JP2005296733A - 触媒の製造方法 - Google Patents
触媒の製造方法 Download PDFInfo
- Publication number
- JP2005296733A JP2005296733A JP2004113507A JP2004113507A JP2005296733A JP 2005296733 A JP2005296733 A JP 2005296733A JP 2004113507 A JP2004113507 A JP 2004113507A JP 2004113507 A JP2004113507 A JP 2004113507A JP 2005296733 A JP2005296733 A JP 2005296733A
- Authority
- JP
- Japan
- Prior art keywords
- metal
- supported
- catalyst
- colloid
- amount
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 239000003054 catalyst Substances 0.000 title claims abstract description 69
- 238000004519 manufacturing process Methods 0.000 title claims description 9
- 229910052751 metal Inorganic materials 0.000 claims abstract description 106
- 239000002184 metal Substances 0.000 claims abstract description 106
- 239000000084 colloidal system Substances 0.000 claims abstract description 75
- 239000002245 particle Substances 0.000 claims abstract description 36
- 230000003197 catalytic effect Effects 0.000 claims abstract description 29
- 239000011148 porous material Substances 0.000 claims abstract description 28
- 239000003223 protective agent Substances 0.000 claims abstract description 21
- 238000000034 method Methods 0.000 claims abstract description 18
- 238000011068 loading method Methods 0.000 claims abstract description 10
- 238000005470 impregnation Methods 0.000 abstract description 9
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 64
- 239000007789 gas Substances 0.000 description 40
- 239000000843 powder Substances 0.000 description 33
- 239000000243 solution Substances 0.000 description 27
- 229910000510 noble metal Inorganic materials 0.000 description 23
- 238000001179 sorption measurement Methods 0.000 description 12
- 238000012360 testing method Methods 0.000 description 10
- 238000006243 chemical reaction Methods 0.000 description 9
- 238000009826 distribution Methods 0.000 description 9
- 239000000203 mixture Substances 0.000 description 9
- 229910018072 Al 2 O 3 Inorganic materials 0.000 description 8
- 239000007864 aqueous solution Substances 0.000 description 8
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 7
- 229910052697 platinum Inorganic materials 0.000 description 7
- 239000002131 composite material Substances 0.000 description 6
- 239000002244 precipitate Substances 0.000 description 6
- 239000011164 primary particle Substances 0.000 description 6
- 239000010948 rhodium Substances 0.000 description 6
- 229920006395 saturated elastomer Polymers 0.000 description 6
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 5
- 239000012298 atmosphere Substances 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- 238000001816 cooling Methods 0.000 description 5
- 230000007246 mechanism Effects 0.000 description 5
- 229910052760 oxygen Inorganic materials 0.000 description 5
- 229910052703 rhodium Inorganic materials 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- 238000001514 detection method Methods 0.000 description 4
- 230000000694 effects Effects 0.000 description 4
- 239000010419 fine particle Substances 0.000 description 4
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 4
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 4
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 4
- 239000011163 secondary particle Substances 0.000 description 4
- 239000006228 supernatant Substances 0.000 description 4
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 3
- HSJPMRKMPBAUAU-UHFFFAOYSA-N cerium(3+);trinitrate Chemical compound [Ce+3].[O-][N+]([O-])=O.[O-][N+]([O-])=O.[O-][N+]([O-])=O HSJPMRKMPBAUAU-UHFFFAOYSA-N 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 238000009792 diffusion process Methods 0.000 description 3
- 239000006185 dispersion Substances 0.000 description 3
- 235000019441 ethanol Nutrition 0.000 description 3
- 239000000706 filtrate Substances 0.000 description 3
- 239000001301 oxygen Substances 0.000 description 3
- 229910052763 palladium Inorganic materials 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 239000003507 refrigerant Substances 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- 229910002651 NO3 Inorganic materials 0.000 description 2
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 2
- MCMNRKCIXSYSNV-UHFFFAOYSA-N Zirconium dioxide Chemical compound O=[Zr]=O MCMNRKCIXSYSNV-UHFFFAOYSA-N 0.000 description 2
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 2
- 235000011114 ammonium hydroxide Nutrition 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 229910052739 hydrogen Inorganic materials 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 2
- 238000012795 verification Methods 0.000 description 2
- BNGXYYYYKUGPPF-UHFFFAOYSA-M (3-methylphenyl)methyl-triphenylphosphanium;chloride Chemical compound [Cl-].CC1=CC=CC(C[P+](C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 BNGXYYYYKUGPPF-UHFFFAOYSA-M 0.000 description 1
- NGDQQLAVJWUYSF-UHFFFAOYSA-N 4-methyl-2-phenyl-1,3-thiazole-5-sulfonyl chloride Chemical compound S1C(S(Cl)(=O)=O)=C(C)N=C1C1=CC=CC=C1 NGDQQLAVJWUYSF-UHFFFAOYSA-N 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonium chloride Substances [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 1
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- 229920002873 Polyethylenimine Polymers 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 229920002125 Sokalan® Polymers 0.000 description 1
- DGEZNRSVGBDHLK-UHFFFAOYSA-N [1,10]phenanthroline Chemical compound C1=CN=C2C3=NC=CC=C3C=CC2=C1 DGEZNRSVGBDHLK-UHFFFAOYSA-N 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 238000004220 aggregation Methods 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-N ammonia Natural products N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 239000003945 anionic surfactant Substances 0.000 description 1
- 235000011089 carbon dioxide Nutrition 0.000 description 1
- 239000003093 cationic surfactant Substances 0.000 description 1
- CETPSERCERDGAM-UHFFFAOYSA-N ceric oxide Chemical compound O=[Ce]=O CETPSERCERDGAM-UHFFFAOYSA-N 0.000 description 1
- 229910000422 cerium(IV) oxide Inorganic materials 0.000 description 1
- 230000000536 complexating effect Effects 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 150000004696 coordination complex Chemical class 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 238000005238 degreasing Methods 0.000 description 1
- 238000003795 desorption Methods 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 238000010304 firing Methods 0.000 description 1
- -1 for example Substances 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- QOSATHPSBFQAML-UHFFFAOYSA-N hydrogen peroxide;hydrate Chemical compound O.OO QOSATHPSBFQAML-UHFFFAOYSA-N 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- 150000002605 large molecules Chemical class 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 229910052748 manganese Inorganic materials 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 150000002736 metal compounds Chemical class 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 230000003472 neutralizing effect Effects 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- UJVRJBAUJYZFIX-UHFFFAOYSA-N nitric acid;oxozirconium Chemical compound [Zr]=O.O[N+]([O-])=O.O[N+]([O-])=O UJVRJBAUJYZFIX-UHFFFAOYSA-N 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 239000004584 polyacrylic acid Substances 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 229920006316 polyvinylpyrrolidine Polymers 0.000 description 1
- 238000010992 reflux Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- MHOVAHRLVXNVSD-UHFFFAOYSA-N rhodium atom Chemical compound [Rh] MHOVAHRLVXNVSD-UHFFFAOYSA-N 0.000 description 1
- 238000007788 roughening Methods 0.000 description 1
- 238000009738 saturating Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 229910052723 transition metal Inorganic materials 0.000 description 1
- 150000003624 transition metals Chemical class 0.000 description 1
- 229910052721 tungsten Inorganic materials 0.000 description 1
Images
Landscapes
- Exhaust Gas Treatment By Means Of Catalyst (AREA)
- Catalysts (AREA)
Abstract
【課題】金属コロイドを用いて含浸法で担持したとしても、触媒金属を高分散で担持できるようにする。
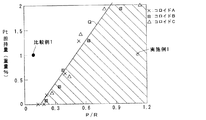
【解決手段】金属コロイドにおける触媒金属に対する保護剤の重量比(保護剤重量/触媒金属重量)をRと表し、担体における金属コロイドの粒径より大きな径をもつ細孔の積分細孔容積(cc/g)をPと表したとき、比P/Rと目的とする触媒金属の担持量との関係が図1に示す斜線の範囲となるように担体と金属コロイドを組み合わせて触媒金属を担体に吸着担持する。
比P/Rが触媒金属の担持量と正の相関関係を有するので、担体と金属コロイドとの組み合わせが最適化され、用いる金属コロイドのほぼ全量が吸着担持される。
【選択図】 なし
【解決手段】金属コロイドにおける触媒金属に対する保護剤の重量比(保護剤重量/触媒金属重量)をRと表し、担体における金属コロイドの粒径より大きな径をもつ細孔の積分細孔容積(cc/g)をPと表したとき、比P/Rと目的とする触媒金属の担持量との関係が図1に示す斜線の範囲となるように担体と金属コロイドを組み合わせて触媒金属を担体に吸着担持する。
比P/Rが触媒金属の担持量と正の相関関係を有するので、担体と金属コロイドとの組み合わせが最適化され、用いる金属コロイドのほぼ全量が吸着担持される。
【選択図】 なし
Description
本発明は、自動車の排ガス浄化用触媒などを製造するにあたり、多孔質酸化物よりなる担体に金属コロイドを用いて触媒金属を担持する方法に関する。
自動車エンジンの排ガスを浄化する排ガス浄化用触媒として、アルミナ( Al2O3)などの多孔質酸化物よりなる担体に白金(Pt)、ロジウム(Rh)、パラジウム(Pd)などの貴金属を担持した触媒が広く用いられている。例えば三元触媒は、γ-Al2O3などの多孔質酸化物にPtやRhを担持してなり、排ガス中のHC及びCOを酸化して浄化するとともに、排ガス中のNOx を還元して浄化するものである。
この三元触媒などの排ガス浄化用触媒では、貴金属の塩化物、貴金属のニトロ錯体、貴金属のアンモニウム錯体などの水溶液に、粉末状あるいはハニカム基材にコートされた状態の多孔質酸化物担体を接触させ、その後乾燥・焼成することで貴金属を担持している。このような担持方法で担持された貴金属は、原子状にきわめて高分散に担持され、その触媒はきわめて高い触媒活性を有している。
ところが従来の排ガス浄化用触媒においては、使用初期は高い触媒活性を示すものの、経時により徐々に触媒活性が低下するという不具合があった。この不具合は、リーンバーンエンジンからの排ガスを浄化する触媒などに特に顕著に現れ、これまでの研究から経時による触媒活性低下の原因は、使用中に貴金属、特にPtが酸素過剰の高温のリーン雰囲気中で著しく粒成長し、表面積の低下により触媒活性点が減少することに起因するものであることがわかっている。
すなわち従来の触媒では、例えばPtが原子状に高分散担持されているため、以下に示す二つの機構により粒成長が生じると考えられる。
(1)高温で酸素過剰のリーン雰囲気では、Ptは酸化されて揮発性のPtO2となり、担持位置から離脱・拡散して他のPt原子又はPt微粒子に捕捉されるために粒成長が生じる。
(2)例えばPtとAl2O3とは親和力が小さいために、Al2O3 担体表面をPt原子又はPt微粒子が移動し易く、衝突・融合を繰り返して粒成長が生じる。
(1)高温で酸素過剰のリーン雰囲気では、Ptは酸化されて揮発性のPtO2となり、担持位置から離脱・拡散して他のPt原子又はPt微粒子に捕捉されるために粒成長が生じる。
(2)例えばPtとAl2O3とは親和力が小さいために、Al2O3 担体表面をPt原子又はPt微粒子が移動し易く、衝突・融合を繰り返して粒成長が生じる。
上記の機構のうち(1)においては、PtO2の離脱・拡散はその蒸気圧に依存し、蒸気圧の大きな微細粒子ほど離脱・拡散し易く、それが粒成長して蒸気圧の小さい粗化粒子となることで安定するため粒成長が生じる。したがってPt粒子を予め離脱・拡散しにくい粒径で担持すれば、粒成長を抑制することができる。このような粒径をもつ原子団は、一般にクラスタと呼ばれている。
一方(2)の機構においては、PtとAl2O3との親和力を高めることで粒成長を抑制することができる。
そこで特開平11−151436号公報には触媒用金属コロイドが記載され、国際公開WO1999/032223号公報には、貴金属を複合貴金属コロイドの状態で担持した触媒が記載されている。この触媒によれば、貴金属は10〜数1000の原子が集まった貴金属クラスタ粒子として担持されているため、原子状で担持された従来の触媒に比べて高温で酸素過剰のリーン雰囲気におけるPtO2の離脱・拡散が抑制される。これにより上記(1)の機構による粒成長が抑制される。
また、貴金属は複数種の貴金属が複合化した複合貴金属コロイドの状態で担持されている。したがって、例えばPtとRh、あるいはPtとPdとを複合化することにより、Al2O3 などの担体と親和力の大きな Rh2O3、 RhO、PdOなどが生成する。また複合貴金属クラスタとAl2O3 との親和力も大きい。したがって複合貴金属クラスタが担体上を移動するのが抑制され、(2)の機構による粒成長が抑制される。
ところが貴金属コロイドを用いて含浸法で貴金属を担持した場合には、担体種と貴金属コロイドの組み合わせによっては、担持された貴金属の分散性が低くなり所望の浄化活性が得られないという問題があった。
特開平11−151436号
国際公開WO1999/032223号
本発明は上記した事情に鑑みてなされたものであり、金属コロイドを用いて含浸法で担持したとしても触媒金属を高分散で担持できるようにすることを解決すべき課題とする。
上記課題を解決する本発明の触媒の製造方法の特徴は、多孔質酸化物よりなる担体に保護剤と触媒金属とよりなる金属コロイドを用いて触媒金属を担持する方法であって、金属コロイドにおける触媒金属に対する保護剤の重量比(保護剤重量/触媒金属重量)をRと表し、担体における金属コロイドの粒径より大きな径をもつ細孔の積分細孔容積(cc/g)をPと表したとき、比P/Rと目的とする触媒金属の担持量との関係が図1に示す斜線の範囲となるように担体と金属コロイドを組み合わせて触媒金属を担体に吸着担持することにある。
比P/Rと目的とする触媒金属の担持量との関係が、図1に示す直線Qの範囲となるように担体と金属コロイドを組み合わせることが望ましい。
なお図1においては、触媒金属担持量が2重量%までしか図示していないが、触媒金属担持量をさらに多くする場合には、直線Qを延長するとともに斜線の範囲をその下側に同様に延長すればよい。
本発明の触媒の製造方法によれば、担体と金属コロイドとの組み合わせが最適化されるため、用いる金属コロイドのほぼ全量を吸着担持することができる。したがって含浸法を用いて担持しても、ほぼ全量が吸着担持されるため、触媒金属はほぼ全量が担体の細孔に担持されることになり高分散で担持することができる。
金属コロイドを用いて吸着法で触媒金属を担持する場合、金属錯体水溶液を用いる場合と同様に、触媒金属は担体の表面に担持される。担体表面とは酸化物担体の一次粒子の表面であるが、一次粒子は凝集して二次粒子を形成しているから、触媒金属は二次粒子間及び一次粒子間の細孔に担持される。しかし一次粒子間の細孔は二次粒子間の細孔より細孔径が小さく、約15nm以上の粒径をもつ金属コロイドは一次粒子間の細孔には物理的に進入できないので、吸着担持され得ないことになる。
そのため金属コロイドを用いて含浸法で触媒金属を担持した場合には、吸着担持される触媒金属が少ないために、担体の表面に触媒金属が集中して付着担持され、それによって分散性が低下すると考えられる。
吸着法とは、金属コロイド溶液と担体とを所定時間接触させ、濾過した後に焼成する担持方法をいう。担持される部位は、上記したように一次粒子間あるいは二次粒子間の細孔内である。濾液中には吸着されなかった金属コロイドが存在する場合があり、それを分析することで吸着担持された量を知ることができる。また含浸法とは、金属コロイドの溶液を担体に含浸させそのまま蒸発乾固して焼成する担持方法をいう。この場合は金属コロイド溶液中の金属コロイドは全量が担持され、担持される部位は細孔内に限らない。
金属コロイドとは、溶媒に不溶な1〜 100nmの金属が溶液中に分散、懸濁した状態をいい、一般に溶媒が液体である金属コロイド溶液として用いられている。金属コロイドは、金属クラスタと、これを溶液中で安定に分散させるための保護剤とから構成されている。
この保護剤は、コロイド溶液中で金属クラスタの周辺に化学的または物理的に結合、吸着することで金属クラスタどうしの凝集を抑制し、粒径分布を適正範囲に制御し安定化させる。したがって保護剤を添加することで、細かな粒径の金属クラスタが懸濁した状態を維持し、触媒製造においては触媒粒子の粒径を小さくして触媒の有効表面積を可能な限り大きくすることができるようになる。
そして本発明者らの研究によれば、触媒金属に対する保護剤の比(保護剤/触媒金属)Rによって金属コロイドの粒径を制御できることが見出された。すなわちRが大きいほど金属コロイドの粒径が小さくなることが明らかとなった。したがって金属コロイドの粒径を任意に調整することが可能になり、さらに研究を進めた結果、担体における金属コロイドの粒径より大きな径をもつ細孔の積分細孔容積をPとしたとき、比P/Rが触媒金属の担持量と正の相関関係を有することが明らかとなった。本発明はこの発見に基づいてなされたものである。
すなわち本発明では、金属コロイドにおける触媒金属に対する保護剤の重量比(保護剤重量/触媒金属重量)をRと表し、担体における金属コロイドの粒径より大きな径をもつ細孔の積分細孔容積(cc/g)をPと表したとき、比P/Rと目的とする触媒金属の担持量との関係が図1に示す斜線の範囲となるように担体と金属コロイドを組み合わせ、触媒金属を担体に吸着担持することとしている。比P/Rと目的とする触媒金属の担持量との関係が図1に示す斜線の範囲を超えた組成で含浸法により担持すると、吸着担持される触媒金属量が少なくなるために、担持された触媒金属の分散性が低下し活性が低下する。
多孔質酸化物としては、アルミナ、セリア、チタニア、ジルコニア、シリカなどから選ばれる少なくとも一種、あるいはこれらから選ばれる複数種の複合酸化物など、従来用いられているものを用いることができる。
金属コロイドとしては、Pt、Rh、Pdなどの貴金属、あるいはFe、Co、Ni、Cu、W、Mnなどの遷移金属から選ばれる触媒金属を金属クラスタとして含むものを用いることができる。複数種の触媒金属を含む複合金属コロイドを用いることもできる。
保護剤としては、ポリビニルピロリドン、ポリビニルアルコール、ポリアクリル酸、ポリエチレンイミンなどの高分子化合物、金属イオンへの配位作用を有するクエン酸、トリフェニルホスフィン、フェナントロリン、テトラメテルアンモニウム塩などの低分子化合物などが例示される。金属コロイド溶液中で金属クラスタを安定させる作用に優れたポリビニルピロリドンが特に好ましい。
触媒金属に対する保護剤の重量比(保護剤重量/触媒金属重量)Rは、目的に応じて種々選択することができる。Rが大きいほど金属コロイドの粒径が小さくなるので、用いる担体の細孔分布に応じて金属コロイドの粒径を決定しそれに応じてRを決定する、あるいはRに対応する金属コロイドの粒径に応じて細孔分布を鑑みて担体を決定すればよい。
例えば目的とする粒径をもつ貴金属コロイドを製造するには、可溶性の貴金属化合物とコロイドの保護剤とを任意の組成でコロイド溶液を調製する工程と、得られたコロイド溶液を構成するコロイド粒子の粒径を測定する工程と、を含む開始ステップと、
開始ステップで得られた粒径が目的の粒径より大きい場合には保護剤の組成割合を相対的に増やし、逆に粒径が目的の粒径より小さい場合には保護剤の組成割合を相対的に減じて再度コロイド溶液を調製する工程と、得られたコロイド溶液を構成するコロイド粒子の粒径を測定する工程と、を含む検証ステップと、
目的の粒径に到達するまで検証ステップを繰り返す再検証ステップと、目的の粒径が得られたときのRでコロイド溶液を調製する製造ステップと、を行うことができる。
開始ステップで得られた粒径が目的の粒径より大きい場合には保護剤の組成割合を相対的に増やし、逆に粒径が目的の粒径より小さい場合には保護剤の組成割合を相対的に減じて再度コロイド溶液を調製する工程と、得られたコロイド溶液を構成するコロイド粒子の粒径を測定する工程と、を含む検証ステップと、
目的の粒径に到達するまで検証ステップを繰り返す再検証ステップと、目的の粒径が得られたときのRでコロイド溶液を調製する製造ステップと、を行うことができる。
本発明では、比P/Rと目的とする触媒金属の担持量との関係が図1に示す斜線の範囲となるように担体と金属コロイドを組み合わせている。図1に示す直線Qは、触媒金属の飽和吸着担持量を意味している。したがって比P/Rと目的とする触媒金属の担持量との関係が図1に示す斜線の範囲を超えると、触媒金属の吸着担持量が飽和するため、それ以上の濃度で金属コロイドを含む場合には過剰の金属コロイドが含まれているので、含浸法で担持するとその分によって担持された触媒金属の分散性が低下する。図1に示す斜線の範囲内であれば、触媒金属は全て吸着によって担持されるので、確実に高分散担持することができる。
以下、試験例、実施例及び比較例により本発明を具体的に説明する。
(試験例1)
特許文献1の第1実施形態の記載に従って、ポリビニルピロリドンとPtの重量比R(ポリビニルピロリドン重量/Pt重量)が 2.5、1.25、1の3種類のPtコロイド溶液(A,B,C)を調製した。
特許文献1の第1実施形態の記載に従って、ポリビニルピロリドンとPtの重量比R(ポリビニルピロリドン重量/Pt重量)が 2.5、1.25、1の3種類のPtコロイド溶液(A,B,C)を調製した。
代表例として重量比Rが 2.5のPtコロイドの合成方法を説明する。まず、22gのシス−ジアンミンジアクア白金(II)硝酸塩と 2.5gのポリビニルピロリドン(K-30)を1000mlの水に溶解した。この溶解液に 250mlのエチルアルコールを加え、水分の蒸発およびエチルアルコールの揮散を防止するため還流冷却器を用いて、11時間の還流を行った。このようにしてポリビニルピロリドン保護Ptコロイド溶液を得た。
得られたそれぞれのPtコロイド溶液(A,B,C)中のPtコロイドの粒子径をナノトラック粒度分布測定装置(「UPA−150EX」日機装社製)にて測定したところ、表1に示すように、粒子径はそれぞれ17.2nm、33.9nm、39.4nmであった。
得られた沈殿物を遠心分離器にかけて上澄み液を捨て、これに捨てた上澄み液と同量のイオン交換水を加えて撹拌し再び遠心分離器にかけた。この操作をさらに2回行うことにより、沈殿物を洗浄した。
最後に上澄み液を捨てた後の沈殿物を再び3リットルのビーカに移し、所定量のイオン交換水を加えてプロペラ撹拌器とホモジナイザを用いて撹拌した。そこへ陽イオン性界面活性剤(「アーマック」ライオン社製)と陰イオン性界面活性剤(「アーモフロー」ライオン社製)を加え、さらに5分間撹拌した。
この分散液を遠心分離器にかけ、沈殿物を洗浄した。最後に上澄み液を捨てた後の沈殿物を、脱脂炉を用い大気中にて 400℃で5時間焼成し、さらに大気中 700℃で5時間焼成してCeO2−ZrO2−Y2O3担体粉末を調製した。界面活性剤の添加量を調製することで、細孔分布が異なる3種類の担体粉末(1,2,3)を調製した。
また所定濃度の硝酸セリウム(III)の水溶液と、所定濃度のオキシ硝酸ジルコニルの水容液及び所定濃度の硝酸アルミニウムの水溶液をそれぞれ調製し、この3種の水溶液とセリウムイオンの 1.1倍モルのH2O2を含む過酸化水素水を混合して充分に撹拌した。モル比Al/Ce/Zrは5/3/2である。
この混合水溶液に全ての硝酸根を中和できる量の 1.2倍モルの NH3を含むアンモニア水を添加し、メカニカルスターラー及びホモジナイザで1時間撹拌した。得られた共沈物(酸化物前駆体)を濾過・洗浄し、大気中にて 300℃で3時間乾燥し、さらに 500℃で1時間焼成した。
得られた酸化物粉末を、H2を5%含むN2気流中にて 700℃で5時間還元処理し、 Al2O3−CeO2−ZrO2担体粉末を調製した。ホモジナイザによる撹拌時間を調製することで、細孔分布が異なる2種類の担体粉末(4,5)を調製した。各担体粉末(1〜5)の細孔分布を図2に示す。なお細孔容積は水銀ポロシメータにより測定し、図2には各細孔径に対する積分細孔容積を示している。
全てのPtが担持された場合にPt担持量が2重量%となるように、3種類のPtコロイド溶液(A,B,C)と5種類の担体粉末(1〜5)をそれぞれ秤量し、試験管中で総当たり(3×5=15通り)に混合してそれぞれ24時間放置した。その後メンブランフィルタで濾過し、濾液中のPt量をICP(「ICPS−2000」島津製作所(株)製)でそれぞれ定量した。そして用いたPtコロイド溶液中のPt量と濾液中のPt量との差から、各担体粉末に担持されたPt量をそれぞれ算出した。このPt担持量は、吸着によって担持されるPt吸着担持量が飽和した値であり、Pt飽和吸着担持量という。
図2に示す各担体粉末の細孔分布と各Ptコロイドの粒子径とから、各Ptコロイド粒子径より大きな細孔の積分容積を算出してP値とし、各Ptコロイド溶液の重量比R値に対する比(P/R)をそれぞれ算出した。そして比(P/R)を横軸に、Pt担持量(重量%)を縦軸に取って各値をプロットし、結果を図1に示す。
図1から、比(P/R)とPt飽和吸着担持量とは直線Qの関係にあり、きわめて良い相関を示していることがわかる。すなわち、図1に示す斜線の範囲内であれば、Ptコロイドは全て吸着によって担持されることになる。なおPtコロイド溶液Cと担体粉末3との組み合わせでは、試験管中のPtコロイドが全て担体粉末3に吸着担持されても、担体粉末3にはさらに吸着担持できる余力があるため、図1の直線から外れている。
(実施例1)
試験例で用いたPtコロイド溶液Cと担体粉末3との組み合わせでは、Pt飽和吸着担持量は2重量%以上であった。そこで全てのPtが担持された場合にPt担持量が1重量%となるように、Ptコロイド溶液Cと担体粉末3をそれぞれ秤量し、試験管中で24時間放置した。Pt担持量が1重量%となるのは、図1に◎で示すように斜線の範囲にある。その後、混合物をそのまま蒸発・乾固し、 250℃で1時間焼成して実施例1の触媒粉末を調製した。
試験例で用いたPtコロイド溶液Cと担体粉末3との組み合わせでは、Pt飽和吸着担持量は2重量%以上であった。そこで全てのPtが担持された場合にPt担持量が1重量%となるように、Ptコロイド溶液Cと担体粉末3をそれぞれ秤量し、試験管中で24時間放置した。Pt担持量が1重量%となるのは、図1に◎で示すように斜線の範囲にある。その後、混合物をそのまま蒸発・乾固し、 250℃で1時間焼成して実施例1の触媒粉末を調製した。
(比較例1)
試験例で用いたPtコロイド溶液Aと担体粉末1との組み合わせでは、Pt飽和吸着担持量は0重量%であった。そこで全てのPtが担持された場合にPt担持量が1重量%となるように、Ptコロイド溶液Aと担体粉末1をそれぞれ秤量し、試験管中で24時間放置した。Pt担持量が1重量%となるのは、図1に●で示すように斜線の範囲外にある。その後、混合物をそのまま蒸発・乾固し、 250℃で1時間焼成して比較例1の触媒粉末を調製した。
試験例で用いたPtコロイド溶液Aと担体粉末1との組み合わせでは、Pt飽和吸着担持量は0重量%であった。そこで全てのPtが担持された場合にPt担持量が1重量%となるように、Ptコロイド溶液Aと担体粉末1をそれぞれ秤量し、試験管中で24時間放置した。Pt担持量が1重量%となるのは、図1に●で示すように斜線の範囲外にある。その後、混合物をそのまま蒸発・乾固し、 250℃で1時間焼成して比較例1の触媒粉末を調製した。
(試験例2)
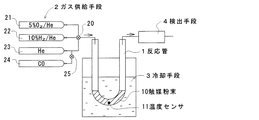
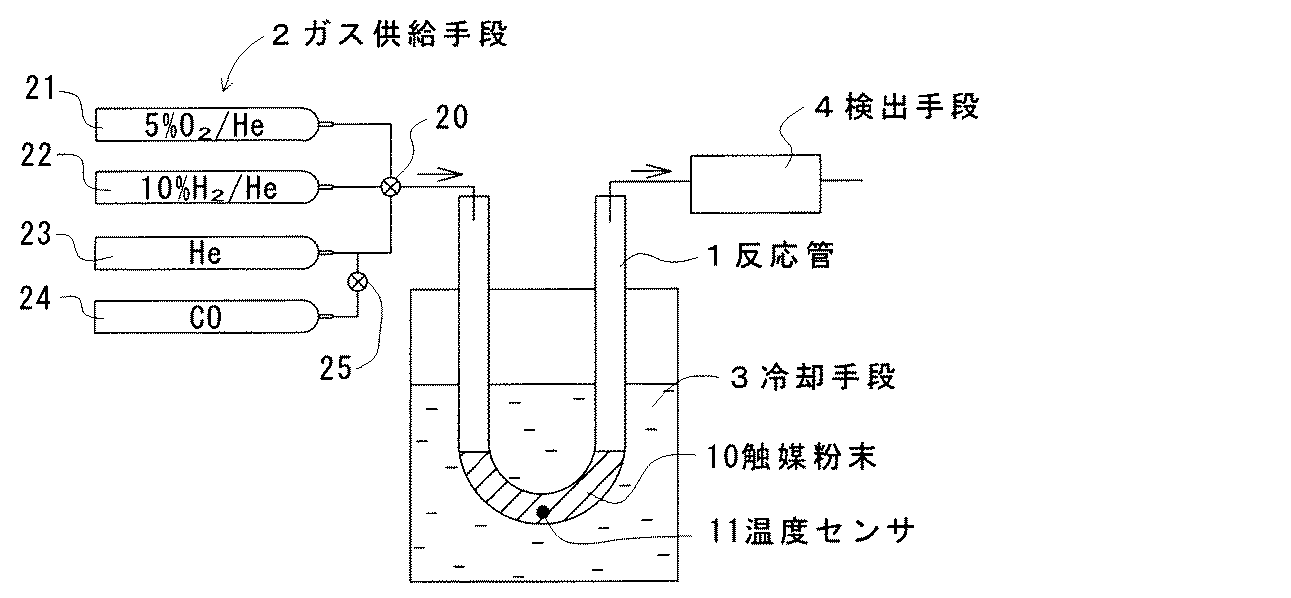
実施例1及び比較例1の触媒粉末について、図3に示す測定装置を用いてPt分散性を測定した。この測定装置は、反応管1と、ガス供給手段2と、冷却手段3と、検出手段4と、からなる。反応管1は石英ガラス製のU字形の筒状をなし、内部に触媒粉末10が詰められている。反応管1には温度センサ11が設けられ、触媒粉末10の温度を検出可能とされている。
実施例1及び比較例1の触媒粉末について、図3に示す測定装置を用いてPt分散性を測定した。この測定装置は、反応管1と、ガス供給手段2と、冷却手段3と、検出手段4と、からなる。反応管1は石英ガラス製のU字形の筒状をなし、内部に触媒粉末10が詰められている。反応管1には温度センサ11が設けられ、触媒粉末10の温度を検出可能とされている。
ガス供給手段2は4種のガスボンベ21〜24からなり、切替コック20を介して反応管1の一端開口に接続されている。ガスボンベ21には5%のO2を含むHeガスが充填され、ガスボンベ22には10%のH2を含むHeガスが充填され、ガスボンベ23にはHeガスが充填され、ガスボンベ24にはCOガスが充填されている。またガスボンベ24は、切替コック25を介してガスボンベ23のガス流路に接続されている。
冷却手段3は、エタノールにドライアイスを投入することで約−80℃に冷却された冷媒が入れられた容器からなり、反応管1の触媒粉末10が詰められた部分が冷媒中に浸漬されている。また反応管1の他端はガスクロマトグラフと質量分析計からなる検出手段4に連結され、出ガス中のCO濃度を定量可能とされている。
先ず、冷却手段3に代えてヒータを配置した。次に実施例1及び比較例1の触媒粉末のそれぞれ 0.5gを反応管1内にそれぞれ詰め、ガスボンベ23からHeガスを30ml/分の流量で流通させながら、ヒーターで触媒粉末10の温度が 400℃となるように加熱した。触媒粉末10の温度を 400℃に保持した状態で、ガスボンベ21からO2を5%含むHeガスを15分間供給し、続いてガスボンベ22からH2を10%含むHeガスを15分間供給し、その後ガスボンベ23からHeガスを15分間供給する前処理を行った。いずれもガス流量は30ml/分である。
この前処理後にヒータを除去し、ガスボンベ23からHeガスを30ml/分の流量で流通させながら触媒粉末10を冷却した。触媒粉末10の温度が室温付近になった時点で、冷却手段3を配置して反応管1を冷媒中に浸漬し、触媒粉末10をさらに冷却した。
触媒粉末10の温度が−78℃になった状態で、ガスボンベ24から所定量のCOガスをHeキャリア中にパルス状に供給し、そのときの出ガス中のCO濃度を検出手段4で測定し、出ガス中のCO量を算出した。そして供給されたCO量と出ガス中のCO量との差分から触媒粉末10によるCO吸着量を算出した。さらにCO吸着量からCOの吸着に関わった活性Pt量を算出し、触媒粉末 0.5gに担持されているPtの全量に対する活性Pt量の割合をPt分散性として算出した。算出されたPt分散性を表2に示す。
本発明の触媒の製造方法は、酸化触媒、三元触媒、NOx 吸蔵還元触媒などの自動車の排ガス浄化用触媒ばかりでなく、金属コロイド溶液を用いて触媒金属を担持する場合全てに利用することができる。
1:反応管 2:ガス供給手段 3:冷却手段
4:検出手段 10:触媒粉末
4:検出手段 10:触媒粉末
Claims (2)
- 多孔質酸化物よりなる担体に保護剤と触媒金属とよりなる金属コロイドを用いて該触媒金属を担持する方法であって、該金属コロイドにおける該触媒金属に対する該保護剤の重量比(保護剤重量/触媒金属重量)をRと表し、該担体における該金属コロイドの粒径より大きな径をもつ細孔の積分細孔容積(cc/g)をPと表したとき、比P/Rと目的とする該触媒金属の担持量との関係が図1に示す斜線の範囲となるように該担体と該金属コロイドを組み合わせて該触媒金属を該担体に吸着担持することを特徴とする触媒の製造方法。
- 前記比P/Rと目的とする前記触媒金属の担持量との関係が、図1に示す直線Qの範囲となるように前記担体と前記金属コロイドを組み合わせる請求項1に記載の触媒の製造方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004113507A JP2005296733A (ja) | 2004-04-07 | 2004-04-07 | 触媒の製造方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004113507A JP2005296733A (ja) | 2004-04-07 | 2004-04-07 | 触媒の製造方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005296733A true JP2005296733A (ja) | 2005-10-27 |
Family
ID=35328931
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004113507A Pending JP2005296733A (ja) | 2004-04-07 | 2004-04-07 | 触媒の製造方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005296733A (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006055748A (ja) * | 2004-08-20 | 2006-03-02 | Tanaka Kikinzoku Kogyo Kk | 触媒の製造方法 |
| WO2008054026A1 (en) | 2006-11-01 | 2008-05-08 | Toyota Jidosha Kabushiki Kaisha | Automobile exhaust gas purifying catalyst and method for producing the same |
| WO2008069003A1 (ja) * | 2006-12-05 | 2008-06-12 | Tanaka Kikinzoku Kogyo K. K. | 排ガス浄化用触媒及びその製造方法 |
-
2004
- 2004-04-07 JP JP2004113507A patent/JP2005296733A/ja active Pending
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2006055748A (ja) * | 2004-08-20 | 2006-03-02 | Tanaka Kikinzoku Kogyo Kk | 触媒の製造方法 |
| WO2008054026A1 (en) | 2006-11-01 | 2008-05-08 | Toyota Jidosha Kabushiki Kaisha | Automobile exhaust gas purifying catalyst and method for producing the same |
| US8288310B2 (en) | 2006-11-01 | 2012-10-16 | Toyota Jidosha Kabushiki Kaisha | Automobile exhaust gas purification catalyst and method of production of same |
| WO2008069003A1 (ja) * | 2006-12-05 | 2008-06-12 | Tanaka Kikinzoku Kogyo K. K. | 排ガス浄化用触媒及びその製造方法 |
| KR100965738B1 (ko) | 2006-12-05 | 2010-06-24 | 다나까 홀딩스 가부시끼가이샤 | 배기가스 정화용 촉매 및 그 제조방법 |
| US7781367B2 (en) * | 2006-12-05 | 2010-08-24 | Tanaka Kikinzoku Kogyo K.K. | Exhaust gas cleaning catalyst and process for producing the same |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP4006976B2 (ja) | 複合酸化物粉末とその製造方法及び触媒 | |
| JP5889756B2 (ja) | 排気ガス浄化用触媒担体 | |
| JP4465352B2 (ja) | 排ガス浄化触媒 | |
| JPWO2009001962A1 (ja) | 排ガス浄化触媒担体の製造方法および排ガス浄化触媒担体 | |
| JP2006055748A (ja) | 触媒の製造方法 | |
| JP2012239982A (ja) | 内燃機関の排気浄化用触媒 | |
| JP4346215B2 (ja) | 排ガス浄化触媒の製造方法 | |
| JP3997783B2 (ja) | 触媒担体の製造方法 | |
| CN104114276B (zh) | 利用贱金属的排气净化催化剂系统及其控制方法 | |
| JP2013169480A (ja) | メタン酸化触媒およびその製造方法 | |
| JP5706476B2 (ja) | 一酸化炭素酸化触媒、及びその製造方法 | |
| JP5503155B2 (ja) | 一酸化炭素除去フィルター | |
| JP2005296733A (ja) | 触媒の製造方法 | |
| JP5299603B2 (ja) | 酸化物複合体前駆体水溶液、酸化物複合体の製造方法、酸化物複合体、その酸化物複合体を備える排ガス浄化用触媒及びその排ガス浄化用触媒を用いた排ガス浄化方法 | |
| JP2008279319A (ja) | 排ガス浄化用触媒及びそれに用いられる酸性酸化物担持アルミナの製造方法 | |
| JP2013198888A (ja) | 排ガス浄化用触媒担体、それを用いた窒素酸化物浄化用触媒、及びそれらの製造方法 | |
| JP4599817B2 (ja) | NOx吸蔵材の担持方法 | |
| JP4807620B2 (ja) | 排ガス浄化用触媒及びそれを用いた排ガス浄化方法 | |
| JP2006043637A (ja) | 排ガス浄化用触媒 | |
| JP4324856B2 (ja) | 排ガス浄化触媒用担体と触媒 | |
| JP6096818B2 (ja) | 排ガス浄化触媒、その製造方法、及び、それを用いた排ガス浄化方法 | |
| JP2000051705A (ja) | 排ガス浄化用触媒及びその製造方法 | |
| JP2014213272A (ja) | 排気浄化触媒及び排気浄化装置 | |
| JP4737149B2 (ja) | 触媒担体及び触媒 | |
| JP5104352B2 (ja) | 排ガス浄化用触媒 |