JP2005201765A - 固体状の核分裂生成物含有物の核種分離方法 - Google Patents
固体状の核分裂生成物含有物の核種分離方法 Download PDFInfo
- Publication number
- JP2005201765A JP2005201765A JP2004008204A JP2004008204A JP2005201765A JP 2005201765 A JP2005201765 A JP 2005201765A JP 2004008204 A JP2004008204 A JP 2004008204A JP 2004008204 A JP2004008204 A JP 2004008204A JP 2005201765 A JP2005201765 A JP 2005201765A
- Authority
- JP
- Japan
- Prior art keywords
- fission product
- temperature
- oxygen
- solid
- technetium
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
- 230000004992 fission Effects 0.000 title claims abstract description 84
- 239000007787 solid Substances 0.000 title claims abstract description 68
- 238000000034 method Methods 0.000 title claims abstract description 61
- 229910052760 oxygen Inorganic materials 0.000 claims abstract description 90
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 claims abstract description 89
- 239000001301 oxygen Substances 0.000 claims abstract description 89
- 229910052713 technetium Inorganic materials 0.000 claims abstract description 65
- 239000000463 material Substances 0.000 claims abstract description 63
- 229910052750 molybdenum Inorganic materials 0.000 claims abstract description 59
- GKLVYJBZJHMRIY-UHFFFAOYSA-N technetium atom Chemical compound [Tc] GKLVYJBZJHMRIY-UHFFFAOYSA-N 0.000 claims abstract description 45
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 claims abstract description 42
- 239000011733 molybdenum Substances 0.000 claims abstract description 42
- 229910000510 noble metal Inorganic materials 0.000 claims abstract description 41
- 230000003647 oxidation Effects 0.000 claims abstract description 36
- 238000007254 oxidation reaction Methods 0.000 claims abstract description 36
- 230000008569 process Effects 0.000 claims abstract description 25
- 238000010438 heat treatment Methods 0.000 claims abstract description 14
- IOWOAQVVLHHFTL-UHFFFAOYSA-N technetium(vii) oxide Chemical compound [O-2].[O-2].[O-2].[O-2].[O-2].[O-2].[O-2].[Tc+7].[Tc+7] IOWOAQVVLHHFTL-UHFFFAOYSA-N 0.000 claims abstract description 8
- 229910000476 molybdenum oxide Inorganic materials 0.000 claims abstract description 5
- PQQKPALAQIIWST-UHFFFAOYSA-N oxomolybdenum Chemical compound [Mo]=O PQQKPALAQIIWST-UHFFFAOYSA-N 0.000 claims abstract description 5
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 claims description 85
- 239000010948 rhodium Substances 0.000 claims description 82
- 229910052751 metal Inorganic materials 0.000 claims description 66
- 239000002184 metal Substances 0.000 claims description 63
- 229910052707 ruthenium Inorganic materials 0.000 claims description 61
- 229910052763 palladium Inorganic materials 0.000 claims description 57
- 229910052703 rhodium Inorganic materials 0.000 claims description 55
- 238000000926 separation method Methods 0.000 claims description 51
- 238000012958 reprocessing Methods 0.000 claims description 48
- 239000010814 metallic waste Substances 0.000 claims description 36
- 229910052768 actinide Inorganic materials 0.000 claims description 31
- 150000001255 actinides Chemical class 0.000 claims description 31
- 150000003839 salts Chemical class 0.000 claims description 20
- 239000002910 solid waste Substances 0.000 claims description 20
- KJTLSVCANCCWHF-UHFFFAOYSA-N Ruthenium Chemical compound [Ru] KJTLSVCANCCWHF-UHFFFAOYSA-N 0.000 claims description 18
- 239000002915 spent fuel radioactive waste Substances 0.000 claims description 18
- 229910052726 zirconium Inorganic materials 0.000 claims description 17
- QCWXUUIWCKQGHC-UHFFFAOYSA-N Zirconium Chemical compound [Zr] QCWXUUIWCKQGHC-UHFFFAOYSA-N 0.000 claims description 13
- MHOVAHRLVXNVSD-UHFFFAOYSA-N rhodium atom Chemical compound [Rh] MHOVAHRLVXNVSD-UHFFFAOYSA-N 0.000 claims description 12
- 239000002253 acid Substances 0.000 claims description 7
- 229910001338 liquidmetal Inorganic materials 0.000 claims description 7
- 230000001590 oxidative effect Effects 0.000 claims description 7
- 230000000903 blocking effect Effects 0.000 claims description 5
- 230000008016 vaporization Effects 0.000 claims description 4
- 239000000126 substance Substances 0.000 abstract description 7
- 238000012360 testing method Methods 0.000 description 51
- 238000006243 chemical reaction Methods 0.000 description 25
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 20
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 20
- 229910001882 dioxygen Inorganic materials 0.000 description 20
- 239000007789 gas Substances 0.000 description 18
- 239000011261 inert gas Substances 0.000 description 17
- 239000007788 liquid Substances 0.000 description 16
- 230000009467 reduction Effects 0.000 description 13
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 11
- 230000005496 eutectics Effects 0.000 description 11
- 229910017604 nitric acid Inorganic materials 0.000 description 11
- 229910052786 argon Inorganic materials 0.000 description 10
- 239000011521 glass Substances 0.000 description 9
- 150000002739 metals Chemical class 0.000 description 9
- 229910052702 rhenium Inorganic materials 0.000 description 9
- 239000002927 high level radioactive waste Substances 0.000 description 8
- 239000010970 precious metal Substances 0.000 description 8
- 238000002441 X-ray diffraction Methods 0.000 description 7
- 239000002699 waste material Substances 0.000 description 7
- 230000008859 change Effects 0.000 description 6
- 238000004090 dissolution Methods 0.000 description 6
- 239000000446 fuel Substances 0.000 description 6
- 230000005484 gravity Effects 0.000 description 6
- 239000000203 mixture Substances 0.000 description 6
- WUAPFZMCVAUBPE-UHFFFAOYSA-N rhenium atom Chemical compound [Re] WUAPFZMCVAUBPE-UHFFFAOYSA-N 0.000 description 6
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 5
- 229910052778 Plutonium Inorganic materials 0.000 description 4
- 229910000310 actinide oxide Inorganic materials 0.000 description 4
- 238000000354 decomposition reaction Methods 0.000 description 4
- 238000004821 distillation Methods 0.000 description 4
- 239000000843 powder Substances 0.000 description 4
- 238000003860 storage Methods 0.000 description 4
- 230000004580 weight loss Effects 0.000 description 4
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 229910052770 Uranium Inorganic materials 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- 238000010586 diagram Methods 0.000 description 3
- 238000001914 filtration Methods 0.000 description 3
- 231100001252 long-term toxicity Toxicity 0.000 description 3
- 239000011159 matrix material Substances 0.000 description 3
- 239000012071 phase Substances 0.000 description 3
- 230000035484 reaction time Effects 0.000 description 3
- 238000011084 recovery Methods 0.000 description 3
- 238000007711 solidification Methods 0.000 description 3
- 230000008023 solidification Effects 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- 229910052793 cadmium Inorganic materials 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 238000005868 electrolysis reaction Methods 0.000 description 2
- 230000008018 melting Effects 0.000 description 2
- 238000002844 melting Methods 0.000 description 2
- 239000011824 nuclear material Substances 0.000 description 2
- 238000009377 nuclear transmutation Methods 0.000 description 2
- SJLOMQIUPFZJAN-UHFFFAOYSA-N oxorhodium Chemical compound [Rh]=O SJLOMQIUPFZJAN-UHFFFAOYSA-N 0.000 description 2
- 229910003445 palladium oxide Inorganic materials 0.000 description 2
- JQPTYAILLJKUCY-UHFFFAOYSA-N palladium(ii) oxide Chemical compound [O-2].[Pd+2] JQPTYAILLJKUCY-UHFFFAOYSA-N 0.000 description 2
- 238000005191 phase separation Methods 0.000 description 2
- OYEHPCDNVJXUIW-UHFFFAOYSA-N plutonium atom Chemical compound [Pu] OYEHPCDNVJXUIW-UHFFFAOYSA-N 0.000 description 2
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M potassium chloride Inorganic materials [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 2
- 239000002994 raw material Substances 0.000 description 2
- 229910003450 rhodium oxide Inorganic materials 0.000 description 2
- 239000007790 solid phase Substances 0.000 description 2
- 238000002076 thermal analysis method Methods 0.000 description 2
- 238000012795 verification Methods 0.000 description 2
- 238000004017 vitrification Methods 0.000 description 2
- 239000003039 volatile agent Substances 0.000 description 2
- 239000013585 weight reducing agent Substances 0.000 description 2
- 229910013618 LiCl—KCl Inorganic materials 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 229910045601 alloy Inorganic materials 0.000 description 1
- 239000000956 alloy Substances 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- BDOSMKKIYDKNTQ-UHFFFAOYSA-N cadmium atom Chemical compound [Cd] BDOSMKKIYDKNTQ-UHFFFAOYSA-N 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 238000012812 general test Methods 0.000 description 1
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 230000033116 oxidation-reduction process Effects 0.000 description 1
- 239000010908 plant waste Substances 0.000 description 1
- 239000001103 potassium chloride Substances 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 239000012857 radioactive material Substances 0.000 description 1
- 238000007670 refining Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000000630 rising effect Effects 0.000 description 1
- VSZWPYCFIRKVQL-UHFFFAOYSA-N selanylidenegallium;selenium Chemical compound [Se].[Se]=[Ga].[Se]=[Ga] VSZWPYCFIRKVQL-UHFFFAOYSA-N 0.000 description 1
- KKCBUQHMOMHUOY-UHFFFAOYSA-N sodium oxide Chemical compound [O-2].[Na+].[Na+] KKCBUQHMOMHUOY-UHFFFAOYSA-N 0.000 description 1
- 229910001948 sodium oxide Inorganic materials 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000000638 solvent extraction Methods 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- JFALSRSLKYAFGM-UHFFFAOYSA-N uranium(0) Chemical compound [U] JFALSRSLKYAFGM-UHFFFAOYSA-N 0.000 description 1
- 238000009834 vaporization Methods 0.000 description 1
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E30/00—Energy generation of nuclear origin
- Y02E30/30—Nuclear fission reactors
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02W—CLIMATE CHANGE MITIGATION TECHNOLOGIES RELATED TO WASTEWATER TREATMENT OR WASTE MANAGEMENT
- Y02W30/00—Technologies for solid waste management
- Y02W30/50—Reuse, recycling or recovery technologies
Landscapes
- Manufacture And Refinement Of Metals (AREA)
Abstract
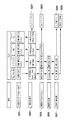
【解決手段】TcとMoを含む固体状の核分裂生成物含有物を不活性雰囲気中で450℃〜600℃に昇温する第1の加熱工程S21と、450℃〜600℃の温度範囲でTcを酸化させて揮発させる酸化工程S22と、揮発した酸化テクネチウムを捕捉するテクネチウム捕捉工程S23と、酸化テクネチウムの揮発後に酸素雰囲気中で650℃以上に昇温しMoを酸化させて気化させる第2の加熱工程S24と、気化した酸化モリブデンを捕捉するモリブデン捕捉工程S25とを備えている。
【選択図】図1
Description
熱分析装置による酸化/還元挙動の観察試験と、ガラス製カラムを用いた反応/揮発の試験の2種類の試験を必要に応じて行った。
幾つかの条件でガラス製カラムでの試験を終えた後のReの分布を表1に示した。表1の1段目の結果でガラス製カラム内に固体が6.4%残留しているのは、試験時間(反応時間)が足りなかった為であると考えた。また、2段目の結果でガラス製カラム内の残留量が42.1%と極めて多いのは、試験温度(反応時間)が低すぎたからであると考えた。3段目の結果で試験時間が長いにもかかわらず残留量が20.0%と多いのは、Arの流量が多く、O2の流量が少なすぎたからであると考えた。これらの結果より、試験温度、試験時間、O2の流量がパラメータになると考えた。即ち、表中最下段(4段目)のように十分な反応時間と反応温度および酸素が存在すれば、レニウムはほぼ全量が揮発してトラップへと移行することが示された。これにより、450℃以上に昇温させてレニウムを酸化させることで、レニウムを実用的な速度で揮発させて分離回収できることが確認された。
Moの酸化と揮発の挙動はまず熱分析装置を用いて調べられた。熱分析ではArを0.15L/分で、酸素を0.10L/分で流しながら徐々に昇温して酸化の著しくなる温度と揮発の著しくなる温度および酸素を絶った場合の挙動を調べた。結果を図6(A)(B)に示す。
Rh単体の試験は熱分析装置を用いて行った。2回の試験の結果を図7(A)(B)に示す。図7(A)に示した試験では昇温の開始前から降温終了までの間、常に0.2L/分の流量のArと0.1L/分の酸素を流していた。Rhは温度が約600℃から酸化し始めた。Rhの酸化物としてはIII価のRh2O3のみが安定であるとされており、この前提に立つと降温を開始した時点の酸化率は約45%で、Rhは一部が酸化され一部が金属で残っていると考えられた。
Pd単体の試験は熱分析装置を用いて行った。2回の試験の結果を図9(A)(B)に示す。図9(A)に示した試験では昇温の開始前から降温終了までの間、常に0.2L/分の流量のArと0.1L/分の酸素を流していた。Pdも約600℃から酸化し始めた。Pdの酸化物としてはII価のPdOのみが安定であるとされているが、この前提に立つと重量が最大になった際の酸化率は約30%で、Pdは一部が酸化され一部が金属で残っていると考えられた。しかしその後、温度が800℃を上回ると重量は急に減少に転じ、数分のうちには原料金属と同じ重量まで低下した。重量減少が原料の重さに達すると同時に終わり以後は定常であったことから、この重量減少は生成した酸化物などの揮発によるものではなく、PdOが高温で不安定になってPdとO2に分解されたものであると考えられた。
Ruの挙動はReと共にガラス製カラムに装荷した試験を行って調べた。試験では525mgのRu金属と500mgのRe金属の粉末をガラスカラムに装荷してまずArを0.15L/分で流しながら450℃まで昇温し、定常に達してから0.1L/分で酸素ガスを流した。この後6時間のあいだ酸素ガスを流しながら450℃に保持し、6時間後に酸素を流すのをやめて同時に降温を開始した。冷却後に調べたところ装荷したReは98%が揮発してトラップに捕捉されていることが分かった。一方で反応容器の中には549mgの固体が残っていた。この固体のXRD観察の結果を図10に示す。
試験は熱分析装置(TG/DTA)に金属Rhの粉を45.3mg装荷して、まず0.15L/分のArガスと0.1L/分の酸素ガスを流しながら昇温し、酸化があるていど進行したところでガスを流したまま降温することで酸化物を得た。温度は約30分で1000℃まで昇温し、この温度で60分間保持したのち降温した。この際の経過時間に対する温度と重量の変化を図11(A)に示す。Rhは全量がRh2O3になった場合を100%とする「酸化率」が約43%になった。
試験は熱分析装置(TG/DTA)に金属Pdの粉を46.9mg装荷して、まず0.15L/分のArガスと0.1L/分の酸素ガスを流しながら昇温し、酸化があるていど進行したところでガスを流したまま降温することで酸化物を得た。温度は約25分で750℃まで昇温し、この温度で60分間保持したのち降温した。この際の経過時間に対する温度と重量の変化を図12(A)に示す。Pdは全量がPdOになった場合を100%とする「酸化率」が約32%になった。
S22 酸化工程
S23 テクネチウム捕捉工程
S24 第2の加熱工程
S25 モリブデン捕捉工程
Claims (10)
- テクネチウムとモリブデンを含む固体状の核分裂生成物含有物を不活性雰囲気中で450℃〜600℃に昇温する第1の加熱工程と、450℃〜600℃の温度範囲で前記テクネチウムを酸化させて揮発させる酸化工程と、揮発した酸化テクネチウムを捕捉するテクネチウム捕捉工程と、酸化テクネチウムの揮発後に酸素雰囲気中で650℃以上に昇温し前記モリブデンを酸化させて気化させる第2の加熱工程と、気化した酸化モリブデンを捕捉するモリブデン捕捉工程とを備えることを特徴とする固体状の核分裂生成物含有物の核種分離方法。
- 前記核分裂生成物含有物は使用済み核燃料の再処理工程で生じた固体廃棄物であって貴金属元素を含むものであり、前記テクネチウムと前記モリブデンを分離した後、前記650℃以上の温度で酸素を遮断して酸化していた前記貴金属元素の少なくとも一部を金属に還元して回収することを特徴とする請求項1記載の固体状の核分裂生成物含有物の核種分離方法。
- 前記使用済み核燃料の再処理工程は湿式再処理工程であり、前記固体廃棄物はアクチニドを含む不溶解残渣であり、前記酸化していた貴金属元素の少なくとも一部を金属に還元した後、冷却して酸溶解し、溶解した前記アクチニドと不溶解の前記貴金属元素とを分離して回収することを特徴とする請求項2記載の固体状の核分裂生成物含有物の核種分離方法。
- 前記使用済み核燃料の再処理工程は乾式再処理工程であり、前記固体廃棄物はジルコニウムを含む金属廃棄物であり、前記酸化していた貴金属元素の少なくとも一部を金属に還元した後、溶融塩/液体金属系に移送し、前記溶融塩側に移行した前記ジルコニウムと前記液体金属に移行した前記貴金属元素とを分離して回収することを特徴とする請求項2記載の固体状の核分裂生成物含有物の核種分離方法。
- 前記酸素を遮断する温度は900℃以上であることを特徴とする請求項2から4のいずれか一つに記載の固体状の核分裂生成物含有物の核種分離方法。
- テクネチウムを含む固体状の核分裂生成物含有物を450℃以上に昇温して酸素を供給し、前記テクネチウムを酸化させて揮発させることで分離回収することを特徴とする固体状の核分裂生成物含有物の核種分離方法。
- モリブデンを含む固体状の核分裂生成物含有物を650℃以上に昇温して酸素を供給し、前記モリブデンを酸化させて気化させることで分離回収することを特徴とする固体状の核分裂生成物含有物の核種分離方法。
- ロジウムを含む固体状の核分裂生成物含有物に酸素を供給しながら前記ロジウム以外の核種を分離した後、900℃以上の温度で酸素を遮断し、前記酸素の供給で酸化したロジウムを金属に還元して回収することを特徴とする固体状の核分裂生成物含有物の核種分離方法。
- パラジウムを含む固体状の核分裂生成物含有物に酸素を供給しながら前記パラジウム以外の核種を分離した後、700℃以上の温度で酸素を遮断し、前記酸素の供給で酸化したパラジウムを金属に還元して回収することを特徴とする固体状の核分裂生成物含有物の核種分離方法。
- ルテニウムを含む固体状の核分裂生成物含有物に酸素を供給しながら前記ルテニウム以外の核種を分離した後、前記酸素の供給で酸化したRuO4を108℃以上の温度でRuO2又はRuに還元し、その後108℃未満の温度では酸素を遮断し、前記ルテニウムをRuO2又はRuの状態で残存させて回収することを特徴とする固体状の核分裂生成物含有物の核種分離方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004008204A JP2005201765A (ja) | 2004-01-15 | 2004-01-15 | 固体状の核分裂生成物含有物の核種分離方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2004008204A JP2005201765A (ja) | 2004-01-15 | 2004-01-15 | 固体状の核分裂生成物含有物の核種分離方法 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| JP2005201765A true JP2005201765A (ja) | 2005-07-28 |
Family
ID=34821648
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2004008204A Pending JP2005201765A (ja) | 2004-01-15 | 2004-01-15 | 固体状の核分裂生成物含有物の核種分離方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2005201765A (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010285680A (ja) * | 2009-06-15 | 2010-12-24 | Toshiba Corp | レアメタルの製造方法及び製造システム |
| JP2015127659A (ja) * | 2013-12-27 | 2015-07-09 | 株式会社Ihi | 高レベル放射性廃液ガラス固化設備 |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63243232A (ja) * | 1987-03-31 | 1988-10-11 | Ishikawajima Harima Heavy Ind Co Ltd | 放射性廃棄物からのルテニウム回収方法 |
| JPH02201199A (ja) * | 1989-01-28 | 1990-08-09 | Power Reactor & Nuclear Fuel Dev Corp | 高放射性廃棄物の処理方法 |
| JPH04154924A (ja) * | 1990-10-15 | 1992-05-27 | Univ Nagoya | 核燃料再処理廃棄物からの白金族元素の回収法 |
| JPH0691163A (ja) * | 1993-01-18 | 1994-04-05 | Hitachi Ltd | 溶存物質の酸化又は還元方法 |
| JPH1123793A (ja) * | 1997-06-27 | 1999-01-29 | Toshiba Corp | イオン交換樹脂の処理方法 |
| JPH1164577A (ja) * | 1997-08-15 | 1999-03-05 | Toshiba Corp | 使用済み燃料の溶融塩電解再処理方法 |
| JP2000061423A (ja) * | 1998-08-17 | 2000-02-29 | Toshiba Corp | 廃棄物処理方法および廃棄物処理装置 |
-
2004
- 2004-01-15 JP JP2004008204A patent/JP2005201765A/ja active Pending
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS63243232A (ja) * | 1987-03-31 | 1988-10-11 | Ishikawajima Harima Heavy Ind Co Ltd | 放射性廃棄物からのルテニウム回収方法 |
| JPH02201199A (ja) * | 1989-01-28 | 1990-08-09 | Power Reactor & Nuclear Fuel Dev Corp | 高放射性廃棄物の処理方法 |
| JPH04154924A (ja) * | 1990-10-15 | 1992-05-27 | Univ Nagoya | 核燃料再処理廃棄物からの白金族元素の回収法 |
| JPH0691163A (ja) * | 1993-01-18 | 1994-04-05 | Hitachi Ltd | 溶存物質の酸化又は還元方法 |
| JPH1123793A (ja) * | 1997-06-27 | 1999-01-29 | Toshiba Corp | イオン交換樹脂の処理方法 |
| JPH1164577A (ja) * | 1997-08-15 | 1999-03-05 | Toshiba Corp | 使用済み燃料の溶融塩電解再処理方法 |
| JP2000061423A (ja) * | 1998-08-17 | 2000-02-29 | Toshiba Corp | 廃棄物処理方法および廃棄物処理装置 |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010285680A (ja) * | 2009-06-15 | 2010-12-24 | Toshiba Corp | レアメタルの製造方法及び製造システム |
| US8221609B2 (en) | 2009-06-15 | 2012-07-17 | Kabushiki Kaisha Toshiba | Process for producing rare metal and production system thereof |
| JP2015127659A (ja) * | 2013-12-27 | 2015-07-09 | 株式会社Ihi | 高レベル放射性廃液ガラス固化設備 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Simpson | Developments of spent nuclear fuel pyroprocessing technology at Idaho National Laboratory | |
| RU2403634C1 (ru) | Способ регенерации отработанного топлива | |
| US8475747B1 (en) | Processing fissile material mixtures containing zirconium and/or carbon | |
| Souček et al. | Pyrochemical reprocessing of spent fuel by electrochemical techniques using solid aluminium cathodes | |
| JP3940632B2 (ja) | ジルコニウム廃棄物のリサイクルシステム | |
| JP2016507008A (ja) | イオン液体からのアクチニドの常温電着 | |
| Zaikov et al. | Research and development of the pyrochemical processing for the mixed nitride uranium-plutonium fuel | |
| JP3120002B2 (ja) | 使用済み燃料の再処理方法 | |
| CN104428429B (zh) | 使用含特殊熔盐介质的、将至少一种第一化学元素e1与至少一种第二化学元素e2分离的方法 | |
| JP3763980B2 (ja) | 使用済み酸化物燃料の還元装置およびその還元方法 | |
| JP4487031B2 (ja) | 使用済酸化物燃料の乾式再処理方法 | |
| JP2005201765A (ja) | 固体状の核分裂生成物含有物の核種分離方法 | |
| US20130233716A1 (en) | Room Temperature Electrodeposition of Actinides from Ionic Solutions | |
| US6767444B1 (en) | Method for processing spent (TRU, Zr)N fuel | |
| JP4679070B2 (ja) | 使用済み酸化物燃料の再処理方法 | |
| JP5017069B2 (ja) | 使用済燃料の再処理方法 | |
| Iizuka et al. | Development of treatment process for anode residue from molten salt electrorefining of spent metallic fast reactor fuel | |
| JPH09257985A (ja) | 使用済み燃料の再処理方法 | |
| JP2018100910A (ja) | ガラス固化体の分解方法及び前記ガラス固化体からの化学種及び元素の分離方法とその分離装置 | |
| WO2003063178A1 (fr) | Procede de reduction electrolytique | |
| Arm | Flowsheet Evaluation of Dissolving Used Nuclear Fuel in PUREX Solvent | |
| JP2004028808A (ja) | 使用済み燃料の再処理方法 | |
| WO2011144937A1 (en) | Novel reprocessing method | |
| JP6515369B1 (ja) | 不溶解性残渣処理プロセス | |
| JP2014132249A (ja) | セシウム抽出法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20061115 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20080403 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20081022 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20081222 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20090204 |