JP2004523223A - 微生物を特異的に検出するためのinsituハイブリダイゼーション装置 - Google Patents
微生物を特異的に検出するためのinsituハイブリダイゼーション装置 Download PDFInfo
- Publication number
- JP2004523223A JP2004523223A JP2002550112A JP2002550112A JP2004523223A JP 2004523223 A JP2004523223 A JP 2004523223A JP 2002550112 A JP2002550112 A JP 2002550112A JP 2002550112 A JP2002550112 A JP 2002550112A JP 2004523223 A JP2004523223 A JP 2004523223A
- Authority
- JP
- Japan
- Prior art keywords
- slide
- sample
- container
- hybridization
- nucleic acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6841—In situ hybridisation
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6888—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for detection or identification of organisms
- C12Q1/689—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for detection or identification of organisms for bacteria
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Analytical Chemistry (AREA)
- Zoology (AREA)
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- Microbiology (AREA)
- Physics & Mathematics (AREA)
- Molecular Biology (AREA)
- Immunology (AREA)
- Biotechnology (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Measuring Or Testing Involving Enzymes Or Micro-Organisms (AREA)
- Apparatus Associated With Microorganisms And Enzymes (AREA)
Abstract
本発明は、微生物を特異的に検出するためのin situハイブリダイゼーションシステム、in situハイブリダイゼーションにより微生物を特異的に検出する方法、および試料中の微生物の同定および視覚化を可能にするキットに関する。本発明は、特に微生物を特異的に同定するためのin situハイブリダイゼーションシステムに関する。前記システムは、少なくとも1つの開口部(2)を有する容器(1)と、ハイブリダイゼーション溶液用支持台(3)と、標本スライド(4)と、標本スライド用固定手段(5)とを備える。
Description
【技術分野】
【0001】
本発明は、微生物を特異的に検出するためのin situハイブリダイゼーション装置、in situハイブリダイゼーションにより微生物を特異的に検出する方法、および試料中の微生物の同定および視覚化を可能にするキットに関する。
【背景技術】
【0002】
現行の細菌判別法はいずれも共通の目標を有しており、細菌培養の必要性を排除することにより培養の不利点を回避しようとしている。
【0003】
PCR、すなわちポリメラーゼ連鎖反応では、細菌特異的プライマーを用いて細菌ゲノムの特定の特性セグメントを増幅させる。プライマーがその標的部位を見つけると、その遺伝情報セグメントの何百万もの増幅産物が生成される。DNAフラグメントを分離するためのアガロースゲルによるその後の分析で定性評価を行うことができる。最も簡単なケースでは、これによって、分析試料中に標的部位が存在するという情報が得られる。標的部位は、生細菌、死細菌または裸のDNA由来であり得るので、他の結論は得られない。この場合、判別は不可能である。この技術をさらに発展させたものが定量PCRであり、これは、存在する細菌の量と、得られ、増幅されたDNAの量との間に相関関係を生成させようとするものである。
【0004】
しかし、細菌の同定には生化学的パラメータも用いられる。キノン分析に基づいて細菌プロファイルを得る方法は、出来る限り偏りを少なく細菌群を示すのに役立つ〔ヒライシ エー(Hiraishi,A.)、Respiratory quinone profiles as tools for identifying different bacterial populations in activated sludge、J.Gen.Appl.Microbiol.第34巻:39−56ページ(1988年)〕。しかし、この方法も、参照データベースの作製に単一培養細菌のキノンプロファイルを必要とするので、個々の細菌の培養に依存する。さらに、細菌のキノンプロファイルが決定されても、試料中に実際に存在する集団分布の実像は得られない。
【0005】
上記とは対照的に、抗体による細菌検出法はもっと直接的な方法である〔ブリグモン アール エル(Brigmon,R.L.)、ジー ビットン(G.Bitton)、エス ジー ザム(S.G.Zam)、およびビー オブライエン(B.O’Brien)、Development and application of a monoclonal antibody against Thiothrix spp.、Appl.Environ.Microbiol.第61巻:13−20ページ(1995年)〕。蛍光標識した抗体を試料と混ぜ、細菌の抗原に高特異的に結合させる。次いで、エピ蛍光顕微鏡で、発せられる蛍光により細菌を検出する。このようにして、細菌は菌株レベルまで同定することができる。しかし、この方法の適用は3つの重要な不利点によって制限される。第1に、抗体の産生に単一培養が必要である。第2に、抗体−蛍光分子複合体は、体積が大きくて扱いにくいことが多く、そのために標的細胞に侵入する際に問題が生じる。第3に、検出が特異的に過ぎることが多い。抗体の生産には費用がかかり、1種類の特異的細菌株だけしか検出されないことが多く、同じ細菌種の他の株を検出することができない。しかし、多くの場合、細菌の株特異的検出は不要であり、それよりむしろ細菌種または細菌群全体の検出の方が必要とされる。第4に、抗体の生産は比較的冗長で費用のかかる手順である。
【0006】
PCRなどの分子生物学的方法の特異性と、抗体法に代表されるような細菌視覚化の可能性とを組み合わせたユニークな方法は、蛍光in situハイブリダイゼーション法〔FISH;アマン アール アイ(Amann,R.I.)、ダブリュー ルドウィッヒ(W.Ludwig)、およびケー−エイチ シュライファー(K.−H.Schleifer)、Phylogenetic identification and in situ detection of individual microbial cells without cultivation、Microbiol.Rev.第59巻:143−169ページ(1995年)〕である。この方法によって、細菌の種、属または群を試料中で直接、高特異的に視覚化し、同定することができる。この方法は、生物群の実際のあるがままの(in situ)分布についての偏りのない実像を与える唯一の方法である。これまでに培養されたことのない細菌、したがって、特性決定されていない細菌でさえ、試料中で直接同定可能であり、視覚化することもできる。
【0007】
FISH法は、その極めて重要な機能ゆえに進化の過程において極くわずかしか突然変異しなかった特定の分子、すなわち、16Sおよび23Sリボソームリボ核酸(rRNA)が細菌細胞中に存在するという事実に基づいている。どちらのリボ核酸も、タンパク質生合成の場であるリボソームの構成成分であり、それらの遍在分布、サイズ、および構造的かつ機能的不変性により、系統発生のマーカーとして役立ち得る〔ウーズ シー アール(Woese,C.R.)、Bacterial evolution、Microbiol.Rev.第51巻:221−271ページ(1987年)〕。比較配列分析に基づき、専らこれらのデータから系統発生関係を誘導することができる。このためには、これらの配列データを整列化(アライン)しなければならない。これらの巨大分子の二次構造および三次構造についての知識に基づいて整列化する際には、リボソーム核酸の相同部位を相関させる。図1は、16S rRNAの二次構造モデルを示している。
【0008】
これらのデータに基づき、系統学的な計算を実施し得る。最新のコンピュータテクノロジーを用いることにより、例えこれらのデータが大規模であっても迅速かつ効率的な計算が可能になるだけでなく、16S rRNAおよび23S rRNAの整列化された配列を含む大きなデータベースを確立することができる。このデータ材料に高速アクセスすることにより、新規に得られた配列を短時間で系統学的に解析することができる。これらのrRNAデータベースは、特異的遺伝子プローブの構築に用い得る。それによって、すべての利用可能なrRNA配列を比較し、細菌の種、属または群を特異的に検出する特定配列部分用プローブを設計する。
【0009】
FISH(蛍光in situハイブリダイゼーション)においては、リボソーム標的配列上の特定の領域に相補的なこれらの遺伝子プローブを細胞に導入する。通常、これらの遺伝子プローブは、16〜20塩基長の小さい一本鎖デオキシリボ核酸フラグメントであり、細菌種または細菌群に特有な標的領域用につくられている。蛍光標識遺伝子プローブが細菌細胞内で標的配列を見つけると、このプローブは標的配列に結合し、それらの蛍光により細菌細胞を蛍光顕微鏡で検出することができる。図2は、in situハイブリダイゼーションの手順を示している。
【0010】
培養に依存した方法では、微生物群の構成および動態に対して極めて偏った認識しか得られない。FISH法を用いて、例えば、活性汚泥の微生物相(フローラ)の検出の際に、培養することにより培養シフトが生じることを証明することができた〔ワグナー エム(Wagner,M.)、アール アマン(R.Amann)、エイチ レマー(H.Lemmer)、およびケー エイチ シュライファー、Probing activated sludge with oligonucleotides specific for proteobacteria:inadequacy of culture−dependent methods for describing microbial community structure、Appl.Environ.Mcrobiol.第59巻:1520−1525ページ(1993年)〕。
【0011】
実際の細菌群構造がこのように培地依存的に偏ることによって、活性汚泥中では副次的な役割しか果たさないが使用培養条件には十分に適合した細菌の重要性が劇的に過大評価される。したがって、そのような培養のアーチファクトにより、アシネトバクター(Acinetobacter)属細菌が、廃水処理における生物学的リン酸除去剤としてのその役割に関してまったく不正確に評価されてきたことを証明することができた。そのような誤った評価の結果として、コスト集約的で、欠陥があるかまたは不的確なプラントが設計される。そのようなシミュレーション計算の効率および再現性は低い。
【0012】
培養を用いる細菌同定法と比べたFISH法の利点は多岐にわたる。第1に、遺伝子プローブを用いた方がより多くの細胞を検出できる。培養では、1つの試料の細菌群の最大15%しか視覚化できないのに対し、FISHでは、多くの試料の全細菌群の100%まで検出できる。第2に、細菌群の活性部分を全細菌用につくられたプローブと非特異的な細胞染色との割合によって測定し得る。第3に、細菌は、直接in situ(その場)で視覚化される。したがって、種々の細菌群間で起こり得る相互作用を見分けて、分析することができる。第4に、FISH法を用いた細菌の検出は培養を用いた場合よりはるかに迅速である。培養を用いた細菌の同定には数日を要することが多いのに対し、FISH法を用いると、試料の採取から細菌の同定までに要する時間は、種レベルの同定においてさえ数時間しかかからない。第5に、遺伝子プローブは、それらの特異性にほとんど制限されることなく選択することができる。1つのプローブで、属または細菌群全体だけでなく個々の種をも検出し得る。第6に、細菌種または全細菌群を試料中で直接正確に定量し得る。培養とそれに伴う不十分な定量は必要ない。
【0013】
ある試料中に存在する細菌を生物分類学的に調べるときには、トップ・ダウンアプローチを利用する。これは、先ず、特異性が出来得る限りおおまかである、すなわち、特異性が低い、細菌群全体のみを検出する遺伝子プローブを用いて細菌試料を分析する。用いるプローブの特異性を連続的に高めることにより、最終的に未知の細菌が同定される。
【0014】
このように、FISH法は、試料中で直接細菌を迅速かつ高特異的に検出するための優れたツールである。培養を用いる方法とは対照的に、FISH法は直接的な手順であり、現行の方法とは異なり、細菌の視覚化だけでなくさらに細菌の正確な定量をも可能にする。
【0015】
細菌は評価中に高エネルギー光を照射することにより視覚化されるので、FISH分析は原則としてスライド上で実施される。ハイブリダイゼーション緩衝液またはハイブリダイゼーション溶液および洗浄緩衝液または洗浄溶液などの個々の溶液の組成は当業者には周知であり、例えば、スナイドルら(Snaidr et al.)〔ジェイ スナイドル(J.Snaidr)、アール アマン、アイ フーバー(I.Huber)、ダブリュー ルドウィッヒ、およびケイ−エイチ シュライファー、Phylogenetic analysis and in situ identification of bacteria in activated sludge、Appl.Env.Microb.第63巻7号:2884−2896ページ(1997年)〕に詳細に記載されている。スライド上での微生物分析のFISH手順は、通常、以下のステップを含む:
1. 反応バイアルに微生物試料のアリコート(一定分量)を導入し、アリコートを適当な固定溶液と混合するステップ;
2. 試料が固定され、遺伝子プローブにアクセス可能になるまで数回遠心、洗浄するステップ;
3. 固定された微生物試料のアリコートをスライド上のウエルに加えるステップ;
4. スライド上の微生物をオーブン中40〜90℃で10〜30分間インキュベートして乾燥させるステップ;
5. スライドを50%、70%および100%エタノールを含む溶液中に順次浸して、エタノール濃度を増大させることで微生物細胞を脱水するステップ;
6. 微生物を含有するウエルにハイブリダイゼーション溶液を加えるステップ;
7. 同ウエルにプローブ溶液を加えるステップ;
8. セルロース片を折り曲げてプラスチックチューブに挿入し、次いで、チャンバ内のセルロースを数mlのハイブリダイゼーション溶液で湿らせて湿潤チャンバを作成するステップ;
9. スライドを湿潤チャンバ内のセルロース上に水平に配置するステップ;
10. 湿潤チャンバをインキュベーションオーブンに移し、1〜2時間インキュベートするステップ;
11. 湿潤チャンバを開き、スライドを取り出して、蒸留水で手短にリンスするステップ;
12. 湿潤チャンバを廃棄するステップ;
13. 新たなプラスチックチューブに洗浄緩衝溶液を充填するステップ;
14. 洗浄溶液を充填したプラスチックチューブにリンスしたスライドを挿入するステップ;
15. プラスチックチューブに挿入したスライドを、インキュベーションオーブン中で10〜30分間インキュベートするステップ;
16. プラスチックチューブからスライドを取り出し、蒸留水で洗浄するステップ;
17. スライドを上下に動かして風乾するステップ;
18. 褪色防止剤をスライド上に加えた後、エピ蛍光顕微鏡でスライドを視検することができる。
【発明の開示】
【発明が解決しようとする課題】
【0016】
しかし、上述の微生物を検出するための従来のFISH法は、実質的な不利点を有している。上記方法は、複雑かつ冗長で、いくつかの誤差源のために一貫した質で再現することができない。これを以下に詳細に説明する。
【0017】
何回もの洗浄、遠心ステップのために、試料の固定効率にばらつきが生じ得る。この結果、後続のハイブリダイゼーションステップにおいて、遺伝子プローブが様々な効率で細胞に侵入するために、エピ蛍光顕微鏡で細胞を検出するときに明度の変動が生じる。しかし、明度は細胞のリボソーム含量と相関している。したがって、例えばFISH分析の例で言えば、蛍光強度は、細胞の増殖状態が試料採取時に良好であったかまたは不良であったかを判定する尺度である。この情報は、特に医学微生物学、それだけでなく食品または環境微生物学においても、試料の微生物についての状態を全体的に評価するために重要である。したがって、分析試料固定時に効率が変動することにより、試料の増殖状態ひいては全体的な状態について偏った情報がもたらされる。
【0018】
さらに、非効率的固定によるシグナル強度不良は、エピ蛍光顕微鏡で視覚化するときに、小細胞またはリボソーム含量が低い細胞をも検出する検査者の能力を低下させる。それに加え、種々の洗浄、遠心ステップのために、反応バイアルで固定プロセスを実施している間に細胞が失われることがある。
【0019】
従来のFISH法の別の問題は、数回のインキュベーション間の細胞脱水時に、細胞がスライドから剥離したり、他のウエルに移ってしまう可能性があることである。
【0020】
さらに、プローブ溶液とハイブリダイゼーション溶液とを別々にすると、2種の異なる溶液をスライドウエルに加えなければならないので、作業費用が高くなる。
【0021】
さらに、湿潤チャンバの作成は不便であり、スライドの水平配置が保証されない。そのために、異なるウエル中に存在する別の溶液が混じってしまう可能性がある。
【0022】
上記文献に引用されているようなハイブリダイゼーションチャンバとして丸いプラスチックチューブを用いる際の別の問題は、インキュベーションオーブン中で、湿潤チャンバがいつも不安定な状態にあることである。この不安定な状態により、スライドも不安定になって、異なるスライドウエルの溶液が混ざってしまうことがある。
【0023】
さらに、スライドを、先ず洗浄ステップでリンスし、次いで、別の容器に移さなければならない。この比較的冗長なプロセス中にハイブリダイゼーション温度が低下することにより、核酸プローブ分子と細胞との非特異的結合が生じ得る。
【0024】
従来のFISH法の他の問題は、蒸留水を用いた洗浄ステップ中に細胞が洗い落とされるか、別のスライドウエルに流入し得ること、および、垂直状態で風乾している間にスライドから流れ落ちる液滴を介して、細胞が1つのスライドウエルから次のスライドウエルに移り得ることである。スライドが不安定状態にあるために、スライドがひっくり返ったり、細胞が剥がれたりし得る。
【0025】
再現性不良で、操作が複雑、冗長かつ不便であることによって、in situハイブリダイゼーション一般、特にFISH分析は、これまで産業にはめったに利用されなかった。しかし、これらの手順を用いた細菌分析は、現在産業に用いられている他のすべての微生物学的分析法に比べて有意な利点を有しているので、in situハイブリダイゼーション、特にFISH法による微生物の簡単かつ再現性のある同定を可能にするデバイスまたは方法が求められている。
【0026】
したがって、上述した従来技術の不利点を克服し、試料中の微生物の迅速な同定を容易かつ再現性よく実施し得るデバイスまたは装置および方法を提供することが本発明の目的である。
【0027】
他の目的は本発明の以下の説明から明らかにされる。
【課題を解決するための手段】
【0028】
上述の目的は、本発明にしたがって独立クレームの特徴により解決される。さらなる実施形態は従属クレームの特徴に由来する。
【0029】
本発明により、微生物を特異的に検出するためのin situハイブリダイゼーション装置が提供され、この装置は、少なくとも1つの開口部2を有する容器1と、ハイブリダイゼーション溶液用支持台3と、スライド4と、スライド用固定手段5とを備えている。この装置は、容器開口部の密閉、特に、水密および/または気密シールに適した蓋6を備えているのが好ましい。この文脈における用語「密」とは、容器内に存在する湿分が閉鎖された容器から実質的に漏れないことを意味する。
【0030】
スライドは、分析試料や、場合により、ネガティブコントロールまたはポジティブコントロールとなる試料を互いに別々に加え得るウエル9を備えているのが好ましい。スライド上のウエルは、一次元でのみ他のウエルに隣接し、例えば一列に配置されているのが特に好ましいが、ウエルが列内でジグザグ配置されていてもよい。
【0031】
本発明のin situハイブリダイゼーション装置の好ましい実施形態において、蓋はスライド用固定手段5を備えている。蓋は、スライド用固定手段として、スライドの一方の端部7を差し込み得るスロット5を有しているのが特に好ましい。
【0032】
代替例として、スライドを、容器の構成部品、例えば容器底部のスロット形態の固定手段5と係合させてもよいことは勿論であり、この場合、底部は容器の開口部の反対側に配置される。
【0033】
本発明の装置の別の好ましい実施形態において、蓋は、スライドが水平に配置されているときに、固定スライドを有する蓋を蓋のない装置から離れて安定させ得る構造要素8を有している。
【0034】
蓋は、スライドが水平または垂直または横向き配置されているときに、固定スライドを有する蓋を蓋のない装置から離れて立っていられるように構成するのが特に好ましい。
【0035】
本発明の範囲内でスライドの水平配置とは、試料またはプローブをわきに流さずにスライド上に加え得るようなスライド配置を意味する。
【0036】
本発明の範囲内で横向き配置とは、水平配置に比べて90°回転させた配置を意味し、スライドは、ウエルが一次元でのみ他のウエルに隣接しているならば、液滴が、場合によりスライド上の別のウエルに流入することなくスライドを流れ落ち得るように90°回転されている。
【0037】
本発明の範囲内でスライドの垂直配置とは、水平配置に比べても横向き配置に比べても90°回転させた配置を意味する。
【0038】
本発明の装置の特に好ましい実施形態において、容器および/または蓋は、蓋が閉鎖されていないときも閉鎖されているときも、スライドが水平、垂直または横向き配置されているときに装置を安定配置し得るように構成される。
【0039】
さらに、本発明によれば、容器または装置内でスライドを安定化するために容器がスライド用の横軸受10もしくはガイドレールを備えている装置であって、そのような軸受10が容器の構成部品である装置が好ましい。
【0040】
さらに、ハイブリダイゼーション溶液用支持台3は、取り外し可能であるか、挿入可能であるのが好ましい。さらに、本発明によれば、ハイブリダイゼーション溶液用支持台3は容器内に完全に挿入し得るのが好ましい。しかし、ハイブリダイゼーション溶液用支持台3は、また、段階的に、特に連続的に、容器1内に挿入し得るのも好ましい。
【0041】
別の好ましい実施形態において、容器1は、内部でハイブリダイゼーション溶液用支持台3を安定化させるためにハイブリダイゼーション溶液用支持台3用の横軸受11を備えているか、またはそのような軸受11は容器1の構成部品である。
【0042】
代替例として、ハイブリダイゼーション溶液用支持台は、容器の固定部品、特に容器内のウエルまたは凹みである。
【0043】
本発明の装置の特に好ましい実施形態において、ハイブリダイゼーション溶液用支持台は、トレイ3、特に、液体取り込み用および/または液浸パッド取り込み用ウエル12を備えたトレイである。
【0044】
スライドを除く装置の全部品の材料は、好ましくはプラスチック、特に好ましくはポリエチレンおよび/またはポリプロピレンを包含する。さらに、上述の装置部品の材料は金属も包含し得る。
【0045】
スライドは、好ましくはガラス製、特に好ましくはDIN 12111に基く加水分解等級1〜4に相当するガラス製である。
【0046】
本発明の他の態様において、in situハイブリダイゼーションにより微生物を特異的に検出する方法が提供され、この方法は、以下のステップ:
(a) 試料中に含まれている微生物を固定するステップ;
(b) 固定細胞を検出可能な核酸プローブ分子と共にインキュベートするステップ;
(c) ハイブリダイズしなかった核酸プローブ分子を除去または洗い落とすステップ;および
(d) 核酸プローブ分子とハイブリダイズした細胞を検出するステップ
を含み、
ステップ(a)〜(c)と、場合によりステップ(d)は、本発明のin situハイブリダイゼーション装置を用いて実施する。
【0047】
固定ステップおよび/または場合により乾燥ステップは、スライド上で実施するのが好ましい。
【0048】
さらに、本発明によれば、スライドが横向きに配置されているときにスライドの最終乾燥を行い、かつ/またはスライドが水平配置されているときにインキュベーションを行い、かつ/またはスライドが垂直配置されているときに洗浄を行うのが好ましい。
【0049】
本発明の方法の別の好ましい実施形態では、ステップ(b)で、ハイブリダイゼーション溶液と核酸プローブ分子溶液との混合物をスライドに加える。
【0050】
上述の混合物は滴下容器を用いて加えるのが特に好ましい。この滴下容器は、別の好ましい実施形態では、使い捨て滴下容器または複数回使用可能な滴下容器である。
【0051】
本発明の方法によれば、湿潤チャンバに必要とされるハイブリダイゼーション溶液を、ハイブリダイゼーション溶液用支持台内に配置されたハイブリダイゼーション溶液浸漬パッドを介して本発明の装置内に注入可能である。
【0052】
ステップ(b)で用いられる核酸プローブ分子は、検出対象微生物の染色体DNAもしくはエピソームのDNA、mRNAまたはrRNAに相補的であることが好ましい。
【0053】
本発明によれば、核酸プローブ分子は検出可能なマーカーに共有結合しているのがさらに好ましい。この検出可能なマーカーは、以下のマーカー:
− 蛍光マーカー、
− 化学発光マーカー、
− 放射性マーカー、
− 酵素活性を有する基、
− ハプテン、
− ハイブリダイゼーションにより検出可能な核酸
からなる群から選択するのが好ましい。
【0054】
本発明の方法における微生物は単細胞微生物であるのが好ましい。この微生物は、酵母、細菌、藻類または真菌類であるのが特に好ましい。別の好ましい実施形態において、微生物は廃水細菌である。
【0055】
本発明の方法のさらなる実施形態において、試料は、環境試料であって水、土壌または空気から採取された試料;食品試料、特に、牛乳もしくは乳製品、飲用水、飲料、パン製品または肉製品由来の試料;医学試料、特に、組織、分泌物もしくは糞便から採取された試料;廃水試料、特に、活性汚泥、消化汚泥もしくは嫌気性汚泥から採取された試料;バイオフィルムから採取された試料、特に、バイオフィルムが産業施設から採取されるか、排水処理の過程で生成されるか、もしくは天然バイオフィルムである試料;または、医薬品もしくは化粧品から採取された試料である。
【0056】
さらに、本発明により、in situハイブリダイゼーションにより微生物を特異的に検出するためのキットが提供され、このキットは、微生物を特異的に検出するための少なくとも1つの核酸プローブ分子と、少なくとも1種のハイブリダイゼーション溶液と、場合により、ネガティブコントロールとなる核酸プローブ分子と、場合により、ポジティブコントロールとなる核酸プローブ分子と、場合により、洗浄溶液と、場合により、固定溶液と、場合により、褪色防止剤と、本発明のin situハイブリダイゼーション装置とを含む。
【0057】
本発明のキット中の核酸プローブ分子は、検出対象微生物の染色体もしくはエピソームのDNA、mRNAまたはrRNAに相補的であるのが好ましい。
【0058】
本発明の好ましい実施形態において、本発明のキット中の核酸プローブ分子は、検出可能なマーカーに共有結合しているのが好ましい。検出可能なマーカーは、蛍光マーカー、化学発光マーカー、放射性マーカー、酵素活性を有する基、ハプテンおよびハイブリダイゼーションにより検出可能な核酸からなる群から選択するのが特に好ましい。
【0059】
本発明の別の主題は、in situハイブリダイゼーションにより微生物を特異的に検出するための本発明のin situハイブリダイゼーション装置の利用法である。
【0060】
最後に、本発明の別の主題は、本発明の方法における本発明のキットの利用法である。
【発明を実施するための最良の形態】
【0061】
この度、驚くべきことには、簡単かつ再現可能な方法で微生物を迅速かつ安全に同定し得るin situハイブリダイゼーション装置を提供することが可能になった。本発明の装置は、少なくとも1つの開口部を有し、以後チャンバとも称される容器と;容器もしくはチャンバに完全に挿入し得るか、または容器の一部であるハイブリダイゼーション溶液用支持台、特にトレイと;スライド用固定手段とを備えている。さらに、この装置は、in situハイブリダイゼーション用チャンバ内に挿入可能なスライドを備えている。本発明の装置の構造は図3に示されている。
【0062】
本発明の装置は、容器開口部の密閉、特に、水密および/または気密シールに適した蓋をさらに備えているのが好ましい。スライドはこの蓋に固定されるのが好ましく、スライドがこの蓋に挿し込まれるのが特に好ましい。この好ましい実施形態において、スライドは、蓋にきっちりかつ安全に挿し込まれるが、最終的な分析のために極度の力を加えなくても再び手で蓋から取外すことができる。蓋を固定するか、きっちり締めることにより、本発明の装置が垂直配置されているときでも洗浄手順を確実に実施することができる。
【0063】
本発明の装置の特に好ましい実施形態において、蓋は、スライドが水平または垂直配置されているときに固定スライドを有する蓋を装置から離れて安定させ得る構造部品を備えているか、またはそのような構造部品を有している。本発明に従って、例えば蓋に支持脚を取り付けることによって得られるこの蓋の安定性により、実施されるいずれの反応時にもスライドを水平状態に維持することができる。
【0064】
取り扱いを容易にするためには、スライドをin situハイブリダイゼーション装置の蓋に固定するのが好ましい(図4参照)。この場合、スライドを、本発明のハイブリダイゼーション法の初めから終わりまで蓋に固定された状態に保ち得る。さらに、洗浄、固定などのすべての処理手順を同じ反応チャンバ内で実行することもできる。スライドが水平または垂直配置されているときに蓋を装置から離れて安定配置し得る構造部品を蓋が備えていることは、試料およびプローブの使用時にもスライドを蓋に付いたままにしておけるだけでなく、試料使用時にスライドが平坦かつ安定に配置されるという重要な利点を有する。さらに、蓋の構造部品または支持脚により、スライドが蓋に固定された状態で、スライド上で核酸プローブと細胞とのハイブリダイゼーションを実現させるための個別反応を実施することができる。さらに、上記構造部品を備えた蓋を用いて、すべての乾燥ステップをチャンバ外で実施することもできる。固定スライドを有する蓋が平坦かつ安定して立っていられるので、スライド上での試料の混合を防止することができる。
【0065】
本発明の別の好ましい実施形態において、容器および/または蓋は、蓋を閉めた状態で、スライドが水平配置されているときに装置が安定な状態に置かれるように構成される。したがって、特に本発明の方法のステップ(a)および(b)におけるスライドの水平配置は、本発明のin situハイブリダイゼーション装置部品の支持面の構成により得られる。
【0066】
トレイをハイブリダイゼーション溶液用支持台として用いることにより、湿潤チャンバに必要なハイブリダイゼーション溶液を安全かつ清潔に本発明の装置に導入することができる。トレイは、液体を取り込むための小さなウエルまたは凹みを有しているのが好ましい(図5参照)。湿潤チャンバを作成するのに必要なハイブリダイゼーション溶液をトレイに充填し得るように、先ずトレイの一部のみをチャンバ内に挿入するのが特に好ましい。次いで、トレイを完全にチャンバ内に挿入する(図6参照)。
【0067】
あるいは、ハイブリダイゼーション溶液用支持台としてセルロースを用いてもよい。
【0068】
ハイブリダイゼーション溶液を滴下し、使用後に取り外すことができる交換可能なトレイを構成することは、規定量のハイブリダイゼーション溶液を本発明のin situハイブリダイゼーション装置に迅速導入し得るという利点を有する。セルロースの利用は不可欠ではないが、排除もされない。
【0069】
ハイブリダイゼーション溶液を本発明のin situハイブリダイゼーション装置に導入するための別の代替案は、トレイに配置された使い捨てパッドを介してハイブリダイゼーション溶液を反応装置に導入する方法である。使い捨てパッドは鮮度保持シールでシールするのが好ましく、トレイをチャンバに挿入した後直ぐにシールを除去すると、ハイブリダイゼーション溶液がチャンバ内で蒸散し得る。
【0070】
微生物を特異的に分析するためのin situハイブリダイゼーションを迅速かつ簡単に実施するために本発明のin situハイブリダイゼーション装置で実施される方法の好ましい実施形態は、以下のステップ:
(a) スライド上で試料中に含まれている微生物を固定するステップ;
(b) ハイブリダイゼーションを実現させるために本発明の装置で固定細胞を核酸プローブと共にインキュベートするステップ;
(c) ハイブリダイズしなかったオリゴヌクレオチドを除去または洗い落とすステップ;
(d) オリゴヌクレオチドにハイブリダイズした細胞を検出するステップ
を含む。
【0071】
インキュベーションおよび洗浄手順は、本発明のin situハイブリダイゼーション装置内で行うのが好ましい。
【0072】
微生物は、通常行なわれているように最初に反応容器内で固定してから固定化するのではなく、固定および/または場合により乾燥をスライド上で直接行うのが好ましい。
【0073】
上記のようにスライド上で固定すると、細胞の損失が回避され、その取扱いが著しく容易になり、実施がはるかに簡単になる。さらに、スライド上で固定することにより、固定ステップとその後の脱水を1つの手順に組み合わせることができる。
【0074】
本発明によれば、核酸プローブ分子のハイブリダイゼーションおよび添加は、通常行われているように、ピペットを用いて、先ず規定量のハイブリダイゼーション溶液、次いで規定量のプローブ溶液をスライドウエルに加えるのではなく、スライド上にハイブリダイゼーション溶液とヌクレオチドプローブ分子溶液との混合物を加えるのが好ましい。
【0075】
ハイブリダイゼーション溶液と核酸プローブ分子溶液との混合物を加えることにより、核酸プローブ分子が比較的安定な状態で迅速かつ完璧に処置することが可能になる。
【0076】
上述の混合物は、滴下容器に軽く圧力を加えて滴下するのが好ましい。滴下容器は、複数回使用可能でハイブリダイゼーション溶液とプローブ溶液との混合溶液を数滴分含むものであってもよいし、または代替例として死容積を顧慮した必要量の試薬を入れた小型の使い捨て滴下容器であってもよい。
【0077】
滴下容器を用いると、高価なピペットを使わなくて済むだけでなく、取扱いおよび注入も容易になる。
【0078】
次いで、好ましくは蓋に固定されたスライドをチャンバ内に挿入する(図7参照)。スライドのチャンバ内への挿入、さらには固定または安定化を容易にするために、チャンバ内に横軸受またはガイドレールを取り付けるのが好ましい(図8参照)。
【0079】
チャンバおよび/または蓋は、安定した水平配置だけでなく垂直または横向き配置が確実になるように構成するのが好ましい。
【0080】
その後のインキュベーションは、スライドを水平に配置した状態で実施するのが好ましい。続くスライドの洗浄は、本発明に従って、好ましくはチャンバ内で、特に好ましくはスライドを垂直に配置した状態で実施する。
【0081】
スライドを最終乾燥、特に最終風乾するためには、蓋を横向きに配置し得るように構成するのが好ましい。このようにすると、液滴がスライドの別のウエルに流れ込まずにスライドを流れ落ちるので特に好都合である。
【0082】
結果として、ほとんどの処置ステップを、チャンバと好ましくは装置の蓋とからなる単一容器内で実施するのが好ましい。
【0083】
図9に、蓋と、チャンバと、トレイと、挿入されたスライドとを有する本発明のin situハイブリダイゼーション装置の好ましい実施形態の全構造を示す。図10〜図12は、蓋、トレイおよびチャンバの寸法を示している。
【0084】
したがって、従来のin situハイブリダイゼーション法、特に従来のFISH法と比較した、微生物を特異的に検出するための本発明のin situハイブリダイゼーション装置および本発明の方法の極めて重要な利点は、取扱いが非常に容易であることと、試料中の微生物の特異的検出を可能にする速度および再現性である。
【0085】
本発明の範囲内において、微生物の「固定」とは、微生物の細胞エンベロープを核酸プローブに対して透過性にする処理を意味する。それによって、オリゴヌクレオチドとこれに結合させたマーカーとからなる核酸プローブは、細胞内の核酸プローブに対応する標的配列に結合するべく細胞エンベロープを透過することができる。結合とは、相補的核酸領域間の水素結合の生成と解釈されるべきものである。エンベロープは、ウイルスをコートする脂質エンベロープ、細菌の細胞壁または単細胞真核生物の細胞膜であってよい。固定には通常エタノールを用いる。これらの手段を用いても細胞壁を核酸プローブに対して透過性にし得ない場合、専門家は同じ結果をもたらす他の手段を知っているであろう。そのような手段には、例えば、低濃度のパラホルムアルデヒド溶液またはホルムアルデヒド希釈液、メタノール、アルコール混合物、酵素処理などが含まれる。
【0086】
本発明の意味での核酸プローブは、通常12〜1000ヌクレオチド、好ましくは12〜50ヌクレオチド、特に好ましくは17〜25ヌクレオチドを有するDNAまたはRNAプローブであってよい。核酸プローブは、相補配列が検出対象微生物中に存在するかどうかという基準に従って選択される。規定配列を選択することにより、細菌種、細菌属または全細菌群を検出し得る。12〜15ヌクレオチド長のプローブでは、配列は100%相補的でなければならない。15を越えるヌクレオチドを有するオリゴヌクレオチドでは、1〜数個のミスマッチが許容される。ストリンジェントなハイブリダイゼーション条件に従って、核酸プローブ分子が標的配列に実際にハイブリダイズする。本発明の意味での穏和な条件とは、例えば、実施例1に記載のようなハイブリダイゼーション溶液中0%のホルムアミドである。本発明の意味でのストリンジェントな条件とは、例えばハイブリダイゼーション溶液中20〜80%ホルムアミドである。
【0087】
ハイブリダイゼーションの持続時間は通常10分〜12時間であるが、ハイブリダイゼーションは約2時間持続するのが好ましい。ハイブリダイゼーション温度は、好ましくは44〜48℃、特に好ましくは46℃であり、ハイブリダイゼーション温度のパラメータならびにハイブリダイゼーション溶液中の塩および界面活性剤の濃度は、1種類または複数のプローブに応じて、特にその長さや検出対象細胞中の標的配列に対する相補度に応じて最適化し得る。この点で標準的な計算法は当業者には公知である。
【0088】
本発明の方法の範囲内で、標準的なハイブリダイゼーション溶液は、0.1〜1.5M、好ましくは0.9Mの塩濃度を有し、塩は塩化ナトリウムであるのが好ましい。さらに、ハイブリダイゼーション溶液は、通常、0.001〜0.1%の濃度、好ましくは0.01%の濃度のドデシル硫酸ナトリウム(SDS)などの界面活性剤と、0.001〜0.1Mの範囲の濃度、好ましくは0.02Mの濃度のトリス/HClとを含んでいる。トリス/HClのpHは、通常6〜10であるが、約8.0のpHが好ましい。上述のように、ハイブリダイゼーション溶液は、所望または要求されるストリンジェンシーの度合いに応じて、0〜80%のホルムアミドをさらに含み得る。
【0089】
ハイブリダイゼーション溶液には、可能なら15〜1000ngの量の核酸プローブが存在しなければならないが、この量は、8〜100μl、好ましくは40μlのハイブリダイゼーション溶液量中に含まれていなければならない。プローブ濃度は、111ng/40μlハイブリダイゼーション溶液が特に好ましい。
【0090】
ハイブリダイゼーション終了後、ハイブリダイズしなかった過剰なプローブ分子を除去しなければならないが、これは、普通、通常の洗浄溶液または通常の洗浄緩衝液を用いて実施する。この洗浄溶液は、所望なら、0.001〜0.1%、好ましくは0.01%の濃度のSDSなどの界面活性剤と、0.001〜0.1M、好ましくは0.02Mの濃度のトリス/HClとを含んでいてよく、トリス/HClのpHは、6.0〜10.0の範囲、好ましくは8.0である。洗浄溶液中には界面活性剤が存在し得るが、これは絶対要件ではない。洗浄溶液は、通常、NaClをさらに含んでいてよく、その濃度は、要求されるストリンジェンシーに応じて、0.003〜0.9M、好ましくは0.01〜0.9Mである。洗浄溶液はさらにEDTAを含んでいてよく、その濃度は、0.005Mであるのが好ましい。洗浄溶液はさらに、当業者には公知の通常の保存剤を適量含み得る。
【0091】
結合しなかったプローブ分子の「洗い落とし」は、通常、44〜52℃、好ましくは44〜50℃の範囲、特に好ましくは46℃で、10〜40分間、好ましくは15分間行う。
【0092】
それぞれの核酸プローブは検出対象微生物に基づいて選択する。この場合、核酸プローブは、検出対象微生物の染色体またはエピソームのDNAにも、mRNAまたはrRNAにも相補的であり得る。検出対象微生物中に2以上のコピー数存在する領域に相補的な核酸プローブを選択するのが有利である。検出対象配列は、細胞当たり、好ましくは500〜100000、特に好ましくは1000〜50000のコピー数存在する。このために、標的部位としてrRNAを用いるのが好ましい。というのは、細胞のリボソームはタンパク質生合成部位であり、各活性細胞中に数千コピー存在するからである。
【0093】
本発明に従って、核酸プローブ分子を微生物に透過させ、核酸プローブ分子と微生物の核酸とをハイブリダイズさせるために、核酸プローブを上記の意味で固定された微生物と共にインキュベートする。次いで、ハイブリダイズしなかった核酸プローブ分子を通常の洗浄ステップで除去する。その後、各細胞で特異的にハイブリダイズした核酸プローブ分子を検出することができる。
【0094】
同定および定量の必要条件は、本発明に従って用いられる核酸プローブ分子が検出可能であることである。この検出能は、例えば、核酸プローブ分子と検出可能なマーカーとの共有結合によって得られる。検出可能なマーカーとしては、例えば、いずれも専門家には周知の、CY2、CY3、CY5、FITC、FLUOS、TRITC、またはFLUOS−PRIMEなどの蛍光団が用いられる。蛍光団の例は以下の表1にリストされている。
【0095】
【表1】
あるいは、化学発光団、または35S、32P、33P、125Jなどの放射性標識を用いる。しかし、検出能は、核酸プローブ分子と酵素活性分子、例えば、アルカリホスファターゼ、酸ホスファターゼ、ペルオキシダーゼ、西洋ワサビペルオキシダーゼ、β−D−ガラクトシダーゼ、またはグルコースオキダーゼとを結合させても得られる。これらの酵素それぞれについて、天然基質の代わりに変換可能で、着色産物または蛍光産物に変換可能な多くの色素原が知られている。そのような色素原の例を以下の表2に示す。
【0096】
【表2】
最後に、核酸プローブ分子を、その5′または3′末端にハイブリダイゼーションに適した別の核酸配列を有するように作成することができる。この核酸配列も、約12〜1000、好ましくは15〜50ヌクレオチドを有する。この第2の核酸部分も、上述の化合物または作用物質のいずれかで検出し得るオリゴヌクレオチドプローブによって認識され得る。
【0097】
別の可能性は、検出可能な核酸プローブ分子とハプテンとを結合させることである。標的核酸から核酸プローブ分子を分離した後、今や独立して存在する核酸プローブ分子を検出可能なハプテン認識抗体と接触させることができる。そのようなハプテンの周知例は、ジゴキシゲニンまたはその誘導体である。当業者は、ハイブリダイゼーションに利用されるオリゴヌクレオチドを検出、定量するためのここに挙げた例とは別の多くの実行可能な手段を知っている。
【0098】
さらに、多くの可能な標識によって、2つ以上のオーバーラップする集団またはオーバーラップしない集団を同時に検出することができる。したがって、例えば2つ以上の異なる蛍光マーカーを用いて、数種の細菌群を検出し得る〔アール アマン、ジェイ スナイドル、ダブリュー ルドウィッヒ,およびケイ−エイチ シュライファー、In situ visualization of high genetic diversity in a natural microbial community,J.Bacteriol.第178巻、第12号:3496−3500ページ(1996年)〕。
【0099】
評価は、利用されるプローブの標識の種類に依存する。本発明の範囲内において、評価は、光学顕微鏡、エピ蛍光顕微鏡、化学発光測定装置、蛍光光度計などを用いて有利に実施し得る。
【0100】
本発明の方法を用いて検出される微生物は、原核または真核微生物であってよい。ほとんどの場合、単細胞微生物を検出するのが望ましいであろう。これらの単細胞微生物は、大きな細胞塊、いわゆる糸状体中にも存在し得る。ここで適切な微生物は、主として、酵母、藻類、細菌または真菌類である。
【0101】
本発明の特に好ましい実施形態において、微生物は、廃水処理施設の廃水中に存在する細菌である。
【0102】
本発明の方法は多方面に利用し得る。微生物の存在について環境試料を分析し得る。このために、これらの試料を、空気、水または土壌から採取し得る。
【0103】
本発明の方法の別の適用分野は食品管理である。好ましい実施形態において、食品試料は、牛乳または乳製品(ヨーグルト、チーズ、カッテージチーズ、バター、バターミルク)、飲用水、飲料(レモネード、ビール、ジュース)、パン製品または肉製品から採取する。食品中の微生物を検出するには、場合により、微生物が十分な量で存在することを確実にするために培養してもよい。
【0104】
本発明の方法は、さらに、医学試料の分析にも利用し得る。本発明の方法は、例えば、肺、腫瘍または炎症組織由来、汗、唾液、精液および鼻分泌物などの分泌物由来の生検材料、尿道または膣排出物などの組織標本、ならびに尿または排泄物試料の分析に適している。
【0105】
本発明の方法のさらなる適用分野は、廃水、例えば、活性汚泥、消化汚泥または嫌気性汚泥の分析である。さらに、本発明の方法は、産業施設のバイオフィルムの分析、および天然バイオフィルムまたは廃水処理時に生成されるバイオフィルムの分析に適している。本発明の方法を用いて、医薬品および化粧品、例えば、軟膏、クリーム剤、チンキ、液体製剤などを分析することができる。
【0106】
本発明により、本発明のさらなる態様において、試料中の微生物の検出に本発明の方法を適用するためのキットが提供される。そのようなキットの内容は、実質的に検出対象微生物の性質に基づく。このキットは、主要構成要素として、検出対象微生物それぞれに特異的な1つ以上の核酸プローブと、好ましくは、ネガティブまたはポジティブコントロールとなり得る他の核酸プローブとを含む。さらに、このキットは、ハイブリダイゼーション溶液と洗浄溶液とを含んでいるのが好ましい。ハイブリダイゼーション溶液の選択は、主として、用いられる核酸プローブの長さに依存する。したがって、当業者には公知のように、長さ15ヌクレオチドの核酸プローブのハイブリダイゼーションには、長さ75ヌクレオチドのプローブのハイブリダイゼーションの場合よりストリンジェントでない条件を選択しなければならない。ハイブリダイゼーション条件の例は、例えば、スタール&アマン(Stahl & Amann)(1991年),スタッケブランド&グッドフェロー(Stackebrand and Goodfellow)(編),Nucleic Acid Techniques in Bacterial Systematics;ジョンワイリー&サンズ社(John Wiley & Sons Ltd.),英国チチェスター所在、に記載されている。
【0107】
したがって、本発明により、上述の本発明の方法を実施し得るキットが提供される。好ましい実施形態において、本発明のキットは、微生物を特異的に検出するための少なくとも1つの核酸プローブ分子と、少なくとも1種のハイブリダイゼーション溶液と、場合により、ネガティブコントロールとなる核酸プローブ分子と、場合により、ポジティブコントロールとなる核酸プローブ分子と、場合により、洗浄溶液と、場合により、固定溶液と、場合により、褪色防止剤と、本発明のin situハイブリダイゼーション装置とを含み、この装置またはこの装置の一部で、以下のステップ:
(a) 試料中に含まれている微生物をスライド上で固定するステップ;
(b) ハイブリダイゼーションを実現させるために固定された細胞を核酸プローブと共にインキュベートするステップ;
(c) ハイブリダイズしなかったヌクレオチドプローブ分子を除去または洗い落とすステップ
を実施し得る。
【0108】
好ましい実施形態において、本発明のキットは、廃水処理施設の廃水中に存在する細菌の検出に特異的なプローブを含む。
【0109】
本発明の方法を用いて、in situハイブリダイゼーションを実際に成立させることができる。
【0110】
以下の実施例および図面は本発明の説明に役立つが、決して本発明を制限するものと解釈されるものではない。
(実施例: 廃水試料中の細菌の検出)
1.一般的な説明
以下に「VIT反応容器」とも称される本発明のin situハイブリダイゼーション装置における、以下に「VIT法」とも称される本発明の方法の以下の実施例は、廃水試料中に存在する細菌の定性分析に役立つ。同定は数時間内に完了する。
2.基本原理
この手順では、細菌を蛍光標識オリゴヌクレオチドプローブとハイブリダイズさせ、次いで、エピ蛍光顕微鏡下、スライド上で検出し得る。
3.材料
46℃に予熱した乾燥チャンバ
洗浄溶液を調製、加熱するためのボトル
洗浄溶液を調製するための目盛付きシリンダー
温度計
タイマー
VIT溶液:特異的核酸プローブ分子を含有する溶液
ネガティブコントロール:ネガティブコントロール用溶液
ポジティブコントロール:ポジティブコントロール用溶液
溶液AおよびB:固定溶液
溶液C:ハイブリダイゼーション溶液
溶液D:洗浄溶液
仕上剤:褪色防止剤
3つのウエルを有するスライド(「VIT」マークを付けた実際のハイブリダイゼーション用ウエル;「−」マークを付けたネガティブコントロール用ウエル;「+」マークを付けたポジティブコントロール用ウエル)
カバーグラス
4.手順
分析に先立ち、乾燥チャンバを46℃に予熱する。
試料を適用し、固定する。
【0111】
1.VIT反応容器の蓋にスライドを挿し込む。
【0112】
2.スライド上の3つのウエルそれぞれに1滴の試料材料を移し、(VIT反応容器の外で)スライドを水平状態で(46℃、30分間または完全に乾燥するまで)インキュベートする。
【0113】
3.スライド上の各ウエルに1滴の「溶液A」を加え、(VIT反応容器の外で)スライドを水平状態で(46℃、30分間または完全に乾燥するまで)インキュベートする。
【0114】
4.スライド上の各ウエルに1滴の「溶液B」を加え、(VIT反応容器の外で)スライドを水平状態で(室温、1分間または完全に乾燥するまで)インキュベートする。
ハイブリダイゼーション
5.「−」マークを付けたスライドウエルに1滴の「ネガティブコントロール」を加える。
【0115】
6.「+」マークを付けたスライドウエルに1滴の「ポジティブコントロール」を加える。
【0116】
7.「VIT」マークを付けたスライドウエルに1滴の「VIT」を加える。
【0117】
8.VIT反応容器にトレイを半分まで挿し込む。
【0118】
9.VIT反応容器のトレイに約20〜30滴の「溶液C」を加え、トレイを反応容器に完全に挿し込む。
【0119】
10.スライドを慎重かつ水平にVIT反応容器に挿し込み、VIT反応容器を閉め、水平状態でインキュベートする(46℃、1.5時間)。
注意:個々の液滴を混合させてはならない!
11.洗浄溶液を調製する。
【0120】
各VIT反応容器には25mlの洗浄溶液が必要である。このために、「溶液D」を蒸留水で10倍希釈する。表3に希釈率の例を示す。
【0121】
【表3】
12.ハイブリダイゼーション中、乾燥チャンバ内の密閉容器中の洗浄溶液を46℃に予熱する。
洗浄
13.VIT反応容器を注意深く開き、スライドを取り出す。
【0122】
14.注意:個々の液滴を混合させてはならない。
【0123】
15.VIT反応容器を適切な位置に置き、予熱済み(ステップ5.2.7参照)洗浄溶液を目盛まで加える。スライドを垂直に挿し込み、VIT反応容器を閉じ、垂直状態でインキュベートする(46℃、15分)。
【0124】
16.VIT反応容器を開き、スライドを取り出す。洗浄溶液を浴びせる。
【0125】
17.VIT反応容器に蒸留水を目盛まで加える。スライドを垂直に挿し込み、次いで素早く取り出す。水を浴びせる。
【0126】
18.スライドを垂直に配置し、(46℃、15分間または完全に乾燥するまで)インキュベートする。
【0127】
19.各スライドウエル間に1滴の「仕上剤」を加え、カバーガラスを乗せる。
【図面の簡単な説明】
【0128】
【図1】16S rRNAの二次構造モデルの図。
【図2】FISH法の略図。in situハイブリダイゼーション中、異なる標識を付けたプローブAおよびBが細胞AおよびCに侵入する。細胞Aは、タイプAプローブ結合部位を有するがタイプBプローブ結合部位は有していないリボソーム核酸を含んでおり、したがって、タイプBのプローブは結合できない。細胞Cは、プローブA結合部位もプローブB結合部位も有しておらず、したがって、2種のプローブのいずれとも結合できない。続く洗浄ステップの後、細胞中には結合したプローブのみが存在する。細胞Aは、その蛍光シグナルにより、蛍光顕微鏡で検出することができる。
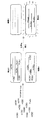
【図3】本発明のin situハイブリダイゼーション装置の特別な実施形態の構成部品の平面図: (左から右に)容器1、トレイ3、スライド4、支持脚8を有する蓋6。
【図4】スライド4を固定するためのスロット5と支持脚8とスライド4とを有する蓋6の特に好ましい実施形態の略図。
【図5】本発明のin situハイブリダイゼーション装置の好ましい実施形態の略図。トレイ3は、液体取り込み用の小さいウエルを有し、最初は、湿潤チャンバ1に必要なハイブリダイゼーション溶液を充填し得るように一部分だけ湿潤チャンバ1に挿し差し込まれる。
【図6】トレイ3が完全に差し込まれている本発明のin situハイブリダイゼーション装置の特別な実施形態の略図。
【図7】蓋6に固定されたスライドが挿し込まれる、本発明のin situハイブリダイゼーション装置の特に好ましい実施形態の略図。
【図8】本発明のin situハイブリダイゼーション装置の好ましい実施形態の略図。湿潤チャンバ内の横軸受またはガイドレールにより、スライドおよびトレイのチャンバ内への挿し込みが容易になり、チャンバ内でスライドおよびトレイがさらに固定または安定化される。チャンバおよび蓋は、水平状態でも垂直状態でも安定しているような構造を有する。(a)分り易くするために本発明のin situハイブリダイゼーション装置の部品が透けて示されている略斜視図。(b)(a)の輪郭図。
【図9】本発明のin situハイブリダイゼーション装置を用いたin situハイブリダイゼーションにより微生物を特異的に検出するための本発明のin situハイブリダイゼーション装置の個々の構成部品のアセンブリの略図。
【図10】蓋6の好ましい実施形態の尺度図。
【図11】トレイ3の好ましい実施形態の尺度図。
【図12】容器1すなわちチャンバ1の好ましい実施形態の尺度図。
【0001】
本発明は、微生物を特異的に検出するためのin situハイブリダイゼーション装置、in situハイブリダイゼーションにより微生物を特異的に検出する方法、および試料中の微生物の同定および視覚化を可能にするキットに関する。
【背景技術】
【0002】
現行の細菌判別法はいずれも共通の目標を有しており、細菌培養の必要性を排除することにより培養の不利点を回避しようとしている。
【0003】
PCR、すなわちポリメラーゼ連鎖反応では、細菌特異的プライマーを用いて細菌ゲノムの特定の特性セグメントを増幅させる。プライマーがその標的部位を見つけると、その遺伝情報セグメントの何百万もの増幅産物が生成される。DNAフラグメントを分離するためのアガロースゲルによるその後の分析で定性評価を行うことができる。最も簡単なケースでは、これによって、分析試料中に標的部位が存在するという情報が得られる。標的部位は、生細菌、死細菌または裸のDNA由来であり得るので、他の結論は得られない。この場合、判別は不可能である。この技術をさらに発展させたものが定量PCRであり、これは、存在する細菌の量と、得られ、増幅されたDNAの量との間に相関関係を生成させようとするものである。
【0004】
しかし、細菌の同定には生化学的パラメータも用いられる。キノン分析に基づいて細菌プロファイルを得る方法は、出来る限り偏りを少なく細菌群を示すのに役立つ〔ヒライシ エー(Hiraishi,A.)、Respiratory quinone profiles as tools for identifying different bacterial populations in activated sludge、J.Gen.Appl.Microbiol.第34巻:39−56ページ(1988年)〕。しかし、この方法も、参照データベースの作製に単一培養細菌のキノンプロファイルを必要とするので、個々の細菌の培養に依存する。さらに、細菌のキノンプロファイルが決定されても、試料中に実際に存在する集団分布の実像は得られない。
【0005】
上記とは対照的に、抗体による細菌検出法はもっと直接的な方法である〔ブリグモン アール エル(Brigmon,R.L.)、ジー ビットン(G.Bitton)、エス ジー ザム(S.G.Zam)、およびビー オブライエン(B.O’Brien)、Development and application of a monoclonal antibody against Thiothrix spp.、Appl.Environ.Microbiol.第61巻:13−20ページ(1995年)〕。蛍光標識した抗体を試料と混ぜ、細菌の抗原に高特異的に結合させる。次いで、エピ蛍光顕微鏡で、発せられる蛍光により細菌を検出する。このようにして、細菌は菌株レベルまで同定することができる。しかし、この方法の適用は3つの重要な不利点によって制限される。第1に、抗体の産生に単一培養が必要である。第2に、抗体−蛍光分子複合体は、体積が大きくて扱いにくいことが多く、そのために標的細胞に侵入する際に問題が生じる。第3に、検出が特異的に過ぎることが多い。抗体の生産には費用がかかり、1種類の特異的細菌株だけしか検出されないことが多く、同じ細菌種の他の株を検出することができない。しかし、多くの場合、細菌の株特異的検出は不要であり、それよりむしろ細菌種または細菌群全体の検出の方が必要とされる。第4に、抗体の生産は比較的冗長で費用のかかる手順である。
【0006】
PCRなどの分子生物学的方法の特異性と、抗体法に代表されるような細菌視覚化の可能性とを組み合わせたユニークな方法は、蛍光in situハイブリダイゼーション法〔FISH;アマン アール アイ(Amann,R.I.)、ダブリュー ルドウィッヒ(W.Ludwig)、およびケー−エイチ シュライファー(K.−H.Schleifer)、Phylogenetic identification and in situ detection of individual microbial cells without cultivation、Microbiol.Rev.第59巻:143−169ページ(1995年)〕である。この方法によって、細菌の種、属または群を試料中で直接、高特異的に視覚化し、同定することができる。この方法は、生物群の実際のあるがままの(in situ)分布についての偏りのない実像を与える唯一の方法である。これまでに培養されたことのない細菌、したがって、特性決定されていない細菌でさえ、試料中で直接同定可能であり、視覚化することもできる。
【0007】
FISH法は、その極めて重要な機能ゆえに進化の過程において極くわずかしか突然変異しなかった特定の分子、すなわち、16Sおよび23Sリボソームリボ核酸(rRNA)が細菌細胞中に存在するという事実に基づいている。どちらのリボ核酸も、タンパク質生合成の場であるリボソームの構成成分であり、それらの遍在分布、サイズ、および構造的かつ機能的不変性により、系統発生のマーカーとして役立ち得る〔ウーズ シー アール(Woese,C.R.)、Bacterial evolution、Microbiol.Rev.第51巻:221−271ページ(1987年)〕。比較配列分析に基づき、専らこれらのデータから系統発生関係を誘導することができる。このためには、これらの配列データを整列化(アライン)しなければならない。これらの巨大分子の二次構造および三次構造についての知識に基づいて整列化する際には、リボソーム核酸の相同部位を相関させる。図1は、16S rRNAの二次構造モデルを示している。
【0008】
これらのデータに基づき、系統学的な計算を実施し得る。最新のコンピュータテクノロジーを用いることにより、例えこれらのデータが大規模であっても迅速かつ効率的な計算が可能になるだけでなく、16S rRNAおよび23S rRNAの整列化された配列を含む大きなデータベースを確立することができる。このデータ材料に高速アクセスすることにより、新規に得られた配列を短時間で系統学的に解析することができる。これらのrRNAデータベースは、特異的遺伝子プローブの構築に用い得る。それによって、すべての利用可能なrRNA配列を比較し、細菌の種、属または群を特異的に検出する特定配列部分用プローブを設計する。
【0009】
FISH(蛍光in situハイブリダイゼーション)においては、リボソーム標的配列上の特定の領域に相補的なこれらの遺伝子プローブを細胞に導入する。通常、これらの遺伝子プローブは、16〜20塩基長の小さい一本鎖デオキシリボ核酸フラグメントであり、細菌種または細菌群に特有な標的領域用につくられている。蛍光標識遺伝子プローブが細菌細胞内で標的配列を見つけると、このプローブは標的配列に結合し、それらの蛍光により細菌細胞を蛍光顕微鏡で検出することができる。図2は、in situハイブリダイゼーションの手順を示している。
【0010】
培養に依存した方法では、微生物群の構成および動態に対して極めて偏った認識しか得られない。FISH法を用いて、例えば、活性汚泥の微生物相(フローラ)の検出の際に、培養することにより培養シフトが生じることを証明することができた〔ワグナー エム(Wagner,M.)、アール アマン(R.Amann)、エイチ レマー(H.Lemmer)、およびケー エイチ シュライファー、Probing activated sludge with oligonucleotides specific for proteobacteria:inadequacy of culture−dependent methods for describing microbial community structure、Appl.Environ.Mcrobiol.第59巻:1520−1525ページ(1993年)〕。
【0011】
実際の細菌群構造がこのように培地依存的に偏ることによって、活性汚泥中では副次的な役割しか果たさないが使用培養条件には十分に適合した細菌の重要性が劇的に過大評価される。したがって、そのような培養のアーチファクトにより、アシネトバクター(Acinetobacter)属細菌が、廃水処理における生物学的リン酸除去剤としてのその役割に関してまったく不正確に評価されてきたことを証明することができた。そのような誤った評価の結果として、コスト集約的で、欠陥があるかまたは不的確なプラントが設計される。そのようなシミュレーション計算の効率および再現性は低い。
【0012】
培養を用いる細菌同定法と比べたFISH法の利点は多岐にわたる。第1に、遺伝子プローブを用いた方がより多くの細胞を検出できる。培養では、1つの試料の細菌群の最大15%しか視覚化できないのに対し、FISHでは、多くの試料の全細菌群の100%まで検出できる。第2に、細菌群の活性部分を全細菌用につくられたプローブと非特異的な細胞染色との割合によって測定し得る。第3に、細菌は、直接in situ(その場)で視覚化される。したがって、種々の細菌群間で起こり得る相互作用を見分けて、分析することができる。第4に、FISH法を用いた細菌の検出は培養を用いた場合よりはるかに迅速である。培養を用いた細菌の同定には数日を要することが多いのに対し、FISH法を用いると、試料の採取から細菌の同定までに要する時間は、種レベルの同定においてさえ数時間しかかからない。第5に、遺伝子プローブは、それらの特異性にほとんど制限されることなく選択することができる。1つのプローブで、属または細菌群全体だけでなく個々の種をも検出し得る。第6に、細菌種または全細菌群を試料中で直接正確に定量し得る。培養とそれに伴う不十分な定量は必要ない。
【0013】
ある試料中に存在する細菌を生物分類学的に調べるときには、トップ・ダウンアプローチを利用する。これは、先ず、特異性が出来得る限りおおまかである、すなわち、特異性が低い、細菌群全体のみを検出する遺伝子プローブを用いて細菌試料を分析する。用いるプローブの特異性を連続的に高めることにより、最終的に未知の細菌が同定される。
【0014】
このように、FISH法は、試料中で直接細菌を迅速かつ高特異的に検出するための優れたツールである。培養を用いる方法とは対照的に、FISH法は直接的な手順であり、現行の方法とは異なり、細菌の視覚化だけでなくさらに細菌の正確な定量をも可能にする。
【0015】
細菌は評価中に高エネルギー光を照射することにより視覚化されるので、FISH分析は原則としてスライド上で実施される。ハイブリダイゼーション緩衝液またはハイブリダイゼーション溶液および洗浄緩衝液または洗浄溶液などの個々の溶液の組成は当業者には周知であり、例えば、スナイドルら(Snaidr et al.)〔ジェイ スナイドル(J.Snaidr)、アール アマン、アイ フーバー(I.Huber)、ダブリュー ルドウィッヒ、およびケイ−エイチ シュライファー、Phylogenetic analysis and in situ identification of bacteria in activated sludge、Appl.Env.Microb.第63巻7号:2884−2896ページ(1997年)〕に詳細に記載されている。スライド上での微生物分析のFISH手順は、通常、以下のステップを含む:
1. 反応バイアルに微生物試料のアリコート(一定分量)を導入し、アリコートを適当な固定溶液と混合するステップ;
2. 試料が固定され、遺伝子プローブにアクセス可能になるまで数回遠心、洗浄するステップ;
3. 固定された微生物試料のアリコートをスライド上のウエルに加えるステップ;
4. スライド上の微生物をオーブン中40〜90℃で10〜30分間インキュベートして乾燥させるステップ;
5. スライドを50%、70%および100%エタノールを含む溶液中に順次浸して、エタノール濃度を増大させることで微生物細胞を脱水するステップ;
6. 微生物を含有するウエルにハイブリダイゼーション溶液を加えるステップ;
7. 同ウエルにプローブ溶液を加えるステップ;
8. セルロース片を折り曲げてプラスチックチューブに挿入し、次いで、チャンバ内のセルロースを数mlのハイブリダイゼーション溶液で湿らせて湿潤チャンバを作成するステップ;
9. スライドを湿潤チャンバ内のセルロース上に水平に配置するステップ;
10. 湿潤チャンバをインキュベーションオーブンに移し、1〜2時間インキュベートするステップ;
11. 湿潤チャンバを開き、スライドを取り出して、蒸留水で手短にリンスするステップ;
12. 湿潤チャンバを廃棄するステップ;
13. 新たなプラスチックチューブに洗浄緩衝溶液を充填するステップ;
14. 洗浄溶液を充填したプラスチックチューブにリンスしたスライドを挿入するステップ;
15. プラスチックチューブに挿入したスライドを、インキュベーションオーブン中で10〜30分間インキュベートするステップ;
16. プラスチックチューブからスライドを取り出し、蒸留水で洗浄するステップ;
17. スライドを上下に動かして風乾するステップ;
18. 褪色防止剤をスライド上に加えた後、エピ蛍光顕微鏡でスライドを視検することができる。
【発明の開示】
【発明が解決しようとする課題】
【0016】
しかし、上述の微生物を検出するための従来のFISH法は、実質的な不利点を有している。上記方法は、複雑かつ冗長で、いくつかの誤差源のために一貫した質で再現することができない。これを以下に詳細に説明する。
【0017】
何回もの洗浄、遠心ステップのために、試料の固定効率にばらつきが生じ得る。この結果、後続のハイブリダイゼーションステップにおいて、遺伝子プローブが様々な効率で細胞に侵入するために、エピ蛍光顕微鏡で細胞を検出するときに明度の変動が生じる。しかし、明度は細胞のリボソーム含量と相関している。したがって、例えばFISH分析の例で言えば、蛍光強度は、細胞の増殖状態が試料採取時に良好であったかまたは不良であったかを判定する尺度である。この情報は、特に医学微生物学、それだけでなく食品または環境微生物学においても、試料の微生物についての状態を全体的に評価するために重要である。したがって、分析試料固定時に効率が変動することにより、試料の増殖状態ひいては全体的な状態について偏った情報がもたらされる。
【0018】
さらに、非効率的固定によるシグナル強度不良は、エピ蛍光顕微鏡で視覚化するときに、小細胞またはリボソーム含量が低い細胞をも検出する検査者の能力を低下させる。それに加え、種々の洗浄、遠心ステップのために、反応バイアルで固定プロセスを実施している間に細胞が失われることがある。
【0019】
従来のFISH法の別の問題は、数回のインキュベーション間の細胞脱水時に、細胞がスライドから剥離したり、他のウエルに移ってしまう可能性があることである。
【0020】
さらに、プローブ溶液とハイブリダイゼーション溶液とを別々にすると、2種の異なる溶液をスライドウエルに加えなければならないので、作業費用が高くなる。
【0021】
さらに、湿潤チャンバの作成は不便であり、スライドの水平配置が保証されない。そのために、異なるウエル中に存在する別の溶液が混じってしまう可能性がある。
【0022】
上記文献に引用されているようなハイブリダイゼーションチャンバとして丸いプラスチックチューブを用いる際の別の問題は、インキュベーションオーブン中で、湿潤チャンバがいつも不安定な状態にあることである。この不安定な状態により、スライドも不安定になって、異なるスライドウエルの溶液が混ざってしまうことがある。
【0023】
さらに、スライドを、先ず洗浄ステップでリンスし、次いで、別の容器に移さなければならない。この比較的冗長なプロセス中にハイブリダイゼーション温度が低下することにより、核酸プローブ分子と細胞との非特異的結合が生じ得る。
【0024】
従来のFISH法の他の問題は、蒸留水を用いた洗浄ステップ中に細胞が洗い落とされるか、別のスライドウエルに流入し得ること、および、垂直状態で風乾している間にスライドから流れ落ちる液滴を介して、細胞が1つのスライドウエルから次のスライドウエルに移り得ることである。スライドが不安定状態にあるために、スライドがひっくり返ったり、細胞が剥がれたりし得る。
【0025】
再現性不良で、操作が複雑、冗長かつ不便であることによって、in situハイブリダイゼーション一般、特にFISH分析は、これまで産業にはめったに利用されなかった。しかし、これらの手順を用いた細菌分析は、現在産業に用いられている他のすべての微生物学的分析法に比べて有意な利点を有しているので、in situハイブリダイゼーション、特にFISH法による微生物の簡単かつ再現性のある同定を可能にするデバイスまたは方法が求められている。
【0026】
したがって、上述した従来技術の不利点を克服し、試料中の微生物の迅速な同定を容易かつ再現性よく実施し得るデバイスまたは装置および方法を提供することが本発明の目的である。
【0027】
他の目的は本発明の以下の説明から明らかにされる。
【課題を解決するための手段】
【0028】
上述の目的は、本発明にしたがって独立クレームの特徴により解決される。さらなる実施形態は従属クレームの特徴に由来する。
【0029】
本発明により、微生物を特異的に検出するためのin situハイブリダイゼーション装置が提供され、この装置は、少なくとも1つの開口部2を有する容器1と、ハイブリダイゼーション溶液用支持台3と、スライド4と、スライド用固定手段5とを備えている。この装置は、容器開口部の密閉、特に、水密および/または気密シールに適した蓋6を備えているのが好ましい。この文脈における用語「密」とは、容器内に存在する湿分が閉鎖された容器から実質的に漏れないことを意味する。
【0030】
スライドは、分析試料や、場合により、ネガティブコントロールまたはポジティブコントロールとなる試料を互いに別々に加え得るウエル9を備えているのが好ましい。スライド上のウエルは、一次元でのみ他のウエルに隣接し、例えば一列に配置されているのが特に好ましいが、ウエルが列内でジグザグ配置されていてもよい。
【0031】
本発明のin situハイブリダイゼーション装置の好ましい実施形態において、蓋はスライド用固定手段5を備えている。蓋は、スライド用固定手段として、スライドの一方の端部7を差し込み得るスロット5を有しているのが特に好ましい。
【0032】
代替例として、スライドを、容器の構成部品、例えば容器底部のスロット形態の固定手段5と係合させてもよいことは勿論であり、この場合、底部は容器の開口部の反対側に配置される。
【0033】
本発明の装置の別の好ましい実施形態において、蓋は、スライドが水平に配置されているときに、固定スライドを有する蓋を蓋のない装置から離れて安定させ得る構造要素8を有している。
【0034】
蓋は、スライドが水平または垂直または横向き配置されているときに、固定スライドを有する蓋を蓋のない装置から離れて立っていられるように構成するのが特に好ましい。
【0035】
本発明の範囲内でスライドの水平配置とは、試料またはプローブをわきに流さずにスライド上に加え得るようなスライド配置を意味する。
【0036】
本発明の範囲内で横向き配置とは、水平配置に比べて90°回転させた配置を意味し、スライドは、ウエルが一次元でのみ他のウエルに隣接しているならば、液滴が、場合によりスライド上の別のウエルに流入することなくスライドを流れ落ち得るように90°回転されている。
【0037】
本発明の範囲内でスライドの垂直配置とは、水平配置に比べても横向き配置に比べても90°回転させた配置を意味する。
【0038】
本発明の装置の特に好ましい実施形態において、容器および/または蓋は、蓋が閉鎖されていないときも閉鎖されているときも、スライドが水平、垂直または横向き配置されているときに装置を安定配置し得るように構成される。
【0039】
さらに、本発明によれば、容器または装置内でスライドを安定化するために容器がスライド用の横軸受10もしくはガイドレールを備えている装置であって、そのような軸受10が容器の構成部品である装置が好ましい。
【0040】
さらに、ハイブリダイゼーション溶液用支持台3は、取り外し可能であるか、挿入可能であるのが好ましい。さらに、本発明によれば、ハイブリダイゼーション溶液用支持台3は容器内に完全に挿入し得るのが好ましい。しかし、ハイブリダイゼーション溶液用支持台3は、また、段階的に、特に連続的に、容器1内に挿入し得るのも好ましい。
【0041】
別の好ましい実施形態において、容器1は、内部でハイブリダイゼーション溶液用支持台3を安定化させるためにハイブリダイゼーション溶液用支持台3用の横軸受11を備えているか、またはそのような軸受11は容器1の構成部品である。
【0042】
代替例として、ハイブリダイゼーション溶液用支持台は、容器の固定部品、特に容器内のウエルまたは凹みである。
【0043】
本発明の装置の特に好ましい実施形態において、ハイブリダイゼーション溶液用支持台は、トレイ3、特に、液体取り込み用および/または液浸パッド取り込み用ウエル12を備えたトレイである。
【0044】
スライドを除く装置の全部品の材料は、好ましくはプラスチック、特に好ましくはポリエチレンおよび/またはポリプロピレンを包含する。さらに、上述の装置部品の材料は金属も包含し得る。
【0045】
スライドは、好ましくはガラス製、特に好ましくはDIN 12111に基く加水分解等級1〜4に相当するガラス製である。
【0046】
本発明の他の態様において、in situハイブリダイゼーションにより微生物を特異的に検出する方法が提供され、この方法は、以下のステップ:
(a) 試料中に含まれている微生物を固定するステップ;
(b) 固定細胞を検出可能な核酸プローブ分子と共にインキュベートするステップ;
(c) ハイブリダイズしなかった核酸プローブ分子を除去または洗い落とすステップ;および
(d) 核酸プローブ分子とハイブリダイズした細胞を検出するステップ
を含み、
ステップ(a)〜(c)と、場合によりステップ(d)は、本発明のin situハイブリダイゼーション装置を用いて実施する。
【0047】
固定ステップおよび/または場合により乾燥ステップは、スライド上で実施するのが好ましい。
【0048】
さらに、本発明によれば、スライドが横向きに配置されているときにスライドの最終乾燥を行い、かつ/またはスライドが水平配置されているときにインキュベーションを行い、かつ/またはスライドが垂直配置されているときに洗浄を行うのが好ましい。
【0049】
本発明の方法の別の好ましい実施形態では、ステップ(b)で、ハイブリダイゼーション溶液と核酸プローブ分子溶液との混合物をスライドに加える。
【0050】
上述の混合物は滴下容器を用いて加えるのが特に好ましい。この滴下容器は、別の好ましい実施形態では、使い捨て滴下容器または複数回使用可能な滴下容器である。
【0051】
本発明の方法によれば、湿潤チャンバに必要とされるハイブリダイゼーション溶液を、ハイブリダイゼーション溶液用支持台内に配置されたハイブリダイゼーション溶液浸漬パッドを介して本発明の装置内に注入可能である。
【0052】
ステップ(b)で用いられる核酸プローブ分子は、検出対象微生物の染色体DNAもしくはエピソームのDNA、mRNAまたはrRNAに相補的であることが好ましい。
【0053】
本発明によれば、核酸プローブ分子は検出可能なマーカーに共有結合しているのがさらに好ましい。この検出可能なマーカーは、以下のマーカー:
− 蛍光マーカー、
− 化学発光マーカー、
− 放射性マーカー、
− 酵素活性を有する基、
− ハプテン、
− ハイブリダイゼーションにより検出可能な核酸
からなる群から選択するのが好ましい。
【0054】
本発明の方法における微生物は単細胞微生物であるのが好ましい。この微生物は、酵母、細菌、藻類または真菌類であるのが特に好ましい。別の好ましい実施形態において、微生物は廃水細菌である。
【0055】
本発明の方法のさらなる実施形態において、試料は、環境試料であって水、土壌または空気から採取された試料;食品試料、特に、牛乳もしくは乳製品、飲用水、飲料、パン製品または肉製品由来の試料;医学試料、特に、組織、分泌物もしくは糞便から採取された試料;廃水試料、特に、活性汚泥、消化汚泥もしくは嫌気性汚泥から採取された試料;バイオフィルムから採取された試料、特に、バイオフィルムが産業施設から採取されるか、排水処理の過程で生成されるか、もしくは天然バイオフィルムである試料;または、医薬品もしくは化粧品から採取された試料である。
【0056】
さらに、本発明により、in situハイブリダイゼーションにより微生物を特異的に検出するためのキットが提供され、このキットは、微生物を特異的に検出するための少なくとも1つの核酸プローブ分子と、少なくとも1種のハイブリダイゼーション溶液と、場合により、ネガティブコントロールとなる核酸プローブ分子と、場合により、ポジティブコントロールとなる核酸プローブ分子と、場合により、洗浄溶液と、場合により、固定溶液と、場合により、褪色防止剤と、本発明のin situハイブリダイゼーション装置とを含む。
【0057】
本発明のキット中の核酸プローブ分子は、検出対象微生物の染色体もしくはエピソームのDNA、mRNAまたはrRNAに相補的であるのが好ましい。
【0058】
本発明の好ましい実施形態において、本発明のキット中の核酸プローブ分子は、検出可能なマーカーに共有結合しているのが好ましい。検出可能なマーカーは、蛍光マーカー、化学発光マーカー、放射性マーカー、酵素活性を有する基、ハプテンおよびハイブリダイゼーションにより検出可能な核酸からなる群から選択するのが特に好ましい。
【0059】
本発明の別の主題は、in situハイブリダイゼーションにより微生物を特異的に検出するための本発明のin situハイブリダイゼーション装置の利用法である。
【0060】
最後に、本発明の別の主題は、本発明の方法における本発明のキットの利用法である。
【発明を実施するための最良の形態】
【0061】
この度、驚くべきことには、簡単かつ再現可能な方法で微生物を迅速かつ安全に同定し得るin situハイブリダイゼーション装置を提供することが可能になった。本発明の装置は、少なくとも1つの開口部を有し、以後チャンバとも称される容器と;容器もしくはチャンバに完全に挿入し得るか、または容器の一部であるハイブリダイゼーション溶液用支持台、特にトレイと;スライド用固定手段とを備えている。さらに、この装置は、in situハイブリダイゼーション用チャンバ内に挿入可能なスライドを備えている。本発明の装置の構造は図3に示されている。
【0062】
本発明の装置は、容器開口部の密閉、特に、水密および/または気密シールに適した蓋をさらに備えているのが好ましい。スライドはこの蓋に固定されるのが好ましく、スライドがこの蓋に挿し込まれるのが特に好ましい。この好ましい実施形態において、スライドは、蓋にきっちりかつ安全に挿し込まれるが、最終的な分析のために極度の力を加えなくても再び手で蓋から取外すことができる。蓋を固定するか、きっちり締めることにより、本発明の装置が垂直配置されているときでも洗浄手順を確実に実施することができる。
【0063】
本発明の装置の特に好ましい実施形態において、蓋は、スライドが水平または垂直配置されているときに固定スライドを有する蓋を装置から離れて安定させ得る構造部品を備えているか、またはそのような構造部品を有している。本発明に従って、例えば蓋に支持脚を取り付けることによって得られるこの蓋の安定性により、実施されるいずれの反応時にもスライドを水平状態に維持することができる。
【0064】
取り扱いを容易にするためには、スライドをin situハイブリダイゼーション装置の蓋に固定するのが好ましい(図4参照)。この場合、スライドを、本発明のハイブリダイゼーション法の初めから終わりまで蓋に固定された状態に保ち得る。さらに、洗浄、固定などのすべての処理手順を同じ反応チャンバ内で実行することもできる。スライドが水平または垂直配置されているときに蓋を装置から離れて安定配置し得る構造部品を蓋が備えていることは、試料およびプローブの使用時にもスライドを蓋に付いたままにしておけるだけでなく、試料使用時にスライドが平坦かつ安定に配置されるという重要な利点を有する。さらに、蓋の構造部品または支持脚により、スライドが蓋に固定された状態で、スライド上で核酸プローブと細胞とのハイブリダイゼーションを実現させるための個別反応を実施することができる。さらに、上記構造部品を備えた蓋を用いて、すべての乾燥ステップをチャンバ外で実施することもできる。固定スライドを有する蓋が平坦かつ安定して立っていられるので、スライド上での試料の混合を防止することができる。
【0065】
本発明の別の好ましい実施形態において、容器および/または蓋は、蓋を閉めた状態で、スライドが水平配置されているときに装置が安定な状態に置かれるように構成される。したがって、特に本発明の方法のステップ(a)および(b)におけるスライドの水平配置は、本発明のin situハイブリダイゼーション装置部品の支持面の構成により得られる。
【0066】
トレイをハイブリダイゼーション溶液用支持台として用いることにより、湿潤チャンバに必要なハイブリダイゼーション溶液を安全かつ清潔に本発明の装置に導入することができる。トレイは、液体を取り込むための小さなウエルまたは凹みを有しているのが好ましい(図5参照)。湿潤チャンバを作成するのに必要なハイブリダイゼーション溶液をトレイに充填し得るように、先ずトレイの一部のみをチャンバ内に挿入するのが特に好ましい。次いで、トレイを完全にチャンバ内に挿入する(図6参照)。
【0067】
あるいは、ハイブリダイゼーション溶液用支持台としてセルロースを用いてもよい。
【0068】
ハイブリダイゼーション溶液を滴下し、使用後に取り外すことができる交換可能なトレイを構成することは、規定量のハイブリダイゼーション溶液を本発明のin situハイブリダイゼーション装置に迅速導入し得るという利点を有する。セルロースの利用は不可欠ではないが、排除もされない。
【0069】
ハイブリダイゼーション溶液を本発明のin situハイブリダイゼーション装置に導入するための別の代替案は、トレイに配置された使い捨てパッドを介してハイブリダイゼーション溶液を反応装置に導入する方法である。使い捨てパッドは鮮度保持シールでシールするのが好ましく、トレイをチャンバに挿入した後直ぐにシールを除去すると、ハイブリダイゼーション溶液がチャンバ内で蒸散し得る。
【0070】
微生物を特異的に分析するためのin situハイブリダイゼーションを迅速かつ簡単に実施するために本発明のin situハイブリダイゼーション装置で実施される方法の好ましい実施形態は、以下のステップ:
(a) スライド上で試料中に含まれている微生物を固定するステップ;
(b) ハイブリダイゼーションを実現させるために本発明の装置で固定細胞を核酸プローブと共にインキュベートするステップ;
(c) ハイブリダイズしなかったオリゴヌクレオチドを除去または洗い落とすステップ;
(d) オリゴヌクレオチドにハイブリダイズした細胞を検出するステップ
を含む。
【0071】
インキュベーションおよび洗浄手順は、本発明のin situハイブリダイゼーション装置内で行うのが好ましい。
【0072】
微生物は、通常行なわれているように最初に反応容器内で固定してから固定化するのではなく、固定および/または場合により乾燥をスライド上で直接行うのが好ましい。
【0073】
上記のようにスライド上で固定すると、細胞の損失が回避され、その取扱いが著しく容易になり、実施がはるかに簡単になる。さらに、スライド上で固定することにより、固定ステップとその後の脱水を1つの手順に組み合わせることができる。
【0074】
本発明によれば、核酸プローブ分子のハイブリダイゼーションおよび添加は、通常行われているように、ピペットを用いて、先ず規定量のハイブリダイゼーション溶液、次いで規定量のプローブ溶液をスライドウエルに加えるのではなく、スライド上にハイブリダイゼーション溶液とヌクレオチドプローブ分子溶液との混合物を加えるのが好ましい。
【0075】
ハイブリダイゼーション溶液と核酸プローブ分子溶液との混合物を加えることにより、核酸プローブ分子が比較的安定な状態で迅速かつ完璧に処置することが可能になる。
【0076】
上述の混合物は、滴下容器に軽く圧力を加えて滴下するのが好ましい。滴下容器は、複数回使用可能でハイブリダイゼーション溶液とプローブ溶液との混合溶液を数滴分含むものであってもよいし、または代替例として死容積を顧慮した必要量の試薬を入れた小型の使い捨て滴下容器であってもよい。
【0077】
滴下容器を用いると、高価なピペットを使わなくて済むだけでなく、取扱いおよび注入も容易になる。
【0078】
次いで、好ましくは蓋に固定されたスライドをチャンバ内に挿入する(図7参照)。スライドのチャンバ内への挿入、さらには固定または安定化を容易にするために、チャンバ内に横軸受またはガイドレールを取り付けるのが好ましい(図8参照)。
【0079】
チャンバおよび/または蓋は、安定した水平配置だけでなく垂直または横向き配置が確実になるように構成するのが好ましい。
【0080】
その後のインキュベーションは、スライドを水平に配置した状態で実施するのが好ましい。続くスライドの洗浄は、本発明に従って、好ましくはチャンバ内で、特に好ましくはスライドを垂直に配置した状態で実施する。
【0081】
スライドを最終乾燥、特に最終風乾するためには、蓋を横向きに配置し得るように構成するのが好ましい。このようにすると、液滴がスライドの別のウエルに流れ込まずにスライドを流れ落ちるので特に好都合である。
【0082】
結果として、ほとんどの処置ステップを、チャンバと好ましくは装置の蓋とからなる単一容器内で実施するのが好ましい。
【0083】
図9に、蓋と、チャンバと、トレイと、挿入されたスライドとを有する本発明のin situハイブリダイゼーション装置の好ましい実施形態の全構造を示す。図10〜図12は、蓋、トレイおよびチャンバの寸法を示している。
【0084】
したがって、従来のin situハイブリダイゼーション法、特に従来のFISH法と比較した、微生物を特異的に検出するための本発明のin situハイブリダイゼーション装置および本発明の方法の極めて重要な利点は、取扱いが非常に容易であることと、試料中の微生物の特異的検出を可能にする速度および再現性である。
【0085】
本発明の範囲内において、微生物の「固定」とは、微生物の細胞エンベロープを核酸プローブに対して透過性にする処理を意味する。それによって、オリゴヌクレオチドとこれに結合させたマーカーとからなる核酸プローブは、細胞内の核酸プローブに対応する標的配列に結合するべく細胞エンベロープを透過することができる。結合とは、相補的核酸領域間の水素結合の生成と解釈されるべきものである。エンベロープは、ウイルスをコートする脂質エンベロープ、細菌の細胞壁または単細胞真核生物の細胞膜であってよい。固定には通常エタノールを用いる。これらの手段を用いても細胞壁を核酸プローブに対して透過性にし得ない場合、専門家は同じ結果をもたらす他の手段を知っているであろう。そのような手段には、例えば、低濃度のパラホルムアルデヒド溶液またはホルムアルデヒド希釈液、メタノール、アルコール混合物、酵素処理などが含まれる。
【0086】
本発明の意味での核酸プローブは、通常12〜1000ヌクレオチド、好ましくは12〜50ヌクレオチド、特に好ましくは17〜25ヌクレオチドを有するDNAまたはRNAプローブであってよい。核酸プローブは、相補配列が検出対象微生物中に存在するかどうかという基準に従って選択される。規定配列を選択することにより、細菌種、細菌属または全細菌群を検出し得る。12〜15ヌクレオチド長のプローブでは、配列は100%相補的でなければならない。15を越えるヌクレオチドを有するオリゴヌクレオチドでは、1〜数個のミスマッチが許容される。ストリンジェントなハイブリダイゼーション条件に従って、核酸プローブ分子が標的配列に実際にハイブリダイズする。本発明の意味での穏和な条件とは、例えば、実施例1に記載のようなハイブリダイゼーション溶液中0%のホルムアミドである。本発明の意味でのストリンジェントな条件とは、例えばハイブリダイゼーション溶液中20〜80%ホルムアミドである。
【0087】
ハイブリダイゼーションの持続時間は通常10分〜12時間であるが、ハイブリダイゼーションは約2時間持続するのが好ましい。ハイブリダイゼーション温度は、好ましくは44〜48℃、特に好ましくは46℃であり、ハイブリダイゼーション温度のパラメータならびにハイブリダイゼーション溶液中の塩および界面活性剤の濃度は、1種類または複数のプローブに応じて、特にその長さや検出対象細胞中の標的配列に対する相補度に応じて最適化し得る。この点で標準的な計算法は当業者には公知である。
【0088】
本発明の方法の範囲内で、標準的なハイブリダイゼーション溶液は、0.1〜1.5M、好ましくは0.9Mの塩濃度を有し、塩は塩化ナトリウムであるのが好ましい。さらに、ハイブリダイゼーション溶液は、通常、0.001〜0.1%の濃度、好ましくは0.01%の濃度のドデシル硫酸ナトリウム(SDS)などの界面活性剤と、0.001〜0.1Mの範囲の濃度、好ましくは0.02Mの濃度のトリス/HClとを含んでいる。トリス/HClのpHは、通常6〜10であるが、約8.0のpHが好ましい。上述のように、ハイブリダイゼーション溶液は、所望または要求されるストリンジェンシーの度合いに応じて、0〜80%のホルムアミドをさらに含み得る。
【0089】
ハイブリダイゼーション溶液には、可能なら15〜1000ngの量の核酸プローブが存在しなければならないが、この量は、8〜100μl、好ましくは40μlのハイブリダイゼーション溶液量中に含まれていなければならない。プローブ濃度は、111ng/40μlハイブリダイゼーション溶液が特に好ましい。
【0090】
ハイブリダイゼーション終了後、ハイブリダイズしなかった過剰なプローブ分子を除去しなければならないが、これは、普通、通常の洗浄溶液または通常の洗浄緩衝液を用いて実施する。この洗浄溶液は、所望なら、0.001〜0.1%、好ましくは0.01%の濃度のSDSなどの界面活性剤と、0.001〜0.1M、好ましくは0.02Mの濃度のトリス/HClとを含んでいてよく、トリス/HClのpHは、6.0〜10.0の範囲、好ましくは8.0である。洗浄溶液中には界面活性剤が存在し得るが、これは絶対要件ではない。洗浄溶液は、通常、NaClをさらに含んでいてよく、その濃度は、要求されるストリンジェンシーに応じて、0.003〜0.9M、好ましくは0.01〜0.9Mである。洗浄溶液はさらにEDTAを含んでいてよく、その濃度は、0.005Mであるのが好ましい。洗浄溶液はさらに、当業者には公知の通常の保存剤を適量含み得る。
【0091】
結合しなかったプローブ分子の「洗い落とし」は、通常、44〜52℃、好ましくは44〜50℃の範囲、特に好ましくは46℃で、10〜40分間、好ましくは15分間行う。
【0092】
それぞれの核酸プローブは検出対象微生物に基づいて選択する。この場合、核酸プローブは、検出対象微生物の染色体またはエピソームのDNAにも、mRNAまたはrRNAにも相補的であり得る。検出対象微生物中に2以上のコピー数存在する領域に相補的な核酸プローブを選択するのが有利である。検出対象配列は、細胞当たり、好ましくは500〜100000、特に好ましくは1000〜50000のコピー数存在する。このために、標的部位としてrRNAを用いるのが好ましい。というのは、細胞のリボソームはタンパク質生合成部位であり、各活性細胞中に数千コピー存在するからである。
【0093】
本発明に従って、核酸プローブ分子を微生物に透過させ、核酸プローブ分子と微生物の核酸とをハイブリダイズさせるために、核酸プローブを上記の意味で固定された微生物と共にインキュベートする。次いで、ハイブリダイズしなかった核酸プローブ分子を通常の洗浄ステップで除去する。その後、各細胞で特異的にハイブリダイズした核酸プローブ分子を検出することができる。
【0094】
同定および定量の必要条件は、本発明に従って用いられる核酸プローブ分子が検出可能であることである。この検出能は、例えば、核酸プローブ分子と検出可能なマーカーとの共有結合によって得られる。検出可能なマーカーとしては、例えば、いずれも専門家には周知の、CY2、CY3、CY5、FITC、FLUOS、TRITC、またはFLUOS−PRIMEなどの蛍光団が用いられる。蛍光団の例は以下の表1にリストされている。
【0095】
【表1】
あるいは、化学発光団、または35S、32P、33P、125Jなどの放射性標識を用いる。しかし、検出能は、核酸プローブ分子と酵素活性分子、例えば、アルカリホスファターゼ、酸ホスファターゼ、ペルオキシダーゼ、西洋ワサビペルオキシダーゼ、β−D−ガラクトシダーゼ、またはグルコースオキダーゼとを結合させても得られる。これらの酵素それぞれについて、天然基質の代わりに変換可能で、着色産物または蛍光産物に変換可能な多くの色素原が知られている。そのような色素原の例を以下の表2に示す。
【0096】
【表2】
最後に、核酸プローブ分子を、その5′または3′末端にハイブリダイゼーションに適した別の核酸配列を有するように作成することができる。この核酸配列も、約12〜1000、好ましくは15〜50ヌクレオチドを有する。この第2の核酸部分も、上述の化合物または作用物質のいずれかで検出し得るオリゴヌクレオチドプローブによって認識され得る。
【0097】
別の可能性は、検出可能な核酸プローブ分子とハプテンとを結合させることである。標的核酸から核酸プローブ分子を分離した後、今や独立して存在する核酸プローブ分子を検出可能なハプテン認識抗体と接触させることができる。そのようなハプテンの周知例は、ジゴキシゲニンまたはその誘導体である。当業者は、ハイブリダイゼーションに利用されるオリゴヌクレオチドを検出、定量するためのここに挙げた例とは別の多くの実行可能な手段を知っている。
【0098】
さらに、多くの可能な標識によって、2つ以上のオーバーラップする集団またはオーバーラップしない集団を同時に検出することができる。したがって、例えば2つ以上の異なる蛍光マーカーを用いて、数種の細菌群を検出し得る〔アール アマン、ジェイ スナイドル、ダブリュー ルドウィッヒ,およびケイ−エイチ シュライファー、In situ visualization of high genetic diversity in a natural microbial community,J.Bacteriol.第178巻、第12号:3496−3500ページ(1996年)〕。
【0099】
評価は、利用されるプローブの標識の種類に依存する。本発明の範囲内において、評価は、光学顕微鏡、エピ蛍光顕微鏡、化学発光測定装置、蛍光光度計などを用いて有利に実施し得る。
【0100】
本発明の方法を用いて検出される微生物は、原核または真核微生物であってよい。ほとんどの場合、単細胞微生物を検出するのが望ましいであろう。これらの単細胞微生物は、大きな細胞塊、いわゆる糸状体中にも存在し得る。ここで適切な微生物は、主として、酵母、藻類、細菌または真菌類である。
【0101】
本発明の特に好ましい実施形態において、微生物は、廃水処理施設の廃水中に存在する細菌である。
【0102】
本発明の方法は多方面に利用し得る。微生物の存在について環境試料を分析し得る。このために、これらの試料を、空気、水または土壌から採取し得る。
【0103】
本発明の方法の別の適用分野は食品管理である。好ましい実施形態において、食品試料は、牛乳または乳製品(ヨーグルト、チーズ、カッテージチーズ、バター、バターミルク)、飲用水、飲料(レモネード、ビール、ジュース)、パン製品または肉製品から採取する。食品中の微生物を検出するには、場合により、微生物が十分な量で存在することを確実にするために培養してもよい。
【0104】
本発明の方法は、さらに、医学試料の分析にも利用し得る。本発明の方法は、例えば、肺、腫瘍または炎症組織由来、汗、唾液、精液および鼻分泌物などの分泌物由来の生検材料、尿道または膣排出物などの組織標本、ならびに尿または排泄物試料の分析に適している。
【0105】
本発明の方法のさらなる適用分野は、廃水、例えば、活性汚泥、消化汚泥または嫌気性汚泥の分析である。さらに、本発明の方法は、産業施設のバイオフィルムの分析、および天然バイオフィルムまたは廃水処理時に生成されるバイオフィルムの分析に適している。本発明の方法を用いて、医薬品および化粧品、例えば、軟膏、クリーム剤、チンキ、液体製剤などを分析することができる。
【0106】
本発明により、本発明のさらなる態様において、試料中の微生物の検出に本発明の方法を適用するためのキットが提供される。そのようなキットの内容は、実質的に検出対象微生物の性質に基づく。このキットは、主要構成要素として、検出対象微生物それぞれに特異的な1つ以上の核酸プローブと、好ましくは、ネガティブまたはポジティブコントロールとなり得る他の核酸プローブとを含む。さらに、このキットは、ハイブリダイゼーション溶液と洗浄溶液とを含んでいるのが好ましい。ハイブリダイゼーション溶液の選択は、主として、用いられる核酸プローブの長さに依存する。したがって、当業者には公知のように、長さ15ヌクレオチドの核酸プローブのハイブリダイゼーションには、長さ75ヌクレオチドのプローブのハイブリダイゼーションの場合よりストリンジェントでない条件を選択しなければならない。ハイブリダイゼーション条件の例は、例えば、スタール&アマン(Stahl & Amann)(1991年),スタッケブランド&グッドフェロー(Stackebrand and Goodfellow)(編),Nucleic Acid Techniques in Bacterial Systematics;ジョンワイリー&サンズ社(John Wiley & Sons Ltd.),英国チチェスター所在、に記載されている。
【0107】
したがって、本発明により、上述の本発明の方法を実施し得るキットが提供される。好ましい実施形態において、本発明のキットは、微生物を特異的に検出するための少なくとも1つの核酸プローブ分子と、少なくとも1種のハイブリダイゼーション溶液と、場合により、ネガティブコントロールとなる核酸プローブ分子と、場合により、ポジティブコントロールとなる核酸プローブ分子と、場合により、洗浄溶液と、場合により、固定溶液と、場合により、褪色防止剤と、本発明のin situハイブリダイゼーション装置とを含み、この装置またはこの装置の一部で、以下のステップ:
(a) 試料中に含まれている微生物をスライド上で固定するステップ;
(b) ハイブリダイゼーションを実現させるために固定された細胞を核酸プローブと共にインキュベートするステップ;
(c) ハイブリダイズしなかったヌクレオチドプローブ分子を除去または洗い落とすステップ
を実施し得る。
【0108】
好ましい実施形態において、本発明のキットは、廃水処理施設の廃水中に存在する細菌の検出に特異的なプローブを含む。
【0109】
本発明の方法を用いて、in situハイブリダイゼーションを実際に成立させることができる。
【0110】
以下の実施例および図面は本発明の説明に役立つが、決して本発明を制限するものと解釈されるものではない。
(実施例: 廃水試料中の細菌の検出)
1.一般的な説明
以下に「VIT反応容器」とも称される本発明のin situハイブリダイゼーション装置における、以下に「VIT法」とも称される本発明の方法の以下の実施例は、廃水試料中に存在する細菌の定性分析に役立つ。同定は数時間内に完了する。
2.基本原理
この手順では、細菌を蛍光標識オリゴヌクレオチドプローブとハイブリダイズさせ、次いで、エピ蛍光顕微鏡下、スライド上で検出し得る。
3.材料
46℃に予熱した乾燥チャンバ
洗浄溶液を調製、加熱するためのボトル
洗浄溶液を調製するための目盛付きシリンダー
温度計
タイマー
VIT溶液:特異的核酸プローブ分子を含有する溶液
ネガティブコントロール:ネガティブコントロール用溶液
ポジティブコントロール:ポジティブコントロール用溶液
溶液AおよびB:固定溶液
溶液C:ハイブリダイゼーション溶液
溶液D:洗浄溶液
仕上剤:褪色防止剤
3つのウエルを有するスライド(「VIT」マークを付けた実際のハイブリダイゼーション用ウエル;「−」マークを付けたネガティブコントロール用ウエル;「+」マークを付けたポジティブコントロール用ウエル)
カバーグラス
4.手順
分析に先立ち、乾燥チャンバを46℃に予熱する。
試料を適用し、固定する。
【0111】
1.VIT反応容器の蓋にスライドを挿し込む。
【0112】
2.スライド上の3つのウエルそれぞれに1滴の試料材料を移し、(VIT反応容器の外で)スライドを水平状態で(46℃、30分間または完全に乾燥するまで)インキュベートする。
【0113】
3.スライド上の各ウエルに1滴の「溶液A」を加え、(VIT反応容器の外で)スライドを水平状態で(46℃、30分間または完全に乾燥するまで)インキュベートする。
【0114】
4.スライド上の各ウエルに1滴の「溶液B」を加え、(VIT反応容器の外で)スライドを水平状態で(室温、1分間または完全に乾燥するまで)インキュベートする。
ハイブリダイゼーション
5.「−」マークを付けたスライドウエルに1滴の「ネガティブコントロール」を加える。
【0115】
6.「+」マークを付けたスライドウエルに1滴の「ポジティブコントロール」を加える。
【0116】
7.「VIT」マークを付けたスライドウエルに1滴の「VIT」を加える。
【0117】
8.VIT反応容器にトレイを半分まで挿し込む。
【0118】
9.VIT反応容器のトレイに約20〜30滴の「溶液C」を加え、トレイを反応容器に完全に挿し込む。
【0119】
10.スライドを慎重かつ水平にVIT反応容器に挿し込み、VIT反応容器を閉め、水平状態でインキュベートする(46℃、1.5時間)。
注意:個々の液滴を混合させてはならない!
11.洗浄溶液を調製する。
【0120】
各VIT反応容器には25mlの洗浄溶液が必要である。このために、「溶液D」を蒸留水で10倍希釈する。表3に希釈率の例を示す。
【0121】
【表3】
12.ハイブリダイゼーション中、乾燥チャンバ内の密閉容器中の洗浄溶液を46℃に予熱する。
洗浄
13.VIT反応容器を注意深く開き、スライドを取り出す。
【0122】
14.注意:個々の液滴を混合させてはならない。
【0123】
15.VIT反応容器を適切な位置に置き、予熱済み(ステップ5.2.7参照)洗浄溶液を目盛まで加える。スライドを垂直に挿し込み、VIT反応容器を閉じ、垂直状態でインキュベートする(46℃、15分)。
【0124】
16.VIT反応容器を開き、スライドを取り出す。洗浄溶液を浴びせる。
【0125】
17.VIT反応容器に蒸留水を目盛まで加える。スライドを垂直に挿し込み、次いで素早く取り出す。水を浴びせる。
【0126】
18.スライドを垂直に配置し、(46℃、15分間または完全に乾燥するまで)インキュベートする。
【0127】
19.各スライドウエル間に1滴の「仕上剤」を加え、カバーガラスを乗せる。
【図面の簡単な説明】
【0128】
【図1】16S rRNAの二次構造モデルの図。
【図2】FISH法の略図。in situハイブリダイゼーション中、異なる標識を付けたプローブAおよびBが細胞AおよびCに侵入する。細胞Aは、タイプAプローブ結合部位を有するがタイプBプローブ結合部位は有していないリボソーム核酸を含んでおり、したがって、タイプBのプローブは結合できない。細胞Cは、プローブA結合部位もプローブB結合部位も有しておらず、したがって、2種のプローブのいずれとも結合できない。続く洗浄ステップの後、細胞中には結合したプローブのみが存在する。細胞Aは、その蛍光シグナルにより、蛍光顕微鏡で検出することができる。
【図3】本発明のin situハイブリダイゼーション装置の特別な実施形態の構成部品の平面図: (左から右に)容器1、トレイ3、スライド4、支持脚8を有する蓋6。
【図4】スライド4を固定するためのスロット5と支持脚8とスライド4とを有する蓋6の特に好ましい実施形態の略図。
【図5】本発明のin situハイブリダイゼーション装置の好ましい実施形態の略図。トレイ3は、液体取り込み用の小さいウエルを有し、最初は、湿潤チャンバ1に必要なハイブリダイゼーション溶液を充填し得るように一部分だけ湿潤チャンバ1に挿し差し込まれる。
【図6】トレイ3が完全に差し込まれている本発明のin situハイブリダイゼーション装置の特別な実施形態の略図。
【図7】蓋6に固定されたスライドが挿し込まれる、本発明のin situハイブリダイゼーション装置の特に好ましい実施形態の略図。
【図8】本発明のin situハイブリダイゼーション装置の好ましい実施形態の略図。湿潤チャンバ内の横軸受またはガイドレールにより、スライドおよびトレイのチャンバ内への挿し込みが容易になり、チャンバ内でスライドおよびトレイがさらに固定または安定化される。チャンバおよび蓋は、水平状態でも垂直状態でも安定しているような構造を有する。(a)分り易くするために本発明のin situハイブリダイゼーション装置の部品が透けて示されている略斜視図。(b)(a)の輪郭図。
【図9】本発明のin situハイブリダイゼーション装置を用いたin situハイブリダイゼーションにより微生物を特異的に検出するための本発明のin situハイブリダイゼーション装置の個々の構成部品のアセンブリの略図。
【図10】蓋6の好ましい実施形態の尺度図。
【図11】トレイ3の好ましい実施形態の尺度図。
【図12】容器1すなわちチャンバ1の好ましい実施形態の尺度図。
Claims (50)
- 試料中の微生物を特異的に検出するためのin situハイブリダイゼーション装置であって、
− 少なくとも1つの開口部(2)を有する容器、
− ハイブリダイゼーション溶液用支持台(3)、
− スライド(4)、および
− スライド(4)用固定手段(5)
を備えた装置。 - 装置が、容器(1)の開口部(2)を密閉するのに適した蓋(6)を有する、請求項1に記載の装置。
- 蓋(6)がスライド(4)用固定手段(5)を有する、請求項2に記載の装置。
- 蓋(6)が、スライド(4)用固定手段(5)として、スライド(4)の一方の端部(7)を挿し込み得るスロット(5)を有する、請求項3に記載の装置。
- スライド(4)が水平に配置されているときに、固定スライド(4)を有する蓋(6)を、蓋(6)のない装置から離れて安定させ得る構造部品(8)を蓋(6)が備えている、請求項2〜4のいずれか1項に記載の装置。
- スライド(4)が水平、垂直または横向き配置されているときに、固定スライド(4)を有する蓋(6)が、蓋(6)のない装置から離れて立っていられるように蓋(6)が構成されている、請求項2〜5のいずれか1項に記載の装置。
- 蓋(6)が閉鎖されているときも閉鎖されていないときも、スライド(4)が水平、垂直または横向き配置されているときに装置を安定させ得るように、容器(1)および蓋(6)の少なくともいずれかが構成されている、請求項2〜6のいずれか1項に記載の装置。
- スライド(4)が、分析試料と、場合により、ネガティブコントロールとなる試料またはポジティブコントロールとなる試料とを互いに別々に加え得るウエル(9)を備えている、請求項1〜7のいずれか1項に記載の装置。
- スライド(4)上のウエル(9)が他のウエル(9)に一次元でのみ隣接している、請求項1〜8のいずれか1項に記載の装置。
- 容器(1)が、容器(1)内でスライド(4)を安定化させるためにスライド(4)用の横軸受(10)を備えている、請求項1〜9のいずれか1項に記載の装置。
- ハイブリダイゼーション溶液用支持台(3)が取外し可能または挿し込み可能である、請求項1〜10のいずれか1項に記載の装置。
- ハイブリダイゼーション溶液用支持台(3)を容器(1)内に完全に挿し込み得る、請求項1〜11のいずれか1項に記載の装置。
- ハイブリダイゼーション溶液用支持台(3)を容器(1)内に部分的に挿し込み得る、請求項1〜12のいずれか1項に記載の装置。
- 容器(1)が、ハイブリダイゼーション溶液用支持台(3)を容器(1)内で安定化させ
るためにハイブリダイゼーション溶液用支持台(3)用の横軸受(11)を備えている、請求項1〜13のいずれか1項に記載の装置。 - ハイブリダイゼーション溶液用支持台(3)が容器(1)の固定部品である、請求項1〜10のいずれか1項に記載の装置。
- ハイブリダイゼーション溶液用支持台(3)が容器(1)内のウエルである、請求項15に記載の装置。
- ハイブリダイゼーション溶液用支持台(3)が、トレイ(3)、特に、液体取り込み用および液浸パッド取り込み用の少なくともいずれかのウエル(12)を備えたトレイ(3)である、請求項1〜16のいずれか1項に記載の装置。
- スライド(4)を除く装置の全部品の材料が、プラスチック、特に、ポリエチレンおよびポリプロピレンの少なくともいずれかを含んでなる、請求項1〜17のいずれか1項に記載の装置。
- スライド(4)が、ガラス、特に、DIN 12111に基づく加水分解等級1〜4に相当するガラス製である、請求項1〜18のいずれか1項に記載の装置。
- in situハイブリダイゼーションにより試料中の微生物を特異的に検出する方法であって、以下のステップ:
(a)試料中に含まれている微生物を固定するステップ、
(b)固定細胞を検出可能な核酸プローブ分子と共にインキュベートするステップ、
(c)ハイブリダイズしなかった核酸プローブ分子を除去または洗い落とすステップ、および
(d)核酸プローブ分子とハイブリダイズした細胞を検出するステップ
を含んでなり、
ステップ(a)〜(c)と、場合により、ステップ(d)が、請求項1〜19のいずれか1項に記載のin situハイブリダイゼーション装置で実施される方法。 - スライド(4)上で固定ステップおよび場合により乾燥ステップの少なくともいずれかを実施する、請求項20に記載の方法。
- スライド(4)が横向きに配置されているときにスライド(4)の乾燥、特に最終乾燥を行う、請求項20または21に記載の方法。
- スライド(4)が水平に配置されているときにインキュベーションを行う、請求項20〜22のいずれか1項に記載の方法。
- スライド(4)が垂直配置されているときに洗浄を行う、請求項20〜23のいずれか1項に記載の方法。
- 方法のステップ(b)で、ハイブリダイゼーション溶液と核酸プローブ分子溶液との混合物をスライド(4)に加える、請求項20〜24のいずれか1項に記載の方法。
- 滴下容器を用いて混合物を加える、請求項25に記載の方法。
- 滴下容器が、使い捨て滴下容器または複数回使用可能な滴下容器である、請求項26に記載の方法。
- ハイブリダイゼーション溶液用支持台(3)内に配置されたハイブリダイゼーション溶液浸漬パッドを介して、請求項1〜19のいずれか1項に記載の装置にハイブリダイゼーション溶液を導入する、請求項20〜25のいずれか1項に記載の方法。
- 核酸プローブ分子が、検出対象微生物の染色体もしくはエピソームのDNA、mRNAまたはrRNAと相補的である、請求項20〜28のいずれか1項に記載の方法。
- 核酸プローブ分子が検出可能なマーカーに共有結合している、請求項20〜29のいずれか1項に記載の方法。
- 検出可能なマーカーが、以下のマーカー:
− 蛍光マーカー、
− 化学発光マーカー、
− 放射性マーカー、
− 酵素活性を有する基、
− ハプテン、
− ハイブリダイゼーションにより検出可能な核酸
からなる群から選択される、請求項30に記載の方法。 - 微生物が単細胞微生物である、請求項20〜31のいずれか1項に記載の方法。
- 微生物が、酵母、細菌、藻類または真菌類である、請求項20〜32のいずれか1項に記載の方法。
- 微生物が廃水細菌である、請求項33に記載の方法。
- 試料が、水、土壌または空気から採取された環境試料である、請求項20〜34のいずれか1項に記載の方法。
- 試料が食品試料である、請求項20〜34のいずれか1項に記載の方法。
- 試料が、牛乳もしくは乳製品、飲用水、飲料、パン製品または肉製品から採取される、請求項36に記載の方法。
- 試料が医学試料である、請求項20〜34のいずれか1項に記載の方法。
- 試料が、組織、分泌物または糞便から採取される、請求項38に記載の方法。
- 試料が廃水から採取される、請求項20〜34のいずれか1項に記載の方法。
- 試料が、活性汚泥、消化汚泥または嫌気性汚泥から採取される、請求項40に記載の方法。
- 試料がバイオフィルムから採取される、請求項20〜34のいずれか1項に記載の方法。
- バイオフィルムが、産業施設から採取されるか、廃水処理工程中に生成されるか、または天然バイオフィルムである、請求項42に記載の方法。
- 試料が医薬品または化粧品から採取される、請求項20〜34のいずれか1項に記載の方
法。 - in situハイブリダイゼーションにより微生物を特異的に検出するためのキットであって、
− 微生物を特異的に検出するための少なくとも1種の核酸プローブ分子、
− 少なくとも1種のハイブリダイゼーション溶液、
− 場合により、ネガティブコントロールとするための核酸プローブ分子、
− 場合により、ポジティブコントロールとするための核酸プローブ分子、
− 場合により、洗浄溶液、
− 場合により、固定溶液、および
− 請求項1〜19のいずれか1項に記載のin situハイブリダイゼーション装置を含んでなるキット。 - 核酸プローブ分子が、検出対象微生物の染色体もしくはエピソームのDNA、mRNAまたはrRNAと相補的である、請求項45に記載のキット。
- 核酸プローブ分子が検出可能なマーカーに共有結合している、請求項45または46に記載のキット。
- 検出可能なマーカーが、以下のマーカー:
− 蛍光マーカー、
− 化学発光マーカー、
− 放射性マーカー、
− 酵素活性を有する基、
− ハプテン、
− ハイブリダイゼーションにより検出可能な核酸
からなる群から選択される、請求項47に記載のキット。 - in situハイブリダイゼーションにより微生物を特異的に検出するための、請求項1〜19のいずれか1項に記載の装置の利用法。
- 請求項20〜44のいずれか1項に記載の方法における請求項45〜48のいずれか1項に記載のキットの利用法。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE10061655A DE10061655A1 (de) | 2000-12-11 | 2000-12-11 | In situ-Hybridisierungs-Anordnung zum spezifischen Nachweis von Mikroorganismen |
| PCT/EP2001/014543 WO2002048398A2 (de) | 2000-12-11 | 2001-12-11 | In situ-hybridisierungs-anordnung zum spezifischen nachweis von mikroorganismen |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2004523223A true JP2004523223A (ja) | 2004-08-05 |
| JP2004523223A5 JP2004523223A5 (ja) | 2005-12-22 |
Family
ID=7666693
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002550112A Pending JP2004523223A (ja) | 2000-12-11 | 2001-12-11 | 微生物を特異的に検出するためのinsituハイブリダイゼーション装置 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20040038270A1 (ja) |
| EP (1) | EP1341897B1 (ja) |
| JP (1) | JP2004523223A (ja) |
| AT (1) | ATE298786T1 (ja) |
| AU (1) | AU2002231689A1 (ja) |
| CA (1) | CA2430894A1 (ja) |
| DE (2) | DE10061655A1 (ja) |
| WO (1) | WO2002048398A2 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007020528A (ja) * | 2005-07-21 | 2007-02-01 | Hakodate Chiiki Sangyo Shinko Zaidan | 培養併用蛍光インサイチューハイブリダイゼーション法による食品の微生物検査法 |
| JP2012507288A (ja) * | 2008-11-03 | 2012-03-29 | ゼネラル・エレクトリック・カンパニイ | 水性媒体中の微生物含有量の測定方法及びシステム |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10323197B4 (de) * | 2003-05-22 | 2008-10-02 | Clondiag Chip Technologies Gmbh | Vorrichtung zur Halterung und Detektion von Substanzbibliotheken |
| US8062897B2 (en) | 2003-07-21 | 2011-11-22 | Aureon Laboratories, Inc. | Diagnostic histopathology using multiplex gene expression FISH |
| US6995020B2 (en) * | 2003-07-21 | 2006-02-07 | Aureon Laboratories, Inc. | Methods and compositions for the preparation and use of fixed-treated cell-lines and tissue in fluorescence in situ hybridization |
| ES2387903B1 (es) * | 2010-07-16 | 2013-08-13 | María Albiñana Blanco | Procedimiento y kit para verificar, en una muestra de semen humano o animal, la existencia de espermatozoides fecundantes. |
| DE102011004449B4 (de) * | 2011-02-21 | 2019-01-24 | Fraunhofer-Gesellschaft zur Förderung der angewandten Forschung e.V. | Biopsieplättchen, Einbettkassette und Diagnosevorrichtung |
| CN106442020B (zh) * | 2016-11-18 | 2022-05-24 | 何耀 | 一种尿液取样检测装置 |
| CN110672811A (zh) * | 2019-10-21 | 2020-01-10 | 远大可建科技有限公司 | 一种芯板内腔检测装置及其方法 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3618265A (en) * | 1969-01-08 | 1971-11-09 | Remington Arms Co Inc | Finishing machine for metal surfaces |
| US3616265A (en) * | 1969-08-07 | 1971-10-26 | Smith Kline French Lab | Device for making a culture of microorganisms |
| FR2525233B1 (fr) * | 1982-04-14 | 1985-12-06 | Lille Inst Pasteur | Dispositif de culture microbiologique |
| US4640895A (en) * | 1982-10-15 | 1987-02-03 | Gibco Division, The Mogul Corporation | Biphasic media culture apparatus |
| DE8309876U1 (de) * | 1983-04-02 | 1983-12-22 | Biotest-Serum-Institut Gmbh, 6000 Frankfurt | Zweiphasige blutkulturflasche |
| IT1205100B (it) * | 1987-06-25 | 1989-03-10 | Sta Te Spa | Dispositivo per culture microbiologiche |
| US4886741A (en) * | 1987-12-09 | 1989-12-12 | Microprobe Corporation | Use of volume exclusion agents for the enhancement of in situ hybridization |
| US5192503A (en) * | 1990-05-23 | 1993-03-09 | Mcgrath Charles M | Probe clip in situ assay apparatus |
| US5380492A (en) * | 1990-12-18 | 1995-01-10 | Seymour; Eugene H. | Sampling device and sample adequacy system |
| EP0497464A1 (en) * | 1991-01-31 | 1992-08-05 | Amoco Corporation | Rapid microbial diagnostics by in situ hybridization in aqueous suspension |
| US5128476A (en) * | 1991-02-20 | 1992-07-07 | The Midland Certified Reagent Company | Biotinylated oligonucleotides and reagents for preparing the same |
| EP0667894B1 (en) * | 1991-11-15 | 1997-01-02 | Nunc A/S | A cell cultivating device |
| DE4409705A1 (de) * | 1994-03-22 | 1995-09-28 | Boehringer Mannheim Gmbh | Vorrichtung zur Bearbeitung von Nukleinsäuren in Präparationen |
| US5750340A (en) * | 1995-04-07 | 1998-05-12 | University Of New Mexico | In situ hybridization solution and process |
| US6022689A (en) * | 1995-04-07 | 2000-02-08 | University Of New Mexico | Situ hybridization slide processes |
| US6007994A (en) * | 1995-12-22 | 1999-12-28 | Yale University | Multiparametric fluorescence in situ hybridization |
| WO2000065093A2 (en) * | 1999-04-22 | 2000-11-02 | Science And Technology Corporation | In situ hybridization methods for reducing the occurrence of false positives and for targeting multiple microorganisms |
-
2000
- 2000-12-11 DE DE10061655A patent/DE10061655A1/de not_active Ceased
-
2001
- 2001-12-11 CA CA002430894A patent/CA2430894A1/en not_active Abandoned
- 2001-12-11 WO PCT/EP2001/014543 patent/WO2002048398A2/de active IP Right Grant
- 2001-12-11 DE DE50106653T patent/DE50106653D1/de not_active Expired - Lifetime
- 2001-12-11 AT AT01991823T patent/ATE298786T1/de active
- 2001-12-11 AU AU2002231689A patent/AU2002231689A1/en not_active Abandoned
- 2001-12-11 EP EP01991823A patent/EP1341897B1/de not_active Expired - Lifetime
- 2001-12-11 JP JP2002550112A patent/JP2004523223A/ja active Pending
-
2003
- 2003-06-10 US US10/458,775 patent/US20040038270A1/en not_active Abandoned
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007020528A (ja) * | 2005-07-21 | 2007-02-01 | Hakodate Chiiki Sangyo Shinko Zaidan | 培養併用蛍光インサイチューハイブリダイゼーション法による食品の微生物検査法 |
| JP2012507288A (ja) * | 2008-11-03 | 2012-03-29 | ゼネラル・エレクトリック・カンパニイ | 水性媒体中の微生物含有量の測定方法及びシステム |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2002048398A2 (de) | 2002-06-20 |
| EP1341897B1 (de) | 2005-06-29 |
| WO2002048398A3 (de) | 2003-05-15 |
| EP1341897A2 (de) | 2003-09-10 |
| DE50106653D1 (de) | 2005-08-04 |
| US20040038270A1 (en) | 2004-02-26 |
| AU2002231689A1 (en) | 2002-06-24 |
| DE10061655A1 (de) | 2002-06-20 |
| CA2430894A1 (en) | 2002-06-20 |
| ATE298786T1 (de) | 2005-07-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2347011B1 (en) | Fast results hybrid capture assay and system | |
| JP5596891B2 (ja) | プローブセット、プローブ固定担体及び遺伝子検査方法 | |
| JP5201818B2 (ja) | プローブセット、プローブ固定担体及び遺伝子検査方法 | |
| JP5596894B2 (ja) | プローブセット、プローブ固定担体及び遺伝子検査方法 | |
| JP2008118914A (ja) | プローブ、プローブセット、プローブ固定担体及び遺伝子検査方法 | |
| JP2012506705A5 (ja) | ||
| AU773559B2 (en) | Method for detecting microorganisms in a sample | |
| JP2004523223A (ja) | 微生物を特異的に検出するためのinsituハイブリダイゼーション装置 | |
| WO2003052128A1 (en) | A method and a kit for determination of a microbial count | |
| CN111172301A (zh) | 一种艰难梭菌毒素b的pcr荧光检测试剂盒及其应用 | |
| US20090136930A1 (en) | Method for the identification of microorganisms by means of in situ hybridization and flow cytometry | |
| CN102936625B (zh) | 一种用于副溶血性弧菌分子分型的分子马达生物传感器试剂盒 | |
| FI91888C (fi) | Menetelmä mykoplasmabakteerien laskemiseksi ja toteamiseksi | |
| US5948618A (en) | Primer for gene amplification, method for nucleic acid discrimination with the use of the same, and nucleic acid discrimination kit | |
| JP2008161170A (ja) | 高感度なサルモネラ属菌検出用オリゴヌクレオチド、それを用いた検出方法および検出キット | |
| JP2005525804A (ja) | insituハイブリダイゼーションおよびフローサイトメトリーを用いる微生物の同定方法 | |
| JP2004290171A (ja) | 微生物の分子生物学的同定技術 | |
| US20230374570A1 (en) | Method and system for detecting fungal genes and kit for use with same | |
| CN106198968A (zh) | 一种支原体的检测方法及检测试剂盒 | |
| JP2004534536A (ja) | グラム陽性菌の検出方法 | |
| Singh et al. | Molecular Methods for the Assessment of Microbial Biofilms | |
| CN117144026A (zh) | 一种检测解脲脲原体的居家自检试剂盒 | |
| CN117512158A (zh) | 基于RPA-CRISPR/Cas12a检测刚地弓形虫的试剂盒及检测方法 | |
| JP5137441B2 (ja) | プローブセット、プローブ固定担体及び検査方法 | |
| JP5121281B2 (ja) | プローブセット、プローブ固定担体及び検査方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20041210 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20041210 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20071023 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20080318 |