JP2004187545A - 核酸配列の検査方法及び試料調製方法 - Google Patents
核酸配列の検査方法及び試料調製方法 Download PDFInfo
- Publication number
- JP2004187545A JP2004187545A JP2002357804A JP2002357804A JP2004187545A JP 2004187545 A JP2004187545 A JP 2004187545A JP 2002357804 A JP2002357804 A JP 2002357804A JP 2002357804 A JP2002357804 A JP 2002357804A JP 2004187545 A JP2004187545 A JP 2004187545A
- Authority
- JP
- Japan
- Prior art keywords
- sequence
- test region
- primer
- dna
- bases
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Abstract
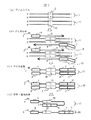
【解決手段】多型位置を含む検査領域20の配列として想定される配列7をアンカー配列として付加したプライマー10を用いてPCR反応を行い、配列7の相補配列7’と検査領域20および21のハイブリダイゼーションの融解温度の中間の温度でPCR産物の電気泳動分析を行う。
【効果】多型によって異なる融解温度の中間の温度で電気泳動を行うと、ヘアピン状態の有無という大きな立体構造の変化が生じて泳動速度の差が大きくなるため、SSCP分析の分離能を大きく改善でき、多型のタイピングやLOHを用いたがん診断の高精度化などに大きな効果がある。また、融解温度を予測してアンカー配列を設計できるため、温度条件の探索など分離の最適化作業を減らせるだけでなく、自動キャピラリー電気泳動装置に適した温度領域に設計することで、ルーチン検査にも好適となる。
【選択図】 図1
Description
【発明の属する技術分野】
本発明は、遺伝子における1塩基多型等の多型及び変異の分離検出方法に関する。さらに言えば、ゲル電気泳動法を用いるDNAの一本鎖高次構造多型(Single Strand Conformation Polymorphism: SSCP)解析法の分離能改良法およびその解析法を用いた遺伝子診断法に関する。
【0002】
【従来の技術】
近年、ヒトゲノムの解析が急速に進み、ヒトのゲノムには、ほぼ1000塩基毎に1つの頻度で一塩基レベルの個人差(多型)があることがわかってきた。これをSingle Nucleotide Polymorphism (SNP)と呼ぶ。この多型は、ゲノム上に高密度に存在するため、ゲノム上での位置を示す詳細な目印となる。例えば、ある病気の疾患集団と正常集団との間で、このゲノム上にマッピングされたSNPの出現頻度の差異を解析することにより、ゲノム上のどの位置にその疾患に関連した遺伝子が配置しているかをつきとめられる。ゲノム上の遺伝子の位置関係が詳細にわかれば、遺伝子間の相互作用などの新しい機能情報の取得につながり、新しい創薬・診断・治療につながる知見が得られるものと期待されている。
【0003】
また、一塩基レベルの遺伝子多型が検出できるということは、遺伝子配列中の突然変異の検出が可能であることを意味する。発がんや転移のメカニズムに関しては、遺伝子変異の関与が示唆されているため、一塩基の多型や変異の分析技術は、がんを始めとする多くの疾病の診断の基礎技術になると期待される。
【0004】
このような、一塩基レベルの多型を分析する方法の1つに一本鎖DNA高次構造多型解析(Single Starnd Conformation Polymorphism:SSCP)法がある。この方法は、M.Oritaらによって報告されている(例えば非特許文献1参照)。これは、一本鎖DNAを非変性ポリアクリルアミドゲル中で電気泳動した時の泳動速度が、同じ長さのDNAであっても、一塩基の配列の違いによって異なることを利用して、一塩基の多型を分離検出する方法である。一塩基の違いによって一本鎖DNAがもつ高次構造(立体構造)が異なり、その高次構造の違いが泳動速度の違いを引き起こしていると考えられている。近年では、生体試料から抽出したDNAの標的部分をPCR(Polymerase Chain Reaction)によって選択的に増幅して分析するPCR−SSCP法が広く行われている。
【0005】
PCR−SSCP法を利用したがんの診断法の一例として、ヘテロ接合性欠損(Loss of Heterozygosity, LOH)という現象に基づくものがある。細胞から抽出したゲノムDNAには、通常は父親由来の遺伝子と母親由来の遺伝子が同数含まれている(ヘテロ接合性)。ところが、がん化した細胞では、特定遺伝子座について欠落や異常な複製が起こっているため、この平衡が失われているという現象 (LOH) がよく見られる。M. Shigyoらの報告(例えば非特許文献2参照)によれば、尿中の細胞のLOHと膀胱の悪性腫瘍に高い相関があることが報告されている。
このLOHを測定する際に、父親由来の遺伝子と母親由来の遺伝子を区別するマーカーとして一塩基多型を用い、SSCP法によってこの一塩基多型を分離検出する。父親由来の遺伝子と母親由来の遺伝子の存在量の不均衡は、電気泳動によって分離されたこの一塩基多型のピーク強度の比によって定量化される。
【0006】
一方、従来、SSCP法には平板ゲル電気泳動またはキャピラリーゲル電気泳動が利用されてきた。平板ゲル(スラブゲル)電気泳動装置には、例えば、アマシャム・ファルマシアバイオテク社の製品GenePhorなどがある。平板ゲル電気泳動装置は、装置構成が簡単で価格も安いが、ゲルの作製、泳動槽への設置、試料の導入、ゲルの泳動槽からの取りだし、ゲルの写真撮影等、手作業の工程が多い。そこで、例えば特許文献1に記載のように、自動化に適し、かつ、内径が100ミクロン以下と細いために電気泳動に伴うジュール熱の放熱が早いキャピラリーゲルを用い、高電圧で高速分析を行うSSCP法が提案されている。キャピラリー電気泳動装置には、アプライドバイオシステムズ社の製品ABI Prism 310のように、分離媒体として流動性ポリマーを用い、測定終了毎にポリマーを自動交換する機能を有していて、多数のサンプルを全自動で連続測定できる装置が、近年急速に普及している。
【0007】
【特許文献1】
特開平6−138090号公報
【非特許文献1】
オリタ(M.Orita)ら、「プロシーディング オブ ナショナル アカデミー オブ サイエンス USA(Proceeding of National Academy of Science of U.S.A.)」 (米国) 1989年、第86巻 p.2766−p.2770
【非特許文献2】
シギョウ(M. Shigyo)、「インターナショナル ジャーナル オブ キャンサー(International Journal of Cancer)」、(米国) 1998年、78巻 p.425−p.429
【0008】
【発明が解決しようとする課題】
上記のように、SSCP法は一塩基多型を測定するのに簡便で有効な方法であり、さらに、キャピラリー電気泳動装置を用いれば、迅速な自動分析も可能である。しかし、SSCP法はその原理からも示唆されるように、一本鎖DNAに一塩基多型が存在しても、その高次構造の違いがもたらす泳動速度の違いが、ゲル電気泳動の分離能に比べて小さい場合には分離できない。また、高次構造およびその構造と泳動速度との関係を理論的に予測することは困難であるため、検査の対象となる一塩基多型の1つ1つについて、電気泳動条件を少しずつ変えて測定を繰り返すことによって、分離が得られる条件を探索しなければならなかった。
特にLOHによる遺伝子診断のような場合には、ピーク強度比を正確に求める必要があるため、一塩基多型の2つのピークが重ならないように十分高い分離能を得ることが必要であり、条件検討に大変な手間を要していた。
【0009】
前出の平板ゲル電気泳動装置GenePhorでは、SSCP法による一塩基多型の分離能は、温度が低くゲル濃度が高い方が良くなる場合が多いことを利用して、15%濃度で架橋度3%程度の架橋ポリアクリルアミドゲルを用い、温度を5−20℃程度の範囲に設定し、最適な測定条件を探索するための作業を支援する配慮がなされている。しかし、前出のABI Prism 310のような全自動キャピラリー電気泳動装置では、測定が終了する毎にキャピラリーに分離媒体(架橋していないポリアクリルアミドなどからなるポリマー溶液)を詰替えるため、架橋ゲルは使用できない。また、架橋していない場合でも高濃度のポリマー溶液は粘性が高いため、詰替えの際の圧力損失が大きく、詰替えに要する時間も長くなるという不都合を招く。
【0010】
また、15℃程度以下の低温では、結露による高電圧のリークや感電を防止するために、装置全体を密閉して内部の湿度を下げるなどの対策が必要になる。前出の平板ゲル電気泳動装置では、泳動とゲルの画像測定は別の装置によって行われ、かつ電気泳動装置は小型であるのであまり問題ではない。しかし、全自動キャピラリー電気泳動装置では、電気泳動とDNAの検出とを同時に行うため、装置が比較的大型である。このため、結露対策が大掛かりにならざるを得なかった。
【0011】
本発明は、上記の問題点に鑑みてなされたものであり、SSCP法による一塩基多型の分析条件の最適化にかかる手間を軽減することを目的とする。さらに言えば、ルーチン分析や診断用途に適した全自動キャピラリー電気泳動装置において、低温や高濃度のポリマーを用いなくても高い分離が得られるようにSSCP法を改良することを目的とする。
【0012】
【課題を解決するための手段】
上記の問題点を解決するために種々検討した結果、一塩基多型の有無によって一本鎖DNAの高次構造を大きく変化させるような塩基配列をPCR反応の際に導入し、それによってSSCP法の条件検討に要する手間及び分離能を顕著に改善することが可能となった。
【0013】
すなわち本発明は、検査領域中に存在する一塩基多型等の塩基配列の差異によってPCR反応で増幅されるDNA断片の高次構造が変化するように設計したプライマーを用い、検査領域を含むDNA断片を増幅する工程を含む、核酸配列の検査方法、試料調製方法、及び上記プライマーを含む核酸配列の検査のためのキットを提供する。
【0014】
【発明の実施の形態】
以下、本発明の試料調製方法及び検査方法の概要を以下に述べる。
【0015】
鋳型となるDNAは、例えば、被験者の血液や組織細胞等から抽出したゲノムDNAや、mRNAからの逆転写によって得られるcDNA等であり、一本鎖DNAであっても二本鎖DNAであっても良い。本発明において、このDNA上にある検査対象となる検査領域は、一塩基多型等の多型部位とそれに隣接する部分からなり、この検査領域の配列を含む領域をPCR反応で増幅する。ゲノム解析の進展の結果、一塩基多型等の変異に関しては既に情報が蓄積されつつあり、検査領域及びその近辺の配列は予め判明していることが多く、本発明は検査領域の配列が予め想定されていることが前提となる。この際、一方のプライマー(第1のプライマー)には、一本鎖DNAまたは二本鎖DNAの一方の鎖における検査領域より3’末端側の配列にハイブリダイズする配列(第1の配列部分)の他に、この第1の配列部分の5’末端側に続いて、アンカー配列(プライマーの5’末端側に付加してあり、一般的には鋳型DNAの配列とは相補でない配列)を設け、そのアンカー配列を、前記検査領域の配列として想定される配列と同一の配列にする(第2の配列部分)。他方のプライマー(第2のプライマー)は、上記のプライマーが鋳型とするDNA鎖の相補鎖(二本鎖DNAにおける他方の鎖)を鋳型とするが、この相補鎖における検査領域より3’末端側の配列にハイブリダイズする配列を有するように設計し、5’末端を蛍光色素等の標識体で標識する。
【0016】
別の観点において、第1のプライマーは、一本鎖DNAまたは二本鎖DNAの一方の鎖における第1の所定の塩基数からなる検査領域の3’末端から5’→3’方向に第2の所定の塩基数だけ離れた第3の所定の塩基数の配列にハイブリダイズする第1の配列部分と、前記第1の所定の塩基数からなり、前記検査領域の配列として想定される配列と同一の配列を持ち、かつ前記第1の配列部分の5’末端側に続く第2の配列部分とを有する。第1の所定の塩基数としては、自己ハイブリダイゼーションを生じる配列であることから、特に限定するものではないが、好ましくは7〜15塩基である。第3の所定の塩基数としては、通常プライマーの配列として用いる範囲であれば良く、特に限定するものではないが、好ましくは17〜30塩基である。第2の所定の塩基数としては、自己ハイブリダイゼーションを妨げず、PCRが好適に行える範囲であれば良く、特に限定するものではないが、好ましくは30〜100塩基である。
【0017】
上記の観点において、第2のプライマーは、前記検査領域の配列の5’末端から3’→5’方向に第4の所定の塩基数だけ離れた第5の所定の塩基数の配列に相補な配列にハイブリダイズする配列を有し、5’末端が標識されている。第4の所定の塩基数としては、PCRが好適に行える範囲であれば良く、特に限定するものではないが、好ましくは30〜100塩基である。第5の所定の塩基数としては、上記の第3の所定の塩基数と同様、通常プライマーの配列として用いる範囲であれば良く、特に限定するものではないが、好ましくは17〜30塩基である。尚、第1のプライマーと第2のプライマーは、当分野において通常行われているように、PCR反応の進行条件を考慮して、Tm値がほぼ等しい値になるように設計する。
【0018】
これらのプライマーを用い、上記DNAを鋳型とするPCR反応を行うことにより、上記検査領域を含むDNA断片を増幅することができ、目的の核酸配列の検査方法に必要な試料(増幅されたDNA断片)が調製される。
【0019】
増幅されたDNA断片は二本鎖の状態であり、これを一本鎖DNA断片に変性することによって、各DNA断片は、その塩基配列に応じて自己ハイブリダイゼーション等を生じ、エネルギー的に安定な高次構造をとるようになる。この場合に、増幅されたDNA断片は検査領域を含む鋳型DNAの配列に加えて上記第1のプライマーのアンカー配列に対応する配列をも含んでいる。
【0020】
従って、一方の鎖の検査領域の配列を含むDNA断片は、その3’末端側に、検査領域の配列として想定される配列と同一の配列であるアンカー配列に相補の配列(第3の配列部分)が付加されており、検査領域の配列が想定された配列そのものである場合には第3の配列部分の配列と完全に相補となり、自己ハイブリダイゼーションを容易に生じる。検査領域の配列が想定された配列と異なる場合、例えば一塩基多型によって第3の配列部分と一塩基のミスマッチがある場合には、自己ハイブリダイゼーションを生じにくくなる。尚、本発明においては、一塩基のみのミスマッチでも明確に識別できる検査方法を提供するが、一塩基多型以外の多型、例えば複数個の塩基の挿入、欠失、置換等の多型及び変異を検出することもできるものであり、特に一塩基多型のみに限定するものではない。
【0021】
一方、上記のDNA断片と対となって増幅されたDNA断片においては、上記他方の鎖における検査領域の配列(上記一方の鎖における検査領域の配列と相補となる配列)を含み、その5’末端側に、アンカー配列と同一の配列、すなわち上記一方の鎖における検査領域の配列を有しているので、上記と同様に、検査領域の配列が想定された配列そのものである場合には自己ハイブリダイゼーションを容易に生じ、検査領域の配列が想定された配列と異なる場合には、自己ハイブリダイゼーションを生じにくくなる。
【0022】
検査領域の配列と第3の配列部分の配列が完全に相補的な場合にのみ自己ハイブリダイゼーションを生じ、一塩基ミスマッチの場合に自己ハイブリダイゼーションを生じないようにするためには、具体的には以下のようにすれば良い。
【0023】
すなわち、検査領域の配列に一塩基の多型が存在すると、一塩基の違いによって融解温度(Tm)は異なる値となる。したがって、例えば、電気泳動の温度を、完全に相補的な場合のハイブリダイゼーションのTm以下にすると、自己ハイブリダイゼーションを生じてヘアピン型の構造を作ることになる。Tm以上に温度を上げると、このヘアピン型構造は解離する。一塩基ミスマッチの場合のハイブリダーゼーションのTmはこれよりも低い値となる。
【0024】
アンカー配列を多型の一方の種類の塩基を含む検査領域の配列と完全に一致する(完全マッチ)ように設計した場合、他方の種類の塩基を含む検査領域の配列とは一塩基ミスマッチとなりTmは下がる。したがって、電気泳動の温度を、完全マッチのTmと一塩基ミスマッチのTmとの間、例えば中間の温度に設定すると、完全マッチのDNAはヘアピン構造を取り、一塩基ミスマッチのDNAはヘアピン構造を取らないことになる。Tm値はハイブリダイゼーションをする塩基配列に応じて変動する値であるが、予め塩基配列が明らかである場合には当業者に公知の手段によって計算することが可能である。
【0025】
上記のように、増幅されたDNA断片が検査領域における多型または変異の状態に応じて一本鎖化した場合の高次構造が、適当な温度を設定することによって、上記アンカー配列の存在によって顕著に異なることとなるため、これらを電気泳動で分離し、レーザー励起蛍光検出法を用いることによって、蛍光色素等で標識されている方の一本鎖DNAを検出することができる。
【0026】
本方法によると、第1に、ヘアピン型構造とそうでない構造という高次構造の違いが、従来のSSCP法における構造変化に比べて大きいため、分離が改善される。このため、粘性の高い高濃度ポリマーや低温を使用しなくても高い分離が得られる。第2に、検査領域の配列のTmの値は公知の方法により計算が可能であることから、分離に好適な温度条件を予め推定できるため、SSCP分析の温度条件を最適化するための作業量を軽減できる。第3に、Tmの計算値から予測される分離に最適な温度が、キャピラリー電気泳動装置に適した30−60℃程度になるように検査領域の配列を設定できる。加えて、複数の多型部位について、分離に最適な温度がほぼ等しくなるように検査領域の配列を設計することによって、同時に一定の温度条件で複数の多型部位の検査を行うことが可能となる。
【0027】
本発明の方法は、一塩基多型の存在を容易に検出することができ、予め多型と電気泳動におけるピーク位置との関係を対照データとして得ておけば、検査対象のDNAにおける一塩基多型の型をDNA断片の泳動ピークの位置から直ちに検出することができる。また、検査領域の配列が異なる複数のDNAが存在する場合に、その存在比をピークの位置及び強度比から算出することができる。
【0028】
更に本発明により、核酸配列の検査のためのキットが提供される。キットは、上記第1のプライマー及び上記第2のプライマーを含み、必要に応じてPCR反応に必要なその他の試薬、例えば酵素、ヌクレオチド、バッファー等、及び好適なPCR反応条件に関するデータ等を含んでいても良い。プライマーそのものの代わりに、プライマーの塩基配列データをキットに含めても良い。その場合には、プライマーを合成する必要があるため、合成のための試薬、プライマーを標識するための蛍光色素等の標識体を含んでいても良い。
【0029】
キットには更に、一塩基多型等の多型または変異を上記プライマーを用いたPCR反応によって増幅されるDNA断片による自己ハイブリダイゼーションの有無を電気泳動で分析するための温度条件のデータを含むものであっても良い。温度条件のデータは、予め検査領域の配列及び想定される多型または変異の型を考慮して、計算値または実測値として提供することができる。
【0030】
本発明のキットは、検査領域に含まれる多型または変異を電気泳動で分析するために使用することができ、具体的には、検査領域における1塩基多型の型を解析したり、検査領域の配列が異なる複数のDNAの存在比を解析するために使用することができる。
【0031】
【実施例】
以下、本発明の実施例を図1により説明する。本発明による核酸配列の検査方法は、DNAの抽出、PCR反応、PCR産物の変性(一本鎖化)、電気泳動分析という4つの工程からなるが、以下工程を追ってその詳細を説明する。
【0032】
工程1では、ヒトの血液や組織細胞などの生体試料から公知技術によりゲノムDNAを抽出する。図1(a)に示すように、ゲノムDNAは、父親由来1と母親由来11の一対の二本鎖DNAからなり、その多型部位を2、12で示す。図1(a)では、多型の塩基位置が父親由来のDNAではA−Tの組に、母親由来のDNAではG−Cの組になっているものとし、この多型以外の配列の違いはないものとする。また、ゲノムDNA1、11において両端の3’または5’の記号は、それぞれのDNA分子の末端が5’末端、3’末端のいずれであるかを示している。
【0033】
工程2では、ゲノムDNA上の検査領域20、21を間にはさんだ領域をPCR反応で増幅する。図1(b)に示すように、PCRに用いるプライマー組は、蛍光色素8で標識されたプライマー4と、配列7と配列6が5’末端から3’末端に向かってこの順につながった構造のプライマー10とからなる。プライマー10の配列7の部分は、ゲノムDNA1上の多型位置を含む領域(検査領域)20と同じ配列に設計されている。PCRにおいて、これらのプライマー4と10はゲノムDNA上のあらかじめ決めた配列位置にハイブリダイズして伸長する。プライマー4、10からの伸長反応によって形成されるDNA鎖をそれぞれ9,9’で表す。ゲノムDNA11上でも同様の伸長反応が起こる。PCR反応終了後の生成物を図1(c)に示す。父親由来ゲノムDNA1を鋳型として生成される二本鎖のPCR産物13の蛍光色素8で標識された方の鎖は、プライマー4の配列、ゲノムDNA1の検査領域20と同じ配列、プライマー10の相補配列(配列6の相補配列6’と配列7の相補配列7’からなる)が5’末端側からこの順でつながった構造となり、母親由来ゲノムDNA11を鋳型として生成されるPCR産物23の蛍光色素8で標識された方の鎖は、プライマー4の配列、ゲノムDNA11の検査領域21と同じ配列、プライマー10の相補配列(配列6’と配列7’からなる)が5’末端側からこの順でつながった構造となる。
【0034】
工程3では、PCR産物13、23を熱あるいはホルムアミドなどの変性剤を使った公知の方法で変性して一本鎖DNAを得る。
【0035】
工程4では、工程3で得られた一本鎖DNAを電気泳動によって検出する。DNAの検出をレーザー励起蛍光法で行う場合には、図1(d)に示す蛍光色素8が5’末端側に標識された一本鎖DNA14および24が検出される。一本鎖DNA14はゲノムDNA1からのPCR産物であり、多型位置を含む検査領域の配列20はプライマー10のアンカー配列部分7の相補配列7’と完全に相補になっている。一方、一本鎖DNA24はゲノムDNA11からのPCR産物であり、多型位置を含む検査領域の配列21はプライマー10のアンカー配列部分7の相補配列7’と多型位置においてC−Aのミスマッチになっている。従って、配列20と配列7’との融解温度(Tm2)と配列21と配列7’との融解温度(Tm1)を比較すると、Tm2はTm1よりも高くなっている。従って、電気泳動の温度をTm1とTm2の間に設定すれば、図1(d)に示すように、DNA14は自己ハイブリダイゼーションを起こしたヘアピン型になり、DNA24とは大きく異なる立体構造を持つものとなる。このように積極的に構造を変化させることにより、SSCP法の分離能を向上させることができる。
【0036】
本実施例では、プライマー10のアンカー部分の配列7は検査領域の配列20と全く同じ配列であるとしたが、原理的には検査領域の配列20および検査領域の配列21でTmに十分な差が生ずるものであれば配列7はどのような配列であっても構わない。また、Tmは、キャピラリー電気泳動で分析する場合には、20−60℃程度になるように設計するのが好適である。
【0037】
本実施例を、具体的な鋳型DNA配列を用いた実験結果により、さらに詳細に、以下の図2、図3、図4、図5を用いて説明する。
【0038】
実験の条件を以下1.〜9.に示す。
1.検査対象の多型位置
VAV2遺伝子のイントロン領域にある多型であり、ヒト染色体9q34領域(GenBank Accession 番号:AC002111、全長39702塩基)の5680番目の塩基位置。
【0039】
2.検査対象の多型の塩基型
TまたはCの一塩基多型である。
【0040】
3.PCRプライマー配列
Shigyoらの報告(インターナショナル ジャーナル オブ キャンサー、78巻425頁から429頁 1998年(M. Shigyo et al., Int. J. Cancer, 78, pp. 425−429 (1998))に則って以下の配列を有するプライマーペアをPCRに用いた。以下これらをオリジナルのプライマーと呼ぶ。
・オリジナルフォワードプライマーの配列(図1のプライマー4に対応):配列番号2
・オリジナルリバースプライマーの配列(図1の配列6に対応):配列番号3
上記のオリジナルフォワードプライマーとオリジナルリバースプライマーを用いたPCR反応によりVAV2遺伝子のイントロン領域(138塩基長)が増幅される。この領域のフォワード鎖の配列を配列番号1で示す。配列番号1中にyの表記で示しているのは、この塩基位置がTとCのヘテロ構造であることを示している。
【0041】
4.アンカー配列
VAV2遺伝子のイントロン領域(以下簡単のため単にVAV2遺伝子領域と呼ぶ)のフォワード鎖を検出する場合には、オリジナルフォワードプライマーの5’末端を蛍光色素(本実験ではROXを用いた)で標識する。オリジナルリバースプライマーには以下の2種類のアンカー配列を5’側に付加し、2種類のアンカー付加プライマー(図1のプライマー10に対応)を準備した。
・アンカー配列1(11塩基長):配列番号4
・アンカー配列2(13塩基長):配列番号5
すなわち、図1の検査領域の配列20および21の塩基数として、アンカー配列1を用いる場合は11塩基、アンカー配列2を用いる場合は13塩基のように決めたことを示す。また、ここでは、11塩基および13塩基の真中(それぞれ6番目および7番目の塩基位置)に多型の塩基位置を配置した。
【0042】
VAV2遺伝子のリバース鎖を検出する場合には、オリジナルリバースプライマーの5’末端に蛍光色素(本実験ではFAMを用いた)を標識する。オリジナルフォワードプライマーには以下のアンカー配列を5’側に付加した。
【0043】
アンカー配列3(11塩基長):配列番号6
すなわち、図1の検査領域の20、21の塩基数として11塩基に決めたことを示す。また、11塩基の真中(6番目の塩基位置)に多型の塩基位置を配置した。
【0044】
5.ゲノム溶液の調製
公知の方法(例えば、QIA−mini キット;キアゲン社)を用いて全血からゲノムDNAを抽出し、50μg/mLの水溶液に調製した。このゲノムDNAのVAV2遺伝子の所定の多型部分は、T−AペアとC−Gペアのヘテロ構造(父母由来の配列が異なる)であることを、DNAシーケンサで解析して確認した。
【0045】
6.PCR反応
PCR反応キット(Platinum Genotype Tsp DNAポリメラーゼ;Life Technologies社)の標準プロトコールに従って、所定の反応バッファー溶液中のdNTP濃度を0.2mM, MgCl2 濃度を1.5mMに調整した。ゲノムDNA量50‐100ng、酵素量0.6U、プライマー量5‐30pmolを用いて、反応液全量15μLでPCR反応を行った。反応容器は200μLのPCR反応用チューブで、サーマルサイクラーにはUno−ThermoBlock (Biometra社)を用いた。
【0046】
温度条件は、94℃2分間の熱変性後、94℃30秒、55℃30秒、72℃60秒のサイクルを30回行い、最後に72℃10分間の最終伸長反応を行った。上記で55℃のアニ−ル温度は、プライマーの配列に応じて、55〜61℃の範囲で、所望以外のDNAが増幅されないように適宜選択した。
【0047】
7.電気泳動装置
分析装置には、ABI Prism 310 Genetic Analyzerを用いた。キャピラリーは内径50μm、外径350μm、長さ47cmである。このとき、試料の注入端から検出点(レーザーの照射点)までの距離は36cmであった。キャピラリー温度は30℃から60℃の範囲で設定した。試料溶液からのDNA注入は電界注入法によって行い、具体的には、15kVの電圧を5秒間印加した。電気泳動は15kVの電圧を印加しておこなった。
【0048】
8.電気泳動試薬
電気泳動用のバッファーには、1×TBE、10%グリセロールを用いた。分離媒体であるポリマーには非変性ポリマーであるGenescan(アプライド・バイオシステムズ社)を用いた。Genescanは重量比7%濃度で供給されているが、電気泳動用バッファーと同じ1×TBE、10%グリセロール溶液中でポリマー濃度が重量比で6%になるように調製した。
【0049】
9.分析する試料溶液の調製
PCR反応溶液を精製キット(QIA‐quick PCR Purificationキット;キアゲン社)を用いてプライマー除去と脱塩を行い、50μLの滅菌純水で溶出した。ついで、この溶液を水で10倍程度に希釈した後、その希釈液1μLと脱イオン化したホルムアミド10μLとを混合し、94℃で5分間加熱してPCR産物を熱変成(一本鎖化)した後、自然空冷して試料溶液とした。尚、上記において水による希釈の倍率は、測定装置ABI Prism 310において適切な信号強度が得られるように適宜調整した。
【0050】
以上1.〜9.に記載した条件で得られた結果の一例を図2に示す。
図2(a)は、蛍光色素(ROX)で標識したオリジナルフォワードプライマーとオリジナルリバースプライマーを用いてPCR反応を行い、36℃でSSCP分析をした例である。横軸は泳動時間、縦軸は蛍光強度を表す。蛍光色素はフォワードプライマーに標識されているので、検出されているのはフォワード鎖である。試料に用いたゲノムDNAが一塩基多型位置においてT/Cヘテロ構造であることに対応して、2つのピークが検出されている。
【0051】
図2(b)は、オリジナルリバースプライマーにアンカー配列1(11塩基長)を付加したプライマーと蛍光色素(ROX)で標識したオリジナルフォワードプライマーを用いてPCR反応を行い、46℃でSSCP分析をした例である。蛍光色素はフォワードプライマーに標識されているので、検出されているのはフォワード鎖である。試料に用いたゲノムDNAが一塩基多型位置においてT/Cヘテロ構造であることに対応して、2つのピークが検出されている。泳動時間が短いほうのピーク32がT、長いほうのピーク33がCの配列を持つものであることを、Tホモ構造およびCホモ構造である別の二種類のゲノムDNAを用いて検証している。図2(a)との比較からわかるように、オリジナルリバースプライマーにアンカー配列1を付加することにより、格段によい分離が得られた。
【0052】
図2(c)は、オリジナルリバースプライマーにアンカー配列2(13塩基長)を付加したプライマーと蛍光色素(ROX)で標識したオリジナルフォワードプライマーを用いてPCR反応を行い、49℃でSSCP分析をした例である。図2(b)の場合と同様に、泳動時間が短いほうのピーク34がT、長いほうのピーク35がCの配列を持つものであることを、Tホモ構造およびCホモ構造である別の二種類のゲノムDNAを用いて検証している。アンカー配列2を付加した場合にもアンカー配列1を付加した場合には若干及ばないものの、オリジナルプライマーと比べた場合には、やはり格段によい分離が得られた。
【0053】
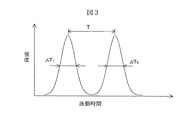
図3を用いて分離能RSの定義を説明する。2つのピークの泳動時間差をTとし、それぞれのピークの半値幅の時間をΔT1、ΔT2とした場合、RS=√(2ln2)・[T/(ΔT1+ΔT2)]で表される。ここでlnは自然対数をあらわす。
【0054】
図4に電気泳動の温度を変化させて分離能RSを測定した結果を示す。曲線36,37,38は、それぞれ、図2(a)(b)(c)の実験結果を得るのに用いたプライマーの組み合わせを用い、電気泳動の温度を変化させて分離能RSを測定した結果を示している。オリジナルのプライマー配列を用いた場合(曲線36)に比べ、リバースプライマーにアンカー配列1(配列番号4)を導入した場合(曲線38)、アンカー配列2(配列番号5)を導入した場合(曲線37)では、分離の最高値は5〜6倍向上した。最高の分離能が得られた温度は、オリジナルプライマーでは36℃、アンカー配列1を導入した場合には49℃、アンカー配列2を導入した場合は46℃であった。
【0055】
図5には、同じくVAV2遺伝子を用い、リバース鎖を検出した結果を示す。
図5(a)はオリジナルプライマーの組を用いた場合、図5(b)はアンカー配列3(配列番号6)をオリジナルフォワードプライマーの5’末端側に付加したプライマーを用いた場合である。図5(c)には図4と同じように、分離能の温度依存性を示した。この場合には、オリジナルプライマーでは分離できなかった(図5(a)のピーク39)ヘテロ構造が、図5(b)のピーク40、41で示すように、アンカー配列の導入で明確に分離できた。このときの温度は39℃であった。一塩基多型は泳動時間が短いほうのピーク40がA、長いほうのピーク33がGであるであることを、フォワード鎖がTホモ構造およびCホモ構造(リバース鎖では、それぞれAホモ、Gホモ)である別の二種類のゲノムDNAを用いて検証している。図5(c)で示すように、最高分離能が得られる温度は39℃であった。
【0056】
以下の表1には、上述の実験結果から得られた最高分離を与える温度の実測値と、アンカー配列のハイブリダイゼーションの融解温度の計算値から得られた最高分離を与える温度の計算値とを示す。
【0057】
表1
最高の分離を与える泳動温度の計算値と実測値、および多型によるヘアピン構造の融解温度の計算値の差と分離能の実測値
【表1】
【0058】
ここで、融解温度の計算には、一塩基ミスマッチを考慮に入れたNearest Neighbor法に基づく熱力学パラメータを用いたが、特に限定するものではない。Nearest Neighbor法の詳細は主に、SantaLucia他による文献:プロシーディング オブ ナショナル アカデミー オブ サイエンス USA 第95巻 1460頁から1465頁 1998年(Proceeding of National Academy of Science of U.S.A., Vol. 95, pp.1460〜1465, (1998))、およびPeyret他による文献:バイオケミストリー 第38巻 12号 3468頁から3477頁 1999年(Biochemistry, Vol. 38,No. 12, pp.3468〜3477, (1999))に開示されている。最高分離を与える温度は、完全マッチと一塩基ミスマッチのTmの平均値とした。
【0059】
表1に示すように、最高分離を与える温度の計算結果と実験結果とは、約7℃以内でほぼ一致している。この結果は、従来のSSCP法では予測不可能であった分離最適温度を、本実施例においては、ある程度あらかじめ予測できることを示している。このため、計算結果に従って電気泳動の温度を設定しても、ある程度の分離が得られる。また、実験的に最高分離が得られるような泳動温度を探索する場合にも、少ない実験量で最適の値を容易に得ることができる。さらに、最高分離が得られる温度をキャピラリー電気泳動装置で設定しやすい温度条件に設定できるように、アンカー配列を適宜設計することもできる。
【0060】
さらに表1には、一塩基多型によるアンカー配列の融解温度の違い(差)の計算値と、最高分離能の実測値を示した。融解温度差の計算値の大小関係と、最高分離能の実測値の大小関係は一致している。すなわち、一塩基多型による融解温度の計算値の差が最も大きくなるようにアンカー配列を設計することによって、高い分離能が得られる。
【0061】
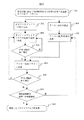
図6には、以上に説明してきた結果を踏まえた、本発明のプライマー設計の工程をフローチャートで示す。
【0062】
検査対象DNAの塩基配列および検査する多型の塩基位置と塩基種のデータセット301を用い、工程302では、まず公知の技術を用いて、PCRプライマーの配列の内の、検査対象のDNAにハイブリダイズする部分(図1に4および6で示した部分であり、オリジナルプライマーと呼ぶ)の塩基配列を設計する。
設計に当たっては、公知の技術により、17ないし30塩基長程度で、一組のプライマーの融解温度がほぼ等しい値になるように、また、プライマーの自己ハイブリダイゼーションや3’末端側でのプライマー同士のハイブリダイゼーションなど、PCRを阻害する要因を除くように考慮する。さらに、PCR増幅産物の長さは、従来のSSCP法で良く用いられている塩基長数十から300塩基長程度になるようにする。このようにして複数組のオリジナルプライマー組の候補を設計しておく。尚、プライマーの設計には、市販のソフトウェアを用いることができる。工程303では、設計した候補の内、一組のオリジナルプライマーを選び、オリゴヌクレオチドを合成する。次いで工程304では、合成したオリジナルプライマーペアを用いてPCR反応を行い、単一長さの特異的な増幅が良好に起こるか否かを、アガロース電気泳動などの適当な公知技術を用いて検定する。
増幅が良好であれば、そのプライマーペアを選定して工程305に進む。増幅が悪い場合は、工程302で設計した別のオリジナルプライマーペアを用いて工程303と304を行う。この過程を繰り返してオリジナルプライマーペアを決定する。
【0063】
尚、過去の文献等で、検査対象の多型部位を含む領域を特異的に増幅できることが実験的に検証されているプライマー配列が報告されている場合には、工程303においてその配列をオリジナルプライマー配列に用いることもできる。
【0064】
一方、工程306では、データセット301を用いて、アンカー配列を設計する。できるだけ高い分離能を得るためには、アンカー配列が多型部位を含む領域と特異的にハイブリダイズし、かつ多型部位の塩基が異なることによる融解温度の差が最も大きくなるようにする。さらに、キャピラリー電気泳動に適した測定条件にするために、融解温度の計算値が30℃から60℃位になるように、またアンカー配列の長さをおおよそ7−15塩基長程度にする。より単純には、アンカー配列は、多型部位を含む7から15塩基長程度の範囲の配列で、多型部位に相当する塩基位置を除いて鋳型DNAと完全に同じ配列とする。アンカー配列が短すぎると類似配列の出現率が高くなり、長すぎるとTm値が高くなりすぎて好ましくない場合がある。アンカー配列内の多型部位に相当する位置とその塩基種類は、多型による融解温度の計算値の差が最も大きくなるようにする。この考え方で、複数のアンカー配列候補を設計する工程が306である。
【0065】
工程307では、工程306で設計したアンカー配列候補のうち、1つを選ぶ。工程305では、工程304で選択したオリジナルプライマー組の片方に工程307で選んだアンカー配列を付加したプライマーを合成する。
【0066】
次いで、工程308では、アンカー配列を付加したプライマーともう一方のオリジナルプライマーを用いて、再びPCR反応を行い、特異的増幅の良否をチェックする。増幅が好ましい時は、次の工程309に進み、好ましくないときは、工程303に戻って別のオリジナルプライマーペアを選択し、再び工程をやりなおす。
【0067】
工程309では、電気泳動分析により、多型の分離能を検定する。この工程において、全自動キャピラリー電気泳動装置を用いる場合には、アンカー配列を付加していないオリジナルプライマーに蛍光標識を行い、PCR増幅を行ってから測定する。電気泳動の温度は、アンカー配列の融解温度から計算される値を初期値として、10℃程度の範囲で前後数点の測定を行えば、最適値を得ることができる。分離が良好な場合は、この工程309で用いたプライマー組と泳動温度の条件が、確立されたプライマーと分析条件310となる。分離が悪い場合には、工程307に戻り、別のアンカー配列候補を用いて工程305からやりなおす。
【0068】
上述のような一連の工程を経て、検査対象の多型部位について実験的にも保証されたプライマーと分析条件を得ることができる。
【0069】
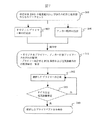
本発明のプライマー設計の一連のプロセスについて、別の実施例を図7に示す。検査対象DNAの塩基配列および検査する多型の塩基位置と塩基種のデータセット301を用い、オリジナルプライマーの設計工程302とアンカー配列の設計工程306により、プライマーペアの候補とそれを用いる場合の推奨PCR条件と電気泳動条件の一覧表311を得ることができる。一覧表311から選択したプライマーペアを工程312において合成し、工程313でPCR反応と電気泳動分析を行い、多型の分離を検証する。良好な分離が得られた場合、プライマーと分析条件310を確定する。良好でない場合には、工程312に戻り、別のプライマーを合成するところからやりなおす。本実施例においては、単純なフローチャートであるため、候補となるプライマーペアを複数一度に評価するのには都合がよい。
【0070】
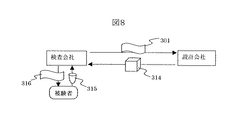
図8と図9には、上記図6と図7で示したプライマーと分析条件の確立を行うサービスビジネスの実施例を示す。
【0071】
図9では、検査会社は、図6および図7で示したデータセット301を設計会社に提示する。設計会社は、図6または図7に示したようなフローチャートに従って、プライマーと分析条件を確立し、試薬としてのプライマーと測定条件を記載したドキュメントを含む検査キット314を提供し対価を得る。検査会社は、被験者から血液や組織などの生体試料315を受け取り、その分析結果316を報告して対価を得る。本実施例では、検査会社においては、自社で多くの時間と人手をかけなくても、所定の多型に関する検査キットを入手できる効果があり、設計会社においては、従来のSSCP法に比べて分析に最適な条件の予測性がよい本発明によって、キットを確立するのに必要な時間と労力を短縮でき、低価格でサービスを提供できるメリットがある。
【0072】
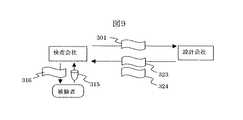
図9では、本発明に基づくサービスビジネスの別の実施例を示す。本実施例では、図8で説明した実施例と同様に、検査対象の多型を含むDNAの配列と多型の配列情報(データセット301)に基づいてプライマー配列を設計して、プライマー組の配列のいくつかの候補をリストアップ(プライマー組の配列一覧表323)し、それに推奨する分析条件(条件のデータ324)を添付する。実験に基づく検証は行わない。実験条件の決定は検査会社が行う。検査会社は設計結果に基づいて実験を行い、最終的なプライマーの選定と分析条件を確立する。そして確立した分析条件を用いて被験者から提供を受けた生体試料315に対する分析結果316を報告する。検査会社は被験者から検査費用を受け取り、設計会社には設計費用を支払う。
【0073】
この実施例においては、設計会社と検査会社の間には、試料やプライマーなどの物のやり取りはなく、データのやりとりだけなので、設計会社にとっては、インターネット上のホームページによってサービスを提供する形態も可能となる。
このため、低価格のサービスが提供できる。本発明においては、従来の技術と異なり、分離に最適な条件が予測可能なため、実験による保証はないものの、ユーザに推奨条件を提示することは可能である。実験設備やノウハウの十分に整った検査会社などの依頼者に対しては、低価格で設計結果のみを提供できる効果がある。
【0074】
【発明の効果】
本発明によれば、PCR−SSCP法に用いるPCRプライマーに、検査領域の配列として想定される配列と同一の配列をアンカー配列として付加することにより、電気泳動測定時にヘアピン状態を起こさせる。ヘアピン状態の融解温度が一塩基の違いによって異なることを利用して、その中間の温度で電気泳動を行うことにより、SSCP法による一塩基多型の分離能を著しく改善することができる。また、分離に最適な温度を予測することが可能となり、従来のSSCP法で必須であった分析条件の最適化に要する手間を大きく低減できる。また、最高の分離を与える電気泳動温度がキャピラリー電気泳動装置に適した温度範囲に入るように、アンカー配列を設計することができる。このため、遺伝子診断の自動化・高精度化に大きな効果がある。さらに、本発明によって、一塩基多型を分離分析するための推奨の実験条件を添付した形で、PCRプライマーの配列あるいは合成したPCRプライマーを提供するサービスビジネスが実現できる。
【0075】
【配列表】
【0076】
【配列表フリーテキスト】
配列番号2:合成ポリヌクレオチド
配列番号3:合成ポリヌクレオチド
配列番号4:合成ポリヌクレオチド
配列番号5:合成ポリヌクレオチド
配列番号6:合成ポリヌクレオチド
【図面の簡単な説明】
【図1】本発明の原理を工程に沿って示す。
【図2】本発明の原理に基づく電気泳動測定結果の一例を示す。
(a)従来のSSCP法でフォワード鎖を検出して得られた電気泳動スペクトル
(b)本発明でアンカー配列として配列番号4の配列からなるポリヌクレオチドを用いフォワード鎖を検出して得られた電気泳動スペクトル
(c)本発明でアンカー配列として配列番号5の配列からなるポリヌクレオチドを用いフォワード鎖を検出して得られた電気泳動スペクトル
【図3】分離能の定義の説明図を示す。
【図4】図2(a)(b)(c)で示したそれぞれの場合について、分離能と温度との関係を測定した結果を示す。
【図5】(a)従来のSSCP法でリバース鎖を検出して得られた電気泳動スペクトルを示す。
(b)本発明でアンカー配列として配列番号6の配列からなるポリヌクレオチドを用いリバース鎖を検出して得られた電気泳動スペクトルを示す。
(c)(a)(b)それぞれの場合で、分離能の電気泳動温度に対する依存性を示す。
【図6】本発明のPCRプライマーの設計手順のフローチャートを示す。
【図7】本発明のPCRプライマーの別の設計手順のフローチャートを示す。
【図8】図6及び図7で示した設計フローの全部または一部を実施する設計会社を含むビジネスモデルの一実施例を示す。
【図9】図6及び図7で示した設計フローの一部を実施する設計会社を含むビジネスモデルの別の実施例を示す。
【符号の説明】
1.ゲノムDNA(父由来)
11.ゲノムDNA(母由来)
2,12.多型部位
4,10.プライマー
8.蛍光色素
20、21.検査領域の配列
20’、21’.検査領域の配列
20、21の相補配列
7、7’.アンカー配列およびその相補配列
13、23.PCR産物
14、24.一本鎖化したPCR産物のうち、蛍光色素8で標識されている鎖
315.生体試料(血液、組織など)
316.検査結果を記載した書類
301.検査対象の多型部位を含む領域のDNA配列及び多型の位置と塩基種からなるデータ。
314.プライマー及び反応・測定条件が記載された書類を含む検査キット
323.プライマー配列
324.推奨する反応・測定条件が記載された書類
Claims (15)
- 二本鎖DNAの一方の鎖における検査領域より3’末端側の配列にハイブリダイズする第1の配列部分と、前記検査領域の配列として想定される配列と同一の配列を持ち、かつ前記第1の配列部分の5’末端側に続く第2の配列部分とを有する第1のプライマーと、前記DNAの他方の鎖における検査領域より3’末端側の配列にハイブリダイズする第2のプライマーとを使用して、前記DNAを鋳型とするPCR反応により前記検査領域を含むDNA断片を増幅する工程と、
増幅された前記DNA断片を一本鎖化した後に電気泳動分離する工程と
を含むことを特徴とする、核酸配列の検査方法。 - 一本鎖DNAまたは二本鎖DNAの一方の鎖における第1の所定の塩基数からなる検査領域の3’末端から5’→3’方向に第2の所定の塩基数だけ離れた第3の所定の塩基数の配列にハイブリダイズする第1の配列部分と、前記第1の所定の塩基数からなり、前記検査領域の配列として想定される配列と同一の配列を持ち、かつ前記第1の配列部分の5’末端側に続く第2の配列部分とを有する第1のプライマーと、前記検査領域の配列の5’末端から3’→5’方向に第4の所定の塩基数だけ離れた第5の所定の塩基数の配列に相補な配列にハイブリダイズする配列を有し、5’末端が標識された第2のプライマーとを使用して、前記DNAを鋳型とするPCR反応により前記検査領域を含むDNA断片を増幅する工程と、
増幅された前記DNA断片を一本鎖化した後に電気泳動分離する工程と
を含むことを特徴とする、核酸配列の検査方法。 - 得られた一本鎖DNA断片の3’末端側に形成された、前記第2の配列部分の配列に相補な第3の配列部分の配列と、前記検査領域の配列との自己ハイブリダイゼーションの有無を指標として前記検査領域の配列を同定する工程を更に含む、請求項1または2に記載の核酸配列の検査方法。
- 二本鎖DNAの一方の鎖における検査領域より3’末端側の配列にハイブリダイズする第1の配列部分と、前記検査領域の配列として想定される配列と同一の配列を持ち、かつ前記第1の配列部分の5’末端側に続く第2の配列部分とを有する第1のプライマーと、前記DNAの他方の鎖における検査領域より3’末端側の配列にハイブリダイズする第2のプライマーとを使用して、前記DNAを鋳型とするPCR反応により前記検査領域を含むDNA断片を増幅する工程と、
増幅された前記DNA断片の自己ハイブリダイゼーションの有無により、前記検査領域の配列を同定する工程と
を含むことを特徴とする、核酸配列の検査方法。 - 二本鎖DNAの一方の鎖における検査領域より3’末端側の配列にハイブリダイズする第1の配列部分と、前記検査領域の配列を検出するための配列を持ち、かつ前記第1の配列部分の5’末端側に続く第2の配列部分とを有する第1のプライマーと、前記DNAの他方の鎖における検査領域より3’末端側の配列にハイブリダイズする第2のプライマーとを使用して、前記DNAを鋳型とするPCR反応により前記検査領域を含むDNA断片を増幅する工程と、
増幅された前記DNA断片を一本鎖化した後に電気泳動分離する工程と
を含むことを特徴とする、核酸配列の検査方法。 - 検査領域が1塩基多型の塩基位置を含む、請求項1〜5のいずれか1項に記載の核酸配列の検査方法。
- 検査領域の配列が異なる複数のDNAの存在比を、前記複数のDNAから増幅された複数のDNA断片の泳動ピークの強度比から求めることを特徴とする、請求項1〜5のいずれか1項に記載の核酸配列の検査方法。
- 二本鎖DNAの一方の鎖における検査領域より3’末端側の配列にハイブリダイズする第1の配列部分と、前記検査領域の配列として想定される配列と同一の配列を持ち、かつ前記第1の配列部分の5’末端側に続く第2の配列部分とを有する第1のプライマーと、前記DNAの他方の鎖における検査領域より3’末端側の配列にハイブリダイズする第2のプライマーとを使用して、前記DNAを鋳型とするPCR反応により前記検査領域を含むDNA断片を増幅する工程を含むことを特徴とする、試料調製方法。
- 一本鎖DNAまたは二本鎖DNAの一方の鎖における第1の所定の塩基数からなる検査領域の3’末端から5’→3’方向に第2の所定の塩基数だけ離れた第3の所定の塩基数の配列にハイブリダイズする第1の配列部分と、前記第1の所定の塩基数からなり、前記検査領域の配列として想定される配列と同一の配列を持ち、かつ前記第1の配列部分の5’末端側に続く第2の配列部分とを有する第1のプライマーと、前記検査領域の配列の5’末端から3’→5’方向に第4の所定の塩基数だけ離れた第5の所定の塩基数の配列に相補な配列にハイブリダイズする配列を有する第2のプライマーとを使用して、前記DNAを鋳型とするPCR反応により前記検査領域を含むDNA断片を増幅する工程を含むことを特徴とする、試料調製方法。
- 二本鎖DNAの一方の鎖における検査領域より3’末端側の配列にハイブリダイズする第1の配列部分と、前記検査領域の配列として想定される配列と同一の配列を持ち、かつ前記第1の配列部分の5’末端側に続く第2の配列部分とを有する第1のプライマー、及び
前記DNAの他方の鎖における検査領域より3’末端側の配列にハイブリダイズする第2のプライマー
を含むことを特徴とする、核酸配列の検査のためのキット。 - 一本鎖DNAまたは二本鎖DNAの一方の鎖における第1の所定の塩基数からなる検査領域の3’末端から5’→3’方向に第2の所定の塩基数だけ離れた第3の所定の塩基数の配列にハイブリダイズする第1の配列部分と、前記第1の所定の塩基数からなり、前記検査領域の配列として想定される配列と同一の配列を持ち、かつ前記第1の配列部分の5’末端側に続く第2の配列部分とを有する第1のプライマー、
前記検査領域の配列の5’末端から3’→5’方向に第4の所定の塩基数だけ離れた第5の所定の塩基数の配列に相補な配列にハイブリダイズする配列を有し、5’末端が標識された第2のプライマー
を含むことを特徴とする、核酸配列の検査のためのキット。 - 増幅されたDNA断片の3’末端側に形成された、前記第2の配列部分の配列に相補な第3の配列部分の配列と前記検査領域の配列との自己ハイブリダイゼーションの有無を電気泳動で分析するための温度条件のデータを更に含むことを特徴とする、請求項10または11に記載のキット。
- 検査領域に含まれる多型または変異を電気泳動で分析するための、請求項10〜12のいずれか1項に記載のキット。
- 検査領域における1塩基多型を解析するためのものである、請求項10〜13のいずれか1項に記載のキット。
- 検査領域の配列が異なる複数のDNAの存在比を解析するためのものである、請求項10〜13のいずれか1項に記載のキット。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002357804A JP2004187545A (ja) | 2002-12-10 | 2002-12-10 | 核酸配列の検査方法及び試料調製方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2002357804A JP2004187545A (ja) | 2002-12-10 | 2002-12-10 | 核酸配列の検査方法及び試料調製方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2004187545A true JP2004187545A (ja) | 2004-07-08 |
| JP2004187545A5 JP2004187545A5 (ja) | 2005-10-06 |
Family
ID=32757705
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2002357804A Pending JP2004187545A (ja) | 2002-12-10 | 2002-12-10 | 核酸配列の検査方法及び試料調製方法 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP2004187545A (ja) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR100825154B1 (ko) | 2006-09-27 | 2008-04-24 | 포항공과대학교 산학협력단 | 모세관 전기영동-단일쇄 형태변환 다형성을 이용한 세포내mRNA 정량 방법 |
| US7833716B2 (en) | 2006-06-06 | 2010-11-16 | Gen-Probe Incorporated | Tagged oligonucleotides and their use in nucleic acid amplification methods |
| JP2012511923A (ja) * | 2008-12-17 | 2012-05-31 | ビオコールテク | 気分障害および自殺を誘発する、薬剤の潜在的なリスクの評価:専用プラットフォームの使用 |
| WO2015015585A1 (ja) * | 2013-07-31 | 2015-02-05 | 株式会社日立製作所 | 遺伝子変異分析装置、遺伝子変異分析システム及び遺伝子変異分析方法 |
| JP5723993B2 (ja) * | 2012-10-19 | 2015-05-27 | 株式会社日立製作所 | 遺伝子分析方法および遺伝子分析装置および分析用キット |
-
2002
- 2002-12-10 JP JP2002357804A patent/JP2004187545A/ja active Pending
Cited By (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9284549B2 (en) | 2006-06-06 | 2016-03-15 | Gen-Probe Incorporated | Tagged oligonucleotides and their use in nucleic acid amplification methods |
| US7833716B2 (en) | 2006-06-06 | 2010-11-16 | Gen-Probe Incorporated | Tagged oligonucleotides and their use in nucleic acid amplification methods |
| US8034570B2 (en) | 2006-06-06 | 2011-10-11 | Gen-Probe Incorporated | Tagged oligonucleotides and their use in nucleic acid amplification methods |
| USRE48909E1 (en) | 2006-06-06 | 2022-02-01 | Gen-Probe Incorporated | Tagged oligonucleotides and their use in nucleic acid amplification methods |
| US8278052B2 (en) | 2006-06-06 | 2012-10-02 | Gen-Probe Incorporated | Tagged oligonucleotides and their use in nucleic acid amplification methods |
| US8580510B2 (en) | 2006-06-06 | 2013-11-12 | Gen-Probe Incorporated | Tagged oligonucleotides and their use in nucleic acid amplification methods |
| US10167500B2 (en) | 2006-06-06 | 2019-01-01 | Gen-Probe Incorporated | Tagged oligonucleotides and their use in nucleic acid amplification methods |
| KR100825154B1 (ko) | 2006-09-27 | 2008-04-24 | 포항공과대학교 산학협력단 | 모세관 전기영동-단일쇄 형태변환 다형성을 이용한 세포내mRNA 정량 방법 |
| JP2017169571A (ja) * | 2008-12-17 | 2017-09-28 | アルスディアグAlcediag | 気分障害および自殺を誘発する、薬剤の潜在的なリスクの評価:専用プラットフォームの使用 |
| JP2012511923A (ja) * | 2008-12-17 | 2012-05-31 | ビオコールテク | 気分障害および自殺を誘発する、薬剤の潜在的なリスクの評価:専用プラットフォームの使用 |
| JP5723993B2 (ja) * | 2012-10-19 | 2015-05-27 | 株式会社日立製作所 | 遺伝子分析方法および遺伝子分析装置および分析用キット |
| WO2015015585A1 (ja) * | 2013-07-31 | 2015-02-05 | 株式会社日立製作所 | 遺伝子変異分析装置、遺伝子変異分析システム及び遺伝子変異分析方法 |
| US10274459B2 (en) | 2013-07-31 | 2019-04-30 | Hitachi, Ltd. | Gene mutation analyzer, gene mutation analysis system, and gene mutation analysis method |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0907752B1 (en) | Method for determination of nucleic acid sequences and diagnostic applications thereof | |
| US11913066B2 (en) | SE33 mutations impacting genotype concordance | |
| WO2008059578A1 (fr) | Procédé d'amplification pcr multiplex | |
| JP3844996B2 (ja) | 反復性pcr産物の融解曲線解析方法 | |
| WO2008118839A1 (en) | Exon grouping analysis | |
| CN104894256A (zh) | 检测乙醛脱氢酶2基因rs671多态性位点的引物、试剂盒及其PCR方法 | |
| Dearlove | High throughput genotyping technologies | |
| CN108823294B (zh) | 基于20个单倍群d的y-snp遗传标记的法医学复合检测试剂盒 | |
| CN110564861A (zh) | 人类Y染色体STR基因座和InDel位点的荧光标记复合扩增试剂盒及其应用 | |
| KR101119417B1 (ko) | 비만 유전자 증폭용 프라이머 세트, 그것을 포함하는 비만 유전자 증폭용 시약 및 그 용도 | |
| CN104830991A (zh) | 检测pdgfra基因d842v多态性位点的引物、试剂盒及其pcr方法 | |
| CN104830992A (zh) | 检测亚甲基四氢叶酸还原酶c677t多态性位点的引物、试剂盒及其pcr方法 | |
| JP2004187545A (ja) | 核酸配列の検査方法及び試料調製方法 | |
| JP5319148B2 (ja) | 標的核酸中の変異の検出方法及びアレイ | |
| JP4243262B2 (ja) | オリゴヌクレオチドプローブ、前記プローブが固定化されているマイクロアレイ及び前記プローブを設計する方法 | |
| JP4336877B2 (ja) | β3アドレナリン受容体変異遺伝子の検出法ならびにそのための核酸プローブおよびキット | |
| CN113234838A (zh) | 高分辨率熔解曲线鉴定绵羊FecB基因型的引物对、产品和方法 | |
| USRE44894E1 (en) | Method of detecting or quantitatively determining mitochondrial DNA 3243 variation, and kit therefor | |
| JP4437207B2 (ja) | Cyp2d6の変異の検出法ならびにそのための核酸プローブおよびキット | |
| JP2008125471A (ja) | マルチプレックスな核酸増幅方法 | |
| JP2007143420A (ja) | 塩基配列の判別方法 | |
| CN114438173B (zh) | 同时检测60个InDel遗传多态性位点复合扩增试剂盒及应用 | |
| JP4505839B2 (ja) | Cyp2d6*4の変異の検出法ならびにそのための核酸プローブおよびキット | |
| CN109312397A (zh) | Penta E基因座多态性人体鉴定 | |
| JP4437206B2 (ja) | Cyp2c9の変異の検出法ならびにそのための核酸プローブおよびキット |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20050517 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20050517 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080205 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20080404 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20080507 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20080909 |