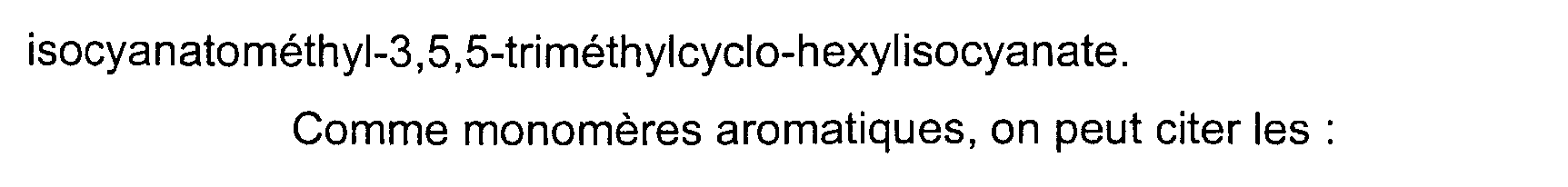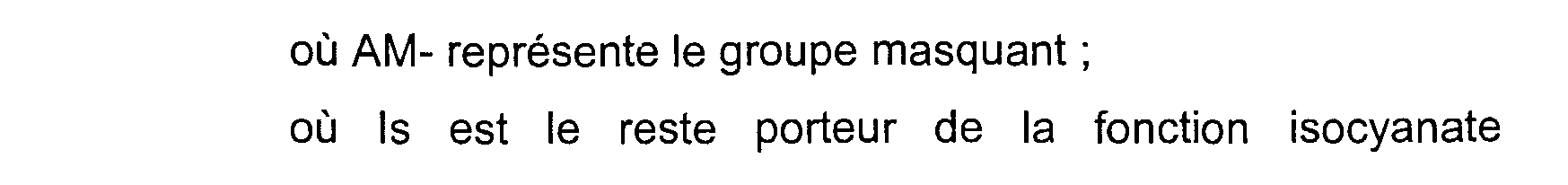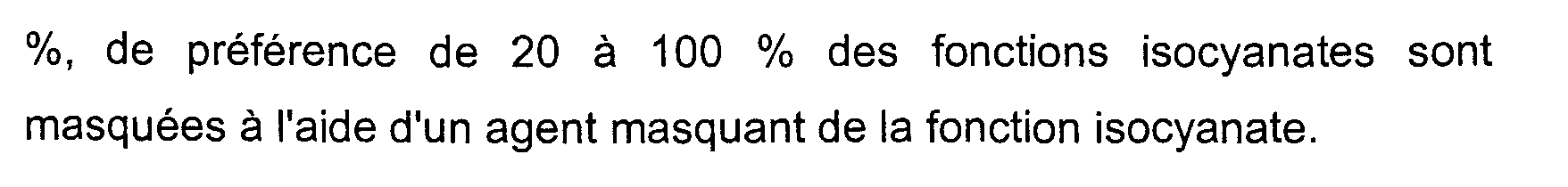FR2818973A1 - Nouveau procede de (cyclo) condensation d'isocyanates au moyen d'un sel de silazane d'etain - Google Patents
Nouveau procede de (cyclo) condensation d'isocyanates au moyen d'un sel de silazane d'etain Download PDFInfo
- Publication number
- FR2818973A1 FR2818973A1 FR0017315A FR0017315A FR2818973A1 FR 2818973 A1 FR2818973 A1 FR 2818973A1 FR 0017315 A FR0017315 A FR 0017315A FR 0017315 A FR0017315 A FR 0017315A FR 2818973 A1 FR2818973 A1 FR 2818973A1
- Authority
- FR
- France
- Prior art keywords
- isocyanate
- group
- advantageously
- weight
- compounds
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 0 CC(*)(*N*)N Chemical compound CC(*)(*N*)N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D251/00—Heterocyclic compounds containing 1,3,5-triazine rings
- C07D251/02—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings
- C07D251/12—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D251/26—Heterocyclic compounds containing 1,3,5-triazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with only hetero atoms directly attached to ring carbon atoms
- C07D251/40—Nitrogen atoms
- C07D251/42—One nitrogen atom
- C07D251/46—One nitrogen atom with oxygen or sulfur atoms attached to the two other ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D229/00—Heterocyclic compounds containing rings of less than five members having two nitrogen atoms as the only ring hetero atoms
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/02—Polymeric products of isocyanates or isothiocyanates of isocyanates or isothiocyanates only
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/08—Processes
- C08G18/09—Processes comprising oligomerisation of isocyanates or isothiocyanates involving reaction of a part of the isocyanate or isothiocyanate groups with each other in the reaction mixture
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G18/00—Polymeric products of isocyanates or isothiocyanates
- C08G18/06—Polymeric products of isocyanates or isothiocyanates with compounds having active hydrogen
- C08G18/08—Processes
- C08G18/16—Catalysts
- C08G18/22—Catalysts containing metal compounds
- C08G18/24—Catalysts containing metal compounds of tin
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Polyurethanes Or Polyureas (AREA)
Abstract
Cette invention concerne un procédé de (cyclo) condensation, catalytique d'isocyanates monomères caractérisé en ce qu'il comprend :a) la réaction des isocyanates monomères de départ avec un catalyseur comprenant un sel d'étain (II) d'un composé de formule (1), (CF DESSIN DANS BOPI) ou un précurseur dudit composé,à une température d'au moins 20degreC et avantageusement d'au moins 40degreC et d'au plus 100degreC, avantageusement d'au plus 80degreC, b) l'arrêt de la réaction de la (cyclo) condensation au taux de transformation souhaité compris entre 5 et 95 %, avantageusement entre 10 et 50% et c) l'élimination éventuelle des monomères n'ayant pas réagi ou la réaction avec d'autres composés réactifs avec la fonction isocyanate.
Description
<Desc/Clms Page number 1>
L'invention concerne un nouveau procédé de (cyclo)condensation catalytique d'isocyanates.
L'invention concerne plus particulièrement un procédé de (cyclo) condensation d'isocyanates conduisant à la production de composés 2-imino-4-oxo-1, 3-diazétidine et d'oligomères de ceux-ci.
Il est connu de préparer des 2-imino-4-oxo-1, 3-diazétidines par cycloaddition (2 + 2) d'isocyanates sur des carbodiimides (Houben Weyl, Methoden der Organischen Chemie, Vierte Auflage ; Georg Thieme Verlag, 1983, pp 1111-1113).
Par ailleurs, EP 576 53 (Rhône-Poulenc) décrit des catalyseurs de trimérisation diisocyanates aliphatiques consistant en composés à groupement amino silylés, notamment des silazans.
Grâce à l'invention, il a été découvert de manière surprenante que les isocyanates en présence de certains sels de silazane conduisaient par (cyclo) addition ou (cyclo) condensation à un mélange réactionnel contenant en proportion importante, variant suivant le taux de transformation des composés à cycle 2-imino-4-oxo-1, 3-diazétidine.
On a, en outre, découvert de manière surprenante que ces sels de silazane permettaient de catalyser la (cyclo) condensation d'isocyanates dans lesquels la fonction isocyanate est peu accessible, notamment les isocyanates dans lesquels la fonction isocyanate est portée par un atome de carbone d'un cycle aliphatique, secondaire, tertiaire ou néopentylique, ou dans lesquels le squelette hydrocarboné comportait une ramification en a ou en ss de la fonction NCO.
L'invention a pour objet un procédé de (cyclo) condensation catalytique d'isocyanates monomères qui comprend : a) la réaction des isocyanates monomères de départ avec un catalyseur comprenant un sel d'étain (II) d'un composé de formule (1),
<Desc/Clms Page number 2>
dans laquelle les symboles : - Ri, R2, R3, R4, R5 et R6 identiques ou différents représentent un groupe monovalent de nature hydrocarbonée ayant de 1 à 30 atomes de carbone, aliphatique, cycloaliphatique saturé ou insaturé, aryle, aralkyl ou alkylaryle, éventuellement substitué par des atomes d'halogène, des groupements CN, ou ester, et/ou éventuellement interrompu par un ou plusieurs atomes choisis parmi 0, S, N et Si, ou - l'un de Ri, R2, R3, R4, R5 et R6 représente un motif de formule (2) :
A étant un groupe alkylène ayant de 1 à 30, avantageusement 2 à 20 atomes de carbone éventuellement substitué par des atomes d'halogène, des groupements CN, ou ester, et/ou éventuellement interrompu par un ou plusieurs atomes choisis parmi 0, S, N et Si, A étant de préférence (CH2) n' avec n'compris entre 1 et 6, et R'1 à R'5 identiques ou différents représentant un groupe monovalent de nature hydrocarbonée ayant de 1 à 30 atomes de carbone, aliphatique, cycloaliphatique saturé ou insaturé, aryle, aralkyl ou alkylaryle, éventuellement substitué par des atomes d'halogène, des groupements CN, ou ester éventuellement interrompu par un ou plusieurs atomes choisis parmi 0, S, N et Si, et n est un nombre entier entre 1 et 50, ou
<Desc/Clms Page number 3>
- deux parmi R1, R2 et R3 d'une part et/ou R4, R5 et R6 d'autre part, constituent ensemble un groupe hydrocarboné divalent ayant de 1 à 30 atomes de carbone éventuellement substitué par des atomes d'halogène, des groupements CN, ou ester, et/ou éventuellement interrompu par un ou plusieurs atomes choisis parmi 0, S, N et Si, et/ou - au moins un groupe choisi parmi R1, R2 et R3 forme avec au moins un groupe parmi R4, R5 et R6 un groupe hydrocarboné divalent ayant de 1 à 30 atomes de carbone éventuellement substitué par des atomes d'halogène, des groupements CN, ou ester, et/ou éventuellement interrompu par un ou plusieurs atomes choisis parmi 0, S, N et Si, ou un précurseur dudit composé,
à une température d'au moins 20 C et avantageusement d'au moins 40 C et d'au p ! us 100 C, avantageusement d'au plus 80oC, b) l'arrêt de la réaction de (cyclo) condensation au taux de transformation souhaité compris entre 5 et 95 %, avantageusement entre 10 et 50 % ; et
c) l'élimination éventuelle des monomères n'ayant pas réagi ou la réaction avec d'autres composés réactifs avec la fonction isocyanate.
à une température d'au moins 20 C et avantageusement d'au moins 40 C et d'au p ! us 100 C, avantageusement d'au plus 80oC, b) l'arrêt de la réaction de (cyclo) condensation au taux de transformation souhaité compris entre 5 et 95 %, avantageusement entre 10 et 50 % ; et
c) l'élimination éventuelle des monomères n'ayant pas réagi ou la réaction avec d'autres composés réactifs avec la fonction isocyanate.
A l'issue du procédé tel que défini ci-dessus, on obtient une composition comprenant outre les isocyanates monomères de départ n'ayant pas réagi des composés 2-imino-4-oxo-1,3-diazétidines de formule (3) :
dans lequel R est le reste d'un composé monomère isocyanate de formule :
dans lequel R est le reste d'un composé monomère isocyanate de formule :
<Desc/Clms Page number 4>
R-N-CO, dans laquelle R est notamment un reste hydrocarboné aliphatique, linéaire ou ramifié, cycloaliphatique ou aromatique ayant de 4 à 30 atomes de carbone comportant éventuellement un ou plusieurs substituants choisis parmi un groupe NCO, un groupe carbamate, allophanate, ester, éther, etc.
La présence d'une teneur substantielle en composés de formule (3) dans une composition polyisocyanate est particulièrement intéressante dans la mesure où ces composés ont une fonctionnalité NCO de trois et une masse plus faible en comparaison des monoisocyanurates correspondants de même fonctionnalité.
Avantageusement Ri à R6 et R'1 à R's identiques ou différents représentent : un groupe alkyle, alkényle, halogénoalkyle ou halogénoalkényle ayant de 1 à 20, de préférence de 1 à 6 atomes de carbone, et comportant éventuellement des atomes de chlore et/ou de fluor, - un groupe cycloalkyl, cycloalkényle, halogénocycloalkyle ou halogénocycloalkényle ayant de 3 à 30, de préférence 3 à 10 atomes de carbone et contenant des atomes de chlore et/ou de fluor, - un groupe aryle, alkylaryl ou halogénoaryle ayant de 6 à 30, de préférence 6 à 10 atomes de carbone et contenant des atomes de chlore et/ou de fluor, - un groupe cyanoalkyl ayant de 1 à 30, de préférence 1 à 6 atomes de carbone, - ou deux groupes parmi Ri, R2 et R3 ou R3, R4 et R5 forment ensemble un radical divalent comprenant de 2 à 5 atomes de carbone, - ou deux parmi Ri, R2 et R3 d'une part et/ou R4, Rs et R6 d'autre part, constituent ensemble un groupe hydrocarboné divalent, ou - au moins un groupe choisi parmi Ri, R2 et R3 forme avec au moins un groupe parmi R4, Rs et R6 un groupe hydrocarboné divalent, comprenant de 2 à 5 atomes de carbone.
<Desc/Clms Page number 5>
De préférence, R1 à R6 identiques ou différents sont choisis parmi les groupes méthyle, éthyle, propyle, ispropyle, butyle, isobutyle, a-pentyle, t-butyle, chlorométhyle, dichlorométhyle, α-chloro-éthyle, a, ss--dichloroéthyle, fluorométhyle, difluorométhyle, a, ss-difluoroéthyle, trifluoro-3, 3,3 propyle, trifluoro cyclopropyle, trifluoro-4, 4,4 butyle, heptafluoro-3, 3,3, 4,4, 5,5 pentyle, ss-cyanoéthyle, y-cyanopropyle, phényle, p-chlorophényle, m-chlorophényle, dichloro-3, 5 phényle, trichlorophényle,
tétrachlorophényle, o-, p-, ou m-tolyle, a, a, a-trifluorotolyle ; et
tétrachlorophényle, o-, p-, ou m-tolyle, a, a, a-trifluorotolyle ; et
<Desc/Clms Page number 6>
xylyles (diméthyl-2, 3 phényle ; diméthyl-3, 4 phényle) ; ou deux groupes parmi Ri, R2 et R3, d'une part et/ou R4, R5 et R6, d'autre part pris ensemble représentent un groupe propylène, butylène, pentylène, de préférence leurs isomères linéaires, triméthylène, tétraméthylène ou pentaméthy ! ène, et/ou Ri et R4 pris ensemble représentent un groupe choisi parmi éthylène, propylène, butylène, pentylène, de préférence les isomères non ramifiés, diméthylène et triméthylène, ou deux groupes parmi les groupes mentionnés ci-dessus représentent ensemble une chaîne-N--Si (CH3) 2-N-.
Des groupes R1 à R6 et R'1 à R'5 particulièrement préférés sont choisis parmi méthyle, éthyle, propyle, linéaires ou ramifiés le cas échéant, vinyle et phényle, pouvant éventuellement être chloré et/ou fluoré.
Lorsque les groupes Ri à R6 et R'1 à R'5 sont chlorés et/ou fluorés, le nombre d'atomes d'halogène varie de 1 à la totalité des valences disponibles.
On peut tout particulièrement citer les sels des composés silazans suivants : hexaméthyldisilazane, diéthyl 1-3, tétraméthyl-1, 1,3, 3 disilazane, divinyl-1, 3 tétraméthyl-1, 1,3, 3 disilazane, hexaéthyldisliazane, diphényl-1, 3 tétraméthyl-1, 1,3, 3 disilazane, hexaméthylcyclotrisilazane, et éthylène-2, 5-tétraméthyl 2, 2,5, 5-cyclodisilazane.
Le sel selon l'invention peut comprendre outre un ligand de formule (1) ci-dessus, éventuellement un ligand différent.
Généralement, on préfère que tous les ligands soient des composés de formule (1) auquel cas la formule des composés de l'invention se lira lorsque n'représente zéro :
<Desc/Clms Page number 7>
Les sels selon l'invention sont des composés existant dans le commerce ou pouvant être préparés à partir des silazans correspondants, par exemple par réaction avec un amidure ou hydrure métallique ou un alkyl-métal en milieu éther à température ambiante.
Les sels de l'invention peuvent également être obtenus par échange du cation lithium d'un sel de lithium avec un étain au moyen du chlorure d'étain.
Les silazans de départ sont des composés connus disponibles dans le commerce ou peuvent être obtenus à partir des chlorosilazanes correspondants au moyen de réaction simples usuelles dans le domaine en question.
Pour la préparation des silazans cycliques, on pourra se reporter à Houben-Weyl : Methoden der Organische Chemie"Organosilicum Verbindungen", Georg Thieme Verlag, Stuttgart, 1980.
Pour plus de précisions concernant la préparation des sels de silazane, on pourra se reporter au même ouvrage ou se référer aux méthodes décrites dans Organomet. Chem. (1983), 461 (1-2), 75-80 ; Chem. Prum (1977), 27 (11), 566-8 ; Zh. Obstich. Khim (1988), 58 (8), 934- 5 ; Inorg. Synth. (1966), 8,19-22 ou Inorg. Chem. (1966) ; 8,15-19.
Lorsque le composé de formule (1) ou (2) est formé in situ, on part d'un précurseur dudit composé qui est libéré par un moyen connu en soi, pour former le composé actif correspondant.
Dans l'étape c), les autres composés réactifs avec la fonction isocyanate peuvent être des isocyanates ou des composés porteurs d'un atome d'hydrogène mobile, notamment les amines, alcools, imidazoles, pyrazoles, malonate, etc.... substitués ou non substitués.
<Desc/Clms Page number 8>
Ainsi, les composés 2-imino-4-oxo-1, 3-diazétines conduisent en présence d'HCI par réaction avec un composé isocyanate, notamment dans lequel la fonction isocyanate est portée par un atome de carbone appartenant à un cycle aromatique à des dérivés asymétriques à cycle 4, 6-dioxo-2-imino-hexahydro-1, 3,5-triazine de formule :
dans lequel R est tel que défini ci-dessus.
dans lequel R est tel que défini ci-dessus.
Les catalyseurs de l'invention sont appropriés à la polycondensation, notamment l'oligomérisation et en particulier la (cyclo) trimérisation des isocyanates aliphatiques linéaires, ramifiés, cycloaliphatiques ou aromatiques.
La présente invention vise l'oligomérisation, notamment la trimérisation de composés isocyanates en général et, de préférence, porteurs de deux fonctions isocyanates, désignés dans la présente description par isocyanates monomères.
Il peut s'agir de monomères isocyanates à squelette hydrocarboné exclusivement de nature aliphatique, linéaire, ramifiés ou cycliques ou d'isocyanates aromatiques.
On peut citer également les monomères aliphatiques dont le squelette hydrocarboné est ramifié mais dont les fonctions isocyanates sont portées par des atomes de carbone primaire, par exemple le 2-méthyl pentane diisocyanate.
<Desc/Clms Page number 9>
On peut encore citer les monomères dont au moins une fonction isocyanate est en position cycloaliphatique, secondaire, tertiaire ou néopentylique.
Ainsi, parmi ces produits, ceux qui donnent d'excellents résultats avec les catalyseurs de l'invention, à la différence des autres catalyseurs avec lesquels ils n'ont qu'un taux de transformation médiocre, sont les monomères dans lesquels la fonction isocyanate est portée par un atome de carbone cycloaliphatique, secondaire, tertiaire ou néopentylique, en particulier les isocyanates cycloaliphatiques. Ces monomères sont tels qu'au moins l'une avantageusement des deux fonctions isocyanates est distante du cycle le plus proche d'au plus un carbone et, de préférence, est reliée directement à lui. En outre, ces monomères cycloaliphatiques présentent avantageusement au moins une, de préférence deux fonctions isocyanates choisies parmi les fonctions isocyanates secondaire, tertiaire ou néopentylique.
De manière surprenante, on obtient de bons résultats pour des isocyanates dans lesquels la liberté conformationnelle du carbone portant la fonction NCO est faible. On peut citer à titre d'exemple les monomères suivants : - les composés correspondant à l'hydrogénation du ou des noyaux aromatiques porteurs des fonctions isocyanates de monomères d'isocyanates aromatiques et notamment du TDI (toluènediisocyanate) et des diisocyanato-biphényles, le composé connu sous le sigle H12MDI (4,4' bis- (isocyanato cyclohexyl) méthane), les divers BIC [Bis (isocyanato- méthylcyclohexane)] et les cyclohexyldiisocyanates éventuellement substitués ; et surtout - le norbornanediisocyanate, souvent désigné par son sigle NBDI ; - l'isophoronediisocyanate, ou IPDI, ou plus précisément 3-
isocyanatométhyl-3, 5, 5-triméthylcyclo-hexylisocyanate.
isocyanatométhyl-3, 5, 5-triméthylcyclo-hexylisocyanate.
Comme monomères aromatiques, on peut citer les :
<Desc/Clms Page number 10>
- 2, 4- ou 2, 6- toluène diisocyanate (TDI) ; - 2, 6-4, 4'-diphénylméthane diisocyanate (MDI) ; - 1, 5-naphtalène diisocyanate (NDI) ; - tolidine diisocyanate (TODI) ;
- p-phénylène diisocyanate (PPDI).
- p-phénylène diisocyanate (PPDI).
Les monomères de départ peuvent également être des produits d'oligomérisation d'isocyanates de plus faible masse moléculaire, ces produits d'oligomérisation étant porteurs de fonctions isocyanates.
Dans ce cas, il n'est pas nécessaire de séparer l'oligomère non transformé du produit réactionnel formé à l'issue de la réaction de trimérisation.
Le catalyseur est de préférence utilisé tel quel ou dissous dans un solvant inerte avant introduction dans le milieu réactionnel. Le solvant de formulation du catalyseur est de préférence inerte vis-à-vis des isocyanates du milieu réactionnel. Dans le cas où le solvant est réactif vis- à-vis des isocyanates, on ajuste la concentration du catalyseur de telle manière que la quantité de solvant ne soit pas préjudiciable à l'obtention du composé de l'application visée.
Le solvant est de préférence choisi de façon à ce que son point d'ébullition soit supérieur à la température de réaction. On peut citer les hydrocarbures aliphatiques tels que l'hexane ou aromatiques tels que le toluène.
On peut toutefois travailler sous pression avec des solvants ou des gaz à l'état supercritique.
La quantité de catalyseur varie en fonction de l'isocyanate de départ, la réactivité des isocyanates aromatiques étant supérieure à celle des isocyanates aliphatiques linéaires ou ramifiés, elle-même supérieure à celle des isocyanates cycloaliphatiques.
Le ratio molaire quantité catalyseur métallique/quantité
fonctions NCO est avantageusement d'au moins 10-3, et d'au plus 10-1, à 60 C.
fonctions NCO est avantageusement d'au moins 10-3, et d'au plus 10-1, à 60 C.
Lorsque les gaz dissous dans les isocyanates monomères de départ sont éliminés, la quantité de catalyseur peut être réduite.
<Desc/Clms Page number 11>
En outre, lorsque l'on élimine les gaz dissous dans les isocyanates monomères de départ, la réactivité des catalyseurs est améliorée.
Les gaz dissous (Co2, gaz halogénés, Os...) peuvent être éliminés par tout moyen connu, notamment par barbotage d'un gaz inerte tel que l'azote ou l'argon, ou par mise sous vide du milieu réactionnel.
On choisira donc la quantité de catalyseur en fonction de la cinétique de réaction et des propriétés physicochimiques (viscosité, etc) attendues, des quantités trop faibles ne permettant pas l'obtention de trimères en quantité notable mais donnant des produits de faible viscosité avec un taux de trimères vrais (un seul motif isocyanurate) élevé. A l'inverse, des quantités trop élevées risquent de créer un emballement de la réaction.
La température de réaction est d'au moins 20 C, avantageusement d'au moins 30 C.
Dès que la réaction démarre, elle est exothermique. Il est donc généralement préférable de contrôler la température du milieu réactionnel pour éviter un emballement de la réaction susceptible de conduire à une polymérisation non contrôlée de l'isocyanate.
Il est généralement préférable d'introduire le catalyseur dilué progressivement par exemple par coulée lente.
La réaction de cyclocondensation est stoppée au taux de transformation voulu, généralement entre 5% et 95 %, avantageusement entre 8 % et 60% des fonctions NCO, par addition d'un désactivateur du catalyseur ou par élimination de celui-ci par tout moyen connu de l'homme du métier, tel qu'absorption sur colonne, etc...
On peut, notamment, stopper la réaction par addition d'un composé acide ou un composé pouvant générer dans le milieu réactionnel un composé acide susceptible de neutraliser l'activité du catalyseur, notamment un sel d'acide.
Au cours de l'étude qui a mené à la présente invention, il a été montré qu'il était préférable d'ajouter un acide de force élevée,
<Desc/Clms Page number 12>
généralement ayant un pKa 3, tel que les acides sulfuriques ou sulfoniques, par exemple les acides mésylique, tosylique, ou halogénosulfoniques, ou un acide phosphorique, ou phosphoniques de pKa plus élevée, de préférence un ester d'acide phosphor.
Comme esters d'acides phosphors, on peut citer les esters de phosphate, notamment les monoesters, diesters ou leurs mélanges.
On peut citer les phosphonates, de préférence monoestérifiés, et les phosphinates.
On peut également citer les acides minéraux, de préférence halogénés, par exemple HF, HCI, HBr.
L'empoisonnement du catalyseur est toutefois de préférence réalisé au moyen d'esters acides de l'acide phosphorique, et notamment des esters phosphoriques de dialcoyle, en particulier le phosphate de
dibutyl et le phosphate de di-2-éthylhexyle.
dibutyl et le phosphate de di-2-éthylhexyle.
On peut aussi utiliser des composés précurseurs d'un composé acide tels que des acides de Lewis (AICI3, ZnCI2) ou des triflates métalliques.
Le produit réactionnel contient des produits de polycondensation, notamment de (cyclo) condensation des isocyanates de départ.
Il s'agit principalement, outre les produits isocyanates de départ, de composés à cycle 2-imino-4-oxo-1,3-diazétidine possédant un seul cycle de ce type.
Il peut s'agir également de composés oligomères ayant deux voire plus de deux cycles 2-imino-4-oxo-1,3-diazétidine.
Selon le taux de transformation, le mélange final comprend une quantité variable de composés lourds de plus haut poids moléculaire.
Les compositions polyisocyanates obtenues par le procédé de l'invention comprennent avantageusement : - de 50 à 75 %, avantageusement de 55 à 75 % en poids de composés mono-2-imino-4-oxo-1, 3-diazétidine ;
<Desc/Clms Page number 13>
- de 10 à 25 % en poids, avantageusement de 12 à 20 % en poids de composés bis- (2-imino-4-oxo-1, 3-diazétidine) ; - de 10 à 25 %, avantageusement de 14 à 20 % en poids d'isocyanates-urées ; et - moins de 1 % en poids d'isocyanates monomères, par rapport au poids total des composés isocyanates présents dan la composition.
Ainsi, pour un taux de transformation de 25 % des fonctions NCO initiales, la composition polyisocyanate selon l'invention comprend avantageusement au moins 50 %, de préférence au moins 60 % en poids de composés mono- (2-imino-4-oxo-1, 3-diazétidine).
Lorsque le taux de transformation augmente, la quantité de
mono- (2-imino-4-oxo-3-diazétidine) augmente mais également la quantité de produits lourds.
mono- (2-imino-4-oxo-3-diazétidine) augmente mais également la quantité de produits lourds.
Les compositions telles que définies ci-dessus représentent un autre objet de l'invention.
L'invention a également pour objet une composition polyisocyanate masquée comprenant : - de 50 à 75 %, avantageusement de 55 à 70 % en poids de composés mono-2-imino-4-oxo-1,3-diazétidine ; - de 10 à 25 % en poids, avantageusement de 12 à 20 % en
poids de composés bis- (2-imino-4-oxo-1, 3-diazétidine) ; - de 10 à 25 %, avantageusement de 14 à 20 % en poids d'isocyanates-urées ; et - moins de 1 % en poids d'isocyanates monomères par rapport au poids total des composés isocyanates présents dan la composition ; dans laquelle de 0,5 à 100 %, avantageusement de 10 à 100
%, de préférence de 20 à 100 % des fonctions isocyanates sont masquées à l'aide d'un agent masquant de la fonction isocyanate.
poids de composés bis- (2-imino-4-oxo-1, 3-diazétidine) ; - de 10 à 25 %, avantageusement de 14 à 20 % en poids d'isocyanates-urées ; et - moins de 1 % en poids d'isocyanates monomères par rapport au poids total des composés isocyanates présents dan la composition ; dans laquelle de 0,5 à 100 %, avantageusement de 10 à 100
%, de préférence de 20 à 100 % des fonctions isocyanates sont masquées à l'aide d'un agent masquant de la fonction isocyanate.
<Desc/Clms Page number 14>
L'agent masquant, qui peut être un mélange d'agents masquants, présente le plus souvent au moins un hydrogène mobile de manière que la réaction de masquage puisse s'écrire :
Is-N=C=O + AM-H-------------- > Is-NH-CO (AM) où AM-H représente l'agent masquant ;
où AM-représente le groupe masquant ; où Is est le reste porteur de la fonction isocyanate considérée, notamment d'une composition telle que définie ci-dessus.
Is-N=C=O + AM-H-------------- > Is-NH-CO (AM) où AM-H représente l'agent masquant ;
où AM-représente le groupe masquant ; où Is est le reste porteur de la fonction isocyanate considérée, notamment d'une composition telle que définie ci-dessus.
Ledit agent masquant présente au moins une fonction portant un hydrogène mobile, ou plus exactement réactif, fonction pour laquelle on peut définir un pKa lequel correspond, soit à l'ionisation d'un acide, y compris l'hydrogène des fonctions, phénols et alcools, soit à l'acide associé d'une base, en général azotée. Le pKa de la fonction présentant des hydrogènes est au moins égal à 4, avantageusement à 5, de préférence à 6 et est au plus égal à 14, avantageusement à 13, de préférence à 12, et de manière plus préférée à 10, une exception devant être faite pour les lactames dont le pKa est supérieur à ces valeurs et qui constituent des agents masquants néanmoins acceptables bien que non préférés pour l'invention.
Avantageusement, l'agent masquant ne comporte qu'un seul hydrogène mobile.
A titre d'exemples non limitatifs, des agents de masquage selon l'invention, on peut citer les dérivés de l'hydroxylamine tels que
l'hydroxysuccinimide et les oximes telles tel que la méthyl éthylcétoxime, les dérivés des phénols ou assimilés, les dérivés des amides tels les imides et les lactames, ainsi que les malonate ou cétoesters et les hydroxamates.
l'hydroxysuccinimide et les oximes telles tel que la méthyl éthylcétoxime, les dérivés des phénols ou assimilés, les dérivés des amides tels les imides et les lactames, ainsi que les malonate ou cétoesters et les hydroxamates.
On peut également citer les groupes hétérocycliques azotés comprenant 2 à 9 atomes de carbone et, outre l'atome d'azote, de 1 à 3 autres hétéroatomes choisis parmi l'azote, l'oxygène et le soufre. On préfère en particulier les hétérocycles comportant de 2 à 4 atomes de carbone et de 1 à 3 atomes d'azote, tels les groupes pyrolyle, 2H-
<Desc/Clms Page number 15>
pyrrolyl, imidazolyle, pyrimidinyle, pyridazinyle, pyrazinyle, pyrimidinyle, pyridazinyle, indolizinyle, iso-indolyle, indolyle, indolyle, indozolyle, purinyle, quinolizinyle, isoquinolyle, pyrazolidinyle, imidazolidinyle et triazolyl, ces groupes étant éventuellement substitués par un à trois substituants choisis parmi NH2, NH (alkyle en C1-C6), N- (dialkyle en C1-C6), OH, SH, CF3, alkyle en Ci-Ce, cycloalkyl en C3-C6, aryle en C5-C12, notamment phényle, aralkyl en C6-C18 ayant de 5 à 12 atomes de carbone dans le groupe aryle, notamment benzyle ou alkaryl en C6-C18 ayant de 5 à 12 atomes de carbone dans le groupe aryle.
Particulièrement préférés sont les groupes 1,2, 3-triazolyl ou 1,2, 4-triazolyl.
Pour la détermination des pKa, on pourra se reporter à"The determination of ionization constants, a laboratory manual, A. Albert of E. P. Serjeant ; Chapman and Hall Ltd, London".
Pour la liste des agents bloquants, on pourra se reporter à Z.
Wicks (Prog. Org. Chem., 1975,3, 73 et Prog. Org. Chem., 1989,9, 7) et Petersen (Justus Liebigs, Annalen der Chemie 562,205, (1949).
De préférence, l'isocyanate est l'IPDI.
Les compositions polyisocyanates masquées selon l'invention sont obtenues par réaction du produit de l'étape b) ou c) avec un agent masquant tel que défini ci-dessus dans les conditions habituelles.
Lorsque l'agent masquant est mis à réagir avec le produit de l'étape b), il est opportun de réaliser une étape c) d'élimination des isocyanates monomères masqués, le cas échéant à l'issue de l'étape de masquage proprement dite.
Le procédé selon l'invention présente l'avantage d'obtenir directement des composés 2-imino-4-oxo-1,3-diazétidine à partir d'isocyanates sans passage par un carbodiimide et au moyen d'un seul catalyseur.
<Desc/Clms Page number 16>
Les compositions obtenues par le procédé de l'invention présentent une fonctionnalité élevée en groupes NCO, tout en ayant une faible viscosité.
Les exemples suivants sont destinés à illustrer l'invention.
Sauf indications contraires, les pourcentages sont exprimés en poids.
Exemple
Dans un réacteur de 50 ml à double enveloppe muni d'un agitateur, d'un réfrigérant, d'un dispositif de chauffage et d'un bain Huber
pour la régulation de la température, on place sous agitation 20 g d'IPDI (0,09 mole, 0,18 moles NCO). On chauffe le milieu réactionnel à 60 C. On ajoute 1 g de bis (triméthyl silyl) amide d'étain (2,275. 10-3 mole) représentant une quantité de catalyseur de 5 % en poids par rapport à l'IPDI de départ.
Dans un réacteur de 50 ml à double enveloppe muni d'un agitateur, d'un réfrigérant, d'un dispositif de chauffage et d'un bain Huber
pour la régulation de la température, on place sous agitation 20 g d'IPDI (0,09 mole, 0,18 moles NCO). On chauffe le milieu réactionnel à 60 C. On ajoute 1 g de bis (triméthyl silyl) amide d'étain (2,275. 10-3 mole) représentant une quantité de catalyseur de 5 % en poids par rapport à l'IPDI de départ.
Après 5 heures de réaction à 60 C, on ajoute 300 mg de dibutyl phosphate. Il se produit un arrêt de la réaction.
Le taux de transformation de l'IPDI est de 26, 5 %.
Les résultats de l'essai sont récapitulés dans le tableau cidessous.
<tb>
<tb> Produit/Elément <SEP> Ex. <SEP> 1
<tb> IPDI <SEP> (%) <SEP> 74, <SEP> 5 <SEP> %
<tb> Trimethylsilyl <SEP> urée <SEP> d'IPDI <SEP> 4,7 <SEP> % <SEP> *
<tb> IUT** <SEP> 16, <SEP> 3%
<tb> Bis-IUT <SEP> 4, <SEP> 3%
<tb>
% en poids par rapport au poids d'isocyanate * présence de fonctions carbodiimide ** IUT : 2-imino-4-oxo-1, 3-diazétidine
<tb> Produit/Elément <SEP> Ex. <SEP> 1
<tb> IPDI <SEP> (%) <SEP> 74, <SEP> 5 <SEP> %
<tb> Trimethylsilyl <SEP> urée <SEP> d'IPDI <SEP> 4,7 <SEP> % <SEP> *
<tb> IUT** <SEP> 16, <SEP> 3%
<tb> Bis-IUT <SEP> 4, <SEP> 3%
<tb>
% en poids par rapport au poids d'isocyanate * présence de fonctions carbodiimide ** IUT : 2-imino-4-oxo-1, 3-diazétidine
Claims (15)
1. Procédé de (cyclo) condensation, catalytique d'isocyanates monomères caractérisé en ce qu'il comprend : a) la réaction des isocyanates monomères de départ avec un catalyseur comprenant un sel d'étain (II) d'un composé de formule (1),
dans laquelle les symboles : - R1, R2, R3, R4, R5 et R6 identiques ou différents représentent un groupe monovalent de nature hydrocarbonée ayant de 1 à 30 atomes de carbone, aliphatique, cycloaliphatique saturé ou insaturé, aryle, aralkyle ou alkylaryle, éventuellement substitué par des atomes d'halogène, des groupements CN, ou ester, et/ou éventuellement interrompu par un ou plusieurs atomes choisis parmi 0, S, N et Si, ou - !'um de Ri, R2, R3, R4, R5 et R6 représente un motif de formule (2) :
A étant un groupe alkylène ayant de 1 à 30, avantageusement 2 à 20 atomes de carbone éventuellement substitué par des atomes d'halogène, des groupements CN, ou ester, et/ou
<Desc/Clms Page number 18>
à une température d'au moins 20 C et avantageusement d'au moins 40 C et d'au plus 1 OOOC, avantageusement d'au plus 80OC, b) l'arrêt de la réaction de (cyclo) condensation au taux de transformation souhaité compris entre 5 et 95 %, avantageusement entre 10 et 50 % ; et c) l'élimination éventuelle des monomères n'ayant pas réagi ou la réaction avec d'autres composés réactifs avec la fonction isocyanate.
- deux parmi R1, R2 et R3 d'une part et/ou R4, Rs et R6 d'autre part, constituent ensemble un groupe hydrocarboné divalent en Cm-so éventuellement substitué par des atomes d'halogène, des groupements CN, ou ester, et/ou éventuellement interrompu par un ou plusieurs atomes choisis parmi 0, S, N et Si, et/ou - au moins un groupe choisi parmi R1, R2 et R3 forme avec au moins un groupe parmi R4, R5 et R6 un groupe hydrocarboné divalent en C1-C30 éventuellement substitué par des atomes d'halogène, des groupements CN, ou ester, et/ou éventuellement interrompu par un ou plusieurs atomes choisis parmi 0, S, N et Si, ou un précurseur dudit composé,
éventuellement interrompu par un ou plusieurs atomes choisis parmi 0, S, N et Si, A étant de préférence (CH2) n' avec n'compris entre 1 et 6, et R'1 à R'5 identiques ou différents représentant un groupe monovalent de nature hydrocarbonée en C1-C30, aliphatique, cycloaliphatique saturé ou insaturé, aryle, aralkyl ou alkylaryl, éventuellement substitué par des atomes d'halogène, des groupements CN, ou ester éventuellement interrompu par un ou plusieurs atomes choisis parmi 0, S, N et Si, et n est un nombre entier entre 1 et 50, ou
2. Procédé selon la revendication 1, caractérisé en ce que Ri à R6 et R'1 à R'5 identiques ou différents représentent :
<Desc/Clms Page number 19>
un groupe alkyle, alkényle, halogénoalkyle ou halogénoalkényle ayant de 1 à 20 atomes de carbone et comportant un ou plusieurs atomes de chlore et/ou de fluor, - un groupe cycloalkyl, cycloalkényle, halogénocycloalkyle ou halogénocycloalkényle ayant de 3 à 30 atomes de carbone et contenant un ou plusieurs atomes de chlore et/ou de fluor, - un groupe aryle, alkylaryle ou halogénoaryle ayant de 6 à 30 atomes de carbone et contenant un ou plusieurs atomes de chlore et/ou de fluor, - un groupe cyanoalkyl ayant de 1 à 30, de préférence 1 à 6 atomes de carbone, ou deux groupes parmi R1, R2 et R3 ou R3, R4 et R5 forment ensemble un radical divalent comprenant de 2 à 5 atomes de carbone, et/ou - au moins un groupe choisi parmi R, R2 et R3 forme avec au moins un groupe parmi R4, R5 et R6 un groupe hydrocarboné divalent, comprenant de 2 à 5 atomes de carbone.
3. Procédé selon l'une quelconque des revendications précédentes, caractérisé en ce que R1 à R6 identiques ou différents sont choisis parmi les groupes : méthyle, éthyle, propyl, isopropyl, butyle, Isobutyl, α-Dpentyle, t-butyle, chlorométhyle, dichlorométhyle, α-chloro-éthyle,
<Desc/Clms Page number 20>
tétrachlorophényle, o-, p-, ou m-tolyle, a, a, a-trifluorotolyle ; et xylyles ou deux groupes parm ! Ri, ? 2 et R3 ou R4, R5 et R6 représentent un groupe diméthylène, triméthylène, tétraméthylène ou pentaméthylène et/ou R1 et R4 pris ensemble représentent un groupe choisi parmi éthylène, propylène, butylène, pentylène, de préférence les isomères non ramifiés, de méthylène et triméthylène.
a, ss--dichloroéthyle, fluorométhyle, difluorométhyle, a, ss-difluoroéthyle, trifluoro-3, 3,3 propyle, trifluoro cyclopropyle, trifluoro-4, 4,4 butyle, heptafluoro-3, 3,3, 4,4, 5,5 pentyle, ss-cyanoéthyle, y-cyanopropyle, phényle, p-chlorophényle, m-chlorophényle, dichloro-3, 5 phényle, trichlorophényle,
4. Procédé selon la revendication 3 caractérisé en ce que Ri à R6 et R'1 R'5 identiques ou différents sont choisis parmi méthyle, éthyle, propyle vinyle et phényle, ces groupes étant éventuellement chlorés et/ou fluorés.
<Desc/Clms Page number 21>
5. Procédé selon l'une quelconque des revendications précédentes, caractérisé en ce que le composé de formule (1) est choisi parmi les sels des composés suivants : hexaméthyldisilazane, diéthyl 1-3, tétraméthyl-1, 1,3, 3 disilazane, divinyl-1, 3 tétraméthyl-1, 1,3, 3 disilazane, hexaéthyldisilazane, et diphényl-1, 3 tétraméthyl-1, 1,3, 3 disilazane.
6. Procédé selon l'une quelconque des revendications précédentes, caractérisé en ce que l'isocyanate de départ est un diisocyanate dans lequel au moins une, avantageusement les deux fonctions isocyanates sont portées par un atome de carbone en position cycloaliphatique, secondaire, tertiaire ou néopentylique.
7. Procédé selon l'une des revendications 1 à 6, caractérisé en ce que ledit isocyanate est un isocyanate cycloaliphatique dans lequel au moins une, avantageusement les deux fonctions isocyanates est distante du cycle le plus proche d'au plus un atome de carbone, de préférence reliée directement à lui.
8. Procédé selon la revendication 7, caractérisé en ce que l'isocyanate est l'IPDI.
10. Composition polyisocyanate susceptible d'être obtenue selon le procédé tel que défini aux revendications1 à 9.
<Desc/Clms Page number 22>
11. Composition polyisocyanate selon la revendication 10, caractérisée en ce qu'elle comprend : - de 50 à 75 %, avantageusement de 55 à 75 % en poids de composés mono-2-imino-4-oxo-1, 3-diazétidine ; - de 10 à 25 % en poids, avantageusement de 12 à 20 % en
poids de composés bis- (2-imino-4-oxo-1, 3-diazétidine) ; - de 10 à 25 %, avantageusement de 14 à 20 % en poids d'isocyanates-urées ; et - moins de 1 % en poids d'isocyanates monomères, par rapport au poids total des composés isocyanates présents dan la composition.
12. Composition polyisocyanate masquée obtenue par le procédé de la revendication 1, dans lequel une étape de masquage avec un agent masquant de la fonction isocyanate est réalisée à l'issue de l'étape b) ou de l'étape c).
13. Composition polyisocyanate masquée selon la revendication 12, caractérisé en ce qu'elle comprend : - de 50 à 75 %, avantageusement de 55 à 70 % en poids de composés mono-2-imino-4-oxo-1, 3-diazétidine ; - de 10 à 25 % en poids, avantageusement de 12 à 20 % en
poids de composés bis- (2-imino-4-oxo-1, 3-diazétidine) ; - de 10 à 25 %, avantageusement de 14 à 20 % en poids d'isocyanates-urées ; et - moins de 1 % en poids d'isocyanates monomères par rapport au poids total des composés isocyanates présents dan la composition ; dans laquelle de 0,5 à 100 %, avantageusement de 10 à 100
%, de préférence de 20 à 100 % des fonctions isocyanates sont masquées à l'aide d'un agent masquant de la fonction isocyanate.
<Desc/Clms Page number 23>
14. Composition polyisocyanate masquée selon la revendication 11 ou la revendication 13, dans laquelle l'isocyanate monomère est l'isophorone diisocyanate.
15. Composition polyisocyanate masquée selon la revendication 13 ou la revendication 14, dans laquelle l'agent masquant est choisi parmi les oximes et les composés hétérocycliques azotés ayant de 2 à 9 atomes de carbone.
Priority Applications (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0017315A FR2818973B1 (fr) | 2000-12-29 | 2000-12-29 | Nouveau procede de (cyclo) condensation d'isocyanates au moyen d'un sel de silazane d'etain |
| PCT/FR2001/004228 WO2002053614A1 (fr) | 2000-12-29 | 2001-12-28 | Catalyseur de condensation pour isocyanate, composition en contenant, procede d'utilisation, et compositions obtenues |
| US10/450,261 US6946538B2 (en) | 2000-12-29 | 2001-12-28 | Catalyst for isocyanate condensation, composition containing same, method for use, and resulting compositions |
| BR0116559-3A BR0116559A (pt) | 2000-12-29 | 2001-12-28 | Catalisador de condensação para isocianato, composição compreendendo o mesmo, processo de utilização, e composições obtidas |
| DE60141771T DE60141771D1 (de) | 2000-12-29 | 2001-12-28 | Katalysator zur isocyanatkondensation, zusammensetzung, die diesen enthält, verfahren zur verwendung und erhaltene zusammensetzungen |
| AT01989673T ATE463522T1 (de) | 2000-12-29 | 2001-12-28 | Katalysator zur isocyanatkondensation, zusammensetzung, die diesen enthält, verfahren zur verwendung und erhaltene zusammensetzungen |
| EP01989673A EP1358238B1 (fr) | 2000-12-29 | 2001-12-28 | Catalyseur de condensation pour isocyanate, composition en contenant, procede d'utilisation, et compositions obtenues |
| CA002432960A CA2432960A1 (fr) | 2000-12-29 | 2001-12-28 | Catalyseur de condensation pour isocyanate, composition en contenant, procede d'utilisation, et compositions obtenues |
| CNB018215599A CN1215100C (zh) | 2000-12-29 | 2001-12-28 | 异氰酸酯的缩合催化剂,包括该催化剂的组合物,使用方法,和所得组合物 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| FR0017315A FR2818973B1 (fr) | 2000-12-29 | 2000-12-29 | Nouveau procede de (cyclo) condensation d'isocyanates au moyen d'un sel de silazane d'etain |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| FR2818973A1 true FR2818973A1 (fr) | 2002-07-05 |
| FR2818973B1 FR2818973B1 (fr) | 2003-10-24 |
Family
ID=8858417
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| FR0017315A Expired - Fee Related FR2818973B1 (fr) | 2000-12-29 | 2000-12-29 | Nouveau procede de (cyclo) condensation d'isocyanates au moyen d'un sel de silazane d'etain |
Country Status (1)
| Country | Link |
|---|---|
| FR (1) | FR2818973B1 (fr) |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4003859A (en) * | 1974-01-30 | 1977-01-18 | The Upjohn Company | Novel process for trimerizing polyisocyanates |
| US4412874A (en) * | 1981-11-19 | 1983-11-01 | The United States Of America As Represented By The Secretary Of The Army | Silane ballistic modifier containing propellant |
| US4675401A (en) * | 1984-10-30 | 1987-06-23 | Rhone-Poulenc Specialites Chimiques | Process for preparing polyisocyanato/polyisocyanurates by catalytic cyclotrimerization of polyisocyanates |
-
2000
- 2000-12-29 FR FR0017315A patent/FR2818973B1/fr not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4003859A (en) * | 1974-01-30 | 1977-01-18 | The Upjohn Company | Novel process for trimerizing polyisocyanates |
| US4412874A (en) * | 1981-11-19 | 1983-11-01 | The United States Of America As Represented By The Secretary Of The Army | Silane ballistic modifier containing propellant |
| US4675401A (en) * | 1984-10-30 | 1987-06-23 | Rhone-Poulenc Specialites Chimiques | Process for preparing polyisocyanato/polyisocyanurates by catalytic cyclotrimerization of polyisocyanates |
Also Published As
| Publication number | Publication date |
|---|---|
| FR2818973B1 (fr) | 2003-10-24 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP3995300B2 (ja) | イミノオキサジアジンジオン基を含むイソシアネート三量体、その製造及び使用 | |
| JP4490813B2 (ja) | ウレトジオン基を含むイソシアネート | |
| JPH0211554A (ja) | イソシアヌレート基含有ポリイソシアネートの製造方法およびそれらの使用 | |
| JP4029047B2 (ja) | ウレトジオン、イソシアヌレートおよびイミノオキサジアジンジオン構造を有する脂肪族ポリイソシアネートの製造方法 | |
| JPH0324471B2 (fr) | ||
| EP1129120B1 (fr) | Polyisocyanates modifies | |
| JP3729857B2 (ja) | ビウレット基含有ポリイソシアネートの製法 | |
| EP1833785B1 (fr) | Compositions isocyanates presentant de bonnes proprietes de melange et utilisation de derives silyles comme adjuvants de compositions isocyanates, notamment de melange | |
| JPH04482B2 (fr) | ||
| TWI423995B (zh) | A reaction catalyst for forming a isocyanurate link, and a method for producing the modified polyisocyanate mixture containing the isocyanurate link thereof | |
| JP2004534871A5 (fr) | ||
| FR2818974A1 (fr) | (cyclo) condensation de composes isocyanates | |
| FR2818973A1 (fr) | Nouveau procede de (cyclo) condensation d'isocyanates au moyen d'un sel de silazane d'etain | |
| JP4498749B2 (ja) | 高い官能価を有する低粘度ポリイソシアネート組成物及びその製造方法 | |
| FR2818976A1 (fr) | Procede de (cyclo) condensation au moyen d'un sel de silazane d'erbium | |
| EP1358238B1 (fr) | Catalyseur de condensation pour isocyanate, composition en contenant, procede d'utilisation, et compositions obtenues | |
| FR2864537A1 (fr) | Synthese de biurets et d'isocyanates a fonctions alcoxysilanes, formulations en contenant et leurs applications | |
| EP0203874A1 (fr) | Procédé de stabilisation de solutions organiques de polyisocyanates | |
| FR2818975A1 (fr) | Nouveau procede de (cyclo) condensation, notamment de (cyclo) trimerisation catalytique d'isocyanates | |
| EP1352006B1 (fr) | Procede de dimerisation catalytique d'isocyanates | |
| JPS6321659B2 (fr) | ||
| WO2002012366A1 (fr) | Composition polyisocyanate | |
| EP4067403A1 (fr) | Agent de blocage pour groupe isocyanate, et isocyanate protégé par ledit agent de blocage | |
| JP2012504562A (ja) | 1,4,2−ジアザホスホリジン誘導体 | |
| FR2833864A1 (fr) | Catalyseur de condensation pour isocyanate, composition en contenant, procede d'utilisation, et compositions obtenues |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ST | Notification of lapse |