ES2899665T3 - Derivados de 2-(3-(1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol y compuestos relacionados como inhibidores de PRS para el tratamiento, p. ej., del cáncer - Google Patents
Derivados de 2-(3-(1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol y compuestos relacionados como inhibidores de PRS para el tratamiento, p. ej., del cáncer Download PDFInfo
- Publication number
- ES2899665T3 ES2899665T3 ES18750794T ES18750794T ES2899665T3 ES 2899665 T3 ES2899665 T3 ES 2899665T3 ES 18750794 T ES18750794 T ES 18750794T ES 18750794 T ES18750794 T ES 18750794T ES 2899665 T3 ES2899665 T3 ES 2899665T3
- Authority
- ES
- Spain
- Prior art keywords
- benzo
- propyl
- piperidin
- imidazol
- chloro
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4184—1,3-Diazoles condensed with carbocyclic rings, e.g. benzimidazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/454—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. pimozide, domperidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/06—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a carbon chain containing only aliphatic carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/14—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D473/00—Heterocyclic compounds containing purine ring systems
- C07D473/02—Heterocyclic compounds containing purine ring systems with oxygen, sulphur, or nitrogen atoms directly attached in positions 2 and 6
- C07D473/04—Heterocyclic compounds containing purine ring systems with oxygen, sulphur, or nitrogen atoms directly attached in positions 2 and 6 two oxygen atoms
- C07D473/06—Heterocyclic compounds containing purine ring systems with oxygen, sulphur, or nitrogen atoms directly attached in positions 2 and 6 two oxygen atoms with radicals containing only hydrogen and carbon atoms, attached in position 1 or 3
- C07D473/12—Heterocyclic compounds containing purine ring systems with oxygen, sulphur, or nitrogen atoms directly attached in positions 2 and 6 two oxygen atoms with radicals containing only hydrogen and carbon atoms, attached in position 1 or 3 with methyl radicals in positions 1, 3, and 7, e.g. caffeine
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Abstract
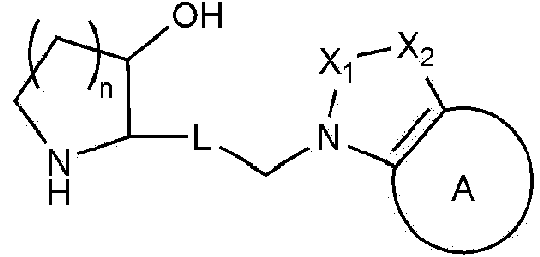
Un compuesto representado por la siguiente Fórmula Química 1, o una de sus sales farmacéuticamente aceptables: [Fórmula Química 1] **(Ver fórmula)** en la Fórmula Química 1, n es 1 o 2, L es -CH2CH2-, -CH=C(R')- o -C≡C-, en donde R' es hidrógeno, alquilo C1-4 o halógeno, X1 es CR1R2, NR1 o -CO-, X2 es CR3R4 o NR3, en donde cada uno de R1 a R4 son independientemente hidrógeno, alquilo C1-4, hidroxialquilo C1-4, hidroxi, amino, carboxi, -COO(alquilo C1-4), -CONH2, -CONH(alquilo C1-4), -CON (alquilo C1-4)2, o pirazolilo no sustituido o sustituido con haloalquilo C1-4; o R1 y R3, uno junto con el otro, conectan X1 y X2 a través de un doble enlace, y A es un anillo de benceno, piridina, pirimidina o pirimidinodiona, en donde A no está sustituido o está sustituido con de uno a tres sustituyentes seleccionados cada uno independientemente del grupo que consiste en un sustituyente de tipo anular seleccionado del grupo que consiste en furanilo, imidazolilo, isoxazolilo, fenilo, pirazolilo, piridinonilo, piridinilo, pirrolilo, tiazolilo y tiofenilo; alquilo C1-4; alcoxi C1-4; haloalquilo C1-4; haloalcoxi C1-4; halógeno; di(alquil C1-4)amino; nitro; -COO(alquilo C1- 4); dihidropiranilo; morfolino; piperidinilo; y pirrolidinilo; y en donde el sustituyente de tipo anular no está sustituido o está sustituido con uno o dos sustituyentes seleccionados cada uno independientemente del grupo que consiste en alquilo C1-5, haloalquilo C1-4, cicloalquilo C3-6, monovalente de carbonato de alquileno C2-5, -COO(alquilo C1-4), halógeno, ciano, tiazolilo y (1,3-dioxolan-2-il)metilo.
Description
DESCRIPCIÓN
Derivados de 2-(3-(1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol y compuestos relacionados como inhibidores de PRS para el tratamiento, p. ej., del cáncer
CAMPO TÉCNICO
La presente invención se refiere a un compuesto heterocíclico que tiene una nueva estructura que se puede usar para la prevención o el tratamiento de enfermedades provocadas por una anormalidad en una actividad de PRS (prolil-ARNt sintetasa), a un método para preparar el mismo y a una composición farmacéutica que comprende el mismo.
ANTECEDENTES DE LA TÉCNICA
LA PRS (prolil-ARNt sintetasa) es una de la familia de aminoacil-ARNt sintetasas (ARS) y sirve para activar un aminoácido para la síntesis de proteínas. Esto es, la ARS realiza una función de traducción para formar adenilato de aminoacilo (Aa -AMP) y a continuación transferir el aminoácido activado al extremo 3 del ARNt correspondiente. Puesto que la ARS representa un papel importante en la síntesis de proteína, los inhibidores de ARS suprimen el crecimiento de todas las células. Así, la ARS se ha identificado como una diana prometedora para un agente terapéutico para tratar enfermedades que deberían suprimir antibióticos o sobreexpresión celular (Nature, 2013, 494:121-125).
La PRS está presente en, o funciona como, un complejo de multisintetasa (MSC) en la forma de EPRS (glutamil-prolil-ARNt sintetasa). En particular, entre diversos MSCs, la EPRS funciona como un silenciador de la traducción que suprime la producción de VEGF A (factor de crecimiento endotelial vascular A) que es un factor clave en la angiogénesis. Además, se presenta que la EPRS está estrechamente relacionada con diversos tumores sólidos (Nat. Rev. Cancer, 2011,11,708-718).
La única sustancia conocida como el inhibidor de PRS es la halofuginona. La halofuginona es un derivado de febrifugina derivado de productos naturales y tiene efectos antimaláricos y diversos efectos antinflamatorios. También se puede usar como un aditivo para piensos. Además, se ha presentado que la halofuginona incrementa la fosforilación de GCN2 cinasa a través de la inhibición de PRS, lo que induce la expresión de ATF4 y CHOP, y así promueve la muerte celular (Nat. Chem. Biol. 2012, 8, 311-317). Actualmente, la halofuginona se está estudiando clínicamente como agente anticanceroso, un agente antinflamatorio (J Immunol, 2014, 192(5), 2167-76), agentes terapéuticos para el tratamiento de enfermedades autoinmunitarias (Arthritis Rheumatol, 2014,66 (5), 1195-207), agentes terapéuticos para el tratamiento de enfermedades fibróticas (World J Gastroenterol, 2014,20 (40), 14778-14786), y similares (Bioorg. Med. Chem. 2014, 22, 1993-2004).
Sin embargo, se ha presentado que la halofuginona actúa sobre diversas dianas y tiene una toxicidad muy intensa y además existe un riesgo de genotoxicidad (The EFSA Journal, 2003, 8: 1-45). Por lo tanto, el descubrimiento de inhibidores de PRS que tengan una seguridad superior para el cuerpo humano entre sustancias capaces de inhibir PRS como halofuginona tiene una significación en cuanto al desarrollo de un agente anticanceroso de la siguiente generación que se pueda usar como un agente antifibrótico, un agente antinflamatorio, un agente terapéutico autoinmunitario solo o en combinación con un agente anticanceroso elegido existente.
De WO2016/200116A1, se conocen inhibidores de PRS, que son compuestos representados por la siguiente fórmula
En la que
A es un benceno o un anillo de piridina,
X es CO o CHOH
R1 es hidrógeno o hidroxialquilo C1-14 y
R2 es fenilo, pirazolilo, piridin-2-onilo, pirrolidinilo o tiazolilo no sustituido o sustituido.
El documento EP3159335A2 (equivalente al documento WO2015/199418A1) divulga compuestos para ser usados en las mismas aplicaciones que los compuestos anteriores, estando representados dichos compuestos por la siguiente fórmula
en la que
n es 1 o 2,
R1 es hidrógeno o hidroxi,
R1 ' es hidrógeno,
R2 es hidroxi, halógeno, amino, (alquil C1-4)-amino, di(alquil C1-4)amino o alcoxi C1-4;
R3 es hidrógeno, halógeno, alquilo C1-4 o haloalquilo C1-4; o R2 y R3 forman juntos un oxo (=O), hidroxiimino (=N-OH) o (alcoxi C1-4)-imino (=N-O-(alquilo C1-4));
Y es
en donde Y1 es N, CH o CR4, siendo R4 alquilo C1-4, hidroxialquilo C1-4, alquilo C1-4 sustituido con alcoxi C1-4, haloalquilo C1-4 o -(CH2)mNR9R10, en donde m es un número entero de 1 a 4, y R9 y R10 son cada uno independientemente hidrógeno o alquilo C1-4,
Y2 es N o CH,
A es benceno, heteroarilo que tiene de 1 a 4 átomos de nitrógeno, o ciclohexeno, como un anillo de seis miembros,
k es un número entero de 0 a 4, y
cada Ra es independientemente alquilo C1-4, alcoxi C1-4, haloalquilo C1-4, haloalcoxi C1-4, halógeno, ciano o carboxi.
A este respecto, los presentes inventores han efectuado numerosos estudios para desarrollar un nuevo compuesto con toxicidad reducida mientras que tenga un efecto inhibidor de la enzima PRS, y han encontrado que el compuesto que tiene una nueva estructura que se describirá más tarde inhibe selectivamente la PRS, completando de ese modo la presente invención. Los compuestos pertenecientes a la presente invención, por sí mismos, tienen principalmente una actividad inhibidora de la enzima PRS, pero no excluyen una posibilidad de exhibir una acción farmacológica como un agente eficaz por un ambiente corporal especial o por productos del proceso metabólico, después de la absorción en el cuerpo.
DESCRIPCIÓN DETALLADA DE LA INVENCIÓN
PROBLEMA TÉCNICO
Un objetivo de la presente invención es proporcionar un compuesto heterocíclico que tenga una nueva estructura que se pueda usar para la prevención o el tratamiento de cánceres, enfermedades inflamatorias, enfermedades autoinmunitarias o fibrosis, un método para preparar el mismo y una composición farmacéutica que comprenda el mismo.
SOLUCIÓN TÉCNICA
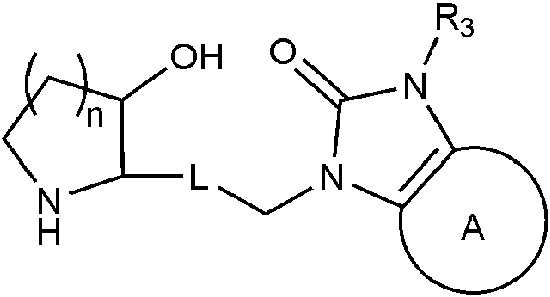
A fin de alcanzar el objetivo anterior, la presente invención proporciona un compuesto representado por la siguiente Fórmula Química 1, o una de sus sales farmacéuticamente aceptables:
[Fórmula Química 1]
en la Fórmula Química 1,
n es 1 o 2,
L es -CH2CH2-, -CH=C(R')- o -C=C-,
en donde R' es hidrógeno, alquilo C1-4 o halógeno,
X1 es CR1 R2 , NR1 o -CO-,
X2 es CR3R4 o NR3,
en donde cada uno de R1 a R4 son independientemente hidrógeno, alquilo C1-4, hidroxialquilo C1-4, hidroxi, amino, carboxi, -COO(alquilo C1-4), -CONH2, -CONH(alquilo C1-4), -CON (alquilo C1-4)2, o pirazolilo no sustituido o sustituido con haloalquilo C1-4; o R1 y R3 , uno junto con el otro, conectan X1 y X2 a través de un doble enlace, y
A es un anillo de benceno, piridina, pirimidina o pirimidinodiona,
en donde A no está sustituido o está sustituido con de uno a tres sustituyentes seleccionados cada uno independientemente del grupo que consiste en un sustituyente de tipo anular seleccionado del grupo que consiste en furanilo, imidazolilo, isoxazolilo, fenilo, pirazolilo, piridinonilo, piridinilo, pirrolilo, tiazolilo y tiofenilo; alquilo C1-4; alcoxi C1-4; haloalquilo C1-4; haloalcoxi C1-4; halógeno; di(alquil C1-4)amino; nitro; -COO(alquilo C1-4); dihidropiranilo; morfolino; piperidinilo; y pirrolidinilo; y
en donde el sustituyente de tipo anular no está sustituido o está sustituido con uno o dos sustituyentes seleccionados cada uno independientemente del grupo que consiste en alquilo C1-5, haloalquilo C1-4, cicloalquilo C3-6, monovalente de carbonato de alquileno C2-5, -COO(alquilo C1-4), halógeno, ciano, tiazolilo y (1,3-dioxolan-2-il)metilo.
Preferiblemente, cuando el sustituyente de tipo anular es furanilo, no está sustituido o está sustituido con -COO(alquilo C1-4). Cuando el sustituyente de tipo anular es imidazolilo, no está sustituido o está sustituido con alquilo C1-5. Cuando el sustituyente de tipo anular es isoxazolilo, no está sustituido o está sustituido con dos alquilos C1-5. Cuando el sustituyente de tipo anular es fenilo, no está sustituido o está sustituido con halógeno o haloalquilo C1-4. Cuando el sustituyente de tipo anular es pirazolilo, no está sustituido o está sustituido con alquilo C1-5, haloalquilo C1-4, monovalente de carbonato de alquileno C2-5, tiazolilo y (1,3-dioxolan-2-il)metilo. Cuando el sustituyente de tipo anular es piridinonilo, no está sustituido o está sustituido con alquilo C1-5. Cuando el sustituyente de tipo anular es piridinilo, no está sustituido o está sustituido con halógeno. Cuando el sustituyente de tipo anular es pirrolilo, no está sustituido o está sustituido con alquilo C1-5 y -COO(alquilo C1-4). Cuando el sustituyente de tipo anular es tiazolilo, no está
sustituido o está sustituido con alquilo C1-5, cicloalquilo C3-6, ciano o monovalente de carbonato de alquileno C2-5. Cuando el sustituyente de tipo anular es tiofenilo, no está sustituido o está sustituido con uno o dos sustituyentes seleccionados cada uno independientemente del grupo que consiste en alquilo C1-5 y -COO(alquilo C1-4).
Preferiblemente, A no está sustituido o está sustituido con de uno a tres sustituyentes seleccionados cada uno independientemente del grupo que consiste en alquilo C 1-4; alcoxi C1-4; haloalquilo C1-4; halógeno; fenilo no sustituido o sustituido con halógeno o haloalquilo C 1-4; pirazolilo no sustituido o sustituido con alquilo C1-5, tiazolilo o haloalquilo C1-4; tiofenilo no sustituido o sustituido con alquilo C1-5 o -COO(alquilo C1-4); pirrolilo no sustituido o sustituido con alquilo C1-5 y/o -COO(alquilo C1-4); di(alquil C1-4)amino; morfolino; piperidinilo; furanilo; y pirrolidinilo.
Preferiblemente, L es -CH2CH2-, -CH=CH-, -CH=CF-, -CH=C(CH3)- o -C=C-.
Preferiblemente, según X1 y X2 , el compuesto representado por la Fórmula Química 1 se representa mediante las siguientes Fórmulas Químicas 1-1 a 1-5:
[Fórmula Química 1-1]
[Fórmula Química 1-2]
[Fórmula Química 1-3]
[Fórmula Química 1 -4]
[Fórmula Química 1-5]
en las Fórmulas Químicas 1-1 a 1-5,
n, L, R1 a R4 y A son como se definen previamente.
Preferiblemente, cada uno de Ri a R4 son independientemente hidrógeno, metilo, hidroximetilo, hidroxi, amino, carboxi, -COOCH3 , -CONH2 , -CONHCH3 o -CON(CH3)2 ; o R1 y R3 , uno junto con el otro, conectan X1 y X2 a través de un doble enlace.
Preferiblemente, A es un anillo de benceno, piridina, pirimidina o pirimidinodiona, en donde A no está sustituido o está sustituido con de uno a tres sustituyentes seleccionados cada uno independientemente del grupo que consiste en metilo, isobutilo, metoxi, trifluorometilo, fluoro, cloro, bromo, fenilo, fenilo sustituido con fluoro, fenilo sustituido con cloro, fenilo sustituido con trifluorometilo, tiofenilo, tiofenilo sustituido con metilo, tiofenilo sustituido con -COOCH3, pirazolilo sustituido con difluorometilo, pirazolilo sustituido con metilo, pirazolilo sustituido con tiazolilo, pirrolilo sustituido con metilo y -COOCH2CH3, furanilo, dimetilamino, dietilamino, metiletilamino, morfolino, piperidinilo y pirrolidinilo.
Preferiblemente, A es benceno, en donde A no está sustituido o está sustituido con de uno a tres sustituyentes seleccionados cada uno independientemente del grupo que consiste en alquilo C1-4; alcoxi C1-4; halógeno; y fenilo no sustituido o sustituido con halógeno o haloalquilo C1-4.
Preferiblemente, A es piridina, en donde A no está sustituido o está sustituido con uno o dos sustituyentes seleccionados cada uno independientemente del grupo que consiste en alquilo C1-4; haloalquilo C1-4; halógeno; y fenilo sustituido con halógeno.
Preferiblemente, A es pirimidina, en donde A está sustituido con un sustituyente seleccionado del grupo que consiste en halógeno; di(alquil C1-4)amino; morfolino; piperidinilo; y pirrolidinilo.
Preferiblemente, A es pirimidinodiona, en donde A no está sustituido o está sustituido con uno o dos alquilo C1-4. Ejemplos típicos de los compuestos representados por la Fórmula Química 1 son como sigue:
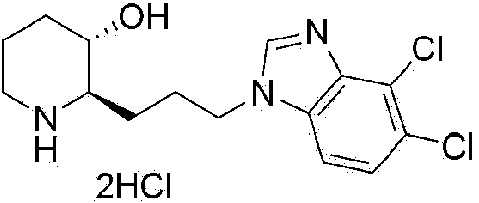
1) (2R,3S)-2-(3-(6-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
2) (2R,3S)-2-(3-(4-bromo-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
3) (2R,3S)-2-(3-(5-bromo-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
4) (2R,3S)-2-(3-(6-bromo-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
5) (2R,3S)-2-(3-(7-bromo-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
6) (2R,3S)-2-(3-(4-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
7) (2R,3S)-2-(3-(5-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
8) (2R,3S)-2-(3-(6-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
9) (2R,3S)-2-(3-(7-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
10) (2R,3S)-2-(3-(4-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
11) (2R,3S)-2-(3-(5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
12) (2R,3S)-2-(3-(7-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
13) (2R,3S)-2-(3-(6-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
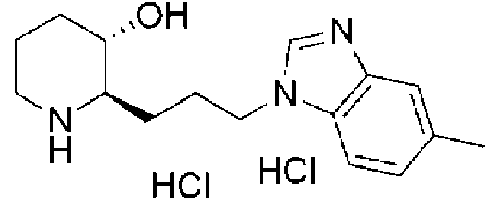
14) (2R,3S)-2-(3-(5-metil-1 H-benzo[d]imidazol-1-il)propil)piperidin-3-ol,
15) (2R,3S)-2-(3-(6-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
16) (2R,3S)-2-(3-(7-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
17) (2R,3S)-2-(3-(7-(trifluorometoxi)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(4-(pirrolidin-1 -il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(4-(piperidin-1 -il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(4-(3-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(4-(3-clorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(5-(3-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(6-(2-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(6-(3-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(6-(4-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(7-(2-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(7-(3-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(7-(4-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(5-(1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(6-(1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(7-(1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(6-cloro-5-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(6-bromo-5-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(5-cloro-6-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(5-bromo-6-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(6-bromo-5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(6-cloro-5-metoxi-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(6-fluoro-5-metoxi-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(5-fluoro-6-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(4,5-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2S,3S)-2-(3-(4,5-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2S,3R)-2-(3-(4,5-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3R)-2-(3-(4,5-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(4-cloro-5-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(5-bromo-4-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(5-bromo-4-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-bromo-7-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(4,5-difluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6,7-difluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(4,5-dimetil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5,6-difluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5,6-dibromo-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5,6-dimetil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6,7-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(4,6-difluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5,7-difluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(4-cloro-5-metoxi-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(7-cloro-6-metoxi-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(4-cloro-5-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-bromo-4-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-fluoro-4-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-fluoro-7-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(4-cloro-5-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(7-cloro-6-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
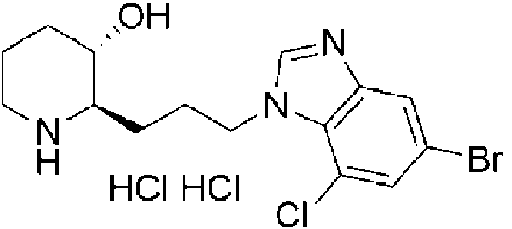
) 7-bromo-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-5-carboxilato de metilo, ) (2R,3S)-2-(3-(7-bromo-5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-bromo-7-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(7-bromo-5-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-bromo-4-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-bromo-7-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(7-cloro-4-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-bromo-4-nitro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-bromo-7-nitro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(7-cloro-5-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3 -ol,
) (2R,3S)-2-(3-(5-cloro-7-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5,7-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-7-(1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3 -ol,
) (2R,3S)-2-(3-(7-(1 H-pirazol-4-il)-5-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3 -ol,
) (2R,3S)-2-(3-(5-cloro-7-(3-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3 -ol,
) (2R,3S)-2-(3-(7-(3-fluorofenil)-5-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3 -ol,
) (2R,3S)-2-(3-(5-cloro-7-(2-metiltiazol-5-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3 -ol,
) (2R,3S)-2-(3-(5-cloro-7-(piridin-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3 -ol,
) (2R,3S)-2-(3-(5-cloro-7-(5-fluoropiridin-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3 -ol,
) 5-(5-cloro-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-7-il)-1 -metilpiridin-2(1 H)-ona, ) (2R,3S)-2-(3-(5-cloro-7-(1 -(difluorometil)-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(5-cloro-7-(isoxazol-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-7-(tiofen-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3 -ol,
) (2R,3S)-2-(3-(5-cloro-7-(2-metiltiofen-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3 -ol,
) (2R,3S)-2-(3-(5-cloro-7-(3,5-dimetilisoxazol-4-il)-1 H-benzo[d]imidazol-1-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-7-(3,6-dihidro-2H-piran-4-il)-1 H-benzo[d]imidazol-1-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(7-(1 -((1,3-dioxolan-2-il)metil)-1 H-pirazol-4-il)-5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-7-(1 -metil-1 H-imidazol-5-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-7-(1 -metil-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
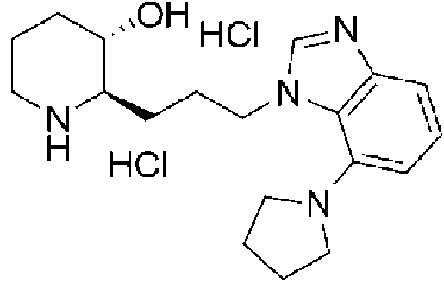
) (2R,3S)-2-(3-(7-(pirrolidin-1 -il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-7-(pirrolidin-1 -il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
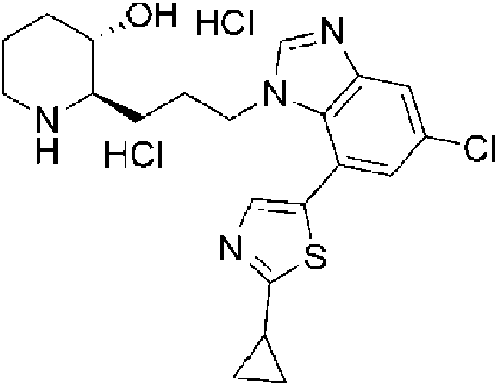
0) (2R,3S)-2-(3-(5-cloro-7-(2-ciclopropiltiazol-5-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
1) (2R,3S)-2-(3-(5-cloro-7-(1 -(tiazol-2-il)-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-7-(1 -(oxetan-3-il)-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(5-cloro-7-(2-(tetrahidro-2H-piran-4-il)tiazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(5-cloro-7-(furan-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) 4-(5-cloro-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-7-il)tiazol-2-carbonitrilo, ) (2R,3S)-2-(3-(7-(1 -(terc-butil)-1 H-pirazol-4-il)-5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(5-cloro-7-(1 -isopentil-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-7-(1 -isopropil-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-7-(4-metiltiofen-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) 3-(5-cloro-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-7-il)furano-2-carboxilato de etilo, ) 4-(5-cloro-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-7-il)tiofeno-2-carboxilato de metilo,
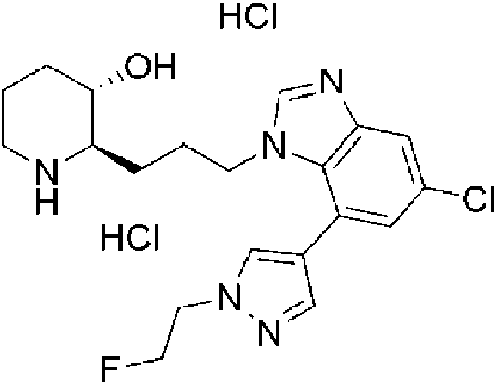
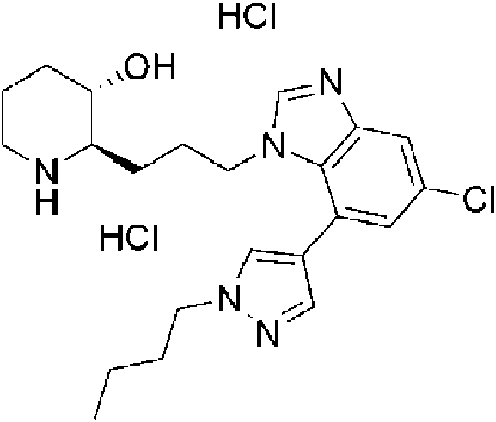
) (2R,3S)-2-(3-(5-cloro-7-(1 -(2-fluoroetil)-1 H-pirazol-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(7-(1 -butil-1 H-pirazol-4-il)-5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
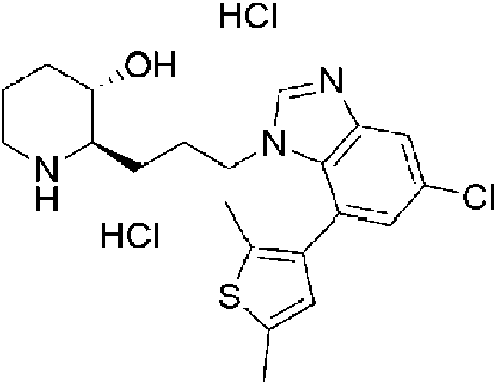
) (2R,3S)-2-(3-(5-cloro-7-(2,5-dimetiltiofen-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-7-(1 -isobutil-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
) 4-(5-cloro-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-7-il)-1 -metil-1 H-pirrol-2-carboxilato de etilo,
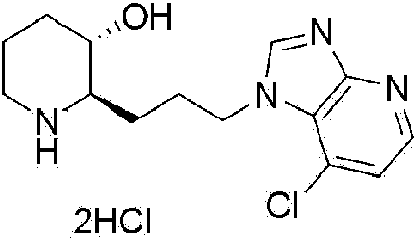
) (2R,3S)-2-(3-(5-cloro-1 H-imidazo[4,5-b]piridin-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol,
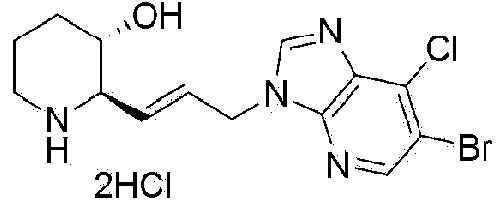
) (2R,3S)-2-(3-(5-bromo-1 H-imidazo[4,5-b]piridin-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-bromo-1 H-imidazo[4,5-b]piridin-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-metil-1 H-imidazo[4,5-b]piridin-1 -il)propil)piperidin-3-ol,
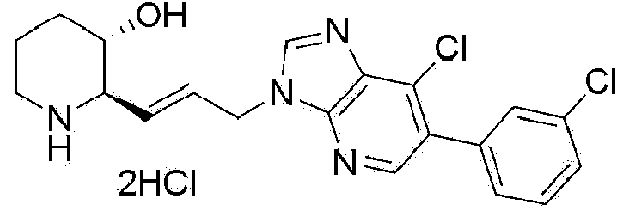
) (2R,3S)-2-(3-(6-cloro-1 H-imidazo[4,5-c]piridin-1 -il)propil)piperidin-3-ol.
) (2R,3S)-2-(3-(6-cloro-3H-imidazo[4,5-c]piridin-3-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-bromo-1 H-imidazo[4,5-c]piridin-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-bromo-3H-imidazo[4,5-c]piridin-3-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(7-cloro-1 H-imidazo[4,5-b]piridin-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5,6-dicloro-1 H-imidazo[4,5-b]piridin-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(7-bromo-1 H-imidazo[4,5-c]piridin-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-(trifluorometil)-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6,7-dicloro-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol,
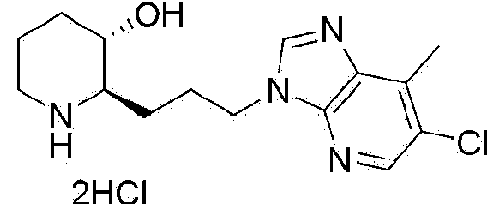
) (2R,3S)-2-(3-(6-cloro-7-metil-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-bromo-7-metil-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-bromo-7-cloro-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(7-cloro-6-(3-clorofenil)-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(2-cloro-7H-purin-7-il)propil)piperidin-3-ol,
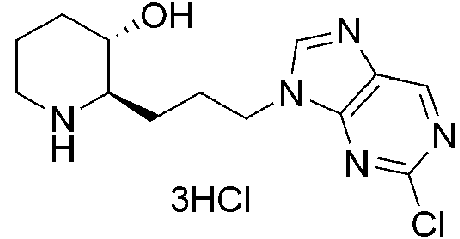
) (2R,3S)-2-(3-(2-cloro-9H-purin-9-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-(dimetilamino)-9H-purin-9-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-(dietilamino)-9H-purin-9-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-(etil(metil)amino)-9H-purin-9-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-morfolino-9H-purin-9-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-(piperidin-1 -il)-9H-purin-9-il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(6-(pirrolidin-1 -il)-9H-purin-9-il)propil)piperidin-3-ol,
) 1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-2-ol,
) 5,6-dicloro-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-2-ol, ) (2R,3S)-2-(3-(2-(hidroximetil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
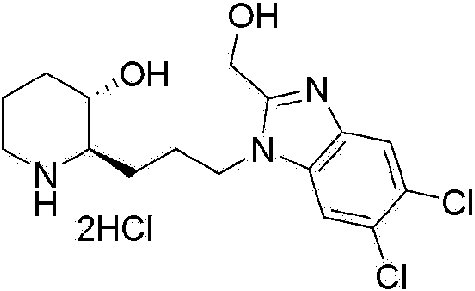
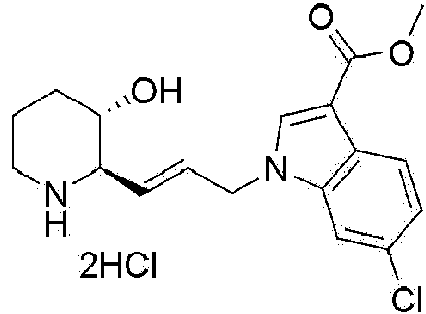
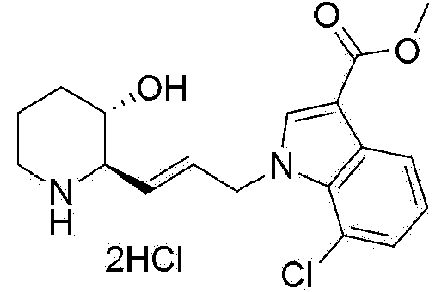
) (2R,3S)-2-(3-(2-(hidroximetil)-4,5-dimetil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, .147)(2R,3S)-2-(3-(5,6-dicloro-2-(hidroximetil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(2-amino-5,6-dicloro-1 H-benzo[d]imidazol-1-il)propil)piperidin-3-ol, ) 7-bromo-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo, ) 5-bromo-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo, ) 6-bromo-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-indol-3-carboxilato de metilo, ) 4-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo, ) 6-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo, ) 7-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo, ) (2R,3S)-2-(3-(5-cloro-3-ciclopropil-1 H-indazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-3-(trifluorometil)-1 H-indazol-1 -il)propil)piperidin-3-ol,
) (2R,3S)-2-(3-(5-cloro-3-(1 -(difluorometil)-l H-pirazol-4-il)-1 H-indazol-1 -il)propil)piperidin-3-ol, ) (2R,3S)-2-(3-(6-cloro-3-(1 -(difluorometil)-1 H-pirazol-4-il)-1 H-indazol-1 -il)propil)piperidin-3-ol, ) 1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-3-metil-1 H-benzo[d]imidazol-2(3H)-ona,
) 5-bromo-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-2(3H)-ona,
) 6-bromo-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-2(3H)-ona,
) 7-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1,3-dimetil-1 H-purino-2,6(3H,7H)-diona,
) 7-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-3-metil-1 H-purino-2,6(3H,7H)-diona,
) 9-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 -metil-1 H-purino-2,6(3H,9H)-diona,
) 7-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-3-isobutil-1 -metil-1 H-purino-2,6(3H,7H)-diona, ) (2R,3S)-2-((E)-3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(5-fluoro-4-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(5-bromo-4-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(5,6-dimetil-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(5,6-dibromo-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
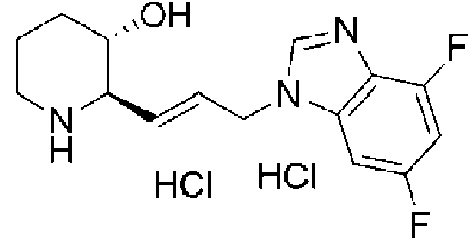
) (2R,3S)-2-((E)-3-(5,6-difluoro-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(4,5-dimetil-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(5-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(4,5-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(4-cloro-5-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(5-bromo-4-nitro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(6-bromo-7-nitro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(4-cloro-5-nitro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(4,6-difluoro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(6-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(7-cloro-5-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(5,7-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(5-cloro-7-fluoro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(5-bromo-1 H-imidazo[4,5-b]piridin-1 -il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(7-cloro-6-(3-clorofenil)-3H-imidazo[4,5-b]piridin-3-il)prop-1-enil)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(6-bromo-7-metil-3H-imidazo[4,5-b]piridin-3-il)prop-1-enil)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(6-bromo-7-cloro-3H-imidazo[4,5-b]piridin-3-il)prop-1-enil)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(6-cloro-7-metil-3H-imidazo[4,5-b]piridin-3-il)prop-1-enil)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(6,7-dicloro-3H-imidazo[4,5-b]piridin-3-il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(6-(3-clorofenil)-1 H-benzo[d]imidazol-1-il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(6-(3-fluorofenil)-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(6-(3-(trifluorometil)fenil)-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(5-bromo-6,7-difluoro-2-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol, ) (2R,3S)-2-((E)-3-(indolin-1 -il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(5-cloroindolin-1 -il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(1 H-pirrolo[2,3-b]piridin-1 -il)prop-1 -enil)piperidin-3-ol,
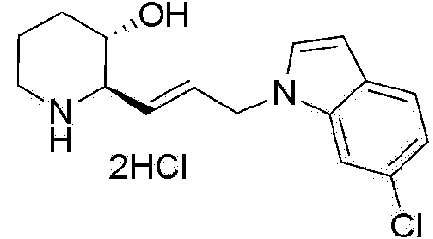
) (2R,3S)-2-((E)-3-(6-cloro-1 H-indol-1 -il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(6-cloro-1 H-indazol-1 -il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(4-cloro-7H-pirrolo[2,3-d]pirimidin-7-il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(5-cloro-1 H-pirazolo[3,4-b]piridin-1 -il)prop-1 -enil)piperidin-3-ol,
) (2R,3S)-2-((E)-3-(3,5-dimetil-1 H-indazol-1 -il)prop-1 -enil)piperidin-3-ol,
) 7-bromo-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxilato de metilo,
) ácido 7-bromo-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
) ácido 5-bromo-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
) ácido 4-cloro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
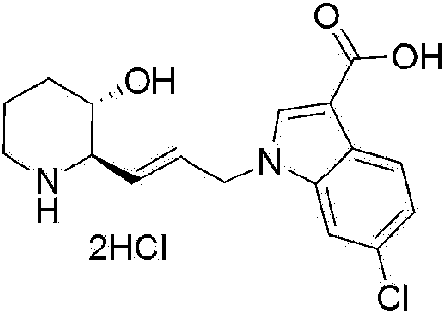
) ácido 6-cloro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
) ácido 7-cloro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
) ácido 6-fluoro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
) ácido 1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
) 4-cloro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxilato de metilo,
) 6-cloro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxilato de metilo,
) 7-cloro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxilato de metilo,
213) 5-bromo-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxilato de metilo,
214) 6-bromo-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxilato de metilo,
215) 5-bromo-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-N-metil-1 H-indol-3-carboxamida,
216) 5-bromo-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-N,N-dimetil-1 H-indol-3-carboxamida,
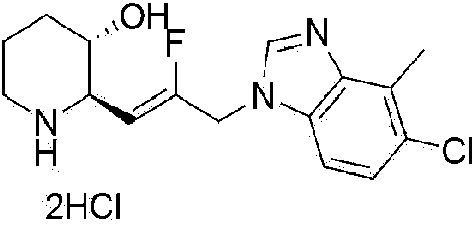
217) (2R,3S)-2-((Z)-3-(5-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)-2-fluoroprop-1 -enil)piperidin-3-ol,
218) (2R,3S)-2-((Z)-3-(5-bromo-4-metil-1 H-benzo[d]imidazol-1 -il)-2-fluoroprop-1 -enil)piperidin-3-ol,
219) (2R,3S)-2-((Z)-3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)-2-fluoroprop-1 -enil)piperidin-3-ol,
220) (2R,3S)-2-((Z)-3-(5,6-dicloro-2-(hidroximetil)-1 H-benzo[d]imidazol-1 -il)-2-fluoroprop-1 -enil)piperidin-3-ol, 221) (2R,3S)-2-((E)-3-(5-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)-2-metilprop-1 -enil)piperidin-3-ol,
222) (2R,3S)-2-((E)-3-(5-bromo-4-metil-1 H-benzo[d]imidazol-1 -il)-2-metilprop-1 -enil)piperidin-3-ol,
223) (2R,3S)-2-((E)-3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)-2-metilprop-1 -enil)piperidin-3-ol,
224) (2R,3S)-2-((E)-3-(5,6-dicloro-2-(hidroximetil)-1 H-benzo[d]imidazol-1 -il)-2-metilprop-1 -enil)piperidin-3-ol, 225) (2R,3S)-2-(3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -inil)piperidin-3-ol,
226) (2R,3S)-2-(3-(5-bromo-4-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -inil)piperidin-3-ol,
227) (2R,3S)-2-(3-(5-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -inil)piperidin-3-ol,
228) (2R,3S)-2-(3-(5,6-dibromo-1 H-benzo[d]imidazol-1 -il)prop-1 -inil)piperidin-3-ol,
229) (2R,3S)-2-(3-(5-fluoro-4-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -inil)piperidin-3-ol, y
230) (2R,3S)-2-((E)-3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)pirrolidin-3 -ol.
Además, los compuestos de la presente invención pueden existir en la forma de una sal farmacéuticamente aceptable. Como sal, es útil una sal por adición de ácido formada por un ácido libre farmacéuticamente aceptable. Como el ácido libre, se puede usar un ácido inorgánico y un ácido orgánico. Ejemplos del ácido inorgánico pueden incluir ácido bromhídrico, ácido brómico, ácido sulfúrico, ácido fosfórico, y similares. Ejemplos del ácido orgánico pueden incluir ácido cítrico, ácido acético, ácido láctico, ácido maleico, ácido glucónico, ácido metanosulfónico, ácido succínico, ácido 4-toluenosulfónico, ácido glutámico, ácido aspártico o similares.
Sales o solvatos de los compuestos representados por la Fórmula Química 1 que sean farmacéuticamente no aceptables se pueden usar como productos intermedios en la preparación del compuesto representado por la Fórmula Química 1, una de sus sales farmacéuticamente aceptables o uno de sus solvatos.
El compuesto representado por la Fórmula Química 1 según la presente invención incluye sus sales farmacéuticamente aceptables así como tanto solvatos como hidratos que se pueden preparar a partir de las mismas. Las sales o los solvatos del compuesto representado por la Fórmula Química 1 se pueden preparar a partir de los compuestos representados por la Fórmula Química 1 usando métodos convencionales en el campo técnico del que trata la presente invención.
Además, el compuesto representado por la Fórmula Química 1 según la presente invención se puede preparar en forma cristalina o en forma no cristalina. Cuando el compuesto representado por la Fórmula Química 1 se produce en forma cristalina, opcionalmente se puede hidratar o solvatar. La presente invención puede incluir no solo hidratos estequiométricos del compuesto representado por la Fórmula Química 1 sino también compuestos que contienen una cantidad diversa de agua. Los solvatos del compuesto representado por la Fórmula Química 1 según la presente invención incluyen tanto solvatos estequiométricos como solvatos no estequiométricos.
La presente invención también proporciona un método para preparar un compuesto representado por la Fórmula Química 1 según se muestra en el siguiente Esquema de Reacción 1:
[Esquema de Reacción 1]
(en el Esquema de Reacción 1, n, L, X1, X2 y A son como se definen previamente, X es halógeno (preferiblemente bromo), y cada uno de R' y R" significa independientemente un grupo protector. El grupo protector puede ser terc -butildimetilsililo o terc-butiloxicarbonilo.)
La etapa 1 es una etapa de preparación de un compuesto representado por la Fórmula Química 1-C al hacer reaccionar un compuesto representado por la Fórmula Química 1-A con un compuesto representado por la Fórmula Química 1-B en presencia de una base. Se pueden usar como la base bases inorgánicas y bases orgánicas convencionales. Ejemplos no limitativos de bases orgánicas pueden incluir diisopropiletilamina o trietilamina. Ejemplos no limitativos de las bases inorgánicas pueden incluir carbonato potásico, carbonato sódico, hidrogenocarbonato sódico, carbonato de cesio o carbonato cálcico. Además, la reacción se puede llevar a cabo en un disolvente polar tal como metanol, etanol, butanol, tetrahidrofurano, acetona, tolueno, dimetilformamida, dimetilformsulfóxido, cloroformo, dioxano, éter dietílico de acetonitrilo, o diclorometano, a de 20°C a 150°C durante de 10 minutos a 24 horas.
La etapa 2 es una etapa de preparación de un compuesto representado por la Fórmula Química 1 al hacer reaccionar un compuesto representado por la Fórmula Química 1-C en presencia de un ácido. Ejemplos no limitativos del ácido pueden incluir ácido clorhídrico, ácido brómico, ácido fluorhídrico, ácido trifluoroacético o similares. Preferiblemente, el disolvente de reacción puede usar o no un disolvente orgánico polar. Preferiblemente, cuando se usa un disolvente orgánico polar, se puede usar diclorometano, cloroformo, tolueno, dimetilformamida, dioxano, tetrahidrofurano o similares, y la reacción se puede llevar a cabo a de 20°C a 100°C durante de 10 minutos a 6 horas.
Como otro ejemplo, el compuesto representado por la Fórmula Química 1-1 se puede preparar como se muestra en el siguiente Esquema de Reacción 2:
[Esquema de Reacción 2]
(en el Esquema de Reacción 2, n, L, R2 y A son como se definen previamente, y cada uno de R' y R" significa independientemente un grupo protector. El grupo protector puede ser terc-butildimetilsililo o terc-butiloxicarbonilo.)
La etapa 1' es una etapa de preparación de un compuesto representado por la Fórmula Química 2-C al hacer reaccionar un compuesto representado por la Fórmula Química 2-A con un compuesto representado por la Fórmula Química 2-B en presencia de una base. Se pueden usar como la base bases inorgánicas y bases orgánicas convencionales. Ejemplos no limitativos de bases orgánicas pueden incluir diisopropiletilamina o trietilamina. Ejemplos no limitativos de las bases inorgánicas pueden incluir carbonato potásico, carbonato sódico, hidrogenocarbonato sódico, carbonato de cesio o carbonato cálcico. Además, la reacción se puede llevar a cabo en un disolvente polar tal como metanol, etanol, butanol, tetrahidrofurano, acetona, tolueno, dimetilformamida, dimetilformsulfóxido, cloroformo, dioxano, éter dietílico de acetonitrilo o diclorometano a de 20°C a 150°C durante de 10 minutos a 24 horas.
La etapa 2' es una etapa de preparación de un compuesto representado por la Fórmula Química 2-D al hacer reaccionar un grupo amina y un grupo nitro del compuesto representado por la Fórmula Química 2-C para formar un anillo. La etapa anterior se lleva a cabo sustancialmente en dos fases. En primer lugar, un compuesto representado por la Fórmula Química 2-C se hace reaccionar con hidrógeno en presencia de níquel Raney y a continuación se hace reaccionar con ortoformiato de trimetilo. La primera reacción se lleva a cabo en un disolvente polar tal como metanol, etanol, butanol, tetrahidrofurano, acetona, tolueno, dimetilformamida, dimetilformsulfóxido, cloroformo, dioxano, éter dietílico de acetonitrilo, o diclorometano, a de 20°C a 150°C durante de 10 minutos a 24 horas. La última reacción se lleva a cabo preferiblemente en presencia de ácido paratoluenosulfónico, y la reacción se puede llevar a cabo en un disolvente polar tal como metanol, etanol, butanol, tetrahidrofurano, acetona, tolueno, dimetilformamida, dimetilformsulfóxido, cloroformo, dioxano, éter dietílico de acetonitrilo, o diclorometano, a de 20°C a 150°C durante de 10 minutos a 24 horas.
La etapa 3' es una etapa de preparación de un compuesto representado por la Fórmula Química 1 -1 al hacer reaccionar un compuesto representado por la Fórmula Química 2-D en presencia de un ácido. Las condiciones de reacción específicas de la etapa 3' se pueden aplicar de forma similar a las condiciones de reacción de la etapa 2 del Esquema de Reacción 1 descrito anteriormente.
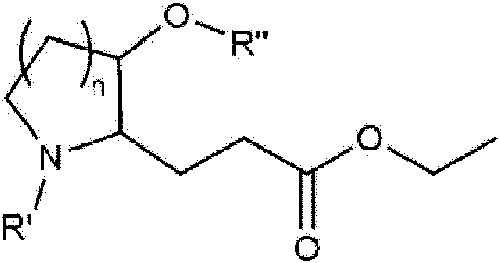
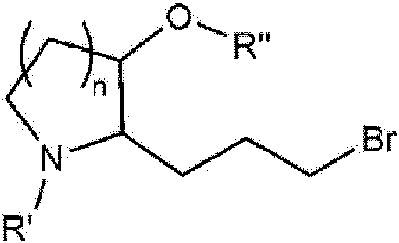
Además, como un ejemplo, entre los compuestos de Fórmula Química 2-A mostrados en el Esquema de Reacción 2, un compuesto en el que L es etileno y R2 es hidrógeno (un compuesto representado por la siguiente Fórmula Química 3) se puede preparar mediante un método como el mostrado en el siguiente Esquema de Reacción 3:
[Esquema de Reacción 3]
(en el Esquema de Reacción 3, n es como se define previamente, y cada uno de R' y R" significa independientemente un grupo protector. El grupo protector puede ser terc-butildimetilsililo o terc-butiloxicarbonilo.)
La etapa 1" es una etapa de preparación de un compuesto representado por la Fórmula Química 3-B al hacer reaccionar el compuesto representado por la Fórmula Química 3-A con (carbetoximetilen)trifenilfosforano. Preferiblemente, el compuesto representado por la Fórmula Química 3-A se hace reaccionar en primer lugar con cloruro de oxalilo y a continuación se hace reaccionar con trifenilfosforano. La primera reacción se lleva a cabo preferiblemente en presencia de cloruro de metileno, N,N-dimetilsulfóxido y trietilamina. La última reacción también se puede llevar a cabo a de -78°C a 20°C durante de 10 minutos a 12 horas. Además, en la reacción con trifenilfosforano, se puede usar diclorometano como el disolvente, y la reacción se puede llevar a cabo a de 20°C a 150°C durante de 10 minutos a 24 horas.
La etapa 2" es una etapa de preparación de un compuesto representado por la Fórmula Química 3-C al hidrogenar el compuesto representado por la Fórmula Química 3-B. Preferiblemente, la reacción se lleva a cabo en presencia de hidrógeno y un catalizador de hidrogenación (p. ej., hidróxido de paladio). Además, se puede usar tetrahidrofurano
como un disolvente para la reacción. Además, la reacción se puede llevar a cabo a de 20°C a 150°C durante de 10 minutos a 24 horas.
La etapa 3" es una etapa de preparación de un compuesto representado por la Fórmula Química 3-D al hidrolizar el compuesto representado por la Fórmula Química 3-C. Preferiblemente, la reacción se puede llevar a cabo bajo una condición básica, y se puede usar hidróxido sódico como la base. Además, se puede usar agua o metanol como un disolvente para la reacción. Adicionalmente, la reacción se puede llevar a cabo a de 20°C a 150°C durante de 10 minutos a 24 horas.
La etapa 4" es una etapa de preparación de un compuesto representado por la Fórmula Química 3-E al someter el compuesto representado por la Fórmula Química 3-D a una reacción de reducción de carbonilo. Preferiblemente, la reacción se puede llevar a cabo en presencia de hidruro de litio y aluminio. Además, se puede usar tetrahidrofurano como un disolvente para la reacción. Adicionalmente, la reacción se puede llevar a cabo a de -78°C a 20°C durante de 10 minutos a 12 horas.
La etapa 5" es una etapa de preparación de un compuesto representado por la Fórmula Química 3-F al bromar el compuesto representado por la Fórmula Química 3-F. Preferiblemente, la reacción se lleva a cabo en presencia de trifenilfosfina y tetrabromometano. Además, se puede usar cloruro de metileno como un disolvente para la reacción. Adicionalmente, la reacción se puede llevar a cabo a de 20°C a 150°C durante de 10 minutos a 24 horas.
La etapa 6" es una etapa de preparación de un compuesto representado por la Fórmula Química 3-G al someter el compuesto representado por la Fórmula Química 3-F a una reacción con azida. Preferiblemente, la reacción se lleva a cabo en presencia de azida sódica. Además, se puede usar N,N-dimetilformamida como un disolvente para la reacción. Adicionalmente, la reacción se puede llevar a cabo a de 20°C a 150°C durante de 10 minutos a 24 horas.
La etapa 7" es una etapa de preparación de un compuesto representado por la Fórmula Química 3 al aminar el compuesto representado por la Fórmula Química 3-G. Preferiblemente, la reacción se lleva a cabo en presencia de trifenilfosfina. Además, se puede usar tetrahidrofurano como un disolvente para la reacción. Adicionalmente, la reacción se puede llevar a cabo a de 20°C a 150°C durante de 10 minutos a 24 horas.
Adicionalmente, la presente invención proporciona una composición farmacéutica para la prevención o el tratamiento de enfermedades provocadas por una anormalidad en una actividad de PRS (prolil-ARNt sintetasa), que comprende un compuesto representado por la Fórmula Química 1 o una de sus sales farmacéuticamente aceptables.
El compuesto representado por la Fórmula Química 1 según la presente invención puede inhibir la actividad enzimática de PRS y así se puede usar para la prevención o el tratamiento de enfermedades provocadas por una anormalidad en una actividad de PRS (prolil-ARNt sintetasa). Ejemplos de enfermedades provocadas por una anormalidad en la actividad de PRS (prolil-ARNt sintetasa) pueden incluir un cáncer, una enfermedad inflamatoria, una enfermedad autoinmunitaria y una fibrosis.
Como se muestra en los Ejemplos que se describirán posteriormente, el compuesto representado por la Fórmula Química 1 según la presente invención puede inhibir significativamente la actividad enzimática de PRS y también inhibir el crecimiento de células cancerosas. Así, este compuesto se puede usar eficazmente para la prevención o el tratamiento de las enfermedades.
La composición farmacéutica según la presente invención se puede formular en tipos para administraciones orales o parenterales según una práctica farmacéutica estándar. Estas formulaciones pueden contener aditivos tales como un portador, adyuvante o diluyente farmacéuticamente aceptable además del ingrediente activo. Portadores adecuados pueden incluir, por ejemplo, solución salina fisiológica, polietilenglicol, etanol, aceite vegetal y miristato de isopropilo, y el diluyente puede incluir, por ejemplo, lactosa, dextrosa, sacarosa, manitol, sorbitol, celulosa y/o glicina, pero no se limitan a estos. Adicionalmente, los compuestos de la presente invención se pueden disolver en aceites, propilenglicol u otros disolventes que se usan habitualmente para la preparación de soluciones inyectables. Además, los compuestos de la presente invención se pueden formular como pomadas o cremas para aplicación tópica.
Una dosis preferida del compuesto representado por la Fórmula Química 1 según la presente invención se puede variar dependiendo de la condición y el peso de un paciente, la gravedad de una enfermedad, el tipo de un fármaco y la vía y la duración de la administración, pero se puede seleccionar adecuadamente por los expertos en la técnica. Sin embargo, a fin de alcanzar los efectos deseados , el compuesto representado por la Fórmula Química 1 según la presente invención se puede administrar diariamente en una dosis de 0,0001 a 100 mg/kg (de peso corporal), y preferiblemente de 0,001 a 100 mg/kg (de peso corporal). La administración se puede realizar una vez al día o en dosis divididas cada día a través de una vía oral o parenteral.
Dependiendo del método de administración, la composición farmacéutica según la presente invención puede contener el compuesto representado por la Fórmula Química 1 o una de sus sales farmacéuticamente aceptables en una cantidad de 0,001 a 99% en peso, preferiblemente de 0,01 a 60% en peso.
La composición farmacéutica según la presente invención se puede administrar a mamíferos tales como una rata, un ratón, un animal doméstico, un ser humano o similares, a través de diversas vías. La administración se puede llevar a cabo a través de todos los métodos posibles, por ejemplo, inyección oral, rectal, intravenosa, intramuscular, subcutánea, intraendometrial, intracerebroventricular.
EFECTOS VENTAJOSOS
El compuesto representado por la Fórmula Química 1 según la presente invención puede inhibir la actividad enzimática de PRS y así se puede usar eficazmente para la prevención o el tratamiento de enfermedades provocadas por una anormalidad en una actividad de PRS (prolil-ARNt sintetasa), por ejemplo, cánceres, enfermedades inflamatorias, enfermedades autoinmunitarias y fibrosis.
DESCRIPCIÓN DETALLADA DE LAS REALIZACIONES
Posteriormente, la presente invención se describirá con más detalle por medio de ejemplos que se proporcionan solamente para ilustrar la presente invención.
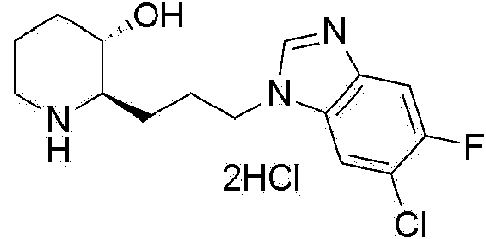
Ejemplo 1: Preparación de dih idrocloruro de (2R,3S)-2-(3-(6-cloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
Etapa 1-1: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(E)-3-etoxi-3-oxoprop-1-en-1-il)piperidino-1-carboxilato de terc-butilo
Se añadieron cloruro de metileno (47 ml, 0,12 M) y cloruro de oxalilo (1,0 ml, 11,6 mmol) a un matraz cargado con argón y la solución de reacción se enfrió hasta -78°C. A continuación, se añadió N,N-dimetilsulfóxido (1,7 ml, 23,2 mmol) a la misma temperatura y se agitó durante 30 minutos. A continuación, se disolvió (2R,3S)-3-((tercbutildimetilsilil)oxi)-2-(hidroximetil)piperidino-1 -carboxilato de terc-butilo (2,0 g, 5,8 mmol) en una pequeña cantidad de cloruro de metileno y se añadió lentamente. Después de agitar a la misma temperatura durante 1 hora, se añadió trietilamina (3,3 ml, 23,2 mmol) y la temperatura de la solución de reacción se elevó hasta temperatura ambiente desde -78°C. Cuando la reacción se completaba, el disolvente se retiraba y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó con sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se disolvió en cloruro de metileno (47 ml, 0,12 M). Se añadió a esto (carbetoximetilen)trifenilfosforano (4,0 g, 11,6 mmol) a temperatura ambiente y se agitó durante 2 horas. Cuando la reacción se completaba, el disolvente se retiraba y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (hexano:acetato de etilo = 4:1) para dar el compuesto del epígrafe (2,1 g, 89% de rendimiento a lo largo de dos etapas).
Etapa 1-2: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-etoxi-3-oxopropil)piperidino-1-carboxilato de tercbutilo
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(E)-3-etoxi-3-oxoprop-1-en-1-il)piperidino-1-carboxilato de terc-butilo (3,2 g, 7,7 mmol) obtenido a partir de la Etapa 1-1 se disolvió en tetrahidrofurano (50 ml, 0,15 M), y a continuación se añadió a esto hidróxido de paladio (104 mg, 0,77 mmol). Después de la conexión de un globo de hidrógeno, la mezcla se agitó a temperatura ambiente durante 5 horas. Cuando la reacción se completaba, la solución de reacción se filtraba a través de Celite y se concentraba bajo presión reducida. Las reacciones posteriores se llevaron a cabo sin un procedimiento de purificación.
Etapa 1-3: Preparación de ácido 3-((2R,3S)-1-(terc-butoxicarbonil)-3-(terc-butildimetilsilil)oxi)piperidin-2-il)propenoico
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-etoxi-3-oxopropil)piperidino-1-carboxilato de terc-butilo (3,0 g, 7,2 mmol) obtenido a partir de la Etapa 1-2 se disolvió en metanol (20 ml, 0,36 M), y a continuación se añadió a esto solución acuosa de hidróxido sódico 2 N (10 ml) y se agitó a temperatura ambiente durante 3 horas. Cuando la reacción se completaba, la solución de reacción se neutralizaba con solución acuosa de ácido clorhídrico 1 N, se acidificaba y a continuación se diluía con acetato de etilo, y se lavaba con solución saturada de cloruro sódico. La capa orgánica se
recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida. Las reacciones posteriores se llevaron a cabo sin un procedimiento de purificación.
Etapa 1-4: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-hidroxipropil)piperidino-1 -carboxilato de terc-butilo
El ácido 3-((2R,3S)-1-(terc-butoxicarbonil)-3-(terc-butildimetilsilil)oxi)piperidin-2-il)propenoico (1,6 g, 4,0 mmol) obtenido a partir de la Etapa 1-1 se disolvió en tetrahidrofurano (50 ml, 0,08 M), y la solución de reacción se enfrió hasta 0°C. A continuación, se añadió lentamente a esto una solución de hidruro de litio y aluminio (1,6 ml, 4,0 mmol), se hizo reaccionar a la misma temperatura durante 30 minutos y a continuación se agitó a temperatura ambiente durante 2 horas. Se añadió una pequeña cantidad de agua para completar la reacción, se diluyó con acetato de etilo y se lavó con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (diclorometano:metanol = 10:1) para dar el compuesto del epígrafe (1,3 g, rendimiento: 85%).
Etapa 1-5: Preparación de (2R,3S)-2-(3-bromopropil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(-3-hidroxipropil)piperidino-1 -carboxilato de terc-butilo (5,1 g, 13,8 mmol) obtenido a partir de la Etapa 1-4 se añadió a cloruro de metileno (100 ml, 0,14 M). La solución de reacción se enfrió hasta 0°C, y a continuación se añadieron secuencialmente trifenilfosfina (4,3 g, 16,5 mmol) y tetrabromometano (5,5 g, 16,5 mmol) a la misma temperatura, seguido por agitación a temperatura ambiente durante 2 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y a continuación se concentró bajo presión reducida, y se purificó mediante cromatografía en columna (hexano:acetato de etilo = 5:1) para dar el compuesto del epígrafe (4,6 g, rendimiento: 76%).
Etapa 1-6: Preparación de (2R,3S)-2-(3-azidopropil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo
El (2R,3S)-2-(3-bromopropil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo (7,4 g, 17,0 mmol) obtenido a partir de la Etapa 1 -5 se disolvió en N,N-dimetilformamida (25 ml, 0,67 M). A continuación, se añadió a esto azida sódica (3,3 g, 17,0 mmol) y la mezcla se agitó a temperatura ambiente durante 4 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluían con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato sódico, se filtró y a continuación se concentró bajo presión reducida, y se purificó mediante cromatografía en columna (hexano:acetato de etilo = 7:1) para dar el compuesto del epígrafe (5,8 g, rendimiento 85%).
Etapa 1-7: Preparación de (2R,3S)-2-(3-aminopropil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo
El (2R,3S)-2-(3-azidopropil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo (5,5 g, 13,8 mmol) obtenido a partir de la Etapa 1-6 se disolvió en tetrahidrofurano (24 ml, 0,57 M), y a continuación se añadió a esto trifenilfosfina (4,3 g, 16,5 mmol) y se agitó a temperatura ambiente durante 30 minutos. A continuación, se añadió a esto agua (24 ml, 0,57 M) y se agitó a temperatura ambiente durante 1 hora. Cuando la reacción se completaba, la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato sódico, se filtró y a continuación se concentró bajo presión reducida, y se purificó mediante cromatografía en columna (diclorometano:metanol= 10:1 trietilamina 2%) para dar el compuesto del epígrafe (4,0 g, rendimiento: 78%).
Etapa 1-8: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-((4-cloro-2-nitrofenil)amino)propil)piperidino-1-carboxilato de terc-butilo
El (2R,3S)-2-(3-aminopropil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo (1,0 g, 2,7 mmol) obtenido a partir de la Etapa 1-7 se disolvió en N,N-dimetilformamida (25 ml, 0,67 M). Se añadieron a esto 4-cloro-2-fluoro-1-nitrobenceno (518 mg, 3,0 mmol) y N,N-diisopropiletilamina (0,93 ml, 5,4 mmol), y la mezcla se calentó y se agitó a 60°C durante 2 horas. Cuando la reacción se completaba, la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato sódico, se filtró y se concentró bajo presión reducida, y se purificó mediante cromatografía en columna (hexano:acetato de etilo = 5:1) para dar el compuesto del epígrafe (1,2 g, rendimiento: 87%).
Etapa 1-9: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-(5-cloro-1H-benzo[d]imidazol-1-il)propil)piperidino-1 -carboxilato de terc-butilo
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-((4-cloro-2-nitrofenil)amino)propil)piperidino-1 -carboxilato de terc-butilo (2,6 mg, 4,9 mmol) obtenido a partir de la Etapa 1 -8 se disolvió en metanol (25 ml, 0,2 M), y a continuación se añadió
a esto una cantidad apropiada de níquel Raney. Después de conectar un globo de hidrógeno, la mezcla se agitó a temperatura ambiente durante 1 hora. Cuando la reacción se completaba, la solución de reacción se filtraba a través de Celite y se concentraba bajo presión reducida. Las reacciones posteriores se llevaron a cabo sin un procedimiento de purificación. El compuesto concentrado se disolvió en tolueno (30 ml, 0,16 M), y a continuación se añadieron a esto ortoformiato de trimetilo (1,6 ml, 14,6 mmol) y ácido paratoluenosulfónico (168 mg, 0,98 mmol), seguido por calentamiento y agitación a 50°C durante 6 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida, y se purificó mediante cromatografía en columna (hexano:acetato de etilo = 1:1) para dar el compuesto del epígrafe (1,8 g, rendimiento: 74%).
Etapa 1-10: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-cloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-(5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidino-1 -carboxilato de tercbutilo (1,8 g, 3,6 mmol) obtenido a partir de la Etapa 1-9 se disolvió en una pequeña cantidad de tetrahidrofurano. A continuación, se añadió a esto solución en dioxano de cloruro de hidrógeno 4 N (30 ml, 0,12 M), y la mezcla se agitó a temperatura ambiente durante 12 horas. Cuando la reacción se completaba, la solución de reacción se concentraba bajo presión reducida para retirar el disolvente, se disolvía mediante la adición de una pequeña cantidad de metanol, y a continuación se cristalizaba con éter dietílico para dar el compuesto del epígrafe (1,1 g, rendimiento: 81%).
1H-RMN (500 MHz, MeOD) : 59,56 (s, 1H), 8,18 (d, 1H), 7,86 (d, 1H), 7,70 (dd, 1H), 4,58 (t, 2H), 3,58 (m, 2H), 2,99 (m, 2H), 2,21 (m, 2H), 2,07 (m, 2H), 1,97 (m, 1H), 1,75 (m, 2H), 1,58 (m, 1H)
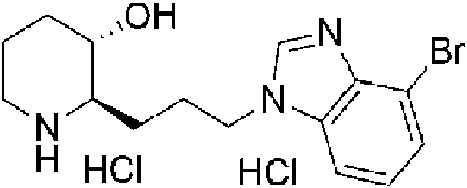
Ejemplo 2: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 93%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1 -bromo-3-fluoro-2-nitrobenceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 9,63(s, 1H), 8,02(d, 1H), 7,86(d, 1H), 7,59(t, 1H), 4,61 (t, 2H), 3,56(m, 2H), 3,46(m, 1H), 3,27(m, 1H), 2,95(m, 2H), 2,20(m, 2H), 2,03(m, 2H), 1,98(m, 1 H), 1,78(m, 2H), 1,53(m, 1 H)
Ejemplo 3: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-bromo-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (13 mg, rendimiento: 91%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 4-bromo-1 -fluoro-2-nitrobenceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,53(s, 1 H), 8,08(d, 1H), 7,98(d, 1 H), 7,83(dd, 1H), 4,63(t, 2H), 3,74(t, 1 H), 3,67(m, 1H), 3,58(m, 2H), 2,97(m, 2H), 2,30(m, 2H), 2,14(m, 2H), 2,02(m, 1 H), 1,78(m, 2H), 1,55(m, 1 H)
Ejemplo 4: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-bromo-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (10 mg, rendimiento: 90%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 4-bromo-2-fluoro-1 -nitrobenceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 9,51 (s, 1 H), 8,32(s, 1H), 7,81 (m, 2H), 4,59(t, 2H), 3,58(m, 1 H), 2,97(m, 2H), 2,20(m, 2H), 2,12(m, 2H), 2,02(m, 1H), 1,79(m, 2H), 1,59(m, 1H)
Ejemplo 5: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-bromo-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (14 mg, rendimiento: 93%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1 -bromo-2-fluoro-3-nitrobenceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 9,59(s, 1 H), 7,89(dd, 2H), 7,56(t, 1H), 3,59(m, 1H), 2,98(m, 2H), 2,30(m, 2H), 2,13(m, 2H), 2,04(m, 1H), 1,79(m, 2H), 1,56(m, 1 H)
Ejemplo 6: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (13 mg, rendimiento: 92%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1,3-difluoro-2-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,52(s, 1H), 7,82(d, 1H), 7,65(m, 1 H), 7,44(m, 1 H), 4,61 (t, 2H), 3,66(m, 1H), 3,58(m, 1H), 3,27(m, 1H), 2,97(m, 2H), 2,24(m, 2H), 2,08(m, 2H), 2,02(m, 1 H), 1,75(m, 2H), 1,54(m, 1 H)
Ejemplo 7: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (11 mg, rendimiento: 90%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1,4-difluoro-2-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,56(s, 1H), 8,07(m, 1 H), 7,65(d, 1 H), 7,50(t, 1H), 4,63(m, 2H), 3,58(m, 1H), 3,00(m, 2H), 2,24(m, 2H), 2,12(m, 2H), 2,02(m, 1 H), 1,74(m, 2H), 1,54(m, 1 H)
Ejemplo 8: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (12 mg, rendimiento: 91%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 2,4-difluoro-1 -nitrobenceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 5 9,56(s, 1H), 7,89(m, 2H), 7,48(t, 1H), 4,59(m, 2H), 3,57(m, 1H), 3,03(m, 2H), 2,29(m, 2H), 2,11(m, 2H), 2,03(m, 1H), 1,76(m, 2H), 1,54(m, 1H)
Ejemplo 9: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (10 mg, rendimiento: 90%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1,2-difluoro-3-nitrobenceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 5 9,57(s, 1H), 7,68(m, 1H), 7,63(m, 1H), 7,46(m, 1H), 4,69(t, 2H), 3,58(m, 1H), 3,25(m, 1H), 2,97(m, 2H), 2,30(m, 2H), 2,15(m, 2H), 2,03(m, 1H), 1,75(m, 2H), 1,54(m, 1H)
Ejemplo 10: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-cloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (11 mg, rendimiento: 91%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1 -cloro-3-fluoro-2-nitrobenceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,55(s, 1 H), 7,96(d, 1H), 7,67(d, 1H), 7,63(m, 1H), 4,61 (t, 2H), 3,60(m, 1H), 3,34(m, 1 H), 3,00(m, 2H), 2,28(m, 2H), 2,14(m, 2H), 2,03(m, 1H), 1,75(m, 2H), 1,54(m, 1 H)
Ejemplo 11: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (8 mg, rendimiento: 87%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 4-cloro-1 -fluoro-2-nitrobenceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,55(s, 1H), 8,03(d, 1 H), 7,93(s, 1H), 7,69(d, 1H), 4,61 (m, 2H), 3,58(m, 1H), 3,01 (m, 2H), 2,29(m, 2H), 2,09(m, 2H), 2,00(m, 1 H), 1,74(m, 2H), 1,52(m, 1H)
Ejemplo 12: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-cloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (10 mg, rendimiento: 90%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1 -cloro-2-fluoro-3-nitrobenceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,59(s, 1 H), 7,83(d, 1H), 7,66(d, 1 H), 7,61 (d, 1 H), 3,59(m, 1H), 3,00(m, 2H), 2,30(m, 2H), 2,16(m, 2H), 2,03(m, 1 H), 1,83(m, 2H), 1,55(m, 1H)
Ejemplo 13: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-metil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (14 mg, rendimiento: 85%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 2-fluoro-4-metil-1-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,42(s, 1H), 7,83(s, 1H), 7,73(d, 1H), 7,52(d, 1H), 4,59(m, 2H), 3,57(m, 1H), 2,95(m, 2H), 2,59(s, 3H), 2,24(m, 2H), 2,11 (m, 2H), 2,01 (m, 1 H), 1,74(m, 2H), 1,54(m, 1 H)
Ejemplo 14: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-metil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (12 mg, rendimiento: 82%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1-fluoro-4-metil-2-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 5 9,41(s, 1H), 7,89(d, 1H), 7,65(d, 1H), 7,52(m, 1H), 4,56(m, 2H), 3,36(m, 2H), 2,95(m, 2H), 2,66(s, 3H), 2,24(m, 2H), 2,07(m 3H), 1,95(m, 2H), 1,72(m, 1 H)
Ejemplo 15: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-(trifluorometil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (17 mg, rendimiento: 92%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 2-fluoro-1 -nitro-4-(trifluorometil)benceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,62(s, 1H), 8,45(s, 1H), 8,06(d, 1H), 7,95(d, 1H), 4,67(m, 2H), 3,62(m, 1H), 2,98(m, 2H), 2,22(m, 2H), 2,08(m, 2H), 2,01 (m, 1 H), 1,71 (m, 2H), 1,54(m, 1H)
Ejemplo 16: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-(trifluorometil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 89%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 2-fluoro-1 -nitro-3-(trifluorometil)benceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,32(m, 1H), 8,35(m, 2H), 7,97(m, 1 H), 5,02(m, 1H), 4,89(m, 1 H), 3,77(m, 1H), 3,59(m, 2H), 3,01 (m, 2H), 2,39(m, 4H), 1,78(m, 3H)
Ejemplo 17: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-(trifluorometoxi)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (14 mg, rendimiento: 87%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 2-fluoro-1-nitro-3-(trifluorometoxi)benceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 5 9,68(s, 1H), 7,87-7,64(m, 3H), 4,81(m, 3H), 3,59(m, 1H), 2,99(m, 2H), 2,24(m, 2H), 2,08(m, 3H), 1,77(m, 2H), 1,56(m, 1 H)
Ejemplo 18: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-(pirrolidin-1-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
Etapa 18-1: Preparación de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo
El compuesto del epígrafe (1,7 g, rendimiento: 73%) se obtuvo del mismo modo que en las Etapas 1-1 a 1-9 del Ejemplo 1.
Etapa 18-2: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-(4-(pirrolidin-1-il)-1H-benzo[d]imidazol-1-il)propil)piperidino-1-carboxilato de terc-butilo
El (2R,3S)-2-(3-(4-bromo-1 H-benzo[d]imidazol-1 -il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de tercbutilo (100 mg, 0,2 mmol) obtenido en la Etapa 18-1 se disolvió en N,N-dimetilformamida (2 ml, 0,09 M). Se añadieron a esto pirrolidina (14 mg, 0,2 mmol), 2,2'-bis(difenilfosfino)-1,1 '-binaftilo) (25 mg, 0,04 mmol), acetato de paladio (II) (5 mg, 0,02 mmol) y carbonato de cesio (130 mg, 0,4 mmol), y a continuación se agitaron en un microondas a 100°C durante 30 minutos. Cuando la reacción se completaba, se filtraba con Celite, se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió y se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida. El residuo se purificó mediante cromatografía en columna (hexano:acetato de etilo = 1:5) para dar el compuesto del epígrafe (60 mg, rendimiento: 45%).
Etapa 18-3: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-(pirrolidin-1-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (10 mg, rendimiento: 90%) se obtuvo del mismo modo que en la Etapa 1-9 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,32(s, 1H), 7,45(t, 1H), 7,17(d, 1H), 6,76(d, 1H), 4,52(t, 2H), 3,64(m, 3H), 3,57(m, 1H), 3,48(m, 1 H), 2,92(m, 2H), 2,27(m, 1 H), 2,18(m, 4H), 2,11 (m, 2H), 2,02(m, 1 H), 1,72(m, 2H), 1,55(m, 1H)
Ejemplo 19: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-(piperidin-1-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 96%) se obtuvo del mismo modo que en el Ejemplo 18, con la excepción de que se usó piperidina en lugar de pirrolidina en la Etapa 18-2 del Ejemplo 18.
1H RMN (500MHz, MeOD): 59,05(s, 1 H), 7,69(d, 1 H), 7,53(t, 1H), 7,35(d, 1 H), 4,52(t, 2H), 3,50(m, 5H), 3,34(m, 1H), 3,26(m, 1 H), 2,95(m, 2H), 2,25(m, 2H), 2,09(m, 2H), 2,02(m, 4H), 1,75(m,4H), 1,53(m, 1H)
Ejemplo 20: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-(3-fluorofenil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
Etapa 20-1: (2R,3S)-2-(3-(4-bromo-1 H-benzo[d]imidazol-1 -il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo
El compuesto del epígrafe (1,7 g, rendimiento: 73%) se obtuvo del mismo modo que en las Etapas 1-1 a 1-9 del Ejemplo 1.
Etapa 20-2: (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-(4-(3-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidino-1 -carboxilato de terc-butilo
El (2R,3S)-2-(3-(4-bromo-1 H-benzo[d]imidazol-1 -il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de tercbutilo (100 mg, 0,2 mmol) obtenido en la Etapa 20-1 se disolvió en N,N-dimetilformamida (2 ml, 0,09 M). Se añadieron a esto ácido (3-fluorofenil)borónico (22 mg, 0,2 mmol), tetraquis(trifenilfosfina)paladio(0) (23 mg, 0,04 mmol) y carbonato sódico 2 N (0,3 ml, 0,76 mmol), y se agitaron en un microondas a 130°C durante 45 minutos. Cuando la reacción se completaba, se filtraba con Celite, se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió y se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida. El residuo se purificó mediante cromatografía en columna (hexano:acetato de etilo = 1:5) para dar el compuesto del epígrafe (60 mg, rendimiento: 45%).
Etapa 20-3: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-(3-fluorofenil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (19 mg, rendimiento: 91%) se obtuvo del mismo modo que en la Etapa 1-9 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,57(d, 1H), 8,03(d, 1H), 7,77(t, 1H), 7,72(d, 1H), 7,62(m, 1H), 7,49(d, 1H), 7,45(m, 1 H), 7,29(t, 1H), 4,66(t, 2H), 3,57(m, 1H), 2,97(m, 2H), 2,25(m, 2H), 2,14(m, 2H), 2,02(m, 1H), 1,75(m, 2H), 1,55(m, 1H)
Ejemplo 21: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-(3-clorofenil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (18 mg, rendimiento: 89%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó ácido (3-clorofenil)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,63(s, 1H), 8,07(d, 1H), 7,79(t, 1H), 7,71 (m, 2H), 7,58(m, 3H), 4,67(t, 2H), 3,60(m, 1H), 2,97(m, 2H), 2,28(m, 2H) 2,10(m, 2H), 2,02(m, 1H), 1,85(m, 2H), 1,55(m, 1H)
Ejemplo 22: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-(3-fluorofenil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (7 mg, rendimiento: 26%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(5-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,56(s, 1H), 8,11(m, 2H), 7,98(m, 1H), 7,54(m, 2H), 7,20(m, 1H), 7,16(m,1H), 4,67(m, 2H), 3,61(m, 2H), 3,03(m, 2H), 2,30(m, 2H), 2,12(m, 2H), 1,98(m, 1H), 1,78(m, 2H), 1,59(m, 1H)
Ejemplo 23: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-(2-fluorofenil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (13 mg, rendimiento: 34%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(6-bromo-1 H-benzo[d]imidazol-1 -il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (2-fluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 57,98(s, 1H), 7,88(m, 1H), 7,71(m, 1H), 7,59(m, 1H), 7,44(m, 1H), 7,32(m, 1H), 7,25(m, 1H), 4,58(m, 2H), 3,55(m, 1H), 2,94(m, 2H), 2,19(m, 2H), 2,06(m, 2H), 2,00(m, 1H), 1,70(m, 2H), 1,53(m, 1H)
Ejemplo 24: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-(3-fluorofenil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (11 mg, rendimiento: 30%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(6-bromo-1 H-benzo[d]imidazol-1 -il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,27(s, 1H), 8,18(m, 1H), 7,91(m, 2H), 7,58(m, 1H), 7,52(m, 2H), 7,17(t, 1H), 4,65(m, 2H), 3,57(m, 1 H), 2,96(m, 2H), 2,23(m, 2H), 2,08(m, 2H), 2,00(m, 1H), 1,73(m, 2H), 1,57(m, 1 H)
Ejemplo 25: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-(4-fluorofenil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (8 mg, rendimiento: 28%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(6-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (4-fluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 5 7,97(s, 1H), 7,83-7,74(m, 4H), 7,23(m, 2H), 4,55(m, 2H), 3,54(m, 1H), 2,94(m, 2H), 2,20(m, 2H), 2,05(m, 2H), 2,00(m, 1 H), 1,69(m, 2H), 1,53(m, 1H)
Ejemplo 26: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-(2-fluorofenil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (11 mg, rendimiento: 30%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-1 H-benzo[d]imidazol-1 -il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (2-fluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,50(s, 1 H), 7,94(d, 1H), 7,75(t, 1H), 7,62(m, 1 H), 7,57(m, 1 H), 7,53(d, 1H), 7,43(m, 1H), 7,38(t, 1H), 4,27(m, 1H), 4,09(m, 1H), 3,42(m, 1H), 3,16(m, 1H), 2,90(m, 1 H), 2,73(m, 1 H), 1,97(m, 2H), 1,77-1,62(m, 3H), 1,47(m, 2H), 1,27(m, 1H)
Ejemplo 27: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-(3-fluorofenil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (7 mg, rendimiento: 28%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,49(s, 1 H), 7,91 (d, 1H), 7,72(t, 1H), 7,59(m, 1 H), 7,50(d, 1H), 7,36(m, 3H), 4,17(m, 2H), 3,37(m, 1H), 3,16(m, 1H), 2,90(m, 1H), 2,73(m, 1H), 1,96(m, 2H), 1,67(m, 3H), 1,50(m, 2H), 1,32(m, 1H)
Ejemplo 28: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-(4-fluorofenil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (13 mg, rendimiento: 32%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-1 H-benzo[d]imidazol-1 -il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (4-fluorofenil)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,48(s, 1H), 7,89(d, 1H), 7,68(t, 1H), 7,54(m, 2H), 7,50(d, 1H), 7,33(t, 2H), 4,14(m, 2H), 3,42(m, 1H), 3,16(m, 1H), 2,90(m, 1 H), 2,72(m, 1H), 1,97(m, 2H), 1,72(m, 3H), 1,50(m, 2H), 1,31 (m, 1 H)
Ejemplo 29: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-(1H-pirazol-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (7 mg, rendimiento: 19%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(6-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1 H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,53(s, 1H), 8,32(s, 1H), 8,07(m, 1H), 7,70(m, 2H), 7,58(m, 1H), 4,63(m, 2H), 3,60(m, 1H), 3,00(m, 2H), 2,30(m, 2H), 2,14(m, 2H), 2,05(m, 1 H), 1,78(m,2H), 1,55(m, 1 H)
Ejemplo 30: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-(1H-pirazol-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (6 mg, rendimiento: 15%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(6-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc
butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1 H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,52(s, 1H), 8,48(s, 1H), 8,03(d, 1H), 7,87(d, 1H), 7,68(m, 1H), 7,58(m, 1H), 4,66(m, 2H), 3,60(m, 1 H), 2,97(m, 2H), 2,31(m, 2H), 2,14(m, 2H), 2,00(m, 1H), 1,77(m, 2H), 1,54(m, 1H)
Ejemplo 31: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-(1H-pirazol-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (5 mg, rendimiento: 12%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1 H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,55(s, 1H), 7,99(s, 1 H), 7,87(d, 1H), 7,69(t, 1H), 7,51 (d, 1 H), 4,35(m, 2H), 3,50(m, 2H), 3,21 (m, 1 H), 2,97(m, 1 H), 2,77(m, 1 H), 2,01 (m, 2H), 1,76(m, 2H), 1,70(m, 2H), 1,55(m, 1 H), 1,45(m, 1H) Ejemplo 32: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-cloro-5-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 83%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1-cloro-2,5-difluoro-4-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H-RMN (500 MHz, MeOD) : 59,55 (s, 1 H), 8,33 (d, 1 H), 7,82 (d, 1 H), 4,58 (td, 2H), 3,59 (m, 2H), 2,98 (m, 2H), 2,23 (m, 2H), 2,08 (m, 2H), 1,98 (m, 1 H), 1,77 (m, 2H), 1,76 (m, 1H)
Ejemplo 33: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-bromo-5-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 81%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1-bromo-2,5-difluoro-4-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H-RMN (500 MHz, MeOD): 59,55 (s, 1H), 8,46 (d, 1 H), 7,79 (d, 1 H), 4,59 (t, 2H), 3,59 (m, 1 H), 2,97 (m, 2H), 2,22 (m, 2H), 2,08 (m, 2H), 1,97 (m, 1H), 1,76 (m, 2H), 1,56 (m, 1 H)
Ejemplo 34: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-6-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (20 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1-cloro-2,4-difluoro-5-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H-RMN (500 MHz, MeOD) : 59,55 (s, 1H), 8,09 (d, 1 H), 8,06 (d, 1H), 4,58 (t, 2H), 3,60 (m, 2H), 2,98 (m, 2H), 2,21 (m, 2H), 2,09 (m, 2H), 1,97 (m, 1H), 1,76 (m, 2H), 1,56 (m, 1H)
Ejemplo 35: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-bromo-6-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (22 mg, rendimiento: 83%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1-bromo-2,4-difluoro-5-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H-RMN (500 MHz, MeOD) : 59,58 (s, 1H), 8,19 (d, 1H), 8,07 (d, 1H), 4,58 (t, 2H), 3,59 (m, 2H), 2,98 (m, 2H), 2,22 (m, 2H), 2,08 (m, 2H), 1,96 (m, 1H), 1,76 (m, 2H), 1,56 (m, 1H)
Ejemplo 36: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (22 mg, rendimiento: 83%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1-bromo-2-cloro-5-fluoro-4-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H-RMN (500 MHz, MeOD) : 59,54 (s, 1 H), 8,51 (s, 1 H), 8,10 (s, 1 H), 4,58 (t, 2H), 3,66 (m, 2H), 2,98 (m, 2H), 2,23 (m, 2H), 2,08 (m, 2H), 1,97 (m, 1 H), 1,76 (m, 2H), 1,56 (m, 1 H)
Ejemplo 37: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-cloro-5-metoxi-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (18 mg, rendimiento: 81 %) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1 -cloro-5-fluoro-2-metoxi-4-nitrobenceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H-RMN (500 MHz, MeOD) : 59,44 (s, 1H), 8,17 (s, 1H), 7,45 (s, 1H), 4,56 (t, 2H), 4,02 (s, 3H), 3,58 (t, 1H), 2,98 (m, 2H), 2,21 (m, 2H), 2,05 (m, 2H), 1,97 (m, 1 H), 1,76 (m, 2H), 1,54 (m, 1 H)
Ejemplo 38: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-fluoro-5-metoxi-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (18 mg, rendimiento: 81%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1,5-difluoro-2-metoxi-4-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H-RMN (500 MHz, MeOD) : 59,45 (s, 1H), 7,92 (d, 1H), 7,48 (d, 1 H), 4,55 (t, 2H), 4,00 (s, 3H), 3,58 (m, 2H), 2,99 (m, 2H), 2,22 (m, 2H), 2,06 (m, 2H), 1,97 (m, 1 H), 1,77 (m, 2H)
Ejemplo 39: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-fluoro-6-metil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 79%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1,4-difluoro-2-metil-5-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H-RMN (500 MHz, MeOD) : 59,49 (s, 1H), 7,96 (d, 2H), 7,58 (d, 1 H), 4,59 (t, 2H), 3,59 (m, 1H), 3,00 (m, 2H), 2,50 (s, 3H), 2,22 (m, 2H), 2,08 (m, 2H), 1,97 (m, 1 H), 1,77 (m, 2H), 1,56 (m, 1 H)
Ejemplo 40: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4,5-dicloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (26 mg, rendimiento: 81%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1,2-dicloro-4-fluoro-3-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H-RMN (500 MHz, MeOD): 59,67 (s, 1H). 8,02 (d, 1H), 7,82 (d, 1H), 4,62 (m, 2H), 3,60 (m, 1H), 3,28 (m, 1H), 2,99 (m, 2H), 2,25 (m, 2H), 2,08 (m, 2H), 1,99 (m, 1 H), 1,78 (m, 2H), 1,54 (m, 1H)
Ejemplo 41: Preparación de dihidrocloruro de (2S,3S)-2-(3-(4,5-dicloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (19 mg, rendimiento: 85%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó (2S,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-hidroxipropil)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-hidroxipropil)piperidino-1 -carboxilato de terc-butilo en la Etapa 1-5 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,58(d, 1 H), 7,97(d, 1H), 7,81 (d, 1 H), 4,59(m, 2H), 4,02(s, 1H), 3,27(s, 1H), 3,20(m, 1 H), 3,00(t, 1H), 2,18-2,05(m, 3H), 1,94(m, 1H), 1,87(m, 1H), 1,72-1,67(m, 3H)
Ejemplo 42: Preparación de dihidrocloruro de (2S,3R)-2-(3-(4,5-dicloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (33 mg, rendimiento: 84%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó (2S,3R)-3-((terc-butildimetilsilil)oxi)-2-(3-hidroxipropil)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-hidroxipropil)piperidino-1 -carboxilato de terc-butilo en la Etapa 1-5 del Ejemplo 1.
1H RMN (500MHz, MeOD): 5 9,64(d, 1H), 8,00(dd, 1H), 7,82(d, 1H), 4,61(m, 2H), 3,59(m, 1H), 3,27(s, 1H), 3,02-2,93(m, 2H), 2,29-2,18(m, 2H), 2,07(m, 2H), 1,99(m, 1H), 1,58(m, 2H), 1,51(m, 1H)
Ejemplo 43: Preparación de dihidrocloruro de (2R,3R)-2-(3-(4,5-dicloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (23 mg, rendimiento: 85%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó (2R,3R)-3-((terc-butildimetilsilil)oxi)-2-(3-hidroxipropil)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-hidroxipropil)piperidino-1 -carboxilato de terc-butilo en la Etapa 1-5 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,66(d, 1H), 7,97(d, 1H), 7,83(d, 1H), 4,60(t, 2H), 4,01(s, 1H), 3,27(s, 1H), 3,20(t, 1H), 3,00(t, 1H), 2,20-2,05(m, 3H), 1,94(m, 1H), 1,88(m, 1 H), 1,73-1,66(m, 3H)
Ejemplo 44: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-cloro-5-metil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 2-cloro-4-fluoro-1-metil-3-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H-RMN (500 MHz, MeOD): 5961 (s, 1 H), 7,88 (d, 1 H), 7,62 (d, 1H), 4,60 (t, 2H), 3,58 (m, 2H), 2,97 (m, 2H), 2,58 (s, 3H), 2,23 (m, 2H), 2,06 (m, 2H), 1,96 (m, 1 H), 1,76 (m, 2H), 1,54 (m, 1 H)
Ejemplo 45: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-bromo-4-metil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
Etapa 45-1: Preparación de (2R,3S)-2-(3-(5-bromo-4-metil-1H-benzo[d]imidazol-1-il)propil)-3-(tercbutildimetilsilil)oxi)piperidin-1 -carboxilato de te rc-butilo
El (2R,3S)-2-(3-bromopropil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo (40 mg, 0,09 mmol) obtenido a partir de la Etapa 1 -5 del Ejemplo 1 se disolvió en N,N-dimetilformamida (2 ml, 0,05 M). A continuación, se añadieron a esto carbonato potásico (25 mg, 0,18 mmol) y 5-bromo-4-metil-1 H-benzo[d]imidazol (18 mg, 0,09 mmol), y la mezcla se agitó a temperatura ambiente durante 4 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato sódico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (hexano:acetato de etilo = 1:1) para dar el compuesto del epígrafe (43 mg, rendimiento: 85%).
Etapa 45-2: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-bromo-4-metil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El (2R,3S)-2-(3-(5-bromo-4-metil-1 H-benzo[d]imidazol-1 -il)propil)-3-(terc-butildimetilsilil)oxi)piperidin-1 -carboxilato de terc-butilo (43 mg, 0,08 mmol) obtenido a partir de la Etapa 45-1 se disolvió en una pequeña cantidad de tetrahidrofurano. A continuación, se añadió solución en dioxano de cloruro de hidrógeno 4 N (2,0 ml, 0,04 M), y la mezcla se agitó a temperatura ambiente durante 12 horas. Cuando la reacción se completaba, la solución de reacción se concentraba bajo presión reducida para retirar el disolvente, se disolvía mediante la adición de una pequeña cantidad de metanol, y a continuación se cristalizaba con éter dietílico para obtener el compuesto del epígrafe (27 mg, rendimiento: 85%).
1H-RMN (500 MHz, DMSO-d6): ó 9,19 (s, 1 H), 7,82 (d, 1H), 7,76 (s, 1 H), 4,47 (m, 2H), 3,38 (m, 1 H), 3,09 (d, 1 H), 2,81 (m, 2H), 2,65 (s, 3H), 2,19 (m, 1 H), 2,10 (m, 1 H), 1,88 (m, 2H), 1,75 (m, 1H), 1,72 (m, 1H), 1,58 (m, 1 H), 1,37 (m, 1H)
Ejemplo 46: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-4-metil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (30 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-cloro-4-metil-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,53 (s, 1H), 7,83 (d, 1 H), 7,69 (d, 1H), 4,58 (t, 2H), 3,58 (m, 1 H), 3,28 (m, 1H), 2,96 (m, 2H), 2,70 (s, 3H), 2,22 (m, 2H), 2,05 (m, 2H), 2,00 (m, 1H), 1,75 (m, 2H), 1,55 (m, 1 H)
Ejemplo 47: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-bromo-4-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (10 mg, rendimiento: 40%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-bromo-4-fluoro-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,47 (s, 1H), 7,84 (dd, 1H), 7,79 (d, 1H), 4,60 (m, 2H), 3,59 (m, 1 H), 3,27 (m, 1H), 2,99 (m, 2H), 2,20 (m, 2H), 2,07 (m, 2H), 1,98 (m, 1 H), 1,75 (m, 2H), 1,56 (m, 1H)
Ejemplo 48: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-bromo-7-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (11 mg, rendimiento: 43%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-bromo-7-fluoro-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,53 (S, 1H), 7,85 (dd, 1H), 7,64 (d, 1H), 4,67 (m, 2H), 3,59 (m, 1H), 3,27 (m, 1H), 2,98 (m, 2H), 2,23 (m, 2H), 2,09 (m, 2H), 1,98 (m, 1 H), 1,77 (m, 2H), 1,54 (m, 1H)
Ejemplo 49: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4,5-difluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (9 mg, rendimiento: 39%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 4,5-difluoro-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, DMSO-d6): 58,58 (s, 1 H), 7,58 (dd, 1 H), 7,40 (dd, 1H), 4,33 (m, 2H), 3,38 (m, 1 H), 3,09 (d, 1H), 2,98 (m, 2H), 2,10 (m, 1H), 1,96 (m, 1H), 1,87 (m, 2H), 1,77 (m, 1H), 1,65 (m, 1H), 1,54 (m, 1H), 1,36 (m, 1H)
Ejemplo 50: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6,7-difluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (10 mg, rendimiento: 41%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6,7-difluoro-1H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, DMSO-d6): 58,94 (s, 1 H), 7,59 (dd, 1 H), 7,44 (dd, 1H), 4,44 (m, 2H), 3,41 (m, 1 H), 3,09 (d, 1H), 2,78 (m, 2H), 2,13 (m, 1H), 2,03 (m, 1 H), 1,89 (m, 2H), 1,76 (d, 1 H), 1,66 (m, 1H), 1,57 (m, 1H), 1,35 (m, 1H)
Ejemplo 51: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4,5-dimetil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (30 mg, rendimiento: 86%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 4,5-dimetil-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,48 (s, 1H), 7,71 (d, 1 H), 7,51 (d, 1H), 4,57 (t, 2H), 3,58 (m, 1 H), 3,27 (m, 1H), 2,98 (m, 2H), 2,56 (s, 3H), 2,48 (s, 3H), 2,23 (m, 2H), 2,06 (m, 2H), 1,98 (m, 1 H), 1,76 (m, 2H), 1,55 (m, 1 H)
Ejemplo 52: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5,6-difluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (32 mg, rendimiento: 84%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5,6-difluoro-1H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,58 (s, 1H), 8,17 (dd, 1H), 7,88 (dd, 1H), 4,59 (t, 2H), 3,59 (m, 1H), 3,28 (m, 1H), 2,99 (m, 2H), 2,23 (m, 2H), 2,08 (m, 2H), 1,97 (m, 1H), 1,77 (m, 2H), 1,56 (m, 1H)
Ejemplo 53: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5,6-dicloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (37 mg, rendimiento: 85%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5,6-dicloro-1H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, DMSO-d6): 59,10 (s, 1H), 8,08 (s, 1H), 4,39 (m, 2H), 3,41 (m, 1H), 3,10 (m, 1H), 2,80 (m, 2H), 2,11 (m, 1H), 2,01 (m, 1 H), 1,90 (m, 2H), 1,77 (m, 1 H), 1,67 (m, 1H), 1,57 (m, 1H), 1,35 (m, 1 H)
Ejemplo 54: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5,6-dibromo-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (31 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5,6-dibromo-1H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, DMSO-d6): 58,93 (s, 1H), 8,38 (s, 1H), 8,17 (2, 1H), 4,37 (m, 2H), 3,40 (m, 1H), 3,10(d, 1H), 2,79 (m, 2H), 2,07 (m, 1H), 1,99 (m, 1H), 1,89 (m, 2H), 1,77 (d, 1H), 1,65 (m, 1 H), 1,53 (m, 1 H), 1,35 (m, 1H)
Ejemplo 55: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5,6-dimetil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (36 mg, rendimiento: 85%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5,6-dimetil-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,38 (s, 1H), 7,80 (s, 1H), 7,62 (s, 1H), 4,59 (m, 2H), 3,59 (m, 1H), 3,27 (m, 1H), 2,99 (m, 2H), 2,51 (s, 3H), 2,49 (s, 3H), 2,24 (m, 2H), 2,08 (m, 2H), 1,97 (m, 1 H), 1,77 (m, 2H), 1,56 (m, 1H)
Ejemplo 56: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6,7-dicloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 30%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6,7-dicloro-1H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,43 (s, 1H), 7,80 (s, 2H), 4,83 (m, 2H), 3,58 (t, 1H), 3,28 (m, 1H), 2,99 (m, 2H), 2,21 (m, 2H), 2,10 (m, 2H), 2,09 (m, 1H), 1,77 (m, 2H), 1,76 (m, 1H)
Ejemplo 57: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4,6-difluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (26 mg, rendimiento: 92%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 4,6-difluoro-1H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 59,56(s, 1 H), 7,76(d, 1 H), 7,39(t, 1H), 4,57(m, 2H), 3,62(m, 1 H), 2,99(m, 2H), 2,68(m, 1 H), 2,28(m, 2H), 2,12(m, 2H), 2,05(m, 1 H), 1,80(m, 2H), 1,55(m, 1H)
Ejemplo 58: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5,7-difluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 90%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 4,6-difluoro-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 59,60(d, 1H), 7,51 (d, 1H), 7,42(t, 1 H), 4,66(m, 2H), 3,58(m, 1H), 2,98(m, 2H), 2,30(m, 2H), 2,12(m, 2H), 2,02(m, 1H), 1,74(m, 2H), 1,54(m, 1H)
Ejemplo 59: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-cloro-5-metoxi-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (23 mg, rendimiento: 91%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 4-cloro-5-metoxi-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 59,55(s, 1H), 7,97(d, 1 H), 7,52(d, 1 H), 4,59(t, 2H), 4,04(s, 3H), 3,57(m, 1 H), 2,99(m, 2H), 2,31 (m, 2H), 2,10(m, 2H), 2,02(m, 1 H), 1,79(m, 2H), 1,55(m, 1 H)
Ejemplo 60: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-cloro-6-metoxi-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (22 mg, rendimiento: 90%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 4-cloro-5-metoxi-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 59,48(s, 1H), 7,79(d, 1 H), 7,52(d, 1H), 4,82(m, 2H), 4,03(s, 3H), 3,62(m, 1 H), 2,99(m, 2H), 2,30(m, 2H), 2,14(m, 2H), 2,02(m, 1 H), 1,80(m, 2H), 1,55(m, 1H)
Ejemplo 61: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-cloro-4-metil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (24 mg, rendimiento: 91%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-cloro-4-metil-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 59,59(s, 1H), 7,97(s, 1 H), 7,52(s, 1 H), 4,58(m, 2H), 3,59(m, 1H), 2,97(m, 2H), 2,67(s, 3H), 2,20(m, 2H), 2,10(m, 2H), 2,01(m, 1H), 1,76(m, 2H), 1,55(m, 1H)
Ejemplo 62: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-cloro-5-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (19 mg, rendimiento: 89%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 4-cloro-5-fluoro-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 59,54(s, 1 H), 7,95(d, 1H), 7,50(d, 1 H), 4,58(t, 2H), 3,56(m, 1H), 3,42(m, 1H), 2,98(m, 2H), 2,30(m, 2H), 2,08(m, 2H), 2,00(m, 1 H), 1,72(m, 2H), 1,52(m, 1H)
Ejemplo 63: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-bromo-4-metil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (26 mg, rendimiento: 93%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-bromo-4-metil-1H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 59,58(s, 1H), 8,12(s, 1 H), 7,66(s, 1 H), 4,57(m, 2H), 3,60(m, 1H), 2,99(m, 2H), 2,65(s, 3H), 2,24(m, 2H), 210(m, 2H), 2,02(m, 1H), 1,79(m, 2H), 1,59(m, 1H)
Ejemplo 64: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-fluoro-4-metil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (22 mg, rendimiento: 90%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-fluoro-4-metil-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 59,62(s, 1H), 7,88(dd, 1H), 7,46(t, 1H), 4,61(m, 2H), 3,58(m, 1H), 2,99(m, 2H), 2,59(s, 3H), 2,25(m, 2H), 2,12(m 2H), 2,01(m, 1H), 1,79(m, 2H), 1,59(m, 1H)
Ejemplo 65: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-fluoro-7-metil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (20 mg, rendimiento: 88%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-fluoro-4-metil-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 59,50(s, 1H), 7,69(dd, 1H), 7,46(t, 1H), 4,76(m, 2H), 3,61(m, 1H), 3,00(m, 2H), 2,77(s, 3H), 2,25(m, 2H), 2,13(m, 2H), 2,02(m, 1H), 1,79(m, 2H), 1,57(m, 1H)
Ejemplo 66: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-cloro-5-(trifluorometil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (27 mg, rendimiento: 95%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 4-cloro-5-(trifluorometil)-1H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 5 9,65(s, 1H), 8,13(d, 1H), 8,01(d, 1H), 4,64(m, 2H), 3,61(m, 2H), 2,98(m, 2H), 2,26(m, 2H), 2,10(m, 2H), 1,98(m, 1H), 1,76(m, 2H), 1,56(m, 1H)
Ejemplo 67: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-cloro-6-(trifluorometil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (23 mg, rendimiento: 91%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 4-cloro-5-(trifluorometil)-1H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 5 9,59(s, 1H), 8,01(d, 1H), 7,96(d, 1H), 4,91(m, 2H), 3,61(m, 1H), 2,98(m, 2H), 2,27(m, 2H), 2,10(m, 2H), 2,01(m, 1H), 1,80(m, 2H), 1,56(m, 1H)
Ejemplo 68: dihidrocloruro de 7-bromo-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-benzo[d]imidazol-5-carboxilato de metilo
El compuesto del epígrafe (22 mg, rendimiento: 89%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 3-bromo-4-fluoro-5-nitrobenzoato de metilo en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 58,85(s, 1 H),8,38(s, 1 H), 8,27(s, 1H), 4,75(m, 2H), 3,96(s, 3H), 3,57(m, 1 H), 2,98(m, 2H), 2,25-1,98(m, 5H), 1,72(m, 2H), 1,54(m, 1H)
Ejemplo 69: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (24 mg, rendimiento: 90%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1 -bromo-5-cloro-2-fluoro-3-nitrobenceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,28(s, 1H), 7,87(m, 2H), 4,77(m, 2H), 3,59(m, 1H), 2,93(m, 2H), 2,18(m, 2H), 2,08(m, 2H), 2,02(m, 1H), 1,75(m, 2H), 1,55(m, 1H)
Ejemplo 70: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-bromo-7-cloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (23 mg, rendimiento: 89%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 5-bromo-1 -cloro-2-fluoro-3-nitrobenceno en lugar de 4-cloro-2-fluoro-1 -nitrobenceno en la Etapa 1 -8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,35(s, 1H), 8,00(s, 1H), 7,84(s, 1 H), 4,78(m, 2H), 3,58(m, 1H), 2,97(m, 2H), 2,21 (m, 2H), 2,08(m, 2H), 1,99(m, 1 H), 1,74(m, 2H), 1,53(m, 1H)
Ejemplo 71: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-bromo-5-(trifluorometil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (19 mg, rendimiento: 89%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1-bromo-2-fluoro-3-nitro-5-(trifluorometil)benceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,26(s, 1H), 8,11 (s, 1H), 8,02(s, 1 H), 3,55(m, 1 H), 2,90(m, 2H), 2,18(m, 2H), 2,05(m, 2H), 1,94(m, 1 H), 1,71 (m, 2H), 1,52(m, 1 H)
Ejemplo 72: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-bromo-4-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (23 mg, rendimiento: 90%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-bromo-4-fluoro-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 59,44(s, 1H), 8,12(s, 1H), 7,65(d, 1H), 4,55(m, 2H), 3,65(m, 1H), 3,57(m, 1H), 2,98(m, 2H), 2,26(m, 2H), 2,10(m, 2H), 1,98(m, 1 H), 1,74(m, 2H), 1,54(m, 1H)
Ejemplo 73: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-bromo-7-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (24 mg, rendimiento: 92%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-bromo-4-fluoro-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.1
1H RMN (500MHz, MeOD): 59,55(s, 1H), 7,92(s, 1H), 7,69(d, 1H), 4,65(m, 2H), 3,61(m, 1H), 2,96(m, 2H), 2,15(m, 2H), 2,07(m, 2H), 1,98(m, 1 H), 1,75(m, 2H), 1,53(m, 1 H)
Ejemplo 74: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-cloro-4-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (9 mg, rendimiento: 45%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 7-cloro-4-fluoro-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45 1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 59,43(s, 1H), 7,60(dd, 1H), 7,38(t, 1H), 4,82(m, 2H), 3,54(m, 1H), 2,98(m, 2H), 2,24(m, 2H), 2,16(m, 2H), 1,99(m, 1 H), 1,72(m, 2H), 1,55(m, 1 H)
Ejemplo 75: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-bromo-4-nitro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (23 mg, rendimiento: 90%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-bromo-4-nitro-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 5 8,81(s, 1H), 7,95(d, 1H), 7,82(d, 1H), 4,51(m, 2H), 3,53(m, 1H), 2,92(m, 2H), 2,10(m, 2H), 2,04(m, 3H), 1,68(m, 2H), 1,57(m, 1 H)
Ejemplo 76: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-bromo-7-nitro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (18 mg, rendimiento: 87%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-bromo-4-nitro-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 58,51 (s, 1 H), 7,84(d, 1H), 7,68(d, 1H), 4,24(t, 1H), 3,52(m, 1H), 2,97(m, 2H), 2,00(m, 5H), 1,73(m, 1 H), 1,63(m, 1 H), 1,53(m, 1 H)
Ejemplo 77: Preparación de dihidrocloruro de (2R,3S)-2-(3-(4-cloro-5-nitro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (23 mg, rendimiento: 92%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 4-cloro-5-nitro-1 H-benzo[d]imidazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.1
1H RMN (500MHz, MeOD): 5 8,76(s, 1H), 8,06(d, 1H), 7,86(d, 1H), 4,51(m, 2H), 3,66(m, 1H), 2,98(m, 2H), 2,08(m, 2H), 1,99(m 3H), 1,74(m, 3H), 1,56(m, 1H)
Ejemplo 78: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-cloro-5-(trifluorometil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (19 mg, rendimiento: 87%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1-cloro-2-fluoro-3-nitro-5-(trifluorometil)benceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 5 9,32(m, 1H), 8,07(d, 1H), 7,83(d, 1H), 4,78(s, 1H), 3,58(m, 1H), 3,44(m, 1H), 3,00(m, 1H), 2,93(m, 2H), 2,20-2,05(m, 4H), 2,02(m, 1H), 1,97(m, 2H), 1,52(m, 1 H)
Ejemplo 79: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-fluoro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (22 mg, rendimiento: 88%) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 5-cloro-1,2-difluoro-3-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,39(m, 1H), 7,71(m, 1H), 7,49(m, 1H), 4,59(m, 2H), 3,57(m, 1H), 3,44(m, 1H), 3,29(m, 1H), 2,97(m, 2H), 2,18(m, 2H), 2,07(m, 1 H), 1,72(m, 2H), 1,51 (m, 1H)
Ejemplo 80: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5,7-dicloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (7 mg, rendimiento: 31 %) se obtuvo del mismo modo que en el Ejemplo 1, con la excepción de que se usó 1,5-dicloro-2-fluoro-3-nitrobenceno en lugar de 4-cloro-2-fluoro-1-nitrobenceno en la Etapa 1-8 del Ejemplo 1.
1H RMN (500MHz, MeOD): 59,30(s, 1H), 7,84(s, 1H), 7,69(s, 1 H), 4,78(m, 2H), 3,69(m, 1H), 3,30(m, 1 H), 2,99(m, 2H), 2,25(m, 2H), 2,16(m, 2H), 2,06(m, 1 H), 1,78(m, 2H), 1,51 (m, 1H)
Ejemplo 81: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(1H-pirazol-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (8 mg, rendimiento: 14%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc
butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1 H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,37(s, 1H), 7,97(s, 2H), 7,88(s, 1 H), 7,49(s, 1 H), 4,28(m, 2H), 3,44(m, 1H), 2,91 (m, 1H), 2,75(m, 1H), 1,96(m, 2H), 1,74-1,62(m, 3H), 1,50(m, 1H), 1,36(m, 1H)
Ejemplo 82: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-(1H-pirazol-4-il)-5-(trifluorometil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (9 mg, rendimiento: 15%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-(trifluorometil)-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,06(m, 1 H), 8,10(s, 1 H), 7,97(s, 2H), 7,61 (s, 1 H), 4,26(m, 2H), 3,44(m, 1H), 3,17(m, 1H), 2,93(m, 1H), 2,76(m, 1H), 1,99(m, 2H), 1,67(m, 3H), 1,53(m, 1H), 1,49(m, 1 H)
Ejemplo 83: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(3-fluorofenil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (13 mg, rendimiento: 22%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,39(s, 1H), 7,95(d, 1H), 7,64(m, 1H), 7,62(m, 1H), 7,39(m, 2H), 7,34(m, 1H), 4,15(m, 1H), 4,05(m, 2H), 3,44(m, 1H), 3,18(m, 1H), 2,91 (t, 1H), 2,87(s, 1H), 2,01(m, 2H), 1,96(m, 2H), 1,50(m, 2H), 1,33(m, 1H)
Ejemplo 84: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-(3-fluorofenil)-5-(trifluorometil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (11 mg, rendimiento: 20%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-(trifluorometil)-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,62(s, 1H), 8,24(m, 2H), 7,74(m, 1H), 7,64(m, 1H), 7,42(m, 3H), 4,15(m, 2H), 3,43(m, 1H), 3,21 (m, 1 H), 2,91 (m, 1H), 2,74(m, 1 H), 1,97(m, 2H), 1,73(m, 3H), 1,52(m, 2H), 1,33(m, 1 H)
Ejemplo 85: Preparación de (2R,3S)-2-(3-(5-cloro-7-(2-metiltiazol-5-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (6 mg, rendimiento: 12%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (2-metiltiazol-5-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,68(s, 1H), 8,06(m, 2H), 7,71(s, 1H), 4,30(t, 2H), 3,52(m, 1H), 3,27(m, 1H), 2,95(m, 1H), 2,84(s, 3H), 2,83(s, 1 H), 2,05-1,89(m, 4H), 1,88(m, 2H), 1,74(m, 2H)
Ejemplo 86: Preparación de trihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(piridin-3-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (8 mg, rendimiento: 15%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1 H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido piridin-3-ilborónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,55(s, 1H), 9,16(s, 1H), 9,03(s, 1H), 8,74(s, 1H), 8,18(s, 1H), 8,09(s, 1H), 7,68(s, 1H), 4,10(m, 2H), 3,46(m, 1H), 3,24(m, 1H), 2,92(m, 1 H), 2,78(m, 1 H), 2,03(m, 1H), 1,98(m, 1 H), 1,95-1,93(m, 3H), 1,52(m, 1H), 1,44(m 2H)
Ejemplo 87: Preparación de trihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(5-fluoropiridin-3-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (9 mg, rendimiento: 16%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (5-fluoropiridin-3-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,70(s, 1H), 8,86-8,75(m, 2H), 8,19(m, 1H), 8,07(s, 1 H), 7,67(s, 1H), 4,11 (m, 2H), 3,47(m, 1H), 3,24(m, 1H), 2,93(td, 1 H), 2,77(s, 1H), 2,01 -2,00 (m, 2H), 1,93-1,82(m, 3H), 1,73(s, 1 H), 1,65(m, 1H)
Ejemplo 88: dihidrocloruro de 5-(5-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-benzo[d]imidazol-7-il)-1-metilpiridin-2(1 H)-ona
El compuesto del epígrafe (10 mg, rendimiento: 16%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1-metil-6-oxo-1,6-dihidropiridin-3-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,55(m, 1 H), 7,98(d, 2H), 7,74(d, 1H), 7,57(s, 1H), 6,71 (d, 1H), 4,32(m, 2H), 3,67(s, 3H), 3,44(s, 1H), 3,24(m, 1H), 2,88(t, 1 H), 2,80(s, 1H), 2,03-1,89(m, 4H), 1,71 (m, 2H), 1,49(m, 2H)
Ejemplo 89: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(1-(difluorometil)-1H-pirazol-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (9 mg, rendimiento: 14%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1-(difluorometil)-1H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,46(s, 1 H), 8,50(s, 1 H), 8,05(s, 1H), 7,94(s, H), 7,56(s, 1H), 4,28(m, 2H), 3,49(m, 1H), 3,24(m, 1 H), 2,94(t, 1H), 2,89(m, 1 H), 2,01 (m, 2H), 1,80(m, 2H), 1,72(m, 2H), 1,64(m, 1 H), 1,55(m, 1 H)
Ejemplo 90: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(isoxazol-3-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (7 mg, rendimiento: 12%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido isoxazol-3-ilborónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,53(s, 1H), 8,04(m, 2H), 7,92(s, 1H), 7,69(m, 1H), 4,61(m, 2H), 3,61 (m, 1H), 3,02(m, 2H), 2,28(m, 2H), 2,04(m, 2H), 1,99(m, H), 1,78(m, 2H), 1,52(m, 1 H)
Ejemplo 91: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(tiofen-3-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (24 mg, rendimiento: 3 1%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido tiofen-3-ilborónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,52 (s 1 H), 7,93(s, 1H), 7,73(d, 2H), 7,52(s, 1H), 7,36(d, 1H), 4,22(m, 2H), 3,48(m, 1H), 3,23(m, 1 H), 2,93(t, 1 H), 2,76(m, 1H), 2,02(m, 2H), 1,78-1,63(m, 3H), 1,62(m, 1H), 1,57(m, 1H), 1,55(m, 1 H)
Ejemplo 92: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(2-metiltiofen-3-il)-1H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol
El compuesto del epígrafe (20 mg, rendimiento: 25%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (2-metiltiofen-3-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,56(s, 1H), 7,95(s, 1H), 7,47(d, 2H), 7,15(d, 1H), 4,22(m, 1H), 4,15(m, 1H), 3,50(m, 1H), 3,25(m, 1H), 2,91 (t, 1H), 2,81 (m, 1H), 2,34(d, 3H), 2,01 (m, 2H), 1,99-1,96(m, 3H), 1,79(m, 1H), 1,65(m, 1 H), 1,56(m, 1H)
Ejemplo 93: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(3,5-dimetilisoxazol-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (19 mg, rendimiento: 24%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (3,5-dimetilisoxazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.1
1H RMN(500MHz, MeOD): 59,58(s, 1 H), 8,04(s, 1H), 7,71 (s, 1H), 4,23(m, 2H), 3,61 (m, 1H), 3,01 (m, 1H), 2,97(m, 1H), 2,39(s, 3H), 2,18(s, 3H), 2,17-2,11(m, 3H), 2,04(m, 2H), 1,86(m, 2H), 1,71(m, 2H)
Ejemplo 94: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(3,6-dihidro-2H-piran-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (22 mg, rendimiento: 27%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (3,6-dihidro-2H-piran-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
H RMN (500MHz, MeOD): 5 9,60(s, 1H), 7,85(s, 1H), 7,51(s, 1H), 6,08(s, 1H), 4,60(t, 2H), 4,39(s, 2H), 4,03(t, 2H), 3,61(m, 1 H), 2,99(m,2H), 2,58(s, 2H), 2,12-1,96(m, 5H), 1,72(m, 2H), 1,51(m, 1H)
Ejemplo 95: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-(1-((1,3-dioxolan-2-il)metil)-1H-pirazol-4-il)-5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol
El compuesto del epígrafe (17 mg, rendimiento: 22%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1-((1,3-dioxolan-2-il)metil)-1 H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,62(s, 1H), 8,07(s, 1H), 7,93(s, 1H), 7,82(s, 1 H), 7,53(s, 1H), 4,43(m, 2H), 4,41 (m, 2H), 3,97(m, 2H), 3,56(m, 1H), 3,25(m, 1 H), 2,96(t, 1 H), 2,96(s, 1 H), 2,01 (m, 1H), 1,82-1,65(m, 5H), 1,56(m, 1 H), 1,51 (m, 1H)
Ejemplo 96: Preparación de trihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(1-metil-1H-imidazol-5-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (20 mg, rendimiento: 29%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1-metil-1H-imidazol-5-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.1
1H RMN (500MHz, MeOD): 59,20(s, 1H), 9,12(d, 1H), 8,01(s, 1H), 8,00(s, 1H), 7,68(s, 1H), 4,20(s, 1H), 3,94(s, 1H), 3,78(s, 3H), 3,47(m, 1 H), 2,94(t, 1H), 2,89(m, 1H), 2,06(m, 1H), 1,97(m, 1H), 1,85(m, 2H), 1,83-1,74(m, 3H), 1,53(m, 2H)
Ejemplo 97: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(1-metil-1H-pirazol-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 25%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1-metil-1H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,30(s, 1H), 7,97(s, 1H), 7,87(s, 1H), 7,76(s, 1H), 7,45(s, 1H), 4,32(m, 2H), 4,02(s, 3H), 3,24(m, 1H), 2,92(m, 1H), 2,77(m, 1H), 2,00(m, 2H), 1,71(m, 4H), 1,51(m, 1H), 1,40(m, 1H)
Ejemplo 98: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-(pirrolidin-1-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (12 mg, rendimiento: 20%) se obtuvo del mismo modo que en el Ejemplo 18, con la excepción de que se usó (2R,3 S)-2-(3-(7-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en la Etapa 18-2 del Ejemplo 18.
1H RMN (500MHz, MeOD): 5 9,44(s, 1H), 7,55(m, 3H), 4,76(t, 2H), 3,56(m, 1H), 3,20(m, 4H), 2,94(m, 2H), 2,20(m, 2H), 2,07(m, 5H), 2,00(m, 3H), 1,74(m, 2H), 1,53(m, 1 H)
Ejemplo 99: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(pirrolidin-1-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (13 mg, rendimiento: 21%) se obtuvo del mismo modo que en el Ejemplo 18, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en la Etapa 18-2 del Ejemplo 18.
1H RMN (500MHz, MeOD): 5 9,46(s, 1H), 7,58(d, 1H), 7,47(d, 1H), 4,72(m, 2H), 3,53(m, 1H), 3,21 (m, 4H), 2,94(m, 2H), 2,20(m, 2H), 2,11 (m, 5H), 1,96(m, 2H), 1,77(m, 1 H), 1,63(m, 1 H), 1,52(m, 1H)
Ejemplo 100: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(2-ciclopropiltiazol-5-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (12 mg, rendimiento: 25%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (2-ciclopropiltiazol-5-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,51 (s, 1H), 7,97(s, 1H), 7,73(s, 1 H), 7,70(s, 1H), 4,63(m, 2H), 3,42(m, 1H), 3,22(m, 1 H), 2,93(m, 1H), 2,77(m, 1 H), 2,50(m, 1 H), 1,95(m, 2H), 1,68(m, 4H), 1,50(m, 2H), 1,23(m, 2H), 1,11 (m, 2H)
Ejemplo 101: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(1-(tiazol-2-il)-1H-pirazol-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (17 mg, rendimiento: 30%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1-(tiazol-2-il)-1 H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,41(s, 1H), 8,83(s, 1H), 8,10(s, 1H), 7,95(s, 1H), 7,65(s, 1H), 7,61(s, 1H), 7,47(s, 1H), 4,37(m, 2H), 3,44(m, 1H), 3,18(m, 1H), 2,87(m, 1H), 2,78(m, 1H), 1,92(m, 2H), 1,82(m, 2H), 1,65(m, 2H), 1,43(m, 2H) Ejemplo 102: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(1-(oxetan-3-il)-1H-pirazol-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (12 mg, rendimiento: 23%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1-(oxetan-3-il)-1H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,58(s, 1H), 8,15(s, 1H), 7,92(s, 1H), 7,87(s, 1H), 7,54(s, 1H), 4,68(m, 1H), 4,34(m, 2H), 4,03(m, 2H), 3,50(m, 1 H), 3,22(m, 1 H), 2,92(m, 1 H), 2,85(m, 1 H), 1,95(m, 2H), 1,78(m, 4H), 1,64(m, 1 H), 1,42(m, 1H)
Ejemplo 103: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(2-(tetrahidro-2H-piran-4-il)tiazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol
El compuesto del epígrafe (10 mg, rendimiento: 18%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (2-(tetrahidro-2H-piran-4-il)tiazol-5-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,63(s, 1 H), 7,98(s, 1 H), 7,73(S, 1H), 7,21 (s, 1 H), 4,65(m, 2H), 3,84(m, 4H), 3,62(m, 4H), 3,48(m, 1 H), 3,25(m, 1 H), 2,94(m, 1 H), 2,81 (m, 1H), 1,99(m, 3H), 1,82(m, 4H), 1,54(m, 2H)
Ejemplo 104: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(furan-3-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (9 mg, rendimiento: 15%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido furan-3-ilborónico en lugar de ácido (3 fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,55(s, 1H), 8,05(d, 1 H), 7,93(s, 1H), 7,69(d, 1H), 7,50(m, 1H), 7,32(m, 1H), 4,63(m, 2H), 3,61(m, 1 H), 3,02(m, 1H), 2,94(m, 1H), 2,26(m, 2H), 2,09(m, 2H), 2,01(m, 1H), 1,78(m, 2H), 1,53(m, 1H)
Ejemplo 105: dihidrocloruro de 4-(5-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-benzo[d]imidazol-7-il)tiazol-2-carbonitrilo
El compuesto del epígrafe (14 mg, rendimiento: 20%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (2-cianotiazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,54(s, 1H), 8,29(s, 1 H), 8,02(s, 1H), 7,79(s, 1 H), 4,57(m, 2H), 3,42(m, 1H), 3,20(m, 1H), 2,91 (m, 1 H), 2,76(m, 1H), 1,95(m, 2H), 1,60(m, 4H), 1,52(m, 1H), 1,41(m, 1H)
Ejemplo 106: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-(1-(terc-butil)-1H-pirazol-4-il)-5-cloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (10 mg, rendimiento: 18%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3 -(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1-(terc-butil)-1 H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,52(s, 1H), 8,14(s, 1H), 7,89(s, 1H), 7,80(s, 1H), 7,51(s, 1H), 4,36(m, 2H), 3,48(m, 1H), 3,23(m, 1H), 2,95(m, 1H), 2,82(m, 1 H), 2,01 (m, 2H), 1,81 (m, 2H), 1,73(m, 11H), 1,53(m, 1 H), 1,43(m, 1 H)
Ejemplo 107: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(1-isopentil-1H-pirazol-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (17 mg, rendimiento: 25%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1 -isopentil-1 H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,47(s, 1H), 8,04(s, 1 H), 7,89(s, 1 H), 7,78(s, 1H), 7,50(s, 1 H), 4,32(m, 4H), 3,45(m, 1H), 3,23(m, 1 H), 2,95(m, 1H), 2,78(m, 1 H), 2,00(m, 2H), 1,87(m, 2H), 1,76(m, 2H), 1,64(m, 4H), 1,54(m, 1H), 1,42(m, 1H), 1,02(s, 6H)
Ejemplo 108: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(1-isopropil-1H-pirazol-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 21%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1 -isopropil-1 H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,48(s, 1H), 8,07(s, 1 H), 7,90(s, 1 H), 7,79(s, 1H), 7,52(s, 1 H), 4,70(m, 1 H), 4,30(m, 2H), 3,45(m, 1H), 3,24(m, 1 H), 2,93(m, 1 H), 2,80(m, 1H), 1,99(m, 2H), 1,71 (m, 2H), 1,67(m, 2H), 1,59(s, 6H), 1,53(m, 1H), 1,40(m, 1H)
Ejemplo 109: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(4-metiltiofen-3-il)-1 H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (20 mg, rendimiento: 31%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (4-metiltiofen-3-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,53(s, 1H), 7,95(s, 1 H), 7,63(s, 1H), 7,48(s, 1H), 7,34(s, 1 H), 4,23(m, 1 H), 3,96(m, 1H), 3,51 (m, 1 H), 3,23(m, 1 H), 2,96(m, 1 H), 2,81 (m, 1H), 2,06(d, 3H), 1,99(m, 2H), 1,76(m, 3H), 1,57(m, 2H), 1,42(m, 1H)
Ejemplo 110: dihidrocloruro de 3-(5-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-benzo[d]imidazol-7-il)furano-2-carboxilato de etilo
El compuesto del epígrafe (10 mg, rendimiento: 21%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (2-(etoxicarbonil)furan-3-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,53(s, 1H), 8,00(s, 1 H), 7,97(s, 1H), 7,55(s, 1H), 6,96(s, 1 H), 4,29(m, 1 H), 4,15(m, 3H), 3,47(m, 1 H), 3,24(m, 2H), 2,94(m, 1 H), 2,79(m, 1H), 1,97(m, 3H), 1,84(m, 2H), 1,72(m, 2H), 1,53(m, 2H), 1,08(t, 3H)
Ejemplo 111: dihidrocloruro de 4-(5-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-benzo[d]imidazol-7-il)tiofeno-2-carboxilato de metilo
El compuesto del epígrafe (9 mg, rendimiento: 19%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (5-(metoxicarbonil)tiofen-3-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.1
1H RMN (500MHz, MeOD): 59,54(s, 1H), 8,05(d, 2H), 7,97(s, 1H), 7,57(s, 1 H), 4,80(m, 1H), 4,22(m, 2H), 3,93(s, 3H), 3,43(m, 1 H), 3,22(m, 2H), 2,93(m, 1 H), 2,78(m, 1H), 2,01 (m, 2H), 1,78(m, 3H), 1,63(m, 1 H), 1,53(m, 1H), 1,41 (m, 1 H)
Ejemplo 112: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(1-(2-fluoroetil)-1H-pirazol-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 29%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1-(2-fluoroetil)-1H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,53(s, 1H), 8,09(s, 1 H), 7,91 (s, 1H), 7,85(s, 1H), 7,53(s, 1 H), 4,92(m, 1 H), 4,64(m, 1H), 4,56(m, 1H), 4,32(m, 2H), 3,49(m, 1 H), 3,23(m, 1 H), 2,94(m, 1 H), 2,80(m, 1H), 1,96(m, 3H), 1,74(m, 4H), 1,54(m, 1H), 1,47(m, 1 H)
Ejemplo 113: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-(1-butil-1H-pirazol-4-il)-5-cloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (18 mg, rendimiento: 34%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1 -butil-1 H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,43(s, 1H), 8,02(S, 1H), 7,89(s, 1 H), 7,79(s, 1 H), 7,50(s, 1 H), 4,30(m, 3H), 3,45(m, 1 H), 3,36(m, 1 H), 3,22(m, 1 H), 2,95(m, 1 H), 2,78(m, 1H), 2,01 (m, 4H), 1,75(m, 4H), 1,54(m, 1 H), 1,42(m, 3H), 1,01 (m, 3H)
Ejemplo 114: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(2,5-dimetiltiofen-3-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (12 mg, rendimiento: 20%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3 -(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (2,5-dimetiltiofen-3-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,54(m, 1 H), 7,92(s, 1H), 7,44(s, 1 H), 6,80(s, 1H), 4,25(m, 1H), 4,09(m, 1 H), 3,48(m, 1H), 3,25(m, 2H), 2,95(m, 1H), 2,80(m, 1H), 2,51(s, 3H), 2,24(d, 3H), 1,99(m, 3H), 1,80(m, 2H), 1,66(m, 3H), 1,56(m, 1H), 1,47(m, 1 H)
Ejemplo 115: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-7-(1-isobutil-1H-pirazol-4-il)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (18 mg, rendimiento: 27%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (1 -isobutil-1 H-pirazol-4-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,53(s, 1H), 8,03(s, 1H), 7,90(s, 1H), 7,80(s, 1H), 7,50(s, 1H), 4,33(m, 2H), 4,10(m, 2H), 3,48(m, 1H), 3,23(m, 1H), 2,92(m, 1H), 2,81(m, 1H), 2,30(m, 1H), 1,99(m, 2H), 1,81(m, 2H), 1,74(m, 2H), 1,54(m, 1H), 1,44(m, 1 H), 0,99(d, 6H)
Ejemplo 116: dihidrocloruro de 4-(5-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-benzo[d]imidazol-7-il)-1-metil-1H-pirrol-2-carboxilato de etilo
El compuesto del epígrafe (18 mg, rendimiento: 31%) se obtuvo del mismo modo que en el Ejemplo 20, con la excepción de que se usó (2R,3S)-2-(3-(7-bromo-5-cloro-1H-benzo[d]imidazol-1-il)propil)-3-((tercbutildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo en lugar de (2R,3S)-2-(3-(4-bromo-1H-benzo[d]imidazol-1-il)propil)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo y que se usó ácido (5-(etoxicarbonil)-1-metil-1 H-pirrol-3-il)borónico en lugar de ácido (3-fluorofenil)borónico en la Etapa 20-2 del Ejemplo 20.
1H RMN (500MHz, MeOD): 59,50(s, 1H), 7,87(s, 1H), 7,49(s, 1H), 731(s, 1H), 7,15(s, 1H), 4,41(m, 2H), 4,32(m, 2H), 4,04(s, 3H), 3,42(m, 1H), 3,21 (m, 1 H), 2,92(m, 1 H), 2,76(m, 1H), 1,96(m, 2H), 1,88-1,62(m, 5H), 1,52(m, 2H), 1,40(m, 3H)
Ejemplo 117: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-1H-imidazo[4,5-b]piridin-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (17 mg, rendimiento: 35%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-cloro-1 H-imidazo[4,5-b]piridina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.1
1H-RMN (500 MHz, MeOD): 59,48 (s, 1H), 8,29 (d, 1 H), 7,68 (d, 1 H), 4,58 (t, 2H), 3,66 (m, 2H), 3,00 (m, 2H), 2,20 (m, 2H), 2,07 (m, 2H), 1,98 (m, 1H), 1,74 (m, 2H), 1,56 (m, 1 H)
Ejemplo 118: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 40%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-cloro-3H-imidazo[4,5-b]piridina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,50 (s, 1H), 8,46 (d, 1 H), 7,69 (d, 1H), 4,59 (t, 2H), 3,65 (m, 1 H), 3,58 (m, 1H), 2,99 (m, 2H), 2,20 (m, 2H), 2,05 (m, 2H), 1,97 (m, 1 H), 1,73 (m, H), 1,54 (m, 1H)
Ejemplo 119: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-bromo-1H-imidazo[4,5-b]piridin-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (30 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-bromo-1H-imidazo[4,5-b]piridina en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,54 (s, 1H), 8,20 (d, 1 H), 7,84 (d, 1H), 4,59 (t, 2H), 3,58 (m, 2H), 2,99 (m, 2H), 2,24 (m, 2H), 2,07 (m, 2H), 1,98 (m, 1 H), 1,74 (m, 2H), 1,56 (m, 1 H)
Ejemplo 120: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-bromo-1H-imidazo[4,5-b]piridin-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (33 mg, rendimiento: 82%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-bromo-1H-imidazo[4,5-b]piridina en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,50 (s, 1 H), 8,78 (d, 1H), 8,53 (d, 1 H), 4,60 (t, 2H), 3,56 (t, 1H), 2,98 (m, 2H), 2,26 (m, 2H), 2,21 (m, 2H), 1,97 (m, 1 H), 1,74 (m, 2H), 1,55 (m, 1 H)
Ejemplo 121: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-metil-1H-imidazo[4,5-b]piridin-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (19 mg, rendimiento: 49%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-metil-1 H-imidazo[4,5-b]piridina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.1
1H-RMN(500 MHz, MeOD): 59,55 (s, 1H), 8,18 (d, 1H), 7,58 (d, 1H), 4,63 (t, 2H), 3,58 (m, 2H), 3,00 (m, 2H), 2,74 (s, 3H), 2,24 (m, 2H), 2,06 (m, 2H), 1,98 (m, 1 H), 1,74 (m, 2H), 1,56 (m, 2H), 1,56 (m, 1 H)
Ejemplo 122: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-cloro-1H-imidazo[4,5-c]piridin-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 40%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-cloro-1 H-imidazo[4,5-c]piridina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,30 (s, 1H), 9,09 (s, 1 H), 7,91 (s, 1H), 4,62 (t, 2H), 3,60 (m, 2H), 2,99 (m, 2H), 2,22 (m, 2H), 2,06 (m, 2H), 1,98 (m, 1 H), 1,73 (m, 2H), 1,56 (m, 1 H)
Ejemplo 123: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-cloro-3H-imidazo[4,5-c]piridin-3-il)propil)piperidin-3-ol
El compuesto del epígrafe (18 mg, rendimiento: 37%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-cloro-3H-imidazo[4,5-c]piridina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,21 (s, 1H), 8,97 (s, 1H), 8,18 (s, 1H), 4,52 (t, 2H), 3,58 (m, 1H), 2,98 (m, 2H), 2,19 (m, 2H), 2,05 (m, 2H), 1,97 (m, 1 H), 1,73 (m, 2H), 1,56 (m, 1 H)
Ejemplo 124: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-bromo-1H-imidazo[4,5-c]piridin-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (18 mg, rendimiento: 35%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-bromo-3H-imidazo[4,5-c]piridina en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,43 (s, 1H), 9,16 (s, 1 H), 8,12 (s, 1H), 4,64 (t, 2H), 3,65 (m, 2H), 3,01 (m, 2H), 2,26 (m, 2H), 2,07 (m, 2H), 1,97 (m, 1 H), 1,75 (m, 2H), 1,56 (m, 1 H)
Ejemplo 125: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-bromo-3H-imidazo[4,5-c]piridin-3-il)propil)piperidin-3-ol
El compuesto del epígrafe (20 mg, rendimiento: 40%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-bromo-3H-imidazo[4,5-c]piridina en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,18 (s, 1H), 9,01 (s, 1H), 8,38 (s, 1H), 4,53 (t, 2H), 3,58 (m, 2H), 2,97 (m, 2H), 2,19 (m, 2H), 2,05 (m, 2H), 1,97 (m, 1H), 1,74 (m, 2H), 1,56 (m, 1 H)
Ejemplo 126: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-cloro-1H-imidazo[4,5-b]piridin-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 32%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 7-cloro-1 H-imidazo[4,5-b]piridina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
Ejemplo 127: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5,6-dicloro-1H-imidazo[4,5-b]piridin-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (35 mg, rendimiento: 48%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5,6-dicloro-1 H-imidazo[4,5-b]piridina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,10 (s, 1H), 8,45 (s, 1H), 4,50 (t, 2H), 3,56 (m, 1H), 2,98 (m, 2H), 2,21 (m, 2H), 2,03 (m, 3H), 1,69 (m, 2H), 1,53 (m, 1H)
Ejemplo 128: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-bromo-1H-imidazo[4,5-c]piridin-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (18 mg, rendimiento: 35%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 7-bromo-1H-imidazo[4,5-c]piridina en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,66 (s, 1H), 9,07 (s, 1H), 8,89 (s, 1 H), 4,62 (t, 2H), 3,58 (m, 2H), 2,99 (m, 2H), 2,21 (m, 2H), 2,00 (m, 3H), 1,74 (m, 2H), 1,55 (m, 1 H)
Ejemplo 129: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-(trifluorometil)-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol
El compuesto del epígrafe (20 mg, rendimiento: 45%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-(trifluorometil)-3H-imidazo[4,5-b]piridina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN(500 MHz, MeOD): 59,71 (s, 1H), 8,53 (d, 1 H), 8,08 (d, 1H), 4,67 (t, 2H), 3,59 (m, 1H), 2,95 (m, 2H), 2,28 (m, 2H), 2,07 (m, 2H), 1,98 (m, 1 H), 1,75 (m, 2H), 1,55 (m, 1 H)
Ejemplo 130: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6,7-dicloro-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6,7-dicloro-3H-imidazo[4,5-b]piridina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 58,62 (s, 1 H), 8,51 (s, 1 H), 4,43 (m, 2H), 3,51 (m, 1 H), 3,22 (m, 1H), 2,91 (m, 2H), 2,08 (m, 2H), 1,96 (m, 3H), 1,55 (m, 3H)
Ejemplo 131: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-cloro-7-metil-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol
El compuesto del epígrafe (31 mg, rendimiento: 84%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-cloro-7-metil-3H-imidazo[4,5-b]piridina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,68 (s, 1H), 8,67 (s, 1 H), 4,62 (t, 2H), 3,57 (m, 2H), 2,97 (m, 2H), 2,74 (s, 3H), 2,25 (m, 2H), 2,06 (m, 2H), 1,97 (m, 1 H), 1,75 (m, 2H), 1,53 (m, 1 H)
Ejemplo 132: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-bromo-7-metil-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol
El compuesto del epígrafe (35 mg, rendimiento: 85%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-bromo-7-metil-3H-imidazo[4,5-b]piridina en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,74 (s, 1 H), 8,80 (d, 1 H), 4,63 (t, 2H), 3,57 (m, 1 H), 2,96 (m, 2H), 2,76 (s, 3H), 2,28 (m, 2H), 2,06 (m, 2H), 1,97 (m, 1 H), 1,74 (m, 2H), 1,55 (m, 1 H)
Ejemplo 133: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-bromo-7-cloro-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol
El compuesto del epígrafe (30 mg, rendimiento: 78%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-bromo-7-cloro-3H-imidazo[4,5-b]piridina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,24 (s, 1H), 8,77 (s, 1H), 4,55 (t, 2H), 3,55 (m, 1H), 3,26 (m, 1H), 2,97 (m, 2H), 2,23 (m, 2H), 2,03 (m, 3H), 1,70 (m, 2H), 1,54 (m, 1 H)
Ejemplo 134: Preparación de dihidrocloruro de (2R,3S)-2-(3-(7-cloro-6-(3-clorofenil)-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol
El compuesto del epígrafe (28 mg, rendimiento: 70%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 7-cloro-6-(3-clorofenil)-3H-imidazo[4,5-b]piridina en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,69 (s, 1H), 8,67 (s, 1H), 7,55 (m, 4H), 4,66 (t, 2H), 3,59 (m, 1H), 3,02 (m, 2H), 2,33 (m, 2H), 2,07 (m, 2H), 1,97 (m, 1 H), 1,56 (m, 2H), 1,55 (m, 1H)
Ejemplo 135: Preparación de trihidrocloruro de (2R,3S)-2-(3-(2-cloro-7H-purin-7-il)propil)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 35%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 2-cloro-7H-purina en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,05 (s, 1H), 8,81 (s, 1H), 4,44 (t, 2H), 3,55 (m, 1H), 3,28 (m, 1H), 2,98 (m, 2H), 2,19 (m, 2H), 2,03 (m, 3H), 1,70 (m, 2H), 1,55 (m, 1 H)
Ejemplo 136: Preparación de trihidrocloruro de (2R,3S)-2-(3-(2-cloro-9H-purin-9-il)propil)piperidin-3-ol
El compuesto del epígrafe (12 mg, rendimiento: 30%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 2-cloro-9H-purina en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 59,19 (s, 1H), 8,87 (s, 1H), 4,52 (m, 2H), 3,55 (m, 1H), 3,25 (m, 1H), 2,97 (m, 2H), 2,16 (m, 2H), 2,00 (m, 3H), 1,65 (m, 2H), 1,55 (m, 1 H)
Ejemplo 137: Preparación de trihidrocloruro de (2R,3S)-2-(3-(6-(dimetilamino)-9H-purin-9-il)propil)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 75%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó N,N-dimetil-9H-purin-6-amina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 58,38 (s, 1 H), 8,37 (s, 1 H), 4,41 (t, 2H), 3,98 (a, 2H), 3,56 (t, 1H), 3,42 (a, 3H), 3,26 (m, 1H), 2,97 (m, 2H), 2,19 (m, 5H), 1,78 (m, 1 H), 1,67 (m, 1 H), 1,53 (m, 1 H)
Ejemplo 138: Preparación de trihidrocloruro de (2R,3S)-2-(3-(6-(dietilamino)-9H-purin-9-il)propil)piperidin-3-ol
El compuesto del epígrafe (27 mg, rendimiento: 77%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó N,N-dietilamino-9H-purin-6-amina en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 58,34 (s, 1H), 8,32 (d, 1H), 4,38 (m, 2H), 3,66 (a, 4H), 3,55 (m, 1H), 3,27 (m, 1H), 2,96 (m, 2H), 2,14-2,00 (m, 6H), 1,68 (m, 1H), 1,53 (m, 1H), 1,38 (a, 6H)
Ejemplo 139: Preparación de trihidrocloruro de (2R,3S)-2-(3-(6-(etil(metil)amino)-9H-purin-9-il)propil)piperidin-3-ol
El compuesto del epígrafe (28 mg, rendimiento: 78%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó N-etil-N-metil-9H-purin-6-amina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 58,39 (s, 1 H), 8,38 (s, 1 H), 4,51 (a, 2H), 4,41 (t, 2H), 3,56 (m, 1 H), 3,41 (m, 1H), 3,27 (m, 3H), 2,96 (m, 2H), 2,19-1,99 (m, 5H), 1,75 (m, 1H), 1,68 (m, 1H), 1,53 (t, 3H)
Ejemplo 140: Preparación de trihidrocloruro de (2R,3S)-2-(3-(6-morfolino-9H-purin-9-il)propil)piperidin-3-ol
El compuesto del epígrafe (27 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 4-(9H-purin-6-il)morfolina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45 1 del Ejemplo 45.
1H-RMN(500 MHz, MeOD): 58,35 (s, 1H), 8,33 (d, 1H), 4,39 (m, 2H), 3,66 (s, 6H), 3,54 (m, 1H), 3,25 (m, 1H), 2,96 (m, 2H), 2,14-1,98 (m, 5H), 1,84 (s, 6H), 1,72 (m, 2H), 1,53 (m, 1H)
Ejemplo 141: Preparación de trihidrocloruro de (2R,3S)-2-(3-(6-(piperidin-1-il)-9H-purin-9-il)propil)piperidin-3-ol
El compuesto del epígrafe (30 mg, rendimiento: 81%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-(piperidin-1 -il)-9H-purina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45 1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 58,43 (s, 1H), 8,36 (s, 1H), 4,40 (m, 4H), 3,91 (m, 4H), 3,66 (s, 6H), 3,27 (m, 1H), 2,96 (m, 2H), 2,03 (m, 5H), 1,69 (m, 2H), 1,53 (m, 1 H)
Ejemplo 142: Preparación de trihidrocloruro de (2R,3S)-2-(3-(6-(pirrolidin-1-il)-9H-purin-9-il)propil)piperidin-3-ol
El compuesto del epígrafe (29 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-(pirrolidin-1 -il)-9H-purina en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45 1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 58,33 (a, 2H), 4,37 (m, 4H), 3,75 (a, 2H), 3,66 (m, 1 H), 2,96 (m, 2H), 2,17 (a, 6H), 2,00 (m, 4H), 1,73 (m, 2H), 1,53 (m, 1H)
Ejemplo 143: Preparación de dihidrocloruro de 1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-benzo[d]imidazol-2-ol
El compuesto del epígrafe (25 mg, rendimiento: 79%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 1 H-benzo[d]imidazol-2-ol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 57,16 (d, 1H), 7,10 (m, 3H), 3,96 (m, 2H), 3,53 (m, 1H), 3,20 (m, 1H), 2,91 (m, 2H), 2,00 (m, 5H), 1,62 (m, 2H), 1,51 (m, 1H)
Ejemplo 144: Preparación de dihidrocloruro de 5,6-dicloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-benzo[d]imidazol-2-ol
El compuesto del epígrafe (27 mg, rendimiento: 84%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5,6-dicloro-1 H-benzo[d]imidazol-2-ol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 57,38 (s, 1H), 7,21 (s, 1H), 3,92 (m, 2H), 3,48 (m, 2H), 3,20 (m, 3H), 2,89 (m, 3H), 2,04 1,92 (m, 7H), 1,67 (m, 5H)
Ejemplo 145: Preparación de dihidrocloruro de (2R,3S)-2-(3-(2-(hidroximetil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó (1 H-benzo[d]imidazol-2-il)metanol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 57,99 (d, 1 H), 7,81 (d, 1 H), 7,64 (m, 2H), 5,20 (s, 2H), 4,51 (m, 2H), 3,59 (m, 1H), 3,27 (m, 1 H), 2,97 (m, 2H), 2,20 (m, 1 H), 2,08 (m, 3H), 1,96 (m, 1H), 1,87 (m,2H), 1,55 (m, 1H)
Ejemplo 146: Preparación de dihidrocloruro de (2R,3S)-2-(3-(2-(hidroximetil)-4,5-dimetil-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (31 mg, rendimiento: 83%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó (4,5-dimetil-1 H-benzo[d]imidazol-2-il)metanol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 57,67 (d, 1 H), 7,47 (d, 1 H), 5,14 (s, 2H), 4,53 (m, 2H), 3,59 (m, 1H), 3,28 (m, 1H), 2,97 (m, 2H), 2,57 (s, 3H), 2,47 (s, 3H), 2,20 (m, 1 H), 2,10 (m, 3H), 1,97 (m, 1 H), 1,76 (m, 2H), 1,54 (m, 1 H)
Ejemplo 147: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5,6-dicloro-2-(hidroximetil)-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (28 mg, rendimiento: 79%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó (5,6-dicloro-1H-benzo[d]imidazol-2-il)metanol en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, DMSO-de): 58,37 (s, 1H), 7,99 (s, 1H), 4,99 (s, 2H), 4,40 (m, 2H), 3,41 (m, 1H), 3,09 (d, 1 H), 2,78 (m, 2H), 2,08 (m, 1H), 1,98 (m, 2H), 1,89 (m, 1 H), 1,77 (m, 1H), 1,64 (m, 2H), 1,35 (m, 1H)
Ejemplo 148: Preparación de dihidrocloruro de (2R,3S)-2-(3-(2-amino-5,6-dicloro-1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 81%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5,6-dicloro-1H-benzo[d]imidazol-2-amina en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 57,84 (s, 1 H), 7,57 (s, 1 H), 4,20 (t, 2H), 3,58 (m, 1H), 2,97 (m, 1H), 2,98 (m, 2H), 2,07 1,95 (m, 5H), 1,77 (m, 2H), 1,54 (m, 1 H)
Ejemplo 149: Preparación de dihidrocloruro de 7-bromo-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo
El compuesto del epígrafe (30 mg, rendimiento: 75%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó metilo 7-bromo-1H-indol-3-carboxilato de metilo en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 58,13 (d, 1 H), 8,05 (s, 1H), 7,45 (d, 1H), 7,09 (t, 1 H), 4,69 (m, 2H), 3,88 (s, 3H), 3,48 (m, 1H), 3,16 (m, 1 H), 2,88 (m, 2H), 2,00 (m, 5H), 1,64 (m, 2H), 1,52 (m, 1H)
Ejemplo 150: Preparación de dihidrocloruro de 5-bromo-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo
El compuesto del epígrafe (29 mg, rendimiento: 73%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó metilo 5-bromo-1H-indol-3-carboxilato de metilo en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 58,20 (s, 1H), 8,05 (s, 1 H), 7,49 (d, 1 H), 7,38 (d, 1H), 4,33 (m, 2H), 3,88 (s, 3H), 3,50 (m, 1H), 3,20 (d, 1 H), 2,90 (m, 2H), 1,99 (m, 5H), 1,65 (m, 1H), 1,52 (m, 2H)
Ejemplo 151: Preparación de dihidrocloruro de 6-bromo-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo
El compuesto del epígrafe (25 mg, rendimiento: 77%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó metilo 6-bromo-1H-indol-3-carboxilato de metilo en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.1
1H-RMN (500 MHz, MeOD): 58,03 (s, 1H), 7,97 (d, 1 H), 7,78 (s, 1H), 7,34 (d, 1H), 4,30 (m, 2H), 3,87 (s, 3H), 3,50 (m, 1H), 3,20 (d, 1 H), 2,91 (m, 2H), 1,97 (m, 5H), 1,67 (m, 1H), 1,53 (m, 2H)
Ejemplo 152: Preparación de dihidrocloruro de 4-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo
El compuesto del epígrafe (27 mg, rendimiento: 70%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó metilo 4-cloro-1 H-indol-3-carboxilato de metilo en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 58,07 (s, 1 H), 7,51 (d, 1 H), 7,24 (s, 1 H), 7,23 (s, 1 H), 4,33 (m, 2H), 3,84 (s, 3H), 3,20 (m, 1H), 2,91 (m, 2H), 2,00 (m, 5H), 1,67 (m, 1H), 1,52 (m, 2H)
Ejemplo 153: Preparación de dihidrocloruro de 6-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo
El compuesto del epígrafe (21 mg, rendimiento: 73%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó metilo 6-cloro-1H-indol-3-carboxilato de metilo en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 58,04 (s, 1 H), 8,02 (d, 1H), 7,62 (s, 1H), 7,21 (d, 1H), 4,31 (m, 2H), 3,87 (s, 3H), 3,50 (m, 1H), 3,19 (d, 1H), 2,91 (m, 2H), 1,97 (m, 5H), 1,65 (m, 1H), 1,53 (m, 2H)
Ejemplo 154: Preparación de dihidrocloruro de 7-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo
El compuesto del epígrafe (19 mg, rendimiento: 77%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó metilo 7-cloro-1 H-indol-3-carboxilato de metilo en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 58,07 (d, 1H), 8,04 (s, 1H), 7,25 (d, 1H), 7,17 (t, 1H), 4,66 (m, 2H), 3,88 (s, 3H), 3,51 (m, 1H), 3,20 (d, 1H), 2,91 (m, 2H), 3,11 (m, 1H), 2,08 (m, 4H), 1,69 (m, 2H), 1,55 (m, 1H)
Ejemplo 155: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-3-ciclopropil-1H-indazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (20 mg, rendimiento: 65%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-cloro-3-ciclopropil-1 H-indazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 57,93(s, 1H), 7,47(s, 2H), 4,35(m, 2H), 3,51(m, 1H), 3,20(m, 1H), 2,92(m, 2H), 2,22(m, 1H), 2,10-1,91(m, 4H), 1,68(m, 1H), 1,51(m,2H), 1,04)m, 2H), 0,97(m, 2H)
Ejemplo 156: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-3-(trifluorometil)-1H-indazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (17 mg, rendimiento: 31%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-cloro-3-(trifluorometil)-1 H-indazol en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 5 7,96(s, 1H), 7,72(d, 1H), 7,65(d, 1H), 4,57(m, 2H), 3,52(m, 1H), 3,22(m, 1H), 2,92(m, 2H), 2,20(m, 1H), 2,12(m, 1H), 2,00(m, 3H), 1,68(m, 1H), 1,62(m, 1H), 1,50(m, 1H)
Ejemplo 157: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-3-(1-(difluorometil)-1H-pirazol-4-il)-1H-indazol-1-il)propil)piperidin-3-ol
El compuesto del epígrafe (16 mg, rendimiento: 29%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-cloro-3-(1-(difluorometil)-1H-pirazol-4-il)-1H-indazol en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1HNMR (500MHz, MeOD): 58,69(s, 1H), 8,27(s, 1 H), 8,03(s, 1 H), 7,65(d, 1 H), 7,44(d, 1 H), 4,52(m, 2H), 3,50(m, 1H), 3,16(m, 1H), 2,90(m, 2H), 2,21(m, 1H), 2,12(m, 1H), 2,07(m, 3H), 1,66(m, 2H), 1,50(m, 1H)
Ejemplo 158: Preparación de dihidrocloruro de (2R,3S)-2-(3-(6-cloro-3-(1-(difluorometil)-1H-pirazol-4-il)-1H-indazol-1 -il)propil)piperidin-3-ol
El compuesto del epígrafe (17 mg, rendimiento: 30%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 6-cloro-3-(1-(difluorometil)-1H-pirazol-4-il)-1H-indazol en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H RMN (500MHz, MeOD): 58,66(s, 1 H), 8,27(s, 1H), 7,99(d, 1 H), 7,70(s, 1H), 7,23(d, 1H), 4,51 (m, 2H), 3,50(m, 1H), 3,21 (m, 1H), 2,92(m, 2H), 2,18(m, 1H), 2,10(m, 1H), 2,07(m, 3H), 1,66(m, 2H), 1,55(m, 1H)
Ejemplo 159: Preparación de dihidrocloruro de 1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-3-metil-1H-benzo[d]imidazol-2(3H)-ona
El compuesto del epígrafe (18 mg, rendimiento: 69%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 1-metil-1,3-dihidro-2H-benzo[d]imidazol-2-ona en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 57,16 (m, 4H), 3,99 (m, 2H), 3,66 (s, 2H), 3,53 (m, 2H), 3,43 (s, 3H), 2,94 (m, 2H), 2,00 (m, 4H), 1,88 (m, 1H), 1,62 (m, 2H), 1,52 (m, 1H)
Ejemplo 160: Preparación de dihidrocloruro de 5-bromo-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-benzo[d]imidazol-2(3H)-ona
El compuesto del epígrafe (15 mg, rendimiento: 42%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-bromo-1,3-dihidro-2H-benzo[d]imidazol-2-ona en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 57,37 (s, 1 H), 7,21 (d, 1H), 6,99 (d, 1 H), 3,94 (m, 2H), 3,54 (m, 1H), 3,23 (m, 1H), 2,94 (m, 2H), 2,05-1,87 (m, 5H), 1,65 (m, 2H), 1,53 (m, 1H)
Ejemplo 161: Preparación de dihidrocloruro de 6-bromo-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-benzo[d]imidazol-2(3H)-ona
El compuesto del epígrafe (14 mg, rendimiento: 40%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 5-bromo-1,3-dihidro-2H-benzo[d]imidazol-2-ona en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 57,23 (d, 1 H), 7,22 (s, 1H), 7,09 (d, 1 H), 3,95 (m, 2H), 3,53 (m, 1H), 3,23 (m, 1H), 2,94 (m, 2H), 2,02-1,87 (m, 5H), 1,66 (m, 2H), 1,53 (m, 1H)
Ejemplo 162: Preparación de dihidrocloruro de 7-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1,3-dimetil-1H-urino-2,6(3H,7H)-diona
El compuesto del epígrafe (21 mg, rendimiento: 75%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 1,3-dimetil-3,7-dihidro-1 H-purino-2,6-diona en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 58,15 (s, 1H), 4,40 (a, 2H), 3,57 (m, 1H), 3,34 (s, 6H), 3,26 (m, 1H), 2,98 (m, 2H), 2,00 (m, 5H), 1,72 (m, 2H), 1,55 (m, 1H)
Ejemplo 163: Preparación de dihidrocloruro de 7-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-3-metil-1H-purino-2,6(3H,7H)-diona
El compuesto del epígrafe (21 mg, rendimiento: 72%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 3-metil-3,7-dihidro-1 H-purino-2,6-diona en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 57,95 (s, 1H), 4,34 (m, 2H), 3,48 (m, 3H), 3,22 (m, 1 H), 2,89 (m, 2H), 1,95 (m, 5H), 1,68 (m, 1 H), 1,52 (m, 2H)
Ejemplo 164: Preparación de dihidrocloruro de 9-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1-metil-1H-purino-2,6(3H,9H)-diona
El compuesto del epígrafe (25 mg, rendimiento: 70%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 1-metil-3,9-dihidro-1 H-purino-2,6-diona en lugar de 5-bromo-4-metil-1 H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 57,89 (s, 1H), 4,36 (m, 2H), 3,66 (m, 1H), 3,23 (m, 1 H), 2,98 (m, 2H), 1,99 (m, 5H), 1,69 (m, 1 H), 1,56 (m, 2H)
Ejemplo 165: Preparación de dihidrocloruro de 7-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-3-isobutil-1-metil-1 H-urino-2,6(3H,7H)-diona
El compuesto del epígrafe (25 mg, rendimiento: 70%) se obtuvo del mismo modo que en el Ejemplo 45, con la excepción de que se usó 3-isobutil-1-metil-3,7-dihidro-1H-purino-2,6-diona en lugar de 5-bromo-4-metil-1H-benzo[d]imidazol en la Etapa 45-1 del Ejemplo 45.
1H-RMN (500 MHz, MeOD): 57,95 (s, 1H), 4,38 (m, 2H), 3,90 (m, 3H), 3,54 (m, 1 H), 3,36 (m, 4H), 3,28 (m, 1H), 2,99 (m, 2H), 2,26 (m, 1H), 2,04 (m, 5H), 1,69 (m, 1 H), 1,63 (m, 1H), 1,54 (m, 1H), 0,94 (m, 8H)
Ejemplo 166: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5,6-dicloro-1H-benzo[d]imidazol-1-il)prop-1-enil)piperidin-3-ol
Etapa 166-1: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-((E)-3-etoxi-3-oxoprop-1-en-1-il)piperidino-1-carboxilato de terc-butilo
Se añadieron cloruro de metileno (47 ml, 0,12 M) y cloruro de oxalilo (1,0 ml, 11,6 mmol) a un matraz cargado con argón y la solución de reacción se enfrió hasta -78°C. A continuación, se añadió dimetilsulfóxido (1,7 ml, 23,2 mmol)
a la misma temperatura y se agitó durante 30 minutos. A continuación, se disolvió (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(hidroximetil)piperidino-1 -carboxilato de terc-butilo (2,0 g, 5,8 mmol) en una pequeña cantidad de cloruro de metileno y se añadió lentamente. Después de agitar a la misma temperatura durante 1 hora, se añadió trietilamina (3,3 ml, 23,2 mmol) y la temperatura de la solución de reacción se elevó hasta temperatura ambiente desde -78°C. Cuando la reacción se completaba, el disolvente se retiraba y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó con sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se disolvió en cloruro de metileno (47 ml, 0,12 M). A continuación, se añadió a esto (carbetoximetilen)trifenilfosforano (4,0 g, 11,6 mmol) y se agitó durante 2 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y a continuación se concentró bajo presión reducida y se purificó mediante cromatografía en columna (hexano:acetato de etilo = 4:1) para dar el compuesto del epígrafe (2,1 g, rendimiento: 89%).
Etapa 166-2: Preparación de ácido (E)-3-((2R,3S)-1-(terc-butoxicarbonil)-3-((terc-butildimetilsilil)oxi)piperidin-2-il)acrílico
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-((E)-3-etoxi-3-oxoprop-1-en-1-il)piperidino-1-carboxilato de terc-butilo (3,0 g, 7,2 mmol) obtenido a partir de la Etapa 166-1 se disolvió en metanol (20 ml, 0,36 mmol). A continuación, se añadió a esto solución acuosa de hidróxido sódico 2 N (10 ml) y se agitó a temperatura ambiente durante 3 horas. Cuando la reacción se completaba, la solución de reacción se neutralizaba con solución acuosa de ácido clorhídrico 1 N, se acidificaba, se diluía con acetato de etilo y a continuación se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida. Las reacciones posteriores se llevaron a cabo sin un procedimiento de purificación.
Etapa 166-3: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-((E)-3-hidroxiprop-en-1-il) piperidino-1 -carboxilato de terc-butilo
El ácido (E)-3-((2R,3S)-1-(terc-butoxicarbonil)-3-((terc-butildimetilsilil)oxi)piperidin-2-il)acrílico (1,6 g, 4,0 mmol) obtenido a partir de la Etapa 166-2 se disolvió en tetrahidrofurano (50 ml, 0,08 M), y la solución de reacción se enfrió hasta 0°C. A continuación, se añadió lentamente a esto una solución de hidruro de litio y aluminio (1,6 ml, 4,0 mmol), se hizo reaccionar a la misma temperatura durante 30 minutos y a continuación se agitó a temperatura ambiente durante 2 horas. Se añadió una pequeña cantidad de agua para completar la reacción, se diluyó con acetato de etilo y se lavó con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (diclorometano:metanol = 10:1) para dar el compuesto del epígrafe (1,3 g, rendimiento: 85%).
Etapa 166-4: Preparación de (2R,3S)-2-((E)-3-bromoprop-1-en-1-il)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-((E)-3-hidroxiprop-en-1 -il)piperidino-1 -carboxilato de terc-butilo (100 mg, 0,27 mmol) obtenido a partir de la Etapa 166-3 se añadió a cloruro de metileno (10 ml, 0,03 M). La solución de reacción se enfrió hasta 0°C, y a continuación se añadieron secuencialmente a la misma temperatura trifenilfosfina (106 g, 0,40 mmol) y tetrabromometano (134 mg, 0,40 mmol), seguido por agitación a temperatura ambiente durante 2 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (hexano:acetato de etilo = 5:1) para dar el compuesto del epígrafe (89 mg, rendimiento: 76%).
Etapa 166-5: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-((E)-3-(5,6-dicloro-1 H-benzo[d]imidazol-1-il)prop-1-en-1-il)piperidino-1-carboxilato de terc-butilo
El (2R,3S)-2-((E)-3-bromoprop-1-en-1-il)-3-((terc-butildimetilsilil)oxi)piperidino-1-carboxilato de terc-butilo (83 mg, 0,19 mmol) obtenido a partir de la Etapa 166-4 se disolvió en N,N-dimetilformamida (3 ml, 0,06 M). Se añadieron a esto carbonato potásico (53 mg, 0,38 mmol) y 5,6-dicloro-1H-benzo[d]imidazol (35 mg, 0,19 mmol) y la mezcla se agitó a temperatura ambiente durante 4 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato sódico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (hexano:acetato de etilo = 1:2) para dar el compuesto del epígrafe (88 g, rendimiento: 85%).
Etapa 166-6: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5,6-dicloro-1H-benzo[d]imidazol-il)prop-1-en-1-il)piperidin-3-ol
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-((E)-3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidino-1 -carboxilato de terc-butilo (85 mg, 0.16 mmol) obtenido a partir de la Etapa 166-5 se disolvió en una pequeña cantidad de tetrahidrofurano. A continuación, se añadió a esto solución en dioxano de cloruro de hidrógeno 4 N (5 ml, 0,03 M) y se agitó a temperatura ambiente durante 12 horas. Cuando la reacción se completaba, la solución de reacción se concentraba bajo presión reducida para retirar el disolvente, se disolvía mediante la adición de una pequeña cantidad de metanol y a continuación se cristalizaba con éter dietílico para obtener el compuesto del epígrafe (51 mg, rendimiento: 81 %).
1H-RMN (500 MHz, DMSO-d6) : 58,86 (s, 1H), 8,12 (s, 1H), 8,04 (s, 1H), 6,11 (dt,1H), 5,85 (d, 1H), 5,03 (d, 2H), 3,54 (m, 1H), 3,40 (m, 1H), 3,13 (d, 1H), 2,79 (m, 1H), 1,94 (m, 1H), 1,79 (d, 1H), 1,68 (m, 1H), 1,41 (m, 1H)
Ejemplo 167: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5-fluoro-4-metil-1H-benzo[d]imidazol-1-il)prop-1 -enil)piperidin-3-ol
El compuesto del epígrafe (24 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5-fluoro-4-metil-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 59,45 (d, 1H), 7,73 (m, 1H), 7,42 (m, 1H), 6,25 (m, 1H), 5,98 (m, 1 H), 5,23 (s, 2H), 3,55 (m, 2H), 2,96 (m, 1H), 2,56 (s, 3H), 2,00 (m, 3H), 1,74 (m, 1H), 1,56 (m, 1 H)
Ejemplo 168: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5-bromo-4-metil-1H-benzo[d]imidazol-1-il)prop-1 -enil)piperidin-3-ol
El compuesto del epígrafe (30 mg, rendimiento: 85%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5-bromo-4-metil-1H-benzo[d]imidazol en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 59,38 (d, 1H), 7,68 (m, 1H), 7,37 (m, 1H), 6,15 (m, 1H), 5,88 (m, 1H), 5,00 (s, 2H), 3,34 (m, 2H), 2,78 (m, 1H), 2,54 (s, 3H), 1,97 (m, 3H), 1,68 (m, 1H), 1,48 (m, 1 H)
Ejemplo 169: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5,6-dimetil-1H-benzo[d]imidazol-1-il)prop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (30 mg, rendimiento: 85%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5,6-dimetil-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166 5 del Ejemplo 166.1
1H-RMN (500 MHz, MeOD): 57,64 (m, 1H), 7,61 (s, 1H), 6,25 (m, 1 H), 5,91 (m, 1 H), 5,20 (s, 2H), 3,56 (m, 2H), 2,95 (m, 1H), 2,46 (m, 1H), 2,45 (s, 6H), 2,09 (m, 1 H), 2,00 (m, 2H), 1,72 (m, 1 H), 1,56 (m, 1H)
Ejemplo 170: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5,6-dibromo-1H-benzo[d]imidazol-1-il)prop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (24 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5,6-dibromo-1H-benzo[d]imidazol en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 59,21 (m, 1H), 8,30 (m, 1H), 8,21 (m, 1H), 6,22 (m, 1H), 5,92 (m, 1H), 5,16 (m, 2H), 3,56 (m, 2H), 2,95 (m, 1H), 1,99 (m, 3H), 1,72 (m, 1 H), 1,56 (m, 1H)
Ejemplo 171: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5,6-dicloro-1H-benzo[d]imidazol-1 il)prop-1-en-1 -il)piperidin-3-ol
El compuesto del epígrafe (20 mg, rendimiento: 86%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5,6-difluoro-1H-benzo[d]imidazol en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 57,76 (m, 1H), 6,22 (m, 1H), 5,88 (m, 1H), 5,12 (m, 2H), 3,57 (m, 3H), 2,92 (m, 1H), 2,20 (m, 4H), 1,72 (m, 1H), 1,56 (m, 1H)
Ejemplo 172: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(4,5-dimetil-1H-benzo[d]imidazol-1-il)prop-1-en-1 -il)piperidin-3-ol
El compuesto del epígrafe (19 mg, rendimiento: 81%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 4,5-dimetil-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166 5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 59,42 (m, 1H), 7,62 (m, 1H), 7,47 (m, 1H), 6,25 (m, 1H), 5,94 (m, 1 H), 5,21 (m, 2H), 3,55 (m, 2H), 3,34 (m, 1H), 2,95 (m, 1 H), 1,99 (m, 2H), 1,74 (m, 1H), 1,53 (m, 1H)
Ejemplo 173: Preparación de hidrocloruro de (2R,3S)-2-((E)-3-(5-cloro-4-metil-1H-benzo[d]imidazol-1-il)prop-1-en-1 -il)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 82%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5-cloro-4-metil-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 59,50 (s, 1H), 7,76 (d, 1H), 7,67 (d, 1H), 5,98 (m, 1H), 5,23 (m, 2H), 3,63 (m, 1H), 3,55 (m, 1 H), 2,96 (m, 1H), 2,66 (s, 3H), 2,09 (m, 1H), 2,00 (m, 1H), 1,74 (m, 1H), 1,53 (m, 1H)
Ejemplo 174: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(4,5-dicloro-1H-benzo[d]imidazol-1-il)prop-1-en-1 -il)piperidin-3-ol
El compuesto del epígrafe (20 mg, rendimiento: 89%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 4,5-dicloro-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166 5 del Ejemplo 166.
1H RMN (500MHz, MeOD): 59,58(s, 1 H), 7,91 (d, 1H), 7,79(d, 1 H), 6,30(m, 1 H), 6,03(m, 1 H), 5,25(d, 2H), 3,69(m, 1H), 3,58(m, 1 H), 3,01 (m, 1 H), 2,11 (m, 1 H), 2,03(m, 1H), 1,80(m, 1H), 1,55(m, 1 H)
Ejemplo 175: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(4-cloro-5-metil-1H-benzo[d]imidazol-1-il)prop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (23 mg, rendimiento: 91%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 4-cloro-5-metil-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H RMN (500MHz, MeOD): 59,52(s, 1 H), 7,88(d, 1H), 7,70(d, 1 H), 6,25(m, 1 H), 6,01 (m, 1 H), 5,20(d, 2H), 3,62(m, 1H), 3,49(m, 1 H), 3,00(m, 1 H), 2,65(s, 3H), 2,05(m, 1 H), 2,00(m, 1H), 1,74(m, 1 H), 1,51 (m, 1H)
Ejemplo 176: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5-bromo-4-nitro-1H-benzo[d]imidazol-1-il)prop-1 -en-1 -il)piperidin-3-ol
El compuesto del epígrafe (9 mg, rendimiento: 45%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5-bromo-4-nitro-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H RMN (500MHz, MeOD): 5 8,94(s, 1H), 7,93(d, 1H), 7,83(d, 1H), 6,27(m, 1H), 5,84(m, 1H), 5,20(m, 2H), 3,62(m, 2H), 3,58(m 1H), 2,99(m, 1 H), 2,11 (m, 1H), 2,08(m, 1H), 1,98(m, 1H), 1,59(m, 1H)
Ejemplo 177: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(6-bromo-7-nitro-1H-benzo[d]imidazol-1-il)prop-l-en-1-il)piperidin-3-ol
El compuesto del epígrafe (10 mg, rendimiento: 51%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5-bromo-4-nitro-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.1
1H RMN (500MHz, MeOD): 5 8,45(s, 1H), 7,85(d, 1H), 7,69(d, 1H), 6,11(m, 1H), 5,59(m, 1H), 4,28(m, 2H), 3,62(m, 2H), 2,96(m 1H), 2,24(m, 1 H), 1,72(m, 2H), 1,58(m, 1H), 1,53(m, 1H)
Ejemplo 178: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(4-cloro-5-nitro-1H-benzo[d]imidazol-1-il)prop-1 -en-1 -il)piperidin-3-ol
El compuesto del epígrafe (11 mg, rendimiento: 52%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 4-cloro-5-nitro-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H RMN (500MHz, MeOD): 5 9,06(s, 1H), 8,04(m, 1H), 7,92(m, 1H), 7,87(m, 1H), 6,26(m, 1H), 5,86(m, H), 5,26(m, 2H), 3,60(m, 2H), 2,96(m, 2H), 2,07(m, 1 H), 1,99(m 2H), 1,77(m, 1H), 1,51 (m, 1H)
Ejemplo 179: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(4,6-difluoro-1H-benzo[d]imidazol-1-il)prop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 62%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 4,6-difluoro-1H-benzo[d]imidazol en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H RMN (500MHz, MeOD): 59,22(m, 1H), 7,58(m, 1H), 7,32(m, 1H), 6,38(m, 1H), 5,99(m, 1H), 5,27(d, 1H), 3,65(m, 2H), 2,99(t, 1H), 2,19(m, 1H), 2,08(m, 2H), 1,87(m, 2H), 1,65(m, 1H)
Ejemplo 180: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(6-cloro-4-metil-1H-benzo[d]imidazol-1-il)propl-en-1 -il)piperidin-3-ol
El compuesto del epígrafe (14 mg, rendimiento: 58%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 6-cloro-4-metil-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H RMN (500MHz, MeOD): 59,53(m, 1H), 7,85(m, 1H, 7,50(m, 1H), 6,31(m, 1H), 6,01(m, 1H), 5,41 (m, 1H), 3,66(m, 1H), 3,00(m, 2H), 2,64(s, 3H), 2,08(m, 3H), 1,73(m, 1H)
Ejemplo 181: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(7-cloro-5-(trifluorometil)-1 H-benzo[d]imidazol-1-il)prop-l-en-1-il)piperidin-3-ol
El compuesto del epígrafe (19 mg, rendimiento: 75%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 7-cloro-5-(trifluorometil)-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.1
1H RMN (500MHz, MeOD): 59,51(m, 1H), 8,20(m, 1H, 7,99(m, 1H), 6,37(m, 1H), 5,89(m, 1H), 5,47(m, 2H), 3,59(m, 2H), 2,93(m, 1H), 2,08(m, 2H), 2,06(m, 1 H), 1,75(m, 1 H), 1,58(m, 1H), 1,51 (m, 1 H)
Ejemplo 182: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5,7-dicloro-1H-benzo[d]imidazol-1-il)prop-1-en-1 -il)piperidin-3-ol
El compuesto del epígrafe (22 mg, rendimiento: 85%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5,7-dicloro-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166 5 del Ejemplo 166.
1H RMN (500MHz, MeOD): 59,04(s, 1H), 7,81 (s, 1 H), 7,61 (s, 1H), 6,36(m, 1H), 5,74(m, 1H), 5,42(m, 1H).3,63-3,53(m, 2H), 2,99(m, 1H), 2,09(m, 1 H), 2,01 (m, 1 H), 1,76(m, 1 H), 1,59(m, 1H), 1,51 (m, 1 H)
Ejemplo 183: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5-cloro-7-fluoro-1H-benzo[d]imidazol-1-il)prop-1 -en-1 -il)piperidin-3-ol
El compuesto del epígrafe (18 mg, rendimiento: 72%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5-cloro-7-fluoro-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H RMN (500MHz, MeOD): 59,56(s, 1H), 7,75(m, 1H), 7,47(m, 1H), 6,33(m, 1H), 6,02(m, 1H), 5,28(m, 2H), 3,66(m, 2H), 2,99(m, 1H), 2,11 (m, 2H). 1,78(m, 2H), 1,55(m, 1 H)
Ejemplo 184: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5-bromo-1H-imidazo[4,5-b]piridin-1-il)prop-1-en-1 -il)piperidin-3-ol
El compuesto del epígrafe (18 mg, rendimiento: 40%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5-bromo-1 H-imidazo[4,5-b]piridina en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,37 (s, 1H), 7,94 (m, 1H), 7,46 (m, 1H), 6,24 (m, 1 H), 5,70 (m, 1 H), 5,08 (m, 2H), 3,49 (m, 2H), 3,24 (m, 1H), 2,91 (m, 1 H), 1,97 (m, 2H), 1,68 (m, 1H), 1,51 (m, 1H)
Ejemplo 185: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(7-cloro-6-(3-clorofenil)-3H-imidazo[4,5-b]piridin-3-il)prop-1 -en-1 -il)piperidin-3-ol
El compuesto del epígrafe (20 mg, rendimiento: 41%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 7-cloro-6-(3-clorofenil)-3H-imidazo[4,5-b]piridina en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,52 (s, 1H), 8,38 (s, 1 H), 7,42 (m, 4H), 6,26 (m, 1H), 5,68 (m, 1 H), 5,12 (m, 2H), 3,51 (m, 2H), 3,34 (m 1 H), 2,92 (m, 1H), 1,99 (m, 2H), 1,53 (m, 2H)
Ejemplo 186: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(6-bromo-7-metil-3H-imidazo[4,5-b]piridin-3-il)prop-1 -en-1 -il)piperidin-3-ol
El compuesto del epígrafe (18 mg, rendimiento: 40%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 6-bromo-7-metil-3H-imidazo[4,5-b]piridina en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,39 (s, 1 H), 8,34 (s, 1 H), 6,24 (m, 1 H), 5,70 (m, 1 H), 5,08 (m, 2H), 3,49 (m, 2H), 3,24 (m, 1H), 2,91 (m, 1H), 2,23 (s, 3H), 1,97 (m, 2H), 1,68 (m, 1H), 1,51 (m, 1H)
Ejemplo 187: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(6-bromo-7-cloro-3H-imidazo[4,5-b]piridin-3-il)prop-1 -en-1 -il)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 45%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 6-bromo-7-cloro-3H-imidazo[4,5-b]piridina en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,58 (m, 2H), 6,24 (m, 1H), 5,70 (m, 1H), 5,08 (m, 2H), 3,49 (m, 2H), 3,24 (m, 1 H), 2,91 (m, 1H), 1,97 (m, 2H), 1,68 (m, 1H), 1,51 (m, 1H)
Ejemplo 188: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(6-cloro-7-metil-3H-imidazo[4,5-b]piridin-3-il)prop-1 -en-1 -il)piperidin-3-ol
El compuesto del epígrafe (32 mg, rendimiento: 84%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 6-cloro-7-metil-3H-imidazo[4,5-b]piridina en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,37 (s, 1 H), 8,31 (s, 1 H), 6,22 (m, 1 H), 5,68 (m, 1 H), 5,06 (m, 2H), 3,38 (m, 2H), 3,20 (m, 1H), 2,84 (m, 1H), 2,20 (s, 3H), 1,87 (m, 2H), 1,54 (m, 1H), 1,48 (m, 1H)
Ejemplo 189: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(6,7-dicloro-3H-imidazo[4,5-b]piridin-3-il)prop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 60%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 6,7-dicloro-3H-imidazo[4,5-b]piridina en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, DMSO-de): 58,68 (s, 1H), 8,57 (s, 1H), 6,15 (dd, 1H), 5,76 (dd, 1H), 4,98 (d, 2H), 3,52 (m, 1H), 3,40 (m, 1H), 3,09 (d, 1H), 2,78 (dd, 1 H), 1,92 (m, 1 H), 1,77 (m, 1 H), 1,68 (m, 1 H), 1,37 (m, 1H)
Ejemplo 190: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(6-(3-clorofenil)-1H-benzo[d]imidazol-1-il)prop-1 -en-1 -il)piperidin-3-ol
El compuesto del epígrafe (18 mg, rendimiento: 40%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 6-(3-clorofenil)-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 59,53 (s, 1H), 8,18 (s, 1H), 7,96 (s, 2H), 7,80 (s, 1H), 6,69 (d, 1H), 7,50 (t, 1H), 7,45 (d, 1H) 6,34 (dd, 1H), 6,00 (dd, 1H), 5,32 (d, 2H), 3,64 (m, 2H), 2,97 (m, 1H), 2,10 (m, 1H), 1,98 (m, 1H), 1,75 (m, 1H), 1,56 (m, 1 H), 1,30 (m, 1H)
Ejemplo 191: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(6-(3-fluorofenil)-1H-benzo[d]imidazol-1-il)prop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 42%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 6-(3-fluorofenil)-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 59,35 (s, 1H), 8,23 (d, 1H), 7,93 (s, 2H), 7,57 (d, 1H), 7,52 (d, 2H), 7,17 (t, 1H), 6,32 (d, 1H), 5,94 (m, 1 H), 5,31 (m, 2H), 3,56 (m, 3H), 2,97 (m, 1 H), 2,10 (m, 1H), 2,01 (m, 1 H), 1,72 (m, 1 H), 1,55 (m, 1 H) Ejemplo 192: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(6-(3-(trifluorometil)fenil)-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol
El compuesto del epígrafe (15 mg, rendimiento: 40%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 6-(3- (trifluorometil)fenil)-1H-benzo[d]imidazol en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 59,48 (s, 1H), 8,21 (s, 1H), 8,03 (m, 2H), 8,01 (s, 2H), 7,73 (m, 2H), 6,34 (td, 1H), 5,99 (dd, 1H), 5,34 (m, 2H), 3,60 (td, 2H), 2,95 (m, 1H), 2,10 (d, 1H), 2,01 (d, 1H), 1,74 (m, 1H), 1,55 (m, 1H), 1,31 (m, 1H) Ejemplo 193: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5-bromo-6,7-difluoro-2-metil-1H-benzo[d]imidazol-1-il)prop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (12 mg, rendimiento: 40%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5-bromo-6,7-difluoro-2-metil-1H-benzo[d]imidazol en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,37 (s, 1H), 8,31 (s, 1 H), 6,22 (m, 1H), 5,68 (m, 1H), 5,06 (m, 2H), 3,38 (m, 2H), 3,20 (m, 1 H), 2,84 (m, 1H), 2,20 (s, 3H), 1,87 (m, 2H), 1,54 (m, 1H), 1,48 (m, 1H)
Ejemplo 194: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(indolin-1-il)prop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó indolina en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166. 1H-RMN (500 MHz, MeOD): 57,29 (m, 4H), 6,89 (s, 2H), 4,14 (m, 2H), 3,82 (m, 2H), 3,56 (m, 2H), 3,25 (m, 5H), 2,95 (m, 1 H), 1,99 (m, 2H), 1,74 (m 1H), 1,56 (m, 1H)
Ejemplo 195: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5-cloroindolin-1-il)prop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (27 mg, rendimiento: 82%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5-cloroindolina en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 57,10 (s, 1H), 6,89 (m, 2H), 6,04 (s, 2H), 4,12 (m, 2H), 3,74 (m, 2H), 3,42 (m, 2H), 3,20 (m, 5H), 2,84 (m, 1H), 1,97 (m, 2H), 1,68 (m, 1 H), 1,52 (m, 1H)
Ejemplo 196: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(1H-pirrolo[2,3-b]piridin-1-il)prop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (30 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 1H-pirrolo[2,3-b]piridina en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,21 (d, 1H), 7,98 (m, 1 H), 7,37 (m, 1 H), 7,09 (m, 1H), 6,51 (m, 1 H), 6,20 (m, 1H), 5,90 (m, 1H), 4,87 (m, 2H), 3,61 (m, 1 H), 3,52 (m, 1 H), 3,27 (m, 1H), 2,95 (m, 1H), 2,00 (m, 2H), 1,71 (m, 1H), 1,56 (m, 1 H) Ejemplo 197: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(6-cloro-1H-indol-1-il)prop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (37 mg, rendimiento: 83%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 6-cloro-1 H-indol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 57,36 (m, 3H), 7,08 (d, 1 H), 6,90 (m, 1 H), 6,13 (m, 1H), 5,38 (m, 1 H), 4,87 (m, 2H), 3,44 (m, 2H), 3,15 (m, 1H), 2,88 (m, 1H), 1,94 (m, 2H), 1,65 (m, 1H), 1,48 (m, 1H)
Ejemplo 198: Preparación de dihidrocloruro de (2X3S)-2-((E)-3-(6-cloro-1 H-indazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 79%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 6-cloro-1 H-indazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,02 (s, 1H), 7,71 (m, 1H), 7,63 (s, 1 H), 7,12 (m, 1 H), 6,20 (m, 1H), 5,62 (m, 1 H), 5,21 (m 2H), 3,54 (m, 1 H), 3,46 (m, 1H), 3,22 (m, 1H), 2,90 (m, 1H), 2,05 (m, 1 H), 1,96 (m, 1 H), 1,65 (m, 1 H), 1,50 (m, 1H)
Ejemplo 199: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(4-cloro-7H-pirrolo[2,3-d]pirimidin-7-il)prop-1-en-1 -il)piperidin-3-ol
El compuesto del epígrafe (27 mg, rendimiento: 85%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 4-cloro-7H-pirrolo[2,3-d]pirimidina en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,53 (s, 1H), 7,60 (s, 1H), 6,69 (m, 1H), 6,18 (m, 1H), 5,53 (m, 1H), 5,04 (m, 2H), 3,46 (m, 2H), 3,21 (m, 1H), 2,90 (m, 1 H), 1,96 (m, 2H), 1,56 (m, 1H), 1,50 (m, 1H)
Ejemplo 200: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5-cloro-1H-pirazolo[3,4-b]piridin-1-il)prop-1-en-1 -il)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 81%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó cloro-1 H-pirazolo[3,4-b]piridina en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166 5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,52 (m, 1H), 8,26 (m, 1 H), 8,13 (s, 1H), 6,20 (m, 1 H), 5,62 (m, 1H), 5,21 (m 2H), 3,54 (m, 1 H), 3,46 (m, 1H), 3,22 (m, 1 H), 2,90 (m, 1 H), 2,05 (m, 1H), 1,96 (m, 1H), 1,65 (m, 1H), 1,50 (m, 1H)
Ejemplo 201: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(3,5-dimetil-1H-indazol-1-il)prop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (28 mg, rendimiento: 79%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 3,5-dimetil-1H-indazol en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 57,74 (s, 1 H), 7,50 (m, 1 H), 7,37 (m, 1 H), 6,13 (m, 1H), 5,49 (m, 1H), 5,02 (m, 2H), 3,50 (m, 1H), 3,44 (m, 1H), 3,32 (s, 3H), 3,21 (m, 1 H), 2,90 (m, 1H), 2,51 (s, 3H), 2,04 (m, 1 H), 1,95 (m, 1 H), 1,56 (m, 1 H), 1,49 (m, 1 H)
Ejemplo 202: Preparación de dihidrocloruro de 7-bromo-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxilato de metilo
El compuesto del epígrafe (30 mg, rendimiento: 82%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó metilo 7-bromo-1 H-indol-3-carboxilato de metilo en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,14 (m, 1H), 8,04 (s, 1 H), 7,44 (m, 1 H), 7,09 (m, 1H), 6,26 (m, 1H), 5,43 (m, 1H), 5,31 (m, 1H), 3,50 (m, 2H), 3,15 (m, 1H), 2,88 (m, 1H), 1,94 (m, 2H), 1,62 (m, 1H), 1,50 (m, 1H)
Ejemplo 203: Preparación de dihidrocloruro de ácido 7-bromo-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico
El compuesto del epígrafe (28 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó ácido 7-bromo-1 H-indol-3-carboxílico en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,02 (m, 2H), 7,39 (d, 1 H), 7,09 (m, 1H), 6,21 (m, 1 H), 5,91 (m, 1H), 4,83 (m, 2H), 3,62 (m, 1H), 3,51 (m, 1H), 3,26 (m, 1H), 2,94 (m, 1H), 1,98 (m, 2H), 1,71 (m, 1H), 1,52 (m, 1H)
Ejemplo 204: Preparación de dihidrocloruro de ácido 5-bromo-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxílico
El compuesto del epígrafe (35 mg, rendimiento: 82%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó ácido 5-bromo-1 H-indol-3-carboxílico en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,18 (s, 1H), 8,01 (m, 1H), 7,31 (m, 2H), 6,21 (m, 1H), 5,90 (m, 1H), 4,89 (m, 2H), 3,61 (m, 1H), 3,53 (m, 1H), 3,23 (m, 1H), 2,95 (m, 1H), 1,99 (m, 2H), 1,68 (m, 1 H), 1,53 (m, 1H)
Ejemplo 205: Preparación de dihidrocloruro de ácido 4-cloro-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxílico
El compuesto del epígrafe (31 mg, rendimiento: 83%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó ácido 4-cloro-1 H-indol-3-carboxílico en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,06 (s, 1 H), 7,41 (d, 1H), 7,15 (m, 2H), 6,20 (m, 1H), 5,90 (m, 1 H), 4,87 (m, 2H), 3,61 (m, 1 H), 3,52 (m, 1H), 3,27 (m, 1 H), 2,95 (m, 1 H), 2,00 (m, 2H), 1,71 (m, 1H), 1,56 (m, 1H)
Ejemplo 206: Preparación de dihidrocloruro de ácido 6-cloro-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxílico
El compuesto del epígrafe (27 mg, rendimiento: 79%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó ácido 6-cloro-1 H-indol-3-carboxílico en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,01 (d, 1H), 7,46 (m, 1H), 7,17 (d, 1H), 6,22 (m, 1H), 5,91 (m, 1H), 4,88 (m, 2H), 4,36 (m, 1 H), 3,61 (m, 1H), 3,27 (m, 1 H), 2,94 (m, 1 H), 2,05 (m, 2H), 1,72 (m, 1H), 1,56 (m, 1H)
Ejemplo 207: Preparación de dihidrocloruro de ácido 7-cloro-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxílico
El compuesto del epígrafe (25 mg, rendimiento: 77%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó ácido 7-cloro-1 H-indol-3-carboxílico en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,00 (m, 2H), 7,16 (m, 2H), 6,22 (m, 1H), 5,91 (m, 1H), 4,90 (m, 2H), 3,53 (m, 2H), 2,96 (m, 1 H), 1,99 (m, 2H), 1,71 (m 1H), 1,55 (m, 1H)
Ejemplo 208: Preparación de dihidrocloruro de ácido 6-fluoro-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxílico
El compuesto del epígrafe (24 mg, rendimiento: 81%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó ácido 6-fluoro-1 H-indol-3-carboxílico en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 57,99 (m, 2H), 7,15 (m, 1H), 6,95 (m, 1H), 6,21 (m, 1H), 5,90 (m, 1 H), 4,87 (m, 2H), 3,60 (m, 1 H), 3,51 (m, 1H), 3,26 (m, 1 H), 2,94 (m, 1 H), 2,01 (m, 2H), 1,71 (m, 1H), 1,56 (m, 1H)
Ejemplo 209: Preparación de dihidrocloruro de ácido 1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico
El compuesto del epígrafe (20 mg, rendimiento: 78%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó ácido 1H-indol-3-carboxílico en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,05 (d, 1H), 7,99 (d, 1H), 7,45 (d, 1H), 7,16 (m, 2H), 6,22 (m, 1H), 5,91 (m, 1H), 4,83 (m, 2H), 4,37 (m, 1H), 3,61 (m, 1 H), 3,52 (m, 1 H), 2,94 (m, 1H), 2,00 (m, 2H), 1,69 (m, 1H), 1,53 (m, 1H) Ejemplo 210: Preparación de dihidrocloruro de 4-cloro-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxilato de metilo
El compuesto del epígrafe (18 mg, rendimiento: 82%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó metilo 4-cloro-1 H-indol-3-carboxilato de metilo en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,05 (s, 1H), 7,44 (d, 1H), 7,20 (m, 2H), 6,17 (m, 1H), 5,42 (m, 1H), 4,98 (m, 2H), 3,84 (s, 3H), 3,45 (m, 2H), 3,18 (m, 1H), 2,89 (m, 1H), 1,94 (m, 2H), 1,64 (m, 1H), 1,50 (m, 1H)
Ejemplo 211: Preparación de dihidrocloruro de 6-cloro-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxilato de metilo
El compuesto del epígrafe (28 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó metilo 6-cloro-1 H-indol-3-carboxilato de metilo en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,02 (m, 2H), 7,56 (s, 1H), 7,22 (t, 1H), 6,17 (m, 1H), 5,45 (m, 1H), 4,96 (m, 2H), 3,87 (s, 3H), 3,46 (m, 2H), 3,20 (m, 1H), 2,89 (m, 1H), 1,95 (m, 2H), 1,65 (m, 1H), 1,51 (m, 1H)
Ejemplo 212: Preparación de dihidrocloruro de 7-cloro-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxilato de metilo
El compuesto del epígrafe (28 mg, rendimiento: 84%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó metilo 7-cloro-1 H-indol-3-carboxilato de metilo en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,08 (d, 1H), 8,03 (s, 1H), 7,25 (d, 1H), 7,16 (m, 1H), 6,26 (m, 1H), 5,28 (m, 2H), 3,89 (s, 3H), 3,65 (s, 1H), 3,46 (m, 2H), 3,16 (m, 1H), 2,90 (m, 1H), 1,95 (m, 2H), 1,60 (m, 1H), 1,50 (m, 1H)
Ejemplo 213: Preparación de dihidrocloruro de 5-bromo-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxilato de metilo
El compuesto del epígrafe (30 mg, rendimiento: 85%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó metilo 5-bromo-1 H-indol-3-carboxilato de metilo en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,19 (d, 1H), 8,04 (d, 1H), 7,36 (m, 2H), 6,17 (m, 1H), 5,46 (m, 1H), 4,97 (m, 2H), 3,90 (s, 3H), 3,43 (m, 2H), 3,20 (m, 1 H), 2,88 (m, 1 H), 1,97 (m, 2H), 1,66 (m, 1H), 1,51 (m, 1H)
Ejemplo 214: Preparación de dihidrocloruro de 6-bromo-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxilato de metilo
El compuesto del epígrafe (31 mg, rendimiento: 83%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó metilo 6-bromo-1 H-indol-3-carboxilato de metilo en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 57,96 (m, 2H), 7,71 (s, 1H), 7,33 (m, 1H), 6,17 (m, 1H), 5,44 (m, 1H), 4,96 (m, 2H), 3,87 (s, 3H), 3,47 (m, 2H), 3,19 (m, 1 H), 2,89 (m, 1 H), 1,97 (m, 2H), 1,65 (m, 1 H), 1,51 (m, 1H)
Ejemplo 215: Preparación de dihidrocloruro de 5-bromo-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-N-metil-1H-indol-3-carboxamida
El compuesto del epígrafe (21 mg, rendimiento: 86%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5-bromo-N-metil-1 H-indol-3-carboxamida en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,25 (m, 1H), 7,84 (s, 1H), 7,34 (m, 2H), 6,16 (m, 1H), 5,38 (m, 1H), 4,89 (m, 2H), 3,44 (m, 2H), 3,16 (m, 1H), 2,86 (m, 4H), 1,94 (m, 2H), 1,63 (m, 1H), 1,48 (m, 1H)
Ejemplo 216: Preparación de dihidrocloruro de 5-bromo-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-N,N-dimetil-1 H-indol-3-carboxamida
El compuesto del epígrafe (21 mg, rendimiento: 86%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 5-bromo-N,N-dimetil-1H-indol-3-carboxilamida en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN(500MHz, MeOD): 57,95 (s, 1H), 7,71 (s, 1H), 7,41 (d, 1H), 7,34 (m, 1 H), 6,14 (m, 1H), 5,39 (m, 1H), 4,96 (m, 2H), 3,45 (m, 2H), 3,16 (m, 7H), 2,89 (m, 1H), 1,97 (m, 2H), 1,65 (m, 1H), 1,50 (m, 1H)
Ejemplo 217: Preparación de dihidrocloruro de (2R,3S)-2-((Z)-3-(5-cloro-4-metil-1H-benzo[d]imidazol-1-il)-2-fluoroprop-1-enil)piperidin-3-ol
El compuesto del epígrafe (25 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 2-fluoro-2-fosfonoacetato de trietilo en lugar de (carbetoximetilen)trifenilfosforano en la Etapa 166-1 del Ejemplo 166, y 5-cloro-4-metil-1H-benzo[d]imidazol en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,30 (s, 1H), 7,52 (d, 1H), 7,32 (d, 1H), 5,36 (m, 1H), 5,25 (m, 1H), 5,19 (m, 1H), 3,36 (t, 1 H), 3,31 (m, 1H), 3,10 (d, 1H), 2,79 (m, 1H), 2,61 (s, 3H), 2,15 (m, 1H), 1,87 (m, 1H), 1,68 (m, 1H), 1,56 (m, 1H)
Ejemplo 218: Preparación de dihidrocloruro de (2R,3S)-2-((Z)-3-(5-bromo-4-metil-1H-benzo[d]imidazol-1-il)-2-fluoroprop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (27 mg, rendimiento: 81%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 2-fluoro-2-fosfonoacetato de trietilo en lugar de (carbetoximetilen)trifenilfosforano en la Etapa 166-1 del Ejemplo 166, y 5-bromo-4-metil-1H-benzo[d]imidazol en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,29 (s, 1H), 7,46 (s, 2H), 5,35 (m, 1H), 5,25 (m, 1H), 5,21 (m, 1H), 3,54 (t, 1H), 3,41 (m, 1H), 3,12 (d, 1 H), 2,77 (m, 1 H), 2,63 (s, 3H), 2,15 (m, 1 H), 1,87 (m, 1 H), 1,68 (m, 1 H), 1,56 (m, 1H)
Ejemplo 219: Preparación de dihidrocloruro de (2R,3S)-2-((Z)-3-(5,6-dicloro-1H-benzo[d]imidazol-1-il)-2-fluoroprop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (35 mg, rendimiento: 84%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 2-fluoro-2-fosfonoacetato de trietilo en lugar de (carbetoximetilen)trifenilfosforano en la Etapa 166-1 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,38 (s, 1 H), 8,00 (s, 1H), 7,80 (s, 1H), 5,26 (m, 3H), 3,59 (t, 1H), 3,42 (m, 1 H), 3,14 (d, 1H), 2,83 (t, 1H), 2,14 (m, 1H), 1,89 (d, 1 H), 1,69 (m, 1 H), 1,58 (m, 1H)
Ejemplo 220: Preparación de dihidrocloruro de (2R,3S)-2-((Z)-3-(5,6-dicloro-2-(hidroximetil)-1H-benzo[d]imidazol-1-il)-2-fluoroprop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (30 mg, rendimiento: 79%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó 2-fluoro-2-fosfonoacetato de trietilo en lugar de (carbetoximetilen)trifenilfosforano en la Etapa 166-1 del Ejemplo 166, y (5,6-dicloro-1 H-benzo[d]imidazol-2-il)metanol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,01 (s, 1 H), 7,71 (s, 1 H), 5,41 (m, 3H), 4,85 (m, 2H), 3,80 (m, 1H), 3,57 (m, 2H), 3,26 (s, 1H), 2,96 (t, 1 H), 2,18 (m, 1H), 1,98 (m, 1H), 1,73 (m, 1 H), 1,63 (m, 1 H)
Ejemplo 221: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5-cloro-4-metil-1H-benzo[d]imidazol-1-il)-2-metilprop-1 -en-1 -il)piperidin-3-ol
El compuesto del epígrafe (27 mg, rendimiento: 81%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó (1 -etoxicarboniletilidenodien)trifenilfosforano en lugar de (carbetoximetilen)trifenilfosforano en la Etapa 166-1 del Ejemplo 166, y 5-cloro-4-metil-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,21 (s, 1 H), 7,39 (d, 1H), 7,31 (d, 1H), 5,13 (d, 1H), 4,93 (m, 2H), 3,62 (t, 1 H), 3,39 (m, 1H), 3,15 (m, 1 H), 2,87 (m, 1H), 2,62 (s, 3H), 2,06 (m, 1H) 1,93 (m, 1H), 1,78 (s, 3H), 1,62 (m, 1H), 1,57 (m, 1H) Ejemplo 222: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5-bromo-4-metil-1H-benzo[d]imidazol-1-il)-2-metilprop-1 -en-1 -il)piperidin-3-ol
El compuesto del epígrafe (34 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó (1 -etoxicarboniletilidenodien)trifenilfosforano en lugar de (carbetoximetilen)trifenilfosforano en la Etapa 166-1 del Ejemplo 166, y 5-bromo-4-metil-1H-benzo[d]imidazol en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 58,20 (s, 1 H), 7,47 (d, 1H), 7,35 (d, 1H), 5,12 (d, 1H), 4,93 (m, 2H), 3,62 (t, 1 H), 3,40 (m, 1H), 3,15 (m, 1 H), 2,86 (m, 1 H), 2,64 (s, 3H), 2,06 (m, 1H), 1,92 (m, 1H), 1,78 (s, 3H), 1,66 (m, 1 H), 1,56 (m, 1 H) Ejemplo 223: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5,6-dicloro-1H-benzo[d]imidazol-1-il)-2-metilprop-1 -en-1 -il)piperidin-3-ol
El compuesto del epígrafe (28 mg, rendimiento: 78%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó (1-etoxicarboniletiliden)trifenilfosforano en lugar de (carbetoximetilen)trifenilfosforano en la Etapa 166-1 del Ejemplo 166.1
1H-RMN(500 MHz, MeOD): 58,28 (s, 1H), 7,83 (s, 2H), 5,18 (d, 1H), 4,91 (m, 2H), 3,48 (t, 1H), 3,07 (d, 1H), 2,76 (t, 1H), 2,07 (m, 1 H), 1,86 (m, 1 H), 1,76 (s, 3H), 1,62 (m, 1H), 1,46 (m, 1H)
Ejemplo 224: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5,6-dicloro-2-(hidroximetil)-1H-benzo[d]imidazol-1-il)-2-metilprop-1-en-1-il)piperidin-3-ol
El compuesto del epígrafe (31 mg, rendimiento: 78%) se obtuvo del mismo modo que en el Ejemplo 166, con la excepción de que se usó (1-etoxicarboniletiliden)trifenilfosforano en lugar de (carbetoximetilen)trifenilfosforano en la Etapa 166-1 del Ejemplo 166, y 5,6-dicloro-1H-benzo[d]imidazol-2-il)metanol en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 166-5 del Ejemplo 166.
1H-RMN (500 MHz, MeOD): 57,79 (s, 2H), 5,03 (m, 2H), 4,89 (m, 3H), 3,70 (t, 1H), 3,40 (m, 1H), 3,14 (m, 1H), 2,92 (m, 1 H), 2,03 (m, 1H), 1,94 (m, 1 H), 1,84 (s, 3H), 1,65 (m, 1H), 1,55 (m, 1 H)
Ejemplo 225: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5,6-dicloro-1H-benzo[d]imidazol-1-il)prop-1-in-1-il)piperidin-3-ol
Etapa 225-1: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(E)-3-etoxi-3-oxoprop-1-en-1-il)piperidino-1-carboxilato de terc-butilo
Se añadieron cloruro de metileno (47 ml, 0,12 M) y cloruro de oxalilo (1,0 ml, 11,6 mmol) a un matraz cargado con argón y la solución de reacción se enfrió hasta -78°C. A continuación, se añadió dimetilsulfóxido (1,7 ml, 23,2 mmol) a la misma temperatura y se agitó durante 30 minutos. A continuación, se disolvió (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(hidroximetil)piperidino-1 -carboxilato de terc-butilo (2,0 g, 5,8 mmol) en una pequeña cantidad de cloruro de metileno y se añadió lentamente. Después de agitar a la misma temperatura durante 1 hora, se añadió trietilamina (3,3 ml, 23,2 mmol) y la temperatura de la solución de reacción se elevó hasta temperatura ambiente desde -78°C. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió y se secó con sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se disolvió en cloruro de metileno (47 ml, 0,12 M), y se añadió a esto (carbetoximetilen)trifenilfosforano (4,0 g, 11,6 mmol) a temperatura ambiente y se agitó durante 2 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida, y se purificó mediante cromatografía en columna (hexano:acetato de etilo = 4:1) para dar el compuesto del epígrafe (2,1 g, 89% de rendimiento a lo largo de dos etapas).
Etapa 225-2: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-etoxi-3-oxoprop-1 -in-1 -il)piperidino-1 -carboxilato de terc-butilo
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(E)-3-etoxi-3-oxoprop-1-en-1-il)piperidino-1-carboxilato de terc-butilo (3,2 g, 7,7 mmol) obtenido a partir de la Etapa 225-1 se disolvió en metanol (50 ml, 0,15 M), y se añadió a esto un catalizador de Lindlar (82 mg, 0,77 mmol). Después de conectar un globo de hidrógeno, la mezcla se agitó a temperatura ambiente durante 5 horas. Cuando la reacción se completaba, la solución de reacción se filtraba a través de Celite y se concentraba bajo presión reducida. Las reacciones posteriores se llevaron a cabo sin un procedimiento de purificación.
Etapa 225-3: Preparación de ácido 3-((2R,3S)-1-(terc-butoxicarbonil)-3-(terc-butildimetilsilil)oxi)piperidin-2-il)propenoico
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-etoxi-3-oxoprop-1-in-1 -il)piperidino-1 -carboxilato de terc-butilo (3,0 g, 7,2 mmol) obtenido a partir de la Etapa 225-2 se disolvió en metanol (20 ml, 0,36 M), y a continuación se añadió a esto solución acuosa de hidróxido sódico 2 N (10 ml) y se agitó a temperatura ambiente durante 3 horas. Cuando la reacción
se completaba, la solución de reacción se neutralizaba con solución acuosa de ácido clorhídrico 1 N, se acidificaba, se diluía con acetato de etilo y a continuación se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida. Las reacciones posteriores se llevaron a cabo sin un procedimiento de purificación.
Etapa 225-4: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-hidroxiprop-1 -in-1 -il)piperidino-1 -carboxilato de terc-butilo
El ácido 3-((2R,3S)-1-(terc-butoxicarbonil)-3-(terc-butildimetilsilil)oxi)piperidin-2-il)propenoico (1,6 g, 4,0 mmol) obtenido a partir de la Etapa 225-3 se disolvió en tetrahidrofurano (50 ml, 0,08 M), y la solución de reacción se enfrió hasta 0°C. A continuación, se añadió lentamente a esto una solución de hidruro de litio y aluminio (1,6 ml, 4,0 mmol), se hizo reaccionar a la misma temperatura durante 30 minutos y a continuación se agitó a temperatura ambiente durante 2 horas. Se añadió una pequeña cantidad de agua para completar la reacción, se diluyó con acetato de etilo y se lavó con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (diclorometano:metanol = 10:1) para dar el compuesto del epígrafe (1,3 g, rendimiento: 85%).
Etapa 225-5: Preparación de (2R,3S)-2-(3-bromoprop-1 -in-1 -il)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-hidroxiprop-1 -in-1 -il)piperidino-1 -carboxilato de terc-butilo (100 mg, 0,27 mmol) obtenido a partir de la Etapa 225-4 se añadió a cloruro de metileno (100 ml, 0,03 M). La solución de reacción se enfrió hasta 0°C, y a continuación se añadieron secuencialmente a la misma temperatura trifenilfosfina (107 g, 0,41 mmol) y tetrabromometano (135 g, 0,41 mmol), seguido por agitación a temperatura ambiente durante 2 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió y se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (hexano:acetato de etilo = 5:1) para dar el compuesto del epígrafe (89 g, rendimiento: 76%).
Etapa 225-6: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-(5,6-dicloro-1H-benzo[d]imidazol-1-il)prop-1-in-1 -il)piperidino-1 -carboxilato de terc-butilo
El (2R,3S)-2-(3-bromoprop-1 -in-1 -il)-3-((terc-butildimetilsilil)oxi)piperidino-1 -carboxilato de terc-butilo (200 mg, 0,46 mmol) obtenido a partir de la Etapa 225-5 se disolvió en N,N-dimetilformamida (5 ml, 0,69 M). A continuación, se añadieron a esto carbonato potásico (127 mg, 0,92 mmol) y 5,6-dicloro-1 H-benzo[d]imidazol (86 mg, 0,46 mmol), y la mezcla se agitó a temperatura ambiente durante 4 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato sódico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (hexano:acetato de etilo = 1:2) para dar el compuesto del epígrafe (293 mg, rendimiento 85%).
Etapa 225-7: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5,6-dicloro-1H-benzo[d]imidazol-1-il)prop-1-in-1-il)piperidin-3-ol
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -in-1 -il)piperidino-1 -carboxilato de terc-butilo (293 mg, 0.54 mmol) obtenido a partir de la Etapa 225-6 se disolvió en una pequeña cantidad de tetrahidrofurano y se añadió a esto solución en dioxano de cloruro de hidrógeno 4 N (5 ml, 0,10 M), y la mezcla se calentó y se agitó a temperatura ambiente durante 12 horas. Cuando la reacción se completaba, la solución de reacción se concentraba bajo presión reducida para retirar el disolvente, se disolvía mediante la adición de una pequeña cantidad de metanol y a continuación se cristalizaba en éter dietílico para dar el compuesto del epígrafe (176 mg, rendimiento: 82%).
1H-RMN (500 MHz, MeOD): 58,44 (a, 1H), 7,99 (s, 1H), 7,88 (s, 1 H), 5,34 (s, 2H), 4,11 (m, 1 H), 3,90 (m, 1H), 3,22 (m, 1H), 3,04 (m, 1 H), 1,99 (m, 2H), 1,65 (m, 2H)
Ejemplo 226: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-bromo-4-metil-1H-benzo[d]imidazol-1-il)prop-1-in-1-il)piperidin-3-ol
El compuesto del epígrafe (42 mg, rendimiento: 85%) se obtuvo del mismo modo que en el Ejemplo 225, con la excepción de que se usó 5-bromo-4-metil-1H-benzo[d]imidazol en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 225-6 del Ejemplo 225.
1H-RMN (500 MHz, MeOD): 5961 (m, 1H), 7,86 (m, 1H), 7,78 (m, 1H), 5,57 (d, 2H), 4,86 (m, 1H), 4,16 (m, 1H), 3,97 (m, 1H), 3,06 (m, 1H), 2,72 (s, 3H), 2,02 (m, 2H), 1,65 (m, 2H)
Ejemplo 227: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-cloro-4-metil-1H-benzo[d]imidazol-1-il)prop-1-in-1 -il)piperidin-3-ol
El compuesto del epígrafe (35 mg, rendimiento: 81%) se obtuvo del mismo modo que en el Ejemplo 225, con la excepción de que se usó 5-cloro-4-metil-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 225-6 del Ejemplo 225.
1H-RMN (500 MHz, MeOD): 59,65 (s, 1H), 7,86 (d, 1H), 7,71 (d, 1H), 5,57 (s, 2H), 4,82 (m, 1H), 4,16 (m, 1H), 3,95 (m, 1H), 3,05 (m, 1H), 2,17 (s, 3H), 2,00 (m, 2H), 1,63 (m, 2H)
Ejemplo 228: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5,6-dibromo-1H-benzo[d]imidazol-1-il)prop-1-in-1-il)piperidin-3-ol
El compuesto del epígrafe (30 mg, rendimiento: 80%) se obtuvo del mismo modo que en el Ejemplo 225, con la excepción de que se usó 5,6-dibromo-1H-benzo[d]imidazol en lugar de 5,6-dicloro-1H-benzo[d]imidazol en la Etapa 225-6 del Ejemplo 225.
1H-RMN (500 MHz, MeOD): 59,18 (a, 1H), 8,39 (s, 1H), 8,20 (m, 1H), 5,47 (s, 2H), 4,88 (m, 1H), 4,16 (m, 1H), 3,94 (m, 1H), 3,06 (m, 1H), 1,99 (m, 2H), 1,68 (m, 2H)
Ejemplo 229: Preparación de dihidrocloruro de (2R,3S)-2-(3-(5-fluoro-4-metil-1H-benzo[d]imidazol-1-il)prop-1-in-1 -il)piperidin-3-ol
El compuesto del epígrafe (28 mg, rendimiento: 75%) se obtuvo del mismo modo que en el Ejemplo 225, con la excepción de que se usó 5-fluoro-4-metil-1 H-benzo[d]imidazol en lugar de 5,6-dicloro-1 H-benzo[d]imidazol en la Etapa 225-6 del Ejemplo 225.
1H-RMN (500 MHz, MeOD): 58,44 (a, 1H), 7,99 (s, 1H), 7,88 (s, 1 H), 5,34 (s, 2H), 4,11 (m, 1 H), 3,90 (m, 1H), 3,22 (m, 1H), 3,04 (m, 1 H), 1,99 (m, 2H), 1,65 (m, 2H)
Ejemplo 230: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5,6-dicloro-1H-benzo[d]imidazol-1-il)prop-1-en-1 -il)pirrolidin-3-ol
Etapa 230-1: Preparación de ácido (2R,3S)-1 -(terc-butoxicarbonil)-3-((terc-butildimetilsilil)oxi)pirrolidino-2-carboxílico
Se disolvió ácido (2R,3S)-1-(terc-butoxicarbonil)-3-hidroxipirrolidino-2-carboxílico (10,7 g, 46,2 mmol) en N,N-dimetilformamida (100 ml, 0,46 M). A continuación, la solución de reacción se enfrió hasta 0°C, y se añadieron a esto cloruro de terc-butildimetilsililo (20,9 g, 138,6 mmol) y trietilamina (32,2 ml, 231,0 mmol). La solución de reacción se agitó a temperatura ambiente durante 12 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (diclorometano:metanol = 7: 1) para dar el compuesto del epígrafe (14,4 g, rendimiento: 90%).
Etapa 230-2: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-(hidroximetil)pirrolidino-1 -carboxilato de terc-butilo
El ácido (2R,3S)-1-(terc-butoxicarbonil)-3-((terc-butildimetilsilil)oxi)pirrolidino-2-carboxílico (2,0 g, 4,3 mmol) obtenido a partir de la Etapa 230-1 se disolvió en tetrahidrofurano (50 ml, 0,09 M). A continuación, la solución de reacción se enfrió hasta 0°C y se añadió a esto una solución de borano (5,2 ml, 4,7 mmol). La solución de reacción se agitó a la misma temperatura durante 1 hora y a continuación se agitó a temperatura ambiente durante 2 horas. Se añadió una pequeña cantidad de metanol para completar la reacción. Después de retirar el disolvente, la solución de reacción se diluyó con acetato de etilo y se lavó con solución saturada de cloruro sódico. La capa orgánica se recogió y la mezcla resultante se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (hexano:acetato de etilo = 3:1) para dar el compuesto del epígrafe (1,1 g, rendimiento 80%).
Etapa 230-3: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-((E)-3-etoxi-3-oxoprop-1 -en-1 -il)pirrolidino-1 -carboxilato de terc-butilo
Se añadieron cloruro de metileno (61 ml, 0,12 M) y cloruro de oxalilo (0,76 ml, 8,7 mmol) a un matraz cargado con argón y la solución de reacción se enfrió hasta -78°C. A continuación se añadió a la misma temperatura N,N-dimetilsulfóxido (1,2 ml, 17,4 mmol) y se agitó durante 30 minutos. A continuación, el (2R,3S)-3-((tercbutildimetilsilil)oxi)-2-(hidroximetil)pirrolidino-1 -carboxilato de terc-butilo (1.4 g, 4,3 mmol) obtenido a partir de la Etapa 230-2 se disolvió en una pequeña cantidad de cloruro de metileno y se añadió lentamente. Después de agitar a la misma temperatura durante 1 hora, se añadió trietilamina (2,4 ml, 17,4 mmol) y la temperatura de la solución de reacción se elevó hasta temperatura ambiente desde -78°C. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó con sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se disolvió en cloruro de metileno (20 ml, 0,22 M), y se añadió a esto a temperatura ambiente (carbetoximetilen)trifenilfosforano (3,0 g, 8,7 mmol) y se agitó durante 2 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (hexano:acetato de etilo = 4:1) para dar el compuesto del epígrafe (1,5 g, rendimiento: 87%).
Etapa 230-4: Preparación de ácido (E)-3-((2R,3S)-1-(terc-butoxicarbonil)-3-((terc-butildimetilsilil)oxi)pirrolidin-2-il)acrílico
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-((E)-3-etoxi-3-oxoprop-1-en-1-il)pirrolidino-1-carboxilato de terc-butilo (1,5 g, 3,8 mmol) obtenido a partir de la Etapa 230-3 se disolvió en etanol (27 ml, 0,14 M), y a continuación se añadió a esto solución acuosa de hidróxido sódico 2 N (8 ml) y se agitó a temperatura ambiente durante 3 horas. Cuando la reacción se completaba, la solución de reacción se neutralizaba con solución acuosa de ácido clorhídrico 1 N, se acidificaba y a continuación se diluía con acetato de etilo, y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida. Las reacciones posteriores se llevaron a cabo sin un procedimiento de purificación.
Etapa 230-5: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-((E)-3-hidroxiprop-1 -en-1 -il)pirrolidin-1 -carboxilato de terc-butilo
El ácido (E)-3-((2R,3S)-1-(terc-butoxicarbonil)-3-((terc-butildimetilsilil)oxi)pirrolidin-2-il)acrílico (400 mg, 1,1 mmol) obtenido a partir de la Etapa 230-4 se disolvió en tetrahidrofurano (10 ml, 0,1 M), y la solución de reacción se enfrió hasta 0°C. A continuación, se añadió lentamente a esto una solución de hidruro de litio y aluminio (0,43 ml, 1,1 mmol), se hizo reaccionar a la misma temperatura durante 30 minutos y a continuación se agitó a temperatura ambiente durante 2 horas. Se añadió una pequeña cantidad de agua para completar la reacción, se diluyó con acetato de etilo y se lavó con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato magnésico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (diclorometano:metanol = 10:1) para dar el compuesto del epígrafe (328 g, rendimiento: 85%).
Etapa 230-6: Preparación de (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-((E)-3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)pirrolidino-1 -carboxilato de terc-butilo
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-((E)-3-hidroxiprop-1 -en-1 -il)pirrolidin-1 -carboxilato de terc-butilo (177 mg, 0,49 mmol) obtenido a partir de la Etapa 230-5 se añadió a cloruro de metileno (5 ml, 0,1 M). La solución de reacción se enfrió hasta 0°C, y a continuación se añadieron secuencialmente a la misma temperatura una solución acuosa al 50% de hidróxido potásico (0,05 ml, 0,49 mmol) y cloruro de paratoluenosulfonilo (104 mg, 0,55 mmol), seguido por agitación a temperatura ambiente durante 2 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió y se secó sobre sulfato magnésico, se filtró y a continuación se concentró bajo presión reducida, y se disolvió en N,N-dimetilformamida (3 ml, 0,16 M). A continuación, se añadieron a esto carbonato potásico (53 mg, 0,38 mmol) y 5,6-dicloro-1H-benzo[d]imidazol (92 mg, 0.49 mmol) y se agitaron a temperatura ambiente durante 4 horas. Cuando la reacción se completaba, el disolvente se retiraba, y la mezcla resultante se diluía con acetato de etilo y se lavaba con solución saturada de cloruro sódico. La capa orgánica se recogió, se secó sobre sulfato sódico, se filtró y se concentró bajo presión reducida, y a continuación se purificó mediante cromatografía en columna (hexano:acetato de etilo =1:1) para dar el compuesto del epígrafe (155 mg, rendimiento: 60%).
Etapa 230-7: Preparación de dihidrocloruro de (2R,3S)-2-((E)-3-(5,6-dicloro- 1H-benzo[d]imidazol-1-il)prop-1-en-1-il)pirrolidin-3-ol
El (2R,3S)-3-((terc-butildimetilsilil)oxi)-2-((E)-3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)pirrolidino-1 -carboxilato de terc-butilo (43 mg, 0,08 mmol) obtenido a partir de la Etapa 230-6 se disolvió en una pequeña cantidad de tetrahidrofurano y a continuación se añadió a esto solución de dioxano de cloruro de hidrógeno 4 N (2 ml, 0,04 M) y la mezcla se agitó a temperatura ambiente durante 12 horas. Cuando la reacción se completaba, la solución de reacción se concentraba bajo presión reducida para retirar el disolvente, se disolvía mediante la adición de una pequeña cantidad de metanol, y a continuación se cristalizaba con éter dietílico para dar el compuesto del epígrafe (25 mg, rendimiento 79%).
1H-RMN (500 MHz, DMSO-ds): 58,80 (s, 1H), 8,11 (s, 1H), 8,04 (s, 1H), 6,12 (m, 1H), 5,78 (m, 1H), 5,02 (d, 2H), 4,05 (m, 1H), 3,81 (m, 1H), 3,22 (m, 2H), 2,10 (m, 1H), 1,79 (m, 1H)
Ejemplo Experimental: Experimento de inhibición de la actividad de la enzima PRS
A fin de confirmar las actividades biológicas de los compuestos preparados en los Ejemplos, se calcularon valores del % de inhibición o IC50 de las actividades de la enzima PRS (fosforribosilpirofosfato sintetasa).
Específicamente, se subclonó la poción correspondiente a PRS en ADNc de EPRS, y la proteína PRS de alta pureza obtenida se purificó y se usó en el experimento. Los compuestos (1 pM) preparados en los Ejemplos se añadieron al tampón de reacción (KPO4 20 mM (pH 7,4), MgAc 6 mM, ATP 5 mM, 400 mg/ml de ARNt, DTT 0,5 mM, 20 mCi[3H]prolina (1 mCi/ml)) y se dejaron reaccionar a 37°C durante de 5 a 10 minutos. La reacción se terminó con papel 3M que se secaba por adelantado mediante la adición de TCA al 5%. La radiactividad se midió usando un contador de centelleo de líquido.
Los valores de % de inhibición e IC50 de los compuestos respectivos se calcularon y se analizaron usando Microsoft Excel o Sigma Plot 8.0. Los resultados se muestran en las Tablas 1 a 3 posteriormente. En las Tablas 1 a 3, los resultados se dividen en A, B y C según el intervalo de IC50. El caso en el que la IC50 derivada es 100 nM o menos está representado por "A", el caso en el que la IC50 es de 100 a 500 nM está representado por "B", y el caso en el que la IC50 es 500 nM o más está representado por "C".
[Tabla 1]
[Tabla 2]
[Tabla 3]
Claims (230)
1. Un compuesto representado por la siguiente Fórmula Química 1, o una de sus sales farmacéuticamente aceptables:
[Fórmula Química 1]
en la Fórmula Química 1,
n es 1 o 2,
L es -CH2CH2-, -CH=C(R')- o -C=C-,
en donde R' es hidrógeno, alquilo C1-4 o halógeno,
X1 es CR1 R2, NR1 o -CO-,
X2 es CR3R4 o NR3,
en donde cada uno de R1 a R4 son independientemente hidrógeno, alquilo C 1-4, hidroxialquilo C1-4, hidroxi, amino, carboxi, -COO(alquilo C1-4), -CONH2, -CONH(alquilo C1-4), -CON (alquilo C1-4)2, o pirazolilo no sustituido o sustituido con haloalquilo C1-4; o R1 y R3, uno junto con el otro, conectan X1 y X2 a través de un doble enlace, y
A es un anillo de benceno, piridina, pirimidina o pirimidinodiona,
en donde A no está sustituido o está sustituido con de uno a tres sustituyentes seleccionados cada uno independientemente del grupo que consiste en un sustituyente de tipo anular seleccionado del grupo que consiste en furanilo, imidazolilo, isoxazolilo, fenilo, pirazolilo, piridinonilo, piridinilo, pirrolilo, tiazolilo y tiofenilo; alquilo C1-4; alcoxi C1-4; haloalquilo C1-4; haloalcoxi C1-4; halógeno; di(alquil C1-4)amino; nitro; -COO(alquilo C1-4); dihidropiranilo; morfolino; piperidinilo; y pirrolidinilo; y
en donde el sustituyente de tipo anular no está sustituido o está sustituido con uno o dos sustituyentes seleccionados cada uno independientemente del grupo que consiste en alquilo C 1-5, haloalquilo C1-4, cicloalquilo C3-6, monovalente de carbonato de alquileno C2-5, -COO(alquilo C1-4), halógeno, ciano, tiazolilo y (1,3-dioxolan-2-il)metilo.
2. El compuesto o una de sus sales farmacéuticamente aceptables según la reivindicación 1, en donde A no está sustituido o está sustituido con de uno a tres sustituyentes seleccionados cada uno independientemente del grupo que consiste en alquilo C1-4; alcoxi C1-4; haloalquilo C1-4; halógeno; fenilo no sustituido o sustituido con halógeno o haloalquilo C1-4; pirazolilo no sustituido o sustituido con alquilo C1-5, tiazolilo o haloalquilo C1-4; tiofenilo no sustituido o sustituido con alquilo C1-5 o -COO(alquil C1-4); pirrolilo no sustituido o sustituido con alquilo C1-5 y/o -COO(alquilo C1-4); di(alquil C1-4)amino; morfolino; piperidinilo; furanilo; y pirrolidinilo.
3. El compuesto o una de sus sales farmacéuticamente aceptables según la reivindicación 1, en donde L es -CH2CH2-, -CH=CH-, -CH=CF-, -CH=C(CH3)- o -C=C-.
4. El compuesto o una de sus sales farmacéuticamente aceptables según la reivindicación 1, en donde el compuesto representado por la Fórmula Química 1 está representado por las siguientes Fórmulas Químicas 1-1 a 1-5:
[Fórmula Química 1-1]
[Fórmula Química 1-2]
[Fórmula Química 1-3]
[Fórmula Química 1-4]
[Fórmula Química 1-5]
en las Fórmulas Químicas 1-1 a 1-5,
n, L, R1 a R4 y A son como se definen en la reivindicación 1.
5. El compuesto o una de sus sales farmacéuticamente aceptables según la reivindicación 1, en donde cada uno de R1 a R4 son independientemente hidrógeno, metilo, hidroximetilo, hidroxi, amino, carboxi, -COOCH3, -CONH2 , -CONHCH3 o -CON(CH3)2; o R1 y R3, uno junto con el otro, conectan X1 y X2 a través de un doble enlace.
6. El compuesto o una de sus sales farmacéuticamente aceptables según la reivindicación 1, en donde A es un anillo de benceno, piridina, pirimidina o pirimidinodiona, y A no está sustituido o está sustituido con de uno a tres sustituyentes seleccionados cada uno independientemente del grupo que consiste en metilo, isobutilo, metoxi, trifluorometilo, fluoro, cloro, bromo, fenilo, fenilo sustituido con fluoro, fenilo sustituido con cloro, fenilo sustituido con trifluorometilo, tiofenilo, tiofenilo sustituido con metilo, tiofenilo sustituido con -COOCH3, pirazolilo sustituido con difluorometilo, pirazolilo sustituido con metilo, pirazolilo sustituido con tiazolilo, pirrolilo sustituido con metilo y -COOCH2CH3, furanilo, dimetilamino, dietilamino, metiletilamino, morfolino, piperidinilo, y pirrolidinilo.
7. El compuesto o una de sus sales farmacéuticamente aceptables según la reivindicación 1, en donde A es benceno, y A no está sustituido o está sustituido con de uno a tres sustituyentes seleccionados cada uno independientemente del grupo que consiste en alquilo C1-4; alcoxi C1-4; halógeno; y fenilo no sustituido o sustituido con halógeno o haloalquilo C1-4.
8. El compuesto o una de sus sales farmacéuticamente aceptables según la reivindicación 1, en donde A es piridina, y A no está sustituido o está sustituido con uno o dos sustituyentes seleccionados cada uno independientemente del grupo que consiste en alquilo C1-4; alcoxi C1-4; halógeno; y fenilo sustituido con halógeno.
9. El compuesto o una de sus sales farmacéuticamente aceptables según la reivindicación 1, en donde A es pirimidina, y A está sustituido con un sustituyente seleccionado del grupo que consiste en halógeno; di(alquil C1-4)amino; morfolino; piperidinilo; y pirrolidinilo.
10. El compuesto o una de sus sales farmacéuticamente aceptables según la reivindicación 1, en donde A es pirimidinodiona, y A no está sustituido o está sustituido con uno o dos alquilo C1-4.
11. Un compuesto o una de sus sales farmacéuticamente aceptables, en donde el compuesto se selecciona del grupo que consiste en:
1) (2R,3S)-2-(3-(6-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
2) (2R,3S)-2-(3-(4-bromo-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
3) (2R,3S)-2-(3-(5-bromo-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
4) (2R,3S)-2-(3-(6-bromo-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
5) (2R,3S)-2-(3-(7-bromo-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
6) (2R,3S)-2-(3-(4-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
7) (2R,3S)-2-(3-(5-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
8) (2R,3S)-2-(3-(6-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
9) (2R,3S)-2-(3-(7-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
10) (2R,3S)-2-(3-(4-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
11) (2R,3S)-2-(3-(5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
12) (2R,3S)-2-(3-(7-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
13) (2R,3S)-2-(3-(6-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
14) (2R,3S)-2-(3-(5-metil-1 H-benzo[d]imidazol-1-il)propil)piperidin-3-ol,
15) (2R,3S)-2-(3-(6-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
16) (2R,3S)-2-(3-(7-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
17) (2R,3S)-2-(3-(7-(trifluorometoxi)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
18) (2R,3S)-2-(3-(4-(pirrolidin-1 -il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
19) (2R,3S)-2-(3-(4-(piperidin-1 -il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
20) (2R,3S)-2-(3-(4-(3-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
21) (2R,3S)-2-(3-(4-(3-clorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
22) (2R,3S)-2-(3-(5-(3-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
23) (2R,3S)-2-(3-(6-(2-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
24) (2R,3S)-2-(3-(6-(3-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
25) (2R,3S)-2-(3-(6-(4-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
26) (2R,3S)-2-(3-(7-(2-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
27) (2R,3S)-2-(3-(7-(3-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
28) (2R,3S)-2-(3-(7-(4-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
29) (2R,3S)-2-(3-(5-(1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
30) (2R,3S)-2-(3-(6-(1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
31) (2R,3S)-2-(3-(7-(1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
32) (2R,3S)-2-(3-(6-cloro-5-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
33) (2R,3S)-2-(3-(6-bromo-5-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
34) (2R,3S)-2-(3-(5-cloro-6-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
35) (2R,3S)-2-(3-(5-bromo-6-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
36) (2R,3S)-2-(3-(6-bromo-5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
37) (2R,3S)-2-(3-(6-cloro-5-metoxi-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
38) (2R,3S)-2-(3-(6-fluoro-5-metoxi-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
39) (2R,3S)-2-(3-(5-fluoro-6-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
40) (2R,3S)-2-(3-(4,5-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
41) (2S,3S)-2-(3-(4,5-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
42) (2S,3R)-2-(3-(4,5-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
43) (2R,3R)-2-(3-(4,5-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
44) (2R,3S)-2-(3-(4-cloro-5-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
45) (2R,3S)-2-(3-(5-bromo-4-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
46) (2R,3S)-2-(3-(5-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
47) (2R,3S)-2-(3-(5-bromo-4-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
48) (2R,3S)-2-(3-(6-bromo-7-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
49) (2R,3S)-2-(3-(4,5-difluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
50) (2R,3S)-2-(3-(6,7-difluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
51) (2R,3S)-2-(3-(4,5-dimetil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
52) (2R,3S)-2-(3-(5,6-difluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
53) (2R,3S)-2-(3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
54) (2R,3S)-2-(3-(5,6-dibromo-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
55) (2R,3S)-2-(3-(5,6-dimetil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
56) (2R,3S)-2-(3-(6,7-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
57) (2R,3S)-2-(3-(4,6-difluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
58) (2R,3S)-2-(3-(5,7-difluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
59) (2R,3S)-2-(3-(4-cloro-5-metoxi-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
60) (2R,3S)-2-(3-(7-cloro-6-metoxi-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
61) (2R,3S)-2-(3-(6-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
62) (2R,3S)-2-(3-(4-cloro-5-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
63) (2R,3S)-2-(3-(6-bromo-4-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
64) (2R,3S)-2-(3-(5-fluoro-4-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
65) (2R,3S)-2-(3-(6-fluoro-7-metil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
66) (2R,3S)-2-(3-(4-cloro-5-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
67) (2R,3S)-2-(3-(7-cloro-6-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
68) 7-bromo-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-5-carboxilato de metilo,
69) (2R,3S)-2-(3-(7-bromo-5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
70) (2R,3S)-2-(3-(5-bromo-7-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
71) (2R,3S)-2-(3-(7-bromo-5-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
72) (2R,3S)-2-(3-(6-bromo-4-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
73) (2R,3S)-2-(3-(5-bromo-7-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
74) (2R,3S)-2-(3-(7-cloro-4-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
75) (2R,3S)-2-(3-(5-bromo-4-nitro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
76) (2R,3S)-2-(3-(6-bromo-7-nitro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
77) (2R,3S)-2-(3-(4-cloro-5-nitro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
78) (2R,3S)-2-(3-(7-cloro-5-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
79) (2R,3S)-2-(3-(5-cloro-7-fluoro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
80) (2R,3S)-2-(3-(5,7-dicloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
81) (2R,3S)-2-(3-(5-cloro-7-(1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
82) (2R,3S)-2-(3-(7-(1 H-pirazol-4-il)-5-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
83) (2R,3S)-2-(3-(5-cloro-7-(3-fluorofenil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
84) (2R,3S)-2-(3-(7-(3-fluorofenil)-5-(trifluorometil)-1 H-benzo[d]imidazol-1-il)propil)piperidin-3-ol,
85) (2R,3S)-2-(3-(5-cloro-7-(2-metiltiazol-5-il)-1 H-benzo[d]imidazol-1-il)propil)piperidin-3-ol,
86) (2R,3S)-2-(3-(5-cloro-7-(piridin-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
87) (2R,3S)-2-(3-(5-cloro-7-(5-fluoropiridin-3-il)-1 H-benzo[d]imidazol-1-il)propil)piperidin-3-ol,
88) 5-(5-cloro-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-7-il)-1 -metilpiridin-2(1 H)-ona,
89) (2R,3S)-2-(3-(5-cloro-7-(1 -(difluorometil)-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
90) (2R,3S)-2-(3-(5-cloro-7-(isoxazol-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
91) (2R,3S)-2-(3-(5-cloro-7-(tiofen-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
92) (2R,3S)-2-(3-(5-cloro-7-(2-metiltiofen-3-il)-1 H-benzo[d]imidazol-1-il)propil)piperidin-3-ol,
93) (2R,3S)-2-(3-(5-cloro-7-(3,5-dimetilisoxazol-4-il)-1 H-benzo[d]imidazol-1-il)propil)piperidin-3-ol,
94) (2R,3S)-2-(3-(5-cloro-7-(3,6-dihidro-2H-piran-4-il)-1 H-benzo[d]imidazol-1-il)propil)piperidin-3-ol,
95) (2R,3S)-2-(3-(7-(1 -((1,3-dioxolan-2-il)metil)-1 H-pirazol-4-il)-5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
96) (2R,3S)-2-(3-(5-cloro-7-(1 -metil-1 H-imidazol-5-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
97) (2R,3S)-2-(3-(5-cloro-7-(1 -metil-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
98) (2R,3S)-2-(3-(7-(pirrolidin-1 -il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
99) (2R,3S)-2-(3-(5-cloro-7-(pirrolidin-1 -il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
100) (2R,3S)-2-(3-(5-cloro-7-(2-ciclopropiltiazol-5-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
101) (2R,3S)-2-(3-(5-cloro-7-(1 -(tiazol-2-il)-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
102) (2R,3S)-2-(3-(5-cloro-7-(1 -(oxetan-3-il)-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
103) (2R,3S)-2-(3-(5-cloro-7-(2-(tetrahidro-2H-piran-4-il)tiazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
104) (2R,3S)-2-(3-(5-cloro-7-(furan-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
105) 4-(5-cloro-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-7-il)tiazol-2-carbonitrilo,
106) (2R,3S)-2-(3-(7-(1 -(terc-butil)-l H-pirazol-4-il)-5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
107) (2R,3S)-2-(3-(5-cloro-7-(1 -isopentil-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
108) (2R,3S)-2-(3-(5-cloro-7-(1 -isopropil-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
109) (2R,3S)-2-(3-(5-cloro-7-(4-metiltiofen-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
110) 3-(5-cloro-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-7-il)furano-2-carboxilato de etilo,
111) 4-(5-cloro-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-7-il)tiofeno-2-carboxilato de metilo,
112) (2R,3S)-2-(3-(5-cloro-7-(1 -(2-fluoroetil)-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
113) (2R,3S)-2-(3-(7-(1 -butil-1 H-pirazol-4-il)-5-cloro-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
114) (2R,3S)-2-(3-(5-cloro-7-(2,5-dimetiltiofen-3-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
115) (2R,3S)-2-(3-(5-cloro-7-(1 -isobutil-1 H-pirazol-4-il)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
116) 4-(5-cloro-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-7-il)-1 -metil-1 H-pirrol-2-carboxilato de etilo,
117) (2R,3S)-2-(3-(5-cloro-1 H-imidazo[4,5-b]piridin-1 -il)propil)piperidin-3-ol,
118) (2R,3S)-2-(3-(5-cloro-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol,
119) (2R,3S)-2-(3-(5-bromo-1 H-imidazo[4,5-b]piridin-1 -il)propil)piperidin-3-ol,
120) (2R,3S)-2-(3-(6-bromo-1 H-imidazo[4,5-b]piridin-1 -il)propil)piperidin-3-ol,
121) (2R,3S)-2-(3-(5-metil-1 H-imidazo[4,5-b]piridin-1 -il)propil)piperidin-3-ol,
122) (2R,3S)-2-(3-(6-cloro-1 H-imidazo[4,5-c]piridin-1 -il)propil)piperidin-3-ol.
123) (2R,3S)-2-(3-(6-cloro-3H-imidazo[4,5-c]piridin-3-il)propil)piperidin-3-ol,
124) (2R,3S)-2-(3-(6-bromo-1 H-imidazo[4,5-c]piridin-1 -il)propil)piperidin-3-ol,
125) (2R,3S)-2-(3-(6-bromo-3H-imidazo[4,5-c]piridin-3-il)propil)piperidin-3-ol,
126) (2R,3S)-2-(3-(7-cloro-1 H-imidazo[4,5-b]piridin-1 -il)propil)piperidin-3-ol,
127) (2R,3S)-2-(3-(5,6-dicloro-1 H-imidazo[4,5-b]piridin-1 -il)propil)piperidin-3-ol,
128) (2R,3S)-2-(3-(7-bromo-1 H-imidazo[4,5-c]piridin-1 -il)propil)piperidin-3-ol,
129) (2R,3S)-2-(3-(5-(trifluorometil)-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol,
130) (2R,3S)-2-(3-(6,7-dicloro-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol,
131) (2R,3S)-2-(3-(6-cloro-7-metil-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol,
132) (2R,3S)-2-(3-(6-bromo-7-metil-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol,
133) (2R,3S)-2-(3-(6-bromo-7-cloro-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol,
134) (2R,3S)-2-(3-(7-cloro-6-(3-clorofenil)-3H-imidazo[4,5-b]piridin-3-il)propil)piperidin-3-ol,
135) (2R,3S)-2-(3-(2-cloro-7H-purin-7-il)propil)piperidin-3-ol,
136) (2R,3S)-2-(3-(2-cloro-9H-purin-9-il)propil)piperidin-3-ol,
137) (2R,3S)-2-(3-(6-(dimetilamino)-9H-purin-9-il)propil)piperidin-3-ol,
138) (2R,3S)-2-(3-(6-(dietilamino)-9H-purin-9-il)propil)piperidin-3-ol,
139) (2R,3S)-2-(3-(6-(etil(metil)amino)-9H-purin-9-il)propil)piperidin-3-ol,
140) (2R,3S)-2-(3-(6-morfolino-9H-purin-9-il)propil)piperidin-3-ol,
141) (2R,3S)-2-(3-(6-(piperidin-1 -il)-9H-purin-9-il)propil)piperidin-3-ol,
142) (2R,3S)-2-(3-(6-(pirrolidin-1 -il)-9H-purin-9-il)propil)piperidin-3-ol,
143) 1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-2-ol,
144) 5,6-dicloro-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-2-ol,
145) (2R,3S)-2-(3-(2-(hidroximetil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
146) (2R,3S)-2-(3-(2-(hidroximetil)-4,5-dimetil-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
147) (2R,3S)-2-(3-(5,6-dicloro-2-(hidroximetil)-1 H-benzo[d]imidazol-1 -il)propil)piperidin-3-ol,
148) (2R,3S)-2-(3-(2-amino-5,6-dicloro-1 H-benzo[d]imidazol-1-il)propil)piperidin-3-ol,
149) 7-bromo-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo,
150) 5-bromo-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo,
151) 6-bromo-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-indol-3-carboxilato de metilo,
152) 4-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo,
153) 6-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo,
154) 7-cloro-1-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1H-indol-3-carboxilato de metilo,
155) (2R,3S)-2-(3-(5-cloro-3-ciclopropil-1 H-indazol-1 -il)propil)piperidin-3-ol,
156) (2R,3S)-2-(3-(5-cloro-3-(trifluorometil)-1 H-indazol-1 -il)propil)piperidin-3-ol,
157) (2R,3S)-2-(3-(5-cloro-3-(1 -(difluorometil)-1 H-pirazol-4-il)-1 H-indazol-1 -il)propil)piperidin-3-ol,
158) (2R,3S)-2-(3-(6-cloro-3-(1 -(difluorometil)-1 H-pirazol-4-il)-1 H-indazol-1 -il)propil)piperidin-3-ol,
159) 1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-3-metil-1 H-benzo[d]imidazol-2(3H)-ona,
160) 5-bromo-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-2(3H)-ona,
161) 6-bromo-1 -(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 H-benzo[d]imidazol-2(3H)-ona,
162) 7-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1,3-dimetil-1 H-purino-2,6(3H,7H)-diona,
163) 7-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-3-metil-1 H-purino-2,6(3H,7H)-diona,
164) 9-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-1 -metil-1 H-purino-2,6(3H,9H)-diona,
165) 7-(3-((2R,3S)-3-hidroxipiperidin-2-il)propil)-3-isobutil-1 -metil-1 H-purino-2,6(3H,7H)-diona,
166) (2R,3S)-2-((E)-3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
167) (2R,3S)-2-((E)-3-(5-fluoro-4-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
168) (2R,3S)-2-((E)-3-(5-bromo-4-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
169) (2R,3S)-2-((E)-3-(5,6-dimetil-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
170) (2R,3S)-2-((E)-3-(5,6-dibromo-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
171) (2R,3S)-2-((E)-3-(5,6-difluoro-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
172) (2R,3S)-2-((E)-3-(4,5-dimetil-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
173) (2R,3S)-2-((E)-3-(5-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
174) (2R,3S)-2-((E)-3-(4,5-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol,
175) (2R,3S)-2-((E)-3-(4-cloro-5-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol,
176) (2R,3S)-2-((E)-3-(5-bromo-4-nitro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol,
177) (2R,3S)-2-((E)-3-(6-bromo-7-nitro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol,
178) (2R,3S)-2-((E)-3-(4-cloro-5-nitro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol,
179) (2R,3S)-2-((E)-3-(4,6-difluoro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol,
180) (2R,3S)-2-((E)-3-(6-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol,
181) (2R,3S)-2-((E)-3-(7-cloro-5-(trifluorometil)-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol,
182) (2R,3S)-2-((E)-3-(5,7-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol,
183) (2R,3S)-2-((E)-3-(5-cloro-7-fluoro-1 H-benzo[d]imidazol-1 -il)prop-1 -en-1 -il)piperidin-3-ol,
184) (2R,3S)-2-((E)-3-(5-bromo-1 H-imidazo[4,5-b]piridin-1 -il)prop-1 -enil)piperidin-3-ol,
185) (2R,3S)-2-((E)-3-(7-cloro-6-(3-clorofenil)-3H-imidazo[4,5-b]piridin-3-il)prop-1-enil)piperidin-3-ol,
186) (2R,3S)-2-((E)-3-(6-bromo-7-metil-3H-imidazo[4,5-b]piridin-3-il)prop-1-enil)piperidin-3-ol,
187) (2R,3S)-2-((E)-3-(6-bromo-7-cloro-3H-imidazo[4,5-b]piridin-3-il)prop-1-enil)piperidin-3-ol,
188) (2R,3S)-2-((E)-3-(6-cloro-7-metil-3H-imidazo[4,5-b]piridin-3-il)prop-1-enil)piperidin-3-ol,
189) (2R,3S)-2-((E)-3-(6,7-dicloro-3H-imidazo[4,5-b]piridin-3-il)prop-1 -enil)piperidin-3-ol,
190) (2R,3S)-2-((E)-3-(6-(3-clorofenil)-1 H-benzo[d]imidazol-1-il)prop-1-enil)piperidin-3-ol,
191) (2R,3S)-2-((E)-3-(6-(3-fluorofenil)-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
192) (2R,3S)-2-((E)-3-(6-(3-(trifluorometil)fenil)-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
193) (2R,3S)-2-((E)-3-(5-bromo-6,7-difluoro-2-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)piperidin-3-ol,
194) (2R,3S)-2-((E)-3-(indolin-1 -il)prop-1 -enil)piperidin-3-ol,
195) (2R,3S)-2-((E)-3-(5-cloroindolin-1 -il)prop-1 -enil)piperidin-3-ol,
196) (2R,3S)-2-((E)-3-(1 H-pirrolo[2,3-b]piridin-1 -il)prop-1 -enil)piperidin-3-ol,
197) (2R,3S)-2-((E)-3-(6-cloro-1 H-indol-1 -il)prop-1 -enil)piperidin-3-ol,
198) (2R,3S)-2-((E)-3-(6-cloro-1 H-indazol-1 -il)prop-1 -enil)piperidin-3-ol,
199) (2R,3S)-2-((E)-3-(4-cloro-7H-pirrolo[2,3-d]pirimidin-7-il)prop-1 -enil)piperidin-3-ol,
200) (2R,3S)-2-((E)-3-(5-cloro-1 H-pirazolo[3,4-b]piridin-1 -il)prop-1 -enil)piperidin-3-ol,
201) (2R,3S)-2-((E)-3-(3,5-dimetil-1 H-indazol-1 -il)prop-1 -enil)piperidin-3-ol,
202) 7-bromo-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxilato de metilo,
203) ácido 7-bromo-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
204) ácido 5-bromo-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
205) ácido 4-cloro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
206) ácido 6-cloro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
207) ácido 7-cloro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
208) ácido 6-fluoro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
209) ácido 1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxílico,
210) 4-cloro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxilato de metilo,
211) 6-cloro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxilato de metilo,
212) 7-cloro-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1 H-indol-3-carboxilato de metilo,
213) 5-bromo-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxilato de metilo,
214) 6-bromo-1-((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-1H-indol-3-carboxilato de metilo,
215) 5-bromo-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-N-metil-1 H-indol-3-carboxamida,
216) 5-bromo-1 -((E)-3-((2R,3S)-3-hidroxipiperidin-2-il)alil)-N,N-dimetil-1 H-indol-3-carboxamida,
217) (2R,3S)-2-((Z)-3-(5-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)-2-fluoroprop-1 -enil)piperidin-3-ol,
218) (2R,3S)-2-((Z)-3-(5-bromo-4-metil-1 H-benzo[d]imidazol-1 -il)-2-fluoroprop-1 -enil)piperidin-3-ol,
219) (2R,3S)-2-((Z)-3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)-2-fluoroprop-1 -enil)piperidin-3-ol,
220) (2R,3S)-2-((Z)-3-(5,6-dicloro-2-(hidroximetil)-1 H-benzo[d]imidazol-1 -il)-2-fluoroprop-1 -enil)piperidin-3-ol,
221) (2R,3S)-2-((E)-3-(5-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)-2-metilprop-1 -enil)piperidin-3-ol,
222) (2R,3S)-2-((E)-3-(5-bromo-4-metil-1 H-benzo[d]imidazol-1 -il)-2-metilprop-1 -enil)piperidin-3-ol,
223) (2R,3S)-2-((E)-3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)-2-metilprop-1 -enil)piperidin-3-ol,
224) (2R,3S)-2-((E)-3-(5,6-dicloro-2-(hidroximetil)-1 H-benzo[d]imidazol-1 -il)-2-metilprop-1 -enil)piperidin-3-ol,
225) (2R,3S)-2-(3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -inil)piperidin-3-ol,
226) (2R,3S)-2-(3-(5-bromo-4-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -inil)piperidin-3-ol,
227) (2R,3S)-2-(3-(5-cloro-4-metil-1 H-benzo[d]imidazol-1 -il)prop-1 -inil)piperidin-3-ol,
228) (2R,3S)-2-(3-(5,6-dibromo-1 H-benzo[d]imidazol-1 -il)prop-1 -inil)piperidin-3-ol,
229) (2R,3S)-2-(3-(5-fluoro-4-metil-1 H-benzo[d]imidazol-1-il)prop-1-inil)piperidin-3-ol, and
230) (2R,3S)-2-((E)-3-(5,6-dicloro-1 H-benzo[d]imidazol-1 -il)prop-1 -enil)pirrolidin-3-ol.
12. Una composición farmacéutica para el uso en la prevención o el tratamiento de cánceres, enfermedades inflamatorias, enfermedades autoinmunitarias o fibrosis, que comprende el compuesto según una cualquiera de las reivindicaciones 1 a 11 o una de sus sales farmacéuticamente aceptables.
13. Un método para preparar un compuesto representado por la siguiente Fórmula Química 1, que comprende las etapas de:
hacer reaccionar un compuesto representado por la siguiente Fórmula Química 1-A con un compuesto representado por la siguiente Fórmula Química 1-B en presencia de una base para preparar un compuesto representado por la siguiente Fórmula Química 1-C; y
hacer reaccionar un compuesto representado por la Fórmula Química 1-C en presencia de un ácido para preparar un compuesto representado por la siguiente Fórmula Química 1:
[Fórmula Química 1]
[Fórmula Química 1-A]
[Fórmula Química 1-B]
[Fórmula Química 1-C]
en las Fórmulas Químicas 1, 1-A, 1-B, y 1 -C,
n, L, X1 , X2 y A son como se definen en la reivindicación 1,
X es halógeno, y
cada uno de R' y R" son independientemente un grupo protector.
14. Un método para preparar un compuesto representado por la siguiente Fórmula Química 1-1, que comprende las etapas de:
hacer reaccionar un compuesto representado por la siguiente Fórmula Química 2-A con un compuesto representado por la siguiente Fórmula Química 2-B en presencia de una base para preparar un compuesto representado por la siguiente Fórmula Química 2-C;
hacer reaccionar un grupo amina y un grupo nitro del compuesto representado por la Fórmula Química 2-C para formar un anillo, preparando de ese modo un compuesto representado por la siguiente Fórmula Química 2-D; y
hacer reaccionar un compuesto representado por la Fórmula Química 2-D en presencia de un ácido para preparar un compuesto representado por la siguiente Fórmula Química 1-1:
[Fórmula Química 1-1]
[Fórmula Química 2-A]
[Fórmula Química 2-B]
[Fórmula Química 2-C]
[Fórmula Química 2-D]
en las Fórmulas Químicas 1 -1,2-A, 2-B, 2-C y 2-D,
n, L, R2 y A son como se definen en la reivindicación 1, y
cada uno de R' y R" son independientemente un grupo protector.
15. Un método para preparar un compuesto representado por la siguiente Fórmula Química 3, que comprende las etapas de:
hacer reaccionar el compuesto representado por la siguiente Fórmula Química 3-A con (carbetoximetilen)trifenilfosforano para preparar un compuesto representado por la siguiente Fórmula Química 3-B;
hidrogenar el compuesto representado por la siguiente Fórmula Química 3-B para preparar un compuesto representado por la siguiente Fórmula Química 3-C;
hidrolizar el compuesto representado por la Fórmula Química 3-C para preparar un compuesto representado por la siguiente Fórmula Química 3-D;
someter el compuesto representado por la Fórmula Química 3-D a una reacción de reducción de carbonilo para preparar un compuesto representado por la siguiente Fórmula Química 3-E;
bromar el compuesto representado por la Fórmula Química 3-E para preparar un compuesto representado por la siguiente Fórmula Química 3-F;
someter el compuesto representado por la Fórmula Química 3-F a una reacción con azida para preparar un compuesto representado por la siguiente Fórmula Química 3-G; y
aminar el compuesto representado por la Fórmula Química 3-G para preparar un compuesto representado por la siguiente Fórmula Química 3:
[Fórmula Química 3]
[Fórmula Química 3-A]
[Fórmula Química 3-B]
[Fórmula Química 3-C]
[Fórmula Química 3-D]
[Fórmula Química 3-E]
[Fórmula Química 3-F]
[Fórmula Química 3-G]
en las Fórmulas Químicas 3, 3-A, 3-B, 3-C, 3-D, 3-E, 3-F y 3-G, n es como se define en la reivindicación 1, y
cada uno de R' y R" son independientemente un grupo protector.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20170016971 | 2017-02-07 | ||
| PCT/KR2018/001625 WO2018147626A1 (en) | 2017-02-07 | 2018-02-07 | Novel heterocyclic compound, its preparation method, and pharmaceutical composition comprising the same |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2899665T3 true ES2899665T3 (es) | 2022-03-14 |
Family
ID=63107680
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES18750794T Active ES2899665T3 (es) | 2017-02-07 | 2018-02-07 | Derivados de 2-(3-(1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol y compuestos relacionados como inhibidores de PRS para el tratamiento, p. ej., del cáncer |
Country Status (31)
| Country | Link |
|---|---|
| US (1) | US10981917B2 (es) |
| EP (1) | EP3580208B1 (es) |
| JP (1) | JP6785384B2 (es) |
| KR (1) | KR102084772B1 (es) |
| CN (1) | CN110191882B (es) |
| AR (1) | AR110963A1 (es) |
| AU (1) | AU2018218965B2 (es) |
| BR (1) | BR112019016291A2 (es) |
| CA (1) | CA3049643C (es) |
| CL (1) | CL2019002019A1 (es) |
| CO (1) | CO2019007834A2 (es) |
| DO (1) | DOP2019000193A (es) |
| EC (1) | ECSP19051409A (es) |
| ES (1) | ES2899665T3 (es) |
| HR (1) | HRP20211483T1 (es) |
| HU (1) | HUE056218T2 (es) |
| MA (1) | MA47469B1 (es) |
| MX (1) | MX2019009185A (es) |
| MY (1) | MY196538A (es) |
| PE (1) | PE20191477A1 (es) |
| PH (1) | PH12019501811A1 (es) |
| PL (1) | PL3580208T3 (es) |
| PT (1) | PT3580208T (es) |
| RS (1) | RS62541B1 (es) |
| RU (1) | RU2733384C1 (es) |
| SA (1) | SA519402180B1 (es) |
| SG (1) | SG11201906436VA (es) |
| SI (1) | SI3580208T1 (es) |
| TN (1) | TN2019000204A1 (es) |
| TW (4) | TWI694070B (es) |
| WO (1) | WO2018147626A1 (es) |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018213211A1 (en) * | 2017-05-15 | 2018-11-22 | The Regents Of The University Of Michigan | Pyrrolo[2,3-c]pyridines and related analogs as lsd-1 inhibitors |
| KR102346187B1 (ko) * | 2019-12-26 | 2021-12-31 | 울산과학기술원 | 디히드로퓨란 유도체 및 이의 합성 방법 |
| WO2022240035A1 (ko) | 2021-05-13 | 2022-11-17 | 주식회사 대웅제약 | 섬유화증의 예방 또는 치료용 약학적 조성물 |
| BR112023023670A2 (pt) | 2021-05-13 | 2024-01-30 | Daewoong Pharmaceutical Co Ltd | Composição farmacêutica para prevenir ou tratar fibrose |
| CN117693343A (zh) | 2021-07-23 | 2024-03-12 | 株式会社大熊制药 | 用于预防或治疗系统性硬化症的药物组合物 |
| KR20230047910A (ko) * | 2021-10-01 | 2023-04-10 | 주식회사유한양행 | 바이사이클릭 융합환 유도체 또는 이의 염 및 이를 포함하는 약학 조성물 |
| KR20230092630A (ko) * | 2021-12-17 | 2023-06-26 | 주식회사 대웅제약 | (2R, 3S)-2-(벤조[d]이미다졸일프로필)피페리딘-3-올 유도체의 제조 방법 |
| TW202334112A (zh) * | 2021-12-17 | 2023-09-01 | 南韓商大熊製藥股份有限公司 | (2R, 3S)-2-(3-(4,5-二氯-1H-苯并[d]咪唑-1-基)丙基)哌啶-3-醇的新穎酸加成鹽及晶形 |
| WO2023239166A1 (ko) * | 2022-06-08 | 2023-12-14 | 주식회사 대웅제약 | 아르기나아제 저해제 및 이를 포함하는 약학적 조성물 |
| WO2024080777A1 (ko) * | 2022-10-12 | 2024-04-18 | 주식회사 대웅제약 | 신장염의 예방 또는 치료용 약학적 조성물 |
Family Cites Families (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB8900719D0 (en) | 1989-01-13 | 1989-03-08 | Nycomed As | Compounds |
| DE59504622D1 (de) | 1994-10-31 | 1999-02-04 | Merck Patent Gmbh | Benzylpiperidinderivate mit hoher Affinität zu Bindungsstellen von Aminosäure-Rezeptoren |
| IL114951A (en) | 1995-08-15 | 1999-08-17 | Hadasit Med Res Service | Quinazolinone-containing pharmaceutical compositions for prevention of neovascularization |
| WO1997034895A1 (de) * | 1996-03-15 | 1997-09-25 | Novartis Ag | NEUE N-7 HETEROCYCLYL-PYRROLO[2,3-d]PYRIMIDINE UND IHRE VERWENDUNG |
| CN1333028C (zh) * | 1999-08-20 | 2007-08-22 | Csl硅树脂公司 | 用作防腐蚀涂层的单组分有机聚硅氧烷橡胶组合物 |
| MXPA03008180A (es) | 2001-03-15 | 2003-12-12 | Astrazeneca Ab | Inhibidores de metaloproteinasa. |
| US7307088B2 (en) * | 2002-07-09 | 2007-12-11 | Amgen Inc. | Substituted anthranilic amide derivatives and methods of use |
| CN101247853B (zh) | 2005-04-13 | 2014-11-12 | 轴突公司 | 具有nos抑制活性的取代的吲哚化合物 |
| EP1939199A4 (en) * | 2005-09-22 | 2010-10-20 | Dainippon Sumitomo Pharma Co | NEW ADENINE CONNECTION |
| WO2008101867A1 (en) | 2007-02-19 | 2008-08-28 | Smithkline Beecham Corporation | Purine derivatives as immunomodulators |
| KR101649881B1 (ko) * | 2008-08-11 | 2016-08-30 | 글락소스미스클라인 엘엘씨 | 신규의 아데닌 유도체 |
| CA2737219C (en) | 2008-08-11 | 2017-02-28 | Tracy Keller | Halofuginone analogs for inhibition of trna synthetases and uses thereof |
| US20130338201A1 (en) | 2009-11-02 | 2013-12-19 | Ahr Pharmaceuticals, Inc. | Method of Cancer Treatment with 2-(1H-Indole-3-Carbonyl)-Thiazole-4-Carboxylic Acid Methyl Ester |
| AU2013237881B2 (en) | 2012-03-29 | 2017-10-12 | Akashi Therapeutics, Inc. | Dosage forms of halofuginone and methods of use |
| WO2014145576A2 (en) | 2013-03-15 | 2014-09-18 | Northwestern University | Substituted pyrrolo(2,3-d)pyrimidines for the treatment of cancer |
| WO2015199418A2 (ko) * | 2014-06-23 | 2015-12-30 | 주식회사 대웅제약 | 신규한 헤테로고리 화합물 |
| KR102277538B1 (ko) * | 2015-06-08 | 2021-07-14 | 주식회사 대웅제약 | 신규한 헤테로 고리 화합물, 이의 제조 방법 및 이를 포함하는 약학적 조성물 |
-
2018
- 2018-02-06 AR ARP180100277A patent/AR110963A1/es unknown
- 2018-02-07 CA CA3049643A patent/CA3049643C/en active Active
- 2018-02-07 CN CN201880006571.2A patent/CN110191882B/zh active Active
- 2018-02-07 MX MX2019009185A patent/MX2019009185A/es unknown
- 2018-02-07 TW TW107104338A patent/TWI694070B/zh active
- 2018-02-07 RS RS20211375A patent/RS62541B1/sr unknown
- 2018-02-07 MY MYPI2019004122A patent/MY196538A/en unknown
- 2018-02-07 TN TNP/2019/000204A patent/TN2019000204A1/en unknown
- 2018-02-07 TW TW109107089A patent/TWI772759B/zh active
- 2018-02-07 AU AU2018218965A patent/AU2018218965B2/en active Active
- 2018-02-07 MA MA47469A patent/MA47469B1/fr unknown
- 2018-02-07 SI SI201830416T patent/SI3580208T1/sl unknown
- 2018-02-07 PL PL18750794T patent/PL3580208T3/pl unknown
- 2018-02-07 JP JP2019542437A patent/JP6785384B2/ja active Active
- 2018-02-07 TW TW110116961A patent/TWI782525B/zh active
- 2018-02-07 HR HRP20211483TT patent/HRP20211483T1/hr unknown
- 2018-02-07 HU HUE18750794A patent/HUE056218T2/hu unknown
- 2018-02-07 SG SG11201906436VA patent/SG11201906436VA/en unknown
- 2018-02-07 PT PT187507942T patent/PT3580208T/pt unknown
- 2018-02-07 US US16/477,575 patent/US10981917B2/en active Active
- 2018-02-07 KR KR1020180015091A patent/KR102084772B1/ko active IP Right Grant
- 2018-02-07 WO PCT/KR2018/001625 patent/WO2018147626A1/en unknown
- 2018-02-07 TW TW108107266A patent/TWI700280B/zh active
- 2018-02-07 PE PE2019001462A patent/PE20191477A1/es unknown
- 2018-02-07 RU RU2019124878A patent/RU2733384C1/ru active
- 2018-02-07 BR BR112019016291A patent/BR112019016291A2/pt active Search and Examination
- 2018-02-07 ES ES18750794T patent/ES2899665T3/es active Active
- 2018-02-07 EP EP18750794.2A patent/EP3580208B1/en active Active
-
2019
- 2019-07-08 SA SA519402180A patent/SA519402180B1/ar unknown
- 2019-07-17 EC ECSENADI201951409A patent/ECSP19051409A/es unknown
- 2019-07-18 CL CL2019002019A patent/CL2019002019A1/es unknown
- 2019-07-22 CO CONC2019/0007834A patent/CO2019007834A2/es unknown
- 2019-07-24 DO DO2019000193A patent/DOP2019000193A/es unknown
- 2019-08-06 PH PH12019501811A patent/PH12019501811A1/en unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2899665T3 (es) | Derivados de 2-(3-(1H-benzo[d]imidazol-1-il)propil)piperidin-3-ol y compuestos relacionados como inhibidores de PRS para el tratamiento, p. ej., del cáncer | |
| ES2788856T3 (es) | Composiciones de pirrolopirrol como activadores de quinasa de piruvato (PKR) | |
| AU2017221865B2 (en) | Viral replication inhibitors | |
| ES2555224T3 (es) | Inhibidores de aminopirimidina cinasa | |
| AU2007209689B2 (en) | Pyrrolo [3,2-c] pyridine-4-one 2-indolinone protein kinase inhibitors | |
| KR20230157463A (ko) | 피리미딘-융합된 환형 화합물, 이의 제조 방법 및 이의 용도 | |
| CA2629228A1 (en) | Pyrrolopyridines as kinase inhibitors | |
| ES2717510T3 (es) | Inhibidores macrocíclicos de cinasa LRRK2 | |
| EP3481824B1 (en) | 2-phenylimidazo[4,5-b]pyridin-7-amine derivates useful as inhibitors of mammalian tyrosine kinase ror1 activity | |
| WO2018078360A1 (en) | Modulators of hedgehog (hh) signalling pathway | |
| ES2763344T3 (es) | Inhibidores macrocíclicos de la cinasa RIP2 | |
| EP4347579A1 (en) | Targeted protein degradation using bifunctional compounds that bind ubiquitin ligase and target mcl-1 protein | |
| WO2021108581A1 (en) | Potent and selective azaindole inhibitors of cdk8 and cdk19 | |
| NZ755300B2 (en) | Novel heterocyclic compound, its preparation method, and pharmaceutical composition comprising the same |