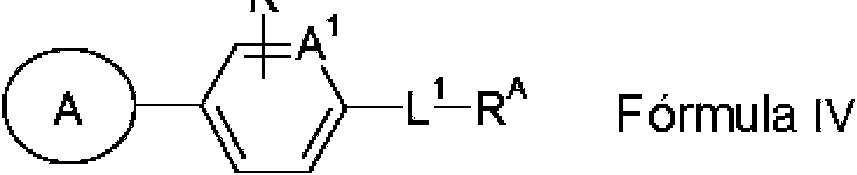ES2855173T3 - Compuestos heterocíclicos útiles para el tratamiento de una enfermedad - Google Patents
Compuestos heterocíclicos útiles para el tratamiento de una enfermedad Download PDFInfo
- Publication number
- ES2855173T3 ES2855173T3 ES14762555T ES14762555T ES2855173T3 ES 2855173 T3 ES2855173 T3 ES 2855173T3 ES 14762555 T ES14762555 T ES 14762555T ES 14762555 T ES14762555 T ES 14762555T ES 2855173 T3 ES2855173 T3 ES 2855173T3
- Authority
- ES
- Spain
- Prior art keywords
- substituted
- unsubstituted
- phenyl
- acid
- alkyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 C1[C@]2*CC[C@@]1C2 Chemical compound C1[C@]2*CC[C@@]1C2 0.000 description 11
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D261/00—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings
- C07D261/02—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings not condensed with other rings
- C07D261/06—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings not condensed with other rings having two or more double bonds between ring members or between ring members and non-ring members
- C07D261/10—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings not condensed with other rings having two or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D261/14—Nitrogen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/18—Drugs for disorders of the alimentary tract or the digestive system for pancreatic disorders, e.g. pancreatic enzymes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/02—Drugs for disorders of the urinary system of urine or of the urinary tract, e.g. urine acidifiers
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/02—Drugs for disorders of the nervous system for peripheral neuropathies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/06—Antiglaucoma agents or miotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/12—Antihypertensives
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/14—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D231/38—Nitrogen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D231/00—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings
- C07D231/02—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings
- C07D231/10—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D231/14—Heterocyclic compounds containing 1,2-diazole or hydrogenated 1,2-diazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D231/44—Oxygen and nitrogen or sulfur and nitrogen atoms
- C07D231/52—Oxygen atom in position 3 and nitrogen atom in position 5, or vice versa
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D233/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings
- C07D233/54—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members
- C07D233/66—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, not condensed with other rings having two double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D233/88—Nitrogen atoms, e.g. allantoin
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D239/00—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings
- C07D239/02—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings
- C07D239/24—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members
- C07D239/28—Heterocyclic compounds containing 1,3-diazine or hydrogenated 1,3-diazine rings not condensed with other rings having three or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, directly attached to ring carbon atoms
- C07D239/32—One oxygen, sulfur or nitrogen atom
- C07D239/42—One nitrogen atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D263/00—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings
- C07D263/02—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings
- C07D263/30—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D263/34—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D263/48—Nitrogen atoms not forming part of a nitro radical
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/04—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Urology & Nephrology (AREA)
- Ophthalmology & Optometry (AREA)
- Diabetes (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Hematology (AREA)
- Heart & Thoracic Surgery (AREA)
- Oncology (AREA)
- Cardiology (AREA)
- Pain & Pain Management (AREA)
- Epidemiology (AREA)
- Vascular Medicine (AREA)
- Rheumatology (AREA)
- Dermatology (AREA)
- Emergency Medicine (AREA)
- Endocrinology (AREA)
- Obesity (AREA)
- Pulmonology (AREA)
- Gastroenterology & Hepatology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
Abstract
Un compuesto donde el compuesto tiene la estructura de fórmula I **(Ver fórmula)** o una sal farmacéuticamente aceptable de este, donde RA es -CO2H, -CO2RB, -CN, tetrazolilo, -C(=O)NH2, -C(=O)NHRB, -C(=O)NHSO2RB o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico seleccionado del grupo que consiste en **(Ver fórmula)** donde RB es -H o -alquilo C1-C4, o tiene la estructura de uno de: **(Ver fórmula)** L1 está ausente o es alquileno C1-C6 sustituido o no sustituido, cicloalquileno C3-C6 sustituido o no sustituido, fluoroalquileno C1-C6, heteroalquileno C1-C6 sustituido o no sustituido; L2 está ausente; El anillo B es arileno sustituido o no sustituido, heteroarileno sustituido o no sustituido, donde si el anillo B está sustituido entonces el anillo B está sustituido con 1, 2 o 3 RH seleccionados independientemente; donde el anillo B tiene la estructura de: **(Ver fórmula)** donde A1, A2 y A3 son independientemente -N=, =N-, =CH- o -CH=; El anillo A es un heteroareno de 5 miembros que se selecciona de uno de: **(Ver fórmula)** donde la línea punteada indica el punto de unión del anillo A al anillo B; donde RC es -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, o fluoroalquilo C1-C4, y RD es -N(RF)-C(=O)XCH(RG)-CY, -N(RF)C(=O)XC(RG)2-CY, -N(RF)C(=O)X-CY, -C(=O)N(RF)CH(RG)X-CY, o - C(=O)-N(RF)C(RG)2X-CY, donde X está ausente, es -O-, -NH- o -CH2-; RE es -H, -alquilo C1-C4 o -fluoroalquilo C1-C4; RF es -H o alquilo C1-C4; RG se selecciona independientemente de RE, o un RG es alquilo C1-C4 y se toma junto con el átomo de carbono al que se une RG y el carbono o heteroátomo al que se une CY para definir un carbociclo sustituido o no sustituido o un heterociclo sustituido o no sustituido, y el otro RG, si está presente, es como se define por RE; CY es alquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C10 sustituido o no sustituido, heterocicloalquilo C2-C10 sustituido o no sustituido, arilo sustituido o no sustituido, o heteroarilo sustituido o no sustituido, donde si CY está sustituido, entonces CY está sustituido con 1, 2, o 3 RH seleccionados independientemente; donde cada RH se selecciona independientemente de -H, halógeno, -CN, -NO2, -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2RJ, -N(RJ)S(=O)2RJ, -S(=O)2N(RL)2, -C(=O)RJ, OC(=O)RJ, -C(=O)ORJ, -OC(=O)ORJ, -N(RL)2, -C(=O)N(RL)2, - OC(=O)N(RL)2, -N(RJ)C(=O)N(RL)2, -N(RJ)C(=O)RJ, -N(RJ)C(=O)ORJ, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4, y heteroalquilo C1-C4, donde cada RJ es independientemente alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3- C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido); donde cada RL es independientemente -H, alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido), o cuando RH es -S(=O)2N(RL)2, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2 o N(RF)C(=O)N(RL)2, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al átomo de N al que están unidos para definir un heterociclo sustituido o no sustituido; El anillo C es cicloalquileno C3-C10 sustituido o no sustituido, heterocicloalquileno C2-C10 sustituido o no sustituido, arileno sustituido o no sustituido, o heteroarileno sustituido o no sustituido, donde si el anillo C está sustituido entonces el anillo C está sustituido con 1, 2 o 3 RH seleccionados independentemente, donde RH es como se ha definido previamente, donde si RJ, RL y o RH está sustituido, está sustituido con uno o más seleccionados entre alquilo, cicloalquilo, arilo, heteroarilo, heteroalicíclico, hidroxi, alcoxi, ariloxi, alquiltio, ariltio, alquilsulfóxido, arilsulfóxido, alquilsulfona, arilsulfona, ciano, halo, nitro, haloalquilo, fluoroalquilo, fluoroalcoxi y amino, incluidos grupos amino mono- y disustituidos, -CN, NO2 o LsRs, donde cada Ls se selecciona independientemente entre un enlace, -O-, -C(=O)-, -C(=O)O-, -S-, -S(=O)-, -S(=O)2-, -NH-, -NHC(=O)-, -C(=O)NH-, S(=O)2NH-, -NHS(=O)2, - OC(=O)NH-, -NHC(=O)O-, o -(alquileno C1-C6)-; y cada Rs se selecciona entre -H, alquilo, fluoroalquilo, heteroalquilo, cicloalquilo, arilo, heteroarilo o heterocicloalquilo.
Description
DESCRIPCIÓN
Compuestos heterocíclicos útiles para el tratamiento de una enfermedad
DECLARACIÓN DE INTERÉS DEL GOBIERNO
Esta invención se realizó con el apoyo del gobierno mediante las Subvenciones DK092005 y CA174019 otorgadas por los Institutos Nacionales de la Salud. El gobierno de los Estados Unidos tiene algunos derechos en la invención.
CAMPO DE LA INVENCIÓN
La presente invención se refiere a compuestos que tienen actividad farmacológica, a procedimientos para la preparación de dichos compuestos, a composiciones farmacéuticas que los comprenden y a su uso en la terapia y profilaxis de la enfermedad en un sujeto en necesidad de tratamiento, en particular, para tratamientos humanos y veterinarios de dolor, prurito, cáncer, inflamación y enfermedades fibrósicas.
ANTECEDENTES DE LA INVENCIÓN
Los lisofosfolípidos afectan las funciones celulares fundamentales, que incluyen proliferación, diferenciación, supervivencia, migración, adhesión, invasión y morfogénesis. Las funciones anormales influyen en muchos procesos biológicos, que resultan en enfermedades, entre las que se incluyen, a modo no taxativo, la enfermedad fibrósica, la inflamación, el cáncer y la lesión del nervio periférico. El ácido lisofosfatídico (LPA) es un lisofosfolípido, que se ha demostrado que actúa a través de receptores específicos acoplados a la proteína G (GPCRs) de manera autocrina y paracrina. Los antagonistas de los receptores del LPA son útiles en el tratamiento de enfermedades, trastornos o afecciones en las que el LPA cumple un papel.
Los agentes que interactúan con los receptores del ácido lisofosfatídico [LPAR] para reducir la transducción de señales a través de esos receptores (es decir, por inhibición competitiva o no competitiva o que actúan como agonistas inversos) reducen las manifestaciones de las enfermedades descritas en la presente. Las enfermedades y afecciones cuya etiología, progresión o persistencia tiene lugar, total o parcialmente, mediante la señalización a través del subtipo de receptor de ácido lisofosfatídico 1 (LPA1R) se consideran LPA-dependientes. Se necesitan nuevos agentes con utilidad terapéutica para el tratamiento de dichas afecciones y enfermedades LPA-dependientes y las demás enfermedades y afecciones descritas en la presente.
SUMARIO DE LA INVENCIÓN
En la presente se divulgan compuestos, que inhiben la actividad fisiológica del ácido lisofosfatídico (LPA) y, por lo tanto, son útiles como agentes para el tratamiento o la prevención de enfermedades en las que la inhibición de la actividad fisiológica del LPA resulta útil.
En un aspecto, dichos compuestos son útiles para el tratamiento de la fibrosis de órganos (por ejemplo, hígado, riñón, pulmón, corazón y similares), enfermedades del hígado (por ejemplo, hepatitis aguda, hepatitis crónica, fibrosis hepática, cirrosis hepática, hipertensión portal, insuficiencia regenerativa, esteatohepatitis no alcohólica (EHNA), hipofunción hepática, trastorno del flujo sanguíneo hepático y similares), enfermedad proliferativa celular, como cánceres (que incluyen, a modo no taxativo, tumor sólido, metástasis de tumor sólido, fibroma vascular, mieloma, mieloma múltiple, sarcoma de Kaposi, leucemia, leucemia linfocítica crónica (LLC), metástasis invasiva de las células cancerosas y similares), enfermedades inflamatorias (que incluyen, a modo no taxativo, psoriasis, nefropatía, neumonía y similares), enfermedades del tracto gastrointestinal (que incluyen, a modo no taxativo, síndrome del intestino irritable (SII), enfermedad inflamatoria intestinal (EII), secreción pancreática anormal y similares), enfermedades renales, enfermedades asociadas al tracto urinario (que incluyen, a modo no taxativo, hiperplasia prostática benigna o síntomas asociados a la enfermedad de la vejiga neuropática), tumor en la médula espinal, hernia de disco intervertebral, estenosis del canal espinal, síntomas derivados de la diabetes, enfermedades del tracto urinario inferior (que incluyen, a modo no taxativo, obstrucción del tracto urinario inferior y enfermedades similares), enfermedades inflamatorias del tracto urinario inferior (que incluyen, a modo no taxativo, disuria, micción frecuente y similares), enfermedades del páncreas, enfermedades asociadas a la angiogénesis anormal (que incluyen, a modo no taxativo, obstrucción arterial y enfermedades similares), esclerodermia, enfermedades asociadas al cerebro (que incluyen, a modo no taxativo, infarto cerebral, hemorragia cerebral y similares), enfermedades del sistema nervioso (que incluyen, a modo no taxativo, dolor neuropático, neuropatía periférica, prurito y similares), enfermedades oculares (que incluyen, a modo no taxativo, degeneración macular asociada a la edad (DMAE), retinopatía diabética, vitreorretinopatía proliferativa (VR), penfigoide cicatricial, cicatrices de cirugía de filtración de glaucoma y enfermedades similares).
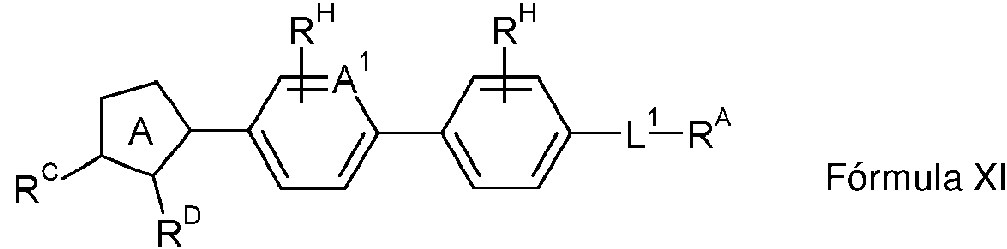
Los compuestos de la invención incluyen compuestos de fórmula I que tienen la estructura:
donde RA es -CO2H, -CÜ2RB, -CN, tetrazolilo, -C(=O)NH2, -C(=O)NHRB, -C(=O)NHSO2RB o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico seleccionado de
y
L1 está ausente o es alquileno C1-C6 sustituido o no sustituido, cicloalquileno C3-C6 sustituido o no sustituido, fluoroalquileno C1-C6, o heteroalquileno C1-C6 sustituido o no sustituido;
L2 está ausente;
donde RB es -H o alquilo-C1-C4, o tiene la estructura de uno de:
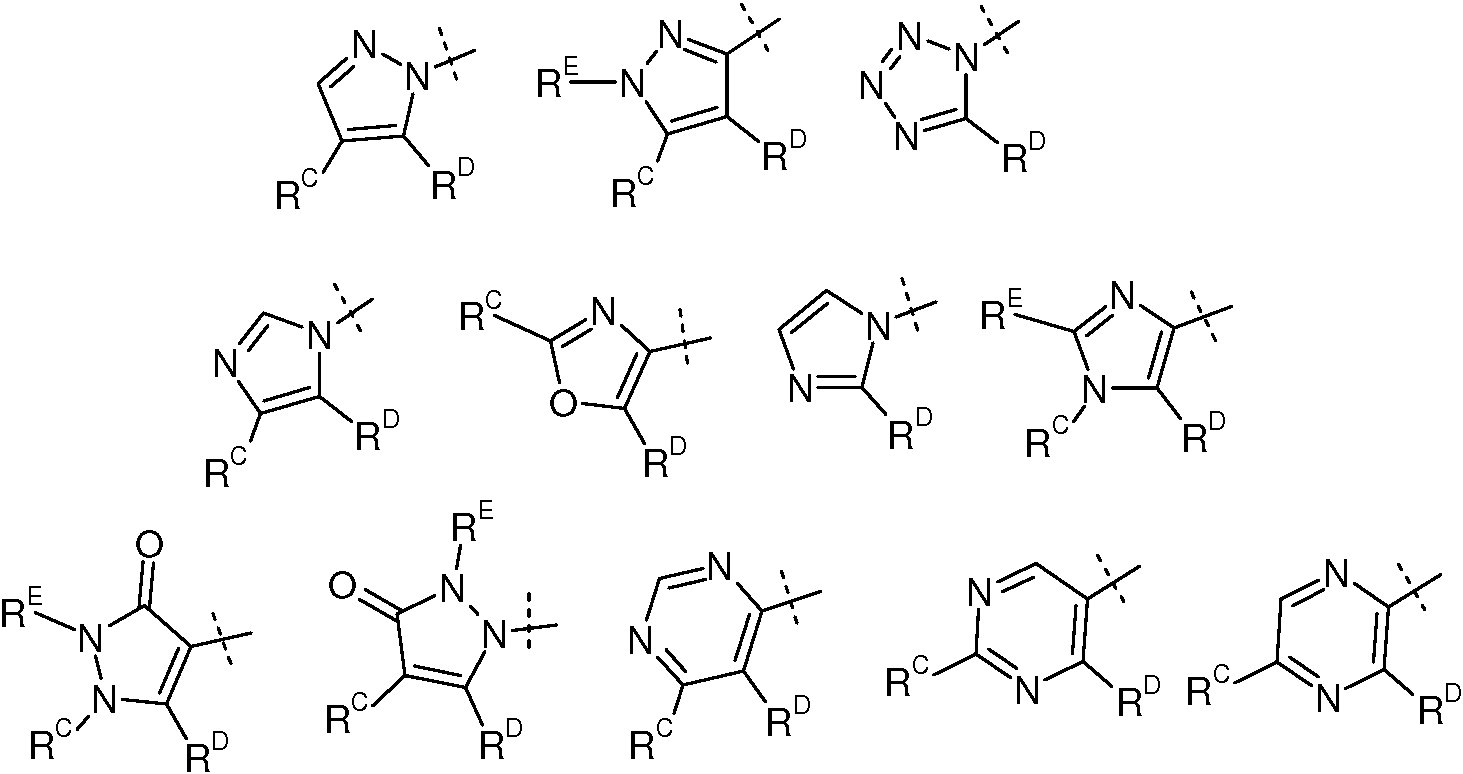
El anillo A es un heteroareno de 5 miembros que tiene la estructura de uno de:
donde la línea punteada indica el punto de unión del anillo A al anillo B;
donde RC es -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4 o fluoroalquilo C1-C4,
y RD es -N(RF)C(=O)XCH(RG)-CY, -N(RF)C(=O)XC(RG)2-CY, -N(RF)C(=O)X-CY, -C(=O)-N(RF)-CH(RG)X-CY, o -C(=O)-N(Rf)-C(Rg)2X-CY, donde X está ausente, es -O-, -NH- o -CH2-;
RE es -H, alquilo C1-C4 o fluoroalquilo C1-C4;
RF es -H o alquilo C1-C4;
RG es RE seleccionado independientemente, o un RG es alquileno C1-C4 y se toma junto con el átomo de carbono al que RG está unido y el carbono o heteroátomo al que CY está unido para definir un carbociclo sustituido o no sustituido o un heterociclo sustituido o no sustituido, y el otro RG, si está presente, es como se define por RE;
CY es alquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C10 sustituido o no sustituido, heterocicloalquilo C2-C10 sustituido o no sustituido, arilo sustituido o no sustituido, o heteroarilo sustituido o no sustituido, donde si CY está sustituido, entonces CY está sustituido con 1,2, o 3 RH seleccionados independientemente,
donde cada RH es independientemente -H, halógeno, -CN, -NO2, -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2RJ, -N(Rj)S(=O)2Rj, -S(=O)2N(Rl)2, -C(=O)Rj, OC(=O)Rj, -C(=O)ORj, -OC=O)ORj, -N(Rl)2, -C(=O)N(Rl)2, -OC(=O)N(Rl)2, -N(Rj)C(=O)N(Rl)2, -N(Rj)C(=O)Rj, -N(Rj)C(=O)ORj, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4, o heteroalquilo C1-C4;
donde cada RJ es independientemente alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido), y donde cada RL es independientemente -H, alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4
(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-Ci -C4-(heterocicloalquilo sustituido o no sustituido), alquileno-Ci -C4-(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido),
o cuando RH es -S(=O)2N(RL)2, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2 o -N(RJ)C(=O)N(RL)2, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al el átomo de N al que están unidos para definir un heterociclo sustituido o no sustituido,
El anillo B es un arileno sustituido o no sustituido, o heteroarileno sustituido o no sustituido, donde si el anillo B está sustituido, entonces el anillo B está sustituido con 1, 2, o 3 RH seleccionados independientemente, donde RH es como se definió previamente; donde el anillo B tiene la estructura
El anillo C es cicloalquileno C3-C10 sustituido o no sustituido, heterocicloalquileno C2-C10 sustituido o no sustituido, arileno sustituido o no sustituido, o heteroarileno sustituido o no sustituido, donde si el anillo C está sustituido, entonces el anillo C está sustituido con 1, 2, o 3 RH seleccionados independientemente, donde RH es como se definió previamente;
donde si RJ, RL y o RH está sustituido, está sustituido con uno o más seleccionados entre alquilo, cicloalquilo, arilo, heteroarilo, heteroalicíclico, hidroxi, alcoxi, ariloxi, alquiltio, ariltio, alquilsulfóxido, arilsulfóxido, alquilsulfona, arilsulfona, ciano, halo, nitro, haloalquilo, fluoroalquilo, fluoroalcoxi y amino, incluidos grupos amino mono- y disustituidos, haluro, -CN, -NO2, o LsRs, donde cada Ls se selecciona independientemente entre un enlace, -O-, -C(=O)-, -C(=O)O-, -S-, -S(=O)-, -S(=O)2-, -NH-, -NHC(=O)-, - C(=O)NH-, S(=O)2NH-, -NHS(=O)2, -OC(=O)NH-, -NHC(=O)O-, o -(alquileno C1-C6)-; y cada Rs se selecciona entre -H, alquilo, fluoroalquilo, heteroalquilo, cicloalquilo, arilo, heteroarilo o heterocicloalquilo.
Otros compuestos de la invención tienen las estructuras que se indican mediante las realizaciones y reivindicaciones enumeradas en la presente.
DESCRIPCIÓN DETALLADA DE LA INVENCIÓN
Definiciones
Salvo que el contexto indique lo contrario, los términos que se utilizan en este documento tienen los significados definidos a continuación. A menos que se indique o infiera lo contrario, por ejemplo, mediante la inclusión de elementos u opciones mutuamente excluyentes, en estas definiciones y en la totalidad de la memoria descriptiva, los términos "un" y "una" significan uno o más y el término "o" significa y/o cuando el contexto lo permita. Como se utiliza en la memoria descriptiva y las reivindicaciones adjuntas, las formas en singular "un/una" y "el/la" incluyen términos en plural, a menos que el contexto indique claramente lo contrario.
En varios lugares de la presente divulgación, por ejemplo, en cualquiera de las realizaciones descritas o en las reivindicaciones, se hace referencia a compuestos, composiciones o métodos que "comprenden" uno o más componentes, elementos o etapas específicas. Las realizaciones de la invención también incluyen específicamente los compuestos, las composiciones o los métodos, que son componentes, elementos o etapas especificadas o que consisten, o consisten esencialmente, en los componentes, los elementos o las etapas especificadas. Los términos "que comprende", "consiste en" y "consiste esencialmente en" tienen los significados normalmente aceptados en virtud de la legislación de patentes de los Estados Unidos, a menos que expresamente se indique lo contrario. El término "compuesto por" se usa indistintamente con el término "que comprende" y se reconocen como términos equivalentes. Por ejemplo, las composiciones, los dispositivos, los artículos de fabricación o los métodos divulgados, que "comprenden" un componente o una etapa son abiertos e incluyen uno o más componentes o etapas adicionales o están incluidos en estos. De manera similar, las composiciones, los dispositivos, los artículos de fabricación o los métodos divulgados, que "consisten en" un componente o una etapa son cerrados y no incluirían otros componentes o etapas adicionales ni estarían incluidos en estos. Además, el uso del término "que incluye", así como otras formas, como "incluyen", "incluye" e "incluido", no es limitante. Los títulos de las secciones, que se incluyen en la presente, son a fines meramente organizativos y no deben interpretarse como limitantes del objeto descrito. A menos que se indique lo contrario, se emplean los procedimientos convencionales de espectroscopía de masas, RMN, HPLC, química de proteínas, bioquímica, técnicas de ADN recombinante y farmacología.
El término "enlace" o "enlace simple", como se utiliza en la presente, significa un enlace químico entre dos átomos o dos porciones cuando los átomos unidos por el enlace se consideran parte de una subestructura mayor. Como se indica expresamente, o se infiere a partir del contexto, cuando un grupo descrito en la presente es un enlace, el grupo de referencia está ausente, lo que permite que se forme un enlace entre los restantes grupos identificados.
Como se utiliza en la presente, el término "anillo de [x] miembros" significa cualquier estructura cíclica. El término "miembros" denota el número de átomos que constituyen el anillo. En consecuencia, a modo de ejemplo, los anillos que incluyen ciclohexilo, piridinilo, piranilo y tiopiranilo son anillos de 6 miembros, y los anillos que incluyen ciclopentilo, pirrolilo, furanilo, y tienilo son anillos de 5 miembros.
Como se utiliza en la presente, "porción" significa un segmento, fragmento o grupo funcional específico de una molécula o un compuesto. A veces, las porciones químicas se indican como entidades químicas, que están incorporadas o adosadas a una molécula o compuesto (p.ej. un grupo variable o sustituyente).
Un "alquilo", como se utiliza en la presente, se refiere a un grupo de átomos de carbono que están unidos covalentemente en disposiciones normales, secundarias, terciarias o cíclicas, es decir, en cadenas lineales, ramificadas, cíclicas o cualquier combinación de estas. Un sustituyente alquilo a una estructura es la cadena de átomos de carbono que se encuentra unida covalentemente a la estructura mediante un carbono sp3 del sustituyente. El sustituyente alquilo, como se utiliza en la presente, contiene una o más porciones o grupos saturados y puede contener además porciones o grupos alquilo no saturados, es decir, el sustituyente puede comprender uno, dos, tres o más enlaces dobles o triples de una combinación de estos, seleccionados independientemente, por lo general, un enlace doble o un enlace triple cuando se encuentran presentes dichas porciones o grupos alquilo no saturados.
Las porciones o grupos alquilo no saturados incluyen las porciones o los grupos descritos a continuación para porciones alquenilo, alquinilo, cicloalquilo y arilo. Las porciones alquilo saturadas contienen átomos de carbono saturados (sp3) y átomos de carbono no aromático sp2 o sp. El número de átomos de carbono en una porción o un grupo alquilo puede variar y, generalmente, oscila entre 1 y aproximadamente 50, por ejemplo, aproximadamente 1 30 o aproximadamente 1-20, a menos que se especifique lo contrario, por ejemplo, alquilo C1-8 o alquilo C1-C8 significa una porción alquilo, que contiene 1, 2, 3, 4, 5, 6, 7 u 8 átomos de carbono y alquilo C1-6 o alquilo C1-C6 significa una porción alquilo, que contiene 1, 2, 3, 4, 5 o 6 átomos de carbono.
Cuando se especifica un sustituyente, una porción o un grupo alquilo, las especies pueden incluir metilo, etilo, 1-propilo (n-propilo), 2-propilo (iso-propilo, -CH(CH3)2), 1 -butilo (n-butilo), 2-metil-1 -propilo (iso-butilo, -CH2CH(CH3)2), 2-butilo (sec-butilo, -CH(CH3) CH2CH3), 2-metil-2-propilo (t-butilo, -C(CH3)3), amilo, isoamilo, sec-amilo y otras porciones alquilo de cadena lineal, cíclica y ramificada. A menos que se especifique lo contrario, los grupos alquilo pueden contener las especies y los grupos descritos a continuación para cicloalquilo, alquenilo, grupos alquinilo, grupos arilo, grupos arilalquilo, grupos alquilarilo y similares.
Como se utiliza en la presente, cicloalquilo es un sistema de anillos monocíclico, bicíclico o tricíclico, compuesto únicamente por átomos de carbono. El término "cicloalquilo" abarca un radical alifático no aromático monocíclico o policíclico, en el que cada uno de los átomos que forman el anillo (es decir, los átomos del esqueleto) es un átomo de carbono. El número de átomos de carbono en un sustituyente, una porción o un grupo cicloalquilo puede variar y, generalmente, oscila entre 3 y aproximadamente 50, por ejemplo, aproximadamente 1-30 o aproximadamente 1-20, a menos que se especifique lo contrario, por ejemplo, alquilo C3-8 o alquilo C3-C8 significa un sustituyente, una porción o un grupo cicloalquilo, que contiene 3, 4, 5, 6, 7 u 8 átomos de carbono y alquilo C3-6 o alquilo C3-C6 significa un sustituyente, una porción o un grupo cicloalquilo, que contiene 3, 4, 5 o 6 átomos de carbono. Por lo general, los sustituyentes, las porciones o los grupos cicloalquilo tendrán 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 o 20 átomos de carbono y pueden contener enlaces dobles exo o endocíclicos, enlaces triples exo o endocíclicos o una combinación de ambos, donde los enlaces dobles o triples endocíclicos, o la combinación de ambos, no forman un sistema conjugado cíclico de 4n 2 electrones; en el que el sistema de anillos bicíclico puede compartir uno (es decir, sistema de anillos espiro) o dos átomos de carbono y el sistema de anillos tricíclico puede compartir un total de 2, 3 o 4 átomos de carbono, típicamente 2 o 3.
A menos que se especifique lo contrario, los sustituyentes, las porciones o los grupos cicloalquilo pueden contener las porciones y los grupos descritos para alquenilo, alquinilo, arilo, arilalquilo, alquilarilo y similares, y pueden contener también una o más porciones cicloalquilo. Por lo tanto, los cicloalquilos pueden ser saturados o parcialmente insaturados. Los cicloalquilos se pueden condensar con un anillo aromático, y los puntos de unión al anillo aromático son en un carbono o carbonos del sustituyente, la porción o el grupo cicloalquilo, que no es un átomo de carbono del anillo aromático. Los grupos cicloalquilo incluyen grupos, que tienen un anillo de 3 a 10 átomos. Los sustituyentes, las porciones o los grupos cicloalquilo incluyen ciclopropilo, ciclopropenilo, ciclohexilo u otros compuestos cíclicos, donde todos los carbonos contienen porciones cicloalquilo. Los cicloalquilos incluyen además ciclobutilo, ciclopentilo, ciclohexenilo, cicloheptilo y ciclooctilo. Los grupos cicloalquilo pueden ser sustituidos o no sustituidos. En función de la estructura del sustituyente, un sustituyente cicloalquilo puede ser un monorradical o un dirradical (es decir, un cicloalquileno, por ejemplo, ciclopropano-1,1-diilo, ciclobutan-1,1 -diilo, ciclopentan-1, 1-diilo, ciclohexan-1, 1 -diilo, ciclohexan-1,4-diilo, cicloheptan-1, 1 -diilo y similares). Cuando el cicloalquilo se utiliza como un grupo Markush (es decir, un sustituyente), el cicloalquilo está unido a una fórmula Markush con la que se asocia a través de un carbono, que participa en un sistema de anillo de carbono cíclico del grupo cicloalquilo, que no es un carbono aromático.
Como se utiliza en la presente, "alquilamina" significa un grupo, una porción o un sustituyente -N(alquilo)xHy, donde x e y se seleccionan independientemente del grupo x = 1, y = 1 y x = 2, y = O. La alquilamina incluye aquellos grupos N(alquilo)xHy , donde x = 2 e y = 0 y los grupos alquilo tomados junto con el átomo de nitrógeno al que están unidos forman un sistema de anillos cíclico.
Como se utiliza en la presente, "heteroalquileno" significa un grupo, una porción o un sustituyente alquileno (es decir, alcanodiilo) en el que uno o más átomos del esqueleto del alquilo se seleccionan entre un átomo distinto de carbono, por ejemplo, oxígeno, nitrógeno, azufre, fósforo o combinaciones de estos. Los heteroalquilenos incluyen heteroalquilenos C1-C6 o heteroalquilenos C1-C4. Los heteroalquilenos ejemplares incluyen, a modo no taxativo, -OCH2-, -OCH(CH3)-, -OC(CH3)2-, -OCH2CH2-, -CH2O-, -CH(CH3)O-, C(CH3)2O-, -CH2CH2O-, -CH2OCH2-, -CH2OCH2CH2-, -CH2CH2OCH2-, -SCH2-, -SCH(CH3)-, -SC(CH3)2-, -SCH2CH2-, -CH2S-, - CH(CH3)S-, -C(CH3)2S-, -CH2CH2S-, -CH2SCH2-,-CH2SCH2CH2-, -CH2CH2SCH2-, - S(=O)2CH2-, -S(=O)2CH(CH3)-, -S(=O)2C(CH3)2-, -S(=O)2CH2CH2-, -CH2S(=O)2-, -CH(CH3)S(=O)2-, -C(CH3)2S(=O)2-, -CH2CH2S(=O)2-, -CH2S(=O)2CH2-, -CH2S(=O)2CH2CH2-, CH2CH2S(=O)2CH2-, -NHCH2-, -NHCH(CH3)-, -NHC(CH3)2-, -NHCH2CH2-, -CH2NH-, -CH(CH3)NH-, -C(CH3)2NH-, -CH2CH2NH-, -CH2NHCH2-, -CH2NHCH2CH2-, -CH2CH2NHCH2-, y similares.
Como se utiliza en la presente, "bioisóstero de ácido carboxílico" significa un grupo, una porción o un sustituyente funcional, que exhibe propiedades físicas, biológicas y/o químicas similares a las de una porción ácido carboxílico. A modo de ejemplo, los bioisósteros de ácido carboxílico incluyen,
[51] Como se utiliza en la presente, "alquenilo" significa un sustituyente, una porción o un grupo, que comprende una o más porciones de enlace doble (p.ej. -CH=CH-) o 1, 2, 3, 4, 5 o 6 o más, generalmente 1, 2 o 3 de dichas porciones y puede incluir una porción o grupo arilo, como benceno, y adicionalmente comprende átomos de carbono normales, secundarios, terciarios o cíclicos, es decir, de cadena lineal, ramificada, cíclica o cualquier combinación de estos, a menos que la porción alquenilo sea un radical de vinilo (por ejemplo, -CH=CH2). Una porción, un grupo o un sustituyente alquenilo con múltiples enlaces dobles puede tener enlaces dobles dispuestos en forma contigua (es decir, porción 1,3 butadienilo) o no contigua, con uno o más átomos de carbono intermedios saturados o una combinación de estos, siempre que una disposición cíclica, contigua de enlaces dobles no forme un sistema cíclicamente conjugado de 4n 2 electrones (es decir, aromático). El número de átomos de carbono en una porción o un grupo alquenilo puede variar y, generalmente, oscila entre 2 y aproximadamente 50, por ejemplo, aproximadamente 2-30 o aproximadamente 2-20, a menos que se especifique lo contrario, por ejemplo, alquenilo C2-8 o alquenilo C2-C8 significa una porción alquenilo, que contiene 2, 3, 4, 5, 6, 7 u 8 átomos de carbono y alquenilo C2-6 o alquenilo C2-C6 significa una porción alquenilo, que contiene 2, 3, 4, 5 o 6 átomos de carbono. Por lo general, las porciones o los grupos alquenilo tendrán 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 o 20 átomos de carbono.
Cuando se especifica una porción, un grupo o un sustituyente alquenilo, las especies incluyen, a modo de ejemplo, cualquiera de los grupos, las porciones o los sustituyentes alquilo o cicloalquilo descritos en la presente, que tienen uno o más enlaces dobles, metileno (=CH2), metilmetileno (=CH-CH3), etilmetileno (=CH-CH2-CH3), =CH-CH2-CH2-CH3, vinilo (-CH=CH2), alilo, 1 -metilvinilo, butenilo, iso-butenilo, 3-metil-2-butenilo, 1-pentenilo, ciclopentenilo, 1-metilciclopentenilo, 1-hexenilo, 3-hexenilo, ciclohexenilo y otra cadena lineal, cíclica y ramificada, donde todos los carbonos comprenden porciones, que contienen al menos un enlace doble. Cuando el alquenilo se utiliza como un grupo Markush (es decir, un sustituyente), el alquenilo está unido a una fórmula Markush con la que se asocia a través de un carbono no saturado de enlace doble de la porción o el grupo alquenilo, salvo que se especifique lo contrario.
Como se usa en la presente, ''alquinilo'' significa un sustituyente, una porción o un grupo, que contiene una o más porciones de enlace triple (es decir, -C=C-), p.ej. 1, 2, 3, 4, 5, 6 o más, generalmente 1 o 2, enlaces triples, y opcionalmente 1, 2, 3, 4, 5, 6 o más enlaces dobles, y el resto de los enlaces (de existir) son enlaces simples, con átomos de carbono de cadena secundaria, terciaria o cíclicas o cualquier combinación de estos, salvo que la porción alquinilo sea etinilo. El número de átomos de carbono en una porción o un grupo alquenilo puede variar y, generalmente, oscila entre 2 y aproximadamente 50, por ejemplo, aproximadamente 2-30 o aproximadamente 2-20, a menos que se especifique lo contrario, por ejemplo, alquinilo C2-8 o alquinilo C2-C8 significa una porción alquinilo, que contiene 2, 3, 4, 5, 6, 7 u 8 átomos de carbono. Por lo general, las porciones o los grupos alquinilo tendrán 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18, 19 o 20 átomos de carbono.
Cuando se especifica una porción, un grupo o un sustituyente alquinilo, las especies incluyen, a modo de ejemplo, cualquiera de los grupos, las porciones o los sustituyentes alquilo descritos en la presente, que tienen uno o más
enlaces dobles, etinilo, propinilo, butinilo, iso-butinilo, 3-metil-2-butin¡lo, 1-pentilo, ciclopentilo, 1-metil-ciclopentinilo, 1 -hexinilo, 3-hexinilo, ciclohexinilo y otras cadenas lineales, cíclicas y ramificadas, donde todos los carbonos comprenden porciones, que contienen al menos un enlace doble. Cuando el alquinilo se utiliza como un grupo Markush (es decir, un sustituyente), el alquinilo está unido a una fórmula Markush con la que se asocia a través de uno de los carbonos no saturados del grupo funcional alquinilo.
Como se utiliza en la presente, "aromático" se refiere a un anillo plano, que tiene un sistema de electrones pi deslocalizados, que contiene 4n+2 electrones pi, donde n es un entero positivo. Los anillos aromáticos pueden formarse a partir de cinco, seis, siete, ocho, nueve, diez, o más de diez átomos. Los aromáticos son opcionalmente sustituidos. El término "aromático" incluye tanto grupos arilo carboxílico ("arilo", p.ej. fenilo) como grupos arilo heterocíclico (o "heteroarilo" o "heteroaromático") (p.ej. piridina). El término incluye grupos monocíclicos o policíclicos de anillos condensados (es decir, anillos que comparten pares de átomos de carbono adyacentes).
Como se utiliza en la presente, "arilo" significa un sistema de anillos aromáticos o un sistema de anillos condensados sin heteroátomos en el anillo, que comprende 1, 2, 3 o de 4 a 6 anillos, generalmente de 1 a 3 anillos, donde los anillos se componen de átomos de carbono únicamente; y se refiere a un sistema cíclicamente conjugados de 4n+2 electrones (regla de Hückel), generalmente 6, 10 o 14 electrones, algunos de los cuales pueden participar, además, en la conjugación exocíclica (crosconjugado (por ejemplo, quinona)). Los sustituyentes, las porciones y los grupos arilo se forman generalmente con cinco, seis, siete, ocho, nueve o más de nueve átomos de carbono. Los sustituyentes, las porciones o los grupos arilos son opcionalmente sustituidos. Los arilos ejemplares incluyen arilos C6-C10, como fenilo y naftafenilo y fenantrilo. En función de la estructura del sustituyente, un grupo arilo puede ser un monorradical o un dirradical (es decir, un grupo arileno). Los arilenos ejemplares incluyen, a modo no taxativo, fenil-1-2-eno, fenil-1,3-eno y fenil-1-4 eno. Cuando el arilo se utiliza como un grupo Markush (es decir, un sustituyente), el arilo está unido a una fórmula Markush con la que se asocia a través de un carbono aromático del grupo arilo.
Como se utiliza en la presente, "arilalquilo" significa un sustituyente, una porción o un grupo, donde la porción arilo está unida a una porción alquilo, es decir, -alquil-arilo, donde los grupos alquilo y arilo son como se describe anteriormente, por ejemplo, -CH2-C6H5 o -CH2CH(CH3)-C6H5. Cuando el arilalquilo se utiliza como un grupo Markush (es decir, un sustituyente), el arilalquilo está unido a una fórmula Markush con la que se asocia a través de un carbono sp3 de la porción alquilo.
Como se utiliza en la presente, "alquilarilo" significa un sustituyente, una porción o un grupo, donde la porción alquilo está unida a una porción arilo, es decir, -aril-alquilo, donde los grupos arilo y alquilo son como se describe anteriormente, por ejemplo, -C6H4-CH3 o -C6H4-CH2CH(CH3). Cuando el alquilarilo se utiliza como un grupo Markush (es decir, un sustituyente), el alquilarilo está unido a una fórmula Markush con la que se asocia a través de un carbono sp2 de la porción arilo.
Como se utilizan en la presente, "alquilo sustituido", "cicloalquilo sustituido", "alquenilo sustituido", "alquinilo sustituido", "alquilarilo sustituido", "arilalquilo sustituido", "heterociclo sustituido", "arilo sustituido" y similares significan un grupo alquilo, alquenilo, alquinilo, alquilarilo, heterociclo arilalquilo, arilo u otro grupo o porción como se define o divulga en la presente, que tiene uno o más sustituyentes, que sustituyen a uno o más átomos de hidrógeno o uno o más sustituyentes, que interrumpen una cadena de átomos de carbono. Los grupos alquenilo y alquinilo, que comprenden uno o más sustituyentes están opcionalmente sustituidos en un carbono, que consiste en una o más porciones metileno, removidas de un enlace doble.
Como se utilizan en la presente, "alquilo opcionalmente sustituido", "alquenilo opcionalmente sustituido", "alquinilo opcionalmente sustituido", alquilarilo opcionalmente sustituido ","arilalquilo opcionalmente sustituido", "heterociclo opcionalmente sustituido", "arilo opcionalmente sustituido", "heteroarilo opcionalmente sustituido", "alquilheteroarilo opcionalmente sustituido", "heteroarilalquilo opcionalmente sustituido" y similares significan un grupo alquilo, alquenilo, alquinilo, alquilarilo, heterociclo arilalquilo, arilo, heteroarilo, alquilheteroarilo, heteroarilalquilo u otro sustituyente, grupo o porción como se define o divulga en la presente, que tiene uno o más sustituyentes, que reemplazan opcionalmente a uno o más átomos de hidrógeno o uno o más sustituyentes, que interrumpen una cadena de átomos de carbono. Dichos sustituyentes se describen en la presente. Para una porción fenilo, la disposición de cualquiera de los dos sustituyentes presentes en el anillo aromático puede ser orto (o), meta (m) o para (p). Un fluoroalquilo opcionalmente sustituido es una porción alquilo o cicloalquilo, típicamente un alquilo lineal, donde uno o más átomos de hidrógeno es reemplazado por flúor y al menos otro átomo distinto de carbono y flúor.
Un sustituyente, una porción o un grupo opcionalmente sustituido o sustituido incluye aquellos que tienen uno o más grupos, que reemplazan su o sus átomos de hidrógeno individual e independientemente seleccionado entre alquilo, cicloalquilo, arilo, heteroarilo, heteroalicíclico, hidroxi, alcoxi, ariloxi, alquiltio, ariltio, alquilsulfóxido, arilsulfoxida, alquilsulfona, arilsulfona, ciano, halo, nitro, haloalquilo, fluoroalquilo, fluoroalcoxi, y amino, incluso grupos amino mono y disustituidos, y sus derivados protegidos. A modo de ejemplo, un sustituyente opcional puede ser haluro, -CN, -NO2, o LsRs, donde cada Ls se selecciona independientemente entre un enlace, -O-, -C(=O)-, -C(=O)O-, -S-, -S(=O)-, -S(=O)2-, -NH-, -NHC(=O)-, -C(=O)NH-, S(=O)2NH-, -NHS(=O)2, -OC(=O)NH-, -NHC(=O)O- o - (alquileno C1-C6) -; y cada Rs se selecciona de -H, alquilo, fluoroalquilo, heteroalquilo, cicloalquilo, arilo, heteroarilo o heterocicloalquilo. Los grupos protectores, que pueden formar los derivados protectores de los sustituyentes
anteriores se pueden encontrar en fuentes como Greene y Wuts. Los sustituyentes opcionales incluyen los seleccionados del grupo que consiste en halógeno, -CN, -NH2, -OH, -N (CH3)2, alquilo, fluoroalquilo, heteroalquilo, cicloalquilo, heterocicloalquilo, arilo, heteroarilo, alcoxi, ariloxi, alquiltio, ariltio, alquilsulfóxido, arilsulfóxido, alquilsulfona y arilsulfona, los seleccionados del grupo que consiste en halógeno, -CN, -NH2, -OH, NH(CH3), -N(CH3)2, -CO2H, -CO2alquilo, -C(=O)NH2, -C(=O)NHalquilo, -C(=O)N(alquilo)2, -S(=O)2NH2, -S(=O)2NH(alquilo), -S(=O)2N(alquilo)2, alquilo, cicloalquilo, fluoroalquilo, heteroalquilo, alcoxi, fluoroalcoxi, -S-alquilo y-S(=0)2alquilo o los seleccionados del grupo que consiste en halógeno, -CN, -NH2, -OH, -NH(CH3), -N(CH3)2, -CH3, -CH2CH3, -CF3, -OCH3, y -OCF3. Por lo general, un sustituyente, una porción o un grupo opcionalmente sustituido está sustituido con uno o dos de los grupos anteriores o, más comúnmente, con uno de los grupos anteriores. Un sustituyente opcional en un átomo de carbono alifático (átomos de carbono acíclicos o cíclicos, saturados o insaturados, con exclusión de los átomos de carbono aromáticos) incluye, además, oxo (= O).
Como se utiliza en la presente, "heterociclo" o ''heterocíclico'' significa un sistema cicloalquilo o de anillo aromático, donde uno o más, generalmente 1, 2 o 3, pero no todos los átomos de carbono que comprenden el sistema de anillos se sustituyen por un heteroátomo, que es un átomo distinto de carbono, incluso N, O, S, Se, B, Si, P, generalmente N, O S, donde dos o más heteroátomos pueden ser adyacentes entre sí o estar separados por uno o más átomos de carbono, generalmente 1-17 átomos de carbono, 1-7 átomos o 1-3 átomos. Los heterociclos incluyen anillos heteroaromáticos (también conocidos como heteroarilos) y anillos heterocicloalquilo (también conocidos como grupos heteroalicíclicos), que contienen de uno a cuatro heteroátomos en el o los anillos, donde cada heteroátomo en el o los anillos se selecciona entre O, S y N, donde cada grupo heterocíclico tiene de 4 a 10 átomos en su sistema de anillos, y con la salvedad que ningún anillo contiene dos átomos S u O adyacentes.
Los sustituyentes, las porciones o los grupos heterocíclicos no aromáticos (también conocidos como heterocicloalquilos) tienen al menos 3 átomos en su sistema de anillos, y los grupos heterocíclicos aromáticos tienen al menos 5 átomos en su sistema de anillos e incluyen sistemas de anillos benzo-condensados. Los heterociclos con 3, 4, 5, 6 y 10 átomos incluyen aziridinilo azetidinilo, tiazolilo, piridilo y quinolinilo, respectivamente. Los sustituyentes, las porciones o los grupos no aromáticos heterocíclicos son pirrolidinilo, tetrahidrofuranilo, dihidrofuranilo, tetrahidrotienilo, oxazolidinonilo, tetrahidropiranilo, dihidropiranilo, tetrahidrotiopiranilo, piperidinilo, morfolinilo, tiomorfolinilo, tioxanilo, piperazinilo, aziridinilo, azetidinilo, oxetanilo, tietanilo, homopiperidinilo, oxepanilo, tiepanilo, oxazepinilo, diazepinilo, tiazepinilo, 1,2,3,6-tetrahidropiridinilo, pirrolin-2-ilo, pirrolin-3-ilo, indolinilo, 2H-piranilo, 4H-piranilo, dioxanilo, 1,3-dioxolanilo, pirazolinilo, ditianilo, ditiolanilo, dihidropiranilo, dihidrotienilo, dihidrofuranilo, pirazolidinilo, imidazolinilo, imidazolidinilo, 3-azabiciclo [3.1.0) hexanilo, 3azabicyclo [4.1.0) heptanilo, 3H-indolilo y quinolizinilo. Los heterocíclicos aromáticos incluyen, a modo de ejemplo, piridinilo, imidazolilo, pirimidinilo, pirazolilo, triazolilo, pirazinilo, tetrazolilo, furilo, tienilo, isoxazolilo, tiazolilo, oxazolilo, isotiazolilo, pirrolilo, quinolinilo, isoquinolinilo, indolilo, bencimidazolilo, benzofuranilo, cinnolinilo, indazolilo, indolizinilo, ftalazinilo, piridazinilo, triazinilo, isoindolilo, pteridinilo, purinilo, oxadiazolilo, tiadiazolilo, furazanilo, benzofurazanilo, benzo-tiofenilo, benzotiazolilo, benzoxazolilo, quinazolinilo, quinoxalinilo, naftiridinilo y furopiridinilo. Los heterociclos no aromáticos pueden estar sustituidos con una o dos porciones oxo (=O) e incluyen pirrolidin-2-ona.
Cuando el heterociclo se utiliza como un grupo Markush (es decir, un sustituyente) el heterociclo está unido a una fórmula Markush con la que se asocia a través de un carbono o un heteroátomo del heterociclo, donde dicha unión no resulta en un estado de oxidación formal inestable o no permitido de dicho carbono o heteroátomo. Un heterociclo con enlace C está unido a una molécula a través de un átomo de carbono, e incluye porciones como -(CH2)nheterociclo, donde n es 1,2 o 3 o -C<heterociclo, donde C<representa un átomo de carbono en un anillo heterociclo. Un heterociclo con enlace N es un heterociclo que contiene nitrógeno, que está unido a un nitrógeno del anillo heterociclo a veces descrito como -N<heterociclo, donde N<representa un átomo de nitrógeno en un anillo heterociclo. Por lo tanto, los heterociclos que contienen nitrógeno pueden tener enlaces C o N e incluir sustituyentes pirrol, por ejemplo, pirrol-1-ilo (con enlace N) o pirrol-3-ilo (con enlace C), sustituyentes imidazol, por ejemplo, imidazol-1-ilo o imidazol-3-ilo (ambos con enlace N) o imidazol-2-ilo, imidazol-4-ilo o imidazol-5-il (todos con enlace C).
Como se utiliza en la presente, "heteroarilo" significa un sistema de anillos arilo, donde uno o más, generalmente 1, 2 o 3, pero no todos los átomos de carbono que comprenden el sistema de anillo arilo se sustituyen por un heteroátomo, que es un átomo distinto de carbono, incluso N, O, S, Se, B, Si, P, oxígeno (-O-), nitrógeno (-NX-) o azufre (-S-), donde X es -H, un grupo protector o alquilo C1-6 opcionalmente sustituido, donde el heteroátomo participa en el sistema conjugado ya sea a través de un enlace pi con un átomo adyacente en el sistema de anillo o a través de un único par de electrones en el heteroátomo y puede estar opcionalmente sustituido en uno o más carbonos o heteroátomos o una combinación de ambos, de una manera que conserva el sistema cíclicamente conjugado.
Los heterociclos y heteroarilos incluyen, a modo de ejemplo, los heterociclos y heteroarilos descritos en Paquette, Leo A.; "Principles of Modern Heterocyclic Chemistry" (W. A. Benjamin, New York, 1968), especialmente en los Capítulos 1,3, 4, 6, 7 y 9; "The Chemistry of Heterocyclic Compounds, A series of Monographs" (John Wiley & Sons, New York, 1950 to present), en particular los Volúmenes 13, 14, 16, 19 y 28; y J. Am. Chem. Soc. 1960, 82:5545-5473, particularmente 5566-5573). Los heteroarilos incluyen, a modo no taxativo, piridilo, tiazolilo, pirimidinilo, furanilo, tienilo, pirrolilo, pirazolilo, purinilo, imidazolilo, benzofuranilo, indolilo, isoindoilo, quinolinilo, isoquinolinilo, bencimidazolilo, piridazinilo, pirazinilo, benzotiopirano, benzotriazina, isoxazolilo, pirazolopirimidinilo, quinoxalinilo,
tiadiazolilo, triazolilo y similares. Los heterociclos que no son heteroarilos incluyen, a modo no taxativo, tetrahidrotiofenilo, tetrahidrofuranilo, indolenilo, piperidinilo, pirrolidinilo, 2-pirrolidonilo, tetrahidroquinolinilo, tetrahidroisoquinolinilo, decahidroquinolinilo, octahidroisoquinolinilo, 2H-pirrolilo, 3H-indolilo, 4H-quinolizinilo, imidazolidinilo, imidazolinilo, pirazolidinilo, piperazinilo, quinuclidinilo, morfolinilo, oxazolidinilo y similares.
Otros heteroarilos incluyen, a modo no taxativo, las siguientes porciones:
Los heteroarilos monocíclicos incluyen, a modo no taxativo, piridinilo, imidazolilo, pirimidinilo, pirazolilo, triazolilo, pirazinilo, tetrazolilo, furilo, tienilo, isoxazolilo, tiazolilo, oxazolilo, isotiazolilo, pirrolilo, piridazinilo, triazinilo, oxadiazolilo, tiadiazolilo, y furazanilo. Los heteroarilos incluyen los sustituyentes, las porciones o los grupos que contienen 0-3 átomos de N, 1-3 átomos de N o 0-3 átomos de N, 0-1 átomos de O y 0-1 átomos de S. Un heteroarilo puede ser monocíclico o bicíclico. El sistema de anillos de un anillo heteroarilo contiene generalmente 1-9 átomos de carbono (es decir, heteroarilo Cl-C9). Los heteroarilos monocíclicos incluyen heteroarilos C1-C5. Los heteroarilos monocíclicos incluyen aquellos que tienen sistemas de anillos de cinco o seis miembros. Los heteroarilos bicíclicos incluyen heteroarilos C6-C9. En función de la estructura del sustituyente, un grupo heteroarilo puede ser un monorradical o un dirradical (es decir, un grupo heteroarileno).
Como se utiliza en la presente, "heterocicloalquilo" o "heteroalicíclico" significa un grupo, una porción o un sustituyente cicloalquilo, donde al menos un carbono de la cadena de cicloalquilo se reemplaza por un heteroátomo seleccionado del grupo, que consiste en nitrógeno, oxígeno y azufre. El heterocicloalquilo se puede condensar con un arilo o un heteroarilo. Los heterocicloalquilos, también denominados heterociclos no aromáticos, incluyen, a modo no taxativo:
Los heterocicloalquilos incluyen, a modo no taxativo, oxazolidinonilo, pirrolidinilo, tetrahidrofuranilo, tetrahidrotienilo, tetrahidropiranilo, tetrahidrotiopiranilo, piperidinilo, morfolinilo, tiomorfolinilo, piperazinilo e indolinilo. Los heteroalicíclicos también incluyen todas las formas de anillos de carbohidratos, incluso, a modo no taxativo, monosacáridos, disacáridos y oligosacáridos. Por lo general, un heterocicloalquilo es un heterocicloalquilo C2-C10 e incluye heterocicloalquilo C4-C10. Un heterocicloalquilo puede c-2 átomos de contener 0-2 átomos de N, 0-2 átomos de O 0-2 átomos de S.
Como se utiliza en la presente, "heteroarilalquilo" significa un sustituyente, una porción o un grupo, donde una porción heteroarilo se encuentra ligada a una porción alquilo, es decir, -alquil-heteroarilo, donde los grupos alquilo y heteroarilo son como se describen anteriormente. Cuando el heteroarilalquilo se utiliza como un grupo Markush (es
decir, un sustituyente), la porción alquilo del heteroarilalquilo está unida a una fórmula Markush con la que se asocia a través de un carbono sp3 de la porción alquilo.
Como se utiliza en la presente, "alquilheteroarilo" significa un sustituyente, una porción o un grupo, donde una porción heteroarilo se encuentra ligada a una porción alquilo, es decir, -heteroaril-alquilo, donde los grupos heteroarilo y alquilo son como se describen anteriormente. Cuando el heteroarilalquilo se utiliza como un grupo Markush (es decir, un sustituyente), la porción heteroarilo del heteroarilalquilo está unida a una fórmula Markush con la que se asocia a través de un carbono sp2 o heteroátomo de la porción alquilo.
Como se utiliza en la presente, "halógeno" o "halo" significa flúor, cloro, bromo o yodo.
Como se utiliza en la presente, "haloalquilo" significa un sustituyente, una porción o un grupo alquilo, donde uno o más de los átomos de hidrógeno se reemplazan con uno o más átomos de halogenuros seleccionados independientemente. Los haloalquilos incluyen haloalquilo C1-C4. Los haloalquilos C1-C4 incluyen, a modo no taxativo, -CH2Cl, ChbBr, -CH2I, -CHBrCl, -CHCl-ChbCl y -CHCFCH2I.
Como se utiliza en la presente, "haloalquileno" significa un sustituyente, una porción o un grupo alquileno, donde uno o más de los átomos de hidrógeno se reemplazan con uno o más átomos de halogenuros. Los haloalquilenos incluyen haloalquilenos C1-C6 o haloalquilenos C1-C4.
Como se utiliza en la presente, "fluoroalquilo" significa un alquilo, en el que uno o más de los átomos de hidrógeno se reemplazan con un átomo de flúor. Los fluoroalquilos incluyen fluoroalquilos C1-C6 y fluoroalquilos C1-C4. Los fluoroalquilos ejemplares incluyen, a modo no taxativo, -CH3F, -CH2F2 y -CF3 y perfluoroalquilos.
Como se utiliza en la presente, "fluoroalquileno" significa un alquileno, en el que uno o más de los átomos de hidrógeno se reemplazan con un átomo de flúor. Los fluoroalquilenos incluyen fluoroalquilenos C1-C6 o fluoroalquilenos C1-C4.
Como se utiliza en la presente, "heteroalquilo" significa un grupo alquilo, en el que uno o más átomos del esqueleto del alquilo se seleccionan entre un átomo distinto de carbono, por ejemplo, oxígeno, nitrógeno, azufre, fósforo o combinaciones de estos. En un aspecto, un heteroalquilo es un heteroalquilo C1-C6.
Como se utiliza en la presente, "grupo protector" significa una porción que anula o reduce la capacidad del átomo o grupo funcional al que está vinculado de participar en reacciones no deseadas. Existen ejemplos no limitantes para -ORPR, donde RPR es un grupo protector para el átomo de oxígeno, que se encuentra en un grupo hidroxilo, mientras que para -C(O)-ORPR, Rpr puede ser un grupo protector ácido carboxílico; para -SRPR, RPR puede ser un grupo protector para el azufre en los tioles y para -NHRPR o -N(RPR)2-, al menos uno de RPR es un grupo protector del átomo de nitrógeno para aminas primarias o secundarias. Los grupos hidroxilo, amina, cetona y otros grupos reactivos pueden requerir protección contra reacciones, que tienen lugar en otras partes de la molécula. Los grupos protectores de los átomos de oxígeno, azufre o nitrógeno se utilizan generalmente para evitar reacciones no deseadas con compuestos electrófilos, como agentes de acilación. En Greene (1999), "Protective groups in organic synthesis, 3rd ed.", Wiley Interscience se proporcionan grupos protectores comunes para átomos o grupos funcionales.
Como se utiliza en la presente, "éster" significa un sustituyente, una porción o un grupo, que contiene: estructura -C(O)-O- (es decir, grupo funcional éster), donde el átomo de carbono de la estructura no está conectado directamente a otro heteroátomo y está directamente conectado a -H u otro átomo de carbono. Por lo general, los ésteres comprenden, o consisten en, una porción orgánica, que contiene 1-50 átomos de carbono, 1-20 átomos de carbono o 1-8 átomos de carbono y de 0 a 10 heteroátomos seleccionados independientemente (por ejemplo, O, S, N, P, Si), generalmente 0-2, donde la porción orgánica está ligada a través de la estructura -C(O)-O- e incluye porciones éster como porciones orgánicas-C(O)-O-. La porción orgánica comprende comúnmente uno o más de cualquiera de los grupos orgánicos descritos en la presente, por ejemplo, porciones alquilo C1-20, porciones alquenilo C2-20, porciones alquinilo C2-20, porciones arilo, heterociclos C3-8 o derivados sustituidos de cualquiera de estos, por ejemplo, que comprenden 1, 2, 3, 4 o más sustituyentes, donde cada sustituyente se elige independientemente. Las sustituciones ejemplares no limitantes de átomos de hidrógeno o carbono en estos grupos orgánicos son como se describen anteriormente para alquilo sustituido y otras porciones sustituidas y se eligen de forma independiente. Las sustituciones mencionadas anteriormente son típicamente sustituyentes, que se pueden utilizar para reemplazar uno o más átomos de carbono, por ejemplo, -O- o -C(O)- o uno o más átomos de hidrógeno, por ejemplo, halógeno, -NH2 u -OH. Los ésteres ejemplares incluyen, a modo no taxativo, uno o más acetatos, propionatos, isopropionatos, isobutiratos, butiratos, valeratos, isovaleratos, caproatos, isocaproatos, hexanoatos, heptanoatos, octanoatos, ésteres de fenilacetato o ésteres de benzoato seleccionados independientemente. Cuando un éster se utiliza como grupo Markush (es decir, un sustituyente), el oxígeno de enlace simple del grupo funcional éster está unido a una fórmula Markush con la que se asocia.
Como se utiliza en la presente "acetal", "tioacetal", "cetal", "tiocetal" y similares significan una porción, un grupo o un sustituyente, que comprende, o que consiste en, un átomo de carbono al que están unidos dos de los heteroátomos iguales o diferentes, donde los heteroátomos son S y O independientemente seleccionados. Para el acetal, el carbono tiene dos átomos de oxígeno unidos, un átomo de hidrógeno y una porción orgánica. Para el cetal, el
carbono tiene dos átomos de oxígeno unidos y dos porciones orgánicas independientemente seleccionadas, donde la porción orgánica es como se describe en la presente, un grupo alquilo o un grupo alquilo opcionalmente sustituido. Para el tioacetal y el tiocetal, uno de los átomos de oxígeno o ambos átomos de oxígeno en el acetal o cetal, respectivamente, se reemplazan con azufre. Los átomos de oxígeno o azufre en el cetal o tiocetal se encuentran, a veces, unidos por una porción alquilo opcionalmente sustituido. Por lo general, la porción alquilo es un alquilo opcionalmente sustituido C1-8 o una estructura alquilo ramificada, como -C(CH3)2-, -CH(CH3)-, -CH2-, -CH2-CH2-, -C[(alquilo C2-C4)2]i, 2, 3- o -[CH(alquilo C2-C4)]i, 2, 3-. Algunas de estas porciones pueden servir como grupos protectores para un aldehído o cetona, por ejemplo, acetales y cetales de aldehídos para cetonas, y contienen porciones -O-CH2-CH2-CH2-O- u -O-CH2-CH2-O-. que forman un anillo espiro con el carbono carbonilo y se pueden remover mediante métodos de síntesis química o a través del metabolismo en células o fluidos biológicos.
"Éter", como se usa en la presente, significa una porción, un grupo o un sustituyente orgánico que comprende o consiste en 1, 2, 3, 4 o más porciones -O-, generalmente 1 o 2, donde no hay dos porciones -O- inmediatamente adyacentes (es decir, unidas directamente) entre sí. Típicamente, los éteres comprenden una porción orgánica que contiene 1-50 átomos de carbono, 1-20 átomos de carbono o 1-8 átomos de carbono y de 0 a 10 heteroátomos seleccionados independientemente (por ejemplo, O, S, N, P, Si), típicamente 0-2. Una porción, un grupo o un sustituyente éter que incluye una porción orgánica-O- donde la porción orgánica es como se describe en la presente para alquilo o un grupo alquilo opcionalmente sustituido. Cuando el éter se utiliza como un grupo Markush (es decir, un sustituyente), el oxígeno del grupo funcional éter está unido a una fórmula Markush con la que está asociado. Cuando el éter se utiliza como sustituyente en un grupo Markush, a veces se llama grupo "alcoxi". Alcoxi incluye sustituyentes de éter C1-C4, que incluye, a modo no taxativo, metoxi, etoxi, propoxi, iso-propoxi y butoxi. Éter incluye además aquellos sustituyentes, aquellas porciones o aquellos grupos que contienen una (sin incluir cetal) o más porciones -OCH2CH2O- en la secuencia (es decir, polietileno o porciones PEG).
"Carbonato", como se usa en la presente, significa un sustituyente, una porción o un grupo que contiene una estructura -OC(=O)-O-(es decir, grupo funcional carbonato). Típicamente, los grupos carbonato, como se usan en la presente, comprenden o consisten en una porción orgánica, que contiene 1-50 átomos de carbono, 1-20 átomos de carbono o 1-8 átomos de carbono y de 0 a 10 heteroátomos seleccionados independientemente (por ejemplo, O, S, N, P, Si), típicamente 0-2 unidos a través de la estructura -O-C(=O)-O-, por ejemplo, porción orgánica -O-C (=O)-O-. Cuando el carbonato se utiliza como un grupo Markush (es decir, un sustituyente), uno de los átomos de oxígeno de unión simple del grupo funcional carbonato está unido a una fórmula Markush con la que está asociado.
"Carbamato" o "uretano", como se utiliza en la presente, significa un sustituyente, una porción o un grupo que contiene una estructura -O-C(=O)N(RPR)-, -O-C(=O)N(Rpr)2, -O-C(=O)NH (alquilo opcionalmente sustituido) o -O-C(=O)N(alquilo opcionalmente sustituido^ (es decir, grupo funcional carbamato), donde RPR y alquilo opcionalmente sustituido se seleccionan independientemente y RPR son independientemente -H, un grupo protector o una porción orgánica como se describió para éster, alquilo o alquilo opcionalmente sustituido. Típicamente, los grupos carbamato, como se usan en la presente, comprende o consiste en una porción orgánica que contiene 1-50 átomos de carbono, 1-20 átomos de carbono o 1-8 átomos de carbono y de 0 a 10 heteroátomos seleccionados independientemente (por ejemplo, O, S, N, P, Si), típicamente 0-2 unidos a través de la estructura -O-C(=O)-NRPR-, por ejemplo, la porción orgánica -O-C(=O)-NRPR- o la porción orgánica -O-C(=O)-NRPR. Cuando el carbamato se utiliza como un grupo Markush (es decir, un sustituyente), el oxígeno (unión O) o nitrógeno (unión N) de unión simple del grupo funcional carbamato está unido a una fórmula Markush con la que está asociado. La unión del sustituyente carbamato se indica de forma explícita (unión N- u O-) o implícita en el contexto al que se refiere este sustituyente.
Para cualquier porción o grupo sustituyente descrito por un rango de átomos de carbono, el rango designado significa que se describe cualquier número individual de átomos de carbono. Por lo tanto, la referencia a, por ejemplo, "alquilo C1-C4 opcionalmente sustituido", "alquenilo C2-6 alquenilo opcionalmente sustituido", "heterociclo C3-C8 opcionalmente sustituido" significa específicamente que está presente una porción alquilo opcionalmente sustituido de 1, 2, 3 o 4 carbonos, como se define en la presente, o un alquenilo de 2, 3, 4, 5 o 6 carbonos, o una porción de 3, 4, 5, 6, 7 u 8 carbonos comprende un heterociclo o porción alquenilo opcionalmente sustituido, como se define en la presente. Todas estas designaciones tienen el propósito expreso de divulgar todos los grupos de átomos de carbono individuales y, por lo tanto, "alquilo C1-C4 opcionalmente sustituido" incluye, por ejemplo, alquilo 3 de carbono, alquilo sustituido 4 de carbono y alquilo de carbono 4, lo que incluye todos los isómeros posicionales y similares; estos pueden denominarse o referirse expresamente. Para ésteres, carbonatos y carbamatos definidos por un rango de átomos de carbono, el rango designado incluye el carbono carbonilo del grupo funcional respectivo. Así, un éster C1 se refiere a un éster de formiato y un éster C2 se refiere a un éster de acetato. Los sustituyentes orgánicos, las porciones y los grupos descritos en la presente, y para otras porciones cualesquiera descritas en la presente, por lo general excluirá porciones inestables, excepto cuando dichas porciones inestables son especies transitorias que se pueden utilizar para elaborar un compuesto con la suficiente estabilidad química para uno o más de los usos que se describen en la presente. Los sustituyentes, las porciones o los grupos por operación de las definiciones de la presente que se traduce en los que tienen un carbono pentavalente se excluyen específicamente.
"Dependiente de LPA", "mediado por LPA" o términos similares, como se usa en la presente, significa una enfermedad o trastorno cuya etiología, avance o persistencia se efectúa en todo o en parte por la señalización a través de uno o más subtipos de receptores de ácido lisofosfatidico, que incluyo a modo enunciativo, subtipos de receptores de ácido lisofosfatídico 1-6 (LPAR). Las enfermedades y los trastornos dependientes de LPA o mediados
por LPA incluyen, a modo no taxativo, la fibrosis de órganos (por ejemplo, hígado, riñón, pulmón, corazón y similares), enfermedades del hígado (por ejemplo, hepatitis aguda, hepatitis crónica, fibrosis hepática, cirrosis hepática, hipertensión portal, insuficiencia regenerativa, esteatohepatitis no alcohólica (EHNA), hipofunción hepática, trastorno hepático del flujo sanguíneo y similares), enfermedad proliferativa celular (por ejemplo, cánceres, incluido a modo no taxativo, metástasis de tumor sólido, fibroma vascular, mieloma, mieloma múltiple, sarcoma de Kaposi, leucemia, leucemia linfocítica crónica (LLC), metástasis invasiva de las células cancerígenas y similares), enfermedad inflamatoria (por ejemplo, psoriasis, nefropatía, neumonía y similares), enfermedad del tracto gastrointestinal (por ejemplo. síndrome del intestino irritable (ISS), enfermedad inflamatoria intestinal (EII), secreción pancreática anormal, y similares), enfermedad renal, enfermedad asociada al tracto urinario (por ejemplo, hiperplasia prostática benigna o síntomas asociados con la enfermedad neuropática de la vesícula), tumor de la médula espinal, hernia de disco intervertebral, estenosis del canal espinal, síntomas derivados de la diabetes, enfermedad del tracto urinario inferior (por ejemplo, obstrucción del tracto urinario inferior y similares), enfermedad inflamatoria del tracto urinario inferior (por ejemplo, disuria, micción frecuente y similares), enfermedad del páncreas, enfermedad asociada con angiogénesis anormal (por ejemplo, obstrucción arterial y similares), esclerodermia, enfermedades asociadas con el cerebro (por ejemplo, infarto cerebral, hemorragia cerebral y similares), enfermedades del sistema nervioso (por ejemplo, dolor neuropático, neuropatía periférica, prurito y similares), enfermedad ocular (por ejemplo, degeneración macular relacionada con la edad (AMD), retinopatía diabética, retinopatía proliferativa vítrea (PVR), penfigoide cicatricial, cicatrices por cirugía de filtración de glaucoma y similares).
"Agentes LPA1R selectivos", "compuestos selectivos LPA1R" y términos similares, como se usan en la presente, significan agentes o compuestos que interactúan con el subtipo 1 de receptor de ácido lisofosfatidico con preferencia sobre el receptor del ácido lisofosfatídico 2-6. Típicamente, esa preferencia se manifiesta por una afinidad de unión 10 veces más fuerte del agente a LPA1R en comparación con otros LPAR conocidos, de conformidad con lo medido por los valores de Kd determinados experimentalmente.
"Formulación farmacéuticamente aceptable", como se usa en la presente, significa una composición que comprende un ingrediente farmacéuticamente activo, como un compuesto que tiene la fórmula I-VI, además de uno o más excipientes farmacéuticamente aceptables o se refiere a una composición preparada a partir de un ingrediente farmacéuticamente activo y uno o más excipientes farmacéuticamente aceptables, donde la composición es adecuada para la administración a un individuo que lo necesita, como un ser humano o un animal. Para que una formulación farmacéuticamente aceptable sea adecuada para la administración a un ser humano, la formulación debe tener actividad biológica para tratar o prevenir una enfermedad o trastorno descrito en la presente o debe existir una expectativa de que la formulación tendría una actividad deseada hacia una "intención de tratar" la enfermedad o trastorno. Típicamente, la "intención de tratar" una enfermedad o trastorno es una enfermedad o trastorno mediada por el receptor de ácido lisofosfatídico. Más típicamente, la enfermedad o trastorno que se busca tratar o prevenir es una enfermedad o trastorno mediado por un receptor tipo 1 de ácido lisofosfatídico. Una formulación farmacéuticamente aceptable que es adecuada para su administración a un animal no requiere necesariamente una actividad biológica para tratar o prevenir una enfermedad o trastorno y se puede administrar al animal a fin de evaluar una actividad biológica o farmacológica potencial de un compuesto de Fórmula I-XII. Por consiguiente, estas formulaciones deben ser adecuadas para tratar o prevenir una enfermedad o trastorno descrito en la presente en un animal que las necesita o adecuadas para evaluar una actividad farmacológica o biológica de un compuesto de Fórmula I-XII. Las composiciones que son adecuadas solo para su uso en ensayos in vitro o que contienen un vehículo, componente o excipiente en una cantidad no permitida de un producto farmacéutico están específicamente excluidas de la definición de una formulación farmacéuticamente aceptable.
La formulación farmacéuticamente aceptable puede estar compuesta de uno, dos o más compuestos de Fórmula I-XII o prepararse a partir de ellos, típicamente uno o dos, y uno o más excipientes farmacéuticamente aceptables. Más típicamente, las formulaciones consisten esencialmente o consisten en un único compuesto de Fórmula I-XII y uno o más excipientes farmacéuticamente aceptables. Otras formulaciones pueden estar compuestas, consistir esencialmente, o consistir en uno, dos o más compuestos de Fórmula I-XII y uno, dos o más compuestos en uso actual para el tratamiento de una enfermedad o trastorno mediado por el receptor tipo 1 de ácido lisofosfatídico descrito en la presente y uno o más excipientes farmacéuticamente aceptables. Típicamente, las formulaciones consisten esencialmente o consisten en un único compuesto de Fórmula I-XII, un compuesto único actualmente en uso para el tratamiento de una enfermedad o trastorno mediado por el receptor tipo 1 de ácido lisofosfatídico descrito en la presente y uno o más excipientes farmacéuticamente aceptables.
"Formulación sólida", como se utiliza en la presente, se refiere a una formulación farmacéuticamente aceptable que comprende al menos un compuesto de Fórmula I-XII y uno o más excipientes farmacéuticamente aceptables en forma sólida, donde la formulación tiene una forma de dosificación unitaria adecuada para la administración de un sólido. Las unidades de dosificación incluyen comprimidos, cápsulas, comprimidos oblongos, cápsulas de gel, suspensiones y otras unidades de dosificación típicamente asociadas con administración por vía parenteral o enteral (oral) de un sólido.
"Formulación líquida", como se utiliza en la presente, se refiere a una formulación farmacéuticamente aceptable donde al menos un compuesto de Fórmula I-XII se ha mezclado o ha entrado en contacto con uno o más excipientes farmacéuticamente aceptables, donde al menos uno de los excipientes está en forma líquida en proporciones exigidas para una formulación líquida, es decir, que la mayoría de la cantidad de masa del compuesto de Fórmula IXII se disuelve en el excipiente no sólido. Las unidades de dosificación que contienen una formulación líquida incluyen jarabes, geles, ungüentos y otras unidades de dosificación típicamente asociadas con la administración por vía parenteral o enteral de una formulación farmacéutica en forma líquida a un individuo que la necesita.
"Prevenir", "previene" y similar, como se usa en la presente, tiene el significado normal y habitual de las técnicas médicas y, por lo tanto, #no exige que cada instancia a la que se refiere el término se evite con certeza.
Realizaciones numeradas
En la presente se divulgan las siguientes formas de realización. En ciertas realizaciones, los compuestos presentados en la presente poseen uno o más estereocentros y cada centro existe independientemente, ya sea en la configuración R o S. Los compuestos presentados en la presente incluyen diastereoisómeros, enantiómeros y epiméros así como mezclas apropiadas de estos. Los estereoisómeros se obtienen por métodos tales como, síntesis estereoselectiva y/o separación de estereoisómeros por columnas cromatográficas quirales. Los métodos y formulaciones descritas en la presente incluyen el uso de sales farmacéuticamente aceptables de los compuestos que tienen la estructura de Fórmulas (I-VI), así como metabolitos activos de estos compuestos que tienen el mismo tipo de actividad. En algunas situaciones, los compuestos pueden existir como tautómeros. Todos los tautómeros están incluidos dentro del alcance de los compuestos presentados en la presente. En realizaciones específicas, los compuestos descritos en la presente existirán en forma de sales, incluso sales farmacéuticamente aceptables. Las formas de sales incluyen sales de adición inorgánicas, como F- Cl-, Br-, I- y sales de sulfato y sales de adición orgánicas, como mesilato, besilato, tosilato, citrato, succinato, fumarato y malonato. En otras formas de realización, los compuestos descritos en la presente existen como sales de amonio cuaternario.
1. Un compuesto de fórmula I que tiene la estructura
o una sal farmacéuticamente aceptable de este,
donde RA es -CO2H, -CO2RB, -CN, tetrazolilo, -C(=O)NH2, -C(=O)NHRB, -C(=O)NHSO2RB o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico como se indica anteriormente;
L1 está ausente o es alquileno C1-C6 sustituido o no sustituido, fluoroalquileno C1-C6, cicloalquileno C3-C6 sustituido o no sustituido, heteroalquileno C1-C6 sustituido o no sustituido;
L2 está ausente;
donde RB es -H o alquilo C1-C4, o tiene la estructura de uno de:
El anillo A es un heteroareno de 5 miembros que tiene la estructura de uno de:
donde la línea punteada indica el punto de unión del anillo A al anillo B;
donde RC es -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, alquilo C1-C4, cicloalquilo C3-C6, o fluoroalquilo C1-C4,
y RD es -NRFC(=O)XCH(RG)-CY, -N(RF)C(=O)XC(RG)2-CY, o -NRFC(=O)X-CY, -C(=O)-N(RF)-CH(RG)X-CY, o -C(=O)-N(RF)-C(RG)2X-CY,
donde X está ausente, es -O-, -NH- o -CH2-;
RE es -H, -alquilo C1-C4 o -fluoroalquilo C1-C4,
RF es -H o alquilo C1-C4, y
RG es RE seleccionado independientemente o un RG es alquilo C1-C4 y se toma junto con CY y el átomo de carbono al que RG está unido y el carbono o heteroátomo al que CY está unido para definir un carbociclo sustituido o no sustituido o heterociclo sustituido o no sustituido y el otro RG, si está presente, es como se define por RE;
donde CY es alquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C10 sustituido o no sustituido, heterocicloalquilo
C2-C10 sustituido o no sustituido, arilo sustituido o no sustituido, o heteroarilo sustituido o no sustituido, donde si CY está sustituido, entonces CY está sustituido con 1,2, o 3 RH seleccionados independientemente,
RH es independientemente -H, halógeno, -CN, -NO2, -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2RJ, -N(RJ)S(=O)2RJ, -S(=O)2N(Rl)2, -C(=O)Rj, OC(=O)Rj, -CO2Rj, -OCO2Rj, -N(Rl)2, -C(=O)N(Rl)2, -OC(=O)N(Rl)2, N(Rj)C(=O)N N(RJ)C(=O)RJ,
-N(RJ)C(=O)ORJ, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4, o heteroalquilo C1-C4,
donde cada RJ es independientemente alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), y alquileno-C1-C4-(heteroarilo sustituido o no sustituido), y
donde cada RL es independientemente -H, alquilo C1-C6, C1-C6 heteroalquilo, fluoroalquilo C1-C6, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido), o
Cuando RH es -S(=O)2N(RL)2, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2 o
-N(Rj)C(=O)N(Rl)2, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al el átomo de N al que están unidos para definir un heterociclo sustituido o no sustituido,
o cuando W o Z es -C(RL)2-cada RL es independientemente -H, alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al átomo de carbono al que están unidos para definir un carbociclo;
El anillo B es arileno sustituido o no sustituido, o heteroarileno sustituido o no sustituido, donde si el anillo B está sustituido, entonces el anillo B está sustituido con 1, 2, o 3 RH seleccionados independientemente, donde el anillo B tiene la estructura
donde A1, A2 y A3 se seleccionan independientemente de -N=, =N-, =CH- o -CH=;
RH es como se definió previamente; y
El anillo C está ausente o es cicloalquileno C3-C10 sustituido o no sustituido, heterocicloalquileno C2-C10 sustituido o no sustituido, arileno sustituido o no sustituido, o heteroarileno sustituido o no sustituido, donde si el anillo C está sustituido, entonces el anillo C está sustituido con 1, 2, o 3 RH seleccionados independientemente, donde RH es como se definió previamente, y
donde los sustituyentes de RJ, RL y RH, si están presentes, son como se indican.
En algunas realizaciones RC es -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, alquilo C1-C4, cicloalquilo C3-C6, o fluoroalquilo
C1-C4 y RD es -N(RF)-C(=O)XCH(RG)-CY, -N(RF)-, -C(=O)XC(RG)2-CY o -N(RF)-C(=O)X-CY, donde RF y cada RG son independientemente -H o alquilo C1-C4.
RA es -CO2H, -CO2Rb, -CN, tetrazolilo, -C(=O)NH2,
-C(=O)NHRB, C(=O)NHSO2Rb o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico como se indica anteriormente.
En realizaciones preferidas RA es -CO2H, -CO2RB, -CN, o -C(=O)NHSO2RB, donde RB es alquilo C1-C4 sustituido o no sustituido o tiene la estructura de uno de:
En algunas realizaciones L1 está ausente o es alquileno C1-C6 sustituido o no sustituido, fluoroalquileno C1-C6, o heteroalquileno C1-C6 sustituido o no sustituido.
En algunas realizaciones preferidas L1 está ausente o es alquileno C1-C6 sustituido o no sustituido.
En realizaciones particularmente preferidas L1 es -CH2-, , o dimetilmetano (es decir, -C(CH3)2-).
L2 está ausente.
El anillo A es un heteroareno de 5 miembros que tiene una de las estructuras de:
Los compuestos de Fórmula I tienen RC que se define como -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, alquilo C1-C4, o fluoroalquilo C1-C4.
En realizaciones más preferidas, los compuestos de Fórmula I tienen RC que se define como -F, -CN, -CH3, o -CF3. En algunas realizaciones, los compuestos de Fórmula I tienen RD que se define como -N(RF)C(=O)-XCH(RG)-CY, -N(Rf)C(=O)XC(Rg)2-CY, o -N(RF)C(=O)X-CY, donde X está ausente, es -O-, -NH- o -CH2-, donde RF es -H o alquilo C1-C4 y X, Cy y RG son como se definieron previamente.
En realizaciones más preferidas, los compuestos de Fórmula I tienen RD que se define como -N(RF)C(=O)OCH(RG)-CY, -N(RF)C(=O)NHC(RG)-CY, o -N(RF)C(=O)CH2-CY, donde RF es -H o alquilo C1-C4 y X, CY y RG son como se definieron previamente.
Los compuestos de Fórmula I tienen RE que se define como -H o alquilo C1-C4, o fluoroalquilo C1-C4.
En realizaciones más preferidas, los compuestos de Fórmula I tienen RE que se define como -H, -CH3, ciclopropilo o -CF3.
Los compuestos de Fórmula I tienen RF que se define como H, o alquilo C1-C4.
En realizaciones más preferidas, los compuestos de Fórmula I tienen RF que se define como -H.
En algunas realizaciones de fórmula I los compuestos un RG es -alquilo C1-C4 y se toma junto con CY y el átomo de carbono al que RG y CY están unidos para definir un carbociclo sustituido o no sustituido o un heterociclo sustituido o no sustituido y el otro RG, si está presente es -H.
En otras realizaciones de fórmula I los compuestos RG es independientemente -H o alquilo C1-C4.
En la fórmula I los compuestos de anillo B son como se indica anteriormente. En la fórmula I los compuestos de anillo C son cicloalquileno C3-C10 sustituido o no sustituido, heterocicloalquileno C2-C10 sustituido o no sustituido, un arileno sustituido o no sustituido, o heteroarileno sustituido o no sustituido, donde si el anillo C está sustituido, entonces el anillo C está sustituido con 1,2, o 3 RH seleccionados independientemente.
En la fórmula I los compuestos CY son alquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C10 sustituido o no sustituido, heterocicloalquilo C2-C10 sustituido o no sustituido, arilo sustituido o no sustituido, o heteroarilo sustituido o no sustituido, donde si CY está sustituido, entonces CY está sustituido con 1, 2, o 3 RH seleccionados independientemente.
Los compuestos particularmente preferidos de Fórmula I tienen el anillo B y el anillo C cada uno definido independientemente como arilo o heteroarilo 1,4-sustituido, RA es -CO2H, RC es -F o -CN, RD es -NRFC(=O)OCH(RG)-CY, RE es -CH3, y RF, RG, y CY son como se definieron previamente.
Otros compuestos particularmente preferidos de Fórmula I tienen el anillo B que se define como arilo o heteroarilo 1,4-sustituido, RA es -CO2H, RD es -N(RF)C(=O)OCH(RG)-CY, RE es -CH3, y RC, RF, RG, y CY son como se definieron previamente.
2. El compuesto de la realización 1 donde Rc es -CN, -F, -CH3 o -CF3.
3. El compuesto de la realización 1 o 2 donde RC es -F o -CN.
4. El compuesto de la realización 1, 2 o 3 donde L1, cuando está presente es un alquilo geminalmente sustituido, grupo cicloalquilo o heterocicloalquilo.
6. El compuesto de cualquiera de las realizaciones 1 -5 donde RF es -H.
7. El compuesto de cualquiera de las realizaciones 1-6 donde RG es -CH3.
8. El compuesto de cualquiera de las realizaciones 1-7 donde CY es fenilo sustituido o no sustituido.
9. El compuesto de cualquiera de las realizaciones 1-8 donde RH es -H, halógeno, -CN, -NO2, -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2Rj, -N(Rl)2, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4, y heteroalquilo C1-C4.
10. El compuesto de cualquiera de las realizaciones 1-9 donde RH se seleccionan independiente de -H, halógeno o alquilo C1-C4 sustituido o no sustituido o alcoxi C1-C4 sustituido.
11. El compuesto de cualquiera de las realizaciones 1-10 donde RH es independientemente -H, -Cl, -F, -CH3, -CF3, -OCH3 o -OCF3.
Se divulga adicionalmente un compuesto de fórmula II que tiene la estructura:
donde RA es -CO2H, -CO2RB, -CN, tetrazolilo, -C(=O)NH2, -C(=O)NHRB, C(=O)NHSO2RB o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico,
RB es alquilo C1-C4 opcionalmente sustituido o tiene la estructura de uno de:
L1 está ausente o es alquileno C1-C6 opcionalmente sustituido; fluoroalquileno C1-C6 opcionalmente sustituido, o heteroalquileno C1-C6 opcionalmente sustituido o -UV-Z-, donde -UV- se define mediante -OW-, -WO-, -N(RJ)W-, -WN(RJ)-, -N(RJ)C(=O)-, -SW-, -S(=O)nW-, o
-C(=O)N(RJ)-, donde W es alquileno C1-C3 opcionalmente sustituido o W es -C(RL)2-, Z es alquileno C1-C6 opcionalmente sustituido o fluoroalquileno C1-C6 o Z es -C(RL)2-; y n es 0, 1, o 2;
El anillo A es un heteroareno de 5 o 6 miembros que tiene la estructura de uno de:
donde RC es -H, -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, alquilo C1-C4, cicloalquilo C3-C6, o fluoroalquilo C1-C4;
RD es -N(RF)C(=O)XCH(RG)-CY, -N(RF)C(=O)XC(RG)2-CY, o -N(RF)C(=O)X-CY; donde X está ausente, es -O-, -NH-o -CH2-;
RE es -H o alquilo C1-C4, cicloalquilo C1-C6 o fluoroalquilo C1-C4;
RF es -H, alquilo C1-C4 o cicloalquilo C1-C6;
RG es RE seleccionado independientemente, o uno de RG es alquilo C1-C4 y se toma junto con CY y el átomo de carbono al que RG y CY están unidos para definir un carbociclo sustituido o no sustituido o un heterociclo sustituido o no sustituido y el otro RG, si está presente, es como se define por RE ;
El anillo B está cicloalquileno C3-C10 opcionalmente sustituido, heterocicloalquileno C2-C10 opcionalmente sustituido, arileno opcionalmente sustituido, o heteroarileno opcionalmente sustituido, donde si el anillo B está sustituido, entonces el anillo B está sustituido con 1,2, o 3 RH independientemente seleccionados;
El anillo C está ausente o es cicloalquileno C3-C10 opcionalmente sustituido, heterocicloalquileno C2-C10 opcionalmente sustituido, arileno opcionalmente sustituido, o heteroarileno opcionalmente sustituido, donde si el anillo C está sustituido, entonces el anillo C está sustituido con 1, 2, o 3 RH seleccionados independientemente;
CY es alquilo C1-C6 opcionalmente sustituido, cicloalquilo C3-C10 opcionalmente sustituido, heterocicloalquilo C2-C10 opcionalmente sustituido, arilo opcionalmente sustituido, u heteroarilo opcionalmente sustituido, donde si CY está sustituido, entonces CY está sustituido con 1,2, o 3 RH seleccionados independientemente, o
donde cada RH es seleccionados independientemente -H, halógeno, -CN, -NO2, -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2RJ, -N(RJ)S(=O)2RJ, -S(=O)2N(RL)2, -C(=O)RJ, -OC(=O)RJ, -C(=O)ORJ, -OC(=O)ORJ, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(Rl)2, -N(Rj)C(=O)N(Rl)2, -N(Rj)C(=O)Rj, -N(Rj)C(=O)ORj, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4, o heteroalquilo C1-C4, y
donde RJ es alquilo C1-C6 opcionalmente sustituido, heteroalquilo C1-C6 opcionalmente sustituido, fluoroalquilo C1-C6 opcionalmente sustituido, cicloalquilo C3-C6 opcionalmente sustituido, heterocicloalquilo opcionalmente sustituido, arilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 opcionalmente sustituido), alquileno-C1-C4-(heterocicloalquilo opcionalmente sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo opcionalmente sustituido), y
cada RL es independientemente -H, alquilo C1-C6 opcionalmente sustituido, heteroalquilo C1-C6 opcionalmente sustituido, fluoroalquilo C1-C6 opcionalmente sustituido, cicloalquilo C3-C6 opcionalmente sustituido, heterocicloalquilo opcionalmente sustituido, arilo opcionalmente sustituido, heteroarilo opcionalmente sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 opcionalmente sustituido), alquileno-C1-C4-(heterocicloalquilo opcionalmente sustituido), alquileno-C1-C4-(arilo opcionalmente sustituido), o alquileno-C1-C4-(heteroarilo opcionalmente sustituido), o
cuando RH es -S(=O)2N(RL)2, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2 o -N(RJ)C(=O)N(RL)2, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al el átomo de N al que están unidos para definir un heterociclo opcionalmente sustituido,
o cuando W o Z es -C(RL)2-, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al átomo de carbono al que están unidos para definir un carbociclo;
donde cuando el anillo B es arileno sustituido o no sustituido, el anillo C está ausente, L1 es -UV-Z, donde -UV- es -N(RJ)-C(=O)-, donde RJ es -H, RD es -N(RF)C(=O)XCH(RG)-CY, donde X es -O-, RG es -CH3 y RF es -H, y RC es -H, -CH3 o -CF3, o cuando el anillo B es arileno sustituido o no sustituido y el anillo C es arileno sustituido o no sustituido o es cicloalquileno C3-C10 sustituido o no sustituido, o el anillo B es cicloalquileno C3-C10 sustituido o no sustituido y el anillo C es arileno sustituido o no sustituido y L1 es alquileno C1-C6,
y RC es -H o -CH3 y RA es -CO2H o -CO2RB,
entonces el anillo A tiene la estructura de uno de:
y cuando el anillo B es heterocicloalquileno C2-C10, el anillo C es arileno sustituido o no sustituido, L1 es alquileno C1-C6, RC es -CH3 y RA es -CO2H o -CO2RB,
entonces el anillo A tiene la estructura de uno de:
El anillo A puede tener la estructura de uno de:
Los compuestos de Fórmula II pueden tener el anillo B y el anillo C cada uno definidos como arilo o heteroarilo 1,4-sustituido, RA es CO2H, y RD es -N(RF)C(=O)OCH(RG)-CY.
Los compuestos de Fórmula II pueden tener el anillo B que se define como arilo o heteroarilo 1,4-sustituido, L1 es -UV-Z-, donde -UV- se define mediante -WO-, -WN(RJ)-, o -C(=O)N(RJ)-, donde W es -CH2-, Z es alquileno C1-C6 sustituido o no sustituido, RA es -CO2H, RD es -N(RF)C(=O)OCH(RG)-CY.
Se divulga adicionalmente un compuesto de fórmula III que tiene la estructura:
o una sal o profármaco farmacéuticamente aceptable de este,
donde RA es -CO2H, -CO2RB, -CN, tetrazolilo, -C(=O)NH2, -C(=O)NHRB, C(=O)NHSO2RB o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico;
RB es alquilo C1-C4 sustituido o no sustituido o tiene la estructura de uno de
L1 está ausente o es alquileno C1-C6 sustituido o no sustituido, fluoroalquileno C1-C6; o heteroalquileno C1-C6 sustituido o no sustituido o -UV-Z-donde -UV- se define mediante -OW-, -WO-, -N(Rj)W-, -WN(Rj )-, -N(Rj)C(=O)-, -SW-, -S(=O)nW-, o -C(=O)N(RJ)-, donde W es alquileno C1-C3 sustituido o no sustituido o W es -C(RL)2-, Z es alquileno C1-C6 sustituido o no sustituido o fluoroalquileno C1-C6; y n es 0,1, o 2;
El anillo A es un heteroareno de 5-6 miembros que tiene la estructura de uno de:
donde RC es -H, -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, alquilo C1-C4, cicloalquilo C3-C6, o fluoroalquilo C1-C4;
RD es -N(RF)C(=O)XCH(RG)-CY, -N(RF)C(=O)XC(RG)2-CY, o -N(RF)C(=O)X-CY. donde X está ausente, es -O-, -NH-o -CH2-;
RE es -H o alquilo C1-C4, cicloalquilo C1-C6 o fluoroalquilo C1-C4;
RF -H, alquilo C1-C4 o cicloalquilo C1-C6;
RG es RE seleccionado independientemente, o un RG es -alquilo C1-C4 y se toma junto con CY y el átomo de carbono al que RG y CY están unidos para definir un carbociclo sustituido o no sustituido o un heterociclo sustituido o no sustituido y el otro RG, si está presente, es como se define por RE;,
A1, A2 y A3 son independientemente =NH-, -N=, =CH- o -CH=;
El anillo C está ausente o es cicloalquileno C3-C10 sustituido o no sustituido, heterocicloalquileno C2-C10 sustituido o no sustituido, arileno sustituido o no sustituido, o heteroarileno sustituido o no sustituido, donde si el anillo C está sustituido, entonces el anillo C está sustituido con 1, 2, o 3 RH seleccionados independientemente;
CY es alquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C10 sustituido o no sustituido, heterocicloalquilo C2-C10 sustituido o no sustituido, arilo sustituido o no sustituido, o heteroarilo sustituido o no sustituido, donde si CY está sustituido, entonces CY está sustituido con 1, 2, o 3 RH ;
donde cada RH es independientemente -H, halógeno, -CN, -NO2, -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2RJ, -N(Rj)S(=O)2Rj, -S(=O)2N(Rl)2, -C(=O)Rj, -OC(=O)Rj, -C(=O)ORj, -OC(=O)ORj, -N(Rl)2, -C(=O)N(Rl)2, -OC(=O)N(Rl)2, N(Rj)C(=O)N(Rl)2, -N(Rj)C(=O)Rj, -NRjC(=O)ORj, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4, o heteroalquilo C1-C4;
cada RJ es independientemente alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o C1-C4 alquileno-(heteroarilo sustituido o no sustituido);
cada RL es independientemente -H, alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo sustituido o no sustituido, un heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido), o
cuando RH es -S(=O)2N(RL)2, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2 o N(RJ)C(=O)N(RL)2, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al el átomo de N al que están unidos para definir un heterociclo sustituido o no sustituido, o
cuando W o Z es -C(RL)2-, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al átomo de carbono al que están unidos para definir un carbociclo;
donde cuando A1, A2 y A3 son =CH- o -CH=, el anillo C está ausente, L1 es -UV-Z, donde -UV- es -N(RJ)C(=O)-, donde RJ es -H, RD es -N(RF)C(=O)XCH(RG)-CY, donde X es -O-, RG es -CH3 y RF es -H, y RC es -H, -CH3 o -CF3, o cuando el anillo C es arileno sustituido o no sustituido o cicloalquileno C3-C10 sustituido o no sustituido y RC es -H o -CH3 y RA es -CO2H o -CO2RB,
entonces el anillo A tiene la estructura de uno de:
y cuando el anillo C es arileno sustituido o no sustituido, L1 es alquileno C1-C6, RC es -CH3 y RA es -CO2H o -CO2RB entonces el anillo A tiene la estructura de uno de:
El anillo A puede tener la estructura de uno de:
Los compuestos de Fórmula III pueden tener el anillo C que se define como fenilo o piridilo 1,4-sustituido, RA es -CO2H, y RD es -N(RF)C(=O)OCH(RG)-CY; L1 es -UV-Z- donde -UV- se define mediante -WO-, -WN(RJ)-, o -C(=O)N(RJ)-, donde W es -CH2-, Z es alquileno C1-C6 sustituido o no sustituido, RA es -CO2H, y RD es -N(RF)C(=O)OCH(RG)-CY.
Se divulga adicionalmente un compuesto de fórmula IV que tiene la estructura:
o una sal o profármaco farmacéuticamente aceptable de este,
donde RA es -CO2H, -CO2RB, -CN, tetrazolilo, -C(=O)NH2, -C(=O)NHRB, -C(=O)NHSO2RB o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico;
RB está opcionalmente sustituido -alquilo C1-C4 o tiene la estructura de uno de:
L1 es -UV-Z-, donde -UV- se define mediante -OW-, -WO-, -N(RJ)W-, -WN(RJ)-, -N(RJ)C(=O)-, -SW-, -S(=O)nW-, o -C(=O)N(RJ)-, donde W es alquileno C1-C3 sustituido o no sustituido o W es -C(RL)2-, Z es alquileno C1-C6 sustituido o no sustituido o fluoroalquileno C1-C6 sustituido o no sustituido o Z es -C(RL)2-; y n es 0, 1, o 2;
A1 es independientemente =N- o =CH-;
El anillo A es un heteroareno de 5 o 6 miembros que tiene una de las estructuras de:
donde RC es -H, -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, alquilo C1-C4, cicloalquilo C3-C6, o fluoroalquilo C1-C4;
RD es -N(RF)C(=O)XCH(RG)-CY, -N(RF)C(=O)XC(RG)2-CY, o -N(RF)C(=O)X-CY, donde X está ausente, es -O-, -NH-o -CH2-;
RE es -H o alquilo C1-C4, cicloalquilo C3-C6 o fluoroalquilo C1-C4;
RF es -H, alquilo C1-C4 o cicloalquilo C3-C6;
RG es RE seleccionado independientemente, o un RG es -alquilo C1-C4 y se toma junto con CY y el átomo de carbono al que RG y CY están unidos para definir un carbociclo sustituido o no sustituido o un heterociclo sustituido o no sustituido, y el otro RG, si está presente, es como se define por RE;
CY es alquilo C1-C6, a cicloalquilo C3-C10 sustituido o no sustituido, un heterocicloalquilo C2-C10 sustituido o no sustituido, un arilo sustituido o no sustituido, o un heteroarilo sustituido o no sustituido, donde si CY está sustituido, entonces CY está sustituido con 1,2, o 3 RH;
donde cada RH es independientemente -H, halógeno, -CN, -NO2, -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2RJ, -N(RJ)S(=O)2RJ, -S(=O)2N(RL)2, -C(=O)RJ, -OC(=O)RJ, -C(=O)ORJ, -OC(=O)ORJ, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2, N(RJ)C(=O)N(RL)2, -N(RJ)C(=O)RJ, -N(RJ)C(=O)ORJ, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4, o heteroalquilo C1-C4;
donde RJ es independientemente alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o C1-C4 alquileno-(heteroarilo sustituido o no sustituido); y
cada RL es independientemente -H, alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido),
o cuando RH es -S(=O)2N(RL)2, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2 o -N(RJ)C(=O)N(RL)2, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al átomo de N al que están unidos para definir un heterociclo sustituido o no sustituido,
o cuando W o Z es -C(RL)2-, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al átomo de carbono al que están unidos para definir un carbociclo,
o cuando RH es -S(=O)2N(RL)2, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2 o -N(RJ)C(=O)N(RL)2, cada RL es independientemente es -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al átomo de N al que están unidos para definir un heterociclo sustituido o no sustituido,
o cuando W es -C(RL)2-, cada RL es independientemente -H, alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al átomo de carbono al que están unidos para definir un carbociclo;
donde A1 es =CH-, L1 es -UV-Z, donde -UV- es -N(RJ)-C(=O)-, donde 0RJ es -H, RD es -N(RF)-C(=O)XCH(RG)-CY, donde X es -O-, RG es -CH3 y RF es -H, y RC es -H, -CH3 o -CF3,
y RC es -H o -CH3 y RA es -CO2H o CO2RB
entonces el anillo A tiene la estructura de uno de:
El anillo A puede tener la estructura de uno de:
Los compuestos de Fórmula IV pueden tener L1 que se define como -UV-Z-, donde -UV- se define mediante -WO-, -WN(RJ)-, o -C(=O)N(RJ)-, donde W es -CH2-, Z es alquileno C1-C6 sustituido o no sustituido, RA es -CO2H, y RD es -N(RF)C(=O)OCH(RG)-CY.
Se divulga adicionalmente un compuesto de fórmula V que tiene la estructura:
o una sal o profármaco farmacéuticamente aceptable de este,
donde RA es -CO2H, -CO2RB, -CN, tetrazolilo, -C(=O)NH2, -C(=O)NHRB, C(=O)NHSO2RB o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico,
donde RB es alquilo C1-C4 opcionalmente sustituido o tiene la estructura de uno de
L1 es -UV-Z-, donde -UV-se define mediante -OW-, -WO-, -N(RJ)W-, -WN(RJ)-, -N(RJ)C(=O)-, -SW-, -S(=O)nW-, o -C(=O)N(RJ)-, donde W es alquileno C1-C3 sustituido o no sustituido o W es -C(Rl)2-, Z es alquileno C1-C6 sustituido o no sustituido o fluoroalquileno C1-C6 sustituido o no sustituido o Z es -C(RL)2-; y n es 0, 1, o 2;
A1 es =N- o =CH-;
El anillo A es un heteroareno de 5 miembros que tiene la estructura de uno de:
donde Rc es -H, -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, alquilo C1-C4, cicloalquilo C3-C6, o fluoroalquilo C1-C4;
Rd es -N(Rf)C(=O)XCH(Rg)-CY, -N(Rf)C(=O)XC(Rg)2-CY, o -N(Rf)C(=O)X-CY; donde X está ausente, es -O-, -NH-o -CH2-;
Re es -H o alquilo C1-C4, cicloalquilo C3-C6 o fluoroalquilo C1-C4;
Rf es -H, alquilo C1-C4 o -cicloalquilo C3-C6;
Rg es Re seleccionado independientemente, o un Rg es -alquilo C1-C4 y se toma junto con CY y el átomo de carbono al que Rg y CY están unidos para definir un carbociclo sustituido o no sustituido o un heterociclo sustituido o no sustituido, y el otro Rg, si está presente, es como se define por Re;
CY es alquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C10 sustituido o no sustituido, heterocicloalquilo C2-C10 sustituido o no sustituido, arilo sustituido o no sustituido, o un heteroarilo sustituido o no sustituido, donde si CY está sustituido, entonces CY está sustituido con 1,2, o 3 Rh seleccionados independientemente;
Rh es independientemente -H, halógeno, -CN, -NO2, -OH, -ORj, -SRj, -S(=O)Rj, -S(=O)2Rj, -N(Rj)S(=O)2Rj, -S(=O)2N(RL)2, -C(=O)RJ, -OC(=O)RJ, -C(=O)ORJ, -OC(=O)ORJ, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2, NRjC(=O)N(Rl)2, -NrjC(=O)Rj, -NRjC(=O)ORj, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4, y heteroalquilo C1-C4;
donde cada Rj es independientemente alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o C1-C4 alquileno-(heteroarilo sustituido o no sustituido);
donde cada Rl es independientemente -H, alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido),
o cuando Rh es -S(=O)2N(Rl)2, -N(Rl)2, -C(=O)N(Rl)2, -OC(=O)N(Rl)2 o -N(Rj)C(=O)N(Rl)2, cada Rl es independientemente -H o alquilo C1-C6, o los grupos Rl son independientemente alquilo C1-C6 que se toman junto al el átomo de N al que están unidos para definir un heterociclo sustituido o no sustituido,
o cuando W o Z es -C(Rl)2-, cada Rl es independientemente -H o alquilo C1-C6, o los grupos Rl son independientemente alquilo C1-C6 que se toman junto al átomo de carbono al que están unidos para definir un carbociclo.
donde cuando A1 es =CH-, L1 es -UV-Z, donde -UV- es -NHC(=O)-, y Rc es -H, -CH3 o -CF3, entonces el anillo A tiene la estructura de uno de:
Los compuestos particularmente preferidos de Fórmula V tienen L1 que se define como UV-Z-, donde -UV- se define mediante -WO-, -Wn (Rj )-, o -C(=O)N(RJ)-, donde W es -CH2-, Z es alquileno C1-C6 sustituido o no sustituido, Ra es -CO2H, y Rd es -N(RF)C(=O)OCH(RG)-CY.
Se divulga adicionalmente un compuesto de fórmula VI que tiene la estructura:
o una sal o profármaco farmacéuticamente aceptable de este,
donde Ra es -CO2H, -CO2Rb, -CN, tetrazolilo, -C(=O)NH2, -C(=O)NHRB, -C(=O)NHSO2Rb o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico, donde
Rb es alquilo C1-C4 opcionalmente sustituido o tiene la estructura de uno de:
L1 es UV-Z- donde -UV- se define mediante -OW-, -WO-, -N(Rj)W-, -WN(Rj)-, -N(Rj)C(=O)-, -SW-, -S(=O)nW-, o -C(=O)N(RJ)-, donde W es alquileno C1-C3 sustituido o no sustituido o W es -C(Rl)2-, Z es alquileno C1-C6 sustituido o no sustituido o fluoroalquileno C1-C6 sustituido o no sustituido o Z es -C(Rl)2-; y n es 0, 1, o 2;
A1 es independientemente =N- o =CH-;
El anillo A es un heteroareno de 5 miembros que tiene una de las estructuras de:
donde RC que se define como -H, -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, alquilo C1-C4, cicloalquilo C3-C6, o fluoroalquilo C1-C4;
donde RD es el sustituyente -N(RF)C(=O)CH(RG)-CY de fórmula VI donde CY es fenilo sustituido con un RH;
RG es RE seleccionado independientemente, o un RG es -alquilo C1-C4 y se toma junto con CY y el átomo de carbono al que RG y CY están unidos para definir un carbociclo sustituido o no sustituido o un heterociclo sustituido o no sustituido, y el otro RG, si está presente, es como se define por RE;
RF es -H, -alquilo C1-C4 o -cicloalquilo C3-C6;
RH se selecciona independientemente de -H, halógeno, -CN, -NO2, -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2RJ, -N(RJ)S(=O)2RJ, -S(=O)2N(RL)2, -C(=O)RJ, OC(=O)RJ, -CO2RJ, -OC(=O)ORJ, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2, N(Rj)C(=O)N(Rl)2, -N(Rj)C(=O)Rj, -N(Rj)C(=O)ORj, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4, y heteroalquilo C1-C4;
donde RJ es alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, un heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o C1-C4 alquileno-(heteroarilo sustituido o no sustituido);
donde cada RL es independientemente -H, alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido),
o cuando RH es -S(=O)2N(RL)2, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2 o N(RJ)C(=O)N(RL)2, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al el átomo de N al que están unidos para definir un heterociclo sustituido o no sustituido,
o cuando W o Z es -C(RL)2-, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al átomo de carbono al que están unidos para definir un carbociclo.
El anillo A puede tener la estructura de uno de:
Los compuestos de Fórmula VI pueden tener L1 como -UV-Z- donde -UV- es -C(=O)NH-, -CH2O- o -CH2NH-, Z es -CH-sustituido, y RA es -CO2H.
Se divulga adicionalmente un compuesto de fórmula VII que tiene la estructura de:
donde RA es -CO2H, -CO2RB -CN, tetrazolilo, -C(=O)NH2, -C(=O)NHRB, -C(=O)NHSO2RB o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico;
RB es alquilo C1-C4 opcionalmente sustituido o tiene la estructura de uno de:
A1 es independientemente =N- o =CH-;
El anillo A tiene la estructura de uno de:
RC es -H, -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, alquilo C1-C4, cicloalquilo C3-C6, o fluoroalquilo C1-C4;
donde RD es el sustituyente -N(RF)C(=O)CH(RG)-CY de fórmula VII donde CY es fenilo sustituido con un RH;
RE, RF y RG son independientemente -H o alquilo C1-C4;
Z es -C(Rl)2-;
RH es independientemente -H, halógeno, -CN, -NO2, -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2RJ, -N(RJ)S(=O)2RJ, -S(=O)2N(RL)2, -C(=O)RJ, -OC(=O)RJ, -CO2RJ, -OCO2RJ, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2, NRJC(=O)N(RL)2, -NRJC(=O)RJ, -NRjC(=o )o Rj, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4, y heteroalquilo C1-C4;
RJ es alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido);
RL es -H, alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido.
fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido),
o cuando RH es -S(=O)2N(RL)2, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2 o -N(RJ)C(=O)N(RL)2, cada RL es independentemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto con el átomo de N al que están unidos para definir un heterociclo sustituido o no sustituido,
o cada RL en Z es independientemente -H o alquilo C1-C6, o los grupos RL independientemente son alquilo C1-C6 que se toman junto con el átomo de carbono al que están unidos para definir un carbociclo.
Los compuestos de Fórmula VII pueden tener RF definido como -H, alquilo C1-C4 o cicloalquilo C1-C6 y cada RH RJ y RL son como se han definido previamente;
En algunos compuestos de Fórmula VII RA es -CO2H.
Se divulga además un compuesto de Fórmula VIII que tiene la estructura:
o una sal o profármaco farmacéuticamente aceptable de este,
donde RA es -CO2H, -CO2RB, -CN, tetrazolilo, -C(=O)NH2, -C(=O)NHRB, -C(=O)NHSO2RB o -C(=O)NHCH2CH2SO3H o un isóstero de ácido carboxílico;
RB es alquilo C1-C4 opcionalmente sustituido o tiene la estructura de uno de:
A1 es =N- or =CH-;
El anillo A tiene la estructura de uno de:
RC -H, -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, alquilo C1-C4, cicloalquilo C3-C6, o fluoroalquilo C1-C4;
donde RD es el sustituyente -N(RF)C(=O)CH(RG)-CY de Fórmula VII donde CY es un fenilo sustituido con un RH; RF y RE son independientemente -H o alquilo C1-C4 o cicloalquilo C3-C6;
RG es -H o alquilo C1-C4 o es alquilo C1-C4 que se toma junto con la la porción fenilo con RH del sustituyente RD del anillo A y el átomo de carbono al que RG y dicha porción fenilo están unidos para definir un carbociclo;
W es -C(Rl)2-;
Z es -C(Rl)2-;
RH es -H, halógeno, -CN, -NO2, -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2RJ, - N(RJ)S(=O)2RJ, -S(=O)2N(RL)2, -C(=O)RJ, -OC(=O)RJ, -CO2Rj, -OCO2Rj, -N(Rl)2, - C(=O)N(Rl)2, -OC(=O)N(Rl)2, NRjC(=O)N(Rl)2, -NRjC(=O)Rj, -NRJC(=O)ORJ, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4 y heteroalquilo C1-C4;
RJ es alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido);
RL es independientemente -H, alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido),
o cuando RH es -S(=O)2N(RL)2, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2 o -N(RJ)C(=O)N(RL)2, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al el átomo de N al que están unidos para definir un heterociclo sustituido o no sustituido,
o cada RL es en W o Z independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-6 que se toman junto al átomo de carbono al que están unidos para definir un carbociclo.
En algunas realizaciones, compuestos de Fórmula VIII tienen RF que se define como -H, alquilo C1-C4 o cicloalquilo C3-C6.
En algunos compuestos de Fórmula VIII RA es -CO2H y RJ es -H.
Se divulga adicionalmente un compuesto de fórmula IX que tiene la estructura:
o una sal o profármaco farmacéuticamente aceptable de este,
donde RA es -CO2H, -CO2RB, -CN, tetrazolilo, -C(=O)NH2, -C(=O)NHRB, C(=O)NHSO2RB o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico;
RB es alquilo C1-C4 opcionalmente sustituido o tiene la estructura de uno de:
El anillo tiene la estructura de uno de:
RC -H, -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, alquilo C1-C4, cicloalquilo C3-C6, o fluoroalquilo C1-C4;
donde RD es el sustituyente -N(RF)C(=O)CH(RG)-CY en Fórmula IX donde CY es fenilo sustituido con un RH;
RE, RF y RG son independientemente -H, alquilo C1-C4 o cicloalquilo C1-C6 o RE y RF son independientemente -H, alquilo C1-C4 o cicloalquilo C1-C6 y RG es alquilo C1-C4 que se toma junto con el grupo funcional fenilo RH del anillo A sustituyente RD y el átomo de carbono al que RG y dicho grupo funcional fenilo está unido para definir un carbociclo; RH es independientemente -H, halógeno, -CN, -NO2, -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2RJ, -N(RJ)S(=O)2RJ, -S(=O)2N(RL)2, -C(=O)RJ, -OC(=O)RJ, -CO2RJ, -OCO2RJ,
-N(Rl)2, -C(=°)N(Rl)2, -OC(=°)N(Rl)2, NRjC(=°)N(Rl)2, -NRJC(=O)RJ, -NRJC(=O)ORJ, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4, y heteroalquilo C1-C4;
RJ es alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido,
arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, -alquileno Ci -C4-(cicloalquilo C3-C6 sustituido o no sustituido), -alquileno C1-C4-(heterocicloalquilo sustituido o no sustituido), -alquileno C1-C4-(arilo sustituido o no sustituido) o alquileno C1-C4-(heteroarilo sustituido o no sustituido);
W es -C(Rl)2-;
Z es -C(Rl)2-;
RL es independientemente -H, alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o C1-C4 alquileno-(heteroarilo sustituido o no sustituido),
cada RL es en W o Z independientemente alquilo C1-C6 que se toma junto al átomo de carbono al que están unidos para definir un carbociclo.
En algunos compuestos de Fórmula IX RA es -CO2H.
12. Un compuesto de fórmula X que tiene la estructura:
o una sal farmacéuticamente aceptable de este,
donde RA es -CO2H, -CO2RB -CN, tetrazolilo, -C(=O)NH2, -C(=O)NHRB, C(=O)NHSO2RB o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico como se define anteriormente;
RB es alquilo C1-C4 o tiene la estructura de uno de:
L1 está ausente o es alquileno C1-C6 opcionalmente sustituido; fluoroalquileno C1-C6; o heteroalquileno C1-C6
opcionalmente sustituido o L1, cuando está presente es -CH2- o dimetilmetano disustituido.
A1 es =N- o =CH-;
El anillo A tiene la estructura de uno de:
RC es -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, o fluoroalquilo C1-C4;
RD es -NRFC(=O)XCH(RG)-CY, -NRF)C(=O)XC(RG)2-CY, o -NRFC(=O)X-CY; donde X está ausente, es -O-, -NH- o -CH2-;
RE es -H, alquilo C1-C4 o fluoroalquilo C1-C4, RF es -H o alquilo C1-C4 y RG se selecciona independientemente de -H, alquilo C1-C4 o fluoroalquilo C1-C4 o un RG es alquilo C1-C4 y se toma junto con el CY y el átomo de carbono al que RG y CY están unidos para definir un carbociclo sustituido o no sustituido o un heterociclo sustituido o no sustituido, y el otro RG, si está presente, es como se define por RE;
RH es -H, halógeno, -CN, -NO2, -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2RJ, -N(RJ)S(=O)2RJ, -S(=O)2N(RL)2, -C(=O)RJ, -OC(=O)RJ, -CO2Rj, -OCO2Rj, -N(Rl)2, -C(=O)N(Rl)2, -OC(=O)N(Rl)2, NRjC(=O)N(Rl)2, -NRjC(=O)Rj, -NRJC(=O)ORJ, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4, y heteroalquilo C1-C4;
RJ es alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o C1-C4 alquileno-(heteroarilo sustituido o no sustituido);
RL es independientemente -H, alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido),
o cuando RH es -S(=O)2N(RL)2, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2 o -N(RJ)C(=O)N(RL)2, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independentemente alquilo C1-C6 que se toman junto com el átomo de N al que están unidos para definir un heterociclo sustituido o no sustituido;
CY es alquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C10 sustituido o no sustituido, heterocicloalquilo C2-C10 sustituido o no sustituido, arilo sustituido o no sustituido o heteroarilo sustituido o no sustituido, donde si CY está sustituido entonces CY está sustituido con 1,2 o 3 RH.
13. Un compuesto de Fórmula XI que tiene la estructura
o una sal farmacéuticamente aceptable de este,
donde RA es -CO2H, -CO2RB, -CN, tetrazolilo, -C(=O)NH2, -C(=O)NHRB, C(=O)NHSO2RB o -C(=O)NHCH2CH2SO3H o un isóstero de ácido carboxílico;
RB es alquilo C1-C4 o tiene la estructura de uno de:
L1 está ausente o es alquileno C1-C6 opcionalmente sustituido; fluoroalquileno C1-C6; o heteroalquileno C1-C6
opcionalmente sustituido o L1, cuando está presente es -CH2-, > o dimetilmetano disustituido.
A1 es =N- or =CH-;
El anillo A tiene la estructura de uno de:
RC es -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, alquilo C1-C4, cicloalquilo C3-C6, o fluoroalquilo C1-C4;
RD es -N(RF)C(=O)XCH(RG)-CY, -N(RF)C(=O)XC(RG)2-CY o -N(RF)C(=O)X-CY; donde X está ausente, es -O-, -NH- o -CH2-;
RE es -H, -alquilo C1-C4 o -fluoroalquilo C1-C4, RF es -H o -alquilo C1-C4 y RG es independientemente -H, alquilo C1-C4 o -fluoroalquilo C1-C4 un RG es alquilo C1-C4 y se toma junto con CY y el átomo de carbono al que RG y CY se unen para definir un carbociclo sustituido o no sustituido o un heterociclo sustituido o no sustituido, y el otro RG, si está presente, es como se ha definido para RE;
RH es -H, halógeno, -CN, -NO2, -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2RJ, -N(RJ)S(=O)2RJ, -S(=O)2N(RL)2, -C(=O)RJ, -OC(=O)RJ, -CO2RJ, -OCO2RJ, -N(RL)2, - C(=O)N(RL)2, -OC(=O)N(RL)2, NRJC(=O)N(RL)2, -NRJC(=O)RJ, -NRJC(=O)ORJ, alquilo C1-C4, fluoroalquilo C1-C4, fluoroalcoxi C1-C4, alcoxi C1-C4 y heteroalquilo C1-C4;
RJ es alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, -alquileno C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), -alquileno C1-C4-(heterocicloalquilo sustituido o no sustituido), -alquileno C1-C4-(arilo sustituido o no sustituido) o alquileno C1-C4-(heteroarilo sustituido o no sustituido);
RL son independientemente -H, alquilo C1-C6 sustituido o no sustituido, heteroalquilo C1-C6 sustituido o no sustituido, fluoroalquilo C1-C6 sustituido o no sustituido, cicloalquilo C3-C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, -alquileno C1-C4-(cicloalquilo C3-C6 sustituido o no sustituido), -alquileno C1-C4-(heterocicloalquilo sustituido o no sustituido), -alquileno C1-C4-(arilo sustituido o no sustituido) o alquileno C1-C4-(heteroarilo sustituido o no sustituido);
o cuando RH es -S(=O)2N(RL)2, -N(RL)2, -C(=O)N(RL)2, -OC(=O)N(RL)2 o -N(RJ)C(=O)N(RL)2, cada RL es independientemente -H o alquilo C1-C6, o los grupos RL son independientemente alquilo C1-C6 que se toman junto al el átomo de N al que están unidos para definir un heterociclo sustituido o no sustituido,
CY es alquilo C1-C6, a cicloalquilo C3-C10 sustituido o no sustituido, un heterocicloalquilo C2-C10 sustituido o no sustituido, un arilo sustituido o no sustituido, o un heteroarilo sustituido o no sustituido, donde si CY está sustituido, entonces CY está sustituido con 1, 2, o 3 RH.
En compuestos particularmente preferidos de Fórmula XI compuestos RA es -CO2H, y RD es
-NRFC(=O)OCH(RG)-CY.
14. Un compuesto de fórmula XII que tiene la estructura:
o una sal farmacéuticamente aceptable de este,
donde RA es -CO2H o -CO2RB, -;
El anillo A tiene la estructura de uno de:
RC es -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4 , alquilo C1 -C4 , o fluoroalquilo C1-C4 ;
donde RD es el sustituyente -N(RF)C(=O)CH(RG)-CY en Fórmula XII donde CY es fenilo sustituido con un RH;
RG es -H o -CH3 ; y
RH es independientemente -H, halógeno, -CH3 o CF3.
15. Una composición que comprende, consiste esencialmente de o consiste de uno o más compuestos de fórmula I o X-XII y uno o más excipientes.
En realizaciones preferidas la composición comprende, consiste esencialmente de, o consiste de un compuesto de fórmula I o X-XII y uno o más excipientes.
En otras realizaciones preferidas la composición es una formulación farmacéuticamente aceptable que comprende, consiste esencialmente de, o consiste de un compuesto de fórmula I o X-XII y uno o más excipientes farmacéuticamente aceptable.
16. Un compuesto de fórmula I o X-XII o una sal farmacéuticamente aceptable de este donde la afinidad de unión del compuesto al receptor-1 del ácido lisofosfatídico (LPA1R) es entre aproximadamente 10 qM y 1 pM o menos.
17. Un compuesto de fórmula I o X-XII o una sal farmacéuticamente aceptable del mismo donde el compuesto es un compuesto selectivo del receptor-1 del ácido lisofosfátidico (LPA1R).
18. El compuesto de la realización 12 donde el compuesto es un compuesto receptor-1 selectivo del ácido lisofosfátidico (LPA1R) donde la afinidad de unión (es decir, Kd) del compuesto LPA1 R es entre aproximadamente 1 qM y 1 pM o menos. En realizaciones preferidas la Kd es 100 nM o menos, más preferentemente 10 nM o menos.
A continuación se describirán compuestos específicos que no se incluyen necesariamente dentro del alcance de esta invención: Un compuesto de Tabla 1.
El compuesto donde el compuesto es ácido 1-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-ciclopropano-carboxílico, ácido 2-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-indan-2-carboxílico, ácido 2-(S)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxi-carbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)feniloacético, ácido 2-(R)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino) fenilopropanoico, ácido 2(R)-[[4-[3-metil-4-((R)-1 -feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico, ácido 2(S)-[[4-[3-metil-4-((R)-feniletoxicarbonil-amino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico, ácido (R)-2-{4-[3-metil-4-((S)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-benzoilamino}-3-fenil-propiónico, ácido (S)-2-{4-[3-metil-4-((S)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-benzoilamino}-3-fenil-propiónico, ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-fenil-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-fluoro-fenil)-propiónico, ácido (R)-3-(4-clorofenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(3,4-difluoro-fenil)-propiónico, ácido (R)-3-(2-cloro-fenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico, ácido (R)-3-(4-bromo-fenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(2-fluorofenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-ptolil-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-trifluorometil-fenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-ciano-fenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metilisoxazol-5-il}-benzoilamino)-3-ciclopropil-propiónico.
32. El compuesto de la realización 30 donde el compuesto es ácido (fi)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-fenil-propanoico, ácido (R)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]aminoÍ-3-(4-fluorofenil)propanoico, ácido (R)-3-(4-bromofenil)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-3-(4-clorofenil)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico o ácido (R)-3-(3,4-difluorofenil)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico.
El compuesto donde el compuesto es 2-[4-[4-[2,5-dimetil-4-(1-feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]acético, ácido 2-[4-[4-[4-[1 -(2-cloro-fenil)etoxicarbonilamino]-2,5-dimetil-pirazol-3-il]fenil]fenil]acético, ácido 2-[4-[4-[4-[1 -(2-fluorofenil)etoxicarbonilamino]-2,5-dimetil-pirazol-3-il]fenil]-fenil]acético, ácido 2-[4-[4-[4-[1-(2,6
difluorofenil)etoxicarbonilamino]-2,5-dimetil-pirazol-3-il]-fenil]fenil]acético, ácido 2-[4-[4-[4-[1-(2-metoxifenil)etoxicarbonil-amino]-2,5-di-metil-pirazol-3-il]fenil]fenil]acético, ácido 1 -[4-[4-[2,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]ciclopropanocarboxílico, ácido 1 -[4-[6-[2,5-di-metil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]-3-piridil]fenil]ciclo-propanocarboxílico, ácido 1-[4-[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-2,5-dimetil-pirazol-3-il]fenil]fenil]ciclopropanocarboxílico, ácido 1-[4-[4-[4-[1-(2-fluorofenil)-etoxicarbonil-amino]-2,5-dimetil-pirazol-3-il]fenil]fenil]ciclopropanocarboxílico, ácido 1-[4-[4-[4-[1-(2,6-difluorofenil)etoxicarbonilamino]-2,5-dimetil-pirazol-3-il]fenil]fenil]ciclo-propanocarboxílico ácido 1 -[4-[4-[4-[1 -(2-metoxifenil)etoxi-carbonilamino]-2,5-dimetil-pirazol-3-il]fenil]fenil]ciclopropanocarboxílico, ácido 2-[4-[4-[2,5-dimetil-4-(1-fenil-etoxicarbonilamino)pirazol-3-il]fenil]fenil]-2-metil-propanoico, ácido 2-[4-[4-[4-[1 -(2-clorofenil)etoxicarbonilamino]-2,5-dimetil-pirazol-3-il]fenil]fenil]-2-metil-propanoico, ácido 2-[4-[4-[4-[1 -(2-fluorofenil)etoxicarbonil-amino]-2,5-dimetil-pirazol-3-il]fenil]fenil]-2-metil-propanoico, ácido 2-[4-[4-[4-[1 -(2,6-difluorofenil)etoxicarbonil-amino]-2,5-dimetil-pirazol-3-il]fenil]fenil]-2-metil-propanoico o ácido 2-[4-[4-[4-[1 -(2-metoxifenil)etoxicarbonilamino]-2,5-dimetil-pirazol-3-il]fenil]-fenil]-2-metil-propanoico.
El compuesto donde el compuesto es ácido (R)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-fenil-propanoico, ácido (R)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-fluorofenil)propanoico, ácido (R)-3-(4-bromofenil)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]propanoico, ácido ((R)-3-(4-clorofenil)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]propanoico o ácido (R)-3-(3,4-difluorofenil)-2-[[4-[1,5-dimetil-4-((R)-1 -feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico.
El compuesto donde el compuesto es ácido (R)-2-(4-{5-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-4-metil-pirazol-1-il}-benzoilamino)-3-fenil-propiónico.
El compuesto donde el compuesto es ácido (R)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-3-fenil-propiónico, ácido (R)-3-(2-fluoro-fenil)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-3-(4-trifluorometil-fenil)-propiónico, ácido (R)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-3-(2-cloro-fenil)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-3-(4-cloro-fenil)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-fenil-propiónico, ácido (R)-2-(4-{4-[(R)_1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-(2-fluoro-fenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-(4-trifluorometil-fenil)-propiónico, ácido (R)-3-(2-cloro-fenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-propiónico o ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-ciclopropil-propiónico.
El compuesto donde el compuesto es ácido 2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-3-fenil-propiónico, ácido 2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-3-fenil-propiónico, ácido (RS)-3-ciclopropil-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-propiónico o ácido (RS)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-propiónico.
El compuesto donde el compuesto es ácido 2-[4-[4-[5-[1-(2-clorofenil)etoxicarbonilamino]-4-ciano-pirazol-1-il]fenil]fenil]acético, ácido (R)-1 -[4-[4-[1,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]ciclo-propano carboxílico, ácido (R)-1 -[4-[4-[2,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]ciclopropano carboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonil-amino]-4-fluoro-pirazol-1 -il}-3-fluoro-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-2-fluoro-bifenil-4-il)-ciclo-propanocarboxílico, ácido (R)-1 -(2-cloro-4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1-(4'-{5-[1-(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1-il}-2-metil-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -{4'-[5-(1 -fenil-etoxicarbonilamino)-4-trifluorometil-pirazol-1 -il]-bifenil-4-il}-ciclopropanocarboxílico, ácido (R)-1 -{2-fluoro-4'-[5-(1 -fenil-etoxicarbonilamino)-4-trifluorometil-pirazol-1 -il]-bifenil-4-il}-ciclopropanocarboxílico o ácido (R)-1 -(4-{5-[5-(1 -fenil-etoxicarbonilamino)-pirazol-1 -il]-piridin-2-il}-fenil)-ciclopropanocarboxílico.
El compuesto donde el compuesto es ácido 2-[[4-[3-metil-4-(1-feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico, ácido 3-ciclopropil-2-[[4-[3-metil-4-(1-feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-propanoico, ácido 2-[[4-[3-metil-4-(1 -feniletoxicarbonilamino)isoxazol-5-il]benzoil]-amino]-3-fenoxi-propanoico, ácido 2-[[4-[3-metil-4-(1 -feniletoxicarbonilamino)-isoxazol-5-il]benzoil]amino]-4-fenil-butanoico, ácido 2-[[4-[4-[1 -(2-clorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-fenil-propanoico, ácido 2-[[4-[4-[1 -(2-clorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-ciclopropil-propanoico, ácido 2-[[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]-benzoil]amino]-4-fenil-butanoico, ácido 2-[[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-fenoxi-propanoico, ácido 2-[[4-[4-[1 -(2-fluorofenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-4-fenil-butanoico, ácido 2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-fenoxi-propanoico, ácido 3-ciclopropil-2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]propanoico, ácido 2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-fenil-propanoico, ácido 3-(4-metoxifenil)-2-[[4-[3-metil-4-(1feniletoxicarbonilamino)isoxazol-5-il]benzoil]-amino]propanoico, ácido 3-(4-fluorofenil)-2-[[4-[3-metil-4-(1-feniletoxicarbonilamino)-isoxazol-5-il]benzoil]amino]propanoico, ácido 3-(2,6-difluorofenil)-2-[[4-[3-metil-4-(1-feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]propanoico, ácido 3-(3-ciano-fenil)-2-[[4-[3-metil-4-(1-feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-propanoico, ácido 3-(2-clorofenil)-2-[[4-[3-metil-4-(1-feniletoxicarbonilamino)-isoxazol-5-il]benzoil]amino]propanoico, ácido 3-(4-clorofenil)-2-[[4-[3-metil-4-(1-feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]propanoico, ácido 2-[[4-[3-metil-4-(1 -feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-[4-(trifluorometil)fenil]-propanoico, ácido 3-(4-hidroxifenil)-2-[[4-[3-metil-4-(1-feniletoxicarbonilamino)-isoxazol-5-il]benzoil]amino]propanoico, ácido 3-(3,4-difluorofenil)-2-[[4-[3-metil-4-(1 -feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]propanoico, ácido 3-(4-bromo-fenil)-2-[[4-[3-metil-4-(1 -feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-propanoico, ácido 2-[[4-[3-metil-4-(1 -feniletoxicarbonilamino)isoxazol-5-il]benzoil]-amino]-3-[4-(trifluorometoxi)fenil]propanoico, ácido 2-[[4-[4-[1-(2-clorofenil)etoxi-carbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-(4-metoxifenil)propanoico, ácido 2-[[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-(4-fluorofenil)propanoico, ácido 2-[[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-(2,6-difluorofenil)propanoico, ácido 2-[[4-[4-[1-(2-cloro-fenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-(3-cianofenil)-propanoico, ácido 3-(2-clorofenil)-2-[[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]propanoico, ácido 3-(4-clorofenil)-2-[[4-[4-[1 -(2-clorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]propanoico, ácido 2-[[4-[4-[1 -(2-clorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-[4-(trifluorometil)fenil]propanoico, ácido 2-[[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-(4-hidroxifenil)propanoico, ácido 3-(4-bromo-fenil)-2-[[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]-amino]propanoico, ácido 2-[[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-(3,4-difluorofenil)propanoico, ácido 2-[[4-[4-[1-(2-clorofenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-[4-(trifluorometoxi)-fenil]propanoico, ácido 2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-(4-metoxifenil)propanoico, ácido 3-(4-fluorofenil)-2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]propanoico, ácido 3-(2,6-difluorofenil)-2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]propanoico, ácido 3-(3-cianofenil)-2-[[4-[4-[1-(2-fluorofenil)etoxi-carbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]propanoico, ácido 3-(2-clorofenil)-2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-propanoico, ácido 3-(4-clorofenil)-2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]propanoico, ácido 2-[[4-[4-[1-(2-fluorofenil)etoxi-carbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-[4-(trifluorometil)fenil]-propanoico, ácido 2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-(4-hidroxifenil)propanoico, ácido 3-(3,4-difluorofenil)-2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]propanoico, ácido 3-(4-bromofenil)-2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]propanoico, ácido 2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-3-metil-isoxazol-5-il]benzoil]amino]-3-[4-(trifluorometoxi)fenil]propanoico, ácido (±)-(4-{4-[1-(2-cloro-fenil)-etoxicarbonil-amino]-3-metil-isoxazol-5-il}-benzoilamino)-acético, ácido (±)-2-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-2-metil-propiónico, ácido (±)-2-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico, ácido (±)-2-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-hidroxi-propiónico, ácido (±)-1 -(4-{4-[1 -(2-cloro-fenil)etoxicarbonil-amino]-3-metil-isoxazol-5-il}-benzoil)-pirrolidina-2-carboxílico o ácido (±)-2-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico.
El compuesto donde el compuesto es ácido 2-{p-[3-fluoro-4-(1-feniletoxicarbonilamino)-5-isoxazolil]benzoilamino}-3-fenilpropiónico, ácido 2-(p-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}benzoilamino)-3-fenil-propiónico, ácido 3-ciclopropil-2-{p-[3-fluoro-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-benzoilamino}propiónico, ácido 2-(p-{4-[1 -(o-clorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}benzoilamino)-3-ciclopropilpropiónico, ácido 2-[({p-[3-fluoro-4-(1 -feniletoxi-carbonilamino)-5-isoxazolil]fenil}metil)amino]-3-fenilpropiónico, ácido 2-{[(p-{4-[1 -(oclorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}fenil)metil]amino}-3-fenilpropiónico, ácido 3-ciclopropil-2-[({p-[3-fluoro-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]fenil}metil)amino]propiónico, ácido 2-{[(p-{4-[1 -(oclorofenil)etoxicarbonil-amino]-3-fluoro-5-isoxazolil}fenil)metil]amino}-3-ciclopropilpropiónico, ácido 2-({p-[3-fluoro-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]fenil}metoxi)-3-fenilpropiónico, ácido 2-[(p-{4-[1 -(oclorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}fenil)-metoxi]-3-fenilpropiónico, ácido 3-ciclopropil-2-({p-[3-fluoro-4-(1 -feniletoxicarbonil-amino)-5-isoxazolil]fenil}metoxi)propiónico o ácido 2-[(p-{4-[1 -(o-clorofenil)etoxi-carbonilamino]-3-fluoro-5-isoxazolil}fenil)metoxi]-3-ciclopropilpropiónico.
El compuesto donde el compuesto es ácido 2-bencil-3-{5-[3-fluoro-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}propiónico, ácido 2-bencil-3-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}-2-piridilamino)propiónico, ácido 2-(ciclopropilmetil)-3-{5-[3-fluoro-4-(1-feniletoxicarbonil-amino)-5-isoxazolil]-2-piridilamino}propiónico, ácido 3-(5-{4-[1-(o-clorofenil)etoxi-carbonilamino]-3-fluoro-5-isoxazolil}-2-piridilamino)-2-(ciclopropilmetil)propiónico, ácido 2-bencil-3-{5-[3-fluoro-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}-propiónico, ácido 2-bencil-3-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}-2-piridiloxi)propiónico, ácido 2-bencil-3-(5-{4-[1 -(o-clorofenil)etoxicarbonil-amino]-3-fluoro-5-isoxazolil}-2-piridiloxi)propiónico, ácido 2-(ciclopropilmetil)-3-{5-[3-fluoro-4-(1-feniletoxicarbonil-amino)-5-isoxazolil]-2-piridiloxi}propiónico, ácido 3-(5-{4-[1-(oclorofenil)etoxi-carbonilamino]-3-fluoro-5-isoxazolil}-2-piridiloxi)-2-(ciclo-propilmetil)propiónico, ácido 2-{5-[3-fluoro-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}-3-fenil-propiónico, ácido 2-(5-{4-[1 -(oclorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}-2-piridilamino)-3-fenilpropiónico, ácido 3-ciclopropil-2-{5-[3-fluoro-4-(1 -feniletoxi-carbonilamino)-5-isoxazolil]-2-piridilamino}propiónico, ácido 2-(5-{4-[1 -(o-clorofenil)-etoxicarbonilamino]-3-fluoro-5-isoxazolil}-2-piridilamino)-3-ciclopropil-propiónico, ácido 2-{5-[3-fluoro-4-(1feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}-3-fenil-propiónico, ácido 2-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-fluoro-5-iso-xazolil}-2-piridiloxi)-3-fenilpropiónico, ácido 3-ciclopropil-2-{5-[3-fluoro-4-(1-fenil-etoxi-carbonilamino)-5-isoxazolil]-2-piridiloxi}propiónico, ácido 2-(5-{4-[1-(o-cloro-fenil)-etoxicarbonilamino]-3-fluoro-5-isoxazolil}-2-piridiloxi)-3-ciclopropilpropiónico, ácido 2-{p-[3-fluoro-4-(1-feniletoxicarbonilamino)-5-isoxazolil]benzoilamino}-3-fenilpropiónico, ácido 2-(p-{4-[1 -(o-clorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}benzoil-amino)-3-fenilpropiónico, ácido 3-ciclopropil-2-{p-[3-fluoro-4-(1 -feniletoxicarbonil-amino)-5-isoxazolil]benzoilamino}propiónico, ácido 2-(p-{4-[1 -(oclorofenil)etoxi-carbonilamino]-3-fluoro-5-isoxazolil}benzoilamino)-3-ciclopropilpropiónico, ácido 2-[({p-[3-fluoro-4-(1-feniletoxicarbonilamino)-5-isoxazolil]fenil}metil)amino]-3-fenil-propiónico, ácido 2-{[(p-{4-[1-(oclorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}-fenil)metil]amino}-3-fenilpropiónico, ácido 3-ciclopropil-2-[({p-[3-fluoro-4-(1 -fenil-etoxicarbonilamino)-5-isoxazolil]fenil}metil)amino]propiónico, ácido 2-{[(p-{4-[1 -(oclorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}fenil)metil]amino}-3-ciclo-propilpropiónico, ácido 2-({p-[3-fluoro-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-fenil}metoxi)-3-fenilpropiónico, ácido 2-[(p-{4-[1 -(o-clorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}fenil)metoxi]-3-fenilpropiónico, ácido 3-ciclopropil-2-({p-[3-fluoro-4-(1-feniletoxicarbonilamino)-5-isoxazolil]fenil}metoxi)propiónico, ácido 2-[(p-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}fenil)metoxi]-3-ciclopropilpropiónico, ácido 2-bencil-3-{5-[3-fluoro-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}propiónico, ácido 2-bencil-3-(5-{4-[1-(o-clorofenil)etoxi-carbonilamino]-3-fluoro-5-isoxazolil}-2-piridilamino)propiónico, ácido 2-(ciclopropil-metil)-3-{5-[3-fluoro-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}-propiónico, ácido 3-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}-2-piridil-amino)-2-(ciclopropilmetil)propiónico, ácido 2-bencil-3-{5-[3-fluoro-4-(1-feniletoxi-carbonilamino)-5-isoxazolil]-2-piridiloxi}propiónico, ácido 2-bencil-3-(5-{4-[1-(o-cloro-fenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}-2-piridiloxi)propiónico, ácido 2-(ciclo-propilmetil)-3-{5-[3-fluoro-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}-propiónico, ácido 3-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}-2-piridiloxi)-2-(ciclopropilmetil)propiónico, ácido 2-{5-[3-fluoro-4-(1-feniletoxicarbonil-amino)-5-isoxazolil]-2-piridilamino}-3-fenilpropiónico, ácido 2-(5-{4-[1-(o-clorofenil)-etoxicarbonilamino]-3-fluoro-5-isoxazolil}-2-piridilamino)-3-fenilpropiónico, ácido 3-ciclopropil-2-{5-[3-fluoro-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}-propiónico, ácido 2-(5-{4-[1 -(o-clorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}-2-piridilamino)-3-ciclopropilpropiónico, ácido 2-{5-[3-fluoro-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}-3-fenilpropiónico, ácido 2-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}-2-piridiloxi)-3-fenil-propiónico, ácido 3-ciclopropil-2-{5-[3-fluoro-4-(1-feniletoxicarbonilamino)-5-iso-xazolil]-2-piridiloxi}propiónico o ácido 2-(5-{4-[1 -(o-clorofenil)etoxicarbonilamino]-3-fluoro-5-isoxazolil}-2-piridiloxi)-3-ciclopropilpropiónico.
El compuesto donde el compuesto es ácido 2-{p-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]benzoilamino}-3-fenilpropiónico, ácido 2-(p-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}benzoilamino)-3-fenil-propiónico, ácido 2-{p-[3-ciano-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]benzoil-amino}-3-ciclopropilpropiónico, ácido 2-(p-{4-[1 -(o-clorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}benzoilamino)-3-ciclopropilpropiónico, ácido 2-[({p-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]fenil}metil)amino]-3-fenilpropiónico, ácido 2-{[(p-{4-[1-(oclorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}fenil)metil]-amino}-3-fenilpropiónico, ácido 2-[({p-[3-ciano-4-(1-feniletoxicarbonilamino)-5-iso-xazolil]fenil}metil)amino]-3-ciclopropilpropiónico, ácido 2-{[(p-{4-[1-(o-clorofenil)-etoxicarbonilamino]-3-ciano-5-isoxazolil}fenil)metil]amino}-3-ciclopropilpropiónico, ácido 2-({p-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]fenil}metoxi)-3-fenilpropiónico, ácido 2-[(p-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-ciano-5-iso-xazolil}fenil)metoxi]-3-fenilpropiónico, ácido 2-({p-[3-ciano-4-(1-feniletoxicarbonil-amino)-5-isoxazolil]fenil}metoxi)-3-ciclopropilpropiónico o ácido 2-[(p-{4-[1 -(o-cloro-fenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}fenil)metoxi]-3-ciclopropilpropiónico.
Un compuesto donde el compuesto es ácido 2-bencil-3-{5-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}propiónico, ácido 2-bencil-3-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}-2-piridilamino)-propiónico, ácido 3-{5-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridil-amino}-2-(ciclopropilmetil)propiónico, ácido 3-(5-{4-[1-(o-clorofenil)etoxicarbonil-amino]-3-ciano-5-isoxazolil}-2-piridilamino)-2-(ciclopropilmetil)propiónico, ácido 2-bencil-3-{5-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}propiónico, ácido 2-bencil-3-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}-2-piridiloxi)propiónico, ácido 3-{5-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}-2-(ciclopropilmetil)propiónico, ácido 3-(5-{4-[1-(o-clorofenil)etoxicarbonil-amino]-3-ciano-5-isoxazolil}-2-piridiloxi)-2-(ciclopropilmetil)propiónico, ácido 2-{5-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}-3-fenilpropiónico, ácido 2-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}-2-piridil-amino)-3-fenilpropiónico, ácido 2-{5-[3-ciano-4-(1-feniletoxicarbonilamino)-5-iso-xazolil]-2-piridilamino}-3-ciclopropilpropiónico, ácido 2-(5-{4-[1 -(o-clorofenil)etoxi-carbonilamino]-3-ciano-5-isoxazolil}-2-piridilamino)-3-ciclopropilpropiónico, ácido 2-{5-[3-ciano-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}-3-fenilpropiónico, ácido 2-(5-{4-[1 -(oclorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}-2-piridiloxi)-3-fenilpropiónico, ácido 2-{5-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}-3-ciclopropilpropiónico, ácido 2-(5-{4-[1-(oclorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}-2-piridiloxi)-3-ciclopropilpropiónico, ácido 2-{p-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]benzoilamino}-3-fenilpropiónico, ácido 2-(p-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}benzoilamino)-3-fenilpropiónico, ácido 2-{p-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]benzoilamino}-3-ciclo-propilpropiónico, ácido 2-(p-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}benzoilamino)-3-ciclopropilpropiónico, ácido 2-[({p-[3-ciano-4-(1-feniletoxi-carbonilamino)-5-isoxazolil]fenil}metil)amino]-3-fenilpropiónico, ácido 2-{[(p-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}fenil)metil]amino}-3-fenil-propiónico, ácido 2-[({p-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]fenil}metil)amino]-3-ciclopropilpropiónico, ácido 2-{[(p-{4-[1-(o-clorofenil)etoxicarbonil-amino]-3-ciano-5-isoxazolil}fenil)metil]amino}-3-ciclopropilpropiónico, ácido 2-({p-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]fenil}metoxi)-3-fenilpropiónico, ácido 2-[(p-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}fenil)-metoxi]-3-fenilpropiónico, ácido 2-({p-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]fenil}metoxi)-3-ciclopropilpropiónico, ácido 2-[(p-{4-[1-(o-clorofenil)etoxi-carbonilamino]-3-ciano-5-isoxazolil}fenil)metoxi]-3-ciclopropilpropiónico, ácido 2-bencil-3-{5-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}-propiónico, ácido 2-bencil-3-(5-{4-[1 -(o-clorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}-2-piridilamino)propiónico, ácido 3-{5-[3-ciano-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}-2-(ciclopropilmetil)propiónico, ácido 3-(5-{4-[1 -(ocloro-fenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}-2-piridilamino)-2-(ciclopropilmetil)-propiónico, ácido 2-bencil-3-{5-[3-ciano-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}propiónico, ácido 2-bencil-3-(5-{4-[1 -(oclorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}-2-piridiloxi)propiónico, ácido 3-{5-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}-2-(ciclopropilmetil)propiónico, ácido 3-(5-{4-[1-(o-cloro-fenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}-2-piridiloxi)-2-(ciclopropilmetil)-propiónico, ácido 2-{5-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridil-amino}-3-fenilpropiónico, ácido 2-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}-2-piridilamino)-3-fenilpropiónico, ácido 2-{5-[3-ciano-4-(1-feniletoxi-carbonilamino)-5-isoxazolil]-2-piridilamino}-3-ciclopropilpropiónico, ácido 2-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-ciano-5-isoxazolil}-2-piridilamino)-3-ciclopropil-propiónico, ácido 2-{5-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}-3-fenilpropiónico, ácido 2-(5-{4-[1 -(o-clorofenil)etoxicarbonilamino]-3-ciano-5-iso-xazolil}-2-piridiloxi)-3-fenilpropiónico, ácido 2-{5-[3-ciano-4-(1 -feniletoxicarbonil-amino)-5-isoxazolil]-2-piridiloxi}-3-ciclopropilpropiónico o ácido 2-(5-{4-[1 -(o-clorofenil)-etoxicarbonilamino]-3-ciano-5-isoxazolil}-2-piridiloxi)-3-ciclopropilpropiónico.
Un compuesto donde el compuesto es ácido 2-bencil-3-{5-[3-metil-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}propiónico, ácido 2-bencil-3-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridilamino)-propiónico, ácido 2-(ciclopropilmetil)-3-{5-[3-metil-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}propiónico, ácido 3-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridilamino)-2-(ciclopropilmetil)propiónico, ácido 2-bencil-3-{5-[3-metil-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}propiónico, ácido 2-bencil-3-(5-{4-[1 -(o-clorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridil-oxi)propiónico, ácido 2-(ciclopropilmetil)-3-{5-[3-metil-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}propiónico, ácido 3-(5-{4-[1 -(o-clorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridiloxi)-2-(ciclopropilmetil)propiónico, ácido 2-{5-[3-metil-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}-3-fenilpropiónico, ácido 2-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridilamino)-3-fenilpropiónico, ácido 2-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridilamino)-3-ciclopropilpropiónico, ácido 2-{5-[3-metil-4-(1-feniletoxi-carbonilamino)-5-isoxazolil]-2-piridiloxi}-3-fenilpropiónico, ácido 2-(5-{4-[1 -(o-cloro-fenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridiloxi)-3-fenilpropiónico, ácido 3-ciclopropil-2-{5-[3-metil-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridil-oxi}propiónico, ácido 2-(5-{4-[1 -(oclorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridiloxi)-3-ciclopropilpropiónico, ácido 2-bencil-3-{5-[3-metil-4-(1-fenil-etoxicarbonilamino)-5-isoxazolil]-2-piridilamino}propiónico, ácido 2-bencil-3-(5-{4-[1-(oclorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridilamino)propiónico, ácido 2-(ciclopropilmetil)-3-{5-[3-metil-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}propiónico, ácido 3-(5-{4-[1 -(o-clorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridilamino)-2-(ciclopropilmetil)propiónico, ácido 2-bencil-3-{5-[3-metil-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}propiónico, ácido 2-bencil-3-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridiloxi)propiónico, ácido 2-(ciclopropilmetil)-3-{5-[3-metil-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}propiónico, ácido 3-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridiloxi)-2-(ciclopropilmetil)propiónico, ácido 2-{5-[3-metil-4-(1-fenil-etoxicarbonilamino)-5-isoxazolil]-2-piridilamino}-3-fenilpropiónico, ácido 2-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridilamino)-3-fenil-propiónico, ácido 3-ciclopropil-2-{5-[3-metil-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}propiónico, ácido 2-(5-{4-[1 -(o-clorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridilamino)-3-ciclopropilpropiónico, ácido 2-{5-[3-metil-4-(1-feniletoxi-carbonilamino)-5-isoxazolil]-2-piridiloxi}-3-fenilpropiónico, ácido 2-(5-{4-[1-(o-cloro-fenil)etoxicarbonilamino]-3- metil-5-isoxazolil}-2-piridiloxi)-3-fenilpropiónico, ácido 3-ciclopropil-2-{5-[3-metil-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}-propiónico, ácido 2-(5-{4-[1-(o-clorofenil)etoxicarbonilamino]-3-metil-5-isoxazolil}-2-piridiloxi)-3-ciclopropilpropiónico, ácido 3-{p-[3-metil-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]benzoilamino}-4-fenilbutírico, ácido 4- ciclopropil-3-{p-[3-metil-4-(1 -fenil-etoxicarbonilamino)-5-isoxazolil]benzoilamino}butírico, ácido 3-[({p-[3-metil-4-(1 -fenil-etoxicarbonilamino)-5-isoxazolil]fenil}metil)amino]-4-fenilbutírico, ácido 4-ciclo-propil-3-[({p-[3-metil-4-(1-feniletoxicarbonilamino)-5-isoxazolil]fenil}metil)-amino]butírico, ácido 3-({p-[3-metil-4-(1-feniletoxicarbonilamino)-5-isoxazolil]fenil}-metoxi)-4-fenilbutírico, ácido 4-ciclopropil-3-({p-[3-metil-4-(1-feniletoxicarbonil-amino)-5-isoxazolil]fenil}metoxi)butírico, ácido 3-{5-[3-metil-4-(1-feniletoxicarbonil-amino)-5-isoxazolil]-2-piridilamino}-4-fenilbutírico, ácido 4-ciclopropil-3-{5-[3-metil-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridilamino}butírico, ácido 3-{5-[3-metil-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}-4-fenilbutírico, ácido 4-ciclo-propil-3-{5-[3-metil-4-(1-feniletoxicarbonilamino)-5-isoxazolil]-2-piridiloxi}butírico.
45. Un compuesto de la realización 30 donde el compuesto es ácido 2-[[4-[1,5-dimetil-4-(1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-metoxifenil)propanoico, ácido 2-[[4-[1,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-fluorofenil)propanoico, ácido 3-(2,6-difluorofenil)-2-[[4-[1,5-dimetil-4-(1 -feniletoxi-carbonilamino)pirazol-3-il]benzoil]amino]propanoico, ácido 3-(3-cianofenil)-2-[[4-[1,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]propanoico, ácido 3-(2-clorofenil)-2-[[4-[1,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]-amino]propanoico, ácido 3-(4-clorofenil)-2-[[4-[1,5-dimetil-4-(1 -feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido 2-[[4-[1,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-[4-(trifluorometil)fenil]propanoico, ácido 2-[[4-[1,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-hidroxifenil)propanoico, ácido 3-(3,4-difluorofenil)-2-[[4-[1,5-dimetil-4-(1 -feniletoxi-carbonilamino)pirazol-3-il]benzoil]amino]propanoico, ácido 3-(4-bromofenil)-2-[[4-[1,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]propanoico, ácido 2-[[4-[1,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-[4-(trifluoro-metoxi)fenil]propanoico, ácido 2-[[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]-3-(4-metoxifenil)propanoico, ácido 2-[[4-[4-[1 -(2-clorofenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]-3-(4-fluoro-fenil)propanoico, ácido 2-[[4-[4-[1 -(2-clorofenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]-3-(2,6-difluorofenil)propanoico, ácido 2-[[4-[4-[1 -(2-cloro-fenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]-3-(3-cianofenil)-propanoico, ácido 3-(2-clorofenil)-2-[[4-[4-[1 -(2-clorofenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]propanoico, ácido 3-(4-clorofenil)-2-[[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]propanoico, ácido 2-[[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]-amino]-3-[4-(trifluorometil)fenil]propanoico, ácido 2-[[4-[4-[1 -(2-clorofenil)etoxi-carbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]-3-(4-hidroxifenil)propanoico, ácido 2-[[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]-amino]-3-(3,4-difluorofenil)propanoico, ácido 3-(4-bromofenil)-2-[[4-[4-[1-(2-cloro-fenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]propanoico, ácido 2- [[4-[4-[1-(2-clorofenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]-3-[4-(trifluorometoxi)fenil]propanoico, ácido 2-[[4-[4-[1-(2-fluorofenil)etoxicarbonil-amino]-1,5-dimetil-pirazol-3-il]benzoil]amino]-3-(4-metoxifenil)propanoico, ácido 3-(4-fluorofenil)-2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]propanoico, ácido 3-(2,6-difluorofenil)-2-[[4-[4-[1-(2-fluorofenil)etoxi-carbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]propanoico, ácido 3-(3-cianofenil)-2-[[4-[4-[1 -(2-fluorofenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]-propanoico, ácido 3-(2-clorofenil)-2-[[4-[4-[1 -(2-fluorofenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]propanoico, ácido 3-(4-clorofenil)-2-[[4-[4-[1 -(2-fluorofenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]propanoico, ácido 2-[[4-[4-[1 -(2-fluorofenil)etoxicarbonilamino]-1,5-dimetil-pirazol-3-il]benzoil]amino]-3-[4-(trifluorometil)fenil]propanoico, ácido 2-[[4-[4-[1 -(2-fluorofenil)etoxicarbonil-amino]-1,5-dimetil-pirazol-3-il]benzoil]amino]-3-(4-hidroxifenil)propanoico, ácido 3-(3,4-difluorofenil)-2-[[4-[4-[1-(2-fluorofenil)etoxicarbonilamino]-1.5- dimetil-pirazol-3-il]benzoil]amino]propanoico, ácido 3-(4-bromofenil)-2-[[4-[4-[1 -(2-fluorofenil)etoxi-carbonilamino]-1.5- dimetil-pirazol-3-il]benzoil]amino]propanoico, ácido 2-[[4-[4-[1 -(2-fluorofenil)etoxicarbonilamino]-1,5-dimetilpirazol-3-il]benzoil]amino]-3-[4-(trifluorometoxi)fenil]propanoico, ácido 2-{p-[1 -metil-5-metil-4-(1 -feniletoxicarbonilamino)-1 H-pirazol-3-il]benzoilamino}-3-fenilpropiónico, ácido 3-ciclopropil-2-{p-[1 -metil-5-metil-4-(1 -feniletoxicarbonilamino)-1 H-pirazol-3-il]benzoilamino}-propiónico, ácido 2-(p-{4-[1 -(o-clorofenil)etoxicarbonilamino]-1 -metil-5-metil-1 H-pirazol-3-il}benzoilamino)-3-fenilpropiónico, ácido 2-(p-{4-[1 -(o-clorofenil)etoxi-carbonilamino]-1 -metil-5-metil-1 H-pirazol-3-il}benzoilamino)-3-ciclopropilpropiónico, ácido 2-[({p-[1 -metil-5-metil-4-(1 -feniletoxicarbonilamino)-1H-pirazol-3-il]fenil}-metil)amino]-3-fenilpropiónico, ácido 3-ciclopropil-2-[({p-[1-metil-5-metil-4-(1 -fenil-etoxicarbonilamino)-1 H-pirazol-3-il]fenil}metil)amino]propiónico, ácido 2-{[(p-{4-[1 -(oclorofenil)etoxicarbonilamino]-1 -metil-5-metil-1 H-pirazol-3-il}fenil)metil]-amino}-3-fenilpropiónico, ácido 2-{[(p-{4-[1 -(oclorofenil)etoxicarbonilamino]-1 -metil-5-metil-1 H-pirazol-3-il}fenil)metil]amino}-3-ciclopropilpropiónico, ácido 2-({p-[1 -metil-5-metil-4-(1 -feniletoxicarbonilamino)-1 H-pirazol-3-il]fenil}metoxi)-3-fenil-propiónico, ácido 3-ciclopropil-2-({p-[1 -metil-5-metil-4-(1 -feniletoxicarbonilamino)-1 H-pirazol-3-il]fenil}metoxi)propiónico, ácido 2-[(p-{4-[1 -(oclorofenil)etoxicarbonil-amino]-1 -metil-5-metil-1 H-pirazol-3-il}fenil)metoxi]-3-fenilpropiónico, ácido 2-[(p-{4-[1 -(oclorofenil)etoxicarbonilamino]-1 -metil-5-metil-1 H-pirazol-3-il}fenil)-metoxi]-3-ciclopropilpropiónico, ácido 3-{p-[1 -metil-5- metil-4-(1 -feniletoxicarbonil-amino)-1 H-pirazol-3-il]benzoilamino}-4-fenilbutírico, ácido 4-ciclopropil-3-{p-[1 -metil-5-metil-4-(1 -feniletoxicarbonilamino)-1 H-pirazol-3-il]benzoilamino}butírico, ácido 3-[({p-[1 -metil-5-metil-4-(1 -feniletoxicarbonilamino)-1 H-pirazol-3-il]fenil}metil)amino]-4-fenilbutírico, ácido 4-ciclopropil-3-[({p-[1 -metil-5-metil-4-(1 -feniletoxicarbonil-amino)-1 H-pirazol-3-il]fenil}metil)amino]butírico, ácido 3-({p-[1 -metil-5-metil-4-(1 -feniletoxicarbonilamino)-1 H-pirazol-3-il]fenil}metoxi)-4-fenilbutírico o ácido 4-ciclopropil-3-({p-[1 -metil-5-metil-4-(1 -feniletoxicarbonilamino)-1H-pirazol-3-il]fenil}metoxi)butírico.
Un compuesto donde el compuesto es ácido 2-[4-[4-[4-ciano-5-(1-feniletoxicarbonilamino)pirazol-1-il]fenil]fenil]acético, ácido 1 -[4-[4-[4-ciano-5-(1 -feniletoxicarbonilamino)pirazol-1 -il]fenil]fenil]ciclopropanocarboxílico, ácido 1-[4-[4-[5-[1-(2-clorofenil)etoxicarbonilamino]-4-ciano-pirazol-1-il]fenil]fenil]ciclo-propanocarboxílico, ácido 2-[4-[4-[4-ciano-5-(1 -feniletoxicarbonilamino)pirazol-1 -il]-fenil]fenil]-2-metil-propanoico, ácido 2-[4-[4-[5-[1 -(2-clorofenil)etoxicarbonil-amino]-4-ciano-pirazol-1 -il]fenil]fenil]-2-metil-propanoico, ácido 1 -{4'-[4-fluoro-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-4-bifenilil}ciclopropanocarboxílico, ácido 1 -(4'-{5-[1 -(oclorofenil)etoxicarbonilamino]-4-fluoro-1 H-pirazol-1 -il}-4-bifenilil)-ciclopropanocarboxílico, ácido 1 -{3-fluoro-4'-[4-fluoro-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-4-bifenilil}ciclopropanocarboxílico, ácido 1 -(4'-{5-[1 -(oclorofenil)etoxi-carbonilamino]-4-fluoro-1 H-pirazol-1 -il}-3-fluoro-4-bifenilil)ciclopropanocarboxílico, ácido 1 -{2-fluoro-4'-[4-fluoro-5-(1-feniletoxicarbonilamino)-1 H-pirazol-1 -il]-4-bifenilil}-ciclopropanocarboxílico, ácido 1 -(4'-{5-[1 -(oclorofenil)etoxicarbonilamino]-4-fluoro-1 H-pirazol-1 -il}-2-fluoro-4-bifenilil)ciclopropanocarboxílico, ácido 1 -(2-cloro-4'-{5-[1 -(o-clorofenil)etoxicarbonilamino]-4-fluoro-1 H-pirazol-1 -il}-4-bifenilil)ciclopropano-carboxílico, ácido 1 -(4-{p-[4-fluoro-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-fenil}tolil)ciclopropanocarboxílico, ácido 1 -[4-(p-{5-[1 -(oclorofenil)etoxicarbonil-amino]-4-fluoro-1 H-pirazol-1 -il}fenil)tolil]ciclopropanocarboxílico, ácido 1 -(p-{5-[5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}fenil)ciclopropanocarboxílico, ácido 1 -[p-(5-{5-[1 -(oclorofenil)etoxicarbonilamino]-1 H-pirazol-1 -il}-2-piridil)-fenil]ciclopropanocarboxílico, ácido 1 -(p-{5-[4-metil-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}fenil)ciclopropanocarboxílico, ácido 1 -[p-(5-{5-[1 -(o-clorofenil)etoxicarbonilamino]-4-metil-1 H-pirazol-1 -il}-2-piridil)fenil]ciclopropano-carboxílico, ácido 1 -(2-fluoro-4-{5-[5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}fenil)ciclopropanocarboxílico, ácido 1 -[4-(5-{5-[1 -(oclorofenil)etoxicarbonil-amino]-1 H-pirazol-1 -il}-2-piridil)-2-fluorofenil]ciclopropanocarboxílico, ácido 1 -(3-fluoro-4-{5-[5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}fenil)ciclopropano-carboxílico, ácido 1 -[4-(5-{5-[1 -(oclorofenil)etoxicarbonilamino]-1 H-pirazol-1 -il}-2-piridil)-3-fluorofenil]ciclopropanocarboxílico, ácido 1 -(p-{5-[4-metil-5-(1 -feniletoxi-carbonilamino)-1 H-pirazol-1 -il]-2-piridil}fenil)ciclopropanocarboxílico, ácido 1 -(p-{5-[4-metil-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}fenil)ciclopropano-carboxílico, ácido 1 -[p-(5-{5-[1 -(oclorofenil)etoxicarbonilamino]-4-metil-1 H-pirazol-1 -il}-2-piridil)fenil]ciclopropanocarboxílico, ácido 1 -(2-fluoro-4-{5-[4-metil-5-(1 -fenil-etoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}fenil)ciclopropanocarboxílico, ácido 1 -[4-(5-{5-[1 -(oclorofenil)etoxicarbonilamino]-4-metil-1 H-pirazol-1 -il}-2-piridil)-2-fluorofenil]ciclopropanocarboxílico, ácido 1 -(3-fluoro-4- {5-[4-metil-5-(1 -feniletoxi-carbonilamino)-1 H-pirazol-1 -il]-2-piridil}fenil)ciclopropanocarboxílico, ácido 1 -[4-(5-{5-[1 -(o-clorofenil)etoxicarbonilamino]-4-metil-1 H-pirazol-1 -il}-2-piridil)-3-fluoro-fenil]ciclopropanocarboxílico, ácido 1 -(p-{5-[4-fluoro-5-(1-feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}fenil)ciclopropanocarboxílico, ácido 1 -[p-(5-{5-[1 -(ocloro-fenil)etoxicarbonilamino]-4-fluoro-1 H-pirazol-1 -il}-2-piridil)fenil]ciclopropano-carboxílico, ácido 1 -(2-fluoro-4-{5-[4-fluoro-5-(1-feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}fenil)ciclopropanocarboxílico, ácido 1 -[4-(5-{5-[1 -(oclorofenil)etoxi-carbonilamino]-4-fluoro-1 H-pirazol-1 -il}-2-piridil)-2-fluorofenil]ciclopropanocarboxílico, ácido 1 -(3-fluoro-4-{5-[4-fluoro-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}fenil)ciclopropanocarboxílico, ácido 1 -[4-(5-{5-[1 -(o-clorofenil)etoxicarbonil-amino]-4-fluoro-1 H-pirazol-1 -il}-2-piridil)-3-fluorofenil]ciclopropanocarboxílico, ácido 1 -(p-{5-[4-ciano-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}fenil)ciclo-propanocarboxílico, ácido 1 -[p-(5-{5-[1 -(o-clorofenil)etoxicarbonilamino]-4-ciano-1 H-pirazol-1 -il}-2-piridil)fenil]ciclopropanocarboxílico, ácido 1 -(4-{5-[4-ciano-5-(1 -fenil-etoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}-2-fluorofenil)ciclopropanocarboxílico, ácido 1 -[4-(5-{5-[1 -(oclorofenil)etoxicarbonilamino]-4-ciano-1 H-pirazol-1 -il}-2-piridil)-2-fluorofenil]ciclopropanocarboxílico, ácido 1 -(4-{5-[4-ciano-5-(1 -feniletoxi-carbonilamino)-1 H-pirazol-1 -il]-2-piridil}-3-fluorofenil)ciclopropano-carboxílico o ácido 1 -[4-(5-{5-[1-(o-clorofenil)etoxicarbonilamino]-4-ciano-1 H-pirazol-1-il}-2-piridil)-3-fluorofenil]ciclopropanocarboxílico.
Un compuesto donde el compuesto es ácido 3-fenil-2-[[4-[5-(1-feniletoxicarbonilamino)oxazol-4-il]benzoil]amino]propanoico, ácido 3-ciclopropil-2-[[4-[5-(1-feniletoxicarbonilamino)oxazol-4-il]benzoil]amino]propanoico, ácido 4-fenil-2-[[4-[5-(1-feniletoxicarbonilamino)oxazol-4-il]benzoil]amino]butanoico, ácido 3-fenoxi-2-[[4-[5-(1 -feniletoxicarbonilamino)oxazol-4-il]benzoil]amino]propanoico, ácido 3-fenil-2-[({p-[5-(1 -feniletoxicarbonilamino)-1,3-oxazol-4-il]fenil}metil)-amino]propiónico, ácido 3-ciclopropil-2-[({p-[5-(1 -feniletoxicarbonilamino)-1,3-oxazol-4-il]fenil}-metil)amino]propiónico, ácido 3-fenil-2-({p-[5-(1 -feniletoxicarbonilamino)-1,3-oxazol-4-il]fenil}metoxi)propiónico, ácido 4-fenil-3-({p-[5-(1 -feniletoxi-carbonilamino)-1,3-oxazol-4-il]fenil}metoxi)butírico o ácido 4-ciclopropil-3-({p-[5-(1 -feniletoxicarbonil-amino)-1,3-oxazol-4-il]fenil}metoxi)butírico.
Un compuesto donde el compuesto es ácido 2-[[4-[1-metil-5-(1-feniletoxicarbonilamino)imidazol-4-il]benzoil]amino]-3-fenil-propanoico, ácido 3-ciclopropil-2-[[4-[1 -metil-5-(1 -feniletoxicarbonilamino)imidazol-4-il]benzoil]-amino]propanoico, ácido 2-[[4-[1 -metil-5-(1 -feniletoxicarbonilamino)imidazol-4-il]benzoil]amino]-4-fenil-butanoico, ácido 2-[[4-[1 -metil-5-(1 -feniletoxicarbonil-amino)imidazol-4-il]benzoil]amino]-3-fenoxi-propanoico, ácido 2-[({p-[1 -metil-5-(1 -feniletoxicarbonilamino)-1 H-imidazol-4-il]fenil}metil)amino]-3-fenilpropiónico, ácido 3-ciclopropil-2-[({p-[1 -metil-5-(1 -feniletoxicarbonilamino)-1 H-imidazol-4-il]fenil}metil)amino]propiónico, ácido 2-({p-[1 -metil-5-(1 -feniletoxicarbonilamino)-1 H-imidazol-4-il]fenil}metoxi)-3-fenilpropiónico, ácido 3-ciclopropil-2-({p-[1 -metil-5-(1 -feniletoxicarbonilamino)-1 H-imidazol-4-il]fenil}metoxi)propiónico, ácido 3-[({p-[1 -metil-5-(1 -feniletoxicarbonilamino)-1 H-imidazol-4-il]fenil}metil)amino]-4-fenilbutírico, 4-ciclopropil-3-[({p-[1 -metil-5-(1 -feniletoxicarbonilamino)-1 H-imidazol-4-il]fenil}metil)amino]butírico ácido, ácido 3-({p-[1 -metil-5-(1 -feniletoxicarbonil-amino)-1 H-imidazol-4-il]fenil}metoxi)-4-fenilbutírico o ácido 4-ciclopropil-3-({p-[1 -metil-5-(1 -feniletoxicarbonilamino)-1 H-imidazol-4-il]fenil}metoxi)butírico.
Un compuesto donde el compuesto es ácido 2-[[4-[1,2-dimetil-3-oxo-5-(1-feniletoxicarbonilamino)pirazol-4-il]benzoil]amino]-3-fenil-propanoico, ácido 3-ciclopropil-2-[[4-[1,2-dimetil-3-oxo-5-(1 -feniletoxicarbonilamino)pirazol-4-il]benzoil]amino]propanoico, ácido 2-[[4-[1,2-dimetil-3-oxo-5-(1 -feniletoxicarbonil-amino)pirazol-4-il]benzoil]amino]-4-fenil-butanoico, ácido 2-[[4-[1,2-dimetil-3-oxo-5-(1 -feniletoxicarbonilamino)pirazol-4-il]benzoil]amino]-3-fenoxipropanoico, ácido 2-[({p-[1,2-dimetil-3-oxo-5-(1 -feniletoxicarbonilamino)-1,2-dihidropirazol-4-il]-fenil}-metil)amino]-3-fenilpropiónico, ácido 3-ciclopropil-2-[({p-[1,2-dimetil-3-oxo-5-(1 -feniletoxicarbonilamino)-1,2-dihidropirazol-4-il]fenil}metil)amino]propiónico, ácido 2-({p-[1,2-dimetil-3-oxo-5-(1 -feniletoxicarbonilamino)-1,2-dihidropirazol-4-il]-fenil}metoxi)-3-fenilpropiónico, ácido 3-ciclopropil-2-({p-[1,2-dimetil-3-oxo-5-(1 -feniletoxicarbonilamino)-1,2-dihidropirazol-4-il]fenil}metoxi)propiónico, ácido 3-[({p-[1,2-dimetil-3-oxo-5-(1 -feniletoxicarbonilamino)-1,2-dihidropirazol-4-il]-fenil}-metil)amino]-4-fenilbutírico, ácido 4-ciclopropil-3-[({p-[1,2-dimetil-3-oxo-5-(1 -feniletoxicarbonilamino)-1,2-dihidropirazol-4-il]fenil}metil)amino]butírico, ácido 3-({p-[1,2-dimetil-3-oxo-5-(1 -feniletoxicarbonilamino)-1,2-dihidropirazol-4-il]-fenil}-metoxi)-4-fenilbutírico o ácido 4-ciclopropil-3-({p-[1,2-dimetil-3-oxo-5-(1-feniletoxi-carbonilamino)-1,2-dihidropirazol-4-il]fenil}metoxi)butírico.
Un compuesto donde el compuesto es ácido 3-fenil-2-[[4-[5-(1-feniletoxicarbonilamino)pirimidin-4-il]benzoil]amino]propanoico, ácido 3-ciclopropil-2-[[4-[5-(1-feniletoxicarbonilamino)pirimidin-4-il]benzoil]amino]propanoico, ácido 4-fenil-2-[[4-[5-(1-feniletoxicarbonilamino)pirimidin-4-il]benzoil]amino]butanoico, ácido 3-fenoxi-2-[[4-[5-(1 -feniletoxicarbonilamino)pirimidin-4-il]benzoil]amino]-propanoico, ácido 3-fenil-2-[({p-[5-(1 -feniletoxicarbonilamino)-4-pirimidinil]fenil}-metil)-amino]propiónico, ácido 3-ciclopropil-2-[({p-[5-(1-feniletoxicarbonilamino)-4-pirimidinil]-fenil}metil)amino]propiónico, ácido 3-fenil-2-({p-[5-(1-feniletoxi-carbonilamino)-4-pirimidinil]fenil}metoxi)propiónico, ácido 3-ciclopropil-2-({p-[5-(1-feniletoxicarbonil-amino)-4-pirimidinil]fenil}metoxi)propiónico, ácido 4-fenil-3-[({p-[5-(1 -feniletoxi-carbonilamino)-4pirimidinil]fenil}metil)amino]butírico, ácido 4-ciclopropil-3-[({p-[5-(1-feniletoxicarbonilamino)-4-pirimidinil]fenil}metil)amino]-butírico, ácido 4-fenil-3-({p-[5-(1-feniletoxicarbonilamino)-4-pirimidinil]fenil}-metoxi)butírico, ácido 4-ciclopropil-3-({p-[5-(1 -feniletoxicarbonilamino)-4-pirimidinil]fenil}metoxi)butírico, ácido 2-[[4-[6-metil-5-(1-feniletoxicarbonil-amino)pirimidin-4-il]benzoil]amino]-3-fenil-propanoico, ácido 3-ciclopropil-2-[[4-[6-metil-5-(1 -feniletoxicarbonilamino)-pirimidin-4-il]benzoil]amino]propanoico, ácido 2-[[4-[6-metil-5-(1 -feniletoxicarbonilamino)pirimidin-4-il]benzoil]amino]-4-fenil-butanoico o ácido 2-[[4-[6-metil-5-(1 -fenil-etoxicarbonilamino)pirimidin-4-il]benzoil]-amino]-3-fenoxi-propanoico.
Un compuesto donde el compuesto es ácido 3-fenil-2-[[4-[4-(1-feniletoxicarbonilamino)pirimidin-5-il]benzoil]amino]propanoico, ácido 3-ciclopropil-2-[[4-[4-(1-feniletoxicarbonilamino)pirimidin-5-il]benzoil]amino]propanoico, ácido 4-fenil-2-[[4-[4-(1 -feniletoxicarbonilamino)pirimidin-5-il]benzoil]amino]butanoico o ácido 3-fenoxi-2-[[4-[4-(1-feniletoxicarbonilamino)pirimidin-5-il]benzoil]amino]-propanoico,
Un compuesto donde el compuesto es ácido 3-fenil-2-[[4-[3-(1-feniletoxicarbonilamino)pirazin-2-il]benzoil]amino]propanoico, ácido 3-ciclopropil-2-[[4-[3-(1-feniletoxicarbonilamino)pirazin-2-il]benzoil]amino]propanoico, ácido 4-fenil-2-[[4-[3-(1 -feniletoxicarbonilamino)pirazin-2-il]benzoil]amino]butanoico o ácido 3-fenoxi-2-[[4-[3-(1-feniletoxicarbonilamino)pirazin-2-il]benzoil]amino]propanoico.
Un compuesto donde el compuesto es ácido 1-{p-[3-metil-4-(1-feniletoxicarbonilamino)-5-isoxazolil]fenil}-4-piperidinacarboxílico, ácido (1-{p-[3-metil-4-(1-feniletoxicarbonilamino)-5-isoxazolil]fenil}-4-piperidil)acético, ácido 1-(1 -{p-[3-metil-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]fenil}-4-piperidil)ciclo-propanocarboxílico, ácido [1 -(1 -{p-[3-metil-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-fenil}-4-piperidil)ciclopropil]acético, ácido 1 -{5-[3-metil-4-(1 -feniletoxicarbonil-amino)-5-isoxazolil]-2-piridil}-4-piperidinacarboxílico, ácido (1 -{5-[3-metil-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridil}-4-piperidil)acético, ácido 1 -(1 -{5-[3-metil-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridil}-4-piperidil)ciclopropanocarboxílico, ácido [1 -(1 -{5-[3-metil-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridil}-4-piperidil)ciclopropil] acético, ácido 1 -{p-[3-fluoro-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]fenil}-4- piperidinacarboxílico, ácido (1 -{p-[3-fluoro-4-(1 -feniletoxicarbonil-amino)-5-isoxazolil]fenil}-4-piperidil)acético, ácido 1 -(1 -{p-[3-fluoro-4-(1 -feniletoxi-carbonilamino)-5-isoxazolil]fenil}-4-piperidil)ciclopropanocarboxílico, ácido [1 -(1 -{p-[3-fluoro-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]fenil}-4-piperidil)ciclopropil]acético, ácido 1 -{5-[3-fluoro-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridil}-4-piperidina-carboxílico, ácido (1 -{5-[3-fluoro-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridil}-4-piperidil)acético, ácido 1 -(1 -{5-[3-fluoro-4-(1 -feniletoxicarbonilamino)-5- isoxazolil]-2-piridil}-4-piperidil)ciclopropanocarboxílico, ácido [1 -(1 -{5-[3-fluoro-4-(1 -feniletoxi-carbonilamino)-5-isoxazolil]-2-piridil}-4-piperidil)ciclopropil]acético, ácido 1-{p-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]fenil}-4-piperidinacarboxílico, ácido (1-{p-[3-ciano-4-(1-feniletoxicarbonilamino)-5-isoxazolil]fenil}-4-piperidil)acético, ácido 1-(1 -{p-[3-ciano-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]fenil}-4-piperidil)ciclo-propanocarboxílico, ácido [1 -(1 -{p-[3-ciano-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-fenil}-4-piperidil)ciclopropil]acético, ácido 1 -{5-[3-ciano-4-(1 -feniletoxicarbonil-amino)-5-isoxazolil]-2-piridil}-4-piperidinacarboxílico, ácido (1 -{5-[3-ciano-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridil}-4-piperidil)acético, ácido 1 -(1 -{5-[3-ciano-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridil}-4-piperidil)ciclopropanocarboxílico, ácido [1 -(1 -{5-[3-ciano-4-(1 -feniletoxicarbonilamino)-5-isoxazolil]-2-piridil}-4-piperidil)ciclopropil]acético, ácido 1 -{p-[5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]fenil}-4-piperidinacarboxílico, ácido (1 -{p-[5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]fenil}-4-piperidil)acético, ácido 1-(1-{p-[5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]fenil}-4-piperidil)ciclopropanocarboxílico, ácido [1 -(1 -{p-[5-(1 -feniletoxicarbonil-amino)-1 H-pirazol-1 -il]fenil}-4-piperidil)ciclopropil]acético, ácido 1-{5-[5-(1-feniletoxi-carbonilamino)-1 H-pirazol-1 -il]-2-piridil}-4-piperidinacarboxílico, ácido (1 -{5-[5-(1 -fenil-etoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}-4-piperidil)acético, ácido 1 -(1 -{5-[5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}-4-piperidil)ciclopropanocarboxílico, ácido [1 -(1 -{5-[5-(1-feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}-4-piperidil)-ciclopropil] acético, ácido 1 -{p-[4-metil-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]fenil}-4-piperidinacarboxílico, ácido (1 -{p-[4-metil-5-(1-feniletoxicarbonilamino)-1 H-pirazol-1 -il]fenil}-4-piperidil)acético, ácido 1 -(1 -{p-[4-metil-5-(1 -feniletoxi-carbonilamino)-1 H-pirazol-1-il]fenil}-4-piperidil)ciclopropanocarboxílico, ácido [1-(1-{p-[4-metil-5-(1-feniletoxicarbonilamino)-1 H-pirazol-1 il]fenil}-4-piperidil)ciclopropil-]acético, ácido 1-{5-[4-metil-5-(1-feniletoxicarbonilamino)-1 H-pirazol-1 - il]-2-piridil}-4-piperidinacarboxílico, ácido (1-{5-[4-metil-5-(1-feniletoxicarbonilamino)-1 H-pirazol-1 - il]-2-piridil}-4-piperidil)acético, ácido 1-(1-{5-[4-metil-5-(1-feniletoxicarbonilamino)-1 H-pirazol-1 il]-2-piridil}-4-piperidil)ciclopropanocarboxílico, ácido [1-(1-{5-[4-metil-5-(1-feniletoxicarbonilamino)-1 H-pirazol-1 - il]-2-piridil}-4-piperidil)ciclopropil]acético, ácido 1-{p-[4-fluoro-5-(1-feniletoxicarbonilamino)-1 H-pirazol-1 il]fenil}-4-piperidina-carboxílico, ácido (1-{p-[4-fluoro-5-(1-feniletoxicarbonilamino)-1 H-pirazol-1 il]fenil}-4-piperidil)acético, ácido 1 -(1 -{p-[4-fluoro-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1-il]fenil}-4-piperidil)ciclopropanocarboxílico, ácido [1 -(1 -{p-[4-fluoro-5-(1 -feniletoxi-carbonilamino)-1 H-pirazol-1 -il]fenil}-4-piperidil)ciclopropil]acético, ácido 1 -{5-[4-fluoro-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}-4-piperidinacarboxílico, ácido (1 -{5-[4-fluoro-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}-4-piperidil)acético, ácido 1 -(1 -{5-[4-fluoro-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}-4-piperidil)ciclopropanocarboxílico, ácido [1 -(1 -{5-[4-fluoro-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}-4-piperidil)ciclopropil]acético, ácido 1 -{p-[4-ciano-5-(1 -fenil-etoxicarbonilamino)-1 H-pirazol-1 -il]fenil}-4-piperidinacarboxílico, ácido (1 -{p-[4-ciano-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]fenil}-4-piperidil)acético, ácido 1 -(1 -{p-[4-ciano-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]fenil}-4-piperidil)ciclopropano-carboxílico, ácido [1 -(1 -{p-[4-ciano-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-fenil}-4-piperidil)ciclopropil]acético, ácido 1 -{5-[4-ciano-5-(1 -feniletoxicarbonil-amino)-1 H-pirazol-1 -il]-2-piridil}-4-piperidinacarboxílico, ácido (1 -{5-[4-ciano-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}-4-piperidil)acético, ácido 1 -(1 -{5-[4-ciano-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}-4-piperidil)ciclopropano-carboxílico o ácido [1 -(1 -{5-[4-ciano-5-(1 -feniletoxicarbonilamino)-1 H-pirazol-1 -il]-2-piridil}-4-piperidil)ciclopropil]acético.
Una formulación farmacéuticamente aceptable que comprende, consiste esencialmente de, o consiste de un compuesto de Tabla 1 y uno o más excipientes farmacéuticamente aceptable.
Se divulga adicionalmente un método que comprende administrar una cantidad efectiva de un compuesto de Fórmula I-XII a un individuo que tiene una enfermedad o trastorno mediado por LPA o dependiente de LPA.
En una realización la enfermedad o trastorno mediado por LPA o dependiente de LPA es una enfermedad con fibrosis de órganos.
En una realización la fibrosis se produce en el hígado, riñón, pulmón, corazón, ojo y similares.
En una realización la enfermedad o trastorno mediado por LPA o dependiente de LPA es dolor crónico.
En una realización la enfermedad o trastorno mediado por LPA o dependiente de LPA es prurito.
En una realización la enfermedad mediada por LPA es una enfermedad proliferativa, como cáncer (tumores sólidos, metástasis de tumor sólido, fibroma vascular, mieloma, mieloma múltiple, sarcoma de Kaposi, leucemia, leucemia linfocítica crónica (LLC) y similares) y metástasis invasiva de células cancerosas, incluido cáncer de ovario, de mama y cáncer de mama triple negativo y similares.
En una realización la enfermedad mediada por LPA es una enfermedad inflamatoria que incluye psoriasis, nefropatía, neumonía y similares.
En una realización la enfermedad mediada por LPA es una enfermedad gastrointestinal, como enfermedad inflamatoria intestinal.
En una realización la enfermedad mediada por LPA es una enfermedad ocular que incluye degeneración macular relacionada con la edad (AMD), retinopatía diabética, retinopatía proliferativa vítrea (PVR), penfigoide cicatricial, cicatrices por cirugía de filtración de glaucoma, uveítis y similares.
En una realización 78 la enfermedad mediada por LPA es una enfermedad hepática que incluye hepatitis aguda, hepatitis crónica, fibrosis hepática, cirrosis hepática, prurito colestásica, hipertensión portal, insuficiencia regenerativa, esteatohepatitis no alcohólica (ENAH), hipofunción hepática, trastorno del flujo sanguíneo hepático y similares.
En una realización la enfermedad mediada por LPA es una enfermedad renal, que incluye insuficiencia renal crónica, enfermedad renal en etapa terminal, prurito urémico, nefropatía diabética, incluida nefropatía, y similares.
En una realización la enfermedad mediada por LPA es una enfermedad de la piel que incluye escleroderma, cicatrices en la piel, dermatitis atópica, psoriasis y similares.
En una realización el individuo es un humano.
En una realización el compuesto se selecciona de la Tabla 1.
En una realización el compuesto es ácido 1-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-ciclo-propanocarboxílico, ácido 2-(4-{4-[1-(2-cloro-fenil)-etoxicarbonil-amino]-3-metil-iso-xazol-5-il}-benzoilamino)-indan-2-carboxílico, ácido 2-(S)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)feniloacético, ácido 2-(R)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-iso-xazol-5-il}-benzoilamino) fenilopropanoico, ácido 2(R)-[[4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico, ácido 2(S)-[[4-[3-metil-4-((R)-feniletoxicarbonil-amino)isoxazol-5-il]benzoil]amino]-3-fenilpropanoico, ácido (R)-2-{4-[3-metil-4-((S)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benzoilamino}-3-fenil-propiónico, ácido (S)-2-{4-[3-metil-4-((S)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-benzoilamino}-3-fenil-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-fenil-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-fluoro-fenil)-propiónico, ácido (R)-3-(4-cloro-fenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(3,4-difluoro-fenil)-propiónico, ácido (R)-3-(2-cloro-fenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico, ácido (R)-3-(4-bromo-fenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metilisoxazol-5-il}-benzoilamino)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(2-fluoro-fenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metilisoxazol-5-il}-benzoilamino)-3-p-tolil-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metilisoxazol-5-il}-benzoilamino)-3-(4-trifluorometil-fenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-ciano-fenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-clorofenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-ciclopropil-propiónico, ácido (R)-2-[[4-[2,5-dimetil-4((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-fenil-propanoico, ácido (R)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-fluorofenil)propanoico, ácido (R)-3-(4-bromofenil)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-3-(4-clorofenil)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-3-(3,4-difluorofenil)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-2-[[4-[1,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-fenil-propanoico, ácido (R)-2-[[4-[1,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-fluorofenil)propanoico, ácido (R)-3-(4-bromofenil)-2-[[4-[1,5-dimetil-4-((R)-1 -feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido ((R)-3-(4-clorofenil)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-3-(3,4-difluorofenil)-2-[[4-[1,5-dimetil-4-((R)-1 -feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-2-(4-{5-[(R)-1 -(2-clorofenil)-etoxicarbonilamino]-4-metil-pirazol-1 -il}-benzoilamino)-3-fenil-propiónico, ácido (R)-2-{4-[3-metil-4-((R)-1 -feniletoxicarbonilamino)-isoxazol-5-il]-bencilamino}-3-fenil-propiónico, ácido (R)-3-(2-fluoro-fenil)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-2-{4-[3-metil-4-((R)-1-feniletoxicarbonilamino)-isoxazol-5-il]-bencilamino}-3-(4-trifluorometil-fenil)-propiónico, ácido (R)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-3-(2-cloro-fenil)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-3-(4-cloro-fenil)-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-fenil-propiónico, ácido (R)-2-(4-{4-[(R)_1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-(2-fluoro-fenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-clorofenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-(4-trifluorometil-fenil)-propiónico, ácido (R)-3-(2-clorofenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-ciclopropil-propiónico, ácido 2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-3-fenil-propiónico, ácido 2-{4-[3-metil-4-((R)-1 -feniletoxicarbonilamino)-isoxazol-5-il]-benciloxi}-3-fenil-propiónico, ácido (RS)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-feniletoxicarbonilamino)-isoxazol-5-il]-benciloxi}-propiónico, ácido (RS)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-feniletoxicarbonilamino)-isoxazol-5-il]-benciloxi}-propiónico, ácido 2-[4-[4-[5-[1-(2-clorofenil)etoxicarbonilamino]-4-cianopirazol-1 -il]fenil]fenil]acético, ácido (R)-1 -[4-[4-[1,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]fenil]fenilciclopropano carboxílico, ácido (R)-1 -[4-[4-[2,5-dimetil-4-(1 -feniletoxicarbonilamino)-pirazol-3-il]fenil]fenil]ciclopropano carboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonil-amino]-4-fluoro-pirazol-1 -il}-3-fluoro-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-2-fluoro-bifenil-4-il)-ciclo-propanocarboxílico, ácido (R)-1 -(2-cloro-4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-2-metil-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxi-carbonilamino]-4-fluoro-pirazol-1 -il}-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -{4'-[5-(1 -fenil-etoxicarbonilamino)-4-trifluorometil-pirazol-1 -il]-bifenil-4-il}-ciclo-propanocarboxílico, ácido (R)-1 -{2-fluoro-4'-[5-(1 -fenil-etoxicarbonilamino)-4-trifluoro-metil-pirazol-1 -il]-bifenil-4-il}-ciclopropanocarboxílico, ácido (R)-1 -(4-{5-[5-(1 -fenil-etoxicarbonilamino)-pirazol-1 -il]-piridin-2-il}-fenil)-ciclopropanocarboxílico,
Los compuestos de la invención se pueden formular en una composición que comprende, consiste esencialmente o consiste en uno o más compuestos de Fórmula (I o XXII) y uno o más agentes actualmente usados para tratar una enfermedad o trastorno dependiente de LPA o mediado por LPA o una enfermedad o trastorno descrito en la presente.
Los compuestos de la invención se pueden formular en una formulación farmacéuticamente aceptable que comprende, consiste esencialmente o consiste en uno o más compuestos de Fórmula (I o X-XII), uno o más agentes utilizados actualmente para tratar una enfermedad o trastorno dependiente de LPA o mediado por LPA y uno o más excipientes farmacéuticamente aceptables.
Se divulga adicionalmente un método que comprende administrar en manera combinada o co-administrar un compuesto de Fórmula (I-XII) a un individuo con una enfermedad o trastorno dependiente de LPA o mediado por LPA y un agente utilizado actualmente para tratar una enfermedad o trastorno dependiente de LPA o mediado por LPA.
Uno o más agentes terapéuticamente activos adicionales distintos de los compuestos de Fórmula (I-XII) se seleccionan de: corticosteroides, inmunosupresores, analgésicos, agentes anti-cáncer, antiinflamatorios, antagonistas del receptor de quimioquinas, broncodilatadores, antagonistas de los receptores de leucotrienos, inhibidores de la formación de leucotrienos, antagonistas de los receptores para el factor de activación plaquetaria, inhibidores de monoacilglicerol quinasa, inhibidores de fosfolipasa A 1 , inhibidores de fosfolipasa A2 e inhibidores de lisofosfolipasa D (lisoPLD), inhibidores de autotaxina, descongestivos, estabilizadores de mastocitos, antihistamínicos, mucolíticos, anticolinérgicos, antitusivos, expectorantes y agonistas p-2.
Los agentes que se utilizan actualmente se pueden seleccionar de los descritos en el Índice Merck de los que afectan a la señalización del receptor de ácido lisofosfatídico. El compuesto de Fórmula (I-XII) se puede seleccionar de la Tabla 1.
Las terapias que combinan un compuesto de Fórmula (I-XII) con agentes utilizados actualmente que actúan sobre diferentes vías de señalización a la síntesis LPA o vía de señalización a fin de proporcionar resultados clínicos complementarios se incluyen en la presente para tratar enfermedades o trastornos mediados por LPA o dependientes de LPA.
Entre los ejemplos de agentes terapéuticos adicionales se incluyen, a modo no taxativo, cualquiera de los siguientes: gosipol, genasense, polifenol E, Clorofusin, todo ácido trans-retinoico (ATRA), briostatina, ligando inductor de apoptosis relacionada con el factor de necrosis tumoral (TRAIL), 5-aza-2 'desoxicitidina, todo ácido trans-retinoico, doxorrubicina, vincristina, etopósido, gemcitabina, imatinib, geldanamicina, 17-N-alilamino-17-Demethoxygeldanamycin (17 -AAG), flavopiridol, LY294002, bortezomib, trastuzumab, BAY 11-7082, PKC412, o PD 184352, TaxolTM (paclitaxel) y análogos de Taxol ™, como Taxotere ™, U0126, PD98059, PD184352, PD0325901, ARRY-142886, s B239063, SP600 125, BAY 43-9006 , wortmanina o LY294002, adriamicina, dactinomicina, bleomicina, vinblastina, cisplatino, acivicina; aclarrubicina; hidrocloruro de acodazol; acronina; adozelesina; aldesleukina; altretamina; ambomicina; acetato ametantrona; amino-glutetimida; amsacrina; anastrozol; antramicina; asparaginasa; asperlina; azacitidina; azetepa; azotomicina; batimastat; benzodepa; bicalutamida; hidrocloruro de bisantreno; dimesilato de bisnafida; bizelesina; sulfato de bleomicina; brequinar sodio; bropirimina; busulfán; cactinomicina; calusterona; caracemida; carbetímero; carboplatino; carmustina; hidrocloruro de carubicina; carzelesina; cedefingol; clorambucil; cirolemicina; cladribina; mesilato de crisnatol; ciclofosfamida; citarabina; dacarbazina; hidrocloruro de daunorubicina; decitabina; dexormaplatino; desazaguanina; mesilato de desazaguanina; diaziquona; doxorrubicina; hidrocloruro de doxorrubicina; droloxifeno; citrato de droloxifeno; propionato de dromostanolona; duazomicina; edatrexato; hidrocloruro de eflornitina; elsamitrucina; enloplatino; enpromato; epipropidina; hidrocloruro de epirubicina; erbulozol; hidrocloruro de esorubicina; estramustina; fosfato sódico de estramustina; etanidazol; etopósido; fosfato de etopósido; etoprina; hidrocloruro de fadrozol; fazarabina; fenretinida; floxuridina; fosfato de fludarabina; fluorouracilo; flurocitabina; fosquidona; fostriecin de sodio; gemcitabina; hidrocloruro de gemcitabina; hidroxiurea; hidrocloruro de idarubicina; ifosfamida; iimofosina; interleucina II (incluida interleucina recombinante II, o rIL2), interferón alfa-2a; interferón alfa-2b; interferón alfa-n1; interferón alfa-n3; interferón beta-l a; interferón gamma-l b; iproplatino; hidrocloruro de irinotecán; acetato de lanreotida; letrozol; acetato de leuprolide; hidrocloruro de liarozol; lometrexol de sodio; lomustina; hidrocloruro de osoxantrona; masoprocol; maitansina; hidrocloruro de mecloretamina; acetato de megestrol; acetato de melengestrol; melfalán; menogaril; mercaptopurina; metotrexato; metotrexato de sodio; metoprina; meturedepa; mitindomida; mitocarcina; mitocromina; mitogilina; mitomalcina; mitomicina; mitosper; mitotano; hidrocloruro de mitoxantrona; ácido micofenólico; nocodazoie; nogalamicina; ormaplatino; oxisuran; pegaspargasa; peliomicina; pentamustina; sulfato de peplomicina; perfosfamida; pipobromán; piposulfan; hidrocloruro de piroxantrona; plicamicina; plomestano; porfímero sódico; porfiromicina; prednimustina; hidrocloruro de procarbazina; puromicina; hidrocloruro de puromicina; pirazofurina; riboprina; rogletimida; safingol; hidrocloruro de safingol; semustina; simtraceno; esparfosato de sodio; esparsomicina; hidrocloruro de germanio espiro; espiromustina; espiroplatino; estreptonigrina; estreptozotocina; sulofenur; talisomicina; tecogalán de sodio; tegafur; hidrocloruro de teloxantrona; temoporfm; tenipósido; teroxirona; testolactona; tiamiprina; tioguanina; tiotepa; tiazofurina; tirapazamina; citrato de toremifeno; acetato de trestolona; fosfato de triciribina; trimetrexato; trimetrexato de glucuronato; triptorelina; hidrocloruro de tubulozol; mostaza de uracilo; uredepa; vapreotida; verteporfina; sulfato de vinblastina; sulfato de vincristina; vindesina; sulfato de vindesina; sulfato de vinepidina; sulfato de vinglicinato; sulfato de vinleurosina; tartrato de vinorelbina; sulfato de vinrosidina; sulfato de vinzolidina; vorozol; zeniplatino; zinostatina; hidrocloruro de zorubicina, mecloroetamina, ciclofosfamida, clorambucilo, meiphalan, etc.), etilenimina, hexametilmelamina, tiotepa, busulfán), carmustina, lomusitne, semustina, estreptozocina, ortriazenes, dacarbazina, metotrexato, fluorouracilo, floxouridina, citarabina, mercaptopurina, tioguanina, pentostatina, caproato de hidroxiprogesterona, acetato de megestrol, acetato de medroxiprogesterona, estrógenos, dietilstilbestrol, etinilestradiol, tamoxifeno), propionato de testosterona, fluoximesterona, flutamida, leuprolida, cisplatino, carboblatina, mitoxantrona), procarbazina, mitotano, amino-glutetimida, Erbulozol, Dolastatina 10, Mivobulina isetionato, Vincristina, NSC-639829, Discodermolida, ABT-751, (Altorirtin A y Altorirtin C), Espongistatinas 1-9, Hidrocloruro de cemadotina, Epotilona A, Epotilona B, Epotilona C, Epotilona D, Epotilona E, Epotilona F, N-Óxido de Epotilona B, AN-Óxido de Epotilona, Epotilona B 16-Aza, 21-Aminoepotilona B, 21-Hidroxiepotilona D, 26-Fluoroepotilona, Auristatina PE, Soblidotina, Criptoficina 52, Vitilevuamide, Tubulisina A, Canadensol, Centaureidina, Oncocidina Al Fijianolide B, Laulimalida, Narcosina, Nascapina, Hemiasterlina, Acetilacetonato de Vanadoceno, Eleuterobinas Indanocina (como Desmetileleuterobina, Desaetileleuterobina, Isoeleuterobina A y Z-Eleuterobina), Caribaeósido, Caribaeolina, Halicondrina B, Diazonamida A, Tacalonolida A, Diozostatina, (-)-Fenilahistina, Mioseverina B, Fosfato sódico de resverastatina, Aprepitante, cannabis, Marinol, dronabinol, eritropoyetina-a, Filgrastim, rituximab, natalizumab, ciclofosfamida, penicilamina, ciclosporina, nitrosoureas, cisplatino, carboplatino, oxaliplatino, metotrexato, azatioprina, mercaptopurina, análogos de pirimidina, inhibidores de la síntesis de proteínas, dactinomicina, antraciclinas, mitomicina C, bleomicina, mitramicina, Atgam® Thymoglobuline®, OKT3®, basiliximab, daclizumab, ciclosporina, tacrolimus, sirolimus, interferones, opioides, infliximab, etanercept, adalimumab, golimumab, leflunomida, sulfasalazina, hidroxicloroquina, minociclina, rapamicina, ácido micofenólico, micofenolato mofetil, FTY720, ciclosporina A (CsA) o tacrolimus (FK506), aspirina, ácido salicílico, ácido gentísico, salicilato de colina y magnesio, salicilato de colina, salicilato de colina y magnesio, salicilato de colina, salicilato de magnesio, salicilato de sodio, diflunisal, carprofeno, fenoprofeno, calcio fenoprofeno, flurobiprofeno, ibuprofeno, ketoprofeno, nabutone, ketolorac, ketorolaco trometamina, naproxeno, oxaprozina, diclofenac, etodolac, indometacina, sulindac, tolmetina, meclofenamato, meclofenamato de sodio, ácido mefenámico, piroxicam, meloxicam, valdecoxib, parecoxib, etoricoxib, lumiracoxib, betametasona, prednisona, alclometasona,
aldosterona, amcinonida, beclometasona, betametasona, budesonida, ciclesonida, clobetasol, clobetasona, clocortolona, cloprednol, cortisona, cortivazol, deflazacort, desoxicorticosterona, desonida, desoximetasona, desoxicortona, dexametasona, diflorasona, diflucortolona, difluprednato , fluclorolona,fludrocortisona, fludroxicortida, flumetasona, flunisolida, acetónido de fluocinolona,fluocinonida, fluocortina, fluocortolona, fluorometolona, fluperolona, fluprednideno, fluticasona, formocorta1, halcinonida, halometasona, hidrocortisona/cortisol, aceponato de hidrocortisona, buteprato de hidrocortisona, butirato de hidrocortisona, lotepredno1, medrisona, meprednisona, metilprednisolona,aceponato de metilprednisolona,furoato de mometasona, parametasona, prednicarbato, prednisona/prednisolona,rimexolona,tixocortol, triamcinolona, ulobetasol, pioglitazona, clofibrato, gemfibrozil fenofibrato, ácido fólico, isbogrel, ozagrel, ridogrel, dazoxibén, lovastatina, simvastatina, pravastatina , fluvastatina, atorvastatina, nisvastatina, y rosuvastatina, edaravona, vitamina C, TROLOX™, citicolina y miniciclina, ácido (2R)-2-propiloctanoico, propanolol, nadolol, timolol, pindolol, labetalol, metoprolol, atenolol, esmolol y acebutolol, memantina, traxoprodil, tirofibán lamifibán, argatroban, enalapril, ciclandelato, losartán, valsartán, candesartán, irbesartán, telmisartán, olmesartán mepiramina (pirilamina), antazolina, difenhidramina, carbinoxamina, doxilamina, clemastina, dimenhidrinato, feniramina, clorfenamina (clorfeniramina), dexclorfeniramina, bromfeniramina, triprolidina, cetirizina, ciclizina clorciclizina, hidroxizina, meclizina, loratadina, desloratadina, prometazina, alimemazina (trimeprazina), ciproheptadina, azatadina, ketotifeno, acrivastina, astemizol, cetirizina, mizolastina, terfenadina, azelastina, epinastina, levocabastina, olopatadina, levocetirizina, fexofenadina , rupatadina, bepotastina), mucolíticos, anticolinérgicos, antitusígenos, analgésicos, expectorantes, albuterol, efedrina, epinefrina, fomoterol, metaproterenol, terbutalina, budesonida, ciclesonida, dexametasona, flunisolida, propionato de fluticasona, triamcinolona, bromuro de ipratropio, pseudoefedrina, teofilina, montelukast, pranlukast, tomelukast, zafirlukast, ambrisentan, bosentan, enrasentán, sitaxsentán, tezosentán, iloprost, treprostinil, pirfenidona, epinefrina, isoproterenol, orciprenalina, xantinas, zileutón.
En el método anterior el individuo puede ser un humano.
En el método anterior los compuestos de Fórmula I-XII se pueden seleccionar de la Tabla 1.
En el método anterior los compuestos de Fórmula I-XII se pueden seleccionar del grupo que consiste en ácido 1-(4-{4-[1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-ciclo-propanocarboxílico, ácido 2-(4-{4-[1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-indan-2-carboxílico, ácido 2-(S)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)feniloacético, ácido 2-(R)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino) fenilopropanoico, ácido 2(R)-[[4-[3-metil-4-((R)-1 -feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico, ácido 2(S)-[[4-[3-metil-4-((R)-feniletoxicarbonil-amino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico, ácido (R) -2-{4-[3-metil-4-((S)-1-feniletoxicarbonilamino)-isoxazol-5-il]-benzoilamino}-3-fenil-propiónico, ácido (S) -2-{4-[3-metil-4-((S)-1-feniletoxicarbonilamino)-isoxazol-5-il]-benzoilamino}-3-fenil-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-fenil-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-fluoro-fenil)-propiónico, ácido (R)-3-(4-cloro-fenil)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico, ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(3,4-difluoro-fenil)-propiónico, ácido (R)-3-(2-cloro-fenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico, ácido (R)-3-(4-bromo-fenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(2-fluoro-fenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-p-tolilpropiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-trifluorometil-fenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-ciano-fenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metilisoxazol-5-il}-benzoilamino)-3-ciclopropil-propiónico, ácido (fí)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-fenil-propanoico, ácido (R)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-fluorofenil)propanoico, ácido (R)-3-(4-bromofenil)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-3-(4-clorofenil)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-3-(3,4-difluorofenil)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-2-[[4-[1,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-fenil-propanoico, ácido (R)-2-[[4-[1,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-fluorofenil)propanoico, ácido (R)-3-(4-bromofenil)-2-[[4-[1,5-dimetil-4-((R)-1 -feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-3-(4-clorofenil)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-3-(3,4-difluorofenil)-2-[[4-[1,5-dimetil-4-((R)-1 -feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-2-(4-{5-[(R)-1 -(2-clorofenil)-etoxicarbonilamino]-4-metil-pirazol-1 -il}-benzoilamino)-3-fenil-propiónico, ácido (R)-2-{4-[3-metil-4-((R)-1 -feniletoxicarbonilamino)-isoxazol-5-il]-bencilamino}-3-fenil-propiónico, ácido (R)-3-(2-fluoro-fenil)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-2-{4-[3-metil-4-((R)-1-feniletoxicarbonilamino)-isoxazol-5-il]-bencilamino}-3-(4-trifluorometil-fenil)-propiónico, ácido (R)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-3-(2-cloro-fenil)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-3-(4-cloro-fenil)-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-fenil-propiónico, ácido (R)-2-(4-{4-[(R)_1-(2-cloro-fenil)etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-(2-fluoro-fenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-clorofenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-(4-trifluorometil-fenil)-propiónico, ácido (R)-3-(2-clorofenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-ciclopropil-propiónico, ácido 2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-3-fenil-propiónico, ácido 2-{4-[3-metil-4-((R)-1 -feniletoxicarbonilamino)-isoxazol-5-il]-benciloxi}-3-fenil-propiónico, ácido (RS)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-feniletoxicarbonilamino)-isoxazol-5-il]-benciloxi}-propiónico, ácido (RS)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-feniletoxicarbonilamino)-isoxazol-5-il]-benciloxi}-propiónico, ácido 2-[4-[4-[5-[1-(2-clorofenil)etoxi-carbonilamino]-4-cianopirazol-1 -il]fenil]fenil]acético, ácido (R)-1 -[4-[4-[1,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]ciclopropano carboxílico, ácido (R)-1-[4-[4-[2,5-dimetil-4-(1-feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]-ciclopropano carboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonil-amino]-4-fluoro-pirazol-1 -il}-3-fluoro-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-2-fluoro-bifenil-4-il)-ciclo-propanocarboxílico, ácido (R)-1 -(2-cloro-4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-2-metil-bifenil-4-il)-ciclopropano-carboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -{4'-[5-(1 -fenil-etoxicarbonil-amino)-4-trifluorometil-pirazol-1 -il]-bifenil-4-il}-ciclopropanocarboxílico, ácido (R)-1 -{2-fluoro-4'-[5-(1 -fenil-etoxicarbonilamino)-4-trifluorometil-pirazol-1 -il]-bifenil-4-il}-ciclopropanocarboxílico, ácido (R)-1 -(4-{5-[5-(1 -fenil-etoxicarbonilamino)-pirazol-1 -il]-piridin-2-il}-fenil)-ciclopropanocarboxílico,
En la composición anterior el agente que se usa actualmente puede ser un estabilizador de mastósitos celular
En la composición anterior el agente que se usa actualmente puede ser un factor activador de plaquetas de los receptores antagonistas,
El agente estabilizador de los mastocitos puede ser cromoglicato, nedocromil, azelastina, bepotastina, epinastina, ketotifeno, olopatadina y rupatadina.
El factor activador de plaquetas de los receptores antagonista puede ser rupatadina, SM-12502, CV-3988 y WEB 2170.
Los siguientes compuestos se describen a modo de referencia:
1A. Un compuesto donde el compuesto tiene la estructura de fórmula I
o una sal o profármaco farmacéuticamente aceptable de este,
donde RA es -CO2 H, -CO2 RB, -CN, tetrazolilo, -C(=O)NH2 , -C(=O)NHRB, -C(=O)NHSO2 RB o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico;
donde RB es -H o -alquilo C1-C4 , o tiene la estructura de uno de:
L1 está ausente o es alquileno C1-C6 sustituido o no sustituido, cicloalquileno C3 -C6 sustituido o no sustituido, fluoroalquileno C1-C6 , heteroalquileno C1-C6 sustituido o no sustituido, o -UV-Z-, donde -UV- se define mediante -OW-, -WO-, -N(RJ)W-, -WN(RJ)-, -N(RJ)C(=O)-, -SW-, -S(=O)nW- o -C(=O)N(RJ)-, donde W es alquileno C1-C3 sustituido o no sustituido o cicloalquileno C3 -C6 sustituido o no sustituido o W es -C(RL)2 -, y donde Z es alquileno C1-C6 sustituido o no sustituido, cicloalquileno C3 -C6 sustituido o no sustituido, o fluoroalquileno C1-C6 o Z es -C(RL)2 -; donde n es 0, 1, o 2;
L2 está ausente o es alquileno C1-C6 sustituido o no sustituido, cicloalquileno C3 -C6 sustituido o no sustituido, fluoroalquileno C1-C6 , heteroalquileno C1-C6 sustituido o no sustituido, -O-, -S-, -S(=O)-, -S(=O)2 -, -N(RJ)-, -C(=O)-, o -C(=O)N(RJ)-;
El anillo A es un heteroareno de 5-6 miembros que se selecciona de uno de:
d o n d e la línea p u n te a d a ind ica e l p un to de un ión de l an illo A al an illo B; d o n d e uno de RC y RD es -H , -C N , -F, -C l, -Br, -I, -O a lq u ilo C1-C4, -a lqu ilo C1-C4, -c ic lo a lq u ilo C3-C6, o - flu o ro a lq u ilo C1-C4, y el o tro RC o RD es -N (R F)-C (= O )X C H (R G)-C Y , -N (R F)-C (= O )X C (R G)2-C Y , -N (R F)-C (= O )X -C Y , -C (= O )-N (R F)-C H (R G)X -C Y , -C (= O )-N (R F)-C(Rg)2X-CY, o -C (= O )X -N (R F)-X -C Y , d o n d e X e s tá ause n te , es -O -, -N H - o -CH2-;
RE es -H, -a lqu ilo C1-C4 o - flu o ro a lq u ilo C1-C4; RF es -H o a lq u ilo C1-C4; RG es RE s e le cc io n a d o in d e p en d ie n te m e n te , o un RG es -a lqu ilo C1-C4 y se to m a ju n to con el á to m o de c a rb o n o al qu e RG e s tá u n ido y el ca rb o n o o he te ro á to m o al q ue C Y e s tá un ido p a ra d e fin ir un c a rb o c ic lo su s titu id o o no su s titu id o o un h e te ro c ic lo su s titu id o o no su s titu id o , y el o tro RG, si e s tá p rese n te , es co m o se d e fin e p o r RE;
C Y es a lq u ilo C1-C6 su s titu id o o no sus titu ido , c ic lo a lq u ilo C3-C10 su s titu id o o no sus titu ido , h e te ro c ic lo a lq u ilo C2-C10 su s titu id o o no su s titu id o , arilo su s titu id o o no su s titu id o , o he te ro a rilo su s titu id o o no sus titu ido , d o n d e si C Y e s tá su s titu id o , e n to n ce s C Y e s tá su s titu id o con 1, 2, o 3 RH se le cc io n a d o s in d e p en d ie n te m e n te ;
d o n d e ca d a RH se se le cc io n a in d e p e n d ie n te m e n te de -H , h a lógeno , -C N , -NO2, -O H , -O R J, -S R J, -S (= O )R J, -S(=O)2Rj , -N (R J)S (= O )2RJ, -S (= O )2N (R L)2, -C(=O)Rj , OC(=O)Rj, -CO2Rj , -OCO2Rj , -N (R L)2, -C (= O )N (R L)2, -O C (= O )N (R L)2, -N (R J)C (= O )N (R L)2, -N (R J)C (= O )R J, -N (R J)C (= O )O R J, a lq u ilo C1-C4, flu o ro a lq u ilo C1-C4, flu o ro a lco x i C1-C4, a lcox i C1-C4, y h e te ro a lq u ilo C1-C4, d o n d e ca d a RJ es in d e p e n d ie n te m e n te a lq u ilo C1-C6 su s titu id o o no su s titu id o , h e te ro a lq u ilo C1-C6 su s titu id o o no sus titu ido , flu o ro a lq u ilo C1-C6, c ic lo a lq u ilo C3-C6 su s titu id o o no su s titu id o , h e te ro c ic lo a lq u ilo su s titu id o o no su s titu id o , a rilo su s titu id o o no sus titu ido , h e te ro a rilo su s titu id o o no su s titu id o , a lq u ile n o -C 1-C 4-(c ic lo a lq u ilo C3-C6 su s titu id o o no su s titu id o ), a lq u ile n o -C 1-C 4-(h e te ro c ic lo a lq u ilo sus titu ido o no sus titu id o ), a lq u ile n o -C 1-C 4-(a rilo su s titu id o o no sus titu id o ), o a lq u ile n o -C 1-C 4-(h e te ro a rilo su s titu id o o no su s titu id o );
d o n d e ca d a RL es in d e p e n d ie n te m e n te -H , a lqu ilo C1-C6 su s titu id o o no sus titu ido , h e te ro a lq u ilo C1-C6 su s titu id o o no su s titu id o , flu o ro a lq u ilo C1-C6, c ic lo a lq u ilo C3-C6 su s titu id o o no su s titu id o , h e te ro c ic lo a lq u ilo su s titu id o o no sus titu id o , a rilo su s titu id o o no sus titu ido , he te ro a rilo su s titu id o o no su s titu id o , a lq u ile n o -C 1-C 4-(c ic lo a lq u ilo su s titu id o o no su s titu id o ), a lq u ile n o -C 1-C 4-(h e te ro c ic lo a lq u ilo su s titu id o o no sus titu id o ), a lq u ile n o -C 1-C 4(a rilo su s titu id o o no su s titu id o ), o a lq u ile n o -C 1-C 4-(h e te ro a rilo su s titu id o o no su s titu id o ), o c u a n d o RH es -S (=O )2N (R L)2, -N (R L)2, -C (= O )N (R L)2, -O C (= O )N (R L)2 o -N (R F)C (= O )N (R L)2, ca d a RL es in d e p e n d ie n te m e n te -H o a lq u ilo C1-C6, o los g ru p o s RL son in d e p e n d ie n te m e n te a lqu ilo C1-C6 qu e se to m a n ju n to al e l á to m o de N al qu e es tán un id o s pa ra d e fin ir un h e te ro c ic lo su s titu id o o no su s titu id o , o cu a n do W es -C(Rl)2- o Z es -C (R L)2-, ca d a RL es in d e p e n d ie n te m e n te -H, a lq u ilo C1-C6, o los g ru p o s RL son in d e p e n d ie n te m e n te a lq u ilo C1-C6 q ue se to m a n ju n to al á to m o de c a rb o n o al que es tán un id o s pa ra d e fin ir un ca rb o c ic lo ;
El an illo B es c ic lo a lq u ile n o C3-C10 su s titu id o o no sus titu ido , h e te ro c ic lo a lq u ile n o C2-C10 su s titu id o o no sus titu id o , a rile no su s titu id o o no su s titu id o , o h e te ro a rile no su s titu id o o no su s titu id o , d o n de si e l an illo B e s tá sus titu id o , e n to n ce s el an illo B e s tá su s titu id o con 1, 2, o 3 RH s e le cc io n a d o s in d e p en d ie n te m e n te , d o n d e RH es co m o se d e fin ió p re v ia m e n te ;
El an illo C e s tá a u se n te o es c ic lo a lq u ile n o C3-C10 su s titu id o o no sus titu ido , h e te ro c ic lo a lq u ile n o C2-C10 su s titu id o o no su s titu id o , a rileno su s titu id o o no sus titu ido , o h e te ro a rile no su s titu id o o no sus titu ido , d o n d e si e l an illo C e s tá su s titu id o , e n to n ce s e l an illo C e s tá su s titu id o con 1, 2, o 3 RH s e le cc io n a d o s in d e p en d ie n te m e n te , d o n de RH es co m o se d e fin ió p rev ia m e n te ,
d o n d e c u a n d o el an illo B es a rile no su s titu id o o no sus titu ido , e l an illo C e s tá ause n te , L2 e s tá ausen te , L 1 es -U V -Z -, d o n d e -U V - es -N (R J)-C (= O )-, d o n d e RJ es -H, RD es -N (R F)-C (= O )X C H (R G)-C Y , d o n d e X es -O -, RG es -CH3 y RF es -H, y RC es -H, -CH3 o -CF3,
o cu a n do e l an illo B es a rile no su s titu id o o no su s titu id o y e l a n illo C es a rileno su s titu id o o no su s titu id o o es c ic lo a lq u ile n o C3-C10 su s titu id o o no su s titu id o , o e l an illo B es c ic lo a lq u ile n o C3-C10 su s titu id o o no su s titu id o y el an illo C es a rileno su s titu id o o no sus titu ido , L2 e s tá ause n te , L 1 es a lq u ile n o C1-C6,
y RC es -H o -CH3 y RA es -CO2H o C O 2R B,
e n to n ce s e l an illo A tie n e la e s tru c tu ra de uno de:
y cu a n d o e l an illo B es h e te ro c ic lo a lq u ile n o C2-C10, el an illo C es a rile no su s titu id o o no sus titu ido , L2 e s tá ausen te , L1 es a lq u ile n o C1-C6, RC es -CH3 y RA es -CO2H o C O 2R B, e n to n ce s e l an illo A tie n e la e s tru c tu ra de uno de:
2A. El co m p u e s to de la rea lizac ión 1A d o n de RC es -H , -C N , -F, -C l, -B r, -I, -O a lq u ilo C1-C4, -a lqu ilo C1-C4, -c ic lo a lq u ilo C3-C6, o -fluo ro a lq u ilo C1-C4 y RD es -N (R F)-C (= O )X C H (R G)-C Y , -N (R F)-C (= O )X C (R G)2-CY, -N (R F)-C (= O )X -C Y , d o n d e RF y ca d a RG son in d e p e n d ie n te m e n te -H o a lqu ilo C1-C4.
3A. El c o m p u e s to de la rea lizac ión 2A d o n de e l an illo A se se le cc io n a de uno de:
d o n d e RD es -N (R F)-C (= O )X C H (R G)-C Y , y RC es -H , -CH3 o -CF3,
El an illo B es a rile no su s titu id o o no su s titu id o o h e te ro a rile no su s titu id o o no su s titu id o , e l an illo C e s tá a u se n te ; L2 e s tá a u se n te ; L1 es -U V -Z -, d o n d e -U V -e s -O W -, -W O -, -N (R J)W -, -W N (R J)-, -N (R J)C (=O )-, -S W -, -S (=O )nW -, o -(= O )N (R J)-, d o n d e W es a lq u ile n o C1-C3 su s titu id o o no su s titu id o ; y n es 0, 1, o 2 ; o el an illo B y el an illo C son in d e p e n d ie n te m e n te a rile no su s titu id o o no su s titu id o o a rile no su s titu id o o no su s titu id o L2 e s tá ausen te , L1 es a lq u ile n o C1-C6.
4A. El c o m p u e s to de la rea lizac ión 2A d o n de e l an illo A tie n e la e s tru c tu ra de uno de:
d o n d e el an illo B es a rile no su s titu id o o no su s titu id o y el an illo C es a rile no su s titu id o o no su s titu id o o es c ic lo a lq u ile n o C3-C10 su s titu id o o no su s titu id o , o e l an illo B es c ic lo a lq u ile n o C3-C10 su s titu id o o no su s titu id o y el an illo C es a rileno su s titu id o o no sus titu ido , L2 e s tá a u se n te y L1 es a lq u ile n o C1-C6.
5A. El co m p u e s to de la rea lizac ión 2A d o n d e L2 e s tá au se n te y L1 es a lq u ile n o C1-C6, o c ic lo a lq u ile n o C3-C6 su s titu id o o no su s titu id o , h e te ro a lq u ile n o C1-C6 su s titu id o o no su s titu id o o L2 y e l an illo C es tán a u se n te s y L1 es -U V -Z -, d o n de -U V - se d e fin e m ed ia n te -O W -, -W O -, -N (R J)W -, -W N (R J)-, -N (R J)C (= O )-, -S W -, -S (=O )nW -, o -C (= O )N (R J)-, d o n d e W es a lq u ile n o C1-C3 su s titu id o o no su s titu id o ; y n es 0, 1, o 2.
6A. El co m p u e s to de la rea lizac ión 5A d o n de L1 es -U V -Z - d o n d e -U V - se d e fin e m ed ia n te -O W -, -W O -, -N (R J)W -, -W N (R J)- o -C (= O )N (R J)-, d o n d e W es a lq u ile n o C1-C3 su s titu id o o no sus titu id o .
7A. El co m p u e s to de la rea lizac ión 5A d o n de L1 es -U V -Z -, d o n de -U V - se d e fin e m ed ia n te -W O -, -W N (R J)- o -(= O )N (R J)-, d o n d e W es a lq u ile n o C1-C3 su s titu id o o no sus titu ido , y L2 e s tá ausente .
8A. El c o m p u e s to de la rea lizac ión 7A d o n de Z es a lq u ile n o C1-C6 su s titu id o o no sus titu ido .
9A. El c o m p u e s to de la rea lizac ión 7A d o n de Z es a lq u ile n o C1-C6 su s titu id o o no su s titu id o y RA es -CO2H o -C O 2R B.
10A. El compuesto de la realización 7A, donde L1 es -UV-Z-, donde -UV- se define mediante -C(=O)N(RJ)-, donde RJ es -H o -CH3.
11A. El compuesto de la realización 7A donde L1 es UV-Z-, donde -UV-, se define mediante -WO-.
12A. El compuesto de la realización 7A donde L1 es UV-Z-, donde -UV-, se define mediante -WN(RJ)-, donde RJ es -H o -CH3.
13A. El compuesto de la realización 2A donde L1 está ausente o un C1-C4 alquileno sustituido o no sustituido o a sustituido o no sustituido C3 cicloalquileno (es decir, ciclopropil-di-ilo).
14A. El compuesto de la realización 2 donde L1 es -CH2-, o -C(CH3)2-.
15A. El compuesto de la realización 2 donde el anillo A tiene la estructura de uno de:
donde RC es -H, -CN, -CH3, o -CF3, RD es -N(RF)C(=O)XCH(RG)-CY, -N(RF)C(=O)XC(RG)2-CY, o -N(RF)C(=O)X-CY y L1 es -UV-Z- donde -UV- se define mediante -WO-, -WN(RJ)- o -C(=O)N(RJ)-.
16A. El compuesto de la realización 15A donde RC es -H, -CH3 o -CF3 y RD es -N(RF)C(=O)XCH(RG)-CY.
17A. El compuesto de la realización 15A donde RD es -N(RF)C(=O)XCH(RG)-CY, donde -X- es -N(RF)- o -O-; y donde RG y cada RF, seleccionados independientemente, son -H o -CH3.
18A. El compuesto de la realización 17A donde RG es -CH3, en la configuración R o S, y CY es fenilo sustituido o no sustituido o heteroarilo sustituido o no sustituido.
19A. El compuesto de la realización 17A donde RD es -N(RF)C(=O)OCH(RG)-CY, donde CY es no sustituido o sustituido fenilo, donde el fenilo sustituido es fenilo que está sustituido con uno o dos RJ seleccionados independientemente.
20A. El compuesto de la realización 17A, donde RD es -N(RF)C(=O)OCH(CH3)-CY, donde RF es -H, y donde CY es fenilo no sustituido.
21A. El compuesto de la realización 17A, donde RD es -N(RF)-C(=O)OCH(CH3)-CY, donde RF es -H, y donde CY es fenilo sustituido, donde el fenilo sustituido es fenilo que está sustituido con uno o dos RH seleccionados independientemente, donde RH son halógenos.
22A. El compuesto de la realización 21A, donde RD es -NH-C(=O)OCH(CH3)-CY donde CY es fenilo sustituido, donde el fenilo sustituido es fenilo que está sustituido con un RH, donde RH es -F, -Cl o -Br.
23A. El compuesto de la realización 21A, donde RD es -NH-C(=O)OCH(CH3)-CY, donde CY es fenilo sustituido, donde el fenilo sustituido es fenilo que está sustituido con un RH, donde RH es -Cl.
24A. El compuesto de la realización 19A, donde RD es -NH-C(=0)0CH(CH3)-CY que tiene la estructura de
25A. El compuesto de la reivindicación 19A donde RD es -NH-C(=O)OCH(CH3)-CY donde el grupo metilo en RD es de configuración R .
donde L2 está ausente y el anillo B es arileno sustituido o no sustituido, o heteroarileno sustituido o no sustituido,
siempre que el anillo C no está ausente y L1 es alquileno C1-C6, o el anillo C está ausente y L1 es -UV-Z, donde -UV es -N(RJ)-C(=O)-, y RD tiene la estructura de -N(RF)-C(=O)XCH(RG)-CY, -N(RF)-C(=O)XC(RG)2-CY o -N(RF)-C(=O)X-CY, y RA es -CO2H, entonces RC es diferente a -H, -CH3 y -CF3.
27A. El compuesto de la realización 26A donde RC es -H, -CH3 o -CF3, y RD es -NH-C(=O)OCH(RG)-CY, donde RG es -H o -CH3, en la configuración R o S, y -CY es fenilo sustituido o no sustituido.
28A. El compuesto de la realización 26A donde L2 y el anillo C están ausentes, el anillo B es arileno sustituido o no sustituido, o heteroarileno sustituido o no sustituido, y L1 es -UV-Z-, donde -UV-, se define mediante -WO-, -WN(RJ)-o -C(=O)N(RJ)-.
29A. El compuesto de la realización 26A donde L2 y el anillo C están ausentes, el anillo B es arileno sustituido o no sustituido, o heteroarileno sustituido o no sustituido, y L1 es -UV-Z-, donde -UV-, se define mediante -WN(RJ)- o -C(=O)N(RJ)-, donde RJ es -H o -CH3.
30A. El compuesto de la realización 29A donde L1 es -UV-Z-, donde -UV- se define mediante -C(=O)NH-, y donde Z es alquileno C1-C6 sustituido o no sustituido.
31A. El compuesto de la realización 29A donde L1 es -UV-Z-, donde -UV- se define mediante -WO-, donde W es alquileno C1-C3 sustituido o no sustituido, y donde Z es alquileno C1-C6 sustituido o no sustituido.
32A. El compuesto de la realización 29A donde L1 es -UV-Z-, donde -UV- se define mediante -W-NH-, donde W es alquileno C1-C3 sustituido o no sustituido, y donde Z es alquileno C1-C6 sustituido o no sustituido.
33A. El compuesto de la realización 26A donde L1 es -UV-Z-, donde -UV- se define mediante -WO-, -WN(RJ)- o -C(=O)N(RJ), donde RJ es -H o -CH3, y donde Z es alquileno C1-C6 sustituido o no sustituido, donde el alquileno es -CH(CH2-ciclopropilo)-, -CH(CH2-arilo) o -CH(CH2-heteroarilo), donde el arilo o heteroarilo está sustituido o no sustituido.
34A. El compuesto de la realización 33A donde L1 es -UV-Z-, donde -UV- se define mediante -C(=O)NH-, -WO- o -W-NH-, donde -W- es -CH2-.
35A. El compuesto de la realización 33A donde RA es -CO2H o -CO2RB.
36A. El compuesto de la realización 33A donde L1 es -UV-Z-, donde -UV- se define mediante -CH2O-, -CH2-NH- o -C(=O)NH-, donde Z es alquileno C1-C6 sustituido o no sustituido, donde el alquileno es -CH(CH2-ciclopropilo)-, -CH(CH2-arilo) o -CH(CH2-heteroarilo), donde el arilo o heteroarilo está sustituido o no sustituido con 1, 2, o 3 alquilo C1-C4 sustituido o no sustituido o halógeno seleccionados independientemente.
37A. El compuesto de la realización 36A donde dicho sustituyente o sustituyentes alquilo C1-C4 sustituido o no sustituido o halógeno del arilo o heteroarilo de -CH(CH2-arilo) o -CH(CH2-heteroarilo) se seleccionan del grupo que consiste en -CH3, -CF3, -F, -Cl o -Br.
38A. El compuesto de la realización 33A, donde L1 es -UV-Z-y donde RA es -CO2H al que Z está unido para definir -L1-RA (es decir, -UV-Z-RA), donde -UV- se define mediante -C(=O)NH-, -WO- o -W-NH-, donde -W- es -CH2-, y Z es -CH(CH2-arilo), donde el arilo está sustituido o no sustituido, que tiene la estructura de uno de
39A. El compuesto de la realización 36A donde el sustituyente -CH(CH2-arilo) de Z en el -L1-RA tiene la configuración R.
40A. El compuesto de la realización 33A donde L1 es -UV-Z-y donde RA es -CO2H al que Z está unido para definir -L1-RA (es decir, -UV-Z-RA), donde -UV- se define mediante -C(=O)NH-, -WO- o -W-NH-, donde -W- es -CH2 -, y Z es -CH(CH2-ciclopropilo)-, que tiene la estructura de
41A. El compuesto de la realización 1A, 2A, 3A, o 4A, donde el compuesto tiene la estructura de fórmula III
donde A1, A2 y A3 son independientemente -N=, =N-CH- o -CH=
42A. El compuesto de la realización 41A donde el anillo A donde el anillo A tiene la estructura de uno de:
, donde cuando L1 es alquileno C1-C6, RD es -N(RF)-C(=°)XCH(RG)-CY, -N(RF)-C(=°)XC(RG)2-CY, donde RF es -H, RG es -H o -CH3; RA es -CO2H o CO2RB, y
43A. El compuesto de la realización 41A, donde el anillo A donde el anillo A tiene la estructura de uno de:
donde el anillo C es un arileno sustituido o no sustituido o heteroarileno, L1 es alquileno C1-C6, RA es -CO2H o CO2RB, RD es -N(RF)-C(=O)XCH(RG)-CY, - N ^ - C ^ O ^ R ^ - C Y , donde RF es -H, RG es -CH3 y CY es fenilo sustituido y RC es -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, alquilo-C2-C4, -cicloalquilo C3-C6, o fluoroalquilo-C2-C4.
44A. El compuesto de la realización 41A, donde el anillo A tiene la estructura de uno de:
o no sustituido o heteroarileno, L1 es alquileno C1-C6, RA es -CO2H o -CÜ2RB, RD es -N(RF)-C(=O)XCH(RG)-CY, -N(RF)-C(=O)XC(RG)2-CY, donde X es -O-, RF es -CH3, RG es -H o -CH3 y CY es fenilo sustituido y RC es -H, -CN, -F, -Cl, -Br, -I, -Oalquilo C1-C4, -alquilo C1-C4, -cicloalquilo C3-C6, o -fluoroalquilo C1-C4.
45A. El compuesto de la realización 1A, 2A o 5A donde el compuesto tiene la estructura de fórmula IV
donde el anillo A tiene la estructura de uno de:
son independientemente -H o -CH3; y RA es -CO2H o -CO2RB.
46A. El compuesto de la realización 2A donde el compuesto tiene la estructura de fórmula VII
sustituyente -N(RF)C(=O)CH(RG)-CY de fórmula VI donde CY es fenilo sustituido con un RH, y RC es -H, -CH3, CF3 o -F; RA es -CO2H o -CO2RB; y RF y RG son independientemente -H o -CH3; y RH son independientemente -H, halógeno, -CH3 o -CF3.
47A. El compuesto de la realización 2A donde el compuesto tiene la estructura de fórmula VII
,
N(RF)C(=O)CH(RG)-CY de fórmula VII donde CY es fenilo sustituido con un RH; y RC es -H, -CH3, CF3 o -F; RA es CO2H o -CO2Rb ; Re y RF son independientemente -H o alquilo C1-C4; RG es -H o -CH3; RH son independientemente H, halógeno, -CH3 o -CF3; y Z es -C(RL)2, donde un RL es -H y el otro RL es -H o alquilo C1-C4.
48A El compuesto de la realización 2A donde el compuesto tiene la estructura de fórmula VIII
independientemente -H, halógeno, -CH3 o -CF3; y Z es -C(RL)2, donde un RL es -H y el otro RL es -H o alquilo C1-C4.
49A. El compuesto de la realización 2A donde el compuesto tiene la estructura de fórmula IX
donde RD es el sustituyente -N(RF)C(=O)CH(RG)-CY de fórmula VII donde CY es fenilo sustituido con un RH; RA es -CO2H o -CO2RB
donde W es -C(RL)2- o ; RE y RF son independientemente -H o alquilo C1-C4; RG es -H o -CH3; RH son independientemente -H, halógeno, -CH3 o -CF3; y Z es -C(RL)2, donde un RL es -H y el otro RL es -H o alquilo C1-C4.
50A. El compuesto de la realización 2A donde el compuesto tiene la estructura de fórmula XII
independientemente -H, halógeno, -CH3 o -CF3; y Z es -C(RL)2, donde un RL es -H y el otro RL es -H o alquilo C1-C4.
51A. El compuesto de la realización 2A donde el compuesto se selecciona de Tabla 1.
52A. El compuesto de la realización 51A donde el compuesto es ácido 1-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-ciclopropanocarboxílico, ácido 2-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-indan-2-carboxílico, ácido 2-(S)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino"]-3-metil-isoxazol-5-il}-benzoilamino)fenilacético, ácido 2-(R)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metilisoxazol-5-il}-benzoilamino) fenilpropanoico, ácido 2(R)-[[4-[3-metil-4-((R)-1 -feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico, ácido 2(S)-[[4-[3-metil-4-((R)-1-feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico, ácido (fí)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino~]-3-fenil-propanoico, ácido (R)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-fenil-propanoico, ácido (R)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-fluorofenil)propanoico, ácido (R)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-fluorofenil)propanoico, ácido (R)-3-(4-bromofenil)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-3-(4-bromofenil)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-3-(4-clorofenil)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-3-(4-clorofenil)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-3-(3,4-difluorofenil)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico, ácido (R)-3-(3,4-difluorofenil)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-ciclopropil-propiónico, ácido (R)-2-{4-[3-metil-4-((S)-1-feniletoxicarbonilamino)-isoxazol-5-il]-benzoilamino}-3-fenil-propiónico, ácido (S)-2-{4-[3-metil-4-((S)-1-feniletoxicarbonilamino)-isoxazol-5-il]-benzoilamino}-3-fenil-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-fenil-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-fluoro-fenil)-propiónico, ácido (R)-3-(4-cloro-fenil)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico, ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(3,4-difluoro-fenil)-propiónico, ácido (R)-3-(2-cloro-fenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico, ácido (R)-3- (4-bromo-fenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico, ácido (R)-3-(4-bromo-fenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(2-fluorofenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-ptolil-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-trifluorometil-fenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-ciano-fenil)-propiónico, ácido (R)-2-(4-{5-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-4-metil-pirazol-1 -il}-benzoilamino)-3-fenil-propiónico, ácido (R)-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-3-fenil-propiónico, ácido (R)-3-(2-fluoro-fenil)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-3-(4-trifluorometil-fenil)-propiónico, ácido (R)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-3-(2-cloro-fenil)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-3-(4-cloro-fenil)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-fenil-propiónico, ácido (R)-2-(4-{4-[(R)_1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-(2-fluoro-fenil)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-(4-trifluorometil-fenil)-propiónico, ácido (R)-3-(2-cloro-fenil)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-propiónico, ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilaminoÍ-3-metil-isoxazol-5-il}-bencilamino)-3-ciclopropil-propiónico, ácido 2-{4-[3-metil-4-((R)-1 -feniletoxicarbonilamino)-isoxazol-5-il]-benciloxi}-3-fenil-propiónico, ácido (RS)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-feniletoxicarbonilamino)-isoxazol-5-il]-benciloxi}-propiónico, ácido (RS)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-feniletoxicarbonilamino)-isoxazol-5-il]-benciloxi}-propiónico, ácido 2-[4-[4-[5-[1-(2-clorofenil)etoxicarbonilamino]-4-cianopirazol-1 -il]fenil]fenil]acético, ácido (R)-1 -[4-[4-[1,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]ciclopropano carboxílico, ácido (R)-1 -[4-[4-[2,5-dimetil-4-(1 -feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]ciclopropano carboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-3-fluoro-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-2-fluoro-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -(2-cloro-4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-2-metil-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4- fluoro-pirazol-1 -il}-bifenil-4-il)-ciclopropanocarboxílico, ácido (R)-1 -{4'-[5-(1 -fenil-etoxicarbonilamino)-4-trifluorometilpirazol-1 -il]-bifenil-4-il}-ciclopropanocarboxílico, ácido (R)-1 -{2-fluoro-4'-[5-(1 -fenil-etoxicarbonilamino)-4-trifluorometilpirazol-1 -il]-bifenil-4-il}-ciclopropanocarboxílico, ácido (R)-1 -(4-{5-[5-(1 -fenil-etoxicarbonilamino)-pirazol-1 -il]-piridin-2-il}-fenil)-ciclopropanocarboxílico.
53A. Un compuesto de cualquiera de las realizaciones 1A-52A para la preparación de un medicamento para tratar la enfermedad o afección LPA-dependiente.
Los compuestos de Tabla 1 son ejemplificantes pero no necesariamente de acuerdo con la invención, donde los compuestos 57-458 se preparan de conformidad con los procedimientos modificados apropiadamente de los Ejemplos para la preparación de los compuestos 1-458.
TABLA 1
EJEMPLOS
M éto d o s H P LC
S e reg is tra ron los ras tros de H P LC pa ra los e je m p lo s s in te tiza d o s u tiliza n d o un a H P LC qu e co n s is te de bom bas S h im a d zu H P LC , d e g a s ific a d o r y d e te c to r UV, e q u ip a d o con un a u to -m u e s tre o A g ile n t se rie 1100. Un d e te c to r MS (A P C I) PE S c ie x AP I 150 EX se in co rp o ró con el p ro p ó s ito de re g is tra r los d a tos de e sp e c tro de m asa. Se ob tuv ie ro n los ras tros H P L C /m a sa u tiliza n d o uno de tres m é to d o s c ro m a to g rá fic o s :
Método 1: C o lu m n a Z o rb a x C 18, ta m a ñ o 4.6 m m X 7.5 cm ; d iso lve n te A : T F A 0.05 % en agua, d iso lve n te B: T FA 0.05% en a ce to n itr ilo ; T a s a de flu jo - 0.7 m L /m in ; G rad ie n te : 5% B a 100% B en 9 m in, en e s p e ra a 100% B d u ra n te 4 m in y 100% B a 5% B en 0.5 m in ; d e te c to r U V - cana l 1 = 220 nm, ca n a l 2 = 254 nm.
Método 2: C o lu m n a Z o rb a x C 18, ta m a ñ o 4.6 mm X 7.5 cm ;
S o lve n te A : T F A 0.05 % en agua, d iso lve n te B: T F A 0.05 % en a ce ton itr ilo ;
T asa de f lu jo - 0.7 m L /m in ; G rad ie n te : 5% B a 100% B en 5 m in, en e sp e ra a 100% B d u ra n te 2 m in y 100% B a 5% B en 0.5 m in; d e te c to r U V - cana l 1 = 220 nm, cana l 2 = 254 nm.
Método 3 : C o lu m n a S u nF ire™ (W a te rs ) C18, ta m a ñ o 2.1 m m X 50 m m ;
S o lve n te A : T F A 0.05 % en agua, d iso lve n te B: T F A 0.05 % en a ce ton itr ilo ;
T asa de f lu jo - 0.8 m L/m in ; G rad ie n te : 10% B a 90 % B en 2.4 m in, en e sp e ra at 90% B d u ra n te 1.25 m in y 90 % B a 10% B en 0.25 m in, en e sp e ra a 10% B d u ra n te 1.5 m in .; d e te c to r U V - cana l 1 = 220 nm, ca n a l 2 = 254 nm.
Ejemplo 1 : ác ido 1 -(4 -{4 -[1 -(2 -c lo ro -fe n il)-e to x ic a rb o n ila m in o ]-3 -m e til- is o x a z o l-5 - il} -b e n z o ila m in o )-c ic lo p ro p a n o ca rb o x ílico
Etapa 1: S e a g re g ó t-bu til a ce to a ce ta to de l t-bu til é s te r de l á c ido 2 -(4 -ca rb o x im e til-b e n z o il)-3 -o x o -b u tír ic o (15.1 mL, 89.0 m m o l) a un a susp e ns ión de c lo ru ro de m ag n e s io (8.48 g, 89.0 m m o l) en d ic lo ro m e ta n o (88 m L) qu e se hab ía e n fria d o a 0oC. A la m ezc la se ag re g ó p ir id in a (13.8 m L, 171 m m o l) y la a g itac ión co n tin u ó d u ra n te 15 m inu tos a d ic io n a les . S e ag re g ó p o r g o teo m etil é s te r de l ác ido 4 -(c lo ro c a rb o n il)b e n z o ic o (17.0 g, 85.6 m m ol) en d ic lo ro m e ta n o (88 m L) a la reacc ión . E sta m ezc la se ag itó a 0oC d u ra n te 90 m in u to s y a te m p e ra tu ra am b ie n te d u ra n te 90 m inu tos. En es te m om e n to la m ezc la se tra tó con un a so lu c ió n de ác ido c lo rh íd r ic o 0.2M (10 m L). La
capa orgánica se diluyó con diclorometano (70 mL), se lavó con una solución de ácido clorhídrico 0.2M (30 mL), se separó, se secó sobre Na2SO4 anhidro, se filtró y se concentró al vacío. El aceite amarillo que se obtuvo se utilizó directamente en la siguiente etapa (17.1 g, 6 8 %).
Método 2, Rt 5.4 min. MS (ESI) m/z 321.2 [M H+].
Etapa 2 : terc-butil éster del ácido 5-(4-metoxicarbonil-fenil)-3-metil-isoxazol-4-carboxílico
t-butil éster del ácido 5-(4-metilcarboxi-fenil)-3-metil-isoxazol-4-il-carboxílico
Una mezcla de t-butil éster del ácido 2-(4-carboximetil-benzoil)-3-oxo-butírico [Ejemplo 1, etapa 1] (7.45 g, 23.2 mmol), hidrocloruro de hidroxilamina (5.17 g, 74.4 mmol), etanol (46.5 mL) y agua (32.2 mL) se calentó a 60-62oC durante 2 horas. En este momento la reacción se dejó enfriar y la mezcla resultante se repartió entre acetato de etilo y agua. La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío. Se obtuvo un producto en bruto que se purificó mediante cromatografía de gel de sílice inicialmente con hexano/acetato de etilo 9/1 como disolvente de elución para proporcionar terc-butil éster del ácido 5-(4-metoxicarbonil-fenil)-3-metil-isoxazol-4-carboxílico (4.69 g, 64%)
Método 2, Rt 6.14 min. MS (ESI) m/z 318.2 [M H+].
Etapa 3 : ácido 5-(4-metoxicarbonil-fenil)-3-metil-isoxazol-4-carboxílico
Se disolvió terc-butil éster del ácido 5-(4-metoxicarbonil-fenil)-3-metil-isoxazol-4-carboxílico [Ejemplo 1, etapa 2] (6.35 g mg, 20 mmol) en diclorometano (100 mL) y a este se agregó ácido trifluoroacético (50 mL). La mezcla se agitó durante 2 horas a temperatura ambiente cuando Los extractos volátiles se eliminaron. El producto (5.2 g, 99%) se utilizó como tal en Etapa 4.
Método 2, Rt 4.08 min. MS (ESI) m/z 262 [M H+];
Etapa 4 : metil éster del ácido 1-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico
Se suspendió ácido 5-(4-metilcarboxi-fenil)-3-metil-isoxazol-4-il-carboxílico
[Ejemplo 1, etapa 3] (3.91 g, 15.0 mmol) en tolueno (120 mL) y a este se agregó diisopropiletilamina (3.13 mL, 18.0 mmol). A la solución resultante se agregó difenilfosforil azida (3.56 mL, 16.5 mmol) y esta mezcla se calentó hasta 90oC. Después de 15 minutos, se agregó 1-(2-clorofenil)-etanol (2.98 mL, 22.5 mmol) con calentamiento lento que se mantuvo durante 4 horas. La reacción se dejó enfriar durante la noche. Esta mezcla se diluyó con tolueno, se transfirió a un embudo separador, se extrajo con agua. La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar un producto en bruto (8.34 g). El producto bruto se purificó mediante cromatografía de gel de sílice eluyendo con un gradiente de 30% a 40% acetato de etilo en hexanos para proporcionar producto purificado (3.59 g, 58%) como tres fracciones. Método 2, Rt 5.70 min. MS (ESI) m/z 415.4 [M H+].
Etapa 5 : ácido 1-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico
Se disolvió ácido 1-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico metil éster [Ejemplo 1, etapa 4] (1.5 g, 3.62 mmol) en THF/agua (1/1: 20 mL) y se trató con LiOH (5.1 mL de una solución 1M acuosa). La mezcla resultante se agitó a temperatura ambiente durante 3 horas. La reacción se acidificó hasta un pH de 2, se transfirió a un embudo separador, se diluyó con agua y se extrajo con diclorometano. La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar el producto (0.8 g, 55%). Método 2, Rt 4.77 min. MS (ESI) m/z 401.3 [M H+].
Etapa 6: metil éster del ácido 1-aminociclopropanocarboxílico
Se enfrió ácido 1-aminociclopropanocarboxílico (202 mg, 2 mmol) en metanol (4 mL) a -10oC y a este se agregó por goteo cloruro de tionilo (581pL, 8 mmol). La mezcla se dejó calentar y se sometió a reflujo durante 2 horas. Los disolventes se evaporaron y el residuo se volvió a disolver en alcohol hirviente. A la solución fría se agregó dietil éter hasta el punto de turbidez cuando la mezcla se refrigeró durante 2 días. El precipitado resultantes proporcionó el producto afford el producto (223 mg, 67%) que se usó en Etapa 7.
Etapa 7: metil éster del ácido 1-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-ciclopropanocarboxílico
Al ácido 1-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 1, etapa 5] (49.8 mg, 0.12 mmol) se agregó 1-hidroxibenzotriazolo (18 mg, 0.13 mmol), N-(3-dimetilaminopropil)-etilcarbodiimida (EDCI: 25 mg, 0.13 mmol), diclorometano (2 mL), diisopropiletilamina (52pL, 0.30 mmol), y metil éster del ácido 1-aminociclopropanocarboxílico [Ejemplo 1, etapa 6](20 mg, 0.13 mmol) y esta mezcla se agitó durante la noche. En este momento la mezcla se diluyó con acetato de etilo (20 mL) y se lavó con una solución saturada de bicarbonato de sodio (10 mL), ácido cítrico solución (5 mL) y agua. La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se
concentró al vacío para proporcionar un producto en bruto (101 mg). El residuo se purificó mediante TLC preparativa, eluyendo con una mezcla de 40% de acetato de etilo en hexano v/v. Después de la extracción de la banda purificada, el producto se obtuvo (55 mg, 92%). Método 2, Rt 4.76 min. MS (ESI) m/z 498.4 [M H+].
Etapa 8: ácido 1 -(4-{4-[1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-ciclopropanocarboxílico
Se disolvió metil éster del ácido 1-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-ciclopropanocarboxílico [Ejemplo 1, etapa 7] (55 mg, 0.11 mmol) en una mezcla 1:1 de THF/agua y se trató con hidróxido de litio ( 8 mg, 0.33 mmol). La mezcla resultante se agitó a temperatura ambiente durante 2 días. A este punto el pH se ajustó a 2 con ácido clorhídrico y la mezcla se extrajo con acetato de etilo (3x20 mL). La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar un producto en bruto (190 mg). El residuo se purificó mediante TLC preparativa, eluyendo con una mezcla al 45% de acetona en diclorometano v/v. Después de la extracción de la banda purificada, se obtuvo el producto (22 mg, 41%).
Método 2, Rt 4.30 min. MS (ESI) m/z 484.6 [M H+].
Ejemplo 2 : ácido 2-(4-{4-[1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-indan-2-carboxílico
Etapa 1 : metil éster del ácido 2-amino-2-indancarboxílico
Se preparó metil éster del ácido 2-amino-2-indancarboxílico de conformidad con un procedimiento similar descrito en el Ejemplo 1, etapa 6 a partir de hidrocloruro del ácido 2-amino-2-indancarboxílico (214 mg, 1 mmol) que se utilizó directamente. Rendimiento 155 mg (6 8 %)
Etapa 2 : metil éster del ácido 2-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-indan-2 -carboxílico
Se preparó metil éster del ácido 2-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-indan-2-carboxílico de conformidad con un procedimiento similar descrito en el Ejemplo 1, etapa 7 a partir de ácido 1-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 1, etapa 5] (49.8 mg, 0.12 mmol) y metil éster del ácido 2 -amino-2 -indancarboxílico [Ejemplo 2 , etapa 1 ]. Rendimiento 55 mg, (81%). Método 2 , Rt 5.49 min. MS (ESI) m/z 574.6 [M H+].
Etapa 3: ácido 2-(4-{4-[1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-indan-2-carboxílico
Se preparó ácido 2-(4-{4-[1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-indan-2-carboxílico de conformidad con un procedimiento similar descrito en el Ejemplo 1 , etapa 8 a partir de metil éster del ácido 2-(4-{4-[1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-indan-2-carboxílico [Ejemplo 2, etapa 7](55 mg, 0.11 mmol). Rendimiento 6 mg, (11%). Método 2, Rt 5.00 min. Ms (ESI) m /z 560.3[M H+].
Ejemplo 3 ácido 2-(S)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)fenilacético
Etapa 1: se preparó metil éster L-fenilglicina de conformidad con un procedimiento similar descrito en el Ejemplo 1, etapa 6 a partir de L-fenilglicina (756 mg, 5 mmol) que se utilizó directamente. Rendimiento 480 mg (58%).
Etapa 2 : metil éster del ácido 2-(S)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)fenilacético
Se preparó metil éster del ácido 2-(S)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)fenilacético de conformidad con un procedimiento similar descrito en el Ejemplo 1, etapa 7 a partir de ácido 1-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 1, etapa 5] (58.1 mg, 0.14 mmol) y L-fenilglicina metil éster [Ejemplo 3, etapa 1] que se utilizó sin purificación. Rendimiento 60 mg (76%) Método 2, Rt 5.41 min. MS (ESI) m/z 548.6 [M H+].
Etapa 3: ácido 2-(S)-(4-{4-[(R,S)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)fenilacético
Se preparó ácido 2-(S)-(4-{4-[(R,S)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)fenilacético de conformidad con un procedimiento similar descrito en el Ejemplo 1, etapa 8 a partir de metil éster del ácido 2-(S)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)fenilacético [Ejemplo 3, etapa 2](60 mg, 0 .11 mmol). Rendimiento 4 mg (11%). Método 2 , Rt 4.90 min. MS (ESI) m/z 534.4 [M H+].
Ejemplo 4 : ácido 2-(R)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino) fenilopropanoico
Etapa 1 : metil éster D-fenilalanina
Se preparó metil éster D-fenilalanina de conformidad con un procedimiento similar descrito en el Ejemplo 1, etapa 6 a partir de D-fenilalanina (1.12 g, 7 mmol). Rendimiento 650 mg (53%).
Etapa 2 : metil éster del ácido 2-(R)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)fenilopropanoico
Se preparó metil éster del ácido 2-(R)-(4-{4-[(R,S)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino) fenilopropanoico de conformidad con un procedimiento similar descrito en el Ejemplo 1, etapa 7 a partir de ácido 1-(4-{4-[1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 1, etapa 5] (58.1 mg, 0.14 mmol) y metil éster D-fenilalanina [Ejemplo 4, etapa 1] para proporcionar el producto (40 mg, 49%) que se utilizó directamente. Método 2, Rt 5.6 min. MS (ESI) m/z 562.2 [M H+].
Etapa 3: ácido 2-(R)-(4-{4-[(R,S)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino) fenilpropanoico
ácido 2-(R)-(4-{4-[(R,S)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino) fenilpropanoico se preparó de conformidad con un procedimiento similar descrito en el Ejemplo 1, etapa 8 a partir de metil éster del ácido 2-(R)-(4-{4-[(R,S)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino) fenilo propanoico [Ejemplo 4, etapa 2](40 mg, 0.07 mmol). Rendimiento 8 mg (21%).Método 2, Rt 4.94 min. MS (ESI) m/z 548.5 [M H+].
Ejemplo 5 -ácido 2(R)-[[4-[3-metil-4-((R)-1 -feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico
Etapa 1 : metil éster del ácido 2(R)-[[4-[3-metil-4-((R)-1 -feniletoxicarbonilamino)isoxazol-5-il]benzoico
Se preparó metil éster del ácido 2(R)-[[4-[3-metil-4-((R)-1-feniletoxicarbonilamino)isoxazol-5-il]benzoico de conformidad con un procedimiento similar descrito en el Ejemplo 1, etapa 4 a partir de ácido 5-(4-metoxicarbonilfenil)-3-metil-isoxazol-4-carboxílico [Ejemplo 1, etapa 3] (1.55 g, 5.9 mmol) y 1-(R)-(+)-fenil-etanol. Rendimiento 1.18 g (52%).
Etapa 2 : ácido 2(R)-[[4-[3-metil-4-((R)-1-feniletoxicarbonilamino)isoxazol-5-il] benzoico
Se preparó ácido 2(R)-[[4-[3-metil-4-((R)-1-feniletoxicarbonilamino)isoxazol-5-il]benzoico de conformidad con un procedimiento similar descrito en el Ejemplo 1, etapa 5 a partir de metil éster del ácido 2(R)-[[4-[3-metil-4-((R)-1-feniletoxicarbonilamino)isoxazol-5-il]benzoico [Ejemplo 5, etapa 1] (1.5 g, 3.62 mmol). Rendimiento 1.04 g, (91%). Método 3, Rt 2.72 min. MS (ESI) m/z 367.3 [M H+].
Etapa 3: metil éster del ácido 2(R)-[[4-[3-metil-4-((R)-1-feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-fenilpropanoico
metil éster del ácido 2(R)-[[4-[3-metil-4-((R)-1-feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico se preparó de conformidad con un procedimiento similar descrito en el Ejemplo 1, etapa 7 a partir de ácido 2(R)-[[4-[3-metil-4-((R)-1-feniletoxicarbonilamino)isoxazol-5-il]benzoico [Ejemplo 5, etapa 2] (64,7 mg, 0.18 mmol) y D-fenilalanina metil éster [Ejemplo 4, etapa 1]. Rendimiento 100 mg, 92%).
Método 3, Rt 3.04 min. MS (ESI) m/z 528.3 [M H+].
Etapa 4: ácido 2(R)-[[4-[3-metil-4-((R)-1-feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico (sal de sodio)
Se preparó ácido 2(R)-[[4-[3-metil-4-((R)-1-feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico de conformidad con un procedimiento similar descrito en el Ejemplo 1, etapa 8 a partir de metil éster del ácido 2(R)-[[4-[3-metil-4-((R)-1-feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico [Ejemplo 5, etapa 3](100 mg, 0.19 mmol). El material en bruto (21 mg) se disolvió en metanol y se trató con hidróxido de sodio 1N (40pL) antes de secarse para proporcionar el producto como su sal de sodio (22 mg, 22%). Método 3, Rt 3.04 min. MS (ESI) m/z 514.3 [M H+].
Ejemplo 6: ácido 2(S)-[[4-[3-metil-4-((R)-1 -feniletoxicarbonilamino)isoxazol-5-il]benzoil]amino]-3-fenil-propanoico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 5 a partir de 5-(4-metoxicarbonil-fenil)-3-metil-isoxazol-4-carboxílico ácido [Ejemplo 1, etapa 3] (64.7 mg, 0.18 mmol) y L-fenilalanina metil éster para proporcionar el producto como su sal de sodio (18 mg, 18%). Método 3 Rt 3.05 min. MS (ESI) m/z 514.3 [M H+].
Ejemplo 7 : ácido (R)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-fenil-propanoico
Etapa 1 : terc-butil éster del ácido 5-(4-metoxicarbonil-fenil)-1,3-dimetil-1H-pirazol-4-carboxílico y terc-butil éster del ácido 3-(4-metoxicarbonil-fenil)-1,5-dimetil-1 H-pirazol-4-carboxílico:
Se disolvió metil éster del ácido 4-(2-terc-butoxicarbonil-3-oxo-butiril)-benzoico [Ejemplo 1, Etapa 1] (en bruto 76.0 g, 208.8 mmol en 100% de pureza base) en etanol (2.2 L). Se agregó metil hidrazina (9.72 g, 210.9 mmol) a la solución anterior por goteo bajo agitación a temperatura ambiente. La mezcla de reacción se agitó otras 3 hrs a temperatura ambiente después de finalizar la adición. Se confirmó que la reacción estaba completa mediante LC/MS. El disolvente se eliminó al vacío. El residuo se disolvió en EtOAc (700 mL) y se lavó con agua (2 X 500 mL). Los extractos orgánicos se secaron Na2SO4 , se filtraron y se evaporaron. La mezcla de los productos obtenida como un aceite, que se utilizó en la siguiente etapa sin purificación adicional. Rendimiento bruto 72.6 g. Método 3, Rt 3.12 min. MS (ESI) m/z 331.0 [M H+].
Etapa 2: ácido 5-(4-metoxicarbonil-fenil)-1,3-dimetil-1H-pirazol-4-carboxílico y ácido 3-(4-metoxicarbonil-fenil)-1,5-dimetil-1 H-pirazol-4-carboxílico :
Una mezcla de terc-butil éster del ácido 5-(4-metoxicarbonil-fenil)-1,3-dimetil-1H-pirazol-4-carboxílico y terc-butil éster del ácido 3-(4-metoxicarbonil-fenil)-1,5-dimetil-1H-pirazol-4-carboxílico [Ejemplo 7, Etapa 1] (5.00 g., 15.13 mmol) se disolvió en CH2Cl2 (120.0 mL) y ácido trifluoroacético (40.0 mL) se agregó y la mezcla de reacción se agitó durante 3 h a temperatura ambiente. Los extractos volátiles se eliminaron al vacío. El residuo se disolvió en acetato de etilo (50.0 mL). Se extrajo con una solución saturada ac. de Na2CO3 (40 mL). Se separó la capa acuosa que se lavó con acetato de etilo (2x20 mL). Posteriormente se trató con HCl 1 M hasta un pH de 2. Posteriormente se extrajo con acetato de etilo (2x35 mL), se secó (Na2SO4), se filtró y se concentró para proporcionar sólido blanco mezcla de ácidos (3.0 g., 72%). TLC en plato de sílice (15% de acetona en DCM): dos puntos fluorescentes de dos Isómeros Rf: 0.2 y Rf: 0.125. Método 3, Rt 2.94 min. MS (ESI) m /z 275.0 [M H+];
Etapa 3 : metil éster del ácido 4-[2,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoico y metil éster del ácido 4-[1,5-dimetil-4-((R)-1 -fenil-etoxicarbonilamino)-1 H-pirazol-3-il]-benzoico:
La mezcla de ácido Isómeros [Ejemplo 7, Etapa 2] (6.0 g., 21. 88 mmol), se suspendió en tolueno anhidro (180.0 mL), bajo nitrógeno y se agitó. Posteriormente se agregó diisopropiletilo amina (3.39 g., 26.24 mmol). Una solución transparente se generó al que se agregó difenil fosforil azida 7.22 g, 26.24 mmol). La mezcla de reacción se calentó hasta 950 C. Posteriormente se agregó por goteo (R)-(+)-1 -feniletil alcohol (4.008 g, 32.8 mmol) a 950 C durante un periodo de 40 minutos. Posteriormente la mezcla de reacción se calentó durante otras 5 hr adicionales a 950 C, seguido por agitación a temperatura ambiente durante la noche. Al siguiente día se diluyó con EtOAc (300 mL), se lavó con una solución sat. ac. de Na2CO3 (200.0 mL) y agua (2x500 mL), se secó (Na2SO4), se filtró y se concentró para proporcionar carbamato en bruto aceitoso (12.5 g). El producto bruto se purificó mediante cromatografía en columna (SO 2), elución inicial con DCM (250 mL) y posteriormente gradiente de elución Acetona:DCM (2% de acetona en DCM a 10% de acetona en DCM). Se obtuvieron dos isómeros puros. Se obtuvieron un isómero de movimiento rápido (1.667 g, 19.4%) y un isómero de movimiento lento (2.132 g, 24.77%) [> 95% de pureza mediante HPLC]. Se obtuvo una fracción que contenía una mezcla de isómeros (0.812 g, 9.4%). A) Punto de movimiento lento: Método 3, Rt 2.78 min. MS (ESI) m/z 394.2 [M H+]; asignado tentativamente como metil éster del ácido (R)-4-[1,5-dimetil-4-(1-fenil-etoxicarbonilamino)-1H-pirazol-3-il]-benzoico. B) Punto de movimiento rápido: Método 3, Rt 2.80 min. MS (ESI) m/z 394.4 [M H+]; asignado tentativamente como metil éster del ácido (R)-4-[2,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoico.
Etapa 4 : ácido 4-[2,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoico:
Se disolvió metil éster del ácido 4-[2,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoico [Ejemplo 7, Etapa 3B] (240 mg, 0.61 mmol) en THF/agua (2/1 v/v, 2.25 mL) y se trató con LíOh (1.2 mL de una solución 1M acuosa, 2 eq.). La mezcla resultante se agitó a temperatura ambiente durante la noche. La reacción se acidificó hasta un pH de2, se diluyó con agua y se extrajo con EtOAc (2 X 40 mL). La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar el producto (180 mg, 78%). Método 3, Rt 2.81 min. MS (ESI) m/z 380.2 [M H+].
Etapa 5 : metil éster del ácido (R)-2-{4-[2,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoilamino}-3-fenil-propiónico:
A ácido 4-[2,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoico [Ejemplo 7, etapa 4] (100 mg, 0.26 mmol) se agregó 1-hidroxibenzotriazolo (43 mg, 0.32 mmol), EDCI (67 mg, 0.34 mmol), dimetilformamida (2 mL), diisopropiletilamina (184 pL, 1.06 mmol), y D-fenilalanina metil éster [Ejemplo 4, Etapa 1] ( 86 mg, 0.39 mmol) y esta mezcla se agitó durante la noche. En este momento la mezcla se diluyó con acetato de etilo (20 mL) y se lavó con una solución de hidróxido de sodio 1N (10 mL), y agua. La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar el producto en bruto (193 mg), que se purificó mediante cromatografía de gel de sílice, eluyendo con un acetato de gradiente de etilo/diclorometano para proporcionar el compuesto del título (95 mg, 6 8 %). > 95% de pureza mediante HPLC. Método 3, Rt 2.91 min. m S (ESI) m/z 541.3 [M H+].
Etapa 6 : ácido (R)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-fenil-propanoico:
Se disolvió metil éster del ácido (R)-2-{4-[2,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoilamino}-3-fenil-propiónico [Ejemplo 7, etapa 5] (95 mg, 0.176 mmol) en una mezcla 2:1 de THF/agua (2.25 mL) y se trató con una solución 1M de hidróxido de litio (2 mL). La mezcla resultante se agitó a temperatura ambiente durante la
noche. El pH de la capa acuosa se ajustó a 2 con ácido clorhídrico y la mezcla se extrajo con acetato de etilo (3x20 mL). La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar el producto en bruto (112 mg). El material en bruto se purificó mediante cromatografía de gel de sílice, eluyendo con un gradiente de diclorometano/acetona. (90 mg, 97%). Método 3, Rt 2.90 min. MS (ESI) m/z 527.5 [M H+].
Ejemplo 8 : ácido (R)-2-[[4-[1,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-fenil-propanoico
Etapa 1 : ácido 4-[1,5-dimetil-4-((R)-1 -fenil-etoxicarbonilamino)-1 H-pirazol-3-il]-benzoico:
Se disolvió metil éster ácido 4-[1,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-1H-pirazol-3-il]-benzoico [Ejemplo 7, Etapa 3A] (240 mg, 0.61 mmol) en THF/agua (2/1 v/v, 2.25 mL) y se trató con LiOH (1.2 mL de una solución 1M acuosa, 2 eq.). La mezcla resultante se agitó a temperatura ambiente durante la noche. La reacción se acidificó hasta un pH de 2, se transfirió a un embudo separador, se diluyó con agua y se extrajo con EtOAc (2 X 40 mL). La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar el producto (205 mg, 89%). La pureza resultó de un 97% mediante HPLC. Método 3, Rt 2.43 min. MS (eS i) m/z 380.2 [M H+].
Etapa 2 : metil éster del ácido (R)-2-{4-[1,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-1H-pirazol-3-il]-benzoilamino}-3-fenil-propiónico:
Se agregó ácido 4-[1,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-1H-pirazol-3-il]-benzoico [Ejemplo 8 , Etapa 1] (100 mg, 0.26 mmol) 1-hidroxibenzotriazolo (43 mg, 0.32 mmol), EDCI (67 mg, 0.34 mmol), dimetilformamida (2 mL), diisopropiletilamina (184 pL, 1.06 mmol), y D-fenilalanina metil éster [Ejemplo 4, Etapa 1] ( 86 mg, 0.39 mmol) y esta mezcla se agitó durante la noche. En este momento la mezcla se diluyó con acetato de etilo (20 mL) y se lavó con una solución de hidróxido de sodio 1N (10 mL), y agua. La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar el producto en bruto (150 mg) que se purificó mediante cromatografía de gel de sílice, eluyendo con a acetato de gradiente de etilo/diclorometano para proporcionar el producto (75 mg, 53%). De pureza > 97% mediante HPLC. Método 3, Rt 3.05 min. MS (ESI) m/z 541.2 [M H+].
Etapa 3 : ácido (R)-2-[[4-[1,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-fenil-propanoico:
Se disolvió metil éster del ácido (R)-2-{4-[1,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-1H-pirazol-3-il]-benzoilamino}-3-fenil-propiónico [Ejemplo 8 , etapa 2] (75 mg, 0.139 mmol) en una mezcla 2:1 de THF/agua (1.5 mL) y se trató con una solución 1M de hidróxido de litio (0.28 mL). La mezcla resultante se agitó a temperatura ambiente durante la noche. El pH de la capa acuosa se ajustó a 2 con ácido clorhídrico y la mezcla se extrajo con acetato de etilo (3x20 mL). La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar el producto [>95% HPLC de pureza] (60 mg, 82%). Método 3, Rt 2.69 min. MS (ESI) m /z 527.5 [M H+].
Ejemplo 9: ácido (R)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-fluorofenil)propanoico
Etapa 1 : Hidrocloruro de metil éster del ácido (R)-2-amino-3-(4-fluoro-fenil)-propiónico:
Se preparó hidrocloruro de metil éster del ácido (R)-2-amino-3-(4-fluoro-fenil)-propiónico de conformidad con un procedimiento similar descrito en el Ejemplo 1, etapa 6 a partir de D-4-fluorofenil alanina (1 g, 5.46 mmol). Rendimiento 900 mg, (71%). Método 3, Rt 0.54 min. m S (ESI) m/z 198.3 [M H+].
Etapa 2 : metil éster del ácido (R)-2-{4-[2,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoilamino}-3-(4-fluoro-fenil)-propiónico:
Se preparó metil éster del ácido (R)-2-{4-[2,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoilamino}-3-(4-fluoro-fenil)-propiónico de conformidad con un procedimiento similar descrito en el Ejemplo 7, etapa 5 a partir de ácido (R)-4-[2,5-dimetil-4-(1-fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoico [Ejemplo 7, Etapa 4] (50 mg, 0.132 mmol) e hidrocloruro de metil éster del ácido (R)-2-amino-3-(4-fluoro-fenil)-propiónico [Ejemplo 9, Etapa 1]. Rendimiento 59 mg (80%).
Etapa 3 : ácido (R)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-fluorofenil)propanoico:
Se preparó ácido (R)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-fluorofenil)propanoico de conformidad con un procedimiento similar descrito en el Ejemplo 7, etapa 6 a partir de metil éster del ácido (R)-2-{4-[2,5-dimetil-4-((R)-1 -fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoilamino}-3-(4-fluoro-fenil)-propiónico [Ejemplo 9, Etapa 2] (59 mg, 0.11 mmol) para proporcionar el producto 55 mg (87%). Método 3, Rt 2.73 min. MS (ESI) m/z 545.4 [M H+].
Ejemplo 10: ácido (R)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonilamino)pirazol-3-il]benzoil]amino]-3-(4-fluorofenil)propanoico. El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 8 a partir de ácido 4-[1,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-1H-pirazol-3-il]-benzoico [Ejemplo 8 , Etapa 1] (50 mg, 0.132 mmol) e hidrocloruro de metil éster del ácido (R)-2-amino-3-(4-fluoro-fenil)-propiónico [Ejemplo 9, Etapa 1]. Rendimiento 55 mg, (87%). Método 3, Rt 2.69 min. MS (ESI) m/z 545.4 [M H+].
Ejemplo 11: ácido (R)-3-(4-bromofenil)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico
Etapa 1 : hidrocloruro de metil éster del ácido (R)-2-amino-3-(4-bromo-fenil)-propiónico:
El compuesto del título se preparó utilizando un procedimiento similar al que se describe en el Ejemplo 1, etapa 6 a partir de D-4-bromofenil alanina (1 g, 4.1 mmol). Rendimiento 550 mg (4 6 %). Método 3, Rt 1.70 min. MS (ESI) m/z 258.1 [M H+].
Etapa 2 : ácido (R)-3-(4-bromofenil)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)-pirazol-3-il]benzoil]amino]propanoico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 9 (etapas 2 & 3) a partir de ácido 4-[2,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoico [Ejemplo 7, Etapa 4] e hidrocloruro de metil éster del ácido (R)-2-amino-3-(4-bromo-fenil)-propiónico [Ejemplo 1 1 , Etapa 1 ]. Rendimiento 30 mg (65%). Método 3, Rt 3.03 min. MS (ESI) m/z 607.4 [M H+].
Ejemplo 12: ácido (R)-3-(4-bromofenil)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico. El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 8 a partir de ácido 4-[1,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-1H-pirazol-3-il]-benzoico [Ejemplo 8 , Etapa 1] (50 mg, 0.132 mmol) y hidrocloruro de metil éster del ácido 3-(4-bromo-fenil)-propiónico [Ejemplo 11, Etapa 1]. Rendimiento 60 mg, (80%). Método 3, Rt 3.02 min. MS (ESI) m /z 619.2 [M H+].
Ejemplo 13: ácido (R)-3-(4-clorofenil)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico
Etapa 1 : hidrocloruro de metil éster del ácido (R)-2-amino-3-(4-cloro-fenil)-propiónico:
Se preparó hidrocloruro de metil éster del ácido (R)-2-amino-3-(4-cloro-fenil)-propiónico utilizando un procedimiento similar al que se describe en el Ejemplo 1, etapa 6 a partir de D-4-clorofenil alanina (1 g, 5 mmol). Rendimiento 940 mg (75%). Método 3, Rt 0.03 min. MS (ESI) m/z 214.0 [M H+].
Etapa 2 : ácido (R,R)-3-(4-clorofenil)-2-[[4-[2,5-dimetil-4-(1 -feniletoxicarbonilamino)-pirazol-3-il]benzoil]amino]propanoico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 9 (etapas 2 & 3) a partir de ácido (R)-4-[2,5-dimetil-4-(1-fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoico [Ejemplo 7, Etapa 4] e hidrocloruro de metil éster del ácido (R)-2-amino-3-(4-cloro-fenil)-propiónico [Ejemplo 13, Etapa 1 ]. Rendimiento 40 mg (55%). Método 3, Rt 2.80 min. m S (ESI) m/z 561.3 [M H+].
Ejemplo 14: ácido (R)-3-(4-clorofenil)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 8 a partir de ácido 4-[1,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-1H-pirazol-3-il]-benzoico [Ejemplo 8 , Etapa 1] e hidrocloruro de metil éster del ácido (R)-2-amino-3-(4-cloro-fenil)-propiónico [Ejemplo 8 , Etapa 1 ]. Rendimiento 40 mg (54%) Método 3, Rt 3.00 min. MS (eS i) m/z 561.3 [M H+].
Ejemplo 15: ácido (R)-3-(3,4-difluorofenil)-2-[[4-[2,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico
Etapa 1 : hidrocloruro de metil éster del ácido (R)-2-amino-3-(3,4-difluoro-fenil)-propiónico:
Se preparó hidrocloruro de metil éster del ácido (R)-2-amino-3-(3,4-difluoro-fenil)-propiónico utilizando un procedimiento similar al que se describe en el Ejemplo 1, etapa 6 a partir de D-3,4-difluorofenil alanina (1 g, 4.97 mmol). Rendimiento 1.04 g, 83%). Método 3, Rt 0.16 min. MS (ESI) m/z 216.0 [M H+];
Etapa 2 : ácido (R)-3-(3,4-difluorofenil)-2-[[4-[2,5-dimetil-4-((R)-1 -feniletoxicarbonilamino)-pirazol-3-il]benzoil]amino]propanoico:
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 9 (etapas 2 & 3) a partir de ácido (R)-4-[2,5-dimetil-4-(1-fenil-etoxicarbonilamino)-2H-pirazol-3-il]-benzoico [Ejemplo 7, Etapa 4] (50 mg, 0.132 mmol) e hidrocloruro de metil éster del ácido (R)-2-amino-3-(3,4-difluoro-fenil)-propiónico [Ejemplo 15, Etapa 1]. Rendimiento 30 mg (61%). Método 3, Rt 2.96 min. m S (ESI) m/z 563.4 [M H+].
Ejemplo 16: ácido (R)-3-(3,4-difluorofenil)-2-[[4-[1,5-dimetil-4-((R)-1-feniletoxicarbonil-amino)pirazol-3-il]benzoil]amino]propanoico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 8 a partir de ácido 4-[1,5-dimetil-4-((R)-1-fenil-etoxicarbonilamino)-1H-pirazol-3-il]-benzoico [Ejemplo 8 , Etapa 1] (50 mg, 0.132 mmol) e hidrocloruro de metil éster del ácido (R)-2-amino-3-(3,4-difluoro-fenil)-propiónico [Ejemplo 15, Etapa 1]. Rendimiento 20 mg (56%). Método 3, Rt 2.71 min. Ms (ESI) m/z 563.3 [M H+].
Ejemplo 17: ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-ciclopropil-propiónico
Etapa 1: hidrocloruro de metil éster del ácido (R)-2-amino-3-ciclopropilpropiónico:
Se preparó hidrocloruro de metil éster del ácido (R)-2-amino-3-ciclopropilpropiónico utilizando un procedimiento similar al que se describe en el Ejemplo 1, etapa 6 a partir de ácido (R)-2-amino-3-ciclopropilpropiónico y se utilizó directamente. Rendimiento 350 mg (100%).
Etapa 2: metil éster del ácido 4-{4-[1-((R)-2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico
Se preparó de manera análoga a la del Ejemplo 5 Etapa 1 utilizando ácido 5-(4-metoxicarbonil-fenil)-3-metil-isoxazol-4-carboxílico [Ejemplo 1, etapa 3] (3.47 g, 13.28 mmol) y (R)-1-(2-clorofenil)-etanol. Rendimiento = 1.81 g (4.36 mmol, 25%). Hp LC (254 nm): Método 3 Rt 3.31 min. MS (ESI) m/z 415.5 [M H+].
Etapa 3: ácido 4-{4-[1-((R-2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico
Se preparó de manera análoga a la del Ejemplo 5, Etapa 2 utilizando metil éster del ácido 4-{4-[1-((R)-2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 17, etapa 2](1.81 g, 4.46 mmol). Rendimiento = 1.70 g (4.25 mmol, 95%). HPLC (254 nm): Método 3 Rt 3.01 min. MS (ESI) m/z 401.2 [M H+].
Etapa 4: ácido (R)-2-(4-{4-[1 -((R)-2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-ciclopropilpropiónico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 5 a partir de ácido 4-{4-[1-((R)-2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 17, etapa 3] (50 mg, 0.13 mmol) y hidrocloruro de metil éster del ácido (R)-2-amino-3-ciclopropilpropiónico [Ejemplo 17, etapa 1 ]. Rendimiento 22 mg (34%). Método 3, Rt 3.27min. MS (ESI) m/z 512.5 [M H+].
Ejemplo 18: ácido (R)-2-{4-[3-metil-4-((S)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benzoilamino}-3-fenil-propiónico Etapa 1: ácido 4-[3-metil-4-((S)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benzoico
Se preparó ácido 4-[3-metil-4-((S)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benzoico de una manera análoga a la del Ejemplo 17 [etapas & 3] a partir de ácido 5-(4-metoxicarbonil-fenil)-3-metil-isoxazol-4-carboxílico [Ejemplo 1, etapa 3] (1 g, 3.3 mmol) y (S)-1-(2-clorofenil)-etanol. Rendimiento = 800 mg (2.19 mmol, 60%). HPLC (254 nm): Método 3 Rt 2.67 min. MS (ESI) m/z 367.4 [M H+].
Etapa 2 : ácido (S,R)-2-{4-[3-metil-4-(1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benzoilamino}-3-fenil-propiónico El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 5 a partir de ácido (S)-4-[3-metil-4-(1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benzoico [Ejemplo 18, etapa 2] (61 mg, 0.12 mmol) e hidrocloruro de metil éster D-fenilalanina. Rendimiento = 30 mg (0.06 mmol, 49%). HPLC (254 nm): Método 3 Rt 3.05 min. MS (ESI) m/z 514.5 [M H+].
Ejemplo 19: ácido (S)-2-{4-[3-metil-4-((S)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benzoilamino}-3-fenil-propiónico El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 18 a partir de ácido 4-[3-metil-4-((S)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benzoico [Ejemplo 18, etapa 2] (61 mg, 0.12 mmol) e hidrocloruro de metil éster de L-fenilalanina. Rendimiento = 22 mg (0.04 mmol, 36%). HPLC (254 nm): Método 3 Rt 2.87 min. MS (ESI) m/z 514.5 [M H+].
Ejemplo 20: ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-fenilpropiónico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 17 a partir de ácido 4-{4-[1-((R)-2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 17, etapa 3] (60 mg, 0.15 mmol) y D-fenilalanina metil éster. Rendimiento = 65 mg (0.12 mmol, 77%). HPLC (254 nm): Método 3 Rt 2.93 min. MS (ESI) m/z 566.3 [M H+].
Ejemplo 21: ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-fluoro-fenil)-propiónico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 17 a partir de ácido 4-{4-[1-((R)-2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 17, etapa 3] (60
mg, 0.15 mmol) y D-4-fluorofenilalanina metil éster. Rendimiento = 65 mg (0.12 mmol, 77%). HPLC (254 nm): Método 3 Rt 2.93 min. MS (ESI) m/z 566.3 [M H+].
Ejemplo 22 ácido (R)-3-(4-cloro-fenil)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 17 a partir de ácido 4-{4-[1-((R)-2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 17, etapa 3] (60 mg, 0.15 mmol) y D-4-clorofenilalanina metil éster. Rendimiento = 64 mg (0.11 mmol, 74%). HPLC (254 nm): Método 3 Rt 3.11 min. MS (ESI) m/z 583.4 [M H+].
Ejemplo 23: ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(3,4-difluoro-fenil)-propiónico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 17 a partir de ácido 4-{4-[1-((R)-2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 17, etapa 3] (60 mg, 0.15 mmol) e hidrocloruro de metil éster D-3,4-difluorofenilalanina. Rendimiento = 41 mg (0.07 mmol, 47%). HPLC (254 nm): Método 3 Rt 2.96 min. MS (ESI) m/z 584.1 [M H+].
Ejemplo 24 : ácido (R)-3-(2-cloro-fenil)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 17 a partir de ácido 4-{4-[1-((R)-2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 17, etapa 3] (60 mg, 0.15 mmol) e hidrocloruro de metil éster D-2-clorofenilalanina. Rendimiento = 41 mg (0.07 mmol, 47%). HPLC (254 nm): Método 3 Rt 3.06 min. MS (ESI) m/z 584.2 [M H+].
Ejemplo 25 : ácido (R)-3-(4-bromo-fenil)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-propiónico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 17 a partir de ácido 4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 17, etapa 3] (60 mg, 0.15 mmol) e hidrocloruro de metil éster D-4-bromofenilalanina. Rendimiento = 65 mg (0.10 mmol, 35%). HPLC (254 nm): Método 3 Rt 3.28 min. MS (ESI) m/z 626.3, 628.4 [M H+].
Ejemplo 26 : ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(2-fluoro-fenil)-propiónico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 17 a partir de ácido 4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 17, etapa 3] (60 mg, 0.15 mmol) e hidrocloruro de metil éster D-2-fluorofenilalanina. Rendimiento = 70 mg (0.12 mmol, 52%). HPLC (254 nm): Método 3 Rt 3.12 min. MS (ESI) m/z 566.5, 567.8 [M H+].
Ejemplo 27 : ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-p-tolilpropiónico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 17 a partir de ácido 4-{4-[(R)-1-(4-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 17, etapa 3] (60 mg, 0.15 mmol) e hidrocloruro de metil éster D-4-metilfenilalanina. Rendimiento = 37 mg (0.07 mmol, 43%). HPLC (254 nm): Método 3 Rt 3.13 min. MS (ESI) m/z 562.3 [M H+].
Ejemplo 28 : ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-trifluorometil-fenil)-propiónico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 17 a partir de ácido 4-{4-[(R)-1-(4-bromo-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 17, etapa 3] (60 mg, 0.15 mmol) e hidrocloruro de metil éster D-4-trifluorometilfenilalanina. Rendimiento = 40 mg (0.06 mmol, 44%). HPLC (254 nm): Método 3 Rt 3.00 min. MS (ESI) m/z 616.2 [M H+].
Ejemplo 29 : ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoilamino)-3-(4-ciano-fenil)-propiónico
El compuesto del título se preparó de conformidad con el procedimiento análogo que se describe en el Ejemplo 17 a partir de ácido 4-{4-[(R)-1-(4-bromo-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-benzoico [Ejemplo 17, etapa 3] (60 mg, 0.15 mmol) e hidrocloruro de metil éster D-4-cianofenilalanina. Rendimiento = 17 mg (0.03 mmol, 20%). HPLC (254 nm): Método 3 Rt 2.93 min. MS (ESI) m/z 573.2 [M H+].
Ejemplo 30: ácido (R)-2-(4-{5-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-4-metil-pirazol-1 -il}-benzoilamino)-3-fenilpropiónico Etapa 1 : etil éster del ácido 2-(4-ciano-fenil)-4-metil-2H-pirazol-3-carboxílico
Una solución de triclorocloruro de acetilo (12.92 mL, 115.8 mmol) en diclorometano (30 mL) se enfrió a -10 oC bajo una atmósfera de nitrógeno. Una solución de etil propenil éter (12.82 mL, 115.8 mmol) y piridina (9.36 mL, 115.8 mmol) se agregó por goteo a una tasa tal que mantuvo la temperatura a -10 oC. Después de completarse la adición, la reacción se calentó a temperatura ambiente y se agitó durante 24 horas. La mezcla se filtró y los sólidos se lavó con diclorometano (50 mL). El filtrados se evaporaron a sequedad al vacío para proporcionar un aceite (31.71 g). Este material se disolvió en etanol (400 mL) y se trató con hidrocloruro de 4-cianofenilhidrazina (24.81 g, 139 mmol). La mezcla resultante se sometió a reflujo durante 3 horas y posteriormente se enfrió a temperatura ambiente. Los extractos volátiles se evaporaron al vacío, el residuo se disolvió en EtOAc (1 L) y se lavó con una solución acuosa de HCl 1N (2 X 300 mL). La capa orgánica se separó, se lavó con agua, se secó sobre Na2SO4 anhidro, se filtró y se concentró al vacío para obtener un sólido amarillo (27.8 g). Esto se trituró con EtOAc (130 mL) y los sólidos restantes se eliminaron por filtración (no contiene producto). Los filtrados se concentraron a 50 mL de volumen y los sólido precipitados se filtraron (no contiene producto). Los filtrados se concentraron y se purificó mediante cromatografía de gel de sílice, eluyendo con un gradiente de 100/0 a 88/12 hexanos/acetona. Las fracciones que se recogieron contenían una mezcla de los dos productos isómeroicos, que se concentraron a sequedad y se trituraron con metanol para proporcionar el isómero deseado [etil éster del ácido 2-(4-ciano-fenil)-4-metil-2H-pirazol-3-carboxílico] como un sólido amarillo (3.77 g, 14.8 mmol, 13%). HPLC (254 nm): Método 3 Rt 2.93 min. MS (ESI) m/z 256.3 [M H+]. 1H NMR (500 MHz, CDCb) 57.73 (d, J = 8.5 Hz, 2 H); 7.58 (s, 1 H); 7.52 (d, J = 8.5 Hz, 2 H); 4.27 (q, J = 7.1 Hz, 2 H); 2.35 (s, 3 H); 1.26 (t, J = 7.1 Hz, 3 H).
Etapa 2 : ácido 2-(4-ciano-fenil)-4-metil-2H-pirazol-3-carboxílico
a una solución agitada de etil éster del ácido 2-(4-ciano-fenil)-4-metil-2H-pirazol-3-carboxílico [Ejemplo 30, etapa 1](500 mg, 1.96 mmol) en THF (10 mL) se trató con una solución acuosa de LiOH 1N (10 mL) y la mezcla resultante se agitó a temperatura ambiente durante 6 horas, después de dicho tiempo el análisis mediante HPLC/MS indicó aproximadamente un 60% de conversión a producto. La mezcla de reacción se diluyó con acetato de etilo (100 mL) y se lavó con una solución 1N acuosa de NaOH (100 mL). La capa orgánica contenía material de partida sin reaccionar. La capa acuosa se acidificó hasta un pH de 1 con una solución acuosa de HCl 1N y la suspensión resultante se extrajo con acetato de etilo (100 mL). La capa orgánica se separó, se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar el producto puro como un sólido blanco (289 mg, 1.27 mmol, 65%). HPLC (254 nm): Método 3 Rt 2.56 min. MS (ESI) m /z 228.3 [M H+].
Etapa 3 : etil éster del ácido [2-(4-ciano-fenil)-4-metil-2H-pirazol-3-il]-carbámico (R)-1-(2-cloro-fenil)-
Se suspendió ácido 2-(4-ciano-fenil)-4-metil-2H-pirazol-3-carboxílico [Ejemplo 30, etapa 2] (218 mg, 0.96 mmol) en tolueno (10 mL) y se trató con diisopropiletilamina (200 pL, 1.16 mmol). La solución resultante se trató con difenilfosforil azida (230 pL, 1.06 mmol) y calentó hasta 65 oC. Se agregó (R)-1-(2-cloro-fenil)-etanol (227 mg, 1.44 mmol) a la mezcla de reacción y la temperatura se incrementó a 105 oC durante 30 minutos, Durante dicho tiempo se observó una vigorosa evolución gaseosa. La reacción se llevó a 65 oC y se agitó a esa temperatura durante 4 horas. La reacción se consideró completa mediante HPLC/MS. Luego de enfriar, los extractos se eliminaron los volátiles al vacío y el residuo en bruto se purificó mediante cromatografía de gel de sílice, eluyendo con un gradiente de hexanos/acetato de etilo. El producto se aisló como un sólido blanco (120 mg, 0.31 mmol, 33%). HPLC (254 nm): Método 3 Rt 3.84 min. MS (ESI) m/z 381.2 [M H+].
Etapa 4 : ácido 4-{5-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-4-metil-pirazol-1-il}- benzoico
Una solución que contenía 1-(2-cloro-fenil)-etil éster del ácido (R)-[2-(4-ciano-fenil)-4-metil-2H-pirazol-3-il]-carbámico (120 mg, 0.32 mmol) y THF (1.5 mL) se trató con una solución acuosa de LiOH 1N (1.5 mL) y la mezcla resultante se agitó a temperatura ambiente durante 36 horas, seguido por calentamiento a 45 oC durante 24 horas. La mezcla de reacción se diluyó con acetato de etilo (50 mL) y se lavó con una solución 1N acuosa de NaOH (50 mL). La capa acuosa se acidificó hasta un pH de 1 con una solución acuosa de HCl 1N y la suspensión resultante se extrajo con acetato de etilo (50 mL). La capa orgánica se separó, se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar el producto puro como un sólido blanco. Rendimiento = 62 mg (0.16 mmol, 49%). HPLC (254 nm): Método 3 Rt 3.14 min. MS (ESI) m/z 399.2 [M H+].
Etapa 3 : metil éster del ácido (R)-2-(4-{5-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-4-metil-pirazol-1-il}-benzoilamino)-3-fenil-propiónico
Se disolvió ácido 4-{5-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-4-metil-pirazol-1-il}-benzoico (62 mg, 0.16 mmol), en DMF (1.4 mL) y se trató con di-isopropiletilamina (112 pL, 0.62 mmol) bajo nitrógeno. Se agregó EDCI (40 mg, 0.20 mmol) y HOBt (26 mg, 0.19 mmol) y la mezcla resultante se agitó durante 30 minutos. Se agregó hidrocloruro de metil éster de D-fenilalanina (50 mg, 0.23 mmol) y la mezcla resultante se agitó a temperatura ambiente durante la noche. La reacción se diluyó con EtOAc (50 mL) y se transfirió a un embudo separador. Los extractos orgánicos se lavaron con una solución acuosa de HCl 1N y salmuera, se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío. El residuo en bruto se purificó mediante plato TLC preparativa (1000 pm), eluyendo con a 7:3 v/v hexanos/acetato de etilo mezcla. El producto se obtuvo como un sólido blanco. Rendimiento = 35 mg (0.06 mmol, 39%). HPLC (254 nm): Método 3 Rt 3.28 min. MS (ESI) m/z 561.3, 563.3 [M H+].
Etapa 4 : ácido (R)-2-(4-{5-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-4-metil-pirazol-1 -il}-benzoilamino)-3-fenilpropiónico
Una solución que contenía metil éster del ácido (R)-2-(4-{5-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-4-metil-pirazol-1-il}-benzoilamino)-3-fenil-propiónico (35 mg, 0.06 mmol), y THF (1 mL) se trató con una solución acuosa de LiOH 1N (125 pL) y la mezcla resultante se agitó a temperatura ambiente durante 18 horas. La mezcla de reacción se diluyó con acetato de etilo (50 mL) y se acidificó hasta un pH de 1 con una solución acuosa de HCl 1N. La capa orgánica se separó, se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar el producto puro como un sólido blanco. Rendimiento = 20 mg (0.04 mmol, 61%). HPLC (254 nm): Método 3 Rt 3.19 min. MS (ESI) m/z 547.6, 550.6 [M H+].
Ejemplo 31 : ácido (R)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-3-fenil-propiónico
Etapa 1 : terc-butil éster del ácido 5-(4-clorometil-fenil)-3-metil-isoxazol-4-carboxílico
Una suspensión agitada de MgCl2 (2.97 g, 31.2 mmol) en diclorometano (30 mL) bajo nitrógeno se trató por goteo con acetoacetato de terc-butilo (5.17 mL, 31.2 mmol) y la mezcla resultante se enfrió a 0 oC. La mezcla se agitó a esa temperatura durante 15 minutos y posteriormente se trató con la adición por goteo de piridina (4.85 mL, 60.0 mmol). Después de 15 minutos, se agregó por goteo una solución de cloruro de 4-(clorometil)benzoilo (5.67 g, 30.0 mmol) en diclorometano (30 mL). La mezcla resultante se mantuvo a 0 oC durante 1 hora y a temperatura ambiente durante una hora adicional. La reacción se inactivó con adición cuidadosa de agua ( 1 00 mL) y la mezcla se transfirió a un embudo separador. La capa orgánica se lavó con una solución acuosa de HCl 1N (2 X 100 mL) y posteriormente se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío. El residuo en bruto se disolvió en etanol (60 mL) y se trató con una solución de NH2OH.HCl (6.67 g, 96.0 mmol) en agua (13 mL). Esta mezcla se calentó hasta 60 oC durante 2 horas y a temperatura ambiente durante la noche. Un precipitado blanco espeso se formó que se filtró, se lavó con etanol y se secó al aire. EL licor madre se concentró y se enfrió a 0 oC para proporcionar una segunda partida del sólido que se filtró y se secó al aire. Rendimiento combinado = 5.82 g (19.0 mmol, 63%). HPLC (254 nm): Método 3 Rt 3.49 min. MS (ESI) m/z 308.4 [M H+].
Etapa 2 : ácido 5-(4-clorometil-fenil)-3-metil-isoxazol-4-carboxílico
Se disolvió terc-butil éster del ácido 5-(4-clorometil-fenil)-3-metil-isoxazol-4-carboxílico (4.61 g, 15.0 mmol) en diclorometano (7.5 mL) y se trató con ácido trifluoroacético (7.5 mL). La mezcla resultante se agitó a temperatura ambiente durante 18 horas, después de dicho tiempo la reacción se consideró completa mediante HPLC/MS. Se eliminaron los extractos volátiles al vacío para proporcionar el producto en bruto como un sólido blanco (3.8 g, 15.0 mmol, cuant.), que se utilizó como tal en la siguiente etapa.
Etapa 3 : (R)-1 -fenil-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico
Se suspendió ácido 5-(4-clorometil-fenil)-3-metil-isoxazol-4-carboxílico (3.0 g, 12.0 mmol) en tolueno (120 mL) y se trató con trietilamina (2.02 mL, 14.4 mmol). La solución resultante se trató con difenilfosforil azida (2.85 mL, 13.2 mmol) y se calentó hasta 65 oC. Se agregó (R)-1-(fenil)-etanol (1.9 g, 15.6 mmol) a la mezcla de reacción y la temperatura se incrementó a 105 oC durante 30 minutos, durante dicho tiempo se observó una vigorosa evolución gaseosa. La reacción se llevó a 65 oC y se agitó a esa temperatura durante 4 horas. La reacción se consideró completa mediante HPLC/MS. Luego de enfriar, los extractos se eliminaron los volátiles al vacío y el residuo en bruto se purificó mediante cromatografía de gel de sílice, eluyendo con un gradiente de hexanos/acetato de etilo. El producto se aisló como un sólido blanco (3.16 g, 8.52 mmol, 71%). HPLC (254 nm): Método 3 Rt 3.02 min. MS (ESI) m/z 371.2 [M H+].
Etapa 4 : metil éster del ácido (R)-2-{4-[3-metil-4-((R-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-3-fenilpropiónico
Una solución que contenía (R)-1 -fenil-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico (74 mg, 0.2 mmol), DMF (2 mL) y trietilamina (224 pL, 1.6 mmol) se trató con hidrocloruro de metil éster de D-fenilalanina (173 mg, 0.80 mmol) y calentó hasta 80 oC durante 3 horas. La reacción se consideró completa mediante HPLC/MS. La reacción se enfrió, se repartió entre EtOAc y agua y se transfirió a un embudo separador. La capa orgánica se lavó con agua y salmuera, se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío. El residuo de aceite amarillento en bruto se purificó mediante cromatografía de gel de sílice eluyendo con un gradiente de hexanos/EtOAc. El producto se obtuvo como una película incolora (77 mg, 0.15 mmol, 75%). HPLC (254 nm): Método 3 Rt 2.67 min. MS (ESI) m/z 514.4 [M H+].
Etapa 5 : ácido (R)-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-3-fenil-propiónico
Una solución que contenía metil éster del ácido (R)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-3-fenil-propiónico (77 mg, 0.15 mmol) y THF (1.5 mL) se trató con una solución acuosa de LiOH 1N (1.5 mL) y la mezcla resultante se agitó a temperatura ambiente durante 18 horas. La mezcla de reacción se diluyó con acetato de etilo (50 mL) y se acidificó hasta un pH de ~ 5 con una solución acuosa de HCl 1N. La capa orgánica se separó, se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío. El residuo se trituró con dietil éter para
proporcionar el producto puro como un sólido blanco (9 mg, 0.018 mmol, 12%). HPLC (254 nm): Método 3 Rt 2.74 min. MS (ESI) m/z 500.5 [M H+].
Ejemplo 32 : ácido (R)-3-(2-fluoro-fenil)-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico
El compuesto del título se preparó de manera análoga a la del Ejemplo 31 utilizando (R)-1 -fenil-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 31, etapa 3](100 mg, 0.27 mmol), e hidrocloruro de metil éster D-2-fluorofenil-alanina. Rendimiento = 10 mg (0.02 mmol, 7%). Hp Lc (254 nm): Método 3 Rt 2.64 min. MS (ESI) m/z 518.4 [M H+].
Ejemplo 33 : ácido (R)-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-3-(4-trifluorometilfenil)-propiónico
El compuesto del título se preparó de manera análoga a la del Ejemplo 31 utilizando (R)-1 -fenil-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 31, etapa 3](100 mg, 0.27 mmol), e hidrocloruro de metil éster D-4-trifluorometilfenil-alanina. Rendimiento = 18 mg (0.03 mmol, 11%). HPLC (254 nm): Método 3 Rt 3.10 min. MS (ESI) m/z 568.5 [M H+].
Ejemplo 34 : ácido (R)-3-ciclopropil-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico
El compuesto del título se preparó de manera análoga a la del Ejemplo 31 utilizando (R)-1 -fenil-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 31, etapa 3](100 mg, 0.27 mmol), e hidrocloruro de metil éster del ácido (R)-2-amino-3-ciclopropilpropiónico [Ejemplo 17, etapa 1]. Rendimiento = 13 mg (0.03 mmol, 35%). HPLC (254 nm): Método 3 Rt 2.82 min. Ms (ESI) m/z 464.5 [M H+].
Ejemplo 35 : ácido (R)-3-(2-cloro-fenil)-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico
El compuesto del título se preparó de manera análoga a la del Ejemplo 31 utilizando (R)-1 -fenil-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 31, etapa 3](100 mg, 0.27 mmol), e hidrocloruro de metil éster D-2 -clorofenil-alanina. Rendimiento = 38 mg (0.07 mmol, 27%). Hp LC (254 nm): Método 3 Rt 3.05 min. MS (ESI) m/z 534.2 [M H+].
Ejemplo 36 : ácido (R)-3-(4-cloro-fenil)-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-bencilamino}-propiónico
El compuesto del título se preparó de manera análoga a la del Ejemplo 31 utilizando (R)-1 -fenil-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 31, etapa 3](100 mg, 0.27 mmol), e hidrocloruro de metil éster D-4-clorofenil-alanina. Rendimiento = 8 mg (0.01 mmol, 5%). HPLC (254 nm): Método 3 Rt 3.13 min. MS (ESI) m/z 534.4 [M H+].
Ejemplo 37 : ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-fenilpropiónico
Etapa 1 : (R)-1-(2-cloro-fenil)-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico
Se preparó (R)-1-(2-cloro-fenil)-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico de manera análoga a la del Ejemplo 31, etapas 1-3 a partir de ácido 5-(4-clorometil-fenil)-3-metil-isoxazol-4-carboxílico [Ejemplo 31, etapa 2](1.95 g, 7.75 mmol) y (R)-1 -(2-clorofenil)-etanol (1.82 g, 11.62 mmol). Rendimiento = 1.33 g (3.28 mmol, 42%). HPLC (254 nm): Método 3 Rt 3.31 min. MS (ESI) m /z 405.3 [M H+].
Etapa 2 : metil éster del ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-fenil-propiónico
Se preparó metil éster del ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-fenil-propiónico de manera análoga a la del Ejemplo 31, etapas 4 a partir de (R)-1-(2-cloro-fenil)-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 37, etapa 1] (101 mg, 0.25 mmol) e hidrocloruro de D-fenilalanina metil éster. Rendimiento = 45 mg (0.08 mmol, 33%). HPLC (254 nm): Método 3 Rt 2.90 min. MS (ESI) m/z 548.5 [M H+].
Etapa 3 : ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-fenilpropiónico
Se preparó de manera análoga a la del Ejemplo J, Etapa 5 utilizando los siguientes reagentes y cantidades: metil éster del ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-fenilpropiónico [Ejemplo 37, etapa 2] (45 mg, 0.08 mmol). Rendimiento = 6 mg (0.01 mmol, 14%). HPLC (254 nm): Método 3 Rt 2.69 min. MS (ESI) m/z 534.3 [M H+].
Ejemplo 38: ácido (R)-2-(4-{4-[(R)_1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-(2-fluoro-fenil)-propiónico
El compuesto del título se preparó de manera análoga a la del Ejemplo 31 utilizando (R)-1 -(2-cloro-fenil)-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 37, etapa 1](101 mg, 0.25 mmol), e hidrocloruro de metil éster D-2-fluorofenil-alanina. Rendimiento = 30 mg (0.05 mmol, 22%). HPLC (254 nm): Método 3 Rt 2.57 min. MS (ESI) m/z 552.3 [M H+].
Ejemplo 39: ácido (R)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-(4-trifluorometil-fenil)-propiónico
El compuesto del título se preparó de manera análoga a la del Ejemplo 31 utilizando (R)-1-(2-cloro-fenil)-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 37, etapa 1](101 mg, 0.25 mmol), e hidrocloruro de metil éster D-4-trifluorometilfenil-alanina. Rendimiento = 38 mg (0.06 mmol, 25%). HPLC (254 nm): Método 3 Rt 3.06 min. MS (ESI) m/z 602.6 [M H+].
Ejemplo 40 : ácido (R)-3-(2-cloro-fenil)-2-(4-{4-[(R)-1 -(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-propiónico
El compuesto del título se preparó de manera análoga a la del Ejemplo 31 utilizando (R)-1-(2-cloro-fenil)-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 37, etapa 1](101 mg, 0.25 mmol), e hidrocloruro de metil éster D-2-clorofenil-alanina. Rendimiento = 8 mg (0.01 mmol, 5%). HPLC (254 nm): Método 3 Rt 2.78 min. MS (ESI) m/z 569.3 [M H+].
Ejemplo 41 : ácido (R)-2-(4-{4-[(R)-1-(2-cloro-fenil)-etoxicarbonilamino]-3-metil-isoxazol-5-il}-bencilamino)-3-ciclopropil-propiónico
El compuesto del título se preparó de manera análoga a la del Ejemplo 31 utilizando (R)-1-(2-cloro-fenil)-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 37, etapa 1](101 mg, 0.25 mmol), e hidrocloruro de metil éster del ácido (R)-2-amino-3-ciclopropilpropiónico [Ejemplo 17, etapa 1 ]. Rendimiento = 8 mg (0 .01 mmol, 3%). HPLC (254 nm): Método 3 Rt 2.80 min. MS (ESI) m/z 498.4 [M H+].
Ejemplo 42 : ácido 2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-3-fenil-propiónico
Etapa 1 : acetato de {p-[3-metil-4-((R)-1-feniletoxicarbonilamino)-5-isoxazolil]fenil}metilo
(R)-1 -fenil-etil éster del ácido [5-(4-clorometil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 31, etapa 3] (1 g, 2.8 mmol) se mezcló con acetato de potasio (2 g, 14 mmol) y yoduro de sodio (0.5 g, 2.8 mmol) y a este se agregó N,N-dimetilacetamida (20 mL). La mezcla se sometió a sonicación y se calentó hasta 80oC durante 1.5hrs. La mezcla se enfrió a temperatura ambiente y se repartió entre solución saturada de cloruro de sodio y acetato de etilo. La capa orgánica se lavó adicionalmente con agua 4 times y con una solución saturada de cloruro de sodio antes de secarse sobre sulfato de magnesio. La solución filtrada se evaporó para proporcionar un sólido que se utilizó directamente. Rendimiento = 0.94 g (2.4 mmol, 87%). HPLC (254 nm): Método 3 Rt 2.89 min. MS (ESI) m/z 395.3 [M H+].
Etapa 2 : (R)-1 -fenil-etil éster del ácido [5-(4-hidroximetil-fenil)-3-metil-isoxazol-4-il]-carbámico
Se disolvió {p-[3-metil-4-((R)-1-feniletoxicarbonilamino)-5-isoxazolil]fenil}acetato de metilo [Ejemplo 42, etapa 1](0.94 g, 2.4 mmol) en THF (20 mL) y metanol (20 mL) y a este se agregó carbonato de potasio (981 mg, 7.1 mmol). La mezcla resultante se dejó en agitación durante 1.5 horas a temperatura ambiente cuando LC/MS indicó la formación de un producto único [Hp LC (254 nm): Método 3 Rt 2.93 min. MS (ESI) m/z 353.2 [M H+]. Los disolventes se evaporaron y el residuo se repartió entre solución saturada de cloruro de sodio y acetato de etilo. La fase orgánica se secó sobre sulfato de magnesio, se filtró y se evaporó para proporcionar un residuo que se sometió a cromatografía en un gradiente de 0-50% acetato de etilo en hexanos para proporcionar el producto. Rendimiento 0.63 g (1.79 mmol, 74%).
Etapa 3 : metil-2-diazo-fenilpropanoato
Se repartió hidrocloruro de metil éster de D-fenilalanina (2 g, 9.3 mmol) entre solución saturada de bicarbonato de sodio y acetato de etilo. La fase orgánica se secó sobre sulfato de magnesio, se filtró y se evaporó para proporcionar un residuo que se utilizó directamente. Se disolvió metil éster de D-fenilalanina (836 mg, 4.7 mmol) en cloroformo (20 mL) y se agregó ácido acético (0.055 mL, 0.94 mmol). La solución se calentó a reflujo con la adición lenta por goteo de nitrato de isoamilo (0.76 mL, 5.6 mmol) que se completó antes de la ebullición del disolvente. La mezcla se sometió a reflujo durante 30 minutos adicionales para proporcionar una solución amarilla que se enfrió a 0oC. La solución orgánica se lavó con ácido sulfúrico 1N (25 mL), agua (20 mL), solución saturada de bicarbonato de sodio (25 mL), agua (25 mL) y ácido sulfúrico 1N (25 mL). La fase orgánica se secó sobre sulfato de magnesio, se filtró y se evaporó para proporcionar un residuo que se sometió a cromatografía en un gradiente de 0-5% acetato de etilo en hexanos para proporcionar el producto. Rendimiento 0.65 g (3.4 mmol, 72%).
Etapa 4 : metil éster del ácido 2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-3-fenilpropiónico
(R)-1 -fenil-etil éster del ácido [5-(4-hidroximetil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 42, etapa 2] (100 mg, 0.28 mmol) y metil-2-diazo-fenilpropanoato [Ejemplo 42, etapa 3] (61 mg, 0.39 mmol) se suspendieron en benceno (3 mL) en un recipiente con tapa de rosca. A esto se agregó tetraacetato de dirodio (1 mg, 0.002 mmol). Después de 10 minutos a temperatura ambiente el recipiente se calentó hasta 90oC durante 1 hora. La mezcla se enfrió a temperatura ambiente y la mezcla se sometió a cromatografía en un gradiente de 0 -2 0 % acetato de etilo en hexanos para proporcionar el producto. Rendimiento = 52 mg (0.1 mmol, 36%). HPLC (254 nm): Método 3 Rt 3.56 min. MS (ESI) m/z 515.5 [M H+].
Etapa 5 : ácido 2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-3-fenil-propiónico
Se disolvió metil éster del ácido 2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-3-fenilpropiónico (52 mg, 0 . 10 mmol) en 2 / 1 v/v THF/agua (4.5 mL) y la mezcla se agitó durante 24 horas. La mezcla de reacción se diluyó con acetato de etilo (50 mL) y se lavó con una solución saturada de bicarbonato de sodio. La capa acuosa se acidificó hasta un pH de ~ 3 con HCl 6 N y se extrajo con acetato de etilo. La capa orgánica se separó, se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío. El residuo se evaporó con dietil éter para proporcionar el producto puro como un sólido blanco (22 mg, 0.043 mmol, 44%). HPLC (254 nm): Método 3 Rt 3.03 min. MS (ESI) m/z 501.5 [M H+].
Ejemplo 43 : ácido 2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-3-fenil-propiónico
Ejemplo 43 se preparó de una manera análoga a la del Ejemplo 42 a partir de (R)-1 -fenil-etil éster del ácido [5-(4-hidroximetil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 42, etapa 2] (100 mg, 0.28 mmol) se disolvió en 15% de THF en benceno (1.15 mL) utilizando metil-2-diazo-fenilpropanoato que se sintetizó a partir hidrocloruro de metil éster L-fenilalanina (2 g, 9.3 mmol). Rendimiento 20 mg (0.04 mmol, 14%). HPLC (254 nm): Método 3 Rt 2.96 min. MS (ESI) m/z 501.6 [M H+].
Ejemplo 44 : ácido (RS)-3-ciclopropil-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-propiónico
Etapa 1: metil éster del ácido D,L-2-amino-ciclopropilpropanoico
Se preparó de una manera análoga a la del Ejemplo 1, etapa 6 a partir de ácido D,L-2-amino-ciclopropilpropanoico (500 mg, 3.87 mmol). El residuo en bruto se repartió entre solución saturada de bicarbonato de sodio y acetato de etilo. La fase orgánica se secó sobre sulfato de magnesio, se filtró y se evaporó para proporcionar un residuo que se utilizó directamente. Rendimiento 295 mg (2.06 mmol, 53%)
Etapa 2: R,S metil-2-diazo-ciclopropilpropanoato
Se preparó de una manera análoga a la del Ejemplo 42, etapa 3 a partir de metil éster del ácido D,L-2-aminociclopropilpropanoico (295 mg, 2.06 mmol) y se utilizó directamente. Rendimiento 200 mg (1.29 mmol, 62%)
Etapa 3: metil éster del ácido (RS)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-propiónico
Se preparó de una manera análoga a la del Ejemplo 42, etapa 4 a partir de (R)-1 -fenil-etil éster del ácido [5-(4-hidroximetil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 42, etapa 2] (90 mg, 0.25 mmol) se disolvió en 15% de THF en benceno (1 mL) y R,S metil-2-diazo-ciclopropilpropanoato [Ejemplo 44, etapa 2] (118 mg, 0.75 mmol]. Rendimiento 50 mg (0.1 mmol, 40%). HPLC (254 nm): Método 3 Rt 2.99 min. MS (ESI) m/z 479.1 [M H+].
Etapa 4: ácido (RS)-3-ciclopropil-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-propiónico
Se preparó de una manera análoga a la del Ejemplo 42, etapa 5 a partir de metil éster del ácido (RS)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-propiónico [Ejemplo 44, etapa 3] (50 mg, 0.1 mmol). Rendimiento 21 mg (0.1 mmol, 40%). HPLC (254 nm): Método 3 Rt 3.06 min. Ms (ESI) m/z 465 [M H+].
Ejemplo 45 : ácido (RS)-3-(4-cloro-fenil)-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarboniloxi)-isoxazol-5-il]-benciloxi}-propiónico
Etapa 1: metil éster del ácido D,L-2-amino-3(4-clorofenil)propanoico
Se preparó de una manera análoga a la del Ejemplo 1, etapa 6 a partir de ácido D,L-2-amino-3(4-clorofenil)propanoico (600 mg, 3 mmol). El residuo en bruto se repartió entre solución saturada de bicarbonato de sodio y acetato de etilo. La fase orgánica se secó sobre sulfato de magnesio, se filtró y se evaporó para proporcionar un residuo que se utilizó directamente. Rendimiento 698 mg (3.3 mmol, 100%)
Etapa 2: R,S metil-2-diazo-3(4-clorofenil)propanoato
Se preparó de una manera análoga a la del Ejemplo 42, etapa 3 a partir de metil éster del ácido D,L-2-amino-3(4-clorofenil)propanoico [Ejemplo 45, etapa 1](698 mg, 3.3 mmol) y se utilizó directamente. Rendimiento 275 mg (1.33 mmol, 40%)
Etapa 3: metil éster del ácido (RS)-3-(4-cloro-fenil)-2-{4-[3-metil-4-((R)-1-fenil-etoxicarboniloxi)-isoxazol-5-il]-benciloxi}-propiónico
Se preparó de una manera análoga a la del Ejemplo 42, etapa 4 a partir de (R)-1 -fenil-etil éster del ácido [5-(4-hidroximetil-fenil)-3-metil-isoxazol-4-il]-carbámico [Ejemplo 42, etapa 2] (90 mg, 0.25 mmol) se disolvió en 15% de THF en benceno (1 mL) y R,S metil-2-diazo-3(4-clorofenil)propanoato [Ejemplo 45, etapa 2] (200 mg, 0.89 mmol). Rendimiento 55 mg (0.1 mmol, 40%). HPLC (254 nm): Método 3 Rt 3.49 min. MS (ESI) m/z 549.6 [M H+].
Etapa 4: ácido (RS)-3-(4-cloro-fenil)-2-{4-[3-metil-4-((R)-1 -fenil-etoxicarboniloxi)-isoxazol-5-il]-benciloxi}-propiónico
Se preparó de una manera análoga a la del Ejemplo 42, etapa 5 a partir de metil éster del ácido (RS)-3-ciclopropil-2-{4-[3-metil-4-((R)-1-fenil-etoxicarbonilamino)-isoxazol-5-il]-benciloxi}-propiónico [Ejemplo 44, etapa 3] (55 mg, 0.1 mmol). Rendimiento 20 mg (0.04 mmol, 37%). HPLC (254 nm): Método 3 Rt 3.26 min. MS (ESI) m /z 535 [M H+].
Ejemplo 46 : ácido 2-[4-[4-[5-[1 -(2-clorofenil)etoxicarbonilamino]-4-ciano-pirazol-1 -il]fenil]fenil]acético
Etapa 1 -5-amino-1-(4-bromofenil)pirazol-4-carbonitrilo
Se suspendió hidrocloruro de (4-bromofenil)hidrazina (2.24 g, 10 mmol) en etanol (20 mL) y se trató con trietilamina (1.53 mL, 11 mmol). La solución resultante que se trató con malononitrilo (1.22 g, 10 mmol) se agregó en porciones. Después de se observó una pequeña exoterma, la reacción se calentó a reflujo durante 1 hora. La reacción se enfrió a temperatura ambiente; Los sólidos se recogieron mediante filtración al vacío y se lavaron con etanol frío. Los sólidos se secaron al aire. Rendimiento = 0.93 g, 3.5 mmol (35%). HPLC (254 nm): Método 2, Rt 5.82 min. MS (ESI) m/z 265 [M H+]; 263 [M H+]; 184 [(M - Br) H+].
Etapa 2 -1-(2-clorofenil)etil N-[2-(4-bromofenil)-4-ciano-pirazol-3-il]carbamato
Una solución de 5-amino-1-(4-bromofenil)pirazol-4-carbonitrilo [Ejemplo 46, etapa 1] (26 mg, 0.1 mmol) en CH2 Cl2 (1 mL) se trató con trietilamina (28 pL, 0.2 mmol), seguido por fosgeno (100 pL de una solución 20% v/v en tolueno, 0.2 mmol est.). La solución resultante se agitó a temperatura ambiente durante 30 minutos. Se agregó (±)-1-(2-clorofenil)etanol (23 mg, 0.15 mmol) y la mezcla resultante se agitó a temperatura ambiente durante la noche. La reacción se concentró al vacío para eliminar los volátiles, y el residuo se purificó mediante cromatografía sobre sílice-gel, eluyendo con una mezcla 4:1 de hexanos/acetato de etilo v/v. El producto se obtuvo como una película incolora. Rendimiento = 27 mg (0.06 mmol, 61%). HPLC (254 nm): Método 1, Rt 6.31 min. MS (ESI) m/z 447 [M ± H±]; 445 [M ± H±]. 1H NMR (500 MHz, CDCh) 57.90 (s, 1 H); 7.57 (d, J = 8 . 8 Hz, 2 H); 7.37 - 7.35 (m, 1 H); 7.32 (d, J = 8 . 8 Hz, 2 H); 7.27 (m, 3 H); 6.70 (a, 1 H); 6.14 (q, J = 6.5 Hz, 1 H); 1.54 (d, J = 6.5 Hz, 3 H).
Etapa 3 -2-[4-[4-[5-[1-(2-clorofenil)etoxicarbonilamino]-4-ciano-pirazol-1-il]fenil]fenil]acetato de etilo
En un recipiente de presión, se disolvió 1-(2-clorofenil)etil N-[2-(4-bromofenil)-4-ciano-pirazol-3-il]carbamato [Ejemplo 46, etapa 2] (80 mg, 0.18 mmol) en una mezcla 2:1 v/v de tolueno y etanol (2 mL) y se trató con Na2CÜ3 (0.6 mL de una solución 2N acuosa) y ácido [4-(2-etoxi-2-oxo-etil)fenil]borónico (75 mg, 0.36 mmol). La mezcla resultante se desgasificó bajo Ar durante 15 minutos, después se trató con Pd[Ph3P]4 ( 8 mg, 0.007 mmol). El recipiente se tapó y se sumergió en un baño de aceite a 80 oC, con agitación magnética. La reacción se consideró completa después de 14 horas. La reacción se enfrió a temperatura ambiente y se repartió entre acetato de etilo y agua. La capa orgánica se lavó con agua y salmuera. Las capas acuosas combinadas se extrajeron nuevamente con acetato de etilo. Las capas orgánicas combinadas se secaron MgSÜ4 anhidro, se filtraron y se concentraron al vacío. El residuo se purificó mediante cromatografía sobre sílice-gel, eluyendo con una mezcla 4:1 de hexanos/acetato de etilo v/v. El producto se obtuvo como un sólido blanco. Rendimiento = 82 mg (0.16 mmol, 89%). HPLC (254 nm): Método 1, Rt 6.94 min. MS (ESI) m/z 529.3 [M ± H±]; 485.1 [(M - EtO) ± H±].
Etapa 4 : ácido 2-[4-[4-[5-[1 -(2-clorofenil)etoxicarbonilamino]-4-ciano-pirazol-1 -il]fenil]fenil]acético
Se disolvió 2-[4-[4-[5-[1-(2-clorofenil)etoxicarbonilamino]-4-ciano-pirazol-1-il]fenil]fenil]acetato de etilo [Ejemplo 46, etapa 3] (45 mg, 0.085 mmol) en THF (1 mL) y se trató con LiOH (1 mL de una solución 1M acuosa). La mezcla resultante se agitó a temperatura ambiente durante 2 horas. La reacción se transfirió a un embudo separador, se diluyó con agua y se extrajo con acetato de etilo. La capa orgánica se eliminó y la capa acuosa se llevó hasta un pH de 2 con una solución de HCl 1N. El producto se extrajo con acetato de etilo. La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar un sólido blanco como el producto puro. Rendimiento = 42 mg (0 . 08 5 mmol, cuantitativa). HPLC (254 nm): Método 1, Rt 6.99 min. MS (ESI) m/z 501.3 [M ± H±]; 457.2 [(M - CO2 H) ± H±]. 1H NMR (500 MHz, DMSO-afe) 5 12.39 (a, 1 H); 10.42 (a, 1 H); 8.31 (s, 1 H); 7.82 (d, J = 8 . 6 Hz, 2 H); 7.67 (d, J = 8.3 Hz, 2 H); 7.56 (d, J = 8 . 6 Hz, 2 H); 7.43 (d, J = 7.7 Hz, 1 H); 7.39 (d, J = 8.3 Hz, 2 H); 7.33 - 7.29 (m, 3 H); 5.94 (q, J = 6.5 Hz, 1 H); 3.64 (s, 2 H); 1.44 (a, 3 H).
Ejemplo 47: ácido (R)-1-[4-[4-[1,5-dimetil-4-(1-feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]ciclopropano carboxílico
Etapa 1: etil éster del ácido 2-(4-bromo-benzoil)-3-oxo-butírico
Se agregó acetoacetato de etilo (1.97 mL, 15.6 mmol) a una suspensión de cloruro de magnesio (1.49 g, 15.6 mmol) en diclorometano (15 mL) que se había enfriado a 0oC. A la mezcla se agregó piridina (2.43 mL, 30 mmol) y la agitación continuó durante 15 minutos adicionales. Se agregó cloruro de 4-bromobenzoilo (3.29 g, 15 mmol) en diclorometano (15 mL) a la reacción. Esta mezcla se agitó a 0oC durante 15 minutos y a temperatura ambiente durante 1 hora. En este momento la mezcla se trató con una solución 6 N de ácido clorhídrico (20 mL). La capa orgánica se separó, se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar a aceite incoloro que se utilizó directamente en la siguiente etapa.
Etapa 2: etil éster del ácido 3-(4-bromo-fenil)-1,5-dimetil-1H-pirazol-4-carboxílico y etil éster del ácido 5-(4-bromofenil)-1,3-dimetil-1 H-pirazol-4-carboxílico
Se mezclaron etil éster del ácido 2-(4-bromo-benzoil)-3-oxo-butírico [Ejemplo 47, etapa 1] (4.7 g, 15 mmol), metilhidrazina (0.79 mL, 15.1 mmol), ácido p-Toluenosulfónico (0.15 g) con etanol (150 mL) y esta mezcla se calentó hasta 78oC durante 2 horas. En este momento la reacción se dejó enfriar y la mezcla resultante se repartió entre acetato de etilo y agua. La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío. Se obtuvo un producto en bruto que se purificó mediante cromatografía de gel de sílice inicialmente con hexano/acetato de etilo 95/5 como disolvente de elución y posteriormente con hexano/acetato de etilo 88/12 para proporcionar etil éster del ácido 3-(4-bromo-fenil)-1,5-dimetil-1H-pirazol-4-carboxílico (600 mg, 12%) y etil éster del ácido 5-(4-bromo-fenil)-1,3-dimetil-1H-pirazol-4-carboxílico (190 mg, 4%).
Etapa 3: ácido 3-(4-bromofenil)-1,5-dimetil-1H-pirazol-4-carboxílico
Una mezcla de etil éster del ácido 3-(4-bromofenil)-1,5-dimetil-1H-pirazol-4-carboxílico [Ejemplo 47, etapa 2] (600 mg, 1.85 mmol), solución de hidróxido de sodio 1N (18.5 mL) y dioxano (18.5 mL) se agitó a 100oC durante 3 horas. Al enfriarse, la mezcla se acidificó hasta un pH de 3-4 con una solución de ácido clorhídrico 3N y se extrajo con acetato de etilo. La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar el producto como un sólido (422 mg, 77%).
Etapa 4: (R)-1 -(fenil)etil N-[2-(4-bromofenil)-1,5-dimetil-1H-pirazol-3-il]carbamato
Una suspensión de ácido 3-(4-bromofenil)-1,5-dimetil-1H-pirazol-4-carboxílico [Ejemplo 47, etapa 3] (50 mg, 0.17 mmol) en tolueno (1 mL) y trietilamina (17 mg, 0.17 mmol) se trató con difenilfosforil azida (44pL, 0.20 mmol) y la mezcla se agitó a 45oC durante 3 horas y posteriormente a 95oC con la evolución de un gas. Después de 30 minutos se agregó (R)-(+)-1-feniletanol (25 mg, 0.20 mmol). Se continuó el calentamiento durante 1 hora adicional antes de dejar enfriar la mezcla. La reacción se concentró al vacío y el residuo se disolvió en acetato de etilo y la solución se lavó con una solución de carbonato de potasio 0.1M y posteriormente salmuera. La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar el producto (64 mg, 91%) que se utilizó directamente en la siguiente etapa. HPLC (254 nm): Método 3 Rt 3.10 min. Ms (ESI) m/z 416.2, 414.4 [M H+].
Etapa 5: metil éster del ácido 2-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenil]ciclopropano carboxílico.
Se mezclaron 1-(4-bromofenil)ciclopropanocarboxilato de metilo (1 g, 3.92 mmol), acetato de potasio (461 mg, 4.7 mmol), y bis(pinacolato)diboron (1.19 g, 4.70 mmol) en dioxano (10 mL) y de desgasificó durante 10 minutos bajo una corriente de argón. Se agregó dicloruro de [1,1'-bis(difenilfosfino)ferroceno]palladium(II) (32 mg) y la mezcla se calentó a 95oC durante 2 horas. En este momento la mezcla se dejó enfriar y la mezcla se repartió entre acetato de etilo y agua. La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío. Se obtuvo un producto en bruto que se purificó mediante cromatografía de gel de sílice con hexano/acetato de etilo 95/5 como disolvente de elución para proporcionar el producto como un sólido blanco (1 . 0 2 g, 8 6 %).
Etapa 6 : metil éster del ácido (R)-1-[4-[4-[1,5-dimetil-4-(1-feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]ciclopropanocarboxílico
En un recipiente de presión, (R)-1 -(fenil)etil N-[2-(4-bromofenil)-1,5-dimetil-1H-pirazol-3-il]carbamato [Ejemplo 47, etapa 4) (64 mg, 0.16 mmol) se disolvió en una mezcla 2:1 v/v de tolueno y etanol (2 mL) y se trató con Na2CO3 (0.5 mL de una solución 2N acuosa) y metil éster del ácido 2-[4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2-il)fenil]ciclopropano carboxílico [Ejemplo 47, etapa 5] (52 mg, 0.17 mmol). La mezcla resultante se desgasificó bajo argón durante 15 minutos, y posteriormente se trató con tetraquis (trifenil-fosfina)paladio(0) (1 mg, 0.006 mmol). El recipiente se tapó y se sumergió en un baño de aceite a 80 oC, con agitación magnética vigorosa durante la noche. Esta reacción se enfrió a temperatura ambiente y se repartió entre acetato de etilo y agua. La capa orgánica se lavó con agua y salmuera. Las capas acuosas combinadas se extrajeron nuevamente con acetato de etilo. Las capas orgánicas combinadas se secaron MgSO4 anhidro, se filtraron y se concentraron al vacío. Este material se purificó mediante TLC preparativa eluyendo con hexano/acetato de etilo 1/1 v/v para proporcionar el producto como una película amarilla (10 mg, 13%).
Etapa 7 : ácido (R)-1-[4-[4-[2,5-dimetil-4-(1-feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]ciclopropanocarboxílico
Se disolvió metil éster del ácido (R)-1-[4-[4-[1,5-dimetil-4-(1-feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]ciclopropanocarboxílico [Ejemplo 47, etapa 6 ] (10 mg, 0.02 mmol) en THF (1 mL) y se trató con LiOH (1 mL de una solución 2M acuosa). La mezcla resultante se agitó durante la noche y posteriormente se sometió a reflujo durante 5 horas. La reacción se enfrió y se transfirió a un embudo separador, se diluyó con agua y se extrajo con acetato de etilo. La capa orgánica se eliminó y la capa acuosa se llevó hasta un pH de 1 con una solución de HCl 1N cuando el producto se extrajo con acetato de etilo. Esta capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío. Se obtuvo un residuo que se trituró con dimetoxietano. Los sólidos se filtró y el filtrado se evaporó a sequedad para proporcionar un residuo que se purificó mediante TLC preparativa, eluyendo con acetato de etilo/hexano 2/1 v/v. El producto se obtuvo como un sólido blanco (3 mg, 28%). HPLC (254 nm): Método 3 Rt 3.12 min. MS (ESI) m/z 496.6 [M H+].
Ejemplo 48: ácido (R)-1-[4-[4-[2,5-dimetil-4-(1-feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]ciclopropano carboxílico
Etapa 1: ácido 5-(4-bromo-fenil)-1,3-dimetil-1 H-pirazol-4-carboxílico
Una mezcla de etil éster del ácido 5-(4-bromo-fenil)-1,3-dimetil-1H-pirazol-4-carboxílico [Ejemplo 47, etapa 2] (190 mg, 0.59 mmol), solución de hidróxido de sodio 1N (5.9 mL) y dioxano (5.9 mL) se agitó a 100oC durante 1 hora. Al enfriarse, la mezcla se acidificó hasta un pH de 3-4 con una solución de ácido clorhídrico 3N y se extrajo con acetato de etilo. La capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío para proporcionar el producto como un sólido (170 mg, 98%).
Etapa 2: (R)-1 -(fenil)etil N-[5-(4-bromo-fenil)-1,3-dimetil-1H-pirazol-4-il]-carbamato
ácido 5-(4-bromo-fenil)-1,3-dimetil-1H-pirazol-4-carboxílico [Ejemplo 48, etapa 1] (50 mg, 0.17 mmol) se usó para preparar (R) -1 -(fenil)etil N-[5-(4-bromo-fenil)-1,3-dimetil-1H-pirazol-4-il]carbamato de conformidad con el procedimiento descrito en el Ejemplo 47, etapa 4 para proporcionar el producto (64 mg, 91%) que se usó en la siguiente etapa. HPLC (254 nm): Método 3 Rt 3.03 min. MS (ESI) m/z 416.5 [M H+].
Etapa 3 : metil éster del ácido (R)-1-[4-[4-[2,5-dimetil-4-(1-feniletoxicarbonilamino)pirazol-3-il]fenil]-fenil]ciclopropano carboxílico
En un recipiente de presión, se usó (R)-1 -(fenil)etil N-[5-(4-bromo-fenil)-1,3-dimetil-1H-pirazol-4-il]carbamato [Ejemplo 48, etapa 2) (64 mg, 0.16 mmol) para preparar el producto como un aceite (32 mg, 41%) utilizando un procedimiento similar al descrito en el Ejemplo 47, etapa 6
Etapa 4 : ácido (R)-1-[4-[4-[2,5-dimetil-4-(1-feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]ciclopropano carboxílico
Se disolvió metil éster del ácido (R)-1-[4-[4-[2,5-dimetil-4-(1-feniletoxicarbonilamino)pirazol-3-il]fenil]fenil]ciclopropano carboxílico [Ejemplo 48, etapa 3] (32 mg, 0.06 mmol) en THF (3 mL) y se trató con LiOH (3 mL de una solución 2M acuosa). La mezcla resultante se agitó durante la noche y posteriormente se sometió a reflujo durante 5 horas. La reacción se enfrió y se transfirió a un embudo separador, se diluyó con agua y se extrajo con acetato de etilo. La capa orgánica se eliminó y la capa acuosa se llevó hasta un pH de 1 con una solución de HCl 1N cuando el producto se extrajo con acetato de etilo. Esta capa orgánica se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío. Se obtuvo un residuo que se trituró con dimetoxietano. Los sólidos se filtró y el filtrado se evaporó a sequedad para proporcionar un residuo que se purificó mediante TLC preparativa, eluyendo con acetato de etilo/hexano 2/1 v/v. El producto se obtuvo como un sólido blanco (10 mg, 32%). HPLC (254 nm): Método 3 Rt 2.92 min. MS (ESI) m/z 496.6 [M H+].
Ejemplo 49: ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-3-fluoro-bifenil-4-il)-ciclopropanocarboxílico
Etapa 1: (E)-4-(dimetilamino)-2-oxo-but-3-enoato de etilo
Se disolvió piruvato de etilo (5 g, 43.1 mmol) en CH2Cl2 ( 86 mL) y se trató con dimetilformamida dimetilacetal (5.73 mL, 43.1 mmol). La reacción se agitó a temperatura ambiente durante 2 horas y se concentró al vacío. El producto bruto se utilizó como tal en la siguiente etapa. Rendimiento = 7.4 g.
Etapa 2 : 2-(4-bromofenil)pirazol-3-carboxilato de etilo
Se disolvió hidrocloruro de 4-bromofenil hidrazina (2.0 g, 8.95 mmol) en MeOH (18 mL) y se trató con (E)-4-(dimetilamino)-2-oxo-but-3-enoato de etilo en bruto [Ejemplo 3, etapa 1] (1.54 g, 9.0 mmol). La mezcla resultante se agitó a temperatura ambiente durante 6 horas. Los extractos se eliminaron los volátiles al vacío y el residuo se purificó mediante cromatografía sobre sílice-gel, eluyendo con una mezcla 95:5 de hexanos/acetato de etilo v/v, lo que incrementó al poliraridad a 9:1 con el tiempo. Se aislaron dos productos isoméricos: 2-(4-bromofenil)pirazol-3-carboxilato de etilo como un sólido anaranjado (0.82 g, 2.78 mmol, 31%) y 1-(4-bromofenil)pirazol-3-carboxilato de etilo como un sólido rojo (0.44 g, 1.49 mmol, 17%).
2-(4-bromofenil)pirazol-3-carboxilato de etilo: HPLC (254 nm): Método 2 Rt 5.22 min. MS (ESI) m/z 297 [M H+]; 294.8 [M H+]; 252 [(M - EtO) H+]; 250 [(M - EtO) H+]. 1H NMR (500 MHz, CDCl3) 5 7.69 (d, J = 1.9 Hz, 1 H); 7.58 (d, J = 8.7 Hz, 2 H); 7.32 (d, J = 8.7 Hz, 2 H); 7.03 (d, J = 1.9 Hz, 1 H); 4.26 (q, J = 7.1 Hz, 2 H); 1.28 (t, J = 7.1 Hz, 3 H).
1-(4-bromofenil)pirazol-3-carboxilato de etilo: 1H NMR (500 MHz, CDCb) 57.91 (d, J = 2.4 Hz, 1 H); 7.65 (d, J = 7.2 Hz, 2 H); 7.60 (d, J = 7.2 Hz, 2 H); 7.00 (d, J = 2.4 Hz, 1 H); 4.44 (q, J = 7.0 Hz, 2 H); 1.43 (t, J = 7.0 Hz, 3 H).
Etapa 3 : etil éster del ácido 2-(4-bromo-fenil)-4-fluoro-2H-pirazol-3-carboxílico
Se disolvió 2-(4-bromofenil)pirazol-3-carboxilato de etilo (1.08 g, 3.68 mmol) en acetonitrilo (12 mL) y la mezcla resultante se trató con ácido acético helado (4.6 mL). A esta solución, se agregó 1-clorometil-4-fluoro-1,4-diazoniabiciclo[2.2.2]octano bis(tetrafluoroborato) (Selectfluor®, 3.91 g, 11.04 mmol) en una porción y la mezcla resultante se calentó hasta 105 oC durante 18 horas. La mezcla se enfrió a temperatura ambiente y los extractos volátiles se eliminaron al vacío. El residuo en bruto se cargó directamente en una columna de gel de sílice y se purificó mediante elución con mezcla 95:5 de hexanos/acetato de etilo v/v, lo que incrementó al poliraridad a 9:1 con el tiempo. El producto se aisló como un sólido blanco (410 mg, 1.31 mmol, 36%) y material de partida se recuperó (272 mg, 0.93 mmol, 25%). Para etil éster del ácido 2-(4-bromo-fenil)-4-fluoro-2H-pirazol-3-carboxílico: HPLC (254 nm): Método 3 Rt 2.97 min. MS (ESI) m/z 313.1 [M H+]. 1H NMR (500 MHz, CDCb) 57.60 (s, 1 H); 7.58 (d, J = 9 Hz, 2 H); 7.29 (d, J = 9 Hz, 2 H); 4.30 (q, J = 7.1 Hz, 2 H); 1.28 (t, J = 7.1 Hz, 3 H).
Etapa 4 : ácido 2-(4-bromo-fenil)-4-fluoro-2H-pirazol-3-carboxílico
A una solución agitada de etil éster del ácido 2-(4-bromo-fenil)-4-fluoro-2H-pirazol-3-carboxílico (410 mg, 1.31 mmol) en THF (13 mL) se trató con una solución acuosa de LiOH 1N (13 mL) y la mezcla resultante se agitó a temperatura ambiente durante la noche. La reacción se consideró completa mediante cromatografía de capa delgada y HPLC/MS. La mezcla de reacción se repartió entre acetato de etilo y solución acuosa de HCl 1N (100 mL v/v) y se transfirió a un embudo separador. La capa orgánica se separó y la capa acuosa se extrajo nuevamente con acetato de etilo (30 mL). Las capas orgánicas combinadas se secaron MgSO4 anhidro, se filtraron y se concentraron al vacío para proporcionar el producto puro como un sólido blanco (347 mg, 1.22 mmol, 93%). HPLC (254 nm): Método 3 Rt 2.82 min. MS (ESI) m/z 285.1 [M H+].
Etapa 5 : 1-(2-cloro-fenil)-etil éster del ácido (R)-[2-(4-bromo-fenil)-4-fluoro-2H-pirazol-3-il]-carbámico
Se suspendió ácido 2-(4-bromo-fenil)-4-fluoro-2H-pirazol-3-carboxílico (347 mg, 1.22 mmol) en tolueno (12 mL) y se trató con trietilamina (205 pL, 1.46 mmol). La solución resultante se trató con difenilfosforil azida (316 pL, 1.46 mmol) y se calentó hasta 65 oC. Se agregó (R)-1-(2-cloro-fenil)-etanol (230 mg, 1.46 mmol) a la mezcla de reacción y la temperatura se incrementó a 105 oC durante 30 minutos, durante dicho tiempo se observó una vigorosa evolución gaseosa. La reacción se llevó a 65 oC y se agitó a esa temperatura durante 4 horas. La reacción se consideró completa mediante HPLC/MS. Luego de enfriar, los extractos se eliminaron los volátiles al vacío y el residuo en bruto se purificó mediante cromatografía de gel de sílice, eluyendo con un gradiente de hexanos/acetato de etilo. El producto se aisló como un sólido blanco (452 mg, 1.03 mmol, 85%). HPLC (254 nm): Método 3 Rt 3.16 min. MS (ESI) m/z 440.1 [M H+].
Etapa 6 : ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-3-fluoro-bifenil-4-il)-ciclopropanocarboxílico
Una suspensión agitada de 1-(2-cloro-fenil)-etil éster del ácido (R)-[2-(4-bromo-fenil)-4-fluoro-2H-pirazol-3-il]-carbámico ( 88 mg, 0.2 mmol), 2:1 v/v tolueno/etanol (2 mL), solución acuosa de Na2CO3 2M (670 pL) y ácido 1-(4-borono-2-fluorofenil)ciclopropano-1-carboxílico (45 mg, 0.2 mmol) se desgasificó bajo nitrógeno durante 10 minutos y se trató con Pd[Ph3 P]4 (12 mg, 0.01 mmol). La mezcla resultante se sumergió en un baño de aceite, agitándose a 90 oC durante 12 horas. La reacción se enfrió, se transfirió a un embudo separador y se diluyó con acetato de etilo (50 mL). La mezcla se trató cuidadosamente con una solución acuosa de HCl 1N (20 mL). La capa orgánica se separó, se lavó con salmuera, se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío. El residuo en bruto se purificó mediante plato TLC preparativa (1000 pm), eluyendo con una mezcla 1:1 v/v hexanos/acetato de etilo. El producto se obtuvo como un sólido tostado. Rendimiento = 35 mg (35%). HPLC (254 nm): Método 3, Rt 3.11 min. MS (ESI) m/z 538.3 [M H+].
Ejemplo 50: ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-2-fluoro-bifenil-4-il)-ciclopropanocarboxílico
El compuesto del título se preparó de manera análoga a la del Ejemplo 49 utilizando 1-(2-cloro-fenil)-etil éster del ácido (R)-[2-(4-bromo-fenil)-4-fluoro-2H-pirazol-3-il]-carbámico (Ejemplo 49, Etapa 5 ( 88 mg, 0.2 mmol), y ácido 1-[4-(dihidroxiboranil)-3-fluorofenil]-ciclopropano-1-carboxílico. Rendimiento 40 mg (37%) como un sólido amarillo claro. HPLC (254 nm): Método 3, Rt 3.14 min. MS (ESI) m/z 538.3 [M H+].
Ejemplo 51 : ácido (R)-1-(2-cloro-4'-{5-[1-(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1-il}-bifenil-4-il)-ciclopropanocarboxílico
El compuesto del título se preparó de manera análoga a la del Ejemplo 49 utilizando 1-(2-cloro-fenil)-etil éster del ácido (R)-[2-(4-bromo-fenil)-4-fluoro-2H-pirazol-3-il]-carbámico (Ejemplo 49, Etapa 5 ( 88 mg, 0.2 mmol), y ácido 1-[3-cloro-4-(dihidroxiboranil)fenil]-ciclopropano-1-carboxílico. Rendimiento 24 mg (22%) como un sólido amarillo claro. HPLC (254 nm): Método 3, Rt 3.40 min. MS (ESI) m/z 554.4 [M H+].
Ejemplo 52 : ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-2-metil-bifenil-4-il)-ciclopropanocarboxílico
El compuesto del título se preparó de manera análoga a la del Ejemplo 49 utilizando 1-(2-cloro-fenil)-etil éster del ácido (R)-[2-(4-bromo-fenil)-4-fluoro-2H-pirazol-3-il]-carbámico (Ejemplo 49, Etapa 5 ( 88 mg, 0.2 mmol), y ácido 1-[4-(dihidroxiboranil)-3-metilfenil]ciclo-propano-1-carboxílico. Rendimiento 36 mg (34%) como un sólido amarillo claro. HPLC (254 nm): Método 3, Rt 3.19 min. MS (ESI) m/z 534.3 [M H+].
Ejemplo 53 : ácido (R)-1 -(4'-{5-[1 -(2-cloro-fenil)-etoxicarbonilamino]-4-fluoro-pirazol-1 -il}-bifenil-4-il)-ciclopropanocarboxílico
El compuesto del título se preparó de manera análoga a la del Ejemplo 49 utilizando 1-(2-cloro-fenil)-etil éster del ácido (R)-[2-(4-bromo-fenil)-4-fluoro-2H-pirazol-3-il]-carbámico (Ejemplo 49, Etapa 5 ( 88 mg, 0.2 mmol), y ácido 4-(1-carboxiciclopropil)fenilborónico, pinacol éster. Rendimiento 9 mg (9%) como un sólido blanco. HPLC (254 nm): Método 3, Rt 3.20 min. MS (ESI) m/z 520.0 [M H+].
Ejemplo 54 : ácido (R)-1 -{4'-[5-(1 -fenil-etoxicarbonilamino)-4-trifluorometil-pirazol-1-il]-bifenil-4-il}-ciclopropanocarboxílico
Etapa 1 : etil éster del ácido 2-(4-bromo-fenil)-4-yodo-2H-pirazol-3-carboxílico
Se disolvió 2-(4-bromofenil)pirazol-3-carboxilato de etilo (Ejemplo 49, Etapa 2, 294 mg, 1.0 mmol) en metanol (3 mL) y se trató por goteo con monocloruro de yodo (115 pL, 2.3 mmol). La mezcla resultante se calentó hasta 50 oC durante 3 horas. Otra parte de monocloruro de yodo (120 pL) se agregó y se continuó calentando durante 3 horas adicionales. La reacción se consideró completa mediante HPLC/MS. Luego de enfriar a temperatura ambiente, la mezcla de reacción se diluyó con acetato de etilo (30 mL) y se transfirió a un embudo separador. La capa orgánica se lavó sucesivamente con Na2S2O3 acuoso 1N (30 mL) y salmuera (30 mL). La capa orgánica se separó, se lavó con salmuera, se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío. Se obtuvo el producto [2-(4-bromofenil)-4-yodo-2H-pirazol-3-carboxílico etil éster del ácido] como un sólido amarillo claro (420 mg, cuant.) y utilizado como tal en la siguiente etapa. HPLC (254 nm): Método 3, Rt 3.33 min. MS (ESI) m/z 421.0, 423.0 [M H+].
Etapa 2 : etil éster del ácido 2-(4-bromo-fenil)-4-trifluorometil-2H-pirazol-3-carboxílico
Se disolvió etil éster del ácido 2-(4-bromo-fenil)-4-yodo-2H-pirazol-3-carboxílico (420 mg, 1.0 mmol) en DMF (4 mL) y la solución resultante se desgasificó con nitrógeno durante 10 minutos. Se agregó (1,10-Fenantrolina) (trifluorometil) cobre (I) (Trifluorometilator™, 520 mg, 1.5 mmol) en una porción bajo una atmósfera inerte y la mezcla resultante se agitó a 50 oC durante 18 horas. La reacción se enfrió a temperatura ambiente y se filtró a través una almohadilla de celite y se lavó bien con acetato de etilo. El filtrado se lavó con HCl 1N acuoso, salmuera, se secó sobre MgSO4 anhidro, se filtró y se concentró al vacío. El producto en bruto etil éster del ácido 2-(4-bromo-fenil)-4-trifluorometil-2H-pirazol-3-carboxílico se utilizó como tal en la siguiente etapa (291 mg, 0.80 mmol, 80%). HPLC (254 nm): Método 3, Rt 3.23 min. MS (ESI) m/z 365.2 [M H+].
Etapa 3 : ácido 2-(4-bromo-fenil)-4-trifluorometil-2H-pirazol-3-carboxílico
Se trató etil éster del ácido 2-(4-bromo-fenil)-4-trifluorometil-2H-pirazol-3-carboxílico (291 mg, 0.80 mmol) en THF ( 8 mL) con una solución acuosa de LiOH 1N ( 8 mL) y la mezcla resultante se agitó a temperatura ambiente durante 3 horas. La reacción se consideró completa mediante cromatografía de capa delgada y HPLC/MS. La mezcla de reacción se repartió entre acetato de etilo y solución acuosa de HCl 1N (100 mL v/v) y se transfirió a un embudo separador. La capa orgánica se separó y la capa acuosa se extrajo nuevamente con acetato de etilo (30 mL). Las capas orgánicas combinadas se secaron sobre MgSO4 anhidro, se filtraron y se concentraron al vacío para proporcionar el producto puro como un sólido blanco (268 mg, 0.80 mmol, cuant.). HPLC (254 nm): Método 3 Rt 2.97 min. MS (ESI) m/z 335.2 [M H+].
Etapa 4 : 1 -fenil-etil éster del ácido (R)-[2-(4-bromo-fenil)-4-trifluorometil-2H-pirazol-3-il]-carbámico
Se suspendió ácido 2-(4-bromo-fenil)-4-trifluorometil-2H-pirazol-3-carboxílico (268 mg, 0.80 mmol) en tolueno ( 8 mL) y se trató con trietilamina (135 pL, 0.97 mmol). La solución resultante se trató con difenilfosforil azida (209 pL, 0.97 mmol) y se calentó hasta 65 oC. Se agregó (R)-1-(fenil)-etanol (118 mg, 0.97 mmol) a la mezcla de reacción y la temperatura se incrementó a 105 oC durante 30 minutos, durante dicho tiempo se observó una vigorosa evolución gaseosa. La reacción se llevó a 65 oC y se agitó a esa temperatura durante 4 horas. La reacción se consideró completa mediante HPLC/MS. Luego de enfriar, los extractos se eliminaron los volátiles al vacío y el residuo en bruto se purificó mediante cromatografía de gel de sílice, eluyendo con un gradiente de hexanos/acetato de etilo. El
producto se aisló como un sólido blanco (195 mg, 0.43 mmol, 54%). HPLC (254 nm): Método 3 Rt 3.23 min. MS (ESI) m/z 454.0, 456.1 [M H+].
Etapa 5 : ácido (R)-1 -{4'-[5-(1 -fenil-etoxicarbonilamino)-4-trifluorometil-pirazol-1 -il]-bifenil-4-il}-ciclopropanocarboxílico
Una suspensión agitada de 1 -fenil-etil éster del ácido (R)-[2-(4-bromo-fenil)-4-trifluorometil-2H-pirazol-3-il]-carbámico (98 mg, 0.22 mmol), 2:1 v/v tolueno/etanol (2.2 mL), solución acuosa de Na2CÜ3 2M (720 pL) y ácido 4-(1-carboxiciclopropil)fenilborónico, pinacol éster (124 mg, 0.43 mmol) se desgasificó bajo nitrógeno durante 10 minutos y se trató con Pd[Ph3 P]4 (12 mg, 0.01 mmol). La mezcla resultante se sumergió en un baño de aceite, agitándose a 95 oC durante 3 horas. La reacción se enfrió, se transfirió a un embudo separador y se diluyó con acetato de etilo (50 mL). La mezcla se trató cuidadosamente con una solución acuosa de HCl 1N (20 mL). La capa orgánica se separó, se lavó con salmuera, se secó sobre MgSÜ4 anhidro, se filtró y se concentró al vacío. El residuo en bruto se purificó mediante plato de TLC preparativa (1000 pm), eluyendo con una mezcla 1:1 v/v hexanos/acetato de etilo. El producto se obtuvo como un sólido tostado. Rendimiento = 6 . 8 mg (6 %). HPLC (254 nm): Método 3, Rt 3.21 min. MS (ESI) m/z 536.3 [M H+].
Ejemplo 55: ácido (R)-1 -{2-fluoro-4'-[5-(1 -fenil-etoxicarbonilamino)-4-trifluorometil-pirazol-1 -il]-bifenil-4-il}-ciclopropanocarboxílico
El compuesto del título se preparó de manera análoga a la del Ejemplo 54 utilizando 1 -fenil-etil éster del ácido (R)-[2-(4-bromo-fenil)-4-trifluorometil-2H-pirazol-3-il]-carbámico (Ejemplo 54, Etapa 4 (98 mg, 0.22 mmol) y ácido 1-[4-(dihidroxiboranil)-3-fluorofenil]ciclopropano-1-carboxílico. Rendimiento 7 mg (6 %) como un sólido blanco. HPLC (254 nm): Método 3, Rt 3.11 min. Ms (ESI) m/z 554.4 [M H+]
Ejemplo 56 : ácido (R)-1 -(4-{5-[5-(1 -fenil-etoxicarbonilamino)-pirazol-1 -il]-piridin-2-il}-fenil)-ciclopropanocarboxílico
Etapa 1 : etil éster del ácido 2-(6-cloro-piridin-3-il)-2H-pirazol-3-carboxílico
Se preparó etil éster del ácido 2-(6-cloro-piridin-3-il)-2H-pirazol-3-carboxílico de manera análoga a la del Ejemplo 49, Etapa 2 utilizando hidrocloruro de (6-cloro-piridin-3-il)-hidrazina (9.89 g, 48.68 mmol; que se preparó de conformidad con el WO2005/92856A1) y (E)-4-(dimetilamino)-2-oxo-but-3-enoato de etilo (7.82 g, 45.68 mmol, Ejemplo 49, Etapa 1). Rendimiento = 1.35 g (5.38 mmol, 12%). HPLC (254 nm): Método 3 Rt 2.87 min. MS (ESI) m/z 252.2 [M H+]. 1H NMR (500 MHz, CDCb) 58.50 (d, J = 3.0 Hz, 1 H); 7.77 (dd, Ji = 3.0 Hz, J 2 = 8.5 Hz, 1 H); 7.74 (d, J = 2.0 Hz, 1 H); 7.43 (d, J = 8.5 Hz, 1 H); 7.08 (d, J = 2.0 Hz, 1 H); 4.28 (q, J = 7.5 Hz, 2 H); 1.30 (t, J = 7.5 Hz, 3 H).
Etapa 2: sal hidrocloruro del ácido 2-(6-cloro-piridin-3-il)-2H-pirazol-3-carboxílico
A una solución agitada de etil éster del ácido 2-(6-cloro-piridin-3-il)-2H-pirazol-3-carboxílico [Ejemplo 56, etapa 1] (1.35 g, 5.4 mmol) en THF/agua 8:2 v/v (35 mL) se trató con una solución acuosa de LiOH 1N (6.5 mL) y la mezcla resultante se agitó a temperatura ambiente durante 3 horas. La reacción se consideró completa mediante cromatografía de capa delgada y HPLC/MS. La mezcla de reacción se diluyó con agua (100 mL) y se lavó con diclorometano (60 mL). La capa acuosa se acidificó con una solución acuosa de HCl 1N hasta un pH de 2 lo que resultó en una suspensión blanca. Los sólidos se filtraron, se lavaron con agua y se secaron al aire para proporcionar el compuesto del título como un sólido blanco. Rendimiento = 0.90 g (3.46 mmol, 64%). HPLC (254 nm): Método 3 Rt 2.65 min. MS (ESI) m/z 224.3 [M H+].
Etapa 3 : (R)-[2-(6-cloro-piridin-3-il)-2H-pirazol-3-il]-carbámico 1 -fenil-etil éster del ácido
Se suspendió sal hidrocloruro del ácido 2-(6-cloro-piridin-3-il)-2H-pirazol-3-carboxílico [Ejemplo 56, etapa 2](0.90 g, 4.03 mmol) en tolueno (27 mL) y se trató con di-isopropriletilamina (1.28 mL, 8 . 86 mmol). La solución resultante se trató con difenilfosforil azida (855 pL, 4.83 mmol) y se calentó hasta 65 oC. Se agregó (R)-1-(fenil)-etanol (600 pL, 6.03 mmol) a la mezcla de reacción y la temperatura se incrementó a 105 oC durante 30 minutos, Durante dicho tiempo se observó una vigorosa evolución gaseosa. La reacción se llevó a 65 oC y se agitó a esa temperatura durante 4 horas. La reacción se consideró completa mediante HPLC/MS. Luego de enfriar, se eliminaron los volátiles al vacío y el residuo en bruto se purificó mediante cromatografía de gel de sílice, eluyendo con un gradiente de hexanos/acetato de etilo. El producto se aisló como un sólido blanco. Rendimiento = 0.60 g (1.75 mmol, 44%). HPLC (254 nm): Método 3 Rt 3.05 min. MS (ESI) m/z 343.2 [M H+].
Etapa 4 : metil éster del ácido (R)-1-(4-{5-[4-metil-5-(1-fenil-etoxicarbonilamino)-pirazol-1-il]-piridin-2-il}-fenil)-ciclopropanocarboxílico
Una suspensión agitada de 1 -fenil-etil éster del ácido (R)-[2-(6-cloro-piridin-3-il)-2H-pirazol-3-il]-carbámico [Ejemplo 56, etapa 3] (240 mg, 0.70 mmol) en 2 : 1 v/v tolueno/etanol (7 mL), solución 2 M acuosa de Na2CO3 (1.5 mL) y metil éster del ácido 1-[4-(4,4,5,5-tetrametil-[1,3,2]dioxaborolan-2-il)-fenil]-ciclopropanocarboxílico (260 mg, 0.84 mmol) se desgasificó bajo nitrógeno durante 10 minutos y se trató con Pd[Ph3 P]4 (42 mg, 0.036 mmol). La mezcla resultante se sumergió en un baño de aceite, agitándose a 90 oC durante 15 horas. La reacción se enfrió, se transfirió a un embudo separador y se diluyó con acetato de etilo (50 mL). La mezcla se trató cuidadosamente con una solución acuosa de HCl 1N (20 mL). La capa orgánica se separó, se lavó con salmuera, se secó sobre MgSO4 anhidro, se
filtró y se concentró al vacío. El residuo en bruto se purificó mediante cromatografía de gel de sílice, eluyendo con un gradiente de 0-30% de hexanos/acetato de etilo de polaridad en aumento. El producto se obtuvo como un sólido tostado. Rendimiento = 136 mg (0.28 mmol, 40%). h PlC (254 nm): Método 3 Rt 2.93 min. MS (ESI) m/z 483.4 [M H+].
Etapa 6 : ácido (R)-1 -(4-{5-[5-(1 -fenil-etoxicarbonilamino)-pirazol-1 -il]-piridin-2-il}-fenil)-ciclopropanocarboxílico
Una solución de metil éster del ácido (R)-1-(4-{5-[4-metil-5-(1-fenil-etoxicarbonilamino)-pirazoM-il]-piridin-2-il}-fenil)-ciclopropanocarboxílico (136 mg, 0.28 mmol) en una mezcla 2:1 v/v de THF/agua (3 mL) se trató con una solución acuosa de LiOH 1N (420 gL) y se agitó a temperatura ambiente durante 16 horas. La reacción se llevó hasta un pH de 1 mediante la adición de una solución acuosa de HCl 1N. La mezcla se extrajo con EtOAc y se lavó con agua. La capa orgánica se secó sobre Na2SO4 anhidro, se filtró y se concentró al vacío. El producto se obtuvo como un sólido blanquecino Se preparó de manera análoga a la del Ejemplo M1, Etapa 6 utilizando los siguientes reagentes y cantidades: metil éster del ácido (R)-1-(4-{5-[5-(1-fenil-etoxicarbonilamino)-pirazol-1-il]-piridin-2-il}-fenil)-ciclopropanocarboxílico (136 mg, 0.28 mmol), THF/agua 2:1 v/v (3 mL), solución acuosa de LiOH 1N (420 gL). Rendimiento = 15 mg (0.032 mmol, 11 %). Hp Lc (254 nm): Método 3 Rt 2.93 min. MS (ESI) m/z 483.3 [M H+].
Los compuestos 57 a 458 de la Tabla 1 y derivados de estos se preparan de conformidad con los procedimientos descritos para los compuestos 1-56. Las aminas heterocíclicas o ésteres necesarios para ensamblar los carbamatos correspondientes se preparan de conformidad con los métodos descritos en las citas 1-24.
Ciertas sustituciones de isoxazol se preparan de conformidad con la construcción del isoxazol de arilo apropiado (3, Esquema 1). La fluorinación directa o bromación y cianación permite obtener bromuro de arilo (4) o ácido (5) después de la carbonilación catalizada por paladio.
Esquema 1
seguido de
Ácido (5, esquema 2) puede unirse directamente con aminas para obtener intermedios de amida (6 ) que se puede convertir en productos de carbamato (7) después de la hidrólisis ácida, transposición de Curtius y desprotección con ácido.
Esquema 2
El ácido (5) puede reducirse a alcohol (8 ) y/o convertirse en su cloruro (9), como en el esquema 3. Los alcoholes se pueden convertir en sus análogos de éter (10) mediante la inserción catalizada por rodio en intermedios diazo 2 N+-z-Rb o se pueden generar aminas (11) a partir de cloruros (IX).
Esquema 3
F= F,
De forma alternativa, los bromuros (4) se pueden unir directamente a alcoholes o aminas (UV-Z-RB) donde U es -OH o -NH2 por desplazamiento de haluro de metal o térmico catalizado, como en el Esquema 4. Todos los intermedios clave (10-12) se pueden modificar adicionalmente para producir productos finales, como se describe en el Esquema 1, mediante el uso de hidrólisis ácida y transposición de Curtius seguida por desprotección del ácido.
Esquema 4
4 12
Ejemplo 57. Ensayos de unión de receptores
La afinidad de unión de los compuestos de Fórmula I-XII se determinaron sobre la base de su capacidad para desplazar el ácido lisofosfatídico tritiado ([3H]-LPA) a partir de células CHO que expresan LPA1R en un protocolo similar al descrito en la referencia 17. En un formato de 96 pocillos, las células CHO que expresan LPA1R humana [Cerep] se trataron con [3H]-LPA (2nM). Los compuestos de ensayo se añadieron en concentraciones mayores en cada pocillo y se incubaron a temperatura ambiente durante 90 minutos. En este momento, las placas se lavaron y los pocillos se contaron a los fines de la radioactividad. Los resultados se compararon con un control en el que las células se trataron con [3H]-LPA en presencia de LPA no marcado de 10 |jM. El ligando específico unido a los receptores se definió como la diferencia entre la unión total y la unión no específica determinada en presencia de un exceso de ligando no marcado. Los resultados se expresaron como un porcentaje de unión específica de control ((miden la unión específica/unión específica de control) x 100) y como un porcentaje de inhibición de unión específica de control (100-((mide la unión específica de control/unión específica) x 100)), obtenido en presencia de los compuestos de ensayo. El valor de IC50 (concentración que produce una inhibición media máxima de la unión específica de control) y el coeficiente de Hill (nH) se determinaron mediante análisis de regresión no lineal de la curva de competencia generada con valores de replicación media, mediante el uso del ajuste de la curva de la ecuación de Hill (Y = D [(A - D)/(1 (C/C50) nH)], donde Y = unión específica, D = unión específica mínima, A = unión específica máxima, C = concentración del compuesto, C50 = IC50 y nH = factor de pendiente). Este análisis se realizó con un software desarrollado en Cerep (software Hill) y se validó por comparación con los datos generados por SigmaPlot® 4.0 para Windows® (© 1997 de SPSS Inc.). La constante de inhibición (Ki) se calculó con la ecuación de Cheng Prusoff (Ki = IC50/(1+(L/KD)), donde L = concentración de radioligando en el ensayo y KD = afinidad del radioligando para el receptor). Se utilizó un gráfico de Scatchard para determinar la Kd.
Ejemplo 58. Ensayo de flujo de calcio
Se utilizó la inhibición de flujo de Ca2+ estimulado por LPA para evaluar la potencia del compuesto mediante el uso de tecnología FLIPR en un formato de placa de 96 pocillos. El buffer de ensayo utilizado era una solución salina equilibrada de Hanks (HBSS) donde HBSS se complementó para contener 20 mM de HEPES y 2.5 mM de Probenecid a un pH 7.4 (Millipore, GPCR Profiler®). Las células que expresan LPA1R (Millipore) se colocaron en
p la ca s y se p re p a ra ro n 24 ho ras an tes de l e n sa yo de los a rtícu lo s de en sa yo . El f lu jo de iones C a 2+ se e va lu ó a p a rtir de la f lu o re s c e n c ia de un co lo ra n te no lavab le C a 2+ a base de flú o r. Los d a tos so b re a n ta g o n is ta s se g e n e ra n a p a rtir de p la ca s con c o n c e n tra c io n e s LP A su fic ie n tes p a ra g e n e ra r un a e fe c tiv id a d de l 80% [E C 80]. El p o rce n ta je de inh ib ic ió n se ca lcu ló a p a rtir de un a reducc ión de la e fe c tiv id a d de co n fo rm id a d con la co n ce n tra c ió n de los c o m p u e s to s de F ó rm u la I-V I. P a ra la d o s is -re s p u e s ta se u tiliza ron d a to s sob re inh ib ic ión pa ra c a lc u la r un co m p u e s to IC50.
El e n sa yo a g o n is ta se llevó a ca b o en un in s tru m e n to F L IP R TETRA d o n d e se añ a d ie ro n co m p u e s to s de l ensayo , co n tro le s de ve h ícu lo y a g o n is ta de re fe re n c ia a la p la ca de e n sa yo d e s p u é s de e s ta b le c e r un a línea de base de f lu o re sce n c ia . El e n sa yo de a g o n is ta du ró un to ta l de 180 se g u nd o s y se u tilizó p a ra e v a lu a r la ca p a c id ad de ca d a c o m p u e s to p a ra a c tiva r ca d a G P C R su je ta a en sa yo . A l f in a liz a r el e n sa yo de ago n is ta , la p la ca de e n sa yo se retiró de la F L IP R TETRA y se incubó a 25 °C d u ra n te s ie te (7) m inu tos . D e spués de l pe río d o de incubac ión , la p la ca de e n sa yo se co lo có n u e vam e n te en la F L IP R TETRA y se in ic ió e l e n sa yo an tag o n is ta .
Ensayo Antagonista: M ed ia n te el uso de va lo re s de p o te n c ia E C 80 d e te rm in a d o s d u ra n te e l e n sa yo de agon is ta , to d o s los p o c illo s con c o m p u e s to s de m ue s tra p re - in cu b a d o s se d e sa fia ro n con una c o n ce n tra c ió n E C 80 de ago n is ta de re fe re n c ia d e sp u é s de l e s ta b le c im ie n to de un a línea de base de f lu o re sce n c ia . El e n sa yo a n ta g o n is ta se llevó a ca b o con la m ism a p laca de e n sa yo que se u tilizó p a ra e l e n sa yo ago n is ta . El e n sa yo a n ta g o n is ta se llevó a ca b o en un in s tru m e n to F L IP R TETRA d o n de se añ a d ie ro n 9 co n tro le s de l ve h íc u lo y la co n ce n tra c ió n E C 80 de a g o n is ta de re fe re n c ia a los poc illo s ap ro p ia d o s . El e n sa yo a n ta g o n is ta du ró un to ta l de 180 se g u nd o s y se u tilizó pa ra e v a lu a r la ca p a c id ad de ca d a c o m p u e s to pa ra in h ib ir ca d a G P C R su je ta a ensayo .
Procesamiento de datos: T od o s los d a tos de p la ca de e n sa yo se so m e tie ro n a co rre cc io n e s de re fe re n c ia a p ro p ia d o s . D espués de rea lizad a s las co rre cc io n e s de línea de base , los va lo re s m áx im o s de f lu o re s c e n c ia se e xp o rta ron y los d a tos se p ro ce sa ro n p a ra c a lc u la r e l po rce n ta je de a c tiva c ió n (con resp e c to a los va lo re s de con tro l de l ve h ícu lo y e l a g o n is ta de re fe re n c ia E m ax), p o rce n ta je de inh ib ic ión (con resp e c to a los va lo re s de E C 80 y los va lo re s de l ve h ícu lo de co n tro l) y los va lo re s e s ta d ís tico s a d ic io n a le s (es dec ir, Z ', la va ria c ió n po rce n tu a l e n tre los va lo re s de los d a tos rep licad o s ) pa ra e v a lu a r la ca lid a d de ca d a p la to . C ua n d o los d a tos de p la ca de e n sa yo fue ron re ch a za d o s se lleva ron a cab o e x p e rim e n to s ad ic io n a les . T o d a s las cu rva s d o s is -re s p u e s ta se g e n e ra ron u tilizando G rap h P a d P rism . Las cu rva s se a jus tan m ed ia n te la u tiliza c ió n de la e cu a c ió n "d o s is -re sp u e s ta s ig m o ide a (pe n d ie n te va ria b le )" d o n de el p a rá m e tro in fe rio r se fija en "0". El p a rá m e tro de su p e rio r se f ija en "100 " pa ra p re d e c ir m e jo r los va lo re s de p o te n c ia cu a n d o un a cu rva co m p le ta no se ha g e n e ra d o p o r las c o n c e n tra c io n e s su je ta s a en sa yo .
Los d a tos de la ac tiv idad a n ta g o n is ta pa ra c o m p u e s to s rep re se n ta tivo s p re p a ra d o s de co n fo rm id a d con los m é todos s in té tico s d e sc rito s en la p re sen te se p re sen tan en la T ab la 2.
T a b la 2. D a tos b io ló g ico s in v itro pa ra co m p u e s to s rep re se n ta tivo s de F ó rm u la I-XII. A m enos qu e se ind ique lo co n tra rio , los c o m p u e s to s que se p ro b a ro n te n ían un IC 50 de m enos de 50 pM en el e n sa yo fu n c io n a l de flu jo LP A 1R de C a 2+ .
A m enos qu e se ind ique lo co n tra rio , los c o m p u e s to s qu e se p ro ba ron te n ían un IC50 de m enos de 50 pM en el e n sa yo fu n c io n a l de flu jo LP A 1R de C a 2+ . A = m en o r a 0.3 pM ; B = m a yo r a 0.3 pM y m en o s a 1 pM ; C = m ayo r a 1 pM y m e n o r a 50 pM ; D = m a yo r a 50 pM
C IT A S
1) G yo rko s A. C., C o rre tte C. P., C hoS . Y ., T u rn e r T. M., A so K., Kori M., G yo ten M., C o n d ro sk i K. R., S iedem C. S., B oyd S. A. W O 2005099688 , 2005
2) M aiti, S w a ru p a n a n d a ; S ridha ran , V e lla isa m y ; M enendez , J. C a rlos ; Jo u rn a l o f C o m b in a to r ia l C hem is try , 2010 , vo l. 12, # 5 p. 713 - 722
3) T a ka g i M., N a ka m u ra T., M a tsu d a I., K iguch i T., O g a w a N., O zek i H. U S 2009 /36450 A 1 ,2009
4) Lee, Len F.; S ch le p p n ik , F ranc is M .; H ow e, R obert K.; Jo u rn a l o f H e te ro cyc lic C hem is try , 1985, vo l. 22, p.
1621 - 1630
5) D ehm e l, F lorian ; A ba rb ri, M oham ed ; K noche l, Pau l; S yn le tt, 2000 , # 3 p. 345 - 346
6) A b a rb ri, M oh a m e d ; T h ib o n n e t, Je ro m e ; B erillon , K au ren t; D ahm e l, F lo rian ; R o ttlaende r, M ario ; K noche l, P au l; Jo u rn a l o f O rga n ic C hem is try , 2000 , vo l. 65, # 15 p. 4618 - 4634
7) G a g no n e t a l.; C a nad ian Jo u rn a l o f C h e m is try , 1953, vo l. 31, p. 673 ,682
8) M alk i, Fatiha ; T oua ti, A b d e lka d e r; R ahal, S a id ; M ou lay, S aad ; A s ian Jo u rn a l o f C h e m is try , 2011 , vo l. 23, # 3 p. 961 - 967
9) O h a ta S., K a to K., T o riya b e K., Ito Y ., H a m ag u ch i R., N akano Y., E P 2202226 A 1 ,2010
10) M ae ka w a T., H a ra R., O d a ka H., K im u ra H., M izu fu n e H., F uka tsu K., W O 03099793 , 2003
11) S am , S ik K im ; Bo, S eung C ho i; Jae , H oon Lee; Ki, Kon Lee; Tae , H ee Lee; S h in , H yun ik ; Y o u n g , Ho K im ; S yn le tt, 2009 , # 4 p. 599 - 602
12) Z hu , Y u lin ; Pan, Y u a n jia n g ; H uang, S h e n lin ; S yn th e tic C o m m u n ica tio n s , 2004 , vo l. 34, # 17 p. 3167 - 3174 13) P a thak, V ija i N a th ; G up ta , R ag in i; V a rsh n ey , B indu ; Ind ian Jo u rn a l o f C h e m is try , S ec tion B: O rga n ic C h e m is try Inc lud ing M ed ic ina l C h e m is try , 2008 , vo l. 47, # 3 p. 434 - 438
14) P ierre, F abrice ; O 'B rien , S ean E.; H addach , M ustapha ; B ou rbon , P au line ; S ch w a e b e , M ichae l K .; S te fan , E ric; D arjan ia , Levan ; S tans fie ld , R yan; Ho, C a ro lin e ; S id d iq u i-Ja in , A d a m ; S tre ine r, N ico le ; R ice, W illiam G.; A n d e res , K enna ; R yckm an, D avid M.; B io o rg a n ic and M ed ic ina l C h e m is try Le tte rs , 2011, vo l. 21, # 6 p. 1687 - 1691
15) B oes M., G a lle y G ., G ode l T., H o ffm a n n T., H u n ke le r W ., S ch n id e r P., S ta d le r H. U S 6756380 , 2004 16) A issa o u i H., B oss C., H azem ann J., K o be rs te in R., S ie g ris t R., S iffe rle n T. U S 2011105491 ,2011
17) An S., D ickens M. A ., B leu T., H a llm a rk O. G., G oe tz l E. J. B ioch e m ica l and B io p h ys ica l R esearch C o m m u n ica tio n s (1997) 231,619 -622
18) P S ch e n o n e , P Fossa , G M enozz i, (1991 ) Jo u rn a l o f H e te ro cyc lic C h e m is try , 1991, vo l. 28, # 2 p. 453 - 457 19) T K im ura , N O hkaw a , A N akao , T N agasak i, T S h im o za to , (2006). E P 1632488 A 1 ,
20) ND S m ith , SP G ovek, M K a h ra m a n , JD Ju lien , JY N agasaw a , KL D oug las, C L B onne fous , AG Lai. (2013) W O 2013 /142266 A1
21) B C o ttyn , F T e rrie r, D V ich a rd , P N ioche , P ie rre ; R am an . 2007.
S yn le tt, # 8 p. 1203 - 1206
22) S L B uchw a ld , TD S eneca l, W S hu, W e i. (2013) A n g e w a n d te C h e m ie - In te rn a tio n a l E d ition , 2013, vo l. 52, # 38 p.
10035 - 10039.
23) X G uo, W Hu, H H uang , (2007) A n g e w a n d te C h e m ie - In te rn a tio n a l Ed ition , 2007 , vo l. 46, # 8 p. 1337 - 1339 24) S K S hah , Q T T ru o n g , H Qi, W K H a gm ann (2005). W O 2005044785A 1
S e hace re fe re n c ia a d ic io n a lm e n te a los d o cu m e n to s W O 2013 /025733 y W O 2012 /138648.
Claims (1)
- REIVINDICACIONES1. Un compuesto donde el compuesto tiene la estructura de fórmula Io una sal farmacéuticamente aceptable de este,donde RA es -CO2H, -CO2RB, -CN, tetrazolilo, -C(=O)NH2 , -C(=O)NHRB,-C(=O)NHSO2Rb o -C(=O)NHCH2CH2SO3H o un ácido isostero carboxílico seleccionado del grupo que consiste endonde RB es -H o -alquilo C1-C4 , o tiene la estructura de uno de:L1 está ausente o es alquileno C1-C6 sustituido o no sustituido, cicloalquileno C3-C6 sustituido o no sustituido, fluoroalquileno C1-C6 , heteroalquileno C1-C6 sustituido o no sustituido;L2 está ausente;El anillo B es arileno sustituido o no sustituido, heteroarileno sustituido o no sustituido, donde si el anillo B está sustituido entonces el anillo B está sustituido con 1, 2 o 3 RH seleccionados independientemente; donde el anillo B tiene la estructura de:donde A1, A2 y A3 son independientemente -N=, =N-, =CH- o -CH=;El anillo A es un heteroareno de 5 miembros que se selecciona de uno de:donde la línea punteada indica el punto de unión del anillo A al anillo B;donde RC es -CN, -F, -Cl, -Br, -I, -Oalquilo C1 -C4 , o fluoroalquilo C1 -C4 ,y RD es -N(RF)-C(=O)XCH(RG)-CY, -N(RF)C(=O)XC(RG)2 -CY, -N(RF)C(=O)X-CY, -C(=O)N(RF)CH(RG)X-CY, o -C(=O)-N(Rf )C(Rg )2 X-CY, donde X está ausente, es -O-, -NH- o -CH2 -;RE es -H, -alquilo C1 -C4 o -fluoroalquilo C1 -C4 ;RF es -H o alquilo C1 -C4 ;RG se selecciona independientemente de RE, o un RG es alquilo C1 -C4 y se toma junto con el átomo de carbono al que se une RG y el carbono o heteroátomo al que se une CY para definir un carbociclo sustituido o no sustituido o un heterociclo sustituido o no sustituido, y el otro RG , si está presente, es como se define por RE ;CY es alquilo C1 -C6 sustituido o no sustituido, cicloalquilo C3 -C10 sustituido o no sustituido, heterocicloalquilo C2 -C10 sustituido o no sustituido, arilo sustituido o no sustituido, o heteroarilo sustituido o no sustituido, donde si CY está sustituido, entonces CY está sustituido con 1, 2, o 3 RH seleccionados independientemente;donde cada RH se selecciona independientemente de -H, halógeno, -CN, -NO2 , -OH, -ORJ, -SRJ, -S(=O)RJ, -S(=O)2 RJ, -N(RJ)S(=O)2 RJ, -S(=O)2N(RL)2 , -C(=O)RJ , OC(=O)RJ , -C(=O)ORJ, -OC(=O)ORJ, -N(RL)2 , -C(=O)N(RL)2 , -OC(=O)N(Rl )2 , -N(Rj )C(=O)N(Rl )2 , -N(Rj )C(=O)Rj , -N(Rj )C(=O)ORj , alquilo C1 -C4 , fluoroalquilo C1 -C4 , fluoroalcoxi C1 -C4 , alcoxi C1 -C4 , y heteroalquilo C1 -C4 ,donde cada RJ es independientemente alquilo C1 -C6 sustituido o no sustituido, heteroalquilo C1 -C6 sustituido o no sustituido, fluoroalquilo C1 -C6 , cicloalquilo C3 -C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo C3 -C6 sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o alquileno-C1-C4-(heteroarilo sustituido o no sustituido);donde cada RL es independientemente -H, alquilo C1 -C6 sustituido o no sustituido, heteroalquilo C1 -C6 sustituido o no sustituido, fluoroalquilo C1 -C6 , cicloalquilo C3 -C6 sustituido o no sustituido, heterocicloalquilo sustituido o no sustituido, arilo sustituido o no sustituido, heteroarilo sustituido o no sustituido, alquileno-C1-C4-(cicloalquilo sustituido o no sustituido), alquileno-C1-C4-(heterocicloalquilo sustituido o no sustituido), alquileno-C1-C4-(arilo sustituido o no sustituido), o alquileno-C1 -C4 -(heteroarilo sustituido o no sustituido),o cuando RH es -S(=O)2 N(RL)2 , -N(RL)2 , -C(=O)N(RL)2 , -OC(=O)N(RL)2 o N(RF)C(=O)N(RL)2 , cada RL es independientemente -H o alquilo C1 -C6 , o los grupos RL son independientemente alquilo C1 -C6 que se toman junto al átomo de N al que están unidos para definir un heterociclo sustituido o no sustituido;El anillo C es cicloalquileno C3 -C10 sustituido o no sustituido, heterocicloalquileno C2 -C10 sustituido o no sustituido, arileno sustituido o no sustituido, o heteroarileno sustituido o no sustituido, donde si el anillo C está sustituido entonces el anillo C está sustituido con 1, 2 o 3 RH seleccionados independentemente, donde RH es como se ha definido previamente, donde si RJ , RL y o RH está sustituido, está sustituido con uno o más seleccionados entre alquilo, cicloalquilo, arilo, heteroarilo, heteroalicíclico, hidroxi, alcoxi, ariloxi, alquiltio, ariltio, alquilsulfóxido, arilsulfóxido, alquilsulfona, arilsulfona, ciano, halo, nitro, haloalquilo, fluoroalquilo, fluoroalcoxi y amino, incluidos grupos amino mono- y disustituidos, -CN, NO2 o LsRs, donde cada Ls se selecciona independientemente entre un enlace, -O-, -C(=O)-, -C(=O)O-, -S-, -S(=O)-, -S(=O)2 -, -NH-, -NHC(=O)-, -C(=O)NH-, S(=O)2 NH-, -NHS(=O)2 , -OC(=O)NH-, -NHC(=O)O-, o -(alquileno C1 -C6 )-; y cada Rs se selecciona entre -H, alquilo, fluoroalquilo, heteroalquilo, cicloalquilo, arilo, heteroarilo o heterocicloalquilo.2. El compuesto de la reivindicación 1 donde RD es -N(RF)-C(=O)XCH(RG)-CY, -N(RF)C(=O)XC(RG)2 -CY, -N(Rf )C(=o )X-CY, donde RF y cada RG son independientemente -H o alquilo C1 -C4.3. El compuesto de la reivindicación 2 donde el anillo A tiene la estructura:donde el anillo B es arileno sustituido o no sustituido y el anillo C es arileno sustituido o no sustituido o es cicloalquileno C3 -C10 sustituido o no sustituido.4. El compuesto de la reivindicación 2 donde L1 está ausente o es un alquileno C1 -C4 sustituido o no sustituido o un cicloalquileno C3 sustituido o no sustituido.7. E l c o m p u e s t o d e la r e iv i n d ic a c ió n 2 d o n d e X e s - N H - u - O ; d o n d e R G y c a d a R F , s e l e c c io n a d o s i n d e p e n d ie n t e m e n t e , s o n - H o - a lq u i lo C 1 ; d o n d e - C Y e s a r i l o s u s t i t u id o c o n 1 o 2 R H s e l e c c io n a d o s in d e p e n d ie n t e m e n t e e n t r e - H , - F , - C l o - a lq u i lo C 1.8. E l c o m p u e s t o d e la r e iv i n d ic a c ió n 2 , d o n d e e l a n i l l o C e s a r i l e n o s u s t i t u i d o o n o s u s t i t u id o , d o n d e s i e l a n i l l o C e s t á s u s t i t u i d o e n t o n c e s e l a n i l l o C e s t á s u s t i t u id o c o n 1 R H s e l e c c io n a d o e n t r e - F , - C l o - a lq u i lo C 1.9. E l c o m p u e s t o d e la r e i v i n d i c a c ió n 5 , d o n d e e l c o m p u e s t o t i e n e la e s t r u c t u r ad o n d e A 2 e s = C H - o = N - ; d o n d e e l a n i l l o A e s u n h e t e r o a r e n o d e 5 m ie m b r o s q u e t i e n e la e s t r u c t u r a d e :d o n d e R D e n la r e iv i n d ic a c ió n 2 a n t e r i o r e s - N ( R F) - C ( = O ) O C H ( R G) - C Y y d o n d e C Y e s f e n i l o s u s t i t u id o c o n u n R H ; R A e s - C O 2 H o - C O 2 R BR G e s - H o - C H 3 ;R H s o n in d e p e n d ie n t e m e n t e - H , h a ló g e n o , - C H 3 o - C F 3 .10. E l c o m p u e s t o d e la r e iv i n d ic a c ió n 2 d o n d e e l c o m p u e s t o s e s e l e c c io n a e n t r e : á c i d o 2 -[ 4 -[ 4 -[ 5 -[ 1 -( 2 -c l o r o f e n i l ) e t o x i c a r b o n i l a m i n o ] - 4 - c ia n o - p i r a z o l - 1 - i l ] f e n i l ] f e n i l ] a c é t i c o , á c id o ( R ) - 1 -( 4 ' - { 5 -[ 1 -( 2 - c l o r o - f e n i l ) -e t o x i c a r b o n i l a m i n o ] - 4 - f l u o r o - p i r a z o l - 1 - i l } - 3 - f l u o r o - b i f e n i l - 4 - i l ) - c i c l o p r o p a n o c a r b o x í l i c o , á c id o ( R ) - 1 -( 4 ' - { 5 -[ 1 -( 2 - c l o r o -f e n i l ) - e t o x ic a r b o n i l a m i n o ] - 4 - f l u o r o - p i r a z o l - 1 - i l } - 2 - f l u o r o - b i f e n i l - 4 - i l ) - c i c l o p r o p a n o c a r b o x í l i c o , á c id o ( R ) - 1 -( 2 - c lo r o - 4 ' - { 5 -[1 -( 2 - c l o r o - f e n i l ) - e t o x i c a r b o n i l a m in o ] - 4 - f l u o r o - p i r a z o l - 1 - i l } - b i f e n i l - 4 - i l ) - c i c l o p r o p a n o c a r b o x í l i o , á c id o ( R ) - 1 -( 4 ' - { 5 -[ 1 -( 2 -c l o r o - f e n i l ) - e t o x i c a r b o n i l a m i n o ] - 4 - f l u o r o - p i r a z o l - 1 - i l } - 2 - m e t i l b i f e n i l - 4 - i l ) - c i c l o p r o p a n o c a r b o x í l i c o , á c i d o ( R ) - 1 -( 4 ' - { 5 -[ 1 -( 2 - c lo r o - f e n i l ) - e t o x i c a r b o n i l a m in o ] - 4 - f l u o r o - p i r a z o l - 1 - i l } - b i f e n i l - 4 - i l ) - c i c l o p r o p a n o c a r b o x í l i c o , á c i d o ( R ) - 1 - { 4 ' -[ 5 -( 1 - f e n i l -e t o x i c a r b o n i l a m i n o ) - 4 - t r i f l u o r o m e t i l - p i r a z o l - 1 - i l ] - b i f e n i l - 4 - i l } - c i c l o p r o p a n o c a r b o x í l i c o , á c i d o ( R ) - 1 - { 2 - f lu o r o - 4 ' -[ 5 -( 1 - f e n i l -e t o x i c a r b o n i l a m i n o ) - 4 - t r i f l u o r o m e t i l - p i r a z o l - 1 - i l ] - b i f e n i l - 4 - i l } - c i c l o p r o p a n o c a r b o x í l i c o , á c i d o 2 -[ 4 -[ 4 -[ 4 - c ia n o - 5 -( 1 -f e n i l e t o x i c a r b o n i l a m i n o ) p i r a z o l - 1 - i l ] f e n i l ] f e n i l ] a c é t i c o , á c id o 1 -[ 4 -[ 4 -[ 4 - c ia n o - 5 -( 1 - f e n i l e t o x i c a r b o n i l a m in o ) p i r a z o l - 1 -i l ] f e n i l ] f e n i l ] c i c l o p r o p a n o c a r b o x í l i c o , á c i d o 1 -[ 4 -[ 4 -[ 5 -[ 1 -( 2 - c l o r o f e n i l ) e t o x i c a r b o n i l a m i n o ] - 4 - c i a n o - p i r a z o l - 1 -i l ] f e n i l ] f e n i l ] c i c l o p r o p a n o c a r b o x í l i c o , á c id o 2 -[ 4 -[ 4 -[ 4 - c ia n o - 5 -( 1 - f e n i l e t o x i c a r b o n i l a m in o ) p i r a z o l - 1 - i l ] f e n i l ] f e n i l ] - 2 - m e t i l -p r o p a n o ic o , á c i d o 2 -[ 4 -[ 4 -[ 5 -[ 1 -( 2 - c l o r o f e n i l ) e t o x i c a r b o n i l a m i n o ] - 4 - c i a n o - p i r a z o l - 1 - i l ] f e n i l ] f e n i l ] - 2 - m e t i l - p r o p a n o i c o , á c id o 1 - { 4 ' -[ 4 - f l u o r o - 5 -( 1 - f e n i l e t o x i c a r b o n i l a m in o ) - 1 H - p i r a z o l - 1 - i l ] - 4 - b i f e n i l i l } c i c l o p r o p a n o c a r b o x í l i c o , á c i d o 1 -( 4 ' - { 5 -[ 1 -( o - c l o r o f e n i l ) e t o x i c a r b o n i l a m in o ] - 4 - f l u o r o - 1 H - p i r a z o l - 1 - i l } - 4 - b i f e n i l i l ) c i c l o p r o p a n o c a r b o x í l i c o , á c i d o 1 - { 3 - f l u o r o - 4 ' -[ 4 -f lu o r o - 5 -( 1 - f e n i le t o x i c a r b o n i la m in o ) - 1 H - p i r a z o l - 1 - i l ] - 4 - b i f e n i l i l } c i c l o p r o p a n o c a r b o x í l i c o , á c i d o 1 -( 4 ' - { 5 -[ 1 -( o c lo ro fe n il)e to x ica rb o n ila m in o ]-4 -flu o ro -1 H -p irazo l-1 - il}-3 -flu o ro -4 -b ife n ilil)c ic lo p ro p a n o ca rb o x ílico , á c ido 1 -{2 -flu o ro -4 '-[4 -fluo ro -5 -(1 -fen ile to x ica rb on ila m in o )-1 H -p irazo l-1 - il]-4 -b ife n ilil}c ic lo p ro p a n o ca rb o x ílico , 1 -(4 '-{5-[1 -(oc lo ro fe n il)e to x ica rb o n ila m in o ]-4 -flu o ro -1 H -p irazo l-1 - il}-2 -flu o ro -4 -b ife n ilil)c ic lo p ro p a n o ca rb o x ílico , ác ido 1 -(2 -c lo ro -4 '-{5-[1 -(o -c lo ro fe n il)e to x ica rb o n ila m in o ]-4 -flu o ro -1 H -p irazo l-1 - il} -4 -b ife n ilil)c ic lo p ro p a n o ca rb o x ílico , ác ido 1 -(4 -{p -[4 -fluo ro -5 -(1 - fe n ile to x ica rb on ila m in o )-1 H -p irazo l-1 - il]fen il}to lil)c ic lo p ro p a n o ca rb o x ílico , á c ido 1 -[4-(p-{5 -[1 -(oc lo ro fe n il)e to x ica rb o n ila m in o ]-4 -flu o ro -1 H -p irazo l-1 - il} fe n il) to lil]c ic lo p ro p a n o ca rb o x ílico , á c ido 1 -(p -{5 -[4 -flu o ro -5 -(1 -fe n ile to x ica rb o n ila m in o )-1 H -p irazo l-1 - il]-2 -p irid il}fe n il)c ic lo p ro p a n o ca rb o x ílico , ác ido 1 -[p-(5-{5 -[1 -(oc lo ro fe n il)e to x ica rb o n ila m in o ]-4 -flu o ro -1 H -p irazo l-1 - il}-2 -p ir id il) fe n il]c ic lo p ro p a n o ca rb o x ílico , á c ido 1 -(2 -flu o ro -4 -{5 -[4 -fluo ro -5 -(1 - fe n ile to x ica rb on ila m in o )-1 H -p irazo l-1 - il]-2 -p ir id il}fe n il)c ic lo p ro p a n o ca rb o x ílico , ác ido 1 -[4-(5-{5 -[1 -(oc lo ro fe n il)e to x ica rb o n ila m in o ]-4 -flu o ro -1 H -p irazo l-1 - il}-2 -p ir id il) -2 -flu o ro fe n il]c ic lo p ro p a n o ca rb o x ílico , á c ido 1 -(3 -flu o ro -4 -{5 -[4 -flu o ro -5 -(1 - fe n ile to x ica rb on ila m in o )-1 H -p irazo l-1 - il]-2 -p ir id il}fe n il)c ic lo p ro p a n o ca rb o x ílico , ác ido 1 -[4-(5-{5 -[1 -(o -c lo ro fe n il)e to x ica rb o n ila m in o ]-4 -flu o ro -1 H -p irazo l-1 - il}-2 -p ir id il) -3 -flu o ro fe n il]c ic lo p ro p a n o ca rb o x ílico , á c ido 1 -(p -{5 -[4 -c iano -5 -(1 - fe n ile to x ica rb on ila m in o )-1 H -p irazo l-1 - il]-2 -p ir id il}fe n il)c ic lo p ro p a n o ca rb o x ílico , ác ido 1 -[p-(5-{5 -[1 -(oc lo ro fe n il)e to x ica rb o n ila m in o ]-4 -c ia n o -1 H -p irazo l-1 - il}-2 -p ir id il) fe n il]c ic lo p ro p a n o ca rb o x ílico , á c ido 1 -(4 -{5 -[4 -c ia n o -5 -(1 - fe n ile to x ica rb on ila m in o )-1 H -p irazo l-1 - il]-2 -p ir id il}-2 -flu o ro fe n il)c ic lo p ro p a n o ca rb o x ílico , ác ido 1 -[4-(5-{5 -[1 -(oc lo ro fe n il)e to x ica rb o n ila m in o ]-4 -c ia n o -1 H -p irazo l-1 - il}-2 -p ir id il) -2 -flu o ro fe n il]c ic lo p ro p a n o ca rb o x ílico , ác ido 1 -(4 -{5 -[4 -c iano -5 -(1 - fe n ile to x ica rb on ila m in o )-1 H -p irazo l-1 - il]-2 -p ir id il}-3 -flu o ro fe n il)c ic lo p ro p a n o c a rb o x ílic o y ác ido 1 -[4-(5-{5 -[1 -(o -c lo ro fe n il)e to x ica rb o n ila m in o ]-4 -c ia n o -1 H -p ira zo l-1 -il} -2 -p ir id il) -3 -flu o ro fe n il]c ic lo p ro p a n o ca rb o x ílico .11. El c o m p u e s to de la re iv in d icac ió n 10 d o n de e l co m p u e s to es á c ido 2 -[4 -[4 -[5 -[1 -(2 -c lo ro fe n il)e to x ic a rb o n ila m in o ]-4 -c ian o -p ira zo l-1 -il]fe n il]fe n il]a cé tico , ác ido (R )-1 -(4 '-{5 -[1 -(2 -c lo ro -fe n il)-e to x ic a rb o n ila m in o ]-4 -flu o ro -p ira z o l-1 - il} -3 -flu o ro -b ife n il-4 - il) -c ic lo p ro p a n o c a rb o x ílic o , ác ido (R)-1 -(4 '-{5-[1 - (2 -c lo ro -fe n il)-e to x ica rb o n ila m in o ]-4 -flu o ro -p ira zo l-1 -il}-2 -flu o ro -b ife n il-4 - il) -c ic lo p ro p a n o ca rb o x ílico , ác ido (R)-1 -(2 -c lo ro -4 '-{5 -[1 -(2 -c lo ro -fe n il)-e to x ica rb o n ila m in o ]-4 -fluo ro -p irazo l-1 - il}-b ife n il-4 - il) -c ic lo p ro p a n o ca rb o x ílico , ác ido (R)-1 -(4 '-{5-[1 -(2 -c lo ro -fe n il)-e to x ica rb o n ila m in o ]-4 -fluo ro -p irazo l-1 - il}-2 -m e tilb ife n il-4 -il) -c ic lo p ro p a n o ca rb o x ílico , á c ido (R)-1 -(4 '-{5-[1 -(2 -c lo ro -fe n il)-e to x ica rb o n ila m in o ]-4 -fluo ro -p ira zo l-1 - il} -b ife n il-4 - il) -c ic lo p ro p a n o ca rb o x ílico , á c ido (R )- 1 -{4 '-[5 -(1 - fe n il-e to x ica rb o n ila m in o )-4 -tr if lu o ro m e til-p irazo l-1 - il]-b ife n il-4 -il} -c ic lo p ro p a n o c a rb o x ílic o o ác ido (R)-1 -{2 -fluo ro -4 '-[5 -(1 - fe n il-e to x ica rb o n ila m in o )-4 -tr iflu o ro m e til-p ira z o l-1 - il]-b ife n il-4 - il} -c ic lo p ro p a n o c a rb o x ílic o .12. El co m p u e s to de la re iv in d icac ió n 10 d o n d e e l co m p u e s to es á c ido (R )-1 -(4 '-{5 -[1 -(2 -c lo ro -fe n il)-e to x ic a rb o n ila m in o ]-4 -flu o ro -p ira z o l-1 - il} -2 -flu o ro -b ife n il-4 -il)-c ic lo p ro p a n o c a rb o x ílic o .13. El co m p u e s to de la re iv in d icac ió n 1 pa ra uso en m ed ic ina .14. Un m e d ica m e n to p a ra uso en el tra ta m ie n to de un su je to con un a e n fe rm e d a d o a fecc ió n d e p en d ie n te de l ác ido liso fo s fa tíd ico , qu e c o m p re n d e e l co m p u e s to de la re iv in d icac ió n 1, d o n de la e n fe rm e d a d o a fecc ió n d e p en d ie n te del á c ido liso fo s fa tíd ico se se le cc io n a e n tre fib ro s is de ó rg a n o s in c lu idos h ígado , riñón, pu lm ón y co ra zó n ; e n fe rm e d a d e s de l h ígado inc lu id a s hep a titis aguda , hepa titis c rón ica , fib ro s is hepá tica , c irro s is hepá tica , h ipe rte n s ió n po rta l, in su fic ie n c ia rege n e ra tiva , e s te a to h e p a tit is no a lco h ó lica (E H N A ), h ip o fun c ió n h e p á tica y tra s to rn o de l flu jo sa n g u ín e o hepá tico ; e n fe rm e d a d p ro life ra tiva ce lu la r, co m o cá n ce re s inc lu idos , a m odo no ta xa tivo , tu m o r só lido , m e tá s ta s is de tu m o r só lido , f ib ro m a va scu la r, m ie lom a , m ie lo m a m ú ltip le , sa rco m a de K apos i, leucem ia , leu ce m ia lin fo c ítica c ró n ica (LLC ), m e tá s ta s is in va s iva de las cé lu la s c a n ce ro sa s ; e n fe rm e d a d e s in fla m a to ria s inc lu idas , a m odo no ta xa tivo , pso ria s is , ne fro p a tía , ne u m o n ía ; e n fe rm e d a d e s de l tra c to g a s tro in te s tin a l in c lu idos , a m odo no ta xa tivo , s ín d ro m e de l in te s tin o irritab le (S II), e n fe rm e d a d in fla m a to ria in tes tina l (E II), secre c ió n p a n c re á tica a n o rm a l; e n fe rm e d a d e s rena les, e n fe rm e d a d e s a so c ia d as al tra c to u rina rio inc lu idas , a m odo no ta xa tivo , h ip e rp la s ia p ro s tá tica b e n ig n a o s ín to m a s a so c ia d os a la e n fe rm e da d de la v e jig a neu ro p á tica , tu m o r en la m éd u la esp ina l, h e rn ia de d isco in te rve rte b ra l, e s te n o s is de l cana l esp in a l, s ín to m a s d e riva d o s de la d iabe te s , e n fe rm e d a d e s de l tra c to u rina rio in fe rio r inc lu ida , a m odo no ta xa tivo , o b s tru cc ió n de l tra c to u rina rio in fe rio r, e n fe rm e d a d e s in fla m a to ria s de l tra c to u rina rio in fe rio r inc lu idas , a m odo no ta xa tivo , d isu ria , m icc ión fre cu e n te ; e n fe rm e d a d e s de l p á n creas , e n fe rm e d a d e s a so c ia d as a la a n g io g é n e s is ano rm a l inc lu ida , a m odo no ta xa tivo , o b s tru cc ió n a rte ria l; e sc le ro d e rm ia , e n fe rm e d a d e s a s o c ia d a s al ce re b ro inc lu idos , a m odo no taxa tivo , in fa rto ce re b ra l, h e m o rra g ia ce re b ra l; e n fe rm e d a d e s de l s is te m a ne rv io so inc lu idos , a m odo no ta xa tivo , d o lo r neu ro p á tico , n e u ro p a tía pe rifé rica , p ru rito ; y e n fe rm e d a d e s o cu la re s inc lu idas , a m odo no taxa tivo , d e g en e ra c ió n m a cu la r a so c ia d a a la edad (D M A E ), re tin o p a tía d ia b é tica , v itre o rre tin o p a tía p ro life ra tiva (VR ), p e n figo id e c ica tric ia l, c ica tr ice s de c iru g ía de filtrac ión de g la u co m a .15. El c o m p u e s to de la re iv in d icac ió n 10 d o n de e l co m p u e s to es ác ido 1 -{4 '-[4 -flu o ro -5 -(1 -fe n ile to x ica rb o n ila m in o )-1 H -p ira zo l-1 -il]-4 -b ife n ilil}c ic lo p ro p a n o ca rb o x ílico .16. El co m p u e s to de la re iv in d icac ió n 1 pa ra uso en un m é to d o de tra ta m ie n to de una e n fe rm e d a d o a fecc ión d e p en d ie n te de l ác ido liso fo s fa tíd ico en un su je to qu e lo neces ita , c a ra c ta r iza d o p o r qu e se a d m in is tra al su je to una ca n tid ad te ra p é u tic a m e n te e ficaz de l c o m p u e s to de la re iv in d icac ió n 1, d o n d e la e n fe rm e da d o a fecc ión d e p e n d ie n te de l ác ido liso fo s fa tíd ico se se le cc io n a e n tre fib ro s is de ó rg a n o s inc lu id o s h ígado, riñón , pu lm ón y co ra zó n ; e n fe rm e d a d e s de l h ígado inc lu id a s hep a titis aguda , hepa titis c rón ica , fib ro s is hepá tica , c irro s is hepá tica , h ipe rte n s ió n po rta l, in su fic ie n c ia rege n e ra tiva , e s te a to h e p a tit is no a lco h ó lica (E H N A ), h ip o fun c ió n h e p á tica y tra s to rn o de l flu jo sa n g u ín e o hepá tico ; e n fe rm e d a d p ro life ra tiva ce lu la r, co m o cá n ce re s inc lu idos , a m odo no ta xa tivo , tu m o r só lido , m e tá s ta s is de tu m o r só lido , f ib ro m a va scu la r, m ie lom a , m ie lo m a m ú ltip le , sa rco m a de K apos i, leucem ia , leu ce m ia a so c ia d a s al tra c to u rina rio inc lu idas , a m odo no ta xa tivo , h ip e rp la s ia p ro s té tica b e n ig n a o s ín to m a s a so c ia d os a la e n fe rm e d a d de la v e jig a neu ro p á tica , tu m o r en la m éd u la esp in a l, h e rn ia de d isco in te rve rte b ra l, e s te n o s is de l cana l esp in a l, s ín to m a s d e riva d o s de la d ia b e te s , e n fe rm e d a d e s de l tra c to u rina rio in fe rio r inc lu ida , a m odo no taxa tivo , o b s tru cc ió n de l tra c to u rina rio in fe rio r, e n fe rm e d a d e s in fla m a to ria s de l trac to u rina rio in fe rio r inc lu idas , a m odo no ta xa tivo , d isu ria , m icc ión fre c u e n te ; e n fe rm e d a d e s de l p á n c re a s , e n fe rm e d a d e s a so c ia d as a la a n g io g é n e s is ano rm a l inc lu ida , a m odo no ta xa tivo , o b s tru cc ió n a rte ria l; e sc le ro d e rm ia , e n fe rm e d a d e s a so c ia d as al ce re b ro inc lu idos , a m odo no ta xa tivo , in fa rto ce re b ra l, h e m o rra g ia ce re b ra l; e n fe rm e d a d e s de l s is te m a ne rv io so inc lu id o s , a m odo no ta xa tivo , d o lo r n e u ro p á tico , n e u ro p a tía p e rifé rica , p ru rito ; y e n fe rm e d a d e s o cu la re s inc lu idas , a m odo no taxa tivo , d e g e n e ra c ió n m a cu la r a so c ia d a a la edad (D M A E ), re tin o p a tía d ia b é tica , v itre o rre tin o p a tía p ro life ra tiva (VR), p e n fig o id e c ica tric ia l, c ica trice s de c iru g ía de filtra c ió n de g la u co m a .21. El c o m p u e s to pa ra uso de a cu e rd o con la re iv in d icac ió n 20 d o n d e la e n fe rm e d a d o a fecc ió n d e p e n d ie n te de l ác ido liso fo s fa tíd ico es fib ro s is de los ó rga n o s .22. El c o m p u e s to pa ra uso de a cu e rd o con la re iv in d icac ió n 20 d o n d e la e n fe rm e d a d o a fecc ió n d e p e n d ie n te de l ác ido liso fo s fa tíd ico es un a e n fe rm e d a d hepática .23. El c o m p u e s to pa ra uso de a cu e rd o con la re iv in d icac ió n 20 d o n d e la e n fe rm e d a d o a fecc ió n d e p e n d ie n te de l ác ido liso fo s fa tíd ico es un a e n fe rm e d a d renal.24. El c o m p u e s to pa ra uso de a cu e rd o con la re iv in d icac ió n 20 d o n d e la e n fe rm e d a d o a fecc ió n d e p e n d ie n te de l ác ido liso fo s fa tíd ico es n e fro p a tía d iab é tica .25. U na fo rm u la c ió n fa rm a c é u tic a m e n te a ce p ta b le q ue c o m p re n d e un c o m p u e s to de un a cu a lq u ie ra de las re iv in d ica c io n e s 10-12, 15 y uno o m ás e xc ip ie n te s fa rm a c é u tic a m e n te ace p ta b le s .
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201361801426P | 2013-03-15 | 2013-03-15 | |
| US201361801231P | 2013-03-15 | 2013-03-15 | |
| US201361827409P | 2013-05-24 | 2013-05-24 | |
| PCT/US2014/030712 WO2014145873A2 (en) | 2013-03-15 | 2014-03-17 | Heterocyclic compounds useful in the treatment of disease |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2855173T3 true ES2855173T3 (es) | 2021-09-23 |
Family
ID=51538557
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES14762555T Active ES2855173T3 (es) | 2013-03-15 | 2014-03-17 | Compuestos heterocíclicos útiles para el tratamiento de una enfermedad |
Country Status (16)
| Country | Link |
|---|---|
| US (5) | US10000459B2 (es) |
| EP (1) | EP2988743B1 (es) |
| JP (3) | JP6482086B2 (es) |
| KR (1) | KR102090231B1 (es) |
| CN (3) | CN105142635B (es) |
| AU (3) | AU2014232383B2 (es) |
| BR (2) | BR112015023267B1 (es) |
| CA (1) | CA2906931C (es) |
| DK (1) | DK2988743T3 (es) |
| EA (1) | EA033923B1 (es) |
| ES (1) | ES2855173T3 (es) |
| HK (1) | HK1221167A1 (es) |
| MX (2) | MX2015013303A (es) |
| PT (1) | PT2988743T (es) |
| SG (3) | SG11201507459YA (es) |
| WO (1) | WO2014145873A2 (es) |
Families Citing this family (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2019246109A1 (en) * | 2018-06-18 | 2019-12-26 | Epigen Biosciences, Inc. | Heterocyclic compounds useful in the treatment of disease |
| DK2988743T3 (da) * | 2013-03-15 | 2021-03-01 | Epigen Biosciences Inc | Heterocykliske forbindelser, der kan anvendes til behandling af sygdom |
| US20180360803A1 (en) * | 2015-11-20 | 2018-12-20 | Ube Industries, Ltd. | Pharmaceutical composition for treatment or prevention of nash |
| KR102292989B1 (ko) * | 2017-03-29 | 2021-08-26 | 재단법인 아산사회복지재단 | S1pr4를 타겟으로 하는 비알코올성 지방간염 예방 또는 치료용 조성물 |
| EP3728222B1 (en) * | 2017-12-19 | 2023-03-29 | Bristol-Myers Squibb Company | Cyclohexyl acid pyrazole azines as lpa antagonists |
| US11319309B2 (en) | 2017-12-19 | 2022-05-03 | Bristol-Myers Squibb Company | Cyclohexyl acid isoxazole azines as LPA antagonists |
| ES2942767T3 (es) | 2017-12-19 | 2023-06-06 | Bristol Myers Squibb Co | Isoxazol azoles del ácido ciclohexílico como antagonistas del LPA |
| JP7274486B6 (ja) | 2017-12-19 | 2024-02-15 | ブリストル-マイヤーズ スクイブ カンパニー | Lpaアンタゴニストとしてのトリアゾールn結合カルバモイルシクロヘキシル酸 |
| JP7212047B2 (ja) * | 2017-12-19 | 2023-01-24 | ブリストル-マイヤーズ スクイブ カンパニー | Lpaアンタゴニストとしてのシクロヘキシル酸ピラゾールアゾール |
| CN112041302A (zh) * | 2017-12-19 | 2020-12-04 | 百时美施贵宝公司 | 作为lpa拮抗剂的吡唑o-连接的氨基甲酰基环己基酸 |
| WO2019126099A1 (en) * | 2017-12-19 | 2019-06-27 | Bristol-Myers Squibb Company | Isoxazole n-linked carbamoyl cyclohexyl acids as lpa antagonists |
| EA202091500A1 (ru) | 2017-12-19 | 2020-09-14 | Бристол-Маерс Сквибб Компани | Пиразол n-связанные карбамоилциклогексильные кислоты в качестве антагонистов lpa |
| US11180488B2 (en) | 2017-12-19 | 2021-11-23 | Bristol-Myers Squibb Company | Isoxazole o-linked carbamoyl cyclohexyl acids as LPA antagonists |
| AU2019387370A1 (en) | 2018-11-30 | 2021-06-10 | Nuvation Bio Inc. | Pyrrole and pyrazole compounds and methods of use thereof |
| JOP20210298A1 (ar) | 2019-05-14 | 2023-01-30 | Provention Bio Inc | طرق وتركيبات للوقاية من مرض السكري من النوع الأول |
| US20240122934A1 (en) * | 2019-10-16 | 2024-04-18 | University Of South Florida | Compositions and methods of treatment for inhibiting capillary tube regression |
| US11548871B2 (en) | 2019-11-15 | 2023-01-10 | Gilead Sciences, Inc. | Triazole carbamate pyridyl sulfonamides as LPA receptor antagonists and uses thereof |
| AU2021282986B2 (en) | 2020-06-03 | 2024-03-07 | Gilead Sciences, Inc. | LPA receptor antagonists and uses thereof |
| TWI838626B (zh) | 2020-06-03 | 2024-04-11 | 美商基利科學股份有限公司 | Lpa受體拮抗劑及其用途 |
| IL298999A (en) | 2020-06-11 | 2023-02-01 | Provention Bio Inc | Methods and compositions for the prevention of type 1 diabetes |
| US20230250093A1 (en) * | 2020-07-16 | 2023-08-10 | Chiesi Farmaceutici S.P.A. | Amido cyclohexane acid derivatives as lpa receptor inhibitors |
| CN116669727A (zh) * | 2020-08-11 | 2023-08-29 | 唯久生物有限公司 | 作为lpa受体拮抗剂的三唑-吡啶基取代的氮杂环己基乙酸化合物 |
| CA3218917A1 (en) | 2021-05-11 | 2022-11-17 | Gilead Sciences, Inc. | Lpa receptor antagonists and uses thereof |
| AU2022405082A1 (en) | 2021-12-08 | 2024-07-11 | Gilead Sciences, Inc. | Lpa receptor antagonists and uses thereof |
| WO2024112895A1 (en) * | 2022-11-24 | 2024-05-30 | Lhotse Bio, Inc. | Compounds and compositions for treating conditions associated with lpa receptor activity |
Family Cites Families (40)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JO2308B1 (en) | 1999-05-31 | 2005-09-12 | اف. هوفمان- لاروش أيه جي | Derivatives of phenylpyrmidine |
| TWI288136B (en) * | 2000-02-18 | 2007-10-11 | Kirin Brewery | Novel isoxazole and thiazole compounds and use thereof as drugs |
| EP1364659B1 (en) | 2001-02-08 | 2009-11-11 | Ono Pharmaceutical Co., Ltd. | Remedies for urinary diseases comprising lpa receptor controlling agents |
| CA2487315A1 (en) | 2002-05-24 | 2003-12-04 | Takeda Pharmaceutical Company Limited | 1,2-azole derivatives with hypoglycemic and hypolipidemic activity |
| BRPI0411221A (pt) | 2003-06-11 | 2006-07-18 | Sankyo Co | composto, medicamento, métodos para inibir a produção de citocinas inflamatórias, e para a prevenção ou tratamento de doenças associadas com citocinas inflamatórias, método para o tratamento ou alìvio de febre, dor e/ou inflamação e, métodos para a prevenção ou tratamento de artrite reumatóide, de osteoartrite, de doença septicêmica, psorìase, doença de crohn, colite ulcerativa, diabete melito ou, hepatite |
| WO2005012269A1 (ja) | 2003-08-05 | 2005-02-10 | Ajinomoto Co., Inc. | 新規アゾール化合物 |
| US7390835B2 (en) | 2003-10-30 | 2008-06-24 | Merck & Co., Inc. | Aralkyl amines as cannabinoid receptor modulators |
| PL1732892T3 (pl) | 2004-03-26 | 2009-03-31 | Hoffmann La Roche | Tetrahydrokarbazole i pochodne |
| EP2522670A1 (en) | 2004-04-07 | 2012-11-14 | Takeda Pharmaceutical Company Limited | Heterocyclic CRF receptor antagonists |
| AU2006261841B8 (en) * | 2005-06-27 | 2012-12-06 | Exelixis Patent Company Llc | Pyrazole based LXR modulators |
| TW200803740A (en) * | 2005-12-16 | 2008-01-16 | Du Pont | 5-aryl isoxazolines for controlling invertebrate pests |
| EP2096111A1 (en) | 2006-11-20 | 2009-09-02 | Japan Tobacco Inc. | Pyrazoles and use thereof as drugs |
| BRPI0817844B1 (pt) | 2007-10-18 | 2018-10-23 | Ihara Chemical Ind Co | derivados de 3-alcóxi-1-fenilpirazol, pesticida, inseticida agrícola ou hortícola, acaricida, nematocida e método para o controle de uma peste campo técnico |
| US20110105491A1 (en) | 2008-07-07 | 2011-05-05 | Hamed Aissaoui | Thiazolidine compounds as orexin receptor antagonists |
| GB2466121B (en) | 2008-12-15 | 2010-12-08 | Amira Pharmaceuticals Inc | Antagonists of lysophosphatidic acid receptors |
| GB2470833B (en) | 2009-06-03 | 2011-06-01 | Amira Pharmaceuticals Inc | Polycyclic antagonists of lysophosphatidic acid receptors |
| CN102574822A (zh) * | 2009-08-04 | 2012-07-11 | 阿米拉制药公司 | 作为溶血磷脂酸受体拮抗剂的化合物 |
| JP4683154B2 (ja) | 2009-08-12 | 2011-05-11 | 横浜ゴム株式会社 | 冷媒移送用ホース |
| GB2474120B (en) * | 2009-10-01 | 2011-12-21 | Amira Pharmaceuticals Inc | Compounds as Lysophosphatidic acid receptor antagonists |
| GB2474748B (en) | 2009-10-01 | 2011-10-12 | Amira Pharmaceuticals Inc | Polycyclic compounds as lysophosphatidic acid receptor antagonists |
| WO2011159633A1 (en) | 2010-06-15 | 2011-12-22 | Amira Pharmaceuticals, Inc. | Inhalable formulations of lysophosphatdic acid receptor antagonists |
| US20130253019A1 (en) | 2010-06-15 | 2013-09-26 | John Howard Hutchinson | Lysophosphatidic acid receptor antagonists for the treatment of conditions or diseases of the eye |
| WO2011159635A1 (en) | 2010-06-15 | 2011-12-22 | Amira Pharmaceuticals, Inc. | Lysophosphatidic acid receptor antagonist for the treatment of dermal conditions |
| US20120031985A1 (en) | 2010-08-09 | 2012-02-09 | Terry Lien Do | Fault tolerant appliance |
| BR112013014019A2 (pt) | 2010-12-07 | 2016-09-13 | Amira Pharmaceuticals Inc | antagonistas do receptor do ácido lisofosfatídico e seus usos |
| CN107721940A (zh) | 2010-12-07 | 2018-02-23 | 阿米拉制药公司 | 多环lpa1拮抗剂及其使用 |
| WO2012100436A1 (en) * | 2011-01-30 | 2012-08-02 | Curegenix Inc. | Compound as antagonist of lysophosphatidic acid receptor, composition, and use thereof |
| WO2012138648A1 (en) * | 2011-04-06 | 2012-10-11 | Irm Llc | Compositions and methods for modulating lpa receptors |
| EP2744807A4 (en) * | 2011-08-15 | 2015-03-04 | Intermune Inc | COMPOUNDS AS LYSOPHOSPHIC ACID RECEPTOR ANTAGONISTS |
| WO2013070879A1 (en) | 2011-11-10 | 2013-05-16 | Bristol-Myers Squibb Company | Methods for treating spinal cord injury with lpa receptor antagonists |
| US20140329871A1 (en) | 2011-12-04 | 2014-11-06 | Angion Biomedica Corp. | Small molecule anti-fibrotic compounds and uses thereof |
| EA201491530A1 (ru) | 2012-03-20 | 2015-07-30 | Серагон Фармасьютикалс, Инк. | Модуляторы рецепторов эстрогенов и их применение |
| PE20142448A1 (es) | 2012-06-20 | 2015-01-28 | Hoffmann La Roche | Compuestos de n-alquiltriazol como antagonistas de lpar |
| AU2013279513A1 (en) | 2012-06-20 | 2014-10-16 | F. Hoffmann-La Roche Ag | N-aryltriazole compounds as LPAR antagonists |
| CA2869602A1 (en) | 2012-06-20 | 2013-12-27 | F. Hoffmann-La Roche Ag | Substituted pyrazole compounds as lpar antagonists |
| EP2940013B1 (en) | 2012-12-28 | 2018-02-21 | Ube Industries, Ltd. | Halogen-substituted heterocyclic compound |
| WO2014113485A1 (en) | 2013-01-15 | 2014-07-24 | Intermune, Inc. | Lysophosphatidic acid receptor antagonists |
| DK2988743T3 (da) * | 2013-03-15 | 2021-03-01 | Epigen Biosciences Inc | Heterocykliske forbindelser, der kan anvendes til behandling af sygdom |
| WO2015066456A1 (en) | 2013-10-31 | 2015-05-07 | Bristol-Myers Squibb Company | Radioligands for imaging the lpa-1 receptor |
| US10023554B2 (en) | 2014-06-27 | 2018-07-17 | Ube Industries, Ltd. | Halogen-substituted heterocyclic compound salt |
-
2014
- 2014-03-17 DK DK14762555.2T patent/DK2988743T3/da active
- 2014-03-17 KR KR1020157028061A patent/KR102090231B1/ko active IP Right Grant
- 2014-03-17 BR BR112015023267-1A patent/BR112015023267B1/pt active IP Right Grant
- 2014-03-17 JP JP2016503448A patent/JP6482086B2/ja active Active
- 2014-03-17 EA EA201591607A patent/EA033923B1/ru unknown
- 2014-03-17 PT PT147625552T patent/PT2988743T/pt unknown
- 2014-03-17 MX MX2015013303A patent/MX2015013303A/es unknown
- 2014-03-17 US US14/776,954 patent/US10000459B2/en active Active
- 2014-03-17 EP EP14762555.2A patent/EP2988743B1/en active Active
- 2014-03-17 AU AU2014232383A patent/AU2014232383B2/en active Active
- 2014-03-17 SG SG11201507459YA patent/SG11201507459YA/en unknown
- 2014-03-17 WO PCT/US2014/030712 patent/WO2014145873A2/en active Application Filing
- 2014-03-17 SG SG10201803833WA patent/SG10201803833WA/en unknown
- 2014-03-17 CA CA2906931A patent/CA2906931C/en active Active
- 2014-03-17 ES ES14762555T patent/ES2855173T3/es active Active
- 2014-03-17 CN CN201480015333.XA patent/CN105142635B/zh active Active
-
2016
- 2016-08-05 HK HK16109390.9A patent/HK1221167A1/zh unknown
-
2018
- 2018-06-05 US US16/000,283 patent/US10570103B2/en active Active
- 2018-06-18 US US16/010,755 patent/US10526298B2/en active Active
-
2019
- 2019-02-07 JP JP2019020553A patent/JP6843903B2/ja active Active
- 2019-04-17 AU AU2019202731A patent/AU2019202731B2/en active Active
- 2019-06-18 MX MX2020014300A patent/MX2020014300A/es unknown
- 2019-06-18 BR BR112020025927-6A patent/BR112020025927A2/pt unknown
- 2019-06-18 CN CN201980047732.7A patent/CN112424174B/zh active Active
- 2019-06-18 SG SG11202012656WA patent/SG11202012656WA/en unknown
- 2019-06-18 US US18/015,289 patent/US20230286928A1/en active Pending
- 2019-06-18 CN CN202410150847.1A patent/CN118290357A/zh active Pending
- 2019-06-18 AU AU2019288275A patent/AU2019288275B2/en active Active
-
2020
- 2020-02-07 US US16/784,486 patent/US11427552B2/en active Active
-
2024
- 2024-04-03 JP JP2024059851A patent/JP2024084796A/ja active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2855173T3 (es) | Compuestos heterocíclicos útiles para el tratamiento de una enfermedad | |
| CN103201262B (zh) | 自分泌运动因子抑制剂及其用途 | |
| EP2714680B1 (en) | Heterocyclic autotaxin inhibitors and uses thereof | |
| CN103596947A (zh) | 用于治疗纤维化、疼痛、癌症和呼吸、过敏性、神经系统疾病或心血管疾病的基于3-或5-联苯-4-基异噁唑的化合物 | |
| JP7467361B2 (ja) | 疾患の治療に有用な複素環化合物 | |
| EA038294B1 (ru) | Гетероциклические соединения, применимые в лечении заболеваний | |
| RU2818246C2 (ru) | Гетероциклические соединения, применимые в лечении заболевания | |
| NZ712889B2 (en) | Heterocyclic compounds useful in the treatment of disease | |
| NZ751063B2 (en) | Heterocyclic compounds useful in the treatment of disease | |
| NZ751063A (en) | Heterocyclic compounds useful in the treatment of disease |