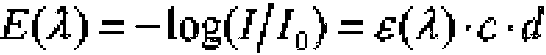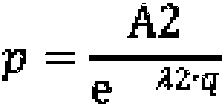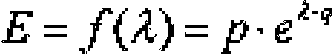ES2852382T3 - Procedimiento para la determinación de lípidos, hemoglobina y bilirrubina en muestras de fluido corporal - Google Patents
Procedimiento para la determinación de lípidos, hemoglobina y bilirrubina en muestras de fluido corporal Download PDFInfo
- Publication number
- ES2852382T3 ES2852382T3 ES18181329T ES18181329T ES2852382T3 ES 2852382 T3 ES2852382 T3 ES 2852382T3 ES 18181329 T ES18181329 T ES 18181329T ES 18181329 T ES18181329 T ES 18181329T ES 2852382 T3 ES2852382 T3 ES 2852382T3
- Authority
- ES
- Spain
- Prior art keywords
- extinction
- hemoglobin
- value
- wavelength
- bilirubin
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/17—Systems in which incident light is modified in accordance with the properties of the material investigated
- G01N21/25—Colour; Spectral properties, i.e. comparison of effect of material on the light at two or more different wavelengths or wavelength bands
- G01N21/31—Investigating relative effect of material at wavelengths characteristic of specific elements or molecules, e.g. atomic absorption spectrometry
- G01N21/314—Investigating relative effect of material at wavelengths characteristic of specific elements or molecules, e.g. atomic absorption spectrometry with comparison of measurements at specific and non-specific wavelengths
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/487—Physical analysis of biological material of liquid biological material
- G01N33/49—Blood
- G01N33/492—Determining multiple analytes
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/17—Systems in which incident light is modified in accordance with the properties of the material investigated
- G01N21/25—Colour; Spectral properties, i.e. comparison of effect of material on the light at two or more different wavelengths or wavelength bands
- G01N21/31—Investigating relative effect of material at wavelengths characteristic of specific elements or molecules, e.g. atomic absorption spectrometry
- G01N21/314—Investigating relative effect of material at wavelengths characteristic of specific elements or molecules, e.g. atomic absorption spectrometry with comparison of measurements at specific and non-specific wavelengths
- G01N2021/3148—Investigating relative effect of material at wavelengths characteristic of specific elements or molecules, e.g. atomic absorption spectrometry with comparison of measurements at specific and non-specific wavelengths using three or more wavelengths
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2201/00—Features of devices classified in G01N21/00
- G01N2201/12—Circuits of general importance; Signal processing
- G01N2201/129—Using chemometrical methods
Landscapes
- Health & Medical Sciences (AREA)
- Physics & Mathematics (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Chemical & Material Sciences (AREA)
- Biomedical Technology (AREA)
- Pathology (AREA)
- Analytical Chemistry (AREA)
- Immunology (AREA)
- General Health & Medical Sciences (AREA)
- General Physics & Mathematics (AREA)
- Hematology (AREA)
- Biochemistry (AREA)
- Ecology (AREA)
- Biophysics (AREA)
- Molecular Biology (AREA)
- Urology & Nephrology (AREA)
- Food Science & Technology (AREA)
- Medicinal Chemistry (AREA)
- Investigating Or Analysing Biological Materials (AREA)
- Investigating Or Analysing Materials By Optical Means (AREA)
Abstract
Procedimiento para la determinación cuantitativa de lípidos, hemoglobina y bilirrubina en una muestra de fluido corporal con los pasos: a) irradiación de la muestra de fluido corporal con luz para una variedad de longitudes de onda λ; b) detección de un primer valor medido A1 a una primera longitud de onda λ1, a la que la extinción no causada por lípidos es insignificante; c) detección de un segundo valor medido A2 a una segunda longitud de onda λ2, a la que la extinción no causada por bilirrubina y hemoglobina y lípidos es insignificante; d) detección de un tercer valor medido A3 a una tercera longitud de onda λ3, a la que la hemoglobina presenta un máximo de extinción; e) detección de un cuarto valor medido A4 a una cuarta longitud de onda λ4, a la que la extinción no causada por bilirrubina y hemoglobina y lípidos es insignificante; f) determinación de un parámetro q con la Fórmula: **(Ver fórmula)** y de un parámetro p con la Fórmula: **(Ver fórmula)** g) cálculo de una curva de aproximación exponencial (L0) de la forma: **(Ver fórmula)** para la extinción E de los lípidos; h) determinación de un primer valor teórico de extinción EH1 para la hemoglobina, que corresponde a la diferencia entre el tercer valor medido A3 y el valor de la curva de aproximación (L0) a la tercera longitud de onda λ3; i) examinar si el primer valor teórico de extinción EH1 para la hemoglobina es mayor que 0 y, cuando sea mayor que 0, determinación de un segundo valor teórico de extinción EH2 para la hemoglobina multiplicando el primer valor teórico de extinción EH1 para la hemoglobina con un primer factor de proporcionalidad predeterminado, que refleja la relación entre los valores de extinción para la hemoglobina a la tercera longitud de onda λ3 y los valores de extinción para la hemoglobina a la cuarta longitud de onda λ4; j) determinación de un primer valor teórico de extinción EB1 para la bilirrubina, que corresponde a la diferencia entre el cuarto valor medido A4 y la suma del valor de la curva de aproximación (L0) a la cuarta longitud de onda λ4 y del segundo valor teórico de extinción EH2 para la hemoglobina; k) examinar si el primer valor teórico de extinción EB1 para la bilirrubina es mayor que 0; y l) cuando en el examen del paso i) resulte que el primer valor teórico de extinción EH1 para la hemoglobina sea mayor que 0, asignación del primer valor teórico de extinción EH1 para la hemoglobina a uno de varios niveles de concentración de hemoglobina predeterminados, y m) cuando en el examen del paso i) resulte que el primer valor teórico de extinción EB1 para la bilirrubina sea mayor que 0, asignación del primer valor teórico de extinción EB1 para la bilirrubina a uno de varios niveles de concentración de bilirrubina predeterminados, y n) asignación del primer valor medido A1 a uno de varios niveles de concentración de lípidos previamente definidos.
Description
DESCRIPCIÓN
Procedimiento para la determinación de lípidos, hemoglobina y bilirrubina en muestras de fluido corporal
La presente invención pertenece al campo del diagnóstico in vitro y se refiere a un procedimiento y un aparato de análisis automático para la determinación cuantitativa de lípidos, hemoglobina y bilirrubina en muestras de suero sanguíneo y plasma sanguíneo.
Numerosos procedimientos de detección y análisis para determinar parámetros fisiológicos en muestras de fluidos corporales se basan en principios de medición fotométrica. Los procedimientos fotométricos permiten la detección cualitativa y cuantitativa de analitos en muestras líquidas.
La determinación de parámetros clínicamente relevantes, como, por ejemplo, la concentración o la actividad de un analito, a menudo se realiza mezclando in vitro una alícuota del líquido corporal de un paciente con uno o varios reactivos de prueba, con lo que se pone en marcha una reacción bioquímica, que provoca un cambio medible en una propiedad óptica del lote de prueba. La fotometría examina y utiliza el debilitamiento de un flujo luminoso cuando atraviesa un medio absorbente y/o dispersante. En función del tipo de reacción bioquímica o biofísica desencadenada, se utilizan diferentes procedimientos de medición fotométrica, que permiten la medición de un lote de prueba líquido turbio.
Para ello pueden utilizarse procedimientos turbidimétricos, en los que se mide la turbidez o la densidad óptica de una solución o suspensión, en base a la atenuación luminosa o extinción de un haz de luz que atraviesa directamente la suspensión.
La intensidad del haz de luz disminuye al atravesar una celda de medición o cubeta que contenga una muestra líquida. Las pérdidas pueden verse influenciadas por interacciones del haz de luz con la muestra ubicada en la celda de medición, por ejemplo, por efectos de absorción, difracción, dispersión y/o reflexión. En general, los efectos de difracción, flexión y reflexión pueden despreciarse o compensarse mediante mediciones de referencia, de forma que principalmente la absorción contribuye a la atenuación del haz de luz.
Por tanto, las determinaciones fotométricas de concentración se basan en una dependencia regular de la extinción o absorción de la concentración de las sustancias disueltas y del espesor de capa de la celda de medida a una determinada longitud de onda de la luz incidente. La ley de Lambert-Beer describe esta relación:
donde E(A) es la extinción dependiente de la longitud de onda A del haz de luz, I es la intensidad de la luz tras atravesar la muestra, lo es la intensidad de la luz antes de atravesar la muestra, £(A) es el coeficiente de extinción molar dependiente de la longitud de onda de una sustancia irradiada, c es la concentración molar de la sustancia irradiada y d es el espesor de capa a través del cual pasa el haz de luz, por ejemplo, la celda de medición.
La concentración de una sustancia en una solución se puede determinar en base a la extinción E (A) de una muestra. Para ello es necesario que previamente se haya determinado la extinción de al menos una solución patrón de concentración conocida. Dado que la extinción es proporcional a la concentración, la concentración de una sustancia disuelta en una muestra desconocida se puede determinar por calibración midiendo la extinción de varias soluciones estándar de concentraciones conocidas.
Sin embargo, la extinción de una muestra depende no solo de la concentración de la propia sustancia a determinar, sino también del tipo de matriz de muestras. Las extinciones de diferentes sustancias se comportan de forma aditiva en una mezcla, siempre que las sustancias no interactúen entre sí. Los fluidos corporales, como el plasma sanguíneo o el suero sanguíneo, son mezclas complejas y, además del analito a determinar, contienen un gran número de otras sustancias que influyen en la absorción global de la muestra.
Sin embargo, en casos individuales, las muestras de fluidos corporales pueden contener concentraciones anormalmente altas de una o varias sustancias intrínsecas, es decir, endógenas, que, al superar una concentración tolerable, resultan perjudiciales en los procedimientos de detección fotométrica y pueden dar lugar a un error sistemático.
Como se sabe, los problemas causan muestras de suero o plasma hemolíticas, ictéricas y/o lipémicas, que tienen concentraciones anormalmente altas de hemoglobina, bilirrubina y/o lípidos. Las concentraciones anormalmente altas de estas sustancias interferentes pueden estar originadas por un estado patológico del paciente o por una obtención o almacenamiento incorrecta/o de la muestra. Si dichas muestras se someten a un procedimiento
fotométrico, que sirve para determinar un parámetro analítico relevante para el diagnóstico, existe el riesgo de una determinación incorrecta, que posiblemente puede resultar en un diagnóstico erróneo y, en el peor de los casos, en un tratamiento incorrecto del paciente. Por tanto, la identificación preanalítica de muestras hemolíticas, ictéricas, así como lipémicas es de especial importancia para evitar resultados de análisis incorrectos.
Por tanto, existe la necesidad de un procedimiento para determinar los efectos espectrométricos de las sustancias interferentes en las muestras de fluidos corporales o para identificar las muestras de fluidos corporales que contengan concentraciones incrementadas de una o varias sustancias interferentes.
En la EP-A1-1059522, la US 4,263,512, la US 2009/0009750 A1 y la US 2010/0174491 A1 se describen diversos procedimientos para la determinación de bilirrubina, hemoglobina y lípidos en muestras de plasma o suero. En la EPA1-1059522 se aproxima localmente de forma lineal, por ejemplo, la extinción que queda tras la retirada de la extinción debida a la hemoglobina y bilirrubina, que contiene particularmente también la extinción provocada por lípidos.
Sin embargo, el último método mencionado tiene también la desventaja de que precisamente una concentración de lípidos comparativamente alta puede influir en la determinación de bilirrubina y hemoglobina en la misma muestra y, por lo tanto, alterar los valores medidos.
La WO 2013/010970 A1 y la EP-A2-3051272 ya describen procedimientos, que permiten determinar con precisión la bilirrubina y la hemoglobina y también determinar la concentración de lípidos en una muestra, incluso en presencia de concentraciones elevadas de lípidos. Estos procedimientos incluyen esencialmente la medición de la extinción de la muestra a diferentes longitudes de onda, el cálculo de una curva de aproximación, función de la potencia, para la extinción de los lípidos, la sustracción de la proporción de hemoglobina y bilirrubina de las extinciones hasta que quede una curva de lípidos y finalmente la determinación de los valores teóricos de extinción utilizando coeficientes de extinción específicos de la sustancia.
Sin embargo, el problema es que los aparatos de análisis ya existentes a menudo solo disponen de un número limitado de fuentes de luz con longitudes de onda predeterminadas. Dado que los procedimientos conocidos de la técnica anterior para determinar las sustancias interferentes requieren una combinación específica de longitudes de onda de medición, no todos los procedimientos conocidos pueden implementarse fácilmente en todos los aparatos de análisis existentes. Por tanto, la presente invención se basa en el objeto de modificar el procedimiento según la EP-A2-3051272 de tal manera que permita una determinación más precisa de la concentración de lípidos, hemoglobina y bilirrubina en muestras de fluidos corporales, cuando estén disponibles otras longitudes de onda diferentes de las mencionadas en la EP-A2 -3051272 (A1: 600-660 nm; A2: 400-480 nm, A3: 400-440 nm; A4: 350 370 nm), especialmente si está disponible la siguiente combinación de longitudes de onda: una longitud de onda, en el que la extinción no causada por lípidos es insignificante (como, por ejemplo, 660 nm); dos longitudes de onda, en las que la extinción no causada por la bilirrubina y la hemoglobina y los lípidos es insignificante (como, por ejemplo, 340 nm y 405 nm); y una longitud de onda, a la que la hemoglobina tiene un máximo de extinción (como, por ejemplo, 575 nm).
Este objeto se resuelve, entre otros, por el hecho de que, en lugar de calcular una curva de aproximación función de la potencia para la extinción de los lípidos, se calcula una curva de aproximación exponencial para la extinción de los lípidos y, en lugar de los coeficientes de extinción de las sustancias interferentes, se utilizan factores de proporcionalidad predeterminados para determinar los valores teóricos de extinción.
Objeto de la presente invención es, en consecuencia, un procedimiento para la determinación cuantitativa de lípidos, hemoglobina y bilirrubina en una muestra de fluido corporal con los pasos:
a) irradiación de la muestra de fluido corporal con luz para una variedad de longitudes de onda A;
b) detección de un primer valor medido A1 a una primera longitud de onda A1, a la que la extinción no causada por lípidos es insignificante;
c) detección de un segundo valor medido A2 a una segunda longitud de onda A2, a la que la extinción no causada por bilirrubina y hemoglobina y lípidos es insignificante;
d) detección de un tercer valor medido A3 a una tercera longitud de onda A3, a la que la hemoglobina presenta un máximo de extinción;
e) detección de un cuarto valor medido A4 a una cuarta longitud de onda A4, a la que la extinción no causada por bilirrubina y hemoglobina y lípidos es insignificante;
f) determinación de un parámetro q con la Fórmula:
y de un parámetro p con la Fórmula:
g) cálculo de una curva de aproximación exponencial (L0) de la forma:
para la extinción E de los lípidos;
h) determinación de un primer valor teórico de extinción Eh1 para la hemoglobina, que corresponde a la diferencia entre el tercer valor medido A3 y el valor de la curva de aproximación (Lo) a la tercera longitud de onda A3;
i) comprobación de si el primer valor teórico de extinción Ehi para la hemoglobina es mayor que 0 y, cuando sea mayor que 0, determinación de un segundo valor teórico de extinción Eh2 para la hemoglobina, multiplicando el primer valor teórico de extinción Ehi para la hemoglobina con un primer factor de proporcionalidad predeterminado, que refleja la relación entre los valores de extinción para la hemoglobina a la tercera longitud de onda A3 y los valores de extinción para la hemoglobina a la cuarta longitud de onda A4;
j) determinación de un primer valor teórico de extinción Ebi para la bilirrubina, que corresponde a la diferencia entre el cuarto valor medido A4 y la suma del valor de la curva de aproximación (Lo) a la cuarta longitud de onda A4 y del segundo valor teórico de extinción EH2 para la hemoglobina;
k) comprobación de si el primer valor teórico de extinción Ebi para la bilirrubina es mayor que 0; y
l) cuando en el examen del paso i) resulte que el primer valor teórico de extinción Ehi para la hemoglobina sea mayor que 0, asignación del primer valor teórico de extinción Ehi para la hemoglobina a uno de varios niveles de concentración de hemoglobina predeterminados, y
m) cuando en el examen del paso i) resulte que el primer valor teórico de extinción Ebi para la bilirrubina sea mayor que 0, asignación del primer valor teórico de extinción Ebi para la bilirrubina a uno de varios niveles de concentración de bilirrubina predeterminados, y
n) asignación del primer valor medido A1 a uno de varios niveles de concentración de lípidos previamente definidos. En una forma de ejecución del procedimiento conforme a la invención, la primera longitud de onda A1, a la que la extinción no causada por lípidos es insignificante, se encuentra entre 600 nm y 660 nm; preferentemente asciende a 660 nm.
En otra forma de ejecución del procedimiento conforme a la invención, la segunda longitud de onda A2, a la que la extinción no causada por bilirrubina y hemoglobina y lípidos es insignificante, se encuentra entre 320 nm y 360 nm; preferentemente asciende a 340 nm.
En otra forma de ejecución del procedimiento conforme a la invención, la tercera longitud de onda A3, a la que la hemoglobina presenta un máximo de extinción, se encuentra entre 540 nm y 580 nm; preferentemente asciende a 575 nm.
En otra forma de ejecución del procedimiento conforme a la invención, la cuarta longitud de onda A4, a la que la extinción no causada por bilirrubina y hemoglobina y lípidos es insignificante, se encuentra entre 380 nm y 440 nm; preferentemente asciende a 405 nm.
En una forma de ejecución especialmente preferente, la primera longitud de onda A1 asciende a 660 nm y la segunda longitud de onda A2 a 340 nm y la tercera longitud de onda A3 a 575 nm y la cuarta longitud de onda A4 a 405 nm.
Los "valores medidos" (A1; A2; A3, etc.) en el sentido de la presente invención son valores medidos de extinción, que pueden registrarse con dispositivos de medición fotométricos. Un valor medido puede ser una variable adimensional, que indique una medida, dependiente de la longitud de onda, de la opacidad de una muestra de fluido corporal con respecto al paso de rayos de luz en el rango de longitud de onda visible, infrarroja y/o ultravioleta. Igualmente, también puede ser posible especificar valores de medición de extinción respecto a un grosor unitario de una celda o cubeta de medición, en la que se almacenan muestras de fluidos corporales durante el paso de haces de luz con el fin de registrar valores medidos de intensidad. En este caso, los valores medidos pueden tener una dimensión de [1/mm]. En cualquier caso, los valores medidos indicados de las siguientes formas de ejecución son solo de naturaleza ejemplar y dependen del dispositivo de medición, de las propiedades de la muestra y de la composición de la muestra. A continuación, los valores de extinción medidos se equiparan, en cada caso, con los valores de absorción, aunque está claro para el experto que, con esta consideración, aunque la difracción, la dispersión y la reflexión contribuyen a los valores de extinción, son esencialmente despreciables en comparación con la absorción en el rango de longitudes de onda considerado.
Los "valores teóricos de extinción " (Eh, Eb, Ehbl, etc.) en el sentido de la presente invención no son realmente valores de extinción medidos, sino valores calculados.
Los "lípidos" en el sentido de la presente solicitud incluyen particularmente las grasas o triglicéridos o triacilgliceroles que se encuentran en el organismo humano o animal.
Tras la incorporación de los valores medidos A1 a A4 (pasos a) a e) del procedimiento conforme a la invención) y la posterior determinación de la curva de aproximación teórica para lípidos (pasos f) y g) del procedimiento conforme a la invención), se determina inicialmente la fracción de extinción de la hemoglobina. A tal efecto se determina inicialmente un primer valor teórico de extinción Ehi para la hemoglobina, haciendo que la diferencia entre el tercer valor medido a 3 y el valor de la curva de aproximación (Lo) a la tercera longitud de onda corresponda a A3, y se comprueba si el primer valor teórico de extinción Ehi para la hemoglobina es mayor que 0. Si la comprobación demuestra que es menor o igual que 0, se confirma la ausencia de hemoglobina. Para cálculos posteriores se usa un valor teórico de extinción para la hemoglobina de 0. Si la comprobación demuestra que es mayor que 0, este primer valor teórico de extinción Ehi para la hemoglobina se asigna a uno de varios niveles de concentración de hemoglobina previamente definidos.
Para determinar la fracción de extinción de la bilirrubina, se determina inicialmente un segundo valor teórico de extinción Eh2 para la hemoglobina, multiplicando el primer valor de extinción teórico Ehi para la hemoglobina por un primer factor de proporcionalidad predeterminado.
El primer factor de proporcionalidad refleja la relación entre los valores de extinción de la hemoglobina a la tercera longitud de onda A3 y los valores de extinción de la hemoglobina a la cuarta longitud de onda A4 y puede predeterminarse, por ejemplo, midiendo la extinción de un gran número de muestras con diferentes concentraciones de hemoglobina (por ejemplo, de 20 a 400 mg/dl) se mide en la tercera longitud de onda A3 y en la cuarta longitud de onda A4 y determinando el valor medio de los cocientes a partir del valor medido en la cuarta longitud de onda A4 y el valor medido en la tercera longitud de onda A3.
A continuación, se determina un primer valor teórico de extinción Ebi para la bilirrubina, determinando la diferencia entre el cuarto valor medido A4 y la suma del valor de la curva de aproximación (L0) a la cuarta longitud de onda A4 y el segundo valor teórico de extinción Eh2 para la hemoglobina. Se comprueba si el primer valor teórico de extinción Ebi de la bilirrubina es superior a 0. Si la comprobación demuestra que es menor o igual a 0, se confirma la ausencia de bilirrubina. Si, por el contrario, la comprobación demuestra que es mayor que 0, este primer valor teórico de extinción Ebi para la bilirrubina se asigna a uno de varios niveles de concentración de bilirrubina previamente definidos.
Además, el primer valor de medición A1 se asigna a uno de varios niveles de concentración de lípidos establecidos de antemano.
Por un "nivel de concentración predeterminado" (para la hemoglobina, bilirrubina o lípidos) debe entenderse un subrango del rango de concentraciones de la sustancia interferente, que es relevante para la identificación preanalítica de muestras hemolíticas, ictéricas y lipémicas. Típicamente, se consideran relevantes el rango de concentraciones de 0 a 1000 mg/dl para la hemoglobina, el rango de concentraciones de 0 a 60 mg/dl para la bilirrubina y el rango de concentraciones de 0 a 2000 mg/dl para los lípidos. El rango de concentraciones relevante se subdivide típicamente en al menos 5 subrangos de diferentes niveles de concentración, a los que se asignan valores de índice (1, 2, 3, etc.). Cuanto mayor sea la concentración de la sustancia interferente, mayor será el valor
del índice. Estos llamados "índices HIL" son marcadores semicuantitativos, que permiten la identificación preanalítica de muestras hemolíticas, ictéricas y lipémicas.
Los niveles de concentración de hemoglobina, bilirrubina y lípidos son definidos típicamente por el fabricante del sistema de análisis, y luego se determina qué valores medidos determinados con el procedimiento conforme a la invención o valores de extinción determinados teóricamente corresponden a qué nivel de concentración. Esto se hace típicamente analizando un gran número de muestras con diferentes concentraciones de hemoglobina (por ejemplo, de 0 a 1000 mg/dl de hemoglobina) y un gran número adicional de muestras con diferentes concentraciones de bilirrubina (por ejemplo, de 0 a 60 mg/dl de bilirrubina) y un gran número adicional de muestras con diferentes concentraciones de lípidos (por ejemplo, de 0 a 2.000 mg/dl de intralípidos) con el procedimiento conforme a la invención y asignando los valores medidos o valores de extinción determinados teóricamente a los niveles de concentración definidos.
En una forma de ejecución del procedimiento conforme a la invención, tras el cálculo de la curva de aproximación L0 para la extinción E de los lípidos en el paso g), se crea una curva de aproximación corregida Lk para la extinción E de los lípidos, corrigiendo la curva de aproximación L0 por medio de un procedimiento iterativo. Esto da lugar a una determinación más precisa de las sustancias interferentes, particularmente en muestras que tengan un alto contenido en lípidos.
Preferentemente, una curva de aproximación corregida Lk para la extinción E de los lípidos sólo se crea cuando se determine que el cociente de la diferencia entre el cuarto valor medido A4 y el valor de la curva de aproximación (L0) a la cuarta longitud de onda A4 y el cuarto valor medido A4 es mayor que 0,2.
Preferentemente, para la creación de la curva de aproximación corregida Lk se determinan un tercer valor teórico de extinción Eh3 para la hemoglobina, un segundo valor teórico de extinción Eb2 para la bilirrubina y un primer valor teórico de extinción ELikorr para los lípidos.
El tercer valor teórico de extinción Eh3 para la hemoglobina se determina multiplicando el primer valor teórico de extinción Ehi para la hemoglobina por un segundo factor de proporcionalidad predeterminado.
El segundo factor de proporcionalidad refleja la relación entre los valores de extinción para la hemoglobina a la tercera longitud de onda A3 y los valores de extinción para la hemoglobina a la segunda longitud de onda A2 y puede predeterminarse, por ejemplo, midiendo en un ensayo preliminar la extinción de un gran número de muestras con diferentes concentraciones de hemoglobina (por ejemplo, de 20 a 400 mg/dl) a la tercera longitud de onda A3 y a la segunda longitud de onda A2 y determinando el valor medio de los cocientes del valor medido a la segunda longitud de onda A2 y el valor medido a la tercera longitud de onda A3.
El segundo valor teórico de extinción Eb2 para la bilirrubina se determina multiplicando el primer valor teórico de extinción Ebi para la bilirrubina por un tercer factor de proporcionalidad predeterminado.
El tercer factor de proporcionalidad refleja la relación entre los valores de extinción para la bilirrubina a la segunda longitud de onda A2 y los valores de extinción para la bilirrubina a la cuarta longitud de onda A4 y puede predeterminarse, por ejemplo, midiendo en un ensayo preliminar la extinción de un gran número de muestras con diferentes concentraciones de bilirrubina (por ejemplo, de 1 a 60 mg/dl) a la segunda longitud de onda A2 y a la cuarta longitud de onda A4 y determinando el valor medio de los cocientes del valor medido a la segunda longitud de onda A2 y el valor medido a la cuarta longitud de onda A4.
El primer valor teórico de extinción ELikorr para lípidos se determina determinando la diferencia entre el segundo valor medido A2 y la suma del tercer valor teórico de extinción Eh3 para la hemoglobina y del segundo valor teórico de extinción Eb2 para la bilirrubina.
La irradiación de la muestra de fluido corporal se realiza favorablemente con luz de una variedad de longitudes de onda con la ayuda de diodos láser o emisores de luz o con la ayuda de una fuente de luz con diferentes filtros ópticos y la detección de la variedad de valores medidos (Ai; a 2; A3; A4) con la ayuda de un fotodetector, por ejemplo, con un sensor CCD, un sensor CMOS, fotosensores o dispositivos similares, que sean adecuados para detectar la intensidad de un haz de luz en función de la longitud de onda. "Muestras de fluidos corporales" en el sentido de la presente invención pueden ser todas las muestras de origen biológico que tengan una consistencia líquida y un gran número de sustancias biológicamente activas en diferentes concentraciones. Por ejemplo, las muestras de fluidos corporales pueden incluir suero sanguíneo, plasma sanguíneo, sangre, orina, fluido linfático, fluido biliar o fluidos similares.
Otro objeto de la presente invención es un aparato de diálisis automático con un dispositivo de medición, donde el dispositivo de medición comprende al menos una fuente de luz y varios filtros ópticos o varias fuentes de luz, preferentemente varios diodos emisores de luz o láser y al menos un fotodetector, donde el dispositivo de medición
está diseñado para ejecutar los pasos procedimentales a) a e) del procedimiento conforme a la invención y que comprende además un dispositivo de cálculo, por ejemplo, un procesador, que está diseñado para ejecutar los demás pasos procedimentales f) a n) para la determinación cuantitativa de lípidos, hemoglobina y bilirrubina del procedimiento conforme a la invención anteriormente descrito.
En una forma de ejecución, el dispositivo de medición del aparato de análisis automático comprende al menos una fuente de luz y varios filtros ópticos para generar luz de diferentes longitudes de onda. En otra forma de ejecución, el dispositivo de medición comprende varias fuentes de luz, preferentemente varios diodos emisores de luz o láser. En una forma de ejecución especialmente preferente, el dispositivo de medición del aparato de análisis automático comprende al menos cuatro fuentes de luz, donde la primera fuente de luz emite luz de una longitud de onda en el rango entre 600 nm y 660 nm, y la segunda fuente de luz emite luz de una longitud de onda en el rango entre 320 nm y 360 nm, y la tercera fuente de luz emite luz de una longitud de onda en el rango entre 540 nm y 580 nm, y la cuarta fuente de luz emite luz de una longitud de onda en el rango entre 380 nm y 440 nm.
En una forma de ejecución especialmente preferente, el dispositivo de medición del aparato de análisis automático comprende al menos cuatro fuentes de luz, donde la primera fuente de luz emite luz de una longitud de onda de 660 nm, y la segunda fuente de luz emite luz de una longitud de onda de 340 nm, y la tercera fuente de luz emite luz de una longitud de onda de 575 nm, y la cuarta fuente de luz emite luz de una longitud de onda de 405 nm.
Ventajosamente, el dispositivo de medición también comprende al menos un fotodetector, por ejemplo, un sensor CCD, un sensor CMOS, fotosensores o dispositivos similares, que sean adecuados para detectar la intensidad de un haz de luz en función de la longitud de onda.
Ahora se describirán con más detalle diversos ejemplos de ejecución y configuraciones de la presente invención con referencia a los dibujos adjuntos.
DESCRIPCIÓN DE LAS FIGURAS
La FIG. 1 muestra el curso de extinción realmente medido de una muestra (n° 3417; A1-A4; diamantes) así como las curvas de lípidos calculadas L0 (cuadrados), Lk (triángulos) y Lkfinal (cruces).
EJEMPLO
a) Longitudes de onda
El procedimiento conforme a la invención se realizó en un aparato de análisis automático comprendiendo una disposición fotométrica con cuatro diodos láser. Se irradiaron muestras de plasma humano en un espesor de capa de d = 1 mm con luz de las siguientes longitudes de onda:
660 nm primera longitud de onda A1, a la que la extinción no causada por lípidos es insignificante;
340 nm segunda longitud de onda A2, a la que la extinción no causada por bilirrubina y hemoglobina y lípidos es insignificante;
575 nm tercera longitud de onda A3, a la que la hemoglobina presenta un máximo de extinción;
405 nm cuarta longitud de onda A4, a la que la extinción no causada por bilirrubina y hemoglobina y lípidos es insignificante.
Se registraron los cuatro valores medidos anteriormente mencionados (A1 = A660, A2 = A340, A3 = A575 y A4 = A405). b) Predeterminación de los valores de proporcionalidad
Primer y segundo valor de proporcionalidad
El primer factor de proporcionalidad (Fhb405) refleja la relación entre los valores de extinción para la hemoglobina a la tercera longitud de onda A3 = 575 nm y los valores de extinción para la hemoglobina a la cuarta longitud de onda A4 = 405 nm. El segundo factor de proporcionalidad (Fhb340) refleja la relación entre los valores de extinción para la hemoglobina a la tercera longitud de onda A3 = 575 nm y los valores de extinción para la hemoglobina a la segunda longitud de onda A2 = 340 nm. En un ensayo preliminar se midió la extinción de 16 muestras con diferentes concentraciones de hemoglobina (de 20 a 400 mg/dl) a575 nm, a 405 nm y a 340 nm, y se determinó el valor medio de los cocientes de los valores medidos a 405 nm y los valores medidos a 575 nm (primer factor de
proporcionalidad) y/o el valor medio de los cocientes de los valores medidos a 340 nm y los valores medidos a 575 nm (segundo factor de proporcionalidad. Los valores medidos determinados en las diferentes muestras y los cocientes determinados a partir de ellos se muestran en la Tabla 1. Para el primer factor de proporcionalidad (Fhb405) se determinó así un valor de 6,3. Para el segundo factor de proporcionalidad (Fhb34o) se determinó así un valor de 1,9.
Tabla 1
Tercer factor de proporcionalidad
El tercer factor de proporcionalidad (Fb34o) refleja la relación entre los valores de extinción para la bilirrubina a la segunda longitud de onda A2 = 340 nm y los valores de extinción para la bilirrubina a la cuarta longitud de onda A4 = 405 nm.
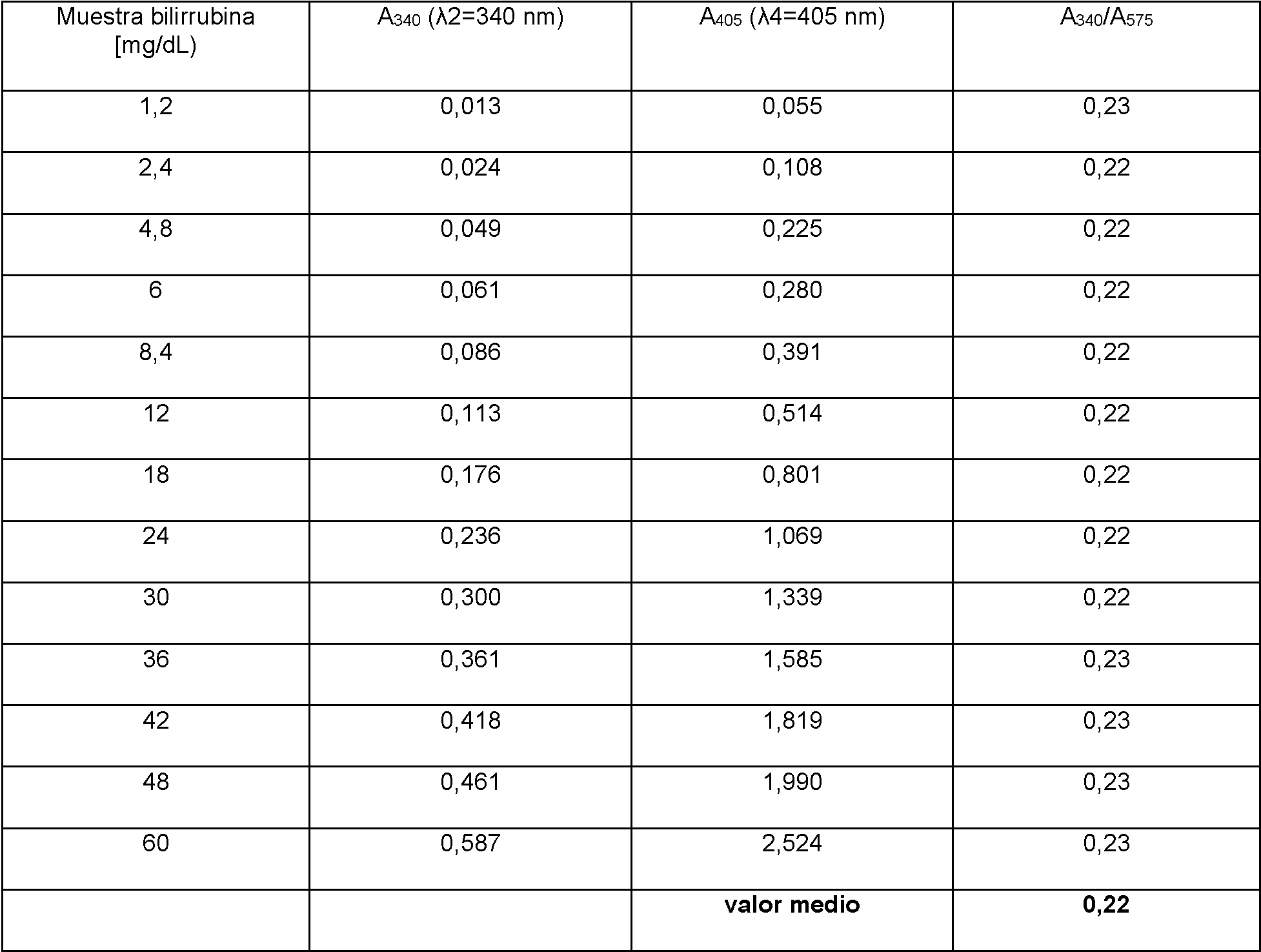
En un ensayo preliminar se midió la extinción de 13 muestras con diferentes concentraciones de bilirrubina (de 1,2 a 60 mg/dl) a 340 nm y a 405 nm, y se determinó el valor medio de los cocientes de los valores medidos a 340 nm y los valores medidos a 405 nm. Los valores medidos determinados en las diferentes muestras y los cocientes determinados a partir de ellos se muestran en la Tabla 2. Para el tercer factor de proporcionalidad (Fb34o) se determinó así un valor de 0,22.
Tabla 2
c) Determinación de los niveles de concentración y valores de índice
Una muestra de plasma humano con una concentración de hemoglobina de 120 mg/dl se irradió con luz a una longitud de onda de 575 nm (A3) en un espesor de capa de d = 5 mm, y se midió un valor medido de extinción de aproximadamente 619 mE, redondeando, 0,6 E. Una extinción de 0 a 0,6 E corresponde, por consiguiente, a un nivel de concentración de 0 a 120 mg/dL de hemoglobina; este rango se definió como "nivel 0". Dado que la hemoglobina se comporta proporcionalmente en la absorción, la definición del nivel se continuó en consecuencia hasta el nivel 5, es decir, hasta 1,2 E es el nivel 1, hasta 1,8 E es el nivel 2 y así sucesivamente.
Para la bilirrubina (concentración de bilirrubina de 4 mg/dl; medición de extinción a 405 nm) y lípidos (concentración intralipídica de 60 mg/dl; medición de extinción a 660 nm) el procedimiento fue análogo.
Los niveles de concentración así determinados se especifican en la Tabla 3.
Tabla 3
d) Ejemplos de ejecución
Se irradiaron cuatro muestras de plasma con concentraciones conocidas de elemento interferente (Tabla 4) en un espesor de capa de d = 5 mm con luz de las longitudes de onda 660 nm (A1), 340 nm (A2), 575 nm (A3) y 405 nm (A4), y se midieron en cada caso los valores medidos de extinción A1-A4 (Tabla 5).
Tabla 4
Tabla 5
e) Muestra n° 3417
La muestra con el n° de muestra 3417 tiene un contenido en hemoglobina ligeramente incrementado y niveles relativamente bajos de bilirrubina y lípidos.
Paso 1: Determinación de la curva lipídica Lo
Para determinar la curva de aproximación exponencial para la extinción de los lípidos (curva de lípidos Lo), primero se asignan las extinciones medidas A1 y A2 a la curva de lípidos; A1 no se altera (punto de anclaje):
A1 = A660 = EL660
A2 = A340 = EL340
Las extinciones teóricas de lípidos a las longitudes de onda de 405 nm (El405) y 575 nm (EL575) se determinan usando la fórmula.
Inicialmente, sin embargo, se determinan los parámetros q y p, usando las siguientes Fórmulas:
y
es decir,
Con estos parámetros se calculan ahora las die extinciones teóricas de la curva de lípidos L0 a las longitudes de onda A3 (575 nm) y A4 (405 nm). Se utiliza la siguiente Fórmula:
con ni = 405 nm, n2= 575 nm, entonces
Etm = 76,25 ■ em ' °’M90 = 1,992E
El .15 = 76,25 - e™Amm = 0,431E
La FIG. 1 muestra el curso de extinción realmente medido (A1-A4; diamantes) de la muestra n° 3417, así como la curva de lípidos Lo así calculada (cuadrados).
Paso 2: Determinación de las fracciones de extinción de hemoglobina y bilirrubina y del nivel de concentración de hemoglobina, bilirrubina y lípidos.
Hemoglobina
Para determinar la fracción de extinción de la hemoglobina, se determina un primer valor teórico de extinción Ehi, determinando primero la diferencia entre el valor de extinción medido real A3 y la curva de lípidos L0 a A3 (575 nm), y cuando el valor de extinción Ehi determinado de esta manera sea mayor que 0, se determina un segundo valor teórico de extinción Eh2, multiplicando el valor de extinción Ehi por el primer factor de proporcionalidad predeterminado Fh405 (= 6,3; ver arriba en b) y la Tabla 1), que refleja la relación entre los valores de extinción para
la hemoglobina a la tercera longitud de onda A3 (575 nm) y los valores de extinción para la hemoglobina a la cuarta longitud de onda A4 (405 nm):
EH1 = A3 - EL575 = 1 , 240 E - 0 , 431 E = 0 , 309 E;
EH2 = FH405 • EHi = 6 ,3 - 0 , 809 E = 5 , 097 E.
Se comprueba si Ehi es mayor o menor que cero.
En el caso de Ehi> 0, el valor de extinción teórico Ehi se asigna a un nivel de concentración de hemoglobina (ver Tabla 3).
En el presente caso, el valor de extinción Ehi = 0,809 E corresponde al nivel de concentración de hemoglobina 1 (ver Tabla 3).
Bilirrubina
Para determinar la fracción de extinción de la bilirrubina, se determina un primer valor de extinción teórico Ebi, determinando primero la diferencia entre el valor medido de extinción real A4 y la suma del valor de la curva de lípidos L0 a A4 (405 nm) y el segundo valor de extinción teórico Eh2 y cuando el valor de extinción Ebi determinado de esta manera sea menor que 0, el valor de extinción Ebi se establece igual a cero:
Ebi = A4 - EL405 - Eh2
= 5 , 441 E - 1, 992 E - 5 , 097 E
= - 1, 648 E
= 0 E.
La muestra no. 3417 no contiene, en consecuencia, ninguna concentración significativa de bilirrubina o ninguna en absoluto.
En el presente caso, el valor de extinción Ebi= 0 E corresponde al nivel de concentración de bilirrubina 0 (ver Tabla 3).
Lípido
El valor real de extinción A1 se asigna a un nivel de concentración de lípidos (ver Tabla 3).
En el presente caso, el valor de extinción A1 = 0,198 E corresponde al nivel de concentración de lípidos 0 (ver Tabla 3).
Tabla 6: Resultado para muestras n° 3417:
Todos los niveles determinados corresponden a las concentraciones de sustancias interferentes contenidas en la muestra.
Creación de una curva lipídica corregida Lk
Además, tras calcular la curva de aproximación Lo para la extinción E de los lípidos, puede crearse una curva de aproximación corregida Lk para la extinción E de los lípidos, corrigiendo la curva de aproximación L0 mediante un procedimiento iterativo. Esto da como resultado una determinación más precisa de las sustancias interferentes, especialmente en muestras que tengan un alto contenido en lípidos.
Normalmente, solo se crea una curva de aproximación corregida Lk para la extinción E de los lípidos cuando se determine que el cociente (VL) de la diferencia entre el cuarto valor medido A4 y el valor de la curva de aproximación (Lo) a la cuarta longitud de onda A4 y el cuarto valor medido A4 es mayor que 0,2.
En el caso de la muestra n° 3417, el cociente VL es mayor que 0,2:
entonces
La extinción para lípidos a la longitud de onda A2 (340 nm (correspondiente al valor medido real A2) se corrige restando la fracción de extinción de hemoglobina y bilirrubina a esta longitud de onda.
Para ello se determinan primero las fracciones de extinción de hemoglobina y bilirrubina en la extinción total a A2 (340 nm).
Para determinar la fracción de extinción de la hemoglobina, se determina un tercer valor de extinción teórico EH3, multiplicando el valor de extinción Ehi para la hemoglobina por el segundo factor de proporcionalidad predeterminado Fhb340 (= 1,9; ver arriba en b) y la Tabla 1), que refleja la relación entre los valores de extinción para la hemoglobina a la tercera longitud de onda A3 (575 nm) y los valores de extinción para la hemoglobina a la segunda longitud de onda A2 (340 nm):
Eh3= FHb340•Ehi= 1,9 * 0,809 E = 1,537 E
Para determinar la fracción de extinción de la bilirrubina, se determina un segundo valor de extinción teórico Eb2, multiplicando el valor de extinción Ebi de la bilirrubina por el tercer factor de proporcionalidad predeterminado Fb340 (= 0,22; ver arriba en b) y la Tabla 2), que refleja la relación entre los valores de extinción para la bilirrubina a la segunda longitud de onda A2 (340 nm) y los valores de extinción para la bilirrubina a la cuarta longitud de onda A4 (405 nm):
EB2 = Fb340 • Ebi = 0 , 22 . 0 E = 0 E
Ahora puede determinarse el valor teórico de extinción ELikorr para lípidos a 340 nm, formando la diferencia entre el segundo valor medido A2 y la suma del tercer valor teórico de extinción Eh3 para la hemoglobina y del segundo valor teórico de extinción Eb2 para la bilirrubina:
ELikorr — A 2 - E h3 ~ Eg2
= 3,575 E - 1,537 E - 0 E
= 2,038 E,
Con este valor de extinción corregido calculado, se calculan ahora los nuevos parámetros q y p para la función exponencial:
y
entonces
y
P e S4Ü -0,<m 73 £ 4 , 38.
Con estos parámetros se calculan ahora las extinciones teóricas de la curva lipídica corregida Lk a las longitudes de onda A3 (575 nm) y A4 (405 nm). Se usa la siguiente Fórmula:
EM05korr = 24 , 38 ♦ e 405 ' - 0 ' 0073 = 1 , 268 E
EL575korr = 2 4 , 38 . e 575 * -0 ' 0073 = 0 , 367 E
Tal y como se muestra en la FIG. 1, la curva lipídica corregida Lk (triángulos) "migra" hacia abajo. El objetivo es empujar la curva hacia abajo hasta que la diferencia de extinción entre el valor medido real A2 y el valor de extinción calculado teóricamente para lípidos a 340 nm corresponda a la suma de las fracciones de extinción causadas por la hemoglobina y la bilirrubina.
Para ello, las fracciones de extinción para la hemoglobina y la bilirrubina se determinan como ya se ha descrito anteriormente y se restan de A2. Todo el procedimiento se repite iterativamente con, en cada caso, parámetros q y p de la función exponencial a calcular nuevamente hasta que se alcance uno de los siguientes criterios de terminación: Elikorr <0 o q> 0 o El575 <A4 o EBi(n) <EBi(n-1). En la Fig. 1 se muestra la curva lipídica corregida iterativamente Lkfinal (cruces), en la que se alcanza el criterio de terminación ELikorr <0. Los valores de extinción corregidos de esta curva se utilizan entonces para calcular los valores de extinción teóricos para la hemoglobina y la bilirrubina, que luego se asignan a un nivel de concentración (ver Tabla 3).
Con la curva de lípidos Lkfinal corregida iterativamente, se determinaron los siguientes valores teóricos de extinción de hemoglobina y bilirrubina:
Eh = 1,003 E
EB = 0 E
El valor de extinción Eh = 1,003 E corresponde al nivel de concentración de hemoglobina 1 (ver Tabla 3).
El valor de extinción Eb = 0 E corresponde al nivel de concentración de bilirrubina 0 (ver Tabla 3).
También en este caso, el valor de extinción real A1 = 0,198 E corresponde al nivel de concentración de lípidos 0 (ver Tabla 3).
f) Muestras n° 5763, 4217 y 3283
Las muestras restantes se midieron y evaluaron de manera análoga y se determinaron los niveles de concentración. Como puede deducirse de la Tabla 7, los niveles de concentración esperados en base a las concentraciones reales se determinaron de manera casi completamente correcta para las tres sustancias interferentes. Solo con la muestra n° 4217, los niveles de hemoglobina y bilirrubina se determinaron cada uno 1 nivel demasiado bajo. Sin embargo, las desviaciones de /- 20% son aceptables para los procesos ópticos. La experiencia ha demostrado que, en muestras con una alta concentración de bilirrubina, también la extinción a 575 nm (A3), es decir, a la longitud de onda a la que la hemoglobina tiene un máximo de extinción, puede ser reducida, de forma puede provocarse que se determine demasiado poca hemoglobina. Sin embargo, esto no es clínicamente relevante, ya que la alta concentración de bilirrubina ya deja claro que la muestra contiene variables interferentes.
Tabla 7: Resultado para las muestras n° 5763, 4217 y 3283:
Claims (14)
1. Procedimiento para la determinación cuantitativa de lípidos, hemoglobina y bilirrubina en una muestra de fluido corporal con los pasos:
a) irradiación de la muestra de fluido corporal con luz para una variedad de longitudes de onda A;
b) detección de un primer valor medido A1 a una primera longitud de onda A1, a la que la extinción no causada por lípidos es insignificante;
c) detección de un segundo valor medido A2 a una segunda longitud de onda A2, a la que la extinción no causada por bilirrubina y hemoglobina y lípidos es insignificante;
d) detección de un tercer valor medido A3 a una tercera longitud de onda A3, a la que la hemoglobina presenta un máximo de extinción;
e) detección de un cuarto valor medido A4 a una cuarta longitud de onda A4, a la que la extinción no causada por bilirrubina y hemoglobina y lípidos es insignificante;
f) determinación de un parámetro q con la Fórmula:
y de un parámetro p con la Fórmula:
g) cálculo de una curva de aproximación exponencial (Lo) de la forma:
para la extinción E de los lípidos;
h) determinación de un primer valor teórico de extinción Ehi para la hemoglobina, que corresponde a la diferencia entre el tercer valor medido A3 y el valor de la curva de aproximación (Lo) a la tercera longitud de onda A3;
i) examinar si el primer valor teórico de extinción Ehi para la hemoglobina es mayor que 0 y, cuando sea mayor que 0, determinación de un segundo valor teórico de extinción Eh2 para la hemoglobina multiplicando el primer valor teórico de extinción Ehi para la hemoglobina con un primer factor de proporcionalidad predeterminado, que refleja la relación entre los valores de extinción para la hemoglobina a la tercera longitud de onda A3 y los valores de extinción para la hemoglobina a la cuarta longitud de onda A4;
j) determinación de un primer valor teórico de extinción Ebi para la bilirrubina, que corresponde a la diferencia entre el cuarto valor medido A4 y la suma del valor de la curva de aproximación (Lo) a la cuarta longitud de onda A4 y del segundo valor teórico de extinción Eh2 para la hemoglobina;
k) examinar si el primer valor teórico de extinción Ebi para la bilirrubina es mayor que 0; y
l) cuando en el examen del paso i) resulte que el primer valor teórico de extinción Ehi para la hemoglobina sea mayor que 0, asignación del primer valor teórico de extinción Ehi para la hemoglobina a uno de varios niveles de concentración de hemoglobina predeterminados, y
m) cuando en el examen del paso i) resulte que el primer valor teórico de extinción Ebi para la bilirrubina sea mayor que 0, asignación del primer valor teórico de extinción Ebi para la bilirrubina a uno de varios niveles de concentración de bilirrubina predeterminados, y
n) asignación del primer valor medido A1 a uno de varios niveles de concentración de lípidos previamente definidos.
2. Procedimiento según la reivindicación 1, donde, cuando en el examen del paso i) para determinar si el primer valor teórico de extinción Eh1 para la hemoglobina es mayor que 0, resulta que es menor o igual que 0, se confirma la ausencia de hemoglobina.
3. Procedimiento según la reivindicación 1, donde, cuando en el examen del paso k) para determinar si el primer valor teórico de extinción Eb1 para bilirrubina es mayor que 0, resulta que es menor o igual que 0, se confirma la ausencia de bilirrubina.
4. Procedimiento según la reivindicación 1, donde, tras calcular la curva de aproximación L0 para la extinción E de los lípidos, se crea una curva de aproximación corregida Lk para la extinción E de los lípidos, corrigiendo la curva de aproximación L0 por medio de un procedimiento iterativo.
5. Procedimiento según la reivindicación 4, donde para crear la curva de aproximación corregida Lk
• se determina un tercer valor teórico de extinción Eh3 para la hemoglobina multiplicando el primer valor de extinción teórico Eh1 para la hemoglobina con un segundo predeterminado factor de proporcionalidad, que refleja la relación entre los valores de extinción para la hemoglobina a la tercera longitud de onda A3 y los valores de extinción para la hemoglobina a la segunda longitud de onda A2; y
• se determina un segundo valor de extinción teórico Eb2 para bilirrubina multiplicando el primer valor de extinción teórico Ebi para bilirrubina con un tercer factor de proporcionalidad predeterminado, que refleja la relación entre los valores de extinción para bilirrubina a la segunda longitud de onda A2 y los valores de extinción para bilirrubina a la cuarta longitud de onda A4; y
• se determina un primer valor de extinción teórico Eukorr para lípidos, que corresponde a la diferencia entre el segundo valor medido A2 y la suma del tercer valor de extinción teórico Eh3 para la hemoglobina y del segundo valor teórico de extinción Eb2 para bilirrubina y el primer valor teórico de extinción Eukorr se emplea para calcular nuevos parámetros q=(ln Ai-ln ELikorr)/(Ai-A2) y p=Ei_ikorr/eA2*q y una curva de aproximación corregida Lk=p*eA*q.
6. Procedimiento según la reivindicación 4, donde una curva de aproximación corregida Lk para la extinción E de los lípidos sólo se crea cuando se determine que el cociente de la diferencia entre el cuarto valor medido A4 y el valor de la curva de aproximación (L0) para la cuarta longitud de onda A4 y del cuarto valor medido A4 es mayor que 0,2.
7. Procedimiento según una de las anteriores reivindicaciones, donde la primera longitud de onda Ai se encuentra en el rango entre 600 nm y 660 nm y la segunda longitud de onda A2 en el rango entre 320 nm y 360 nm y la tercera longitud de onda A3 en el rango entre 540 nm y 580 nm y la cuarta longitud de onda A4 en el rango entre 380 nm y 440 nm.
8. Procedimiento según la reivindicación 7, donde la primera longitud de onda Ai asciende a 660 nm y la segunda longitud de onda A2 a 340 nm y la tercera longitud de onda A3 a 575 nm y la cuarta longitud de onda A4 a 405 nm.
9. Procedimiento según una de las anteriores reivindicaciones, donde la muestra de fluido corporal es suero sanguíneo o plasma sanguíneo.
10. Procedimiento según una de las anteriores reivindicaciones, donde la irradiación de la muestra de fluido corporal con luz se realiza para una variedad de longitudes de onda con la ayuda de diodos láser o emisores de luz o con la ayuda de una fuente de luz con diferentes filtros ópticos y donde la detección de la variedad de valores medidos (Ai; A2; A3; A4) se realiza con la ayuda de un fotodetector.
11. Aparato de diálisis automático con un dispositivo de medición, donde el dispositivo de medición comprende al menos una fuente de luz y varios filtros ópticos y al menos un fotodetector, donde el dispositivo de medición está diseñado para ejecutar los pasos procedimentales a) a e) según la reivindicación i, caracterizado porque el aparato de análisis comprende además un dispositivo de cálculo, que está diseñado para ejecutar los demás pasos procedimentales para la determinación cuantitativa de lípidos, hemoglobina y bilirrubina según la reivindicación i .
12. Aparato de diálisis automático con un dispositivo de medición, donde el dispositivo de medición comprende varias fuentes de luz, preferentemente varios diodos emisores de luz o láser, y al menos un fotodetector, donde el dispositivo de medición está diseñado para ejecutar los pasos procedimentales a) a e) según la reivindicación i, caracterizado porque el aparato de análisis comprende además un dispositivo de cálculo, que está diseñado para
ejecutar los demás pasos procedimentales para la determinación cuantitativa de lípidos, hemoglobina y bilirrubina según la reivindicación 1.
13. Aparato de diálisis automático según la reivindicación 11 o la reivindicación 12, donde el dispositivo de medición comprende al menos cuatro fuentes de luz, donde la primera fuente de luz emite luz de una longitud de onda en el rango entre 600 nm y 660 nm, y la segunda fuente de luz emite luz de una longitud de onda en el rango entre 320 nm y 360 nm, y la tercera fuente de luz emite luz de una longitud de onda en el rango entre 540 nm y 580 nm, y la cuarta fuente de luz emite luz de una longitud de onda en el rango entre 380 nm y 440 nm.
14. Aparato de diálisis automático según la reivindicación 13, donde la primera fuente de luz emite luz de una longitud de onda de 660 nm, y la segunda fuente de luz emite luz de una longitud de onda de 340 nm, y la tercera fuente de luz emite luz de una longitud de onda de 575 nm, y la cuarta fuente de luz emite luz de una longitud de onda de 405 nm.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP18181329.6A EP3591378B1 (de) | 2018-07-03 | 2018-07-03 | Verfahren zur bestimmung von lipiden, hämoglobin und bilirubin in körperflüssigkeitsproben |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2852382T3 true ES2852382T3 (es) | 2021-09-13 |
Family
ID=62846014
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES18181329T Active ES2852382T3 (es) | 2018-07-03 | 2018-07-03 | Procedimiento para la determinación de lípidos, hemoglobina y bilirrubina en muestras de fluido corporal |
Country Status (3)
| Country | Link |
|---|---|
| EP (1) | EP3591378B1 (es) |
| JP (1) | JP7373315B2 (es) |
| ES (1) | ES2852382T3 (es) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2020159599A1 (en) | 2019-01-29 | 2020-08-06 | Siemens Healthcare Diagnostics Inc. | TURBIDITY NORMALIZATION ALGORITHM AND METHODS OF REDUCING INTRALIPID/LIPEMIA INTERFERENCE IN HEMOGLOBIN A1c ASSAYS |
| CN114577743B (zh) * | 2022-05-05 | 2022-09-27 | 深圳市帝迈生物技术有限公司 | 样本中的干扰物确定方法及装置、设备及存储介质 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2847176C2 (de) | 1977-10-31 | 1982-05-06 | Hitachi, Ltd., Tokyo | Verfahren zur photometrischen Bestimmung von Substanzen im Blutserum |
| US5353790A (en) * | 1992-01-17 | 1994-10-11 | Board Of Regents, The University Of Texas System | Method and apparatus for optical measurement of bilirubin in tissue |
| JP3203798B2 (ja) * | 1992-08-17 | 2001-08-27 | 株式会社島津製作所 | クロモゲンの測定方法 |
| EP1059522A1 (en) * | 1999-06-11 | 2000-12-13 | F. Hoffmann-La Roche Ag | Method and apparatus for examining fluids of biological origin |
| EP1802959A1 (en) | 2004-10-11 | 2007-07-04 | Thermo Fisher Scientific Oy | Method for automatically detecting factors that disturb analysis by a photometer |
| JP4758793B2 (ja) * | 2006-03-16 | 2011-08-31 | シスメックス株式会社 | 試料分析方法および試料分析装置 |
| KR101306340B1 (ko) | 2009-01-08 | 2013-09-06 | 삼성전자주식회사 | 생화학 시료에 포함된 성분의 농도 측정 방법 및 이를 이용한 검사 결과의 신뢰도 추정 방법 |
| EP2549264A1 (de) * | 2011-07-18 | 2013-01-23 | Siemens Healthcare Diagnostics Products GmbH | Verfahren und System zum Bestimmen der Konzentration von Substanzen in Körperflüssigkeiten |
| EP2657681A1 (en) * | 2012-04-26 | 2013-10-30 | Roche Diagnostics GmbH | Improvement of the sensitivity and the dynamic range of photometric assays by generating multiple calibration curves |
| EP3051271A1 (de) | 2015-01-27 | 2016-08-03 | Siemens Healthcare Diagnostics Products GmbH | Verfahren zur Bestimmung von Lipiden und anderen Störsubstanzen in Körperflüssigkeitsproben |
-
2018
- 2018-07-03 EP EP18181329.6A patent/EP3591378B1/de active Active
- 2018-07-03 ES ES18181329T patent/ES2852382T3/es active Active
-
2019
- 2019-07-02 JP JP2019123326A patent/JP7373315B2/ja active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP3591378B1 (de) | 2020-11-18 |
| EP3591378A1 (de) | 2020-01-08 |
| JP2020008578A (ja) | 2020-01-16 |
| JP7373315B2 (ja) | 2023-11-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2895091T3 (es) | Procedimiento y dispositivo de análisis automático para la determinación de lípidos y otras sustancias interferentes en muestras de fluidos corporales | |
| RU2302638C2 (ru) | Способ анализа гемоглобина и система для его осуществления | |
| US9395300B2 (en) | Method and system for determining the concentration of substances in body fluids | |
| US6470279B1 (en) | Method for calibrating spectrophotometric apparatus with synthetic fluids to measure plasma and serum analytes | |
| US20090075324A1 (en) | Method and System for Quantitative Hemoglobin Determination | |
| CN104870977B (zh) | 检测样品中的组分的装置 | |
| WO2003056312A1 (fr) | Procede de mesure de la concentration | |
| ES2852382T3 (es) | Procedimiento para la determinación de lípidos, hemoglobina y bilirrubina en muestras de fluido corporal | |
| RU2664786C2 (ru) | Способ и устройство для определения концентрации | |
| CA2283154C (en) | Method and apparatus for measurement of blood substitutes | |
| JP7203739B2 (ja) | 液体中の血液または血液成分を検出するためのデバイスを校正するための方法およびアセンブリ | |
| JP2007127661A (ja) | 分光光度計をカリブレーションする方法 | |
| JP5427362B2 (ja) | ヘマトクリット値または血液成分濃度の測定方法および測定装置 | |
| JP7568885B2 (ja) | 光透過凝集測定法での基準値を決定するためのデータベースを作成するための方法、並びに光透過凝集測定法での測定を行う方法及びデバイス | |
| CN113777333A (zh) | 自动分析仪及其反应杯污染的判定方法和存储介质 | |
| JP5635436B2 (ja) | 化学発光測定装置および化学発光測定方法 | |
| EP1496361B1 (en) | Immunoassay method and immunoassay system using a Fourier transformation to judge the occurrence of zone phenomena. | |
| JP2005274568A (ja) | 全ヘモグロビン測定のための分光分析方法および装置 | |
| US20240044790A1 (en) | Determining time response value of an analyte in a liquid | |
| JP2008008901A (ja) | 診断用分析器に用いられる固体制御および較正要素 | |
| JP6666702B2 (ja) | 測定方法および測定装置 | |
| Oliveira et al. | Point-of-care testing device for diabetes mellitus and renal function analysis of biological fluids | |
| EP4267940A1 (en) | Determining time response value of an analyte in a liquid | |
| Kasagani | Optical quantification of hemolysis, icterus, and lipemia in human serum |