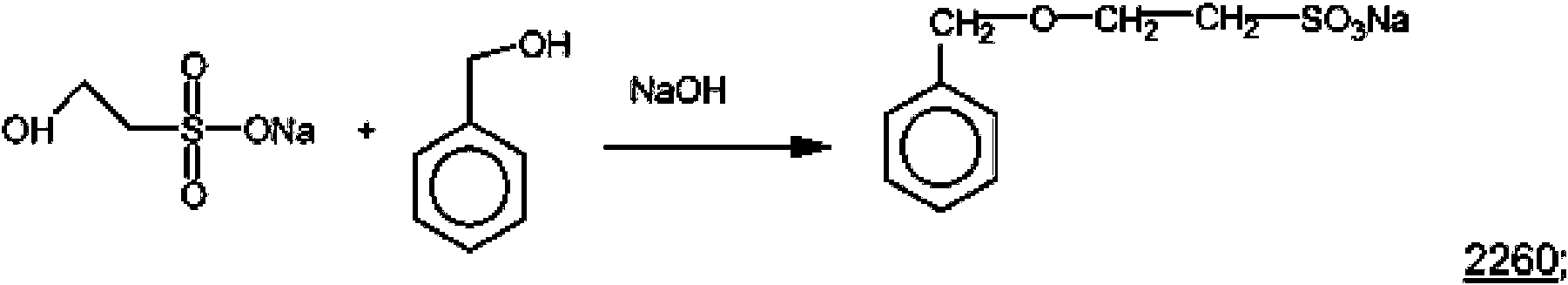ES2807558T3 - Procedimiento de preparación de compuestos de tipo oxatiazina - Google Patents
Procedimiento de preparación de compuestos de tipo oxatiazina Download PDFInfo
- Publication number
- ES2807558T3 ES2807558T3 ES17722874T ES17722874T ES2807558T3 ES 2807558 T3 ES2807558 T3 ES 2807558T3 ES 17722874 T ES17722874 T ES 17722874T ES 17722874 T ES17722874 T ES 17722874T ES 2807558 T3 ES2807558 T3 ES 2807558T3
- Authority
- ES
- Spain
- Prior art keywords
- oxathiazine
- compounds
- reaction
- cancer
- type compounds
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- WVDDGKGOMKODPV-UHFFFAOYSA-N OCc1ccccc1 Chemical compound OCc1ccccc1 WVDDGKGOMKODPV-UHFFFAOYSA-N 0.000 description 1
- AJZRLIIDXGWDDY-UHFFFAOYSA-N [NH3+]OS(CCO)(=O)=O Chemical compound [NH3+]OS(CCO)(=O)=O AJZRLIIDXGWDDY-UHFFFAOYSA-N 0.000 description 1
- FUKCVMLONUSXMC-UHFFFAOYSA-M [O-]S(CCOCc1ccccc1)(=O)=O Chemical compound [O-]S(CCOCc1ccccc1)(=O)=O FUKCVMLONUSXMC-UHFFFAOYSA-M 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C303/00—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides
- C07C303/02—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides of sulfonic acids or halides thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C303/00—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides
- C07C303/02—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides of sulfonic acids or halides thereof
- C07C303/22—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides of sulfonic acids or halides thereof from sulfonic acids, by reactions not involving the formation of sulfo or halosulfonyl groups; from sulfonic halides by reactions not involving the formation of halosulfonyl groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C303/00—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides
- C07C303/32—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides of salts of sulfonic acids
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C303/00—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides
- C07C303/36—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides of amides of sulfonic acids
- C07C303/38—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides of amides of sulfonic acids by reaction of ammonia or amines with sulfonic acids, or with esters, anhydrides, or halides thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C303/00—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides
- C07C303/36—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides of amides of sulfonic acids
- C07C303/40—Preparation of esters or amides of sulfuric acids; Preparation of sulfonic acids or of their esters, halides, anhydrides or amides of amides of sulfonic acids by reactions not involving the formation of sulfonamide groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C309/00—Sulfonic acids; Halides, esters, or anhydrides thereof
- C07C309/01—Sulfonic acids
- C07C309/02—Sulfonic acids having sulfo groups bound to acyclic carbon atoms
- C07C309/24—Sulfonic acids having sulfo groups bound to acyclic carbon atoms of a carbon skeleton containing six-membered aromatic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C309/00—Sulfonic acids; Halides, esters, or anhydrides thereof
- C07C309/78—Halides of sulfonic acids
- C07C309/79—Halides of sulfonic acids having halosulfonyl groups bound to acyclic carbon atoms
- C07C309/82—Halides of sulfonic acids having halosulfonyl groups bound to acyclic carbon atoms of a carbon skeleton substituted by singly-bound oxygen atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C311/00—Amides of sulfonic acids, i.e. compounds having singly-bound oxygen atoms of sulfo groups replaced by nitrogen atoms, not being part of nitro or nitroso groups
- C07C311/22—Sulfonamides, the carbon skeleton of the acid part being further substituted by singly-bound oxygen atoms
- C07C311/23—Sulfonamides, the carbon skeleton of the acid part being further substituted by singly-bound oxygen atoms having the sulfur atoms of the sulfonamide groups bound to acyclic carbon atoms
- C07C311/27—Sulfonamides, the carbon skeleton of the acid part being further substituted by singly-bound oxygen atoms having the sulfur atoms of the sulfonamide groups bound to acyclic carbon atoms of an unsaturated carbon skeleton containing rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D291/00—Heterocyclic compounds containing rings having nitrogen, oxygen and sulfur atoms as the only ring hetero atoms
- C07D291/02—Heterocyclic compounds containing rings having nitrogen, oxygen and sulfur atoms as the only ring hetero atoms not condensed with other rings
- C07D291/06—Six-membered rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
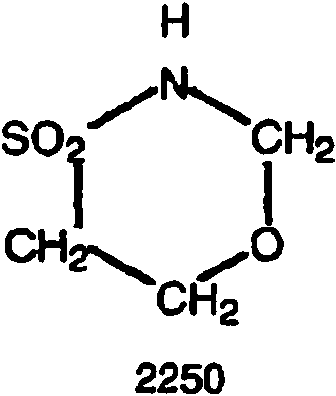
Un procedimiento que comprende hacer reaccionar el ácido isetiónico o una sal del mismo con alcohol bencílico para producir un compuesto que tiene la estructura **(Ver fórmula)** o una sal del mismo.
Description
DESCRIPCIÓN
Procedimiento de preparación de compuestos de tipo oxatiazina
Antecedentes de la invención
Campo de la invención
La presente invención se refiere a nuevos compuestos, procedimientos de preparación de nuevos compuestos y usos de los mismos.
Descripción de la técnica antecedente
Los compuestos de tipo oxatiazina se conocen por el documento WO 2013/190355, la Patente de los Estados Unidos No. 3,202,657 y la Patente de los Estados Unidos No. 3,394,109.
Sigue existiendo la necesidad en la técnica de procedimientos más eficientes y seguros para hacer que tales compuestos proporcionen compuestos con una actividad antineoplásica y antimicrobiana más potente, menos toxicidad y efectos secundarios, y menos resistencia al tratamiento por células tumorales o microbianas.
Sumario de la invención
De acuerdo con la presente invención, se describen procedimientos más eficientes y seguros para fabricar nuevos compuestos de tipo oxatiazina, compuestos útiles para fabricar compuestos de tipo oxatiazina y sus usos.
Descripción detallada de la invención
Según ciertas realizaciones, la presente invención se refiere a procedimientos y compuestos altamente eficientes y seguros de preparación de compuestos tipo oxatiazina en etapas, y derivados de los mismos. Los procedimientos de fabricación y uso de compuestos tipo oxatiazina (nombres IUPAC: tetrahidro-1,4,5-oxatiazindioxid-4,4, o 1,4,5-oxatiazandioxido-4,4) se describen en el documento WO 2016/0989054.
Los compuestos de tipo oxatiazina y derivados de los mismos según ciertas realizaciones de la presente invención tienen actividades antineoplásicas, actividades antimicrobianas y/u otras actividades.
Los procedimientos de fabricación de compuestos de tipo oxatiazina y derivados de los mismos según ciertas realizaciones de esta invención proporcionan métodos ventajosos para fabricar compuestos que tienen actividades antineoplásicas, actividades antimicrobianas y/u otras actividades. En ciertas realizaciones, los compuestos de tipo oxatiazina y derivados de los mismos son útiles, entre otros, en el tratamiento de cánceres y tumores en un sujeto, tal como un paciente humano. De acuerdo con lo anterior, en ciertas realizaciones, la presente invención también se refiere al tratamiento de cánceres y tumores usando compuestos descritos en este documento. Cánceres tales como los cánceres del sistema nervioso central que incluyen glioblastoma, glioma, neuroblastoma, astrocitoma y meningitis carcinomatosa, cáncer de colon, cáncer rectal y cáncer colorrectal, cáncer de ovario, cáncer de mama, cáncer de próstata, cáncer de pulmón, mesotelioma, melanoma, cáncer renal, cáncer de hígado, cáncer de páncreas, cáncer gástrico, cáncer de esófago, cáncer de vejiga urinaria, cáncer de cuello uterino, cáncer cardíaco, cáncer de vesícula biliar, cáncer de piel, cáncer de huesos, cánceres de cabeza y cuello, leucemia, linfoma, linfosarcoma, adenocarcinoma, fibrosarcoma y metástasis de los mismos, por ejemplo, son enfermedades contempladas para el tratamiento según ciertas realizaciones de la invención. Los tumores resistentes a fármacos, por ejemplo, un tumor resistente a múltiples fármacos (MDR), también son útiles en ciertas realizaciones que usan los compuestos de la invención, que incluyen tumores resistentes a fármacos que son tumores sólidos, tumores no sólidos y linfomas. Actualmente se cree que cualquier célula neoplásica se puede tratar usando los métodos descritos en este documento.
En ciertas realizaciones, los compuestos de ejemplo y procedimientos de preparación de compuestos de la invención incluyen lo siguiente:
Hacer reaccionar el ácido isetiónico o una sal del mismo con alcohol bencílico para producir un compuesto que tiene la estructura
o una sal del mismo. Por ejemplo, un procedimiento puede incluir:
En la reacción anterior, la sal sódica del ácido isetiónico se hace reaccionar con alcohol bencílico en presencia de pellas de catalizador de NaOH (99%) para producir el compuesto 2260 y agua. La reacción es altamente eficiente y segura. La reacción de la presente invención evita los olores nocivos y la irritación causados por el uso de reactivos tales como cloruro de bencilo y/o sodio elemental.
Era inesperado que se pudiera lograr una alta pureza y rendimiento usando la reacción de esta divulgación. Esta divulgación describe un procedimiento que es comercialmente útil para producir lotes grandes, por ejemplo, 100-200 kg, con alto rendimiento, baja toxicidad y económicamente.
En ciertas realizaciones, la reacción se puede llevar a cabo a una temperatura de 200 °C o menos, por ejemplo, 160 190 °C o 170-180 °C. La temperatura se puede reducir al vacío, por ejemplo, 130-140 °C a 100 mmHg.
En ciertas realizaciones, el tiempo de reacción es de 30 minutos a 5 horas incluyendo, por ejemplo, 1, 2, 3, 4 o 5 horas o una fracción del mismo.
Los compuestos pueden estar en forma cristalina, por ejemplo, después de la cristalización y/o recristalización en un alcohol, cetona, éster o una combinación de los mismos. Por ejemplo, los compuestos de la presente invención se pueden cristalizar y/o recristalizar en un alcohol tal como etanol.
Síntesis de 2250
Síntesis A
Etapa 1)
Etapa
y
Etapa 4)
Síntesis B
Etapa 1
Exceso de alcohol bencílico por destilación de agua a vacío (por ejemplo, a aproximadamente 140 °C y aproximadamente 100 mmHg de vacío);
Etapa 2)
Etapa 3)
y
Etapa 4)
y
Etapa 5)
Más específicamente, la presente divulgación se refiere a los materiales, productos y métodos descritos a continuación. Esta invención se ilustra mediante los siguientes ejemplos, que son meramente ilustrativos y no deben considerarse como limitativos del alcance de la invención o de la manera en que se puede llevar a la práctica.
Ejemplo 1
14.8 g de ácido isetiónico-Na y
150 mg de NaOH y
100 ml de alcohol bencílico se hicieron reaccionar en un matraz de fondo redondo de 250 ml con un puente de destilación y se calentó lentamente a 180 a 200 °C, durante aproximadamente 3 horas. A esta temperatura, se destilaron aproximadamente 1.8 g de agua.
El producto de reacción se dejó enfriar, formando cristales, y luego se filtró bajo succión. El precipitado muy fino se secó.
Se recuperaron 18.7 g de una sustancia de color blanco con un rendimiento del 78.6%.
El IR confirmó que el producto de reacción era 99% puro.
Ejemplo 2
La sal sódica de ácido isetiónico y las pellas de NaOH en un exceso de alcohol bencílico se calientan en un matraz de vidrio a aproximadamente 170-180 °C. Se destiló aproximadamente 1 mol de agua. El resto se enfría, luego se agrega éster acético o éter de petróleo. El material se extrae a través de papel de filtro bajo succión, dejando un producto puro al 98%.
Por lo general, la reacción se puede llevar a cabo a temperaturas dentro de un intervalo de aproximadamente 160 190 °C hasta que los reactivos estén en solución. El alcohol bencílico tiene un punto de ebullición de aproximadamente 205 °C. De este modo, a las temperaturas de reacción típicas, es posible hervir el agua que se produce sin afectar negativamente la reacción. Como se señaló anteriormente, la reacción puede tener lugar al vacío a temperaturas más bajas, por ejemplo, en exceso de alcohol bencílico o un derivado activo del mismo, con destilación de agua a vacío parcial (por ejemplo, a aproximadamente 130-140 °C y aproximadamente 100 mmHg de vacío).
Claims (9)
2. El procedimiento de la reivindicación 1, que comprende el uso de hidróxido de sodio como catalizador.
3. El procedimiento de la reivindicación 1, en el que la sal del ácido isetiónico es la sal sódica del ácido isetiónico.
7. El procedimiento de la reivindicación 1, en el que dicha reacción se realiza a una temperatura entre 160 °C y 190 °C.
8. El procedimiento de la reivindicación 1, en el que dicha reacción se realiza a una temperatura entre 170 °C y 180 °C.
9. El procedimiento de la reivindicación 1, en el que dicha reacción se realiza a una temperatura entre 130 °C y 140 °C al vacío.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201662319675P | 2016-04-07 | 2016-04-07 | |
| PCT/IB2017/051992 WO2017175177A1 (en) | 2016-04-07 | 2017-04-06 | Process for preparing oxathiazin-like compounds |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2807558T3 true ES2807558T3 (es) | 2021-02-23 |
Family
ID=58699193
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES17722874T Active ES2807558T3 (es) | 2016-04-07 | 2017-04-06 | Procedimiento de preparación de compuestos de tipo oxatiazina |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US10544114B2 (es) |
| EP (1) | EP3440064B1 (es) |
| JP (1) | JP6913692B2 (es) |
| KR (1) | KR20190012148A (es) |
| CN (1) | CN109476615A (es) |
| AU (1) | AU2017245930A1 (es) |
| BR (1) | BR112018070662A2 (es) |
| CA (1) | CA3020239C (es) |
| ES (1) | ES2807558T3 (es) |
| IL (1) | IL262151B (es) |
| MX (1) | MX2018012237A (es) |
| WO (1) | WO2017175177A1 (es) |
| ZA (1) | ZA201807441B (es) |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE1160443B (de) * | 1961-11-30 | 1964-01-02 | Hoechst Ag | Verfahren zur Herstellung von Tetrahydro-oxathiazin-dioxyden |
| DE1234988B (de) | 1964-11-28 | 1967-02-23 | Bayer Ag | Verfahren zur Herstellung von Copolymerisaten des Trioxans |
| US5354864A (en) * | 1992-05-21 | 1994-10-11 | Sloan-Kettering Institute For Cancer Research | 3-(9-acridinylamino)-5-hydroxymethylaniline derivatives as anticancer agents |
| KR101052462B1 (ko) * | 2004-09-21 | 2011-07-28 | 아스텔라스세이야쿠 가부시키가이샤 | 아미노알콜 유도체 |
| DK2861573T3 (da) | 2012-06-18 | 2017-11-13 | Geistlich Pharma Ag | Oxathiazin-derivater som antibakterielle og anticancer-stoffer |
| JP6746605B2 (ja) | 2014-12-19 | 2020-08-26 | ガイストリッヒ・ファルマ・アーゲーGeistlich Pharma Ag | オキサチアジン様化合物を作製する方法 |
-
2017
- 2017-04-06 CA CA3020239A patent/CA3020239C/en active Active
- 2017-04-06 US US16/091,596 patent/US10544114B2/en active Active
- 2017-04-06 BR BR112018070662A patent/BR112018070662A2/pt not_active IP Right Cessation
- 2017-04-06 WO PCT/IB2017/051992 patent/WO2017175177A1/en active Application Filing
- 2017-04-06 CN CN201780027182.3A patent/CN109476615A/zh active Pending
- 2017-04-06 ES ES17722874T patent/ES2807558T3/es active Active
- 2017-04-06 JP JP2018552774A patent/JP6913692B2/ja active Active
- 2017-04-06 EP EP17722874.9A patent/EP3440064B1/en active Active
- 2017-04-06 MX MX2018012237A patent/MX2018012237A/es unknown
- 2017-04-06 KR KR1020187031238A patent/KR20190012148A/ko not_active Application Discontinuation
- 2017-04-06 AU AU2017245930A patent/AU2017245930A1/en not_active Abandoned
-
2018
- 2018-10-04 IL IL262151A patent/IL262151B/en active IP Right Grant
- 2018-11-06 ZA ZA2018/07441A patent/ZA201807441B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| BR112018070662A2 (pt) | 2019-02-05 |
| EP3440064A1 (en) | 2019-02-13 |
| MX2018012237A (es) | 2019-09-04 |
| KR20190012148A (ko) | 2019-02-08 |
| IL262151B (en) | 2020-10-29 |
| JP2019513744A (ja) | 2019-05-30 |
| WO2017175177A1 (en) | 2017-10-12 |
| IL262151A (en) | 2018-11-29 |
| AU2017245930A1 (en) | 2018-10-25 |
| CA3020239A1 (en) | 2017-10-12 |
| CN109476615A (zh) | 2019-03-15 |
| US20190084950A1 (en) | 2019-03-21 |
| JP6913692B2 (ja) | 2021-08-04 |
| US10544114B2 (en) | 2020-01-28 |
| EP3440064B1 (en) | 2020-05-13 |
| CA3020239C (en) | 2024-01-02 |
| ZA201807441B (en) | 2019-08-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2659549T3 (es) | Sales cristalinas de Raltegravir sódico | |
| CA2958139A1 (en) | Solid state forms of ibrutinib | |
| ES2907592T3 (es) | Procesos para preparar compuestos de tipo oxatiazina | |
| ES2470740T3 (es) | Sal de amina orgánica de 6-fluoro-3-hidroxi-2-pirazinocarbonitrilo y método para su producción | |
| ES2612033T3 (es) | Procedimiento para la preparación de bosentán | |
| JP2018527328A (ja) | 置換3−(3−アニリノ−1−シクロヘキシル−1h−ベンズイミダゾール−5−イル)プロパン酸誘導体を調製する方法 | |
| JP2018528199A5 (es) | ||
| ES2879294T3 (es) | Formas polimórficas de Belinostat y procesos para la preparación de las mismas | |
| US20080275265A1 (en) | Process for the Preparation of (Aminoalkylamino)Alkyl Halides and Conversion to Amifostine | |
| CA3183040A1 (en) | Processes for the preparation of an apoptosis-inducing agent | |
| ES2361189T3 (es) | Método para la preparación de ácido 3-o-alquil-ascórbico. | |
| ES2807558T3 (es) | Procedimiento de preparación de compuestos de tipo oxatiazina | |
| ES2223626T3 (es) | Procedimiento para la preparacion de 4-(heteroarilmetil)-1(2h)-ftalazinonas. | |
| JP2017503020A (ja) | Hx塩の形態の(e)−4−n,n−ジアルキルアミノクロトン酸の製造方法、およびegfrチロシンキナーゼ阻害剤の合成のためのその使用 | |
| ES2837014T3 (es) | Procedimiento para la síntesis de curcumina | |
| US20120208787A1 (en) | Crystalline form of fosamprenavir calcium | |
| JP2007015937A (ja) | 5−アミノレブリン酸エステルリン酸類塩、その製造方法及びその用途 | |
| CN113620931A (zh) | 一种雄激素受体抑制剂及其用途 | |
| ES2851499T3 (es) | Proceso para fabricar una forma cristalina de gefitinib | |
| JP2018502901A (ja) | プロドラッグ及び標的治療用化合物を製造する方法 | |
| ES2887268T3 (es) | Proceso para la síntesis de 2-bencidril-3 quinuclidinona | |
| ES2868633T3 (es) | Método de aislamiento y purificación de la naltrexona | |
| ES2538880B1 (es) | Un procedimiento para obtener 4-amino-1-isobutil-1H-imidazo[4,5-c]quinoleína | |
| CN107382942B (zh) | 8-多胺基二氢杨梅素衍生物及其制备方法和应用 | |
| RU2433998C1 (ru) | Способ получения периндоприла и его фармацевтически приемлемых солей |