EP0983994A2 - Dimethyl-(3-aryl-but-3-enyl)-aminverbindungen als pharmazeutische Wirkstoffe - Google Patents
Dimethyl-(3-aryl-but-3-enyl)-aminverbindungen als pharmazeutische Wirkstoffe Download PDFInfo
- Publication number
- EP0983994A2 EP0983994A2 EP99119108A EP99119108A EP0983994A2 EP 0983994 A2 EP0983994 A2 EP 0983994A2 EP 99119108 A EP99119108 A EP 99119108A EP 99119108 A EP99119108 A EP 99119108A EP 0983994 A2 EP0983994 A2 EP 0983994A2
- Authority
- EP
- European Patent Office
- Prior art keywords
- alkyl
- formula
- aryl
- chr
- enyl
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
- 0 CN(C)CC(*)C(C(*)**)=O Chemical compound CN(C)CC(*)C(C(*)**)=O 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D333/00—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom
- C07D333/50—Heterocyclic compounds containing five-membered rings having one sulfur atom as the only ring hetero atom condensed with carbocyclic rings or ring systems
- C07D333/52—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes
- C07D333/54—Benzo[b]thiophenes; Hydrogenated benzo[b]thiophenes with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the hetero ring
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/01—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to acyclic carbon atoms
- C07C211/26—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to acyclic carbon atoms of an unsaturated carbon skeleton containing at least one six-membered aromatic ring
- C07C211/28—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to acyclic carbon atoms of an unsaturated carbon skeleton containing at least one six-membered aromatic ring having amino groups linked to the six-membered aromatic ring by unsaturated carbon chains
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C211/00—Compounds containing amino groups bound to a carbon skeleton
- C07C211/01—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to acyclic carbon atoms
- C07C211/26—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to acyclic carbon atoms of an unsaturated carbon skeleton containing at least one six-membered aromatic ring
- C07C211/29—Compounds containing amino groups bound to a carbon skeleton having amino groups bound to acyclic carbon atoms of an unsaturated carbon skeleton containing at least one six-membered aromatic ring the carbon skeleton being further substituted by halogen atoms or by nitro or nitroso groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C215/00—Compounds containing amino and hydroxy groups bound to the same carbon skeleton
- C07C215/46—Compounds containing amino and hydroxy groups bound to the same carbon skeleton having hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton
- C07C215/48—Compounds containing amino and hydroxy groups bound to the same carbon skeleton having hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton with amino groups linked to the six-membered aromatic ring, or to the condensed ring system containing that ring, by carbon chains not further substituted by hydroxy groups
- C07C215/54—Compounds containing amino and hydroxy groups bound to the same carbon skeleton having hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton with amino groups linked to the six-membered aromatic ring, or to the condensed ring system containing that ring, by carbon chains not further substituted by hydroxy groups linked by carbon chains having at least three carbon atoms between the amino groups and the six-membered aromatic ring or the condensed ring system containing that ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C215/00—Compounds containing amino and hydroxy groups bound to the same carbon skeleton
- C07C215/46—Compounds containing amino and hydroxy groups bound to the same carbon skeleton having hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton
- C07C215/64—Compounds containing amino and hydroxy groups bound to the same carbon skeleton having hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton with rings other than six-membered aromatic rings being part of the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C217/00—Compounds containing amino and etherified hydroxy groups bound to the same carbon skeleton
- C07C217/54—Compounds containing amino and etherified hydroxy groups bound to the same carbon skeleton having etherified hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton
- C07C217/56—Compounds containing amino and etherified hydroxy groups bound to the same carbon skeleton having etherified hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton with amino groups linked to the six-membered aromatic ring, or to the condensed ring system containing that ring, by carbon chains not further substituted by singly-bound oxygen atoms
- C07C217/62—Compounds containing amino and etherified hydroxy groups bound to the same carbon skeleton having etherified hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton with amino groups linked to the six-membered aromatic ring, or to the condensed ring system containing that ring, by carbon chains not further substituted by singly-bound oxygen atoms linked by carbon chains having at least three carbon atoms between the amino groups and the six-membered aromatic ring or the condensed ring system containing that ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C217/00—Compounds containing amino and etherified hydroxy groups bound to the same carbon skeleton
- C07C217/54—Compounds containing amino and etherified hydroxy groups bound to the same carbon skeleton having etherified hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton
- C07C217/74—Compounds containing amino and etherified hydroxy groups bound to the same carbon skeleton having etherified hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton with rings other than six-membered aromatic rings being part of the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C219/00—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton
- C07C219/26—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton having esterified hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton
- C07C219/28—Compounds containing amino and esterified hydroxy groups bound to the same carbon skeleton having esterified hydroxy groups bound to carbon atoms of at least one six-membered aromatic ring and amino groups bound to acyclic carbon atoms or to carbon atoms of rings other than six-membered aromatic rings of the same carbon skeleton having amino groups bound to acyclic carbon atoms of the carbon skeleton
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07B—GENERAL METHODS OF ORGANIC CHEMISTRY; APPARATUS THEREFOR
- C07B2200/00—Indexing scheme relating to specific properties of organic compounds
- C07B2200/07—Optical isomers
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/06—Systems containing only non-condensed rings with a five-membered ring
- C07C2601/10—Systems containing only non-condensed rings with a five-membered ring the ring being unsaturated
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/12—Systems containing only non-condensed rings with a six-membered ring
- C07C2601/16—Systems containing only non-condensed rings with a six-membered ring the ring being unsaturated
Definitions
- the invention relates to dimethyl (3-aryl-but-3-enyl) amine compounds, Process for their preparation and their use Compounds in drugs.
- Opioids have been used as analgesics for pain relief for many years used, although they have a number of side effects, for example Addiction and addiction, respiratory depression, gastrointestinal inhibitory effects and constipation. You can therefore only under special Precautions such as special regulations on given for a longer period or in higher doses (Goodman, Gilman, The Pharmacological Basis of Therapeutics, Pergamon Press, New York 1990).
- Tramadol is a racemate and consists of equal amounts of (+) - and (-) - enantiomer. In vivo, the active ingredient forms the metabolite O-desmethyl-tramadol, which is also present as a mixture of enantiomers.
- the object underlying the invention was to develop of analgesically active substances that are used to treat strong Pain is suitable without the side effects typical of opioids cause.
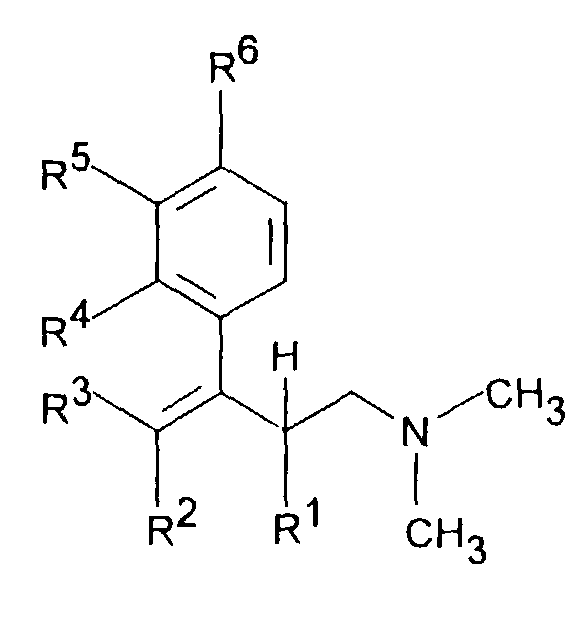
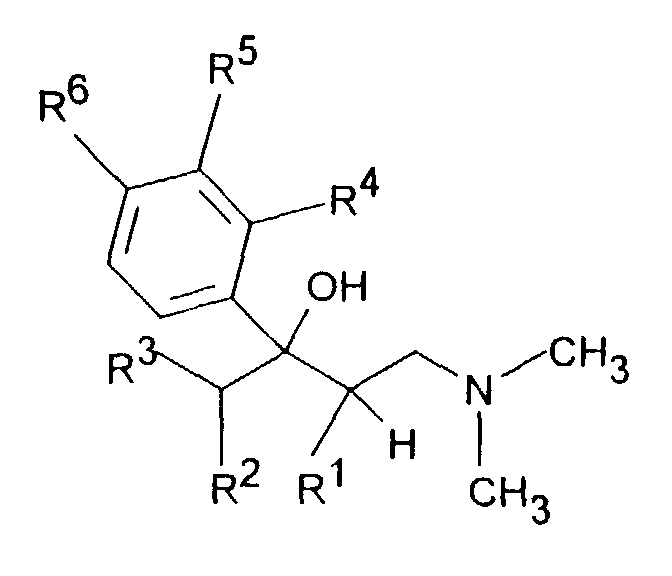
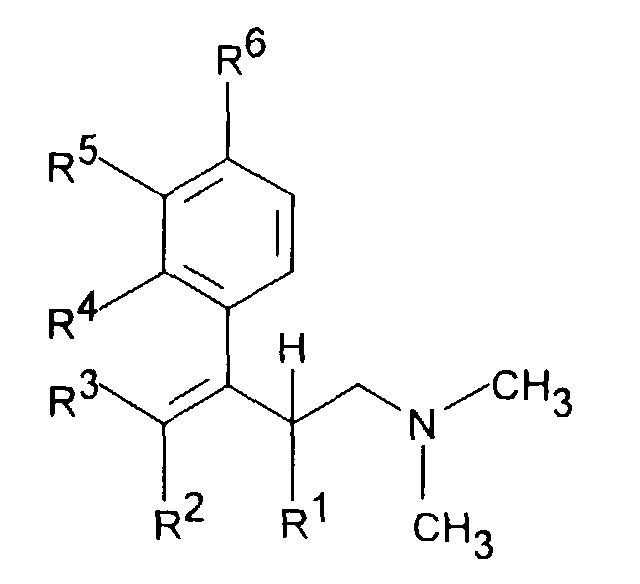
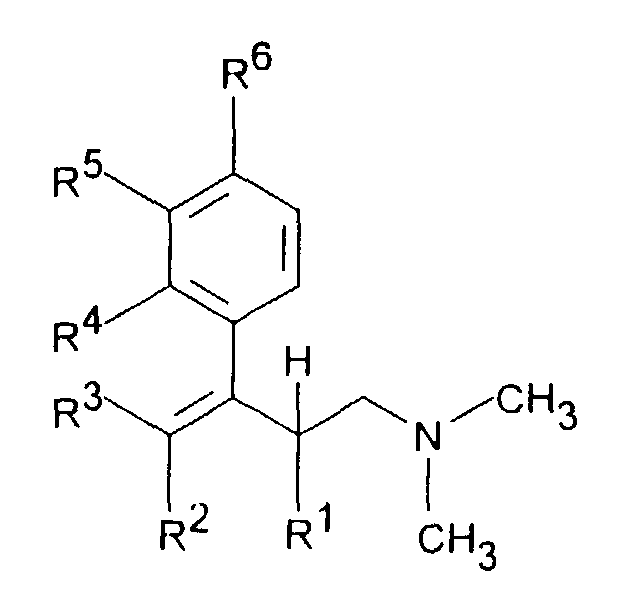
- the invention accordingly relates to dimethyl (3-aryl-but-3-enyl) amine compounds of the formula I.
- R 1 and R 2 together represent - (CH 2 ) 2-4 -, - (CH 2 ) 2 -CHR 7 or -CH 2 -CHR 7 -CH 2 -
- R 3 is H or C 1-5 alkyl
- R 4 is H, OH, C 1-4 alkyl, OC 1-4 alkyl, O-benzyl, CF 3 , O-CF 3 , Cl, F or OR 8
- R 5 is H, OH, C 1 -4 alkyl, OC 1-4 alkyl, O-benzyl, CHF 2 , CF 3 , O-CF 3 , Cl, F or OR 8
- R 6 is H, OH, C 1-4 alkyl, OC 1 -4- alkyl, O-benzyl, CF 3 , O-CF 3 , Cl, F or OR 8
- R 6 is H, OH, C
- R 8 CO-C 1-5 alkyl, PO (OC 1-4 alkyl) 2 , CO-C 6 H 4 -R 11 , CO (OC 1-5 alkyl), CO-CHR 12 -NHR 13 , CO-NH-C 6 H 3 - (R 14 ) 2 or an unsubstituted or substituted pyridyl, thienyl, thiazoyl or phenyl group
- R 9 is H or C 1-4 alkyl
- R 10 is H or C 1-3 alkyl
- R 11 is OC (O) -C 1-3 alkyl in the ortho position or CH 2 -N- (R 15 ) 2 in the meta or para position, where R 15 is C 1-4 alkyl or both radicals R 15 together with N form the 4-morpolino radical
- means R 12 and R 13 are identical or different and H, C 1 -6- alkyl or C 3-8 -cycloalkyl or R 12 and R 13 together - (CH 2 ) 3-8 -
- R 1 and R 2 together are - (CH 2 ) 2-3 - or - (CH 2 ) 2 -CHR 7 ,
- Another subject of the invention is a process for the preparation of dimethyl- (3-aryl-but-3-enyl) amine compounds of the formula I in which R 1 and R 2 together - (CH 2 ) 2-4 -, - (CH 2 ) 2 -CHR 7 or -CH 2 -CHR 7 -CH 2 - represent, R 3 is H or C 1-5 -alkyl, R 4 is H, C 1-4 -alkyl, OC 1-4 -alkyl, O-benzyl , CF 3 , O-CF 3 , Cl or F means R 5 H, C 1-4 alkyl, OC 1-4 alkyl, O-benzyl, CHF 2 , CF 3 , O-CF 3 , Cl or F represents and R 6 is H, C 1-4 alkyl, OC 1-4 alkyl, O-benzyl, CF 3 , O-CF 3 , Cl or F, with the proviso that two of the radicals R 4 , R 5 or R 6 are
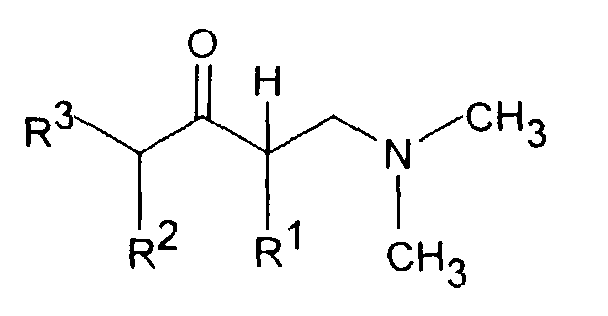
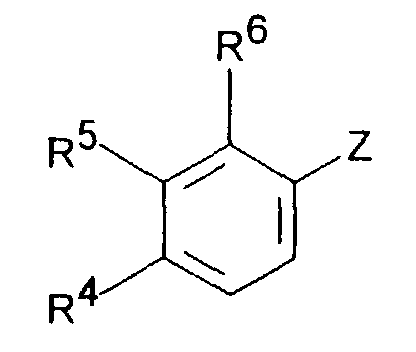
- the reaction of a ⁇ -dimethylamine ketone with a Grignard compound of the formula III, in which Z is MgCl, MgBr or MgJ, or with one organolithium compound of formula III can in an aliphatic Ethers, for example diethyl ether and / or tetrahydrofuran Temperatures between -70 ° and + 60 ° C can be carried out.
- the Implementation with a Grignard connection can be done with or without addition a carry-along reagent, preferably 1,2-dibromoethane.
- lithium Organic Compounds of formula III can be implemented a compound of the formula III in which Z is Cl, Br or J, with for example an n-butyllithium / hexane solution by halogen / lithium exchange receive.
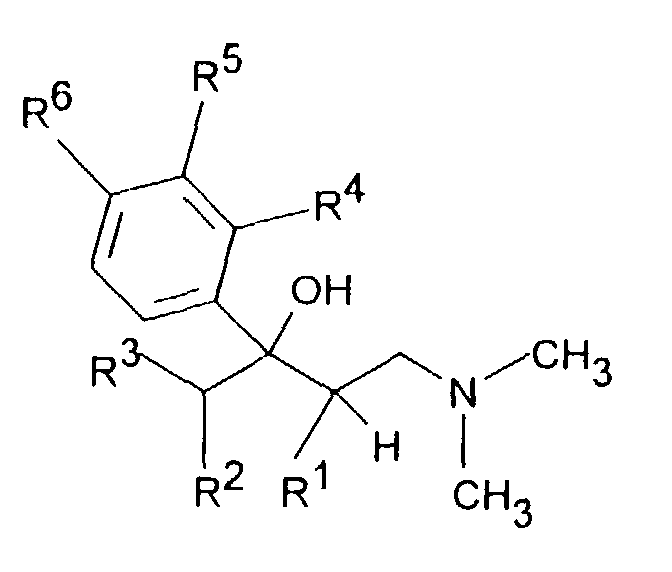
- the tertiary alcohols of the formula IV obtained can be reacted with acids, especially formic acid or hydrochloric acid, at temperatures between Dehydrate at 0 ° and 100 ° C.
- Another object of the invention is a process for the preparation of a dimethyl- (3-aryl-but-3-enyl) amine compound of the formula I in which R 1 and R 2 together - (CH 2 ) 2-4 -, - (CH 2 ) 2 -CHR 7 or -CH 2 -CHR 7 -CH 2 mean, R 3 is H or C 1-5 alkyl, one of the radicals R 4 , R 5 or R 6 is OH and the other two radicals are H, R 7 is C 1-8 alkyl, C 3-8 cycloalkyl, OC 1-4 alkyl, O-benzyl, CF 3 , Cl or F, which is characterized in that a compound of the formula I in which one of the radicals R 4 , R 5 or R 6 is O-CH 3 and the other two radicals are H, reacted with diisobutylaluminium hydride or a compound of the formula I in which one of the radicals R 4 , R 5 or R 6 is O-benz
- reaction of a dimethyl (3-aryl-but-3-enyl) amine compound with diisobutyl aluminum hydride is usually carried out in an aromatic hydrocarbon, for example toluene, at a temperature between 60 ° and 130 ° C (Synthesis 1975 , 617; DE 24 09 990, DE 24 09 991; Chem. Abstr. 84 59862 (1974)).
- aromatic hydrocarbon for example toluene
- the reductive debenzylation of a compound of the formula I according to the invention in which one of the radicals R 4 , R 5 or R 6 is O-benzyl, can be carried out in the presence of platinum or palladium on a support material, for example activated carbon, in the presence of hydrogen in a solvent , for example acetic acid or C 1-4 alkyl alcohol, at pressures between 1 and 100 bar and temperatures between 20 ° and 100 ° C.
- a support material for example activated carbon
- Dimethyl- (3-aryl-but-3-enyl) amine compounds of the formula I in which OR 8 represents an ⁇ -aminocarboxylate group are obtained by reacting a corresponding dimethyl- [3- (hydroxy-phenyl) but-3-enyl ] -amine compound of formula I, in which R 4 , R 5 and / or R 6 represent an OH group, with a corresponding 2-t-butoxycarbonylamino-carboxylic acid using triethylamine and coupling reagents such as benzotriazol-1-yl-oxy tripyrrolidinophosphonium hexafluorophosphate in a solvent, for example dichloromethane, available.
- a solvent for example dichloromethane
- the compounds of formula I can be physiologically tolerated Acids, for example hydrochloric acid, hydrobromic acid, sulfuric acid, Methanesulfonic acid, formic acid, acetic acid, oxalic acid, Succinic acid, tartaric acid, mandelic acid, fumaric acid, lactic acid, citric acid, Glutamic acid and / or aspartic acid, known per se Transfer them to their salts.
- Salt formation is preferably carried out in a solvent, for example diethyl ether, diisopropyl ether, Alkyl acetate, acetone and / or 2-butanone performed.
- the production of the hydrochloride is also suitable Trimethylohlorsilane in aqueous solution.
- the compounds according to the invention have a pronounced analgesic Effect and are toxicologically harmless. They are suitable therefore as active pharmaceutical ingredients. Is accordingly Subject of the invention also the use of a dimethyl (3-aryl-but-3-enyl) amine compound of formula I as an active ingredient in pharmaceuticals, preferably as an active ingredient in pain relievers.
- Medicaments according to the invention contain at least one Dimethyl- (3-aryl-but-3-enyl) amine compound of the formula I.
- Carrier materials, fillers, solvents, diluents, dyes and / or binders The selection of auxiliary materials and the ones to be used Amounts depend on whether the drug is oral, intravenous, intraperitoneal, intradermal, intramuscular, intranasal, buccal or local to Example for infections on the skin, on the mucous membranes or on the Eyes to be applied.
- the amount of active ingredient to be administered to the patient varies in Depends on the weight of the patient, on the type of application, the Indication and the severity of the disease. Usually 10 to 500 mg per kg of at least one dimethyl- (3-aryl-but-3-enyl) amine compound of formula I applied.
- the indication ether means diethyl ether.
- the methoxy compounds (-37) and (+37) from the 2nd stage were under the conditions given in Example 5 into the hydrochloride (+38) and (-38) in a yield of 87% of theory and with a melting point transferred from 122 - 123 ° C.
- the analgesic activity was in phenylquinone-induced writhing on the mouse, modified according to IC Hendershot, J. Forsaith, J. Pharmacol. Exp. Ther. 125 , 237-240 (1959).
- Male NMRI mice weighing 25-30 g were used for this.
- Groups of 10 animals per substance dose were given 10 minutes after intravenous administration of a compound according to the invention to 0.3 ml / mouse of a 0.02% strength aqueous solution of phenylquinone (phenylbenzoquinone, from Sigma, Deisenhofen; preparation of the solution with addition of 5% ethanol and Storage in a water bath at 45 ° C) applied intraperitoneally.
- the animals were placed individually in observation cages.
- the ED 50 values of the writhing reaction were calculated from the dose-dependent decrease in the writhing reactions compared to animal groups examined in parallel, to which no compounds according to the invention were applied, using regression analysis (evaluation program Martens EDV Service, Eckental).
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Pain & Pain Management (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Rheumatology (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
Description
Die reduktive Debenzylierung einer erfindungsgemäßen Verbindung der Formel I, in der einer der Reste R4, R5 oder R6 O-Benzyl bedeutet, läßt sich in Gegenwart von Platin oder Paladium auf einem Trägermaterial, beispielsweise Aktivkohle, in Gegenwart von Wasserstoff in einem Lösungsmittel, beispielsweise Essigsäure oder C1-4-Alkylalkohol, bei Drücken zwischen 1 und 100 bar und Temperaturen zwischen 20° und 100° C durchführen.
und
- (+27):
- Ausbeute: 42 % der Theorie
[α] RT / D = +33,8° (c = 1,00; Methanol) - (-27):
- Ausbeute: 44 % der Theorie
[α] RT / D = -34,3° (c = 1,06; Methanol)
und
- (+29):
- Ausbeute: 43 % der Theorie
[α] RT / D = +24,1° (c = 0,96; Methanol) - (-29):
- Ausbeute: 44 % der Theorie
[α] RT / D = -23,5° (c = 0,94; Methanol)
und
und
- (+37):
- Ausbeute: 43 % der Theorie
[α] RT / D = +36,4° (c = 1,01; Methanol) - (-37):
- Ausbeute: 44 % der Theorie
[α] RT / D = -37,7° (c = 1,01; Methanol)
und
und
- (-36):
- [α] RT / D = - 75,5° (c = 0,96; Methanol)
- (+36):
- [α] RT / D = + 77,7° (c = 1,08; Methanol)
- (-39):
- [α] RT / D = -96,6° (c = 1,04; Methanol)
- (+39):
- [α] RT / D = +89,0° (c = 0,99; Methanol)
| Analgesieprüfung im Writhing-Test an der Maus | |
| erfindungsgemäße Verbindung hergestellt nach Beispiel | ED50 (mg/kg) |
| 2 (+)-Enantiomer | 1,40 |
| 4 (-)-Enantiomer | 2,12 |
| 6 | 1,35 |
| 7 (-)-Enantiomer | 0,90 |
| 8 (-)-Enantiomer | 1,04 |
| 9 (+)-Enantiomer | 1,60 |
| zum Vergleich: Tramadol | 3,68 |
Claims (9)
- Dimethyl-(3-aryl-but-3-enyl)-aminverbindungen der Formel I,ausgenommen sind.in der R1 und R2 zusammen -(CH2)2-4-, -(CH2)2-CHR7 oder -CH2-CHR7-CH2- darstellen,R3 H oder C1-5-Alkyl bedeutet,R4 H bedeutet,R5 OH, C1-4-Alkyl, O-C1-4-Alkyl, O-Benzyl, CHF2, CF3, O-CF3, Cl, F oder OR8 darstellt undR6 H bedeutet,R7 C1-8-Alkyl, C3-8-Cycloalkyl, O-C1-4-Alkyl, O-Benzyl, CF3, Cl oder F bedeutetR8 CO-C1-5-Alkyl, PO(O-C1-4-Alkyl)2, CO-C6H4-R11, CO(O-C1-5-Alkyl), CO-CHR12-NHR13, CO-NH-C6H3-(R14)2 oder eine unsubstituierte oder substituierte Pyridyl-, Thienyl-, Thiazoyl- oder Phenylgruppe bedeutet,R11 OC(O)-C1-3-Alkyl in ortho-Stellung oder CH2-N-(R15)2 in meta- oder para-Stellung, wobei R15 C1-4-Alkyl oder beide Reste R15 zusammen mit N den 4-Morpolino-Rest bilden, bedeutetR12 und R13 gleich oder verschieden sind und H, C1-6-Alkyl oder C3-8-Cycloalkyl oder R12 und R13 zusammen -(CH2)3-8- bedeuten,R14 H, OH, C1-7Alkyl, O-C1-7-Alkyl, Phenyl, O-Aryl, CF3, Cl oder F bedeutet, mit der Maßgabe, daß die beiden Reste R14 gleich oder verschieden sind,in Form ihrer Basen und/oder Salze von physiologisch verträglichen Säuren, als Enantiomere oder Racemate mit der Maßgabe, daß die Racemate der Verbindungen der Formel I,in der R1 und R2 zusammen -(CH2)3- sind, R3, R4 und R6 H bedeuten und R5 OCH3 ist,
oderin der R1 und R2 zusammen -(CH2)3- sind, R3, R4 und R6 H bedeuten und R5 O-CO-CH3 ist,
oderin der R1 und R2 zusammen -(CH2)2- sind, R3, R4 und R6 H bedeuten und R5 OH ist, als Hydrochlorid,
oderin der R1 und R2 zusammen -(CH2)3- sind, R3, R4 und R6 H bedeuten und R5 OH ist, als Hydrochlorid,
oderin der R1 und R2 zusammen -(CH2)4- sind, R3, R4 und R6 H bedeuten und R5 OH ist, als Hydrochlorid, - Dimethyl-(3-aryl-but-3-enyl)-aminverbindungen gemäß Anspruch 1, dadurch gekennzeichnet, daßR1 und R2 zusammen -(CH2)2-4- oder -(CH2)2-CHR7 bedeuten,R3 H oder C1-3-Alkyl bedeutet,R4 H bedeutet,R5 OH, C1-4-Alkyl, O-C1-4-Alkyl, O-Benzyl, CHF2, CF3, Cl, F oder OR8 darstellt undR6 H bedeutet,R7 C1-4-Alkyl, CF3, Cl oder F bedeutet.
- Dimethyl-(3-aryl-but-3-enyl)-aminverbindungen gemäß Anspruch 1 oder 2, dadurch gekennzeichnet, daßR1 und R2 zusammen -(CH2)2-3- oder -(CH2)2-CHR7 bedeuten,R3 H, CH3 oder CH2CH3 bedeutet,R4 H, R5 OH, OCH3, CHF2 oder OR8 und R6 H bedeutet,R8 CO-C6H4-R11 mit R11 OC(O)-C1-3-Alkyl in ortho-Stellung darstellt.
- Dimethyl-(3-aryl-but-3-enyl)-aminverbindungen gemäß einem oder mehreren der Ansprüche 1 bis 3, dadurch gekennzeichnet, daßR1 und R2 zusammen -(CH2)2-3- oder -(CH2)2-CH(CH3)- darstellen,R3 H oder CH3 bedeutet,R4 H ist, R5 OH oder OR8 bedeutet, R6 H ist, und R8 CO-C6H4-R11 mit R11 OC(O)-CH3 in ortho-Stellung bedeutet.
- Verfahren zur Herstellung einer Dimethyl-(3-aryl-but-3-enyl)-aminverbindung der Formel I,ausgenommen sind, dadurch gekennzeichnet, daß man ein β-Dimethylaminoketon der Formel II mit einer metallorganischen Verbindung der Formel III in der Z MgCl, MgBr, MgI oder Li bedeutet, zu einem tertiären Alkohol der Formel IV umsetzt, welcher anschließend zu einer Verbindung der Formel I dehydratisiert wird.in der R1 und R2 zusammen -(CH2)2-4-, -(CH2)2-CHR7 oder -CH2-CHR7-CH2- darstellen,R3 H oder C1-5-Alkyl bedeutet,R4 H bedeutet,R5 C1-4-Alkyl, O-C1-4-Alkyl, O-Benzyl, CHF2, CF3, O-CF3, Cl oder F darstellt undR6 H bedeutet,R7 C1-8-Alkyl, C3-8-Cycloalkyl, O-C1-4-Alkyl, O-Benzyl, CF3, Cl oder F bedeutet, wobei die Racemate der Verbindungen der Formel I,in der R1 und R2 zusammen -(CH2)3- sind, R3, R4 und R6 H bedeuten und R5 OCH3 ist,
oderin der R1 und R2 zusammen -(CH2)3- sind, R3, R4 und R6 H bedeuten und R5 O-CO-CH3 ist,
oderin der R1 und R2 zusammen -(CH2)2- sind, R3, R4 und R6 H bedeuten und R5 OH ist, als Hydrochlorid,
oderin der R1 und R2 zusammen -(CH2)3- sind, R3, R4 und R6 H bedeuten und R5 OH ist, als Hydrochlorid,
oderin der R1 und R2 zusammen -(CH2)4- sind, R3, R4 und R6 H bedeuten und R5 OH ist, als Hydrochlorid, - Verfahren zur Herstellung einer Dimethyl-(3-aryl-but-3-enyl)-aminverbindung der Formel I,in der R1 und R2 zusammen -(CH2)2-4-, -(CH2)2-CHR7 oder -CH2-CHR7-CH2- bedeuten,R3 H oder C1-5-Alkyl bedeutet,der Rest R5 OH bedeutet und die Reste R4 und R6 H sind,R7 C1-8-Alkyl, C3-8-Cycloalkyl, O-C1-4-Alkyl, O-Benzyl, CF3, Cl oder F bedeutet
dadurch gekennzeichnet, daß man eine Verbindung der Formel I, in der der Rest R5 O-CH3 bedeutet und die Reste R4 und R6 H sind, mit Diisobutylaluminiumhydrid umsetzt oder eine Verbindung der Formel I, in der der Rest R5 O-Benzyl bedeutet und die Reste R4 und R6 H sind, reduktiv debenzyliert. - Arzneimittel enthaltend als pharmazeutischen Wirkstoff wenigstens eine Dimethyl-(3-aryl-but-3-enyl)-aminverbindung der allgemeinen Formel I,ausgenommen sindin der R1 und R2 zusammen -(CH2)2-4-, -(CH2)2-CHR7 oder -CH2-CHR7-CH2- darstellen,R3 H oder C1-5-Alkyl bedeutet,R4 H bedeutet,R5 OH, C1-4-Alkyl, O-C1-4-Alkyl, O-Benzyl, CHF2, CF3, O-CF3, Cl, F oder OR8 darstellt undR6 H bedeutet,R7 C1-8-Alkyl, C3-8-Cycloalkyl, O-C1-4-Alkyl, O-Benzyl, CF3, Cl oder F bedeutet,R8 CO-C1-5-Alkyl, PO(O-C1-4-Alkyl)2, CO-C6H4-R11, CO(O-C1-5-Alkyl), CO-CHR12-NHR13, CO-NH-C6H3-(R14)2 oder eine unsubstituierte oder substituierte Pyridyl-, Thienyl-, Thiazoyl- oder Phenylgruppe bedeutet,R11 OC(O)-C1-3-Alkyl in ortho-Stellung oder CH2-N-(R15)2 in meta- oder para-Stellung, wobei R15 C1-4-Alkyl oder beide Reste R15 zusammen mit N den 4-Morpolino-Rest bilden, bedeutet,R12 und R13 gleich oder verschieden sind und H, C1-6-Alkyl oder C3-8-Cycloalkyl oder R12 und R13 zusammen -(CH2)3-8- bedeuten,R14 H, OH, C1-7-Alkyl, O-C1-7-Alkyl, Phenyl, O-Aryl, CF3, Cl oder F bedeutet, mit der Maßgabe, daß die beiden Reste R14 gleich oder verschieden sind,mit der Maßgabe, daß die Racemate der Verbindungen der Formel I,in der R1 und R2 zusammen -(CH2)3- sind, R3, R4 und R6 H bedeuten und R5 OCH3 ist
oderin der R1 und R2 zusammen -(CH2)3- sind, R3, R4 und R6 H bedeuten und R5 O-CO-CH3 istin Form ihrer Base und/oder ihres Salzes einer physiologisch verträglichen Säure, als Enantiomer oder Racemat und gegebenfalls weitere Wirkstoffe und/oder Hilfsstoffe. - Arzneimittel nach Anspruch 7 zur Bekämpfung von Schmerz.
- Verwendung wenigstens einer Dimethyl-(3-aryl-but-3-enyl)-aminverbindung der Formel I gemäß Anspruch 7 in Form ihrer Base und/oder ihres Salzes einer physiologisch verträglichen Säure, als Enantiomer oder Racemat zur Herstellung eines Arzneimittels zur Bekämpfung von Schmerzen.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE19609847 | 1996-03-13 | ||
| DE19609847A DE19609847A1 (de) | 1996-03-13 | 1996-03-13 | Dimethyl-(3-aryl-but-3-enyl)-aminverbindungen als pharmazeutische Wirkstoffe |
| EP97102923A EP0799819B1 (de) | 1996-03-13 | 1997-02-22 | 1-Dimethylaminomethyl-2-phenyl-cycloalk-2-enverbindungen mit analgetischer Wirkung |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP97102923A Division EP0799819B1 (de) | 1996-03-13 | 1997-02-22 | 1-Dimethylaminomethyl-2-phenyl-cycloalk-2-enverbindungen mit analgetischer Wirkung |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| EP0983994A2 true EP0983994A2 (de) | 2000-03-08 |
| EP0983994A3 EP0983994A3 (de) | 2001-01-10 |
Family
ID=7788151
Family Applications (4)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP99119109A Expired - Lifetime EP0983995B1 (de) | 1996-03-13 | 1997-02-22 | Dimethyl-(3-aryl-but-3-enyl)-aminverbindungen als pharmazeutische Wirkstoffe |
| EP99119108A Withdrawn EP0983994A3 (de) | 1996-03-13 | 1997-02-22 | Dimethyl-(3-aryl-but-3-enyl)-aminverbindungen als pharmazeutische Wirkstoffe |
| EP00116745A Expired - Lifetime EP1069106B1 (de) | 1996-03-13 | 1997-02-22 | Dimethyl-(3-aryl-but-3-enyl)-amin-verbindungen mit analgetischer Wirkung |
| EP97102923A Expired - Lifetime EP0799819B1 (de) | 1996-03-13 | 1997-02-22 | 1-Dimethylaminomethyl-2-phenyl-cycloalk-2-enverbindungen mit analgetischer Wirkung |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP99119109A Expired - Lifetime EP0983995B1 (de) | 1996-03-13 | 1997-02-22 | Dimethyl-(3-aryl-but-3-enyl)-aminverbindungen als pharmazeutische Wirkstoffe |
Family Applications After (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP00116745A Expired - Lifetime EP1069106B1 (de) | 1996-03-13 | 1997-02-22 | Dimethyl-(3-aryl-but-3-enyl)-amin-verbindungen mit analgetischer Wirkung |
| EP97102923A Expired - Lifetime EP0799819B1 (de) | 1996-03-13 | 1997-02-22 | 1-Dimethylaminomethyl-2-phenyl-cycloalk-2-enverbindungen mit analgetischer Wirkung |
Country Status (27)
| Country | Link |
|---|---|
| US (1) | US5811582A (de) |
| EP (4) | EP0983995B1 (de) |
| JP (2) | JP4205182B2 (de) |
| KR (2) | KR100538662B1 (de) |
| CN (1) | CN1157366C (de) |
| AR (1) | AR008991A1 (de) |
| AT (3) | ATE258544T1 (de) |
| AU (1) | AU725430B2 (de) |
| BR (1) | BR9700369B1 (de) |
| CA (1) | CA2199679C (de) |
| CO (1) | CO4520279A1 (de) |
| CZ (1) | CZ293971B6 (de) |
| DE (4) | DE19609847A1 (de) |
| DK (3) | DK1069106T3 (de) |
| ES (3) | ES2213526T3 (de) |
| HU (1) | HU224819B1 (de) |
| IL (1) | IL120430A (de) |
| NO (1) | NO308294B1 (de) |
| NZ (1) | NZ314384A (de) |
| PE (1) | PE55798A1 (de) |
| PL (1) | PL186050B1 (de) |
| PT (3) | PT983995E (de) |
| RU (1) | RU2167146C2 (de) |
| SI (3) | SI1069106T1 (de) |
| SK (1) | SK284328B6 (de) |
| UA (1) | UA55373C2 (de) |
| ZA (1) | ZA972147B (de) |
Families Citing this family (30)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE4426245A1 (de) * | 1994-07-23 | 1996-02-22 | Gruenenthal Gmbh | 1-Phenyl-3-dimethylamino-propanverbindungen mit pharmakologischer Wirkung |
| DE19732928C2 (de) * | 1997-07-31 | 2000-05-18 | Gruenenthal Gmbh | Verwendung substituierter Imidazolidin-2,4-dion-Verbindungen als Schmerzmittel |
| DE19830105C1 (de) * | 1998-07-06 | 2000-02-17 | Gruenenthal Gmbh | Acridinderivate |
| ES2141688B1 (es) * | 1998-11-06 | 2001-02-01 | Vita Invest Sa | Nuevos esteres derivados de compuestos fenil-ciclohexil sustituidos. |
| DE10000311A1 (de) * | 2000-01-05 | 2001-07-12 | Gruenenthal Gmbh | Aminomethyl-Phonyl-Cyclohexanonderivate |
| DE10025948A1 (de) * | 2000-05-26 | 2001-11-29 | Gruenenthal Gmbh | Wirkstoffkombination |
| DE10049481A1 (de) * | 2000-09-29 | 2002-05-02 | Gruenenthal Gmbh | Substituierte C-Cyclohexylmethylamin-Derivate |
| DE10049483A1 (de) * | 2000-09-29 | 2002-05-02 | Gruenenthal Gmbh | Substituierte 1-Aminobutan-3-ol-Derivate |
| DE10059413A1 (de) * | 2000-11-30 | 2002-06-20 | Gruenenthal Gmbh | Verwendung von substituierten 6-Dimethylaminomethyl-1-phenyl-cyclohexanverbindungen zur Therapie der Harninkontinenz |
| DE10059411A1 (de) * | 2000-11-30 | 2002-06-13 | Gruenenthal Gmbh | Verwendung von 6-Dimethylaminomethyl-1-phenyl-cyclohexanverbindungen zur Therapie der Harninkontinenz |
| US20050176790A1 (en) | 2001-02-28 | 2005-08-11 | Johannes Bartholomaus | Pharmaceutical salts |
| EP1397126B9 (de) | 2001-03-16 | 2007-02-21 | DMI Biosciences, Inc. | Verwendung von Tramadol zur Verzögerung der Ejakulation |
| DE10132747A1 (de) * | 2001-07-05 | 2003-01-23 | Gruenenthal Gmbh | Substituierte 1-Aryl-but-3-enylamin- und 1-Aryl-but-2-enylaminverbindungen |
| DE10146275A1 (de) | 2001-09-18 | 2003-04-24 | Gruenenthal Gmbh | Kombination ausgewählter Opioide mit Muscarin-Antagonisten zur Therapie der Harninkontinenz |
| PE20030527A1 (es) | 2001-10-24 | 2003-07-26 | Gruenenthal Chemie | Formulacion farmaceutica con liberacion retardada que contiene 3-(3-dimetilamino-1-etil-2-metil-propil) fenol o una sal farmaceuticamente aceptable del mismo y tabletas para administracion oral que la contienen |
| DE10224624A1 (de) * | 2002-05-30 | 2003-12-11 | Gruenenthal Gmbh | Metabolite und Prodrugs von 1-Dimethylamino-3-(3-methoxy-phenyl)-2-methyl-pentan-3-ol |
| DE10225315A1 (de) * | 2002-06-06 | 2003-12-24 | Gruenenthal Gmbh | Wirkstoffsalze und Ester von 1-Dimethylamino-3-(3-methoxy-phenyl)-2-methyl- pentan-3-ol und 3-(3-Dimethylamino-1-ethyl-1-hydroxy-2-methyl- propyl)-phenol |
| DE10261091A1 (de) * | 2002-12-20 | 2004-07-01 | Grünenthal GmbH | Gesättigte und ungesättigte Heteroarylcycloalkylmethyl-Amine |
| DE10315917A1 (de) * | 2003-04-08 | 2004-11-18 | Schwarz Pharma Ag | Hochreine Basen von 3,3-Diphenylpropylaminmonoestern |
| DE10326097A1 (de) | 2003-06-06 | 2005-01-05 | Grünenthal GmbH | Verfahren zur Herstellung von Dimethyl-(3-aryl-butyl)-aminverbindungen |
| DE10328316A1 (de) * | 2003-06-23 | 2005-01-20 | Grünenthal GmbH | Verfahren zur Herstellung von Dimethyl-(3-aryl-buthyl)-aminverbindungen als pharmazeutische Wirkstoffe |
| DE102004034619A1 (de) * | 2004-07-16 | 2006-02-23 | Grünenthal GmbH | Substituierte Aminoverbindungen als 5-HT/NA Uptakehemmer |
| DE102005033732B4 (de) * | 2005-05-27 | 2014-02-13 | Grünenthal GmbH | Trennung stereoisomerer N,N-Dialkylamino-2-alkyl-3-hydroxy-3-phenyl-alkane |
| DE102005052588A1 (de) | 2005-11-02 | 2007-05-10 | Grünenthal GmbH | Verfahren zur Herstellung substituierter Dimethyl-(3-aryl-butyl)-amin-Verbindungen mittels homogener Katalyse |
| DE102005061429A1 (de) * | 2005-12-22 | 2007-06-28 | Grünenthal GmbH | Substituierte Oxazol-Derivate |
| TWI496762B (zh) | 2006-07-24 | 2015-08-21 | 製備(1r,2r)-3-(3-二甲胺基-1-乙基-2-甲基-丙基)-酚之方法 | |
| WO2008012283A1 (en) * | 2006-07-24 | 2008-01-31 | Janssen Pharmaceutica Nv | Preparation of (2r,3r)-3-(3-methoxyphenyl)-n,n,2-trimethylpentanamine |
| CN101948397A (zh) * | 2010-09-07 | 2011-01-19 | 天津泰普药品科技发展有限公司 | 镇痛药他喷他多重要中间体的制备方法 |
| EP2619174A4 (de) * | 2010-09-20 | 2014-05-14 | Ind Swift Lab Ltd | Verfahren zur herstellung eines l-phenyl-3-dimethylaminopropanderivats |
| EP2674414A1 (de) | 2012-06-15 | 2013-12-18 | Siegfried AG | Verfahren zur Herstellung von 1-aryl-1-alkyl-3-dialkylaminopropan-Verbindungen |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE1518663A1 (de) * | 1965-08-02 | 1969-12-18 | Gruenenthal Chemie | Basisch substituierte Cycloalken-derivate und Verfahren zu ihrer Herstellung |
| US3652589A (en) * | 1967-07-27 | 1972-03-28 | Gruenenthal Chemie | 1-(m-substituted phenyl)-2-aminomethyl cyclohexanols |
| US3978129A (en) * | 1972-01-28 | 1976-08-31 | A. H. Robins Company, Incorporated | Alkenyl- and alkanylamines |
| NL7403348A (de) * | 1973-03-19 | 1974-09-23 | ||
| GB1502635A (en) * | 1974-02-27 | 1978-03-01 | Schering Ag | Process for splitting steroid ethers |
| DE2409990C2 (de) * | 1974-02-27 | 1982-11-25 | Siemens AG, 1000 Berlin und 8000 München | Meßwandler für Hochspannungsschaltanlagen mit Metallkapselung |
| JPS598259B2 (ja) * | 1976-01-01 | 1984-02-23 | 武田薬品工業株式会社 | 新規シクロヘキセン誘導体 |
| US4173649A (en) * | 1978-02-27 | 1979-11-06 | E. R. Squibb & Sons, Inc. | 5-Phenyl-2,4-pentadien-1-amines and method for inhibiting prostaglandin dehydrogenase |
| FR2559765B1 (fr) * | 1984-02-16 | 1986-06-13 | Rhone Poulenc Sante | Nouveaux derives de la phenyl-3 propene-2 amine, leur preparation et les medicaments qui les contiennent |
| IT1213219B (it) * | 1984-09-28 | 1989-12-14 | Consiglio Nazionale Ricerche | Derivati amminoalchilnaftalenici ad attivita' farmacologica. |
| US5430044A (en) * | 1987-02-06 | 1995-07-04 | Fisons Corporation | Arylalkyl-amines and -amides having anticonvulsant and neuroprotective properties |
| SE9202218D0 (sv) * | 1992-07-22 | 1992-07-22 | Kabi Pharmacia Ab | Pharmacologically active alfa-(tertiary-aminomethyl)-benzenemethanol derivatives, pharmaceutical composition containing them, therapeutical use thereof and processes for their preparation |
| DE4426245A1 (de) * | 1994-07-23 | 1996-02-22 | Gruenenthal Gmbh | 1-Phenyl-3-dimethylamino-propanverbindungen mit pharmakologischer Wirkung |
-
1996
- 1996-03-13 DE DE19609847A patent/DE19609847A1/de not_active Withdrawn
-
1997
- 1997-02-22 AT AT00116745T patent/ATE258544T1/de active
- 1997-02-22 ES ES00116745T patent/ES2213526T3/es not_active Expired - Lifetime
- 1997-02-22 DK DK00116745T patent/DK1069106T3/da active
- 1997-02-22 DK DK99119109T patent/DK0983995T3/da active
- 1997-02-22 SI SI9730618T patent/SI1069106T1/xx unknown
- 1997-02-22 PT PT99119109T patent/PT983995E/pt unknown
- 1997-02-22 PT PT00116745T patent/PT1069106E/pt unknown
- 1997-02-22 DE DE59711477T patent/DE59711477D1/de not_active Expired - Lifetime
- 1997-02-22 AT AT97102923T patent/ATE223888T1/de active
- 1997-02-22 PT PT97102923T patent/PT799819E/pt unknown
- 1997-02-22 DK DK97102923T patent/DK0799819T3/da active
- 1997-02-22 SI SI9730653T patent/SI0983995T1/xx unknown
- 1997-02-22 ES ES99119109T patent/ES2218924T3/es not_active Expired - Lifetime
- 1997-02-22 DE DE59711267T patent/DE59711267D1/de not_active Expired - Lifetime
- 1997-02-22 ES ES97102923T patent/ES2183030T3/es not_active Expired - Lifetime
- 1997-02-22 EP EP99119109A patent/EP0983995B1/de not_active Expired - Lifetime
- 1997-02-22 DE DE59708160T patent/DE59708160D1/de not_active Expired - Lifetime
- 1997-02-22 EP EP99119108A patent/EP0983994A3/de not_active Withdrawn
- 1997-02-22 AT AT99119109T patent/ATE263140T1/de active
- 1997-02-22 SI SI9730428T patent/SI0799819T1/xx unknown
- 1997-02-22 EP EP00116745A patent/EP1069106B1/de not_active Expired - Lifetime
- 1997-02-22 EP EP97102923A patent/EP0799819B1/de not_active Expired - Lifetime
- 1997-03-07 BR BRPI9700369-7A patent/BR9700369B1/pt not_active IP Right Cessation
- 1997-03-07 PE PE1997000175A patent/PE55798A1/es not_active Application Discontinuation
- 1997-03-11 NZ NZ314384A patent/NZ314384A/xx unknown
- 1997-03-11 KR KR1019970008046A patent/KR100538662B1/ko not_active Expired - Fee Related
- 1997-03-11 CA CA002199679A patent/CA2199679C/en not_active Expired - Fee Related
- 1997-03-11 AR ARP970100969A patent/AR008991A1/es active IP Right Grant
- 1997-03-12 NO NO971137A patent/NO308294B1/no not_active IP Right Cessation
- 1997-03-12 RU RU97103580/04A patent/RU2167146C2/ru active
- 1997-03-12 CZ CZ1997759A patent/CZ293971B6/cs not_active IP Right Cessation
- 1997-03-12 US US08/820,377 patent/US5811582A/en not_active Expired - Lifetime
- 1997-03-12 HU HU9700574A patent/HU224819B1/hu not_active IP Right Cessation
- 1997-03-12 CN CNB971034877A patent/CN1157366C/zh not_active Expired - Fee Related
- 1997-03-12 UA UA97031138A patent/UA55373C2/uk unknown
- 1997-03-12 CO CO97013358A patent/CO4520279A1/es unknown
- 1997-03-12 AU AU16251/97A patent/AU725430B2/en not_active Ceased
- 1997-03-12 JP JP05769597A patent/JP4205182B2/ja not_active Expired - Fee Related
- 1997-03-12 ZA ZA9702147A patent/ZA972147B/xx unknown
- 1997-03-12 IL IL12043097A patent/IL120430A/xx not_active IP Right Cessation
- 1997-03-12 SK SK321-97A patent/SK284328B6/sk not_active IP Right Cessation
- 1997-03-12 PL PL97318922A patent/PL186050B1/pl not_active IP Right Cessation
-
2005
- 2005-06-03 KR KR1020050047916A patent/KR100602810B1/ko not_active Expired - Fee Related
-
2008
- 2008-03-17 JP JP2008066934A patent/JP4846750B2/ja not_active Expired - Fee Related
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0983995B1 (de) | Dimethyl-(3-aryl-but-3-enyl)-aminverbindungen als pharmazeutische Wirkstoffe | |
| EP0753506B1 (de) | 6-Dimethylaminomethyl-1-phenyl-cyclo-hexanverbindungen als pharmazeutische Wirkstoffe | |
| EP0693475B1 (de) | 1-Phenyl-3-dimethylamino-propanverbindungen mit pharmakologischer Wirkung | |
| EP0780369B1 (de) | 1-Phenyl-2-dimethylaminomethyl-cyclohexan-1-olverbindungen als pharmazeutische Wirkstoffe | |
| EP0786450B1 (de) | Verfahren zur Herstellung der Enantiomeren von O-Demethyltramadol | |
| EP1202953B1 (de) | Substituierte 2-dialkylaminoalkylbiphenyl-derivate | |
| EP1246793B1 (de) | Substituierte aminomethyl-phenyl-cyclohexanderivate | |
| KR100748378B1 (ko) | 아미노메틸-페닐-사이클로헥사논 유도체 | |
| EP1043306B1 (de) | 3-Amino-3-arylpropan-1-ol-Derivate, deren Herstellung und Verwendung | |
| DE10132747A1 (de) | Substituierte 1-Aryl-but-3-enylamin- und 1-Aryl-but-2-enylaminverbindungen | |
| HK1026197B (en) | Pharmaceutically-active dimethyl-(3-aryl-but-3-enyl)-amine compounds |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| 17P | Request for examination filed |
Effective date: 19991004 |
|
| AC | Divisional application: reference to earlier application |
Ref document number: 799819 Country of ref document: EP |
|
| AK | Designated contracting states |
Kind code of ref document: A2 Designated state(s): AT BE CH DE DK ES FI FR GB GR IE IT LI LU MC NL PT SE |
|
| AX | Request for extension of the european patent |
Free format text: AL;LT PAYMENT 19991004;LV PAYMENT 19991004;RO;SI PAYMENT 19991004 |
|
| PUAL | Search report despatched |
Free format text: ORIGINAL CODE: 0009013 |
|
| AK | Designated contracting states |
Kind code of ref document: A3 Designated state(s): AT BE CH DE DK ES FI FR GB GR IE IT LI LU MC NL PT SE |
|
| AX | Request for extension of the european patent |
Free format text: AL;LT PAYMENT 19991004;LV PAYMENT 19991004;RO;SI PAYMENT 19991004 |
|
| RIC1 | Information provided on ipc code assigned before grant |
Free format text: 7C 07C 217/62 A, 7C 07C 215/54 B, 7C 07C 219/28 B, 7C 07C 211/28 B, 7C 07C 211/29 B, 7C 07C 215/64 B, 7C 07D 333/58 B, 7A 61K 31/135 B, 7A 61K 31/235 B, 7A 61K 31/38 B |
|
| AKX | Designation fees paid |
Free format text: AT BE CH DE DK ES FI FR GB GR IE IT LI LU MC NL PT SE |
|
| AXX | Extension fees paid |
Free format text: LT PAYMENT 19991004;LV PAYMENT 19991004;SI PAYMENT 19991004 |
|
| 17Q | First examination report despatched |
Effective date: 20010905 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: THE APPLICATION IS DEEMED TO BE WITHDRAWN |
|
| 18D | Application deemed to be withdrawn |
Effective date: 20020316 |
|
| REG | Reference to a national code |
Ref country code: HK Ref legal event code: WD Ref document number: 1026196 Country of ref document: HK |