DK152256B - Fremgangsmaade til fremstilling af en stabil bloderstatning - Google Patents
Fremgangsmaade til fremstilling af en stabil bloderstatning Download PDFInfo
- Publication number
- DK152256B DK152256B DK307276AA DK307276A DK152256B DK 152256 B DK152256 B DK 152256B DK 307276A A DK307276A A DK 307276AA DK 307276 A DK307276 A DK 307276A DK 152256 B DK152256 B DK 152256B
- Authority
- DK
- Denmark
- Prior art keywords
- emulsion
- plasma
- blood
- tests
- particle size
- Prior art date
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
- A61K9/0026—Blood substitute; Oxygen transporting formulations; Plasma extender
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/08—Plasma substitutes; Perfusion solutions; Dialytics or haemodialytics; Drugs for electrolytic or acid-base disorders, e.g. hypovolemic shock
Landscapes
- Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Hematology (AREA)
- Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Dermatology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Diabetes (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Epidemiology (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Description
Opfindelsen angår en fremgangsmåde til fremstilling af en stabil bloderstatning, ved hvilken man homogent blander fysiologisk acceptabelt vand, oxygen-overførende perfluorcarbonforbin-delser og emulgatorer til opnåelse af en grov emulsion, hvorefter denne emulgeres ved, at den injiceres ved en temperatur på op til 55 °C igennem en spalte under et tryk på fra omkring 10 til omkring 50 MPa og derved underkastes forskydningskræfter og blandingsvirkning baseret på en stærk hastighedsgradient, indtil perfluorcarbonforbindelsernes partikelstørrelse i den resulterende emulsion når 0,05 - 0,3 ^um.
Det er allerede blevet rapporteret af et antal forskere, at fluor-carbonforbindelse-emulsioner eventuelt kan anvendes som kunstig bloderstatning til pattedyr og som perfusionsvæske til konservering af indre organer, som skal transplanteres, især som en infusionsvæskeerstatning, der er i stand til at transportere oxygen [Leland C. Clark, Jr., F. Becattini, and S. Kaplan: The physiology of syn-thetic biood, Journal of Thoracic Cardiovascular Surgery, 60, 757-773 (1970); R. P. Geyer: Fluorocarbon-polyol artificial biood substitutes, New England Journal of Medicine, 289» 1077-1082 (1973)J ·
Disse emulsioner, kan imidlertid ikke antages at være tilfredsstillende nok til praktisk brug med hensyn til deres farmaceutiske stabilitet og sikkerhed for den levende organisme. For at fluor-carbonforbindelse-emulsioner skal være kvalificeret til praktisk brug som kimstig bloderstatning, er det nødvendigt at udvikle et præparat, som er tilstrækkeligt stabilt til at kunne opbevares i lang tid uden ændring i partikelstørrelse.
I fluorcarbonforbindelse-emulsioner spiller partikelstørrelsen en vigtig rolle for emulsionens toxic.it et og effektivitet [k. Yokoyama, K. Yamanouchi, M. Watanabe, R. Murashima, T. Matsumoto, T. Hamano, H. Ikamoto, T. Suyama, R. Watanabe, and R. Naito: Preparation of perfluorodecalin emulsion, an approach to the red cells substitute, Federation Proceedings, 34, 1478-1483 (May, 1975)]· En emulsion med større partikelstørrelse er mere toxisk og har kortere opholdstid af partiklerne i blodstrømmen. Når fluorcarbonforbindelse-emulsionen er beregnet til brug som kunstig bloderstatning til opretholdelse af livet hos en patient, der lider af massiv blødning, må dens gennemsnitlige partikelstørrelse derfor være 0,3 ^um eller mindre, fortrinsvis 0,2 ^,um eller derunder Cjapansk patentskrift nr. 849 412].
Foruden partikelstørrelsen er det nødvendigt, for at fluorcarbon-forbindelse-emulsionen er anvendelig som kunstig bloderstatning, at den intravenøst indgivne fluorcarbonforbindelse efter at være elimineret fra blodstrømmen udskilles fra kroppen så hurtigt som muligt. Yed tidligere undersøgelser af udskillelseshastigheden og toxiciteten af flere slags fluorcarbonforbindelse-emulsioner er det fundet, at perfluorcarbonforbindelser med 9-11 carbonato-mer er anvendelige som materiale i kunstig bloderstatning, idet den bedste forbindelse er perfluordecalin £k.Yokoyama, K. Yamanouchi, and R. Murashima: Excretion of perfluorochemicals after intravenous injection of their emulsion, Chemical Pharmaceutical Bulletin, 23, 1368-1373 (Juni 1975)].
Desuden er det fundet, at der kan fremstilles fine og stabile fluor-carbonforbindelse-emulsioner ud fra disse udvalgte fluorcarbonfor-bindelser med 9-11 carbonatomer ved emulgering af fluorcarbonfor-bindelserne med en blanding af æggeblomme-phospholipider eller soyabønne-phospholipider og en lille mængde fedtsyrer med 8-22 carbonatomer eller salte eller monoglycerider deraf {^japansk patentskrift nr. 954 944 og det tilsvarende DE offentliggørelsesskrift nr. 24 04 564] .
Sammenlignet med en perfluortributylamin-emulsion stabiliseret med en højmolekylær polyoxyethylen-polyoxypropylen-copolymer (R.P.
Geyer, loc.cit.), er den ovennævnte emulsion stabiliseret med både phospholipider og fedtsyrer bedre med hensyn til udskillelseshastighed, men dårligere med hensyn til stabilitet i den cirkulerende blodstrøm efter intravenøs injektion, idet halveringstiden er omkring 2/3 af den førstnævntes.
Endvidere kan en fluorcarbonforbindelse-emulsion, fremstillet med et højmolekylært ikke-ionisk overfladeaktivt middel, såsom perfluortributylamin-emulsion, anvendes som en blanding i ethvert forhold med de kommercielle plasmaforstrækningsmidler, såsom dextran- eller hydroxyethylstivelse- eller modificeret gelatineopløsning, medens den i JP 954 944 og DE 24 04 564 beskrevne perfluordecalin-emulsion ikke kan anvendes i kombination med de nævnte plasmaforstrækningsmidler på grund af dannelse af bundfald, når den blandes med de sidstnævnte. Det ser ud til, at udfældningen skyldes nedbrydningen af emulgerede partikler forårsaget af gensidig indvirkning mellem phospholipiderne, der indeholdes i høj koncentration i emulsionen, og plasmaforstrækningsmidlet, såsom dextran eller hydroxyethyl-stivelse, der er et højmolekylært kolloidt stof.
Når en fluorcarbonforbindelse-emulsion skal anvendes som infusionvæske eller som kunstig bloderstatning til at redde en patients liv i tilfælde af massiv blødning, bliver kombinationen med et plasmaforstrækningsmiddel vigtig for at frembringe isotonicitet, d.v.s. at udligne de onkotiske tryk af de to kolloidale opløsnin ger, nemlig emulsionen og blodet. Fluorcarbonforbindelse-emulsio-nen leverer oxygen, medens plasmaforstrækningsmidlet gør det muligt at holde det cirkulerende blodvolumen på et passende niveau. Derfor foretrækkes det at anvende et højmolekylært ikke-ionisk overfladeaktivt middel, som er inaktivt over for plasmaforstræknings-midlet, til fremstilling af en fluorcarbonforbindelse-emulsion til anvendelse som kunstigt blod. Selv om disse højmolekylære ikke-iohiske overfladeaktive midler er effektive som emulgeringsmiddel for nogle fluorcarbonforbindelser, såsom perfluortributylamin og andre fluorcarbonforbindelser af amintype, er de ikke egnede for fluorcarbonforbindelser med 9-11 carbonatomer, såsom perfluordeca-lin, som har en.høj udskillelseshastighed.
Under disse omstændigheder har opfinderne gennemført omfattende undersøgelser for'at finde en fremgangsmåde til emulgering af perfluordecalin uden at anvende et phospholipid som hovedemulgeringsmiddel og har som resultat fundet, at når perfluordecalin emulgeres som en blanding med perfluortripropylamin, kan den ønskede emulsion fremstilles ved anvendelse af et ikke-ionisk overfladeaktivt middel som hovedemulgeringsmiddel. Endvidere blev det ved anvendelse af et ikke-ionisk overfladeaktivt middel muligt at tilsætte et plasmaforstrækningsmiddel, som gør emulsionens onkotiske tryk isotonisk. Som resultat heraf nedsættes den hæmo-lytiske virkning, som ellers frembringes af en emulsion, således at dyrets overlevelse bliver mulig, når emulsionen anvendes som kunstig bloderstatning. Det er således udvælgelsen af bestemte perfluorcarbonforbindelser og ikke-ionisk overfladeaktivt middel i forbindelse med et plasmaforstrækningsmiddel, som har gjort . det muligt at fremstille en udmærket fluorcarbonemulsion, der er stabil i den cirkulerende blodstrøm og har lav toxicitet i den levende krop og ønskede egenskaber, så den for første gang i verden har kunnet anvendes som kunstig bloderstatning inden for det kliniske område.
Det ejendommelige ved fremgangsmåden ifølge opfindelsen ligger således i udvælgelsen af de optimale komponenter og anvendelsen af disse i det optimale forhold, hvorved der opnås et overraskende fordelagtigt resultat.
I overensstemmelse hermed er fremgangsmåden ifølge opfindelsen ejendommelig ved det i kravets kendetegnende del anførte.
Symbolet "% (vægt/vol.)n betyder mængdeforholdet af et materiale beregnet som vægt (gram) per 100 ml af den resulterende emulsion.
I resten af beskrivelsen betegnes dette mængdeforhold blot som
De polyoxyethylen-polyoxypropylen-copolymere, der anvendes som emulgeringsmiddel, har en molekylvægt på 2000-20000. Koncentrationen af dette højmolekylære ikke-ioniske overfladeaktive middel i emulsionen er fra omkring 2,0 til omkring 5,0 %, fortrinsvis 3,0 -3,5 %.
De phospholipider, der anvendes som emulgeringsmiddel i emulsionen, er sådanne der almindeligt anvendes inden for teknikken, og de, der omfatter æggeblomme-phospholipid eller soyabønne-phos-pholipid, foretrækkes. Den tilstedeværende mængde i emulsionen kan varierer fra omkring 0,1 til 1,0 %, og fortrinsvis omkring 0,4 til omkring 0,6 %.
Den fedtsyreforbindelse, der anvendes som emulgeringsmiddel, er en fedtsyre med 8-22 carbonatomer, et fysiologisk acceptabelt salt deraf, såsom natrium- eller kaliumsaltet, eller et monogly-cerid deraf. Sådanne fedtsyreforbindelser inkluderer f.eks. capryl-syre, caprinsyre, laurinsyre, myristinsyre, palmitinsyre, stearinsyre, behensyre, palmitolsyre, oliesyre, linolsyre og arachidon-syre samt natrium- og kaliumsaltet deraf og monoglycerider deraf. Disse fedtsyreforbindelser kan anvendes alene eller som en blanding af to eller flere slags deraf i så lille en mængde som 0,004-0,1 %, og fortrinsvis fra omkring 0,02 til omkring omkring 0,04 %. Blandt disse fedtsyreforbindelser foretrækkes sådanne med 14-20 carbonatomer og deres fysiologisk acceptable salte, og de mest foretrukne er kaliumpalmitat og kaliumoleat i betragtning af deres gode opløselighed og den lette fremstilling af emulsionen dermed.
Fremgangsmåden ifølge opfindelsen gennemføres ved homogent at blande foreskrevne mængder af de førnævnte komponenter i en hvilken som helst rækkefølge i et fysiologisk acceptabelt vandigt medium, såsom destilleret vand, eller en isotonisk opløsning, til opnåelse af en rå emulsion og derpå emulgere den rå emulsion ved at injicere den ved en temperatur på op til 55 °C igennem en spalte under et tryk på fra omkring 10 til omkring 50 MPa, hvorved den underkastes forskydningskræfter og blandingsvirkning baseret på en stærk hastighedsgradient, indtil den førnævnte ønskede partikelstørrelse er opnået.
Den homogene sammenblanding af materialerne udføres ved anvendelse af en konventionel blander, såsom en homoblander eller propel-omrører.
Emulgeringen af den rå emulsion opnås ved hjælp af en højtryksho-mogenisator, som er en højtrykspumpe, der homogeniserer en blanding af to ublandbare væsker ved at injicere den igennem en spalte under et højt tryk med en meget høj hastighed til frembringelse af en forskydning og sammenblanding af væskerne. Den typiske homogenisator på markedet er af Manton-Gaulin-typen (handelsnavn for en homogenisator forhandlet af Manton-Gaulin Manufacturing Co., Inc., U.S.A.), som har en flertrinsventil i kombination af to eller flere ventiler, der hver indeholder en fjeder, hvoraf spalterne dannes.
Blandingen cirkuleres i denne type homogenisator flere gange under et totaltryk på omkring 50 MPa, hvorved der opnås en stabil emulsion. Arbejdstemperaturen holdes i området op til 55 °C, og fortrinsvis ved 25-40 °C.
Den ved fremgangsmåden ifølge opfindelsen fremstillede emulsion har en dispers fase af ultrafine partikler, hvis diameter er mindre end 0,2 ^um eller i hvert fald mindre end 0,3 yum. Endvidere er den stabil, idet den ikke viser nogen vækst i partikelstørrelse, selv når den opvarmes eller opbevares i lang tid. Derfor sikrer emulsionen i høj grad det dyr, hvortil den indgives imod skadelig virkning på grund af agglomerering af emulsionspartiklerne.
Emulsionen har endvidere en lang tilbageholdelsestid i den cirkulerende blodstrøm, således at den oxygenbærende evne opretholdes i lang tid.
F.eks. forbliver den ifølge opfindelsen fremstillede emulsion meget længere i dyrets blodstrøm end en fluorcarbonforbindelse-emulsion fremstillet ved anvendelse af phospholipider som emulgeringsmiddel ifølge JP 954 944 og DE 24 04 564. Udskillelsen af den ifølge opfindelsen fremstillede emulsion fra kroppen er meget hurtigere end af en perfluortributylamin-emulsion.
Den foreliggende emulsion kan anvendes som infusionsvæske, da den er gjort fysiologisk isotonisk med kommercielle plasmaforstrækningsmidler, såsom dextran og hydroxyethylstivelse. Endvidere kan den anvendes som bloderstatning for pattedyr og som per-fusat til konservering af indre organer.
Opfindelsen belyses nærmere ved de følgende eksempler, i hvilke partikelstørrelsen blev målt ved centrifugalsedimenteringsmetoden, som er foreslået af K. Yokoyama, A. Suzuki, I. Utsumi and R. Naito. Chem. Pharm. Buil. 22 (12), 2966-2971 (1974).
EKSEMPEL 1 181 destilleret vand opløstes 300 g af en polyoxyethylen-polyoxy-propylen-copolymer (molekylvægt 10800). Til opløsningen sattes 40 g soyabørme-phospholipider, 2 g kaliumo.leat og en blanding bestående af 3 kg perfluordecalin og 300 g perfluortripropylamin.
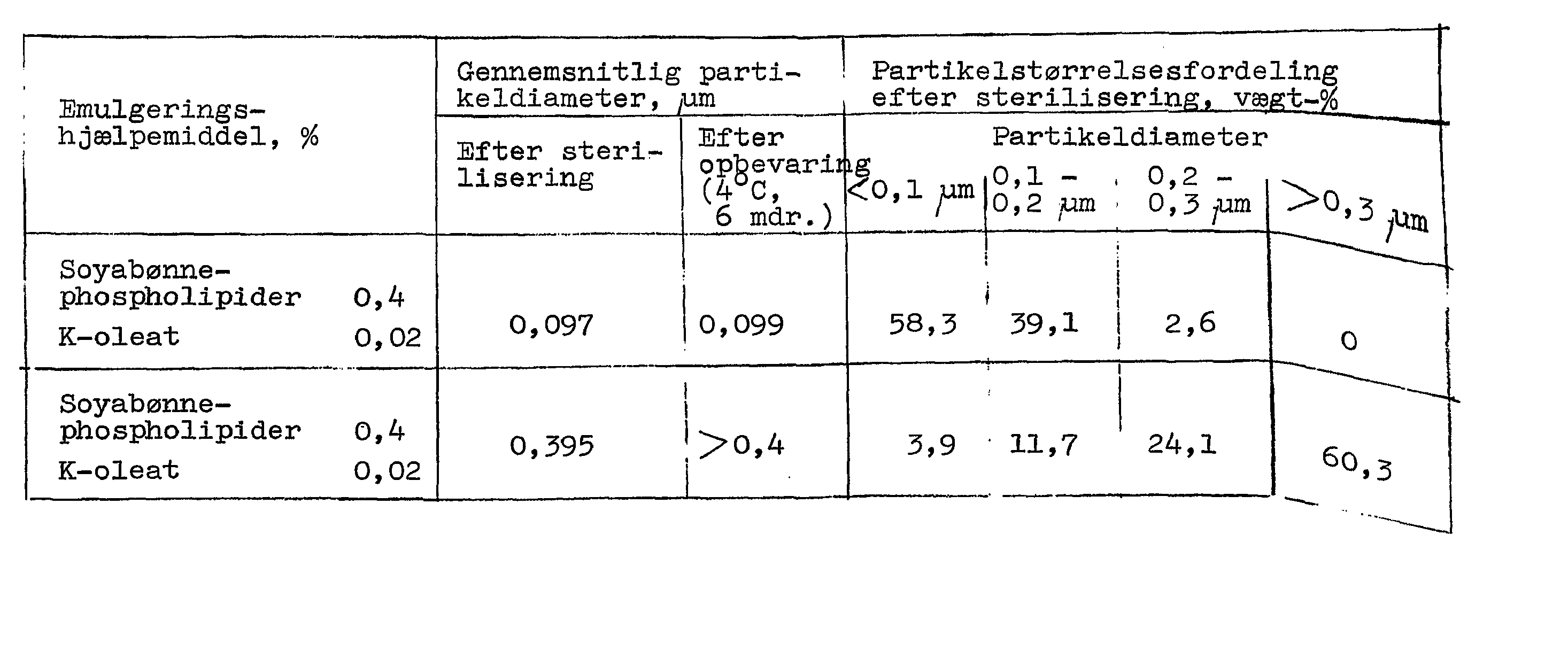
Den resulterende blanding blev omrørt i en blander til dannelse af en grov emulsion. Den resulterende grove emulsion blev fyldt i væsketanken på en jetemulgator (fremstillet af Manton-Gaulin Co.) og emulgeret ved passage 12 gange gange igennem en ventil ved et højt tryk på 20-49 MPa, medens væsketemperaturen holdtes ved 35-5 °C, til frembringelse af emulgering. Den resulterende emulsion indeholdt 30,5 % perfluordecalin og 2,9 % perfluortripropylamin. Den gennemsnitlige partikeldiameter var 0,09 - 0,1 ^um, målt ved centrifugalsedimenteringsmetoden. Emulsionen viste i det væsentlige ingen vækst i partikelstørrelse, når den blev indesluttet i en ampul til injektion og underkastet termisk sterilisering ved 115 °C i 12 minutter i den specielt udformede rotationssterili-sator. I tabel 1 er anført partikelstørrelsesfordelingen af denne emulsion og af en emulsion af perfluordecalin alene, fremstillet uden anvendelse af perfluortripropylamin.
Som det ses af tabel 1, viste den foreliggende emulsion, når den blev opbevaret ved 4 °C i 6 måneder ingen agglomerering, idet mid-delpartikeldiameteren var i det væsentlige uændret.
Tabel 1. Partikelstørrelsesfordeling af forskellige emulsioner
(Tabellen fortsætter herfra på næste side.
* = polyoxyethylen-polyoxypropylen-copolymer, gennemsnitsmolekylvægt 10 800.
Tabel 1 (fortsat)
(fortsat fra side 9 )
Til fremstilling af en bloderstatning ved fremgangsmåden ifølge opfindelsen tilsættes emulsionen et plasmaforstrækningsmiddel til at udfylde manglen på onkotisk tryk. Når denne emulsion blev blandet med et plasmaforstrækningsmiddel, blev den reversible udfældning, som kan forårsages af gensidig indvirkning mellem kolloidale opløsninger, ikke iagttaget, hvilket viser, at en af de vanskeligheder, som kunne forventes ved anvendelse af den ifølge opfindelsen fremstillede bloderstatning som infusionsvæske, er elimineret.
Perfluordecalin/perfluortripropylamin-(10:1)-emulsioner af forskellige koncentrationer fremstillet på samme måde som ovenfor og som reference perfluordecalinemulsioner af forskellige koncentrationer fremstillet ifølge DE offentliggørelsesskrift nr. 24 04 564 [æggeblomme-phospholipid 4%; kaliumoleat 0,02%1 blev hver for sig gjort isotoniske med lactatholdig Ringer's opløsning eller Krebs-Ringer-hydrogencarbonat-opløsning, og derpå blandet med en plasmaerstatning, således at den endelige koncentration af plasmaforstrækningsmidlet blev 1-6%, hvorpå dannelsen af bundfald blev iagttaget visuelt i løbet af 6 timer efter blanding ved stuetemperatur. De anvendte plasmaerstatninger er hydroxyethylstivelse (gennemsnitlig molekylvægt 200 000, 20% i fysiologisk saltopløsning; leveret af Ajinomoto Co., Ltd.) og "Dextran 40" Cgennemsnitlig molekylvægt 40 000, 10% i fysiologisk saltopløsning; leveret af The Green Cross Corp.J.
Ved "plasmaerstatning" forstås en opløsning af de højmolekylære forbindelser, "plasmaforstrækningsmidlerne", i et fysiologisk acceptabelt vandigt medium i en sådan koncentration, at de kan anvendes til erstatning af plasma.
Resultaterne er anført i tabel 2 og 3.
Tabel 2
Tabel 3
Note: intet bundfald +: dannelse af bundfald
Af de ovenstående resultater fremgår det, at bloderstatningen fremstillet ved fremgangsmåden ifølge opfindelsen påvirkes meget mindre af tilstedeværelsen af et plasmaforstrækningsmiddel end emulsionen ifølge DE offentliggørelsesskrift nr. 24 04 564, hvilket viser, at emulsionen, der anvendes ved fremgangsmåden ifølge opfindelsen kan blandes med "Dextran 40"- og hydroxyethylstivel-seplasmaerstatning i ethvert forhold til at give en bloderstatning med den fysiologisk kolloidale isotonicitet, som opnås ved tilsætning af "Dextran 40" og hydroxyethylstivelse i en endelig koncentration op til henholdsvis 2% og 4%.
Sammen!iqningsforsøq
Bloderstatningsemulsionerne blev fremstillet ved proceduren fra eksempel 1 og deres bestanddele var som anført i den efterfølgende tabel 4.
Som udgangsmaterialer anvendtes følgende forbindelser:
Komponent (A): Perfluordecalin Komponent (B): Perfluortripropylamin
Emulgeringsmiddel: Polyoxyethylen-polyoxypropylencopolymer ("PLURONIC F-68") i prøverne fremstillet ifølge opfindelsen; phospholipid (æggeblomme) i sammenligningsprøverne .
Emulgeringshjælpemiddel: Phospholipid (æggeblomme) og fedtsyre i prøverne fremstillet ifølge opfindelsen; fedtsyre i sammenligningsprøverne.
Fysiologisk acceptabel bærer: Vandig opløsning indeholdende glycerol (0,8 vægt/vol.%), NaCl (0,6 vægt/vol.%), KCl (0,034 vægt/vol.%), MgCl2 (0,02 vægt-vol.%), CaCl2 (0,028 vægt/vol.%), NaHCO^ (0,21 vægt/vol.%) og glucose (0,18 vægt/vol.%).
Plasmaforstrækningsmiddel: Hydroxyethylstivelse.
Sammenligningsforsøgene blev udført med hensyn til følgende emner: 1) Emulsionens partikelstørrelse:
Emulsionens gennemsnitlige partikelstørrelse blev bestemt efter sterilisering og efter 6 måneders opbevaring ved 4 °C ifølge centrifugalsedimenteringsmetoden, som er beskrevet af K. Yokoyama et al. tchem. Pharm. Buil., 22 (12), 2966-2971 (1974)'].
2) Virkning af plasmaforstrækningsmidlet:
Hydroxyethylstivelse anvendtes som plasmaforstrækningsmiddel i en mængde på 3 vægt/vol.-%, og forekomsten af bundfald blev iagttaget visuelt efter 6 timers opbevaring ved stuetempratur.
Hvis der dannes et reversibelt bundfald ved gensidig indvirkning af fluorcarbon(FC)-emulsionen og plasmaforstrækningsmidlet, kan emulsionen ikke anvendes som bloderstatning.
3) Udskiftningstransfusion på rotter:
Der gennemførtes sammenligningsforsøg med udskiftningstransfusion under anvendelse af rotter (Wistar-stamme, hanner, vægt 200 -250 g) ved gentagen blødning fra carotidarterien og erstatningstransfusion igennem halevenen skiftevis op til en hæmatokritværdi på 4,0 under 100 % oxygenatmosfære. Derpå bestemtes overlevelsestiden af de udskiftningstransfuserede rotter.
4) Hæmolytiske virkninger:
Forsøg med FC-emulsionens hæmolytiske virkning i det ekstrakorpo-rale kredsløbssystem blev udført in vivo ved anvendelse af røde blodceller fra kaniner.
FC-emulsionen blev blandet med en lactatholdig Ringer"s opløsning, således at den blev i hovedsagen fysiologisk isotonisk, og det resulterende isotoniske emulsionspræparat blev blandet med hepari-niseret kaninblod i et forhold på 1:1 til fremstilling af en prøveopløsning til prøvningen. 8 ml af prøveopløsningen holdtes ved 37 °C i 6 timer, og derpå bestemtes indholdet af frit hæmo- globin ved cyanmethæmoglobinmetoden (Kampen, E.J. and Ziilstram, W.J., Clin. Chim. Acta. 6, 538, 1961). I tilfælde, hvor en lac-tatholdig Ringer's opløsning anvendtes alene som kontrol uden anvendelse af FC-emulsion var det frie hæmoglobinindhold 128 mg.
5) Udåndingshastighed af FC-emulsion in vivo.
Udåndingshastigheden af FC-emulsionen in vivo blev bestemt ved den metode, som er beskrevet i Chemical Pharmacological Buil.
26, (3) 956-966, 1978, (K. Yokoyama, "Fate of perfluorochemicals in aminals after intraveneous injection or hemodilution with their emulsions").
FC-emulsionen blev indgivet intravenøst til rotten med en hastighed på 4 g/kg legemsvægt, og udåndningshastigheden blev vist ved antallet af dage, indtil halvdelen af det indgivne FC var forbrugt ved udånding.
De opnåede resultater er anført i tabel 4.
_________Tabel 4_.______
NOTE: (A) : Perfluordecalin (B) : Perfluortripropylamin F : "PLURONIC F68" L : Phospholipid FA : Fedtsyre HES : Hydroxyethylstivelse
Af de viste resultater kan udledes følgende.
I tilfælde af prøve nr. 1 er den resulterende FC-emulsion utilstrækkelig m.h.t. emulgering og har lav stabilitet, således at der ikke kunne opnås en emulsion med en gennemsnitlig partikelstørrelse på under 0,2 yum. Således er den resulterende emulsion helt uegnet som lægemiddel.
I tilfælde af prøve nr. 2 var den resulterende emulsion udmærket m.h.t. emulgering og stabilitet, men den dannede bundfald ved blanding med hydroxyethylstivelse, og desuden udviste den en bemærkelsesværdig hæmolytisk virkning, og rotter kunne ikke overleve behandlingen ved udskiftningstransfusion. Således kan denne emulsion heller ikke anvendes som lægemiddel.
I tilfælde af prøve nr. 3 har den resulterende emulsion lav stabilitet, men den kan indgives in vivo som lægemiddel, lige efter at den er fremstillet.
Prøve nr. 4 viste det samme resultat som nr. 2.
Prøverne nr. 5, 7 og 9 viste meget udmærkede egenskaber. Derfor kan de anvendes som bloderstatning.
Prøverne nr. 6, 8, 10, 12 og 14 viste de samme resultater som nr. 2.
Prøve nr. 11 har lav udåndingshastighed af FC i en levende krop sammenlignet med prøverne nr. 5, 7 og 9, men vil kunne anvendes som lægemiddel under en tilstrækkelig kontrol.
Prøve nr. 13 har meget lav udåndingshastighed, således at den kan forårsage uforudsigelige ulemper i den levende krop. I dette tilfælde døde rotter efter 69 timer, når de blev underkastet udskiftningstransfusion.
Som det kan ses af disse sammenligningsforsøg viser bloderstat- ningen fremstillet ved fremgangsmåden ifølge opfindelsen (prøverne nr. 3, 5, 7, 9 og 11) væsentlig virkning med hensyn til partiklernes stabilitet, den samtidige anvendelse af plasmaforstrækningsmiddel, udskiftningstransfusion og sikkerhed i kredsløbssystemer uden for legemet sammenlignet med FC-emulsionerne ifølge de tidligere nævnte patentskrifter (prøve nr. 1 er sammensat ifølge DE fremlæggelsesskrift nr. 21 44 094, og prøverne nr. 2, 4, 6, 8, 10, 12 og 14 er sammensat ifølge DE offentliggørelsesskrift nr.
24 04 564). Den ovennævnte forskel i virkning mellem den ifølge opfindelsen fremstillede bloderstatning og de kendte FC-emulsioner skyldes forskellen i FC-emulsionernes bestanddele, som medførte et så væsentligt fremskridt som, at FC-emulsionens toxicitet næsten forsvandt, og det for første gang var muligt at anvende en sådan FC-emulsion til klinisk behandling.
Klinisk afprøvning På basis af de tidligere rapporterede prøvningsresultater og omfattende yderligere undersøgelser med hensyn til toxicitet, farmakologi, farmakodynamik og effektivitet hos dyr er den ifølge opfindelsen fremstillede bloderstatning, som er kendt under navnet "Fluosol-DA", blevet påvist at være sikker og effektiv som kunstig bloderstatning. Undersøgelserne er nu nået ind i det kliniske stadium.
Sammensætningen i vægt/vol.?i af "Fluosol-DA (20 %)" er som følger:
Perfluordecalin 14,0
Per fluortripropylamin 6,0 "Pluronic F-68" 2,7 Æggeblommephospholipider 0,4
Kaliumoleat 0,04
Glycerol 0,8
NaCl 0,600 KC1 0,034
MgCl2 0,020
CaCl2 0,028
NaHC03 0,210
Glucose 0,180
Hydroxyethylstivelse 3,0 1 marts 1979 er fase I undersøgelsen af "Fluosol-DA" hos mennesker blevet gennemført i Japan af professor Mitsuno og Dr. Ohyanagi ved Kobe University Medical School. 10 normale voksne mandlige frivillige, herunder 7 læger, blev infuseret med fra 20 til 500 ml "Fluosol-DA", idet de tre individer, som modtog 500 ml, forinden blev tappet for 200 ml blod.
Blodprøver blev taget før infusionen og 3, 24 og 48 timer og 1, 2 og 4 uger efter infusionen. De individer, som modtog enten 200 ml eller 500 ml, fik yderligere taget prøver 8 og 14 uger efter infusionen. På prøverne undersøgtes følgende parametre: Hæmatologi
Fuldstændig blodtælling Reticulocyttælling B1odp1adetæl1ing Tælling og differentialtælling af hvide blodceller Serumprotein-elektrophorese
Kemi
Thymolturbiditetsprøvning Amylase
Bilirubin, total og direkte Lactatdehydrogenase (LDH)
Cobaltreaktion Cholinesterase
Serum-glutamatoxaloacetattransami- nase (SGOT) Blod-urin-nitrogen (BUN)
Serum-glutamatpyruvattransaminase (SGPT) Total cholesterol
Alkalisk phosphatase Creatinin
Total protein
Desuden udførtes et thromboelastogram, og komplementaktiviteten blev bestemt på blodprøverne taget 3 og 24 timer efter infusionen.
Der blev ikke iagttaget nogen ændringer i blodtryk, pulshastighed, åndedrætshastighed, legemstemperatur eller ECE. Ingen andre symptomer blev iagttaget. Ingen skadelige reaktioner eller klager blev rapporteret af nogen af de 10 individer. Under hele undersø-
Claims (1)
- gelsen var prøverne for alle individer inden for de normale områder for de ovennævnte prøvninger. Det viser, at "Fluosol-DA" er sikker og kan anvendes på patienter. Patentkrav : Fremgangsmåde til fremstilling af en stabil bloderstatning, ved hvilken man homogent blander fysiologisk acceptabelt vand, oxygen-overførende perfluorcarbonforbindelser og emulgatorer til opnåelse af en grov emulsion, hvorefter denne emulgeres ved, at den injiceres ved en temperatur på op til 55 °C igennem en spalte under et tryk på fra omkring 10 til omkring 50 MPa og derved underkastes forskydningskræfter og blandingsvirkning baseret på en stærk hastighedsgradient, indtil perfluorcarbonforbindelsernes partikelstørrelse i den resulterende emulsion når 0,05 - 0,3 ^um, kendetegnet ved, at man som perfluorcarbonforbindelser anvender 10 - 50 % (vægt/vol.) af (A) perfluordecalin og (B) per-fluortripropylamin, hvor vægtforholdet A:B er mellem 95:5 og 50:50, og som emulgatorer anvender 2,0 - 5,0 % (vægt/vol.) af en polyoxy-ethylen/polyoxypropylen-copolymer med en molekylvægt på 2000 -20 000, 0,1 - 1,0 % (vægt/vol.) af et phospholipid og 0,004 -0,1 % (vægt/vol.) af mindst én fedtsyreforbindelse udvalgt blandt fedtsyrer med 8-22 carbonatomer og fysiologisk acceptable salte og monoglycerider deraf, og at man efter fremstillingen af den fine emulsion blander den med en mængde plasmaerstatning, der tilfører 1 - 2 % (vægt/vol.) Dextran 40 eller 1 - 4 % (vægt/vol.) hydroxyethylstivelse som plasmaforstrækningsmiddel.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US65496476A | 1976-02-03 | 1976-02-03 | |
| US65496476 | 1976-02-03 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| DK307276A DK307276A (da) | 1977-08-04 |
| DK152256B true DK152256B (da) | 1988-02-15 |
| DK152256C DK152256C (da) | 1988-08-29 |
Family
ID=24626936
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| DK307276A DK152256C (da) | 1976-02-03 | 1976-07-07 | Fremgangsmaade til fremstilling af en stabil bloderstatning |
Country Status (22)
| Country | Link |
|---|---|
| JP (1) | JPS5835485B2 (da) |
| AR (1) | AR218864A1 (da) |
| AT (1) | AT355214B (da) |
| BE (1) | BE850992A (da) |
| CA (1) | CA1072446A (da) |
| CH (1) | CH633674A5 (da) |
| DD (1) | DD132231A5 (da) |
| DE (1) | DE2630586C2 (da) |
| DK (1) | DK152256C (da) |
| ES (1) | ES449635A1 (da) |
| FI (1) | FI58071C (da) |
| FR (1) | FR2361867A1 (da) |
| GB (1) | GB1549038A (da) |
| IL (1) | IL51325A (da) |
| LU (1) | LU76698A1 (da) |
| MX (1) | MX4136E (da) |
| NL (1) | NL171533C (da) |
| NO (1) | NO145370C (da) |
| NZ (1) | NZ183096A (da) |
| SE (1) | SE442706B (da) |
| SU (1) | SU797546A3 (da) |
| ZA (1) | ZA77229B (da) |
Families Citing this family (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4186253A (en) * | 1978-10-10 | 1980-01-29 | The Green Cross Corporation | Perfusate for preserving organ to be transplanted and preserving method |
| JPS55100312A (en) * | 1979-01-25 | 1980-07-31 | Toshiro Wada | Contrast medium for blood vessel |
| DE3277769D1 (en) * | 1981-09-08 | 1988-01-14 | Green Cross Corp | Perfluorochemicals, process for preparing the same and their use as blood substitutes |
| US4423077A (en) * | 1982-07-27 | 1983-12-27 | The University Of Pennsylvania | Perfluorochemical emulsion artificial blood |
| JPS5946218A (ja) * | 1982-09-09 | 1984-03-15 | Green Cross Corp:The | フルオロカ−ボン乳化製剤 |
| JPS59175421A (ja) * | 1983-03-24 | 1984-10-04 | Tetsuzou Agishi | 血液浄化剤 |
| AU2441592A (en) * | 1991-08-08 | 1993-03-02 | Leigh D. Segel | Fluorocarbon blood substitute |
| US5658962A (en) | 1994-05-20 | 1997-08-19 | Minnesota Mining And Manufacturing Company | Omega-hydrofluoroalkyl ethers, precursor carboxylic acids and derivatives thereof, and their preparation and application |
| US5502094A (en) * | 1994-05-20 | 1996-03-26 | Minnesota Mining And Manufacturing Company | Physiologically acceptable emulsions containing perfluorocarbon ether hydrides and methods for use |
| WO1997025978A1 (en) * | 1996-01-15 | 1997-07-24 | BELOYARTSEV, Arkady Felixovich | Method of obtaining perfluorocarbon emulsions for medical purposes |
| CN1068778C (zh) * | 1998-05-15 | 2001-07-25 | 赵超英 | 救治用的药物组合物及其制备方法 |
| US7357937B2 (en) | 2002-09-24 | 2008-04-15 | Therox, Inc. | Perfluorocarbon emulsions with non-fluorinated surfactants |
| RU2259819C1 (ru) | 2004-03-01 | 2005-09-10 | Кузнецова Ирина Николаевна | Эмульсия перфторорганических соединений медицинского назначения и способ её получения |
| EP2005948A2 (en) | 2006-03-14 | 2008-12-24 | Sergey Ivanovich Vorobyev | Perfluorocarbon gas transferring emulsion for medico-biological use, the composition and the production method thereof a medicinal agent |
| US8063020B2 (en) * | 2007-12-22 | 2011-11-22 | Simpkins Cuthbert O | Resuscitation fluid |
| GB2467353B (en) | 2009-01-30 | 2011-07-20 | Steven Skill | Apparatus for treatment of fluid streams and method of conducting the same |
| ES2541226B2 (es) * | 2014-01-15 | 2016-02-12 | MONDRAGÓN GOI ESKOLA POLITEKNIKOA J. Mª. ARIZMENDIARRIETA, S.C | Fantoma de sangre |
| RU2745290C2 (ru) * | 2019-04-12 | 2021-03-23 | Ирина Николаевна Кузнецова | Эмульсия перфторуглеродных соединений медико-биологического назначения и способ её получения |
| EP4580680A1 (de) * | 2022-08-31 | 2025-07-09 | Universität Duisburg-Essen | Lecithin-modifizierte nanoskalierte sauerstoffträger (lenox) |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2404564A1 (de) * | 1973-10-05 | 1975-04-17 | Green Cross Corp | Waessrige emulsion von gesaettigten aliphatischen perfluorkohlenstoffverbindungen, verfahren zu ihrer herstellung und ihre verwendung als blutersatzmittel und perfusionsfluessigkeit |
| DE2144094B2 (de) * | 1970-09-05 | 1980-02-14 | Tanabe Seiyaku Co. Ltd. | Verfahren zur Herstellung einer zum Sauerstofftransport befähigten, injizierbaren Fluorkohlenstoffteilchenemulsion |
-
1976
- 1976-07-01 JP JP51078127A patent/JPS5835485B2/ja not_active Expired
- 1976-07-02 GB GB27739/76A patent/GB1549038A/en not_active Expired
- 1976-07-06 SE SE7607727A patent/SE442706B/xx not_active IP Right Cessation
- 1976-07-07 NL NLAANVRAGE7607514,A patent/NL171533C/xx not_active IP Right Cessation
- 1976-07-07 DK DK307276A patent/DK152256C/da not_active IP Right Cessation
- 1976-07-07 AT AT496676A patent/AT355214B/de not_active IP Right Cessation
- 1976-07-07 ES ES449635A patent/ES449635A1/es not_active Expired
- 1976-07-07 CH CH869676A patent/CH633674A5/de not_active IP Right Cessation
- 1976-07-07 DE DE2630586A patent/DE2630586C2/de not_active Expired
- 1976-07-08 CA CA256,571A patent/CA1072446A/en not_active Expired
- 1976-07-08 FR FR7620907A patent/FR2361867A1/fr active Granted
-
1977
- 1977-01-17 NZ NZ183096A patent/NZ183096A/xx unknown
- 1977-01-17 ZA ZA770229A patent/ZA77229B/xx unknown
- 1977-01-21 MX MX775377U patent/MX4136E/es unknown
- 1977-01-25 IL IL51325A patent/IL51325A/xx unknown
- 1977-01-31 AR AR266381A patent/AR218864A1/es active
- 1977-02-01 FI FI770354A patent/FI58071C/fi not_active IP Right Cessation
- 1977-02-01 NO NO770324A patent/NO145370C/no unknown
- 1977-02-02 SU SU772447657A patent/SU797546A3/ru active
- 1977-02-02 BE BE174577A patent/BE850992A/xx not_active IP Right Cessation
- 1977-02-03 DD DD7700197227A patent/DD132231A5/xx unknown
- 1977-02-03 LU LU76698A patent/LU76698A1/xx unknown
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2144094B2 (de) * | 1970-09-05 | 1980-02-14 | Tanabe Seiyaku Co. Ltd. | Verfahren zur Herstellung einer zum Sauerstofftransport befähigten, injizierbaren Fluorkohlenstoffteilchenemulsion |
| DE2404564A1 (de) * | 1973-10-05 | 1975-04-17 | Green Cross Corp | Waessrige emulsion von gesaettigten aliphatischen perfluorkohlenstoffverbindungen, verfahren zu ihrer herstellung und ihre verwendung als blutersatzmittel und perfusionsfluessigkeit |
| DK137433B (da) * | 1973-10-05 | 1978-03-06 | Green Cross Corp | Fremgangsmåde til fremstilling af en stabil emulsion af en oxygen-overførende mættet perfluorcarbonforbindelse. |
Also Published As
| Publication number | Publication date |
|---|---|
| FI58071C (fi) | 1980-12-10 |
| DD132231A5 (de) | 1978-09-13 |
| FI58071B (fi) | 1980-08-29 |
| GB1549038A (en) | 1979-08-01 |
| FR2361867A1 (fr) | 1978-03-17 |
| AT355214B (de) | 1980-02-25 |
| NL7607514A (nl) | 1977-08-05 |
| NO145370B (no) | 1981-11-30 |
| IL51325A0 (en) | 1977-03-31 |
| NO770324L (no) | 1977-08-04 |
| SE7607727L (sv) | 1977-08-04 |
| JPS5296722A (en) | 1977-08-13 |
| BE850992A (fr) | 1977-05-31 |
| ES449635A1 (es) | 1977-11-16 |
| NL171533B (nl) | 1982-11-16 |
| DK307276A (da) | 1977-08-04 |
| DE2630586C2 (de) | 1984-06-07 |
| NO145370C (no) | 1982-03-10 |
| NZ183096A (en) | 1979-04-26 |
| CH633674A5 (en) | 1982-12-31 |
| AU1550576A (en) | 1977-07-28 |
| ATA496676A (de) | 1979-07-15 |
| CA1072446A (en) | 1980-02-26 |
| FR2361867B1 (da) | 1978-12-15 |
| ZA77229B (en) | 1977-11-30 |
| SE442706B (sv) | 1986-01-27 |
| MX4136E (es) | 1982-01-06 |
| FI770354A7 (da) | 1977-08-04 |
| DK152256C (da) | 1988-08-29 |
| JPS5835485B2 (ja) | 1983-08-03 |
| IL51325A (en) | 1980-05-30 |
| NL171533C (nl) | 1983-04-18 |
| SU797546A3 (ru) | 1981-01-15 |
| LU76698A1 (da) | 1977-06-28 |
| DE2630586A1 (de) | 1977-08-11 |
| AR218864A1 (es) | 1980-07-15 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US4252827A (en) | Oxygen-transferable fluorocarbon emulsion | |
| DK152256B (da) | Fremgangsmaade til fremstilling af en stabil bloderstatning | |
| AU629832B2 (en) | Improved emulsions of highly fluorinated organic compounds | |
| EP0063149B1 (fr) | Microemulsions aqueuses de fluorocarbures indefiniment stables a une temperature donnee, procede d'obtention et applications | |
| CA1337969C (en) | Stable emulsions of highly fluorinated organic compounds | |
| EP2749268B1 (en) | Resuscitation Fluid | |
| US4397870A (en) | Process for prolonging retention of emulsion particles in the bloodstream | |
| US4343797A (en) | Synthetic whole blood and a method of making the same | |
| US4439424A (en) | Synthetic whole blood | |
| US4497829A (en) | Process for preparing perfluorochemical emulsion artificial blood | |
| CN101448485A (zh) | 用于血液替代品和其他治疗用途的优化的氟碳乳剂 | |
| RU2070033C1 (ru) | Способ получения перфторуглеродных эмульсий для медицинских целей | |
| Vorob’ev | First-and second-generation perfluorocarbon emulsions | |
| RU2162692C1 (ru) | Состав на основе эмульсии перфторорганических соединений для медико-биологических целей | |
| RU2199311C2 (ru) | Состав перфторуглеродного кровезаменителя на основе эмульсии перфторорганических соединений для медико-биологических целей | |
| JPS5946218A (ja) | フルオロカ−ボン乳化製剤 | |
| RU2393849C2 (ru) | Эмульсия перфторорганических соединений медицинского назначения, способ ее приготовления и способ ее применения | |
| US4874742A (en) | Synthetic whole blood and a process for preparing the same | |
| RU2745290C2 (ru) | Эмульсия перфторуглеродных соединений медико-биологического назначения и способ её получения | |
| KR810000695B1 (ko) | 산소 운반 가능한 플루오로카아본 유탁액의 제조방법 | |
| JPS59130813A (ja) | 癌化学療法補助剤 | |
| WO2000013501A1 (en) | Improved artificial blood fluids | |
| GEYER | Surfactants and perfluorochemical emulsions for use in blood replacement preparations | |
| FI65009C (fi) | Perfusionsvaetska foer konservering av ett organ som skall transplanteras och konserveringsfoerfaras | |
| HK1133185B (en) | Optimized fluorocarbon emulsions for blood substitutes and other therapeutic uses |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PBP | Patent lapsed |