-
HINTERGRUND
DER ERFINDUNG
-
Diese
Erfindung betrifft eine Einrichtung zur Erkennung von Extravasation
und insbesondere die Erkennung von Extravasation ionischer und nicht-ionischer
Kontrastmittel.
-
Extravasation
oder Infiltration ist eine Komplikation, welche mit der Verwendung
von Power-Injektoren während
des Injektionsvorgangs von Kontrastmitteln verbunden ist. Wenn eine
Extravasation auftritt, wird Kontrastmittel in das das Blutgefäß umgebende
Gewebe injiziert, statt in das Blutgefäß selbst. Die Gründe für die Extravasation
sind unterschiedlich und reichen von Fehlern des Bedieners bei der
Platzierung der Nadel zu physiologischen Grenzen des Blutgefäßes hinsichtlich
der Aufnahmefähigkeit
der Fluid-Zufuhrrate.
-
Die
die Extravasation betreffenden Komplikationen können ziemlich schwerwiegend
sein und auch Gewebenekrose einschließen. Zur Wiederherstellung
kann dies eine rekonstruktive chirurgische Behandlung erfordern.
-
Gegenwärtig besteht
ein Verfahren zur Erkennung einer Extravasation in einer visuellen Überwachung durch
die Bedienungsperson. Jedoch kann zu dem Zeitpunkt, zu dem eine
Extravasation visuell beobachtbar ist, ein großer Teil des beschriebenen
Schadens bereits aufgetreten sein. Andere bekannte Verfahren schließen die
Erfassung von Temperaturveränderungen
(US-A-4010749) oder die Verwendung von elektromagnetischen Wellen
(US-A-4877034, US-A-5334141) ein.
-
Entsprechend
ist es eine Aufgabe der vorliegenden Erfindung sichere, effiziente,
kostengünstige
und zuverlässige
Mittel zur frühen
Erkennung von Extravasationen bereit zu stellen.
-
In
den Vereinigten Staaten werden jedes Jahr eine große Anzahl
von Kontrastmittel-Injektionen vorgenommen; eine Zahl etwa in der
Größenordnung
von 10 Millionen. Weniger als 0,2% dieser Vorgänge führen zu einer Extravasation.
Jedoch ist die absolute Zahl beträchtlich, da die Basiszahl so
groß ist.
Das Auftreten einer Extravasation erfordert den Abbruch und den
Neubeginn des Vorgangs. Dementsprechend ist bei einer normalen Situation,
in der eine Extravasation auftritt, die frühe Erkennung hinsichtlich der
Minimierung der Auswirkung auf den Patienten wichtig, spart Zeit
und ermöglicht
einen frühen
Neubeginn des Vorgangs.
-
Obwohl
eine Extravasation nicht lebensbedrohlich ist, verursacht sie beim
Auftreten Beschwerden für den
Patienten. Es erfordert eine hohe Aufmerksamkeit von dem Arzt und
bedeutet üblicherweise,
daß ein
Vorgang unterbrochen werden muß.
Es ist daher wichtig, daß eine
Methode zur Erkennung von Extravasation eine falsche Anzeige von
Extravasationen vermeidet.
-
In
verhältnismäßig seltenen
Fällen
kann die Extravasation ziemlich gesundheitsschädlich für den Patienten sein. Die frühe Erkennung
vermeidet daher ein Trauma oder andere Verletzungen des Patienten
vermeiden.
-
Die
falsche Erkennung einer Extravasation führt zu einem Abbruch eines
Vorgangs. Der Beginn des Vorgangs verursacht ein unnötiges Trauma
für den
Patienten und Kosten. Daher wird jede Erkennungsmethode, welche
eine wahrnehmbare Anzahl von falschen Anzeigen liefert, durch den
Arzt nicht verwendet werden.
-
Dementsprechend
ist es wichtig, daß jede
akzeptable Erkennungsmethode eine äußerst geringe Anzahl von falschen
Anzeigen von Extravasationen in Verbindung mit einer ausreichend
hohen Spezifität
für die Erkennung
des Extravasationsvorkommens kombiniert.
-
Die
relativ große
Anzahl von vorgenommenen Kontrastmittel-Injektionen in Verbindung mit dem relativ kleinen
Prozentanteil auftretender Extravasationen bedeutet, daß jeder
für den
medizinischen Berufsstand akzeptable Vorgang nicht-invasiv sein
muß.
-
Es
ist eine anerkannte Tatsache, daß jeder invasive Vorgang Risiken
und Traumata mit sich bringt. Diese sind zu vermeiden, solange die
Vorteile nicht überwiegen.
-
Damit
eine Extravasations-Erkennungsmethode in diesem Zusammenhang akzeptabel
ist, muß sie die
folgenden Aufgaben erfüllen.
-
Zunächst muß sie kostengünstig und
ein Einwegartikel für
den einmaligen Gebrauch sein.
-
Zweitens
muß sie
für den
Patienten verhältnismäßig akzeptabel
sein. Daher sollte sie nicht-invasiv sein und keine Schmerzen oder
andere Probleme beim Patienten verursachen.
-
Drittens
muß sie
für den
Techniker oder Arzt einfach handhabbar sein und sich leicht in den
Ablauf der Kontrastmittel-Injektion
einfügen.
-
Viertens,
und möglicherweise
wichtiger, darf sie nahezu keine falschen Anzeigen von Extravasation liefern.
Eine falsche Anzeige bedeutet den Abbruch eines Vorgangs, der nicht
abgebrochen werden müßte. Daraus
folgt, daß die
Methode spezifisch für
Extravasationen sein muß und
auf andere Vorkommnisse, wie zum Beispiel eine Bewegung des Armes
durch den Patienten/die Patientin, unempfindlich sein muß.
-
Nur
eine die obigen Kriterien erfüllende
Einrichtung (a) wird sicher sein, (b) veranlaßt Techniker und Ärzte zur
Benutzung, (c) führt
zu Akzeptanz durch die Patienten und (d) paßt zu den ökonomischen Anforderungen der
Institution, welche den Injektionsvorgang für das Medium bereitstellt.
-
Die
vorliegende Erfindung betrifft ein Gerät zur Erkennung von Extravasation.
Das Extravasations-Gerät
ist ein Elektrodenpflaster zum Erfassen bestimmter elektrischer
Informationen.
-
Das
Elektrodenpflaster weist einen Körperabschnitt
auf, der lösbar
an der Haut eines Patienten befestigt werden kann. Außen- und
Innenpaare von länglichen
Elektroden sind längs
des Körpers
des Pflasters angeordnet. Das Innenpaar definiert eine Meßzone, die
zum Umfassen der Nadelspitze innerhalb dieser Zone geformt und bemessen
ist. Die Zone ist klein genug, um die Empfindlichkeit zu optimieren
und groß genug,
um das Auflegen des Pflasters über
der Nadelspitze zu ermöglichen.
Wenn der Körper
des Pflasters an der Haut des Patienten fixiert ist und eine elektrische
Wechselsspannung an die Außenelektroden
angelegt wird, so wird ein Feld bereitgestellt, welches ein Signal
in den Innenelektroden hervorruft, wobei das Feld eine Funktion
der Impedanz des Gewebes der Meßzone
ist.
-
Informationen
von dem Elektrodenpflaster werden gesammelt und zur Berechnung der
Gewebeimpedanz verarbeitet. Das Vorliegen einer Extravasation wird
durch Auswerten der Gewebeimpedanzmessung bestimmt und auf diese
Weise können
Extravasationen früh
erkannt werden. Ein Verfahren zum Bestimmen der Extravasation enthält einen
ersten Schritt des Bestimmens einer Vor-Injektions-Grundlinienmessung
der Gewebeimpedanz.
-
Das
Elektrodenpflaster wird derart fixiert, daß die Meßzone die Nadelspitze umfaßt. Das
Anlegen einer Spannung an das Außenelektrodenpaar induziert
ein Signal in dem Innenelektrodenpaar als Funktion der Impedanz
des Körpergewebes
in der Meßzone.
Die Gewebeimpedanz wird während
des Injektionsvorgangs des Mediums unter Verwendung der elektrischen
Informationen gemessen, die von dem Innenelektrodenpaar erfaßt werden.
Die Charakteristika der Veränderung
dieser Impedanz von der Grundlinien-Impedanzmessung wird bestimmt.
Die Gewebeimpedanz wird während
des Injektionsvorgangs überwacht.
Eine vorgegebene Charakteristik der Gewebeimpedanzveränderung
zeigt Extravasation an.
-
Kurzbeschreibung
der Zeichnungen
-
1 zeigt eine perspektivische
Gesamtansicht mit von der Unterseite der bevorzugten Ausführungsform
getrennten Bestandteilen und stellt das Abziehen des Abdeckpapiers
von dem Klebstoff-beschichteten Körper des Elektrodenpflasters
mit einem daneben befindlichen geöffneten Federclip-Verbinder
dar.
-
2 zeigt eine Ansicht des
Elektrodenpflasters von oben und zeigt die leitenden Elektrodenstreifen in
dem Pflaster.
-
3 zeigt die untere Klemmbacke
des Federclip-Verbinders in einer perspektivischen Ansicht mit einem üblichen
Kontakt und Bestandteilen in explodierter Darstellung.
-
4 zeigt eine übliche Art
der Anwendung in einer perspektivischen Darstellung, wobei Pflaster
und Clip gezeigt sind bevor sie über
dem Einführungspunkt
der Nadel angeordnet werden.
-
5 zeigt eine schematische
Draufsicht einer üblichen
Anwendung und die Verbindung der Einrichtung.
-
6 zeigt eine schematische
Draufsicht des auf einem Patienten angeordneten Pflasters und zeigt, in
idealisierter Weise, die Beziehung zwischen einer Extravasation
und der Meßzone.
-
7 zeigt eine Draufsicht
von unten einer gegenwärtig
bevorzugten Ausführungsform
des Pflasters, das ähnlich
dem in 2 gezeigten ist,
bis auf das durchsichtige Trägermaterial
oder die Trägerschicht 68, welche
die Unter- oder Grundschicht bildet und in 7 weggelassen ist.
-
8 zeigt eine Explosionsansicht
des Pflasters aus 7 und
zeigt die Schichten und Elemente, aus denen das Pflaster besteht.
-
Beschreibung
der bevorzugten Ausführungsform
-
Unter
Bezug auf die Zeichnungen bezeichnet das Bezugszeichen 10 ein
Extravasations-Erkennungssystem.
-
Das
Extravasations-Erkennungssystem 10 enthält ein Elektrodenpflaster 12,
das bestimmte elektrische Informationen erfassen kann. Das Elektrodenpflaster 12,
wie es am besten in 1 gezeigt
ist, weist eine PVC-Körper 15 und
eine klebende Rückseite 17 auf.
Die klebende Rückseite 17 ist
durch ein durchsichtiges Trägermaterial 19 geschützt. Das
Elektrodenpflaster 12 weist vier darauf befindliche beabstandete
Elektroden auf, zwei inneren Flächenelektroden 18, 19 und
zwei äußeren Flächenelektroden 22 und 24.
Zwischen den inneren Elektroden 18, 20 befindet
sich ein Bereich 26. Der Bereich 26 ist geformt
und bemessen, um darunter eine Nadel 21 zu platzieren und
die Empfindlichkeit des Systems für die Tiefe der Nadelspitze
in dem Gewebe während
einer üblichen
Injektion zu optimieren. Durch Verwenden der klebenden Rückseite 15 kann
das Elektrodenpflaster 12 leicht auf der Haut angebracht
und von dort entfernt werden.
-
Das
Elektrodenpflaster 12 weist eine Kopplungsbereich 23 auf,
der so geformt und bemessen ist, daß er in einen Clip 28 paßt. Der
Clip 28 ist mit elektrischen Kontakten 30, 32, 34, 36 versehen,
die in dem Clip derart angeordnet sind, daß sie die Flächenelektroden 18, 19, 22, 24 kontaktieren
können,
wenn das Leiter-Pflaster 12 in den Clip 28 eingebracht
ist. Bei einer bevorzugten Ausführungsform
weist der Clip 28 eine Feder 25 auf. Der Clip 28 weist
elektrische Anschlußdrähte 50, 52 auf,
die mit einer Stromquelle eines konstanten Wechselstroms verbunden
sind und elektrische Anschlußdrähte 54, 56,
die mit einer Spannungs-Potential-Meßschaltung verbunden sind.
Der Clip 28 weist ferner eine die Anschlußdrähte 50, 52, 54, 56 aufnehmende
erste Leitung 27 auf, die mit einem Gerät 29 verbunden ist,
wobei das Gerät
die durch das Elektrodenpflaster 12 erfaßten Daten
auswertet und eine zweite Leitung 40, die mit einem CT-Injektor 42 verbunden
ist. Die Leitung 40 kann den Betrieb des Injektors 42 anhalten,
wenn eine Extravasation erkannt wurde oder diese Information an
den Injektor 42 weiterleiten.
-
Bei
einer Ausführungsform
sind die Elektroden 18, 20, 22, 24 Silber/Silberchlorid-Streifen.
Jede der Elektroden weist einen ersten relativ kurzen vertikalen
Abschnitt 18a, 20a, 22a, 24a auf
und einen zweiten relativ langen vertikalen Abschnitt 18b, 20b, 22b, 24b.
Jede Elektrode hat eine Gesamtlänge
von etwa 7,62 cm (3 Zoll) und eine Breite von etwa 0,47 cm (3/16
Zoll). Die inneren Elektroden 18, 19 sind voneinander
um 1,905 cm (0,75 Zoll) beabstandet und die äußeren Elektroden 22, 24 sind
voneinander um etwa 3,81 cm (1,5 Zoll) beabstandet.
-
Bei
dieser Ausführungsform
hat das Elektrodenpflaster 12 eine Länge von etwa 7,62 cm (3 Zoll)
und an seinem breitesten Punkt eine Breite von etwa 5,08 cm (2 Zoll).
-
Bei
Verwendung arbeitet das Extravasations-Erkennungssystem wie folgt.
Eine Spritzennadel 21 wird in das Gefäßsystem des Patienten eingeführt. Das
Trägermaterial 19 wird
von dem Pflasterkörper 15 entfernt und
das Elektrodenpflaster 12 wird mit Hilfe der klebenden
Rückseite 17 auf
die Haut des Patienten geklebt. Wie bereits erwähnt, wird das Pflaster 12 derart
angeordnet, daß die
Nadelspitze durch den Bereich 26 bedeckt wird. Das Elektrodenpflaster 12 wird
in den Clip 28 mit Hilfe des Kopplungsbereichs 23 derart
festgeklemmt, daß die
Flächenelektroden 18, 20, 22, 24 in
Kontakt mit den elektrischen Kontakten 30, 32, 34, 36 stehen.
Der Clip 28 wird dann durch die Leitung 27 mit
der Impedanzüberwachung
und Auswerteschaltung in dem Gerät 29 verbunden.
Die Bereitstellung der kurzen vertikalen Abschnitte ermöglicht die
Verwendung eines Clips für
alle elektrischen Verbindungen, ohne den Abstand der Flächenelektroden
in dem Meßbereich 26 des Elektrodenpflasters
zu beeinträchtigen,
in dem Messungen vorgenommen werden.
-
Vorbereitungsdaten
werden zur Bestimmung der Gewebeimpedanz gesammelt, bevor eine Injektion vorgenommen
wird. Dann wird eine Injektion unter Verwendung des Injektors 42 begonnen.
Während
des Injektionsvorgangs werden fortlaufende Berechnungen der Gewebeimpedanz
durchgeführt.
Es wird eine auftretenden Extravasation angenommen, wenn während des
Injektionsvorgangs die Impedanzänderung
eine ungefähr
gleichmäßige Steigerung
von mindestens plus oder minus 0,5 Ohm pro Sekunde zeigt, wenn eine
Materialinfusion in das Gefäßsystem
bei einer Rate von mehr als 0,25 ml pro Sekunde verabreicht wird.
Es ist beabsichtigt, daß bei
bestimmten Ausführungsformen
ein automatischer Stop-Mechanismus bei Festellung einer aufgetretenen
Extravasation die Injektion des Mediums durch die Leitung 40 beendet
oder als Alternative ein visuelles oder andersartiges Warnsignal
ausgelöst
wird. Ionisches Kontrastmittel hat eine geringere Impedanz als Gewebe
und verursacht eine Verringerung der Gewebeimpedanz während einer
Extravasation. Nichtionisches Kontrastmittel hat eine höhere Impedanz
als Gewebe und verursacht eine Zunahme der Gewebeimpedanz während einer
Extravasation.
-
Um
die geeigneten Daten von dem Elektrodenpflaster 12 abzuleiten,
wird ein Wechselstrom konstanter Stärke an die zwei äußeren Elektroden 22, 24 angelegt.
Der verwendete Strom und die verwendete Frequenz betragen etwa 200
Mikroampere Sinusstrom bei 20 Kilohertz. Die inneren Elektroden 18, 19 ermöglichen
die Messung der Spannung.
-
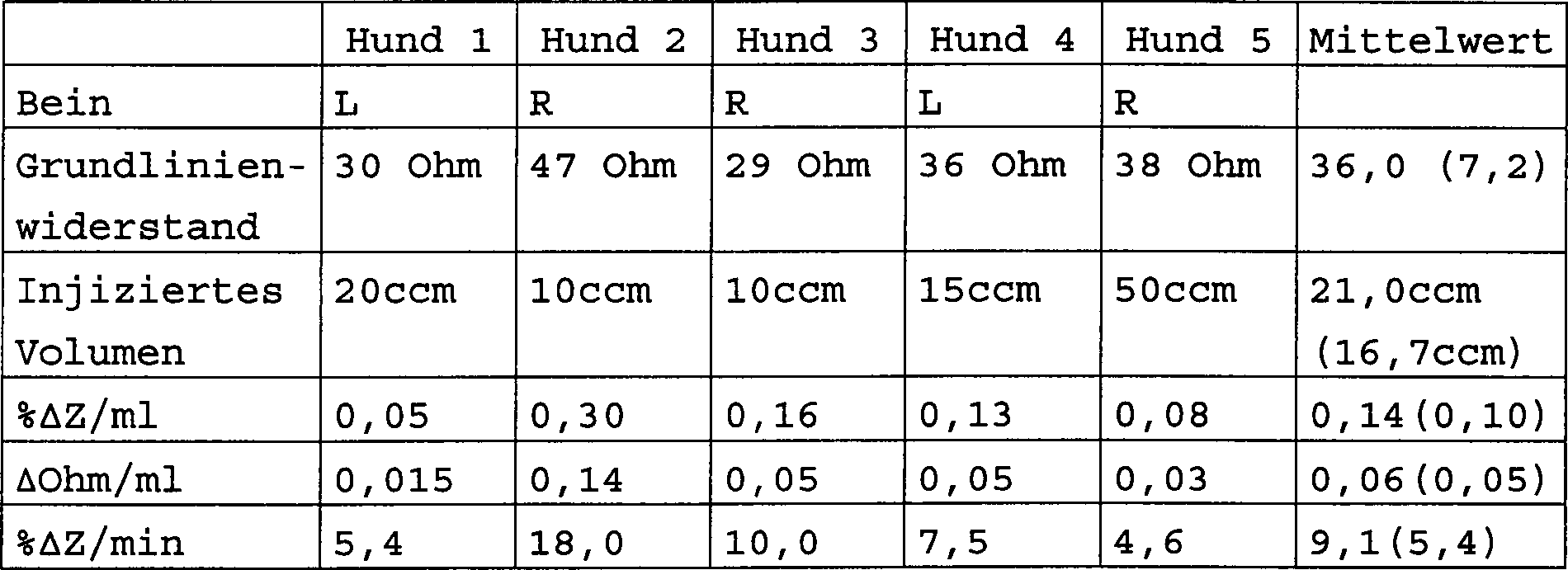
Tabelle
1
Zusammenfassung der Daten von fünf Hunden
-
Tabelle
2
Ergebnisse der intravenösen
Injektion von ionischem Kontrastmittel bei fünf Hunden
-
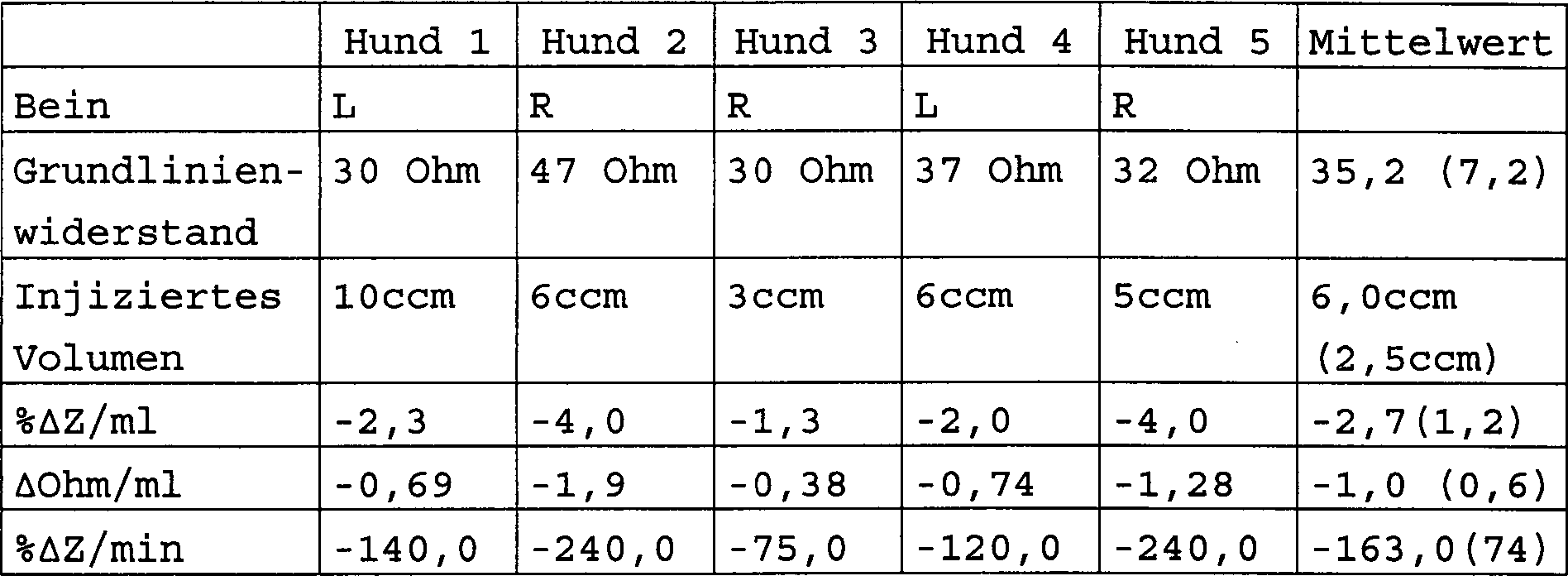
Tabelle
3
Ergebnisse der Extravasation von ionischem Kontrastmittel
bei fünf
Hunden
-
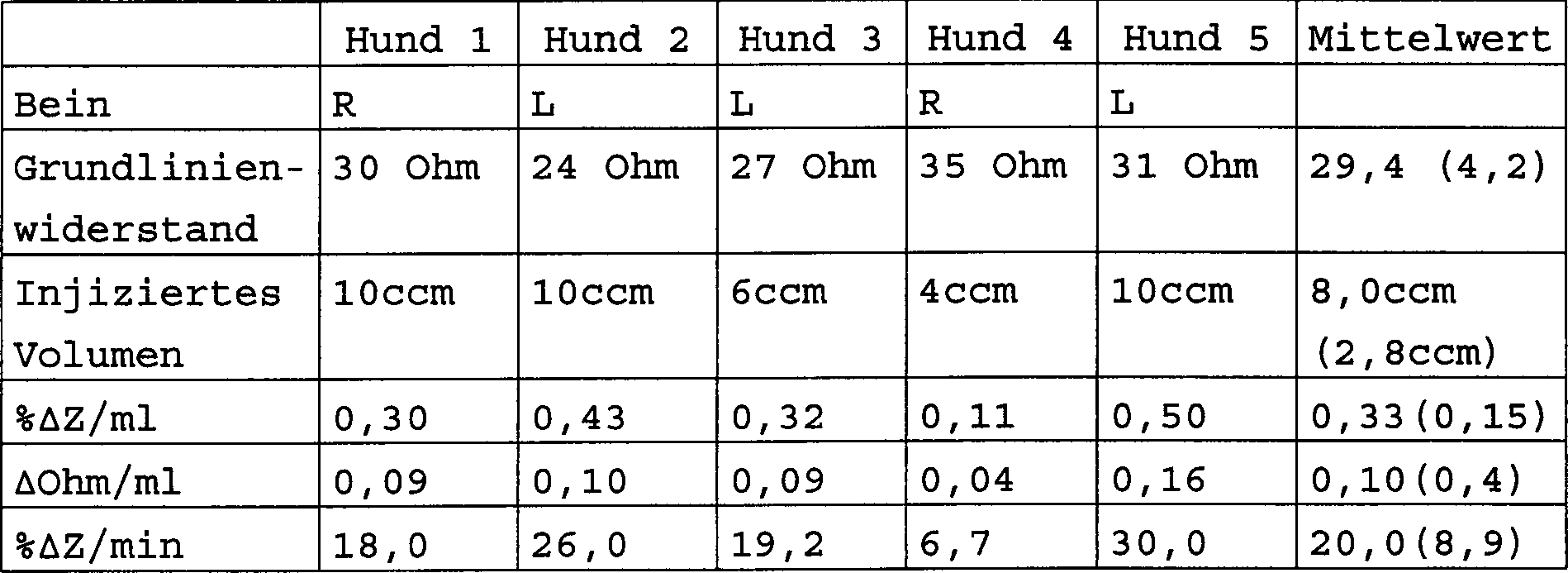
Tabelle
4
Ergebnisse der intravenösen
Injektion von nicht-ionischem Kontrastmittel bei fünf Hunden
-
Tabelle
5
Ergebnisse der Extravasation von nicht-ionischem Kontrastmittel
bei fünf
Hunden
-
Obwohl
das Gerät 10 und
das diesbezügliche
Verfahren bislang nur zur Erkennung von Extravasationen von ionischen
und nicht-ionischen Kontrastmitteln verwendet wurden, können sie
zur Erkennung von Extravasationen anderer Arten von injizierbaren
Fluiden nützlich
sein.
-
Ein
Vorteil eines Extravasation-Erkennungssystems unter Verwendung eines
Elektrodenpflasters gemäß Anspruch
1 ist, daß es
einen nicht-invasiven Ablauf bedeutet. Eine andere wichtige Überlegung
ist, daß die
Elektrodenkonfiguration in angemessener Weise die Extravasation
umfaßt
und darauf reagiert.
-
Wenn
die Nadel während
eines Vorgangs in einer Vene angeordnet ist, kann man sich kein
genaues Bild davon machen, wo sich die Nadelspitze befindet. Da
die Extravasation an der Nadelspitze auftritt, kann man nicht sicher
sein, wo die Extravasation entlang dem Verlauf des Blutgefäßes genau
auftritt. Das Elektrodenpflaster mit seiner länglichen Meßzone 26 (zwischen
den Aufnahmeelektroden 18 und 20 aus 2) stellt den erforderlichen
Erfassungsbereich zur Verfügung.
-
Ferner
ist es wichtig, daß zwischen
den Erfassungselektroden 18 und 20 die in 2 gezeigte Öffnung 26 liegt,
so daß die
Zone unter dem Bereich 26 in dem Körper des Patienten abgetastet
wird, wenn eine Extravasation auftritt.
-
Die
länglichen
Abtastelektroden 18, 20 und die parallelen länglichen
Stromversorgungselektroden 22, 24 stellen die
erforderliche Konfiguration zur Verfügung, um eine Extravasation
beim Auftreten zuverlässig
zu erfassen. Dies ist in 6 gezeigt.
Diese Empfindlichkeit wird insbesondere dadurch ermöglicht,
daß der
vom Anmelder vorgeschlagene Aufbau eine Platzierung der Elektroden 18, 20, 22, 24 um
den Punkt herum sicherstellt, an dem die Nadel 21 in die
Haut eintritt. Daher ist die Extravasation 44 im wesentlichen
in dem Meßbereich
zentriert, der durch die inneren Elektroden 18, 20 gebildet
wird. Im allgemeinen wird die Extravasation in zehn bis zwanzig
ccms einer Extravasation erkannt.
-
Die
dargelegte geometrische Konfiguration der oben genannten Anwendung
erfüllt
die Aufgaben, eine gute Sicherheit dafür bereit zu stellen, daß eine Extravasation
erkannt wird und eine Fehlanzeige von Extravasation nahezu vollständig vermieden
wird.
-
Die 7 und 8 zeigen eine gegenwärtig bevorzugte Ausführungsform
des Pflasters. Wie in der explodierten Ansicht in 8 am besten zu sehen ist, ist die Oberseite
des Pflasters eine durchsichtige Vinylschicht 60. Diese
Schicht 60 weist auf der dem Patienten zugewandten Seite
einen Klebstoff auf, der dazu dient, die Elektroden zu halten und
das Pflaster auf den Patienten zu kleben. Unter dieser Vinylschicht 60 befindet
sich eine Verstärkungsschicht 62,
welche dem durch die Klammer 28 (siehe 1) zu haltenden Ende des Pflasters Steifheit
verleiht. Direkt unterhalb der Verstärkung 62 und großteils im
Kontakt und gehalten durch die klebende Seite der Schicht 60,
befindet sich der Satz aus vier Elektroden 64. Wie unter
Bezugnahme auf 2 beschrieben,
weist jede Elektrode einen länglichen
Abschnitt auf. Diese länglichen
Abschnitte sind die aktiven Abschnitte zum Bereitstellen des Feldes
und zum Aufnehmen des Signals. Diese Elektroden 64 gleichen
im wesentlichen der Elektrodenanordnung aus 1. Die dem Patienten zugewandte Seite
jeder Elektrode weist eine Hydrogel- Beschichtung auf, um guten Kontakt mit
der Haut des Patienten sicher zu stellen. Da Hydrogel leitend ist,
ist es wichtig, daß die
Hydrogelbeschichtung sich nur auf der Elektrode befindet und nicht
auf einer Fläche
zwischen den Elektroden, da sie sonst zum Kurzschluß der betroffenen
Signale führen
könnte.
Ein durchsichtiges Isolierband 66 entlang den kurzen Abschnitten
der Elektroden hat die wichtige Funktion, die Wechselwirkung zwischen
den kurzen Abschnitten der Elektroden und dem Patienten zu minimieren,
so daß die
langen Abschnitte der Elektroden 64 als Stromversorgung
und Erfassungselektroden wirken. Schließlich gibt es das durchsichtige
Trägermaterial 68,
welches die Grundschicht des Pflasters bildet, mit einer perforierten
Linie 70. Wie in 1 gezeigt,
kann das Trägermaterial
(die Schicht 19 in 1)
zu Beginn umgebogen werden, so daß das Pflaster in der Klemme 28 angeordnet
werden kann, bevor es verwendet wird. Wenn es dann verwendet wird,
kann der Hauptteil der Schicht 68 durch Abreißen an der
Perforationslinie 70 entfernt werden, so daß die Elektroden 64 auf
der Haut des Patienten platziert werden können. Die dem Patienten zugewandte
Seite der Vinylschicht 60 trägt den druckempfindlichen Klebstoff,
der das Pflaster stabil an der Haut des Patienten festklebt.
-
7 zeigt die Anordnung der
Schichten aus 8, wobei
die klare Vinylschicht weggelassen ist. Die Gesamtabmessungen betragen
etwa 9,4 cm mal 5,84 cm (3,7 Zoll mal 2,3 Zoll). Die Elektroden 64 sind
jeweils etwa 0,51 cm (0.2 Zoll) breit und die länglichen Abschnitte sind etwa
5,08 cm (2 Zoll) lang. Die Hydrogelbeschichtung der Elektroden 64 endet
an der Linie 72. Der Abstand zwischen den inneren Rändern der
inneren Elektroden beträgt
etwa 1,78 cm (0,7 Zoll) und der Abstand zwischen den inneren Rändern der äußeren Elektrodenpaare
beträgt
etwa 3,81 cm (1,5 Zoll).