-
Hintergrund der Erfindung
-
Die
vorliegende Erfindung betrifft Benzimidazol-Derivate, Zusammensetzungen
und Medikamente, die diese enthalten, sowie Verfahren zur Herstellung
und Verwendung solcher Verbindungen, Zusammensetzungen und Medikamente.
Solche Benzimidazol-Derivate sind nützlich in der Behandlung von
Krankheiten, die mit unangemessener Angiogenese assoziiert sind.
-
Der
Prozeß der
Angiogenese ist die Entwicklung von neuen Blutgefäßen, im
allgemeinen Kapillargefäße, aus
einer vorher vorhandenen Gefäßanordnung.
Angiogenese wird definiert als mit sich bringend: (i) Aktivierung
von Endothelzellen; (ii) zunehmende vaskuläre Permeabilität; (iii)
nachfolgende Auflösung
der Basalmembran und Extravasation von Plasmakomponenten, was zur
Bildung einer vorläufigen
extrazellulären
Fibringel-Matrix führt;
(iv) Proliferation und Mobilisierung von Endothelzellen; (v) Neuorganisierung
von mobilisierten Endothelzellen zur Ausbildung funktioneller Kapillargefäße; (vi)
Ausbildung einer Gefäßschleife;
und (vii) Ablagerung der Basalmembran und Rekrutierung von perivaskulären Zellen,
um Gefäße neu auszubilden. Normale
Angiogenese wird während
des Gewebewachstums, von der embryonalen Entwicklung bis zur Reife, aktiviert
und tritt dann in eine Periode relativer Ruhe während des Erwachsenenstadiums.
Normale Angiogenese wird ebenfalls während der Wundheilung und in
bestimmten Stadien des weiblichen Reproduktionszyklusses aktiviert.
Unangemessene Angiogenese wurde mit mehreren Krankheitszuständen assoziiert,
einschließlich
verschiedener Retinopathien; ischämischer Krankheit; Atherosklerose;
chronischer Entzündungsstörungen;
und Krebs. Die Rolle der Angiogenese in Krankheitszuständen wird
zum Beispiel in Fan et al., Trends in Pharmacol. Sci. 16:54-66; Shawver et al.,
DDT Bd. 2, Nr. 2, Februar 1997; Folkmann, 1995, Nature Medicine
1:27-31 diskutiert.
-
Für das Wachstum
von soliden Tumoren in Krebs wurde gezeigt, daß dieses angiogeneseabhängig ist (siehe
J. Folkmann, J. Nat'l.
Cancer Inst., 1990, 82, 4-6). Konsequenterweise ist das Abzielen
auf proangiogene Stoffwechselwege in der Krebsbehandlung eine Strategie,
die weitläufig
verfolgt wird, um neue Therapeutika auf diesen Gebieten des großen, unerreichten
medizinischen Bedarfs bereitzustellen. Die Rolle von Tyrosinkinasen,
die an der Angiogenese und in der Vaskulisierung von soliden Tumoren
beteiligt sind, hat Interesse geweckt. Bis vor kurzem wurde das
meiste Interesse auf diesem Gebiet auf Wachstumsfaktoren, wie zum
Beispiel Gefäßzell-Wachstumsfaktor
(VEGF), und seinen Rezeptoren, die als Gefäßzelle-Wachstumsfaktorrezeptor(en)
(VEGFR) bezeichnet werden, fokussiert. VEGF, ein Polypeptid, ist
Mitose-auslösend
für Endothelzellen in
vitro und stimuliert angiogene Antworten in vivo. VEGF wurde ebenfalls
mit unangemessener Angiogenes verbunden (H.M. Pinedo et al., The
Oncologist, Bd. 5, Nr. 90001, 1-2, April 2000). VEGFR(s) sind Proteintyrosinkinasen
(PTKs). PTKs katalysieren die Phosphorylierung spezifischer Tyrosinreste
in Proteinen, die an der Regulierung des Zellwachstums und der Differentierung
beteiligt sind (A.F. Wilks, Progress in Growth Factor Research,
1990, 2, 97-111; S.A. Courtneidge, Dev. Supp. I, 1993, 57-64; J.A.
Cooper, Semin, Cell Biol., 1994, 5(6), 377-387; R.F. Paulson, Semin.
Immunol., 1995, 7(4), 267-277; A.C. Chan, Curr. Opin. Immunol.,
1996, 8(3), 394-401).
-
Drei
PTK-Rezeptoren für
VEGF wurden identifziert: VEGFR-1 (Flt-1); VEGFR-2 (Flk-1 oder KDR)
und VEGFR-3 (Flt-4). Diese Rezeptoren sind an der Angiogenese beteiligt
und partizipieren an der Signaltransduktion (T. Mustonen et al,
J. Cell Biol. 1995:129:895-898). Von besonderen Interesse ist VEGFR-2,
das ein Transmembranrezeptor-PTK ist, der primär in Endothelzellen exprimiert
wird. Die Aktivierung von VEGFR-2 durch VEGF ist ein kritischer
Schritt im Signaltransduktionsweg, der Tumorangiogenese einleitet.
Die VEGF-Expression kann konstitutiv für Tumorzellen sein und kann
ebenfalls in Antwort auf bestimmte Stimuli hochreguliert werden.
Ein solches Stimuli ist Hypoxie, bei der die VEGF-Expression sowohl
im Tumor als auch im assoziierten Wirtsgewebe hochreguliert wird.
Der VEGF-Ligand aktiviert VEGFR-2 durch Binden an dessen extrazelluläre VEGF-Bindestelle.
Dies führt
zur einer Rezeptordimerisierung von VEGFRs und Autophosphorylierung von
Tyrosinresten in der intrazellulären
Kinasedomäne
von VEGFR-2. Die Kinasedomäne
führt zum
Transfer eines Phosphats von ATP auf die Tyrosinreste, woduch Bindestellen
für Signalproteine
stromabwärts
von VEGFR-2 bereitgestellt werden, was letztendlich zur Einleitung
der Angiogenese führt
(G. McMahon, The Oncologist, Bd. 5, Nr. 90001, 3-10, April 2000).
-
Angiopoieten
1 (Ang1), ein Ligand für
die endothel-spezifische Rezeptortyrosinkinase TIE-2, ist ein neuer
angiogener Faktor (Davis et al., Cell, 1996, 87:1161-1169; Partanen
et al., Mol. Cell Biol., 12:1698-1707 (1992);
US-Patente 5,521,073 ;
5,879,672 ;
5,877,020 und
6,030,831 ). Das Acronym TIE stellt "Tyrosinkinase-enthaltendes
Ig und EGF Homologdomänen" dar. TIE wird verwendet,
um eine Klasse von Rezeptortyrosinkinasen zu identifizieren, die
exklusiv in vaskulären
Endothelzellen und frühen
hämopoetischen
Zellen exprimiert werden. Typischerweise werden TIE-Rezeptorkinasen durch
die Gegenwart einer EGF-ähnlichen
Domäne
und einer Immunglobulin (IG)-ähnlichen
Domäne
gekennzeichnet, die aus extrazellulären Faltungseinheiten, die
durch Disulfidbrückenbindungen
innerhalb der Kette stabilisiert werden, besteht (Partanen et al., Curr.
Tropics Microbiol. Immunol., 1999, 237:159-172). Im Gegensatz zu
VEGF, das während
des frühen
Stadiums der vaskulären
Entwicklung wirkt, wirkt Ang1 und sein Rezeptor TIE-2 in den späten Stadien
der vaskulären
Entwicklung, d.h. während
der vaskulären
Ummodulierung (Ummodulierung bezieht sich auf die Ausbildung eines
vaskulären
Lumens) und Reifung (Yancopoulus et al., Cell, 1998, 93:661-664;
K.G. Peters, Circ. Res., 1998, 83(3):342-3; Suri et al, Cell 87,
1171-1180 (1996)).
-
Konsequenterweise
würde zu
erwarten sein, daß die
Inhibierung von TIE-2 zur Unterbrechung des Ummodulierens und der
Reifung einer neuen Gefäßanordnung,
die durch Angiogenese eingeleitet wird, dienen könnte, wodurch der angiogene
Prozeß unterbrochen
wird. Des weiteren würde
die Inhibierung an der Kinasedomänebindestelle
von VEGFR-2 die Phosphorylierung von Tyrosinresten blockieren und
zum Unterbrechen der Einleitung der Angiogenese dienen. Wahrscheinlich
sollte Inhibierung von TIE-2 und/oder VEGFR-2 dann die Tumorangiogenese
unterbinden und zum Verzögern
oder Auslöschen
des Tumorwachstums dienen. Entsprechend könnte eine Behandlung für Krebs
oder anders Störungen,
die mit einer unangemessenen Angiogenese assoziiert sind, bereitgestellt
werden.
-
WO 97/19065 offenbart substituierte
2-Anilinopyrimidine, die nützlich
als Inhibitoren von Proteinkinasen sind, insbesondere für p56
lck, p59
fyn, ZAP-70
und Proteinkinase C.
-
Die
vorliegenden Erfinder haben neue Benzimidazol-Verbindungen gefunden,
die Inhibitoren von TIE-2- und/oder VEGFR-2-Kinaseaktivität sind.
Solche Benzimidazol-Derivate sind nützlich in der Behandlung von
Störungen,
einschließlich
Krebs, die mit einer unangemessenen Angiogenese assoziiert sind.
-
Kurze Zusammensetzung der Erfindung
-
In
einem Aspekt der vorliegenden Erfindung wird eine Verbindung der
Formel (I) bereitgestellt:
oder ein Salz oder Solvat
davon:
worin:
D -NRR
1, -OR, -SR,
-S(O)R oder -S(O)
2R ist,
R Wasserstoff,
C
1-8-Alkyl, C
3-7-Cycloalkyl,
Aralkyl, Aryl, Heteroaryl, -C(O)NR
1R
1, -C(O)OR
1, Acyl,
Aroyl oder Heteroaroyl ist;
R
1 Wasserstoff,
C
1-8-Alkyl, C
3-7-Cycloalkyl,
Aralkyl oder Aryl ist;
R
2 C
1-6-Alkyl oder C
3-7-Cycloalkyl
ist;
R
3 Wasserstoff, C
1-4-Alkyl,
C
1-4-Halogenalkyl, Aralkyl, Cyanoalkyl,
-(CH
2)
pC=CH(CH
2)
tH, -(CH
2)
pC≡C(CH
2)
tH oder C
3-7-Cycloalkyl ist;
p 1, 2 oder 3 ist;
t
0 oder 1 ist;
R
4 Wasserstoff, Halogen
oder Cyano ist;
Q
1 Wasserstoff, Halogen,
C
1-2-Halogenalkyl, C
1-2-Alkyl,
C
1-2-Alkoxy oder C
1-2-Halogenalkoxy
ist;
Q
2 A
1 oder
A
2 ist;
Q
3 A
1 ist, wenn Q
2 A
2 ist, und Q
3 A
2 ist, wenn Q
2 A
1 ist; worin
A
1 Wasserstoff,
Halogen, C
1-3-Alkyl, C
1-3-Halogenalkyl,
-OR
5 ist, und
A
2 die
Gruppe ist, die durch -(Z)
m(Z
1)-(Z
2) definiert ist, worin
Z CH
2 ist und m 0, 1, 2 oder 3 ist, oder
Z
NR
5 ist und m 0 oder 1 ist, oder
Z
Sauerstoff ist und m 0 oder 1 ist, oder
Z CH
2NR
6 ist und m 0 oder 1 ist;
Z
1 S(O)
2, S(O) oder C(O) ist; und
Z
2 C
1-4-Alkyl, Cycloalkyl,
Heterocyclyl, -NR
8R
9,
Aryl, Arylamino, Aralkyl, Aralkoxy oder Heteroaryl ist;
R
5 und R
6 jeweils
unabhängig
ausgewählt
sind aus Wasserstoff, Hydroxyl, Alkoxy, Aryloxy, Aralkoxy, C
1-4-Alkyl, C
3-7-Cycloalkyl,
Heterocyclyl, -S(O)
2R
7 oder
-C(O)R
7;
R
7 C
1-4-Alkyl oder C
3-7-Cycloalkyl
ist;
R
8 Wasserstoff, Hydroxyl, C
1-6-Alkyl, C
1-6-Alkoxy,
Aryloxy, Aralkoxy, C
3-7-Cycloalkyl oder
C
3-7-Cycloalkoxy ist; und
R
9 Wasserstoff, C
1-6-Alkyl,
C
3-7-Cycloalkyl, Aryl, Acyl, Carbamoyl oder
Heterocyclyl ist.
-
In
einem zweiten Aspekt der vorliegenden Erfindung wird eine Verbindung
der Formel (II) bereitgestellt:
oder ein Salz oder Solvat
davon, worin:
R Wasserstoff, C
1-8-Alkyl,
C
3-7-Cycloalkyl, Aralkyl, Aryl, Heteroaryl,
-C(O)NR
1R
1, -C(O)OR
1, Acyl, Aroyl oder Heteroaryl ist;
R
1 Wasserstoff, C
1-8-Alkyl,
C
3-7-Cycloalkyl, Aralkyl oder Aryl ist;
R
2 C
1-6-Alkyl oder
C
3-7-Cycloalkyl ist;
R
3 Wasserstoff,
C
1-4-Alkyl, C
1-4-Halogenalkyl,
Aralkyl, Cyanoalkyl, (CH
2)
tH-(CH
2)
pC=CH(CH
2)
tH, -(CH
2)
pC≡C(CH
2)
tH oder C
3-7-Cycloalkyl ist;
p 1, 2 oder ist;
t
0 oder 1 ist;
R
4 Wasserstoff, Halogen
oder Cyano ist;
Q
1 Wasserstoff, Halogen,
C
1-2-Halogenalkyl, C
1-2-Alkyl,
C
1-2-Alkoxy oder C
1-2-Halogenalkoxy
ist;
Q
2 A
1 oder
A
2 ist;
Q
3 A
1 ist, wenn Q
2 A
2 ist, und Q
3 A
2 ist, wenn Q
2 A
1 ist;
worin
A
1 Wasserstoff,
Halogen, C
1-3-Alkyl, C
1-3-Halogenalkyl,
-OR
5 ist, und
A
2 die
Gruppe ist, die durch -(Z)
m(Z
1)-(Z
2) definiert ist, worin
Z CH
2 ist und m 0, 1, 2 oder 3 ist, oder
Z
NR
5 ist und m 0 oder 1 ist, oder
Z
Sauerstoff ist und m 0 oder 1 ist, oder
Z CH
2NR
6 ist und m 0 oder 1 ist;
Z
1 S(O)
2, S(O) oder C(O) ist; und
Z
2 C
1-4-Alkyl, Cycloalkyl,
Heterocyclyl, -NR
8R
9,
Aryl, Arylamino, Aralkyl, Aralkoxy oder Heteroaryl ist;
R
5 und R
6 jeweils
unabhängig
ausgewählt
sind aus Wasserstoff, Hydroxyl, Alkoxy, Aryloxy, Aralkoxy, C
1-4-Alkyl, C
3-7-Cycloalkyl,
Heterocyclyl, -S(O)
2R
7 oder
-C(O)R
7;
R
7 C
1-4-Alkyl oder C
3-7-Cycloalkyl
ist;
R
8 Wasserstoff, Hydroxyl, C
1-6-Alkyl, C
1-6-Alkoxy,
Aryloxy, Aralkoxy, C
3-7-Cycloalkyl oder
C
3-7-Cycloalkoxy ist; und
R
9 Wasserstoff, C
1-6-Alkyl,
C
3-7-Cycloalkyl, Aryl, Acyl, Carbamoyl oder
Heterocyclyl ist.
-
In
einem dritten Aspekt der vorliegenden Erfindung wird eine pharmazeutische
Zusammensetzung bereitgestellt, die eine therapeutisch effektive
Menge einer Verbindung der Formel (I) oder eines Salzes oder Solvats
davon und einen oder mehrere pharmazeutisch annehmbare Träger, Verdünnungsstoffe
und Exzipienten umfaßt.
-
In
einem fünften
Aspekt der vorliegenden Erfindung wird eine Verbindung der Formel
(I) oder ein Salz oder Solvat davon zur Verwendung in der Therapie
bereitgestellt.
-
In
einem sechsten Aspekt der vorliegenden Erfindung wird die Verwendung
einer Verbindung der Formel (I) oder eines Salzes oder Solvats davon
in der Herstellung eines Medikaments zur Verwendung in der Behandlung
einer Störung,
die durch mindestens eine aus unangemessener TIE-2- und VEGFR-2-Aktivität vermittelt
wird, bereitgestellt.
-
In
einem achten Aspekt der vorliegenden Erfindung wird die Verwendung
einer Verbindung der Formel (I) oder eines Salzes oder Solvats davon
in der Herstellung eines Medikaments zur Verwendung in der Behandlung
einer Störung
in einem Säugetier
bereitgestellt, wobei die Störung
durch unangemessene Angiogenese gekennzeichnet ist.
-
Ausführliche
Beschreibung
-
Wie
hier verwendet bedeutet der Begriff "effektive Menge" diejenige Menge eines Arzneistoffs
oder pharmazeutischen Mittels, die die biologische oder medizinische
Antwort eines Gewebes, Systems, Tiers oder Menschen auslöst, die
zum Beispiel durch einen Forscher oder Kliniker begehrt wird. Des
weiteren bedeutet der Begriff "therapeutisch
effektive Menge" jedwede
Menge, die im Vergleich zu einem entsprechenden Probanden, der eine
solche Menge nicht erhalten hat, in einer verbesserten Behandlung,
Heilung, Prävention
oder Verbesserung einer Krankheit, Störung oder Nebenwirkung oder
in einer Abnahme der Rate des Fortschreitens einer Krankheit oder
Störung
resultiert. Der Begriff schließt
ebenfalls innerhalb seines Umfangs Mengen ein, die effektiv zum
Steigern einer normalen physiologischen Funktion sind.
-
Wie
hier verwendet bezeichnet der Begriff "Alkyl" ein geradkettiges oder verzweigtkettige
Kohlenwasserstoffradikal mit 1 bis 12 Kohlenstoffatomen, das gegebenenfalls
mit Substituenten substituiert ist, die aus der Gruppe ausgewählt sind,
die aus C1-6-Alkyl, C1-6-Hydroxyalkyl,
C1-6-Alkoxy,
C1-6-Alkylsulfanyl, C1-6-Alkylsulfenyl,
C1-6-Alkylsulfonyl, Oxo, Hydroxy, Mercapto,
Amino, das gegebenenfalls mit Alkyl substituiert ist, Carboxy, Carbamoyl,
das gegebenenfalls mit Alkyl substituiert ist, Aryl, Aryloxy, Heteroaryl,
Aminosulfonyl, das gegebenenfalls mit Alkyl substituiert ist, Nitro,
Cyano, Halogen oder C1-6-Perfluoralkyl besteht,
wobei mehrere Substitutionsgrade möglich sind. Beispiele für "Alkyl", wie hier verwendet,
schließen
uneingeschränkt
Methyl, Ethyl, n-Propyl, Isopropyl, n-Butyl, Isobutyl, t-Butyl,
n-Pentyl, Isopentyl und dgl. ein.
-
Wie
hier verwendet bezeichnen die Begriffe "C1-3-Alkyl", "C1-4-Alkyl", "C1-6-Alkyl" und "C1-8-Alkyl" eine wie oben definierte
Alkyl-Gruppe, die
mindestens 1 und höchstens
3, 4, 6 bzw. 8 Kohlenstoffatome enthält. Beispiele für solche
verzweigten oder geradkettigen Alkyl-Gruppen, die in der vorliegenden
Erfindung nützlich sind,
schließen
uneingeschränkt
Methyl, Ethyl, n-Propyl, Isopropyl, Isobutyl, n-Butyl, t-Butyl,
n-Pentyl, Isopentyl, n-Hexyl und n-Septyl ein.
-
Wie
hier verwendet bezeichnet der Begriff "Alkylen" ein geradkettiges oder verzweigtkettiges
zweiwertiges Kohlenwasserstoffradikal mit 1 bis 10 Kohlenstoffatomen,
das gegebenenfalls mit Substituenten substituiert ist, die aus der
Gruppe ausgewählt
sind, die C1-6-Alkyl, C1-6-Alkoxy,
C1-6-Alkylsulfanyl,
C1-6-Alkylsulfenyl, C1-6-Alkylsulfonyl,
Oxo, Hydroxy, Mercapto, Amino, das gegebenenfalls mit Alkyl substituiert
ist, Carboxy, Carbamoyl, das gegebenenfalls mit Alkyl substituiert
ist, Aminosulfonyl, das gegebenenfalls mit Alkyl substituiert ist,
Nitro, Cyano, Halogen und C1-6-Perfluoralkyl
einschließt,
wobei mehrere Grade an Substitutionen möglich sind. Beispiele für "Alkylen", wie hier verwendet,
schließen
uneingeschränkt
Methylen, Ethylen, n-Propylen, n-Butylen und dgl. ein.
-
Wie
hier verwendet bezeichnet der Begriff "C1-3-Alkylen" eine wie oben definierte
Alkylen-Gruppe, die mindestens 1 bzw. höchstens 3 Kohlenstoffatome
enthält.
Beispiele für "C1-3-Alkylen"-Gruppen, die nützlich in der
vorliegenden Erfindung sind, schließen uneingeschränkt Methylen,
Ethylen und n-Propylen ein.
-
Wie
hier verwendet bezeichnet der Begriff "Halogen" Fluor (F), Chlor (Cl), Brom (Br) oder
Iod (I) und der Begriff "Halogen" bezeichnet die Halogenradikale
Fluor (-F), Chlor (-Cl), Brom (-Br) und Iod (-I).
-
Wie
hier verwendet bezeichnen die Begriffe "C1-2-Halogenalkyl", "C1-3-Halogenalkyl", "C1-4-Halogenalkyl" und "C1-6-Halogenalkyl" eine wie oben definierte
Alkyl-Gruppe, die mindestens 1 und höchstens 2, 3, 4 bzw. 6 Kohlenstoffatome
enthält,
die mit mindestens einer Halogen-Gruppe substituiert sind, wobei
das Halogen wie hier definiert ist. Beispiele für solche verzweigtkettigen
oder geradkettigen Halogenalkyl-Gruppen, die nützlich in der vorliegenden
Erfindung sind, schließen
uneingeschränkt
Methyl, Ethyl, Propyl, Isopropyl, Isobutyl und n-Butyl ein, die
unabhängig
mit einem oder mehreren Halogenen, z.B. Fluor, Chlor, Brom und Iod,
substituiert sind.
-
Wie
hier verwendet, bezeichnet der Begriff "Cycloalkyl" einen nichtaromatischen cyclischen
Kohlenwasserstoffring. In ähnlicher
Weise bezeichnet der Begriff "C3-7-Cycloalkyl" einen nicht-aromatischen cyclischen
Kohlenwasserstoffring mit 3 bis 7 Kohlenstoffatomen, der gegebenenfalls
eine C1-6-Alkyl-Verknüpfung einschließt, durch
die er angehängt
sein kann. Die C1-6-Alkyl-Gruppe ist wie
oben definiert. Beispielhafte "C3-7-Cycloalkyl"-Gruppen, die nützlich in der vorliegenden
Erfindung sind, schließen
uneingeschränkt
Cyclopropyl, Cyclobutyl, Cyclopentyl, Cyclohexyl und Cycloheptyl
ein.
-
Wie
hier verwendet bezeichnet der Begriff "heterocyclisch" oder der Begriff "Heterocyclyl" einen nicht-aromatischen Heterocyclylring
mit 3 bis 12 Gliedern, der gesättigt
ist oder einen oder mehrere Grade an Unsättigung hat, der ein oder mehrere
Heteroatomsubstitutionen enthält,
die aus S, S(O), S(O)2, O oder N ausgewählt sind,
gegebenenfalls substituiert mit Substituenten, die aus der Gruppe
ausgewählt
sind, die C1-6-Alkyl, C1-6- Alkoxy, C1-6-Alkylsulfanyl, C1-6-Alkylsulfenyl,
C1-6-Alkylsulfonyl, Oxo, Hydroxy, Mercapto,
Amino, das gegebenenfalls mit Alkyl substituiert ist, Carboxy, Carbamoyl,
das gegebenenfalls mit Alkyl substituiert ist, Aminosulfonyl, das
gegebenenfalls mit Alkyl substituiert ist, Nitro, Cyano, Halogen
oder C1-6-Perfluoralkyl besteht, wobei mehrere
Grade an Substitution möglich
sind. Solch ein Ring kann gegebenenfalls an einen oder mehrere andere "heterocyclische(n)" Ring(e) oder Cycloalkylring(e)
kondensiert sein. Beispiele für "heterocyclische" Reste schließen uneingeschränkt Tetrahydrofuran,
Pyran, 1,4-Dioxan, 1,3-Dioxan, Piperidin, Piperazin, 2,4-Piperazindion,
Pyrrolidin, Imidazolidin, Pyrazolidin, Morpholin, Thiomorpholin,
Tetrahydrothiopyran, Tetrahydrothiophen und dgl. ein.
-
Wie
hier verwendet bezieht sich der Begriff "Aryl" auf
einen gegebenenfalls substituierten Benzolring oder auf ein gegebenenfalls
substituiertes Benzolringsystem, das mit einem oder mehreren gegebenenfalls substituierten
Benzolringen kondensiert ist, um zum Beispiel Anthracen-, Phenanthren-
oder Naphthalinringsysteme zu bilden. Beispielhafte optionale Substituenten
schließen
C1-6-Alkyl, C1-6-Alkoxy,
C1-6-Halogenalkyl, C1-6-Halogenalkoxy, C1-6-Alkylsulfanyl, C1-6-Alkylsulfenyl,
C1-6-Alkylsulfonyl, C1-6-Alkylsulfonylamino,
Arylsulfonoamino, Alkylcarboxy, Alkylcarboxyamid, Oxo, Hydroxy,
Mercapto, Amino, das gegebenenfalls mit Alkyl oder Acyl substituiert
ist, Carboxy, Tetrazolyl, Carbamoyl, das gegebenenfalls mit Alkyl,
Aryl oder Heteroaryl substituiert ist, Aminosulfonyl, das gegebenenfalls
mit Alkyl substituiert ist, Acyl, Aroyl, Aroylamino, Heteroaroyl,
Acyloxy, Aroyloxy, Heteroaroyloxy, Alkoxycarbonyl, Nitro, Cyano,
Halogen, Heteroaryl, Heterocyclyl, Aryl, das gegebenenfalls mit
Aryl, Halogen, C1-6-Alkyl, C1-6-Halogenalkyl
oder C1-6-Alkylsulfonyl substituiert ist,
Ureido, Arylharnstoff, Alkylharnstoff, Cycloalkylharnstoff, Alkylthioharnstoff,
Aryloxy oder Aralkoxy ein, wobei mehrere Grade an Substitution möglich sind.
Beispiele für "Aryl"-Gruppen schließen uneingeschränkt Phenyl,
2-Naphthyl, 1-Naphthyl, Biphenyl sowie substituierte Derivate davon
ein.
-
Wie
hier verwendet bezieht sich der Begriff "Aralkyl" auf eine Aryl- oder Heteroaryl-Gruppe, wie hier definiert,
die durch einen C1-3-Alkylenlinker verknüpft ist,
worin das C1-3-Alkylen wie hier definiert
ist. Beispiele für "Aralkyl" schließen uneingeschränkt Benzyl,
Phenylpropyl, 2-Pyridylmethyl, 3-Isoxazolylmethyl, 5-Methyl, 3-Isoxazolylmethyl
und 2-Imidazoylethyl ein.
-
Wie
hier verwendet bezieht sich der Begriff "Heteroaryl" auf einen monocyclischen aromatischen
Ring mit 5 bis 7 Gliedern oder auf ein kondensiertes bicyclisches
oder tricyclisches aromatisches Ringsystem, das zwei solcher monocyclischen
aromatischen Ringe mit 5 bis 7 Gliedern umfaßt. Diese Heteroarylringe enthalten ein
oder mehrere Stickstoff-, Schwefelund/oder Sauerstoffheteroatome,
wobei N-Oxide und Schwefeloxide und Dioxide zulässige Heteroatomsubstituenten
sind, und gegebenenfalls mit bis zu drei Mitgliedern substituiert
sein können,
die aus der Gruppe ausgewählt
sind, die aus C1-6-Alkyl, C1-6-Alkoxy,
C1-6-Alkylsulfanyl, C1-6-Alkylsulfenyl,
C1-6-Alkylsulfonyl, Oxo, Hydroxy, Mercapto,
Amino, das gegebenenfalls mit Alkyl substituiert ist, Carboxy, Tetrazolyl,
Carbamoyl, das gegebenenfalls mit Alkyl substituiert ist, Aminosulfonyl,
das gegebenenfalls mit Alkyl substituiert ist, Acyl, Aroyl, Heteroaroyl,
Acyloxy, Aroyloxy, Heteroaroyloxy, Alkoxycarbonyl, Nitro, Cyano,
Halogen, C1-6-Perfluoralkyl, Heteroaryl
oder Aryl besteht, wobei mehrere Grade an Substitution möglich sind.
Beispiel für
hier verwendete "Heteroaryl"-Gruppen schließen Furanyl,
Thiophenyl, Pyrrolyl, Imidazolyl, Pyrazolyl, Triazolyl, Tetrazolyl,
Thiazolyl, Oxazolyl, Isoxazolyl, Oxadiazolyl, Oxopyridyl, Thiadiazolyl,
Isothiazolyl, Pyridyl, Pyridazyl, Pyrazinyl, Pyrimidyl, Chinolinyl,
Isochinolinyl, Benzofuranyl, Benzothiophenyl, Indolyl, Indazolyl
und substituierte Versionen davon ein.
-
Wie
hier verwendet bezieht sich der Begriff "Alkoxy" auf die Gruppe RaO-,
worin Ra ein wie oben definiertes Alkyl
ist, und der Begriff "C1-6-Alkoxy" bezieht sich auf
eine wie hier definierte Alkoxy-Gruppe, worin der Alkyl-Rest mindestens
ein 1 und höchstens
6 Kohlenstoffatome enthält.
Beispielhafte C1-6-Alkoxy-Gruppen, die in
der vorliegenden Erfindung nützlich
sind, schließen
uneingeschränkt
Methoxy, Ethoxy, n-Propoxy, Isopropoxy, n-Butoxy und t-Butoxy ein.
-
Wie
hier verwendet bezieht sich der Begriff "Amino" auf die Gruppe -NH2.
-
Wie
hier verwendet bezieht sich der Begriff "Alkylamino" auf die Gruppe -NHRa,
worin Ra ein wie oben definiertes Alkyl
ist.
-
Wie
hier verwendet bezieht sich der Begriff "arylamino" auf die Gruppe -NHRa,
worin Ra ein wie oben definiertes Aryl ist.
-
Wie
hier verwendet bezieht sich der Begriff "Aralkylamino" auf die Gruppe -NHRa,
worin Ra eine wie oben definierte Aralkyl-Gruppe
ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Aralkoxy" auf die Gruppe RbRaO-, worin Ra Alkylen
ist und Rb alle wie oben definierten Aryl- oder Heteroaryl-Gruppen
ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Aryloxy" auf die Gruppe RaO-,
worin Ra Aryl oder Heteroaryl ist, wobei
beide wie oben definiert sind.
-
Wie
hierin verwendet bezieht sich der Begriff "Ureido" auf die Gruppe -NHC(O)NH2.
-
Wie
hierin verwendet bezieht sich der Begriff "Arylharnstoff" auf die Gruppe -NHC(O)NHRa,
worin Ra ein wie oben definiertes Aryl ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Arylthioharnstoff" auf die Gruppe -NHC(S)NHRa,
worin Ra ein wie oben definiertes Aryl ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Alkylharnstoff" auf die Gruppe -NHC(O)NHRa,
worin Ra ein wie oben definiertes Alkyl
ist.
-
Wie
hier verwendet bezieht sich der Begriff "Cycloalkylharnstoff" auf die Gruppe -NHC(O)NHRa,
worin Ra ein wie oben definiertes Cycloalkyl
ist.
-
Wie
hierin verwendet bezieht sich der Begriff "C3-7-Cycloalkoxy" auf die Gruppe RaO-, worin Ra ein
wie oben definiertes C3-7-Cycloalkyl ist.
Beispielhafte C3-7-Cycloalkoxy-Gruppen,
die in der vorliegenden Erfindung nützlich sind, schließen uneingeschränkt Cyclobutoxy
und Cyclopentoxy ein.
-
Wie
hierin verwendet bezieht sich der Begriff "Halogenalkoxy" auf die Gruppe RaO-,
worin Ra ein wie oben definiertes Halogenalkyl
ist, und der Begriff "C1-6-Halogenalkoxy" bezieht sich auf eine wie hier definierte Halogenalkoxy-Gruppe,
worin der Halogenalkyl-Rest mindestens 1 und höchstens 6 Kohlenstoffatome
enthält. Beispielhafte
C1-6-Halogenalkoxy-Gruppen, die in der vorliegenden Erfindung
nützlich
sind, schließen
uneingeschränkt
Trifluormethoxy ein.
-
Wie
hierin verwendet bezieht sich der Begriff "Alkylsulfanyl" auf die Gruppe RaS-,
worin Ra ein wie oben definiertes Alkyl
ist, und der Begriff "C1-6-Alkylsulfanyl" bezieht sich auf eine wie hier definierte
Alkylsulfanyl-Gruppe, worin der Alkylrest mindestens 1 und höchstens
6 Kohlenstoffatome enthält.
-
Wie
hierin verwendet bezieht sich der Begriff "Halogenalkylsulfanyl" auf die Gruppe RaS-,
worin Ra ein wie oben definiertes Halogenalkyl
ist, und der Begriff "C1-6-Halogenalkylsulfanyl" bezieht sich auf eine wie hier definierte
Halogenalkylsulfanyl-Gruppe, worin der Alkylrest mindestens 1 und
höchstens
6 Kohlenstoffatome enthält.
-
Wie
hier verwendet bezieht sich der Begriff "Alkylsulfenyl" auf die Gruppe RSS(O)-,
worin Ra ein wie oben definiertes Alkyl
ist, und der Begriff "C1-6-Alkylsulfenyl" bezieht sich auf eine wie hier definierte
Alkylsulfenyl-Gruppe, worin der Alkylrest mindestens 1 und höchstens
6 Kohlenstoffatome enthält.
-
Wie
hierin verwendet bezieht sich der Begriff "Alkylsulfonyl" auf die Gruppe RaS(O)2-, worin Ra ein
wie oben definiertes Alkyl ist, und der Begriff "C1-6-Alkylsulfonyl" bezieht sich auf
eine wie hier definierte Alkylsulfonyl-Gruppe, worin der Alkyl-Rest
mindestens 1 und höchstens
6 Kohlenstoffatome enthält.
-
Wie
hierin verwendet bezieht sich der Begriff "Alkylsulfonylamino" auf die Gruppe -NHS(O)2Ra, worin Ra ein wie
oben definiertes Alkyl ist, und der Begriff "C1-6-Alkylsulfonylamino" bezieht sich auf
eine wie hier definierte Alkylsulfonylamino-Gruppe, worin der Alkylrest
mindestens 1 und höchstens
6 Kohlenstoffatome enthält.
-
Wie
hierin verwendet bezieht sich der Begriff "Arylsulfonylamino" auf die Gruppe -NHS(O)2Ra, worin Ra ein wie
oben definiertes Aryl ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Alkylcarboxyamid" auf die Gruppe -NHC(O)Ra,
worin Ra ein wie oben definiertes Alkyl,
Amino oder Amino ist, das mit Alkyl, Aryl oder Heteroaryl substituiert
ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Alkylcarboxy" auf die Gruppe -C(O)Ra,
worin Ra ein wie oben beschriebenes Alkyl
ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Oxo" auf
die Gruppe =O.
-
Wie
hierin verwendet bezieht sich der Begriff "Mercapto" auf die Gruppe -SH.
-
Wie
hierin verwendet bezieht sich der Begriff "Carboxy" auf die Gruppe -C(O)OH.
-
Wie
hierin verwendet bezieht sich der Begriff "Cyano" auf die Gruppe -CN.
-
Wie
hierin verwendet bezieht sich der Begriff "Cyanoalkyl" auf die Gruppe -CNRa,
worin Ra ein wie oben definiertes Alkyl
ist. Beispielhafte "Cyanoalkyl"-Gruppen, die in
der vorliegenden Erfindung nützlich
sind, schließen
uneingeschränkt
Cyanomethyl, Cyanoethyl und Cyanoisopropyl ein.
-
Wie
hierin verwendet bezieht sich der Begriff "Aminosulfonyl" auf die Gruppe -S(O)2NH2.
-
Wie
hier verwendet bezieht sich der Begriff "Carbamoyl" auf die Gruppe -C(O)NH2.
-
Wie
hier verwendet bezieht sich der Begriff "Sulfanyl" auf die Gruppe -S-.
-
Wie
hierin verwendet bezieht sich der Begriff "Sulfenyl" auf die Gruppe -S(O)-.
-
Wie
hierin verwendet bezieht sich der Begriff "Sulfonyl" auf die Gruppe -S(O)2-
oder -SO2-.
-
Wie
hierin verwendet bezieht sich der Begriff "Acyl" auf
die Gruppe RaC(O)-, worin Ra ein
wie hier definiertes Alkyl, Cycloalkyl oder Heterocyclyl ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Aroyl" auf die Gruppe RaC(O)-,
worin Ra ein wie hier definiertes Aryl ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Aroylamino" auf die Gruppe RaC(O)NH-,
worin Ra ein wie hier definiertes Aryl ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Heteroaroyl" auf die Gruppe RaC(O)-,
worin Ra ein wie hier definiertes Heteroaryl
ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Alkoxycarbonyl" auf die Gruppe RaOC(O)-,
worin Ra ein wie hier definiertes Alkyl
ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Acyloxy" auf die Gruppe RaC(O)O-,
worin Ra ein wie hier definiertes Alkyl,
Cycloalkyl oder Heterocyclyl ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Aroyloxy" auf die Gruppe RaC(O)O-,
worin Ra ein wie hier definiertes Aryl ist.
-
Wie
hierin verwendet bezieht sich der Begriff "Heteroaryloxy" auf die Gruppe RaC(O)O-,
worin Ra ein wie hier definiertes Heteroaroyl
ist.
-
Wie
hierin verwendet bedeutet der Begriff "gegebenenfalls", daß die nachfolgend beschriebenen
Ereignisse auftreten können
oder nicht, und schließt
sowohl Ereignisse, die auftreten, als auch Ereignisse, die nicht
auftreten, ein.
-
Wie
hier verwendet bezieht sich der Begriff "Solvat" auf einen Komplex von variabler Stöchiometrie, der
durch einen gelösten
Stoff (in dieser Erfindung eine Verbindung der Formel (I) oder ein
Salz davon) und einem Lösungsmittel
gebildet wird. Solche Lösungsmittel
können
zum Zwecke der Erfindung nicht die biologische Aktivität des gelösten Stoffs
stören.
Beispiele für
geeignete Lösungsmittel
schließen
uneingeschränkt Wasser,
Methanol, Ethanol und Essigsäure
ein. Vorzugsweise ist das verwendete Lösungsmittel ein pharmazeutisch
annehmbares Lösungsmittel.
Beispiele für
geeignete pharmazeutisch annehmbare Lösungsmittel schließen uneingeschränkt Wasser,
Ethanol und Essigsäure
ein. Am meisten bevorzugt ist das verwendete Lösungsmittel Wasser.
-
Wie
hier verwendet bezieht sich der Begriff "substituiert" auf eine Substitution mit dem bezeichneten Substituent
oder Substituenten, wobei mehrere Grade an Substitution, sofern
nicht anders angegeben, möglich
sind.
-
Bestimmte
der hier beschriebenen Verbindungen können ein oder mehrere chirale
Atome enthalten oder können
andererseits in der Lagesein, als zwei Enantiomere vorzuliegen.
Die Verbindungen dieser Erfindung schließen Gemische von Enantiomeren
als auch aufgereinigte Enantiomere oder enantiomerisch angereicherte
Gemische ein. Ebenfalls vom Schutzumfang der Erfindung eingeschlossen
sind die individuellen Isomere der Verbindungen, die durch die oben
angegebene Formel (I) dargestellt sind, als auch jede vollständig oder
partiell äquilibrierten
Gemische davon ein. Die vorliegende Erfindung umfaßt ebenfalls
die individuellen Isomere der Verbindung, die durch die oben angegebenen
Formeln dargestellt sind, als Gemische mit Isomeren davon, worin
ein oder mehrere chirale Zentren invertiert sind. Ebenfalls ist
es verständlich,
daß jede
Tautomere und Gemische von Tautomeren der Verbindungen der Formel
(I) im Umfang der Verbindungen der Formel (I) eingeschlossen sind.
-
Es
ist selbstverständlich,
daß der
Verweis auf Verbindungen der oben angegebenen Formeln (I) und (II)
sich auf Verbindungen innerhalb des Umfangs der oben definierten
Formeln (I) und (II) hinsichtlich D, Q1, Q2, Q3, A1,
A2, Z, Z1, Z2, R1, R2,
R3, R4, R5, R6, R7,
R8 und R9 beziehen,
sofern nicht andersweitig spezifisch eingeschränkt.
-
In
einer Ausführungsform
ist D -NRR1. In einer Ausführungsform
ist D -NRR1, worin R C1-8-Alkyl,
Aryl oder Aralkyl ist und R1 Wasserstoff
ist. In einer bevorzugten Ausführungsform
ist D -NRR1, worin R Methyl, Isopropyl,
Benzyl oder Phenyl ist und R1 Wasserstoff
ist. In einer anderen Ausführungsform
ist D -NRR1, worin R Wasserstoff, C1-8-Alkyl, C3-7-Cycloalkyl
ist. In einer anderen Ausführungsform
ist D -NRR1, worin C3-7-Cycloalkyl ist.
In einer weiteren Ausführungsform
ist D -NRR1, worin R -C(O)NR1R1 ist. In einer anderen Ausführungsform ist
D -NRR1, worin R C(O)OR1 ist.
In noch einer anderen Ausführungsform
ist D -NRR1, worin R Acyl ist. In einer anderen
Ausführungsform
ist D -NRR1, worin R Aroyl ist. In noch
einer anderen Ausführungsform
ist D -NRR1, worin R Heteroaroyl ist.
-
In
einer anderen Ausführungsform
ist R2 C1-8-Alkyl.
In einer bevorzugten Ausführungsform
ist R2 Methyl.
-
In
einer Ausführungsform
ist R3 Wasserstoff, C1-4-Alkyl,
Cyanoalkyl oder -(CH2)pC≡C(CH2)tH. In einer bevorzugten
Ausführungsform
ist R3 Wasserstoff, Methyl, Ethyl, Isopropyl,
Cyanomethyl oder -(CH2)pC≡C(CH2)tH, worin p 1 ist
und t 0 ist. In einer besonders bevorzugten Ausführungsform ist R3 Methyl.
-
In
einer Ausführungsform
ist R4 Wasserstoff oder Halogen. In einer
bevorzugten Ausführungsform
ist R4 Wasserstoff.
-
In
einer anderen Ausführungsform
ist Q1 Wasserstoff, Halogen, C1-2-Alkyl oder C1-2-Alkoxy. In einer bevorzugten Ausführungsform
ist Q1 Wasserstoff, Chlor, Methyl oder Methoxy.
-
In
einer Ausführungsform
ist Q2 A1 und Q3 ist A2. In einer
alternativen Ausführungsform
ist Q2A2 und Q3 ist A1.
-
In
einer Ausführungsform
ist Q2 A2 und Q3 ist A1, worin A1 Wasserstoff, Halogen oder C1-3-Halogenalkyl ist
und A2 die Gruppe ist, die durch -(Z)m-(Z1)-(Z2) definiert ist, worin Z CH2 ist
und m 0 oder 1 ist; Z1 S(O)2 ist; und Z2 C1-4-Alkyl oder
NR8R9 ist, und worin
R8 Wasserstoff, C1-4-Alkyl
oder Alkoxy ist und R9 Wasserstoff, C1-4-Alkyl oder Alkoxy ist. In einer bevorzugten
Ausführungsform
ist Q2 A2 und Q3 ist A1, worin A1 Wasserstoff oder Chlor ist und A2 die Gruppe ist, die durch -(Z)m-(Z1)-(Z2) definiert
ist, worin Z CH2 ist und m 0 oder 1 ist;
Z1 S(O)2 ist; und
Z2 Methyl oder -NH2 ist.
-
In
einer Ausführungsform
is Q2 A1 und Q3 ist A2, worin A1 Wasserstoff, Halogen oder C1-3-Alkyl
ist und A2 die Gruppe ist, die durch -(Z)m-(Z1)-(Z2) definiert ist, worin Z CH2 ist
und m 0 oder 1 ist; Z1 S(O)2 ist; und Z2 C1-4-Alkyl oder
NR8R9 ist, und worin
R8 Wasserstoff, C1-4-Alkyl
oder Alkoxy ist und R9 Wasserstoff, C1-4-Alkyl oder Alkoxy ist. In einer bevorzugten
Ausführungsform
ist Q2 A1 und Q3 ist A2, worin A1 Wasserstoff, Methyl oder Chlor ist und
A2 die Gruppe ist, die durch -(Z)m-(Z1)-(Z2) definiert ist, worin Z CH2 ist
und m 0 oder 1 ist; 21 S(O)2 ist;
und Z2 NR8R9 ist,
worin R8 Methoxy ist und R9 Wasserstoff
ist.
-
In
einer bevorzugten Ausführungsform
ist D -NRR1, worin R C1-8-Alkyl,
Aryl oder Aralkyl ist und R1 Wasserstoff
ist; R2 C1-8-Alkyl
ist; R2 Methyl ist; R3 Methyl
ist; R4 Wasserstoff ist; Q1 Wasserstoff,
Chlor, Methyl oder Methoxy ist; Q2 A2 ist und Q3 A1 ist, worin A1 Wasserstoff
oder Chlor ist und A2 die Gruppe ist, die
durch -(Z)m-(Z1)-(Z2) definiert ist, worin Z CH2 ist
und m 0 oder 1 ist; Z1 S(O)2 ist;
und Z2 Methyl oder -NH2 ist.
-
In
einer bevorzugten Ausführungsform
ist D -NRR1, worin R C1-8-Alkyl,
Aryl oder Aralkyl ist und R1 Wasserstoff
ist; R2 C1-8-Alkyl
ist; R2 Methyl ist; R3 Methyl
ist; R4 Wasserstoff ist; Q1 Wasserstoff,
Chlor, Methyl oder Methoxy ist; Q2 A1 ist und Q3 ist
A2, worin A1 Wasserstoff,
Methyl oder Chlor ist und A2 die Gruppe
ist, die durch -(Z)m-(Z1)-(Z2) definiert ist, worin Z CH2 ist
und m 0 oder 1 ist; Z1 S(O)2 ist;
und Z2 NR8R9 ist, worin R8 Methoxy ist
und R9 Wasserstoff ist.
-
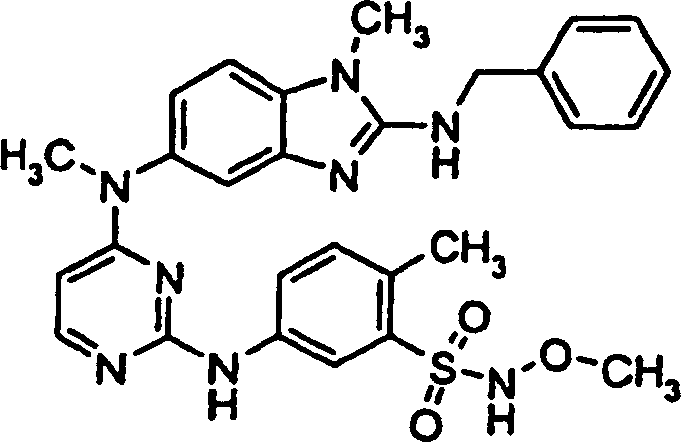
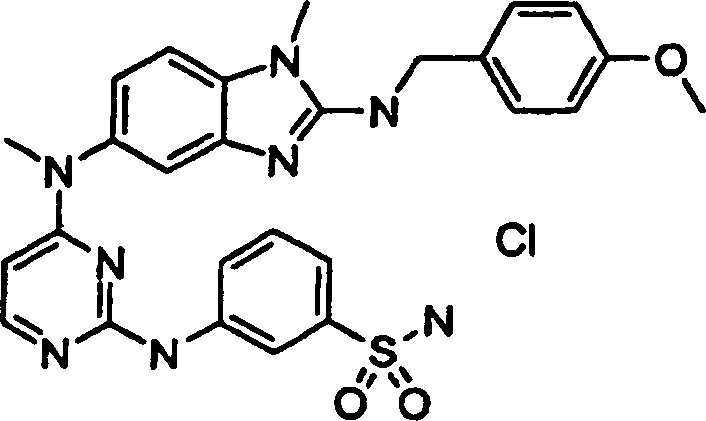
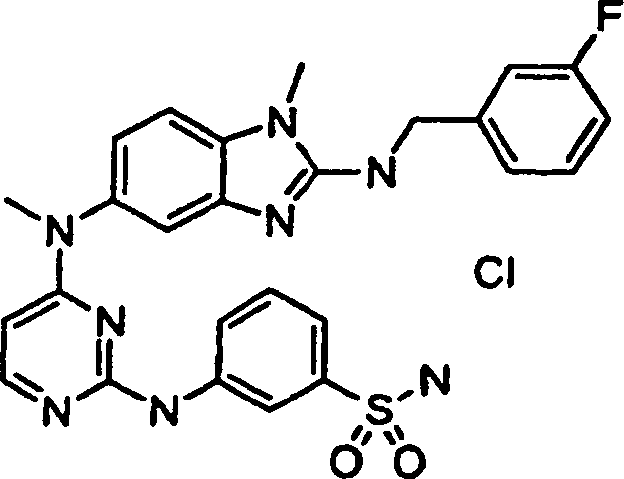
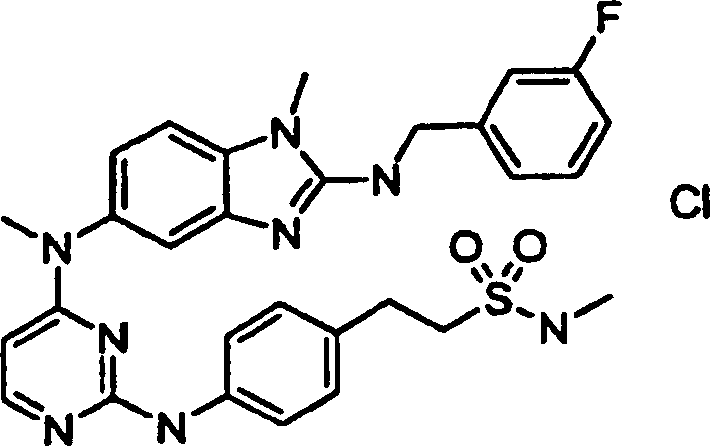
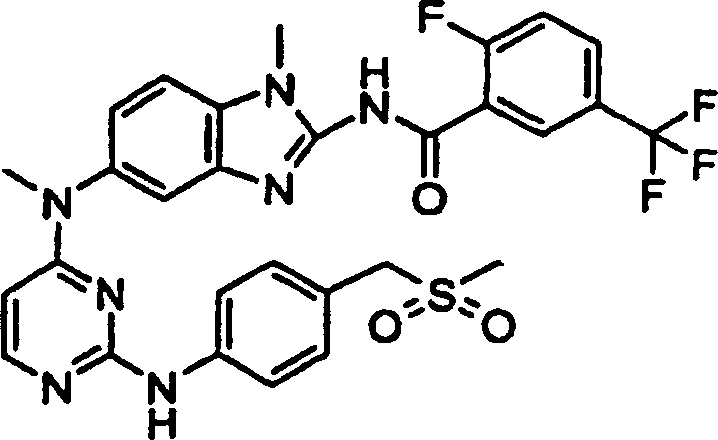
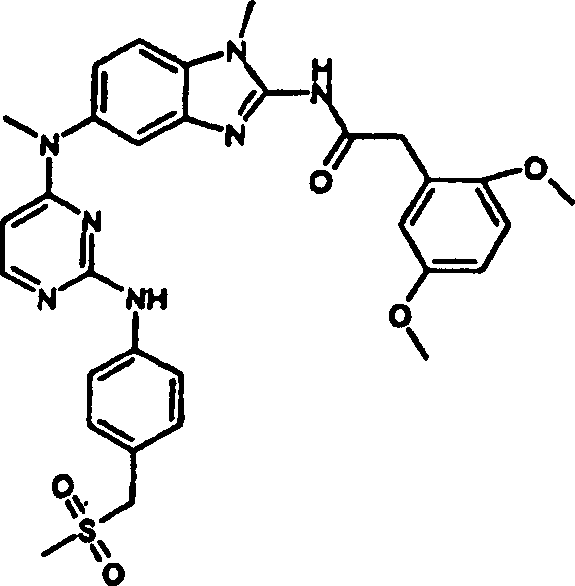
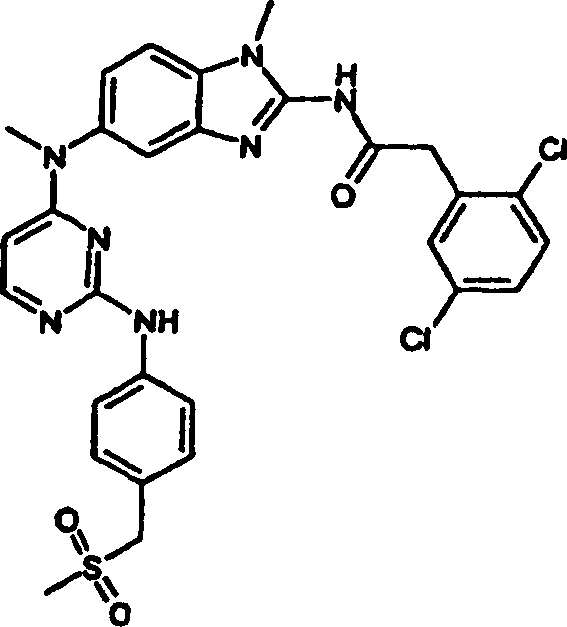
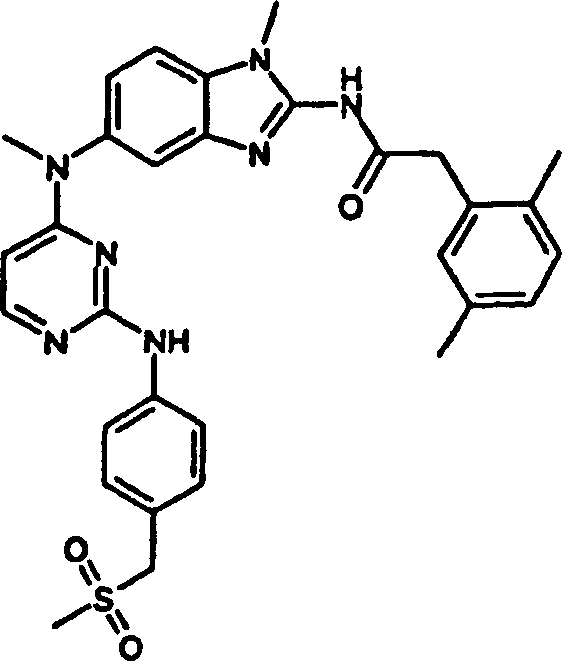
Besondere
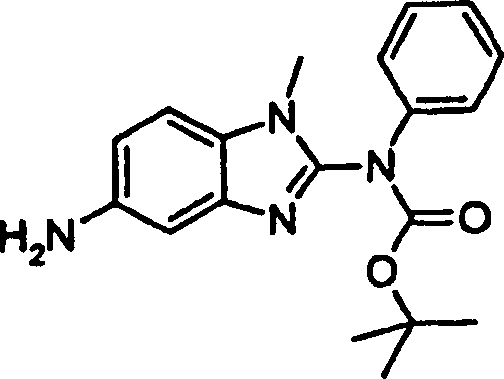
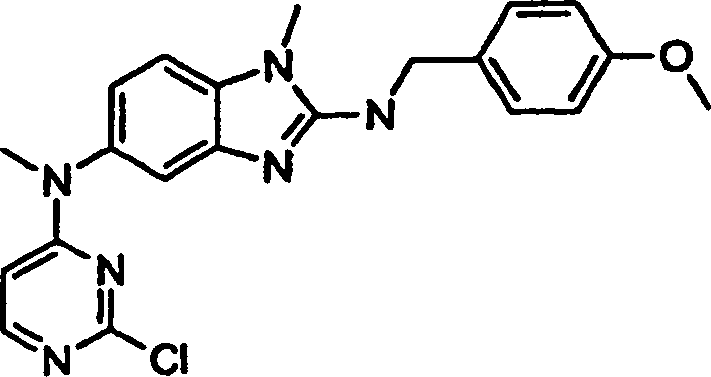
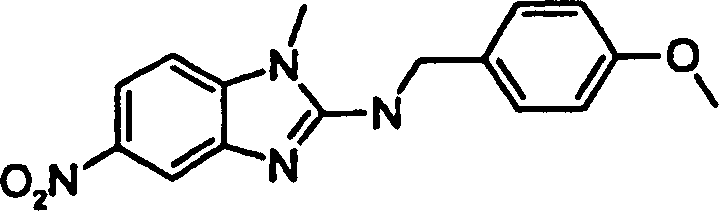
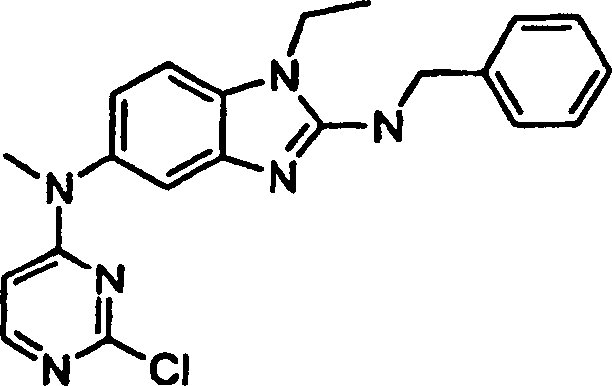
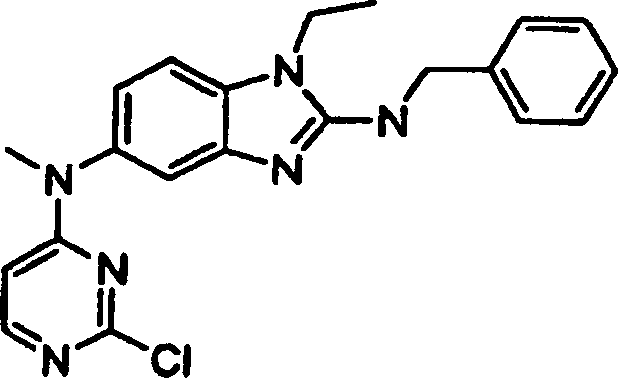
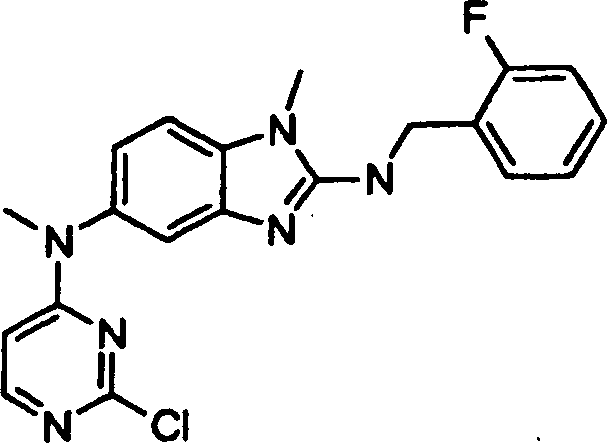
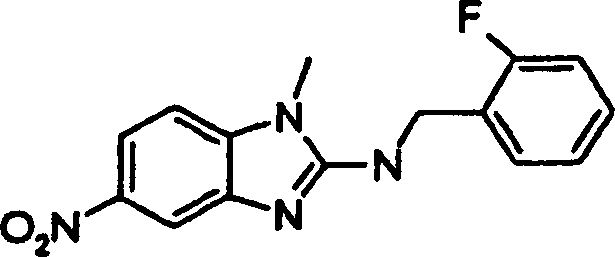
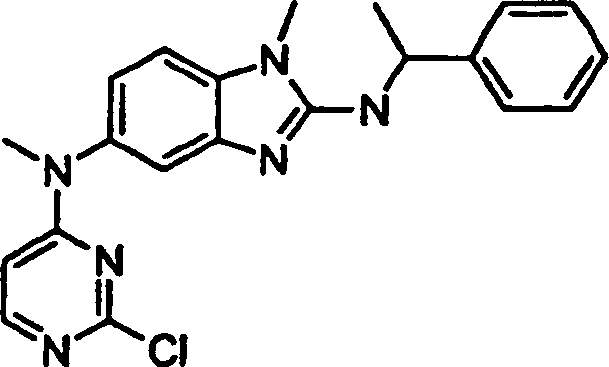
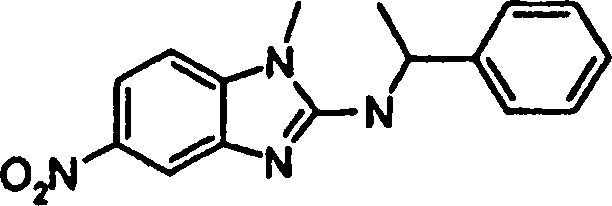
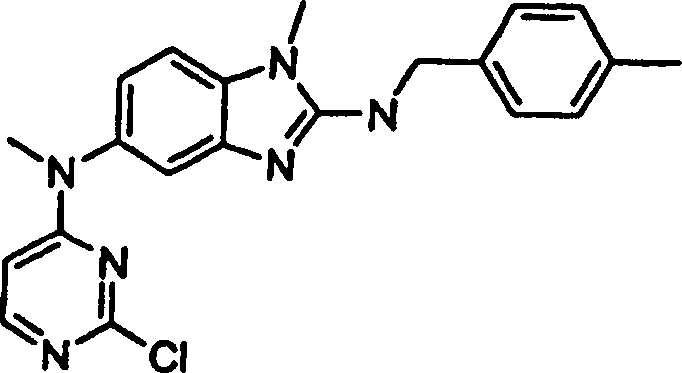
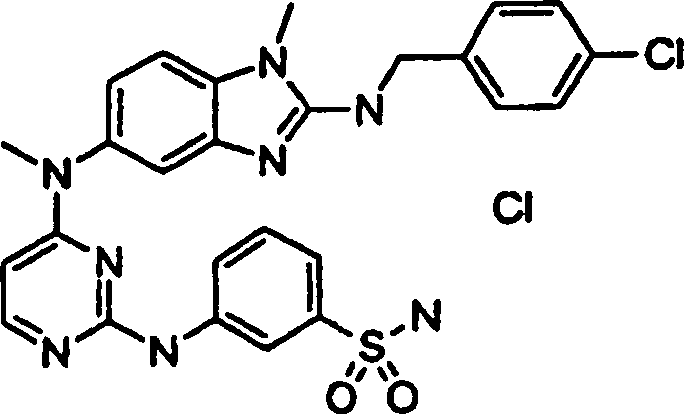
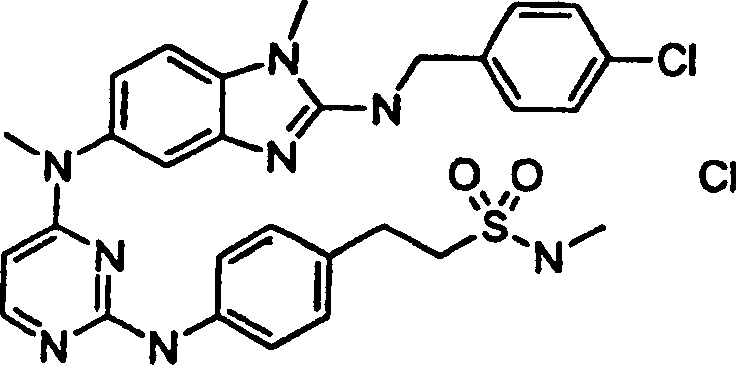
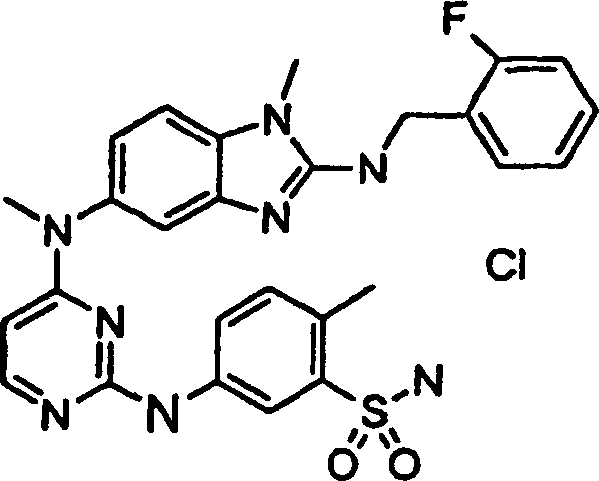
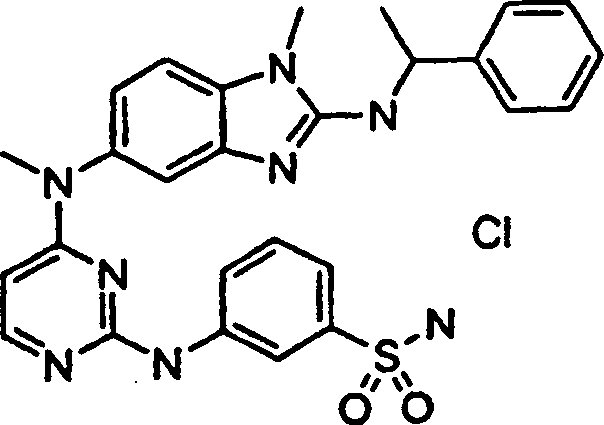
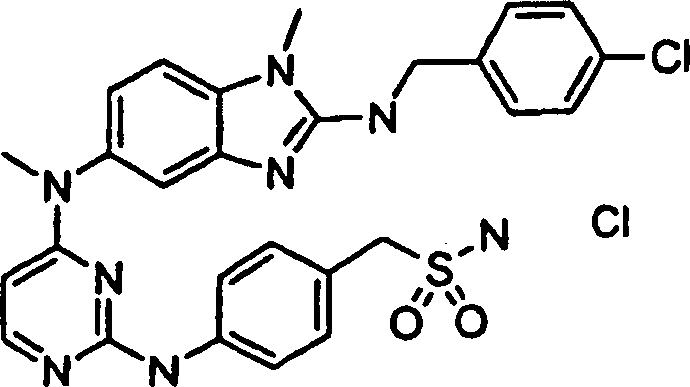
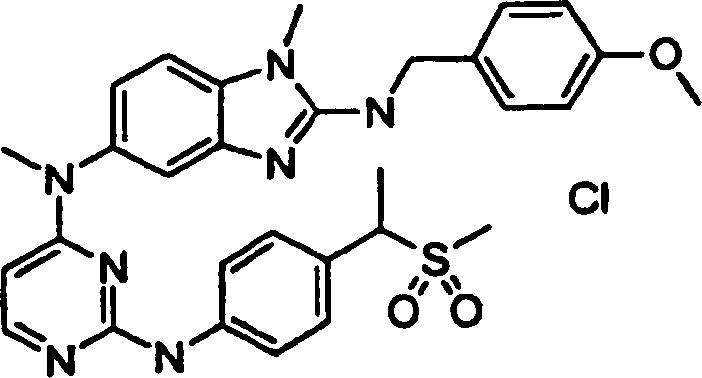
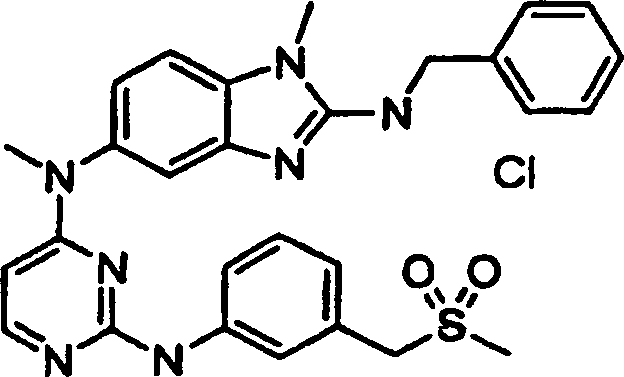
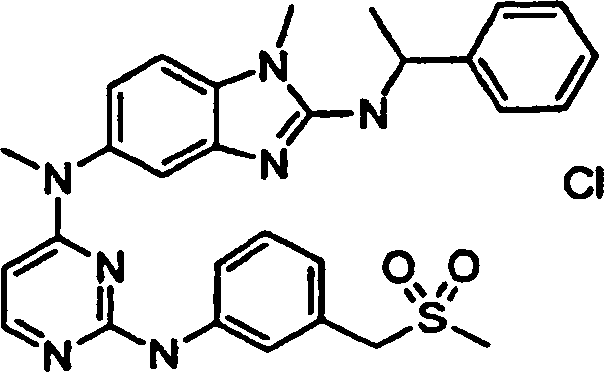
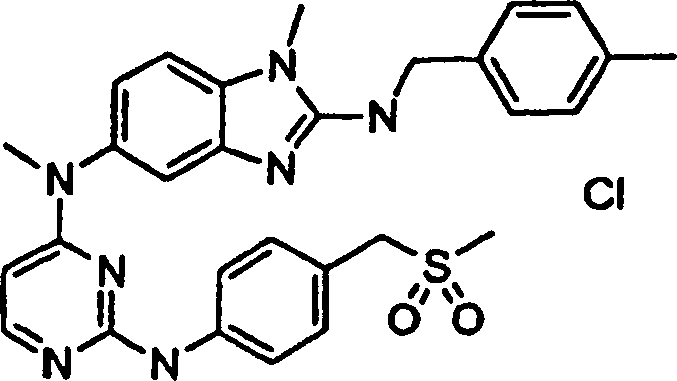
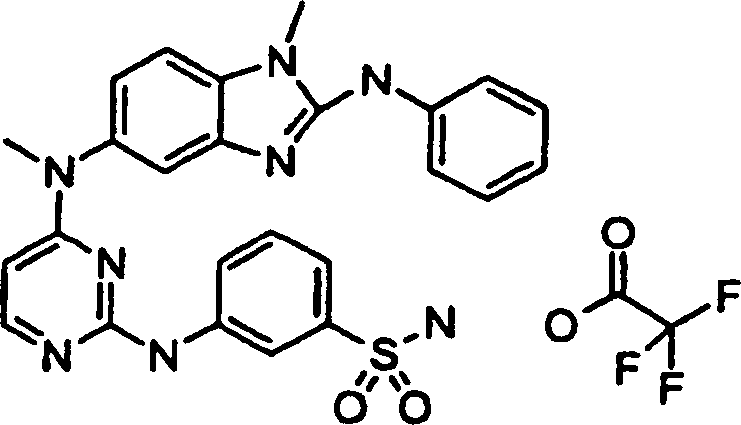
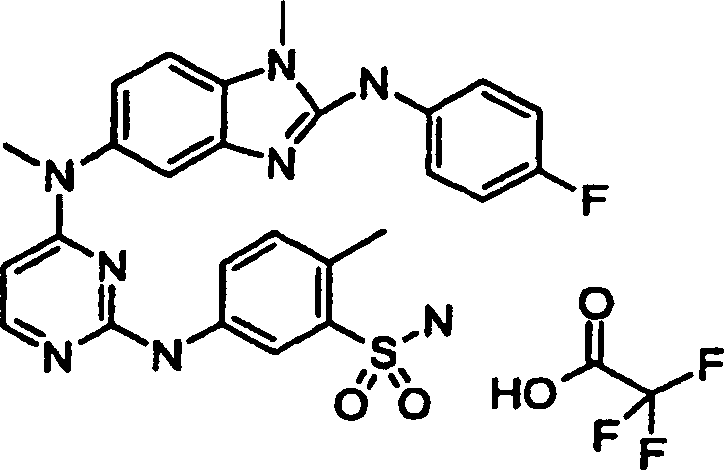
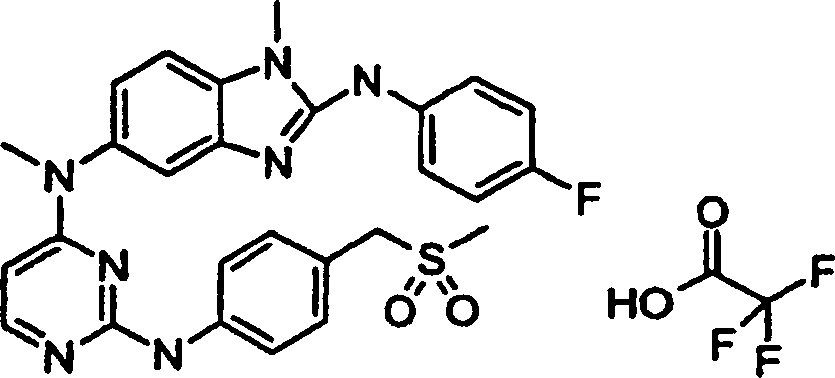
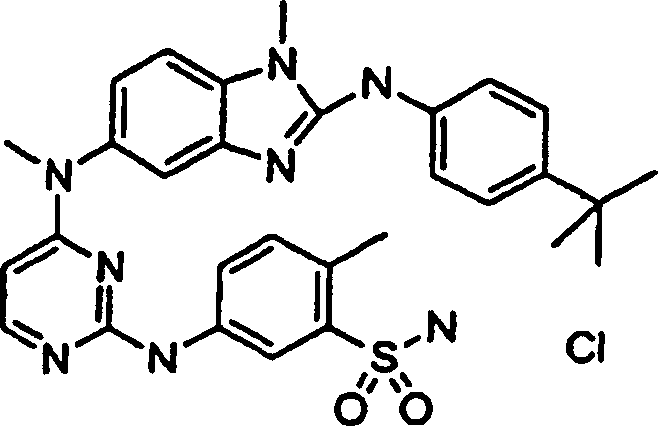
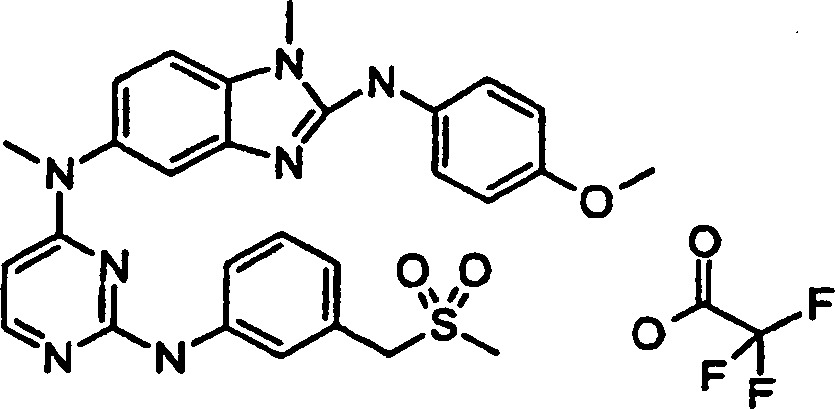
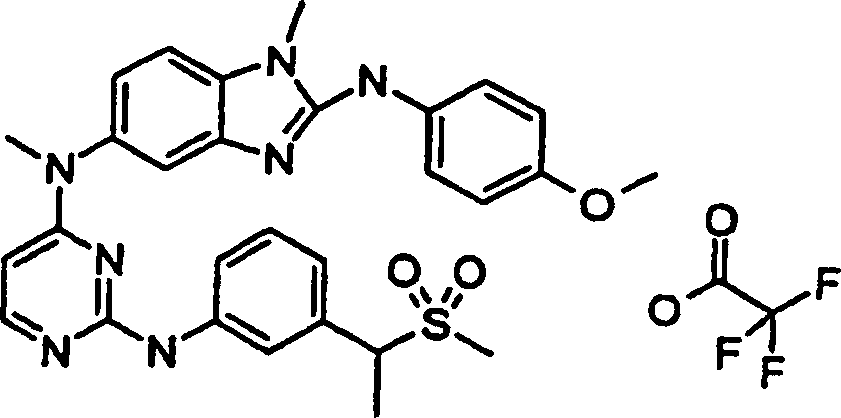
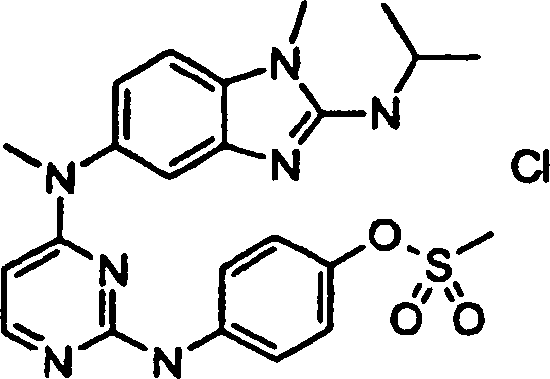
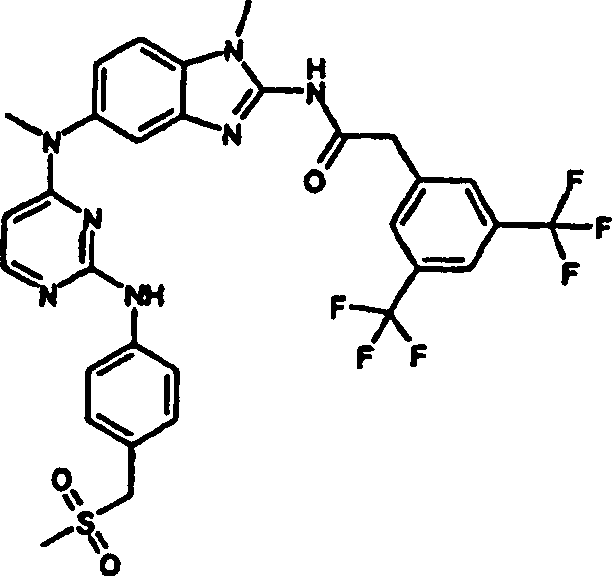
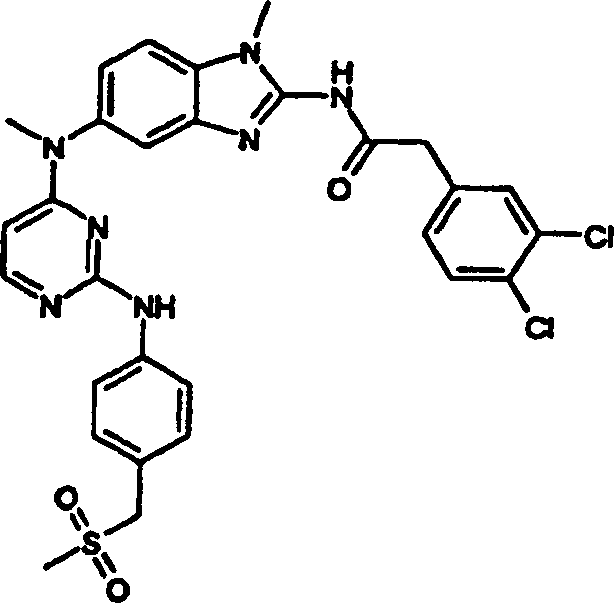
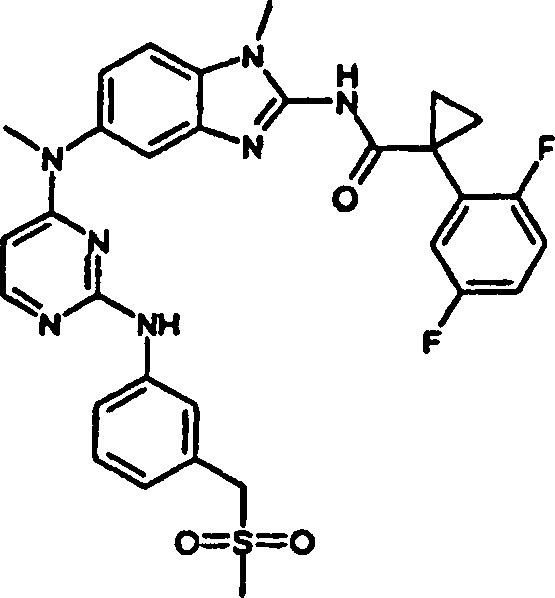
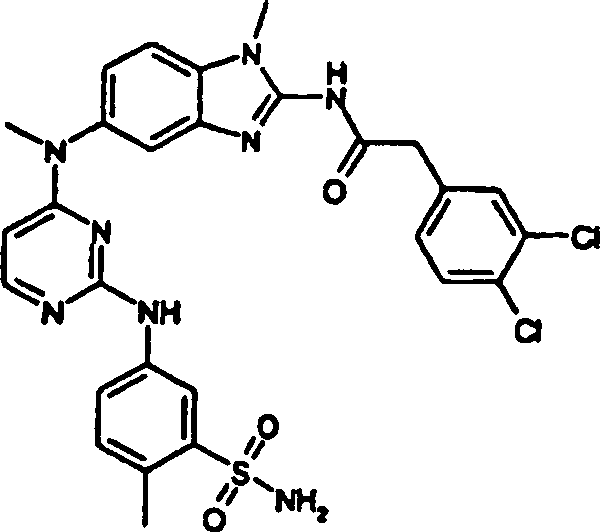
Beispiele der Verbindungen der vorliegenden Erfindung schließen die
folgenden ein:
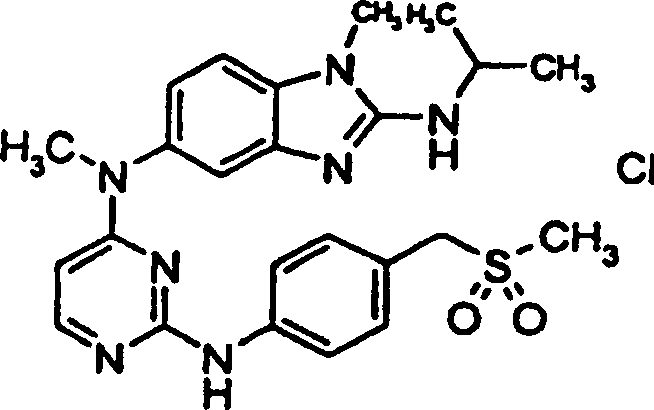
- N5,1-Dimethyl-N2-(1-methylethyl)-N5-[({4-[(methylsulfonyl)methyl]-phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
- 1-(4-{[4-(Methyl{1-methyl-2-[(1-methylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)methansulfonamidhydrochlorid,
- N2,N5,1-Trimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
- N5,1-Dimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N2-(phenylmethyl)-1H-benzimidazol-2,5-diaminhydrochlorid,
- N5,1-Dimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N2-phenyl-1H-benzimidazol-2,5-diamin,
- 2-Methyl-5-{[4-(methyl{1-methyl-2-[(Phenylmethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}-N-(methyloxy)benzolsulfonamid,
- 3-{[4-(Methyl{1-methyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamidhydrochlorid,
- 2-Methyl-5-{[4-(methyl{1-methyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamidhydrochlorid,
- 1-(4-{[4-(methyl{1-methyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)methansulfonamidhydrochlorid,
- N-Methyl-2-(4-{[4-(methyl{1-methyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)ethansulfonamidhydrochlorid,
- 3-({4-[(2-{[(4-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid,
- 5-({4-[(2-{[(4-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid,
- N2-[(4-Fluorphenyl)methyl]-N5,1-dimethyl-N5-[2-({4-[(methylsulfonyl)-methyl]phenyl}amino-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
- 1-[4-({4-[(2-{[(4-fluorpheriyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidhydrochlorid,
- 2-[4-({4-[(2-{[(4-fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyl]-N-methylethansulfonamidhydrochlorid,
- 3-[(4-(Methyl[1-methyl-2-({[4-(methyloxy)phenyl]methyl}amino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]benzolsulfonamidhydrochlorid,
- 2-Methyl-5-[(4-{methyl[1-methyl-2-({[4-(methyloxy)phenyl]methyl}amino-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]benzolsulfonamidhydrochlorid,
- N5,1-Dimethyl-N2{[4-(methyoxy)phenyl]methyl}-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
- 1-{4-[(4{Methyl[1-methyl-2-({[4-(methyloxy)phenyl]methyl}amino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino}phenyl}methansulfonamidhydrochlorid,
- N-Methyl-2-{4-[(4-{methyl[1-methyl-2-({[4-(methyloxy)phenyl]methyl}amino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]phenyl}ethansulfonamidhydrochlorid,
- 5-({4-[(2-{[(3-fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid,
- 3-({4-[(2-{[(3-fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid,
- N2[(3-Fluorphenyl)methyl]-N5,1-dimethyl-N5-[2-([4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
- 1-[4-({4[(2-{[(3-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidhydrochlorid,
- 2-[4-({4-[(2-{[(3-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyl]-N-methylethansulfonamidhydrochlorid,
- 3-({4-[(2-{[(4-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimdazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid,
- 5-({4-[(2-{[(4-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid,
- 2-[4-({4-[(2-{[(4-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimdazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyl]-N-methylethansulfonamidhydrochlorid,
- N2-[(4-Chlorphenyl)methyl]-N5,1-dimetyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diaminhydrochlorid,
- 3-({4-[{1-Ethyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid
- 5-({4-[{1-Ethyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid,
- 1-Ethyl-N5-methyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N2-(phenylmethyl)-1H-benzimidazol-2,5-diaminhydrochlorid,
- 1-[4-({4-[{1-Ethyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidhydrochlorid,
- 3-({4-[(2-{[(2-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid,
- 5-({4-[(2-{[(2-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid,
- 1-[4-({4-[(2-{[(2-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimdazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidhydrochlorid,
- 2-[4-({4-[{1-Ethyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)phenyl]-N-methylethansulfonamidhydrochlorid,
- 3-{[4-(Methyl{1-methyl-2-[(1-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamidhydrochlorid,
- 2-Methyl-5-{[4-(methyl{1-methyl-2-[(1-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamidhydrochlorid,
- N5,1-Dimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N2-(1-phenylethyl)-1H-benzimidazol-2,5-diaminhydrochlorid,
- 1-(4-{[4-(Methyl{1-methyl-2-[(1-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)methansulfonamidhydrochlorid,
- 3-([4-[(2-{[(3-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimdazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid,
- 5-([4-[(2-{[(3-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimdazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid,
- 1-[4-({4-[(2-{[(4-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidhydrochlorid,
- 3-({4-[(2-{[(4-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenylmethansulfonathydrochlorid,
- N5,1-Dimethyl-N2-{[4-(methyloxy)phenyl]methyl}-N5-[2-([4-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diaminhydrochlorid,
- N5,1-Dimethyl-N2-{[4-(methyloxy)phenyl]methyl}-N5-[2-({3-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diaminhydrochlorid,
- N5,1-Dimethyl-N2-{[4-(methyloxy)phenyl]methyl}-N5-[2-({4-[1-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diaminhydrochlorid,
- N5,1-Dimethyl-N2-{[4-(methyloxy)phenyl]methyl}-N5-[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diaminhydrochlorid,
- N5,1-Dimethyl-N5-[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N2-(phenylmethyl)-1H-benzimidazol-2,5-diaminhydrochlorid,
- N5,1-Dimethyl-N5-[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N2-(1-phenylethyl)-1H-benzimidazol-2,5-diaminhydrochlorid,
- N5,1-Dimethyl-N5-[2-({3-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-N2-(1-phenylethyl)-1H-benzimidazol-2,5-diaminhydrochlorid,
- N5,1-Dimethyl-N5-[2-({4-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-N2-(1-phenylethyl)-1H-benzimidazol-2,5-diaminhydrochlorid,
- 2-Methyl-5-({4-[methyl(1-methyl-2-{[(4-methylphenyl)methyl]amino}-1H-benzimidazol-5-yl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid,
- N5,1-Dimethyl-N2-[(4-methylphenyl)methyl]-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
- N5,1-Dimethyl-N2-[(4-methylphenyl)methyl]-N5-[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
- N5,1-Dimethyl-N2-[(4-methylphenyl)methyl]-N5-[2-({4-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
- N5,1-Dimethyl-N2-[(4-methylphenyl)methyl]-N5-[2-({3-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
- N5,1-Dimethyl-N2-[(4-methylphenyl)methyl]-N5-[2-({4-[1-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
- 1,1-Dimethyl{5-[(2-{[3-(aminosulfonyl)phenyl]amino}-4-pyrimidinyl(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}phenylcarbamathydrochlorid,
- 3-[(4-{Methyl[1-methyl-2-(phenylamino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]benzolsulfonamidtrifluoracetat,
- 1,1-Dimethylethyl[5-[(2-{[3-(aminosulfonyl)-4-methylphenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}phenylcarbamathydrochlorid,
- N5,1-Dimethyl-N5-(2-{[4-methyl-3-(methylsulfonyl)phenyl]amino}-4-pyrimidinyl)-N2-phenyl-1H-benzimidazol-2,5-diamintrifluoracetat,
- N5,1-Dimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N2-phenyl-1H-benzimidazol-2,5-diamintrifluoracetat,
- 1-{4-[(4-[Methyl[1-methyl-2-(phenylamino)-1H-benzimdazol-5-yl]amino}-2-pyrimidinyl)amino]phenyl}methansulfonamidtrifluoracetat,
- 4-[(4-(Methyl[1-methyl-2-(phenylamino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]phenylmethansulfonattrifluoracetat,
- 3-({4-[{2-[(4-Fluorphenyl)amino]-1-methyl-1H-benzimdazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidtrifluoracetat,
- 5-({4-[{2-[(4-Fluorphenyl)amino]-1-methyl-1H-benzimdazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidtrifluoracetat,
- N2-(4-Fluorphenyl)-N5,1-dimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamintrifluoracetat,
- 1-[4-({4-[{2-[(4-Fluorphenyl)amino]-1-methyl-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidtrifluoracetat,
- 4-({4-[{2-[(4-Fluorphenyl)amino]-1-methyl-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)phenylmethansulfonattrifluoracetat,
- 3-({4-[{2-[(4-Fluorphenyl)amino]-1-methyl-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)phenylmethansulfonattrifluoracetat,
- N5,1-Dimethyl-N2-(4-methylphenyl)-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamintrifluoracetat,
- 1-[4-({4-[(2-{[4-(1,1-Dimethylethyl)phenyl]amino}-1-methyl-1H-benzimidazol-5-yl)methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidtrifluoracetat,
- 3-({4-[(2-{[4-(1,1-Dimethylethyl)phenyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidtrifluoracetat,
- 5-({4-[(2-{[4-(1,1-Dimethylethyl)phenyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid,
- N2-[4-(1,1-Dimethylethyl)phenyl]-N5,1-dimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamintrifluoracetat,
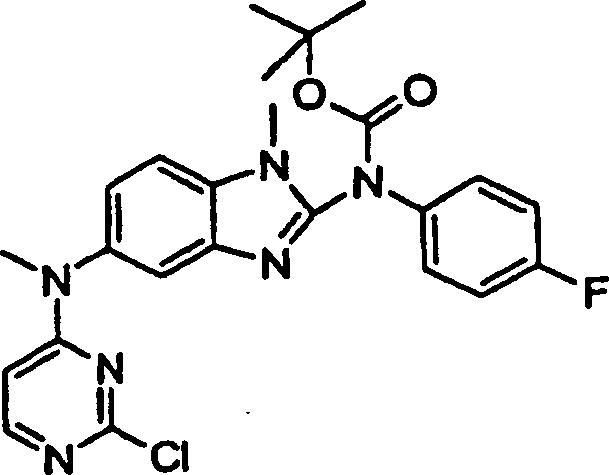
- 1,1-Dimethylethyl(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)[4-(methyloxy)phenyl]carbamat,
- N5,1-Dimethyl-N2-[4-(methyloxy)phenyl]-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamintrifluoracetat,
- 1,1-Dimethylethyl{5-[[2-({4-[(aminosulfonyl)methyl]phenyl}amino)-4-pyrimidinyl](methyl)amino]-1-methyl-1H-benzimdazol-2-yl}[4-(methyloxy)phenyl]carbamat,
- 1-[4-({4-[Methyl(1-methyl-2-{[4-(methyloxy)phenyl]amino}-1Hbenzimdazol-5-yl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidtrifluoracetat,
- 1,1-Dimethylethyl(1-methyl-5-{methyl[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimdazol-2-yl)[4-(methyloxy)phenyl]carbamat,
- N5,1-Dimethyl-N2-[4-(methyloxy)phenyl]-N5-[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diamintrifluoracetat,
- 1,1-Dimethylethyl(1-methyl-5-{methyl[2-({4-[1-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimdazol-2-yl)[4-(methyloxy)phenyl]carbamat,
- N5,1-Dimethyl-N2-[4-(methyloxy)phenyl]-N5-[2-({4-[1-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diamintrifluoracetat,
- N5,1-Dimethyl-N2-[4-(methyloxy)phenyl]-N5-[2-({3-[1-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diamintrifluoracetat,
- 3-{[4-(Methyl{1-methyl-2-[(1-methylethyl)amino]-1H-benzimdazol-5-yl}amino)-2-pyrimidinyl]amino)benzolsulfonamidhydrochlorid,
- 2-Chlor-5-{[4-(methyl{1-methyl-2-[(1-methylethyl)amino]-1H-benzimdazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamid,
- 2-Methyl-5-{[4-methyl[1-methyl-2-(1-methylethyl)amino]-1H-benzimdazol-5-yl)amino)-2-pyrimidinyl]amino}benzolsulfonamidhydrochlorid,
- N-Methyl-2-(4-{[4-(methyl[1-methyl-2-[(1-methylethyl)amino]-1H-benzimdazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)ethansulfonamidhydrochlorid,
- 4-{[4-(Methyl{1-methyl-2-[(1-methylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenylmethansulfonathydrochlorid,
- 3-{[4-(Methyl{1-methyl-2-[(1-methylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenylmethansulfonathydrochlorid,
- N5,1-Dimethyl-N2-(1-methylethyl)-N5-[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydochlorid,
- 3-{[4-(Methyl{1-methyl-2-[(2-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamidhydrochlorid,
- 2-Methyl-5-{[4-(methyl[1-methyl-2-[(2-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyljamino}benzolsulfonamidhydrochlorid,
- 1-(4-{[4-(Methyl[1-methyl-2-[{2-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)methansulfonamidhydrochlorid,
- N5,1-Dimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N2-(2-phenylethyl)-1H-benzimidazol-2,5-diaminhydrochlorid,
- N-Methyl-2-(4-{[4-(methyl{1-methyl-2-{(2-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)ethansulfonamidhydrochlorid,
- N2-(1,1-Dimethylethyl)-N5,1-dimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
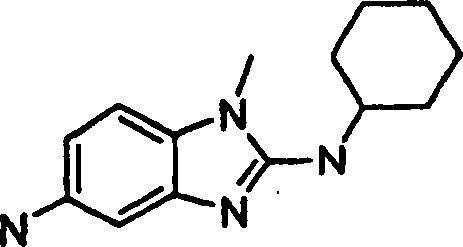
- N2-Cyclohexyl-N5,1-dimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamin,
- 5-({4-[[2-(Cyclohekylamino)-1-methyl-1H-benzimidazol-5-yl](methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid,
- N2-Cyclohexyl-N5,1-dimethyl-N5-[2-({3-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
- N2-Cyclohexyl-N5,1-dimethyl-N5-[2-({4-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
- N2-Cyclohexyl-N5,1-dimethyl-N5-[2-({4-[1-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid,
- 2-Methyl-5-[(4-(methyl[1-methyl-2-(methylamino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]benzolsulfonamidhydrochlorid,
- 1-{4-[(4-{Methyl[1-methyl-2-(methylamino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]phenyl}methansulfonamidhydrochlorid,
- 3-[(4-{Methyl[1-methyl-2-(methylamino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]benzolsulfonamidhydrochlorid,
- N2,N5,1-Trimethyl-N5-[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamin,
- 1-[4-({4-[[1-Ethyl-2-(methylamino)-1H-benzimidazol-5-yl](methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidhydrochlorid,
- N5,1-Dimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N2-[4-(trifluormethyl)phenyl]-1H-benzimidazol-2,5-diamin.
- 4-{4-[Methyl-(1-methyl-2-methylsulfanyl-1H-benzoimidazol-5-yl)-
amino]-pyrimidin-2-ylamino}-benzolsulfonamid,
- 4-{4-[(2-Methansulfinyl-1-methyl-1H-benzoimidazol-5-yl)-methylamino]-pyrimidin-2-ylamino}-benzolsulfonamid,
- 4-(4-{Methyl-[1-methyl-2-(4-trifluormethyl-phenylamino)-1H-benzoimidazol-5-yl]-amino}-pyrimidin-2-ylamino)-benzolsulfonamid,
- N5-[2-(4-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-N1,N5-dimethyl-N2-(3-trifluormethyl-phenyl)-1H-benzoimidazol-2,5-diamin,
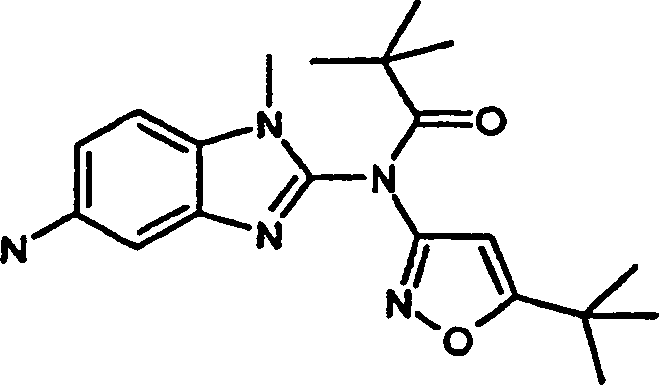
- N2-(5-tert-Butyl-isoxazol-3-yl)-N5-[2-(4-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-1,N5-dimethyl-1H-methyl-amino-benzoimidazol-2,5-diamin,
- N2-[5-(1,1-dimethylethyl)-3-isoxazolyl)-N5,1-dimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamin,
- N2-(5-tert-Butyl-isoxazol-3-yl)-N5-[2-(4-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-1-methyl-1-1H-benzimidazol-2,5-diamintrifluoracetat,
- N2-(5-tert-Butyl-isoxazol-3-yl)-N5-[2-(3-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-1-methyl-1H-benzimidazol-2,5-diamin,
- N2-(5-tert-Butyl-isoxazol-3-yl)-N5-[2-(3-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-1,N5-dimethyl-1-H-benzoimidazol-2,5-diamin,
- N2-(5-tert-Butyl-isoxazol-3-yl)-N5-[2-(3-methansulfonyl-4-methylphenylamino)-pyrimidin-4-yl]-1-methyl-1H-benzimidazol-2,5-diamin,
- 5-(4-{[2-(5-tert-Butyl-isoxazol-3-ylamino)-1-methyl-1-H-benzoimidazol-5-yl]-methyl-amino}-pyrimidin-2-ylamino)-2-methyl-benzolsulfonamid,
- N2-(6-Fluor-4-H-benzo[1,3]dioxin-8-ylmethyl)-N5-[2-(3-methansulfonyl-4-methyl-phenylamino)-pyrimidin-4-yl]-1-methyl-1H-benzoimidazol-2,5-diamin,
- N2-5-(tert-Butyl-isoxazol-3-yl)-1-methyl-N5-{2-[3-(morpholin-4-sulfonyl)-phenylamino]-pyrimidin-4-yl}-1H-benzoimidazol-2,5-diamin,
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-N'-phenylharnstoff,
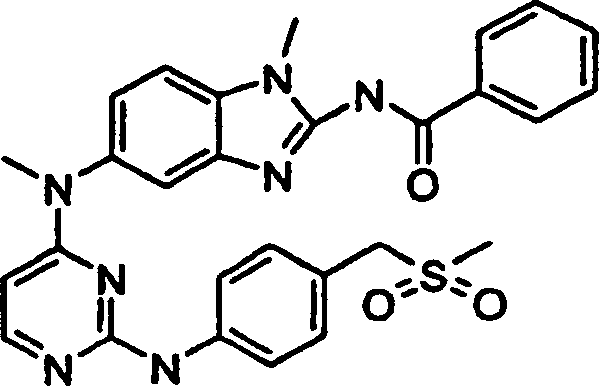
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)benzamid,
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidiriyl]amino}-1H-benzimidazol-2-yl)-2,3-dihydro-1H-indol-1-carboxamid,
- N-[5-(1,1-Dimethylethyl)-3-isoxazolyl]-N'-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)harnstoff,
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-phenylacetamid,
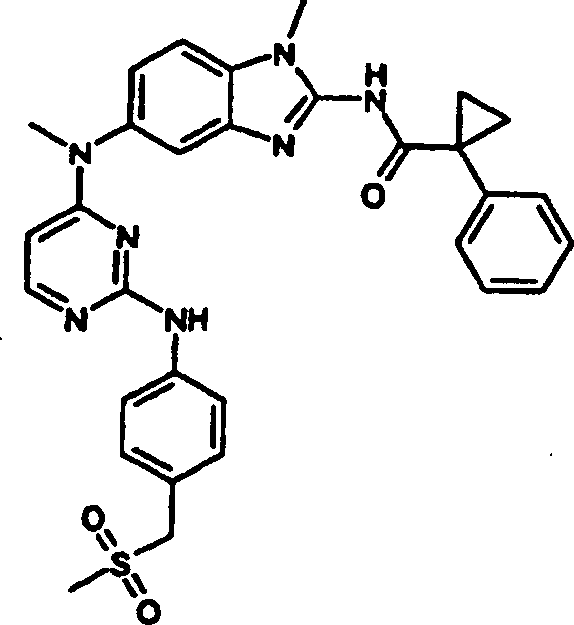
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-1-phenylcyclopropancarboxamid,
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-4-pyridincarboxamid,
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)cyclohexancarboxamid,
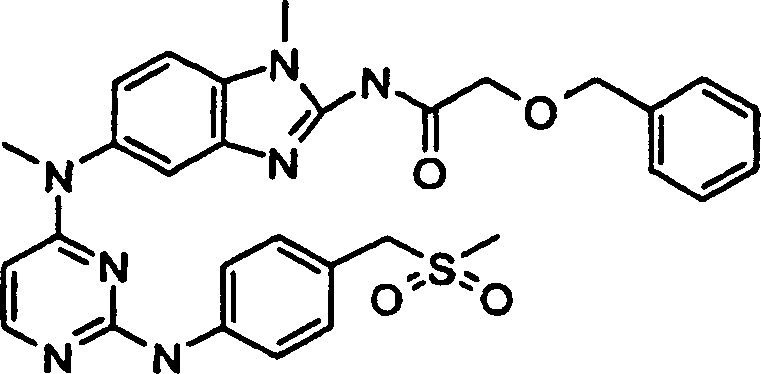
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-[(phenylmethyl)oxa]acetamid,
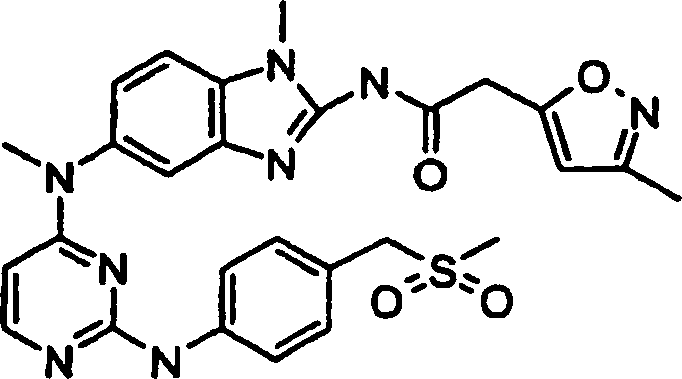
- 2-(3-Methyl-5-isoxazolyl)-N-(1-methyl-5-{methyl[2-((4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
- 3-[(Dimethylamino)methyl]-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)benzamid,
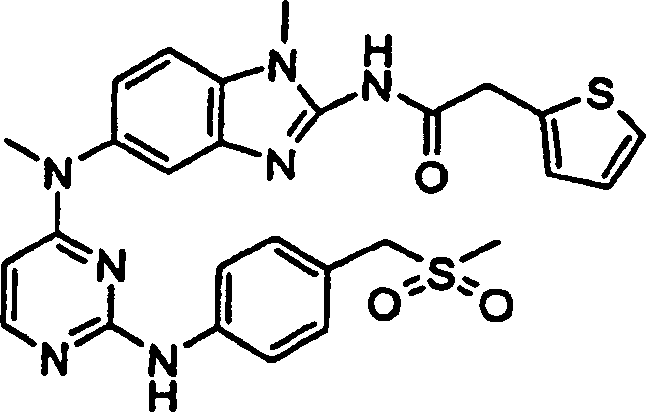
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-(2-thienyl)acetamid,
- 2-Fluor-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-5-(trifluormethyl)benzamid,
- Difluor-N-({[2-(3-methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]methyl-amino}-methyl-1H-benzoimidazol-2-yl)-benzamid,
- N-({[2-(3-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methylamino}-methyl-1H-benzoimidazol-2-yl)-3,5-bis-trifluormethyl-benzamid,
- Cyclohexancarbonsäure({[2-(3-methansulfonylmethyl-phenylamino)pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-amid,
- N-({[2-(3-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)methyl-benzamid,
- N-({[2-(3-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-4-methoxy-benzamid,
- C-(Chlor-trifluormethyl-phenyl)-N-({[2-(3-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)acetamid,
- (3,5-Bis-trifluormethyl-phenyl)-N-({[2-(3-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)acetamid,
- N-(5-{[2-(3-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methylamino}-1-methyl-1H-benzoimidazol-2-yl)-2-(3-trifluormethylsulfanyl-phenyl)acetamid,
- (2,4-Bis-trifluormethyl-phenyl)-N-({[2-(3-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)acetamid,
- (2-Fluor-5-trifluormethyl-phenyl)-N-({[2-(3-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)acetamid,
- 3H-Benzotriazol-5-carbonsäure({[2-(3-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)amid,
- 3H-Benzoimidazol-5-carbonsäure({[2-(3-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)amid,
- Thiophen-2-carbonsäure({[2-(3-methansulfonylmethyl-phenylamino)pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-amid,
- Thiophen-3-carbonsäure({[2-(3-methansulfonylmethyl-phenylamino)pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-amid,
- N-({[2-(3-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methylamino}-methyl-1H-benzoimidazol-2-yl)-C-thiophen-2-yl-acetamid,
- 3-Methyl-thiophen-2-carbonsäure({[2-(4-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-amid,
- Furan-3-carbonsäure({[2-(4-methansulfonylmethyl-phenylamino)pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-amid,
- 3-Methyl-furan-2-carbonsäure({[2-(4-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-amid,
- N-({[2-(4-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methylamino}-methyl-1H-benzoimidazol-2-yl)-2-(3-methyl-isoxazol-5-yl)-acetamid,
- C-(Chlor-trifluormethyl-phenyl)-N-({[2-(4-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)acetamid,
- N-(5-{[2-(4-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methylamino}-1-methyl-1H-benzoimidazol-2-yl)-2-(3-trifluormethylsulfanyl-phenyl)acetamid,
- C-(Fluor-trifluormethyl-phenyl)-N-({[2-(4-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-acetamid,
- N-({[2-(4-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methylamino}-methyl-1H-benzoimidazol-2-yl)-dimethyl-butyramid,
- 2-Propyl-pentansäure({[2-(4-methansulfonylmethyl-phenylamino)pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-amid,
- N-({[2-(4-Methansulfonylmethyl-phenylamino-pyrimidin-4-yl]-methylamino}-methyl-1H-benzoimidazol-2-yl)-isobutyramid,
- Cyclopropancarbonsäure({[2-(4-methansulfonylmethyl-phenylamino)pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-amid,
- N-({[2-(4-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methylamino}-methyl-1H-benzoimidazol-2-yl)-4-methoxy-benzamid,
- 4-Methoxy-N-(methyl-{methyl-[2-(4-methyl-3-sulfamoyl-phenylamino)-pyrimidin-4-yl]-amino}-1H-benzoimidazol-2-yl)-benzamid,
- Furan-2-carbonsäure({[2-(4-methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-amid,
- N-(Methyl-{methyl-[2-(4-methyl-3-sulfamoyl-phenylamino)-pyrimidin-4-yl]-amino}-1H-benzoimidazol-2-yl)-C-thiophen-2-yl-acetamid,
- C-(Chlor-trifluormethyl-phenyl)-N-(methyl-{methyl-[2-(4-methyl-3-sulfamoyl-phenylamino)-pyrimidin-4-yl]-amino}-1H-benzoimidazol-2-yl)-acetamid,
- 4-Methoxy-N-[methyl-(methyl-{2-[3-(morpholin-4-sulfonyl)-phenylamino]-pyrimidin-4-yl}-amino)-1H-benzoimidazol-2-yl]-benzamid,
- N-[Methyl-(methyl-{2-[3-(morpholin-4-sulfonyl)-phenylamino]-pyrimidin-4-yl}-amino)-1H-benzoimidazol-2-yl]-C-thiophen-2-yl-acetamid,
- Thiophen-2-carbonsäure[methyl-(methyl-{2-[3-(morpholin-4-sulfonyl)-phenylamino]-pyrimidin-4-yl}-amino)-1H-benzoimidazol-2-yl]-amid,
- Furan-2-carbonsäure[methyl-(methyl-{2-[3-(morpholin-4-sulfonyl)-phenylamino]-pyrimidin-4-yl}-amino)-1H-benzoimidazol-2-yl]-amid,
- N-({[2-(3-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methylamino}-methyl-1H-benzoimidazol-2-yl)-2-(3-methyl-isoxazol-5-yl)-acetamid,
- Furan-2-carbonsäure-({[2-(3-methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-amid,
- 2-(3-Methyl-isoxazol-5-yl)-N-[methyl-(methyl-{2-[3-(morpholin-4-sulfonyl)-phenylamino]-pyrimidin-4-yl}-amino)-1H-benzoimidazol-2-yl]-acetamid,
- 3-Methyl-furan-2-carbonsäure-({[2-(3-methansulfonylmethylphenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-amid,
- N-[Methyl-(methyl-{2-[3-(4-methyl-piperazin-1-sulfonyl)-phenylamino]-pyrimidin-4-yl}-amino)-1H-benzoimidazol-2-yl]-C-thiophen-2-yl-acetamid,
- Thiophen-2-carbonsäure[methyl-(methyl-{2-[3-(4-methyl-piperazin-1-sulfonyl)-phenylamino]-pyrimidin-4-yl}-amino)-1H-benzoimidazol-2-yl]-amid,
- Furan-2-carbonsäure[methyl-(methyl-{2-[3-(4-methyl-piperazin-1-sulfonyl)-phenylamino]-pyrimidin-4-yl}-amino)-1H-benzoimidazol-2-yl]-amid,
- 2-(3-Methyl-isoxazol-5-yl)-N-[methyl-(methyl-{2-[3-(4-methylpiperazin-1-sulfonyl)-phenylamino]-pyrimidin-4-yl}-amino)-1H-benzoimidazol-2-yl]-acetamid,
- N-({[2-(3-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methylamino}-methyl-1H-benzoimidazol-2-yl)-dimethylbutyramid,
- N-({[2-(3-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methylamino}-methyl-1H-benzoimidazol-2-yl)-propionamid,
- Pentansäure-({[2-(3-methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-amid,
- N-({[2-(3-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methylamino}-methyl-1H-berizoimidazol-2-yl)-butyramid,
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-phenylacetamid,
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-1-phenylcyclopropancarboxamid,
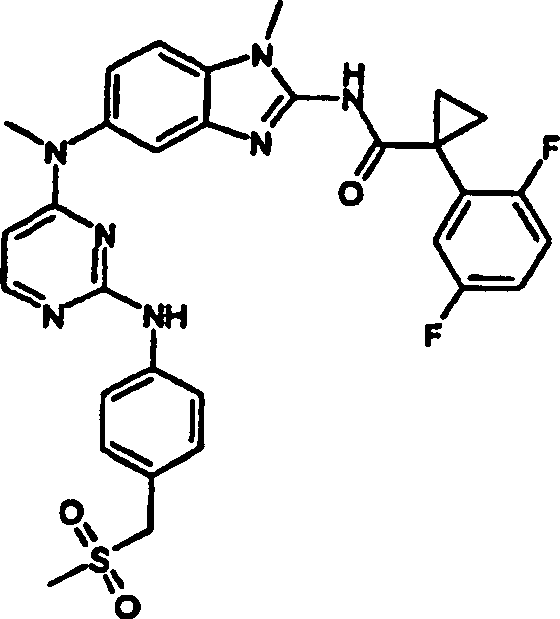
- 1-(2,5-Difluorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-cyclopropancarboxamid,
- 1-(4-Chlorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-cyclopropancarboxamid,
- 2-(4-Fluorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
- 2-[3,5-Bis(trifluormethyl)phenyl]-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
- 2-(3,4-Dichlorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
- 1-(2,5-Difluorphenyl)-N-(1-methyl-5-{methyl[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-cyclopropancarboxamid,
- 2-(2,5-Difluorphenyl)-N-(1-methyl-5-{methyl[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
- 2-(3,4-Dichlorphenyl)-N-(1-methyl-5-{methyl[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
- 1-(2,5-Difluorphenyl)-N-{5-[(2-{[5-(ethylsulfonyl)-2-(methyloxy)phenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}cyclopropancarboxamid,
- 2-(2,5-Difluorphenyl)-N-{5-[(2-{[5-(ethylsulfonyl)-2-(methyloxy)phenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}acetamid,
- 1-(3,4-Dichlorphenyl)-N-{5-[(2-{[5-(ethylsulfonyl)-2-(methyloxy)phenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}cyclopropancarboxamid,
- 2-(3,4-Dichlorphenyl)-N-{5-[(2-{[5-(ethylsulfonyl)-2-(methyloxy)phenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}acetamid,
- N-{5-[(2-{[3-(Aminosulfonyl)-4-methylphenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}-1-(2,5-difluorphenyl)cyclopropancarboxamid,
- N-{5-[(2-{[3-(Aminosulfonyl)-4-methylphenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}-1-(3,4-dichlorphenyl)cyclopropancarboxamid,
- N-{5-[(2-{[3-(Aminosulfonyl)-4-methylphenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}-2-(3,4-dichlorphenyl)-acetamid,
- 2-[2,3-Bis(methyloxy)phenyl]-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
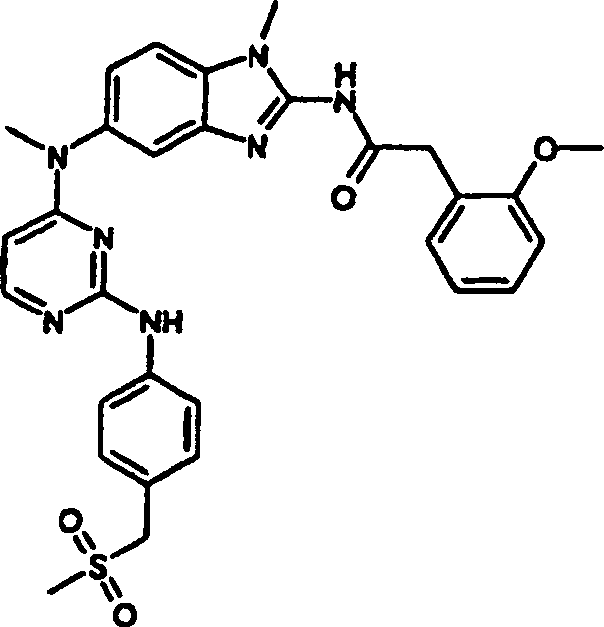
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-[2-(methyloxy)phenyl]acetamid,
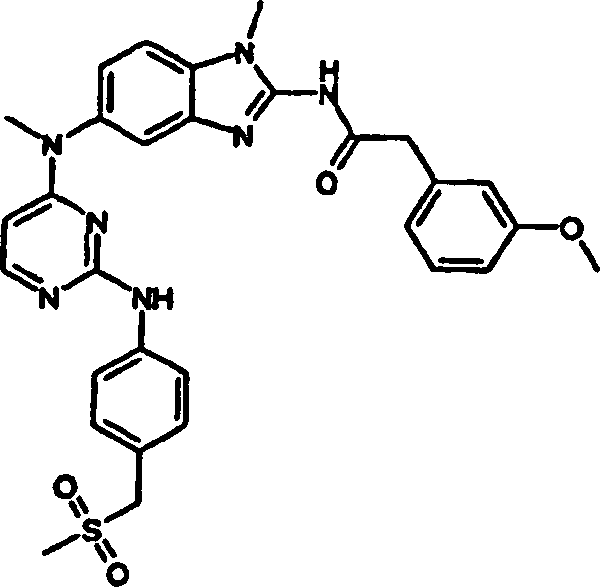
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-[3-(methyloxy)phenyl]acetamid,
- N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-[4-(methyloxy)phenyl]acetamid,
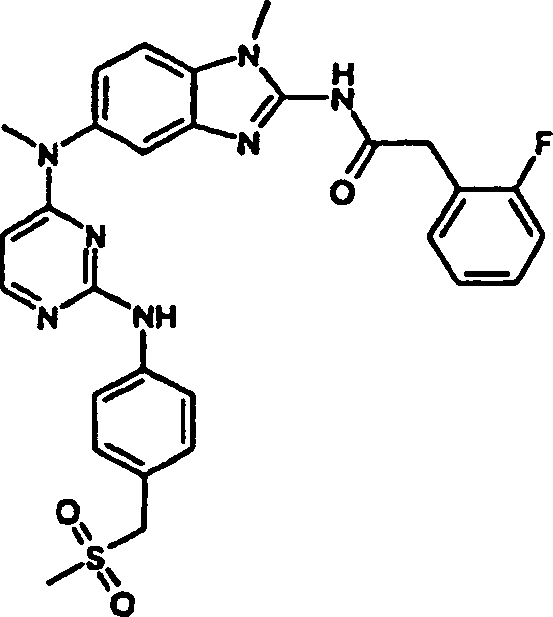
- 2-(2-Fluorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
- 2-(3-Fluorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
- 2-(2,6-Difluorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
- 2-(2,3-Difluorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
- 2-[3,4-Bis(methyloxy)phenyl]-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
- N-{5-[(2-{[3-(Aminosulfonyl)-4-methylphenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}-2-(2,5-difluorphenyl)-acetamid,
- 1-(3,4-Dichlorphenyl)-N-(1-methyl-5-{methyl[2-([3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)cyclopropancarboxamid,
- 2-(2-Chlorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
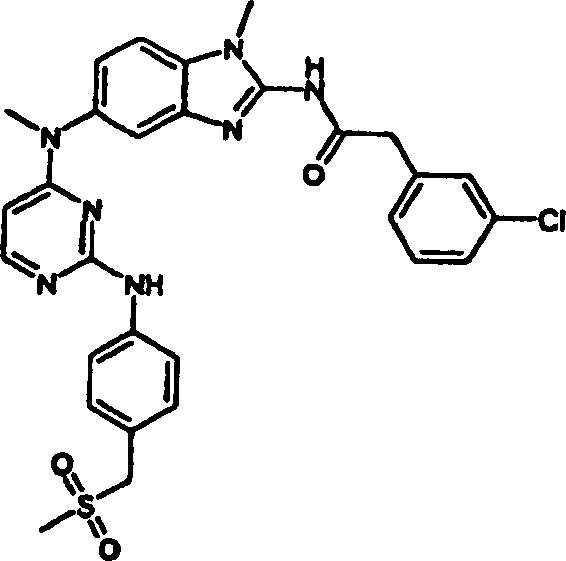
- 2-(3-Chlorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
- 2-(4-Chlorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid,
- 2-[3,5-Bis(methyloxy)phenyl]-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl-acetamid,
- 2-[2,5-Bis(methyloxy)phenyl]-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl-acetamid,
- 2-(2,5-Dichlorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl-acetamid,
- 3-Methyl-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-phenylbutanamid,
- 2-(2,5-Dimethylphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl-acetamid,
- 2-Methyl-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-phenylpropanamid,
- 2-(1,3-Benzodioxol-5-yl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
oder
ein Salz oder Solvat davon.
-
Typischerweise
sind Salze der vorliegenden Erfindung pharmazeutisch annehmbare
Salze. Salze, die von dem Begriff "pharmazeutisch annehmbare Salze" umfaßt sind,
beziehen sich auf nicht-toxische Salze der Verbindungen dieser Erfindung.
Salze der Verbindungen der vorliegenden Erfindung können Säureadditionssalze,
die von einem Stickstoff auf einem Substituenten in der Verbindung
(I) abgeleiter sind, umfassen. Repräsentative Salze schließen die
folgenden Salze ein: Acetat, Benzolsulfonat, Benzoat, Bicarbonat,
Bisulfat, Bitartrat, Borat, Bromid Calciumedetat, Camsylat, Carbonat,
Chlorid, Clavulanat, Citrat, Dihydrochlorid, Edetat, Edisylat, Estolat,
Esylat, Fumarat, Gluceptat, Gluconat, Glutamat, Glycollylarsanilat,
Hexylresorcinat, Hydrabamin, Hydrobromid, Hydrochlorid, Hydroxynaphthoat,
Iodid, Isethionat, Lactat, Lactobionat, Laurat, Malst, Malest, Mandelat,
Mesylat, Methylbromid, Methylnitrat, Methylsulfat, Monokaliummaleat,
Mucat, Napsylat, Nitrat, N-Methylglucamin, Oxalat, Pamoat (Embonat),
Palmitat, Pantothenat, Phosphat/Diphosphat, Polygalacturonat, Kalium,
Salicylat, Natrium, Stearat, Subacetat, Succinat, Tannst, Tartrat,
Teoclat, Tosylat, Triethiodid, Trimethylammonium und Valerat. Andere
Salze, die nicht pharmazeutisch annehmbar sind, können nützlich in der
Herstellung von Verbindungen dieser Erfindung sein, und diese bilden
einen weiteren Aspekt der Erfindung.
-
Während es
möglich
ist, zur Verwendung in der Therapie, daß therapeutisch effektive Mengen
einer Verbindung der Formel (I) als auch Salzen und Solvaten davon
als die Rohchemikalie verabreicht werden können, ist es möglich, den
Wirkstoff als eine pharmazeutische Zusammensetzung anzubieten. Entsprechend stellt
die Erfindung ferner pharmazeutische Zusammensetzungen bereit, die
therapeutisch effektive Mengen der Verbindungen der Formel (I) und
Salzen und Solvaten davon, und ein oder mehrere pharmazeutisch annehmbare
Träger,
Verdünnungsmittel
oder Exzipienten einschließen.
Die Verbindungen der Formel (I) und Salze und Solvate davon sind
wie oben beschrieben. Die Träger,
Verdünnungsmittel
oder Exzipienten müssen
annehmbar im Sinne der Kompatibilität mit den anderen Bestandteilen
der Formulierung sein und dürfen
nicht schädlich
für den
Empfänger
sein. Gemäß einem
anderen Aspekt der Erfindung wird ebenfalls ein Verfahren zur Herstellung
einer pharmazeutischen Formulierung bereitgestellt, das das Mischen
einer Verbindung der Formel (I) oder eines Salzes oder Solvates
davon mit ein oder mehreren pharmazeutisch annehmbaren Trägern, Verdünnungsmitteln
oder Exzipienten einschließt.
-
Pharmazeutische
Formulierungen können
in Einheitdosisformen vorliegen, die eine vorbestimmte Menge des
Wirkstoff pro Einheitsdosis enthalten. Solch eine Einheit kann zum
Beispiel 0,5 mg bis 1 g enthalten, vorzugsweise 1 mg bis 700 mg,
besonders bevorzugt 5 mg bis 100 mg der Verbindung der Formel (I),
abhängig
des zu behandelnden Zustands, vom Weg der Verabreichung und dem
Alter, Gewicht und Zustand des Patienten, oder pharmazeutische Formulierungen
können
in Einheitsdosisformen vorliegen, die eine vorbestimmte Menge des
Wirkstoffs pro Einheitsdosis enthalten. Bevorzugte Einheitsdosierungsformulierungen
sind die, die ein tägliche
Dosis oder Subdosis, wie bereits oben vorgetragen, oder eine angemessene
Fraktion davon, eines Wirkstoff enthalten. Außerdem können solche pharmazeutischen
Formulierungen durch jede dem auf dem Gebiet der Pharmazie vertrauten
Fachmann bekannten Verfahren hergestellt werden.
-
Pharmazeutische
Formulierungen können
für die
Verabreichung über
jeden angemessenen Weg angepaßt
sein, zum Beispiel über
den oralen (einschließlich
bukkalen oder sublingualen), rektalen, nasalen, topischen (einschließlich bukkalen,
sublingualen oder transdermalen), vaginalen oder parenteralen (einschließlich subkutanen,
intramuskulären,
intravenösen
oder intradermalen) Weg. Solche Formulierungen können durch jede dem auf dem
Gebiet der Pharmazie vertrauten Fachmann bekannten Verfahren hergestellt
werden, zum Beispiel durch das Verbinden des Wirkstoffs mit den
Trägern
oder Exzipienten.
-
Pharmazeutische
Formulierungen, die für
die orale Verabreichung angepaßt
sind, können
als separate Einheiten vorliegen, wie zum Beispiel als Kapseln oder
Tabletten; Pulver oder Granalien; Lösungen oder Suspensionen in
wäßrigen oder
nicht-wäßrigen Flüssigkeiten;
eßbare
Schäume
oder geschlagene Cremes; oder Öl-in-Wasser-Flüssigemulsionen
oder Wasser-in-Öl-Flüssigemulsionen.
-
Zum
Beispiel für
die orale Verabreichung in der Form einer Tablette oder Kapsel kann
die aktive Arzneimittelkomponente mit einem oralen, nichttoxischen
pharmazeutisch annehmbaren inerten Träger kombiniert sein, wie zum
Beispiel Ethanol, Glycerin, Wasser und dgl. Pulver werden durch
Zerkleinern der Verbindung in eine geeignete feine Größe und Mischen
mit einem ähnlich
zerkleinerten pharmazeutischen Träger hergestellt, wie zum Beispiel
einem eßbaren
Kohlenhydrat, wie zum Beispiel Stärke oder Mannit. Aromastoffe, Konservierungsstoffe,
Dispergiermittel und Farbstoffe können ebenfalls vorliegen.
-
Kapseln
werden durch Herstellen des Pulvergemisches, wie oben beschrieben,
und Füllen
in geformte Gelatinehüllen
hergestellt. Gleitmittel und Schmiermittel, wie zum Beispiel kolloidale
Kieselerde, Talk, Magnesiumstearat, Calciumstearat oder festes Polyethylenglykol
können
dem Pulvergemisch vor der Abfüllung
zugesetzt werden. Ein Spreng- oder Solubilisierungsmittel, wie zum
Beispiel Agar-Agar, Calciumcarbonat oder Natriumcarbonat, können ebenfalls
zugesetzt werden, um die Verfügbarkeit
des Medikaments, wenn die Kapsel aufgenommen wird, zu verbessern.
-
Des
weiteren, falls erwünscht
oder notwendig, können
geeignete Bindemittel, Schmiermittel, Sprengmittel und Farbstoffe
ebenfalls in das Gemisch eingebracht werden. Geeignete Bindemittel
schließen
Stärke, Gelatine,
natürliche
Zucker, wie Glucose oder beta-Lactose, Maissüßstoffe, natürliche und
synthetische Gummis, wie Gummi arabicum, Tragacanthgummi oder Natriumalginat,
Carboxymethylcellulose, Polyethylenglykol, Wachse und dgl. ein.
Schmiermittel, die in diesen Dosierungsformen verwendet werden,
schließen
Natriumoleat, Natriumstearat, Magnesiumstearat, Natriumbenzoat,
Natriumacetat, Natriumchlorid und dgl. ein. Sprengmittel schließen uneingeschränkt Stärke, Methylcellulose,
Agar, Bentonit, Xanthangummi und dgl. ein. Tabletten werden zum
Beispiel durch Herstellen eines Pulvergemisches, granulierend oder
schlagend, Zugeben eine Schmier- und Sprengmittels und Pressen in
Tabletten formuliert. Ein Pulvergemisch wird durch Mischen der Verbindung,
geeigneterweise zerkleinert, mit einem Verdünnungsmittel oder einer Basis,
wie oben beschrieben, und gegebenenfalls mit einem Bindemittel,
wie zum Beispiel Carboxymethylcellulose, einem Alginat, Gelatine,
oder Polyvinylpyrrolidon, ein Auflösungsverzögerer, wie zum Beispiel Paraffin,
einem Abbaubeschleuniger, wie zum Beispiel ein quaternäres Salz,
und/oder einem Absorptionsmittel, wie zum Beispiel Bentonit, Kaolin
oder Dicalciumphosphat, hergestellt. Das Pulvergemisch kann durch
Befeuchten mit einem Bindemittel, wie zum Beispiel Sirup, Stärkepaste,
Akazienschleim oder Lösungen
von Cellulose-basierenden oder polymeren Materialien, und Treiben
durch ein Drahtsieb granuliert werden. Als eine Alternative zur
Granulierung kann das Pulvergemisch durch die Tablettiermaschine
laufen gelassen werden, und das Ergebnis sind unvollkommen geformte
Rohlinge, die in Granalien zerbrochen sind. Die Granalien können durch
die Zugabe von Stearinsäure,
eines Stearatsalzes, Talk oder Mineralöl eingeschmiert sein, um zu
verhindern, daß sie
an den Tabletten-formenden Prägestempel
haften bleiben. Das eingeschmierte Gemisch wird dann in Tabletten
verpreßt. Die
Verbindungen der vorliegenden Erfindung können ebenfalls mit einem freifließenden inerten
Träger
kombiniert sein und direkt ohne das Durchführen der Granulierungs- oder
Schlagungsschritte in Tabletten verpreßt werden. Eine klare oder
undurchsichtige Schutzbeschichtung kann bereitgestellt werden, die
aus einer versiegelnden Schicht von Schellack, einer Beschichtung
aus Zucker oder polymeren Materials und einer Polierbeschichtung
aus Wachs besteht. Farbstoffe können
zu diesen Beschichtungen hinzugegeben werden, um die verschiedenen
Einheitsdosierungen zu unterscheiden.
-
Orale
Flüssigkeiten,
wie zum Beispiel Lösungen,
Sirupe und Elixiere können
in einer Dosierungseinheitsform hergestellt werden, so daß eine gegebene
Menge eine vorbestimmte Menge der Verbindung enthält. Sirupe
können
durch Auflösen
der Verbindung in eine geeignete mit Geschmack versehenen wäßrige Lösung hergestellt
werden, während
Elixiere durch die Verwendung eines nicht-toxischen alkoholischen
Vehikels hergestellt wird. Suspensionen können durch Dispergieren der
Verbindung in einem nichttoxischen Vehikel formuliert sein. Solubilisierungsmittel
und Emulgatoren, wie zum Beispiel ethoxylierte Isostearylalkohole
und Polyoxyethylensorbitester, Konservierungsmittel, Geschmackszusätze, wie
zum Beispiel Pfefferminzöl
oder natürliche
Süßstoffe
oder Saccharin oder andere nützliche
Süßstofffe,
und dgl. können
ebenfalls zugesetzt werden.
-
Wo
angebracht, können
die Dosierungseinheitsformulierungen für die orale Verabreichung mikroeingekapselt
sein. Die Formulierung kann ebenfalls hergerichtet sein, um die
Freisetzung zu verlängern
oder fortzusetzen, wie zum Beispiel durch Beschichten oder Einbetten
von partikulären
Material in Polymere, Wachs oder dgl.
-
Die
Verbindungen der Formel (I) und Salze oder Solvate davon können ebenfalls
in der Form von Liposomen-Übertragungssystemen,
wie zum Beispiel kleine unilamellierte Vesikel, große unilamellierte
Vesikel und multilamellierte Vesikel, verabreicht werden. Liposome
können
aus einer Vielfalt von Phospholipiden gebildet werden, wie zum Beispiel
Cholesterol, Stearylamin oder Phosphatidylcholinen.
-
Die
Verbindungen der Formel (I) und Salze oder Solvate davon können ebenfalls
durch Verwendung von monoklonalen Antikörpern als individuelle Träger zugeführt werden,
die an die Verbindungsmoleküle
gekoppelt sind. Die Verbindungen können ebenfalls mit löslichen
Polymeren als aufs Ziel eingestellte Arzneimittelträger verknüpft sein.
Solche Polymere können
Polyvinylpyrrolidon, Pyran-Copolymer, Polyhydroxypropylmethacrylamidphenol,
Polyhydroxyethylaspartamidphenol oder Polyethylenoxidpolylysin,
das mit Palmitoyl-Resten substituiert ist, einschließen. Des
weiteren können
die Verbindungen an eine Klasse von bioabbaubaren Polymeren gekoppelt
sein, die nützlich
im Erreichen des kontrollierten Freisetzens eines Arzneistoffs sind,
wie zum Beispiel Polymilchsäure,
Polepsiloncaprolacton, Polyhydroxybuttersäure, Polyorthoester, Polyacetale,
Polydihydropyrane, Polycyanoacrylate und vernetzte oder amphipathische
Blockcopolymere von Hydrogelen.
-
Pharmazeutische
Formulierungen, die für
die transdermale Verabreichung angpaßt sind, können als absondernde Pflaster
vorliegen, die beabsichtigt sind den unmittelbaren Kontakt mit der
Epidermis des Empfängers
für eine
verlängernde
Zeit beizubehalten. Zum Beispiel kann der Wirkstoff von dem Pflaster
durch Iontophorese, wie allgemein beschrieben in Pharmaceutical
Research, 3(6), 318 (1986), zugeführt werden.
-
Pharmazeutische
Formulierungen, die für
die topische Verabreichung angepaßt sind, können als Salben, Cremen, Suspensionen,
Lotionen, Puder, Lösungen,
Pasten, Gele, Sprays, Aerosole oder Öle formuliert sein.
-
Zur
Behandlung des Auges oder anderer äußerer Gewebe, zum Beispiel
Mund und Haut, werden die Formulierungen vorzugsweise als eine topische
Salbe oder Creme aufgetragen. Wenn in einer Salbe formuliert, kann
der Wirkstoff mit sowohl einer Paraffin-basierenden oder einer wassermischbaren
Salbenbasis eingesetzt werden. Alternativ kann der Wirkstoff in
einer Creme mit einer Öl-in-Wasser-Cremebasis
oder einer Wasser-in-Öl-Basis
formuliert sein.
-
Pharmazeutische
Formulierungen, die für
die topische Verabreichung in das Auge angepaßt sind, schließen Augentropfen
ein, worin der Wirkstoff in einem geeigneten Träger, speziell einem wäßrigen Lösungsmittel,
aufgelöst
oder suspendiert wird.
-
Pharmazeutische
Formulierungen, die für
die topische Verabreichung in den Mund angepaßt sind, schließen Lutschtabletten,
Pastillen und Mundwässer
ein.
-
Pharmazeutische
Formulierungen, die für
die rektale Verabreichung angepaßt sind, können als Suppositorien oder
als Klisterien vorliegen.
-
Pharmazeutische
Formulierungen, die für
die nasale Verabreichung angepaßt
sind, worin der Träger ein
Feststoff ist, schließen
ein grobkörnigse
Pulver ein, das eine Teilchengröße zum Beispiel
im Bereich von 20 bis 500 μm
hat, das auf ähnliche
Weise wie Schnupftabak genommen wird verabreicht wird, d.h. durch
rasches Inhalieren über
den Nasengang aus einem Pulverbehälter, der nah an die Nase gehalten
wird. Geeigte Formulierungen für
die Verabreichung als ein Nasenspray oder als Nasentropfen, worin
der Träger
ein Feststoff ist, schließen
wäßrige oder Öl-Lösungen des
Wirkstoff ein.
-
Pharmazeutische
Formulierungen, die für
die Verabreichung durch Inhalation angepaßt sind, schließen feine
Partikelstäube
oder -nebel ein, die durch verschiedene Arten an dosierten, Dosis-druckverdichteten Aerosolen,
Nebulisatoren oder Insufflatoren erzeugt werden.
-
Pharmazeutische
Formulierungen, die für
die vaginale Verabreichung angepaßt sind, können als Pessare, Tampons,
Cremen, Gelen, Pasten, Schäumen
oder Sprayformulierungen vorliegen.
-
Pharmazeutische
Formulierungen, die für
die parenterale Verabreichung angepaßt sind, schließen wäßrige und
nicht-wäßrige sterile
Injektionslösungen,
die Antioxidantien, Puffer, Baktkeriozide und gelöste Substanzen,
die die Formulierung isotonisch mit dem Blut des beabsichtigten
Empfängers
machen, enthalten können;
und wäßrige und
nicht-wäßrige sterile
Suspension ein, die Suspendiermittel und Verdickungsmittel einschließen können. Die
Formulierungen können
in Einheitsdosis- oder Mehrfachdosisbehälter vorliegen, zum Beispiel
versiegelte Ampullen und Fläschchen,
und können
in einem gefriergetrockneten (lyophilisierten) Zustand gelagert
werden, was nur die Zugabe eines sterilen Flüssigkeitsträgers unmittelbar vor der Verwendung
erfordert, wie zum Beispiel Wasser für Injektionen. Unvorbe reitete
Injektionslösungen
und -suspensionen können
aus sterilen Pulvern, Granalien und Tabletten zubereitet werden.
-
Es
ist selbstverständlich,
daß zusätzlich zu
den besonderen oben erwähnten
Bestandteilen die Formulierungen andere Mittel, die üblich auf
dem Gebiet mit Hinsicht auf die Art der in Frage kommenden Formulierung
sind, einschließen
kann, zum Beispiel solche geeignet für die orale Verabreichung können Aromastoffe einschließen.
-
Eine
therapeutisch effektive Menge einer Verbindung der vorliegenden
Erfindung hängt
von einer Anzahl von Faktoren ab, einschließlich zum Beispiel dem Alter
und dem Gewicht des Tiers, dem genauen Zustand, der die Behandlung
erfordert, und seine Schwere, der Art der Formulierung und dem Weg
der Verabreichung, und unterliegt letztendlich der Ermessensfreiheit
des behandelnden Arztes oder Veterinärs. Jedoch wird eine effektive
Menge einer Verbindung der Formel (I) für die Behandlung von neoplastischem
Wachstum, zum Beispiel Darm- oder Brustcarcinoma, im allgemeinen
im Bereich von 0,1 bis 100 mg/kg Körper des Empfängers (Säugetier)
pro Tag sein, und mehr gewöhnlich
im Bereich von 1 bis 10 mg/kg Körpergewicht
pro Tag. Daher würde
die eigentliche Menge für
ein erwachsenes Säugetier
gewöhnlich
von 70 kg pro Tag von 70 bis 700 Mg sein, und diese Menge kann in
einer einzelnen Dosis pro Tag oder mehr gewöhnlich in einer Anzahl (wie
zwei, drei, vier, fünf
oder sechs) an Subdosen pro Tag gegeben werden, so daß die gesamte
Tagesdosis die gleiche ist. Eine effektive Menge eines Salzes oder
Solvats davon kann als ein Anteil der effektiven Menge der Verbindung
der Formel (I) alleine bestimmt werden. Es wird ersichtlich, daß gleiche
Dosierungen angemessen für
die Behandlung der anderen Zustände,
auf die oben bezug genommen wurde, sein würden.
-
Die
Verbindungen der vorliegenden Erfindung und ihre Salze und Solvate
davon können
allein oder in Kombination mit anderen Therapeutika zur Behandlung
der oben genannten Zustände
eingesetzt werden. Insbesondere ist in der Antikrebstherapie eine
Kombination mit anderen Chemotherapeutika, hormonellen Mitteln oder
Antikörpermittel
vorgesehen sowie eine Kombination mit der chirurgischen Therapie
und Radiotherapie. Erfindungsgemäße Kombinationstherapien
umfassen daher die Verabreichung mindestens einer Verbindung der
Formel (I) oder eines pharmazeutisch annehmbaren Salzes oder Solvats
davon und die Verwendung mindestens einer anderen Krebsbehandlungsmethode.
Vorzugsweise umfassen die erfindungsgemäßen Kombinationstherapien die
Verabreichung mindestens einer Verbindung der Formel (I) oder eines
pharmazeutisch annehmbaren Salzes oder Solvats davon und mindestens
eines anderen pharmazeutisch wirksamen Mittels, vorzugsweise eines
antineoplastischen Mittels. Die Verbindung(en) der Formel (I) und
das/die andere(n) pharmazeutisch wirksamen Mittel können zusammen
oder getrennt verabreicht werden, und wenn getrennt verabreicht,
dann kann dies simultan oder in einer nacheinanderfolgenden Reihe
erfolgen. Die Mengen der Verbindung(en) der Formel (I) und des/der
anderen pharmazeutisch wirksamen Mittels(n) und die relative zeitliche Koordinierung
der Verabreichung wird ausgewählt,
um den gewünschten
kombinierten therapeutischen Effekt zu erhalten.
-
Die
Verbindungen der Formel (I) oder Salze oder Solvate davon und mindestens
eine zusätzliche Krebsbehandlungstherapie
können
in Kombination, gleichzeitig oder sequentiell in jeder therapeutisch
angemessenen Kombination mit solch anderen Antikrebstherapien eingesetzt
werden. In einer Ausführungsform
ist die andere Antikrebstherapie mindestens eine zusätzliche
chemotherapeutische Therapie, die die Verabreichung mindestens eines
antineoplastischen Mittels einschließt. Die Verabreichung in Kombination
einer Verbindung der Formel (I) oder Salzes oder Solvats davon mit
anderen neoplastischen Mitteln kann in Kombination gemäß der Erfindung
durch gleichzeitige Verabreichung in (1) einer einheitlichen pharmazeutischen
Zusammensetzung, die beide Verbindungen einschließt, oder
(2) getrennte pharmazeutische Zusammensetzung, die jeweils eine
der Verbindungen einschließt,
sein. Alternativ kann die Kombination getrennt in einer sequentiellen
Art und Weise verabreicht werden, worin ein antineoplastisches Mittel
zuerst verabreicht wird und das andere als zweites oder umgekehrt.
Solch eine sequentielle Verabreichung kann zeitlich nah oder zeitlich
entfernt vorliegen.
-
Antineoplastische
Mittel können
antineoplastische Effekte in einer Zellzyklus-spezifischen Art induzieren,
d.h. sie sind phasenspezifisch und wirken in einer spezifischen
Phase des Zellzyklusses, oder binden DNA und wirken in einer Nicht-Zellzyklus-spezifischen
Art, d.h. sie sind Nicht-Zellzyklus-spezifisch
und agieren durch andere Mechanismen.
-
Antineoplastische
Mittel, die nützlich
in Kombination mit den Verbindungen der Formel (I) und Salzen oder
Solvaten davon sind, schließen
die folgenden ein:
- (1) Zellzyklus-spezifische
antineoplastische Mittel, die uneingeschränkt Diterpenoide wie zum Beispiel
Paclitaxel und sein Analog Docetaxel; Vincaalkaloide, wie zum Beispiel
Vinblastin, Vincristin, Vindesin und Vinorelbin; Epipodophyllotoxine,
wie zum Beispiel Etoposid und Teniposid; Gemcitabin; Fluorpyrimidine,
wie zum Beispiel 5-Fluoruracil und Fluordesoxyuridin; Antimetabolite,
wie zum Beispiel Allopurinol, Fludurabin, Methotrexat, Cladrabin,
Cytarabin, Mercaptopurin und Thioguanin; und Camptothecine, wie
zum Beispiel 9-Aminocamptothecin, Irinotecan, Topotecan, CPT-11
und verschiedene optische Formen von 7-(4-Methylpiperazinomethylen)-10,11-ethylendioxy-20-camptothecin
einschließen;
- (2) cytotoxische chemotherapeutische Mittel, die uneingeschränkt alkylierende
Mittel, wie zum Beispiel Melphalan, Chlorambucil, Cyclophosphamid,
Mechlorethamin, Hexamethylmelamin, Busulfan, Carmustin, Iomustin
und Dacarbazin; Antitumor-Antibiotika, wie zum Beispiel Doxorubicin,
Daunomycin, Epirubicin, Idarubicin, Mitomycin-C, Dacttinomycin und
Mithramycin; und Platin-Koordinationskomplexe, wie zum Beispiel Cisplatin,
Carboplatin und Oxaliplatin einschließen; und
- (3) andere chemotherapeutische Mittel, die uneingeschränkt Anti-Östrogene wie zum Beispiel Tamoxifen, Toremifen,
Raloxifen, Droloxifen und Iodoxyfen; Progesterone, wie zum Beispiel
Megestrolacetat; Aromataseinhibitoren, wie zum Beispiel Anastrozol,
Letrazol, Vorazol und Exemestan; Antiandrogene, wie zum Beispiel
Flutamid, Nilutamid, Bicalutamid und Cyproteronacetat; LHRH-Agonisten
und -Antagonisten, wie zum Beispiel Goserelinacetat und Luprolid,
Testosteron-5α-dihydroreduktaseinhibitoren,
wie zum Beispiel Finasterid; Metalloproteinaseinhibitoren, wie zum
Beispiel Marimastat; Antiprogestone; Inhibitoren der Urokinaseplasminogen-Aktivatorrezeptorfunktion;
Inhibitoren der Wachstumsfaktorfunktion, wie zum Beispiel Inhibitoren
der Funktion des Hepatozytenwachstumsfaktors; für erb-B2, erb-B4, epidermalen Wachstumsfaktorrezeptor
(EGFR), Blutplättchen-abgeleiteten
Wachstumsfaktorrezeptor (PDGFR), vaskulären endothelialer Wachstumsfaktorrezeptor
(VEGFR) und TIE-2 (verschieden von solchen VEGFR- und TIE-2-Inhibitoren, die
in der vorliegenden Erfindung beschrieben sind); und andere Tyrosinkinase-Inhibitoren
einschließen,
wie zum Beispiel Inhibitoren des CDK1 und CDK4-Inhibitoren.
-
Für die Verbindungen
der Formel (I) und deren Salze oder Solvate wird angenommen, daß sie eine Antikrebswirkung
haben, als ein Ergebnis der Inhibierung der Proteinkinase TIE-2
und/oder VEGFR-2 und ihres Effekt auf ausgewählte Zelllinien, deren Wachstum
von TIE-2- und/oder VEGFR-2-Proteinkinaseaktivität abhängig sind.
-
Die
vorliegende Erfindung stellt daher Verbindungen der Formel (I) und
pharmazeutisch annehmbare Salze oder Solvate davon zur Verwendung
in der medizinischen Therapie bereit, und im speziellen in der Behandlung
von Störungen,
die durch mindestens eine unangemessene TIE-2- und VEGFR-2-Aktivität vermittelt werden.
-
Die
unangemessene TIE-2- und/oder VEGFR-2-Aktivität, auf die hier Bezug genommen
wird, ist jede TIE-2- und/oder VEGFR-2-Aktivität, die von der normalen TIE-2-
und/oder VEGFR-2-Aktivität,
die in einem bestimmten Säugetierprobanden
erwartet wird, abweicht. Eine unangemessene TIE-2- und/oder VEGFR-2-Aktivität kann die
Form von zum Beispiel einer abnormalen Zunahme in der Aktivität oder einer
Abnormalle in der Zeitsteuerung und/oder Kontrolle der TIE-2- und/oder
VEGFR-2-Aktivität
annehmen. Eine solche unangemessene Aktivität kann dann von zum Beispiel
einer Überexpression
oder Mutation der Proteinkinase resultieren, die zu einer unangemessenen
oder unkontrollierten Aktivierung führt. Des weiteren ist es selbstverständlich, daß eine unerwünschte TIE-2-
und/oder VEGFR-2-Aktivität
in einer abnormalen Quelle liegen kann, wie zum Beispiel einem bösartigen
Tumor. Das heißt,
das Level der TIE-2- und/oder VEGFR-2-Aktivität muß nicht abnormal sein, um als
unangemessen erachtet zu werden, vielmehr stammt die Aktivität von einer
abnormalen Quelle. In ähnlicher
Weise bezieht sich die unangemessene Angiogenese auf jede angiogene
Aktivität,
die von der normalen angiogenen Aktivität, die in einem bestimmten
Säugetierprobanden
erwartet wird, abweicht. Die unangemessene Angiogenese kann die
Form von zum Beispiel einer abnormalen Zunahme in der Aktivität oder einer
Anomalie in der Zeitsteuerung und/oder Kontrolle der angiogenen
Aktivität
annehmen. Eine solche unangemessene Aktivität kann dann zum Beispiel aus
einer Überexpression
oder Mutation einer Proteinkinase resultieren, die zu einer unangemessenen
oder unkontrollierten Aktivierung führen. Des weiteren ist es selbstverständlich,
daß unerwünschte angiogene
Aktivität
in einer abnormalen Quelle liegen kann, wie zum Beispiel einem bösartigen
Tumor. Das heißt,
das Level der angiogenen Aktivität
muß nicht
abnormal sein, um als unangemessen angesehen zu werden, vielmehr
stammt die Aktivität
aus einer abnormalen Quelle.
-
Die
vorliegende Erfindung ist auf die Verbindungen der Erfindung zur
Verwendung in Verfahren zur Regulierung, Modulierung und Inhibierung
von TIE-2 und/oder VEGFR-2 zur Prävention und/oder Behandlung von
Störungen,
die einer unregulierten TIE-2- und/oder VEGFR-2-Aktivität zugeordnet
sind, gerichtet. Insbesondere können
Verbindungen der vorliegenden Erfindung ebenfalls in der Behandlung
von bestimmten Formen von Krebs verwendet werden. Des weiteren können die
Verbindungen der vorliegenden Erfindung verwendet werden, um zusätzliche
oder synergetische Effekte mit bestimmten existierenden Krebschemotherapien
bereitzustellen, und/oder können
verwendet werden, um die Effektivität bestimmter existierender
Krebschemotherapien und Bestrahlung wieder herzustellen.
-
Die
Verbindungen der vorliegenden Erfindung sind ebenfalls nützlich in
der Behandlung von einer oder mehreren Krankheiten, die Säugetiere
plagen, die durch zelluläre
Proliferation im Bereich der Störung,
die mit Neovaskularisierung und/oder vaskulärer Permeabilität assoziiert
sind, gekennzeichnet sind, einschließlich Arthritis und Restenose;
fibrotische Störungen,
einschließlich
hepatische Zirrhose und Atherosklerose; mesangioproliverative Störungen,
einschließlich
Glomerulonephritis, diabetische Nephropathie, bösartige Nephrosklerose, thrombotische
Mikroangiopathiesyndrome, Organtransplantatabsoßung und Glomerulopathien;
und Stoffwechselstörungen,
einschließlich
Psoriasis, Diabetes mellitus, chronische Wundheilung, Entzündung und neurodegenerative
Krankheiten.
-
Ein
weiterer Aspekt der vorliegenden Erfindung stellt die Verwendung
einer Verbindung der Formel (I) oder eines pharmazeutisch annehmbaren
Salzes oder Solvats davon in der Herstellung eines Medikaments zur
Behandlung einer Störung
bereit, die durch mindestens eine der unangemessenen TIE-2- und
VEGFR-2-Aktivität
gekennzeichnet ist. In einer bevorzugten Ausführungsform ist die Störung ein
empfänglicher Krebs.
-
Ein
weiterer Aspekt der vorliegenden Erfindung stellt die Verwendung
einer Verbindung der Formel (I) oder eines pharmazeutisch annehmbaren
Salzes oder Solvats davon in der Herstellung eines Medikaments zur
Behandlung von Krebs und bösartigen
Tumoren bereit.
-
Das
Säugetier,
das der Behandlung mit einer Verbindung der vorliegenden Erfindung
bedarf, ist typischerweise ein Mensch.
-
In
einer anderen Ausführungsform
werden therapeutisch effektive Mengen von Verbindungen der Formel
(I) oder Salzen oder Solvaten davon und Mitteln, die eine Wachstumsfaktorrezeptorfunktion
inhibieren, in Kombination an ein Säugetier zur Behandlung einer
Störung
verabreicht, die durch mindestens eine unangemessene TIE-2- und
VEGFR-2-Aktivität
vermittelt wird, zum Beispiel in der Behandlung von Krebs. Solche Wachstumsfaktorrezeptoren
schließen
zum Beispiel EGFR, PDGFR, erbB2, erbB4, VEGFR und/oder TIE-2 ein.
Wachstumsfaktorrezeptoren und Mittel, die die Wachstumsfaktorrezeptorfunktion
inhibieren, sind zum Beispiel in Kath, John C., Exp. Opin. Ther.
Patents (2000), 10(6):803-818 und in Shawver et al., DDT Bd. 2,
Nr. 2, Februar 1997 beschrieben.
-
Die
Verbindungen der Formel (I) oder Salze oder Solvate davon und das
Mittel zur Inhibierung einer Wachstumsfaktorrezeptorfunktion können in
Kombination, gleichzeitig oder sequentiell, in jeder therapeutisch annehmbaren
Kombination eingesetzt werden. Die Kombination kann in Kombinationen
gemäß der Erfindung durch
gleichzeitige Verabreichung in (1) einer einheitlichen pharmazeutischen
Zusammensetzung, die beide Verbindungen einschließt, oder
(2) getrennte pharmazeutische Zusammensetzung, die jeweils eine
der Verbindungen einschließt,
eingesetzt werden. Alternativ kann die Kombination getrennt in einer
sequentiellen Art und Weise verabreicht werden, wobei eine Verbindung
zuerst verabreicht wird und die andere als zweite oder umgekehrt.
Solch eine sequenzelle Verabreichung kann zeitlich nahe oder zeitlich
entfernt sein.
-
In
einem anderen Aspekt der vorliegenden Erfindung wird die Verwendung
einer Verbindung der Formel (I) oder eines Salzes oder Solvats davon
in der Herstellung eines Medikaments zur Verwendung in der Behandlung
einer Störung
in einem Säugetier
bereitgestellt, wobei die Störung
durch unangemessene Angiogenese gekennzeichnet ist. In einer Ausführungsform
ist die unangemessene angiogene Aktivität aufgrund mindestens einer
unangemessenen VEGFR1-, VEGFR2-, VEGFR3- oder TIE-2-Aktivität. In einer
anderen Ausführungsform
ist die unangemessene Angiogenese aufgrund einer unangemessenen
VEGFR2- und TIE-2-Aktivität.
In einer weiteren Ausführungsform
schließt
die Verwendung ferner die Verwendung eines VEGFR2-Inhibitors zur
Herstellung des Medikaments zusammen mit den Verbindungen der Formel
(I) oder Salzen oder Solvaten davon ein. Vorzugsweise ist die Störung ein
empfänglicher
Krebs.
-
Die
Kombination einer Verbindung der Formel (I) oder eines Salzes oder
Silvats davon mit einem VEGFR2-Inhibitor kann in Kombination gemäß der Erfindung
durch gleichzeitige Verabreichung in (1) einer einheitlichen pharmazeutischen
Zusammensetzung, die beide Verbindungen einschließt, oder
(2) getrennten pharmazeutischen Zusammensetzungen, die jeweils eine
der Verbindungen einschließt,
eingesetzt werden. Alternativ kann die Kombination getrennt in einer
sequentiellen Art und Weise verabreicht werden, wobei eine Verbindung
zuerst verabreicht wird und die andere als zweite oder umgekehrt.
Solch eine sequentielle Verabreichung kann zeitlich nah oder zeitlich
entfernt sein.
-
Die
Verbindungen dieser Erfindung können
durch eine Vielzahl an Verfahren erzeugt werden, einschließlich Standardchemie.
Jede zuvor definierte Variante behält soweit nicht anderweitig
angegeben weiterhin die zuvor definierte Bedeutung. Illustrative
allgemeine synthetische Verfahren werden nachfolgend dargelegt,
und spezifische Verbindungen der Erfindung werden dann in den Arbeitsbeispielen
hergestellt.
-
Die
Verbindungen der allgemeinen Formel (I) können durch Verfahren, die auf
dem Gebiet der organischen Synthese fachbekannt sind, wie im Teil
durch die nachfolgenden Syntheseschemata dargelegt, hergestellt
werden. In all den nachfolgend beschriebenen Schemata ist es selbstverständlich,
daß Schutzgruppen für sensitive
oder reaktive Gruppen da eingesetzt werden, wo es gemäß den allgemeinen
Prinzipien der Chemie notwendig ist. Schutzgruppen werden gemäß den Standardverfahren
der organischen Synthese manipuliert (T.W. Green und P.G.M. Wuts
(1991), Protecting Groups in Organic Synthesis, John Wiley & Sons). Diese Gruppen
werden in einem passenden Arbeitsgang in der Verbindungssynthese
unter Verwendung von Verfahren, die den Fachleuten leicht ersichtlich
werden, entfernt. Die Auswahl der Verfahren sowie die Reaktionsbedingungen
und Reihenfolge ihrer Ausführung
wird übereinstimmend
mit der Herstellung der Verbindung der Formel (I) sein. Die Fachleute
werden erkennen, wenn ein Stereozentrum in Verbindungen der Formel
(I) existiert. Entsprechend schließt die vorliegende Erfindung
beide mögliche
Stereoisomere ein, und schließt
nicht nur racemische Verbindungen sondern auch die individuellen
Enantiomere ein. Wenn eine Verbindung als ein einzelnes Enantiomer
erwünscht
ist, kann es durch stereospezifische Synthese oder durch Auflösung des
Endprodukts oder jedes konventionellen Zwischenprodukts erhalten
werden. Auflösung
des Endprodukts, eines Zwischenprodukts oder eines Ausgangsmaterials
kann durch jedes geeignete fachbekannte Verfahren besorgt werden.
Siehe zum Beispiel Stereochemistry of Organic Compounds by E.L.
Eliel, S.H. Wilen und L.N. Mander (Wiley-Interscience, 1994).
-
Die
Verbindungen der Formel (I) können
gemäß den synthetischen
Sequenzen, die in Schemata 1, 2, 3, 4 und 5 geschildert sind, hergestellt
werden und ferner im nachfolgenden Beispielsabschnitt ausführlicher beschrieben
sind.
-
Schema
1 zeigt das Syntheseschema zur Herstellung von N-Alkyl- und N-Benzyl-2-aminobenzimidazol-Derivaten
der Formel (I). Das heißt,
solche Verbindungen der Formel (I), worin D -NRR
1 ist.
In diesem Schema ist R Wasserstoff, R
1 ist
wie oben definiert und Q stellt 1 oder mehrere Substituenten, wie
durch Q
1, Q
2 und
Q
3 oben definiert, dar. Schema
1
-
Schema
2 zeigt das Syntheseschema zur Herstellung von N-Aryl-2-aminobenzimidazol-Derivaten
der Formel (I). Das heißt,
solche Verbindungen der Formel (I), worin D -NRR
1 ist.
In diesem Schema ist R Wasserstoff, R
1 ist
Aryl oder Arylalkyl und Q stellt einen oder mehrere Substituenten,
wie durch Q
1, Q
2 und
Q
3 oben definiert, dar. Schema
2
-
Schema
3 zeigt das Syntheseschema zur Herstellung von Alkylthiobenzimidazol-Derivaten
der Formel (I). Das heißt,
solche Verbindungen der Formel (I), worin D -SR
1,
-S(O)R
1 oder -S(O)
2R
1 ist. In diesem Schema ist R
1 wie
oben definiert, n ist 1 oder 2, und Q stellt einen oder mehrere
Substituenten, wie durch Q
1, Q
2 und Q
3 oben definiert, dar. Schema
3
-
Schema
4 zeigt das Syntheseschema zur Herstellung von Endstücken von
Aminobenzimidazol-Derivaten der Formel (I). Das heißt, solche
Verbindungen der Formel (I), worin Q 1 oder mehrere Substituenten, wie
durch Q
1, Q
2 und
Q
3 oben definiert, darstellt. Ebenfalls
sind R
8 und R
9 wie
oben definiert. Schema
4
-
Schema
5 zeigt das Syntheseschema zur Herstellung von 2-Alkoxy-, 2-Phenoxy-
und 2-Thiophenoxybenzimidazol-Derivaten der Formel (I). Das heißt, solche
Verbindungen der Formel (I), worin X ein Heteroatom von D, wie oben
definiert, ist, R
1 Alkoxy, Aryloxy oder
Aralkoxy ist, n 1 oder 2 ist, und Q 1 oder mehrere Substituenten,
wie durch Q
1, Q
2 und
Q
3 oben definiert, darstellt. Schema
5
-
Schema
6 zeigt das Syntheseschema zur Herstellung von Benzimidazolheteroarylamin-Derivaten
der Formel (I), worin Oxazol als eine spezifische Heteroaryl-Gruppe
verwendet wird: Schema
6
-
Schema
7 zeigt nachfolgend ein Syntheseschema für die Herstellung von Benzimidazolamiden
der Formel (I) und (II). R
1 ist wie oben
definiert und Q stellt Q
1, Q
2 und/oder
Q
3, wie oben definiert, dar. Schema
7
-
Bestimmte
Ausführungsformen
der vorliegenden Erfindung werden nun durch Beispiele alleine veranschaulicht.
Die physikalischen Daten, die für
exemplarischen Verbindungen angegeben sind, sind konsistent mit
den zugeordneten Strukturen dieser Verbindungen.
-
Beispiele
-
Wie
hier verwendet sind die in diesen Verfahren, Schemata und Beispielen
verwendeten Symbole und Konventionen konsistent mit denen, die in
der wissenschaftlichen Gegenwartsliteratur, zum Beispiel dem Journal
of the American Chemical Society oder dem Journal of Biological
Chemistry, verwendet werden. Standard-Ein-Buchstaben- oder Drei-Buchstaben-Abkürzungen
werden im allgemeinen verwendet, um Aminosäurereste soweit nicht anders
vermerkt zu bezeichnen, von denen angenommen wird, daß sie in
der L-Konfiguration
sind. Soweit nicht anders vermerkt, wurden alle Ausgangsmaterialien
von kommerziellen Lieferanten erhalten, und ohne weitere Rufreinigung
verwendet. Speziell die folgenden Abkürzungen können in den Beispielen über die
gesamte Beschreibung verwendet werden:
- g
- (Gramm);
- mg
- (Milligramm);
- l
- (Liter);
- ml
- (Milliliter);
- μl
- (Mikroliter);
- psi
- (Pfund pro Quadratinch);
- M
- (molar);
- mM
- (Millimolar;
- i.v.
- (intravenös);
- Hz
- (Hertz);
- MHz
- (Megahertz);
- mol
- (Mol);
- mmol
- (Millimol);
- Rt
- (Raumtemperatur);
- min
- (Minuten);
- h
- (Stunden);
- Smp.
- (Schmelzpunkt);
- TLC
- (Dünnschichtchromatographie);
- Tr
- (Retentionszeit);
- RP
- (reverse-Phase);
- MeOH
- (Methanol);
- i-PrOH
- (Isopropanol);
- TEA
- (Triethylamin);
- TFA
- (Trifluoressigsäure);
- TFAA
- (Trifluoressigsäureanhydrid);
- THF
- (Tetrahydrofuran);
- DMSO
- (Dimethylsulfoxid);
- AcOEt
- (Ethylacetat);
- DME
- (1,2-Dimethoxyethan);
- DCM
- (Dichlormethan);
- DCE
- (Dichlorethan);
- DMF
- (N,N-Dimethylformamid);
- DMPU
- (N,N'-Dimethylpropylenharnstoff);
- CDI
- (1,1-Carbonyldiimidazol);
- IBCF:
- (Isobutylchlorformiat);
- HOAc
- (Essigsäure);
- HOSu
- (N-Hydroxysuccinimid);
- HOBt
- (1-Hydroxybenzotriazol;
- mCPBA
- (meta-Chlorperbenzoesäure;
- EDC
- (Ethylcarbodiimidhydrochlorid);
- BOC
- (tert-Butyloxycarbonyl);
- FMOC
- (9-Fluorenylmethoxycarbonyl);
- DCC
- (Dicyclohexylcarbodiimid);
- CBZ
- (Benzyloxycarbonyl);
- Ac
- (Acetyl);
- atm
- (Atmosphäre);
- TMSE
- (2-(Trimethylsilyl)ethyl);
- TMS
- (Trimethylsilyl);
- TIPS
- (Triisopropylsilyl);
- TBS
- (t-Butyldimethylsilyl);
- DMAP
- (4-Dimethylaminopyridin);
- BSA
- (Rinderserumalbumin);
- ATP
- (Adenosintriphosphat);
- HRP
- (Meerrettichperoxidase);
- DMEM
- (Dulbecco's modifiziertes Eaglemedium);
- HPLC
- (Hochdruckflüssigchromatographie);
- BOP
- (Bis(2-oxo-3-oxazolidinyl)phosphinchlorid);
- TRAF
- (tetra-n-Butylammoniumfluorid);
- HBTU
- (O-Benzotriazol-1-yl-N,N,N',N'-tetramethyluroniumhexa
fluorphosphat);
- HEPES
- (4-(2-Hydroxyethyl)-1-piperazinethansulfonsäure);
- DPPA
- (Diphenylphosphorylazid);
- fHNO3
- (rauchendes HNO3); und
- EDTA
- (Ethylendiamintetraessigsäure).
-
Alle
Verweise auf Ether beziehen sich auf Diethylether; Salzlösung bezieht
sich auf eine gesättigte wäßrige Lösung aus
NaCl. Soweit nicht anders angegeben, werden alle Temperaturen in °C (Grad Celsius) ausgedrückt. Alle
Reaktionen werden unter einer inerten Atmosphäre bei Raumtemperatur, soweit
nicht anders angegeben, durchgeführt.
-
1H-NMR-Spektren wurden auf einem Varian VXR-300,
einem Varian Unity-300,
einem Varian Unity-400-Instrument, einem Brucker AVANCE-400, oder
einem General Electric QE-300 aufgenommen. Chemische Verschiebungen
werden in Teile pro Million (ppm, 6-Einheiten) ausgedrückt. Kupplungskonstanten
sind in Hertz (Hz)-Einheiten. "Splitting-Muster" beschreiben die
apparenten Multiplizitäten
und werden als s (Singulett), d (Doublett), t (Triplett), q (Quartett),
quint (Quintett), m (Multiplett), br (breit) bezeichnet.
-
HPLC
wurden auf einem Gilson-HPLC- oder Shimazi-HPLC-System mit den folgenden
Bedingungen aufgezeichnet. Säule:
50 × 4,6
mm (id) rostfreier Stahl, gepackt mit 5 μm Phenomenex Lunda C-18; Flußrate: 2,0
ml/min; mobile Phase: A-Phase = 50 mM Ammoniumacetat (pH 7,4), B-Phase
= Acetonitril, 0-0,5
min (A: 100 %, B: 0 %), 0,5-3,0 min (A: 100-0 %, B: 0-100 %), 3,0- 3,5 min (A: 0 %,
B: 100 %), 3,5-3,7 min (A: 0-100 %, B: 100-0 %), 3,7-4,5 min (A: 100 %,
B: 0 %); Detektion: UV 254 nm; Injektionsvolumen: 3 μl.
-
Niedrig-Auflösungsmassenspektren
(MS) wurden auf einem JOEL JMS-AX505HA-,
JOEL SX-102- oder einem SCIEX-APIiii-Spektrometer aufgezeichnet;
LC-MS wurden auf einem Micromass 2MD und Waters 2690 aufgezeichnet;
Hochauflösungs-MS
wurde unter Verwendung eines JOEL SX-102A-Spektrometers erhalten.
Alle Massenspektren wurden unter Elektrosprayionisation (ESI), chemischer
Ionisation (CI), Elektronenimpact (EI) oder durch "fast atom bombardment
(FAB)"-Verfahren
genommen. Infrarot (IR)-Spektren wurde auf einem Nicolet 510 FT-IR-Spektrometer
unter Verwendung einer 1-mm-NaCl-Zelle erhalten. Zusätzliche Massenspektren
wurden auf einem Open-Access-LC/MS-System unter Verwendung von Elektrosprayionisation
durchgeführt.
LC-Bedingungen:
4,5 % bis 90 % CH3CN (0,02 % TFA) in 3,2
min mit einer Haltezeit von 0,4 min und 1,4 min Reäquilibrierung;
Detektion durch MS, UV bei 214 nm, und einem Lichtstreuungsdetektor (ELS).
Säule:
1 × 40
mm Aquasil (C18).
-
Die
meisten der Reaktionen wurden durch Dünnschichtchromatographie auf
0,25 mm E. Merck Kieselgelplatten (60F-254) überwacht, und mit UV-Licht, 5 % ethanolische
Phosphomolybdänsäure oder
p-Anisaldehyd-Lösung
sichtbar gemacht. "Flash"-Säulenchromatographie
wurde auf Kieselgel (230-400
mesh, Merck) durchgeführt.
-
Zwischenprodukt Beispiel 1
-
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-N
2-(1-methylethyl-1H-benzimidazol-2,5-diamin
-
(A)
N
1-Methyl-4-nitro-1,2-benzoldiamin
-
Zu
einer Lösung
aus 2-Fluor-5-nitroanilin (5 g, 32 mmol) in 40 ml N-Methylpyrrolidinon
in einem versiegelten Reaktionsgefäß wurde Kaliumcarbonat (9,0
g, 50,0 mmol) und eine Lösung
aus Methylamin (32 ml, 2M in THF) hinzugegeben, und die Reaktion
wurde auf 120°C
erhitzt. Nach 16 h wurde das Reaktionsgemisch auf Raumtemperatur
abgekühlt
und in 400 ml Wasser gegossen. Das resultierende Präzipitat
wurde filtriert und getrocknet, um die Titelverbindung als einen
roten Feststoff hervorzubringen.
1H-NMR
(300 MHz, d
6-DMSO) δ: 7,54 (dd, J = 8,7 und 2,7Hz,
1H), 7,39 (d, J = 2,7Hz, 1H), 6,41 (d, J = 8,7Hz, 1H), 6,13 (s,
1H), 5,08 (s, 2H), 2,83 (s, 3H). (B)
1-Methyl-N-(1-methylethyl)-5-nitro-1H-benzimidazol-2-amin
-
Zu
einer Lösung
aus N
1-Methyl-4-nitro-1,2-benzoldiamin (2,0
g, 12,0 mmol) in Pyridin (20 ml) wurde Isopropylisothiocyanat (1,41
g, 13,2 mmol) hinzugegeben und das Gemisch auf 90°C erhitzt.
Nach 1 h wurde 1-Cyclohexyl-3-(2-morpholinoethyl)carbodiimidmetho-p-toluolsulfonat
(6,6 g, 15,6 mmol) hinzugegeben und das Gemisch auf 90°C erhitzt.
Nach 16 h wurde das Reaktionsgemisch auf Raumtemperatur abgekühlt, filtriert und
zu einem roten Rückstand
aufkonzentriert. Dieser wurde in EtOAc aufgelöst und mit Wasser (4 × 125 ml) gewaschen.
Die organische Schicht wurde über
MgSO
4 getrocknet und zu einem orangefarbenen
Feststoff aufkonzentriert. MeOH wurde hinzugegeben und der Feststoff
filtriert und getrocknet, um die Titelverbindung als einen orangefarbenen
Feststoff hervorzubringen (2,4 g, 85 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 7,88 (dd, j = 8,7 und 2,4Hz),
7,30 (d, J = 8,7Hz, 1H), 6,89 (d, J = 7,5Hz, 1H), 4,08 (m, 1H),
3,56 (s, 3), 1,25 (d, J = 6,6Hz, 6H).
MS (ESI) m/z = 235 [M+H]
+. (C)
1-Methyl-N
2-(1-methylethyl)-1H-benzimidazol-2,5-diamin
-
Zu
einer Lösung
aus 1-Methyl-N-(1-methylethyl)-5-nitro-1H-benzimidazol-2-amin (2,15 g, 9,2 mmol) und
10 % Pd/C(500 mg) in Ethanol (60 ml) wurde Hydrazin (5 ml) hinzugegeben
und das Reaktionsgemisch auf 80°C
erhitzt. Nachdem eine TLC zeigte, daß das Ausgangsmaterial aufgebraucht
war, wurde die Reaktion auf Raumtemperatur abgekühlt und durch einen Pfropfen
aus Celite passiert. Das Filtrat wurde aufkonzentriert, um die Titelverbindung
als einen cremefarbenen Feststoff zu ergeben.
1H-NMR
(300 MHz, d
6-DMSO) δ: 6,75 (d, J = 8,1Hz, 1H), 6,45
(d, J = 1,8Hz, 1H), 6,20 (dd, J = 8,1 und 2,1Hz, 1H), 6,06 (d, J
= 7,8Hz, 1H), 4,43 (br s, 2H), 3,96 (m, 1H), 3,35 (s, 3H), 1,19
(d, J = 6,6Hz, 6H). (D)
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-N
2-(1-methylethyl)-1H-benzimidazol-2,5-diamin
-
Zu
einer Lösung
aus 1-Methyl-N2-(1-methylethyl)-1H-benzimidazol-2,5-diamin (1,46 g, 7,2
mmol) in THF (7 ml) und Ethanol (21 ml) wurde NaHCO3 (1,81
g, 21,6 mmol) und 2,4-Dichlorpyrimidin (2,68 g, 18 mmol) hinzugegeben
und die Reaktion auf 75°C
erhitzt. Nach 5 h wurde die Reaktion heiß abfiltriert und zu einem grauen
Schaum aufkonzentriert. Ether wurde hinzugegeben, und der Feststoff
wurde filtriert und getrocknet, um N5-(2-Chlor-pyrimidin-4-yl)-N2-isopropyl-1-methyl-1H-benzimidazol-2,5-diamin
als einen cremefarbenen Feststoff zu ergeben.
-
N5-(2-Chlor-pyrimidin-4-yl)-N2-isopropyl-1-methyl-1H-benzimidazol-2,5-diamin wurde
in DMF (21 ml) aufgelöst
und Cäsiumcarbonat
(6,84 g, 21 mmol) wurde hinzugegeben. Nach 15 min wurde Iodmethan
(0,70 ml, 11,2 mmol) hinzugegeben und die Reaktion bei RT gerührt. Nachdem
eine TLC zeigte, daß das
Ausgangsmaterial aufgebraucht war, wurde die Reaktion mit Wasser
verdünnt.
Die wäßrige Schicht
wurde mit EtOAc extrahiert. Die kombinierten organischen Schicht
wurdem mit Wasser gewaschen, über
MgSO4 getrocknet und zu einem roten Schaum
aufkonzentriert. Das Rohmaterial wurde mit Kieselgel gereinigt,
um die Titelverbindung als weißen
Feststoff zu ergeben (1,10 g, 46 % über zwei Schritte).
1H-NMR (300 MHz, d6-DMSO) δ: 7,87 (d,
J = 6,0Hz, 1H), 7,22 (d, J = 8,1Hz, 1H), 7,11 (1,8Hz, 1H), 6,82
(dd, J = 8,1 und 1,8Hz, 1H), 6,53 (d, J = 7,5Hz, 1H), 6,09 (d, J
= 6,0Hz, 1H), 4,04 (m, 1H), 3,51 (s, 3H), 3,37 (s, 3H), 1,23 (d,
J = 6,6Hz, 6H).
MS (ESI) m/z = 331 [M+H]+.
-
Zwischenprodukt Beispiel 2
-
N
2-(2-Chlor-4-pyrimidinyl)-N
2,N
5,1-trimethyl-1H-benzimidazol-2,5-diamin
-
(A)
N,1-Dimethyl-5-nitro-1H-benzimidazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (2,0 g,
12,0 mmol) und Methylisothiocyanat (0,90 ml, 13,2 mmol) wurden unter
Verwendung des Verfahrens von Beispiel 1, Teil B, verknüpft, um
die Titelverbindung als einen gelben Feststoff zu ergeben (1,32
g, 53 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
7,98 (d, J = 2,1Hz, 1H), 7,90 (dd, J = 8,7 und 2,4Hz, 1H), 7,32
(d, J = 8,7Hz, 1H), 7,15 (m, 1H), 3,55 (d, 3H), 2,95 (d, J = 4,5Hz,
3H). (B)
N
2,1-Dimethyl-1H-benzimidazol-2,5-diamin
-
N,1-Dimethyl-5-nitro-1H-benzimidazol-2-amin
wurde unter Verwendung des Verfahrens aus Beispiel 1, Teil C, reduziert,
um die Titelverbindung als einen weißen Feststoff zu ergeben.
1H-NMR: δ (300
MHz, CD
3OD) δ: 7,50 (m, 2H), 7,31 (dd, J
= 8,7 und 2,1Hz, 1H), 3,13 (s, 3H).
MS (ESI) m/z = 163 [M+H]
+. (C)
N
5-(2-Chlor-4-pyrimidinyl)-N
2,N
5,1-trimethyl-1H-benzimidazol-2,5-diamin
-
N2,1-Dimethyl-1H-benzimidazol-2,5-diamin wurde
gemäß dem Verfahren
aus Beispiel 1, Teil D, verknüpft
und methyliert, um die Titelverbindung als einen weißen Feststoff
zu ergeben.
1H-NMR (400 MHz, d6-DMSO) δ:
7,85 (d, J = 6,0Hz, 1H), 7,21 (d, J = 8,0Hz, 1H), 6,92 (dd, J =
8,4 und 2,0Hz, 1H), 6,77 (m, 1H), 6,07 (br s, 1H), 3,48 (s, 3H),
3,36 (s, 3H), 2,89 (d, J = 4,4Hz, 3H).
-
Zwischenprodukt Beispiel 3
-
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-N
2-(phenylmethyl)-1H-benzimidazol-2,5-diamin
-
(A)
1-Methyl-5-nitro-N-(phenylmethyl)-1H-benzimidazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (2,0 g,
12,0 mmol) und Benzylisothiocyanat (1,75 ml, 13,2 mmol) wurden unter
Verwendung des Verfahrens aus Beispiel 1, Teil B, verknüpft, um
die Titelverbindung als einen gelben Feststoff zu ergeben (2,4 g,
71 %).
1H-NMR (300 MHz, d
6-DMSO) δ: 7,97 (d,
J = 2,4Hz, 1H), 7,90 (dd, J = 8,7 und 2,4Hz, 1H), 7,77 (t, J = 5,7Hz, 1H),
7,21-7,41 (m, 6H), 4,63 (d, J = 5,7Hz, 2H), 3,62 (s, 3H) ppm. (B)
1-Methyl-N
2-(phenylmethyl)-1H-benzimidazol-2,5-diamin
-
1-Methyl-5-nitro-N-(phenylmethyl)-1H-benzimidazol-2-amin
(2,4 g, 8,5 mmol) wurde unter Verwendung des Verfahrens aus Beispiel
1, Teil C, reduziert, um die Titelverbindung als einen weißen Schaum
zu ergeben (2,01 g, 94 %).
1H-NMR (300
MHz, d
6-DMSO) δ: 7,28-7,39 (m, 4H), 7,22 (m,
1H), 7,01 (t, J = 5,7Hz, 1H), 6,79 (d, J = 8,1Hz, 1H), 6,44 (d,
J = 1,8Hz, 1H), 6,23 (dd, J = 8,2 und 1,9Hz, 1H), 4,54 (d, J = 5,7Hz,
2H), 3,42 (s, 3H). (C)
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-N
2-(phenylmethyl)-1H-benzimidazol-2,5-diamin
-
1-Methyl-N2-(phenylmethyl)-1H-benzimidazol-2,5-diamin
(2,01 g, 8 mmol) wurde gemäß dem Verfahren
aus Beispiel 1, Teil D, verknüpft
und methyliert, um die Titelverbindung als einen weißen Feststoff
zu ergeben (1,20 g, 40 %).
1H-NMR (300
MHz, d6-DMSO) δ: 7,86 (d, J = 6,0Hz, 1H), 7,23-7,46
(m, 7H), 7,11 (d, J = 1,8Hz, 1H), 6,84 (dd, J = 8,2 und 1,9Hz, 1H),
6,08 (d, J = 5,4Hz, 1H), 4,60 (d, J = 5,7Hz, 2H), 3,57 (s, 3H),
3,36 (s, 3H).
MS (ESI) m/z = 379 [M+H]+.
-
Zwischenprodukt Beispiel 4
-
1,1-Dimethylethyl{5-(2-chlor-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}phenylcarbamat
-
(A)
1-Methyl-5-nitro-N-phenyl-1H-benzimidazol-2-amin
-
Eine
Lösung
Phenylisothiocyanat (1,58 ml, 13,2 mmol) und 1-Cyclohexyl-3-(2-morpholinoethyl)carbodiimid-metho-p-toluolsulfonat
(6,6 g, 15,6 mmol) wurde in Pyridin (20 ml) bei 90°C gerührt. Nach
2 Stunden wurde N
1-Methyl-4-nitro-benzol-1,2-diamin
zugegeben und die Reaktion über
Nacht erhitzt. Die Reaktion wurde abgekühlt und zu einem roten Feststoff
aufkonzentriert. Dieser wurde in EtOAc aufgelöst und mit Wasser gewaschen.
Die organische Schicht wurde über
MgSO
4 getrocknet und zu einem roten Feststoff
aufkonzentriert. Dieser wurde in MeOH gerührt, filtriert und getrocknet,
um die Titelverbindung als einen orangefarbenen Feststoff zu ergeben
(1,97 g, 62 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
8,23 (s, 1H), 8,17 (d, J = 1,8Hz, 1H), 8,02 (dd, J = 8,7 und 2,1Hz,
1H), 7,89 (d, J = 8,1Hz, 2H), 7,50 (d, J = 8,7Hz, 1H), 7,36 (m,
2H), 7,02 (m, 1H), 3,79 (s, 1H) ppm.
MS (ESI) m/z = 269 [M+H]
+. (B)
1,1-Dimethylethyl(1-methyl-5-nitro-1H-benzimidazol-2-yl)phenyl carbamat
-
Zu
einer Lösung
aus Methyl-5-nitro-N-phenyl-1H-benzimidazol-2-amin (1,97 g, 7,4
mmol) in THF (30 ml) wurde Cäsiumcarbonat
(4,82 g, 14,8 mmol) und Di-tert-butyldicarbonat (2,42 g, 11,1 mmol)
hinzugegeben und die Reaktion bei Raumtemperatur für 18 h gerührt. Die
Reaktion wurde mit Wasser verdünnt
und mit EtOAc extrahiert. Die vereinigten organischen Schichten
wurden mit Wasser gewaschen, über
MgSO
4 getrocknet und zu einem gelben Feststoff
aufkonzentriert. Das Rohmaterial wurde durch Kieselgel aufgereinigt,
um die Titelverbindung als einen gelben Feststoff zu ergeben (1,11
g, 41 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
8,50 (d, J = 2,4Hz, 1H), 8,23 (dd, J = 9,0 und 2,1Hz, 1H), 7,84
(d, J = 9,0Hz, 1H), 7,40 (m, 4H), 7,29 (m, 1H), 3,83 (s, 3H), 1,40
(s, 9H) ppm. (C)
1,1-Dimethylethyl(5-amino-1-methyl-1H-benzimidazol-2-yl)phenylcarbamat
-
1,1-Dimethyl(1-methyl-5-nitro-1H-benzimidazol-2-yl)phenylcarbamat
(1,11 g, 3 mmol) wurde durch das Verfahren aus Beispiel 1, Teil
C, reduziert, um die Titelverbindung als einen weißen Feststoff
zu ergeben (1,03 g, > 95
%).
1H-NMR (300 MHz, d
6-DMSO) δ: 7,31-7,40
(m, 4H), 7,19-7,26 (m, 2H), 6,70 (d, J = 1,8Hz, 1H), 6,63 (dd, J
= 8,1 und 1,8Hz, 1H), 4,78 (br s, 2H), 3,60 (s, 3H), 1,39 (s, 9H). (D)
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)amino]-1-methyl-1H- benzimidazol-2-yl}phenylcarbamat
-
Zu
einer Lösung
aus 1,1-Dimethylethyl(5-amino-1-methyl-1H-benzimidazol-2-yl)phenylcarbamat (1,03 g,
3,0 mmol) in THF (3 ml) und Ethanol (9 ml) wurde NaHCO
3 (0,76
g, 9,0 mmol) und 2,4-Dichlorpyrimidin (0,89 g, 6,0 mmol) hinzugegeben,
und die Reaktion wurde auf 75°C
erhitzt. Nach 5 h wurde die Reaktion heiß filtriert und zu einem grauen
Schaum aufkonzentriert. Das Rohmaterial wurde auf Kieselgel aufgereinigt,
um die Titelverbindung als einen weißen Schaum zu ergeben (0,98
g, 73 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
10,00 (s, 1H), 8,10 (d, J = 5,7Hz, 1H), 7,89 (s, 1H), 7,58 (d, J
= 9,0Hz, 1H), 7,36-7,39 (m, 5H), 7,24-7,34 (m, 1H), 6,70 (d, J =
6,0Hz, 1H), 3,73 (s, 3H), 1,40 (s, 9H). (E)
1,1-Dimethyl{5-[(2-chlor-4-pyrimidinyl)(methyl)amino}-1-methyl-1H-benzimidazol-2-yl}phenylcarbamat
-
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)amino]-1-methyl-1H-benzimidazol-2-yl}phenylcarbamat (0,97
g, 2,2 mmol) wurde in DMF (10 ml) aufgelöst und Cäsiumcarbonat (2,15 g, 6,6 mmol)
hinzugegeben. Nach 15 min wurde Iodmethan (0,20 ml, 3,3 mmol) zugegeben,
und die Reaktion wurde bei Raumtemperatur gerührt. Nachdem eine TLC zeigte,
daß das
Ausgangsmaterial verbraucht wurde, wurde die Reaktion mit Wasser
verdünnt.
Die wäßrige Schicht
wurde mit EtOAc extrahiert. Die vereinigten organischen Schichten
wurden mit Wasser gewaschen, über
MgSO4 getrocknet und zu einem roten Schaum
aufkonzentriert. Das Rohmaterial wurde durch Kieselgel aufgereinigt,
um die Titelverbindung als einen weißen Feststoff zu ergeben (0,80
g, 78 % über
zwei Schritte).
1H-NMR (300 MHz, d6-DMSO) δ:
7,90 (d, J = 6,3Hz, 1H), 7,72 (d, J = 8,7Hz, 1H), 7,60 (d, J = 1,8Hz,
1H), 7,38 (m, 4H), 7,25-7,29 (m, 2H), 6,17 (d, J = 5,7Hz, 1H), 3,78
(s, 3H), 3,41 (s, 3H), 1,41 (s, 9H).
MS (ESI) m/z = 465 [M+H]+.
-
Zwischenprodukt Beispiel 5
-
2-Methyl-N-(methyloxy)-5-nitrobenzolsulfonamid
-
4-Nitrotoluol
(15 g, 73 mmol) wurde zu kalter Chlorsulfonsäure (25 ml, 365 mmol) in 0,5
g-Portionen über
einen Zeitraum von 10 Minuten hinzugegeben. Die Lösung wurde
in einem Eisbad für
10 min gerührt, dann
in ein 65°C-Ölbad plaziert
und bis zu 7 h bei offener Luftzufuhr erhitzt. Die resultierende
dunkelbraune Lösung
wurde auf Raumtemperatur abgekühlt,
dann langsam in eine Eiswasserlösung
(400 ml) gegossen. Die wäßrige Suspension
wurde mit EtOAc extrahiert. Die organischen Schichten wurden mit
MgSO4 getrocknet und zu einem braunen Öl aufkonzentriert,
das in 1,4-Dioxan (100 ml) aufgelöst und mit Methoxylaminhydrochlorid
(50 ml einer 25%igen wäßrigen Lösung, 1,65
mmol, Aldrich) vereinigt. Diese Lösung wurde in einem Eisbad
gekühlt,
und mit Triethylamin (30 ml) behandelt, dann bei Raumtemperatur
für 18
h gerührt.
Eiswasser wurde hinzugegeben (100 ml) und die Lösung wurde mit EtOAc extrahiert.
Die organischen Schichten wurden mit MgSO4 getrocknet
und zu einem braunen Feststoff aufkonzentriert (16 g, 67 mmol).
1H-NMR (300 MHz, d6-DMSO) δ: 10,9 (s,
1H), 8,58 (s, 1H), 8,42 (d, J = 8,4Hz, 1H), 7,76 (d, J = 8,4Hz,
1H), 3,68/sm 3H), 2,72 (s, 3H).
-
Zwischenprodukt Beispiel 6
-
5-Amino-2-methyl-N-(methyloxy)benzolsulfonamid
-
N-Methoxy-2-methyl-5-nitrobenzolsulfonamid
(0,5 g, 2 mmol) wurde mit 10 % Palladium auf Aktivkohle (0,05 g),
Ethanol (10 ml) und Hydrazin (1 ml) vereinigt und unter Rückfluß für 18 h erhitzt.
Die Lösung
wurde durch Celite filtriert, aufkonzentriert und auf Kieselgel
mit Methanol in Dichlormethan aufgereinigt. Das Produkt war ein
cremefarbene Feststoff (0,28 g, 1,3 mmol).
1H-NMR
(300 MHz, d6-DMSO) δ: 10,3 (s, 1H), 7,11 (s, 1H),
7,02 (d, J = 8,2Hz, 1H), 6,7 (d, J = 8,2Hz, 1H), 5,37 (s, 2H), 3,57
(s, 3H), 2,38 (s, 3H).
-
Zwischenprodukt Beispiel 7
-
N
5-(2-Chlor-4-pyrimidinyl)-N
2-[(4-fluorphenyl)methyl]-N
5,1-dimethyl-1H-benzimidazol-2,5-diamin
-
(A)
N-[(4-Fluorphenyl)methyl]-1-methyl-5-nitro-1H-benzimidazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (2,0 g,
12 mmol) und 4-Fluorbenzylisothiocyanat (2,21 g, 13,2 mmol) wurden
unter Verwendung des Verfahrens aus Zwischenprodukt Beispiel 1,
Teil B, verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (2,16
g, 60 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
7,96 (d, J = 1,8hz, 1H), 7,89 (dd, J = 6,6 und 1,8Hz, 1H), 7,76
(t, J = 4,5Hz, 1H), 7,42 (m, 2H), 7,34 (d, J = 6,6Hz, 1H), 7,13
(t, J = 6,6Hz, 2H), 4,59 (d, J = 4,5Hz, 2H), 3,60 (s, 3H). (B)
N
2-[(4-Fluorphenyl)methyl]-1-methyl-1H-benzimidazol-2,5-diamin
-
N-[(4-Fluorphenyl)methyl]-1-methyl-5-nitro-1H-benzimidazol-2-amin
(2,16 g, 7,2 mmol) wurde unter Verwendung des Verfahrens aus Zwischenprodukt
Beispiel 1, Teil C, reduziert, um die Titelverbindung als einen
weißen
Feststoff zu ergeben (1,77 g, 70 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 7,39-7,44 (m, 2H), 7,10-7,16
(m, 2H), 6,96-6,99 (m, 1H), 6,79 (d, J = 8,1Hz, 1H), 6,44 (d, J
= 2,1Hz, 1H), 6,23 (dd, J = 8,1 und 1,8Hz, 1H), 4,51 (s, 2H), 3,93
(s, 2H), 3,42 (s, 3H). (C)
N
5-(2-Chlor-4-pyrimidinyl)-N
2-[(4-fluorphenyl)methyl]-N
5,1-dimethyl-1H-benzimidazol-2,5-diamin
-
N2-[(4-Fluorphenyl)methyl]-1-methyl-1H-benzimidazol-2,5-diamin
wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil D, verknüpft und methyliert, um die
Titelverbindung als einen weißen
Feststoff zu ergeben (603 mg, 23 % über zwei Schritte).
1H-NMR (300 MHz, d6-DMSO) δ: 7,86 (d,
J = 6,0Hz, 1H), 7,40-7,47 (m, 3H), 7,26 (d, J = 8,1Hz, 1H), 7,11-7,14 (m,
3H), 6,85 (dd, J = 8,1 und 1,8Hz, 1H), 6,08 (d, J = 5,4Hz, 1H),
4,57 (d, J = 5,7Hz, 2H), 3,56 (s, 3H), 3,37 (s, 3H).
MS (ESI)
m/z = 397 [M+H]+.
-
Zwischenprodukt Beispiel 8
-
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-N
2-{[4-(methyloxy)phenyl]methyl}-1H-benzimidazol-2,5-diamin
-
(A)
1-Methyl-N-{[4-(methyloxy)phenyl]methyl}-5-nitro-1H-benzimidazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (2,0 g,
12 mmol) und 4-Methoxybenzylisothiocyanat (2,37 g, 13,2 mmol) wurden
unter Verwendung des Verfahrens aus Zwischenprodukt Beispiel 1,
Teil B, verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (2,00
g, 41 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
7,98 (d, J = 2,1Hz, 1H), 7,90 (dd, J = 8,7 und 2,1Hz, 1H), 7,68
(t, J = 5,7Hz, 1H), 7,32-7,35 (m, 3H), 6,859 (d, J = 8,7Hz, 2H),
4,55 (d, J = 5,7Hz, 2H), 3,72 (s, 3H), 3,61 (s, 3H). (B)
1-Methyl-N
2-{[4-(methyloxy)phenyl]methyl}-1H-benzimidazol-2,5-diamin
-
1-Methyl-N-{[4-(methyloxy)phenyl]methyl}-5-nitro-1H-benzimidazol-2-amin (1,99 g, 4,9
mmol) wurden unter Verwendung des Verfahrens aus Zwischenprodukt
Beispiel 1, Teil C, reduziert, um die Titelverbindung als einen
weißen
Feststoff zu ergeben (1,68 g, 91 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 7,30 (d, J = 8,1Hz, 2H), 6,87
(m, 3H), 6,78 (d, J = 8,4Hz, 1H), 6,45 (s, 1H), 6,22 (d, J = 8,1Hz,
1H), 4,45 (d, J = 2,1Hz, 2H), 4,21 (br s, 2H), 3,71 (s, 3H), 3,39
(s, 3H). (C)
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-N
2-{[4-(methyloxy)phenyl]methyl}-1H-benzimidazol-2,5-diamin
-
1-Methyl-N2-{[4-(methyloxy)phenyl]methyl}-1H-benzimidazol-2,5-diamin
wurden gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil D, verknüpft und methyliert, um die
Titelverbindung als einen cremefarbenen Feststoff zu ergeben (910
mg, 51 % über
zwei Schritte).
1H-NMR (300 MHz, d6-DMSO) δ:
7,86 (d, J = 6,0Hz, 1H), 7,30-7,37 (m, 3H), 7,24 (d, J = 8,1Hz,
1H), 7,11 (d, J = 1,5Hz, 1H), 6,82-6,89 (M, 3H), 6,09 (d, J = 5,4Hz,
1H), 4,52 (d, J = 5,7Hz, 2H), 3,72 (s, 3H), 3,55 (s, 3H), 3,37 (s,
3H).
MS (ESI) m/z = 409 [M+H]+.
-
Zwischenprodukt Beispiel 9
-
N
5-(2-Chlor-4-pyrimidinyl)-N
2-[(3-fluorphenyl)methyl]-N
5,1-dimethyl-1H-benzimidazol-2,5-diamin
-
(A)
N-[(3-Fluorphenyl)methyl]-1-methyl-5-nitro-1H-benzimidazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (1,4 g,
8,4 mmol) und 3-Fluorbenzylisothiocyanat (1,26 ml 9,2 mmol) wurde
unter Verwendung des Verfahrens aus Zwischenprodukt Beispiel 1,
Teil B, verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergebe (1,40
g, 56 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
7,98 (d, J = 2,1Hz, 1H), 7,92 (dd, J = 8,4 und 2,1Hz, 1H), 7,81
(t, J = 5,7Hz, 1H), 7,34-7,41 (m, 2H), 7,20-7,25 (M, 2H), 7,07 (dt,
J = 8,7 und 2,4Hz, 1H), 4,65 (d, J = 5,7Hz, 2H), 3,64 (s, 3H). (B)
N
2-[(Fluorphenyl)methyl]-1-methyl-1H-benzimidazol-2,5-diamin
-
N-[(3-Fluorphenyl)methyl]-1-methyl-5-nitro-1H-benzimidazol-2-amin
(1,39 g, 4,6 mmol) wurden unter Verwendung des Verfahrens aus Zwischenprodukt
Beispiel 1, Teil C, reduziert, um die Titelverbindung als einen
weißen
Feststoff zu ergeben (1,12 g, 90 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 7,30-7,38 (m, 1H), 7,16-7,22
(m, 2H), 7,00-7,06 (M, 2H), 6,79 (d, J = 8,4Hz, 1H), 6,43 (d, J
= 1,8Hz, 1H), 6,23 (dd, J = 8,1 und 2,1Hz, 1H), 4,54 (d, J = 4,5Hz,
2H), 4,42 (br s, 2H), 3,42 (s, 3H). (C)
N
5-(2-Chlor-4-pyrimidinyl)-N
2-[(3-fluorphenyl)methyl]-N
5,1-dimethyl-1H-benzimidazol-2,5-diamin
-
N2-[(Fluorphenyl)methyl]-1-methyl-1H-benzimidazol-2,5-diamin
wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil D, verknüpft und methyliert, um die
Titelverbindung als einen gelben Feststoff zu ergeben.
1H-NMR (300 MHz, d6-DMSO) δ: 7,85 (d,
J = 6,0Hz, 1H), 7,48 (t, J = 6,0Hz, 1H), 7,32-7,39 (m, 1H), 7,17-7,27 (m,
3H), 7,11 (d, J = 1,8Hz, 1H), 7,04 (m, 1H), 6,85 (dd, J = 8,1 und
1,8Hz, 1H), 6,07 (d, J = 5,7Hz, 1H), 4,60 (d, J = 6,0Hz, 2H), 3,58
(s, 3H), 3,36 (s, 3H).
-
Zwischenprodukt Beispiel 10
-
N
2-[(4-Chlorphenyl)methyl]-N
5-(2-Chlor-4-pyrimidinyl-N
5,1-dimethyl-1H-benzimidazol-2,5-diamin
-
(A)
N-[(4-Chlorphenyl)methyl]-1-methyl-5-nitro-1H-benzimdazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (2,0 g,
12,0 mmol) und 4-Chlorbenzylisothiocyanat (2,42 g, 13,2 mmol) wurden
unter Verwendung des Verfahrens aus Zwischenprodukt Beispiel 1,
Teil B, verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (2,82
g, 74 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
7,96 (d, J = 2,1Hz, 1H), 7,90 (dd, J = 8,7 und 2,4Hz, 1H), 7,98
(t, J = 6,0Hz, 1H), 7,33-7,43 (m, 5H), 4,60 (d, J = 5,7Hz, 2H),
3,61 (s, 3H).
MS (ESI) m/z = 317 [M+H]
+. (B)
N
2-[(4-Chlorphenyl)methyl]-1-methyl-1H-benzimidazol-2,5-diamin
-
N-[(4-Chlorphenyl)methyl]-1-methyl-5-nitro-1H-benzimdazol-2-amin
(2,82 g, 8,9 mmol) wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil C, reduziert, um die Titelverbindung
als einen weißen Feststoff
zu ergeben (2,43 g, 96 %).
1H-NMR (300
MHz, d
6-DMSO) δ: 7,33-7,41 (m, 4H), 7,00 (m.
1H), 6,78 (d, J = 8,1Hz, 1H), 6,43 (d, J = 1,8Hz, 1H), 6,22 (dd,
J = 8,4 und 1,8Hz, 1H), 4,51 (m, 2H), 3,40 (s, 3H). (C)
N
2-[(4-Chlorphenyl)methyl]-N
5-(2-Chlor-4-pyrimidinyl-N
5,1-dimethyl-1H-benzimidazol-2,5-diamin
-
N2-[(4-Chlorphenyl)methyl]-1-methyl-1H-benzimidazol-2,5-diamin
(2,43 g, 8,5 mmol) wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil D, verknüpft und methyliert, um die
Titelverbindung als einen rosafarbenen Feststoff zu ergeben (1,93
g, 55 %).
1H-NMR (300 MHz, d6-DMSO) δ:
7,85 (d, J = 6,0Hz, 1H), 7,47 (t, J = 5,7Hz, 1H), 7,34-7,42 (M,
4H), 7,25 (d, J = 8,4Hz, 1H), 7,10 (s, 1H), 6,83 (d, J = 8,4Hz,
1H), 6,01 (D, J = 4,8Hz, 1H), 4,57 (d, J = 5,7Hz, 2H), 3,56 (s, 3H),
3,35 (s, 3H).
MS (ESI) m/z = 413 [M+H]+.
-
Zwischenprodukt Beispiel 11
-
N
5-(2-Chlor-4-pyrimidinyl)-1-ethyl-N
5-methyl-N
2-(phenylmethyl)-1H-benzimidazol-2,5-diamin
-
(A)
N
1-Ethyl-4-nitro-1,2-benzoldiamin(2-amino-4-nitrophenyl)ethylamin
-
2-Fluor-5-nitroanilin
(5 g, 32 mmol) und eine Lösung
aus Ethylamin (32 ml, 2M in THF) wurden gemäß dem Verfahren aus Zwischenprodukt
Beispiel 1, Teil A, verknüpft,
um die Titelverbindung als einen dunkelroten Feststoff zu ergeben
(4,16 g, 72 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
7,51 (dd, J = 8,7 und 2,7Hz, 1H), 7,38 (d, J = 2,7Hz, 1H), 6,44
(d, J = 8,7Hz, 1H), 5,86 (t, J = 4,6Hz, 1H), 5,15 (s, 2H), 3,20
(m, 2H), 1,21 (t, J = 7,2Hz, 3H). (B)
1-Ethyl-5-nitro-N-(phenylmethyl-IH-benzimidazol-2-amin
-
N
1-Ethyl-4-nitro-1,2-benzoldiamin und (2-Amino-4-nitrophenyl)ethylamin
(2,0 g, 11,0 mmol) und Benzylisothiocyanat (1,60 ml, 12,1 mmol)
wurden unter Verwendung des Verfahrens aus Zwischenprodukt Beispiel 1,
Teil B, verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (2,0
g, 61 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
7,96 (d, J = 2,1Hz, 1H), 7,89 (dd, J = 8,7 und 2,1Hz, 1H), 7,80
(t, J = 5,7Hz, 1H), 7,21-7,39 (m, 6H), 4,63 (d, J = 5,7Hz, 2H),
4,16 (q, J = 6,9Hz, 2H), 1,24 (t, J = 6,9Hz, 3H). (C)
1-Ethyl-N
2-(phenylmethyl)-1H-benzimidazol-2,5-diamin
-
1-Methyl-5-nitro-N-(phenylmethyl-1H-benzimidazol-2-amin
(2,0 g, 6,7 mmol) wurden gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil C, reduziert, um die Titelverbindung
als einen weißen
Feststoff zu ergeben (1,6 g, 90 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 7,24-7,38 (m, 4H), 7,21 (m,
1H), 6,99 (m, 1H), 6,80 (d, J = 8,1Hz, 1H), 6,44 (d, J = 1,8Hz,
1H), 6,22 (dd, J = 8,1 und 1,8Hz, 1H), 4,55 (s, 2H), 4,20 (br s,
2H), 3,94 (q, J = 7,2Hz, 2H), 1,17 (t, J = 7,2Hz, 3H). (D)
N
5-(2-Chlor-4-pyrimidinyl)-1-ethyl-N
5-methyl-N
2-(phenylmethyl)-1H-benzimidazol-2,5-diamin
-
1-Ethyl-N2-(phenylmethyl)-1H-benzimidazol-2,5-(1,6
g, 6 mmol) wurde gemäß dem Verfahren
aus dem Zwischenprodukt Beispiel 1, Teil D, verknüpft und
methyliert, um die Titelverbindung als einen weißen Feststoff zu ergeben.
1H-NMR (300 MHz, d6-DMSO) δ: 7,86 (d,
J = 6,0Hz, 1H), 7,47 (t, J = 6,0Hz, 1H), 7,22-7,39 (m, 6H), 7,11
(d, J = 1,8Hz, 1H), 6,84 (dd, J = 8,1 und 1,8Hz, 1H), 6,11 (d, J
= 5,7Hz, 1H), 4,61 (d, J = 5,7Hz, 2H), 4,11 (q, J = 7,2Hz, 2H),
3,37 (s, 3H), 1,25 (t, J = 7,2Hz, 3H).
MS (ESI) m/z = 393 [M+H]+.
-
Zwischenprodukt Beispiel 12
-
N
5-(2-Chlor-4-pyrimidinyl)-N
2-[(2-fluorphenyl)methyl]-N
5,1-dimethyl-1H-benzimdazol-2,5-diamin
-
(A)
N-[(2-Fluorphenyl)methyl]-1-methyl-5-nitro-1H-benzimidazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (2,0 g,
12 mmol) und 2-Fluorbenzylisothiocyanat (1,81 ml, 13,2 mmol) wurden
unter Verwendung des Verfahrens aus Zwischenprodukt Beispiel 1,
Teil B, verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (2,0
g, 56 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
7,98 (s, 1H), 7,92 (d, J = 8,7Hz, 1H), 7,76 (t, J = 5,7Hz, 1H),
7,47 (m, 1H), 7,28-7,38 (m, 2H), 7,13-7,23 (m, 2H), 4,67 (d, J =
5,7Hz, 2H), 3,64 (s, 3H).
MS (ESI) m/z = 543 [M+H]
+. (B)
N
2-[(2-Fluorphenyl)methyl]-1-methyl-1H-benzimidazol-2,5-diamin
-
N-[(2-Fluorphenyl)methyl]-1-methyl-5-nitro-1H-benzimdazol-2-amin
wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil C, reduziert, um die Titelverbindung
als einen weißen
Feststoff zu ergeben (1,74 g, 97 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 7,42-7,47 (m, 1H), 7,26-7,30
(m, 1H), 7,11-7,10 (m, 2H), 6,97-7,01 (m, 1H), 6,80 (d, J = 8,1Hz,
1H), 6,44/dm H) 2,1Hz, 1H), 6,24 (dd, J = 8,2 und 2,2Hz, 1H), 5,00
(br s, 2H), 4,58 (m, 2H), 3,43 (s, 3H). (C)
N
5-(2-Chlor-4-pyrimidinyl)-N
2-[(2-fluorphenyl)methyl]-N
5,1-dimethyl-1H-benzimdazol-2,5-diamin
-
N2-[(2-Fluorphenyl)methyl]-1-methyl-1H-benzimidazol-2,5-diamin
wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil D, verknüpft und methyliert, um die
Titelverbindung als einen weißen
Feststoff zu ergeben.
1H-NMR (300 MHz,
d6-DMSO) δ:
7,86 (d, J = 6,3Hz, 1H), 7,41-7,48 (m, 2H), 7,26-7,31 (m, 2H), 7,12-7,22
(m, 3H), 6,86 (dd, J = 8,1 und 1,8Hz, 1H), 6,08 (d, J = 5,7Hz, 1H),
4,64 (d, J = 5,7Hz, 2H), 3,59 (s, 3H), 3,37 (s, 3H).
MS (ESI)
m/z = 397 [M+H]+.
-
Zwischenprodukt Beispiel 13
-
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-N
2-(1-phenylethyl)-1H-benzimidazol-2,5-diamin
-
(A)
1-Methyl-5-nitro-N-(1-phenylethyl)-1H-benzimidazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (2,0 g,
12 mmol) und 1-Phenylethylisothiocyanat (2,15 g, 13,2 mmol) wurden
unter Verfahrens aus Zwischenprodukt Beispiel 1, Teil B, verknüpft, um
die Titelverbindung als einen gelben Feststoff zu ergeben (1,2 g,
34 %).
1H-NMR (300 MHz, d
6-DMSO) δ: 7,87-7,94
(m, 2H), 7,44-7,52 (m, 3H), 7,29-7,34 (m, 3H), 7,21 (m, 1H), 5,18 (m,
1H), 3,65 (s, 3H), 1,55 (d, J = 6,9Hz, 3H). (B)
1-Methyl-N
2-(1-phenylethyl)-1H-benzimdazol-2,5-diamin
-
1-Methyl-5-nitro-N-(1-phenylethyl)-1H-benzimidazol-2-amin
wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil C, reduziert, um die Titelverbindung
als einen weißen
Feststoff zu ergeben (1,2 g, 97 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 7,42 (d, J = 7,5Hz, 2H), 7,27-7,32
(m, 2H), 7,18-7,21 (m, 1H), 6,70-6,78 (m, 2H), 6,40 (d, J = 1,8Hz,
1H), 6,21 (dd, J = 8,5 und 2,0Hz, 1H), 5,09 (m, 1H), 4,37 (br s,
2H), 3,44 (s, 3H), 1,49 (d, J = 7,2Hz, 3H). (C)
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-N
2-(1-phenylethyl)-1H-benzimidazol-2,5-diamin
-
1-Methyl-N2-(1-phenylethyl)-1H-benzimdazol-2,5-diamin
wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil D, verknüpft und methyliert, um die
Titelverbindung als einen gelben Schaum zu ergeben.
1H-NMR (300 MHz, d6-DMSO) δ: 7,84 (d,
J = 6,3Hz, 1H), 7,44 (d, J = 7,5Hz, 2H), 7,28-7,34 (m, 2H), 7,16-7,25 (m,
3H), 7,07 (d, J = 1,8Hz, 1H), 6,83 (dd, J = 8,1 und 1,8Hz, 1H),
6,06 (d, J = 5,7Hz, 1H), 5,14 (m, 1H), 3,60 (s, 3H), 3,35 (s, 3H).
MS
(ESI) m/z = 393 [M+H]+.
-
Zwischenprodukt Beispiel 14
-
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-N
2-[(4-methylphenyl)methyl]-1H-benzimidazol-2,5-diamin
-
(A)
1-Methyl-N-[(4-methylphenyl)methyl]-5-nitro-1H-benzimidazol-2- amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (2,0 g,
12 mmol) und 4-Methylbenzylisothiocyanat (2,15 g, 13,2 mmol) wurden
unter Verwendung des Verfahrens aus Zwischenprodukt Beispiel 1,
Teil B, verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (2,1
g, 59 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
7,97 (d, J = 2,4Hz, 1H), 7,90 (dd, J = 8,7 und 2,1Hz, 1H)), 7,71
(t, J = 6,0H, 1H), 7,34 (d, JH = 8,7Hz, 1H), 7,28 (d, J = 7,8Hz,
2H), 7,13 (d, J = 8,1Hz, 2H), 4,58 (d, J = 6,0Hz, 2H), 3,61 (s, 3H),
2,27 (s, 3H). (B)
1-Methyl-N
2-[(4-methylphenyl)methyl]-1H-benzimidazol-2,5-diamin
-
1-Methyl-N-[(4-methylphenyl)methyl]-5-nitro-1H-benzimidazol-2-amin
wurde gemäß dem Verfahren aus
Zwischenprodukt Beispiel 1, Teil C, reduziert, um die Titelverbindung
als einen weißen
Feststoff zu ergeben (1,8 g, 95 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 7,26 (d, J = 8,1Hz, 2H), 7,11
(d, J = 7,8Hz, 2H), 6,88 (t, J = 6,0Hz, 1H), 6,77 (d, J = 8,1Hz,
1H), 6,43 (d, J = 1,8Hz, 1H), 6,22 (dd, J = 8,1 und 2,1Hz, 1H),
4,48 (d, J = 5,7Hz, 2H), 4,37 (s, 2H), 3,40 (s, 3H), 2,26 (s, 3H). (C)
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-N
2-[(4-methylphenyl)methyl]-1H-benzimidazol-2,5-diamin
-
1-Methyl-N2-[(4-methylphenyl)methyl]-1H-benzimidazol-2,5-diamin
wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil D, verknüpft und methyliert, um die
Titelverbindung als einen weißen
Feststoff zu ergeben.
1H-NMR (300 MHz,
d6-DMSO) δ:
7,86 (d, J = 6,0Hz, 1H), 7,38 (t, J = 6,0Hz, 1H), 7,23-7,28 (m,
3H), 7,11-7,13 (m, 3H), 6,84 (dd, J = 8,1 und 1,8Hz, 1H), 6,08 (d,
J = 5,4Hz, 1H), 4,54 (d, J = 5,7Hz, 2H), 3,56 (s, 3H), 3,37 (s,
3H), 2,26 (s, 3H).
MS (ESI) m/z = 393 [M+H]+.
-
Zwischenprodukt Beispiel 15
-
N
2-[(3-Chlorphenyl)methyl]-N
5-(2-chlor-4-pyrimidinyl)-N
5,1-dimethyl-1H-benzimidazol-2,5-diamin
-
(A)
N-[(3-Chlorphenyl)methyl]-1-methyl-5-nitro-1H-benzimidazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (2,0 g,
12,0 mmol) und 3-Chlorbenzylisothiocyanat (1,94 ml, 13,2 mmol) wurde
unter Verwendung des Verfahrens aus Zwischenprodukt Beispiel 1,
Teil B, verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (2,2
g, 58 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
7,98 (d, J = 2,1Hz, 1H), 7,90-7,93 (m, 1H), 7,82 (t, J = 5,7Hz,
1H), 7,46 (s, 1H), 7,30-7,38 (m, 4H), 4,63 (d, J = 5,7Hz, 2H), 3,64
(s, 3H). (B)
N
2-[(3-Chlorphenyl)methyl]-1-methyl-1H-benzimidazol-2,5-diamin
-
N-[(3-Chlorphenyl)methyl]-1-methyl-5-nitro-1H-benzimidazol-2-amin
wurde gemäß dem Verfahren aus
Zwischenprodukt Beispiel 1, Teil C, reduziert, um die Titelverbindung
als einen weißen
Feststoff zu ergeben (0,67 g, 34 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 7,22-7,43 (m, 5H), 6,80 (m,
1H), 6,44 (d, J = 1,8Hz, 1H), 6,23 (m, 1H), 4,54 (s, 2H), 3,42 (s,
3H). (C)
N
2-[(3-Chlorphenyl)methyl]-N
5-(2-chlor-4-pyrimidinyl)-N
5,1-dimethyl-1H-benzimidazol-2,5-diamin
-
N2-[(3-Chlorphenyl)methyl]-1-methyl-1H-benzimidazol-2,5-diamin
wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil D, verknüpft und methyliert, um die
Titelverbindung als einen weißen
Feststoff zu ergeben.
1H-NMR (300 MHz,
d6-DMSO) δ:
7,86 (d, J = 6,0Hz, 1H), 7,24-7,52 (m, 6H), 7,12 (m, 1H), 6,86 (dd,
J = 8,1 und 2,1Hz, 1H), 6,09 (d, J = 5,4Hz, 1H), 4,60 (d, J = 5,7Hz,
2H), 3,58 (s, 3H), 3,37 (s, 3H).
MS (ESI) m/z = 413 [M+H]+.
-
Zwischenprodukt Beispiel 16
-
-
Die
Titelverbindung ist kommerziell erhältlich: CAS # 98-18-0.
-
Zwischenprodukt Beispiel 17
-
5-Amino-2-methylbenzolsulfonamid
-
Die
Titelverbindung ist in der Literatur beschrieben: CAS # 6973-09-7.
-
Zwischenprodukt Beispiel 18
-
4-[(Methylsulfonyl)methyl]anilin
-
Die
Titelverbindung ist in der Literatur beschrieben: CAS # 24176-70-3.
-
Zwischenprodukt Beispiel 19
-
1-(4-Aminophenyl)methansulfonamid
-
Die
Titelverbindung ist in der Literatur beschrieben: CAS # 4403-84-3.
-
Zwischenprodukt Beispiel 20
-
2-(4-Aminophenyl)-N-methylethansulfonamid
-
Die
Titelverbindung ist in der Literatur beschrieben: CAS # 98623-16-6.
-
Zwischenprodukt Beispiel 21
-
4-[2-(Methylsulfonyl)ethyl]anilin
-
Die
Synthese der Titelverbindung ist in der internationalen Patentanmeldung
PCT/US 03/03816 , eingereicht
am 7. Februar 2003 (
WO 03/066601 )
beschrieben.
-
Zwischenprodukt Beispiel 22
-
3-[(Methylsulfonyl)methyl]anilin
-
Die
Titelverbindung ist in der Literatur beschrieben: CAS # 261925-02-4.
-
Zwischenprodukt Beispiel 23
-
3-Aminohenlmethansulfonat
-
Die
Titelverbindung ist in der Literatur beschrieben: CAS # 38164-50-0.
-
Zwischenprodukt Beispiel 24
-
3-[2-(Methylsulfonyl)ethyl]anilin
-
Die
Synthese der Titelverbindung ist in der internationalen Patentanmeldung
PCT/US 03/03816 , eingereicht
am 7. Februar 2003, beschrieben.
-
Zwischenprodukt Beispiel 25
-
4-[1-(Methylsulfonyl)ethyl]anilin
-
Die
Synthese der Titelverbindung ist in der internationalen Patentanmeldung
PCT/US 03/03816 , eingericht
am 7. Februar 2003, beschrieben.
-
Zwischenprodukt Beispiel 26
-
1,1-Dimethyl{5-[(2-chlor-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}(4-fluorphenyl)carbamat
-
(A)
N-(4-Fluorphenyl-5-nitro-1H-benzimidazol-2-amin
-
N1-Methyl-4-nitro-benzol-1,2-diamin (2,0 g,
12 mmol) und 4-Fluorphenylisothiocyanat (1,58 ml, 13,2 mmol) wurden
unter Verwendung des Verfahrens aus aus Zwischenprodukt Beispiel
4, Teil A, verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (1,49
g, 43 %).
1H-NMR (300 MHz, d6-DMSO) δ:
9,29 (s, 1H), 8,17 (m, 1H), 8,01-8,04 (m, 1H), 7,89-7,90 (m, 2H),
7,49-7,52 (m, 1H), 7,18-7,25 (m, 2H), 3,79 (s, 3H).
-
(B)
1,1-Dimethylethyl(1-methyl-5-nitro-1H-benzimidazol-2-yl)phenylcarbamat
-
N-(4-Fluorphenyl-5-nitro-1H-benzimidazol-2-amin
(1,49 g, 5,2 mmol) wurden gemäß dem Verfahren aus
Zwischenprodukt Beispiel 4, Teil B, geschützt, um die Titelverbindung
als einen leichtgelben Feststoff zu ergeben (1,08 g, 54 %).
1H-NMR (300 MHz, d6-DMSO) δ: 8,50 (d,
J = 2,1Hz, 1H), 8,23 (dd, J = 9,0 und 2,1Hz, 1H), 7,85 (d, J = 9,0Hz, 1H),
7,47-7,51 (m, 2H), 7,22-7,27 (m, 2H), 3,84 (s, 3H), 1,40 (s, 9H).
-
(C)
1,1-Dimethylethy(5-amino-1-methyl-1H-benzimidazol-2-yl)(4-fluorphenyl)carbamat
-
1,1-Dimethylethyl(1-methyl-5-nitro-1H-benzimidazol-2-yl)phenylcarbamat
(1,08 g, 2,8 mmol) wurden durch das Verfahren aus Zwischenprodukt
Beispiel 1, Teil C, reduziert, um die Titelverbindung als einen
weißen
Feststoff zu ergeben (0,99 g, 99 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 7,39-7,447 (m, 2H), 7,17-7,23
(m, 3H), 6,70 (d, J = 1,5Hz, 1H), 6,63 (dd, J = 8,5 und 2,0Hz, 1H),
4,78 (s, 2H), 3,61 (s, 3H).
-
(D)
1,1-Dimethyl{5-[(2-chlor-4-pyrimidinyl)amino]-1-methyl-1H-benzimidazol-2-yl}(4-fluorphenyl)carbamat
-
1,1-Dimethylethy(5-amino-1-methyl-1H-benzimidazol-2-yl)(4-fluorphenyl)carbamat
(0,99 g, 2,8 mmol) wurden gemäß dem Verfahren
aus Zwischenprodukt Beispiel 4, Teil D, verknüpft, um die Titelverbindung
als einen weißen
Feststoff zu ergeben (1,00 g, 76 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 10,00 (s, 1H), 8,10 (d, J
= 6,0Hz, 1H), 7,89 (m, 1H), 7,58 (d, J = 8,4Hz, 1H), 7,44-7,49 (m,
2H), 7,34 (d, J = 8,7Hz, 1H), 7,20-7,26 (m, 2H), 6,69 (d, J = 6,0Hz,
1H), 3,74 (s, 3H), 1,40 (s, 9H).
-
(E)
1,1-Dimethyl{5-[(2-chlor-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}(4-fluorphenyl)carbamat
-
1,1-Dimethyl{5-[(2-chlor-4-pyrimidinyl)amino]-1-methyl-1H-benzimidazol-2-yl}(4-fluorphenyl)carbamat
wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 4, Teil E, methyliert, um die Titelverbindung als
einen orangefarbenen Schaum zu ergeben.
1H-NMR
(300 MHz, d6-DMSO) δ: 7,91 (d, J = 6,0Hz, 1H), 7,72
(d, J = 8,4Hz, 1H), 7,61 (d, J = 1,5Hz, 1H), 7,45-7,50 (m, 2H),
7,20-7,29 (m, 3H), 6,17 (d, J = 5,7Hz, 1H), 3,79 (s, 3H), 3,41 (s,
3H), 1,42 (s, 9H).
MS (ESI) m/z = 483 [M+H]+.
-
Zwischenprodukt Beispiel 27
-
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}(4-methylphenyl)carbamat
-
(A)
1-Methyl-N-(4-methylphenyl)-5-nitro-1H-benzimidazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (2,5 g,
15 mmol) und p-Tolylisothiocyanat (2,46 g, 16,5 mmol) wurden unter
Verwendung des Verfahrens aus Zwischenprodukt Beispiel 4, Teil A,
verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (1,99
g, 47 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
9,14 (s, 1H), 8,15 (d, J = 2,1Hz, 1H), 8,00 (dd, J = 8,7 und 2,1Hz,
1H), 7,76 (d, J = 8,4Hz, 2H), 7,47 (d, J = 8,7Hz, 1H), 7,16 (d,
J = 8,4Hz, 2H), 3,77 (s, 3H), 2,28 (s, 3H). (B)
1,1-Dimethyl(1-methyl-5-nitro-1H-benzimidazol-1-yl)(4-methylphenyl)carbamat
-
1-Methyl-N-(4-methylphenyl)-5-nitro-1H-benzimidazol-2-amin
wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 4, Teil B, geschützt, um die Titelverbindung
als einen hellgelben Feststoff zu ergeben (1,50 g, 55 %).
1H-NMR (300 MHz, d
6-DMSO) δ: 8,49 (d,
J = 2,1Hz, 1H), 8,22 (dd, J = 9,0 und 2,1Hz, 1H), 7,83 (d, J = 9,3Hz, 1H),
7,28 (d, J = 8,4Hz, 2H), 7,20 (d, J = 8,1Hz, 2H), 3,82 (s, 3H),
2,29 (s, 3H), 1,40 (s, 9H.
MS (ESI) m/z = 405 [M+Na]
+. (C)
1,1-Dimethylethyl(5-amino-1-methyl-1H-benzimidazol-2-yl)(4-methylpheriyl)carbamat
-
1,1-Dimethyl(1-methyl-5-nitro-1H-benzimidazol-1-yl)(4-methylphenyl)carbamat
(1,50 g, 3,9 mmol) wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil C, reduziert, um die Titelverbindung
als weißen
Feststoff (1,31 g, 96 %) zu ergeben.
1H-NMR
(300 MHz, d
6-DMSO) δ: 7,14-7,23 (m, 5H), 6,69 (d,
J = 1,5Hz, 1H), 6,62 (dd, J = 8,5 und 1,9Hz, 1H), 4,77 (s, 2H),
3,58 (s, 3H), 2,27 (s, 3H), 1,38 (s, 9H). (D)
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)amino]-1-methyl-1H-berizimidazol-2-yl}(4-methylphenyl)carbamat
-
1,1-Dimethylethyl(5-amino-1-methyl-1H-benzimidazol-2-yl)(4-methylphenyl)carbamat
(1,31 g, 3,7 mmol) wurden gemäß dem Verfahren
aus Zwischenprodukt Beispiel 4, Teil D, verknüpft um die Titelverbindung als
einen weißen
Feststoff zu ergeben (0,75 g, 44 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 10,00 (s, 1H), 8,10 (d, J
= 6,0Hz, 1H), 7,87 (s, 1H), 7,57 (d, J = 8,7Hz, 1H), 7,34 (d, J
= 8,7Hz, 1H), 7,26 (d, J = 8,4Hz, 2H), 7,18 (d, J = 8,4Hz, 2H),
6,69 (d, J = 6,0Hz, 1H), 3,72 (s, 3H), 2,28 (s, 3H), 1,40 (s, 9H).
MS
(ESI) m/z = 465 [M+H]
+. (E)
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)(methyl)amino]-1-methl-1H-benzimidazol-2-yl}(4-methylphenyl)carbamat
-
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)amino]-1-methyl-1H-benzimidazol-2-yl}(4-methylphenyl)carbamat
(0,75 g, 1,62 mmol) wurd gemäß dem Verfahren
aus Zwischenprodukt Beispiel 4, eil E, methyliert, um die Titelverbindung
als einen weißen
Feststoff zu ergeben.
1H-NMR (300 MHz,
d6-DMSO) δ:
7,91 (d, J = 6,0Hz, 1H), 7,71 (d, J = 8,4Hz, 1H), 7,59 (d, J = 1,2Hz,
1H), 7,27 (d, J = 8,4Hz, 3H), 7,19 (d, J = 8,4Hz, 2H), 6,17 (d,
J = 5,4Hz, 1H), 3,76 (s, 3H), 3,41 (s, 3H), 2,28 (s, 3H), 1,41 (s,
9H).
MS (ESI) m/z = 479 [M+H]+.
-
Zwischenprodukt Beispiel 28
-
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}]4-(1,1-dimethylethyl)phenyl]carbamat
-
(A)
N-[4-(1,1-Dimethylethyl)phenyl]-1-methyl-5-nitro-1H-benzimidazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (1,89
g, 11,3 mmol) und p-tert-Butylphenylisothiocyanat
(2,37 g, 12,4 mmol) wurden unter Verwendung des Verfahrens aus Zwischenprodukt
Beispiel 4, Teil A, verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (1,39
g, 38 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
9,17 (s, 1H), 8,14 (d, J = 2,7Hz, 1H), 8,00 (dd, J = 9,0 und 2,4Hz,
1H), 7,76 (d, J = 8,7Hz, 2H), 7,48 (d, J = 9,0Hz, 1H), 7,37 (d,
J = 8,7kz, 2H), 3,78 (s, 3k), 1,29 (s, 9H). (B)
1,1-Dimethylethyl[4-(1,1-dimethylethyl)phenyl](1-methyl-5-nitro-1H-benzimidazol-2-yl)carbamat
-
N-[4-(1,1-Dimethylethyl)phenyl]-1-methyl-5-nitro-1H-benzimidazol-2-amin (1,38 g, 4,3
mmol) wurden gemäß dem Verfahren
aus Zwischenprodukt Beispiel 4, Teil B, geschützt, um die Titelverbindung
als einen leichtgelben Feststoff zu ergeben (0,86 g, 47 %).
1H-NMR (300 MHz, d
6-DMSO) δ: 8,49 (d,
J = 2,1Hz, 1H), 8,23 (dd, J = 9,0 und 2,1Hz, 1H), 7,84 (d, J = 9,3Hz, 1H),
7,41 (d, J = 8,4Hz, 2H), 7,31 (d, J = 8,7Hz, 2H), 3,83 (s, 3H),
1,40 (s, 9H), 1,26 (s, 9H). (C)
1,1-Dimethylethyl(5-amino-1-methyl-1H-benzimidazol-2-yl)[4-(1,1-dimethylethyl)phenyl]carbamat
-
1,1-Dimethylethyl[4-(1,1-dimethylethyl)phenyl](1-methyl-5-nitro-1H-benzimidazol-2-yl)carbamat
(0,86 g, 2,1 mmol) wurden durch das Verfahren aus Zwischenprodukt
Beispiel 1, Teil C, reduziert, um die Titelverbindung als einen
weißen
Feststoff zu ergeben (0,81 g), 98 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 7,37 (d, J = 8,4Hz, 2H), 7,18-7,25
(m, 2H), 6,69 (d, J = 1,8Hz, 1H), 6,62 (dd, J = 8,7 und 2,1Hz, 1H),
4,78 (s, 2H), 3,60 (s, 3H), 1,38 (s, 9H), 1,25 (s, 9H). (D)
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)amino]-1-methyl-1H-benzimidazol-2-yl}]4-(1,1-dimethylethyl)phenyl]carbamat
-
1,1-Dimethylethyl(5-amino-1-methyl-1H-benzimidazol-2-yl)[4-(1,1-dimethylethyl)phenyl]carbamat (0,81
g, 2,1 mmol) wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 4, Teil D, verknüpft, um die Titelverbindung
als einen weißen
Feststoff zu ergeben (0,76 g, 72 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 10,00 (s, 1H), 8,10 (d, J
= 5,7Hz, 1H), 7,88 (s, 1H), 7,57 (d, J = 8,7Hz, 1H), 7,27-7,41 (m,
6H), 6,69 (d, J = 6,0Hz, 1H), 3,73 (s, 3H), 1,40 (s, 9H), 1,26 (s,
9H). (E)
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}]4-(1,1-dimethylethyl)phenyl]carbamat
-
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)amino]-1-methyl-1H-benzimidazol-2-yl}]4-(1,1-dimethylethyl)phenyl]carbamat
(0,76 g, 1,50 mmol) wurden gemäß dem Verfahren
aus Zwischenprodukt Beispiel 4, Teil E, methyliert, um die die Titelverbindung
als einen weißen
Feststoff zu ergeben.
1H-NMR (300 MHz,
d6-DMSO) δ:
7,90 (d, J = 6,0Hz, 1H), 7,72 (d, J = 8,7Hz, 1H), 7,60 (d, J = 1,5Hz,
1H), 7,40 (d, J = 8,7Hz, 2H), 7,25-7,31 (m, 3H), 7,16 (d, J = 5,7Hz,
1H), 3,78 (s, 3H), 3,41 (s, 3H), 1,41 (s, 9H), 1,26 (s, 9H).
MS
(ESI) m/z = 521 [M+H]+.
-
Zwischenprodukt Beispiel 29
-
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-N
2-[4-(methyloxy)phenyl]-1H-benzimidazol-2,5-diamin
-
(A)
1-Methyl-N-[4-(methyloxy)phenyl]-5-nitro-1H-benzimidazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (2,0 g,
12,0 mmol) und p-Methoxyphenylisocyanat (1,82 ml, 13,2 mmol) wurden
unter Verwendung des Verfahrens aus Zwischenprodukt Beispiel 4,
Teil A, verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (1,88
g, 53 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
9,08 (s, 1H), 8,12 (d, J = 2,1Hz, 1H), 7,99 (dd, J = 8,7 und 2,1Hz,
1H), 7,76 (d, J = 9,0Hz, 2H), 7,46 (d, J = 9,0Hz, 1H), 6,95 (d,
J = 9,0Hz, 2H), 3,76 (s, 3H), 3,75 (s, 3H).
MS (ESI) m/z =
299 [M+H]
+. (B)
1,1-Dimethylethyl(1-methyl-5-nitro-1H-benzimidazol-2-yl)[4-(methyloxy)phenyl]carbamat
-
1-Methyl-N-[4-(methyloxy)phenyl]-5-nitro-1H-benzimidazol-2-amin
(1,88 g, 6,3 mmol) wurden gemäß dem Verfahren
aus Zwischenprodukt Beispiel 4, Teil B, geschützt, um die Titelverbindung
als einen leichtgelben Feststoff zu ergeben (1,09 g, 43 %).
1H-NMR (300 MHz, d
6-DMSO) δ: 8,48 (d,
J = 2,1Hz, 1H), 8,22 (dd, J = 9,0 und 2,1Hz, 1H), 7,82 (d, J = 9,0Hz, 1H),
7,35 (d, J = 9,0Hz, 2H), 6,94 (d, J = 8,7Hz, 2H), 3,83 (s, 3H),
3,74 (s, 3H), 1,40 (s, 9H).
MS (ESI) m/z = 399 [M+H]
+. (C)
1,1-Dimethylethyl(5-amino-1-methyl-1H-benzimidazol-2-yl)[4-(methyloxy)phenyl]carbamat
-
1,1-Dimethylethyl(1-methyl-5-nitro-1H-benzimidazol-2-yl)[4-(methyloxy)phenyl]carbamat
(1,09 g, 2,7 mol) wurden durch das Verfahren qus Zwischenprodukt
Beispiel 1, Teil C, reduziert, um die Titelverbindung als einen
weißen
Feststoff zu ergeben (1,05 g, 98 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 7,28 (d, J = 8,7Hz, 2H), 7,18
(d, J = 8,4Hz, 1H), 6,91 (d, J = 9,0Hz, 2H), 6,68 (d, J = 1,5Hz,
1H), 6,61, J = 8,4 und 1,5Hz, 1H), 4,76 (s, 2H), 3,73 (s, 3H), 3,60
(s, 3H), 1,38 (s, 9H). (D)
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)amino)-1-methyl-1H-benzimidazol-2-yl}[4-(methyloxy)phenyl]carbamat
-
1,1-Dimethylethyl(5-amino-1-methyl-1H-benzimidazol-2-yl)[4-(methyloxy)phenyl]carbamat
(1,05 g, 2,85 mmol) wurden gemäß dem Verfahren
aus Zwischenprodukt Beispiel 4, Teil D, verknüpft, um die Titelverbindung
als einen weißen
Feststoff zu ergeben (0,96 g, 70 %).
1H-NMR
(300 MHz, d
6-DMSO) δ: 9,99 (s, 1H), 8,09 (d, J =
6,0Hz, 1H), 7,87 (br s, 1H), 7,56 (d, J = 8,7Hz, 1H), 7,33 (d, J
= 9,0Hz, 2H), 6,93 (d, J = 9,0Hz, 2H), 6,69 (d, J = 6,0Hz, 1H),
3,74 (s, 3H), 3,73 (s, 3H), 1,39 (s, 9H).
MS (ESI) m/z = 481
[M+H]
+. (E)
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}[4-(methyloxy)phenyl]carbamat
-
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)amino]-1-methyl-1H-benzimidazol-2-yl}[4-(methyloxy)phenyl]carbamat
wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 4, Teil E, methyliert, um die Titelverbindung
als einen weißen
Feststoff zu ergeben.
1H-NMR (300 MHz,
d6-DMSO) δ:
7,90 (d, J = 6,0Hz, 1H), 7,70 (d, J = 8,4Hz, 1H), 7,59 (d, J = 1,8Hz,
1H), 7,34 (d, J = 9,0Hz, 2H), 7,26 (dd, J = 8,5 und 1,9Hz, 1H),
6,93 (d, J = 9,0Hz, 2H), 6,16 (d, J = 5,4Hz, 1H), 3,78 (s, 3H),
3,74 (s, 3H), 3,41 (s, 3H), 3,41 (s, 3H), 1,41 (s, 9H).
MS
(ESI) m/z = 495 [M+H]+.
-
Zwischenprodukt Beispiel 30
-
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-N
2-(2-phenylethyl)-1H-benzimidazol-2,5-diamin
-
(A)
1-Methyl-5-nitro-N-(2-phenylethyl)-1H-benzimidazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (2,0 g,
12,0 mmol) und Phenethylisocyanat (2,15 g, 13,2 mmol) wurden unter
Verwendung des Verfahrens aus Zwischenprodukt Beispiel 1, Teil B,
verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (2,36
g, 66 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
8,01 (d, J = 2,1Hz, 1H), 7,90 (dd, J = 8,7 und 2,4Hz, 1H), 7,21-7,35
(m, 7H), 3,58-3,65 (m, 2H), 3,56 (s, 3H), 2,93-2,98 (m, 2H) ppm. (B)
1-Methyl-N
2-(2-phenylethyl)-1H-benzimidazol-2,5-diamin
-
1-Methyl-5-nitro-N-(2-phenylethyl)-1H-benzimidazol-2-amin
(2,36 g, 8 mmol) wurden unter Verwendung des Verfahrens aus Zwischenprodukt
Beispiel 1, Teil C, reduziert, um die Titelverbindung als einen
weißen
Feststoff zu ergeben (1,98 g, 93 %).
1H-NMR: δ (300 MHZ,
CD
3OD) δ: (C)
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-N
2-(2-phenylethyl)-1H-benzimidazol-2,5-diamin
-
1-Methyl-N2-(2-phenylethyl)-1H-benzimidazol-2,5-diamin
wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil D, verknüpft und methyliert, um die
Titelverbindung als einen weißen
Feststoff zu ergeben (1,43 g, 49 % über 2 Schritte).
1H-NMR (300 MHz, d6-DMSO) δ: 7,87 (d,
J = 6,0Hz, 1H), 7,20-7,34 (m, 6H), 7,15 (d, J = 2,1Hz, 1H), 6,97
(t, J = 5,4Hz, 1H), 6,84 (dd, J = 8,4 und 1,8Hz, 1H), 6,10 (d, J
= 5,7Hz, 1H), 3,54-3,61 (m, 2H), 3,50 (s, 3H), 3,38 (s, 3H), 2,92-2,97
(m, 2H) ppm.
MS (ESI) m/z = 393 [M+H]+.
-
Zwischenprodukt Beispiel 31
-
N
5-(2-Chlor-4-pyrimidinyl)-N
2-(1,1-dimethylethyl)-N
5,1-dimethyl-1H-benzimidazol-2,5-diamin
-
(A)
N-(1,1-Dimethylethyl)-1-methyl-5-nitro-1H-benzimdazol-2-amin
-
N-Methyl-4-nitro-benzol-1,2-diamin
(2,0 g, 12,0 mmol) und tert-Butylisothiocyanat
(1,67 ml, 13,2 mmol) wurden unter Verwendung des Verfahrens aus
Zwischenprodukt Beispiel 1, Teil B, verknüpft, um die Titelverbindung
als einen gelben Feststoff zu ergeben.
1H-NMR
(300 MHz, d
6-DMSO) δ: 8,01 (d, J = 2,1Hz, 1H), 7,90
(dd, J = 8,7 und 2,1Hz, 1H), 7,32 (d, J = 8,7Hz, 1H), 6,41 (s, 1H),
3,58 (s, 3H), 1,48 (s, 9H) ppm. (B)
N
2-(1,1-Dimethylethyl)-1-methyl-1H-benzimidazol-2,5-diamin
-
N-(1,1-Dimethylethyl)-1-methyl-5-nitro-1H-benzimidazol-2-amin
(700 mg, 2,8 mmol) wurde unter Verwendung des Verfahren aus Zwischenprodukt Beispiel
1, Teil C, reduziert, um die Titelverbindung als einen braunen Feststoff
zu ergeben (240 mg, 39 %).
1H-NMR: δ (300 MHZ,
CD
3OD) δ:
6,76 (d, J = 8,1Hz, 1H), 6,48 (d, J = 1,8Hz, 1H), 622 (dd, J = 8,1
und 1,8Hz, 1H), 5,64 (s, 1H), 4,40 (br s, 2H), 3,36 (s, 3H), 1,43
(s, 9H) ppm. (C)
N
5-(2-Chlor-4-pyrimidinyl)-N
2-(1,1-dimethylethyl)-N
5,1-dimethyl-1H-benzimidazol-2,5-diamin
-
N2-(1,1-Dimethylethyl)-1-methyl-1H-benzimidazol-2,5-diamin
(240 mg, 1,1 mmol) wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil D, verknüpft und methyliert, um die
Titelverbindung als einen weißen
Feststoff zu ergeben (348 mg, 92 % über 2 Schritte).
1H-NMR (300 MHz, d6-DMSO) δ: 7,86 (d,
J = 6,0Hz, 1H), 7,23 (d, J = 8,4Hz, 1H), 7,16 (d, J = 1,8Hz, 1H),
6,84 (dd, J = 8,1 und 1,8Hz, 1H), 6,08 (br s, 2H), 3,52 (s, 3H),
3,38 (s, 3H), 1,46 (s, 9H) ppm.
MS (ESI) m/z = 345 [M+H]+.
-
Zwischenprodukt Beispiel 32
-
N
5-(2-Chlor-4-pyrimidinyl)-N
2-cyclohexyl-N
5,1-dimethyl-1H-benzimidazol-2,5-diamin
-
(A)
N-Cyclohexyl-1-methyl-5-nitro-1H-benzimidazol-2-amin
-
N
1-Methyl-4-nitro-benzol-1,2-diamin (2,0 g,
12,0 mmol) und Cyclohexylisothiocyanat (1,80 ml, 13,2 mmol) wurden
unter Verwendung des Verfahrens aus Zwischenprodukt Beispiel 1,
Teil B, verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (2,41
g, 73 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
7,98 (d, J = 2,4Hz, 1H), 7,88 (dd, J = 8,7 und 2,4Hz, 1H), 7,30
(d, J = 8,7Hz, 1H), 6,88 (d, J = 7,8Hz, 1H), 3,74 (m, 1H), 3,56
(s, 3H), 2,00 (m, 2H), 1,75 (m, 2H), 1,63 (m, 1H), 1,25-1,36 (M, 4H),
1,17 (m, 1H) ppm. (B)
N
2-Cyclohexyl-1-methyl-1H-benzimidazol-2,5-diamin
-
N-Cyclohexyl-1-methyl-5-nitro-1H-benzimidazol-2-amin
(2,4 g, 8,8 mmol) wurden unter Verwendung des Verfahrens aus Zwischenprodukt
Beispiel 1, Teil C, reduziert, um die Titelverbindung als einen
weißen Feststoff
zu ergeben (2,05 g, 95 %).
1H-NMR (300
MHz, d
6-DMSO) δ: 6,74 (d, J = 8,1Hz, 1H), 6,44
(d, J = 1,8Hz, 1H), 6,20 (dd, J = 8,2 und 2,0Hz, 1H), 6,05 (d, J
= 7,5Hz, 1H), 4,32 (br s, 2H), 3,62 (m, 1H), 3,35 (s, 3H), 1,96-1,99
(m, 2H), 1,71-1,75 (m, 2H), 1,60-1,67 (m, 1H), 1,03-1,34 (m, 5H)
ppm.
MS (ESI) m/z = 245 [M+H]
+. (C)
N
5-(2-Chlor-4-pyrimidinyl)-N
2-cyclohexyl-N
5,1-dimethyl-1H-benzimidazol-2,5-diamin
-
N2-Cyclohexyl-1-methyl-1H-benzimidazol-2,5-diamin
(2,03 g, 8,3 mmol) wurde gemäß dem Verfahren aus
Zwischenprodukt Beispiel 1, Teil D, verknüpft und methyliert, um die
Titelverbindung als einen weißen Feststoff
zu ergeben (2,45 g, 80 % über
2 Schritte).
1H-NMR (300 MHz, d6-DMSO) δ:
7,87 (d, J = 6,3Hz, 1H), 7,21 (d, J = 8,4Hz, 1H), 7,11 (d, J = 1,8Hz,
1H), 6,82 (dd, J = 8,2 und 2,0Hz, 1H), 6,52 (d, J = 7,8Hz, 1H),
6,09 (d, J = 5,7Hz, 1H), 3,70 (m, 1H), 3,51 (s, 3H), 3,37 (s, 3H),
1,99 (m, 2H), 1,74 (m, 2H), 1,62 (m, 1H), 1,14-1,31 (m, 5H) ppm.
MS
(ESI) m/z = 371 [M+H]+.
-
Zwischenprodukt Beispiel 33
-
N
5-(2-Chlor-4-pyrimidinyl)-1-ethyl-N
2,N
5-dimethyl-1H-benzimidazol-2,5-diamin
-
(A)
1-Ethyl-N-methyl-5-nitro-1H-benzimidazol-2-amin
-
N-Ethyl-4-nitro-benzol-1,2-diamin
(2,0 g, 11,0 mmol) und Methylisothiocyanat (0,83 ml, 12,1 mmol) wurden
unter Verwendung des Verfahrens aus Zwischenprodukt Beispiel 1,
Teil B, verknüpft,
um die Titelverbindung als einen gelben Feststoff zu ergeben (0,99
g, 41 %).
1H-NMR (300 MHz, d
6-DMSO) δ:
7,99 (d, J = 2,4Hz, 1H), 7,90 (dd, J = 8,7 und 2,1Hz, 1H), 7,36
(d, J = 8,7Hz, 1H), 7,16 (m, 1H), 4,08 (q, J = 7,2Hz, 2H), 2,96
(d, J = 4,5Hz, 3H), 1,21 (t, J = 7,2Hz, 3H).
MS (ESI) m/z =
221 [M+H]
+. (B)
1-Ethyl-N
2-methyl-1H-benzimidazol-2,5-diamin
-
1-Ethyl-N-methyl-5-nitro-1H-benzimidazol-2-amin
wurde durch das Verfahren aus Zwischenprodukt Beispiel 1, Teil C,
reduziert, um die Titelverbindung als einen weißen Feststoff zu ergeben (0,95
g, > 95 %).
1H-NMR (300 MHz, d
6-DMSO) δ: 6,78 (d,
J = 8,4Hz, 1H), 6,47 (d, J = 1,8Hz, 1H), 6,32 (br s, 1H), 6,21 (dd,
J = 8,4 und 1,8Hz, 1H), 4,15 (br s, 2H), 3,85 (q, J = 7,1Hz, 2H),
2,86 (s, 3H), 1,13 (t, J = 7,1Hz, 3H).
MS (ESI) m/z = 191 [M+H]
+. (C)
N
5-(2-Chlor-4-pyrimidinyl)-1-ethyl-N
2,N
5-dimethyl-1H-benzimidazol-2,5-diamin
-
1-Ethyl-N2-methyl-1H-benzimidazol-2,5-diamin (0,95
g, 4,9 mmol) wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 1, Teil D, verknüpft und methyliert, um die
Titelverbindung als einen weißen
Feststoff zu ergeben.
1H-NMR (300 MHz,
d6-DMSO) δ:
7,88 (d, J = 6,0Hz, 1H), 7,26 (d, J = 8,1Hz, 1H), 7,13 (d, J = 108Hz,
1H), 6,78-6,85 (m, 2H), 6,11 (d, J = 5,7Hz, 1H), 4,02 (q, J = 7,1Hz,
2H), 3,38 (s, 3H), 2,92 (d, J = 4,5Hz, 3H), 1,21 (t, J = 7,1Hz,
3H).
MS (ESI) m/z = 317 [M+H]+.
-
Zwischenprodukt Beispiel 34
-
1-Methyl-5-nitro-1,3-dihydro-2H-benzimidazol-2-thion
-
Eine
Lösung
aus Thiophosgen (2,3 ml, 30 mmol) in THF (300 ml) wurde zu einer
Lösung,
die N1-Methyl-4-nitro-benzol-1,2-diamin
(5,01 g, 30 mmol) und Et3N (9,2 ml, 66 mmol)
in THF (300 ml) enthielt, bei 0°C über 90 min
zugetropft. Nach Rühren
bei 0°C
für eine
weitere Stunde wurde dem Gemisch ermöglicht auf Raumtemperatur zu
erwärmen.
Das Gemisch wurde dann auf 100 ml aufkonzentriert, Wasser (200 ml)
wurde hinzugegeben, das Gemisch wurde für 20 min gerührt, das
Produkt wurde durch Filtration gesammelt und mit einer kleinen Menge
an kaltem CH2Cl2 gewaschen,
wobei nach Trocknung 5,16 g als ein senfgelber Feststoff zurückblieb:
LC/MS
(m/e) bei 210,0 [M+H]+, Rt bei 1,49 min.
-
Zwischenprodukt Beispiel 35
-
1-Methyl-2-(methylthio)-5-nitro-1H-benzimdazol
-
Ein
Gemisch aus 1-Methyl-5-nitro-1,3-dihydro-benzoimidazol-2-thion (5,16
g, 24,7 mmol), Na2CO3 (2,88
g, 27,2 mmol) und MeI (3,68 g, 25,94 mmol) in Aceton (150 ml) wurde über Nacht
refluxsiert. Das Gemisch wurde heiß filtriert, und das Filtrat
wurde auf ungefähr
50 ml aufkonzentriert, das Produkt durch Filtration gesammelt und
mit einer kleinen Menge an kaltem CH2Cl2 gewaschen, wobei nach Trocknung 4,58 g
als ein senfgelber Feststoff zurückblieb:
LC/MS
(m/e) bei 224,0 [M+H]+, Rt bei 1,55 min.
-
Zwischenprodukt Beispiel 36
-
1-Methyl-2-(methylthio)-1H-benzimidazol-5-amin
-
Zink
(9,52 g, 145,6 mmol) wurde zu einem Gemisch aus 1-Methyl-2-methylsulfanyl-5-nitro-1H-benzoimidazol
(4,64 g, 20,8 mmol) in EtOH (100 ml) und Eisessig (200 ml) hinzugegeben,
das resultierende Gemisch wurde bei Raumtemperatur für 2 h gerührt und
filtriert. Das Filtrat wurde aufkonzentriert, der Rückstand
in Wasser (100 ml) gegeben und durch NaOH neutralisiert, und das
Produkt wurde durch CH2Cl2 extrahiert
bis das gesamte Produkt aus der wäßrigen Phase extrahiert war.
Die vereinigten Extrakte wurden mit Salzlösung gewaschen, getrocknet
und aufkonzentriert, was 3,86 g als staubrosanen Feststoff ergab:
LC/MS
(m/e) bei 194,0 [M+H]+, Rt bei 1,02 min.
-
Zwischenprodukt Beispiel 37
-
N-(2-Chlor-4-pyrimidinyl)-N,1-dimethyl-2-(methylthio)-1H-benzimdazol-5-amin
-
Entsprechend
dem Verfahren aus Zwischenprodukt Beispiel 1D, wobei N2-Isopropyl-1-methyl-1H-benzoimidazol-2,5-diamin
durch 1-Methyl-2-methylsulfanyl-11H-benzoimidazol-5-ylamin ersetzt
wurde, wurde die Titelverbindung als ein weißer Feststoff erhalten:
LC/MS
(m/e) bei 320,0 [M+H]+, Rt bei 1,53 min.
-
Zwischenprodukt Beispiel 38
-
N
4-Methyl-N
4-[1-methyl-2-(methylthio)-1H-benzimidazol-5-yl]-N
2-{4-[(methylsulfonyl)methyl]phenyl}-2,4-pyrimidindiamin
-
Ein
Gemisch aus (2-Chlor-pyrimidin-4-yl)-methyl-(1-methyl-2-methylsulfanyl-1H-benzoimidazol-5-yl)-amin
(3,19 g, 10 mmol), 4-Methansulfonylmethyl-phenylamin (1,85 g, 10
mmol) und (833 μl,
12N, 10 mmol) wurde in Isopropanol (100 ml) über Nacht refluxiert. Das Gemisch
wurde dann bis zur Trockenheit aufkonzentriert und der Rückstand
in MeOH aufgenommen und mit NaHCO3 (3 g)
bei Raumtemperatur für
20 Minuten gerührt
und filtriert. Das Filtrat wurde aufkonzentriert und der Rückstand
durch Kiselsäure "flash" aufgereinigt, was
3,35 g als einen bleichgelben Feststoff ergab.
LC/MS (m/e)
469,2 [M+H]+, Rt bei 1,37 min.
-
Zwischenprodukt Beispiel 39
-
N
4-Methyl-N
4-[1-methyl-2-(methylsulfinyl)-1H-benzimidazol-5-yl]-N
2-{4-[(methylsulfonyl)methyl]phenyl}-2,4-pyrimidindiamin
-
mCPBA
(1,27 g, 5,61 mmol) wurde zu einer Lösung aus N2-(4-Methansulfonylmethyl-phenyl)-N4-methyl-N4-(1-methyl-2-methylsulfanyl-1H-benzoimidazol-5-yl)-pyrimidin-2,4-diamin
(2,4 g, 5,1 mmol) in CHCl3 (60 ml) bei -20°C zugegeben.
Das resultierende Gemisch wurde bei -20°C für 6 h gerührt und durch CHCl3 verdünnt, mit
NaHCO3 gewaschen (10 %, x4). Alle Extrakte
wurden vereinigt und mit Salzlösung
gewaschen, getrocknet und aufkonzentriert, und der Rückstand
wurde durch Kieselsäure "flash" aufgereinigt, was
1,22 g als einen leichtgelben Feststoff ergab:
LC/MS (m/e)
485 [M+H]+, Rt bei 1,29 min.
-
Zwischenprodukt Beispiel 40
-
(2-Amino-4-nitrophenyl)methylamin
-
Zu
einer Lösung
aus 2-Fluor-5-nitroanilin (3,0 g, 19,2 mmol) in 24 ml N-Methylpyrrolidinon
in einem versiegelten Reaktionsgefäß wurde Kaliumcarbonat (5,4
g, 30,0 mmol) und eine Lösung
aus Methylamin (20 ml, 2M in THF) hinzugegeben, und die Reaktion
wurde auf 120°C
erhitzt. Nach 16 h wurde das Reaktionsgemisch auf Raumtemperatur
abgekühlt
und in 200 ml Wasser gegossen. Das resultierende Präzipitat
wurde filtriert und getrocknet, um die Titelverbindung als einen
roten Feststoff zu ergeben.
MS (ESI) m/z = 168 [M+H].
-
Zwischenprodukt Beispiel 41
-
1-Methyl-5-nitro-1,3-dihydro-2H-benzimidazol-2-thion
-
Zu
einer Lösung
aus N1-Methyl-4-nitro-benzol-1,2-diamin
(1,0 g, 6,0 mmol) und Triethylamin (2,5 ml, 18 mmol) in THF (60
ml) wurde Thiophosgen (0,46 ml, 6,0 mmol) bei 0°C hinzugegeben. Nach 1 h wurde
das Reaktionsgemisch bis auf Raumtemperatur erwärmt und bei Raumtemperatur
für 3 h
gerührt.
Nachdem das Ausgangsmaterial aufgebraucht war, wurde die Reaktion
filtriert. Der gesammelte Feststoff wurde mit EtOAc:Hexan = 1:1
(10 ml × 2)
und Wasser gewaschen. Der resultierende gelbe Feststoff wurde getrocknet, um
die Titelverbindung zu ergeben (0,82 g, 66 %).
MS (ESI) m/z
= 209 [M+H].
-
Zwischenprodukt Beispiel 42
-
2-Chlor-1-methyl-5-nitro-1H-benzimidazol
-
Die
Verbindung 1-Methyl-5-nitro-1,3-dihydro-benzoimidazol-2-thion (5,8
g, 27,9 mmol) wurde bis auf Reflux mit SOCl2 (30
ml) über
Nacht erhitzt. Das Reaktionsgemisch wurde auf Raumtemperatur abgekühlt und in
300 ml Eiswasser gegossen und mit CH2Cl2 extrahiert. Die organischen Schichten wurden
mit 10 % NaHCO3-Wasser-Lösung und Salzlösung gewaschen, über Na2SO4 getrocknet und
aufkonzentriert, um die Titelverbindung als einen gelben Feststoff
zu ergeben.
MS (ESI) m/z = 212 [M+H].
-
Zwischenprodukt Beispiel 43
-
N-[5-(1,1-Dimethylethyl)-3-isoxazolyl]-1-methyl-5-nitro-1H-benzimidazol-2-amin
-
Zu
einer Lösung
aus 2-Chlor-1-methyl-5-nitro-1H-benzoimidazol (200 mg, 0,19 mmol)
und 5-tert-Butyl-isoxazol-3-ylamin (265 mg,. 0,190 mmol) in Isopropanol
(15 ml) wurde eine Lösung
aus HCl (3 Tropfen, 4,0 mmol in Dioxan) hinzugegeben. Die Reaktion
wurde auf 80°C
erhitzt, und nach 20 h wurde das Reaktionsgemisch auf Raumtemperatur
abgekühlt.
Das Lösungsmittel
wurde bis zur Trockene eingedampft, und der resultierende Feststoff
wurde in EtOAc aufgelöst
und durch eine 10%ige NaHCO3-Wasser-Lösung neutralisiert. Die vereinigten
organischen Schichten wurden mit Wasser gewaschen, über MgSO4 getrocknet und aufkonzentriert, um einen
Schaum zu ergeben. Das Rohmaterial wurde durch Kieselgel aufgereinigt,
um die Titelverbindung als einen gelben Feststoff zu ergeben (190
mg, 63 %).
MS (ESI) m/z = 316 [M+H].
-
Zwischenprodukt Beispiel 44
-
N-[5-(1,1-Dimethylethyl)-3-isoxazolyl]-2,
2-dimethyl-N-(1-methyl-5-nitro-1H-benzimidazol-2-yl)propanamid
-
Zu
einer Lösung
aus (1,97 g, 7,4 mmol) (5-tert-Butyl-isoxazol-3-yl)(1-methyl-5-nitro-1-H-benzoimidazol-2-yl)-amin
(439 μg,
1,38 mmol) in THF (30 ml) wurde Cäsiumcarbonat (906 mg, 2,78
mmol) und Di-tert-butyldicarbonat-THF-Lösung (2,1 ml, 2,09 mmol, 1M
THF-Lösung)
hinzugegeben. Die Reaktion wurde bei Raumtemperatur für 16 h gerührt, und
die Reaktion wurde dann mit Wasser verdünnt und mit EtOAc extrahiert.
Die vereinigten organischen Schichten wurden mit Wasser gewaschen, über MgSO4 getrocknet und aufkonzentriert, um ein
gelbes Öl
hervorzubringen. Das Rohmaterial wurde durch Kieselgel aufgereinigt,
um die Titelverbindung als einen gelben Feststoff zu ergeben (190
mg, 33 %).
MS (ESI) m/z = 416 [M+H].
-
Zwischenprodukt Beispiel 45
-
N-(5-Amino-1-methyl-1H-benzimidazol-2-yl)-N-[5-(1,1-dimethylethyl)-3-isoxazolyl]-2,2-dimethylpropanamid
-
Zu
einer Lösung
aus N-(5-tert-Butyl-isoxazol-3-yl)-2,2-dimethyl-N-(1-methyl-5-nitro-1-H-benzoimidazol-2-yl)-propinamid
(190 mg, 0,48 mmol) in Essigsäure
(12 ml und 3 ml) Ethanol wurde Zinkpulver (290 mg) hinzugegeben. Das
Reaktionsgemisch wurde bei Raumtemperatur gerührt bis das Ausgangsmaterial
aufgebraucht war, und die Reaktion wurde dann filtriert. Das Lösungsmittel
wurde verdampft, um einen braunen Rückstand zu ergeben, der dann
in CH2Cl2 aufgelöst und mit
einer 10%igen NaHCO3-Wasser-Lösung und Salzlösung gewaschen
wurde. Die organischen Schichten wurden über MgSO4 getrocknet
und aufkonzentriert, um die Titelverbindung als einen gelben Feststoff
zu ergeben (140 mg, 73 %).
MS (ESI) m/z = 450 [M+H].
-
Zwischenprodukt Beispiel 46
-
N-{5-[(2-Chlor-4-pyrimidinyl)amino]-1-methyl-1H-benzimidazol-2-yl}-N-[5-(1,1-dimethylethyl)-3-isoxazolyl]-2,2-dimethylpropanamid
-
Zu
einer Lösung
aus N-(5-Amino-1-methyl-1-H-benzoimidazol-2-yl)-N-(5-tert-butyl-isoxazol-3-yl)-2,2-dimethyl-propinamid
(149 mg, 0,39 mmol) in THF (3 ml) und Ethanol (9 ml) wurde NaHCO3 (66 mg, 0,78 mmol) und 2,4-Dichlorpyrimidin
(78 mg, 0,52 mmol) hinzugegeben, und die Reaktion wurde auf 75°C erhitzt.
Nach 5 h wurde die Reaktion heiß filtriert
und aufkonzentriert, um einen braunen Rückstand zu ergeben. Das Rohmaterial
wurde mit Ether verdünnt
und die Titelverbindung wurde durch die Zugabe von Hexan auspräzipitiert
(140 mg, 73 %).
MS (ESI) m/z = 498 [M+H].
-
Zwischenprodukt Beispiel 47
-
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}[5-(1,1-dimethylethyl)-3-isoxazolyl]carbamat
-
N-(5-tert-Butyl-isoxazol-3-yl)-2,2-dimethyl-N-[1-methyl-5-(2-methylpyrimidin-4-ylamino)-1H-benzoimidazol-2-yl]-propionamid
(200 mg, 0,37 mmol) wurde in DMF (10 ml) aufgelöst und Cäsiumcarbonat (244 mg, 0,75
mmol) wurde hinzugegeben. Nach 15 min wurde Iodmethan (25 μl, 0,41 mmol)
hinzugegeben, und die Reaktion wurde bei Raumtemperatur gerührt bis
das Ausgangsmaterial verbraucht war. Die Reaktion wurde mit Wasser
verdünnt
und die wäßrige Schicht
wurde mit EtOAc extrahiert. Die vereinigten organischen Schichten
wurden mit Wasser gewaschen, über
Na2SO4 getrocknet,
und aufkonzentriert, um einen weißen Feststoff hervorzubringen
(195 mg, 96 %).
MS (ESI) m/z = 512 [M+H]+.
-
Zwischenprodukt Beispiel 48
-
1-Methyl-5-nitro-1H-benzimidazol-2-amin
-
Zu
einer Lösung
aus N1-Methyl-4-nitro-benzol-1,2-diamin
(200 mg, 1,20 mmol) in Methanol (12 ml) wurde Cyanogenbromid (190,1
mg, 1,79 mmol) hinzugegeben. Nach Rühren bei Raumtemperatur für 16 h wurde
das Methanol im Vakuum entfernt, und der resultierende Feststoff
wurde mit Diethylether (40 ml) für
5 Minuten gerührt.
Das resultierende Hydrobromidsalz der Titelverbindung wurde filtriert
und luftgetrocknet.
1H-NMR (300 MHz,
d6-DMSO) δ:
7,91 (s, 1H), 7,88 (d, J = 8,6Hz, 1H), 7,31 (d, J = 8,5Hz, 1H),
6,96 (s, 2H), 3,57 (s, 3H).
-
Zwischenprodukt Beispiel 49
-
1-Methyl-1H-benzimidazol-2,5-diamin
-
Die
Titelverbindung wurde unter Verwendung des Verfahrens aus Zwischenprodukt
von Beispiel 1C hergestellt, mit der Ausnahme, daß 1-Methyl-5-nitro-1H-benzimidazol-2-amin
als das Ausgangsmaterial verwendet wurde.
1H-NMR
(400 MHz, d6-DMSO) δ: 6,72 (d, J = 8,6Hz, 1H), 6,37
(s, 1H), 6,17 (d, J = 8,1Hz, 1H), 6,04 (m, 2H), 4,36 (br s, 2H),
3,34 (s, 3H).
-
Zwischenprodukt Beispiel 50
-
N
5-(2-Chlor-5-pyrimidinyl)-1-methyl-1H-benmzimidazol-2,5-diamin
-
Die
Titelverbindung wurde unter Verwendung des Verfahrens aus Zwischenprodukt
von Beispiel 1D hergestellt, mit der Ausnahme, daß 1-Methyl-1H-benzimidazol-2,5-diamin
als das Ausgangsmaterial verwendet wurde.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,75 (s, 1H), 8,02 (d, J =
5,9Hz, 1H), 7,29 (br s, 1H), 7,09 (d, J = 8,3Hz, 1H), 6,93 (br m,
1H), 6,58 (d, J = 5,2Hz, 1H), 6,44 (s, 2H), 3,47 (s, 3H).
-
Zwischenprodukt Beispiel 51
-
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)amino]-1-methyl-1H-benzimidazol-2-yl}carbamat
-
Zu
einer Lösung
aus N5-(2-Chlorpyrimidin-4-yl)-1-methyl-1H-benzimidazol-2,5-diamin
(200 mg, 0,728 mmol) in THF (10 ml) wurde Triethylamin (0,101 ml,
0,728 mmol) und Di-tert-butyldicarbonat (175 mg, 0,801 mmol) zugegeben.
Nach Rühren
für 16
h bei Raumtemperatur wurde die Reaktion mit Wasser verdünnt und mit
EtOAc extrahiert. Die vereinigten Schichten wurden mit Wasser gewaschen, über MgSO4 getrocknet und im Vakuum aufkonzentriert.
1H-NMR (400 MHz, d6-DMSO) δ: 9,92 (s,
1H), 8,09 (d, J = 5,8Hz, 1H), 7,74 (br s, 1H), 7,21-7,19 (m, 2H),
7,02 (d, J = 8,2Hz, 1H), 6,66 (d, J = 5,9Hz, 1H), 3,24 (s, 3H),
1,61 (s, 9H).
-
Zwischenprodukt Beispiel 52
-
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}carbamat
-
Die
Titelverbindung wurde unter Verwendung des Verfahrens aus Zwischenprodukt
Beispiel 4E hergestellt, mit der Ausnahme, daß tert-Butyl- 5-[(2-chlorpyrimidin-4-yl)amino]-1-methyl-1H-benzimidazol-2-ylcarbamat
als das Ausgangsmaterial verwendet wurde.
1H-NMR
(400 MHz, d6-DMSO) δ: 7,98 (d, J = 6,0Hz, 1H), 7,44
(s, 1H), 7,21-7,16 (m, 3H), 6,31 (d, J = 5,8Hz, 1H), 3,38 (s, 3H),
3,29 (s, 3H), 1,58/(s, 9H).
-
Zwischenprodukt Beispiel 53
-
N
5,1-Dimethyl-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamin
-
Die
Titelverbindung wurde unter Verwendung des Verfahrens aus Schema
1 und Beispiel 1 hergestellt, mit der Ausnahme, daß N5-(2-Chlorpyrimidin-4-yl)-N2,N5,1-dimethyl-1H-benzimidazol-2,5-diamin
als das Ausgangsmaterial verwendet wurde.
1H-NMR
(400 MHz, d6-DMSO) δ: 9,23 (s, 1H), 7,81-7,78 (m,
3H), 7,25-7,19 (m, 3H), 7,04 (m, 1H), 6,82 (m, 1H), 6,56 (br s,
2H), 5,65 (d, J = 5,9Hz, 1H), 4,36 (s, 2H), 3,53 (s, 3H), 3,44 (s,
3H), 2,86 (s, 3H).
MS (ESI) m/z = 438 [M+H]+.
-
Zwischenprodukt Beispiel 54
-
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}carbamat
-
(A)
1-Methyl-5-nitro-1H-benzimidazol-2-amin
-
Zu
einer Lösung
aus N
1-Methyl-4-nitro-benzol-1,2-diamin
(5 g, 30 mmol) in MeOH wurde Bromidisothiocyanat (4,4 g, 42 mmol)
hinzugegeben, und das Gemisch wurde bei Raumtemperatur gerührt. Nach
16 h wurde 6N NaOH-Lösung zu
dem Reaktionsgemisch gegeben bis Ph~10, und MeOH wurde dann im Vakuum entfernt.
H
2O wurde hinzugegeben und der Feststoff
wurde filtriert und getrocknet, um die Titelverbindung als einen
cremefarbenen Feststoff zu ergeben (5,2 g, 90 %).
MS (ESI)
m/z = 193 [M+H]
+. (C)
1-Methyl-1H-benzimidazol-2,5-diamin
-
Eine
Lösung
aus 1-Methyl-5-nitro-1H-benzimidazol-2-amin (0,19 g, 1 mmol), 10
% Pd/C (50 mg) in Ethanol (10 ml) wurden Hydrazin (0,5 ml) hinzugegeben,
und die Reaktion wurde bis auf 80°C
erhitzt. Nachdem eine TLC zeigte, daß das Ausgangsmaterial aufgebraucht
war, wurde die Reaktion auf Raumtemperatur abgekühlt und durch einen Pfropfen
aus Celite passiert. Das Filtrat wurde aufkonzentriert, um die Titelverbindung
als einen cremefarbenen Feststoff zu ergeben.
MS (ESI) m/z
= 163 [M+H]
+. (D)
N
5-(2-Chlor-4-pyrimidinyl)-N
5,1-dimethyl-1H-benzimidazol-2,5-diamin
-
Zu
einer Lösung
aus 1-Methyl-1H-benzimidazol-2,5-diamin (0,63 g, 3,89 mmol) in THF
(4 ml) und Ethanol (12 ml) wurde NaHCO
3 (0,98
g, 11,67 mmol) und 2,4-Dichlorpyrimidin (1,45 g, 9,7 mmol) hinzugegeben,
und die Reaktion wurde auf 80°C
erhitzt. Nach 5 h wurde die Reaktion heiß filtriert und zu einem grauen Schaum
aufkonzentriert. Ether wurde hinzugegeben und der Feststoff wurde
filtriert und getrocknet, um N
5-(2-Chlor-pyrimidin-4-yl)-1-methyl-1H-benzoimidazol-2,5-diamin
als einen roten Feststoff zu ergeben.
MS (ESI) m/z = 275 [M+H]
+. (E)
1,1-Dimethylethyl{5-[(2-chlor-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}carbamat
-
Zu
einer Lösung
aus N5-(2-Chlor-4-pyrimidinyl)-N5,1-dimethyl-1H-benzimidazol-2,5-diamin (137 mg, 0,5
mmol) in THF (17 ml) wurde Triethylamin (0,7 ml, 0,5 mmol) und Di-tert-butyldicarbonat
1M in THF (0,5 ml, 0,5 mmol) hinzugegeben, und die Reaktion wurde
bei Raumtemperatur für
16 h gerührt.
Die Reaktion wurde mit Wasser verdünnt und mit CH2Cl2 extrahiert. Die vereinigten organischen
Schichten wurden mit Wasser gewaschen, über MgSO4 getrocknet
und zu einem cremefarbenen Feststoff aufkonzentriert.
-
Dieser
Feststoff wurde in DMF (2 ml) aufgelöst und Cäsiumcarbonat (0,2 g, 0,626
mmol) hinzugegeben, und das Reaktionsgemisch wurde bei Raumtemperatur
gerührt.
Nach 15 min wurde Iodmethan (0,022 ml, 0,344 mmol) hinzugegeben,
und die Reaktion wurde bei Raumtemperatur gerührt. Nachdem eine TLC zeigt, daß das Ausgangsmaterial
aufgebraucht war, wurde die Reaktion mit Wasser verdünnt. Die
wäßrige Schicht wurde
mit CH2Cl2 extrahiert.
Die vereinigten organischen Schichten wurden mit Wasser gewaschen, über MgSO4 getrocknet und zu einem roten Schaum aufkonzentriert.
Das Rohmaterial wurde mit Kieselgelchromatographie aufgereinigt,
um die Titelverbindung als einen weißen Feststoff zu ergeben (0,058
mg, 45 % über zwei
Schritte).
MS (ESI) m/z = 389 [M+H]+.
-
Zwischenprodukt Beispiel 55
-
3-(4-Morpholinylsulfonyl)anilin
-
Morpholin
(2,2 ml, 25 mmol) wurde langsam zu 3-Nitro-benzolsulfonylchlorid
(5,5 g, 25 mmol) in CH2Cl2 bei
0°C hinzugegeben.
Die Reaktion wurde innerhalb von 0,5 h auf Raumtemperatur erwärmt. Nachdem
CH2Cl2 im Vakuum
entfernt wurde, wurde eine gesättigte
NaHCO3-Lösung
hinzugegeben, und der Feststoff wurde filtriert und getrocknet,
um 4-(3-Nitro-benzolsulfonyl)morpholin als einen cremefarbenen Feststoff zu
ergeben (5,9 g, 87 %).
MS (ESI) m/z = 273 [M+H]+.
-
4-(3-Nitro-benzolsulfonyl)-morpholin
(5,9 g, 21,7 mmol) wurde mit 10 % Palladium auf Aktivkohle (1 g), Ethanol
(60 ml) und Hydrazin (5 ml) vereinigt und bei Reflux für 18 h erhitzt.
Die Lösung
wurde duch Celite filtriert, aufkonzentriert und auf 0°C abgekühlt. Das
Produkt präzipitierte
als ein farbloses Kristall aus (4,7 g, 89 %).
MS (ESI) m/z
= 243 [M+H]+.
-
Zwischenprodukt Beispiel 56
-
3-[(4-Methyl-1-piperazinyl)sulfonyl]anilin
-
Die
Titelverbindung wurde entsprechend dem Verfahren aus Zwischenprodukt
Beispiel 2 mit 3-Nitro-benzolsulfonylchlorid (4,4 g, 20 mmol) und
N-Methyl-piperazin (2,2 ml, 20 mmol) als einen cremefarbenen Feststoff
hergestellt (3,6 g, 70 %).
MS (ESI) m/z = 256 [M+H]+.
-
Zwischenprodukt Beispiel 57
-
4-Amino-N,N-dimethylbenzolsulfonamid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Zwischenprodukt Beispiel 2 mit 3-Nitro-benzolsulfonylchlorid
(6,6 g, 30 mmol) und Dimethylamin 2M in MeOH (15 ml, 30 mmol) als
einen cremefarbenen Feststoff hergestellt (4,8 g, 70 %).
MS
(ESI) m/z = 232 [M+H]+.
-
Beispiel 1
-
N
5,1-Dimethyl-N
2-(1-methylethyl)-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Zu
einer Lösung
aus N5-(2-chlor-4-pyrimidinyl)-N5,1-dimethyl-N2-(1-methylethyl)-1H-benzimidazol-2,5-diamin
(83 mg, 0,25 mmol) und 4-[(Methylsulfonyl)methyl]anilin (46 mg,
0,25 mmol) in Ethanol (2,5 ml) wurde eine Lösung aus HCl (0,25 ml, 1M in
Diethylether) gegeben, und die Reaktion wurde auf 70°C erhitzt. Nach
5 h wurde das Präzipitat
abfiltriert und mit Ethanol gewaschen und getrocknet, um die Titelverbindung als
einen weißen
Feststoff zu ergeben (104 mg, 87 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 10,1 (s, 1H), 8,74 (m, 1H),
7,93 (d, J = 6,6Hz, 1H), 7,60-7,65 (m, 3H), 7,41 (s, 1H), 7,24-7,29
(m, 3H), 5,90 (s, 1H), 4,39 (s, 2H), 4,09 (m, 1H), 3,69 (s, 3H),
3,49 (s, 3H), 2,87 (s, 3H), 1,33 (d, J = 6,6Hz, 611), ppm.
MS
(ESI) m/z = 480 [M+H]+.
-
Beispiel 2
-
1-(4-{[4-(Methyl{1-methyl-2-[(1-methylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)methansulfonamidhydrochlorid
-
Zu
einer Lösung
aus N5-(2-Chlor-4-pyrimidinyl)-N5,1-dimethyl-N2-(1-methylethyl)-1H-benzimidazol-2,5-diamin
(83 mg, 0,25 mmol) und 1-(4-(Aminophenyl)methan-sulfonamid
(47 mg, 0,25 mmol) in Ehtanol (2,5 ml) wurde eine Lösung aus
HCl (0,25 ml, 1M in Diethylether) gegeben, und die Reaktion wurde
auf 70°C erhitzt.
Nach 20 Stunden wurde das Reaktionsgemisch mit der Zugabe von festem
NaHCO3 neutralisiert. Das Gemisch wurde
filtriert, und das Filtrat wurde mit Kieselgel aufgereinigt, um
die Titelverbindung als einen weißen Feststoff zu ergeben.
1H-NMR (300 MHz, d6-DMSO) δ: 9,16 (s,
1H), 7,78 (m, 3H), 7,19 (d, J = 8,1Hz, 3H), 7,09 (d, J = 1,8Hz,
1H), 6,82 (dd, J = 8,1 und 1,8Hz, 1H), 6,75 (s, 2H), 6,49 (d, J
= 7,8Hz, 1H), 5,62 (d, J = 6,0Hz, 1H), 4,15 (s, 2H), 4,02 (m, 1H),
3,51 (s, 3H), 3,44 (s, 3H), 1,24 (d, J = 6,6Hz, 611) ppm.
MS
(ESI) m/z = 481 [M+H]+.
-
Beispiel 3
-
N
2,N
5,1-Trimethyl-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlorpyrimidin-4-yl)-N2,N5-1-trimethyl-1H-benzimidazol-2,5-diamin
(62 mg, 0,21 mmol) und 4-[(Methylsulfonyl)methyl]anilin (39 mg,
0,21 mmol) als einen weißen
Feststoff hergestellt (73 mg, 72 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 10,22 (s, 1H), 9,32 (d, J
= 4,5Hz, 1H), 7,94 (d, J = 6,6Hz, 1H), 7,62 (d, J = 8,4Hz, 3H),
7,43 (d, J = 1,8Hz, 1H), 7,24-7,30 (m, 3H), 5,91 (d, J = 5,7Hz,
1H), 4,40 (s, 2H), 3,69 (s, 3H), 3,49 (s, 3H), 3,07 (d, 1 = 4,5Hz,
3H), 2,87 (s, 3H).
MS (ESI) m/z = 452 [M+H]+.
-
Beispiel 4
-
N
5,1-Dimethyl-N
5-(2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N
2-(phenylmethyl)-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-Benzyl-N5-(2-chlorpyrimidin-4-yl)-N5,1-dimethyl-1H-benzimidazol-2,5-diamin (95
mg, 0,25 mmol) und 4-[(Methylsulfonyl)methyl]anilin (46 mg, 0,25
mmol) als einen weißen
Feststoff hergestellt (138 mg, 95 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 9,20 (s, 1H), 7,76-7,80 (m,
3H), 7,38-7,41 (m, 3H), 7,29-7,34 (m, 2H), 7,22-7,24 (m, 4H), 7,08
(d, J = 1,8Hz, 1H), 6,84 (dd, J = 8,1 und 1,8Hz, 1H), 5,63 (d, J
= 6,0Hz, 1H), 4,60 (d, J = 6,0Hz, 2H), 4,34 (s, 2H), 3,58 (s, 3H),
3,43 (s, 3H), 2,85 (s, 3H).
MS (ESI) m/z = 527 [M+H]+.
-
Beispiel 5
-
N
5,1-Dimethyl-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N
2-(phenyl-1H-benzimidazol-2,5-diamintrifluoracetat
-
Zu
einer Lösung
aus tert-Butyl-5-[(2-chlorpyrimidin-4-yl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl(phenyl)carbamat
(100 mg, 0,22 mmol) und 4-[(Methylsulfonyl)methyl]anilin (41 mg,
0,22 mmol) in Ethanol (2,5 ml) wurde eine Lösung aus HCl (1 Tropfen, 1M
in Diethylether) hinzugegeben, und die Reaktion wurde auf 70°C erhitzt.
Nach 20 Stunden wurden das Reaktionsgemisch mit der Zugabe von festem
NaHCO3 neutralisiert. Das Gemisch wurde
filtriert, und das Filtrat wurde mit Kieselgel aufgereinigt. Das
gesammelte Produkt wurde in 5 ml einer 1:1 TFA/Methylenchlorid-Lösung für 3 h gerührt. Die
Reaktion wurde aufkonzentriert, um die Titelverbindung als einen
weißen
Feststoff zu ergeben (116 mg, 84 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 10,6 (s, 1H), 9,83 (br s,
1H), 7,78 (d, J = 6,9Hz, 1H), 7,70 (d, J = 8,1Hz, 2H), 7,57-7,60
(m, 3H), 7,32-7,44 (m, 5H), 7,11-7,21 (m, 2H), 5,93 (br s, 1H),
4,43 (s, 2H), 3,79 (s, 3H), 3,53 (s, 3H), 2,87 (s, 3H).
MS
(ESI) m/z = 514 [M+H]+.
-
Beispiel 6
-
2-Methyl-5-{[4-(methyl{1-methyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}-N-(methyloxy)benzolsulfonamid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N2-Benzyl-N5-(2-chlorpyrimidin-4-yl)-N5,1-dimethyl-1H-benzimidazol-2,5-diamin (50
mg, 0,13 mmol) und 5-Amino-N-methoxy-2-methylbenzolsulfonamid (30
mg, 0,14 mmol) als einen weißen
Feststoff (58 mg, 0,10 mmol) nach Kieselgel-Chromatographie mit Ethanol in Dichlormethan
hergestellt.
1H-NMR (300 MHz, d6-DMSO) δ:
10,3 (s, 1H), 9,42 (s, 1H), 8,73 (s, 1H), 7,76-7,80 (m, 2H), 7,40-7,23
(m, 8H), 7,09 (br s, 1H), 6,84 (d, J = 7,4Hz, 1H), 5,61 (d, J =
5,3Hz, 1H), 4,60 (br s, 2H), 4,34 (s, 2H), 3,58 (s, 6H), 3,46 (s,
3H).
MS (ESI) m/z = 559 [M+H]+.
-
Beispiel 7
-
3-{[4-(Methyl{1-methyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-Benzyl-N5-(2-chlorpyrimidin-4-yl)-N5,1-dimethyl-1H-benzimidazol-2,5-diamin (95
mg, 0,25 mmol) und 3-Amino-benzolsulfonamid (43 mg, 0,25 mmol) als
einen leichtrosanen Feststoff hergestellt (112 mg, 82 %).
1H-NMR (300 MHz, d6-DMSO
+ NaHCO3) δ: 10,03 (br s, 2H), 9,55 (br
s, 1H), 8,48 (s, 1H), 7,89 (d, J = 6,3Hz, 1H), 7,74 (m, 1H), 7,59
(d, J = 8,7Hz, 1H), 7,51 (m, 2H), 7,22-7,41 (m, 8H), 5,76 (d, J
= 6,3Hz, 1H), 4,76 (d, J = 5,7Hz, 2H), 3,763 (s, 3H), 3,48 (s, 3H).
MS
(ESI) m/z = 515 [M+H]+.
-
Beispiel 8
-
2-Methyl-5-{[4-(methyl{1-methyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-Benzyl-N5-(2-chlorpyrimidin-4-yl)-N5,1-dimethyl-1H-benzimidazol-2,5-diamin (95
mg, 0,25 mmol) und 5-Amino-2-methyl-benzolsulfonamid (47 mg, 0,25
mmol) hergestellt, um das gewünschte
Produkt als einen rosafarbenen Feststoff zu ergeben (114 mg, 81
%).
1H-NMR (300 MHz, d6-DMSO
+ NaHCO3) δ: 10,31 (br s, 2H), 9,61 (br
s, 1H), 8,46 (s, 1H), 7,88 (d, J = 6,6Hz, 1H), 7,63 (m, 2H), 7,51
(d, J = 7,5Hz, 2H), 7,23-7,39 (m, 7H), 5,77 (d, J = 6,3Hz, 1H),
4,77 (d, H = 6,0Hz, 2H), 3,74 (s, 3H), 3,50 (s, 3H), 2,52 (s, 3H).
MS
(ESI) m/z = 529 [M+H]+.
-
Beispiel 9
-
1-(4-{[4-(methyl{1-methyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)methansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß denm Verfahren
aus Beispiel 1 mit N2-Benzyl-N5-(2-chlorpyrimidin-4-yl)-N5,1-dimethyl-1H-benzimidazol-2,5-diamin (95
mg, 0,25 mmol) und (4-Amino-phenyl)-methansulfonamid (46 mg, 0,25
mmol) hergestellt, um das gewünschte
Produkt als einen weißen
Feststoff zu ergeben (85 mg, 60 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 10,17 (br
s, 2H), 9,53 (br s, 1H), 7,90 (d, J = 6,6Hz, 1H), 7,61 (d, J = 8,4Hz,
3H), 7,51 (d, J = 7,5Hz, 2H), 7,22-7,39 (m, 6H), 6,82 (s, 2H), 5,87
(d, J = 6,0Hz, 1H), 4,76 (d, J = 5,7Hz, 2H), 4,19 (s, 2H), 3,74
(s, 3H), 3,49 (s, 3H).
MS (ESI) m/z = 529 [M+H]+.
-
Beispiel 10
-
N-Methyl-2-(4-{[4-(methyl{1-methyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)ethansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-Benzyl-N5-(2-chlorpyrimidin-4-yl)-N5,1-dimethyl-1H-benzimidazol-2,5-diamin (95
mg, 0,25 mmol) und 2-(4-Amino-phenyl)-ethansulfonsäuremethylamid
(54 mg, 0,25 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben (49 mg, 33 %).
1H-NMR (300
MHz, d6-DMSO + NaHCO3) δ: 9,97 (br
s, 1H), 9,34 (br s, 1H), 7,85 (d, J = 6,6Hz, 1H), 7,49-7,59 (m,
5H), 7,25-7,37 (m, 4H), 7,17 (d, J = 8,1Hz, 3H), 7,03 (q, J = 5,4Hz,
1H), 5,77 (d, J = 6,6Hz, 1H), 4,74 (d, J = 5,1Hz, 2H), 3,72 (s,
3H), 3,46 (s, 3H), 3,21-3,27 (m, 2H), 2,85-2,91 (m, 2H), 2,58 (d,
J = 4,8Hz, 3H).
MS (ESI) m/z = 557 [M+H]+.
-
Beispiel 11
-
3-({4-[(2-{[(4-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(4-fluor-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (99 mg, 0,25
mmol) und 3-Amino-benzolsulfonamid (43 mg, 0,25 mmol) als einen
weißen
Feststoff hergestellt (104 mg, 73 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 10,08 (br,
s, 1H), 9,57 (br s, 1H), 8,46 (s, 1H), 7,87 (d, J = 1,8Hz, 1H),
7,73 (m, 1H), 7,55-7,58 (m, 3H), 7,40 (d, J = 3,3Hz, 2H), 7,35 (s,
1H), 7,30 (s, 2H), 7,16-7,23 (m, 3H), 5,74 (d, J = 4,5Hz, 1H), 4,73
(d, J = 4,2Hz, 2H), 3,71 (s, 3H), 3,47 (s, 3H).
MS (ESI) m/z
= 533 [M+H]+.
-
Beispiel 12
-
5-({4-[(2-{[(4-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(4-fluor-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (99 mg, 0,25
mmol) und 5-Amino-2-methyl benzolsulfonamid (47 mg, 0,25 mmol) als
einen weißen
Feststoff hergestellt (69 mg, 48 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 10,28 (br
s, 1H), 9,61 (br s, 1H), 8,45 (s, 1H), 7,86 (d, J = 2,1Hz, 1H),
7,63 (m, 1H), 7,52-7,59 (m, 3H), 7,37 (s, 1H), 7,31 (s, 2H), 7,13-7,26
(m, 4H), 5,74 (d, J = 4,5Hz, 1H), 4,73 (d, J = 4,5Hz, 2H), 3,71
(s, 3H), 3,48 (s, 3H), 2,50 (s, 3H).
MS (ESI) m/z = 547 [M+H]+.
-
Beispiel 13
-
N
2-[(4-Fluorphenyl)methyl]-N
5,1-dimethyl-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(4-fluor-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (99 mg, 0,25
mmol) und 4-[(Methylsulfonyl)methyl]anilin (46 mg, 0,25 mmol) als
einen weißen
Feststoff hergestellt (69 mg, 48 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 9,20 (s, 1H), 7,76-7,80 (m,
3H), 7,41-7,46 (m, 3H), 7,23 (d, J = 8,4Hz, 3H), 7,09-7,17 (m, 3H),
6,84 (dd, J = 8,4 und 1,8Hz, 1H), 5,63 (d, J = 6,0Hz, 1H), 4,57
(d, J = 5,7Hz, 2H), 4,34 (s, 2H), 3,57 (s, 3H), 3,43 (s, 3H), 2,85
(s, 3H).
MS (ESI) m/z = 546 [M+H]+.
-
Beispiel 14
-
1-[4-({4-[(2-{[(4-fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(4-fluor-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (99 mg, 0,25
mmol) und (4-Amino-phenyl)methansulfonamid (46 mg, 0,25 mmol) als
einen weißen
Feststoff hergestellt (50 mg, 34 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 9,16 (s, 1H), 7,75-7,78 (m,
3H), 7,38-7,46 (m, 3H), 7,08-7,24 (m, 6H), 6,84 (dd, J = 8,2 und
1,6Hz, 1H), 6,75 (br s, 2H), 5,61 (d, J = 6,0Hz, 1H), 4,57 (d, J
= 5,7Hz, 2H), 4,15 (s, 2H), 3,56 (s, 3H), 3,43 (s, 3H).
MS
(ESI) m/z = 547 [M+H]+.
-
Beispiel 15
-
2-[4-({4-[(2-{[(4-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyl]-N-methylethansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(4-fluor-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (99 mg, 0,25
mmol) und 2-(4-Amino-phenyl)ethansulfonsäuremethylamid (54 mg, 0,25
mmol) hergestellt, um das gewünschte
Produkt als einen weißen
Feststoff zu ergeben (90 mg, 59 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 9,04 (s, 1H), 7,68-7,75 (m,
3H), 7,41-7,46 (m, 3H), 7,23 (d, J = 8,1Hz, 1H), 7,08-7,17 (m, 4H),
6,94 (q, J = 5,1Hz, 1H), 6,83 (dd, J = 8,1 und 1,5Hz, 1H), 5,59
(d, J = 6,0Hz, 1H), 4,57 (d, J = 5,4Hz, 2H), 3,56 (s, 3H), 3,41
(s, 3H), 3,20-3,26 (m, 2H), 2,83-2,88
(m, 2H), 2,59 (d, J = 5,1Hz, 2H).
MS (ESI) m/z = 575 [M+H]+.
-
Beispiel 16
-
3-[(4-(Methyl[1-methyl-2-({[4-(methyloxy)phenyl]methyl}amino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino}benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(4-methoxy-benzyl)-1,N5-dimethyl-1H- benzoimidazol-2,5-diamin (82 mg, 0,20
mmol) und 3-Amino-benzolsulfonamid (34 mg, 0,20 mmol) als einen
weißen
Feststoff hergestellt (83 mg, 72 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 10,28 (br
s, 2H), 9,53 (br s, 1H), 8,44 (s, 1H), 7,91 (d, J = 6,6Hz, 1H),
7,73 (m, 1H), 7,64 (d, J = 8,4Hz, 1H), 7,43 (d, J = 8,4Hz, 4H),
7,28-7,34 (m, 3H), 6,94 (d, J = 8,4Hz, 2H), 5,81 (m, 1H), 4,67 (d,
J = 5,7Hz, 2H), 3,74 (s, 3H), 3,71 (s, 3H), 3,50 (s, 3H).
MS
(ESI) m/z = 545 [M+H]+.
-
Beispiel 17
-
2-Methyl-5-[(4-{methyl[1-methyl-2-({[4-(methyloxy)phenyl]methyl}amino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(4-methoxy-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin
(82 mg, 0,20 mmol) und 5-Amino-2-methylbenzolsulfonamid (37 mg,
0,20 mmol) als einen weißen
Feststoff hergestellt (89 mg, 75 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 10,25 (br
s, 2H), 9,50 (br s, 1H), 8,46 (s, 1H), 7,88 (d, J = 6,6Hz, 1H),
7,60-7,67 (m, 2H), 7,41-7,46 (m, 3H), 7,23-7,32 (m, 4H), 6,93 (d,
J = 8,7Hz, 2H), 5,78 (d, J = 6,3Hz, 1H), 6,68 (d, J = 5,7Hz, 2H),
3,74 (s, 3H), 3,71 (s, 3H), 3,51 (s, 3H), 2,53 (s, 3H).
MS
(ESI) m/z = 559 [M+H]+.
-
Beispiel 18
-
N
5,1-Dimethyl-N
2{[4-(methyoxy)phenyl]methyl}-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(4-methoxy-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (82 mg, 0,20
mmol) und 4-[(Methylsulfonyl)methyl]anilin (37 mg, 0,20 mmol) als
einen weißen
Feststoff hergestellt (86 mg, 72 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 9,21 (s, 1H), 7,76-7,81 (m,
3H), 7,29-7,34 (m, 3H), 7,21-7,25 (m, 3H), 7,09 (d, J = 1,8Hz, 1H),
6,82-6,90 (m, 3H), 5,64 (d, J = 6,0Hz, 1H), 4,52 (d, J = 5,7Hz,
2H), 4,35 (s, 2H), 3,72 (s, 3H), 3,56 (s, 3H), 3,43 (s, 3H), 2,85
(s, 3H).
MS (ESI) m/z = 558 [M+H]+.
-
Beispiel 19
-
1-{4-[(4{Methyl[1-methyl-2-({[4-(methyloxy)phenyl]methyl}amino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino}phenyl}methansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(4-methoxy-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (82 mg, 0,20
mmol) und (4-Amino-phenyl)methansulfonamid ((37 mg, 0,20 mmol) als
einen weißen
Feststoff hergestellt (49 mg, 41 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 9,58 (br s, 1H), 9,00 (br
s, 1H), 7,85 (d, J = 6,0Hz, 1H), 7,68 (d, J = 8,1Hz, 2H), 7,42-7,50
(m, 3H), 7,29 (s, 1H), 7,12-7,21 (m, 3H), 6,91 (d, J = 8,4Hz, 2H),
6,80 (s, 2H), 5,75 (d, J = 5,7Hz, 1H), 4,64 (d, J = 5,1Hz, 2H),
4,17 (s, 2H), 3,73 (s, 3H), 3,68 (s, 3H), 3,46 (s, 3H).
MS
(ESI) m/z = 559 [M+H]+.
-
Beispiel 20
-
N-Methyl-2-{4-[(4-{methyl[1-methyl-2-({[4-(methyloxy)phenyl]-methyl}amino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]phenyl}ethansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-chlor-pyrimidin-4-yl)-N2-(4-methoxy-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin
(82 mg, 0,20 mmol) und 2-(4-Amino-phenyl)ethansulfonsäuremethylamid
(43 mg, 0,20 mmol) als einen weißen Feststoff hergestellt (105
g, 85 %).
1H-NMR (300 MHz, d6-DMSO) δ:
10,18 (br s, 1H), 9,46 (br s, 1H), 7,88 (d, J = 6,6Hz, 1H), 7,54-7,62
(m, 3H), 7,40-7,47 (m, 3H), 7,18-7,26 (m, 3H), 7,01 (m, 1H), 6,92
(d, J = 8,4Hz, 2H), 5,83 (d, J = 6,3Hz, 1H), 4,68 (d, J = 5,4Hz,
2H), 3,73 (s, 3H), 3,72 (s, 3H), 3,48 (s, 3H), 3,23-3,28 (m, 2H),
2,87-2,93 (m, 2H), 2,60 (d, J = 4,8Hz, 3H).
MS (ESI) m/z =
587 [M+H]+.
-
Beispiel 21
-
5-({4-[(2-{[(3-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(3-fluor-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (99 mg, 0,25
mmol) und 5-Amino-2-methylbenzolsulfonamid (47 mg, 0,25 mmol) als
einen weißen
Feststoff hergestellt (96 mg, 66 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 10,06 (br
s, 1H), 9,34 (br s, 1H), 8,49 (s, 1H), 7,84 (d, J = 6,6Hz, 1H),
7,65 (d, J = 6,6Hz, 1H), 7,56 (d, J = 8,4Hz, 1H), 7,08-7,44 (m,
9H), 5,72 (d, J = 6,6Hz, 1H), 4,75 (d, J = 6,6Hz, 2H), 3,71 (s,
3H), 3,48 (s, 3H), 2,51 (s, 3H).
MS (ESI) m/z = 547 [M+H]+.
-
Beispiel 22
-
3-({4-[(2-{[(3-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5- yl)(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(3-fluor-berizyl)-1,N5-dimethyl-1H-berizoimidazol-2,5-diamin
(99 mg, 0,25 mmol) und 3-Amino-benzolsulfonamid (43 mg, 0,25 mmol)
als einen weißen
Feststoff hergestellt (62 mg, 44 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,70 (s,
2H), 8,53 (s, 1H), 7,83 (d, J = 6,0Hz, 1H), 7,74 (d, J = 6,6Hz,
1H), 7,26-7,50 (m, 8H), 7,10 (m, 2H), 5,69 (d, J = 6,0Hz, 1H), 4,70
(d, J = 5,1Hz, 2H), 3,67 (s, 3H), 3,46 (s, 3H).
MS (ESI) m/z
= 533 [M+H]+.
-
Beispiel 23
-
N
2-[(3-Fluorphenyl)methyl]-N
5,1-dimethyl-N
5-[2-([4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(2-fluor-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin
(99 mg, 0,25 mmol) und 4-[(Methylsulfonyl)methyl]anilin (46 mg,
0,25 mmol) als einen weißen
Feststoff hergestellt (44 mg, 30 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 10,64 (s, 1H), 9,82 (s, 1H),
7,93 (d, J = 6,9Hz, 1H), 7,57-7,66 (m, 3H), 7,28-7,43 (m, 7H, 7,12
(m, 1H), 5,94 (s, 1H), 4,80 (d, J = 5,7Hz, 2H), 4,41 (s, 2H), 3,76
(s, 3H), 3,50 (s, 3H), 2,87 (s, 3H).
MS (ESI) m/z = 546 [M+H]+.
-
Beispiel 24
-
1-[4-({4[(2-{[(3-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyljmethansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimjidin-4-yl)-N2-(3-fluor-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin
(99 mg, 0,25 mmol) und (4-Amino-phenyl)methansulfonamid (46 mg,
0,25 mmol) als einen weißen
Feststoff hergestellt (1H mg, 76 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 10,03 (br
s, 2H), 9,37 (br s, 1H), 7,87 (d, J = 6,6Hz, 1H), 7,54-7,64 (m,
2H), 7,32-7,44 (m, 3H), 7,19-7,24 (m, 3H), 7,08-7,14 (m, 1H), 6,81
(s, 2H), 5,82 (d, J = 6,0Hz, 1H), 4,76 (d, J = 5,7Hz, 2H), 4,18
(s, 2H), 3,72 (s, 3H), 3,47 (s, 3H).
MS (ESI) m/z = 547 [M+H]+.
-
Beispiel 25
-
2-[4-({4-[(2-{[(3-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyl]-N-methylethansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(3-fluor-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (99 mg, 0,25
mmol) und 2-(4-Amino-phenyl)ethansulfonsäuremethylamid (54 mg, 0,25
mmol) als einen weißen
Feststoffher (74 mg, 49 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,66 (br
s, 1H), 8,73 (br s, 1H), 7,81 (d, J = 6,6Hz, 1H), 7,62 (d, J = 8,1Hz,
2H), 7,36-7,49 (m, 2H), 7,27-7,31 (m, 3), 7,08-7,18 (m, 4H), 6,99
(q, J = 4,8Hz, 1H), 5,73 (d, J = 6,3Hz, 1H), 4,71 (d, J = 5,4Hz,
2H), 3,68 (s, 3H), 3,45 (s, 3H), 3,22-3,27 (m, 2H), 2,86-2,91 (m,
2H), 2,59 (d, J = 4,8Hz, 3H).
MS (ESI) m/z = 575 [M+H]+.
-
Beispiel 26
-
3-({4-[(2-{[(4-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimdazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-(4-Chlor-benzyl)-N5-(2-chlor-pyrimidin-4-yl)-1,N5-dimethyl-1Hbenzoimidazol-2,5-diamin (103
mg, 0,25 mmol) und 3-Amino-benzolsulfonamid (43 mg, 0,25 mmol) als
einen weißen
Feststoff hergestellt (68 mg, 47 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,89 (br
s, 1H), 8,49 (s, 1H), 7,86 (d, J = 6,3Hz, 1H), 7,73 (m, 1H), 7,18-7,74
(m, 1011), 5,73 (d, J = 6,3Hz, 1H), 4,71 (d, J = 5,7Hz, 2H), 3,69
(s, 3H), 3,47 (s, 3H).
MS (ESI) m/z = 549 [M+H]+.
-
Beispiel 27
-
5-({4-[(2-{[(4-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-(4-Chlor-benzyl)-N5-(2-chlor-pyrimidin-4-yl)-1,N5-dimethyl-1H-benzimidazol-2,5-diamin
(103 mg, 0,25 mmol) und 5-Amino-2-methylbenzolsulfonamid (47 mg,
0,25 mmol) als einen weißen
Feststoff hergestellt (106 mg, 71 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 10,17 (br
s, 1H), 9,40 (br s, 1H), 8,45 (s, 1H), 7,85 (d, J = 6,6Hz, 1H),
7,62 (m, 2H), 7,49-7,52 (m, 2H), 7,42-7,45 (m, 2H), 7,37 (s, 1H),
7,23-7,31 (m, 4H), 5,75 (m, 1H), 4,72 (d, J = 5,7Hz, 2H), 3,70 (s,
3H), 3,49 (s, 3H), 2,52 (s, 3H).
MS (ESI) m/z = 561 [M+H]+.
-
Beispiel 28
-
2-[4-({4-[(2-{[(4-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimdazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyl]-N-methylethansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-(4-Chlor-benzyl)-N5-(2-chlor-pyrimidin-4-yl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (103 mg, 0,25
mmol) und 2-(4-Amino-phenyl)ethansulfonsäuremethylamid (54 mg, 0,25
mmol) als einen weißen
Feststoff hergestellt (96 mg, 64 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 10,27 (br
s, 1H), 9,34 (br s, 1H), 7,85 (d, J = 7,2Hz, 1H), 7,61 (d, J = 8,4Hz,
1H), 7,49-7,54 (m, 4H), 7,38-7,44 (m, 3H), 7,20-7,26 (m, 3H), 6,99
(q, J = 5,1Hz, 1H), 5,83 (br s, 1H), 4,72 (d, J = 5,7Hz, 2H), 3,71
(s, 3H), 3,48 (s, 3H), 3,22-3,28 (m, 2H), 2,87-2,93 (m, 2H), 2,58
(d, J = 4,8Hz, 3H).
MS (ESI) m/z = 562 [M+H]+.
-
Beispiel 29
-
N
2-[(4-Chlorphenyl)methyl]-N
5,1-dimetyl-N
5-[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-(4-Chlor-benzyl)-N5-(2-chlor-pyrimidin-4-yl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin
(103 mg, 0,25 mmol) und 4-[(Methylsulfonyl)-methyl]anilin (46 mg, 0,25 mmol) als
einen weißen
Feststoff hergestellt (61 mg, 41 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,20 (s,
1H), 7,76-7,80 (m, 3H), 7,36-7,43 (m, 5H), 7,24 (d, J = 8,1Hz, 2H),
7,08 (d, J = 1,8Hz, 1H), 6,85 (dd, J = 8,1 und 1,8Hz, 1H), 5,63
(d, J = 6,0Hz, 1H), 4,58 (d, J = 5,7Hz, 2H), 4,34 (s, 2H), 3,58
(s, 3H), 3,43 (s, 3H), 2,85 (s, 3H).
MS (ESI) m/z = 562 [M+H]+.
-
Beispiel 30
-
3-({4-[{1-Ethyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-Benzyl-N5-(2-chlor-pyrimidin-4-yl)-1-ethyl-N5-methyl-1H-benzoimidazol-2,5-diamin (98 mg, 0,25 mmol) und 3-Amino-benzolsulfonamid (43
mg, 0,25 mmol) als einen weißen
Feststoff hergestellt (43 mg, 24 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,61 (s,
1H), 8,56 (s, 1H), 7,75-7,84 (m, 2H), 7,23-7,45 (m, 11H), 7,04 (d,
J = 7,2Hz, 1H), 5,71 (d, J = 5,7Hz, 1H), 4,68 (d, J = 5,1Hz, 2H),
4,21 (m, 2H), 3,46 (s, 3H), 1,28 (mm, 3H).
MS (ESI) m/z = 529
[M+H]+.
-
Beispiel 31
-
5-({4-[{1-Ethyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-Benzyl-N5-(2-chlor-pyrimidin-4-yl)-1-ethyl-N5-methyl-1H-benzoimidazol-2,5-diamin (98 mg, 0,25 mmol) und 5-Amino-2-methyl-benzolsulfonamid
(46 mg, 0,25 mmol) als einen weißen Feststoff hergestellt (83
mg, 58 %).
1H-NMR (300 MHz, d6-DMSO + NaHCO3) δ: 9,54 (s,
1H), 8,56 (s, 1H), 7,80 (d, J = 6,3Hz, 1H), 7,68 (dd, J = 8,25 und
1,6Hz, 1H), 7,15-7,47 (m, 1011), 7,03 (d, J = 7,8Hz, 1H), 5,69 (d,
J = 6,0Hz, 1H), 4,68 (d, J = 5,7Hz, 2H), 4,21 (m, 2H), 3,46 (s,
3H), 2,50 (s, 3H), 1,28 (t, J = 6,9Hz, 3H).
MS (ESI) m/z =
543 [M+H]+.
-
Beispiel 32
-
1-Ethyl-N
5-methyl-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N
2-(phenylmethyl)-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N2-Benzyl-N5-(2-chlor-pyrimidin-4-yl)-1-ethyl-N5-methyl-1H-benzoimidazol-2,5-diamin (98 mg, 0,25 mmol) und 4-[(Methylsulfonyl)methyl]anilin
(46 mg, 0,25 mmol) als einen weißen Feststoff hergestellt (65
mg, 45 %).
1H-NMR (300 MHz, d6-DMSO + NaHCO3) δ: 9,53 (s,
1H), 7,75 (m, 3H), 7,19-7,40 (m, 9H), 7,10 (s, 1H), 6,87 (m, 1H),
5,66 (m, 1H), 4,60 (m, 2H), 4,32 (s, 2H), 4,11 (m, 2H), 6,41 (s,
3H), 2,83 (s, 3H), 1,24 (m, 3H).
-
Beispiel 33
-
1-[4-({4-[{1-Ethyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N2-Benzyl-N5-(2-chlor-pyrimidin-4-yl)-1-ethyl-N5-methyl-1H-benzoimidazol-2,5-diamin (98 mg, 0,25 mmol) und (4-Amino-phenyl)-methansulfonamid
(46 mg, 0,25 mmol) als einen weißen Feststoff hergestellt (97
mg, 67 %).
1H-NMR (300 MHz, d6-DMSO + NaHCO3) δ: 9,30 (s,
1H), 7,79 (d, J = 6,0Hz, 1H), 7,75 (d, J = 8,7Hz, 2H), 7,15-7,42
(m, 9H), 6,9 + 5 (d, J = 8,1Hz, 1H), 6,77 (s, 2H), 5,69 (d, J =
6,0Hz, 1H), 4,65 (d, J = 5,7Hz, 2H), 4,16-4,18 (m, 4H), 3,44 (s,
3H), 1,27 (t, J = 7,2Hz, 3H).
MS (ESI) m/z = 543 [M+H]+.
-
Beispiel 34
-
3-({4-[(2-{[(2-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid,
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5(2-Chlor-pyrimidin-4-yl)-N2-(2-fluor-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin
(60 mg, 0,15 mmol) und 3-Amino-benzolsulfonamid (26 mg, 0,15 mmmol)
als einen weißen
Feststoff hergestellt (52 mg, 61 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,51 (s,
1H), 8,60 (s, 1H), 7,78 (d, J = 6,0Hz, 2H), 7,62 (br s, 1H), 7,47
(t, J = 7,8Hz, 1H), 7,12-7,41 (m, 9H), 6,89 (d, J = 8,1Hz, 1H),
5,64 (d, J = 6,3Hz, 1H), 4,66 (d, J = 5,4Hz, 2H), 3,61 (s, 3H),
3,45 (s, 3H).
MS (ESI) m/z = 533 [M+H]+.
-
Beispiel 35
-
5-({4-[(2-{[(2-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(2-fluor-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin
(60 mg, 0,15 mmol) und 3-Amino-2-methylbenzolsulfonamid (28 mg,
0,15 mmmol) als einen weißen
Feststoff hergestellt (69 mg, 79 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,71 (s,
1H), 8,55 (s, 1H), 7,81 (d, J = 6,0Hz, 1H), 7,68 (dd, J = 8,1 und
1,8Hz, 1H), 7,44-7,54 (m, 2H), 7,16-7,36 (m, 7H), 7,07 (d, J = 8,4Hz,
1H), 5,68 (d, J = 6,3Hz, 1H), 4,73 (d, J = 5,1Hz, 2H), 3,67 (s,
3H), 3,47 (s, 3H), 2,50 (s, 2H).
MS (ESI) m/z = 547 [M+H]+.
-
Beispiel 36
-
1-[4-({4-[(2-{[(2-Fluorphenyl)methyl]amino}-1-methyl-1H-benzimdazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5(2-Chlor-pyrimidin-4-yl)-N2-(2-fluor-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin
(60 mg, 0,15 mmol) und (4-Amino-phenyl)-methansulfonamid (28 mg,
0,15 mmmol) als einen weißen
Feststoff hergestellt (30 mg, 34 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,58 (s,
1H), 7,83 (d, J = 6,3Hz, 1H), 7,68 (d, J = 8,4Hz, 2H), 7,49-7,53
(m, 2H), 7,33-7,40 (m, 1H), 7,17-7,27 (m, 4H), 7,09-7,12 (m, 1H),
6,79 (s, 2H), 5,76 (d, J = 6,0Hz, 1H), 4,72 (d, J = 5,4Hz, 2H),
4,18 (s, 2H), 3,67 (s, 3H), 3,46 (s, 3H).
MS (ESI) m/z = 547
[M+H]+.
-
Beispiel 37
-
2-[4-({4-[{1-Ethyl-2-[(phenylmethyl)amino]-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)phenyl]-N-methylethansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N2-Benzyl-N5-(2-chlor-pyrimidin-4-yl)-1-ethyl-N5-methyl-1H-benzoimidazol-2,5-diamin (98 mg, 0,25
mmol) und 2-(4--Amino-phenyl)-ethansulfonsäuremethylamid (54 mg, 0,25
mmmol) als einen weißen
Feststoff hergestellt (74 mg, 49 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,04 (s,
1H), 7,75 (d, J = 6,0Hz, 1H), 7,69 (d, J = 8,4Hz, 2H), 7,23-7,42
(m, 7H), 7,07-7,12 (m, 3H), 6,94 (q, J = 5,1Hz, 1H), 6,83 (dd, J
= 8,4 und 2,1Hz, 1H), 5,63 (d, J = 5,7Hz, 1H), 4,61 (d, J = 5,7Hz,
2H), 4,H (q, J = 6,9Hz, 2H), 3,41 (s, 3H), 3,32 (s, 3H), 3,20-3,25
(m, 2H), 2,83-2,88 (m, 2H), 2,59 (d, J = 4,8HZ, 3H), 1,26 (t, J
= 6,9Hz, 3H).
MS (ESI) m/z = 571 [M+H]+.
-
Beispiel 38
-
3-{[4-(Methyl{1-methyl-2-[(1-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-(1-phenyl-ethyl)-1H-benzoimidazol-2,5-diamin
(98 mg, 0,25 mmol) und 3-Amino-benzolsulfonamid (43 mg, 0,25 mmmol)
als einen weißen
Feststoff hergestellt (65 mg, 46 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,58 (s,
2H), 8,57 (s, 1H), 7,75-7,81 (m, 2H), 7,48-7,51 (m, 2H), 7,32-7,41
(m, 5H), 7,17-7,26 (m, 4H), 6,98-7,00 (m, 1H), 5,65 (d, J = 6,3Hz,
1H), 5,17 (m, 1H), 3,67 (s, 3H), 3,44 (s, 3H), 1,58 (d, J = 6,9Hz,
3H).
MS (ESI) m/z = 529 [M+H]+.
-
Beispiel 39
-
2-Methyl-5-{[4-(methyl{1-methyl-2-[(1-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-(1-phenyl-ethyl)-1H-benzoimidazol-2,5-diamin
(98 mg, 0,25 mmol) und 5-Amino-2-methylbenzolsulfonamid (46 mg,
0,25 mmmol) als einen weißen
Feststoff hergestellt (90 mg, 63 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,85 (br
s, 2H), 8,52 (s, 1H), 7,83 (d, J = 6,3Hz, 1H), 7,65-7,68 (dd, J
= 8,1 und 1,8Hz, 1H), 7,51-7,57 (m, 3H), 7,34-7,39 (m, 2H), 7,25-7,30
(m, 4H), 7,15-7,22 (m, 2H), 5,70 (d, J = 6,3Hz, 1H), 5,22 (m, 1H),
3,74 (s, 3H), 3,47 (s, 3H), 2,51 (s, 3H), 1,63 (d, J = 6,6Hz, 3H).
MS
(ESI) m/z = 543 [M+H]+.
-
Beispiel 40
-
N
5,1-Dimethyl-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N
2-(1-phenylethyl)-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-(1-phenyl-ethyl)-1H-benzoimidazol-2,5-diamin
(98 mg, 0,25 mmol) und 4-[(Methylsulfonyl)methyl]aminilin (46 mg,
0,25 mmmol) als einen weißen
Feststoff hergestellt (66 mg, 46 %).
1H-NMR
(400 MHz, d6-DMSO) δ: 9,18 (s, 1H), 7,72-7,77 (m,
3H), 7,42 (d, J = 7,6Hz, 2H), 7,16-7,21 (m, 4H), 7,10 (d, J = 8,0Hz,
1H), 7,02 (d, J = 2,0Hz, 1H), 6,79 (dd, J = 8,4 und 2,0Hz, 1H),
5,58 (d, J = 5,6Hz, 1H), 5,12 (m, 1H), 4,31 (s, 2H), 3,58 (s, 3H),
3,38 (s, 3H), 2,82 (s, 3H), 1,50 (d, J = 6,8Hz, 3H).
MS (ESI)
m/z = 542 [M+H]+.
-
Beispiel 41
-
1-(4-{[4-(Methyl[1-methyl-2-[(1-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)methansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-(1-phenyl-ethyl)-1H-benzoimidazol-2,5-diamin
(98 mg, 0,25 mmol) und (4-Amino-phenyl)-methansulfonamid (46 mg,
0,25 mmmol) als einen weißen
Feststoff hergestellt (90 mg, 62 %).
1H-NMR
(400 MHz, d6-DMSO) δ: 9,13 (s, 1H), 7,71-7,75 (m,
3H), 7,42 (d, J = 7,6Hz, 2H), 7,26-7,30 (m, 2H), 7,16-7,19 (m, 4H),
7,11 (d, J = 8,0Hz, 1H), 7,02 (d, J = 2,0Hz, 1H), 6,79 (dd, J =
8,4 und 2,0Hz, 1H), 6,73 (s, 2H), 5,56 (d, J = 6,0Hz, 1H), 5,12
(m, 1H), 4,12 (s, 2H), 3,58 (s, 3H), 1,50 (d, J = 7,2Hz, 3H).
MS
(ESI) m/z = 543 [M+H]+.
-
Beispiel 42
-
3-([4-[(2-{[(3-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimdazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-(3-Chlor-benzyl)-N5-(2-chlor-pyrimidin-4-yl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (50 mg, 0,12
mmol) und 3-Amino-benzolsulfonamid (21 mg, 0,12 mmol) als einen
weißen
Feststoff hergestellt (31 mg, 44 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,51 (s,
1H), 8,60 (s, 1H), 7,76-7,80 (m, 2H), 7,25-7,47 (m, 10H), 7,13 (s,
1H), 6,90 (d, J = 7,8Hz, 1H), 5,64 (d, J = 6,0Hz, 1H), 4,62 (d,
J = 5,4Hz, 2H), 3,61 (s, 3H), 3,45 (s, 3H).
MS (ESI) m/z =
549 [M+H]+.
-
Beispiel 43
-
5-([4-[(2-{[(3-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimdazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-(3-Chlor-benzyl)-N5-(2-chlor-pyrimidin-4-yl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (50 mg, 0,12
mmol) und 5-Amino-2-methylbenzolsulfonamid (22 mg, 0,12 mmmol) als
einen weißen
Feststoff hergestellt (42 mg, 58 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,79 (s,
1H), 8,54 (s, 1H), 7,81-7,84 (m, 1H), 7,66-7,69 (m, 1H), 7,H-7,56
(m, 11H), 5,69 (d, J = 6,0Hz, 1H), 4,72 (d, J = 5,4Hz, 2H), 3,70
(s, 3H), 3,48 (s, 3H), 2,51 (s, 3H).
MS (ESI) m/z = 563 [M+H]+.
-
Beispiel 44
-
1-[4-({4-[(2-{[(4-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-(4-Chlor-benzyl)-N5-(2-chlor-pyrimidin-4-yl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (103 mg, 0,25
mmol) und (4-Amino-phenyl)methansulfonamid (46 mg, 0,25 mmmol) als
einen weißen
Feststoff hergestellt (90 mg, 60 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,31 (s,
1H), 8,05 (br s, 1H), 7,72-7,80 (m, 3H), 7,46 (d, J = 8,4Hz, 2H),
7,38 (d, J = 8,4Hz, 2H), 7,32 (d, J = 8,4Hz, 1H), 7,20 (d, J = 8,4Hz,
2H), 7,14 (s, 1H), 6,93 (d, J = 8,4Hz, 1H), 6,78 (s, 2H), 5,66 (d,
J = 6,0H, 1H), 4,62 (d, J = 5,4Hz, 2H), 4,17 (s, 2H), 3,63 (s, 3H),
3,44 (s, 3H).
MS (ESI) m/z = 563 [M+H]+.
-
Beispiel 45
-
3-({4-[(2-{[(4-Chlorphenyl)methyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)phenylmethansulfonathydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-(4-Chlor-benzyl)-N5-(2-chlor-pyrimidin-4-yl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (103 mg, 0,25
mmol) und Methansulfonsäure-3-aminophenylester
(56 mg, 0,25 mmmol) als einen weißen Feststoff hergestellt (87
mg, 58 %).
1H-NMR (300 MHz, d6-DMSO + NaHCO3) δ: 9,40 (s,
1H), 8,00 (s, 1H), 7,79 (d, J = 6,0Hz, 1H), 7,64 (d, J = 8,1Hz,
1H), 7,50 (t, J = 5,7Hz, 1H), 7,36- 7,44 (m, 4H), 7,23-7,29 (m, 25),
7,08 (s, 15), 6,84 (d, J = 8,1Hz, 2H), 5,65 (d, J = 5,7Hz, 1H),
4,58 (d, J = 5,7Hz, 2H), 3,58 (s, 35), 3,43 (s, 35), 3,34 (s, 3H).
MS
(ESI) m/z = 564 [M+H]+.
-
Beispiel 46
-
N
5,1-Dimethyl-N
2-{[4-(methyloxy)phenyl]methyl}-N
5-[2-([4-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(4-methoxy-benzyl)-1,N5-dimethyl-1Hbenzoimidazol-2,5-diamin (82
mg, 0,20 mmol) und 4-(2-Methansulfonyl-ethyl)phenylamin (40 mg,
0,20 mmol) als einen weißen
Feststoff hergestellt (57 mg, 47 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 9,28 (s, 15), 7,78 (d, J =
6,0Hz, 15), 7,67 (d, J = 8,4Hz, 2H), 7,34-7,38 (m, 35), 7,13-7,18
(m, 3H), 6,94 (d, J = 8,4Hz, 1H), 6,89 (d, J = 8,7Hz, 2H), 5,66
(d, J = 6,0Hz, 1H), 4,57 (d, J = 5,4Hz, 2H), 3,72 (s, 35), 3,62
(s, 35), 3,43 (s, 35), 3,35-3,43 (m, 2H), 2,96 (s, 35), 2,90-2,96
(m, 2H).
MS (ESI) m/z = 572 [M+H]+.
-
Beispiel 47
-
N
5,1-Dimethyl-N
2-{[4-(methyloxy)phenyl]methyl}-N
5-[2-({3-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(4-methoxy-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (82 mg, 0,20
mmol) und 3-(2-Methansulfonyl-ethyl) phenylamin (40 mg, 0,20 mmol)
als einen weißen
Feststoff hergestellt (69 mg, 57 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 9,08 (s, 1H), 7,76 (d, J =
6,0Hz, 2H), 7,59 (d, J = 8,4Hz, 1H), 7,28-7,34 (m, 3H), 7,08-7,23
(m, 3H), 6,79-6,89 (m, 4H), 5,61 (d, J = 5,7Hz, 1H), 4,52 (d, J
= 5,7Hz, 2H), 3,72 (s, 3H), 3,55 (s, 3H), 3,43 (s, 3H), 3,35-3,40
(m, 2H), 2,97 (s, 3H), 2,90-2,94 (m, 2H).
MS (ESI) m/z = 572
[M+H]+.
-
Beispiel 48
-
N
5,1-Dimethyl-N
2-{[4-(methyloxy)phenyl]methyl}-N
5-[2-({4-[1-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)N2-(4-methoxy-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (82 mg, 0,20
mmol) und 4-(1-Methansulfonyl-ethyl)phenylamin (47 mg, 0,20 mmmol)
als einen weißen
Feststoff hergestellt (49 mg, 40 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,24 (s,
1H), 7,75-7,80 (m, 3H), 7,60 (br s, 1H), 7,34 (d, J = 8,7Hz, 2H),
7,26 (d, J = 7,8Hz, 3H), 7,12 (s, 1H), 6,89 (d, J = 8,4Hz, 3H),
5,66 (d, J = 6,0Hz, 1H), 4,53 (d, J = 5,7Hz, 2H), 4,40 (m, 1H),
3,72 (s, 3H), 3,58 (s, 3H), 3,43 (s, 3H), 2,76 (s, 3H), 1,59 (d,
J = 7,2Hz, 3H).
MS (ESI) m/z = 572 [M+H]+.
-
Beispiel 49
-
N
5,1-Dimethyl-N
2-{[4-(methyloxy)phenyl]methyl}-N
5-[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(4-methoxy-benzyl)-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (82 mg, 0,20
mmol) und Methansulfonylmethylphenylamin (37 mg, 0,20 mmmol) als
einen weißen
Feststoff hergestellt (105 mg, 88 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 9,19 (s, 1H), 7,90 (s, 1H),
7,77 (d, J = 6,0Hz, 1H), 7,69 (d, J = 8,4Hz, 1H), 7,28-7,34 (m,
3H), 7,19-7,24 (m, 2H), 7,09 (d, J = 1,8Hz, 1H), 6,81-6,92 (m, 4H),
5,64 (d, J = 6,0Hz, 1H), 4,52 (d, J = 5,7Hz, 2H), 4,32 (s, 2H),
3,72 (s, 3H), 3,55 (s, 3H), 3,43 (s, 3H), 2,88 (s, 3H).
MS
(ESI) m/z = 558 [M+H]+.
-
Beispiel 50
-
N
5,1-Dimethyl-N
5-[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N
2-(phenylmethyl)-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N2-Benzyl-N5-(2-chlorpyrimidin-4-yl)-N5,1-dimethyl-1H-benzoimidazol-2,5-diamin
(95 mg, 0,25 mmol) und Methansulfonylmethylphenylamin (46 mg, 0,25
mmmol) hergestellt, um das gewünschte
Produkt als einen weißen
Feststoff zu ergeben (121 mg, 86 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 9,26 (s, 1H), 7,87 (s, 1H),
7,78 (d, J = 6,0Hz, 1H), 7,67 (d, J = 8,4Hz, 1H), 7,42 (m, 1H),
7,21-7,40 (m, 7H), 7,12 (s, 1H), 6,88-6,93 (m, 2H), 5,66 (d, J =
5,7Hz, 1H), 4,62 (d, J = 5,4Hz, 2H), 4,32 (s, 2H), 3,60 (s, 3H),
3,43 (s, 3H), 2,88 (s, 3H).
MS (ESI) m/z = 528 [M+H]+.
-
Beispiel 51
-
N
5,1-Dimethyl-N
5-[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N
2-(1-phenylethyl)-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-(1-phenyl-ethyl)-1H-benzoimidazol-2,5-diamin
(98 mg, 0,25 mmol) und Methansulfonylmethylphenylamin (46 mg, 0,25
mmmol) als einen weißen
Feststoff hergestellt (90 mg, 62 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 9,19 (s, 1H), 7,88 (s, 1H),
7,75 (d, J = 6,0Hz, 1H), 7,68 (d, J = 8,1Hz, 1H), 7,45 (d, J = 7,5Hz,
2H), 7,29-7,34 (m, 2H), 7,16-7,23 (m, 4H), 7,05 (d, J = 1,8Hz, 1H),
6,90 (d, J = 7,5Hz, 1H), 5,62 (dd, J = 8,1 und 1,8Hz, 1H), 5,62
(d, J = 6,0Hz, 1H), 5,15 (m, 1H), 4,31 (s, 2H), 3,61 (s, 3H), 3,41
(s, 3H), 2,87 (s, 3H), 1,53 (d, J = 6,9Hz, 3H).
MS (ESI) m/z
= 542 [M+H]+.
-
Beispiel 52
-
N
5,1-Dimethyl-N
5-[2-({3-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-N
2-(1-phenylethyl)-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-(1-phenyl-ethyl)-1H-benzoimidazol-2,5-diamin
(98 mg, 0,25 mmol) und 3-(2-Methansulfonylethyl)phenylamin (50 mg,
0,25 mmmol) als einen weißen
Feststoff hergestellt (48 mg, 32 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 9,08 (s, 1H), 7,73-7,77 (m,
2H), 7,58 (d, J = 8,4Hz, 1H), 7,44 (d, J = 7,5Hz, 2H), 7,29-7,34
(m, 2H), 7,12-7,23 (m, 4H), 7,05 (d, J = 1,5Hz, 1H), 6,79-6,84 (m,
2H), 5,59 (d, J = 5,7Hz, 1H), 5,14 (m, 1H), 3,60 (s, 3H), 3,41 (s,
3H), 3,32-3,41 (m, 2H), 2,90-2,96 (m, 5H), 1,53 (d, J = 3,9Hz, 3H).
MS
(ESI) m/z = 556 [M+H]+.
-
Beispiel 53
-
N
5,1-Dimethyl-N
5-[2-({4-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-N
2-(1-phenylethyl)-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 2 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-(1-phenyl-ethyl)-1H-benzoimidazol-2,5-diamin
(98 mg, 0,25 mmol) und 4-(2-Methansulfonylethyl)phenylamin (50 mg,
0,25 mmmol) als einen weißen
Feststoff hergestellt (81 mg, 55 %).
1H-NMR
(300 MHz, d6-DMSO) δ: 10,09 (s, 1H), 8,87 (s, 1H),
7,84 (d, J = 6,9Hz, 1H), 7,48-7,61 (m, 5H), 7,36-7,40 (m, 3H), 7,20-7,31
(m, 4H), 5,82 (d, J = 5,7Hz, 1H), 5,09 (m, 1H), 3,74 (s, 3H), 3,47
(s, 3H), 3,37-3,42 (m, 2H), 2,94-2,99 (m, 5H), 1,63 (d, J = 6,6Hz,
3H).
MS (ESI) m/z = 556 [M+H]+.
-
Beispiel 54
-
2-Methyl-5-({4-[methyl(1-methyl-2-{[(4-methylphenyl)methyl]amino}-1H-benzimidazol-5-yl)amino]-2-pyrimidinyl}amino)benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-(4-methyl-benzyl)-1H-benzoimidazol-2,5-diamin
(98 mg, 0,25 mmol) und 5-Amino-2-methylbenzolsulfonamid (46 mg,
0,25 mmmol) als einen weißen
Feststoff hergestellt (127 mg, 88 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,34 (s,
1H), 8,62 (s, 1H), 7,70-7,76 (m, 2H), 7,50 (br s, 1H), 7,09-7,30
(m, 9H), 6,85 (d, J = 8,1Hz, 1H), 5,60 (d, J = 5,7Hz, 1H), 4,55
(d, J = 5,4Hz, 1H), 3,58 (s, 3H), 3,44 (s, 3H), 2,50 (s, 3H), 2,26
(s, 3H).
MS (ESI) m/z = 543 [M+H]+.
-
Beispiel 55
-
N
5,1-Dimethyl-N
2-[(4-methylphenyl)methyl]-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-(4-methyl-benzyl)-1H-benzoimidazol-2,5-diamin
(98 mg, 0,25 mmol) und 4-[(Methylsulfonyl)methyl]anilin (46 mg,
0,25 mmmol) als einen weißen
Feststoff hergestellt (141 mg, 97 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,21 (s,
1H), 7,76-7,79 (m, 3H), 7,50 (br s, 1H), 7,22-7,30 (m, 5H), 7,09-7,14
(m, 3H), 6,86 (d, J = 8,4Hz, 1H), 5,64 (d, J = 6,0Hz, 1H), 4,55
(d, J = 5,4Hz, 2H), 4,34 (s, 2H), 3,58 (s, 3H), 3,43 (s, 3H), 2,85
(s, 3H), 2,26 (s, 3H).
MS (ESI) m/z = 542 [M+H]+.
-
Beispiel 56
-
N
5,1-Dimethyl-N
2-[(4-methylphenyl)methyl]-N
5-[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-(4-methyl-benzyl)-1H-benzoimidazol-2,5-diamin
(98 mg, 0,25 mmol) und Methansulfonylmethylphenylamin (46 mg, 0,25
mmmol) als einen weißen
Feststoff hergestellt (142 mg, 97 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,18 (s,
1H), 7,89 (s, 1H), 7,77 (d, J = 6,0Hz, 1H), 7,68 (d, J = 8,1Hz,
1H), 7,36 (t, J = 6,0Hz, 1H), 7,19-7,29 (m, 4H), 7,07-7,13 (m, 3H),
6,91 (d, J = 7,5Hz, 1H), 6,83 (dd, J = 8,1 und 1,8Hz, 1H), 5,64
(d, J = 6,0Hz, 1H), 4,54 (d, J = 5,4Hz, 2H), 4,32-4,35 (m, 2H),
3,57 (s, 3H), 3,42 (s, 3H), 2,88 (s, 3H), 2,26 (s, 3H).
MS
(ESI) m/z = 542 [M+H]+.
-
Beispiel 57
-
N
5,1-Dimethyl-N
2-[(4-methylphenyl)methyl]-N
5-[2-({4-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-(4-methyl-benzyl)-1H-benzoimidazol-2,5-diamin
(98 mg, 0,25 mmol) und 4-(2-Methansulfonyl-ethyl)phenylamin (50
mg, 0,25 mmmol) als einen weißen
Feststoff hergestellt (104 mg, 70 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,05 (s,
1H), 7,70-7,75 (m, 3H), 7,36 (t, J = 5,7Hz, 1H), 7,20-7,29 (m, 3H),
7,07-7,14 (m, 5H), 6,82 (dd, J = 8,1 und 1,5H, 1H), 5,60 (d, J =
5,7Hz, 1H), 4,54 (d, J = 5,4Hz, 2H), 3,57 (s, 3H), 3,42 (s, 3H),
3,30-3,37 (m, 2H), 2,90-2,95 (m, 5H), 2,26 (s, 3H).
MS (ESI)
m/z = 556 [M+H]+.
-
Beispiel 58
-
N
5,1-Dimethyl-N
2-[(4-methylphenyl)methyl]-N
5-[2-({3-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-(4-methyl-benzyl)-1H-benzoimidazol-2,5-diamin
(98 mg, 0,25 mmol) und 3-(2-Methansulfonyl-ethyl)phenylamin (50
mg, 0,25 mmmol) als einen weißen
Feststoff hergestellt (126 mg, 85 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,07 (s,
1H), 7,75-7,77 (m, 2H), 7,59 (d, J = 8,1Hz, 1H), 7,36 (t, J = 6,0Hz,
1H), 7,07-7,29 (m, 7H), 6,79-6,85 (m, 2H), 5,61 (d, J = 5,7Hz, 1H),
4,54 (d, J = 5,7Hz, 2H), 3,57 (s, 3H), 3,43 (s, 3H), 3,32-3,40 (m,
2H), 2,97 (s, 3H), 2,90-2,97 (m, 2H), 2,26 (s, 3H).
MS (ESI)
m/z = 556 [M+H]+.
-
Beispiel 59
-
N
5,1-Dimethyl-N
2-[(4-methylphenyl)methyl]-N
5-[2-({4-[1-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-(4-methyl-benzyl)-1H-benzoimidazol-2,5-diamin
(98 mg, 0,25 mmol) und 4-(1-Methansulfonyl-ethyl)phenylamin (50
mg, 0,25 mmmol) als einen weißen
Feststoff hergestellt (151 mg, 97 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,20 (s,
1H), 7,76-7,79 (m, 3H), 7,38 (m, 1H), 7,21-7,29 (m, 5H), 7,08-7,13
(m, 3H), 6,83 (d, J = 8,1Hz, 1H), 5,64 (d, J = 6,0Hz, 1H), 4,54
(d, J = 5,1Hz, 2H), 4,39 (m, 1H), 3,57 (s, 3H), 3,43 (s, 3H), 2,76
(s, 3H), 2,26 (s, 3H), 1,59 (d, J = 7,2Hz, 3H).
-
Beispiel 60
-
1,1-Dimethyl{5-[(2-{[3-(aminosulfonyl)phenyl]amino}-4-pyrimidinyl(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}phenylcarbamathydrochlorid
-
Zu
einer Lösung
von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl]-phenyl-carbaminsäure-tert-butylester
(100 mg, 0,22 mmol) und 3-Amino-benzolsulfonamid (38 mg, 0,22 mmol)
in Ethanol wurde HCl (1 Tropfen, 1M in Diethylether) hinzugegeben
und die Reaktion auf 70°C
erhitzt. Nach 20 h wurde das Reaktionsgemisch abfiltriert, um die
Titelverbindung als einen weißen
Feststoff zu ergeben.
1H-NMR (300 MHz,
d6-DMSO + NaHCO3) δ: 10,15 (s,
1H), 8,44 (s, 1H), 7,84 (d, J = 6,6Hz, 1H), 7,72 (d, J = 8,4Hz,
2H), 7,61 (s, 1H), 7,27-7,39 (m, 10H), 5,79 (d, J = 5,1Hz, 1H),
3,78 (s, 3H), 3,51 (s, 3H), 1,41 (s, 9H).
MS (ESI) m/z = 601
[M+H]+.
-
Beispiel 61
-
3-[(4-{Methyl[1-methyl-2-(phenylamino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]benzolsulfonamidtrifluoracetat
-
(1-Methyl-5-{methyl-[2-(3-sulfamoyl-phenylamino)-pyrimidin-4-yl]amino}-1H-benzoimidazol-2-yl)-phenyl-carbaminsäure-tert-butylesterhydrochlorid
wurde in eine Lösung
aus 50 % Trifluoressigsäure
und Methylenchlorid gerührt
und aufkonzentriert, um die Titelverbindung als einen weißen Feststoff
zu ergeben.
1H-NMR (300 MHz, d6-DMSO + NaHCO3) δ: 10,32 (br
s, 1H), 9,54 (br s, 1H), 8,49 (s, 1H), 7,86 (d, J = 6,9Hz, 1H),
7,73-7,78 (m, 3H), 7,47-7,54 (m, 3H), 7,34-7,41 (m, 4H), 7,06-7,14
(m, m 2H), 5,80 d, J = 6,6Hz, 1H), 3,78 (s, 3H), 3,53 (s, 3H).
MS
(ESI) m/z = 501 [M+H]+.
-
Beispiel 62
-
1,1-Dimethylethyl[5-[(2-{[3-(aminosulfonyl)-4-methylphenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}phenylcarbamathydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 60 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-phenyl-carbaminsäure-tert-butylester
(100 mg, 0,22 mmol) und 5-Amino-2-methyl-benzolsulfonamid (41 mg,
0,22 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben.
1H-NMR (300 MHz, d6-DMSO + NaHCO3) δ: 9,48 (s,
1H), 8,54 (s, 1H), 7,79 (d, J = 6,3Hz, 1H), 7,66-7,71 (m, 2H), 7,56
(d, J = 1,5Hz, 1H), 7,38 (m, 4H), 7,23-7,29 (m, 4H), 7,12 (m, 1H),
5,68 (d, J = 6,0Hz, 1H), 3,78 (s, 3H), 3,48 (s, 3H), 2,49 (s, 3H),
1,42 (s, 9H).
MS (ESI) m/z = 615 [M+H]+.
-
Beispiel 63
-
N
5,1-Dimethyl-N
5-(2-{[4-methyl-3-(methylsulfonyl)phenyl]amino}-4-pyrimidinyl)-N
2-phenyl-1H-benzimidazol-2,5-diamintrifluoracetat
-
(1-Methyl-5-{methyl-[2-(4-methyl-3-sulfamoyl-phenylamino)-pyrimidin-4-yl]-amino}-1H-benzoimidazol-2-yl)-phenyl-carbaminsäure-tert-butylesterhydrochlorid
wurde gemäß dem Verfahren
aus Beispiel 61 entschützt,
um die Titelverbindung als einen weißen Feststoff zu ergeben.
1H-NMR (300 MHz, d6-DMSO
+ NaHCO3) δ: 10,52 (br s, 1H), 9,55 (br
s, 1H), 8,45 (s, 1H), 7,83 (d, J = 6,9Hz, 1H), 7,76 (d, J = 8,1Hz,
2H), 7,64 (dd, J = 8,1 und 1,5Hz, 1H), 7,53 (d, J = 8,7Hz, 1H),
7,29-7,40 (m, 5H), 7,04-7,14 (m, 2H), 5,80 (d, J = 6,3Hz, 1H), 3,77
(s, 3H), 3,54 (s, 3H), 2,54 (s, 3H).
MS (ESI) m/z = 515 [M+H]+.
-
Beispiel 64
-
N
5,1-Dimethyl-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N
2-phenyl-1H-benzimidazol-2,5-diamintrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-phenyl-carbaminsure-tert-butylester
(100 mg, 0,22 mmol) und 4-[(Methylsulfonyl)methyl]anilin (41 mg,
0,22 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben (116 mg, 84 %).
1H-NMR (300
MHz, d6-DMSO + NaHCO3) δ: 10,55 (s,
1H), 9,83 (br s, 1H), 7,87 (d, J = 6,9Hz, 1H), 7,70 (d, J = 8,1Hz,
2H), 7,57-7,60 (m, 3H), 7,32-7,44 (m, 5H), 7,H-7,21 (m, 2H), 5,93
(br s, 1H), 4,43 (s, 2H), 3,79 (s, 3H), 3,53 (s, 3H), 2,87 (s, 3H).
MS
(ESI) m/z = 514 [M+H]+.
-
Beispiel 65
-
1-{4-[(4-[Methyl[1-methyl-2-(phenylamino)-1H-benzimdazol-5-yl]amino}-2-pyrimidinyl)amino]phenyl}methansulfonamidtrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-phenyl-carbaminsäure-tert-butylester
(100 mg, 0,22 mmol) und (4-Amino-phenyl)-methansulfonamid (39 mg,
0,22 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben (53 mg, 40 %).
1H-NMR (300
MHz, d6-DMSO + NaHCO3) δ: 9,47 (s,
1H), 9,10 (s, 1H), 7,73-7,87 (m, 5H), 7,41 (d, J = 8,4Hz, 1H), 7,30-7,36
(m, 3H), 7,23 (d, J = 8,4Hz, 1H), 6,95-7,03 (m, 2H), 6,78 (s, 2H),
5,71 (d, J = 6,0Hz, 1H), 4,18 (s, 2H), 3,76 (s, 3H), 3,49 (s, 3H).
MS
(ESI) m/z = 515 [M+H]+.
-
Beispiel 66
-
4-[(4-(Methyl[1-methyl-2-(phenylamino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]
phenylmethansulfonattrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-phenyl-carbaminsäure-tert-butylester
(100 mg, 0,22 mmol) und Sulfaminsäure-4-aminophenylester (39
mg, 0,22 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben (86 mg, 65 %).
1H-NMR (300
MHz, d6-DMSO + NaHCO3) δ: 9,32 (s,
1H), 9,02 (s, 1H), 7,80-7,88 (m, 5H), 7,30-7,41 (m, 4H), 7,18 (d,
J = 8,7Hz, 2H), 6,93-7,01 (m, 2H), 5,71 (d, J = 6,0Hz, 1H), 3,76
(s, 3H), 3,47 (s, 3H), 3,30 (s, 3H).
MS (ESI) m/z = 516 [M+H]+.
-
Beispiel 67
-
3-({4-[{2-[(4-Fluorphenyl)amino]-1-methyl-1H-benzimdazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidtrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-(4-fluor-phenyl)-carbaminsäure-tert-butylester
(120 mg, 0,25 mmol) und 3-Amino-benzolsulfonamid (43 mg, 0,25 mmol)
hergestellt, um das gewünschte
Produkt als einen weißen
Feststoff zu ergeben (76 mg, 48 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,80 (br
s, 1H), 9,21 (br s, 1H), 8,57 (s, 1H), 7,76-7,89 (m, 4H), 7,38-7,45
(m, 3H), 7,29-7,33 (m, 3H), 7,13-7,22 (m, 2H), 7,01-7,05 (m, 1H),
5,71 (d, J = 6,0Hz, 1H), 3,75 (s, 3H), 3,50 (s, 3H).
MS (ESI)
m/z = 519 [M+H]+.
-
Beispiel 68
-
5-({4-[{2-[(4-Fluorphenyl)amino]-1-methyl-1H-benzimdazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidtrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-(4-fluor-phenyl)-carbaminsäure-tert-butylester
(120 mg, 0,25 mmol) und 5-Amino-2-methyl-benzolsulfonamid (46 mg,
0,25 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben (150 mg, 93 %).
1H-NMR (300
MHz, d6-DMSO + NaHCO3) δ: 10,28 (br
s, 1H), 9,36 (br s, 1H), 8,51 (s, 1H), 7,80-7,87 (m, 3H), 7,66 (dd,
J = 8,4 und 2,1Hz, 1H), 7,48 (d, J = 8,4Hz, 1H), 7,27-7,37 (m, 4H),
7,17-7,23 (m, 2H), 7,08 (dd, J = 8,2 und 1,8Hz, 1H), 5,76 (d, J
= 6,3Hz, 1H), 3,76 (s, 3H), 2,54 (s, 3H).
MS (ESI) m/z = 533
[M+H]+.
-
Beispiel 69
-
N
2-(4-Fluorphenyl)-N
5,1-dimethyl-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamintrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-(4-fluor-phenyl)-carbaminsäure-tert-butylester
(100 mg, 0,21 mmol) und 4-[(Methylsulfonyl)methyl]anilin (39 mg,
0,21 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben (109 mg, 81 %).
1H-NMR (300
MHz, d6-DMSO + NaHCO3) δ: 9,81 (br
s, 1H), 9,23 (br s, 1H), 7,81-7,88 (m, 3H), 7,72 (d, J = 8,1Hz,
2H), 7,44 (d, J = 8,4Hz, 1H), 7,28-7,34 (m, 3H), 7,16-7,22 (m, 2H),
7,05 (dd, J = 8,5 und 1,6Hz, 1H), 5,78 (d, J = 6,0Hz, 1H), 4,39
(s, 2H), 3,75 (s, 3H), 3,50 (s, 3H), 2,86 (s, 3H).
MS (ESI)
m/z = 532 [M+H]+.
-
Beispiel 70
-
1-[4-({4-[{2-[(4-Fluorphenyl)amino]-1-methyl-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidnyl}amino)phenyl]methansulfonamidtrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-(4-fluor-phenyl)-carbaminsure-tert-butylester
(100 mg, 0,21 mmol) und (4-Amino-phenyl)-methansulfonamid (39 mg,
0,21 mmol) hergestellt, um das gewünschte Produkt als einen gelben
Feststoff zu ergeben (89 mg, 65 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,54 (br
s, 1H), 9,16 (br s, 1H), 7,72-7,90 (m, 5H), 7,41 (d, J = 8,4Hz,
1H), 7,32 (s, 2H), 7,14-7,25 (m, 4H), 7,01 (d, J = 8,1Hz, 1H), 6,78
(s, 2H), 5,71 (d, J = 6,0Hz, 1H), 4,18 (s, 2H), 3,75 (s, 3H), 3,49
(s, 3H).
MS (ESI) m/z = 533 [M+H]+.
-
Beispiel 71
-
4-({4-[{2-[(4-Fluorphenyl)amino]-1-methyl-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)phenylmethansulfonattrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-(4-fluor-phenyl)-carbaminsure-tert-butylester
(96 mg, 0,20 mmol) und Sulfaminsäure-4-amino-phenylester
(37 mg, 0,19 mmol) hergestellt, um das gewünschte Produkt als einen gelben
Feststoff zu ergeben (66 mg, 51 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,33 (s,
1H), 9,10 (s, 1H), 7,80-7,92 (m, 5H), 7,39 (d, J = 8,4Hz, 1H), 7,30
(s, 1H), 7,14-7,20 (m, 4H), 6,99 (dd, J = 8,4 und 1,6Hz, 1H), 5,71
(d, J = 6,0Hz, 2H), 3,74 (s, 3H), 3,47 (s, 3H), 2,50 (s, 3H).
MS
(ESI) m/z = 534 [M+H]+.
-
Beispiel 72
-
3-({4-[{2-[(4-Fluorphenyl)amino]-1-methyl-1H-benzimidazol-5-yl}(methyl)amino]-2-pyrimidinyl}amino)phenylmethansulfonattrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-(4-fluor-phenyl)-carbaminsäure-tert-butylester
(92 mg, 0,19 mmol) und Methansulfonsäure-3-amino-phenylesterhydrochlorid
(42 mg, 0,19 mmol) hergestellt, um das gewünschte Produkt als einen gelben
Feststoff zu ergeben (73 mg, 59 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,46 (s,
1H), 9,10 (s, 1H), 8,00 (m, 1H), 7,87-7,91 (m, 2H), 7,82 (d, J =
6,0Hz, 1H), 7,64 (d, J = 8,4Hz, 1H), 7,40 (d, J = 8,1Hz, 1H), 7,27-7,23
(m, 2H), 7,14-7,20 (m, 2H), 7,00 (dd, J = 8,2 und 1,6Hz, 1H), 6,85
(dd, J = 8,1 und 2,1Hz, 1H), 5,71 (d, J = 6,0Hz, 1H), 3,74 (s, 3H),
3,47 (s, 3H), 3,34 (s, 3H).
MS (ESI) m/z = 534 [M+H]+.
-
Beispiel 73
-
N
5,1-Dimethyl-N
2-(4-methylphenyl)-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamintrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-p-tolyl-carbaminsäure-tert-butylester
(66 mg, 0,14 mmol) und 4-[(Methylsulfonyl)methyl]anilin (26 mg,
0,14 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben (32 mg, 36 %).
1H-NMR (300
MHz, d6-DMSO + NaHCO3) δ: 9,26 (s,
1H), 8,92 (s, 1H), 7,73-7,81 (m, 5H), 7,37 (d, J = 8,4Hz, 1H), 7,29
(d, J = 1,5Hz, 1H), 7,24 (d, J = 8,4Hz, 2H), 7,13 (d, J = 8,4Hz,
2H), 6,98 (dd, J = 8,4 und 1,5Hz, 1H), 5,69 (d, J = 6,0Hz, 1H),
4,35 (s, 2H), 3,74 (s, 3H), 3,47 (s, 3H), 2,85 (s, 3H), 2,26 (s,
3H).
MS (ESI) m/z = 534 [M+H]+.
-
Beispiel 74
-
1-[4-({4-[(2-{[4-(1,1-Dimethylethyl)phenyl]amino}-1-methyl-1H-benzimidazol-5-yl)methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidtrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von (4-tert-Butyl-phenyl){5-[(2-chlor-pyrimidin-4-yl)-methylamino]-1-methyl-1H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
(104 mg, 0,2 mmol) und (4-Amino-phenyl)-ethansulfonamid (37 mg,
0,2 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben 116 mg, 84 %).
1H-NMR (300
MHz, d6-DMSO + NaHCO3) δ: 9,42 (s,
1H), 9,04 (s, 1H), 7,80 (d, J = 6,0Hz, 1H), 7,71-7,75 (m, 4H), 7,33-7,41
(m, 3H), 7,29 (s, 1H), 7,22 (d, J = 8,4Hz, 2H), 7,00 (d, J = 7,8Hz,
2H), 6,77 (s, 2H), 5,70 (d, J = 6,0Hz, 1H), 4,17 (s, 2H), 3,74 (s,
3H), 3,48 (s, 3H), 1,28 (m, 9H).
MS (ESI) m/z = 571 [M+H]+.
-
Beispiel 75
-
3-({4-[(2-{[4-(1,1-Dimethylethyl)phenyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)benzolsulfonamidtrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von (4-tert-Butyl-phenyl)-{5-[(2-chlor-pyrimidin-4-yl)-methylamino]-1-methyl-1H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
(104 mg, 0,20 mmol) und 3-Amino-benzolsulfonamid (34 mg, 0,20 mmol)
hergestellt, um das gewünschte
Produkt als einen weißen
Feststoff zu ergeben (85 mg, 63 %).
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,57 (s,
1H), 9,01 (s, 1H), 8,60 (s, 1H), 7,72-7,82 (m, 4H), 7,33-7,42 (m,
5H), 7,26-7,29 (m, 3H), 6,98 (dd, J = 8,4 und 1,5Hz, 1H), 5,68 (d,
J = 6,0Hz, 1H), 3,73 (s, 3H), 3,49 (s, 3H), 1,28 (s, 9H).
MS
(ESI) m/z = 557 [M+H]+.
-
Beispiel 76
-
5-({4-[(2-{[4-(1,1-Dimethylethyl)phenyl]amino}-1-methyl-1H-benzimidazol-5-yl)(methyl)amino]-2-pyrimidinyl}amino)-2-methylbenzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von (4-tert-Butyl-phenyl)-{5-[(2-chlor-pyrimidin-4-yl)-methylamino]-1-methyl-1H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
(104 mg, 0,20 mmol) und 5-Amino-2-methyl-benzolsulfonamid (37 mg,
0,20 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben (66 mg, 48 %).
1H-NMR (300
MHz, d6-DMSO + NaHCO3) δ: 9,35 (s,
1H), 8,96 (s, 1H), 8,62 (s, 1H), 7,71-7,78 (m, 4H), 7,32-7,38 (m,
3H), 7,27 (s, 1H), 7,17-7,23 (m, 3H), 6,96 (d, J = 8,4Hz, 1H), 5,63
(d, J = 6,0Hz, 1H), 3,74 (s, 3H), 3,48 (s, 3H), 2,50 (s, 3H), 1,28
(s, 9H).
MS (ESI) m/z = 571 [M+H]+.
-
Beispiel 77
-
N
2-[4-(1,1-Dimethylethyl)phenyl]-N
5,1-dimethyl-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamintrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von (4-tert-Butyl-phenyl)-{5-[(2-chlor-pyrimidin-4-yl)-methylamino]-1-methyl-1H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
(104 mg, 0,20 mmol) und 4-[(Methylsulfonyl)methyl]anilin (37 mg,
0,20 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben.
1H-NMR (300 MHz, d6-DMSO + NaHCO3) δ: 9,51 (s,
1H), 9,07 (s, 1H), 7,81 (d, J = 6,3Hz, 1H), 7,71-7,77 (m, 4H), 7,24-7,41
(m, 6H), 7,00 (dd, J = 8,4 und 1,5Hz, 1H), 5,72 (d, J = 6,0Hz, 1H),
4,36 (s, 2H), 3,74 (s, 3H), 3,48 (s, 3H), 2,85 (s, 3H), 1,28 (s,
9H).
MS (ESI) m/z = 570 [M+H]+.
-
Beispiel 78
-
1,1-Dimethylethyl(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)[4-(methyloxy)phenyl]carbamat
-
Zu
einer Lösung
aus {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-(4-methoxy-phenyl)carbaminsure-tert-butylester (100 mg,
0,20 mmol) und 4-[(Methylsulfonyl)methyl]anilin (37 mg, 0,20 mmol)
wurde kat. HCl hinzugegeben, und die Reaktion wurde auf 70°C über Nacht
erhitzt. Die Reaktion wurde mit festem NaHCO3 neutralisiert,
filtriert und aufkonzentriert. Das Rohmaterial wurde durch Kieselgel
aufgereinigt, um die Titelverbindung als einen weißen Feststoff
zu ergeben.
1H-NMR (300 MHz, d6-DMSO) δ:
9,24 (s, 1H), 7,82 (d, J = 6,0Hz, 1H), 7,65-7,74 (m, 3H), 7,54 (d,
J = 1,5Hz, 1H), 7,35 (d, J = 8,7Hz, 2H), 7,24 (dd, J = 8,7 und 1,5Hz,
1H), 7,18 (d, J = 8,4Hz, 2H), 6,94 (d, J = 9,0Hz, 2H), 5,72 (d,
J = 5,7Hz, 1H), 4,32 (s, 2H), 3,78 (s, 3H), 3,74 (s, 3H), 3,46 (s,
3H), 2,84 (s, 3H), 1,41 (s, 9H).
MS (ESI) m/z = 644 [M+H]+.
-
Beispiel 79
-
N
5,1-Dimethyl-N
2-[4-(methyloxy)phenyl]-N
5-[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamintrifluoracetat
-
(5-{[2-(4-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methylamino]-1-methyl-1H-benzoimidazol-2-yl)-(4-methoxy-phenyl)-carbaminsäuretert-butylester
wurde gemäß dem Verfahren
aus Beispiel 61 entschützt,
um die Titelverbindung als einen weißen Feststoff zu ergeben.
1H-NMR (300 MHz, d6-DMSO
+ NaHCO3) δ: 9,48 (s, 1H), 9,12 (s, 1H),
7,81 (d, J = 6,0Hz, 1H), 7,69-7,76 (m, 4H), 7,41 (d, J = 8,1Hz,
1H), 7,24-7,27 (m, 3H), 7,02 (d, J = 8,1Hz, 1H), 6,95 (d, J = 9,0Hz,
2H), 5,73 (d, J = 6,0Hz, 1H), 4,36 (d, 2H), 3,74 (s, 3H), 3,73 (s,
3H), 3,47 (s, 3H), 2,86 (s, 3H).
MS (ESI) m/z = 544 [M+H]+.
-
Beispiel 80
-
1,1-Dimethylethyl{5-[[2-({4-[(aminosulfonyl)methyl]phenyl}amino)-4-pyrimidinyl](methyl)amino]-1-methyl-1H-benzimdazol-2-yl}[4-(methyloxy)phenyl]carbamat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 78 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-(4-methoxy-phenyl)-carbaminsure-tert-butylester
(100 mg, 0,20 mmol) und (4-Amino-phenyl)-methansulfonamid (37 mg, 0,20
mmol) hergestellt, um das gewünschte
Produkt als einen weißen
Feststoff zu ergeben.
1H-NMR (300 MHz,
d6-DMSO + NaHCO3) δ: 9,20 (s,
1H), 7,81 (d, J = 6,0Hz, 1H), 7,65-7,73 (m, 3H), 7,54 (d, J = 1,8Hz,
1H), 7,34 (d, J = 8,7Hz, 2H), 7,24 (dd, J = 8,4 und 1,8Hz, 1H),
7,16 (d, J = 8,4Hz, 2H), 6,97 (d, J = 9,0Hz, 2H), 6,75 (s, 2H),
5,69 (d, J = 6,0Hz, 1H), 4,14 (s, 2H), 3,78 (s, 3H), 3,74 (s, 3H),
3,46 (s, 3H), 1,41 (s, 9H).
MS (ESI) m/z = 645 [M+H]+.
-
Beispiel 81
-
1-[4-({4-[Methyl(1-methyl-2-{[4-(methyloxy)phenyl]amino}-1-1H-benzimdazol-5-yl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidtrifluoracetat
-
(4-Methoxy-phenyl)-(1-methyl-5-{methyl-[2-(4-sulfamoylmethylphenylamino)-pyrimidin-4-yl]-amino}-1H-benzoimidazol-2-yl)carbaminsäuretert-butylester
wurde gemäß dem Verfahren
aus Beispiel 78 entschützt,
um die Titelverbindung als einen weißen Feststoff zu ergeben.
1H-NMR (300 MHz, d6-DMSO
+ NaHCO3) δ: 9,70 (s, 1H), 9,22 (s, 1H),
7,82 (d, J = 6,3Hz, 1H), 7,68-7,71 (m, 4H), 7,43 (d, J = 8,1Hz,
1H), 7,22-7,33 (m, 3H), 7,04 (d, J = 8,1Hz, 1H), 6,95 (d, J = 8,7Hz,
2H), 6,79 (s, 2H), 5,74 (d, J = 5,4Hz, 1H), 4,18 (s, 2H), 3,74 (s,
6H), 3,48 (s, 3H).
MS (ESI) m/z = 545 [M+H]+.
-
Beispiel 82
-
1,1-Dimethylethyl(1-methyl-5-{methyl[2-({3-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimdazol-2-yl)[4-(methyloxy)phenyl]carbamat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 78 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-(4-methoxy-phenyl)-carbaminsure-tert-butylester
(100 mg, 0,20 mmol) und 3-Methansulfonylmethyl-phenylamin (37 mg,
0,20 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben.
1H-NMR (300 MHz, d6-DMSO) δ:
9,44 (s, 1H), 7,80-7,82 (m, 2H), 7,63-7,70 (m, 2H), 7,56 (d, J =
1,5Hz, 1H), 7,34 (d, J = 8,7Hz, 2H), 7,25 (dd, J = 8,6 und 1,2Hz,
1H), 7,18 (t, J = 7,5Hz, 1H), 6,94 (d, J = 9,0Hz, 2H), 5,75 (d,
J = 6,0Hz, 1H), 4,34 (s, 2H), 3,79 (s, 3H), 3,74 (s, 3H), 3,47 (s,
3H), 2,87 (s, 3H), 1,41 (s, 9H).
MS (ESI) m/z = 644 [M+H]+.
-
Beispiel 83
-
N
5,1-Dimethyl-N
2-[4-(methyloxy)phenyl]-N
5-[2-({3-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diamintrifluoracetat,
-
(5-{[2-(3-Methansulfonylmethyl-phenylamino)-pyrimidin-4-yl]-methylamino}-1-methyl-1H-benzoimidazol-2-yl)-(4-methoxy-phenyl)-carbaminsäuretert-butylester
wurde gemäß dem Verfahren
aus Beispiel 61 entschützt,
um die Titelverbindung als einen weißen Feststoff zu ergeben.
1H-NMR (300 MHz, d6-DMSO
+ NaHCO3) δ: 9,36 (s, 1H), 8,94 (s, 1H),
7,87 (s, 1H), 7,80 (d, J = 6,0Hz, 1H), 7,67-7,75 (m, 3H), 7,21-7,26
(m, 2H), 7,37 (d, J = 8,4Hz, 1H), 6,91-6,99 (m, 4H), 5,70 (d, J
= 6,0Hz, 1H), 4,34 (s, 2H), 3,73 (s, 3H), 3,72 (s, 3H), 3,46 (s,
3H), 2,89 (s, 3H).
MS (ESI) m/z = 544 [M+H]+.
-
Beispiel 84
-
1,1-Dimethylethyl(1-methyl-5-{methyl[2-({4-[1-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimdazol-2-yl)[4-(methyloxy)phenyl]carbamat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 78 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-(4-methoxy-phenyl)-carbaminsure-tert-butylester
(100 mg, 0,20 mmol) und 4-(1-Methylsulfony-ethyl)-phenylamin (40
mg, 0,20 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben.
1H-NMR (300 MHz, d6-DMSO) δ:
9,25 (s, 1H), 7,82 (d, J = 6,0Hz, 1H), 7,65-7,74 (m, 3H), 7,54 (s,
1H), 7,35 (d, J = 8,7Hz, 2H), 7,21-7,25 (m, 3H), 6,94 (d, J = 9,0Hz,
2H), 5,72 (d, J = 6,0Hz, 1H), 4,37 (m, 1H), 3,78 (s, 3H), 3,74 (s,
3H), 3,46 (s, 3H), 2,75 (s, 3H), 1,58 (d, J = 7,2Hz, 3H), 1,41 (s,
9H).
MS (ESI) m/z = 658 [M+H]+.
-
Beispiel 85
-
N
5,1-Dimethyl-N
2-[4-(methyloxy)phenyl]-N
5-[2-({4-[1-(methylsulfonyl)ethyl]phenl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diamintrifluoracetat
-
[5-({2-[4-(1-Methansulfonyl-ethyl)-phenylamino]-pyrimidin-4-yl}-methyl-amino)-1-methyl-1H-benzoimidazol-2-yl]-(4-methoxy-phenyl)-carbaminsäure-tert-butylester
wurde gemäß dem Verfahren
aus Beispiel 61 entschützt, um
die Titelverbindung als einen weißen Feststoff zu ergeben.
1H-NMR (300 MHz, d6-DMSO
+ NaHCO3) δ: 9,38 (s, 1H), 9,00 (s, 1H),
7,81 (d, J = 6,0Hz, 1H), 7,72-7,74 (m, 4H), 7,38 (d, J = 8,4Hz,
1H), 7,26-7,28 (m, 3H), 6,92-7,00 (m, 3H), 5,72 (d, J = 5,7Hz, 1H),
4,40 (m, 1H), 3,73 (s, 6H), 3,47 (s, 3H), 2,76 (s, 3H), 1,59 (d,
J = 7,2Hz, 3H).
MS (ESI) m/z = 558 [M+H]+.
-
Beispiel 86
-
N
5,1-Dimethyl-N
2-[4-(methyloxy)phenyl]-N
5-[2-({3-[1-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimdazol-2,5-diamintrifluoracetat
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 5 unter Verwendung von {5-[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-(4-methoxy-phenyl)-carbaminsure-tert-butylester
(100 mg, 0,20 mmol) und 3-(1-Methansulfonyl-ethyl)-phenylaminhydrochlorid
(47 mg, 0,20 mmol) hergestellt, um das gewünschte Produkt als einen weißen Feststoff
zu ergeben.
1H-NMR (300 MHz, d6-DMSO + NaHCO3) δ: 9,23 (s,
1H), 8,86 (s, 1H), 7,96 (s, 1H), 7,80 (d, J = 6,0Hz, 1H), 7,75 (d,
J = 8,7Hz, 2H), 7,64 (d, J = 8,1Hz, 1H), 7,36 (d, J = 8,4Hz, 1H),
7,19-7,26 (m, 2H), 6,90-6,98 (m, 4H), 5,69 (d, J = 5,7Hz, 1H), 4,28
(m, 1H), 3,73 (d, 3H), 3,72 (s, 3H), 3,47 (s, 3H), 2,77 (s, 3H),
1,59 (d, J = 7,2Hz, 3H).
MS (ESI) m/z = 558 [M+H]+.
-
Beispiel 87
-
3-{[4-(Methyl{1-methyl-2-[(1-methylethyl)amino]-1H-benzimdazol-5-yl}amino)-2-pyrimidinyl]amino)benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-4-pyrimidinyl)-N5,1-dimethyl-N2-(1-methylethyl)-1H-benzimidazol-2,5-diamin (83 mg,
0,25 mmol) und 3-Amino-benzolsulfonamid (43 mg, 0,25 mmol) als einen
weißen
Feststoff (59 mg, 47 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 11,03 (s, 1H), 8,94 (d, J
= 8,1Hz, 1H), 8,35 (s, 1H), 7,97 (d, J = 7,2Hz, 1H), 7,71 (d, J
= 7,2Hz, 1H), 7,66 (d, J = 8,4Hz, 1H), 7,48-7,57 (m, 3H), 7,40 (s,
1H), 7,33 (dd, J = 8,4 und 1,5Hz, 1H), 5,90 (s, 1H), 4,12 (m, 1H),
3,70 (s, 3H), 3,54 (s, 3H), 1,33 (d, J = 6,3Hz, 6H) ppm.
MS
(ESI) m/z = 467 [M+H]+.
-
Beispiel 88
-
2-Chlor-5-{[4-(methyl{1-methyl-2-[(1-methylethyl)amino]-1Hbenzimdazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-4-pyrimidinyl)-N5,1-dimethyl-N2-(1-methylethyl)-1H-benzimidazol-2,5-diamin (83 mg,
0,25 mmol) und 5-Amino-2-chlor-benzolsulfonamid (52 mg, 0,25 mmol)
als einen weißen
Feststoff (74 mg, 59 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,58 (s, 1H), 8,78 (s, 1H),
7,83 (dd, J = 8,7 und 2,1Hz, 1H), 7,78 (d, J = 5,7Hz, 1H), 7,55
(br s, 1H), 7,40 (d, J = 8,7Hz, 1H), 7,19 (d, J = 8,4Hz, 1H), 7,08
(s, 12H), 6,80 (d, J = 8,1Hz, 1H), 6,61 (d, J = 7,5Hz, 1H), 5,64
(d, J = 6,0Hz, 1H), 4,04 (m, 1H), 3,52 (s, 3H), 3,45 (s, 3H), 1,23
(d, J = 6,3Hz, 6H) ppm.
MS (ESI) m/z = 501 [M+H]+.
-
Beispiel 89
-
2-Methyl-5-{[4-(methyl{1-methyl-2-[(1-methylethyl)amino]-1H-benzimdazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-4-pyrimidinyl)-N5,1-dimethyl-N2-(1-methylethyl)-1H-benzimidazol-2,5-diamin (60 mg,
0,18 mmol) und 5-Amino-2-methyl-benzolsulfonamid (34 mg, 0,18 mmol)
als einen weißen
Feststoff (42 mg, 45 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,85 (s, 1H), 8,67 (s, 1H),
8,51 (s, 1H), 7,87 (d, J = 6,3Hz, 1H), 7,67 (d, J = 8,1Hz, 1H),
7,57 (d, J = 8,4Hz, 1H), 7,37 (s, 1H), 7,18-7,27 (m, 3H), 5,73 (d,
J = 6,0Hz, 1H), 4,11 (m, 1H), 3,68 (s, 3H), 3,48 (s, 3H), 1,32 (d,
J = 6,3Hz, 6H) ppm.
MS (ESI) m/z = 481 [M+H]+.
-
Beispiel 90
-
N-Methyl-2-(4-{[4-(methyl{1-methyl-2-[(1-methylethyl)amino]-1H-benzimdazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)ethansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-4-pyrimidinyl)-N5,1-dimethyl-N2-(1-methylethyl)-1H-benzimidazol-2,5-diamin (83 mg,
0,25 mmol) und 2-(4-Amino-phenyl)-ethansulfonsäuremethylamid (54 mg, 0,25
mmol) als einen weißen
Feststoff (71 mg, 52 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,05 (s, 1H), 7,68-7,76 (m,
3H), 7,19 (d, J = 8,4Hz, 1H), 7,08-7,13 (m, 3H), 6,96 (q, M = 5,1Hz,
1H), 6,81 (dd, J = 8,1 und 1,8Hz, 1H), 6,53 (d, J = 6,9Hz, 1H),
5,60 (d, J = 5,7Hz, 1H), 4,04 (m, 1H), 3,51 (s, 3H), 3,42 (s, 3H),
3,21-3,30 (m, 2H), 2,83-2,88 (m, 2H), 2,59 (d, J = 5,1Hz, 3H), 1,23
(d, J = 6,6Hz, 6H) ppm.
MS (ESI) m/z = 509 [M+H]+.
-
Beispiel 91
-
4-{[4-(Methyl{1-methyl-2-[(1-methylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenylmethansulfonathydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-4-pyrimidinyl)-N5,1-dimethyl-N2-(1-methylethyl)-1H-benzimidazol-2,5-diamin (83 mg,
0,25 mmol) und Methansulfonsäure-4-amino-phenylester
(47 mg, 0,25 mmol) als einen weißen Feststoff (45 mg, 35 %)
hergestellt.
1H-NMR (300 MHz, d6-DMSO) δ:
9,30 (s, 1H), 7,78-7,86 (m, 3H), 7,17-7,21 (m, 3H), 7,09 (d, J =
1,5Hz, 1H), 6,82 (dd, J = 8,1 und 1,8Hz, 1H), 6,51 (d, J = 7,5Hz,
1H), 5,67 (d, J = 6,0Hz, 1H), 4,05 (m, 1H), 3,52 (s, 3H), 3,43 (s,
3H), 3,31 (s, 3H), 1,24 (d, J = 6,6Hz, 6H) ppm.
MS (ESI) m/z
= 482 [M+H]+.
-
Beispiel 92
-
3-{[4-(Methyl{1-methyl-2-[(1-methylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenylmethansulfonathydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-4-pyrimidinyl)-N5,1-dimethyl-N2-(1-methylethyl)-1H-benzimidazol-2,5-diamin (83 mg,
0,25 mmol) und Methansulfonsäure-3-amino-phenylesterhydrochlorid
(56 mg, 0,25 mmol) als einen weißen Feststoff (55 mg, 43 %)
hergestellt.
1H-NMR (300 MHz, d6-DMSO) δ:
9,41 (s, 1H), 8,02 (s, 1H), 7,79 (d, J = 6,0Hz, 1H), 7,65 (d, J
= 8,4Hz, 1H), 7,30 (t, J = 8,2Hz, 1H), 7,20 (d, J = 8,1Hz, 1H),
7,10 (s, 1H), 6,81-6,86 (m, 2H), 6,55 (d, J = 7,8Hz, 1H), 5,46 (d,
J = 5,7Hz, 1H), 4,05 (m, 1H), 3,52 (s, 3H), 3,44 (s, 3H), 3,34 (s
unter H20, 3H) ppm.
MS (ESI) m/z =
482 [M+H]+.
-
Beispiel 93
-
N
5,1-Dimethyl-N
2-(1-methylethyl)-N
5-[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-4-pyrimidinyl)-N5,1-dimethyl-N2-(1-methylethyl)-1H-benzimidazol-2,5-diamin (83 mg,
0,25 mmol) und 3-Methansulfonylmethyl-phenylamin (46 mg, 0,25 mmol)
als einen weißen
Feststoff (69 mg, 53 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,20 (s, 1H), 7,90 (s, 1H),
7,77 (d, J = 6,0Hz, 1H), 7,69 (d, J = 8,1Hz, 1H), 7,18-7,25 (m,
2H), 7,09 (d, J = 1,8Hz, 1H), 6,91 (d, J = 7,5Hz, 1H), 6,82 (dd,
J = 8,1 und 1,8Hz, 1H), 6,49 (d, J = 7,5Hz, 1H), 5,64 (d, J = 6,0Hz,
1H), 4,34 (s, 2H), 4,03 (m, 1H), 3,51 (s, 3H), 3,43 (s, 3H), 2,89
(s, 3H), 1,24 (d, J = 6,6Hz, 6H) ppm.
MS (ESI) m/z = 480 [M+H]+.
-
Beispiel 94
-
3-{[4-(Methyl{1-methyl-2-[(2-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-phenethyl-1H-benzimidazol-2,5-diamin (98 mg, 0,25
mmol) und 3-Amino-benzolsulfonamid (43 mg, 0,25 mmol) als einen
weißen
Feststoff (95 mg, 67 %) hergestellt.
1H-NMR
(400 MHz, d6-DMSO) δ: 9,83 (br s, 1H), 9,04 (br
s, 1H), 8,49 (d, 1H), 7,87 (d, J = 6,0Hz, 1H), 7,72-7,74 (m, 1H),
7,56 (d, J = 8,4Hz, 1H), 7,18-7,40 (m, 11H), 5,72 (d, J = 5,6Hz,
1H), 3,65-3,71 (m, 2H), 3,64 (s, 3H), 3,46 (s, 3H), 2,96 (m, 2H)
ppm.
MS (ESI) m/z = 529 [M+H]+.
-
Beispiel 95
-
2-Methyl-5-{[4-(methyl{1-methyl-2-[(2-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-phenethyl-1H-benzoimidazol-2,5-diamin (98 mg, 0,25
mmol) und 5-Amino-2-methylbenzolsulfonamid (46 mg, 0,25 mmol) als
einen weißen
Feststoff (88 mg, 61 %) hergestellt.
1H-NMR
(400 MHz, d6-DMSO) δ: 10,25 (br s, 1H), 9,22 (br
s, 1H), 8,44 (s, 1H), 7,87 (d, J = 6,8Hz, 1H), 7,58-7,64 (m, 2H),
7,18-7,41 (m, 10H), 5,75 (d, J = 5,6Hz, 1H), 3,68-3,73 (m, 2H),
3,66 (s, 3H), 3,48 (s, 3H), 2,97 (m, 2H), 2,50 (s, 3H) ppm.
MS
(ESI) m/z = 543 [M+H]+.
-
Beispiel 96
-
1-(4-{[4-(Methyl{1-methyl-2-[{2-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)methansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-phenethyl-1H-benzimidazol-2,5-diamin (98 mg, 0,25
mmol) und (4-Amino-phenyl)-methansulfonamid (46 mg, 0,25 mmol) als
einen weißen
Feststoff (37 mg, 26 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,17 (s, 1H), 7,76-7,78 (m,
3H), 7,21-7,34 (m, 8H), 7,19 (s, 1H), 7,13 (d, J = 1,8Hz, 1H), 7,00
(br s, 1H), 6,84 (dd, J = 8,1 und 1,5Hz, 1H), 6,77 (s, 2H), 5,63
(d, J = 6,0Hz, 1H), 4,16 (s, 2H), 3,54-3,61 (m, 2H), 3,52 (s, 3H),
3,45 (s, 3H), 2,92-2,97 (m, 2H) ppm.
MS (ESI) m/z = 543 [M+H]+.
-
Beispiel 97
-
N
5,1-Dimethyl-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N
2-(2-phenylethyl)-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-4-pyrimidin-4-yl)-1,N5-dimethyl-N2-phenethyl-1H-benzoimidazol-2,5- diamin (98 mg, 0,25
mmol) und 4-[(Methylsulfonyl)methyl]anilin (46 mg, 0,25 mmol) als
einen weißen
Feststoff (120 mg, 83 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,21 (s, 1H), 7,77-7,81 (m,
3H), 7,18-7,33 (m, 8H), 7,12 (d, J = 1,5Hz, 1H), 7,00 (t, J = 5,7Hz,
1H), 6,83 (dd, J = 8,1 und 1,5Hz, 1H), 5,65 (d, J = 6,0Hz, 1H),
4,35 (s, 2H), 3,54-3,61 (m, 2H), 3,52 (s, 3H), 3,44 (s, 3H), 2,92-2,97
(m, 2H), 2,86 (s, 3H) ppm.
MS (ESI) m/z = 542 [M+H]+.
-
Beispiel 98
-
N-Methyl-2-(4-{[4-(methyl{1-methyl-2-[(2-phenylethyl)amino]-1H-benzimidazol-5-yl}amino)-2-pyrimidinyl]amino}phenyl)ethansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-1,N5-dimethyl-N2-phenethyl-1H-benzoimidazol-2,5-diamin (98 mg, 0,25
mmol) und 2-(4-Amino-phenyl)ethansulfonsduremethylamid (54 mg, 0,25
mmol) als einen weißen
Feststoff (100 mg, 66 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,30 (s, 1H), 7,82 (d, J =
6,0Hz, 1H), 7,65 (d, J = 8,4Hz, 2H), 7,43 (d, J = 8,4Hz, 1H), 7,20-7,33
(m, 5H), 7,06-7,14 (m, 3H), 6,98 (q, J = 6,2Hz, 1H), 5,70 (d, J
= 6,0Hz, 1H), 3,65 (m, 2H), 3,60 (s, 3H), 3,45 (s, 3H), 3,21-3,26
(m, 2H), 2,95-3,00 (m, 2H), 2,84-2,90 (m, 2H), 2,59 (d, J = 5,1Hz,
3H) ppm.
MS (ESI) m/z = 571 [M+H]+.
-
Beispiel 99
-
N
2-(1,1-Dimethylethyl)-N
5,1-dimethyl-N
5-[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-tert-Butyl-N5-(2-chlor-pyrimidin-4-yl)-1,N5-dimethyl-1H-benzoimidazol-2,5- diamin (69 mg, 0,20
mmol) und 4-[(Methylsulfonyl)methyl]anilin (37 mg, 0,20 mol) als
einen weißen
Feststoff (111 mg, 95 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,28 (s, 1H), 7,77-7,79 (m,
3H), 7,24 (d, J = 8,4Hz, 3H), 7,16 (d, J = 1,5Hz, 1H), 6,88 (d,
J = 7,8Hz, 1H), 6,21 (br s, 1H), 5,67 (d, J = 6,0Hz, 1H), 4,35 (s,
2H), 3,54 (s, 3H), 3,45 (s, 3H), 2,86 (s, 3H), 1,47 (s, 9H) ppm.
MS
(ESI) m/z = 494 [M+H]+.
-
Beispiel 100
-
N
2-Cyclohexyl-N
5,1-dimethyl-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamin
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-cyclohexyl-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (92 mg, 0,25
mmol) und 4-[(Methylsulfonyl)methyl]anilin (46 mg, 0,25 mmol) als
einen weißen
Feststoff (31 mg, 24 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,20 (s, 1H), 7,77-7,80 (m,
3H), 7,10 (s, 1H), 6,82 (d, J = 7,8Hz, 1H), 6,50 (d, J = 7,5Hz,
1H), 5,64 (d, J = 6,0Hz, 1H), 4,34 (s, 2H), 3,70 (br s, 1H), 3,51
(s, 3H), 3,44 (s, 3H), 2,85 (s, 3H), 2,01 (br s, 2H), 1,74 (br s,
2H), 1,62 (d, J = 11,1Hz, 1H), 1,16-1,32 (m, 5H) ppm.
MS (ESI)
m/z = 520 [M+H]+.
-
Beispiel 101
-
5-({4-[[2-(Cyclohexylamino)-1-methyl-1H-benzimidazol-5-yl](methyl)amino-2-rimidinl}amino)-2-methylbenzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-cyclohexyl-1,N5-dimethyl-1H-benzoimidazol-2,5- diamin (92 mg, 0,25
mmol) und 5-Amino-2-methyl-benzolsulfonamid (46 mg, 0,25 mmol) als
einen weißen
Feststoff (95 mg, 68 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,51 (s, 1H), 8,56 (s, 1H),
8,18 (br s, 1H), 7,83 (d, J = 6,0Hz, 1H), 7,69 (dd, J = 8,4 und
2,1Hz, 1H), 7,48 (d, J = 8,1Hz, 1H), 7,30 (s, 1H), 7,24 (s, 2H),
7,13-7,18 (m, 2H), 5,69 (d, J = 6,0Hz, 1H), 3,70 (m, 1H), 3,64 (s,
3H), 3,47 (s, 3H), 2,50 (s, 3H), 1,98-2,01 (m, 2H), 1,76-1,79 (m,
2H), 1,62-1,66 (m, 1H), 1,29-1,48 (m, 4H), 1,14-1,17 (m, 1H) ppm.
MS
(ESI) m/z = 521 [M+H]+.
-
Beispiel 102
-
N
2-Cyclohexyl-N
5,1-dimethyl-N
5-[2-({3-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-cyclohexyl-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (74 mg, 0,20
mmol) und 3-(2-Methansulfonylethyl)-phenylamin (47 mg, 0,20 mmol)
als einen weißen
Feststoff (59 mg, 52 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,07 (s, 1H), 7,76-7,78 (m,
2H), 7,60 (d, J = 8,4Hz, 1H), 7,13-7,20 (m, 2H), 7,09 (d, J = 1,8Hz,
1H), 6,79-6,82 (m, 2H), 6,47 (d, J = 7,8Hz, 1H), 5,61 (d, J = 6,0Hz,
1H), 3,70 (m, 1H), 3,51 (s, 3H), 3,44 (s, 3H), 3,35-3,40 (m, 2H),
2,97 (s, 3H), 2,91-2,95 (m, 2H), 2,01 (m, 2H), 1,74 (m, 2H), 1,63
(m, 1H), 1,16-1,31 (m, 5H), ppm.
MS (ESI) m/z = 534 [M+H]+.
-
Beispiel 103
-
N
2-Cyclohexyl-N
5,1-dimethyl-N
5-[2-({4-[2-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-cyclohexyl-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (74 mg, 0,20
mmol) und 4-(2-Methansulfonylethyl)-phenylamin (40 mg, 0,20 mmol)
als einen weißen
Feststoff (100 mg, 88 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,12 (s, 1H), 7,78 (d, J =
6,0Hz, 1H), 7,69 (d, J = 8,4Hz, 2H), 7,27 (d, J = 8,4Hz, 1H), 7,11-7,14
(m, 3H), 6,90 (d, J = 8,1Hz, 1H), 5,64 (d, J = 6,0Hz, 1H), 3,72
(m, 1H), 3,56 (s, 3H), 3,43 (s, 3H), 3,30-3,43 (m, 2H), 2,90-2,95
(m, 5H), 1,98 (m, 2H), 1,76 (m, 2H), 1,62 (m, 1H), 1,36 (m, 4H),
1,10 (m, 1H) ppm.
MS (ESI) m/z = 534 [M+H]+.
-
Beispiel 104
-
N
2-Cyclohexyl-N
5,1-dimethyl-N
5-[2-({4-[1-(methylsulfonyl)ethyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diaminhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-cyclohexyl-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (74 mg, 0,20
mmol) und 4-(1-Methansulfonylethyl)-phenylamin (40 mg, 0,20 mmol)
als einen weißen
Feststoff (104 mg, 91 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,34 (s, 1H), 7,85 (d, J =
6,0Hz, 1H), 7,71 (d, J = 8,4Hz, 2H), 7,43 (d, J = 8,1Hz, 1H), 7,22-7,26
(m, 3H), 7,08 (d, J = 8,1Hz, 1H), 5,76 (d, J = 6,0Hz, 1H), 4,40
(m, 1H), 3,72 (m, 1H), 3,63 (s, 3H), 3,45 (s, 3H), 2,76 (s, 3H),
1,99 (m, 2H), 1,76 (m, 2H), 1,58-1,65 (m, 4H), 1,33-1,43 (m, 4H),
1,15 (m, 1H) ppm.
MS (ESI) m/z = 534 [M+H]+.
-
Beispiel 105
-
2-Methyl-5-[(4-(methyl[1-methyl-2-(methylamino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-N2,N5,1-trimethyl-1H-benzimidazol-2,5-diamin
(58 mg, 0,20 mmol) und 5-Amino-2-methyl-benzolsulfonamid (35 mg,
0,20 mmol) als einen rosafarbenen Feststoff (78 mg, 84 %) hergestellt.
1H-NMR (300 MHz, d6-DMSO) δ: 10,63 (br
s, 1H), 9,22 (d, J = 4,2Hz, 1H), 8,40 (br s, 2H), 7,91 (d, J = 6,9Hz, 1H),
7,67 (m, 2H), 7,47 (d, J = 1,5Hz, 1H), 7,28-7,36 (m, 3H), 5,83 (m,
1H), 3,67 (s, 3H), 3,53 (s, 3H), 3,08 (d, J = 4,5Hz, 3H), 2,54 (s,
3H).
MS (ESI) m/z = 453 [M+H]+.
-
Beispiel 106
-
1-{4-[(4-{Methyl[1-methyl-2-(methylamino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]phenyl}methansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlorpyrimidin-4-yl)-N2,N5,1-trimethyl-1H-benzimidazol-2,5-diamin
(50 mg, 0,17 mmol) und (4-Amino-phenyl)-methansulfonamid (32 mg,
0,17 mmol) als einen weißen
Feststoff (38 mg, 46 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,71 (br
s, 1H), 9,00 (br s, 2H), 7,90 (d, J = 6,3Hz, 1H), 7,61 (m, 3H),
7,39 (s, 1H), 7,26 (d, J = 8,4Hz, 1H), 7,19 (d, J = 8,1Hz, 1H),
6,79 (s, 2H), 5,83 (d, J = 5,7Hz, 1H), 4,17 (s, 2H), 3,66 (s, 3H),
3,48 (s, 3H), 3,06 (d, J = 4,5Hz, 3H).
MS (ESI) m/z = 453 [M+H]+.
-
Beispiel 107
-
3-[(4-{Methyl[1-methyl-2-(methylamino)-1H-benzimidazol-5-yl]amino}-2-pyrimidinyl)amino]benzolsulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlorpyrimidin-4-yl)-N2,N5,1-trimethyl-1H-benzimidazol-2,5-diamin (60
mg, 0,20 mmol) und 3-Amino-benzolsulfonamid (34 mg, 0,20 mmol) als
einen weißen
Feststoff (40 mg, 42 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO + NaHCO3) δ: 9,51 (s,
1H), 8,61 (s, 1H), 7,77-7,82 (m, 2H), 7,26-7,39 (m, 6H), 7,17 (s,
1H), 6,92 (d, J = 7,8Hz, 1H), 5,66 (d, J = 6,0Hz, 1H), 3,55 (s,
3H), 3,47 (s, 3H), 2,95 (d, J = 4,2Hz, 3H).
MS (ESI) m/z =
439 [M+H]+.
-
Beispiel 108
-
N
2,N
5,1-Trimethyl-N
5-[2-({3-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-1H-benzimidazol-2,5-diamin
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlorpyrimidin-4-yl)-N2,N5,1-trimethyl-1H-benzimidazol-2,5-diamin
(48 mg, 0,16 mmol) und 3-Methansulfonylmethyl-phenylamin (30 mg,
0,16 mmol) als einen weißen
Feststoff (75 mg, 83 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,23 (s, 1H), 7,89 (s, 1H),
7,79 (d, J = 6,0Hz, 1H), 7,68 (d, J = 8,1Hz, 1H), 7,19-7,27 (m,
3H), 7,13 (s, 1H), 6,87-6,93 (m, 2H), 5,66 (d, J = 6,0Hz, 1H), 4,33
(s, 2H), 3,54 (s, 3H), 3,43 (s, 3H), 2,93 (d, J = 4,5Hz, 3H), 2,89
s, 3H).
MS (ESI) m/z = 452 [M+H]+.
-
Beispiel 109
-
1-[4-({4-[[1-Ethyl-2-(methylamino)-1H-benzimidazol-5-yl](methyl)amino]-2-pyrimidinyl}amino)phenyl]methansulfonamidhydrochlorid
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N5-(2-Chlor-pyrimidin-4-yl)-1-ethyl-N2,N5-dimethyl-1H-benzoimidazol-2,5-diamin
(79 mg, 0,25 mmol) und (4-Amino-phenyl)-methansulfonamid (46 mg,
0,25 mmol) als einen weißen
Feststoff (110 mg, 88 %) hergestellt.
1H-NMR
(300 MHz, d6-DMSO) δ: 9,24 (s, 1H), 7,81 (d, J =
6,0Hz, 1H), 7,74 (m, 3H), 7,36 (d, J = 8,1Hz, 1H), 7,17-7,20 (m,
3H), 6,96 (d, J = 8,4Hz, 1H), 6,78 (s, 2H), 5,70 (d, J = 6,0Hz,
1H), 4,09-4,16 (m, 4H), 3,45 (s, 3H), 2,97 (d, J = 4,5Hz, 3H), 1,24
(t, J = 6,9Hz, 3H) ppm.
MS (ESI) m/z = 467 [M+H]+.
-
Beispiel 110
-
N
5,1-Dimethyl-N
5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]-N
2-[4-(trifluormethyl)phenyl]-1H-benzimidazol-2,5-diamin
-
Ein
Gemisch aus N4-(2-Methansulfonyl-1-methyl-1H-benzoimidazol-5-yl)-N2-(4-methansulfonylmethyl-phenyl)-N4-methyl-pyrimidin-2,4-diamin (89 mg, 0,18
mmol), 4-(Trifluormethyl)anilin (148 mg, 0,9 mmol) und eine katalytische
Menge an HCl (1 Tropfen, konzentriert) in Isopropanol wurde in einem
Smith-Syntherisator bei 150°C
für 10
min erhitzt. Das Reaktionsgemisch wurde aufkonzentriert und durch
präparative
HPLC aufgereinigt, und nach Rufkonzentrierung wurde das Produkt
mit HCl (0,1 ml, 1M in Ether) behandelt, um die Titelverbindung
als einen blaßgelben
Feststoff zu ergeben:
LC/MS (m/e) 582,2 [M+H]+,
Rt bei 1,34 min.
-
Die
folgenden Verbindungen der Beispiele 111-125 der Formel I
a wurden gemäß dem Verfahren aus Beispiel
110 hergestellt
-
Beispiel 126
-
Das
Verfahren aus Beispiel 5 wurde verwendet, wobei 4-Methansulfonylmethylphenylamin
durch 4-Amino-benzolsulfonamid ersetzt wurde, was die Titelverbindung
als einen weißen
Feststoff ergab:
LC/MS (m/e) 456,02 [M+H]+,
Rt bei 1,37 min.
-
Beispiel 127
-
Das
Verfahren aus Beispiel 6 wurde verwendet, wobei N2-(4-Methansulfonylmethyl-phenyl)-N4-methyl-N4-(1-methyl-2-methylsulfanyl-1H-benzolimidazol-5-yl)-pyrimidin-2,4-diamin
durch 4-{4-[Methyl-(1-methyl-2- methylsulfanyl-1H-benzoimidazol-5-yl)-amino]-pyrimidin-2-ylamino}-benzolsulfonamid
ersetzt wurde, was die Titelverbindung ergab:
LC/MS (m/e) 472,2
[M+H]+, Rt bei 1,24 min.
-
Beispiel 128
-
Das
Verfahren aus Beispiel 7 wurde verwendet, wobei N4-(2-Methansulfonyl-1-methyl-1H-benzoimidazol-5-yl)-N2-(4-methansulfonylmethylphenyl)-N4-methyl-pyrimidin-2,4-diamin durch 4-{4-[(2-Methansulfinyl-1-methyl-1H-benzOimidazol-5-yl)methyl-amino]-pyrimidin-2-ylamino}-benzolsulfonamid
ersetzt wurde, was die Titelverbindung als ein gelbes 151 ergab:
LC/MS
(m/e) 569,4 [M+H]+, Rt bei 1,41 min.
-
Beispiel 129
-
Das
Verfahren aus Zwischenprodukt Beispiel 1B wurde verwendet, wobei
Isothiocyanat durch 3-Trifluormethyl-phenylamin ersetzt wurde, was
die Titelverbindung als einen dunkelorangen Feststoff ergab:
LC/MS
(m/e) 337,2 [M+H]+.
-
Beispiel 130
-
(Methyl-nitro-1H-benzoimidazol-2-yl)-(3-trifluormethyl-phenyl)-amin
(2,34 g) und Cäsiumcarbonat (5,61
g, 17,2 mmol) wurden in DMF für
15 min gerührt,
und dann wurde (BOC)2O (2,81 g, 12,9 mmol)
hinzugegeben. Das resultierende Gemisch wurde bei Raumtemperatur
für 4 Tage
gerührt.
Das Reaktionsgemisch wurde dann aufkonzentriert und der Rückstand
in EtOAc aufgenommen und mit Wasser und dann mit Salzlösung gewaschen,
getrocknet und aufkonzentriert, Kieselsäure "Flash", was 1,45 g der Titelverbindung als
einen gelben Schaum ergag.
LC/MS (m/e) 437 [M+H]+,
Rt bei 2,34 min.
-
Beispiel 131
-
Das
Verfahren aus Beispiel 3 wurde verwendet, wobei 1-Methyl-2-methylsulfanyl-5-nitro-1H-benzoimidazol
durch (Methyl-nitro-1H-benzoimidazol-2-yl)-(3-trifluormethyl-phenyl)-carbaminsäuredimethylethylester ersetzt
wurde, was die Titelverbindung als einen gelbbräunlichen gegebenenfalls ergab:
LC/MS
(m/e) 407,4 [M+H]+, Rt bei 1,62 min.
-
Beispiel 132
-
Das
Verfahren aus Zwischenprodukt Beispiel 1D wurde verwendet, wobei
N2-Isopropyl-1-methyl-1H-benzoimidazol-2,5-diamin
durch (Amino-methyl-1-benzoimidazol-2-yl)-(3-trifluormethyl-phenyl)-carbaminsäuredimethylethylester
ersetzt wurde, was die Titelverbindung als einen weißen Feststoff
ergab:
LC/MS (m/e) 533,2 [M+H]+, Rt
bei 2,44 min.
-
Beispiel 133
-
Das
Verfahren aus Beispiel 7 wurde verwendet, wobei N4-(2-Methansulfonyl-1-methyl-1H-benzoimidazol-5-yl)-N2-(4-methansulfonylmethylphenyl)-N4-methyl-pyrimidin-2,4-diamin durch [(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-1H-benzoimidazol-2-yl}-(3-trifluormethyl-phenyl)-carbaminsäuredimethyl-ethylester
ersetzt wurde, was die Titelverbindung als einen gelben Feststoff
ergab:
LC/MS (m/e) 582,0 [M+H]+, Rt
bei 1,14 min.
-
Beispiel 134
-
N
2-[5-(1,1-Dimethylethyl)-3-isoxazolyl]-N
5,1-dimethyl-N
5-[2({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl)-1H-benzimidazol-2 ‚5-diamin
-
N-(5-tert-Butyl-isoxazol-3-yl)-N-{5-[(2-chlor-pyrimidin-4-yl)-methylamino]-1-methyl-1H-benzoimidazol-2-yl}-2,2-dimethyl-propionamid
(50 mg, 0,10 mmol) und 4-[(Methylsulfonyl)methyl]anilin (19 mg,
0,10 mmol) wurden in Isopropanol (2,5 ml) aufgelöst. Zu dieser Lösung wurde
eine katalytische Menge an HCl zugegeben, und die Reaktion wurde
auf 70°C
12 Stunden erhitzt. Das Lösungsmittel
wurde entfernt, und das Reaktionsgemisch durch RP-HPLC und unter
Verwendung von CH3CN:H2O:0,1
% TFA-Lösungsmittel
als mobile Phase aufgereinigt. Der Feststoff wurde in CH2Cl2 aufgelöst und durch
eine 10%ige NaHCO3-Lösung neutralisiert. Die CH2Cl2-Phase wurde über Na2SO4 getrocknet und
eingedampft, um die Titelverbindung zu ergeben.
1H-NMR
(400 MHz, d6-DMSO) δ: 11,3 und 10,6 (s, 1H), 9,6
(d, J = 10,9Hz, 1H), 7,85 (d, 5,8Hz, 1H), 7,75 (m, 2H), 7,45 (d,
J = 5,8Hz, 1H), 7,25-7,45 (m, 2H), 7,05-7,10 (m, 2H), 5,75 (m, 1H),
4,35 (s, 2H), 3,52 (s, 3H), 3,51 (d, J = 12Hz, 3H), 2,85 (s, 3H),
1,29 (s, 9H) ppm.
MS (ESI) m/z = 560 [M+H]+.
-
Die
folgenden Verbindungen der Beispiel 135-141 der Formel Ib wurden gemäß dem Verfahren aus Beispiel
134 mit dem im jeweiligen Beispiel angegebenem Ausgangsmaterial
hergestellt.
-
-
Beispiel 135
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 134 mit N2-(5-tert-Butyl-isoxazol-3-yl)-N5-(2-chlor-pyrimidin-4-yl)-1-methyl-1H-benzoimidazol-2,5-diamin
(50 mg, 0,126 mmol) und 4-[(Methylsulfonyl)-methyl]anilin (26 mg, 0,139 mmol) hergestellt,
um einen weißen
Feststoff hervorzubringen (36 mg, 0,06 mmol).
MS (ESI) m/z
= 547 [M+H]+.
-
Beispiel 136
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 134 mit N2-(5-tert-Butyl-isoxazol-3-yl)-N5-(2-chlor-pyrimidin-4-yl)-1-methyl-1H-benzoimidazol-2,5-diamin
(50 mg, 0,126 mmol) und 4-[(Methylsulfonyl)-methyl]anilin (26 mg, 0,139 mmol) hergestellt,
um einen weißen
Feststoff hervorzubringen (16 mg, 0,03 mmol).
MS (ESI) m/z
= 547 [M+H]+.
-
Beispiel 137
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 134 mit N-(5-tert-Butyl-isoxazol-3-yl)-N-{5-[(2-chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-2,2-dimethyl-propionamid
(23 mg, 0,045 mmol) und 3-[(Methylsulfonyl)methyl]anilin (10 mg,
0,139 mmol) hergestellt, um einen weißen Feststoff hervorzubringen
(5 mg, 0,01 mmol).
MS (ESI) m/z = 561 [M+H]+.
-
Beispiel 138
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 134 mit N2-(5-tert-Butyl-isoxazol-3-yl)-N5-(2-chlor-pyrimidin-4-yl)-1-methyl-1H-benzoimidazol-2,5-diamin
(40 mg, 0,10 mmol) und 5-Amino-2-methyl-benzolsulfonamid (27 mg, 0,11 mmol)
hergestellt, um einen weißen
Feststoff hervorzubringen (26 mg, 0,048 mmol).
MS (ESI) m/z
= 547 [M+H]+.
-
Beispiel 139
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 134 mit N-(5-tert-Butyl-isoxazol-3-yl)-N-{5-[(2-chlor-pyrimidin-4-yl)-methyl-amino]-1-methyl-1H-benzoimidazol-2-yl}-2,2-dimethyl-propionamid
(50 mg, 0,10 mmol) und 3-[(Methylsulfonyl)methyl]anilin (23 mg,
0,10 mmol) hergestellt, um einen weißen Feststoff hervorzubringen
(20 mg, mmol).
MS (ESI) m/z = 562 [M+H]+.
-
Beispiel 140
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 134 mit N5-(2-Chlor-pyrimidin-4-yl)-N2-(6-fluor-4-H-benzo[1,3]dioxin-8-ylmethyl)-1H-benzoimidazol-2,5-diamin
(35 mg, 0,08 mmol) und 3-[(Methylsulfonyl)- methyl]anilin (16 mg, 0,08 mmol) hergestellt,
um einen weißen
Feststoff hervorzubringen (12 mg, 0,02 mmol).
MS (ESI) m/z
= 590 [M+H]+.
-
Beispiel 141
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 1 mit N2-(5-tert-Butyl-isoxazol-3-yl)-NS-(2-chlor-pyrimidin-4-yl)-1-methyl-1H-benzoimidazol-2,5-diamin
(35 mg. 0,09 mmol) und 3-(Morpholin-4-sulfonyl)-phenylamin (23 mg, 0,10 mmol) hergestellt,
um einen cremefarbenen Feststoff hervorzubringen (32 mg, 0,05 mmol).
MS
(ESI) m/z = 605 [M+H]+.
-
Beispiel
142
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-N'-phenylharnstoff
-
Zu
einer Lösung
aus N5,1-Dimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)pyrimidin-4-yl]-1H-benzimidazol-2,5-diamin
(150 mg, 0,343 mmol) in N,N-Dimethylacetamid (3 ml) wurde 1,1'-Carbonyldiimidazol
(167 mg, 1,03 mmol) hinzugegeben. Das Gemisch wurde für 24 h gerührt und
Anilin (192 mg, 2,06 mmol) wurde dann zugegeben. Die Reaktion mit
gesättigter
Natriumbicarbonat-Lösung
(30 ml) abgeschreckt und das Produkt präzipitiert. Das Rohprodukt wurde
filtriert, mit Wasser und Diethylether gewaschen und luftgetrocknet,
um das gewünschte
Produkt ohne weitere Rufreinigung zu ergeben.
1H-NMR
(300 MHz, d6-DMSO) δ: 12,14 (s, 1H), 9,26 (s, 1H),
9,12 (s, 1H), 7,86 (d, J = 5,8Hz, 1H), 7,76-7,68 (m, 4H), 7,42 (d,
J = 8,2Hz, 1H), 7,30-7,20 (m, 5H), 7,12 (d, J = 8,2Hz, 1H), 6,89
(t, J = 7,1Hz, 1H), 5,75 (d, J = 5,7Hz, 1H), 4,34 (s, 2H), 3,57
(s, 3H), 3,44 (s, 3H), 2,84 (s, 3H).
MS (ESI) m/z = 557 [M+H]+.
-
Beispiel 143
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)benzamid
-
Zu
einer Lösung
aus Benzoesäure
(51 mg, 0,402 mmol) in N,N-Dimethylformamid
(2 ml) wurde 1,1'-Carbonyldiimidazol
(65,2 mg, 0,400 mmol) hinzugegeben. Das Gemisch wurde für 30 Minuten
bei Raumtemperatur gerührt,
und dann wurde eine Lösung
aus N5,1-Dimethyl-N5-[2-({4-[(methylsulfonyl)methyl]phenyl}amino)pyrimidin-4-yl]-1H-benzimidazol-2,5-diamin (88 mg, 0,201
mmol) und Triethylamin (0,03 ml, 0,201 mmol) in N,N-Dimethylformamid
(2 ml) hinzugegeben. Das Reaktionsgemisch wurde für 16 Stunden
gerührt, mit
gesättigter
Natriumbicarbonat-Lösung
(30 ml) abgeschreckt und das Produkt dann präzipitiert. Das Rohprodukt wurde
filtriert, mit Wasser und Diethylether gewaschen und luftgetrocknet,
um das gewünschte
Produkt ohne weitere Aufreinigung zu ergeben.
1H-NMR
(400 MHz, d6-DMSO) δ: 12,82 (s, 1H), 9,28 (s, 1H),
8,28 (d, J = 7,3Hz, 2H), 7,89 (d, J = 6,1Hz, 1H), 7,74 (d, J = 8,2Hz,
2H), 7,59 (d, J = 8,4Hz, 1H), 7,51-7,44 (m, 4H), 7,25-7,20 (m, 3H),
5,79 (d, J = 5,9Hz, 1H), 4,34 (s, 2H), 3,77 (s, 3H), 3,47 (s, 3H),
2,84 (s, 3H).
MS (ESI) m/z = 542 [M+H]+.
-
Die
nachfolgenden Beispiele 144-152 wurden in gleicher Weise wie Beispiele
142 oder 143 hergestellt.
-
Beispiel 144
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2,3-dihydro-1H-indol-1-carboxamid
-
- 1H-NMR (300 MHz, d6-DMSO) δ: 12,23 (s,
1H), 9,25 (s, 1H), 7,86 (d, J = 5,9Hz, 1H), 7,74 (d, J = 8,2Hz,
2H), 7,65 (d, J = 7,4Hz, 1H), 7,45 (d, J = 8,5Hz, 1H), 7,32 (s,
1H), 7,21-7,12 (m, 5H), 6,85 (m, 1H), 5,75 (d, J = 6,1Hz, 1H), 4,33
(s, 2H), 3,60 (s, 3H), 3,48-3,43 (m, 5H), 3,06 (m, 2H), 2,83 (s,
3H).
MS (ESI) m/z = 583 [M+H]+.
-
Beispiel 145
-
N-[5-(1,1-Dimethylethyl)-3-isoxazolyl-N'-(1-methyl-5-{methyl[2-){4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)harnstoff
-
- 1H-NMR (300 MHz, d6-DMSO) δ: 12,22 (s,
1H), 9,79 (br s, 1H), 9,28 (s, 1H), 7,88 (d, J = 5,9Hz, 1H), 7,75
(d, J = 8,2Hz, 2H), 7,46 (d, J = 8,4Hz, 1H), 7,31 (br s, 1H), 7,22
(d, J = 8,4Hz, 2H), 7,16 (m, 1H), 6,67 (s, 1H), 5,76 (d, J = 5,9Hz,
1H), 4,35 (s, 2H), 3,58 (s, 3H), 3,45 (s, 3H), 2,85 (s, 3H), 1,30
(s, 9H.
MS (ESI) m/z = 604 [M+H]+.
-
Beispiel 146
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-phenylacetamid
-
- 1H-NMR (400 MHz, d6-DMSO) δ: 10,92 (s,
1H), 9,24 (s, 1H), 7,85 (m, 1H), 7,73 (d, J = 8,1Hz, 2H), 7,59 (d,
J = 8,3Hz, 1H), 7,52 (s, 1H), 7,38-7,29 (m, 5H), 7,19 (m, 3H), 5,75 (d,
J = 4,8Hz, 1H), 4,34 (s, 2H), 3,81 (s, 3H), 3,58 (s, 3H), 3,48 (s,
3H), 2,48 (s, 3H).
MS (ESI) m/z = 556 [M+H]+.
-
Beispiel 147
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-1-phenylcyclopropancarboxamid
-
- 1H-NMR (400 MHz, d6-DMSO) δ: 12,44 (s,
1H), 9,26 (s, 1H), 7,87 (d, J = 6,0Hz, 1H), 7,72 (d, J = 8,3Hz,
2H), 7,45 (d, J = 8,4Hz, 1H), 7,38 (d, J = 7,3Hz, 2H), 7,31-7,27
(m, 3H), 7,21-7,16 (m, 4H), 5,75 (d, J = 5,8Hz, 1H), 4,34 (s, 2H),
3,43 (s, 611), 2,84 (s, 3H), 1,60 (m, 2H), 1,10 (m, 2H).
MS
(ESI) m/z = 582 [M+H]+.
-
Beispiel 148
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-4-pyridincarboxamid
-
- 1H-NMR (400 MHz, d6-DMSO) δ: 12,92 (s,
1H), 9,29 (s, 1H), 8,75 (d, J = 5,7Hz, 2H), 8,11 (d, J = 5,7Hz,
2H), 7,90 (d, J = 6,1Hz, 1H), 7,74 (d, J = 8,4Hz, 2H), 7,64 (d,
J = 8,4Hz, 1H), 7,47 (s, 1H), 7,29 (m, 1H), 7,21 (d, J = 8,4Hz,
2H), 5,81 (d, J = 5,9Hz, 1H), 4,34 (d, 2H), 3,80 (s, 3H), 3,48 (s,
3H), 2,85 (s, 3H).
MS (ESI) m/z = 543 [M+H]+.
-
Beispiel 149
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)cyclohexancarboxamid
-
- 1H-NMR (400 MHz, d6-DMSO) δ: 10,56 (s,
1H), 9,23 (s, 1H), 7,85 (d, J = 5,3Hz, 1H), 7,85 (d, J = 7,3Hz,
2H), 7,73 (d, J = 8,4Hz, 1H), 7,60 (d, J = 8,4Hz, 1H), 7,51 (s,
1H), 7,19-7,18 (m, 3H), 5,81 (d, J = 4,9Hz, 1H), 4,34 (s, 2H), 3,60
(s, 3H), 3,48 (s, 3H), 2,85 (s, 3H), 1,92 (m, 2H), 1,77 (m, 2H),
1,66 (m., 1H), 1,47 (m, 2H), 1,36-1,20 (m, 4H).
MS (ESI) m/z
= 548 [M+H]+.
-
Beispiel 150
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-[(phenylmethyl)oxy]acetamid
-
- 1H-NMR (400 MHz, d6-DMSO) δ: 8,84 (s,
1H), 7,87 (d, J = 5,5Hz, 1H), 7,73 (d, J = 8,6Hz, 2H), 7,53 (d,
J = 8,0Hz, 1H), 7,47-7,18 (m, 10H), 5,81 (d, J = 5,4Hz, 1H), 4,69
(s, 2H), 4,31 (s, 2H), 3,64 (s, 3H), 3,48 (s, 3H), 3,47 (s, 2H),
2,85 (s, 3H).
MS (ESI) m/z = 586 [M+H]+.
-
Beispiel 151
-
2-(3-Methyl-5-isoxazolyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
- 1H-NMR (400 MHz, d6-DMSO) δ: 8,84 (s,
1H), 7,88 (d, J = 6,2Hz, 1H), 7,72 (d, J = 8,4Hz, 2H), 7,53 (d,
J = 8,6Hz, 1H), 7,46 (s, 1H), 7,23-7,19 (m, 3H), 6,23 (s, 1H), 5,82
(d, J = 5,7Hz, 1H), 4,30 (s, 2H), 3,63 (s, 3H), 3,48-3,47 (m, 5H),
2,82 (s, 3H), 2,23 (s, 3H).
MS (ESI) m/z = 561 [M+H]+.
-
Beispiel 152
-
3-[(Dimethylamino)methyl]-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)benzamid
-
- 1H-NMR (400 MHz, d6-DMSO) δ: 8,86 (s,
1H), 8,16-8,14 (m, 2H), 7,89 (d, J = 5,8Hz, 1H), 7,74 (d, J = 8,4Hz, 2H),
7,55-7,41 (m, 4H), 7,24-7,19 (m, 3H), 5,85 (d, J = 5,9Hz, 1H), 4,31
(s, 2H), 3,75 (s, 3H), 3,50 (s, 2H), 3,59 (s, 3H), 2,82 (s, 3H),
2,22 (s, 6H).
MS (ESI) m/z = 599 [M+H]+,
-
Beispiel 153
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-(2-thienyl)acetamid
-
Zu
einer Lösung
aus {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
(3,88 g, 10 mmol) und 4-[(Methylsulfonyl)methyl]anilin (1,9 g, 12
mmol) in Isopropanol (100 ml) wurde eine Lösung aus HCl (1 Tropfen, 4M
in Dioxan) hinzugegeben, und die Reaktion wurde auf 85°C erhitzt.
Nach 48 Stunden wurde das Reaktionsgemisch im Vakuum aufkonzentriert
und mit der Zugabe von gesättigter
NaHCO3-Lösung
neutralisiert. Das Gemisch wurde filtriert, um N5-[3-(4-Methansulfonylmethyl-phenylamino)-phenyl]-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin als
einen cremefarbenen Feststoff zu ergeben, der zur Herstellung der
Titelverbindung verwendet wurde.
-
Zu
einer Lösung
aus Thiophen-2-yl-essigsäure
(78 mg, 0,58 mmol) und Carbonyldiimidazol (88 mg, 0,55 mmol) in
DMF, die bei Raumtemperatur für
15 min gerührt
wurde, wurde eine Lösung
aus N5-[3-(4-Methansulfonylmethylphenylamino)-phenyl]-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin (120
mg, 0,29 mmol) und Triethylamin (40 μl, 0,29 mmol) in DMF zugegeben.
Das Reaktionsgemisch wurde bei Raumtemperatur für 16 h gerührt und N-({[3-(4-Methansulfonylmethyl-phenylamino)-phenyl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)-C-thiophen-2-yl-acetamid
(54 mg, 17 %) wurde mit reverser Phase-HPLC aufgereinigt.
1H-NMR (400 MHz, d6-DMSO) δ: 9,23 (s,
1H), 7,74-7,84 (m, 4H), 7,46-6,95 (m, 8H), 5,73 (d, J = 5,6Hz, 1H), 4,35
(s, 2H), 3,91 (s, 2H), 3,60 (s, 3H), 3,46 (s, 3H), 2,85 (s, 3H).
MS
(ESI) m/z = 562 [M+H]+.
LC/MS Rt (min)
1,47.
-
Beispiel 154
-
2-Fluor-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}-amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-5-(trifluormethyl)benzamid
-
Zu
einer Lösung
aus {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
(2,86 g, 7,4 mmol) und 3-[(methylsulfonyl)methyl]anilin (1,5 g,
8,1 mmol) in Isopropanol (70 ml) wurde eine Lösung von HCl (1 Tropfen, 4M
in Dioxan) hinzugegeben, und die Reaktion wurde auf 70°C erhitzt.
Nach 16 Stunden wurde das Reaktionsgemisch im Vakuum aufkonzentriert
und mit der Zugabe von gesättigter
NaHCO3-Lösung
neutralisiert. Das Gemisch wurde filtriert, um N5-[3-(3-Methansulfonylmethyl-phenylamino)-phenyl]-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin als
einen cremefarbenen Feststoff zu ergeben, der zur Herstellung der
Titelverbindung verwendet wurde.
-
Zu
der Lösung
aus N5-[3-(3-Methansulfonylmethyl-phenylamino)-phenyl]-1,N5-dimethyl-1H-benzoimidazol-2,5-diamin
(36 mg, 0,083 mmol) in NMP wurde Fluor-trifluormethyl-benzoylchlorid
(38 μl,
0,25 mmol) hinzugegeben. Das Reaktionsgemisch wurde bei Raumtemperatur
für 24
h gerührt
und dann mit einer Gilson-HPLC aufgereinigt, um C-Fluor-N-({[3-(3-methansulfonylmethyl-phenylamino)-phenyl]-methyl-amino}-methyl-1H-benzoimidazol-2-yl)trifluormethylbenzamid
(20 mg, 38 %) zu ergeben.
MS (ESI) m/z = 628 [M+H]+.
LC/MS
Rt (min) 2,03.
-
Die
folgenden Verbindungen der Beispiele 155-239 der Formel I
c wurden gemäß den Verfahren der Beispiele
153 oder 154 mit den entsprechenden Ausgangsmaterialien hergestellt
-
Beispiel 155
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 154 mit 3,4-Difluor-benzoylchlorid, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
hergestellt.
MS (ESI) m/z = 578 [M+H]+.
-
Beispiel 156
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 154 mit Bis-trifluormethyl-benzoylchlorid, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
hergestellt.
MS (ESI) m/z = 678 [M+H]+.
-
Beispiel 157
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 154 mit Cyclohexancarbonsäurechlorid, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 548 [M+H]+.
-
Beispiel 158
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 154 mit 3-Methyl-benzoylchlorid, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester in
Pyridin hergestellt.
MS (ESI) m/z = 556 [M+H]+.
-
Beispiel 159
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 4-Methoxy-benzoesäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester hergestellt.
MS
(ESI) m/z = 572 [M+H]+.
-
Beispiel 160
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit (Chlor-trifluormethyl-phenyl)essigsäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
hergestellt.
MS (ESI) m/z = 658 [M+H]+.
-
Beispiel 161
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 3,5-Bis-trifluormethyl-essigsäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 692 [M+H]+.
-
Beispiel 162
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit (3-Trifluormethylsulfanyl-phenyl)-essigsäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 656 [M+H]+.
-
Beispiel 163
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 2,4-Bis-trifluormethyl-phenylessigsäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 692 [M+H]+.
-
Beispiel 164
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 2-Fluor-5-trifluormethyl-phenylessigsäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 642 [M+H]+.
-
Beispiel 165
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 3H-Benzotriazol-5-carbonsäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 583 [M+H]+.
-
Beispiel 166
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 3H-Benzoimidazol-5-carbonsäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 582 [M+H]+.
-
Beispiel 167
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Thiophen-2-carbonsäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäuretert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 548 [M+H]+.
-
Beispiel 168
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Thiophen-3-carbonsäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäuretert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 548 [M+H]+.
-
Beispiel 169
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Thiophen-2-yl-essigsäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäuretert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 562 [M+H]+.
-
Beispiel 170
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 3-Methyl-thiophen-2-carbonsäure, 4-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
hergestellt.
MS (ESI) m/z = 562 [M+H]+.
-
Beispiel 171
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Furan-3-carbonsäure, 4-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäuretert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 532 [M+H]+.
-
Beispiel 172
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 3-Methyl-furan-2-carbonsäure, 4-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 546 [M+H]+.
-
Beispiel 173
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 3-Methyl-isoxazol-5-yl-essigsäure 4-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 561 [M+H]+.
-
Beispiel 174
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 2-Chlor-5-trifluormethyl-phenylessigsäure, 4-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 658 [M+H]+.
-
Beispiel 175
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 3-Trifluormethylsulfanyl-phenylessigsäure, 4-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 656 [M+H]+.
-
Beispiel 176
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 2-Fluor-5-trifluormethyl-phenylessigsäure, 4-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 642 [M+H]+.
-
Beispiel 177
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 3,3-Dimethyl-buttersäure, 4-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester in
Pyridin hergestellt.
MS (ESI) m/z = 536 [M+H]+.
-
Beispiel 178
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 2-Propyl-pentansäure, 4-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester in
Pyridin hergestellt.
MS (ESI) m/z = 564 [M+H]+.
-
Beispiel 179
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Isobuttersäure,
4-[(Methylsulfonyl)methyl]anilin und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester in Pyridin
hergestellt.
MS (ESI) m/z = 508 [M+H]+.
-
Beispiel 180
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Cyclopropancarbonsäure, 4-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlorpyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäuretert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 506 [M+H]+.
-
Beispiel 181
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 4-Methoxy-benzoesäure, 4-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäuretert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 572 [M+H]+.
-
Beispiel 182
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 4-Methoxy-benzoesäure, 5-Amino-2-methyl-benzolsulfonamid
und {[(2-Chlorpyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäuretert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 573 [M+H]+.
-
Beispiel 183
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Furan-3-carbonsäure, 4-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester in
Pyridin hergestellt.
MS (ESI) m/z = 532 [M+H]+.
-
Beispiel 184
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Thiophen-2-yl-essigsäure, 5-Amino-2-methyl-benzolsulfonamid
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester in
Pyridin hergestellt.
MS (ESI) m/z = 563 [M+H]+.
-
Beispiel 185
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 2-Chlor-5-trifluormethyl-phenylsäure, 5-Amino-2-methyl-benzolsulfonamid
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 660 [M+H]+.
-
Beispiel 186
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 4-Methoxybenzoesäure, 3-(Morpholin-4-sulfonyl)-phenylamin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester in
Pyridin hergestellt.
MS (ESI) m/z = 629 [M+H]+.
-
Beispiel 187
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Thiophen-2-yl-essigsäure, 3-(Morpholin-4-sulfonyl)-phenylamin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 619 [M+H]+.
-
Beispiel 188
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Thiophen-2-yl-carbonsäure, 3-(Morpholin-4-sulfonyl)-phenylamin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 605 [M+H]+.
-
Beispiel 189
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Furan-3-carbonsäure, 3-(Morpholin-4-sulfonyl)-phenylamin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester in
Pyridin hergestellt.
MS (ESI) m/z = 589 [M+H]+.
-
Beispiel 190
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 3-Methyl-isoxazol-5-yl-essigsäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 561 [M+H]+.
-
Beispiel 191
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Furan-2-carbonsäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäuretert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 532 [M+H]+.
-
Beispiel 192
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 3-Methyl-isoxazol-5-yl-essigsäure, 3-(Morpholin-4-sulfonyl)-phenylamin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 618 [M+H]+.
-
Beispiel 193
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 3-Methyl-furan-2-carbonsäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 546 [M+H]+.
-
Beispiel 194
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Thiophen-2-yl-essigsäure, 3-(4-Methyl-piperazin-1-sulfonyl)-phenylamin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 632 [M+H]+.
-
Beispiel 195
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Thiophen-2-yl-carbonsäure, 3-(4-Methyl-piperazin-1-sulfonyl)-phenylamin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 618 [M+H]+.
-
Beispiel 196
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Furan-2-carbonsäure, 3-(4-Methyl-piperazin-1-sulfonyl)-phenylamin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 602 [M+H]+.
-
Beispiel 197
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 3-Methyl-isoxazol-5-yl-essigsäure, 3-(4-Methyl-piperazin-1-sulfonyl)phenylamin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 631 [M+H]+.
-
Beispiel 198
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit 3,3-Dimethyl-buttersäure, 3-[(Methylsulfonyl)methyl]anilin
und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäuretert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 536 [M+H]+.
-
Beispiel 199
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Propionsäure,
3-[(Methylsulfonyl)methyl]anilin und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tert-butylester
in Pyridin hergestellt.
MS (ESI) m/z = 494 [M+H]+.
-
Beispiel 200
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Pentansäure,
3-[(Methylsulfonyl)methyl]anilin und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tertbutylester
in Pyridin hergestellt.
MS (ESI) m/z = 522 [M+H]+.
-
Beispiel 201
-
Die
Titelverbindung wurde gemäß dem Verfahren
aus Beispiel 153 mit Buttersäure,
3-[(Methylsulfonyl)methyl]anilin und {[(2-Chlor-pyrimidin-4-yl)-methyl-amino]-methyl-H-benzoimidazol-2-yl}-carbaminsäure-tertbutylester
in Pyridin hergestellt.
MS (ESI) m/z = 508 [M+H]+.
-
Beispiel 202
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-phenylacetamid
-
Beispiel 203
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-1-phenylcyclopropancarboxamid
-
Beispiel 204
-
1-(2,5-Difluorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)cyclopropancarboxamid
-
Beispiel 205
-
1-(4-Chlorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)cyclopropancarboxamid
-
Beispiel 206
-
2-(4-Fluorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 207
-
2-[3,5-Bis(trifluormethyl)phenyl]-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 208
-
2-(3,4-Dichlorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 209
-
1-(2,5-Difluorphenyl)-N-(1-methyl-5-{methyl[2-({3-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)cyclopropancarboxamid
-
Beispiel 210
-
2-(2,5-Difluorphenyl)-N-(1-methyl-5-{methyl[2-({3-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 211
-
2-(3,4-Dichlorphenyl)-N-(1-methyl-5-{methyl[2-({3-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 212
-
1-(2,5-Difluorphenyl)-N-{5-[(2-{[5-(ethylsulfonyl)-2-(methyloxy)phenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}cyclopropancarboxamid
-
Beispiel 213
-
1-(2,5-Difluorphenyl)-N-{5-[(2-{[5-(ethylsulfonyl)-2-(methyloxy)phenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}acetamid
-
Beispiel 214
-
1-(3,4-Dichlorphenyl)-N-{5-[(2-{[5-(ethylsulfonyl)-2-(methyloxy)phenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}cyclopropancarboxamid
-
Beispiel 215
-
2-(3,4-Dichlorphenyl)-N-{5-[(2-{[5-(ethylsulfonyl)-2-(methyloxy)phenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}acetamid
-
Beispiel 216
-
N-{5-[(2-{[3-(Aminosulfonyl)-4-methylphenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}-1-(2,5-difluorphenyl)cyclopropancarboxamid
-
Beispiel 217
-
N-{5-[(2-{[3-(Aminosulfonyl)-4-methylphenyl]amino}-4-pyrimidinyl)(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}-1-(3,4-dichlorphenyl)cyclopropancarboxamid
-
Beispiel 218
-
N-{5-[(2-{[3-(Aminosulfonyl)-4-methylphenyl]amino}-4-pyrimidinyl)(methyl)aminoj-1-methyl-1H-benzimidazol-2-yl}-2-(3,4-dichlorphenyl)acetamid
-
Beispiel 219
-
2-[2,3-Bis(methyloxy)phenyl]-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 220
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-[2-(methyloxy)phenyl]acetamid
-
Beispiel 221
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-[3-(methyloxy)phenyl]acetamid
-
Beispiel 222
-
N-(1-Methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-[4-(methyloxy)phenyl]acetamid
-
Beispiel 223
-
2-(2-Fluorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 224
-
2-(3-Fluorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 225
-
2-(2,6-Difluorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 226
-
2-(2,3-Difluorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 227
-
2-[3,4-Bis(methyloxy)phenyl]-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 228
-
N-{5-[(2-{[3-(Aminosulfonyl)-4-methylphenyl]amino}-4-pyrimidinyl)-(methyl)amino]-1-methyl-1H-benzimidazol-2-yl}-2-(2,5-difluorphenyl)acetamid
-
Beispiel 229
-
1-(3,4-Dichlorphenyl)-N-(1-methyl-5-(methyl[2-({3-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)cyclopropancarboxamid
-
Beispiel 230
-
2-(2-Chlorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 231
-
2-(3-Chlorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-ylacetamid
-
Beispiel 232
-
2-(4-Chlorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 233
-
2-[3,5-Bis(methyloxy)phenyl]-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 234
-
2-[2,5-Bis(methyloxy)phenyl]-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 235
-
2-(2,5-Dichlorphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 236
-
3-Methyl-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-phenylbutanamid
-
Beispiel 237
-
2-(2,5-Dimethylphenyl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)-methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Beispiel 238
-
2-Methyl-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)-2-phenylpropanamid
-
Beispiel 239
-
2-(1,3-Benzodioxol-5-yl)-N-(1-methyl-5-{methyl[2-({4-[(methylsulfonyl)methyl]phenyl}amino)-4-pyrimidinyl]amino}-1H-benzimidazol-2-yl)acetamid
-
Biologische Daten
-
Tie2-Fluoreszenzpolarisations-Kinaseaktivitäts-Assay:
(TIE2-FP) Aktivierung der rekombinanten Tie2-Aktivierung:
-
Rekombinantes
GST-Tie2 wurde durch Inkubieren des Enzym in 20 mM Tris-HCl, pH
7,5, 12 mM MgCl2, 100 mM NaCl, 20 μM Natriumvanidat,
1 mM DTT und 300 μM
ATP bei Raumtemperatur für
2 Stunden aktiviert. Das Aktivierungsgemisch wurde dann durch eine
NAP-25-Entsalzungssäule
(Pharmacia Biotech Kat. Nr.. 17-0852-02) passiert, um freies ATP
zu entfernen. Das aktivierte Enzym wurde als Aliquots bei -80°C in 20 mM
Tris-HCl, pH 7,5 und 100 mM NaCl gelagert.
-
Testbedingungen:
-
Die
Endtestbedingungen waren 50 mM HEPES, pH 7,5, 5 % DMSO (wenn Verbindungen
durchgemustert werden), 200 μM
ATP, 5 mM MgCl2, 1 mM DTT, 50 μM Natriumvanidat,
1 nM aktiviertes Enzym und 200 μM
Peptid. IC50-Werte der Verbindungen wurden
unter subsättigenden
ATP (200 μM)
und variierenden Konzentrationen an aktiviertem Tie2 und Peptid-Substrat
(RFWKYEFWR-OH; MW 1873 Da, TFA-Salz). Panvera-Anti-Phosphotyrosin-Antikörper (Kat#P2840) und
PTK Green Tracer (Kat#P2842) wurden verwendet, um das phosphorylierte
Peptid zu detektieren. Die Polarisierung wurde auf einem TECAN-Polarion
in 138 Sekundenzyklen für
30 Minuten bei Raumtemperatur gemessen. IC50-Werte
wurden dann von % Polarisierung unter Verwendung normaler Berechnungsverfahren
bestimmt. Die Resultate sind nachfolgend angegeben.
-
VEGF-R2-Enzymtest (VEGF-E)
-
Der
VEGF-Enzymtest verwendete das LANCE-Verfahren (Wallac) und GST-VEGFR2, Baculovirus-exprimierte
rekombinante Konstrukte der intrazellulären Domänen des humanen TIE2, das durch
GST getagged ist. Das Verfahren maß die Fähigkeit des aufgereinigten
Enzyms den Transfer des γ-Phosphats
vom ATP auf Tyrosinreste in einem biotinylierten synthetischen Peptid
(Biotin-Aminohexyl-EEEEYFELVAKKKK-NH2)
zu katalysieren. Diese Peptid-Phosphorylierung wurde unter Verwendung
des folgenden Verfahrens detektiert: GST-VEGFR2 wurde für 40-60 Minuten bei Raumtemperatur
mit 75 μM
ATP, 5 mM MgCl2, 0,1 mM DTT, 0,1 mg/ml BSA
und der Testverbindung (verdünnt
von einer 10 mM-Stammlösung
in DMSO auf die gewünschte
Konzentration) in 100 mM hepes-Puffer inkubiert. Die Reaktion wurde
durch die Zugabe von EDTA (50 mM Endkonzentration) angehalten. Streptavidin-verknüpftes APC
(Allophycocyanin, Molecular Probe) und Europium-markierter anti-phosphoryliertes
Tyrosin-Antikörper
(Wallac) wurden dann bei einer Endkonzentration von 15 nM bzw. 1
nM hinzugegeben. Das APC-Signal wurde unter Verwendung einer ARVO "Multilabe-Zählers" (Wallac Berthold,
Japan) gemessen. Die Prozentinhibierung der Aktivität wurde
relativ zu Blindkontrolllöchern
berechnet. Die Konzentration der Testverbindung, bei der 50 % der
Aktivität
inhibiert wird (IC50), wurde unter Verwendung
einer nicht-linearen Regression (Levernberg-Marquardt) und der Gleichung
y = Vmax (1-x/(K+x)) + Y2 interpoliert, wobei "K" dem
IC50-Wert gleich war. Die IC50-Werte
wurden zu pIC50-Werte umgewandelt, d.h.
-log IC50 in Molarkonzentration. Die Ergebnisse
sind nachfolgend in Tabelle 1 dargestellt.
-
VEGF-geführter zellulärer Proliferationstest:
BrdU-Incorporationstest (VEGF-C)
-
Humane
Nabelschnur-Endothelzellen (HUVEC, Clonetics, CC25196) wurden in
TypI-Collagen-beschichtete 100 mm-Petrischalen in EGM-MV-Medium
(Clonetics, CC3125) bei 37°C
in einem befeuchteten Inkubator mit 5 % CO
2 und
95 % Luft passagiert. (HUVEC, die mehr als 6-mal in vitro passagiert
wurden, wurden verworfen und keinem Test unterzogen). Die Zellen
wurden unter Verwendung von Trypsin/EDTA geerntet, unter Verwendung
eines Hämocytometers
gezählt
und bei 5000 Zellen/Loch in eine Typ I-Collagen beschichtete 96-Loch-Platte
(Becton Dickinson, 354407) in M199 Medium (Gibco BRL, 12340-030)
ausplattiert, das 5 % FBS (Hyclone, A 1115-L) und Gentamicin (bei
50 μg/ml,
Gibco BRL) enthielt. Nach Inkubation über Nach bei 37°C wurde das
Medium mit 100 μl
an M199-serumfreien Medium, das Verbindungen bei verschiedenen Konzentrationen
mit 0,6 % DMSO und Gentamicin enthielt, ausgetauscht. Die Verbindungen
wurden in serumfrein M199-Medium von einer 10 mM-Stammlösung, die
in 100 % DMSO hergestellt wurde, verdünnt. Nach einer 30-minütigen Inkubation
bei 37°C
wurden die Zellen mit 100 μl
an serumfreien M199-Medium, das Gentamicin, 0,2 % Rinderserumalbumin
von Kulturgrad (BSA, Sigma A1993) und 20 ng/ml an VEGF (R&D Systems, 293-Ve)
oder 0,6 ng/ml an basischem FGF (R&D Systems, 233-FB) enthielt, gefüttert und
bei 37°C
für weitere 24
h kultiviert. Die Zellen wurden mit Bromdesoxyuridin (BrdU bei 10 μM in serumfreien
M199) bei 37°C
für zusätzliche
24 h pulsiert. Der Einbau von BrdU in die proliferierenden HUVEC
wurden unter Verwendung eines BrdU-Zell-Proliferations-ELISA (Roche
Molecular Biochemicals, 1647229) gemäß dem Protokoll des Herstellers
analysiert. Die optische Dichte bei 450 nm wurde mit einem "Multilabel-Zähler" (ARVO SX, Wallac) gemessen. Die Prozent-Inhibierung
des Zellwachstums wurde relativ zu den Blank-Kontrolllöchern berechnet.
die Konzentration der Testverbindung, bei der 50 % des Zellwachstums
inhibiert wurde (IC
50) wurde unter Verwendung
einer linearen Regression (Levernberg-Marquardt) und der Gleichung y = Vmax
(1-x/(K+x)) + Y2, wobei "K" zu dem IC
50 gleich war, interpoliert. Die IC
50-Werte wurden zu pIC
50-Werte
umgewandelt, d.h. -log IC
50 in Molarkonzentration.
Die Ergebnisse sind nachfolgend in Tabelle 1 dargestellt. Tabelle I
| Bsp.-Nr. | TIE2-FP | VEGF-E | VEGF- |
| 1 | | +++ | +++ |
| 2 | | +++ | +++ |
| 3 | | +++ | +++ |
| 4 | | +++ | +++ |
| 5 | | +++ | +++ |
| 6 | | +++ | +++ |
| 11 | | +++ | |
| 90 | | +++ | |
| 92 | + | ++ | |
| 95 | ++ | +++ | |
| 110 | +++ | +++ | |
| 112 | +++ | +++ | |
| 117 | + | +++ | |
| 118 | ++ | +++ | |
| 124 | ++ | +++ | |
| 125 | +++ | +++ | |
| 135 | + | +++ | |
| 136 | + | +++ | |
| 142 | | +++ | |
| 153 | + | +++ | |
| 156 | | ++ | |
| 157 | | +++ | |
| 161 | + | ++ | |
| 162 | + | +++ | |
| 167 | + | +++ | |
| 169 | + | +++ | |
| 173 | + | +++ | |
| 177 | + | +++ | |
| 202 | | +++ | |
| 203 | +++ | +++ | |
| 204 | + | ++ | |
| 206 | + | +++ | |
| 219 | | +++ | |
| 226 | + | +++ | |
| 229 | + | ++ | |
| 230 | + | +++ | |
| 239 | | ++ | |
- + = pIC50 von 5,0-6,0;
++ = pIC50 von 6,0-7,0; +++ = pIC50 von >7,0;