-
HINTERGRUND
DER ERFINDUNG
-
Erfindungsgebiet:
-
Vorliegende
Erfindung betrifft einen neuen Keramikartikel, einen Träger für einen
Katalysator, Verfahren zu deren Herstellung, einen Katalysator zur
Herstellung von Ethylenoxid unter Verwendung des Trägers sowie
ein Verfahren zur Herstellung von Ethylenoxid. Insbesondere betrifft
sie einen Keramikartikel, der bei erhöhten Temperaturen kalziniert
und mit sauren Punkten ausgestattet ist, einen Träger zur
Verwendung bei einem Katalysator, Verfahren zu dessen Herstellung,
einen Katalysator zur Herstellung von Ethylenoxid unter Verwendung
des Trägers
sowie ein Verfahren zur Herstellung von Ethylenoxid. Insbesondere
betrifft sie einen Keramikartikel mit einem Gehalt an Aluminium,
Silizium und Titan, der infolge seiner Kalzinierung bei 1.000°–2.000°C starke
saure Punkte aufweist, einen Träger
zur Verwendung bei einem Katalysator, Verfahren zu dessen Herstellung
sowie ein Verfahren zur Herstellung von Ethylenoxid.
-
BESCHREIBUNG DES STANDS
DER TECHNIK:
-
Die
Keramikartikel, welche die Oxide von Aluminium, Silizium, Titan
usw. als Grundmaterialien benutzen, besitzen in der Regel außerordentlich
hervorragende thermische, mechanische, elektrische und chemische
Eigenschaften und finden bei Anwendungen Gebrauch, die zu zahlreich
sind, um aufgezählt
zu werden. Diejenigen der Keramikartikel, welche sich durch thermische
und mechanische Festigkeit auszeichnen, werden intensiv auf dem
Gebiet der chemischen Industrie und als Träger für einen Katalysator sowie als
Raffinierungsmaterial und auf dem Gebiet von Biokeramiken als künstliche
Knochen und künstliche
Zähne,
welche Affinität
für lebende
Organismen aufweisen müssen,
Verwendung. Diejenigen Keramikartikel, welche chemische Eigenschaften
besitzen, werden für
die Analyse unter Verwendung der Adsorbierungs-/Desorbierungseigenschaft
einer chemischen Substanz benutzt, und insbesondere diejenigen Keramikartikel,
welche saure Punkte besitzen, werden als Katalysator für die Oxidation
von Olefinen und die Dehydrierung hydratisierter Verbindungen verwendet.
-
Beispielsweise
offenbart JP-A-54-32.408 einen nicht-sauren Füllstoff mit einem Gehalt an
Aluminium-, Silizium- und Titanoxid in einer Gesamtmenge von nicht
weniger als 99 Gew.% mit einem Gehalt an Metallen der Gruppen Va,
VIa, VIIa, VIII, Ib und IIb im Periodensystem der Elemente in einer
Gesamtmenge von weniger als 0,1 Gew.%, zurückgeführt auf Metalloxide, welcher
in Methylrot mit einem pKa-Wert von + 4,8 keine Säurefarbe
annimmt.
-
Ferner
offenbart JP-A-55-145.677 ein Verfahren zur Herstellung von Ethylenoxid,
gekennzeichnet durch die Verwendung eines Silberkatalysators, gebildet
unter Verwendung des nicht-sauren, zuvor erwähnten Füllstoffs als Katalysatorträger und
Silberablagerung hierauf, und erforderlichenfalls ferner einer Alkalimetallkomponente
oder einer Erdalkalimetallkomponente. U.S.-A-4.812.437 offenbart
einen hauptsächlich
aus α-Aluminiumoxid
zusammengesetzten Träger
mit einer spezifischen Oberfläche,
einem Wasserabsorptionsverhältnis,
mittleren Porendurchmesser, Siliziumdioxidgehalt und Natriumgehalt,
der in einem Indikator mit einem pKa-Wert von + 4,8 eine Säurefarbe
annimmt.
-
JP-A-62-4.444
offenbart, dass ein Träger
mit einer geringen Menge an Verunreinigungen erhalten wird, indem
man eine Aluminiumverbindung mit einem Salz eines Metalls der Gruppe
IA im Periodensystem der Elemente und dessen Kalzinierung erhalten
wird, und der den Träger
verwendende Katalysator hat eine hervorragende Stabilität. JP-A-4-363.139
offenbart einen Träger,
der ein Element von 4–6
Zyklen der Gruppen IIIa–VIIa
und IIIb–Vb
im Periodensystem der Elemente in α-Aluminiumoxid enthält, und
der Katalysator, der einen derartigen Träger verwendet, ergibt eine
hohe Selektivität
und eine lange Betriebsdauer. Ferner offenbart U.S.-A- 5.100.859 einen Träger, umfassend
ein α-Aluminiumoxid
hoher Reinheit, ein Erdalkalimetalloxid, ein Siliziumoxid und Zirkonoxid,
und der einen derartigen Träger
verwendende Katalysator ergibt eine hohe Anfangsselektivität und eine
lange Betriebsdauer.
-
Andererseits
wurden ein Träger
für einen
Katalysator, der an der Oberfläche
von α-Aluminiumoxid
mit einer Überzugsschicht
aus amorpher Kieselsäure
versehen ist, und für
die Herstellung von Ethylenoxid verwendet wird (US-A-5.077.256)
verwendet wird, und ein Träger
für einen
an der Oberfläche
von α-Aluminiumoxid
mit einer Überzugsschicht
aus amorphem Siliziumaluminiumoxid, und der zur Herstellung von
Ethylenoxid verwendet wird (US-A-5.395.812), bekannt. Diese Patentveröffentlichungen
legen jedoch weder irgendetwas im Zusammenhang mit einem Aluminium,
Silicium und Titan enthaltenden, eine Azidität aufweisenden Keramikartikel
nahe, noch schlägt
sie irgendetwas im Zusammenhang mit einem Verfahren zur Herstellung
des Keramikartikels vor.
-
Weitere
Dokumente, die sich mit Katalysatorträgern, welche Aluminiumoxid,
Siliziumdioxid und Titandioxid umfassen, befassen, sind
GB 1602777 , WO 97/46317,
WO 99/39825 und
US 4.483.944 .
-
GB 1602777 befasst sich
mit einem Hydrosol und einem hieraus erhaltenen Crackkatalysator.
Es wurde gefunden, dass ein Titandioxid-Aluminiumoxid-Siliziumdioxid-Hydrosol,
das besonders brauchbar für
die Herstellung von gebundenen Ton-/Zeolit-Katalysatorzusammensetzungen
brauchbar ist, hergestellt werden kann, indem man gemischte Säuresalzlösungen von
Titan und Aluminium mit Alkalimetallsilicatlösungen unter Bildung von Hydrosolen
mit einem pH-Wert von 2,5 bis 3,5 herstellen kann. Die Gewichtsbereiche
von Titandioxid, Aluminiumoxid, Siliziumdioxid und Wasser im Hydrosol
pro Gewichtsteil SiO
2 sind: H
2O
= 6–25
Teile pro Teil SiO
2, TiO
2 =
0,01–0,12
Teile und Al
2O
3 =
0,01–0,15
Teile. Wenn das Hydrosolbindemittel in ein getrocknetes Gelprodukt übergeführt wird,
enthält
es folgende Menge an SiO
2, TiO
2 und
Al
2O
3, ausgedrückt als
Gew.% auf Trockenbasis: SiO
2 = 78–98, TiO
2 = 1–10
und Al
2O
3 = 1–12.
-
WO
97/463127 betrifft einen Epoxidierungskatalysator, der Silber, einen
oder mehrere Alkalimetallpromotoren, gegebenenfalls Rhenium als
Co-Promotor, getragen auf einem α-Aluminiumoxidträger, bei
dem ein kalzinierter Trägerkörper mit
einer Titandioxidquelle in einem flüssigen Medium imprägniert wird,
das beim Erhitzen Titandioxid liefert und sodann vorzugsweise bei
400–700°C 30–60 Minuten
kalziniert wird, um im Träger gleichmäßig dispergiertes
Titandioxid in einer Menge von bis zu 10 Gew.%, bezogen auf das
Gesamtgewicht des Trägers,
dispergiert ist, zu erzeugen.
-
WO
99/39825 befasst sich mit Träger
für Fischer-Tropsch-Katalysatoren
mit erhöhter
Festigkeit und Abriebbeständigkeit,
die durch Einarbeitung von sowohl Siliziumdioxid als auch Aluminiumoxid
in einen Träger gebildet
werden, der in erster Linie Titandioxid umfasst. Der Träger kann
mit aktiven Fischer-Tropsch-Metallen vermischt sein. Der Katalysator
ist insbesondere bei Aufschlämmungsreaktionen
brauchbar.
-
US 4.483.944 richtet sich
auf die Herstellung gesinterter Keramikartikel, wobei Aluminiumtitanat
und Mullit die vorherrschenden Kristallphasen bilden und wobei deren
Mikrostruktur die Korngrenze und das intrakristalline Mikrospalten
offensichtlich macht. Die Gegenstände haben Basiszusammensetzungen,
denen 0,5–5%
Fe
2O
3 und/oder 0,5–5% ein
Seltene-Erden-Metalloxid zugegeben werden können.
-
In
der Regel werden Keramikartikel, welche saure Punkte aufweisen,
als dynamische und statische Schaufel einer Gasturbine und eine
Verbrennungskammer einer Kolbenkraftmaschine als Konstruktionsmaterial
zum Sprühen
auf eine Turbinenschaufel oder ein Korn als thermisches Isoliermaterial
und für
ein thermisches Absorptionsmaterial unter Gebrauchmachen deren Azidität verwendet,
jedoch werden sie in ihrer chemischen Anwendung als Katalysator
oder Träger
zur Ver wendung bei Katalysatoren benutzt, welche für verschiedene
Oxidationen, Reduktionen, Additionen und Zersetzungen brauchbar
sind. Es ist erforderlich, dass sie eine hohe thermische Stabilität bei allen
diesen Anwendungen besitzen, und sie leiten große wirtschaftliche Wirkungen
aus der hohen thermischen Stabilität ab. Es wird vorhergesagt,
dass eine Hochtemperatur-Wärmebehandlung
ausreicht, um derartigen Trägern
eine hohe thermische Stabilität
und mechanische Festigkeit zu verleihen. Tatsache ist ebenfalls,
dass die bei einer hohen Temperatur durchgeführte Wärmebehandlung derartige Träger ihrer
sauren Punkte beraubt.
-
Ein
Ziel vorliegender Erfindung ist deshalb die Bereitstellung eines
neuen Keramikartikels, eines Trägers
für einen
Katalysator, Verfahren zu deren Herstellung, eines Katalysators
zur Herstellung von Ethylenoxid unter Verwendung des Trägers sowie
eines Verfahrens zur Herstellung von Ethylenoxid. Ein anderes Ziel
vorliegender Erfindung ist die Bereitstellung eines bei hoher Temperatur
kalzinierten Keramikartikels, der mit hoher thermischer Stabilität und sauren
Punkten ausgestattet ist, eines Trägers für einen Katalysator, eines
Verfahrens zu dessen Herstellung, eines Katalysators zur Herstellung
von Ethylenoxid unter Verwendung des Trägers sowie eines Verfahrens
zur Herstellung von Ethylenoxid.
-
Ein
weiteres Ziel vorliegender Erfindung ist die Bereitstellung eines
Katalysators zur Herstellung von Ethylenoxid, der sich durch seine
Katalysatorleistung, d.h., Aktivität, Selektivität und Betriebsdauer,
auszeichnet, sowie eines Verfahrens zur Herstellung von Ethylenoxids
unter Verwendung eines derartigen Katalysators.
-
ZUSAMMENFASSUNG
DER ERFINDUNG
-
Diese
Ziele werden durch folgende Punkte (1) bis (15) erreicht:
- (1) ein Keramikartikel mit einem Gehalt an
Aluminium, Silizium und Titan in einer Gesamtmenge von mindestens
99 Gew.%, zurückgeführt auf
die Oxide (Al2O3 +
SiO2 + TiO2) und
der in Methylrot, einem Indikator mit einem pKa-Wert von + 4,8, eine
Säurefarbe
annimmt, wobei der Aluminiumgehalt im Bereich von 70,0 bis 99,5
Gew.%, berechnet als Al2O3,
liegt, der Siliziumgehalt im Bereich von 0,06–12 Gew.%, berechnet als SiO2 liegt, und der Titangehalt im Bereich von
0,08–30
Gew.%, berechnet als TiO2, liegt, welcher
durch Kalzinieren eines eine Aluminiumverbindung, Siliziumverbindung
und Titanverbindung enthaltenden Gemischs bei einer Temperatur im
Bereich von 1.000°–2000°C erhältlich ist;
- (2) ein Verfahren zur Herstellung eines Keramikartikels mit
einem Gehalt an Aluminium, Silizium und Titan in einer Gesamtmenge
von mindestens 99 Gew.%, zurückgeführt auf
die Oxide (Al2O3 +
SiO2 + TiO2), der in
Methylrot, einem Indikator eines pKa-Werts von + 4,8, eine Säurefarbe
annimmt, wobei der Aluminiumgehalt im Bereich von 70,0–99,5 Gew.%,
berechnet als Al2O3,
der Siliziumgehalt im Bereich von 0,06–12 Gew.%, berechnet als SiO2, und der Titangehalt im Bereich von 0,08–30 Gew.%,
berechnet als TiO2 liegt, wobei das Verfahren
das Kalzinieren eines eine Aluminiumverbindung, eine Siliziumverbindung
und eine Titanverbindung enthaltenden Gemischs bei einer Temperatur
im Bereich von 1.000°–2.000°C umfasst;
- (3) ein in (2) oben, dargelegtes Verfahren, bei dem die Aluminiumverbindung α-Aluminiumoxid
ist;
- (4) ein in (2) oder (3), oben, dargelegtes Verfahren, bei dem
die Siliziumverbindung und die Titanverbindung Verbindungen sind,
welche einer Bildung einer amorphen Schicht von Siliziumdioxid und
Titandioxid durch ein Kalzinieren zusammen fähig sind;
- (5) ein in (3), oben, dargelegtes Verfahren, bei dem das α-Aluminiumoxid
einen Aluminiumkristalldurchmesser im Bereich von 0,1 bis 5 μm, einen
Teilchendurchmesser im Bereich von 50–100 μm und eine spezifische BET-Oberfläche im Bereich
von 0,1–4
m2/g aufweist;
- (6) ein Träger
für einen
aus einem Formkörper
eines Keramikartikels mit einem Gehalt an Aluminium, Silizium und
Titan in einer Gesamtmenge von mindestens 99 Gew.%, zurückgeführt auf
die Oxide (Al2O3 +
SiO2 + TiO2) gebildeten
Katalysators, der eine Säurefarbe
in Methylrot, einem Indikator eines pKa-Werts von + 4,8 annimmt,
bei dem der Aluminiumgehalt im Bereich von 70,0–99,5 Gew.%, berechnet als
Al2O3, der Siliziumgehalt
im Bereich von 0,06–12
Gew.%, berechnet als SiO2, und der Titangehalt
im Bereich von 0,08–30
Gew.%, berechnet als TiO2, liegen, erhältlich durch
Kalzinieren eines eine Aluminiumverbindung, Siliziumverbindung und
Titanverbindung enthaltenden Gemischs bei einer Temperatur im Bereich
von 1.000°–2.000°C;
- (7) ein Träger,
dargelegt in (6), oben, bei dem der Formkörper in Form von Kugeln, Pellets
oder Ringen vorliegt;
- (8) ein Verfahren zur Herstellung eines Trägers für einen Katalysator mit einem
Gehalt an Aluminium, Silizium und Titan in einer Gesamtmenge von
mindestens 99 Gew.%, zurückgeführt auf
die Oxide Al2O3 +
SiO2 + TiO2), der
in Methylrot, einem Indikator mit einem kPa-Wert von 4,0, eine Säurefarbe
annimmt, bei dem der Aluminiumgehalt im Träger im Bereich von 70,0–99,5 Gew.%,
berechnet als Al2O3,
der Siliziumgehalt in der Keramik im Bereich von 0,06–12 Gew.%,
berechnet als SiO2, und der Titangehalt
im Bereich von 0,08–30
Gew.%, berechnet als TiO2 in der Keramik,
liegen, wobei das Verfahren die Bildung eines Gemischs mit einem
Gehalt an einer Aluminiumverbindung, einer Siliziumverbindung und
einer Titanverbindung angegebener Form und das anschließende Kalzinieren
des geformten Gemischs bei einer Temperatur im Bereich von 1.000° bis 2.000°C umfasst;
- (9) in (8), oben, dargelegtes Verfahren, bei dem die Aluminiumverbindung
ein α-Aluminiumoxid
ist;
- (10) in (8) oder (9), oben, dargelegtes Verfahren, bei dem die
Siliziumverbindung und die Titanverbindung Verbindungen sind, welche
der Bildung einer amorphen Schicht von Siliziumdioxid und Titandioxid
fähig sind,
wenn man sie zusammen kalziniert;
- (11) in (9), oben, dargelegtes Verfahren, bei dem das α-Aluminiumoxid
einen Aluminiumoxidkristalldurchmesser im Bereich von 0,1 bis 5 μm, einen
Teilchendurchmesser im Bereich von 50–100 μm und eine spezifische BET-Oberfläche im Bereich
von 0,1 bis 4 m2/g besitzt;
- (12) ein Katalysator zur Herstellung von Ethylenoxid, welcher
das Ablagern einer Silberkomponente und mindestens eines, aus der
Gruppe ausgewählten
Elements, die aus einem Alkalimetall und einem Erdalkalimetall besteht,
auf einem, in (6) oder (7), oben, dargelegten Träger umfasst;
- (13) ein in (12), oben, dargelegten Katalysator, bei dem das
Alkalimetall Cäsium
ist;
- (14) ein Verfahren zur Herstellung eines Katalysators zur Herstellung
von Etyhlenoxid, das das Ablagern einer Silberkomponente und eines
Reaktionspromotors als Komponente auf dem in (6) oder (7) dargelegten Träger, dessen
Kalzinierung in einer oxidativen Atmosphäre bei einer Temperatur von
150–450°C während 0,1
bis 10 Stunden und sein anschließendes Kalzinieren in einer
Inertgasatmosphäre
bei einer Temperatur von 450° bis
800°C, während 0,1
bis 10 Stunden umfasst;
- (15) ein Verfahren zur Herstellung von Ethylenoxid, welches
die Oxidation von Ethylen in Dampfphase durch einen molekularen
Sauerstoff enthaltendes Gas in Gegenwart des in (12) oder (13),
oben, dargelegten Katalysators, umfasst.
-
Da
der Keramikartikel gemäß vorliegender
Erfindung eine hohe thermische Stabilität und starke saure Punkte besitzt,
ist der aus ihm bestehende Formkörper
als Katalysator oder Träger
für einen
Katalysator, wie bei Oxidationen, Reduktionen, Additionen und Zersetzungen
brauchbar und besitzt eine hervorragende Betriebsdauer sowie Leistung
bei Hochtemperatur-Reaktionen. Ferner ist der Katalysator zur Herstellung
von Ethylenoxid, erhalten unter Verwendung des erfindungsgemäßen Trägers hinsichtlich
seiner Katalysatorleistung, insbesondere seiner Selektivität, hervorragend.
-
ERKLÄRUNG DER
BEVORZUGTEN AUSFÜHRUNGSFORM
-
Der
erfindungsgemäße Keramikartikel
wird, wie zuvor beschrieben, erhalten, indem man ein Gemisch mit
einem Gehalt an einer Aluminium-, Silizium Titanverbindung bei einer
Temperatur im Bereich von 1.000° bis
2.000°C
erhalten.
-
Als
typische Beispiele für
die bei vorliegender Erfindung zu verwendende Aluminiumverbindung
können α-Aluminiumoxid, β-Aluminiumoxid
und γ-Aluminiumoxid
genannt werden. Unter anderen, zuvor erwähnten Aluminiumverbindungen
erweist sich α-Aluminiumoxid
als besonders vorteilhaft. Das α-Aluminiumoxid selbst
braucht nicht besonders beschränkt
zu werden. Es kann irgendeine von derartigen Verbindungen sein, wie
sie allgemein als α-Aluminiumoxid
verwendet werden. Besonders bevorzugt wird, dass es einen Alkalimetallgehalt
im Bereich von 1 bis 70 mMol, insbesondere im Bereich von 2–3 mMol,
pro kg besitzt (in vorliegender Erfindung ausgedrückt als
1–70 mMol/kg
(α-Aluminiumoxidpulver).
Wenn das Endprodukt darunter leidet, dass Aluminiumoxid hierin in
einer Menge von nicht weniger als 99,5 Gew.%, vorliegt, zeigt es
saure Punkte nur mit Schwierigkeit. Zweckmäßigerweise liegt der Aluminiumgehalt
im Endprodukt im Bereich von 70,0–99,5 Gew.%, vorzugsweise 80,0–99,0 Gew.%,
bevorzugter im Bereich von 90,0–98,5
Gew.%.
-
Damit
es bei vorliegender Erfindung wirksam verwendet wird, besitzt das α-Aluminiumoxid einen
Aluminiumoxidkristalldurchmesser (mittlerer Primärteilchendurchmesser) im Bereich
von 0,1 bis 5 μm,
vorzugsweise 0,5 bis 4 μm,
einen Teilchendurchmesser (mittlerer sekundärer Teilchendurchmesser) im
Bereich von 30–100 μm, vorzugsweise
50–80 μm, ferner
eine spezifische BET-Oberfläche
im Bereich von 0,1–4
m2/g, vorzugsweise 0,5–3,0 m2/g,
und überdies
einen Koeffizienten der linearen Kontraktion durch zweistündige Kalzinierung
bei 1.700°C
im Bereich von 12–20%.
Der Ausdruck „Koeffizient" der linearen Kontraktion
durch zweistündige
Kalzinierung bei 1.700°C", der im vorliegenden
benutzt wird, bedeutet den Koeffizienten der linearen Kontraktion,
der erhalten wird, wenn eine Probe, die aus dem Pulverisieren von α-Aluminiumoxid
auf eine Größe von α-Kristallen
(Primärteilchen),
Formgebung der Probe unter einem Druck von 1 Tonne/cm2 und
Kalzinieren des Formkörpers
bei 1.700°C
während
2 Stunden erhalten wird.
-
Der
erfindungsgemäße Keramikartikel
enthält
Aluminium, Silizium und Titan in einer Gesamtmenge von mindestens
99 Gew.%, zurückgeführt auf
die Oxide (Al2O3 +
SiO2 + TiO2), vorzugsweise
mindestens 99,5 Gew.%. Er wird beispielsweise erhalten, indem man α-Aluminiumoxid
mit zuvor erwähntem
geringen Alkalimetallgehalt mit einer Titanverbindung und einer
Siliziumverbindung zusammen mit einem organischen Bindemittel und
einem Porenbildungsmittel, die normalerweise benutzt werden, vermischt,
und das erhaltene Gemisch bei einer Temperatur im Bereich von 1.000° bis 2.000°C kalziniert.
Es wird angenommen, dass dieser Kalzinierungsarbeitsgang auf der äußeren Oberfläche von α-Aluminiumoxid
und der inneren Oberfläche
von dessen Poren eine amorphe Siliziumdioxid-Titandioxid-Überzugsschicht
bildet.
-
Eine
der Eigenschaften vorliegender Erfindung beruht auf der Bildung
einer derartigen amorphen Siliziumdioxid-Titandioxid-Überzugsschicht
auf der Oberfläche
des α-Aluminiumoxids
und das anschließende Äußern von
starken Säurepunkten,
die offensichtlich in der Überzugsschicht
ihren Ursprung haben. Die Säurestärke kann
leicht nach einem Verfahren bestimmt werden, das auf Seite 161 ff.
in der Monographie „Acid-Base Catalysts" von Koho Tanabe
und Tsuneichi Takeshita, veröffentlicht
von Sangyo Tosho K.K. am 26. April 1966 beschrieben ist. Der erfindungsgemäße Keramikartikel
enthält
Aluminium, Silizium und Titan und besitzt ein Gesamtgehalt an Aluminiumoxid
(Al2O3), Siliziumdioxid
(SiO2) und Titandioxid (TiO2)
von mindestens 99 Gew.% und nimmt eine Säurefarbe in Methylrot als Indikator
mit einem pKa-Wert von + 4,8 an. Ferner wird es durch Regulieren
der Zusammensetzung und Herstellungsbedingungen des Keramikartikels
möglich
gemacht, einen Keramikartikel vom Typ Aluminiumoxid-Siliziumdioxid-Titandioxid
herzustellen, der eine Farbe in Phenylazonaphthylamin, einem Indikator
mit einem pKa-Wert von + 4,0, p-Dimethylaminoazobenzol, einem Indikator
mit einem pKa-Wert von + 3,3, 2-Amino-5-azotoluol,
einem Indikator mit einem pKa-Wert von + 2,0 oder sogar Dicinnamalaceton,
einem Indikator mit einem kPa-Wert von – 3,0, annimmt. Es ist zu erwarten,
dass dieser Keramikartikel vom Typ Aluminiumoxid-Siliziumdioxid-Titandioxid
bei verschiedenen Anwendungen Brauchbarkeit findet, je nach der
Säurestärke und
der Säuremenge.
Insbesondere ist es möglich,
einen Träger herzustellen,
der starke Säurepunkte
besitzt und eine Farbe bei einem pKa-Wert von + 2,0 oder – 3,0 annimmt, und
der Träger,
welcher diese Eigenschaften besitzt, ist für einen Katalysator geeignet,
welcher zur Herstellung von Ethylenoxid beabsichtigt ist.
-
Als
die zuvor erwähnte
Titanverbindung kann irgendeine der Titanverbindungen verwendet
werden, solange sie der Bildung einer amorphen Siliziumdioxid-Titandioxid-Schicht
durch Kalzinierung zusammen mit einer Siliziumverbindung fähig ist,
welche nachfolgend genauer beschrieben wird. Als typische Beispiele
für die
Titanverbindung können
Titanhydrat und Titanoxide (Anatas, Rutil und eine amorphe Form)
genannt werden. Diese Titanverbindungen können entweder allein oder in
Form von zwei oder mehreren Verbindungen verwendet werden. Sie können in
Form von Syntheseprodukten oder natürlichen Produkten benutzt werden. Die
Titanverbindung braucht nicht besonders in Anbetracht des Aggregatzustands
unterschieden werden. Sie kann in das Gemisch in irgendeinem beliebigen
Zustand, wie z. B. einem Pulver, Sol oder einer wässerigen Lösung eingearbeitet
werden. Wenn die Titanverbindung im Zustand eines Pulvers vorliegt,
hat sie zweckmäßigerweise
einen Teilchendurchmesser im Bereich von 1–300 nm, vorzugsweise im Bereich
von 1–20
nm. Unter anderen Titanverbindungen wird besonders vorteilhaft kolloidales
Titandioxid mit einem Teilchendurchmesser im Bereich von 1–300 nm,
vorzugsweise 1–20
nm, verwendet. Unter dem Gesichtspunkt einer Leichtigkeit der Dispersion
wird bevorzugt, dass dieses kolloidale Titandioxid in Form von einem
Titandioxidsol verwendet wird. Dieses Titandioxidsol kann beispielsweise
nach einem Verfahren erhalten werden, welches das Hydrolysieren
eines Titansalzes oder einem Verfahren erhalten werden, welches
das Neutralisieren einer wässerigen Titansalzlösung mit
einem Alkali umfasst, wodurch sich vorläufig ein Gel bildet und sodann
das Gel peptisiert wird.
-
Damit
die zuvor erwähnte
Siliziumverbindung im vorliegenden wirksam verwendet wird, ist es
lediglich erforderlich, dass sie der Bildung eines amorphen Siliziumdioxid-Titandioxids
beim Kalzinieren zusammen mit einer Aluminiumverbindung und einer
Titanverbindung fähig
ist. Als typische Beispiele für
die Siliziumverbindung können
Kieselsäure,
Feldspat, Ton, Siliziumnitrit, Siliziumcarbid, Silan und Silicate
genannt werden. Daneben sind auch solche Aluminosilicate als Siliziumdioxid-Aluminiumoxid
sowie Mullit brauchbar. Diese Siliziumverbindungen können entweder
allein oder in Form von zwei oder mehreren Verbindungen verwendet
werden. Sie können
in Form von synthetischen oder natürlichen Produkten benutzt werden.
Die Siliziumverbindung braucht nicht in Anbetracht des Aggregatzustands
besonders unterschieden werden. Sie kann in das Gemisch in einem
beliebigen Zustand eingearbeitet werden, beispielsweise als Pulver,
Sol oder wässerige
Lösung.
Wenn die Siliziumverbindung im Zustand eines Pulvers vorliegt, hat
sie zweckmäßigerweise
einen Teilchendurchmesser im Bereich von 1–300 nm, vorzugsweise im Bereich
von 1–20
nm. Unter anderen Siliziumverbindungen wird besonders vorteilhaft
kolloidale Kieselsäure
mit einem Teilchendurchmesser im Bereich von 1–300 nm, vorzugsweise 1–20 nm verwendet.
Infolge hoher Dispergierbarkeit wird bevorzugt, dass diese kolloidale
Kieselsäure
in Form einer wässerigen
Lösung
verwendet wird. Diese kolloidale Kieselsäure kann z. B. nach einem Verfahren
erhalten werden, welches das Neutralisieren einer wässerigen
Natriumsilikatlösung
mit einer Säure
umfasst, wodurch sich ein Gel vorläufig bildet, wonach sodann
das Gel peptisiert wird, oder nach einem Verfahren, welches einer
wässerigen
Natriumsilikatlösung
mittels Ionenaustausch Natrium entzieht.
-
Als
zuvor erwähntes
organisches Bindemittel können
irgendwelche organische Bindemittel verwendet werden, welche allgemein
bei der Herstellung von irgendwelchen üblichen Keramikartikeln, insbesondere
Träger,
benutzt werden können.
Als typische Beispiele für
das organische Bindemittel können
Gummiarabicum, Polyvinylalkohol, Hydroxyethylcellulose, Methylcellulose,
Carboxymethylcellulose und Maisstärke angegeben werden. Unter
anderen organischen Bindemitteln, die zuvor erwähnt wurden, können besonders
vorteilhaft im Hinblick auf die Tatsache Methylcellulose und Maisstärke verwendet
werden, dass sie zu Aschen lediglich in einer geringen Menge nach
der Kalzinierungsstufe führen.
Der Siliziumgehalt in dem neuen Keramikartikel oder Träger gemäß vorliegender
Erfindung liegt im Bereich von 0,06–12 Gew.%, berechnet als SiO2 des Keramikartikels oder Trägers. Der
Siliziumgehalt in dem Keramikartikel oder dem Träger liegt vorzugsweise im Bereich
von 0,6–6
Gew.%, bevorzugter im Bereich von 1,2–3 Gew.%.
-
Die
Gesamtmenge des Aluminiums, Siliziums und Titans, berechnet als
Al2O3, SiO2 und TiO2 beträgt mindestens
99 Gew.%.
-
Der
Titangehalt liegt im Bereich von 0,08–30 Gew.%, berechnet als TiO2 des Keramikartikels oder Trägers. Der
Titangehalt in dem Keramikartikel oder Träger liegt vorzugsweise im Bereich
von 0,8–25
Gew.%, bevorzugter im Bereich von 1,6–16 Gew.%. Der Silizium- und
Titangehalt in dem Keramikartikel oder Träger kann aus den Ergebnissen
der Fluoreszenz-Röntgenstrahlenbeugungsanalyse
des Keramikartikels für
die Zusammensetzung berechnet werden.
-
Die
Mengen der Aluminiumverbindung, Siliziumverbindung und Titanverbindung,
die bei der Herstellung des neuen Keramikartikels gemäß vorliegender
Erfindung zu verwenden sind, können
zweckmäßigerweise
so entschieden werden, dass die Gehalte an Aluminium, Silizium und
Titan im hergestellten Keramikartikel in die jeweiligen, zuvor genannten
Bereiche fallen. Zweckmäßigerweise
liegt das Verhältnis
Ti/Si im Bereich von 0,005–20,
vorzugsweise 0,5–10,
bevorzugter 3–6.
Die zu verwendende Menge des organischen Bindemittels braucht nicht
besonders beschränkt
werden, sie kann aber zweckmäßigerweise
ausgewählt
werden, um dem Verwendungszweck optimal zu entsprechen.
-
Das
Verfahren zur Herstellung des neuen Keramikartikels gemäß vorliegender
Erfindung braucht nicht besonders unterschieden werden. Beispielsweise
kann die Herstellung erreicht werden, indem man eine Aluminiumverbindung,
eine Siliziumverbindung, eine Titanverbindung und ein organisches
Bindemittel vermischt, das erhaltene Gemisch formt, und sodann das
geformte Gemisch bei einer Temperatur im Bereich von 1.000°–2.000°C kalziniert.
Um genauer zu sein: Das Verfahren umfasst die Zugabe einer Siliziumverbindung, einer
Titanverbindung und eines organischen Bindemittels zu α-Aluminiumoxid,
gegebenenfalls die Zugabe von Wasser und sorgfältiges Vermischen derselben
unter Anwendung einer Mischvorrichtung, wie einem Kneter, die anschließende Extrusionsformung
des erhaltenen Gemischs, das Granulieren des geformten Gemischs,
das Trocknen der Granalien und das Kalzinieren der trockenen Granalien
bei einer Temperatur im Bereich von 1.000°–2.000°C, vorzugsweise 1.200°–1.700°C, bevorzugter
1.300°–1.600°C. Obgleich
die Extrusionsformung in einer trockenen oder einer feuchten Form
bewirkt werden kann, wird sie in der Regel in einer feuchten Form
durchgeführt.
Der Arbeitsgang des zuvor genannten Trocknens wird in der Regel
bei einer Temperatur im Bereich von 80°–900°C durchgeführt. Gelegentlich kann er weggelassen
werden.
-
Das
organische Bindemittel kann zusammen mit einem Porenbildungsmittel,
wie z. B. einem Pulver, erhalten durch Pulverisieren von Schalen
und Samen von Pfirsichen, Aprikosen und Walnüssen auf einen gleichmäßigen Teilchendurchmesser
oder einer Substanz erhalten werden, welche einen gleichmäßigen Teilchendurchmesser
hat, und die Fähigkeit
besitzt, beim Kalzinieren zu verschwinden.
-
Der
erfindungsgemäße Keramikartikel
wird in Anbetracht seiner ihm eigenen chemischen Eigenschaft vorteilhafterweise
als Katalysator oder Träger
für einen
Katalysator verwendet. Wenn er als Katalysator oder Träger für einen
Katalysator verwendet wird, braucht er nicht besonders hinsichtlich
seiner Form begrenzt werden.
-
In
der Regel wird er in solch einer granularen Form, wie Kugeln, Pellets
und Ringen benutzt. Hinsichtlich seiner Größe hat er einen mittleren Äquivalentdurchmesser
in der Regel im Bereich von 3–20
nm, vorzugsweise 5–10
nm.
-
Im
Speziellen wird aus dem zuvor erwähnten Keramikartikel ein Träger für einen
Katalysator durch Formung des Keramikartikels in die zuvor genannte
Form vor der Stufe der Kalzinierung und Kalzinierung des hergestellten
geformten Gegenstands unter den zuvor genannten Bedingungen erhalten.
Der derart erhaltene Träger
wird vorteilhafterweise besonders für einen Silberkatalysator benutzt,
auf dem Silber und ein Alkalimetalloxid abgelagert sind, und zur
Herstellung von Ethylenoxid durch Oxidation von Ethylen mit einem
molekularen Sauerstoff enthaltenden Gas verwendet.
-
Die
spezifische Oberfläche
des Trägers,
welche bei vorliegender Erfindung in Betracht gezogen wird, liegt
in der Regel im Bereich von 0,03–10 m2/g,
vorzugsweise 0,1–5
m2/g, bevorzugter 0,3–2 m2/g.
Wenn die spezifische Oberfläche übermäßig gering
ist, zeigt die Verringerung den Nachteil, dass sie darunter leidet,
dass die Sinterung übermäßig fortschreitet
und dass ein Verleihen eines befriedigenden Koeffizienten der Wasserabsorption
dem Träger
verhindert wird, und eine Ablagerung einer Katalysatorkomponente
auf dem Träger schwierig
gemacht wird.
-
Umgekehrt
bringt, wenn die spezifische Oberfläche übermäßig groß ist, der Überschuss den Nachteil einer
Verringerung des Porendurchmessers und eine Beschleunigung der nachfolgenden
Oxidation des hergestellten Ethylenoxids. Der Koeffizient der Wasserabsorption
liegt in der Regel im Bereich von 10–70%, vorzugsweise 20–60%, bevorzugter
30–50%.
Wenn der Koeffizient der Wasserabsorption übermäßig gering ist, bringt der
Unterschuss den Nachteil mit sich, dass die Ablagerung einer Katalysatorkomponente
schwierig wird. Umgekehrt bringt, wenn er übermäßig hoch ist, der Überschuss
den Nachteil mit sich, dass ein Erreichen einer ausreichenden Druckfestigkeit
unmöglich
wird. Der mittlere Porendurchmesser liegt in der Regel im Bereich
von 0,1 bis 5 μm,
vorzugsweise 0,2 bis 3 μm,
bevorzugter 0,3 bis 0,9 μm.
Wenn der mittlere Porendurchmesser übermäßig groß ist, bringt der Überschuss
den Nachteil einer Verringerung der Aktivität mit sich. Umgekehrt bringt,
wenn er übermäßig gering
ist, der Unterschuss den Nachteil mit sich, dass ein Gasstillstand bewirkt
und eine nachfolgende Oxidation des hergestellten Ethylenoxids gefördert wird.
Die Porosität
liegt in der Regel im Bereich von 40–80%, vorzugsweise 50–70%. Wenn
die Porosität übermäßig gering
ist, bringt der Unterschuss den Nachteil mit sich, dass das spezifische
Gewicht des Trägers übermäßig groß wird.
Wenn er übermäßig hoch
ist, bringt der Überschuss
den Nachteil mit sich, dass der Träger daran gehindert wird, eine befriedigende
Druckfestigkeit zu erreichen.
-
Der
Katalysator zur Herstellung von Ethylenoxid gemäß vorliegender Erfindung kann
nach einem allgemeinen Verfahren gebildet werden, welches beim Katalysator
zur Herstellung von Ethylenoxid mit Ausnahme des zuvor genannten
Trägers
angewandt wird. Die auf dem Träger
niedergeschlagene Katalysatorkomponente kann Silber allein oder
in Kombination von Silber mit einem Reaktionspromotor wie Cäsium sein.
-
Die „Ablagerungen
einer Silberkomponente" vorliegender
Erfindung sind Ablagerungen von Silber, zusätzlich zur Ausführungsform
der Ablagerung von Silber und eines Reaktionspromotors.
-
Typischerweise
wird beispielsweise eine Silberverbindung allein zur Bildung von
Silber, die Silberverbindung, ein Komplexierungsmittel für die Bildung
eines Silberkomplexes oder ferner eine wässerige Lösung mit einem Gehalt an dem
Reaktionspromotor erforderlichenfalls hergestellt, und nach Imprägnieren
des Trägers
damit, getrocknet und kalziniert. Das Trocknen wird vorzugsweise
in Luft, Sauerstoffgas oder einer Inertgasatmosphäre wie Stickstoffgas
bei einer Temperatur von 80° bis
120°C durchgeführt. Das
Kalzinieren wird vorzugsweise in Luft, Sauerstoffgas oder einer
Inertgasatmosphäre
bei einer Temperatur von 150°C
bis 800°C vorgenommen.
Ferner können
die Kalzinierungen in einer Stufe oder in zwei oder mehreren Stufen
durchgeführt
werden. Unter diesen wird es bevorzugt, dass die erste Stufe in
einer oxidieren Atmosphäre
wie Luft bei einer Temperatur von 150° bis 250°C während 0,1 bis 10 Stunden, und
die zweite Stufe in einer oxidierenden Atmosphäre wie Luft bei einer Temperatur
von 250° bis
450°C während 0,1
bis 10 Stunden durchgeführt
werden. Ferner wird die dritte Stufe vorzugsweise in einer aus der
Gruppe ausgewählten
Inertgasatmosphäre
vorgenommen, welche aus Stickstoff, Helium und Argon besteht, und
zwar bei einer Temperatur von 450° bis 800°C während 0,1
bis 10 Stunden. Typische Beispiele für die zuvor erwähnte Silberverbindung
sind Silbernitrat, Silbercarbonat, Silberoxalat, Silberacetat, Silberpropionat,
Silberlactat, Silbercitrat, Silberneodecanat usw.. Als typisches
Beispiel für
das Komplexierungsmittel können
genannt werden: Monoethanolamin, Diethanolamin, Triethanolamin,
Ethylendiamin, Propylendiamin, usw.. Als typischer Reaktionspromotor
können
Alkalimetalle wie Lithium, Natrium, Kalium, Rubidium und Cäsium, ferner
Thallium, Schwefel, Chrom, Molybdän, Wolfram usw. angegeben werden.
Diese können
allein oder als Kombination von zwei oder mehreren Verbindungen
benutzt werden.
-
Als
Katalysator zur Herstellung von Ethylenoxid gemäß vorliegender Erfindung wird
der Katalysator bevorzugt, auf dem Silber und ein Reaktionspromotor
als Katalysatorkomponente abgelagert sind. Als Reaktionspromotor
können
ein Oxid eines Alkalimetalls wie Natrium, Kalium, Cäsium usw.
und ein Oxid eines Erdalkalimetalls wie Barium, Kalzium, Magnesium
usw. genannt werden, und unter diesen wird das Alkalimetall, insbesondere
Cäsium,
bevorzugt. Die aufzubringende Silbermenge beträgt in der Regel 1–30 Gew.%
des Katalysators, vorzugsweise 5 bis 20 Gew.% des Katalysators.
Die aufzutragende Menge des Reaktionspromotors liegt in der Regel
von 0,001 bis 1 Gew.% des Katalysators, vorzugsweise 0,01 bis 0,5
Gew.% des Katalysators, bevorzugter 0,4 bis 0,3 Gew.% des Katalysators.
-
Ethylenoxid
kann durch Oxidation von Ethylen durch ein molekularen Sauerstoff
enthaltendes Gas in Gegenwart des so erhaltenen Katalysators in
Dampfphase erhalten werden.
-
Die
Standardbedingungen, welche bei der Herstellung in kommerziellem
Maßstab
vorherrschen, sind eine Reaktionstemperatur im Bereich von 180° bis 300°C, vorzugsweise
200° bis
260°C, ein
Reaktionsdruck im Bereich von 0,2 bis 4 MPa, vorzugsweise 1,5 bis
4 MPa, sowie eine Raumgeschwindigkeit im Bereich von 1.000 bis 30.000
Stdn.–1 (STP),
vorzugsweise 3.000 bis 8.000 Stdn.–1 (STP).
Hinsichtlich der Zusammensetzung des Beschickungsgases, welches
durch den Katalysator geleitet wird, kann in geeigneter Weise das
Verfahren übernommen
werden, welches 0,5 bis 40 Vol.% Ethylen, 3–10 Vol.% Sauerstoff, 5–30 Vol.%
Kohlendioxidgas, Rest eines solchen Inertgases wie z. B. Stickstoff
oder Argon, und ferner Wasserdampf und ein niederer Kohlenwasserstoff
wie Methan oder Ethan sowie als Reaktionsinhibitor 0,1 bis 10 ppm
(bezogen auf das Volumen) einer organischen Chloridverbindung wie
Ethylendichlorid, Ethylchlorid oder Vinylchlorid benutzt werden.
-
Als
typische Beispiele für
das den molekularen Sauerstoff enthaltende Gas, das bei vorliegender
Erfindung zu verwenden ist, können
Luft, Sauerstoff und angereicherte Luft angegeben werden.
-
Im
Folgenden wird nun vorliegende Erfindung spezieller unter Bezugnahme
auf Arbeitsbeispiele beschrieben.
-
BEISPIEL 1
-
In
einem Kneter wurden 89,5 Gewichtsteile α-Aluminiumoxidpulver (A) (mittlerer
Aluminiumoxidkristalldurchmesser: 1 μm, mittlerer Teilchendurchmesser:
65 μm, spezifische
BET-Oberfläche:
2,2 m2/g, Koeffzient der linearen Kontraktion
durch Kalzinieren bei 1.700°C
während
2 Stunden: 15%, und Natriumgehalt: 16 mMol/kg) 0,5 Gewichtsteile
Kieselsäuresol
mit einem mittleren Teilchendurchmesser im Bereich von 1 bis 20 nm
(zurückgeführt auf
SiO2) (hergestellt von Nissan Chemicals
Industries Ltd. und unter dem Warenzeichen „Snowtex-O" verkauft), 10 Gewichtsteile Titandioxidpulver
(hergestellt von Wako Pure Chemical Industries, Ltd.), 6 Gewichtsteile
Methylcellulose, 6 Gewichtsteile Maisstärke und 30 Gewichtsteile Walnussschalen
(100 bis 170 μm)
sorgfältig
vermischt, und das erhaltene Gemisch wurde weiter mit 40 Gewichtsteilen
zugegebenem Wasser vermischt. Das hergestellte Gemisch wurde zu
einer Ringform extrudiert, getrocknet und bei 1.500°C 2 Stunden
kalziniert, um einen Keramikartikel (A) zu ergeben.
-
Es
wurde gefunden, dass dieser Keramikartikel (A) einen Siliziumgehalt
von 0,5 Gew.%, berechnet als SiO2, und einen
Titangehalt von 10 Gew.%, berechnet als TiO2 hatte.
Die Gesamtzusammensetzung des Keramikartikels war nachgewiesenermaßen 99,9
Gew.%, zurückgeführt auf
Al2O3 + SiO2 + TiO2. Es wurde
gefunden, dass er einen mittleren äquivalenten Durchmesser von
8 mm, eine spezifische BET-Oberfläche von
1,1 m2/g, einen Koeffizienten der Wasserabsorption
von 41 %, einen mittleren Porendurchmesser von 0,7 μm und eine
Porosität
von 61 % hatte. Durch Messung der Säurestärke zeigte er in einem Indikator
mit einem pKa-Wert von + 4,8, einem Indikator mit einem pKa-Wert
von + 4,0 und einem Indikator mit einem pKa-Wert von + 3,3 sowie einem Indikator
mit einem pKa-Wert von + 2,0 Säurefarbe.
Dieser wird im folgenden als Träger
(A) bezeichnet.
-
Der
derart erhaltene Träger
(A) wurde mit siedendem Wasser dreimal gewaschen und getrocknet.
210 g des gewaschenen Trägers
wurden mit einer Komplexlösung
mit einem Gehalt an 57,3 g Silberoxalat, 38,6 ml Monoethanolamin,
41,4 ml Wasser und 0,22 g Cäsiumnitrat
imprägniert
und sodann erwärmt,
konzentriert, abermals bei einer Temperatur von 120°C 40 Minuten
getrocknet und in einem Luftstrom bei einer Temperatur von 170°C 30 Minuten
und einer Temperatur von 270°C
30 Minuten erhitzt, wobei ein Katalysator (a) zur Herstellung von
Ethylenoxid erhalten wurde.
-
BEISPIEL 2
-
In
einem Kneter wurden 93 Gewichtsteile des gleichen α-Aluminiumoxidpulvers
(A), wie im Beispiel 1 verwendet, 1,1 Gewichtsteile (zurückgeführt auf SiO2) des gleichen Kieselsäuresols wie im Beispiel 1 benutzt, 6
Gewichtsteile Titandioxidpulver, 6 Gewichtsteile Methylcellulose
und 6 Gewichtsteile Maisstärke
sorgfältig vermischt,
und das erhaltene Gemisch wurde ferner mit 40 Gewichtsteilen Wasser
vermischt. Das gebildete Gemisch wurde extrudiert, granuliert, getrocknet
und bei 1.400°C
2 Stunden kalziniert, um zu einem Keramikartikel (B) zu führen. Es
wurde gefunden, dass dieser Keramikartikel (B) einen Siliziumgehalt
von 1 Gew.%, berechnet als SiO2, einen Titangehalt
von 6 Gew.%, berechnet als TiO2 und eine
Gesamtzusammensetzung von 99,9 Gew.%, zurückgeführt auf Al2O3 + SiO2 + TiO2 hatte. Ferner wurde gefunden, dass er einen
mittleren äquivalenten
Durchmesser von 8 mm, eine spezifische BET-Oberfläche von
1,6 m2/g, einen Koeffizienten der Wasserabsorption
von 45%, einen mittleren Porendurchmesser von 0,8 μm und eine
Porosität
von 64% hatte.
-
Durch
Messung der Säurestärke wurde
nachgewiesen, dass er eine Säurefarbe
in einem Indikator eines pKa-Werts von + 4,8, einem Indikator mit
einem pKa-Wert von
+ 4,0, einem Indikator eines pKa-Werts von + 3,3 und einem Indikator
eines pKa-Werts von + 2,0 Säurefarbe
zeigte. Im folgenden wird dies auf einen Träger (B) bezogen.
-
Ein
Katalysator (b) zur Herstellung von Ethylenoxid wurde nach dem gleichen
Verfahren wie im Beispiel 1 mit der Ausnahme erhalten, dass der
Träger
(B) verwendet wurde.
-
BEISPIEL 3
-
In
einem Kneter wurden 95 Gewichtsteile des gleichen α-Aluminiumoxidpulvers
A, wie im Beispiel 1 verwendet, 4 Gewichtsteile (zurückgeführt auf
SiO2) des gleichen Kieselsäuresols,
wie im Beispiel 1 verwendet, [sic!] Gewichtsteile Titandioxidpulver,
6 Gewichtsteile Methylcellulose und 6 Gewichtsteile Maisstärke sorgfältig vermischt,
und das erhaltene Gemisch wurde ferner mit 40 Gewichtsteilen Wasser
vermischt. Das erhaltene Gemisch wurde extrudiert, granuliert, getrocknet und
bei 1.550°C
2 Stunden kalziniert, wobei ein Keramikartikel (C) anfiel. Es wurde
gefunden, dass dieser Keramikartikel (C) ein Siliziumgehalt von
4 Gew.%, berechnet als SiO2, ein Titangehalt
von 1 Gew.%, berechnet als TiO2, und eine
Gesamtzusammensetzung von 99,9 Gew.%, zurückgeführt auf Al2O3 + SiO2 + TiO2 hatte. Ferner wurde gefunden, dass er einen
mittleren äquivalenten
Durchmesser von 8 mm, eine spezifische BET-Oberfläche von
0,7 m2/g, einen Koeffizienten der Wasserabsorption
von 38%, einen mittleren Porendurchmesser von 0,6 μm und eine
Porosität
von 58% besaß. Durch
Messung der Säurestärke wurde
nachgewiesen, dass er in einem Indikator mit einem pKa-Wert von
+ 4,8, einem Indikator mit einem pKa-Wert von + 4,0, einem Indikator mit
einem pKa-Wert von + 3,3 und einem Indikator mit einem pKa-Wert
von + 2,0 Säurefarbe
zeigte. Dies ist im folgenden auf einen Träger (C) bezogen.
-
Ein
Katalysator (c) zur Herstellung von Ethylenoxid wurde nach dem gleichen
Verfahren des Beispiels 1 mit der Ausnahme erhalten, dass der Träger (C)
verwendet wurde.
-
BEISPIEL 4
-
In
einem Kneter wurden 93 Gewichtsteile α-Aluminiumoxidpulver (B) (mittlerer
Aluminiumoxid-Kristalldurchmesser: 1 μm, mittlerer Teilchendurchmesser:
65 μm, spezifische
BET-Oberfläche:
0,9 m2/g, Koeffizient der linearen Kontraktion
durch Kalzinieren bei 1.700°C
während
2 Stunden: 15%, und Natriumgehalt: 16 mMol/kg), 1 Gewichtsteil Kieselsäuresol (zurückgeführt auf
SiO2), 4 Gewichtsteile Titandioxidpulver,
6 Gewichtsteile Methylcellulose und 6 Gewichtsteile Maisstärke sorgfältig vermischt
und das erhaltene Gemisch wurde weiter mit 40 Gewichtsteilen zugegebenem
Wasser vermischt. Das erhaltene Gemisch wurde extrudiert, granuliert,
getrocknet und bei 1.600°C
2 Stunden kalziniert, wobei ein Keramikartikel (D) anfiel.
-
Es
wurde gefunden, dass dieser Keramikartikel (D) ein Siliziumgehalt
von 1 Gew.%, berechnet als SiO2, und einen
Titangehalt von 4 Gew.%, berechnet als TiO2 hatte.
Die Gesamtzusammensetzung des Keramikartikels war nachgewiesenermaßen 99,9
Gew.%, zurückgeführt auf
Al2O3 + SiO2 + TiO2. Es wurde
gefunden, dass er einen mittleren äquivalenten Durchmesser von
8 mm, eine spezifische BET-Oberfläche von
0,6 m2/g, einen Koeffizienten der Wasserabsorption
von 34%, einen mittleren Porendurchmesser von 0,5 μm und eine
Porosität
von 56% hatte. Durch Messung der Säurestärke wurde nachgewiesen, dass
er in einem Indikator mit einem pKa-Wert von + 4,8, einem Indikator
mit einem pKa-Wert von + 4,0, einem Indikator mit einem pKa-Wert
von + 3,3 und einem Indikator mit einem pKa-Wert von + 2,0 Säurefarbe
zeigte. Dies ist im folgenden auf einen Träger (D) bezogen.
-
Der
so erhaltene Träger
(D) wurde mit siedendem Wasser dreimal gewaschen und getrocknet.
210 g des gewaschenen Trägers
wurden mit einer Komplexlösung
mit einem Gehalt von 57,3 g Silberoxalat, 38,8 ml Monoethanolamin,
41,4 ml Wasser und 0,81 g Cäsiumnitrat
imprägniert
und sodann erwärmt,
eingeengt, abermals bei einer Temperatur von 120°C 40 Minuten getrocknet und
in einem Luftstrom bei einer Temperatur von 170°C 30 Minuten und bei einer Temperatur
von 270°C
30 Minuten erwärmt,
weiter in einem Stickstoffstrom bei einer Temperatur von 650°C 2 Stunden
kalziniert, wobei ein Katalysator (d) zur Herstellung von Ethylenoxid erhalten
wurde.
-
Kontrolle 1
-
In
einem Kneter wurden 99,6 Gewichtsteile des gleichen α-Aluminiumoxidpulvers
A, wie im Beispiel 1 benutzt, 0,4 Gewichtsteile (berechnet als TiO2)
des gleichen Titandioxidpulvers, wie im Beispiel 1 benutzt, 6 Gewichtsteile
Methylcellulose und 6 Gewichtsteilen Maisstärke sorgfältig vermischt, und das erhaltene
Gemisch wurde weiter mit 40 Gewichtsteilen zugegebenem Wassers vermischt.
Das erhaltene Gemisch wurde extrudiert, granuliert, getrocknet und
bei 1.200°C
2 Stunden kalziniert, wobei ein Keramikartikel (E) erhalten wurde.
Durch Messung der Säurestärke wurde
nachgewiesen, dass er in einem Indikator mit einem pKa-Wert von
+ 4,8, einem Indikator mit einem pKa-Wert von + 4,0, einem Indikator
mit einem pKa-Wert von + 3,3 und einem Indikator mit einem pKa-Wert
von + 2,0 keine Säurefarbe
zeigte. Dies wird im folgenden auf einen Träger (E) bezogen.
-
Ein
Katalysator (e) zur Herstellung von Ethylenoxid wurde nach dem gleichen
Verfahren des Beispiels 1 mit der Ausnahme erhalten, dass der Träger (E)
verwendet wurde.
-
Kontrolle 2
-
In
einem Kneter wurden 97,5 Gewichtsteile des gleichen α-Aluminiumoxidpulvers
A, wie im Beispiel 1 benutzt, 1 Gewichtsteil (berechnet als TiO2) des gleichen Titandioxidpulvers, wie im
Beispiel 1 verwendet, und 12 Gewichtsteile Carboxymethylcellulose
(8 Gew.% berechnet als Na2O) sorgfältig gemischt,
und das erhaltene Gemisch wurde weiter mit 40 Gewichtsteilen zugegebenem
Wasser vermischt. Das erhaltene Gemisch wurde extrudiert, granuliert,
getrocknet und bei 1.100°C
2 Stunden kalziniert, wobei ein Keramikartikel (F) erhalten wurde.
-
Durch
Messung der Säurestärke wurde
nachgewiesen, dass er in einem Indikator mit einem pKa-Wert von
+ 4,8, einem Indikator mit einem pKa-Wert von + 4,0 und einem Indikator
mit einem pKa-Wert von + 3,3 sowie einem Indikator mit einem pKa-Wert
von + 2,0 keine Säurefarbe
zeigte. Dies wird im folgenden auf einen Träger (F) bezogen.
-
Ein
Katalysator (f) zur Herstellung von Ethylenoxid wurde nach dem gleichen
Verfahren des Beispiels 1 mit der Ausnahme erhalten, dass der Träger (F)
verwendet wurde.
-
Kontrolle 3
-
In
einem Kneter wurden 99,9 Gewichtsteile eines α-Aluminiumoxidpulvers (C) (mittleres
Aluminiumkristallteilchen: 3,0 μm,
mittlerer Teilchendurchmesser: 100 μm, spezifische BET-Oberfläche: 0,7
m2/g, Koeffizient der linearen Kontraktion
durch Kalzinieren bei 1.700°C
während
2 Stunden: 13%, und Natriumgehalt: 90 mMol/kg), 0,1 Gewichtsteil
(zurückgeführt auf
SiO2) des gleichen Kieselsäuresols,
wie im Beispiel 1 benutzt, 6 Gewichtsteile Methylcellulose und 6
Gewichtsteile Maisstärke
sorgfältig
vermischt, und das erhaltene Gemisch wurde ferner mit 40 Gewichtsteilen
zugegebenem Wasser vermischt. Das erhaltene Gemisch wurde extrudiert, granuliert,
getrocknet und bei 1.700°C
2 Stunden kalziniert, wobei ein Keramikartikel (G) anfiel. Es wurde
gefunden, dass dieser Keramikartikel (G) einen mittleren äquivalenten
Durchmesser von 8 mm, eine spezifische BET-Oberfläche von
1,0 m2/g, einen Koeffizienten der Wasserabsorption
von 32%, einen mittleren Porendurchmesser von 0,6 μm und eine
Porosität
von 55% hatte.
-
Durch
Messung der Säurestärke wurde
nachgewiesen, dass er in einem Indikator mit einem pKa-Wert von
+ 4,8, einem Indikator mit einem pKa-Wert von + 4,0, einem Indikator
mit einem pKa-Wert von + 3,3 und einem Indikator mit einem pKa-Wert von + 2,0 keine
Säurefarbe
zeigte. Dies wird im folgenden auf einen Träger (G) bezogen.
-
Ein
Katalysator (g) zur Herstellung von Ethylenoxid wurde nach dem gleichen
Verfahren des Beispiels 1 mit der Ausnahme erhalten, dass der Träger (G)
verwendet wurde.
-
BEISPIEL 5
-
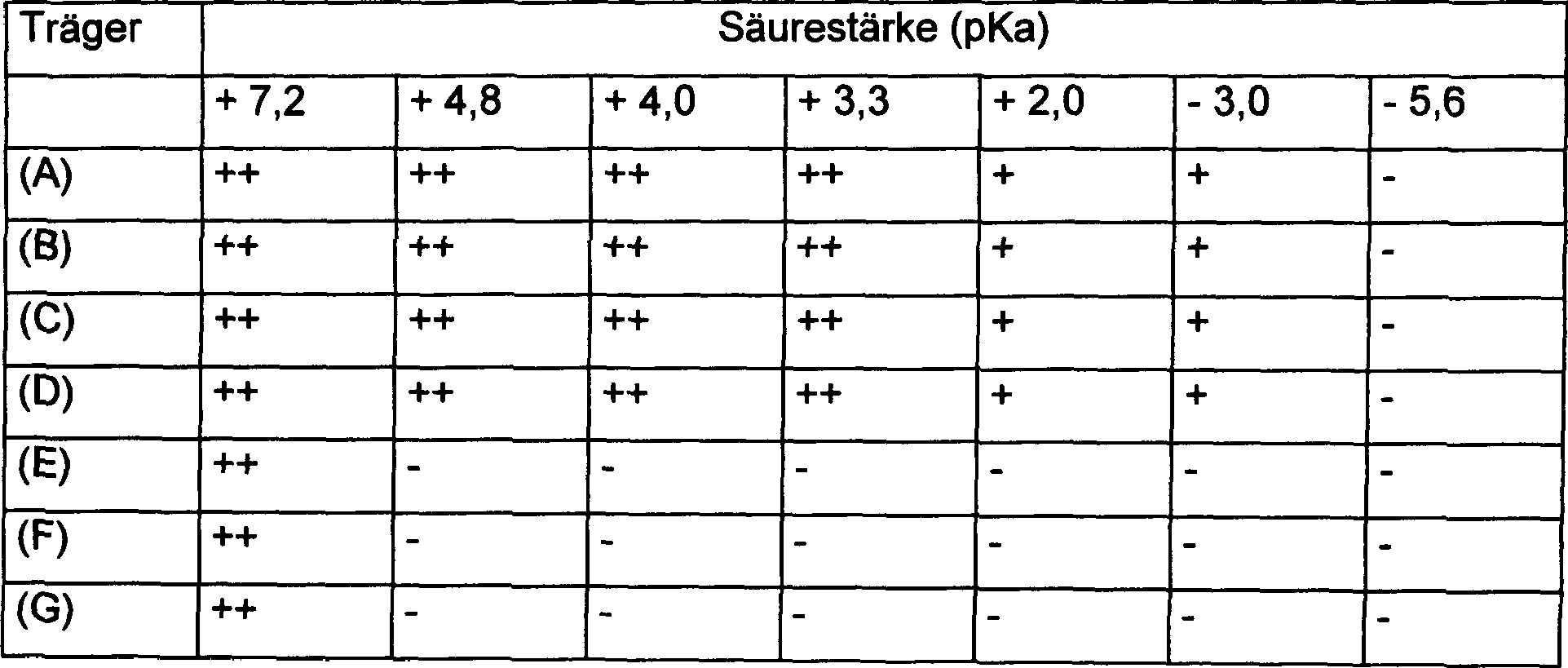
Die
Träger
(A) bis (G) wurden auf ihre Säurestärke in Übereinstimmung
mit dem Verfahren getestet, welches in der Monographie „Acid-Base
Catalysts" von Kozo
Tanabe und Tsuneichi Takeshita gemeinsam geschrieben und veröffentlicht
von Sangyo Tosho K.K. am 26. April 1966 ab Seite 161 beschrieben
ist. Die in dem Test verwendeten Proben waren jeweils durch Sieden
zur Reinigung eines gegebenen kalzinierten Keramikartikels im 10fachen
ihres Eigengewichts gereinigten Wassers während 30 Minuten, zweimalige
Wiederholung dieser Siedebehandlung, anschlie ßendes Trocknen des gereinigten
Keramikartikels bei 120°C
während
18 Stunden, Abkühlenlassen
des getrockneten Artikels auf normale Raumtemperatur, Klassieren
des abgekühlten
Keramikartikels in Größen von
100–200
meshes, Abwiegen eines Teils von 0,1 g des abgetrennten Pulvers in
einer Probeampulle und Trocknen des Anteils in der Ampulle bei 120°C während 5
Stunden hergestellt. Die Ergebnisse des Tests sind in Tabelle 1
gezeigt.
-
-
BEISPIEL 6
-
Die
Katalysatoren (a) bis (g) wurden jeweils pulverisiert und in Größen von
600 bis 850 μm
klassiert. Die Reaktionsrohre aus rostfreiem Stahl mit einem Innendurchmesser
von 3 mm und einer Länge
von 600 mm wurden jeweils mit den demgemäß hergestellten Pulver eines
Gewichts von 1,2 g gepackt und für
die Gasphasenoxidation von Ethylen unter folgenden Bedingungen verwendet.
Wenn der Umwandlungsgrad von Ethylen 10% erreichte, wurden die Selektivität für Ethylenoxid
und die Reaktionstemperatur des Katalysatorbetts gemessen. Die Ergebnisse
sind in Tabelle 2 gezeigt. Reaktionsbedingungen:
| Raumgeschwindigkeit: | 6.150
Stdn.–1 |
| Reaktionsdruck: | 2,1
Mpa |
-
Zusammensetzung
des Ausgangsmaterialgases: Ethylen 20%, Sauerstoff 7,6%, Kohlendioxid
5,7%, Ethylendichlorid 2,2 ppm (Methan, Stickstoff, Argon und Ethan
Rest).
-