-
Diese Erfindung betrifft kosmetische
Zusammensetzungen, die Maulbeerbaum-Extrakt in Kombination mit Retinoiden
enthalten, und Verfahren zur Behandlung der Haut durch die Auftragung
derartiger Zusammensetzungen.
-
Retinol (Vitamin A) ist eine endogene
Verbindung, die natürlich
im menschlichen Körper
vorkommt und für
eine normale Epithelzellen-Differenzierung wesentlich ist. Natürliche und
synthetische Vitamin A-Derivate sind
in großem
Umfang bei der Behandlung einer Vielfalt von Hautstörungen und
als Hautreparatur- und Erneuerungsmittel verwendet worden. Retinoesäure ist
verwendet worden, um eine Vielfalt von Hautzuständen, wie Akne, Falten, Psoriasis,
Altersflecken und Hautverfärbung,
zu behandeln.
-
Innerhalb der Zellen sind Retinol
und Retinoesäure
an spezielle zelluläre
Bindungsproteine gebunden, wobei zwei der Hauptproteine CRABP-1
und CRABP-2 sind (Roos et al., Pharmacological Reviews: 50, 315–333, 1998).
Diese Proteine wirken bei der Regulierung der intrazellulären Konzentration
von Retinoiden, indem sie sowohl als Speicher- als auch als Shuttle-Proteine
im Retinoid-Metabolismus wirken. Die Mengen dieses Proteins werden
durch die Menge an Retinoesäure
innerhalb der Zellen reguliert. Höhere zelluläre Konzentrationen an Retinoiden
erhöhen
die Expression von CRABP-2. Deshalb ist die Menge dieses Proteins
in den Zellen ein Maß der
Retinoid-Aktivität
der Zellen. Hautzellen enthalten CRABP-2 sowohl in der Epidermis als
auch in der Dermis. Die CRABP-2-Antwort auf eine Retinoid-Verabreichung in
Fibroblasten in vitro wird als reproduzierbares Maß der Retinoid-Bioaktivität verwendet,
welches menschliche Hautantworten voraussagt (Elder et al., J. Invest.
Dermatol., 106: 517–521,
1996). Deshalb ist die CRABP-2-Expression von Fibroblasten ein Maß der Retinoid-Aktivität, die zu
verschiedenen kosmetischen Vorteilen für die Haut (Alterungshemmung, Faltenbildungshemmung,
Hautkonditionierung usw.) führt.
-
Kosmetische Zusammensetzungen, die
Maulbeerbaum und Retinoide enthalten, sind in der Technik bekannt.
Siehe z. B. die
EP 815838 (Shiseido),
EP 887070 (Kibun Food Chemifa
Co.),
US 5,676,948 ,
US 5,676,949 und
US 5,607,692 . Die
US 5332575 beschreibt ein
Verfahren zum Anzielen von Melanocyten mit einer Verbindung, die
einen Fucose-Rest enthält,
um das Produkt an die Melanocyten-Membran zu binden. Als Beispiel wird
eine kosmetische Zusammensetzung angeführt, die einen Extrakt von
trockener Maulbeerbaum-Wurzelrinde in einer Konzentration von 0,5%
enthält.
In einem weiteren Beispiel wird beta-Carotin oder 0,25% Vitamin
A-Propionat verwendet.
-
Die vorliegende Erfindung beruht
auf der Entdeckung, daß Maulbeerbaum-Extrakt
in Kombination mit ausgewählten
Retinoiden eine Synergie zeigt, wenn sie innerhalb eines speziellen
Verhältnisbereiches
kombiniert werden.
-
Die vorliegende Erfindung schließt eine
kosmetische Hautpflege-Zusammensetzung ein, welche umfasst:
- (i) einen glycolischen Extrakt von Maulbeerbaum-Wurzel
in einer Menge von 0,00001 bis 10 Gew.-%,
- (ii) ein Retinoid, das aus Retinylacetat, Retinylpalmitat und
Retinyllinoleat ausgewählt
ist, und
- (iii) ein kosmetisch annehmbares Vehikel,
wobei
das Gewichtsverhältnis
von Retinylacetat zu dem Maulbeerbaum-Extrakt im Bereich von 1 :
80 bis 120 : 1 liegt, das Gewichtsverhältnis von Retinyllinoleat zu
dem Maulbeerbaum-Extrakt im Bereich von 1 8 bis 120 : 1 liegt und
das Gewichtsverhältnis
von Retinylpalmitat zu dem Maulbeerbaum-Extrakt im Bereich von 1
: 16 bis 6 : 1 liegt.
-
Die vorliegende Erfindung umfasst
auch ein kosmetisches Verfahren zur Verbesserung oder Verhütung des
Zustandes von faltiger, gefurchter, trockener, schuppiger, gealterter
oder lichtgeschädigter
Haut und Verbesserung der Hautdicke, -elastizität, -flexibilität, des Hautglanzes,
der Hautröte
und -prallheit, wobei das Verfahren das Auftragen der erfindungsgemäßen Zusammensetzung
auf der Haut einschließt.
Die Zusammensetzungen der Erfindung sind für die topische Anwendung auf
Säugerhaut
gedacht, die bereits trocken, schuppig, gefurcht, faltig, gealtert,
lichtgeschädigt
ist, oder die erfindungsgemäßen Zusammensetzungen
können
prophylaktisch aufgebracht werden, um Verschleißänderungen zu verringern.
-
Außer in den Beispielen oder
wo ansonsten ausdrücklich
angezeigt sind alle Zahlen in dieser Beschreibung, die Mengen an
Material oder Reaktionsbedingungen, physikalische Eigenschaften
von Materialien und/oder eine Verwendung anzeigen, so zu verstehen,
dass sie durch das Wort „etwa" modifiziert sind.
Alle Mengen sind bezüglich
Gewicht der Zusammensetzung, falls nicht anders angegeben.
-
Der Maulbeerbaum-Extrakt, der zur
Verwendung in der vorliegenden Erfindung geeignet ist, ist ein glycolischer
Extrakt aus der Wurzel des weißen
Maulbeerbaums. Der weiße
Maulbeerbaum ist auch als Morus alba bekannt. Der Extrakt kann von
Bioland (Südkorea)
erhalten werden.
-
Im Allgemeinen liegt die Menge des
Maulbeerbaum-Extraktes in den erfindungsgemäßen Zusammensetzungen im Bereich
von 0,001 bis 20 Gew.-% der Zusammensetzung. Vorzugsweise liegt,
um die Kosten zu erniedrigen und die Wirkung zu maximieren, die
Menge des Maulbeerbaum-Extraktes im Bereich von 0,01 bis 10% und
am bevorzugtesten im Bereich von 0,1 bis 5%.
-
Die erfindungsgemäßen Zusammensetzungen umfassen
weiter ein Retinoid, das aus Retinylacetat, Retinylpalmitat und
Retinyllinoleat ausgewählt
ist. Es wurde gefunden, dass diese Retinoide synergistisch mit dem
Maulbeerbaum-Extrakt zusammenwirken, wenn das Retinoid und der Maulbeerbaum-Extrakt
in einem speziellen Gewichtsverhältnis
kombiniert werden; das Gewichtsverhältnis von Retinylacetat zu
dem Maulbeerbaum-Extrakt liegt im Bereich von 1 : 8 bis 120 : 1,
bevorzugt von 1 : 8 bis 12 : 1, am bevorzugtesten von 1 : 8 bis
1,2 : 1; das Gewichtsverhältnis
von Retinyllinoleat zu dem Maulbeerbaum-Extrakt liegt im Bereich von 1 : 8 bis
120 : 1, vorzugsweise von 1 : 8 bis 12 : 1, am bevorzugtesten von
1 8 bis 1,2 : 1, und das Gewichtsverhältnis von Retinylpalmitat zu
dem Maulbeerbaum-Extrakt liegt im Bereich von 1 : 16 bis 6 : 1,
bevorzugt von 1 : 8 bis 8 : 1, am bevorzugtesten von 1 : 8 bis 1,2
: 1.
-
Die Zusammensetzung gemäß der Erfindung
umfasst auch ein kosmetisch annehmbares Vehikel, das als Verdünnungsmittel,
Dispergiermittel oder Träger
für den
Maulbeerbaum-Extrakt und das Retinoid in der Zusammensetzung wirkt,
um deren Verteilung zu erleichtern, wenn die Zusammensetzung auf
der Haut aufgebracht wird.
-
Vehikel außer oder zusätzlich zu
Wasser können
flüssige
oder feste Erweichungsmittel, Lösungsmittel, Befeuchtungsmittel,
Verdickungsmittel und Puder einschließen. Ein besonders bevorzugter
nicht-wässriger Träger ist
ein Polydimethylsiloxan und/oder ein Polydimethylphenylsiloxan.
Bei Silikonen dieser Erfindung kann es sich um diejenigen mit Viskositäten im Bereich
irgendwo von etwa 10 bis 10 000 000 mm2/s
(Centistoke) bei 25°C
handeln. Besonders wünschenswert
sind Mischungen von niedrig- und hochviskosen Silikonen. Diese Silikone
sind von der General Electric Company unter den eingetragenen Marken
Vicasil SE und SF und von der Dow Corning Company unter der 200-
und 550-Reihe erhältlich.
Mengen an Silikon, die in den Zusammensetzungen dieser Erfindung
verwendet werden können,
liegen im Bereich irgendwo von 5 bis 95, vorzugsweise von 25 bis
90 Gew.-% der Zusammensetzung.
-
Das kosmetisch annehmbare Vehikel
umfasst gewöhnlich
5 bis 99,9, vorzugsweise 25 bis 80 Gew.-% der Zusammensetzung und
kann in Abwesenheit von anderen kosmetischen Zusätzen den Rest der Zusammensetzung
bilden. Vorzugsweise ist das Vehikel mindestens 80 Gew.-% Wasser,
bezogen auf das Gewicht des Vehikels. Vorzugsweise umfasst Wasser
mindestens 50 Gew.-% der erfindungsgemäßen Zusammensetzung, am bevorzugtesten
60 bis 80 Gew.-%, bezogen auf das Gewicht der Zusammensetzung.
-
Die Zusammensetzung kann fakultative
hautnützliche
Materialien und kosmetische Zusätze
umfassen. Ein Öl
oder öliges
Material kann zusammen mit einem Emulgator anwesend sein, um entweder
eine Wasser-in-Öl-Emulsion
oder eine Öl-in-Wasser-Emulsion
zu liefern, im großen
und ganzen abhängig
von dem durchschnittlichen hydrophil-lipophilen Gleichgewicht (HLB)
des verwendeten Emulgators.
-
Die erfindungsgemäßen Zusammensetzungen schließen bevorzugt
einen Sonnenschutz ein. Ein Sonnenschutz schließt diejenigen Materialien ein,
die üblicherweise
verwendet werden, um Ultraviolettlicht abzublocken. Erläuternde
Verbindungen sind die Derivate von PABA, Cinnamat und Salicylat.
Beispielsweise können
Octylmethoxycinnamat und 2-Hydroxy-4-methoxybenzophenon (auch als
Oxybenzon bekannt) verwendet werden. Octylmethoxycinnamat und 2-Hydroxy-4-methoxybenzophenon
sind im Handel unter den eingetragenen Marken Parsol MCX bzw. Benzophenon-3
erhältlich.
Die genaue Menge an Sonnenschutz, die in den Emulsionen verwendet
wird, kann abhängig
von dem gewünschten
Grad des Schutzes vor der UV-Strahlung der Sonne variieren.
-
Erweichungsmittel werden häufig den
kosmetischen Zusammensetzungen der vorliegenden Erfindung einverleibt.
Konzentrationen derartiger Erweichungsmittel können im Bereich von 0,5 bis
50, bevorzugt zwischen 5 und 30 Gew.-% der Gesamtzusammensetzung
liegen. Erweichungsmittel können
in solche allgemeine chemische Kategorien wie Ester, Fettsäuren und
Alkohole, Polyole und Kohlenwasserstoffe klassifiziert werden.
-
Bei Estern kann es sich um Mono-
oder Diester handeln. Annehmbare Beispiele für Fettdiester schließen Dibutyladipat,
Dibutylsebacat, Diethylsebacat, Diisopropyldimerat und Dioctylsuccinat
ein. Annehmbare verzweigtkettige Diester schließen 2-Ethylhexylmyristat, Isopropylstearat
und Isostearylpalmitat ein. Annehmbare Ester von dreibasigen Säuren schließen Triisopropyltrilinoleat
und Trilaurylcitrat ein. Annehmbare geradkettige Fettester schließen Laurylpalmitat,
Myristyllactat und Stearyloleat ein. Bevorzugte Ester umfassen Kokoscaprylat/caprat
(eine Mischung von Kokoscaprylat und Kokoscaprat), Propylenglycolmyristyletheracetat, Diisopropyladipat
und Cetyloctanoat.
-
Geeignete Fettalkohole und -säuren schließen die
Verbindungen mit 10 bis 20 Kohlenstoffatomen ein. Besonders bevorzugt
sind Verbindungen wie Cetyl-, Myristyl-, Palmitin- und Stearylalkohole
und -säuren.
-
Unter den Polyolen, die als Erweichungsmittel
dienen können,
befinden sich lineare und ver zweigtkettige Alkylpolyhydroxyl-Verbindungen.
Beispielsweise sind Propylenglycol, Sorbit und Glycerin bevorzugt. Ebenfalls
nützlich
können
polymere Polyole sein, wie Polypropylenglycol und Polyethylenglycol.
Butylen- und Propylenglycol sind auch als Penetrationsverstärker besonders
bevorzugt.
-
Beispielhafte Kohlenwasserstoffe,
die als Erweichungsmittel dienen können, sind diejenigen mit Kohlenwasserstoff-Ketten
irgendwo von 12 bis 30 Kohlenstoff-Atomen. Spezielle Beispiele umfassen
Mineralöl, Erdölgallerte,
Squalen und Isoparaffine.
-
Eine weitere Kategorie von funktionellen
Bestandteilen, die in den kosmetischen Zusammensetzungen der vorliegenden
Erfindung vorliegen können,
sind Verdickungsmittel. Ein Verdickungsmittel ist gewöhnlich in
einer Menge im Bereich von 0,1 bis 20 Gew.-%, bevorzugt von etwa
0,5 bis 10 Gew.-% der Zusammensetzung vorhanden. Beispielhafte Verdickungsmittel
sind vernetzte Polyacrylat-Materialien, die unter der eingetragenen
Marke Carbopol von der B. F. Goodrich Company erhältlich sind.
Gummis können
verwendet werden, wie Xanthan-, Carrageenan-, Gelatine-, Karaya-,
Pectin- und Johannisbrotgummi. Unter gewissen Umständen kann
die Verdickungsfunktion durch ein Material bereitgestellt werden,
das auch als Silikon oder Erweichungsmittel dient. Beispielsweise
weisen Silikongummis mit mehr als 10 Centistoke und Ester, wie Glycerinstearat,
eine doppelte Funktionalität
auf.
-
Puder können der kosmetischen Zusammensetzung
der Erfindung einverleibt werden. Diese Puder umfassen Kreide, Talk,
Kaolin, Stärke,
Smektit-Tone, chemisch modifiziertes Magnesiumaluminiumsilicat,
organisch modifizierten Montmorillonit-Ton, hydratisiertes Aluminiumsilicat,
Kieselpuder, Aluminiumstärkeoctenylsuccinat
und deren Mischungen.
-
Andere geringfügige Zusatzkomponenten können den
kosmetischen Zusammensetzungen ebenfalls einverleibt werden. Diese
Bestandteile können
Färbemittel,
Opakmacher und Parfüme
einschließen.
Die Mengen dieser anderen geringfügigen Zusatzkomponenten können im
Bereich von 0,001 bis zu 20 Gew.-% der Zusammensetzung liegen.
-
Die Zusammensetzung gemäß der Erfindung
ist hauptsächlich
als Produkt für
die topische kosmetische Auftragung auf menschliche Haut gedacht,
insbesondere als eine zum Konditionieren, Befeuchten und Glätten der
Haut und zur Verhütung
oder Verringerung des Aussehens von gefurchter, faltiger oder gealterter Haut.
-
Bei der Verwendung wird eine geringe
Menge der Zusammensetzung, beispielsweise 1 bis 100 ml, aus einem
geeigneten Behälter
oder Applikator auf freiliegende Hautflächen aufgetragen und, falls
erforderlich, unter Verwendung der Hand oder von Fingern oder einer
geeigneten Vorrichtung auf der Haut ausgebreitet und/oder in diese
eingerieben.
-
Die topische Hautbehandlungs-Zusammensetzung
der Erfindung kann als Lotion, Creme oder Gel formuliert werden.
Die Zusammensetzung kann in einem geeigneten Behälter abgepackt werden, der
für ihre
Viskosität
und die vom Verbraucher beabsichtigte Verwendung geeignet ist. Beispielsweise
kann eine Lotion oder Creme ein einer Flasche oder einem Rollkugel-Applikator
oder einer Treibmittel-getriebenen Aerosolvorrichtung oder einem
Behälter
abgepackt werden, welcher mit einer Pumpe versehen ist, die für einen
Betrieb mit dem Finger geeignet ist. Wenn die Zusammensetzung eine
Creme ist, kann sie einfach in einer nicht-verformbaren Flasche
oder in einem ausdrückbaren
Behälter
aufbewahrt werden, wie einer Tube oder einem Gefäß mit Deckel. Die Zusammensetzung
kann auch in Kapseln eingeschlossen werden, wie diejenigen, die
im US-Patent 5,063,507 beschrieben sind, das hierin durch Bezugnahme
auf genommen wird. Die Erfindung stellt demgemäß auch einen geschlossenen
Behälter
bereit, der eine kosmetisch annehmbare Zusammensetzung, wie hierin
definiert, enthält.
-
Die folgenden speziellen Beispiele
erläutern
die Erfindung weiter, aber die Erfindung ist nicht darauf beschränkt. In
allen Beispielen wurde Resveratrol von Sigma erhalten. Retinoide
wurden von Sigma erhalten. Der Student-„t-Test" wurde verwendet, um alle p-Werte zu
berechnen.
-
BEISPIELE
-
Die folgenden Methoden wurden verwendet.
-
(1) Zellkulturmethode:
-
Menschliche erwachsene Fibroblasten,
die aus dem sonnengeschützten
Innenarm eines weiblichen Freiwilligen von 25–30 Jahren erhalten wurden,
wurden verwendet. Die Zellen wurden in 1 : 1 DMEM/Hams F12-Medium
gezüchtet,
das 10% FBS enthielt und bei 37°C
in einer 5% CO2-Atmosphäre unter normalem atmosphärischem
Sauerstoffdruck gehalten wurde. Erwachsene Fibroblasten der dritten
Passage wurden in DMEM-Medium mit 10% FBS in einer Platte mit 12
Vertiefungen bei einer Beimpfungsdichte von 40000 Zellen/ml/Vertiefung
gezüchtet.
Die Zellen mit 80% Konfluenz wurden zweimal mit serumfreien und
Phenolrot-freiem (PRF) DMEM-Medium gespült, 4 Stunden mit Phytoaktiv
vorbehandelt, mit Retinoiden versetzt und 48 Stunden inkubiert.
-
Nach Inkubation wurden die Vertiefungen
zweimal mit 1 × PBS
gewaschen, und die Zell-Monoschicht wurde
in 100 μl
Zelllyse-Puffer (enthält
1 × PBS,
1% TritonX, 0,5% Natriumdesoxycholat, 0,1% SDS, das Proteaseinhibitor
(10 mg/ml PMSF in Isopropanol, 10 μl/m) enthält) geerntet. Die Suspension
wurde 10 Minuten bei 14000 U/min zentrifugiert, der Überstand
wurde gesammelt, und eine Aliquote des Überstands wurde für die quantitative
Proteinbestimmung verwendet. Die Proteinkonzentration wurde unter
Verwendung eines Pierce-Proteinkits bestimmt. Der Rest der 100 μl Überstand
(Zelllysat) wurde in einer Mischung aus 40 μl Probenpuffer (NOVEX) und 0,5%
beta-Mercaptoethanol (BME) durch fünfminütiges Kochen der Probe denaturiert. Gleiche
Mengen an Protein wurden dann auf 16% Tris-Glycin-Gele für die Proteinanalyse
mittels SDS-PAGE und Western-Immuno-Blotting für die CRABP-2-Proteinexpression
geladen.
-
3. Nachweis des zellulären Retinoesäure-bindenen
Proteins 2 (CRABP-2) in Fibroblasten und Schweinehaut-Biopsien:
-
Um die Konzentrationen an CRABP-2
in den Fibroblasten- und Schweinehaut-Extrakten, die wie oben beschrieben
hergestellt wurden, zu messen, wurde der Zellüberstand in 4 × Probenpuffer
und 10 BME resuspendiert, 5 Minuten gekocht und für ein Western-Blotting
verwendet. Gleiche Mengen an Proteinen wurden auf 16% Tris-Glycin-Gele
für die
CRABP-Protein-Analyse mittels SDS-PAGE und Western-Immuno-Blotting
geladen. Die Gele wurden auf Nitrocellulose-Blots überführt, und
das Western-Blotting
wurde unter Verwendung von monoklonalen Antikörpern gegen CRABP-2 gemäß Standardverfahren
durchgeführt.
Die CRABP-2-Proteinbande wurde unter Verwendung des Chemielumineszenz-Systems,
das von Santa Cruz Biotechnology (Santa Cruz, CA) erhalten wurde,
in den Western-Blots sichtbar gemacht. Die Banden in der Folie wurden durch
densiometrisches Scanning quantifiziert, die Daten aus dreifachen
Proben wurden als Prozent der Kontrolle berechnet und in den folgenden
Tabellen als Prozent Zunahme gegen Kontrolle (mit Kontrolle als
100%) +/- SA von Dreifachversuchen ausgedrückt.
-
1. Berechnungen des Retinoid:
Maulbeerbaum-Verhältnisses
-
Der in diesen Studien verwendete
Maulbeerbaum-Extrakt enthält
2% Feststoffe. Deshalb entspricht 1 μl Maulbeerbaum-Extrakt, der
in diesen Studien zu 1 ml Medium gegeben wird, 0,1% Extrakt × 0,02
Feststoff
= 0,002% Maulbeerbaum-Feststoffe,
1 μM Retinoid entspricht etwa 500 μg/l Retinylester;
was äquivalent
zu 50 μg/100
ml oder 0,00005% Retinylestern ist.
-
Deshalb weist 1 μM Retinoid : 1 μl Maulbeerbaum-Extrakt,
was in diesem In-vitro-Assay-System verwendet wurde, ein Verhältnis von
0,00005 zu 0,002 oder ein Verhältnis
von 1 : 80 auf.
-
Die verschiedenen Verhältnisse
von Retinoiden zu Maulbeerbaum, die in den in dieser Patentanmeldung
beschriebenen In-vitro-Studien verwendet wurden, und potentielle
Konzentrationen von Retinoiden zu Maulbeerbaum, um diesem Verhältnis in
Formulierungen zu entsprechen, die in Hauptpflegeprodukten verwendet
werden können,
sind in der nachstehenden Tabelle 1 gezeigt.
-
-
Es ist aus Tabelle 1 ersichtlich,
dass die Verhältnisse
den nützlichen
Bereich an Retinoiden von 0,007% bis 1,2% und des Maulbeerbaum-Extrakts
von 0,5% bis 8% abdecken.
-
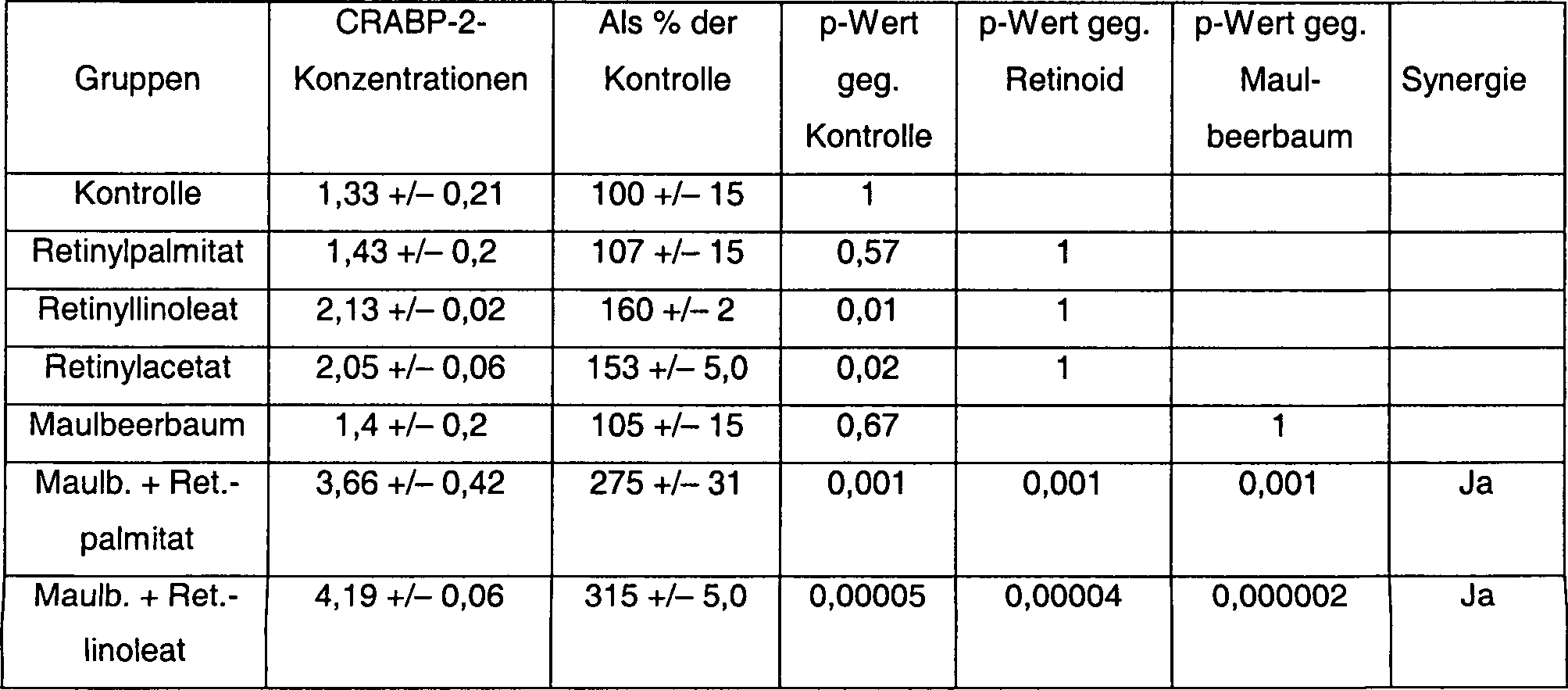
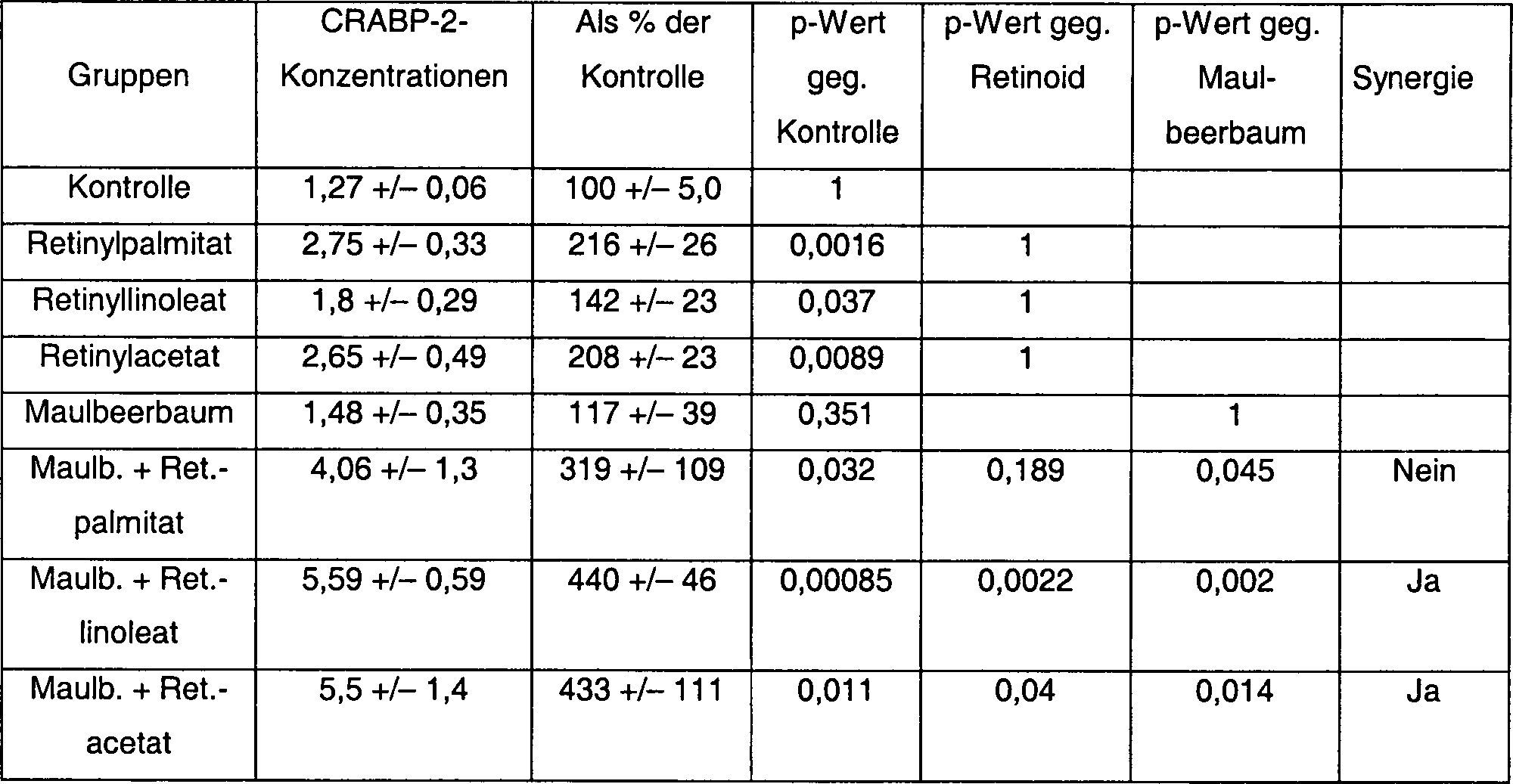
Die nachstehenden Tabellen 2–10 zeigen
die CRABP-2-Expression von Fibroblasten in Experimenten unter Verwendung
von Retinyllinoleat, Retinylpalmitat und Retinylacetat mit Maulbeerbaum-Extrakt in verschiedenen
Verhältnissen
von 1 : 80 (Tabellen 2, 3), 1 : 16 (Tabelle 4), 1 : 8 (Tabelle 5),
1 16 (Tabelle 6), 1,2 : 1 (Tabelle 7), 6 : 1 (Tabelle 8), 12 : 1
(Tabelle 9) oder 120 : 1 (Tabelle 10). Tabelle 11 fasst alle Daten
aus den Tabellen 2–10
zusammen.
-
TABELLE
2
1 μM
Retinylester und 1 μl
Maulbeerbaum-Extrakt (Retinoid : Maulbeerbaum-Verhältnis =
1 : 80)
-
TABELLE
3
100 nM Retinylester und 0,1 μl Maulbeerbaum-Extrakt (Retinoid
: Maulbeerbaum-Verhältnis
= 1 : 80)
-
TABELLE
4
500 nM Retinylester und 0,1 μl Maulbeerbaum-Extrakt (Retinoid
: Maulbeerbaum-Verhältnis
= 1 : 16)
-
-
TABELLE
5
1 μM
Retinylester und 0,1 μl
Maulbeerbaum-Extrakt (Retinoid : Maulbeerbaum-Verhältnis =
1 : 8)
-
TABELLE
6
500 nM Retinylester und 0,1 μl Maulbeerbaum-Extrakt (Retinoid
: Maulbeerbaum-Verhältnis
= 1 : 1,6)
-
-
TABELLE
7
100 nM Retinylester und 0,001 μl Maulbeerbaum-Extrakt (Retinoid
: Maulbeerbaum-Verhältnis
= 1 : 0,8 oder 1,2 : 1)
-
TABELLE
8
500 nM Retinylester und 0,001 μl Maulbeerbaum-Extrakt (Retinoid
: Maulbeerbaum-Verhältnis
= 6 : 1)
-
TABELLE
9
10 μM
Retinylester und 0,01 μl
Maulbeerbaum-Extrakt (Retinoid : Maulbeerbaum-Verhältnis =
12 : 1)
-
TABELLE
10
10 μM
Retinylester und 0,001 μl
Maulbeerbaum-Extrakt (Retinoid : Maulbeerbaum-Verhältnis =
120 : 1)
-
-
-
Zusammenfassend zeige Retinylacetat
eine Synergie mit Maulbeerbaum-Extrakt bei einem Verhältnis von
1 : 80 bis 120 : 1 in Hautzellen. Retinyllinoleat zeigte eine Synergie
von 1 : 8 bis 120 : 1 und Retinylpalmitat zeigte eine Synergie bei
Verhältnissen
von 1 : 16 bis 6 : 1.
-
Es versteht sich, daß die speziellen,
hierin erläuterten
und beschriebenen Formen der Erfindung nur repräsentativ sein sollen. Änderungen,
einschließlich,
ohne darauf beschränkt
zu sein, derjenigen, die in dieser Beschreibung vorgeschlagen werden,
können
in den erläuterten
Ausführungsformen
vorgenommen werden, ohne von den klaren Lehren der Offenbarung abzuweichen.
Demgemäß sollte
bei der Bestimmung des vollen Bereichs der Erfindung auf die folgenden
beigefügten
Ansprüche
Bezug genommen werden.