CN1615135A - 磺酰胺前药如帕瑞考昔的口服剂型 - Google Patents
磺酰胺前药如帕瑞考昔的口服剂型 Download PDFInfo
- Publication number
- CN1615135A CN1615135A CNA028270843A CN02827084A CN1615135A CN 1615135 A CN1615135 A CN 1615135A CN A028270843 A CNA028270843 A CN A028270843A CN 02827084 A CN02827084 A CN 02827084A CN 1615135 A CN1615135 A CN 1615135A
- Authority
- CN
- China
- Prior art keywords
- carbonyl
- compositions
- parecoxib
- alkyl
- fructus
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/18—Sulfonamides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/365—Lactones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/42—Oxazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
Abstract
一种基本上不含水的药物组合物,包括至少可口服给予的一个剂量单位,其含有治疗有效量的磺酰胺前药,其中前药在体外容易被降解,在口服之前有办法抑制这种降解。说明性地,该前药是帕瑞考昔或其水溶性盐,以及该组合物有办法抑制帕瑞考昔转化为伐地考昔。一种治疗或预防COX-2介导的疾病的方法,包括(a)在药学上可接受的含水赋形剂中溶解至少一个剂量单位的这种组合物以制备一种溶液,以及(b)在溶液中形成大量不溶物质沉淀前,患者口服该溶液。
Description
发明领域
本发明涉及磺酰胺药物的前药包括帕瑞考昔(parecoxib),一种选择性环加氧酶-2(COX-2)抑制药物伐地考昔(valdecoxib)的前药。更具体地说,本发明涉及这种前药的可口服给予的剂型。本发明还涉及使用这种剂型进行治疗的方法。
发明背景
环加氧酶(COX)酶的抑制至少被认为是非甾体抗炎药(NSAIDs)通过抑制前列腺素合成发挥它们特有的消炎、退热和止痛作用的主要机理。在治疗剂量,常规的NSAIDs例如酮咯酸、双氯酚酸、萘普生和它们的盐不仅抑制组成性表达的COX-1,而且抑制与炎症有关的或由炎症引起的环加氧酶的COX-2同工型。COX-1的抑制,其中COX-1生成正常细胞功能所需的前列腺素,看起来是与使用常规的NSAIDs有关的某些不良副作用的原因。相反,基本上不抑制COX-1的选择性地抑制COX-2,将产生消炎、退热、止痛和其它有益的治疗作用,并同时减少或消除这种不良副作用。选择性的COX-2抑制药物如塞来考昔和罗非考昔,首次在1999年市售,代表了该领域的主要进展。这些药物被配制成各种可口服给予的剂型。
帕瑞考昔,公开在Talley等人的US 5,932,598中,在此引入作为参考,是具有磺酰胺部分的选择性COX-2抑制药物的N-取代的水溶性前药这一类中的一种。对给药后,帕瑞考昔转变成基本上不溶于水的选择性COX-2抑制药物伐地考昔。在暴露于水时,例如溶解在水中时,帕瑞考昔也转变成伐地考昔。
具有下面结构式(I)的帕瑞考昔,其本身在体外对COX-1和COX-2显示出弱的抑制活性,而伐地考昔(II)对COX-2具有强的抑制活性,但它同时是一种弱的COX-1抑制剂。
上面所引的US 5,932,598同时还公开了可比较的具有磺酰胺部分的其它选择性COX-2抑制剂的N-取代的前药。例如,在US5,932,598中,将化合物N-[[4-[5-(4-甲基苯基)-3-(三氟甲基)-1H-吡唑-1-基]苯基]磺酰基]乙酰胺(III)和它的钠盐用作选择性COX-2抑制药物塞来考昔(celecoxib)(IV)的前药。
与选择性强的COX-2抑制药物例如塞来考昔和伐地考昔相比,由于帕瑞考昔的高水溶性,特别是帕瑞考昔的盐例如钠盐的高水溶性,前药帕瑞考昔已经建议用于肠胃外使用。参见Talley等人(2000),J.Med.Chem.43,1661-1663。
上面所引的US 5,932,598指出:治疗炎症的优选方法是通过注射给予在那里公开的水溶性化合物。然而,上面所引的专利还公开了可以口服给予这种化合物或包含这种化合物的组合物,例如可以以片剂、硬胶囊剂或软胶囊剂、锭剂、可分散的粉剂、悬液或液剂的形式口服给予该组合物。
由于帕瑞考昔在暴露于水时趋向于迅速转变成不溶解的伐地考昔,因此迄今为止,对口服给予帕瑞考昔或开发一种帕瑞考昔的实际口服剂型没有多大的兴趣。
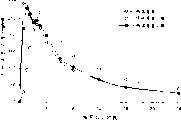
图1表示药动学研究结果,其中在11个健康成年患者中测定血浆中伐地考昔的浓度,这些患者一次性静脉注射(IV)在1ml丸剂中的20mg剂量的帕瑞考昔,例如帕瑞考昔钠,或者以立即释放片剂形式一次性口服给予20毫克剂量的伐地考昔,用240ml水吞服。 服用一、二和三小时后,患者喝180ml水。血浆中伐地考昔的浓度用有效的高效液相色谱法(HPLC)进行测定。从图1中可以清楚地看出,IV给予帕瑞考昔时,在服药后约1小时达到最大血浆浓度,比伐地考昔口服给予时(服药后约3小时)更早达到最大血浆浓度。通过IV给予帕瑞考昔,可以更快地在血液中建立伐地考昔的治疗有效浓度,这一点是非常重要的,因为它可以迅速产生治疗作用。对于许多COX-2介导的疾病,特别是伴随剧烈疼痛的那些疾病,快速起作用是一种非常理想的特点。
IV给药,对于许多遭受或处于这种疾病危险之中的人们来说,尤其对那些需要自己给药的患者来说,是不方便的并且使人不愉快的。通常,口服给予药物比较方便并且有助于更高程度的患者适应性。
因此,在治疗和/或预防由COX-2介导的疾病的领域中,人们希望通过口服,获得伐地考昔最大血浆浓度的时间(Tmax),显著地比那些通过口服立即释放片剂形式的伐地考昔获得的最大血浆浓度的时间要短,优选与通过IV给予帕瑞考昔获得的最大血浆浓度的时间相当。
人们还希望提供这样一种口服剂型,它可以改善其它选择性COX-2抑制磺酰胺药物包括塞来考昔以及一般性磺酰胺药物的的Tmax。
发明概述
本发明提供一种基本上不含水并且包含至少一种剂量单位的药物组合物,其中至少一种剂量单位包含一种治疗有效量的化合物X-SO2-NHR1或其药学上可接受的盐,其中X是这样的一个部分,它使化合物X-SO2-NH2是一种已知的药物,以及其中R1是一个具有至多8个碳原子的基团,该基团选自烷基、羟基烷基、烷氧基烷基、羧基烷基、酰基、烷基羰基、烷氧基羰基、羟基烷基羰基、烷氧基烷基羰基、羧基烷基羰基、氨基烷基-羰基、苯基羰基、苄基羰基、苯基(羟基)甲基羰基、烷氧基羰基羰基、烷氧基羰基烷基羰基、烷氧基羰基烷基羰基、烷基羰基氨基烷基羰基、烷氧基羰基氨基烷基羰基、烷氧基-羰基羰基、氨基酸残基和杂芳基羰基。该组合物可口服给予并且,其中化合物X-SO2-NHR1很容易地在体外降解成药物X-SO2-NH2,在口服前有手段抑制这种降解。说明性地,药物X-SO2-NH2是一种选择性COX-2抑制药物,例如伐地考昔、塞来考昔或地拉考昔。
特别地,本发明提供一种基本上不含水并且包含至少一个剂量单位的药物组合物,其中至少一个剂量单位包含治疗有效量的帕瑞考昔或其水溶性盐,该组合物是可口服给予的并且在口服前有手段抑制帕瑞考昔转化成伐地考昔。
本发明还提供一种包括一种基本上不透水的包装的产品,其包含一种单一剂量单位的可口服给予的药物组合物,其中该药物组合物基本上不含水并且包括一种治疗有效量的化合物X-SO2-NHR1或其药学上可接受的盐,其中X是这样的一个部分,它使化合物X-SO2-NH2是一种已知的药物,以及其中R1是一个具有至多8个碳原子的基团,该基团选自烷基、羟基烷基、烷氧基烷基、羧基烷基、酰基、烷基羰基、烷氧基羰基、羟基烷基羰基、烷氧基烷基羰基、羧基烷基羰基、氨基烷基-羰基、苯基羰基、苄基羰基、苯基(羟基)甲基羰基、烷氧基羰基羰基、烷氧基羰基烷基羰基、烷氧基羰基烷基羰基、烷基羰基氨基烷基羰基、烷氧基羰基氨基烷基羰基、烷氧基羰基羰基、氨基酸残基和杂芳基羰基。在根据本发明具体实施方案制备的一种产品中,化合物X-SO2-NHR1是帕瑞考昔并且优选以水溶性盐的形式存在。
在此″可口服给予的″是指这样的组合物,(a)如上面提供的,即基本上不含水的组合物,或者(b)组合物分散和/或溶解在一种药学上可接受的含水赋形剂中后,适于患者口服。
本发明另外还提供一种治疗或预防COX-2介导的疾病的方法,该方法包括(a)将至少一个剂量单位的基本上不含水并且包含治疗有效量的帕瑞考昔或其水溶性盐的一种药物组合物,溶解在一种药学上可接受的含水赋形剂中,以形成一种溶液,以及(b)在该溶液在出现不溶物质的沉淀(substantialprecipitation)之前,患者口服该溶液。
意外地发现,受试验的人通过口服一种本发明的帕瑞考昔或其水溶性盐的组合物的溶液,在受试者的血浆中的伐地考昔浓度迅速地提高到治疗有效水平。这种水平要比伐地考昔本身作为一种立即释放片剂配方(Pharmacia Corp.的Bextra)口服给予更快地达到。更令人惊讶地是,根据本发明,在伐地考昔血浆浓度的药动学方面,口服给予帕瑞考昔可以与IV给予帕瑞考昔相比或基本上相当。
同样地发现,受试验的狗通过口服一种本发明的塞来考昔前药的组合物的溶液,在受试验的狗的血浆中的塞来考昔浓度非常快地提高到治疗有效水平。从前药中得到的塞来考昔的生物利用率要比塞来考昔本身以市场上买到的胶囊配方(Pharmacia Corp.的西乐葆)形式口服给予大很多,并且与通过口服在苹果汁中的细小塞来考昔混悬液的生物利用度类似或者更大。
重要的是,在本发明的一种方法中,其中前药是帕瑞考昔或其水溶性盐,在含水赋形剂中的溶液在服药前很短的时间内配制,以使帕瑞考昔尽量少地转化为伐地考昔,其中在水介质中这种转化趋向快速地发生。这种转化可以通过在溶液中出现不溶性沉淀物进行观察,因此根据本发明的方法,在溶液中出现不溶物质的沉淀之前,口服给予该溶液。
附图的简要描述
图1表示如上所述的人药动学数据,显示(a)静脉注射在1ml丸剂中20mg帕瑞考昔后,以及(b)以商业上的立即释放片剂形式口服给予20mg伐地考昔后,伐地考昔在0-24小时之间的平均血浆浓度变化。
图2表示同样的药动学研究数据,显示在(c)口服给予水溶液形式的20mg帕瑞考昔后,在0-24小时之间的伐地考昔的平均血浆浓度。
图3表示狗的药动学研究数据,表示在口服给予(a)商业上胶囊形式的塞来考昔后;(b)在苹果汁中的塞来考昔悬浮液后;以及(c)在水溶液中的如下文定义的塞来考昔前药化合物Z后;所有都相当于给予200mg的塞来考昔,塞来考昔的平均血浆浓度在0-24小时内的变化。
发明的详细说明
本发明在此特别是涉及帕瑞考昔,更特别是帕瑞考昔钠,其是选择性COX-2抑制磺酰胺药物伐地考昔的一种前药。但是,应该清楚,本发明的范围延伸到一般性磺酰胺药物的前药,其中这种前药由如上定义的磺酰胺部分被N-取代生成。
任何已知的磺酰胺药物可以作为前药的基药,磺酰胺药物的例子包括但不限于Eisai的ABT-751(N-(2-((4-羟苯基)氨基)-3-吡啶基)4-甲氧基苯磺酰胺);阿吡必利;氨碘洛尔;安普那韦;安沙可林;阿加曲班;asulacrine;阿佐酰胺;Bayer的BAY-38-4766(N-[4-[[[5-(二甲氨基)-1-萘基]磺酰基]氨基]苯基]-3-羟基-2,2-二甲基丙酰胺);苄氟噻嗪;Bristol Myers Squibb的BMS-193884(N-(3,4-二甲基-5-异噁唑基)-4′-(2-噁唑基)-[1,1′-联苯基]-2-磺酰胺);波色坦;布美他尼;塞来考昔;氯噻酮;地拉韦啶;地拉考昔;多非利特;多米曲班;杜塞酰胺;决奈达隆;Eisai的E-7070(N-(3-氯-1H-吲哚-7-基)-1,4-苯-二磺酰胺);Schwartz Pharma的EF-7412(N-3-[4-[4-(四氢-1,3-二氧代-1H-吡咯并[1,2-c]咪唑-2(3H)-基)丁基]-1-哌嗪基]苯基]乙烷-磺酰胺);苯喹唑酮;呋塞米;格列本脲;格列齐特;格列美脲;格列太特;格列吡嗪;格列喹酮;格列索脲;Glaxo SmithKline的GW-8510(4-[[(6,7-二氢-7-氧代-8H-吡咯并[2,3-g]苯并噻唑-8-亚基)甲基]氨基]-N-2-吡啶基苯磺酰胺);Ivax的GYKI-16638(N-[4-[2-[[2-(2,6-二甲氧基-苯氧基)-1-甲基乙基]甲基氨基]乙基]苯基]甲磺酰胺);Aventis的HMR-1098(5-氯-2-甲氧基-N-[2-[4-甲氧基-3-[[[(甲基氨基)-硫代甲基]氨基]磺酰基]苯基]乙基]苯甲酰胺);双氢氯噻嗪;伊布利特;吲达帕胺;Ishihara的IS-741(N-[2-[(乙基磺酰基)氨基]-5-(三氟甲基)-3-吡啶基]环己烷羧酰胺);Japan Tobacco的JTE-522(4-(4-环己基-2-甲基-5-噁唑基)-2-氟苯磺酰胺);Chugai的KCB-328(N-[3-氨基-4-[2-[[2-(3,4-二甲氧基苯基)乙基]甲基氨基]乙氧基]苯基]甲磺酰胺);Kotobuki的KT2-962(3-[4-[[(4-氯苯基)磺酰基]氨基]丁基]-6-(1-甲基乙基)-1-薁磺酸);左舒必利;Eli Lilly的LY-295501(N-[[(3,4-二氯苯基)氨基]羰基]-2,3-二氢-5-苯并呋喃磺酰胺)和LY-404187(N-2-(4-(4-氰基苯基)苯基)丙基-2-丙磺酰胺);美托拉宗;那拉曲坦;尼美舒利;Nippon的NS-49((R)-N-[3-(2-氨基-1-羟乙基)-4-氟苯基]甲磺酰胺);Ono的ONO-8711((5Z)-6-[(2R,3S)-3-[[[(4-氯-2-甲基苯基)磺酰基]氨基]甲基]二环[2.2.2]辛-2-基]-5-己烯酸);吡咯他尼;Pharmacia的PNU-103657(1-[5-甲磺酰胺基吲哚-2-基羰基]-4-(N-甲基-N-(3-(2-甲基丙基)-2-吡啶基)氨基)哌啶);多噻嗪;雷马曲班;Hoffmann LaRoche的RO-61-1790(N-[6-(2-羟基乙氧基)-5-(2-甲氧基苯氧基)-2-[2-(1H-四唑-5-基)-4-吡啶基]-4-嘧啶基]-5-甲基-2-吡啶磺酰胺);Aventis的RPR-130737(4-羟基-3-[2-氧代-3(S)-[5-(3-吡啶基)噻吩-2-基磺酰氨基]-吡咯烷-1-基甲基]苯甲酰胺)和RPR-208707;Servier的S-18886(3-[(6-(4-氯苯基磺酰氨基)-2-甲基-5,6,7,8-四氢化萘]-1-基)丙酸)和S-32080(3-[6-(4-氯苯基磺酰胺基)-2-丙基-3-(3-吡啶基-甲基)-5,6,7,8-四氢化萘-1-基]丙酸);Kaken的S-36496(2-磺酰基-[N-(4-氯苯基)磺酰氨基-丁基-N-[(4-环丁基-噻唑-2-基)乙烯基苯基-3-基-甲基]]氨基苯甲酸);山帕曲拉;Glaxo SmithKline的SB-203208(L-苯基丙氨酸,b-甲基-,(4aR,6S,7R,7aS)-4-(氨基羰基)-7-[[[[[(2S,3S)-2-氨基-3-甲基-1-氧代戊基]氨基]磺酰基]乙酰基]氨基]-7-羧基-2,4a,5,6,7,7a-六氢-2-甲基-1H-环戊二烯并[c]吡啶-6-基酯,(bS)-);DuPont的SE-170(2-(5-脒基-1H-吲哚-3-基)N-[2’-(氨基磺酰基)-3-溴(1,1′-联苯基)-4-基]乙酰胺);西维来司;Senju的SJA-6017(N-(4-氟苯基磺酰基)-L-缬氨酰基L-亮氨醛);Sumitomo的SM-19712(4-氯N-[[(4-氰基-3-甲基-1-苯基-1H-吡唑-5-基)氨基]羰基]苯磺酰胺);索奈哌唑;梭达罗;磺胺嘧啶;磺胺胍诺;柳氮磺胺吡啶;舒必利;硫前列酮;舒马曲坦;Toyama的T-614(N-[3-(甲酰基氨基)-4-氧代-6-苯氧基-4H-1-苯并吡喃-7-基]甲磺酰胺);Tularik的T-138067(2,3,4,5,6-五氟-N-(3-氟-4-甲氧基苯基)苯磺酰胺)和T-900607(2,3,4,5,6-五氟-N-(3-脲基-4-甲氧基苯基)苯磺酰胺);Takeda的TAK-661(2,2-二甲基-3-[[7-(1-甲基乙基)[1,2,4]三唑并[1,5-b]-哒嗪-6-基]氧]-1-丙磺酰胺);坦索罗辛;替唑生坦;替拉那韦;替罗非班;托拉塞米;三氯噻嗪;曲帕胺;伐地考昔;维拉必利;氯磺水杨胺;Zeria的Z-335(2-[2-(4-氯苯基磺酰氨基甲基)茚满-5-基]乙酸);扎鲁司特;唑尼沙胺;和它们的盐。
在一种实施方案中,磺酰胺药物是一种选择性COX-2抑制药物,这种药物优选选自塞来考昔、地拉考昔和伐地考昔。本发明尤其适合使用在水中具有低溶解度的磺酰胺药物的前药,和这些前药的盐。特别地,其中这些前药或其盐本身是水溶性的。在此″在水中低溶解度″是指在25℃的纯水中,溶解度不大于约10μg/ml,优选不大于约1μg/ml。
作为在此公开的令人惊讶的帕瑞考昔结果代表更宽的范围的证据,本发明还提供下面新化合物N-[[4-[5-(4-甲基苯基)-3-(三氟甲基)-1H-吡唑-1-基]苯基]磺酰基]丙酰胺,钠盐(在此也描述成″化合物Z″)的数据,其是塞来考昔的一种前药。
本发明的第一种实施方案:药物组合物
帕瑞考昔组合物暴露于水汽将使得大量的帕瑞考昔转化为伐地考昔。在这样的环境中该组合物是治疗有效的,其中伐地考昔是活性药物,而帕瑞考昔是一种前药,但是本发明的优点,特别是快速达到治疗血浆浓度并随后快速开始治疗作用的优点,由于这种暴露,趋向于减少。
因此,在第一种实施方案中,本发明提供一种药物组合物,其基本上不含水,即一种干燥的组合物。在本发明的上下文中,术语″基本上不含水″是指存在于组合物中以及与帕瑞考昔反应获得的水的量足够地低,使得当组合物在室温(约20-25℃)下储存在一个密封不透水的容器中时,组合物中的帕瑞考昔表现出可接受的化学稳定性,帕瑞考昔至少稳定存在约30天,优选至少稳定存在约6个月,最优选至少稳定存在约2年。在此″可接受的化学稳定性″是指组合物,在规定的期限(例如,约30天、约6个月或约2年)后,通过治疗剂的化学纯度的标准试验,在一种优选实施方案中,帕瑞考昔或其水溶性盐例如可达到有关当局需要批准的稳定性。这种试验的一个例子是″5%总杂质,1%单个杂质规则″,其中制备这样一种候选药物或前药,其总杂质的含量不超过5%,并且任何一种杂质的含量不超过1%。
一般地,为了提供可接受的化学稳定性的帕瑞考昔,按重量计算,组合物中水含量小于约5%,优选小于约2%,更优选小于约1%。
在第一种实施方案中,组合物包括至少一个剂量单位,其中该剂量单位包含治疗有效量的帕瑞考昔或其水溶性盐。在此″剂量单位″是指一份药物组合物,其包含适于一次口服的药物量以提供治疗作用。通常,一个剂量单位或数个(至多约4个)剂量单位,提供足够数量的药剂以产生预期效果。关于这一点,尽管术语″治疗作用″、″治疗有效的″和″治疗剂″在此用来表示一种前药,例如帕瑞考昔或其水溶性盐,但是应该明白,这些术语可以广义地适用于转变为治疗活性物质的前药。在这里,还应该理解,″治疗″包括预防。
在它的广泛实施方案中,本发明组合物的一个剂量单位包括一种前药,其数量等于或者理论上产生100%转化率时等于在文献中已知是治疗有效的磺酰胺药物的数量。例如,化合物Z的治疗有效量等价于约10-约1000mg,更通常约为50-约400mg,优选约为100-约200mg的塞来考昔。
本发明帕瑞考昔组合物的剂量单位通常包含约1mg-约200mg,优选包含约5mg-约120mg,更优选包含约10mg-约100mg,例如约20mg,约40mg或约80mg的帕瑞考昔。
在此使用的术语″帕瑞考昔″有时包括帕瑞考昔的盐,并且有时在更严格意义上来说是指前药的游离酸形式。含义在出现该术语的上下文中是清楚的。在帕瑞考昔盐的情况中,可以使用能够生成帕瑞考昔的水溶性盐的任何药学上可接受的阳离子。优选的水溶性盐是碱金属盐,钠盐(帕瑞考昔钠)是尤其优选的。
在第一种实施方案中,干燥组合物溶解在含水赋形剂中之前,有抑制帕瑞考昔转化为伐地考昔的手段(means)。这种手段可以以一种或多种方式对抑制转化起作用,包括下面就要指出的那些。所有这些手段,其与在此提供的组合物一同存在,包括在本发明的范围之内。
在本发明的干燥组合物中,抑制帕瑞考昔转化为伐地考昔的一种手段的实例是:在贮存和运输期间,充分地防止组合物暴露在水中,包括防止组合物暴露在潮湿大气中。例如,通过将组合物包装在一个密封的和基本上不透水的包装或容器中,可以充分地防止暴露在水中。或者或另外,组合物可以用一种基本上不透水的包膜材料包上,例如一种基于乙基纤维素的包膜材料。组合物的单个固体颗粒或微粒,或者是组合物较大的珠粒或整个片剂,也可以这样包膜。如果使用,包膜应该选择在胃肠道内容易降解的那些,以便药物或前药迅速吸收的优点不会因为药物或前药从摄取组合物中的延误释放而抵消。
在本发明的干燥组合物中,抑制帕瑞考昔转化为伐地考昔的另一个手段是帕瑞考昔尽量避免与任何非水赋形剂接触,或者帕瑞考昔与任何非水赋形剂尽可能地少接触,否则将促进帕瑞考昔转化为伐地考昔。例如,在一种实施方案中,在组合物中不存在这样的赋形剂。在另一种实施方案中,在帕瑞考昔和任何这种赋形剂之间存在一个隔离层。
说明性地,在本发明的组合物中用作赋形剂的某些糖,例如甘露糖醇,在赋形剂与帕瑞考昔密切接触的干燥组合物中,倾向于将帕瑞考昔转化为伐地考昔。通过使用一种物质对至少一种赋形剂和帕瑞考昔进行预包衣,使它们之间的接触最小化,可以抑制这种转化。
在本发明的干燥组合物中,其它抑制帕瑞考昔转化为伐地考昔的手段对本领域熟练技术人员来说是显而易见的。
本发明的干燥组合物优选充分地可溶于一种药学上可接受的含水赋形剂中,以形成一种可口服给予的溶液。术语″充分可溶解的″是指剂量单位的组合物溶于不大于约100ml,优选不大于约50ml的含水赋形剂中,除选择性地有少量混浊从组合物或含水赋形剂的赋形剂组分中出现之外,肉眼没有观察到有不溶残渣存在。
任何药学上可接受的水成液合适作为赋形剂或溶解组合物的介质。水,例如自来水或瓶装水是特别合适的。或者,可以使用变甜的、加香的和/或充碳酸气的饮料例如糖液、果汁、苏打、浸剂(例如茶)、萃取物(例如牛肉浸抽提物、麦芽抽提物、酵母抽提物)等等。
本发明的第一种实施方案的组合物可以基本上由帕瑞考昔或其水溶性盐组成,但是任选另外包括其它组分,例如药学上可接受的赋形剂。这种其它组分的用量优选与帕瑞考昔是化学相容的,特别是在基本上没有水的情况下,不会促进帕瑞考昔转化为伐地考昔。如果发现想要的赋形剂促进这种转化,如上所述,包含这种赋形剂的组合物应该用一种隔离层配制,以避免赋形剂和帕瑞考昔之间的接触,或使赋形剂和帕瑞考昔之间的接触最小化。
可以包括在本发明组合物中的赋形剂的例子是便于制备组合物的那些,例如通过在下文中描述的方法。这样的赋形剂包括药学上可接受的填充剂、缓冲剂、抗结块剂等等,没有限制。
可以包括在本发明组合物中的其它赋形剂的例子是在溶解组合物上可以提高感官性质的试剂。已经发现,帕瑞考昔,特别是帕瑞考昔钠,具有一种不愉快的苦味。在一种优选实施方案中,组合物包括至少一种改善器官感觉的试剂,选自甜味剂、调味剂和味觉调节剂。合适的甜味剂包括可溶性糖例如右旋糖、果糖、蔗糖和甘露糖醇,合成甜味剂例如糖精、环拉酸、丁磺氨、阿斯巴特、新甜素(neotame)和它们的盐。合适的天然的或合成的调味剂可以选自标准手册,例如Fenaroli′s Handbook of FlavorIngredients,3rd edition(1995)。合适的天然调味剂的非限定性例子,其中有一些可以很容易地用合成的试剂或其组合模仿,包括杏仁、茴香、苹果、杏、香柠檬、黑莓、黑醋栗、蓝莓、可可、焦糖、樱桃、肉桂、丁子香、咖啡、芫荽、红莓、枯茗、莳萝、桉树、小茴香、无花果、姜、葡萄、葡萄柚、番石榴、蛇麻、柠檬、甘草、白柠檬、麦芽、桔、糖浆、肉豆蔻、甜橙、桃子、梨、薄荷、悬钩子、玫瑰、留兰香、草莓、橘子、茶叶、香子兰、冬青等等。味觉调节剂是影响受试者味觉感觉的那些试剂,包括麻醉剂。
优选的赋形剂是完全溶解在含水赋形剂中的那些。可以选择性地包含从属的赋形剂以改善其它组分的溶解性;这样的从属赋形剂包括药学上可接受的润湿剂、环糊精等等。
干燥组合物可以以任何合适的形式存在,但是优选以快速溶解的形式存在,例如以粉剂(例如,通过下文所述的冷冻干燥制备的粉剂)或快速崩解的片剂的形式存在。任选地,可以包括一种泡腾剂,例如碳酸氢盐例如碳酸氢钠,以加快溶解和提供泡腾的器官感觉好处。
本发明的粉剂组合物优选具有足够的多孔性,以使其在加入到一种含水赋形剂中时,可以快速地溶解。通过使用冷冻干燥方法制备下文中所述的粉剂,可以获得高的孔隙度。
在一种说明性的方法中,将帕瑞考昔钠和一种缓冲剂,例如磷酸二钠七水合物,溶解在水中以制备一种水溶液。在溶液中的帕瑞考昔钠和缓冲剂的各自浓度与这些组分在最终组合物中想要的相对浓度一致。这些组分的绝对浓度不是关键的;然而考虑到方法的效力,通常,帕瑞考昔钠的浓度优选尽可能地高以不超出溶解度的范围内方便地制备。如果需要,在此阶段也可以加入其它的配方组分。加入的顺序不是关键的,但是为了确保快速和彻底地溶解,以及使帕瑞考昔暴露在水中的时间最短,强烈优选最后加入帕瑞考昔钠。
将该溶液计量到一个或多个冷冻干燥容器中,例如小瓶中。每个容器接受测定体积的溶液,其中该溶液具有想要剂量的帕瑞考昔钠。具有开口的塞子位于容器上,其中该开口允许升华发生。然后,将塞紧的容器放入冷冻干燥室中,对容器中的物质进行冷冻干燥,优选在三相循环中。
在冷冻干燥循环的第一阶段,每个容器中的溶液在低于溶液的玻璃态转化温度下冷冻。包含帕瑞考昔钠和磷酸二钠的组合物的玻璃态转化温度约为-20℃。可以通过本领域已知的任何技术测量玻璃态转化温度,例如使用冷冻干燥显微镜或通过电阻测量的方法测量玻璃态转化温度。冷冻阶段的合适的温度通常约为-30℃-约-60℃,例如约-40℃-约-50℃。通常在约1-约5小时内,更通常在约2-约4小时内,温度逐渐从室温降低到需要的冷冻温度。然后,温度在冷冻温度保持通常约0.5-约24小时,更通常约0.75-约3小时。
在一种优选的冷冻干燥方法的冷冻阶段,例如在约0.25-约1小时内,更优选在约0.5-约0.75小时内,温度从室温十分快速地下降到约-20℃。然后,例如在约1-约4小时内,更优选在约1.5-约3小时内,温度从约-20℃更逐渐地下降到约-30℃。不受理论的束缚,有理由相信这种逐渐下降的温度可以确保溶液完全冷冻。然后,例如在约0.1-约1小时内,更优选在约0.25-约0.5小时内,温度从约-30℃十分快速地下降到最终冷冻温度,优选约为-40℃。已经发现,如上所述的逐步冷冻阶段有助于提供没有裂纹的最终冻干制品。
在冷冻干燥循环的第二阶段,通过在冷冻干燥室中抽真空进行冷冻干燥。这个阶段在此被描述成″初次干燥″阶段。通常,约25-约500μmHg(约25-约500毫托)的真空,优选约50-约300μmHg的真空是合适的。在初次干燥阶段期间,温度逐渐被升高,当温度保持恒定时,任选地通过周期分阶段分开。优选用氮气吹扫保持真空。在此阶段,冰从冷冻溶液中升华,形成部分干燥的饼状物。
在优选冷冻干燥方法的初次干燥阶段,首先在约1-约5小时内,优选在约2-约4小时内,温度从冷冻温度,例如约-40℃上升到约0℃,然后在约0℃下保持一段时间,例如约6-约12小时,优选约8-约10小时。在初次干燥阶段,优选约150-约300μmHg的真空。
在冷冻干燥循环的第三阶段,干燥在真空下完成。这个阶段在此被描述成″二次干燥″阶段。再次,通常约25-约500μmHg,优选约50-约300μmHg的真空是合适的,优选用氮气吹扫保持真空。在二次干燥阶段,温度优选被升高到室温以上,例如约40℃,以赶走剩余的水汽,并获得一种含水量小于约5wt%,优选小于约2wt%,更优选小于约1wt%的粉剂。
在一种优选冷冻干燥方法的二次干燥阶段,首先在约1-约1小时内,优选在约1.5-约3小时内,温度从约0℃,升高到约40℃,然后在约40℃下保持约3-约12小时,优选约4-约8小时。在二次干燥期间,优选使用约为150-约300μmHg的真空。任选地在二次干燥阶段的后半部分期间,温度保持在约40℃,同时真空下降到约25-约75μmHg。
整个冷冻干燥循环时间通常约为18-约36小时。延长循环时间通常不会损害最终产品的质量,但会增加操作费用。产品质量和操作经济的最佳组合可以基于在此公开的信息通过常规测试获得,并随几个因素而改变,包括使用的具体冷冻干燥设备、选择的容器、冷冻干燥的溶液中组分的确切组成和浓度等等。然而,通常,发现约18-约24小时的循环时间是合适的。在磷酸二钠作为缓冲剂的帕瑞考昔钠组合物的情况中,现已发现循环时间小于约18小时,例如16.5小时,将使最终产品破裂的发生率增加,这反过来对加入到一种含水赋形剂中快速溶解没有帮助。
在完成冷冻干燥循环后,释放真空,温度回到室温。然后,密封容器以防止从空气中再吸收水分。
适于口服的帕瑞考昔的离散剂型例如片剂和胶囊,可以通过本领域已知的方法制备。最少量的水与帕瑞考昔接触和/或帕瑞考昔与水最短接触时间的方法是优选的。
本发明的第二种实施方案:一种制备的产品
在第二种实施方案中,本发明提供一种包括一种基本上不透水的包装的制备的产品,其中该包装中包含一种单一剂量单位的可口服给予的药物组合物,该药物组合物基本上不含水并且包含一种治疗有效量的帕瑞考昔或其水溶性盐。该组合物优选充分地可溶于一种药学上可接受的含水赋形剂中,以形成一种可口服给予的溶液。
在此″基本上不透水的″是指这样的包装,当该包装存储在常规空气条件下时,在至少约30天,优选至少约6个月以及更优选至少约2年的储存期内,可以充分地阻止水汽进入,以使组合物基本上不含水。
合适的包装材料包括但不限于玻璃、聚丙烯、铝等等。该包装必须密封以防止水汽通过任何开口或裂缝进入。因为该包装仅仅包含单一剂量单位的组合物,因此使用后不必再密封。
上面描述的是一种制备的产品,包括多个连接在一起的基本上不透水的包装,每个包装中包含单一剂量单位的本发明的组合物。例如,遇水可迅速分散的(例如泡腾的)单位剂量片剂可以单个地包装在多个不透水的常规的箔包装或泡罩包装的间隔中。
本发明的第三种实施方案:一种治疗或预防方法
在第三种实施方案中,为患者提供一种治疗或预防COX-2调节的病症的方法。该方法包括(a)在一种药学上可接受的含水赋形剂中,溶解至少一个剂量单位的基本上不含水并且包含一种治疗有效量的帕瑞考昔或其水溶性盐的药物组合物,以形成一种溶液,以及(b)在该溶液在出现不溶物质的沉淀之前,患者口服该溶液。
含水赋形剂可以是任何药学上可接受的水成液,包括在上文指出的那些。无论该干燥组合物是否包括这些组分,任选地,含水赋形剂可以包含一种或多种组分例如甜味剂或调味剂以抵消帕瑞考昔的不愉快的味道。
对于口服的剂量单位的组合物,可以使用任何适宜体积的水成液作为赋形剂。通常,体积优选不大于约100ml,以及体积更优选不大于约50ml。
当该干燥组合物以粉剂的形式存在时,例如以冷冻干燥粉剂的形式存在时,通常将水成液加入到包装有粉剂的容器中是最方便的。为此,容器优选足够大以容纳适宜体积的液体,一旦容器开口,可以在服药前溶解组合物。
当干燥组合物以离散的剂型存在时,例如片剂,可以在一个喝水容器中将一片或多片药剂加入到适宜体积的水成液中,其中在服药前溶解该组合物。
搅拌或搅动发生溶解的溶液或贮器是有利的,可以加快溶解的过程。本发明的组合物优选仅仅需要温和的搅拌或搅动或没有搅拌或搅动。
优选溶解完就马上服用所得溶液。迟延服药会在溶液中产生不溶解的伐地考昔沉淀,这降低了通过本发明的方法获得的好处。通常,在溶液制备完成后,口服在约15分钟内完成,优选在约5分钟内完成。
本发明的组合物用于治疗和预防非常宽范围的由COX-2调节的病症,包括但不限于以炎症、疼痛和/或发烧为特征的病症。这样的组合物尤其可用作消炎药,例如用于治疗关节炎,具有比相对于COX-1上缺乏对COX-2选择性的常规的NSAIDs的组合物具有明显较少的有害副作用的额外的益处。特别地,与常规的NSAIDs组合物相比,本发明的组合物具有降低胃肠毒性和胃肠刺激性的潜能,包括上胃肠道溃疡和出血。因此,本发明的组合物特别是用作常规NSAIDs的代替品,其中这样的NSAIDs例如在患有消化性溃疡、胃炎、局限性肠炎、溃疡性结肠炎、憩室炎或具有复发史的胃肠损伤;胃肠出血、凝固障碍包括贫血例如低凝血酶原血、血友病或其它的出血问题;肾病的患者中;或者手术前的患者中或服用抗凝血剂的患者中是禁忌的。
本发明的组合物可以用于治疗各种关节炎,包括但不限于,类风湿性关节炎、脊椎关节病、痛风性关节炎、骨关节炎、系统性红斑狼疮和少年关节炎。
这样的组合物可以用于治疗哮喘、支气管炎、月经痛、预产期前的阵痛、肌腱炎、粘液囊炎、变应性神经炎、巨细胞病毒感染、细胞程序死亡包括HIV-诱导的细胞程序死亡、腰痛、肝脏疾病包括肝炎、与皮肤有关的病症例如牛皮癣、湿疹、粉刺、烧伤、皮炎和紫外线损伤包括晒斑、以及手术后炎症包括眼睛手术例如白内障手术或曲光手术后炎症。
这样的组合物可以用于治疗胃肠疾病例如炎症性肠病、克罗恩氏病、胃炎、过敏性肠综合征和溃疡性结肠炎。
这样的组合物可以用于治疗在这样的疾病中的炎症,例如偏头痛、结节性动脉周围炎、甲状腺炎、再生障碍性贫血、何杰金氏病、硬皮病、风湿热、I型糖尿病、神经肌肉接头疾病包括重症肌无力、白质疾病包括多发性硬化症、结节病、肾病综合征、贝切特氏综合征、多肌炎、龈炎、肾炎、超敏性、损伤后的肿胀包括脑脑水肿、心肌缺血等等。
这样的组合物可以用于治疗眼睛疾病,包括但不限于,炎性疾病例如内眼炎、巩膜外层炎、视网膜炎、虹膜炎、睫状体炎、脉络膜炎、角膜炎、结膜炎和睑炎,眼睛的多于一个部分的炎性疾病例如视网膜脉络膜炎、虹膜睫状体炎、虹膜睫状体脉络膜炎(亦称眼色素层炎)、角膜结膜炎、睑结膜炎等等;其它COX-2调节的视网膜病包括糖尿病性视网膜病;畏光症、任何眼睛组织的急性损伤包括术后创伤例如白内障或角膜移植手术后的创伤;术后眼睛炎症;手术中的瞳孔缩小;角膜移植排斥;眼睛的例如视网膜的新血管形成包括下述的损伤或感染;黄斑变性;黄斑囊样水肿;晶状体后纤维增生症;新生血管性青光眼;以及眼睛疼痛。
这样的组合物可以用于治疗肺部炎症例如与病毒感染和囊性纤维化有关的那些疾病,并且这样的组合物可以用于治疗骨吸收例如与骨质疏松症有关的那些疾病。
这样的组合物可以用于治疗某些中枢神经系统疾病例如皮质痴呆包括阿尔茨海默氏病、由于中风、局部缺血和创伤造成的神经变性和中枢神经系统损伤。术语″治疗″在本发明的上下文中包括部分或全部抑制痴呆,包括阿尔茨海默氏病、血管性痴呆、多发梗塞性痴呆、早老年性痴呆、酒精中毒性痴呆和老年性痴呆。
这样的组合物可以用于治疗过敏性鼻炎、呼吸窘迫综合征、内毒素休克综合症和肝脏疾病。
这样的组合物可以用于治疗疼痛,包括但不限于术后疼痛、牙痛、肌肉疼痛和由癌症引起的疼痛。例如,这样的组合物可以在各种病症中用于缓减疼痛、发烧和炎症,这些病症包括风湿热、流感、及其他病毒感染包括普通感冒、背下部和颈部疼痛、痛经、头痛、牙痛、扭伤和劳损、肌炎、神经痛、滑膜炎、关节炎包括类风湿性关节炎、关节变性病(骨关节炎)、痛风和强直性脊柱炎、粘液囊炎、烧伤、外科和牙科手术后的创伤。
这样的组合物可以用于治疗和预防与炎症有关的心血管疾病,包括血管疾病、冠状动脉病、动脉瘤、血管排斥反应、动脉硬化、动脉粥样硬化包括心脏移植动脉粥样硬化、心肌梗塞、栓塞、中风、血栓形成包括静脉血栓形成、心绞痛包括不稳定的心绞痛、冠状血小板炎症、细菌引起的炎症包括衣原体引起的炎症、病毒导致的炎症以及与外科手术有关的炎症例如血管移植术包括冠状动脉旁路术、再血管化手术包括血管成形术、支架放置、动脉内膜切除术、或涉及动脉、静脉和毛细管的其它侵入方法。
这样的组合物可以用于治疗患者与血管形成有关的疾病例如抑制肿瘤血管生成。这样的组合物可以用于治疗肿瘤形成包括肿瘤转移;眼科病症例如角膜移植排斥、眼睛新血管形成、视网膜新血管形成包括损伤或感染后的新血管形成、糖尿病性视网膜病、黄斑变性、晶状体后纤维增生症和新生血管性青光眼;溃疡性疾病例如胃溃疡;病理的但非恶性的病症例如血管瘤包括婴儿血管瘤、鼻咽的血管纤维瘤和骨的无血管形成性坏死;以及雌性生殖系统疾病例如子宫内膜异位症。
这样的组合物可以用于预防和治疗良性的和恶性的肿瘤以及肿瘤形成包括癌症,例如结肠直肠癌、脑癌、骨癌、源自上皮细胞的肿瘤形成(上皮癌)例如基底细胞癌、腺癌、胃肠癌例如唇癌、口腔癌、食道癌、小肠癌、胃癌、结肠癌、肝癌、膀胱癌、胰腺癌、卵巢癌、子宫颈恶性肿瘤、肺癌、乳腺癌、皮肤癌例如鳞状上皮细胞和基细胞癌、前列腺癌、肾细胞癌、及其它已知的作用整个身体的上皮细胞的癌症。对于肿瘤形成,本发明的组合物特别是可以用于胃肠癌、巴雷特食管、肝癌、膀胱癌、胰腺癌、卵巢癌、前列腺癌、子宫颈癌、肺癌、乳腺癌和皮肤癌。这样的组合物还可以用于治疗放射治疗时发生的纤维化。这样的组合物可以用于治疗患有腺瘤性息肉包括家族性多发性腺癌(PAP)的那些患者。此外,这样的组合物可以用于预防患者处于FAP危险之中形成的息肉。
这样的组合物通过抑制收缩性前列腺素的合成,从而前列腺素引起的平滑肌收缩,因此可以用于治疗痛经、早产、哮喘和与嗜曙红细胞有关的疾病。它们还可以用于减少骨损失特别是减少绝经后妇女的骨损失(即治疗骨质疏松症),以及用于治疗青光眼。
本发明的组合物优选用于治疗类风湿性关节炎和骨关节炎,通常用于疼痛控制(特别是口腔外科手术后疼痛、普通外科手术后疼痛、矫形外科手术后疼痛、以及骨关节炎的急性潮红),用于预防和治疗头痛和偏头痛,用于治疗阿尔茨海默氏病,以及用于结肠癌的化学预防。
因为本发明的组合物可以表现出快速开始的治疗作用,这些可口服给予的选择性COX-2抑制药物的组合物在治疗急性COX-2介导的疾病上特别有利,尤其是在缓减疼痛例如头痛包括窦性头痛和偏头痛。
本发明的组合物除用于人类治疗之外,还可以用于结伴动物、外来动物、家畜等等,特别是哺乳动物的治疗。更特别地是,本发明的组合物可以用于治疗马、狗和猫的COX-2介导的疾病。
预防、从病症或疾病中得到减轻、或改善病症和疾病的给药方案优选一天一次或一天两次,但是给药方案可以根据各种因素改变。这些因此包括患者的类型、年龄、体重、性别、饮食和医疗条件,以及疾病的性质和严重程度。因此,实际使用的给药方案在很大程度上可以改变,因此可以偏离上面所述的优选给药方案。
初步治疗可以用上面给出的给药方案开始。根据需要,治疗通常持续几个星期至几个月或几年,直到病症或疾病得到控制或消除。通常,患者用本发明的组合物进行治疗可以通过本领域公知的任何方法进行监测,以确定治疗的有效性。连续分析监测数据可以允许在治疗期间改变剂量方案,以便在任何一时间点上给予最佳有效剂量,这样可以确定治疗的时间。以这种方式,在整个治疗期间,治疗方案和剂量安排可以合理的进行改变,以使给予最少量的组合物获得令人满意的效果,只要可以成功地治疗病症或疾病,此药物组合物可以连续服用。
现已发现,当口服给予患病的人时,帕瑞考昔快速地并且完全地转化为伐地考昔。因此,令人惊讶地是,当需要快速开始治疗作用时,口服给予治疗有效量的帕瑞考昔,例如以帕瑞考昔钠盐的形式,这等于口服给予治疗有效量的伐地考昔。在这里,术语″等于″是指在摩尔量或绝对量(即重量)上相等。基于分子量,1mg帕瑞考昔完全转化,产生约0.85mg的伐地考昔。从实际角度来说,认为1mg帕瑞考昔相当于1mg伐地考昔不会造成大的误差。
因此根据本发明的一种实施方案,本发明提供一种在患病的人中治疗COX-2介导的疾病的方法,包括患者口服给予帕瑞考昔或其盐,其中帕瑞考昔剂量等于治疗有效剂量的伐地考昔。帕瑞考昔或其盐例如钠盐的每日剂量优选为约1mg-约200mg。每日剂量更优选约为5mg-约120mg,更优选约为10mg-约100mg,例如约20mg,约40mg或约80mg的帕瑞考昔。
在一种尤其令人惊讶的发现中,其在图2中所示,帕瑞考昔如此迅速和完全地转化为伐地考昔,以致口服帕瑞考昔的患者可以比口服相同剂量的以立即释放形式伐地考昔本身要更早获得伐地考昔的血浆浓度峰值。
本发明的治疗方法还包括帕瑞考昔或本发明的组合物与一种或多种选自下面的药物的联合治疗,这些药物选自鸦片及其它镇痛药包括麻醉性镇痛药、Mu受体拮抗剂、Kappa受体拮抗剂、非麻醉药(即非成瘾的)镇痛药、单胺吸收抑制剂、腺苷调节剂、大麻素衍生物、P物质拮抗剂、神经激肽-1受体拮抗剂和钠通道阻滞剂等等。联合治疗优选包括使用本发明的组合物与一种或多种选自下面的化合物,这些化合物选自醋氯芬酸、阿西美辛、ε-乙酰胺基己酸、阿仙达明那芬、乙酰氨萨罗、乙酰苯胺、乙酰基水杨基水杨酸、S-腺苷甲硫氨酸、阿氯芬酸、阿芬他尼、烯丙苯哌啶、阿明洛芬、阿洛泼林、阿法罗定、二(乙酰水杨酸)铝、氨芬酸、氨氯苯嗪、3-氨基-4-羟丁酸、2-氨基-4-皮考啉、甲胺丙胺安替比林、氨基比林、阿米曲林、水杨酸铵、安吡昔康、呱氨托美丁、安那里丁、安替比林、水杨酸安替比林、安拉非宁、阿扎丙宗、阿斯匹林、巴柳氮、苄达酸、贝诺酯、苯噁洛芬、苄哌吡酮、苄达明、苄吗啡、黄连素、贝尔洛芬、氰苯咪呱啶、α-没药醇、溴芬酸、对溴乙酰苯胺、5-溴水杨酸乙酸酯、5-溴水杨醇、布西丁、氯环己苯酰丙酸、布可龙、丁苯羟酸、丁丙二苯肼、丁丙诺啡、布他西丁、布替布芬、布托啡诺、乙酰水杨酸钙、酰胺咪嗪、卡必芬、卡布洛芬、卡沙兰、氯代丁醇、氯西诺泰、水杨酸胆碱、辛可芬、桂美辛、西拉马多、环氯茚酸、氯美辛、氯尼他秦、氯尼辛、氯吡酸、丁香、可待因、可待因甲基溴、磷酸可待因、硫酸可待因、克罗丙胺、克罗乙胺、二氢脱氧吗啡、右旋二苯哌啶二噁烷、右旋吗拉迈得、地佐辛、地恩丙胺、双氯酚酸钠、二苯酰胺吡唑、双苯哌醋胺、二氟苯水杨酸、二氢可待因、二氢可待因酮、乙酸烯醇酯、二氢吗啡、乙酰水杨酸二羟化铝、地美沙多、美沙醇、二甲噻丁、吗苯丁酯、地匹哌酮、地匹乙酯、安乃近、地他唑、哚昔康、依莫法宗、苯乙氨茴酸、依匹唑、依他佐辛、依那西普、依特柳酯、乙柳酰胺、乙庚嗪、二氨乙氧重氮苯、乙基甲基噻吩丁烯胺、乙基吗啡、依托度酸、依托芬那酯、乙氧硝唑、丁香酚、联苯乙酸、联苯丁酮酸、芬克洛酸、芬度柳、非诺洛芬、芬太尼、芬替酸、非普地醇、非泼拉酮、氟喹氨苯酯、氟灭酸、氟诺洛芬、对氟苯乙砜、氟吡汀、氟丙喹酮、氟比洛芬、磷酸柳酯、龙胆酸、格拉非宁、葡卡美新、水杨酸乙二醇酯、愈创木薁、氢可酮、氢化吗啡酮、羟基哌替啶、异丁苯乙酸、布洛芬、异丁普生、水杨酸咪唑酯、吲哚美辛、吲哚布洛芬、英夫利昔单抗、白介素-10、三苯唑酸、isoladol、异美沙酮、羟烟甲苯胺、依索克酸、伊索昔康、甲哌酮、酮基布洛芬、酮咯酸、乳酰乙氧苯胺、来苯胺、利富吩、来苷帕泛、罗芬太尼、氯苯唑酸、氯诺西康、乐活布洛芬、乙酰水杨酸赖氨酸酯、乙酰水杨酸镁、甲氯灭酸、甲灭酸、派替啶、美他西诺、美沙拉嗪、美他佐辛、美沙酮、甲氧异丁嗪、甲吩噻嗪乙酸、甲氧夫啉、美托酮、莫非保松、莫芬唑酸、吗拉宗、吗啡、盐酸吗啡、硫酸吗啡、水杨酸吗啉、麦罗啡、纳布美通、纳布啡、水杨酸1-萘基酯、萘普生、那碎因。萘福潘、二烟酰吗啡、烟胺比林、尼氟灭酸、尼美舒利、5′-硝基-2′-丙氧基N-乙酰苯胺、左旋3-羟吗啡烷、去甲美沙酮、去甲吗啡、二苯哌己酮、奥沙拉嗪、鸦片、醋羟脯氨酸、吲肟酸、噁丙嗪、氧可酮、氧吗啡酮、羟保松、阿片金碱、胍苯叉芴、帕沙米特、喷他佐辛、哌立索唑、非那西汀、非那多松、非那佐辛、非那吡啶、盐酸盐、非诺可、苯哌利定、非诺吡酮、乙酰水杨酸苯酯、苯基保泰松、水杨酸苯酯、非尼拉朵、吡酮洛芬、去痛定、哌布宗、哌吡唑酮、吡拉唑酸、哌腈米特、吡罗昔康、吡洛芬、普拉洛芬、丙谷美辛、普罗庚嗪、二甲哌替啶、丙帕他莫、丙吡胺、丙氧酚、异丙安替比林、普罗喹宗、丙替嗪酸、雷米那酮、瑞芬太尼、甲硫酸吡嘧乙酯、醋水杨胺、水杨苷、水杨酰胺、邻氨甲酰基苯氧乙酸、水杨酸硫酸酯、萨利萨尔、胺乙氧苯酰苯胺、西美曲特、水杨酸钠、舒芬太尼、柳氮磺胺吡啶、舒林酸、过氧化物歧化酶、噻丙吩、琥保松、氟烟酞酯、替尼达普、替诺昔康、特罗芬那酯、汉防己碱、thiazolinobutazone、噻洛芬酸、噻拉米特、替立定、氨苄噻吡酯、托灭酸、托美丁、曲马多、tropesin、氯苄吡醇、联苯丁酸、肟环苯丙酸、扎托洛芬、齐考诺肽和苯酰吡酸钠(参见Merck Index,13th Edition(2001),治疗种类和生物活性索引,其标题为″止痛″、″消炎″和″退热″)。
使用帕瑞考昔或本发明的组合物与鸦片化合物的联合治疗是特别优选的,更特别地是鸦片化合物是可待因、派替啶、吗啡或其衍生物。
与帕瑞考昔或本发明的组合物一起进行联合治疗的药物可以以任何途径给予,包括胃肠外、口服、局部等等。其中帕瑞考昔和药物两个都通过口服给予时,它们可以单独配制,或者一起配制在本发明的组合物中。其中帕瑞考昔与第二种药物例如鸦片药物一起配制,第二种药物可以以直接配制成释放、迅速开始、持久释放或二元的释放的形式。
在本发明的一种实施方案中,其中特别是当COX-2调节的病症是头痛或偏头痛时,本发明的帕瑞考昔组合物与血管调节剂,优选具有血管调节功能的黄嘌呤衍生物,更优选烷基黄嘌呤化合物一起进行联合治疗。
本发明的实施方案包括联合治疗,其中烷基黄嘌呤化合物与在此提供的帕瑞考昔组合物一起给予,不管烷基黄嘌呤是否是一种血管调节剂,也不管联合治疗的疗效在任何程度上可导致血管调节作用。此处的术语″烷基黄嘌呤″包括具有一个或多个C1-C4烷基取代基,优选甲基的黄嘌呤衍生物,以及这种黄嘌呤衍生物的药学上可接受的盐。二甲基黄嘌呤和三甲基黄嘌呤包括咖啡因、可可碱和茶碱,其中茶碱是尤其优选的。烷基黄嘌呤化合物最优选是咖啡因。
选择帕瑞考昔和血管调节剂或烷基黄嘌呤的总剂量和相对剂量,以有效地治疗和/或预防与头痛或偏头痛有关的疼痛。合适的剂量将取决于所选自的具体血管调节剂或烷基黄嘌呤。例如,在用帕瑞考昔和咖啡因进行联合治疗时,通常帕瑞考昔的日剂量约为10mg-约100mg,优选约20mg-约80mg,咖啡因的日剂量约为1mg-约500mg,优选约10mg-约400mg,更优选约20mg-约300mg。
联合治疗的血管调节剂或烷基黄嘌呤成分可以以任何合适的剂型通过任何合适的途径优选口服给予。血管调节剂或烷基黄嘌呤可以任选地与帕瑞考昔以单一口服剂量形式一起配制。因此,本发明的组合物任选地包括帕瑞考昔和血管调节剂或烷基黄嘌呤例如咖啡因,它们的总剂量和相对剂量与前面所述的一致。或者,帕瑞考昔可以存在于一个干燥组合物中,该干燥组合物适于溶解在在此提供的含水赋形剂中,以及血管调节剂或烷基黄嘌呤可以存在于含水赋形剂中。例如,咖啡因化的饮料例如茶叶、咖啡或咖啡因化的苏打水或运动饮料可以作为赋形剂用于溶解本发明的帕瑞考昔组合物。
在上述组合物、制品和治疗方法中的帕瑞考昔可以上文通式给出的任何磺酰胺药物的前药代替。特别地,本发明还涉及新的具有结构式(V)的塞来考昔前药。
即,N-[[4-[5-(4-甲基苯基)-3-(三氟甲基)-1H-吡唑-1-基]苯基]-磺酰基]丙酰胺,和其药学上可接受的盐,例如钠盐(VI)
在此也称为化合物Z,可以在本发明的组合物中口服给予。
这些化合物可以通过上面所引的US 5,932,598,分别是实施例13和14中描述的方法制备,其中用适当的磺酰胺(在塞来考昔的情况下)和酐(在丙酸酐的情况下)代替。
实施例
以下实施例阐明本发明的一个方面,但是不应该解释为限制本发明的范围。
实施例1
在药动学研究中,测定11个健康成年男性患者的伐地考昔的血浆浓度。每个研究对象接受三个处理中的每一个,以随机顺序,治疗被15天分开。处理是:
(a)单一静脉注射(IV)20mg剂量的帕瑞考昔钠,从冷冻干燥粉剂中在1ml水中重新组成并一次推注给予;
(b)单一口服20mg剂量的伐地考昔,以直接释放伐地考昔片剂形式,与240ml水一起服用;和
(c)单一20mg剂量的帕瑞考昔钠,从冷冻干燥粉剂中在50ml水中重新组成,口服给予,接着用两个25ml的水洗涤容器。
每个处理后,研究对象在处理一、二和三小时后喝180ml的水。
血浆中伐地考昔浓度用有效的高效液相色谱法(HPLC)进行测定。服药后的0-24小时内,的伐地考昔的平均血浆浓度表示在图2中。下面计算的伐地考昔的血浆药物动力学参数列于表1中:
Cmax:最大浓度(ng/ml);
Tmax:达到最大浓度的时间(小时);
T1/2:血浆浓度的终点半衰期(小时);
AUC0-48:从0-48小时之间的血浆浓度曲线下面积(ng.hr/ml)-生物利用度的测定。
表1:伐地考昔在血浆中的药动学参数(平均±s.d.)
| 参数 | 帕瑞考昔IV | 伐地考昔口服 | 帕瑞考昔口服 |
| Cmax(ng/ml) | 312±39 | 284±62 | 297±69 |
| Tmax(小时) | 1.33±0.93 | 3.11±0.55 | 1.22±0.56 |
| T1/2(小时) | 7.41±2.29 | 7.69±2.45 | 7.33±2.49 |
| AUC0-48(ng.hr/ml) | 2555±684 | 3116±604 | 2590±809 |
当帕瑞考昔静脉内给予时,伐地考昔获得最大血浆浓度的时间(Tmax=1.33小时),要比伐地考昔口服给予时,伐地考昔获得最大血浆浓度的时间(Tmax=3.11小时)伐地考昔要早。
令人惊讶地,当根据本发明帕瑞考昔口服给予时获得的伐地考昔最大血浆浓度的时间(Tmax=1.22小时),并不比当帕瑞考昔通过静脉内给予时获得的伐地考昔最大血浆浓度的时间长。此外,达到最大伐地考昔浓度(Cmax=297ng/ml)与用静脉注射帕瑞考昔(Cmax=312ng/ml)或口服伐地考昔(Cmax=284ng/ml)相似。
实施例2
在药动学研究中,测定6个健康成年雄性比格犬的塞来考昔的血浆浓度。每个研究对象接受如下描述的三种处理中的每一种。处理(a)和(b)比治疗(c)在更早的时间给予以随机的顺序进行,但是对相同的狗进行处理。
处理是:
(a)单一口服200mg剂量的以西乐葆胶囊形式的塞来考昔;
(b)单一口服200mg剂量的塞来考昔,以在苹果汁中新配制的悬浮液的形式;并且
(c)单一口服剂量的化合物Z水溶液,浓度24.1mg/ml,等于20mg/ml的塞来考昔,用量10ml。
每种处理通过胃插管法以一次给予,接着给予10ml水。
血浆中塞来考昔浓度用有效的高效液相色谱法(HPLC)进行测定。服药后的0-24小时内的塞来考昔平均血浆浓度表示在图3中。塞来考昔计算的血浆药动学参数在表2中给出。
表2:血浆中塞来考昔的药动学参数(平均±s.d.)
| 参数 | 塞来考昔胶囊 | 塞来考昔苹果计悬浮液 | 化合物Z溶液 |
| Cmax(ng/ml) | 852±690 | 4602±1305 | 5040±1298 |
| Tmax(小时) | 1.05±1.10 | 0.33±0.13 | 1.83±0.68 |
| AUC(ng.hr/ml) | 6792±5822 | 30635±16590 | 55733±32451 |
Claims (34)
1.一种药物组合物,其基本上不含水并包含至少一个剂量单位,该剂量单位含有治疗有效量的化合物X-SO2-NHR1或其药学上可接受的盐,其中X是一个以使化合物X-SO2-NH2是一种已知的药物的选择部分,化合物X-SO2-NHR1很容易地在体外被降解成药物X-SO2-NH2;以及其中R1是一个至多8个碳原子的基团,选自烷基、羟基烷基、烷氧基烷基、羧基烷基、酰基、烷基羰基、烷氧基羰基、羟基烷基羰基、烷氧基烷基羰基、羧基烷基羰基、氨基烷基羰基、苯基羰基、苄基羰基、苯基(羟基)甲基羰基、烷氧基羰基羰基、烷氧基羰基烷基羰基、烷基羰基氨基烷基羰基、烷氧基羰基氨基烷基羰基、烷氧基羰基羰基、氨基酸残基和杂芳基羰基;所述组合物是可口服给予的并且有手段抑制化合物X-SO2-NHR1或其盐在口服前降解成药物X-SO2-NH2。
2.权利要求1的组合物,其中药物X-SO2-NH2是一种选择性COX-2抑制药物。
3.权利要求1的组合物,其中药物X-SO2-NH2选自由伐地考昔、塞来考昔和地拉考昔。
4.权利要求1的组合物,其中化合物X-SO2-NHR1是帕瑞考昔并且以帕瑞考昔游离酸或其药学上可接受的水溶性盐的形式存在。
5.权利要求4的组合物,其中在每个剂量单位中,帕瑞考昔或其水溶性盐的量为约1mg-约200mg。
6.权利要求4的组合物,其中在每个剂量单位中,帕瑞考昔或其水溶性盐的量为约5mg-约120mg。
7.权利要求4的组合物,其中在每个剂量单位中,帕瑞考昔或其水溶性盐的量为约10mg-约100mg。
8.权利要求4的组合物,有抑制帕瑞考昔或其水溶性盐转化为伐地考昔的手段,这些办法包括防止组合物充分暴露于水。
9.权利要求8的组合物,其中充分防止组合物暴露在水中的办法包括一种密封的和基本上不透水的包装或容器。
10.权利要求8的组合物,其中充分防止组合物暴露在水中的办法包括一种基本上不透水的包衣。
11.权利要求4的组合物,其有手段抑制帕瑞考昔或其水溶性盐转化为伐地考昔,包括一种组合物的制剂,当与帕瑞考昔或其水溶性盐密切接触时,其基本上没有任何趋于促进这种转化的赋形剂。
12.权利要求4的组合物,其有手段抑制帕瑞考昔或其水溶性盐转化为伐地考昔,其包括一种组合物的制剂,所述制剂包括促进所述转化的赋形剂以及在所述赋形剂以及帕瑞考昔或其水溶性盐之间的隔离层。
13.权利要求4的组合物,其基本上可溶于一种药学上可接受的含水赋形剂中以制备一种可口服给予的溶液。
14.权利要求13的组合物,其以粉末的形式存在。
15.权利要求14的组合物,其中粉末通过包括冷冻干燥的方法进行制备。
16.权利要求13的组合物,其以可迅速崩解的片剂的形式存在。
17.权利要求16的组合物,其中片剂是泡腾剂。
18.权利要求13的组合物,还包括至少一种试剂以改善溶液的感官特性。
19.权利要求18的组合物,其中改善溶液感官特性的至少一种试剂选自由甜味剂、调味剂和口味调节剂。
20.权利要求18的组合物,其中改善溶液感官特性的至少一种试剂是一种甜味剂。
21.权利要求20的组合物,其中甜味剂是一种可溶性糖,选自由右旋糖、左旋糖、蔗糖和甘露糖醇。
22.权利要求20的组合物,其中甜味剂是一种合成甜味剂,选自由糖精、环拉酸、丁磺氨、阿斯帕坦、新甜素和其盐。
23.权利要求18的组合物,其中改善溶液感官特性的至少一种试剂是一种调味剂。
24.权利要求23的组合物,其中调味剂选自由杏仁、茴香、苹果、杏、香柠檬、黑莓、黑醋栗、蓝莓、可可、焦糖、樱桃、肉桂、丁子香、咖啡、芫荽、红莓、枯茗、莳萝、桉树、小茴香、无花果、姜、葡萄、葡萄柚、番石榴、蛇麻、柠檬、甘草、白柠檬、麦芽、桔、糖浆、肉豆蔻、甜橙、桃子、梨、薄荷、悬钩子、玫瑰、留兰香、草莓、橘子、茶叶、香子兰、冬青调味剂以及它们的合成类似物。
25.一种包含一种基本上不透水的包装的制品,含有单一剂量单位的可口服给予的药物组合物,该药物组合物基本上不含水并且包含一种治疗有效量的X-SO2-NHR1化合物或其药学上可接受的盐,其中X是以致化合物X-SO2-NH2是一种已知的药物的部分,和其中R1是一个至多8个碳原子的基团,选自烷基、羟基烷基、烷氧基烷基、羧基烷基、酰基、烷基羰基、烷氧基羰基、羟基烷基羰基、烷氧基烷基羰基、羧基烷基羰基、氨基烷基羰基、苯基羰基、苄基羰基、苯基(羟基)甲基羰基、烷氧基羰基羰基、烷氧基羰基烷基羰基、烷氧基羰基烷基羰基、烷基羰基氨基烷基羰基、烷氧基羰基氨基烷基羰基、烷氧基羰基羰基、氨基酸残基和杂芳基羰基。
26.权利要求25的制品,其中药物X-SO2-NH2是一种选择性的COX-2抑制药物。
27.权利要求25的制品,其中药物X-SO2-NH2选自由伐地考昔、塞来考昔和地拉考昔。
28.权利要求25的制品,其中化合物X-SO2-NHR1是帕瑞考昔并且以帕瑞考昔游离酸或其药学上可接受的水溶性盐的形式存在。
29.权利要求28的制品,其中组合物是粉末的形式,并且包装是一种合适的密封容器,并且当打开时,可以加入一种可以溶解组合物的含水赋形剂。
30.权利要求28的制品,其中组合物是片剂的形式,以及该包装是薄箔包装或泡罩包装。
31.权利要求30的制品,其中多个片剂分别包装在薄箔包装或泡罩包装的隔室中。
32.一种治疗或预防COX-2调节疾病的方法,该方法包括(a)在一种药学上可接受的含水赋形剂中溶解至少一个剂量单位的一种药物组合物,该药物组合物基本上不含水并且包含一种治疗有效量的X-SO2-NHR1化合物或其药学上可接受的盐,其中X是以致化合物X-SO2-NH2是一种选择性COX-2抑制药物的部分,和其中R1是一个至多8个碳原子的基团,选自烷基、羟基烷基、烷氧基烷基、羧基烷基、酰基、烷基羰基、烷氧基羰基、羟基烷基羰基、烷氧基烷基羰基、羧基烷基羰基、氨基烷基羰基、苯基羰基、苄基羰基、苯基(羟基)甲基羰基、烷氧基羰基羰基、烷氧基羰基烷基羰基、烷氧基羰基烷基羰基、烷基羰基氨基烷基羰基、烷氧基羰基氨基烷基羰基、烷氧基羰基羰基、氨基酸残基和杂芳基羰基,以形成一种溶液;(b)在该溶液没有出现不溶性物质沉淀之前,口服给予患者该溶液。
33.权利要求32的方法,其中选择性COX-2抑制药物选自由伐地考昔、塞来考昔和地拉考昔。
34.权利要求32的方法,其中化合物X-SO2-NHR1是帕瑞考昔并且以帕瑞考昔游离酸或其药学上可接受的水溶性盐的形式存在。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US35059601P | 2001-11-13 | 2001-11-13 | |
| US60/350,596 | 2001-11-13 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN1615135A true CN1615135A (zh) | 2005-05-11 |
Family
ID=23377399
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNA028270843A Pending CN1615135A (zh) | 2001-11-13 | 2002-11-12 | 磺酰胺前药如帕瑞考昔的口服剂型 |
Country Status (20)
| Country | Link |
|---|---|
| US (1) | US20030100595A1 (zh) |
| EP (1) | EP1446118B1 (zh) |
| JP (1) | JP2005509002A (zh) |
| KR (1) | KR20050044459A (zh) |
| CN (1) | CN1615135A (zh) |
| AR (1) | AR037356A1 (zh) |
| AT (1) | ATE383156T1 (zh) |
| BR (1) | BR0214081A (zh) |
| CA (1) | CA2466504A1 (zh) |
| CO (1) | CO5580744A2 (zh) |
| DE (1) | DE60224558T2 (zh) |
| ES (1) | ES2297032T3 (zh) |
| IL (1) | IL161991A0 (zh) |
| MX (1) | MXPA04004476A (zh) |
| NO (1) | NO20042440L (zh) |
| PL (1) | PL369962A1 (zh) |
| RU (1) | RU2004114552A (zh) |
| TW (1) | TW200300680A (zh) |
| WO (1) | WO2003041705A1 (zh) |
| ZA (1) | ZA200403328B (zh) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112979572A (zh) * | 2020-11-24 | 2021-06-18 | 苏州璞正医药有限公司 | 一种帕瑞昔布衍生物及其制备方法和应用 |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7785640B2 (en) | 2004-01-16 | 2010-08-31 | Amerilab Technologies, Inc. | Effervescent composition including cranberry extract |
| ES2523796T1 (es) | 2004-10-08 | 2014-12-01 | Forward Pharma A/S | Composición farmacéutica de liberación controlada que comprende éster de ácido fumárico |
| WO2007038421A2 (en) * | 2005-09-27 | 2007-04-05 | University Of Kentucky Research Foundation | Berry preparations and extracts |
| EP1940382A2 (en) * | 2005-10-07 | 2008-07-09 | Aditech Pharma AB | Combination therapy with fumaric acid esters for the treatment of autoimmune and/or inflammatory disorders |
| CA2661274A1 (en) * | 2006-08-29 | 2008-03-06 | University Of Kentucky Research Foundation | Compositions and methods for oral cancer chemoprevention using berry preparations and extracts |
| EP1902708A1 (de) * | 2006-09-25 | 2008-03-26 | Losan Pharma GmbH | Wirkstoff enthaltende stabilisierte feste Arzneimittelformen und Verfahren zu ihrer Herstellung |
| DK2209501T3 (da) * | 2007-10-12 | 2012-02-27 | Astrazeneca Ab | Zibotentan-sammensætning, der indeholder mannitol og mikrokrystallinsk cellulose |
| DK2564839T3 (en) | 2009-01-09 | 2016-07-25 | Forward Pharma As | A pharmaceutical formulation comprising one or more fumaric acid esters in an erosion matrix |
| JP6102120B2 (ja) * | 2012-08-16 | 2017-03-29 | ニプロ株式会社 | 医薬製剤およびその製造方法 |
| CN104771370B (zh) * | 2014-01-14 | 2020-07-24 | 南京圣和药业股份有限公司 | 帕瑞昔布钠冻干粉针剂及其制备方法 |
| CN104965041B (zh) * | 2015-06-11 | 2016-06-29 | 成都克莱蒙医药科技有限公司 | 一种帕瑞昔布钠异构体的高效液相色谱检测方法 |
| CN106074399B (zh) * | 2016-06-21 | 2018-11-02 | 马鞍山丰原制药有限公司 | 一种帕瑞昔布钠冻干制剂及其制备方法 |
Family Cites Families (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE69432186T2 (de) * | 1993-11-18 | 2004-05-06 | Nippon Shinyaku Co., Ltd. | Verfahren zur herstellung stabiler arzneimittel |
| GB9523833D0 (en) * | 1995-11-22 | 1996-01-24 | Boots Co Plc | Medical treatment |
| DE69739003D1 (de) * | 1996-04-12 | 2008-10-30 | Searle Llc | Substituierte Benzensulfonamid-Derivate als Wirkstoff-Vorläufer von COX-2 Inhibitoren |
| SE9703693D0 (sv) * | 1997-10-10 | 1997-10-10 | Astra Pharma Prod | Novel combination |
| US6323226B1 (en) * | 1999-10-19 | 2001-11-27 | Texas Heart Institute | Treatment of heart disease with cox-2 inhibitors |
| AU1930301A (en) * | 1999-12-08 | 2001-06-18 | Pharmacia Corporation | Valdecoxib compositions |
| DE60027464T2 (de) * | 1999-12-22 | 2006-08-31 | Pharmacia Corp. | Arzneizubereitungen mit zwei verschiedenen freisetzungsraten enthaltend einen cyclooxygenase-2 hemmer |
| AU2001247745B2 (en) * | 2000-03-24 | 2006-08-31 | Pharmacia Corporation | Amidino compounds useful as nitric oxide synthase inhibitors |
| AR035642A1 (es) * | 2000-05-26 | 2004-06-23 | Pharmacia Corp | Uso de una composicion de celecoxib para el alivio rapido del dolor |
| US6306842B1 (en) * | 2000-06-02 | 2001-10-23 | Medinox, Inc. | Protected forms of a combination of pharmacologically active agents and uses therefor |
| WO2002005799A2 (en) * | 2000-07-13 | 2002-01-24 | Pharmacia Corporation | Combination of a cox-2 inhibitor and a vasomodulator for treating pain and headache pain |
| US7695736B2 (en) * | 2001-04-03 | 2010-04-13 | Pfizer Inc. | Reconstitutable parenteral composition |
-
2002
- 2002-11-12 KR KR1020047007335A patent/KR20050044459A/ko not_active Application Discontinuation
- 2002-11-12 US US10/292,682 patent/US20030100595A1/en not_active Abandoned
- 2002-11-12 EP EP02789593A patent/EP1446118B1/en not_active Expired - Lifetime
- 2002-11-12 PL PL02369962A patent/PL369962A1/xx not_active Application Discontinuation
- 2002-11-12 MX MXPA04004476A patent/MXPA04004476A/es active IP Right Grant
- 2002-11-12 TW TW091133146A patent/TW200300680A/zh unknown
- 2002-11-12 BR BR0214081-0A patent/BR0214081A/pt not_active IP Right Cessation
- 2002-11-12 RU RU2004114552/14A patent/RU2004114552A/ru not_active Application Discontinuation
- 2002-11-12 JP JP2003543592A patent/JP2005509002A/ja active Pending
- 2002-11-12 AT AT02789593T patent/ATE383156T1/de not_active IP Right Cessation
- 2002-11-12 CA CA002466504A patent/CA2466504A1/en not_active Abandoned
- 2002-11-12 AR ARP020104341A patent/AR037356A1/es unknown
- 2002-11-12 WO PCT/US2002/036253 patent/WO2003041705A1/en active IP Right Grant
- 2002-11-12 DE DE60224558T patent/DE60224558T2/de not_active Expired - Fee Related
- 2002-11-12 ES ES02789593T patent/ES2297032T3/es not_active Expired - Lifetime
- 2002-11-12 IL IL16199102A patent/IL161991A0/xx unknown
- 2002-11-12 CN CNA028270843A patent/CN1615135A/zh active Pending
-
2004
- 2004-05-03 ZA ZA200403328A patent/ZA200403328B/en unknown
- 2004-05-07 CO CO04042439A patent/CO5580744A2/es not_active Application Discontinuation
- 2004-06-11 NO NO20042440A patent/NO20042440L/no not_active Application Discontinuation
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112979572A (zh) * | 2020-11-24 | 2021-06-18 | 苏州璞正医药有限公司 | 一种帕瑞昔布衍生物及其制备方法和应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| DE60224558D1 (de) | 2008-02-21 |
| ZA200403328B (en) | 2005-04-13 |
| PL369962A1 (en) | 2005-05-02 |
| AR037356A1 (es) | 2004-11-03 |
| DE60224558T2 (de) | 2009-01-22 |
| EP1446118B1 (en) | 2008-01-09 |
| TW200300680A (en) | 2003-06-16 |
| KR20050044459A (ko) | 2005-05-12 |
| WO2003041705A1 (en) | 2003-05-22 |
| EP1446118A1 (en) | 2004-08-18 |
| IL161991A0 (en) | 2005-11-20 |
| NO20042440L (no) | 2004-08-09 |
| RU2004114552A (ru) | 2005-02-20 |
| JP2005509002A (ja) | 2005-04-07 |
| ATE383156T1 (de) | 2008-01-15 |
| ES2297032T3 (es) | 2008-05-01 |
| CO5580744A2 (es) | 2005-11-30 |
| CA2466504A1 (en) | 2003-05-22 |
| US20030100595A1 (en) | 2003-05-29 |
| BR0214081A (pt) | 2004-09-28 |
| MXPA04004476A (es) | 2004-08-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2002254609B2 (en) | Orally deliverable pharmaceutical composition comprising an active compound having an aminosulfonyl group (COX-2 inhibitor), a polyethylene glycol and a free-radical scavenging antioxidant | |
| ES2236007T3 (es) | Composiciones de inhibidor de ciclooxigenasa-2 ue tiene un efecto terapeutico rapido. | |
| US8362062B2 (en) | Pharmaceutical compositions with improved dissolution | |
| AU2002254609A1 (en) | Orally deliverable pharmaceutical composition comprising an active compound having an aminosulfonyl group (COX-2 inhibitor), a polyethylene glycol and a free-radical scavenging antioxidant | |
| CN1615135A (zh) | 磺酰胺前药如帕瑞考昔的口服剂型 | |
| EP1814517B1 (en) | Nonaqueous liquid parenteral aceclofenac formulation | |
| JP2005509002A6 (ja) | スルホンアミドプロドラックの経口剤形 | |
| ZA200503188B (en) | Celecoxib prodrug | |
| US20060052432A1 (en) | Pharmaceutical compositions with improved dissolution | |
| JP2005535644A (ja) | 安定な非経口パレコキシブ液体製剤 | |
| MXPA04011323A (es) | Compuestos de celecoxib amorfo estable y su proceso de obtencion. | |
| EP2339328A2 (en) | Pharmaceutical co-crystal compositions of celecoxib | |
| AU2002352646A1 (en) | Oral dosage form of a sulfonamide prodrug such as parecoxib | |
| ZA200307576B (en) | Orally deliverable pharmaceutical composition comprising an active compound having an aminosulfonyl group (Cox-2 inhibitor), a polyethylene glycol and a free-radical scavenging antioxidant. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |