CN1507464A - 具有全氟烷基的电活性芴聚合物、制备这种聚合物的方法以及用这种聚合物制造的器件 - Google Patents
具有全氟烷基的电活性芴聚合物、制备这种聚合物的方法以及用这种聚合物制造的器件 Download PDFInfo
- Publication number
- CN1507464A CN1507464A CNA028094476A CN02809447A CN1507464A CN 1507464 A CN1507464 A CN 1507464A CN A028094476 A CNA028094476 A CN A028094476A CN 02809447 A CN02809447 A CN 02809447A CN 1507464 A CN1507464 A CN 1507464A
- Authority
- CN
- China
- Prior art keywords
- general formula
- alkyl
- group
- aryl
- polymkeric substance
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/02—Macromolecular compounds containing only carbon atoms in the main chain of the macromolecule, e.g. polyxylylenes
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G61/00—Macromolecular compounds obtained by reactions forming a carbon-to-carbon link in the main chain of the macromolecule
- C08G61/12—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule
- C08G61/122—Macromolecular compounds containing atoms other than carbon in the main chain of the macromolecule derived from five- or six-membered heterocyclic compounds, other than imides
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Polyoxymethylene Polymers And Polymers With Carbon-To-Carbon Bonds (AREA)
- Electroluminescent Light Sources (AREA)
Abstract
本发明一般涉及全氟烷基化的芴聚合物。还涉及制备所述聚合物的方法和用所述聚合物制造的器件。
Description
发明背景
发明领域
本发明涉及具有全氟烷基的电活性芴聚合物,以及制备这种聚合物的方法。本发明还涉及其中包含这种聚合材料的电子器件。
有关技术的说明
在多种不同电子设备中存在有机电子器件。在所有这些器件中,有机活性层被夹在两层电接触层之间。有机电子器件的例子包括发光器件,如用于制造显示器的发光二极管(LED)。在LED中,至少一层电接触层是透光的,因此,光可通过电接触层。在横跨电接触层通电时,有机活性层发出的光通过透光的电接触层。
众所周知用有机的电致发光化合物作为发光二极管中的活性组分。已知简单的有机分子,如蒽、噻二唑衍生物和香豆素衍生物显示电致发光性。也已公开了几类发光聚合物。它们包括例如,聚(1,4-亚苯基亚乙烯基)和衍生物;聚噻吩,具体为聚(3-烷基噻吩)和聚(对-亚苯基)。聚芴的烷基和二烷基衍生物还在美国专利5708130和5900327中已公开。
对具有改进效率的光活性化合物及其制备方法仍有需求。
发明的概述
本发明涉及一种芴和芴衍生物的聚合物,其中,所述聚合物的芳环上具有全氟烷基取代基。
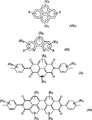
在一个实施方式中,所述芴聚合物包含一种或多种具有图1所示的通式I的单体单元,其中:
R在各自存在时可以相同或不同,是芳环中碳原子上的取代基,选自:氢、烷基、芳基、杂烷基、杂芳基、F、-CN、-OR1、-CO2R1、CψHθFλ、-OCψHθFλ、-SR1、-N(R1)2、-P(R1)2、-SOR1、-SO2R1、-NO2,具有图12所示的通式XII并且如以下“通式XII”进一步所描述的β-二羰基;或相邻的R基团一起可形成选自烷基、芳基、和杂芳基环的5-或6-元环,其中:
R1在各自存在时可以相同或不同,是杂原子上的取代基,选自烷基、芳基、杂烷基和杂芳基;
ψ是1-20的整数,θ和λ是满足下面等式A1的整数:
θ+λ=2ψ+1; (等式A1);
R2是不在芳环上的碳原子上的取代基,它可以相同或者不同,并选自氢、烷基、芳基、杂烷基、杂芳基和-CψHθFλ,前提是所述芴聚合物包含至少一个具有通式-CψF2ψ+1的R取代基,其中ψ如以上所定义的。
在另一实施方式中,所述芴聚合物包含至少一种具有图1所示通式I的第一单体单元,和至少一种第二单体单元,其中所述至少一种第二单体单元选自:(i)具有图2所示通式II的芳族基团,(ii)具有图6所示通式III的6元杂芳基,(iii)具有图7所示通式IV的5元杂芳基,(iv)具有图8所示的通式V的芳族基团,(v)具有图9所示通式VI-VIII、图10所示的通式IX-XI的二价稠环芳族基团,以及(6)它们的组合,其中:
在各通式II、III、IV、V、VI、VII、VIII和IX中:
R、R1、R2、ψ、θ和λ如以上通式I中所定义的;
E在各自存在时可以是相同或不同的,是单键或选自亚芳基和亚杂芳基的连接基团;
在通式IV中:
A在各自存在时分别为C或N,γ是0或选自1或2的整数,这样,如果两个A是N,则γ是0;或者如果一个A是N,一个A是C,则γ是1;或者如果两个A是C,则γ是2;
Q是O、S、SO2或NR1,其中:
R1在各自存在时可以相同或不同,是杂原子上的取代基,选自烷基、芳基、杂烷基和杂芳基;
在通式V中:
Q1是羰基、O、S、SO2或NR1,其中:
R1在各自存在时可以相同或不同,是杂原子上的取代基,选自烷基、芳基、杂烷基和杂芳基;
W是H、烷基或杂烷基;或两个W一起可代表一个单键;
在通式VI中:
两个E是在1,4-,1,5-,1,8-,2,3-或2,6-位;
在通式VII中:
两个E是在1,4-,1,5-,1,8-,2,3-,2,6-或9,10-位;
在通式VIII中:
第一个E是在1,2或3位;第二个E是在6,7或8位;
在通式IX中:
第一个E是在2,3或4位;第二个E是在7,8或9位;
在通式XII中:
R3选自氢、烷基、芳基、杂烷基和杂芳基;
δ是0或1-12整数;
其前提是所述芴聚合物包含至少一个具有通式-CψF2ψ+1的R取代基,其中ψ如上所述。
本发明还涉及制备具有全氟烷基的芴聚合物的方法,所述方法包括:
形成具有至少一种单体单元的聚合物,所述单体单元具有图1所示通式I;
在钌(II)催化剂存在下,用全氟烷基化试剂处理所述聚合物,所述试剂选自(i)全氟烷基碘化物,和(ii)全氟烷基磺酰氯。
本发明还针对有机电子器件,它具有至少一层包括上述全氟烷基化芴聚合物的发射层。
本文使用的术语“烷基”意指衍生自脂肪烃的基团,包括直链的、支链的和环状基团,它可以是未取代的或取代的。术语“杂烷基”意指衍生自具有至少一个杂原子在主链上的脂肪烃基团,该基团可以是未取代的或取代的。术语“芳基”意指衍生自芳烃的基团,它可以是未取代的或取代的。术语“杂芳基”意指衍生自含有至少一个杂原子的芳族基团,该基团可以是未取代的或取代的。术语“亚芳基”意指衍生自芳烃的、具有两连接点的基团,该基团可以是未取代的或取代的。术语“亚杂芳基”意指衍生自具有至少一个杂原子的芳基并具有两连接点的基团,该基团可以是未取代的或取代的。短语“相邻于”,当用于表示器件中的层时,不一定指:一层紧靠另一层。另一方面,短语“相邻的R基团”,用于表示化学式(即,多个R基团用键连接在多个原子上)中互相邻近的R基团。术语“芴聚合物”和“全氟烷基化芴聚合物”是指均聚物和共聚物。术语“基础芴聚合物”是指没有任何全氟烷基的芴聚合物。术语“光活性的”与任何显示电致发光和/或光敏性的材料有关。术语“电活性”涉及显示空穴输运/注入性质,电子输运/注入性质,电致发光和/或光敏性的任何材料。术语“单体单元”指聚合物中的重复单元。另外,通篇使用IUPAC编号体系,其中来自周期表的族,从左到右编号为1-18(化学和物理的CRC手册,第81版,2000年)。
附图说明
图1为本发明中使用的第一单体单元的通式I和通式I(a)。
图2为本发明中使用的第二单体单元的通式II。
图3为本发明中使用的第二单体单元的通式II(a)-II(j)。
图4为本发明中使用的第二单体单元的通式II(k)-II(s)。
图5为本发明中使用的第二单体单元的通式II(t)-II(z)。
图6为本发明中使用的第二单体单元的通式III和通式III(a)-III(g)。
图7为本发明中使用的第二单体单元的通式IV和通式IV(a)-IV(h)。
图8为本发明中使用的第二单体单元的通式V和通式V(a)-V(e)。
图9为本发明中使用的第二单体单元的通式VI和通式VI(a)-VI(d)。
图10为本发明中使用的第二单体单元的通式VII和通式VII(a)。
图11为本发明中使用的第二单体单元的通式VIII-通式XI。
图12为本发明中使用的第二单体单元取代基的通式XII。
图13是可装有本发明全氟烷基化芴聚合物的电子器件示意图。
较佳实例的详细说明
本发明芴聚合物包含至少一种芴基单体单元(通式I),并可以包含其它芳族单体单元(通式II、III、IV、V、VI、VII、VIII、IX、X和XI),其中,所述聚合物中至少一个芳环被至少一个全氟烷基取代。
第一单体单元
所述基础芴聚合物至少具有第一单体单元,所述单元具有图1所示的通式I。所述芴聚合物可以是两种或多种具有通式I的不同单体单元的共聚物。优选的R基团是具有1-30个碳原子的烷基,具有1-30个碳原子和一个或多个杂原子S、N、或O的杂烷基,具有6-20个碳原子的芳基,具有2-20个碳原子(或2-18个碳原子)和一个或多个杂原子S、N或0的杂芳基。适合的R基团的例子包括正丁基和异丁基、各种戊基,直链的或支链的;各种己基,各种辛基,包括2-乙基己基,直至十六烷基以上,可带有或不带有烯烃不饱和度;苯基,噻吩,咔唑,烷氧基,苯氧基和氰基。芴单体单元的苯基环上更优选的R基团是H,C1-C12烷氧基(或C1-C4烷氧基或C6-C12烷氧基)、苯氧基、C1-C12烷基(或C1-C4烷基或C6-C12烷基)、苯基或氰基。
优选的R2是具有1-30个碳原子的烷基,具有1-30个碳原子和一个或多个杂原子S、N、或O的杂烷基。更加优选的R2选自直链C6-C12烷基(或者直链C6-C10烷基),和支链C6-C12烷基(或者支链C6-C10烷基)。
适合的第一单体单元的例子在图1中如通式I(a)所示。
第二单体单元
在通式II、III、IV、V、VI、VII、VIII和IX中,当任意一种或多种E连接基选自杂亚芳基,则所述杂亚芳基可以选自具有通式XIII和图12所示XIV的基团,其中:
在通式XIII中:
R如上述通式I、II、III、IV、V、VI、VII、VIII-IX中所述的;
E1是单键;
在通式XII中:
R和Q如上述通式I、II、III、IV、V、VI、VII、VIII-IX中所述的;
E1是单键。
通式II:
第二单体单元可以是具有图2中通式II所示结构的芳基。R基团优选选自:
氢;
烷基;
芳基;
杂烷基;
杂芳基;
F;
-CN;
-NO2;
具有图12中所示通式XII的β-二羰基,并如上进一步所述;
-CψHθFλ;
-OCψHθFλ;和
-P(R1)2、-SOR1,-OR1、-CO2R1、-SR1、-N(R1)2和-SO2R1,其中R1是1-20个碳原子的直链或支链烷基,或者直链或支链的杂烷基;或者相邻的R基团一起可形成选自环烷基环、芳环和杂芳环的5-或6-元环。
或者,通式II中的R基团可选自:
1-12个碳原子的烷基;
部分或全部氟化的具有1-12个碳原子的烷基,尤其CF3;
具有6-20个碳原子的芳基;
具有4-20个碳原子,并用O、S或N取代的杂芳基;
具有1-12个碳原子的烷氧基;和具有3-15个碳原子的酯。
具有通式II的合适的第二单体单元的例子是图3-5中如通式II(a)-II(z)所示,其中:
在通式II(v)-II(y)中:
R是如上面对各个通式I、II、III、IV、V、VI、VII、VIII-XI所描述。
通式III:
或者,第二单体单元可以是具有如图6中通式III所示结构的二价6元环杂芳基。优选的R基团是氢、C6-C12烷基(或者C1-C5烷基或者C6-C12烷基),C6-C20芳基、C2-C20杂芳基。合适的E连接基团的例子包括亚吡啶基(pyridinediyl,-C5H4N-)和亚联吡啶基(bipyridinediyl,-C5H4N-C5H4N-)。
具有通式III的合适的第二单体单元的例子如图6中所示的通式III(a)-III(g)。
通式IV:
或者,第二单体单元可以是具有如图7中通式IV所示结构的5元环杂芳基。优选的R基团是氢、C1-C12烷基(或者,C1-C6烷基或C6-C12烷基),C6-C20芳基(或者C6-C10芳基)、C2-C20杂芳基(或者C6-C10杂芳基)、更优选C6-C12芳基。合适的E连接基团的例子包括亚吡咯基(pyrroledi yl,-C4H3N-)和亚噻吩基(thiophenediyl,-C4H3S-)。
合适的具有通式IV的第二单体单元的例子是图7所示通式IV(a)-IV(h),这里:
在通式IV(a)中:
R是如上面对各个通式I、II、III、IV、V、VI、VII、VIII-XI所描述。
在通式IV(h)中:
R1在各自存在时可以相同或不同,是杂原子上的取代基,选自烷基,芳基,杂烷基,和杂芳基。
通式V:
或者,第二单体单元可以是具有如图8中通式V所示结构的芳族基团。R基团优选是氢、C1-C12烷基(或者,C1-C6烷基或C6-C12烷基),C6-C20芳基(或者C6-C10芳基)、C2-C20杂芳基(或者C6-C10杂芳基)。优选两个W代表一个单键。
合适的这种类型的第二单体单元的例子是具有通式V(a)-V(e)的结构的单元,这里:
在通式V(a),V(b)中:
R是如上面对各个通式I、II、III、IV、V、VI、VII、VIII-XI所描述的。
在通式V(e)中:
R1在各自存在时可以相同或不同,是杂原子上的取代基,选自烷基,芳基,杂烷基,和杂芳基。
通式VI-通式XI:
或者,第二单体单元可以是具有如图9中通式VI、图10通式VII、图11通式IX-XI所示结构的二价稠合芳族基团。优选的R基团是氢、C1-C20烷基(或者,C1-C6烷基或C6-C12烷基)、C6-C20芳基和C2-C20杂芳基。
在通式VI中,E优选在1,4-,1,5-,1,8-,2,3-,或2,6-位。合适的具有通式VI的第二单体单元的例子示于图9的通式VI(a)-VI(d)。
在通式VII中,E优选在1,4-,1,5-,1,8-,2,3-,2,6-或9,10-位。合适的具有通式VII的第二单体单元的例子示于图10通式VII(a)。
在本发明的共聚物中,R基团基本上是聚合物主链之外的侧链。因此,R基团的最后选择应考虑这些侧链在最后聚合物性质中所起的作用。这些性质包括电子性能,溶解性,加工性,成膜性,增强或降低链间的相互作用,导致在有机溶剂中的溶解性,导致在掺混物中与主聚合物的相容性,引起高介电常数使离子溶剂化,增强离子的迁移性等。另外,在R基团被取代时,这些取代基的空间影响应在取代基选择时予以考虑。
在本发明的芴聚合物中,一种以上的第二单体单元可与第一单体单元一起存在。第一单体单元对至少一种第二单体单元的相对摩尔比可从99.9∶0.1到1∶99或99.5∶0.5到10∶90;或99∶1到20∶80,或99∶1到50∶50。分子量以从几千到几十万之间变化。在生成聚合物时单体的结合可以是无规的或控制的,结果是共聚物包括,但不限于,无规共聚物,交替共聚物和嵌段共聚物。
本发明的芴聚合物包含至少一种具有通式-CψF2ψ+1的R取代基,其中ψ是1-20之间的整数,较好是1-12。
所述全氟烷基是芳环上的取代基。所述具有全氟烷基取代基的单体单元的比例通常为5-100摩尔%,较好是10-50摩尔%。
方法
本发明的全氟烷基化芴聚合物可以通过首先形成全氟烷基化单体,然后聚合形成所述聚合物来制备。但是,这种途径要求单独合成各单体,这会比较困难。在本发明的另一实施方式中,提供更加通用的制备全氟烷基化芴聚合物的方法,包括首先制备所述基础芴聚合物,然后用能将全氟烷基引入聚合物芳环上的原料处理所述基础聚合物。
合成
形成所述基础芴聚合物的聚合反应一般可通过三条已知的合成途径来进行。在第一种合成方法中,如Yamamoto在《聚合物科学的进展》,第17卷,1153页(1992)中所述的,单体单元的二卤(宜为二溴)衍生物与化学计量的零价镍化合物,如双(1,5-环辛二烯)镍(0)反应。在第二种方法中,如Colon等在《聚合物科学杂志》,部分A,聚合物化学版,28卷,367页(1990)中所述的,单体单元的二卤衍生物与催化量的Ni(II)化合物在化学计量的可将二价镍离子还原成零价镍的物质的存在下反应。合适的物质包括锌、镁、钙和锂。在第三种合成方法中,如美国专利5962631和发表的PCT申请WO00/53565中所述的,在零价钯催化剂下,如四(三苯基膦)Pd的存在下,一种单体单元的二卤衍生物与具有两个反应基团的另一种单体单元的衍生物反应,该反应基团选自硼酸、硼酸酯和硼烷。这种第三反应可以在需要相变催化剂的两相介质中进行。
在本发明的一些实施例中,共聚物可与封端化合物反应,将活性端基转化成非活性端基。封端化合物一般加到预制的聚合物中,并终止聚合反应。封端化合物一般是具有单一活性基团的芳族化合物,如具有单一卤化物基团或硼酸或硼酸酯基团的芳环。合适的封端化合物的例子包括9-溴蒽,4-溴-1,2-二甲氧基苯,1-溴芘,碘苯,溴苯,2-溴-9-芴酮,苯硼酸和4-甲基苯硼酸。封端基团也可设计成增加功能性,如电荷迁移性和色移。它也可影响链间聚集。
在形成所述基础芴聚合物之后,在钌(II)催化剂存在下,和全氟烷基化试剂反应,所述试剂选自(i)全氟烷基碘化物,(ii)全氟烷基磺酰氯。
合适的全氟碘化物包括具有1-20个,宜为1-12个碳原子的全氟烷基碘化物,它可以是直链、支链或环状的。许多全氟烷基碘化物可以商业购得。其它的可以由已知的合成技术制得。
合适的全氟烷基磺酰氯包括具有1-20个,较好是1-12个碳原子的全氟烷基磺酰氯,它可以是直链、支链或者环状的。许多全氟烷基磺酰氯可以商业购得。其它的可以由已知的合成技术制得。
合适的钌(II)催化剂是具有配位基如膦,尤其是三苯基膦、一氧化碳、环辛二烯、氯化物和氢化物的中性有机金属配合物。优选的催化剂是二氯三(三苯基膦)钌(II)。许多钌(II)催化剂可以商业购得。其它可以通过已知的合成技术制得,如N.Kamigata,T.Fukushima和M.Yoshida所著J.Chem.Soc.PerkinTrans.,1,1989,1559中所述的。
所述全氟烷基化反应通常在溶剂中进行,所述溶剂不和所述全氟烷基化试剂反应,所述基础芴聚合物至少部分溶解在其中。合适的溶剂例子包括缺电子的芳香族类,如氯苯。若要求更高的反应温度,那么使用更高沸点的溶剂。所述反应通常在惰性气氛中进行,如在氮气中。温度通常约为100-250℃。反应时间在约1小时到三天内变化。所述反应产物可以使用已知的技术进行分离,如用另一种溶剂进行萃取或者沉淀,并进行干燥。
所得产物在聚合物中的至少一些芳环上具有全氟烷基取代基。每个聚合物中全氟烷基取代基的数目以及它们的取代位置,即在芳基上取代,取决于用于制备所述聚合物的单体单元的化学反应活性。空间效应也是一个因素。
芴聚合物和共聚物的全氟烷基化反应会影响所述聚合物的电子性能。所述全氟烷基化的芴聚合物更加缺电子,且LUMO能级更低。这提高了所述聚合物的电子传导性,并便于电子注入/输运。全氟烷基化反应也会影响其它聚合物的性能,如聚合物薄膜的溶解性、加工性和形态。
电子器件
本发明还涉及包括至少一层光活性层的电子器件,该层位于两个电接触层之间,其中器件的至少一层电活性层包括本发明的共聚物。如图13所示,典型的器件100具有阳极层110和阴极层150,以及阳极110和阴极150之间的电活性层120、130及任选的140。相邻于阳极的是空穴注入/输运层120。相邻于阴极的是任选的包括电子输运材料的层140。在空穴注入/输运层120和阴极(或任选电子输运层)之间是光活性层130。本发明的共聚物可用在空穴注入/输运层120和/或光活性层130和/或任选的电子注入/输运层140中。
器件一般还包括可相邻于阳极或阴极的支承(未显示)。通常支承相邻阳极。支承可以是柔性的或刚性的,有机的或无机的。通常,玻璃或柔性有机薄膜可用作支承。阳极110是对注入或收集正电荷载流子等特别有效的电极。阳极优选由包含金属、混合的金属、合金、金属氧化物或混合的金属氧化物的材料制造。合适的金属包括第11族金属,在第4、5和6族中的金属,以及第8-10族过渡金属。如果阳极是透光的,则通常使用第12、13和14族的混合金属氧化物,如铟-锡氧化物。阳极110也可包括有机材料,如“Flexible light-emitting diodes made from soluble conducting polymer”,Nature vol.357,pp477-479(1992年6月11日)中所述的聚苯胺。
阳极层110,一般用物理蒸气淀积的方法或旋转浇铸的方法施涂。术语“物理蒸气淀积”指的是涉及在真空中进行的各种淀积方法。于是,例如,物理蒸气淀积包括所有形式的溅射,包括离子束溅射,以及所有形式的蒸气淀积,如电子束蒸发和电阻蒸发。有用的物理蒸气淀积的具体形式是射频磁控管溅射。
本发明的共聚物可起层120中的空穴注入/输运材料的作用。其他有利于空穴注入/输运的材料包括:N,N’-二苯基-N,N’-双(3-甲基苯基)-[1,1’-联苯基]-4,4’-二胺(TPD)和双[4-(N,N’-二乙基氨基)-2-甲基苯基](4-甲基苯基)甲烷(MPMP),空穴注入/输运聚合物,如聚乙烯基咔唑(PVK),(苯基甲基)聚硅烷,聚(3,4-亚乙基二氧噻吩)(PEDOT),聚苯胺(PANI);电子和空穴注入/输运材料,如4,4-N,N’-二咔唑联苯(BCP);或具有良好电子和空穴注入/输运性质的发光材料,比如螯合的oxinoid化合物,如三(8-羟基喹啉(quinolato))铝(Alq3)。
可使用常规的方法涂布空穴注入/输运层120,包括:旋涂、浇铸和印刷,如凹版印刷。层的涂布,也可以通过喷墨印刷、热布线图案形成或物理蒸气淀积。
通常,所述无机阳极和空穴注入/输运层120是有图案的。可以理解,该图案可按要求变化。可通过例如在涂布第一电接触层材料前,用位于第一柔性复合阻挡结构上的有图案的掩模或光刻胶的图案对上述层进行涂布。或者上述层可作为整体层涂布,随后用例如光刻胶和湿化学蚀刻来形成图案。空穴注入/输运层也可以喷墨印刷、平版印刷或热转移印刷图案涂布。
根据器件100的应用,光活性层130可以是通过施加电压而被激活(如在发光二极管或发光电化学电池中)的发光层,响应辐射能并在施加或不施加偏电压下产生信号的材料层(比如,在光电探测器中)。光电探测器的例子包括光电导管、光敏电阻器、光控开关、光敏晶体管、光电管和光伏电池,这些术语按照在Markus,John,Electronics and Nucleonics Dictionary,470 and476(McGraw-Hill,Inc.1966)中描述的。
在器件100是发光器件时,光活性层130在足够的偏压施加到电接触层时会发光。本发明的共聚物可用在发光活性层130中。其他已知的发光材料包括小分子材料,如Tang,美国专利4356429;Van Slyke等,美国专利4539507中描述的材料,它们的相关部分结合在此供参考。或者,这些材料可以是聚合材料,如Friend等在美国专利5247190中,Heeger等在美国专利5408109中,Nakano等在美国专利5317169中描述的材料,它们的相关部分结合在此供参考。发光材料可分散在另一种材料的基质中,可有或没有添加剂,但优选单独地形成层。活性有机层一般的厚度在50-500纳米的范围内。
电子器件100是光电探测器时,光活性层130响应辐射能,并在有或没有偏压下产生信号。响应辐射能并能在偏压下产生信号的材料(如在光电导管,光敏电阻器,光控开关、光敏晶体管、光电管的情况中)包括,例如许多共轭的聚合物和电致发光材料。响应辐射能并能在无偏压下产生信号的材料(如在光电导管或光伏电池的情况中)包括对光起化学反应并由此产生信号的材料。这些光敏的化学反应性材料例如包括许多共轭的聚合物和电致和光致发光材料。具体的例子包括,但不限于,MEH-PPV(“Optocoupler made fromsemiconducting polymers”,G.Yu,K.Pakbaz,和A.J.Heeger,Journal ofElectronic materials,Vol.23,pp925-928(1994));和MEH-PPV Compositeswith CN-PPV(“Efficient Photodiodes from Interpenetrating PolymerNetworks’,J.J.M.Halls等。(Cambridge group)Nature Vol.376,pp498-500,1995)。
含活性有机材料的活性层130,可从溶液通过常用的方法,包括旋涂,浇铸和印刷进行涂布。根据材料的性质,活性有机材料可直接通过蒸气淀积方法涂布。也可涂布活性聚合物前体,然后一般通过加热转化成聚合物。
阴极150是对注入,或者收集电子或负电荷载流子特别有效的电极。阴极可以是具有比第一电接触层(在这情况中,阳极)低的工作功能的任何金属或非金属。第二接触层的材料可选自第1族的碱金属(例如Li,,Cs),第2族(碱土金属)金属,第12族金属,稀土金属,镧系元素和锕系元素。也可使用如铝、铟、钙,钡和镁及其组合。
阴极层150经常通过物理蒸气淀积方法涂布。一般,阴极层是有图案的,如上面关于阳极层110和导电聚合物层120所讨论的。可用类似的加工方法使阴极层形成图案。
任选层140可起便于电子输运的作用,也可用作防止在层界面外骤冷作用的缓冲层或密封层。该层优选促进电子迁移性和减少骤冷作用。任选层140的电子输运材料的例子包括金属螯合的8-羟基喹啉(oxinoid)化合物,如三(8-羟基喹啉)铝(Alq3),菲咯啉基化合物,如2,9-二甲基-4,7-二苯基-1,10菲咯啉(DDPA)或4,7-二苯基-1,10-菲咯啉(DPA),吡咯化合物,如2-(4-联苯基)-5-(4-叔丁基苯基)-1,3,4-噁二唑(PBD)和3-(4-联苯基)-4-苯基-5-(4-叔丁基苯基)-1,2,4-三唑(TAZ)。
已知在有机电子器件中有其他层。例如,在导电的聚合物层120和活性层130之间可以有一层(未显示),以便于正电荷输运和/或层的带隙匹配,或起保护层的作用。类似地,在活性层130和阴极层150之间可存在额外层,以便于负电荷输运和/或层间的带隙匹配,或起保护层的作用。可使用技术上已知的层。另外,上述任何层可由二层或多层组成。或者,一些或所有无机阳极层110,导电聚合物层120,活性层130,和阴极层150,可以表面处理,增加电荷载流子输运效率。每层构成层的材料选择宜通过权衡提供有高器件效率的器件的目标来确定。
器件100可通过在合适的基片上顺序淀积各层制备。可使用的基片如玻璃和聚合膜。在大多数情况下,将阳极涂布到基片上,并从那里形成各层。然而,可首先将阴极涂布到基片,并以相反的次序加上各层。一般,不同的层具有下面的厚度范围:无机阳极110,500-5000埃,优选1000-2000埃;导电聚合物层,50-2500埃,优选200-2000埃;发光层130,10-1000埃,优选100-800埃;任选电子输运层140,50-1000埃,优选200-800埃;阴极150,200-10000埃,优选300-5000埃。
实施例
下面的实施例阐明本发明的某些特性和优点。它们是发明的说明,而不是限制。除非另行说明,所有的百分率按重量计。
实施例1
本实施例说明基础芴聚合物,2,7-聚(9,9-二(2-乙基己基)芴)的制备。
在惰性条件下,将DMF(5毫升)加到装有搅拌条的50毫升Schlenck管中,管内含有双(1,5-环辛二烯)镍(0)(2.231克,8.11毫摩尔),2,2’-联吡啶(1.267克,8.11毫摩尔),和1,5-环辛二烯(0.877克,8.11毫摩尔)。在60℃搅拌随后的深蓝/紫色溶液30分钟,然后将2,7-二溴-9,9-双(2-乙基己基)芴在甲苯(20毫升)中的溶液经注射器加入。反应混合物然后在75℃搅拌5天。混合物冷却至室温,并沉淀到甲醇(100毫升),丙酮(100毫升)和浓盐酸(5毫升)的溶液中。搅拌2小时后,过滤混合物。然后将固体残留物溶解在氯仿中,再沉淀到甲醇(1 00毫升),丙酮(100毫升)和浓盐酸(5毫升)的溶液中。搅拌1小时后,过滤混合物。最后,残留物依次用甲醇,水和甲醇洗涤,并真空干燥。所述共聚物通过核磁共振(NMR)表征,并通过凝胶渗透色谱(GPC)确定数均分子量(Mn)。
实施例1A
重复实施例1的步骤,除了反应混合物在75℃搅拌24小时,而不是5天。另外,混合物过滤后,在残留物依次用甲醇,水和甲醇洗涤并真空干燥前,所得的固体再溶解在氯仿中,并沉淀在纯甲醇中。基本上得到下面表1中提供的相同分子量。
实施例2-4
实施例2-4说明了本发明全氟烷基化芴共聚物的制备。
实施例2
在本实施例中,将全氟癸基取代基加到实施例1制得的基础芴聚合物中。在氮气气氛下,将来自实施例1的2,7-聚(9,9-双(2-乙基己基)芴)(0.50g,1.29mmol)、1-碘代全氟癸烷(1.83g,2.84mmol)和1,2,4-三氯代苯(50ml)加入装有水冷凝管的100ml圆底烧瓶中。然后加热所述容器至190℃,并保持24小时。冷却到室温之后,所述反应溶液用氯仿萃取。所述氯仿层依次用稀的亚硫酸氢钠水溶液、稀的碳酸氢钠水溶液、稀的氢氧化钠水溶液和水洗涤。所述有机层用硫酸镁干燥,然后蒸干。所得聚合物通过F19NMR进行分析,表明加入了约10-15摩尔%的全氟癸基。
实施例3
在本实施例中,将全氟甲基取代基加到实施例1制得的基础芴聚合物中。
在氮气气氛下,将来自实施例1的2,7-聚(9,9-双(2-乙基己基)芴)(0.50g,1.29mmol)、三氟甲基磺酰氯(0.48g,2.84mmol)、二氯三(三苯基膦)钌(II)(12mg,0.0125mmol)和1,2,4-三氯代苯(50ml)加入玻璃压力容器中。在干冰/丙酮浴中将所述容器冷却至-30℃,并进行抽空,然后充氮气。重复这一循环2次以上。然后将所述容器升温至室温,并置于高压釜(antoclave)中,在此加热至130℃,并保持24小时。然后,将所述容器冷却至室温,并用氮气吹扫。所述三氯代苯溶液沉淀在丙酮中。收集固体残留物,用丙酮洗涤并在真空中干燥。所得聚合物通过F19NMR进行分析,表明加入了约10-15摩尔%的三氟甲基。
实施例4
在本实施例中,将全氟丁基取代基加到实施例1制得的基础芴聚合物中。
在氮气气氛下,将来自实施例1的2,7-聚(9,9-双(2-乙基己基)芴)(0.50g,1.29mmol)、三氟丁基磺酰氯(0.905g,2.84mmol)、二氯三(三苯基膦)钌(II)(12mg,0.0125mmol)和1,2,4-三氯代苯(20ml)加入装有水冷凝管的100ml圆底烧瓶中。然后加热所述容器至120℃,并保持24小时。冷却到室温之后,所述反应溶液沉淀在丙酮中。收集固体残留物,用丙酮洗涤并在真空中干燥。所得聚合物通过F19NMR进行分析,表明加入了约10-15摩尔%的全氟丁基。
尽管本发明已对目前认为是优选的实例进行描述,但应理解本发明不限于公开的实例。相反,发明涵盖包括在所附权利要求书的精神和范围中的各种改良和等同的结构。下面权利要求书的范围给予最概括的解释,以包括所有这些改良和等同的阐述及功能。
Claims (12)
1.一种聚合物,所述聚合物包含一种或多种图1所示通式I的第一单体单元,其中,
R在各自存在时可以相同或不同,是芳环中碳原子上的取代基,选自:氢、烷基、芳基、杂烷基、杂芳基、F、-CN、-OR1、-CO2R1、CψHθFλ、-OCψHθFλ、-SR1、-N(R1)2、-P(R1)2、-SOR1、-SO2R1、-NO2,具有图12所示的通式XII的β-二羰基;或相邻的R基团一起可形成选自5元环烷基、6元环烷基、5元芳基、6元芳基、5元杂芳基和6元杂芳基的环,其中:
R1在各自存在时可以相同或不同,是杂原子上的取代基,选自烷基、芳基、杂烷基和杂芳基;和
ψ是1-20的整数,θ和λ是满足下面等式A1的整数:
θ+λ=2ψ+1; (等式A1);
R2是不在芳环上的碳原子上的取代基,它在各自存在时可以相同或者不同,并选自氢、烷基、芳基、杂烷基、杂芳基和-CψHθFλ,前提是所述聚合物包含至少一个具有通式-CψF2ψ+1的R取代基。
2.权利要求1所述的聚合物,所述聚合物还包含至少一种第二单体单元,所述第二单体单元选自:(i)具有图1所示通式I的芳基,(ii)具有图2所示通式II的芳族基团,(iii)具有图6所示通式III的6元杂芳基,(iv)具有图7所示通式IV的5元杂芳基,(v)具有图8所示的通式V的芳族基团,(vi)具有图9所示通式VI-VII、图10中所示的通式IX-XI的二价稠环芳族基团,以及(vii)它们的组合,其中:
在各通式II、III、IV、V、VI、VII、VIII和IX中:
R、R1、R2、ψ、θ和λ如以上所定义的;
E在各自存在时可以是相同或不同的,是单键或选自亚芳基和亚杂芳基的连接基团;
在通式IV中:
A在各自存在时分别为C或N,γ是0或选自1或2的整数,这样,如果两个A是N,则γ是0;或者如果一个A是N,一个A是C,则γ是1;或者如果两个A是C,则γ是2;
Q是O、S、SO2或NR1,其中:
R1在各自存在时可以相同或不同,是杂原子上的取代基,选自烷基、芳基、杂烷基和杂芳基;
在通式V中:
Q1是羰基、O、S、SO2或NR1,其中:
R1在各自存在时可以相同或不同,是杂原子上的取代基,选自烷基、芳基、杂烷基和杂芳基;
W是H、烷基或杂烷基;或两个W一起可代表一个单键;
在通式VI中:
两个E是在1,4-,1,5-,1,8-,2,3-或2,6-位;
在通式VII中:
两个E是在1,4-,1,5-,1,8-,2,3-,2,6-或9,10-位;
在通式VIII中:
第一个E是在1,2或3位;第二个E是在6,7或8位;
在通式IX中:
第一个E是在2,3或4位;第二个E是在7,8或9位;
在通式XII中:
R3选自氢、烷基、芳基、杂烷基和杂芳基;
δ是0或1-12整数。
3.权利要求2所述的聚合物,其特征在于,在一种或多种所述至少一种第一单体单元中,所述至少一种R基团分别选自:直链或支链正丁基、直链或支链异丁基、直链或支链戊基、可带有或不带有烯烃不饱和度的各种己基和各种辛基;苯基,噻吩基,咔唑基,烷氧基,苯氧基和氰基。
4.权利要求2所述的聚合物,其特征在于,在一种或多种所述至少一种第一单体单元中,所述至少一种R基团分别选自:氢原子、C6-C12烷氧基、苯氧基、C6-C12烷基、苯基和氰基。
5.权利要求2所述的聚合物,其特征在于,一种或多种所述至少一种第二单体单元选自通式II(a)-II(z)、III(a)-III(g)、IV(a)-IV(h)、V(a)-V(e)、VI(a)-VI(d)和VII(a),其中:
在通式II(v)-II(y)、IV(a)、V(a)和V(b)中:
R如上述各通式I、II、III、IV、V、VI、VII、VIII-XI中所述的;
在通式IV(h)中:
R1在各自存在时可以相同或不同,是杂原子上的取代基,选自烷基,芳基,杂烷基,和杂芳基;和
在通式V(e)中:
R1在各自存在时可以相同或不同,是杂原子上的取代基,选自烷基,芳基,杂烷基,和杂芳基。
6.权利要求1所述的聚合物,其特征在于,一种或多种所述至少一种第二单体单元具有通式II,式中,R选自:
氢;
烷基;
芳基;
杂烷基;
杂芳基;
F;
-CN;
-NO2;
具有图12中所示通式XII的β-二羰基;
-CψHθFλ;
-OCψHθFλ;和
-P(R1)2、-SOR1,-OR1、-CO2R1、-SR1、-N(R1)2和-SO2R1,其中R1是1-20个碳原子的直链或支链烷基,或者直链或支链的杂烷基。
7.权利要求1所述的聚合物,其特征在于,一种或多种所述至少一种第二单体单元具有通式II,式中,R选自:
具有1-12个碳原子的烷基;
部分或全部氟化的具有1-12个碳原子的烷基,尤其CF3;
具有6-20个碳原子的芳基;
具有4-20个碳原子,并用O、S或N取代的杂芳基;
具有1-12个碳原子的烷氧基;和
具有3-15个碳原子的酯。
8.权利要求1-7任一项所述的聚合物,所述聚合物还包含具有芳族基团的封端基团。
9.一种电子器件(100),所述器件包含至少一层电活性层(120、130、140),该电活性层包含权利要求1-7任一项所述的聚合物。
10.权利要求9所述的器件,其特征在于,所述器件中所述至少一层电活性层中的一层或多层是光活性层(130)、或者空穴注入/输运层(120)或者电子注入/输运层(140)。
11.权利要求9所述的器件,其特征在于,所述器件选自发光器件、光电探测器和光伏器件。
12.用于制备权利要求1-7任一项所述聚合物的方法,其步骤包括:
形成具有至少一种第一单体单元的聚合物,所述单体单元具有图1所示通式I;其中:
R在各自存在时可以相同或不同,是芳环中碳原子上的取代基,选自:氢、烷基、芳基、杂烷基、杂芳基、F、-CN、-OR1、-CO2R1、CψHθFλ、-OCψHθFλ、-SR1、-N(R1)2、-P(R1)2、-SOR1、-SO2R1、-NO2,具有图12所示的通式XII的β-二羰基;或相邻的R基团一起可形成选自5元环烷基或6元环烷基、5元芳基、6元芳基、5元杂芳基和6元杂芳基的环,其中:
R1在各自存在时可以相同或不同,是杂原子上的取代基,选自烷基、芳基、杂烷基和杂芳基;
ψ是1-20的整数,θ和λ是满足下面等式A1的整数:
θ+λ=2ψ+1; (等式A1);
R2是不在芳环上的碳原子上的取代基,它可以相同或者不同,并选自氢、烷基、芳基、杂烷基、杂芳基和-CψHθfλ,前提是所述聚合物包含至少一个具有通式-CψF2ψ+1的R取代基;
在钌(II)催化剂存在下,用全氟烷基化试剂处理所述聚合物,所述试剂选自(i)全氟烷基碘化物,和(ii)全氟烷基磺酰氯。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US28933301P | 2001-05-07 | 2001-05-07 | |
| US60/289,333 | 2001-05-07 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN1507464A true CN1507464A (zh) | 2004-06-23 |
Family
ID=23111073
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNA028094476A Pending CN1507464A (zh) | 2001-05-07 | 2002-05-06 | 具有全氟烷基的电活性芴聚合物、制备这种聚合物的方法以及用这种聚合物制造的器件 |
Country Status (9)
| Country | Link |
|---|---|
| US (3) | US7074886B2 (zh) |
| EP (1) | EP1397410A4 (zh) |
| JP (1) | JP2005513170A (zh) |
| KR (1) | KR20030093334A (zh) |
| CN (1) | CN1507464A (zh) |
| CA (1) | CA2442125A1 (zh) |
| IL (1) | IL158073A0 (zh) |
| TW (1) | TW593405B (zh) |
| WO (1) | WO2002090416A1 (zh) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6770904B2 (en) | 2002-01-11 | 2004-08-03 | Xerox Corporation | Polythiophenes and electronic devices generated therefrom |
| US7250625B2 (en) | 2002-01-11 | 2007-07-31 | Xerox Corporation | Polythiophenes and electronic devices generated therefrom |
| DE10248876B4 (de) * | 2002-10-18 | 2006-07-06 | H.C. Starck Gmbh | Verfahren zur Herstellung linearer organischer Oligomere |
| WO2005014691A2 (en) * | 2003-08-06 | 2005-02-17 | Merck Patent Gmbh | Process of preparing regioregular polymers |
| US20060094859A1 (en) * | 2004-11-03 | 2006-05-04 | Marrocco Matthew L Iii | Class of bridged biphenylene polymers |
| US20090220857A1 (en) * | 2005-09-02 | 2009-09-03 | Toyota Motor Engineering & Manufacturing North America, Inc. | Chemical protection of metal surface |
| US20070082268A1 (en) * | 2005-09-02 | 2007-04-12 | Kurt Star | Chemical protection of metal surface |
| US7659410B2 (en) * | 2006-04-25 | 2010-02-09 | Fuji Xerox Co., Ltd. | Thiophene-containing compound and thiophene-containing compound polymer, organic electroluminescent device, production method thereof, and image display medium |
| JP4935172B2 (ja) * | 2006-04-25 | 2012-05-23 | 富士ゼロックス株式会社 | 有機電界発光素子およびその製造方法、並びに画像表示媒体 |
| WO2012008556A1 (ja) * | 2010-07-14 | 2012-01-19 | 住友化学株式会社 | 光電変換素子 |
| GB2483269A (en) * | 2010-09-02 | 2012-03-07 | Cambridge Display Tech Ltd | Organic Electroluminescent Device containing Fluorinated Compounds |
| CN102086338B (zh) * | 2010-12-22 | 2012-12-12 | 浙江工业大学 | 一种乙烯基酯树脂强防腐耐热碳系导电涂料及制备方法 |
Family Cites Families (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2527618A1 (fr) * | 1982-05-25 | 1983-12-02 | Thomson Csf | Polymeres contenant des heterocycles et des noyaux aromatiques et materiaux organiques conducteurs formes a partir de ces polymeres |
| FR2603288B1 (fr) | 1986-09-03 | 1988-12-09 | France Etat | Polyfluorenes 9,9'-disubstitues, leur procede de preparation et leurs applications en electro-optique et electrochimie |
| DE4331401A1 (de) * | 1993-09-15 | 1995-03-16 | Hoechst Ag | Verwendung von Polymeren mit isolierten Chromophoren als Elektrolumineszenzmaterialen |
| US5770070A (en) * | 1994-10-03 | 1998-06-23 | Genomyx Corporation | Radioactive waste disposal cartridge |
| DE4436773A1 (de) * | 1994-10-14 | 1996-04-18 | Hoechst Ag | Konjugierte Polymere mit Spirozentren und ihre Verwendung als Elektrolumineszenzmaterialien |
| TW334474B (en) * | 1995-02-01 | 1998-06-21 | Sumitomo Kagaku Kk | Method for making a polymeric fluorescent substrate and organic electrolumninescent element |
| DE69608446T3 (de) | 1995-07-28 | 2010-03-11 | Sumitomo Chemical Company, Ltd. | 2,7-aryl-9-substituierte fluorene und 9-substituierte fluorenoligomere und polymere |
| US5708130A (en) | 1995-07-28 | 1998-01-13 | The Dow Chemical Company | 2,7-aryl-9-substituted fluorenes and 9-substituted fluorene oligomers and polymers |
| WO1997009394A1 (de) * | 1995-09-04 | 1997-03-13 | Hoechst Research & Technology Deutschland Gmbh & Co. Kg | Polymere mit triarylamin-einheiten als elektrolumineszenzmaterialien |
| JP4112007B2 (ja) | 1996-03-04 | 2008-07-02 | デュポン ディスプレイズ, インコーポレイテッド | フォトルミネセンスおよびエレクトロルミネセンス用材料としてのポリフルオレン |
| KR100471935B1 (ko) | 1997-01-30 | 2005-03-07 | 제이에스알 가부시끼가이샤 | 페닐렌-함유 중합체의 제조 방법 및 필름 형성재 |
| US6309763B1 (en) * | 1997-05-21 | 2001-10-30 | The Dow Chemical Company | Fluorene-containing polymers and electroluminescent devices therefrom |
| US5998045A (en) * | 1997-07-03 | 1999-12-07 | International Business Machines Corporation | Polymeric light-emitting device |
| US5777070A (en) * | 1997-10-23 | 1998-07-07 | The Dow Chemical Company | Process for preparing conjugated polymers |
| KR100697861B1 (ko) | 1998-03-13 | 2007-03-22 | 캠브리지 디스플레이 테크놀로지 리미티드 | 전장 발광 디바이스들 |
| WO1999054943A1 (en) | 1998-04-21 | 1999-10-28 | The Dow Chemical Company | Organic electroluminescent devices with improved stability in air |
| DE19846768A1 (de) * | 1998-10-10 | 2000-04-20 | Aventis Res & Tech Gmbh & Co | Konjugierte Polymere enthaltend 2,7-Fluorenyleinheiten mit verbesserten Eigenschaften |
| DE19846766A1 (de) * | 1998-10-10 | 2000-04-20 | Aventis Res & Tech Gmbh & Co | Konjugierte Polymere, enthaltend spezielle Fluorenbausteine mit verbesserten Eigenschaften |
| EP1151484A1 (en) * | 1999-01-15 | 2001-11-07 | The Dow Chemical Company | Semiconducting polymer field effect transistor |
| US6353083B1 (en) * | 1999-02-04 | 2002-03-05 | The Dow Chemical Company | Fluorene copolymers and devices made therefrom |
| JP3310658B1 (ja) | 1999-03-05 | 2002-08-05 | ケンブリッジ ディスプレイ テクノロジー リミテッド | 高分子の合成方法 |
| FR2790815B1 (fr) | 1999-03-08 | 2001-04-27 | Jean Michel Pretceille | Procede de raccordement, ensemble a compteur et robinet sur console, et raccord pour sa mise en oeuvre |
| GB9917356D0 (en) | 1999-07-24 | 1999-09-22 | Univ Cambridge Tech | Aromatic monomers and polymers for optoelectronic devices |
| AU1540001A (en) * | 1999-12-09 | 2001-06-18 | Cambridge Display Technology Limited | Fluorene-perylene copolymers and uses thereof |
-
2002
- 2002-05-03 US US10/139,002 patent/US7074886B2/en not_active Expired - Fee Related
- 2002-05-06 IL IL15807302A patent/IL158073A0/xx unknown
- 2002-05-06 EP EP02744278A patent/EP1397410A4/en not_active Withdrawn
- 2002-05-06 CN CNA028094476A patent/CN1507464A/zh active Pending
- 2002-05-06 KR KR10-2003-7014231A patent/KR20030093334A/ko not_active Application Discontinuation
- 2002-05-06 JP JP2002587490A patent/JP2005513170A/ja active Pending
- 2002-05-06 WO PCT/US2002/018399 patent/WO2002090416A1/en not_active Application Discontinuation
- 2002-05-06 CA CA002442125A patent/CA2442125A1/en not_active Abandoned
- 2002-05-07 TW TW091109463A patent/TW593405B/zh not_active IP Right Cessation
-
2004
- 2004-04-01 US US10/816,153 patent/US7183365B2/en not_active Expired - Lifetime
- 2004-04-01 US US10/816,160 patent/US7259229B2/en not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| EP1397410A4 (en) | 2005-03-16 |
| US20040186255A1 (en) | 2004-09-23 |
| EP1397410A1 (en) | 2004-03-17 |
| US7183365B2 (en) | 2007-02-27 |
| US20020177679A1 (en) | 2002-11-28 |
| KR20030093334A (ko) | 2003-12-06 |
| WO2002090416A1 (en) | 2002-11-14 |
| TW593405B (en) | 2004-06-21 |
| US20040219391A1 (en) | 2004-11-04 |
| CA2442125A1 (en) | 2002-11-14 |
| US7074886B2 (en) | 2006-07-11 |
| IL158073A0 (en) | 2004-03-28 |
| US7259229B2 (en) | 2007-08-21 |
| JP2005513170A (ja) | 2005-05-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5602191B2 (ja) | 電荷輸送材料として使用するトリアリールアミン化合物 | |
| KR101135745B1 (ko) | 방향족 아민 조성물 및 상기 조성물로 제조된 전자디바이스 | |
| KR101197802B1 (ko) | 방향족 아민 조성물 및 상기 조성물로 제조된 전자디바이스 | |
| KR101295484B1 (ko) | 신규한 공중합체를 포함하는 조성물 및 상기 조성물로제조된 전자 장치 | |
| CN1216928C (zh) | 含有螺二芴单元和氟单元的共轭聚合物及其应用 | |
| JP4050988B2 (ja) | 置換フルオレンポリマー、その製造方法、及びこれを用いた光学装置 | |
| JP5048995B2 (ja) | ポリマーのガラス転移温度制御方法及びこれを用いたポリマー | |
| CN1419575A (zh) | 可溶性聚芳基噁二唑共轭聚合物 | |
| CN1729229A (zh) | 三环芳基胺单体及其聚合物和器件 | |
| CN1910261A (zh) | 具有9,9-二(芴基)-2,7-芴基单元的有机场致发光聚合物及使用该聚合物制得的有机场致发光装置 | |
| CN1882632A (zh) | 可交联的取代芴化合物和基于其的共轭低聚物或聚合物 | |
| CN1768090A (zh) | 聚合物 | |
| CN1711301A (zh) | 用于有机电致发光器件的芳基取代的聚茚并芴 | |
| CN1947274A (zh) | 包含平面芳基胺单元的电致发光聚合物,其制备和用途 | |
| JP5363306B2 (ja) | 多層構造を有する光電子デバイス | |
| CN1800298A (zh) | 蓝光发射聚合物和使用其的有机电致发光器件 | |
| CN1646660A (zh) | 空穴输运聚合物以及用该聚合物制成的器件 | |
| KR101387213B1 (ko) | 신규한 화합물을 포함하는 조성물 및 상기 조성물로 제조된전자 장치 | |
| CN1507464A (zh) | 具有全氟烷基的电活性芴聚合物、制备这种聚合物的方法以及用这种聚合物制造的器件 | |
| CN1524100A (zh) | 电活性芴共聚物和用这种共聚物制造的器件 | |
| KR20200069453A (ko) | 벤조페논 작용기 함유 화합물, 상기 화합물의 광경화물을 포함한 유기물층을 구비한 유기전자소자 | |
| CN1761693A (zh) | 聚酯及其制备和用途 | |
| CN1582310A (zh) | 芳族聚合物的制备方法 | |
| CN1818010A (zh) | 蓝光电致发光聚合物和使用其的有机电致发光器件 | |
| JP5198428B2 (ja) | 多層構造を有する光電子デバイス |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| REG | Reference to a national code |
Ref country code: HK Ref legal event code: DE Ref document number: 1063810 Country of ref document: HK |
|
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication | ||
| REG | Reference to a national code |
Ref country code: HK Ref legal event code: WD Ref document number: 1063810 Country of ref document: HK |