CN1497360A - 具有含甲苯胺基团化合物的有机光感受器 - Google Patents
具有含甲苯胺基团化合物的有机光感受器 Download PDFInfo
- Publication number
- CN1497360A CN1497360A CNA031248772A CN03124877A CN1497360A CN 1497360 A CN1497360 A CN 1497360A CN A031248772 A CNA031248772 A CN A031248772A CN 03124877 A CN03124877 A CN 03124877A CN 1497360 A CN1497360 A CN 1497360A
- Authority
- CN
- China
- Prior art keywords
- organophotoreceptorswith
- compound
- charge
- layer
- branching
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03G—ELECTROGRAPHY; ELECTROPHOTOGRAPHY; MAGNETOGRAPHY
- G03G5/00—Recording members for original recording by exposure, e.g. to light, to heat, to electrons; Manufacture thereof; Selection of materials therefor
- G03G5/02—Charge-receiving layers
- G03G5/04—Photoconductive layers; Charge-generation layers or charge-transporting layers; Additives therefor; Binders therefor
- G03G5/06—Photoconductive layers; Charge-generation layers or charge-transporting layers; Additives therefor; Binders therefor characterised by the photoconductive material being organic
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/56—Ring systems containing three or more rings
- C07D209/80—[b, c]- or [b, d]-condensed
- C07D209/82—Carbazoles; Hydrogenated carbazoles
- C07D209/86—Carbazoles; Hydrogenated carbazoles with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to carbon atoms of the ring system
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03G—ELECTROGRAPHY; ELECTROPHOTOGRAPHY; MAGNETOGRAPHY
- G03G5/00—Recording members for original recording by exposure, e.g. to light, to heat, to electrons; Manufacture thereof; Selection of materials therefor
- G03G5/02—Charge-receiving layers
- G03G5/04—Photoconductive layers; Charge-generation layers or charge-transporting layers; Additives therefor; Binders therefor
- G03G5/06—Photoconductive layers; Charge-generation layers or charge-transporting layers; Additives therefor; Binders therefor characterised by the photoconductive material being organic
- G03G5/0601—Acyclic or carbocyclic compounds
- G03G5/0612—Acyclic or carbocyclic compounds containing nitrogen
- G03G5/0614—Amines
- G03G5/06142—Amines arylamine
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03G—ELECTROGRAPHY; ELECTROPHOTOGRAPHY; MAGNETOGRAPHY
- G03G5/00—Recording members for original recording by exposure, e.g. to light, to heat, to electrons; Manufacture thereof; Selection of materials therefor
- G03G5/02—Charge-receiving layers
- G03G5/04—Photoconductive layers; Charge-generation layers or charge-transporting layers; Additives therefor; Binders therefor
- G03G5/06—Photoconductive layers; Charge-generation layers or charge-transporting layers; Additives therefor; Binders therefor characterised by the photoconductive material being organic
- G03G5/0622—Heterocyclic compounds
- G03G5/0644—Heterocyclic compounds containing two or more hetero rings
- G03G5/0661—Heterocyclic compounds containing two or more hetero rings in different ring systems, each system containing at least one hetero ring
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Photoreceptors In Electrophotography (AREA)
- Liquid Developers In Electrophotography (AREA)
- Indole Compounds (AREA)
Abstract
一种改进有机光感受器,包括导电基底和在导电基底上的光导元件,其中光电导元件具有(a)具有下列通式的电荷转移材料,其中R1和R2各自独立是,咔唑基、N,N-双取代的氨基芳基、例如三苯基胺基、或久洛尼定基,R3和R4各自独立是氢、支化或线性烷基(例如C1-C20烷基)、支化或线性不饱和烃基、环烷基(例如环己基)、或芳基(例如苯基、茋基、萘基、(9H-芴基-9-亚基)苯甲基,或二苯乙炔基)。(b)任选的电荷转移化合物;和(c)电荷产生化合物。
Description
交叉引用相关申请
本申请要求待批美国临时专利申请号60/414,822的优先权,Jubran等2002年9月30日提交,名称为″具有甲苯胺基团的新型电子转移化合物的有机光感受器″在这里引入作为参考。
本发明领域
本发明涉及适用于电子照相的有机光感受器,更准确地说涉及具有含甲苯胺基团(可以取代)化合物的有机光感受器。
本发明背景
在电子照相中,板状、盘状、薄片、带状、鼓状等形状有机光感受器在导电基底上具有电绝缘光导电元件,首先均匀地静电充电于光导电元件表面,然后使充电表面曝光形成光图像。光照射有选择地释放照明区域(光照射的表面)内的电荷,因此形成充电和未充电区的图案,称为潜影。随后在潜影附近提供液体调色剂或固体调色剂,调色剂微滴或颗粒可取决于调色剂的性能沉积在充电或未充电的区域,以在光导电元件表面上形成调色的图像。得到的调色图像可以转移到最终或中间接收表面,例如纸、或光导电元件可以作为图像的最终接受体。成像过程可以重复多次,以完成单一图像,图像可以包括,例如清楚的呈色组分的重叠图象,或者产生阴影像以得到全色完全图,和/或复制其它的图像。
已经使用单层和多层光导电元件。在单层实施方式中,选自电荷转移化合物、电子转移化合物和其两者组合物的电荷产生化合物和电荷转移材料与聚合粘结剂结合,然后沉积在导电基底上。在多层实施方式中,基于电荷转移化合物,电荷转移化合物和电荷产生化合物以分开的层,其每个可以选择性地结合聚合粘结剂,沉积在导电的基底上。两种排列是可能的。在一种排列(″双层″排列)中,电荷产生层沉积在导电的基底上,电荷转移层沉积在电荷产生层顶部,在另一个排列(″反向双层″排列)中,电荷转移层和电荷产生层的顺序是相反的。
在单层和多层光导电元件中,电荷产生材料的用途是在其上曝光时产生电荷载体(即空穴和/或电子)。电荷转移材料的用途是接受这些电荷载体,并转移它们穿过电荷转移层以放出光导电元件上的表面电荷。当使用电荷转移化合物时,电荷转移化合物接受空穴载体,并转移它们穿过电荷转移化合物所在的层。当使用电子转移化合物时,电子转移化合物接受电子载体,并转移它们穿过电子转移化合物所在的层。
本发明摘要
本发明涉及具有优良静电性能例如高Vacc和低Vdis的有机光感受器。
在第一方面,本发明特征为有机光感受器,包括导电基底和在导电基底上的光导电元件,其中光导电元件具有
a)一种具有下列通式的电荷转移材料
其中R1和R2独立地是咔唑基、(N,N-双取代的)氨基芳香基、例如三苯胺基、或久洛尼定基(julalidine),R3和R4独立地是氢、支化或线性烷基(例如C1-C20烷基),支化或线性不饱和烃基、环烷基(例如环己基)、或芳基(例如苯基、萘基、芪基、(9H-芴-9-亚基(ylidene))苯甲基、二苯乙炔基);
(b)任选的电荷转移化合物;和
(c)电荷产生化合物。
例如,有机光感受器可以是板状、柔性带状、柔性盘状、薄片状、刚性鼓状、围绕刚性或柔性鼓状的薄片。在一个实施方式中,有机光感受器包括:(a)一种光导电元件,包括电荷转移化合物、电荷产生化合物、电子转移化合物、和聚合粘结剂;和(b)导电的基底。
在第二方面,本发明特征为电子照相成像装置,包括(a)光成像元件;和(b)上述的有机光感受器用于接收来自光成像元件的光线。装置可以进一步包括调色剂分配器,例如液体调色剂分配器。也描述了具有含这些改进的转移材料的光感受器的电子照相成像方法。
在第三方面,本发明特征为电子照相成像过程,包括(a)对上述有机光感受器表面进行充电;(b)成象地曝光有机光感受器表面以辐射释放选择区域的电荷,并从而在表面上形成至少相对充电和未充电区域的图案;(c)使表面接触调色剂,例如液体调色剂(包括分散在有机液体中的色料颗粒),以产生调色图像;和(d)转移调色图像至基底。
在第四方面,本发明特征为具有上述通式的电荷转移材料。
本发明提供了用于有机光感受器的电荷转移材料,特征为具有优良机械和静电性能的组合。这些光感受器可以成功地和液体调色剂一起使用以产生高质量的图像。成像系统的高质量在重复周期之后得以保持。
从下列优选实施方式的说明和权利要求,本发明的其它特征和优点将清晰可见。
附图摘要
图1是在导电基底上的具有光电导层的有机光感受器侧视图。
图2是有机光感受器的侧视图,其在导电基底上依次具有电荷产生层和电荷转移层。
图3是有机光感受器的侧视图,其在导电的基底上依次具有电荷转移层和电荷产生层。
图4是有机光感受器的侧视图,其在导电基底上依次具有电荷转移层、电荷产生层和电子转移层。
图5有机光感受器的侧视图,其在导电的基底上依次具有电子转移层、电荷产生层和电荷转移层。
优选实施方式的详细说明
改进的有机光感受器包括通常作为电荷转移材料的化合物,具有下列通式:
其中R1和R2独立地是(N,N-双取代的)氨基芳香基、例如三苯胺基、咔唑基或久洛尼定基,R3和R4独立地是氢、支化或线性烷基(例如,C1-C20烷基)、支化或线性不饱和烃基、环烷基基(例如环己基)、或芳基(例如苯基、萘基、芪基、(9H-芴-9-亚基)苯甲基、或二苯乙炔基);本领域已知,可以广泛选择取代基以实现对化合物性能的各种物理影响,例如流动性、灵敏性、可溶性、稳定性等。上述通式的化合物也包括上述通式的同分异构体,意味着R1和R2可互换,R3和R4可互换。在一些实施方式中,这些化合物作为电子转移化合物是特别有效的。
通常,有机光感受器包括导电基底,在导电基底的表面具有光导电元件,其中光导电元件可包括一层或多层,即其结构内部的分层。光电导体的一层或多层可以包含电子转移化合物。具有电子转移化合物的层还可以包括聚合粘结剂、电荷转移化合物、紫外光稳定剂、和/或电荷产生化合物。
为了产生高质量的图像,特别在多次循环之后,合乎需要的是有机光感受器的化合物和聚合粘结剂形成均匀溶液,并在材料循环期间保持大致均匀地分散在有机光感受器中。此外,为了产生高质量图像,合乎需要的是增加有机光感受器可以接受的电荷量(用参数标明为已知的接受电压或“Vacc”),并减少放电时的电荷保留(用参数标明为已知的放电电压或“Vdis”)。
在这里描述的改进的有机光感受器根据循环试验、结晶、弯曲和伸展,具有高Vacc、低Vdis、和高稳定性。有机光感受器特别适用于激光打印机等以及复印机、扫描仪、其他基于电子照相的电子设备、和其组合。尽管由电子照相操作的其它装置中的应用可以从以下讨论中概括,这些有机光感受器的用途在以下激光打印机应用的内容中更详细地公开。
通常,电子转移化合物与电荷转移化合物(通常转移空穴(即正电荷)更有效)相比具有适当的转移电子能力。在电子照相应用中,有机光感受器内的电荷产生化合物吸收光以形成电子-空穴对。电子和/或空穴可以在大电场下的适当时间范围内转移以放出部分表面电荷,也就是说产生电场。在具体位置的电场的放电产生表面电荷图案,该图案基本上符合以光形成的图案。随后该电荷图案可用于引导调色剂沉积。为了使用有机光感受器印刷二维图像,有机光感受器具有用于形成至少部分图像的二维表面。随后通过循环使用有机光感受器以完成全部图像的形成和/或用于随后图像的处理而继续成像过程。
有机光感受器可以是板状、柔性带状、盘状、刚性鼓状、围绕刚性或柔性鼓的薄片等形状。电荷转移化合物和/或电子转移化合物可与电荷产生化合物在同一层,和/或与电荷产生化合物在不同的层。例如,电子转移化合物可以在外涂层。在一些实施方式中,有机光感受器材料为单一层、在聚合粘结剂内具有电荷转移化合物和电荷产生化合物。在另一实施方式中,电荷转移化合物可以在不同于电荷产生层的电荷转移层中。对于使用电子转移层和单独的电荷转移层的实施方式,电荷产生层通常是在电荷转移层和电子转移层间的中间。对于电子转移层在外涂层的实施方式,电荷转移层可以是在电荷产生层和导电基底间的中间。也可以使用附加层,如以下公开的。
有机光感受器可以并入电子照相成像装置,例如激光打印机。在这些装置中,图像由物理设备形成,并转变成光图像,扫描到有机光感受器上以形成表面潜像。表面潜像可用于吸引有机光感受器表面上的调色剂,其中调色剂图像与投射到有机光感受器上的光图像相同或相反。调色剂可以是液体调色剂或干燥调色剂。随后调色剂可以从有机光感受器表面转移至接收表面,例如一张纸。在调色剂转移之后,整个表面可以放电,材料准备再次循环。例如,成像装置可以进一步包括,多个用于转移纸接收介质和/或移动光感受器的支承辊,具有合适光学器件以形成光成像的光成像组件、光源,例如激光器、调色剂源和输送系统以及适当的控制系统。
电子照相成像过程通常可以包括(a)在上述公开的有机光感受器表面进行充电;(b)曝光有机光感受器表面,以辐射释放选择区域内的电荷,并因此在表面上形成充电和未充电的图案;(c)使表面暴露于调色剂,例如液体调色剂(包括分散在有机液体中的色料颗粒)以吸引调色剂至有机光感受器充电或放电区域以产生调色剂图像;和(d)转移调色剂图像至基底。
在公开的以具有化学取代基的结构式表示的化学试剂中,某些术语可用于反映通式代表的全部范围。例如,术语″基团″、″部分″、和″衍生物″可以具有特定的含义。术语“基团”指通常在所述的化学物质(例如烷基、苯基、亚芴基丙二腈基、咔唑腙基等)上可以有任何与该基团的键结构一致的取代基。因此,术语“基团”容许在指定类材料上存在其它取代基,只要取代基仍然是属类内可认识的。例如,烷基包括,例如未被取代的线性、支化和环烷基,例如甲基、乙基、异丙基、叔丁基、环己基、十二烷基等,也包括诸如取代的烷基例如氯甲基、二溴乙基、1,3-二氰基丙基、1,3,5-三羟基己基、1,3,5-三氟环己基、1-甲氧基-十二烷基、苯丙基等。然而,与这类术语相一致,该术语不包括改变基础基团的基本键结构的取代。例如,当述及苯环基团时,取代基例如1-羟苯基,2,4-氟苯基、正氰基苯基、1,3,5-三甲氧基苯基等是该命名法可接受的,而1,1,2,2,3,3-六甲基苯基是不可接受的,因为该取代基要求苯基的环键结构改变为非芳香形式。类似地,当涉及咔唑基时,列举的化合物或取代基包括不实质上改变环基团化学性质或通式中其它特征的键结构(例如氮间双键等)的任何取代基。例如,咔唑基不包括用饱和环中双键而除去芳香结构的环变化,但是包括加入长链脂肪酸基团取代咔唑基上的氢原子。
当使用术语“部分”时,例如烷基部分或苯基部分,术语代表没有被取代的化学物质。例如,术语烷基部分仅代表未被取代的烷基烃类基团,不论支化、直链、或环。当使用术语衍生物时,该术语代表从另一物质衍生或获得的并包含母体物质基本单元的化合物。
许多电子转移化合物适用于电子照相。某些本领域普通的电子转移化合物列举如下。通常,这些电子转移化合物在各种电子照相应用中的至少一种具有某些缺点。因此,一直需要另一种电子转移化合物以满足电子照相应用的各种要求。在这里公开的化合物的某些具体实例具有甲苯胺基团,可用于满足这些需要。
有机光接受器
有机光感受器可以是例如,板状、片状、柔性带状、盘状、刚性鼓状、或围绕刚性或柔性鼓的片状,柔性带状并刚性鼓状通常用于商业用途。有机光感受器可以包括,例如,导电基底和一层或多层形式的光导电元件。有机光感受器通常包括在聚合粘结剂中的电荷转移化合物和电荷产生化合物(可以在相同或不同的层)。类似地,电子转移化合物与电荷产生化合物可以在或不在相同层。如果电子转移化合物与电荷产生化合物在不同的层,电子转移化合物可以是外涂层,即,在相对于导电基底的一侧,或是内涂层,与电荷产生层在相同一边如导电基底。在某些实施方式中,具有电子转移化合物的层可以进一步包括紫外光稳定剂。
至于电荷产生化合物和电荷转移化合物,在某些单层结构实施方式中,电荷转移化合物和电荷产生化合物是在单一层中。然而在其它实施方式中,光导电元件包括双层结构,特征为电荷产生层和单独的电荷转移层。电荷产生层可以位于导电基底和电荷转移层间的中间。或者,光导电元件可以具有其中电荷转移层是在导电基底和电荷产生层间的中间的结构。可比较的有机光感受器可以仅由电子转移化合物形成,而没有电荷转移化合物,尽管特别感兴趣的有机光感受器的具体实例具有电荷转移化合物。
基于电荷产生层和电荷转移层的三种基本结构,可以根据电子转移化合物的存在而概括有机光感受器的结构。例如,对于电子转移化合物与电荷产生化合物在相同层的具体实例,有图1-3示意显示出的三种可能结构。参见图1,有机光感受器100包括导电基底102和光电导层104,光电导层包括电荷产生化合物、电荷转移化合物和电子转移化合物。参见图2,有机光感受器110包括导电基底112,包含电荷产生化合物和电子转移化合物的电荷产生层114,和包含电荷转移化合物的电荷转移层116。参见图3,有机光感受器120包含导电基底122,包含电荷转移化合物的电荷转移层124,和包含电荷产生化合物和电子转移化合物的电荷产生层126。
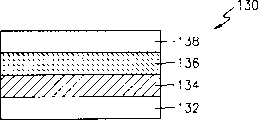
对于电子转移化合物与电荷产生化合物在不同层的具体实例,有两种主要感兴趣的结构,在图4和5中所示。参见图4,有机光感受器130包括导电基底132,包含电荷转移化合物的电荷转移层134,包含电荷产生化合物的电荷产生层136,和包含电子转移化合物的电子转移层138。参见图5,有机光感受器150包括导电基底152,包含电子转移化合物的电子转移层154,包含电荷产生化合物的电荷产生层156,和包括电荷转移化合物的电荷转移层158。
当图1-5的具体实例在单一层中具有电子转移化合物时,则多层可以包含电子转移化合物。特别地,电子转移层和电荷产生层可以都包含电子转移化合物。此外,在图1-5显示的有机光感受器结构可以进一步包含其它的内涂层和/或外涂层,例如以下进一步公开的。此外,在图1-5显示的特别感兴趣的具体实例以外可以形成其它分层的有机光感受器结构,这些其它的结构可以具有不同的分层顺序和/或多种公开的层类型(具有或没有不同的组合物)。
导电基底与导电基底支持的电绝缘衬底一起可以是柔性的,例如柔性网或带状物形式,或刚性,例如鼓状物形式。鼓状物可以具有中空的圆柱状结构,以提供使鼓状物安装到在成像过程期间旋转鼓状物的驱动设备上。一般地,复合基底包括电绝缘衬底和导电材料薄层,在导电基底上施加光电导材料。
电绝缘衬底可以是纸或成膜聚合物例如聚酯,例如聚对苯二甲酸乙二酯或聚萘酸乙二酯、聚酰亚胺、聚砜、聚烯烃、例如聚乙烯或聚丙烯,尼龙、聚碳酸酯、聚乙烯树脂、聚氟乙烯、聚苯乙烯,其适当的共聚物,其混合物等。用于支持基底的聚合物特定实例包括,例如,聚醚砜(StabarTM S-100,可从ICI获得),聚氟乙烯(Tedlar,可从E.I.DuPont de Nemours & Company获得),聚双酚-A聚碳酸酯(MakrofolTM可从Mobay Chemical Comnpany获得)和无定形的聚对苯二甲酸乙二酯(MelinarTM,可从ICI Americas,Inc获得.)。导电材料,通常为涂层形式,可以包括石墨、分散的炭黑、碘化物、导电聚合物、例如聚吡咯(polypyroles)和Calgo导电聚合物261(可商购自CalgonCorporation,Inc.,Pittsburgh,Pa.),金属,例如铝,钛、铬、黄铜、金、铜、钯、镍、不锈钢或其合金,金属氧化物例如氧化锡或氧化铟或其组合物。在特别感兴趣的具体实例中,导电材料包括铝金属。通常,光导电基底具有足够厚度以提供所需的机械稳定性。例如,柔性网基底通常厚度约0.01-约1毫米,而鼓状基底通常厚度约0.5毫米-约2毫米。
电荷产生化合物通常例如是能够吸收光以产生电荷载体的材料如染料或颜料。适当的电荷产生化合物的非限定实例包括,例如,不含金属的酞菁(例如CGM-XO1,可从Sanyo Color Works,Ltd获得.),金属酞菁例如钛酞菁、铜酞菁、氧钛(oxytitanium)酞菁(也称为钛氧基羟酞菁,并包括可以作为电荷产生化合物的任何晶相或晶相混合体),羟基镓酞菁、方形酸鎓盐(squarglium)染料和颜料,羟基取代的方形酸鎓盐颜料、苝酰胺(perylimides)、多核醌,可从Allied Chemical Corporation以商品名IndofastDouble Scarlet、IndofastViolet Lake B、IndofastBrilliant Scarlet和IndofastOrange获得、喹吖啶酮,可从DuPont以商品名MonastralTM Red、MonastralTM Violet和MonastralTM Red Y获得,萘1,4,5,8-四羧酸衍生的颜料包括perinones、四苯并卟啉和四萘并卟啉,靛类和硫靛类染料、苯并噻吨衍生物,苝3,4,9,10-四羧酸衍生的颜料,多偶氮颜料,包括双偶氮、三偶氮和四偶氮颜料,多次甲基染料,含喹唑啉基团的染料,叔胺,无定形硒,硒合金例如硒-碲、硒-碲-砷和硒-砷、硫硒化镉,硒化镉,硫化镉和其混合物。对于某些具体实例,电荷产生化合物包括氧钛基酞菁(例如其任何晶相),羟基镓酞菁或其混合物。
有许多种电荷转移化合物适用于电子照相。例如,任何本领域已知的电荷转移化合物可用于形成本文公开的有机光导电体。合适的电荷转移化合物包括,但是不局限于吡唑啉酮衍生物,芴衍生物、二唑衍生物、芪衍生物、腙衍生物、咔唑腙衍生物,三芳基胺、聚乙烯咔唑、聚乙烯芘、聚苊、或包含至少二个腙基团的多腙化合物,至少二个基团选自三苯胺和杂环例如咔唑、久洛尼定、吩噻嗪、吩嗪、吩嗪、吩氧硫杂环己二烯(phenoxathiin)、噻唑、唑、异唑、二苯并(1,4)二烯、噻蒽、咪唑、苯并噻唑、苯并三唑、苯并唑、苯并咪唑、喹啉、异喹啉、喹喔啉、吲哚、吲唑、吡咯、嘌呤、吡啶、哒嗪、嘧啶、吡嗪、三唑、二唑、四唑、噻二唑、苯并异唑、苯并异噻唑、氧芴、硫芴、噻吩、硫茚、喹唑啉、肉啉或其组合物。在某些具体实例中,电荷转移化合物是烯胺芪化合物例如来自Mitsubishi Paper Mills(Tokyo,Japan)的MPCT-10,MPCT 38和MPCT-46。
适用于适当层或多层的适宜的电子转移化合物通常具有对于电子捕获电势较大的电子亲合性,在与聚合物混合时产生适当电子迁移率。在某些具体实例中,电子转移化合物具有小于O2的还原电位。通常、电子转移组合物易于还原,并难于氧化,而电荷转移组合物通常易于氧化,难于还原。在某些具体实例中,电子转移化合物在室温、零电场下的电子迁移率至少约1×10-13cm2/Vs,在另一些具体实例中至少约1×10-10cm2/Vs,在另一些具体实例中至少约1×10-8cm2/Vs,在另一些具体实例中至少约1×10-6cm2/Vs。本领域熟练技术人员参考详述的范围,将认识到本发明范围内电子迁移率的其它范围。
用于有机光接受体的电子转移化合物可以是具有甲苯胺基团化合物(即甲苯胺基化合物),例如以下所公开的。一种或多种甲苯胺基化合物可用于光电导体选择层作为电子转移化合物,或甲苯胺基化合物可用于与另一种非甲苯胺基电子转移化合物的组合。适宜的非甲苯胺基电子转移化合物的非限定实例包括,例如溴苯胺、四氰乙烯、四氰基醌二甲烷、2,4,7-三硝基-9-芴酮、2,4,5,7-四硝基-9-芴酮、2,4,5,7-四硝基呫吨酮、2,4,8-三硝基硫代呫吨酮、2,6,8-三硝基-茚并4H-茚并[1,2-b]噻吩-4-酮,和1,3,7-三硝基二苯并噻吩-5,5-二氧化物,(2,3-二苯基-1-亚茚基)丙二腈,4H-噻喃-1,1-二氧化物、和其衍生物,例如4-二氰基亚甲基-2,6-二苯基-4H-噻喃-1,1-二氧化物、4-二氰基亚甲基-2,6-二间甲苯基-4H-噻喃-1,1-二氧化物、和非对称取代的2,6-二芳基-4H-噻喃-1,1-二氧化物例如4H-1,1-二氧代-2-(对异丙苯基)-6-苯基-4-(二氰基亚甲基)噻喃和4H-1,1-二氧代-2-(对异丙苯基)-6-(2-噻嗯基)-4-(二氰基亚甲基)噻喃,磷杂2,5-环己二烯的衍生物、烷氧羰基-9-亚芴基)丙二腈衍生物例如(4-正丁氧基羰基-9-亚芴基)-丙腈、(4-苯乙氧基,羰基-9-亚芴基)丙二腈、(4-卡必氧基-9-亚芴基)丙二腈、和二乙基(4-n-丁氧基羰基-2,7-二硝基-9-亚芴基)二丙酯、蒽醌(anthraquino)二甲烷衍生物例如11,11,12,12-四氰基-2-烷基蒽醌二甲烷和11,11-二氰基-12,12-双(乙氧基羰基)蒽醌二甲烷,蒽酮衍生物例如I-氯-10[双(乙氧基羰基)亚甲基]蒽酮,1,8-二氯-10[双(乙氧羰基)亚甲基]蒽酮,1,8-二羟基-10[双(乙氧羰基)亚甲基]蒽酮,和1-氰基-10-[双(乙氧羰基)亚甲基]蒽酮,7-硝基-2-氮杂-9-亚芴基-丙二腈,双酚醌衍生物、苯并醌衍生物、萘并醌衍生物、奎宁衍生物、四氰基亚乙基氰基乙烯、2,4,8-三硝基噻吨酮(thioxantone)、二硝基苯衍生物、二硝基蒽衍生物、二硝基吖啶衍生物、硝基蒽醌衍生物、二硝基蒽醌衍生物、琥珀酸酐、马来酸酐、二溴代马来酸酐、芘衍生物、咔唑衍生物、腙衍生物、N,N-二烷基苯胺衍生物、二苯胺衍生物、三苯胺衍生物、三苯甲烷衍生物、四氰基醌二甲烷,2,4,5,7-四硝基-9-芴酮,2,4,7-三硝基-9-二氰基亚甲基芴酮,2,4,5,7-四硝基噻吨酮衍生物,2,4,8-三硝基噻吨酮衍生物和其组合物。
电子转移化合物和紫外线光稳定剂可以具有协同关系,用于提供想要的光电导体内部的电子流。紫外线光稳定剂的存在改变电子转移化合物的电子转移性能以改善复合物的电子转移性能。紫外线光稳定剂可以是紫外线吸收剂或捕捉自由基的紫外线抑制剂。
紫外线光吸收剂可以吸收紫外辐射,并在加热时散逸。紫外线抑制剂被认为是捕捉紫外线产生的自由基,并在捕捉自由基后随着能量损耗再生活性稳定剂部分。由于紫外线稳定剂和电子转移化合物的协同关系,紫外线稳定剂的特定优点可能不是其紫外线稳定能力,尽管紫外线稳定能力可以进一步有利地减少有机光感受器随时间的降解。而不受理论的限制,紫外线稳定剂贡献的协同关系可能与化合物的电子性能(该性能有助于紫外线稳定功能)有关,与电子转移化合物结合进一步有助于建立电子传导通道。特别地,具有电子转移化合物和紫外线稳定剂组合物的有机光感受器证明可以具有更稳定的循环接受电压Vacc。具有含电子转移化合物和紫外线稳定剂层的有机光感受器的改善的协同性能公开于待批美国专利申请号10/425,333,Zhu,2003年4月28日提交,名称为“具有光稳定剂的有机光感受器”在这里引入作为参考。
合适的光稳定剂的非限定实例包括,例如,位阻三烷基胺例如Tinuvin144和Tinuvin 292(来自Ciba Specialty Chemicals,Terrytown NY),位阻烷氧基二烷基胺例如Tinuvin 123(来自Ciba Specialty Chemicals),苯并三唑例如Tinuvan 328、Tinuvin 900和Tinuvin 928(来自Ciba Specialty Chemicals),二苯甲酮例如Sanduvor 3041(来自Clariant Corp,Charlotte,N.C.),镍化合物例如Arbestab(来自Robinson Brothers Ltd,West Midlands、Great Britain),水杨酸酯,氰基桂皮酸酯、亚苄基丙二酸酯、苯甲酸酯、草酰二苯胺例如SanduvorVSU(来自Clariant Corp.Charlotte,N.C.),三嗪例如Cyagard UV-1164(来自Cytec Industries Inc.N.J.),聚合位阻胺例如Luchem(来自Atochem NorthAmerica,Buffalo,NY)。在某些具体实例中,光稳定剂选自具有下列通式的位阻三烷基胺:
其中R1、R2、R3、R4、R6、R7、R8、R10、R11、R12、R13和R15各自独立是氢、烷基或酯、或醚基团;R5、R9、和R14各自独立是烷基;X是连接基团选自-O-CO-(CH2)m-CO-O,m在2-20之间。
用于有机光感受器任何特定层的聚合物粘合剂通常能够分散或溶解相应的官能化合物,例如电子转移组合物、电荷转移化合物、电荷产生化合物和/或紫外线光稳定化合物。合适的聚合物粘合剂实例通常包括,例如苯乙烯--丁二烯共聚物、苯乙烯--丙烯腈共聚物,改性丙烯酸聚合物、聚醋酸乙烯酯、苯乙烯醇酸树脂、大豆脂肪酸-烷基树脂、聚氯乙烯、聚偏氯乙烯、聚丙烯腈、聚碳酸酯、聚丙烯酸、聚丙烯酸脂、聚甲基丙烯酸酯、苯乙烯聚合物、聚乙烯醇缩丁醛、醇酸树脂、聚酰胺、聚氨酯、聚酯、聚砜、聚醚、聚酮、苯氧基树脂、环氧树脂、有机硅树脂、聚硅氧烷、聚(羟基醚)树脂、聚羟基苯乙烯树脂、酚醛清漆、(苯基缩水甘油醚)--双环戊二烯共聚物,用于上述聚合物单体的共聚物、和其组合物。在某些特别感兴趣的具体实例中,粘结剂选自聚碳酸酯、聚乙烯醇缩丁醛和其组合物。合适的聚碳酸酯粘结剂实例包括,例如,衍生自双酚-A的聚碳酸酯A、衍生自亚环己基双酚的聚碳酸酯Z、衍生自甲基双酚A的聚碳酸酯C和聚酯碳酸酯。合适的聚乙烯醇缩丁醛的实例是BX-1和BX-5,来自Sekisui Chemical Co.Ltd.,Japan。对于释放层,合乎需要的可以是,例如,氟化聚合物、硅氧烷聚合物、氟硅酮聚合物、聚硅烷、聚乙烯、聚丙烯、聚丙烯酸酯、(异丁烯酸甲酯--甲基丙烯酸)共聚物、聚氨酯树脂、氨基甲酸乙酯-环氧树脂、丙烯酸酯-氨基甲酸乙酯树脂、氨基甲酸乙酯-丙烯酸树脂、其交联聚合物或其组合物。
任何一个或多个层的适合的任选添加剂包括,例如抗氧化剂、偶联剂、分散剂、固化剂、表面活性剂和其组合物。
光导电元件的总厚度一般为约10-约45微米。在双层具体实例中具有单独的电荷产生层和单独的电荷转移层,电荷产生层通常厚度约0.5-约2微米,电荷转移层厚度约5-约35微米。在电荷转移化合物和电荷产生化合物在同一层的具体实例中,具有电荷产生化合物和电荷转移组合物的层通常厚度从7-约30微米。在具有特定的电子转移层的具体实例中,电子转移层平均厚度约0.5微米-约10微米,在另一些具体实例中约1微米-约3微米。通常,电子转移外涂层可以增加机械抗磨性、增加对载液和大气湿度的抵抗性,并减少由电晕气体引起的光感受器降解。本领域熟练技术人员参考详述的范围,将认识到本发明范围内厚度的其它的范围。
通常,对于在这里公开的有机光感受器,电荷产生化合物的含量基于光电导层的重量约0.5-约20wt%,在另一些具体实例中约1-约10wt%。电荷转移化合物的含量基于光电导层的重量约10-约80wt%,在另一些具体实例中基于光电导层的重量约35-约60wt%。电子转移化合物的含量基于光电导层的重量约2.5-约25wt%,在另一些具体实例中基于光电导层的重量约4wt%-约20wt%。粘结剂的含量基于光电导层的重量约15-约80wt%,在另一些具体实例中基于光电导层的重量约20-50wt%。
对于具有单独的电荷产生层和电荷转移层的双层具体实例,电荷产生层通常基于电荷产生层的重量包含约10-约90wt%的粘结剂,在另一些具体实例中约15-约80wt%,在某些具体实例中约20-约75wt%。如果在电荷产生层存在任选的电子转移化合物,通常含量基于电荷产生层的重量至少约2.5wt%,在另一些具体实例中约4-约30wt%,在其它具体实例中约10-约25wt%。电荷转移层通常包含约30wt%-约70wt%的粘结剂。本领域熟练技术人员参考详述的范围,将认识到本发明范围内双层具体实例中粘合剂含量的其它范围。
对于含电荷产生化合物和电荷转移化合物的单一层的具体实例,光电导层一般包含粘结剂、电荷转移化合物和电荷产生化合物。电荷产生化合物含量基于光电导层的重量可以约0.05-约25wt%,在另一些具体实例中含量约2-约15wt%。电荷转移化合物的含量可以约10-约80wt%、在另一些具体实例中约25-约65wt%,在另一些具体实例中约20-约60wt%,在另一些具体实例中含量约35-约55wt%,都基于光电导层的重量,光电导层的其余部分包括粘结剂和任选的添加剂,例如任一常规添加剂。具有电荷转移化合物和电荷产生化合物的单一层通常包含约10wt%-约75wt%的粘结剂,在另一些具体实例中约20wt%-约60wt%,在另一些具体实例中约25wt%-约50wt%。任选地,具有电荷产生化合物和电荷转移化合物的层可以包含电子转移化合物。如果存在任选的电子转移化合物,基于光电导层的重量通常含量至少约2.5wt%,在另一些具体实例中含量约4-约30wt%,在另一些具体实例中含量约10-约25wt%。本领域熟练技术人员参考详述的范围,将认识到本发明范围内其它组分的范围。
通常,任何具有电子转移层的层可以有利地进一步包含紫外线光稳定剂。特别地,电子转移层通常可以包含电子转移化合物、粘结剂和任选的紫外线光稳定剂。包含电子转移化合物的外涂层公开于待批美国专利申请号10/396,536,Zhu等名称为,″具有电子转移层的有机光感受器″,在这里引入作为参考。例如,如上所述的电子转移化合物可以用于此处公开的光电导体的释放层。电子转移层中的电子转移化合物含量基于电子转移层的重量约10-约50wt%,在另一些具体实例中约20-约40wt%。本领域熟练技术人员参考详述的范围和本发明公开的范围,将认识到组分的其它范围。
如果存在紫外线光稳定剂,在光电导体任何适当的一层或多层中含量基于特定层的重量约0.5-约25wt%,在某些具体实例中含量约1-约10wt%。
可以根据本领域任何适当的已知技术形成光导电元件,例如浸涂、喷涂、挤出等。本领域熟练技术人员根据详述的范围将认识到本发明范围内其它成分的范围和厚度。
光感受器可以同时选择性地具有附加层。该附加层可以是,例如,内层和/或外涂层。内层可以是位于导电基底和光导电元件之间的电荷阻挡层。内层也可以改善导电基底和光导电元件之间的粘着力。
外涂层可以是,例如阻挡层、释放层、保护层和粘结层。对于外涂层,光感受器可以包含一个或多个具有电子转移化合物的外涂层(例如电子转移层)。例如,释放层或保护层可以包含电子转移化合物。如上所述的一种或多种电子转移化合物可以用于释放层或保护层。
在释放层或保护层中的电子转移化合物含量通常可以为约2-约50wt%,在另一些具体实例中,含量约10-约40wt%,都基于释放层或保护层的重量。本领域熟练技术人员根据详述的范围将认识到本发明范围内成分的其它范围。虽然外涂层可以具有或没有电子转移化合物,存在于每个外涂层的电子转移化合物(可以与其它外涂层组合物相同或不同)可以提供电荷产生层和表面间的连续的电导率,这可以改善有机光感受器的性能。
释放层或保护层形成光电导体层的最上层。例如,当不通过静电力或磁力促进调色剂转移时,顶层释放层促进调色剂从有机光感受器转移至中间传送介质例如带状物或鼓状物、或接受介质例如纸。释放层可以具有比调色剂从有机光感受器转移到的介质更低的表面能。顶层为保护层,它为下层提供磨擦和耐溶剂的保护。一层可以同时是保护层和释放层。阻挡层可以夹在释放层和光导电元件之间,或用于光导电元件外涂层。阻挡层为下层提供磨擦和耐溶剂的保护。粘结层位于并改善电荷产生层和外涂层间或两个外涂层间的粘附力。
合适的阻挡层包括,例如,涂层例如可交联的硅氧烷醇-胶态的二氧化硅涂层和羟基化硅倍半烷(silsesquioxane)-胶态的二氧化硅涂层,和有机粘结剂例如聚乙烯醇、甲基乙烯基醚/马来酸酐共聚物、酪蛋白、聚乙烯基吡咯烷酮、聚丙烯酸、明胶、淀粉、聚氨酯、聚酰亚胺、聚酯、聚酰胺、聚醋酸乙烯酯、聚氯乙烯、聚亚乙烯基氯化物、聚碳酸酯、聚乙烯缩丁醛、聚乙烯乙酰缩乙醛、聚乙烯缩甲醛、聚丙烯腈、聚甲基丙烯酸甲酯、聚丙烯酸酯、聚乙烯咔唑,用于上述聚合物单体的共聚物,氯乙烯/醋酸乙烯酯/乙烯醇三元共聚物,氯乙烯/醋酸乙烯酯/马来酸三元共聚物,乙烯/醋酸乙烯酯共聚物,氯乙烯/亚乙烯基氯化物共聚物,纤维素聚合物,和其混合物。上述阻挡层聚合物选择性地可以包含少量的无机颗粒例如热解法二氧化硅、二氧化硅、二氧化钛、氧化铝,氧化锆或其结合物。阻挡层进一步公开于Woo等人的美国专利6,001,522,名称为“用于光电导体元件的包含有机聚合物和二氧化硅的阻挡层”,此处引入作为参考。
是顶层的释放层可以包含,例如,任何本领域已知的释放层组分。在一些具体实例中,释放层是氟化聚合物、硅氧烷聚合物、氟硅氧烷聚合物、聚硅烷、聚乙烯、聚丙烯、聚丙烯酸酯、异丁烯酸甲酯--甲基丙烯酸共聚物、氨基甲酸乙酯树脂、氨基甲酸乙酯-环氧树脂、丙烯酸化的氨基甲酸乙酯树脂、氨基甲酸乙酯-丙烯酸树脂,或其组合物。释放层可以包含交联聚合物。
保护层保护有机光感受器以防化学和机械降解。保护层可以包含,例如,任何本领域已知的保护层组合物。在某些具体实例中,保护层是氟化聚合物、硅氧烷聚合物、氟硅酮聚合物、聚硅烷、聚乙烯、聚丙烯、聚丙烯酸酯、甲基丙烯酸甲酯--甲基丙烯酸共聚物、氨基甲酸乙酯树脂、氨基甲酸乙酯-环氧树脂、丙烯酸酯化-氨基甲酸乙酯树脂、氨基甲酸乙酯-丙烯酸树脂、或其组合物。在某些具体实例中,保护层包含交联聚合物。
通常,粘结层包含成膜的聚合物、例如聚酯、聚乙烯醇缩丁醛、聚乙烯吡咯烷酮、聚氨酯、聚甲基丙烯酸甲酯、聚(羟基氨基醚)等。外涂层进一步公开于Ackley等人的美国专利6,180,305,名称为″用于液体电子照相的有机光感受器″,此处引入作为参考。
内层可以包含,例如聚乙烯醇缩丁醛、有机硅烷、可水解的硅烷、环氧树脂、聚酯、聚酰胺、聚氨酯、硅氧烷等。在某些具体实施例中,内层干燥厚度为约20埃-约2,000埃。内层包含厚度1-25微米厚的金属氧化物导电颗粒。本领域熟练技术人员根据详述的范围将认识到本发明范围内成分的其它范围和厚度。
此处公开的有机光感受器适用于使用干燥或液体调色剂显影的成像过程,调色剂包括例如,本领域已知的固体调色剂和液体调色剂。因为液体调色剂显影提供较高分辩率图像的优点,因而是合乎需要的。合适的液体调色剂实例是本领域已知的。液体调色剂通常包含分散在载体液体中的调色剂颗粒。调色剂颗粒通常可以包含色料/颜料,树脂粘合剂、和/或电荷导向剂(director)。在液体调色剂的某些具体实例中,树脂与颜料比例从2∶1到10∶1,在另一些具体实例中从4∶1到8∶1。液体调色剂进一步公开于美国专利申请号2002/0128349,名称为″包含稳定有机溶胶的液体油墨”,2002/0086916,名称为“包含处理过的色料颗粒的液体油墨”,和2002/0197552,名称为″用于液体电子照相的相变显影剂″,此处全部引入作为参考。
甲苯胺基电荷转移材料
此处公开的有机光感受器包含具有下式的电子转移化合物:
其中R1和R2各自独立是,(N,N-双取代的)氨基芳基(例如三苯胺基)、咔唑基、或久洛尼定基,R3和R4各自独立是氢、支化或线性烷基(例如C1-C20烷基)、支化或线性不饱和烃基、环烷基(例如环己基)、或芳基(例如苯基、萘基、均二苯乙烯基、(9H-芴-9-亚基)苯甲基,或二苯乙炔基)。
具体的,合适的电荷转移材料的非限制实例在具有下列结构的甲苯胺基化合物通式内。
甲苯胺基化合物可以合成,例如,从N,N-双取代氨基苯甲醛和相应的芳族加成物。例如,可以分别从对-二乙氨基苯甲醛或对二苯氨基苯甲醛分别与N-乙基咔唑合成化合物2和3(三种物质均可从Aldrich,Milwaukee,WI.获得)。其它N,N-双取代的氨基苯甲醛也是商业上可得的。其它的芳族加合物,例如三苯基胺和久洛尼定可从Aldrich商购(Milwaukee,WI)。下面详细叙述了化合物2的合成。基于此处的详细说明,可以类似地合成其它的甲苯胺基化合物。
具有甲苯胺基化合物的有机光感量器性质
以下实施例证明,具有甲苯胺基化合物的有机光感受器在静电试验中可以具有改善的循环性能。使用如下所述的测试方法,改善的有机光感受器在4000个循环后可以具有至少约500伏的Vacc值,在另一些具体实例中至少约600伏,在另一些具体实例中至少约675伏。此外,有机光感受器在4000个周期之后可以具有至少约425伏特的对比电压(Vcan),在另一些具体实例中至少约450伏特,在另一些具体实例中至少约475伏。本领域熟练技术人员根据这些确切值将认识到本发明范围内其它的静电性能值。
有机光感受器(OPR)制备方法
通常,光导电元件可以由分散的或溶解的组分化合物而形成,例如在有机溶剂中的电荷产生化合物、电荷转移化合物、光稳定剂、电子转移化合物、和/或聚合粘结剂,在各底层上涂布分散物和/或溶液,并干燥涂层。在某些具体实例中,成分可以用高剪切均化器、球磨、研磨、高能珠粒(沙粒)碾磨或其它的磨细方法或本领域已知用于减少粒径的混合技术进行分散以形成分散剂。可以使用刮涂法、挤出、浸涂或其它适当的涂布技术(包括本领域已知的技术)施加涂层。在某些具体实例中,对多层进行依次涂布。可以在应用后一层前干燥层。某些具体的实例如下。
现在通过以下实施例进一步描述本发明。
实施例
实施例1-合成电子转移化合物
本实施例公开了两种电子转移化合物的合成。一种化合物具有甲苯胺基,上述的化合物2。第二种化合物用于制备对比有机光感受器。
化合物2的制备
将20g N-乙基咔唑(0.1摩尔,商购自Aldrich,Milwaukee,WI),7.4g对-二乙基氨基苯甲醛(0.042摩尔,商购自Aldrich,Milwaukee,WI),40ml异丙醇加入到装有回流冷凝器和机械搅拌器的100m 3-颈烧瓶。以~1毫升/2分钟的速度向溶液逐滴加入7毫升浓硫酸。在酸加完后,加入脲(5g,0.08摩尔,商购自Aldrich,Milwaukee,WI)。回流混合物4小时,冷却至室温,然后慢慢搅拌下加入到装有1500g冰水中的1%碳酸氢钠的烧瓶中。继续搅拌2小时。然后,滤出固体,重复用水洗涤直至洗涤水的pH为中性。从丙酮和甲醇的混合物中重结晶产物3次,得到11g浅蓝色固体,产率48%。发现固体熔点为152℃。在CDCl3中得到质子核磁共振谱(H-NMR)。发现峰在(ppm):1.01-1.24(t,6H);1.30-1.56(t,6H);3.19-3.42(q,4H);4.19-4.43(q,4H);6.53(s,1H);6.94-7.52(m,14H);7.75-8.05(m,4H)。
(4-正丁氧基羰基-9-亚芴基)丙二腈的制备
将460g浓硫酸(4.7摩尔,分析级,商购自Sigma-Aldrich,Milwaukee,WI)和100g-联苯甲酸(0.41摩尔,商购自Acros Fisher Scientific Company Inc.,Hanover Park,IL)加入到1-升的装有温度计、机械搅拌器和回流冷凝器的3-颈圆底烧瓶中。使用加热套,加热烧瓶到135-145℃保持12分钟,然后冷却到室温。在冷却到室温后,溶液加入到装有3升水的4-升锥形烧瓶中。机械搅拌混合物,并温和地沸腾一小时。滤出黄色热固体,用热水洗至洗涤水的pH为中性,风干过夜。该黄色固体为芴酮-4-羧酸。产量为75g(80%)。然后表征产物。熔点(m.p.)为223-224℃。用Bruker Instrument以300MHz NMR得到芴酮-4-羧酸在d6-DMSO溶剂中的1H-NMR谱。发现峰在(ppm)δ=7.39-7.50(m,2H);δ=7.79-7.70(q,2H);δ=7.74-7.85(d,1H);δ=7.88-8.00(d,1H);δ=8.18-8.30(d,1H),其中d为双重态,t为三重态,m为多重态,dd为双偶重态,q为五重态。
将70g(0.312摩尔)芴酮-4-羧酸,480g(6.5摩尔)正丁醇(商购自FisherScientific Company Inc.,Hanover Park,IL),1000ml甲苯和4ml浓硫酸加入到2-升装有机械搅拌器和具有Dean Stark设备的回流冷凝器的圆底烧瓶中。在强搅拌和回流下回流溶液5小时,期间在Dean Stark装置中收集~6g水。冷却烧瓶至室温。蒸发溶剂,并将剩余物搅拌下加入到4-升3%碳酸氢钠水溶液中。滤出固体,用水洗至洗涤水的pH为中性,并在通风橱中干燥过夜。产物为正丁基芴酮-4-羧酸酯。产量为70g(80%)。用由Bruker Instrument的300MHz NMR得到在CDCl3中的正丁基芴酮-4-羧酸酯的1H-NMR谱。峰为(ppm)δ=0.87-1.09(t,3H);δ=1.42-1.70(m,2H);δ=1.75-1.88(q,2H);δ=4.26-4.64(t,2H);δ=7.29-7.45(m,2H);δ=7.46-7.58(m,1H);δ=7.60-7.68(dd,1H);δ=7.75-7.82(dd,1H);δ=7.90-8.00(dd,1H);δ=8.25-8.35(dd,1H)。
将70g(0.25摩尔)正丁基芴酮-4-羧基酯,,750毫升无水甲醇,37g(0.55摩尔)丙二腈(商购自Sigma-Aidrich、Milwaukee,WI),20滴哌啶(商购自Sigma-Aldrich,Milwaukee,WI)加入到2-升装有机械搅拌器和回流冷凝器的3-颈圆底烧瓶中。回流溶液8小时。然后,冷却烧瓶至室温。滤出橙色粗制品,用70毫升甲醇洗涤两次,用50毫升水洗涤一次,在通风橱中干燥过夜。使用活性碳从600毫升丙酮和300毫升甲醇的混合物重结晶橙色粗制品。烧瓶置于0℃下16小时。滤出晶体并在真空炉中以50℃干燥6小时,得到60g纯(4-正丁氧基羰基-9-亚芴基)丙二腈。熔点(m.p.)为99-100℃。用由BrukerInstrurnent的300MHz NMR得到(4-正丁氧基羰基-9-亚芴基)丙二腈在CDCl3中的1H-NMR谱。峰为(ppm)δ=0.74-1.16(t,3H);δ=1.38-1.72(m,2H);δ=1.70-1.90(q,2H);δ=4.29-4.55(t 2H);δ=7.31-7.43(m,2H);δ=7.45-7.58(m,1H);δ=7.81-7.91(dd,1H);δ=8.15-8.25(dd,1H);δ=8.42-8.52(dd,1H);δ=8.56-8.66(dd,1H)。
实施例2-有机光感受器的制备
在本实施例中描述了三种有机光感受器样品和三种相应对比有机光感受器样品的制备。在下列实施例中表征样品。
样品1
样品1是单层有机光感受器,它具有含蒸气涂布的铝层(商购自CP Films,Martinsville,VA)的76.2微米(3mil)厚聚酯基底。通过预搅拌在四氢呋喃中的2.4g 20wt%化合物2的溶液,在四氢呋喃中的6.66g 25wt%的MPCT-10溶液(电荷转移材料,商购自Mitsubishi Paper Mills,Tokyo,Japan),在四氢呋喃中的7.65g 12wt%聚乙烯醇缩丁醛树脂(BX-1,商购自Sekisui ChemicalCo.Ltd.,Japan)制备单层有机光感受器的涂布溶液。然后将0.74g含19wt%氧钛基羟酞菁的CGM研磨基料和聚乙烯缩丁醛树脂(Bx-5,商购自SekisitiChemical Co Ltd,Japan)以2.3∶1的重量比加入到上述混合物中。通过在水平砂磨机(型号LMC12 DCMS,商购自Netzsch Incorporated,Exton,PA)上对112.7g氧钛基羟酞菁(商购自H.W.Sands Corp,Jupiter,FL)和49g聚乙烯醇缩丁醛树脂(BX-5)和1-微米锆珠粒,以循环模式研磨4小时制备CGM研磨基料。在机械摇动器上混合约1小时后,使用有94微米缝隙距离的刮刀涂布机在上述基底上涂布单层涂布溶液。在烘箱中以110℃干燥有涂布溶液的基底5分钟。干燥的层厚度为9微米。
样品2
按照制备样品1的方法制备样品2,除了在机械摇动器上混合约1小时后,使用有145微米的缝隙距离的刮刀涂布机在上述基底上涂布单层涂布溶液。在烘箱中以110℃干燥有涂布溶液的基底5分钟。干燥的层厚度为14微米。
样品3
按照制备样品1的方法制备样品3,除了在机械摇动器上混合约1小时后,使用有200微米的缝隙距离的刮刀涂布机在上述基底上涂布单层涂布溶液。在烘箱中以110℃干燥有涂布溶液的基底5分钟。干燥的层厚度为19微米。
对比样品A
对比样品A是单层有机光感受器,它具有含蒸气涂布的铝层(商购自CPFilms,Martinsville,VA)的76.2微米(3mil)厚聚酯基底。通过预混合在四氢呋喃中的2.4g 20wt%(4-正丁氧基羰基-9-亚芴基)丙二腈,在四氢呋喃中的6.66g 25wt%的MPCT-10(电荷转移材料,商购自Mitsubishi Paper Mills,Tokyo,Japan),在四氢呋喃中的7.65g 12wt%聚乙烯醇缩丁醛(BX-1,商购自Sekisui Chemical Co.Ltd.,Japan)制备单层有机光感受器的涂布溶液。然后将0.74g含19wt%氧钛基羟酞菁的CGM研磨基料和聚乙烯基缩丁醛(BX-5,商购自Sekisui Chejnical Co Ltd,Japan)以2.3∶1的重量比加入到上述混合物中。通过对112.7g氧钛基羟酞菁(商购自H.W.Sands Corp,Jupiter,FL)和49g聚乙烯醇缩丁醛(BX-5)在651g甲乙酮中与1微米锆珠粒在水平砂磨机(型号LMC12 DCMS,商购自Netzsch Incorporated,Exton,PA)上以循环模式研磨4小时制备CGM研磨基料。在机械摇动器上混合约1小时后,使用有94微米缝隙距离的刮刀涂布机在上述基底上涂布单层涂布溶液。在烘箱中以110℃干燥有涂布溶液的基底5分钟。干燥的层厚度为10微米。
对比样品B
按照制备对比样品A的方法制备样品B,除了在机械摇动器上混合约1小时后,使用有145微米的缝隙距离的刮刀涂布机在上述基底上涂布单层涂布溶液。在烘箱中以110℃干燥有涂布溶液的基底5分钟。干燥的层厚度为15微米。
对比样品C
按照制备对比样品A的方法制备样品C,除了在机械摇动器上混合约1小时后,使用有200微米的缝隙距离的刮刀涂布机在上述基底上涂布单层涂布溶液。在烘箱中以110℃干燥有涂布溶液的基底5分钟。干燥的层厚度为20微米。
实施例3-静电测试和有机光接受剂的性能
本实施例提供了对按照实施例2制备的有机光感受器样品的静电测试结果。
例如,使用可以测试多达三个缠绕在约160毫米直径鼓的样品条的内部设计和显影测试台测定此处公开的具有甲苯胺-基化合物的有机光感受器静电循环性能。这些样品的测试结果表明可得到具有用于支持有机光感受器的其它支撑结构例如带状、鼓状等的结果。
对于使用160毫米直径鼓状物测试,将三个每个50厘米长、8.8厘米宽的涂布样品条并排栓紧然后完全围绕铝鼓(周长50.3厘米)。在某些具体实例中,至少一个样品条是精确用丝网涂覆的对比样品,并用作内部参考点。对比样品用作对照物。在该静电循环测试仪中,鼓状物以8.13厘米/秒(3.2ips)的速度转动,测试仪中的每个测量点位置(距离和每一循环经过的时间)如下表所示:
表1
在8.13厘米/秒的160mm鼓状物周围的静电测试点
| 测试点 | 角度 | 总距离,cm | 总时间,秒 |
| 前清除杆边缘 | 0° | 起始,0cm | 起始,0s |
| 清除杆 | 0-7.2° | 0-1.0 | 0-0.12 |
| Scorotron充电器 | 113.1-135.3° | 15.8-18.9 | 1.94-2.33 |
| 激光冲击 | 161.0° | 22.5 | 2.77 |
| 探针#1 | 181.1° | 25.3 | 3.11 |
| 探针#2 | 251.2° | 35.1 | 4.32 |
| 清除杆 | 360° | 50.3 | 6.19 |
清除杆是一排720nm波长的激光发射二极管(LBD)。对有机光感受器的表面进行放电。scorotron充电器包含一条可以将所需量电荷转移至有机光感受器表面的金属线。
从上表可知,第一个静电探针(Trek 344TM静电计,Trek,Inc.Medina,NY)位于激光照射点后0.34s,和scorotron后0.78s,第二探针(Trek 344TM静电计)位于距离第一探针1.21s,距离scorotron 1.99s。全部测量在环境温度和相对湿度下进行。
根据测试台上几次运行汇编得到静电测量结果。首先三个诊断测试(最初的探针测试,最初的VlogE,最初的暗衰减))是用来评价新样品的静电周期,最后的三个相同诊断测试(最后的探针测试,最后的VIogE,最后的暗衰减)在样品循环后进行。此外,在测试期间周期性地进行测量,如同以下描述的“长期运行”。激光运行于780nm波长,600dpi,50微米光斑尺寸,60毫微秒/像素曝光时间,1,800行/秒扫描速度,100%占空系数。占空系数是像素时钟周期的曝光百分率,即以100%占空系数激光在每个像素上照满60毫微秒。
静电测试系列:
1)探针测试:通过使样品经受用于三个完整鼓旋转(激光关闭)的晕电荷(清除条总是打开)而建立电荷接受(Vacc)和放电电压(Vdis);在第四个旋转使用@780nm & 600dpi的激光放电(50um光斑尺寸,曝光60毫微秒/像素,扫描速度1,800行/秒,占空系数100%);之后三个旋转彻底地充电;在第八个旋转只用@720nm清除灯放电(电晕和激光关闭)以得到残留电压(Vres);最后的三个旋转彻底地充电(激光关闭)。对比电压(Vcon)是Vacc和Vdis间的差值,功能暗衰减(Vdd)是探针#1和#2测量的电荷接收电位差值。
2)VLOGE:该测试测量光导体对各种激光功率的光致放电,通过以固定曝光时间和恒定初始电位监测样品的放电电压作为激光功率(曝光持续时间50ns)的函数。根据该测试确定功能感光性,S780nm和操作功率设置。
3)暗衰减:该测试测量在黑暗中没有激光或清除90秒照明下随时间的可接受的电荷损失,用作指示i)将剩余空穴从电荷产生层注入到电荷转移层,ii)俘获电荷的热释放,和iii)从表面或铝接地层注入电荷。
4)长期运行:根据下列每个样品-鼓旋转序列对4,000个鼓旋转样品进行静电循环。对样品电晕充电,激光循环打开关闭(80-100°区域)对样品部分放电,最后清除灯对全部样品放电以准备下次循环。激光循环开关以致样品的第一区域从不曝光,第二区域总是曝光,第三区域从不曝光,最后的区域总是曝光。重复该方式总共4,000个鼓旋转,并周期性地对4,000个循环运行中的每第50个循环记录数据。
5)在长期运行测试后,再进行一次探针测试、VLOGE、暗衰减测试。
下表列出最初探针测试和最后探针测试的结果。给出了最初和最后循环的电荷接受电压值(Vacc,从第三个循环获得的探针#1平均电压),放电电压(Vdis,从第四个循环获得的探针#1平均电压)。
表2在4000个循环后干燥静电测验结果
| 实施例 | 最初探针测试 | 最后探针测试 | |||||||||
| Vacc | Vdis | Vcon | S780nm | 暗衰减 | Vres | Vacc | Vdis | Vcon | 暗衰减 | Vres | |
| 实施例1 | 418 | 61 | 357 | 322 | 60 | 30 | 512 | 65 | 447 | 84 | 19 |
| 实施例2 | 457 | 59 | 398 | 330 | 87 | 24 | 564 | 92 | 472 | 94 | 26 |
| 实施例3 | 522 | 90 | 432 | 210 | 96 | 29 | 685 | 193 | 492 | 63 | 67 |
| 对比实施例A | 605 | 37 | 568 | 356 | 38 | 12 | 326 | 34 | 292 | 82 | 13 |
| 对比实施例B | 716 | 32 | 684 | 424 | 34 | 10 | 319 | 30 | 289 | 127 | 8 |
| 对比实施例C | 730 | 57 | 673 | 430 | 42 | 18 | 450 | 47 | 403 | 148 | 11 |
注:数据是在样品开始循环和4,000个充电-放电循环后得到的。
在上表中,根据VLOGE诊断期间得到的数据,来计算对光感受器放电至初始电位的1/2所需要的激光功率与曝露时间和1/光斑尺寸乘积的倒数,来确定静电印刷过程的辐射敏感性(在780nm的敏感性m2/J)。
表2的结果表明相对于用对比电子转移化合物形成的有机光感受器,化合物2改善了有机光感受器的性能。具体地说,与对比样品的明显降低接受电压小相比,该有机光感受器样品显示出接受电压(Vacc)的增加。因此,虽然相对于对比例样品的放电电压较高,和对比样品相比,4000个循环后样品的对比电压(Vcon)较高。
可以理解,本领域熟练技术人员可以在本发明公开的范围和意图内作出其它的替换、改变取代基,使用替代的合成方法。上述具体实例中是用来例举说明的,而不是用来限定。其它的具体实例在权利要求范围之内。尽管本发明已经参考特定具体实例作出说明,本领域熟练技术人员将认识到在不脱离本发明精神和范围下可以进行变化。
Claims (28)
1.一种有机光感受器,包括导电基底和在所述导电基底上的光电导元件,其中光电导层包含
(a)具有下列通式的电荷转移材料
其中R1和R2各自独立是(N,N-双取代的)氨基芳基、咔唑基、或久洛尼定基,R3和R4各自独立是氢、支化或线性烷基、支化或线性不饱和烃基、环烷基或芳基;和
(b)电荷产生化合物。
2.权利要求1的有机光感受器,其中,所述光电导层进一步包含粘结剂。
3.权利要求1的有机光感受器,其中,所述电荷转移化合物具有下列通式
其中R3、R4、R5、R6、各自独立是氢、支化或线性烷基、支化或线性不饱和烃基、环烷基、或芳基。
4.权利要求1的有机光感受器,进一步包括在所述光电导元件上的外涂层。
5.权利要求1的有机光感受器,其中,所述光电导元件进一步包括紫外线稳定剂。
6.权利要求1的有机光感受器,其中,所述电荷产生化合物和所述电荷转移材料是在所述光电导元件的同一层。
7.权利要求1的有机光感受器,其中,所述光电导元件包括第一层和第二层,所述第一层包含所述电荷产生化合物,所述第二层包含所述电荷转移化合物。
8.权利要求1的有机光感受器,进一步包括电荷转移化合物,其中,所述电荷产生化合物、所述电荷转移材料和所述电荷转移化合物在所述光电导元件的同一层。
9.权利要求1的有机光感受器,进一步包括电荷转移化合物,其中,所述光电导元件包括第一层和第二层,所述第一层包含所述电荷产生化合物和所述电荷转移化合物,所述第二层包含所述电荷电荷转移材料。
10.权利要求1的有机光感受器,进一步包括电荷转移化合物,其中,所述光电导元件包括第一层第二层和第三层,所述第一层包含所述电荷产生化合物,所述第二层包含所述电荷转移化合物,所述第三层包含所述电荷转移材料。
11.权利要求1的有机光感受器,其中,R1和R2是咔唑基。
12.权利要求1的有机光感受器,其中,(N,N-双取代的)氨基苯基是三苯基胺基。
13.权利要求1的有机光感受器,其对比电压(Vcon)在4000个测试循环后至少约425伏特。
15.权利要求14的电子照相成像装置,其中,所述电荷转移材料具有下列通式
其中R3、R4、R5、R6、各自独立是氢、支化或线性烷基、支化或线性不饱和烃基、环烷基、或芳基。
16.权利要求14的电子照相成像装置,还包括在所述光电导元件上的外涂层。
17.权利要求14的电子照相成像装置,其中,所述光电导元件进一步包括紫外线稳定剂。
18.权利要求14的电子照相成像装置,其中,所述光电导元件进一步包括电荷转移化合物。
19.一种电子照相成像方法,包括:
a)在包括导电基底和在所述导电基底上的光电导元件的有机光感受器表面施加电荷,其中所述光电导元件包括
(i)具有下列通式的电荷转移材料
其中R1和R2各自独立是咔唑基、(N,N-双取代的)氨基芳基、或久洛尼定基,R3和R4各自独立是氢、支化或线性烷基、支化或线性不饱和烃基、环烷基或芳基;和
(ii)电荷产生化合物;
(b)成像地曝光所述有机光感受器的所述表面以辐射释放选择区域的电荷,从而在所述表面形成充电和未充电的图案;
(c)使所述表面和调色剂接触以形成调色图像;和
(d)转移所述调色图像至基底。
20.权利要求19的电子照相成像方法,其中,所述调色剂包括液体调色剂,液体调色剂包括在有机液体中分散的色料颗粒。
22.权利要求19的电子照相成像方法,进一步包括在所述光电导元件上的外涂层。
23.权利要求19的电子照相成像方法,其中,光电导元件进一步包括光稳定剂。
24.权利要求19的电子照相成像方法,其中,所述光电导层包括电荷转移化合物。
25.一种具有下列通式的电荷转移材料
其中R1和R2各自独立是咔唑基、(N,N-双取代的)氨基芳基、或久洛尼定基,R3和R4各自独立是氢、支化或线性烷基、支化或线性不饱烃基、环烷基或芳基。
26.权利要求25的电荷转移材料,其中所述电荷转移材料具有下列通式:
其中R3、R4、R5、R6、各自独立物是氢、支化或线性烷基、支化或线性不饱和烃基、环烷基、或芳基。
27.权利要求25的电荷转移材料,其中,R1和R2是咔唑基。
28.权利要求25的电荷转移材料,其中,所述(N,N-双取代的)氨基苯基是三苯基胺基。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US41482202P | 2002-09-30 | 2002-09-30 | |
| US60/414,822 | 2002-09-30 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN1497360A true CN1497360A (zh) | 2004-05-19 |
Family
ID=31994273
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNA031248772A Pending CN1497360A (zh) | 2002-09-30 | 2003-09-29 | 具有含甲苯胺基团化合物的有机光感受器 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20040063012A1 (zh) |
| EP (1) | EP1406127A3 (zh) |
| JP (1) | JP2004126583A (zh) |
| KR (1) | KR100522612B1 (zh) |
| CN (1) | CN1497360A (zh) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US7867675B2 (en) * | 2007-12-20 | 2011-01-11 | Xerox Corporation | Nitrogen heterocyclics in photoconductor charge transport layer |
| US7989127B2 (en) * | 2008-04-30 | 2011-08-02 | Xerox Corporation | Carbazole containing charge transport layer photoconductors |
Family Cites Families (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4202820A (en) * | 1976-10-26 | 1980-05-13 | Ciba-Geigy Corporation | Pressure-sensitive or heat-sensitive recording material containing a carbazolyl methane compound |
| LU76074A1 (zh) * | 1976-10-26 | 1978-05-16 | ||
| US4304829A (en) * | 1977-09-22 | 1981-12-08 | Xerox Corporation | Imaging system with amino substituted phenyl methane charge transport layer |
| US4369326A (en) * | 1978-04-24 | 1983-01-18 | Ciba-Geigy Corporation | Carbazolylmethane compounds |
| CH633533A5 (de) * | 1978-04-24 | 1982-12-15 | Ciba Geigy Ag | Carbazolylmethanverbindungen, ihre herstellung und verwendung als farbbildner in druckempfindlichen oder waermeempfindlichen aufzeichnungsmaterialien. |
| US4403791A (en) * | 1981-08-06 | 1983-09-13 | Sterling Drug Inc. | Carbonless duplicating and marking systems |
| US4402791A (en) * | 1981-08-10 | 1983-09-06 | Brewer John C | Apparatus for pyrolyzing shredded tires |
| DE3582576D1 (de) * | 1985-01-03 | 1991-05-23 | Ciba Geigy Ag | Dithioketo-pyrrolo-pyrrole, verfahren zu deren herstellung und verwendung. |
| DE69027697T2 (de) * | 1989-03-31 | 1997-01-23 | Toshiba Kawasaki Kk | Organische elektrolumineszente Vorrichtung |
| JPH03262170A (ja) * | 1990-03-13 | 1991-11-21 | Toshiba Corp | 有機/無機接合型半導体素子 |
| US5093698A (en) * | 1991-02-12 | 1992-03-03 | Kabushiki Kaisha Toshiba | Organic electroluminescent device |
| US6361913B1 (en) * | 1993-12-21 | 2002-03-26 | Xerox Corporation | Long life photoreceptor |
| US6004708A (en) * | 1999-04-15 | 1999-12-21 | Lexmark International, Inc. | Electrophotographic photoconductor containing fluorenyl-azine derivatives as charge transport additives |
| KR100457510B1 (ko) * | 2000-10-23 | 2004-11-17 | 삼성전자주식회사 | 전하 수송 화합물, 이를 포함하는 전자사진 유기 감광체 및 전자사진 화상 형성장치 및 방법 |
| EP1291723B1 (en) * | 2001-09-06 | 2011-03-16 | Ricoh Company, Ltd. | Electrophotographic photoreceptor, and image forming method, image forming apparatus and process cartridge therefor using the photoreceptor |
-
2003
- 2003-06-09 US US10/457,756 patent/US20040063012A1/en not_active Abandoned
- 2003-09-04 KR KR10-2003-0061703A patent/KR100522612B1/ko not_active IP Right Cessation
- 2003-09-23 EP EP03255986A patent/EP1406127A3/en not_active Withdrawn
- 2003-09-29 CN CNA031248772A patent/CN1497360A/zh active Pending
- 2003-09-30 JP JP2003340718A patent/JP2004126583A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| KR100522612B1 (ko) | 2005-10-19 |
| EP1406127A3 (en) | 2005-02-02 |
| EP1406127A2 (en) | 2004-04-07 |
| KR20040028508A (ko) | 2004-04-03 |
| US20040063012A1 (en) | 2004-04-01 |
| JP2004126583A (ja) | 2004-04-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1287227C (zh) | 具有电荷转移物质的电照相有机感光体 | |
| CN1276308C (zh) | 具有电荷转移化合物的电子照相有机感光体 | |
| CN100435028C (zh) | 含带环氧基的电荷转移化合物的有机感光体 | |
| CN1598700A (zh) | 具有环氧改性的含吖嗪基电荷传输化合物的有机光接受器 | |
| KR100510135B1 (ko) | 전자 수송층을 가진 유기감광체 | |
| CN1484101A (zh) | 具有光稳定剂的有机光感受器 | |
| CN1550916A (zh) | 具有氨基取代的腙基团和环氧基团的电荷转移材料的有机感光器 | |
| KR100522609B1 (ko) | 복수개의 광도전층을 포함하는 유기 감광체 | |
| CN100356271C (zh) | 具有带芴酮吖嗪基团的电荷传输材料的有机光接受器 | |
| CN100394308C (zh) | 具有双(9-芴酮)吖嗪基团的电荷传输材料的有机光接受器 | |
| CN1519655A (zh) | 用于电子照相的具有含盐外涂层的感光体 | |
| CN1497360A (zh) | 具有含甲苯胺基团化合物的有机光感受器 | |
| CN1609719A (zh) | 具有带两个n,n,n-三取代氨基的电荷传输材料的有机光接受器 | |
| JP2001265033A (ja) | 電子写真感光体、並びにそれを用いたプロセスカートリッジおよび電子写真装置 | |
| CN100401194C (zh) | 电子照相的有机感光体、成像装置、成像方法和电荷迁移化合物 | |
| CN1598698A (zh) | 具有吖嗪基电荷传输化合物的有机光接受器 | |
| CN1573577A (zh) | 具有吖嗪类化合物的有机光感受器 | |
| CN100394307C (zh) | 吖嗪基电荷转移材料 | |
| CN1637625A (zh) | 含有具有两个环氧化腙基的电荷传输材料的有机感光体 | |
| CN1573599A (zh) | 含有芳香杂环腙基团的新型电荷转移材料 | |
| KR100514754B1 (ko) | 플루오란계 화합물을 갖는 유기감광체 | |
| CN100401195C (zh) | 具有电子传输化合物盐的电子照相用受光体 | |
| CN1603963A (zh) | 具有带两个吖嗪基团的电荷传输材料的有机光接受器 | |
| CN1677250A (zh) | 聚(吖嗪)类电荷传输材料 | |
| CN1641489A (zh) | 含有具有两个环氧化咔唑基的电荷传输材料的有机感光体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C02 | Deemed withdrawal of patent application after publication (patent law 2001) | ||
| WD01 | Invention patent application deemed withdrawn after publication |