CN1392902A - 由氯化物促进氧化加压浸提回收硫化浮选精矿中的镍及钴 - Google Patents
由氯化物促进氧化加压浸提回收硫化浮选精矿中的镍及钴 Download PDFInfo
- Publication number
- CN1392902A CN1392902A CN01802786A CN01802786A CN1392902A CN 1392902 A CN1392902 A CN 1392902A CN 01802786 A CN01802786 A CN 01802786A CN 01802786 A CN01802786 A CN 01802786A CN 1392902 A CN1392902 A CN 1392902A
- Authority
- CN
- China
- Prior art keywords
- nickel
- leach
- cobalt
- copper
- solution
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C22—METALLURGY; FERROUS OR NON-FERROUS ALLOYS; TREATMENT OF ALLOYS OR NON-FERROUS METALS
- C22B—PRODUCTION AND REFINING OF METALS; PRETREATMENT OF RAW MATERIALS
- C22B23/00—Obtaining nickel or cobalt
- C22B23/04—Obtaining nickel or cobalt by wet processes
- C22B23/0453—Treatment or purification of solutions, e.g. obtained by leaching
- C22B23/0461—Treatment or purification of solutions, e.g. obtained by leaching by chemical methods
-
- C—CHEMISTRY; METALLURGY
- C22—METALLURGY; FERROUS OR NON-FERROUS ALLOYS; TREATMENT OF ALLOYS OR NON-FERROUS METALS
- C22B—PRODUCTION AND REFINING OF METALS; PRETREATMENT OF RAW MATERIALS
- C22B23/00—Obtaining nickel or cobalt
- C22B23/04—Obtaining nickel or cobalt by wet processes
- C22B23/0407—Leaching processes
- C22B23/0415—Leaching processes with acids or salt solutions except ammonium salts solutions
- C22B23/0423—Halogenated acids or salts thereof
-
- C—CHEMISTRY; METALLURGY
- C22—METALLURGY; FERROUS OR NON-FERROUS ALLOYS; TREATMENT OF ALLOYS OR NON-FERROUS METALS
- C22B—PRODUCTION AND REFINING OF METALS; PRETREATMENT OF RAW MATERIALS
- C22B23/00—Obtaining nickel or cobalt
- C22B23/04—Obtaining nickel or cobalt by wet processes
- C22B23/0407—Leaching processes
- C22B23/0415—Leaching processes with acids or salt solutions except ammonium salts solutions
- C22B23/043—Sulfurated acids or salts thereof
-
- C—CHEMISTRY; METALLURGY
- C22—METALLURGY; FERROUS OR NON-FERROUS ALLOYS; TREATMENT OF ALLOYS OR NON-FERROUS METALS
- C22B—PRODUCTION AND REFINING OF METALS; PRETREATMENT OF RAW MATERIALS
- C22B3/00—Extraction of metal compounds from ores or concentrates by wet processes
- C22B3/04—Extraction of metal compounds from ores or concentrates by wet processes by leaching
- C22B3/06—Extraction of metal compounds from ores or concentrates by wet processes by leaching in inorganic acid solutions, e.g. with acids generated in situ; in inorganic salt solutions other than ammonium salt solutions
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P10/00—Technologies related to metal processing
- Y02P10/20—Recycling
Landscapes
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Materials Engineering (AREA)
- Mechanical Engineering (AREA)
- Metallurgy (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Inorganic Chemistry (AREA)
- Environmental & Geological Engineering (AREA)
- General Life Sciences & Earth Sciences (AREA)
- Geochemistry & Mineralogy (AREA)
- Geology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Manufacture And Refinement Of Metals (AREA)
- Electrolytic Production Of Metals (AREA)
- Extraction Or Liquid Replacement (AREA)
- Inorganic Compounds Of Heavy Metals (AREA)
Abstract
本发明提供一种从硫化物浮选精矿中回收镍及钴的方法。本方法涉及在硫酸溶液中形成一种浮选精矿浆液,然后在常压下对此浆化浮选精矿进行氯浸提,接着在升温及酸性条件下对其进行氧化加压浸提。经液体-固粒分离、提纯及脱钴之后,通过电解提取直接处理该含镍溶液,从其中回收阴极镍。
Description
发明领域
本发明涉及一种湿法冶金分离,萃取及回收硫化物浮选精矿中有用镍及钴的方法。更具体地说,本方法涉及在酸性条件下进行常压氯浸提,接着进行氧化高压酸浸提,和通过电解提取步骤回收镍。
发明背景
长期以来,为了回收硫化物浮选精矿中的基底金属,冶金工作者一直在寻求研发经济可行的湿法冶金方法,作为替代常规熔炼及精炼的方法。由于对环境排放物控制更为严格,熔炉修建及操作都变得越来越昂贵。过去五十年所研究的许多方法都在空气或氧气氛下在高压反应釜中利用对硫化物浮选精矿的一种水浆液进行浸提,实现对该提浓物铁、硫及矸石组分中的有用金属初步分离。但这些方法几乎均未工业成功。
1950年代初期,加拿大Sherribt Gordon矿山有限公司,在含氨的硫酸铵溶液中在95℃及空气气氛下对基于加压浸提镍-铜硫化物浮选精矿的湿法冶金方法进行了工业化(J.R.Boldt,Jr.and P.E.Queneau,
The Winning of Nickel,Longmans Canada Limited,Toronto,1967,pp 299-314),并成功运行了四十年。由于能耗较高,必需对副产物硫酸铵肥料找寻市场,这种方法并没被其它镍厂家广泛采纳,因为它特别适合于Sherritt Gordon装置的一般位置和可提供的原料。
自1981年,对硫化锌浮选精矿处理的硫酸基加压浸提方法工业运行取得成功,接着被几家锌厂家采纳,替代了常规煅烧技术。这种方法于150℃下在硫酸溶液中对硫化锌浮选精矿进行氧化加压浸提,产生一种硫酸锌的溶液和一种由元素硫和氧化铁组成的残渣。对硫酸锌溶液进行提纯,脱除微量杂质金属,并用长期确立的电解提取方法从提纯后的浸提溶液中回收金属锌。在加压浸提中,该提浓物中通常不足10%的硫化物被氧化为硫酸盐,其余的则作为固态元素硫加以回收,销售或存储。这种方法中硫的形态大大优于老的煅烧方法,老方法中硫全被转化为硫酸,硫酸必须经常亏本销售,或将其转化为固体废物诸如石膏填埋处理。
已经做过许多尝试,以图使这种氧化加压酸浸提技术延伸至直接处理铜和镍-铜硫化物浮选精矿,但迄今这种方法仍未工业化成功。采用在硫熔点以上的温度下氧化加压浸提方法,来处理含黄铜矿浮选精矿的主要障碍在于,熔融硫有覆盖金属硫化物颗粒表面的趋势。这样就抑制并阻碍了金属硫化物与酸溶液的反应。因此,于温度120℃下在硫酸中对铜提浓物的氧化加压浸提一般都导致反应速率慢和金属萃取率低的结果。硫化锌与镍的颗粒对熔融硫亲合力低于硫化铜对熔融硫的亲合力,而且如上所述的锌氧化加压浸提成功方法利用有机添加剂如木素磺化盐类或白坚木,来防止浸提过程中对硫化物颗粒的覆盖。这些添加剂对硫化铜提浓物无效,但最近发现(参见USP 5,730,776,Collins等人的专利),添加劣质煤可阻止在150℃下于硫酸溶液中进行氧化加压浸提中对硫化锌及硫化铜二者的覆盖。
USP 4,039,406中(Stanley)中描述了一种不同的解决熔融硫阻塞硫化物颗粒表面问题的方法。此专利披露在高于120℃温度的硫酸溶液中对黄铜矿提浓物氧化加压浸提的浸提溶液中添加低浓度的氯离子。添加氯化物的好处表明可大大提高黄铜矿的浸提速率和显著减少硫化物氧化为硫酸盐的数量,其结果回收了实际上所有固体残渣中赤铁矿提浓物的铁含量。于150℃下在硫酸中对黄铜矿的氧化加压浸提,在不添加氯离子时一般产生的浸提溶液含酸及溶解铁浓度高。而添加氯化物时,其浸提液一般pH值2.5-3,铁浓度在1克/升以下。硫氧化深度低的另一后果,以及含氯化物浸提溶液中所造成的低酸度,可使大部分浸提铜被再沉淀为碱性硫酸铜。这种作用的大小可通过调节浸提中添加的酸量而加以改变。这种可对溶液与浸提残渣间铜的形态进行控制的性能,为设计铜回收方法提供了相当大的灵活性。
后来在Subramanian等人标题为“Oxygen pressure Leaching ofFe-Ni-Cu sulfide Concentrates at 110℃-Effect of Low ChlorideAddition”(“110℃下氧压浸提铁-镍-铜硫化物提浓物---氯化物低添加量的影响”)的论文中,对在加压浸提含镍硫化物浮选精矿的硫酸盐溶液中添加氯离于的氧化加压浸提的实用性进行了描述(见(Hydrometallurgy 2,(1976)pp.117-125))。
近年来,D.L.Jones在USP 5,431,788、5,645,708、5,650,057、5,855,858、5,874,055及5,902,474中,披露了使以氯化物促进的硫酸氧化加压浸提硫化铜提浓物与各种基于常规溶剂萃取及电解提取的工艺流程回收铜的方法结合一起使用。
Jones在USP 5,650,057中描述了一种萃取矿石或提浓物中的铜的湿法冶金方法。这种方法广义地包括在含卤离子和硫酸氢根或硫酸根离子源的酸性溶液中对矿石或提浓物进行氧化加压浸提。这种方法延伸至萃取无亚铜的金属如锌、镍和钴。显然,在氧化加压浸提过程中,金属可被沉淀为不溶性碱式盐,诸如碱式硫酸铜,或后来又基本完全被增溶并沉淀为碱式铜盐。在也由Jones发布的USP 5,855,858中更详细地描述了这种方法对含镍-钴硫化物提浓物的具体应用。
在USP 5,855,858的图1中说明的方法对本发明是有兴趣的。这种方法涉及对铜-镍浮选精矿进行氧化加压浸提。在分离浸提溶液与浸提残渣后,将浸提溶液送至溶剂萃取铜流程中。然后将来自铜萃取步骤的萃取液送至利用石灰的常规氢氧化镍沉淀步骤。在进行液/固分离后,对基本含全部有用镍及钴的残渣进行含氨浸提,并将其中的浸提溶液先送至一种溶剂萃取流程中脱除钴。最后,将来自钴萃取步骤的萃取液送至进行镍的溶剂萃取和电解提取,从而产出阴极镍。
应当注意的是,在回收矿石或提浓物中的镍的过程中,包括在该方法中的氯化物促进的氧化加压浸提,迄今仍有必要对无铜含镍的浸提物流进行溶剂萃取处理步骤,以便产生一种高浓度的提纯硫酸镍溶液,适于从其中电解提取回收有用镍。
在七十年代Gerlach等人(“Activation and Leaching ofChalcopyrite Concentrates in Dilute Sulfuric Acid” (“在稀硫硫酸中对黄铜矿提浓物的活化和浸提”),
International Symposium on Hydrometallurgy(湿法冶金国际讨论会),1973,pp.401-416)和Pawlek(“The Influence of Grain Size and MineralogicalComposition on the Leachability of Copper Concentrates”(“粒度和矿物成分对铜提浓物的可浸提性的影响”),
International Symposium on Cooper Extraction and Refining(铜萃取和精炼国际讨论会),1976,pp,690-705)首先确定了在氧化加压浸提前使基底金属硫化物浮选精矿研磨得很细的好处。在那时,由于已有研磨技术能耗高,将浮选精矿细研磨至粒度约30微米以下被认为是不经济的。过去了三十年,精细研磨技术出现了明显进步,现在可工业提供各种研磨机,可使基底金属浮选精矿的粒度减小至20微米以下,而不过度消耗能量。最近提出了许多湿法冶金的方法,都依赖于金属溶解步骤之前的精细研磨,以达到高的金属萃取率,而浸提条件比对常规粒径的浮选精矿所需的条件更温和得多。这类方法的实例描述于USP5,232,491(Corrans等人)和5,917,116(Johnson等发布)中。专利USP 5,232,491提出了一种活化矿物物种的方法,采用在氧化湿法冶金处理之前对其进行精细或超细研磨的方法。专利USP 5,917,116提出了一种采用初期研磨矿物至粒径2-20微米范围的处理铜矿物的方法。然后,在氯离子存在下及在低于元素硫熔点的温度下对该矿物进行氧化加压浸提。
不利地是,不管利用混合氯化物-硫酸盐溶液进行氧化加压浸提方法的优点如何,上述系列参考美国专利中由Jones提出的处理含镍矿石或提浓物的工艺流程都比较复杂,而且许多分离步骤的效率低。他们还在寻求工业认可。因此,仍然需要一种硫化镍浮选精矿的处理方法,它兼有在混合氯化物硫酸盐溶液中氧化加压浸提的优点,并使溶液净化和金属回收方法更简单和更直接。
发明综述
本发明的一个主要目的在于提供一种从硫化物浮选精矿中回收有用镍及钴的新湿法冶金方法,该方法包括常压的酸氯浸提(acidchlorine leach),接着氧化加压浸提,而且其中可将由其所得提纯镍浸提溶液直接送至电解提取流程中,产生阴极镍。此外,重要的要求在于,使有用金属溶解迅速而且元素硫的回收率高。
本发明的第二个目的在于提供一种来自常压酸氯浸提的可用于氧化加压浸提的含氯化物进料液,从而达到如上所述的主要目的。
本发明的另一目的还在于,利用电解提取镍步骤中产生的氯作为硫化物浮选精矿浸提中的一种氧化剂。
此外,本发明的目的还在于提供一种工序最少且试剂费用最低的方法。
最后,与采用可能工业可行的所有湿法冶金方法一样,人们总要追求有用金属回收率最大和投资与操作费用最少。
按照本发明,这里提供一种从含镍-钴-铜硫化物浮选精矿中萃取,分离和回收镍、钴和铜的方法。该方法包括制备含硫化物浮选精矿的浆液和使所述浆液与在常压酸性浸提阶段含氧及氯的气流进行接触的步骤,从而产生一种其中含预定浓度氯离子的加压浸提进料浆液。然后,在酸性及高温条件下对此加压浸提进料浆液进行氧化加压浸提,从中选择性地浸提出大部分镍、钴和铜,形成一种含镍-钴-铜的浸提溶液和浸取残渣。对从中分离浸取残渣之后的含镍-钴-铜的浸提溶液进行处理,分别回收铜和钴,并脱除杂质,从而形成一种提纯后的镍浸提溶液。然后电解提取出所述提纯后的镍浸提溶液中的镍,由此产生阴极镍及氧、氯及硫酸。优选在常压酰基氯浸提(acidchloride leach)之前将硫化物浮选精矿研磨得很细,最优选研磨至粒度约10-30微米的范围。加压浸提进料浆液中优选氯化物浓度范围应在约2-40克/升之间。
在本发明一组优选实施方案中,广义提供一种用于从含镍-钴-铜硫化物浮选精矿中萃取,分离及回收有用镍、钴及铜的方法,包括制备一种含浮选精矿的浆液和使所述浆液与常压酸性浸提中的含氧及氯的气流进行接触,从而产生一种其中含预定浓度氯离子的加压浸提的进料浆液。对此加压浸提进料浆液在酸性条件及高温下进行氧化加压浸提,从中选择性地浸提出大部分镍、钴和铜,形成含镍-钴-铜的浸提溶液和浸取残渣。随后将此含镍-钴-铜的浸提溶液与所述浸取残渣分离。从所述含镍及钴的浸提溶液中脱除所含的铜,并对此脱铜后的含镍及钴的浸提溶液进行中和,并脱除其中的铁。使此含镍及钴的浸提溶液经历提纯步骤,由此脱除含镍-钴的浸提溶液中的杂质,一般为钙、锌及铅。利用溶剂萃取过程脱除所述含镍钴的浸提溶液中的钴,并通过电解提取方法从所述提纯后的含镍溶液中提取镍。此外,精细研磨后的硫化物浮选精矿的优选粒度应是如上所述的那样,应当达到在加压浸提料液中的氯离子的浓度。
本发明还延伸至一种由含镍-钴-铜硫化物浮选精矿制备加压浸提进料浆液的方法,包括步骤:精细研磨所述浮选精矿达到预定的粒度;制备含所述精细研磨的浮选精矿酸性溶液的浆液,并使所述浆液与含氧及氯的气流接触,从而产生-种其中含预定浓度的氯离子的加压浸提的进料浆液。
另外,本发明考虑了将电解提取提镍步骤产生的氧/氯形成合并气流再循环至常压酸氯浸提中。此外,使含硫酸的镍阳极液流再循环至常压酸氯浸提步骤中会特别有利。
在氧化加压浸提之前先对硫化物浮选精矿进行常压酸氯浸提,对提高硫化矿物氧化速率并由此显著降低氧化加压浸提方法所需反应釜的尺寸及费用有利。
有利地是,由于实施本发明方法,有可能直接电解提取来自氧化加压浸提的含氯化物高浓度硫酸镍提纯浸提液中的镍,从而产生镍并因此不必进行镍改质及提纯步骤而涉及中间物沉淀、再溶解及溶剂萃取。此外,由于实施了从含氯化物硫酸镍溶液中电解提取镍,和与再循环阳极产生的气流至常压浸提的结合,回收氯可采用溶解氯离子的理想方式,而免除了通过回收气流与氢气反应再产生盐酸的必要性。
本发明方法的基本要求是,对硫化物浮选精矿的常压酸氯浸提必须在氧化加压浸提之前进行。
在这种工艺相对不复杂,涉及步骤比已有技术更少,工业上可行的方法中,镍回收率得以提高,氧化加压浸提中的反应时间也大大缩短。
同样不想受约束,据认为在氯作为氧化剂的存在下,在进行氧化加压浸提之前新加常压酸浸的步骤有助于达到如上所述目的。
其另一优点是,规定在常压酸氯浸提步骤之前对硫化物浮选精矿进行精细研磨的步骤,促进了金属回收率的提高。
附图简要说明
图1是本发明的一般化示意流程图。
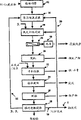
图2是图1方法实施方案的一种示意流程图。
图3是表明间歇氧化加压浸提试验中氧消耗速率的对照图,试验是针对按照本发明方法制得的常压酸氯浸取残渣和针对按照已有技术直接氧化加压浸提处理镍-铜-钴硫化物浮选精矿完成的。
本发明优选实施方案
以数字10表示的图1描述了本方法的流程,图2描述了这种方法的实施方案。现参看图2,本方法包括在步骤12对含镍-铜-钴硫化物浮选精矿进行精细研磨,接着进行常压酸氯浸提14。常压酸氯浸提的残渣在含酸性氯化物溶液中的浆液,此后简称加压浸提进料浆液,被送至氧化加压浸提步骤15。经液/固分离步骤后,含镍-钴-铜的氧化加压浸提溶液被送至脱铜步骤20。脱除铜后,含镍-钴的浸提溶液经合并中和及经历除铁步骤22,然后进行溶液提纯步骤24。在步骤26经分离溶液中的钴之后,镍在电解提取法提镍步骤28中被从所述提纯镍硫酸盐-氯化物浸提溶液中电解提取出来,产生阴极镍,并生成硫酸及释放出氧气及氯气。在精细研磨步骤12中,将一种其粒度d80 40-80微米一般含5-25%Ni、1-10%Cu及0.2-1.0%Co的镍-钴-铜硫化物浮选精矿的水成浆液注入一立式球磨中,使其粒度d80减小至10-30微米范围。将此经过精细研磨的硫化物浮选精矿的浆液与来自电解提取法提镍步骤28的再循环镍阳极液30相混合,它一般含45-55克/升Ni及10-50克/升H2SO4,和在常压酸氯浸提步骤14中进行浸提,用氯与氧的混合物对其进行鼓泡,也通过电解提取法提镍步骤28再循环。这种浸提通过一系列两个或更多个串联排列的搅拌反应槽完成,其反应温度约40-90℃,保留时间至少30分钟。氯、氧及酸与含镍矿物、磁黄铁矿及镍黄铁矿反应按照以下反应式进行:
一般,常压酸氯浸提14之后,在所述浸提溶液中氯化物浓度在约2-40克/升范围,最优选在约2-20克/升范围。
在一系列数值前的术语“约”均应当理解为用于系列中的各数值,除非另有陈述。
氯与硫化矿物间的反应快速而完全,所以基本上所有在电解提取法提镍步骤28中的阳极产生的氯气都被回收及转化为常压酸氯浸提产物溶液中,即加压浸提进料浆液中的氯化物。因此,常压浸提槽排放气体中无氯。氧及硫酸与硫化矿物的反应较慢,在常压酸浸提条件下利用氧比较少,所以可能提供附加空气或氧有利,以使硫酸与硫化矿物的反应达到最大。据观察发现,氯与酸二者对磁黄铁矿的选择性攻击都超过对镍黄铁矿的,以致对铁萃取百分比一般比对镍的萃取率高。一般,该提浓物中最多15%含量的铁及5-10%含量的镍被溶解在常压酸氯浸提中。因此,常压酸氯浸提的主要可溶性产物是氯化亚铁和较少量的氯化镍。但更重要地是,在常压酸氯浸提中硫化物浮选精矿有15-20%的硫化物料反应形成了元素硫或硫酸盐。
通过常压酸氯浸提先处理镍-钴-铜硫化物浮选精矿的氧化加压浸提操作产生了二个明显的好处。令人惊讶地是,现已发现,凡先在常压酸氯浸提步骤中对硫化物浮选精矿进行过处理的,在氧化加压浸提中这种硫化矿的氧化速率就较快。这种有利的结果被认为是由于在常压酸氯浸提中,有很大部分的硫化物浮选精矿的铁含量被溶解,因此提高了氧化加压浸提溶液中溶解铁的浓度。众所周知,溶解的铁会促进硫化矿物在氧化加压浸提中氧的传递。一般,在氧化加压浸提中达到镍提取率93%所需要的时间缩短了约33%,如从30分钟减到20分钟,相应显著增大了反应釜的生产能力。
由于在将浆液引入氧化加压浸提反应釜之前,最多约20%的高发热硫化物氧化反应发生在常压酸浸提中,所以使必须从反应釜中移出的热量显著降低。在工业实施中,氧化加压浸提反应釜的生产能力基本上完全取决于它所能脱除反应热的速率。因此,使很大部分的氧化反应在常压酸氯浸提中完成,会使反应釜的生产能力显著提高。
将常压酸氯浸提产物的浆液,即加压浸提进料浆液,作为进料直接泵送至步骤16的氧化加压浸提反应釜中,使之在预选总酸对提浓物的比例下进行处理,一般为每公吨硫化物浮选精矿150-250千克的H2SO4,其处理温度100-150℃,氧分压0.5-1.0兆帕。达到镍及钴萃取率98%所需的停留时间一般范围从在130℃时约20-30分钟到在105℃时约1.5-3小时。在氧化加压浸提步骤中发生的主要化学反应可由以下反应式表示:
在此体系中氯离子的精确作用还未明白,但非常肯定的是,氯化物浓度达到约2克/升以上,会显著增加基底金属的溶解及硫化物氧化为元素硫的速率。同时氯离子会抑制硫化物及/或元素硫氧化为硫酸盐的反应。因此,由于使中和及需要除铁量减至最少,氧化加压浸提过程中消耗的氧量显著降低,同样随后处理氧化加压浸提溶液的费用降低。据报导,硫化物浮选精矿中通常不超过10%含量的的硫化物对氧化加压浸提溶液为溶解硫酸盐,其余部分主要为浸取残渣中的固体元素硫。
通过调节固粒对反应釜内总溶液流量的比例,使氧化加压浸提的排放溶液中镍浓度一般维持在70-80克/升的范围。这种氧化加压浸提产物的溶液一般含2~10克/升的Cu及0.5~3克/升的Co,其pH值为1.8~3.0。在这种加压浸提放溶液中溶解铁的含量取决于pH值,其范围为pH 2.5时低于0.1克/升到pH 1.8时达到~5克/升。最终pH值取决于加至浸提步骤14及16的阳极液流中硫酸量和硫化物氧化为硫酸盐的程度。这种氧化加压浸提溶液也含痕量其它金属杂质,如锌和铅,而且可以是硫酸钙饱和的。氧化加压浸提残渣主要由元素硫(20-25%)和赤铁矿(40-45%Fe)及来自硫化物浮选精矿的不溶性矸石材料组成。
反应釜排放浆液经固液分离步骤18,从高浓度含镍溶液中分离出脱金属后的固体残渣。由于氧化加压浸提溶液含镍浓度高,重要的是应充分洗涤其残渣,保证分离出废弃固粒中所有被夹带的氧化加压浸提溶液。氧化高压残渣洗涤步骤19可包括利用增稠剂的逆流倾注洗涤流程,或利用带式过滤器上的逆流洗涤完成。洗涤后,将贫瘠的氧化加压浸提残渣废弃至适宜保管体系中。任选可通过熔融硫的常规泡沫浮选和过滤方法,分离在氧化加压浸提残渣赤铁矿和矸石成分中的元素硫。只要经济上允许,就可进一步处理这种氧化加压浸提残渣,回收贵重及铂族金属。
氧化加压浸提溶液,在pH 2.0~3.0时通常含不足5克/升的Cu,经脱铜步骤20处理,用硫化物试剂沉淀硫化铜中间产物或通过常规溶剂萃取和电解提取产生铜阴极产物的方法,脱除铜。两种方法都产生硫酸,从而降低了含镍及钴溶液的pH,例如:
脱除铜步骤20后,脱铜后的镍及钴的硫酸盐-氯化物溶液一般含约10克/升的游离硫酸及约1克/升的Fe,接着在氧化条件下对其进行中和,使pH值升高至2.5-4.0的范围,通过水解作用在中和及除铁步骤22中沉淀铁。工艺步骤22通常在60-80℃温度下在一系列串联排列的搅拌槽中完成。精细粉碎的石灰石及消石灰是优选的中和剂,用空气或氧气对浆液鼓泡,氧化溶解二价铁为三价形态,使之水解沉淀为氢氧化铁及石膏:
通过过滤(未示出)分离无铁的镍硫酸盐-氯化物溶液中的沉淀硫酸钙及氢氧化铁,并用水充分洗涤固粒,回收夹带的含镍溶液,然后将固粒摈弃至保管体系中。
在中和及脱铁步骤22后,部分提纯后的高浓度镍-钴溶液仍然含杂质,如锌及铅以及残余痕量的铜及铁,而且是硫酸钙饱和的。在回收溶液中纯产品钴及镍之前,必须脱除基底金属的杂质,而在进一步处理之前还需脱除至少一部分钙,因为硫酸钙可引起后序工艺中的各种问题。利用与可溶性硫化物如硫氢化钠的常规沉淀作用,可以脱除基底金属,同时利用有机磷酸溶剂萃取试剂,如二2-乙基己基磷酸(D2EHPA),可在溶液提纯步骤24中脱除基底金属及钙。两种提纯方法在提纯后的镍-钴溶液中都产生游离硫酸,在处理过程中都必须进行中和。在此步骤中2 4优选中和剂是氢氧化钠、碳酸钠或氢氧化铵,因为此刻应避免用钙试剂。D2EHPA溶剂萃取步骤,在55℃及pH 3.5~4.0下操作,可通过常规混合澄清槽或逆流萃取塔完成。使含镍及钴溶液中的钙含量从500毫克/升以上降低到100毫克/升以下,并使锌及铁定量脱除。铜及铅的含量也显著降低。通过与酸性含氯化物的水溶液如盐酸进行接触的方法,汽提该负荷金属的有机溶液,并进一步对含氯化钙洗提液进行处理,以分离及脱除所含有用金属。
提纯后的含镍及钴的溶液进至钴分离步骤26,通过溶剂萃取,例如利用Cyanex272(一种有机次膦酸萃取剂,由加拿大Cytec公司制造),选择性地脱除含镍及钴溶液中99%以上的钴。在pH值约4时钴被负荷于有机萃取剂中,经过常规洗涤该负荷的有机溶液,脱除夹带及/或共萃取的镍之后,使之与酸性洗涤水溶液进行接触,再萃取有机溶液中的钴。这个步骤优选在50~55℃下完成。对高浓度钴洗提溶液进一步地处理,回收目的产物形态的钴,如阴极金属、氧化钴、碳酸钴或钴盐。在进行到电解提取法提镍步骤28之前,对来自脱钴步骤26的含镍提余液进行常规处理,脱除任何夹带的有机溶液。这种溶液一般含约80克/升的镍及pH值约4.0。在电解提取法提镍步骤28中,来自步骤26提纯后的镍硫酸盐-氯化物溶液经电解,使金属镍沉淀在阴极上,并在阳极产生氯气、氧气及硫酸。
将提纯后的高浓度镍的硫酸盐-氯化物溶液加到常规电解提取池中,电解提取池内装有多个不溶解阳极并交替插入多个阴极,阴极可以是镍起动器薄片或由钛或不锈钢造的永久阴极基材。通过将镍电镀在镍起动器薄片上制成整板阴极,或通过电镀在部分遮盖的不锈钢基材上制成为离散片如ROUNDSTM。(ROUNDS是Inco Limited(国际镍有限公司)的商标)。这种不溶性阳极包括金属钛基材,或为网或整板,其上涂布一层或多层过渡金属氧化物的覆盖层,过渡金属氧化物优选选自钽、钌及铱的氧化物。各阳极被封闭在半透膜制成的鞘或袋子中,采用一种罩盖方法使之隔离氧及氯气及阳极液,如USP4,201,653(O′Neill等)及4,288,305(Garriteen等)专利中所述,两者均授权于Inco Limited公司。
电解提取法提镍工艺步骤28操作于电流密度200~350安培/平方米及55~60℃下。应当注意,电解提取法提镍流程的进料液中氯化物浓度始终保持在约2~20克/升范围。提纯后的镍硫酸盐-氯化物溶液一般含70~80克/升的Ni,将其加至阴极室中,使金属镍镀到阴极上,并形成氢离子。脱镍后的酸性溶液渗透穿过封闭阳极空间的薄膜,达到阳极表面,在阳极表面形成氯气及氧气。镍阳极液流30,它与氯气及氧气一起在阳极室被回收,一般含50克/升的Ni,1克/升以下的Cl及20~50克/升的H2SO4。
氯与氧气流32与部分阳极液30一起被再循环至常压酸氯浸提步骤14中。另一部分阳极液30被再循环至氧化加压浸提步骤16中。为了保持工艺中所需水及硫酸盐的平衡,要从流程中放出平衡的阳极液30和洗涤液,构成一种排放液34。用石灰石及石灰处理排放液34,中和酸并沉淀所含的镍为返回流程中(未示出)的氢氧化镍。现在参考以下非限制性实施例描述本发明的方法。
实施例I
此实施例说明,在氧化加压浸提之前,利用氯及氧的气体混合物作为氧化剂,在硫酸溶液中进行常压酸浸提含镍-铜-钴硫化物浮选精矿的好处。常压浸提试验利用再研磨(d80~24微米)的镍-铜-钴硫化物浮选精矿样品完成,再研磨样品分析结果为10.5%Ni,2.5%Cu,44%Fe及33%S。在环境温度下,对含55%固粒的硫化物浮选精矿浆液在含不同浓度硫酸的酸性水溶液中进行间歇常压浸提试验。在各试验中用一种由氯或氧或其混合物组成的气流对该硫化物浮选精矿浆液进行鼓泡,气流用量示于表1中。
表I
| 试验 | 添加率,千克/吨提浓物 | %Fe溶解 | %S2-氧化 | |||
| 氯 | 氧 | 酸 | S0 | SO4 2- | ||
| 1 | 30 | 31 | 0 | 4.1 | 16.2 | 3.1 |
| 2 | 20 | 21 | 0 | 4.9 | 9.7 | <1 |
| 3 | 20 | 0 | 74 | 9.1 | 11.1 | <1 |
| 4 | 20 | 21 | 110 | 14.3 | 12.0 | 3.4 |
| 5 | 21 | 21 | 148 | 14.3 | 11.1 | 3.1 |
这些试验数据说明,在常压酸浸提中用氯及氧气对浆液进行鼓泡时,增加酸用量对铁溶解程度、对硫化物氧化为元素硫和氧化为硫酸盐的相对程度的影响。
随后用水及/或稀硫酸溶液对试验4及5中形成的常压酸浸提浆液进行稀释,调整溶液中氯离子含量至5克/升,并调整两浸提段中总酸用量至160千克H2SO4/吨提浓物。对各氧化加压浸提(OPL)进料浆液加入少量水溶性木素磺化盐,以保证熔融硫充分分散。然后在间歇反应釜中,在150℃及700千帕氧分压下,对各浆液氧化加压浸提30分钟。在两组OPL试验中,30分钟后镍萃取率超过98%。为了比较,在相同条件即没有以前的常压酸氯气浸提,直接对同样再研磨的含镍-铜-钴硫化物浮选精矿样品进行氧化加压浸提。在这组OPL试验中30分钟后镍萃取率为97%。在所有三组试验中氧化为元素硫(S0)的硫化物量超过75%,氧化为硫酸盐的硫化物量约15%。
图3表示三组OPL试验的累积耗氧速率图。在间歇氧化加压浸提过程中,按气体质量流量计测定的氧消耗速率,提供了一种对硫化矿物氧化速率的方便和可靠的量度,它对基底金属萃取速率可给出良好显示。图3图形表明,对试验4及5的常压浸取残渣的OPL试验中,在约20分钟后,硫化物氧化反应的氧消耗基本完全。相反,在直接对含镍-铜-钴硫化物浮选精矿的OPL试验中,到30分钟才观察到明显的氧消耗速率。这些数据表明,先在常压酸氯气浸提中对硫化物浮选精矿进行处理后,使氧化加压浸提中镍萃取率达到98%的目标所需的停留时间会大大缩短。
实施例II
这个实施例说明进料颗粒粒度对含10%Ni、2.6%Cu和29%S的镍-钴-铜硫化物浮选精矿在含5克/升氯化物和35克/升H2SO4的硫酸盐-氯化物溶液中进行浸提的影响。利用立式球磨机精细研磨提浓物(d80~48微米),使其形成分别达到d80值约13和6微米的材料。在常压酸氯浸提溶液中对各硫化物浮选精矿样品进行再浆化,形成一种含250克/固粒的浆液,并使之在150℃下经受氧化加压浸提。间歇试验在约700千帕氧分压下和停留时间在20~60分钟的范围内完成。对氧化加压浸提进料浆液加入了少量水溶性的木素磺化盐,以保证熔融硫充分分散。结果示于以下表II中:
表II
| 提浓物粒度,d80微米 | 48 | 13 | 6 |
| 加压浸提时间,分 | 60 | 30 | 20 |
| 产物溶液pH值 | 2.3 | 1.8 | 1.6 |
| 萃取率% NiCu | 96 | 98 | 98 |
| 75 | 90 | 93 |
这些试验表明,超细研磨含镍-铜-钴硫化物的浮选精矿,显著地缩短了氧化加压浸提中达到镍萃取率98%目标所需要的浸提时间。较精细研磨也提高了对更难浸提的黄铜矿物中铜的萃取率。但是,氧化加压浸提残渣也因硫化物浮选精矿的粒度降低逐渐变得更难沉降和过滤。实际上,据认为最佳粒度在15-30微米的范围。
实施例III
以下实施例说明氯化物添加量及浸提温度对氧化加压浸提性能的影响。为了比较在100及150℃两个条件下氧化加压浸提的性能,对研磨得非常细的硫化物浮选精矿(d80~7微米)进行了一系列间歇加压浸提试验。镍-铜-钴硫化物浮选精矿含15%镍、2.6%钴及34%硫。采用一种合成氯化物-硫酸盐溶液(5克/升的Cu,5克/升的Cl及10-40克/升的H2SO4)在氯化物-硫酸盐溶液中进行氧化加压浸提试验。采用一种含5克/升的Cu及40克/升的H2SO4的溶液进行在无氯化物的硫酸盐溶液中的氧化加压浸提试验。将水溶性的木素磺化盐加至氧化加压浸提浆液中,在150℃下进行氧化加压浸提试验。其结果列于以下表III中。
表III
| 浸提时间,分 | 180 | 30 | |||
| 浸提温度,℃ | 100 | 150 | |||
| 氯添加量,克/升 | 0 | 5 | 0 | 5 | 11 |
| 产物溶液 pH | 1.7 | 3.2 | 1.2 | 1.9 | 2.6 |
| Fe,克/升 | 9 | <1 | 1 | <1 | <1 |
| 金属萃取率 %,NiCu | 99 | 96 | 99 | 98 | 98 |
| 78 | 75 | 70 | 85 | 60 | |
实施例IV
此实施例说明少量氯化物及多量硫酸盐的镍溶液在电解提取法提镍中的性能,试验在电流密度300安培/平方米及电池电压3.0伏特下完成。电解提取池是一种装有不锈钢阴极和双阳极的隔膜电池,双阳极由涂有钽、钌及铱氧化物的组合物的钛基材组成。进料液中含有75克/升Ni,pH 2.5及温度60℃,氯化物浓度范围在2.5~10克/升。产物阳极液的组成列于表IV中。
表IV
| 氯化物浓度,克/升 | 产物阳极液组成,克/升 | ||
| Ni | Cl | H2SO4 | |
| 2.5 | 45 | 0.2 | 47 |
| 5.0 | 47 | 0.5 | 40 |
| 10.0 | 48 | 1.2 | 33 |
在各试验中,从溶液中以氯气形式脱除约90%的氯离子,同时在阴极以金属态析出进料液中的镍约35%。随进料液中的氯化物量的增加,产物溶液中硫酸量成比例地减少。
尽管根据章程的规定,这里说明及描述了本发明的具体实施方案,但本领域技术人员会理解,可做出一些为本发明权利要求书所覆盖类型的变化,而且有时可利用本发明的某些特征而不相应利用另一些特征。
Claims (17)
1.一种从含镍-钴-铜硫化物浮选精矿中萃取、分离和回收镍、钴和铜的方法,包括:
制备一种含所述浮选精矿的浆液,并在常压酸浸提过程中使所述浆液与含氧及氯的气流进行接触,从而产生一种其中含预定浓度氯离子的加压浸提的进料浆液;
使所述加压浸提进料浆液在酸性条件及高温下经受氧化加压浸提,选择性地从中浸提大部分镍、钴和铜,形成一种含镍-钴-铜的浸提溶液和一种浸提残渣;
在分离其中浸提残渣之后,对所述含镍-钴-铜的氧化加压浸提溶液进行处理,以分别回收铜和钴,并脱除杂质,从而形成一种提纯后的含镍的氧化加压浸提溶液;及
从所述提纯后的含镍的氧化加压浸提溶液中电解提取法提镍,从而从中产生阴极镍、氯、氧及硫酸。
2.按照权利要求1的方法,其中氧化加压浸提进料浆液的氯化物浓度范围在约2~40克/升之间。
3.按照权利要求1的方法,包括在引入至所述常压酸氯浸提之前,对所述硫化物浮选精矿进行精细研磨,使之达到预定的粒度。
4.按照权利要求3的方法,其中该硫化物浮选精矿被研磨至d8010~30微米之间。
5.按照权利要求1的方法,包括将至少一部分电解提取法提镍步骤中形成的硫酸再循环至常压酸浸提过程中。
6.按照权利要求1的方法,包括将至少一部分在电解提取法提镍步骤中形成的氯气及氧气再循环至常压酸浸提过程中。
7.按照权利要求1的方法,其中在加压浸提进料浆液中氯离子的预定浓度范围在约5~10克/升之间。
8.一种从含镍-钴-铜的硫化物浮选精矿中萃取、分离和回收镍、钴和铜的方法,包括:
制备一种含所述浮选精矿的浆液,并在常压酸浸提过程中使所述浆液与含氧及氯的气流进行接触,从而产生一种其中含预定浓度氯离子的加压浸提进料浆液;
使所述加压浸提进料浆液在酸性条件及高温下经受氧化加压浸提,选择性地从中浸提大部分镍、钴和铜,以形成一种含镍、钴及铜的浸提溶液和一种浸提残渣。
分离所述含镍-钴-铜的氧化加压浸提溶液与所述氧化加压浸提残渣;
从所述含镍及钴的氧化加压浸提溶液中脱除所含的铜;中和所述脱铜后的含镍及钴的氧化加压浸提溶液,并从其中脱除铁;
提纯所述含镍及钴的氧化加压浸提溶液,从而脱除含镍及钴的氧化加压浸提溶液中的杂质;
利用溶剂萃取,脱除所述含镍钴的氧化加压浸提溶液中的钴;并
电解提取所述含镍的氧化加压浸提溶液,从而在其中形成阴极镍、氯、氧及硫酸。
9.按照权利要求8的方法,包括精细研磨所述浮选精矿至预定粒度。
10.按照权利要求9的方法,其中将所述浮选精矿研磨至粒度范围在约10~30微米之间。
11.按照权利要求8的方法,其中加压浸提进料液的氯化物浓度范围在约2~40克/升之间。
12.按照权利要求8的方法,包括将至少一部分在镍的电解提取法步骤中产生的硫酸再循环至所述常压酸浸提过程中。
13.按照权利要求8的方法,包括将所述镍的电解提取法步骤中产生的氧及氯再循环至所述常压酸浸提过程中。
14.按照权利要求8的方法,其中所述高压浸提进料浆液中氯离子的预定浓度在约5-10克/升范围之间。
15.一种由含镍-钴-铜硫化物浮选精矿制备高压浸提进料浆液的方法包括:
精细研磨所述浮选精矿至预定粒度;制备含所述精细研磨浮选精矿的浆液;并使所述浆液与含氧及氯的气流在常压酸浸提中接触,从而产生一种其中含预定浓度氯离子的高压浸提进料浆液。
16.按照权利要求15的方法,其中所述浮选精矿颗粒被精细研磨至粒度在10-30微米范围之间。
17.按照权利要求15的方法,其中所述高压浸提进料浆液中所述氯离子预定浓度在约2-40克/升范围之间。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US09/664,475 | 2000-09-18 | ||
| US09/664,475 US6428604B1 (en) | 2000-09-18 | 2000-09-18 | Hydrometallurgical process for the recovery of nickel and cobalt values from a sulfidic flotation concentrate |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN1392902A true CN1392902A (zh) | 2003-01-22 |
| CN1210417C CN1210417C (zh) | 2005-07-13 |
Family
ID=24666118
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CNB018027865A Expired - Fee Related CN1210417C (zh) | 2000-09-18 | 2001-02-26 | 从硫化物浮选精矿中回收镍、钴和铜的湿法冶金方法 |
Country Status (13)
| Country | Link |
|---|---|
| US (2) | US6428604B1 (zh) |
| EP (1) | EP1325165B1 (zh) |
| JP (1) | JP3946633B2 (zh) |
| CN (1) | CN1210417C (zh) |
| AT (1) | ATE338833T1 (zh) |
| AU (1) | AU774519B2 (zh) |
| BR (1) | BR0107217A (zh) |
| CA (1) | CA2376883C (zh) |
| DE (1) | DE60122914T2 (zh) |
| FI (1) | FI123376B (zh) |
| RU (1) | RU2221881C1 (zh) |
| WO (1) | WO2002024966A1 (zh) |
| ZA (1) | ZA200202941B (zh) |
Cited By (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN100420760C (zh) * | 2004-05-21 | 2008-09-24 | Wmc资源有限公司 | 镍的回收 |
| CN102002586A (zh) * | 2010-12-04 | 2011-04-06 | 金川集团有限公司 | 一种含镍高钴硫化物浸出技术 |
| CN101705371B (zh) * | 2009-11-20 | 2011-04-06 | 北京矿冶研究总院 | 一种硫化铜钴矿中提取钴的方法 |
| CN101760616B (zh) * | 2008-12-02 | 2011-08-10 | 中国恩菲工程技术有限公司 | 含钴矿石的浸出方法 |
| CN102206834A (zh) * | 2011-05-03 | 2011-10-05 | 四川省尼科国润新材料有限公司 | 一种用低冰镍直接生产电解镍的方法 |
| CN102344163A (zh) * | 2011-07-01 | 2012-02-08 | 王嘉兴 | 用废渣铜泥制备硫化铜,碳酸铜和氯化钠的方法 |
| CN102344118A (zh) * | 2011-07-01 | 2012-02-08 | 王嘉兴 | 用废渣铜泥制备硫化铜,氢氧化铜和氯化钠的方法 |
| CN102367176A (zh) * | 2011-07-01 | 2012-03-07 | 王嘉兴 | 用废渣铜泥制备硫化铜,磷酸铜和磷酸钠的方法 |
| CN102367179A (zh) * | 2011-07-01 | 2012-03-07 | 王嘉兴 | 用废渣铜泥制备硫化铜,氯化铜和氯化钠的方法 |
| CN102367175A (zh) * | 2011-07-01 | 2012-03-07 | 王嘉兴 | 用废渣铜泥制备硫化铜,氢氧化铜和氯化钠的方法 |
| CN102367173A (zh) * | 2011-07-01 | 2012-03-07 | 王嘉兴 | 用废渣铜泥制备硫化铜和氯化钠的方法 |
| CN101356292B (zh) * | 2005-11-10 | 2012-11-14 | 瓦利·德·利奥多斯公司 | 组合浸出方法 |
| CN103725887A (zh) * | 2013-12-13 | 2014-04-16 | 金川集团股份有限公司 | 一种浸出海绵铜的方法 |
| CN103958416A (zh) * | 2011-12-26 | 2014-07-30 | 住友金属矿山株式会社 | 硫酸钴的制造方法 |
| CN108103311A (zh) * | 2017-12-14 | 2018-06-01 | 中南大学 | 一种铜镍混合矿的湿法冶炼方法 |
| CN108118149A (zh) * | 2017-12-14 | 2018-06-05 | 中南大学 | 一种用硫化镍精矿制备动力电池正极材料前驱体的方法 |
| CN112680602A (zh) * | 2020-12-18 | 2021-04-20 | 衢州华友钴新材料有限公司 | 一种提升含铜硫化矿浸出效率的处理方法 |
| CN113957264A (zh) * | 2021-09-13 | 2022-01-21 | 广东邦普循环科技有限公司 | 一种由低冰镍制备硫酸镍的方法 |
Families Citing this family (43)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AP1752A (en) * | 2000-07-25 | 2007-07-12 | Freeport Mcmoran Corp | Method for recovery of copper from sulfidic ore materials using super-fine grinding and medium temperature pressure leaching |
| US6428604B1 (en) * | 2000-09-18 | 2002-08-06 | Inco Limited | Hydrometallurgical process for the recovery of nickel and cobalt values from a sulfidic flotation concentrate |
| US20050126923A1 (en) * | 2001-07-25 | 2005-06-16 | Phelps Dodge Corporation | Process for recovery of copper from copper-bearing material using medium temperature pressure leaching, direct electrowinning and solvent/solution extraction |
| US7476308B2 (en) * | 2001-07-25 | 2009-01-13 | Phelps Dodge Corporation | Process for multiple stage direct electrowinning of copper |
| US6863825B2 (en) | 2003-01-29 | 2005-03-08 | Union Oil Company Of California | Process for removing arsenic from aqueous streams |
| US20040156765A1 (en) * | 2003-02-12 | 2004-08-12 | Nichromet Extraction Inc. | Gold and silver recovery from polymetallic sulfides by treatment with halogens |
| US7736487B2 (en) | 2004-10-29 | 2010-06-15 | Freeport-Mcmoran Corporation | Process for recovery of copper from copper-bearing material using pressure leaching, direct electrowinning and solution extraction |
| EA010942B1 (ru) * | 2004-10-29 | 2008-12-30 | Фелпс Додж Корпорейшн | Способ извлечения меди из медьсодержащего материала |
| JP2008540834A (ja) * | 2005-05-13 | 2008-11-20 | ビーエイチピー・ビリトン・エスエスエム・テクノロジー・ピーティーワイ・リミテッド | 含ニッケル酸化鉱石のヒープリーチングのための改良法 |
| WO2007039663A1 (en) * | 2005-10-03 | 2007-04-12 | Outotec Oyj. | Processing of nickel sulphide ore or concentrates with sodium chloride |
| US7572317B2 (en) * | 2005-11-10 | 2009-08-11 | Barrick Gold Corporation | Thiosulfate generation in situ in precious metal recovery |
| US8066874B2 (en) | 2006-12-28 | 2011-11-29 | Molycorp Minerals, Llc | Apparatus for treating a flow of an aqueous solution containing arsenic |
| US20080308429A1 (en) * | 2007-06-18 | 2008-12-18 | Cvrd Inco Limited | Method for improving cathode morphology |
| US7998441B2 (en) * | 2007-09-20 | 2011-08-16 | Cvrd Inco Limited | Method for selective removal of cadmium |
| US8252087B2 (en) | 2007-10-31 | 2012-08-28 | Molycorp Minerals, Llc | Process and apparatus for treating a gas containing a contaminant |
| US8349764B2 (en) | 2007-10-31 | 2013-01-08 | Molycorp Minerals, Llc | Composition for treating a fluid |
| RU2444573C2 (ru) * | 2010-01-20 | 2012-03-10 | Открытое акционерное общество "Кольская горно-металлургическая компания" | Способ производства концентрата драгоценных металлов из сульфидного медно-никелевого сырья |
| CA2788369A1 (en) * | 2010-01-28 | 2011-08-04 | Mcmaster University | Nanoparticle flotation collectors |
| FI122188B (fi) * | 2010-03-18 | 2011-09-30 | Outotec Oyj | Hydrometallurginen menetelmä metallisen nikkelin valmistamiseksi |
| JP5445777B2 (ja) | 2010-07-28 | 2014-03-19 | 住友金属鉱山株式会社 | 低品位ニッケル酸化鉱石からのフェロニッケル製錬原料の製造方法 |
| US10662503B2 (en) * | 2011-01-25 | 2020-05-26 | The University Of Queensland | Method of ore processing using mixture including acidic leach solution and oxidizing agent |
| PT2668303T (pt) * | 2011-01-25 | 2019-07-15 | Univ Queensland | Método melhorado para a transformação de minério |
| US9233863B2 (en) | 2011-04-13 | 2016-01-12 | Molycorp Minerals, Llc | Rare earth removal of hydrated and hydroxyl species |
| FI20110279A0 (fi) | 2011-08-29 | 2011-08-29 | Outotec Oyj | Menetelmä metallien talteenottamiseksi niitä sisältävästä materiaalista |
| JP5842684B2 (ja) * | 2012-03-13 | 2016-01-13 | 住友金属鉱山株式会社 | 湿式製錬方法 |
| JP5424139B2 (ja) * | 2012-03-19 | 2014-02-26 | 住友金属鉱山株式会社 | 製鉄用ヘマタイトの製造方法 |
| FI124883B (fi) | 2012-12-20 | 2015-03-13 | Outotec Oyj | Menetelmä ja laitteisto metallikiven happogranuloimiseksi |
| CN103272700B (zh) * | 2013-06-07 | 2014-11-05 | 浙江华友钴业股份有限公司 | 一种从铜钴矿酸浸冶炼渣中浮选回收铜钴的方法 |
| CN103386359A (zh) * | 2013-07-19 | 2013-11-13 | 广州有色金属研究院 | 一种氧化铜钴矿的选矿方法 |
| JP5440823B1 (ja) * | 2013-09-18 | 2014-03-12 | 住友金属鉱山株式会社 | 製鉄用ヘマタイトの製造方法 |
| US9975787B2 (en) | 2014-03-07 | 2018-05-22 | Secure Natural Resources Llc | Removal of arsenic from aqueous streams with cerium (IV) oxide compositions |
| JP5884870B1 (ja) | 2014-08-13 | 2016-03-15 | 住友金属鉱山株式会社 | ニッケルの回収方法 |
| US10457565B2 (en) | 2014-09-18 | 2019-10-29 | Sumitomo Metal Mining Co., Ltd. | Production method for hematite for iron production |
| CN107429311B (zh) * | 2014-12-19 | 2019-09-03 | Fl史密斯公司 | 用于快速浸出黄铜矿的方法 |
| RU2613823C1 (ru) * | 2015-12-18 | 2017-03-21 | Федеральное государственное бюджетное учреждение науки Институт химии и технологии редких элементов и минерального сырья им. И.В. Тананаева Кольского научного центра Российской академии наук (ИХТРЭМС КНЦ РАН) | Способ получения концентрата драгоценных металлов из медно-никелевого файнштейна |
| WO2017197417A1 (en) * | 2016-05-09 | 2017-11-16 | Mintek | Method of recovering a target metal |
| JP7062996B2 (ja) * | 2017-03-29 | 2022-05-09 | 住友金属鉱山株式会社 | チオン酸を含む溶液の保存方法および定量方法、ならびにチオン酸を含む試料溶液およびその作製方法 |
| JP6957974B2 (ja) * | 2017-05-23 | 2021-11-02 | 住友金属鉱山株式会社 | 塩素浸出方法、電気ニッケルの製造方法 |
| CN111278998A (zh) * | 2017-06-08 | 2020-06-12 | 城市采矿有限公司 | 从废锂基电池和其它进料中回收钴、锂和其它金属的方法 |
| EP3926061A4 (en) * | 2019-02-13 | 2022-11-02 | Korea Zinc Co., Ltd. | ECONOMIC PROCESS USING A COMBINATION OF WET AND DRY PROCESSES FOR MELTING NICKEL FROM NICKEL SULFIDE ORES |
| WO2023092480A1 (zh) * | 2021-11-26 | 2023-06-01 | 深圳市坤鹏冶金工程技术有限公司 | 一种从高冰镍中提取硫酸镍的方法 |
| WO2024103106A1 (en) * | 2022-11-14 | 2024-05-23 | Hydromet WA Pty Limited | "method for the preferential leach of value metals from sulphide concentrates" |
| CN115818739B (zh) * | 2022-12-22 | 2024-07-09 | 广西中伟新能源科技有限公司 | 使用高冰镍制备硫酸镍的方法 |
Family Cites Families (24)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4039406A (en) | 1973-08-10 | 1977-08-02 | Noranda Mines Limited | Recovering copper from concentrates with insoluble sulfate forming leach |
| JPS50115614A (zh) * | 1974-02-16 | 1975-09-10 | ||
| US3981962A (en) * | 1975-06-30 | 1976-09-21 | The United States Of America As Represented By The Secretary Of The Interior | Decomposition leach of sulfide ores with chlorine and oxygen |
| CA1092056A (en) | 1977-10-11 | 1980-12-23 | Victor A. Ettel | Electrowinning cell with bagged anode |
| CA1107678A (en) | 1978-04-12 | 1981-08-25 | Kohur N. Subramanian | Nickel recovery from sulfur-deficient mattes |
| CA1125228A (en) | 1979-10-10 | 1982-06-08 | Daniel P. Young | Process for electrowinning nickel or cobalt |
| US4384940A (en) * | 1982-01-21 | 1983-05-24 | Inco Limited | Chlorine leaching of nickel-cobalt-iron sulphides |
| NO833784L (no) * | 1983-10-18 | 1985-04-19 | Thomas Thomassen | Autoklav-klorluting av kobbersulfidkonsentrater |
| FI88728C (fi) * | 1986-04-24 | 1993-06-28 | Falconbridge Ltd | Separering av nickel fraon koppar i autoklav |
| US5232491A (en) | 1991-10-25 | 1993-08-03 | Dominion Mining Limited | Activation of a mineral species |
| US5431788A (en) | 1993-06-28 | 1995-07-11 | Cominco Engineering Services Ltd. | Chloride assisted hydrometallurgical copper extraction |
| US5650057A (en) | 1993-07-29 | 1997-07-22 | Cominco Engineering Services Ltd. | Chloride assisted hydrometallurgical extraction of metal |
| US5874055A (en) | 1993-07-29 | 1999-02-23 | Cominco Engineering Services Ltd. | Chloride assisted hydrometallurgical extraction of metal |
| US5855858A (en) | 1993-07-29 | 1999-01-05 | Cominco Engineering Services Ltd. | Process for the recovery of nickel and/or cobalt from an ore or concentrate |
| US5902474A (en) | 1993-07-29 | 1999-05-11 | Cominco Engineering Services Ltd. | Chloride assisted hydrometallurgical extraction of metal |
| US5378262A (en) * | 1994-03-22 | 1995-01-03 | Inco Limited | Process for the extraction and separation of nickel and/or cobalt |
| CA2137124C (en) * | 1994-12-01 | 1999-03-16 | Tao Xue | Pressure leaching of nickel and cobalt sulphides with chlorine under controlled redox potential conditions |
| GB9503877D0 (en) | 1995-02-27 | 1995-04-19 | Sherritt Inc | Recovery of copper from sulphidic concentrates |
| AUPN191395A0 (en) * | 1995-03-22 | 1995-04-27 | M.I.M. Holdings Limited | Atmospheric mineral leaching process |
| AUPN476695A0 (en) | 1995-08-14 | 1995-09-07 | Dominion Mining Limited | Method of processing a copper mineral species |
| FI98073C (fi) * | 1995-08-14 | 1997-04-10 | Outokumpu Eng Oy | Menetelmä nikkelin talteenottamiseksi hydrometallurgisesti kahdesta eri nikkelikivestä |
| JPH10140257A (ja) | 1996-11-07 | 1998-05-26 | Sumitomo Metal Mining Co Ltd | 塩素浸出電解採取法によるニッケルの湿式精錬方法 |
| US5993514A (en) * | 1997-10-24 | 1999-11-30 | Dynatec Corporation | Process for upgrading copper sulphide residues containing nickel and iron |
| US6428604B1 (en) * | 2000-09-18 | 2002-08-06 | Inco Limited | Hydrometallurgical process for the recovery of nickel and cobalt values from a sulfidic flotation concentrate |
-
2000
- 2000-09-18 US US09/664,475 patent/US6428604B1/en not_active Expired - Fee Related
-
2001
- 2001-02-26 CN CNB018027865A patent/CN1210417C/zh not_active Expired - Fee Related
- 2001-02-26 JP JP2002529558A patent/JP3946633B2/ja not_active Expired - Lifetime
- 2001-02-26 RU RU2002113102/02A patent/RU2221881C1/ru not_active IP Right Cessation
- 2001-02-26 CA CA002376883A patent/CA2376883C/en not_active Expired - Lifetime
- 2001-02-26 BR BR0107217-0A patent/BR0107217A/pt not_active IP Right Cessation
- 2001-02-26 AU AU37169/01A patent/AU774519B2/en not_active Ceased
- 2001-02-26 DE DE60122914T patent/DE60122914T2/de not_active Expired - Lifetime
- 2001-02-26 WO PCT/CA2001/000227 patent/WO2002024966A1/en active IP Right Grant
- 2001-02-26 AT AT01909372T patent/ATE338833T1/de not_active IP Right Cessation
- 2001-02-26 EP EP01909372A patent/EP1325165B1/en not_active Expired - Lifetime
-
2002
- 2002-04-15 ZA ZA200202941A patent/ZA200202941B/xx unknown
- 2002-04-23 FI FI20020784A patent/FI123376B/fi not_active IP Right Cessation
- 2002-06-19 US US10/175,023 patent/US6569224B2/en not_active Expired - Lifetime
Cited By (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN100420760C (zh) * | 2004-05-21 | 2008-09-24 | Wmc资源有限公司 | 镍的回收 |
| CN101356292B (zh) * | 2005-11-10 | 2012-11-14 | 瓦利·德·利奥多斯公司 | 组合浸出方法 |
| CN101760616B (zh) * | 2008-12-02 | 2011-08-10 | 中国恩菲工程技术有限公司 | 含钴矿石的浸出方法 |
| CN101705371B (zh) * | 2009-11-20 | 2011-04-06 | 北京矿冶研究总院 | 一种硫化铜钴矿中提取钴的方法 |
| CN102002586A (zh) * | 2010-12-04 | 2011-04-06 | 金川集团有限公司 | 一种含镍高钴硫化物浸出技术 |
| CN102002586B (zh) * | 2010-12-04 | 2012-09-26 | 金川集团有限公司 | 一种含镍高钴硫化物浸出工艺 |
| CN102206834A (zh) * | 2011-05-03 | 2011-10-05 | 四川省尼科国润新材料有限公司 | 一种用低冰镍直接生产电解镍的方法 |
| CN102206834B (zh) * | 2011-05-03 | 2012-12-26 | 四川省尼科国润新材料有限公司 | 一种用低冰镍直接生产电解镍的方法 |
| CN102367173A (zh) * | 2011-07-01 | 2012-03-07 | 王嘉兴 | 用废渣铜泥制备硫化铜和氯化钠的方法 |
| CN102367175A (zh) * | 2011-07-01 | 2012-03-07 | 王嘉兴 | 用废渣铜泥制备硫化铜,氢氧化铜和氯化钠的方法 |
| CN102367179A (zh) * | 2011-07-01 | 2012-03-07 | 王嘉兴 | 用废渣铜泥制备硫化铜,氯化铜和氯化钠的方法 |
| CN102367176A (zh) * | 2011-07-01 | 2012-03-07 | 王嘉兴 | 用废渣铜泥制备硫化铜,磷酸铜和磷酸钠的方法 |
| CN102344118A (zh) * | 2011-07-01 | 2012-02-08 | 王嘉兴 | 用废渣铜泥制备硫化铜,氢氧化铜和氯化钠的方法 |
| CN102344163A (zh) * | 2011-07-01 | 2012-02-08 | 王嘉兴 | 用废渣铜泥制备硫化铜,碳酸铜和氯化钠的方法 |
| CN103958416A (zh) * | 2011-12-26 | 2014-07-30 | 住友金属矿山株式会社 | 硫酸钴的制造方法 |
| CN103958416B (zh) * | 2011-12-26 | 2016-04-13 | 住友金属矿山株式会社 | 硫酸钴的制造方法 |
| CN103725887A (zh) * | 2013-12-13 | 2014-04-16 | 金川集团股份有限公司 | 一种浸出海绵铜的方法 |
| CN108103311A (zh) * | 2017-12-14 | 2018-06-01 | 中南大学 | 一种铜镍混合矿的湿法冶炼方法 |
| CN108118149A (zh) * | 2017-12-14 | 2018-06-05 | 中南大学 | 一种用硫化镍精矿制备动力电池正极材料前驱体的方法 |
| CN112680602A (zh) * | 2020-12-18 | 2021-04-20 | 衢州华友钴新材料有限公司 | 一种提升含铜硫化矿浸出效率的处理方法 |
| CN113957264A (zh) * | 2021-09-13 | 2022-01-21 | 广东邦普循环科技有限公司 | 一种由低冰镍制备硫酸镍的方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP3946633B2 (ja) | 2007-07-18 |
| BR0107217A (pt) | 2002-07-09 |
| ZA200202941B (en) | 2003-04-15 |
| AU774519B2 (en) | 2004-07-01 |
| JP2004509232A (ja) | 2004-03-25 |
| EP1325165B1 (en) | 2006-09-06 |
| EP1325165A1 (en) | 2003-07-09 |
| FI123376B (fi) | 2013-03-15 |
| US6428604B1 (en) | 2002-08-06 |
| CN1210417C (zh) | 2005-07-13 |
| CA2376883C (en) | 2002-12-03 |
| DE60122914D1 (de) | 2006-10-19 |
| ATE338833T1 (de) | 2006-09-15 |
| RU2002113102A (ru) | 2004-01-27 |
| US6569224B2 (en) | 2003-05-27 |
| US20030033906A1 (en) | 2003-02-20 |
| RU2221881C1 (ru) | 2004-01-20 |
| WO2002024966A1 (en) | 2002-03-28 |
| DE60122914T2 (de) | 2007-04-26 |
| FI20020784A (fi) | 2002-04-23 |
| AU3716901A (en) | 2002-04-02 |
| CA2376883A1 (en) | 2002-03-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN1392902A (zh) | 由氯化物促进氧化加压浸提回收硫化浮选精矿中的镍及钴 | |
| EP0924307B1 (en) | Solvent extraction of cobalt and nickel values from a magnesium containing solution | |
| CN101278064B (zh) | 以基于氯化物的浸出方式处理含镍原料的方法 | |
| US6171564B1 (en) | Process for extraction of metal from an ore or concentrate containing nickel and/or cobalt | |
| US6383460B2 (en) | Process for the recovery of nickel and/or cobalt from a concentrate | |
| AU2014270210B2 (en) | Method for recovering metals | |
| US20020034465A1 (en) | Method for recovering metal values from metal-containing materials using high temperature pressure leaching | |
| CN102859012B (zh) | 处理含镍原料的方法 | |
| USRE37251E1 (en) | Chloride assisted hydrometallurgical extraction of metal | |
| AU728941B2 (en) | Process for the recovery of nickel and/or cobalt from a concentrate |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| CF01 | Termination of patent right due to non-payment of annual fee | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20050713 Termination date: 20200226 |