CN113372579B - 可注射大孔水凝胶 - Google Patents
可注射大孔水凝胶 Download PDFInfo
- Publication number
- CN113372579B CN113372579B CN202110629796.7A CN202110629796A CN113372579B CN 113372579 B CN113372579 B CN 113372579B CN 202110629796 A CN202110629796 A CN 202110629796A CN 113372579 B CN113372579 B CN 113372579B
- Authority
- CN
- China
- Prior art keywords
- peg
- gel
- solute
- macroporous
- mol
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 239000000017 hydrogel Substances 0.000 title claims abstract description 41
- 229920001223 polyethylene glycol Polymers 0.000 claims abstract description 121
- 239000002202 Polyethylene glycol Substances 0.000 claims abstract description 118
- 238000000034 method Methods 0.000 claims abstract description 33
- 238000001879 gelation Methods 0.000 claims abstract description 25
- 239000007864 aqueous solution Substances 0.000 claims abstract description 17
- 239000003431 cross linking reagent Substances 0.000 claims abstract description 17
- 238000005191 phase separation Methods 0.000 claims abstract description 14
- 239000003795 chemical substances by application Substances 0.000 claims abstract description 11
- 229920002674 hyaluronan Polymers 0.000 claims description 69
- 108090000765 processed proteins & peptides Proteins 0.000 claims description 45
- 150000004676 glycans Chemical class 0.000 claims description 33
- 229920001282 polysaccharide Polymers 0.000 claims description 32
- 239000005017 polysaccharide Substances 0.000 claims description 32
- 229920002307 Dextran Polymers 0.000 claims description 19
- 238000004132 cross linking Methods 0.000 claims description 17
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 claims description 9
- 229960003160 hyaluronic acid Drugs 0.000 claims description 9
- 239000004971 Cross linker Substances 0.000 claims description 6
- 150000004662 dithiols Chemical class 0.000 claims description 3
- 230000000977 initiatory effect Effects 0.000 claims description 2
- 229920000642 polymer Polymers 0.000 abstract description 56
- 229920000765 poly(2-oxazolines) Polymers 0.000 abstract description 25
- 239000000243 solution Substances 0.000 abstract description 21
- 229920006037 cross link polymer Polymers 0.000 abstract description 6
- 239000000499 gel Substances 0.000 description 152
- 210000004027 cell Anatomy 0.000 description 67
- KIUKXJAPPMFGSW-MNSSHETKSA-N hyaluronan Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)C1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H](C(O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-MNSSHETKSA-N 0.000 description 61
- 229940099552 hyaluronan Drugs 0.000 description 60
- 210000002569 neuron Anatomy 0.000 description 37
- 239000011148 porous material Substances 0.000 description 36
- 210000002241 neurite Anatomy 0.000 description 31
- AEMOLEFTQBMNLQ-VANFPWTGSA-N D-mannopyranuronic acid Chemical compound OC1O[C@H](C(O)=O)[C@@H](O)[C@H](O)[C@@H]1O AEMOLEFTQBMNLQ-VANFPWTGSA-N 0.000 description 29
- IAJILQKETJEXLJ-UHFFFAOYSA-N Galacturonsaeure Natural products O=CC(O)C(O)C(O)C(O)C(O)=O IAJILQKETJEXLJ-UHFFFAOYSA-N 0.000 description 29
- 125000003396 thiol group Chemical class [H]S* 0.000 description 29
- 230000015572 biosynthetic process Effects 0.000 description 27
- 230000014511 neuron projection development Effects 0.000 description 23
- 239000002609 medium Substances 0.000 description 21
- AFOSIXZFDONLBT-UHFFFAOYSA-N divinyl sulfone Chemical class C=CS(=O)(=O)C=C AFOSIXZFDONLBT-UHFFFAOYSA-N 0.000 description 17
- 238000005538 encapsulation Methods 0.000 description 17
- 238000003384 imaging method Methods 0.000 description 16
- 230000015556 catabolic process Effects 0.000 description 15
- 238000006731 degradation reaction Methods 0.000 description 15
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 15
- 102000004196 processed proteins & peptides Human genes 0.000 description 13
- 230000035899 viability Effects 0.000 description 13
- 239000000872 buffer Substances 0.000 description 12
- 230000000694 effects Effects 0.000 description 12
- 210000003594 spinal ganglia Anatomy 0.000 description 11
- 239000000203 mixture Substances 0.000 description 10
- 230000001537 neural effect Effects 0.000 description 10
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 9
- 108010000684 Matrix Metalloproteinases Proteins 0.000 description 9
- 102000002274 Matrix Metalloproteinases Human genes 0.000 description 9
- 238000006845 Michael addition reaction Methods 0.000 description 9
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 9
- 108060008539 Transglutaminase Proteins 0.000 description 9
- 210000005056 cell body Anatomy 0.000 description 9
- VYFYYTLLBUKUHU-UHFFFAOYSA-N dopamine Chemical compound NCCC1=CC=C(O)C(O)=C1 VYFYYTLLBUKUHU-UHFFFAOYSA-N 0.000 description 9
- 239000001963 growth medium Substances 0.000 description 9
- 239000003999 initiator Substances 0.000 description 9
- 102000003601 transglutaminase Human genes 0.000 description 9
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 8
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 8
- 229910052791 calcium Inorganic materials 0.000 description 8
- 239000011575 calcium Substances 0.000 description 8
- 210000003618 cortical neuron Anatomy 0.000 description 8
- 108010088381 isoleucyl-lysyl-valyl-alanyl-valine Proteins 0.000 description 8
- 210000001519 tissue Anatomy 0.000 description 8
- DZGWFCGJZKJUFP-UHFFFAOYSA-N tyramine Chemical compound NCCC1=CC=C(O)C=C1 DZGWFCGJZKJUFP-UHFFFAOYSA-N 0.000 description 8
- -1 1,3, 5-tribromophenyl Chemical group 0.000 description 7
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 7
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 7
- 239000007995 HEPES buffer Substances 0.000 description 7
- 239000004205 dimethyl polysiloxane Substances 0.000 description 7
- 235000013870 dimethyl polysiloxane Nutrition 0.000 description 7
- CXQXSVUQTKDNFP-UHFFFAOYSA-N octamethyltrisiloxane Chemical compound C[Si](C)(C)O[Si](C)(C)O[Si](C)(C)C CXQXSVUQTKDNFP-UHFFFAOYSA-N 0.000 description 7
- 238000004987 plasma desorption mass spectroscopy Methods 0.000 description 7
- 229920000435 poly(dimethylsiloxane) Polymers 0.000 description 7
- 239000000758 substrate Substances 0.000 description 7
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 6
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 6
- 229940072056 alginate Drugs 0.000 description 6
- 235000010443 alginic acid Nutrition 0.000 description 6
- 229920000615 alginic acid Polymers 0.000 description 6
- 230000008901 benefit Effects 0.000 description 6
- 229920001577 copolymer Polymers 0.000 description 6
- 239000011159 matrix material Substances 0.000 description 6
- 239000000178 monomer Substances 0.000 description 6
- 238000011002 quantification Methods 0.000 description 6
- 150000003254 radicals Chemical class 0.000 description 6
- 230000002829 reductive effect Effects 0.000 description 6
- XQQUSYWGKLRJRA-RABCQHRBSA-N (2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-6-amino-2-[[(2s,3s)-2-amino-3-methylpentanoyl]amino]hexanoyl]amino]-3-methylbutanoyl]amino]propanoyl]amino]-3-methylbutanoic acid Chemical compound CC[C@H](C)[C@H](N)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](C(C)C)C(O)=O XQQUSYWGKLRJRA-RABCQHRBSA-N 0.000 description 5
- IMSODMZESSGVBE-UHFFFAOYSA-N 2-Oxazoline Chemical compound C1CN=CO1 IMSODMZESSGVBE-UHFFFAOYSA-N 0.000 description 5
- 238000013528 artificial neural network Methods 0.000 description 5
- 238000006243 chemical reaction Methods 0.000 description 5
- 230000005284 excitation Effects 0.000 description 5
- 230000007717 exclusion Effects 0.000 description 5
- 238000002474 experimental method Methods 0.000 description 5
- 238000004108 freeze drying Methods 0.000 description 5
- 238000011065 in-situ storage Methods 0.000 description 5
- 230000001965 increasing effect Effects 0.000 description 5
- 230000003993 interaction Effects 0.000 description 5
- 229920002521 macromolecule Polymers 0.000 description 5
- 239000003550 marker Substances 0.000 description 5
- 238000002156 mixing Methods 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 235000018102 proteins Nutrition 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 238000010186 staining Methods 0.000 description 5
- 238000003860 storage Methods 0.000 description 5
- 229920001567 vinyl ester resin Polymers 0.000 description 5
- 150000003923 2,5-pyrrolediones Chemical class 0.000 description 4
- GJKGAPPUXSSCFI-UHFFFAOYSA-N 2-Hydroxy-4'-(2-hydroxyethoxy)-2-methylpropiophenone Chemical group CC(C)(O)C(=O)C1=CC=C(OCCO)C=C1 GJKGAPPUXSSCFI-UHFFFAOYSA-N 0.000 description 4
- NYEZZYQZRQDLEH-UHFFFAOYSA-N 2-ethyl-4,5-dihydro-1,3-oxazole Chemical compound CCC1=NCCO1 NYEZZYQZRQDLEH-UHFFFAOYSA-N 0.000 description 4
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 4
- IICCLYANAQEHCI-UHFFFAOYSA-N 4,5,6,7-tetrachloro-3',6'-dihydroxy-2',4',5',7'-tetraiodospiro[2-benzofuran-3,9'-xanthene]-1-one Chemical compound O1C(=O)C(C(=C(Cl)C(Cl)=C2Cl)Cl)=C2C21C1=CC(I)=C(O)C(I)=C1OC1=C(I)C(O)=C(I)C=C21 IICCLYANAQEHCI-UHFFFAOYSA-N 0.000 description 4
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 4
- 102000009123 Fibrin Human genes 0.000 description 4
- 108010073385 Fibrin Proteins 0.000 description 4
- BWGVNKXGVNDBDI-UHFFFAOYSA-N Fibrin monomer Chemical compound CNC(=O)CNC(=O)CN BWGVNKXGVNDBDI-UHFFFAOYSA-N 0.000 description 4
- 239000004365 Protease Substances 0.000 description 4
- AUNGANRZJHBGPY-SCRDCRAPSA-N Riboflavin Chemical compound OC[C@@H](O)[C@@H](O)[C@@H](O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O AUNGANRZJHBGPY-SCRDCRAPSA-N 0.000 description 4
- 150000001252 acrylic acid derivatives Chemical class 0.000 description 4
- 150000001299 aldehydes Chemical class 0.000 description 4
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 4
- 235000001014 amino acid Nutrition 0.000 description 4
- 150000001540 azides Chemical class 0.000 description 4
- 230000004071 biological effect Effects 0.000 description 4
- 230000000903 blocking effect Effects 0.000 description 4
- DEGAKNSWVGKMLS-UHFFFAOYSA-N calcein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC(CN(CC(O)=O)CC(O)=O)=C(O)C=C1OC1=C2C=C(CN(CC(O)=O)CC(=O)O)C(O)=C1 DEGAKNSWVGKMLS-UHFFFAOYSA-N 0.000 description 4
- ACTIUHUUMQJHFO-UPTCCGCDSA-N coenzyme Q10 Chemical compound COC1=C(OC)C(=O)C(C\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CC\C=C(/C)CCC=C(C)C)=C(C)C1=O ACTIUHUUMQJHFO-UPTCCGCDSA-N 0.000 description 4
- 238000001218 confocal laser scanning microscopy Methods 0.000 description 4
- 230000006378 damage Effects 0.000 description 4
- 230000001419 dependent effect Effects 0.000 description 4
- 229960003638 dopamine Drugs 0.000 description 4
- 229950003499 fibrin Drugs 0.000 description 4
- 238000012744 immunostaining Methods 0.000 description 4
- 238000001727 in vivo Methods 0.000 description 4
- 238000011534 incubation Methods 0.000 description 4
- 238000002347 injection Methods 0.000 description 4
- 239000007924 injection Substances 0.000 description 4
- 150000002734 metacrylic acid derivatives Chemical class 0.000 description 4
- 229960002378 oftasceine Drugs 0.000 description 4
- 230000000704 physical effect Effects 0.000 description 4
- 229920000671 polyethylene glycol diacrylate Polymers 0.000 description 4
- 239000000047 product Substances 0.000 description 4
- 229940000960 q-gel Drugs 0.000 description 4
- 229930187593 rose bengal Natural products 0.000 description 4
- 229940081623 rose bengal Drugs 0.000 description 4
- STRXNPAVPKGJQR-UHFFFAOYSA-N rose bengal A Natural products O1C(=O)C(C(=CC=C2Cl)Cl)=C2C21C1=CC(I)=C(O)C(I)=C1OC1=C(I)C(O)=C(I)C=C21 STRXNPAVPKGJQR-UHFFFAOYSA-N 0.000 description 4
- 150000003839 salts Chemical class 0.000 description 4
- 239000011550 stock solution Substances 0.000 description 4
- 238000012546 transfer Methods 0.000 description 4
- 238000011282 treatment Methods 0.000 description 4
- 229960003732 tyramine Drugs 0.000 description 4
- TXBCBTDQIULDIA-UHFFFAOYSA-N 2-[[3-hydroxy-2,2-bis(hydroxymethyl)propoxy]methyl]-2-(hydroxymethyl)propane-1,3-diol Chemical compound OCC(CO)(CO)COCC(CO)(CO)CO TXBCBTDQIULDIA-UHFFFAOYSA-N 0.000 description 3
- GUXJXWKCUUWCLX-UHFFFAOYSA-N 2-methyl-2-oxazoline Chemical compound CC1=NCCO1 GUXJXWKCUUWCLX-UHFFFAOYSA-N 0.000 description 3
- 108010035532 Collagen Proteins 0.000 description 3
- 102000008186 Collagen Human genes 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- 102100039289 Glial fibrillary acidic protein Human genes 0.000 description 3
- 101710193519 Glial fibrillary acidic protein Proteins 0.000 description 3
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 3
- 102100021118 Microtubule-associated protein 2 Human genes 0.000 description 3
- 102000008763 Neurofilament Proteins Human genes 0.000 description 3
- 108010088373 Neurofilament Proteins Proteins 0.000 description 3
- BELBBZDIHDAJOR-UHFFFAOYSA-N Phenolsulfonephthalein Chemical compound C1=CC(O)=CC=C1C1(C=2C=CC(O)=CC=2)C2=CC=CC=C2S(=O)(=O)O1 BELBBZDIHDAJOR-UHFFFAOYSA-N 0.000 description 3
- 150000003926 acrylamides Chemical class 0.000 description 3
- 150000001345 alkine derivatives Chemical class 0.000 description 3
- 150000001413 amino acids Chemical class 0.000 description 3
- 229920006187 aquazol Polymers 0.000 description 3
- 210000001130 astrocyte Anatomy 0.000 description 3
- 238000005311 autocorrelation function Methods 0.000 description 3
- BQRGNLJZBFXNCZ-UHFFFAOYSA-N calcein am Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC(CN(CC(=O)OCOC(C)=O)CC(=O)OCOC(C)=O)=C(OC(C)=O)C=C1OC1=C2C=C(CN(CC(=O)OCOC(C)=O)CC(=O)OCOC(=O)C)C(OC(C)=O)=C1 BQRGNLJZBFXNCZ-UHFFFAOYSA-N 0.000 description 3
- 238000004113 cell culture Methods 0.000 description 3
- 230000004709 cell invasion Effects 0.000 description 3
- 229920001436 collagen Polymers 0.000 description 3
- 235000018417 cysteine Nutrition 0.000 description 3
- 125000000151 cysteine group Chemical class N[C@@H](CS)C(=O)* 0.000 description 3
- 238000009792 diffusion process Methods 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- 229940012444 factor xiii Drugs 0.000 description 3
- 238000000799 fluorescence microscopy Methods 0.000 description 3
- 238000005227 gel permeation chromatography Methods 0.000 description 3
- 210000005046 glial fibrillary acidic protein Anatomy 0.000 description 3
- 239000012456 homogeneous solution Substances 0.000 description 3
- 238000003365 immunocytochemistry Methods 0.000 description 3
- 238000007373 indentation Methods 0.000 description 3
- 208000014674 injury Diseases 0.000 description 3
- FZWBNHMXJMCXLU-BLAUPYHCSA-N isomaltotriose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@@H](OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O)O1 FZWBNHMXJMCXLU-BLAUPYHCSA-N 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 229910052751 metal Inorganic materials 0.000 description 3
- 239000002184 metal Substances 0.000 description 3
- 210000005044 neurofilament Anatomy 0.000 description 3
- WXZMFSXDPGVJKK-UHFFFAOYSA-N pentaerythritol Chemical compound OCC(CO)(CO)CO WXZMFSXDPGVJKK-UHFFFAOYSA-N 0.000 description 3
- 229960003531 phenolsulfonphthalein Drugs 0.000 description 3
- 229920003023 plastic Polymers 0.000 description 3
- 239000004033 plastic Substances 0.000 description 3
- 229920001610 polycaprolactone Polymers 0.000 description 3
- 229920001451 polypropylene glycol Polymers 0.000 description 3
- 210000002243 primary neuron Anatomy 0.000 description 3
- 230000008929 regeneration Effects 0.000 description 3
- 238000011069 regeneration method Methods 0.000 description 3
- 238000000518 rheometry Methods 0.000 description 3
- 239000007787 solid Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 239000006228 supernatant Substances 0.000 description 3
- 230000000946 synaptic effect Effects 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- 230000001960 triggered effect Effects 0.000 description 3
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 3
- GJZKNORRVIUCCH-UHFFFAOYSA-N 1,4-dibromo-2,3-bis(bromomethyl)but-2-ene Chemical group BrCC(CBr)=C(CBr)CBr GJZKNORRVIUCCH-UHFFFAOYSA-N 0.000 description 2
- VGIRNWJSIRVFRT-UHFFFAOYSA-N 2',7'-difluorofluorescein Chemical compound OC(=O)C1=CC=CC=C1C1=C2C=C(F)C(=O)C=C2OC2=CC(O)=C(F)C=C21 VGIRNWJSIRVFRT-UHFFFAOYSA-N 0.000 description 2
- SFRDXVJWXWOTEW-UHFFFAOYSA-N 2-(hydroxymethyl)propane-1,3-diol Chemical compound OCC(CO)CO SFRDXVJWXWOTEW-UHFFFAOYSA-N 0.000 description 2
- PTJWCLYPVFJWMP-UHFFFAOYSA-N 2-[[3-hydroxy-2-[[3-hydroxy-2,2-bis(hydroxymethyl)propoxy]methyl]-2-(hydroxymethyl)propoxy]methyl]-2-(hydroxymethyl)propane-1,3-diol Chemical compound OCC(CO)(CO)COCC(CO)(CO)COCC(CO)(CO)CO PTJWCLYPVFJWMP-UHFFFAOYSA-N 0.000 description 2
- HATKUFQZJPLPGN-UHFFFAOYSA-N 2-phosphanylethane-1,1,1-tricarboxylic acid Chemical compound OC(=O)C(CP)(C(O)=O)C(O)=O HATKUFQZJPLPGN-UHFFFAOYSA-N 0.000 description 2
- RCUKTMOISQQFBQ-UHFFFAOYSA-N 3-(4,5-dihydro-1,3-oxazol-2-yl)propanoic acid Chemical compound OC(=O)CCC1=NCCO1 RCUKTMOISQQFBQ-UHFFFAOYSA-N 0.000 description 2
- RPXVIAFEQBNEAX-UHFFFAOYSA-N 6-Cyano-7-nitroquinoxaline-2,3-dione Chemical compound N1C(=O)C(=O)NC2=C1C=C([N+](=O)[O-])C(C#N)=C2 RPXVIAFEQBNEAX-UHFFFAOYSA-N 0.000 description 2
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 2
- 108091006146 Channels Proteins 0.000 description 2
- AUNGANRZJHBGPY-UHFFFAOYSA-N D-Lyxoflavin Natural products OCC(O)C(O)C(O)CN1C=2C=C(C)C(C)=CC=2N=C2C1=NC(=O)NC2=O AUNGANRZJHBGPY-UHFFFAOYSA-N 0.000 description 2
- 238000005698 Diels-Alder reaction Methods 0.000 description 2
- 108010071289 Factor XIII Proteins 0.000 description 2
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 2
- 229920002148 Gellan gum Polymers 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 101000979001 Homo sapiens Methionine aminopeptidase 2 Proteins 0.000 description 2
- 101000969087 Homo sapiens Microtubule-associated protein 2 Proteins 0.000 description 2
- 108010003272 Hyaluronate lyase Proteins 0.000 description 2
- 102000001974 Hyaluronidases Human genes 0.000 description 2
- 108010085895 Laminin Proteins 0.000 description 2
- 102000007547 Laminin Human genes 0.000 description 2
- PEEHTFAAVSWFBL-UHFFFAOYSA-N Maleimide Chemical compound O=C1NC(=O)C=C1 PEEHTFAAVSWFBL-UHFFFAOYSA-N 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- CERQOIWHTDAKMF-UHFFFAOYSA-M Methacrylate Chemical compound CC(=C)C([O-])=O CERQOIWHTDAKMF-UHFFFAOYSA-M 0.000 description 2
- 108090000192 Methionyl aminopeptidases Proteins 0.000 description 2
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 2
- 208000012902 Nervous system disease Diseases 0.000 description 2
- 208000025966 Neurological disease Diseases 0.000 description 2
- 108090000526 Papain Proteins 0.000 description 2
- 102000035195 Peptidases Human genes 0.000 description 2
- 108091005804 Peptidases Proteins 0.000 description 2
- 239000004698 Polyethylene Substances 0.000 description 2
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 2
- 208000027418 Wounds and injury Diseases 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 239000003513 alkali Substances 0.000 description 2
- 150000001342 alkaline earth metals Chemical class 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- 125000003275 alpha amino acid group Chemical group 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- 210000003050 axon Anatomy 0.000 description 2
- 230000003376 axonal effect Effects 0.000 description 2
- 229920001222 biopolymer Polymers 0.000 description 2
- 239000007844 bleaching agent Substances 0.000 description 2
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 2
- 150000001732 carboxylic acid derivatives Chemical group 0.000 description 2
- 150000001735 carboxylic acids Chemical class 0.000 description 2
- 239000006143 cell culture medium Substances 0.000 description 2
- 239000001913 cellulose Substances 0.000 description 2
- 229920002678 cellulose Polymers 0.000 description 2
- 235000010980 cellulose Nutrition 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 210000003837 chick embryo Anatomy 0.000 description 2
- 230000021615 conjugation Effects 0.000 description 2
- 238000012937 correction Methods 0.000 description 2
- 238000005314 correlation function Methods 0.000 description 2
- ZYGHJZDHTFUPRJ-UHFFFAOYSA-N coumarin Chemical compound C1=CC=C2OC(=O)C=CC2=C1 ZYGHJZDHTFUPRJ-UHFFFAOYSA-N 0.000 description 2
- 230000034994 death Effects 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- 238000000502 dialysis Methods 0.000 description 2
- 229920000359 diblock copolymer Polymers 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-M dihydrogenphosphate Chemical compound OP(O)([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-M 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 238000006073 displacement reaction Methods 0.000 description 2
- 210000002257 embryonic structure Anatomy 0.000 description 2
- SEACYXSIPDVVMV-UHFFFAOYSA-L eosin Y Chemical compound [Na+].[Na+].[O-]C(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C([O-])=C(Br)C=C21 SEACYXSIPDVVMV-UHFFFAOYSA-L 0.000 description 2
- 238000007667 floating Methods 0.000 description 2
- 238000002073 fluorescence micrograph Methods 0.000 description 2
- 230000004927 fusion Effects 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 230000000848 glutamatergic effect Effects 0.000 description 2
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 2
- 238000009499 grossing Methods 0.000 description 2
- 229960002773 hyaluronidase Drugs 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 230000002452 interceptive effect Effects 0.000 description 2
- 230000003834 intracellular effect Effects 0.000 description 2
- 230000009545 invasion Effects 0.000 description 2
- 238000002386 leaching Methods 0.000 description 2
- 239000012705 liquid precursor Substances 0.000 description 2
- 230000007774 longterm Effects 0.000 description 2
- 108010082117 matrigel Proteins 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- CXKWCBBOMKCUKX-UHFFFAOYSA-M methylene blue Chemical compound [Cl-].C1=CC(N(C)C)=CC2=[S+]C3=CC(N(C)C)=CC=C3N=C21 CXKWCBBOMKCUKX-UHFFFAOYSA-M 0.000 description 2
- 229960000907 methylthioninium chloride Drugs 0.000 description 2
- 239000004005 microsphere Substances 0.000 description 2
- 238000012544 monitoring process Methods 0.000 description 2
- 210000005036 nerve Anatomy 0.000 description 2
- 210000005155 neural progenitor cell Anatomy 0.000 description 2
- 108010087904 neutravidin Proteins 0.000 description 2
- 230000003647 oxidation Effects 0.000 description 2
- 238000007254 oxidation reaction Methods 0.000 description 2
- 229940055729 papain Drugs 0.000 description 2
- 235000019834 papain Nutrition 0.000 description 2
- 229920001277 pectin Polymers 0.000 description 2
- 239000001814 pectin Substances 0.000 description 2
- 235000010987 pectin Nutrition 0.000 description 2
- 230000002093 peripheral effect Effects 0.000 description 2
- 239000007793 ph indicator Substances 0.000 description 2
- 229920000747 poly(lactic acid) Polymers 0.000 description 2
- 229920000867 polyelectrolyte Polymers 0.000 description 2
- 229920000573 polyethylene Polymers 0.000 description 2
- 239000003361 porogen Substances 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 230000003518 presynaptic effect Effects 0.000 description 2
- XJMOSONTPMZWPB-UHFFFAOYSA-M propidium iodide Chemical compound [I-].[I-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CCC[N+](C)(CC)CC)=C1C1=CC=CC=C1 XJMOSONTPMZWPB-UHFFFAOYSA-M 0.000 description 2
- 238000010526 radical polymerization reaction Methods 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 230000001172 regenerating effect Effects 0.000 description 2
- 238000009877 rendering Methods 0.000 description 2
- 229960002477 riboflavin Drugs 0.000 description 2
- 235000019192 riboflavin Nutrition 0.000 description 2
- 239000002151 riboflavin Substances 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 238000013341 scale-up Methods 0.000 description 2
- 238000004062 sedimentation Methods 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 2
- 239000013589 supplement Substances 0.000 description 2
- 230000009469 supplementation Effects 0.000 description 2
- 210000000225 synapse Anatomy 0.000 description 2
- 102000003137 synaptotagmin Human genes 0.000 description 2
- 108060008004 synaptotagmin Proteins 0.000 description 2
- CFMYXEVWODSLAX-QOZOJKKESA-N tetrodotoxin Chemical compound O([C@@]([C@H]1O)(O)O[C@H]2[C@@]3(O)CO)[C@H]3[C@@H](O)[C@]11[C@H]2[C@@H](O)N=C(N)N1 CFMYXEVWODSLAX-QOZOJKKESA-N 0.000 description 2
- 229950010357 tetrodotoxin Drugs 0.000 description 2
- CFMYXEVWODSLAX-UHFFFAOYSA-N tetrodotoxin Natural products C12C(O)NC(=N)NC2(C2O)C(O)C3C(CO)(O)C1OC2(O)O3 CFMYXEVWODSLAX-UHFFFAOYSA-N 0.000 description 2
- 150000004764 thiosulfuric acid derivatives Chemical class 0.000 description 2
- 229920000428 triblock copolymer Polymers 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- WCDDVEOXEIYWFB-VXORFPGASA-N (2s,3s,4r,5r,6r)-3-[(2s,3r,5s,6r)-3-acetamido-5-hydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-4,5,6-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@@H]1C[C@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](C(O)=O)O[C@@H](O)[C@H](O)[C@H]1O WCDDVEOXEIYWFB-VXORFPGASA-N 0.000 description 1
- AEMOLEFTQBMNLQ-SYJWYVCOSA-N (2s,3s,4s,5s,6r)-3,4,5,6-tetrahydroxyoxane-2-carboxylic acid Chemical group O[C@@H]1O[C@H](C(O)=O)[C@@H](O)[C@H](O)[C@@H]1O AEMOLEFTQBMNLQ-SYJWYVCOSA-N 0.000 description 1
- OXBLVCZKDOZZOJ-UHFFFAOYSA-N 2,3-Dihydrothiophene Chemical compound C1CC=CS1 OXBLVCZKDOZZOJ-UHFFFAOYSA-N 0.000 description 1
- PAWVJRPRVYDHLQ-UHFFFAOYSA-N 2-(4,5-dihydro-1,3-oxazol-2-yl)ethanol Chemical compound OCCC1=NCCO1 PAWVJRPRVYDHLQ-UHFFFAOYSA-N 0.000 description 1
- SUAYFRHPQLERMW-UHFFFAOYSA-N 2-methyl-1,2-diphenylpropan-1-one Chemical group C=1C=CC=CC=1C(C)(C)C(=O)C1=CC=CC=C1 SUAYFRHPQLERMW-UHFFFAOYSA-N 0.000 description 1
- BYDNGJQDDNBAHI-UHFFFAOYSA-N 4-methyl-7-sulfanylchromen-2-one Chemical compound C1=C(S)C=CC2=C1OC(=O)C=C2C BYDNGJQDDNBAHI-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- BHPQYMZQTOCNFJ-UHFFFAOYSA-N Calcium cation Chemical compound [Ca+2] BHPQYMZQTOCNFJ-UHFFFAOYSA-N 0.000 description 1
- 229920001661 Chitosan Polymers 0.000 description 1
- 229920001287 Chondroitin sulfate Polymers 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- AEMOLEFTQBMNLQ-BZINKQHNSA-N D-Guluronic Acid Chemical compound OC1O[C@H](C(O)=O)[C@H](O)[C@@H](O)[C@H]1O AEMOLEFTQBMNLQ-BZINKQHNSA-N 0.000 description 1
- 102000016911 Deoxyribonucleases Human genes 0.000 description 1
- 108010053770 Deoxyribonucleases Proteins 0.000 description 1
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 238000003072 Ellman's test Methods 0.000 description 1
- 102000005593 Endopeptidases Human genes 0.000 description 1
- 108010059378 Endopeptidases Proteins 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- 108010000196 Factor XIIIa Proteins 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- LEVWYRKDKASIDU-IMJSIDKUSA-N L-cystine Chemical compound [O-]C(=O)[C@@H]([NH3+])CSSC[C@H]([NH3+])C([O-])=O LEVWYRKDKASIDU-IMJSIDKUSA-N 0.000 description 1
- 241000283986 Lepus Species 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 239000007987 MES buffer Substances 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 102100023174 Methionine aminopeptidase 2 Human genes 0.000 description 1
- OVRNDRQMDRJTHS-FMDGEEDCSA-N N-acetyl-beta-D-glucosamine Chemical group CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O OVRNDRQMDRJTHS-FMDGEEDCSA-N 0.000 description 1
- 208000028389 Nerve injury Diseases 0.000 description 1
- 108010057166 PA22-2 Proteins 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 229920002873 Polyethylenimine Polymers 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 239000002262 Schiff base Substances 0.000 description 1
- 150000004753 Schiff bases Chemical class 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 229920002125 Sokalan® Polymers 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 229920002807 Thiomer Polymers 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 229920004890 Triton X-100 Polymers 0.000 description 1
- 239000013504 Triton X-100 Substances 0.000 description 1
- 102000004142 Trypsin Human genes 0.000 description 1
- 108090000631 Trypsin Proteins 0.000 description 1
- 238000010162 Tukey test Methods 0.000 description 1
- LUTSRLYCMSCGCS-BWOMAWGNSA-N [(3s,8r,9s,10r,13s)-10,13-dimethyl-17-oxo-1,2,3,4,7,8,9,11,12,16-decahydrocyclopenta[a]phenanthren-3-yl] acetate Chemical compound C([C@@H]12)C[C@]3(C)C(=O)CC=C3[C@@H]1CC=C1[C@]2(C)CC[C@H](OC(=O)C)C1 LUTSRLYCMSCGCS-BWOMAWGNSA-N 0.000 description 1
- 238000011481 absorbance measurement Methods 0.000 description 1
- 239000000370 acceptor Substances 0.000 description 1
- 230000036982 action potential Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 150000001336 alkenes Chemical class 0.000 description 1
- AEMOLEFTQBMNLQ-WAXACMCWSA-N alpha-D-glucuronic acid Chemical group O[C@H]1O[C@H](C(O)=O)[C@@H](O)[C@H](O)[C@H]1O AEMOLEFTQBMNLQ-WAXACMCWSA-N 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 238000004873 anchoring Methods 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- 239000012861 aquazol Substances 0.000 description 1
- 239000012062 aqueous buffer Substances 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 230000004009 axon guidance Effects 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 239000002585 base Substances 0.000 description 1
- 229960002685 biotin Drugs 0.000 description 1
- 239000011616 biotin Substances 0.000 description 1
- 230000002051 biphasic effect Effects 0.000 description 1
- 239000003114 blood coagulation factor Substances 0.000 description 1
- 238000009835 boiling Methods 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 210000002449 bone cell Anatomy 0.000 description 1
- 229940098773 bovine serum albumin Drugs 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 229910001424 calcium ion Inorganic materials 0.000 description 1
- 238000004364 calculation method Methods 0.000 description 1
- 238000011088 calibration curve Methods 0.000 description 1
- 239000012482 calibration solution Substances 0.000 description 1
- MPBRYMWMMKKRGC-UHFFFAOYSA-M carbocyanin DBTC Chemical compound [Br-].C1=CC=CC2=C([N+](=C(C=C(C)C=C3N(C4=C5C=CC=CC5=CC=C4S3)CC)S3)CC)C3=CC=C21 MPBRYMWMMKKRGC-UHFFFAOYSA-M 0.000 description 1
- 150000001718 carbodiimides Chemical class 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 150000001733 carboxylic acid esters Chemical class 0.000 description 1
- 125000002843 carboxylic acid group Chemical group 0.000 description 1
- 235000010418 carrageenan Nutrition 0.000 description 1
- 239000000679 carrageenan Substances 0.000 description 1
- 229920001525 carrageenan Polymers 0.000 description 1
- 229940113118 carrageenan Drugs 0.000 description 1
- 210000000845 cartilage Anatomy 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 230000021164 cell adhesion Effects 0.000 description 1
- 239000012578 cell culture reagent Substances 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 239000006285 cell suspension Substances 0.000 description 1
- 230000001413 cellular effect Effects 0.000 description 1
- 210000003850 cellular structure Anatomy 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 230000002490 cerebral effect Effects 0.000 description 1
- 210000001612 chondrocyte Anatomy 0.000 description 1
- 239000000512 collagen gel Substances 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 239000013065 commercial product Substances 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 230000001054 cortical effect Effects 0.000 description 1
- 229960000956 coumarin Drugs 0.000 description 1
- 235000001671 coumarin Nutrition 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 238000006352 cycloaddition reaction Methods 0.000 description 1
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 1
- 210000000805 cytoplasm Anatomy 0.000 description 1
- 238000010908 decantation Methods 0.000 description 1
- 230000000593 degrading effect Effects 0.000 description 1
- 230000008021 deposition Effects 0.000 description 1
- 230000001066 destructive effect Effects 0.000 description 1
- 239000003599 detergent Substances 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 150000001354 dialkyl silanes Chemical group 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 230000001079 digestive effect Effects 0.000 description 1
- 238000010494 dissociation reaction Methods 0.000 description 1
- 230000005593 dissociations Effects 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 230000000857 drug effect Effects 0.000 description 1
- 238000007877 drug screening Methods 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 230000007831 electrophysiology Effects 0.000 description 1
- 238000002001 electrophysiology Methods 0.000 description 1
- 238000001523 electrospinning Methods 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 229940066758 endopeptidases Drugs 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 230000007515 enzymatic degradation Effects 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- ZMMJGEGLRURXTF-UHFFFAOYSA-N ethidium bromide Chemical compound [Br-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CC)=C1C1=CC=CC=C1 ZMMJGEGLRURXTF-UHFFFAOYSA-N 0.000 description 1
- 229960005542 ethidium bromide Drugs 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 238000010304 firing Methods 0.000 description 1
- GNBHRKFJIUUOQI-UHFFFAOYSA-N fluorescein Chemical compound O1C(=O)C2=CC=CC=C2C21C1=CC=C(O)C=C1OC1=CC(O)=CC=C21 GNBHRKFJIUUOQI-UHFFFAOYSA-N 0.000 description 1
- 238000002376 fluorescence recovery after photobleaching Methods 0.000 description 1
- 239000007850 fluorescent dye Substances 0.000 description 1
- 239000003269 fluorescent indicator Substances 0.000 description 1
- 239000012634 fragment Substances 0.000 description 1
- 239000012737 fresh medium Substances 0.000 description 1
- 235000011389 fruit/vegetable juice Nutrition 0.000 description 1
- 238000001641 gel filtration chromatography Methods 0.000 description 1
- 239000007863 gel particle Substances 0.000 description 1
- 235000010492 gellan gum Nutrition 0.000 description 1
- 239000000216 gellan gum Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 210000000020 growth cone Anatomy 0.000 description 1
- 239000003102 growth factor Substances 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 125000004404 heteroalkyl group Chemical group 0.000 description 1
- 125000005842 heteroatom Chemical group 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 229940014041 hyaluronate Drugs 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 1
- 239000001341 hydroxy propyl starch Substances 0.000 description 1
- 235000013828 hydroxypropyl starch Nutrition 0.000 description 1
- 238000005286 illumination Methods 0.000 description 1
- 230000002163 immunogen Effects 0.000 description 1
- 230000005847 immunogenicity Effects 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 230000001976 improved effect Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000010874 in vitro model Methods 0.000 description 1
- 238000010952 in-situ formation Methods 0.000 description 1
- 210000004263 induced pluripotent stem cell Anatomy 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 238000007689 inspection Methods 0.000 description 1
- 102000006495 integrins Human genes 0.000 description 1
- 108010044426 integrins Proteins 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 238000002955 isolation Methods 0.000 description 1
- 230000002147 killing effect Effects 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 108010042502 laminin A Proteins 0.000 description 1
- 125000005647 linker group Chemical group 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- 239000006193 liquid solution Substances 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 210000002901 mesenchymal stem cell Anatomy 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 239000011859 microparticle Substances 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 238000003801 milling Methods 0.000 description 1
- 230000000877 morphologic effect Effects 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 210000003098 myoblast Anatomy 0.000 description 1
- 210000000653 nervous system Anatomy 0.000 description 1
- 210000001178 neural stem cell Anatomy 0.000 description 1
- 230000036403 neuro physiology Effects 0.000 description 1
- 230000004007 neuromodulation Effects 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 239000012299 nitrogen atmosphere Substances 0.000 description 1
- 238000010606 normalization Methods 0.000 description 1
- 238000012758 nuclear staining Methods 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 210000004248 oligodendroglia Anatomy 0.000 description 1
- 238000001543 one-way ANOVA Methods 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 238000012634 optical imaging Methods 0.000 description 1
- 230000010355 oscillation Effects 0.000 description 1
- 230000003204 osmotic effect Effects 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 230000000149 penetrating effect Effects 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- ACVYVLVWPXVTIT-UHFFFAOYSA-M phosphinate Chemical compound [O-][PH2]=O ACVYVLVWPXVTIT-UHFFFAOYSA-M 0.000 description 1
- 229920001983 poloxamer Polymers 0.000 description 1
- 229920000773 poly(2-methyl-2-oxazoline) polymer Polymers 0.000 description 1
- 239000004584 polyacrylic acid Substances 0.000 description 1
- 238000006116 polymerization reaction Methods 0.000 description 1
- 150000004804 polysaccharides Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- XAEFZNCEHLXOMS-UHFFFAOYSA-M potassium benzoate Chemical compound [K+].[O-]C(=O)C1=CC=CC=C1 XAEFZNCEHLXOMS-UHFFFAOYSA-M 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 230000037452 priming Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000000644 propagated effect Effects 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000000751 protein extraction Methods 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- 238000010791 quenching Methods 0.000 description 1
- 230000000171 quenching effect Effects 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 229920005604 random copolymer Polymers 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 239000012047 saturated solution Substances 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 125000000467 secondary amino group Chemical group [H]N([*:1])[*:2] 0.000 description 1
- 238000001338 self-assembly Methods 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 239000012679 serum free medium Substances 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 238000004088 simulation Methods 0.000 description 1
- 210000003491 skin Anatomy 0.000 description 1
- 239000002002 slurry Substances 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 238000012421 spiking Methods 0.000 description 1
- 208000020431 spinal cord injury Diseases 0.000 description 1
- 210000001032 spinal nerve Anatomy 0.000 description 1
- 230000008925 spontaneous activity Effects 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 238000007155 step growth polymerization reaction Methods 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 125000000446 sulfanediyl group Chemical group *S* 0.000 description 1
- 230000000153 supplemental effect Effects 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- WGTODYJZXSJIAG-UHFFFAOYSA-N tetramethylrhodamine chloride Chemical compound [Cl-].C=12C=CC(N(C)C)=CC2=[O+]C2=CC(N(C)C)=CC=C2C=1C1=CC=CC=C1C(O)=O WGTODYJZXSJIAG-UHFFFAOYSA-N 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- OFBPGACXRPVDQW-UHFFFAOYSA-N thiirane 1,1-dioxide Chemical compound O=S1(=O)CC1 OFBPGACXRPVDQW-UHFFFAOYSA-N 0.000 description 1
- 238000001269 time-of-flight mass spectrometry Methods 0.000 description 1
- 230000017423 tissue regeneration Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 230000008733 trauma Effects 0.000 description 1
- 239000012588 trypsin Substances 0.000 description 1
- 229910021642 ultra pure water Inorganic materials 0.000 description 1
- 239000012498 ultrapure water Substances 0.000 description 1
- 231100000747 viability assay Toxicity 0.000 description 1
- 238000003026 viability measurement method Methods 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 239000003932 viscosupplement Substances 0.000 description 1
- 239000000664 voltage gated sodium channel blocking agent Substances 0.000 description 1
- 238000003260 vortexing Methods 0.000 description 1
- UHVMMEOXYDMDKI-JKYCWFKZSA-L zinc;1-(5-cyanopyridin-2-yl)-3-[(1s,2s)-2-(6-fluoro-2-hydroxy-3-propanoylphenyl)cyclopropyl]urea;diacetate Chemical compound [Zn+2].CC([O-])=O.CC([O-])=O.CCC(=O)C1=CC=C(F)C([C@H]2[C@H](C2)NC(=O)NC=2N=CC(=CC=2)C#N)=C1O UHVMMEOXYDMDKI-JKYCWFKZSA-L 0.000 description 1
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/52—Hydrogels or hydrocolloids
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J3/00—Processes of treating or compounding macromolecular substances
- C08J3/02—Making solutions, dispersions, lattices or gels by other methods than by solution, emulsion or suspension polymerisation techniques
- C08J3/03—Making solutions, dispersions, lattices or gels by other methods than by solution, emulsion or suspension polymerisation techniques in aqueous media
- C08J3/075—Macromolecular gels
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/14—Macromolecular materials
- A61L27/18—Macromolecular materials obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/14—Macromolecular materials
- A61L27/20—Polysaccharides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/14—Macromolecular materials
- A61L27/22—Polypeptides or derivatives thereof, e.g. degradation products
- A61L27/227—Other specific proteins or polypeptides not covered by A61L27/222, A61L27/225 or A61L27/24
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/14—Macromolecular materials
- A61L27/26—Mixtures of macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/36—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix
- A61L27/38—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells
- A61L27/3804—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells characterised by specific cells or progenitors thereof, e.g. fibroblasts, connective tissue cells, kidney cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/50—Materials characterised by their function or physical properties, e.g. injectable or lubricating compositions, shape-memory materials, surface modified materials
- A61L27/56—Porous materials, e.g. foams or sponges
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/04—Drugs for skeletal disorders for non-specific disorders of the connective tissue
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G65/00—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule
- C08G65/02—Macromolecular compounds obtained by reactions forming an ether link in the main chain of the macromolecule from cyclic ethers by opening of the heterocyclic ring
- C08G65/32—Polymers modified by chemical after-treatment
- C08G65/329—Polymers modified by chemical after-treatment with organic compounds
- C08G65/331—Polymers modified by chemical after-treatment with organic compounds containing oxygen
- C08G65/332—Polymers modified by chemical after-treatment with organic compounds containing oxygen containing carboxyl groups, or halides, or esters thereof
- C08G65/3322—Polymers modified by chemical after-treatment with organic compounds containing oxygen containing carboxyl groups, or halides, or esters thereof acyclic
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J9/00—Working-up of macromolecular substances to porous or cellular articles or materials; After-treatment thereof
- C08J9/28—Working-up of macromolecular substances to porous or cellular articles or materials; After-treatment thereof by elimination of a liquid phase from a macromolecular composition or article, e.g. drying of coagulum
- C08J9/286—Working-up of macromolecular substances to porous or cellular articles or materials; After-treatment thereof by elimination of a liquid phase from a macromolecular composition or article, e.g. drying of coagulum the liquid phase being a solvent for the monomers but not for the resulting macromolecular composition, i.e. macroporous or macroreticular polymers
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L5/00—Compositions of polysaccharides or of their derivatives not provided for in groups C08L1/00 or C08L3/00
- C08L5/02—Dextran; Derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L5/00—Compositions of polysaccharides or of their derivatives not provided for in groups C08L1/00 or C08L3/00
- C08L5/08—Chitin; Chondroitin sulfate; Hyaluronic acid; Derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L53/00—Compositions of block copolymers containing at least one sequence of a polymer obtained by reactions only involving carbon-to-carbon unsaturated bonds; Compositions of derivatives of such polymers
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L71/00—Compositions of polyethers obtained by reactions forming an ether link in the main chain; Compositions of derivatives of such polymers
- C08L71/02—Polyalkylene oxides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L71/00—Compositions of polyethers obtained by reactions forming an ether link in the main chain; Compositions of derivatives of such polymers
- C08L71/08—Polyethers derived from hydroxy compounds or from their metallic derivatives
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L79/00—Compositions of macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing nitrogen with or without oxygen or carbon only, not provided for in groups C08L61/00 - C08L77/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2400/00—Materials characterised by their function or physical properties
- A61L2400/06—Flowable or injectable implant compositions
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J2371/00—Characterised by the use of polyethers obtained by reactions forming an ether link in the main chain; Derivatives of such polymers
- C08J2371/02—Polyalkylene oxides
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J2405/00—Characterised by the use of polysaccharides or of their derivatives not provided for in groups C08J2401/00 or C08J2403/00
- C08J2405/02—Dextran; Derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J2405/00—Characterised by the use of polysaccharides or of their derivatives not provided for in groups C08J2401/00 or C08J2403/00
- C08J2405/08—Chitin; Chondroitin sulfate; Hyaluronic acid; Derivatives thereof
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L2201/00—Properties
- C08L2201/54—Aqueous solutions or dispersions
Abstract
本发明涉及可注射大孔水凝胶,并且还涉及生成大孔水凝胶的方法。在第一步,产生两种溶质的水性溶液。所述第一溶质是可以交联的聚合物,并且是聚乙二醇(PEG)或聚噁唑啉(POx)的衍生物,所述第二溶质是有序构造性试剂。在第二步,向溶液添加交联剂。这同时引发所述聚合物的胶凝和相分离,由此生成大孔水凝胶。本发明还涉及大孔水凝胶,其能够通过本发明方法获得。该大孔水凝胶由交联聚合物组成,交联聚合物是聚乙二醇(PEG)或聚噁唑啉(POx)的衍生物。所述水凝胶展现出尺寸为200nm至1000μm、特别是500nm至100μm的互连大孔,并且特征在于pH是7.0至8.0,特别是约7.4。
Description
本申请是分案申请,其原申请的国际申请号是PCT/EP2016/071238,国际申请日是2016年09月08日,中国国家申请号为201680051583.8,进入中国的日期为2018年03月06日,发明名称为“可注射大孔水凝胶”。
技术领域
本发明涉及大孔(macroporous)水凝胶及其在组织工程化和再生药品中的用途。
背景技术
大孔水凝胶在组织工程化领域是重要的,因为它们在机械性质、稳定性、分子扩散/传输性质和细胞侵入方面比均质材料具有重要优势。但是,已经建立的形成大孔水凝胶的方法(盐浸提、冷冻干燥、气囊形成)通常需要在苛刻的条件下先进行材料的模板化,然后进行细胞接种;并且它们不是可注射的,这在最终植入患者内时导致更多的创伤。报道用于产生细胞相容性的可注射水凝胶的少数方法(例如微粒融合、或牺牲性致孔剂包含和降解)分别具有非常繁重的预处理步骤,以形成凝胶颗粒,或由于缓慢的致孔剂降解而导致缓慢的孔形成。它们对可获得的孔径也具有有限的控制。也已经使用两相系统来生产多孔凝胶,但不能在与可注射性和细胞包封相容的条件下进行。
本发明的目的在于改进现有技术并提供用于再生药品的可注射的组织相容性大孔水凝胶。该目的通过独立权利要求的主题而实现。
术语和定义
在本说明书的上下文中,术语“聚噁唑啉(POx)”是指噁唑啉或噁嗪的烷基衍生物(特别是经甲基、乙基或丙基取代)的聚合物。
在本说明书的上下文中,“聚乙二醇(PEG)”是指通式H-(O-CH2-CH2)n-OH(CAS编号25322-68-3)的聚合物。
在本说明书的上下文中,术语“星形PEG/POx”是指支化聚合物,其由与中央核心链接的数个(大于3)线性PEG/Pox链组成。聚合物的核心可以是单个原子、分子或大分子。连接聚乙二醇或聚烷基噁唑啉链特别常见的是季戊四醇(CAS 115-77-5)、2-羟甲基-1,3-丙二醇(CAS 4704-94-3)、二季戊四醇(CAS126-58-9)、三季戊四醇(CAS78-24-0)、甘油、四(溴甲基)亚乙基(CAS 30432-16-7)、1,3,5-三溴苯基、1,3,5-三羟基苯基、硅和二烷基硅烷部分。
在本说明书的上下文中,术语“透明质素”(或其同义词透明质酸或透明质酸盐/酯)缩写为HA,是指以下述通式的交替β-1,3和β-1,4键包含D-葡糖醛酸部分和N-乙酰葡糖胺部分的重复单元的聚合物
重复单元的分子量为379g/mol。体内的透明质素可以超过每摩尔2500个重复单元。透明质素标注为CAS编号9004-61-9(酸)、9067-32-7(钠盐)和31700-91-4(钾盐)。
“甘露糖醛酸(MA)”是指通过(1-4)键连接的β-D-甘露糖醛酸残基的线性聚合物(CAS编号6814-36-4)。
应当理解的是,当在本文中使用时,用于本文所述的任何聚合物的术语聚合物可以表示所提及单体的聚合物,其中一部分单体被反应性基团取代以允许交联。
分子量值(数均分子量)在本文中用于定义聚合物或其它大分子时,除非另外指出,是使用用于校准的同一聚合物的近似单分散标准品通过凝胶渗透色谱(GPC)确定的,详细地如描述于Andre Striegel,Wallace W.Yau,Joseph J.Kirkland和Donald D.Bly,“Modern Size-Exclusion Liquid Chromatography:Practice of Gel Permeation andGel Filtration Chromatography”,John Wiley&Sons,2009。标准品的质量使用基质辅助激光吸附/离子化飞行时间质谱(MALDI-TOF)测量。
在本说明书的上下文中,术语“有序构造性(kosmotropic)试剂”是指在水性溶液中可以与PEG或Pox的水性溶液形成两相体系的任何试剂。
发明内容
根据本发明,提供了一种提供大孔凝胶的方法,所述方法包括下述步骤:
a)提供包含第一溶质和第二溶质的水性溶液,其中所述第一溶质是选自聚乙二醇(PEG)的可交联衍生物和聚噁唑啉(POx)的可交联衍生物的可交联聚合物;并且所述第二溶质是有序构造性试剂;和
b)向该混合物添加能够交联所述可交联聚合物的交联剂,由此同时引发所述可交联聚合物的胶凝和相分离。
在一些实施方式中,所述可交联聚合物选自:包含星形聚乙二醇、聚乙二醇二嵌段共聚物和聚乙二醇三嵌段共聚物的组;或包含聚甲基噁唑啉、聚乙基噁唑啉、聚丙基噁唑啉和聚丁基噁唑啉的组;或包含星形聚噁唑啉和噁唑啉共聚物、特别是2-甲基噁唑啉和2-乙基噁唑啉与含有噁唑啉的羧酸或醇(特别是2-羧乙基噁唑啉或2-羟乙基噁唑啉)的共聚物的组;或包含部分水解的聚2-甲基噁唑啉或聚2-乙基噁唑啉的组。
在一些实施方式中,可交联聚合物是线性聚乙二醇。
在一些实施方式中,可交联聚合物是星形聚乙二醇,其具有季戊四醇核,分子量为10kg/mol至40kg/mol,特别是约20kg/mol(例如Sigma产品编号JKA7025)。在一些实施方式中,可交联聚合物是10kg/mol至40kg/mol的星形聚乙二醇,其具有二季戊四醇核(例如Sigma产品编号JKA10034)。在一些实施方式中,可交联聚合物是具有甘油核的星形聚乙二醇。
在一些实施方式中,可交联聚合物是聚乙二醇二嵌段共聚物,其包含聚乙二醇与聚乙烯(PE)或聚丙交酯(PLA)或聚丙交酯-co-乙交酯(PLGA)或聚-ε-己内酯(PCL)和聚苯乙烯的共聚物。
在一些实施方式中,可交联聚合物是聚乙二醇三嵌段共聚物,其包含聚乙二醇与聚丙二醇(PPG)的共聚物或者聚乙二醇与聚丙交酯-co-乙交酯(PLGA)的共聚物。
在一些实施方式中,可交联聚合物是聚乙二醇共聚物,其包含至少50%PEG和选自PCL、PPG和PLGA中的至少一种其它聚合物。
在一些实施方式中,可交联聚合物是包含甲基噁唑啉或乙基噁唑啉与羧乙基噁唑啉的无规共聚物的聚噁唑啉,并且羧酸取代有反应性部分,特别是取代有一个或多个选自由下述组成的组的反应性部分:硫醇、乙烯基砜、马来酰亚胺、转谷氨酰胺酶底物肽、酪胺、多巴胺、丙烯酸酯、甲基丙烯酸酯、乙烯基酯、炔、叠氮化物、醛和丙烯酰胺,所述反应性部分更特别选自由下述组成的组:硫醇、乙烯基砜、马来酰亚胺、丙烯酸酯和甲基丙烯酸酯。
在一些实施方式中,可交联聚合物是由四(溴甲基)亚乙基引发剂聚合的星形聚噁唑啉。在一些实施方式中,可交联聚合物是由1,3,5-三溴苯基引发剂聚合的星形聚噁唑啉。
在一些实施方式中,本文提及的任何星形聚噁唑啉聚合物以羟基、氨基或羧酸基团封端,在某些进一步的实施方案中,其进一步取代有一个或多个如本文所述的反应性部分,特别选自硫醇、乙烯基砜、马来酰亚胺、转谷氨酰胺酶底物肽、酪胺、多巴胺、丙烯酸酯、甲基丙烯酸酯、乙烯基酯、炔、叠氮化物、醛和丙烯酰胺。在一些替代性实施方式中,通过用所需的可交联基团猝灭噁唑啉聚合,从而将星形聚噁唑啉直接以反应性部分封端。
在一些实施方式中,通过在酸或碱的存在下在水中煮沸,使线性聚噁唑啉部分水解以除去其1%至40%的侧链(例如从聚(2-甲基-2-噁唑啉)释放乙酸酯),并且所释放的仲胺取代有反应性部分。
在一些实施方式中,可交联聚合物包含反应性部分,反应性部分选自包含下述的组:丙烯酸酯、甲基丙烯酸酯、丙烯酰胺、乙烯基酯、马来酰亚胺、乙烯基砜、炔、叠氮化物、醛、酪胺、多巴胺和巯基部分。反应性部分添加在星形聚合物链的末端,或者添加在线性聚合物的约5%至25%的侧链上。
在一些实施方式中,可交联聚合物包含转谷氨酰胺酶底物肽作为反应性部分,特别是凝血因子XIII底物肽,更特别是含有序列FKGG和NQEQVSPL的肽。
在一些实施方式中,可交联聚合物经乙烯基砜改性,并且所述交联剂是包含两个巯基(-SH)部分的短接头分子,特别是包含由含有2至10个碳原子或杂原子的烷基或杂烷基链隔开的两个SH基团的分子;或含有两个半胱氨酸氨基酸构成嵌段(building block)的肽。
在一些实施方式中,可交联聚合物经乙烯基砜改性,并且所述交联剂选自包含下述的组:取代有巯基部分、特别是伯巯基部分的亲水性聚合物,特别是包含伯巯基(-CH2SH)部分的星形聚乙二醇或包含伯巯基(-CH2SH)部分的线性聚乙二醇;和含有2至100个、特别是2至20个、更特别是4至16个氨基酸的肽,其中两个所述氨基酸是半胱氨酸;特别是适合被内肽酶、更特别是基质金属蛋白酶切割的肽,还更特别是氨基酸序列为GCRD-GPQGIWGQ-DRCG或GCRE-GPQGIAGQ-ERCG的肽。
在一些实施方式中,可交联聚合物的分子量为1000g/mol至1000000g/mol,特别是10000g/mol至40000g/mol。
在一些实施方式中,可交联聚合物是线性聚合物,长度为50至1000个单体,长度特别是75至500个单体、还更特别是100至300个单体、最优选150个单体。
在一些实施方式中,水性溶液中可交联聚合物的浓度为0.2%(w/v)至50%(w/v),特别是0.5%(w/v)至10%(w/v)。
在一些实施方式中,水性溶液包含0.5%(w/v)至3%(w/v)的所述聚乙二醇的可交联衍生物或1%(w/v)至10%(w/v)的所述聚噁唑啉的可交联衍生物。
在一些实施方式中,有序构造性试剂选自包含多糖、聚电解质和金属(特别是碱金属和碱土金属)碳酸盐、硫酸盐、硫代硫酸盐和磷酸二氢盐的组。
在一些实施方式中,有序构造性试剂是多糖,特别是选自包含透明质素、甘露糖醛酸、角叉菜胶、肝素、硫酸软骨素、葡聚糖、羟丙基葡聚糖、果胶、藻酸盐、结冷胶、纤维素、甲基纤维素、乙基纤维素、乙酸纤维素酯、淀粉、羟丙基淀粉的组,并且其中特别是所述多糖的特征在于分子量为1000g/mol至10000000g/mol,更特别是10000g/mol至2000000g/mol,还更特别是100000g/mol至1000000g/mol,还更特别是约150000g/mol。
在一些实施方式中,水性溶液中多糖的浓度是0.1%(w/v)至50%(w/v),特别是0.1(w/v)至5%,还更特别是0.35(w/v)至0.5%(w/v)。
在一些实施方式中,水性溶液包含0.1%至1%的透明质素、特别是约0.4%的透明质素,或者0.5%至5%的甘露糖醛酸、特别是约2%的甘露糖醛酸,或者0.1%至10%的葡聚糖,或者其混合物。
在一些实施方式中,有序构造性试剂是特征在于分子量为1000g/mol至10000000/mol、特别是10000g/mol至100000g/mol的聚电解质,特别是聚乙烯亚胺或聚丙烯酸。
在一些实施方式中,可交联聚合物是20000g/mol的4臂-PEG-乙烯基砜,多糖是甘露糖醛酸,交联剂是基质金属蛋白酶可切割肽,特别是包含氨基酸序列GPQGIWGQ的肽。在一些实施方式中,可交联聚合物是20000g/mol的4臂-PEG-乙烯基砜,多糖是甘露糖醛酸,交联剂是肽GCRD-GPQGIWGQ-DRCG。
在一些实施方式中,可交联聚合物是丙烯酸酯、甲基丙烯酸酯、丙烯酰胺、乙烯基酯或马来酰亚胺衍生物,并且使用自由基引发剂来在加热或暴露于光下时触发胶凝。特别是在光触发的自由基引发剂存在下的1kg/mol至10kg/mol的线性PEG-二丙烯酸酯或PEG-二甲基丙烯酸酯,或者1kg/mol至10kg/mol的POx-二丙烯酸酯或POx-二甲基丙烯酸酯。
在一些实施方式中,自由基引发剂是浓度为0.01%(w/v)至1%(w/v)、特别是0.025%(w/v)至0.1%(w/v)的Irgacure 2959,并且使用蓝光至近紫外光、特别是约365nm和10mW/cm2的光来触发交联。
在一些实施方式中,,自由基引发剂是2,2-二甲基-2-苯基-苯乙酮(特别是在N-乙烯基吡咯烷酮的存在下),或者在胺(诸如在N-乙烯基吡咯烷酮的存在下的三乙醇胺)的存在下的酰基次膦酸锂或孟加拉玫瑰红(rose bengale)。
在一些实施方式中,可交联聚合物是转谷氨酰胺酶底物肽衍生物,并且添加转谷氨酰胺酶以触发胶凝。特别地,通过加入活化的转谷氨酰胺酶凝血因子XIII使以含有序列FKGG和NQEQVSPL的肽封端的星形PEG交联。
在一些实施方式中,可交联聚合物是酪胺或多巴胺衍生物,并且使用辣根过氧化物酶和过氧化氢来触发交联。作为另外的选择,或者将诸如孟加拉玫瑰红、曙红-Y、亚甲蓝或核黄素等感光性单线态氧引发剂与在可见光或近紫外线中的可见光暴露组合使用。特别地,使用浓度为1μmol/L~100μmol/L的核黄素和浓度为0.01%%(w/v)至1%(w/v)的孟加拉玫瑰红、曙红-Y或亚甲蓝,并将其暴露至近紫外线/可见光以触发胶凝。将0.1单位/mL至10单位/mL的辣根过氧化物酶与0.01mmol/L~1mmol/L过氧化氢一起使用,特别是将1单位/mL辣根过氧化物酶与0.1mmol/L过氧化氢一起使用。
在一些实施方式中,水性溶液的特征在于pH是7.0~8.0,特别是约7.4;并且所述交联剂的添加发生在20℃至40℃,特别是约37℃。
在一些实施方式中,在交联之前向水性溶液添加细胞,特别是哺乳动物细胞。
在一些实施方式中,添加交联剂后10秒至15分钟使水性混合物通过注射器,和/或添加交联剂后约1~60分钟观察到固体大孔凝胶。
在一些实施方式中,将交联剂和可交联聚合物分别装载入双筒注射器中,而有序构造性试剂在任一侧,注射时将两个筒混合,从而导致在1分钟至30分钟后形成固体大孔凝胶。
根据本发明的第二方面,提供大孔水凝胶,其特征在于,其由交联聚合物组成,其中所述交联聚合物是聚乙二醇的衍生物或聚噁唑啉的衍生物;和其展现出特征在于尺寸为200nm至1000μm、特别是特征在于500nm至100μm的互连大孔;并且所述凝胶的特征进一步在于pH是7.0至8.0,特别是约7.4。
在一些实施方式中,所述凝胶由作为可交联聚合物的任一种上述聚合物制成。
在一些实施方式中,大孔水凝胶是透明的;并且其刚度为1Pa~500000Pa,特别是10Pa~10000Pa,特别是10Pa~1000Pa,还更特别是50Pa~500Pa。
在一些实施方式中,大孔水凝胶包含活细胞。
在一些实施方式中,大孔水凝胶包含含有功能性、突触连接的神经突的神经元。
在一些实施方式中,将大孔水凝胶用于治疗神经或脊髓损伤的方法中,其中将所述凝胶移植在损伤部位或使其在损伤部位原位胶凝,可以使用或不使用额外的支撑导管。
在一些实施方式中,使用大孔水凝胶来支持组织再生。特别地,将大孔水凝胶在具有或不具有细胞的情况下预培养并移植,或者将大孔水凝胶在具有或不具有细胞的情况下在损伤部位原位胶凝以支持再生。更特别地,将神经元、神经干细胞、神经祖细胞、星形胶质细胞、少突胶质细胞、成纤维细胞、内皮细胞、骨细胞、软骨细胞、间充质干细胞或成肌细胞包封在凝胶中,将凝胶递送至神经、脊髓、皮肤、骨、软骨或椎间盘中。
附图说明
图1.高粘度多糖与PEG形成两相体系,这产生多孔凝胶。(a)无多糖下胶凝的对照的CLSM成像。该结构是完全均匀的,并且在185nm的分辨率下没有孔。(b)在0.35%(w/v)的高粘度HA存在下形成的1.5%PEG具有0.5μm至1.5μm的多孔结构。(c)在1.4%(w/v)的高粘度MA存在下形成的1.5%PEG具有数微米的多孔结构。(d)多孔网络的三维检查显示孔是完全互连的。(e)孔的自相关函数。相关函数的圆对称性表明多孔网络是各向同性的。(f)因此自相关函数可以仅作为半径的函数分析。显示了两种类型的多孔凝胶的实验数据(虚线)以及它们与可穿透球模型(线)的拟合。对于HA而言孔直径为0.82+/-0.1μm获得最佳拟合,对于MA而言孔直径为2.39+/-0.16μm获得最佳拟合。误差棒:标准偏差(n=3)。(a-c)来自共聚焦显微镜的单个切片。(d)凝胶中25μm立方体的渲染。比例尺:5μm。
图2.体积排阻增强了用Michael加成的PEG胶凝的动力学。(a)凝胶的流变学监测。HA补充使凝胶能够在生理pH下形成,具有与在pH8.0下用纯PEG凝胶获得的动力学几乎相同的动力学。(b)在37℃于完全生长培养基中HA和MA原液的复数粘度。(c)胶凝时间。较高的PEG含量或pH导致较快的胶凝,如以粘性HA原液代替胶凝介质那样。给出Q-凝胶作为市售PEG凝胶的参考。(d)凝胶形成60分钟后的刚度(初始平稳)。1.2%至1.9%(w/v)的PEG浓度跨越了与发育中的神经系统有关的刚度范围,其假定为提供轴突生长的最佳条件。在胶凝10分钟后也显示Q-凝胶刚度,因为这是制造商推荐添加介质的时间。误差棒:标准偏差(n=3)。
图3.不可降解的大孔PEG凝胶中的背根神经节(DRGs)。(a)培养30天后的整体凝胶成像显示被来自DRG中的轴突完全侵入(中心中的簇,荧光成像1.5mm最大强度投影(MIP))。(b)显示高神经突密度的中心特写(顶视图,1.5毫米MIP)。(c)先前显示神经突的侧视图分布在凝胶的整个深度(1.5mm MIP)。DRG的位置是突出显示的,因为只有其下表面是可见的,其剩余部分和后面的锥体中的神经突不易接近光并且看起来黑。(d)DRG横截面的活/死成像。死细胞的冠冕是可见的,但内部细胞是活的。比例尺:1mm(a)250μm(b)250μm(c)125μm(d)。
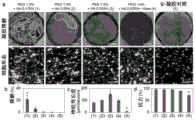
图4.用HA进行微结构化改善了软凝胶的稳定性,并允许快速的神经突向外生长,在pH7.4时形成凝胶和高活力。透明质素可以在胶凝后被去除而不杀死神经元,降解凝胶或防止神经突向外生长。(a)在第2天的明视野中看到的宏观凝胶降解,白色突出显示降解部分和绿色为PDMS支持体,以及如通过荧光显微镜(200μm堆叠的投影)看到的神经元形态的特写。不使用HA形成的PEG1.5%凝胶未显示,因为它们在2天内不稳定,因此不能定量。染色是钙黄绿素/DAPI(1至3)和βIII-微管蛋白/DAPI(4和5)。两种方法都能染色所有神经突/细胞体,但部分降解的凝胶不能经受免疫染色,所以细胞形态直接成像在经钙黄绿素染色的活样品上。(b)在第2天宏观降解相对于凝胶面积的百分比。(c)在第2天总神经突长度除以样品体积中的细胞体数量。(d)在第2天的活力。误差棒:标准偏差(对于降解n=6,对于活力和神经突长度n=3)。*:不同于所有其它条件(p<0.01)。其他是可比的(p>0.01)。比例尺:1mm(第一行)和25μm(第二行)。
图5.包封在多孔PEG凝胶中的来自E17大鼠胚胎的原代皮质神经元形成长期稳定的电活性三维神经网络。(a)具有颜色编码深度的200微米MIPs显示,包封的神经元均匀分布,并使三维形式的神经突延伸通过基质。包封后两天已经可见长神经突,以增加的速率继续生长,从而至第5天形成密集网络。到第26天,整个凝胶充满了密集的神经突网络。(b)免疫细胞化学标记物(来自双光子激光扫描显微镜堆叠采集的200μm MIPs):βIII-微管蛋白是染色胚胎神经元的所有神经突的中性标记物,突触结合蛋白是突触前末梢的标记物,MAP2是此时已知仅染色细胞体和近端神经突的分化神经元标记物。(c)用细胞内钙离子荧光报道物俄勒冈绿BAPTA-1观察凝胶中的尖峰活性。观察到独立的自发活性(例如细胞体1至3)以及同步活性(10s时的细胞体5至11),证明在合成ECM中通过16天建立了功能性突触连接网络。比例尺:100μm,200μm颜色编码深度(a)和50μm(b,c)。
图6.该方法翻译成人iPSC衍生神经元。(a)在第2天(200μm MIP)通过双光子激发荧光显微镜(Calcein/Hoechst)在D2(200μmMIP)看到的在利用0.525%HA微结构化的PEG凝胶中细胞密度和刚度对细胞形态的影响。(b-c)活力和神经突向外生长在高刚度或低细胞密度下受损。(d)在第5天凝胶的定性描述:较软的凝胶和较高的细胞密度导致更快的降解,产生在最极端的组合中不稳定的凝胶。(e)免疫细胞化学。实际上,所有活细胞对于神经元标记物神经丝、βIII-微管蛋白和MAP2都是阳性的,并且对于星形细胞标记物GFAP是阴性的。误差棒:标准偏差(n=3)。*统计学上不同于其他所有条件(p<0.01)。否则为p>0.01。比例尺:40μm。
图7.监测胶凝过程中的相分离。样品是在MA 2%(w/v)存在下使用PEG-二硫醇作为交联剂于室温(比文章其它部分使用的37℃慢)胶凝的经TMR标记的PEG 1.5%(w/v),用CLSM成像。标出混合后时间。比例尺:5μm。
图8.如差分干涉对比(DIC)中所看到的凝胶透明度。(a)很难在形成后立即将凝胶与水区别开。(b)除了在神经元包封两周半之后的一些散在的细胞碎片之外,凝胶仍然是完全透明的。比例尺:50μm。
图9.典型的胶凝曲线以及本工作中使用的刚度和胶凝时间定义。初始刚度被认为是60分钟时的刚度,此时的刚度接近平稳水平,并且加入培养基以停止胶凝并进行细胞培养。胶凝时间被认为是储存模量在对数标度上达到最大值的一半时的时间——由于待比较样品的粘度非常不同(因此损耗模量不同),因此该定义相对于储存模量和损耗模量交叉的时间是优选的。该曲线是在HA 0.525%(w/v)存在下胶凝的PEG 1.9%。
图10.透明质酸降解监测。透明质酸在补充有1mg/ml HAse的培养基中迅速降解,这使其能够从多孔PEG凝胶中除去。误差棒:标准偏差(n=3)。
图11.当在三维培养中使用优化的机械条件时,不需要粘附肽。(a)IKVAV肽以剂量依赖性方式促进组织培养塑料(TCP)上的细胞粘附和神经突延伸。(b)多孔PEG凝胶中的神经突向外生长即使在高浓度(显示100μM)下,在不存在和存在IKVAV时也是相似的,与用于产生孔的多糖无关。注意由MA产生的大孔中的神经元所采用的畸形形态。比例尺:40μm。
图12.PEG成分与神经元的相互作用。(a)非常高分子量的PEG不能用作粘性补充剂,因为它立即引起悬浮液的神经元成簇。(b)用于凝胶形成的官能化高分子量星形PEG由神经元摄取,如使用经TMR标记的变体所看出的。比例尺:50μm。
图13.来自在多孔不可降解性PEG凝胶中的经包封皮层神经元的神经突向外生长。神经突向外生长即使在MMP可切割肽的不存在下也会发生,即使活力降低。这也作为MMP-可切割肽在其余工作中不用于粘附的对照,因为这些凝胶仅在MA存在下与PEG-二硫醇交联。200μm MIP,比例尺:50μm。
图14.从βIII-微管蛋白双光子成像定量神经突向外生长。(a)在包封2天和5天后神经突向外生长。在HA微结构化的存在下,在超过一个数量级(20Pa至250Pa)上未看到强的刚度依赖性,只有较软的凝胶由于部分降解而具有降低的神经突向外生长。在未微结构化下、由较高pH值的多糖替换体积排阻的加速效果的情况下制造的凝胶,在第一天内降解(降解时发生灰色交叉)。Q-凝胶用作自由浮动凝胶(经典方案)和用作支持凝胶(与本发明的方案相同的模具)的参考。误差棒:SEM(n=3)。
图15显示大孔凝胶的稳定性增加是由于交联聚合物含量较低时的稳定性,而不是较高的酶降解抗性。a)大孔凝胶被蛋白酶以与非大孔凝胶类似的速率降解(对于大孔凝胶,在0.525%(w/v)的1.6kg/mol透明质素的存在下,通过亚乙基砜上硫醇的迈克尔加成,20kg/mol 1.5%(w/v)的4臂PEG-乙烯基砜与MMP-敏感性肽ERCG-GPQGIWGQ-GCRE交联。消化液为在磷酸盐缓冲液中0.5mg/ml的木瓜蛋白酶+1mg/ml牛血清白蛋白。反应通过用于压痕的纹理分析仪监测,压痕模量被标准化为每次测量的初始压痕模量)。误差棒:来自n=3的标准偏差。b)大孔凝胶在交联聚合物含量低于正常凝胶时保持稳定(在图例中指出的重量/体积为20kg/mol的4臂PEG-乙烯基砜,与3.8kg/mol的PEG-二硫醇交联。在另外存在0.5%(w/v)透明质素和1%(w/v)葡聚糖的存在下形成大孔凝胶。在用1mg/ml透明质酸酶的PBS溶液然后超纯水各自洗涤盐和未结合的聚合物1天并且冻干后测量凝胶的干质量)。误差棒:n=11至16的平均值的标准偏差。
图16显示PEG凝胶中的大分子平衡浓度低于上清液中的大分子平衡浓度,但是大孔凝胶使得大分子在孔中达到完全浓度,这使得它们最终可用于凝胶中深度包封的细胞。A)由1.5%(w/v)的20kg/mol的4臂-PEG-VS和3.8kg/mol的PEG-二硫醇交联剂形成的PEG凝胶浸入经荧光标记的中性链亲和素溶液中,将PEG凝胶内中性链亲和素的浓度与上清液中的浓度进行比较,并从各自的荧光强度测量孔。在荧光图像下标出浓度比,显示底部的凝胶和顶部的上清液。B)荧光标记的琥珀酰化壳聚糖也是如此。C)500kg/mol的经荧光标记的葡聚糖也是如此。
图17显示可以通过使用透明质素补充剂来增加粘度和使用不同量的葡聚糖以增加PEG从多糖相的斥力来形成具有可调孔径的大孔PEG凝胶。在图中证明形成孔径大小范围从小于1微米到大于50微米的大孔PEG凝胶(在上述荧光显微照片上标出的多糖的存在下1.5%(w/v)的20kg/mol的4臂-PEG-乙烯基砜与3.8kg/mol的PEG-二硫醇交联。荧光标签与PEG聚合物结合以可视化。
图18显示了与乙烯基砜上的硫醇的迈克尔加成相比,用其他交联化学方法形成的大孔PEG凝胶。即使由特定多糖浓度产生的孔径不同,该方法的原理仍然是相同的。转谷氨酰胺酶交联的PEG在此由PEG凝胶说明,所述PEG凝胶由被肽末端官能化的20kg/mol的4臂-PEG前体形成,所述肽是转谷氨酰胺酶活化的血液凝固因子XIII的底物(FKGG-ERCG andNQEQVSPL-ERCG)。
将分子量为10kg/mol的线性PEG-二丙烯酸酯以10%(w/v)溶解于水性缓冲液(葡萄糖100mmol/L,TRIS 50mmol/L,钙50mmol/L)中。分子量为450-550kg/mol的葡聚糖以5%(w/v)溶解在相同的缓冲液中。将可光活化的自由基引发剂Irgacure 2959以0.2%(w/v)溶解在相同的缓冲液中。然后将该溶液与40μl PEG溶液、40μl葡聚糖溶液和10μl Irgacure2959溶液合并。该混合物是一种清澈的均匀溶液,将其置于两个间隔1mm的盖玻片之间,并暴露至光强度为约10mW/cm^2的365nm紫外线10分钟以进行交联。为了评估孔形成,将所得水凝胶在4-甲基7-硫代香豆素的饱和溶液中温育20分钟,所述4-甲基7-硫代香豆素与少量未反应的丙烯酸酯基团反应,由此用蓝色荧光标记PEG。荧光多孔PEG凝胶用双光子激发荧光在710nm激发和400-500nm光收集下成像,显示三维结构化的均匀多孔结构。
在活化因子XIII和钙存在下,4臂-PEG前体交联成凝胶。PEG-二丙烯酸酯的自由基聚合在此用10kg/mol的PEG-二丙烯酸酯(末端官能化的)和使用0.025%(w/v)的Irgacure2959作为在365nmUV照射下活化的自由基引发剂进行说明。透明质素(HA)和葡聚糖用于制造大孔。使用配备有差分干涉对比度(DIC)滤光片的显微镜获取图像。比例尺:10微米。
图19显示了通过迈克尔加成形成的大孔聚噁唑啉水凝胶,对其荧光标记,并使用双光子激发荧光激光扫描共聚焦显微镜成像。
使用93%2-乙基-2-噁唑啉和7%2-羧乙基2-噁唑啉的150单位长的共聚物作为原料。这是一种线性聚2-乙基-2-噁唑啉,其含有用于引入可交联部分的羧酸。通过对羧酸酯进行标准EDC活化而获得含硫醇衍生物,以用于与2倍过量的3,3'-二硫代双(丙酸二酰肼)(DTPHY)在pH4.5的300mM MES缓冲液中反应,然后用10倍过量的三羧乙基膦(TCEP)还原,接着透析和冻干。通过使硫醇衍生物与50倍过量的二乙烯基砜在三乙醇胺缓冲液(pH8.0)中在氮气气氛下反应1小时,然后透析和冷冻干燥,而获得乙烯基砜衍生物。
将聚(2-乙基-2-噁唑啉)的硫代衍生物和乙烯基砜衍生物以10%(w/v)分别重悬浮于mQ水和300mM三乙醇胺缓冲液(pH8.0)中。将分子量1000至2000kg/mol的透明质素以7.5mg/ml溶于相同的缓冲液中。将溶液合并,每种聚噁唑啉衍生物20μl用于40μl透明质素溶液。为了使多孔结构可视化,可以在乙烯基砜官能化的聚噁唑啉上预先反应少量的缀合有荧光香豆素的硫醇。充分混合后,将通过迈克尔加成进行的胶凝在室温下静置以继续1小时,并且在扫描共聚焦荧光显微镜上将经荧光标记的大孔聚噁唑啉水凝胶成像。
图20显示了包封在PEG凝胶中的大鼠皮质神经元中测量的钙尖峰活性是由于神经元的谷氨酸能激发和动作电位启动导致的,因为它们被谷氨酸能传递抑制剂d,l-3[(±)-2-羧基哌嗪-4-基]-丙基-1-膦酸(CPP)和6-氰基-7-硝基喹喔啉-2,3-二酮(CNQX)和被电压门控钠通道抑制剂河豚毒素(TTX)抑制。在宽视野显微镜中在用5x物镜获得的90s荧光视频的视野中,对在荧光指示剂俄勒冈州绿BAPTA-1报告的钙尖峰计数。
具体实施方式
在本发明中,提供了两种溶质的水溶液。已知这两种溶质能够形成水性两相体系。两种溶质的浓度没有高至足以产生相分离,因此它们最初是可混溶的。两种溶质中的一种是聚合物,然后其进行化学交联,这意味着聚合物分子量随时间增加,导致凝胶形成。但是在该过程中,分子量的增加触发相分离,在大多数情况下更高的分子量促进相分离。这导致胶凝过程期间的动态孔形成。该过程与注射至动物或患者以及与细胞包封相容。在典型的实施方式中,星形聚乙二醇(PEG)或者聚甲基-或聚乙基-噁唑啉(POx)用乙烯基砜改性并用作可交联聚合物,所述可交联聚合物将在交联剂(含有两个以上巯基的分子)存在下形成凝胶相。第二溶质是有序构造性试剂,其可以与PEG和Pox一起形成水性两相体系。第二溶质可以是多糖,例如透明质素、甘露糖醛酸和葡聚糖,或者它可以选自包含金属(特别是碱金属和碱土金属)碳酸盐、硫酸盐、硫代硫酸盐和磷酸二氢盐的组。也可以将数种PEG/Pox衍生物或数种有序构造性试剂组合。将这三种组分混合在一起,最初形成均匀的溶液。该混合物可以用于使细胞悬浮,并且可以将其注射或放入模具中成型或放在细胞培养支持物上,因为其是均匀的液体溶液。随着交联的进行,触发相分离,具有富交联聚合物(PEG/POx)相和富多糖相。只有PEG/POx相会产生凝胶,多糖相将保持为液体,从而形成大孔水凝胶。
在所有实施方式中,可交联聚合物包含可以被交联的反应性部分,或者已经用所述反应性部分改性。
共价交联通过本领域技术人员已知的任何化学手段实现,包括但不限于:甲基丙烯酸酯、丙烯酸酯、丙烯酰胺、乙烯基酯或其它含烯分子的自由基聚合;巯基-烯加成、在其它受体如马来酰亚胺或丙烯酸酯上的迈克尔加成。硫醇(thiol)可以是含有数个巯基的任何肽或蛋白质,典型地但不是必须地通过半胱氨酸残基引入。硫醇组分也可以是硫醇化聚合物,例如带有硫醇末端的线性或支化PEG,或者在侧链上或在具有线性或支化形状的末端上具有巯基的POx。也可以使用通过酪胺或多巴胺的氧化或用转谷氨酰胺酶进行的酶促交联。其他经典手段是由醛形成氨基的席夫碱形成、叠氮化物点击铜催化或应变促进化学、狄尔斯-阿尔德反应(Diels alder reaction)、2+2环加成、胺叠氮化物或酰肼偶联到碳化二亚胺活化的羧酸上,等等。
交联也可以通过非共价相互作用例如疏水性相互作用(例如普朗尼克类(pluronics))或特异性识别(例如链亲和素-生物素)而发生。
任何其他多糖或多糖衍生物可用于第二有序构造性溶质,例如以果胶、藻酸盐、结冷胶、纤维素、甘露糖醛酸、透明质素、葡聚糖或任何这些天然多糖的衍生物为代表的天然/自然多糖。这些多糖的特征在于分子量为1000g/mol至10000000g/mol,特别是10000g/mol至2000000g/mol,更特别是100000g/mol至1000000g/mol,还更特别是约150000g/mol。不含聚合物的相也可以是非多糖或合成的新型多糖聚合物,只要不丧失相分离即可。
本发明的方法非常廉价、使用方便快捷并且容易上规模,而其他方法则不然。与现有技术的方法和凝胶相反,本发明的方法和凝胶同时提供可注射大孔水凝胶的所有所需性质。这些包括与细胞包封的生物相容性、原位孔形成(理论上包括在患者体内)、在大范围内大孔尺寸的完全可调性以及容易处理。另外,该方法还提供孔的互连性、完美的水凝胶透明度、优异的水凝胶对细胞侵入的容许度以及改善的稳定性。
直接用途是用于筛选的体外三维培养。即使存在其它替代物(例如纤维蛋白凝胶、胶原凝胶和基质胶),水凝胶也表现得与现有的黄金标准一样好,特别是对于三维神经元培养物而言。但是这些基质是动物源的,这造成了免疫原性或病毒污染风险的严重问题以及更高的成本,并且它们通常在细胞存在下降解过快,而所有这些问题都被本发明的水凝胶克服。还没有其它的完全合成的水凝胶像本文的情形那样被描述为提供优良的活力和包封的神经元的三维神经突向外生长。
对于细胞体内递送和大孔凝胶形成,已知的替代方法具有严重限制,仅本发明克服了它们。之前没有解决方案能够使可注射大孔水凝胶具有容易的规模扩大处理、直接孔形成和细胞相容性。本策略也特别容易实施,并且在容易获得的孔径和刚度范围方面更灵活。
通过下面的实施例和附图进一步说明本发明,可以从其得出其它的实施方式和优点。这些实施例是为了说明本发明而不是限制其范围。
实施例
提供了一种策略,其基于互连的大孔网络的形成,在包封的DRG和分离的中枢神经元(源自原代大鼠皮质和人类iPSC)存在的情况下展现了前所未有的三维神经突向外生长和稳定性。该策略的关键是使用未改性的高分子量多糖(PS)以进行聚乙二醇(PEG)排除(透明质素(HA)或非交互式甘露糖醛酸(MA))。通过将硫醇在乙烯基砜(VS)上的迈克尔加成,从PS相中排除PEG改善了交联的动力学,使得在生理pH值的介质中在几分钟内进行胶凝,而不要求pH值为8.0(pH 8.0对诸如神经元等敏感细胞是破坏性的)。PEG和多糖之间的相分离也产生与非微结构化等价物相比稳定性和神经突向外生长增加的凝胶。诸如蛋白质或整合素结合肽等粘附提示物(adhesion cue)在该系统中是不必要的,这举例说明了物理性质在将神经突允许性ECM工程化中的绝对重要性。在优化的条件下,包封的皮质神经元从第一周起以100μm/神经元/天的典型速率延伸神经突并在合成基质中形成突触,这在两周后产生具有自发协调电活性的三维神经网络,其在培养物中保持稳定至少一个月。
用PS将PEG水凝胶微结构化
由于PEG的水组织化性质,长期以来已知PEG与葡聚糖和一些盐一起形成水性双相体系。这种物理效应已被广泛用于蛋白质提取,并显示用于凝胶微球形成,但尚未显示其对于大孔支架的原位自组装的潜力。这可能是因为相分离通常通过快速微球形成进行,随后进行融合和倾析,其不提供孔和凝胶的渗透网络。可以通过使高百分比PEG-葡聚糖混合物中的葡聚糖在翻滚下过夜光交联来获得互连的网络。尽管有其优点,但该方法不能实现原位胶凝和细胞包封,并且所得到的支架具有低透明度。本发明人发现,以与细胞包封和注射相容的方式产生大孔水凝胶的关键在于将低的聚合物含量和高的粘度组合。低的聚合物含量保证了PEG和多糖溶液最初是可混溶的。然后,由在交联剂存在下发生的PEG链延伸触发相分离(其在水性体系中高度依赖于分子量)(图7)。
图1显示了该方法的两种典型实施方式,其产生具有完全不同的微观结构的凝胶:与MMP-可切割肽(含有两个半胱氨酸,为通过迈克尔加成的交联提供巯基)交联的4臂-PEG-VS(星形聚乙二醇,乙烯基砜封端)1.5%(w/v),分别具有70%(v/v)的2%(w/v)甘露糖醛酸(MA)溶液或0.5%(w/v)透明质素(HA)溶液(表示为PEG+MA和PEG+HA)。胶凝在补充有pH7.4的HEPES缓冲液的细胞培养基(Neurobasal+B27)中进行。多糖经选择为具化学惰性、以高分子量可获得以保证低浓度下的高粘度并且不具有(对于MA而言)或几乎不具有(对于HA而言)特定的生物学效应。在较大的频率范围内调节HA/MA原液的浓度以获得相似的复数粘度(图2b),静态粘度接近1Pa(类似于室温的甘油)。从均匀溶液开始的优点是,只要起始溶液充分混合,最终的微观结构就不依赖于确切的混合或注射策略:这是形成可重现的、均匀的和各向同性的孔的基础。为了将孔径、连接性和各向同性定量,使用具有荧光标签的4臂-PEG-VS衍生物和共焦激光扫描显微镜(CLSM)。不存在多糖时形成的PEG凝胶看起来是完全均匀的(PEG链之间的距离估计为5nm至50nm,并且所使用的成像条件下的衍射极限为185nm),而在HA或MA存在下形成的PEG凝胶是大孔的(图1a、1c)。三维检查显示孔完全互连(interconnected)。计算自相关函数(图1e),发现是各向同性的。通过将数据与可穿透球体模型拟合(图1f)来完成孔径定量,对于PEG+HA产生0.82±0.1μm的典型孔径,对于PEG+MA产生2.39±0.16μm的典型孔径。R2值>0.8,显示出与模型的良好一致性。对于PEG+MA,发现孔体积分数S2(0)为58±4%,对于PEG+HA,发现孔体积分数为43±1.6%(最后这个值应谨慎考虑,因为在HA存在下形成的孔接近衍射极限,因此显得模糊;另一方面PEG+MA中的孔得到良好分辨)。值得注意的是,相同粘度的HA和MA溶液产生显著不同的多孔结构:这是预料到的,因为已知相分离动力学不仅取决于粘度,还取决于界面张力。孔径也可以通过添加不同量的葡聚糖来调节,这可以在不明显改变粘度的情况下更快地进行PEG排除,从而产生可调尺寸的孔(数据未显示)。
低的聚合物含量也保证两相之间密度和光学指数的差异小。前者受关注是在于避免了会导致凝胶顶部和底部的孔径差异的沉降。后者避免了凝胶内的光衍射,这导致了完美的凝胶透明度(图8),这是对于大孔支架相对独特的特性。这使得能够在几毫米的深度上进行光学成像,并且易于在差分干涉对比法(DIC)中观察细胞。此类渗透性大孔凝胶对于组织工程化应用而言受到极大关注,因为它们具有最大化运输性质并且能够根据孔尺寸实现快速的神经突延伸或细胞侵入的自由通道。此类互连的大孔通常见于天然纤维状基质如胶原蛋白和纤维蛋白中,但在经典的化学交联的水凝胶(典型地具有5nm至50nm的孔径)中未发现。
胶凝动力学
粘度的增加使得扩散更慢,因此动力学更慢。但是该效应不仅是经由体积排阻由浓度制衡,而且因此形成了具有增强动力学的多孔PEG凝胶。这尤其值得关注,因为这使得能在生理pH下形成具有最佳动力学的凝胶,而类似的良好胶凝时机通常仅在pH8.0达到(图2a/2c),而pH 8.0对于细胞通常是应激性的并且可以导致诸如神经元等敏感细胞的损伤或死亡。高粘度也防止了在胶凝发生之前的细胞沉降。
背根神经节(DRG)包封
DRG是外周轴突再生最常见的体外模型,并且由于其对化学和生物胁迫的抗性,所以完整的外植体易于培养。它们通常以二维生长以测试各种底物的生物活性,并且在纤维蛋白或胶原蛋白中以三维生长,但由于外植体周围的高浓度蛋白酶,这些蛋白在几天内会降解。研究者发现,不可降解的多孔PEG凝胶允许外周轴突侵入,且在较长时间内稳定(图3)。为此,将来自E9.5鸡胚的DRG外植体包封在由4臂-PEG-VS 0.8%(w/v)形成的PEG凝胶盘(4mm×1.5mm)中,该PEG凝胶盘在HA 0.525%(w/v)和葡聚糖1.4%(w/v))的存在下与化学计量的PEG二硫醇进行了交联。30天后活细胞处理(由钙黄绿素染色)的完整凝胶成像显示整个凝胶已被致密的轴突网格侵入,显示容许性以及长期稳定性。由碘化丙啶(PI,死亡)/钙黄绿素AM(活)染色图案可见,细胞死亡在外植体表面上显而易见,而在内部不明显。这表明外部细胞层有助于保护内层细胞免受与包封相关的胁迫影响。
多孔PEG中来自大鼠皮质神经元的三维神经网络
将原代大鼠皮质神经元包封在用渐增量的HA形成的大孔凝胶中(图4)。将神经元活力、神经突向外生长速率和凝胶降解定量,因为它们是优化三维神经网络形成的最关键的参数。商业产品Q-凝胶用作无孔经典PEG凝胶对照,因为它代表了当前的黄金标准并且已经成功用于包封许多不同类型的细胞。
对于该系列的实验,由于已知神经元在非常柔软的纤维蛋白和胶原蛋白基质中生长最好,所以研究者选择浓度为1.5%(w/v)的PEG,其在刚胶凝后具有70Pa的储存模量。也使用了MMP可切割的肽以用于交联,因为先期实验显示当使用不可切割的交联剂时活力显著降低(图13)。为了解释这一点,研究者发现经TMR标记的4臂-PEG-VS可以在凝胶形成时被神经元摄取(图12),因此假设神经元应该能够代谢凝胶片段来避免毒性。该限制不适用于作为簇生长的神经元,因为外部神经元提供对PEG暴露的屏蔽,并且簇可以直接在不可降解的多孔PEG凝胶中生长(例如图3)。包封后两天(D2)的定量显示神经元在多孔凝胶中保留了非常高的活力(>95%)(图4d),这是重要的起点,其远远超过可能是目前最成功的合成神经元支持凝胶(Puramatrix)所达到的。Q-凝胶对照的活力降低至70%,这可能是由于短时间暴露于较高的pH值以及暴露于经典途径中使用的较高含量的PEG所致。神经突延伸在第2天平均约100μm/神经元,与HA百分比无关(图4c),这表明选择的低刚度适合支持快速神经突延伸。微结构化对凝胶的稳定性有重要影响:HA的量增加导致更少的宏观降解(图4b)。未使用HA形成的凝胶在两天内完全降解(因此图4中没有这种情况),而用0.525%(w/v)HA形成的凝胶在超过一个月后完全稳定。这是所预料到的,因为微结构化凝胶具有更致密和稳健的浓缩PEG凝胶支柱,其由未交联的HA留下的弱通道所隔开。这使得这些微结构化凝胶更耐降解,同时保持其支持快速神经突向外生长的潜力。
用MA微结构化的水凝胶具有大的开放孔结构,其导致细胞形态畸形,因为细胞体使其形状适应它们所处的尺寸为数微米的孔,并且神经突随着它们出现急转弯(图11、13)。因此,未针对该应用进一步研究它们。反而由HA形成的亚微米孔形成了薄而致密的网络,其中细胞体和神经看起来光滑,如同它们在体内一样。虽然长期以来认定层粘连蛋白或层粘连蛋白肽对于三维水凝胶中的神经突向外生长是必需的,但是研究者在此呈现出在不存在任何粘附提示物时在PEG+HA微结构化凝胶中的优异的神经突向外生长。鉴于PEG的隐形性、防粘性和非交互性,这一点尤其值得注意。几个系列数据表明神经突延伸主要依赖于物理性质。
为了测试凝胶是否因HA的存在而具有固有的粘附提示,在凝胶形成后立即用1mg/ml透明质酸酶(HAse)消化。在这些条件下,HA在数秒内降解,如通过流变测定法所见(图10),并且蛋白质穿过凝胶的扩散不成其为问题(例如,可容易地进行全凝胶免疫染色)。此外,当选择MA用于相排阻微结构化时,神经元虽然缺乏针对该海洋/细菌聚合物的受体却仍然生长。另外,当将PEG+HA和PEG+MA凝胶用IKVAV共价官能化时,即使在高浓度下,神经突向外生长在性质上与没有IKVAV的对照相似,而在二维组织培养塑料对照上,肽以浓度依赖性方式有效地诱导神经突向外生长(图11)。这表明具体提示物(specific cue)在已经最佳的物理背景下不是必需的。由于研究者在无血清条件下工作且不使用生长因子,神经元也不太可能非特异性地粘附至凝胶中夹带的蛋白质。此外,最初的神经突向外生长对于通过细胞进行的基质沉积而言发生得过快,从而无法起主要作用(典型地,在包封后1小时内可见许多约10μm的神经突)。最后,研究者排除了对MMP可切割肽的非选择性粘附:与PEG-二硫醇交联的微结构化的不可降解PEG凝胶完全不含氨基酸或电荷,却仍然容许神经突向外生长,尽管活力降低(图13)。总体而言,研究者的数据由此表明,物理性质才对于三维的快速神经突延伸具有极大的重要性,而不是特定的粘附线索物。大分子含量从1.2%(w/v)到1.9%(w/v)(18Pa~250Pa)的变化在两天或五天内不会显著影响神经突向外生长(图14)。最柔软的凝胶更不稳定,这能够导致更多的损伤和神经突的损失。在没有HA的情况下在pH8.0胶凝的1.5%(w/v)和1.9%(w/v)的无孔对照,在几天后降解。Q-凝胶是完全稳定的,但不能使神经突向外生长像多孔PEG那样好。在优化条件下,包封的原代神经元在几天内形成广泛的网络,其密度增加并保持稳定至少一个月(图5a)。主要分化的神经元标志物表达类似于已知的二维培养物(图5b),并且存在大量的突触前密度。在使用细胞内钙的荧光报道物在培养16天后观察固体尖峰活性(spiking activity)。显见协调的活动(图5c),这证明在合成ECM中形成了具有功能性突触连接的三维网络。
向hiPSC衍生神经元的转换
原代大鼠神经元培养物长期以来一直是细胞生物学研究的参考模型,但是hiPSC衍生的神经元正在成为人类神经疾病的更相关的模型。它们提供其中可以研究特定突变或药物效应的规定细胞的可再生来源,并且据认为它们具有治疗潜力。它们通常在规定的无血清培养基中二维生长,但是基质胶通常用于三维培养。此处,研究者建立了hiPSC衍生神经元的有效限定的三维培养系统,其不依赖于会阻碍转换至临床应用的免疫原性材料。将hiPSC衍生的神经元包封在具有高活力(高达85%)的用0.525%(w/v)HA微结构化的PEG凝胶中,并以与原代神经元相同的高速率延伸神经突(图6)。它们对刚度和细胞密度非常敏感,并且使凝胶降解明显更快。因此,凝胶在形成连通的网络所需的5天内是稳定的,但是不幸的是,在对于获得尖峰活性所需的2至3周内不稳定。在这些微结构化条件下采用2%(w/v)PEG和5M细胞/ml是提供具有快速神经突延伸和高活力的稳定超过一周的凝胶的最好折衷方案。细胞出现完全分化,对神经元标记物神经丝(βIII-微管蛋白和MAP2)呈阳性,对星形细胞标记物GFAP呈阴性。
讨论
已经开发了许多方法来创建具有宏观或分层孔隙的支架,其典型地通过盐浸、冷冻干燥或静电纺丝进行。然而,这些方法不能使细胞包封或原位形成。此处,研究者提出了一种独特的方法,其允许细胞被直接包封在多孔结构中,该多孔结构通过随着PEG进行步进生长聚合时在PEG和高粘度多糖之间的相分离所创建。能够使得神经突快速向外生长和突触形成的受限的三维培养,对于依赖于神经元-基质相互作用(例如轴突指导、生长锥机制、突触组装和再生)的研究而言最受关注。在空白背景下研究细胞外提示物的生物活性的可能性是一个重要的工具,特别是在结合hiPSC衍生的神经元时,因为后者可以商购获自各种患者特异性的转基因细胞系,这些细胞系提供了神经疾病的重要可重现模型。由于其完美的透明性,所描述的微结构化凝胶特别适合于成像研究。
电活性三维模型也代表了相对于二维模型的显著改进。体外神经网络对于研究电生理学、神经调节、神经毒理学而言或对于药物筛选而言是重要工具。其三维对应物具有显着不同的连接性,这会产生与体内状况更相关的数据。进来对网络连接性(networkconnectivity)在堆叠的二维表面上进行了研究,然而,研究者所描述的系统通过将神经元置于完全三维环境中而更进一步。
本研究中描述的大孔水凝胶提供了神经细胞外基质的生物物理性质的优异模拟,从而首次允许在合成PEG凝胶中形成稳定的功能性网络。对于体内应用,令人关注的是此处使用的组分和交联化学都是生物相容性的。特别是,PEG、HA和藻酸盐已经在诊所中使用。由于系统在微米范围内的直接可调性,还可以设想包封其他细胞类型以控制其在三维空间中的迁移、组装和相互作用。这些水凝胶的中孔隙度(mesoporosity)/大孔隙度(macroporosity)提供了非常高的表面积,改善了传质,并且可允许开发与均相体系相比更具组织化的组织类似物。
方法
除非另有说明,否则所有化学品均来自Sigma-Aldrich,细胞培养试剂来自Invitrogen,实验一式三份地进行,并且图像被最小程度地修改(对所有图片的亮度/对比度进行调整,且仅对于神经元图片的伽马值进行调整,以使神经突和细胞体清晰可辨)。
4臂-PEG-乙烯基砜(4臂-PEG-VS)
将1g(50μmol)的20kDa 4臂-PEG-硫醇(Laysan Bio)溶解于4ml三乙醇胺(TEOA)缓冲液(300mM,pH8.0)中,立即在剧烈搅拌下滴加至1004μl(10mmol)二乙烯基砜的4ml相同的缓冲液中。反应在几分钟内基本完成,并且放置进行2小时。将产物相对于mQ水透析(每次至少6小时至少换水6次),并冻干。发现硫醇在质子NMR(在氘代氯仿中,Bruker 400Mhz仪器)的检出限内被完全取代。将产物以4%(w/v)重悬浮于mQ水中,无菌过滤,以200μl(8mg)等分,冻干,并在使用前储存于-20℃。
基质金属蛋白酶(MMP)可切割肽处理
具有序列Ac-GCRD-GPQGIWGQ-DRCG-NH2(1746Da)的MMP-可切割肽(Nagase,H.,Biopolymers 40,339–416,1996;Lutolf,B.M.P.,Adv.Mater.15,888–892,2003)来自Anawa(瑞士),纯度>95%。将经HPLC纯化的肽作为需要中和的酸性TFA盐。为此目的,将约100mg肽粉末分散在少量水(约1ml)中,补充最少量的酚红作为pH指示剂,并用300mM NaOH水溶液中和(黄色溶液变成橙色)。肽的质子化形式溶解性差,但在加工过程中初始浆液变得清澈。避免加入过量的NaOH是重要的,因为硫醇在pH>7.0(指示器变成红橙色)时迅速氧化。然后将经中和的肽在mQ水中稀释至1%(w/v),无菌过滤,以400μl(4mg)等分,冻干,密封并储存在-20℃直至使用。发现以这种形式至少6个月是稳定的。肽粉末通常含有显著量的抗衡离子和少量氧化的肽,因此对于每一批,重悬浮的等分试样中的游离硫醇的精确浓度使用Ellman测定法(Ellman,G.L.,Arch.Biochem.Biophys.70–77,1959)利用β-巯基乙醇校准曲线确定。将用于pH平衡的少量酚红在该测定的情况下控制为具有可忽略的吸光度。
缓冲液
特别小心地制备HEPES缓冲液(200mM HEPES和100mM NaOH的mQ水溶液,调节至pH7.4),因为其用于通过迈克尔加成形成凝胶,这是非常pH敏感的(Lutolf,M.P.,Biomacromolecules 4,713–722,2003)。发现pH指示剂酚红在558/433nm处的吸光度测量提供最可靠的pH值,从而保证可再现的实验而不依靠更易于漂移的校准溶液和电极。将558/433nm处的吸光度比率调整为2,其对应于在24℃和300mM离子强度下的pH7.40(Yao,W.,Environ.Sci.Technol.35,1197–201,2001)(假设两性离子携带两个电荷;如果相反地像无电荷分子一样处理它们,这相当于100mM离子强度和pH 7.5)。
类似地制备pH8.0的TEOA,同时通过用HCl 300mM降低pH7.4的PBS(Gibco)的pH而制备pH6.0的PBS。
甘露糖醛酸(MA)
高粘度(参见图S1)细菌MA(H.,Methods Biotechnol.10,71–78,1999)是Prof./>教授(Norwegian University of Science and Technology,BiopolymerLaboratory)所惠赠。与HA不同,藻酸盐不存在于哺乳动物中,因此预期不会被任何神经元受体特异性识别。另外,这种形式的藻酸盐是纯粘性的,因为其缺乏古洛糖醛酸盐(其使得野生型藻酸盐能够交联钙)。
凝胶形成
事先准备支持体。将PDMS(Sylgard 184,10%(w/w)交联剂)的1mm层在50℃在陪替氏培养皿中加热2小时。用4mm和6mm的连续同心冲孔获得环形模具(来自Kai Medical的皮肤冲孔器)。准备24孔板,每个孔具有一个无菌盖玻片,在其上放置一个PDMS模具。PDMS粘在玻璃上,凝胶可以直接在该支持体上制作,这使得能够容易转移、成像或免疫染色,所有这些都不会机械性干扰神经元。试图保持凝胶像其他细胞类型通常的那样自由浮动,给出了更差的结果:神经突通常在介质变化或凝胶转移过程中机械破裂。在用洗涤剂洗涤和紫外线消毒后,可以回收PDMS模具。应该避免乙醇,因为它可以加载在PDMS中并释放到培养物中。在即将制作凝胶之前,将4臂-PEG-VS的等分试样以20%(w/v)重悬浮于pH7.4的HEPES中(提供40mM乙烯基砜)。将MMP-可切割肽以8%(w/v)重悬浮于pH6.0的PBS中(根据Ellman测试,典型地提供50mM的硫醇)。肽溶液的微酸性pH值对于避免硫醇氧化是重要的,硫醇氧化在pH7.4时几小时就变得显著。将补充有0.75%(w/v)透明质素(HA,Sigma53747)的无菌过滤完全培养基的等分试样保持在4℃。由于高粘度,必须使用容积式移液管(例如GilsonMicroman M50E)来准确吸取含有大于0.5%(w/v)HA的溶液。为了制备100μl含有2%(w/v)PEG、0.525%(w/v)HA和1e7个细胞/ml的典型凝胶,如下合并原液:10μl of 4臂-PEG-VS原液、12μl的HEPES pH7.4缓冲液、在HA补充培养基中1.43e7个细胞/ml的70μl细胞悬浮液,最后在试管侧壁滴加8μl的MMP-可切割肽。快速涡旋并用容积式移液管剧烈混合约10秒后,液体前体可以用15μl/PDMS模具分配。在此浓度下3至4分钟内发生胶凝,但更软的凝胶可能会花费多达15分钟,因此在添加1ml生长培养基之前,在细胞培养箱(37℃,5%CO2)中使每次胶凝进行1小时。胶凝混合物具有生理pH值和渗透压以及大比例的完全培养基:结果,细胞受到最小的胁迫,并且在1小时停止胶凝时在相差中已经可以看到神经突延伸。通过约20%(v/v)的强缓冲的HEPES溶液(pH7.4)使pH保持稳定。其它条件通过下述获得:相应地改变在混合物中加入的4臂-PEG-VS和MMP肽原液的体积,用pH8.0的TEOA代替缓冲液,改变原液中的HA和细胞浓度,将培养基改变为适于各细胞类型的培养基,或者用另一种高粘性补充剂代替HA,如各实验所指明。在相同的缓冲液和硫醇摩尔浓度下通过用PEG-二硫醇(LaysanBio,3.4kDa)代替MMP-可切割肽而形成不可降解的凝胶。在所指定的情形中加入具有序列CSRARKQAASIKVAVSADR-NH2(简称为IKVAV,ANAWA)的层粘连蛋白α1(2110-2127)肽。为此,首先将IKVAV肽从4mg/ml原液添加到4臂-PEG-VS溶液中,静置缀合30分钟,然后进行所述策略的其余部分(在该情况下,HEPES缓冲液的添加量相应减少以保持相同的总体积)。使用香豆素标记的IKVAV肽进行的FRAP测试来验证肽成功地锚定在凝胶中。根据公开的策略以二维检验IKVAV的生物活性(Tashiro,K.,J.Biol.Chem.264,16174–82,1989)。
流变测定法
在Anton Paar MCR 301流变仪上进行动态剪切测量。如上所述制备凝胶的液体前体,其具有完全的生长培养基但没有细胞,并插入在金属底板和20mm直径的平行板几何体之间。在5%应变、0.25mm间隙、37℃珀耳帖控制温度和水饱和气氛下,以1Hz振荡监测存储模量G'和损耗模量G″的增加。选择该菌株以完全落入凝胶的线性粘弹性区内(在1Hz下延伸至少1%至400%)。将刚度定义为在60分钟时的储存模量(所有样品达到平稳水平并且通过添加细胞培养基来停止胶凝的点),胶凝时间被定义为在对数标度上达到平稳水平刚度的一半时的时间,如在典型实验曲线上的补充图1所示。在2%应变、0.2mm间隙、37℃和水饱和气氛下以0.01至10Hz测量0.5%(w/v)HA和2%(w/v)MA的复数粘度。
四甲基罗丹明标记的4臂-PEG-乙烯基砜(TMR-标记的4臂-PEG-VS)
将100mg(5μmol)的20kDa的4臂-PEG-硫醇溶解于2ml mQ水中。然后在搅拌下滴加0.12mg(0.25μmol)四甲基罗丹明-5-马来酰亚胺(sigma 94506)的2ml PBS(pH7.4)溶液。缀合在几秒钟内发生,但静置额外10分钟。将所得的混合物滴加在220μl(2.2mmol)二乙烯基砜的4ml TEOA缓冲液(300mM,pH8.0)中,静置反应30分钟,透析并冻干。所有的处理都在黑暗中进行。
该策略在100%缀合效率的上限情况下取代了4臂-PEG端点的1/80,这确保对凝胶形成的影响可忽略不计。
孔隙成像和量化
如上所述用PEG 1.9%(w/v),不使用细胞,并使用TMR标记的4臂-PEG-VS制备凝胶。为了产生不同的孔径,培养基(混合物的70%)补充有0或0.5%(w/v)HA或2%MA。在具有63x/1.4油物镜和520nm激发的Leica SP8共聚焦显微镜中,在pH7.4的PBS中温育3天后,将每个凝胶的微结构成像为具有50×50×200nm3像素尺寸的25μm的立方体堆栈。将LeicaHyDs用于检测,优点是在具有非常低噪声的光子计数下运行,因此提供了“真”黑色电平。通过漂白校正、2px高斯平滑、阈值化、使用Matlab等值面进行曲面三角剖分和减少贴片函数(patch function)以及Blender渲染来获得孔连通性的三维视图。对于孔径定量,每个条件的三个堆栈中的每一个都用漂白校正(Fiji,简单比例,背景电平0)和1px高斯平滑进行过滤。然后对堆栈进行阈值化和倒置以获得标记为1的孔和标记为0的荧光PEG的二值图像,并且使用定制的Matlab脚本来计算二阶相关函数S2(x,y)。由于观察到各向同性,所以将数据减少至r使用50nm面元(bin)。最后,使用可穿透球模型将所得到的数据拟合(Berryman,J.G.,J.Appl.Phys.57,2374–2384,1985)。
大鼠E17解离皮层神经元
如前所述解剖来自E17Wistar大鼠胚胎的皮质并解离(Buerli,T.,Nat.Protoc.2,3090–101,2007)。简言之,将切碎的皮质在补充有1mg/ml BSA、10mM葡萄糖、0.5μg/ml DNA酶(Sigma,D-5025)和0.5mg/ml木瓜蛋白酶(Sigma,P-4762)的PBS中于37℃温育15分钟,并用由DMEM+10%FBS组成的阻断培养基(blocking medium)洗涤。然后将其重悬浮在2ml阻断培养基中,并使用火抛光的巴斯德移液管通过研磨进行解离。将解离的细胞重悬浮于无血清生长培养基中,所述培养基由补充有1x Glutamax和青霉素/链霉素的Neurobasal+B27(Gibco 21103-049和17504-044)组成,并且在PLL包被的烧瓶(50ug/ml PLL的硼酸盐缓冲液,pH8.4,在37℃温育1h)中铺平板过夜。次日,首先用TrypLE快速洗涤平板5分钟,以使弱粘附的非活细胞和细胞碎片脱离。然后将剩余的健康细胞用胰蛋白酶/EDTA(Gibco 12605-010和25200-072)脱离。加入两倍体积的阻断培养基后,将细胞离心并重悬浮于无血清生长培养基中。所有随后的二维或三维细胞培养都在无血清生长培养基中进行,每周一次更换其中一半培养基。
背根神经节(DRG)分离和培养
在即将包封前从E10鸡胚中分离DRG。将它们在补充有1mg/ml白蛋白和50ng/mlNGF的无血清生长培养基中培养。在HA 0.525%(w/v)和葡聚糖1.4%(w/v))的存在下,在交联有化学计量量的PEG-二硫醇的4臂-PEG-VS 0.8%(w/v)中完成包封,如凝胶形成部分所述。
人诱导多能干细胞(hiPSC)衍生的神经元
hiPSC衍生的神经祖细胞(Axol ax0016)根据在线供应商策略进行繁殖和分化。然后在HA 0.525%(w/v)的存在下,以与原代神经元相同的策略,将衍生的人大脑皮质神经元包封在凝胶中,以用于微结构化,并用Axol维持培养基(也无血清)代替生长培养基。
用钙离子传感器尖峰成像
取出用于钙成像的凝胶的培养基,替换为来自1mM无水DMSO溶液的补充有6μM的Oregon Green BAPTA-1(Life technologies)的新鲜完全培养基。温育1h后,将凝胶在其原始培养基中洗涤1h,并使用具有8KHz共振扫描仪的20x/0.95水物镜和488nm照射,在LeicaSP8共焦显微镜上成像。所得成像速率为7.44Hz。
活力测定
通过用钙黄绿素AM(绿色细胞质,活细胞,2μM,来自4mM在DMSO中的原液)补充凝胶培养基和细胞核染色完成活力测定,所述细胞核染色为Hoechst(蓝色细胞核,所有细胞,10μg/ml,来自10mg/ml的mQ水溶液)、溴化乙啶同二聚体-1(红色细胞核,死细胞,2μM,来自在DMSO/水1:4中的2mM原液)和碘化丙锭(红色细胞核,死细胞,6.6μg/ml,来自0.33mg/ml的mQ水溶液)。将凝胶在补充培养基中温育1小时,然后在新鲜的培养基中洗涤1小时,并在LeicaSP8多光子显微镜上对解离的细胞成像,所述多光子显微镜具有超过200μM深度的20x/0.95水物镜,或者具有10x/0.3空气物镜,作为DRG外植体的单个切片。活细胞和死细胞手动计数。
凝胶降解
通过采用在5x空气物镜的明视野中覆盖Zeiss Observer 2显微镜上整个凝胶的铺瓦扫描,在4mm直径的凝胶层上,在2天后对凝胶稳定性定量(此时将在培养一个月内溶解的条件已经可见化地降解)。铺瓦与Microsoft Image Composite Editor组装在一起。由于其没有悬浮的细胞体,并被大致呈现为簇集在降解部分的侧面和底部的黑暗细胞聚集体,因此降解的区域清晰可见。将其使用Fiji手动分段,将降解百分比报告为相对于总凝胶面积的降解面积(来自6个样品的平均值和标准偏差)。
PEG诱导的成簇和PEG摄取
当用10%(w/v)高分子量PEG(Sigma,200kDa)作为粘性组分进行神经元包封时,在混合后立即观察到细胞成簇。使用PlasDIC在20x空气物镜上完成成像。为了在最佳可见度条件下研究PEG吸收,使神经元在PLL包被的组织培养塑料中二维生长6天,以确保从组织解离完全恢复。然后在其培养基中补充1%(w/v)TMR标记的4臂-PEG-VS,以模拟在包封过程中暴露于PEG。用新的生长培养基仔细洗涤培养物5次10分钟,立即在PlasDIC中成像,并在20x空气物镜上进行荧光以观察PEG与细胞的结合。在培养另外12天后进行相同的观察,以观察PEG保留。通过背景减法和3px中值滤波对荧光通道进行光不均匀性和噪声校正。
神经突向外生长定量
在第2天神经突长度通过手工追踪进行定量,因为它提供了最大的准确性和可靠性,但是第5天自动追踪,因为在这个时间点的长度变得几乎难以手动追踪。对来自自动跟踪的每个图像进行目视检查以适当跟踪。使用简单的神经突示踪剂进行手动追踪(Longair,M.H.,Bioinformatics 27,2453–2454,2011),使用NeuriteQuant进行自动跟踪(Dehmelt,L.,BMC Neurosci.12,100,2011)。追踪是在200μm深和620μm宽的双光子成像三维堆栈上进行的。对于含有部分降解的凝胶的系列(其太弱而不能经受免疫染色),荧光染色是缺省的βIII-微管蛋白(对固定样品上的所有神经突染色)和钙黄绿素AM(对活样品上的所有过程染色)(图4和图6中的HA响应曲线)。对DAPI染色的细胞核进行计数并用于相对于细胞数量标准化。
免疫细胞化学和成像
原代抗体:βIII-微管蛋白(Sigma T5076,1:500)、神经丝(Sigma N4142,1:150)、突触结合蛋白(DSHB mAB 30,由Reichardt博士开发,来自UCSF,8μg/ml)、MAP-2(SigmaM3696,1:200)、GFAP(R&D Systems AF2594,10μg/ml)。以1:200使用与Alexa488和594缀合的二抗(Invitrogen A11005,A11008,A10680,A11015)。研究者采用标准的免疫细胞化学策略,以对整个凝胶进行直接染色和成像。将样品固定并在4℃于具有0.1%Triton X-100的10%福尔马林透化1小时,用5%BSA的PBS溶液阻断过夜,并用PBS洗涤(1h两次,一次过夜)。然后将它们在一抗中温育(室温在温和摇动下过夜,用3%BSA的PBS溶液稀释),用PBS洗涤,在二抗中温育过夜,用PBS洗涤,用DAPI 0.3μM的PBS溶液染色1小时,最后用PBS洗涤。在具有20x/0.95水物镜、超过620μm宽和200μm深的Leica SP8多光子显微镜上,使用1μm步进,600Hz扫描速率,1024×1024px,并且使用MaiTai Deepsee and Insight Deepsee fs激光器(Spectra Physics)分别在710nm和1100nm同时激发,而进行经免疫染色样品的成像。同时采集2至3种颜色。对所得到的堆栈施加最大强度投影(MIP),通过除以荧光素参考图像而补偿光的不均匀性,并调节其颜色显示(亮度/对比度/伽马值)。
统计分析
使用单因素方差分析和Tukey事后检验来定量系列内的差异,p<0.01被认为是显著的。
Claims (4)
1.一种提供大孔水凝胶的方法,所述方法包括下述步骤:
-提供包含第一溶质和第二溶质的水性溶液,其中
i)所述第一溶质是聚乙二醇(PEG)的可交联衍生物;并且
ii)所述第二溶质是多糖有序构造性试剂,
-添加能够交联所述PEG的可交联衍生物的交联剂,由此同时引发所述PEG的可交联衍生物的胶凝和相分离;
a)其中所述水性溶液包含0.8%(w/v)4臂-PEG-乙烯基砜作为第一溶质,以及0.525%(w/v)透明质酸和1.4%(w/v)葡聚糖的组合作为第二溶质;并且其中所述交联剂是PEG二硫醇;或者
b)其中所述水性溶液包含1.5%(w/v)TMR标记的4臂-PEG-乙烯基砜作为第一溶质和0.525%(w/v)透明质酸作为第二溶质;并且其中所述交联剂是MMP-可切割肽;或者
c)其中所述水性溶液包含1.5%(w/v)4臂-PEG-乙烯基砜作为第一溶质和70%(v/v)的0.5%(w/v)透明质酸作为第二溶质;并且其中所述交联剂是MMP-可切割肽。
2.如权利要求1所述的方法,其中
-所述第一溶质是0.8%(w/v)4臂-PEG-乙烯基砜;
-所述第二溶质是0.525%(w/v)透明质酸和1.4%(w/v)葡聚糖的组合;
-所述交联剂是PEG二硫醇。
3.如权利要求1所述的方法,其中
-所述第一溶质是1.5%(w/v)TMR标记的4臂-PEG-乙烯基砜;
-所述第二溶质是0.525%(w/v)透明质酸;
-所述交联剂是MMP-可切割肽。
4.如权利要求1所述的方法,其中
-所述第一溶质是1.5%(w/v)4臂-PEG-乙烯基砜;
-所述第二溶质是70%(v/v)的0.5%(w/v)透明质酸;
-所述交联剂是MMP-可切割肽。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN202110629796.7A CN113372579B (zh) | 2015-09-09 | 2016-09-08 | 可注射大孔水凝胶 |
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP15184552.6 | 2015-09-09 | ||
| EP15184552 | 2015-09-09 | ||
| CN201680051583.8A CN108025110B (zh) | 2015-09-09 | 2016-09-08 | 可注射大孔水凝胶 |
| CN202110629796.7A CN113372579B (zh) | 2015-09-09 | 2016-09-08 | 可注射大孔水凝胶 |
| PCT/EP2016/071238 WO2017042301A1 (en) | 2015-09-09 | 2016-09-08 | Injectable macroporous hydrogels |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201680051583.8A Division CN108025110B (zh) | 2015-09-09 | 2016-09-08 | 可注射大孔水凝胶 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN113372579A CN113372579A (zh) | 2021-09-10 |
| CN113372579B true CN113372579B (zh) | 2023-07-14 |
Family
ID=54150245
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN202110629796.7A Active CN113372579B (zh) | 2015-09-09 | 2016-09-08 | 可注射大孔水凝胶 |
| CN201680051583.8A Active CN108025110B (zh) | 2015-09-09 | 2016-09-08 | 可注射大孔水凝胶 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201680051583.8A Active CN108025110B (zh) | 2015-09-09 | 2016-09-08 | 可注射大孔水凝胶 |
Country Status (18)
| Country | Link |
|---|---|
| US (1) | US20180264176A1 (zh) |
| EP (2) | EP3868416B1 (zh) |
| JP (1) | JP6829898B2 (zh) |
| CN (2) | CN113372579B (zh) |
| AU (1) | AU2016320395B2 (zh) |
| CA (1) | CA2992692C (zh) |
| CY (1) | CY1124571T1 (zh) |
| DK (2) | DK3347061T3 (zh) |
| ES (1) | ES2883235T3 (zh) |
| HR (1) | HRP20211306T1 (zh) |
| HU (1) | HUE055937T2 (zh) |
| IL (1) | IL257024B (zh) |
| LT (1) | LT3347061T (zh) |
| PL (1) | PL3347061T3 (zh) |
| PT (1) | PT3347061T (zh) |
| RS (1) | RS62239B1 (zh) |
| SI (1) | SI3347061T1 (zh) |
| WO (1) | WO2017042301A1 (zh) |
Families Citing this family (34)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012044753A2 (en) | 2010-10-01 | 2012-04-05 | Applied Medical Resources Corporation | Portable laparoscopic trainer |
| KR101963610B1 (ko) | 2011-10-21 | 2019-03-29 | 어플라이드 메디컬 리소시스 코포레이션 | 수술 트레이닝용 모의 조직 구조 |
| JP2015503961A (ja) | 2011-12-20 | 2015-02-05 | アプライド メディカル リソーシーズ コーポレイション | 高度手術シミュレーション |
| KR102105979B1 (ko) | 2012-09-26 | 2020-05-04 | 어플라이드 메디컬 리소시스 코포레이션 | 복강경 절차들을 위한 수술 훈련 모델 |
| US10679520B2 (en) | 2012-09-27 | 2020-06-09 | Applied Medical Resources Corporation | Surgical training model for laparoscopic procedures |
| US9940849B2 (en) | 2013-03-01 | 2018-04-10 | Applied Medical Resources Corporation | Advanced surgical simulation constructions and methods |
| CA3232626A1 (en) | 2013-06-18 | 2014-12-24 | Applied Medical Resources Corporation | Gallbladder model |
| AU2014293036B2 (en) | 2013-07-24 | 2017-12-21 | Applied Medical Resources Corporation | First entry model |
| US10198966B2 (en) | 2013-07-24 | 2019-02-05 | Applied Medical Resources Corporation | Advanced first entry model for surgical simulation |
| WO2015148817A1 (en) | 2014-03-26 | 2015-10-01 | Applied Medical Resources Corporation | Simulated dissectible tissue |
| WO2016077195A1 (en) | 2014-11-13 | 2016-05-19 | Applied Medical Resources Corporation | Simulated tissue models and methods |
| KR20230143198A (ko) | 2015-02-19 | 2023-10-11 | 어플라이드 메디컬 리소시스 코포레이션 | 시뮬레이션된 조직 구조체들 및 방법들 |
| JP2018514805A (ja) | 2015-05-14 | 2018-06-07 | アプライド メディカル リソーシーズ コーポレイション | 電気手術トレーニングおよびシミュレーション用の合成組織構造 |
| ES2925028T3 (es) | 2015-06-09 | 2022-10-13 | Applied Med Resources | Modelo de histerectomía |
| KR20180030178A (ko) | 2015-07-16 | 2018-03-21 | 어플라이드 메디컬 리소시스 코포레이션 | 시뮬레이션된 절개가능 조직 |
| ES2883261T3 (es) | 2015-07-22 | 2021-12-07 | Applied Med Resources | Modelo de apendicectomía |
| KR102649261B1 (ko) | 2015-10-02 | 2024-03-20 | 어플라이드 메디컬 리소시스 코포레이션 | 자궁 절제술 모델 |
| KR20180083919A (ko) | 2015-11-20 | 2018-07-23 | 어플라이드 메디컬 리소시스 코포레이션 | 시뮬레이션된 절개가능 조직 |
| EP4151661A1 (en) | 2016-03-24 | 2023-03-22 | Takeda Pharmaceutical Company Limited | Alginate hydrogel compositions |
| JP6925579B2 (ja) * | 2016-03-31 | 2021-08-25 | 日油株式会社 | 環状ベンジリデンアセタール構造を有する生分解性ヒドロゲル |
| KR102405187B1 (ko) | 2016-06-27 | 2022-06-07 | 어플라이드 메디컬 리소시스 코포레이션 | 시뮬레이션된 복벽 |
| EP3554569A1 (en) * | 2016-12-13 | 2019-10-23 | Millennium Pharmaceuticals, Inc. | Conformal coating of biological surfaces |
| WO2018152122A1 (en) | 2017-02-14 | 2018-08-23 | Applied Medical Resources Corporation | Laparoscopic training system |
| US10847057B2 (en) | 2017-02-23 | 2020-11-24 | Applied Medical Resources Corporation | Synthetic tissue structures for electrosurgical training and simulation |
| AU2018330610A1 (en) * | 2017-09-11 | 2020-04-02 | Evorion Biotechnologies Gmbh | Systems, methods and hydrogels for cell culture and analysis |
| CN108893445A (zh) * | 2018-07-26 | 2018-11-27 | 南方医科大学 | 一种引导视网膜神经节细胞及其轴突生长延展的方法 |
| CN109316628B (zh) * | 2018-09-21 | 2021-04-20 | 广州远想生物科技有限公司 | 一种凝胶及其制备方法和应用 |
| CN109731133B (zh) * | 2019-02-01 | 2020-09-01 | 浙江大学 | 一种抗菌、抗粘附、可注射式温敏壳聚糖凝胶敷料及其制备方法 |
| US11680107B2 (en) * | 2019-03-22 | 2023-06-20 | Taipei Medical University | Hydrogel composition for drug delivery and uses thereof |
| US11807720B2 (en) | 2019-08-28 | 2023-11-07 | Boston Scientific Scimed, Inc. | Multi-armed polyoxazolines and compositions, systems and methods pertaining to the same |
| WO2021138588A1 (en) * | 2020-01-03 | 2021-07-08 | Repertoire Immune Medicines, Inc. | Compositions of hydrogels and methods of use thereof |
| CN112898600B (zh) * | 2021-02-07 | 2023-05-23 | 西安工业大学 | 一种聚多巴胺可逆粘附凝胶的分相制备方法 |
| WO2023135155A1 (en) | 2022-01-12 | 2023-07-20 | Eth Zurich | Photocurable phase-separating hydrogels |
| WO2023242189A1 (en) | 2022-06-13 | 2023-12-21 | Eth Zurich | Collagen visualization on microfluidic device |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1668697A (zh) * | 2001-11-07 | 2005-09-14 | 苏黎世大学 | 用于控制细胞向内生长和组织再生的合成基质 |
| CN1835792A (zh) * | 2003-01-17 | 2006-09-20 | 康乃尔研究基金会有限公司 | 含水两相体系的可注射水凝胶微球 |
| CN1918219A (zh) * | 2004-02-03 | 2007-02-21 | 安特易斯有限公司 | 生物相容性交联凝胶 |
| CN102573941A (zh) * | 2009-07-30 | 2012-07-11 | 卡比兰生物外科公司 | 改性透明质酸聚合物组合物和相关的方法 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20070264227A1 (en) * | 2001-11-07 | 2007-11-15 | Eidgenossische Technische Hochschule Zurich | Synthetic Matrix for Controlled Cell Ingrowth and Tissue Regeneration |
| AU2002358272B2 (en) * | 2001-12-18 | 2009-01-22 | Eidgenossische Technische Hochschule Zurich | Growth factor modified protein matrices for tissue engineering |
| KR100699278B1 (ko) * | 2005-05-12 | 2007-03-23 | 학교법인 포항공과대학교 | 수화젤레이터로 유용한 바이오틴-아미노산 결합체 및이로부터 제조된 수화젤 |
| US20070212385A1 (en) * | 2006-03-13 | 2007-09-13 | David Nathaniel E | Fluidic Tissue Augmentation Compositions and Methods |
| CA2780294C (en) * | 2009-11-09 | 2018-01-16 | Spotlight Technology Partners Llc | Polysaccharide based hydrogels |
| CN107648668B (zh) * | 2010-10-06 | 2021-06-18 | 哈佛学院董事会 | 用于基于材料的细胞疗法的可注射的成孔水凝胶 |
| EP2825582B1 (en) * | 2012-03-16 | 2016-01-13 | Bender Analytical Holding B.V. | Cross-linked polymers and medical products derived from nucleophilically activated polyoxazoline |
| ES2769503T3 (es) * | 2012-11-07 | 2020-06-26 | Eth Zuerich | Hidrogeles de alginato sulfatados para cultivo celular y terapia |
-
2016
- 2016-09-08 DK DK16763035.9T patent/DK3347061T3/da active
- 2016-09-08 DK DK21168993.0T patent/DK3868416T3/da active
- 2016-09-08 HU HUE16763035A patent/HUE055937T2/hu unknown
- 2016-09-08 US US15/758,390 patent/US20180264176A1/en not_active Abandoned
- 2016-09-08 PL PL16763035T patent/PL3347061T3/pl unknown
- 2016-09-08 WO PCT/EP2016/071238 patent/WO2017042301A1/en active Application Filing
- 2016-09-08 JP JP2018511412A patent/JP6829898B2/ja active Active
- 2016-09-08 ES ES16763035T patent/ES2883235T3/es active Active
- 2016-09-08 LT LTEP16763035.9T patent/LT3347061T/lt unknown
- 2016-09-08 CN CN202110629796.7A patent/CN113372579B/zh active Active
- 2016-09-08 AU AU2016320395A patent/AU2016320395B2/en active Active
- 2016-09-08 EP EP21168993.0A patent/EP3868416B1/en active Active
- 2016-09-08 CN CN201680051583.8A patent/CN108025110B/zh active Active
- 2016-09-08 RS RS20211024A patent/RS62239B1/sr unknown
- 2016-09-08 SI SI201631296T patent/SI3347061T1/sl unknown
- 2016-09-08 EP EP16763035.9A patent/EP3347061B1/en active Active
- 2016-09-08 CA CA2992692A patent/CA2992692C/en active Active
- 2016-09-08 PT PT167630359T patent/PT3347061T/pt unknown
-
2018
- 2018-01-18 IL IL257024A patent/IL257024B/en unknown
-
2021
- 2021-08-13 HR HRP20211306TT patent/HRP20211306T1/hr unknown
- 2021-08-18 CY CY20211100738T patent/CY1124571T1/el unknown
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1668697A (zh) * | 2001-11-07 | 2005-09-14 | 苏黎世大学 | 用于控制细胞向内生长和组织再生的合成基质 |
| CN1835792A (zh) * | 2003-01-17 | 2006-09-20 | 康乃尔研究基金会有限公司 | 含水两相体系的可注射水凝胶微球 |
| CN1918219A (zh) * | 2004-02-03 | 2007-02-21 | 安特易斯有限公司 | 生物相容性交联凝胶 |
| CN102573941A (zh) * | 2009-07-30 | 2012-07-11 | 卡比兰生物外科公司 | 改性透明质酸聚合物组合物和相关的方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN108025110A (zh) | 2018-05-11 |
| EP3868416A1 (en) | 2021-08-25 |
| CY1124571T1 (el) | 2022-07-22 |
| EP3347061A1 (en) | 2018-07-18 |
| CA2992692C (en) | 2021-12-21 |
| DK3347061T3 (da) | 2021-08-23 |
| DK3868416T3 (da) | 2022-10-31 |
| EP3347061B1 (en) | 2021-05-19 |
| SI3347061T1 (sl) | 2021-11-30 |
| WO2017042301A1 (en) | 2017-03-16 |
| CA2992692A1 (en) | 2017-03-16 |
| CN113372579A (zh) | 2021-09-10 |
| EP3868416B1 (en) | 2022-08-10 |
| IL257024B (en) | 2022-02-01 |
| IL257024A (en) | 2018-03-29 |
| PL3347061T3 (pl) | 2021-11-22 |
| AU2016320395B2 (en) | 2020-09-17 |
| JP6829898B2 (ja) | 2021-02-17 |
| LT3347061T (lt) | 2021-09-10 |
| AU2016320395A1 (en) | 2018-02-22 |
| CN108025110B (zh) | 2021-08-20 |
| RS62239B1 (sr) | 2021-09-30 |
| HUE055937T2 (hu) | 2022-01-28 |
| US20180264176A1 (en) | 2018-09-20 |
| ES2883235T3 (es) | 2021-12-07 |
| JP2018535704A (ja) | 2018-12-06 |
| PT3347061T (pt) | 2021-08-25 |
| HRP20211306T1 (hr) | 2021-11-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN113372579B (zh) | 可注射大孔水凝胶 | |
| US11511016B2 (en) | Method for preparing porous scaffold for tissue engineering, cell culture and cell delivery | |
| Wang et al. | Bioactive silk fibroin scaffold with nanoarchitecture for wound healing | |
| Yang et al. | Bioinspired poly (γ-glutamic acid) hydrogels for enhanced chondrogenesis of bone marrow-derived mesenchymal stem cells | |
| Lee et al. | Advanced gellan gum-based glycol chitosan hydrogel for cartilage tissue engineering biomaterial | |
| US20130142763A1 (en) | Crosslinked cellulosic polymers | |
| Fiorica et al. | Hyaluronic acid and beta cyclodextrins films for the release of corneal epithelial cells and dexamethasone | |
| WO2018197688A1 (en) | Non-covalently assembled conductive hydrogel | |
| WO2021041372A1 (en) | Universal orthogonal network bioinks for three-dimensional bioprinting | |
| Diao et al. | Highly fluorescent and photostable polymeric nanofibers as scaffolds for cell interfacing and long-term tracking | |
| US10576042B2 (en) | Composition comprising polyelectrolyte complexes, methods and uses thereof | |
| Kirwale et al. | Chitosan, chondroitin sulfate, and hyaluronic acid based in-situ forming scaffold for efficient cell grafting | |
| Sharma et al. | Designing ECM-inspired supramolecular scaffolds by utilizing the interactions between a minimalistic neuroactive peptide and heparin | |
| Ramos Ferrer et al. | Sustained neurotrophin‐3 delivery from hyaluronic acid hydrogels for neural tissue regeneration | |
| Broguiere | Engineering of synthetic extracellular matrix analogues supporting and guiding neurons | |
| Diamond | Decellularized Porcine Brain Matrix for Neural Tissue Engineering | |
| Srisuk | Alginate based composite scaffold for biomedical engineering applications | |
| Smith | Cellular hitchhiking via injectable microparticles | |
| Pizzolitto | SVILUPPO E CARATTERIZZAZIONE DI STRUTTURE 3D E DI IDROGELI A BASE DI POLISACCARIDI NATURALI E MODIFICATI E LORO APPLICAZIONE IN CAMPO BIOMEDICO | |
| Karvinen | Hydrazone Crosslinked Polysaccharide-based Hydrogels for Soft Tissue Engineering | |
| Shi | Differentiation of neural stem cell using small molecules in 2D and 3D culture system | |
| Gonçalves | Bacterial cellulose as a novel substrate for retinal pigment epithelium cells transplantation in age-related macular degeneration |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |