CN108567970B - 注射用还原型谷胱甘肽的制备方法 - Google Patents
注射用还原型谷胱甘肽的制备方法 Download PDFInfo
- Publication number
- CN108567970B CN108567970B CN201810530808.9A CN201810530808A CN108567970B CN 108567970 B CN108567970 B CN 108567970B CN 201810530808 A CN201810530808 A CN 201810530808A CN 108567970 B CN108567970 B CN 108567970B
- Authority
- CN
- China
- Prior art keywords
- injection
- reduced glutathione
- temperature
- solution
- plate layer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/06—Tripeptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/14—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles
- A61K9/19—Particulate form, e.g. powders, Processes for size reducing of pure drugs or the resulting products, Pure drug nanoparticles lyophilised, i.e. freeze-dried, solutions or dispersions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Diabetes (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Obesity (AREA)
- Dermatology (AREA)
- Gastroenterology & Hepatology (AREA)
- Emergency Medicine (AREA)
- Endocrinology (AREA)
- Hematology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
Abstract
本发明公开了一种高稳定注射用还原型谷胱甘肽的制备方法。它为0.6g规格注射用还原型谷胱甘肽,配方组分为:还原型谷胱甘肽0.6g,10%氢氧化钠溶液调pH至6.0~7.0,注射用水加至2g;当为1.0g规格注射用还原型谷胱甘肽,配方组分为:还原型谷胱甘肽1.0g,10%氢氧化钠溶液调pH至6.0~7.0,注射用水加至3.3g;当为1.5g规格注射用还原型谷胱甘肽,配方组分为:其中,在配液过程中,配液和灌装过程中不断充氮气保持溶液中氧含量在1.5ppm以下。本发明具有质量稳定、可控,安全的优点。
Description
技术领域
本发明涉及医药制剂领域,更具体地说它是高稳定注射用还原型谷胱甘肽的制备方法。
背景技术
还原型谷胱甘肽(GSH)是人类细胞中自然合成的一种三肽,由谷氨酸、半胱氨酸和甘氨酸组成,含有巯基(-SH),广泛分布于人体各器官内,对维持细胞生物功能,保护细胞膜的完整性有着重要作用;还原型谷胱甘肽作为一种细胞内重要的调节代谢物质,其既是甘油醛磷酸脱氢酶的辅基,又是乙二醛酶及丙糖脱氢酶的辅酶,参与体内三羧酸循环及糖代谢,并能激活多种酶,如巯基(-SH)酶-辅酶等,从而促进糖类、脂肪和蛋白质代谢。
GSH分子特点是具有活性巯基(-SH)和谷氨酰键;巯基是GSH最重要的功能集团,可参与机体多种重要的生化反应,保护体内重要酶蛋白巯基不被氧化、灭活,保证能量代谢、细胞利用;通过巯基与体内的自由基结合,可直接使自由基还原,使之转化成容易代谢的酸类物质从而加速自由基的排泄,同时还可对抗自由基对重要脏器的损害; GSH是非酶性抗氧化剂,是细胞合成的抗氧化剂,通过其巯基氧化-还原态的转换,作为可逆的供氧体,主要在细胞内的水相提供氧化保护;GSH对贫血、中毒或组织炎症造成的全身或局部低氧血症患者,可减轻细胞损伤,促进修复;由于其临床作用广泛,因此广泛用于肝、肾损害及糖尿病等多系统、多脏器疾病的辅助治疗。
目前,注射用还原型谷胱甘肽剂型为粉针剂,粉针主要有无菌粉末和冻干粉末,由于无菌粉末在制备过程中存在较多的问题,如:装量差异、溶解性及澄明度较差、容易造成污染,特别是涉及到生化药品时,对原辅料和制备工艺要求更高。
而冻干粉末的制备,现在已有的冻干工艺分为两种,第一种是将原料冻干,在无菌操作条件下经过粉碎过筛后进行粉末灌装,虽然其冻干成本较低,但经该方法制备的注射用还原型谷胱甘肽药粉易吸潮,易分解变质,影响用药安全,还易造成装量不足;第二种是将药物配制成液体后直接进行无菌分装,然后进行冷冻干燥,其优点是装量差异容易控制,可增强药物的稳定性,缺点是对于还原型谷胱甘肽而言,冻干的条件不易控制,造成废品率较高,乃至于影响药品在有效期内的稳定性;现有的第二种方法对于还原型谷胱甘肽这个产品冻干效果并不好,业界内都认为这个产品很难,主要是在处方的选择、溶液的配置及冻干过程的控制等环节造成的。
发明内容
本发明的目的是提供一种高稳定注射用还原型谷胱甘肽的制备方法,稳定性较好,单杂、总杂较少。
为了实现上述目的,本发明的技术方案为:高稳定注射用还原型谷胱甘肽,其特征在于:当为0.6g规格注射用还原型谷胱甘肽,配方组分为:
还原型谷胱甘肽0.6g
10%氢氧化钠溶液调pH至6.0~7.0
注射用水加至2g
当为1.0g规格注射用还原型谷胱甘肽,配方组分为:
还原型谷胱甘肽1.0g
10%氢氧化钠溶液调pH至6.0~7.0
注射用水加至3.3g
当为1.5g规格注射用还原型谷胱甘肽,配方组分为:
还原型谷胱甘肽1.5g
10%氢氧化钠溶液调pH至6.0~7.0
注射用水加至5.0g
其中,在配液过程中,配液和灌装过程中不断充氮气保持溶液中氧含量在1.5ppm以下;
制备所述的高稳定注射用还原型谷胱甘肽的方法,包括如下步骤:
步骤1:称取处方量30%的注射用水,冷至20℃~30℃,往注射用水中充高纯氮气置换溶液中的氧气至溶液中氧含量小于1.5ppm;
步骤2:加入处方量谷胱甘肽原料药,搅拌;同时加入10%氢氧化钠溶液,配液和灌装过程中不断充氮气保持溶液中氧含量小于1.5ppm;
步骤3:搅拌使配液溶解澄清,加注射用水至全量,并通过10%氢氧化钠溶液调节pH值至6.0~7.0;
步骤4:加入0.1%的针剂用活性炭,加入后搅拌10分钟;用0.22μm的孔滤膜初滤除炭,再用0.22μm的微孔滤膜精滤;
步骤5:采用7ml低硼硅玻璃管制注射剂瓶灌装,每瓶灌装2g,进行冷冻干燥;
冷冻干燥包括如下步骤,
在20℃至30℃条件下配液灌装,将样品放入冻干机中,迅速将板层温度降至-40℃,保温1h,当隔板温度温至-10℃±2℃时,保温1h,再在1h内迅速将板层温度降至-40℃,保温2~4h,转冷阱-50℃后抽真空到10Pa以下,第一次板层温度-5℃,保持2~4h,然后在3h内将板层加热到10℃,当制品到0℃时,开始升板层温度至40℃,当制品升至30℃以后,保温4~6h;
步骤6:出箱,轧盖,得到成品。
在上述技术方案中,注射用水温度为20℃~30℃,注射用水中氧含量小于1.5ppm。
在上述技术方案中,步骤5中,冷冻干燥包括如下步骤,
在20℃至30℃条件下配液灌装,将样品放入冻干机中,迅速将板层温度降至-40℃,保温1h,当隔板温度温至-10℃±2℃时,保温1h,再在1h内迅速将板层温度降至-40℃,保温3h,转冷阱-50℃后抽真空到10Pa以下,第一次板层温度-5℃,保持3h,然后在 3h内将板层加热到10℃,当制品到0℃时,开始升板层温度至40℃,当制品升至30℃以后,保温5h。
在上述技术方案中,步骤3中,搅拌使配液溶解澄清,加注射用水至全量,并通过10%氢氧化钠溶液调节pH值至6.9。
本发明具有如下优点:
(1)本发明制得的最终产品为按产品规格定量冻干于管制瓶中的产品,本发明采用反复冻融工艺,其外观为白色多孔的块状物,稳定性较好,单杂、总杂较少;本发明方法制得的产品质量符合国家标准的规定;
(2)本发明的产品制备中并不添加晶体骨架支撑剂等辅料,制得的产品即能得到装量和外观均符合规定的终产品,排除了因添加辅料而带来的产品质量风险,提高用药安全;
(3)本发明制得的产品免去了粉碎和分装操作过程,水分含量低(本发明的水分控制在较低范围内,本发明水分含量小于或等于2.0%),较好地解决了产品在粉碎和分装过程中易吸潮、易氧化分解和被微生物污染的问题;
(4)本发明方法工艺参数简单、易控,产品质量稳定,适宜标准化工业生产,经验证,本发明制备的注射用还原型谷胱甘肽的处方和工艺适合大生产的要求,按照本发明开发的处方和工艺进行本品的生产能有效保证产品的质量,能生产出符合国家标准的规定的产品;本发明制得的最终产品的水分(干燥失重)、有关物质(氧化型谷胱甘肽)等指标均比现有技术制得的产品下降,有效成分(还原型谷胱甘肽)含量指标有所提高;
(5)本发明在生产全过程中采用氮气保护,避免产品与空气中的氧接触,避免产品的氧化。
具体实施方式
下面结合实施例详细说明本发明的实施情况,但它们并不构成对本发明的限定,仅作举例而已。同时通过说明使本发明的优点更加清楚和容易理解。
高稳定注射用还原型谷胱甘肽,其特征在于:当为0.6g规格注射用还原型谷胱甘肽,配方组分为:
还原型谷胱甘肽0.6g
10%氢氧化钠溶液调pH至6.0~7.0
注射用水加至2g
当为1.0g规格注射用还原型谷胱甘肽,配方组分为:
还原型谷胱甘肽1.0g
10%氢氧化钠溶液调pH至6.0~7.0
注射用水加至3.3g
当为1.5g规格注射用还原型谷胱甘肽,配方组分为:
还原型谷胱甘肽1.5g
10%氢氧化钠溶液调pH至6.0~7.0
注射用水加至5.0g
其中,在配液过程中,配液和灌装过程中不断充氮气保持溶液中氧含量在1.5ppm以下;
制备所述的高稳定注射用还原型谷胱甘肽的方法,包括如下步骤:
步骤1:称取处方量约30%的注射用水,冷至20℃~30℃,往注射用水中充高纯氮气置换溶液中的氧气至溶液中氧含量小于1.5ppm;
步骤2:加入处方量谷胱甘肽原料药,搅拌;同时加入10%氢氧化钠溶液,配液和灌装过程中不断充氮气保持溶液中氧含量小于1.5ppm;
步骤3:搅拌使配液溶解澄清,加注射用水至全量,并通过10%氢氧化钠溶液调节pH值至6.0~7.0;
步骤4:加入0.1%的针剂用活性炭,加入后搅拌10分钟;用0.22μm的孔滤膜初滤除炭,再用0.22μm的微孔滤膜精滤;
步骤5:采用7ml低硼硅玻璃管制注射剂瓶灌装,每瓶灌装2g,进行冷冻干燥;
冷冻干燥包括如下步骤,
在20℃至30℃条件下配液灌装,将样品放入冻干机中,迅速将板层温度降至-40℃,保温1h,当隔板温度温至-10℃±2℃时,保温1h,再在1h内迅速将板层温度降至-40℃,保温2~4h,转冷阱-50℃后抽真空到10Pa以下,第一次板层温度-5℃,保持2~4h,然后在3h内将板层加热到10℃,当制品到0℃时,开始升板层温度至40℃,当制品升至30℃以后,保温4~6h;
步骤6:出箱,轧盖,得到成品,配液灌装时间为2h;
低硼硅胶玻璃管制注射剂瓶和注射用无菌粉末用卤化丁基橡胶塞(溴化)包装,再压铝塑组合盖密封,后置纸盒的包装。
进一步地,注射用水温度为20℃~30℃,注射用水中氧含量小于1.5ppm。
进一步地,步骤5中,冷冻干燥包括如下步骤,
在20℃至30℃条件下配液灌装,将样品放入冻干机中,迅速将板层温度降至-40℃,保温1h,当隔板温度温至-10℃±2℃时,保温1h,再在1h内迅速将板层温度降至-40℃,保温3h,转冷阱-50℃后抽真空到10Pa以下,第一次板层温度-5℃,保持3h,然后在 3h内将板层加热到10℃,当制品到0℃时,开始升板层温度至40℃,当制品升至30℃以后,保温5h。
更进一步地,步骤3中,搅拌使配液溶解澄清,加注射用水至全量,并通过10%氢氧化钠溶液调节pH值至6.9。
实施例
现以0.6g规格注射用还原型谷胱甘肽及其制备方法为实施例进行说明,对其他规格注射用还原型谷胱甘肽及其制备方法同样具有指导作用。
实施例1
步骤1:称取处方量约30%的注射用水,冷至20℃~30℃,往注射用水中充高纯氮气置换溶液中的氧气至溶液中氧含量小于1.5ppm;
步骤2:加入处方量谷胱甘肽原料药,搅拌;同时加入10%氢氧化钠溶液,配液和灌装过程中不断充氮气保持溶液中氧含量小于1.5ppm;
步骤3:搅拌使配液溶解澄清,加注射用水至全量,并通过10%氢氧化钠溶液调节pH值至6.0;
步骤4:加入0.1%的针剂用活性炭,加入后搅拌10分钟;用0.22μm的孔滤膜初滤除炭,再用0.22μm的微孔滤膜精滤;
步骤5:采用7ml低硼硅玻璃管制注射剂瓶灌装,每瓶灌装2g,进行冷冻干燥;
冷冻干燥包括如下步骤,
在20℃至30℃条件下配液灌装,将样品放入冻干机中,迅速将板层温度降至-40℃,保温1h,当隔板温度温至-10℃±2℃时,保温1h,再在1h内迅速将板层温度降至-40℃,保温2h,转冷阱-50℃后抽真空到10Pa以下,第一次板层温度-5℃,保持4h,然后在3h内将板层加热到10℃,当制品到0℃时,开始升板层温度至40℃,当制品升至30℃以后,保温4h;
步骤6:出箱,轧盖,得到成品。
实施例2
步骤1:称取处方量约30%的注射用水,冷至20℃~30℃,往注射用水中充高纯氮气置换溶液中的氧气至溶液中氧含量小于1.5ppm;
步骤2:加入处方量谷胱甘肽原料药,搅拌;同时加入10%氢氧化钠溶液,配液和灌装过程中不断充氮气保持溶液中氧含量小于1.5ppm;
步骤3:搅拌使配液溶解澄清,加注射用水至全量,并通过10%氢氧化钠溶液调节pH值至7.0;
步骤4:加入0.1%的针剂用活性炭,加入后搅拌10分钟;用0.22μm的孔滤膜初滤除炭,再用0.22μm的微孔滤膜精滤;
步骤5:采用7ml低硼硅玻璃管制注射剂瓶灌装,每瓶灌装2g,进行冷冻干燥;
冷冻干燥包括如下步骤,
在20℃至30℃条件下配液灌装,将样品放入冻干机中,迅速将板层温度降至-40℃,保温1h,当隔板温度温至-10℃±2℃时,保温1h,再在1h内迅速将板层温度降至-40℃,保温4h,转冷阱-50℃后抽真空到10Pa以下,第一次板层温度-5℃,保持2h,然后在 3h内将板层加热到10℃,当制品到0℃时,开始升板层温度至40℃,当制品升至30℃以后,保温6h;
步骤6:出箱,轧盖,得到成品。
实施例3
步骤1:称取处方量约30%的注射用水,冷至20℃~30℃,往注射用水中充高纯氮气置换溶液中的氧气至溶液中氧含量小于1.5ppm;
步骤2:加入处方量谷胱甘肽原料药,搅拌;同时加入的10%氢氧化钠溶液,配液和灌装过程中不断充氮气保持溶液中氧含量小于1.5ppm;
步骤3:搅拌使配液溶解澄清,加注射用水至全量,并通过10%氢氧化钠溶液调节pH值至6.9;
步骤4:加入0.1%的针剂用活性炭,加入后搅拌10分钟;用0.22μm的孔滤膜初滤除炭,再用0.22μm的微孔滤膜精滤;
步骤5:采用7ml低硼硅玻璃管制注射剂瓶灌装,每瓶灌装2g,进行冷冻干燥;
冷冻干燥包括如下步骤,
在20℃至30℃条件下配液灌装,将样品放入冻干机中,迅速将板层温度降至-40℃,保温1h,当隔板温度温至-10℃±2℃时,保温1h,再在1h内迅速将板层温度降至-40℃,保温3h,转冷阱-50℃后抽真空到10Pa以下,第一次板层温度-5℃,保持3h,然后在 3h内将板层加热到10℃,当制品到0℃时,开始升板层温度至40℃,当制品升至30℃以后,保温3h;
步骤6:出箱,轧盖,得到成品。
实施例4
步骤1:称取处方量约30%的注射用水,冷至20℃~30℃,往注射用水中充高纯氮气置换溶液中的氧气至溶液中氧含量小于1.5ppm;
步骤2:加入处方量谷胱甘肽原料药,搅拌;同时加入的10%氢氧化钠溶液,配液和灌装过程中不断充氮气保持溶液中氧含量小于1.5ppm;
步骤3:搅拌使配液溶解澄清,加注射用水至全量,并通过10%氢氧化钠溶液调节pH值至6.8;
步骤4:加入0.1%的针剂用活性炭,加入后搅拌10分钟;用0.22μm的孔滤膜初滤除炭,再用0.22μm的微孔滤膜精滤;
步骤5:采用7ml低硼硅玻璃管制注射剂瓶灌装,每瓶灌装2g,进行冷冻干燥;
冷冻干燥包括如下步骤,
在20℃至30℃条件下配液灌装,将样品放入冻干机中,迅速将板层温度降至-40℃,保温1h,当隔板温度温至-10℃±2℃时,保温1h,再在1h内迅速将板层温度降至-40℃,保温4h,转冷阱-50℃后抽真空到10Pa以下,第一次板层温度-5℃,保持2h,然后在3h内将板层加热到10℃,当制品到0℃时,开始升板层温度至40℃,当制品升至30℃以后,保温5h;
步骤6:出箱,轧盖,得到成品。
质量及稳定性研究结果
取上述实施例1-4制得的注射用还原型谷胱甘肽,进行质量及稳定性研究,
表1质量对比表
由上表可知,上述实施例制得的注射用还原型谷胱甘肽性状均符合要求,所有批次样品的冻干前后pH值基本一致,实施例3制得的注射用还原型谷胱甘肽的干燥失重较低,实施例1制得的注射用还原型谷胱甘肽的干燥失重较高。
表2高温试验对比表
由上表可知,经过高温40℃考察10天后,各实施例制得的注射用还原型谷胱甘肽性状均未发生变化,单杂和总杂增加幅度基本一致,其中实施例1制得的注射用还原型谷胱甘肽单杂和总杂较高。
现对实施例1制得的注射用还原型谷胱甘肽的稳定性进行试验,试验结果如下:
表3稳定性对比表
由上表可知,与0天的结果进行比较,除60℃高温杂质变化较大外,光照10天和加速2月样品的各检测指标均没有发生显著性变化,各项指标仍符合国家标准的规定,表明实施例1制备出的注射用还原型谷胱甘肽稳定性能良好。
选取代表性的批次,分别为实施例1配方的中试放大批的试生产和工艺验证三批的生产,详见表4;
表4代表性批次汇总表
按照拟定的注射还原型谷胱甘肽质量标准草案对中试样品和验证样品进行检测,并和市售品的主要指标进行对比分析,验证批样品和市售品的检测结果见表5-表6。
表5代表性批次样品和市售品质量检测结果一
表6代表性批次样品和市售品质量检测结果二
经检测批中试样品和三批验证样品的各项指标均符合拟定的注射还原型谷胱甘肽质量标准草案,且几批样品杂质个数、位置、单杂和总杂含量基本一致,说明样品的批间差异小;与市售品比较,本品六批样品杂质个数和位置与市售品一致,单杂和总杂略小于市售品;其它重要指标,如干燥失重、pH值和含量与市售品基本一致,表明本发明产品和市售品的质量一致。
综上,本发明所述的注射用还原型谷胱甘肽的处方和工艺适合大生产的要求,按照本发明处方和工艺进行本品的生产能有效保证产品的质量,能生产出和市售品质量一致的产品。
还原型谷胱甘肽的杂质内容如下所示:
杂质A
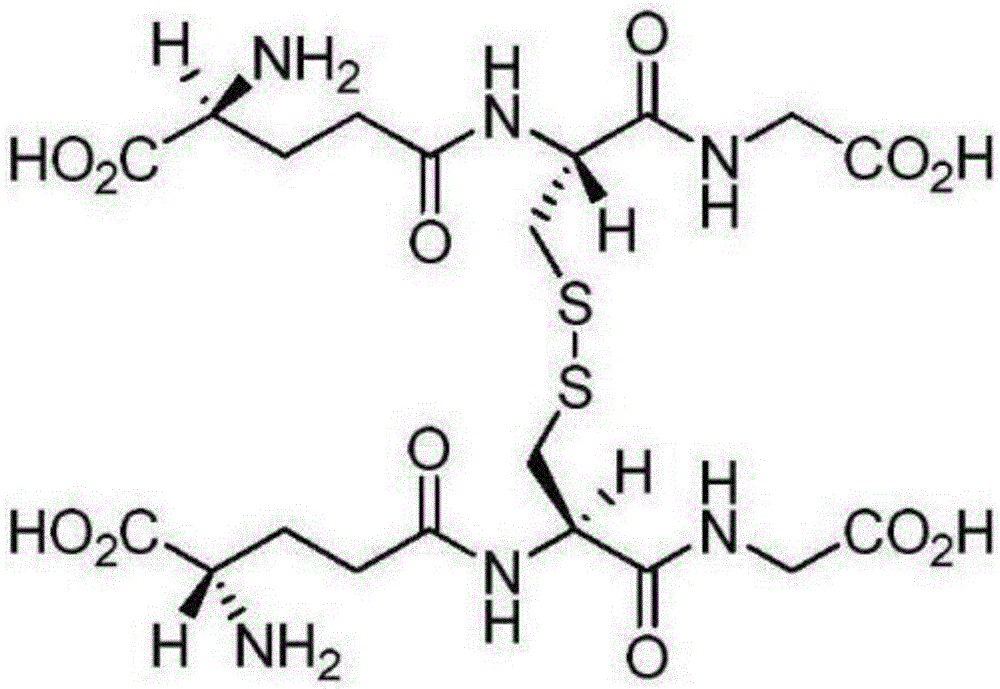
化学名称:双(L-γ-谷氨酰基-L-半胱氨酰基甘氨酸)二硫化物(L-氧化型谷胱甘肽)
结构式:
分子式:C20H32N6O12S2
分子量:612.63
杂质B
化学名称:L-半胱氨酰甘氨酸
结构式:
分子式:C5H10N2O3S
分子量:178.21
杂质D
化学名称:(5S)-2-吡咯烷酮-5-羧酸
结构式:
分子式:C5H7NO3
分子量:129.11
配伍试验结果
结合国内的注射剂常用溶剂,选择0.9%氯化钠注射液、5%葡萄糖注射液、10%葡萄糖注射液、注射用水进行本品常温条件下的配伍实验。
样品名称:本发明产品(批号P-110201,规格0.6g)
配伍注射液:
0.9%氯化钠注射液,重庆迪康长江制药有限公司生产
5%葡萄糖注射液,太极西南药业股份有限公司生产
10%葡萄糖注射液,太极西南药业股份有限公司生产
注射用水,自制
考察时间:0h、2h、4h、6h
考察指标:澄清度、pH值、可见异物、不溶性微粒、有关物质(面积归一化法计)(分别稀释成测定浓度,仅在0h、2h、4h、6h测定)常温条件下本发明产品在四种注射液中结果见表7-表8。
表7常温条件下本发明产品配伍试验结果(一)
表8配伍稳定性试验结果(二)(以面积归一化法计)
本发明产品分别与0.9%氯化钠注射液、5%葡萄糖注射液、10%葡萄糖注射液、注射用水配伍后,溶液在常温下放置6h,除有关物质中杂质A(氧化型谷胱甘肽)可能由于与各溶剂中的氧气发生反应增大外,其它指标均未发生明显变化,各项检测指标均符合国家标准的规定,由此可见,本发明配伍性较好。
本发明产品与市售品的主要指标对比结果
(1)有关物质
样品:中试样品(生产批号:P-110201)、工艺验证样品(生产批号:YJ110401、YJ110402和YJ110403)和市售品(生产批号:31002)。
对比条件:0月、加速6月试验。
本发明产品和市售品的有关物质对比见表9。
表9有关物质的对比结果(以面积归一化法计)
(2)其它指标
样品:中试样品(生产批号:P-110201)、三批工艺验证样品(生产批号:YJ110401、YJ110402和YJ110403)和市售品(生产批号::31002)。
对比条件:0月、加速6月和长期12月试验。
考察指标:性状、酸度、溶液澄清度与颜色、干燥失重、可见异物、不溶性微粒、细菌内毒素、无菌和含量。
其它指标的对比结果见10-表12。
表10 0.6g规格其它指标的对比结果
表11 1.0g规格其它指标的对比结果
表12 1.5g规格其它指标的对比结果
按照拟定的注射还原型谷胱甘肽质量标准草案对中试样品和验证样品进行检测,并和市售品的主要指标进行对比分析,验证批样品和市售品的检测结果见上表10-表12。
经检测批中试样品和三批验证样品的各项指标均符合拟定的注射还原型谷胱甘肽质量标准草案,且几批样品杂质个数、位置、单杂和总杂含量基本一致,说明样品的批间差异小;与市售品比较,本品六批样品杂质个数和位置与市售品一致,单杂和总杂略小于市售品;其它重要指标,如性状、酸度、溶液澄清度与颜色、干燥失重、可见异物、不溶性微粒、细菌内毒素、无菌和含量与市售品基本一致,表明本发明产品和市售品的质量一致。
动物实验
高稳定注射用还原型谷胱甘肽由湖北人民制药有限公司提供,由成都岐黄药物非临床研究有限公司完成该药的特殊安全性试验研究。
按国家食品药品监督管理局《药品注册管理办法》的规定要求,设计了本试验方案并完成了试验工作,结果如下:
(1)高稳定注射用还原型谷胱甘肽血管刺激性试验中,家兔耳缘静脉对照组、市售组及受试组均无充血、出血和变性坏死现象出现,亦无病理性损害,表明本发明高稳定注射用还原型谷胱甘肽(本发明选用批号为YJ110401的样品)静脉给药对家兔耳血管未产生刺激反应;
(2)高稳定注射用还原型谷胱甘肽肌肉单次给药刺激性试验中,家兔腿股二头肌对照组、市售组及受试组无红肿、充血和变性坏死现象出现,亦无病理性损害,表明本发明高稳定注射用还原型谷胱甘肽(批号为YJ110401)肌内单次注射对家兔股二头肌未产生刺激反应;
(3)高稳定注射用还原型谷胱甘肽肌肉多次给药刺激性试验中,家兔腿股二头肌对照组无红肿、充血和变性坏死现象出现,亦无病理性损害;市售组及受试组停药48小时各有一只家兔股二头肌可见变性、坏死及炎细胞浸润;市售组恢复7天可见一只家兔股二头肌变性、坏死及炎细胞浸润;表明本发明高稳定注射用还原型谷胱甘肽(批号为YJ110401)肌内多次注射对家兔股二头肌有一定刺激性,但具有可恢复性;
(4)高稳定注射用还原型谷胱甘肽溶血性试验中,本发明高稳定注射用还原型谷胱甘肽(批号为YJ110401)受试管均无溶血现象发生,振摇后红细胞可分散,无凝聚现象;
(5)高稳定注射用还原型谷胱甘肽全身主动过敏性试验中,受试组豚鼠激发时(脚背静脉注射)未出现全身过敏反应,表明本发明高稳定注射用还原型谷胱甘肽(批号为YJ110401)对豚鼠未产生全身主动过敏反应;
(6)高稳定注射用还原型谷胱甘肽被动皮肤过敏试验中,豚鼠激发后,受试组蓝斑直径、浸出液吸光度与阴性组比较无差异,与阳性组比较有显著差异,表明本发明高稳定注射用还原型谷胱甘肽(批号为YJ110401)对豚鼠未产生被动皮肤过敏反应。
结论:本发明批号为YJ110401的高稳定注射用还原型谷胱甘肽特殊安全性试验中,血管刺激性试验、肌肉单次给药刺激性试验未见相关刺激,未见溶血和过敏反应;肌肉多次给药刺激性试验显示肌内多次注射对家兔股二头肌有一定刺激性,但具有可恢复性;结合药品说明书的注意事项:肌内注射仅限于需要此途径给药时使用,并应避免同一部位反复注射;提示临床使用时应避免同一部位多次肌内注射给药。
其它未说明的部分均属于现有技术。
Claims (3)
1.高稳定注射用还原型谷胱甘肽的制备方法,其特征在于:当为0.6g规格注射用还原型谷胱甘肽,配方组分为:
还原型谷胱甘肽0.6g
10%氢氧化钠溶液调pH至6.0~7.0
注射用水加至2g
当为1.0g规格注射用还原型谷胱甘肽,配方组分为:
还原型谷胱甘肽1.0g
10%氢氧化钠溶液调pH至6.0~7.0
注射用水加至3.3g
当为1.5g规格注射用还原型谷胱甘肽,配方组分为:
还原型谷胱甘肽1.5g
10%氢氧化钠溶液调pH至6.0~7.0
注射用水加至5.0g
其中,在配液过程中,配液和灌装过程中不断充氮气保持溶液中氧含量在1.5ppm以下;
制备所述的高稳定注射用还原型谷胱甘肽的方法,由如下依次执行的步骤组成:
步骤1:称取处方量30%的注射用水,冷至20℃~30℃,往注射用水中充高纯氮气置换溶液中的氧气至溶液中氧含量小于1.5ppm;
步骤2:加入处方量谷胱甘肽原料药,搅拌;同时加入10%氢氧化钠溶液,配液和灌装过程中不断充氮气保持溶液中氧含量小于1.5ppm;
步骤3:搅拌使配液溶解澄清,加注射用水至全量,并通过10%氢氧化钠溶液调节pH值至6.0~7.0;
步骤4:加入0.1%的针剂用活性炭,加入后搅拌10分钟;用0.22μm的孔滤膜初滤除炭,再用0.22μm的微孔滤膜精滤;
步骤5:采用7ml低硼硅玻璃管制注射剂瓶灌装,每瓶灌装2g,进行冷冻干燥;
冷冻干燥包括如下步骤,
在20℃至30℃条件下配液灌装,将样品放入冻干机中,迅速将板层温度降至-40℃,保温1h,当隔板温度温至-10℃±2℃时,保温1h,再在1h内迅速将板层温度降至-40℃,保温2~4h,转冷阱-50℃后抽真空到10Pa以下,第一次板层温度-5℃,保持2~4h,然后在3h内将板层加热到10℃,当制品到0℃时,开始升板层温度至40℃,当制品升至30℃以后,保温4~6h;
步骤6:出箱,轧盖,得到成品。
2.根据权利要求1所述的高稳定注射用还原型谷胱甘肽的制备方法,其特征在于:步骤5中,冷冻干燥包括如下步骤,
在20℃至30℃条件下配液灌装,将样品放入冻干机中,迅速将板层温度降至-40℃,保温1h,当隔板温度温至-10℃±2℃时,保温1h,再在1h内迅速将板层温度降至-40℃,保温3h,转冷阱-50℃后抽真空到10Pa以下,第一次板层温度-5℃,保持3h,然后在3h内将板层加热到10℃,当制品到0℃时,开始升板层温度至40℃,当制品升至30℃以后,保温5h。
3.根据权利要求2所述的高稳定注射用还原型谷胱甘肽的制备方法,其特征在于:步骤3中,搅拌使配液溶解澄清,加注射用水至全量,并通过10%氢氧化钠溶液调节pH值至6.9。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201810530808.9A CN108567970B (zh) | 2018-05-25 | 2018-05-25 | 注射用还原型谷胱甘肽的制备方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201810530808.9A CN108567970B (zh) | 2018-05-25 | 2018-05-25 | 注射用还原型谷胱甘肽的制备方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN108567970A CN108567970A (zh) | 2018-09-25 |
| CN108567970B true CN108567970B (zh) | 2021-09-24 |
Family
ID=63572971
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201810530808.9A Active CN108567970B (zh) | 2018-05-25 | 2018-05-25 | 注射用还原型谷胱甘肽的制备方法 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN108567970B (zh) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN112535725A (zh) * | 2020-12-29 | 2021-03-23 | 山东罗欣药业集团股份有限公司 | 一种注射用还原型谷胱甘肽及其制备方法 |
Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB741498A (en) * | 1952-05-24 | 1955-12-07 | Schwarz Lab Inc | Improvements in or relating to a glutathione composition for parenteral injection and process of preparing such composition |
| CN1970075A (zh) * | 2005-11-24 | 2007-05-30 | 山东绿叶制药有限公司 | 还原型谷胱甘肽冻干粉针制剂及其制备工艺 |
| CN1994461A (zh) * | 2006-01-06 | 2007-07-11 | 上海复旦复华药业有限公司 | 一种制备注射用还原型谷胱甘肽的冻干工艺 |
| CN101074202A (zh) * | 2006-05-16 | 2007-11-21 | 重庆药友制药有限责任公司 | 一种注射用还原型谷胱甘肽的制备方法 |
| CN101642441A (zh) * | 2009-08-31 | 2010-02-10 | 重庆福安药业有限公司 | 一种头孢磺啶钠冻干粉、其制剂及制备方法 |
| CN101647783A (zh) * | 2009-07-24 | 2010-02-17 | 上海复旦复华药业有限公司 | 一种用冻干法制备注射用还原型谷胱甘肽时的预冻方法 |
| CN101991548A (zh) * | 2009-08-11 | 2011-03-30 | 安英 | 还原型谷胱甘肽冻干粉针剂及其制备方法 |
| CN102151251A (zh) * | 2011-01-11 | 2011-08-17 | 山东绿叶制药有限公司 | 一种注射用还原型谷胱甘肽的冻干方法 |
| CN102670523A (zh) * | 2011-03-18 | 2012-09-19 | 海南中化联合制药工业股份有限公司 | 一种注射用还原型谷胱甘肽冻干粉制备方法 |
| CN105434368A (zh) * | 2014-11-27 | 2016-03-30 | 广州白云山明兴制药有限公司 | 一种注射用还原型谷胱甘肽及其预冻方法 |
-
2018
- 2018-05-25 CN CN201810530808.9A patent/CN108567970B/zh active Active
Patent Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB741498A (en) * | 1952-05-24 | 1955-12-07 | Schwarz Lab Inc | Improvements in or relating to a glutathione composition for parenteral injection and process of preparing such composition |
| CN1970075A (zh) * | 2005-11-24 | 2007-05-30 | 山东绿叶制药有限公司 | 还原型谷胱甘肽冻干粉针制剂及其制备工艺 |
| CN1994461A (zh) * | 2006-01-06 | 2007-07-11 | 上海复旦复华药业有限公司 | 一种制备注射用还原型谷胱甘肽的冻干工艺 |
| CN101074202A (zh) * | 2006-05-16 | 2007-11-21 | 重庆药友制药有限责任公司 | 一种注射用还原型谷胱甘肽的制备方法 |
| CN101647783A (zh) * | 2009-07-24 | 2010-02-17 | 上海复旦复华药业有限公司 | 一种用冻干法制备注射用还原型谷胱甘肽时的预冻方法 |
| CN101991548A (zh) * | 2009-08-11 | 2011-03-30 | 安英 | 还原型谷胱甘肽冻干粉针剂及其制备方法 |
| CN101642441A (zh) * | 2009-08-31 | 2010-02-10 | 重庆福安药业有限公司 | 一种头孢磺啶钠冻干粉、其制剂及制备方法 |
| CN102151251A (zh) * | 2011-01-11 | 2011-08-17 | 山东绿叶制药有限公司 | 一种注射用还原型谷胱甘肽的冻干方法 |
| CN102670523A (zh) * | 2011-03-18 | 2012-09-19 | 海南中化联合制药工业股份有限公司 | 一种注射用还原型谷胱甘肽冻干粉制备方法 |
| CN105434368A (zh) * | 2014-11-27 | 2016-03-30 | 广州白云山明兴制药有限公司 | 一种注射用还原型谷胱甘肽及其预冻方法 |
Non-Patent Citations (1)
| Title |
|---|
| 注射用还原型谷胱甘肽的处方工艺研究;宋涵,等;《医药制剂》;20151031;第104-105页 * |
Also Published As
| Publication number | Publication date |
|---|---|
| CN108567970A (zh) | 2018-09-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN113150867B (zh) | 一种富含灵芝三萜的灵芝萃取油的制备方法 | |
| CN106420398A (zh) | 一种免洗水性喷雾型护发素及其制备方法 | |
| CN104140949B (zh) | 囊胚培养液及其制备方法 | |
| CN110218756B (zh) | 一种具有抗衰作用的富硒鲟鱼骨肽提取方法及产品 | |
| CN100500145C (zh) | 炎琥宁冻干粉针剂及其制备方法 | |
| CN108498468B (zh) | 注射用甲泼尼龙琥珀酸钠 | |
| CN108567970B (zh) | 注射用还原型谷胱甘肽的制备方法 | |
| CN104490795B (zh) | 一种含缩宫素药物组合物的注射剂及其制备方法 | |
| CN104140948A (zh) | 卵子与胚胎处理液及其制备方法 | |
| CN112353734A (zh) | 一种积雪草发酵产物的发酵方法及其在修复功效化妆品中的应用 | |
| CN103494780A (zh) | 一种注射用加米霉素组合物冻干粉及制备方法 | |
| CN103110576A (zh) | 一种香菇多糖注射液制剂及其制备方法 | |
| CN103142507B (zh) | 一种注射用克林霉素磷酸酯制剂及其制备方法 | |
| CN114601792A (zh) | 一种甲钴胺注射液的制备方法 | |
| CN106674225B (zh) | 一种核黄素磷酸钠化合物及其药物组合物 | |
| CN102488706B (zh) | 一种防治尿结石的药物及其制备方法和应用 | |
| CN100497650C (zh) | 一种富锌亮菌多糖及其制备方法和用途 | |
| CN114656576B (zh) | 一种环磷酸腺苷-大枣酸性多糖复合物及制备方法与应用 | |
| CN107281122A (zh) | 一种左旋奥拉西坦冻干粉针及其制备方法 | |
| CN107281135A (zh) | 一种注射用左旋奥拉西坦冻干粉及其制备方法 | |
| CN108815166A (zh) | 一种复方维生素注射液及其制备方法 | |
| CN107281126B (zh) | 一种稳定性好的(s)-4-羟基-2氧代-1-吡咯烷乙酰胺冻干粉针及其制备方法 | |
| CN105769776A (zh) | 一种治疗非霍奇金淋巴瘤的冻干组合物及其制备方法 | |
| CN107281128A (zh) | 一种杂质少的左旋奥拉西坦无菌粉末及其制备方法 | |
| CN113143850A (zh) | 一种猫用眼睛凝胶及其制备方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PB01 | Publication | ||
| PB01 | Publication | ||
| SE01 | Entry into force of request for substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| GR01 | Patent grant | ||
| GR01 | Patent grant |