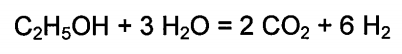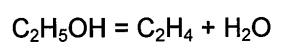BRPI1002970B1 - processo para a produção de hidrogênio a partir do etanol - Google Patents
processo para a produção de hidrogênio a partir do etanol Download PDFInfo
- Publication number
- BRPI1002970B1 BRPI1002970B1 BRPI1002970-2A BRPI1002970A BRPI1002970B1 BR PI1002970 B1 BRPI1002970 B1 BR PI1002970B1 BR PI1002970 A BRPI1002970 A BR PI1002970A BR PI1002970 B1 BRPI1002970 B1 BR PI1002970B1
- Authority
- BR
- Brazil
- Prior art keywords
- ethanol
- hydrogen
- catalyst
- catalysts
- mol
- Prior art date
Links
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 title claims abstract description 183
- 238000000034 method Methods 0.000 title claims abstract description 80
- 239000001257 hydrogen Substances 0.000 title claims abstract description 78
- 229910052739 hydrogen Inorganic materials 0.000 title claims abstract description 78
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 title claims abstract description 71
- 230000008569 process Effects 0.000 title claims abstract description 54
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 46
- 239000003054 catalyst Substances 0.000 claims abstract description 111
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 claims abstract description 73
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 claims abstract description 58
- 239000007789 gas Substances 0.000 claims abstract description 37
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims abstract description 36
- 238000000629 steam reforming Methods 0.000 claims abstract description 23
- 238000006243 chemical reaction Methods 0.000 claims description 34
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 claims description 26
- 229910052700 potassium Inorganic materials 0.000 claims description 16
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 claims description 15
- 239000000203 mixture Substances 0.000 claims description 15
- 239000011591 potassium Substances 0.000 claims description 15
- -1 magnesium aluminate Chemical class 0.000 claims description 14
- 229910052783 alkali metal Inorganic materials 0.000 claims description 12
- 150000001340 alkali metals Chemical class 0.000 claims description 12
- 239000011777 magnesium Substances 0.000 claims description 9
- 229910052749 magnesium Inorganic materials 0.000 claims description 9
- 229910000480 nickel oxide Inorganic materials 0.000 claims description 9
- GNRSAWUEBMWBQH-UHFFFAOYSA-N oxonickel Chemical compound [Ni]=O GNRSAWUEBMWBQH-UHFFFAOYSA-N 0.000 claims description 9
- XFWJKVMFIVXPKK-UHFFFAOYSA-N calcium;oxido(oxo)alumane Chemical compound [Ca+2].[O-][Al]=O.[O-][Al]=O XFWJKVMFIVXPKK-UHFFFAOYSA-N 0.000 claims description 8
- 230000003197 catalytic effect Effects 0.000 claims description 7
- 150000001875 compounds Chemical class 0.000 claims description 7
- 229910000510 noble metal Inorganic materials 0.000 claims description 7
- AOWKSNWVBZGMTJ-UHFFFAOYSA-N calcium titanate Chemical compound [Ca+2].[O-][Ti]([O-])=O AOWKSNWVBZGMTJ-UHFFFAOYSA-N 0.000 claims description 5
- 230000009467 reduction Effects 0.000 claims description 5
- UGFAIRIUMAVXCW-UHFFFAOYSA-N Carbon monoxide Chemical compound [O+]#[C-] UGFAIRIUMAVXCW-UHFFFAOYSA-N 0.000 claims description 4
- 229910002091 carbon monoxide Inorganic materials 0.000 claims description 4
- 229910052697 platinum Inorganic materials 0.000 claims description 4
- 229910052763 palladium Inorganic materials 0.000 claims description 3
- 229910052751 metal Inorganic materials 0.000 claims 3
- 230000001737 promoting effect Effects 0.000 claims 2
- LFQSCWFLJHTTHZ-HQMMCQRPSA-N Ethanol-14C Chemical compound C[14CH2]O LFQSCWFLJHTTHZ-HQMMCQRPSA-N 0.000 claims 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 claims 1
- 150000001342 alkaline earth metals Chemical class 0.000 claims 1
- 239000002184 metal Substances 0.000 claims 1
- 229910044991 metal oxide Inorganic materials 0.000 claims 1
- 150000004706 metal oxides Chemical class 0.000 claims 1
- 238000004064 recycling Methods 0.000 claims 1
- 230000015572 biosynthetic process Effects 0.000 abstract description 23
- 229910052759 nickel Inorganic materials 0.000 abstract description 21
- 150000001336 alkenes Chemical class 0.000 abstract description 10
- 239000002994 raw material Substances 0.000 abstract description 7
- 238000002203 pretreatment Methods 0.000 abstract description 5
- 238000003786 synthesis reaction Methods 0.000 abstract description 5
- 239000002028 Biomass Substances 0.000 abstract description 3
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 48
- 239000011787 zinc oxide Substances 0.000 description 24
- 235000014692 zinc oxide Nutrition 0.000 description 23
- 239000007864 aqueous solution Substances 0.000 description 18
- 239000000571 coke Substances 0.000 description 17
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 15
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 14
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 12
- 239000005977 Ethylene Substances 0.000 description 12
- 239000000243 solution Substances 0.000 description 11
- 229910018590 Ni(NO3)2-6H2O Inorganic materials 0.000 description 10
- MCMNRKCIXSYSNV-UHFFFAOYSA-N Zirconium dioxide Chemical compound O=[Zr]=O MCMNRKCIXSYSNV-UHFFFAOYSA-N 0.000 description 10
- 238000005470 impregnation Methods 0.000 description 10
- CPLXHLVBOLITMK-UHFFFAOYSA-N Magnesium oxide Chemical compound [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 9
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 9
- CETPSERCERDGAM-UHFFFAOYSA-N ceric oxide Chemical compound O=[Ce]=O CETPSERCERDGAM-UHFFFAOYSA-N 0.000 description 9
- 229910000422 cerium(IV) oxide Inorganic materials 0.000 description 9
- 229930195733 hydrocarbon Natural products 0.000 description 9
- 150000002430 hydrocarbons Chemical class 0.000 description 9
- 239000003345 natural gas Substances 0.000 description 9
- 239000012071 phase Substances 0.000 description 9
- 238000002360 preparation method Methods 0.000 description 9
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 8
- IKHGUXGNUITLKF-UHFFFAOYSA-N Acetaldehyde Chemical class CC=O IKHGUXGNUITLKF-UHFFFAOYSA-N 0.000 description 7
- 229910002092 carbon dioxide Inorganic materials 0.000 description 7
- 150000002431 hydrogen Chemical class 0.000 description 7
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N Propane Chemical compound CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 description 6
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 6
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 6
- 239000011575 calcium Substances 0.000 description 6
- 230000009849 deactivation Effects 0.000 description 6
- 238000009826 distribution Methods 0.000 description 6
- 239000001301 oxygen Substances 0.000 description 6
- 229910052760 oxygen Inorganic materials 0.000 description 6
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Substances [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 description 6
- IKHGUXGNUITLKF-XPULMUKRSA-N acetaldehyde Chemical compound [14CH]([14CH3])=O IKHGUXGNUITLKF-XPULMUKRSA-N 0.000 description 5
- 239000002253 acid Substances 0.000 description 5
- 239000003463 adsorbent Substances 0.000 description 5
- 239000006227 byproduct Substances 0.000 description 5
- 229910052791 calcium Inorganic materials 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- 239000000395 magnesium oxide Substances 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 4
- GNTDGMZSJNCJKK-UHFFFAOYSA-N divanadium pentaoxide Chemical compound O=[V](=O)O[V](=O)=O GNTDGMZSJNCJKK-UHFFFAOYSA-N 0.000 description 4
- 239000000446 fuel Substances 0.000 description 4
- 229910052809 inorganic oxide Inorganic materials 0.000 description 4
- 239000003915 liquefied petroleum gas Substances 0.000 description 4
- KBJMLQFLOWQJNF-UHFFFAOYSA-N nickel(ii) nitrate Chemical compound [Ni+2].[O-][N+]([O-])=O.[O-][N+]([O-])=O KBJMLQFLOWQJNF-UHFFFAOYSA-N 0.000 description 4
- 239000011148 porous material Substances 0.000 description 4
- 238000000746 purification Methods 0.000 description 4
- 239000000377 silicon dioxide Substances 0.000 description 4
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 3
- OTMSDBZUPAUEDD-UHFFFAOYSA-N Ethane Chemical compound CC OTMSDBZUPAUEDD-UHFFFAOYSA-N 0.000 description 3
- 229910002651 NO3 Inorganic materials 0.000 description 3
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 239000001273 butane Substances 0.000 description 3
- 238000001354 calcination Methods 0.000 description 3
- 229910052681 coesite Inorganic materials 0.000 description 3
- 229910052906 cristobalite Inorganic materials 0.000 description 3
- 229910052746 lanthanum Inorganic materials 0.000 description 3
- FZLIPJUXYLNCLC-UHFFFAOYSA-N lanthanum atom Chemical compound [La] FZLIPJUXYLNCLC-UHFFFAOYSA-N 0.000 description 3
- MRELNEQAGSRDBK-UHFFFAOYSA-N lanthanum oxide Inorganic materials [O-2].[O-2].[O-2].[La+3].[La+3] MRELNEQAGSRDBK-UHFFFAOYSA-N 0.000 description 3
- IJDNQMDRQITEOD-UHFFFAOYSA-N n-butane Chemical compound CCCC IJDNQMDRQITEOD-UHFFFAOYSA-N 0.000 description 3
- OFBQJSOFQDEBGM-UHFFFAOYSA-N n-pentane Natural products CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 3
- KTUFCUMIWABKDW-UHFFFAOYSA-N oxo(oxolanthaniooxy)lanthanum Chemical compound O=[La]O[La]=O KTUFCUMIWABKDW-UHFFFAOYSA-N 0.000 description 3
- 239000000047 product Substances 0.000 description 3
- 239000001294 propane Substances 0.000 description 3
- 235000012239 silicon dioxide Nutrition 0.000 description 3
- 238000013112 stability test Methods 0.000 description 3
- 229910052682 stishovite Inorganic materials 0.000 description 3
- 229910052905 tridymite Inorganic materials 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 2
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- ZOKXTWBITQBERF-UHFFFAOYSA-N Molybdenum Chemical compound [Mo] ZOKXTWBITQBERF-UHFFFAOYSA-N 0.000 description 2
- 229910018054 Ni-Cu Inorganic materials 0.000 description 2
- 229910018481 Ni—Cu Inorganic materials 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 150000001412 amines Chemical class 0.000 description 2
- 229910021529 ammonia Inorganic materials 0.000 description 2
- 235000011114 ammonium hydroxide Nutrition 0.000 description 2
- 229910000420 cerium oxide Inorganic materials 0.000 description 2
- 239000003638 chemical reducing agent Substances 0.000 description 2
- 229910017052 cobalt Inorganic materials 0.000 description 2
- 239000010941 cobalt Substances 0.000 description 2
- GUTLYIVDDKVIGB-UHFFFAOYSA-N cobalt atom Chemical compound [Co] GUTLYIVDDKVIGB-UHFFFAOYSA-N 0.000 description 2
- 239000000356 contaminant Substances 0.000 description 2
- 238000000354 decomposition reaction Methods 0.000 description 2
- 238000006297 dehydration reaction Methods 0.000 description 2
- 238000006356 dehydrogenation reaction Methods 0.000 description 2
- 230000008021 deposition Effects 0.000 description 2
- 239000000945 filler Substances 0.000 description 2
- 229910052747 lanthanoid Inorganic materials 0.000 description 2
- 150000002602 lanthanoids Chemical class 0.000 description 2
- YIXJRHPUWRPCBB-UHFFFAOYSA-N magnesium nitrate Chemical compound [Mg+2].[O-][N+]([O-])=O.[O-][N+]([O-])=O YIXJRHPUWRPCBB-UHFFFAOYSA-N 0.000 description 2
- 229910052750 molybdenum Inorganic materials 0.000 description 2
- 239000011733 molybdenum Substances 0.000 description 2
- BMMGVYCKOGBVEV-UHFFFAOYSA-N oxo(oxoceriooxy)cerium Chemical compound [Ce]=O.O=[Ce]=O BMMGVYCKOGBVEV-UHFFFAOYSA-N 0.000 description 2
- FKTOIHSPIPYAPE-UHFFFAOYSA-N samarium(III) oxide Inorganic materials [O-2].[O-2].[O-2].[Sm+3].[Sm+3] FKTOIHSPIPYAPE-UHFFFAOYSA-N 0.000 description 2
- 238000001179 sorption measurement Methods 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- 239000010457 zeolite Substances 0.000 description 2
- BNGXYYYYKUGPPF-UHFFFAOYSA-M (3-methylphenyl)methyl-triphenylphosphanium;chloride Chemical compound [Cl-].CC1=CC=CC(C[P+](C=2C=CC=CC=2)(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 BNGXYYYYKUGPPF-UHFFFAOYSA-M 0.000 description 1
- ZZBAGJPKGRJIJH-UHFFFAOYSA-N 7h-purine-2-carbaldehyde Chemical compound O=CC1=NC=C2NC=NC2=N1 ZZBAGJPKGRJIJH-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- ATRRKUHOCOJYRX-UHFFFAOYSA-N Ammonium bicarbonate Chemical compound [NH4+].OC([O-])=O ATRRKUHOCOJYRX-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 229910052684 Cerium Inorganic materials 0.000 description 1
- 229910017488 Cu K Inorganic materials 0.000 description 1
- 229910017541 Cu-K Inorganic materials 0.000 description 1
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 1
- 229910019427 Mg(NO3)2-6H2O Inorganic materials 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 229910018879 Pt—Pd Inorganic materials 0.000 description 1
- 229910021536 Zeolite Inorganic materials 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 239000001099 ammonium carbonate Substances 0.000 description 1
- 235000012501 ammonium carbonate Nutrition 0.000 description 1
- 239000000908 ammonium hydroxide Substances 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 239000001569 carbon dioxide Substances 0.000 description 1
- 239000002041 carbon nanotube Substances 0.000 description 1
- 229910021393 carbon nanotube Inorganic materials 0.000 description 1
- 239000012159 carrier gas Substances 0.000 description 1
- 238000001193 catalytic steam reforming Methods 0.000 description 1
- ZMIGMASIKSOYAM-UHFFFAOYSA-N cerium Chemical compound [Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce] ZMIGMASIKSOYAM-UHFFFAOYSA-N 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000002485 combustion reaction Methods 0.000 description 1
- 239000004035 construction material Substances 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- HNPSIPDUKPIQMN-UHFFFAOYSA-N dioxosilane;oxo(oxoalumanyloxy)alumane Chemical compound O=[Si]=O.O=[Al]O[Al]=O HNPSIPDUKPIQMN-UHFFFAOYSA-N 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 238000004817 gas chromatography Methods 0.000 description 1
- 239000007792 gaseous phase Substances 0.000 description 1
- 238000005984 hydrogenation reaction Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- FAHBNUUHRFUEAI-UHFFFAOYSA-M hydroxidooxidoaluminium Chemical compound O[Al]=O FAHBNUUHRFUEAI-UHFFFAOYSA-M 0.000 description 1
- 239000013067 intermediate product Substances 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 description 1
- 229910001092 metal group alloy Inorganic materials 0.000 description 1
- 150000002815 nickel Chemical class 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 235000011007 phosphoric acid Nutrition 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 239000012495 reaction gas Substances 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 238000002407 reforming Methods 0.000 description 1
- 239000011819 refractory material Substances 0.000 description 1
- 238000005245 sintering Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
- RNWHGQJWIACOKP-UHFFFAOYSA-N zinc;oxygen(2-) Chemical class [O-2].[Zn+2] RNWHGQJWIACOKP-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B3/00—Hydrogen; Gaseous mixtures containing hydrogen; Separation of hydrogen from mixtures containing it; Purification of hydrogen
- C01B3/02—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen
- C01B3/32—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air
- C01B3/323—Catalytic reaction of gaseous or liquid organic compounds other than hydrocarbons with gasifying agents
- C01B3/326—Catalytic reaction of gaseous or liquid organic compounds other than hydrocarbons with gasifying agents characterised by the catalyst
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/70—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper
- B01J23/76—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/78—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36 with alkali- or alkaline earth metals
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/70—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper
- B01J23/76—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/80—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36 with zinc, cadmium or mercury
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/70—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper
- B01J23/76—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/83—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36 with rare earths or actinides
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/70—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper
- B01J23/89—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of the iron group metals or copper combined with noble metals
- B01J23/892—Nickel and noble metals
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B3/00—Hydrogen; Gaseous mixtures containing hydrogen; Separation of hydrogen from mixtures containing it; Purification of hydrogen
- C01B3/02—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen
- C01B3/32—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air
- C01B3/34—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air by reaction of hydrocarbons with gasifying agents
- C01B3/38—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air by reaction of hydrocarbons with gasifying agents using catalysts
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B3/00—Hydrogen; Gaseous mixtures containing hydrogen; Separation of hydrogen from mixtures containing it; Purification of hydrogen
- C01B3/02—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen
- C01B3/32—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air
- C01B3/34—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air by reaction of hydrocarbons with gasifying agents
- C01B3/38—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air by reaction of hydrocarbons with gasifying agents using catalysts
- C01B3/382—Multi-step processes
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B3/00—Hydrogen; Gaseous mixtures containing hydrogen; Separation of hydrogen from mixtures containing it; Purification of hydrogen
- C01B3/02—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen
- C01B3/32—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air
- C01B3/34—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air by reaction of hydrocarbons with gasifying agents
- C01B3/48—Production of hydrogen or of gaseous mixtures containing a substantial proportion of hydrogen by reaction of gaseous or liquid organic compounds with gasifying agents, e.g. water, carbon dioxide, air by reaction of hydrocarbons with gasifying agents followed by reaction of water vapour with carbon monoxide
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J2523/00—Constitutive chemical elements of heterogeneous catalysts
-
- B01J35/56—
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/02—Impregnation, coating or precipitation
- B01J37/0201—Impregnation
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/16—Reducing
- B01J37/18—Reducing with gases containing free hydrogen
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/02—Processes for making hydrogen or synthesis gas
- C01B2203/0205—Processes for making hydrogen or synthesis gas containing a reforming step
- C01B2203/0227—Processes for making hydrogen or synthesis gas containing a reforming step containing a catalytic reforming step
- C01B2203/0233—Processes for making hydrogen or synthesis gas containing a reforming step containing a catalytic reforming step the reforming step being a steam reforming step
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/02—Processes for making hydrogen or synthesis gas
- C01B2203/0205—Processes for making hydrogen or synthesis gas containing a reforming step
- C01B2203/0227—Processes for making hydrogen or synthesis gas containing a reforming step containing a catalytic reforming step
- C01B2203/0244—Processes for making hydrogen or synthesis gas containing a reforming step containing a catalytic reforming step the reforming step being an autothermal reforming step, e.g. secondary reforming processes
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/02—Processes for making hydrogen or synthesis gas
- C01B2203/0283—Processes for making hydrogen or synthesis gas containing a CO-shift step, i.e. a water gas shift step
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/02—Processes for making hydrogen or synthesis gas
- C01B2203/0283—Processes for making hydrogen or synthesis gas containing a CO-shift step, i.e. a water gas shift step
- C01B2203/0288—Processes for making hydrogen or synthesis gas containing a CO-shift step, i.e. a water gas shift step containing two CO-shift steps
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/04—Integrated processes for the production of hydrogen or synthesis gas containing a purification step for the hydrogen or the synthesis gas
- C01B2203/042—Purification by adsorption on solids
- C01B2203/043—Regenerative adsorption process in two or more beds, one for adsorption, the other for regeneration
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/10—Catalysts for performing the hydrogen forming reactions
- C01B2203/1041—Composition of the catalyst
- C01B2203/1047—Group VIII metal catalysts
- C01B2203/1052—Nickel or cobalt catalysts
- C01B2203/1058—Nickel catalysts
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/10—Catalysts for performing the hydrogen forming reactions
- C01B2203/1041—Composition of the catalyst
- C01B2203/1082—Composition of support materials
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/12—Feeding the process for making hydrogen or synthesis gas
- C01B2203/1205—Composition of the feed
- C01B2203/1211—Organic compounds or organic mixtures used in the process for making hydrogen or synthesis gas
- C01B2203/1217—Alcohols
- C01B2203/1229—Ethanol
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/14—Details of the flowsheet
- C01B2203/142—At least two reforming, decomposition or partial oxidation steps in series
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/14—Details of the flowsheet
- C01B2203/142—At least two reforming, decomposition or partial oxidation steps in series
- C01B2203/143—Three or more reforming, decomposition or partial oxidation steps in series
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B2203/00—Integrated processes for the production of hydrogen or synthesis gas
- C01B2203/14—Details of the flowsheet
- C01B2203/148—Details of the flowsheet involving a recycle stream to the feed of the process for making hydrogen or synthesis gas
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/52—Improvements relating to the production of bulk chemicals using catalysts, e.g. selective catalysts
Abstract
PROCESSO PARA A PRODUÇÃO DE HIDROGÊNIO A PARTIR DO ETANOL. Pelo processo descrito na presente invenção produz-se um gás rico em metano e hidrogênio e com teor inferior a 1% v/v de olefinas, o qual satisfaz plenamente aos requisitos necessários às matérias-primas usadas para produzir hidrogênio ou gas de síntese em larga escala, em unidades de reforma a vapor já existentes em grande número de refinarias de petróleo e unidades petroquímicas. A partir do etanol, vapor de água, catalisadores à base de níquel e o uso de relações adequadas de temperatura, relações molares H20/etanol e H2/etanol, a invenção ensina a produção de hidrogênio e gas de síntese a partir de biomassa, de maneira estável por longos períodos sem perda de desempenho dos catalisadores com o tempo, permitindo a sua aplicação industrial em unidades novas ou em unidades existentes. Como solução para a produção de etanol, a presente invenção reivindica a substituição dos catalisadores à base de ZnO e hidrotratamento da seção de pré-tratamento da carga, por catalisadores à base de níquel e condições de processo em acordo com a presente invenção.
Description
A presente invenção pertence ao campo dos processos catalíticos de reforma com vapor de água e dos catalisadores usados nesses processos. A produção de hidrogênio a partir de biomassa, em particular do etanol, é de grande interesse para novas unidades industriais e células a combustível e objetivo da presente invenção.
O processo mais empregado para produção de hidrogênio em escala industrial é a reforma a vapor (“steam reforming”). Trata-se de um processo de diversas etapas com condições operacionais e catalisadores distintos. Na etapa chamada de “reforma a vapor”, que utiliza catalisador do tipo níquel sobre suportes refratários, tais como alumina, aluminato de cálcio ou aluminato de magnésio, as principais reações que ocorrem são:
O processo de reforma a vapor utiliza como matérias-primas o gás natural, o gás de refinaria, o propano, o butano, o gás liquefeito de petróleo ou a nafta.
O uso de matérias-primas renováveis (biomassa) para a produção do hidrogênio, tal como o etanol, permitiria reduzir a emissão de CO2 no balanço global, uma vez que estas matérias-primas fixam o CO2 da atmosfera. Apesar do benefício ambiental, a tecnologia de produção de H2 em larga escala a partir do etanol ainda não está consolidada tecnicamente.
A desativação dos catalisadores utilizados no processo de reforma a vapor pela formação de coque é a principal dificuldade a ser solucionada, para a viabilização industrial da produção de hidrogênio a partir do etanol.
O eteno formado a partir da desidratação do etanol é um dos principais compostos que favorecem a formação do coque na reforma a vapor do etanol. Numa unidade industrial de reforma a vapor a partir do gás natural ou do gás de refinaria considera-se o teor de eteno máximo admissível na alimentação em torno de 1% v/v. Acima deste valor a perda de atividade dos catalisadores inviabiliza economicamente o processo.
Uma solução técnica que vem sendo investigada é o desenvolvimento de catalisadores mais resistentes à desativação por deposição de coque. Alguns dos tipos de catalisadores investigados são: óxidos e óxidos mistos como MgO, AI2O3, V2O5, ZnO, TiO2, l_a2O3, CeO2, Sm2O3, La2O3-AI2O3, CeO2-AI2O3, MgO-AI2O3; Co suportados como CO/AI2O3, Co/l_a2O3, Co/SiO2, Co/MgO, Co/ZrO2, Co/ZnO, Co/TiO2) Co/V2O5, Co/CeO2, Co/Sm2O3, Co/CeO2-ZrO2, Co/C; Ni suportados como Ni/La2O3 Ni(La2O3-AI2O3), Ni/AI2O3, Ni/MgO, Ni-Cu/SiO2) Ni-Cu/AI2O3, Ni-Cu-K/AI2O3; CU suportados sobre Nb2O5-AI2O3 e sobre ZnO-AI2O3; metais nobres suportados como Rh sobre TiO2, SiO2, CeO2, ZrO2, AI2O3, MgO e CeO2-ZrO2, Pt sobre CeO2, Pd sobre CeO2, AI2O3 e C; ligas metálicas como Rh-Au/CeO2, Rh-Pt/CeO2 e Pt-Pd/CeO2.
No entanto, tais catalisadores ainda apresentam restrições para uso industrial, tais como: não terem a resistência adequada à desativação por formação de coque ou sinterização da fase ativa; apresentarem custo elevado por serem baseados em metais nobres ou formarem subprodutos, como o acetaldeído, acetatos, acetona e etileno, que dificultam a purificação do hidrogênio (ou do gás de síntese) produzido ou acarretam dificuldades e/ou custos adicionais devido à contaminação do condensado gerado no processo a partir da água utilizada em excesso na estequiometria de reação.
Uma segunda solução técnica, e escopo da presente invenção, seria a conversão prévia do etanol em matérias-primas utilizadas industrialmente, que converte o etanol em um gás rico em metano e isento de olefinas e outros contaminantes orgânicos, tais como acetaldeídos, cetonas, acetatos e outros, através da combinação de condições de processo e de catalisadores adequados que apresentam baixa formação de coque. Tal gás pode ser então utilizado como carga de uma unidade convencional de produção de hidrogênio que utilize gás natural, GLP, gás de refinaria, nafta ou combinações destas, como matérias-primas.
A produção de hidrogênio pela reforma a vapor do etanol pode ser descrita teoricamente pela equação global abaixo:
Na prática, podem ocorrer diversas outras reações, dependendo do tipo de catalisador e das condições operacionais utilizadas, tais como: a) a formação de eteno pela reação de desidratação do etanol. b) a formação de acetaldeído pela desidrogenação do etanol. c) a decomposição do etanol e a reação de reforma a vapor do etanol ou de produtos intermediários produzindo CO, CO2 e CH4.
Os catalisadores contendo metal nobre tendem a apresentar maior resistência à formação de coque do que os catalisadores equivalentes utilizando níquel como fase ativa. Entretanto, produzi-los requer custos mais elevados, o que tende a inviabilizar o seu uso industrial. Dessa forma, apesar de conhecidos a longo tempo, tais catalisadores à base de metais nobres não encontraram aplicação industrial na produção de hidrogênio em larga escala.
Industrialmente, os catalisadores utilizados para a produção de hidrogênio a partir do gás natural, propano, butano, GLP, gás de refinaria ou nafta, em unidades de grande capacidade (aqui definidas por terem capacidade de produção acima de 10.000 Nm3/dia), compreendem níquel suportado em materiais refratários, tais como: alumina, aluminato de cálcio ou aluminato de magnésio, podendo ser promovidos por outros elementos, como metais alcalinos (especialmente o potássio) e terras raras (especialmente o lantânio).
Os catalisadores à base de níquel podem sofrer séria desativação por formação de coque quando utilizados para a reforma a vapor do etanol, sendo a taxa de formação de coque influenciada pelo tipo de catalisador e pelas condições operacionais.
O catalisador do tipo Ni/AI2O3 apresenta boa atividade e seletividade para produção de hidrogênio em temperaturas acima de 550°C. Em temperaturas inferiores observa-se o aparecimento de eteno nos produtos acompanhado por rápida perda de atividade associada à deposição de coque.
A tendência à formação de coque, sobre catalisadores do tipo níquel suportado, na reforma a vapor do etanol é bem conhecida. Sun e colaboradores relatam nas publicações J. Sun, X.P. Qiu, F. Wu, W.T. Zhu, HH2 from steam reforming of ethanol at low temperature over NÍ/Y2O3, Ni/La2O3 and NI/AI2O3 catalysts for fuel-celf’, International Journal of Hydrogen Energy 30 (2005) 437-445 e J. Sun, X. Qiu, F. Wu, W. Zhu, W. Wang, S. Hao, “Hydrogen from steam reforming of ethanol in low and middle temperature range for fuel cell application”, International Journal of Hydrogen Energy 29 (2004) 1075-1081 que utilizaram catalisadores do tipo NÍ/Y2O3, Ni/La2O3 e Ni/AI2O3. Os autores ensinaram que o uso de suportes que não tenham acidez, em temperaturas acima de 380°C, reduz a formação de coque.
A invenção descrita no documento de patente WO 2009/004462 A1, ensina a produzir hidrogênio e nanotubos de carbono (um tipo especial de coque) a partir da decomposição do etanol sobre catalisadores à base de níquel suportado em lantânio.
Os resultados divulgados mostram que o desempenho de catalisadores à base de níquel, para a produção de hidrogênio a partir do etanol, é aplicável às unidades industriais de produção de hidrogênio existentes, mas ainda pode ser aperfeiçoado. Uma técnica descrita na literatura para a produção de hidrogênio a partir do etanol, denominada como reforma autotérmica, envolve a adição de oxigênio à mistura de etanol e vapor.
A publicação WO 2009/009844 A2 ensina a adição de oxigênio na alimentação de etanol e vapor de água, associada ao uso de catalisadores específicos, à base de óxido de cério, com promotores selecionados do grupo dos metais alcalinos e dos lantanídeos, para a produção de H2 a partir do etanol.
Outro exemplo dessa técnica é a invenção descrita no documento de patente US 2005/0260123 A1, que ensina um processo para produzir hidrogênio, o qual utiliza catalisadores que compreendem Rh sobre suportes, como o óxido de cério, e é conduzido em condições autotérmicas com introdução de oxigênio no gás reacional.
O uso de oxigênio na alimentação, embora apresente vantagens; como prover o calor de reação através de reações de combustão, e auxilie na remoção do coque formado sobre o catalisador, não é um método prático para produção de hidrogênio em larga escala, devido ao custo associado de produção do oxigênio e à purificação do hidrogênio, quando se usa ar no lugar de oxigênio. Tal método dificilmente seria aplicado em unidades industriais existentes de produção de hidrogênio pela reforma a vapor, devido aos altos investimentos necessários para a alteração dos equipamentos.
Conceitualmente, uma técnica possível de ser aplicada à produção de hidrogênio a partir do etanol seria a sua prévia conversão em matérias- primas, que já são utilizadas industrialmente para a produção de hidrogênio em larga escala, tais como a nafta, o gás natural ou hidrocarbonetos leves, como metano, etano, propano e butano. Após uma primeira etapa de conversão prévia do etanol, a corrente de hidrocarbonetos alimentaria o processo convencional de produção de hidrogênio já existente industrialmente, onde os hidrocarbonetos seriam convertidos à mistura de H2, CO, CO2 e metano residual. Na parte final do processo, o H2 (ou se desejado a mistura H2/CO) seria purificado por técnicas convencionais de absorção em aminas ou via PSA (“pressure swing adsorption”).
O documento de patente US 2006/0057058 A1 ensina um método para a produção de um gás rico em hidrogênio a partir do etanol caracterizado por: a) uma primeira etapa onde o etanol, vapor de água e hidrogênio de reciclo alimentam um reator, onde ocorrem as etapas catalíticas de desidrogenação do etanol a eteno e de hidrogenação do eteno a etano (o catalisador compreende Pt, Pd ou Cu sobre um suporte selecionado do grupo alumina, sílica-alumina, zircônia e zeólitas, particularmente, a zeólita HZSM5); b) uma segunda etapa de pré-reforma adiabática onde a corrente rica em etano é transformada em uma corrente rica em metano; c) alimentação da corrente rica em metano numa configuração típica de unidades industriais de reforma a vapor, contendo um reformador primário e um reator de “shift”.
A invenção não reporta dados sobre a estabilidade dos catalisadores. O hidrogênio produzido em acordo com esta invenção supre uma célula a combustível sendo, portanto, adequado para uso em pequena escala.
O documento de patente WO/2009/130197 relata um método para conversão de etanol em metano, em um pré-reformador. De acordo com o método, etanol e vapor de água são postos para reagir sobre um catalisador que compreende platina sobre um suporte de ZrO2 e CeO2, na faixa de temperatura entre 300°C e 550°C.
Na publicação S. Freni, N. Mondelo, S. Cavallaro et al., React. Kinet. Catai. Lett, 71 (2000) 143, relata-se o uso de uma primeira etapa de conversão de etanol a acetaldeído, na presença de vapor e hidrogênio, sobre um catalisador do tipo Cu suportado em sílica, em temperaturas entre 300°C e 400°C e, em seguida, a reação de reforma a vapor da mistura reacional sobre um catalisador do tipo Ni suportado em óxido de magnésio.
A literatura especializada apresenta ainda várias citações e descrições de processos em duas etapas para a produção de hidrogênio a partir do etanol. Tais processos, no entanto, possuem os inconvenientes de utilizarem catalisadores baseados em metais nobres ou produzirem compostos intermediários, dos quais não se tem experiência do impacto que exercem sobre o desempenho dos catalisadores utilizados industrialmente, na etapa de reforma a vapor, sendo necessária a realização de testes para comprovar a durabilidade dos sistemas catalíticos e sua aplicabilidade em unidades existentes.
A presente invenção diz respeito a um processo de produção de hidrogênio a partir do etanol e a um sistema catalítico específico para utilização no dito processo. Um caráter essencial da presente invenção é a conversão do etanol, numa primeira etapa do processo, em um gás rico em metano, isento de olefinas (<1%), com baixos teores de monóxido de carbono (<2%) e outros contaminantes orgânicos, como acetaldeído.
A presente invenção pode ser implementada em unidades industriais de produção de hidrogênio em larga escala, com substituição dos catalisadores da seção de pré-tratamento (normalmente utilizam-se ZnO e CoMo) e uso das condições de processo nela descritas.
A presente invenção diz respeito a um processo de produção de hidrogênio a partir do etanol e ao uso, no referido processo, de catalisadores específicos à base de níquel. O processo de produção de hidrogênio a partir do etanol é caracterizado por compreender duas etapas, que na verdade resultam da combinação de dois processos executados em série.
Na primeira etapa, um processo de pré-reforma compreende reações que produzem um gás com alto teor de metano e, na segunda etapa, uma configuração típica do processo de reforma a vapor utilizada industrialmente é adequada para receber o produto gerado na primeira etapa. Portanto, a presente invenção pode ser implementada em unidades industriais de produção de hidrogênio já existentes substituindo-se os catalisadores da seção de pré-tratamento ou da seção de pré-reforma por catalisadores adequados e condições de processo apropriadas, para a realização da primeira etapa, em acordo com a presente invenção.
Na primeira etapa o etanol, em presença de hidrogênio com relações molares H2/etanol entre 0,1 mol/mol e 1,0 mol/mol, preferencialmente entre 0,2 mol/mol e 0,6 mol/mol, vapor de água com relações molares H2O/etanol entre 1 mol/mol e 10 mol/mol, temperaturas entre 300°C e 550°C, preferencialmente entre 350°C e 450°C e velocidades espaciais (LHSV considerando somente o etanol) entre 0,1 h’1 e 10 h‘1, preferencialmente entre 0,5 h'1 e 3 h‘1, é convertido na presença de um catalisador à base de níquel em um gás com alto teor de em metano, isento de olefinas e com baixo teor de monóxido de carbono (menos de 2% v/v deste componente em base seca).
A pressão de operação pode ser a utilizada na prática industrial do processo de reforma a vapor, ou seja, pelo estado da técnica atual entre 1 kgf/cm2 e 40 kgf/cm2, preferencialmente entre 10 kgf/cm2 e 25kgf/cm2, sendo o valor máximo definido pelas limitações dos materiais de construção da unidade industrial.
Na segunda etapa, o gás com alto teor de metano é utilizado como carga de uma unidade de produção de hidrogênio pelo processo de reforma a vapor. Uma configuração típica do processo de reforma a vapor, utilizada industrialmente e adequada para receber o gás com alto teor de metano gerado na primeira etapa, compreende as seguintes etapas adicionais: a) reforma primária, onde a mistura entre vapor de água e gás com alto teor de metano é convertida numa mistura, com altos teores de H2, CO e CO2 e baixo teor de metano, e as temperaturas de reação estão na faixa entre 500°C e 850°C e pressões entre 10 kgf/cm2 e 40 kgf/cm2; b) “shift", onde o CO reage com vapor de água em temperaturas entre 300°C e 450°C e pressões entre 10 kgf/cm2 e 40 kgf/cm2; c) purificação, onde através do uso da técnica de “pressurre swing adsorption” produz-se uma corrente com pureza superior a 99% de hidrogênio e um gás residual contendo H2, CO, CO2 e metano, o qual é utilizado como combustível na etapa de reforma primária.
Outras configurações de processo de reforma a vapor conhecidos na prática industrial podem ser utilizadas para processar o gás com alto teor de metano gerado na primeira etapa do processo, tais como as configurações de processo que contém reatores de pré-reforma, reforma secundária, “shift” de média (MTS), “shift” de baixa (LTS) e metanação e purificação do gás rico em hidrogênio através do uso de soluções aquosas de aminas. Também podem ser utilizadas Configurações de processo de reforma a vapor para produção de gás de síntese, como correntes contendo além de hidrogênio, teores significativos de CO para uso em processos petroquímicos como a produção de metanol ou em processos de Fischer Tropsch.
Os catalisadores da presente invenção compreendem níquel sobre um suporte inorgânico de baixa acidez, selecionado entre óxido de zinco, titanato de cálcio e aluminato de cálcio ou magnésio, ou mistura destes, podendo o suporte ser modificado por metais alcalinos, particularmente por meio de adição de potássio, para atingir um teor entre 0,1% p/p e 10% p/p, preferencialmente entre 1% a 5% de potássio.
O processo de preparação do catalisador à base de níquel suportado em óxidos inorgânicos para uso no processo reivindicado pela presénte invenção compreende as seguintes etapas: 1) preparação de uma solução de um sal inorgânico de níquel, preferencialmente nitrato, acetato ou carbonato, podendo conter um ou mais elementos do grupo dos lantanídeos (ou terras raras), preferencialmente lantânio ou cério; 2) impregnação do suporte de óxido inorgânico pelas técnicas conhecidas do volume de poros (ponto úmido) ou pelo método do excesso de solução; 3) secagem do material de óxido inorgânico impregnado com solução contendo níquel ao ar, em temperaturas entre 80°C e 140°C, por 1 a 24 horas; 4) calcinação do material de óxido inorgânico impregnado ao ar, entre 350°C e 650°C, por 1 a 4 horas.
Alternativamente, as etapas 2 a 4 podem ser repetidas mais de uma vez até se atingir o teor desejado de NiO no suporte. Os teores desejados estão entre 10% p/p e 40% p/p de NiO, preferencialmente entre 12% e 20%. Adicionalmente podem-se incluir como aditivos na impregnação, compostos para controle do pH, aumento da solubilidade ou para evitar precipitação de fases. Exemplos não limitantes destes compostos são o ácido nítrico, ácido sulfúrico, ácido fosfórico, hidróxido de amónio, carbonato de amónia, peróxido de hidrogênio (H2O2), açúcares ou combinações destes compostos. Opcionalmente, no preparo do suporte é adicionado um teor de alumina entre 5% e 50 %, para se obter uma resistência mecânica dos catalisadores adequada para uso industrial. As partículas do suporte podem estar em várias formas adequadas ao uso industrial no processo de reforma a vapor, tais como esferas, cilindros, cilindros com um furo central (anéis de “Rashing”) e cilindros com vários furos.
Os catalisadores de óxido de níquel sobre o suporte necessitam de transformação para a fase ativa de níquel metálico sobre o suporte. A transformação, denominada de redução, pode ser realizada antes da alimentação de etanol e vapor de água, por meio de passagem de um fluxo de hidrogênio ou de um agente redutor como amónia, metanol ou acetaldeído, em condições de temperatura entre 300°C e 550°C. Opcionalmente, o catalisador pode ser reduzido externamente, como etapa final do processo de sua produção, pela passagem de um fluxo de hidrogênio ou um agente redutor como amónia, metanol ou de acetaldeído, em condições de temperatura entre 300°C a 550°C, por 1 a 5 horas, e a seguir resfriado e submetido a um fluxo de ar em temperaturas entre 20°C e 60°C, por 1 às 5 horas. Opcionalmente, os catalisadores podem conter baixos teores de metais nobres, particularmente Pd e Pt em teores inferiores a 0,5% p/p, ou preferencialmente inferiores a 0,1% p/p, para acelerar a etapa de redução.
Os catalisadores, assim preparados, podem ser utilizados na produção de um gás com alto teor de metano, teor de olefinas menor que 1% p/p e com baixo teor de CO, em pressões entre 1 kgf/cm e 50 kgf/cm e temperaturas entre 300°C e 550°C, a partir da mistura de etanol, hidrogênio e vapor de água com relações molares H2/etanol entre 0,2 mol/mol e 0,6 mol/mol e relações molares H2O/etanol entre 1 mol/mol e 10 mol/mol, as quais permitem operar-se por longos períodos sem perda de desempenho por formação de coque. O gás com alto teor de metano pode ser utilizado para produção de hidrogênio através do processo de reforma a vapor.
A presente invenção também prevê, opcionalmente, o uso de catalisadores comerciais classificados como de “metanação” ou de catalisadores classificados como de “pré-reforma”, ambos à base de níquel, desde que utilizados nas condições de processo ensinadas. Os exemplos a seguir são apresentados de forma a ilustrar mais completamente a natureza da presente invenção e a maneira de praticar a mesma, sem que, no entanto, possam ser considerados como limitantes do seu conteúdo.
Este exemplo, comparativo do estado da técnica ensina que os adsorventes comerciais à base de oxido de zinco e os catalisadores comerciais de hidrotratamento contendo cobalto e molibdênio, ambos usados industrialmente no processo de reforma a vapor na etapa de pré- tratamento de cargas do processo de reforma a vapor, não são adequados 10 para processarem uma alimentação de etanol e hidrogênio, uma vez que possuem uma elevada taxa de formação de eteno e de outros subprodutos, particularmente o acetaldeído, mesmo quando se utiliza uma elevada relação molar H2/etanol na alimentação (Tabela 1). Tabela 1 15 Distribuição de hidrocarbonetos na fase gasosa obtida na conversão do etanol em presença de hidrogênio sobre adsorventes de óxidos de zinco e catalisadores de hidrotratamento utilizados no processo industrial de reforma a vapor.
Tais subprodutos não são desejáveis por propiciarem a desativação precoce do catalisador utilizado ou de catalisadores de reforma a vapor, utilizados em seguida no processo.
Os resultados foram obtidos em uma unidade de microatividade 5 operando à pressão atmosférica.
Moeram-se os catalisadores, para a faixa entre 100 mesh e 150 mesh. Alimentou-se o etanol, através da passagem do gás de arraste (hidrogênio ou nitrogênio), por um saturador mantido a 10°C.
As análises da carga e do produto formado foram realizadas por meio 10 de cromatografia gasosa.
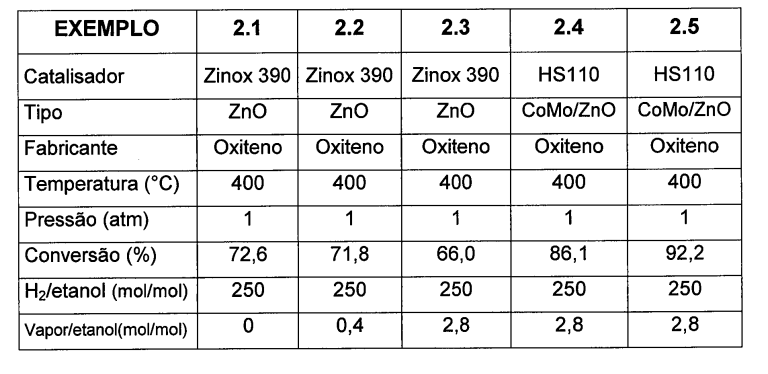
Este exemplo comparativo ensina que os adsorventes comerciais à base de óxido de zinco e os catalisadores de hidrotratamento contendo cobalto e molibdênio, os quais são utilizados na etapa de pré-tratamento de cargas do processo industrial de reforma a vapor, não são adequados para processarem uma alimentação de etanol, hidrogênio e vapor de água, em condições de temperatura industrialmente utilizadas nos reatores de pré- tratamento, uma vez que conduzem a uma elevada taxa de formação de eteno e outros subprodutos, particularmente o acetaldeído e olefinas leves.
Este exemplo ainda ilustra o efeito benéfico da presença de vapor de água (comparação entre os Exemplos 2.1 e 2.2) e da redução da velocidade espacial (comparação entre os Exemplos 2.4 e 2.5) em reduzir a formação de eteno e de outras olefinas leves.
Os catalisadores foram testados por meio de procedimentos semelhantes aos descritos no Exemplo 1.
A presente invenção reivindica a substituição dos catalisadores à base de ZnO e do hidrotratamento da seção de pré-tratamento da carga, por catalisadores à base de níquel, preparados de acordo com a presente invenção como solução para a produção de etanol em unidades de reforma a vapor existentes. Tabela 2
Distribuição de hidrocarbonetos na fase gasosa obtida na conversão de etanol em presença de hidrogênio e vapor de água sobre óxidos de zinco e catalisadores de hidrotratamento, ambos comerciais (Oxiteno), usados no processo industrial de reforma a vapor.
Este exemplo comparativo, em acordo com a presente invenção, ensina o uso de um suporte do tipo óxido de zinco, para o preparo de um catalisador de a base óxido de níquel e seu uso na produção de hidrogênio a 5 partir de etanol. Prepararam-se as seguintes amostras:
Amostra 3A: impregnaram-se 95 gramas de adsorvente comercial à base de óxido de zinco (ZINOX390), pelo método da impregnação incipiente, com 38 ml de solução aquosa contendo 19,5 gramas de Ni(NO3)2 6H2O. Em seguida, secou-se a amostra a 110°C 10 por uma noite e calcinou-se a 450°C ao ar por 4 horas de forma a obter-se 5% p/p de NiO suportado em óxido de zinco;
Amostra 3B: impregnaram-se 94 gramas do catalisador do Exemplo 5, pelo método da impregnação incipiente, com 40 ml de solução aquosa contendo 21,4 gramas de Ni(NO3)2 6H2O. Em seguida, secou-se a amostra a 110°C por uma noite e calcinou-se a 450°C ao ar por 4 horas de forma a obter-se 10% p/p de NiO suportado em óxido de zinco;
Amostra 3C: impregnaram-se 95 gramas do catalisador do Exemplo 6, pelo método da impregnação incipiente, com 40 ml de solução aquosa contendo 21,7 gramas de nitrato de níquel Ni(NO3)2 6H2O. Em seguida, secou-se a amostra a 110°C por uma noite e calcinou-se a 450°C ao ar por 4 horas de forma a obter-se 15% p/p de NiO suportado em óxido de zinco.
Este exemplo comparativo, em acordo com a presente invenção, ensina o uso de um suporte do tipo óxido de zinco promovido por metais alcalinos, para o preparo de um catalisador de a base óxido de níquel e seu uso na produção de hidrogênio a partir do etanol.
Inicialmente, preparou-se um suporte de óxido de zinco promovido por potássio, da seguinte forma: impregnaram-se 150 gramas de adsorvente comercial à base de óxido de zinco (ZINOX390) com 60 ml de solução aquosa contendo 3,1 gramas de hidróxido de potássio; em seguida, secou- se a amostra a 110°C por uma noite e calcinou-se a 450°C por 4 horas, para obter-se 2% de K2O sobre óxido de zinco. Prepararam-se, então, diversos catalisadores contendo óxido de níquel a partir deste suporte, como descrito a seguir:
Amostra 4A: impregnaram-se 95 gramas do material preparado no Exemplo 8, pelo método da impregnação incipiente, com 28 ml de solução aquosa contendo 19,5 gramas de Ni(NO3)2 6H2O. Em seguida, secou-se a amostra a 110°C por uma noite e calcinou-se a 450°C ao ar por 4 horas, para obter-se 5% p/p de NiO suportado em óxido de zinco promovido por potássio.
Amostra 4B: impregnaram-se 87 gramas do catalisador do Exemplo 8, pelo método da impregnação incipiente, com 37 ml de solução aquosa contendo 19,9 gramas de nitrato de níquel Ni(NO3)2 6H2O. Em seguida, secou-se a amostra a 110°C por uma noite e calcinada a 450°C ao ar por 4 horas, para obter-se 10% p/p de NiO suportado em óxido de zinco promovido por potássio.
Amostra 4C: impregnaram-se 79 gramas do catalisador do Exemplo 8, pelo método da impregnação incipiente, com 26 ml de solução aquosa contendo 20,2 gramas de nitrato de níquel Ni(NO3)2 6H2O. Em seguida, secou-se a amostra a 110°C por uma noite e calcinada a 450°C ao ar por 4 horas, para obter-se 15% p/p de NiO suportado em óxido de zinco promovido por potássio.
Os catalisadores preparados nos Exemplos 3 e 4 foram reduzidos previamente em fluxo de hidrogênio e vapor de água a 450°C por 2 horas e, em seguida, testados de forma semelhante à descrita no Exemplo 1.
Os resultados são apresentados na Tabela 3 e mostram que: a) a introdução de óxido de níquel na formulação de um suporte do tipo óxido de zinco produz um catalisador, que favorece a redução de moléculas de subprodutos, especialmente eteno e acetaldeído, tendo ainda como vantagem adicional o aumento da atividade de conversão de etanol; b) a introdução de potássio no catalisador à base de óxido de níquel sobre óxido de zinco acarreta uma redução adicional do teor de eteno e de outras olefinas, que são os principais compostos que aceleram a formação de coque nas condições de conversão do etanol para gás de síntese.
Este exemplo comparativo demonstra que catalisadores comerciais de reforma a vapor do gás natural e da nafta apresentam elevada desativação, mostrado pela acentuada queda da conversão na Tabela 4, quando utilizados para a reforma a vapor do etanol na presença de hidrogênio e em condições de temperatura existentes na seção de pré-tratamento de unidades existentes de geração de hidrogênio. 5 Os catalisadores foram reduzidos previamente em fluxo de hidrogênio e vapor de água a 450°C por 2 horas e a seguir testados de forma semelhante à relatada no Exemplo 1. Tabela 3
Distribuição de hidrocarbonetos na fase gasosa obtida na conversão 10 do etanol em presença de hidrogênio e vapor de água. Relação molar vapor/etanol = 2,8 mol/mol, relação molar H2/etanol = 250 mol/mol, GHSV = 23000 l/gh, temperatura de 400°C e pressão de 1 atm. Tabela 4
Distribuição de hidrocarbonetos na fase gasosa obtida na conversão do etanol em presença de hidrogênio e vapor de água sobre catalisadores comerciais de reforma a vapor do gás natural (G91EW) ou da nafta (46.3Q) 5 utilizados no processo industrial de reforma a vapor. Relação molar vapor/etanol = 2,8 mol/mol e relação molar H2/etanol = 250 mol/mol.
Este exemplo mostra que catalisadores comerciais conhecidos na prática industrial como catalisadores de metanação, originalmente utilizados 10 na conversão de monóxido de carbono e dióxido de carbono com hidrogênio, para a produção de metano, podem ser surpreendentemente utilizados, de acordo com a presente invenção, para a conversão de etanol num gás rico em metano e isento de olefinas, em presença de hidrogênio e vapor de água e nas condições de temperatura utilizadas na seção de pré- tratamento de unidades existentes de geração de hidrogênio pelo processo de reforma a vapor.
Os catalisadores foram reduzidos previamente em fluxo de hidrogênio 5 e vapor de água a 450°C por 2 horas e, em seguida, testados de forma semelhante à descrita no Exemplo 1. No entanto, as propriedades de atividade e de desativação se mostraram influenciadas pelo tipo de catalisador comercial utilizado, indicando que seria desejável o preparo de catalisadores específicos para a conversão de etanol em hidrogênio, de 10 acordo com o proposto na presente invenção. Tabela 5
Distribuição de hidrocarbonetos na fase gasosa obtida na conversão do etanol em presença de hidrogênio e vapor de água sobre catalisadores de metanação comerciais. Relação molar vapor/etanol = 2,8 mol/mol e 15 relação molar H2/etanol = 250 mol/mol.
Este exemplo ensina o preparo de um catalisador, de acordo com a presente invenção, à base de níquel sobre suporte do tipo alumina e promovido por metais alcalinos. Impregnaram-se 300 gramas de hidróxido de alumínio comercial (PURAL SB, comercializado pela SASOL) com 180 ml de solução aquosa contendo 7,1 gramas de hidróxido de potássio. Em seguida, secou-se a amostra a 110°C por 12 horas e calcinou-se ao ar a 1200°C, por 4 horas, para obter-se um suporte do tipo alumina promovida por potássio. Em seguida, impregnou-se a amostra pelo método da impregnação incipiente, com solução aquosa contendo nitrato de níquel, secou-se a 110°C e calcinou-se a 450°C. Repetiu-se o procedimento mais duas vezes de forma a se obter um catalisador contendo 15% de NiO (15% NiO/2%K/alumina).
Este exemplo ensina o preparo de um catalisador, de acordo com a presente invenção, à base de níquel sobre suporte do tipo aluminato de magnésio e promovido por metais alcalinos. Inicialmente, preparou-se um suporte do tipo aluminato de magnésio a partir das seguintes etapas: a) misturar uma solução aquosa de AI(NO3)3 9H20 com uma solução aquosa de Mg(NO3)2 6H2O, à temperatura ambiente; b) adicionar a solução anterior sobre uma solução aquosa contendo 14,5% de NH4OH, mantendo 0 pH igual ou acima de 8,0; c) filtrar e lavar 0 precipitado formado com água desmineralizada; d) secar a 110°C e calcinar ao ar entre 1000°C e 1300°C por 1 a 4 horas (no exemplo, as soluções contém 543 gramas de nitrato de alumínio em 1435 ml de água e 176 gramas de nitrato de magnésio em 679 ml de água, respectivamente).
A temperatura de calcinação utilizada foi de 1100°C. O suporte preparado foi então impregnado ao volume de poros com solução aquosa de KOH e a seguir calcinado a 1200°C, por 4 horas, de forma a se obter um suporte com 1,5% p/p de KOH. Em seguida, impregnaram-se 112 gramas do suporte assim obtido com 39 ml de uma solução aquosa contendo 23 gramas de Ni(NO3)2 6H2O. Secou-se o material e calcinou-se a 450°C, por 4 horas, para obter-se 5% de NiO suportado em aluminato de magnésio promovido por potássio. Repetiu-se o procedimento até se obter 15% de NiO suportado em aluminato de magnésio promovido por potássio.
Este exemplo ensina o preparo de um catalisador, de acordo com a presente invenção, à base de níquel sobre suporte do tipo aluminato de cálcio e promovido por metais alcalinos. Impregnaram-se 300 gramas de aluminato de cálcio comercial (SECAR 80) ao volume de poros com uma solução aquosa de KOH e, em seguida, calcinaram-se a 1200°C por 4 horas, para se obter um suporte de aluminato de cálcio promovido por 1,5% p/p de KOH. Impregnaram-se 114 gramas do suporte assim obtido com 31 ml de uma solução aquosa contendo 23 gramas de Ni(NO3)2 6H2O. Secou-se o material e calcinou-se a 450°C por 4 horas, para se obter 5% de NiO suportado em aluminato de cálcio promovido por potássio. O procedimento foi repetido até se obter 15% de NiO suportado em aluminato de cálcio promovido por potássio.
Este exemplo ensina o preparo de um catalisador, de acordo com a presente invenção, na sua modalidade preferencial, à base de níquel sobre suportes do tipo titanatos de metais alcalinos. Impregnam-se 190 gramas de titanato de cálcio comercial (Certronic) com 68 ml de uma solução aquosa contendo 39 gramas de Ni(NO3)2 6H2O. Em seguida, secou-se a amostra a 110°C por uma noite e calcinou-se a 450°C ao ar por 4 horas de forma a se obter 5% p/p de NiO suportado em titanato de cálcio. Repetiu-se o procedimento mais duas vezes de forma a se obter o catalisador contendo 15% p/p de NiO suportado em titanato de cálcio.
Este exemplo ensina o preparo de um catalisador, de acordo com a presente invenção, à base de níquel sobre suporte do tipo alumina-cálcio. Impregnaram-se 235 gramas de alumina CATAPAL com 141 ml de solução aquosa contendo 63 gramas de Ca(NO3)2 4H2O. Em seguida, secou-se a amostra a 110°C por 1 noite e calcinou-se a 600°C por 4 horas ao ar. Impregnaram-se 230 gramas do suporte acima ao volume de poros com 160 ml de solução aquosa contendo 99,4 gramas de Ni(NO3)2 6H2O. Em seguida, secou-se a amostra a 110°C por uma noite e calcinou-se a 450°C ao ar por 4 horas de forma a se obter 10% p/p de NiO suportado em alumina. Repetiu-se o procedimento de impregnação e calcinação de forma a se obter o catalisador final contendo 20% de NiO suportado em alumina modificada por cálcio.
Este exemplo comparativo (Tabela 6) demonstra que catalisadores preferenciais da presente invenção constituídos de níquel sobre suportes de baixa acidez, apresentam elevada estabilidade e seletividade, para a produção de um gas com alto teor de metano e isento de olefinas, em condições de temperatura existentes na seção de pré-tratamento de unidades existentes de geração de hidrogênio. Reduziram-se os catalisadores previamente em fluxo de hidrogênio e vapor de água a 450°C por 2 horas e, em seguida, testaram-se de forma semelhante à descrita no Exemplo 1. Tabela 6
Distribuição de hidrocarbonetos na fase gasosa obtida na conversão do etanol em presença de hidrogênio e vapor de água sobre catalisadores constituídos de níquel sobre suportes de baixa acidez.
Os resultados mostram que se pode obter um catalisador ativo, estável e seletivo para produção de metano a partir da mistura de etanol, hidrogênio e vapor de água.
O catalisador, de acordo com a presente invenção, é constituído de Ni sobre suportes do tipo alumina, aluminatos de cálcio, aluminatos de magnésio e titanatos de cálcio, podendo ser promovidos por metais alcalinos, como o potássio.
Este exemplo mostra que, de acordo com a presente invenção, o uso de hidrogênio, com relações molares entre 0,1 mol/mol e 1,0 mol/mol na mistura etanol e vapor de água, é essencial para evitar a formação de coque. Na prática, utiliza-se industrialmente uma relação molar típica entre 0,01 mol/mol e 0,05 mol/mol na reforma a vapor do gás natural e entre 0,1 mol/mol a 0,3 mol/mol para a reforma a vapor da nafta. Conduz-se a reação em unidade de bancada utilizando-se 2 gramas de catalisador, pressão de 10 kgf/cm2, temperatura de 400°C, solução 30% p/p de etanol em água (correspondendo a uma relação molar vapor/carbono de 3,0 mol/mol), LHSV = 9h’1 (calculado com base na mistura etanol e água).
As Tabelas 7 e 8 apresentam os resultados obtidos com catalisadores comerciais de pré-reforma e metanação, respectivamente, que são tipicamente utilizados na produção de hidrogênio pelo processo de reforma a vapor. Utilizam-se os catalisadores de pré-reforma e metanação nas etapas de produção de um gás com alto teor de H2, a partir de gás natural, GLP ou nafta. 5 Tabela 7
Teste de estabilidade da conversão de etanol e vapor de água a um gás com alto teor de metano em função da relação molar H2/etanol sobre catalisadores comerciais de pré-reforma. O catalisador RKNGR foi reduzido a 450°C e o catalisador Reformax a 550°C antes do início da reação.
Este exemplo mostra o uso dos catalisadores, de acordo com a presente invenção, em sua modalidade preferencial, do tipo Ni sobre suportes de baixa acidez. As condições de reação foram descritas no 5 Exemplo 14. Os resultados mostram uma excelente estabilidade sem aumento de perda de carga, indicativo da formação de coque sobre os catalisadores (Tabela 9). Tabela 8
Teste de estabilidade de conversão de etanol e vapor de água a um 10 gás com alto teor de metano em função da relação molar H2/etanol sobre catalisadores comerciais (C13-4-04 Sud Chemie) de metanação. Tabela 9
Claims (9)
1- PROCESSO PARA PRODUÇÃO DE HIDROGÊNIO A PARTIR DE ETANOL, caracterizado por compreender as seguintes etapas: a) prover o reator com um sistema catalítico onde o dito sistema catalítico compreende em um catalisador de óxido de níquel sobre um suporte com um teor compreendido na faixa entre 10% p/p e 40% p/p, selecionado do grupo alumina, aluminato de cálcio e aluminato de magnésio ou mistura desses compostos, em qualquer proporção, e com um elemento promotor selecionado do grupo dos metais alcalinos ou alcalinos terrosos, em que o dito elemento promotor de metal alcalino compreender o potássio, presente no catalisador com um teor compreendido na faixa entre 0,5% p/p e 5% p/p; b) prover dito reator com uma carga de alimentação de etanol, com uma velocidade espacial (LHSV) entre 0,5 tr1 e 3,0 tr1 e permitir o contato com o sistema catalítico; c) prover dito reator de maneira simultânea com as etapas (a) e (b) com uma alimentação de hidrogênio, para estabelecer uma relação molar H2/etanol (mol/mol) compreendida na faixa entre 0,2 e 0,6; d) prover dito reator de maneira simultânea com as etapas (a), (b) e (c) com uma alimentação de vapor de água, para estabelecer uma relação molar vapor de água/etanol (mol/mol) compreendida na faixa entre 3,0 e 6,0; e) ajustar as condições operacionais do reator para uma temperatura compreendida na faixa entre 350°C e 550°C; f) permitir a conversão do etanol e uma corrente contendo metano, CO, CO2 e H2, nas condições estabelecidas nas etapas anteriores; g) direcionar a mistura de gases produzida na etapa (f) para uma unidade operando em condições típicas de reforma primária do processo industrial de reforma a vapor para permitir a conversão do metano a CO, CO2 e H2; h) tratar a mistura de gases produzida na etapa (g) por meio de condições típicas da etapa de “shift” do processo industrial de reforma a vapor, para permitir a conversão do monóxido de carbono CO2 e hidrogênio; i) purificar o hidrogênio produzido oriundo do reator de shift, por meio de métodos usados no processo industrial de reforma a vapor.
2- PROCESSO, de acordo com a reivindicação 1, caracterizado por dita carga de etanol compreender etanol anidro, etanol hidratado ou, preferencialmente, etanol cru.
3- PROCESSO, de acordo com a reivindicação 1, caracterizado por dita alimentação de hidrogênio compreender o reciclo do produto obtido na dita conversão do etanol.
4- PROCESSO, de acordo com a reivindicação 1, caracterizado por dito óxido de níquel estar presente no catalisador com um teor compreendido na faixa entre 12% p/p e 20% p/p.
5- PROCESSO, de acordo com a reivindicação 1 e 4, caracterizado por dito elemento promotor de metal alcalino compreender o potássio, presente no catalisador com um teor compreendido na faixa entre 1 % p/p e 3% p/p.
6- PROCESSO, de acordo com a reivindicação 1, caracterizado por dito catalisador compreender um segundo elemento metálico, do grupo dos metais nobres, particularmente Pt e Pd, presente no catalisador com um teor inferior a 0,5% p/p, em relação ao teor de Ni metálico, de forma a favorecer a redução das espécies de óxido metálico na faixa de temperatura compreendida entre 350°C e 550°C.
7- PROCESSO, de acordo com a reivindicação 6, caracterizado pelo segundo elemento metálico, presente no catalisador ter um teor inferior a 0,1% p/p, em relação ao teor de Ni metálico.
8- PROCESSO, de acordo com a reivindicação 1, caracterizado por dito sistema catalítico compreender um catalisador de óxido níquel sobre um suporte selecionado do grupo titanatos de metais alcalinos.
9- PROCESSO, de acordo com as reivindicações 1 e 8, caracterizado por dito suporte compreender o titanato de cálcio.
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| BRPI1002970-2A BRPI1002970B1 (pt) | 2010-08-18 | 2010-08-18 | processo para a produção de hidrogênio a partir do etanol |
| US13/212,772 US8642004B2 (en) | 2010-08-18 | 2011-08-18 | Process for the production of hydrogen from ethanol |
| JP2013524314A JP2013540674A (ja) | 2010-08-18 | 2011-08-18 | エタノールからの水素の製造方法 |
| PCT/BR2011/000291 WO2012031341A1 (pt) | 2010-08-18 | 2011-08-18 | Processo para a produção de hidrogênio a partir do etanol |
| EP11822945.9A EP2607302B1 (en) | 2010-08-18 | 2011-08-18 | A method for producing hydrogen from ethanol |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| BRPI1002970-2A BRPI1002970B1 (pt) | 2010-08-18 | 2010-08-18 | processo para a produção de hidrogênio a partir do etanol |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI1002970A2 BRPI1002970A2 (pt) | 2012-04-17 |
| BRPI1002970B1 true BRPI1002970B1 (pt) | 2020-10-13 |
Family
ID=45810031
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI1002970-2A BRPI1002970B1 (pt) | 2010-08-18 | 2010-08-18 | processo para a produção de hidrogênio a partir do etanol |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US8642004B2 (pt) |
| EP (1) | EP2607302B1 (pt) |
| JP (1) | JP2013540674A (pt) |
| BR (1) | BRPI1002970B1 (pt) |
| WO (1) | WO2012031341A1 (pt) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN104640625A (zh) * | 2012-09-25 | 2015-05-20 | 托普索公司 | 蒸汽重整催化剂 |
| US9181148B2 (en) | 2013-05-22 | 2015-11-10 | Saudi Arabian Oil Company | Ni/CGO and Ni-Ru/CGO based pre-reforming catalysts formulation for methane rich gas production from diesel processing for fuel cell applications |
| US9499403B2 (en) * | 2013-07-10 | 2016-11-22 | Saudi Arabian Oil Company | Catalyst and process for thermo-neutral reforming of liquid hydrocarbons |
| WO2015054755A1 (pt) * | 2013-10-17 | 2015-04-23 | Petróleo Brasileiro S.A. - Petrobras | Catalisador para produção de gás de síntese e processo de obtenção do mesmo |
| CN104258913B (zh) * | 2014-08-06 | 2016-03-30 | 中国科学院广州能源研究所 | 一种用于催化生物质合成气合成低碳混合醇的催化剂的还原装置及还原方法 |
| US10953388B1 (en) | 2019-12-27 | 2021-03-23 | Saudi Arabian Oil Company | Ni—Ru—CgO based pre-reforming catalyst for liquid hydrocarbons |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AR220381A1 (es) * | 1979-04-16 | 1980-10-31 | Sao Paulo Gas | Proceso catalitico para la gasificacion de etanol con vapor |
| US4238371A (en) * | 1979-04-18 | 1980-12-09 | Phillips Petroleum Company | Methanation catalyst |
| GB2068407A (en) * | 1980-01-31 | 1981-08-12 | British Gas Corp | Gas production |
| BR8400305A (pt) * | 1984-01-16 | 1985-06-11 | Catalysts & Chem Europ | Processo para a producao de gases ricos em hidrogenio,metano,oxidos de carbono ou suas misturas |
| JP3313766B2 (ja) * | 1992-07-15 | 2002-08-12 | 財団法人石油産業活性化センター | 水蒸気改質用薄膜状触媒 |
| US7255848B2 (en) | 2002-10-01 | 2007-08-14 | Regents Of The Univeristy Of Minnesota | Production of hydrogen from alcohols |
| US7252692B2 (en) * | 2004-01-21 | 2007-08-07 | Min-Hon Rei | Process and reactor module for quick start hydrogen production |
| US7585339B2 (en) | 2004-09-15 | 2009-09-08 | Haldor Topsoe A/S | Process for reforming ethanol to hydrogen-rich products |
| JP4594011B2 (ja) * | 2004-09-15 | 2010-12-08 | ハルドール・トプサー・アクチエゼルスカベット | エタノール改質方法 |
| JP2010524824A (ja) * | 2007-04-18 | 2010-07-22 | エアー・リキッド・プロセス・アンド・コンストラクション,インコーポレイテッド | 水素製造方法 |
| ATE456691T1 (de) | 2007-07-02 | 2010-02-15 | Centre Nat Rech Scient | Verfahren zur herstellung von wasserstoffgas und kohlenstoffnanoröhrchen aus dem katalytischen abbau von ethanol |
| BRPI0703296A2 (pt) | 2007-07-19 | 2009-03-10 | Inst Nac De Tecnologia Int | catalisadores para a produÇço de hidrogÊnio para cÉlulas a combustÍvel de baixa temperatura a partir da reforma a vapor e da reforma autotÉrmica de Álcoois |
| WO2009130197A2 (de) | 2008-04-22 | 2009-10-29 | Basf Se | Verfahren zum prereforming von ethanol |
-
2010
- 2010-08-18 BR BRPI1002970-2A patent/BRPI1002970B1/pt active IP Right Grant
-
2011
- 2011-08-18 WO PCT/BR2011/000291 patent/WO2012031341A1/pt active Application Filing
- 2011-08-18 EP EP11822945.9A patent/EP2607302B1/en active Active
- 2011-08-18 JP JP2013524314A patent/JP2013540674A/ja active Pending
- 2011-08-18 US US13/212,772 patent/US8642004B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| US20120070367A1 (en) | 2012-03-22 |
| JP2013540674A (ja) | 2013-11-07 |
| EP2607302A4 (en) | 2014-07-23 |
| EP2607302A1 (en) | 2013-06-26 |
| WO2012031341A1 (pt) | 2012-03-15 |
| US8642004B2 (en) | 2014-02-04 |
| BRPI1002970A2 (pt) | 2012-04-17 |
| EP2607302B1 (en) | 2018-08-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US7166268B2 (en) | Catalyst for hydrocarbon reforming and method of reforming hydrocarbon with the same | |
| JP2017052695A (ja) | 液体炭化水素の熱中和改質のための触媒およびプロセス | |
| CA3110894A1 (en) | Processes and catalysts for reforming of impure methane-containing feeds | |
| BRPI1002970B1 (pt) | processo para a produção de hidrogênio a partir do etanol | |
| WO2015054755A1 (pt) | Catalisador para produção de gás de síntese e processo de obtenção do mesmo | |
| JP2016104467A (ja) | 炭化水素含有ガスの水蒸気改質触媒、水素製造装置、及び水素製造方法 | |
| DK180157B1 (en) | Process for pre-reforming olefin-containing hydrocarbon streams, pre-reforming catalyst and process for preparing the catalyst | |
| WO2014078119A1 (en) | Renewable hydrogen production catalysts from oxygenated feedstocks | |
| Belhadi et al. | Methane steam reforming on supported nickel based catalysts. effect of oxide ZrO 2, La 2 O 3 and Nickel Composition | |
| BRPI1107073A2 (pt) | Catalisador de reforma a vapor, processo para a preparação do referido catalisador e processo para a produção de hidrogênio e gás natural sintético | |
| WO2016197211A1 (pt) | Catalisador tolerante a enxofre para uso em reações de deslocamento gás-água, e, processo de deslocamento gás-água | |
| US11111142B2 (en) | Processes and catalysts for reforming of impure methane-containing feeds | |
| US10525449B2 (en) | Process for preparing a nickel-based catalyst, the nickel-based catalyst, and use thereof in a steam reforming process | |
| US11358128B2 (en) | High activity reforming catalyst formulation and process for low temperature steam reforming of hydrocarbons to produce hydrogen | |
| AU2017440226B2 (en) | Noble metal catalysts and processes for reforming of methane and other hydrocarbons | |
| BRPI1105737A2 (pt) | Catalisadores para a remoção de alcatrão de gás de síntese | |
| BR102015030320B1 (pt) | processo para pré-reforma de correntes hidrocarbonetos para produção de hidrogênio e gás de síntese | |
| BR112020009740B1 (pt) | Processo para produzir um produto de gás de síntese | |
| WO2017082752A1 (ru) | Катализатор, способ его приготовления и процесс обогащения смесей углеводородных газов метаном | |
| BR102013012165A2 (pt) | processo de conversão de co2 para obtenção de gás de síntese via reação de shift reversa e o uso de óxidos mistos em reações de shift reversa |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B03A | Publication of a patent application or of a certificate of addition of invention [chapter 3.1 patent gazette] | ||
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 13/10/2020, OBSERVADAS AS CONDICOES LEGAIS. |