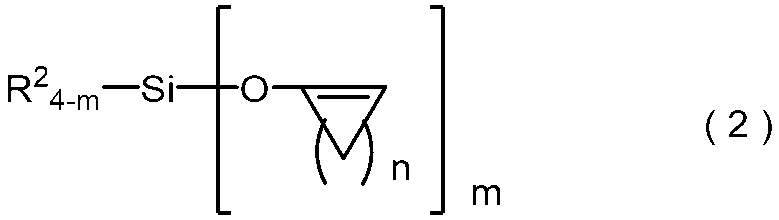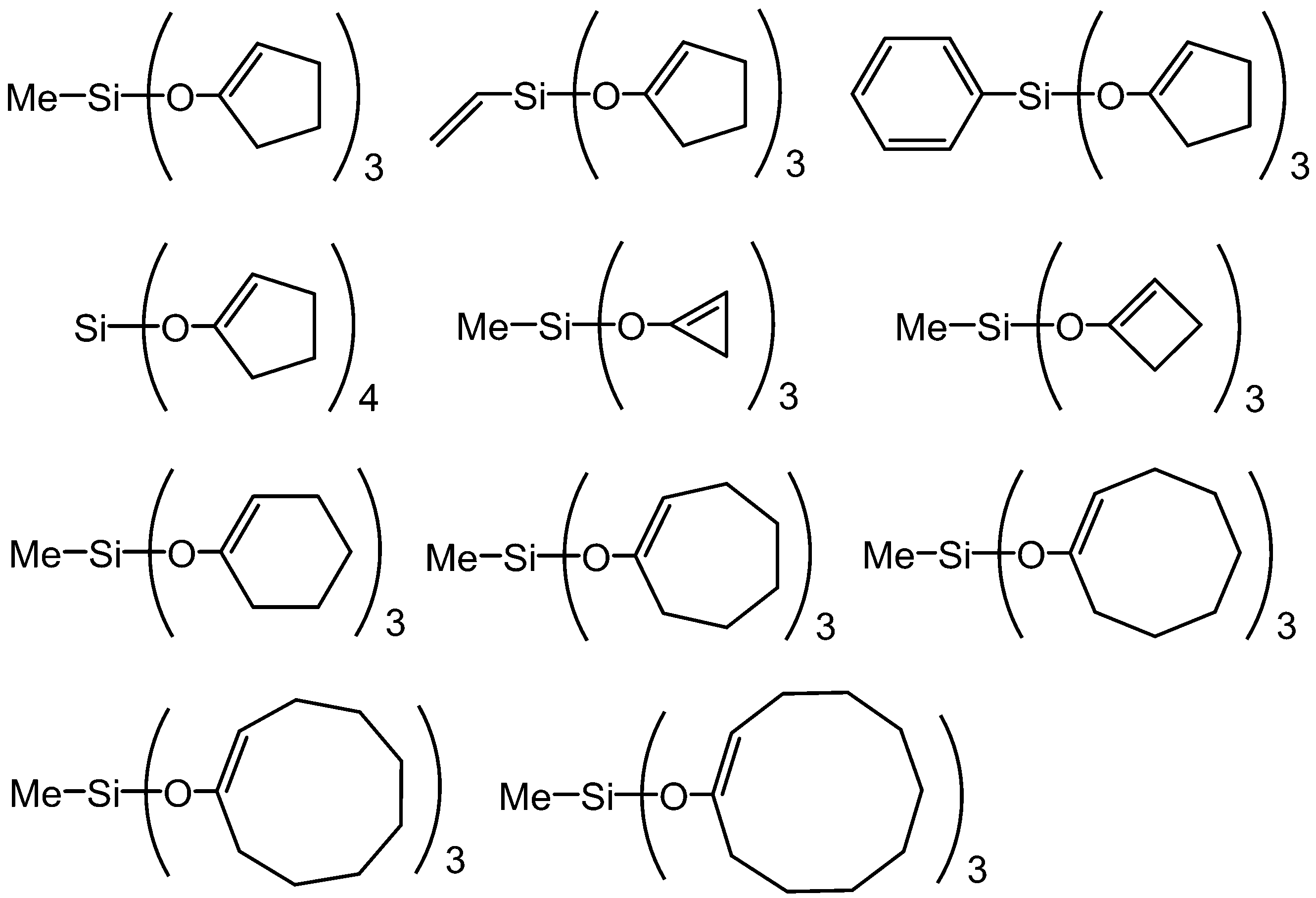WO2022113437A1 - 室温硬化性オルガノポリシロキサン組成物及び物品並びに加水分解性オルガノシラン化合物及びその製造方法 - Google Patents
室温硬化性オルガノポリシロキサン組成物及び物品並びに加水分解性オルガノシラン化合物及びその製造方法 Download PDFInfo
- Publication number
- WO2022113437A1 WO2022113437A1 PCT/JP2021/029897 JP2021029897W WO2022113437A1 WO 2022113437 A1 WO2022113437 A1 WO 2022113437A1 JP 2021029897 W JP2021029897 W JP 2021029897W WO 2022113437 A1 WO2022113437 A1 WO 2022113437A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- room temperature
- temperature curable
- curable organopolysiloxane
- organopolysiloxane composition
- Prior art date
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 182
- -1 organosilane compound Chemical class 0.000 title claims abstract description 144
- 229920001296 polysiloxane Polymers 0.000 title claims abstract description 108
- 238000004519 manufacturing process Methods 0.000 title claims abstract description 23
- 239000003054 catalyst Substances 0.000 claims abstract description 57
- 125000004432 carbon atom Chemical group C* 0.000 claims abstract description 32
- 239000003795 chemical substances by application Substances 0.000 claims abstract description 29
- 125000001183 hydrocarbyl group Chemical group 0.000 claims abstract 5
- BGTOWKSIORTVQH-UHFFFAOYSA-N cyclopentanone Chemical compound O=C1CCCC1 BGTOWKSIORTVQH-UHFFFAOYSA-N 0.000 claims description 89
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims description 51
- 239000000126 substance Substances 0.000 claims description 46
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 claims description 45
- 238000006243 chemical reaction Methods 0.000 claims description 36
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 claims description 30
- 239000000377 silicon dioxide Substances 0.000 claims description 24
- 239000005046 Chlorosilane Substances 0.000 claims description 23
- 238000006460 hydrolysis reaction Methods 0.000 claims description 17
- 239000000853 adhesive Substances 0.000 claims description 16
- 230000001070 adhesive effect Effects 0.000 claims description 16
- 229910000019 calcium carbonate Inorganic materials 0.000 claims description 15
- 230000007062 hydrolysis Effects 0.000 claims description 15
- 239000012974 tin catalyst Substances 0.000 claims description 15
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 14
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 claims description 14
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical group CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 claims description 12
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 claims description 11
- 229910052797 bismuth Inorganic materials 0.000 claims description 11
- JCXGWMGPZLAOME-UHFFFAOYSA-N bismuth atom Chemical compound [Bi] JCXGWMGPZLAOME-UHFFFAOYSA-N 0.000 claims description 11
- 229910052719 titanium Inorganic materials 0.000 claims description 11
- 239000010936 titanium Substances 0.000 claims description 11
- 239000006087 Silane Coupling Agent Substances 0.000 claims description 10
- SHQSVMDWKBRBGB-UHFFFAOYSA-N cyclobutanone Chemical compound O=C1CCC1 SHQSVMDWKBRBGB-UHFFFAOYSA-N 0.000 claims description 10
- 239000011256 inorganic filler Substances 0.000 claims description 10
- 229910003475 inorganic filler Inorganic materials 0.000 claims description 10
- 239000003566 sealing material Substances 0.000 claims description 9
- 239000011248 coating agent Substances 0.000 claims description 8
- 238000004382 potting Methods 0.000 claims description 8
- 239000003921 oil Substances 0.000 claims description 7
- 125000001309 chloro group Chemical group Cl* 0.000 claims description 6
- 125000000524 functional group Chemical group 0.000 claims description 6
- 229910052757 nitrogen Inorganic materials 0.000 claims description 6
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 6
- 125000004430 oxygen atom Chemical group O* 0.000 claims description 6
- 229910052717 sulfur Inorganic materials 0.000 claims description 6
- 125000004434 sulfur atom Chemical group 0.000 claims description 6
- IMFACGCPASFAPR-UHFFFAOYSA-N tributylamine Chemical compound CCCCN(CCCC)CCCC IMFACGCPASFAPR-UHFFFAOYSA-N 0.000 claims description 6
- 239000006229 carbon black Substances 0.000 claims description 5
- 125000005842 heteroatom Chemical group 0.000 claims description 5
- TWNQGVIAIRXVLR-UHFFFAOYSA-N oxo(oxoalumanyloxy)alumane Chemical compound O=[Al]O[Al]=O TWNQGVIAIRXVLR-UHFFFAOYSA-N 0.000 claims description 5
- QDFXRVAOBHEBGJ-UHFFFAOYSA-N 3-(cyclononen-1-yl)-4,5,6,7,8,9-hexahydro-1h-diazonine Chemical compound C1CCCCCCC=C1C1=NNCCCCCC1 QDFXRVAOBHEBGJ-UHFFFAOYSA-N 0.000 claims description 4
- WADSJYLPJPTMLN-UHFFFAOYSA-N 3-(cycloundecen-1-yl)-1,2-diazacycloundec-2-ene Chemical compound C1CCCCCCCCC=C1C1=NNCCCCCCCC1 WADSJYLPJPTMLN-UHFFFAOYSA-N 0.000 claims description 4
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 claims description 4
- ODWXUNBKCRECNW-UHFFFAOYSA-M bromocopper(1+) Chemical compound Br[Cu+] ODWXUNBKCRECNW-UHFFFAOYSA-M 0.000 claims description 4
- 239000004202 carbamide Substances 0.000 claims description 4
- ORTQZVOHEJQUHG-UHFFFAOYSA-L copper(II) chloride Chemical group Cl[Cu]Cl ORTQZVOHEJQUHG-UHFFFAOYSA-L 0.000 claims description 4
- GBRBMTNGQBKBQE-UHFFFAOYSA-L copper;diiodide Chemical compound I[Cu]I GBRBMTNGQBKBQE-UHFFFAOYSA-L 0.000 claims description 4
- YFTHZRPMJXBUME-UHFFFAOYSA-N tripropylamine Chemical compound CCCN(CCC)CCC YFTHZRPMJXBUME-UHFFFAOYSA-N 0.000 claims description 4
- JKFYKCYQEWQPTM-UHFFFAOYSA-N 2-azaniumyl-2-(4-fluorophenyl)acetate Chemical compound OC(=O)C(N)C1=CC=C(F)C=C1 JKFYKCYQEWQPTM-UHFFFAOYSA-N 0.000 claims description 3
- 229910021607 Silver chloride Inorganic materials 0.000 claims description 3
- 229910021612 Silver iodide Inorganic materials 0.000 claims description 3
- 239000003517 fume Substances 0.000 claims description 3
- 229940045105 silver iodide Drugs 0.000 claims description 3
- HKZLPVFGJNLROG-UHFFFAOYSA-M silver monochloride Chemical compound [Cl-].[Ag+] HKZLPVFGJNLROG-UHFFFAOYSA-M 0.000 claims description 3
- ADZWSOLPGZMUMY-UHFFFAOYSA-M silver bromide Chemical compound [Ag]Br ADZWSOLPGZMUMY-UHFFFAOYSA-M 0.000 claims description 2
- 239000000047 product Substances 0.000 abstract description 77
- 229920001971 elastomer Polymers 0.000 abstract description 20
- 230000009931 harmful effect Effects 0.000 abstract description 5
- 239000007859 condensation product Substances 0.000 abstract 1
- 238000003386 deoximation reaction Methods 0.000 abstract 1
- 238000001723 curing Methods 0.000 description 57
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 42
- 150000001875 compounds Chemical class 0.000 description 30
- 239000004205 dimethyl polysiloxane Substances 0.000 description 30
- 235000013870 dimethyl polysiloxane Nutrition 0.000 description 30
- 229920000435 poly(dimethylsiloxane) Polymers 0.000 description 30
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 26
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 21
- 238000002156 mixing Methods 0.000 description 21
- 230000000052 comparative effect Effects 0.000 description 20
- 150000002430 hydrocarbons Chemical group 0.000 description 20
- 239000003431 cross linking reagent Substances 0.000 description 18
- 150000001282 organosilanes Chemical class 0.000 description 17
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical group [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 16
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 16
- 229910052710 silicon Inorganic materials 0.000 description 16
- 230000015572 biosynthetic process Effects 0.000 description 15
- 238000003786 synthesis reaction Methods 0.000 description 15
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 12
- 125000005372 silanol group Chemical group 0.000 description 12
- 229920002379 silicone rubber Polymers 0.000 description 12
- 239000004945 silicone rubber Substances 0.000 description 12
- 239000012188 paraffin wax Substances 0.000 description 11
- 238000000746 purification Methods 0.000 description 11
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 10
- 229910052791 calcium Inorganic materials 0.000 description 10
- 238000000034 method Methods 0.000 description 10
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 9
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 9
- 239000011575 calcium Substances 0.000 description 9
- 238000011156 evaluation Methods 0.000 description 9
- PHQOGHDTIVQXHL-UHFFFAOYSA-N n'-(3-trimethoxysilylpropyl)ethane-1,2-diamine Chemical compound CO[Si](OC)(OC)CCCNCCN PHQOGHDTIVQXHL-UHFFFAOYSA-N 0.000 description 9
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 8
- 239000000383 hazardous chemical Substances 0.000 description 8
- 239000002904 solvent Substances 0.000 description 8
- 238000006482 condensation reaction Methods 0.000 description 7
- LIKFHECYJZWXFJ-UHFFFAOYSA-N dimethyldichlorosilane Chemical compound C[Si](C)(Cl)Cl LIKFHECYJZWXFJ-UHFFFAOYSA-N 0.000 description 7
- 230000007613 environmental effect Effects 0.000 description 7
- 239000002316 fumigant Substances 0.000 description 7
- 230000000704 physical effect Effects 0.000 description 7
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 6
- 229910021591 Copper(I) chloride Inorganic materials 0.000 description 6
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 6
- 229940125904 compound 1 Drugs 0.000 description 6
- OXBLHERUFWYNTN-UHFFFAOYSA-M copper(I) chloride Chemical compound [Cu]Cl OXBLHERUFWYNTN-UHFFFAOYSA-M 0.000 description 6
- 239000000706 filtrate Substances 0.000 description 6
- 238000001914 filtration Methods 0.000 description 6
- 238000010992 reflux Methods 0.000 description 6
- 238000003756 stirring Methods 0.000 description 6
- ILWRPSCZWQJDMK-UHFFFAOYSA-N triethylazanium;chloride Chemical compound Cl.CCN(CC)CC ILWRPSCZWQJDMK-UHFFFAOYSA-N 0.000 description 6
- SJECZPVISLOESU-UHFFFAOYSA-N 3-trimethoxysilylpropan-1-amine Chemical compound CO[Si](OC)(OC)CCCN SJECZPVISLOESU-UHFFFAOYSA-N 0.000 description 5
- XQBCVRSTVUHIGH-UHFFFAOYSA-L [dodecanoyloxy(dioctyl)stannyl] dodecanoate Chemical compound CCCCCCCCCCCC(=O)O[Sn](CCCCCCCC)(CCCCCCCC)OC(=O)CCCCCCCCCCC XQBCVRSTVUHIGH-UHFFFAOYSA-L 0.000 description 5
- 125000003118 aryl group Chemical group 0.000 description 5
- 238000004821 distillation Methods 0.000 description 5
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 5
- WHIVNJATOVLWBW-SNAWJCMRSA-N methylethyl ketone oxime Chemical compound CC\C(C)=N\O WHIVNJATOVLWBW-SNAWJCMRSA-N 0.000 description 5
- BPSIOYPQMFLKFR-UHFFFAOYSA-N trimethoxy-[3-(oxiran-2-ylmethoxy)propyl]silane Chemical compound CO[Si](OC)(OC)CCCOCC1CO1 BPSIOYPQMFLKFR-UHFFFAOYSA-N 0.000 description 5
- 206010007269 Carcinogenicity Diseases 0.000 description 4
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 4
- 239000005749 Copper compound Substances 0.000 description 4
- LCGLNKUTAGEVQW-UHFFFAOYSA-N Dimethyl ether Chemical compound COC LCGLNKUTAGEVQW-UHFFFAOYSA-N 0.000 description 4
- ZRALSGWEFCBTJO-UHFFFAOYSA-N Guanidine Chemical compound NC(N)=N ZRALSGWEFCBTJO-UHFFFAOYSA-N 0.000 description 4
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 4
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 4
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical compound [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 description 4
- 239000000654 additive Substances 0.000 description 4
- 125000003342 alkenyl group Chemical group 0.000 description 4
- 125000000217 alkyl group Chemical group 0.000 description 4
- 125000003710 aryl alkyl group Chemical group 0.000 description 4
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 4
- 230000007670 carcinogenicity Effects 0.000 description 4
- 231100000260 carcinogenicity Toxicity 0.000 description 4
- 229940116318 copper carbonate Drugs 0.000 description 4
- 150000001880 copper compounds Chemical class 0.000 description 4
- GEZOTWYUIKXWOA-UHFFFAOYSA-L copper;carbonate Chemical compound [Cu+2].[O-]C([O-])=O GEZOTWYUIKXWOA-UHFFFAOYSA-L 0.000 description 4
- DIOQZVSQGTUSAI-UHFFFAOYSA-N decane Chemical compound CCCCCCCCCC DIOQZVSQGTUSAI-UHFFFAOYSA-N 0.000 description 4
- LZCLXQDLBQLTDK-UHFFFAOYSA-N ethyl 2-hydroxypropanoate Chemical compound CCOC(=O)C(C)O LZCLXQDLBQLTDK-UHFFFAOYSA-N 0.000 description 4
- 229940093499 ethyl acetate Drugs 0.000 description 4
- 235000019439 ethyl acetate Nutrition 0.000 description 4
- 230000036541 health Effects 0.000 description 4
- 231100000206 health hazard Toxicity 0.000 description 4
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 4
- 230000007246 mechanism Effects 0.000 description 4
- 229910052751 metal Inorganic materials 0.000 description 4
- 239000002184 metal Substances 0.000 description 4
- 125000002524 organometallic group Chemical group 0.000 description 4
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 4
- 230000035484 reaction time Effects 0.000 description 4
- 238000003860 storage Methods 0.000 description 4
- VZGDMQKNWNREIO-UHFFFAOYSA-N tetrachloromethane Chemical compound ClC(Cl)(Cl)Cl VZGDMQKNWNREIO-UHFFFAOYSA-N 0.000 description 4
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 4
- 238000005160 1H NMR spectroscopy Methods 0.000 description 3
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 3
- 229930194542 Keto Natural products 0.000 description 3
- 206010074268 Reproductive toxicity Diseases 0.000 description 3
- 229910052782 aluminium Inorganic materials 0.000 description 3
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 3
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 3
- 125000004369 butenyl group Chemical group C(=CCC)* 0.000 description 3
- 229940125782 compound 2 Drugs 0.000 description 3
- 229940126214 compound 3 Drugs 0.000 description 3
- 229940125898 compound 5 Drugs 0.000 description 3
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 3
- 230000002939 deleterious effect Effects 0.000 description 3
- 238000003795 desorption Methods 0.000 description 3
- 125000006038 hexenyl group Chemical group 0.000 description 3
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 3
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 3
- 125000000555 isopropenyl group Chemical group [H]\C([H])=C(\*)C([H])([H])[H] 0.000 description 3
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 3
- 150000002894 organic compounds Chemical class 0.000 description 3
- 239000003960 organic solvent Substances 0.000 description 3
- 125000005375 organosiloxane group Chemical group 0.000 description 3
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 3
- 125000000286 phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 3
- 238000006116 polymerization reaction Methods 0.000 description 3
- 125000004368 propenyl group Chemical group C(=CC)* 0.000 description 3
- 231100000372 reproductive toxicity Toxicity 0.000 description 3
- 230000007696 reproductive toxicity Effects 0.000 description 3
- 229910000077 silane Inorganic materials 0.000 description 3
- 150000003377 silicon compounds Chemical class 0.000 description 3
- 125000001424 substituent group Chemical group 0.000 description 3
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 3
- UOCLXMDMGBRAIB-UHFFFAOYSA-N 1,1,1-trichloroethane Chemical compound CC(Cl)(Cl)Cl UOCLXMDMGBRAIB-UHFFFAOYSA-N 0.000 description 2
- ZXSQEZNORDWBGZ-UHFFFAOYSA-N 1,3-dihydropyrrolo[2,3-b]pyridin-2-one Chemical compound C1=CN=C2NC(=O)CC2=C1 ZXSQEZNORDWBGZ-UHFFFAOYSA-N 0.000 description 2
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 2
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 2
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 2
- XOBKSJJDNFUZPF-UHFFFAOYSA-N Methoxyethane Chemical compound CCOC XOBKSJJDNFUZPF-UHFFFAOYSA-N 0.000 description 2
- CHJJGSNFBQVOTG-UHFFFAOYSA-N N-methyl-guanidine Natural products CNC(N)=N CHJJGSNFBQVOTG-UHFFFAOYSA-N 0.000 description 2
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 2
- CYTYCFOTNPOANT-UHFFFAOYSA-N Perchloroethylene Chemical group ClC(Cl)=C(Cl)Cl CYTYCFOTNPOANT-UHFFFAOYSA-N 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 2
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 2
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 2
- 125000004423 acyloxy group Chemical group 0.000 description 2
- 238000007259 addition reaction Methods 0.000 description 2
- 230000000996 additive effect Effects 0.000 description 2
- 125000003302 alkenyloxy group Chemical group 0.000 description 2
- 125000003545 alkoxy group Chemical group 0.000 description 2
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 2
- NUMHJBONQMZPBW-UHFFFAOYSA-K bis(2-ethylhexanoyloxy)bismuthanyl 2-ethylhexanoate Chemical compound [Bi+3].CCCCC(CC)C([O-])=O.CCCCC(CC)C([O-])=O.CCCCC(CC)C([O-])=O NUMHJBONQMZPBW-UHFFFAOYSA-K 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 2
- 229910052794 bromium Inorganic materials 0.000 description 2
- 230000000711 cancerogenic effect Effects 0.000 description 2
- 231100000315 carcinogenic Toxicity 0.000 description 2
- 239000007795 chemical reaction product Substances 0.000 description 2
- 239000000460 chlorine Substances 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- 238000013005 condensation curing Methods 0.000 description 2
- 238000012790 confirmation Methods 0.000 description 2
- 238000010276 construction Methods 0.000 description 2
- 229910000365 copper sulfate Inorganic materials 0.000 description 2
- XTVVROIMIGLXTD-UHFFFAOYSA-N copper(II) nitrate Chemical compound [Cu+2].[O-][N+]([O-])=O.[O-][N+]([O-])=O XTVVROIMIGLXTD-UHFFFAOYSA-N 0.000 description 2
- ARUVKPQLZAKDPS-UHFFFAOYSA-L copper(II) sulfate Chemical compound [Cu+2].[O-][S+2]([O-])([O-])[O-] ARUVKPQLZAKDPS-UHFFFAOYSA-L 0.000 description 2
- OPQARKPSCNTWTJ-UHFFFAOYSA-L copper(ii) acetate Chemical compound [Cu+2].CC([O-])=O.CC([O-])=O OPQARKPSCNTWTJ-UHFFFAOYSA-L 0.000 description 2
- PUHAKHQMSBQAKT-UHFFFAOYSA-L copper;butanoate Chemical compound [Cu+2].CCCC([O-])=O.CCCC([O-])=O PUHAKHQMSBQAKT-UHFFFAOYSA-L 0.000 description 2
- HFDWIMBEIXDNQS-UHFFFAOYSA-L copper;diformate Chemical compound [Cu+2].[O-]C=O.[O-]C=O HFDWIMBEIXDNQS-UHFFFAOYSA-L 0.000 description 2
- 238000004132 cross linking Methods 0.000 description 2
- 238000005520 cutting process Methods 0.000 description 2
- 125000000753 cycloalkyl group Chemical group 0.000 description 2
- JHIVVAPYMSGYDF-UHFFFAOYSA-N cyclohexanone Chemical compound O=C1CCCCC1 JHIVVAPYMSGYDF-UHFFFAOYSA-N 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- BAUZLFKYYIVGPM-UHFFFAOYSA-N cyclononanone Chemical compound O=C1CCCCCCCC1 BAUZLFKYYIVGPM-UHFFFAOYSA-N 0.000 description 2
- 230000006837 decompression Effects 0.000 description 2
- SWSQBOPZIKWTGO-UHFFFAOYSA-N dimethylaminoamidine Natural products CN(C)C(N)=N SWSQBOPZIKWTGO-UHFFFAOYSA-N 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 150000002148 esters Chemical class 0.000 description 2
- 150000002170 ethers Chemical class 0.000 description 2
- 229940116333 ethyl lactate Drugs 0.000 description 2
- 230000001747 exhibiting effect Effects 0.000 description 2
- 229910052731 fluorine Inorganic materials 0.000 description 2
- 239000011737 fluorine Substances 0.000 description 2
- 238000005227 gel permeation chromatography Methods 0.000 description 2
- 150000008282 halocarbons Chemical class 0.000 description 2
- 125000005843 halogen group Chemical group 0.000 description 2
- VHHHONWQHHHLTI-UHFFFAOYSA-N hexachloroethane Chemical compound ClC(Cl)(Cl)C(Cl)(Cl)Cl VHHHONWQHHHLTI-UHFFFAOYSA-N 0.000 description 2
- FUZZWVXGSFPDMH-UHFFFAOYSA-M hexanoate Chemical compound CCCCCC([O-])=O FUZZWVXGSFPDMH-UHFFFAOYSA-M 0.000 description 2
- NUKZAGXMHTUAFE-UHFFFAOYSA-N hexanoic acid methyl ester Natural products CCCCCC(=O)OC NUKZAGXMHTUAFE-UHFFFAOYSA-N 0.000 description 2
- 229930195733 hydrocarbon Natural products 0.000 description 2
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 2
- 238000006459 hydrosilylation reaction Methods 0.000 description 2
- 238000009413 insulation Methods 0.000 description 2
- 231100000647 material safety data sheet Toxicity 0.000 description 2
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 2
- BFXIKLCIZHOAAZ-UHFFFAOYSA-N methyltrimethoxysilane Chemical compound CO[Si](C)(OC)OC BFXIKLCIZHOAAZ-UHFFFAOYSA-N 0.000 description 2
- ZCYXXKJEDCHMGH-UHFFFAOYSA-N nonane Chemical compound CCCC[CH]CCCC ZCYXXKJEDCHMGH-UHFFFAOYSA-N 0.000 description 2
- BKIMMITUMNQMOS-UHFFFAOYSA-N normal nonane Natural products CCCCCCCCC BKIMMITUMNQMOS-UHFFFAOYSA-N 0.000 description 2
- TVMXDCGIABBOFY-UHFFFAOYSA-N octane Chemical compound CCCCCCCC TVMXDCGIABBOFY-UHFFFAOYSA-N 0.000 description 2
- 239000005054 phenyltrichlorosilane Substances 0.000 description 2
- 239000004848 polyfunctional curative Substances 0.000 description 2
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 235000012239 silicon dioxide Nutrition 0.000 description 2
- 229910001958 silver carbonate Inorganic materials 0.000 description 2
- LKZMBDSASOBTPN-UHFFFAOYSA-L silver carbonate Substances [Ag].[O-]C([O-])=O LKZMBDSASOBTPN-UHFFFAOYSA-L 0.000 description 2
- 229940100890 silver compound Drugs 0.000 description 2
- 150000003379 silver compounds Chemical class 0.000 description 2
- SQGYOTSLMSWVJD-UHFFFAOYSA-N silver(1+) nitrate Chemical compound [Ag+].[O-]N(=O)=O SQGYOTSLMSWVJD-UHFFFAOYSA-N 0.000 description 2
- 230000002194 synthesizing effect Effects 0.000 description 2
- 238000010998 test method Methods 0.000 description 2
- 231100000331 toxic Toxicity 0.000 description 2
- 230000002588 toxic effect Effects 0.000 description 2
- GQIUQDDJKHLHTB-UHFFFAOYSA-N trichloro(ethenyl)silane Chemical compound Cl[Si](Cl)(Cl)C=C GQIUQDDJKHLHTB-UHFFFAOYSA-N 0.000 description 2
- ORVMIVQULIKXCP-UHFFFAOYSA-N trichloro(phenyl)silane Chemical compound Cl[Si](Cl)(Cl)C1=CC=CC=C1 ORVMIVQULIKXCP-UHFFFAOYSA-N 0.000 description 2
- 125000000725 trifluoropropyl group Chemical group [H]C([H])(*)C([H])([H])C(F)(F)F 0.000 description 2
- 239000005050 vinyl trichlorosilane Substances 0.000 description 2
- 239000008096 xylene Substances 0.000 description 2
- WYTZZXDRDKSJID-UHFFFAOYSA-N (3-aminopropyl)triethoxysilane Chemical compound CCO[Si](OCC)(OCC)CCCN WYTZZXDRDKSJID-UHFFFAOYSA-N 0.000 description 1
- NOGBEXBVDOCGDB-NRFIWDAESA-L (z)-4-ethoxy-4-oxobut-2-en-2-olate;propan-2-olate;titanium(4+) Chemical compound [Ti+4].CC(C)[O-].CC(C)[O-].CCOC(=O)\C=C(\C)[O-].CCOC(=O)\C=C(\C)[O-] NOGBEXBVDOCGDB-NRFIWDAESA-L 0.000 description 1
- KYVBNYUBXIEUFW-UHFFFAOYSA-N 1,1,3,3-tetramethylguanidine Chemical compound CN(C)C(=N)N(C)C KYVBNYUBXIEUFW-UHFFFAOYSA-N 0.000 description 1
- BMVXCPBXGZKUPN-UHFFFAOYSA-N 1-hexanamine Chemical compound CCCCCCN BMVXCPBXGZKUPN-UHFFFAOYSA-N 0.000 description 1
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 1
- OBETXYAYXDNJHR-UHFFFAOYSA-N 2-Ethylhexanoic acid Chemical compound CCCCC(CC)C(O)=O OBETXYAYXDNJHR-UHFFFAOYSA-N 0.000 description 1
- KTXWGMUMDPYXNN-UHFFFAOYSA-N 2-ethylhexan-1-olate;titanium(4+) Chemical compound [Ti+4].CCCCC(CC)C[O-].CCCCC(CC)C[O-].CCCCC(CC)C[O-].CCCCC(CC)C[O-] KTXWGMUMDPYXNN-UHFFFAOYSA-N 0.000 description 1
- UUEWCQRISZBELL-UHFFFAOYSA-N 3-trimethoxysilylpropane-1-thiol Chemical compound CO[Si](OC)(OC)CCCS UUEWCQRISZBELL-UHFFFAOYSA-N 0.000 description 1
- YPIFGDQKSSMYHQ-UHFFFAOYSA-M 7,7-dimethyloctanoate Chemical compound CC(C)(C)CCCCCC([O-])=O YPIFGDQKSSMYHQ-UHFFFAOYSA-M 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- 240000007594 Oryza sativa Species 0.000 description 1
- 235000007164 Oryza sativa Nutrition 0.000 description 1
- 239000004721 Polyphenylene oxide Substances 0.000 description 1
- 229910018540 Si C Inorganic materials 0.000 description 1
- 240000002657 Thymus vulgaris Species 0.000 description 1
- 235000007303 Thymus vulgaris Nutrition 0.000 description 1
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 description 1
- FMRLDPWIRHBCCC-UHFFFAOYSA-L Zinc carbonate Chemical compound [Zn+2].[O-]C([O-])=O FMRLDPWIRHBCCC-UHFFFAOYSA-L 0.000 description 1
- ISKQADXMHQSTHK-UHFFFAOYSA-N [4-(aminomethyl)phenyl]methanamine Chemical compound NCC1=CC=C(CN)C=C1 ISKQADXMHQSTHK-UHFFFAOYSA-N 0.000 description 1
- NOKSMMGULAYSTD-UHFFFAOYSA-N [SiH4].N=C=O Chemical class [SiH4].N=C=O NOKSMMGULAYSTD-UHFFFAOYSA-N 0.000 description 1
- UKLDJPRMSDWDSL-UHFFFAOYSA-L [dibutyl(dodecanoyloxy)stannyl] dodecanoate Chemical compound CCCCCCCCCCCC(=O)O[Sn](CCCC)(CCCC)OC(=O)CCCCCCCCCCC UKLDJPRMSDWDSL-UHFFFAOYSA-L 0.000 description 1
- 125000003668 acetyloxy group Chemical group [H]C([H])([H])C(=O)O[*] 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 150000001338 aliphatic hydrocarbons Chemical class 0.000 description 1
- 125000005083 alkoxyalkoxy group Chemical group 0.000 description 1
- 125000005336 allyloxy group Chemical group 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- 125000003368 amide group Chemical group 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 125000003277 amino group Chemical group 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 229920005601 base polymer Polymers 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- 239000000440 bentonite Substances 0.000 description 1
- 229910000278 bentonite Inorganic materials 0.000 description 1
- SVPXDRXYRYOSEX-UHFFFAOYSA-N bentoquatam Chemical compound O.O=[Si]=O.O=[Al]O[Al]=O SVPXDRXYRYOSEX-UHFFFAOYSA-N 0.000 description 1
- 230000001588 bifunctional effect Effects 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 150000001622 bismuth compounds Chemical class 0.000 description 1
- FPCJKVGGYOAWIZ-UHFFFAOYSA-N butan-1-ol;titanium Chemical compound [Ti].CCCCO.CCCCO.CCCCO.CCCCO FPCJKVGGYOAWIZ-UHFFFAOYSA-N 0.000 description 1
- 125000004106 butoxy group Chemical group [*]OC([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- BRPQOXSCLDDYGP-UHFFFAOYSA-N calcium oxide Chemical compound [O-2].[Ca+2] BRPQOXSCLDDYGP-UHFFFAOYSA-N 0.000 description 1
- 239000000292 calcium oxide Substances 0.000 description 1
- ODINCKMPIJJUCX-UHFFFAOYSA-N calcium oxide Inorganic materials [Ca]=O ODINCKMPIJJUCX-UHFFFAOYSA-N 0.000 description 1
- SHZIWNPUGXLXDT-UHFFFAOYSA-N caproic acid ethyl ester Natural products CCCCCC(=O)OCC SHZIWNPUGXLXDT-UHFFFAOYSA-N 0.000 description 1
- 125000001951 carbamoylamino group Chemical group C(N)(=O)N* 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- KOPOQZFJUQMUML-UHFFFAOYSA-N chlorosilane Chemical compound Cl[SiH3] KOPOQZFJUQMUML-UHFFFAOYSA-N 0.000 description 1
- 238000004040 coloring Methods 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 239000007822 coupling agent Substances 0.000 description 1
- 229910002026 crystalline silica Inorganic materials 0.000 description 1
- 150000001923 cyclic compounds Chemical class 0.000 description 1
- SXOZDDAFVJANJP-UHFFFAOYSA-N cyclodecanone Chemical compound O=C1CCCCCCCCC1 SXOZDDAFVJANJP-UHFFFAOYSA-N 0.000 description 1
- CGZZMOTZOONQIA-UHFFFAOYSA-N cycloheptanone Chemical compound O=C1CCCCCC1 CGZZMOTZOONQIA-UHFFFAOYSA-N 0.000 description 1
- BGTOWKSIORTVQH-HOSYLAQJSA-N cyclopentanone Chemical group O=[13C]1CCCC1 BGTOWKSIORTVQH-HOSYLAQJSA-N 0.000 description 1
- VBBRYJMZLIYUJQ-UHFFFAOYSA-N cyclopropanone Chemical compound O=C1CC1 VBBRYJMZLIYUJQ-UHFFFAOYSA-N 0.000 description 1
- AYOHIQLKSOJJQH-UHFFFAOYSA-N dibutyltin Chemical compound CCCC[Sn]CCCC AYOHIQLKSOJJQH-UHFFFAOYSA-N 0.000 description 1
- 239000012975 dibutyltin dilaurate Substances 0.000 description 1
- ZXDVQYBUEVYUCG-UHFFFAOYSA-N dibutyltin(2+);methanolate Chemical compound CCCC[Sn](OC)(OC)CCCC ZXDVQYBUEVYUCG-UHFFFAOYSA-N 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- NHWNGVQMIQXKCB-UHFFFAOYSA-N dimethoxy(dimethyl)stannane Chemical compound CO[Sn](C)(C)OC NHWNGVQMIQXKCB-UHFFFAOYSA-N 0.000 description 1
- 125000000118 dimethyl group Chemical group [H]C([H])([H])* 0.000 description 1
- SDTDHTCWRNVNAJ-UHFFFAOYSA-L dimethyltin(2+);diacetate Chemical compound CC(=O)O[Sn](C)(C)OC(C)=O SDTDHTCWRNVNAJ-UHFFFAOYSA-L 0.000 description 1
- HGQSXVKHVMGQRG-UHFFFAOYSA-N dioctyltin Chemical compound CCCCCCCC[Sn]CCCCCCCC HGQSXVKHVMGQRG-UHFFFAOYSA-N 0.000 description 1
- 229920005645 diorganopolysiloxane polymer Polymers 0.000 description 1
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical group [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 125000003700 epoxy group Chemical group 0.000 description 1
- NKSJNEHGWDZZQF-UHFFFAOYSA-N ethenyl(trimethoxy)silane Chemical compound CO[Si](OC)(OC)C=C NKSJNEHGWDZZQF-UHFFFAOYSA-N 0.000 description 1
- MABAWBWRUSBLKQ-UHFFFAOYSA-N ethenyl-tri(propan-2-yloxy)silane Chemical compound CC(C)O[Si](OC(C)C)(OC(C)C)C=C MABAWBWRUSBLKQ-UHFFFAOYSA-N 0.000 description 1
- 125000001301 ethoxy group Chemical group [H]C([H])([H])C([H])([H])O* 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 239000006081 fluorescent whitening agent Substances 0.000 description 1
- 229910021485 fumed silica Inorganic materials 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 230000003301 hydrolyzing effect Effects 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 125000001841 imino group Chemical group [H]N=* 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 125000002510 isobutoxy group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])O* 0.000 description 1
- 125000003253 isopropoxy group Chemical group [H]C([H])([H])C([H])(O*)C([H])([H])[H] 0.000 description 1
- 231100001231 less toxic Toxicity 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 231100000053 low toxicity Toxicity 0.000 description 1
- ZLNQQNXFFQJAID-UHFFFAOYSA-L magnesium carbonate Chemical compound [Mg+2].[O-]C([O-])=O ZLNQQNXFFQJAID-UHFFFAOYSA-L 0.000 description 1
- 239000001095 magnesium carbonate Substances 0.000 description 1
- 229910000021 magnesium carbonate Inorganic materials 0.000 description 1
- 239000000395 magnesium oxide Substances 0.000 description 1
- CPLXHLVBOLITMK-UHFFFAOYSA-N magnesium oxide Inorganic materials [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 1
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 description 1
- ZKWONARDNQWFKT-UHFFFAOYSA-N methanolate;titanium(2+) Chemical compound CO[Ti]OC ZKWONARDNQWFKT-UHFFFAOYSA-N 0.000 description 1
- ARYZCSRUUPFYMY-UHFFFAOYSA-N methoxysilane Chemical compound CO[SiH3] ARYZCSRUUPFYMY-UHFFFAOYSA-N 0.000 description 1
- 239000005055 methyl trichlorosilane Substances 0.000 description 1
- JLUFWMXJHAVVNN-UHFFFAOYSA-N methyltrichlorosilane Chemical compound C[Si](Cl)(Cl)Cl JLUFWMXJHAVVNN-UHFFFAOYSA-N 0.000 description 1
- 239000003607 modifier Substances 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- 229910052755 nonmetal Inorganic materials 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 150000003961 organosilicon compounds Chemical class 0.000 description 1
- 150000002923 oximes Chemical class 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 229920000570 polyether Polymers 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- HKJYVRJHDIPMQB-UHFFFAOYSA-N propan-1-olate;titanium(4+) Chemical compound CCCO[Ti](OCCC)(OCCC)OCCC HKJYVRJHDIPMQB-UHFFFAOYSA-N 0.000 description 1
- 125000002572 propoxy group Chemical group [*]OC([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- 239000010453 quartz Substances 0.000 description 1
- 150000003254 radicals Chemical class 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000003014 reinforcing effect Effects 0.000 description 1
- 239000012763 reinforcing filler Substances 0.000 description 1
- 239000005871 repellent Substances 0.000 description 1
- 230000002940 repellent Effects 0.000 description 1
- 235000009566 rice Nutrition 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 239000000523 sample Substances 0.000 description 1
- 239000000565 sealant Substances 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 125000005920 sec-butoxy group Chemical group 0.000 description 1
- FZHAPNGMFPVSLP-UHFFFAOYSA-N silanamine Chemical class [SiH3]N FZHAPNGMFPVSLP-UHFFFAOYSA-N 0.000 description 1
- 150000004756 silanes Chemical class 0.000 description 1
- 229910010271 silicon carbide Inorganic materials 0.000 description 1
- FDNAPBUWERUEDA-UHFFFAOYSA-N silicon tetrachloride Chemical compound Cl[Si](Cl)(Cl)Cl FDNAPBUWERUEDA-UHFFFAOYSA-N 0.000 description 1
- 229920002545 silicone oil Polymers 0.000 description 1
- CQLFBEKRDQMJLZ-UHFFFAOYSA-M silver acetate Chemical compound [Ag+].CC([O-])=O CQLFBEKRDQMJLZ-UHFFFAOYSA-M 0.000 description 1
- 229940071536 silver acetate Drugs 0.000 description 1
- 229910001961 silver nitrate Inorganic materials 0.000 description 1
- YPNVIBVEFVRZPJ-UHFFFAOYSA-L silver sulfate Chemical compound [Ag+].[Ag+].[O-]S([O-])(=O)=O YPNVIBVEFVRZPJ-UHFFFAOYSA-L 0.000 description 1
- 229910000367 silver sulfate Inorganic materials 0.000 description 1
- JKOCEVIXVMBKJA-UHFFFAOYSA-M silver;butanoate Chemical compound [Ag+].CCCC([O-])=O JKOCEVIXVMBKJA-UHFFFAOYSA-M 0.000 description 1
- FTNNQMMAOFBTNJ-UHFFFAOYSA-M silver;formate Chemical compound [Ag+].[O-]C=O FTNNQMMAOFBTNJ-UHFFFAOYSA-M 0.000 description 1
- 239000002689 soil Substances 0.000 description 1
- 238000003980 solgel method Methods 0.000 description 1
- TXDNPSYEJHXKMK-UHFFFAOYSA-N sulfanylsilane Chemical class S[SiH3] TXDNPSYEJHXKMK-UHFFFAOYSA-N 0.000 description 1
- 230000001629 suppression Effects 0.000 description 1
- 239000012756 surface treatment agent Substances 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 125000004213 tert-butoxy group Chemical group [H]C([H])([H])C(O*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 125000003396 thiol group Chemical group [H]S* 0.000 description 1
- 239000001585 thymus vulgaris Substances 0.000 description 1
- 150000003606 tin compounds Chemical class 0.000 description 1
- 150000003609 titanium compounds Chemical class 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- HQYALQRYBUJWDH-UHFFFAOYSA-N trimethoxy(propyl)silane Chemical compound CCC[Si](OC)(OC)OC HQYALQRYBUJWDH-UHFFFAOYSA-N 0.000 description 1
- 239000000341 volatile oil Substances 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 1
- 239000011667 zinc carbonate Substances 0.000 description 1
- 229910000010 zinc carbonate Inorganic materials 0.000 description 1
- 235000004416 zinc carbonate Nutrition 0.000 description 1
- 239000011787 zinc oxide Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D7/00—Features of coating compositions, not provided for in group C09D5/00; Processes for incorporating ingredients in coating compositions
- C09D7/40—Additives
- C09D7/60—Additives non-macromolecular
- C09D7/61—Additives non-macromolecular inorganic
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/54—Silicon-containing compounds
- C08K5/541—Silicon-containing compounds containing oxygen
- C08K5/5415—Silicon-containing compounds containing oxygen containing at least one Si—O bond
- C08K5/5419—Silicon-containing compounds containing oxygen containing at least one Si—O bond containing at least one Si—C bond
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/20—Polysiloxanes containing silicon bound to unsaturated aliphatic groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic System
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/18—Compounds having one or more C—Si linkages as well as one or more C—O—Si linkages
- C07F7/1804—Compounds having Si-O-C linkages
- C07F7/1872—Preparation; Treatments not provided for in C07F7/20
- C07F7/188—Preparation; Treatments not provided for in C07F7/20 by reactions involving the formation of Si-O linkages
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/06—Preparatory processes
- C08G77/08—Preparatory processes characterised by the catalysts used
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/14—Polysiloxanes containing silicon bound to oxygen-containing groups
- C08G77/16—Polysiloxanes containing silicon bound to oxygen-containing groups to hydroxyl groups
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/22—Polysiloxanes containing silicon bound to organic groups containing atoms other than carbon, hydrogen and oxygen
- C08G77/26—Polysiloxanes containing silicon bound to organic groups containing atoms other than carbon, hydrogen and oxygen nitrogen-containing groups
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/02—Elements
- C08K3/04—Carbon
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/18—Oxygen-containing compounds, e.g. metal carbonyls
- C08K3/20—Oxides; Hydroxides
- C08K3/22—Oxides; Hydroxides of metals
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/18—Oxygen-containing compounds, e.g. metal carbonyls
- C08K3/24—Acids; Salts thereof
- C08K3/26—Carbonates; Bicarbonates
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/34—Silicon-containing compounds
- C08K3/36—Silica
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K9/00—Use of pretreated ingredients
- C08K9/04—Ingredients treated with organic substances
- C08K9/06—Ingredients treated with organic substances with silicon-containing compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K9/00—Use of pretreated ingredients
- C08K9/08—Ingredients agglomerated by treatment with a binding agent
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L83/00—Compositions of macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon only; Compositions of derivatives of such polymers
- C08L83/04—Polysiloxanes
- C08L83/06—Polysiloxanes containing silicon bound to oxygen-containing groups
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D183/00—Coating compositions based on macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing silicon, with or without sulfur, nitrogen, oxygen, or carbon only; Coating compositions based on derivatives of such polymers
- C09D183/04—Polysiloxanes
- C09D183/06—Polysiloxanes containing silicon bound to oxygen-containing groups
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D7/00—Features of coating compositions, not provided for in group C09D5/00; Processes for incorporating ingredients in coating compositions
- C09D7/40—Additives
- C09D7/60—Additives non-macromolecular
- C09D7/61—Additives non-macromolecular inorganic
- C09D7/62—Additives non-macromolecular inorganic modified by treatment with other compounds
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D7/00—Features of coating compositions, not provided for in group C09D5/00; Processes for incorporating ingredients in coating compositions
- C09D7/40—Additives
- C09D7/60—Additives non-macromolecular
- C09D7/63—Additives non-macromolecular organic
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J11/00—Features of adhesives not provided for in group C09J9/00, e.g. additives
- C09J11/02—Non-macromolecular additives
- C09J11/04—Non-macromolecular additives inorganic
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J11/00—Features of adhesives not provided for in group C09J9/00, e.g. additives
- C09J11/02—Non-macromolecular additives
- C09J11/06—Non-macromolecular additives organic
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J183/00—Adhesives based on macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing silicon, with or without sulfur, nitrogen, oxygen, or carbon only; Adhesives based on derivatives of such polymers
- C09J183/04—Polysiloxanes
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J183/00—Adhesives based on macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing silicon, with or without sulfur, nitrogen, oxygen, or carbon only; Adhesives based on derivatives of such polymers
- C09J183/04—Polysiloxanes
- C09J183/06—Polysiloxanes containing silicon bound to oxygen-containing groups
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K3/00—Materials not provided for elsewhere
- C09K3/10—Materials in mouldable or extrudable form for sealing or packing joints or covers
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K3/00—Materials not provided for elsewhere
- C09K3/10—Materials in mouldable or extrudable form for sealing or packing joints or covers
- C09K3/1006—Materials in mouldable or extrudable form for sealing or packing joints or covers characterised by the chemical nature of one of its constituents
- C09K3/1018—Macromolecular compounds having one or more carbon-to-silicon linkages
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/18—Oxygen-containing compounds, e.g. metal carbonyls
- C08K3/20—Oxides; Hydroxides
- C08K3/22—Oxides; Hydroxides of metals
- C08K2003/2227—Oxides; Hydroxides of metals of aluminium
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/18—Oxygen-containing compounds, e.g. metal carbonyls
- C08K3/24—Acids; Salts thereof
- C08K3/26—Carbonates; Bicarbonates
- C08K2003/265—Calcium, strontium or barium carbonate
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K3/00—Use of inorganic substances as compounding ingredients
- C08K3/01—Use of inorganic substances as compounding ingredients characterized by their specific function
- C08K3/013—Fillers, pigments or reinforcing additives
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/54—Silicon-containing compounds
- C08K5/541—Silicon-containing compounds containing oxygen
- C08K5/5415—Silicon-containing compounds containing oxygen containing at least one Si—O bond
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J2203/00—Applications of adhesives in processes or use of adhesives in the form of films or foils
- C09J2203/326—Applications of adhesives in processes or use of adhesives in the form of films or foils for bonding electronic components such as wafers, chips or semiconductors
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09J—ADHESIVES; NON-MECHANICAL ASPECTS OF ADHESIVE PROCESSES IN GENERAL; ADHESIVE PROCESSES NOT PROVIDED FOR ELSEWHERE; USE OF MATERIALS AS ADHESIVES
- C09J2203/00—Applications of adhesives in processes or use of adhesives in the form of films or foils
- C09J2203/354—Applications of adhesives in processes or use of adhesives in the form of films or foils for automotive applications
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2200/00—Chemical nature of materials in mouldable or extrudable form for sealing or packing joints or covers
- C09K2200/06—Macromolecular organic compounds, e.g. prepolymers
- C09K2200/068—Containing also other elements than carbon, oxygen or nitrogen in the polymer main chain
- C09K2200/0685—Containing silicon
Definitions
- the present invention is a condensation-curable room-temperature curable organopolysiloxane composition that is cross-linked (cured) by a hydrolysis / condensation reaction due to atmospheric moisture (moisture) at room temperature (23 ° C ⁇ 15 ° C), particularly curing.
- the desorption compound desorbed / generated from the cross-linking agent (hardener) by the hydrolysis reaction at the time is a cyclic ketone compound such as cyclobutanone or cyclopentanone, and is a silicone rubber that cures well by the condensation reaction and has excellent adhesiveness.
- a room temperature curable organopolysiloxane composition that gives a cured product (a cured elastomeric organopolysiloxane), various articles having the composition or a cured product thereof (silicone rubber), and cyclopenta as a desorption group by hydrolysis.
- the present invention relates to a novel hydrolyzable organosilane compound that releases non, and a method for producing the same.
- a room temperature curable organopolysiloxane composition that cures at room temperature to become a silicone rubber has been known for a long time and has been widely used in the industrial world.
- Known mechanisms for curing at room temperature include a mechanism for curing by a hydrosilylation addition reaction, a mechanism for radical curing by ultraviolet rays, and a mechanism for curing by a condensation reaction between a hydrolyzable group bonded to a silicon atom and a hydroxyl group.
- the room temperature curable organopolysiloxane composition that is cured by the condensation reaction has an advantage that it can be easily cured at room temperature and that it is less likely to cause curing inhibition due to impurities that occur in the hydrosilylation addition reaction or the like.
- the cured product (silicone rubber cured product) obtained by curing a room temperature curable organopolysiloxane composition that is cured by a condensation reaction is used for automobiles such as in-vehicle gaskets and sealing materials, construction of building sealants, and electrical / electronic. Widely used in fields such as parts.
- the room temperature curable organopolysiloxane composition that is cured by the condensation reaction contains a hydrolyzable organosilane compound having a hydrolyzable group in the molecule as a curing agent (crosslinking agent) in the composition, and has already been contained in the composition.
- Widely used curing agents include a de-oxime-type hydrolyzable organosilane compound that releases an oxime compound such as 2-butanone oxime at the time of curing, and a de-alcohol-type hydrolyzable compound that releases an alcohol compound such as methanol.
- Organosilane compounds and the like are known.
- the rubber-like cured product obtained by curing the composition containing these curing agents has high heat resistance, chemical resistance, and weather resistance derived from silicone (siloxane structure).
- oxime compounds such as 2-butanone oxime generated when the de-oxime type curing agent is cured are not preferable because they are suspected to be carcinogenic. It is toxic to oxime and is designated as a deleterious substance, which is not preferable from the viewpoint of human health.
- a tin catalyst whose regulations are tightened as an environmentally hazardous substance, is used as the curing catalyst, which is not preferable from the viewpoint of ensuring the safety of workers and protecting the environment in recent years, and is safer. It is required to substitute for a hydrolyzable organosilane compound (hardener) having a highly effective leaving group (leaving compound).
- the curing agent (crosslinking agent) used in the dealcohol type room temperature curable organopolysiloxane composition is more reactive than the curing agent used in the deoxime type room temperature curable organopolysiloxane composition. Since it is inferior to the deoxime type, it has a drawback of being inferior in curability to the deoxime type. From the viewpoint of environmental protection and suppression of health damage, products that are more environmentally friendly and safer as well as improved performance are particularly desired. Room temperature curable organopolysiloxane compositions with high safety of desorbed compounds and excellent performance. Demand is increasing.
- Japanese Patent Laid-Open No. 2018-515634 contains, as a cross-linking agent, a silane compound that desorbs and releases an ⁇ -hydroxycarboxylic acid ester compound typified by ethyl lactate as an alternative to the de-alcohol type and de-oxime type curing agents.
- ethyl lactate which is a leaving group, is a highly safe compound, but it is essential to use a tin catalyst as a catalyst. It has been pointed out that tin catalysts are harmful to aquatic organisms, and the use of tin catalysts is not preferable from the viewpoint of environmental protection.
- Japanese Patent Publication No. 51-39673 proposes a condensation-curable organopolysiloxane composition that releases a ketone compound typified by acetone.
- Acetone is a compound that is less harmful to the human body than 2-butanone oxime and methanol, and further provides a composition that gives a cured silicone rubber product that cures faster and has better durability than the conventional cured form. is doing.
- the flash point of acetone is as low as -20 ° C and it is highly volatile, there is a problem that the usage environment is limited.
- Cyclopentanone is a compound with low toxicity and high biodegradability, and has a flash point of 35 ° C, which is a relatively high compound as an organic solvent.
- Examples of the silane coupling agent having cyclopentanone as a leaving group include Journal of Organometallic Chemistry (1984), 273 (1) (Non-Patent Document 1), Journal of Organometallic Chemistry (1985), 281 (2-3) ( Non-Patent Document 2) has an example of synthesizing tris (1-cyclopenten-1-yloxy) methylsilane having a methyl group as a substituent, but there is no example of using it as a cross-linking agent for a room-temperature curable organopolysiloxane composition.
- the present invention has been made in view of the above circumstances, and there have been no reports of health hazards such as carcinogenicity and reproductive toxicity to the human body and environmental hazards such as aquatic biotoxicity in the room temperature curable organopolysiloxane composition.
- a hydrolyzable organosilane compound having a cyclic ketone compound such as cyclobutanone or cyclopentanone as a desorbing group (desorbing compound) as a curing agent, which has a relatively high flammability
- various catalysts can be used.
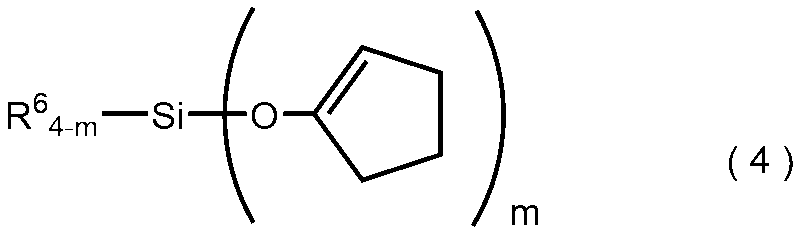
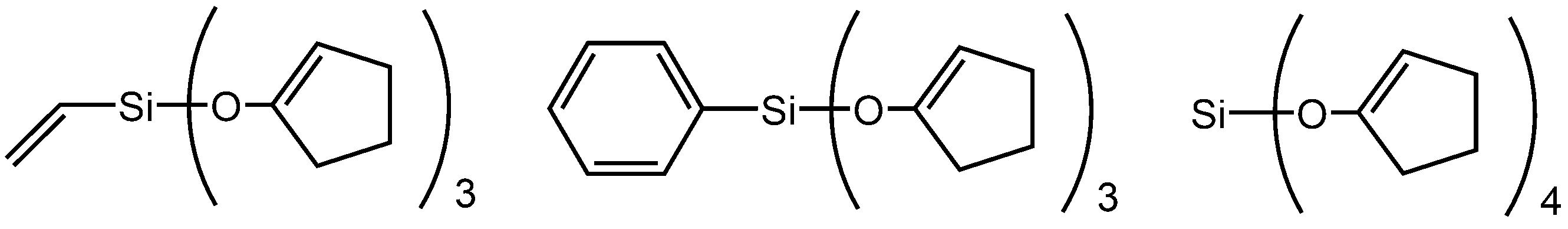
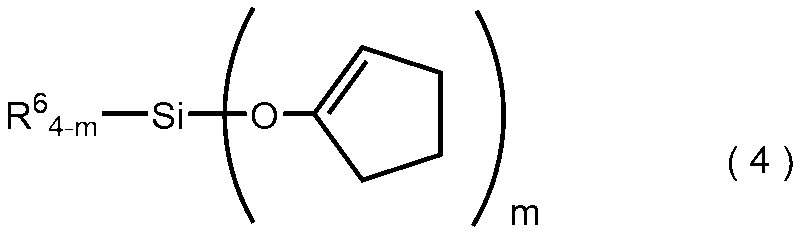
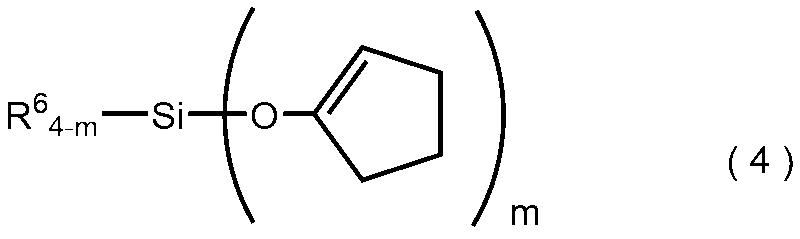
- the present inventor has a vinyl group as a substituent, which is represented by the following general formula (4), which is less toxic to the human body by hydrolysis, releases cyclopentanone, and is a substituent.
- a phenyl group or a tetrafunctional organic silicon compound hydrolyzable organosilane compound
- it has excellent safety and is a conventional curing type (dealcoholization).
- a room-temperature curable organopolysiloxane composition exhibiting rubber properties and fast-curing properties equal to or higher than that of a room-temperature curable organopolysiloxane composition (type or deoxym type) can be provided.
- R 6 is a vinyl group or a phenyl group, and m is 3 or 4.
- a hydrolyzable organic compound that desorbs and releases a cyclic ketone compound such as cyclobutanone or cyclopentanone as a desorbing group represented by the following general formula (2).
- a room-temperature curable organopolysiloxane composition containing a silane compound and / or a partially hydrolyzed condensate thereof as a curing agent solves the above-mentioned problems of harmfulness to the human body and the environment and safety. Further, it was found that even when an organic compound containing titanium, guanidine, etc. is added as a curing catalyst to this composition, the same curability and cured product performance as when a tin catalyst is added are exhibited, and the present invention is made. It came to. (In the formula, R 2 is a monovalent hydrocarbon group having 1 to 10 carbon atoms, n is an integer of 1 to 8, and m is 3 or 4).
- the present invention relates to the following room temperature curable organopolysiloxane composition, and various articles (automobile parts, automobile oil seals, electric / electronic parts, building structures, etc.) having the composition or the cured product thereof. It provides a structure for civil engineering work, an adhesive, a sealing material, a potting agent, a coating agent, etc.), a hydrolyzable organosilane compound, and a method for producing the same.
- (A) Organopolysiloxane having a viscosity of 20 to 1,000,000 mPa ⁇ s at 23 ° C.
- R 1 is an unsubstituted or substituted monovalent hydrocarbon group having 1 to 10 carbon atoms, and each R 1 may be the same group or a different group from each other. A is 50 or more.
- R 2 is a monovalent hydrocarbon group having 1 to 10 carbon atoms, n is an integer of 1 to 8, and m is 3 or 4).
- a room temperature curable organopolysiloxane composition containing.
- (C) The room temperature curable organopolysiloxane composition according to [5], wherein the curing catalyst is at least one selected from a tin catalyst, a titanium catalyst, an organic strong base catalyst and an organic bismuth catalyst.
- (D) contains 0.01 to 10 parts by mass of the silane coupling agent represented by the following general formula (3) and / or a partially hydrolyzed condensate thereof with respect to 100 parts by mass of the component (A).
- R 3 is a monovalent group having at least one functional group (excluding the guanidyl group) containing at least one hetero atom selected from a nitrogen atom, a sulfur atom and an oxygen atom, and having 1 to 20 carbon atoms. It is a hydrocarbon group.
- R 4 is an unsubstituted or substituted monovalent hydrocarbon group having 1 to 10 carbon atoms, X is a hydrolyzable group, and b is 0, 1 or 2).
- a hydrolyzable organosilane compound represented by the following general formula (4).
- the compound (desorption compound) generated from the curing agent (crosslinking agent) by the hydrolysis / condensation reaction at the time of curing is a cyclic compound such as cyclobutanone or cyclopentanone having high safety.
- a silicone rubber cured product evaporative organopolysiloxane cured product
- the room temperature curable organopolysiloxane composition of the present invention has the same curability and cured product performance as the case where a tin catalyst is added even when an organic compound containing titanium, bismuth, guanidine and the like is added as a curing catalyst. Therefore, it can be suitably used as various adhesives, sealing materials, potting agents, coating agents, etc. in consideration of environmental protection (load reduction). Further, the hydrolyzable organosilane compound of the present invention releases a safer compound as a desorbing group (desorbing compound), and is particularly used as a cross-linking agent for a room temperature curable organopolysiloxane composition. Since the composition has excellent curability and rapidly cures when exposed to air to exhibit excellent physical properties, the composition containing this hydrolyzable organosilane compound can be used for construction, automobiles, and electrical and electronic applications. It can be effectively used as an adhesive.
- the viscosity is a measured value by a rotational viscometer according to the method specified in JIS Z8803.
- room temperature means a state where the temperature is 23 ° C. ⁇ 15 ° C. and the humidity is 50% RH ⁇ 5% RH.
- the component (A) used in the room temperature curable organopolysiloxane composition of the present invention is an organopolysiloxane having a viscosity of 20 to 1,000,000 mPa ⁇ s at 23 ° C. represented by the following general formula (1).
- HO- (SiR 1 2 O) a -H (1) (In the formula, R 1 is an unsubstituted or substituted monovalent hydrocarbon group having 1 to 10 carbon atoms, and each R 1 may be the same group or a different group from each other. A is 50 or more. It is an integer.)
- the component (A) has a main chain consisting of repeating diorganosiloxane units as shown in the formula (1), and both ends of the molecular chain are sealed with a hydroxyl group (silanol group) bonded to a silicon atom at 23 ° C. It is a linear diorganopolysiloxane having a viscosity of 20 to 1,000,000 mPa ⁇ s, and acts as a main agent (base polymer) of the room temperature curable organopolysiloxane composition of the present invention.
- R 1 is an unsubstituted or substituted monovalent hydrocarbon group having 1 to 10 carbon atoms, particularly 1 to 6 carbon atoms, and is, for example, a methyl group, an ethyl group, a propyl group or an isopropyl group.
- Alkenyl group such as allyl group, propenyl group, isopropenyl group, butenyl group and hexenyl group, aryl group such as phenyl group and trill group, and aralkyl group such as benzyl group and phenylethyl group.
- a group in which the hydrogen atom of these hydrocarbon groups is partially substituted with a halogen atom such as chlorine, fluorine or bromine, for example, a trifluoropropyl group or the like can be mentioned.
- R 1 As the unsubstituted or substituted monovalent hydrocarbon group of R 1 , those containing no aliphatic unsaturated bond are preferable, and specifically, an alkyl group such as a methyl group and an aryl group such as a phenyl group are more preferable. Methyl groups are particularly preferred.
- This R 1 may be the same group or a different group.
- a indicating the number of repetitions (or degree of polymerization) of the bifunctional diorganosiloxane unit (SiR 1 2 O 2/2 ) constituting the main chain is an integer of 50 or more, preferably an integer of 50 or more. It is an integer of 50 to 2,000, more preferably an integer of 100 to 1,500, and particularly preferably an integer of 200 to 1,200.
- the degree of polymerization is, for example, a polystyrene-equivalent number average degree of polymerization (or number average molecular weight) in gel permeation chromatography (GPC) analysis using toluene, tetrahydrofuran (THF) or the like as a developing solvent.
- GPC gel permeation chromatography
- THF tetrahydrofuran
- the organopolysiloxane of the component (A) has a viscosity at 23 ° C. of 20 to 1,000,000 mPa ⁇ s, preferably 100 to 300,000 mPa ⁇ s, and more preferably 1,000 to 200,000 mPa ⁇ s. It is s, and particularly preferably 10,000 to 100,000 mPa ⁇ s. If the viscosity of the organopolysiloxane is less than the above lower limit value (20 mPa ⁇ s), a large amount of the component (C) described later is required, which is economically disadvantageous. Further, if the viscosity of the organopolysiloxane exceeds the above upper limit value (1,000,000 mPa ⁇ s), the workability is lowered, which is not preferable.
- the organopolysiloxane of the component (A) may be used alone or in combination of two or more.
- the component (B) used in the room temperature curable organopolysiloxane composition of the present invention is a hydrolyzable organosilane compound represented by the following general formula (2) and / or a partially hydrolyzed condensate thereof, and is a cross-linking agent (curing). It is used as an agent), and is characterized by releasing a cyclic ketone compound such as cyclobutanone or cyclopentanone as a desorbing group (desorbing substance) by hydrolysis.
- the "partially hydrolyzable condensate” is preferably three or more residual hydrolyzable groups in the molecule, which is produced by partially hydrolyzing and condensing the hydrolyzable organosilane compound. It means an organosiloxane oligomer having 4 or more.
- R 2 is a monovalent hydrocarbon group having 1 to 10 carbon atoms, n is an integer of 1 to 8, and m is 3 or 4).
- R 2 is a monovalent hydrocarbon group having 1 to 10 carbon atoms, preferably 1 to 6 carbon atoms, and more preferably an alkyl group having 1 to 6 carbon atoms and 2 to 6 carbon atoms. It is an alkenyl group of 6, an aryl group having 6 to 10 carbon atoms or an aralkyl group having 7 to 10 carbon atoms, and the R 2 thereof includes a methyl group, an ethyl group, a propyl group, an isopropyl group, a butyl group, an isobutyl group and sec.
- -Alkyl group such as butyl group, tert-butyl group, pentyl group, hexyl group, octyl group, 2-ethylhexyl group, nonyl group, decyl group, vinyl group, allyl group, propenyl group, isopropenyl group, butenyl group, hexenyl
- alkenyl group such as a group, an aryl group such as a phenyl group and a trill group, and an aralkyl group such as a benzyl group and a phenylethyl group.
- a methyl group, an ethyl group, a vinyl group and a phenyl group are preferable, and a methyl group, a vinyl group and a phenyl group are particularly preferable.
- n is an integer of 1 to 8, preferably an integer of 2 to 6, more preferably an integer of 2 to 4, and even more preferably 2 or 3.
- n is 0, the structure does not have an annular structure.
- n is an integer of 9 or more, the molecular weight of the hydrolyzable organosilane becomes large, which makes purification by distillation difficult and increases the amount of addition required to ensure storage stability, which is disadvantageous in terms of cost. ..
- m is 3 or 4.
- this number is less than 3 (that is, when m is 0, 1 or 2), rubber curing due to the crosslinking reaction does not occur, and it is not suitable as a crosslinking agent for a room temperature curable organopolysiloxane composition.
- the desorbing group (desorbing compound) generated by the hydrolysis of the hydrolyzable organosilane compound represented by the above general formula (2) is cyclopropanone, cyclobutanone, cyclopentanone, cyclohexanone, cycloheptanone, cycloocta. It is a cyclic ketone compound such as non, cyclononanone, and cyclodecanone, preferably cyclobutanone and cyclopentanone, and more preferably cyclopentanone.
- cyclobutanone and cyclopentanone having health hazards such as carcinogenicity and reproductive toxicity to the human body, and environmental hazards such as aquatic biotoxicity.
- cyclopentanone is industrially mass-produced, easily available, and highly cost-competitive. Therefore, as will be described later, cyclopentanone is also advantageous for producing the hydrolyzable organosilane compound of the component (B).
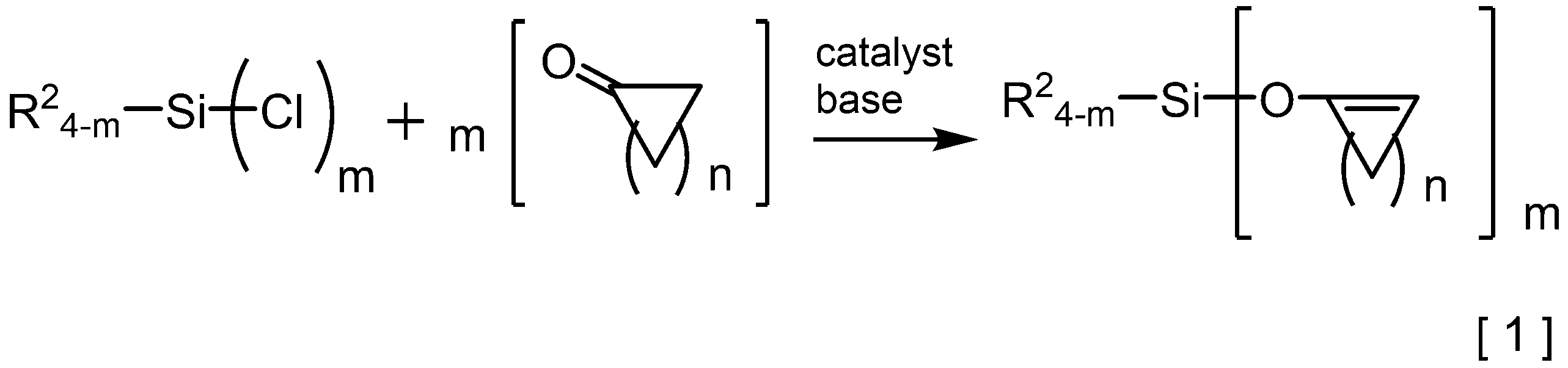
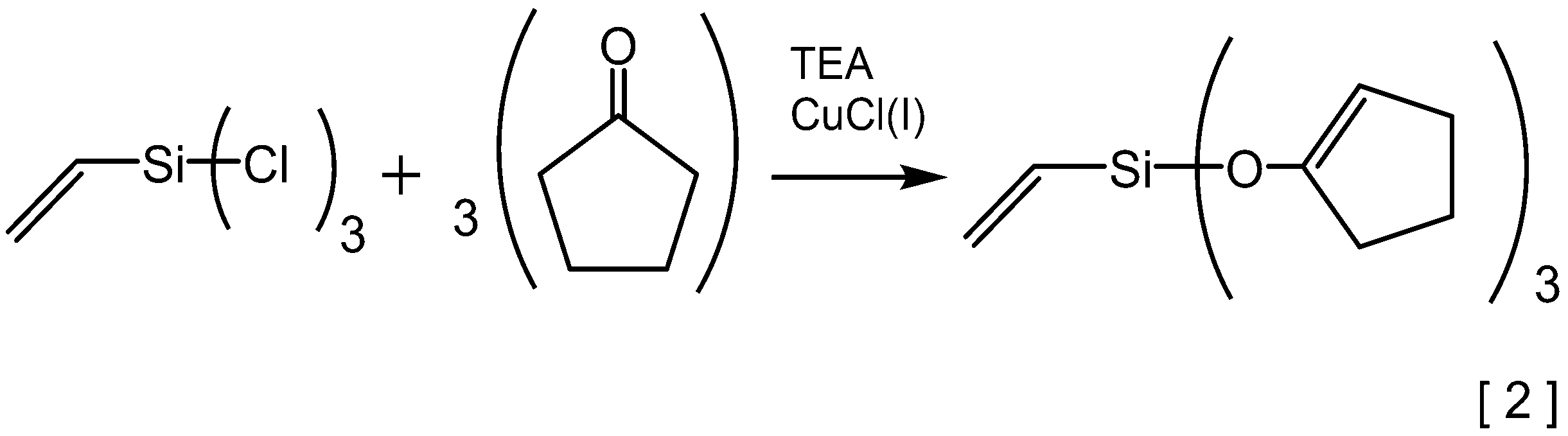
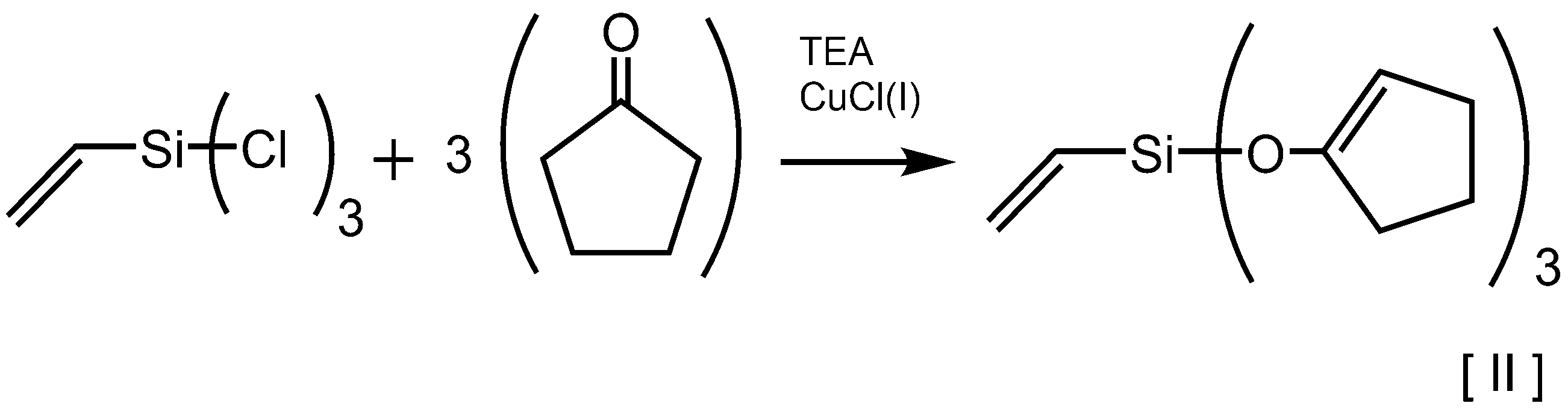
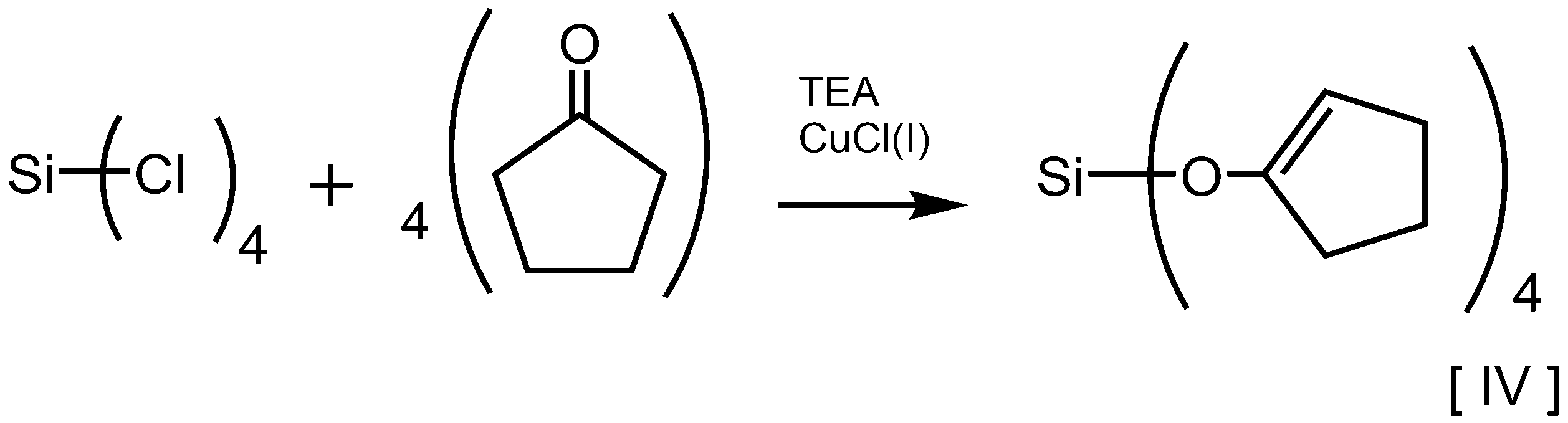
- the hydrolyzable organosilane compound of the component (B) is, for example, a chlorosilane compound corresponding to the hydrolyzable organosilane compound represented by the general formula (2), which is a product, and a cyclic ketone compound as a catalyst and the presence of a basic substance. It can be produced by reacting below (for example, dehydrolysis reaction). This reaction formula is represented by, for example, the following formula [1].
- examples of the chlorosilane compound include those shown below.
- examples of the cyclic ketone compound include those shown below.
- the amount of the cyclic ketone compound to be reacted with the chlorosilane compound is preferably 0.95 to 3.0 mol, more preferably 0.99 to 2.5 mol, with respect to 1 mol of chlorine atoms in the chlorosilane compound. .0 to 2.0 mol is more preferred. If the amount of the cyclic ketone compound added is small, the reaction may not be completed, and if the amount of the cyclic ketone compound added is too large, purification may take time and the production time may increase.
- Examples of the catalyst used in the reaction include monovalent or divalent metallic copper compounds, for example, copper chloride, copper bromide, copper iodide, copper sulfate, copper nitrate, copper carbonate, basic copper carbonate, copper formate. , Copper acetate, copper butyrate, etc., but are not limited thereto.
- the amount of the catalyst (metal copper compound) added is preferably 0.001 to 0.5 mol, more preferably 0.002 to 0.2 mol, and 0.003 to 0.1 mol with respect to 1 mol of the chlorosilane compound. Is more preferable. If the amount of the catalyst added is small, the reaction may not be completed, and if the amount of the catalyst added is too large, it is disadvantageous in terms of cost.
- a basic substance having low nucleophilicity such as trimethylamine, triethylamine, tripropylamine, tributylamine, urea, diazabicycloundecene and diazabicyclononene can be used.
- trimethylamine, triethylamine and tributylamine are preferable, and triethylamine is particularly preferable.
- the amount of the basic substance added is preferably 0.95 to 2.5 mol, more preferably 0.99 to 2.0 mol, and 1.0 to 1. 5 mol is more preferred. If the amount of the basic substance added is small, the reaction may not be completed, and if the amount of the basic substance added is too large, it is economically disadvantageous.
- a commonly used solvent may be used for the production of the hydrolyzable organosilane compound of the component (B), and the solvent may be, for example, aromatic hydrocarbons such as toluene, xylene and benzene, pentane and hexane. , Heptane, nonane, octane, decane and other aliphatic hydrocarbons, dimethyl ether, methyl ethyl ether, tetrahydrofuran, dioxane and other ethers, perchloroethane, perchloroethylene, trichloroethane, chloroform, carbon tetrachloride and other halogenated hydrocarbons.
- aromatic hydrocarbons such as toluene, xylene and benzene
- pentane and hexane pentane and hexane.
- Heptane nonane
- octane decane and other aliphatic hydro
- Amids such as dimethylformamide, and organic solvents such as esters such as ethyl acetate, methyl acetate and butyl acetate.
- the amount of the solvent used is not particularly limited, but is usually in the range of 10 to 500 parts by mass, preferably 30 to 400 parts by mass, more preferably 50 to 300 parts by mass, etc. with respect to 100 parts by mass of the cyclic ketone compound used. Used in.
- the chlorosilane compound is usually added dropwise to the cyclic ketone compound at a temperature of 0 to 120 ° C., preferably 0 to 100 ° C., and 50 to 120 ° C., preferably 60 to 100 ° C. It is preferable to react at ° C. for 1 to 48 hours, more preferably 3 to 30 hours. If the temperature during the reaction is too low, the reaction may not be completed, and if the temperature during the reaction is too high, the coloration of the product may increase. Further, if the reaction time is too short, the reaction may not be completed, and if the reaction time is too long, the productivity is disadvantageous.
- purification after completion of the reaction is possible by distilling the target product in a reduced pressure environment, and the degree of reduced pressure is preferably 1 ⁇ 10 -5 to 3,000 Pa, more preferably 1 ⁇ 10 -5 to 2,000 Pa.
- the temperature at the time of purification is preferably 100 to 250 ° C, more preferably 120 to 230 ° C. Distillation may be difficult if the pressure at the time of depressurization (degree of decompression) is too high. Further, if the temperature at the time of purification is too low, purification by distillation may be difficult, and if it is too high, the reaction product may be colored or decomposed.
- hydrolyzable organosilane compound of the component (B) examples include those represented by the following formula.
- Me represents a methyl group.
- a novel organic silicon compound (hydrolyzable organosilane) that desorbs cyclopentanone as a desorbing group (eliminating compound) generated by hydrolysis, which is particularly represented by the following general formula (4).
- Compound is preferable from the viewpoint of quick curing and the like.
- m is the same as above, and R 6 is a vinyl group or a phenyl group.
- R 6 is a vinyl group or a phenyl group, and a vinyl group is particularly preferable.
- m is 3 or 4 as described above. When this number is less than 3 (that is, when m is 0, 1 or 2), rubber curing due to the crosslinking reaction does not occur, and it is not suitable as a crosslinking agent for a condensation-curing room temperature curable organopolysiloxane composition. ..
- the hydrolyzable organosilane compound of the present invention can be produced, for example, by reacting a chlorosilane compound and cyclopentanone with a catalyst in the presence of a basic substance (for example, a dehydrolysis reaction).
- This reaction formula is represented by, for example, the following formula [I].
- examples of the chlorosilane compound include those shown below.
- the amount of cyclopentanone added to react with the chlorosilane compound is preferably 0.95 to 3.0 mol, more preferably 0.99 to 2.5 mol, with respect to 1 mol of chlorine atoms in the chlorosilane compound. .0 to 2.0 mol is more preferred. If the amount of cyclopentanone added is too small, the reaction may not be completed, and if the amount of cyclopentanone added is too large, purification takes time and the production time increases.
- a basic substance having low nucleophilicity such as trimethylamine, triethylamine, tripropylamine, tributylamine, urea, diazabicycloundecene and diazabicyclononene can be used.
- trimethylamine, triethylamine and tributylamine are preferable, and triethylamine is particularly preferable.
- the amount of the basic substance added is preferably 0.95 to 2.5 mol, more preferably 0.99 to 2.0 mol, and 1.0 to 1. 5 mol is more preferred. If the amount of the basic substance added is small, the reaction may not be completed, and if the amount of the basic substance added is too large, it is economically disadvantageous.
- Examples of the catalyst used in the reaction include monovalent or divalent metallic copper compounds and metallic silver compounds.
- the amount of the catalyst (metal copper compound, metal silver compound) added is preferably 0.001 to 0.5 mol, more preferably 0.002 to 0.2 mol, and 0.003 to 0.003 to 1 mol of the chlorosilane compound. 0.1 mol is more preferred. If the amount of the catalyst added is small, the reaction may not be completed, and if the amount of the catalyst added is too large, it is disadvantageous in terms of cost.
- a commonly used solvent may be used in the production of the hydrolyzable organosilane compound of the present invention, for example, aromatic hydrocarbons such as toluene, xylene and benzene, pentane, hexane, heptane, nonane and octane.
- Aroma group hydrocarbons such as decane, ethers such as dimethyl ether, methyl ethyl ether, tetrahydrofuran, dioxane, halogenated hydrocarbons such as perchloroethane, perchloroethylene, trichloroethane, chloroform, carbon tetrachloride, amides such as dimethylformamide.
- Examples include organic solvents such as esters such as ethyl acetate, methyl acetate and butyl acetate.
- the amount of the solvent used is not particularly limited, but is usually in the range of 10 to 500 parts by mass, preferably 30 to 400 parts by mass, more preferably 50 to 300 parts by mass, etc. with respect to 100 parts by mass of cyclopentanone to be used. Used in.
- the chlorosilane compound is usually added dropwise to cyclopentanone at a temperature of 0 to 130 ° C., preferably 20 to 120 ° C., and 50 to 140 ° C., preferably 60 to 130 ° C. It is preferable to react at ° C. for 0.5 to 48 hours, preferably about 1 to 30 hours. If the temperature during the reaction is too low, the reaction may not be completed, and if the temperature during the reaction is too high, the coloration of the product may increase. Further, if the reaction time is too short, the reaction may not be completed, and if the reaction time is too long, the productivity is disadvantageous.
- purification after completion of the reaction is possible by distilling the target product in a reduced pressure environment, and the degree of reduced pressure is preferably 1 ⁇ 10 -5 to 3,000 Pa, more preferably 1 ⁇ 10 -5 to 2,000 Pa.
- the temperature at the time of purification is preferably 100 to 250 ° C, more preferably 120 to 230 ° C. Distillation may be difficult if the pressure at the time of depressurization (degree of decompression) is too high. Further, if the temperature at the time of purification is too low, purification by distillation may be difficult, and if it is too high, the reaction product may be colored or decomposed.
- hydrolyzable organosilane compound of the present invention include those represented by the following formulas.
- an organic silicon compound (hydrolyzable organosilane compound) that desorbs cyclopentanone is used as a cross-linking agent (curing agent) for a room temperature curable organopolysiloxane composition. ), It can give a cured product having particularly fast curing properties and excellent rubber physical properties.
- Cyclopentanone is a compound that is less harmful to the human body and the environment and has excellent biodegradability as compared with methanol and 2-butanone oxime.
- the novel hydrolyzable organosilane compound of the present invention has cyclopentanone as a leaving group (leaving compound) generated by hydrolysis, and is particularly preferably used as a cross-linking agent for a room temperature curable organopolysiloxane composition.
- such a hydrolyzable organosilane compound can impart higher safety and quick curability.
- a more safe hydrolyzable organosilane compound that releases cyclopentanone as a cross-linking agent (curing agent) as a desorbing group (desorbing compound) generated by hydrolysis the rubber property is excellent.
- a cured product is given to obtain a condensation-curable room-temperature curable organosiloxane composition having fast-curing properties.
- the component (B) may be used alone or in combination of two or more.
- the blending amount of the component (B) is 1 to 40 parts by mass, preferably 3 to 30 parts by mass, and more preferably 5 to 20 parts by mass with respect to 100 parts by mass of the component (A). If the blending amount of the component (B) is less than 1 part by mass of the above lower limit value, the storage stability when stored in a sealed container may deteriorate. Further, if the blending amount of the component (B) exceeds 40 parts by mass of the above upper limit value, the curability of the room temperature curable organopolysiloxane composition may be significantly lowered, and the adhesiveness may be further deteriorated.
- the hydrolyzable organosilane compound of the component (B) and / or its partially hydrolyzed condensate contains a functional group containing one or more atoms selected from a nitrogen atom, a sulfur atom and an oxygen atom in the molecule. It is clearly distinguished from the silane coupling agent of the component (D) and / or its partially hydrolyzed condensate as an optional component described later in that it does not have a monovalent hydrocarbon group having at least one. Is.
- the room temperature curable organopolysiloxane composition of the present invention may contain, if necessary, a curing catalyst of the component (C) as an optional component.
- a curing catalyst of the component (C) a metal-based or non-metal-based condensation catalyst generally used as a curing accelerator for a room temperature curable organopolysiloxane composition can be used.
- organic tin compounds such as dibutyl tin methoxide, dibutyl tin diacetate, dibutyl tin dioctate, dibutyl tin dilaurate, dioctyl tin dilaurate, dioctyl tin dioctate, dimethyl tin dimethoxide, dimethyl tin diacetate, tetrapropyl titanate, tetra.
- tin catalysts such as dibutyl tin methoxide, dibutyl tin diacetate, dibutyl tin dioctate, dibutyl tin dilaurate, dioctyl tin dilaurate, dioctyl tin dioctate, dimethyl tin dimethoxide, dimethyl tin diacetate, tetrapropyl titanate, tetra.
- Organic titanium compounds such as butyl titanate, tetra-2-ethylhexyl titanate, dimethoxytitanium diacetylacetonate, titanium diisopropoxybis (ethylacetoacetate), triethylamine, hexylamine, tetramethylguanidine, ⁇ -tetramethylg.
- Amin compounds such as anidylpropyltrimethoxysilane, organic bismuth compounds such as salts thereof (organic strong base catalyst), bismastris (2-ethylhexanoate), bismastris (neodecanoate), and mixtures thereof (organic bismuth catalysts).
- any of the above catalysts, the titanium catalyst, the organic strong base catalyst, and the organic bismuth catalyst exhibits the same curability and cured product performance as the case where the tin catalyst is blended. From the viewpoint of environmental protection, it is preferable to add a titanium catalyst, an organic strong base catalyst or an organic bismuth catalyst without adding a tin catalyst.
- the blending amount thereof is preferably 0.01 to 10 parts by mass, more preferably 0.05 to 8 parts by mass with respect to 100 parts by mass of the component (A). More preferably, it is 0.1 to 5 parts by mass. If the blending amount of the component (E) is less than 0.01 part by mass of the lower limit value, the catalytic effect may not be obtained, and if it exceeds 10 parts by mass of the upper limit value, the storage stability of the composition is inferior. In some cases.
- the room temperature curable organopolysiloxane composition of the present invention may contain, if necessary, the silane coupling agent of the component (D) and / or a partially hydrolyzed condensate thereof as an optional component.
- the component (D) is a silane coupling agent represented by the following general formula (3) (that is, a hydrolyzable organosilane compound or a carbon functional silane having a functional group-containing monovalent hydrocarbon group) and / or a portion thereof.
- R 3 is a monovalent group having at least one functional group (excluding the guanidyl group) containing at least one hetero atom selected from a nitrogen atom, a sulfur atom and an oxygen atom, and having 1 to 20 carbon atoms. It is a hydrocarbon group.
- R 4 is an unsubstituted or substituted monovalent hydrocarbon group having 1 to 10 carbon atoms, X is a hydrolyzable group, and b is 0, 1 or 2).
- R 3 is a functional group containing one or more heteroatoms selected from a nitrogen atom, a sulfur atom and an oxygen atom (for example, an unsubstituted or substituted amino group, an unsubstituted or substituted imino group, It is a monovalent hydrocarbon group having at least one amide group, ureido group, mercapto group, epoxy group, (meth) acryloxy group, but excluding guanidyl group) and having 1 to 20 carbon atoms.
- ⁇ - (2,3-epoxycyclohexyl) ethyl group ⁇ - (3,4-epoxycyclohexyl) ethyl group, ⁇ -glycidoxypropyl group, ⁇ -methacryloxypropyl group, ⁇ -acryloxypropyl group, N - ⁇ - (Aminoethyl) - ⁇ -aminopropyl group [also known as N-2- (aminoethyl) -3-aminopropyl group], ⁇ -aminopropyl group, N-phenyl- ⁇ -aminopropyl group, ⁇ - It contains at least one heteroatom selected from a nitrogen atom such as a ureidopropyl group, a ⁇ -mercaptopropyl group, and a ⁇ -isocyanappropyl group, a sulfur atom, and an oxygen atom, preferably having 3 to 20 carbon atoms, and more preferably having 3 to 20 carbon atoms
- Examples thereof include monovalent hydrocarbon groups of 3 to 14.
- R 5 a ⁇ -glycidoxypropyl group, a ⁇ -aminopropyl group, and an N- ⁇ - (aminoethyl) - ⁇ -aminopropyl group are particularly preferable.
- R 4 is an unsubstituted or substituted monovalent hydrocarbon group having 1 to 10 carbon atoms, preferably 1 to 6 carbon atoms, and is, for example, a methyl group, an ethyl group or a propyl group.
- Examples thereof include an alkenyl group such as a group, a vinyl group, an allyl group, a propenyl group, an isopropenyl group, a butenyl group and a hexenyl group, an aryl group such as a phenyl group and a trill group, and an aralkyl group such as a benzyl group and a phenylethyl group.
- a group in which the hydrogen atom of these hydrocarbon groups is partially substituted with a halogen atom such as chlorine, fluorine or bromine, for example, a trifluoropropyl group or the like can be mentioned.
- a methyl group, an ethyl group, a propyl group and an isopropyl group are preferable.
- R 4 may be the same group or a different group.
- examples of the hydrolyzable group X include a ketooxime group, an alkoxy group, an alkoxyalkoxy group, an acyloxy group, an alkenyloxy group and the like.
- examples thereof include an acyloxy group having 2 to 4 carbon atoms such as a group and a propionoxy group, an alkenyloxy group having 2 to 4 carbon atoms such as a vinyloxy group, an allyloxy group, a propenoxy group and an isopropenoxy group.
- X it is preferably a methoxy group.
- the hydrolyzable group X may be the same group or a different group.
- silane coupling agent represented by the formula (3) of the component (D) include ⁇ -aminopropyltrimethoxysilane, ⁇ -aminopropyltriethoxysilane, and 3-2- (aminoethylamino) propyltri.
- Aminosilanes such as methoxysilane [also known as N-2- (aminoethyl) -3-aminopropyltrimethoxysilane], ⁇ -glycidoxypropyltrimethoxysilane, ⁇ - (3,4-epoxycyclohexyl) ethyltrimethoxy
- Epoxysilanes such as silanes, (meth) acrylic silanes such as ⁇ - (meth) acryloxipropyltrimethoxysilane, ⁇ - (meth) acryloxipropyltriethoxysilane, and mercaptosilanes such as ⁇ -mercaptopropyltrimethoxysilane.
- isocyanate silanes such as ⁇ -isocyanide propyltrimethoxysilane.
- silane coupling agent of the component (D) and / or its partially hydrolyzed condensate may be used alone or in combination of two or more.
- the blending amount thereof is preferably 0.01 to 10 parts by mass, more preferably 0.1 to 8 parts by mass with respect to 100 parts by mass of the component (A). If it is less than 0.01 parts by mass, the cured product may not exhibit sufficient adhesive performance, and if it is blended in excess of 10 parts by mass, the rubber strength after curing may decrease or the curability may decrease. May be done.
- the room temperature curable organopolysiloxane composition of the present invention may contain, if necessary, the inorganic filler of the component (E) as an optional component.
- the inorganic filler of the component (E) is a reinforcing and non-reinforcing filler for imparting rubber physical characteristics to the room temperature curable organopolysiloxane composition of the present invention.
- Examples of the inorganic filler of the component (E) include calcined silica, molten silica, crushed silica, dry silica such as fuming silica (fumed silica), precipitated silica, and sol-gel method, which are surface hydrophobized or untreated.
- silica such as silica, silica-based filler such as crystalline silica (fine powder quartz), diatomaceous soil, carbon black, talc, bentonite, surface-treated or untreated calcium carbonate, zinc carbonate, magnesium carbonate, surface-treated or untreated.
- Calcium oxide, zinc oxide, magnesium oxide, aluminum oxide, aluminum hydroxide and the like are exemplified, and among them, calcium carbonate, fumes silica, precipitated silica, carbon black and aluminum oxide are preferable, and the surface is more preferably treated with hydrophobic treatment. Calcium carbonate, fuming silica, precipitation silica, carbon black, aluminum oxide. In this case, it is preferable that these inorganic fillers have a small amount of water.
- the type, amount, treatment method, etc. of the surface treatment agent are not particularly limited, but typically, organosilicon compounds such as chlorosilane, alkoxysilane, and organosilazane, fatty acids, and paraffin are used. , Silane coupling agents, titanium coupling agents and other treatment agents can be applied.
- the inorganic filler of the component (E) may be used alone or in combination of two or more.
- the blending amount thereof is preferably 1 to 500 parts by mass, more preferably 20 to 500 parts by mass, and further preferably 20 parts by mass with respect to 100 parts by mass of the component (A). It is about 300 parts by mass, and particularly preferably 50 to 300 parts by mass. If it is less than 1 part by mass, sufficient rubber strength cannot be obtained, which may cause a problem that it is not suitable for the intended use. If it exceeds 500 parts by mass, the dischargeability from the cartridge deteriorates and the storage stability deteriorates. In addition, the mechanical properties of the obtained rubber properties may also deteriorate.
- a generally known additive other than the above-mentioned components may be used as long as the object of the present invention is not impaired.
- the additive include polyether as a thixophilic improver, silicone oil (non-functional organopolysiloxane) as a plasticizer, isoparaffin and the like, and coloring of pigments, dyes, fluorescent whitening agents and the like as necessary.
- Physiologically active additives such as agents, antifungal agents, antibacterial agents, marine biological repellents, phenylsilicone oil as bleed oil, fluorosilicone oil, surface modifiers such as organic liquids incompatible with silicone, solvent volatile oil , Low boiling point isoparaffin and other solvents can also be added.
- the room temperature curable organopolysiloxane composition of the present invention can be obtained by uniformly mixing the above-mentioned components and predetermined amounts of the above-mentioned various additives in a dry atmosphere. Further, the room temperature curable organopolysiloxane composition of the present invention is cured by being left at room temperature, and the molding method, curing conditions, etc. thereof shall adopt known methods and conditions according to the type of composition. Can be done.
- the room temperature curable organopolysiloxane composition of the present invention is stored at room temperature in the absence of moisture, that is, in a closed container protected from moisture, and exposed to moisture in the air during use. It cures easily at (23 ° C ⁇ 15 ° C).
- the compound generated from the cross-linking agent by the hydrolysis reaction at the time of curing is a highly safe cyclic ketone compound such as cyclopentanone, which is considered for the human body and the environment. It is a thing. Further, cyclopentanone has a flash point of 35 ° C., which is higher than that of the de-alcohol type which releases an alcohol compound such as methanol when the composition is cured, and is highly safe.
- a room temperature curable organopolysiloxane composition of the present invention exhibits good curability by using various existing catalysts, and the cured product (silicone rubber) is also excellent in adhesiveness. Further, by using a catalyst other than tin, it is possible to provide a composition in consideration of the environmental load.
- the room temperature curable organopolysiloxane composition of the present invention is useful as an adhesive, a sealing material, a potting agent, a coating agent, or the like.
- the method of using the room temperature curable organopolysiloxane composition of the present invention as an adhesive, a sealing material, a potting agent, or a coating agent may follow a conventionally known method.
- Examples of the target articles include automobile parts, automobile oil seals, electric / electronic parts, building structures, civil engineering structures, and the like.
- the viscosity is a value measured by a rotational viscometer at 23 ° C. according to the method specified in JIS Z8803.
- Me represents a methyl group.
- composition 1 After mixing with (B-1), 8 parts by mass of the hydrolyzable organosilane compound 1 was added, and the mixture was sufficiently mixed. Finally, add 1 part by mass of (D-1) ⁇ -aminopropyltrimethoxysilane (product name; KBM-903, manufactured by Shin-Etsu Chemical Co., Ltd.) and 0.1 part by mass of (C-1) dioctyltin dilaurate. , Completely mixed under reduced pressure to give composition 1.
- (D-1) ⁇ -aminopropyltrimethoxysilane product name; KBM-903, manufactured by Shin-Etsu Chemical Co., Ltd.
- composition 4 After mixing with (B-1), 8 parts by mass of the hydrolyzable organosilane compound 1 was added, and the mixture was sufficiently mixed. Finally, 1 part by mass of (D-1) ⁇ -aminopropyltrimethoxysilane (product name; KBM-903, manufactured by Shin-Etsu Chemical Co., Ltd.), (C-4) bismuth tris (2-ethylhexanoate). 1 part by mass of an organic bismuth catalyst (product name; Neostan U-600, manufactured by Nitto Kasei Co., Ltd.) containing the above as a main component was added and completely mixed under reduced pressure to obtain composition 4.
- an organic bismuth catalyst product name; Neostan U-600, manufactured by Nitto Kasei Co., Ltd.
- E-1 Methyl group
- a dimethylpolysiloxane corresponding to about 620
- composition 7 1 part by mass of (D-1) ⁇ -aminopropyltrimethoxysilane (product name; KBM-903, manufactured by Shin-Etsu Chemical Co., Ltd.) and 0.1 part by mass of (C-1) dioctyltin dilaurate. , Completely mixed under reduced pressure to give composition 7.
- (D-1) ⁇ -aminopropyltrimethoxysilane product name; KBM-903, manufactured by Shin-Etsu Chemical Co., Ltd.
- the curing rate test method is to fill a glass petri dish with an inner diameter of 10 mm with each composition prepared in the above Examples and Comparative Examples, and after 1 day (24 hours) at 23 ° C. and 50% RH, use a probe. The thickness (depth) cured from the part exposed to the air by inserting was measured.
- Rubber Physical Characteristics Each composition prepared in the above Examples and Comparative Examples was poured into a 2 mm mold and cured at 23 ° C. and 50% RH for 7 days to obtain a rubber sheet having a thickness of 2 mm. Rubber physical characteristics (type A durometer hardness, tensile strength, elongation at cutting) were measured according to JIS K 6249.
- Adhesiveness Each of the compositions prepared in the above Examples and Comparative Examples was cured by curing at 23 ° C. and 50% RH for 7 days between two aluminum plates having a width of 25 mm and a length of 100 mm, and the upper and lower aluminum plates were cured. A silicone rubber cured product layer having an adhesive area of 2.5 cm 2 and an adhesive thickness of 1 mm was formed to prepare a shear adhesive test piece. Using each of these test pieces, the shear adhesive force to aluminum and the cohesive fracture rate were measured according to the method specified in JIS K 6249.
- Heat resistance evaluation In order to confirm the heat resistance performance, the obtained cured silicone rubber sheet and shear adhesive test piece were exposed to a dry environment at 150 ° C. and deteriorated for 1,000 hours, and then the same test as in the initial production (initial evaluation) was performed. A heat resistance confirmation test was conducted by performing (rubber physical properties, adhesiveness).
- the room temperature curable organopolysiloxane composition of the present invention has good curability (tack-free) in the initial evaluation regardless of whether a tin catalyst, a titanium catalyst, an organic strong base catalyst, or an organic bismuth catalyst is used. It has thyme, curing rate), rubber physical properties and adhesiveness, and has been shown to have good properties in a moisture resistance test and a heat resistance test.
- the properties of the room temperature curable organopolysiloxane composition of the present invention are not inferior to those of the widely used deoxime type, dealcohol type and deacetone type compositions.
- the room temperature curable organopolysiloxane composition of the present invention exhibits good properties even when an organic bismuth catalyst is used, but dealcoholization using the organic bismuth catalyst of Comparative Example 3 is performed.
- the composition of the mold did not cure. From these results, it can be seen that the hydrolyzable organosilane compound used in the room temperature curable organopolysiloxane composition of the present invention is superior in end-sealing ability and curability to the dealcohol type curing agent.
- the compound released during curing by the composition of the example is cyclopentanone, which is safe because there are no reports of health hazards such as carcinogenicity and reproductive toxicity to the human body and environmental hazards such as aquatic biotoxicity.
- the room temperature curable organopolysiloxane composition of the present invention desorbs a compound having higher safety at the time of curing and has good curability even when various catalysts are used, and the cured product has good curability. It was confirmed that it has good physical properties, adhesiveness, and durability (moisture and heat resistance, heat resistance), and it was found that it can be suitably used in various applications (adhesives, sealing materials, potting agents, coating agents, etc.). rice field.
- compositions prepared in the above composition examples and composition comparative examples were poured into a 2 mm mold and cured at 23 ° C. and 50% RH for 7 days to obtain a rubber sheet having a thickness of 2 mm.
- the tack free time (drying time to the touch) was measured according to the method specified in JIS A 5758, and the rubber physical characteristics (hardness, elongation at cutting, tensile strength) were measured from a 2 mm thick sheet according to JIS K 6249.
- the hydrolyzable organosilane compound of the present invention showed high curability even when a basic catalyst was used, and the tack free time was very short as compared with the conventional cross-linking agent. In addition, the physical properties after curing were also obtained without any problem. On the other hand, in Composition Comparative Examples 1 and 2, the use of a highly toxic tin catalyst was indispensable, the tack free time was long, and the curability was inferior.
Abstract
Description
一方で、脱オキシム型の硬化剤が硬化時に発生する2-ブタノンオキシムなどのオキシム化合物は発がん性のおそれが疑われており好ましくなく、脱アルコール型の硬化剤が硬化時に発生するメタノール等は人体に対して有毒で、劇物に指定されていることから、人体の健康の観点から好ましくない。更に、これらの組成物では、硬化触媒として、環境負荷物質として規制が強化されている錫触媒を使用するケースもあり、近年の作業員の安全性確保や環境保護の観点から好ましくなく、より安全性の高い脱離基(脱離化合物)を有する加水分解性オルガノシラン化合物(硬化剤)に代替することが求められている。
環境保護や健康被害抑制といった観点から、性能向上とともにより環境・安全に配慮された製品が特に望まれており、脱離する化合物の安全性が高く、性能に優れる室温硬化性オルガノポリシロキサン組成物に対する需要が高まっている。
更に室温硬化性オルガノポリシロキサン組成物において、下記一般式(2)で示される、脱離基(脱離化合物)としてシクロブタノンやシクロペンタノン等の環状ケトン化合物を脱離・放出する加水分解性オルガノシラン化合物及び/又はその部分加水分解縮合物を硬化剤(架橋剤)として含有する室温硬化性オルガノポリシロキサン組成物が、上記人体・環境に対する有害性や安全性の問題を解決するものであることを見出し、更にはこの組成物にチタン、グアニジン等を含む有機化合物を硬化触媒として添加した場合でも錫触媒を添加した場合と同等の硬化性及び硬化物性能を示すことを見出し、本発明をなすに至った。
[1]
(A)下記一般式(1)で示される23℃における粘度が20~1,000,000mPa・sのオルガノポリシロキサン:100質量部
HO-(SiR1 2O)a-H (1)
(式中、R1は炭素数1~10の非置換又は置換の一価炭化水素基であり、各R1は互いに同一であっても異種の基であってもよい。aは50以上の整数である。)、及び
(B)下記一般式(2)で示される加水分解性オルガノシラン化合物及び/又はその部分加水分解縮合物:1~40質量部
を含有する室温硬化性オルガノポリシロキサン組成物。
[2]
(B)成分の加水分解性オルガノシラン化合物及び/又はその部分加水分解縮合物が、加水分解によって環状ケトン化合物を脱離するものである[1]に記載の室温硬化性オルガノポリシロキサン組成物。
[3]
脱離する環状ケトン化合物がシクロブタノン又はシクロペンタノンである[2]に記載の室温硬化性オルガノポリシロキサン組成物。
[4]
(B)成分の加水分解性オルガノシラン化合物が、下記一般式(4)で示される加水分解性オルガノシラン化合物である[1]~[3]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物。
[5]
更に、(C)硬化触媒を(A)成分100質量部に対して0.01~10質量部含有するものである[1]~[4]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物。
[6]
(C)硬化触媒が、錫触媒、チタン触媒、有機強塩基触媒及び有機ビスマス触媒から選ばれる少なくとも1種である[5]に記載の室温硬化性オルガノポリシロキサン組成物。
[7]
錫触媒を含有しないものである[1]~[6]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物。
[8]
更に、(D)下記一般式(3)で示されるシランカップリング剤及び/又はその部分加水分解縮合物を(A)成分100質量部に対して0.01~10質量部含有するものである[1]~[7]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物。
R3R4 bSiX3-b (3)
(式中、R3は窒素原子、硫黄原子及び酸素原子から選ばれる1種以上のヘテロ原子を含む官能性基(但し、グアニジル基を除く)を少なくとも1個有する炭素数1~20の一価炭化水素基である。R4は炭素数1~10の非置換又は置換の一価炭化水素基であり、Xは加水分解性基である。bは0、1又は2である。)
[9]
更に、(E)無機質充填剤を(A)成分100質量部に対して1~500質量部含有するものである[1]~[8]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物。
[10]
(E)成分が、炭酸カルシウム、煙霧質シリカ、沈降性シリカ、カーボンブラック及び酸化アルミニウムから選ばれる1種又は2種以上の無機質充填剤である[9]に記載の室温硬化性オルガノポリシロキサン組成物。
[11]
[1]~[10]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物の硬化物を有する自動車用部品。
[12]
[1]~[10]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物の硬化物を有する自動車用オイルシール。
[13]
[1]~[10]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物の硬化物を有する電気・電子用部品。
[14]
[1]~[10]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物の硬化物を有する建築用構造物。
[15]
[1]~[10]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物の硬化物を有する土木工事用構造物。
[16]
[1]~[10]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物を含有する接着剤。
[17]
[1]~[10]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物を含有するシーリング材。
[18]
[1]~[10]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物を含有するポッティング剤。
[19]
[1]~[10]のいずれかに記載の室温硬化性オルガノポリシロキサン組成物を含有するコーティング剤。
[20]
下記一般式(4)で示される加水分解性オルガノシラン化合物。
[21]
加水分解によってシクロペンタノンを脱離するものである[20]に記載の加水分解性オルガノシラン化合物。
[22]
下記反応式[I]
で示される、クロロシラン化合物とシクロペンタノンを塩基性物質及び触媒の存在下で反応させる工程を含む[20]又は[21]に記載の加水分解性オルガノシラン化合物の製造方法。
[23]
上記シクロペンタノンの添加量が、クロロシラン化合物中の塩素原子数1モルに対して、0.95~3.0モルである[22]に記載の加水分解性オルガノシラン化合物の製造方法。
[24]
上記触媒物質が、塩化銅、ヨウ化銅、臭化銅、塩化銀、ヨウ化銀又は臭化銀である[22]又は[23]に記載の加水分解性オルガノシラン化合物の製造方法。
[25]
上記触媒物質の添加量が、クロロシラン化合物1モルに対して0.001~0.5モルである[22]~[24]のいずれかに記載の加水分解性オルガノシラン化合物の製造方法。
[26]
上記塩基性物質が、トリメチルアミン、トリエチルアミン、トリプロピルアミン、トリブチルアミン、尿素、ジアザビシクロウンデセン又はジアザビシクロノネンである[22]~[25]のいずれかに記載の加水分解性オルガノシラン化合物の製造方法。
[27]
上記塩基性物質の添加量が、クロロシラン化合物中の塩素原子数1モルに対して0.95~2.5モルである[22]~[26]のいずれかに記載の加水分解性オルガノシラン化合物の製造方法。
また、本発明の加水分解性オルガノシラン化合物は、脱離基(脱離化合物)としてより安全性の高い化合物を放出し、特に室温硬化性オルガノポリシロキサン組成物の架橋剤として使用した場合に、該組成物は、硬化性に優れ、空気中に曝すと速やかに硬化して、優れた物性を示すことから、この加水分解性オルガノシラン化合物を含む組成物は、建築用途、自動車用途、電気電子用接着剤用途として有効に使用することができる。
本発明の室温硬化性オルガノポリシロキサン組成物に用いられる(A)成分は、下記一般式(1)で示される23℃における粘度が20~1,000,000mPa・sのオルガノポリシロキサンである。
HO-(SiR1 2O)a-H (1)
(式中、R1は炭素数1~10の非置換又は置換の一価炭化水素基であり、各R1は互いに同一であっても異種の基であってもよい。aは50以上の整数である。)
本発明において、重合度(又は分子量)は、例えば、トルエン、テトラヒドロフラン(THF)等を展開溶媒としたゲルパーミエーションクロマトグラフィー(GPC)分析におけるポリスチレン換算の数平均重合度(又は数平均分子量)等として求めることができる。
本発明の室温硬化性オルガノポリシロキサン組成物に用いられる(B)成分は、下記一般式(2)で示される加水分解性オルガノシラン化合物及び/又はその部分加水分解縮合物で、架橋剤(硬化剤)として用いられるものであり、加水分解によってシクロブタノンやシクロペンタノン等の環状ケトン化合物を脱離基(脱離物質)として放出するものであることを特徴とする。
なお、本発明において「部分加水分解縮合物」とは、該加水分解性オルガノシラン化合物を部分的に加水分解・縮合して生成する、分子中に残存加水分解性基を3個以上、好ましくは4個以上有するオルガノシロキサンオリゴマーを意味する。
触媒(金属銅化合物)の添加量としては、クロロシラン化合物1モルに対して0.001~0.5モルが好ましく、0.002~0.2モルがより好ましく、0.003~0.1モルが更に好ましい。触媒の添加量が少ないと反応が終結しないおそれがあり、触媒の添加量が多すぎるとコスト的に不利となる。
塩基性物質の添加量としては、クロロシラン化合物中の塩素原子数1モルに対して0.95~2.5モルが好ましく、0.99~2.0モルがより好ましく、1.0~1.5モルが更に好ましい。塩基性物質の添加量が少ないと反応が終結しないおそれがあり、塩基性物質の添加量が多すぎると経済的に不利である。
溶剤の使用量としては特に限定されないが、通常、使用する環状ケトン化合物100質量部に対して、10~500質量部、好ましくは30~400質量部、より好ましくは50~300質量部等の範囲で使用される。
また、反応終了後の精製は減圧環境下で目的物を蒸留することで可能であり、減圧度は好ましくは1×10-5~3,000Pa、より好ましくは1×10-5~2,000Paであり、精製時の温度は好ましくは100~250℃、より好ましくは120~230℃である。減圧時の圧力(減圧度)が高すぎると蒸留が困難となる場合がある。また、精製時の温度が低すぎると、蒸留による精製が困難となる場合があり、高すぎると反応物の着色や分解を招くおそれがある。
また、mは上述したとおり、3又は4である。この数が3未満である場合(即ち、mが0、1又は2である場合)は架橋反応によるゴム硬化が起こらず、縮合硬化型室温硬化性オルガノポリシロキサン組成物の架橋剤として不適である。
塩基性物質の添加量としては、クロロシラン化合物中の塩素原子数1モルに対して0.95~2.5モルが好ましく、0.99~2.0モルがより好ましく、1.0~1.5モルが更に好ましい。塩基性物質の添加量が少ないと反応が終結しないおそれがあり、塩基性物質の添加量が多すぎると経済的に不利である。
触媒(金属銅化合物、金属銀化合物)の添加量としては、クロロシラン化合物1モルに対して0.001~0.5モルが好ましく、0.002~0.2モルがより好ましく、0.003~0.1モルが更に好ましい。触媒の添加量が少ないと反応が終結しないおそれがあり、触媒の添加量が多すぎるとコスト的に不利となる。
溶剤の使用量としては特に限定されないが、通常、使用するシクロペンタノン100質量部に対して、10~500質量部、好ましくは30~400質量部、より好ましくは50~300質量部等の範囲で使用される。
また、反応終了後の精製は減圧環境下で目的物を蒸留することで可能であり、減圧度は好ましくは1×10-5~3,000Pa、より好ましくは1×10-5~2,000Paであり、精製時の温度は好ましくは100~250℃、より好ましくは120~230℃である。減圧時の圧力(減圧度)が高すぎると蒸留が困難となる場合がある。また、精製時の温度が低すぎると、蒸留による精製が困難となる場合があり、高すぎると反応物の着色や分解を招くおそれがある。
加水分解によって生じる脱離基(脱離化合物)として、より安全性の高い、シクロペンタノンを放出する加水分解性オルガノシラン化合物を架橋剤(硬化剤)として使用することによって、ゴム物性に優れた硬化物を与え、速硬化性を有する縮合硬化型室温硬化性オルガノシロキサン組成物が得られる。
(B)成分の配合量は、(A)成分100質量部に対して1~40質量部であり、好ましくは3~30質量部であり、更に好ましくは5~20質量部である。(B)成分の配合量が上記下限値の1質量部未満であると、密封容器中に保管した際の保存性が悪化する場合がある。また、(B)成分の配合量が上記上限値の40質量部を超えると、室温硬化性オルガノポリシロキサン組成物の硬化性が著しく低下し、更には接着性が悪化する場合がある。
なお、(B)成分の加水分解性オルガノシラン化合物及び/又はその部分加水分解縮合物は、分子中に、窒素原子、硫黄原子及び酸素原子から選ばれる1種以上の原子を含む官能性基を少なくとも1個有する一価炭化水素基を有しないものである点において、後述する任意成分としての(D)成分のシランカップリング剤及び/又はその部分加水分解縮合物とは明確に区別されるものである。
本発明の室温硬化性オルガノポリシロキサン組成物には、必要に応じて(C)成分の硬化触媒を任意成分として配合することができる。(C)成分の硬化触媒としては、室温硬化性オルガノポリシロキサン組成物の硬化促進剤として従来から一般的に使用されている金属系又は非金属系の縮合触媒を使用できる。例えば、ジブチル錫メトキサイド、ジブチル錫ジアセテート、ジブチル錫ジオクテート、ジブチル錫ジラウレート、ジオクチル錫ジラウレート、ジオクチル錫ジオクテート、ジメチル錫ジメトキサイド、ジメチル錫ジアセテート等の有機錫化合物(錫触媒)、テトラプロピルチタネート、テトラブチルチタネート、テトラ-2-エチルヘキシルチタネート、ジメトキシチタンジアセチルアセトナート、チタンジイソプロポキシビス(エチルアセトアセテート)等の有機チタン化合物(チタン触媒)、トリエチルアミン、ヘキシルアミン、テトラメチルグアニジン、γ-テトラメチルグアニジルプロピルトリメトキシシラン等のアミン化合物やこれらの塩(有機強塩基触媒)、ビスマストリス(2-エチルヘキサノエート)、ビスマストリス(ネオデカノエート)等の有機ビスマス化合物及びそれらの混合物(有機ビスマス触媒)などが挙げられ、これらの少なくともいずれか1つ、即ち1種を単独で又は2種以上を組み合わせて使用することができる。
なお、本発明においては、上記触媒のうち、チタン触媒、有機強塩基触媒及び有機ビスマス触媒のいずれを配合しても、錫触媒を配合した場合と同等の硬化性及び硬化物性能を示すことから、錫触媒を配合せずにチタン触媒、有機強塩基触媒又は有機ビスマス触媒を配合することが環境保護の観点から好ましい。
本発明の室温硬化性オルガノポリシロキサン組成物には、必要に応じて(D)成分のシランカップリング剤及び/又はその部分加水分解縮合物を任意成分として配合することができる。(D)成分は、下記一般式(3)で示されるシランカップリング剤(即ち、官能性基含有一価炭化水素基を有する加水分解性オルガノシラン化合物又はカーボンファンクショナルシラン)及び/又はその部分加水分解縮合物であり、本発明の室温硬化性オルガノポリシロキサン組成物の硬化物に良好な接着性を発現させるための成分である。
R3R4 bSiX3-b (3)
(式中、R3は窒素原子、硫黄原子及び酸素原子から選ばれる1種以上のヘテロ原子を含む官能性基(但し、グアニジル基を除く)を少なくとも1個有する炭素数1~20の一価炭化水素基である。R4は炭素数1~10の非置換又は置換の一価炭化水素基であり、Xは加水分解性基である。bは0、1又は2である。)
本発明の室温硬化性オルガノポリシロキサン組成物には、必要に応じて(E)成分の無機質充填剤を任意成分として配合することができる。(E)成分の無機質充填剤は、本発明の室温硬化性オルガノポリシロキサン組成物にゴム物性を付与するための補強性、非補強性充填剤である。(E)成分の無機質充填剤としては、表面疎水化処理又は無処理の、焼成シリカ、溶融シリカ、破砕シリカ、煙霧質シリカ(ヒュームドシリカ)等の乾式シリカ、沈降性シリカ、ゾル-ゲル法シリカ等の湿式シリカ、結晶性シリカ(微粉末石英)などのシリカ系充填剤、珪藻土、カーボンブラック、タルク、ベントナイト、表面処理又は無処理の炭酸カルシウム、炭酸亜鉛、炭酸マグネシウム、表面処理又は無処理の酸化カルシウム、酸化亜鉛、酸化マグネシウム、酸化アルミニウム、水酸化アルミニウム等が例示され、その中でも炭酸カルシウム、煙霧質シリカ、沈降性シリカ、カーボンブラック、酸化アルミニウムが好ましく、より好ましくは表面が疎水化処理された、炭酸カルシウム、煙霧質シリカ、沈降性シリカ、カーボンブラック、酸化アルミニウムである。この場合、これら無機質充填剤は、水分量が少ないことが好ましい。
なお、該表面処理剤(疎水化処理剤)の種類、量や処理方法等については特に制限はないが、代表的には、クロロシラン、アルコキシシラン、オルガノシラザン等の有機ケイ素化合物や、脂肪酸、パラフィン、シランカップリング剤、チタンカップリング剤等の処理剤が適用できる。
(E)成分の無機質充填剤は、1種単独で用いてもよく、2種以上を併用してもよい。
また、本発明の室温硬化性オルガノポリシロキサン組成物には、上記成分以外に一般に知られている添加剤を本発明の目的を損なわない範囲で使用しても差し支えない。添加剤としては、チクソ性向上剤としてのポリエーテル、可塑剤としてのシリコーンオイル(無官能性オルガノポリシロキサン)、イソパラフィン等が挙げられ、必要に応じて顔料、染料、蛍光増白剤等の着色剤、防かび剤、抗菌剤、海洋生物忌避剤等の生理活性添加剤、ブリードオイルとしてのフェニルシリコーンオイル、フロロシリコーンオイル、シリコーンと非相溶の有機液体等の表面改質剤、溶剤揮発油、低沸点イソパラフィン等の溶剤も添加できる。
機械攪拌機、温度計、還流管及び滴下ロートを備えた5,000mLの四つ口セパラブルフラスコに、シクロペンタノン834g(9.9mol)、トリエチルアミン825g(8.2mol)、塩化銅(I)5g(0.05mol)、ヘキサン1,500mlを仕込み、40~60℃の範囲でビニルトリクロロシラン400g(2.47mol)を約2時間かけて滴下した。その後、80℃で12時間撹拌後、生成したトリエチルアミン塩酸塩を濾過して取り除き、ろ液から100℃、常圧の条件でヘキサンを留去したのち、180℃、300Paの条件で蒸留することで加水分解性オルガノシラン化合物1を得た(収量532g、収率69%)。この反応式は、下記式[2]で表される。
機械攪拌機、温度計、還流管及び滴下ロートを備えた5,000mLの四つ口セパラブルフラスコに、シクロペンタノン834g(9.9mol)、トリエチルアミン825g(8.2mol)、塩化銅(I)5g(0.05mol)、ヘキサン1,500mlを仕込み、40~60℃の範囲でメチルトリクロロシラン368g(2.47mol)を約2時間かけて滴下した。その後、80℃で12時間撹拌後、生成したトリエチルアミン塩酸塩を濾過して取り除き、ろ液から100℃、常圧の条件でヘキサンを留去したのち、170℃、300Paの条件で蒸留することで加水分解性オルガノシラン化合物2を得た(収量519g、収率71%)。この反応式は、下記式[3]で表される。
機械攪拌機、温度計、還流管及び滴下ロートを備えた5,000mLの四つ口セパラブルフラスコに、シクロペンタノン834g(9.9mol)、トリエチルアミン825g(8.2mol)、塩化銅(I)5g(0.05mol)、ヘキサン1,500mlを仕込み、40~60℃の範囲でフェニルトリクロロシラン522g(2.47mol)を約2時間かけて滴下した。その後、80℃で12時間撹拌後、生成したトリエチルアミン塩酸塩を濾過して取り除き、ろ液から100℃、常圧の条件でヘキサンを留去したのち、200℃、300Paの条件で蒸留することで加水分解性オルガノシラン化合物3を得た(収量568g、収率65%)。この反応式は、下記式[4]で表される。
(A)23℃における粘度が20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部に、(E-1)表面がパラフィン系で処理された重質炭酸カルシウム(製品名;MCコートP-20、丸尾カルシウム(株)製)を100質量部、(E-2)表面がジメチルジクロロシランにて処理された煙霧質シリカ(製品名;MU-215、信越化学工業(株)製)を10質量部加えて十分に混合した後、(B-1)前記加水分解性オルガノシラン化合物1を8質量部加え、十分に混合した。最後に(D-1)γ-アミノプロピルトリメトキシシラン(製品名;KBM-903、信越化学工業(株)製)を1質量部、(C-1)ジオクチル錫ジラウレートを0.1質量部加え、減圧下で完全に混合し、組成物1を得た。
(A)23℃における粘度が20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部に、(E-1)表面がパラフィン系で処理された重質炭酸カルシウム(製品名;MCコートP-20、丸尾カルシウム(株)製)を100質量部、(E-2)表面がジメチルジクロロシランにて処理された煙霧質シリカ(製品名;MU-215、信越化学工業(株)製)を10質量部加えて十分に混合した後、(B-1)前記加水分解性オルガノシラン化合物1を8質量部加え、十分に混合した。最後に(D-2)γ-グリシドキシプロピルトリメトキシシラン(製品名;KBM-403、信越化学工業(株)製)を1質量部、(C-2)チタンジイソプロポキシビス(エチルアセトアセテート)(製品名;オルガチックスTC750、マツモトファインケミカル(株)製)を4質量部加え、減圧下で完全に混合し、組成物2を得た。
(A)23℃における粘度が20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部に、(E-1)表面がパラフィン系で処理された重質炭酸カルシウム(製品名;MCコートP-20、丸尾カルシウム(株)製)を100質量部、(E-2)表面がジメチルジクロロシランにて処理された煙霧質シリカ(製品名;MU-215、信越化学工業(株)製)を10質量部加えて十分に混合した後、(B-1)前記加水分解性オルガノシラン化合物1を8質量部加え、十分に混合した。最後に(D-3)N-2-(アミノエチル)-3-アミノプロピルトリメトキシシラン(製品名;KBM-603、信越化学工業(株)製)を1質量部、(C-3)γ-テトラメチルグアニジルプロピルトリメトキシシランを0.6質量部加え、減圧下で完全に混合し、組成物3を得た。
(A)23℃における粘度が20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部に、(E-1)表面がパラフィン系で処理された重質炭酸カルシウム(製品名;MCコートP-20、丸尾カルシウム(株)製)を100質量部、(E-2)表面がジメチルジクロロシランにて処理された煙霧質シリカ(製品名;MU-215、信越化学工業(株)製)を10質量部加えて十分に混合した後、(B-1)前記加水分解性オルガノシラン化合物1を8質量部加え、十分に混合した。最後に(D-1)γ-アミノプロピルトリメトキシシラン(製品名;KBM-903、信越化学工業(株)製)を1質量部、(C-4)ビスマストリス(2-エチルヘキサノエート)を主成分とする有機ビスマス触媒(製品名;ネオスタンU-600、日東化成(株)製)を1質量部加え、減圧下で完全に混合し、組成物4を得た。
(A)23℃における粘度が20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部に、(E-1)表面がパラフィン系で処理された重質炭酸カルシウム(製品名;MCコートP-20、丸尾カルシウム(株)製)を100質量部、(E-2)表面がジメチルジクロロシランにて処理された煙霧質シリカ(製品名;MU-215、信越化学工業(株)製)を10質量部加えて十分に混合した後、(B-2)前記加水分解性オルガノシラン化合物2を8質量部加え、十分に混合した。最後に(D-3)N-2-(アミノエチル)-3-アミノプロピルトリメトキシシラン(製品名;KBM-603、信越化学工業(株)製)を1質量部、(C-3)γ-テトラメチルグアニジルプロピルトリメトキシシランを0.6質量部加え、減圧下で完全に混合し、組成物5を得た。
(A)23℃における粘度が20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部に、(E-1)表面がパラフィン系で処理された重質炭酸カルシウム(製品名;MCコートP-20、丸尾カルシウム(株)製)を100質量部、(E-2)表面がジメチルジクロロシランにて処理された煙霧質シリカ(製品名;MU-215、信越化学工業(株)製)を10質量部加えて十分に混合した後、(B-3)前記加水分解性オルガノシラン化合物3を8質量部加え、十分に混合した。最後に(D-3)N-2-(アミノエチル)-3-アミノプロピルトリメトキシシラン(製品名;KBM-603、信越化学工業(株)製)を1質量部、(C-3)γ-テトラメチルグアニジルプロピルトリメトキシシランを0.6質量部加え、減圧下で完全に混合し、組成物6を得た。
(A)23℃における粘度が20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部に、(E-1)表面がパラフィン系で処理された重質炭酸カルシウム(製品名;MCコートP-20、丸尾カルシウム(株)製)を100質量部、(E-2)表面がジメチルジクロロシランにて処理された煙霧質シリカ(製品名;MU-215、信越化学工業(株)製)を10質量部加えて十分に混合した後、(B’)メチルトリスメチルエチルケトオキシムシランを10質量部加え、十分に混合した。最後に(D-1)γ-アミノプロピルトリメトキシシラン(製品名;KBM-903、信越化学工業(株)製)を1質量部、(C-1)ジオクチル錫ジラウレートを0.1質量部加え、減圧下で完全に混合し、組成物7を得た。
(A’)23℃における粘度が20,000mPa・sの分子鎖両末端がメチルジメトキシ基で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部に、(E-1)表面がパラフィン系で処理された重質炭酸カルシウム(製品名;MCコートP-20、丸尾カルシウム(株)製)を100質量部、(E-2)表面がジメチルジクロロシランにて処理された煙霧質シリカ(製品名;MU-215、信越化学工業(株)製)を10質量部加えて十分に混合した後、(B'')メチルトリメトキシシランを10質量部加え、十分に混合した。最後に(D-2)γ-グリシドキシプロピルトリメトキシシラン(製品名;KBM-403、信越化学工業(株)製)を1質量部、(C-2)チタンジイソプロポキシビス(エチルアセトアセテート)(製品名;オルガチックスTC750、マツモトファインケミカル(株)製)を4質量部加え、減圧下で完全に混合し、組成物8を得た。
(A)23℃における粘度が20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部に、(E-1)表面がパラフィン系で処理された重質炭酸カルシウム(製品名;MCコートP-20、丸尾カルシウム(株)製)を100質量部、(E-2)表面がジメチルジクロロシランにて処理された煙霧質シリカ(製品名;MU-215、信越化学工業(株)製)を10質量部加えて十分に混合した後、(B'')メチルトリメトキシシランを10質量部加え、十分に混合した。最後に(D-1)γ-アミノプロピルトリメトキシシラン(製品名;KBM-903、信越化学工業(株)製)を1質量部、(C-4)ビスマストリス(2-エチルヘキサノエート)を主成分とする有機ビスマス触媒(製品名;ネオスタンU-600、日東化成(株)製)を1質量部加え、減圧下で完全に混合し、組成物9を得た。
(A)23℃における粘度が20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部に、(E-1)表面がパラフィン系で処理された重質炭酸カルシウム(製品名;MCコートP-20、丸尾カルシウム(株)製)を100質量部、(E-2)表面がジメチルジクロロシランにて処理された煙霧質シリカ(製品名;MU-215、信越化学工業(株)製)を10質量部加えて十分に混合した後、(B''')ビニルトリスイソプロポキシシランを8質量部加え、十分に混合した。最後に(D-3)N-2-(アミノエチル)-3-アミノプロピルトリメトキシシラン(製品名;KBM-603、信越化学工業(株)製)を1質量部、(C-3)γ-テトラメチルグアニジルプロピルトリメトキシシランを0.6質量部加え、減圧下で完全に混合し、組成物10を得た。
上記実施例1~6、比較例1~4で調製された各組成物(室温硬化性オルガノポリシロキサン組成物)について、下記の評価を行った。実施例1~6、比較例1~4の配合量と共に、下記評価結果を表1に示す。
初期評価として上記調製直後の各組成物を用いて以下のタックフリータイム、硬化速度、ゴム物性、接着性を評価した。
タックフリータイム
上記実施例、比較例で調製された各組成物を用いて、JIS A 5758に規定する方法に準じてタックフリータイム(指触乾燥時間)を測定した。
硬化速度試験方法は、内径10mmのガラスシャーレに、上記実施例、比較例で調製された各組成物を充填し、23℃、50%RHで1日(24時間)後に、探針を差し込むことで空気に触れた部分から硬化した厚さ(深さ)を測定した。
上記実施例、比較例で調製された各組成物を2mmの型枠に流し込み、23℃、50%RHで7日間養生して2mm厚さのゴムシートを得た。JIS K 6249に準じてゴム物性(タイプAデュロメータ硬さ、引張強度、切断時伸び)を測定した。
上記実施例、比較例で調製された各組成物を、幅25mm、長さ100mmのアルミニウム板2枚の間で23℃、50%RHで7日間養生して硬化させ、上下それぞれのアルミニウム板との接着面積2.5cm2、接着厚さ1mmのシリコーンゴム硬化物層を形成して、せん断接着試験体を作製した。この各試験体を用いてアルミニウムに対するせん断接着力と凝集破壊率をJIS K 6249に規定する方法に準じて測定した。
耐湿熱性能を確認するため、得られた硬化後のシリコーンゴムシート及びせん断接着試験体を85℃、85%RHの環境に暴露し、1,000時間劣化させて、その後製造初期(初期評価)と同様の試験(ゴム物性、接着性)を行うことで、耐湿熱性の確認試験を行った。
耐熱性能を確認するため、得られた硬化後のシリコーンゴムシート及びせん断接着試験体を150℃の乾燥環境に暴露し、1,000時間劣化させて、その後製造初期(初期評価)と同様の試験(ゴム物性、接着性)を行うことで、耐熱性の確認試験を行った。
また、実施例の組成物が硬化中に放出する化合物は、シクロペンタノンであり、人体に対しての発がん性や生殖毒性など健康有害性、水生生物毒性など環境有害性の報告例がなく安全性の高い化合物である。一方で、比較例の組成物が硬化中に放出する化合物はいずれもSDS(安全データシート)等で健康有害性が表示されており、発がん性のおそれ、水生生物への毒性を有する2-ブタノンオキシム、劇物に指定され、人体に強い有害性を有しているメタノール、反復暴露による臓器への障害を有するアセトンである。また、メタノール、アセトンは、シクロペンタノンと比較して引火点や沸点が低いことからも、本発明の室温硬化性オルガノポリシロキサン組成物は、人体の健康、環境保護の観点からより優れていることが分かる。
機械攪拌機、温度計、還流管及び滴下ロートを備えた5,000mLの四つ口セパラブルフラスコに、シクロペンタノン834g(9.9mol)、トリエチルアミン825g(8.2mol)、塩化銅(I)5g(0.05mol)、ヘキサン1,500mlを仕込み、40~60℃の範囲でビニルトリクロロシラン400g(2.47mol)を約2時間かけて滴下した。その後、80℃で12時間撹拌後、生成したトリエチルアミン塩酸塩を濾過して取り除き、ろ液から100℃、常圧の条件でヘキサンを留去したのち、180℃、300Paの条件で蒸留することで加水分解性オルガノシラン化合物4を得た(収量532g、収率69%)。この反応式は、下記式[II]で表される。
1H-NMR(400MHz,CDCl3)δ6.11(-CH=CH 2 ,m,2H),δ6.02(-CH=CH2,m,1H),δ4.43(-OC(CH2)=CH-,s,3H),δ2.20(-OC-CH 2 -,t,6H),δ2.15(-OC=CH-CH 2 -,m,6H)δ2.15(-OC-CH2-CH 2 -,m,6H)
機械攪拌機、温度計、還流管及び滴下ロートを備えた5,000mLの四つ口セパラブルフラスコに、シクロペンタノン834g(9.9mol)、トリエチルアミン825g(8.2mol)、塩化銅(I)5g(0.05mol)、ヘキサン1,500mlを仕込み、40~60℃の範囲でフェニルトリクロロシラン522g(2.47mol)を約2時間かけて滴下した。その後、80℃で12時間撹拌後、生成したトリエチルアミン塩酸塩を濾過して取り除き、ろ液から100℃、常圧の条件でヘキサンを留去したのち、200℃、300Paの条件で蒸留することで加水分解性オルガノシラン化合物5を得た(収量568g、収率65%)。この反応式は、下記式[III]で表される。
1H-NMR(400MHz,CDCl3)δ6.64(Si-C6 H 5 ,m,5H),δ4.40(-OC(CH2)=CH-,s,3H),δ2.20(-OC-CH 2 -,t,6H),δ2.15(-OC=CH-CH 2 -,m,6H)δ2.13(-OC-CH2-CH 2 -,m,6H)
機械攪拌機、温度計、還流管及び滴下ロートを備えた5,000mLの四つ口セパラブルフラスコに、シクロペンタノン758g(9.0mol)、トリエチルアミン727g(7.2mol)、塩化銅(I)5g(0.05mol)、ヘキサン1200mlを仕込み、40℃~60℃の範囲でテトラクロロシラン255g(1.5mol)を約2時間かけて滴下した。その後、80℃で12時間撹拌後、生成したトリエチルアミン塩酸塩を濾過して取り除き、ろ液から100℃、常圧の条件でヘキサンを留去したのち、210℃、300Paの条件で蒸留することで加水分解性オルガノシラン化合物6を得た(収量302g、収率56%)。この反応式は、下記式[IV]で表される。
1H-NMR(400MHz,CDCl3)δ4.45(-OC(CH2)=CH-,s,4H),δ2.22(-OC-CH 2 -,t,8H),δ2.15(-OC=CH-CH 2 -,m,8H)δ2.15(-OC-CH2-CH 2 -,m,8H)
粘度20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部と、加水分解性オルガノシラン化合物4を7質量部と、γ-テトラメチルグアニジルプロピルトリメトキシシラン0.5質量部を加え、湿気遮断下で均一になるまで混合して組成物を調製した。
粘度20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部と、加水分解性オルガノシラン化合物5を7質量部と、γ-テトラメチルグアニジルプロピルトリメトキシシラン0.5質量部を加え、湿気遮断下で均一になるまで混合して組成物を調製した。
粘度20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部と、加水分解性オルガノシラン化合物6を7質量部と、γ-テトラメチルグアニジルプロピルトリメトキシシラン0.5質量部を加え、湿気遮断下で均一になるまで混合して組成物を調製した。
粘度20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部と、ビニルトリスケトオキシムシランを7質量部と、ジオクチル錫ジラウレート0.1質量部を加え、湿気遮断下で均一になるまで混合して組成物を調製した。
粘度20,000mPa・sの分子鎖両末端がシラノール基(ケイ素原子に結合した水酸基)で封鎖された直鎖状ジメチルポリシロキサン(前記一般式(1)において、R1=メチル基、a=約620に該当するジメチルポリシロキサン)100質量部と、ビニルトリメトキシシランを7質量部と、ジオクチル錫ジラウレート0.1質量部を加え、湿気遮断下で均一になるまで混合して組成物を調製した。
これらの結果を下記表3に示した。
Claims (27)
- (B)成分の加水分解性オルガノシラン化合物及び/又はその部分加水分解縮合物が、加水分解によって環状ケトン化合物を脱離するものである請求項1に記載の室温硬化性オルガノポリシロキサン組成物。
- 脱離する環状ケトン化合物がシクロブタノン又はシクロペンタノンである請求項2に記載の室温硬化性オルガノポリシロキサン組成物。
- 更に、(C)硬化触媒を(A)成分100質量部に対して0.01~10質量部含有するものである請求項1~4のいずれか1項に記載の室温硬化性オルガノポリシロキサン組成物。
- (C)硬化触媒が、錫触媒、チタン触媒、有機強塩基触媒及び有機ビスマス触媒から選ばれる少なくとも1種である請求項5に記載の室温硬化性オルガノポリシロキサン組成物。
- 錫触媒を含有しないものである請求項1~6のいずれか1項に記載の室温硬化性オルガノポリシロキサン組成物。
- 更に、(D)下記一般式(3)で示されるシランカップリング剤及び/又はその部分加水分解縮合物を(A)成分100質量部に対して0.01~10質量部含有するものである請求項1~7のいずれか1項に記載の室温硬化性オルガノポリシロキサン組成物。
R3R4 bSiX3-b (3)
(式中、R3は窒素原子、硫黄原子及び酸素原子から選ばれる1種以上のヘテロ原子を含む官能性基(但し、グアニジル基を除く)を少なくとも1個有する炭素数1~20の一価炭化水素基である。R4は炭素数1~10の非置換又は置換の一価炭化水素基であり、Xは加水分解性基である。bは0、1又は2である。) - 更に、(E)無機質充填剤を(A)成分100質量部に対して1~500質量部含有するものである請求項1~8のいずれか1項に記載の室温硬化性オルガノポリシロキサン組成物。
- (E)成分が、炭酸カルシウム、煙霧質シリカ、沈降性シリカ、カーボンブラック及び酸化アルミニウムから選ばれる1種又は2種以上の無機質充填剤である請求項9に記載の室温硬化性オルガノポリシロキサン組成物。
- 請求項1~10のいずれか1項に記載の室温硬化性オルガノポリシロキサン組成物の硬化物を有する自動車用部品。
- 請求項1~10のいずれか1項に記載の室温硬化性オルガノポリシロキサン組成物の硬化物を有する自動車用オイルシール。
- 請求項1~10のいずれか1項に記載の室温硬化性オルガノポリシロキサン組成物の硬化物を有する電気・電子用部品。
- 請求項1~10のいずれか1項に記載の室温硬化性オルガノポリシロキサン組成物の硬化物を有する建築用構造物。
- 請求項1~10のいずれか1項に記載の室温硬化性オルガノポリシロキサン組成物の硬化物を有する土木工事用構造物。
- 請求項1~10のいずれか1項に記載の室温硬化性オルガノポリシロキサン組成物を含有する接着剤。
- 請求項1~10のいずれか1項に記載の室温硬化性オルガノポリシロキサン組成物を含有するシーリング材。
- 請求項1~10のいずれか1項に記載の室温硬化性オルガノポリシロキサン組成物を含有するポッティング剤。
- 請求項1~10のいずれか1項に記載の室温硬化性オルガノポリシロキサン組成物を含有するコーティング剤。
- 加水分解によってシクロペンタノンを脱離するものである請求項20に記載の加水分解性オルガノシラン化合物。
- 上記シクロペンタノンの添加量が、クロロシラン化合物中の塩素原子数1モルに対して、0.95~3.0モルである請求項22に記載の加水分解性オルガノシラン化合物の製造方法。
- 上記触媒物質が、塩化銅、ヨウ化銅、臭化銅、塩化銀、ヨウ化銀又は臭化銀である請求項22又は23に記載の加水分解性オルガノシラン化合物の製造方法。
- 上記触媒物質の添加量が、クロロシラン化合物1モルに対して0.001~0.5モルである請求項22~24のいずれか1項に記載の加水分解性オルガノシラン化合物の製造方法。
- 上記塩基性物質が、トリメチルアミン、トリエチルアミン、トリプロピルアミン、トリブチルアミン、尿素、ジアザビシクロウンデセン又はジアザビシクロノネンである請求項22~25のいずれか1項に記載の加水分解性オルガノシラン化合物の製造方法。
- 上記塩基性物質の添加量が、クロロシラン化合物中の塩素原子数1モルに対して0.95~2.5モルである請求項22~26のいずれか1項に記載の加水分解性オルガノシラン化合物の製造方法。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US18/038,805 US20240002606A1 (en) | 2020-11-26 | 2021-08-16 | Room temperature curable organopolysiloxane composition, article, hydrolyzable organosilane compound and method for producing same |
| EP21897416.0A EP4253494A1 (en) | 2020-11-26 | 2021-08-16 | Room temperature curable organopolysiloxane composition, article, hydrolyzable organosilane compound and method for producing same |
| CN202180077951.7A CN116507689A (zh) | 2020-11-26 | 2021-08-16 | 室温固化性有机聚硅氧烷组合物及物品以及水解性有机硅烷化合物及其制造方法 |
| KR1020237020983A KR20230112134A (ko) | 2020-11-26 | 2021-08-16 | 실온경화성 오르가노폴리실록산 조성물 및 물품 그리고 가수분해성 오르가노실란 화합물 및 그 제조 방법 |
| JP2022565054A JPWO2022113437A1 (ja) | 2020-11-26 | 2021-08-16 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020-195627 | 2020-11-26 | ||
| JP2020195627 | 2020-11-26 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2022113437A1 true WO2022113437A1 (ja) | 2022-06-02 |
Family
ID=81754542
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2021/029897 WO2022113437A1 (ja) | 2020-11-26 | 2021-08-16 | 室温硬化性オルガノポリシロキサン組成物及び物品並びに加水分解性オルガノシラン化合物及びその製造方法 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20240002606A1 (ja) |
| EP (1) | EP4253494A1 (ja) |
| JP (1) | JPWO2022113437A1 (ja) |
| KR (1) | KR20230112134A (ja) |
| CN (1) | CN116507689A (ja) |
| WO (1) | WO2022113437A1 (ja) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023032745A1 (ja) * | 2021-09-03 | 2023-03-09 | 信越化学工業株式会社 | オルガノポリシロキサン化合物、室温硬化性オルガノポリシロキサン組成物、及び物品 |
| WO2023127675A1 (ja) * | 2021-12-27 | 2023-07-06 | 信越化学工業株式会社 | 室温硬化性樹脂組成物及び物品 |
| WO2023248723A1 (ja) * | 2022-06-21 | 2023-12-28 | 信越化学工業株式会社 | グアニジン配位子を有する固定化亜鉛錯体およびその製造方法、並びにこれを用いた環状カーボネートの製造方法 |
| WO2024014350A1 (ja) * | 2022-07-14 | 2024-01-18 | 信越化学工業株式会社 | 二成分型室温速硬化性樹脂組成物及び物品 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5139673B2 (ja) | 1972-07-14 | 1976-10-29 | ||
| JP2015113377A (ja) * | 2013-12-10 | 2015-06-22 | 信越化学工業株式会社 | 室温硬化性オルガノポリシロキサン組成物の製造方法、シーリング材及び物品 |
| JP2018515634A (ja) | 2015-03-17 | 2018-06-14 | ヘンケル・アクチェンゲゼルシャフト・ウント・コムパニー・コマンディットゲゼルシャフト・アウフ・アクチェンHenkel AG & Co. KGaA | 硬化性シリコーン組成物 |
| JP2019073670A (ja) * | 2017-10-19 | 2019-05-16 | 信越化学工業株式会社 | 室温硬化性オルガノポリシロキサン組成物及びその製造方法、並びに自動車ロングライフクーラントシール材 |
| JP2020517771A (ja) * | 2017-04-21 | 2020-06-18 | ニトロヘミー、アッシヤウ、ゲーエムベーハー | 硬化性シリコーンゴム化合物 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE2437610A1 (de) | 1974-08-05 | 1976-02-26 | Boehringer Sohn Ingelheim | Neue 5,9-beta-disubstituierte 2-tetrahydrofurfuryl-6,7-benzomorphane, deren saeureadditionssalze, ihre verwendung als arzneimittel und verfahren zu deren herstellung |
-
2021
- 2021-08-16 US US18/038,805 patent/US20240002606A1/en active Pending
- 2021-08-16 CN CN202180077951.7A patent/CN116507689A/zh active Pending
- 2021-08-16 WO PCT/JP2021/029897 patent/WO2022113437A1/ja active Application Filing
- 2021-08-16 EP EP21897416.0A patent/EP4253494A1/en active Pending
- 2021-08-16 KR KR1020237020983A patent/KR20230112134A/ko unknown
- 2021-08-16 JP JP2022565054A patent/JPWO2022113437A1/ja active Pending
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS5139673B2 (ja) | 1972-07-14 | 1976-10-29 | ||
| JP2015113377A (ja) * | 2013-12-10 | 2015-06-22 | 信越化学工業株式会社 | 室温硬化性オルガノポリシロキサン組成物の製造方法、シーリング材及び物品 |
| JP2018515634A (ja) | 2015-03-17 | 2018-06-14 | ヘンケル・アクチェンゲゼルシャフト・ウント・コムパニー・コマンディットゲゼルシャフト・アウフ・アクチェンHenkel AG & Co. KGaA | 硬化性シリコーン組成物 |
| JP2020517771A (ja) * | 2017-04-21 | 2020-06-18 | ニトロヘミー、アッシヤウ、ゲーエムベーハー | 硬化性シリコーンゴム化合物 |
| JP2019073670A (ja) * | 2017-10-19 | 2019-05-16 | 信越化学工業株式会社 | 室温硬化性オルガノポリシロキサン組成物及びその製造方法、並びに自動車ロングライフクーラントシール材 |
Non-Patent Citations (3)
| Title |
|---|
| DATABASE REGISTRY 21 January 1985 (1985-01-21), ANONYMOUS: "/1 -(C) FILE REGISTRY RN -94358-77-7 REGISTRY ED -Entered STN: 21 Jan 1985 CN -Silane, tris(1-cyclopenten-1-yloxy)methyl-(9CI) (CA INDEX NAME)", XP055935616, retrieved from STN Database accession no. 94358-77-7 * |
| JOURNAL OF ORGANOMETALLIC CHEMISTRY, vol. 273, no. 1, 1984 |
| JOURNAL OF ORGANOMETALLIC CHEMISTRY, vol. 281, no. 2-3, 1985 |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023032745A1 (ja) * | 2021-09-03 | 2023-03-09 | 信越化学工業株式会社 | オルガノポリシロキサン化合物、室温硬化性オルガノポリシロキサン組成物、及び物品 |
| WO2023127675A1 (ja) * | 2021-12-27 | 2023-07-06 | 信越化学工業株式会社 | 室温硬化性樹脂組成物及び物品 |
| WO2023248723A1 (ja) * | 2022-06-21 | 2023-12-28 | 信越化学工業株式会社 | グアニジン配位子を有する固定化亜鉛錯体およびその製造方法、並びにこれを用いた環状カーボネートの製造方法 |
| WO2024014350A1 (ja) * | 2022-07-14 | 2024-01-18 | 信越化学工業株式会社 | 二成分型室温速硬化性樹脂組成物及び物品 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN116507689A (zh) | 2023-07-28 |
| US20240002606A1 (en) | 2024-01-04 |
| KR20230112134A (ko) | 2023-07-26 |
| JPWO2022113437A1 (ja) | 2022-06-02 |
| EP4253494A1 (en) | 2023-10-04 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2022113437A1 (ja) | 室温硬化性オルガノポリシロキサン組成物及び物品並びに加水分解性オルガノシラン化合物及びその製造方法 | |
| KR102326223B1 (ko) | 실온 경화성 오르가노폴리실록산 조성물 및 해당 실온 경화성 오르가노폴리실록산 조성물의 경화물인 성형물 | |
| JP6314993B2 (ja) | 多成分系室温硬化性オルガノポリシロキサン組成物、該組成物の硬化物及び該硬化物からなる成型物 | |
| JPWO2019069706A1 (ja) | 室温硬化性オルガノポリシロキサン組成物の製造方法、室温硬化性オルガノポリシロキサン組成物及び物品 | |
| WO2020209083A1 (ja) | オイルシール用室温硬化性オルガノポリシロキサン組成物及び自動車用部品 | |
| US10428183B2 (en) | Room temperature-curable resin composition containing an aluminum chelate compound | |
| WO2022163436A1 (ja) | 二成分型室温速硬化性オルガノポリシロキサン組成物及び物品 | |
| JP6760223B2 (ja) | 室温硬化性オルガノポリシロキサン組成物、およびこれを含有するシール剤、コーティング剤、接着剤、成形物 | |
| WO2022009759A1 (ja) | 二成分型室温速硬化性オルガノポリシロキサン組成物、該組成物の硬化物及び物品 | |
| WO2023127675A1 (ja) | 室温硬化性樹脂組成物及び物品 | |
| JP4879616B2 (ja) | 硬化性シリコーン系樹脂の硬化触媒及び硬化性シリコーン系樹脂組成物 | |
| JP4781810B2 (ja) | 室温硬化性ポリオルガノシロキサン組成物 | |
| JP6315100B2 (ja) | 新規有機チタン化合物、該有機チタン化合物の製造方法、硬化触媒及び室温硬化性オルガノポリシロキサン組成物 | |
| WO2020226076A1 (ja) | 室温硬化性オルガノポリシロキサン組成物、シリコーンゴム及び物品 | |
| WO2023032745A1 (ja) | オルガノポリシロキサン化合物、室温硬化性オルガノポリシロキサン組成物、及び物品 | |
| JP7351264B2 (ja) | 室温硬化性オルガノポリシロキサン組成物及び物品 | |
| JP2023161342A (ja) | 室温硬化性オルガノポリシロキサン組成物及び物品 | |
| JP7176527B2 (ja) | オルガノポリシロキサン組成物、並びに有機ケイ素化合物及びその製造方法 | |
| JP6816681B2 (ja) | 硬化触媒、湿気硬化型室温硬化性オルガノポリシロキサン組成物及び成形体 | |
| JP2711613B2 (ja) | 室温硬化性組成物 | |
| WO2024014350A1 (ja) | 二成分型室温速硬化性樹脂組成物及び物品 | |
| JP2023026886A (ja) | 二成分型室温速硬化性オルガノポリシロキサン組成物及び物品 | |
| JP2021178933A (ja) | 室温硬化性オルガノポリシロキサン組成物及び物品 | |
| JP5915599B2 (ja) | 室温硬化性樹脂組成物 | |
| JP2021066816A (ja) | 室温硬化性オルガノポリシロキサン組成物及び硬化物並びに物品 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 21897416 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2022565054 Country of ref document: JP Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 202180077951.7 Country of ref document: CN |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 18038805 Country of ref document: US |
|
| ENP | Entry into the national phase |
Ref document number: 20237020983 Country of ref document: KR Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2021897416 Country of ref document: EP Effective date: 20230626 |