WO2022049614A1 - Il-31アンタゴニストを有効成分として含有する、透析そう痒症の予防用及び/又は治療用医薬組成物 - Google Patents
Il-31アンタゴニストを有効成分として含有する、透析そう痒症の予防用及び/又は治療用医薬組成物 Download PDFInfo
- Publication number
- WO2022049614A1 WO2022049614A1 PCT/JP2020/032987 JP2020032987W WO2022049614A1 WO 2022049614 A1 WO2022049614 A1 WO 2022049614A1 JP 2020032987 W JP2020032987 W JP 2020032987W WO 2022049614 A1 WO2022049614 A1 WO 2022049614A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- weeks
- pruritus
- dialysis
- group
- dose
- Prior art date
Links
- 208000003251 Pruritus Diseases 0.000 title claims abstract description 270
- 238000000502 dialysis Methods 0.000 title claims abstract description 126
- 239000005557 antagonist Substances 0.000 title claims abstract description 102
- 238000011282 treatment Methods 0.000 title claims abstract description 79
- 239000008194 pharmaceutical composition Substances 0.000 title claims abstract description 58
- 230000002265 prevention Effects 0.000 title claims abstract description 29
- 239000004480 active ingredient Substances 0.000 title claims abstract description 17
- 101710181613 Interleukin-31 Proteins 0.000 claims abstract description 247
- 102100021596 Interleukin-31 Human genes 0.000 claims abstract description 247
- 210000002966 serum Anatomy 0.000 claims description 73
- 230000006872 improvement Effects 0.000 claims description 61
- 230000003472 neutralizing effect Effects 0.000 claims description 31
- 102100021594 Interleukin-31 receptor subunit alpha Human genes 0.000 claims description 23
- 230000007958 sleep Effects 0.000 claims description 22
- 208000019116 sleep disease Diseases 0.000 claims description 17
- 230000004620 sleep latency Effects 0.000 claims description 9
- 208000020685 sleep-wake disease Diseases 0.000 claims description 8
- 241000283973 Oryctolagus cuniculus Species 0.000 claims description 7
- 230000009260 cross reactivity Effects 0.000 claims description 6
- 238000002513 implantation Methods 0.000 claims description 5
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 claims description 4
- 101710131691 Interleukin-31 receptor subunit alpha Proteins 0.000 claims description 2
- 230000000670 limiting effect Effects 0.000 abstract description 30
- 239000000203 mixture Substances 0.000 abstract description 5
- 229940068196 placebo Drugs 0.000 description 71
- 239000000902 placebo Substances 0.000 description 71
- 238000000034 method Methods 0.000 description 51
- 241000282567 Macaca fascicularis Species 0.000 description 37
- 230000037396 body weight Effects 0.000 description 33
- 238000004458 analytical method Methods 0.000 description 31
- 238000007920 subcutaneous administration Methods 0.000 description 31
- 206010012438 Dermatitis atopic Diseases 0.000 description 29
- 201000008937 atopic dermatitis Diseases 0.000 description 29
- 230000000694 effects Effects 0.000 description 29
- 230000006399 behavior Effects 0.000 description 27
- 239000003814 drug Substances 0.000 description 27
- 238000011156 evaluation Methods 0.000 description 27
- XGZZHZMWIXFATA-UEZBDDGYSA-N nalfurafine Chemical compound C([C@]12[C@H]3OC=4C(O)=CC=C(C2=4)C[C@@H]2[C@]1(O)CC[C@H]3N(C)C(=O)\C=C\C1=COC=C1)CN2CC1CC1 XGZZHZMWIXFATA-UEZBDDGYSA-N 0.000 description 27
- 101001043817 Homo sapiens Interleukin-31 receptor subunit alpha Proteins 0.000 description 26
- 102000005962 receptors Human genes 0.000 description 25
- 108020003175 receptors Proteins 0.000 description 25
- 230000007803 itching Effects 0.000 description 23
- 229960000441 nalfurafine Drugs 0.000 description 22
- 229940079593 drug Drugs 0.000 description 20
- 201000004624 Dermatitis Diseases 0.000 description 19
- 210000004027 cell Anatomy 0.000 description 19
- 208000024891 symptom Diseases 0.000 description 18
- 102100035360 Cerebellar degeneration-related antigen 1 Human genes 0.000 description 17
- 238000012360 testing method Methods 0.000 description 17
- 150000001875 compounds Chemical class 0.000 description 16
- 108090000623 proteins and genes Proteins 0.000 description 16
- 230000008859 change Effects 0.000 description 14
- 102000004169 proteins and genes Human genes 0.000 description 14
- 230000027455 binding Effects 0.000 description 12
- 230000007423 decrease Effects 0.000 description 12
- 230000001965 increasing effect Effects 0.000 description 12
- 241000282412 Homo Species 0.000 description 11
- 150000001413 amino acids Chemical class 0.000 description 11
- 102000003987 Oncostatin M Receptors Human genes 0.000 description 10
- 108010082522 Oncostatin M Receptors Proteins 0.000 description 10
- 125000003275 alpha amino acid group Chemical group 0.000 description 10
- 230000033001 locomotion Effects 0.000 description 10
- 150000003431 steroids Chemical class 0.000 description 10
- 238000002965 ELISA Methods 0.000 description 9
- 239000000427 antigen Substances 0.000 description 9
- 102000036639 antigens Human genes 0.000 description 9
- 108091007433 antigens Proteins 0.000 description 9
- 239000002775 capsule Substances 0.000 description 9
- 239000012071 phase Substances 0.000 description 9
- 239000000243 solution Substances 0.000 description 9
- 238000002560 therapeutic procedure Methods 0.000 description 9
- 201000010099 disease Diseases 0.000 description 8
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 8
- 238000001631 haemodialysis Methods 0.000 description 8
- 230000000322 hemodialysis Effects 0.000 description 8
- 206010015150 Erythema Diseases 0.000 description 7
- 208000010668 atopic eczema Diseases 0.000 description 7
- 230000002354 daily effect Effects 0.000 description 7
- 229940000406 drug candidate Drugs 0.000 description 7
- 231100000321 erythema Toxicity 0.000 description 7
- 239000002547 new drug Substances 0.000 description 7
- 230000000699 topical effect Effects 0.000 description 7
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 6
- 241000700159 Rattus Species 0.000 description 6
- 230000003247 decreasing effect Effects 0.000 description 6
- 230000036470 plasma concentration Effects 0.000 description 6
- 238000004393 prognosis Methods 0.000 description 6
- 230000004044 response Effects 0.000 description 6
- 210000000707 wrist Anatomy 0.000 description 6
- 208000013738 Sleep Initiation and Maintenance disease Diseases 0.000 description 5
- 239000000043 antiallergic agent Substances 0.000 description 5
- 239000000739 antihistaminic agent Substances 0.000 description 5
- 238000003556 assay Methods 0.000 description 5
- 239000000090 biomarker Substances 0.000 description 5
- 239000000833 heterodimer Substances 0.000 description 5
- 102000045410 human IL31RA Human genes 0.000 description 5
- 230000002401 inhibitory effect Effects 0.000 description 5
- 206010022437 insomnia Diseases 0.000 description 5
- 239000000047 product Substances 0.000 description 5
- 230000009467 reduction Effects 0.000 description 5
- 230000002829 reductive effect Effects 0.000 description 5
- 238000004088 simulation Methods 0.000 description 5
- 230000003860 sleep quality Effects 0.000 description 5
- 238000009121 systemic therapy Methods 0.000 description 5
- 241000209094 Oryza Species 0.000 description 4
- 235000007164 Oryza sativa Nutrition 0.000 description 4
- 206010033733 Papule Diseases 0.000 description 4
- 229940125715 antihistaminic agent Drugs 0.000 description 4
- 230000000903 blocking effect Effects 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- BMCQMVFGOVHVNG-TUFAYURCSA-N cortisol 17-butyrate Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@@](C(=O)CO)(OC(=O)CCC)[C@@]1(C)C[C@@H]2O BMCQMVFGOVHVNG-TUFAYURCSA-N 0.000 description 4
- 239000012228 culture supernatant Substances 0.000 description 4
- 238000009826 distribution Methods 0.000 description 4
- 210000003141 lower extremity Anatomy 0.000 description 4
- 239000002609 medium Substances 0.000 description 4
- 150000007523 nucleic acids Chemical group 0.000 description 4
- 238000007911 parenteral administration Methods 0.000 description 4
- 235000009566 rice Nutrition 0.000 description 4
- 238000012216 screening Methods 0.000 description 4
- 230000009885 systemic effect Effects 0.000 description 4
- 230000007704 transition Effects 0.000 description 4
- 210000001364 upper extremity Anatomy 0.000 description 4
- 230000000007 visual effect Effects 0.000 description 4
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 3
- 241000282693 Cercopithecidae Species 0.000 description 3
- 102000004190 Enzymes Human genes 0.000 description 3
- 108090000790 Enzymes Proteins 0.000 description 3
- 206010024438 Lichenification Diseases 0.000 description 3
- 239000004909 Moisturizer Substances 0.000 description 3
- 241000699666 Mus <mouse, genus> Species 0.000 description 3
- 241000699670 Mus sp. Species 0.000 description 3
- 206010060875 Uraemic pruritus Diseases 0.000 description 3
- 210000001015 abdomen Anatomy 0.000 description 3
- 238000010521 absorption reaction Methods 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 239000011575 calcium Substances 0.000 description 3
- 229910052791 calcium Inorganic materials 0.000 description 3
- 230000005713 exacerbation Effects 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 238000001990 intravenous administration Methods 0.000 description 3
- 230000003902 lesion Effects 0.000 description 3
- 229940071337 locoid Drugs 0.000 description 3
- 230000001333 moisturizer Effects 0.000 description 3
- 229950010012 nemolizumab Drugs 0.000 description 3
- 108020004707 nucleic acids Proteins 0.000 description 3
- 102000039446 nucleic acids Human genes 0.000 description 3
- 230000002093 peripheral effect Effects 0.000 description 3
- 238000013105 post hoc analysis Methods 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 238000011321 prophylaxis Methods 0.000 description 3
- 238000006748 scratching Methods 0.000 description 3
- 230000002393 scratching effect Effects 0.000 description 3
- 230000011664 signaling Effects 0.000 description 3
- -1 small molecule compound Chemical class 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- NFGXHKASABOEEW-UHFFFAOYSA-N 1-methylethyl 11-methoxy-3,7,11-trimethyl-2,4-dodecadienoate Chemical compound COC(C)(C)CCCC(C)CC=CC(C)=CC(=O)OC(C)C NFGXHKASABOEEW-UHFFFAOYSA-N 0.000 description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 2
- 208000032544 Cicatrix Diseases 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 2
- 206010020751 Hypersensitivity Diseases 0.000 description 2
- 206010060708 Induration Diseases 0.000 description 2
- 206010061218 Inflammation Diseases 0.000 description 2
- 241000699660 Mus musculus Species 0.000 description 2
- 206010030113 Oedema Diseases 0.000 description 2
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 208000005770 Secondary Hyperparathyroidism Diseases 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 210000001744 T-lymphocyte Anatomy 0.000 description 2
- 230000005856 abnormality Effects 0.000 description 2
- 208000026935 allergic disease Diseases 0.000 description 2
- 230000007815 allergy Effects 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 2
- 230000004663 cell proliferation Effects 0.000 description 2
- 239000003795 chemical substances by application Substances 0.000 description 2
- 230000001186 cumulative effect Effects 0.000 description 2
- 230000008034 disappearance Effects 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 230000002878 effect on pruritus Effects 0.000 description 2
- 230000008030 elimination Effects 0.000 description 2
- 238000003379 elimination reaction Methods 0.000 description 2
- 230000008451 emotion Effects 0.000 description 2
- 230000003203 everyday effect Effects 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 230000008595 infiltration Effects 0.000 description 2
- 238000001764 infiltration Methods 0.000 description 2
- 230000004054 inflammatory process Effects 0.000 description 2
- 230000000977 initiatory effect Effects 0.000 description 2
- 230000031146 intracellular signal transduction Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 238000012423 maintenance Methods 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 238000009521 phase II clinical trial Methods 0.000 description 2
- 239000011574 phosphorus Substances 0.000 description 2
- 229910052698 phosphorus Inorganic materials 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 206010037844 rash Diseases 0.000 description 2
- 231100000241 scar Toxicity 0.000 description 2
- 230000037387 scars Effects 0.000 description 2
- QZAYGJVTTNCVMB-UHFFFAOYSA-N serotonin Chemical compound C1=C(O)C=C2C(CCN)=CNC2=C1 QZAYGJVTTNCVMB-UHFFFAOYSA-N 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 239000013589 supplement Substances 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- 238000011830 transgenic mouse model Methods 0.000 description 2
- 230000007306 turnover Effects 0.000 description 2
- 238000009192 ultraviolet light therapy Methods 0.000 description 2
- 239000003981 vehicle Substances 0.000 description 2
- 230000001755 vocal effect Effects 0.000 description 2
- 239000008215 water for injection Substances 0.000 description 2
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 208000019901 Anxiety disease Diseases 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 206010003645 Atopy Diseases 0.000 description 1
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- 108700022150 Designed Ankyrin Repeat Proteins Proteins 0.000 description 1
- 206010013786 Dry skin Diseases 0.000 description 1
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- 208000010201 Exanthema Diseases 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 101001043821 Homo sapiens Interleukin-31 Proteins 0.000 description 1
- 101000586302 Homo sapiens Oncostatin-M-specific receptor subunit beta Proteins 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 1
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 1
- 208000008839 Kidney Neoplasms Diseases 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 108090000189 Neuropeptides Proteins 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- 241000009328 Perro Species 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 206010062519 Poor quality sleep Diseases 0.000 description 1
- 206010038389 Renal cancer Diseases 0.000 description 1
- 206010039509 Scab Diseases 0.000 description 1
- 206010040844 Skin exfoliation Diseases 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- GUGOEEXESWIERI-UHFFFAOYSA-N Terfenadine Chemical compound C1=CC(C(C)(C)C)=CC=C1C(O)CCCN1CCC(C(O)(C=2C=CC=CC=2)C=2C=CC=CC=2)CC1 GUGOEEXESWIERI-UHFFFAOYSA-N 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 1
- VJHCJDRQFCCTHL-UHFFFAOYSA-N acetic acid 2,3,4,5,6-pentahydroxyhexanal Chemical compound CC(O)=O.OCC(O)C(O)C(O)C(O)C=O VJHCJDRQFCCTHL-UHFFFAOYSA-N 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 230000001387 anti-histamine Effects 0.000 description 1
- 230000009830 antibody antigen interaction Effects 0.000 description 1
- 230000036506 anxiety Effects 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 208000006673 asthma Diseases 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 229950008138 carmellose Drugs 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 239000004359 castor oil Substances 0.000 description 1
- 235000019438 castor oil Nutrition 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 235000010980 cellulose Nutrition 0.000 description 1
- 230000007012 clinical effect Effects 0.000 description 1
- 230000000052 comparative effect Effects 0.000 description 1
- 238000012875 competitive assay Methods 0.000 description 1
- 230000024203 complement activation Effects 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 238000002425 crystallisation Methods 0.000 description 1
- 230000008025 crystallization Effects 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 230000035618 desquamation Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- 230000003292 diminished effect Effects 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 230000037336 dry skin Effects 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 230000003090 exacerbative effect Effects 0.000 description 1
- 201000005884 exanthem Diseases 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 239000004744 fabric Substances 0.000 description 1
- 239000012091 fetal bovine serum Substances 0.000 description 1
- 230000001605 fetal effect Effects 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 238000000684 flow cytometry Methods 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 238000009472 formulation Methods 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 238000010353 genetic engineering Methods 0.000 description 1
- 229930195712 glutamate Natural products 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- 125000000404 glutamine group Chemical group N[C@@H](CCC(N)=O)C(=O)* 0.000 description 1
- ZEMPKEQAKRGZGQ-XOQCFJPHSA-N glycerol triricinoleate Natural products CCCCCC[C@@H](O)CC=CCCCCCCCC(=O)OC[C@@H](COC(=O)CCCCCCCC=CC[C@@H](O)CCCCCC)OC(=O)CCCCCCCC=CC[C@H](O)CCCCCC ZEMPKEQAKRGZGQ-XOQCFJPHSA-N 0.000 description 1
- 230000003862 health status Effects 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 229960001340 histamine Drugs 0.000 description 1
- 102000045345 human IL31 Human genes 0.000 description 1
- 102000043719 human OSMR Human genes 0.000 description 1
- 210000004408 hybridoma Anatomy 0.000 description 1
- 229960001524 hydrocortisone butyrate Drugs 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- 230000001900 immune effect Effects 0.000 description 1
- 210000000987 immune system Anatomy 0.000 description 1
- 230000002163 immunogen Effects 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 230000001939 inductive effect Effects 0.000 description 1
- 230000028709 inflammatory response Effects 0.000 description 1
- 239000003112 inhibitor Substances 0.000 description 1
- 230000003834 intracellular effect Effects 0.000 description 1
- 230000004068 intracellular signaling Effects 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 201000010982 kidney cancer Diseases 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 150000002605 large molecules Chemical class 0.000 description 1
- 238000001638 lipofection Methods 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 238000004519 manufacturing process Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000010534 mechanism of action Effects 0.000 description 1
- 150000004667 medium chain fatty acids Chemical class 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- CWWARWOPSKGELM-SARDKLJWSA-N methyl (2s)-2-[[(2s)-2-[[2-[[(2s)-2-[[(2s)-2-[[(2s)-5-amino-2-[[(2s)-5-amino-2-[[(2s)-1-[(2s)-6-amino-2-[[(2s)-1-[(2s)-2-amino-5-(diaminomethylideneamino)pentanoyl]pyrrolidine-2-carbonyl]amino]hexanoyl]pyrrolidine-2-carbonyl]amino]-5-oxopentanoyl]amino]-5 Chemical compound C([C@@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)OC)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](N)CCCN=C(N)N)C1=CC=CC=C1 CWWARWOPSKGELM-SARDKLJWSA-N 0.000 description 1
- 230000003020 moisturizing effect Effects 0.000 description 1
- 230000035772 mutation Effects 0.000 description 1
- 230000010807 negative regulation of binding Effects 0.000 description 1
- 229940005483 opioid analgesics Drugs 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 230000001766 physiological effect Effects 0.000 description 1
- 239000013612 plasmid Substances 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 230000004481 post-translational protein modification Effects 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000003449 preventive effect Effects 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 230000009822 protein phosphorylation Effects 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 230000002285 radioactive effect Effects 0.000 description 1
- 230000004043 responsiveness Effects 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 229940076279 serotonin Drugs 0.000 description 1
- 208000037851 severe atopic dermatitis Diseases 0.000 description 1
- RMAQACBXLXPBSY-UHFFFAOYSA-N silicic acid Chemical compound O[Si](O)(O)O RMAQACBXLXPBSY-UHFFFAOYSA-N 0.000 description 1
- 235000012239 silicon dioxide Nutrition 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 239000007790 solid phase Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 230000003068 static effect Effects 0.000 description 1
- 239000008223 sterile water Substances 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 238000010998 test method Methods 0.000 description 1
- 238000010257 thawing Methods 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 229940126622 therapeutic monoclonal antibody Drugs 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 229920002554 vinyl polymer Polymers 0.000 description 1
- 230000002618 waking effect Effects 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2866—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against receptors for cytokines, lymphokines, interferons
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/24—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against cytokines, lymphokines or interferons
- C07K16/244—Interleukins [IL]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/04—Antipruritics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/54—Medicinal preparations containing antigens or antibodies characterised by the route of administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/545—Medicinal preparations containing antigens or antibodies characterised by the dose, timing or administration schedule
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Dermatology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Animal Behavior & Ethology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Description
〔1〕 IL-31アンタゴニストを有効成分として含有する、透析そう痒症の予防用及び/又は治療用医薬組成物。
〔2〕 前記IL-31アンタゴニストは、0.1mg~1000mg/body/2週、0.1mg~1000mg/body/4週、又は、0.1mg~1000mg/body/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与される、〔1〕に記載の医薬組成物。
〔3〕 前記IL-31アンタゴニストは、25mg~100mg/body/4週で投与される、〔2〕に記載の医薬組成物。
〔4〕 前記IL-31アンタゴニストは、50mg~100mg/body/4週で投与される、〔2〕または〔3〕に記載の医薬組成物。
〔5〕 前記IL-31アンタゴニストは、0.01mg~10mg/kg/2週、0.01mg~10mg/kg/4週、又は、0.01mg~10mg/kg/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与される、〔1〕~〔4〕のいずれかに記載の医薬組成物。
〔6〕 前記IL-31アンタゴニストは、0.2mg~2mg/kg/4週で投与される、〔5〕に記載の医薬組成物。
〔7〕 前記IL-31アンタゴニストは、血清中のIL-31濃度が所定の値以上である、透析そう痒症に罹患した、又は、罹患している恐れのある対象に投与される、〔1〕~〔6〕のいずれかに記載の医薬組成物。
〔7-2〕 透析そう痒症に罹患した、又は、罹患している恐れのある対象から得られた血清中のIL-31濃度を測定すること;ならびに、当該IL-31濃度が所定の値以上である対象をIL-31アンタゴニストによる予防及び/又は治療に対する応答者であると判定することを含む、対象のIL-31アンタゴニストによる予防及び/又は治療に対する応答を予測する方法により、IL-31アンタゴニストによる予防及び/又は治療に対する応答者であると判定された対象にのみ投与するための、〔1〕~〔7〕のいずれかに記載の医薬組成物。
〔7-3〕 血清中のIL-31濃度が測定された、透析そう痒症に罹患した、又は、罹患している恐れのある対象において、当該IL-31濃度が所定の値以上である対象をIL-31アンタゴニストによる予防及び/又は治療に対する応答者であると判定することを含む、対象のIL-31アンタゴニストによる予防及び/又は治療に対する応答を予測する方法により、IL-31アンタゴニストによる予防及び/又は治療に対する応答者であると判定された対象にのみ投与するための、〔1〕~〔7〕のいずれかに記載の医薬組成物。
〔8〕 透析そう痒症によって引き起こされる睡眠障害の改善用の、〔1〕~〔7-3〕のいずれかに記載の医薬組成物。
〔9〕 前記睡眠障害の改善が入眠から覚醒までの時間を増加させるための、及び/又は、睡眠潜時(着床後睡眠までの時間)を短縮させるための、〔8〕に記載の医薬組成物。
〔10〕 前記IL-31アンタゴニストが、IL-31シグナルを阻害する抗体である、〔1〕~〔9〕のいずれかに記載の医薬組成物。
〔11〕 前記抗体が、マウス、ラット、及びウサギのいずれのIL-31RAに対しても交差反応性を示さない、〔10〕に記載の医薬組成物。
〔12〕 前記抗体が、抗IL-31中和抗体または抗IL-31RA中和抗体である、〔10〕又は〔11〕に記載の医薬組成物。
〔13〕 前記抗IL-31RA中和抗体が、
(1)配列番号:1に記載のCDR1、配列番号:2に記載のCDR2、および配列番号:3に記載のCDR3を含むH鎖可変領域、ならびに、配列番号:4に記載のCDR1、配列番号:5に記載のCDR2、および配列番号:6に記載のCDR3を含むL鎖可変領域を含む抗IL-31RA抗体;
(2)配列番号:7に記載のH鎖可変領域、および、配列番号:8に記載のL鎖可変領域を含む抗IL-31RA抗体;又は、
(3)配列番号:9に記載のH鎖、および、配列番号:10に記載のL鎖を含む抗IL-31RA抗体
のいずれかである、〔12〕に記載の医薬組成物。
〔14〕 透析そう痒症が、ナルフラフィン塩酸塩を除く全身療法又は局所療法を行ったことがあり、それらの治療が(十分に)奏効していない透析そう痒症である、〔1〕~〔13〕のいずれかに記載の医薬組成物。
〔15〕 前記全身療法が抗ヒスタミン剤又は抗アレルギー薬による治療であり、前記局所療法が保湿剤又はステロイドによる治療である、〔14〕に記載の医薬組成物。
〔16〕 前記透析そう痒症が、IL-31シグナルに起因する透析そう痒症である、〔1〕~〔15〕のいずれかに記載の医薬組成物。
〔17〕 透析そう痒症に罹患した、又は、罹患している恐れのある対象にIL-31アンタゴニストを投与することを含む、透析そう痒症の予防及び/又は治療方法。
〔18〕 前記IL-31アンタゴニストは、0.1mg~1000mg/body/2週、0.1mg~1000mg/body/4週、又は、0.1mg~1000mg/body/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与される、〔17〕に記載の方法。
〔19〕 前記IL-31アンタゴニストは、0.01mg~10mg/kg/2週、0.01mg~10mg/kg/4週、又は、0.01mg~10mg/kg/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与される、〔17〕に記載の方法。
〔20〕 前記IL-31アンタゴニストは、血清中のIL-31濃度が所定の値以上である、透析そう痒症に罹患した、又は、罹患している恐れのある対象に投与される、〔17〕~〔19〕のいずれかに記載の方法。
〔21〕透析そう痒症に罹患した、又は、罹患している恐れのある対象から得られた血清中のIL-31濃度を測定すること;当該IL-31濃度が所定の値以上である対象をIL-31アンタゴニストによる予防及び/又は治療に対する応答者であると判定すること;ならびに、応答者であると判定された対象にIL-31アンタゴニストを投与することを含む、〔20〕に記載の方法。
〔21-2〕血清中のIL-31濃度が測定された、透析そう痒症に罹患した、又は、罹患している恐れのある対象において、当該IL-31濃度が所定の値以上である対象をIL-31アンタゴニストによる予防及び/又は治療に対する応答者であると判定すること;ならびに、応答者であると判定された対象にIL-31アンタゴニストを投与することを含む、〔20〕に記載の方法。
〔22〕 透析そう痒症の予防及び/又は治療のための医薬の製造における、IL-31アンタゴニストの使用。
〔23〕 前記IL-31アンタゴニストは、0.1mg~1000mg/body/2週、0.1mg~1000mg/body/4週、又は、0.1mg~1000mg/body/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与される、〔22〕に記載の使用。
〔24〕 前記IL-31アンタゴニストは、0.01mg~10mg/kg/2週、0.01mg~10mg/kg/4週、又は、0.01mg~10mg/kg/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与される、〔22〕に記載の使用。
〔25〕 前記IL-31アンタゴニストは、血清中のIL-31濃度が所定の値以上である、透析そう痒症に罹患した、又は、罹患している恐れのある対象に投与される、〔22〕~〔24〕のいずれかに記載の使用。
〔26〕 (i)容器;(ii)IL-31アンタゴニストを有効成分として含有する、前記容器内の医薬組成物;ならびに(iii)前記IL-31アンタゴニストを、0.1mg~1000mg/body/2週、0.1mg~1000mg/body/4週、又は、0.1mg~1000mg/body/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与することを指示する文書;および/あるいは(iv)前記IL-31アンタゴニストを、血清中のIL-31濃度が所定の値以上である、透析そう痒症に罹患した、又は、罹患している恐れのある対象に投与することを指示する文書を含む、製品。
〔27〕 (i)容器;(ii)IL-31アンタゴニストを有効成分として含有する、前記容器内の医薬組成物;ならびに(iii)前記IL-31アンタゴニストは、0.01mg~10mg/kg/2週、0.01mg~10mg/kg/4週、又は、0.01mg~10mg/kg/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与することを指示する文書;および/あるいは(iv)前記IL-31アンタゴニストを、血清中のIL-31濃度が所定の値以上である、透析そう痒症に罹患した、又は、罹患している恐れのある対象に投与することを指示する文書を含む、製品。
〔28〕 IL-31アンタゴニストを有効成分として含有する、透析そう痒症の予防用及び/又は治療用医薬組成物であって、さらには透析そう痒症によって引き起こされる睡眠障害の改善用の、医薬組成物。
〔29〕 前記睡眠障害の改善が入眠から覚醒までの時間を増加させるための、及び/又は、睡眠潜時(着床後睡眠までの時間)を短縮させるための、〔28〕に記載の医薬組成物。
〔30〕 透析そう痒症の予防及び/又は治療における使用のためのIL-31アンタゴニスト。
〔31〕 0.1mg~1000mg/body/1日~12週、0.1mg~1000mg/body/2週、0.1mg~1000mg/body/4週、又は、0.1mg~1000mg/body/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与される、〔30〕に記載のIL-31アンタゴニスト。
〔32〕 0.01mg~10mg/kg/1日~12週、0.01mg~10mg/kg/2週、0.01mg~10mg/kg/4週、又は、0.01mg~10mg/kg/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与される、〔30〕に記載のIL-31アンタゴニスト。
〔33〕 血清中のIL-31濃度が所定の値以上である、透析そう痒症に罹患した、又は、罹患している恐れのある対象に投与される、〔30〕~〔32〕のいずれかに記載のIL-31アンタゴニスト。
〔34〕 IL-31アンタゴニストを有効成分として含有する、透析そう痒症の予防用及び/又は治療用医薬組成物であって、
前記IL-31アンタゴニストは、血清中のIL-31濃度が所定の値以上である、透析そう痒症に罹患した、又は、罹患している恐れのある対象に投与される、医薬組成物。
〔35〕 IL-31アンタゴニストが、0.1mg~1000mg/body/2週、0.1mg~1000mg/body/4週、又は、0.1mg~1000mg/body/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与される、〔28〕又は〔29〕に記載の医薬組成物。
上記〔1〕~〔35〕のいずれかに記載の1又は複数の構成要件(element)の一部又は全部を任意に組み合わせたものも、技術常識に基づいて技術的に矛盾せず、かつ文脈に反しない限り、本開示に含まれる。
また、別の方法として、ある化合物がIL-31シグナルを阻害するかどうかは、IL-31が細胞に作用することによって引き起こされる生理活性がその化合物により阻害されるかどうかを調べることによっても確認することができる。前記生理活性は、何らかの方法により定量的あるいは定性的に測定できる活性であれば特に限定されないが、細胞増殖活性やタンパク質リン酸化活性、遺伝子/タンパク質発現誘導活性などを挙げることができる。例えば、表面にIL-31受容体を発現し、外部からのIL-31刺激に応じて増殖活性が誘導されるような細胞を用意して、そこに化合物を添加した場合に、IL-31により誘導される細胞増殖活性が低下するかどうかを測定することによって、当該化合物がIL-31シグナルを阻害したかどうかを評価することができる。そのような細胞としては、生来的にIL-31受容体を発現している天然の細胞を用いてもよいし、人工的にIL-31受容体を発現させた遺伝子組換え細胞を用いてもよい。遺伝子組換え細胞の好適な例として、IL-31受容体を発現させたBa/F3細胞を挙げることができる。また、さらなる別の方法として、Dillonらの文献(Nat Immunol (2004) 5, 752-760)に記載の方法を用いることもできる。
また、別の好ましい例として、抗ヒトIL-31RA(中和)抗体が挙げられ、具体的には、ヒトIL-31RAのドメイン1及び/又はドメイン2を認識する抗IL-31RA(中和)抗体を挙げることができる。ここでヒトIL-31RAのドメイン1とは、配列番号:11に記載のアミノ酸配列における53番目のアミノ酸から152番目のアミノ酸までの領域(LPAKP~LENIA)を指す。また、ドメイン2とは、配列番号:11に記載のアミノ酸配列における153番目のアミノ酸から259番目のアミノ酸までの領域(KTEPP~EEEAP)をいう。
限定はされないが、抗IL-31RA中和抗体の中でもより好ましくは、配列番号:1に記載のCDR1、配列番号:2に記載のCDR2、および配列番号:3に記載のCDR3を含むH鎖(重鎖)可変領域、ならびに配列番号:4に記載のCDR1、配列番号:5に記載のCDR2、および配列番号:6に記載のCDR3を含むL鎖(軽鎖)可変領域を含む抗IL-31RA抗体であり、さらに好ましくは、配列番号:7に記載のH鎖可変領域、および配列番号:8に記載のL鎖可変領域を含む抗IL-31RA抗体であり、特に好ましくは、配列番号:9に記載のH鎖、および配列番号:10に記載のL鎖を含む抗IL-31RA抗体である。
(1)配列番号:1に記載のCDR1、配列番号:2に記載のCDR2、および配列番号:3に記載のCDR3を含むH鎖可変領域、ならびに配列番号:4に記載のCDR1、配列番号:5に記載のCDR2、および配列番号:6に記載のCDR3を含むL鎖可変領域を含む抗IL-31RA抗体;
(2)配列番号:7に記載のH鎖可変領域、および配列番号:8に記載のL鎖可変領域を含む抗IL-31RA抗体;
(3)配列番号:9に記載のH鎖、および配列番号:10に記載のL鎖を含む抗IL-31RA抗体;又は
(4)ネモリズマブ(nemolizumab))
のいずれかを有効成分として含有する医薬組成物を、
透析そう痒症に罹患した、又は、罹患している恐れのある対象(例えばヒトの患者)に、
(A) 0.1mg~1000mg/body/2週、0.1mg~1000mg/body/4週、0.1mg~1000mg/body/8週、25mg~100mg/body/4週、50mg~100mg/body/4週、5mg~75mg/body/4週、5mg~50mg/body/4週、5mg~25mg/body/4週、5mg~20mg/body/4週、5mg/body/4週、10mg/body/4週、15mg/body/4週、20mg/body/4週、25mg/body/4週、30mg/body/4週(この場合、例えば、初回用量は、60mg/bodyであり、初回用量と1回目の継続用量との投与間隔は4週間であり、継続用量は30mg/body/4週であってよい。)、又は60mg/body/4週;あるいは、
(B) 0.01mg~10mg/kg/2週、0.01mg~10mg/kg/4週、0.01mg~10mg/kg/8週、0.125~2.0mg/kg/4週、0.125~0.5mg/kg/4週、0.5mg~2.0mg/kg/4週、又は0.5mg/kg/4週
で、投与してよい。かかる場合、対象における血清中のIL-31濃度は所定の値以上(例えば、超高感度酵素結合免疫吸着アッセイ(ELISA; SiMoATM, Quanterix, Billerica, MA, USA)を用いて測定した場合に、例えば、0.15 pg/mL以上、0.2 pg/mL以上、0.3 pg/mL以上、0.4 pg/mL以上、0.5 pg/mL以上、0.6 pg/mL以上、0.7 pg/mL以上、0.8 pg/mL以上、0.86 pg/mL以上、0.9 pg/mL以上、1.0 pg/mL以上、1.1 pg/mL以上、1.25 pg/mL以上、1.5 pg/mL以上、1.75 pg/mL以上、2 pg/mL以上、2.25 pg/mL以上、または、2.5 pg/mL以上、またはそれ以上)であってよい。
CDR Kabat Chothia Contact
L1 L24-L34 L24-L34 L30-L36
L2 L50-L56 L50-L56 L46-L55
L3 L89-L97 L89-L97 L89-L96
H1 H31-H35B H26-H32/34 H30-H35B (Kabatナンバリング)
H1 H31-H35 H26-H32 H30-H35 (Chothiaナンバリング)
H2 H50-H65 H52-H56 H47-H58
H3 H95-H102 H95-H102 H93-H101
(1) ナルフラフィン塩酸塩内服(製品名レミッチカプセル)
通常、成人には、ナルフラフィン塩酸塩として1日1回2.5μgを夕食後又は就寝前に経口投与する。なお、症状に応じて増量することができるが、1日1回5μgを限度とする。
例えば、一実施態様において、かゆみの強さをVASで測定して50mm以上に分類された対象を透析そう痒症に罹患していると認定してもよいが、透析そう痒症に対してナルフラフィン塩酸塩を除く全身療法(抗ヒスタミン剤や抗アレルギー薬等)又は局所療法(保湿剤、ステロイド等)を行ったことがあり、それらの治療が十分に奏効していないそう痒症であれば、その対象は特に限定されない。
かかる場合、当該IL-31アンタゴニストは、以下に詳述する、所定の投与間隔で所定の用量(投与量)にて等量かつ同一の投与間隔で反復投与されることが意図されてよい。
特定の実施態様において、本開示の医薬組成物は、IL-31アンタゴニスト投与開始前における血清中のIL-31濃度が所定の値以上である患者における透析そう痒症の予防用及び/又は治療用に用いられてよい。例示的な実施態様において、本開示の医薬組成物は、(1) 透析そう痒症に罹患した、又は、罹患している恐れのある対象から得られた血清中のIL-31濃度を測定すること;ならびに(2) 当該IL-31濃度が所定の値以上である対象をIL-31アンタゴニストによる予防及び/又は治療に対する応答者であると判定することを含む、対象のIL-31アンタゴニストによる予防及び/又は治療に対する応答を予測する方法により、IL-31アンタゴニストによる予防及び/又は治療に対する応答者であると判定された対象にのみ投与するためのものであってよい。
かかる場合、本開示の医薬組成物の投与によって、より高いそう痒改善効果の発揮が期待できる。そのような、高いそう痒改善効果の発揮が期待できる基準となりうる、所定の血清中IL-31濃度は、例えば、0.86 pg/mLである。患者から得られた血清中のIL-31濃度は、当業者に公知の任意の手法により測定することができ、好ましい非限定的な実施態様において、当該所定の血清中IL-31濃度は、超高感度酵素結合免疫吸着アッセイ(ELISA; SiMoATM, Quanterix, Billerica, MA, USA)を用いて測定してよい。
一実施態様において、透析そう痒症の予防と治療は場合によって同義に解されてもよい。
上述のように透析そう痒症の改善は患者のQOL、睡眠の質、又は生命予後の改善のために重要であると考えられている。
したがって、非限定的な別の態様において、本開示は、IL-31アンタゴニストを有効成分として含有する、透析そう痒症の予防用及び/又は治療用医薬組成物であって、さらには透析そう痒症によって引き起こされる睡眠障害の改善用の、医薬組成物に関する。当該睡眠障害の改善は、例えば、入眠から覚醒までの時間の増加、及び/又は、睡眠潜時(着床後睡眠までの時間)の短縮によって特徴づけられてよい。あるいは、非限定的なさらなる態様又は非限定的な別の態様において、本開示は透析そう痒症によって引き起こされるQOLの改善用の医薬組成物に関する。あるいは、非限定的なさらなる態様又は非限定的な別の態様において、本開示は透析そう痒症によって引き起こされる生命予後の改善用の医薬組成物に関する。
例えば、本開示におけるIL-31アンタゴニストを透析そう痒症に罹患した、又は、罹患している恐れのある対象に対して固定用量(mg/body)で投与することが意図される場合には、本開示におけるIL-31アンタゴニストの投与量を、mg/kgからmg/bodyへ換算し、適当な投与量(mg/body)を設定して、対象に投与してもよい。この際、mg/kgからmg/bodyへの換算ロジックとしては、限定はされないが、当業者公知のロジックを用いて適宜決定してよい。そのようなロジックの一例としては以下が考えられ得る:
本開示におけるIL-31アンタゴニストの最低有効血清中濃度と最大忍容(経験)血清中濃度が存在すると仮定し、この濃度範囲に血清中IL-31アンタゴニスト濃度が体重にかかわらず得られるように、mg/kgの投与量からmg/bodyの投与量への変更を検討してよい。そのような対象は、例えば体重が100kg未満又は120kg未満である対象であってよい。限定はされないが、高体重(例えば体重が100kg超又は120kg超)の対象に対してはmg/bodyでの投与量を場合により増大させてもよい。また、低体重の小児用の投与量はmg/bodyでは曝露が著しく増大する可能性がある場合には、mg/kgでの投与を検討してもよい。
あるいは、統計資料等に基づき、一般的な透析そう痒症患者の体重を想定し、当該想定体重に基づき、「体重あたり投与量 x 想定体重 = 固定用量」の計算式により、体重あたりの投与量(mg/kg)を固定用量(mg/body)に換算してもよい。例えば、成人一人あたりの想定体重を例えば60kgとして、体重あたり投与量(0.5mg/kg)から固定用量を30mg/bodyと算出してもよい。同様に、小児一人あたりの想定体重を例えば30kgとして、体重あたり投与量体重あたり投与量(0.5mg/kg)固定用量を15mg/bodyと算出してもよい。
週、146mg/body/6週、146.5mg/body/6週、147mg/body/6週、147.5mg/body/6週、148mg/body/6週、148.5mg/body/6週、149mg/body/6週、149.5mg/body/6週、150mg/body/6週、150.5mg/body/6週、151mg/body/6週、151.5mg/body/6週、152mg/body/6週、152.5mg/body/6週、153mg/body/6週、153.5mg/body/6週、154mg/body/6週、154.5mg/body/6週、155mg/body/6週、155.5mg/body/6週、156mg/body/6週、156.5mg/body/6週、157mg/body/6週、157.5mg/body/6週、158mg/body/6週、158.5mg/body/6週、159mg/body/6週、159.5mg/body/6週、160mg/body/6週、160.5mg/body/6週、161mg/body/6週、161.5mg/body/6週、162mg/body/6週、162.5mg/body/6週、163mg/body/6週、163.5mg/body/6週、164mg/body/6週、164.5mg/body/6週、165mg/body/6週、165.5mg/body/6週、166mg/body/6週、166.5mg/body/6週、167mg/body/6週、167.5mg/body/6週、168mg/body/6週、168.5mg/body/6週、169mg/body/6週、169.5mg/body/6週、170mg/body/6週、170.5mg/body/6週、171mg/body/6週、171.5mg/body/6週、172mg/body/6週、172.5mg/body/6週、173mg/body/6週、173.5mg/body/6週、174mg/body/6週、174.5mg/body/6週、175mg/body/6週、175.5mg/body/6週、176mg/body/6週、176.5mg/body/6週、177mg/body/6週、177.5mg/body/6週、178mg/body/6週、178.5mg/body/6週、179mg/body/6週、179.5mg/body/6週、180mg/body/6週、180.5mg/body/6週、181mg/body/6週、181.5mg/body/6週、182mg/body/6週、182.5mg/body/6週、183mg/body/6週、183.5mg/body/6週、184mg/body/6週、184.5mg/body/6週、185mg/body/6週、185.5mg/body/6週、186mg/body/6週、186.5mg/body/6週、187mg/body/6週、187.5mg/body/6週、188mg/body/6週、188.5mg/body/6週、189mg/body/6週、189.5mg/body/6週、190mg/body/6週、190.5mg/body/6週、191mg/body/6週、191.5mg/body/6週、192mg/body/6週、192.5mg/body/6週、193mg/body/6週、193.5mg/body/6週、194mg/body/6週、194.5mg/body/6週、195mg/body/6週、195.5mg/body/6週、196mg/body/6週、196.5mg/body/6週、197mg/body/6週、197.5mg/body/6週、198mg/body/6週、198.5mg/body/6週、199mg/body/6週、199.5mg/body/6週、200mg/body/6週等であってよい。あるいは、非限定的な一実施態様において、それは例えば、50mg/body/8週、50.5mg/body/8週、51mg/body/8週、51.5mg/body/8週、52mg/body/8週、52.5mg/body/8週、53mg/body/8週、53.5mg/body/8週、54mg/body/8週、54.5mg/body/8週、55mg/body/8週、55.5mg/body/8週、56mg/body/8週、56.5mg/body/8週、57mg/body/8週、57.5mg/body/8週、58mg/body/8週、58.5mg/body/8週、59mg/body/8週、59.5mg/body/8週、60mg/body/8週、60.5mg/body/8週、61mg/body/8週、61.5mg/body/8週、62mg/body/8週、62.5mg/body/8週、63mg/body/8週、63.5mg/body/8週、64mg/body/8週、64.5mg/body/8週、65mg/body/8週、65.5mg/body/8週、66mg/body/8週、66.5mg/body/8週、67mg/body/8週、67.5mg/body/8週、68mg/body/8週、68.5mg/body/8週、69mg/body/8週、69.5mg/body/8週、70mg/body/8週、70.5mg/body/8週、71mg/body/8週、71.5mg/body/8週、72mg/body/8週、72.5mg/body/8週、73mg/body/8週、73.5mg/body/8週、74mg/body/8週、74.5mg/body/8週、75mg/body/8週、75.5mg/body/8週、76mg/body/8週、76.5mg/body/8週、77mg/body/8週、77.5mg/body/8週、78mg/body/8週、78.5mg/body/8週、79mg/body/8週、79.5mg/body/8週、80mg/body/8週、80.5mg/body/8週、81mg/body/8週、81.5mg/body/8週、82mg/body/8週、82.5mg/body/8週、83mg/body/8週、83.5mg/body/8週、84mg/body/8週、84.5mg/body/8週、85mg/body/8週、85.5mg/body/8週、86mg/body/8週、86.5mg/body/8週、87mg/body/8週、87.5mg/body/8週、88mg/body/8週、88.5mg/body/8週、89mg/body/8週、89.5mg/body/8週、90mg/body/8週、90.5mg/body/8週、91mg/body/8週、91.5mg/body/8週、92mg/body/8週、92.5mg/body/8週、93mg/body/8週、93.5mg/body/8週、94mg/body/8週、94.5mg/body/8週、95mg/body/8週、95.5mg/body/8週、96mg/body/8週、96.5mg/body/8週、97mg/body/8週、97.5mg/body/8週、98mg/body/8週、98.5mg/body/8週、99mg/body/8週、99.5mg/body/8週、100mg/body/8週、100.5mg/body/8週、101mg/body/8週、101.5mg/body/8週、102mg/body/8週、102.5mg/body/8週、103mg/body/8週、103.5mg/body/8週、104mg/body/8週、104.5mg/body/8週、105mg/body/8週、105.5mg/body/8週、106mg/body/8週、106.5mg/body/8週、107mg/body/8週、107.5mg/body/8週、108mg/body/8週、108.5mg/body/8週、109mg/body/8週、109.5mg/body/8週、110mg/body/8週、110.5mg/body/8週、111mg/body/8週、111.5mg/body/8週、112mg/body/8週、112.5mg/body/8週、113mg/body/8週、113.5mg/body/8週、114mg/body/8週、114.5mg/body/8週、115mg/body/8週、115.5mg/body/8週、116mg/body/8週、116.5mg/body/8週、117mg/body/8週、117.5mg/body/8週、118mg/body/8週、118.5mg/body/8週、119mg/body/8週、119.5mg/body/8週、120mg/body/8週、120.5mg/body/8週、121mg/body/8週、121.5mg/body/8週、122mg/body/8週、122.5mg/body/8週、123mg/body/8週、123.5mg/body/8週、124mg/body/8週、124.5mg/body/8週、125mg/body/8週、125.5mg/body/8週、126mg/body/8週、126.5mg/body/8週、127mg/body/8週、127.5mg/body/8週、128mg/body/8週、128.5mg/body/8週、129mg/body/8週、129.5mg/body/8週、130mg/body/8週、130.5mg/body/8週、131mg/body/8週、131.5mg/body/8週、132mg/body/8週、132.5mg/body/8週、133mg/body/8週、133.5mg/body/8週、134mg/body/8週、134.5mg/body/8週、135mg/body/8週、135.5mg/body/8週、136mg/body/8週、136.5mg/body/8週、137mg/body/8週、137.5mg/body/8週、138mg/body/8週、138.5mg/body/8週、139mg/body/8週、139.5mg/body/8週、140mg/body/8週、140.5mg/body/8週、141mg/body/8週、141.5mg/body/8週、142mg/body/8週、142.5mg/body/8週、143mg/body/8週、143.5mg/body/8週、144mg/body/8週、144.5mg/body/8週、145mg/body/8週、145.5mg/body/8週、146mg/body/8週、146.5mg/body/8週、147mg/body/8週、147.5mg/body/8週、148mg/body/8週、148.5mg/body/8週、149mg/body/8週、149.5mg/body/8週、150mg/body/8週、150.5mg/body/8週、151mg/body/8週、151.5mg/body/8週、152mg/body/8週、152.5mg/body/8週、153mg/body/8週、153.5mg/body/8週、154mg/body/8週、154.5mg/body/8週、155mg/body/8週、155.5mg/body/8週、156mg/body/8週、156.5mg/body/8週、157mg/body/8週、157.5mg/body/8週、158mg/body/8週、158.5mg/body/8週、159mg/body/8週、159.5mg/body/8週、160mg/body/8週、160.5mg/body/8週、161mg/body/8週、161.5mg/body/8週、162mg/body/8週、162.5mg/body/8週、163mg/body/8週、163.5mg/body/8週、164mg/body/8週、164.5mg/body/8週、165mg/body/8週、165.5mg/body/8週、166mg/body/8週、166.5mg/body/8週、167mg/body/8週、167.5mg/body/8週、168mg/body/8週、168.5mg/body/8週、169mg/body/8週、169.5mg/body/8週、170mg/body/8週、170.5mg/body/8週、171mg/body/8週、171.5mg/body/8週、172mg/body/8週、172.5mg/body/8週、173mg/body/8週、173.5mg/body/8週、174mg/body/8週、174.5mg/body/8週、175mg/body/8週、175.5mg/body/8週、176mg/body/8週、176.5mg/body/8週、177mg/body/8週、177.5mg/body/8週、178mg/body/8週、178.5mg/body/8週、179mg/body/8週、179.5mg/body/8週、180mg/body/8週、180.5mg/body/8週、181mg/body/8週、181.5mg/body/8週、182mg/body/8週、182.5mg/body/8週、183mg/body/8週、183.5mg/body/8週、184mg/body/8週、184.5mg/body/8週、185mg/body/8週、185.5mg/body/8週、186mg/body/8週、186.5mg/body/8週、187mg/body/8週、187.5mg/body/8週、188mg/body/8週、188.5mg/body/8週、189mg/body/8週、189.5mg/body/8週、190mg/body/8週、190.5mg/body/8週、191mg/body/8週、191.5mg/body/8週、192mg/body/8週、192.5mg/body/8週、193mg/body/8週、193.5mg/body/8週、194mg/body/8週、194.5mg/body/8週、195mg/body/8週、195.5mg/body/8週、196mg/body/8週、196.5mg/body/8週、197mg/body/8週、197.5mg/body/8週、198mg/body/8週、198.5mg/body/8週、199mg/body/8週、199.5mg/body/8週、200mg/body/8週等であってよい。あるいは、非限定的な一実施態様において、それは例えば、50mg/body/10週、50.5mg/body/10週、51mg/body/10週、51.5mg/body/10週、52mg/body/10週、52.5mg/body/10週、53mg/body/10週、53.5mg/body/10週、54mg/body/10週、54.5mg/body/10週、55mg/body/10週、55.5mg/body/10週、56mg/body/10週、56.5mg/body/10週、57mg/body/10週、57.5mg/body/10週、58mg/body/10週、58.5mg/body/10週、59mg/body/10週、59.5mg/body/10週、60mg/body/10週、60.5mg/body/10週、61mg/body/10週、61.5mg/body/10週、62mg/body/10週、62.5mg/body/10週、63mg/body/10週、63.5mg/body/10週、64mg/body/10週、64.5mg/body/10週、65mg/body/10週、65.5mg/body/10週、66mg/body/10週、66.5mg/body/10週、67mg/body/10週、67.5mg/body/10週、68mg/body/10週、68.5mg/body/10週、69mg/body/10週、69.5mg/body/10週、70mg/body/10週、70.5mg/body/10週、71mg/body/10週、71.5mg/body/10週、72mg/body/10週、72.5mg/body/10週、73mg/body/10週、73.5mg/body/10週、74mg/body/10週、74.5mg/body/10週、75mg/body/10週、75.5mg/body/10週、76mg/body/10週、76.5mg/body/10週、77mg/body/10週、77.5mg/body/10週、78mg/body/10週、78.5mg/body/10週、79mg/body/10週、79.5mg/body/10週、80mg/body/10週、80.5mg/body/10週、81mg/body/10週、81.5mg/body/10週、82mg/body/10週、82.5mg/body/10週、83mg/body/10週、83.5mg/body/10週、84mg/body/10週、84.5mg/body/10週、85mg/body/10週、85.5mg/body/10週、86mg/body/10週、86.5mg/body/10週、87mg/body/10週、87.5mg/body/10週、88mg/body/10週、88.5mg/body/10週、89mg/body/10週、89.5mg/body/10週、90mg/body/10週、90.5mg/body/10週、91mg/body/10週、91.5mg/body/10週、92mg/body/10週、92.5mg/body/10週、93mg/body/10週、93.5mg/body/10週、94mg/body/10週、94.5mg/body/10週、95mg/body/10週、95.5mg/body/10週、96mg/body/10週、96.5mg/body/10週、97mg/body/10週、97.5mg/body/10週、98mg/body/10週、98.5mg/body/10週、99mg/body/10週、99.5mg/body/10週、100mg/body/10週、100.5mg/body/10週、101mg/body/10週、101.5mg/body/10週、102mg/body/10週、102.5mg/body/10週、103mg/body/10週、103.5mg/body/10週、104mg/body/10週、104.5mg/body/10週、105mg/body/10週、105.5mg/body/10週、106mg/body/10週、106.5mg/body/10週、107mg/body/10週、107.5mg/body/10週、108mg/body/10週、108.5mg/body/10週、109mg/body/10週、109.5mg/body/10週、110mg/body/10週、110.5mg/body/10週、111mg/body/10週、111.5mg/body/10週、112mg/body/10週、112.5mg/body/10週、113mg/body/10週、113.5mg/body/10週、114mg/body/10週、114.5mg/body/10週、115mg/body/10週、115.5mg/body/10週、116mg/body/10週、116.5mg/body/10週、117mg/body/10週、117.5mg/body/10週、118mg/body/10週、118.5mg/body/10週、119mg/body/10週、119.5mg/body/10週、120mg/body/10週、120.5mg/body/10週、121mg/body/10週、121.5mg/body/10週、122mg/body/10週、122.5mg/body/10週、123mg/body/10週、123.5mg/body/10週、124mg/body/10週、124.5mg/body/10週、125mg/body/10週、125.5mg/body/10週、126mg/body/10週、126.5mg/body/10週、127mg/body/10週、127.5mg/body/10週、128mg/body/10週、128.5mg/body/10週、129mg/body/10週、129.5mg/body/10週、130mg/body/10週、130.5mg/body/10週、131mg/body/10週、131.5mg/body/10週、132mg/body/10週、132.5mg/body/10週、133mg/body/10週、133.5mg/body/10週、134mg/body/10週、134.5mg/body/10週、135mg/body/10週、135.5mg/body/10週、136mg/body/10週、136.5mg/body/10週、137mg/body/10週、137.5mg/body/10週、138mg/body/10週、138.5mg/body/10週、139mg/body/10週、139.5mg/body/10週、140mg/body/10週、140.5mg/body/10週、141mg/body/10週、141.5mg/body/10週、142mg/body/10週、142.
5mg/body/10週、143mg/body/10週、143.5mg/body/10週、144mg/body/10週、144.5mg/body/10週、145mg/body/10週、145.5mg/body/10週、146mg/body/10週、146.5mg/body/10週、147mg/body/10週、147.5mg/body/10週、148mg/body/10週、148.5mg/body/10週、149mg/body/10週、149.5mg/body/10週、150mg/body/10週、150.5mg/body/10週、151mg/body/10週、151.5mg/body/10週、152mg/body/10週、152.5mg/body/10週、153mg/body/10週、153.5mg/body/10週、154mg/body/10週、154.5mg/body/10週、155mg/body/10週、155.5mg/body/10週、156mg/body/10週、156.5mg/body/10週、157mg/body/10週、157.5mg/body/10週、158mg/body/10週、158.5mg/body/10週、159mg/body/10週、159.5mg/body/10週、160mg/body/10週、160.5mg/body/10週、161mg/body/10週、161.5mg/body/10週、162mg/body/10週、162.5mg/body/10週、163mg/body/10週、163.5mg/body/10週、164mg/body/10週、164.5mg/body/10週、165mg/body/10週、165.5mg/body/10週、166mg/body/10週、166.5mg/body/10週、167mg/body/10週、167.5mg/body/10週、168mg/body/10週、168.5mg/body/10週、169mg/body/10週、169.5mg/body/10週、170mg/body/10週、170.5mg/body/10週、171mg/body/10週、171.5mg/body/10週、172mg/body/10週、172.5mg/body/10週、173mg/body/10週、173.5mg/body/10週、174mg/body/10週、174.5mg/body/10週、175mg/body/10週、175.5mg/body/10週、176mg/body/10週、176.5mg/body/10週、177mg/body/10週、177.5mg/body/10週、178mg/body/10週、178.5mg/body/10週、179mg/body/10週、179.5mg/body/10週、180mg/body/10週、180.5mg/body/10週、181mg/body/10週、181.5mg/body/10週、182mg/body/10週、182.5mg/body/10週、183mg/body/10週、183.5mg/body/10週、184mg/body/10週、184.5mg/body/10週、185mg/body/10週、185.5mg/body/10週、186mg/body/10週、186.5mg/body/10週、187mg/body/10週、187.5mg/body/10週、188mg/body/10週、188.5mg/body/10週、189mg/body/10週、189.5mg/body/10週、190mg/body/10週、190.5mg/body/10週、191mg/body/10週、191.5mg/body/10週、192mg/body/10週、192.5mg/body/10週、193mg/body/10週、193.5mg/body/10週、194mg/body/10週、194.5mg/body/10週、195mg/body/10週、195.5mg/body/10週、196mg/body/10週、196.5mg/body/10週、197mg/body/10週、197.5mg/body/10週、198mg/body/10週、198.5mg/body/10週、199mg/body/10週、199.5mg/body/10週、200mg/body/10週等であってよい。あるいは、非限定的な一実施態様において、それは例えば、50mg/body/12週、50.5mg/body/12週、51mg/body/12週、51.5mg/body/12週、52mg/body/12週、52.5mg/body/12週、53mg/body/12週、53.5mg/body/12週、54mg/body/12週、54.5mg/body/12週、55mg/body/12週、55.5mg/body/12週、56mg/body/12週、56.5mg/body/12週、57mg/body/12週、57.5mg/body/12週、58mg/body/12週、58.5mg/body/12週、59mg/body/12週、59.5mg/body/12週、60mg/body/12週、60.5mg/body/12週、61mg/body/12週、61.5mg/body/12週、62mg/body/12週、62.5mg/body/12週、63mg/body/12週、63.5mg/body/12週、64mg/body/12週、64.5mg/body/12週、65mg/body/12週、65.5mg/body/12週、66mg/body/12週、66.5mg/body/12週、67mg/body/12週、67.5mg/body/12週、68mg/body/12週、68.5mg/body/12週、69mg/body/12週、69.5mg/body/12週、70mg/body/12週、70.5mg/body/12週、71mg/body/12週、71.5mg/body/12週、72mg/body/12週、72.5mg/body/12週、73mg/body/12週、73.5mg/body/12週、74mg/body/12週、74.5mg/body/12週、75mg/body/12週、75.5mg/body/12週、76mg/body/12週、76.5mg/body/12週、77mg/body/12週、77.5mg/body/12週、78mg/body/12週、78.5mg/body/12週、79mg/body/12週、79.5mg/body/12週、80mg/body/12週、80.5mg/body/12週、81mg/body/12週、81.5mg/body/12週、82mg/body/12週、82.5mg/body/12週、83mg/body/12週、83.5mg/body/12週、84mg/body/12週、84.5mg/body/12週、85mg/body/12週、85.5mg/body/12週、86mg/body/12週、86.5mg/body/12週、87mg/body/12週、87.5mg/body/12週、88mg/body/12週、88.5mg/body/12週、89mg/body/12週、89.5mg/body/12週、90mg/body/12週、90.5mg/body/12週、91mg/body/12週、91.5mg/body/12週、92mg/body/12週、92.5mg/body/12週、93mg/body/12週、93.5mg/body/12週、94mg/body/12週、94.5mg/body/12週、95mg/body/12週、95.5mg/body/12週、96mg/body/12週、96.5mg/body/12週、97mg/body/12週、97.5mg/body/12週、98mg/body/12週、98.5mg/body/12週、99mg/body/12週、99.5mg/body/12週、100mg/body/12週、100.5mg/body/12週、101mg/body/12週、101.5mg/body/12週、102mg/body/12週、102.5mg/body/12週、103mg/body/12週、103.5mg/body/12週、104mg/body/12週、104.5mg/body/12週、105mg/body/12週、105.5mg/body/12週、106mg/body/12週、106.5mg/body/12週、107mg/body/12週、107.5mg/body/12週、108mg/body/12週、108.5mg/body/12週、109mg/body/12週、109.5mg/body/12週、110mg/body/12週、110.5mg/body/12週、111mg/body/12週、111.5mg/body/12週、112mg/body/12週、112.5mg/body/12週、113mg/body/12週、113.5mg/body/12週、114mg/body/12週、114.5mg/body/12週、115mg/body/12週、115.5mg/body/12週、116mg/body/12週、116.5mg/body/12週、117mg/body/12週、117.5mg/body/12週、118mg/body/12週、118.5mg/body/12週、119mg/body/12週、119.5mg/body/12週、120mg/body/12週、120.5mg/body/12週、121mg/body/12週、121.5mg/body/12週、122mg/body/12週、122.5mg/body/12週、123mg/body/12週、123.5mg/body/12週、124mg/body/12週、124.5mg/body/12週、125mg/body/12週、125.5mg/body/12週、126mg/body/12週、126.5mg/body/12週、127mg/body/12週、127.5mg/body/12週、128mg/body/12週、128.5mg/body/12週、129mg/body/12週、129.5mg/body/12週、130mg/body/12週、130.5mg/body/12週、131mg/body/12週、131.5mg/body/12週、132mg/body/12週、132.5mg/body/12週、133mg/body/12週、133.5mg/body/12週、134mg/body/12週、134.5mg/body/12週、135mg/body/12週、135.5mg/body/12週、136mg/body/12週、136.5mg/body/12週、137mg/body/12週、137.5mg/body/12週、138mg/body/12週、138.5mg/body/12週、139mg/body/12週、139.5mg/body/12週、140mg/body/12週、140.5mg/body/12週、141mg/body/12週、141.5mg/body/12週、142mg/body/12週、142.5mg/body/12週、143mg/body/12週、143.5mg/body/12週、144mg/body/12週、144.5mg/body/12週、145mg/body/12週、145.5mg/body/12週、146mg/body/12週、146.5mg/body/12週、147mg/body/12週、147.5mg/body/12週、148mg/body/12週、148.5mg/body/12週、149mg/body/12週、149.5mg/body/12週、150mg/body/12週、150.5mg/body/12週、151mg/body/12週、151.5mg/body/12週、152mg/body/12週、152.5mg/body/12週、153mg/body/12週、153.5mg/body/12週、154mg/body/12週、154.5mg/body/12週、155mg/body/12週、155.5mg/body/12週、156mg/body/12週、156.5mg/body/12週、157mg/body/12週、157.5mg/body/12週、158mg/body/12週、158.5mg/body/12週、159mg/body/12週、159.5mg/body/12週、160mg/body/12週、160.5mg/body/12週、161mg/body/12週、161.5mg/body/12週、162mg/body/12週、162.5mg/body/12週、163mg/body/12週、163.5mg/body/12週、164mg/body/12週、164.5mg/body/12週、165mg/body/12週、165.5mg/body/12週、166mg/body/12週、166.5mg/body/12週、167mg/body/12週、167.5mg/body/12週、168mg/body/12週、168.5mg/body/12週、169mg/body/12週、169.5mg/body/12週、170mg/body/12週、170.5mg/body/12週、171mg/body/12週、171.5mg/body/12週、172mg/body/12週、172.5mg/body/12週、173mg/body/12週、173.5mg/body/12週、174mg/body/12週、174.5mg/body/12週、175mg/body/12週、175.5mg/body/12週、176mg/body/12週、176.5mg/body/12週、177mg/body/12週、177.5mg/body/12週、178mg/body/12週、178.5mg/body/12週、179mg/body/12週、179.5mg/body/12週、180mg/body/12週、180.5mg/body/12週、181mg/body/12週、181.5mg/body/12週、182mg/body/12週、182.5mg/body/12週、183mg/body/12週、183.5mg/body/12週、184mg/body/12週、184.5mg/body/12週、185mg/body/12週、185.5mg/body/12週、186mg/body/12週、186.5mg/body/12週、187mg/body/12週、187.5mg/body/12週、188mg/body/12週、188.5mg/body/12週、189mg/body/12週、189.5mg/body/12週、190mg/body/12週、190.5mg/body/12週、191mg/body/12週、191.5mg/body/12週、192mg/body/12週、192.5mg/body/12週、193mg/body/12週、193.5mg/body/12週、194mg/body/12週、194.5mg/body/12週、195mg/body/12週、195.5mg/body/12週、196mg/body/12週、196.5mg/body/12週、197mg/body/12週、197.5mg/body/12週、198mg/body/12週、198.5mg/body/12週、199mg/body/12週、199.5mg/body/12週、200mg/body/12週等であってよい。
非限定的な一実施態様において、25mg~100mg/body/4週、50mg~100mg/body/4週又は50mg~75mg/body/4週であってよい。非限定的な別の実施態様において、10mg~50mg/body/2週又は20mg~40mg/body/2週であってよい。
えば、0.1mg/kg/8週、0.11mg/kg/8週、0.12mg/kg/8週、0.125mg/kg/8週、0.13mg/kg/8週、0.14mg/kg/8週、0.15mg/kg/8週、0.16mg/kg/8週、0.17mg/kg/8週、0.18mg/kg/8週、0.19mg/kg/8週、0.2mg/kg/8週、0.21mg/kg/8週、0.22mg/kg/8週、0.23mg/kg/8週、0.24mg/kg/8週、0.25mg/kg/8週、0.26mg/kg/8週、0.27mg/kg/8週、0.28mg/kg/8週、0.29mg/kg/8週、0.3mg/kg/8週、0.31mg/kg/8週、0.32mg/kg/8週、0.33mg/kg/8週、0.34mg/kg/8週、0.35mg/kg/8週、0.36mg/kg/8週、0.37mg/kg/8週、0.38mg/kg/8週、0.39mg/kg/8週、0.4mg/kg/8週、0.41mg/kg/8週、0.42mg/kg/8週、0.43mg/kg/8週、0.44mg/kg/8週、0.45mg/kg/8週、0.46mg/kg/8週、0.47mg/kg/8週、0.48mg/kg/8週、0.49mg/kg/8週、0.5mg/kg/8週、0.51mg/kg/8週、0.52mg/kg/8週、0.53mg/kg/8週、0.54mg/kg/8週、0.55mg/kg/8週、0.56mg/kg/8週、0.57mg/kg/8週、0.58mg/kg/8週、0.59mg/kg/8週、0.6mg/kg/8週、0.61mg/kg/8週、0.62mg/kg/8週、0.63mg/kg/8週、0.64mg/kg/8週、0.65mg/kg/8週、0.66mg/kg/8週、0.67mg/kg/8週、0.68mg/kg/8週、0.69mg/kg/8週、0.7mg/kg/8週、0.71mg/kg/8週、0.72mg/kg/8週、0.73mg/kg/8週、0.74mg/kg/8週、0.75mg/kg/8週、0.76mg/kg/8週、0.77mg/kg/8週、0.78mg/kg/8週、0.79mg/kg/8週、0.8mg/kg/8週、0.81mg/kg/8週、0.82mg/kg/8週、0.83mg/kg/8週、0.84mg/kg/8週、0.85mg/kg/8週、0.86mg/kg/8週、0.87mg/kg/8週、0.88mg/kg/8週、0.89mg/kg/8週、0.9mg/kg/8週、0.91mg/kg/8週、0.92mg/kg/8週、0.93mg/kg/8週、0.94mg/kg/8週、0.95mg/kg/8週、0.96mg/kg/8週、0.97mg/kg/8週、0.98mg/kg/8週、0.99mg/kg/8週、1mg/kg/8週、1.01mg/kg/8週、1.02mg/kg/8週、1.03mg/kg/8週、1.04mg/kg/8週、1.05mg/kg/8週、1.06mg/kg/8週、1.07mg/kg/8週、1.08mg/kg/8週、1.09mg/kg/8週、1.1mg/kg/8週、1.11mg/kg/8週、1.12mg/kg/8週、1.13mg/kg/8週、1.14mg/kg/8週、1.15mg/kg/8週、1.16mg/kg/8週、1.17mg/kg/8週、1.18mg/kg/8週、1.19mg/kg/8週、1.2mg/kg/8週、1.21mg/kg/8週、1.22mg/kg/8週、1.23mg/kg/8週、1.24mg/kg/8週、1.25mg/kg/8週、1.26mg/kg/8週、1.27mg/kg/8週、1.28mg/kg/8週、1.29mg/kg/8週、1.3mg/kg/8週、1.31mg/kg/8週、1.32mg/kg/8週、1.33mg/kg/8週、1.34mg/kg/8週、1.35mg/kg/8週、1.36mg/kg/8週、1.37mg/kg/8週、1.38mg/kg/8週、1.39mg/kg/8週、1.4mg/kg/8週、1.41mg/kg/8週、1.42mg/kg/8週、1.43mg/kg/8週、1.44mg/kg/8週、1.45mg/kg/8週、1.46mg/kg/8週、1.47mg/kg/8週、1.48mg/kg/8週、1.49mg/kg/8週、1.5mg/kg/8週、1.51mg/kg/8週、1.52mg/kg/8週、1.53mg/kg/8週、1.54mg/kg/8週、1.55mg/kg/8週、1.56mg/kg/8週、1.57mg/kg/8週、1.58mg/kg/8週、1.59mg/kg/8週、1.6mg/kg/8週、1.61mg/kg/8週、1.62mg/kg/8週、1.63mg/kg/8週、1.64mg/kg/8週、1.65mg/kg/8週、1.66mg/kg/8週、1.67mg/kg/8週、1.68mg/kg/8週、1.69mg/kg/8週、1.7mg/kg/8週、1.71mg/kg/8週、1.72mg/kg/8週、1.73mg/kg/8週、1.74mg/kg/8週、1.75mg/kg/8週、1.76mg/kg/8週、1.77mg/kg/8週、1.78mg/kg/8週、1.79mg/kg/8週、1.8mg/kg/8週、1.81mg/kg/8週、1.82mg/kg/8週、1.83mg/kg/8週、1.84mg/kg/8週、1.85mg/kg/8週、1.86mg/kg/8週、1.87mg/kg/8週、1.88mg/kg/8週、1.89mg/kg/8週、1.9mg/kg/8週、1.91mg/kg/8週、1.92mg/kg/8週、1.93mg/kg/8週、1.94mg/kg/8週、1.95mg/kg/8週、1.96mg/kg/8週、1.97mg/kg/8週、1.98mg/kg/8週、1.99mg/kg/8週、2mg/kg/8週、2.01mg/kg/8週、2.02mg/kg/8週、2.03mg/kg/8週、2.04mg/kg/8週、2.05mg/kg/8週、2.06mg/kg/8週、2.07mg/kg/8週、2.08mg/kg/8週、2.09mg/kg/8週、2.1mg/kg/8週、2.11mg/kg/8週、2.12mg/kg/8週、2.13mg/kg/8週、2.14mg/kg/8週、2.15mg/kg/8週、2.16mg/kg/8週、2.17mg/kg/8週、2.18mg/kg/8週、2.19mg/kg/8週、2.2mg/kg/8週、2.21mg/kg/8週、2.22mg/kg/8週、2.23mg/kg/8週、2.24mg/kg/8週、2.25mg/kg/8週、2.26mg/kg/8週、2.27mg/kg/8週、2.28mg/kg/8週、2.29mg/kg/8週、2.3mg/kg/8週、2.31mg/kg/8週、2.32mg/kg/8週、2.33mg/kg/8週、2.34mg/kg/8週、2.35mg/kg/8週、2.36mg/kg/8週、2.37mg/kg/8週、2.38mg/kg/8週、2.39mg/kg/8週、2.4mg/kg/8週、2.41mg/kg/8週、2.42mg/kg/8週、2.43mg/kg/8週、2.44mg/kg/8週、2.45mg/kg/8週、2.46mg/kg/8週、2.47mg/kg/8週、2.48mg/kg/8週、2.49mg/kg/8週、2.5mg/kg/8週、2.51mg/kg/8週、2.52mg/kg/8週、2.53mg/kg/8週、2.54mg/kg/8週、2.55mg/kg/8週、2.56mg/kg/8週、2.57mg/kg/8週、2.58mg/kg/8週、2.59mg/kg/8週、2.6mg/kg/8週、2.61mg/kg/8週、2.62mg/kg/8週、2.63mg/kg/8週、2.64mg/kg/8週、2.65mg/kg/8週、2.66mg/kg/8週、2.67mg/kg/8週、2.68mg/kg/8週、2.69mg/kg/8週、2.7mg/kg/8週、2.71mg/kg/8週、2.72mg/kg/8週、2.73mg/kg/8週、2.74mg/kg/8週、2.75mg/kg/8週、2.76mg/kg/8週、2.77mg/kg/8週、2.78mg/kg/8週、2.79mg/kg/8週、2.8mg/kg/8週、2.81mg/kg/8週、2.82mg/kg/8週、2.83mg/kg/8週、2.84mg/kg/8週、2.85mg/kg/8週、2.86mg/kg/8週、2.87mg/kg/8週、2.88mg/kg/8週、2.89mg/kg/8週、2.9mg/kg/8週、2.91mg/kg/8週、2.92mg/kg/8週、2.93mg/kg/8週、2.94mg/kg/8週、2.95mg/kg/8週、2.96mg/kg/8週、2.97mg/kg/8週、2.98mg/kg/8週、2.99mg/kg/8週、3mg/kg/8週等であってよい。あるいは、非限定的な一実施態様において、それは例えば、0.1mg/kg/10週、0.11mg/kg/10週、0.12mg/kg/10週、0.125mg/kg/10週、0.13mg/kg/10週、0.14mg/kg/10週、0.15mg/kg/10週、0.16mg/kg/10週、0.17mg/kg/10週、0.18mg/kg/10週、0.19mg/kg/10週、0.2mg/kg/10週、0.21mg/kg/10週、0.22mg/kg/10週、0.23mg/kg/10週、0.24mg/kg/10週、0.25mg/kg/10週、0.26mg/kg/10週、0.27mg/kg/10週、0.28mg/kg/10週、0.29mg/kg/10週、0.3mg/kg/10週、0.31mg/kg/10週、0.32mg/kg/10週、0.33mg/kg/10週、0.34mg/kg/10週、0.35mg/kg/10週、0.36mg/kg/10週、0.37mg/kg/10週、0.38mg/kg/10週、0.39mg/kg/10週、0.4mg/kg/10週、0.41mg/kg/10週、0.42mg/kg/10週、0.43mg/kg/10週、0.44mg/kg/10週、0.45mg/kg/10週、0.46mg/kg/10週、0.47mg/kg/10週、0.48mg/kg/10週、0.49mg/kg/10週、0.5mg/kg/10週、0.51mg/kg/10週、0.52mg/kg/10週、0.53mg/kg/10週、0.54mg/kg/10週、0.55mg/kg/10週、0.56mg/kg/10週、0.57mg/kg/10週、0.58mg/kg/10週、0.59mg/kg/10週、0.6mg/kg/10週、0.61mg/kg/10週、0.62mg/kg/10週、0.63mg/kg/10週、0.64mg/kg/10週、0.65mg/kg/10週、0.66mg/kg/10週、0.67mg/kg/10週、0.68mg/kg/10週、0.69mg/kg/10週、0.7mg/kg/10週、0.71mg/kg/10週、0.72mg/kg/10週、0.73mg/kg/10週、0.74mg/kg/10週、0.75mg/kg/10週、0.76mg/kg/10週、0.77mg/kg/10週、0.78mg/kg/10週、0.79mg/kg/10週、0.8mg/kg/10週、0.81mg/kg/10週、0.82mg/kg/10週、0.83mg/kg/10週、0.84mg/kg/10週、0.85mg/kg/10週、0.86mg/kg/10週、0.87mg/kg/10週、0.88mg/kg/10週、0.89mg/kg/10週、0.9mg/kg/10週、0.91mg/kg/10週、0.92mg/kg/10週、0.93mg/kg/10週、0.94mg/kg/10週、0.95mg/kg/10週、0.96mg/kg/10週、0.97mg/kg/10週、0.98mg/kg/10週、0.99mg/kg/10週、1mg/kg/10週、1.01mg/kg/10週、1.02mg/kg/10週、1.03mg/kg/10週、1.04mg/kg/10週、1.05mg/kg/10週、1.06mg/kg/10週、1.07mg/kg/10週、1.08mg/kg/10週、1.09mg/kg/10週、1.1mg/kg/10週、1.11mg/kg/10週、1.12mg/kg/10週、1.13mg/kg/10週、1.14mg/kg/10週、1.15mg/kg/10週、1.16mg/kg/10週、1.17mg/kg/10週、1.18mg/kg/10週、1.19mg/kg/10週、1.2mg/kg/10週、1.21mg/kg/10週、1.22mg/kg/10週、1.23mg/kg/10週、1.24mg/kg/10週、1.25mg/kg/10週、1.26mg/kg/10週、1.27mg/kg/10週、1.28mg/kg/10週、1.29mg/kg/10週、1.3mg/kg/10週、1.31mg/kg/10週、1.32mg/kg/10週、1.33mg/kg/10週、1.34mg/kg/10週、1.35mg/kg/10週、1.36mg/kg/10週、1.37mg/kg/10週、1.38mg/kg/10週、1.39mg/kg/10週、1.4mg/kg/10週、1.41mg/kg/10週、1.42mg/kg/10週、1.43mg/kg/10週、1.44mg/kg/10週、1.45mg/kg/10週、1.46mg/kg/10週、1.47mg/kg/10週、1.48mg/kg/10週、1.49mg/kg/10週、1.5mg/kg/10週、1.51mg/kg/10週、1.52mg/kg/10週、1.53mg/kg/10週、1.54mg/kg/10週、1.55mg/kg/10週、1.56mg/kg/10週、1.57mg/kg/10週、1.58mg/kg/10週、1.59mg/kg/10週、1.6mg/kg/10週、1.61mg/kg/10週、1.62mg/kg/10週、1.63mg/kg/10週、1.64mg/kg/10週、1.65mg/kg/10週、1.66mg/kg/10週、1.67mg/kg/10週、1.68mg/kg/10週、1.69mg/kg/10週、1.7mg/kg/10週、1.71mg/kg/10週、1.72mg/kg/10週、1.73mg/kg/10週、1.74mg/kg/10週、1.75mg/kg/10週、1.76mg/kg/10週、1.77mg/kg/10週、1.78mg/kg/10週、1.79mg/kg/10週、1.8mg/kg/10週、1.81mg/kg/10週、1.82mg/kg/10週、1.83mg/kg/10週、1.84mg/kg/10週、1.85mg/kg/10週、1.86mg/kg/10週、1.87mg/kg/10週、1.88mg/kg/10週、1.89mg/kg/10週、1.9mg/kg/10週、1.91mg/kg/10週、1.92mg/kg/10週、1.93mg/kg/10週、1.94mg/kg/10週、1.95mg/kg/10週、1.96mg/kg/10週、1.97mg/kg/10週、1.98mg/kg/10週、1.99mg/kg/10週、2mg/kg/10週、2.01mg/kg/10週、2.02mg/kg/10週、2.03mg/kg/10週、2.04mg/kg/10週、2.05mg/kg/10週、2.06mg/kg/10週、2.07mg/kg/10週、2.08mg/kg/10週、2.09mg/kg/10週、2.1mg/kg/10週、2.11mg/kg/10週、2.12mg/kg/10週、2.13mg/kg/10週、2.14mg/kg/10週、2.15mg/kg/10週、2.16mg/kg/10週、2.17mg/kg/10週、2.18mg/kg/10週、2.19mg/kg/10週、2.2mg/kg/10週、2.21mg/kg/10週、2.22mg/kg/10週、2.23mg/kg/10週、2.24mg/kg/10週、2.25mg/kg/10週、2.26mg/kg/10週、2.27mg/kg/10週、2.28mg/kg/10週、2.29mg/kg/10週、2.3mg/kg/10週、2.31mg/kg/10週、2.32mg/kg/10週、2.33mg/kg/10週、2.34mg/kg/10週、2.35mg/kg/10週、2.36mg/kg/10週、2.37mg/kg/10週、2.38mg/kg/10週、2.39mg/kg/10週、2.4mg/kg/10週、2.41mg/kg/10週、2.42mg/kg/10週、2.43mg/kg/10週、2.44mg/kg/10週、2.45mg/kg/10週、2.46mg/kg/10週、2.47mg/kg/10週、2.48mg/kg/10週、2.49mg/kg/10週、2.5mg/kg/10週、2.51mg/kg/10週、2.52mg/kg/10週、2.53mg/kg/10週、2.54mg/kg/10週、2.55mg/kg/10週、2.56mg/kg/10週、2.57mg/kg/10週、2.58mg/kg/10週、2.59mg/kg/10週、2.6mg/kg/10週、2.61mg/kg/10週、2.62mg/kg/10週、2.63mg/kg/10週、2.64mg/kg/10週、2.65mg/kg/10週、2.66mg/kg/10週、2.67mg/kg/10週、2.68mg/kg/10週、2.69mg/kg/10週、2.7mg/kg/10週、2.71mg/kg/10週、2.72mg/kg/10週、2.73mg/kg/10週、2.74mg/kg/10週、2.75mg/kg/10週、2.76mg/kg/10週、2.77mg/kg/10週、2.78mg/kg/10週、2.79mg/kg/10週、2.8mg/kg/10週、2.81mg/kg/10週、2.82mg/kg/10週、2.83mg/kg/10週、2.84mg/kg/10週、2.85mg/kg/10週、2.86mg/kg/10週、2.87mg/kg/10週、2.88mg/kg/10週、2.89mg/kg/10週、2.9mg/kg/10週、2.91mg/kg/10週、2.92mg/kg/10週、2.93mg/kg/10週、2.94mg/kg/10週、2.95mg/kg/10週、2.96mg/kg/10週、2.97mg/kg/10週、2.98mg/kg/10週、2.99mg/kg/10週、3mg/kg/10週等であってよい。あるいは、非限定的な一実施態様において、それは例えば、0.1mg/kg/12週、0.11mg/kg/12週、0.12mg/kg/12週、0.125mg/kg/12週、0.13mg/kg/12週、0.14mg/kg/12週、0.15mg/kg/12週、0.16mg/kg/12週、0.17mg/kg/12週、0.18mg/kg/12週、0.19mg/kg/12週、0.2mg/kg/12週、0.21mg/kg/12週、0.22mg/kg/12週、0.23mg/kg/12週、0.24mg/kg/12週、0.25mg/kg/12週、0.26mg/kg/12週、0.27mg/kg/12週、0.28mg/kg/12週、0.29mg/kg/12週、0.3mg/kg/12週、0.31mg/kg/12週、0.32mg/kg/12週、0.33mg/kg/12週、0.34mg/kg/12週、0.35mg/kg/12週、0.36mg/kg/12週、0.37mg/kg/12週、0.38mg/kg/12週、0.39mg/kg/12週、0.4mg/kg/12週、0.41mg/kg/12週、0.42mg/kg/12週、0.43mg/kg/12週、0.44mg/kg/12週、0.45mg/kg/12週、0.46mg/kg/12週、0.47mg/kg/12週、0.48mg/kg/12週、0.49mg/kg/12週、0.5mg/kg/12週、0.51mg/kg/12週、0.52mg/kg/12週、0.53mg/kg/12週、0.54mg/kg/12週、0.55mg/kg/12週、0.56mg/kg/12週、0.57mg/kg/12週、0.58mg/kg/12週、0.59mg/kg/12週、0.6mg/kg/12週、0.61mg/kg/12週、0.62mg/kg/12週、0.63mg/kg/12週、0.64mg/kg/12週、0.65mg/kg/12週、0.66mg/kg/12週、0.67mg/kg/12週、0.68mg/kg/12週、0.69mg/kg/12週、0.7mg/kg/12週、0.71mg/kg/12週、0.72mg/kg/12週、0.73mg/kg/12週、0.74mg/kg/12週、0.75mg/kg/12週、0.76mg/kg/12週、0.77mg/kg/12週、0.78mg/kg/12週、0.7
9mg/kg/12週、0.8mg/kg/12週、0.81mg/kg/12週、0.82mg/kg/12週、0.83mg/kg/12週、0.84mg/kg/12週、0.85mg/kg/12週、0.86mg/kg/12週、0.87mg/kg/12週、0.88mg/kg/12週、0.89mg/kg/12週、0.9mg/kg/12週、0.91mg/kg/12週、0.92mg/kg/12週、0.93mg/kg/12週、0.94mg/kg/12週、0.95mg/kg/12週、0.96mg/kg/12週、0.97mg/kg/12週、0.98mg/kg/12週、0.99mg/kg/12週、1mg/kg/12週、1.01mg/kg/12週、1.02mg/kg/12週、1.03mg/kg/12週、1.04mg/kg/12週、1.05mg/kg/12週、1.06mg/kg/12週、1.07mg/kg/12週、1.08mg/kg/12週、1.09mg/kg/12週、1.1mg/kg/12週、1.11mg/kg/12週、1.12mg/kg/12週、1.13mg/kg/12週、1.14mg/kg/12週、1.15mg/kg/12週、1.16mg/kg/12週、1.17mg/kg/12週、1.18mg/kg/12週、1.19mg/kg/12週、1.2mg/kg/12週、1.21mg/kg/12週、1.22mg/kg/12週、1.23mg/kg/12週、1.24mg/kg/12週、1.25mg/kg/12週、1.26mg/kg/12週、1.27mg/kg/12週、1.28mg/kg/12週、1.29mg/kg/12週、1.3mg/kg/12週、1.31mg/kg/12週、1.32mg/kg/12週、1.33mg/kg/12週、1.34mg/kg/12週、1.35mg/kg/12週、1.36mg/kg/12週、1.37mg/kg/12週、1.38mg/kg/12週、1.39mg/kg/12週、1.4mg/kg/12週、1.41mg/kg/12週、1.42mg/kg/12週、1.43mg/kg/12週、1.44mg/kg/12週、1.45mg/kg/12週、1.46mg/kg/12週、1.47mg/kg/12週、1.48mg/kg/12週、1.49mg/kg/12週、1.5mg/kg/12週、1.51mg/kg/12週、1.52mg/kg/12週、1.53mg/kg/12週、1.54mg/kg/12週、1.55mg/kg/12週、1.56mg/kg/12週、1.57mg/kg/12週、1.58mg/kg/12週、1.59mg/kg/12週、1.6mg/kg/12週、1.61mg/kg/12週、1.62mg/kg/12週、1.63mg/kg/12週、1.64mg/kg/12週、1.65mg/kg/12週、1.66mg/kg/12週、1.67mg/kg/12週、1.68mg/kg/12週、1.69mg/kg/12週、1.7mg/kg/12週、1.71mg/kg/12週、1.72mg/kg/12週、1.73mg/kg/12週、1.74mg/kg/12週、1.75mg/kg/12週、1.76mg/kg/12週、1.77mg/kg/12週、1.78mg/kg/12週、1.79mg/kg/12週、1.8mg/kg/12週、1.81mg/kg/12週、1.82mg/kg/12週、1.83mg/kg/12週、1.84mg/kg/12週、1.85mg/kg/12週、1.86mg/kg/12週、1.87mg/kg/12週、1.88mg/kg/12週、1.89mg/kg/12週、1.9mg/kg/12週、1.91mg/kg/12週、1.92mg/kg/12週、1.93mg/kg/12週、1.94mg/kg/12週、1.95mg/kg/12週、1.96mg/kg/12週、1.97mg/kg/12週、1.98mg/kg/12週、1.99mg/kg/12週、2mg/kg/12週、2.01mg/kg/12週、2.02mg/kg/12週、2.03mg/kg/12週、2.04mg/kg/12週、2.05mg/kg/12週、2.06mg/kg/12週、2.07mg/kg/12週、2.08mg/kg/12週、2.09mg/kg/12週、2.1mg/kg/12週、2.11mg/kg/12週、2.12mg/kg/12週、2.13mg/kg/12週、2.14mg/kg/12週、2.15mg/kg/12週、2.16mg/kg/12週、2.17mg/kg/12週、2.18mg/kg/12週、2.19mg/kg/12週、2.2mg/kg/12週、2.21mg/kg/12週、2.22mg/kg/12週、2.23mg/kg/12週、2.24mg/kg/12週、2.25mg/kg/12週、2.26mg/kg/12週、2.27mg/kg/12週、2.28mg/kg/12週、2.29mg/kg/12週、2.3mg/kg/12週、2.31mg/kg/12週、2.32mg/kg/12週、2.33mg/kg/12週、2.34mg/kg/12週、2.35mg/kg/12週、2.36mg/kg/12週、2.37mg/kg/12週、2.38mg/kg/12週、2.39mg/kg/12週、2.4mg/kg/12週、2.41mg/kg/12週、2.42mg/kg/12週、2.43mg/kg/12週、2.44mg/kg/12週、2.45mg/kg/12週、2.46mg/kg/12週、2.47mg/kg/12週、2.48mg/kg/12週、2.49mg/kg/12週、2.5mg/kg/12週、2.51mg/kg/12週、2.52mg/kg/12週、2.53mg/kg/12週、2.54mg/kg/12週、2.55mg/kg/12週、2.56mg/kg/12週、2.57mg/kg/12週、2.58mg/kg/12週、2.59mg/kg/12週、2.6mg/kg/12週、2.61mg/kg/12週、2.62mg/kg/12週、2.63mg/kg/12週、2.64mg/kg/12週、2.65mg/kg/12週、2.66mg/kg/12週、2.67mg/kg/12週、2.68mg/kg/12週、2.69mg/kg/12週、2.7mg/kg/12週、2.71mg/kg/12週、2.72mg/kg/12週、2.73mg/kg/12週、2.74mg/kg/12週、2.75mg/kg/12週、2.76mg/kg/12週、2.77mg/kg/12週、2.78mg/kg/12週、2.79mg/kg/12週、2.8mg/kg/12週、2.81mg/kg/12週、2.82mg/kg/12週、2.83mg/kg/12週、2.84mg/kg/12週、2.85mg/kg/12週、2.86mg/kg/12週、2.87mg/kg/12週、2.88mg/kg/12週、2.89mg/kg/12週、2.9mg/kg/12週、2.91mg/kg/12週、2.92mg/kg/12週、2.93mg/kg/12週、2.94mg/kg/12週、2.95mg/kg/12週、2.96mg/kg/12週、2.97mg/kg/12週、2.98mg/kg/12週、2.99mg/kg/12週、3mg/kg/12週等であってよい。
かかる場合、前記IL-31アンタゴニストは、0.1mg~1000mg/body/1日~12週、好ましくは、0.1mg~1000mg/body/2週、0.1mg~1000mg/body/4週、又は、0.1mg~1000mg/body/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与されてもよい。あるいは、前記IL-31アンタゴニストは、0.01mg~10mg/kg/1日~12週、好ましくは、0.01mg~10mg/kg/2週、0.01mg~10mg/kg/4週、又は、0.01mg~10mg/kg/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与されてもよい。また、前記IL-31アンタゴニストは、血清中のIL-31濃度が所定の値以上である、透析そう痒症に罹患した、又は、罹患している恐れのある対象に投与されてもよい。
特定の実施態様において、本開示の予防及び/又は治療方法は、IL-31アンタゴニストを投与する前に、対象から得られた血清中のIL-31濃度が所定の値以上である対象を、予防/治療の対象として選択することをさらに含んでよい。すなわち本開示は、対象から得られた血清中のIL-31濃度が所定の値以上である対象を選択することと、選択された対象にIL-31アンタゴニストを投与することとを含む、透析そう痒症の予防及び/又は治療方法を提供する。本開示のこの実施態様は、前記選択することの前に、透析そう痒症に罹患した、又は、罹患している恐れのある対象から得られた血清中のIL-31濃度を測定することをさらに含んでもよい。あるいは本開示は、透析そう痒症に罹患した、又は、罹患している恐れのある対象から得られた血清中のIL-31濃度を測定すること;当該IL-31濃度が所定の値以上である対象をIL-31アンタゴニストによる予防及び/又は治療に対する応答者であると判定すること;ならびに、応答者であると判定された対象にIL-31アンタゴニストを投与することを含む、透析そう痒症の予防及び/又は治療方法を提供してよい。あるいは、前述の実施態様では、あらかじめ血清中のIL-31濃度が測定された透析そう痒症に罹患した、又は、罹患している恐れのある対象に対して、当該IL-31濃度が所定の値以上である対象をIL-31アンタゴニストによる予防及び/又は治療に対する応答者であると判定してもよい。
抗ヒトIL-31RA抗体の調製
抗ヒトIL-31RA抗体であるCIM331(ネモリズマブ(nemolizumab))(H鎖:配列番号:9;L鎖:配列番号:10のアミノ酸配列で特定される)を、前記特許文献の記載に従って、当業者公知の方法で作製した。WO2010/064697にも記載の通り、CIM331はヒトIL-31RA及びカニクイザルIL-31RAに対して中和活性を有する。
CIM331の臨床試験に先立つ非臨床試験に関連して、特筆すべき重大な事実が見出された。すなわち、CIM331の、マウス、ラット、ウサギの各IL-31RAとの抗原-抗体相互作用を当業者公知の方法を用いてBiacore(Biacore T100 (GE Healthcare))で評価した。その結果、CIM331はマウス、ラット、ウサギのIL-31RAに交差反応性を示さないことが判明した(Sakurai T, Esaki K. Cross-reactivity of CH5427227 with NR10 (IL-31RA) from mice, rats and rabbits (Study No. TOX08-0198S). Chugai Pharmaceutical Co., Ltd. In-house report, 2010.)。
したがって、CIM331のヒトにおける投与量と投与間隔に関する後述する効果としては、当業者といえども、CIM331を実際にヒトに投与して確認するか、あるいは、交差反応性を示すヒトモデル(例えば、カニクイザル)に投与した上でその結果をヒトに対して外挿することで効果を予測しなければならなかった。
カニクイザルにおけるIL-31誘発そう痒に対するCIM331皮下投与の抑制効果
カニクイザルにカニクイザルIL-31を静脈内投与して誘発されるそう痒に対するCIM331皮下投与の影響を検討した。そう痒に対する反応性の指標として、そう痒行動回数を測定した。そう痒行動回数は、ビデオカメラにて記録したサルの行動(2時間)を目視で観察し、前肢又は後肢で体の一部を引っ掻く動作をそう痒行動1回として計測した。ただし、1回及び2回で終了するそう痒行動は偶発的なものであると考え、そう痒行動の回数から除外した。
まずCIM331投与前に、カニクイザルIL-31非投与時の個体行動をビデオカメラで撮影した(2時間)。その後、ビデオ再生により観察し、上記の方法を用いてカニクイザルIL-31非投与時のそう痒行動回数を測定した。
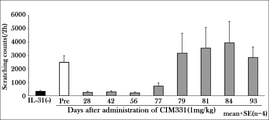
カニクイザルにCIM331 0.2又は1 mg/kgを単回皮下投与し、以下のようにカニクイザルIL-31投与後のそう痒行動回数の測定を行い、CIM331皮下投与の影響を評価した。カニクイザルに0.2 mg/kgのCIM331を単回皮下投与し、CIM331皮下投与前及び皮下投与後3, 15, 28, 42, 56, 93日後に1 μg/kgのカニクイザルIL-31を静脈内投与した。カニクイザルIL-31投与後、ビデオカメラを用いて個体行動を撮影した(2時間)。同様に、カニクイザルに1 mg/kgのCIM331を単回皮下投与し、CIM331皮下投与前及び皮下投与後28, 42, 56, 77, 79, 81, 84, 93日後に1 μg/kgのカニクイザルIL-31を静脈内投与した。カニクイザルIL-31投与後、ビデオカメラを用いて個体行動を撮影した(2時間)。その後、ビデオ再生により観察し、前述の方法を用いて、カニクイザルIL-31投与後のそう痒行動回数を測定した。
カニクイザルに0.2 mg/kgのCIM331を単回皮下投与することにより、CIM331の投与前に比較し、CIM331投与3日後の評価においてカニクイザルIL-31投与後のそう痒行動回数の平均値の減少が認められ、42日後においてもカニクイザルIL-31投与後のそう痒行動回数の平均値の減少が認められた(図6)。また1 mg/kgのCIM331単回皮下投与ではCIM331投与77日後においても、カニクイザルIL-31投与後のそう痒行動回数の平均値の減少が認められた(図7)。
アトピー性皮膚炎患者を対象とした単回皮下投与
第I相単回投与試験の被験薬群において、以下の基準に合致するアトピー性皮膚炎患者36名に対して、体重あたりCIM331投与量0.3 mg/kg、1 mg/kg、3 mg/kgあるいはプラセボのいずれかを、1群あたり9名に対してそれぞれ、腹部に単回で皮下投与した。
CIM331を投与する対象患者としては、外用ステロイド剤による治療を12週以上継続して実施しているにも関わらず以下の基準を満たすアトピー性皮膚炎患者を選択した。
・Eczema Area Severity Indexが10以上、かつ強い炎症を伴う皮疹が体表面積の5%以上
・白取の重症度分類に基づいた日中及び夜間の痒みの程度の評価の合計が4以上
・そう痒VAS平均値≧50mm
なお、治験薬は、1 mL中に100 mgのCIM331抗体を含有する液1 mLを充填したもの、あるいは希釈により目的の投与濃度にしたものを用いた。プラセボは生理食塩水を用いた。
そう痒の強さの評価は、Visual Analog Scale (VAS)により行った。VASは100 mmの直線で、0 mmを痒みなし、100 mmを患者がアトピー性皮膚炎で過去に経験した最も強い痒みとした場合に、起床時及び就寝時におけるかゆみの強さを患者自身が0~100 mmの間に線で示すものである。患者は試験期間中毎日記録を行った。
その結果、プラセボ群では20%程度の低下でVASが推移したのに対し、CIM331投与群ではいずれの用量群においても投与1週後からVASが低下し、投与4週後以降も50%程度の低下が維持された(図1)。
Eczema Area Severity Index(EASI)スコアは、アトピー性皮膚炎の重症度及び範囲を測定するためのツールである。代表的な患部の湿疹の程度及び占める割合を、頭頸部、上肢、体幹及び下肢の4領域のそれぞれについて、発赤(紅斑)、厚さ(硬結、丘疹、浮腫)、ひっかき傷(掻破痕)及び苔癬化の程度を、なし(0)、軽度(1)、中等度(2)、高度(3)で評価した。治験期間中、1週間又は2週間に1回の頻度で医師が判定を行った。投与4週後時点のベースラインからのEASIスコアの平均変化量を、投与4週後におけるそう痒VASスコアの減少率別(すなわち、減少率が50%未満の群と、50%以上の群)に解析した。
その結果、そう痒VASスコアの減少率が50%以上の群では、EASIスコアの平均変化量は-11.5ポイントであり、50%未満の群又はプラセボ群と比較した場合に、EASIスコアの減少量が大きかった(図2)。
(3-3-1)睡眠
Actiwatch(登録商標)は、手首に装着し、全身の動きの指標となる手首の動きを自由行動下で捕捉し、記録及び保存するように設計された非侵襲型測定機器である。投与4週後(Week 4)まで被験者はこの機器を装着した。入眠から覚醒までの実際の時間、睡眠潜時、睡眠効率を含むその他のパラメータを客観的な方法で測定した。睡眠効率は以下の式で算出した。
(3-3-2)DLQI
Dermatology Life Quality Indexは、皮膚科用のQOL評価ツールDLQI(Finlay et al. 1994)であり、10の質問で構成される。DLQIの質問は以下の6項目に分けられる:症状・感情、日常活動、余暇、労働・学校、人間関係、治療。全質問項目のスコアを合計してDLQIを求める。最大は30、最小は0である。スコアが高いほどQOLが低下している。
患者は2週毎あるいは4週毎に記録を行った。その結果、投与4週後における変化はプラセボ群では平均0.7ポイントの低下であったのに対し、CIM331群では平均5.4-6.3ポイントの低下が認められた。
外用ステロイド(ロコイド(登録商標);ヒドロコルチゾン酪酸エステル)はいずれの患者でも併用した。また、外用ステロイドの使用量は、患者の状態により適宜増減可能とした。
その結果、ロコイドの使用量は、プラセボ投与群では増加傾向であったのに対して、CIM331投与群ではいずれの用量群においても投与1週後から減少傾向を示した(図4)。
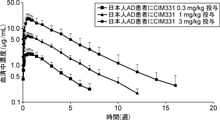
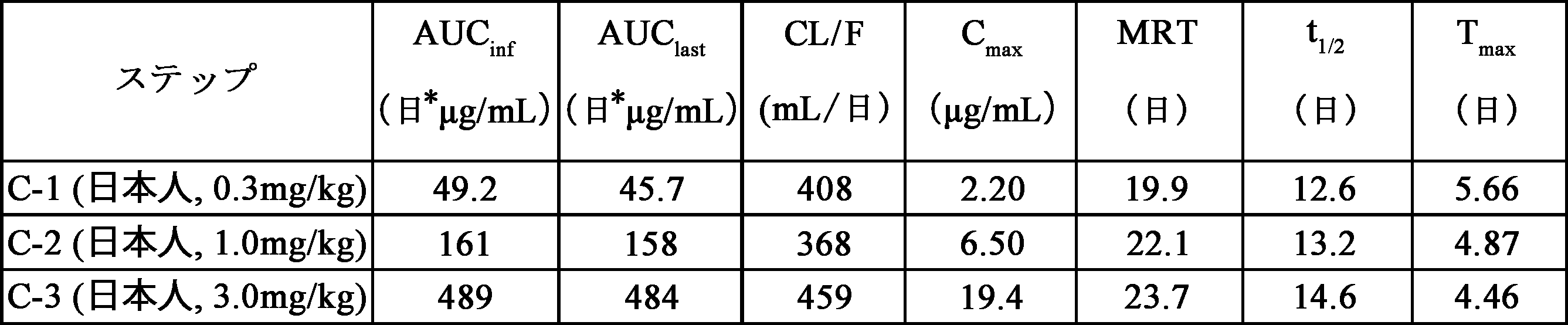
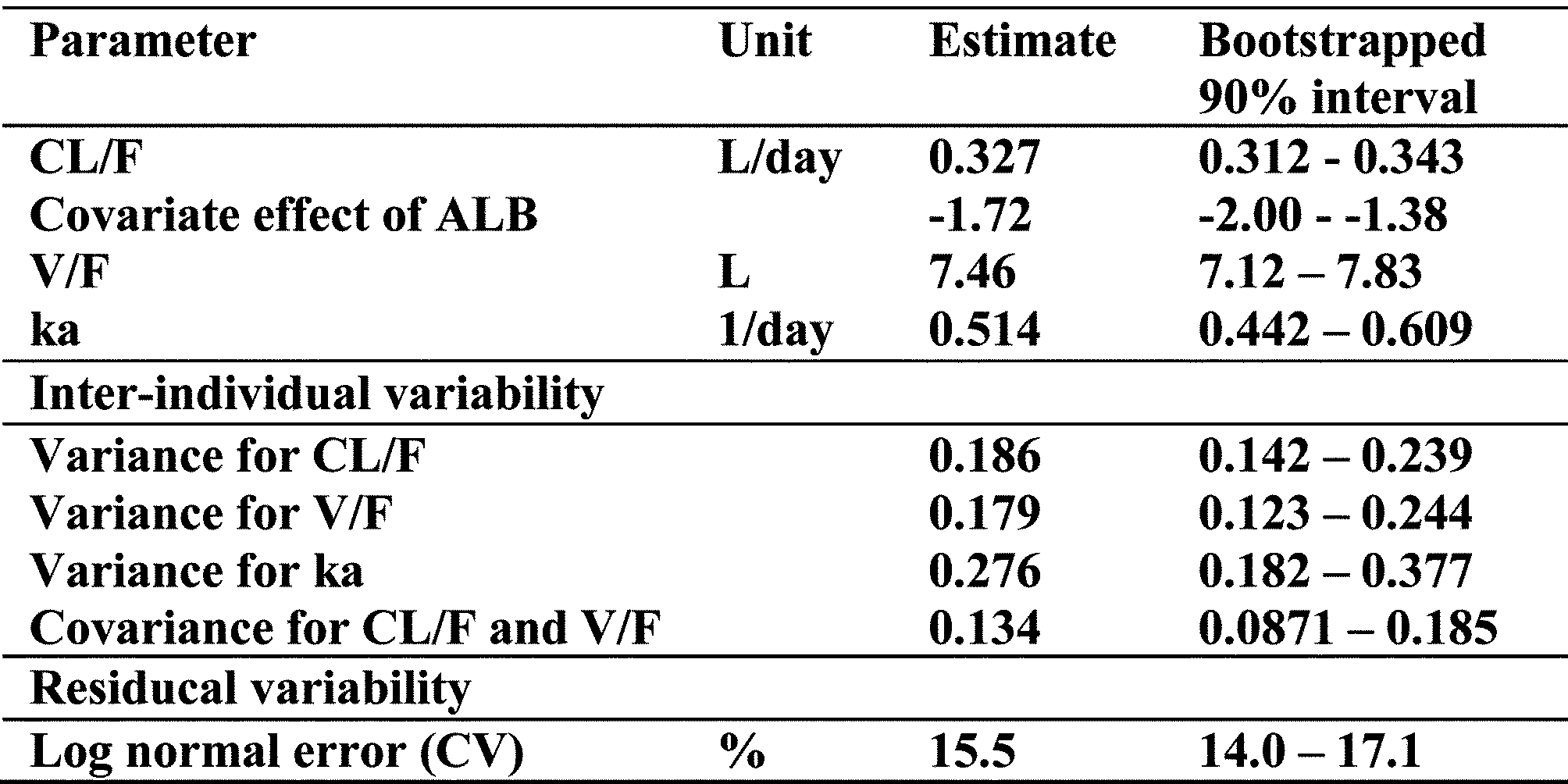
日本人アトピー性皮膚炎患者の血清中CIM331濃度の推移を図5に、薬物動態パラメータ値を表1に示す。
なお、表中、各用語はそれぞれ以下を意味する。
AUCinf: 時間0から無限時間まで外挿したAUC
AUClast: 時間0から血漿中濃度定量可能最終時点までのAUC
CL/F: みかけのクリアランス
Cmax: 最高血中濃度
MRT: 平均滞留時間
t1/2: 消失半減期
Tmax: 最高血中濃度到達時間
これらの結果により、CIM331は、アトピー性皮膚炎患者のそう痒、皮膚炎、及びQOLを改善したことが見出された。本試験は、IL-31アンタゴニストがアトピー性皮膚炎によって生じるそう痒に対して有効であることを示した初の臨床試験成績報告である。これにより、CIM331が、Itch Scratch Cycleの遮断という新しい作用機序に基づき、アトピー性皮膚によって生じるそう痒のみならず、皮膚炎及びQOLの改善をももたらし得ることが期待できる。なお、そう痒を伴うそう破は、皮疹を悪化させる増悪因子であることが知られており、そう破により皮膚が機械的障害を受けてバリア機能が低下し、表皮を通過して侵入した外来抗原により炎症反応が増強され、皮膚炎の悪化及びそう痒の増悪をきたす。このようなそう破-皮膚炎悪化-そう痒悪化の悪循環は、Itch Scratch Cycleとして知られている(例えば、Wahlgren CF et al. J Allergy Clin Immunol 2006;118:178-89)。
アトピー性皮膚炎患者を対象とした反復皮下投与
(4-1)第II相反復投与試験
第II相反復投与試験の被験薬群において、外用治療に効果不十分もしくは忍容性のない、中等症及び重症のアトピー性皮膚炎患者約250名を対象に、以下の要領でCIM331又はプラセボのいずれかを腹部に皮下投与する。CIM331の体重あたりの投与量及び投与液濃度は以下の通りとし、体重あたり20μL/kgの液量でゆっくりと投与する。被験者の体重が120kgを超える場合には体重を120 kgとして治験薬を調製する。なお、治験薬は、1 mL中に100 mgのCIM331抗体を含有する液を1バイアルにつき1.53 mL充填し凍結乾燥させた製剤を、注射用水で溶解して投与液とし、別に溶解させたプラセボ溶液を使用してさらに希釈して目的の投与濃度にする。
・Eczema Area Severity Indexが10以上
・sIGAスコアが3以上
・そう痒VAS≧50mm
Part A
・CIM331(0.1 mg/kg)、4週間ごとに皮下投与(Day 1、Week 4及びWeek 8に投与)
・CIM331(0.5 mg/kg)、4週間ごとに皮下投与(Day 1、Week 4及びWeek 8に投与)
・CIM331(2.0 mg/kg)、4週間ごとに皮下投与(Day 1、Week 4及びWeek 8に投与)
・CIM331(2.0 mg/kg)、8週間ごとに皮下投与(Day 1及びWeek 8に投与、さらにWeek 4にプラセボを投与)
・プラセボを4週間ごとに皮下投与(Day 1、Week 4及びWeek 8に投与)
より具体的には、Part Aにおいて、治験薬あるいはプラセボの投与を1回以上受けた患者は264例で、プラセボ、0.1mg/kg、0.5mg/kg、2.0mg/kgの4週間ごとに皮下投与する群、及び2.0mg/kgを8週間ごとに皮下投与する群で、それぞれ53例、53例、54例、52例及び52例であった。
Part B
Part Aでプラセボ群に割り付けられた被験者は、Part BにおいてCIM331(0.1 mg/kg、0.5 mg/kg、2.0 mg/kg)を4週間ごとに皮下投与する群に再度ランダムに割り付けられる。
Part Aで被験薬群にランダムに割り付けられた被験者は、Part Aと同じ用量群に再度割り付けられ、Week 12以降も同じ治療を継続する。
・CIM331(0.1 mg/kg)、4週間ごとに皮下投与、計52週間
・CIM331(0.5 mg/kg)、4週間ごとに皮下投与、計52週間
・CIM331(2.0 mg/kg)、4週間ごとに皮下投与、計52週間
・CIM331(2.0 mg/kg)、8週間ごとに皮下投与、計52週間(この群の被験者にはCIM331とプラセボを4週毎に交互に投与する。)
そう痒VAS又は皮膚症状の改善が認められない被験者に対し、初回投与4週以後は医師の判断で外用薬を救済治療として使用することを認める。「改善が認められない」の定義は、(1)ベースライン時からsIGAスコアに改善が認められない、
(2)sIGAスコアが3以上、
(3)ベースライン時からのそう痒VAS改善率が10%未満、直近のそう痒VAS が50 mm以上
のすべてを満たす場合とする。
・そう痒の強さの評価は、Visual Analog Scale (VAS)(Furue et al.2013)により行う。VASは100 mmの直線で、0 mmを痒みなし、100 mmを想像され得る最悪の痒みとした場合に、過去24時間におけるかゆみの強さを患者自身が0~100 mmの間に線で示すものである。
・そう痒Verbal rating scale(VRS)は、かゆみなし(0)、軽いかゆみ(1)、中等度のかゆみ(2)、ひどいかゆみ(3)、又は、非常にひどいかゆみ(4)の5段階のVRS(Reich et al. 2012)で過去24時間中のそう痒の程度を被験者が評価する。
・Eczema Area Severity Index(EASI)スコアは、アトピー性皮膚炎の重症度及び範囲を測定するためのツールである。代表的な患部の湿疹の程度及び占める割合を、頭頸部、上肢、体幹及び下肢の4領域のそれぞれについて、発赤(紅斑)、厚さ(硬結、丘疹、浮腫)、ひっかき傷(掻破痕)及び苔癬化の程度を、なし(0)、軽度(1)、中等度(2)、高度(3)で評価する。
・SCORing Atopic dermatitis(SCORAD)は湿疹の範囲及び重症度を評価するための臨床ツールである(European Task Force on Atopic Dermatitis 1993)。
・static Investigator's Global Assessment (sIGA)は、clear からvery severe disease までの6段階(0 = clear, 1 = almost clear, 2 = mild disease, 3= moderate disease, 4 = severe disease, 5 = very severe disease)で、紅斑,浸潤,丘疹,滲出及び痂皮の臨床特性を用いて、評価時点の総合的な重症度を評価する。
・アトピー性皮膚炎病変部のBody surface area(BSA)は全身のうち病変部の占める割合を示す。
・睡眠障害VASは、「睡眠の問題なし」(0)から「全く眠ることができなかった」(10)までのVAS(Furue et al. 2013)で過去24時間中の睡眠障害の程度を被験者が評価する。
・Dermatology Life Quality Indexは、皮膚科用のQOL評価ツールDLQI(Finlay et al. 1994)であり、10の質問で構成される。DLQIの質問は以下の6項目に分けられる:
症状・感情、日常活動、余暇、労働・学校、人間関係、治療。全質問項目のスコアを合計してDLQIを求める。最大は30,最小は0である。スコアが高いほどQOLが低下している。
・アクティグラフィ
Actiwatchは、手首に装着し、全身の動きの指標となる手首の動きを自由行動下で捕捉し、記録及び保存するように設計された非侵襲型測定機器である。前観察期間開始時からWeek 4まで被験者はこの機器を装着する。入眠から覚醒までの実際の時間、睡眠潜時,睡眠効率を含むその他のパラメータを客観的な方法で測定する。
CIM331を4週間ごとに皮下投与する群において、主要評価項目は、投与開始12週後のそう痒VASの投与開始時と比較した改善率とし、4週間に1回CIM331投与の各用量群のプラセボに対する優越性・有効性を確認する。主要な解析方法としては、共分散分析(Analysis of covariance,ANCOVA)を用いる。具体的には、投与開始12週後のそう痒VASの投与開始時と比較した改善率を応答変数とし、治療群を固定効果、投与開始時のそう痒VAS及び地域(日本、欧州、米国)を共変量としたモデルをあてはめる。主要解析では、検定の有意水準は片側0.025を用い、閉検定手順の原理に基づいて高用量から逐次的に2群比較を行うことで、検定の繰り返しによる多重性を考慮する。主要な解析対象集団として、治験実施計画書からの重大な逸脱が認められた被験者の一部、早期に治験を中止した被験者、及び割付けと異なる治験薬を投与された被験者等を除いたper-protocol(PP)集団を用いる。救済治療を受けた後に測定したデータをすべて除外し、欠損値をLOCF(Last Observation value Carrying Forward after baseline)により補完する。
4週間ごとの投与群において、主要評価項目である、投与開始12週後のそう痒VASの開始時からの改善率(最小二乗平均)のプラセボとの差は、0.1mg/kg、0.5mg/kg、2.0mg/kgでそれぞれ-21.39%(p=0.0027)、-41.16%(p<0.0001)、-40.39%(p<0.0001)であった。
また、本事例は探索的な用量設定試験であるため、主要な解析以外にも副次的な解析を実施し、総合的に投与量を検討することができる。その際は、探索的な検討ではあるものの、検定の有意水準は片側0.025を目安とする。限定は意図しないが、具体的には,ANCOVA以外に、Mixed-effects model repeated measures approach(MMRM)の利用や、モデルに依らない要約統計量の集計、治験薬投与後の規定観測時点で得られる利用可能なすべてのデータを用いたIntent-to-Treat(ITT)解析対象集団の利用、救済治療を受けた後に測定したデータの利用、あるいは欠損値を補完しない解析の結果を適宜確認し、包括的に検討してよい。また、そう痒VASに対して、投与開始12週後以外の時点の利用、あるいは、投与開始時と比較した改善率に対応する変化量または各時点の値を利用して、それらの連続量またはある閾値を基準とした改善した症例の割合を応答変数としたモデル解析も評価対象としてよい。このような解析に対し、重要な部分集団を考慮することができる。そう痒VAS以外の副次的有効性評価項目も同様に解析してよい。
CIM331を8週間ごとに皮下投与する群についても同様に探索的な比較を行うことができる。
項目ごとにベースライン時から各時点までに25%,50%及び75%の改善を認めた被験者の割合を算出する。
Part Aの4週間ごとの投与群における結果は、PP集団において救済治療を受けた後に測定したデータを全て除外し欠損値をLOCFして補完した場合、投与開始12週後においてそう痒VASの50%の改善を認めた被験者の割合は、プラセボ群で21%であった一方、0.1mg/kg群、0.5mg/kg群、2.0mg/kg群でそれぞれ41%、67%、59%であった。75%の改善を認めた被験者の割合は、プラセボ群で12%であった一方、0.1mg/kg群、0.5mg/kg群、2.0mg/kg群でそれぞれ14%、49%、44%であった。
同様に、投与開始12週後においてEASIの50%の改善を認めた被験者の割合は、プラセボ群で33%であった一方、0.1mg/kg群、0.5mg/kg群、2.0mg/kg群でそれぞれ43%、51%、41%であった。75%の改善を認めた被験者の割合は、プラセボ群で14%であった一方、0.1mg/kg群、0.5mg/kg群、2.0mg/kg群でそれぞれ23%、37%、22%であった。
投与開始12週後においてSCORADの50%の改善を認めた被験者の割合は、プラセボ群で15%であった一方、0.1mg/kg群、0.5mg/kg群、2.0mg/kg群でそれぞれ18%、39%、31%であった。75%の改善を認めた被験者の割合は、プラセボ群で3%であった一方、0.1mg/kg群、0.5mg/kg群、2.0mg/kg群でそれぞれ0%、15%、17%であった。
各項目のベースライン時から各時点までに2点以上改善した被験者の割合を算出する。
Part Aの4週間ごとの投与群における結果は、投与開始12週後において、sIGAが2点以上改善した被験者の割合は、プラセボ群で12%であった一方、0.1mg/kg群、0.5mg/kg群、2.0mg/kg群でそれぞれ21%、30%、22%であった。
投与開始12週後において、そう痒VRSが2点以上改善した被験者の割合は、プラセボ群で5%であった一方、0.1mg/kg群、0.5mg/kg群、2.0mg/kg群でそれぞれ14%、47%、30%であった。
各項目のベースライン時から各時点までの改善度を記述統計により要約する。
Part Aの4週間ごとの投与群における結果は、PP集団で救済治療を受けた後に測定したデータを全て除外した場合、そう痒VASの改善率は、投与4週後でプラセボ群で12%であった一方、0.1mg/kg群で39%、0.5mg/kg群で55%、2.0mg/kg群で46%の改善を示した。投与12週後ではプラセボ群で24%であった一方、0.1mg/kg群で47%、0.5mg/kg群で68%、2.0mg/kg群で67%の改善率であった。
同様に、EASIの投与12週後の改善率はプラセボ群38%に対し、0.1mg/kg群で34%、0.5mg/kg群で54%、2.0mg/kg群で48%であった。SCORADの投与12週後の改善率は、プラセボ群22%に対し、0.1mg/kg群で37%、0.5mg/kg群で45%、2.0mg/kg群で47%であった。sIGAの投与12週後の改善率はプラセボ群13%に対し、0.1mg/kg群で25%、0.5mg/kg群で34%、2.0mg/kg群で28%であった。BSAの投与12週後の改善率はプラセボ群31%に対し、0.1mg/kg群で25%、0.5mg/kg群で26%、2.0mg/kg群で33%であった。そう痒VRSの投与12週後の改善率はプラセボ群18%に対し、0.1mg/kg群で42%、0.5mg/kg群で58%、2.0mg/kg群で58%であった。睡眠障害VASの投与12週後の改善率はプラセボ群31%に対し、0.1mg/kg群で57%、0.5mg/kg群で65%、2.0mg/kg群で67%であった。
そう痒VAS、EASI及びSCORADにおいて、ベースライン時から25%、50%、75%改善に達するまでの時間、並びに、sIGAにおいてベースライン時から2点改善するまでの時間をKaplan-Meier推定値を用いて経時的な累積発生率として要約する。
Part Aの4週間ごとの投与群における結果は、そう痒VASにおいて、50%の患者がベースライン時から25%、50%、75%改善に達するまでの時間はプラセボ群でそれぞれ11週間、達成せず、達成せずであった一方、0.1mg/kg群でそれぞれ2週間、4週間、達成せず、0.5mg/kg群でそれぞれ2週間、2週間、5週間、2.0mg/kg群でそれぞれ2週間、4週間、達成せずであった。また、Kaplan-Meier推定値を用いた投与開始後12週におけるベースライン時から25%、50%、75%改善の達成率は、プラセボ群でそれぞれ52%、38%、22%であった一方、0.1mg/kg群でそれぞれ84%、66%、38%、0.5mg/kg群でそれぞれ95%、80%、68%、2.0mg/kg群でそれぞれ94%、71%、48%であった。
同様に、EASIにおいて、50%の患者がベースライン時から25%、50%、75%改善に達するまでの時間はプラセボ群でそれぞれ6週間、12週間、達成せずであった一方、0.1mg/kg群でそれぞれ2週間、4週間、達成せず、0.5mg/kg群でそれぞれ2週間、4週間、12週間、2.0mg/kg群でそれぞれ2週間、6週間、達成せずであった。また,Kaplan-Meier推定値を用いた投与開始後12週後におけるベースライン時から25%、50%、75%改善の達成率は、プラセボ群でそれぞれ68%、51%、23%であった一方、0.1mg/kg群でそれぞれ71%、66%、37%、0.5mg/kg群でそれぞれ84%、73%、53%、2.0mg/kg群でそれぞれ93%、67%、28%であった。
SCORADにおいて、50%の患者がベースライン時から25%、50%、75%改善に達するまでの時間はプラセボ群でそれぞれ6週間、達成せず、達成せずであった一方、0.1mg/kg群でそれぞれ2週間、達成せず、達成せず、0.5mg/kg群でそれぞれ3週間、10週間、達成せず、2.0mg/kg群でそれぞれ2週間、達成せず、達成せずであった。また、Kaplan-Meier推定値を用いた投与開始後12週後におけるベースライン時から25%、50%、75%改善の達成率は、プラセボ群でそれぞれ57%、40%、6%であった一方、0.1mg/kg群でそれぞれ78%、46%、9%、0.5mg/kg群でそれぞれ78%、55%、30%、2.0mg/kg群でそれぞれNE(算出できず)、46%、25%であった。
sIGAにおいて、50%の患者がベースライン時から2点改善するまでの時間はプラセボ群、0.1mg/kg群、0.5mg/kg群及び2.0mg/kg群のいずれも12週後までに達成されなかった。また、Kaplan-Meier推定値を用いた投与開始後12週後におけるベースライン時から2点改善の達成率は、プラセボ群で30%であった一方、0.1mg/kg群で36%、0.5mg/kg群で47%、2.0mg/kg群で38%であった。
救済治療を受けるまでの期間をKaplan-Meier推定値を用いて経時的な累積発生率として要約する。救済治療を受けなかった被験者は、Part AのWeek 12での来院(又はPart BのWeek 64での来院)、あるいは治験の早期中止時のいずれか早い方で打ち切りとする。
Part Aの4週間ごとの投与群における結果は、50%の患者がベースライン時から救済治療を受けるまでの時間はプラセボ群、0.1mg/kg群、0.5mg/kg群及び2.0mg/kg群のいずれも12週後までに到達しなかった。また25%の患者がベースライン時から救済治療を受けるまでの時間はプラセボ群、0.1mg/kg群、0.5mg/kg群、及び2.0mg/kg群でそれぞれ5週間、9週間、到達せず、及び9週間であった。
各時点で救済治療を受けている被験者の割合を算出する。
Part Aの4週間ごとの投与群における結果は、救済治療を受けた被験者の割合は、プラセボ群で39.1%であったのに対し、0.1mg/kg群で26.1%、0.5mg/kg群で24.4%、2.0mg/kg群で29.8%であった。
・アクティグラフィ
Part Aの4週間ごとの投与群におけるアクティグラフィの結果から、入眠から覚醒までの実際の時間は、投与4週後において、プラセボ群で7.3分増加であったのに対し、0.1mg/kg群で49.5分増加、0.5mg/kg群で53.1分増加、2.0mg/kg群で48.2分増加した。睡眠潜時(着床後睡眠までの時間)は、投与4週後において、プラセボ群で4.3分短縮であったのに対し、0.1mg/kg群で17.6分短縮、0.5mg/kg群で14.8分短縮、2.0mg/kg群で12.7分短縮した。
投与量について、更なる利便性の改善の観点から、体重当たりの投与量から固定用量での至適用法用量をモデリング&シミュレーションを実施し評価した。
はじめに体重当たりの用量と固定用量の曝露比較を行い、薬物動態の観点から至適用法用量を検討した。CIM331の血清中薬物濃度は1次吸収過程を伴う1コンパートメントモデルに良くあてはまった。また体重を共変量としてallometry式を用いてモデルパラメータに組み込んだ。モデルパラメータを以下に示す。
投与量が50mg固定の場合は体重100kg未満で概ね0.5 mg/kgでの曝露の下限を超えると想定され、また100mg固定の場合は低体重時に2mg/kgの曝露の上限を超えると想定された。また、75mg固定の場合は0.5mg/kgまたは2mg/kgで得られる曝露の範囲に入ると想定された。これらのことより、50mg固定(ただし体重100kg超の場合は100mg)あるいは75mg固定で4週に1度投与することにより、第II相試験で得られた曝露と同様の曝露が得られると考えられた。
4週あたりの固定投与量が25mg/body以上、好ましくは50mg/body以上の場合には、そう痒VASは0.5mg/kgまたは2mg/kgと同様の値を示すものと想定された。
4週毎あるいは8週毎のCIM331の反復投与により、血清中CIM331濃度は定常状態になり、持続的に、アトピー性皮膚炎患者のそう痒に対する効果を発揮できる。また、そう痒改善効果の維持、すなわちItch Scratch Cycle遮断に伴い、皮膚炎が改善可能となり、また、QOLの改善が可能となる。合計64週間における長期の有効性プロファイルが確認できる。
さらに、例えば、4週毎あるいは8週毎のCIM331の反復投与といった治療態様は、アトピー性皮膚炎の現状の全身治療方法が、1日数回、薬を飲んだり、薬を患部に塗布しなければならず、あるいは、紫外線療法の場合には週に1~2回もの通院が必要となり得ることに鑑みても、患者の薬の服用負担や通院負担等を著しく軽減し得ることが期待でき、患者のQOLの向上に一層貢献し得る。
そう痒を有する血液透析患者を対象とした単回皮下投与
(5-1)第II相臨床試験
第II相臨床試験の被験薬群において、そう痒に対してナルフラフィン塩酸塩を除く全身療法又は局所療法の治療が十分に奏効していない血液透析患者約60名、より具体的には69名を対象に、以下の要領でCIM331又はプラセボを腹部に単回皮下投与,又は参照群であるナルフラフィン塩酸塩カプセルを1日1回1カプセル(2.5 μg)夕食後又は就寝前に12週間連日経口投与した。CIM331の体重あたりの投与量及び投与液濃度は以下の通りとし、体重あたり20μLの液量でゆっくりと投与した。なお、治験薬は、1 mL中に100 mgのCIM331抗体を含有する液を1バイアルにつき1.53 mL充填し凍結乾燥させた製剤を、注射用水で溶解して投与液とし、別に溶解させたプラセボ溶液を使用してさらに希釈して目的の投与濃度とした。
・前観察期間1週間のうちそう痒VASが測定された日が5日以上あり,かつ以下のいずれの基準も満たす患者
(1)測定値が20 mm以上となる日が5日以上
(2)測定値の平均が50 mm以上
被験者約60名、より具体的には69名を以下の5群のいずれかに1:1:1:1:1にランダムに割り付けた。
・プラセボ群:CIM331のプラセボを単回皮下投与した
・CIM331 0.125 mg/kg群:CIM331(0.125 mg/kg)を単回皮下投与した
・CIM331 0.5 mg/kg群:CIM331(0.5 mg/kg)を単回皮下投与した
・CIM331 2.0 mg/kg群:CIM331(2.0 mg/kg)を単回皮下投与した
・ナルフラフィン塩酸塩群:ナルフラフィン塩酸塩カプセルを1日1回1カプセル(2.5 μg)12週間連日経口投与した。症状に応じて増量できるが,1日1回2カプセル(5 μg)を限度とした。
29日目のすべての観察及び検査が終了した以降は,そう痒の改善が認められなかった患者又は効果の減弱が認められた患者(ベースラインからのそう痒VASの低下が10 mm未満)に対し,治験責任医師又は治験分担医師が治療の変更が必要と判断した場合,そう痒に対する治療の種類,用法及び用量の変更を可とした。
・そう痒の強さの評価は、Visual Analog Scale (VAS)(Furue et al.2013)により行った。VASは100 mmの直線で、0 mmを痒みなし、100 mmを想像され得る最悪の痒みとした場合に、過去24時間におけるかゆみの強さを患者自身が0~100 mmの間に線で示すものであり、可能な限り同じ時間帯に実施した。
・白取の重症度基準(白取 et al.1983)は、0(症状なし)から4(激烈な痒み)までのそう痒の重症度基準に基づいて、過去24時間以内の日中の症状及び夜間の症状の程度をそれぞれ判定した。本評価については、被験者に加えて治験責任医師又は治験分担医師も評価した。
被験者の評価は可能な限り同じ時間帯に実施した。
・5-D itch scale(江畑 et al.2015)は、過去2週間以内のそう痒が発現した期間、程度、進行状況、障害度、分布を評価した上でスコア化した。
・睡眠障害VASは、「睡眠の問題なし」(0)から「全く眠ることができなかった」(10)までのVAS(Furue et al. 2013)で過去24時間中の睡眠障害の程度を被験者が評価した。
・不眠重症度(Insomnia Severity lndex)(室澤 et al.2009)は、5項目の不眠重症度質問票を用いて不眠の状況をスコア化した。
・EQ-5D-5L(池田 et al.2015)は、「移動の程度」、「身の回りの管理」、「ふだんの活動」、「痛み/不快感」、「不安/ふさぎ込み」の5項目の健康状態をそれぞれ5水準で調査した。
・アクティグラフィ
Actiwatchは、手首に装着し、全身の動きの指標となる手首の動きを自由行動下で捕捉し、記録及び保存するように設計された非侵襲型測定機器である。入眠から覚醒までの実際の時間、睡眠潜時、睡眠効率を含むその他のパラメータを客観的な方法で測定した。
・皮膚症状の評価(医師評価)は、治験責任医師又は治験分担医師が、「厚生労働科学研究班アトピー性皮膚炎治療ガイドライン2008」の「重症度のめやす」を参考に、軽症から最重症までの4段階の皮膚症状の評価を実施した。
・皮膚症状の評価(写真評価)は、治験責任医師又は治験分担医師が、「厚生労働科学研究班アトピー性皮膚炎治療ガイドライン2008」の「重症度のめやす」に示されている皮疹(紅斑、乾燥、落屑、丘疹、びらん、浸潤、苔癬化)に掻破痕を加えた皮疹を撮影対象とし、各被験者における代表的な症状(最も重症度が高い箇所)を選択した。皮膚症状の評価は、日本皮膚科学会アトピー性皮膚炎重症度分類(簡便法)の評価基準に基づき,0(なし)から4(最重症)までの5段階の範囲で医学専門家とは独立した評価委員が実施した。
ベースラインから投与4週後のそう痒VAS変化量について、各CIM331投与群のプラセボ投与群に対する対比較を主要解析とした。仮説は、有意水準両側20%を参考に評価した。探索試験のため、多重性の調整は実施しなかった。
主要評価としては、ベースラインから投与4週後のそう痒VAS変化量を目的変数とし、ベースライン時のそう痒VASを共変量とした共分散分析(ANCOVA)により、プラセボ群とCIM331の各用量群を比較した。平均値の差の95%信頼区間をANCOVAから算出した。欠損値はLOCF(Last Observation Carried Forward after baseline)により補完した。
ナルフラフィン塩酸塩群は、各CIM331投与群及びプラセボ群と探索的に比較を行った。解析は各CIM331投与群及びプラセボ群の主要解析と同様に行った。その他の探索的解析はSAP(解析計画書)に記載した。
主要評価項目である、投与開始4週後におけるそう痒VASの開始時(ベースライン)からの変化量(最小二乗平均)のプラセボとの差は、CIM331 0.125 mg/kg、CIM331 0.5 mg/kg、CIM331 2.0 mg/kgでそれぞれ-2.4 mm(p=0.7806)、-8.7 mm(p=0.3317)、0.4 mm(p=0.9678)であった。なお、参照群であるナルフラフィン塩酸塩のプラセボとの差は5.7 mm(p=0.5154)であった。
投与開始1週後のそう痒VASのベースラインからの変化量は、プラセボ群-18.6 mm、ナルフラフィン塩酸塩群-17.4 mmに対して、CIM331 の0.125 mg/kg群-27.4 mm、 0.5 mg/kg群-30.3 mm、 2.0 mg/kg群-25.9 mmと、いずれのCIM331群も速やかなそう痒の改善効果が確認された。投与開始4週後のそう痒VAS変化量は、プラセボ群-32.8 mm、ナルフラフィン塩酸塩群-27.3 mmに対して、CIM331の 0.125 mg/kg群-34.7 mm、 0.5 mg/kg群-40.1 mm、 2.0 mg/kg群-31.5 mmと、CIM331の0.5 mg/kg群の変化量が最も大きかった(図12)。
・そう痒VAS 30 mm未満に到達する改善を認めた被験者の割合
主要評価項目の評価時期である投与開始4週後にそう痒VASが30 mm未満に到達する改善を認めた被験者の割合は、プラセボ群35.7%、ナルフラフィン塩酸塩群33.3%に対して、CIM331の 0.125 mg/kg群57.1%、 0.5 mg/kg群69.2%、 2.0 mg/kg群42.9%と、プラセボ群、ナルフラフィン塩酸塩群に比べてCIM331群は軽度なそう痒であるVAS 30 mm未満の改善を認めた被験者の割合が多かった。(図13)
投与開始4週後の白取のスコア変化量(日中)は、プラセボ群-0.89、ナルフラフィン塩酸塩群-0.67に対して、CIM331の 0.125 mg/kg群-1.00、 0.5 mg/kg群-1.30、 2.0 mg/kg群-0.79と、CIM331の0.5 mg/kg群の改善が最も大きかった。
投与開始4週後の白取のスコア変化量(夜間)は、プラセボ群-0.81、ナルフラフィン塩酸塩群-0.51に対して、CIM331の 0.125 mg/kg群-0.64、0.5 mg/kg群-1.16、2.0 mg/kg群-0.79と、CIM331の0.5 mg/kg群の改善が最も大きかった。
・5-D itch scaleによるスコア
投与開始4週後の5-D itch scaleのスコア変化量は、プラセボ群-5.4、ナルフラフィン塩酸塩群-3.7に対して、CIM331の0.125 mg/kg群-5.6、0.5 mg/kg群-6.5、2.0 mg/kg群-3.1と、CIM331の0.5 mg/kg群の改善が最も大きかった。
そう痒を有する血液透析患者におけるバイオマーカー解析
(6-1)バイオマーカー評価
CIM331投与前の血清中IL-31濃度と、CIM331投与後の臨床試験成績との相関関係を評価するため、バイオマーカー評価を実施した。
バイオマーカー解析に供するために血清を保管することに同意した全試験患者(n = 68)から血清サンプルを得た。血清中IL-31濃度は、-70℃以下で凍結保管した血清サンプルを室温で融解し、超高感度酵素結合免疫吸着アッセイ(ELISA; SiMoATM, Quanterix, Billerica, MA, USA)を用いて測定した。当該68名のサンプルから得たデータを用いて、スクリーニング段階(CIM331投与前)の血清中IL-31濃度のカットオフ中央値0.86 pg/mLを導き出した。このIL-31カットオフ値を用いて、実施例5に記載のとおりに試験投与を受けた患者(n = 48)について、IL-31と臨床試験結果との間の相関関係を評価した。また、post hoc解析にて、試験患者からのサンプルを、健常人ボランティア由来の市販のサンプルと比較した。
post hoc解析によるIL-31分布のバイオマーカー解析の結果を図14に示す。健常人ボランティア(healthy volunteer:HV;n = 20)と比べて、透析そう痒症(uremic pruritus :UP;n = 68)患者の血清中IL-31レベルは明らかに高かった(図14)。血清サンプルを採取され、試験投与を受けた48名において、血清中IL-31レベルが0.86 pg/mL以上の患者は、血清中IL-31レベルが0.86 pg/mL未満の患者と比べて、CIM331投与によるそう痒VASの顕著な低下が認められた(図15)。この傾向は、プラセボ投与群やナルフラフィン塩酸塩投与群では観察されなかった。
CIM331の単回皮下投与により、血清中CIM331濃度が上昇し、持続的に、透析患者のそう痒に対する効果を発揮できる。また、そう痒改善効果の維持、すなわちItch Scratch Cycle遮断に伴い、皮膚炎が改善可能となり、また、QOLの改善が可能となる。
さらに、例えば、CIM331の単回皮下投与により4週間またはそれ以上の期間に亘りそう痒を抑制できる治療態様は、透析そう痒症の現状の全身治療方法が、1日数回、薬を飲んだり、薬を患部に塗布しなければならず、あるいは、紫外線療法の場合には週に1~2回もの通院が必要となり得ることに鑑みても、患者の薬の服用負担や通院負担等を著しく軽減し得ることが期待でき、患者のQOLの向上に一層貢献し得る。
また、CIM331投与開始前における血清中のIL-31濃度が所定の値以上である透析そう痒症患者は、CIM331の投与によって、より高いそう痒改善効果の発揮が期待できる。そのような、高いそう痒改善効果の発揮が期待できる基準となりうる所定の血清中IL-31濃度は、例えば0.86 pg/mLであり得る。血清中のIL-31濃度が、このような所定の値以上である透析そう痒症患者にCIM331を投与することにより、患者のQOLの向上に一層貢献し得る。
限定はされないが、CIM331は、ナルフラフィン塩酸塩を除く、そう痒に対する既存治療が十分に奏効しない透析患者に投与されてよい。
CIM331は、例えば、2週~12週毎、具体的には、例えば、2週毎、3週毎、4週毎、5週毎、6週毎、7週毎、8週毎、9週毎、10週毎、11週毎、もしくは12週毎に1回、あるいは、1月毎、2月毎、もしくは3月毎に1回、皮下に等量の投与量でかつ同一の投与間隔で反復投与されてよい。
CIM331の体重あたりの投与量及び投与液濃度は、第II相臨床試験結果やそれ以外の試験結果等に基づいて適宜決定してもよい。例えば、透析そう痒症患者の体重が120kgを超える場合には体重を120kgとして治験薬を調製してもよい。また、CIM331を透析そう痒症患者に対してmg/bodyで投与することが意図される場合には、第II相臨床試験結果等から、CIM331の投与量を、mg/kgからmg/bodyへ換算し、適切かつ妥当な投与量(mg/body)を選定して、投与されてもよい。この際、mg/kgからmg/bodyへの換算ロジックとしては、限定はされないが、以下のロジックを用いて当業者が適宜決定できることが理解されよう。
CIM331の最低有効血清中濃度と最大忍容(経験)血清中濃度が存在すると仮定し、この濃度範囲に血清中CIM331濃度が体重にかかわらず得られるよう、mg/kgの投与量からmg/bodyの投与量への変更を第II相試験の結果から検討する。また、低体重の小児用の投与量はmg/bodyでは曝露が著しく増大する可能性があるため、その場合はmg/kgでの投与を検討する。現在実施している第II相試験の結果から、最低有効血清中濃度と最大忍容血清中濃度を決定し、上記のように曝露をそろえることにより、mg/bodyへの変換を行い得る。
あるいは、統計資料等に基づき、一般的な透析そう痒症患者の体重を想定し、当該想定体重に基づき、「体重あたり投与量 x 想定体重 = 固定用量」の計算式により、体重あたりの投与量(mg/kg)を固定用量(mg/body)に換算してもよい。
非限定的な一実施態様において、成人又は小児の透析そう痒症患者には、0.1mg~1000mg/body、例えば、0.2mg~360mg/body、好ましくは10mg~200mg/body、10mg~100mg/body、25mg~100mg/body、50mg~100mg/body、又は50mg~75mg/bodyの中から選択される投与量を一点選択して、上述した投与間隔で皮下に等量かつ同一の投与間隔で反復投与してよい。
あるいは、非限定的な別の実施態様において、小児の透析そう痒症患者には、0.01mg~10mg/kg、例えば、0.1mg~3mg/kg、好ましくは0.2mg~2mg/kg、より好ましくは0.5mg~1.5mg/kgの中から選択される投与量を一点選択して、上述した投与間隔で皮下に等量かつ同一の投与間隔で反復投与してよい。
IgG抗体の発現と精製
抗体の発現は以下の方法を用いて行われた。ヒト胎児腎癌細胞由来HEK293H株(Invitrogen)を10 % Fetal Bovine Serum(Invitrogen)を含むDMEM培地(Invitrogen)へ懸濁し、5~6 × 105細胞/mLの細胞密度で接着細胞用ディッシュ(直径10 cm, CORNING)の各ディッシュへ10 mLずつ蒔きこみCO2インキュベーター(37℃、5 % CO2)内で一昼夜培養した後に、培地を吸引除去し、CHO-S-SFM-II(Invitrogen)培地6.9 mLを添加した。調製したプラスミドをlipofection法により細胞へ導入した。得られた培養上清を回収した後、遠心分離(約2000 g、5分間、室温)して細胞を除去し、さらに0.22μmフィルターMILLEX(R)-GV(Millipore)を通して滅菌して培養上清を得た。得られた培養上清にrProtein A SepharoseTM Fast Flow(Amersham Biosciences)を用いて当業者に公知の方法で精製した。精製抗体の濃度は、分光光度計を用いて280 nmでの吸光度を測定した。得られた値からProtein Science 1995;4:2411-2423に記された方法により算出された吸光係数を用いて抗体濃度を算出した。
Claims (13)
- IL-31アンタゴニストを有効成分として含有する、透析そう痒症の予防用及び/又は治療用医薬組成物。
- 前記IL-31アンタゴニストは、0.1mg~1000mg/body/2週、0.1mg~1000mg/body/4週、又は、0.1mg~1000mg/body/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与される、請求項1に記載の医薬組成物。
- 前記IL-31アンタゴニストは、25mg~100mg/body/4週で投与される、請求項2に記載の医薬組成物。
- 前記IL-31アンタゴニストは、50mg~100mg/body/4週で投与される、請求項3に記載の医薬組成物。
- 前記IL-31アンタゴニストは、0.01mg~10mg/kg/2週、0.01mg~10mg/kg/4週、又は、0.01mg~10mg/kg/8週で、透析そう痒症に罹患した、又は、罹患している恐れのある対象に等量かつ同一の投与間隔で反復投与される、請求項1に記載の医薬組成物。
- 前記IL-31アンタゴニストは、0.2mg~2mg/kg/4週で投与される、請求項5に記載の医薬組成物。
- 前記IL-31アンタゴニストは、血清中のIL-31濃度が所定の値以上である、透析そう痒症に罹患した、又は、罹患している恐れのある対象に投与される、請求項1~6のいずれか一項に記載の医薬組成物。
- 透析そう痒症によって引き起こされる睡眠障害の改善用の、請求項1~7のいずれか一項に記載の医薬組成物。
- 前記睡眠障害の改善が入眠から覚醒までの時間を増加させるための、及び/又は、睡眠潜時(着床後睡眠までの時間)を短縮させるための、請求項8に記載の医薬組成物。
- 前記IL-31アンタゴニストが、IL-31シグナルを阻害する抗体である、請求項1~9のいずれか一項に記載の医薬組成物。
- 前記抗体が、マウス、ラット、及びウサギのいずれのIL-31RAに対しても交差反応性を示さない、請求項10に記載の医薬組成物。
- 前記抗体が、抗IL-31中和抗体または抗IL-31RA中和抗体である、請求項10又は11に記載の医薬組成物。
- 前記抗IL-31RA中和抗体が、
(1)配列番号:1に記載のCDR1、配列番号:2に記載のCDR2、および配列番号:3に記載のCDR3を含むH鎖可変領域、ならびに、配列番号:4に記載のCDR1、配列番号:5に記載のCDR2、および配列番号:6に記載のCDR3を含むL鎖可変領域を含む抗IL-31RA抗体;
(2)配列番号:7に記載のH鎖可変領域、および、配列番号:8に記載のL鎖可変領域を含む抗IL-31RA抗体;又は、
(3)配列番号:9に記載のH鎖、および、配列番号:10に記載のL鎖を含む抗IL-31RA抗体
のいずれかである、請求項12に記載の医薬組成物。
Priority Applications (12)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU2020466800A AU2020466800A1 (en) | 2020-09-01 | 2020-09-01 | Pharmaceutical composition for prevention and/or treatment of dialysis pruritus containing IL-31 antagonist as active ingredient |
| EP20952354.7A EP4209227A1 (en) | 2020-09-01 | 2020-09-01 | Pharmaceutical composition for prevention and/or treatment of dialysis pruritus containing il-31 antagonist as active ingredient |
| IL300694A IL300694A (en) | 2020-09-01 | 2020-09-01 | A pharmaceutical preparation for the prevention and/or treatment of dialysis pruritus that includes an IL-31 antagonist as an active ingredient |
| MX2023002482A MX2023002482A (es) | 2020-09-01 | 2020-09-01 | Composicion farmaceutica para prevencion y/o tratamiento de prurito por dialisis que comprende antagonista de interleucina 31 (il-31) como ingrediente activo. |
| PCT/JP2020/032987 WO2022049614A1 (ja) | 2020-09-01 | 2020-09-01 | Il-31アンタゴニストを有効成分として含有する、透析そう痒症の予防用及び/又は治療用医薬組成物 |
| US18/023,246 US20230391878A1 (en) | 2020-09-01 | 2020-09-01 | Pharmaceutical composition for prevention and/or treatment of dialysis pruritus containing il-31 antagonist as active ingredient |
| KR1020217018823A KR20230048233A (ko) | 2020-09-01 | 2020-09-01 | Il-31 안타고니스트를 유효 성분으로서 함유하는, 투석 소양증의 예방용 및/또는 치료용 의약 조성물 |
| KR1020207030800A KR102269716B1 (ko) | 2020-09-01 | 2020-09-01 | Il-31 안타고니스트를 유효 성분으로서 함유하는, 투석 소양증의 예방용 및/또는 치료용 의약 조성물 |
| CA3189847A CA3189847A1 (en) | 2020-09-01 | 2020-09-01 | Pharmaceutical composition for prevention and/or treatment of dialysis pruritus containing il-31 antagonist as active ingredient |
| JP2020551453A JP6799831B1 (ja) | 2020-09-01 | 2020-09-01 | Il−31アンタゴニストを有効成分として含有する、透析そう痒症の予防用及び/又は治療用医薬組成物 |
| CN202080103639.6A CN116096411A (zh) | 2020-09-01 | 2020-09-01 | 含有作为活性成分的il-31拮抗剂的用于预防和/或治疗透析瘙痒的药物组合物 |
| JP2020187708A JP2022041802A (ja) | 2020-09-01 | 2020-11-11 | Il-31アンタゴニストを有効成分として含有する、透析そう痒症の予防用及び/又は治療用医薬組成物 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/JP2020/032987 WO2022049614A1 (ja) | 2020-09-01 | 2020-09-01 | Il-31アンタゴニストを有効成分として含有する、透析そう痒症の予防用及び/又は治療用医薬組成物 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2022049614A1 true WO2022049614A1 (ja) | 2022-03-10 |
Family
ID=73741045
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2020/032987 WO2022049614A1 (ja) | 2020-09-01 | 2020-09-01 | Il-31アンタゴニストを有効成分として含有する、透析そう痒症の予防用及び/又は治療用医薬組成物 |
Country Status (10)
| Country | Link |
|---|---|
| US (1) | US20230391878A1 (ja) |
| EP (1) | EP4209227A1 (ja) |
| JP (2) | JP6799831B1 (ja) |
| KR (2) | KR102269716B1 (ja) |
| CN (1) | CN116096411A (ja) |
| AU (1) | AU2020466800A1 (ja) |
| CA (1) | CA3189847A1 (ja) |
| IL (1) | IL300694A (ja) |
| MX (1) | MX2023002482A (ja) |
| WO (1) | WO2022049614A1 (ja) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11673946B2 (en) | 2017-02-24 | 2023-06-13 | Kindred Biosciences, Inc. | Methods of treating a companion animal species comprising administering anti-IL31 antibodies |
| US11773173B2 (en) | 2015-04-14 | 2023-10-03 | Chugai Seiyaku Kabushiki Kaisha | Pharmaceutical composition for prevention and/or treatment of atopic dermatitis comprising IL-31 antagonist as active ingredient |
Citations (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1995001937A1 (fr) | 1993-07-09 | 1995-01-19 | Association Gradient | Procede de traitement de residus de combustion et installation de mise en ×uvre dudit procede |
| WO1999054342A1 (en) | 1998-04-20 | 1999-10-28 | Pablo Umana | Glycosylation engineering of antibodies for improving antibody-dependent cellular cytotoxicity |
| WO2000061739A1 (en) | 1999-04-09 | 2000-10-19 | Kyowa Hakko Kogyo Co., Ltd. | Method for controlling the activity of immunologically functional molecule |
| WO2000075314A1 (fr) | 1999-06-02 | 2000-12-14 | Chugai Research Institute For Molecular Medicine, Inc. | Proteine receptrice d'hemopoietine |
| WO2002020565A2 (en) | 2000-09-08 | 2002-03-14 | Universität Zürich | Collections of repeat proteins comprising repeat modules |
| WO2002032925A2 (en) | 2000-10-16 | 2002-04-25 | Phylos, Inc. | Protein scaffolds for antibody mimics and other binding proteins |
| JP2002338476A (ja) * | 2001-05-21 | 2002-11-27 | Health Factor Kenkyusho:Kk | 腎透析に伴う痒みの予防治療剤 |
| WO2004003140A2 (en) | 2002-01-18 | 2004-01-08 | Zymogenetics, Inc. | Cytokine receptor zcytor17 multimers |
| WO2004044011A2 (en) | 2002-11-06 | 2004-05-27 | Avidia Research Institute | Combinatorial libraries of monomer domains |
| WO2005079566A2 (en) | 2004-02-12 | 2005-09-01 | Lexicon Genetics Incorporated | Gene disruptions, compositions and methods relating thereto |
| WO2006063865A2 (en) | 2004-12-15 | 2006-06-22 | Universite D'angers | Compositions for enhancing keratinocyte migration and epidermal repair via a receptor containing osmrbeta as a subunit, and applications thereof |
| WO2006088855A1 (en) | 2005-02-14 | 2006-08-24 | Zymogenetics, Inc. | Methods of treating skin disorders using an il-31ra antagonist |
| WO2006088956A2 (en) | 2005-02-14 | 2006-08-24 | Zymogenetics, Inc. | Methods of predicting therpeutic response in atopic dermatitis to il-31 antagonists |
| WO2006122079A1 (en) | 2005-05-06 | 2006-11-16 | Zymogenetics, Inc. | Il-31 monoclonal antibodies and methods of use |
| WO2007133816A2 (en) | 2006-01-10 | 2007-11-22 | Zymogenetics, Inc. | Methods of treating pain and inflammation in neuronal tissue using il-31ra and osmrb antagonists |
| WO2007142325A1 (ja) | 2006-06-08 | 2007-12-13 | Chugai Seiyaku Kabushiki Kaisha | 炎症性疾患の予防または治療剤 |
| WO2008028192A2 (en) | 2006-09-01 | 2008-03-06 | Zymogenetics, Inc. | Variable region sequences of il-31 monoclonal antibodies and methods of use |
| WO2009071696A2 (en) | 2007-12-07 | 2009-06-11 | Zymogenetics, Inc. | Humanized antibody molecules specific for il-31 |
| WO2009072598A1 (ja) | 2007-12-05 | 2009-06-11 | Chugai Seiyaku Kabushiki Kaisha | 掻痒症治療剤 |
| WO2009072604A1 (ja) | 2007-12-05 | 2009-06-11 | Chugai Seiyaku Kabushiki Kaisha | 抗nr10抗体、およびその利用 |
| WO2010064697A1 (ja) | 2008-12-05 | 2010-06-10 | 中外製薬株式会社 | 抗nr10抗体、およびその利用 |
| WO2014208645A1 (ja) * | 2013-06-28 | 2014-12-31 | 中外製薬株式会社 | そう痒を伴う疾患に罹患した患者のil-31アンタゴニストによる治療に対する応答を予測する方法 |
| WO2015025767A1 (ja) * | 2013-08-21 | 2015-02-26 | 久光製薬株式会社 | 貼付剤 |
| US20190135804A1 (en) * | 2017-11-03 | 2019-05-09 | The United States Of America,As Represented By The Secretary,Department Of Health And Human Services | Compositions and methods for the inhibition of pruritus |
| KR20190059860A (ko) * | 2017-11-23 | 2019-05-31 | 주식회사 헬릭스미스 | 천연추출물을 포함하는 소양증의 예방 또는 치료용 조성물 |
-
2020
- 2020-09-01 KR KR1020207030800A patent/KR102269716B1/ko active IP Right Grant
- 2020-09-01 CN CN202080103639.6A patent/CN116096411A/zh active Pending
- 2020-09-01 AU AU2020466800A patent/AU2020466800A1/en active Pending
- 2020-09-01 JP JP2020551453A patent/JP6799831B1/ja active Active
- 2020-09-01 US US18/023,246 patent/US20230391878A1/en active Pending
- 2020-09-01 WO PCT/JP2020/032987 patent/WO2022049614A1/ja unknown
- 2020-09-01 CA CA3189847A patent/CA3189847A1/en active Pending
- 2020-09-01 IL IL300694A patent/IL300694A/en unknown
- 2020-09-01 MX MX2023002482A patent/MX2023002482A/es unknown
- 2020-09-01 KR KR1020217018823A patent/KR20230048233A/ko not_active Application Discontinuation
- 2020-09-01 EP EP20952354.7A patent/EP4209227A1/en active Pending
- 2020-11-11 JP JP2020187708A patent/JP2022041802A/ja active Pending
Patent Citations (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1995001937A1 (fr) | 1993-07-09 | 1995-01-19 | Association Gradient | Procede de traitement de residus de combustion et installation de mise en ×uvre dudit procede |
| WO1999054342A1 (en) | 1998-04-20 | 1999-10-28 | Pablo Umana | Glycosylation engineering of antibodies for improving antibody-dependent cellular cytotoxicity |
| WO2000061739A1 (en) | 1999-04-09 | 2000-10-19 | Kyowa Hakko Kogyo Co., Ltd. | Method for controlling the activity of immunologically functional molecule |
| WO2000075314A1 (fr) | 1999-06-02 | 2000-12-14 | Chugai Research Institute For Molecular Medicine, Inc. | Proteine receptrice d'hemopoietine |
| WO2002020565A2 (en) | 2000-09-08 | 2002-03-14 | Universität Zürich | Collections of repeat proteins comprising repeat modules |
| WO2002032925A2 (en) | 2000-10-16 | 2002-04-25 | Phylos, Inc. | Protein scaffolds for antibody mimics and other binding proteins |
| JP2002338476A (ja) * | 2001-05-21 | 2002-11-27 | Health Factor Kenkyusho:Kk | 腎透析に伴う痒みの予防治療剤 |
| WO2004003140A2 (en) | 2002-01-18 | 2004-01-08 | Zymogenetics, Inc. | Cytokine receptor zcytor17 multimers |
| WO2004044011A2 (en) | 2002-11-06 | 2004-05-27 | Avidia Research Institute | Combinatorial libraries of monomer domains |
| WO2005079566A2 (en) | 2004-02-12 | 2005-09-01 | Lexicon Genetics Incorporated | Gene disruptions, compositions and methods relating thereto |
| WO2006063865A2 (en) | 2004-12-15 | 2006-06-22 | Universite D'angers | Compositions for enhancing keratinocyte migration and epidermal repair via a receptor containing osmrbeta as a subunit, and applications thereof |
| WO2006063864A2 (en) | 2004-12-15 | 2006-06-22 | Universite D'angers | Compositions for preventing, reducing or treating keratinocyte-mediated inflammation |
| WO2006088955A2 (en) | 2005-02-14 | 2006-08-24 | Zymogenetics, Inc. | Methods of treating diseases which are mediated by cutaneous lymphocyte antigen positive cells |
| WO2006088956A2 (en) | 2005-02-14 | 2006-08-24 | Zymogenetics, Inc. | Methods of predicting therpeutic response in atopic dermatitis to il-31 antagonists |
| WO2006088855A1 (en) | 2005-02-14 | 2006-08-24 | Zymogenetics, Inc. | Methods of treating skin disorders using an il-31ra antagonist |
| WO2006122079A1 (en) | 2005-05-06 | 2006-11-16 | Zymogenetics, Inc. | Il-31 monoclonal antibodies and methods of use |
| WO2007133816A2 (en) | 2006-01-10 | 2007-11-22 | Zymogenetics, Inc. | Methods of treating pain and inflammation in neuronal tissue using il-31ra and osmrb antagonists |
| WO2007143231A2 (en) | 2006-01-10 | 2007-12-13 | Zymogenetics, Inc. | Methods of treating pain and inflammation in neuronal tissue using il-31 antagonists |
| JP2009528264A (ja) * | 2006-01-10 | 2009-08-06 | ザイモジェネティクス,インコーポレイティド | Il−31アンタゴニストを用いて神経組織における疼痛及び炎症を治療する方法 |
| WO2007142325A1 (ja) | 2006-06-08 | 2007-12-13 | Chugai Seiyaku Kabushiki Kaisha | 炎症性疾患の予防または治療剤 |
| WO2008028192A2 (en) | 2006-09-01 | 2008-03-06 | Zymogenetics, Inc. | Variable region sequences of il-31 monoclonal antibodies and methods of use |
| WO2009072598A1 (ja) | 2007-12-05 | 2009-06-11 | Chugai Seiyaku Kabushiki Kaisha | 掻痒症治療剤 |
| WO2009072604A1 (ja) | 2007-12-05 | 2009-06-11 | Chugai Seiyaku Kabushiki Kaisha | 抗nr10抗体、およびその利用 |
| WO2009071696A2 (en) | 2007-12-07 | 2009-06-11 | Zymogenetics, Inc. | Humanized antibody molecules specific for il-31 |
| WO2010064697A1 (ja) | 2008-12-05 | 2010-06-10 | 中外製薬株式会社 | 抗nr10抗体、およびその利用 |
| WO2014208645A1 (ja) * | 2013-06-28 | 2014-12-31 | 中外製薬株式会社 | そう痒を伴う疾患に罹患した患者のil-31アンタゴニストによる治療に対する応答を予測する方法 |
| WO2015025767A1 (ja) * | 2013-08-21 | 2015-02-26 | 久光製薬株式会社 | 貼付剤 |
| US20190135804A1 (en) * | 2017-11-03 | 2019-05-09 | The United States Of America,As Represented By The Secretary,Department Of Health And Human Services | Compositions and methods for the inhibition of pruritus |
| KR20190059860A (ko) * | 2017-11-23 | 2019-05-31 | 주식회사 헬릭스미스 | 천연추출물을 포함하는 소양증의 예방 또는 치료용 조성물 |
Non-Patent Citations (30)
| Title |
|---|
| "Guidelines for Treatment of Atopic Dermatitis", 2008, HEALTH, HEALTH AND LABOR SCIENCES RESEARCH GROUP |
| "Using Antibodies: A Laboratory Manual", 1999, COLD SPRING HARBOR LABORATORY PRESS |
| CHOTHIA ET AL., SCIENCE, vol. 233, 1986, pages 755 - 758 |
| CURR OPIN BIOTECHNOL, vol. 17, 2006, pages 653 - 658 |
| CURR OPIN STRUCT BIOL, vol. 7, 1997, pages 463 - 469 |
| DANNO K.: "Friends of itchiness, The perfect guide for treating itchiness you want to leave in the dialysis room", KINPODO, 2008, pages 1 - 16 |
| DILLON ET AL., NAT IMMUNOL, vol. 5, 2004, pages 752 - 760 |
| GANGEMI SQUARTUCCIO SCASCIARO MTRAPANI GMINCIULLO PLIMBALZANO E: "Interleukin 31 and skin diseases: A systematic review", ALLERGY ASTHMA PROC, vol. 38, no. 6, 2017, pages 401 - 8 |
| IINO, NORIAKI ET AL.: "Dialysis skin pruritus = Uremic Pruritus", JAPANESE JOURNAL OF CLINICAL MEDICINE, no. 18, 20 March 2012 (2012-03-20), JP , pages 259 - 263, XP009542876, ISSN: 0047-1852 * |
| J BIOL CHEM, vol. 270, 1995, pages 21619 - 21625 |
| J BIOL CHEM, vol. 281, 2006, pages 20464 - 20473 |
| J MOL BIOL, vol. 222, 1991, pages 581 - 597 |
| J MOL BIOL, vol. 262, 1996, pages 732 - 745 |
| JENNIFER Q. DONG ET AL.: "Quantitative Prediction of Human Pharmacokinetics for Monoclonal Antibodies", CLIN PHARMACOKINET, vol. 50, no. 2, 2011, pages 131 - 142, XP055307612, DOI: 10.2165/11537430-000000000-00000 |
| JIE LING ET AL.: "Interspecies Scaling of Therapeutic Monoclonal Antibodies: Initial Look", J CLIN PHARMACOL, vol. 49, no. 12, 2009, pages 1382 - 1402 |
| KABAT: "Sequences of Proteins of Immunological Interest", 1991 |
| KASAKURA, SHIMPEI: "A novel cytokine involved in the development of atopic dermatitis: IL-31", JOURNAL OF CLINICAL AND EXPERIMENTAL MEDICINE, vol. 219, no. 3, 21 October 2006 (2006-10-21), JP , pages 229 - 230, XP009542878, ISSN: 0039-2359 * |
| KIMATA N ET AL.: "Pruritus in hemodialysis patients: Results from the Japanese Dialysis Outcomes and Practice Patterns Study (JDOPPS", HEMODIAL INT, vol. 18, 2014, pages 657 - 67 |
| KO MJ ET AL.: "Interleukin-31 is associated with uremic pruritus in patients receiving hemodialysis", J AM ACAD DERMATOL, vol. 71, 2014, pages 1151 - 9 |
| NAKAI S ET AL., CURRENT SITUATION ON CHRONIC DIALYSIS THERAPY IN JAPAN, 31 December 1999 (1999-12-31) |
| NARITA I ET AL.: "Etiology and prognostic significance of severe uremic pruritus in chronic hemodialysis patients", KIDNEY INT, vol. 69, 2006, pages 1626 - 32 |
| NATURE, vol. 256, 1975, pages 495 |
| NATURE, vol. 352, 1991, pages 624 - 628 |
| OMORI K ET AL.: "Situation on dialysis dermal pruritus - Search report on 2474 patients at 41 institutions in the Niigata prefecture", JOURNAL OF THE JAPANESE SOCIETY FOR DIALYSIS THERAPY, vol. 34, 2001, pages 1469 - 77 |
| PISONI RL ET AL.: "Pruritus in haemodialysis patients: International results from the Dialysis Outcomes and Practice Patterns Study (DOPPS", NEPHROL DIAL TRANSPLANT, vol. 21, 2006, pages 3495 - 505 |
| PROTEIN SCI, vol. 15, 2006, pages 14 - 27 |
| PROTEIN SCIENCE, vol. 4, 1995, pages 2411 - 2423 |
| RONG DENG ET AL.: "Projecting human pharmacokinetics of therapeutic antibodies from nonclinical data", MABS, vol. 3, no. 1, 2011, pages 61 - 66, XP055233009, DOI: 10.4161/mabs.3.1.13799 |
| SHIGEKI YAMADA ET AL.: "Questionnaire administered to 1,936 patients from 17 institutions in Tokai area of Japan", vol. 45, 2012, JOURNAL OF THE JAPANESE SOCIETY FOR DIALYSIS THERAPY, article "Investigation of the status of uremic pruritus in hemodialysis patients and the efficacy of nalfurafine hydrochloride", pages: 1133 - 40 |
| WAHLGREN CF ET AL., J ALLERGY CLIN IMMUNOL, vol. 118, 2006, pages 178 - 89 |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11773173B2 (en) | 2015-04-14 | 2023-10-03 | Chugai Seiyaku Kabushiki Kaisha | Pharmaceutical composition for prevention and/or treatment of atopic dermatitis comprising IL-31 antagonist as active ingredient |
| US11673946B2 (en) | 2017-02-24 | 2023-06-13 | Kindred Biosciences, Inc. | Methods of treating a companion animal species comprising administering anti-IL31 antibodies |
| US11697683B2 (en) | 2017-02-24 | 2023-07-11 | Kindred Biosciences, Inc. | Anti-IL31 antibodies for veterinary use |
Also Published As
| Publication number | Publication date |
|---|---|
| MX2023002482A (es) | 2023-03-08 |
| JPWO2022049614A1 (ja) | 2022-03-10 |
| CA3189847A1 (en) | 2022-03-10 |
| KR20230048233A (ko) | 2023-04-11 |
| JP2022041802A (ja) | 2022-03-11 |
| IL300694A (en) | 2023-04-01 |
| JP6799831B1 (ja) | 2020-12-16 |
| AU2020466800A1 (en) | 2023-03-23 |
| US20230391878A1 (en) | 2023-12-07 |
| KR102269716B1 (ko) | 2021-06-28 |
| CN116096411A (zh) | 2023-05-09 |
| EP4209227A1 (en) | 2023-07-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6887212B2 (ja) | Il−31アンタゴニストを有効成分として含有する、アトピー性皮膚炎の予防用及び/又は治療用医薬組成物 | |
| KR20210039402A (ko) | 알츠하이머병의 치료 및 예방 방법 | |
| WO2022049614A1 (ja) | Il-31アンタゴニストを有効成分として含有する、透析そう痒症の予防用及び/又は治療用医薬組成物 | |
| US20240018249A1 (en) | Pharmaceutical composition for prevention and/or treatment of atopic dermatitis comprising il-31 antagonist as active ingredient | |
| JP2023542878A (ja) | 多発性硬化症を治療するためのlou064 | |
| US20210139573A1 (en) | Dosing regimens for treating or preventing c5-associated diseases | |
| TW202210508A (zh) | 含有il-31拮抗劑作為有效成分之透析搔癢症的預防用及/或治療用醫藥組合物 | |
| RU2806304C1 (ru) | Фармацевтическая композиция для профилактики и/или лечения атопического дерматита, включающая антагонист ил-31 в качестве активного ингредиента | |
| US20230053258A1 (en) | Anti-ide antibodies and uses of same | |
| RU2800765C2 (ru) | ЛЕЧЕНИЕ АЛЛЕРГИЧЕСКИХ ЗАБОЛЕВАНИЙ, ОПОСРЕДОВАННЫХ IgE |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| ENP | Entry into the national phase |
Ref document number: 2020551453 Country of ref document: JP Kind code of ref document: A |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 20952354 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 3189847 Country of ref document: CA |
|
| ENP | Entry into the national phase |
Ref document number: 2020466800 Country of ref document: AU Date of ref document: 20200901 Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2020952354 Country of ref document: EP Effective date: 20230403 |