WO2021193561A1 - クロロプレン系ブロック共重合体ラテックス - Google Patents
クロロプレン系ブロック共重合体ラテックス Download PDFInfo
- Publication number
- WO2021193561A1 WO2021193561A1 PCT/JP2021/011777 JP2021011777W WO2021193561A1 WO 2021193561 A1 WO2021193561 A1 WO 2021193561A1 JP 2021011777 W JP2021011777 W JP 2021011777W WO 2021193561 A1 WO2021193561 A1 WO 2021193561A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- chloroprene
- latex
- polymerization
- block copolymer
- polymer block
- Prior art date
Links
- YACLQRRMGMJLJV-UHFFFAOYSA-N chloroprene Chemical compound ClC(=C)C=C YACLQRRMGMJLJV-UHFFFAOYSA-N 0.000 title claims abstract description 266
- 239000004816 latex Substances 0.000 title claims abstract description 235
- 229920000126 latex Polymers 0.000 title claims abstract description 235
- 229920001400 block copolymer Polymers 0.000 title claims abstract description 101
- 229920000642 polymer Polymers 0.000 claims abstract description 194
- 239000000178 monomer Substances 0.000 claims abstract description 102
- 230000009477 glass transition Effects 0.000 claims abstract description 37
- 238000000465 moulding Methods 0.000 claims abstract description 13
- 239000002245 particle Substances 0.000 claims description 34
- 238000005520 cutting process Methods 0.000 claims description 29
- 238000000034 method Methods 0.000 claims description 26
- 238000002296 dynamic light scattering Methods 0.000 claims description 5
- 239000003795 chemical substances by application Substances 0.000 abstract description 44
- 238000004073 vulcanization Methods 0.000 abstract description 37
- 238000010438 heat treatment Methods 0.000 abstract description 27
- 238000003878 thermal aging Methods 0.000 abstract 1
- 238000006116 polymerization reaction Methods 0.000 description 228
- 238000004458 analytical method Methods 0.000 description 88
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 75
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 54
- 230000015572 biosynthetic process Effects 0.000 description 52
- 238000005259 measurement Methods 0.000 description 52
- 238000003786 synthesis reaction Methods 0.000 description 52
- 230000000704 physical effect Effects 0.000 description 44
- 239000000126 substance Substances 0.000 description 37
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 35
- 239000000203 mixture Substances 0.000 description 34
- 229910052757 nitrogen Inorganic materials 0.000 description 31
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical compound C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 29
- 238000001816 cooling Methods 0.000 description 26
- 238000009826 distribution Methods 0.000 description 26
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 25
- 239000003505 polymerization initiator Substances 0.000 description 25
- 239000011591 potassium Substances 0.000 description 25
- 229910052700 potassium Inorganic materials 0.000 description 25
- 238000005292 vacuum distillation Methods 0.000 description 25
- 238000011156 evaluation Methods 0.000 description 24
- YWPOLRBWRRKLMW-UHFFFAOYSA-M sodium;naphthalene-2-sulfonate Chemical compound [Na+].C1=CC=CC2=CC(S(=O)(=O)[O-])=CC=C21 YWPOLRBWRRKLMW-UHFFFAOYSA-M 0.000 description 23
- LWMFAFLIWMPZSX-UHFFFAOYSA-N bis[2-(4,5-dihydro-1h-imidazol-2-yl)propan-2-yl]diazene Chemical compound N=1CCNC=1C(C)(C)N=NC(C)(C)C1=NCCN1 LWMFAFLIWMPZSX-UHFFFAOYSA-N 0.000 description 22
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 21
- 229920001174 Diethylhydroxylamine Polymers 0.000 description 21
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 21
- 239000007864 aqueous solution Substances 0.000 description 21
- FVCOIAYSJZGECG-UHFFFAOYSA-N diethylhydroxylamine Chemical compound CCN(O)CC FVCOIAYSJZGECG-UHFFFAOYSA-N 0.000 description 21
- 239000003112 inhibitor Substances 0.000 description 21
- KNGDIIGATFHORF-UHFFFAOYSA-N 1-phenylpentylsulfanylmethanedithioic acid Chemical compound CCCCC(C1=CC=CC=C1)SC(=S)S KNGDIIGATFHORF-UHFFFAOYSA-N 0.000 description 20
- 238000007654 immersion Methods 0.000 description 19
- 239000000047 product Substances 0.000 description 19
- 239000011248 coating agent Substances 0.000 description 18
- 238000000576 coating method Methods 0.000 description 18
- 230000003712 anti-aging effect Effects 0.000 description 17
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 16
- WSFSSNUMVMOOMR-UHFFFAOYSA-N formaldehyde Natural products O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 16
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 15
- 238000007720 emulsion polymerization reaction Methods 0.000 description 14
- 229920001519 homopolymer Polymers 0.000 description 13
- 230000032683 aging Effects 0.000 description 12
- GXCDLJXPZVCHBX-UHFFFAOYSA-N 3-methylpent-1-yn-3-yl carbamate Chemical compound CCC(C)(C#C)OC(N)=O GXCDLJXPZVCHBX-UHFFFAOYSA-N 0.000 description 11
- -1 aromatic vinyl compound Chemical class 0.000 description 11
- 230000000052 comparative effect Effects 0.000 description 11
- 229920000428 triblock copolymer Polymers 0.000 description 10
- OZAIFHULBGXAKX-UHFFFAOYSA-N 2-(2-cyanopropan-2-yldiazenyl)-2-methylpropanenitrile Chemical compound N#CC(C)(C)N=NC(C)(C)C#N OZAIFHULBGXAKX-UHFFFAOYSA-N 0.000 description 9
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 9
- 229920001577 copolymer Polymers 0.000 description 9
- 238000012360 testing method Methods 0.000 description 9
- 238000004945 emulsification Methods 0.000 description 8
- 238000004519 manufacturing process Methods 0.000 description 8
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 8
- 229920001971 elastomer Polymers 0.000 description 7
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Substances C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 7
- 239000000243 solution Substances 0.000 description 7
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 6
- XLOMVQKBTHCTTD-UHFFFAOYSA-N Zinc monoxide Chemical compound [Zn]=O XLOMVQKBTHCTTD-UHFFFAOYSA-N 0.000 description 6
- 150000001875 compounds Chemical class 0.000 description 6
- 239000012990 dithiocarbamate Substances 0.000 description 6
- 229920001084 poly(chloroprene) Polymers 0.000 description 6
- 239000007787 solid Substances 0.000 description 6
- 206010020751 Hypersensitivity Diseases 0.000 description 5
- 230000003679 aging effect Effects 0.000 description 5
- 230000007815 allergy Effects 0.000 description 5
- DMBHHRLKUKUOEG-UHFFFAOYSA-N diphenylamine Chemical class C=1C=CC=CC=1NC1=CC=CC=C1 DMBHHRLKUKUOEG-UHFFFAOYSA-N 0.000 description 5
- KUDUQBURMYMBIJ-UHFFFAOYSA-N 2-prop-2-enoyloxyethyl prop-2-enoate Chemical compound C=CC(=O)OCCOC(=O)C=C KUDUQBURMYMBIJ-UHFFFAOYSA-N 0.000 description 4
- ZRALSGWEFCBTJO-UHFFFAOYSA-N Guanidine Chemical compound NC(N)=N ZRALSGWEFCBTJO-UHFFFAOYSA-N 0.000 description 4
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 4
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 4
- 239000000853 adhesive Substances 0.000 description 4
- 230000001070 adhesive effect Effects 0.000 description 4
- 125000003118 aryl group Chemical group 0.000 description 4
- AGCPVOYGTAIJAP-UHFFFAOYSA-N benzyl pyrrole-1-carbodithioate Chemical compound C1=CC=CN1C(=S)SCC1=CC=CC=C1 AGCPVOYGTAIJAP-UHFFFAOYSA-N 0.000 description 4
- DKVNPHBNOWQYFE-UHFFFAOYSA-N carbamodithioic acid Chemical compound NC(S)=S DKVNPHBNOWQYFE-UHFFFAOYSA-N 0.000 description 4
- 239000007789 gas Substances 0.000 description 4
- 238000005227 gel permeation chromatography Methods 0.000 description 4
- 230000001771 impaired effect Effects 0.000 description 4
- 238000002156 mixing Methods 0.000 description 4
- IWDCLRJOBJJRNH-UHFFFAOYSA-N p-cresol Chemical compound CC1=CC=C(O)C=C1 IWDCLRJOBJJRNH-UHFFFAOYSA-N 0.000 description 4
- 230000000379 polymerizing effect Effects 0.000 description 4
- 229920006395 saturated elastomer Polymers 0.000 description 4
- 229910052717 sulfur Inorganic materials 0.000 description 4
- 239000011593 sulfur Substances 0.000 description 4
- 125000003396 thiol group Chemical group [H]S* 0.000 description 4
- UMGDCJDMYOKAJW-UHFFFAOYSA-N thiourea Chemical compound NC(N)=S UMGDCJDMYOKAJW-UHFFFAOYSA-N 0.000 description 4
- 229920002554 vinyl polymer Polymers 0.000 description 4
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 3
- 238000005160 1H NMR spectroscopy Methods 0.000 description 3
- OZAIFHULBGXAKX-VAWYXSNFSA-N AIBN Substances N#CC(C)(C)\N=N\C(C)(C)C#N OZAIFHULBGXAKX-VAWYXSNFSA-N 0.000 description 3
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 3
- 239000004793 Polystyrene Substances 0.000 description 3
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 3
- 230000015271 coagulation Effects 0.000 description 3
- 238000005345 coagulation Methods 0.000 description 3
- 125000004122 cyclic group Chemical group 0.000 description 3
- 239000003995 emulsifying agent Substances 0.000 description 3
- 239000000839 emulsion Substances 0.000 description 3
- 150000002430 hydrocarbons Chemical group 0.000 description 3
- 239000002244 precipitate Substances 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 238000000197 pyrolysis Methods 0.000 description 3
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 3
- 229930195734 saturated hydrocarbon Natural products 0.000 description 3
- 229930195735 unsaturated hydrocarbon Natural products 0.000 description 3
- 239000011787 zinc oxide Substances 0.000 description 3
- MYRTYDVEIRVNKP-UHFFFAOYSA-N 1,2-Divinylbenzene Chemical compound C=CC1=CC=CC=C1C=C MYRTYDVEIRVNKP-UHFFFAOYSA-N 0.000 description 2
- WEERVPDNCOGWJF-UHFFFAOYSA-N 1,4-bis(ethenyl)benzene Chemical compound C=CC1=CC=C(C=C)C=C1 WEERVPDNCOGWJF-UHFFFAOYSA-N 0.000 description 2
- HECLRDQVFMWTQS-RGOKHQFPSA-N 1755-01-7 Chemical compound C1[C@H]2[C@@H]3CC=C[C@@H]3[C@@H]1C=C2 HECLRDQVFMWTQS-RGOKHQFPSA-N 0.000 description 2
- XFCMNSHQOZQILR-UHFFFAOYSA-N 2-[2-(2-methylprop-2-enoyloxy)ethoxy]ethyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCOCCOC(=O)C(C)=C XFCMNSHQOZQILR-UHFFFAOYSA-N 0.000 description 2
- INQDDHNZXOAFFD-UHFFFAOYSA-N 2-[2-(2-prop-2-enoyloxyethoxy)ethoxy]ethyl prop-2-enoate Chemical compound C=CC(=O)OCCOCCOCCOC(=O)C=C INQDDHNZXOAFFD-UHFFFAOYSA-N 0.000 description 2
- AISZNMCRXZWVAT-UHFFFAOYSA-N 2-ethylsulfanylcarbothioylsulfanyl-2-methylpropanenitrile Chemical compound CCSC(=S)SC(C)(C)C#N AISZNMCRXZWVAT-UHFFFAOYSA-N 0.000 description 2
- VSKJLJHPAFKHBX-UHFFFAOYSA-N 2-methylbuta-1,3-diene;styrene Chemical compound CC(=C)C=C.C=CC1=CC=CC=C1.C=CC1=CC=CC=C1 VSKJLJHPAFKHBX-UHFFFAOYSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical group COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 2
- CHJJGSNFBQVOTG-UHFFFAOYSA-N N-methyl-guanidine Natural products CNC(N)=N CHJJGSNFBQVOTG-UHFFFAOYSA-N 0.000 description 2
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 239000012987 RAFT agent Substances 0.000 description 2
- UCKMPCXJQFINFW-UHFFFAOYSA-N Sulphide Chemical compound [S-2] UCKMPCXJQFINFW-UHFFFAOYSA-N 0.000 description 2
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 2
- 239000007983 Tris buffer Substances 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Natural products NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- BGYHLZZASRKEJE-UHFFFAOYSA-N [3-[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoyloxy]-2,2-bis[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoyloxymethyl]propyl] 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoate Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)OCC(COC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)(COC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)COC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 BGYHLZZASRKEJE-UHFFFAOYSA-N 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 125000003342 alkenyl group Chemical group 0.000 description 2
- 125000000217 alkyl group Chemical group 0.000 description 2
- 239000003963 antioxidant agent Substances 0.000 description 2
- 230000003078 antioxidant effect Effects 0.000 description 2
- VDLOXZRCFJZRJH-UHFFFAOYSA-N benzyl ethanedithioate Chemical compound CC(=S)SCC1=CC=CC=C1 VDLOXZRCFJZRJH-UHFFFAOYSA-N 0.000 description 2
- 230000006208 butylation Effects 0.000 description 2
- 238000011088 calibration curve Methods 0.000 description 2
- 239000000919 ceramic Substances 0.000 description 2
- 239000007795 chemical reaction product Substances 0.000 description 2
- 239000000460 chlorine Substances 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- 238000001514 detection method Methods 0.000 description 2
- SWSQBOPZIKWTGO-UHFFFAOYSA-N dimethylaminoamidine Natural products CN(C)C(N)=N SWSQBOPZIKWTGO-UHFFFAOYSA-N 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 239000003814 drug Substances 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- STVZJERGLQHEKB-UHFFFAOYSA-N ethylene glycol dimethacrylate Substances CC(=C)C(=O)OCCOC(=O)C(C)=C STVZJERGLQHEKB-UHFFFAOYSA-N 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 125000005842 heteroatom Chemical group 0.000 description 2
- 125000000623 heterocyclic group Chemical group 0.000 description 2
- XXMIOPMDWAUFGU-UHFFFAOYSA-N hexane-1,6-diol Chemical compound OCCCCCCO XXMIOPMDWAUFGU-UHFFFAOYSA-N 0.000 description 2
- 150000002431 hydrogen Chemical class 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 229910052739 hydrogen Inorganic materials 0.000 description 2
- KQNPFQTWMSNSAP-UHFFFAOYSA-N isobutyric acid Chemical compound CC(C)C(O)=O KQNPFQTWMSNSAP-UHFFFAOYSA-N 0.000 description 2
- 239000000395 magnesium oxide Substances 0.000 description 2
- CPLXHLVBOLITMK-UHFFFAOYSA-N magnesium oxide Inorganic materials [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 2
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 description 2
- 238000000691 measurement method Methods 0.000 description 2
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 2
- KVBGVZZKJNLNJU-UHFFFAOYSA-M naphthalene-2-sulfonate Chemical compound C1=CC=CC2=CC(S(=O)(=O)[O-])=CC=C21 KVBGVZZKJNLNJU-UHFFFAOYSA-M 0.000 description 2
- CRSOQBOWXPBRES-UHFFFAOYSA-N neopentane Chemical compound CC(C)(C)C CRSOQBOWXPBRES-UHFFFAOYSA-N 0.000 description 2
- 239000003973 paint Substances 0.000 description 2
- 229950000688 phenothiazine Drugs 0.000 description 2
- OJMIONKXNSYLSR-UHFFFAOYSA-N phosphorous acid Chemical compound OP(O)O OJMIONKXNSYLSR-UHFFFAOYSA-N 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 239000007870 radical polymerization initiator Substances 0.000 description 2
- 239000011347 resin Substances 0.000 description 2
- 229920005989 resin Polymers 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 159000000000 sodium salts Chemical class 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 230000002194 synthesizing effect Effects 0.000 description 2
- 238000009864 tensile test Methods 0.000 description 2
- 229920002725 thermoplastic elastomer Polymers 0.000 description 2
- KUAZQDVKQLNFPE-UHFFFAOYSA-N thiram Chemical compound CN(C)C(=S)SSC(=S)N(C)C KUAZQDVKQLNFPE-UHFFFAOYSA-N 0.000 description 2
- 229960002447 thiram Drugs 0.000 description 2
- HVLLSGMXQDNUAL-UHFFFAOYSA-N triphenyl phosphite Chemical compound C=1C=CC=CC=1OP(OC=1C=CC=CC=1)OC1=CC=CC=C1 HVLLSGMXQDNUAL-UHFFFAOYSA-N 0.000 description 2
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 2
- FGHOOJSIEHYJFQ-UHFFFAOYSA-N (2,4-ditert-butylphenyl) dihydrogen phosphite Chemical compound CC(C)(C)C1=CC=C(OP(O)O)C(C(C)(C)C)=C1 FGHOOJSIEHYJFQ-UHFFFAOYSA-N 0.000 description 1
- PLYLPJCEVQXSHZ-UHFFFAOYSA-N (2-nonylphenyl) diphenyl phosphite Chemical compound CCCCCCCCCC1=CC=CC=C1OP(OC=1C=CC=CC=1)OC1=CC=CC=C1 PLYLPJCEVQXSHZ-UHFFFAOYSA-N 0.000 description 1
- FNBPLKKPMRILKY-UHFFFAOYSA-N (4-ethenylphenyl)methyl benzenecarbodithioate Chemical compound C1=CC(C=C)=CC=C1CSC(=S)C1=CC=CC=C1 FNBPLKKPMRILKY-UHFFFAOYSA-N 0.000 description 1
- QFMZQPDHXULLKC-UHFFFAOYSA-N 1,2-bis(diphenylphosphino)ethane Chemical compound C=1C=CC=CC=1P(C=1C=CC=CC=1)CCP(C=1C=CC=CC=1)C1=CC=CC=C1 QFMZQPDHXULLKC-UHFFFAOYSA-N 0.000 description 1
- ZJQIXGGEADDPQB-UHFFFAOYSA-N 1,2-bis(ethenyl)-3,4-dimethylbenzene Chemical compound CC1=CC=C(C=C)C(C=C)=C1C ZJQIXGGEADDPQB-UHFFFAOYSA-N 0.000 description 1
- QLLUAUADIMPKIH-UHFFFAOYSA-N 1,2-bis(ethenyl)naphthalene Chemical compound C1=CC=CC2=C(C=C)C(C=C)=CC=C21 QLLUAUADIMPKIH-UHFFFAOYSA-N 0.000 description 1
- QWUWMCYKGHVNAV-UHFFFAOYSA-N 1,2-dihydrostilbene Chemical group C=1C=CC=CC=1CCC1=CC=CC=C1 QWUWMCYKGHVNAV-UHFFFAOYSA-N 0.000 description 1
- KOMNUTZXSVSERR-UHFFFAOYSA-N 1,3,5-tris(prop-2-enyl)-1,3,5-triazinane-2,4,6-trione Chemical compound C=CCN1C(=O)N(CC=C)C(=O)N(CC=C)C1=O KOMNUTZXSVSERR-UHFFFAOYSA-N 0.000 description 1
- PRJNEUBECVAVAG-UHFFFAOYSA-N 1,3-bis(ethenyl)benzene Chemical compound C=CC1=CC=CC(C=C)=C1 PRJNEUBECVAVAG-UHFFFAOYSA-N 0.000 description 1
- YHMYGUUIMTVXNW-UHFFFAOYSA-N 1,3-dihydrobenzimidazole-2-thione Chemical compound C1=CC=C2NC(S)=NC2=C1 YHMYGUUIMTVXNW-UHFFFAOYSA-N 0.000 description 1
- VZORBIIKPJNHTD-UHFFFAOYSA-N 1,4-bis(ethenyl)naphthalene Chemical compound C1=CC=C2C(C=C)=CC=C(C=C)C2=C1 VZORBIIKPJNHTD-UHFFFAOYSA-N 0.000 description 1
- XZZWOTQMUOIIFX-UHFFFAOYSA-N 1-(2-diphenoxyphosphanyloxypropoxy)propan-2-yl diphenyl phosphite Chemical compound C=1C=CC=CC=1OP(OC=1C=CC=CC=1)OC(C)COCC(C)OP(OC=1C=CC=CC=1)OC1=CC=CC=C1 XZZWOTQMUOIIFX-UHFFFAOYSA-N 0.000 description 1
- VYDCAOMTIYRSAG-UHFFFAOYSA-N 1-(4-methoxyphenyl)ethyl benzenecarbodithioate Chemical compound C1=CC(OC)=CC=C1C(C)SC(=S)C1=CC=CC=C1 VYDCAOMTIYRSAG-UHFFFAOYSA-N 0.000 description 1
- PXHVIFGBSGEVJJ-UHFFFAOYSA-N 1-benzyl-4-methoxycyclohexa-2,4-diene-1-carbodithioic acid Chemical compound COC1=CCC(C=C1)(CC2=CC=CC=C2)C(=S)S PXHVIFGBSGEVJJ-UHFFFAOYSA-N 0.000 description 1
- VETPHHXZEJAYOB-UHFFFAOYSA-N 1-n,4-n-dinaphthalen-2-ylbenzene-1,4-diamine Chemical compound C1=CC=CC2=CC(NC=3C=CC(NC=4C=C5C=CC=CC5=CC=4)=CC=3)=CC=C21 VETPHHXZEJAYOB-UHFFFAOYSA-N 0.000 description 1
- QEZSTBGQYFCJCW-UHFFFAOYSA-N 1-phenylethyl benzenecarbodithioate Chemical compound C=1C=CC=CC=1C(C)SC(=S)C1=CC=CC=C1 QEZSTBGQYFCJCW-UHFFFAOYSA-N 0.000 description 1
- SDUXJPKZYYBNIX-UHFFFAOYSA-N 1-phenylpropan-2-yl 4-chlorobenzenecarbodithioate Chemical compound ClC1=CC=C(C(=S)SC(C)CC2=CC=CC=C2)C=C1 SDUXJPKZYYBNIX-UHFFFAOYSA-N 0.000 description 1
- UFUXVJFOILLERS-UHFFFAOYSA-N 2,2-dimethylpropane-1,3-diol;prop-2-enoic acid Chemical compound OC(=O)C=C.OCC(C)(C)CO UFUXVJFOILLERS-UHFFFAOYSA-N 0.000 description 1
- LIFLRQVHKGGNSG-UHFFFAOYSA-N 2,3-dichlorobuta-1,3-diene Chemical compound ClC(=C)C(Cl)=C LIFLRQVHKGGNSG-UHFFFAOYSA-N 0.000 description 1
- ICKWICRCANNIBI-UHFFFAOYSA-N 2,4-di-tert-butylphenol Chemical compound CC(C)(C)C1=CC=C(O)C(C(C)(C)C)=C1 ICKWICRCANNIBI-UHFFFAOYSA-N 0.000 description 1
- JAZQIRAEJMLXFV-UHFFFAOYSA-N 2,6-bis(ethenyl)naphthalene Chemical compound C1=C(C=C)C=CC2=CC(C=C)=CC=C21 JAZQIRAEJMLXFV-UHFFFAOYSA-N 0.000 description 1
- GJDRKHHGPHLVNI-UHFFFAOYSA-N 2,6-ditert-butyl-4-(diethoxyphosphorylmethyl)phenol Chemical compound CCOP(=O)(OCC)CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 GJDRKHHGPHLVNI-UHFFFAOYSA-N 0.000 description 1
- KVXWEZPUXPPIBH-UHFFFAOYSA-N 2-(2,4,4-trimethylpentan-2-yl)benzenecarbodithioic acid Chemical compound CC(C)(C)CC(C)(C)C1=CC=CC=C1C(=S)S KVXWEZPUXPPIBH-UHFFFAOYSA-N 0.000 description 1
- XBEIANFIOZTEDE-UHFFFAOYSA-N 2-(benzenecarbonothioylsulfanyl)acetic acid Chemical compound OC(=O)CSC(=S)C1=CC=CC=C1 XBEIANFIOZTEDE-UHFFFAOYSA-N 0.000 description 1
- FIWORJNABUKCGU-UHFFFAOYSA-N 2-[(3-ethenylphenyl)methyl]benzenecarbodithioic acid Chemical compound C=CC1=CC=CC(=C1)CC2=CC=CC=C2C(=S)S FIWORJNABUKCGU-UHFFFAOYSA-N 0.000 description 1
- KJFDMPHFBCONGF-UHFFFAOYSA-N 2-[2-(4-chlorophenyl)propan-2-yl]benzenecarbodithioic acid Chemical compound CC(C)(C1=CC=C(C=C1)Cl)C2=CC=CC=C2C(=S)S KJFDMPHFBCONGF-UHFFFAOYSA-N 0.000 description 1
- HWSSEYVMGDIFMH-UHFFFAOYSA-N 2-[2-[2-(2-methylprop-2-enoyloxy)ethoxy]ethoxy]ethyl 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCCOCCOCCOC(=O)C(C)=C HWSSEYVMGDIFMH-UHFFFAOYSA-N 0.000 description 1
- GHBJFPOIOAVHFC-UHFFFAOYSA-N 2-but-2-enyl-3,4-dichlorobenzenecarbodithioic acid Chemical compound CC=CCC1=C(C=CC(=C1Cl)Cl)C(=S)S GHBJFPOIOAVHFC-UHFFFAOYSA-N 0.000 description 1
- DEDBHVFXKCVOCV-UHFFFAOYSA-N 2-butylsulfanylcarbothioylsulfanylbutanedioic acid Chemical compound CCCCSC(=S)SC(C(O)=O)CC(O)=O DEDBHVFXKCVOCV-UHFFFAOYSA-N 0.000 description 1
- YGQPVBKYIVLGEE-UHFFFAOYSA-N 2-butylsulfanylcarbothioylsulfanylpropanamide Chemical compound CCCCSC(=S)SC(C)C(N)=O YGQPVBKYIVLGEE-UHFFFAOYSA-N 0.000 description 1
- VQUDUXBWOHBISV-UHFFFAOYSA-N 2-butylsulfanylcarbothioylsulfanylpropanoic acid Chemical compound CCCCSC(=S)SC(C)C(O)=O VQUDUXBWOHBISV-UHFFFAOYSA-N 0.000 description 1
- RGRNGKKTVLGVCB-UHFFFAOYSA-N 2-cyanobutan-2-yl N-pyrrol-1-ylcarbamodithioate Chemical compound C(#N)C(C)(CC)SC(NN1C=CC=C1)=S RGRNGKKTVLGVCB-UHFFFAOYSA-N 0.000 description 1
- LINFYYCWDHJMLA-UHFFFAOYSA-N 2-cyanobutan-2-yl pyrrole-1-carbodithioate Chemical compound CCC(C)(C#N)SC(=S)N1C=CC=C1 LINFYYCWDHJMLA-UHFFFAOYSA-N 0.000 description 1
- IDSLBLWCPSAZBL-UHFFFAOYSA-N 2-cyanopropan-2-yl benzenecarbodithioate Chemical compound N#CC(C)(C)SC(=S)C1=CC=CC=C1 IDSLBLWCPSAZBL-UHFFFAOYSA-N 0.000 description 1
- VNJGQXCOPWYQRW-UHFFFAOYSA-N 2-cyanopropan-2-yl n,n-dimethylcarbamodithioate Chemical compound CN(C)C(=S)SC(C)(C)C#N VNJGQXCOPWYQRW-UHFFFAOYSA-N 0.000 description 1
- KOQQFZSGVDYJLH-UHFFFAOYSA-N 2-cyanopropan-2-yl pyrrole-1-carbodithioate Chemical compound N#CC(C)(C)SC(=S)N1C=CC=C1 KOQQFZSGVDYJLH-UHFFFAOYSA-N 0.000 description 1
- QSVOWVXHKOQYIP-UHFFFAOYSA-N 2-dodecylsulfanylcarbothioylsulfanyl-2-methylpropanenitrile Chemical compound CCCCCCCCCCCCSC(=S)SC(C)(C)C#N QSVOWVXHKOQYIP-UHFFFAOYSA-N 0.000 description 1
- DZFGVGDQHQHOKZ-UHFFFAOYSA-N 2-dodecylsulfanylcarbothioylsulfanyl-2-methylpropanoic acid Chemical compound CCCCCCCCCCCCSC(=S)SC(C)(C)C(O)=O DZFGVGDQHQHOKZ-UHFFFAOYSA-N 0.000 description 1
- URUIKGRSOJEVQG-UHFFFAOYSA-N 2-dodecylsulfanylcarbothioylsulfanylacetonitrile Chemical compound CCCCCCCCCCCCSC(=S)SCC#N URUIKGRSOJEVQG-UHFFFAOYSA-N 0.000 description 1
- WMZLRCVBTNRMSP-UHFFFAOYSA-N 2-dodecylsulfanylcarbothioylsulfanylbutanedioic acid Chemical compound CCCCCCCCCCCCSC(=S)SC(C(O)=O)CC(O)=O WMZLRCVBTNRMSP-UHFFFAOYSA-N 0.000 description 1
- CFCFZJHCTNKHGJ-UHFFFAOYSA-N 2-dodecylsulfanylcarbothioylsulfanylpropanoic acid Chemical compound CCCCCCCCCCCCSC(=S)SC(C)C(O)=O CFCFZJHCTNKHGJ-UHFFFAOYSA-N 0.000 description 1
- XKZGIJICHCVXFV-UHFFFAOYSA-N 2-ethylhexyl diphenyl phosphite Chemical compound C=1C=CC=CC=1OP(OCC(CC)CCCC)OC1=CC=CC=C1 XKZGIJICHCVXFV-UHFFFAOYSA-N 0.000 description 1
- JTUKWQIDYANLFR-UHFFFAOYSA-N 2-phenylpropan-2-yl 4-chlorobenzenecarbodithioate Chemical compound C=1C=CC=CC=1C(C)(C)SC(=S)C1=CC=C(Cl)C=C1 JTUKWQIDYANLFR-UHFFFAOYSA-N 0.000 description 1
- KOBJYYDWSKDEGY-UHFFFAOYSA-N 2-phenylpropan-2-yl benzenecarbodithioate Chemical compound C=1C=CC=CC=1C(C)(C)SC(=S)C1=CC=CC=C1 KOBJYYDWSKDEGY-UHFFFAOYSA-N 0.000 description 1
- SDPHVCRQEXFDHR-UHFFFAOYSA-N 2-phenylpropan-2-yl naphthalene-1-carboxylate Chemical compound CC(C)(C1=CC=CC=C1)OC(=O)C1=CC=CC2=CC=CC=C12 SDPHVCRQEXFDHR-UHFFFAOYSA-N 0.000 description 1
- PFANXOISJYKQRP-UHFFFAOYSA-N 2-tert-butyl-4-[1-(5-tert-butyl-4-hydroxy-2-methylphenyl)butyl]-5-methylphenol Chemical compound C=1C(C(C)(C)C)=C(O)C=C(C)C=1C(CCC)C1=CC(C(C)(C)C)=C(O)C=C1C PFANXOISJYKQRP-UHFFFAOYSA-N 0.000 description 1
- PZRWFKGUFWPFID-UHFFFAOYSA-N 3,9-dioctadecoxy-2,4,8,10-tetraoxa-3,9-diphosphaspiro[5.5]undecane Chemical compound C1OP(OCCCCCCCCCCCCCCCCCC)OCC21COP(OCCCCCCCCCCCCCCCCCC)OC2 PZRWFKGUFWPFID-UHFFFAOYSA-N 0.000 description 1
- RDFQSFOGKVZWKF-UHFFFAOYSA-N 3-hydroxy-2,2-dimethylpropanoic acid Chemical compound OCC(C)(C)C(O)=O RDFQSFOGKVZWKF-UHFFFAOYSA-N 0.000 description 1
- KBYXOHPSTSFPHJ-UHFFFAOYSA-N 3-tert-butylsulfanylcarbothioylsulfanylpropanoic acid Chemical compound CC(C)(C)SC(=S)SCCC(O)=O KBYXOHPSTSFPHJ-UHFFFAOYSA-N 0.000 description 1
- BWENLBAVDYTSAM-UHFFFAOYSA-N 4,5,8-tributyl-1,2-bis(ethenyl)naphthalene Chemical compound C(=C)C1=C(C2=C(C=CC(=C2C(=C1)CCCC)CCCC)CCCC)C=C BWENLBAVDYTSAM-UHFFFAOYSA-N 0.000 description 1
- QRLSTWVLSWCGBT-UHFFFAOYSA-N 4-((4,6-bis(octylthio)-1,3,5-triazin-2-yl)amino)-2,6-di-tert-butylphenol Chemical compound CCCCCCCCSC1=NC(SCCCCCCCC)=NC(NC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=N1 QRLSTWVLSWCGBT-UHFFFAOYSA-N 0.000 description 1
- UJAWGGOCYUPCPS-UHFFFAOYSA-N 4-(2-phenylpropan-2-yl)-n-[4-(2-phenylpropan-2-yl)phenyl]aniline Chemical compound C=1C=C(NC=2C=CC(=CC=2)C(C)(C)C=2C=CC=CC=2)C=CC=1C(C)(C)C1=CC=CC=C1 UJAWGGOCYUPCPS-UHFFFAOYSA-N 0.000 description 1
- PRWJPWSKLXYEPD-UHFFFAOYSA-N 4-[4,4-bis(5-tert-butyl-4-hydroxy-2-methylphenyl)butan-2-yl]-2-tert-butyl-5-methylphenol Chemical compound C=1C(C(C)(C)C)=C(O)C=C(C)C=1C(C)CC(C=1C(=CC(O)=C(C=1)C(C)(C)C)C)C1=CC(C(C)(C)C)=C(O)C=C1C PRWJPWSKLXYEPD-UHFFFAOYSA-N 0.000 description 1
- DBCAQXHNJOFNGC-UHFFFAOYSA-N 4-bromo-1,1,1-trifluorobutane Chemical compound FC(F)(F)CCCBr DBCAQXHNJOFNGC-UHFFFAOYSA-N 0.000 description 1
- WLKKWOXFCCFMSO-UHFFFAOYSA-N 4-chloro-2-(2-cyanopropan-2-yl)benzenecarbodithioic acid Chemical compound CC(C)(C#N)C1=C(C=CC(=C1)Cl)C(=S)S WLKKWOXFCCFMSO-UHFFFAOYSA-N 0.000 description 1
- XDVRNILDMPCUQJ-UHFFFAOYSA-N 4-chloro-2-[(4-nitrophenyl)methyl]benzenecarbodithioic acid Chemical compound C1=CC(=CC=C1CC2=C(C=CC(=C2)Cl)C(=S)S)[N+](=O)[O-] XDVRNILDMPCUQJ-UHFFFAOYSA-N 0.000 description 1
- ZZMVLMVFYMGSMY-UHFFFAOYSA-N 4-n-(4-methylpentan-2-yl)-1-n-phenylbenzene-1,4-diamine Chemical compound C1=CC(NC(C)CC(C)C)=CC=C1NC1=CC=CC=C1 ZZMVLMVFYMGSMY-UHFFFAOYSA-N 0.000 description 1
- JSEJKZKNJLSZRM-UHFFFAOYSA-N 5-phenylpentylsulfanylmethanedithioic acid Chemical compound C1=CC=C(C=C1)CCCCCSC(=S)S JSEJKZKNJLSZRM-UHFFFAOYSA-N 0.000 description 1
- ZVVFVKJZNVSANF-UHFFFAOYSA-N 6-[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoyloxy]hexyl 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoate Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)OCCCCCCOC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 ZVVFVKJZNVSANF-UHFFFAOYSA-N 0.000 description 1
- UYQYTUYNNYZATF-UHFFFAOYSA-N 6-methyl-4,6-bis(octylsulfanylmethyl)cyclohexa-1,3-dien-1-ol Chemical compound CCCCCCCCSCC1=CC=C(O)C(C)(CSCCCCCCCC)C1 UYQYTUYNNYZATF-UHFFFAOYSA-N 0.000 description 1
- ADRNSOYXKABLGT-UHFFFAOYSA-N 8-methylnonyl diphenyl phosphite Chemical compound C=1C=CC=CC=1OP(OCCCCCCCC(C)C)OC1=CC=CC=C1 ADRNSOYXKABLGT-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 1
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical group C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 1
- 239000004342 Benzoyl peroxide Substances 0.000 description 1
- OMPJBNCRMGITSC-UHFFFAOYSA-N Benzoylperoxide Chemical compound C=1C=CC=CC=1C(=O)OOC(=O)C1=CC=CC=C1 OMPJBNCRMGITSC-UHFFFAOYSA-N 0.000 description 1
- BADSJZKJOMTNJG-UHFFFAOYSA-N C(CCCCCCCC)C1=C(C=CC=C1)C(O)(C(CO)(CO)CO)C1=C(C=CC=C1)CCCCCCCCC Chemical compound C(CCCCCCCC)C1=C(C=CC=C1)C(O)(C(CO)(CO)CO)C1=C(C=CC=C1)CCCCCCCCC BADSJZKJOMTNJG-UHFFFAOYSA-N 0.000 description 1
- CLZVZBNIOFZSDI-UHFFFAOYSA-N C(N)(S)=S.C1(=CC=CC=C1)C(C)C=1NC=CN1 Chemical compound C(N)(S)=S.C1(=CC=CC=C1)C(C)C=1NC=CN1 CLZVZBNIOFZSDI-UHFFFAOYSA-N 0.000 description 1
- BTJTWYQNBOJOEE-UHFFFAOYSA-N CC(C1=CC=CC=C1)C2=CN=C(N2)C(=S)S Chemical compound CC(C1=CC=CC=C1)C2=CN=C(N2)C(=S)S BTJTWYQNBOJOEE-UHFFFAOYSA-N 0.000 description 1
- UHEWESWHMBTAQP-UHFFFAOYSA-N CC(CC1=CC=CC=C1)(C(NCCO)=O)SSSSC(S)=S Chemical class CC(CC1=CC=CC=C1)(C(NCCO)=O)SSSSC(S)=S UHEWESWHMBTAQP-UHFFFAOYSA-N 0.000 description 1
- LAYUJVUJCLOQIJ-UHFFFAOYSA-N CC1=C(C=CC(=C1C)N)C(=S)S Chemical compound CC1=C(C=CC(=C1C)N)C(=S)S LAYUJVUJCLOQIJ-UHFFFAOYSA-N 0.000 description 1
- BTXXUJXSBTXXHY-UHFFFAOYSA-N CC=CCC1(C=CC=CC1C(=S)S)Cl Chemical compound CC=CCC1(C=CC=CC1C(=S)S)Cl BTXXUJXSBTXXHY-UHFFFAOYSA-N 0.000 description 1
- JAERJOZSIIWZEJ-UHFFFAOYSA-N CCCCC(C1=CC=CC=C1)[SH2]C(S)=S Chemical compound CCCCC(C1=CC=CC=C1)[SH2]C(S)=S JAERJOZSIIWZEJ-UHFFFAOYSA-N 0.000 description 1
- IMKOQCZMBWERGR-UHFFFAOYSA-N CCN(CC)C(C1=CC=CC=C1)[SH2]C(S)=S Chemical compound CCN(CC)C(C1=CC=CC=C1)[SH2]C(S)=S IMKOQCZMBWERGR-UHFFFAOYSA-N 0.000 description 1
- BXDXOXGIVOWTSX-UHFFFAOYSA-N CCN(CC)C([S+](C(C)C)C(C(OCC)=O)C1=CC=CC=C1)=S Chemical compound CCN(CC)C([S+](C(C)C)C(C(OCC)=O)C1=CC=CC=C1)=S BXDXOXGIVOWTSX-UHFFFAOYSA-N 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 201000004624 Dermatitis Diseases 0.000 description 1
- 102100021202 Desmocollin-1 Human genes 0.000 description 1
- 239000012988 Dithioester Substances 0.000 description 1
- 101000968043 Homo sapiens Desmocollin-1 Proteins 0.000 description 1
- 101000880960 Homo sapiens Desmocollin-3 Proteins 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 1
- UTGQNNCQYDRXCH-UHFFFAOYSA-N N,N'-diphenyl-1,4-phenylenediamine Chemical compound C=1C=C(NC=2C=CC=CC=2)C=CC=1NC1=CC=CC=C1 UTGQNNCQYDRXCH-UHFFFAOYSA-N 0.000 description 1
- XQVWYOYUZDUNRW-UHFFFAOYSA-N N-Phenyl-1-naphthylamine Chemical compound C=1C=CC2=CC=CC=C2C=1NC1=CC=CC=C1 XQVWYOYUZDUNRW-UHFFFAOYSA-N 0.000 description 1
- OUBMGJOQLXMSNT-UHFFFAOYSA-N N-isopropyl-N'-phenyl-p-phenylenediamine Chemical compound C1=CC(NC(C)C)=CC=C1NC1=CC=CC=C1 OUBMGJOQLXMSNT-UHFFFAOYSA-N 0.000 description 1
- 239000006057 Non-nutritive feed additive Substances 0.000 description 1
- LZNWGSIDNAGRAJ-UHFFFAOYSA-N P(O)(O)OC(C(C(OP(O)O)(CCCCCCCCCCCCC)C1=CC=CC=C1)(C(OP(O)O)(CCCCCCCCCCCCC)C1=CC=CC=C1)C(OP(O)O)(CCCCCCCCCCCCC)C1=CC=CC=C1)(CCCCCCCCCCCCC)C1=CC=CC=C1 Chemical compound P(O)(O)OC(C(C(OP(O)O)(CCCCCCCCCCCCC)C1=CC=CC=C1)(C(OP(O)O)(CCCCCCCCCCCCC)C1=CC=CC=C1)C(OP(O)O)(CCCCCCCCCCCCC)C1=CC=CC=C1)(CCCCCCCCCCCCC)C1=CC=CC=C1 LZNWGSIDNAGRAJ-UHFFFAOYSA-N 0.000 description 1
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 1
- JKIJEFPNVSHHEI-UHFFFAOYSA-N Phenol, 2,4-bis(1,1-dimethylethyl)-, phosphite (3:1) Chemical compound CC(C)(C)C1=CC(C(C)(C)C)=CC=C1OP(OC=1C(=CC(=CC=1)C(C)(C)C)C(C)(C)C)OC1=CC=C(C(C)(C)C)C=C1C(C)(C)C JKIJEFPNVSHHEI-UHFFFAOYSA-N 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 241001483078 Phyto Species 0.000 description 1
- 239000006087 Silane Coupling Agent Substances 0.000 description 1
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 1
- DAKWPKUUDNSNPN-UHFFFAOYSA-N Trimethylolpropane triacrylate Chemical compound C=CC(=O)OCC(CC)(COC(=O)C=C)COC(=O)C=C DAKWPKUUDNSNPN-UHFFFAOYSA-N 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- ULQMPOIOSDXIGC-UHFFFAOYSA-N [2,2-dimethyl-3-(2-methylprop-2-enoyloxy)propyl] 2-methylprop-2-enoate Chemical compound CC(=C)C(=O)OCC(C)(C)COC(=O)C(C)=C ULQMPOIOSDXIGC-UHFFFAOYSA-N 0.000 description 1
- WJLHMGFCWANTFS-UHFFFAOYSA-N [2-(2-cyanoethyl)phenyl] carbamodithioate Chemical compound C(N)(=S)SC1=C(C=CC=C1)CCC#N WJLHMGFCWANTFS-UHFFFAOYSA-N 0.000 description 1
- CGRTZESQZZGAAU-UHFFFAOYSA-N [2-[3-[1-[3-(3-tert-butyl-4-hydroxy-5-methylphenyl)propanoyloxy]-2-methylpropan-2-yl]-2,4,8,10-tetraoxaspiro[5.5]undecan-9-yl]-2-methylpropyl] 3-(3-tert-butyl-4-hydroxy-5-methylphenyl)propanoate Chemical compound CC(C)(C)C1=C(O)C(C)=CC(CCC(=O)OCC(C)(C)C2OCC3(CO2)COC(OC3)C(C)(C)COC(=O)CCC=2C=C(C(O)=C(C)C=2)C(C)(C)C)=C1 CGRTZESQZZGAAU-UHFFFAOYSA-N 0.000 description 1
- JYSSGQITKNFRQE-UHFFFAOYSA-N [3-(4-anilinoanilino)-2-hydroxypropyl] 2-methylprop-2-enoate Chemical compound C1=CC(NCC(O)COC(=O)C(=C)C)=CC=C1NC1=CC=CC=C1 JYSSGQITKNFRQE-UHFFFAOYSA-N 0.000 description 1
- VMNKHSPZIGIPLL-UHFFFAOYSA-N [3-hydroxy-2,2-bis(hydroxymethyl)propyl] dihydrogen phosphite Chemical compound OCC(CO)(CO)COP(O)O VMNKHSPZIGIPLL-UHFFFAOYSA-N 0.000 description 1
- 125000005396 acrylic acid ester group Chemical group 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 238000006701 autoxidation reaction Methods 0.000 description 1
- 125000000751 azo group Chemical group [*]N=N[*] 0.000 description 1
- 235000019400 benzoyl peroxide Nutrition 0.000 description 1
- NTEOVSMTYUCTKA-UHFFFAOYSA-N benzyl 4-chlorobenzenecarbodithioate Chemical compound C1=CC(Cl)=CC=C1C(=S)SCC1=CC=CC=C1 NTEOVSMTYUCTKA-UHFFFAOYSA-N 0.000 description 1
- OZKGCSSAKRGEEB-UHFFFAOYSA-N benzyl N-(1,3-dioxoisoindol-2-yl)carbamodithioate Chemical compound C1(C=2C(C(N1NC(SCC1=CC=CC=C1)=S)=O)=CC=CC=2)=O OZKGCSSAKRGEEB-UHFFFAOYSA-N 0.000 description 1
- SWZWSQWBVVUAOH-UHFFFAOYSA-N benzyl N-pyrrol-1-ylcarbamodithioate Chemical compound S=C(Nn1cccc1)SCc1ccccc1 SWZWSQWBVVUAOH-UHFFFAOYSA-N 0.000 description 1
- NYGBMYHGSPZAOG-UHFFFAOYSA-N benzyl diethoxyphosphorylmethanedithioate Chemical compound CCOP(=O)(OCC)C(=S)SCC1=CC=CC=C1 NYGBMYHGSPZAOG-UHFFFAOYSA-N 0.000 description 1
- FJBQIWIQQRXHPK-UHFFFAOYSA-N benzyl imidazole-1-carbodithioate Chemical compound C1=CN=CN1C(=S)SCC1=CC=CC=C1 FJBQIWIQQRXHPK-UHFFFAOYSA-N 0.000 description 1
- SNBMGLUIIGFNFE-UHFFFAOYSA-N benzyl n,n-diethylcarbamodithioate Chemical compound CCN(CC)C(=S)SCC1=CC=CC=C1 SNBMGLUIIGFNFE-UHFFFAOYSA-N 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- LAKYXBYUROTWBI-UHFFFAOYSA-N bis(benzylsulfanyl)methanethione Chemical compound C=1C=CC=CC=1CSC(=S)SCC1=CC=CC=C1 LAKYXBYUROTWBI-UHFFFAOYSA-N 0.000 description 1
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical class C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 description 1
- MTAZNLWOLGHBHU-UHFFFAOYSA-N butadiene-styrene rubber Chemical compound C=CC=C.C=CC1=CC=CC=C1 MTAZNLWOLGHBHU-UHFFFAOYSA-N 0.000 description 1
- 239000001273 butane Substances 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-N carbonic acid monoamide Natural products NC(O)=O KXDHJXZQYSOELW-UHFFFAOYSA-N 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 230000001112 coagulating effect Effects 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- OMTFYPHYESIDFH-UHFFFAOYSA-N cyanomethyl 3,5-dimethylpyrazole-1-carbodithioate Chemical compound CC1=NN(C(=C1)C)C(=S)SCC#N OMTFYPHYESIDFH-UHFFFAOYSA-N 0.000 description 1
- FYACMHCOSCVNHO-UHFFFAOYSA-N cyanomethyl n-methyl-n-phenylcarbamodithioate Chemical compound N#CCSC(=S)N(C)C1=CC=CC=C1 FYACMHCOSCVNHO-UHFFFAOYSA-N 0.000 description 1
- 125000000753 cycloalkyl group Chemical group 0.000 description 1
- 125000004386 diacrylate group Chemical group 0.000 description 1
- XWWIKNHJHKAIEI-UHFFFAOYSA-N dibenzyl benzene-1,4-dicarbodithioate Chemical compound C=1C=C(C(=S)SCC=2C=CC=CC=2)C=CC=1C(=S)SCC1=CC=CC=C1 XWWIKNHJHKAIEI-UHFFFAOYSA-N 0.000 description 1
- 229920000359 diblock copolymer Polymers 0.000 description 1
- UZEFVQBWJSFOFE-UHFFFAOYSA-N dibutyl hydrogen phosphite Chemical compound CCCCOP(O)OCCCC UZEFVQBWJSFOFE-UHFFFAOYSA-N 0.000 description 1
- 238000001938 differential scanning calorimetry curve Methods 0.000 description 1
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 1
- OGVJEUDMQQIAPV-UHFFFAOYSA-N diphenyl tridecyl phosphite Chemical compound C=1C=CC=CC=1OP(OCCCCCCCCCCCCC)OC1=CC=CC=C1 OGVJEUDMQQIAPV-UHFFFAOYSA-N 0.000 description 1
- 150000004659 dithiocarbamates Chemical class 0.000 description 1
- 125000005022 dithioester group Chemical group 0.000 description 1
- 239000000806 elastomer Substances 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- ZOOODBUHSVUZEM-UHFFFAOYSA-N ethoxymethanedithioic acid Chemical compound CCOC(S)=S ZOOODBUHSVUZEM-UHFFFAOYSA-N 0.000 description 1
- OEBAUBJJYHXAHH-UHFFFAOYSA-N ethyl 2-ethanethioylsulfanylacetate Chemical compound CCOC(=O)CSC(C)=S OEBAUBJJYHXAHH-UHFFFAOYSA-N 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 1
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 229910017053 inorganic salt Inorganic materials 0.000 description 1
- 238000007689 inspection Methods 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- YDKNBNOOCSNPNS-UHFFFAOYSA-N methyl 1,3-benzoxazole-2-carboxylate Chemical compound C1=CC=C2OC(C(=O)OC)=NC2=C1 YDKNBNOOCSNPNS-UHFFFAOYSA-N 0.000 description 1
- DUWWHGPELOTTOE-UHFFFAOYSA-N n-(5-chloro-2,4-dimethoxyphenyl)-3-oxobutanamide Chemical compound COC1=CC(OC)=C(NC(=O)CC(C)=O)C=C1Cl DUWWHGPELOTTOE-UHFFFAOYSA-N 0.000 description 1
- IJDNQMDRQITEOD-UHFFFAOYSA-N n-butane Chemical compound CCCC IJDNQMDRQITEOD-UHFFFAOYSA-N 0.000 description 1
- OFBQJSOFQDEBGM-UHFFFAOYSA-N n-pentane Natural products CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 1
- 239000012875 nonionic emulsifier Substances 0.000 description 1
- SSDSCDGVMJFTEQ-UHFFFAOYSA-N octadecyl 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoate Chemical compound CCCCCCCCCCCCCCCCCCOC(=O)CCC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 SSDSCDGVMJFTEQ-UHFFFAOYSA-N 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- HLTIDCPTBRVHNR-UHFFFAOYSA-N phenyl 4-chloro-2-methylbenzenecarbodithioate Chemical compound CC1=C(C(=S)SC2=CC=CC=C2)C=CC(=C1)Cl HLTIDCPTBRVHNR-UHFFFAOYSA-N 0.000 description 1
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N phenylbenzene Natural products C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- JDIHPETWTXJUBS-UHFFFAOYSA-M potassium 3,5-dimethylpyrazole-1-carbodithioate Chemical compound [K+].CC=1C=C(C)N(C([S-])=S)N=1 JDIHPETWTXJUBS-UHFFFAOYSA-M 0.000 description 1
- USHAGKDGDHPEEY-UHFFFAOYSA-L potassium persulfate Chemical compound [K+].[K+].[O-]S(=O)(=O)OOS([O-])(=O)=O USHAGKDGDHPEEY-UHFFFAOYSA-L 0.000 description 1
- GEVPMUPAXHXQQS-UHFFFAOYSA-N potassium;nitrate;tetrahydrate Chemical compound O.O.O.O.[K+].[O-][N+]([O-])=O GEVPMUPAXHXQQS-UHFFFAOYSA-N 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 238000010526 radical polymerization reaction Methods 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 239000012744 reinforcing agent Substances 0.000 description 1
- 208000017520 skin disease Diseases 0.000 description 1
- 235000019333 sodium laurylsulphate Nutrition 0.000 description 1
- 125000003011 styrenyl group Chemical group [H]\C(*)=C(/[H])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- 125000000446 sulfanediyl group Chemical group *S* 0.000 description 1
- NHGZJOIUVDLIAW-UHFFFAOYSA-N sulfanyl butanoate Chemical compound CCCC(=O)OS NHGZJOIUVDLIAW-UHFFFAOYSA-N 0.000 description 1
- 238000010059 sulfur vulcanization Methods 0.000 description 1
- NNADJWNJTLVMSL-UHFFFAOYSA-N tert-butyl benzenecarbodithioate Chemical compound CC(C)(C)SC(=S)C1=CC=CC=C1 NNADJWNJTLVMSL-UHFFFAOYSA-N 0.000 description 1
- FIUNVVREDGDHKO-UHFFFAOYSA-N tert-butylsulfanyl benzenecarbodithioate Chemical compound CC(C)(C)SSC(=S)C1=CC=CC=C1 FIUNVVREDGDHKO-UHFFFAOYSA-N 0.000 description 1
- 238000005979 thermal decomposition reaction Methods 0.000 description 1
- KJAMZCVTJDTESW-UHFFFAOYSA-N tiracizine Chemical compound C1CC2=CC=CC=C2N(C(=O)CN(C)C)C2=CC(NC(=O)OCC)=CC=C21 KJAMZCVTJDTESW-UHFFFAOYSA-N 0.000 description 1
- AOQUKZYKYIPBFR-UHFFFAOYSA-N trihydroxy-nonyl-phenyl-$l^{5}-phosphane Chemical compound CCCCCCCCCP(O)(O)(O)C1=CC=CC=C1 AOQUKZYKYIPBFR-UHFFFAOYSA-N 0.000 description 1
- ILLOBGFGKYTZRO-UHFFFAOYSA-N tris(2-ethylhexyl) phosphite Chemical compound CCCCC(CC)COP(OCC(CC)CCCC)OCC(CC)CCCC ILLOBGFGKYTZRO-UHFFFAOYSA-N 0.000 description 1
- WGKLOLBTFWFKOD-UHFFFAOYSA-N tris(2-nonylphenyl) phosphite Chemical compound CCCCCCCCCC1=CC=CC=C1OP(OC=1C(=CC=CC=1)CCCCCCCCC)OC1=CC=CC=C1CCCCCCCCC WGKLOLBTFWFKOD-UHFFFAOYSA-N 0.000 description 1
- QEDNBHNWMHJNAB-UHFFFAOYSA-N tris(8-methylnonyl) phosphite Chemical compound CC(C)CCCCCCCOP(OCCCCCCCC(C)C)OCCCCCCCC(C)C QEDNBHNWMHJNAB-UHFFFAOYSA-N 0.000 description 1
- HIZCIEIDIFGZSS-UHFFFAOYSA-L trithiocarbonate Chemical compound [S-]C([S-])=S HIZCIEIDIFGZSS-UHFFFAOYSA-L 0.000 description 1
- 239000012989 trithiocarbonate Substances 0.000 description 1
- PEXOFOFLXOCMDX-UHFFFAOYSA-N tritridecyl phosphite Chemical compound CCCCCCCCCCCCCOP(OCCCCCCCCCCCCC)OCCCCCCCCCCCCC PEXOFOFLXOCMDX-UHFFFAOYSA-N 0.000 description 1
- 239000004034 viscosity adjusting agent Substances 0.000 description 1
- 239000004636 vulcanized rubber Substances 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 239000012991 xanthate Substances 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F293/00—Macromolecular compounds obtained by polymerisation on to a macromolecule having groups capable of inducing the formation of new polymer chains bound exclusively at one or both ends of the starting macromolecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L53/00—Compositions of block copolymers containing at least one sequence of a polymer obtained by reactions only involving carbon-to-carbon unsaturated bonds; Compositions of derivatives of such polymers
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F293/00—Macromolecular compounds obtained by polymerisation on to a macromolecule having groups capable of inducing the formation of new polymer chains bound exclusively at one or both ends of the starting macromolecule
- C08F293/005—Macromolecular compounds obtained by polymerisation on to a macromolecule having groups capable of inducing the formation of new polymer chains bound exclusively at one or both ends of the starting macromolecule using free radical "living" or "controlled" polymerisation, e.g. using a complexing agent
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F2438/00—Living radical polymerisation
- C08F2438/03—Use of a di- or tri-thiocarbonylthio compound, e.g. di- or tri-thioester, di- or tri-thiocarbamate, or a xanthate as chain transfer agent, e.g . Reversible Addition Fragmentation chain Transfer [RAFT] or Macromolecular Design via Interchange of Xanthates [MADIX]
Definitions
- the present invention relates to a chloroprene-based block copolymer latex.
- Polychloroprene latex is known as a material for immersion molded products such as medical surgical gloves, inspection gloves, industrial gloves, balloons, catheters, and rubber boots. In addition, it is used as a paint, an adhesive, and an adhesive by blending various additives.
- Prior art documents include a copolymer latex of chloroprene and 2,3-dichloro-1,3-butadiene (see, for example, Patent Document 1), and a modified polychloroprene latex obtained by copolymerizing chloroprene and methacrylic acid (for example, Patent Document). 2), a chloroprene-based polymer latex containing no sulfide accelerator (see, for example, Patent Document 3), and a polychloroprene latex containing a composite zinc flower containing an inorganic salt and zinc oxide (see, for example, Patent Document 4) are known. ing.
- a copolymer obtained by polymerizing chloroprene using a polystyrene containing an azo group as an initiator (see, for example, Patent Document 5) and a dithiocarbamate-ized polychloroprene are aromatic.
- a copolymer obtained by polymerizing a group vinyl monomer (see, for example, Patent Document 6), a copolymer in which a hydrophilic oligomer or a hydrophilic polymer is linked to a chloroprene-based polymer (see, for example, Patent Document 7), an aromatic vinyl compound.
- a copolymer having a polymer block and a chloroprene polymer block and specifying the total number average molecular weight and the number average molecular weight of the chloroprene polymer block (see, for example, Patent Document 8), an acrylic acid ester polymer block, and the like.
- a copolymer having a block of a chloroprene polymer (see, for example, Patent Document 9) Further, there is a technique described in Patent Document 10 as a method for chemically bonding molecules between molecules without using vulgarization.
- thermoplastic elastomers have been developed as elastomers that can obtain high strength without using vulcanization.
- a thermoplastic elastomer for dip-molded products a styrene / isoprene / styrene triblock copolymer latex emulsified by a forced emulsification method (see, for example, Patent Document 11) has been developed.
- polychloroprene-based rubber compositions have been vulcanized with sulfur, zinc oxide, magnesium oxide and the like, and thiuram-based, dithiocarbamate-based, thiourea-based, guanidine-based, and xanthate acid in order to obtain the desired mechanical strength.
- the use of salt-based and thiazole-based vulcanization accelerators was indispensable. Since the vulcanization accelerator is a causative substance of type IV allergy that causes skin diseases such as dermatitis, reduction or non-use of the vulcanization accelerator has become an important theme. Further, since the elimination of the use of the vulcanization accelerator leads not only to the reduction of allergies but also to the cost reduction, a rubber composition that exhibits sufficient mechanical strength without using the vulcanization accelerator is desired. There is.
- styrene / isoprene / styrene triblock copolymer latex and styrene / butadiene / styrene triblock copolymer latex can exhibit sufficient mechanical strength without using a sulfide accelerator. Since it is produced by the forced emulsification method, there is a problem that the particle size of the latex cannot be reduced and the mechanical stability of the latex is inferior.
- the present invention provides chloroprene, which has excellent mechanical stability of latex and can obtain a dip-molded film having excellent flexibility, tensile properties, and heat aging resistance without using a vulcanizing agent or a vulcanization accelerator.
- An object of the present invention is to provide a system block copolymer latex.
- the gist of the present invention is as follows. (1) A monomer-derived polymer block (A) in which a polymer having a glass transition temperature of 80 ° C. or higher can be obtained during homopolymerization, and a chloroprene-based polymer block containing 5 to 30% by mass of a chloroprene monomer unit (chloroprene-based polymer block). B) A chloroprene-based block copolymer latex containing a chloroprene-based block copolymer containing 70 to 95% by mass. The film obtained by dip-molding the chloroprene-based block copolymer latex is heat-treated at 130 ° C. for 30 minutes, and then measured in accordance with JIS K 6251. The chloroprene-based block copolymer weight at which the tensile strength at cutting is 17 MPa or more. Combined latex.
- the polymer block (A) 5 to 15% by mass and the chloroprene block (B) 85 to 95% by mass are contained in 100% by mass of the chloroprene block copolymer (1).
- chloroprene-based block according to any one of (1) to (3), wherein the chloroprene-based polymer block (B) has a chloroprene monomer unit and a polyfunctional monomer unit. Monomer latex.
- a chloroprene-based block copolymer latex capable of vulcanization is provided.
- the chloroprene-based block copolymer latex is a chloroprene-based block copolymer containing 5 to 30% by mass of the polymer block (A) and 70 to 95% by mass of the chloroprene-based polymer block (B) containing a chloroprene monomer unit. Includes.
- the polymer block (A) is a monomer-derived polymer block from which a polymer having a glass transition temperature of 80 ° C. or higher can be obtained during homopolymerization. By using such a monomer, the tensile strength at the time of cutting and the heat aging property of the obtained dip-molded coating film are improved. It is preferable to use a monomer that can obtain a polymer having a glass transition temperature of 85 ° C. or higher. From the viewpoint of moldability, a monomer capable of obtaining a polymer having a glass transition temperature of 150 ° C. or lower is preferable, and a monomer capable of obtaining a polymer having a glass transition temperature of 120 ° C.
- the glass transition temperature is, for example, 80, 85, 90, 95, 100, 105, 110, 120, 130, 140, 150 ° C., even if it is within the range between any two of the numerical values exemplified here. good.
- the glass transition temperature is an extrapolated glass transition temperature (Teg) measured in accordance with JIS K 7121.
- Teg extrapolated glass transition temperature measured in accordance with JIS K 7121.
- Examples of the monomer unit constituting the polymer block (A) include an aromatic vinyl monomer unit, a methyl methacrylate monomer unit, and an acrylonitrile monomer unit.
- a unit derived from an aromatic vinyl monomer is preferably used, and a styrene unit is preferably used.
- the polymer block (A) is a polymer block obtained by copolymerizing these monomers or a unit derived from a monomer copolymerizable with these monomers, as long as the object of the present invention is not impaired. It may be a polymer block composed of.
- the number average molecular weight of the polymer block (A) is preferably 10,000 or more from the viewpoint of the tensile properties, heat aging property, and moldability of the obtained immersion molded film.
- the number average molecular weight of the polymer block (A) can be, for example, 10000, 15000, 20000, 25000, 30,000, and may be within the range between any two of the numerical values exemplified here. Further, the molecular weight distribution of the polymer block (A) is preferably 2.0 or less from the viewpoint of moldability.
- the molecular weight distribution of the polymer block (A) is, for example, 1.0, 1.1, 1.2, 1.3, 1.4, 1.5, 1.6, 1.7, 1.8, 1 It can be 9.9 or 2.0, and may be within the range between any two of the numerical values exemplified here.
- the number average molecular weight and the weight average molecular weight are polystyrene-equivalent values measured by gel permeation chromatography (GPC), and are measured values under the following measurement conditions.
- HLC-8320 manufactured by Tosoh
- the chloroprene-based polymer block (B) contains a chloroprene monomer (2-chloro-1,3-butadiene) unit and is mainly composed of a chloroprene monomer unit.
- the chloroprene-based polymer block (B) may contain a polyfunctional monomer unit.
- the chloroprene-based polymer block (B) is derived from a chloroprene monomer unit, a polyfunctional monomer unit, and a monomer copolymerizable with these, as long as the object of the present invention is not impaired. It may be a polymer block composed of units.
- the chloroprene-based polymer block (B) preferably contains 90% by mass or more of structural units derived from the chloroprene monomer, when the chloroprene-based polymer block (B) is 100% by mass.
- each structural unit in the chloroprene-based polymer block (B) is not particularly limited, but is preferably 90 to 99.95% by mass of the chloroprene monomer unit and 0. It is 05 to 10% by mass.
- the content of the polyfunctional monomer unit in the chloroprene-based polymer block (B) is, for example, 0.05, 0.50, 1.00, 2.00, 3.00, 4.00, 5. It is 00, 6.00, 7.00, 8.00, 9.00, 10.00 mass%, and may be within the range between any two of the numerical values exemplified here.
- the polyfunctional monomer is used to improve the tensile properties and heat aging resistance of the obtained dip-molded coating.
- the polyfunctional monomer is a compound having two or more radical polymerization groups in the molecule. From the viewpoints of the flexibility of the obtained dip-molded coating, the tensile strength at the time of cutting, and the moldability, the monomer represented by the chemical formula (1) and the aromatic polyene monomer are preferably used.
- Examples of the monomer represented by the chemical formula (1) include 1.9-nonanediol dimethacrylate, 1.9-nonanediol diacrylate, neopentyl glycol dimethacrylate, neopentyl glycol diacrylate, and 1.6-hexanediol. Dimethacrylate, 1.6-hexanediol diacrylate, ethylene glycol dimethacrylate, diethylene glycol dimethacrylate, triethylene glycol dimethacrylate, triethylene glycol diacrylate, polyethylene glycol dimethacrylate, and polyethylene glycol diacrylate are particularly preferably used.
- the aromatic polyene monomer is an aromatic polyene having 10 or more and 30 or less carbon atoms, having a plurality of double bonds (vinyl groups) and a single or a plurality of aromatic groups, and is, for example, o-divinyl.
- R 1 and R 2 represent hydrogen, chlorine, a substituted or unsubstituted alkyl group, a substituted or unsubstituted alkenyl group, a substituted or unsubstituted aryl group, a mercapto group or a substituted or unsubstituted heterocyclyl group.
- W 1 is a saturated or unsaturated hydrocarbon group, a saturated or unsaturated cyclic hydrocarbon group, a saturated or unsaturated hydrocarbon group containing a hetero atom, or a saturated or unsaturated hydrocarbon group containing a hetero atom. Represents a structure containing one or more of each.
- Z 1 represents oxygen, nitrogen, and sulfur.
- each structural unit of the chloroprene block copolymer is 5 to 30% by mass of the polymer block (A) and 70 to 95% by mass of the chloroprene block (B), preferably the polymer block (A). ) 5 to 15% by mass, and 85 to 95% by mass of the chloroprene-based polymer block (B).
- the polymer block (A) is 5% by mass or more, the tensile strength at the time of cutting and the heat aging property of the obtained dip-molded coating film are improved.
- the polymer block (A) is 30% by mass or less, the flexibility of the obtained dip-molded coating is improved.
- the polymer block (A) is preferably 15% by mass or less.
- the chloroprene-based polymer block (B) is 70% by mass or more, the flexibility of the obtained dip-molded coating is improved.
- the chloroprene-based polymer block (B) is preferably 85% by mass or more.
- the chloroprene-based polymer block (B) is 95% by mass or less, the tensile strength at the time of cutting of the obtained dip-molded coating film is improved.
- the chloroprene-based block copolymer is 100% by mass, the content of the polymer block (A) contained in the chloroprene-based block copolymer is, for example, 5, 10, 15, 20, 25, 30% by mass. Yes, it may be within the range between any two of the numerical values exemplified here.
- the chloroprene-based block copolymer according to one embodiment of the present invention may consist of a polymer block (A) and a polymer block (B), and shall not contain other polymer blocks. Can be done.
- the chloroprene-based block copolymer can be a diblock copolymer of the polymer block (A) -polymer block (B).
- the average particle size of the chloroprene-based block copolymer latex measured by the dynamic light scattering method is preferably 300 nm or less, more preferably 250 nm or less, from the viewpoint of mechanical stability of the latex. It is even more preferably 200 nm or less.
- the lower limit can be, for example, 100 nm or more.
- the average particle size is, for example, 100, 120, 140, 150, 160, 170, 180, 190, 200, 220, 240, 260, 280, 300 nm, and is in the range between any two of the numerical values exemplified here. It may be inside.
- the average particle size is an average particle size measured by a dynamic light scattering method and calculated by a photon correlation method.
- the average particle size can be adjusted by controlling the type and amount of the chloroprene-based block copolymer latex compound and the production conditions.
- the weight average molecular weight of the chloroprene-based block copolymer is not particularly limited, but is preferably 50,000 to 600,000, particularly preferably 100,000 to 500,000 from the viewpoint of molding processability.
- the mechanical stability of the chloroprene-based block copolymer latex according to the embodiment of the present invention is preferably 1% by mass or less, more preferably 0.2% by mass or less, and 0.1% by mass. The following is even more preferable.
- the mechanical stability of the chloroprene-based block copolymer latex can be evaluated by the measuring method described in Examples. Mechanical stability can be adjusted by controlling the type and amount of the chloroprene-based block copolymer latex formulation and the production conditions. For example, the average particle size of the chloroprene-based block copolymer latex is controlled. By doing so, it can be adjusted.
- the chloroprene-based block copolymer latex of the present embodiment is measured according to JIS K 6251 after a dip-molded coating obtained by dip-molding the chloroprene-based block copolymer latex is heat-treated at 130 ° C. for 30 minutes.
- the tensile strength at the time of cutting is 17 MPa or more, and an unvulcanized dip-molded film containing no vulcanizing agent and vulcanization accelerator can be provided.
- the unvulcanized dip-molded coating has flexibility and exhibits sufficient mechanical strength without containing a vulcanizing agent and a vulcanization accelerator.
- the tensile strength at the time of cutting is more preferably 18 MPa or more, further preferably 19 MPa or more, and even more preferably 20 MPa or more.
- the upper limit is not particularly limited, but is, for example, 30 MPa or less.
- the dip-molded coating is heat-treated at 30 ° C. for 30 minutes, and then subjected to a heat aging test at 100 ° C. for 22 hours, and then JIS.
- the tensile strength at cutting measured according to K 6251 is preferably 17 MPa or more, more preferably 18 MPa or more, further preferably 19 MPa or more, and even more preferably 20 MPa or more. preferable.
- the upper limit is not particularly limited, but is, for example, 30 MPa or less.
- the chloroprene-based block copolymer latex of the present embodiment conforms to JIS K 6251 after the dip-molded film obtained by dip-molding the chloroprene-based block copolymer latex is heat-treated at 130 ° C. for 30 minutes.
- the elongation at the time of cutting measured in the above is preferably 900% or more, more preferably 905% or more, and even more preferably 910% or more.
- the upper limit is not particularly limited, but is, for example, 1300% or less.
- the dip-molded coating is heat-treated at 30 ° C.
- the elongation at cutting measured according to K 6251 is preferably 900% or more, more preferably 905% or more, and even more preferably 910% or more.
- the upper limit is not particularly limited, but is, for example, 1300% or less.
- the chloroprene-based block copolymer latex of the present embodiment is measured in accordance with JIS K 6251 after a dip-molded film obtained by dip-molding the chloroprene-based block copolymer latex is heat-treated at 130 ° C. for 30 minutes.
- the 500% stretched modulus is preferably 3.0 MPa or less, more preferably 2.9 MPa or less, and even more preferably 2.8 MPa or less.
- the lower limit is not particularly limited, but is, for example, 1.0 MPa or more.
- the chloroprene-based block copolymer latex according to the embodiment of the present invention is obtained after the dip-molded coating is heat-treated at 30 ° C.
- the 500% elongation modulus measured according to JIS K 6251 is preferably 3.0 MPa or less, more preferably 2.9 MPa or less, and even more preferably 2.8 MPa or less.
- the lower limit is not particularly limited, but is, for example, 1.0 MPa or more.
- the dip-molded film can be obtained by the method described in Examples, and the dip-molded film can be formed without using a vulcanizing agent and a vulcanization accelerator.
- the amount of the polyfunctional monomer added should be adjusted.
- the content of the polyfunctional monomer unit contained in the chloroprene-based polymer block (B) and the content of the chloroprene-based polymer block (B) in the chloroprene-based block copolymer can be adjusted.
- the type and amount of the functional group introduced by polymerizing in the presence of the RAFT agent described later may be adjusted.
- the dip-molded coating obtained from the chloroprene-based block copolymer latex of the present embodiment may contain a vulcanizing agent or a vulcanization accelerator.
- the total content thereof can be 5% by mass or less, more preferably 1% by mass or less, and 0.1% by mass. Is more preferable.
- the unvulcanized dip-molded coating has sufficient mechanical strength even if it does not contain a vulcanizing agent and a vulcanization accelerator, the vulcanizing agent and the vulcanizing agent and the cost are reduced from the viewpoint of reducing allergies and costs. Those containing no vulcanization accelerator are preferable.
- the production method is not particularly limited as long as a desired chloroprene-based block copolymer latex can be obtained, but after the emulsion polymerization step 1 for synthesizing the polymer block (A), emulsification for synthesizing the chloroprene-based block (B). It can be obtained by a production method for obtaining a chloroprene-based block copolymer latex through a two-step polymerization step consisting of the polymerization step 2.
- Emssion polymerization step 1 The emulsion polymerization step 1 will be specifically described.
- the monomer constituting the polymer block (A) is subjected to living radical emulsion polymerization to synthesize the polymer block (A).
- the polymer block (A) obtained here preferably has the above-mentioned glass transition temperature.
- the emulsifier used in the emulsion polymerization is not particularly limited, but an anion-based or nonionic emulsifier is preferable from the viewpoint of emulsion stability.
- the dip-molded coating obtained from the obtained chloroprene-based block copolymer latex can have appropriate strength to prevent excessive shrinkage and breakage.
- the concentration of the emulsifier is preferably 5 to 50% by mass with respect to 100% by mass of the monomers constituting the polymer block (A) from the viewpoint of efficiently performing the polymerization reaction.
- the radical polymerization initiator a known radical polymerization initiator can be used, and for example, potassium persulfate, benzoyl peroxide, hydrogen peroxide, an azo compound and the like can be used.
- the amount of pure water added is preferably 100 to 300% by mass with respect to 100% by mass of the monomers constituting the polymer block (A). When the amount of pure water added is 300% by mass or less, the tensile strength at the time of cutting of the obtained dip-molded coating film is improved.
- the polymerization temperature may be appropriately determined depending on the type of the monomer, but is preferably 10 to 100 ° C, particularly preferably 20 to 80 ° C.
- Emssion polymerization step 2 In the emulsion polymerization step 2, pure water, an emulsifier, a chloroprene monomer, and a polyfunctional monomer are used with respect to the latex containing the polymer block (A) obtained by the living radical emulsion polymerization in the emulsion polymerization step 1. Is added and emulsion-polymerized to obtain a chloroprene-based block copolymer latex. The chloroprene monomer may be added all at once or added.
- the polymerization temperature in the emulsion polymerization step 2 is preferably 10 to 50 ° C. from the viewpoint of ease of polymerization control. The polymerization reaction is stopped by adding a polymerization inhibitor.
- polymerization terminator examples include thiodiphenylamine, 4-thir-butylcatechol, 2,2'-methylenebis-4-methyl-6-thylbutylphenol and the like.
- the unreacted monomer after the completion of emulsion polymerization can be removed by a method such as conventional vacuum distillation.
- the chloroprene-based block copolymer latex obtained in the emulsion polymerization step 2 contains a freeze stabilizer, an emulsion stabilizer, a viscosity modifier, an antioxidant, a preservative, etc. after polymerization as long as the object of the present invention is not impaired. It can be added arbitrarily.
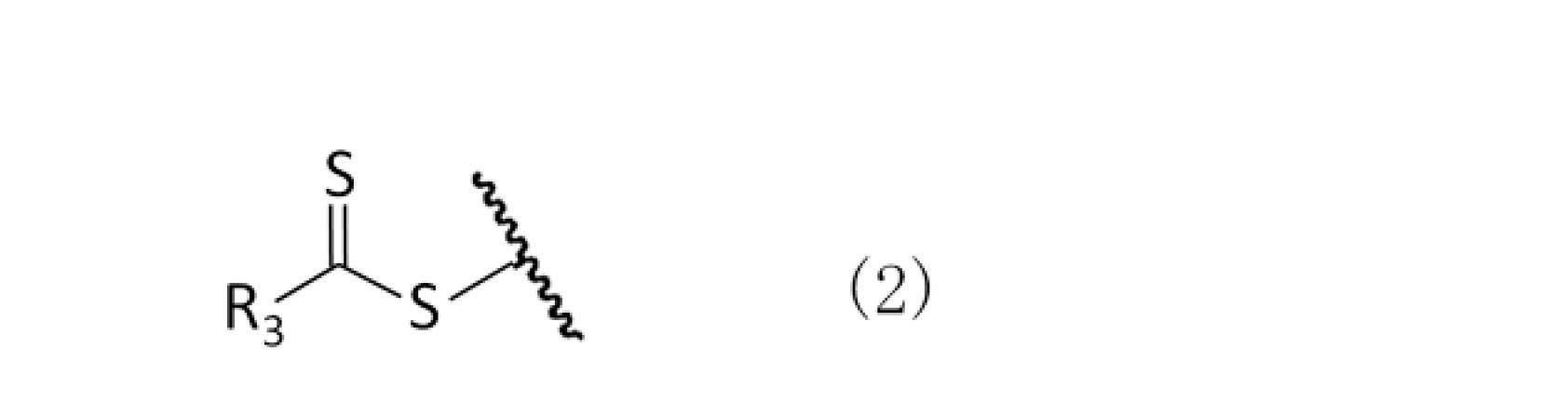
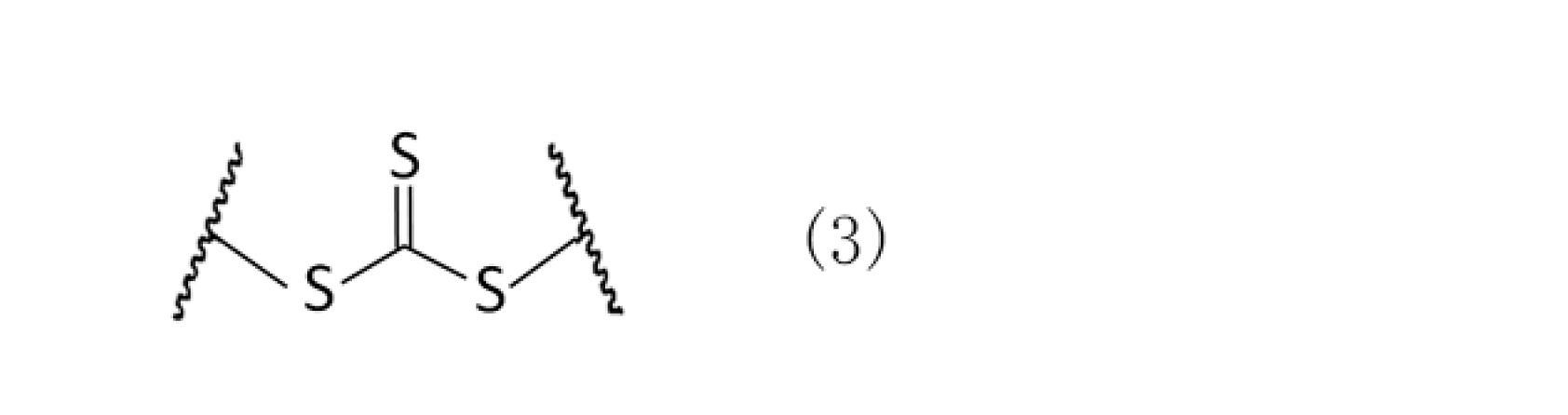
- the chloroprene-based block copolymer preferably has a functional group having a structure represented by the following chemical formula (2) or chemical formula (3).
- R8 represents hydrogen, chlorine, a substituted or unsubstituted alkyl group, a substituted or unsubstituted alkenyl group, a substituted or unsubstituted aryl group, a mercapto group or a substituted or unsubstituted heterocyclyl group.
- the terminal structure represented by the above chemical formula (2) or chemical formula (3) is introduced into a block copolymer by performing emulsion polymerization in the presence of a known RAFT agent.
- the compound that derives the structure represented by the chemical formula (2) is not particularly limited, and general compounds can be used, and examples thereof include dithiocarbamates and dithioesters.
- benzyl1-pyrrolecarbodithioate (common name: benzyl1-pyrroldithiocarbamate), benzylphenylcarbodithioate, 1-benzyl-N, N dimethyl-4-aminodithiobenzoate, 1-benzyl-4- Methoxydithiobenzoate, 1-phenylethylimidazole carbodithioate (common name: 1-phenylethylimidazole dithiocarbamate), benzyl-1- (2-pyrrolidinone) carbodithioate) (common name: benzyl-1- (2-pyrrolidinone) ) Dithiocarbamate), benzylphthalimidylcarbodithioate, (common name: benzylphthalimidyldithiocarbamate), 2-cyanoprop-2-yl-1-pyrrolecarbodithioate, (common name: 2-cyanoprop-2- (Il-1
- benzyl1-pyrrole carbodithioate and benzylphenylcarbodithioate are particularly preferably used.
- the compound that derives the structure represented by the above chemical formula (3) is not particularly limited, and general compounds can be used, for example, 2-cyano-2-propyldodecyltrithiocarbonate and dibenzyl.
- Trithiocarbonate butylbenzyl trithiocarbonate, 2-[[(butylthio) thioxomethyl] thio] propionic acid, 2-[[(dodecylthio) thioxomethyl] thio] propionic acid, 2-[[(butylthio) thioxomethyl] thio ] Succinic acid, 2-[[(dodecylthio) thioxomethyl] thio] succinic acid, 2-[[(dodecylthio) thioxomethyl] thio] -2-methylpropionic acid, 2,2'-[carbonothio oil bis (thio)] Bis [2-methylpropionic acid], 2-amino-1-methyl-2-oxoethylbutyltrithiocarbonate, benzyl2-[(2-hydroxyethyl) amino] -1-methyl-2-oxoethyltrithio Trithiocarbonates such as carbonate, 3-
- the dip-molded article according to the present embodiment is a dip-molded product obtained by dip-molding the above-mentioned chloroprene-based block copolymer latex, has low modulus, is flexible, and has excellent mechanical properties such as tensile strength during cutting and elongation during cutting. It also has excellent heat aging resistance. Gloves, balloons, and catheters are suitable as the immersion molded product.
- the immersion molded product according to the embodiment of the present invention can also be obtained by molding a chloroprene-based block copolymer latex composition containing the above-mentioned chloroprene-based block copolymer latex.
- Examples of the molding method for producing the immersion molded product of the present embodiment include, for example, a coagulation liquid immersion method, but the present invention is not limited to this, and molding may be performed according to a conventional method.
- the immersion molded product of the present embodiment may contain a filler or a reinforcing agent, a plasticizer, a processing aid or a lubricant, an antiaging agent, a silane coupling agent, or the like, as long as the object of the present invention is not impaired.
- a filler or a reinforcing agent e.g., a plasticizer, a processing aid or a lubricant, an antiaging agent, a silane coupling agent, or the like, as long as the object of the present invention is not impaired.
- These agents can be appropriately selected depending on the purpose and use.
- the immersion molded product of the present embodiment may not contain a vulcanizing agent and / or a vulcanization accelerator. That is, the immersion molded product includes a vulcanizing agent and no vulcanization accelerator, a vulcanizing agent and a vulcanization accelerator, and a vulcanizing agent and a vulcanization accelerator. Whether or not to blend the vulcanization agent and the vulcanization accelerator may be determined according to the target immersion molded product. When the immersion molded product according to the embodiment of the present invention contains a vulcanizing agent and / or a vulcanization accelerator, the total content of the vulcanizing agent and the vulcanization accelerator is 100% by mass when the immersion molded product is 100% by mass.
- the immersion molded product according to the embodiment of the present invention may not contain a vulcanizing agent and a vulcanization accelerator from the viewpoint of reducing allergies and reducing costs, and the immersion molded product may contain a vulcanizing agent and a vulcanization accelerator. It has sufficient mechanical strength even if it does not contain a vulcanization accelerator.
- Examples of the vulcanizing agent include sulfur, zinc oxide, magnesium oxide and the like.
- the vulcanization accelerator acts with the vulcanizing agent to increase the vulcanization rate and shorten the vulcanization time, lower the vulcanization temperature, reduce the amount of the vulcanizing agent, and improve the physical properties of the vulcanized rubber.
- It is a drug added for the purpose of, and usually refers to a drug that promotes the sulfur vulcanization reaction.
- Examples of the vulcanization accelerator generally used for vulcanization of chloroprene-based copolymer latex include thiuram-based, dithiocarbamate-based, thiourea-based, guanidine-based, xanthogenate-based, thiazole-based, and the like. It is used alone or in combination of two or more as required.
- the immersion molded product of the present embodiment exhibits excellent mechanical properties regardless of the presence or absence of a vulcanizing agent and a vulcanization accelerator, but from the viewpoint of reducing allergies and reducing costs, the vulcanizing agent and the vulcanization accelerator are exhibited. It is preferable that it does not contain.
- an anti-aging agent to be added to the immersion molded product of the present embodiment a primary anti-aging agent used in ordinary rubber applications to capture radicals and prevent autoxidation, and a secondary anti-aging agent to detoxify hydroperoxide.
- Anti-aging agents can be added. These anti-aging agents can be added at a ratio of 0.1 part by mass or more and 10 parts by mass or less to 100 parts by mass of the rubber component in the chloroprene-based copolymer latex, preferably 2 parts by mass or more and 5 parts by mass. It is in the range of parts by mass or less.
- These anti-aging agents can be used alone or in combination of two or more.
- Examples of the primary anti-aging agent include phenol-based anti-aging agents, amine-based anti-aging agents, acrylate-based anti-aging agents, imidazole-based anti-aging agents, carbamic acid metal salts, and waxes.
- examples of the secondary anti-aging agent include phosphorus-based anti-aging agents, sulfur-based anti-aging agents, and imidazole-based anti-aging agents.
- anti-aging agents are not particularly limited, but are N-phenyl-1-naphthylamine, alkylated diphenylamine, octylated diphenylamine, 4,4'-bis ( ⁇ , ⁇ -dimethylbenzyl) diphenylamine, p- (p).
- -Toluenesulfonylamide diphenylamine, N, N'-di-2-naphthyl-p-phenylenediamine, N, N'-diphenyl-p-phenylenediamine, N-phenyl-N'-isopropyl-p-phenylenediamine, N -Phenyl-N'-(1,3-dimethylbutyl) -p-phenylenediamine, N-phenyl-N'-(3-methacryloyloxy-2-hydroxypropyl) -p-phenylenediamine, 1,1,3- Tris- (2-methyl-4-hydroxy-5-t-butylphenyl) butane, 4,4'-butylidenebis- (3-methyl-6-t-butylphenol), 2,2-thiobis (4-methyl-6) -T-butylphenol), 7-octadecyl-3- (4'-hydroxy-3', 5'-di-
- Example 1 Polymerization Step 1 Synthesis of Polymer Block (A-1) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. Pure water 4666 g, disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 224 g, potassium hydroxide 36.4 g, sodium salt of ⁇ -naphthalene sulfonic acid formalin condensate (manufactured by Kao, trade name: Demor N) 18.7 g , 350 g of styrene monomer and 6.07 g of butylbenzyl trithiocarbonate were charged, the internal temperature was set to 80 ° C., and the mixture was stirred at 200 rpm under a nitrogen stream.
- Pure water 4666 g disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 224 g, potassium hydroxide 36.4 g, sodium salt
- the sampled latex was mixed with a large amount of methanol to precipitate a resin component, which was then filtered and dried to obtain a sample of polymer block (A-1). From the obtained sample, the number average molecular weight, molecular weight distribution, and glass transition temperature of the polymer block (A) were determined by analysis. The analysis results are shown in Table 1. The methods for measuring the "number average molecular weight”, “molecular weight distribution”, and “glass transition temperature” will be described later.
- the average particle size of the latex and the mechanical stability of the latex were measured.
- the analysis results are shown in Table 1. The measurement method will be described later.
- the sampled latex was mixed with a large amount of methanol to precipitate a resin component, which was then filtered and dried to obtain a sample of a chloroprene-based block copolymer. From the obtained sample, the content (mass%) of the polymer block (A-1) and the chloroprene-based polymer block (B-1) of the chloroprene-based block copolymer was determined by analysis. The analysis results are shown in Table 1. The measurement method will be described later.
- Example 2 Polymerization Step 1 Synthesis of Polymer Block (A-2) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. Pure water 3333 g, disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 160 g, potassium hydroxide 26.0 g, sodium salt of ⁇ -naphthalene sulfonic acid formarin condensate (manufactured by Kao, trade name: Demor N) 13.3 g , 250 g of styrene monomer and 4.33 g of butylbenzyl trithiocarbonate were charged, and the mixture was stirred at 200 rpm under a nitrogen stream at an internal temperature of 80 ° C.
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-2) and chloroprene-based polymer blocks (B-2) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- Example 3 Polymerization Step 1 Synthesis of Polymer Block (A-3) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. Pure water 5733 g, disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 275 g, potassium hydroxide 44.7 g, sodium salt of ⁇ -naphthalene sulfonic acid formalin condensate (manufactured by Kao, trade name: Demor N) 22.9 g , 430 g of styrene monomer and 7.45 g of butylbenzyl trithiocarbonate were charged, the internal temperature was set to 80 ° C., and the mixture was stirred at 200 rpm under a nitrogen stream.
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-3) and chloroprene-based polymer blocks (B-3) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- Example 4 (Polymerization Step 1) Synthesis of Polymer Block (A-4) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. Pure water 4666 g, disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 224 g, potassium hydroxide 36.4 g, sodium salt of ⁇ -naphthalene sulfonic acid formalin condensate (manufactured by Kao, trade name: Demor N) 18.7 g , 350 g of styrene monomer and 6.07 g of butylbenzyl trithiocarbonate were charged, the internal temperature was set to 80 ° C., and the mixture was stirred at 200 rpm under a nitrogen stream.
- Pure water 4666 g disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 224 g, potassium hydroxide 36.4 g,
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-4) and chloroprene-based polymer blocks (B-4) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- Example 5 (Polymerization Step 1) Synthesis of Polymer Block (A-5) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. Pure water 4666 g, disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 224 g, potassium hydroxide 36.4 g, sodium salt of ⁇ -naphthalene sulfonic acid formalin condensate (manufactured by Kao, trade name: Demor N) 18.7 g , 350 g of styrene monomer and 6.07 g of butylbenzyl trithiocarbonate were charged, the internal temperature was set to 80 ° C., and the mixture was stirred at 200 rpm under a nitrogen stream.
- Pure water 4666 g disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 224 g, potassium hydroxide 36.4 g,
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-5) and chloroprene-based polymer blocks (B-5) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- Example 6 Polymerization Step 1 Synthesis of Polymer Block (A-6) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. Pure water 4666 g, disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 224 g, potassium hydroxide 36.4 g, sodium salt of ⁇ -naphthalene sulfonic acid formalin condensate (manufactured by Kao, trade name: Demor N) 18.7 g , 350 g of styrene monomer and 6.07 g of butylbenzyl trithiocarbonate were charged, the internal temperature was set to 80 ° C., and the mixture was stirred at 200 rpm under a nitrogen stream.
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-6) and chloroprene-based polymer blocks (B-6) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- Example 7 (Polymerization Step 1) Synthesis of Polymer Block (A-7) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. 5450 g of pure water, 262 g of disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.), 42.5 g of potassium hydroxide, sodium salt of ⁇ -naphthalene sulfonic acid formarin condensate (manufactured by Kao Co., Ltd., trade name: Demor N) 21.8 g , 2500 g of styrene monomer and 43.3 g of butylbenzyl trithiocarbonate were charged, the internal temperature was set to 80 ° C., and the mixture was stirred at 200 rpm under a nitrogen stream.
- Demor N Demor N
- Polymerization Step 2 Synthesis of chloroprene-based polymer block (B-7) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. Pure water 2732 g, disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 131 g, potassium hydroxide 21.3 g, sodium salt of ⁇ -naphthalene sulfonic acid formalin condensate (manufactured by Kao, trade name: Demor N) 10.9 g , 783 g of the latex containing the polymer block (A-2) prepared in the polymerization step 1 was charged, the internal temperature was set to 45 ° C., and the mixture was stirred at 200 rpm under a nitrogen stream.
- Average particle size of latex, mechanical stability of latex, content (% by mass) of polymer block (A-7) and chloroprene-based polymer block (B-7) of chloroprene-based block copolymer, and toluene insoluble content was obtained by analysis in the same manner as in Example 1. The analysis results are shown in Table 1.
- Example 8 (Polymerization Step 1) Synthesis of Polymer Block (A-8) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. Pure water 4666 g, disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 224 g, potassium hydroxide 36.4 g, sodium salt of ⁇ -naphthalene sulfonic acid formalin condensate (manufactured by Kao, trade name: Demor N) 18.7 g , 350 g of styrene monomer and 6.07 g of butylbenzyl trithiocarbonate were charged, the internal temperature was set to 80 ° C., and the mixture was stirred at 200 rpm under a nitrogen stream.
- Pure water 4666 g disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 224 g, potassium hydroxide 36.4 g,
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-8) and chloroprene-based polymer blocks (B-8) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- Example 9 Polymerization Step 1 Synthesis of Polymer Block (A-9) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. Pure water 4666 g, disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 224 g, potassium hydroxide 36.4 g, sodium salt of ⁇ -naphthalene sulfonic acid formalin condensate (manufactured by Kao, trade name: Demor N) 18.7 g , 350 g of styrene monomer and 6.07 g of butylbenzyl trithiocarbonate were charged, the internal temperature was set to 80 ° C., and the mixture was stirred at 200 rpm under a nitrogen stream.
- Pure water 4666 g disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 224 g, potassium hydroxide 36.4 g, sodium salt
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-9) and chloroprene-based polymer blocks (B-9) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- Example 10 Polymerization Step 1 Synthesis of Polymer Block (A-10) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. Pure water 4666 g, disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 224 g, potassium hydroxide 36.4 g, sodium salt of ⁇ -naphthalene sulfonic acid formalin condensate (manufactured by Kao, trade name: Demor N) 18.7 g , 350 g of styrene monomer and 6.07 g of butylbenzyl trithiocarbonate were charged, the internal temperature was set to 80 ° C., and the mixture was stirred at 200 rpm under a nitrogen stream.
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-10) and chloroprene-based polymer blocks (B-10) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- Example 11 (Polymerization Step 1) Synthesis of Polymer Block (A-11) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. 6667 g of pure water, 320 g of disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.), 52.0 g of potassium hydroxide, sodium salt of ⁇ -naphthalene sulfonic acid formarin condensate (manufactured by Kao, trade name: Demor N) 26.7 g , 500 g of styrene monomer and 6.50 g of butylbenzyl trithiocarbonate were charged, and the mixture was stirred at 200 rpm under a nitrogen stream at an internal temperature of 80 ° C.
- Demor N Demor N
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-11) and chloroprene-based polymer blocks (B-11) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- Example 12 (Polymerization Step 1) Synthesis of Polymer Block (A-12) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. 5450 g of pure water, 262 g of disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.), 42.5 g of potassium hydroxide, sodium salt of ⁇ -naphthalene sulfonic acid formarin condensate (manufactured by Kao Co., Ltd., trade name: Demor N) 21.8 g , 2500 g of styrene monomer and 32.5 g of butylbenzyl trithiocarbonate were charged, the internal temperature was set to 80 ° C., and the mixture was stirred at 200 rpm under a nitrogen stream.
- Demor N Demor N
- Polymerization Step 2 Synthesis of chloroprene-based polymer block (B-4) Polymerization was carried out using an autoclave having a capacity of 10 L and a stirrer and a jacket for heating and cooling. Pure water 1188 g, disproportionated potassium rosinate (manufactured by Harima Kasei Co., Ltd.) 57 g, potassium hydroxide 9.3 g, sodium salt of ⁇ -naphthalene sulfonic acid formalin condensate (manufactured by Kao, trade name: Demor N) 4.8 g , 3147 g of the latex containing the polymer block (A-4) prepared in the polymerization step 1 was charged, the internal temperature was set to 45 ° C., and the mixture was stirred at 200 rpm under a nitrogen stream.
- Average particle size of latex, mechanical stability of latex, content (% by mass) of polymer block (A-12) and chloroprene-based polymer block (B-12) of chloroprene-based block copolymer, and toluene insoluble content was obtained by analysis in the same manner as in Example 1. The analysis results are shown in Table 1.
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-13) and chloroprene-based polymer blocks (B-13) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-14) and chloroprene-based polymer blocks (B-14) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-15) and chloroprene-based polymer blocks (B-15) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-17) and chloroprene-based polymer blocks (B-17) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-18) and chloroprene-based polymer blocks (B-18) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 1.
- the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of the first and third blocks of the synthesized triblock copolymer, styrene block, and the second block, chloroprene block, were carried out. It was obtained by analysis in the same manner as in Example 1. The analysis results are shown in Table 2.
- the average particle size of the latex, the mechanical stability of the latex, and the content (% by mass) of the homopolymer of the polymer block (A) and the homopolymer of the chloroprene-based polymer block (B) in the polymer obtained by mixing. ) was obtained by analysis in the same manner as in Example 1. The analysis results are shown in Table 3.
- azobisisobutyronitrile manufactured by Fujifilm Wako Pure Chemical Industries, Ltd., trade name: AIBN
- 20 ml of the obtained solution was sampled, and the remaining latex was used in the next polymerization step.
- the number average molecular weight, molecular weight distribution, and glass transition temperature of the polymer block (A-19) were determined by analysis in the same manner as in Example 1. The analysis results are shown in Table 4.
- Example 1 shows the average particle size of latex, the mechanical stability of latex, and the content (% by mass) of polymer blocks (A-19) and chloroprene-based polymer blocks (B-19) of chloroprene-based block copolymers. It was obtained by analysis in the same manner as above. The analysis results are shown in Table 4.
- Glass transition temperature of polymer block (A) The glass transition temperature was measured by the following method using a differential scanning calorimeter according to JIS K 7121. Device name: DSC1 (manufactured by Mettler Toledo) Procedure: Under a nitrogen stream of 50 ml / min, the temperature is raised to 120 ° C. at a temperature rise rate of 10 ° C./min, kept at 120 ° C. for 10 minutes, then cooled to -60 ° C., and the temperature rise rate is 10 ° C./min.
- a calibration line was prepared from the content of (B).
- a sample of the chloroprene-based block copolymer precipitated by mixing the sampled latex with methanol was measured by a pyrolysis gas chromatogram, and the peak derived from the polymer block (A) and the peak derived from the chloroprene-based polymer block (B) were measured. From the area ratio, the contents of the polymer block (A) and the chloroprene-based polymer block (B) in the chloroprene-based block copolymer were determined using the calibration line prepared above.
- the mechanical stability of latex was measured by the following method using a Maron mechanical stability tester in accordance with JIS K 6392. Procedure: After filtering the sampled latex with a wire mesh to remove impurities, the filtered latex was adjusted to 20 ° C., and 50 g was weighed in a test container. The test container was attached to the testing machine, and the measurement was performed for 10 minutes under a load of 10 kg. The sample in the test container after the measurement was dried in advance at 125 ° C. for 1 hour, filtered through an 80-mesh wire mesh that had been allowed to cool in a desiccator, and the 80-mesh wire mesh and the precipitate were dried in a dryer at 125 ° C.
- the coagulation rate (unit: mass%) of latex was determined using the following formula. [(Weight of 80 mesh wire mesh and precipitate after drying (unit: g))-(Weight of 80 mesh wire mesh (unit: g))] / [50 ⁇ ((Total solid content of latex (unit: mass%)) ) / 100)] ⁇ 100
- the obtained coagulation rate of latex was used as the mechanical stability of latex.
- the mechanical stability of latex was set to 1% by mass or less as a passing level.
- the prepared film was subjected to a heat aging test at 100 ° C. for 22 hours in a forced circulation type heat aging tester, and then, according to JIS K 6251, 500% elongation at elongation, tensile strength at cutting and elongation at cutting Was measured.
- the 500% elongation modulus was 3.0 MPa or less
- the cutting tensile strength was 17 MPa or more
- the cutting elongation was 900% or more.
- the mechanical stability of the latex was 1% by mass or less, and the mechanical stability of the latex was excellent. Further, even without using a vulcanizing agent or a vulcanization accelerator, the film has excellent flexibility with a modulus of 3.0 MPa or less at 500% elongation, a tensile strength at cutting of 17 MPa or more, and an elongation at cutting of 900% or more. It had excellent tensile properties. Further, after the heat aging test, the modulus at 500% elongation of 3.0 MPa or less was excellent in flexibility, the tensile strength at cutting was 17 MPa or more, the elongation at cutting was 900% or more, and the heat aging property was also excellent. On the other hand, Comparative Examples 1 to 8 were inferior in any of the mechanical stability of the latex, the flexibility of the film, the tensile properties, and the heat aging property.
- the immersion molded product obtained from the chloroprene-based block copolymer latex of the present invention is excellent in flexibility, tensile properties, and heat aging resistance, and can be suitably used for surgical gloves, gloves, balloons, catheters, and the like. Further, the chloroprene-based block copolymer latex of the present invention can be suitably used for paints, adhesives, adhesives and the like.
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Manufacture Of Macromolecular Shaped Articles (AREA)
Abstract
ラテックスの機械的安定性に優れ、また加硫剤や加硫促進剤を使用しなくても、柔軟性、引張特性、及び耐熱老化性に優れた浸漬成形被膜が得られるクロロプレン系ブロック共重合体ラテックスを提供する。 本発明によれば、単独重合時にガラス転移温度が80℃以上の重合体が得られる単量体由来の重合体ブロック(A)5~30質量%と、クロロプレン単量体単位を主体とするクロロプレン系重合体ブロック(B)70~95質量%を含むクロロプレン系ブロック共重合体を含むクロロプレン系ブロック共重合体ラテックスであり、前記クロロプレン系ブロック共重合体ラテックスを浸漬成形して得られた被膜を130℃で30分間熱処理した後にJISK6251に準拠して測定した切断時引張強さが17MPa以上であるクロロプレン系ブロック共重合体ラテックスが提供される。
Description
本発明は、クロロプレン系ブロック共重合体ラテックスに関するものである。
ポリクロロプレンラテックスは、医療用手術手袋、検査手袋、工業手袋、風船、カテーテル、ゴム長靴などの浸漬成形品の材料として知られている。また、各種添加剤を配合することで塗料や粘着剤、接着剤として用いられている。
浸漬成形製品用のポリクロロプレンに関する技術は種々提案されている。先行技術文献としては、クロロプレンと2,3-ジクロロ-1,3-ブタジエンとの共重合体ラテックス(例えば特許文献1参照)、クロロプレンとメタクリル酸を共重合させた変性ポリクロロプレンラテックス(例えば特許文献2参照)、加硫促進剤を含まないクロロプレン系重合体ラテックス(例えば特許文献3参照)、無機塩と酸化亜鉛を含む複合亜鉛華を含有するポリクロロプレンラテックス(例えば特許文献4参照)が知られている。
また、クロロプレン系ブロック共重合体に関する技術としては、アゾ基を含有するポリスチレンを開始剤としてクロロプレンを重合して得られる共重合体(例えば特許文献5参照)や、ジチオカルバメート化したポリクロロプレンに芳香族ビニル単量体を重合させた共重合体(例えば特許文献6参照)、クロロプレン系ポリマーに親水性オリゴマー又は親水性ポリマーを連結させた共重合体(例えば特許文献7参照)、芳香族ビニル化合物重合体のブロックとクロロプレン重合体のブロックを有し全体の数平均分子量とクロロプレン重合体のブロックの数平均分子量を特定した共重合体(例えば特許文献8参照)、アクリル酸エステル重合体のブロックとクロロプレン重合体のブロックを有する共重合体(例えば特許文献9参照)さらに、加硫を用いずに、分子間を化学結合する方法として、特許文献10記載の技術がある。
また、クロロプレン系ブロック共重合体に関する技術としては、アゾ基を含有するポリスチレンを開始剤としてクロロプレンを重合して得られる共重合体(例えば特許文献5参照)や、ジチオカルバメート化したポリクロロプレンに芳香族ビニル単量体を重合させた共重合体(例えば特許文献6参照)、クロロプレン系ポリマーに親水性オリゴマー又は親水性ポリマーを連結させた共重合体(例えば特許文献7参照)、芳香族ビニル化合物重合体のブロックとクロロプレン重合体のブロックを有し全体の数平均分子量とクロロプレン重合体のブロックの数平均分子量を特定した共重合体(例えば特許文献8参照)、アクリル酸エステル重合体のブロックとクロロプレン重合体のブロックを有する共重合体(例えば特許文献9参照)さらに、加硫を用いずに、分子間を化学結合する方法として、特許文献10記載の技術がある。
また、加硫を用いずに高い強度が得られるエラストマーとして、種々の熱可塑性エラストマーが開発されている。浸漬成形製品用の熱可塑性エラストマーとして、強制乳化法により乳化させたスチレン・イソプレン・スチレントリブロック共重合体ラテックス(例えば特許文献11参照)が開発されている。
従来、ポリクロロプレン系ゴム組成物は目的とする機械的強度を得るために、硫黄、酸化亜鉛、酸化マグネシウム等の加硫剤、及びチウラム系、ジチオカルバミン酸塩系、チオウレア系、グアニジン系、キサントゲン酸塩系、チアゾール系等の加硫促進剤の使用が不可欠であった。加硫促進剤は皮膚炎等の皮膚疾患を発症させるIV型アレルギーの原因物質であることから、加硫促進剤の削減や不使用化が重要なテーマとなっている。また、加硫促進剤の不使用化は、アレルギーの低減だけではなくコストダウンにも繋がることから、加硫促進剤を使用せずに十分な機械的強度を発現するゴム組成物が望まれている。
一方、スチレン・イソプレン・スチレントリブロック共重合体ラテックスやスチレン・ブタジエン・スチレントリブロック共重合体ラテックスでは加硫促進剤を使用せずに十分な機械的強度を発現することができるが、これらは強制乳化法によって製造されるため、ラテックスの粒子径を小さくすることができず、ラテックスの機械的安定性に劣るという課題がある。
そこで本発明は、ラテックスの機械的安定性に優れ、また加硫剤や加硫促進剤を使用しなくても、柔軟性、引張特性、及び耐熱老化性に優れた浸漬成形被膜が得られるクロロプレン系ブロック共重合体ラテックスを提供することを課題とする。
本発明は、以下を要旨とするものである。
(1)単独重合時にガラス転移温度が80℃以上の重合体が得られる単量体由来の重合体ブロック(A)5~30質量%と、クロロプレン単量体単位を含むクロロプレン系重合体ブロック(B)70~95質量%を含むクロロプレン系ブロック共重合体を含むクロロプレン系ブロック共重合体ラテックスであり、
前記クロロプレン系ブロック共重合体ラテックスを浸漬成形して得られた被膜を130℃で30分間熱処理した後にJIS K 6251に準拠して測定した切断時引張強さが17MPa以上であるクロロプレン系ブロック共重合体ラテックス。
(1)単独重合時にガラス転移温度が80℃以上の重合体が得られる単量体由来の重合体ブロック(A)5~30質量%と、クロロプレン単量体単位を含むクロロプレン系重合体ブロック(B)70~95質量%を含むクロロプレン系ブロック共重合体を含むクロロプレン系ブロック共重合体ラテックスであり、
前記クロロプレン系ブロック共重合体ラテックスを浸漬成形して得られた被膜を130℃で30分間熱処理した後にJIS K 6251に準拠して測定した切断時引張強さが17MPa以上であるクロロプレン系ブロック共重合体ラテックス。
(2)前記クロロプレン系ブロック共重合体100質量%中に、前記重合体ブロック(A)5~15質量%と、前記クロロプレン系重合体ブロック(B)を85~95質量%含有する(1)に記載のクロロプレン系ブロック共重合体ラテックス。
(3)前記クロロプレン系ブロック共重合体ラテックスを動的光散乱法によって測定した平均粒子径が300nm以下である、(1)または(2)に記載のクロロプレン系ブロック共重合体ラテックス。
(4)前記クロロプレン系重合体ブロック(B)が、クロロプレン単量体単位及び多官能性単量体単位を有するものである(1)~(3)のいずれか一項に記載のクロロプレン系ブロック共重合体ラテックス。
(5)浸漬成形体用である(1)~(4)のいずれか一項に記載のクロロプレン系ブロック共重合体ラテックス。
本発明によれば、ラテックスの機械的安定性に優れ、また加硫剤や加硫促進剤を使用しなくても、柔軟性、引張特性、及び耐熱老化性に優れた浸漬成形被膜を得ることができるクロロプレン系ブロック共重合体ラテックスが提供される。
以下、本発明の実施形態について詳細に説明する。なお、本明細書及び特許請求の範囲において、「A~B」という記載は、A以上でありB以下であるという意味である。
<クロロプレン系ブロック共重合体ラテックス>
クロロプレン系ブロック共重合体ラテックスは、重合体ブロック(A)5~30質量%と、クロロプレン単量体単位を含むクロロプレン系重合体ブロック(B)70~95質量%を含むクロロプレン系ブロック共重合体を含むものである。
クロロプレン系ブロック共重合体ラテックスは、重合体ブロック(A)5~30質量%と、クロロプレン単量体単位を含むクロロプレン系重合体ブロック(B)70~95質量%を含むクロロプレン系ブロック共重合体を含むものである。
[重合体ブロック(A)]
重合体ブロック(A)は、単独重合時にガラス転移温度が80℃以上の重合体が得られる単量体由来の重合体ブロックである。このような単量体を用いることで、得られる浸漬成形被膜の切断時引張強さ、耐熱老化性が向上する。好ましくはガラス転移温度が85℃以上の重合体が得られる単量体を用いるとよい。成形性の観点からは、ガラス転移温度が150℃以下の重合体が得られる単量体であれば好ましく、特に好ましくは120℃以下の重合体が得られる単量体である。ガラス転移温度は、例えば、80、85、90、95、100、105、110、120、130、140、150℃であり、ここで例示した数値の何れか2つの間の範囲内であってもよい。なお、本明細書においてガラス転移温度とは、JIS K 7121に準拠して測定した補外ガラス転移温度(T eg)である。重合体ブロック(A)が、単量体(A)を重合することで得られる重合体ブロックである場合、単量体(A)は、単量体Aを単独重合して、数平均分子量10000~30000のホモポリマー(A)としたとき、該ホモポリマー(A)が、上記ガラス転移温度を有する単量体であることが好ましい。
重合体ブロック(A)は、単独重合時にガラス転移温度が80℃以上の重合体が得られる単量体由来の重合体ブロックである。このような単量体を用いることで、得られる浸漬成形被膜の切断時引張強さ、耐熱老化性が向上する。好ましくはガラス転移温度が85℃以上の重合体が得られる単量体を用いるとよい。成形性の観点からは、ガラス転移温度が150℃以下の重合体が得られる単量体であれば好ましく、特に好ましくは120℃以下の重合体が得られる単量体である。ガラス転移温度は、例えば、80、85、90、95、100、105、110、120、130、140、150℃であり、ここで例示した数値の何れか2つの間の範囲内であってもよい。なお、本明細書においてガラス転移温度とは、JIS K 7121に準拠して測定した補外ガラス転移温度(T eg)である。重合体ブロック(A)が、単量体(A)を重合することで得られる重合体ブロックである場合、単量体(A)は、単量体Aを単独重合して、数平均分子量10000~30000のホモポリマー(A)としたとき、該ホモポリマー(A)が、上記ガラス転移温度を有する単量体であることが好ましい。
重合体ブロック(A)を構成する単量体単位としては、芳香族ビニル単量体単位、メタクリル酸メチル単量体単位、アクリロニトリル単量体単位が挙げられる。好ましくは芳香族ビニル単量体に由来する単位が用いられ、スチレン単位が好適に用いられる。重合体ブロック(A)は、本発明の目的を損なわない範囲において、これら単量体同士の共重合により得られる重合体ブロック、またはこれら単量体と共重合可能な単量体に由来する単位からなる重合体ブロックであっても構わない。
重合体ブロック(A)の数平均分子量は、得られる浸漬成形被膜の引張特性、耐熱老化性、成形性の観点から、10,000以上であることが好ましい。重合体ブロック(A)の数平均分子量は、例えば、10000、15000、20000、25000、30000とすることができ、ここで例示した数値の何れか2つの間の範囲内であってもよい。また、重合体ブロック(A)の分子量分布は、成形性の観点から、2.0以下であることが好ましい。重合体ブロック(A)の分子量分布は、例えば、1.0、1.1、1.2、1.3、1.4、1.5、1.6、1.7、1.8、1.9、2.0とすることができ、ここで例示した数値の何れか2つの間の範囲内であってもよい。
なお、本明細書において、数平均分子量及び重量平均分子量とは、ゲルパーミエーションクロマトグラフィー(GPC)にて測定されるポリスチレン換算の値であり、以下記載の測定条件における測定値である。
装置名:HLC-8320(東ソー社製)
カラム:TSKgel GMHHR-Hを3本直列 温度:40℃
検出:示差屈折率
溶媒:テトラヒドロフラン
検量線:標準ポリスチレン(PS)を用いて作製した。
なお、本明細書において、数平均分子量及び重量平均分子量とは、ゲルパーミエーションクロマトグラフィー(GPC)にて測定されるポリスチレン換算の値であり、以下記載の測定条件における測定値である。
装置名:HLC-8320(東ソー社製)
カラム:TSKgel GMHHR-Hを3本直列 温度:40℃
検出:示差屈折率
溶媒:テトラヒドロフラン
検量線:標準ポリスチレン(PS)を用いて作製した。
[クロロプレン系重合体ブロック(B)]
クロロプレン系重合体ブロック(B)は、クロロプレン単量体(2-クロロ-1,3-ブタジエン)単位を含み、クロロプレン単量体単位を主体とする。クロロプレン系重合体ブロック(B)は多官能性単量体単位を含んでいても構わない。なお、本発明の目的を損なわない範囲において、クロロプレン系重合体ブロック(B)は、クロロプレン単量体単位と、多官能性単量体単位と、これらと共重合可能な単量体に由来する単位からなる重合体ブロックであっても構わない。クロロプレン系重合体ブロック(B)は、クロロプレン系重合体ブロック(B)を100質量%としたとき、クロロプレン単量体由来の構造単位を90質量%以上含むことが好ましい。
クロロプレン系重合体ブロック(B)は、クロロプレン単量体(2-クロロ-1,3-ブタジエン)単位を含み、クロロプレン単量体単位を主体とする。クロロプレン系重合体ブロック(B)は多官能性単量体単位を含んでいても構わない。なお、本発明の目的を損なわない範囲において、クロロプレン系重合体ブロック(B)は、クロロプレン単量体単位と、多官能性単量体単位と、これらと共重合可能な単量体に由来する単位からなる重合体ブロックであっても構わない。クロロプレン系重合体ブロック(B)は、クロロプレン系重合体ブロック(B)を100質量%としたとき、クロロプレン単量体由来の構造単位を90質量%以上含むことが好ましい。
クロロプレン系重合体ブロック(B)中の各構造単位の含有量は、特に限定するものではないが、好ましくはクロロプレン単量体単位90~99.95質量%、多官能性単量体単位0.05~10質量%である。クロロプレン系重合体ブロック(B)中の多官能性単量体単位の含有量は、例えば、0.05、0.50、1.00、2.00、3.00、4.00、5.00、6.00、7.00、8.00、9.00、10.00質量%であり、ここで例示した数値の何れか2つの間の範囲内であってもよい。
[多官能性単量体]
多官能性単量体は、得られる浸漬成形被膜の引張特性や耐熱老化性を向上させるために用いるものである。多官能性単量体は、分子中にラジカル性重合基を2個以上有する化合物である。得られる浸漬成形被膜の柔軟性、及び切断時引張強さ、及び成形性の観点から、化学式(1)で表される単量体、芳香族ポリエン単量体が好適に用いられる。化学式(1)で表される単量体としては、1.9-ノナンジオールジメタクリレート、1.9-ノナンジオールジアクリレート、ネオペンチルグリコールジメタクリレート、ネオペンチルグリコールジアクリレート、1.6-ヘキサンジオールジメタクリレート、1.6-ヘキサンジオールジアクリレート、エチレングリコールジメタクリレート、ジエチレングリコールジメタクリレート、トリエチレングリコールジメタクリレート、トリエチレングリコールジアクリレート、ポリエチレングリコールジメタクリレート、ポリエチレングリコールジアクリレートが特に好適に用いられる。芳香族ポリエン単量体としては、10以上30以下の炭素数を持ち、複数の二重結合(ビニル基)と単数又は複数の芳香族基を有した芳香族ポリエンであり、例えば、o-ジビニルベンゼン、p-ジビニルベンゼン、m-ジビニルベンゼン、1,4-ジビニルナフタレン、3,4-ジビニルナフタレン、2,6-ジビニルナフタレン、1,2-ジビニル-3,4-ジメチルベンゼン、1,3-ジビニル-4,5,8-トリブチルナフタレン等、芳香族ポリエン単量体に由来する単位が挙げられ、好ましくはオルトジビニルベンゼン単位、パラジビニルベンゼン単位及びメタジビニルベンゼン単位のいずれか1種又は2種以上の混合物が好適に用いられる。
多官能性単量体は、得られる浸漬成形被膜の引張特性や耐熱老化性を向上させるために用いるものである。多官能性単量体は、分子中にラジカル性重合基を2個以上有する化合物である。得られる浸漬成形被膜の柔軟性、及び切断時引張強さ、及び成形性の観点から、化学式(1)で表される単量体、芳香族ポリエン単量体が好適に用いられる。化学式(1)で表される単量体としては、1.9-ノナンジオールジメタクリレート、1.9-ノナンジオールジアクリレート、ネオペンチルグリコールジメタクリレート、ネオペンチルグリコールジアクリレート、1.6-ヘキサンジオールジメタクリレート、1.6-ヘキサンジオールジアクリレート、エチレングリコールジメタクリレート、ジエチレングリコールジメタクリレート、トリエチレングリコールジメタクリレート、トリエチレングリコールジアクリレート、ポリエチレングリコールジメタクリレート、ポリエチレングリコールジアクリレートが特に好適に用いられる。芳香族ポリエン単量体としては、10以上30以下の炭素数を持ち、複数の二重結合(ビニル基)と単数又は複数の芳香族基を有した芳香族ポリエンであり、例えば、o-ジビニルベンゼン、p-ジビニルベンゼン、m-ジビニルベンゼン、1,4-ジビニルナフタレン、3,4-ジビニルナフタレン、2,6-ジビニルナフタレン、1,2-ジビニル-3,4-ジメチルベンゼン、1,3-ジビニル-4,5,8-トリブチルナフタレン等、芳香族ポリエン単量体に由来する単位が挙げられ、好ましくはオルトジビニルベンゼン単位、パラジビニルベンゼン単位及びメタジビニルベンゼン単位のいずれか1種又は2種以上の混合物が好適に用いられる。
クロロプレン系ブロック共重合体の各構造単位の含有量は、重合体ブロック(A)5~30質量%、クロロプレン系重合体ブロック(B)70~95質量%であり、好ましくは重合体ブロック(A)5~15質量%、クロロプレン系重合体ブロック(B)85~95質量%である。重合体ブロック(A)が5質量%以上である場合に、得られる浸漬成形被膜の切断時引張強さ、耐熱老化性が向上する。重合体ブロック(A)が30質量%以下である場合に、得られる浸漬成形被膜の柔軟性が向上する。重合体ブロック(A)は好ましくは15質量%以下である。クロロプレン系重合体ブロック(B)が70質量%以上である場合に、得られる浸漬成形被膜の柔軟性が向上する。クロロプレン系重合体ブロック(B)は、好ましくは85質量%以上である。クロロプレン系重合体ブロック(B)が95質量%以下である場合に、得られる浸漬成形被膜の切断時引張強さが向上する。クロロプレン系ブロック共重合体を100質量%としたとき、クロロプレン系ブロック共重合体に含まれる重合体ブロック(A)の含有率は、例えば、5、10、15、20、25、30質量%であり、ここで例示した数値の何れか2つの間の範囲内であってもよい。
本発明の一実施形態に係るクロロプレン系ブロック共重合体は、重合体ブロック(A)及び重合体ブロック(B)からなるものとすることができ、他の重合体ブロックを含まないものとすることができる。クロロプレン系ブロック共重合体は、重合体ブロック(A)-重合体ブロック(B)のジブロック共重合体とすることができる。
本発明の一実施形態に係るクロロプレン系ブロック共重合体は、重合体ブロック(A)及び重合体ブロック(B)からなるものとすることができ、他の重合体ブロックを含まないものとすることができる。クロロプレン系ブロック共重合体は、重合体ブロック(A)-重合体ブロック(B)のジブロック共重合体とすることができる。
[ラテックスの平均粒子径]
クロロプレン系ブロック共重合体ラテックスについて、動的光散乱法により測定された平均粒子径は、ラテックスの機械的安定性の観点から、300nm以下であることが好ましく、250nm以下であることが更に好ましく、200nm以下であることがより更に好ましい。下限は、例えば、100nm以上とできる。平均粒子径は、例えば、100、120、140、150、160、170、180、190、200、220、240、260、280、300nmであり、ここで例示した数値の何れか2つの間の範囲内であってもよい。
なお、本明細書において、平均粒子径とは、動的光散乱法により測定され、光子相関法により算出した平均粒子径である。平均粒子径は、クロロプレン系ブロック共重合体ラテックスの配合の種類や量、製造条件を制御することで調整することができる。
クロロプレン系ブロック共重合体ラテックスについて、動的光散乱法により測定された平均粒子径は、ラテックスの機械的安定性の観点から、300nm以下であることが好ましく、250nm以下であることが更に好ましく、200nm以下であることがより更に好ましい。下限は、例えば、100nm以上とできる。平均粒子径は、例えば、100、120、140、150、160、170、180、190、200、220、240、260、280、300nmであり、ここで例示した数値の何れか2つの間の範囲内であってもよい。
なお、本明細書において、平均粒子径とは、動的光散乱法により測定され、光子相関法により算出した平均粒子径である。平均粒子径は、クロロプレン系ブロック共重合体ラテックスの配合の種類や量、製造条件を制御することで調整することができる。
クロロプレン系ブロック共重合体の重量平均分子量は、特に制限はないが、成形加工性の観点から、好ましくは5~60万であり、特に好ましくは10~50万である。
本発明の一実施形態に係るクロロプレン系ブロック共重合体ラテックスの機械的安定性は、1質量%以下であることが好ましく、0.2質量%以下であることがより好ましく、0.1質量%以下であることがさらにより好ましい。なお、クロロプレン系ブロック共重合体ラテックスの機械的安定性は、実施例に記載の測定方法によって評価することができる。機械的安定性は、クロロプレン系ブロック共重合体ラテックスの配合の種類や量、製造条件を制御することで調整することができ、例えば、クロロプレン系ブロック共重合体ラテックスに係る平均粒子径を制御することによって、調整することができる。
[浸漬成形被膜]
本実施形態のクロロプレン系ブロック共重合体ラテックスは、該クロロプレン系ブロック共重合体ラテックスを浸漬成形することで得られる浸漬成形被膜を、130℃で30分間熱処理した後にJIS K 6251に準拠して測定した切断時引張強さが17MPa以上であり、加硫剤及び加硫促進剤を含まない未加硫浸漬成形被膜を与えうる。当該未加硫浸漬成形被膜は、柔軟性を備え、加硫剤及び加硫促進剤を含まずとも十分な機械的強度を発揮する。切断時引張強さは、18MPa以上であることがより好ましく、19MPa以上であることがさらにより好ましく、20MPa以上であることがさらにより好ましい。上限は特に制限されないが、例えば、30MPa以下である。
本発明の一実施形態に係るクロロプレン系ブロック共重合体ラテックスは、上記浸漬成形被膜を、30℃で30分間熱処理した後、さらに、100℃、22時間の条件で熱老化試験を行った後にJIS K 6251に準拠して測定した切断時引張強さが、17MPa以上であることが好ましく、18MPa以上であることがより好ましく、19MPa以上であることがさらにより好ましく、20MPa以上であることがさらにより好ましい。上限は特に制限されないが、例えば、30MPa以下である。
本実施形態のクロロプレン系ブロック共重合体ラテックスは、該クロロプレン系ブロック共重合体ラテックスを浸漬成形することで得られる浸漬成形被膜を、130℃で30分間熱処理した後にJIS K 6251に準拠して測定した切断時引張強さが17MPa以上であり、加硫剤及び加硫促進剤を含まない未加硫浸漬成形被膜を与えうる。当該未加硫浸漬成形被膜は、柔軟性を備え、加硫剤及び加硫促進剤を含まずとも十分な機械的強度を発揮する。切断時引張強さは、18MPa以上であることがより好ましく、19MPa以上であることがさらにより好ましく、20MPa以上であることがさらにより好ましい。上限は特に制限されないが、例えば、30MPa以下である。
本発明の一実施形態に係るクロロプレン系ブロック共重合体ラテックスは、上記浸漬成形被膜を、30℃で30分間熱処理した後、さらに、100℃、22時間の条件で熱老化試験を行った後にJIS K 6251に準拠して測定した切断時引張強さが、17MPa以上であることが好ましく、18MPa以上であることがより好ましく、19MPa以上であることがさらにより好ましく、20MPa以上であることがさらにより好ましい。上限は特に制限されないが、例えば、30MPa以下である。
また、本実施形態のクロロプレン系ブロック共重合体ラテックスは、該クロロプレン系ブロック共重合体ラテックスを浸漬成形することで得られる浸漬成形被膜を、130℃で30分間熱処理した後にJIS K 6251に準拠して測定した切断時伸びが900%以上であることが好ましく、905%以上であることがより好ましく、910%以上であることがさらにより好ましい。上限は特に制限されないが、例えば、1300%以下である。
本発明の一実施形態に係るクロロプレン系ブロック共重合体ラテックスは、上記浸漬成形被膜を、30℃で30分間熱処理した後、さらに、100℃、22時間の条件で熱老化試験を行った後にJIS K 6251に準拠して測定した切断時伸びが900%以上であることが好ましく、905%以上であることがより好ましく、910%以上であることがさらにより好ましい。上限は特に制限されないが、例えば、1300%以下である。
本発明の一実施形態に係るクロロプレン系ブロック共重合体ラテックスは、上記浸漬成形被膜を、30℃で30分間熱処理した後、さらに、100℃、22時間の条件で熱老化試験を行った後にJIS K 6251に準拠して測定した切断時伸びが900%以上であることが好ましく、905%以上であることがより好ましく、910%以上であることがさらにより好ましい。上限は特に制限されないが、例えば、1300%以下である。
本実施形態のクロロプレン系ブロック共重合体ラテックスは、該クロロプレン系ブロック共重合体ラテックスを浸漬成形することで得られる浸漬成形被膜を、130℃で30分間熱処理した後にJIS K 6251に準拠して測定した500%伸長時モジュラスが、3.0MPa以下であることが好ましく、2.9MPa以下であることがより好ましく、2.8MPa以下であることがさらにより好ましい。下限は特に制限されないが、例えば、1.0MPa以上である。
本発明の一実施形態に係るクロロプレン系ブロック共重合体ラテックスは、上記浸漬成形被膜を、30℃で30分間熱処理した後、さらに、100℃、22時間の条件で熱老化試験を行った後に、JIS K 6251に準拠して測定した500%伸長時モジュラスが3.0MPa以下であることが好ましく、2.9MPa以下であることがより好ましく、2.8MPa以下であることがさらにより好ましい。下限は特に制限されないが、例えば、1.0MPa以上である。
なお、上記浸漬成形被膜は、実施例に記載の方法で得ることができ、浸漬成形被膜は、成形に際し、加硫剤及び加硫促進剤を用いないものとできる。
本発明の一実施形態に係るクロロプレン系ブロック共重合体ラテックスは、上記浸漬成形被膜を、30℃で30分間熱処理した後、さらに、100℃、22時間の条件で熱老化試験を行った後に、JIS K 6251に準拠して測定した500%伸長時モジュラスが3.0MPa以下であることが好ましく、2.9MPa以下であることがより好ましく、2.8MPa以下であることがさらにより好ましい。下限は特に制限されないが、例えば、1.0MPa以上である。
なお、上記浸漬成形被膜は、実施例に記載の方法で得ることができ、浸漬成形被膜は、成形に際し、加硫剤及び加硫促進剤を用いないものとできる。
クロロプレン系ブロック共重合体ラテックスを浸漬成形することで得られる浸漬成形被膜の切断時引張強さ、切断時伸び、500%伸長時モジュラスを調整するには、多官能性単量体の添加量を調整したり、クロロプレン系重合体ブロック(B)に含める多官能性単量体単位の含有量やクロロプレン系ブロック共重合体中の当該クロロプレン系重合体ブロック(B)の含有量を調整したり、後述のRAFT剤の存在下で重合することにより導入される官能基の種類や量を調整したりすればよい。
本実施形態のクロロプレン系ブロック共重合体ラテックスから得られる浸漬成形被膜は、加硫剤又は加硫促進剤を含んでもよい。浸漬成形被膜は、加硫剤及び加硫促進剤を含む場合、その合計含有率を5質量%以下とすることができ、1質量%以下とすることがより好ましく、0.1質量%とすることがより好ましい。しかしながら、上記未加硫浸漬成形被膜は、加硫剤及び加硫促進剤を含まずとも、十分な機械的強度を有しているため、アレルギーの低減及びコストダウンの観点から、加硫剤及び加硫促進剤を含まないものが好ましい。
[クロロプレン系ブロック共重合体ラテックスの製造方法]
本発明に係るクロロプレン系ブロック共重合体ラテックスの製造方法について説明する。製造方法は、所望のクロロプレン系ブロック共重合体ラテックスが得られれば特に限定されないが、重合体ブロック(A)を合成する乳化重合工程1の後に、クロロプレン系重合体ブロック(B)を合成する乳化重合工程2からなる二段階の重合工程を経てクロロプレン系ブロック共重合体ラテックスを得る製造方法により得ることが可能である。
本発明に係るクロロプレン系ブロック共重合体ラテックスの製造方法について説明する。製造方法は、所望のクロロプレン系ブロック共重合体ラテックスが得られれば特に限定されないが、重合体ブロック(A)を合成する乳化重合工程1の後に、クロロプレン系重合体ブロック(B)を合成する乳化重合工程2からなる二段階の重合工程を経てクロロプレン系ブロック共重合体ラテックスを得る製造方法により得ることが可能である。
(乳化重合工程1)
乳化重合工程1について具体的に説明する。乳化重合工程1では、重合体ブロック(A)を構成する単量体をリビングラジカル乳化重合して重合体ブロック(A)を合成する。上記したように、ここで得られる重合体ブロック(A)は、上記したガラス転移温度を有することが好ましい。乳化重合で用いる乳化剤としては、特に限定されるものではないが、乳化安定性の観点からアニオン系又はノニオン系の乳化剤が好ましい。特に得られるクロロプレン系ブロック共重合体ラテックスから得られる浸漬成形被膜に適当な強度を持たせて過度の収縮及び破損を防ぐことができるという理由から、ロジン酸アルカリ金属塩を使用することが好ましい。乳化剤の濃度は、重合反応を効率的に行う観点から、重合体ブロック(A)を構成する単量体100質量%に対して、5~50質量%であることが好ましい。ラジカル重合開始剤としては、公知のラジカル重合開始剤を用いることができ、例えば過硫酸カリウム、過酸化ベンゾイル、過酸化水素、アゾ系化合物などを用いることができる。純水の添加量は、重合体ブロック(A)を構成する単量体100質量%に対して、100~300質量%が好ましい。純水の添加量が300質量%以下である場合に、得られる浸漬成形被膜の切断時引張強さが向上する。重合温度は、単量体の種類に応じて適宜決定すればよいが、10~100℃が好ましく、20~80℃が特に好ましい。
乳化重合工程1について具体的に説明する。乳化重合工程1では、重合体ブロック(A)を構成する単量体をリビングラジカル乳化重合して重合体ブロック(A)を合成する。上記したように、ここで得られる重合体ブロック(A)は、上記したガラス転移温度を有することが好ましい。乳化重合で用いる乳化剤としては、特に限定されるものではないが、乳化安定性の観点からアニオン系又はノニオン系の乳化剤が好ましい。特に得られるクロロプレン系ブロック共重合体ラテックスから得られる浸漬成形被膜に適当な強度を持たせて過度の収縮及び破損を防ぐことができるという理由から、ロジン酸アルカリ金属塩を使用することが好ましい。乳化剤の濃度は、重合反応を効率的に行う観点から、重合体ブロック(A)を構成する単量体100質量%に対して、5~50質量%であることが好ましい。ラジカル重合開始剤としては、公知のラジカル重合開始剤を用いることができ、例えば過硫酸カリウム、過酸化ベンゾイル、過酸化水素、アゾ系化合物などを用いることができる。純水の添加量は、重合体ブロック(A)を構成する単量体100質量%に対して、100~300質量%が好ましい。純水の添加量が300質量%以下である場合に、得られる浸漬成形被膜の切断時引張強さが向上する。重合温度は、単量体の種類に応じて適宜決定すればよいが、10~100℃が好ましく、20~80℃が特に好ましい。
(乳化重合工程2)
乳化重合工程2では、上記乳化重合工程1のリビングラジカル乳化重合で得られた重合体ブロック(A)を含むラテックスに対して、純水、乳化剤、クロロプレン単量体、及び多官能性単量体を添加して乳化重合することでクロロプレン系ブロック共重合体ラテックスを得る。クロロプレン単量体は、一括添加でも分添でも構わない。乳化重合工程2の重合温度は、重合制御のしやすさの観点から10~50℃であることが好ましい。重合反応は重合停止剤を加えることにより停止させる。重合停止剤としては、例えばチオジフェニルアミン、4-第3ブチルカテコール、2,2'-メチレンビス-4-メチル-6-第3-ブチルフェノール等がある。乳化重合終了後の未反応単量体は、常法の減圧蒸留等の方法で除去することができる。
乳化重合工程2では、上記乳化重合工程1のリビングラジカル乳化重合で得られた重合体ブロック(A)を含むラテックスに対して、純水、乳化剤、クロロプレン単量体、及び多官能性単量体を添加して乳化重合することでクロロプレン系ブロック共重合体ラテックスを得る。クロロプレン単量体は、一括添加でも分添でも構わない。乳化重合工程2の重合温度は、重合制御のしやすさの観点から10~50℃であることが好ましい。重合反応は重合停止剤を加えることにより停止させる。重合停止剤としては、例えばチオジフェニルアミン、4-第3ブチルカテコール、2,2'-メチレンビス-4-メチル-6-第3-ブチルフェノール等がある。乳化重合終了後の未反応単量体は、常法の減圧蒸留等の方法で除去することができる。
乳化重合工程2で得られたクロロプレン系ブロック共重合体ラテックスには、本発明の目的を損なわない範囲で、重合後に凍結安定剤、乳化安定剤、粘度調整剤、酸化防止剤、防腐剤などを任意に添加することができる。
クロロプレン系ブロック共重合体は、下記化学式(2)又は化学式(3)で表される構造の官能基を有することが好ましい。
上記化学式(2)、又は化学式(3)で表される末端構造は、公知のRAFT剤の存在下で乳化重合を行うことで、ブロック共重合体に導入される。上記化学式(2)で表される構造を導く化合物は特に限定されるものではなく一般的な化合物を使用することができ、例えばジチオカルバメート類、ジチオエステル類が挙げられる。具体的にはベンジル1-ピロールカルボジチオエート(慣用名:ベンジル1-ピロールジチオカルバメート)、ベンジルフェニルカルボジチオエート、1-ベンジル-N,Nジメチル-4-アミノジチオベンゾエート、1-ベンジル-4-メトキシジチオベンゾエート、1-フェニルエチルイミダゾールカルボジチオエート(慣用名:1-フェニルエチルイミダゾールジチオカルバメート)、ベンジル-1-(2-ピロリジノン)カルボジチオエート)(慣用名:ベンジル-1-(2-ピロリジノン)ジチオカルバメート)、ベンジルフタルイミジルカルボジチオエート、(慣用名:ベンジルフタルイミジルジチオカルバメート)、2-シアノプロプ-2-イル-1-ピロールカルボジチオエート、(慣用名:2-シアノプロプ-2-イル-1-ピロールジチオカルバメート)、2-シアノブト-2-イル-1-ピロールカルボジチオエート、(慣用名:2-シアノブト-2-イル-1-ピロールジチオカルバメート)、ベンジル-1-イミダゾールカルボジチオエート、(慣用名ベンジル-1-イミダゾールジチオカルバメート)、2-シアノプロプ-2-イル-N,N-ジメチルジチオカルバメート、ベンジル-N,N-ジエチルジチオカルバメート、シアノメチル-1-(2-ピロリドン)ジチオカルバメート、2-(エトキシカルボニルベンジル)プロプ-2-イル-N,N-ジエチルジチオカルバメート、1-フェニルエチルジチオベンゾエート、2-フェニルプロプ-2-イルジチオベンゾエート、1-酢酸-1-イル-エチルジチオベンゾエート、1-(4-メトキシフェニル)エチルジチオベンゾエート、ベンジルジチオアセテート、エトキシカルボニルメチルジチオアセタート、2-(エトキシカルボニル)プロプ-2-イルジチオベンゾエート、2-シアノプロプ-2-イルジチオベンゾエート、tert-ブチルジチオベンゾエート、2,4,4-トリメチルペンタ-2-イルジチオベンゾエート、2-(4-クロロフェニル)-プロプ-2-イルジチオベンゾエート、3-ビニルベンジルジチオベンゾエート、4-ビニルベンジルジチオベンゾエート、ベンジルジエトキシホスフィニルジチオフォルマート、tert-ブチルトリチオペルベンゾエート、2-フェニルプロプ-2-イル-4-クロロジチオベンゾエート、ナフタレン-1-カルボン酸-1-メチル-1-フェニル-エチルエステル、4-シアノ-4-メチル-4-チオベンジルスルファニル酪酸、ジベンジルテトラチオテレフタラート、カルボキシメチルジチオベンゾエート、ジチオベンゾエート末端基を持つポリ(酸化エチレン)、4-シアノ-4-メチル-4-チオベンジルスルファニル酪酸末端基を持つポリ(酸化エチレン)、2-[(2-フェニルエタンチオイル)スルファニル]プロパン酸、2-[(2-フェニルエタンチオイル)スルファニル]コハク酸、3,5-ジメチル-1H-ピラゾール-1-カルボジチオエートカリウム、シアノメチル-3,5-ジメチル-1H-ピラゾール-1-カルボジチオエート、シアノメチルメチル-(フェニル)ジチオカルバメート、ベンジル-4-クロロジチオベンゾエート、フェニルメチル-4-クロロジチオベンゾエート、4-ニトロベンジル-4-クロロジチオベンゾエート、フェニルプロプ-2-イル-4-クロロジチオベンゾエート、1-シアノ-1-メチルエチル-4-クロロジチオベンゾエート、3-クロロ-2-ブテニル-4-クロロジチオベンゾエート、2-クロロ-2-ブテニルジチオベンゾエート、ベンジルジチオアセテート、3-クロロ-2-ブテニル-1H-ピロール-1-ジチオカルボン酸、2-シアノブタン-2-イル4-クロロ-3,5-ジメチル-1H-ピラゾール-1-カルボジチオエート、シアノメチルメチル(フェニル)カルバモジチオエートが挙げられる。これらのなかでも特に好ましくは、ベンジル1-ピロールカルボジチオエート、ベンジルフェニルカルボジチオエートが用いられる。上記化学式(3)で表される構造を導く化合物は、特に限定されるものではなく一般的な化合物を使用することができ、例えば、2-シアノ-2-プロピルドデシルトリチオカルボナート、ジベンジルトリチオカルボナート、ブチルベンジルトリチオカルボナート、2-[[(ブチルチオ)チオキソメチル]チオ]プロピオン酸、2-[[(ドデシルチオ)チオキソメチル]チオ]プロピオン酸、2-[[(ブチルチオ)チオキソメチル]チオ]コハク酸、2-[[(ドデシルチオ)チオキソメチル]チオ]コハク酸、2-[[(ドデシルチオ)チオキソメチル]チオ]-2-メチルプロピオン酸、2,2′-[カルボノチオイルビス(チオ)]ビス[2-メチルプロピオン酸]、2-アミノ-1-メチル-2-オキソエチルブチルトリチオカルボナート、ベンジル2-[(2-ヒドロキシエチル)アミノ]-1-メチル-2-オキソエチルトリチオカルボナート、3-[[[(tert-ブチル)チオ]チオキソメチル]チオ]プロピオン酸、シアノメチルドデシルトリチオカルボナート、ジエチルアミノベンジルトリチオカルボナート、ジブチルアミノベンジルトリチオカルボナートなどのトリチオカルボナート類が挙げられる。これらのなかでも特に好ましくは、ジベンジルトリチオカルボナート、ブチルベンジルトリチオカルボナートが用いられる。
[浸漬成形体]
本実施形態に係る浸漬成形体は、前述したクロロプレン系ブロック共重合体ラテックスを浸漬成形したものであり、モジュラスが低く柔軟でかつ切断時引張強さや切断時伸びなどの機械的特性に優れ、また耐熱老化性にも優れている。当該浸漬成形体としては、手袋、風船、及びカテーテルが好適である。本発明の一実施形態に係る浸漬成形体は、上記したクロロプレン系ブロック共重合体ラテックスを含む、クロロプレン系ブロック共重合体ラテックス組成物を成形することによって得ることもできる。
本実施形態に係る浸漬成形体は、前述したクロロプレン系ブロック共重合体ラテックスを浸漬成形したものであり、モジュラスが低く柔軟でかつ切断時引張強さや切断時伸びなどの機械的特性に優れ、また耐熱老化性にも優れている。当該浸漬成形体としては、手袋、風船、及びカテーテルが好適である。本発明の一実施形態に係る浸漬成形体は、上記したクロロプレン系ブロック共重合体ラテックスを含む、クロロプレン系ブロック共重合体ラテックス組成物を成形することによって得ることもできる。
本実施形態の浸漬成形体を製造する際の成型方法としては、例えば凝固液浸漬法が挙げられるが、これに限定されるものではなく、常法に従って成形すれば良い。
本実施形態の浸漬成形体は、本発明の目的を損なわない範囲において、充填剤又は補強剤、可塑剤、加工助剤や滑剤、老化防止剤、シランカップリング剤などを含んでいても良い。これら薬剤は、目的や用途に応じて適宜選択することができる。
本実施形態の浸漬成形体は、加硫剤及び/又は加硫促進剤を含まないものであってもよい。すなわち、上記浸漬成形体は、加硫剤を含み加硫促進剤を含まないもの、加硫剤及び加硫促進剤を含むもの、加硫剤及び加硫促進剤を含まないものを包含する。加硫剤及び加硫促進剤を配合するか否かは、目的とする浸漬成形体に応じて決定すればよい。本発明の一実施形態に係る浸漬成形体が加硫剤及び/又は加硫促進剤を含む場合、該浸漬成形体を100質量%としたとき、加硫剤及び加硫促進剤の合計含有率を5質量%以下とすることができ、1質量%以下とすることがより好ましく、0.1質量%とすることがより好ましい。本発明の一実施形態に係る浸漬成形体は、アレルギーの低減及びコストダウンの観点から、加硫剤及び加硫促進剤を含まないものとすることもでき、浸漬成形体は、加硫剤及び加硫促進剤を含まずとも、十分な機械的強度を有する。
加硫剤としては、例えば、硫黄、酸化亜鉛、酸化マグネシウム等が挙げられる。
加硫促進剤は、原料ゴムの加硫に際して、加硫剤と作用して加硫速度を増大させ加硫時間の短縮、加硫温度の低下、加硫剤の減量、加硫ゴムの物性向上を目的として添加する薬剤であり、通常は硫黄加硫反応を促進する薬剤を指す。
クロロプレン系共重合体ラテックスの加硫に一般的に用いられる加硫促進剤としては、チウラム系、ジチオカルバミン酸塩系、チオウレア系、グアニジン系、キサントゲン酸塩系、チアゾール系等が挙げられ、これらは単独で又は必要に応じ2種以上組み合わせて用いられる。
本実施形態の浸漬成形体は、加硫剤及び加硫促進剤の有無を問わず優れた機械的特性を発揮するが、アレルギー低減及びコストダウンの観点からは、加硫剤及び加硫促進剤を含まないものが好ましい。
本実施形態の浸漬成形体に添加する老化防止剤として、通常のゴム用途に使用されている、ラジカルを捕捉して自動酸化を防止する一次老化防止剤と、ハイドロパーオキサイドを無害化する二次老化防止剤を添加することができる。それらの老化防止剤はクロロプレン系共重合体ラテックス中のゴム成分100質量部に対して、それぞれ0.1質量部以上10質量部以下の割合で添加することができ、好ましくは2質量部以上5質量部以下の範囲である。これらの老化防止剤は単独使用のみならず2種以上を併用することも可能である。なお、一次老化防止剤の例としては、フェノール系老化防止剤、アミン系老化防止剤、アクリレート系老化防止剤、イミダゾール系老化防止剤、カルバミン酸金属塩、ワックスを挙げることができる。また、二次老化防止剤として、リン系老化防止剤、硫黄系老化防止剤、イミダゾール系老化防止剤などを挙げることができる。老化防止剤の例として特に限定するものではないが、N-フェニル-1-ナフチルアミン、アルキル化ジフェニルアミン、オクチル化ジフェニルアミン、4,4'-ビス(α,α-ジメチルベンジル)ジフェニルアミン、p-(p-トルエンスルホニルアミド)ジフェニルアミン、N,N'-ジ-2-ナフチル-p-フェニレンジアミン、N,N'-ジフェニル-p-フェニレンジアミン、N-フェニル-N'-イソプロピル-p-フェニレンジアミン、N-フェニル-N'-(1,3-ジメチルブチル)-p-フェニレンジアミン、N-フェニル-N'-(3-メタクリロイルオキシ-2-ヒドロキシプロピル)-p-フェニレンジアミン、1,1,3-トリス-(2-メチル-4-ヒドロキシ-5-t-ブチルフェニル)ブタン、4,4'-ブチリデンビス-(3-メチル-6-t-ブチルフェノール)、2,2-チオビス(4-メチル-6-t-ブチルフェノール)、7-オクタデシル-3-(4'-ヒドロキシ-3',5'-ジ-t-ブチルフェニル)プロピオネート、テトラキス-[メチレン-3-(3',5'-ジ-t-ブチル-4'-ヒドロキシフェニル)プロピオネート]メタン、ペンタエリスリトール-テトラキス[3-(3,5-ジ-t-ブチル-4-ヒドロキシフェニル)プロピオネート]、トリエチレングリコール-ビス[3-(3-t-ブチル-5-メチル-4-ヒドロキシフェニル)プロピオネート]、1,6-ヘキサンジオール-ビス[3-(3,5-ジ-t-ブチル-4-ヒドロキシフェニル)プロピオネート]、2,4-ビス(n-オクチルチオ)-6-(4-ヒドロキシ-3,5-ジ-t-ブチルアニリノ)-1,3,5-トリアジン、トリス-(3,5-ジ-t-ブチル-4-ヒドロキシベンジル)-イソシアヌレート、2,2-チオ-ジエチレンビス[3-(3,5-ジ-t-ブチル-4-ヒドロキシフェニル)プロピオネート]、N,N'-ヘキサメチレンビス(3,5-ジ-t-ブチル-4-ヒドロキシ)-ヒドロシンナアミド、2,4-ビス[(オクチルチオ)メチル]-o-クレゾール、3,5-ジ-t-ブチル-4-ヒドロキシベンジル-ホスホネート-ジエチルエステル、テトラキス[メチレン(3,5-ジ-t-ブチル-4-ヒドロキシヒドロシンナメイト)]メタン、オクタデシル-3-(3,5-ジ-t-ブチル-4-ヒドロキシフェニル)プロピオン酸エステル及び3,9-ビス[2-{3-(3-t-ブチル-4-ヒドロキシ-5-メチルフェニル)プロピオニルオキシ}-1,1-ジメチルエチル]-2,4,8,10-テトラオキサスピロ[5.5]ウンデカン、トリス(ノニル・フェニル)フォスファイト、トリス(混合モノ-及びジ-ノニルフェニル)フォスファイト、ジフェニル・モノ(2-エチルヘキシル)フォスファイト、ジフェニル・モノトリデシル・フォスファイト、ジフェニル・イソデシル・フォスファイト、ジフェニル・イソオクチル・フォスファイト、ジフェニル・ノニルフェニル・フォスファイト、トリフェニルフォスファイト、トリス(トリデシル)フォスファイト、トリイソデシルフォスファイト、トリス(2-エチルヘキシル)フォスファイト、トリス(2,4-ジ-t-ブチルフェニル)フォスファイト、テトラフェニルジプロピレングリコール・ジフォスファイト、テトラフェニルテトラ(トリデシル)ペンタエリスリトールテトラフォスファイト、1,1,3-トリス(2-メチル-4-ジ-トリデシルフォスファイト-5-t-ブチルフェニル)ブタン、4,4'-ブチリデンビス(3-メチル-6-t-ブチル-ジ-トリデシルフォスファイト)、2,2'-エチリデンビス(4,6-ジ-t-ブチルフェノール)フルオロフォスファイト、4,4'-イソプロピリデン-ジフェノールアルキル(C12~C15)フォスファイト、環状ネオペンタンテトライルビス(2,4-ジ-t-ブチルフェニルフォスファイト)、環状ネオペンタンテトライルビス(2,6-ジ-t-ブチル-4-フェニルフォスファイト)、環状ネオペンタンテトライルビス(ノニルフェニルフォスファイト)、ビス(ノニルフェニル)ペンタエリスリトールジフォスファイト、ジブチルハイドロゲンフォスファイト、ジステアリルペンタエリスリトール・ジフォスファイト及び水添ビスフェノールAペンタエリスリトールフォスファイトポリマー、2-メルカプトベンゾイミダゾール、p-クレソールとジシクロペンタジエンのブチル化反応生成物などが挙げられる。
以下、実施例及び比較例をあげて本発明を説明するが、これらは何れも例示的なものであって本発明の内容を限定するものではない。
(実施例1)
(重合工程1)重合体ブロック(A-1)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82gを添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。
(重合工程1)重合体ブロック(A-1)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82gを添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。
サンプリングしたラテックスは、多量のメタノールに混合することで樹脂分を析出させ、濾過、乾燥して重合体ブロック(A-1)のサンプルを得た。得られたサンプルより重合体ブロック(A)の数平均分子量、分子量分布、及びガラス転移温度を分析により求めた。分析結果を表1に示す。なお、「数平均分子量」、「分子量分布」、「ガラス転移温度」の測定方法については後述する。
(重合工程2)クロロプレン系重合体ブロック(B-1)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及び1.9-ノナンジオールジメタクリレート91.4gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及び1.9-ノナンジオールジメタクリレート91.4gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。
サンプリングしたラテックスの一部を用いて、ラテックスの平均粒子径及びラテックスの機械的安定性を測定した。分析結果を表1に示す。なお、測定方法については後述する。またサンプリングしたラテックスを多量のメタノールに混合することで樹脂分を析出させ、濾過、乾燥してクロロプレン系ブロック共重合体のサンプルを得た。得られたサンプルよりクロロプレン系ブロック共重合体の重合体ブロック(A-1)とクロロプレン系重合体ブロック(B-1)の含有量(質量%)を分析により求めた。分析結果を表1に示す。なお、測定方法については後述する。
(実施例2)
(重合工程1)重合体ブロック(A-2)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水3333g、不均化ロジン酸カリウム(ハリマ化成社製)160g、水酸化カリウム26.0g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)13.3g、スチレン単量体250g、ブチルベンジルトリチオカルボナート4.33gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)2.73g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-2)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-2)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水3333g、不均化ロジン酸カリウム(ハリマ化成社製)160g、水酸化カリウム26.0g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)13.3g、スチレン単量体250g、ブチルベンジルトリチオカルボナート4.33gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)2.73g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-2)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-2)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体5584g、及び1.9-ノナンジオールジメタクリレート114.0gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-2)とクロロプレン系重合体ブロック(B-2)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体5584g、及び1.9-ノナンジオールジメタクリレート114.0gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-2)とクロロプレン系重合体ブロック(B-2)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(実施例3)
(重合工程1)重合体ブロック(A-3)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水5733g、不均化ロジン酸カリウム(ハリマ化成社製)275g、水酸化カリウム44.7g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)22.9g、スチレン単量体430g、ブチルベンジルトリチオカルボナート7.45gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)4.69g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-3)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-3)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水5733g、不均化ロジン酸カリウム(ハリマ化成社製)275g、水酸化カリウム44.7g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)22.9g、スチレン単量体430g、ブチルベンジルトリチオカルボナート7.45gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)4.69g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-3)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-3)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体3094g、及び1.9-ノナンジオールジメタクリレート63.1gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-3)とクロロプレン系重合体ブロック(B-3)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体3094g、及び1.9-ノナンジオールジメタクリレート63.1gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-3)とクロロプレン系重合体ブロック(B-3)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(実施例4)
(重合工程1)重合体ブロック(A-4)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-4)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-4)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-4)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-4)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及び1.9-ノナンジオールジアクリレート91.4gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-4)とクロロプレン系重合体ブロック(B-4)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及び1.9-ノナンジオールジアクリレート91.4gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-4)とクロロプレン系重合体ブロック(B-4)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(実施例5)
(重合工程1)重合体ブロック(A-5)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-5)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-5)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-5)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-5)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及びエチレングリコールジアクリレートであるライトエステルEG(共栄社化学社製)91.4gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-5)とクロロプレン系重合体ブロック(B-5)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及びエチレングリコールジアクリレートであるライトエステルEG(共栄社化学社製)91.4gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-5)とクロロプレン系重合体ブロック(B-5)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(実施例6)
(重合工程1)重合体ブロック(A-6)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-6)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-6)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-6)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-6)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及びジビニルベンゼン93.3gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-6)とクロロプレン系重合体ブロック(B-6)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及びジビニルベンゼン93.3gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-6)とクロロプレン系重合体ブロック(B-6)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(実施例7)
(重合工程1)重合体ブロック(A-7)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水5450g、不均化ロジン酸カリウム(ハリマ化成社製)262g、水酸化カリウム42.5g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)21.8g、スチレン単量体2500g、ブチルベンジルトリチオカルボナート43.3gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)27.3g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-7)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-7)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水5450g、不均化ロジン酸カリウム(ハリマ化成社製)262g、水酸化カリウム42.5g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)21.8g、スチレン単量体2500g、ブチルベンジルトリチオカルボナート43.3gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)27.3g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-7)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-7)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水2732g、不均化ロジン酸カリウム(ハリマ化成社製)131g、水酸化カリウム21.3g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)10.9g、重合工程1で作製した重合体ブロック(A-2)を含むラテックス783gを仕込み、内温45℃にし窒素気流下にて200rpmで攪拌した。その後クロロプレン単量体3000gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-7)とクロロプレン系重合体ブロック(B-7)の含有量(質量%)とトルエン不溶分を実施例1と同様に分析により求めた。分析結果を表1に示す。
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水2732g、不均化ロジン酸カリウム(ハリマ化成社製)131g、水酸化カリウム21.3g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)10.9g、重合工程1で作製した重合体ブロック(A-2)を含むラテックス783gを仕込み、内温45℃にし窒素気流下にて200rpmで攪拌した。その後クロロプレン単量体3000gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-7)とクロロプレン系重合体ブロック(B-7)の含有量(質量%)とトルエン不溶分を実施例1と同様に分析により求めた。分析結果を表1に示す。
(実施例8)
(重合工程1)重合体ブロック(A-8)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-8)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-8)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-8)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-8)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及びトリアリルイソシアヌレート91.4gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-8)とクロロプレン系重合体ブロック(B-8)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及びトリアリルイソシアヌレート91.4gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-8)とクロロプレン系重合体ブロック(B-8)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(実施例9)
(重合工程1)重合体ブロック(A-9)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-9)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-9)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-9)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-9)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及びヒドロキシピバリン酸ネオペンチルグリコールアクリル酸付加物(共栄社化学社製)91.4gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-9)とクロロプレン系重合体ブロック(B-9)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及びヒドロキシピバリン酸ネオペンチルグリコールアクリル酸付加物(共栄社化学社製)91.4gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-9)とクロロプレン系重合体ブロック(B-9)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(実施例10)
(重合工程1)重合体ブロック(A-10)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-10)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-10)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-10)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-10)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及びトリメチロールプロパントリアクリレート(共栄社化学社製)91.4gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-10)とクロロプレン系重合体ブロック(B-10)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4480g、及びトリメチロールプロパントリアクリレート(共栄社化学社製)91.4gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-10)とクロロプレン系重合体ブロック(B-10)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(実施例11)
(重合工程1)重合体ブロック(A-11)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水6667g、不均化ロジン酸カリウム(ハリマ化成社製)320g、水酸化カリウム52.0g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)26.7g、スチレン単量体500g、ブチルベンジルトリチオカルボナート6.50gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)4.09g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-11)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-11)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水6667g、不均化ロジン酸カリウム(ハリマ化成社製)320g、水酸化カリウム52.0g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)26.7g、スチレン単量体500g、ブチルベンジルトリチオカルボナート6.50gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)4.09g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-11)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-11)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体1607g、及び1.9-ノナンジオールジメタクリレート32.8gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-11)とクロロプレン系重合体ブロック(B-11)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体1607g、及び1.9-ノナンジオールジメタクリレート32.8gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-11)とクロロプレン系重合体ブロック(B-11)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(実施例12)
(重合工程1)重合体ブロック(A-12)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水5450g、不均化ロジン酸カリウム(ハリマ化成社製)262g、水酸化カリウム42.5g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)21.8g、スチレン単量体2500g、ブチルベンジルトリチオカルボナート32.5gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)20.5g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-12)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-4)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水1188g、不均化ロジン酸カリウム(ハリマ化成社製)57g、水酸化カリウム9.3g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)4.8g、重合工程1で作製した重合体ブロック(A-4)を含むラテックス3147gを仕込み、内温45℃にし窒素気流下にて200rpmで攪拌した。その後クロロプレン単量体3000gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-12)とクロロプレン系重合体ブロック(B-12)の含有量(質量%)とトルエン不溶分を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-12)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水5450g、不均化ロジン酸カリウム(ハリマ化成社製)262g、水酸化カリウム42.5g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)21.8g、スチレン単量体2500g、ブチルベンジルトリチオカルボナート32.5gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)20.5g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-12)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-4)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水1188g、不均化ロジン酸カリウム(ハリマ化成社製)57g、水酸化カリウム9.3g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)4.8g、重合工程1で作製した重合体ブロック(A-4)を含むラテックス3147gを仕込み、内温45℃にし窒素気流下にて200rpmで攪拌した。その後クロロプレン単量体3000gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-12)とクロロプレン系重合体ブロック(B-12)の含有量(質量%)とトルエン不溶分を実施例1と同様に分析により求めた。分析結果を表1に示す。
(実施例13)
(重合工程1)重合体ブロック(A-13)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、メチルメタクリレート単量体350g、ブチル-2-シアノイソプロピルトリチオカルボネート4.14gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)2.87g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-13)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-13)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、メチルメタクリレート単量体350g、ブチル-2-シアノイソプロピルトリチオカルボネート4.14gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)2.87g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-13)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-13)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4424g、及び1.9-ノナンジオールジメタクリレート90.3gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-13)とクロロプレン系重合体ブロック(B-13)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4424g、及び1.9-ノナンジオールジメタクリレート90.3gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-13)とクロロプレン系重合体ブロック(B-13)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(比較例1)
(重合工程1)重合体ブロック(A-14)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水3067g、不均化ロジン酸カリウム(ハリマ化成社製)147g、水酸化カリウム23.9g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)12.3g、スチレン単量体230g、ブチルベンジルトリチオカルボナート3.99gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)2.51g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-14)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-14)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水3067g、不均化ロジン酸カリウム(ハリマ化成社製)147g、水酸化カリウム23.9g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)12.3g、スチレン単量体230g、ブチルベンジルトリチオカルボナート3.99gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)2.51g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-14)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-14)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体7278g、及び1.9-ノナンジオールジメタクリレート148.5gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-14)とクロロプレン系重合体ブロック(B-14)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体7278g、及び1.9-ノナンジオールジメタクリレート148.5gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-14)とクロロプレン系重合体ブロック(B-14)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(比較例2)
(重合工程1)重合体ブロック(A-15)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水6667g、不均化ロジン酸カリウム(ハリマ化成社製)320g、水酸化カリウム52.0g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)26.7g、スチレン単量体500g、ブチルベンジルトリチオカルボナート4.27gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)2.69g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-15)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-15)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水6667g、不均化ロジン酸カリウム(ハリマ化成社製)320g、水酸化カリウム52.0g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)26.7g、スチレン単量体500g、ブチルベンジルトリチオカルボナート4.27gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)2.69g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-15)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-15)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体1607g、及び1.9-ノナンジオールジメタクリレート32.8gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-15)とクロロプレン系重合体ブロック(B-15)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体1607g、及び1.9-ノナンジオールジメタクリレート32.8gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-15)とクロロプレン系重合体ブロック(B-15)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(比較例3)
クロロプレン系重合体ブロック(B-16)のみの共重合体の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水3600g、不均化ロジン酸カリウム(ハリマ化成社製)175g、水酸化カリウム28.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)16.0g、クロロプレン単量体4000g、1.9-ノナンジオールジメタクリレート81.6g、ブチルベンジルトリチオカルボナート4.72gを仕込み、内温45℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)2.96g添加して重合を開始した。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径及びラテックスの機械的安定性を実施例1と同様に分析により求めた。分析結果を表1に示す。
クロロプレン系重合体ブロック(B-16)のみの共重合体の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水3600g、不均化ロジン酸カリウム(ハリマ化成社製)175g、水酸化カリウム28.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)16.0g、クロロプレン単量体4000g、1.9-ノナンジオールジメタクリレート81.6g、ブチルベンジルトリチオカルボナート4.72gを仕込み、内温45℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)2.96g添加して重合を開始した。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径及びラテックスの機械的安定性を実施例1と同様に分析により求めた。分析結果を表1に示す。
(比較例4)
(重合工程1)重合体ブロック(A-17)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4616g、不均化ロジン酸カリウム(ハリマ化成社製)206g、水酸化カリウム2.3g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)46.2g、スチレン単量体462g、ブチルベンジルトリチオカルボナート9.2gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)6.0g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-17)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-17)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4616g、不均化ロジン酸カリウム(ハリマ化成社製)206g、水酸化カリウム2.3g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)46.2g、スチレン単量体462g、ブチルベンジルトリチオカルボナート9.2gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)6.0g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-17)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-17)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4154gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-17)とクロロプレン系重合体ブロック(B-17)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体4154gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-17)とクロロプレン系重合体ブロック(B-17)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(比較例5)
(重合工程1)重合体ブロック(A-18)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4616g、不均化ロジン酸カリウム(ハリマ化成社製)206g、水酸化カリウム2.3g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)46.2g、スチレン単量体692g、ブチルベンジルトリチオカルボナート9.2gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)6.0g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-18)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程1)重合体ブロック(A-18)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4616g、不均化ロジン酸カリウム(ハリマ化成社製)206g、水酸化カリウム2.3g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)46.2g、スチレン単量体692g、ブチルベンジルトリチオカルボナート9.2gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)6.0g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは重合工程2に使用した。重合体ブロック(A-18)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表1に示す。
(重合工程2)クロロプレン系重合体ブロック(B-18)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体3924gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-18)とクロロプレン系重合体ブロック(B-18)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体3924gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-18)とクロロプレン系重合体ブロック(B-18)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表1に示す。
(比較例6)
トリブロック共重合体の合成
(第1ブロックの合成)
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4613g、不均化ロジン酸カリウム(ハリマ化成社製)204.4g、水酸化カリウム2.3g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)46.1g、スチレン単量体230g、ベンジル1-ピロールカルボジチオエート9.2gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)6.0g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは次の重合工程に使用した。第1ブロックの数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表2に示す。
(第2ブロックの合成)
第1ブロックの合成の後、内温が45℃まで下がったところで、クロロプレン単量体4424gを添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。得られたラテックスを用いて次の重合工程に使用した。
(第3ブロックの合成)
第2ブロックの合成の後、内温を80℃まで昇温にし、スチレン単量体230gを仕込み、重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)6.0g添加して重合を開始した。重合を行った後、25℃まで冷却し重合を停止した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及び合成したトリブロック共重合体の第1ブロックと第3ブロックであるスチレンブロックと、第2ブロックであるクロロプレンブロックの含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表2に示す。
トリブロック共重合体の合成
(第1ブロックの合成)
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4613g、不均化ロジン酸カリウム(ハリマ化成社製)204.4g、水酸化カリウム2.3g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)46.1g、スチレン単量体230g、ベンジル1-ピロールカルボジチオエート9.2gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)6.0g添加して重合を開始した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスは次の重合工程に使用した。第1ブロックの数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表2に示す。
(第2ブロックの合成)
第1ブロックの合成の後、内温が45℃まで下がったところで、クロロプレン単量体4424gを添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。得られたラテックスを用いて次の重合工程に使用した。
(第3ブロックの合成)
第2ブロックの合成の後、内温を80℃まで昇温にし、スチレン単量体230gを仕込み、重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)6.0g添加して重合を開始した。重合を行った後、25℃まで冷却し重合を停止した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及び合成したトリブロック共重合体の第1ブロックと第3ブロックであるスチレンブロックと、第2ブロックであるクロロプレンブロックの含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表2に示す。
(比較例7)
重合体ブロック(A)の単独重合体とクロロプレン系重合体ブロック(B)の単独重合体の混合物の作製
(重合体ブロック(A)の単独重合体の合成)
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82gを添加して重合を開始した。スチレン単量体の重合率95%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させた。物性測定のために、得られたラテックスを20mlサンプリングした。重合体ブロック(A)の単独重合体の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表3に示す。
重合体ブロック(A)の単独重合体とクロロプレン系重合体ブロック(B)の単独重合体の混合物の作製
(重合体ブロック(A)の単独重合体の合成)
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水4666g、不均化ロジン酸カリウム(ハリマ化成社製)224g、水酸化カリウム36.4g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)18.7g、スチレン単量体350g、ブチルベンジルトリチオカルボナート6.07gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.82gを添加して重合を開始した。スチレン単量体の重合率95%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させた。物性測定のために、得られたラテックスを20mlサンプリングした。重合体ブロック(A)の単独重合体の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表3に示す。
(クロロプレン系重合体ブロック(B)の単独重合体の合成)
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水3960g、不均化ロジン酸カリウム(ハリマ化成社製)193g、水酸化カリウム31.2g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)17.6g、クロロプレン単量体4400g、1.9-ノナンジオールジメタクリレート89.8g、ブチルベンジルトリチオカルボナート5.19gを仕込み、内温45℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.26g添加して重合を開始した。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。純水3960g、不均化ロジン酸カリウム(ハリマ化成社製)193g、水酸化カリウム31.2g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)17.6g、クロロプレン単量体4400g、1.9-ノナンジオールジメタクリレート89.8g、ブチルベンジルトリチオカルボナート5.19gを仕込み、内温45℃にし窒素気流下にて200rpmで攪拌した。重合開始剤として2,2'-アゾビス[2-(2-イミダゾリン-2-イル)プロパン]2塩化水素(富士フイルム和光純薬社製、商品名:VA-044)3.26g添加して重合を開始した。クロロプレン単量体の重合率80%となった時点で重合停止剤であるN,N-ジエチルヒドロキシルアミンの10重量%水溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体を除去した。
(重合体ブロック(A)の単独重合体ラテックスとクロロプレン系重合体ブロック(B)の単独重合体ラテックスの混合)
得られた重合体ブロック(A)の単独重合体ラテックス4000gとクロロプレン系重合体ブロック(B)の単独重合体のラテックス4000gを容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブに仕込み、内温45℃にして200rpmで攪拌した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及び混合して得られるポリマー中の重合体ブロック(A)の単独重合体とクロロプレン系重合体ブロック(B)の単独重合体の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表3に示す。
得られた重合体ブロック(A)の単独重合体ラテックス4000gとクロロプレン系重合体ブロック(B)の単独重合体のラテックス4000gを容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブに仕込み、内温45℃にして200rpmで攪拌した。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及び混合して得られるポリマー中の重合体ブロック(A)の単独重合体とクロロプレン系重合体ブロック(B)の単独重合体の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表3に示す。
(比較例8)
強制乳化法によるクロロプレン系ブロック共重合体ラテックスの合成
(重合工程1)重合体ブロック(A-19)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。テトラヒドロフラン4616g、スチレン単量体87.5g、ベンジルブチルトリチオカルボナート1.5gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤としてアゾビスイソブチロニトリル(富士フイルム和光純薬社製、商品名:AIBN)0.49g添加して重合を開始した。物性測定のために、得られた溶液を20mlサンプリングし、残りのラテックスは次の重合工程に使用した。重合体ブロック(A-19)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表4に示す。
強制乳化法によるクロロプレン系ブロック共重合体ラテックスの合成
(重合工程1)重合体ブロック(A-19)の合成
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。テトラヒドロフラン4616g、スチレン単量体87.5g、ベンジルブチルトリチオカルボナート1.5gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤としてアゾビスイソブチロニトリル(富士フイルム和光純薬社製、商品名:AIBN)0.49g添加して重合を開始した。物性測定のために、得られた溶液を20mlサンプリングし、残りのラテックスは次の重合工程に使用した。重合体ブロック(A-19)の数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表4に示す。
(重合工程2)クロロプレン系重合体ブロック(B-19)の合成
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体1120g及び1.9-ノナンジオールジメタクリレート22.8gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるフェノチアジンの10重量%テトラヒドロフラン溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体及びテトラヒドロフランを除去してクロロプレン系ブロック共重合体のサンプルを得た。
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体1120g及び1.9-ノナンジオールジメタクリレート22.8gを2時間かけてゆっくり添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるフェノチアジンの10重量%テトラヒドロフラン溶液を添加することで重合を停止させ、減圧蒸留により未反応のクロロプレン単量体及びテトラヒドロフランを除去してクロロプレン系ブロック共重合体のサンプルを得た。
(強制乳化工程)
クロロプレン系ブロック共重合体の強制乳化
重合工程2で得られたクロロプレン系ブロック共重合体350gを4200gのベンゼンに溶解させた。得られた溶液に対して純水4725g、不均化ロジン酸カリウム(ハリマ化成社製)70g、水酸化カリウム0.78g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)1.4gを加え、ホモジナイザーを使用して強制的に乳化させた。得られたラテックスの固形分濃度が50%となるように、減圧蒸留によってベンゼン及び水を除去し、クロロプレン系ブロック共重合体ラテックスを得た。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-19)とクロロプレン系重合体ブロック(B-19)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表4に示す。
クロロプレン系ブロック共重合体の強制乳化
重合工程2で得られたクロロプレン系ブロック共重合体350gを4200gのベンゼンに溶解させた。得られた溶液に対して純水4725g、不均化ロジン酸カリウム(ハリマ化成社製)70g、水酸化カリウム0.78g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)1.4gを加え、ホモジナイザーを使用して強制的に乳化させた。得られたラテックスの固形分濃度が50%となるように、減圧蒸留によってベンゼン及び水を除去し、クロロプレン系ブロック共重合体ラテックスを得た。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及びクロロプレン系ブロック共重合体の重合体ブロック(A-19)とクロロプレン系重合体ブロック(B-19)の含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表4に示す。
(比較例9)
強制乳化法によるトリブロック共重合体ラテックスの合成
(第1ブロックの合成)
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。テトラヒドロフラン4616g、スチレン単量体70g、ベンジル1-ピロールカルボジチオエート2.8gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤としてアゾビスイソブチロニトリル(富士フイルム和光純薬社製、商品名:AIBN)0.93g添加して重合を開始した。物性測定のために、得られた溶液を20mlサンプリングし、残りのラテックスは次の重合工程に使用した。第1ブロックの数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表5に示す。
(第2ブロックの合成)
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体1346gを添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるフェノチアジンの10重量%テトラヒドロフラン溶液を添加することで重合を停止させた。
(第3ブロックの合成)
第2ブロックの合成の後、内温を80℃まで昇温にし、スチレン単量体70gを仕込み、重合開始剤としてアゾビスイソブチロニトリル(富士フイルム和光純薬社製、商品名:AIBN)0.93g添加して重合を開始した。重合を行った後、減圧蒸留により未反応のクロロプレン単量体及びテトラヒドロフランを除去してトリブロック共重合体を得た。
(強制乳化工程)トリブロック共重合体の強制乳化
第3ブロックの合成で得られたトリブロック共重合体350gを4200gのベンゼンに溶解させた。得られた溶液に対して純水4725g、不均化ロジン酸カリウム(ハリマ化成社製)70g、水酸化カリウム0.78g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)1.4gを加え、ホモジナイザーを使用して強制的に乳化させた。得られたラテックスの固形分濃度が50%となるように、減圧蒸留によってベンゼン及び水を除去し、クロロプレン系ブロック共重合体ラテックスを得た。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及び合成したトリブロック共重合体の第1ブロックと第3ブロックであるスチレンブロックと、第2ブロックであるクロロプレンブロックの含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表5に示す。
強制乳化法によるトリブロック共重合体ラテックスの合成
(第1ブロックの合成)
容量10L、攪拌機及び加熱冷却用ジャケット付のオートクレーブを用いて重合を行った。テトラヒドロフラン4616g、スチレン単量体70g、ベンジル1-ピロールカルボジチオエート2.8gを仕込み、内温80℃にし窒素気流下にて200rpmで攪拌した。重合開始剤としてアゾビスイソブチロニトリル(富士フイルム和光純薬社製、商品名:AIBN)0.93g添加して重合を開始した。物性測定のために、得られた溶液を20mlサンプリングし、残りのラテックスは次の重合工程に使用した。第1ブロックの数平均分子量、分子量分布、及びガラス転移温度を実施例1と同様に分析により求めた。分析結果を表5に示す。
(第2ブロックの合成)
重合工程1の後、内温が45℃まで下がったところで、クロロプレン単量体1346gを添加し重合を行った。クロロプレン単量体の重合率80%となった時点で重合停止剤であるフェノチアジンの10重量%テトラヒドロフラン溶液を添加することで重合を停止させた。
(第3ブロックの合成)
第2ブロックの合成の後、内温を80℃まで昇温にし、スチレン単量体70gを仕込み、重合開始剤としてアゾビスイソブチロニトリル(富士フイルム和光純薬社製、商品名:AIBN)0.93g添加して重合を開始した。重合を行った後、減圧蒸留により未反応のクロロプレン単量体及びテトラヒドロフランを除去してトリブロック共重合体を得た。
(強制乳化工程)トリブロック共重合体の強制乳化
第3ブロックの合成で得られたトリブロック共重合体350gを4200gのベンゼンに溶解させた。得られた溶液に対して純水4725g、不均化ロジン酸カリウム(ハリマ化成社製)70g、水酸化カリウム0.78g、β-ナフタレンスルホン酸ホルマリン縮合物のナトリウム塩(花王社製、商品名:デモールN)1.4gを加え、ホモジナイザーを使用して強制的に乳化させた。得られたラテックスの固形分濃度が50%となるように、減圧蒸留によってベンゼン及び水を除去し、クロロプレン系ブロック共重合体ラテックスを得た。物性測定のために、得られたラテックスを20mlサンプリングし、残りのラテックスを用いて評価用のフィルム作製を行った。ラテックスの平均粒子径、ラテックスの機械的安定性及び合成したトリブロック共重合体の第1ブロックと第3ブロックであるスチレンブロックと、第2ブロックであるクロロプレンブロックの含有量(質量%)を実施例1と同様に分析により求めた。分析結果を表5に示す。
[分析]
(重合体ブロック(A)の数平均分子量及び分子量分布測定)
数平均分子量及び分子量分布は、ゲルパーミエーションクロマトグラフィー(GPC)にて測定されるポリスチレン換算の値であり、下記記載の測定条件における測定値である。
装置名:HLC-8320(東ソー社製)
カラム:TSKgel GMHHR-Hを3本直列
温度:40℃
検出:示差屈折率
溶媒:テトラヒドロフラン
検量線:標準ポリスチレン(PS)を用いて作製した。
(重合体ブロック(A)の数平均分子量及び分子量分布測定)
数平均分子量及び分子量分布は、ゲルパーミエーションクロマトグラフィー(GPC)にて測定されるポリスチレン換算の値であり、下記記載の測定条件における測定値である。
装置名:HLC-8320(東ソー社製)
カラム:TSKgel GMHHR-Hを3本直列
温度:40℃
検出:示差屈折率
溶媒:テトラヒドロフラン
検量線:標準ポリスチレン(PS)を用いて作製した。
(重合体ブロック(A)のガラス転移温度)
ガラス転移温度は、JIS K 7121に準拠して示差走査熱量計を用い、以下の方法で測定した。
装置名:DSC1(Mettler Toledo社製)
手順:50ml/minの窒素気流下で、昇温速度10℃/minで120℃まで昇温して、10分間120℃に保った後、-60℃まで冷却し、昇温速度10℃/minで120℃まで昇温して得られたDSC曲線から、高温側のペースラインを低温側に延長した直線と、ピークの高温側の曲線にこう配が最大になるような点で引いた接線との交点の温度をガラス転移温度とした。
ガラス転移温度は、JIS K 7121に準拠して示差走査熱量計を用い、以下の方法で測定した。
装置名:DSC1(Mettler Toledo社製)
手順:50ml/minの窒素気流下で、昇温速度10℃/minで120℃まで昇温して、10分間120℃に保った後、-60℃まで冷却し、昇温速度10℃/minで120℃まで昇温して得られたDSC曲線から、高温側のペースラインを低温側に延長した直線と、ピークの高温側の曲線にこう配が最大になるような点で引いた接線との交点の温度をガラス転移温度とした。
(クロロプレン系ブロック共重合体の重合体ブロック(A)とクロロプレン系重合体ブロック(B)の含有量測定)
熱分解ガスクロマトグラムと1H-NMRを用い、以下の方法で測定した。
熱分解ガスクロマトグラム 装置名:HP5890-II
カラム:DB-5 0.25mmφ×30m(膜厚1.0μm)
カラム温度:50℃(5min)→10℃/min→150℃→25℃/min→300℃
注入口温度:250℃
検出器温度:280℃
検出器:FID
1H-NMR 装置名:JNM-ECX-400(日本電子社製)
手順:重合体ブロック(A)と多官能性単量体単位を含まないクロロプレン系重合体ブロック(B)からなるクロロプレン系ブロック共重合体を熱分解ガスクロマトグラムで測定し、重合体ブロック(A)由来のピークとクロロプレン系重合体ブロック(B)由来のピークの面積比と、1H-NMRを測定して得られたクロロプレン系ブロック共重合体中の重合体ブロック(A)とクロロプレン系重合体ブロック(B)の含有量から検量線を作成した。サンプリングしたラテックスをメタノールに混合して析出したクロロプレン系ブロック共重合体のサンプルを熱分解ガスクロマトグラムで測定し、重合体ブロック(A)由来のピークとクロロプレン系重合体ブロック(B)由来のピークの面積比から、上記で作成した検量線を用いてクロロプレン系ブロック共重合体中の重合体ブロック(A)とクロロプレン系重合体ブロック(B)の含有量を求めた。
熱分解ガスクロマトグラムと1H-NMRを用い、以下の方法で測定した。
熱分解ガスクロマトグラム 装置名:HP5890-II
カラム:DB-5 0.25mmφ×30m(膜厚1.0μm)
カラム温度:50℃(5min)→10℃/min→150℃→25℃/min→300℃
注入口温度:250℃
検出器温度:280℃
検出器:FID
1H-NMR 装置名:JNM-ECX-400(日本電子社製)
手順:重合体ブロック(A)と多官能性単量体単位を含まないクロロプレン系重合体ブロック(B)からなるクロロプレン系ブロック共重合体を熱分解ガスクロマトグラムで測定し、重合体ブロック(A)由来のピークとクロロプレン系重合体ブロック(B)由来のピークの面積比と、1H-NMRを測定して得られたクロロプレン系ブロック共重合体中の重合体ブロック(A)とクロロプレン系重合体ブロック(B)の含有量から検量線を作成した。サンプリングしたラテックスをメタノールに混合して析出したクロロプレン系ブロック共重合体のサンプルを熱分解ガスクロマトグラムで測定し、重合体ブロック(A)由来のピークとクロロプレン系重合体ブロック(B)由来のピークの面積比から、上記で作成した検量線を用いてクロロプレン系ブロック共重合体中の重合体ブロック(A)とクロロプレン系重合体ブロック(B)の含有量を求めた。
(ラテックスの平均粒子径の測定)
サンプリングしたラテックス0.1gを純水50gに溶解したサンプルを用い、大塚電子社製ELSZ-2にて動的光散乱法により測定し、光子相関法でラテックスの平均粒子径を算出した。
サンプリングしたラテックス0.1gを純水50gに溶解したサンプルを用い、大塚電子社製ELSZ-2にて動的光散乱法により測定し、光子相関法でラテックスの平均粒子径を算出した。
(ラテックスの機械的安定性の測定)
ラテックスの機械的安定性は、JIS K 6392に準拠して、マロン機械的安定度試験機を用い、以下の方法で測定した。
手順:サンプリングしたラテックスを金網で濾過し不純物を取り除いた後、濾過したラテックスを20℃に調整し、50gを試験容器に計量した。試験容器を試験機に装着し、荷重10kgで10min測定を行った。測定後の試験容器内の試料を予め125℃×1時間乾燥してデシケータ内で放冷した80メッシュ金網で濾過し、80メッシュ金網と析出物を125℃の乾燥機内で1時間乾燥した後デシケータ内で放冷して、80メッシュ金網と析出物を秤量した。また、サンプリングしたラテックスの全固形分(単位:%)をJIS K 6387に準拠して求めた。次に以下式を用いてラテックスの凝固率(単位:質量%)を求めた。
[(乾燥後の80メッシュ金網と析出物の重量(単位:g))-(80メッシュ金網の重量(単位:g))]/[50×((ラテックスの全固形分(単位:質量%))/100)]×100
求めたラテックスの凝固率をラテックスの機械的安定性とした。ラテックスの機械的安定性は、1質量%以下を合格レベルとした。
ラテックスの機械的安定性は、JIS K 6392に準拠して、マロン機械的安定度試験機を用い、以下の方法で測定した。
手順:サンプリングしたラテックスを金網で濾過し不純物を取り除いた後、濾過したラテックスを20℃に調整し、50gを試験容器に計量した。試験容器を試験機に装着し、荷重10kgで10min測定を行った。測定後の試験容器内の試料を予め125℃×1時間乾燥してデシケータ内で放冷した80メッシュ金網で濾過し、80メッシュ金網と析出物を125℃の乾燥機内で1時間乾燥した後デシケータ内で放冷して、80メッシュ金網と析出物を秤量した。また、サンプリングしたラテックスの全固形分(単位:%)をJIS K 6387に準拠して求めた。次に以下式を用いてラテックスの凝固率(単位:質量%)を求めた。
[(乾燥後の80メッシュ金網と析出物の重量(単位:g))-(80メッシュ金網の重量(単位:g))]/[50×((ラテックスの全固形分(単位:質量%))/100)]×100
求めたラテックスの凝固率をラテックスの機械的安定性とした。ラテックスの機械的安定性は、1質量%以下を合格レベルとした。
[引張試験用サンプルの作製]
(クロロプレン系ブロック共重合体を含むラテックスの調製)
重合工程2で得られたラテックス中のクロロプレン系ブロック共重合体100質量部(固形分換算)に対して、老化防止剤としてp-クレソールとジシクロペンタジエンのブチル化反応生成物(商品名「ノクラックPBK」、大内新興化学工業株式会社製)2質量部、ラウリル硫酸ナトリウム(商品名「エマール10」、花王株式会社製)0.3質量部、及び水を加えて配合物の固形分濃度が30質量%になるように調製し、陶器製ボールミルを用いて、20℃で16時間混合し、調製した。
(フィルムの作製)
外径50mmの陶器製の筒を、水62質量部、硝酸カリウム四水和物35質量部、及び炭酸カルシウム3質量部を混合した凝固液に1秒間浸して取り出した。4分間乾燥させた後、上記で調製したラテックスに2分間浸した。その後45℃の流水で1分間洗浄し、130℃で30分間加熱して水分を除去し、引張試験用のフィルム(140×150mm、厚み:0.2mm)を作製した。
(クロロプレン系ブロック共重合体を含むラテックスの調製)
重合工程2で得られたラテックス中のクロロプレン系ブロック共重合体100質量部(固形分換算)に対して、老化防止剤としてp-クレソールとジシクロペンタジエンのブチル化反応生成物(商品名「ノクラックPBK」、大内新興化学工業株式会社製)2質量部、ラウリル硫酸ナトリウム(商品名「エマール10」、花王株式会社製)0.3質量部、及び水を加えて配合物の固形分濃度が30質量%になるように調製し、陶器製ボールミルを用いて、20℃で16時間混合し、調製した。
(フィルムの作製)
外径50mmの陶器製の筒を、水62質量部、硝酸カリウム四水和物35質量部、及び炭酸カルシウム3質量部を混合した凝固液に1秒間浸して取り出した。4分間乾燥させた後、上記で調製したラテックスに2分間浸した。その後45℃の流水で1分間洗浄し、130℃で30分間加熱して水分を除去し、引張試験用のフィルム(140×150mm、厚み:0.2mm)を作製した。
[引張特性の評価]
作製したフィルムを、130℃で30分間熱処理した後にJIS K 6251に準拠して500%伸長時モジュラス、切断時引張強さ破断強度及び切断時伸びを測定した。なお、500%伸長時モジュラスは3.0MPa以下、切断時引張強さは17MPa以上、切断時伸びは900%以上を合格レベルとした。
作製したフィルムを、130℃で30分間熱処理した後にJIS K 6251に準拠して500%伸長時モジュラス、切断時引張強さ破断強度及び切断時伸びを測定した。なお、500%伸長時モジュラスは3.0MPa以下、切断時引張強さは17MPa以上、切断時伸びは900%以上を合格レベルとした。
[熱老化特性の評価]
作製したフィルムを強制循環型熱老化試験機内で100℃、22時間の条件で熱老化試験を行った後、JIS K 6251に準拠して500%伸長時モジュラス、切断時引張強さ及び切断時伸びを測定した。500%伸長時モジュラスは3.0MPa以下、切断時引張強さは17MPa以上、切断時伸びは900%以上を合格とした。
作製したフィルムを強制循環型熱老化試験機内で100℃、22時間の条件で熱老化試験を行った後、JIS K 6251に準拠して500%伸長時モジュラス、切断時引張強さ及び切断時伸びを測定した。500%伸長時モジュラスは3.0MPa以下、切断時引張強さは17MPa以上、切断時伸びは900%以上を合格とした。
実施例1~13については、いずれもラテックスの機械的安定性が1質量%以下でラテックスの
機械的安定性に優れていた。また加硫剤や加硫促進剤を使用しなくても、フィルムの500%伸長時モジュラス3.0MPa以下で柔軟性に優れ、切断時引張強さ17MPa以上、切断時伸び900%以上であり、引張特性に優れていた。また、熱老化試験後の500%伸長時モジュラス3.0MPa以下で柔軟性に優れ、切断時引張強さ17MPa以上、切断時伸び900%以上であり、耐熱老化性にも優れていた。一方、比較例1~8については、ラテックスの機械的安定性、フィルムの柔軟性、引張特性、及び耐熱老化性のうちいずれかの物性において劣るものであった。
機械的安定性に優れていた。また加硫剤や加硫促進剤を使用しなくても、フィルムの500%伸長時モジュラス3.0MPa以下で柔軟性に優れ、切断時引張強さ17MPa以上、切断時伸び900%以上であり、引張特性に優れていた。また、熱老化試験後の500%伸長時モジュラス3.0MPa以下で柔軟性に優れ、切断時引張強さ17MPa以上、切断時伸び900%以上であり、耐熱老化性にも優れていた。一方、比較例1~8については、ラテックスの機械的安定性、フィルムの柔軟性、引張特性、及び耐熱老化性のうちいずれかの物性において劣るものであった。
本発明のクロロプレン系ブロック共重合体ラテックスから得られる浸漬成形体は、柔軟性、引張特性、耐熱老化性に優れており、手術用手袋、手袋、風船、カテーテルなどに好適に用いることができる。また本発明のクロロプレン系ブロック共重合体ラテックスは、塗料、接着剤、粘着剤などに好適に用いることができる。
Claims (5)
- 単独重合時にガラス転移温度が80℃以上の重合体が得られる単量体由来の重合体ブロック(A)5~30質量%と、クロロプレン単量体単位を含むクロロプレン系重合体ブロック(B)70~95質量%を含むクロロプレン系ブロック共重合体を含むクロロプレン系ブロック共重合体ラテックスであり、
前記クロロプレン系ブロック共重合体ラテックスを浸漬成形して得られた被膜を130℃で30分間熱処理した後にJIS K 6251に準拠して測定した切断時引張強さが17MPa以上であるクロロプレン系ブロック共重合体ラテックス。 - 前記クロロプレン系ブロック共重合体100質量%中に、前記重合体ブロック(A)5~15質量%と、前記クロロプレン系重合体ブロック(B)を85~95質量%を含有する請求項1に記載のクロロプレン系ブロック共重合体ラテックス。
- 前記クロロプレン系ブロック共重合体ラテックスを、動的光散乱法によって測定した平均粒子径が300nm以下である、請求項1または2に記載のクロロプレン系ブロック共重合体ラテックス。
- 前記クロロプレン系重合体ブロック(B)が、クロロプレン単量体単位及び多官能性単量体単位を有するものである請求項1~3のいずれか一項に記載のクロロプレン系ブロック共重合体ラテックス。
- 浸漬成形体用である請求項1~4のいずれか一項に記載のクロロプレン系ブロック共重合体ラテックス。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2022510497A JPWO2021193561A1 (ja) | 2020-03-26 | 2021-03-22 | |
| CN202180024128.XA CN115335422A (zh) | 2020-03-26 | 2021-03-22 | 氯丁二烯系嵌段共聚物乳胶 |
| EP21775670.9A EP4130079A4 (en) | 2020-03-26 | 2021-03-22 | CHLOROPRENE-BASED BLOCK COPOLYMER LATEX |
| US17/788,950 US20230050436A1 (en) | 2020-03-26 | 2021-03-22 | Chloroprene-based block copolymer latex |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020056388 | 2020-03-26 | ||
| JP2020-056388 | 2020-03-26 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2021193561A1 true WO2021193561A1 (ja) | 2021-09-30 |
Family
ID=77890284
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2021/011777 WO2021193561A1 (ja) | 2020-03-26 | 2021-03-22 | クロロプレン系ブロック共重合体ラテックス |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20230050436A1 (ja) |
| EP (1) | EP4130079A4 (ja) |
| JP (1) | JPWO2021193561A1 (ja) |
| CN (1) | CN115335422A (ja) |
| WO (1) | WO2021193561A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023054104A1 (ja) * | 2021-09-28 | 2023-04-06 | デンカ株式会社 | クロロプレン系ブロック共重合体、ラテックス、ラテックス組成物、及びゴム組成物 |
Citations (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3238173A (en) | 1962-09-27 | 1966-03-01 | Shell Oil Co | Polystyrene-polyisoprene-polystyrene block copolymer latices and process for their preparation |
| JPH03207710A (ja) | 1990-01-11 | 1991-09-11 | Tosoh Corp | 共重合体及びその製造方法 |
| JPH03212414A (ja) | 1990-01-18 | 1991-09-18 | Tosoh Corp | クロロプレンブロック共重合体 |
| JP2007297502A (ja) | 2006-04-28 | 2007-11-15 | Tosoh Corp | ソープレスポリクロロプレン系ラテックス及びその製造法 |
| JP2010001458A (ja) * | 2008-05-23 | 2010-01-07 | Tosoh Corp | ポリクロロプレンラテックス及びその製造法 |
| JP2011012196A (ja) * | 2009-07-03 | 2011-01-20 | Tosoh Corp | エマルション及びその製造法 |
| WO2013015043A1 (ja) | 2011-07-25 | 2013-01-31 | 電気化学工業株式会社 | ポリクロロプレンラテックス組成物及び浸漬成形品 |
| JP2014114342A (ja) | 2012-12-07 | 2014-06-26 | Denki Kagaku Kogyo Kk | ポリクロロプレンラテックス、ポリクロロプレンラテックス組成物及び浸漬成形製品 |
| JP2014221901A (ja) | 2008-09-18 | 2014-11-27 | アルケマ フランス | 新規エラストマー材料および該材料を得る方法 |
| WO2016133192A1 (ja) * | 2015-02-19 | 2016-08-25 | デンカ株式会社 | ラテックス組成物及び一液型水系接着剤 |
| WO2016166998A1 (ja) | 2015-04-16 | 2016-10-20 | 昭和電工株式会社 | ゴム用組成物及びその用途 |
| WO2018181801A1 (ja) | 2017-03-30 | 2018-10-04 | デンカ株式会社 | ブロック共重合体及びブロック共重合体の製造方法 |
| CN106433158B (zh) * | 2016-07-07 | 2018-12-04 | 交通运输部科学研究院 | 改性生物沥青的制备方法和改性生物沥青及其用途 |
| WO2019009038A1 (ja) | 2017-07-04 | 2019-01-10 | デンカ株式会社 | メルカプタン変性ポリクロロプレンラテックス及びその製造方法 |
| WO2019026914A1 (ja) | 2017-07-31 | 2019-02-07 | デンカ株式会社 | ブロック共重合体及びブロック共重合体の製造方法 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE69009380T2 (de) * | 1989-09-07 | 1994-09-15 | Tosoh Corp | Chloroprenpolymerisat. |
| JP2860829B2 (ja) * | 1990-10-31 | 1999-02-24 | 電気化学工業株式会社 | 熱可塑性エラストマー組成物 |
| JP2793068B2 (ja) * | 1991-04-24 | 1998-09-03 | 日本ペイント株式会社 | 感光性樹脂組成物 |
| CN101263170A (zh) * | 2005-07-08 | 2008-09-10 | 东曹株式会社 | 氯丁二烯类嵌段共聚物和无皂聚氯丁二烯类胶乳、以及它们的制造方法 |
| IN2014DN08119A (ja) * | 2012-03-02 | 2015-05-01 | Denki Kagaku Kogyo Kk | |
| TWI597320B (zh) * | 2013-10-11 | 2017-09-01 | 科騰聚合物美國有限責任公司 | 烯系不飽和徑向苯乙烯嵌段共聚物及包含水及該徑向苯乙烯嵌段共聚物之經改良不含硫化劑之乳膠 |
-
2021
- 2021-03-22 WO PCT/JP2021/011777 patent/WO2021193561A1/ja unknown
- 2021-03-22 CN CN202180024128.XA patent/CN115335422A/zh active Pending
- 2021-03-22 JP JP2022510497A patent/JPWO2021193561A1/ja active Pending
- 2021-03-22 EP EP21775670.9A patent/EP4130079A4/en active Pending
- 2021-03-22 US US17/788,950 patent/US20230050436A1/en active Pending
Patent Citations (15)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3238173A (en) | 1962-09-27 | 1966-03-01 | Shell Oil Co | Polystyrene-polyisoprene-polystyrene block copolymer latices and process for their preparation |
| JPH03207710A (ja) | 1990-01-11 | 1991-09-11 | Tosoh Corp | 共重合体及びその製造方法 |
| JPH03212414A (ja) | 1990-01-18 | 1991-09-18 | Tosoh Corp | クロロプレンブロック共重合体 |
| JP2007297502A (ja) | 2006-04-28 | 2007-11-15 | Tosoh Corp | ソープレスポリクロロプレン系ラテックス及びその製造法 |
| JP2010001458A (ja) * | 2008-05-23 | 2010-01-07 | Tosoh Corp | ポリクロロプレンラテックス及びその製造法 |
| JP2014221901A (ja) | 2008-09-18 | 2014-11-27 | アルケマ フランス | 新規エラストマー材料および該材料を得る方法 |
| JP2011012196A (ja) * | 2009-07-03 | 2011-01-20 | Tosoh Corp | エマルション及びその製造法 |
| WO2013015043A1 (ja) | 2011-07-25 | 2013-01-31 | 電気化学工業株式会社 | ポリクロロプレンラテックス組成物及び浸漬成形品 |
| JP2014114342A (ja) | 2012-12-07 | 2014-06-26 | Denki Kagaku Kogyo Kk | ポリクロロプレンラテックス、ポリクロロプレンラテックス組成物及び浸漬成形製品 |
| WO2016133192A1 (ja) * | 2015-02-19 | 2016-08-25 | デンカ株式会社 | ラテックス組成物及び一液型水系接着剤 |
| WO2016166998A1 (ja) | 2015-04-16 | 2016-10-20 | 昭和電工株式会社 | ゴム用組成物及びその用途 |
| CN106433158B (zh) * | 2016-07-07 | 2018-12-04 | 交通运输部科学研究院 | 改性生物沥青的制备方法和改性生物沥青及其用途 |
| WO2018181801A1 (ja) | 2017-03-30 | 2018-10-04 | デンカ株式会社 | ブロック共重合体及びブロック共重合体の製造方法 |
| WO2019009038A1 (ja) | 2017-07-04 | 2019-01-10 | デンカ株式会社 | メルカプタン変性ポリクロロプレンラテックス及びその製造方法 |
| WO2019026914A1 (ja) | 2017-07-31 | 2019-02-07 | デンカ株式会社 | ブロック共重合体及びブロック共重合体の製造方法 |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP4130079A4 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2023054104A1 (ja) * | 2021-09-28 | 2023-04-06 | デンカ株式会社 | クロロプレン系ブロック共重合体、ラテックス、ラテックス組成物、及びゴム組成物 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP4130079A1 (en) | 2023-02-08 |
| JPWO2021193561A1 (ja) | 2021-09-30 |
| EP4130079A4 (en) | 2024-02-07 |
| CN115335422A (zh) | 2022-11-11 |
| US20230050436A1 (en) | 2023-02-16 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| NL2007262C2 (en) | A process for preparing articles from a latex comprising water and a styrenic block copolymer and such a latex. | |
| JPWO2012137663A1 (ja) | ポリクロロプレンラテックス、ゴム組成物及び浸漬成形品 | |
| US2474807A (en) | Manufacture of synthetic rubber | |
| JP2019044116A (ja) | クロロプレン共重合体ラテックス組成物及びその成形物 | |
| WO2021193561A1 (ja) | クロロプレン系ブロック共重合体ラテックス | |
| WO2021193562A1 (ja) | 浸漬成形体 | |
| WO2021193563A1 (ja) | クロロプレン系ブロック共重合体、ラテックス、ラテックス組成物及びゴム組成物 | |
| KR20080061927A (ko) | 충격보강제, 그 제조방법 및 이를 이용한 내스크래치성메타크릴레이트계 수지 조성물 | |
| JP2012111860A (ja) | 車両部材用メタクリル樹脂組成物 | |
| WO2021193560A1 (ja) | クロロプレン系ブロック共重合体、ラテックス、ラテックス組成物及びゴム組成物 | |
| US6939917B2 (en) | Impact-resistant composition based on thermoplastic methacrylic (co)polymer | |
| WO2022202555A1 (ja) | (メタ)アクリル系ブロック共重合体、(メタ)アクリル系ブロック共重合体ラテックス、(メタ)アクリル系ブロック共重合体ラテックス組成物、及び成形体 | |
| JP2022147759A (ja) | ジエン系ブロック共重合体、ジエン系ブロック共重合体ラテックス、ジエン系ブロック共重合体ラテックス組成物、及び成形体 | |
| US20240132649A1 (en) | Acrylic block copolymer, (meth)acrylic block copolymer latex, (meth)acrylic block copolymer latex composition, and shaped object | |
| WO2023054104A1 (ja) | クロロプレン系ブロック共重合体、ラテックス、ラテックス組成物、及びゴム組成物 | |
| EP4245778A1 (en) | Chloroprene copolymer latex and method for producing same | |
| US11427701B2 (en) | Chloroprene copolymer latex composition and molded product thereof | |
| KR20240068733A (ko) | 클로로프렌계 블록 공중합체, 라텍스, 라텍스 조성물, 및 고무 조성물 | |
| EP4045106B1 (en) | Styrene butadiene block copolymer compositions for medical devices | |
| JPH1087759A (ja) | ゴム変性スチレン系樹脂及びその組成物 | |
| JP2023128257A (ja) | クロロプレン系重合体ラテックス、浸漬成形体、クロロプレン系重合体ラテックスの製造方法 | |
| CN116323135A (zh) | 氯丁二烯聚合物胶乳及其制造方法、以及浸渍成型体 | |
| WO2020235988A1 (en) | Method for repairing or recycling an elastomeric film | |
| JPS6072953A (ja) | ブロツク共重合体組成物 | |
| JPH04120154A (ja) | 高ニトリル系重合体組成物の製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 21775670 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2022510497 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2021775670 Country of ref document: EP Effective date: 20221026 |