WO2021187601A1 - 心筋細胞の精製方法 - Google Patents
心筋細胞の精製方法 Download PDFInfo
- Publication number
- WO2021187601A1 WO2021187601A1 PCT/JP2021/011231 JP2021011231W WO2021187601A1 WO 2021187601 A1 WO2021187601 A1 WO 2021187601A1 JP 2021011231 W JP2021011231 W JP 2021011231W WO 2021187601 A1 WO2021187601 A1 WO 2021187601A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- cells
- cell
- myocardial
- receptor
- cell population
- Prior art date
Links
- 210000004413 cardiac myocyte Anatomy 0.000 title claims abstract description 171
- 238000000034 method Methods 0.000 title claims abstract description 78
- 238000000746 purification Methods 0.000 title description 12
- 210000004027 cell Anatomy 0.000 claims abstract description 490
- 210000000130 stem cell Anatomy 0.000 claims abstract description 68
- 239000003112 inhibitor Substances 0.000 claims abstract description 52
- 210000001778 pluripotent stem cell Anatomy 0.000 claims abstract description 33
- 238000012258 culturing Methods 0.000 claims abstract description 21
- 102000001301 EGF receptor Human genes 0.000 claims abstract description 15
- 108060006698 EGF receptor Proteins 0.000 claims abstract description 15
- 238000004519 manufacturing process Methods 0.000 claims abstract description 15
- 229940121358 tyrosine kinase inhibitor Drugs 0.000 claims abstract description 10
- 239000005483 tyrosine kinase inhibitor Substances 0.000 claims abstract description 10
- 150000004917 tyrosine kinase inhibitor derivatives Chemical class 0.000 claims abstract description 9
- 230000002107 myocardial effect Effects 0.000 claims description 109
- 230000004069 differentiation Effects 0.000 claims description 103
- 230000006698 induction Effects 0.000 claims description 82
- 229940124617 receptor tyrosine kinase inhibitor Drugs 0.000 claims description 36
- -1 6,7-dimethoxyquinoline-4-yl Chemical group 0.000 claims description 33
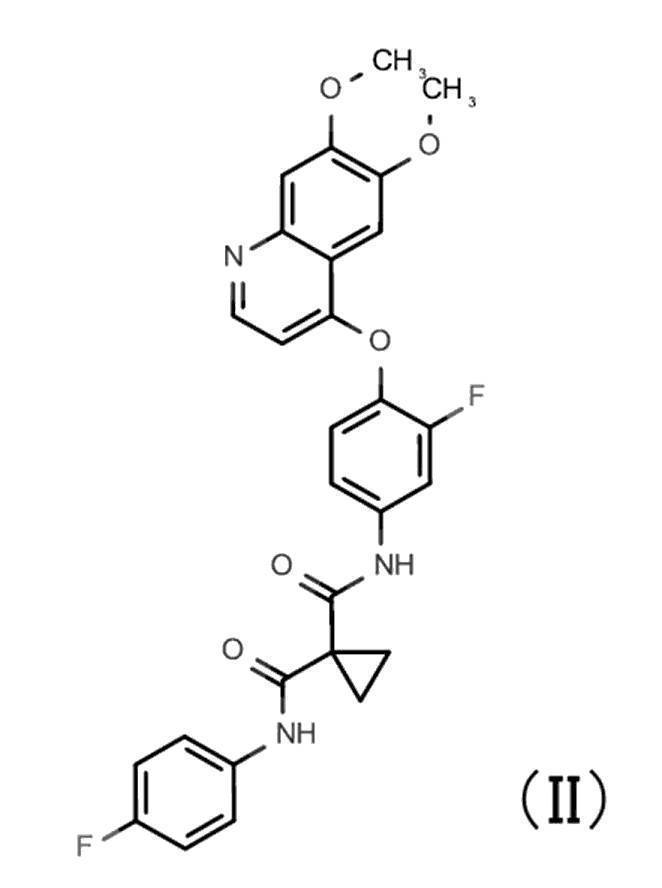
- CXQHYVUVSFXTMY-UHFFFAOYSA-N N1'-[3-fluoro-4-[[6-methoxy-7-[3-(4-morpholinyl)propoxy]-4-quinolinyl]oxy]phenyl]-N1-(4-fluorophenyl)cyclopropane-1,1-dicarboxamide Chemical compound C1=CN=C2C=C(OCCCN3CCOCC3)C(OC)=CC2=C1OC(C(=C1)F)=CC=C1NC(=O)C1(C(=O)NC=2C=CC(F)=CC=2)CC1 CXQHYVUVSFXTMY-UHFFFAOYSA-N 0.000 claims description 14
- VDZZYOJYLLNBTD-UHFFFAOYSA-N 2-[4-[[5-[(2,6-difluoro-3,5-dimethoxyphenyl)methoxy]pyrimidin-2-yl]amino]pyrazol-1-yl]ethanol Chemical compound COC1=CC(OC)=C(F)C(COC=2C=NC(NC3=CN(CCO)N=C3)=NC=2)=C1F VDZZYOJYLLNBTD-UHFFFAOYSA-N 0.000 claims description 13
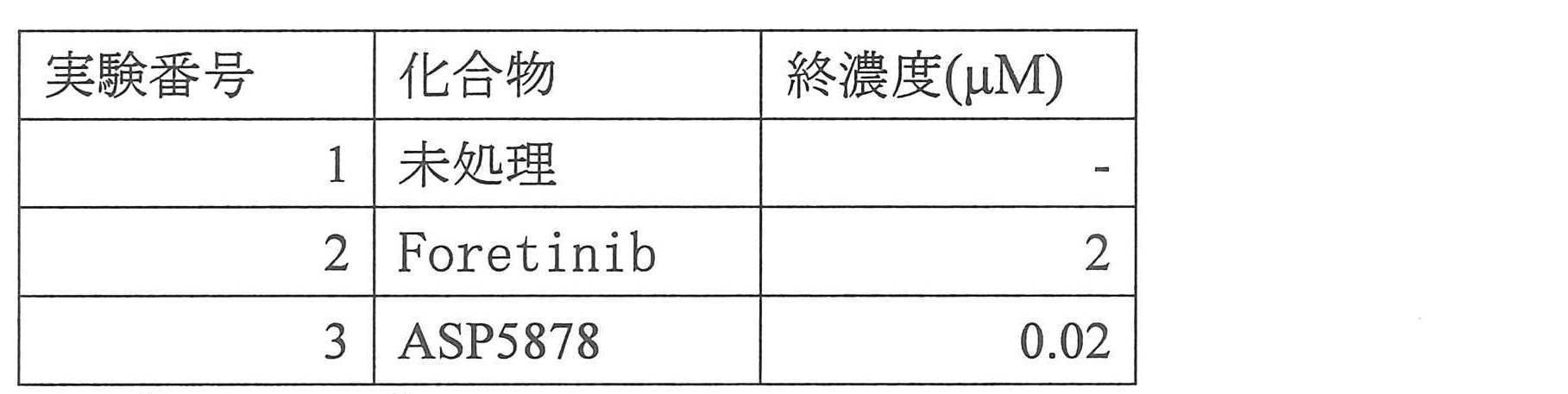
- 229940126287 ASP5878 Drugs 0.000 claims description 13
- 229950008692 foretinib Drugs 0.000 claims description 12
- 108091008598 receptor tyrosine kinases Proteins 0.000 claims description 12
- 210000004263 induced pluripotent stem cell Anatomy 0.000 claims description 11
- 102000027426 receptor tyrosine kinases Human genes 0.000 claims description 11
- 238000002560 therapeutic procedure Methods 0.000 claims description 10
- 230000024245 cell differentiation Effects 0.000 claims description 9
- QADPYRIHXKWUSV-UHFFFAOYSA-N BGJ-398 Chemical compound C1CN(CC)CCN1C(C=C1)=CC=C1NC1=CC(N(C)C(=O)NC=2C(=C(OC)C=C(OC)C=2Cl)Cl)=NC=N1 QADPYRIHXKWUSV-UHFFFAOYSA-N 0.000 claims description 8
- 239000003795 chemical substances by application Substances 0.000 claims description 8
- NVBNDZZLJRYRPD-UHFFFAOYSA-N ZM 323881 Chemical compound C1=C(O)C(C)=CC(F)=C1NC1=NC=NC2=CC(OCC=3C=CC=CC=3)=CC=C12 NVBNDZZLJRYRPD-UHFFFAOYSA-N 0.000 claims description 6
- 108091008603 HGF receptors Proteins 0.000 claims description 5
- DEEOXSOLTLIWMG-UHFFFAOYSA-N 1-[2-[5-(2-methoxyethoxy)-1-benzimidazolyl]-8-quinolinyl]-4-piperidinamine Chemical compound C1=NC2=CC(OCCOC)=CC=C2N1C(N=C12)=CC=C1C=CC=C2N1CCC(N)CC1 DEEOXSOLTLIWMG-UHFFFAOYSA-N 0.000 claims description 4
- 108091008794 FGF receptors Proteins 0.000 claims description 4
- 102000044168 Fibroblast Growth Factor Receptor Human genes 0.000 claims description 4
- 108091008606 PDGF receptors Proteins 0.000 claims description 4
- 102000011653 Platelet-Derived Growth Factor Receptors Human genes 0.000 claims description 4
- 108091008605 VEGF receptors Proteins 0.000 claims description 4
- 102000009484 Vascular Endothelial Growth Factor Receptors Human genes 0.000 claims description 4
- DYNHJHQFHQTFTP-UHFFFAOYSA-N crenolanib Chemical compound C=1C=C2N(C=3N=C4C(N5CCC(N)CC5)=CC=CC4=CC=3)C=NC2=CC=1OCC1(C)COC1 DYNHJHQFHQTFTP-UHFFFAOYSA-N 0.000 claims description 4
- 229950009240 crenolanib Drugs 0.000 claims description 3
- 102000027430 HGF receptors Human genes 0.000 claims 1
- 230000000747 cardiac effect Effects 0.000 abstract description 5
- 150000001875 compounds Chemical class 0.000 description 69
- 239000002609 medium Substances 0.000 description 63
- 238000012360 testing method Methods 0.000 description 55
- 238000002474 experimental method Methods 0.000 description 48
- 230000014509 gene expression Effects 0.000 description 33
- 241000282414 Homo sapiens Species 0.000 description 28
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 27
- 108090000623 proteins and genes Proteins 0.000 description 25
- 150000003839 salts Chemical class 0.000 description 23
- 230000000694 effects Effects 0.000 description 21
- 210000002242 embryoid body Anatomy 0.000 description 20
- 238000005259 measurement Methods 0.000 description 20
- ONIQOQHATWINJY-UHFFFAOYSA-N cabozantinib Chemical compound C=12C=C(OC)C(OC)=CC2=NC=CC=1OC(C=C1)=CC=C1NC(=O)C1(C(=O)NC=2C=CC(F)=CC=2)CC1 ONIQOQHATWINJY-UHFFFAOYSA-N 0.000 description 17
- PIQCTGMSNWUMAF-UHFFFAOYSA-N chembl522892 Chemical compound C1CN(C)CCN1C1=CC=C(NC(=N2)C=3C(NC4=CC=CC(F)=C4C=3N)=O)C2=C1 PIQCTGMSNWUMAF-UHFFFAOYSA-N 0.000 description 17
- 239000002176 L01XE26 - Cabozantinib Substances 0.000 description 16
- 229960001292 cabozantinib Drugs 0.000 description 16
- 239000003814 drug Substances 0.000 description 16
- 229960005070 ascorbic acid Drugs 0.000 description 14
- 208000019622 heart disease Diseases 0.000 description 14
- 230000001939 inductive effect Effects 0.000 description 14
- 102000004169 proteins and genes Human genes 0.000 description 14
- 102000010825 Actinin Human genes 0.000 description 13
- 108010063503 Actinin Proteins 0.000 description 13
- 235000018102 proteins Nutrition 0.000 description 13
- 241000699666 Mus <mouse, genus> Species 0.000 description 12
- 102000013814 Wnt Human genes 0.000 description 12
- 108050003627 Wnt Proteins 0.000 description 12
- 238000011156 evaluation Methods 0.000 description 12
- 210000001082 somatic cell Anatomy 0.000 description 12
- 239000000126 substance Substances 0.000 description 12
- 239000002253 acid Substances 0.000 description 11
- 239000011668 ascorbic acid Substances 0.000 description 11
- 235000010323 ascorbic acid Nutrition 0.000 description 11
- 238000002054 transplantation Methods 0.000 description 11
- 102000003974 Fibroblast growth factor 2 Human genes 0.000 description 10
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 description 10
- 230000001965 increasing effect Effects 0.000 description 10
- 239000006228 supernatant Substances 0.000 description 10
- 229940126062 Compound A Drugs 0.000 description 9
- NLDMNSXOCDLTTB-UHFFFAOYSA-N Heterophylliin A Natural products O1C2COC(=O)C3=CC(O)=C(O)C(O)=C3C3=C(O)C(O)=C(O)C=C3C(=O)OC2C(OC(=O)C=2C=C(O)C(O)=C(O)C=2)C(O)C1OC(=O)C1=CC(O)=C(O)C(O)=C1 NLDMNSXOCDLTTB-UHFFFAOYSA-N 0.000 description 9
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 9
- 229930182816 L-glutamine Natural products 0.000 description 9
- 229940079593 drug Drugs 0.000 description 9
- 210000002950 fibroblast Anatomy 0.000 description 9
- PJUIMOJAAPLTRJ-UHFFFAOYSA-N monothioglycerol Chemical compound OCC(O)CS PJUIMOJAAPLTRJ-UHFFFAOYSA-N 0.000 description 9
- 238000012795 verification Methods 0.000 description 9
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 8
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 8
- 210000002966 serum Anatomy 0.000 description 8
- 102100024505 Bone morphogenetic protein 4 Human genes 0.000 description 7
- 101000762379 Homo sapiens Bone morphogenetic protein 4 Proteins 0.000 description 7
- 102100032352 Leukemia inhibitory factor Human genes 0.000 description 7
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 7
- 230000015572 biosynthetic process Effects 0.000 description 7
- 239000006285 cell suspension Substances 0.000 description 7
- 238000007796 conventional method Methods 0.000 description 7
- 210000002257 embryonic structure Anatomy 0.000 description 7
- 230000002401 inhibitory effect Effects 0.000 description 7
- 239000003550 marker Substances 0.000 description 7
- 229910052760 oxygen Inorganic materials 0.000 description 7
- 239000001301 oxygen Substances 0.000 description 7
- 238000010186 staining Methods 0.000 description 7
- SPMVMDHWKHCIDT-UHFFFAOYSA-N 1-[2-chloro-4-[(6,7-dimethoxy-4-quinolinyl)oxy]phenyl]-3-(5-methyl-3-isoxazolyl)urea Chemical compound C=12C=C(OC)C(OC)=CC2=NC=CC=1OC(C=C1Cl)=CC=C1NC(=O)NC=1C=C(C)ON=1 SPMVMDHWKHCIDT-UHFFFAOYSA-N 0.000 description 6
- 102100022623 Hepatocyte growth factor receptor Human genes 0.000 description 6
- 241000282412 Homo Species 0.000 description 6
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 6
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 6
- 238000004458 analytical method Methods 0.000 description 6
- 229960003005 axitinib Drugs 0.000 description 6
- RITAVMQDGBJQJZ-FMIVXFBMSA-N axitinib Chemical compound CNC(=O)C1=CC=CC=C1SC1=CC=C(C(\C=C\C=2N=CC=CC=2)=NN2)C2=C1 RITAVMQDGBJQJZ-FMIVXFBMSA-N 0.000 description 6
- 239000013078 crystal Substances 0.000 description 6
- 210000001671 embryonic stem cell Anatomy 0.000 description 6
- 210000001900 endoderm Anatomy 0.000 description 6
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 6
- MPVGZUGXCQEXTM-UHFFFAOYSA-N linifanib Chemical compound CC1=CC=C(F)C(NC(=O)NC=2C=CC(=CC=2)C=2C=3C(N)=NNC=3C=CC=2)=C1 MPVGZUGXCQEXTM-UHFFFAOYSA-N 0.000 description 6
- CPMDPSXJELVGJG-UHFFFAOYSA-N methyl 2-hydroxy-3-[N-[4-[methyl-[2-(4-methylpiperazin-1-yl)acetyl]amino]phenyl]-C-phenylcarbonimidoyl]-1H-indole-6-carboxylate Chemical compound OC=1NC2=CC(=CC=C2C=1C(=NC1=CC=C(C=C1)N(C(CN1CCN(CC1)C)=O)C)C1=CC=CC=C1)C(=O)OC CPMDPSXJELVGJG-UHFFFAOYSA-N 0.000 description 6
- DZFZXPPHBWCXPQ-UHFFFAOYSA-N n-[5-[2-(cyclopropanecarbonylamino)imidazo[1,2-b]pyridazin-6-yl]oxy-2-methylphenyl]-2,5-dimethylpyrazole-3-carboxamide Chemical group CN1N=C(C)C=C1C(=O)NC1=CC(OC2=NN3C=C(NC(=O)C4CC4)N=C3C=C2)=CC=C1C DZFZXPPHBWCXPQ-UHFFFAOYSA-N 0.000 description 6
- 239000000243 solution Substances 0.000 description 6
- 238000004114 suspension culture Methods 0.000 description 6
- 229940124597 therapeutic agent Drugs 0.000 description 6
- VUDQSRFCCHQIIU-UHFFFAOYSA-N 1-(3,5-dichloro-2,6-dihydroxy-4-methoxyphenyl)hexan-1-one Chemical compound CCCCCC(=O)C1=C(O)C(Cl)=C(OC)C(Cl)=C1O VUDQSRFCCHQIIU-UHFFFAOYSA-N 0.000 description 5
- GKJCVYLDJWTWQU-CXLRFSCWSA-N 2-[4-[(e)-2-[5-[(1r)-1-(3,5-dichloropyridin-4-yl)ethoxy]-1h-indazol-3-yl]ethenyl]pyrazol-1-yl]ethanol Chemical compound O([C@H](C)C=1C(=CN=CC=1Cl)Cl)C(C=C12)=CC=C1NN=C2\C=C\C=1C=NN(CCO)C=1 GKJCVYLDJWTWQU-CXLRFSCWSA-N 0.000 description 5
- 102000018651 Epithelial Cell Adhesion Molecule Human genes 0.000 description 5
- 101001078158 Homo sapiens Integrin alpha-1 Proteins 0.000 description 5
- 101000942967 Homo sapiens Leukemia inhibitory factor Proteins 0.000 description 5
- 102100025323 Integrin alpha-1 Human genes 0.000 description 5
- 102100024616 Platelet endothelial cell adhesion molecule Human genes 0.000 description 5
- 238000003559 RNA-seq method Methods 0.000 description 5
- 239000012190 activator Substances 0.000 description 5
- KTEIFNKAUNYNJU-GFCCVEGCSA-N crizotinib Chemical compound O([C@H](C)C=1C(=C(F)C=CC=1Cl)Cl)C(C(=NC=1)N)=CC=1C(=C1)C=NN1C1CCNCC1 KTEIFNKAUNYNJU-GFCCVEGCSA-N 0.000 description 5
- 230000003247 decreasing effect Effects 0.000 description 5
- 238000012423 maintenance Methods 0.000 description 5
- 210000001704 mesoblast Anatomy 0.000 description 5
- 239000000203 mixture Substances 0.000 description 5
- 102000005962 receptors Human genes 0.000 description 5
- 108020003175 receptors Proteins 0.000 description 5
- FNHKPVJBJVTLMP-UHFFFAOYSA-N regorafenib Chemical compound C1=NC(C(=O)NC)=CC(OC=2C=C(F)C(NC(=O)NC=3C=C(C(Cl)=CC=3)C(F)(F)F)=CC=2)=C1 FNHKPVJBJVTLMP-UHFFFAOYSA-N 0.000 description 5
- 229940035024 thioglycerol Drugs 0.000 description 5
- 210000001519 tissue Anatomy 0.000 description 5
- NHFDRBXTEDBWCZ-ZROIWOOFSA-N 3-[2,4-dimethyl-5-[(z)-(2-oxo-1h-indol-3-ylidene)methyl]-1h-pyrrol-3-yl]propanoic acid Chemical compound OC(=O)CCC1=C(C)NC(\C=C/2C3=CC=CC=C3NC\2=O)=C1C NHFDRBXTEDBWCZ-ZROIWOOFSA-N 0.000 description 4
- FWBHETKCLVMNFS-UHFFFAOYSA-N 4',6-Diamino-2-phenylindol Chemical compound C1=CC(C(=N)N)=CC=C1C1=CC2=CC=C(C(N)=N)C=C2N1 FWBHETKCLVMNFS-UHFFFAOYSA-N 0.000 description 4
- XXJWYDDUDKYVKI-UHFFFAOYSA-N 4-[(4-fluoro-2-methyl-1H-indol-5-yl)oxy]-6-methoxy-7-[3-(1-pyrrolidinyl)propoxy]quinazoline Chemical compound COC1=CC2=C(OC=3C(=C4C=C(C)NC4=CC=3)F)N=CN=C2C=C1OCCCN1CCCC1 XXJWYDDUDKYVKI-UHFFFAOYSA-N 0.000 description 4
- ZRHDKBOBHHFLBW-UHFFFAOYSA-N 4-amino-5-fluoro-3-[6-(4-methylpiperazin-1-yl)-1H-benzimidazol-2-yl]-1H-quinolin-2-one 2-hydroxypropanoic acid Chemical compound CC(O)C(O)=O.C1CN(C)CCN1C1=CC=C(NC(=N2)C=3C(NC4=CC=CC(F)=C4C=3N)=O)C2=C1 ZRHDKBOBHHFLBW-UHFFFAOYSA-N 0.000 description 4
- VRQMAABPASPXMW-HDICACEKSA-N AZD4547 Chemical compound COC1=CC(OC)=CC(CCC=2NN=C(NC(=O)C=3C=CC(=CC=3)N3C[C@@H](C)N[C@@H](C)C3)C=2)=C1 VRQMAABPASPXMW-HDICACEKSA-N 0.000 description 4
- 241000282693 Cercopithecidae Species 0.000 description 4
- 108010035532 Collagen Proteins 0.000 description 4
- 102000008186 Collagen Human genes 0.000 description 4
- 102000004127 Cytokines Human genes 0.000 description 4
- 108090000695 Cytokines Proteins 0.000 description 4
- 102100027844 Fibroblast growth factor receptor 4 Human genes 0.000 description 4
- 101000917134 Homo sapiens Fibroblast growth factor receptor 4 Proteins 0.000 description 4
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 4
- 239000002147 L01XE04 - Sunitinib Substances 0.000 description 4
- 239000003798 L01XE11 - Pazopanib Substances 0.000 description 4
- 239000002146 L01XE16 - Crizotinib Substances 0.000 description 4
- 241000124008 Mammalia Species 0.000 description 4
- 241000699670 Mus sp. Species 0.000 description 4
- UFICVEHDQUKCEA-UHFFFAOYSA-N N-[[3-fluoro-4-[[2-(1-methyl-4-imidazolyl)-7-thieno[3,2-b]pyridinyl]oxy]anilino]-sulfanylidenemethyl]-2-phenylacetamide Chemical compound CN1C=NC(C=2SC3=C(OC=4C(=CC(NC(=S)NC(=O)CC=5C=CC=CC=5)=CC=4)F)C=CN=C3C=2)=C1 UFICVEHDQUKCEA-UHFFFAOYSA-N 0.000 description 4
- 102100033178 Vascular endothelial growth factor receptor 1 Human genes 0.000 description 4
- 102100033177 Vascular endothelial growth factor receptor 2 Human genes 0.000 description 4
- 235000001014 amino acid Nutrition 0.000 description 4
- 150000001413 amino acids Chemical class 0.000 description 4
- 239000007640 basal medium Substances 0.000 description 4
- 210000002459 blastocyst Anatomy 0.000 description 4
- 229920001436 collagen Polymers 0.000 description 4
- 229960005061 crizotinib Drugs 0.000 description 4
- 238000001514 detection method Methods 0.000 description 4
- 238000010494 dissociation reaction Methods 0.000 description 4
- 230000005593 dissociations Effects 0.000 description 4
- 235000013601 eggs Nutrition 0.000 description 4
- 230000002357 endometrial effect Effects 0.000 description 4
- 238000005516 engineering process Methods 0.000 description 4
- 210000002744 extracellular matrix Anatomy 0.000 description 4
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 4
- 230000007774 longterm Effects 0.000 description 4
- 210000001161 mammalian embryo Anatomy 0.000 description 4
- 210000004165 myocardium Anatomy 0.000 description 4
- 229960004378 nintedanib Drugs 0.000 description 4
- XZXHXSATPCNXJR-ZIADKAODSA-N nintedanib Chemical compound O=C1NC2=CC(C(=O)OC)=CC=C2\C1=C(C=1C=CC=CC=1)\NC(C=C1)=CC=C1N(C)C(=O)CN1CCN(C)CC1 XZXHXSATPCNXJR-ZIADKAODSA-N 0.000 description 4
- 238000010449 nuclear transplantation Methods 0.000 description 4
- 229960000639 pazopanib Drugs 0.000 description 4
- CUIHSIWYWATEQL-UHFFFAOYSA-N pazopanib Chemical compound C1=CC2=C(C)N(C)N=C2C=C1N(C)C(N=1)=CC=NC=1NC1=CC=C(C)C(S(N)(=O)=O)=C1 CUIHSIWYWATEQL-UHFFFAOYSA-N 0.000 description 4
- 239000008188 pellet Substances 0.000 description 4
- 238000011160 research Methods 0.000 description 4
- 210000002235 sarcomere Anatomy 0.000 description 4
- 229960001796 sunitinib Drugs 0.000 description 4
- WINHZLLDWRZWRT-ATVHPVEESA-N sunitinib Chemical compound CCN(CC)CCNC(=O)C1=C(C)NC(\C=C/2C3=CC(F)=CC=C3NC\2=O)=C1C WINHZLLDWRZWRT-ATVHPVEESA-N 0.000 description 4
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 4
- KGWWHPZQLVVAPT-STTJLUEPSA-N (2r,3r)-2,3-dihydroxybutanedioic acid;6-(4-methylpiperazin-1-yl)-n-(5-methyl-1h-pyrazol-3-yl)-2-[(e)-2-phenylethenyl]pyrimidin-4-amine Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O.C1CN(C)CCN1C1=CC(NC2=NNC(C)=C2)=NC(\C=C\C=2C=CC=CC=2)=N1 KGWWHPZQLVVAPT-STTJLUEPSA-N 0.000 description 3
- VPBYZLCHOKSGRX-UHFFFAOYSA-N 1-[2-chloro-4-(6,7-dimethoxyquinazolin-4-yl)oxyphenyl]-3-propylurea Chemical compound C1=C(Cl)C(NC(=O)NCCC)=CC=C1OC1=NC=NC2=CC(OC)=C(OC)C=C12 VPBYZLCHOKSGRX-UHFFFAOYSA-N 0.000 description 3
- XVMHQSDMKWQNBK-UHFFFAOYSA-N 2-[[3-(4-fluorophenyl)-4-oxo-6,7-dihydrothieno[3,2-d]pyrimidin-2-yl]sulfanyl]-n-(6-methyl-1,3-benzothiazol-2-yl)acetamide Chemical compound S1C2=CC(C)=CC=C2N=C1NC(=O)CSC1=NC=2CCSC=2C(=O)N1C1=CC=C(F)C=C1 XVMHQSDMKWQNBK-UHFFFAOYSA-N 0.000 description 3
- JGEBLDKNWBUGRZ-HXUWFJFHSA-N 9-[[[(2r)-1,4-dioxan-2-yl]methyl-methylsulfamoyl]amino]-2-(1-methylpyrazol-4-yl)-11-oxobenzo[1,2]cyclohepta[2,4-b]pyridine Chemical compound C=1C=C2C=CC3=NC=C(C4=CN(C)N=C4)C=C3C(=O)C2=CC=1NS(=O)(=O)N(C)C[C@@H]1COCCO1 JGEBLDKNWBUGRZ-HXUWFJFHSA-N 0.000 description 3
- OONFNUWBHFSNBT-HXUWFJFHSA-N AEE788 Chemical compound C1CN(CC)CCN1CC1=CC=C(C=2NC3=NC=NC(N[C@H](C)C=4C=CC=CC=4)=C3C=2)C=C1 OONFNUWBHFSNBT-HXUWFJFHSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- LQVXSNNAFNGRAH-QHCPKHFHSA-N BMS-754807 Chemical compound C([C@@]1(C)C(=O)NC=2C=NC(F)=CC=2)CCN1C(=NN1C=CC=C11)N=C1NC(=NN1)C=C1C1CC1 LQVXSNNAFNGRAH-QHCPKHFHSA-N 0.000 description 3
- 108060005980 Collagenase Proteins 0.000 description 3
- 102000029816 Collagenase Human genes 0.000 description 3
- 102000016911 Deoxyribonucleases Human genes 0.000 description 3
- 108010053770 Deoxyribonucleases Proteins 0.000 description 3
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 3
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 3
- 108010067306 Fibronectins Proteins 0.000 description 3
- 101001139134 Homo sapiens Krueppel-like factor 4 Proteins 0.000 description 3
- 101001094700 Homo sapiens POU domain, class 5, transcription factor 1 Proteins 0.000 description 3
- 101000984042 Homo sapiens Protein lin-28 homolog A Proteins 0.000 description 3
- 101000713275 Homo sapiens Solute carrier family 22 member 3 Proteins 0.000 description 3
- 101000687905 Homo sapiens Transcription factor SOX-2 Proteins 0.000 description 3
- 102000004877 Insulin Human genes 0.000 description 3
- 108090001061 Insulin Proteins 0.000 description 3
- 102100020677 Krueppel-like factor 4 Human genes 0.000 description 3
- 239000002211 L-ascorbic acid Substances 0.000 description 3
- 239000005551 L01XE03 - Erlotinib Substances 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 102100035423 POU domain, class 5, transcription factor 1 Human genes 0.000 description 3
- 241000288906 Primates Species 0.000 description 3
- 102100025460 Protein lin-28 homolog A Human genes 0.000 description 3
- 108700008625 Reporter Genes Proteins 0.000 description 3
- 102100024270 Transcription factor SOX-2 Human genes 0.000 description 3
- 102000004338 Transferrin Human genes 0.000 description 3
- 108090000901 Transferrin Proteins 0.000 description 3
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 3
- 102000004987 Troponin T Human genes 0.000 description 3
- 108090001108 Troponin T Proteins 0.000 description 3
- 108010053099 Vascular Endothelial Growth Factor Receptor-2 Proteins 0.000 description 3
- 108010053100 Vascular Endothelial Growth Factor Receptor-3 Proteins 0.000 description 3
- 102100033179 Vascular endothelial growth factor receptor 3 Human genes 0.000 description 3
- BEMNJULZEQTDJY-UHFFFAOYSA-N [5-amino-1-(2-methyl-3h-benzimidazol-5-yl)pyrazol-4-yl]-(1h-indol-2-yl)methanone Chemical compound C1=CC=C2NC(C(=O)C=3C=NN(C=3N)C=3C=C4N=C(NC4=CC=3)C)=CC2=C1 BEMNJULZEQTDJY-UHFFFAOYSA-N 0.000 description 3
- 108010023082 activin A Proteins 0.000 description 3
- 239000000853 adhesive Substances 0.000 description 3
- 230000001070 adhesive effect Effects 0.000 description 3
- LTEJRLHKIYCEOX-OCCSQVGLSA-N brivanib alaninate Chemical compound C1=C2NC(C)=CC2=C(F)C(OC2=NC=NN3C=C(C(=C32)C)OC[C@@H](C)OC(=O)[C@H](C)N)=C1 LTEJRLHKIYCEOX-OCCSQVGLSA-N 0.000 description 3
- HFCFMRYTXDINDK-WNQIDUERSA-N cabozantinib malate Chemical compound OC(=O)[C@@H](O)CC(O)=O.C=12C=C(OC)C(OC)=CC2=NC=CC=1OC(C=C1)=CC=C1NC(=O)C1(C(=O)NC=2C=CC(F)=CC=2)CC1 HFCFMRYTXDINDK-WNQIDUERSA-N 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 229960002424 collagenase Drugs 0.000 description 3
- XHBVYDAKJHETMP-UHFFFAOYSA-N dorsomorphin Chemical compound C=1C=C(C2=CN3N=CC(=C3N=C2)C=2C=CN=CC=2)C=CC=1OCCN1CCCCC1 XHBVYDAKJHETMP-UHFFFAOYSA-N 0.000 description 3
- 229960001433 erlotinib Drugs 0.000 description 3
- AAKJLRGGTJKAMG-UHFFFAOYSA-N erlotinib Chemical compound C=12C=C(OCCOC)C(OCCOC)=CC2=NC=NC=1NC1=CC=CC(C#C)=C1 AAKJLRGGTJKAMG-UHFFFAOYSA-N 0.000 description 3
- 230000001605 fetal effect Effects 0.000 description 3
- 238000000684 flow cytometry Methods 0.000 description 3
- 210000004602 germ cell Anatomy 0.000 description 3
- 229940125396 insulin Drugs 0.000 description 3
- 239000000463 material Substances 0.000 description 3
- 208000010125 myocardial infarction Diseases 0.000 description 3
- 210000004940 nucleus Anatomy 0.000 description 3
- MQHIQUBXFFAOMK-UHFFFAOYSA-N pazopanib hydrochloride Chemical compound Cl.C1=CC2=C(C)N(C)N=C2C=C1N(C)C(N=1)=CC=NC=1NC1=CC=C(C)C(S(N)(=O)=O)=C1 MQHIQUBXFFAOMK-UHFFFAOYSA-N 0.000 description 3
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 3
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 3
- 230000001737 promoting effect Effects 0.000 description 3
- 230000008672 reprogramming Effects 0.000 description 3
- 238000010079 rubber tapping Methods 0.000 description 3
- 238000012174 single-cell RNA sequencing Methods 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 238000012546 transfer Methods 0.000 description 3
- 239000012581 transferrin Substances 0.000 description 3
- 239000013598 vector Substances 0.000 description 3
- 229940088594 vitamin Drugs 0.000 description 3
- 229930003231 vitamin Natural products 0.000 description 3
- 235000013343 vitamin Nutrition 0.000 description 3
- 239000011782 vitamin Substances 0.000 description 3
- 239000011534 wash buffer Substances 0.000 description 3
- WCWUXEGQKLTGDX-LLVKDONJSA-N (2R)-1-[[4-[(4-fluoro-2-methyl-1H-indol-5-yl)oxy]-5-methyl-6-pyrrolo[2,1-f][1,2,4]triazinyl]oxy]-2-propanol Chemical compound C1=C2NC(C)=CC2=C(F)C(OC2=NC=NN3C=C(C(=C32)C)OC[C@H](O)C)=C1 WCWUXEGQKLTGDX-LLVKDONJSA-N 0.000 description 2
- LFKQSJNCVRGFCC-UHFFFAOYSA-N 1-(2,4-difluorophenyl)-3-[4-[(6,7-dimethoxy-4-quinolinyl)oxy]-2-fluorophenyl]urea Chemical compound C=12C=C(OC)C(OC)=CC2=NC=CC=1OC(C=C1F)=CC=C1NC(=O)NC1=CC=C(F)C=C1F LFKQSJNCVRGFCC-UHFFFAOYSA-N 0.000 description 2
- RGAZVGZUBCFHRJ-UHFFFAOYSA-N 1-(4-fluorophenyl)-n-[3-fluoro-4-[(3-phenyl-1h-pyrrolo[2,3-b]pyridin-4-yl)oxy]phenyl]-2,3-dimethyl-5-oxopyrazole-4-carboxamide Chemical compound O=C1N(C=2C=CC(F)=CC=2)N(C)C(C)=C1C(=O)NC(C=C1F)=CC=C1OC(C1=2)=CC=NC=2NC=C1C1=CC=CC=C1 RGAZVGZUBCFHRJ-UHFFFAOYSA-N 0.000 description 2
- BJHCYTJNPVGSBZ-YXSASFKJSA-N 1-[4-[6-amino-5-[(Z)-methoxyiminomethyl]pyrimidin-4-yl]oxy-2-chlorophenyl]-3-ethylurea Chemical compound CCNC(=O)Nc1ccc(Oc2ncnc(N)c2\C=N/OC)cc1Cl BJHCYTJNPVGSBZ-YXSASFKJSA-N 0.000 description 2
- LSNPHHKHXUPAIC-UHFFFAOYSA-N 1-amino-5-fluoro-3-[6-(4-methylpiperazin-1-yl)-1h-benzimidazol-2-yl]quinolin-2-one Chemical compound C1CN(C)CCN1C1=CC=C(N=C(N2)C=3C(N(N)C4=CC=CC(F)=C4C=3)=O)C2=C1 LSNPHHKHXUPAIC-UHFFFAOYSA-N 0.000 description 2
- WLAVZAAODLTUSW-UHFFFAOYSA-N 1-n'-[3-fluoro-4-[2-[5-[(2-methoxyethylamino)methyl]pyridin-2-yl]thieno[3,2-b]pyridin-7-yl]oxyphenyl]-1-n-(4-fluorophenyl)cyclopropane-1,1-dicarboxamide Chemical compound N1=CC(CNCCOC)=CC=C1C1=CC2=NC=CC(OC=3C(=CC(NC(=O)C4(CC4)C(=O)NC=4C=CC(F)=CC=4)=CC=3)F)=C2S1 WLAVZAAODLTUSW-UHFFFAOYSA-N 0.000 description 2
- GNNDEPIMDAZHRQ-UHFFFAOYSA-N 1-n'-[4-[2-(cyclopropanecarbonylamino)pyridin-4-yl]oxy-2,5-difluorophenyl]-1-n-(4-fluorophenyl)cyclopropane-1,1-dicarboxamide Chemical compound C1=CC(F)=CC=C1NC(=O)C1(C(=O)NC=2C(=CC(OC=3C=C(NC(=O)C4CC4)N=CC=3)=C(F)C=2)F)CC1 GNNDEPIMDAZHRQ-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- RHUJMHOIQBDFQR-UHFFFAOYSA-N 2-[[3-(2-methoxyphenyl)-4-oxo-6,7-dihydrothieno[3,2-d]pyrimidin-2-yl]sulfanyl]-n-(6-methyl-1,3-benzothiazol-2-yl)acetamide Chemical compound COC1=CC=CC=C1N1C(=O)C(SCC2)=C2N=C1SCC(=O)NC1=NC2=CC=C(C)C=C2S1 RHUJMHOIQBDFQR-UHFFFAOYSA-N 0.000 description 2
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 description 2
- MLDQJTXFUGDVEO-UHFFFAOYSA-N BAY-43-9006 Chemical compound C1=NC(C(=O)NC)=CC(OC=2C=CC(NC(=O)NC=3C=C(C(Cl)=CC=3)C(F)(F)F)=CC=2)=C1 MLDQJTXFUGDVEO-UHFFFAOYSA-N 0.000 description 2
- 102000015735 Beta-catenin Human genes 0.000 description 2
- 108060000903 Beta-catenin Proteins 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- AQGNHMOJWBZFQQ-UHFFFAOYSA-N CT 99021 Chemical compound CC1=CNC(C=2C(=NC(NCCNC=3N=CC(=CC=3)C#N)=NC=2)C=2C(=CC(Cl)=CC=2)Cl)=N1 AQGNHMOJWBZFQQ-UHFFFAOYSA-N 0.000 description 2
- 241000282472 Canis lupus familiaris Species 0.000 description 2
- 208000031229 Cardiomyopathies Diseases 0.000 description 2
- ZEOWTGPWHLSLOG-UHFFFAOYSA-N Cc1ccc(cc1-c1ccc2c(n[nH]c2c1)-c1cnn(c1)C1CC1)C(=O)Nc1cccc(c1)C(F)(F)F Chemical compound Cc1ccc(cc1-c1ccc2c(n[nH]c2c1)-c1cnn(c1)C1CC1)C(=O)Nc1cccc(c1)C(F)(F)F ZEOWTGPWHLSLOG-UHFFFAOYSA-N 0.000 description 2
- LVZWSLJZHVFIQJ-UHFFFAOYSA-N Cyclopropane Chemical compound C1CC1 LVZWSLJZHVFIQJ-UHFFFAOYSA-N 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- ZZZCUOFIHGPKAK-UHFFFAOYSA-N D-erythro-ascorbic acid Natural products OCC1OC(=O)C(O)=C1O ZZZCUOFIHGPKAK-UHFFFAOYSA-N 0.000 description 2
- 241000283073 Equus caballus Species 0.000 description 2
- 102100023593 Fibroblast growth factor receptor 1 Human genes 0.000 description 2
- 101710182386 Fibroblast growth factor receptor 1 Proteins 0.000 description 2
- 102100023600 Fibroblast growth factor receptor 2 Human genes 0.000 description 2
- 101710182389 Fibroblast growth factor receptor 2 Proteins 0.000 description 2
- 102100027842 Fibroblast growth factor receptor 3 Human genes 0.000 description 2
- 101710182396 Fibroblast growth factor receptor 3 Proteins 0.000 description 2
- 102100037362 Fibronectin Human genes 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 206010019280 Heart failures Diseases 0.000 description 2
- 101000972946 Homo sapiens Hepatocyte growth factor receptor Proteins 0.000 description 2
- 101001103036 Homo sapiens Nuclear receptor ROR-alpha Proteins 0.000 description 2
- 101001126417 Homo sapiens Platelet-derived growth factor receptor alpha Proteins 0.000 description 2
- 101000851018 Homo sapiens Vascular endothelial growth factor receptor 1 Proteins 0.000 description 2
- 101000851007 Homo sapiens Vascular endothelial growth factor receptor 2 Proteins 0.000 description 2
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 2
- 206010021143 Hypoxia Diseases 0.000 description 2
- 102000003746 Insulin Receptor Human genes 0.000 description 2
- 108010001127 Insulin Receptor Proteins 0.000 description 2
- 102100039688 Insulin-like growth factor 1 receptor Human genes 0.000 description 2
- 101710184277 Insulin-like growth factor 1 receptor Proteins 0.000 description 2
- 150000000996 L-ascorbic acids Chemical class 0.000 description 2
- 239000005511 L01XE05 - Sorafenib Substances 0.000 description 2
- 239000002138 L01XE21 - Regorafenib Substances 0.000 description 2
- 108010085895 Laminin Proteins 0.000 description 2
- 102000007547 Laminin Human genes 0.000 description 2
- 108090000581 Leukemia inhibitory factor Proteins 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- NWIBSHFKIJFRCO-WUDYKRTCSA-N Mytomycin Chemical compound C1N2C(C(C(C)=C(N)C3=O)=O)=C3[C@@H](COC(N)=O)[C@@]2(OC)[C@@H]2[C@H]1N2 NWIBSHFKIJFRCO-WUDYKRTCSA-N 0.000 description 2
- MOSKATHMXWSZTQ-UHFFFAOYSA-N N-(2,6-difluorophenyl)-5-[3-[2-[5-ethyl-2-methoxy-4-[4-(4-methylsulfonyl-1-piperazinyl)-1-piperidinyl]anilino]-4-pyrimidinyl]-2-imidazo[1,2-a]pyridinyl]-2-methoxybenzamide Chemical compound COC=1C=C(N2CCC(CC2)N2CCN(CC2)S(C)(=O)=O)C(CC)=CC=1NC(N=1)=NC=CC=1C(N1C=CC=CC1=N1)=C1C(C=1)=CC=C(OC)C=1C(=O)NC1=C(F)C=CC=C1F MOSKATHMXWSZTQ-UHFFFAOYSA-N 0.000 description 2
- VNBRGSXVFBYQNN-UHFFFAOYSA-N N-[4-[(2-amino-3-chloro-4-pyridinyl)oxy]-3-fluorophenyl]-4-ethoxy-1-(4-fluorophenyl)-2-oxo-3-pyridinecarboxamide Chemical compound O=C1C(C(=O)NC=2C=C(F)C(OC=3C(=C(N)N=CC=3)Cl)=CC=2)=C(OCC)C=CN1C1=CC=C(F)C=C1 VNBRGSXVFBYQNN-UHFFFAOYSA-N 0.000 description 2
- 108091008604 NGF receptors Proteins 0.000 description 2
- 102000007339 Nerve Growth Factor Receptors Human genes 0.000 description 2
- 102000016979 Other receptors Human genes 0.000 description 2
- 108091005804 Peptidases Proteins 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 102000001393 Platelet-Derived Growth Factor alpha Receptor Human genes 0.000 description 2
- 108010068588 Platelet-Derived Growth Factor alpha Receptor Proteins 0.000 description 2
- 108010051742 Platelet-Derived Growth Factor beta Receptor Proteins 0.000 description 2
- 102100030485 Platelet-derived growth factor receptor alpha Human genes 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 239000004365 Protease Substances 0.000 description 2
- 102000004022 Protein-Tyrosine Kinases Human genes 0.000 description 2
- 108090000412 Protein-Tyrosine Kinases Proteins 0.000 description 2
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- 229940127361 Receptor Tyrosine Kinase Inhibitors Drugs 0.000 description 2
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 102000004357 Transferases Human genes 0.000 description 2
- 108090000992 Transferases Proteins 0.000 description 2
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 2
- 102000004142 Trypsin Human genes 0.000 description 2
- 108090000631 Trypsin Proteins 0.000 description 2
- 108010053096 Vascular Endothelial Growth Factor Receptor-1 Proteins 0.000 description 2
- 229930003268 Vitamin C Natural products 0.000 description 2
- MIJPAVRNWPDMOR-UHFFFAOYSA-N [2-(1,2-dihydroxyethyl)-3-hydroxy-5-oxo-2h-furan-4-yl] dihydrogen phosphate Chemical compound OCC(O)C1OC(=O)C(OP(O)(O)=O)=C1O MIJPAVRNWPDMOR-UHFFFAOYSA-N 0.000 description 2
- 108010076089 accutase Proteins 0.000 description 2
- 230000002378 acidificating effect Effects 0.000 description 2
- 229950005952 altiratinib Drugs 0.000 description 2
- OVDSPTSBIQCAIN-UHFFFAOYSA-N ap26113 Chemical compound COC1=CC(N2CCC(CC2)N(C)C)=CC=C1NC(N=1)=NC=C(Cl)C=1NC1=CC=CC=C1P(C)(C)=O OVDSPTSBIQCAIN-UHFFFAOYSA-N 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 238000010009 beating Methods 0.000 description 2
- WGQKYBSKWIADBV-UHFFFAOYSA-N benzylamine Chemical compound NCC1=CC=CC=C1 WGQKYBSKWIADBV-UHFFFAOYSA-N 0.000 description 2
- 238000002659 cell therapy Methods 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- PAFZNILMFXTMIY-UHFFFAOYSA-N cyclohexylamine Chemical compound NC1CCCCC1 PAFZNILMFXTMIY-UHFFFAOYSA-N 0.000 description 2
- FEHLGOYZDFFMND-UHFFFAOYSA-N cyclopropane-1,1-dicarboxamide Chemical compound NC(=O)C1(C(N)=O)CC1 FEHLGOYZDFFMND-UHFFFAOYSA-N 0.000 description 2
- 230000000850 deacetylating effect Effects 0.000 description 2
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- YUAALFPUEOYPNX-UHFFFAOYSA-N dubermatinib Chemical compound CN(C)S(=O)(=O)C1=CC=CC=C1NC1=NC(NC=2C=CC(CN3CCN(C)CC3)=CC=2)=NC=C1Cl YUAALFPUEOYPNX-UHFFFAOYSA-N 0.000 description 2
- 210000002889 endothelial cell Anatomy 0.000 description 2
- NGOGFTYYXHNFQH-UHFFFAOYSA-N fasudil Chemical compound C=1C=CC2=CN=CC=C2C=1S(=O)(=O)N1CCCNCC1 NGOGFTYYXHNFQH-UHFFFAOYSA-N 0.000 description 2
- 229960002435 fasudil Drugs 0.000 description 2
- 239000007850 fluorescent dye Substances 0.000 description 2
- XGALLCVXEZPNRQ-UHFFFAOYSA-N gefitinib Chemical compound C=12C=C(OCCCN3CCOCC3)C(OC)=CC2=NC=NC=1NC1=CC=C(F)C(Cl)=C1 XGALLCVXEZPNRQ-UHFFFAOYSA-N 0.000 description 2
- 238000007429 general method Methods 0.000 description 2
- 229950007540 glesatinib Drugs 0.000 description 2
- 239000003102 growth factor Substances 0.000 description 2
- IPCSVZSSVZVIGE-UHFFFAOYSA-N hexadecanoic acid Chemical compound CCCCCCCCCCCCCCCC(O)=O IPCSVZSSVZVIGE-UHFFFAOYSA-N 0.000 description 2
- 206010020871 hypertrophic cardiomyopathy Diseases 0.000 description 2
- 230000001146 hypoxic effect Effects 0.000 description 2
- 150000002460 imidazoles Chemical class 0.000 description 2
- 229960003444 immunosuppressant agent Drugs 0.000 description 2
- 239000003018 immunosuppressive agent Substances 0.000 description 2
- 238000000338 in vitro Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 150000007529 inorganic bases Chemical class 0.000 description 2
- BCFGMOOMADDAQU-UHFFFAOYSA-N lapatinib Chemical compound O1C(CNCCS(=O)(=O)C)=CC=C1C1=CC=C(N=CN=C2NC=3C=C(Cl)C(OCC=4C=C(F)C=CC=4)=CC=3)C2=C1 BCFGMOOMADDAQU-UHFFFAOYSA-N 0.000 description 2
- 238000011068 loading method Methods 0.000 description 2
- 108010082117 matrigel Proteins 0.000 description 2
- 210000002901 mesenchymal stem cell Anatomy 0.000 description 2
- 210000003716 mesoderm Anatomy 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- RAHBGWKEPAQNFF-UHFFFAOYSA-N motesanib Chemical compound C=1C=C2C(C)(C)CNC2=CC=1NC(=O)C1=CC=CN=C1NCC1=CC=NC=C1 RAHBGWKEPAQNFF-UHFFFAOYSA-N 0.000 description 2
- 229940028444 muse Drugs 0.000 description 2
- FDMQDKQUTRLUBU-UHFFFAOYSA-N n-[3-[2-[4-(4-methylpiperazin-1-yl)anilino]thieno[3,2-d]pyrimidin-4-yl]oxyphenyl]prop-2-enamide Chemical compound C1CN(C)CCN1C(C=C1)=CC=C1NC1=NC(OC=2C=C(NC(=O)C=C)C=CC=2)=C(SC=C2)C2=N1 FDMQDKQUTRLUBU-UHFFFAOYSA-N 0.000 description 2
- 229950000778 olmutinib Drugs 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 150000007530 organic bases Chemical class 0.000 description 2
- 229960003278 osimertinib Drugs 0.000 description 2
- DUYJMQONPNNFPI-UHFFFAOYSA-N osimertinib Chemical compound COC1=CC(N(C)CCN(C)C)=C(NC(=O)C=C)C=C1NC1=NC=CC(C=2C3=CC=CC=C3N(C)C=2)=N1 DUYJMQONPNNFPI-UHFFFAOYSA-N 0.000 description 2
- 210000004681 ovum Anatomy 0.000 description 2
- XNGIFLGASWRNHJ-UHFFFAOYSA-N phthalic acid Chemical compound OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 229920002338 polyhydroxyethylmethacrylate Polymers 0.000 description 2
- PHXJVRSECIGDHY-UHFFFAOYSA-N ponatinib Chemical compound C1CN(C)CCN1CC(C(=C1)C(F)(F)F)=CC=C1NC(=O)C1=CC=C(C)C(C#CC=2N3N=CC=CC3=NC=2)=C1 PHXJVRSECIGDHY-UHFFFAOYSA-N 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- RXWNCPJZOCPEPQ-NVWDDTSBSA-N puromycin Chemical compound C1=CC(OC)=CC=C1C[C@H](N)C(=O)N[C@H]1[C@@H](O)[C@H](N2C3=NC=NC(=C3N=C2)N(C)C)O[C@@H]1CO RXWNCPJZOCPEPQ-NVWDDTSBSA-N 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 229960004836 regorafenib Drugs 0.000 description 2
- JAABVEXCGCXWRR-FBXFSONDSA-N rel-norcantharidin Chemical compound C1C[C@H]2[C@@H]3C(=O)OC(=O)[C@@H]3[C@@H]1O2 JAABVEXCGCXWRR-FBXFSONDSA-N 0.000 description 2
- 230000004044 response Effects 0.000 description 2
- 230000019491 signal transduction Effects 0.000 description 2
- 229950010611 sitravatinib Drugs 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000012453 solvate Substances 0.000 description 2
- 229960003787 sorafenib Drugs 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 230000008685 targeting Effects 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 2
- 239000012588 trypsin Substances 0.000 description 2
- 229960004441 tyrosine Drugs 0.000 description 2
- 235000019154 vitamin C Nutrition 0.000 description 2
- 239000011718 vitamin C Substances 0.000 description 2
- 150000003722 vitamin derivatives Chemical class 0.000 description 2
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 2
- 229930014124 (-)-epigallocatechin gallate Natural products 0.000 description 1
- 235000004911 (-)-epigallocatechin gallate Nutrition 0.000 description 1
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 1
- FSXCKIBROURMFT-VGSWGCGISA-N (3ar,6ar)-n-[4-(3-ethynylanilino)-7-methoxyquinazolin-6-yl]-1-methyl-2,3,3a,4,6,6a-hexahydropyrrolo[2,3-c]pyrrole-5-carboxamide Chemical compound C=12C=C(NC(=O)N3C[C@@H]4N(C)CC[C@@H]4C3)C(OC)=CC2=NC=NC=1NC1=CC=CC(C#C)=C1 FSXCKIBROURMFT-VGSWGCGISA-N 0.000 description 1
- KCOYQXZDFIIGCY-CZIZESTLSA-N (3e)-4-amino-5-fluoro-3-[5-(4-methylpiperazin-1-yl)-1,3-dihydrobenzimidazol-2-ylidene]quinolin-2-one Chemical compound C1CN(C)CCN1C1=CC=C(N\C(N2)=C/3C(=C4C(F)=CC=CC4=NC\3=O)N)C2=C1 KCOYQXZDFIIGCY-CZIZESTLSA-N 0.000 description 1
- NYNZQNWKBKUAII-KBXCAEBGSA-N (3s)-n-[5-[(2r)-2-(2,5-difluorophenyl)pyrrolidin-1-yl]pyrazolo[1,5-a]pyrimidin-3-yl]-3-hydroxypyrrolidine-1-carboxamide Chemical compound C1[C@@H](O)CCN1C(=O)NC1=C2N=C(N3[C@H](CCC3)C=3C(=CC=C(F)C=3)F)C=CN2N=C1 NYNZQNWKBKUAII-KBXCAEBGSA-N 0.000 description 1
- NXNQLECPAXXYTR-LCYFTJDESA-N (3z)-3-[(1-methylindol-3-yl)methylidene]-1h-pyrrolo[3,2-b]pyridin-2-one Chemical compound C12=CC=CC=C2N(C)C=C1\C=C/1C2=NC=CC=C2NC\1=O NXNQLECPAXXYTR-LCYFTJDESA-N 0.000 description 1
- AWDORCFLUJZUQS-ZDUSSCGKSA-N (S)-2-methyl-1-(4-methylisoquinoline-5-sulfonyl)-1,4-diazepane Chemical compound C[C@H]1CNCCCN1S(=O)(=O)C1=CC=CC2=CN=CC(C)=C12 AWDORCFLUJZUQS-ZDUSSCGKSA-N 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- KZKRRZFCAYOXQE-UHFFFAOYSA-N 1$l^{2}-azinane Chemical group C1CC[N]CC1 KZKRRZFCAYOXQE-UHFFFAOYSA-N 0.000 description 1
- GLBZSOQDAOLMGC-UHFFFAOYSA-N 1-(2-hydroxy-2-methylpropyl)-n-[5-(7-methoxyquinolin-4-yl)oxypyridin-2-yl]-5-methyl-3-oxo-2-phenylpyrazole-4-carboxamide Chemical compound C=1C=NC2=CC(OC)=CC=C2C=1OC(C=N1)=CC=C1NC(=O)C(C1=O)=C(C)N(CC(C)(C)O)N1C1=CC=CC=C1 GLBZSOQDAOLMGC-UHFFFAOYSA-N 0.000 description 1
- KXMZDGSRSGHMMK-VWLOTQADSA-N 1-(6,7-dihydro-5h-benzo[2,3]cyclohepta[2,4-d]pyridazin-3-yl)-3-n-[(7s)-7-pyrrolidin-1-yl-6,7,8,9-tetrahydro-5h-benzo[7]annulen-3-yl]-1,2,4-triazole-3,5-diamine Chemical compound N1([C@H]2CCC3=CC=C(C=C3CC2)NC=2N=C(N(N=2)C=2N=NC=3C4=CC=CC=C4CCCC=3C=2)N)CCCC1 KXMZDGSRSGHMMK-VWLOTQADSA-N 0.000 description 1
- LPFWVDIFUFFKJU-UHFFFAOYSA-N 1-[4-[4-(3,4-dichloro-2-fluoroanilino)-7-methoxyquinazolin-6-yl]oxypiperidin-1-yl]prop-2-en-1-one Chemical compound C=12C=C(OC3CCN(CC3)C(=O)C=C)C(OC)=CC2=NC=NC=1NC1=CC=C(Cl)C(Cl)=C1F LPFWVDIFUFFKJU-UHFFFAOYSA-N 0.000 description 1
- LNMRSSIMGCDUTP-UHFFFAOYSA-N 1-[5-tert-butyl-2-(4-methylphenyl)pyrazol-3-yl]-3-[[5-fluoro-2-[1-(2-hydroxyethyl)indazol-5-yl]oxyphenyl]methyl]urea Chemical compound C1=CC(C)=CC=C1N1C(NC(=O)NCC=2C(=CC=C(F)C=2)OC=2C=C3C=NN(CCO)C3=CC=2)=CC(C(C)(C)C)=N1 LNMRSSIMGCDUTP-UHFFFAOYSA-N 0.000 description 1
- WHTYLRLZUGABTR-UHFFFAOYSA-N 1-n'-(4-fluorophenyl)cyclopropane-1,1-dicarboxamide Chemical compound C=1C=C(F)C=CC=1NC(=O)C1(C(=O)N)CC1 WHTYLRLZUGABTR-UHFFFAOYSA-N 0.000 description 1
- FPYJSJDOHRDAMT-KQWNVCNZSA-N 1h-indole-5-sulfonamide, n-(3-chlorophenyl)-3-[[3,5-dimethyl-4-[(4-methyl-1-piperazinyl)carbonyl]-1h-pyrrol-2-yl]methylene]-2,3-dihydro-n-methyl-2-oxo-, (3z)- Chemical compound C=1C=C2NC(=O)\C(=C/C3=C(C(C(=O)N4CCN(C)CC4)=C(C)N3)C)C2=CC=1S(=O)(=O)N(C)C1=CC=CC(Cl)=C1 FPYJSJDOHRDAMT-KQWNVCNZSA-N 0.000 description 1
- BVYZDBLMCKSKAT-UHFFFAOYSA-N 2,2,3,3-tetrahexyldecanoic acid Chemical compound CCCCCCCC(CCCCCC)(CCCCCC)C(CCCCCC)(CCCCCC)C(O)=O BVYZDBLMCKSKAT-UHFFFAOYSA-N 0.000 description 1
- JJAXTFSPCLZPIW-UHFFFAOYSA-N 2-(2,3,4-trihydroxyphenyl)chromen-4-one Chemical compound OC1=C(O)C(O)=CC=C1C1=CC(=O)C2=CC=CC=C2O1 JJAXTFSPCLZPIW-UHFFFAOYSA-N 0.000 description 1
- NPVXOWLPOFYACO-UHFFFAOYSA-N 2-(butylamino)-4-[(4-hydroxycyclohexyl)amino]-n-[(4-imidazol-1-ylphenyl)methyl]pyrimidine-5-carboxamide Chemical compound C1CC(O)CCC1NC1=NC(NCCCC)=NC=C1C(=O)NCC(C=C1)=CC=C1N1C=CN=C1 NPVXOWLPOFYACO-UHFFFAOYSA-N 0.000 description 1
- KOQIAZNBAWFSQM-UHFFFAOYSA-N 2-[4-(3-ethynylanilino)-7-(2-methoxyethoxy)quinazolin-6-yl]oxyethanol Chemical compound C=12C=C(OCCO)C(OCCOC)=CC2=NC=NC=1NC1=CC=CC(C#C)=C1 KOQIAZNBAWFSQM-UHFFFAOYSA-N 0.000 description 1
- PDMUGYOXRHVNMO-UHFFFAOYSA-N 2-[4-[3-(6-quinolinylmethyl)-5-triazolo[4,5-b]pyrazinyl]-1-pyrazolyl]ethanol Chemical compound C1=NN(CCO)C=C1C1=CN=C(N=NN2CC=3C=C4C=CC=NC4=CC=3)C2=N1 PDMUGYOXRHVNMO-UHFFFAOYSA-N 0.000 description 1
- UYJNQQDJUOUFQJ-UHFFFAOYSA-N 2-[[5-chloro-2-[2-methoxy-4-(4-morpholinyl)anilino]-4-pyrimidinyl]amino]-N-methylbenzamide Chemical compound CNC(=O)C1=CC=CC=C1NC1=NC(NC=2C(=CC(=CC=2)N2CCOCC2)OC)=NC=C1Cl UYJNQQDJUOUFQJ-UHFFFAOYSA-N 0.000 description 1
- PFMPOBVAYMTUOX-GOSISDBHSA-N 2-amino-1-ethyl-7-[(3r)-3-hydroxy-4-methoxy-3-methylbut-1-ynyl]-n-methyl-4-oxo-1,8-naphthyridine-3-carboxamide Chemical compound C1=C(C#C[C@@](C)(O)COC)N=C2N(CC)C(N)=C(C(=O)NC)C(=O)C2=C1 PFMPOBVAYMTUOX-GOSISDBHSA-N 0.000 description 1
- CBIAKDAYHRWZCU-UHFFFAOYSA-N 2-bromo-4-[(6,7-dimethoxyquinazolin-4-yl)amino]phenol Chemical compound C=12C=C(OC)C(OC)=CC2=NC=NC=1NC1=CC=C(O)C(Br)=C1 CBIAKDAYHRWZCU-UHFFFAOYSA-N 0.000 description 1
- LIOLIMKSCNQPLV-UHFFFAOYSA-N 2-fluoro-n-methyl-4-[7-(quinolin-6-ylmethyl)imidazo[1,2-b][1,2,4]triazin-2-yl]benzamide Chemical compound C1=C(F)C(C(=O)NC)=CC=C1C1=NN2C(CC=3C=C4C=CC=NC4=CC=3)=CN=C2N=C1 LIOLIMKSCNQPLV-UHFFFAOYSA-N 0.000 description 1
- BSKHPKMHTQYZBB-UHFFFAOYSA-N 2-methylpyridine Chemical compound CC1=CC=CC=N1 BSKHPKMHTQYZBB-UHFFFAOYSA-N 0.000 description 1
- FGTCROZDHDSNIO-UHFFFAOYSA-N 3-(4-quinolinylmethylamino)-N-[4-(trifluoromethoxy)phenyl]-2-thiophenecarboxamide Chemical compound C1=CC(OC(F)(F)F)=CC=C1NC(=O)C1=C(NCC=2C3=CC=CC=C3N=CC=2)C=CS1 FGTCROZDHDSNIO-UHFFFAOYSA-N 0.000 description 1
- XYDNMOZJKOGZLS-NSHDSACASA-N 3-[(1s)-1-imidazo[1,2-a]pyridin-6-ylethyl]-5-(1-methylpyrazol-4-yl)triazolo[4,5-b]pyrazine Chemical compound N1=C2N([C@H](C3=CN4C=CN=C4C=C3)C)N=NC2=NC=C1C=1C=NN(C)C=1 XYDNMOZJKOGZLS-NSHDSACASA-N 0.000 description 1
- NHFDRBXTEDBWCZ-NTEUORMPSA-N 3-[2,4-dimethyl-5-[(e)-(2-oxo-1h-indol-3-ylidene)methyl]-1h-pyrrol-3-yl]propanoic acid Chemical compound OC(=O)CCC1=C(C)NC(\C=C\2C3=CC=CC=C3NC/2=O)=C1C NHFDRBXTEDBWCZ-NTEUORMPSA-N 0.000 description 1
- DORJQZDOULKINH-QNBGGDODSA-N 3-[4-[(2r)-2-aminopropoxy]phenyl]-n-[(1r)-1-(3-fluorophenyl)ethyl]imidazo[1,2-b]pyridazin-6-amine;hexanedioic acid Chemical compound OC(=O)CCCCC(O)=O.C1=CC(OC[C@H](N)C)=CC=C1C1=CN=C2N1N=C(N[C@H](C)C=1C=C(F)C=CC=1)C=C2 DORJQZDOULKINH-QNBGGDODSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- GSMUHCRTBHLSGL-UHFFFAOYSA-N 4,5-dimethyl-1h-pyrazole-3-carboxamide Chemical compound CC=1NN=C(C(N)=O)C=1C GSMUHCRTBHLSGL-UHFFFAOYSA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- LLSFXOUAPAZFIV-SNVBAGLBSA-N 4-[(1r)-1-aminoethyl]-n-pyridin-4-ylbenzamide Chemical compound C1=CC([C@H](N)C)=CC=C1C(=O)NC1=CC=NC=C1 LLSFXOUAPAZFIV-SNVBAGLBSA-N 0.000 description 1
- MJSHVHLADKXCML-UHFFFAOYSA-N 4-[2-(butylamino)-5-[4-[(4-methylpiperazin-1-yl)methyl]phenyl]pyrrolo[2,3-d]pyrimidin-7-yl]cyclohexan-1-ol Chemical compound C12=NC(NCCCC)=NC=C2C(C=2C=CC(CN3CCN(C)CC3)=CC=2)=CN1C1CCC(O)CC1 MJSHVHLADKXCML-UHFFFAOYSA-N 0.000 description 1
- SINQIEAULQKUPD-UHFFFAOYSA-N 4-[4-(6-methoxy-2-naphthalenyl)-2-(4-methylsulfinylphenyl)-1H-imidazol-5-yl]pyridine Chemical compound C1=CC2=CC(OC)=CC=C2C=C1C=1N=C(C=2C=CC(=CC=2)S(C)=O)NC=1C1=CC=NC=C1 SINQIEAULQKUPD-UHFFFAOYSA-N 0.000 description 1
- CDOVNWNANFFLFJ-UHFFFAOYSA-N 4-[6-[4-(1-piperazinyl)phenyl]-3-pyrazolo[1,5-a]pyrimidinyl]quinoline Chemical compound C1CNCCN1C1=CC=C(C2=CN3N=CC(=C3N=C2)C=2C3=CC=CC=C3N=CC=2)C=C1 CDOVNWNANFFLFJ-UHFFFAOYSA-N 0.000 description 1
- HSYSSKFCQHXOBP-UHFFFAOYSA-N 4-[[2-(butylamino)-5-[5-(morpholin-4-ylmethyl)pyridin-2-yl]pyrimidin-4-yl]amino]cyclohexan-1-ol Chemical compound N=1C(NCCCC)=NC=C(C=2N=CC(CN3CCOCC3)=CC=2)C=1NC1CCC(O)CC1 HSYSSKFCQHXOBP-UHFFFAOYSA-N 0.000 description 1
- QFCXANHHBCGMAS-UHFFFAOYSA-N 4-[[4-(4-chloroanilino)furo[2,3-d]pyridazin-7-yl]oxymethyl]-n-methylpyridine-2-carboxamide Chemical compound C1=NC(C(=O)NC)=CC(COC=2C=3OC=CC=3C(NC=3C=CC(Cl)=CC=3)=NN=2)=C1 QFCXANHHBCGMAS-UHFFFAOYSA-N 0.000 description 1
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 description 1
- WSTUJEXAPHIEIM-UHFFFAOYSA-N 4-fluoro-n-[6-[[4-(2-hydroxypropan-2-yl)piperidin-1-yl]methyl]-1-[4-(propan-2-ylcarbamoyl)cyclohexyl]benzimidazol-2-yl]benzamide Chemical compound C1CC(C(=O)NC(C)C)CCC1N(C=1C(=CC=C(CN2CCC(CC2)C(C)(C)O)C=1)N\1)C/1=N/C(=O)C1=CC=C(F)C=C1 WSTUJEXAPHIEIM-UHFFFAOYSA-N 0.000 description 1
- ZCCPLJOKGAACRT-UHFFFAOYSA-N 4-methyl-3-[[1-methyl-6-(3-pyridinyl)-4-pyrazolo[3,4-d]pyrimidinyl]amino]-N-[3-(trifluoromethyl)phenyl]benzamide Chemical compound CC1=CC=C(C(=O)NC=2C=C(C=CC=2)C(F)(F)F)C=C1NC(C=1C=NN(C)C=1N=1)=NC=1C1=CC=CN=C1 ZCCPLJOKGAACRT-UHFFFAOYSA-N 0.000 description 1
- GPSZYOIFQZPWEJ-UHFFFAOYSA-N 4-methyl-5-[2-(4-morpholin-4-ylanilino)pyrimidin-4-yl]-1,3-thiazol-2-amine Chemical compound N1=C(N)SC(C=2N=C(NC=3C=CC(=CC=3)N3CCOCC3)N=CC=2)=C1C GPSZYOIFQZPWEJ-UHFFFAOYSA-N 0.000 description 1
- NGFFVZQXSRKHBM-UHFFFAOYSA-N 5-[[1-[6-(trifluoromethyl)-1h-benzimidazol-2-yl]-1a,6b-dihydro-1h-cyclopropa[b][1]benzofuran-5-yl]oxy]-3,4-dihydro-1h-1,8-naphthyridin-2-one Chemical compound N1C(=O)CCC2=C1N=CC=C2OC(C=C1C23)=CC=C1OC3C2C1=NC2=CC=C(C(F)(F)F)C=C2N1 NGFFVZQXSRKHBM-UHFFFAOYSA-N 0.000 description 1
- SQDAZGGFXASXDW-UHFFFAOYSA-N 5-bromo-2-(trifluoromethoxy)pyridine Chemical compound FC(F)(F)OC1=CC=C(Br)C=N1 SQDAZGGFXASXDW-UHFFFAOYSA-N 0.000 description 1
- AILRADAXUVEEIR-UHFFFAOYSA-N 5-chloro-4-n-(2-dimethylphosphorylphenyl)-2-n-[2-methoxy-4-[4-(4-methylpiperazin-1-yl)piperidin-1-yl]phenyl]pyrimidine-2,4-diamine Chemical compound COC1=CC(N2CCC(CC2)N2CCN(C)CC2)=CC=C1NC(N=1)=NC=C(Cl)C=1NC1=CC=CC=C1P(C)(C)=O AILRADAXUVEEIR-UHFFFAOYSA-N 0.000 description 1
- DWHXUGDWKAIASB-CQSZACIVSA-N 6-[(1r)-1-[8-fluoro-6-(1-methylpyrazol-4-yl)-[1,2,4]triazolo[4,3-a]pyridin-3-yl]ethyl]-3-(2-methoxyethoxy)-1,6-naphthyridin-5-one Chemical compound C=1N2C([C@@H](C)N3C=CC4=NC=C(C=C4C3=O)OCCOC)=NN=C2C(F)=CC=1C=1C=NN(C)C=1 DWHXUGDWKAIASB-CQSZACIVSA-N 0.000 description 1
- QVMNYGOVNWWFKF-UHFFFAOYSA-N 6-[5-[(2-methylsulfonylethylamino)methyl]furan-2-yl]-n-[3-methyl-4-([1,2,4]triazolo[1,5-a]pyridin-7-yloxy)phenyl]quinazolin-4-amine Chemical compound C=1C=C(OC2=CC3=NC=NN3C=C2)C(C)=CC=1NC(C1=C2)=NC=NC1=CC=C2C1=CC=C(CNCCS(C)(=O)=O)O1 QVMNYGOVNWWFKF-UHFFFAOYSA-N 0.000 description 1
- RNCNPRCUHHDYPC-UHFFFAOYSA-N 6-[[6-(1-methylpyrazol-4-yl)imidazo[1,2-b]pyridazin-3-yl]methyl]quinoline Chemical compound C1=NN(C)C=C1C1=NN2C(CC=3C=C4C=CC=NC4=CC=3)=CN=C2C=C1 RNCNPRCUHHDYPC-UHFFFAOYSA-N 0.000 description 1
- KOAWAWHSMVKCON-UHFFFAOYSA-N 6-[difluoro-(6-pyridin-4-yl-[1,2,4]triazolo[4,3-b]pyridazin-3-yl)methyl]quinoline Chemical compound C=1C=C2N=CC=CC2=CC=1C(F)(F)C(N1N=2)=NN=C1C=CC=2C1=CC=NC=C1 KOAWAWHSMVKCON-UHFFFAOYSA-N 0.000 description 1
- JRWCBEOAFGHNNU-UHFFFAOYSA-N 6-[difluoro-[6-(1-methyl-4-pyrazolyl)-[1,2,4]triazolo[4,3-b]pyridazin-3-yl]methyl]quinoline Chemical compound C1=NN(C)C=C1C1=NN2C(C(F)(F)C=3C=C4C=CC=NC4=CC=3)=NN=C2C=C1 JRWCBEOAFGHNNU-UHFFFAOYSA-N 0.000 description 1
- QKDCLUARMDUUKN-XMMPIXPASA-N 6-ethyl-3-[4-[4-(4-methylpiperazin-1-yl)piperidin-1-yl]anilino]-5-[(3r)-1-prop-2-enoylpyrrolidin-3-yl]oxypyrazine-2-carboxamide Chemical compound N1=C(O[C@H]2CN(CC2)C(=O)C=C)C(CC)=NC(C(N)=O)=C1NC(C=C1)=CC=C1N(CC1)CCC1N1CCN(C)CC1 QKDCLUARMDUUKN-XMMPIXPASA-N 0.000 description 1
- ATEFPOUAMCWAQS-UHFFFAOYSA-N 7,8-dihydroxycoumarin Chemical compound C1=CC(=O)OC2=C(O)C(O)=CC=C21 ATEFPOUAMCWAQS-UHFFFAOYSA-N 0.000 description 1
- TVJRDCQUZMGBAB-UHFFFAOYSA-N 7-(2-hydroxypropan-2-yl)-4-[2-methyl-3-(4-oxoquinazolin-3-yl)phenyl]-9h-carbazole-1-carboxamide Chemical compound N1C2=CC(C(C)(C)O)=CC=C2C2=C1C(C(N)=O)=CC=C2C1=C(C)C(N2C(C3=CC=CC=C3N=C2)=O)=CC=C1 TVJRDCQUZMGBAB-UHFFFAOYSA-N 0.000 description 1
- HEAIZQNMNCHNFD-UHFFFAOYSA-N AMG-208 Chemical compound C=1C=NC2=CC(OC)=CC=C2C=1OCC(N1N=2)=NN=C1C=CC=2C1=CC=CC=C1 HEAIZQNMNCHNFD-UHFFFAOYSA-N 0.000 description 1
- 108010059616 Activins Proteins 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- 102100022014 Angiopoietin-1 receptor Human genes 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 101100481403 Bos taurus TIE1 gene Proteins 0.000 description 1
- 229940126010 CLN-081 Drugs 0.000 description 1
- RYBLECYFLJXEJX-UHFFFAOYSA-N CN1C=C(C=N1)C1=CN2C(C=C1)=NC=C2S(=O)(=O)N1N=CC2=NC=C(C=C12)C1=CN(C)N=C1 Chemical compound CN1C=C(C=N1)C1=CN2C(C=C1)=NC=C2S(=O)(=O)N1N=CC2=NC=C(C=C12)C1=CN(C)N=C1 RYBLECYFLJXEJX-UHFFFAOYSA-N 0.000 description 1
- LLVZBTWPGQVVLW-SNAWJCMRSA-N CP-724714 Chemical compound C12=CC(/C=C/CNC(=O)COC)=CC=C2N=CN=C1NC(C=C1C)=CC=C1OC1=CC=C(C)N=C1 LLVZBTWPGQVVLW-SNAWJCMRSA-N 0.000 description 1
- 101100381481 Caenorhabditis elegans baz-2 gene Proteins 0.000 description 1
- 206010048610 Cardiotoxicity Diseases 0.000 description 1
- 241000700198 Cavia Species 0.000 description 1
- 108010067225 Cell Adhesion Molecules Proteins 0.000 description 1
- 102000016289 Cell Adhesion Molecules Human genes 0.000 description 1
- 229920001287 Chondroitin sulfate Polymers 0.000 description 1
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 description 1
- 206010056370 Congestive cardiomyopathy Diseases 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 108020004414 DNA Proteins 0.000 description 1
- 238000000018 DNA microarray Methods 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 102100030074 Dickkopf-related protein 1 Human genes 0.000 description 1
- XBPCUCUWBYBCDP-UHFFFAOYSA-N Dicyclohexylamine Chemical compound C1CCCCC1NC1CCCCC1 XBPCUCUWBYBCDP-UHFFFAOYSA-N 0.000 description 1
- 201000010046 Dilated cardiomyopathy Diseases 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 238000002965 ELISA Methods 0.000 description 1
- 101150076616 EPHA2 gene Proteins 0.000 description 1
- 101150016325 EPHA3 gene Proteins 0.000 description 1
- 101150097734 EPHB2 gene Proteins 0.000 description 1
- 239000006145 Eagle's minimal essential medium Substances 0.000 description 1
- 108010014258 Elastin Proteins 0.000 description 1
- 102000016942 Elastin Human genes 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 102000050554 Eph Family Receptors Human genes 0.000 description 1
- 108091008815 Eph receptors Proteins 0.000 description 1
- 108010055211 EphA1 Receptor Proteins 0.000 description 1
- 108010055323 EphB4 Receptor Proteins 0.000 description 1
- 101150078651 Epha4 gene Proteins 0.000 description 1
- 101150025643 Epha5 gene Proteins 0.000 description 1
- 102100030322 Ephrin type-A receptor 1 Human genes 0.000 description 1
- 102100021600 Ephrin type-A receptor 10 Human genes 0.000 description 1
- 102100030340 Ephrin type-A receptor 2 Human genes 0.000 description 1
- 102100030324 Ephrin type-A receptor 3 Human genes 0.000 description 1
- 102100021616 Ephrin type-A receptor 4 Human genes 0.000 description 1
- 102100021605 Ephrin type-A receptor 5 Human genes 0.000 description 1
- 102100021604 Ephrin type-A receptor 6 Human genes 0.000 description 1
- 102100021606 Ephrin type-A receptor 7 Human genes 0.000 description 1
- 102100021601 Ephrin type-A receptor 8 Human genes 0.000 description 1
- 102100030779 Ephrin type-B receptor 1 Human genes 0.000 description 1
- 102100031968 Ephrin type-B receptor 2 Human genes 0.000 description 1
- 102100031982 Ephrin type-B receptor 3 Human genes 0.000 description 1
- 102100031983 Ephrin type-B receptor 4 Human genes 0.000 description 1
- 102100031984 Ephrin type-B receptor 6 Human genes 0.000 description 1
- 102100036725 Epithelial discoidin domain-containing receptor 1 Human genes 0.000 description 1
- 101710131668 Epithelial discoidin domain-containing receptor 1 Proteins 0.000 description 1
- 229940091518 ErbB antagonist Drugs 0.000 description 1
- 241000402754 Erythranthe moschata Species 0.000 description 1
- 102000016359 Fibronectins Human genes 0.000 description 1
- 102000016970 Follistatin Human genes 0.000 description 1
- 108010014612 Follistatin Proteins 0.000 description 1
- WMBWREPUVVBILR-UHFFFAOYSA-N GCG Natural products C=1C(O)=C(O)C(O)=CC=1C1OC2=CC(O)=CC(O)=C2CC1OC(=O)C1=CC(O)=C(O)C(O)=C1 WMBWREPUVVBILR-UHFFFAOYSA-N 0.000 description 1
- 102000027587 GPCRs class F Human genes 0.000 description 1
- 108091008884 GPCRs class F Proteins 0.000 description 1
- 101100445395 Gallus gallus EPHB5 gene Proteins 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 102000019058 Glycogen Synthase Kinase 3 beta Human genes 0.000 description 1
- 108010051975 Glycogen Synthase Kinase 3 beta Proteins 0.000 description 1
- 102100028972 HLA class I histocompatibility antigen, A alpha chain Human genes 0.000 description 1
- 102100028976 HLA class I histocompatibility antigen, B alpha chain Human genes 0.000 description 1
- 102100028971 HLA class I histocompatibility antigen, C alpha chain Human genes 0.000 description 1
- 108010075704 HLA-A Antigens Proteins 0.000 description 1
- 108010058607 HLA-B Antigens Proteins 0.000 description 1
- 108010052199 HLA-C Antigens Proteins 0.000 description 1
- 102000006354 HLA-DR Antigens Human genes 0.000 description 1
- 108010058597 HLA-DR Antigens Proteins 0.000 description 1
- 108010033040 Histones Proteins 0.000 description 1
- 102100024208 Homeobox protein MIXL1 Human genes 0.000 description 1
- 101000753291 Homo sapiens Angiopoietin-1 receptor Proteins 0.000 description 1
- 101000864646 Homo sapiens Dickkopf-related protein 1 Proteins 0.000 description 1
- 101000898673 Homo sapiens Ephrin type-A receptor 10 Proteins 0.000 description 1
- 101000898696 Homo sapiens Ephrin type-A receptor 6 Proteins 0.000 description 1
- 101000898708 Homo sapiens Ephrin type-A receptor 7 Proteins 0.000 description 1
- 101000898676 Homo sapiens Ephrin type-A receptor 8 Proteins 0.000 description 1
- 101001064150 Homo sapiens Ephrin type-B receptor 1 Proteins 0.000 description 1
- 101001064458 Homo sapiens Ephrin type-B receptor 3 Proteins 0.000 description 1
- 101001064451 Homo sapiens Ephrin type-B receptor 6 Proteins 0.000 description 1
- 101001052462 Homo sapiens Homeobox protein MIXL1 Proteins 0.000 description 1
- 101001103039 Homo sapiens Inactive tyrosine-protein kinase transmembrane receptor ROR1 Proteins 0.000 description 1
- 101000819074 Homo sapiens Transcription factor GATA-4 Proteins 0.000 description 1
- 101000851334 Homo sapiens Troponin I, cardiac muscle Proteins 0.000 description 1
- 101001103033 Homo sapiens Tyrosine-protein kinase transmembrane receptor ROR2 Proteins 0.000 description 1
- 101000851030 Homo sapiens Vascular endothelial growth factor receptor 3 Proteins 0.000 description 1
- ZGSXEXBYLJIOGF-ALFLXDJESA-N IWR-1-endo Chemical compound C=1C=CC2=CC=CN=C2C=1NC(=O)C(C=C1)=CC=C1N1C(=O)[C@@H]2[C@H](C=C3)C[C@H]3[C@@H]2C1=O ZGSXEXBYLJIOGF-ALFLXDJESA-N 0.000 description 1
- 102100039615 Inactive tyrosine-protein kinase transmembrane receptor ROR1 Human genes 0.000 description 1
- 102100026818 Inhibin beta E chain Human genes 0.000 description 1
- 108090000862 Ion Channels Proteins 0.000 description 1
- 102000004310 Ion Channels Human genes 0.000 description 1
- 108700021430 Kruppel-Like Factor 4 Proteins 0.000 description 1
- AHLPHDHHMVZTML-BYPYZUCNSA-N L-Ornithine Chemical compound NCCC[C@H](N)C(O)=O AHLPHDHHMVZTML-BYPYZUCNSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- 235000000069 L-ascorbic acid Nutrition 0.000 description 1
- MIJPAVRNWPDMOR-ZAFYKAAXSA-N L-ascorbic acid 2-phosphate Chemical compound OC[C@H](O)[C@H]1OC(=O)C(OP(O)(O)=O)=C1O MIJPAVRNWPDMOR-ZAFYKAAXSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- 239000005411 L01XE02 - Gefitinib Substances 0.000 description 1
- 239000002136 L01XE07 - Lapatinib Substances 0.000 description 1
- UCEQXRCJXIVODC-PMACEKPBSA-N LSM-1131 Chemical compound C1CCC2=CC=CC3=C2N1C=C3[C@@H]1C(=O)NC(=O)[C@H]1C1=CNC2=CC=CC=C12 UCEQXRCJXIVODC-PMACEKPBSA-N 0.000 description 1
- JVTAAEKCZFNVCJ-UHFFFAOYSA-M Lactate Chemical compound CC(O)C([O-])=O JVTAAEKCZFNVCJ-UHFFFAOYSA-M 0.000 description 1
- 108010052014 Liberase Proteins 0.000 description 1
- 241000234435 Lilium Species 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 108010018650 MEF2 Transcription Factors Proteins 0.000 description 1
- 241001465754 Metazoa Species 0.000 description 1
- 101100478674 Mus musculus Stk3 gene Proteins 0.000 description 1
- 102100038895 Myc proto-oncogene protein Human genes 0.000 description 1
- 101710135898 Myc proto-oncogene protein Proteins 0.000 description 1
- 102100039229 Myocyte-specific enhancer factor 2C Human genes 0.000 description 1
- FOFDIMHVKGYHRU-UHFFFAOYSA-N N-(1,3-benzodioxol-5-ylmethyl)-4-(4-benzofuro[3,2-d]pyrimidinyl)-1-piperazinecarbothioamide Chemical compound C12=CC=CC=C2OC2=C1N=CN=C2N(CC1)CCN1C(=S)NCC1=CC=C(OCO2)C2=C1 FOFDIMHVKGYHRU-UHFFFAOYSA-N 0.000 description 1
- YHUIUSRCUKUUQA-UHFFFAOYSA-N N-(4-chloro-2-fluorophenyl)-6,7-dimethoxy-4-quinazolinamine Chemical compound C=12C=C(OC)C(OC)=CC2=NC=NC=1NC1=CC=C(Cl)C=C1F YHUIUSRCUKUUQA-UHFFFAOYSA-N 0.000 description 1
- WRKPZSMRWPJJDH-UHFFFAOYSA-N N-(6-methyl-1,3-benzothiazol-2-yl)-2-[(4-oxo-3-phenyl-6,7-dihydrothieno[3,2-d]pyrimidin-2-yl)thio]acetamide Chemical compound S1C2=CC(C)=CC=C2N=C1NC(=O)CSC1=NC=2CCSC=2C(=O)N1C1=CC=CC=C1 WRKPZSMRWPJJDH-UHFFFAOYSA-N 0.000 description 1
- GUYKCXXNIKKSBC-UHFFFAOYSA-N N-[2-chloro-5-[4-(3-chloro-4-fluoroanilino)quinazolin-6-yl]pyridin-3-yl]methanesulfonamide Chemical compound ClC1=NC=C(C=C1NS(=O)(=O)C)C=1C=C2C(=NC=NC2=CC=1)NC1=CC(=C(C=C1)F)Cl GUYKCXXNIKKSBC-UHFFFAOYSA-N 0.000 description 1
- APHGZZPEOCCYNO-UHFFFAOYSA-N N-[3-[[5-chloro-2-[4-(4-methyl-1-piperazinyl)anilino]-4-pyrimidinyl]oxy]phenyl]-2-propenamide Chemical compound C1CN(C)CCN1C(C=C1)=CC=C1NC1=NC=C(Cl)C(OC=2C=C(NC(=O)C=C)C=CC=2)=N1 APHGZZPEOCCYNO-UHFFFAOYSA-N 0.000 description 1
- MVZGYPSXNDCANY-UHFFFAOYSA-N N-[4-[3-chloro-4-[(3-fluorophenyl)methoxy]anilino]-6-quinazolinyl]-2-propenamide Chemical compound FC1=CC=CC(COC=2C(=CC(NC=3C4=CC(NC(=O)C=C)=CC=C4N=CN=3)=CC=2)Cl)=C1 MVZGYPSXNDCANY-UHFFFAOYSA-N 0.000 description 1
- XKFTZKGMDDZMJI-HSZRJFAPSA-N N-[5-[(2R)-2-methoxy-1-oxo-2-phenylethyl]-4,6-dihydro-1H-pyrrolo[3,4-c]pyrazol-3-yl]-4-(4-methyl-1-piperazinyl)benzamide Chemical compound O=C([C@H](OC)C=1C=CC=CC=1)N(CC=12)CC=1NN=C2NC(=O)C(C=C1)=CC=C1N1CCN(C)CC1 XKFTZKGMDDZMJI-HSZRJFAPSA-N 0.000 description 1
- DOEOECWDNSEFDN-UHFFFAOYSA-N N-[5-[[4-(1-cyclopropylindol-3-yl)pyrimidin-2-yl]amino]-2-[2-(dimethylamino)ethyl-methylamino]-4-methoxyphenyl]prop-2-enamide Chemical compound C1(CC1)N1C=C(C2=CC=CC=C12)C1=NC(=NC=C1)NC=1C(=CC(=C(C=1)NC(C=C)=O)N(C)CCN(C)C)OC DOEOECWDNSEFDN-UHFFFAOYSA-N 0.000 description 1
- RRMJMHOQSALEJJ-UHFFFAOYSA-N N-[5-[[4-[4-[(dimethylamino)methyl]-3-phenylpyrazol-1-yl]pyrimidin-2-yl]amino]-4-methoxy-2-morpholin-4-ylphenyl]prop-2-enamide Chemical compound CN(C)CC=1C(=NN(C=1)C1=NC(=NC=C1)NC=1C(=CC(=C(C=1)NC(C=C)=O)N1CCOCC1)OC)C1=CC=CC=C1 RRMJMHOQSALEJJ-UHFFFAOYSA-N 0.000 description 1
- BTYYWOYVBXILOJ-UHFFFAOYSA-N N-{4-[(3-bromophenyl)amino]quinazolin-6-yl}but-2-ynamide Chemical compound C12=CC(NC(=O)C#CC)=CC=C2N=CN=C1NC1=CC=CC(Br)=C1 BTYYWOYVBXILOJ-UHFFFAOYSA-N 0.000 description 1
- ARQFIGQZBRLCPR-UHFFFAOYSA-N NC(COC(C=C(C=C1)C2=C3N=CC(C4=CNN=C4)=CN3N=C2)=C1C#N)C1=CC=CC=C1 Chemical compound NC(COC(C=C(C=C1)C2=C3N=CC(C4=CNN=C4)=CN3N=C2)=C1C#N)C1=CC=CC=C1 ARQFIGQZBRLCPR-UHFFFAOYSA-N 0.000 description 1
- MKCYPWYURWOKST-INIZCTEOSA-N NC1=NC=NC2=C1C(=C1C(=C[C@@H](CN21)NC(C=C)=O)C)C=1C=NC2=CC=CC=C2C=1 Chemical compound NC1=NC=NC2=C1C(=C1C(=C[C@@H](CN21)NC(C=C)=O)C)C=1C=NC2=CC=CC=C2C=1 MKCYPWYURWOKST-INIZCTEOSA-N 0.000 description 1
- 101150111783 NTRK1 gene Proteins 0.000 description 1
- 101150117329 NTRK3 gene Proteins 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 108010025020 Nerve Growth Factor Proteins 0.000 description 1
- 102000007072 Nerve Growth Factors Human genes 0.000 description 1
- 102000048238 Neuregulin-1 Human genes 0.000 description 1
- 108090000556 Neuregulin-1 Proteins 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 101150114527 Nkx2-5 gene Proteins 0.000 description 1
- 101150056950 Ntrk2 gene Proteins 0.000 description 1
- 108091028043 Nucleic acid sequence Proteins 0.000 description 1
- AHLPHDHHMVZTML-UHFFFAOYSA-N Orn-delta-NH2 Natural products NCCCC(N)C(O)=O AHLPHDHHMVZTML-UHFFFAOYSA-N 0.000 description 1
- UTJLXEIPEHZYQJ-UHFFFAOYSA-N Ornithine Natural products OC(=O)C(C)CCCN UTJLXEIPEHZYQJ-UHFFFAOYSA-N 0.000 description 1
- HTUBKQUPEREOGA-UHFFFAOYSA-N PD 168393 Chemical compound BrC1=CC=CC(NC=2C3=CC(NC(=O)C=C)=CC=C3N=CN=2)=C1 HTUBKQUPEREOGA-UHFFFAOYSA-N 0.000 description 1
- LSPANGZZENHZNJ-UHFFFAOYSA-N PD-153035 Chemical compound C=12C=C(OC)C(OC)=CC2=NC=NC=1NC1=CC=CC(Br)=C1 LSPANGZZENHZNJ-UHFFFAOYSA-N 0.000 description 1
- ZJOKWAWPAPMNIM-UHFFFAOYSA-N PD-153035 hydrochloride Chemical compound Cl.C=12C=C(OC)C(OC)=CC2=NC=NC=1NC1=CC=CC(Br)=C1 ZJOKWAWPAPMNIM-UHFFFAOYSA-N 0.000 description 1
- OYONTEXKYJZFHA-SSHUPFPWSA-N PHA-665752 Chemical compound CC=1C(C(=O)N2[C@H](CCC2)CN2CCCC2)=C(C)NC=1\C=C(C1=C2)/C(=O)NC1=CC=C2S(=O)(=O)CC1=C(Cl)C=CC=C1Cl OYONTEXKYJZFHA-SSHUPFPWSA-N 0.000 description 1
- 235000021314 Palmitic acid Nutrition 0.000 description 1
- 241000282579 Pan Species 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- BELBBZDIHDAJOR-UHFFFAOYSA-N Phenolsulfonephthalein Chemical compound C1=CC(O)=CC=C1C1(C=2C=CC(O)=CC=2)C2=CC=CC=C2S(=O)(=O)O1 BELBBZDIHDAJOR-UHFFFAOYSA-N 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- 102100026547 Platelet-derived growth factor receptor beta Human genes 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 241000282405 Pongo abelii Species 0.000 description 1
- HCBIBCJNVBAKAB-UHFFFAOYSA-N Procaine hydrochloride Chemical compound Cl.CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 HCBIBCJNVBAKAB-UHFFFAOYSA-N 0.000 description 1
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 1
- 108010067787 Proteoglycans Proteins 0.000 description 1
- 102000016611 Proteoglycans Human genes 0.000 description 1
- SOLICHUQXFAOEP-YDIXZRNLSA-N Pulsatilla saponin D Chemical compound O[C@@H]1[C@H](O)[C@@H](O)[C@H](C)O[C@H]1O[C@H]1[C@H](O[C@@H]2[C@@]([C@H]3[C@]([C@@H]4[C@@]([C@@]5(CC[C@]6(CCC(C)(C)C[C@H]6C5=CC4)C(O)=O)C)(C)CC3)(C)CC2)(C)CO)OC[C@H](O[C@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)O)[C@@H]1O SOLICHUQXFAOEP-YDIXZRNLSA-N 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 101100372762 Rattus norvegicus Flt1 gene Proteins 0.000 description 1
- 101100247004 Rattus norvegicus Qsox1 gene Proteins 0.000 description 1
- 101710100969 Receptor tyrosine-protein kinase erbB-3 Proteins 0.000 description 1
- 102100029986 Receptor tyrosine-protein kinase erbB-3 Human genes 0.000 description 1
- 102100029981 Receptor tyrosine-protein kinase erbB-4 Human genes 0.000 description 1
- 101710100963 Receptor tyrosine-protein kinase erbB-4 Proteins 0.000 description 1
- BCZUAADEACICHN-UHFFFAOYSA-N SGX-523 Chemical compound C1=NN(C)C=C1C1=NN2C(SC=3C=C4C=CC=NC4=CC=3)=NN=C2C=C1 BCZUAADEACICHN-UHFFFAOYSA-N 0.000 description 1
- 101150086694 SLC22A3 gene Proteins 0.000 description 1
- 101100174722 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) GAA1 gene Proteins 0.000 description 1
- 102100034201 Sclerostin Human genes 0.000 description 1
- 108050006698 Sclerostin Proteins 0.000 description 1
- 238000012300 Sequence Analysis Methods 0.000 description 1
- 108010071390 Serum Albumin Proteins 0.000 description 1
- 102000007562 Serum Albumin Human genes 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 241000282898 Sus scrofa Species 0.000 description 1
- 108091005729 TAM receptors Proteins 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- 108091023040 Transcription factor Proteins 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 102100021380 Transcription factor GATA-4 Human genes 0.000 description 1
- 101710150448 Transcriptional regulator Myc Proteins 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- 102000013394 Troponin I Human genes 0.000 description 1
- 108010065729 Troponin I Proteins 0.000 description 1
- 102100036859 Troponin I, cardiac muscle Human genes 0.000 description 1
- 102100039616 Tyrosine-protein kinase transmembrane receptor ROR2 Human genes 0.000 description 1
- 102000016663 Vascular Endothelial Growth Factor Receptor-3 Human genes 0.000 description 1
- 108010031318 Vitronectin Proteins 0.000 description 1
- 102100035140 Vitronectin Human genes 0.000 description 1
- 230000004156 Wnt signaling pathway Effects 0.000 description 1
- KLGQSVMIPOVQAX-UHFFFAOYSA-N XAV939 Chemical compound N=1C=2CCSCC=2C(O)=NC=1C1=CC=C(C(F)(F)F)C=C1 KLGQSVMIPOVQAX-UHFFFAOYSA-N 0.000 description 1
- 101100460507 Xenopus laevis nkx-2.5 gene Proteins 0.000 description 1
- LUJZZYWHBDHDQX-QFIPXVFZSA-N [(3s)-morpholin-3-yl]methyl n-[4-[[1-[(3-fluorophenyl)methyl]indazol-5-yl]amino]-5-methylpyrrolo[2,1-f][1,2,4]triazin-6-yl]carbamate Chemical compound C=1N2N=CN=C(NC=3C=C4C=NN(CC=5C=C(F)C=CC=5)C4=CC=3)C2=C(C)C=1NC(=O)OC[C@@H]1COCCN1 LUJZZYWHBDHDQX-QFIPXVFZSA-N 0.000 description 1
- MXDSJQHFFDGFDK-CYBMUJFWSA-N [4-(3-chloro-2-fluoroanilino)-7-methoxyquinazolin-6-yl] (2r)-2,4-dimethylpiperazine-1-carboxylate Chemical compound C=12C=C(OC(=O)N3[C@@H](CN(C)CC3)C)C(OC)=CC2=NC=NC=1NC1=CC=CC(Cl)=C1F MXDSJQHFFDGFDK-CYBMUJFWSA-N 0.000 description 1
- AMJJLDJPDLKNJA-UHFFFAOYSA-N [hydroxy(naphthalen-2-yl)methyl]phosphonic acid Chemical compound C1=CC=CC2=CC(C(O)P(O)(O)=O)=CC=C21 AMJJLDJPDLKNJA-UHFFFAOYSA-N 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 239000000488 activin Substances 0.000 description 1
- 238000004115 adherent culture Methods 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- 210000001789 adipocyte Anatomy 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 229960001686 afatinib Drugs 0.000 description 1
- ULXXDDBFHOBEHA-CWDCEQMOSA-N afatinib Chemical compound N1=CN=C2C=C(O[C@@H]3COCC3)C(NC(=O)/C=C/CN(C)C)=CC2=C1NC1=CC=C(F)C(Cl)=C1 ULXXDDBFHOBEHA-CWDCEQMOSA-N 0.000 description 1
- USNRYVNRPYXCSP-JUGPPOIOSA-N afatinib dimaleate Chemical compound OC(=O)\C=C/C(O)=O.OC(=O)\C=C/C(O)=O.N1=CN=C2C=C(O[C@@H]3COCC3)C(NC(=O)/C=C/CN(C)C)=CC2=C1NC1=CC=C(F)C(Cl)=C1 USNRYVNRPYXCSP-JUGPPOIOSA-N 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 125000003545 alkoxy group Chemical group 0.000 description 1
- 238000011316 allogeneic transplantation Methods 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- AZDRQVAHHNSJOQ-UHFFFAOYSA-N alumane Chemical class [AlH3] AZDRQVAHHNSJOQ-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 230000033115 angiogenesis Effects 0.000 description 1
- 210000004102 animal cell Anatomy 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 239000002246 antineoplastic agent Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000006708 antioxidants Nutrition 0.000 description 1
- 229960003982 apatinib Drugs 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 239000007900 aqueous suspension Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 239000005667 attractant Substances 0.000 description 1
- 229960000686 benzalkonium chloride Drugs 0.000 description 1
- SRSXLGNVWSONIS-UHFFFAOYSA-N benzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-N 0.000 description 1
- 229940092714 benzenesulfonic acid Drugs 0.000 description 1
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 210000004703 blastocyst inner cell mass Anatomy 0.000 description 1
- 210000001109 blastomere Anatomy 0.000 description 1
- 210000004271 bone marrow stromal cell Anatomy 0.000 description 1
- 210000004958 brain cell Anatomy 0.000 description 1
- 229950004272 brigatinib Drugs 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 229950005852 capmatinib Drugs 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 231100000259 cardiotoxicity Toxicity 0.000 description 1
- 230000021164 cell adhesion Effects 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 239000006143 cell culture medium Substances 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- VERWOWGGCGHDQE-UHFFFAOYSA-N ceritinib Chemical compound CC=1C=C(NC=2N=C(NC=3C(=CC=CC=3)S(=O)(=O)C(C)C)C(Cl)=CN=2)C(OC(C)C)=CC=1C1CCNCC1 VERWOWGGCGHDQE-UHFFFAOYSA-N 0.000 description 1
- 229960005395 cetuximab Drugs 0.000 description 1
- USVCWSAJUAARAL-MEMLXQNLSA-N chembl551064 Chemical compound C1=2C(N)=NC=NC=2N([C@@H]2C[C@H](C2)N2CCC2)C=C1C(C=1)=CC=CC=1OCC1=CC=CC=C1 USVCWSAJUAARAL-MEMLXQNLSA-N 0.000 description 1
- 230000031902 chemoattractant activity Effects 0.000 description 1
- 229940059329 chondroitin sulfate Drugs 0.000 description 1
- 102000006533 chordin Human genes 0.000 description 1
- 108010008846 chordin Proteins 0.000 description 1
- 229910052804 chromium Inorganic materials 0.000 description 1
- 239000011651 chromium Substances 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 238000002288 cocrystallisation Methods 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 229950002966 danusertib Drugs 0.000 description 1
- YBGKGTOOPNQOKH-UHFFFAOYSA-N daphnetin Natural products OC1=CC=CC2=C1OC(=O)C=C2O YBGKGTOOPNQOKH-UHFFFAOYSA-N 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000007547 defect Effects 0.000 description 1
- 210000005258 dental pulp stem cell Anatomy 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000035475 disorder Diseases 0.000 description 1
- 229950005778 dovitinib Drugs 0.000 description 1
- 238000007877 drug screening Methods 0.000 description 1
- 229940121552 dubermatinib Drugs 0.000 description 1
- 229940121647 egfr inhibitor Drugs 0.000 description 1
- 229920002549 elastin Polymers 0.000 description 1
- 230000005611 electricity Effects 0.000 description 1
- 238000006911 enzymatic reaction Methods 0.000 description 1
- 229940088598 enzyme Drugs 0.000 description 1
- 239000002532 enzyme inhibitor Substances 0.000 description 1
- 229940125532 enzyme inhibitor Drugs 0.000 description 1
- 108060002566 ephrin Proteins 0.000 description 1
- 102000012803 ephrin Human genes 0.000 description 1
- VFSWRBJYBQXUTE-UHFFFAOYSA-N epi-Gallocatechin 3-O-gallate Natural products Oc1ccc2C(=O)C(OC(=O)c3cc(O)c(O)c(O)c3)C(Oc2c1)c4cc(O)c(O)c(O)c4 VFSWRBJYBQXUTE-UHFFFAOYSA-N 0.000 description 1
- 102000052116 epidermal growth factor receptor activity proteins Human genes 0.000 description 1
- 108700015053 epidermal growth factor receptor activity proteins Proteins 0.000 description 1
- 210000000981 epithelium Anatomy 0.000 description 1
- GTTBEUCJPZQMDZ-UHFFFAOYSA-N erlotinib hydrochloride Chemical compound [H+].[Cl-].C=12C=C(OCCOC)C(OCCOC)=CC2=NC=NC=1NC1=CC=CC(C#C)=C1 GTTBEUCJPZQMDZ-UHFFFAOYSA-N 0.000 description 1
- 239000003797 essential amino acid Substances 0.000 description 1
- 235000020776 essential amino acid Nutrition 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 210000002907 exocrine cell Anatomy 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 235000011087 fumaric acid Nutrition 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- 229960002584 gefitinib Drugs 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 210000001368 germline stem cell Anatomy 0.000 description 1
- GYQYAJJFPNQOOW-UHFFFAOYSA-N gilteritinib Chemical compound N1=C(NC2CCOCC2)C(CC)=NC(C(N)=O)=C1NC(C=C1OC)=CC=C1N(CC1)CCC1N1CCN(C)CC1 GYQYAJJFPNQOOW-UHFFFAOYSA-N 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 229930182478 glucoside Natural products 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 229940093915 gynecological organic acid Drugs 0.000 description 1
- 210000002768 hair cell Anatomy 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 1
- 210000003494 hepatocyte Anatomy 0.000 description 1
- 229940121372 histone deacetylase inhibitor Drugs 0.000 description 1
- 239000003276 histone deacetylase inhibitor Substances 0.000 description 1
- 229940088597 hormone Drugs 0.000 description 1
- 239000005556 hormone Substances 0.000 description 1
- 210000005260 human cell Anatomy 0.000 description 1
- 229920002674 hyaluronan Polymers 0.000 description 1
- 229960003160 hyaluronic acid Drugs 0.000 description 1
- 229950007440 icotinib Drugs 0.000 description 1
- QQLKULDARVNMAL-UHFFFAOYSA-N icotinib Chemical compound C#CC1=CC=CC(NC=2C3=CC=4OCCOCCOCCOC=4C=C3N=CN=2)=C1 QQLKULDARVNMAL-UHFFFAOYSA-N 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 238000010324 immunological assay Methods 0.000 description 1
- 238000012744 immunostaining Methods 0.000 description 1
- 230000001861 immunosuppressant effect Effects 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 230000001976 improved effect Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 239000000644 isotonic solution Substances 0.000 description 1
- 229960004891 lapatinib Drugs 0.000 description 1
- 229950003970 larotrectinib Drugs 0.000 description 1
- 229950009640 lazertinib Drugs 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 229950001762 linsitinib Drugs 0.000 description 1
- PKCDDUHJAFVJJB-VLZXCDOPSA-N linsitinib Chemical compound C1[C@](C)(O)C[C@@H]1C1=NC(C=2C=C3N=C(C=CC3=CC=2)C=2C=CC=CC=2)=C2N1C=CN=C2N PKCDDUHJAFVJJB-VLZXCDOPSA-N 0.000 description 1
- 210000005265 lung cell Anatomy 0.000 description 1
- 210000004698 lymphocyte Anatomy 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 230000035800 maturation Effects 0.000 description 1
- 238000000691 measurement method Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 238000002493 microarray Methods 0.000 description 1
- 239000007758 minimum essential medium Substances 0.000 description 1
- 229960004857 mitomycin Drugs 0.000 description 1
- 230000001483 mobilizing effect Effects 0.000 description 1
- 229950003968 motesanib Drugs 0.000 description 1
- 229940124303 multikinase inhibitor Drugs 0.000 description 1
- 210000000663 muscle cell Anatomy 0.000 description 1
- 210000003098 myoblast Anatomy 0.000 description 1
- 208000031225 myocardial ischemia Diseases 0.000 description 1
- ACTNHJDHMQSOGL-UHFFFAOYSA-N n',n'-dibenzylethane-1,2-diamine Chemical compound C=1C=CC=CC=1CN(CCN)CC1=CC=CC=C1 ACTNHJDHMQSOGL-UHFFFAOYSA-N 0.000 description 1
- ONDPWWDPQDCQNJ-UHFFFAOYSA-N n-(3,3-dimethyl-1,2-dihydroindol-6-yl)-2-(pyridin-4-ylmethylamino)pyridine-3-carboxamide;phosphoric acid Chemical compound OP(O)(O)=O.OP(O)(O)=O.C=1C=C2C(C)(C)CNC2=CC=1NC(=O)C1=CC=CN=C1NCC1=CC=NC=C1 ONDPWWDPQDCQNJ-UHFFFAOYSA-N 0.000 description 1
- QUINXWLATMJDQF-UHFFFAOYSA-N n-(3-chloro-4-fluorophenyl)-7-methoxy-6-(3-morpholin-4-ylpropoxy)quinazolin-4-amine;hydrochloride Chemical compound Cl.C=12C=C(OCCCN3CCOCC3)C(OC)=CC2=NC=NC=1NC1=CC=C(F)C(Cl)=C1 QUINXWLATMJDQF-UHFFFAOYSA-N 0.000 description 1
- AZUQEHCMDUSRLH-UHFFFAOYSA-N n-(4-chlorophenyl)-4-(pyridin-4-ylmethyl)phthalazin-1-amine;dihydrochloride Chemical compound Cl.Cl.C1=CC(Cl)=CC=C1NC(C1=CC=CC=C11)=NN=C1CC1=CC=NC=C1 AZUQEHCMDUSRLH-UHFFFAOYSA-N 0.000 description 1
- WQEPLUUGTLDZJY-UHFFFAOYSA-N n-Pentadecanoic acid Natural products CCCCCCCCCCCCCCC(O)=O WQEPLUUGTLDZJY-UHFFFAOYSA-N 0.000 description 1
- JJEDWBQZCRESJL-DEDYPNTBSA-N n-[(e)-(5-methylfuran-2-yl)methylideneamino]-2-phenoxybenzamide Chemical compound O1C(C)=CC=C1\C=N\NC(=O)C1=CC=CC=C1OC1=CC=CC=C1 JJEDWBQZCRESJL-DEDYPNTBSA-N 0.000 description 1
- OQWZIAVXCYIZNN-UHFFFAOYSA-N n-[2-[2-(dimethylamino)ethoxy]-4-(1h-pyrazol-4-yl)phenyl]-2,3-dihydro-1,4-benzodioxine-3-carboxamide Chemical compound C=1C=C(NC(=O)C2OC3=CC=CC=C3OC2)C(OCCN(C)C)=CC=1C=1C=NNC=1 OQWZIAVXCYIZNN-UHFFFAOYSA-N 0.000 description 1
- IQNVEOMHJHBNHC-UHFFFAOYSA-N n-[2-[2-(dimethylamino)ethyl-methylamino]-5-[[4-(1h-indol-3-yl)pyrimidin-2-yl]amino]-4-methoxyphenyl]prop-2-enamide Chemical compound COC1=CC(N(C)CCN(C)C)=C(NC(=O)C=C)C=C1NC1=NC=CC(C=2C3=CC=CC=C3NC=2)=N1 IQNVEOMHJHBNHC-UHFFFAOYSA-N 0.000 description 1
- ZYQXEVJIFYIBHZ-UHFFFAOYSA-N n-[2-[4-[3-chloro-4-[3-(trifluoromethyl)phenoxy]anilino]pyrrolo[3,2-d]pyrimidin-5-yl]ethyl]-3-hydroxy-3-methylbutanamide Chemical compound C=12N(CCNC(=O)CC(C)(O)C)C=CC2=NC=NC=1NC(C=C1Cl)=CC=C1OC1=CC=CC(C(F)(F)F)=C1 ZYQXEVJIFYIBHZ-UHFFFAOYSA-N 0.000 description 1
- YOVNFNXUCOWYSG-UHFFFAOYSA-N n-[3-[2-(4-amino-1,2,5-oxadiazol-3-yl)-1-ethylimidazo[4,5-c]pyridin-6-yl]oxyphenyl]-4-(2-morpholin-4-ylethoxy)benzamide Chemical compound C1=C2N(CC)C(C=3C(=NON=3)N)=NC2=CN=C1OC(C=1)=CC=CC=1NC(=O)C(C=C1)=CC=C1OCCN1CCOCC1 YOVNFNXUCOWYSG-UHFFFAOYSA-N 0.000 description 1
- KIISCIGBPUVZBF-UHFFFAOYSA-N n-[3-[5-chloro-2-[4-(4-methylpiperazin-1-yl)anilino]pyrimidin-4-yl]sulfanylphenyl]prop-2-enamide Chemical compound C1CN(C)CCN1C(C=C1)=CC=C1NC1=NC=C(Cl)C(SC=2C=C(NC(=O)C=C)C=CC=2)=N1 KIISCIGBPUVZBF-UHFFFAOYSA-N 0.000 description 1
- YOHYSYJDKVYCJI-UHFFFAOYSA-N n-[3-[[6-[3-(trifluoromethyl)anilino]pyrimidin-4-yl]amino]phenyl]cyclopropanecarboxamide Chemical compound FC(F)(F)C1=CC=CC(NC=2N=CN=C(NC=3C=C(NC(=O)C4CC4)C=CC=3)C=2)=C1 YOHYSYJDKVYCJI-UHFFFAOYSA-N 0.000 description 1
- QHADVLVFMKEIIP-UHFFFAOYSA-N n-[3-fluoro-4-[1-methyl-6-(1h-pyrazol-4-yl)indazol-5-yl]oxyphenyl]-1-(4-fluorophenyl)-6-methyl-2-oxopyridine-3-carboxamide Chemical compound O=C1N(C=2C=CC(F)=CC=2)C(C)=CC=C1C(=O)NC(C=C1F)=CC=C1OC1=CC=2C=NN(C)C=2C=C1C=1C=NNC=1 QHADVLVFMKEIIP-UHFFFAOYSA-N 0.000 description 1
- WPEWQEMJFLWMLV-UHFFFAOYSA-N n-[4-(1-cyanocyclopentyl)phenyl]-2-(pyridin-4-ylmethylamino)pyridine-3-carboxamide Chemical compound C=1C=CN=C(NCC=2C=CN=CC=2)C=1C(=O)NC(C=C1)=CC=C1C1(C#N)CCCC1 WPEWQEMJFLWMLV-UHFFFAOYSA-N 0.000 description 1
- PDYXPCKITKHFOZ-UHFFFAOYSA-N n-[4-(2-amino-3-chloropyridin-4-yl)oxy-3-fluorophenyl]-5-(4-fluorophenyl)-4-oxo-1h-pyridine-3-carboxamide Chemical compound NC1=NC=CC(OC=2C(=CC(NC(=O)C=3C(C(C=4C=CC(F)=CC=4)=CNC=3)=O)=CC=2)F)=C1Cl PDYXPCKITKHFOZ-UHFFFAOYSA-N 0.000 description 1
- ISPBCAXOSOLFME-UHFFFAOYSA-N n-[4-(6,7-dimethoxyquinolin-4-yl)oxy-3-fluorophenyl]-4-ethoxy-1-(4-fluoro-2-methylphenyl)pyrazole-3-carboxamide Chemical compound N1=C(C(=O)NC=2C=C(F)C(OC=3C4=CC(OC)=C(OC)C=C4N=CC=3)=CC=2)C(OCC)=CN1C1=CC=C(F)C=C1C ISPBCAXOSOLFME-UHFFFAOYSA-N 0.000 description 1
- HAYYBYPASCDWEQ-UHFFFAOYSA-N n-[5-[(3,5-difluorophenyl)methyl]-1h-indazol-3-yl]-4-(4-methylpiperazin-1-yl)-2-(oxan-4-ylamino)benzamide Chemical compound C1CN(C)CCN1C(C=C1NC2CCOCC2)=CC=C1C(=O)NC(C1=C2)=NNC1=CC=C2CC1=CC(F)=CC(F)=C1 HAYYBYPASCDWEQ-UHFFFAOYSA-N 0.000 description 1
- 229950009708 naquotinib Drugs 0.000 description 1
- IOMMMLWIABWRKL-WUTDNEBXSA-N nazartinib Chemical compound C1N(C(=O)/C=C/CN(C)C)CCCC[C@H]1N1C2=C(Cl)C=CC=C2N=C1NC(=O)C1=CC=NC(C)=C1 IOMMMLWIABWRKL-WUTDNEBXSA-N 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 230000001613 neoplastic effect Effects 0.000 description 1
- 210000005036 nerve Anatomy 0.000 description 1
- 210000004498 neuroglial cell Anatomy 0.000 description 1
- 239000003900 neurotrophic factor Substances 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 108700007229 noggin Proteins 0.000 description 1
- 102000045246 noggin Human genes 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 238000010899 nucleation Methods 0.000 description 1
- 238000003199 nucleic acid amplification method Methods 0.000 description 1
- 108020004707 nucleic acids Proteins 0.000 description 1
- 102000039446 nucleic acids Human genes 0.000 description 1
- 150000007523 nucleic acids Chemical class 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 229960003104 ornithine Drugs 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- WVUNYSQLFKLYNI-AATRIKPKSA-N pelitinib Chemical compound C=12C=C(NC(=O)\C=C\CN(C)C)C(OCC)=CC2=NC=C(C#N)C=1NC1=CC=C(F)C(Cl)=C1 WVUNYSQLFKLYNI-AATRIKPKSA-N 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 229940021222 peritoneal dialysis isotonic solution Drugs 0.000 description 1
- 239000007793 ph indicator Substances 0.000 description 1
- 229960003531 phenolsulfonphthalein Drugs 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 230000026731 phosphorylation Effects 0.000 description 1
- 238000006366 phosphorylation reaction Methods 0.000 description 1
- 230000000704 physical effect Effects 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 229920001992 poloxamer 407 Polymers 0.000 description 1
- 229920000747 poly(lactic acid) Polymers 0.000 description 1
- 239000004626 polylactic acid Substances 0.000 description 1
- XAEFZNCEHLXOMS-UHFFFAOYSA-M potassium benzoate Chemical compound [K+].[O-]C(=O)C1=CC=CC=C1 XAEFZNCEHLXOMS-UHFFFAOYSA-M 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 229960001309 procaine hydrochloride Drugs 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 238000002331 protein detection Methods 0.000 description 1
- TXUSTSJRABHHQP-UFGIQYKASA-N pulsatilla saponin D Natural products C[C@@H]1O[C@@H](O[C@@H]2[C@@H](O)[C@H](CO[C@H]2O[C@H]3CC[C@@]4(C)[C@@H](CC[C@]5(C)[C@@H]4CC=C6[C@@H]7CC(C)(C)CC[C@@]7(CC[C@@]56C)C(=O)O)[C@]3(C)O)O[C@@H]8O[C@H](CO)[C@@H](O)[C@H](O)[C@H]8O)[C@H](O)[C@H](O)[C@H]1O TXUSTSJRABHHQP-UFGIQYKASA-N 0.000 description 1
- 229950010131 puromycin Drugs 0.000 description 1
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 230000001172 regenerating effect Effects 0.000 description 1
- 238000003757 reverse transcription PCR Methods 0.000 description 1
- 229950009855 rociletinib Drugs 0.000 description 1
- 239000011435 rock Substances 0.000 description 1
- 238000011076 safety test Methods 0.000 description 1
- DFJSJLGUIXFDJP-UHFFFAOYSA-N sapitinib Chemical compound C1CN(CC(=O)NC)CCC1OC(C(=CC1=NC=N2)OC)=CC1=C2NC1=CC=CC(Cl)=C1F DFJSJLGUIXFDJP-UHFFFAOYSA-N 0.000 description 1
- 229950006474 sapitinib Drugs 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 238000012216 screening Methods 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 238000005204 segregation Methods 0.000 description 1
- OEBIHOVSAMBXIB-SJKOYZFVSA-N selitrectinib Chemical compound C[C@@H]1CCC2=NC=C(F)C=C2[C@H]2CCCN2C2=NC3=C(C=NN3C=C2)C(=O)N1 OEBIHOVSAMBXIB-SJKOYZFVSA-N 0.000 description 1
- WUWDLXZGHZSWQZ-WQLSENKSSA-N semaxanib Chemical compound N1C(C)=CC(C)=C1\C=C/1C2=CC=CC=C2NC\1=O WUWDLXZGHZSWQZ-WQLSENKSSA-N 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 210000004927 skin cell Anatomy 0.000 description 1
- 210000000329 smooth muscle myocyte Anatomy 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 239000007974 sodium acetate buffer Substances 0.000 description 1
- 239000011780 sodium chloride Substances 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 210000001988 somatic stem cell Anatomy 0.000 description 1
- 229960000487 sorafenib tosylate Drugs 0.000 description 1
- IVDHYUQIDRJSTI-UHFFFAOYSA-N sorafenib tosylate Chemical compound [H+].CC1=CC=C(S([O-])(=O)=O)C=C1.C1=NC(C(=O)NC)=CC(OC=2C=CC(NC(=O)NC=3C=C(C(Cl)=CC=3)C(F)(F)F)=CC=2)=C1 IVDHYUQIDRJSTI-UHFFFAOYSA-N 0.000 description 1
- 229960002920 sorbitol Drugs 0.000 description 1
- 230000021595 spermatogenesis Effects 0.000 description 1
- 210000004988 splenocyte Anatomy 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 230000008093 supporting effect Effects 0.000 description 1
- 229920001059 synthetic polymer Polymers 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 229950004186 telatinib Drugs 0.000 description 1
- YBRBMKDOPFTVDT-UHFFFAOYSA-N tert-butylamine Chemical compound CC(C)(C)N YBRBMKDOPFTVDT-UHFFFAOYSA-N 0.000 description 1
- 210000001550 testis Anatomy 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 239000011573 trace mineral Substances 0.000 description 1
- 235000013619 trace mineral Nutrition 0.000 description 1
- 229960000281 trometamol Drugs 0.000 description 1
- TUCIOBMMDDOEMM-RIYZIHGNSA-N tyrphostin B42 Chemical compound C1=C(O)C(O)=CC=C1\C=C(/C#N)C(=O)NCC1=CC=CC=C1 TUCIOBMMDDOEMM-RIYZIHGNSA-N 0.000 description 1
- UHTHHESEBZOYNR-UHFFFAOYSA-N vandetanib Chemical compound COC1=CC(C(/N=CN2)=N/C=3C(=CC(Br)=CC=3)F)=C2C=C1OCC1CCN(C)CC1 UHTHHESEBZOYNR-UHFFFAOYSA-N 0.000 description 1
- 229950000578 vatalanib Drugs 0.000 description 1
- YCOYDOIWSSHVCK-UHFFFAOYSA-N vatalanib Chemical compound C1=CC(Cl)=CC=C1NC(C1=CC=CC=C11)=NN=C1CC1=CC=NC=C1 YCOYDOIWSSHVCK-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0652—Cells of skeletal and connective tissues; Mesenchyme
- C12N5/0657—Cardiomyocytes; Heart cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/34—Muscles; Smooth muscle cells; Heart; Cardiac stem cells; Myoblasts; Myocytes; Cardiomyocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/36—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix
- A61L27/38—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/36—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix
- A61L27/38—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells
- A61L27/3804—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells characterised by specific cells or progenitors thereof, e.g. fibroblasts, connective tissue cells, kidney cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/36—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix
- A61L27/38—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells
- A61L27/3804—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells characterised by specific cells or progenitors thereof, e.g. fibroblasts, connective tissue cells, kidney cells
- A61L27/3834—Cells able to produce different cell types, e.g. hematopoietic stem cells, mesenchymal stem cells, marrow stromal cells, embryonic stem cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L27/00—Materials for grafts or prostheses or for coating grafts or prostheses
- A61L27/36—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix
- A61L27/38—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells
- A61L27/3895—Materials for grafts or prostheses or for coating grafts or prostheses containing ingredients of undetermined constitution or reaction products thereof, e.g. transplant tissue, natural bone, extracellular matrix containing added animal cells using specific culture conditions, e.g. stimulating differentiation of stem cells, pulsatile flow conditions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/04—Inotropic agents, i.e. stimulants of cardiac contraction; Drugs for heart failure
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/11—Epidermal growth factor [EGF]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/70—Enzymes
- C12N2501/72—Transferases [EC 2.]
- C12N2501/727—Kinases (EC 2.7.)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2506/00—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells
- C12N2506/45—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from artificially induced pluripotent stem cells
Definitions
- the present invention relates to a method for producing and purifying cardiomyocytes, and more particularly to a method for producing and purifying cardiomyocytes using a receptor tyrosine kinase inhibitor.
- One of the methods for stably providing uniform myocardial cells is a method for inducing differentiation of myocardial cells from stem cells or myocardial progenitor cells, and in order to establish an efficient method for inducing differentiation into myocardial cells, Various efforts have been made.
- a differentiation-inducing method a method of promoting differentiation induction from pluripotent stem cells to myocardial cells by culturing pluripotent stem cells in a medium containing an EGFR inhibitor (Patent Document 1), artificial pluripotent stem cells
- Patent Document 2 A method of maturing myocardial cells by contacting the myocardial cells with a Neuregulin 1 antagonist or an ErbB antagonist after inducing differentiation into myocardial cells (Patent Document 2), with undifferentiated progenitor cells such as myoblasts.
- a method for promoting differentiation induction of undifferentiated progenitor cells by contacting them with a deacetylating enzyme inhibitor (Patent Document 3), adult progenitor cells such as myocardial progenitor cells, and histone deacetylating enzyme (HDAC).
- a method of promoting differentiation induction of progenitor cells by contacting with an inhibitor (Patent Document 4) has been reported.
- a method that does not undergo a differentiation induction process from stem cells has also been reported.
- myocardial progenitor cells or myocardial cells are produced from somatic cells such as fibroblasts by direct reprogramming. The method is disclosed.
- the present inventors did not promote the induction of differentiation from undifferentiated cells to myocardial cells, but instead promoted myocardium in a cell population already containing myocardial cells.
- Inhibitors targeting proteins that are highly expressed in cells other than cells suppress the proliferation of cells other than the myocardial cells, or reduce the number of cells other than the myocardial cells to reduce the number of cells other than the myocardial cells.
- the present invention provides the following.
- a method for producing a cell population containing cardiomyocytes (1) Receptor-type tyrosine kinase inhibitor (however, EGF receptor) is applied to a cell population containing myocardial cells or myocardial progenitor cells and other cells obtained by culturing pluripotent stem cells in a medium for myocardial cell differentiation. (Excluding body inhibitors) and (2) culturing the cell population, Including methods.
- EGF receptor Receptor-type tyrosine kinase inhibitor
- [3] The method according to [1] or [2], wherein the contact between the cell population of the step (1) and the receptor tyrosine kinase inhibitor is performed for one day or more.
- the inhibitor is an inhibitor against at least one receptor tyrosine kinase selected from the group consisting of VEGF receptor, PDGF receptor, HGF receptor and FGF receptor, [1] to [3]. The method described in any of.
- the inhibitor is N- [5-( ⁇ 2- [(cyclopropanecarbonyl) amino] imidazo [1,2-b] pyridazine-6-yl ⁇ oxy) -2-methylphenyl] -1, 3-Dimethyl-1H-pyrazole-5-carboxamide, N- ⁇ 4-[(6,7-dimethoxyquinoline-4-yl) oxy] -3-fluorophenyl ⁇ -N'-(4-fluorophenyl) cyclopropane -1 the method of.
- the method according to any one of [1] to [5], wherein the pluripotent stem cell is an induced pluripotent stem cell.
- a cell population containing cardiomyocytes obtained by the method according to any one of [1] to [6].
- a cell transplant therapy agent comprising the cell population according to [7].
- a method for purifying cardiomyocytes (1) A step of contacting a cell population containing myocardial cells or myocardial progenitor cells with other cells obtained by culturing pluripotent stem cells in a medium for myocardial cell differentiation with a receptor-type tyrosine kinase inhibitor. And (2) the step of culturing the cell population, Including methods.
- a cell population containing cardiomyocytes with high purity is provided.
- Such a cell population can be suitably used for cell transplantation therapy for heart disease.
- a method of purifying cardiomyocytes with high purity from a cell population containing cardiomyocytes and myocardial progenitor cells is also provided.
- FIG. 1 shows a t-SNE plot of clustering based on single-cell RNA sequencing data of cardiomyocytes induced to differentiate from iPS cells, and the expression levels of sarcomeric- ⁇ -actinin and cTnT (Cardiac Troponin T) of each cluster.
- the circled area in the upper panel indicates the non-cardiomyocyte population.
- the vertical axis of the center and lower panels indicates the gene expression level, and the label of identity on the horizontal axis indicates the cluster number in FIG.
- Each dot indicates an individual cell, and the framed area indicates a non-cardiomyocyte cluster.
- FIG. 1 shows a t-SNE plot of clustering based on single-cell RNA sequencing data of cardiomyocytes induced to differentiate from iPS cells, and the expression levels of sarcomeric- ⁇ -actinin and cTnT (Cardiac Troponin T) of each cluster.
- the circled area in the upper panel indicates the non-cardi
- CM cardiomyocytes
- SMC smooth muscle-like cells
- END endoderm lineage cells
- EC. Endothelium-like cells
- FIG. 2-3 shows the t-SNE plot of the clustering result of iPS cell-derived cardiomyocytes by single RNA sequencing data and the expression of FGFR4, HGFR (c-Met), and EGFR1 genes in each cell.
- FIG. 2-4 shows the t-SNE plot of the clustering results of iPS cell-derived cardiomyocytes based on single RNA sequencing data and the expression of the EGFR3 gene in each cell. Dark gray dots on the panel showing gene expression represent cells with high expression levels and light grays represent cells with low expression levels.
- the highly expressed cell population is circled and the population name is shown in the figure (END: endoderm lineage cell (hereinafter referred to as END)).
- FIG. END endoderm lineage cell
- TNNI1 reporter iPS cell-derived myocardial cells with a myocardial cell rate (TNNI1 positive rate) of 89.6% (leftmost panel) were converted into CD326-positive cell cells (END, cells surrounded by a frame in the center left panel).
- CD326-negative CD31-positive cells EC, cells surrounded by the center right panel
- CD326-negative CD31-negative CD49a-positive cells SMC, cells surrounded by the center right panel
- CD326-negative CD31-negative CD49a-negative cells The cells were separated into cells (Triple Negative: TN, cells located at the lower left of the center right panel). More than 99% of TNs were myocardial marker TNNI1-positive cells (cardiomyocytes) (rightmost panel). For the percentage display of EC and SMC, the values including CD326-negative cells are shown instead of the cells in the panel.
- FIG. 4 shows the cardiomyocyte rate after compound treatment. *: Measurement was not performed because the number of cells was small.
- the vertical axis shows the experiment number, and the horizontal axis shows the Actinin-positive cell rate (cardiomyocyte rate).
- FIG. 5 shows the non-cardiomyocyte rate after compound treatment (END: endoderm lineage cells, SMC: smooth muscle-like cells, EC: endothelial-like cells).
- the vertical axis shows the experiment number, and the horizontal axis shows the non-cardiomyocyte rate.
- the vertical axis shows the experiment number, and the horizontal axis shows the cardiomyocyte rate.
- FIG. 7 shows the non-cardiomyocyte rate after compound treatment (END: endoderm lineage cells, SMC: smooth muscle-like cells, EC: endothelial-like cells).
- the vertical axis shows the experiment number, and the horizontal axis shows the non-cardiomyocyte rate.
- the vertical axis shows the experiment number, and the horizontal axis shows the cardiomyocyte rate.
- the vertical axis shows the experiment number, and the horizontal axis shows the relative ratio of the number of recovered cells.
- the vertical axis shows the experiment number, and the horizontal axis shows the cardiomyocyte count rate.
- the vertical axis shows the experiment number, and the horizontal axis shows the relative ratio of the number of recovered cells.
- the vertical axis shows the experiment number, and the horizontal axis shows the cardiomyocyte rate.
- the vertical axis shows the experiment number, and the horizontal axis shows the non-cardiomyocyte rate.
- the vertical axis shows the experiment number, and the horizontal axis shows the relative ratio of the number of recovered cells.
- FIG. 16 shows the non-cardiomyocyte rate (END: endoderm lineage cells, SMC: smooth muscle-like cells, EC: endothelial-like cells) after compound treatment.
- the vertical axis shows the experiment number, and the horizontal axis shows the non-cardiomyocyte rate. *: Measurement was not performed because the number of cells was small.
- the vertical axis shows the experiment number, and the horizontal axis shows the cardiomyocyte count rate.
- FIG. 16 shows the non-cardiomyocyte rate (END: endoderm lineage cells, SMC: smooth muscle-like cells, EC: endothelial-like cells) after compound treatment.
- the vertical axis shows the experiment number, and the horizontal axis shows the non-cardiomyocyte rate. *: Measurement was not performed
- 5 indicates n 1) (END: endometrial lineage cell, SMC: smooth muscle-like cell, EC: endothelial-like cell).
- the vertical axis shows the experiment number, and the horizontal axis shows the non-cardiomyocyte rate.
- the vertical axis shows the experiment number, and the horizontal axis shows the cardiomyocyte rate.
- the vertical axis shows the experiment number, and the horizontal axis shows the non-cardiomyocyte rate.
- the vertical axis shows the experiment number, and the horizontal axis shows the relative ratio of the number of recovered cells.
- the present invention provides a method for producing a cell population containing cardiomyocytes (hereinafter, also referred to as “the production method of the present invention”).
- the production method of the present invention comprises (1) contacting a cell population containing myocardial cells or myocardial progenitor cells with other cells with a receptor tyrosine kinase inhibitor, and (2) culturing the cell population. include.
- the EGF receptor inhibitor is excluded from the "receptor-type tyrosine kinase inhibitor" in (1) above.
- myocardial cell means a cell in which at least one of sarcomere ⁇ -actinin, myocardial troponin T (cTnT), and troponin I type 1 (TNNI1) is positive. Preferred are sarcomere ⁇ -actinin positive cells. Also, typically, it is a myocardial cell having a self-beating ability.
- the "myocardial progenitor cell” means a progenitor cell of the myocardial cell in which at least one of Nkx2.5, GATA4, MEF2C and MESS1 is positive.
- non-cardiomyocytes mean cells that do not correspond to either cardiomyocytes or myocardial progenitor cells (hereinafter, also referred to as "non-cardiomyocytes"), and specific cells include, for example, smooth muscle cells. , Endothelial cells, stem cells (eg, pluripotent stem cells) and the like.
- Protein detection can be performed using antibody-based immunological assays such as ELISA, immunostaining, and flow cytometry.
- ELISA antibody-based immunological assays
- the reporter protein is expressed together with the protein, and the target protein is detected by detecting the reporter protein.
- Gene detection can be performed using, for example, a nucleic acid amplification method such as RT-PCR, biochip (eg, microarray), RNAseq, and / or a nucleic acid detection method.
- the expression of a protein or gene can be determined by a general method. For example, when flow cytometry is used, the expression of the protein is relatively expressed as compared with the expression level in the negative control group. When the amount is high, it can be determined that the protein is detectable and expressed.
- negative means that the expression level of a protein or gene is less than the lower limit of detection by all or any of the above-mentioned known methods.
- the lower limit of detection of protein or gene expression may differ depending on each method, but can be determined by a general method.
- the term "cell population” means a population consisting of two or more cells of the same type or different types. "Cell population” also means a mass of cells of the same or different types.
- the cell population containing myocardial cells or myocardial progenitor cells and non-myocardial cells used in the step (1) can be produced by culturing pluripotent stem cells in a medium for cardiomyocyte differentiation. Therefore, the production method of the present invention may include a step (0) of inducing differentiation of cardiomyocytes or myocardial progenitor cells from pluripotent stem cells before the step (1).
- pluripotent stem cells used in the present invention include induced pluripotent stem cells (iPS cells), embryonic stem cells (embryonic stem cells: ES cells), and embryos derived from cloned embryos obtained by nuclear transplantation.
- Specified stem cells nuclear transfer Embryonic stem cells: ntES cells
- pluripotent germline stem cells mGS cells
- EG cells embryonic stem cells
- multi-line cells embryonic stem cells
- iPS cells more preferably human iPS cells
- the pluripotent stem cell is an ES cell or an arbitrary cell derived from a human embryo, the cell is a cell produced by destroying an embryo, even if the cell is produced by destroying the embryo.
- the pluripotent stem cells are preferably derived from mammals (eg, mice, rats, hamsters, guinea pigs, dogs, monkeys, orangutans, chimpanzees, humans), and more preferably humans. Therefore, the most preferable pluripotent stem cell used in the present invention is a human iPS cell.
- iPS cell Induced pluripotent stem cell
- iPS cell refers to a cell obtained by introducing a specific factor (nuclear reprogramming factor) into a mammalian somatic cell or an undifferentiated stem cell and reprogramming it.
- a specific factor nuclear reprogramming factor
- iPS cells induced pluripotent stem cells
- iPS cells derived from human cells established by introducing the same four factors into human fibroblasts ( Takahashi K, Yamanaka S., et al. Cell, (2007) 131: 861-872.), After the introduction of the above four factors, selection was performed using the expression of Nanog as an index, and established Nanog-iPS cells (Okita, K., Ichisaka, T., and Yamanaka, S. (2007). Nature 448, 313-317.), C-Myc-free iPS cells (Nakagawa M, Yamanaka S., et al.
- iPS cells established by introducing 6 factors by a virus-free method (Okita K et al. Nat. Methods 2011 May; 8 (5): 409-12, Okita K et al. .Stem Cells.31 (3): 458-66.) Can also be used.
- induced pluripotent stem cells Yu J., Thomason JA. Et al., Science (2007) 318: 1917-1920.
- Induced pluripotent stem cells prepared by Dayy et al. Japanese Patent Laid-Open No. 2008-307007
- any of the induced pluripotent stem cells known in the art can be used.
- As the induced pluripotent stem cell line various iPS cell lines established by NIH, RIKEN, Kyoto University and the like can be used.
- RIKEN's HiPS-RIKEN-1A strain, HiPS-RIKEN-2A strain, HiPS-RIKEN-12A strain, Nippons-B2 strain, Kyoto University's 253G1 strain, 201B7 strain, 409B2 strain examples thereof include 454E2 strain, 606A1 strain, 610B1 strain, 648A1 strain, iPS cell stock for regenerative medicine and the like.
- the term "somatic cell” means any animal cell (preferably a mammalian cell including human) except germline cells such as eggs, egg mother cells, and ES cells or totipotent cells.
- the somatic cells include, but are not limited to, fetal (pup) somatic cells, neonatal (pup) somatic cells, and mature healthy or diseased somatic cells, and primary cultured cells. , Passed cells, and established cells are all included.
- the somatic cells include, for example, (1) tissue stem cells (somatic stem cells) such as nerve stem cells, hematopoietic stem cells, mesenchymal stem cells, and dental pulp stem cells, (2) tissue precursor cells, (3) lymphocytes, and epithelium.
- Endothelial cells muscle cells, fibroblasts (skin cells, etc.), hair cells, hepatocytes, gastric mucosal cells, intestinal cells, splenocytes, pancreatic cells (pancreatic exocrine cells, etc.), brain cells, lung cells, renal cells And differentiated cells such as fat cells are exemplified.
- ES cells are stem cells that are pluripotent and have the ability to proliferate by self-renewal, established from the inner cell mass of early embryos (for example, blastocysts) of mammals such as humans and mice. ES cells were discovered in mice in 1981 (M.J.Evans and MH Kaufman (1981), Nature 292: 154-156), after which ES cell lines were established in primates such as humans and monkeys. (JA Thomason et al. (1998), Science 282: 1145-1147; JA Thomason et al. (1995), Proc. Nature. Acad. Sci. USA, 92: 7844-7884; JA Thomason et al. (1996), Biol.
- ES cells can be established by removing the inner cell mass from the blastocyst of the fertilized egg of the target animal and culturing the inner cell mass on a fibroblast feeder.
- a fibroblast feeder For methods of establishing and maintaining human and monkey ES cells, see, for example, USP 5,843,780; Thomson JA, et al. (1995), Proc. Natl. Acad. Sci. USA. 92: 7844-7884; Thomason JA, et al. (1998), Science. 282: 1145-1147; Suemori H. et al. et al.
- ES cells can be established using only single blastomeres of embryos in the cleavage stage before the blastocyst stage (Chung Y. et al. (2008), Cell Stem Cell 2: 113-). 117), it can also be established using embryos that have stopped developing (Zhang X. et al. (2006), Stem Cells 24: 2669-2676.).
- RIKEN RIKEN
- various mouse ES cell lines established by inGenius targeting laboratory, RIKEN (RIKEN), etc. can be used for mouse ES cells, and Wisconsin University for human ES cells.
- RIKEN inGenius targeting laboratory
- RIKEN RIKEN
- Various human ES cell lines established by NIH, RIKEN, Kyoto University, National Center for Child Health and Development, Cellartis, etc. are available.
- CHB-1 to CHB-12 strains sold by ESI Bio RUES1 strains, RUES2 strains, HUES1 to HUES28 strains, etc.
- H1 strains sold by WiCell Research H9 strains, etc.
- KhES-1, KhES-2, KhES-3, KhES-4, KhES-5, SSES1, SSES2, SSES3 and the like to be sold can be used.
- nt ES cells are ES cells derived from cloned embryos produced by nuclear transplantation technology and have almost the same characteristics as ES cells derived from fertilized eggs (Wakayama T. et al. (Wakayama T. et al.). 2001), Science, 292: 740-743; S. Wakayama et al. (2005), Biol. Report., 72: 923-936; Byrne J. et al. (2007), Nature, 450: 497-502). ..
- ES cells established from the inner cell mass of blastocysts derived from cloned embryos obtained by replacing the nuclei of unfertilized eggs with the nuclei of somatic cells are nt ES (nuclear transfer ES) cells.
- nt ES nuclear transfer ES
- nuclear transplantation technology Cibelli JB et al. (1998), Nature Biotechnol., 16: 642-646)
- ES cell production technology above is used.
- somatic cell nuclei can be injected into enucleated unfertilized eggs of mammals and cultured for several hours to initialize them.
- MGS cells are testis-derived pluripotent stem cells, which are the origin cells for spermatogenesis. Similar to ES cells, these cells can induce differentiation into cells of various lineages, and have properties such as being able to produce chimeric mice when transplanted into mouse blastocysts (Kanatsu-Shinohara M. et al. (Kanatsu-Shinohara M. et al.). 2003) Biol. Report., 69: 612-616; Shinohara K. et al. (2004), Cell, 119: 1001-1012). It is self-renewable in a culture medium containing glial cell line-developed neurotrophic factor (GDNF), and reproduces by repeating passage under the same culture conditions as ES cells. Stem cells can be obtained (Masanori Takebayashi et al. (2008), Experimental Medicine, Vol. 26, No. 5 (Special Edition), pp. 41-46, Yodosha (Tokyo, Japan)).
- GDNF glial
- EG cells are cells with pluripotency similar to ES cells, which are established from embryonic primordial germ cells. It can be established by culturing primordial germ cells in the presence of substances such as LIF, bFGF, stem cell factor (Masui Y. et al. (1992), Cell, 70: 841-847; J. et al. L. Resnick et al. (1992), Nature, 359: 550-551).
- Muse cells are non-neoplastic pluripotent stem cells that are endogenous to the living body, and can be produced, for example, by the method described in WO 2011/007900. Specifically, Muse cells are pluripotent cells obtained by long-term trypsin treatment of fibroblasts or bone marrow stromal cells, preferably 8 or 16 hours of trypsin treatment, followed by suspension culture. SSEA-3 and CD105 are positive.
- the step (0) is not particularly limited as long as the pluripotent stem cells can be induced to differentiate into myocardial cells or myocardial progenitor cells. It can induce differentiation into cells or myocardial progenitor cells.
- the step (0) is (0-1) a step of inducing differentiation of pluripotent stem cells into mesoderm cells, and (0-2) the steps of inducing the differentiation of the mesoderm cells into myocardial cells or It may include the step of inducing differentiation into myocardial progenitor cells.
- the "cardiomyocyte differentiation medium” includes a factor that promotes the induction of differentiation into cardiomyocytes such as cytokines (hereinafter, may be referred to as "cardiomyocyte differentiation inducing factor”) and a basal medium. Means medium.
- the above-mentioned myocardial cell differentiation-inducing factor also includes factors necessary for inducing differentiation of pluripotent stem cells into intermediate cells (for example, mesoderm cells) in the process of inducing differentiation into myocardial cells or myocardial progenitor cells. Shall be.
- basal medium used in the present invention examples include StemFit (eg, StemFit AK03N, StemFit AK02N) (Ajinomoto), StemPro-34 (Thermo Fisher Scientific), PECM (Primate ES Cell Medium), PECM (Primate ES Cell Medium), and Eagle's Medium. : Glasgow Minimum Essential Medium, IMDM (Iskov's Modified Dulbecco's Medium), 199 Medium, Eagle's Minimum Essential Medium (Eagle's Minimum Esentical Dulbecco's moderate Eagle's Medium (DMEM), Ham's F12 medium, RPMI 1640 medium, Fisher's medium, and a mixed medium thereof are included.
- StemFit eg, StemFit AK03N, StemFit AK02N
- Thermo Fisher Scientific Thermo Fisher Scientific
- PECM Primary ES Cell Medium
- PECM Primary ES Cell Medium
- Eagle's Medium Glasgow Minimum Essential Medium
- IMDM Iskov's Modified
- the basal medium includes ROCK inhibitors (eg, Y-27632, Fasudil / HA1077, SR3677, GSK269962, H-1152, Wf-536, etc.), serum (eg, bovine fetal serum (FBS), human serum, horse serum, etc.).
- ROCK inhibitors eg, Y-27632, Fasudil / HA1077, SR3677, GSK269962, H-1152, Wf-536, etc.
- serum eg, bovine fetal serum (FBS), human serum, horse serum, etc.
- serum substitutes insulin, various vitamins (eg vitamin Cs (eg ascorbic acid)), L-glutamine, various amino acids such as non-essential amino acids, 2-mercaptoethanol, thioglycerol (eg ⁇ -monothio) Gglycerol (MTG)), various cytokines, stem cell factors (SCF (Stem cell factor)), activin, etc.), various hormones, various growth factors (leukemia inhibitor (LIF), basic fibroblast growth factor (bFGF), TGF - ⁇ etc.), various extracellular matrices, various cell adhesion molecules, antibiotics such as penicillin / streptomycin and puromycin, pH indicators such as phenol red and the like can be appropriately added.
- Serum alternatives include albumin, transferrin, fatty acids, insulin, collagen precursors, trace elements, Knockout Serum Replacement (KSR), ITS-supplements and mixtures thereof.
- vitamin Cs mean L-ascorbic acid and its derivatives
- L-ascorbic acid derivatives mean those that become vitamin C by an enzymatic reaction in the living body.
- vitamin C phosphate eg, ascorbic acid-2 phosphate
- ascorbic acid glucoside e.g. ascorbic acid-2 phosphate
- ascorbic acid glucoside e.g. ascorbic acid-2 phosphate
- vitamin C ester eg., ascorbic acid phosphate
- ascorbic acid glucoside eg, ascorbic acid glucoside, ascorbic ethyl, vitamin C ester, ascobyl tetrahexyldecanoate, ascobyl stearate and -2 phosphorus ascorbic acid Acid-6 palmitic acid
- Vitamin C phosphate eg, Ascorbic acid 2-phospate
- examples thereof include phosphate-L-ascorbic acid salts such as Na phosphate-L-ascorbic acid or Mg phosphate-L-ascorbic acid. Be done.
- the culture of induced pluripotent stem cells or embryoid bodies may be adhesive culture or suspension culture.
- adhesive culture it may be carried out using a culture vessel coated with an extracellular matrix component, or it may be co-cultured with a feeder cell.
- the feeder cell is not particularly limited, and examples thereof include fibroblasts (mouse fetal fibroblast (MEF), mouse fibroblast (STO), etc.). It is preferable that the feeder cells are inactivated by a method known per se, for example, irradiation with radiation (gamma rays or the like) or treatment with an anticancer agent (mitomycin C or the like).
- matrigel Niwa A, et al.
- fibronectins such as gelatin, collagen and elastin, glucosaminoglycans such as hyaluronic acid and chondroitin sulfate And cell adhesion proteins such as proteoglycan, fibronectin, vitronectin, and laminin.
- the conditions of the culture temperature are not particularly limited, but are preferably about 37 ° C. to 42 ° C. and 37 ° C. to 39 ° C., for example.
- the cells may be cultured under hypoxic conditions, and in the present invention, the hypoxic conditions are exemplified by oxygen concentrations of 15%, 10%, 9%, 8%, 7%, 6%, 5% or less.
- the hypoxic conditions are exemplified by oxygen concentrations of 15%, 10%, 9%, 8%, 7%, 6%, 5% or less.
- Suspension culture refers to culturing cells in a non-adherent state in a culture vessel, and is not particularly limited, but is artificially treated for the purpose of improving adhesion to cells (for example, coating with extracellular matrix or the like).
- Untreated culture vessel or treatment to artificially suppress adhesion for example, coating treatment with polyhydroxyethyl methacrylate (poly-HEMA) or nonionic surfactant (Pluronic F-127, etc.)
- This can be done using the culture vessel that has been prepared.
- stirring blades such as a single-use bioreactor (Biot Co., Ltd.), a single-use bioreactor (Thermo Fisher), a single-use bioreactor (Sartorius Stedium), and a single-use bioreactor (GE Healthcare Life Science).
- Suspension culture may be performed using an incubator.
- the type of incubator to be used and the stirring speed can be appropriately selected by those skilled in the art depending on the type of cells to be cultured. Examples of stirring speeds include, but are not limited to, 0-100 rpm, 20-80 rpm, or 45-65 rpm.
- the step (0) may include a step of forming an embryoid body from pluripotent stem cells.
- a step it is preferable to dissociate the colonized pluripotent stem cells into single cells and then form embryoid bodies.
- the step of dissociating pluripotent stem cells the cells that adhere to each other to form a population are dissociated (separated) into individual cells.
- a method for dissociating pluripotent stem cells for example, a method for mechanically dissociating, a dissociation solution having protease activity and collagenase activity (for example, Accutase TM and Accumax TM ) or a dissociation solution having only collagenase activity was used.
- a dissociation method can be mentioned.
- a method of dissociating pluripotent stem cells using a dissociation solution having protease activity and collagenase activity is used.
- the medium used in the above steps preferably contains thioglycerol, L-glutamine and / or ascorbic acid.
- Examples of the myocardial cell differentiation-inducing factor used in the above step (0-1) include Wnt signal activators, activin A, BMP4, and bFGF, which may be used alone or in combination of two or more. .. In one aspect of the invention, a combination of activin A, BMP4 and bFGF is used.
- the medium used in the above step (0-1) preferably contains thioglycerol, L-glutamine and / or ascorbic acid.
- Wnt signal activator means a substance that activates the Wnt signaling pathway.
- Wnt signal activator examples include Wnt protein, GSK3 ⁇ inhibitor (eg, BIO, CHIR99021, etc.) and the like. These may be used alone or in combination of two or more.
- a Wnt signal activator When a Wnt signal activator is used, its concentration in the medium is not particularly limited.
- BIO or CHIR99021 is used as the Wnt signal activator, it is preferably used at a final concentration of 100 nM to 100 ⁇ M, preferably 1 ⁇ M to 10 ⁇ M in the medium.
- its concentration in the medium is preferably 1 ng / ml to 100 ng / ml, 1 ng / ml, 2 ng / ml, 3 ng / ml, 4 ng / ml, 5 ng / ml, 6 ng / ml, 7 ng / ml, 8 ng / ml, 9 ng / ml, 10 ng / ml, 11 ng / ml, 12 ng / ml, 13 ng / ml, 14 ng / ml, 15 ng / ml, 16 ng / ml, 17 ng / ml, 18 ng / ml, 19 ng / Examples thereof are ml, 20 ng / ml, 30 ng / ml, 40 ng / ml, 50 ng / ml, 60 ng / ml, 70 ng / ml,
- its concentration in the medium is preferably 1 ng / ml to 1 ⁇ g / ml, 1 ng / ml, 2 ng / ml, 3 ng / ml, 4 ng / ml, 5 ng / ml, 6 ng / ml, 7 ng.
- ng / Ml 8 ng / ml, 9 ng / ml, 10 ng / ml, 11 ng / ml, 12 ng / ml, 13 ng / ml, 14 ng / ml, 15 ng / ml, 16 ng / ml, 17 ng / ml, 18 ng / ml, 19 ng / ml , 20 ng / ml, 30 ng / ml, 40 ng / ml, 50 ng / ml, 60 ng / ml, 70 ng / ml, 80 ng / ml, 90 ng / ml, 100 ng / ml, 200 ng / ml, 300 ng / ml, 400 ng / ml, 500 ng Examples include / ml, 600 ng / ml, 700 ng / ml, 800
- its concentration in the medium is preferably 1 ng / ml to 100 ng / ml, 1 ng / ml, 2 ng / ml, 3 ng / ml, 4 ng / ml, 5 ng / ml, 6 ng / ml, 7 ng.
- ng / Ml 8 ng / ml, 9 ng / ml, 10 ng / ml, 11 ng / ml, 12 ng / ml, 13 ng / ml, 14 ng / ml, 15 ng / ml, 16 ng / ml, 17 ng / ml, 18 ng / ml, 19 ng / ml , 20 ng / ml, 30 ng / ml, 40 ng / ml, 50 ng / ml, 60 ng / ml, 70 ng / ml, 80 ng / ml, 90 ng / ml and 100 ng / ml.
- the period of the above step (0-1) is not particularly limited as long as mesoderm cells can be obtained, but is preferably 12 hours or more (example: 1 day, 2 days or more), and 6 days or less (example: 5). Days, 4 days, 3 days or less).
- the mesoderm marker gene include T, MIXL1, NODAL and the like.
- Examples of the myocardial cell differentiation-inducing factor used in the above step (0-2) include a Wnt inhibitor and VEGF, which may be used alone or in combination of two or more.
- the medium used in the above step (0-2) preferably contains thioglycerol, L-glutamine and / or ascorbic acid.
- Wnt inhibitor means a substance that inhibits the signal transduction that follows from the binding of Wnt to the receptor to the accumulation of ⁇ -catenin, and inhibits the binding to the Frizzled family of receptors. It may be a substance or a substance that promotes the decomposition of ⁇ -catenin. Examples of Wnt inhibitors include DKK1 protein (for example, in the case of humans, NCBI accession number: NM_122242), sclerostin (for example, in the case of humans, NCBI accession number: NM_025237), IWR-1 (Merck Millipore).
- DKK1 protein for example, in the case of humans, NCBI accession number: NM_122242
- sclerostin for example, in the case of humans, NCBI accession number: NM_025237
- IWR-1 Merck Millipore
- IWP-2 Sigma-Aldrich
- IWP-3 Sigma-Aldrich
- IWP-4 Sigma-Aldrich
- PNU-74654 Sigma-Aldrich
- XAV939 Sigma-Aldrich
- IWP-3 or IWP-4 is preferable. Only one type of Wnt inhibitor may be used, or a plurality of types may be used in combination.
- a Wnt inhibitor When a Wnt inhibitor is used, its concentration in the medium is preferably 1 nM to 50 ⁇ M, for example, 1 nM, 10 nM, 50 nM, 100 nM, 500 nM, 750 nM, 1 ⁇ M, 2 ⁇ M, 3 ⁇ M, 4 ⁇ M, 5 ⁇ M, 6 ⁇ M, 7 ⁇ M. , 8 ⁇ M, 9 ⁇ M, 10 ⁇ M, 15 ⁇ M, 20 ⁇ M, 25 ⁇ M, 30 ⁇ M, 40 ⁇ M, 50 ⁇ M, but is not limited thereto. More preferably, it is 1 ⁇ M.
- VEGF vascular endothelial growth factor
- its concentration in the medium is preferably 1 to 100 ng / ml, 1 ng / ml, 2 ng / ml, 3 ng / ml, 4 ng / ml, 5 ng / ml, 6 ng / ml, 7 ng / ml.
- a BMP inhibitor and / or a TGF ⁇ inhibitor may be further added to the basal medium as a myocardial cell differentiation inducing factor.
- the "BMP inhibitor” includes a proteinaceous inhibitor such as Chordin, Noggin, and Follistatin, and Dorsomorphin (6- [4- (2-piperidin-1-yl-ethoxy) phenyl] -3-pyridin-. 4-yl-pyrazolo [1,5-a] pyrimidine) and its derivatives (P.B.Yu et al. (2007), Alkoxy, 116: II_60; P.B.Yu et al. (2008), Nat. Chem.
- its concentration in the medium is preferably 1 nM to 50 ⁇ M, for example, 1 nM, 10 nM, 50 nM, 100 nM, 500 nM, 600 nM, 700 nM, 800 nM, 900 nM, 1 ⁇ M, 2 ⁇ M, 3 ⁇ M, 4 ⁇ M. 5, 5 ⁇ M, 6 ⁇ M, 7 ⁇ M, 8 ⁇ M, 9 ⁇ M, 10 ⁇ M, 15 ⁇ M, 20 ⁇ M, 25 ⁇ M, 30 ⁇ M, 40 ⁇ M, 50 ⁇ M, but not limited to these.
- the TGF ⁇ inhibitor means a substance that inhibits the signal transduction of TGF ⁇ from binding to a receptor to SMAD, even if it is a substance that inhibits binding to the ALK family of receptors. , A substance that inhibits the phosphorylation of SMAD by the ALK family.
- TGF ⁇ inhibitor include Lefty-1 (NCBI Accession No. includes mouse: NM_010094 and human: NM_020997), SB431542, SB202190 (above, RK Lindemann et al., Mol. Cancer, etc.).
- SB431542 is preferable.
- a TGF ⁇ inhibitor When a TGF ⁇ inhibitor is used, its concentration in the medium is preferably 1 nM to 50 ⁇ M, for example, 1 nM, 10 nM, 50 nM, 100 nM, 500 nM, 750 nM, 1 ⁇ M, 2 ⁇ M, 3 ⁇ M, 4 ⁇ M, 5 ⁇ M, 5.2 ⁇ M. It is, but is not limited to, 5.4 ⁇ M, 5.6 ⁇ M, 5.8 ⁇ M, 6 ⁇ M, 7 ⁇ M, 8 ⁇ M, 9 ⁇ M, 10 ⁇ M, 15 ⁇ M, 20 ⁇ M, 25 ⁇ M, 30 ⁇ M, 40 ⁇ M, and 50 ⁇ M.
- the period of the above step (0-2) is not particularly limited as long as cardiomyocytes or myocardial progenitor cells can be obtained, but is 1 day or more (eg: 1 day, 2 days, 3 days, 4 days, 5 days, 6 days). , 7 days or more). Further, since the establishment of cardiomyocytes or myocardial progenitor cells is not affected by long-term culture, no upper limit is set, but it is typically 40 days or less. It may also be monitored whether or not myocardial cells or myocardial progenitor cells have been obtained, in which case the number of beating myocardial cells, the expression of markers of myocardial cells or myocardial progenitor cells, the expression of ion channels, electricity. It can be confirmed by the response to physiological stimuli.
- the cardiomyocytes or myocardial progenitor cells obtained in the step (0-2) are further cultured in the presence or absence of the step (0-3) VEGF and / or bFGF. It may include a step of performing.
- the medium used in this step preferably contains thioglycerol, L-glutamine and / or ascorbic acid.
- the medium used in this step is a myocardial maturation compound (eg, N- (1,1-dioxo-2,3-dihydro-1H-1-benzothiophen-5-yl) -2- (4- ⁇ 5).
- VEGF When VEGF is used in step (0-3), its concentration in the medium is preferably 1 to 100 ng / ml, 1 ng / ml, 2 ng / ml, 3 ng / ml, 4 ng / ml, 5 ng / ml, 6 ng.
- ng / Ml 7 ng / ml, 8 ng / ml, 9 ng / ml, 10 ng / ml, 11 ng / ml, 12 ng / ml, 13 ng / ml, 14 ng / ml, 15 ng / ml, 16 ng / ml, 17 ng / ml, 18 ng / ml , 19 ng / ml, 20 ng / ml, 30 ng / ml, 40 ng / ml, 50 ng / ml, 60 ng / ml, 70 ng / ml, 80 ng / ml, 90 ng / ml and 100 ng / ml.
- bFGF When bFGF is used in step (0-3), its concentration in the medium is preferably 1 to 100 ng / ml, 1 ng / ml, 2 ng / ml, 3 ng / ml, 4 ng / ml, 5 ng / ml, 6 ng.
- ng / Ml 7 ng / ml, 8 ng / ml, 9 ng / ml, 10 ng / ml, 11 ng / ml, 12 ng / ml, 13 ng / ml, 14 ng / ml, 15 ng / ml, 16 ng / ml, 17 ng / ml, 18 ng / ml , 19 ng / ml, 20 ng / ml, 30 ng / ml, 40 ng / ml, 50 ng / ml, 60 ng / ml, 70 ng / ml, 80 ng / ml, 90 ng / ml and 100 ng / ml. More preferably, it is 5 ng / ml.
- the period of the above step (0-3) is not particularly limited, but is 1 day or more (eg: 1 day, 2 days, 3 days, 4 days, 5 days, 6 days, 7 days, 8 days, 9 days, 10 days, 11 days, 12 days, 13 days, 14 days, 15 days, 16 days, 17 days, 18 days, 19 days, 20 days, 21 days, 22 days, 23 days, 24 days, 25 days, 26 days , 27 days, 28 days, or more).
- no upper limit is set, but it is typically 60 days or less.
- the embryoid body may be dissociated by the same method as described above before performing the step (0-2) or the step (0-3).
- END2 cells which are mouse-derived supporting cells, and pluripotent stem cells (Mumery, C., et al., Differentiation of human embryonic stem cells to cardiomyocyte cells: roll of cells). Circulation.107 (21), 2733-40 (2003)), a method of inducing myocardial cells by culturing embryo-like bodies with BMP4, FGF2, insulin and serum (Paul, WB, et).
- the cell population containing the myocardial cells or myocardial progenitor cells obtained as described above is contacted with a receptor tyrosine kinase inhibitor, and then the cell population is cultured before contacting the receptor tyrosine kinase inhibitor. It is possible to produce a cell population having a higher purity of myocardial cells as compared with the cell population of. That is, cardiomyocytes can be purified using a receptor tyrosine kinase inhibitor. Therefore, in another aspect of the present invention, (1') a cell population containing myocardial cells or myocardial progenitor cells and non-myocardial cells obtained by culturing pluripotent stem cells in a medium for myocardial cell differentiation.
- the purification method of the present invention comprises a step of contacting a receptor-type tyrosine kinase inhibitor and (2') a step of culturing the cell population. ..
- purifying cardiomyocytes means that a receptor-type tyrosine kinase inhibitor reduces the number of non-cardiomyocytes (“cell count” means the number of living cells; the same applies hereinafter) to cardiomyocytes.
- cell count means the number of living cells; the same applies hereinafter
- Percentage of cardiomyocytes in the cell population (number of cardiomyocytes in the cell population / in the cell population) by exceeding the reduction rate of It means that the total number of cells) increases. Therefore, it is distinguished from the increase in the proportion of myocardial cells due to the promotion of induction of differentiation from myocardial progenitor cells to myocardial cells or the inhibition of induction of differentiation from myocardial progenitor cells to cells other than myocardial cells.
- the reduction in cell number by the receptor tyrosine kinase inhibitor is the result of the induction of cell apoptosis by the receptor tyrosine kinase inhibitor.
- the period of contact between the cell population containing myocardial cells or myocardial progenitor cells and the receptor tyrosine kinase inhibitor is not particularly limited, but is, for example, 1 hour or more (eg, 2). Time, 3 hours, 5 hours, 12 hours, 1 day, 2 days, 3 days or more). In addition, since long-term culture does not affect the establishment of cardiomyocytes or myocardial progenitor cells, there is no particular upper limit, but typically 60 days or less (eg, 50 days, 40 days, 30 days). , 20 days, 14 days, 13 days, 12 days, 11 days or less).
- Contact between a cell population containing myocardial cells or myocardial progenitor cells and a receptor tyrosine kinase inhibitor may be performed by adding a receptor tyrosine kinase inhibitor to a medium containing the cell population, or in advance. This may be done by seeding the cell population in a medium supplemented with a receptor tyrosine kinase inhibitor.
- the timing of contacting the receptor tyrosine kinase inhibitor is also not particularly limited as long as the cell population contains myocardial cells or myocardial progenitor cells, and is not particularly limited. Based on the start date of differentiation induction of pluripotent stem cells, it may be performed on or after the 4th day (eg, 5th day, 6th day, 7th day or later) from the start of differentiation induction. preferable.
- Examples of the receptor-type tyrosine kinase that is inhibited by the receptor-type tyrosine kinase inhibitor used in the present invention include EGF receptors (also referred to as ErbB or HER) (eg, ErbB1 (EGFR), ErbB2 (HER2), ErbB3 (HER3), ErbB4).
- EGF receptors also referred to as ErbB or HER
- EGFR EGF receptors
- HER2 ErbB2
- HER3 ErbB3
- ErbB4 ErbB4
- HER4 insulin receptor
- IR-A, IR-B insulin receptor
- VEGF receptor eg VEGFR-1 (Flt-1), VEGFR-2 (KDR / Flk) -1), VEGFR-3 (Flt-4)
- PDGF receptor eg PDGFR ⁇ , PDGFR ⁇
- HGF receptor also called c-Met
- FGF receptor eg FGFR1, FGFR2, FGFR3, FGFR4
- CCK NGF receptor
- Trk receptor also referred to as Trk receptor
- Trk receptor eg TrkA, TrkB, TrkC
- Eph (Ephrin) receptor eg EPHA1, EPHA2, EPHA3, EPHA4, EPHA5, EPHA6, EPHA7, EPHA8, EPHA9, EPHA10, EPHB1, EPHB2, EPHB3, EPHB4, EPHB5, EPHB6
- AXL also called TAM receptor
- TIE eg TIE-1, TIE-2
- RYK DDR (eg
- VEGF receptor VEGF receptor
- PDGF receptor PDGF receptor
- HGF receptor FGF receptor
- FGF receptor FGF receptor
- the EGF receptor inhibitor is excluded from the receptor tyrosine kinase inhibitor used in the step (1), the EGF receptor inhibitor is used as the receptor tyrosine kinase inhibitor used in the step (1'). Can be used.
- a receptor tyrosine kinase inhibitor has other activities, such as inhibitory activity against other receptor tyrosine kinases, provided that it has at least an inhibitory activity against any of the above receptor tyrosine kinases. Or may have an inhibitory activity specific to one type of receptor tyrosine kinase.
- receptor-type tyrosine kinase inhibitors other than EGF receptor inhibitors exclude those that have inhibitory activity against receptor-type tyrosine kinases other than EGF receptor and also have inhibitory activity against EGF receptor.
- EGF receptor inhibitor is a substance having an EGF receptor inhibitory activity that is superior to other activities, and specifically, it inhibits the EGF receptor by at least 90% or more.
- Examples of the inhibitor against the EGF receptor used in the present invention include Cetuximab, Erlotinib HCl (OSI-744), Gefitinib (ZD1839), Lapatinib (GW-572016) Ditosylate, Afatibin (BIBW2992), Can.
- Insulin receptors or inhibitors of the insulin-like growth factor 1 receptor include, for example, HNMPA, GSK1904529A, Dovitinib (TKI-258) Dynamic Acid, Dovitinib (TKI258) Lactate, NVP-AEW541, Dovitinib (TKI-2). -ADW742, Insulinib (OSI-906), GSK1904529A, BMS-754807, TAE226 (NVP-TAE226), Ceritinib (LDK378) and the like.
- Cabozantinib (XL184, BMS-907351), Cabozantinib malate (XL184), Ki8751, Apatinib, Pontinib (AP24534), ZM323881, LY2874455, Sorafenib, Tyrosine, Sorafenib, Tyrosine, Vandetanib (ZD6474), CYC116, Sunitinib Mate, Sunitinib, PD173704, Semaxanib (SU5416), TSU-68 (SU6668, Orantinib), Axitinib, Cediranib (AZD2171), Cediranib (AZD2171) ), Linifanib (ABT-869), Lenvitanib (E7080), Regorafenib (BAY 73-4506), Telatiib, Tivozanib (AV-951), OSI-930, Cabozantinib (TKI-258) Divic1 Cabozantinib
- Examples of the inhibitor against the HGF receptor include N- ⁇ 4-[(6,7-dimethoxyquinoline-4-yl) oxy] -3-fluorophenyl ⁇ -N'-(4-fluorophenyl) cyclopropane-.
- Examples of the inhibitor against FGFR1 include ASP5878, Ponatinib (AP24534), PD173704, Danusertib (PHA-7393558), Brivanib Alaninate (BMS-582664), Brivanib (BMS-540215), TSU-68 (SU6668). , AZD4547, BGJ398 (NVP-BGJ398), LY2874455, Dovitinib (TKI-258, CHIR-258), Dovitinib (TKI258) Lactate, Dovitinib (TKI-258) Dictic182KiBiBi2Ki (BIBF 1120) and the like.
- Examples of the inhibitor against FGFR2 include ASP5878, BGJ398 (NVP-BGJ398), AZD4547, LY2874455, CH5183284 (Debio-1347), Nintedanib (BIBF 1120), MK-2461 and the like.
- Examples of the inhibitor against FGFR3 include ASP5878, BGJ398 (NVP-BGJ398), AZD4547, LY2874455, Dovitinib (TKI-258) Diractic Acid, Dovitinib (TKI258) Lactate, Dovit, Dovit, Dovit. Debio-1347), MK-2461, Nintedanib (BIBF 1120) and the like.
- Examples of the inhibitor against FGFR4 include ASP5878, LY2874455, AZD4547, CH5183284 (Debio-1347), Nintedanib (BIBF 1120) and the like.
- Examples of the inhibitor against the NGF receptor include BMS-754807, GW441756, DS-6051b, GNF-5738, CH705728, Altiratinib, Seritlectinib (LOXO-195), BMS-935177, Entrectinib (RXDX-101), Sitra. ), PF-06273340, Belizatinib (TSR-011), Larotectiveinib (LOXO-101) sulfate and the like.
- Examples of the inhibitor against the Eph receptor include NVP-BHG712, Sitrabatinib (MGCD516) and the like.
- Examples of the inhibitor against AXL include BMS-777607, Bemcentinib (R428), Cabozantinib malate (XL184), UNC2250, Dubermatinib (TP-0903), UNC-2025, LDC1267, UNC2881, RX. Examples thereof include S49076, Sitlavatinib (MGCD516), 2-D08, Gilteritinib (ASP2215), NPS-1034 and the like.
- Examples of the inhibitor against TIE include MGCD-265 analog, Tie2 kinase inhibitor, Altiratinib, Pexmetinib (ARRY-614) and the like.
- receptor tyrosine kinase inhibitors can be appropriately selected.
- a receptor tyrosine kinase inhibitor N- [5-( ⁇ 2- [(cyclopropanecarbonyl) amino] imidazo [1,2-b] pyridazine-6-yl ⁇ oxy) -2-methylphenyl] -1 , 3-Dimethyl-1H-pyrazole-5-carboxamide, N- ⁇ 4-[(6,7-dimethoxyquinoline-4-yl) oxy] -3-fluorophenyl ⁇ -N'-(4-fluorophenyl) cyclo Propane-1,1-dicarboxamide, AMG337, ASP5878, BGJ398, Foretinib, ZM323881, CP-673451, Crenolanib or Crizotib are preferred.
- receptor tyrosine kinase inhibitor Only one type of receptor tyrosine kinase inhibitor may be used, or a plurality of types may be used in combination. Further, in order to obtain higher purity myocardial cells, another drug (histone deacetylase inhibitor or the like) may be used at the same time as or before and after the receptor tyrosine kinase inhibitor.
- the inhibitor may contain one kind of the above compound or a salt thereof, or may contain two or more kinds.
- Each of the above compounds or salts thereof can be produced according to a method known per se.
- a pharmacologically acceptable salt is preferable, and examples of such a salt include a salt with an inorganic base, a salt with an organic base, a salt with an inorganic acid, and an organic acid. Examples include salts, salts with basic or acidic amino acids, and the like.
- salts with inorganic bases include alkali metal salts such as sodium salt and potassium salt; alkaline earth metal salts such as calcium salt and magnesium salt; aluminum salt; ammonium salt and the like.
- salts with organic bases include trimethylamine, triethylamine, pyridine, picolin, ethanolamine, diethanolamine, triethanolamine, tromethamine [tris (hydroxymethyl) methylamine], tert-butylamine, cyclohexylamine, benzylamine, Examples thereof include salts with dicyclohexylamine, N, N-dibenzylethylenediamine and the like.
- salts with inorganic acids include salts with hydrochloric acid, hydrobromic acid, nitric acid, sulfuric acid, phosphoric acid and the like.
- salts with organic acids are formic acid, acetic acid, trifluoroacetic acid, phthalic acid, fumaric acid, oxalic acid, tartaric acid, maleic acid, citric acid, succinic acid, malic acid, methanesulfonic acid, benzenesulfonic acid. , P-Toluene sulfonic acid and the like.
- salts with basic amino acids include salts with arginine, lysine, ornithine and the like.
- salts with salts with acidic amino acids include salts with aspartic acid, glutamic acid and the like.
- the compound may be a hydrate, a non-hydrate, a solvate, or a non-solvate. Further, the compound is an isotope (eg, 2 H, 3 H, 11 C, 14 C, 18 F, 35 S, etc. 125 I) may be labeled or substituted compounds or the like. A deuterium converter obtained by converting 1 H to 2 H (D) is also included in the above compounds. Tautomers are also included in the above compounds. The compound may be a pharmaceutically acceptable co-crystal or co-crystal salt.
- a co-crystal or a co-crystal salt is unique in two or more kinds at room temperature, each having different physical properties (for example, structure, melting point, heat of fusion, hygroscopicity, solubility and stability). It means a crystalline substance composed of a solid solid.
- the co-crystal or co-crystal salt can be produced according to a co-crystallization method known per se.
- the concentration of the receptor tyrosine kinase inhibitor in the medium can be appropriately selected by those skilled in the art, but for example, 1 nM to 10 ⁇ M is preferable, particularly 10 nM to 3 ⁇ M is more preferable, and specifically, 1 nM and 2 nM, 3nM, 5nM, 10nM, 20nM, 30nM, 40nM, 50nM, 0.1 ⁇ M, 0.2 ⁇ M, 0.3 ⁇ M, 0.4 ⁇ M, 0.5 ⁇ M, 1.0 ⁇ M, 1.5 ⁇ M, 2 ⁇ M, 3 ⁇ M, 4 ⁇ M, 5 ⁇ M, Examples thereof include 6 ⁇ M, 7 ⁇ M, 8 ⁇ M, 9 ⁇ M, and 10 ⁇ M.
- the concentration can be appropriately changed depending on the type of the compound, for example, N- [5-( ⁇ 2-[(cyclopropanecarbonyl) amino] imidazo [1,2-b] pyridazine-6-yl ⁇ oxy. ) -2-Methylphenyl] -1,3-dimethyl-1H-pyrazole-5-carboxamide, preferably 20 nM to 10 ⁇ M, N- ⁇ 4-[(6,7-dimethoxyquinoline-4-yl) ) Oxy] -3-fluorophenyl ⁇ -N'-(4-fluorophenyl) Cyclopropan-1,1-dicarboxamide is preferably 0.2 ⁇ M to 10 ⁇ M, and 0 when AMG337 is used.
- .2 ⁇ M to 10 ⁇ M is preferable, 1 nM to 1 ⁇ M is preferable when ASP5878 is used, 5 nM to 5 ⁇ M is preferable when BGJ398 is used, 5 nM to 5 ⁇ M is preferable when Foretinib is used, and ZM323881 is used.
- 0.1 ⁇ M to 10 ⁇ M is preferable, 0.1 ⁇ M to 10 ⁇ M is preferable when CP-673451 is used, 0.1 ⁇ M to 10 ⁇ M is preferable when using Crenolinib, and 0.1 ⁇ M to 10 ⁇ M is preferable when using Pyrazolenib. It is preferably 0.1 ⁇ M to 10 ⁇ M, but is not limited to these concentrations.
- the method for culturing the cell population in the steps (2) and (2') is the same as in (0-2) or (0-3) above.
- the culture period is the same, and the culture may be continued at least while the cell population is in contact with the receptor tyrosine kinase inhibitor.
- the present invention also provides a cell population containing cardiomyocytes (hereinafter, also referred to as “cell population of the present invention”) obtained by the production method or purification method of the present invention.
- the cell population of the present invention contains cardiomyocytes with high purity. High purity means that the ratio of cardiomyocytes in the cell population (number of cardiomyocytes in the cell population / total number of cells in the cell population) is specifically 80% or more (eg, 85%, 90%, 91). %, 92%, 93%, 94%, 95%, 96%, 97%, 98%, 99% or more).
- the ratio of the cardiomyocytes is before mixing the other cells or the cell population when the cell population is used in combination with other cells or cell populations such as mesenchymal stem cells.
- the cell population of the present invention comprises a higher proportion of cardiomyocytes than the cell population obtained by conventional methods of inducing cardiomyocytes from pluripotent stem cells.
- Such a cell population may be further purified by cell sorting or the like, and the cell population thus purified is also included in the "cell population of the present invention".
- the present invention also provides a cell transplantation therapy agent (hereinafter, also referred to as “the cell transplantation therapy agent of the present invention”), which comprises the cell population of the present invention.
- the cell transplantation therapy agent of the present invention may be used for autologous transplantation or allogeneic transplantation. It may also be used in combination with other drugs, such as immunosuppressants.
- the cell population of the present invention contains myocardial cells with high purity, the cell population of the present invention is suitable for use as a raw material for a cell transplantation therapeutic agent, and the cell population of the present invention or the present invention Cell transplant therapeutic agents are useful in the treatment or prevention of heart disease.
- an effective amount of the cell population or cell transplant therapy agent of the present invention is administered or transplanted to a mammal (eg, human, mouse, rat, monkey, cow, horse, pig, dog, etc.) to be treated or prevented.
- a mammal eg, human, mouse, rat, monkey, cow, horse, pig, dog, etc.
- Methods for treating or preventing heart disease are also included in the present invention.
- Heart diseases to be treated or prevented include diseases or disorders such as heart failure, ischemic heart disease, myocardial infarction, cardiomyopathy, cardiomyopathy, hypertrophic cardiomyopathy, dilated phase hypertrophic cardiomyopathy, and dilated cardiomyopathy. Examples include, but are not limited to, defects.
- the cell population of the present invention is used as a cell transplant therapy agent, it is derived from iPS cells established from somatic cells having the same or substantially the same HLA genotype of the transplanted individual from the viewpoint that rejection does not occur. It is desirable to use a cell population that includes the cells to be used.
- substantially the same means that the transplanted cells have the same HLA genotype to the extent that the immune response can be suppressed by the immunosuppressant, and for example, HLA-A and HLA-B.
- HLA-DR 3 loci or HLA-C added 4 loci matching HLA type somatic cells. It is also possible to implant in a capsule such as polyethylene glycol or silicon, a porous container, or the like to avoid rejection.
- the cell population of the present invention is produced as a parenteral preparation such as an injection, a suspension, or an infusion by mixing with a pharmaceutically acceptable carrier according to conventional means.
- Pharmaceutically acceptable carriers that can be contained in the parenteral preparation include, for example, isotonic solutions containing physiological saline, glucose and other adjuvants (eg, D-sorbitol, D-mannitol, sodium chloride, etc.) and the like.
- An aqueous solution for injection can be mentioned.
- the cell transplantation therapeutic agent of the present invention is, for example, a buffer (for example, phosphate buffer, sodium acetate buffer), a soothing agent (for example, benzalkonium chloride, procaine hydrochloride, etc.), and a stabilizer (for example, human). It may be blended with serum albumin, polyethylene glycol, etc.), preservatives, antioxidants, etc.
- a cell population containing cardiomyocytes is suspended in the aqueous solution so as to have a concentration of about 1 ⁇ 10 6 to about 1 ⁇ 10 8 cells / mL. Just do it.
- the scaffolding material is exemplified by, but is not limited to, a biological component such as collagen and a synthetic polymer such as polylactic acid which substitutes for the component.
- the treatment of heart disease may be performed by sheeting the obtained cardiomyocytes and attaching them to the patient's heart.
- the myocardial sheet is administered, it is achieved by arranging it so as to cover the desired portion.
- the arrangement so as to cover the desired portion can be performed by using a technique well known in the art.
- the tissue may be arranged so as to surround the tissue.
- the administration can also be placed several times in the same portion to obtain the desired effect. When several placements are performed, it is desirable to allow sufficient time for the desired cells to engraft in the tissue and perform angiogenesis.
- the mechanism of treatment for such heart disease may be the effect produced by engraftment of the myocardial sheet, or an indirect effect not dependent on cell engraftment (eg, the recipient by secreting an attractant).
- the effect of mobilizing the derived cells to the damaged site) may be used.
- a cell scaffold material such as collagen, fibronectin, or laminin may be contained in addition to cardiomyocytes.
- any cell type (s) can be included.
- the number of cardiomyocytes used for the treatment of heart disease is not particularly limited as long as the administered myocardial sheet is effective in the treatment of heart disease, and the size of the affected area and the size of the body are not particularly limited. It can be adjusted by increasing or decreasing as appropriate.
- the cell population of the present invention can also be used for drug screening for the treatment of heart disease and cardiotoxicity assessment of the drug.
- the effect and toxicity of the test drug can be evaluated by administering the test drug to the cell population of the present invention and examining the response of cardiomyocytes.
- Example 1 Single-cell RNA sequencing analysis of cells induced to differentiate from iPS cells to cardiomyocytes An evaluation strain of clinical iPS cell lines prepared at the Center for iPS Cell Research and Application (CiRA), Kyoto University was used. The maintenance culture of the iPS cell line was carried out according to the conventional method (Okita K, et al. Stem Cells. 2012 Nov 29. doi: 10.10012 / stem.1293). Induction of differentiation into cardiomyocytes was carried out according to the method described in the paper (Miki et al, Cell Stem Cell. 2015 Jun 4; 16. doi: 10.016 / j. Stem. 2015.04.005.). ..
- RNA passage analysis was performed on cardiomyocytes 22 days after the start of differentiation induction using Chromium manufactured by 10X Genomics. Cell clustering and analysis of each cluster were performed by software (Cellranger, Seurat, Loope Cell Browser). Among the cell populations induced to differentiate from iPS cells to cardiomyocytes, in addition to the cardiomyocyte population expressing sarcomeric- ⁇ -actinin and cardiomyocyte T, three non-myocardiums not expressing sarcomeric- ⁇ -actinin and cardiac Troponin T. It was found that a cell population (which is considered to be smooth muscle-like cells (SMC), endothelial-like cells (EC), and endometrial lineage cells (END) from gene expression) is present (Fig. 1).
- SMC smooth muscle-like cells
- EC endothelial-like cells
- END endometrial lineage cells
- Example 2 Analysis of non-myocardial cells present in a cell population induced to differentiate from iPS cells to myocardium
- the gene expression of receptor tyrosine kinase was analyzed by analysis of single-cell RNA sequencing data by Loope Cell Browser. As a result, it was found that the gene expression of receptor tyrosine kinases such as PDGFRA, PDGFRB, VEGFR1, VEGFR2, c-Met (HGFR), and FGFR4 was high in the non-myocardial cell population and not high in the myocardial cell population (Fig. 2). ..
- Example 3 Staining of non-cardiomyocytes with cell surface markers
- EmGFP EmGFP
- mCherry SEQ ID NO: 2 reporter protein sequence at the TNNI3 locus.
- the human iPS cell line was prepared by an episomal vector (onboard gene; OCT3 / 4, KLF4, SOX2, L-MYC, LIN28, mouse p53DD) using PBMC (LP_167, Sample ID: 2013018) purchased from CTL. (References; Octa K, et al. Stem Cells. 2012 Nov 29. doi: 10.10012 / stem.1293).
- the maintenance culture of the iPS cell line was carried out according to the conventional method (Okita K, et al. Stem Cells. 2012 Nov 29. doi: 10.10012 / stem.1293). Induction of differentiation into cardiomyocytes is performed according to the method described in the paper (Miki et al, Cell Stem Cell. 2015 Jun 4; 16. doi: 10.016 / j. Stem. 2015.04.005.). I went there. Briefly, differentiation into cardiomyocytes is induced by treating the reporter iPS cell line with TripLE select (Life Technologies) diluted in 1/2 with 0.5 mM EDTA / PBS for 4 to 5 minutes, and then using the cell scraper (IWAKI). ), And the cells were dissociated into single cells by pipetting.
- TripLE select Life Technologies
- IWAKI cell scraper
- the medium was removed by centrifugation at 1,000 rpm for 5 min, and the obtained cells were seeded with 2 ⁇ 10 6 cells per 1 well of a 6-well plate, and 1% L-glutamine, transferrin 150 ⁇ g / mL, and ascorbin were seeded in StemPro34 medium.
- Medium 1.5 mL / well supplemented with acid 50 ⁇ g / mL (sigma), monothioglycerol 4 ⁇ 10 -4 M, 10 ⁇ M Y-27632, 2 ng / mL BMP4 (R & D) and 0.5% Growth Factor Reduced Matrigel.
- the cells were cultured under 37 ° C. and 5% oxygen conditions to form embryoid bodies (day 0).
- the 6-well plate was tilted to allow the embryoid bodies to settle, 80-90% of the medium was removed, and then 1.5 mL of IMDM was added to each well.
- the embryoid body was allowed to settle by tilting the well plate again to allow the embryoid body to settle, and after removing 80 to 90% of the medium, 1% L-glutamine, transferase 150 ⁇ g / mL, ascorbic acid 50 ⁇ g / mL (sigma), were added to StemPro34 medium.
- Monothioglycerol 4 ⁇ 10 -4 M, 10 ng / mL VEGF, 1 ⁇ M IWP-3, 0.6 ⁇ M Dorsomorphin and 5.4 ⁇ M SB431542 were cultured in a medium supplemented with 37 ° C. and 5% oxygen conditions for 3 days. ..
- the 6-well plate was tilted and allowed to settle to settle the embryoid body, and after removing 80 to 90% of the medium, 1% L-glutamine, transferrin 150 ⁇ g / mL, ascorbic acid 50 ⁇ g / StemPro34 medium supplemented with mL (sigma), monothioglycerol 4 ⁇ 10 -4 M and 5 ng / mL VEGF was added.
- the cells were cultured for 8 days at 37 ° C. under 5% oxygen conditions. During this period, the medium was replaced with a medium under the same conditions once every 2 to 3 days.
- the cell culture medium containing the embryoid body was centrifuged at 200 g for 1 minute, and the supernatant was removed with an ejector.
- PBS was added, and the mixture was centrifuged at 200 xg for 1 minute, and the supernatant was removed with an ejector.
- 3 mL of a solution prepared by adding 10 ⁇ g / mL of DNase and 100 ⁇ g / mL of Liberase to IMDM (Iscove's Modified Dulbecco's Media) was added to each tube, and the mixture was allowed to stand at 37 ° C. under normal oxygen conditions for 1 hour.
- the tube was centrifuged at 400 g for 5 minutes and the supernatant was removed so as not to suck the embryoid body.
- 2 mL of a solution prepared by adding 10 ⁇ g / mL of DNase to Accutase (Thermo) was added to each tube, and the mixture was allowed to stand at 37 ° C. under normal oxygen conditions for 10 minutes. After standing, a single cell was formed by pipetting, and 2 mL of a medium prepared by adding 10 ⁇ g / mL of DNase to IMDM was added to each tube and mixed by inversion to prepare a single cell suspension.
- the above single cell suspension was centrifuged at 200 xg for 5 minutes, the supernatant was removed, and the suspension was cryopreserved at ⁇ 80 ° C.
- the cryopreserved cells were thawed in a warm bath at 37 ° C., centrifuged at 400 xg for 5 minutes, and the supernatant was removed. After tapping the cell pellet, 1 mL of PBS containing 1% BSA was added, and the mixture was centrifuged at 300 xg for 3 minutes to remove the supernatant.
- the cardiomyocytes induced to differentiate into myocardium from the reporter iPS cells are CD326-positive cells, CD326-negative CD31-positive cells, CD326-negative CD31-negative CD49a-positive cells, and CD326-negative CD31-negative CD49a-negative due to the difference in expression of these three surface markers.
- the cells were separated into four main cell populations.
- the four cell populations include a population mainly composed of three non-myocardial cells expressing one or more of these three surface markers (a population containing many cells not expressing a myocardial reporter gene) and all three markers. It was a negative myocardial cell population (cell population expressing a myocardial reporter gene). For the cell population in which all three markers were negative, more than 99% were cardiomyocytes (cells expressing the myocardial reporter gene) (Fig. 3).
- Example 2 focusing on the receptor tyrosine kinase found in Example 2, whether or not the receptor tyrosine kinase inhibitor can purify myocardial cells in which the expression of the receptor tyrosine kinase is relatively low is determined under various conditions. It was verified (Test Examples 1 to 9). In Test Examples 1 to 9 below, compound A is N- [5-( ⁇ 2-[(cyclopropanecarbonyl) amino] imidazo [1,2-b] pyridazine-6-yl ⁇ oxy) -2-methyl.
- Test example 1 Verification of cardiomyocyte purification effect by receptor tyrosine kinase inhibitor ⁇ Induction of cardiomyocyte differentiation>
- Human iPS cell lines are prepared by episomal vectors (loading genes; OCT3 / 4, KLF4, SOX2, L-MYC, LIN28, mouse p53DD) using PBMC (LP_167, Sample ID: 201303018) purchased from CTL. (Reference; Okita K, et al. Stem Cells. 2012 Nov29. Doi: 10.10012 / stem.1293) Cell line (parent strain of reporter cells used for staining non-myocardial cells with cell surface markers) was used. ..
- the maintenance culture of the iPS cell line was carried out according to the conventional method (Okita K, et al. Stem Cells. 2012 Nov 29. doi: 10.10012 / stem.1293). Induction of differentiation into cardiomyocytes is performed according to the method described in the paper (Miki et al, Cell Stem Cell. 2015 Jun 4; 16. doi: 10.016 / j. Stem. 2015.04.005.). I went there. VEGF was carried out without addition after Day 8. On the 8th day of differentiation induction, the embryoid bodies were collected in one centrifuge tube and allowed to stand at room temperature for several minutes to allow the embryoid bodies to settle, the supernatant was removed with an aspirator, and the medium was added to carry out medium exchange. bottom.
- the embryoid body was precipitated by tilting the 6-well compound and allowing it to stand for several minutes, the supernatant was removed with an aspirator, and the medium was exchanged for each well by adding a medium. The compound was added by adding 1/100 of the evaluation compound having a concentration 100 times the final concentration as in the case of the eyes.
- the embryoid body was precipitated by tilting a 6-well plate, and the embryoid body was transferred to a 1.5 mL tube with a pipette equipped with a wide-diameter 1 mL pipette tip.
- Cell single-cell formation was performed according to staining of non-cardiomyocytes with cell surface markers, and the single-cell suspension was used for cardiomyocyte marker-positive cell rate measurement and non-cardiomyocyte marker-positive cell rate measurement.
- the cell pellet was stained with the fluorescent dye Alexa647 using an anti-Sarcomeric ⁇ -actinin antibody with 1xPerm / Wash Buffer containing 1% BSA, and then further stained with DAPI (4', 6-Diamidino-2-phenylindole Dihydride). Staining was performed. The rate of Sarcomeric ⁇ -actinin-positive cells was analyzed by measuring the amount of fluorescence signal of Alexa647 in the cell population excluding dead cells (cells having a DNA amount of Sub-G1) by measurement with a flow cytometer.
- compound A N- [5-( ⁇ 2- [(cyclopropanecarbonyl) amino] imidazole [1,2-b] pyridazine-6-yl ⁇ oxy) -2-methylphenyl] -1,3- Treatment with dimethyl-1H-pyrazole-5-carboxamide), AMG337, ASP5878, and BGJ398 increased the myocardial cell rate (Actinin-positive cell rate) as compared with the untreated compound (FIG. 4).
- non-cardiomyocyte marker positive cell rate (non-cardiomyocyte rate)> Using an unfrozen single cell suspension, staining, measurement, and analysis were performed according to staining of non-cardiomyocytes with cell surface markers. As a result, treatment with Compound A, AMG337, ASP5878, and BGJ398 reduced the non-cardiomyocyte rate (cell rate positive for any of CD326, CD31, and CD49a) as compared with the untreated compound (FIG. 5).
- Test example 2 Verification of cardiomyocyte purification effect by receptor tyrosine kinase inhibitor ⁇ Induction of cardiomyocyte differentiation>
- human iPS cells the same cell line as in Test Example 1 was used, and differentiation induction into cardiomyocytes was performed in the same manner.
- the medium exchange was carried out on the 8th, 10th, and 13th days of the differentiation induction, the same method as in Test Example 1 on the 8th and 10th days of the differentiation induction, and 10 of Test Example 1 on the 13th day of the differentiation induction. It was done in the same way as on the day.
- the addition of the evaluation compounds (compounds and concentrations of Experiment Nos. 2 and 3 shown in Table 2 below) was carried out in the same manner as in Test Example 1.
- the addition of ASP5878 of Experiment No. 3 was carried out only on the 8th and 10th days of differentiation induction. Each experiment was performed with 4 wells.
- Test example 3 Verification of cardiomyocyte purification effect by receptor tyrosine kinase inhibitor ⁇ Induction of cardiomyocyte differentiation>
- Human iPS cell lines are prepared by episomal vectors (loading genes; OCT3 / 4, KLF4, SOX2, L-MYC, LIN28, mouse p53DD) using PBMC (LP_140, Sample ID: 20120808) purchased from CTL. (References; Octa K, et al. Stem Cells. 2012 Nov 29. doi: 10.10012 / stem.1293) Cell lines were used. The maintenance culture of the iPS cell line was carried out according to the conventional method (Okita K, et al. Stem Cells. 2012 Nov 29. doi: 10.10012 / stem.1293).
- Induction of differentiation into cardiomyocytes was carried out in the same manner as in Example 1.
- VEGF was carried out without addition after Day 10.
- the medium exchange was carried out on the 8th, 10th, and 13th days of the differentiation induction, the same method as in Test Example 1 on the 8th and 10th days of the differentiation induction, and 10 of Test Example 1 on the 13th day of the differentiation induction. It was done in the same way as on the day.
- the addition of the evaluation compounds (compounds and concentrations of Experiment Nos. 2 to 6 shown in Table 3 below) was carried out in the same manner as in Test Example 1.
- cell single cellization and non-cardiomyocyte rate were measured by the same method as in Test Example 1.
- the treatment with Compound A, Foretinib, ZM323881, Crenolinib, and Crizotinib reduced the non-cardiomyocyte rate as compared with the untreated compound (Fig. 7).
- Test example 4 Verification of cardiomyocyte purification effect by receptor tyrosine kinase inhibitor ⁇ Induction of cardiomyocyte differentiation>
- human iPS cells the same cell line as in Test Example 3 was used, and differentiation induction into cardiomyocytes was performed in the same manner.
- the medium exchange was carried out on the 8th, 10th, and 13th days of the differentiation induction, the same method as in Test Example 1 on the 8th and 10th days of the differentiation induction, and 10 of Test Example 1 on the 13th day of the differentiation induction. It was done in the same way as on the day.
- the addition of the evaluation compounds (compounds and concentrations of Experiment Nos. 2 and 3 shown in Table 4 below) was carried out in the same manner as in Test Example 1. Each experiment was performed with 4 wells.
- the above single-cell suspension was added to IMDM medium prepared to be diluted 5-fold in a 1.5 mL tube, mixed by inversion, and the number of cells was measured with a cell counter NC-200 (Chemometec). ..
- NC-200 Cell counter NC-200 (Chemometec). ..
- about 70% of the cells were recovered by the Foretinib treatment as compared with the untreated cells, and about the same number of cells were recovered by the compound A treatment (FIG. 9).
- Test example 5 Verification of cardiomyocyte purification effect by receptor tyrosine kinase inhibitor ⁇ Induction of cardiomyocyte differentiation>
- human iPS cells the same cell line as in Test Example 3 was used, and differentiation induction into cardiomyocytes was performed in the same manner.
- the medium exchange was carried out on the 8th, 10th, and 13th days of the differentiation induction, the same method as in Test Example 1 on the 8th and 10th days of the differentiation induction, and 10 of Test Example 1 on the 13th day of the differentiation induction. It was done in the same way as on the day.
- the addition of the evaluation compounds (compounds and concentrations of Experiment Nos. 2 to 4 shown in Table 5 below) was carried out in the same manner as in Test Example 1.
- the addition of ASP5878 of Experiment No. 4 was carried out only on the 8th and 10th days of differentiation induction. Each experiment was performed with 4 wells.
- the cell number measurement method was carried out by the method described in Test Example 4. As a result, no significant change was observed in the number of cells recovered with or without compound treatment (Fig. 11).
- Test example 6 Verification of cardiomyocyte purification effect by receptor tyrosine kinase inhibitor ⁇ Induction of cardiomyocyte differentiation> A clinical iPS cell line prepared with CiRA was used. The maintenance culture of the iPS cell line was carried out according to the conventional method (Okita K, et al. Stem Cells. 2012 Nov 29. doi: 10.10012 / stem.1293). Induction of differentiation into cardiomyocytes was carried out according to the method described in the paper (Miki et al, Cell Stem Cell. 2015 Jun 4; 16. doi: 10.016 / j. Stem. 2015.04.005.). ..
- the medium exchange was carried out on the 8th, 10th, 14th, 17th and 21st days of the differentiation induction, the same method as in Test Example 1 on the 8th and 10th days of the differentiation induction, and the 14th day and thereafter of the differentiation induction of Test Example 1. The procedure was the same as on the 10th day. On the 14th, 17th, and 21st days of differentiation induction, the addition of compound A, which is one of the evaluation compounds, was carried out in the same manner as in Test Example 1. Each experiment was performed with 4 wells.
- Test example 7 Verification of cardiomyocyte purification effect by receptor tyrosine kinase inhibitor ⁇ Induction of cardiomyocyte differentiation>
- human iPS cells a clinical iPS cell line prepared with CiRA was used. Using the same cell line as in Test Example 6, induction of differentiation into cardiomyocytes was performed in the same manner. The medium exchange was carried out on the 8th, 10th, and 13th days of the differentiation induction, the same method as in Test Example 1 on the 8th and 10th days of the differentiation induction, and 10 of Test Example 1 on the 13th day of the differentiation induction. It was done in the same way as on the day.
- Test example 8 Verification of cardiomyocyte purification effect by receptor tyrosine kinase inhibitor ⁇ Induction of cardiomyocyte differentiation>
- the same cell line as in Test Example 6 was used, and differentiation induction into cardiomyocytes was also carried out in the same manner.
- the medium exchange was carried out on the 8th, 10th, 13th, 17th and 20th days of the differentiation induction, the 8th day of the differentiation induction was the same method as that of the 8th day of the differentiation induction, and the 10th day and thereafter of the differentiation induction of the test example 1 The procedure was the same as on the 10th day.
- Test example 9 Verification of cardiomyocyte purification effect by receptor tyrosine kinase inhibitor ⁇ Induction of cardiomyocyte differentiation>
- the same cell line as in Test Example 6 was used, and differentiation induction into cardiomyocytes was also carried out in the same manner.
- the medium was exchanged on the 8th day of the differentiation induction in the same manner as on the 8th day of Test Example 1, and on the 10th and 13th days of the differentiation induction in the same manner as on the 10th day of Test Example 1.
- the addition of the evaluation compounds (compounds and concentrations of Experiment Nos. 2 and 3 shown in Table 9 below) was carried out in the same manner as in Test Example 1. Each experiment number was carried out in 4 wells.
- cell number measurement was performed in the same manner as in Test Example 1 for cell single cell formation, fixation, cardiomyocyte rate (Sarcomeric ⁇ -actinin positive cell rate) measurement, and non-cardiomyocyte rate measurement. It was carried out in the same manner as in 4.
- the treatment with Foretinib and Crizotinib increased the cardiomyocyte rate (Fig. 19) and decreased the non-cardiomyocyte rate (Fig. 20).
- 80% of the cells were recovered by Crizotinib, and about the same number of cells were recovered by the Foretinib treatment (Fig. 21).
- cardiomyocytes in the embryoid body can be purified in various cell lines by a simple treatment of adding various types of receptor tyrosine kinase inhibitors to the medium.
- Table 10 shows the receptor tyrosine kinases that are the targets of each compound used in Test Examples 1 to 9.
- the present invention provides a cell population containing cardiomyocytes with high purity. Such a cell population is useful because it can be suitably used for cell transplantation therapy for heart disease and screening of therapeutic agents for heart disease.
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Zoology (AREA)
- Cell Biology (AREA)
- Organic Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Cardiology (AREA)
- Biotechnology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Genetics & Genomics (AREA)
- Wood Science & Technology (AREA)
- Epidemiology (AREA)
- Developmental Biology & Embryology (AREA)
- Pharmacology & Pharmacy (AREA)
- Urology & Nephrology (AREA)
- Vascular Medicine (AREA)
- Dermatology (AREA)
- Transplantation (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Botany (AREA)
- Microbiology (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Heart & Thoracic Surgery (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Rheumatology (AREA)
- Virology (AREA)
- Immunology (AREA)
- Hospice & Palliative Care (AREA)
- Hematology (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
Description
近年、心筋梗塞の発生率は減少してきてはいるものの、心筋梗塞を含む心疾患は世界中で依然として主な死亡原因である。重症心不全患者においては、心臓移植が現在唯一の治療法であるが、心臓移植はドナー不足という問題を抱えている。そこで、心筋細胞を用いた細胞治療が、心疾患を改善させる治療法として注目されてきている。また、心筋細胞を用いたインビトロでの薬効評価試験、あるいは薬剤安全性試験の確立にも着目されている。そのため、細胞治療やインビトロでの試験に用いることのできる均一な心筋細胞の安定的な供給が求められている。
[1]心筋細胞を含む細胞集団を製造する方法であって、
(1)多能性幹細胞を心筋細胞分化用培地中で培養して得られた、心筋細胞または心筋前駆細胞とその他の細胞とを含む細胞集団に、受容体型チロシンキナーゼ阻害剤(但し、EGF受容体阻害剤を除く。)を接触させる工程、および
(2)該細胞集団を培養する工程、
を含む、方法。
[2]前記工程(1)の細胞集団と受容体型チロシンキナーゼ阻害剤との接触が、多能性幹細胞の分化誘導開始から4日目以降に行われる、[1]に記載の方法。
[3]前記工程(1)の細胞集団と受容体型チロシンキナーゼ阻害剤との接触が1日以上行われる、[1]または[2]に記載の方法。
[4]前記阻害剤が、VEGF受容体、PDGF受容体、HGF受容体およびFGF受容体からなる群から選択される少なくとも1つの受容体型チロシンキナーゼに対する阻害剤である、[1]~[3]のいずれかに記載の方法。
[5]前記阻害剤が、N-[5-({2-[(シクロプロパンカルボニル)アミノ]イミダゾ[1,2-b]ピリダジン-6-イル}オキシ)-2-メチルフェニル]-1,3-ジメチル-1H-ピラゾール-5-カルボキサミド、N-{4-[(6,7-ジメトキシキノリン-4-イル)オキシ]-3-フルオロフェニル}-N’-(4-フルオロフェニル)シクロプロパン-1,1-ジカルボキサミド、AMG337、ASP5878、BGJ398、Foretinib、ZM323881、CP-673451、CrenolanibおよびCrizotinibからなる群から選択される少なくとも1種である、[1]~[4]のいずれかに記載の方法。
[6]前記多能性幹細胞が人工多能性幹細胞である、[1]~[5]のいずれかに記載の方法。
[7][1]~[6]のいずれかに記載の方法により得られた、心筋細胞を含む細胞集団。
[8][7]に記載の細胞集団を含有してなる、細胞移植療法剤。
[9]心筋細胞を精製する方法であって、
(1)多能性幹細胞を心筋細胞分化用培地中で培養して得られた、心筋細胞または心筋前駆細胞とその他の細胞とを含む細胞集団に、受容体型チロシンキナーゼ阻害剤を接触させる工程、および
(2)該細胞集団を培養する工程、
を含む、方法。
1.心筋細胞を含む細胞集団の製造方法
本発明は、心筋細胞を含む細胞集団を製造する方法(以下、「本発明の製法」ともいう)を提供する。本発明の製法は、(1)心筋細胞または心筋前駆細胞とその他の細胞とを含む細胞集団に、受容体型チロシンキナーゼ阻害剤を接触させる工程、および(2)該細胞集団を培養する工程、を含む。本発明の製法において、上記(1)における「受容体型チロシンキナーゼ阻害剤」からは、EGF受容体阻害剤は除かれる。
このほか、公開されているすべての論文(例えば、Shi Y.,DingS.,et al.,Cell Stem Cell,(2008)Vol3, Issue 5,568-574;、Kim JB.,Scholer HR.,et al.,Nature,(2008)454,646-650;Huangfu D.,Melton,DA.,et al.,Nature Biotechnology,(2008)26,No 7,795-797)、あるいは特許(例えば、特開2008-307007号、特開2008-283972号、US2008-2336610、US2009-047263、WO2007-069666、WO2008-118220、WO2008-124133、WO2008-151058、WO2009-006930、WO2009-006997、WO2009-007852)に記載されている当該分野で公知の人工多能性幹細胞のいずれも用いることができる。人工多能性幹細胞株としては、NIH、理研、京都大学等が樹立した各種iPS細胞株が利用可能である。例えば、ヒトiPS細胞株であれば、理研のHiPS-RIKEN-1A株、HiPS-RIKEN-2A株、HiPS-RIKEN-12A株、Nips-B2株、京都大学の253G1株、201B7株、409B2株、454E2株、606A1株、610B1株、648A1株、再生医療用iPS細胞ストック等が挙げられる。
上記化合物またはその塩は、自体公知の方法に従って、それぞれ製造することができる。
無機塩基との塩の好適な例としては、ナトリウム塩、カリウム塩等のアルカリ金属塩;カルシウム塩、マグネシウム塩等のアルカリ土類金属塩;アルミニウム塩;アンモニウム塩等が挙げられる。
有機塩基との塩の好適な例としては、トリメチルアミン、トリエチルアミン、ピリジン、ピコリン、エタノールアミン、ジエタノールアミン、トリエタノールアミン、トロメタミン[トリス(ヒドロキシメチル)メチルアミン]、tert-ブチルアミン、シクロヘキシルアミン、ベンジルアミン、ジシクロヘキシルアミン、N,N-ジベンジルエチレンジアミン等との塩が挙げられる。
無機酸との塩の好適な例としては、塩酸、臭化水素酸、硝酸、硫酸、リン酸等との塩が挙げられる。
有機酸との塩の好適な例としては、ギ酸、酢酸、トリフルオロ酢酸、フタル酸、フマル酸、シュウ酸、酒石酸、マレイン酸、クエン酸、コハク酸、リンゴ酸、メタンスルホン酸、ベンゼンスルホン酸、p-トルエンスルホン酸等との塩が挙げられる。
塩基性アミノ酸との塩の好適な例としては、アルギニン、リジン、オルニチン等との塩が挙げられる。
酸性アミノ酸との塩の好適な例としては、アスパラギン酸、グルタミン酸等との塩が挙げられる。
また、上記化合物は、同位元素(例、2H、3H、11C、14C、18F、35S、125Iなど)などで標識または置換された化合物であってもよい。
1Hを2H(D)に変換した重水素変換体も、上記化合物に包含される。
互変異性体も、上記化合物に包含される。
上記化合物は、薬学的に許容され得る共結晶または共結晶塩であってもよい。ここで、共結晶または共結晶塩とは、各々が異なる物理的特性(例えば、構造、融点、融解熱、吸湿性、溶解性および安定性等)を持つ、室温で二種またはそれ以上の独特な固体から構成される結晶性物質を意味する。共結晶または共結晶塩は、自体公知の共結晶化法に従い製造することができる。
本発明はまた、本発明の製法または精製方法により得られた、心筋細胞を含む細胞集団(以下、「本発明の細胞集団」ともいう)を提供する。上述の通り、本発明の細胞集団は、高い純度で心筋細胞を含む。高い純度とは、細胞集団中の心筋細胞の割合(細胞集団中の心筋細胞数/細胞集団中の全細胞数)が、具体的には、80%以上(例:85%、90%、91%、92%、93%、94%、95%、96%、97%、98%、99%またはそれ以上)の高純度で含むことを意味する。当然のことながら、上記心筋細胞の割合は、上記細胞集団と、間葉系幹細胞などの他の細胞または細胞集団とを混合して用いる場合には、他の細胞または細胞集団を混合する前の割合を指す。好ましい態様において、本発明の細胞集団は、多能性幹細胞から心筋細胞を誘導する従来の方法で得られる細胞集団よりも、高い割合で心筋細胞を含む。かかる細胞集団は、セルソーティングなどによりさらに精製してもよく、このように精製された細胞集団もまた、「本発明の細胞集団」に包含されるものとする。
本発明はまた、本発明の細胞集団を含有してなる、細胞移植療法剤(以下、「本発明の細胞移植療法剤」ともいう)を提供する。本発明の細胞移植療法剤は、自家移植に用いてもよく、他家移植に用いてもよい。また、他の薬剤、例えば免疫抑制剤、と併用してもよい。上述の通り、本発明の細胞集団は、高純度で心筋細胞を含むため、本発明の細胞集団は、細胞移植療法剤の原料として用いることに適しており、本発明の細胞集団または本発明の細胞移植療法剤は、心疾患の治療または予防に有用である。従って、本発明の細胞集団または細胞移植療法剤の有効量を治療または予防の対象とする哺乳動物(例:ヒト、マウス、ラット、サル、ウシ、ウマ、ブタ、イヌ等)に投与または移植する、心疾患の治療または予防方法も本発明に包含される。治療または予防の対象とする心疾患としては、心不全、虚血性心疾患、心筋梗塞、心筋症、心筋炎、肥大型心筋症、拡張相肥大型心筋症、拡張型心筋症などの疾患または障害による欠損などが挙げられるが、これらに限定されない。
国立大学法人京都大学iPS細胞研究所(CiRA)で作製された臨床用iPS細胞株の評価用株を使用した。iPS細胞株の維持培養は従来法に準じて行った(Okita K,et al.Stem Cells.2012 Nov 29.doi:10.1002/stem.1293)。心筋細胞への分化誘導は、論文(Miki et al,Cell Stem Cell.2015 Jun 4;16.doi:10.1016/j.stem.2015.04.005.)に記載の方法に準じて行った。分化誘導開始後22日目の心筋細胞について10XGenomics社のChromiumを用いてシングルセルRNA sequence解析を行った。ソフトウェア(Cellranger、Seurat、Loupe Cell Browser)により細胞のクラスタリングと各クラスタの解析を行った。iPS細胞から心筋細胞に分化誘導した細胞集団中には、sarcomeric-α-actininとcardiac Troponin Tを発現する心筋細胞集団の他に、sarcomeric-α-actininとcardiac Troponin Tを発現しない3つの非心筋細胞集団(遺伝子発現から平滑筋様の細胞(SMC)、内皮様の細胞(EC)、内胚葉系譜の細胞(END)と考えられる)が、存在していることを見出した(図1)。
シングルセルRNAシークエンシングデータのLoupe Cell Browserによる解析で受容体型チロシンキナーゼの遺伝子発現の解析を行った。その結果、PDGFRA、PDGFRB、VEGFR1、VEGFR2、c-Met(HGFR)、FGFR4等の受容体型チロシンキナーゼの遺伝子発現が非心筋細胞集団において高く、心筋細胞集団では高くないことを見出した(図2)。
TNNI1の遺伝子座にEmGFP(配列番号1)、TNNI3の遺伝子座にmCherry(配列番号2)のレポータータンパク質の配列を挿入したダブルノックインのヒトiPS細胞株を作製した。ヒトiPS細胞株の作製はCTL社より購入したPBMC(LP_167,Sample ID:20130318)を用いてエピソーマルベクター(搭載遺伝子;OCT3/4,KLF4,SOX2,L-MYC,LIN28,mouse p53DD)により行った(参考文献;Okita K,et al.Stem Cells.2012 Nov 29.doi:10.1002/stem.1293)。
心筋細胞への分化誘導は論文(Miki et al,Cell Stem Cell.2015 Jun 4;16.doi:10.1016/j.stem.2015.04.005.)に記載の方法に準じて6 well plateで行った。簡潔に説明すれば、心筋細胞への分化誘導は、レポーターiPS細胞株を0.5mM EDTA/PBSで1/2に希釈したTrypLE select(ライフテクノロジーズ)で4~5分処理後、セルスクレーパー(IWAKI)で細胞を剥離し、ピペッティングによりシングルセルへと解離した。1,000rpm,5minの遠心分離により培地を除去し、得られた細胞を、6ウェルプレート1ウェルあたり2×106cells播種して、StemPro34培地に1%L-グルタミン、トランスフェリン150μg/mL、アスコルビン酸50μg/mL(sigma)、モノチオグリセロール4×10-4M、10μM Y-27632、2ng/mL BMP4(R&D)および0.5%Growth Factor Reduced Matrigelを添加した培地1.5mL/wellで、37℃、5%酸素条件下にて培養して、胚様体を形成させた(0日目)。
翌日(1日目)、StemPro34培地に1%L-グルタミン、トランスフェリン150μg/mL、アスコルビン酸50μg/mL(sigma)、モノチオグリセロール4×10-4M、2ng/mL BMP4(R&D)アクチビンA 12ng/mL、bFGF 5ng/mL、BMP4 18ng/mLを加えた培地を各ウェルに1.5mL添加し、37℃、5%酸素条件にてさらに2日間培養した。
続いて(3日目)、6ウェルプレートを傾けて静置して胚様体を沈降させ、培地の80~90%除去した後、各ウェルにIMDMを1.5mL添加した。再びウェルプレートを傾けて静置して胚様体を沈降させ、培地の80~90%除去した後、StemPro34培地に1%L-グルタミン、トランスフェリン150μg/mL、アスコルビン酸50μg/mL(sigma)、モノチオグリセロール4×10-4M、10ng/mL VEGF、1μM IWP-3、0.6μM Dorsomorphinおよび5.4μM SB431542を添加した培地中で、37℃、5%酸素条件下で、3日間培養した。
続いて(6日目)、6ウェルプレートを傾けて静置して胚様体を沈降させ、培地の80~90%除去した後、1%L-グルタミン、トランスフェリン150μg/mL、アスコルビン酸50μg/mL(sigma)、モノチオグリセロール4×10-4Mおよび5ng/mL VEGFを添加したStemPro34培地を添加した。8日間、37℃、5%酸素条件下で培養した。この間、2~3日に1度同じ条件の培地に交換した。
上記のシングルセル懸濁液を、200xgで5分間遠心後、上清を除去し、-80℃で凍結保存した。
凍結保存した細胞を、37℃の温浴につけて融解し、400xgで5分間遠心後、上清を除去した。
細胞ペレットをタッピング後、1%BSAを含むPBSを1mL加え、300xgで3分間遠心し、上清を除去した。1%BSAを含むPBSでAPCFire750標識抗CD326抗体、PE標識抗CD49a抗体、BV605標識抗CD31抗体、DAPIを用いて染色した。DAPI陽性の死細胞を除去した上で、核細胞の各蛍光色素のシグナル量を測定することで、細胞集団の分離と各細胞集団の割合を測定した。
上記レポーターiPS細胞から心筋に分化誘導した心筋細胞は、これらの3つの表面マーカーの発現の違いにより、CD326陽性細胞、CD326陰性CD31陽性細胞、CD326陰性CD31陰性CD49a陽性細胞、CD326陰性CD31陰性CD49a陰性細胞の主に4つの細胞集団に分離された。4つの細胞集団は、これら3つの表面マーカーのいずれかまたは複数を発現する、3つの非心筋細胞を主とする集団(心筋レポーター遺伝子を発現しない細胞を多く含む集団)と、3つのマーカー全てが陰性の心筋細胞集団(心筋レポーター遺伝子を発現する細胞集団)であった。3つのマーカー全てが陰性の細胞集団については、その99%以上が、心筋細胞(心筋レポーター遺伝子を発現する細胞)であった(図3)。
以下の試験例1~9において、化合物AとはN-[5-({2-[(シクロプロパンカルボニル)アミノ]イミダゾ[1,2-b]ピリダジン-6-イル}オキシ)-2-メチルフェニル]-1,3-ジメチル-1H-ピラゾール-5-カルボキサミドであり、化合物BとはN-{4-[(6,7-ジメトキシキノリン-4-イル)オキシ]-3-フルオロフェニル}-N’-(4-フルオロフェニル)シクロプロパン-1,1-ジカルボキサミドを表す。
<心筋細胞への分化誘導>
ヒトiPS細胞株は、CTL社より購入したPBMC(LP_167,Sample ID:20130318)を用いてエピソーマルベクター(搭載遺伝子;OCT3/4,KLF4,SOX2,L-MYC,LIN28,mouse p53DD)により作製された(参考文献;Okita K,et al.Stem Cells.2012 Nov29.doi:10.1002/stem.1293)細胞株(細胞表面マーカーによる非心筋細胞の染色で使用したレポーター細胞の親株)を使用した。
iPS細胞株の維持培養は従来法に準じて行った(Okita K,et al.Stem Cells.2012 Nov 29.doi:10.1002/stem.1293)。心筋細胞への分化誘導は論文(Miki et al,Cell Stem Cell.2015 Jun 4;16.doi:10.1016/j.stem.2015.04.005.)に記載の方法に準じて6 well plateで行った。VEGFについてはDay8以降は添加せずに実施した。
分化誘導8日目に、胚様体を1つの遠心チューブに集め室温で数分間静置して胚様体を沈降させ、上清をアスピレーターで取り除き、培地を添加することで、培地交換を実施した。胚様体懸濁液を6 well plateに移し、最終濃度の100倍濃度の評価化合物(以下の表1に示す実験番号2から8の化合物と濃度)を各ウェルに100分の1量添加後、プレートを攪拌し、細胞培養を行った。
上記のシングルセル懸濁液を1.5mLチューブに分注後、400gで3分間遠心し、上清を除去した。細胞ペレットをCytofix/Cytoperm Fixation/Permeabilization Solution(BD)に再懸濁して室温で15分静置し、固定した。各チューブに1xPerm/Wash Buffer 1mLを添加し、1500gで3分間遠心後、上清を除去することで細胞を洗浄した。細胞ペレットをタッピング後に、1xPerm/Wash Buffer 1mLを添加し、同様の操作を行うことで細胞を洗浄した。細胞ペレットはタッピング後、1%BSA を含む1xPerm/Wash Bufferで抗Sarcomeric α-actinin抗体を用いて、蛍光色素Alexa647で染色後、さらにDAPI(4’,6-Diamidino-2-phenylindole Dihydrochloride)でDNA染色を行った。フローサイトメーターによる測定で、死細胞(DNA量がSub-G1の細胞)を除いた細胞集団のAlexa647の蛍光シグナル量を測定することで、Sarcomeric α-actinin陽性の細胞率の解析を行った。その結果、化合物A(N-[5-({2-[(シクロプロパンカルボニル)アミノ]イミダゾ[1,2-b]ピリダジン-6-イル}オキシ)-2-メチルフェニル]-1,3-ジメチル-1H-ピラゾール-5-カルボキサミド)、AMG337、ASP5878、BGJ398処理により、化合物未処理に比べ心筋細胞率(Actinin陽性細胞率)が増加した(図4)。
未凍結のシングルセル懸濁液を用いて、細胞表面マーカーによる非心筋細胞の染色に準じて、染色、測定、解析を実施した。その結果、化合物A、AMG337、ASP5878、BGJ398処理により、化合物未処理に比べ、非心筋細胞率(CD326、CD31、CD49aいずれかが陽性の細胞率)が減少した(図5)。
<心筋細胞への分化誘導>
ヒトiPS細胞は試験例1と同じ細胞株を用い、心筋細胞への分化誘導についても同様の方法で行った。培地交換は分化誘導8日目、10日目、13日目に実施し、分化誘導8日目、10日目は試験例1と同様の方法で、分化誘導13日目は試験例1の10日目と同様の方法で行った。分化誘導8日目、10日目、13日目は評価化合物(以下の表2に示す実験番号2、3の化合物と濃度)の添加を試験例1と同様の方法で実施した。ただし、実験番号3のASP5878の添加は分化誘導8日目と10日目のみで実施した。各実験について4ウェルずつで実施した。
<心筋細胞への分化誘導>
ヒトiPS細胞株は、CTL社より購入したPBMC(LP_140,Sample ID:20120808)を用いてエピソーマルベクター(搭載遺伝子;OCT3/4,KLF4,SOX2,L-MYC,LIN28,mouse p53DD)により作製された(参考文献;Okita K,et al.Stem Cells.2012 Nov 29.doi:10.1002/stem.1293)細胞株を使用した。
iPS細胞株の維持培養は従来法に準じて行った(Okita K,et al.Stem Cells.2012 Nov 29.doi:10.1002/stem.1293)。心筋細胞への分化誘導は実施例1と同様の方法で行った。VEGFについてはDay10以降は添加せずに実施した。
培地交換は分化誘導8日目、10日目、13日目に実施し、分化誘導8日目、10日目は試験例1と同様の方法で、分化誘導13日目は試験例1の10日目と同様の方法で行った。分化誘導8日目、10日目、13日目は評価化合物(以下の表3に示す実験番号2から6の化合物と濃度)の添加を試験例1と同様の方法で実施した。
<心筋細胞への分化誘導>
ヒトiPS細胞は試験例3と同じ細胞株を用い、心筋細胞への分化誘導についても同様の方法で行った。
培地交換は分化誘導8日目、10日目、13日目に実施し、分化誘導8日目、10日目は試験例1と同様の方法で、分化誘導13日目は試験例1の10日目と同様の方法で行った。分化誘導8日目、10日目、13日目は評価化合物(以下の表4に示す実験番号2、3の化合物と濃度)の添加を試験例1と同様の方法で実施した。各実験について4ウェルずつで実施した。
<心筋細胞への分化誘導>
ヒトiPS細胞は試験例3と同じ細胞株を用い、心筋細胞への分化誘導についても同様の方法で行った。
培地交換は分化誘導8日目、10日目、13日目に実施し、分化誘導8日目、10日目は試験例1と同様の方法で、分化誘導13日目は試験例1の10日目と同様の方法で行った。分化誘導8日目、10日目、13日目は評価化合物(以下の表5に示す実験番号2から4の化合物と濃度)の添加を試験例1と同様の方法で実施した。ただし、実験番号4のASP5878の添加は分化誘導8日目と10日目のみで実施した。各実験について4ウェルずつで実施した。
<心筋細胞への分化誘導>
CiRAで作製された臨床用iPS細胞株を使用した。iPS細胞株の維持培養は従来法に準じて行った(Okita K,et al.Stem Cells.2012 Nov 29.doi:10.1002/stem.1293)。心筋細胞への分化誘導は、論文(Miki et al,Cell Stem Cell.2015 Jun 4;16.doi:10.1016/j.stem.2015.04.005.)に記載の方法に準じて行った。
培地交換は分化誘導8、10、14、17、21日目に実施し、分化誘導8日目、10日目は試験例1と同様の方法で、分化誘導14日目以降は試験例1の10日目と同様の方法で行った。
分化誘導14日目、17日目、21日目は評価化合物の1つである化合物Aの添加を試験例1と同様の方法で実施した。各実験について4ウェルずつで実施した。
<心筋細胞への分化誘導>
ヒトiPS細胞は、CiRAで作製された臨床用iPS細胞株を使用した。試験例6と同じ細胞株を用い、心筋細胞への分化誘導についても同様の方法で行った。
培地交換は分化誘導8日目、10日目、13日目に実施し、分化誘導8日目、10日目は試験例1と同様の方法で、分化誘導13日目は試験例1の10日目と同様の方法で行った。分化誘導8日目、10日目、13日目は評価化合物(以下の表7に示す実験番号2から9の化合物と濃度、の添加を試験例1と同様の方法で実施した(実験番号1については2ウェル、他は1ウェルで実施した)。
<心筋細胞への分化誘導>
ヒトiPS細胞は試験例6と同じ細胞株を用い、心筋細胞への分化誘導についても同様の方法で行った。
培地交換は分化誘導8、10、13、17、20日目に実施し、分化誘導8日目は試験例1の8日目と同様の方法で、分化誘導10日目以降は試験例1の10日目と同様の方法で行った。分化誘導8、10、13、17、20日目は評価化合物Crenolanibの添加を表8に記載の条件に従い試験例1と同様の方法で実施した。実験番号4は分化誘導8日目以降、実験番号2、3は分化誘導10日目以降から、実験番号5は分化誘導13日目以降から化合物の添加を行った。実験番号1は4ウェル、実験番号2、3は3ウェル、実験番号4、5については1ウェルで実施した。
<心筋細胞への分化誘導>
ヒトiPS細胞は試験例6と同じ細胞株を用い、心筋細胞への分化誘導についても同様の方法で行った。
培地交換は、分化誘導8日目は試験例1の8日目と同様の方法で、分化誘導10日目、13日目は試験例1の10日目と同様の方法で行った。分化誘導8、10、13日目は評価化合物(以下の表9に示す実験番号2、3の化合物と濃度)の添加を試験例1と同様の方法で実施した。各実験番号4ウェルで実施した。
本出願は日本で出願された特願2020-050268(出願日:2020年3月19日)を基礎としており、その内容は本明細書に全て包含されるものである。
Claims (9)
- 心筋細胞を含む細胞集団を製造する方法であって、
(1)多能性幹細胞を心筋細胞分化用培地中で培養して得られた、心筋細胞または心筋前駆細胞とその他の細胞とを含む細胞集団に、受容体型チロシンキナーゼ阻害剤(但し、EGF受容体阻害剤を除く。)を接触させる工程、および
(2)該細胞集団を培養する工程、
を含む、方法。 - 前記工程(1)の細胞集団と受容体型チロシンキナーゼ阻害剤との接触が、多能性幹細胞の分化誘導開始から4日目以降に行われる、請求項1に記載の方法。
- 前記工程(1)の細胞集団と受容体型チロシンキナーゼ阻害剤との接触が1日以上行われる、請求項1または2に記載の方法。
- 前記阻害剤が、VEGF受容体、PDGF受容体、HGF受容体およびFGF受容体からなる群から選択される少なくとも1つの受容体型チロシンキナーゼに対する阻害剤である、請求項1~3のいずれか1項に記載の方法。
- 前記阻害剤が、N-[5-({2-[(シクロプロパンカルボニル)アミノ]イミダゾ[1,2-b]ピリダジン-6-イル}オキシ)-2-メチルフェニル]-1,3-ジメチル-1H-ピラゾール-5-カルボキサミド、N-{4-[(6,7-ジメトキシキノリン-4-イル)オキシ]-3-フルオロフェニル}-N’-(4-フルオロフェニル)シクロプロパン-1,1-ジカルボキサミド、AMG337、ASP5878、BGJ398、Foretinib、ZM323881、CP-673451、CrenolanibおよびCrizotinibからなる群から選択される少なくとも1種である、請求項1~4のいずれか1項に記載の方法。
- 前記多能性幹細胞が人工多能性幹細胞である、請求項1~5のいずれか1項に記載の方法。
- 請求項1~6のいずれか1項に記載の方法により得られた、心筋細胞を含む細胞集団。
- 請求項7に記載の細胞集団を含有してなる、細胞移植療法剤。
- 心筋細胞を精製する方法であって、
(1)多能性幹細胞を心筋細胞分化用培地中で培養して得られた、心筋細胞または心筋前駆細胞とその他の細胞とを含む細胞集団に、受容体型チロシンキナーゼ阻害剤を接触させる工程、および
(2)該細胞集団を培養する工程、
を含む、方法。
Priority Applications (9)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| BR112022018640A BR112022018640A2 (pt) | 2020-03-19 | 2021-03-18 | Métodos para produzir uma população de células compreendendo cardiomiócitos e para purificar cardiomiócitos, população de células contendo cardiomiócitos, e, agente para terapia de transplante de células |
| JP2022508444A JPWO2021187601A1 (ja) | 2020-03-19 | 2021-03-18 | |
| CN202180022395.3A CN115885035A (zh) | 2020-03-19 | 2021-03-18 | 心肌细胞的精制方法 |
| KR1020227034233A KR20220149592A (ko) | 2020-03-19 | 2021-03-18 | 심근세포 정제 방법 |
| IL296317A IL296317A (en) | 2020-03-19 | 2021-03-18 | A method for purifying the cells of the heart |
| AU2021239654A AU2021239654A1 (en) | 2020-03-19 | 2021-03-18 | Cardiomyocyte purification method |
| US17/912,281 US20230136878A1 (en) | 2020-03-19 | 2021-03-18 | Cardiomyocyte purification method |
| EP21772329.5A EP4123015A4 (en) | 2020-03-19 | 2021-03-18 | METHOD FOR PURIFYING CARDIOMYOCYTES |
| CA3175573A CA3175573A1 (en) | 2020-03-19 | 2021-03-18 | Cardiomyocyte purification method |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020050268 | 2020-03-19 | ||
| JP2020-050268 | 2020-03-19 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2021187601A1 true WO2021187601A1 (ja) | 2021-09-23 |
Family
ID=77768142
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2021/011231 WO2021187601A1 (ja) | 2020-03-19 | 2021-03-18 | 心筋細胞の精製方法 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US20230136878A1 (ja) |
| EP (1) | EP4123015A4 (ja) |
| JP (1) | JPWO2021187601A1 (ja) |
| KR (1) | KR20220149592A (ja) |
| CN (1) | CN115885035A (ja) |
| AU (1) | AU2021239654A1 (ja) |
| BR (1) | BR112022018640A2 (ja) |
| CA (1) | CA3175573A1 (ja) |
| IL (1) | IL296317A (ja) |
| TW (1) | TW202200783A (ja) |
| WO (1) | WO2021187601A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024020587A2 (en) | 2022-07-22 | 2024-01-25 | Tome Biosciences, Inc. | Pleiopluripotent stem cell programmable gene insertion |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20230212519A1 (en) * | 2020-03-19 | 2023-07-06 | Orizuru Therapeutics, Inc. | Method for purifying cardiomyocytes |
Citations (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5843780A (en) | 1995-01-20 | 1998-12-01 | Wisconsin Alumni Research Foundation | Primate embryonic stem cells |
| WO2007069666A1 (ja) | 2005-12-13 | 2007-06-21 | Kyoto University | 核初期化因子 |
| US20080236610A1 (en) | 2004-04-10 | 2008-10-02 | Holger Bartels | Hair Rollers |
| WO2008118220A2 (en) | 2006-11-28 | 2008-10-02 | Veritainer Corporation | Radiation detection unit for mounting a radiation sensor to a container crane |
| WO2008124133A1 (en) | 2007-04-07 | 2008-10-16 | Whitehead Institute For Biomedical Research | Reprogramming of somatic cells |
| WO2008151058A2 (en) | 2007-05-30 | 2008-12-11 | The General Hospital Corporation | Methods of generating pluripotent cells from somatic cells |
| JP2008307007A (ja) | 2007-06-15 | 2008-12-25 | Bayer Schering Pharma Ag | 出生後のヒト組織由来未分化幹細胞から誘導したヒト多能性幹細胞 |
| US20090047263A1 (en) | 2005-12-13 | 2009-02-19 | Kyoto University | Nuclear reprogramming factor and induced pluripotent stem cells |
| WO2009146408A1 (en) | 2008-05-30 | 2009-12-03 | Summa Health Systems Llc | Methods for using tgf-b receptor inhibitors or activin-like kinase (alk) 5 inhibitors a-83-01 and sb-431542 to treat eye disease and wound healing conditions |
| WO2011007900A1 (ja) | 2009-07-15 | 2011-01-20 | Dezawa Mari | 生体組織から単離できる多能性幹細胞 |
| JP2017108705A (ja) * | 2015-12-18 | 2017-06-22 | 国立大学法人京都大学 | 心筋細胞の製造方法 |
| JP2018510649A (ja) * | 2015-02-17 | 2018-04-19 | ユニバーシティー ヘルス ネットワーク | 洞房結節様ペースメーカー心筋細胞および心室様心筋細胞を作製および使用するための方法 |
| JP2020050268A (ja) | 2018-09-28 | 2020-04-02 | いすゞ自動車株式会社 | 車両のボディ構造 |
-
2021
- 2021-03-18 TW TW110109790A patent/TW202200783A/zh unknown
- 2021-03-18 EP EP21772329.5A patent/EP4123015A4/en active Pending
- 2021-03-18 AU AU2021239654A patent/AU2021239654A1/en active Pending
- 2021-03-18 IL IL296317A patent/IL296317A/en unknown
- 2021-03-18 CN CN202180022395.3A patent/CN115885035A/zh active Pending
- 2021-03-18 WO PCT/JP2021/011231 patent/WO2021187601A1/ja unknown
- 2021-03-18 JP JP2022508444A patent/JPWO2021187601A1/ja active Pending
- 2021-03-18 BR BR112022018640A patent/BR112022018640A2/pt unknown
- 2021-03-18 US US17/912,281 patent/US20230136878A1/en active Pending
- 2021-03-18 KR KR1020227034233A patent/KR20220149592A/ko unknown
- 2021-03-18 CA CA3175573A patent/CA3175573A1/en active Pending
Patent Citations (17)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5843780A (en) | 1995-01-20 | 1998-12-01 | Wisconsin Alumni Research Foundation | Primate embryonic stem cells |
| US20080236610A1 (en) | 2004-04-10 | 2008-10-02 | Holger Bartels | Hair Rollers |
| WO2007069666A1 (ja) | 2005-12-13 | 2007-06-21 | Kyoto University | 核初期化因子 |
| JP2008283972A (ja) | 2005-12-13 | 2008-11-27 | Kyoto Univ | 誘導多能性幹細胞の製造方法 |
| US20090047263A1 (en) | 2005-12-13 | 2009-02-19 | Kyoto University | Nuclear reprogramming factor and induced pluripotent stem cells |
| WO2008118220A2 (en) | 2006-11-28 | 2008-10-02 | Veritainer Corporation | Radiation detection unit for mounting a radiation sensor to a container crane |
| WO2008124133A1 (en) | 2007-04-07 | 2008-10-16 | Whitehead Institute For Biomedical Research | Reprogramming of somatic cells |
| WO2008151058A2 (en) | 2007-05-30 | 2008-12-11 | The General Hospital Corporation | Methods of generating pluripotent cells from somatic cells |
| WO2009006930A1 (en) | 2007-06-15 | 2009-01-15 | Izumi Bio, Inc. | Human pluripotent stem cells induced from undifferentiated stem cells derived from a human postnatal tissue |
| WO2009006997A1 (en) | 2007-06-15 | 2009-01-15 | Izumi Bio, Inc. | Human pluripotent stem cells and their medical use |
| WO2009007852A2 (en) | 2007-06-15 | 2009-01-15 | Izumi Bio, Inc | Multipotent/pluripotent cells and methods |
| JP2008307007A (ja) | 2007-06-15 | 2008-12-25 | Bayer Schering Pharma Ag | 出生後のヒト組織由来未分化幹細胞から誘導したヒト多能性幹細胞 |
| WO2009146408A1 (en) | 2008-05-30 | 2009-12-03 | Summa Health Systems Llc | Methods for using tgf-b receptor inhibitors or activin-like kinase (alk) 5 inhibitors a-83-01 and sb-431542 to treat eye disease and wound healing conditions |
| WO2011007900A1 (ja) | 2009-07-15 | 2011-01-20 | Dezawa Mari | 生体組織から単離できる多能性幹細胞 |
| JP2018510649A (ja) * | 2015-02-17 | 2018-04-19 | ユニバーシティー ヘルス ネットワーク | 洞房結節様ペースメーカー心筋細胞および心室様心筋細胞を作製および使用するための方法 |
| JP2017108705A (ja) * | 2015-12-18 | 2017-06-22 | 国立大学法人京都大学 | 心筋細胞の製造方法 |
| JP2020050268A (ja) | 2018-09-28 | 2020-04-02 | いすゞ自動車株式会社 | 車両のボディ構造 |
Non-Patent Citations (42)
| Title |
|---|
| "NCBI", Database accession no. NM_025237 |
| CIBELLI J.B. ET AL., NATURE BIOTECHNOL., vol. 16, 1998, pages 642 - 646 |
| HUANGFU D.MELTON, DA. ET AL., NATURE BIOTECHNOLOGY, vol. 26, no. 7, 2008, pages 795 - 797 |
| J. HAO ET AL., PLOS ONE, vol. 3, no. 8, 2008, pages e2904 |
| J.A. THOMSON ET AL., BIOL. REPROD., vol. 55, 1996, pages 254 - 259 |
| J.A. THOMSON ET AL., PROC. NATL. ACAD. SCI. USA, vol. 92, 1995, pages 7844 - 7848 |
| J.A. THOMSON ET AL., SCIENCE, vol. 282, 1998, pages 1145 - 1147 |
| J.A. THOMSONV.S. MARSHALL, CURR. TOP. DEV. BIOL., vol. 38, 1998, pages 133 - 165 |
| J.L. RESNICK ET AL., NATURE, vol. 359, 1992, pages 550 - 551 |
| KANATSU-SHINOHARA M. ET AL., BIOL. REPROD., vol. 69, 2003, pages 612 - 616 |
| KAWASAKI H. ET AL., PROC. NATL. ACAD. SCI. USA, vol. 99, 2002, pages 1580 - 1585 |
| KIM JB.SCHOLER HR. ET AL., NATURE, vol. 454, 2008, pages 646 - 650 |
| KLIMANSKAYA I. ET AL., NATURE, vol. 444, 2006, pages 481 - 485 |
| LIAN X ET AL.: "Robust cardiomyocyte differentiation from human pluripotent stem cells via temporal modulation of canonical Wnt signaling.", PROC NATL ACAD SCI USA., vol. 109, no. 27, 3 July 2012 (2012-07-03), pages E1848 - 57, XP055053519, DOI: 10.1073/pnas.1200250109 |
| M.J. EVANSM.H. KAUFMAN, NATURE, vol. 292, 1981, pages 154 - 156 |
| MASANORI TAKEHASHI ET AL., EXPERIMENTAL MEDICINE, vol. 26, no. 5, 2008, pages 41 - 46 |
| MATSUI Y., CELL, vol. 70, 1992, pages 841 - 847 |
| MIKI ET AL.: "16", CELL STEM CELL, vol. 16, 4 June 2015 (2015-06-04) |
| MINAMI I ET AL.: "A small molecule that promotes cardiac differentiation of human pluripotent stem cells under defined, cytokine-and xeno-free conditions.", CELL REP., vol. 2, no. 5, 29 November 2012 (2012-11-29), pages 1448 - 60, XP055097336, DOI: 10.1016/j.celrep.2012.09.015 |
| MUMMERY, C. ET AL.: "Differentiation of human embryonic stem cells to cardiomyocytes: role of coculture with visceral endoderm-like cells", CIRCULATION, vol. 107, no. 21, 2003, pages 2733 - 40, XP008029536, DOI: 10.1161/01.CIR.0000068356.38592.68 |
| NIWA A ET AL., PLOS ONE, vol. 6, no. 7, 2011, pages e22261 |
| OKITA K ET AL., NAT. METHODS, vol. 8, no. 5, May 2011 (2011-05-01), pages 409 - 12 |
| OKITA K ET AL., STEM CELLS., vol. 31, no. 3, 29 November 2012 (2012-11-29), pages 458 - 66 |
| OKITA, K.ICHISAKA, T.YAMANAKA, S., NATURE, vol. 450, 2007, pages 497 - 502 |
| P. B. YU ET AL., CIRCULATION, vol. 116, 2007, pages 11 - 60 |
| P. B. YU ET AL., NAT. CHEM. BIOL., vol. 4, 2008, pages 33 - 41 |
| PAUL, W B. ET AL.: "A Universal System for Highly Efficient Cardiac Differentiation of Human Induced Pluripotent Stem Cells That Eliminates Interline Variability", PLOSONE, vol. 6, no. 4, 2011, pages e18293, XP009167975, DOI: 10.1371/journal.pone.0018293 |
| R.K. LINDEMANN ET AL., MOL. CANCER, vol. 2, 2003, pages 20 |
| S. WAKAYAMA ET AL., BIOL. REPROD., vol. 72, 2005, pages 932 - 936 |
| See also references of EP4123015A4 |
| SHI Y.DING S. ET AL., CELL STEM CELL, vol. 2, no. 5, 2008, pages 113 - 117 |
| SHINOHARA K. ET AL., CELL, vol. 119, 2004, pages 1001 - 1012 |
| SUEMORI H. ET AL., BIOCHEM. BIOPHYS. RES. COMMUN., vol. 345, 2006, pages 926 - 932 |
| SUEMORI H. ET AL., DEV. DYN., vol. 222, 2001, pages 273 - 279 |
| TAKAHASHI KYAMANAKA S. ET AL., CELL, vol. 131, 2007, pages 861 - 872 |
| TAKAHASHI KYAMANAKA S., CELL, vol. 126, 2006, pages 663 - 676 |
| THOMSON JA ET AL., PROC NATL. ACAD. SCI. U S A., vol. 92, 1995, pages 7844 - 7848 |
| UENO M. ET AL., PROC. NATL. ACAD. SCI. USA, vol. 103, 2006, pages 9554 - 9559 |
| WAKAYAMA T., SCIENCE, vol. 292, 2001, pages 740 - 743 |
| WANG H ET AL.: "Adaptation of human iPSC-derived cardiomyocytes to tyrosine kinase inhibitors reduces acute cardiotoxicity via metabolic reprogramming", CELL SYSTEMS, vol. 8, no. 5, May 2019 (2019-05-01), pages 412 - 426.e7, XP055859363, ISSN: 2405-4712 * |
| YU J.THOMSON JA. ET AL., SCIENCE, vol. 318, 2007, pages 1917 - 1920 |
| ZHANG X. ET AL., STEM CELLS, vol. 24, 2006, pages 2669 - 2676 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024020587A2 (en) | 2022-07-22 | 2024-01-25 | Tome Biosciences, Inc. | Pleiopluripotent stem cell programmable gene insertion |
Also Published As
| Publication number | Publication date |
|---|---|
| CA3175573A1 (en) | 2021-09-23 |
| EP4123015A1 (en) | 2023-01-25 |
| IL296317A (en) | 2022-11-01 |
| BR112022018640A2 (pt) | 2022-11-08 |
| TW202200783A (zh) | 2022-01-01 |
| US20230136878A1 (en) | 2023-05-04 |
| KR20220149592A (ko) | 2022-11-08 |
| JPWO2021187601A1 (ja) | 2021-09-23 |
| AU2021239654A1 (en) | 2022-10-27 |
| EP4123015A4 (en) | 2024-05-22 |
| CN115885035A (zh) | 2023-03-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10947506B2 (en) | Human cardiovascular progenitor cells | |
| US20190032018A1 (en) | Reprogramming cardiomyocytes with one transcription factor | |
| WO2021187601A1 (ja) | 心筋細胞の精製方法 | |
| KR20240125943A (ko) | 신경능 세포의 배양 방법 및 제조 방법 | |
| JP2017108705A (ja) | 心筋細胞の製造方法 | |
| CN116368220A (zh) | 用于大规模制造多能干细胞来源的细胞的封闭制造工艺 | |
| US20220195383A1 (en) | Method for producing pluripotent stem cells | |
| JP7376760B2 (ja) | 多能性幹細胞から各種細胞への段階的製造方法 | |
| WO2020100481A1 (ja) | 脳オルガノイドの製造方法 | |
| RU2813532C1 (ru) | Способ очистки кардиомиоцитов | |
| CN117157388A (zh) | 卵巢体细胞样细胞的制造方法及将灵长类多能干细胞分化诱导成卵巢体细胞样细胞的方法 | |
| JP7344486B2 (ja) | 心筋細胞成熟促進剤 | |
| WO2021187602A1 (ja) | 心筋細胞の精製方法 | |
| US20230078230A1 (en) | Methods for the production of committed cardiac progenitor cells | |
| US20220340871A1 (en) | Method for obtaining or maintaining abcg2-positive corneal limbal stem cells | |
| JPWO2017188082A1 (ja) | 培地添加剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 21772329 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2022508444 Country of ref document: JP Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 3175573 Country of ref document: CA |
|
| REG | Reference to national code |
Ref country code: BR Ref legal event code: B01A Ref document number: 112022018640 Country of ref document: BR |
|
| ENP | Entry into the national phase |
Ref document number: 20227034233 Country of ref document: KR Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2021239654 Country of ref document: AU Date of ref document: 20210318 Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 2021772329 Country of ref document: EP Effective date: 20221019 |
|
| ENP | Entry into the national phase |
Ref document number: 112022018640 Country of ref document: BR Kind code of ref document: A2 Effective date: 20220916 |