WO2020022086A1 - ヘテロ原子をポリマー主鎖中に含むレジスト下層膜形成組成物 - Google Patents
ヘテロ原子をポリマー主鎖中に含むレジスト下層膜形成組成物 Download PDFInfo
- Publication number
- WO2020022086A1 WO2020022086A1 PCT/JP2019/027531 JP2019027531W WO2020022086A1 WO 2020022086 A1 WO2020022086 A1 WO 2020022086A1 JP 2019027531 W JP2019027531 W JP 2019027531W WO 2020022086 A1 WO2020022086 A1 WO 2020022086A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- underlayer film
- resist underlayer
- resist
- compound
- Prior art date
Links
- 0 [O-][N+](C*[N+]([O-])OCC1OC1)OCC1OC1 Chemical compound [O-][N+](C*[N+]([O-])OCC1OC1)OCC1OC1 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D407/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00
- C07D407/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings
- C07D407/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having oxygen atoms as the only ring hetero atoms, not provided for by group C07D405/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G59/00—Polycondensates containing more than one epoxy group per molecule; Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups
- C08G59/18—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing
- C08G59/20—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing characterised by the epoxy compounds used
- C08G59/22—Di-epoxy compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G59/00—Polycondensates containing more than one epoxy group per molecule; Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups
- C08G59/18—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing
- C08G59/40—Macromolecules obtained by polymerising compounds containing more than one epoxy group per molecule using curing agents or catalysts which react with the epoxy groups ; e.g. general methods of curing characterised by the curing agents used
- C08G59/4007—Curing agents not provided for by the groups C08G59/42 - C08G59/66
- C08G59/4064—Curing agents not provided for by the groups C08G59/42 - C08G59/66 sulfur containing compounds
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/09—Photosensitive materials characterised by structural details, e.g. supports, auxiliary layers
- G03F7/11—Photosensitive materials characterised by structural details, e.g. supports, auxiliary layers having cover layers or intermediate layers, e.g. subbing layers
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/20—Exposure; Apparatus therefor
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/26—Processing photosensitive materials; Apparatus therefor
Definitions
- the present invention provides a reaction product of an epoxy adduct-forming compound and a compound having a specific structure having an epoxy group, a resist underlayer film-forming composition containing the reaction product, a resist underlayer film, a method for producing a patterned substrate, and
- the present invention relates to a method for manufacturing a semiconductor device.
- Patent Document 1 discloses a resist underlayer film forming composition for lithography containing a polymer which is a reaction product of at least one compound having two epoxy groups (diepoxy compound) and at least one dicarboxylic acid having a disulfide bond.
- the resist has a large selectivity of the dry etching rate with respect to the resist film, a low k value at a short wavelength such as an ArF excimer laser, and a high n value, and the resist pattern is formed into a desired shape. It discloses that an underlayer film is formed.
- an object of the present invention is to provide a resist underlayer film forming composition that provides a resist underlayer film having higher etching selectivity than conventional products.
- Another object of the present invention is to provide a resist underlayer film that can shorten the dry etching time and suppress undesired etching damage to the underlying substrate.
- a 1 is a carbon atom in which at least one hydrogen atom may be substituted by a halogen atom and is interrupted by an oxygen atom, a sulfur atom, a disulfide group, a sulfonyl group, a carbonyl group or an imino group.
- a linear or branched alkylene group represented by Formulas 2 to 10] and a solvent, and a solvent.
- the epoxy adduct-forming compound is at least one selected from the group consisting of a carboxylic acid-containing compound, a carboxylic anhydride-containing compound, a hydroxy group-containing compound, a thiol group-containing compound, an amino group-containing compound, and an imide group-containing compound.
- the composition for forming a resist underlayer film according to ⁇ 1> which is a compound of the following kind.
- ⁇ 4> The resist underlayer film forming composition according to ⁇ 2> or ⁇ 3>, wherein the carboxylic acid-containing compound is a dicarboxylic acid containing at least one sulfur atom.
- ⁇ 5> The resist underlayer film forming composition according to ⁇ 4>, wherein the dicarboxylic acid containing at least one sulfur atom is an aliphatic dicarboxylic acid containing at least one sulfur atom.
- ⁇ 6> The composition for forming a resist underlayer film according to any one of ⁇ 1> to ⁇ 5>, further comprising a crosslinking catalyst.
- ⁇ 7> The composition for forming a resist underlayer film according to any one of ⁇ 1> to ⁇ 6>, further comprising a crosslinking agent.
- a resist underlayer film which is a baked product of a coating film comprising the resist underlayer film forming composition according to any one of ⁇ 1> to ⁇ 8>.
- a 1 has 2 to 2 carbon atoms in which at least one hydrogen atom may be substituted by a halogen atom and is interrupted by a sulfur atom, a disulfide group, a sulfonyl group, a carbonyl group or an imino group.
- a 1 has 2 to 10 carbon atoms in which at least one hydrogen atom may be substituted by a halogen atom and is interrupted by a sulfur atom, a disulfide group, a sulfonyl group, a carbonyl group or an imino group.
- a reaction product of an epoxy adduct-forming compound such as a carboxylic acid-containing compound and a compound having a specific structure having a hetero atom (O, S, N, etc.) and a glycidyl ester group is prepared by forming a resist underlayer film forming composition
- the resist underlayer film forming composition according to the present invention comprises an epoxy adduct forming compound and the following formula (1):
- a 1 is a carbon atom in which at least one hydrogen atom may be substituted by a halogen atom and is interrupted by an oxygen atom, a sulfur atom, a disulfide group, a sulfonyl group, a carbonyl group or an imino group.
- a linear or branched alkylene group of the formulas 2 to 10] and an epoxy addition product, and a solvent.
- a 1 may have at least one hydrogen atom substituted by a halogen atom and is interrupted by an oxygen atom, a sulfur atom, a disulfide group, a sulfonyl group, a carbonyl group or an imino group.
- Examples of the linear or branched alkylene group having 2 to 10 carbon atoms include ethylene group, n-propylene group, isopropylene group, n-butylene group, s-butylene group, n-pentylene group, 1-methylbutylene group, -Methylbutylene group, 3-methylbutylene group, n-pentylene group, 1,1-dimethylpropylene group, 1,2-dimethylpropylene group, 2,2-dimethylpropylene group, 1,3-dimethylpropylene group, n- Hexylene group, 1-methylheptylene group, 2-methylheptylene group, 3-methylheptylene group, 1,1-dimethylbutylene group, 1,2-dimethylbutylene group, 1,3-dimethylbutylene group, 2,2-dimethylbutylene group, 2,3-dimethylbutylene group, 3,3-dimethylbutylene group, 3,3-dimethylbutane-2-ylene group, 2,
- the term “interrupted” refers to an embodiment in which an oxygen atom, a sulfur atom, a disulfide group, a sulfonyl group, a carbonyl group, or an imino group is inserted between carbon-carbon bonds of the above-mentioned alkylene group.
- the halogen atom include fluorine, chlorine, bromine, and iodine.
- the at least one hydrogen atom may be substituted with a halogen atom means that at least one hydrogen atom of the linear or branched alkylene group having 2 to 10 carbon atoms may be substituted with a halogen atom.
- the number of halogen atom substitutions is preferably 5 or less, more preferably 3 or less, preferably 2 or less, and more preferably 1 or less, and preferably 0 (that is, not substituted with a halogen atom).
- Preferred specific examples are as follows, but are not limited thereto.
- the epoxy adduct-forming compound refers to a compound capable of forming a polymer or oligomer by reacting with the compound represented by the above formula (1). Usually, it is a compound having 1 to 4 functional groups reactive to an epoxy group per molecule.
- the epoxy adduct-forming compound may be used alone, or may be a mixture of two or more. In that case, it is preferable that a compound having two or more functional groups reactive with an epoxy group per molecule occupies the majority of the mixture from the viewpoint of lengthening the main chain of the product to some extent.
- the epoxy adduct-forming compound is preferably at least one selected from the group consisting of carboxylic acid-containing compounds, carboxylic anhydride-containing compounds, hydroxy group-containing compounds, thiol group-containing compounds, amino group-containing compounds and imide group-containing compounds. And more preferably a carboxylic acid-containing compound or a thiol group-containing compound.
- the epoxy adduct-forming compound preferably has a hetero atom.
- the epoxy adduct forming compound preferably has one or more heteroatoms.
- the epoxy adduct-forming compound preferably has 2 to 10 heteroatoms. As the hetero atom, a nitrogen atom, an oxygen atom and a sulfur atom are preferable.
- the carboxylic acid-containing compound is preferably a dicarboxylic acid containing at least one sulfur atom, and more preferably an aliphatic dicarboxylic acid containing at least one sulfur atom.
- epoxy adduct-forming compound ⁇ Specific examples of the epoxy adduct-forming compound are as follows, but are not limited thereto.
- the epoxy addition product is a reaction product of the compound represented by the formula (1) and the epoxy adduct-forming compound. That is, a reaction product of the compound represented by the formula (1), which is a raw material monomer, and an epoxy adduct-forming compound is dissolved in a solvent so as to have an appropriate molar ratio, and a catalyst for activating an epoxy group is used. Obtained by polymerization in the presence.
- the catalyst for activating the epoxy group is, for example, a quaternary phosphonium salt such as triphenylmonoethylphosphonium bromide or a quaternary ammonium salt such as benzyltriethylammonium chloride.
- An appropriate amount can be selected from the range of 0.1% by mass to 10% by mass with respect to the total mass of the compound represented by the formula (1) and the epoxy adduct-forming compound.
- the optimal temperature and time for the polymerization reaction are selected from the range of 80 ° C. to 160 ° C. and 2 hours to 50 hours.
- the above reaction is carried out without a solvent, but is usually carried out using a solvent. All solvents can be used as long as they do not inhibit the reaction.
- solvents such as 1,2-dimethoxyethane, diethylene glycol dimethyl ether, propylene glycol monomethyl ether, tetrahydrofuran, dioxane and the like can be mentioned.
- the weight average molecular weight Mw of the epoxy addition product obtained as described above is usually 500 or 600 or more and 1,000,000 or 500,000 or less.
- solvent for the composition for forming a resist underlayer film according to the present invention
- any solvent can be used without particular limitation as long as it can dissolve the above reaction product.
- the resist underlayer film forming composition according to the present invention is used in a uniform solution state, it is recommended to use a solvent generally used in a lithography step in consideration of its coating performance. .
- Examples of such a solvent include methyl cellosolve acetate, ethyl cellosolve acetate, propylene glycol, propylene glycol monomethyl ether, propylene glycol monoethyl ether, methyl isobutyl carbinol, propylene glycol monobutyl ether, propylene glycol monomethyl ether acetate, and propylene glycol monomethyl ether.
- R 1 , R 2 and R 3 in the formula (i) each represent a hydrogen atom, an oxygen atom, a sulfur atom or an alkyl group having 1 to 20 carbon atoms which may be interrupted by an amide bond. And may be different from each other, and may combine with each other to form a ring structure.
- alkyl group having 1 to 20 carbon atoms examples include a linear or branched alkyl group which may or may not have a substituent, for example, a methyl group, an ethyl group, and an n-propyl group , Isopropyl, n-butyl, sec-butyl, tert-butyl, n-pentyl, isopentyl, neopentyl, n-hexyl, isohexyl, n-heptyl, n-octyl, cyclohexyl , 2-ethylhexyl, n-nonyl, isononyl, p-tert-butylcyclohexyl, n-decyl, n-dodecylnonyl, undecyl, dodecyl, tridecyl, tetradecyl, pentadecyl, hexy
- Oxygen atom the alkyl group of a sulfur atom or an amide interrupted by coupling a 1 to 20 carbon atoms, for example, structural units -CH 2 -O -, - CH 2 -S -, - CH 2 -NHCO- or - Those containing CH 2 —CONH— are exemplified.
- —O—, —S—, —NHCO— or —CONH— may have one unit or two or more units in the alkyl group.
- alkyl group having 1 to 20 carbon atoms interrupted by —O—, —S—, —NHCO— or —CONH— unit include methoxy, ethoxy, propoxy, butoxy, methylthio, ethylthio Group, propylthio group, butylthio group, methylcarbonylamino group, ethylcarbonylamino group, propylcarbonylamino group, butylcarbonylamino group, methylaminocarbonyl group, ethylaminocarbonyl group, propylaminocarbonyl group, butylaminocarbonyl group, etc.
- methyl, ethyl, propyl, butyl, pentyl, hexyl, heptyl, octyl, nonyl, decyl, dodecyl or octadecyl each of which is methoxy, ethoxy Group, propoxy group, butoxy group, methylthio group, Thio group, propylthio group, butylthio group, those substituted methylcarbonyl group, ethylcarbonyl amino group, methylamino group, a ethylamino group or the like.
- these solvents have a relatively high boiling point, they are also effective for imparting a high filling property and a high flattening property to the resist underlayer film forming composition.
- the resist underlayer film forming composition of the present invention can contain a crosslinking agent component.
- the crosslinking agent include a melamine-based, substituted urea-based, or a polymer thereof.
- Preferred are crosslinkers having at least two crosslink-forming substituents, such as methoxymethylated glycoluril, butoxymethylated glycoluril, methoxymethylated melamine, butoxymethylated melamine, methoxymethylated benzoguanamine, butoxymethylated benzoguanamine, Compounds such as methoxymethylated urea, butoxymethylated urea, or methoxymethylated thiourea. Condensates of these compounds can also be used.
- Preferred is tetramethoxymethyl glycoluril (Nippon Cytec Industries, Ltd., trade name: POWDERLINK (registered trademark) 1174).
- crosslinking agent a crosslinking agent having high heat resistance can be used.
- heat-resistant crosslinking agent a compound containing a crosslinking-forming substituent having an aromatic ring (for example, a benzene ring or a naphthalene ring) in the molecule can be preferably used.
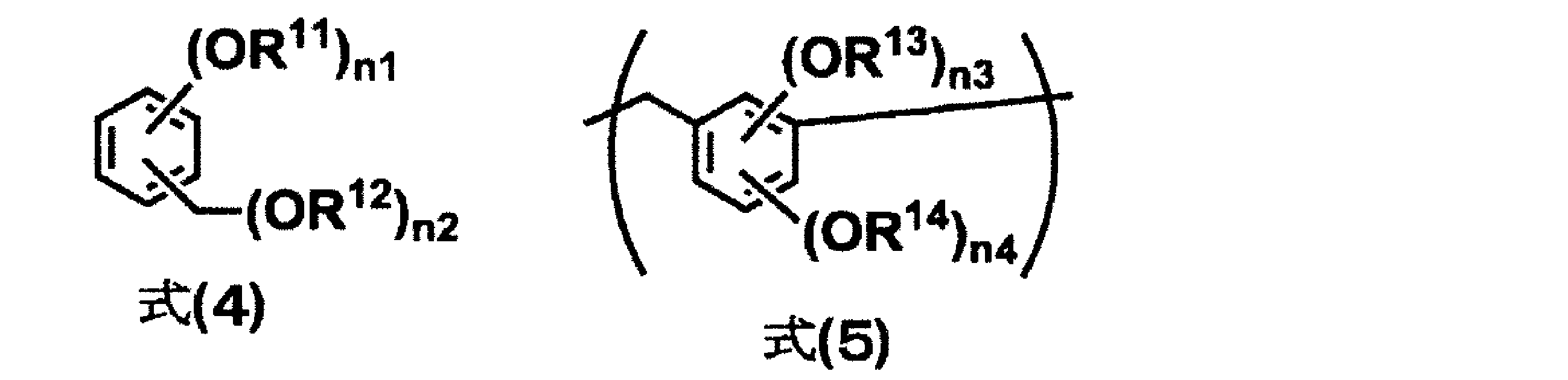
- Examples of the compound include a compound having a partial structure represented by the following formula (4) and a polymer or oligomer having a repeating unit represented by the following formula (5).
- R 11 , R 12 , R 13 , and R 14 are a hydrogen atom or an alkyl group having 1 to 10 carbon atoms, and the above-described examples can be used for these alkyl groups.
- the above compound can be obtained as a product of Asahi Organic Material Industry Co., Ltd. or Honshu Chemical Industry Co., Ltd.
- the compound of the formula (4-24) can be obtained under the trade name TM-BIP-A by Asahi Organic Materials Industry Co., Ltd.
- the addition amount of the crosslinking agent varies depending on the coating solvent used, the base substrate used, the required solution viscosity, the required film shape, and the like, but is 0.001 to 80% by mass based on the total solid content, preferably It is 0.01 to 50% by mass, more preferably 0.05 to 40% by mass.
- These cross-linking agents may cause a cross-linking reaction by self-condensation. However, when a cross-linking substituent is present in the reaction product of the present invention, a cross-linking reaction can be caused with the cross-linking substituent.
- the resist underlayer film forming composition of the present invention may contain an acid and / or an acid generator.
- the acid include p-toluenesulfonic acid, trifluoromethanesulfonic acid, pyridinium p-toluenesulfonic acid, pyridinium trifluoromethanesulfonic acid, pyridinium-p-phenolsulfonic acid, salicylic acid, 5-sulfosalicylic acid, and 4-phenolsulfonic acid.
- Examples include camphorsulfonic acid, 4-chlorobenzenesulfonic acid, benzenedisulfonic acid, 1-naphthalenesulfonic acid, citric acid, benzoic acid, hydroxybenzoic acid, and naphthalenecarboxylic acid.
- the acids can be used alone or in combination of two or more.
- the amount is usually 0.0001 to 20% by mass, preferably 0.0005 to 10% by mass, and more preferably 0.01 to 3% by mass based on the total solid content.
- Examples of the acid generator include a thermal acid generator and a photoacid generator.
- Examples of the thermal acid generator include 2,4,4,6-tetrabromocyclohexadienone, benzoin tosylate, 2-nitrobenzyl tosylate, and other alkyl esters of organic sulfonic acids.
- the photoacid generator generates an acid upon exposure of the resist. Therefore, the acidity of the lower layer film can be adjusted. This is one method for adjusting the acidity of the lower layer film to the acidity of the upper layer resist. Further, by adjusting the acidity of the lower layer film, the pattern shape of the resist formed in the upper layer can be adjusted.
- the photoacid generator contained in the composition for forming a resist underlayer film of the present invention include an onium salt compound, a sulfonimide compound, and a disulfonyldiazomethane compound.
- Examples of the onium salt compound include diphenyliodonium hexafluorophosphate, diphenyliodonium trifluoromethanesulfonate, diphenyliodonium nonafluoronormal butanesulfonate, diphenyliodonium perfluoronormal octanesulfonate, diphenyliodonium camphorsulfonate, and bis (4-tert-butylphenyl) iodonium camphor.
- Iodonium salt compounds such as sulfonate and bis (4-tert-butylphenyl) iodonium trifluoromethanesulfonate, and triphenylsulfonium hexafluoroantimonate, triphenylsulfonium nonafluoronormal butanesulfonate, triphenylsulfonium camphorsulfonate and triphenyls Sulfonium salt compounds such as phosphonium trifluoromethanesulfonate, and the like.
- sulfonimide compound examples include N- (trifluoromethanesulfonyloxy) succinimide, N- (nonafluoronormalbutanesulfonyloxy) succinimide, N- (camphorsulfonyloxy) succinimide, and N- (trifluoromethanesulfonyloxy) naphthalimide. No.
- disulfonyldiazomethane compound examples include bis (trifluoromethylsulfonyl) diazomethane, bis (cyclohexylsulfonyl) diazomethane, bis (phenylsulfonyl) diazomethane, bis (p-toluenesulfonyl) diazomethane, and bis (2,4-dimethylbenzenesulfonyl) ) Diazomethane and methylsulfonyl-p-toluenesulfonyldiazomethane.
- the acid generator may be used alone, or two or more acid generators may be used in combination.
- the proportion thereof is 0.01 to 5 parts by mass, 0.1 to 3 parts by mass, or 0.1 to 3 parts by mass with respect to 100 parts by mass of the solid content of the resist underlayer film forming composition. It is 5 to 1 part by mass.
- the composition for forming a resist underlayer film of the present invention may contain a surfactant in order to prevent the occurrence of pinholes or striations and to further improve the coating property for uneven surface.
- a surfactant for example, polyoxyethylene lauryl ether, polyoxyethylene stearyl ether, polyoxyethylene cetyl ether, polyoxyethylene alkyl ethers such as polyoxyethylene oleyl ether, polyoxyethylene octyl phenol ether, polyoxyethylene nonyl phenol ether Polyoxyethylene alkyl allyl ethers, polyoxyethylene / polyoxypropylene block copolymers, sorbitan monolaurate, sorbitan monopalmitate, sorbitan monostearate, sorbitan monooleate, sorbitan trioleate, sorbitan tristearate, etc.
- Nonionic surfactants such as polyoxyethylene sorbitan fatty acid esters such as tan monopalmitate, polyoxyethylene sorbitan monostearate, polyoxyethylene sorbitan trioleate, and polyoxyethylene sorbitan tristearate; EFTOP EF301, EF303; EF352 (trade name, manufactured by Tochem Products Co., Ltd.), Megafac F171, F173, R-40, R-40N, R-40LM (trade name, manufactured by DIC Corporation), Florard FC430, FC431 (Sumitomo 3M (trade name) Fluorosurfactants such as Asahi Guard AG710, Asahi Guard AG710, Surflon S-382, SC101, SC102, SC103, SC104, SC105, SC106 (trade name, manufactured by Asahi Glass Co., Ltd.), and organosiloxane poly.
- Over KP341 manufactured by Shin-Etsu Chemical Co., Ltd.
- the amount of these surfactants is usually 2.0% by mass or less, preferably 1.0% by mass or less, based on the total solid content of the resist underlayer film material.
- These surfactants may be used alone or in combination of two or more.
- the proportion thereof is 0.0001 to 5 parts by mass, or 0.001 to 1 part by mass, or 0.01 to 100 parts by mass of the solid content of the resist underlayer film forming composition. To 0.5 part by mass.
- a light absorbing agent, a rheology adjusting agent, an adhesion aid, and the like can be added to the resist underlayer forming composition of the present invention.
- the rheology modifier is effective for improving the fluidity of the underlayer film forming composition.
- the adhesion aid is effective for improving the adhesion between the semiconductor substrate or the resist and the lower layer film.
- Examples of the light absorbing agent include commercially available light absorbing agents described in “Technologies and Markets of Industrial Dyes” (CMC Publishing) and “Dye Handbook” (edited by the Society of Synthetic Organic Chemistry), for example, C.I.
- C.I. Disperse Yellow 1,3,4,5,7,8,13,23,31,49,50,51,54,60,64,66,68,79,82,88,90,93,102,114 and 124;
- Disperse Blue 96 C.I. I. C. Fluorescent Brightening Agent 112, 135 and 163; I. Solvent @ Orange 2 and 45; I. Solvent Red 1, 3, 8, 23, 24, 25, 27 and 49; I. Pigment Green 10; I. Pigment Brown 2 or the like can be suitably used.
- the light absorbing agent is generally blended at a ratio of 10% by mass or less, preferably 5% by mass or less, based on the total solid content of the resist underlayer-forming composition.
- the rheology modifier mainly improves the fluidity of the resist underlayer film forming composition, and particularly in the baking step, improves the uniformity of the thickness of the resist underlayer film and the filling property of the resist underlayer film forming composition inside the hole. It is added for the purpose of enhancing.
- phthalic acid derivatives such as dimethyl phthalate, diethyl phthalate, diisobutyl phthalate, dihexyl phthalate, and butyl isodecyl phthalate, dinormal butyl adipate, diisobutyl adipate, adipic acid derivatives such as diisooctyl adipate, and octyl decyl adipate; Normal butyl maleate, diethyl malate, maleic acid derivatives such as dinonyl maleate, methyl oleate, butyl oleate, oleic acid derivatives such as tetrahydrofurfuryl oleate, or normal butyl stearate, stearic acid derivatives such as glyceryl stearate. it can.
- These rheology modifiers are usually blended at a ratio of less than 30% by mass based on the total solids of the resist underlayer-forming composition.
- the adhesion aid is added mainly for the purpose of improving the adhesion between the substrate or the resist and the resist underlayer film forming composition, and particularly preventing the resist from peeling off during development.
- Specific examples include chlorosilanes such as trimethylchlorosilane, dimethylmethylolchlorosilane, methyldiphenylchlorosilane, and chloromethyldimethylchlorosilane; trimethylmethoxysilane, dimethyldiethoxysilane, methyldimethoxysilane, dimethylmethylolethoxysilane, diphenyldimethoxysilane, and phenyltriethoxysilane.
- Alkoxysilanes such as silane, hexamethyldisilazane, silazane such as N, N'-bis (trimethylsilyl) urea, dimethyltrimethylsilylamine, trimethylsilylimidazole, methyloltrichlorosilane, ⁇ -chloropropyltrimethoxysilane, ⁇ -aminopropyl Silanes such as triethoxysilane, ⁇ -glycidoxypropyltrimethoxysilane, benzotriazole, Heterocyclic compounds such as imidazole, indazole, imidazole, 2-mercaptobenzimidazole, 2-mercaptobenzothiazole, 2-mercaptobenzoxazole, urazole, thiouracil, mercaptoimidazole, mercaptopyrimidine, and 1,1-dimethylurea, Urea such as 3-dimethylurea or a thiourea compound can be mentioned
- the solid content of the composition for forming a resist underlayer film according to the present invention is usually 0.1 to 70% by mass, preferably 0.1 to 60% by mass.
- the solid content is the content ratio of all components excluding the solvent from the resist underlayer film forming composition.
- the proportion of the reaction product in the solid content is preferably in the order of 1 to 100% by mass, 1 to 99.9% by mass, 50 to 99.9% by mass, 50 to 95% by mass, 50 to 90% by mass.
- One of the scales to evaluate whether the resist underlayer film forming composition is in a uniform solution state is to observe the permeability of a specific microfilter, but the resist underlayer film forming composition according to the present invention is Through a micro filter having a pore size of 0.1 ⁇ m to exhibit a uniform solution state.
- Examples of the material of the microfilter include fluororesins such as PTFE (polytetrafluoroethylene), PFA (tetrafluoroethylene / perfluoroalkylvinyl ether copolymer), PE (polyethylene), UPE (ultra high molecular weight polyethylene), PP ( Polypropylene), PSF (polysulfone), PES (polyethersulfone), and nylon can be mentioned, and it is preferable that the PTFE (polytetrafluoroethylene) is used.
- PTFE polytetrafluoroethylene
- PFA tetrafluoroethylene / perfluoroalkylvinyl ether copolymer
- PE polyethylene
- UPE ultra high molecular weight polyethylene
- PP Polypropylene
- PSF polysulfone
- PES polyethersulfone
- nylon nylon
- the resist underlayer film forming composition of the present invention is applied by an appropriate application method such as a spinner or a coater, and then baked to form a resist underlayer film.
- Conditions for baking are appropriately selected from a baking temperature of 80 ° C. to 250 ° C. and a baking time of 0.3 to 60 minutes.
- the firing temperature is 150 ° C. to 250 ° C.
- the firing time is 0.5 to 2 minutes.
- the thickness of the formed lower layer film is, for example, 10 to 1000 nm, 20 to 500 nm, 30 to 300 nm, or 50 to 200 nm.
- an inorganic resist underlayer film (hard mask) can be formed on the organic resist underlayer film according to the present invention.
- a Si-based inorganic material film can be formed by a CVD method or the like.
- the resist underlayer film forming composition according to the present invention is applied to a semiconductor substrate having a stepped portion and a portion having no stepped portion (a so-called stepped substrate), and is baked to form the portion having the stepped portion. It is possible to form a resist underlayer film in which a step from a portion having no step is in the range of 3 to 50 nm.
- a resist film for example, a photoresist layer is formed on the resist underlayer film.
- the formation of the photoresist layer can be performed by a well-known method, that is, by applying and baking a photoresist composition solution on an underlayer film.
- the thickness of the photoresist is, for example, 50 to 10000 nm, 100 to 2000 nm, or 200 to 1000 nm.
- the photoresist formed on the resist underlayer film is not particularly limited as long as it is sensitive to light used for exposure. Either a negative photoresist or a positive photoresist can be used.
- a positive photoresist comprising a novolak resin and 1,2-naphthoquinonediazidosulfonic acid ester; a chemically amplified photoresist comprising a binder having a group capable of decomposing by an acid to increase the alkali dissolution rate and a photoacid generator;
- a chemically amplified photoresist comprising a low molecular compound that decomposes and increases the alkali dissolution rate of a photoresist, an alkali-soluble binder and a photoacid generator, and a binder having a group that decomposes with an acid to increase the alkali dissolution rate
- trade name APEX-E manufactured by Shipley Co., Ltd. trade name PAR710 manufactured by Sumitomo Chemical Co., Ltd., and trade name SEPR430 manufactured by Shin-Etsu Chemical Co., Ltd. are exemplified.
- Proc. SPIE, Vol. 3999, 330-334 (2000) Proc. SPIE, Vol. 3999, 357-364 (2000)
- Proc. SPIE, Vol. 3999, 365-374 (2000).
- a resist pattern is formed by light or electron beam irradiation and development.
- exposure is performed through a predetermined mask.
- near ultraviolet rays, far ultraviolet rays, extreme ultraviolet rays for example, EUV (wavelength: 13.5 nm)
- EUV extreme ultraviolet rays
- KrF excimer laser wavelength 248 nm
- ArF excimer laser wavelength 193 nm
- F 2 excimer laser wavelength 157 nm
- post-exposure bake can be performed if necessary.
- the post-exposure heating is performed under conditions appropriately selected from a heating temperature of 70 ° C. to 150 ° C. and a heating time of 0.3 to 10 minutes.
- a resist for electron beam lithography can be used instead of a photoresist as the resist.
- Both negative and positive electron beam resists can be used.
- a chemically amplified resist comprising a binder having a group that decomposes with an acid generator and an acid to change the alkali dissolution rate and a low molecular weight compound that decomposes with an acid and changes the alkali dissolution rate of the resist,
- non-chemically amplified resists made of a binder having a group that changes the alkali dissolution rate by being decomposed by an electron beam and non-chemically amplified resists made of a binder having a site that is cut by
- a developer for example, when a positive photoresist is used, the photoresist in the exposed portion is removed, and a pattern of the photoresist is formed.
- an aqueous solution of an alkali metal hydroxide such as potassium hydroxide or sodium hydroxide
- an aqueous solution of a quaternary ammonium hydroxide such as tetramethylammonium hydroxide, tetraethylammonium hydroxide, or choline
- ethanolamine, propylamine An alkaline aqueous solution such as an aqueous solution of an amine such as ethylenediamine can be given as an example.
- a surfactant or the like can be added to these developers. Conditions for the development are appropriately selected from a temperature of 5 to 50 ° C. and a time of 10 to 600 seconds.
- the inorganic lower layer (intermediate layer) is removed, and then the photoresist and the inorganic lower layer (intermediate layer) are patterned.
- the organic lower layer film (lower layer) is removed.
- the semiconductor substrate is processed using the patterned inorganic lower layer film (intermediate layer) and organic lower layer film (lower layer) as protective films.
- the portion of the inorganic lower layer (intermediate layer) from which the photoresist has been removed is removed by dry etching to expose the semiconductor substrate.
- dry etching of the inorganic lower layer film tetrafluoromethane (CF 4 ), perfluorocyclobutane (C 4 F 8 ), perfluoropropane (C 3 F 8 ), trifluoromethane, carbon monoxide, argon, oxygen, nitrogen, Gases such as sulfur fluoride, difluoromethane, nitrogen trifluoride and chlorine trifluoride, chlorine, trichloroborane and dichloroborane can be used.
- a halogen-based gas for dry etching of the inorganic lower layer film, it is preferable to use a halogen-based gas, more preferably a fluorine-based gas.
- the fluorine-based gas include tetrafluoromethane (CF 4 ), perfluorocyclobutane (C 4 F 8 ), perfluoropropane (C 3 F 8 ), trifluoromethane, and difluoromethane (CH 2 F 2 ).
- the organic underlayer film is removed by using the film composed of the patterned photoresist and the inorganic underlayer film as a protective film.
- the organic lower layer film (lower layer) is preferably formed by dry etching using an oxygen-based gas. This is because an inorganic lower layer film containing a large amount of silicon atoms is not easily removed by dry etching using an oxygen-based gas.
- processing of the semiconductor substrate is preferably performed by dry etching with a fluorine-based gas.
- fluorine-based gas examples include tetrafluoromethane (CF 4 ), perfluorocyclobutane (C 4 F 8 ), perfluoropropane (C 3 F 8 ), trifluoromethane, and difluoromethane (CH 2 F 2 ).
- an organic antireflection film can be formed on the resist underlayer film before forming the photoresist.
- the anti-reflective coating composition used therefor it can be arbitrarily selected from those conventionally used in a lithography process, and a commonly used method, for example, spinner
- the antireflection film can be formed by coating and baking with a coater.
- an inorganic underlayer film can be formed thereon, and a photoresist can be further coated thereon.
- the substrate can be processed by selecting an appropriate etching gas.
- an appropriate etching gas For example, it is possible to process a resist underlayer film using a fluorine-based gas having a sufficiently high etching rate for a photoresist as an etching gas, and to etch a fluorine-based gas having a sufficiently high etching rate for an inorganic underlayer film.
- the substrate can be processed as a gas, and further, the substrate can be processed using an oxygen-based gas, which has a sufficiently high etching rate for the organic underlayer film, as an etching gas.
- the resist underlayer film formed from the resist underlayer film forming composition may have an absorption for the light depending on the wavelength of the light used in the lithography process. In such a case, it can function as an antireflection film having an effect of preventing light reflected from the substrate. Further, the underlayer film formed using the resist underlayer film forming composition of the present invention can also function as a hard mask.
- the underlayer film of the present invention has a layer for preventing interaction between the substrate and the photoresist, and a function for preventing a material used for the photoresist or a substance generated upon exposure to the photoresist from adversely affecting the substrate.
- the underlayer film formed from the composition for forming a resist underlayer film is applied to a substrate having via holes used in a dual damascene process and can be used as a filling material capable of filling holes without gaps. Further, it can be used as a planarizing material for planarizing the surface of a semiconductor substrate having irregularities.
- the weight average molecular weights of the polymers shown in the following synthesis examples of the present specification are the results of measurement by gel permeation chromatography (hereinafter abbreviated as GPC).
- GPC gel permeation chromatography
- a GPC device manufactured by Tosoh Corporation was used for the measurement, and the measurement conditions were as follows.
- the reaction mixture was diluted with 230.0 g of chloroform, and 460.0 g of a 5% aqueous sodium hydrogen carbonate solution was added to carry out liquid separation. Further, the organic layer was separated with 460.0 g of a 10% aqueous sodium hydrogen sulfite solution, 460.0 g of a 5% aqueous sodium hydrogen carbonate solution and 460.0 g of pure water, and then the solvent was distilled off at 40 ° C. under reduced pressure. As a result, 17.63 g of diglycidyl-2,2′-oxydiacetate represented by the above formula (B) was obtained as a white solid (yield: 66.7%).
- the reaction mixture was diluted with 80.0 g of chloroform, and 160.0 g of a 5% aqueous sodium hydrogen carbonate solution was added to carry out liquid separation. Further, the organic layer was separated with 160.0 g of a 10% aqueous sodium hydrogen sulfite solution, 160.0 g of a 5% aqueous sodium hydrogen carbonate solution and 160.0 g of pure water, and then the solvent was distilled off at 30 ° C. under reduced pressure. Thus, 4.36 g of the compound represented by the above formula (D) was obtained as a white solid (yield: 48.6%).
- the ⁇ value of this compound in the 1 H-NMR spectrum (500 MHz, DMSO-d6) was as follows. 4.65 (s, 4H), 4.52 (dd, 2H), 3.98 (dd, 2H), 3.24 (m, 2H), 2.81 (dd, 2H), 2.70 (dd) , 2H)
- composition preparation [Example 1] To 2.650 g of a solution containing 0.424 g of the reaction product (DG-DGA polymer) obtained in Synthesis Example 6, 7.334 g of propylene glycol monomethyl ether and pyridinium trifluoromethanesulfonic acid (Tokyo Chemical Industry Co., Ltd.) were added. 016 g and a surfactant (Dainippon Ink & Chemicals, Inc., trade name: R-40) 0.001 g were added to prepare a solution. Thereafter, the solution was filtered using a polyethylene microfilter having a pore size of 0.02 ⁇ m to prepare a composition for forming a resist underlayer film.
- DG-DGA polymer reaction product obtained in Synthesis Example 6
- a surfactant Dainippon Ink & Chemicals, Inc., trade name: R-40
- Example 2 To 2.924 g of a solution containing 0.482 g of the reaction product (DG-TDGA polymer) obtained in Synthesis Example 7, 7.057 g of propylene glycol monomethyl ether and pyridinium trifluoromethanesulfonic acid (Tokyo Chemical Industry Co., Ltd.) were added. 018 g and a surfactant (Dainippon Ink & Chemicals, Inc., trade name: R-40) 0.001 g were added to obtain a solution. Thereafter, the solution was filtered using a polyethylene microfilter having a pore size of 0.02 ⁇ m to prepare a composition for forming a resist underlayer film.
- DG-TDGA polymer the reaction product obtained in Synthesis Example 7
- a surfactant Dainippon Ink & Chemicals, Inc., trade name: R-40
- Example 3 To 2.486 g of a solution containing 0.482 g of the reaction product (DG-SDGA polymer) obtained in Synthesis Example 8, 7.496 g of propylene glycol monomethyl ether and pyridinium trifluoromethanesulfonic acid (Tokyo Chemical Industry Co., Ltd.) were added. 018 g and a surfactant (Dainippon Ink & Chemicals, Inc., trade name: R-40) 0.001 g were added to obtain a solution. Thereafter, the solution was filtered using a polyethylene microfilter having a pore size of 0.02 ⁇ m to prepare a composition for forming a resist underlayer film.
- DG-SDGA polymer reaction product obtained in Synthesis Example 8
- a surfactant Dainippon Ink & Chemicals, Inc., trade name: R-40
- Example 4 To 2.486 g of a solution containing 0.482 g of the reaction product (DG-DTDGA polymer) obtained in Synthesis Example 9, 7.496 g of propylene glycol monomethyl ether and pyridinium trifluoromethanesulfonic acid (Tokyo Chemical Industry Co., Ltd.) were added. 018 g and a surfactant (Dainippon Ink & Chemicals, Inc., trade name: R-40) 0.001 g were added to obtain a solution. Thereafter, the solution was filtered using a polyethylene microfilter having a pore size of 0.02 ⁇ m to prepare a composition for forming a resist underlayer film.
- DG-DTDGA polymer reaction product obtained in Synthesis Example 9
- a surfactant Dainippon Ink & Chemicals, Inc., trade name: R-40
- Example 5 To 2.486 g of a solution containing 0.482 g of the reaction product (DG-DTDGA polymer (ii)) obtained in Synthesis Example 10, 7.496 g of propylene glycol monomethyl ether and pyridinium trifluoromethanesulfonic acid (Tokyo Chemical Industry Co., Ltd.) ) And 0.001 g of a surfactant (trade name: R-40, manufactured by Dainippon Ink and Chemicals, Incorporated) to form a solution. Thereafter, the solution was filtered using a polyethylene microfilter having a pore size of 0.02 ⁇ m to prepare a composition for forming a resist underlayer film.
- a surfactant trade name: R-40, manufactured by Dainippon Ink and Chemicals, Incorporated
- Examples 1 to 6 have sufficiently higher etching selectivity than Comparative Example 1.
- the composition for forming a resist underlayer film obtained according to the present invention can reduce the etching time during dry etching of the resist underlayer film, and the resist film thickness decreases when the resist underlayer film is removed by dry etching. Can be suppressed. Further, shortening the dry etching time is particularly useful as a resist underlayer film because undesired etching damage to the underlying substrate of the resist underlayer film can be suppressed.
- the resist underlayer film forming composition according to the present invention provides a resist underlayer film having a particularly high dry etching rate.
Abstract
特に高ドライエッチング速度を有するレジスト下層膜、該レジスト下層膜形成組成物、レジストパターン形成方法及び半導体装置の製造方法を提供する。エポキシ付加体形成化合物と、下記式(1): [式(1)中、A1は少なくとも1つの水素原子がハロゲン原子で置換されていてもよく且つ酸素原子、硫黄原子、ジスルフィド基、スルホニル基、カルボニル基若しくはイミノ基で中断されている炭素原子数2乃至10の直鎖若しくは分岐アルキレン基を表す]で表される化合物、とのエポキシ付加生成物と、溶剤とを含む、レジスト下層膜形成組成物とする。
Description
本発明は、エポキシ付加体形成化合物とエポキシ基を有する特定構造の化合物との反応生成物、当該反応生成物を含むレジスト下層膜形成組成物、レジスト下層膜、パターニングされた基板の製造方法、及び半導体装置の製造方法に関する。
特許文献1には、2つのエポキシ基を含む少なくとも1種の化合物(ジエポキシ化合物)と、ジスルフィド結合を含む少なくとも1種のジカルボン酸との反応生成物であるポリマーを含むリソグラフィー用レジスト下層膜形成組成物が、レジスト膜に対するドライエッチング速度の選択比が大きく、ArFエキシマレーザーのような短波長でのk値が低く、且つn値が高い値を示し、レジストパターンが所望の形状に形成されるレジスト下層膜を形成することが開示されている。
しかしながら、従来製品はエッチング選択性がまだ充分には高いとは言い難かった。そこで、本発明が解決しようとする課題は、従来製品に比べエッチング選択性が更に高いレジスト下層膜を与えるレジスト下層膜形成組成物を提供することである。また、本発明が解決しようとする課題は、ドライエッチング時間が短縮でき、下地基板に対して好ましくないエッチングダメージを抑制することができるレジスト下層膜を提供することである。
本発明は以下を包含する。
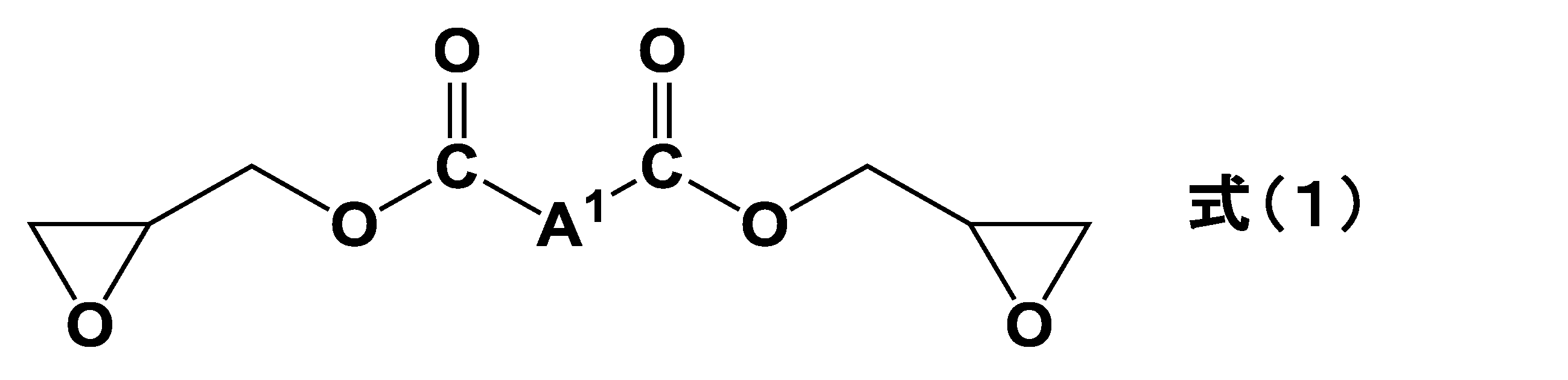
<1> エポキシ付加体形成化合物と、下記式(1):
[式(1)中、A1は少なくとも1つの水素原子がハロゲン原子で置換されていてもよく且つ酸素原子、硫黄原子、ジスルフィド基、スルホニル基、カルボニル基若しくはイミノ基で中断されている炭素原子数2乃至10の直鎖若しくは分岐アルキレン基を表す]で表される化合物、とのエポキシ付加生成物と、溶剤とを含む、レジスト下層膜形成組成物。
<2> 前記エポキシ付加体形成化合物が、カルボン酸含有化合物、カルボン酸無水物含有化合物、ヒドロキシ基含有化合物、チオール基含有化合物、アミノ基含有化合物及びイミド基含有化合物からなる群より選ばれる少なくとも1種の化合物である、<1>に記載のレジスト下層膜形成組成物。
<3> 前記エポキシ付加体形成化合物が、カルボン酸含有化合物またはチオール基含有化合物である、<1>又は<2>に記載のレジスト下層膜形成組成物。
<4> 前記カルボン酸含有化合物が、硫黄原子を少なくとも1つ以上含むジカルボン酸である、<2>又は<3>に記載のレジスト下層膜形成組成物。
<5> 前記硫黄原子を少なくとも1つ以上含むジカルボン酸が、硫黄原子を少なくとも1つ以上含む脂肪族ジカルボン酸である、<4>に記載のレジスト下層膜形成組成物。
<6> 架橋触媒をさらに含む、<1>~<5>のいずれか1項に記載のレジスト下層膜形成組成物。
<7> 架橋剤をさらに含む、<1>~<6>のいずれか1項に記載のレジスト下層膜形成組成物。
<8> 界面活性剤をさらに含む、<1>~<7>のいずれか1項に記載のレジスト下層膜形成組成物。
<9> <1>~<8>のいずれか1項に記載のレジスト下層膜形成組成物からなる塗布膜の焼成物であることを特徴とするレジスト下層膜。
<10> 半導体基板上に、<1>~<8>のいずれか1項に記載のレジスト下層膜形成組成物を塗布しベークしてレジスト下層膜を形成する工程、前記レジスト下層膜上にレジストを塗布しベークしてレジスト膜を形成する工程、前記レジスト下層膜と前記レジストで被覆された半導体基板を露光する工程、露光後の前記レジスト膜を現像し、パターニングする工程を含む、パターニングされた基板の製造方法。
<11> 半導体基板上に、<1>~<8>の何れか1項に記載のレジスト下層膜形成組成物からなるレジスト下層膜を形成する工程と、
前記レジスト下層膜の上にレジスト膜を形成する工程と、
レジスト膜に対する光又は電子線の照射とその後の現像によりレジストパターンを形成する工程と、
形成された前記レジストパターンを介して前記レジスト下層膜をエッチングすることによりパターン化されたレジスト下層膜を形成する工程と、
パターン化された前記レジスト下層膜により半導体基板を加工する工程と、
を含むことを特徴とする、半導体装置の製造方法。
<12> 下記式(1):
(式(1)中、A1は少なくとも1つの水素原子がハロゲン原子で置換されていてもよく且つ硫黄原子、ジスルフィド基、スルホニル基、カルボニル基若しくはイミノ基で中断されている炭素原子数2乃至10の直鎖若しくは分岐アルキレン基を表す)で表される化合物。
<13> 下記式(1):
[式(1)中、A1は少なくとも1つの水素原子がハロゲン原子で置換されてもよく且つ硫黄原子、ジスルフィド基、スルホニル基、カルボニル基若しくはイミノ基で中断されている炭素原子数2乃至10の直鎖若しくは分岐アルキレン基を表す]で表される化合物と、
カルボン酸含有化合物、カルボン酸無水物含有化合物、ヒドロキシ基含有化合物、チオール基含有化合物、アミノ基含有化合物及びイミド基含有化合物からなる群より選択される少なくとも一種のエポキシ付加体形成化合物との反応生成物。
<1> エポキシ付加体形成化合物と、下記式(1):
[式(1)中、A1は少なくとも1つの水素原子がハロゲン原子で置換されていてもよく且つ酸素原子、硫黄原子、ジスルフィド基、スルホニル基、カルボニル基若しくはイミノ基で中断されている炭素原子数2乃至10の直鎖若しくは分岐アルキレン基を表す]で表される化合物、とのエポキシ付加生成物と、溶剤とを含む、レジスト下層膜形成組成物。
<2> 前記エポキシ付加体形成化合物が、カルボン酸含有化合物、カルボン酸無水物含有化合物、ヒドロキシ基含有化合物、チオール基含有化合物、アミノ基含有化合物及びイミド基含有化合物からなる群より選ばれる少なくとも1種の化合物である、<1>に記載のレジスト下層膜形成組成物。
<3> 前記エポキシ付加体形成化合物が、カルボン酸含有化合物またはチオール基含有化合物である、<1>又は<2>に記載のレジスト下層膜形成組成物。
<4> 前記カルボン酸含有化合物が、硫黄原子を少なくとも1つ以上含むジカルボン酸である、<2>又は<3>に記載のレジスト下層膜形成組成物。
<5> 前記硫黄原子を少なくとも1つ以上含むジカルボン酸が、硫黄原子を少なくとも1つ以上含む脂肪族ジカルボン酸である、<4>に記載のレジスト下層膜形成組成物。
<6> 架橋触媒をさらに含む、<1>~<5>のいずれか1項に記載のレジスト下層膜形成組成物。
<7> 架橋剤をさらに含む、<1>~<6>のいずれか1項に記載のレジスト下層膜形成組成物。
<8> 界面活性剤をさらに含む、<1>~<7>のいずれか1項に記載のレジスト下層膜形成組成物。
<9> <1>~<8>のいずれか1項に記載のレジスト下層膜形成組成物からなる塗布膜の焼成物であることを特徴とするレジスト下層膜。
<10> 半導体基板上に、<1>~<8>のいずれか1項に記載のレジスト下層膜形成組成物を塗布しベークしてレジスト下層膜を形成する工程、前記レジスト下層膜上にレジストを塗布しベークしてレジスト膜を形成する工程、前記レジスト下層膜と前記レジストで被覆された半導体基板を露光する工程、露光後の前記レジスト膜を現像し、パターニングする工程を含む、パターニングされた基板の製造方法。
<11> 半導体基板上に、<1>~<8>の何れか1項に記載のレジスト下層膜形成組成物からなるレジスト下層膜を形成する工程と、
前記レジスト下層膜の上にレジスト膜を形成する工程と、
レジスト膜に対する光又は電子線の照射とその後の現像によりレジストパターンを形成する工程と、
形成された前記レジストパターンを介して前記レジスト下層膜をエッチングすることによりパターン化されたレジスト下層膜を形成する工程と、
パターン化された前記レジスト下層膜により半導体基板を加工する工程と、
を含むことを特徴とする、半導体装置の製造方法。
<12> 下記式(1):
(式(1)中、A1は少なくとも1つの水素原子がハロゲン原子で置換されていてもよく且つ硫黄原子、ジスルフィド基、スルホニル基、カルボニル基若しくはイミノ基で中断されている炭素原子数2乃至10の直鎖若しくは分岐アルキレン基を表す)で表される化合物。
<13> 下記式(1):
[式(1)中、A1は少なくとも1つの水素原子がハロゲン原子で置換されてもよく且つ硫黄原子、ジスルフィド基、スルホニル基、カルボニル基若しくはイミノ基で中断されている炭素原子数2乃至10の直鎖若しくは分岐アルキレン基を表す]で表される化合物と、
カルボン酸含有化合物、カルボン酸無水物含有化合物、ヒドロキシ基含有化合物、チオール基含有化合物、アミノ基含有化合物及びイミド基含有化合物からなる群より選択される少なくとも一種のエポキシ付加体形成化合物との反応生成物。
本発明によれば、カルボン酸含有化合物等のエポキシ付加体形成化合物と、ヘテロ原子(O、S、N等)及びグリシジルエステル基を有する特定構造の化合物との反応生成物をレジスト下層膜形成組成物に適用することにより、グリシジルエステル基を持たないヘテロ原子化合物を用いた場合と比較して、高エッチングレートを達成することが可能となった。
[レジスト下層膜形成組成物]
本発明に係るレジスト下層膜形成組成物は、エポキシ付加体形成化合物と、下記式(1):
[式(1)中、A1は少なくとも1つの水素原子がハロゲン原子で置換されていてもよく且つ酸素原子、硫黄原子、ジスルフィド基、スルホニル基、カルボニル基若しくはイミノ基で中断されている炭素原子数2乃至10の直鎖若しくは分岐アルキレン基を表す]で表される化合物、とのエポキシ付加生成物と、溶剤とを含む。以下、順に説明する。
本発明に係るレジスト下層膜形成組成物は、エポキシ付加体形成化合物と、下記式(1):
[式(1)中、A1は少なくとも1つの水素原子がハロゲン原子で置換されていてもよく且つ酸素原子、硫黄原子、ジスルフィド基、スルホニル基、カルボニル基若しくはイミノ基で中断されている炭素原子数2乃至10の直鎖若しくは分岐アルキレン基を表す]で表される化合物、とのエポキシ付加生成物と、溶剤とを含む。以下、順に説明する。
[式(1)で表される化合物]
上記式(1)で表される化合物において、A1は少なくとも1つの水素原子がハロゲン原子で置換されていてもよく且つ酸素原子、硫黄原子、ジスルフィド基、スルホニル基、カルボニル基若しくはイミノ基で中断されている炭素原子数2乃至10の直鎖若しくは分岐アルキレン基を表す。
上記式(1)で表される化合物において、A1は少なくとも1つの水素原子がハロゲン原子で置換されていてもよく且つ酸素原子、硫黄原子、ジスルフィド基、スルホニル基、カルボニル基若しくはイミノ基で中断されている炭素原子数2乃至10の直鎖若しくは分岐アルキレン基を表す。
炭素原子数2乃至10の直鎖若しくは分岐アルキレン基としては、エチレン基、n-プロピレン基、イソプロピレン基、n-ブチレン基、s-ブチレン基、n-ペンチレン基、1-メチルブチレン基、2-メチルブチレン基、3-メチルブチレン基、n-ペンチレン基、1,1-ジメチルプロピレン基、1,2-ジメチルプロピレン基、2,2-ジメチルプロピレン基、1,3-ジメチルプロピレン基、n-ヘキシレン基、1-メチルヘプチレン基、2-メチルヘプチレン基、3-メチルヘプチレン基、1,1-ジメチルブチレン基、1,2-ジメチルブチレン基、1,3-ジメチルブチレン基、2,2-ジメチルブチレン基、2,3-ジメチルブチレン基、3,3-ジメチルブチレン基、3,3-ジメチルブタン-2-イレン基、2,3-ジメチルブタン-2-イレン基、3-ヘキシレン基、2-エチルペンチレン基、2-メチルペンタン-3-イレン基、ヘプチレン基、オクチレン基、ノニレン基、デシレン基等である。
「中断されている」とは、上記アルキレン基の炭素-炭素結合間に、酸素原子、硫黄原子、ジスルフィド基、スルホニル基、カルボニル基若しくはイミノ基が挿入されている態様をいう。
上記ハロゲン原子としては、フッ素、塩素、臭素、及びヨウ素が挙げられる。
上記少なくとも1つの水素原子がハロゲン原子で置換されていてもよい、とは上記炭素原子数2乃至10の直鎖若しくは分岐アルキレン基が有する少なくとも1つの水素原子がハロゲン原子で置換されていてもよいことを言う。ハロゲン原子の置換数としては5以下が好ましく、3以下が好ましく、2以下が好ましく、1以下が好ましく、0(すなわち、ハロゲン原子で置換されていない)が好ましい。
好ましい具体例を挙げると以下のとおりであるが、これらに限定されるわけではない。
-CH2-O-CH2-,-C2H4-O-C2H4-,-C3H6-O-C3H6-,-CH2-S-CH2-,-C2H4-S-C2H4-,-C3H6-S-C3H6-,-CH2-S-C2H4-,-CH2-S-C3H6-,-C2H4-S-C3H6-,-CH2-S-C2H4-S-CH2-,-CH2-SS-CH2-,-C2H4-SS-C2H4-,-C3H6-SS-C3H6-,-CH2-SO2-CH2-,-C2H4-SO2-C2H4-,-C3H6-SO2-C3H6-,-CH2-CO-CH2-,-C2H4-CO-C2H4-,-C3H6-CO-C3H6-,-CH2-NH-CH2-,-C2H4-NH-C2H4-,-C3H6-NH-C3H6-
また、上記アルキレン基が挿入される基によって中断される回数は1回でも良いが、結合の安定性が保たれる限り、2回以上であっても良い。その場合、挿入される基は同一でも良く、異なっていても良い。
上記ハロゲン原子としては、フッ素、塩素、臭素、及びヨウ素が挙げられる。
上記少なくとも1つの水素原子がハロゲン原子で置換されていてもよい、とは上記炭素原子数2乃至10の直鎖若しくは分岐アルキレン基が有する少なくとも1つの水素原子がハロゲン原子で置換されていてもよいことを言う。ハロゲン原子の置換数としては5以下が好ましく、3以下が好ましく、2以下が好ましく、1以下が好ましく、0(すなわち、ハロゲン原子で置換されていない)が好ましい。
好ましい具体例を挙げると以下のとおりであるが、これらに限定されるわけではない。
-CH2-O-CH2-,-C2H4-O-C2H4-,-C3H6-O-C3H6-,-CH2-S-CH2-,-C2H4-S-C2H4-,-C3H6-S-C3H6-,-CH2-S-C2H4-,-CH2-S-C3H6-,-C2H4-S-C3H6-,-CH2-S-C2H4-S-CH2-,-CH2-SS-CH2-,-C2H4-SS-C2H4-,-C3H6-SS-C3H6-,-CH2-SO2-CH2-,-C2H4-SO2-C2H4-,-C3H6-SO2-C3H6-,-CH2-CO-CH2-,-C2H4-CO-C2H4-,-C3H6-CO-C3H6-,-CH2-NH-CH2-,-C2H4-NH-C2H4-,-C3H6-NH-C3H6-
また、上記アルキレン基が挿入される基によって中断される回数は1回でも良いが、結合の安定性が保たれる限り、2回以上であっても良い。その場合、挿入される基は同一でも良く、異なっていても良い。
式(1)で表される化合物の具体例を挙げると以下のとおりであるが、これらに限定されるわけではない。
[エポキシ付加体形成化合物]
エポキシ付加体形成化合物とは、上記式(1)で表される化合物と反応してポリマー又はオリゴマーを生成し得る化合物をいう。通常は、エポキシ基に対する反応性を有する官能基を一分子あたり1乃至4個有している化合物である。エポキシ付加体形成化合物は一種のみを用いることもできるが、二種以上の混合物であってもよい。その場合は、生成物の主鎖を或る程度長くする観点から、エポキシ基と反応性を有する官能基を一分子あたり2個以上有している化合物が混合物の過半量を占めることが好ましい。
エポキシ付加体形成化合物とは、上記式(1)で表される化合物と反応してポリマー又はオリゴマーを生成し得る化合物をいう。通常は、エポキシ基に対する反応性を有する官能基を一分子あたり1乃至4個有している化合物である。エポキシ付加体形成化合物は一種のみを用いることもできるが、二種以上の混合物であってもよい。その場合は、生成物の主鎖を或る程度長くする観点から、エポキシ基と反応性を有する官能基を一分子あたり2個以上有している化合物が混合物の過半量を占めることが好ましい。
エポキシ付加体形成化合物は、好ましくは、カルボン酸含有化合物、カルボン酸無水物含有化合物、ヒドロキシ基含有化合物、チオール基含有化合物、アミノ基含有化合物及びイミド基含有化合物からなる群より選ばれる少なくとも1種の化合物であり、より好ましくは、カルボン酸含有化合物またはチオール基含有化合物である。
エポキシ付加体形成化合物は、ヘテロ原子を有することが好ましい。エポキシ付加体形成化合物は1つ又は2つ以上のヘテロ原子を有することが好ましい。エポキシ付加体形成化合物は2個以上10個以下のヘテロ原子を有することが好ましい。
上記ヘテロ原子としては、窒素原子、酸素原子、硫黄原子が好ましい。
カルボン酸含有化合物は、好ましくは、硫黄原子を少なくとも1つ以上含むジカルボン酸であり、より好ましくは、硫黄原子を少なくとも1つ以上含む脂肪族ジカルボン酸である。
エポキシ付加体形成化合物は、ヘテロ原子を有することが好ましい。エポキシ付加体形成化合物は1つ又は2つ以上のヘテロ原子を有することが好ましい。エポキシ付加体形成化合物は2個以上10個以下のヘテロ原子を有することが好ましい。
上記ヘテロ原子としては、窒素原子、酸素原子、硫黄原子が好ましい。
カルボン酸含有化合物は、好ましくは、硫黄原子を少なくとも1つ以上含むジカルボン酸であり、より好ましくは、硫黄原子を少なくとも1つ以上含む脂肪族ジカルボン酸である。
エポキシ付加体形成化合物の具体例を挙げると以下のとおりであるが、これらに限定されるわけではない。
[エポキシ付加生成物]
エポキシ付加生成物は、前記式(1)で表される化合物とエポキシ付加体形成化合物との反応生成物である。すなわち、原料モノマーである前記式(1)で表される化合物とエポキシ付加体形成化合物との反応生成物とを、適切なモル比になるよう溶剤へ溶解させ、エポキシ基を活性化させる触媒の存在のもと、重合させることによって得られる。
エポキシ付加生成物は、前記式(1)で表される化合物とエポキシ付加体形成化合物との反応生成物である。すなわち、原料モノマーである前記式(1)で表される化合物とエポキシ付加体形成化合物との反応生成物とを、適切なモル比になるよう溶剤へ溶解させ、エポキシ基を活性化させる触媒の存在のもと、重合させることによって得られる。
エポキシ基を活性化させる触媒とは、例えばトリフェニルモノエチルホスホニウムブロミドのような第4級ホスホニウム塩、又はベンジルトリエチルアンモニウムクロリドのような第4級アンモニウム塩であり、原料モノマーである式(1)で表される化合物とエポキシ付加体形成化合物との全質量に対して0.1質量%乃至10質量%の範囲から適量を選択して用いることができる。
重合反応させる温度及び時間は、80℃乃至160℃、2時間乃至50時間の範囲から、最適な条件が選択される。
上記の反応は無溶媒でも行われるが、通常溶媒を用いて行われる。溶媒としては反応を阻害しないものであれば全て使用することができる。例えば1,2-ジメトキシエタン、ジエチレングリコールジメチルエーテル、プロピレングリコールモノメチルエーテル、テトラヒドロフラン、ジオキサン等のエーテル類が挙げられる。
以上のようにして得られるエポキシ付加生成物の重量平均分子量Mwは、通常500又は600以上、1,000,000又は500,000以下である。
[溶剤]
本発明に係るレジスト下層膜形成組成物の溶剤としては、上記反応生成物を溶解できる溶剤であれば、特に制限なく使用することができる。特に、本発明に係るレジスト下層膜形成組成物は均一な溶液状態で用いられるものであるため、その塗布性能を考慮すると、リソグラフィー工程に一般的に使用される溶剤を併用することが推奨される。
本発明に係るレジスト下層膜形成組成物の溶剤としては、上記反応生成物を溶解できる溶剤であれば、特に制限なく使用することができる。特に、本発明に係るレジスト下層膜形成組成物は均一な溶液状態で用いられるものであるため、その塗布性能を考慮すると、リソグラフィー工程に一般的に使用される溶剤を併用することが推奨される。
そのような溶剤としては、例えば、メチルセロソルブアセテート、エチルセロソルブアセテート、プロピレングリコール、プロピレングリコールモノメチルエーテル、プロピレングリコールモノエチルエーテル、メチルイソブチルカルビノール、プロピレングリコールモノブチルエーテル、プロピレングリコールモノメチルエーテルアセテート、プロピレングリコールモノエテルエーテルアセテート、プロピレングリコールモノプロピルエーテルアセテート、プロピレングリコールモノブチルエーテルアセテート、トルエン、キシレン、メチルエチルケトン、シクロペンタノン、シクロヘキサノン、2-ヒドロキシプロピオン酸エチル、2-ヒドロキシ-2-メチルプロピオン酸エチル、エトキシ酢酸エチル、ヒドロキシ酢酸エチル、2-ヒドロキシ-3-メチルブタン酸メチル、3-メトキシプロピオン酸メチル、3-メトキシプロピオン酸エチル、3-エトキシプロピオン酸エチル、3-エトキシプロピオン酸メチル、ピルビン酸メチル、ピルビン酸エチル、エチレングリコールモノメチルエーテル、エチレングリコールモノエチルエーテル、エチレングリコールモノプロピルエーテル、エチレングリコールモノブチルエーテル、エチレングリコールモノメチルエーテルアセテート、エチレングリコールモノエチルエーテルアセテート、エチレングリコールモノプロピルエーテルアセテート、エチレングリコールモノブチルエーテルアセテート、ジエチレングリコールジメチルエーテル、ジエチレングリコールジエチルエーテル、ジエチレングリコールジプロピルエーテル、ジエチレングリコールジブチルエーテルプロピレングリコールモノメチルエーテル、プロピレングリコールジメチルエーテル、プロピレングリコールジエチルエーテル、プロピレングリコールジプロピルエーテル、プロピレングリコールジブチルエーテル、乳酸エチル、乳酸プロピル、乳酸イソプロピル、乳酸ブチル、乳酸イソブチル、ギ酸メチル、ギ酸エチル、ギ酸プロピル、ギ酸イソプロピル、ギ酸ブチル、ギ酸イソブチル、ギ酸アミル、ギ酸イソアミル、酢酸メチル、酢酸エチル、酢酸アミル、酢酸イソアミル、酢酸ヘキシル、プロピオン酸メチル、プロピオン酸エチル、プロピオン酸プロピル、プロピオン酸イソプロピル、プロピオン酸ブチル、プロピオン酸イソブチル、酪酸メチル、酪酸エチル、酪酸プロピル、酪酸イソプロピル、酪酸ブチル、酪酸イソブチル、ヒドロキシ酢酸エチル、2-ヒドロキシ-2-メチルプロピオン酸エチル、3-メトキシ-2-メチルプロピオン酸メチル、2-ヒドロキシ-3-メチル酪酸メチル、メトキシ酢酸エチル、エトキシ酢酸エチル、3-メトキシプロピオン酸メチル、3-エトキシプロピオン酸エチル、3-メトキシプロピオン酸エチル、3-メトキシブチルアセテート、3-メトキシプロピルアセテート、3-メチル-3-メトキシブチルアセテート、3-メチル-3-メトキシブチルプロピオネート、3-メチル-3-メトキシブチルブチレート、アセト酢酸メチル、トルエン、キシレン、メチルエチルケトン、メチルプロピルケトン、メチルブチルケトン、2-ヘプタノン、3-ヘプタノン、4-ヘプタノン、シクロヘキサノン、N、N-ジメチルホルムアミド、N-メチルアセトアミド、N,N-ジメチルアセトアミド、N-メチルピロリドン、4-メチル-2-ペンタノール、及びγ-ブチロラクトン等を挙げることができる。これらの溶剤は単独で、または二種以上の組み合わせで使用することができる。
また、特願2017-140193に記載された下記の化合物を用いることもできる。
(式(i)中のR1、R2及びR3は各々水素原子、酸素原子、硫黄原子又はアミド結合で中断されていてもよい炭素原子数1~20のアルキル基を表し、互いに同一であっても異なっても良く、互いに結合して環構造を形成しても良い。)
(式(i)中のR1、R2及びR3は各々水素原子、酸素原子、硫黄原子又はアミド結合で中断されていてもよい炭素原子数1~20のアルキル基を表し、互いに同一であっても異なっても良く、互いに結合して環構造を形成しても良い。)
炭素原子数1~20のアルキル基としては、置換基を有しても、有さなくてもよい直鎖または分岐を有するアルキル基が挙げられ、例えば、メチル基、エチル基、n-プロピル基、イソプロピル基、n-ブチル基、sec-ブチル基、tert-ブチル基、n-ペンチル基、イソペンチル基、ネオペンチル基、n-ヘキシル基、イソヘキシル基、n-ヘプチル基、n-オクチル基、シクロヘキシル基、2-エチルヘキシル基、n-ノニル基、イソノニル基、p-tert-ブチルシクロヘキシル基、n-デシル基、n-ドデシルノニル基、ウンデシル基、ドデシル基、トリデシル基、テトラデシル基、ペンタデシル基、ヘキサデシル基、ヘプタデシル基、オクタデシル基、ノナデシル基およびエイコシル基などが挙げられる。好ましくは炭素原子数1~12のアルキル基、より好ましくは炭素原子数1~8のアルキル基、更に好ましくは炭素原子数1~4のアルキル基である。
酸素原子、硫黄原子又はアミド結合により中断された炭素原子数1~20のアルキル基としては、例えば、構造単位-CH2-O-、-CH2-S-、-CH2-NHCO-又は-CH2-CONH-を含有するものが挙げられる。-O-、-S-、-NHCO-又は-CONH-は前記アルキル基中に一単位又は二単位以上あってよい。-O-、-S-、-NHCO-又は-CONH-単位により中断された炭素原子数1~20のアルキル基の具体例は、メトキシ基、エトキシ基、プロポキシ基、ブトキシ基、メチルチオ基、エチルチオ基、プロピルチオ基、ブチルチオ基、メチルカルボニルアミノ基、エチルカルボニルアミノ基、プロピルカルボニルアミノ基、ブチルカルボニルアミノ基、メチルアミノカルボニル基、エチルアミノカルボニル基、プロピルアミノカルボニル基、ブチルアミノカルボニル基等であり、更には、メチル基、エチル基、プロピル基、ブチル基、ペンチル基、ヘキシル基、ヘプチル基、オクチル基、ノニル基、デシル基、ドデシル基又はオクタデシル基であって、その各々がメトキシ基、エトキシ基、プロポキシ基、ブトキシ基、メチルチオ基、エチルチオ基、プロピルチオ基、ブチルチオ基、メチルカルボニルアミノ基、エチルカルボニルアミノ基、メチルアミノカルボニル基、エチルアミノカルボニル基等により置換されたものである。好ましくはメトキシ基、エトキシ基、メチルチオ基、エチルチオ基であり、より好ましくはメトキシ基、エトキシ基である。
これらの溶剤は比較的高沸点であることから、レジスト下層膜形成組成物に高埋め込み性や高平坦化性を付与するためにも有効である。
[架橋剤成分]
本発明のレジスト下層膜形成組成物は架橋剤成分を含むことができる。その架橋剤としては、メラミン系、置換尿素系、またはそれらのポリマー系等が挙げられる。好ましくは、少なくとも2個の架橋形成置換基を有する架橋剤であり、メトキシメチル化グリコールウリル、ブトキシメチル化グリコールウリル、メトキシメチル化メラミン、ブトキシメチル化メラミン、メトキシメチル化ベンゾグワナミン、ブトキシメチル化ベンゾグワナミン、メトキシメチル化尿素、ブトキシメチル化尿素、またはメトキシメチル化チオ尿素等の化合物である。また、これらの化合物の縮合体も使用することができる。
好ましいものとして、テトラメトキシメチルグリコールウリル(日本サイテックインダストリーズ(株)、商品名:POWDERLINK〔登録商標〕1174)が挙げられる。
本発明のレジスト下層膜形成組成物は架橋剤成分を含むことができる。その架橋剤としては、メラミン系、置換尿素系、またはそれらのポリマー系等が挙げられる。好ましくは、少なくとも2個の架橋形成置換基を有する架橋剤であり、メトキシメチル化グリコールウリル、ブトキシメチル化グリコールウリル、メトキシメチル化メラミン、ブトキシメチル化メラミン、メトキシメチル化ベンゾグワナミン、ブトキシメチル化ベンゾグワナミン、メトキシメチル化尿素、ブトキシメチル化尿素、またはメトキシメチル化チオ尿素等の化合物である。また、これらの化合物の縮合体も使用することができる。
好ましいものとして、テトラメトキシメチルグリコールウリル(日本サイテックインダストリーズ(株)、商品名:POWDERLINK〔登録商標〕1174)が挙げられる。
また、上記架橋剤としては耐熱性の高い架橋剤を用いることができる。耐熱性の高い架橋剤としては分子内に芳香族環(例えば、ベンゼン環、ナフタレン環)を有する架橋形成置換基を含有する化合物を好ましく用いることができる。
この化合物は下記式(4)の部分構造を有する化合物や、下記式(5)の繰り返し単位を有するポリマー又はオリゴマーが挙げられる。
上記R11、R12、R13、及びR14は水素原子又は炭素数1乃至10のアルキル基であり、これらのアルキル基は上述の例示を用いることができる。
上記R11、R12、R13、及びR14は水素原子又は炭素数1乃至10のアルキル基であり、これらのアルキル基は上述の例示を用いることができる。
上記化合物は旭有機材工業(株)、本州化学工業(株)の製品として入手することができる。例えば上記架橋剤の中で式(4-24)の化合物は旭有機材工業(株)、商品名TM-BIP-Aとして入手することができる。
架橋剤の添加量は、使用する塗布溶媒、使用する下地基板、要求される溶液粘度、要求される膜形状などにより変動するが、全固形分に対して0.001乃至80質量%、好ましくは0.01乃至50質量%、さらに好ましくは0.05乃至40質量%である。これら架橋剤は自己縮合による架橋反応を起こすこともあるが、本発明の上記反応生成物中に架橋性置換基が存在する場合は、それらの架橋性置換基と架橋反応を起こすことができる。
架橋剤の添加量は、使用する塗布溶媒、使用する下地基板、要求される溶液粘度、要求される膜形状などにより変動するが、全固形分に対して0.001乃至80質量%、好ましくは0.01乃至50質量%、さらに好ましくは0.05乃至40質量%である。これら架橋剤は自己縮合による架橋反応を起こすこともあるが、本発明の上記反応生成物中に架橋性置換基が存在する場合は、それらの架橋性置換基と架橋反応を起こすことができる。
[酸及び/又は酸発生剤]
本発明のレジスト下層膜形成組成物は酸及び/又は酸発生剤を含有することができる。
酸としては例えば、p-トルエンスルホン酸、トリフルオロメタンスルホン酸、ピリジニウムp-トルエンスルホン酸、ピリジニウムトリフルオロメタンスルホン酸、ピリジニウム-p-フェノールスルホン酸、サリチル酸、5-スルホサリチル酸、4-フェノールスルホン酸、カンファースルホン酸、4-クロロベンゼンスルホン酸、ベンゼンジスルホン酸、1-ナフタレンスルホン酸、クエン酸、安息香酸、ヒドロキシ安息香酸、ナフタレンカルボン酸等が挙げられる。
酸は一種のみを使用することができ、または二種以上を組み合わせて使用することができる。配合量は全固形分に対して、通常0.0001乃至20質量%、好ましくは0.0005乃至10質量%、さらに好ましくは0.01乃至3質量%である。
本発明のレジスト下層膜形成組成物は酸及び/又は酸発生剤を含有することができる。
酸としては例えば、p-トルエンスルホン酸、トリフルオロメタンスルホン酸、ピリジニウムp-トルエンスルホン酸、ピリジニウムトリフルオロメタンスルホン酸、ピリジニウム-p-フェノールスルホン酸、サリチル酸、5-スルホサリチル酸、4-フェノールスルホン酸、カンファースルホン酸、4-クロロベンゼンスルホン酸、ベンゼンジスルホン酸、1-ナフタレンスルホン酸、クエン酸、安息香酸、ヒドロキシ安息香酸、ナフタレンカルボン酸等が挙げられる。
酸は一種のみを使用することができ、または二種以上を組み合わせて使用することができる。配合量は全固形分に対して、通常0.0001乃至20質量%、好ましくは0.0005乃至10質量%、さらに好ましくは0.01乃至3質量%である。
酸発生剤としては、熱酸発生剤や光酸発生剤が挙げられる。
熱酸発生剤としては、2,4,4,6-テトラブロモシクロヘキサジエノン、ベンゾイントシレート、2-ニトロベンジルトシレート、その他有機スルホン酸アルキルエステル等が挙げられる。
熱酸発生剤としては、2,4,4,6-テトラブロモシクロヘキサジエノン、ベンゾイントシレート、2-ニトロベンジルトシレート、その他有機スルホン酸アルキルエステル等が挙げられる。
光酸発生剤は、レジストの露光時に酸を生ずる。そのため、下層膜の酸性度の調整ができる。これは、下層膜の酸性度を上層のレジストとの酸性度に合わせるための一方法である。また、下層膜の酸性度の調整によって、上層に形成されるレジストのパターン形状の調整ができる。
本発明のレジスト下層膜形成組成物に含まれる光酸発生剤としては、オニウム塩化合物、スルホンイミド化合物、及びジスルホニルジアゾメタン化合物等が挙げられる。
本発明のレジスト下層膜形成組成物に含まれる光酸発生剤としては、オニウム塩化合物、スルホンイミド化合物、及びジスルホニルジアゾメタン化合物等が挙げられる。
オニウム塩化合物としてはジフェニルヨードニウムヘキサフルオロホスフエート、ジフェニルヨードニウムトリフルオロメタンスルホネート、ジフェニルヨードニウムノナフルオロノルマルブタンスルホネート、ジフェニルヨードニウムパーフルオロノルマルオクタンスルホネート、ジフェニルヨードニウムカンファースルホネート、ビス(4-tert-ブチルフェニル)ヨードニウムカンファースルホネート及びビス(4-tert-ブチルフェニル)ヨードニウムトリフルオロメタンスルホネート等のヨードニウム塩化合物、及びトリフェニルスルホニウムヘキサフルオロアンチモネート、トリフェニルスルホニウムノナフルオロノルマルブタンスルホネート、トリフェニルスルホニウムカンファースルホネート及びトリフェニルスルホニウムトリフルオロメタンスルホネート等のスルホニウム塩化合物等が挙げられる。
スルホンイミド化合物としては、例えばN-(トリフルオロメタンスルホニルオキシ)スクシンイミド、N-(ノナフルオロノルマルブタンスルホニルオキシ)スクシンイミド、N-(カンファースルホニルオキシ)スクシンイミド及びN-(トリフルオロメタンスルホニルオキシ)ナフタルイミド等が挙げられる。
ジスルホニルジアゾメタン化合物としては、例えば、ビス(トリフルオロメチルスルホニル)ジアゾメタン、ビス(シクロヘキシルスルホニル)ジアゾメタン、ビス(フェニルスルホニル)ジアゾメタン、ビス(p-トルエンスルホニル)ジアゾメタン、ビス(2,4-ジメチルベンゼンスルホニル)ジアゾメタン、及びメチルスルホニル-p-トルエンスルホニルジアゾメタン等が挙げられる。
酸発生剤は一種のみを使用することができ、または二種以上を組み合わせて使用することができる。
酸発生剤が使用される場合、その割合としては、レジスト下層膜形成組成物の固形分100質量部に対して、0.01乃至5質量部、または0.1乃至3質量部、または0.5乃至1質量部である。
酸発生剤が使用される場合、その割合としては、レジスト下層膜形成組成物の固形分100質量部に対して、0.01乃至5質量部、または0.1乃至3質量部、または0.5乃至1質量部である。
[その他の成分]
本発明のレジスト下膜形成組成物には、ピンホールやストレーション等の発生がなく、表面むらに対する塗布性をさらに向上させるために、界面活性剤を配合することができる。界面活性剤としては、例えばポリオキシエチレンラウリルエーテル、ポリオキシエチレンステアリルエーテル、ポリオキシエチレンセチルエーテル、ポリオキシエチレンオレイルエーテル等のポリオキシエチレンアルキルエーテル類、ポリオキシエチレンオクチルフェノールエーテル、ポリオキシエチレンノニルフェノールエーテル等のポリオキシエチレンアルキルアリルエーテル類、ポリオキシエチレン・ポリオキシプロピレンブロックコポリマー類、ソルビタンモノラウレート、ソルビタンモノパルミテート、ソルビタンモノステアレート、ソルビタンモノオレエート、ソルビタントリオレエート、ソルビタントリステアレート等のソルビタン脂肪酸エステル類、ポリオキシエチレンソルビタンモノラウレート、ポリオキシエチレンソルビタンモノパルミテート、ポリオキシエチレンソルビタンモノステアレート、ポリオキシエチレンソルビタントリオレエート、ポリオキシエチレンソルビタントリステアレート等のポリオキシエチレンソルビタン脂肪酸エステル類等のノニオン系界面活性剤、エフトップEF301、EF303、EF352((株)トーケムプロダクツ製、商品名)、メガファックF171、F173、R-40、R-40N、R-40LM(DIC(株)製、商品名)、フロラードFC430、FC431(住友スリーエム(株)製、商品名)、アサヒガードAG710、サーフロンS-382、SC101、SC102、SC103、SC104、SC105、SC106(旭硝子(株)製、商品名)等のフッ素系界面活性剤、オルガノシロキサンポリマーKP341(信越化学工業(株)製)等を挙げることができる。これらの界面活性剤の配合量は、レジスト下層膜材料の全固形分に対して通常2.0質量%以下、好ましくは1.0質量%以下である。これらの界面活性剤は単独で使用してもよいし、また二種以上の組み合わせで使用することもできる。界面活性剤が使用される場合、その割合としては、レジスト下層膜形成組成物の固形分100質量部に対して0.0001乃至5質量部、または0.001乃至1質量部、または0.01乃至0.5質量部である。
本発明のレジスト下膜形成組成物には、ピンホールやストレーション等の発生がなく、表面むらに対する塗布性をさらに向上させるために、界面活性剤を配合することができる。界面活性剤としては、例えばポリオキシエチレンラウリルエーテル、ポリオキシエチレンステアリルエーテル、ポリオキシエチレンセチルエーテル、ポリオキシエチレンオレイルエーテル等のポリオキシエチレンアルキルエーテル類、ポリオキシエチレンオクチルフェノールエーテル、ポリオキシエチレンノニルフェノールエーテル等のポリオキシエチレンアルキルアリルエーテル類、ポリオキシエチレン・ポリオキシプロピレンブロックコポリマー類、ソルビタンモノラウレート、ソルビタンモノパルミテート、ソルビタンモノステアレート、ソルビタンモノオレエート、ソルビタントリオレエート、ソルビタントリステアレート等のソルビタン脂肪酸エステル類、ポリオキシエチレンソルビタンモノラウレート、ポリオキシエチレンソルビタンモノパルミテート、ポリオキシエチレンソルビタンモノステアレート、ポリオキシエチレンソルビタントリオレエート、ポリオキシエチレンソルビタントリステアレート等のポリオキシエチレンソルビタン脂肪酸エステル類等のノニオン系界面活性剤、エフトップEF301、EF303、EF352((株)トーケムプロダクツ製、商品名)、メガファックF171、F173、R-40、R-40N、R-40LM(DIC(株)製、商品名)、フロラードFC430、FC431(住友スリーエム(株)製、商品名)、アサヒガードAG710、サーフロンS-382、SC101、SC102、SC103、SC104、SC105、SC106(旭硝子(株)製、商品名)等のフッ素系界面活性剤、オルガノシロキサンポリマーKP341(信越化学工業(株)製)等を挙げることができる。これらの界面活性剤の配合量は、レジスト下層膜材料の全固形分に対して通常2.0質量%以下、好ましくは1.0質量%以下である。これらの界面活性剤は単独で使用してもよいし、また二種以上の組み合わせで使用することもできる。界面活性剤が使用される場合、その割合としては、レジスト下層膜形成組成物の固形分100質量部に対して0.0001乃至5質量部、または0.001乃至1質量部、または0.01乃至0.5質量部である。
本発明のレジスト下膜形成組成物には、吸光剤、レオロジー調整剤、接着補助剤などを添加することができる。レオロジー調整剤は、下層膜形成組成物の流動性を向上させるのに有効である。接着補助剤は、半導体基板またはレジストと下層膜の密着性を向上させるのに有効である。
吸光剤としては例えば、「工業用色素の技術と市場」(CMC出版)や「染料便覧」(有機合成化学協会編)に記載の市販の吸光剤、例えば、C.I.Disperse Yellow 1,3,4,5,7,8,13,23,31,49,50,51,54,60,64,66,68,79,82,88,90,93,102,114及び124;C.I.Disperse Orange1,5,13,25,29,30,31,44,57,72及び73;C.I.Disperse Red 1,5,7,13,17,19,43,50,54,58,65,72,73,88,117,137,143,199及び210;C.I.Disperse Violet 43;C.I.Disperse Blue 96;C.I.Fluorescent Brightening Agent 112,135及び163;C.I.Solvent Orange2及び45;C.I.Solvent Red 1,3,8,23,24,25,27及び49;C.I.Pigment Green 10;C.I.Pigment Brown 2等を好適に用いることができる。上記吸光剤は通常、レジスト下膜形成組成物の全固形分に対して10質量%以下、好ましくは5質量%以下の割合で配合される。
レオロジー調整剤は、主にレジスト下層膜形成組成物の流動性を向上させ、特にベーキング工程において、レジスト下層膜の膜厚均一性の向上やホール内部へのレジスト下層膜形成組成物の充填性を高める目的で添加される。具体例としては、ジメチルフタレート、ジエチルフタレート、ジイソブチルフタレート、ジヘキシルフタレート、ブチルイソデシルフタレート等のフタル酸誘導体、ジノルマルブチルアジペート、ジイソブチルアジペート、ジイソオクチルアジペート、オクチルデシルアジペート等のアジピン酸誘導体、ジノルマルブチルマレート、ジエチルマレート、ジノニルマレート等のマレイン酸誘導体、メチルオレート、ブチルオレート、テトラヒドロフルフリルオレート等のオレイン酸誘導体、またはノルマルブチルステアレート、グリセリルステアレート等のステアリン酸誘導体を挙げることができる。これらのレオロジー調整剤は、レジスト下膜形成組成物の全固形分に対して通常30質量%未満の割合で配合される。
接着補助剤は、主に基板あるいはレジストとレジスト下層膜形成組成物の密着性を向上させ、特に現像においてレジストが剥離しないようにするための目的で添加される。具体例としては、トリメチルクロロシラン、ジメチルメチロールクロロシラン、メチルジフェニルクロロシラン、クロロメチルジメチルクロロシラン等のクロロシラン類、トリメチルメトキシシラン、ジメチルジエトキシシラン、メチルジメトキシシラン、ジメチルメチロールエトキシシラン、ジフェニルジメトキシシラン、フェニルトリエトキシシラン等のアルコキシシラン類、ヘキサメチルジシラザン、N,N’-ビス(トリメチルシリル)ウレア、ジメチルトリメチルシリルアミン、トリメチルシリルイミダゾール等のシラザン類、メチロールトリクロロシラン、γ-クロロプロピルトリメトキシシラン、γ-アミノプロピルトリエトキシシラン、γ-グリシドキシプロピルトリメトキシシラン等のシラン類、ベンゾトリアゾール、ベンズイミダゾール、インダゾール、イミダゾール、2-メルカプトベンズイミダゾール、2-メルカプトベンゾチアゾール、2-メルカプトベンゾオキサゾール、ウラゾール、チオウラシル、メルカプトイミダゾール、メルカプトピリミジン等の複素環式化合物や、1,1-ジメチルウレア、1,3-ジメチルウレア等の尿素、またはチオ尿素化合物を挙げることができる。これらの接着補助剤は、レジスト下膜形成組成物の全固形分に対して通常5質量%未満、好ましくは2質量%未満の割合で配合される。
本発明に係るレジスト下層膜形成組成物の固形分は通常0.1乃至70質量%、好ましくは0.1乃至60質量%とする。固形分はレジスト下層膜形成組成物から溶剤を除いた全成分の含有割合である。固形分中における上記反応生成物の割合は、1乃至100質量%、1乃至99.9質量%、50乃至99.9質量%、50乃至95質量%、50乃至90質量%の順で好ましい。
レジスト下層膜形成組成物が均一な溶液状態であるかどうかを評価する尺度の一つは、特定のマイクロフィルターの通過性を観察することであるが、本発明に係るレジスト下層膜形成組成物は、孔径0.1μmのマイクロフィルターを通過し、均一な溶液状態を呈する。
上記マイクロフィルター材質としては、PTFE(ポリテトラフルオロエチレン)、PFA(テトラフルオロエチレン・パーフルオロアルキルビニルエーテル共重合体)などのフッ素系樹脂、PE(ポリエチレン)、UPE(超高分子量ポリエチレン)、PP(ポリプロピレン)、PSF(ポリスルフォン)、PES(ポリエーテルスルホン)、ナイロンが挙げられるが、PTFE(ポリテトラフルオロエチレン)製であることが好ましい。
[レジスト下層膜及び半導体装置の製造方法]
以下、本発明に係るレジスト下層膜形成組成物を用いたレジスト下層膜及び半導体装置の製造方法について説明する。
以下、本発明に係るレジスト下層膜形成組成物を用いたレジスト下層膜及び半導体装置の製造方法について説明する。
半導体装置の製造に使用される基板(例えば、シリコンウエハー基板、シリコン/二酸化シリコン被覆基板、シリコンナイトライド基板、ガラス基板、ITO基板、ポリイミド基板、及び低誘電率材料(low-k材料)被覆基板等)の上に、スピナー、コーター等の適当な塗布方法により本発明のレジスト下層膜形成組成物が塗布され、その後、焼成することによりレジスト下層膜が形成される。焼成する条件としては、焼成温度80℃乃至250℃、焼成時間0.3乃至60分間の中から適宜、選択される。好ましくは、焼成温度150℃乃至250℃、焼成時間0.5乃至2分間である。ここで、形成される下層膜の膜厚としては、例えば、10乃至1000nmであり、または20乃至500nmであり、または30乃至300nmであり、または50乃至200nmである。
また、本発明に係る有機レジスト下層膜上に無機レジスト下層膜(ハードマスク)を形成することもできる。例えば、WO2009/104552A1に記載のシリコン含有レジスト下層膜(無機レジスト下層膜)形成組成物をスピンコートで形成する方法の他、Si系の無機材料膜をCVD法などで形成することができる。
また、本発明に係るレジスト下層膜形成組成物を、段差を有する部分と段差を有しない部分とを有する半導体基板(いわゆる段差基板)上に塗布し、焼成することにより、当該段差を有する部分と段差を有しない部分との段差が3~50nmの範囲内である、レジスト下層膜を形成することができる。
次いでそのレジスト下層膜の上にレジスト膜、例えばフォトレジストの層が形成される。フォトレジストの層の形成は、周知の方法、すなわち、フォトレジスト組成物溶液の下層膜上への塗布及び焼成によって行なうことができる。フォトレジストの膜厚としては例えば50乃至10000nmであり、または100乃至2000nmであり、または200乃至1000nmである。
レジスト下層膜の上に形成されるフォトレジストとしては露光に使用される光に感光するものであれば特に限定はない。ネガ型フォトレジスト及びポジ型フォトレジストのいずれも使用できる。ノボラック樹脂と1,2-ナフトキノンジアジドスルホン酸エステルとからなるポジ型フォトレジスト、酸により分解してアルカリ溶解速度を上昇させる基を有するバインダーと光酸発生剤からなる化学増幅型フォトレジスト、酸により分解してフォトレジストのアルカリ溶解速度を上昇させる低分子化合物とアルカリ可溶性バインダーと光酸発生剤とからなる化学増幅型フォトレジスト、及び酸により分解してアルカリ溶解速度を上昇させる基を有するバインダーと酸により分解してフォトレジストのアルカリ溶解速度を上昇させる低分子化合物と光酸発生剤からなる化学増幅型フォトレジストなどがある。例えば、シプレー社製商品名APEX-E、住友化学工業(株)製商品名PAR710、及び信越化学工業(株)製商品名SEPR430等が挙げられる。また、例えば、Proc.SPIE,Vol.3999,330-334(2000)、Proc.SPIE,Vol.3999,357-364(2000)、やProc.SPIE,Vol.3999,365-374(2000)に記載されているような、含フッ素原子ポリマー系フォトレジストを挙げることができる。
次に、光又は電子線の照射と現像によりレジストパターンを形成する。まず、所定のマスクを通して露光が行なわれる。露光には、近紫外線、遠紫外線、又は極端紫外線(例えば、EUV(波長13.5nm))等が用いられる。具体的には、KrFエキシマレーザー(波長248nm)、ArFエキシマレーザー(波長193nm)及びF2エキシマレーザー(波長157nm)等を使用することができる。これらの中でも、ArFエキシマレーザー(波長193nm)及びEUV(波長13.5nm)が好ましい。露光後、必要に応じて露光後加熱(post exposure bake)を行なうこともできる。露光後加熱は、加熱温度70℃乃至150℃、加熱時間0.3乃至10分間から適宜、選択された条件で行われる。
また、本発明ではレジストとしてフォトレジストに変えて電子線リソグラフィー用レジストを用いることができる。電子線レジストとしてはネガ型、ポジ型いずれも使用できる。酸発生剤と酸により分解してアルカリ溶解速度を変化させる基を有するバインダーからなる化学増幅型レジスト、アルカリ可溶性バインダーと酸発生剤と酸により分解してレジストのアルカリ溶解速度を変化させる低分子化合物からなる化学増幅型レジスト、酸発生剤と酸により分解してアルカリ溶解速度を変化させる基を有するバインダーと酸により分解してレジストのアルカリ溶解速度を変化させる低分子化合物からなる化学増幅型レジスト、電子線によって分解してアルカリ溶解速度を変化させる基を有するバインダーからなる非化学増幅型レジスト、電子線によって切断されアルカリ溶解速度を変化させる部位を有するバインダーからなる非化学増幅型レジストなどがある。これらの電子線レジストを用いた場合も照射源を電子線としてフォトレジストを用いた場合と同様にレジストパターンを形成することができる。
次いで、現像液によって現像が行なわれる。これにより、例えばポジ型フォトレジストが使用された場合は、露光された部分のフォトレジストが除去され、フォトレジストのパターンが形成される。
現像液としては、水酸化カリウム、水酸化ナトリウムなどのアルカリ金属水酸化物の水溶液、水酸化テトラメチルアンモニウム、水酸化テトラエチルアンモニウム、コリンなどの水酸化四級アンモニウムの水溶液、エタノールアミン、プロピルアミン、エチレンジアミンなどのアミン水溶液等のアルカリ性水溶液を例として挙げることができる。さらに、これらの現像液に界面活性剤などを加えることもできる。現像の条件としては、温度5乃至50℃、時間10乃至600秒から適宜選択される。
現像液としては、水酸化カリウム、水酸化ナトリウムなどのアルカリ金属水酸化物の水溶液、水酸化テトラメチルアンモニウム、水酸化テトラエチルアンモニウム、コリンなどの水酸化四級アンモニウムの水溶液、エタノールアミン、プロピルアミン、エチレンジアミンなどのアミン水溶液等のアルカリ性水溶液を例として挙げることができる。さらに、これらの現像液に界面活性剤などを加えることもできる。現像の条件としては、温度5乃至50℃、時間10乃至600秒から適宜選択される。
そして、このようにして形成されたフォトレジスト(上層)のパターンを保護膜として無機下層膜(中間層)の除去が行われ、次いでパターン化されたフォトレジスト及び無機下層膜(中間層)からなる膜を保護膜として、有機下層膜(下層)の除去が行われる。最後に、パターン化された無機下層膜(中間層)及び有機下層膜(下層)を保護膜として、半導体基板の加工が行なわれる。
まず、フォトレジストが除去された部分の無機下層膜(中間層)をドライエッチングによって取り除き、半導体基板を露出させる。無機下層膜のドライエッチングにはテトラフルオロメタン(CF4)、パーフルオロシクロブタン(C4F8)、パーフルオロプロパン(C3F8)、トリフルオロメタン、一酸化炭素、アルゴン、酸素、窒素、六フッ化硫黄、ジフルオロメタン、三フッ化窒素及び三フッ化塩素、塩素、トリクロロボラン及びジクロロボラン等のガスを使用することができる。無機下層膜のドライエッチングにはハロゲン系ガスを使用することが好ましく、フッ素系ガスによることがより好ましい。フッ素系ガスとしては、例えば、テトラフルオロメタン(CF4)、パーフルオロシクロブタン(C4F8)、パーフルオロプロパン(C3F8)、トリフルオロメタン、及びジフルオロメタン(CH2F2)等が挙げられる。
その後、パターン化されたフォトレジスト及び無機下層膜からなる膜を保護膜として有機下層膜の除去が行われる。有機下層膜(下層)は酸素系ガスによるドライエッチングによって行なわれることが好ましい。シリコン原子を多く含む無機下層膜は、酸素系ガスによるドライエッチングでは除去されにくいからである。
最後に、半導体基板の加工が行なわれる。半導体基板の加工はフッ素系ガスによるドライエッチングによって行なわれることが好ましい。
フッ素系ガスとしては、例えば、テトラフルオロメタン(CF4)、パーフルオロシクロブタン(C4F8)、パーフルオロプロパン(C3F8)、トリフルオロメタン、及びジフルオロメタン(CH2F2)等が挙げられる。
フッ素系ガスとしては、例えば、テトラフルオロメタン(CF4)、パーフルオロシクロブタン(C4F8)、パーフルオロプロパン(C3F8)、トリフルオロメタン、及びジフルオロメタン(CH2F2)等が挙げられる。
また、レジスト下層膜の上層には、フォトレジストの形成前に有機系の反射防止膜を形成することができる。そこで使用される反射防止膜組成物としては特に制限はなく、これまでリソグラフィープロセスにおいて慣用されているものの中から任意に選択して使用することができ、また、慣用されている方法、例えば、スピナー、コーターによる塗布及び焼成によって反射防止膜の形成を行なうことができる。
本発明では基板上に有機下層膜を成膜した後、その上に無機下層膜を成膜し、更にその上にフォトレジストを被覆することができる。これによりフォトレジストのパターン幅が狭くなり、パターン倒れを防ぐためにフォトレジストを薄く被覆した場合でも、適切なエッチングガスを選択することにより基板の加工が可能になる。例えば、フォトレジストに対して十分に早いエッチング速度となるフッ素系ガスをエッチングガスとしてレジスト下層膜に加工が可能であり、また無機下層膜に対して十分に早いエッチング速度となるフッ素系ガスをエッチングガスとして基板の加工が可能であり、更に有機下層膜に対して十分に早いエッチング速度となる酸素系ガスをエッチングガスとして基板の加工を行うことができる。
レジスト下層膜形成組成物より形成されるレジスト下層膜は、また、リソグラフィープロセスにおいて使用される光の波長によっては、その光に対する吸収を有することがある。そして、そのような場合には、基板からの反射光を防止する効果を有する反射防止膜として機能することができる。さらに、本発明のレジスト下層膜形成組成物で形成された下層膜はハードマスクとしても機能し得るものである。本発明の下層膜は、基板とフォトレジストとの相互作用の防止するための層、フォトレジストに用いられる材料又はフォトレジストへの露光時に生成する物質の基板への悪作用を防ぐ機能とを有する層、加熱焼成時に基板から生成する物質の上層フォトレジストへの拡散を防ぐ機能を有する層、及び半導体基板誘電体層によるフォトレジスト層のポイズニング効果を減少させるためのバリア層等として使用することも可能である。
また、レジスト下層膜形成組成物より形成される下層膜は、デュアルダマシンプロセスで用いられるビアホールが形成された基板に適用され、ホールを隙間なく充填することができる埋め込み材として使用できる。また、凹凸のある半導体基板の表面を平坦化するための平坦化材として使用することもできる。
次に実施例を挙げ本発明の内容を具体的に説明するが、本発明はこれらに限定されるものではない。
本明細書の下記合成例に示すポリマーの重量平均分子量は、ゲルパーミエーションクロマトグラフィー(以下、GPCと略称する)による測定結果である。測定には東ソー(株)製GPC装置を用い、測定条件等は次のとおりである。
GPCカラム:Shodex〔登録商標〕・Asahipak〔登録商標〕(昭和電工(
株))
カラム温度:40℃
溶媒:テトラヒドロフラン(THF)
流量:0.35ml/min
標準試料:ポリスチレン(東ソー(株))
GPCカラム:Shodex〔登録商標〕・Asahipak〔登録商標〕(昭和電工(
株))
カラム温度:40℃
溶媒:テトラヒドロフラン(THF)
流量:0.35ml/min
標準試料:ポリスチレン(東ソー(株))
(原料モノマーの合成)
<合成例1>
(ジアリル-2,2’-オキシジアセテートの合成)
冷却管、温度計及び攪拌機を備えた1Lフラスコにジグリコール酸50.01g(東京化成工業(株)製)、炭酸カリウム128.81g(0.89mol,関東化学,特級)、アセトン350.0gを入れて5℃以下に冷却し、臭化アリル135.33g(1.12mol,東京化成工業(株)製)を滴下した。その後、55℃に昇温して23時間撹拌した後、室温まで冷却し、不溶物をろ過してアセトン50.0gで2回洗浄した。ろ液を減圧下40℃にて溶媒を留去し、濃縮物にジクロロメタン250.0g及び純水250.0gを加えて分液した。さらに有機層を純水250.0gで2回水洗した後、有機層を減圧下40℃にて溶媒を留去して、上記式(A)で表される化合物を薄黄色の液体として24.47gで得た(収率30.6%)。この化合物の1H-NMRスペクトル(500MHz,Acetone-d6)におけるδ値は下記のとおりであった。
6.00(m,2H),5.38(dd,2H),5.26(s,2H),4.68(d,4H),4.32(s,4H)
<合成例1>
(ジアリル-2,2’-オキシジアセテートの合成)
冷却管、温度計及び攪拌機を備えた1Lフラスコにジグリコール酸50.01g(東京化成工業(株)製)、炭酸カリウム128.81g(0.89mol,関東化学,特級)、アセトン350.0gを入れて5℃以下に冷却し、臭化アリル135.33g(1.12mol,東京化成工業(株)製)を滴下した。その後、55℃に昇温して23時間撹拌した後、室温まで冷却し、不溶物をろ過してアセトン50.0gで2回洗浄した。ろ液を減圧下40℃にて溶媒を留去し、濃縮物にジクロロメタン250.0g及び純水250.0gを加えて分液した。さらに有機層を純水250.0gで2回水洗した後、有機層を減圧下40℃にて溶媒を留去して、上記式(A)で表される化合物を薄黄色の液体として24.47gで得た(収率30.6%)。この化合物の1H-NMRスペクトル(500MHz,Acetone-d6)におけるδ値は下記のとおりであった。
6.00(m,2H),5.38(dd,2H),5.26(s,2H),4.68(d,4H),4.32(s,4H)
<合成例2>
(ジグリシジル-2,2’-オキシジアセテートの合成)(DG-DGA)
温度計及び攪拌機を備えた500mLフラスコに、合成例1で得たジアリル-2,2’-オキシジアセテート23.01g(0.11mol)、クロロホルム230.0gを入れて5℃以下に冷却し、3-クロロ過安息香酸68.41g(0.26mol,東京化成工業(株)製,35%含水品)を徐々に添加した。その後、25℃に昇温して91.5時間撹拌した。反応混合物をクロロホルム230.0gで希釈し、5%炭酸水素ナトリウム水溶液460.0gを加えて分液した。さらに、有機層を10%亜硫酸水素ナトリウム水溶液460.0g、5%炭酸水素ナトリウム水溶液460.0g、純水460.0gで分液した後、有機層を減圧下40℃にて溶媒を留去して、上記式(B)で表されるジグリシジル-2,2’-オキシジアセテートを白色固体として17.63gで得た(収率66.7%)。この化合物の1H-NMRスペクトル(500MHz,DMSO-d6)におけるδ値は下記のとおりであった。
4.46(dd,2H),4.30(s,4H),3.88(dd,2H),3.21(m,2H),2.79(dd,2H),2.65(dd,2H)
(ジグリシジル-2,2’-オキシジアセテートの合成)(DG-DGA)
温度計及び攪拌機を備えた500mLフラスコに、合成例1で得たジアリル-2,2’-オキシジアセテート23.01g(0.11mol)、クロロホルム230.0gを入れて5℃以下に冷却し、3-クロロ過安息香酸68.41g(0.26mol,東京化成工業(株)製,35%含水品)を徐々に添加した。その後、25℃に昇温して91.5時間撹拌した。反応混合物をクロロホルム230.0gで希釈し、5%炭酸水素ナトリウム水溶液460.0gを加えて分液した。さらに、有機層を10%亜硫酸水素ナトリウム水溶液460.0g、5%炭酸水素ナトリウム水溶液460.0g、純水460.0gで分液した後、有機層を減圧下40℃にて溶媒を留去して、上記式(B)で表されるジグリシジル-2,2’-オキシジアセテートを白色固体として17.63gで得た(収率66.7%)。この化合物の1H-NMRスペクトル(500MHz,DMSO-d6)におけるδ値は下記のとおりであった。
4.46(dd,2H),4.30(s,4H),3.88(dd,2H),3.21(m,2H),2.79(dd,2H),2.65(dd,2H)
<合成例3>
(ジグリシジル-2,2’-チオジアセテートの合成)(DG-TDGA)
温度計及び攪拌機を備えた500mLフラスコに、2,2’-チオジグリコール酸30.01g(東京化成工業(株)製)、テトラヒドロフラン90.0g(関東化学,特級)を入れ、5℃に冷却してピリジン32.40g(0.41mol,関東化学,脱水)を添加した。ここにジシクロヘキシルカルボジイミド82.44g(0.40mol,関東化学,鹿特級)をTHF60.0gに溶解させた溶液を滴下して1時間撹拌した。その後、グリシドール(0.40mol,Aldrich製)をTHF30.0gに溶解させた溶液を滴下し、23℃に昇温して20時間撹拌した。反応混合物をTHF120.0gで希釈し、不溶物をろ過してTHF30.0gで2回洗浄した。ろ液を減圧下30℃にて溶媒を留去し、濃縮物に酢酸エチル300.0gを加えて、不溶物をろ過して、酢酸エチル15.0gで2回洗浄した。ここへ純水300.0gを加えて分液し、さらに有機層を純水300.0gで2回水洗した後、減圧下30℃にて溶媒を留去した。得られた残留物をシリカゲルカラムクロマトグラフィー(酢酸エチル/n-ヘプタン=3/2→4/1(容量比))にて精製して、上記式(C)で表される化合物を白色固体として20.67gで得た(収率39.4%)。この化合物の1H-NMRスペクトル(500MHz,DMSO-d6)におけるδ値は下記のとおりであった。
4.43(dd,2H),3.87(dd,2H),3.53(s,4H),3.21(m,2H),2.79(dd,2H),2.66(dd,2H)
(ジグリシジル-2,2’-チオジアセテートの合成)(DG-TDGA)
温度計及び攪拌機を備えた500mLフラスコに、2,2’-チオジグリコール酸30.01g(東京化成工業(株)製)、テトラヒドロフラン90.0g(関東化学,特級)を入れ、5℃に冷却してピリジン32.40g(0.41mol,関東化学,脱水)を添加した。ここにジシクロヘキシルカルボジイミド82.44g(0.40mol,関東化学,鹿特級)をTHF60.0gに溶解させた溶液を滴下して1時間撹拌した。その後、グリシドール(0.40mol,Aldrich製)をTHF30.0gに溶解させた溶液を滴下し、23℃に昇温して20時間撹拌した。反応混合物をTHF120.0gで希釈し、不溶物をろ過してTHF30.0gで2回洗浄した。ろ液を減圧下30℃にて溶媒を留去し、濃縮物に酢酸エチル300.0gを加えて、不溶物をろ過して、酢酸エチル15.0gで2回洗浄した。ここへ純水300.0gを加えて分液し、さらに有機層を純水300.0gで2回水洗した後、減圧下30℃にて溶媒を留去した。得られた残留物をシリカゲルカラムクロマトグラフィー(酢酸エチル/n-ヘプタン=3/2→4/1(容量比))にて精製して、上記式(C)で表される化合物を白色固体として20.67gで得た(収率39.4%)。この化合物の1H-NMRスペクトル(500MHz,DMSO-d6)におけるδ値は下記のとおりであった。
4.43(dd,2H),3.87(dd,2H),3.53(s,4H),3.21(m,2H),2.79(dd,2H),2.66(dd,2H)
<合成例4>
(ジグリシジル-2,2’-スルホニルジアセテートの合成)(DG-SDGA)
温度計及び攪拌機を備えた200mLフラスコに合成例3で得たジグリシジル-2,2’-チオジアセテート8.01g、クロロホルム80.0gを入れて5℃以下に冷却し、3-クロロ過安息香酸19.43g(0.26mol,東京化成工業(株)製)を徐々に添加した。その後、23℃に昇温して4.5時間撹拌した。反応混合物をクロロホルム80.0gで希釈し、5%炭酸水素ナトリウム水溶液160.0gを加えて分液した。さらに、有機層を10%亜硫酸水素ナトリウム水溶液160.0g、5%炭酸水素ナトリウム水溶液160.0g、純水160.0gで分液した後、有機層を減圧下30℃にて溶媒を留去して、上記式(D)で表される化合物を白色固体として4.36gで得た(収率48.6%)。この化合物の1H-NMRスペクトル(500MHz,DMSO-d6)におけるδ値は下記のとおりであった。
4.65(s,4H),4.52(dd,2H),3.98(dd,2H),3.24(m,2H),2.81(dd,2H),2.70(dd,2H)
(ジグリシジル-2,2’-スルホニルジアセテートの合成)(DG-SDGA)
温度計及び攪拌機を備えた200mLフラスコに合成例3で得たジグリシジル-2,2’-チオジアセテート8.01g、クロロホルム80.0gを入れて5℃以下に冷却し、3-クロロ過安息香酸19.43g(0.26mol,東京化成工業(株)製)を徐々に添加した。その後、23℃に昇温して4.5時間撹拌した。反応混合物をクロロホルム80.0gで希釈し、5%炭酸水素ナトリウム水溶液160.0gを加えて分液した。さらに、有機層を10%亜硫酸水素ナトリウム水溶液160.0g、5%炭酸水素ナトリウム水溶液160.0g、純水160.0gで分液した後、有機層を減圧下30℃にて溶媒を留去して、上記式(D)で表される化合物を白色固体として4.36gで得た(収率48.6%)。この化合物の1H-NMRスペクトル(500MHz,DMSO-d6)におけるδ値は下記のとおりであった。
4.65(s,4H),4.52(dd,2H),3.98(dd,2H),3.24(m,2H),2.81(dd,2H),2.70(dd,2H)
<合成例5>
(ジグリシジル-2,2’-ジチオジアセテートの合成)(DG-DTDGA)
200ml四ッ口フラスコに、グリシドール4.5g、塩化メチレン11.55g、1-(3-ジメチルアミノプロピル)-3-エチルカルボジイミド塩酸塩20gを仕込み、氷浴下、マグネチックスターラーで攪拌しながら、ジチオジグリコール酸5gをテトラヒドロフラン10gに溶解させた溶液を3分間掛けて滴下した後、4-ジメチルアミノピリジン0.035gを添加し、室温にて、2時間攪拌した。次に、反応液を酢酸エチル約100gで希釈し、有機層を純水約50gで4回洗浄した後、有機層をエバポレータにて減圧濃縮した。続いて、濃縮物を酢酸エチル約20gで希釈し、シリカゲルのショートカラムを行った後、溶出液をエバポレータにて減圧濃縮し、上記式(E)で表される化合物を3.24gを得た(収率:40%)。この化合物の1H-NMRスペクトル(300MHz,DMSO-d6)におけるδ値は下記のとおりであった。
1H―NMR(300MHz) in DMSO―d6:2.66ppm(m,2H),2.79ppm(dd,J=5.3Hz,J=4.8Hz,2H),3.21ppm(m,2H),3.80ppm(s,4H),3.89ppm(dd,J=12.6Hz,J= 6.6Hz,2H),4.43ppm(dd,J=12.6Hz,J=2.7Hz,2H)
(ジグリシジル-2,2’-ジチオジアセテートの合成)(DG-DTDGA)
200ml四ッ口フラスコに、グリシドール4.5g、塩化メチレン11.55g、1-(3-ジメチルアミノプロピル)-3-エチルカルボジイミド塩酸塩20gを仕込み、氷浴下、マグネチックスターラーで攪拌しながら、ジチオジグリコール酸5gをテトラヒドロフラン10gに溶解させた溶液を3分間掛けて滴下した後、4-ジメチルアミノピリジン0.035gを添加し、室温にて、2時間攪拌した。次に、反応液を酢酸エチル約100gで希釈し、有機層を純水約50gで4回洗浄した後、有機層をエバポレータにて減圧濃縮した。続いて、濃縮物を酢酸エチル約20gで希釈し、シリカゲルのショートカラムを行った後、溶出液をエバポレータにて減圧濃縮し、上記式(E)で表される化合物を3.24gを得た(収率:40%)。この化合物の1H-NMRスペクトル(300MHz,DMSO-d6)におけるδ値は下記のとおりであった。
1H―NMR(300MHz) in DMSO―d6:2.66ppm(m,2H),2.79ppm(dd,J=5.3Hz,J=4.8Hz,2H),3.21ppm(m,2H),3.80ppm(s,4H),3.89ppm(dd,J=12.6Hz,J= 6.6Hz,2H),4.43ppm(dd,J=12.6Hz,J=2.7Hz,2H)
(ポリマーの合成)
<合成例6>(DG-DGAポリマー)
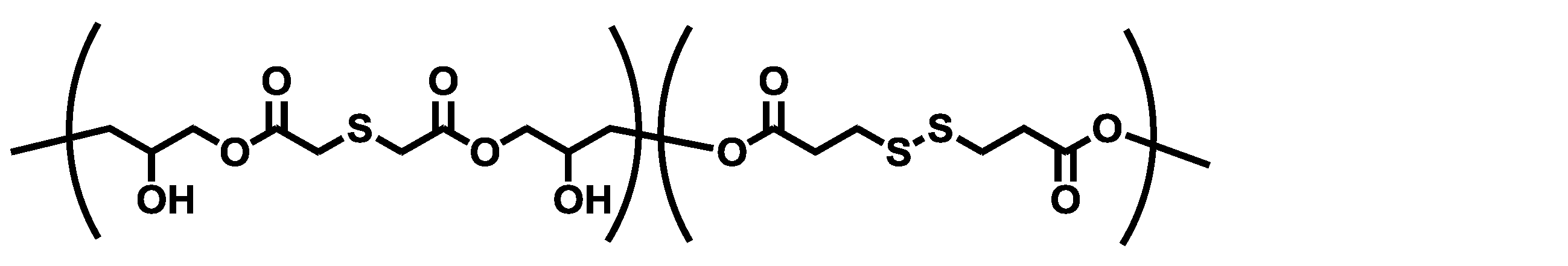
化合物2(DG-DGA)2.50gと3,3’-ジチオジプロピオン酸(堺化学工業(株)、商品名:DTDPA)2.40g、及び触媒として第4級ホスホニウム塩であるテトラブチルホスホニウムブロミド0.12gを、プロピレングリコールモノメチルエーテル20.07gに溶解させた後、105℃に加温し、窒素雰囲気下で24時間撹拌し樹脂化合物の溶液を得た。得られた樹脂のGPC分析を行ったところ、標準ポリスチレン換算にて重量平均分子量は約1700であった。
<合成例6>(DG-DGAポリマー)
化合物2(DG-DGA)2.50gと3,3’-ジチオジプロピオン酸(堺化学工業(株)、商品名:DTDPA)2.40g、及び触媒として第4級ホスホニウム塩であるテトラブチルホスホニウムブロミド0.12gを、プロピレングリコールモノメチルエーテル20.07gに溶解させた後、105℃に加温し、窒素雰囲気下で24時間撹拌し樹脂化合物の溶液を得た。得られた樹脂のGPC分析を行ったところ、標準ポリスチレン換算にて重量平均分子量は約1700であった。
<合成例7>(DG-TDGAポリマー)
化合物3(DG-TDGA)2.30gと3,3’-ジチオジプロピオン酸(堺化学工業(株)、商品名:DTDPA)2.26g、及び触媒として第4級ホスホニウム塩であるテトラブチルホスホニウムブロミド0.17gを、プロピレングリコールモノメチルエーテル18.89gに溶解させた後、105℃に加温し、窒素雰囲気下で24時間撹拌し樹脂化合物の溶液を得た。得られた樹脂のGPC分析を行ったところ、標準ポリスチレン換算にて重量平均分子量は約2300であった。
化合物3(DG-TDGA)2.30gと3,3’-ジチオジプロピオン酸(堺化学工業(株)、商品名:DTDPA)2.26g、及び触媒として第4級ホスホニウム塩であるテトラブチルホスホニウムブロミド0.17gを、プロピレングリコールモノメチルエーテル18.89gに溶解させた後、105℃に加温し、窒素雰囲気下で24時間撹拌し樹脂化合物の溶液を得た。得られた樹脂のGPC分析を行ったところ、標準ポリスチレン換算にて重量平均分子量は約2300であった。
<合成例8>(DG-SDGAポリマー)
化合物4(DG-SDGA)2.50gと3,3’-ジチオジプロピオン酸(堺化学工業(株)、商品名:DTDPA)2.11g、及び触媒として第4級ホスホニウム塩であるテトラブチルホスホニウムブロミド0.16gを、プロピレングリコールモノメチルエーテル19.06gに溶解させた後、105℃に加温し、窒素雰囲気下で24時間撹拌し樹脂化合物の溶液を得た。得られた樹脂のGPC分析を行ったところ、標準ポリスチレン換算にて重量平均分子量は約1000であった。
化合物4(DG-SDGA)2.50gと3,3’-ジチオジプロピオン酸(堺化学工業(株)、商品名:DTDPA)2.11g、及び触媒として第4級ホスホニウム塩であるテトラブチルホスホニウムブロミド0.16gを、プロピレングリコールモノメチルエーテル19.06gに溶解させた後、105℃に加温し、窒素雰囲気下で24時間撹拌し樹脂化合物の溶液を得た。得られた樹脂のGPC分析を行ったところ、標準ポリスチレン換算にて重量平均分子量は約1000であった。
<合成例9>(DG-DTDGAポリマー)
化合物5(DG-DTDGA)2.50gと3,3’-ジチオジプロピオン酸(堺化学工業(株)、商品名:DTDPA)1.73g、及び触媒として第4級ホスホニウム塩であるテトラブチルホスホニウムブロミド0.13gを、プロピレングリコールモノメチルエーテル17.36gに溶解させた後、105℃に加温し、窒素雰囲気下で24時間撹拌し樹脂化合物の溶液を得た。得られた樹脂のGPC分析を行ったところ、標準ポリスチレン換算にて重量平均分子量は約2400であった。
化合物5(DG-DTDGA)2.50gと3,3’-ジチオジプロピオン酸(堺化学工業(株)、商品名:DTDPA)1.73g、及び触媒として第4級ホスホニウム塩であるテトラブチルホスホニウムブロミド0.13gを、プロピレングリコールモノメチルエーテル17.36gに溶解させた後、105℃に加温し、窒素雰囲気下で24時間撹拌し樹脂化合物の溶液を得た。得られた樹脂のGPC分析を行ったところ、標準ポリスチレン換算にて重量平均分子量は約2400であった。
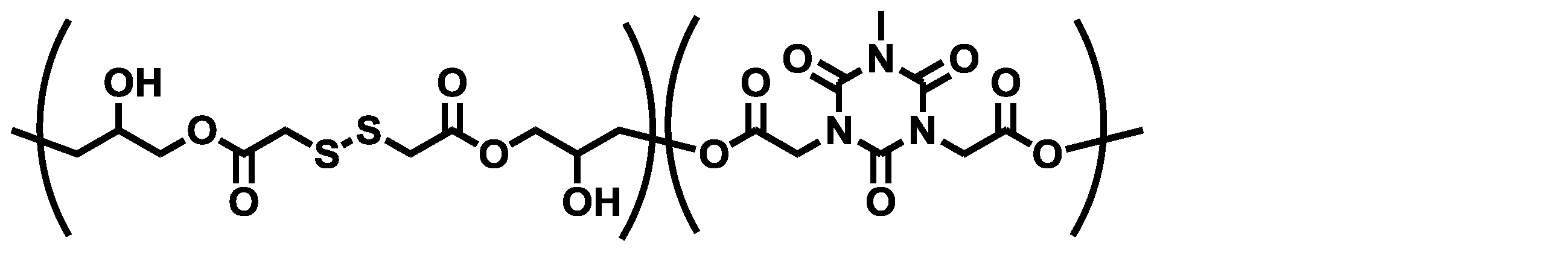
<合成例10>(DG-DTDGAポリマー(ii))
化合物5(DG-DTDGA)2.00gとメチルジカルボキシメチルイソシアヌル酸(四国化成工業(株)、商品名:MeCIC-1)2.36g、及び触媒として第4級ホスホニウム塩であるテトラブチルホスホニウムブロミド0.07gを、プロピレングリコールモノメチルエーテル17.73gに溶解させた後、105℃に加温し、窒素雰囲気下で24時間撹拌し樹脂化合物の溶液を得た。得られた樹脂のGPC分析を行ったところ、標準ポリスチレン換算にて重量平均分子量は約1600であった。
化合物5(DG-DTDGA)2.00gとメチルジカルボキシメチルイソシアヌル酸(四国化成工業(株)、商品名:MeCIC-1)2.36g、及び触媒として第4級ホスホニウム塩であるテトラブチルホスホニウムブロミド0.07gを、プロピレングリコールモノメチルエーテル17.73gに溶解させた後、105℃に加温し、窒素雰囲気下で24時間撹拌し樹脂化合物の溶液を得た。得られた樹脂のGPC分析を行ったところ、標準ポリスチレン換算にて重量平均分子量は約1600であった。
(組成物調製)
[実施例1]
合成例6で得られた反応生成物(DG-DGAポリマー)0.424gを含む溶液2.650gに、プロピレングリコールモノメチルエーテル7.334g、ピリジニウムトリフルオロメタンスルホン酸(東京化成工業(株))0.016g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.001gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
[実施例1]
合成例6で得られた反応生成物(DG-DGAポリマー)0.424gを含む溶液2.650gに、プロピレングリコールモノメチルエーテル7.334g、ピリジニウムトリフルオロメタンスルホン酸(東京化成工業(株))0.016g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.001gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
[実施例2]
合成例7で得られた反応生成物(DG-TDGAポリマー)0.482gを含む溶液2.924gに、プロピレングリコールモノメチルエーテル7.057g、ピリジニウムトリフルオロメタンスルホン酸(東京化成工業(株))0.018g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.001gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
合成例7で得られた反応生成物(DG-TDGAポリマー)0.482gを含む溶液2.924gに、プロピレングリコールモノメチルエーテル7.057g、ピリジニウムトリフルオロメタンスルホン酸(東京化成工業(株))0.018g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.001gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
[実施例3]
合成例8で得られた反応生成物(DG-SDGAポリマー)0.482gを含む溶液2.486gに、プロピレングリコールモノメチルエーテル7.496g、ピリジニウムトリフルオロメタンスルホン酸(東京化成工業(株))0.018g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.001gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
合成例8で得られた反応生成物(DG-SDGAポリマー)0.482gを含む溶液2.486gに、プロピレングリコールモノメチルエーテル7.496g、ピリジニウムトリフルオロメタンスルホン酸(東京化成工業(株))0.018g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.001gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
[実施例4]
合成例9で得られた反応生成物(DG-DTDGAポリマー)0.482gを含む溶液2.486gに、プロピレングリコールモノメチルエーテル7.496g、ピリジニウムトリフルオロメタンスルホン酸(東京化成工業(株))0.018g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.001gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
合成例9で得られた反応生成物(DG-DTDGAポリマー)0.482gを含む溶液2.486gに、プロピレングリコールモノメチルエーテル7.496g、ピリジニウムトリフルオロメタンスルホン酸(東京化成工業(株))0.018g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.001gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
[実施例5]
合成例10で得られた反応生成物(DG-DTDGAポリマー(ii))0.482gを含む溶液2.486gに、プロピレングリコールモノメチルエーテル7.496g、ピリジニウムトリフルオロメタンスルホン酸(東京化成工業(株))0.018g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.001gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
合成例10で得られた反応生成物(DG-DTDGAポリマー(ii))0.482gを含む溶液2.486gに、プロピレングリコールモノメチルエーテル7.496g、ピリジニウムトリフルオロメタンスルホン酸(東京化成工業(株))0.018g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.001gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
[実施例6]
合成例10で得られた反応生成物(DG-DTDGAポリマー(ii))0.357gを含む溶液2.211gに、プロピレングリコールモノメチルエーテル7.689g、テトラメトキシメチルグリコールウリル(日本サイテックインダストリーズ(株)、商品名:POWDERLINK〔登録商標〕1174)0.089g、ピリジニウム-p-フェノールスルホン酸0.013g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.001gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
合成例10で得られた反応生成物(DG-DTDGAポリマー(ii))0.357gを含む溶液2.211gに、プロピレングリコールモノメチルエーテル7.689g、テトラメトキシメチルグリコールウリル(日本サイテックインダストリーズ(株)、商品名:POWDERLINK〔登録商標〕1174)0.089g、ピリジニウム-p-フェノールスルホン酸0.013g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.001gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
[比較例1]
WO2009/096340の合成例1に記載の方法で得られた反応生成物0.723gを含む溶液3.580gに、プロピレングリコールモノメチルエーテル88.431g、プロピレングリコールモノメチルエーテルアセテート9.906g、テトラメトキシメチルグリコールウリル(日本サイテックインダストリーズ(株)、商品名:POWDERLINK〔登録商標〕1174)0.181g、p-フェノールスルホン酸(東京化成工業(株))、ビスフェノールS(東京化成工業(株))0.011g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.007gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
WO2009/096340の合成例1に記載の方法で得られた反応生成物0.723gを含む溶液3.580gに、プロピレングリコールモノメチルエーテル88.431g、プロピレングリコールモノメチルエーテルアセテート9.906g、テトラメトキシメチルグリコールウリル(日本サイテックインダストリーズ(株)、商品名:POWDERLINK〔登録商標〕1174)0.181g、p-フェノールスルホン酸(東京化成工業(株))、ビスフェノールS(東京化成工業(株))0.011g、及び界面活性剤(大日本インキ化学工業(株)、商品名:R-40)0.007gを加え、溶液とした。その後、孔径0.02μmのポリエチレン製ミクロフィルターを用いてろ過して、レジスト下層膜形成用組成物を調製した。
(ドライエッチング速度の測定)
実施例1~実施例6及び比較例1で調製されたレジスト下層膜形成用組成物を、それぞれスピナーによりシリコンウエハー上に塗布し、ホットプレート上、205℃で1分間ベークし、各々膜厚100nmのレジスト下層膜を形成した。これらをサムコ(株)製ドライエッチング装置(RIE-10NR)を用い、ドライエッチングガスとしてCF4及びN2を使用する条件下でドライエッチング速度(単位時間当たりの膜厚の減少量)を測定した。比較例1から得られるレジスト下層膜のエッチング選択比を1.00とした場合の各下層膜のエッチング選択比を表1、2に示す。
実施例1~実施例6及び比較例1で調製されたレジスト下層膜形成用組成物を、それぞれスピナーによりシリコンウエハー上に塗布し、ホットプレート上、205℃で1分間ベークし、各々膜厚100nmのレジスト下層膜を形成した。これらをサムコ(株)製ドライエッチング装置(RIE-10NR)を用い、ドライエッチングガスとしてCF4及びN2を使用する条件下でドライエッチング速度(単位時間当たりの膜厚の減少量)を測定した。比較例1から得られるレジスト下層膜のエッチング選択比を1.00とした場合の各下層膜のエッチング選択比を表1、2に示す。
上記の結果から実施例1~実施例6は比較例1よりも十分高いエッチング選択性を有していることがわかる。その結果、本発明によって得られるレジスト下層膜形成用組成物はレジスト下層膜のドライエッチング時のエッチング時間を短縮することができ、レジスト下層膜をドライエッチングで除去する際に、レジスト膜厚が減少する好ましくない現象を抑制できる。さらに、ドライエッチング時間を短縮できることは、レジスト下層膜の下地基板に対して好ましくないエッチングダメージを抑制することができるため、レジスト下層膜として特に有用である。
本発明に係るレジスト下層膜形成組成物は、特に高ドライエッチング速度を有するレジスト下層膜を提供するものである。
Claims (13)
- 前記エポキシ付加体形成化合物が、カルボン酸含有化合物、カルボン酸無水物含有化合物、ヒドロキシ基含有化合物、チオール基含有化合物、アミノ基含有化合物及びイミド基含有化合物からなる群より選ばれる少なくとも1種の化合物である、請求項1に記載のレジスト下層膜形成組成物。
- 前記エポキシ付加体形成化合物が、カルボン酸含有化合物またはチオール基含有化合物である、請求項1又は2に記載のレジスト下層膜形成組成物。
- 前記カルボン酸含有化合物が、硫黄原子を少なくとも1つ以上含むジカルボン酸である、請求項2又は3に記載のレジスト下層膜形成組成物。
- 前記硫黄原子を少なくとも1つ以上含むジカルボン酸が、硫黄原子を少なくとも1つ以上含む脂肪族ジカルボン酸である、請求項4に記載のレジスト下層膜形成組成物。
- 架橋触媒をさらに含む、請求項1~請求項5のいずれか1項に記載のレジスト下層膜形成組成物。
- 架橋剤をさらに含む、請求項1~請求項6のいずれか1項に記載のレジスト下層膜形成組成物。
- 界面活性剤をさらに含む、請求項1~請求項7のいずれか1項に記載のレジスト下層膜形成組成物。
- 請求項1~請求項8のいずれか1項に記載のレジスト下層膜形成組成物からなる塗布膜の焼成物であることを特徴とするレジスト下層膜。
- 半導体基板上に、請求項1~請求項8のいずれか1項に記載のレジスト下層膜形成組成物を塗布しベークしてレジスト下層膜を形成する工程、前記レジスト下層膜上にレジストを塗布しベークしてレジスト膜を形成する工程、前記レジスト下層膜と前記レジストで被覆された半導体基板を露光する工程、露光後の前記レジスト膜を現像し、パターニングする工程を含む、パターニングされた基板の製造方法。
- 半導体基板上に、請求項1~請求項8の何れか1項に記載のレジスト下層膜形成組成物からなるレジスト下層膜を形成する工程と、
前記レジスト下層膜の上にレジスト膜を形成する工程と、
レジスト膜に対する光又は電子線の照射とその後の現像によりレジストパターンを形成する工程と、
形成された前記レジストパターンを介して前記レジスト下層膜をエッチングすることによりパターン化されたレジスト下層膜を形成する工程と、
パターン化された前記レジスト下層膜により半導体基板を加工する工程と、
を含むことを特徴とする、半導体装置の製造方法。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020217000131A KR20210037659A (ko) | 2018-07-24 | 2019-07-11 | 헤테로원자를 폴리머 주쇄 중에 포함하는 레지스트 하층막 형성 조성물 |
| JP2020532290A JP7375757B2 (ja) | 2018-07-24 | 2019-07-11 | ヘテロ原子をポリマー主鎖中に含むレジスト下層膜形成組成物 |
| CN201980048330.9A CN112437901A (zh) | 2018-07-24 | 2019-07-11 | 聚合物主链中包含杂原子的抗蚀剂下层膜形成用组合物 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2018-138676 | 2018-07-24 | ||
| JP2018138676 | 2018-07-24 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2020022086A1 true WO2020022086A1 (ja) | 2020-01-30 |
Family
ID=69181002
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2019/027531 WO2020022086A1 (ja) | 2018-07-24 | 2019-07-11 | ヘテロ原子をポリマー主鎖中に含むレジスト下層膜形成組成物 |
Country Status (5)
| Country | Link |
|---|---|
| JP (1) | JP7375757B2 (ja) |
| KR (1) | KR20210037659A (ja) |
| CN (1) | CN112437901A (ja) |
| TW (1) | TW202018419A (ja) |
| WO (1) | WO2020022086A1 (ja) |
Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3857875A (en) * | 1972-09-28 | 1974-12-31 | Phillips Petroleum Co | Sulfonyldialkanoic acid esters of 2,3-dibromo-1-alkanols |
| JPH02164875A (ja) * | 1988-10-26 | 1990-06-25 | Shell Internatl Res Maatschappij Bv | 新規ポリグリシジルエステル、それらの製造およびそれらの熱硬化性組成物における使用 |
| EP0518408A2 (en) * | 1991-05-31 | 1992-12-16 | Shell Internationale Researchmaatschappij B.V. | Thermosetting resin composition |
| WO2009096340A1 (ja) * | 2008-01-30 | 2009-08-06 | Nissan Chemical Industries, Ltd. | 硫黄原子を含有するレジスト下層膜形成用組成物及びレジストパターンの形成方法 |
| WO2015098525A1 (ja) * | 2013-12-27 | 2015-07-02 | 日産化学工業株式会社 | トリアジン環及び硫黄原子を主鎖に有する共重合体を含むレジスト下層膜形成組成物 |
| WO2015163195A1 (ja) * | 2014-04-25 | 2015-10-29 | 日産化学工業株式会社 | レジスト下層膜形成組成物及びそれを用いたレジストパターンの形成方法 |
| WO2018203540A1 (ja) * | 2017-05-02 | 2018-11-08 | 日産化学株式会社 | レジスト下層膜形成組成物 |
| WO2019151471A1 (ja) * | 2018-02-02 | 2019-08-08 | 日産化学株式会社 | ジスルフィド構造を有するレジスト下層膜形成組成物 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6323815Y2 (ja) * | 1980-11-11 | 1988-06-30 |
-
2019
- 2019-07-11 CN CN201980048330.9A patent/CN112437901A/zh not_active Withdrawn
- 2019-07-11 JP JP2020532290A patent/JP7375757B2/ja active Active
- 2019-07-11 KR KR1020217000131A patent/KR20210037659A/ko unknown
- 2019-07-11 WO PCT/JP2019/027531 patent/WO2020022086A1/ja active Application Filing
- 2019-07-22 TW TW108125779A patent/TW202018419A/zh unknown
Patent Citations (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3857875A (en) * | 1972-09-28 | 1974-12-31 | Phillips Petroleum Co | Sulfonyldialkanoic acid esters of 2,3-dibromo-1-alkanols |
| JPH02164875A (ja) * | 1988-10-26 | 1990-06-25 | Shell Internatl Res Maatschappij Bv | 新規ポリグリシジルエステル、それらの製造およびそれらの熱硬化性組成物における使用 |
| EP0518408A2 (en) * | 1991-05-31 | 1992-12-16 | Shell Internationale Researchmaatschappij B.V. | Thermosetting resin composition |
| WO2009096340A1 (ja) * | 2008-01-30 | 2009-08-06 | Nissan Chemical Industries, Ltd. | 硫黄原子を含有するレジスト下層膜形成用組成物及びレジストパターンの形成方法 |
| WO2015098525A1 (ja) * | 2013-12-27 | 2015-07-02 | 日産化学工業株式会社 | トリアジン環及び硫黄原子を主鎖に有する共重合体を含むレジスト下層膜形成組成物 |
| WO2015163195A1 (ja) * | 2014-04-25 | 2015-10-29 | 日産化学工業株式会社 | レジスト下層膜形成組成物及びそれを用いたレジストパターンの形成方法 |
| WO2018203540A1 (ja) * | 2017-05-02 | 2018-11-08 | 日産化学株式会社 | レジスト下層膜形成組成物 |
| WO2019151471A1 (ja) * | 2018-02-02 | 2019-08-08 | 日産化学株式会社 | ジスルフィド構造を有するレジスト下層膜形成組成物 |
Non-Patent Citations (1)
| Title |
|---|
| KULSHRESTHA, A. S. ET AL.: "Biomaterials", vol. 1054, part Chapter 9 2010, ISBN: 9780841225688, article "Cyclic Dithiocabonates: Novel in Situ Polymerizing Biomaterials for Medical Applications", pages: 173 - 183, XP009508967, DOI: PUB - 10.1021/bk-2010-1054.ch009 * |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20210037659A (ko) | 2021-04-06 |
| CN112437901A (zh) | 2021-03-02 |
| JP7375757B2 (ja) | 2023-11-08 |
| TW202018419A (zh) | 2020-05-16 |
| JPWO2020022086A1 (ja) | 2021-09-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TWI435179B (zh) | 光阻底層膜形成組成物及使用其之光阻圖型的形成方法 | |
| JP7287389B2 (ja) | 炭素酸素間二重結合を利用したレジスト下層膜形成組成物 | |
| TWI531864B (zh) | 光阻下層膜形成組成物及使用其之光阻圖型之形成方法 | |
| JP7327479B2 (ja) | ジシアノスチリル基を有する複素環化合物を含むウェットエッチング可能なレジスト下層膜形成組成物 | |
| JP2024059666A (ja) | 環式カルボニル化合物を用いたレジスト下層膜形成組成物 | |
| WO2015046149A1 (ja) | レジスト下層膜形成組成物及びそれを用いたレジストパターンの形成方法 | |
| JPWO2018198960A1 (ja) | フルオレン化合物を用いたレジスト下層膜形成組成物 | |
| US11635692B2 (en) | Resist underlying film forming composition | |
| JP2015145944A (ja) | レジスト下層膜形成組成物及びそれを用いたレジストパターンの形成方法 | |
| JP7322949B2 (ja) | ジシアノスチリル基を含むウェットエッチング可能なレジスト下層膜形成組成物 | |
| JP7416062B2 (ja) | レジスト下層膜形成組成物 | |
| JP7375757B2 (ja) | ヘテロ原子をポリマー主鎖中に含むレジスト下層膜形成組成物 | |
| JP2022132962A (ja) | レジスト下層膜形成組成物 | |
| WO2021015181A1 (ja) | レジスト下層膜形成組成物 | |
| US20230203299A1 (en) | Resist underlayer film- forming composition using diarylmethane derivative | |
| US20220334483A1 (en) | Resist underlayer film-forming composition | |
| TW202403454A (zh) | 具有茀骨架之阻劑下層膜形成組成物 | |
| CN115427891A (zh) | 抗蚀剂下层膜形成用组合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 19841143 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2020532290 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 19841143 Country of ref document: EP Kind code of ref document: A1 |