WO2015037716A1 - 含窒素飽和複素環化合物 - Google Patents
含窒素飽和複素環化合物 Download PDFInfo
- Publication number
- WO2015037716A1 WO2015037716A1 PCT/JP2014/074283 JP2014074283W WO2015037716A1 WO 2015037716 A1 WO2015037716 A1 WO 2015037716A1 JP 2014074283 W JP2014074283 W JP 2014074283W WO 2015037716 A1 WO2015037716 A1 WO 2015037716A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- alkyl
- carboxamide
- methylpiperidine
- propan
- substituted
- Prior art date
Links
- 0 **(*)c(cccc1)c1N Chemical compound **(*)c(cccc1)c1N 0.000 description 4
- SZEOQKPDVSRUAR-UHFFFAOYSA-N CC(C)(C)OC(N(C(C1)C(OC)=O)C1=O)=O Chemical compound CC(C)(C)OC(N(C(C1)C(OC)=O)C1=O)=O SZEOQKPDVSRUAR-UHFFFAOYSA-N 0.000 description 1
- MCMQSTZMIVFBRA-UHFFFAOYSA-N CC(C)(C)OC(N(CC(C1)C(OC)=O)CC1(F)F)=O Chemical compound CC(C)(C)OC(N(CC(C1)C(OC)=O)CC1(F)F)=O MCMQSTZMIVFBRA-UHFFFAOYSA-N 0.000 description 1
- DVHUSCHKHCBZKT-UHFFFAOYSA-N CC(C)(C)OC(N(CC1)CC(C(O)=O)=C1c1ccccc1)=O Chemical compound CC(C)(C)OC(N(CC1)CC(C(O)=O)=C1c1ccccc1)=O DVHUSCHKHCBZKT-UHFFFAOYSA-N 0.000 description 1
- UHRXHCZPUWORFZ-UHFFFAOYSA-N CC(C)(C)OC(N(CCC1c2ccccc2)CC1C(O)=O)=O Chemical compound CC(C)(C)OC(N(CCC1c2ccccc2)CC1C(O)=O)=O UHRXHCZPUWORFZ-UHFFFAOYSA-N 0.000 description 1
- LXGWJOIZDQTENM-UHFFFAOYSA-N CC1(c2c(cccc3)c3ccc2)[O](C)=C(C2CNC(CO)CC2)N1 Chemical compound CC1(c2c(cccc3)c3ccc2)[O](C)=C(C2CNC(CO)CC2)N1 LXGWJOIZDQTENM-UHFFFAOYSA-N 0.000 description 1
- AJUGGHOVBBTHCD-NKWVEPMBSA-N C[C@@H](CC1)NC[C@@H]1C(OC)=O Chemical compound C[C@@H](CC1)NC[C@@H]1C(OC)=O AJUGGHOVBBTHCD-NKWVEPMBSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D211/00—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings
- C07D211/04—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D211/06—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D211/36—Heterocyclic compounds containing hydrogenated pyridine rings, not condensed with other rings with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D211/60—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/08—Drugs for disorders of the urinary system of the prostate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/06—Antipsoriatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/08—Antiepileptics; Anticonvulsants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/24—Antidepressants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/06—Antiglaucoma agents or miotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/14—Vasoprotectives; Antihaemorrhoidals; Drugs for varicose therapy; Capillary stabilisers
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D207/00—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D207/02—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom
- C07D207/04—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members
- C07D207/10—Heterocyclic compounds containing five-membered rings not condensed with other rings, with one nitrogen atom as the only ring hetero atom with only hydrogen or carbon atoms directly attached to the ring nitrogen atom having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D207/16—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D405/00—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom
- C07D405/02—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings
- C07D405/12—Heterocyclic compounds containing both one or more hetero rings having oxygen atoms as the only ring hetero atoms, and one or more rings having nitrogen as the only ring hetero atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D409/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms
- C07D409/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings
- C07D409/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having sulfur atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
Definitions
- the present invention relates to a novel nitrogen-containing saturated heterocyclic compound, particularly a novel piperidine derivative, useful as a therapeutic and / or prophylactic agent for a medical disease having somatostatin receptor subtype 4 (SSTR4) selective agonist activity. Furthermore, the present invention relates to a novel nitrogen-containing saturated heterocyclic compound, particularly a novel piperidine derivative, useful as a therapeutic and / or prophylactic agent for neurodegenerative diseases involving A ⁇ such as Alzheimer's disease.
- SSTR4 somatostatin receptor subtype 4
- Alzheimer's disease is a neurodegenerative disease characterized by senile plaque formation and neurofibrillary tangles as well as neuronal degeneration and loss, and is a type of dementia that causes cognitive decline and personality change.
- treatment of Alzheimer's disease is limited to symptomatic treatment with drugs aimed at symptom improvement using acetylcholinesterase inhibitors and the like. No effective method has been found for the treatment and / or prevention of the cause of Alzheimer's disease.
- Neprilysin is known as a degrading enzyme of A ⁇ (sometimes referred to as “amyloid ⁇ protein”, “amyloid ⁇ peptide”, or “beta amyloid”). Neprilysin is capable of degrading soluble A ⁇ oligomers that are thought to cause cognitive decline. Furthermore, it has been reported that somatostatin activates the neprilysin.
- Somatostatin which is an endogenous ligand of somatostatin receptor, has a very short biological half-life and is not suitable for use as a medicine.
- Pyrrolidine derivatives Patent Document 1
- thiourea derivatives Patent Documents 2 and 3
- SSTR4 somatostatin receptor subtype 4
- a thiourea derivative has a highly hydrophilic structure or a relatively large molecular weight, it is generally considered difficult to obtain sufficient oral absorbability or central transferability as a medicine.
- pyrrolidine derivatives are considered to have improved oral absorption or central migration compared to thiourea derivatives, they have not progressed to higher evaluation.
- the pyrrolidine derivative disclosed in Patent Document 1 has a structure represented by the following formula.
- the compound necessarily has a substituent (heterocycle or aryl) represented by R d on the pyrrolidine ring.
- R a and R b are each independently a hydrogen atom or C 1-6 alkyl, or R a and R b together form a C 3-6 cycloalkyl, R c is a hydrogen atom or C 1-6 alkyl, R d is an optionally substituted heterocycle or an optionally substituted aryl (provided that R d is not p-cyanophenyl) , R e is an optionally substituted heterocycle or an optionally substituted aryl (where R e is not p-methoxyphenyl and p-chlorophenyl, or when R e is pyridyl or pyrimidyl) R a is C 1-6 alkyl)]
- the present invention has been made in view of the above circumstances, and an object thereof is to provide a novel compound having somatostatin receptor subtype 4 (hereinafter sometimes referred to as “SSTR4”) selective agonist activity. . Furthermore, a therapeutic agent for the purpose of improving symptoms of neurodegenerative diseases such as Alzheimer's disease by the activation of neprilysin through the action of the compound found in the present invention on somatostatin receptor subtype 4 and the release enhancing action of acetylcholine, and The object is to provide a novel compound useful as a preventive agent.
- SSTR4 somatostatin receptor subtype 4
- the present inventors have found that a novel compound represented by the following formula (I) has a strong SSTR4 binding action and agonist activity, and completed the present invention.
- the nitrogen-containing saturated heterocyclic compound represented by the following formula (I) or a pharmaceutically acceptable salt thereof hereinafter referred to as “the compound of the present invention”, “the compound represented by the formula (I)”) Or “sometimes referred to as a compound of formula (I)”).
- R 1 represents C 1-4 alkyl optionally substituted with 1 to 5 fluorine atoms
- n is an integer of 1 to 4
- R 2 represents a C 1-4 alkyl which may be substituted with the same or different 1 to 5 substituents selected from the group consisting of a fluorine atom and hydroxy, or a hydrogen atom
- R 3 represents C 1-4 alkyl which may be substituted with the same or different 1 to 5 substituents selected from the group consisting of a fluorine atom and hydroxy
- R 3 together with R 2 may contain one —O—, —NR 5 —, —SO— or —SO 2 —.
- the saturated ring may be substituted with 1 to 5 fluorine atoms, C 1-4 alkyl, or substituted with 1 to 5 fluorine atoms.
- R 4a , R 4b , R 4c and R 4d are the same or different and each is optionally substituted with 1 to 5 fluorine atoms, C 1-4 alkyl, C 3-6 cycloalkyl, halogen, 1 to Optionally substituted with 5 fluorine atoms, optionally substituted with 1 to 5 identical or different substituents selected from the group consisting of C 1-4 alkoxy, C 1-4 alkylthio, hydroxy and cyano.
- C 6-14 aryl C 1-4 alkyl optionally substituted by the same or different 1 to 5 substituents selected from the group consisting of fluorine atom, hydroxy and C 1-3 alkoxy; 1-5 number of fluorine may be substituted with atoms C 1-3 alkoxy; hydrogen atom; a fluorine atom, hydroxy, indicates or CO 2 R 9, wherein, when n is 2, R 4a, R 4b R 4c and R 4d are hydrogen atom, with n is 1, 3 or 4, R 4a, R 4b, R 4c and any two or more good C 1-4 alkyl which may be substituted R 4d Wherein two or more of the above optionally substituted C 1-4 alkyls may be taken together to form a 4-7 membered saturated ring; A represents C 6-14 aryl or 5- to 11-membered heteroaryl, and the C 6-14 aryl and the 5- to 11-membered heteroaryl may be substituted with 1 to 5 fluorine atoms.
- R 1 represents C 1-4 alkyl optionally substituted with 1 to 5 fluorine atoms
- n is an integer of 1 to 4
- R 2 represents a C 1-4 alkyl which may be substituted with the same or different 1 to 5 substituents selected from the group consisting of a fluorine atom and hydroxy, or a hydrogen atom
- R 3 represents C 1-4 alkyl which may be substituted with the same or different 1 to 5 substituents selected from the group consisting of a fluorine atom and hydroxy
- R 3 together with R 2 may contain one —O—, —NR 5 —, —SO— or —SO 2 —.
- the saturated ring may be substituted with 1 to 5 fluorine atoms, C 1-4 alkyl, or substituted with 1 to 5 fluorine atoms.
- R 4a , R 4b , R 4c and R 4d are the same or different and each is optionally substituted with 1 to 5 fluorine atoms, C 1-4 alkyl, C 3-6 cycloalkyl, halogen, 1 to Optionally substituted with 5 fluorine atoms, optionally substituted with 1 to 5 identical or different substituents selected from the group consisting of C 1-4 alkoxy, C 1-4 alkylthio, hydroxy and cyano.
- C 6-14 aryl C 1-4 alkyl optionally substituted by the same or different 1 to 5 substituents selected from the group consisting of fluorine atom, hydroxy and C 1-3 alkoxy; 1-5 number of fluorine may be substituted with atoms C 1-3 alkoxy; hydrogen atom; a fluorine atom, hydroxy, indicates or CO 2 R 9, wherein, when n is 2, R 4a, R 4b R 4c and R 4d are hydrogen atom, with n is 1, 3 or 4, R 4a, R 4b, R 4c and any two or more good C 1-4 alkyl which may be substituted R 4d Wherein two or more of the above optionally substituted C 1-4 alkyls may be taken together to form a 4-7 membered saturated ring; A represents C 6-14 aryl or 5- to 11-membered heteroaryl, and the C 6-14 aryl and the 5- to 11-membered heteroaryl may be substituted with 1 to 5 fluorine atoms.
- a saturated heterocycle of R 17 represents a hydrogen atom, C 1-4 alkyl or C 3-6 cycloalkyl, R 18 represents C 1-4 alkyl or C 3-6 cycloalkyl.
- R 18 represents C 1-4 alkyl or C 3-6 cycloalkyl.
- a pharmaceutically acceptable salt thereof Except for the following compounds: N-1- (4-methanesulfonylphenyl) propyl-1-methylpiperidine-3-carboxamide; N-1- (4-pyrrolidin-1-ylphenyl) ethyl-1-methylpiperidine-3-carboxamide; N-1- (2,4-dimethylphenyl) ethyl-1-methylpiperidine-3-carboxamide; N-1-phenylethyl-1-propyl-3- (4-ethylphenyl) piperidine-5-carboxamide; [Section 2] n is 1 or 3, Item 1 or Compound 1-2 or a pharmaceutically acceptable salt thereof; [Section
- Item 3 The compound according to any one of Items 1 to 3 and Item 1-2, or a pharmaceutically acceptable salt thereof; [Clause 4-2] Item 2.
- A is phenyl or 1-naphthyl, and the phenyl or 1-naphthyl is selected from the group consisting of a methyl group, an ethyl group, a methoxy group, a trifluoromethoxy group, a methylthio group, a fluorine atom, a chlorine atom, and a bromine atom.
- A is phenyl or 1-naphthyl, and the phenyl or 1-naphthyl is selected from the group consisting of a methyl group, an ethyl group, a methoxy group, a trifluoromethoxy group, a methylthio group, a fluorine atom, a chlorine atom, and a bromine atom.
- R 1 is C 1-3 alkyl, Item 5.
- R 4a and R 4b are the same or different and each is optionally substituted with 1 to 5 fluorine atoms, C 1-4 alkyl, C 3-6 cycloalkyl, halogen, or 1 to 5 fluorine atoms.
- C 6-14 aryl optionally substituted with 1 to 5 identical or different substituents selected from the group consisting of optionally substituted C 1-4 alkoxy, C 1-4 alkylthio, hydroxy and cyano
- a C 1-4 alkyl which may be substituted with the same or different 1 to 5 substituents selected from the group consisting of a fluorine atom, hydroxy and C 1-3 alkoxy; substituted with 1 to 5 fluorine atoms; Optionally substituted C 1-3 alkoxy; hydrogen atom; fluorine atom; or CO 2 R 9 , where R 4a and R 4b are optionally substituted C 1-4 alkyl
- the optionally substituted C 1-4 alkyl may be taken together to form a 4- to 7-membered saturated ring, R 4c and R 4d are a hydrogen atom, Item 6.
- A is C 6-14 aryl, and the above C 6-14 aryl is C 1-4 alkyl, C 3-6 cycloalkyl, fluorine atom, chlorine atom optionally substituted with 1 to 5 fluorine atoms Substituted with the same or different 1 to 3 substituents selected from the group consisting of C 1-4 alkoxy optionally substituted with 1 to 5 fluorine atoms, bromine atom, C 1-4 alkylthio and cyano May have been, The compound or a pharmaceutically acceptable salt thereof according to any one of Items 1 to 8, Item 1-2, Item 4-2 to Item 4-5, and Item 6-0; [Section 10] When n is 3, R 4a and R 4b are the same or different, 2-position of the piperidine ring, a 5- or 6-position substituent, identical or
- R 4a is a substituent at the 4-position of the piperidine ring, which may be substituted with 1 to 5 fluorine atoms, C 1-4 alkyl, C 3-6 cycloalkyl, halogen, 1 to 5 fluorine atom in an optionally substituted C 1-4 alkoxy, C 1-4 alkylthio, with the same or different 1 to 5 substituents selected from the group consisting of hydroxy and cyano substituted C 6 -14 aryl; or a hydrogen atom, R 4b , R 4c and R 4d are hydrogen atoms, However, the position of R 1 is the 1st position of the piperidine ring and the position of the amide group is the 3rd position of the piperidine ring.
- R 4a is a substituent at the 4-position of the piperidine ring, optionally substituted with 1 to 5 fluorine atoms, C 1-3 alkyl, halogen, or 1 to 5 fluorine atoms.
- a phenyl group which may be substituted with the same or different 1 to 3 substituents selected from the group consisting of C 1-3 alkoxy, C 1-3 alkylthio and hydroxy, R 4b , R 4c and R 4d are hydrogen atoms, Item 11.
- R 4a is a substituent at the 2-position or 6-position of the piperidine ring, and is substituted with the same or different 1 to 5 substituents selected from the group consisting of a fluorine atom, hydroxy and C 1-3 alkoxy
- substituents selected from the group consisting of a fluorine atom, hydroxy and C 1-3 alkoxy
- R 4b , R 4c and R 4d are hydrogen atoms,
- the position of R 1 is the 1st position of the piperidine ring and the position of the amide group is the 3rd position of the piperidine ring.
- R 4a is a substituent at the 5-position of the piperidine ring, and may be substituted with the same or different 1 to 5 substituents selected from the group consisting of a fluorine atom, hydroxy and C 1-3 alkoxy C 1-4 alkyl; C 1-3 alkoxy optionally substituted with 1 to 5 fluorine atoms; fluorine atom; or hydrogen atom
- R 4b , R 4c and R 4d are hydrogen atoms
- the position of R 1 is the 1st position of the piperidine ring and the position of the amide group is the 3rd position of the piperidine ring.
- Item 3 The compound according to any one of Items 3 to 9, Item 4-2 to Item 4-5, Item 5-2 to Item 5-5, and Item 6-0, or a pharmaceutically acceptable salt thereof; [Clause 13-2]
- R 4a is a substituent at the 5-position of the piperidine ring and is C 1-3 alkyl, C 1-3 alkoxy, a fluorine atom or hydroxy
- R 4b , R 4c and R 4d are hydrogen atoms, Provided that the position of R 1 is the 1- position of the piperidine ring and the position of the amide group is the 3-position of the piperidine ring; 5.
- R 4a is a substituent at the 5-position of the piperidine ring and is methyl, methoxy, a fluorine atom or hydroxy;
- R 4c and R 4d are a hydrogen atom, Provided that the position of R 1 is the 1- position of the piperidine ring and the position of the amide group is the 3-position of the piperidine ring; 5.
- R 4a , R 4b , R 4c and R 4d are hydrogen atoms, The compound according to any one of Items 1 to 13, Item 1-2, Item 4-2 to 4-5, Item 5-2 to Item 5-5, and Item 6-0 or a pharmaceutically acceptable salt thereof salt;
- [Section 16] Item 1 to 15, Item 1-2, Item 4-2 to Item 4-5, Item 5-2 to Item 5-5, Item 6-0, Item 11-2, Item 12-2 to Item 12-5 and Item 13.
- a pharmaceutical composition comprising the compound according to any one of Items 13-2 to 13-4 or a pharmaceutically acceptable salt thereof;
- [Section 17] Claims 1-15, 1-2, 4-2 to 4-5, 5-2 to 5-5, 6-0, 11-2, 12-2 to 12-5 And an activator of somatostatin receptor subtype 4, comprising the compound according to any one of Items 13-2 to 13-4 or a pharmaceutically acceptable salt thereof;
- [Section 18] Item 1 to 15, Item 1-2, Item 4-2 to Item 4-5, Item 5-2 to Item 5-5, Item 6-0, Item 11-2, Item 12-2 to Item 12-5 and Treatment or prevention is possible by activating somatostatin receptor subtype 4 containing the compound according to any one of Items 13-2 to 13
- the therapeutic or preventive agent according to Item 18, wherein the disease is epilepsy, depression, behavioral disorder, memory disorder, learning disorder, attention deficit disorder, pain, neurodegenerative disease or neurogenic bladder; [Section 20] Item 19.
- the therapeutic or prophylactic agent according to Item 18, wherein the disease is a hyperproliferative disorder, acromegaly, melanoma, breast cancer, prostate adenoma, prostate cancer, lung cancer, intestinal cancer or skin cancer;
- laim 21 Item 19.
- the therapeutic or prophylactic agent according to Item 18, wherein the disease is arthritis, rheumatoid arthritis or rheumatoid spondylitis; [Item 22] Item 19.
- Item 29 Item 1 to 15, Item 1-2, Item 4-2 to Item 4-5, Item 5-2 to Item 5-5, Item 6-0, Item 11-2, Item 12-2 to Item 12-5 and A method for activating somatostatin receptor subtype 4 comprising administering an effective amount of the compound according to any one of Items 13-2 to 13-4 or a pharmaceutically acceptable salt thereof.
- Proction 30 Item 1-15, Item 1-2, Item 4-2 to Item 4-5, Item 5-2 to Item 5-5, Item 6-0, Item 11 for activating somatostatin receptor subtype 4 -2, the compound according to any one of Items 12-2 to 12-5 and Item 13-2 to Item 13-4, or a pharmaceutically acceptable salt thereof.
- the compound of the present invention is a therapeutic agent for diseases caused by A ⁇ such as Alzheimer's disease, cognitive impairment, memory impairment, learning impairment, mild cognitive impairment, senile dementia, amyloidosis and cerebrovascular angiopathy, pain, cancer, depression, etc. It is useful as a preventive agent.
- the compounds of formula (I) may have one or more asymmetric carbon atoms and may give rise to geometric isomerism or axial chirality.
- the compound of formula (I) may exist as several stereoisomers. In the present invention, these stereoisomers, mixtures thereof and racemates are included in the compound represented by the formula (I) of the present invention.
- a deuterium converter obtained by converting any one or two or more 1 H of the compound represented by the general formula (I) into 2 H (D) is also included in the compound represented by the general formula (I). .
- the compound represented by the formula (I), or a solvate such as a hydrate or ethanol solvate of a pharmaceutically acceptable salt thereof is also encompassed in the compound represented by the general formula (I).
- the compounds of formula (I) may have one or more asymmetric carbon atoms and may give rise to geometric isomerism or axial chirality.
- the compound of formula (I) may exist as several stereoisomers.
- Alkyl means a straight-chain or branched saturated hydrocarbon group.
- C 1-3 alkyl or “C 1-4 alkyl” means an alkyl having 1 to 3 or 1 to 4 carbon atoms. Specific examples thereof include methyl, ethyl, propyl, isopropyl and the like in the case of “C 1-3 alkyl”.
- C 1-4 alkyl in addition to the functional group described above, butyl, isobutyl, sec-butyl, tert-butyl and the like can be mentioned.
- Cycloalkyl means a monocyclic saturated hydrocarbon group or a polycyclic saturated hydrocarbon group.
- C 3-6 cycloalkyl means a cyclic alkyl having 3 to 6 carbon atoms, and includes a partially bridged structure or a structure condensed with aryl or heteroaryl.
- Specific examples of “C 3-6 cycloalkyl” include cyclopropyl, cyclobutyl, cyclopentyl, cyclohexyl and the like.
- “Saturated heterocyclic ring” means a monocyclic group containing 1 to 2 nitrogen atoms, oxygen atoms or sulfur atoms in addition to carbon atoms. “3- to 6-membered saturated heterocyclic ring” means a saturated heterocyclic ring composed of 3 to 6 atoms. Examples include aziridine, azetidine, pyrrolidine and piperidine. “Saturated ring” means the above “cycloalkyl” or “saturated heterocycle”.
- Alkoxy means a group in which a linear or branched saturated hydrocarbon group is interposed via an oxygen atom.
- C 1-3 alkoxy or “C 1-4 alkoxy” means alkoxy having 1 to 3 or 1 to 4 carbon atoms. Specific examples thereof include methoxy, ethoxy, propoxy, isopropoxy and the like in the case of “C 1-3 alkoxy”.
- C 1-4 alkoxy in addition to the functional groups described above, butyloxy and the like can be mentioned.
- Alkylthio means a group in which a linear or branched saturated hydrocarbon group is interposed via a sulfur atom.
- C 1-4 alkylthio means alkylthio having 1 to 4 carbon atoms. Specific examples thereof include methylthio, ethylthio, propylthio, isopropylthio, butylthio and the like in the case of “C 1-4 alkylthio”.
- Halogen means a fluorine atom, a chlorine atom, a bromine atom or an iodine atom. Among them, preferred is a fluorine atom or a chlorine atom.
- Aryl means a monocyclic aromatic hydrocarbon group or a polycyclic aromatic hydrocarbon group.
- C 6-14 aryl means aryl having 6 to 14 carbon atoms constituting the aromatic ring. Specific examples include phenyl, 1-naphthyl, 2-naphthyl, 1-anthracenyl and the like. Of these, 1-naphthyl or phenyl is preferable.
- Aryloxy means a group in which a monocyclic aromatic hydrocarbon group or a polycyclic aromatic hydrocarbon group is interposed via an oxygen atom. Specific examples include phenyloxy, 1-naphthyloxy, 2-naphthyloxy and the like. Of these, phenyloxy is preferable.
- Heteroaryl refers to a monocyclic 5- to 7-membered aromatic heterocyclic group containing 1 to 4 atoms independently selected from the group consisting of a nitrogen atom, an oxygen atom and a sulfur atom, or 2 And an 8- to 11-membered aromatic heterocyclic group of the ring.
- Examples include quinolyl, isoquinolyl, benzofuranyl, benzothienyl, benzoxazolyl, benzothiazolyl, benzisoxazolyl, benzisothiazolyl, benzotriazolyl, benzimidazolyl and the like.
- Preferred heteroaryls include pyridyl, thienyl, pyrimi
- the “position of the 2-position, 4-position, 5-position or 6-position of the piperidine ring” means as shown in the following formula:
- the position of the nitrogen atom of the piperidine ring (position of R 1 ) is the 1st position, and the carbon atom having a substituent when the number of each carbon atom forming the ring is numbered so that the position of the amide group is the 3rd position Means position.
- the “position at the 4-position of the piperidine ring” means that the substituent is located at the fourth carbon atom when a number is assigned so that the position of the amide group is the 3-position with the position of the nitrogen atom as the 1-position. Means replaced.
- R 1 , R 2 , R 3 , R 4a to R 4d , R 5 to R 18 , A and n in the compound of the present invention represented by the formula (I) are those defined in item 1 above.
- the preferred ones are as follows. However, the technical scope of the present invention is not limited to the scope of the compounds listed below.
- R 1 is preferably C 1-4 alkyl, and more preferably C 1-3 alkyl.
- R 1 is more preferably methyl, ethyl, propyl or isopropyl, and most preferably methyl.
- R 2 is preferably C 1-4 alkyl which may be substituted with the same or different 1 to 5 substituents selected from the group consisting of a fluorine atom and hydroxy, more preferably unsubstituted C 1. -4 alkyl.
- R 2 is more preferably methyl, ethyl or isopropyl, and most preferably methyl.
- the R 3 include a fluorine atom and an alkyl of the same or different one to five may be substituted with a substituent C 1-4 selected from the group consisting of hydroxy, preferably unsubstituted C 1- 4 alkyls.
- R 3 is more preferably methyl, ethyl or isopropyl, and more preferably methyl.
- R 3 may combine with R 2 to form a 3- to 6-membered saturated ring. The saturated ring may be substituted with 1 to 5 substituents.
- the unsubstituted 3- to 6-membered saturated ring formed by R 2 and R 3 is preferably a saturated ring which may contain one —O— or —SO 2 —, more preferably A saturated ring optionally containing one —O— is exemplified, and a 3- to 6-membered cycloalkyl is more preferred. Most preferably, the unsubstituted 3- to 6-membered saturated ring formed by R 2 and R 3 is cyclopropyl or cyclohexyl.
- R 4a , R 4b , R 4c and R 4d , R 4a and R 4b are preferably the same or different, and C 1-4 alkyl optionally substituted with 1 to 5 fluorine atoms, C 3- 1 to 5 substituents selected from the group consisting of 6 cycloalkyl, halogen, C 1-4 alkoxy optionally substituted with 1 to 5 fluorine atoms, C 1-4 alkylthio and cyano in an optionally substituted C 6-11 aryl; fluorine atom, may be substituted by the same or different 1 to 5 substituents selected from the group consisting of hydroxy and C 1-3 alkoxy C 1- 4 alkyl; 1-5 which may C 1-3 also be alkoxy substituted by fluorine atoms, hydrogen atoms, fluorine atoms; a, or CO 2 R 9, wherein, R 4a and R 4b are be substituted When it is also good C 1-4 alkyl, said optionally C 1-4 alkyl substituted may form
- R 4a and R 4b are the same or different and may be substituted with the same or different 1 to 5 substituents selected from the group consisting of a fluorine atom, hydroxy and C 1-3 alkoxy.
- R 4a and R 4b are the same or different and are C 1-4 alkyl or a hydrogen atom
- R 4c and R 4d are a hydrogen atom
- most preferably R 4a , R 4 Examples include a combination in which 4b , R 4c and R 4d are hydrogen atoms.
- A is C 6-14 aryl or 5-11 membered heteroaryl.
- the C 6-14 aryl and the 5- to 11-membered heteroaryl may be substituted with 1 to 5 substituents.
- A is preferably C 6-14 aryl, more preferably phenyl or 1-naphthyl. More preferably, A is phenyl.
- the substituent is preferably C 1-4 alkyl, C 3-6 cycloalkyl, fluorine atom, chlorine atom, bromine atom which may be substituted with 1 to 5 fluorine atoms.
- C 1-4 alkoxy optionally substituted with 1 to 5 fluorine atoms, C 1-4 alkylthio, cyano, CO 2 R 10 , CONR 11 R 12 , SO 2 NR 11 R 12 or NR 11 R 12 Is mentioned. More preferably, the substituent is a C 1-4 alkyl, C 3-6 cycloalkyl, fluorine atom, chlorine atom, bromine atom, or 1 to 5 fluorine atom which may be substituted with 1 to 5 fluorine atoms.
- C 1-4 alkoxy atoms an optionally substituted C 1-4 alkoxy atoms, C 1-4 alkylthio, cyano and the like, more preferably, 1 to 5 fluorine atoms which may be substituted with C 1-4 alkyl, fluorine C 1-4 alkoxy which may be substituted with an atom, a chlorine atom or 1 to 5 fluorine atoms.
- the substituent is methyl, ethyl, methoxy, trifluoromethoxy, fluorine atom or chlorine atom.
- the number of substituents substituted for A is preferably 1 to 4, more preferably 1 to 3.
- the number of the substituents is more preferably 1 or 2, and most preferably 2.
- N is preferably 1 to 3, more preferably 2 or 3, and still more preferably 3.
- n is 3, the nitrogen-containing saturated ring is a piperidine ring.
- R 5 is preferably a hydrogen atom, C 1-4 alkyl, C 3-6 cycloalkyl, CONR 15 R 16 or COR 17 , more preferably a hydrogen atom, C 1-3 alkyl or COR 17. It is done. R 5 is more preferably C 1-3 alkyl, and most preferably methyl.
- R 6 and R 9 are the same or different and preferably include C 1-4 alkyl.
- R 6 and R 9 are the same or different, more preferably methyl, ethyl or tert-butyl, and most preferably methyl.
- R 7 and R 8 are the same or different and preferably include a hydrogen atom or C 1-4 alkyl, more preferably C 1-4 alkyl.
- R 7 and R 8 are the same or different, more preferably methyl, ethyl or isopropyl, and most preferably methyl.
- the saturated heterocyclic ring formed by R 7 and R 8 together is preferably pyrrolidine or piperidine, more preferably pyrrolidine.
- R 10 is preferably C 1-4 alkyl or C 3-6 cycloalkyl, and more preferably C 1-4 alkyl.
- R 10 is more preferably methyl, ethyl or tert-butyl, and most preferably methyl.
- R 11 and R 12 are the same or different and preferably include a hydrogen atom or C 1-4 alkyl, more preferably C 1-4 alkyl.
- R 11 and R 12 are the same or different, more preferably methyl, ethyl or isopropyl, and most preferably methyl.
- Preferable examples of the saturated heterocyclic ring formed by R 11 and R 12 together include pyrrolidine or piperidine, more preferably pyrrolidine.
- R 13 is preferably C 1-4 alkyl or C 3-6 cycloalkyl, and more preferably C 1-4 alkyl.
- R 13 is more preferably methyl, ethyl or isopropyl, and most preferably methyl.
- R 14 is preferably C 1-4 alkyl, C 3-6 cycloalkyl or C 6-14 aryl, and more preferably C 1-4 alkyl or C 6-14 aryl.
- R 14 is more preferably methyl, ethyl, isopropyl or phenyl, and most preferably methyl.
- R 15 and R 16 are preferably C 1-4 alkyl, more preferably methyl, ethyl or isopropyl. R 15 and R 16 are more preferably methyl or isopropyl, and most preferably methyl.
- the saturated heterocyclic ring formed by R 15 and R 16 together is preferably pyrrolidine or piperidine, more preferably pyrrolidine.
- R 17 is preferably a hydrogen atom or C 1-4 alkyl, more preferably a hydrogen atom or methyl.
- R 18 is preferably C 1-4 alkyl, more preferably methyl, ethyl or tert-butyl. R 18 is more preferably methyl or ethyl, and most preferably methyl.
- a preferable compound includes, for example, the following compound A, and a more preferable compound includes compound B.
- R 1 is C 1-3 alkyl
- R 2 and R 3 are the same or different and each is a C 1-4 alkyl which may be substituted with the same or different 1 to 5 substituents selected from the group consisting of a fluorine atom and hydroxy
- , R 2 and R 3 together may form a 3-6 membered saturated ring which may contain one —O— or —SO 2 —
- R 4a and R 4b are the same or different and each may be substituted with 1 to 5 substitutable fluorine atoms, C 1-4 alkyl, C 3-6 cycloalkyl, halogen, 1 to 5 fluorine atom in an optionally substituted C 1-4 alkoxy, C 1-4 alkylthio, with the same or different 1 to 5 substituents selected from the group consisting of hydroxy and cyano substituted C 6
- R 1 is C 1-3 alkyl
- R 2 and R 3 are the same or different and each is C 1-4 alkyl
- R 4a and R 4b are the same or different, good fluorine atom, be substituted by the same or different 1 to 5 substituents selected from the group consisting of hydroxy and C 1-3 alkoxy C 1- 4 alkyl; C 1-3 alkoxy optionally substituted with 1 to 5 fluorine atoms; hydrogen atom; or fluorine atom
- R 4c and R 4d are a hydrogen atom
- A is C 6-14 aryl, and the above C 6-14 aryl may be substituted with 1 to 5 fluorine atoms, C 1-4 alkyl, C 3-6 cycloalkyl, fluorine atom, chlorine
- the pharmaceutically acceptable salt of the compound represented by the formula (I) means a pharmaceutically acceptable acid addition salt of the compound of the formula (I) having a group capable of forming an acid addition salt in the structure.
- acid addition salts include hydrochloride, hydrobromide, hydroiodide, sulfate, perchlorate, phosphate, and other inorganic acid salts, oxalate, malonate, maleate Acid, fumarate, lactate, malate, citrate, tartrate, benzoate, trifluoroacetate, acetate, methanesulfonate, p-toluenesulfonate and trifluoromethanesulfonate And amino acid salts such as glutamate and aspartate.
- the compound of the present invention represented by the formula (I) When the compound of the present invention represented by the formula (I) has an acidic functional group such as a carboxyl group, it can form salts with various bases.
- the pharmaceutically acceptable salt in this case include alkali metal salts such as sodium salt and potassium salt, alkaline earth metal salts such as calcium salt, and ammonium salt. These salts can be obtained by a conventional method such as recrystallization after mixing the compound of the present invention represented by the formula (I) with an acid or a base.
- the method for producing the compound of the present invention is described below.
- the compound of the present invention represented by the formula (I) can be produced, for example, by the following production method.
- the compound of the formula (I) can be produced by the following production method.
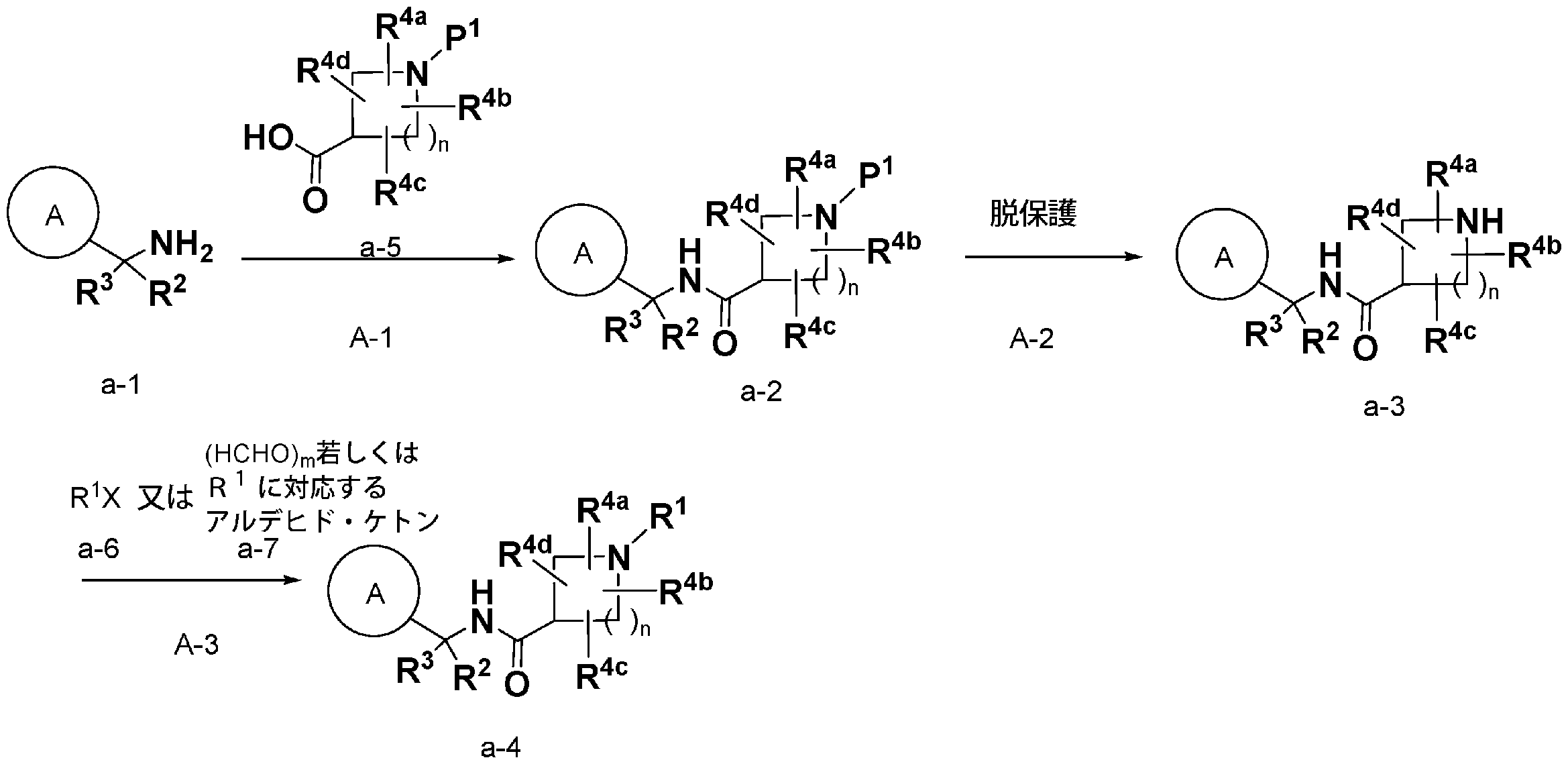
- R 1 , R 2 , R 3 , R 4a to R 4d and n are as defined in item 1
- P 1 is a protecting group for an amino group
- X is a leaving group such as halogen.
- HCHO HCHO
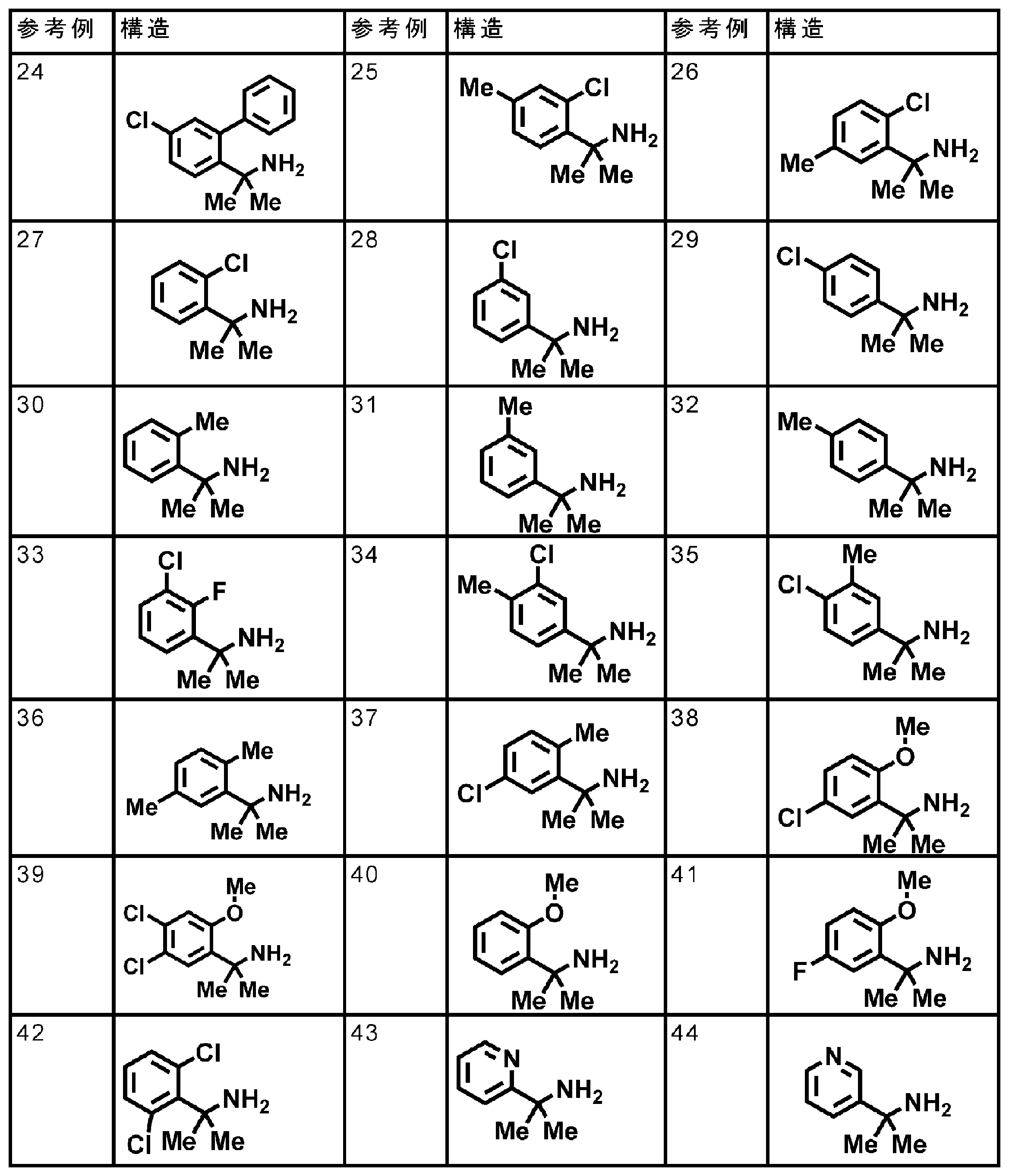
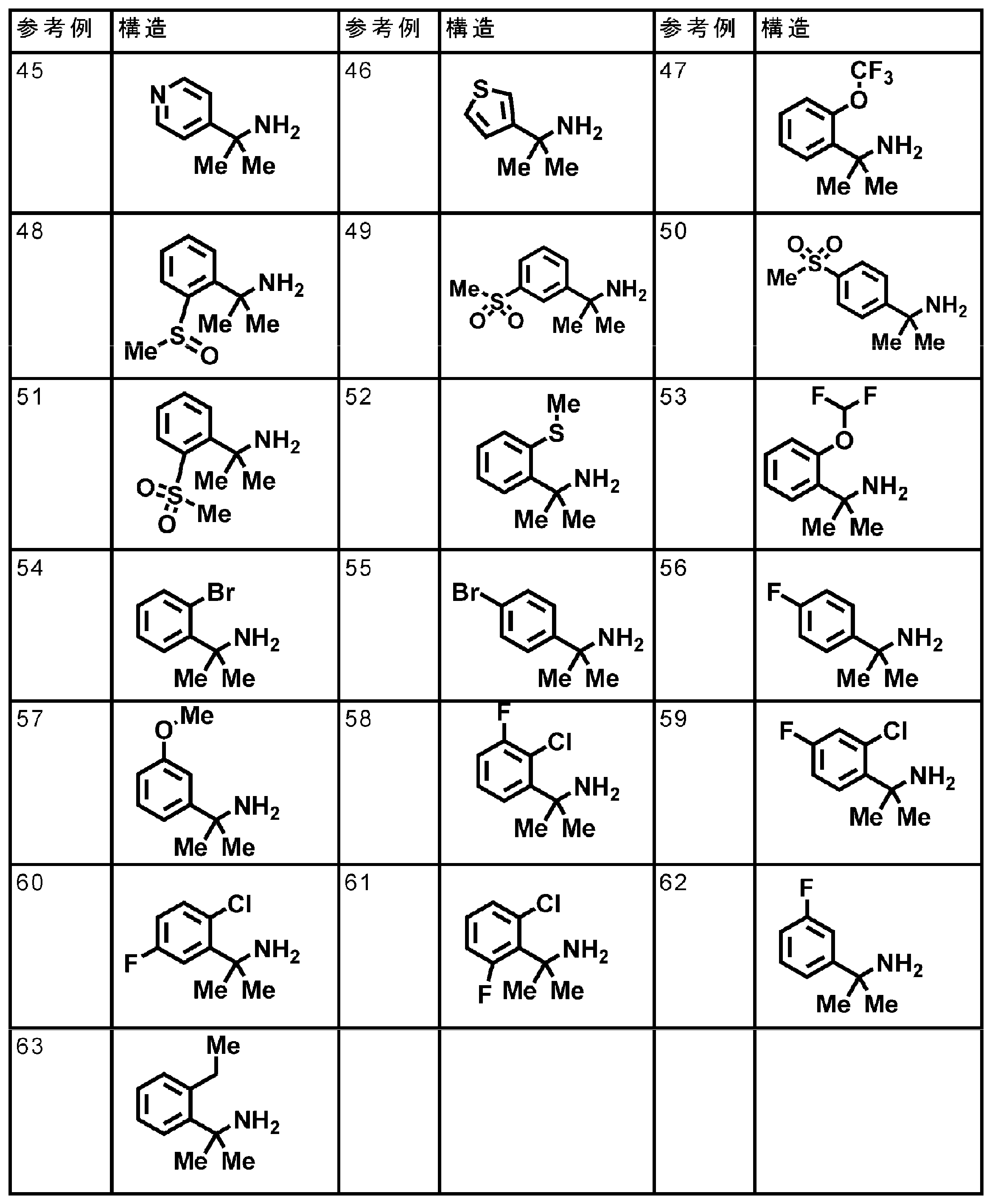
- Compound a-1 can be purchased commercially, for example, Tetrahedron Letters, 1987, 28, 6513-6516, Bioorganic and Medicinal Chemistry, 2011, 19, 5238-5246, International Publication No. 1999/19301, Journal of Mof. It can be synthesized by the method described in Chemistry, 2011, 54, 1836-1846, etc.
- Compound a-5 can be purchased as a commercial product, for example, International Publication No. 2011/26917, Tetrahedron, 2007, 63, 10486-10696, International Publication No. 2006/91697, International Publication No. 2010/118207, International Publication No. Publication No. 2011/26904, Journal of Medicinal Chemistry, 2006, 49, 942-946, International Publication No.
- This step is a step of obtaining compound a-2 by conducting a condensation reaction of compound a-1 and compound a-5.
- This reaction can be performed according to a conventional method.
- this reaction is achieved by converting compound a-5 into a reactive derivative (eg, lower alkyl ester, active ester, acid anhydride, acid halide, etc.) and reacting with compound a-1.
- a reactive derivative eg, lower alkyl ester, active ester, acid anhydride, acid halide, etc.
- the active ester include p-nitrophenyl ester, N-hydroxysuccinimide ester, pentafluorophenyl ester and the like.
- Specific examples of the acid anhydride include mixed acid anhydrides with ethyl chlorocarbonate, isobutyl chlorocarbonate, isovaleric acid, pivalic acid and the like.
- Compound a-2 can also be produced by reacting compound a-1 and compound a-5 in the presence of a condensing agent.
- a condensing agent include DCC, EDCI, HATU, PyBOP and the like. These condensing agents can be used alone or in combination with these condensing agents and peptide synthesis reagents such as N-hydroxysuccinimide, HOBt, and DMAP.
- the reaction between compound a-1 and compound a-5 is carried out in a solvent or without a solvent.
- the solvent should be selected according to the kind of the raw material compound, and examples thereof include toluene, THF, dioxane, DME, dichloromethane, chloroform, ethyl acetate, acetone, acetonitrile, DMF, DMSO and the like.
- the said solvent can be used individually or as a mixed solvent.
- Compound a-1 is used in the form of an acid addition salt such as an aqueous solution or hydrochloride, and a free base may be generated in the reaction system. This reaction is usually carried out in the presence of a base.
- the base used include inorganic bases such as potassium carbonate and sodium hydrogen carbonate, and organic bases such as triethylamine, ethyldiisopropylamine, N-methylmorpholine, pyridine and 4-dimethylaminopyridine.
- the reaction temperature varies depending on the kind of raw material compound used, it is generally about ⁇ 30 ° C. to about 150 ° C., preferably about ⁇ 10 ° C. to about 70 ° C.
- the reaction time varies depending on the type of raw material compound used, it is generally about 30 minutes to 72 hours, preferably about 1 hour to 12 hours.
- Step 3 is a step of obtaining compound a-4 by alkylating the amino group of compound a-3 obtained in step A-2 above, for example, by reductive amination reaction.
- This reaction can be performed according to a conventional method.
- this reaction can be achieved by reacting compound a-3 with various ketones or aldehydes and a reducing agent in the presence or absence of a suitable solvent.
- the reducing agent include sodium borohydride, lithium aluminum hydride, sodium triacetoxyborohydride, sodium cyanoborohydride and the like.
- the solvent should be selected according to the type of the raw material compound, etc., for example, dichloromethane, chloroform, dichloroethane, THF, 1,4-dioxane, DME, acetonitrile, DMF, DMA, NMP, DMSO, acetic acid, Water or alcohols such as methanol, ethanol, isopropanol, and 2,2,2-trifluoroethanol can be mentioned.
- the said solvent can be used individually or as a mixed solvent. While the reaction temperature varies depending on the raw material compound used and the type of reagent, etc., it is generally ⁇ 20 ° C. to 200 ° C., preferably 0 ° C. to 100 ° C. While the reaction time varies depending on the kind of raw material compound used and the like, it is generally 30 minutes to 72 hours, preferably about 1 hour to 12 hours.
- Compound a-4 can also be obtained by reacting compound a-3 with various alkyl halides in a suitable solvent or without solvent.
- the solvent should be selected according to the type of raw material compound, etc., and examples include dichloromethane, chloroform, dichloroethane, THF, 1,4-dioxane, DME, acetonitrile, DMF, DMA, NMP, DMSO and the like. It is done.
- the said solvent can be used individually or as a mixed solvent.
- Compound a-3 is used in the form of an acid addition salt such as hydrochloride, and a free base may be generated in the reaction system. This reaction is usually performed in the presence of a base.
- bases used include inorganic bases such as potassium carbonate, sodium bicarbonate and cesium carbonate, and organic bases such as triethylamine, ethyldiisopropylamine, N-methylmorpholine, pyridine and 4-dimethylaminopyridine. It is done. While the reaction temperature varies depending on the raw material compound used and the type of reagent, etc., it is generally ⁇ 20 ° C. to 200 ° C., preferably 0 ° C. to 100 ° C. While the reaction time varies depending on the kind of raw material compound used and the like, it is generally 30 minutes to 72 hours, preferably about 1 hour to 12 hours.
- the compound of the present invention represented by the formula (I) or an intermediate thereof can be separated and purified by methods known to those skilled in the art. Examples thereof include methods such as extraction, distribution, reprecipitation, column chromatography (for example, silica gel column chromatography, ion exchange column chromatography, preparative liquid chromatography) and recrystallization.
- Examples of the solvent used for recrystallization include alcohol solvents such as methanol, ethanol and 2-propanol, ether solvents such as diethyl ether, ester solvents such as ethyl acetate, aromatic hydrocarbon solvents such as benzene and toluene, A ketone solvent such as acetone, a halogen solvent such as dichloromethane and chloroform, a hydrocarbon solvent such as hexane, an aprotic solvent such as dimethylformamide and acetonitrile, water, and a mixed solvent thereof can be used.
- alcohol solvents such as methanol, ethanol and 2-propanol
- ether solvents such as diethyl ether
- ester solvents such as ethyl acetate
- aromatic hydrocarbon solvents such as benzene and toluene
- a ketone solvent such as acetone
- a halogen solvent such as dichloromethane and chloroform
- the molecular structure of the compound of the present invention is determined by referring to the structure derived from each raw material compound, a spectroscopic method such as a nuclear magnetic resonance method, an infrared absorption method and a circular two-light spectrum analysis method, and a mass. It can be easily done by analytical methods.
- the compound of the present invention represented by the formula (I) or a pharmaceutically acceptable salt thereof may have asymmetry or may have a substituent having an asymmetric carbon.
- optical isomers exist.
- the compounds of the present invention also include mixtures of these isomers and isolated compounds, which can be produced according to conventional methods. Examples of the production method include a method using a raw material having an asymmetric point, or a method of introducing asymmetry at an intermediate stage.
- optical isomers can be obtained by using optically active raw materials or by optical resolution at an appropriate stage of the production process.
- optical resolution method for example, when the compound represented by the formula (I) or an intermediate thereof has a basic functional group, it is used in an inert solvent (for example, alcohol solvents such as methanol, ethanol and 2-propanol).
- Ether solvents such as diethyl ether, ester solvents such as ethyl acetate, hydrocarbon solvents such as toluene, aprotic solvents such as acetonitrile, and mixed solvents thereof
- optically active acids for example, mandelic acid
- Monocarboxylic acids such as N-benzyloxyalanine and lactic acid, tartaric acid, dicarboxylic acids such as o-diisopropylidenetartaric acid and malic acid
- sulfonic acids such as camphorsulfonic acid and bromocamphorsulfonic acid.
- the diastereomer method to form is mentioned.
- an optically active amine for example, 1-phenylethylamine, quinine, quinidine, cinchonidine, cinchonine, and strychnine
- the optical resolution can be carried out by forming a salt using an organic amine such as
- the temperature at which the salt is formed is selected from the range from room temperature to the boiling point of the solvent. In order to improve the optical purity, it is desirable to raise the temperature once to near the boiling point of the solvent. When the precipitated salt is collected by filtration, it can be cooled as necessary to improve the yield.
- the amount of the optically active acid or amine used is suitably in the range of 0.5 to 2.0 chemical equivalents, preferably in the range of 0.8 to 1.2 chemical equivalents relative to the substrate.
- Crystals in an inert solvent as required for example, alcohol solvents such as methanol, ethanol and 2-propanol, ether solvents such as diethyl ether, ester solvents such as ethyl acetate, aromatic hydrocarbon solvents such as toluene, It can also be recrystallized with an aprotic solvent such as acetonitrile or a mixed solvent thereof to obtain a highly pure optically active salt. If necessary, the optically resolved salt can be treated with an acid or base by a conventional method to obtain a free form.
- an optical resolution is achieved by forming an amide using an optically active amine (for example, 1-phenylethylamine). Can also be done.
- the compound of the present invention is useful as an activator of somatostatin receptor subtype 4.
- the compounds of the present invention can be useful therapeutic or prophylactic agents for diseases that can be treated or prevented by activating somatostatin receptor subtype 4.
- diseases include diseases caused by A ⁇ such as Alzheimer's disease, cognitive impairment, memory impairment, learning impairment, mild cognitive impairment, senile dementia, amyloidosis, and cerebrovascular angiopathy, Parkinson's disease, and multiple sclerosis.
- Neurodegenerative diseases such as depression, epilepsy, depression, behavioral disorder, attention deficit disorder, pain, neurogenic bladder, hyperproliferative disorder, acromegaly, melanoma, breast cancer, prostate adenoma, prostate cancer, lung cancer, intestine Cancer such as cancer and skin cancer, arthritis, rheumatoid arthritis, rheumatoid spondylitis, psoriasis, atopic dermatitis, asthma, Graves' disease, inflammatory bowel disease, nephropathy, diabetic vascular disorder, ischemic disease, benign Examples include prostatic hypertrophy, age-related macular degeneration, glaucoma, and diabetic retinopathy. In particular, it can be a useful therapeutic agent for various neurodegenerative diseases including therapeutic agents for Alzheimer's disease.
- the administration route of the compound of the present invention may be any of oral administration, parenteral administration and rectal administration.
- the daily dose of the compound of the present invention varies depending on the type of compound, the method of administration, the symptoms and age of the patient.
- oral administration usually about 0.01 mg to 1000 mg, more preferably about 0.1 mg to 500 mg per 1 kg body weight of a human or mammal can be administered in 1 to several divided doses.
- parenteral administration such as intravenous injection (intravenous injection)
- intravenous injection usually, for example, about 0.01 mg to 300 mg, more preferably about 1 mg to 100 mg per kg body weight of a human or mammal can be administered.
- the compound of the present invention is usually administered in the form of a preparation prepared by mixing with a pharmaceutical carrier when used for pharmaceutical use as described above.
- a pharmaceutical carrier a non-toxic substance that is commonly used in the pharmaceutical field and does not react with the compound of the present invention is used.
- the carrier for the preparation include, for example, citric acid, glutamic acid, glycine, lactose, inositol, glucose, mannitol, dextran, sorbitol, cyclodextrin, starch, partially pregelatinized starch, sucrose, methyl parahydroxybenzoate, and propyl paraoxybenzoate.
- Examples of the dosage form include tablets, capsules, granules, powders, syrups, suspensions, injections, suppositories, eye drops, ointments, coatings, patches, inhalants and the like. These preparations can be prepared according to a conventional method. Liquid preparations may be dissolved or suspended in water or other suitable medium when used. Tablets and granules may be coated by a known method. In addition, these formulations may contain other therapeutically valuable ingredients.
- Me means methyl
- Et means ethyl
- Ph means phenyl
- Bn means benzyl
- Tf means trifluoromethylsulfonyl
- Ac means acetyl
- TBS means tert-butyldimethylsilyl.
- Abbreviations used as reagents include: TFA for trifluoroacetic acid, TBAF for tetra-n-butylammonium fluoride, Boc 2 O for di-tert-butyl dicarbonate, WSCD for 1-ethyl-3- (3-dimethylaminopropyl) ) Carbodiimide, DBU means diazabicycloundecene, and XtalFluor-E means (diethylamino) difluorosulfonium tetrafluoroborate.
- s is a single line
- d is a double line
- dd is a double double line
- t is a triple line
- td is a triple double line
- q is a quadruple line
- m is a multiple line.
- Line, br is broad
- brs is broad singlet
- brd is broad doublet
- brt is broad triplet
- J is coupling constant.
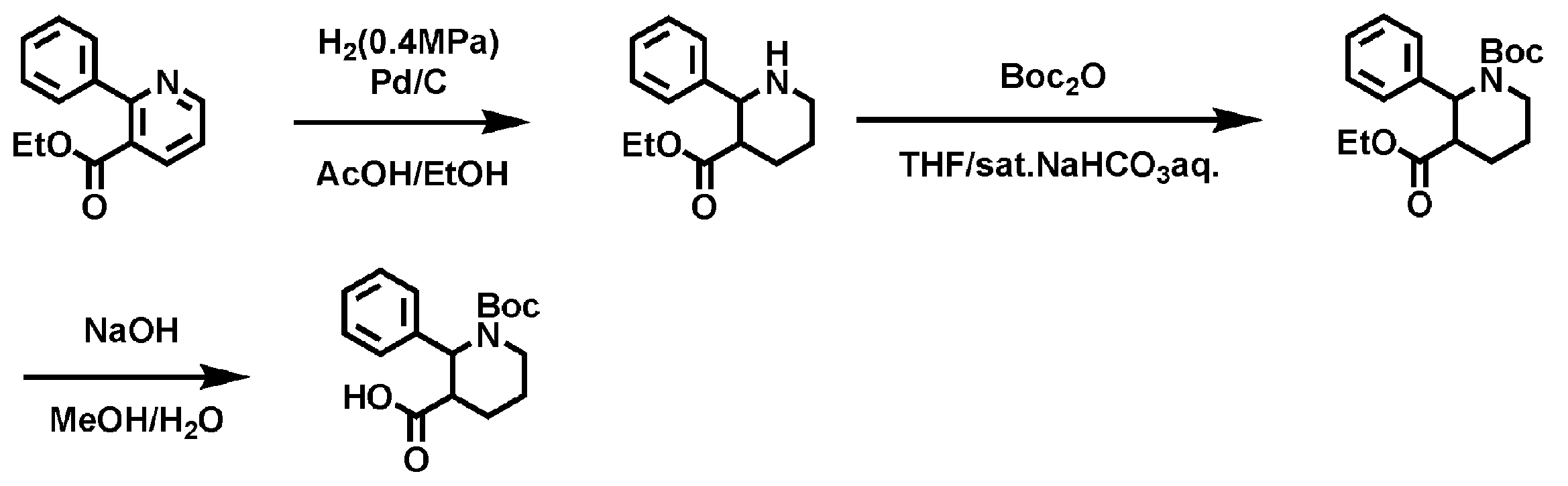
- Trimethylsilyl azide (830 mg) and boron trifluoride diethyl ether complex (1021 mg) were successively added dropwise to a toluene solution (6 mL) of 2- (2-fluorophenyl) propan-2-ol (925 mg) with stirring at room temperature. Stir for 15 minutes. After confirming disappearance of the raw materials, a saturated aqueous sodium hydrogen carbonate solution (50 mL) was added to the reaction solution, and the reaction mixture was extracted with ethyl acetate (40 mL). The organic layer was dried over anhydrous sodium sulfate, and then the reaction mixture was filtered and concentrated under reduced pressure.
- Acetone (1.74 g) and molecular sieves 4A (3.0 g) were added to a toluene (5 mL) solution of benzylamine (1.07 g), and the mixture was heated to reflux at 120 ° C. for 2 hours. After cooling to room temperature, the reaction solution was filtered through celite. The filtrate was concentrated to give 1-phenyl-N- (propane-2-ylidene) methanamine (1.34 g) as an oil.
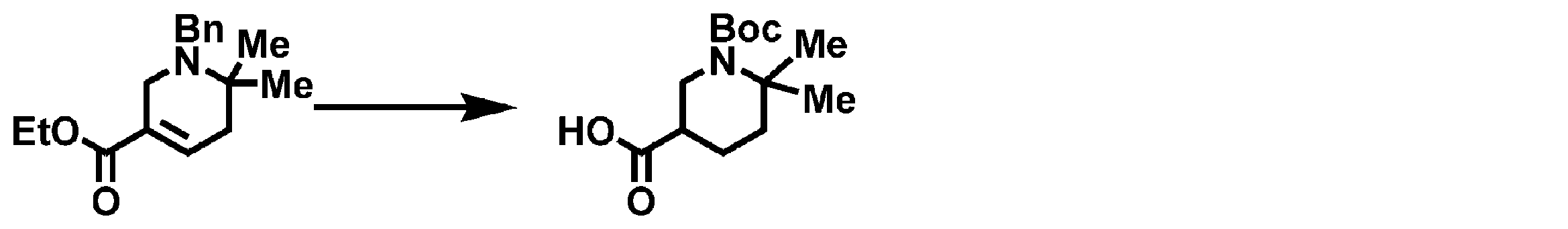
- Step 2 Ethyl 1-benzyl-6,6-dimethylpiperidine-3-carboxylate (137 mg) obtained in Step 1 was added to a pressure-resistant glass container and dissolved in methanol (5 mL). 20% palladium hydroxide / carbon support (68 mg) was added to the reaction mixture, and the mixture was stirred at room temperature for 16 hours under a medium pressure hydrogen atmosphere ( ⁇ 0.40 MPa). The reaction solution was filtered through celite, and the filtrate was concentrated under reduced pressure to obtain ethyl 6,6-dimethylpiperidine-3-carboxylate. The product was directly used in the next reaction without purification.
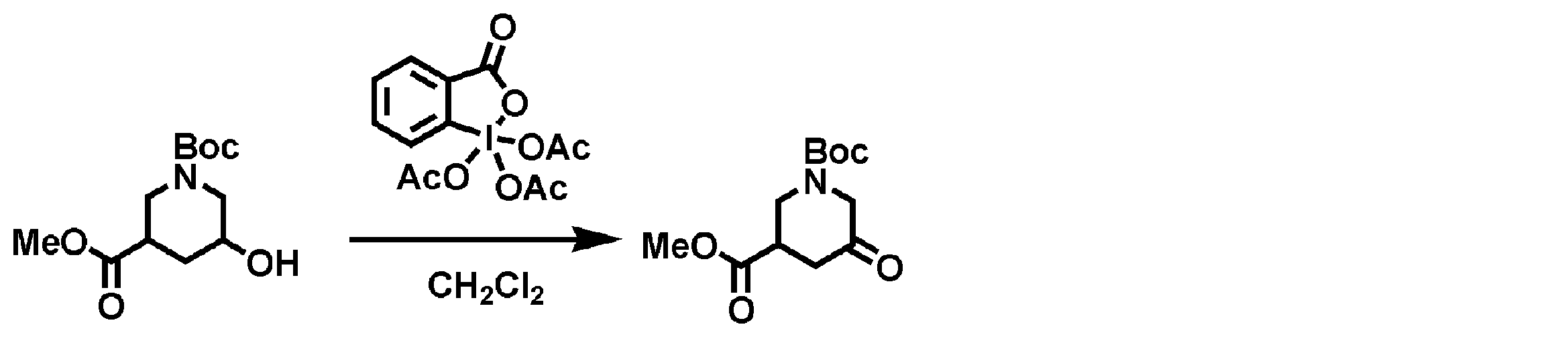
- Dess-Martin reagent (2.33 g) was added to a dichloromethane solution (25 mL) of 1-tert-butyl 3-methyl 5-hydroxypiperidine-1,3-dicarboxylate (1.30 g), and the mixture was stirred at room temperature for 3 hours. .
- a desmartin reagent (1.31 g) was further added to the reaction solution, and the mixture was stirred for 2.5 hours, and then a saturated aqueous sodium hydrogen carbonate solution (50 mL) was added to the reaction solution. Subsequently, 10% aqueous sodium thiosulfate solution (50 mL) was added to the reaction solution, and the organic layer was separated.
- Triethylamine (2.64 g) was added to a dichloromethane solution (40 mL) of methyl 6-methylpiperidine-3-carboxylate (3.90 g) obtained in Step 1, and Boc 2 O (5.68 g) was stirred at room temperature.
- Dichloromethane solution (5 mL) was added. After stirring at room temperature for 70 hours, the reaction solution was washed with 1 mol / L hydrochloric acid (100 mL), and the organic layer was dried over anhydrous sodium sulfate and filtered.
- Cis 1 H NMR (300 MHz, CDCl 3 ) ⁇ 1.13 (d, 3H), 1.46 (s, 9H), 1.50-1.95 (m, 4H), 2.30-2.45 (m, 1H), 2.80-3.00 (m, 1H), 3.69 (s, 3H), 4.15 (br, 1H), 4.40 (br, 1H).
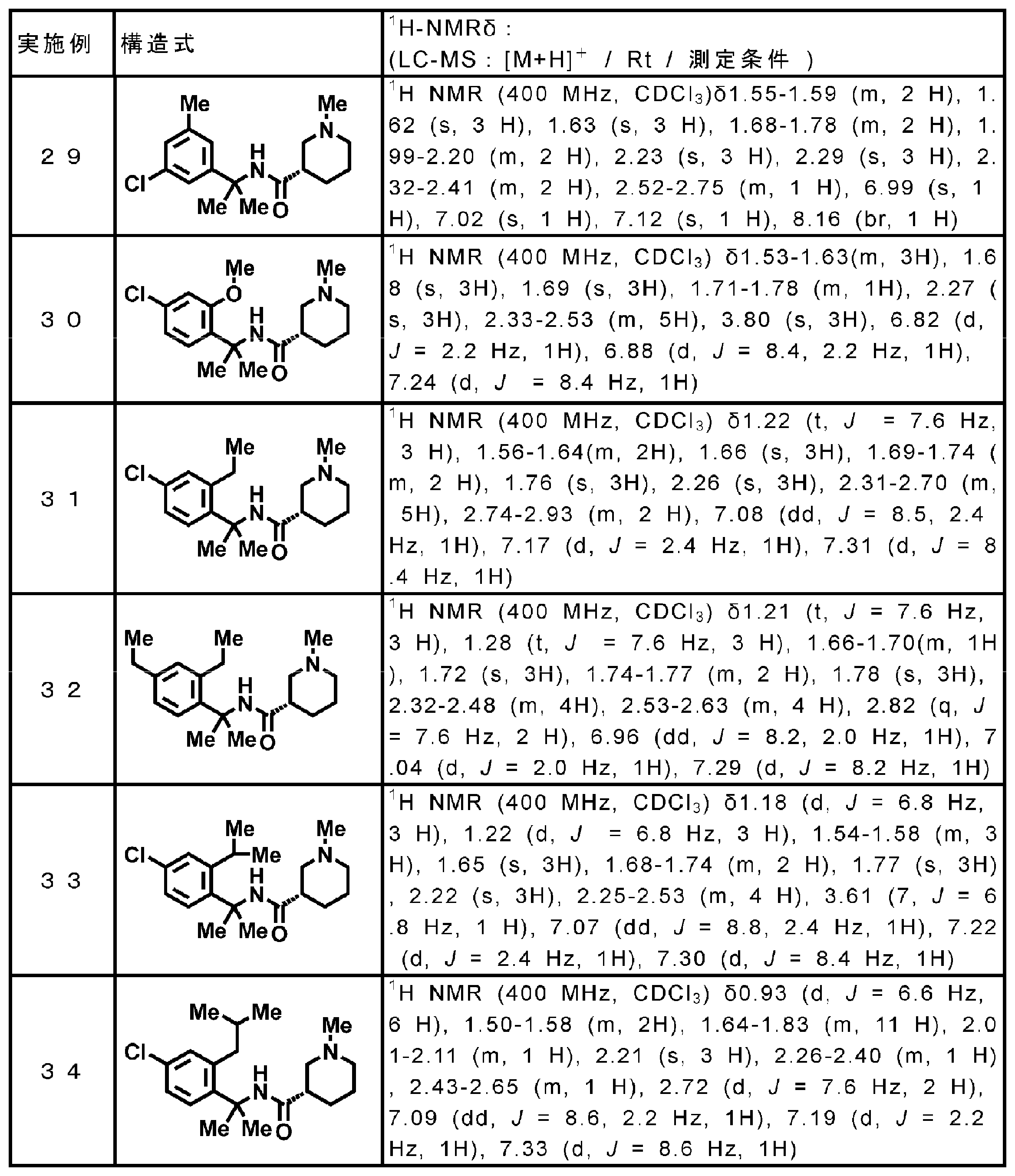
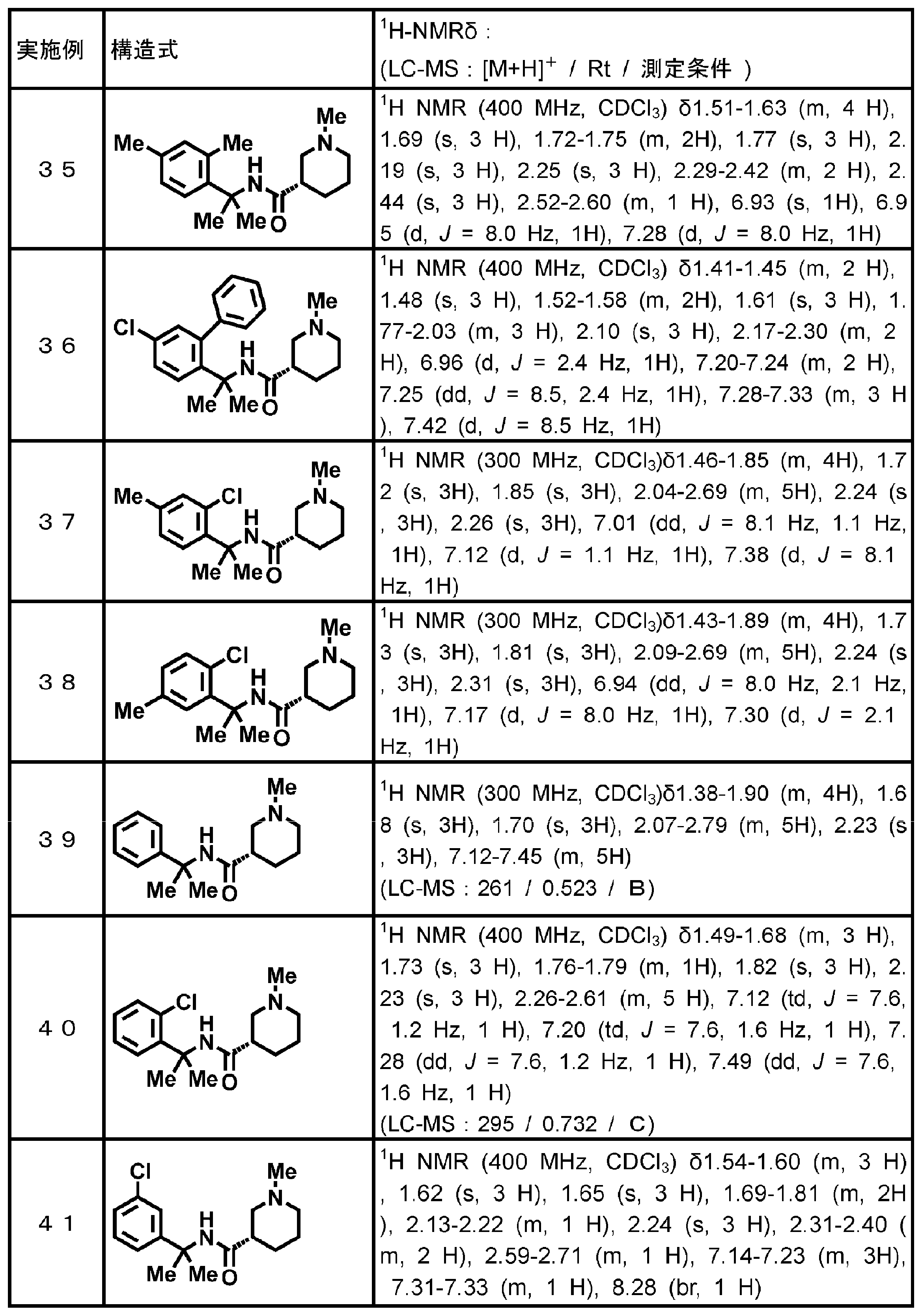
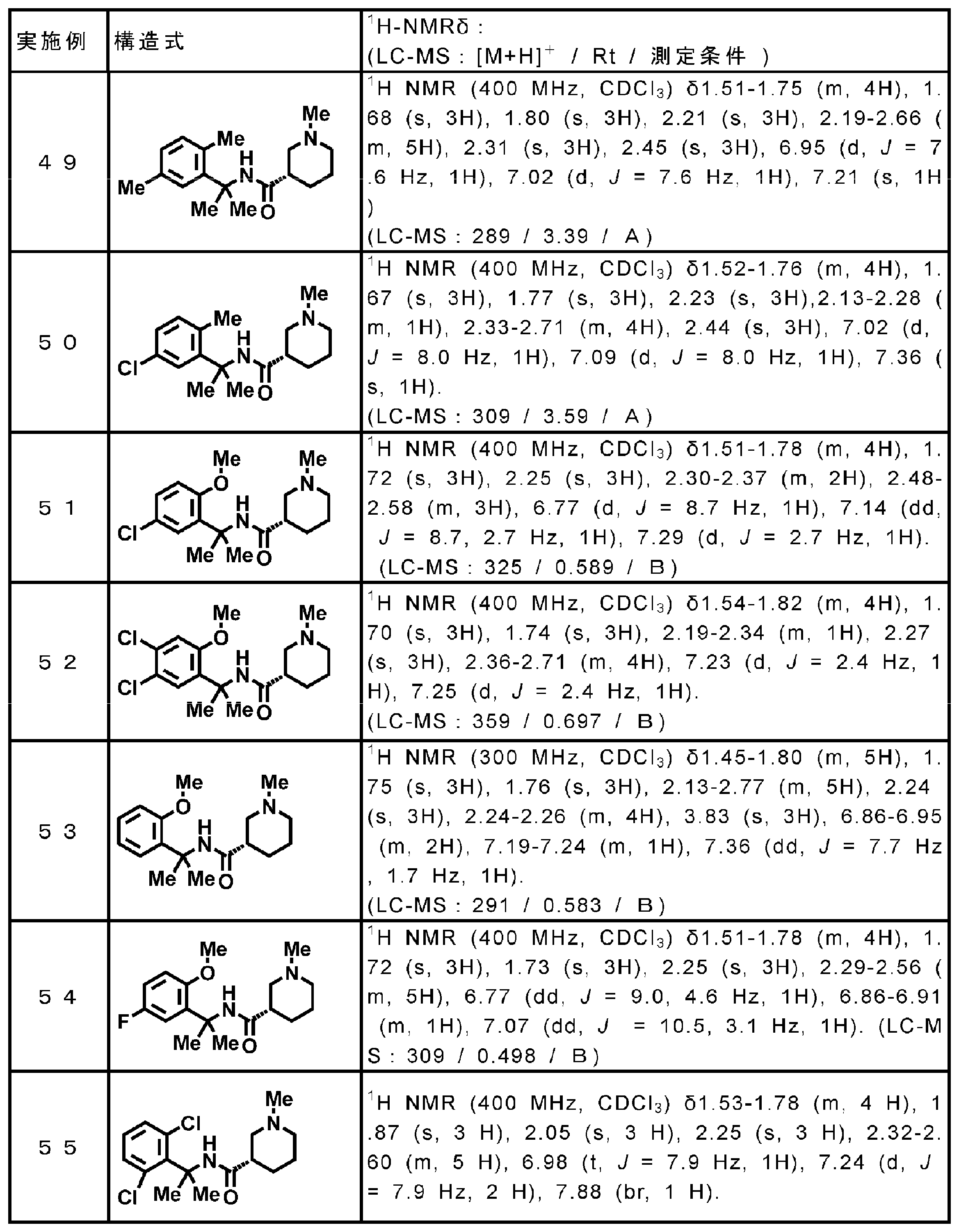
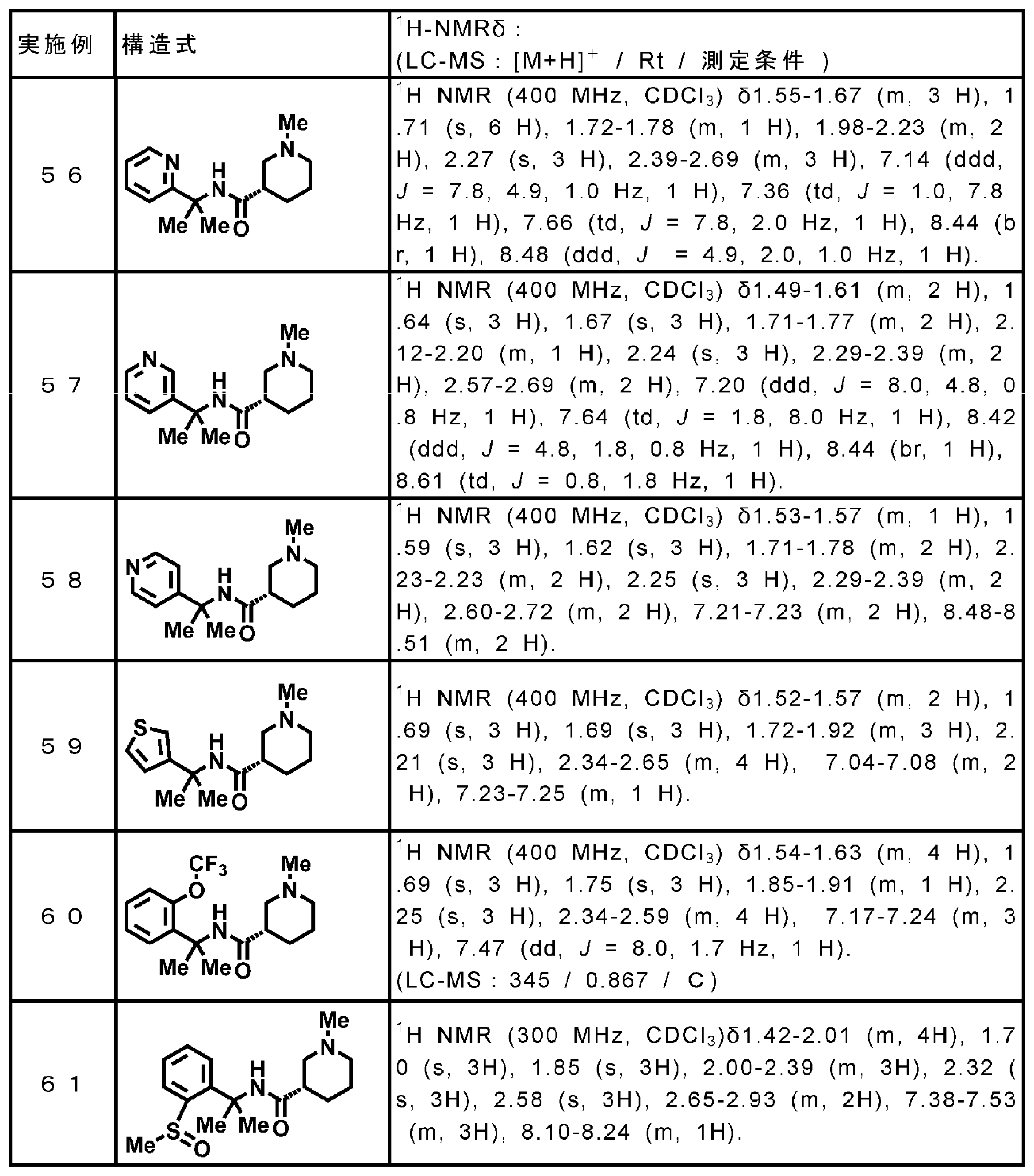
- Examples 111-122 Using the corresponding raw material carboxylic acid compound (commercial product) and raw material amine compound (commercial product), the reaction and treatment similar to the method performed in Example 110 were carried out following Reference Example 64. Tables 22-24 The compounds of Examples 111 to 122 shown below were obtained.
- Test Example 1 Agonist activity evaluation using cells stably expressing human-derived SSTR4 (human SSTR4 stably expressing cells) (1) Human SSTR4 stably expressing cells Human SSTR4 stably expressing cells were prepared and subjected to culture. Specifically, HEK293 cells, which are human kidney-derived cells, were used as host cells. A human SSTR4 stably expressing cell line was obtained by introducing pcDNA3.1 (cat. No. V79020, invitrogen, Carlsbad, CA, USA) into which a human SSTR gene was inserted into HEK293 cells. For selection, G418 (cat. No. 16513-84, Nacalai tesque, Japan) was used. A D-MEM medium (cat. No.
- test compound A DMSO solution was prepared using a test compound so as to have a concentration 1000 times the final concentration.
- the obtained DMSO solution was prepared with Hanks / 20 mmol / L Hepes / 0.1% BSA to a concentration 10 times the final concentration.
- the compounds of the present invention exhibited agonist activity in an evaluation test of agonist activity against SSTR4.
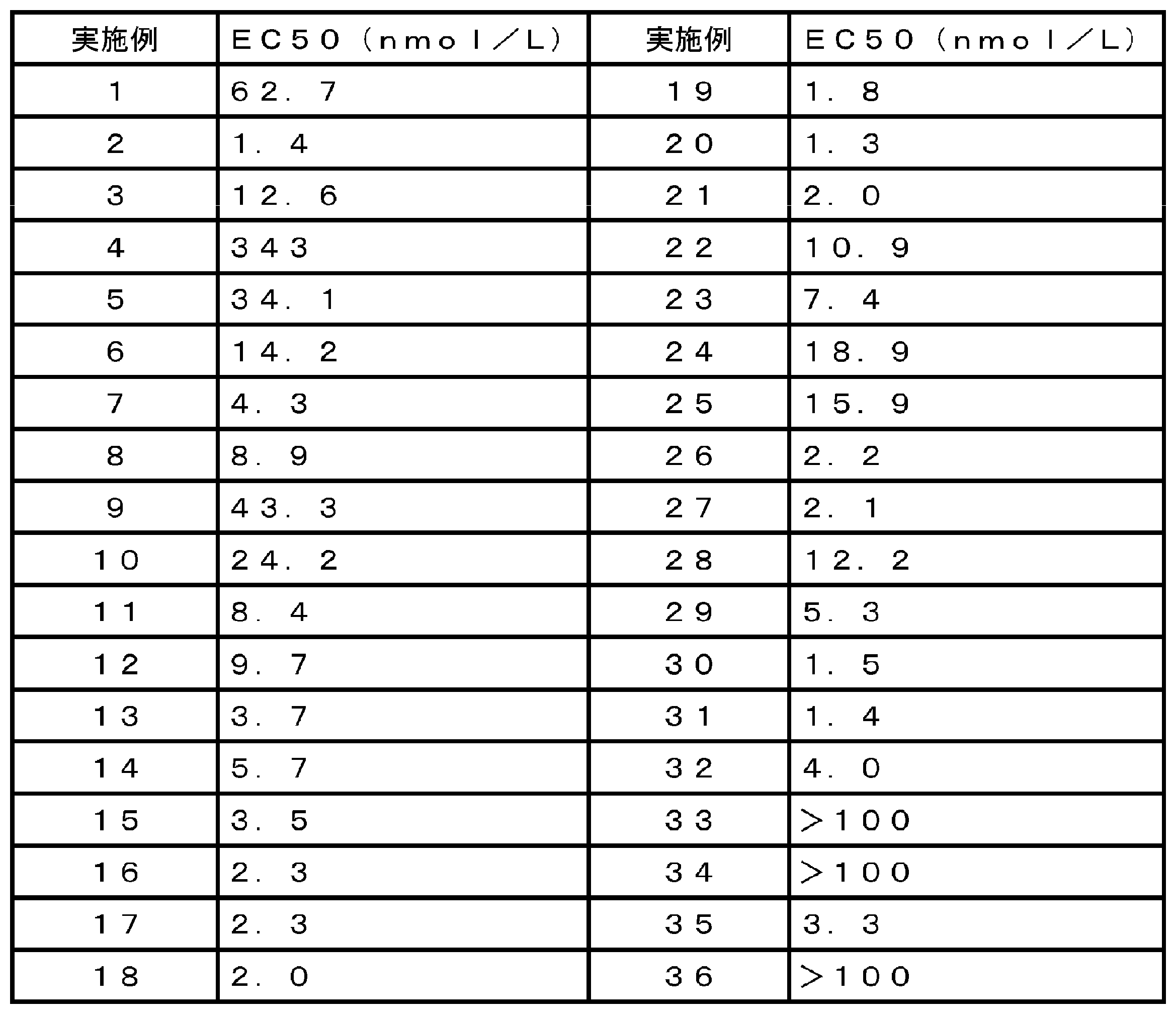
- Examples 2, 7, 13, 15, 16, 17, 18, 19, 20, 21, 26, 27, 30, 31, 37, 52, 67, 72, 76, 77, 81, 82, 85 The compounds obtained with 90, 91, 92, 108, 110, 115 and 116 showed stronger SSTR4 agonist activity compared to other compounds.
- the description “> 100” indicates that the EC50 value is a concentration higher than 100 nmol / L, and detailed numerical values are omitted. Test compounds with an EC50 of> 100 nmol / L were also confirmed to exhibit agonist activity.
- Y-maze test Evaluation of improvement of cognitive impairment using mouse Y-shaped maze test (hereinafter sometimes referred to as “Y-maze test”)
- Y-maze test In a Y-maze test using 25-35 g or 27-30 g Slc: ddY mice (male, SLC Japan), 0.6 mg / kg Scopolamine HBr (cat. No. S0929, Sigma Aldrich, USA) was used as a mouse.
- Subcutaneous administration causes memory impairment and decreases in spontaneous alternation rate. Therefore, the compound according to the present invention was pretreated by oral administration to mice, and the memory impairment improving effect was evaluated. As a result, the compound obtained in Example 2 was confirmed to have a significant memory impairment improving action at 1 or 3 mg / kg (oral).
- Example 21 (Hereinafter, the rate of alternation behavior in each group at the time of evaluation of Example 2 is shown. 0.5% MC administration group: 69.9 ⁇ 3.5, Scopolamine administration group: 43.9 ⁇ 1.9, 1 mg / kg administration) Group: 59.6 ⁇ 3.2, 3 mg / kg administration group: 65.0 ⁇ 1.8). Further, the compound obtained in Example 21 was confirmed to have a significant memory impairment improving effect at 1 or 3 mg / kg (oral). (Hereinafter, the alternation behavior rate in each group at the time of evaluation of Example 21 is shown. 0.5% MC administration group: 71.2 ⁇ 3.5, Scopolamine administration group: 47.5 ⁇ 2.6, 1 mg / kg administration) Group: 60.7 ⁇ 2.6, 3 mg / kg administration group: 64.6 ⁇ 2.2).
- Test Example 3 Evaluation of cognitive function using mouse novel object recognition test (hereinafter sometimes referred to as “mORT”) Reduced memory for known objects in mORT using 25-45g or 35-40g Slc: ddY mice (male, Japan SLC), depending on the time interval between first trial (training) and second trial (test) Is recognized. If the second trial is performed 24 hours after the first trial, significant forgetting is observed. Therefore, the compound according to the present invention was administered before the first trial, and the memory enhancing action in the second trial was evaluated. As a result, it was confirmed that the compound obtained in Example 2 had a memory enhancing effect at 3 mg / kg (oral).
- mORT mouse novel object recognition test
- the identification coefficient is shown as an index of cognitive function at the time of evaluation of Example 2: 0.5% MC administration group: 0.050 ⁇ 0.048, 3 mg / kg administration group: 0.216 ⁇ 0.053) Even in the compound obtained in Example 21, a significant memory enhancing action was confirmed at 3 mg / kg (oral).
- an identification coefficient is shown as an index of cognitive function at the time of evaluation in Example 21: 0.5% MC administration group: 0.014 ⁇ 0.034, 3 mg / kg administration group: 0.214 ⁇ 0.072) Even when the compound of Example 21 was administered after the first trial, a significant memory enhancing action was confirmed at 3 mg / kg (oral).
- a discrimination coefficient is shown as an index of cognitive function. 0.5% MC administration group: 0.054 ⁇ 0.026, 3 mg / kg administration group: 0.245 ⁇ 0.066)
- Test Example 4 Binding Affinity Evaluation Using Human SSTR4-expressing Cell Membrane
- Cell membranes were prepared from Chem-1 cells in which human SSTR4 was forcibly expressed using Hepes Buffer.
- a reaction solution consisting of the prepared cell membrane, 0.1 nmol / L [ 125 I] Tyr11-Somatostatin 14, and the test compound was prepared and incubated at 25 ° C. for 2 hours.
- the cell membrane after incubation was filtered and washed. After the filter was dried, it was immersed in a scintillator and the radioactivity was measured with a scintillation counter.
- the difference in radioactivity between the group not added with the test compound and the group added with 1 ⁇ mol / L Somatostatin 14 was taken as the specific binding amount, and the inhibition rate when the test compound was added was calculated.
- the Ki of the test compound was calculated from the IC50 of the test compound calculated from the inhibition curve, the concentration of [ 125 I] Tyr11-Somatostatin 14, and the Kd of Somatostatin 14.
- the Ki of SSTR4 of the compound obtained in Example 21 was 21 nmol / L.
- the Ki of the compound obtained in Example 21 was a value shown in Table 28 below. It was.
- Test Example 5 Examination of acetylcholine release enhancing action by microdialysis test using rats A guide cannula was placed in the hippocampus of Crlj: WI rats, and the probe was inserted after the animals recovered and microdialysis was performed. After administration of the compound according to the present invention, the perfusate was changed to a high potassium solution for 15 minutes to stimulate the hippocampus. The amount of acetylcholine in the perfusate was analyzed with an HPLC-ECD apparatus. As a result, in the compound obtained in Example 21, the amount of acetylcholine at the time of 60 minutes after administration was significantly increased at 10 mg / kg (oral) compared to the vehicle administration group.
- Test Example 6 Membrane transfer test of neprilysin using human neprilysin / human SSTR4 co-expressing cells SH-SY5Y cells stably expressing human neprilysin / human SSTR4 were seeded on a culture plate and incubated overnight at 37 ° C. in a 5% CO 2 incubator. The next day, the compound according to the present invention was added, and further incubated overnight at 37 ° C. in a 5% CO 2 incubator. The next day, 4% paraformaldehyde was added to fix the cells. Cells were washed and blocked with 3% BSA solution.
- Example 21 transferred neprilysin to the membrane in a concentration-dependent manner, and the EC50 was 9.3 nM.
- Test Example 7 Evaluation of cognitive function improving action and A ⁇ lowering action using Tg2576 mice Tg2576 mice that produce excessive A ⁇ in the brain show cognitive decline caused by A ⁇ .
- a 4-month-old Tg2576 mouse was mixed with the compound of the present invention for 4 months.
- mORT test was performed for cognitive function evaluation, and then the amount of A ⁇ in the brain was quantified by ELISA.
- the compound obtained in Example 21 showed a significant cognitive function improving action at 30 mg / kg / day.
- the identification coefficient is shown as an index of cognitive function evaluation. (Vehicle: 0.064 ⁇ 0.049, 30 mg / kg / day: 0.330 ⁇ 0.062).
- the compound of the present invention has superior pharmacokinetics, central migration, and exposure compared to the pyrrolidine derivative described in Patent Document 1. Confirmed that. Specifically, Test Example 8 shown below was performed.
- Test Example 8 Pharmacokinetic study using rodents (PK study) After the compound of the present invention was orally administered to a mouse at a dose of 10 mg / kg, plasma and brain were collected after 1 hour and after 4 hours, and the concentration of the compound administered using LC / MS / MS was measured. Carried out. Simultaneously, the protein binding rate in plasma and brain was measured by equilibrium dialysis, and the concentration of each non-binding type was calculated. In each of the compounds of Examples 7, 14, 15, 16, 17, 18, 20, 21, 27, 40, and 50, the brain-plasma drug concentration ratio after about 1 hour and 4 hours after administration was about 5 And showed good central migration.
- PK study Pharmacokinetic study using rodents
- the concentration of non-binding drug in the brain at 4 hours after administration exceeded the EC50 value by 10 times or more in the evaluation of agonist activity using cells stably expressing human SSTR4. From the above results, the compound of the present invention has superior pharmacokinetics, central transportability, and exposure compared to the pyrrolidine derivative described in Patent Document 1.
- the derivative represented by the formula (I), or a pharmaceutically acceptable salt thereof has a strong SSTR4 agonist activity, a disease related to the central nervous system and / or the peripheral nervous system, an endocrine disease, It is useful for the treatment of neurodegenerative diseases, diseases such as inflammation or pain, ophthalmic diseases and tumor diseases.
Abstract
Description
R1は、1~5個のフッ素原子で置換されていてもよいC1-4アルキルを示し、
nは、1~4の整数であり、
R2は、フッ素原子及びヒドロキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル、又は、水素原子を示し、
R3は、フッ素原子及びヒドロキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキルを示し、
ここで、nが1、3又は4であるとき、R3はR2と一緒になって、1個の-O-、-NR5-、-SO-又は-SO2-を含んでいてもよい3~6員の飽和環を形成していてもよく、上記飽和環は、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、ハロゲン、ヒドロキシ、シアノ、オキソ、CO2R6、及びCONR7R8からなる群から選択される1~5個の置換基で置換されていてもよく、nが2であるとき、R2及びR3は、一緒になって上記飽和環を形成せず、
R4a、R4b、R4c及びR4dは、それぞれ同一又は異なって、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、ハロゲン、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、ヒドロキシ及びシアノからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC6-14アリール;フッ素原子、ヒドロキシ及びC1-3アルコキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル;1~5個のフッ素原子で置換されていてもよいC1-3アルコキシ;水素原子;フッ素原子;ヒドロキシ;又はCO2R9を示し、ここで、nが2であるとき、R4a、R4b、R4c及びR4dは、水素原子であり、nが1、3又は4で、R4a、R4b、R4c及びR4dのいずれか2個以上が置換されていてもよいC1-4アルキルであるとき、2個以上の上記置換されていてもよいC1-4アルキルは、一緒になって4~7員の飽和環を形成してもよく、
Aは、C6-14アリール又は5~11員のヘテロアリールを示し、上記C6-14アリール及び上記5~11員のへテロアリールは、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、ハロゲン、C6-14アリール、C6-14アリールオキシ、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、ヒドロキシ、シアノ、ニトロ、CO2R10、CONR11R12、NR10COR11、NR10CONR11R12、SOR13、SO2R14、SO2NR11R12及びNR11R12からなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよく、ここで、nが3で、R2が水素原子で、R3がtert-ブチルであるとき、Aは置換基で置換されていないフェニルではなく、
R5は、水素原子、C1-4アルキル、C3-6シクロアルキル、CONR15R16、COR17又はCO2R18を示し、
R6及びR9は、同一又は異なって、水素原子又はC1-4アルキルを示し、
R7及びR8は、それぞれ同一又は異なって、水素原子、C1-4アルキル、C3-6シクロアルキルを示し、ここで、R7及びR8がC1-4アルキルであるとき、一緒になって3~6員の飽和複素環を形成してもよく、
R10は、水素原子、C1-4アルキル、C3-6シクロアルキル、又はC6-14アリールを示し、
R11及びR12は、それぞれ同一又は異なって、水素原子、C1-4アルキル、C3-6シクロアルキル又はC6-14アリールを示し、ここで、R11及びR12がC1-4アルキルであるとき、一緒になって3~6員の飽和複素環を形成してもよく、
R13は、C1-4アルキル、C3-6シクロアルキル又はC6-14アリールを示し、
R14は、ヒドロキシ、C1-4アルキル、C3-6シクロアルキル、C1-4アルコキシ、C6-14アリールオキシ又はC6-14アリールを示し、
R15及びR16は、それぞれ同一又は異なって、水素原子又はC1-4アルキルを示し、ここで、R15及びR16がC1-4アルキルであるとき、一緒になって3~6員の飽和複素環を形成してもよく、
R17は、水素原子、C1-4アルキル又はC3-6シクロアルキルを示し、
R18は、C1-4アルキル又はC3-6シクロアルキルを示す。]
で表される化合物又はその薬学上許容される塩;
下記式(I);
R1は、1~5個のフッ素原子で置換されていてもよいC1-4アルキルを示し、
nは、1~4の整数であり、
R2は、フッ素原子及びヒドロキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル、又は、水素原子を示し、
R3は、フッ素原子及びヒドロキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキルを示し、
ここで、nが1、3又は4であるとき、R3はR2と一緒になって、1個の-O-、-NR5-、-SO-又は-SO2-を含んでいてもよい3~6員の飽和環を形成していてもよく、上記飽和環は、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、ハロゲン、ヒドロキシ、シアノ、オキソ、CO2R6、及びCONR7R8からなる群から選択される1~5個の置換基で置換されていてもよく、nが2であるとき、R2及びR3は、一緒になって上記飽和環を形成せず、
R4a、R4b、R4c及びR4dは、それぞれ同一又は異なって、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、ハロゲン、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、ヒドロキシ及びシアノからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC6-14アリール;フッ素原子、ヒドロキシ及びC1-3アルコキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル;1~5個のフッ素原子で置換されていてもよいC1-3アルコキシ;水素原子;フッ素原子;ヒドロキシ;又はCO2R9を示し、ここで、nが2であるとき、R4a、R4b、R4c及びR4dは、水素原子であり、nが1、3又は4で、R4a、R4b、R4c及びR4dのいずれか2個以上が置換されていてもよいC1-4アルキルであるとき、2個以上の上記置換されていてもよいC1-4アルキルは、一緒になって4~7員の飽和環を形成してもよく、
Aは、C6-14アリール又は5~11員のヘテロアリールを示し、上記C6-14アリール及び上記5~11員のへテロアリールは、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、ハロゲン、C6-14アリール、C6-14アリールオキシ、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、ヒドロキシ、シアノ、ニトロ、CO2R10、CONR11R12、NR10COR11、NR10CONR11R12、SOR13、SO2R14、SO2NR11R12及びNR11R12からなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよく、ここで、nが3で、R2が水素原子で、R3がtert-ブチルであるとき、Aは置換基で置換されていないフェニルではなく、
R5は、水素原子、C1-4アルキル、C3-6シクロアルキル、CONR15R16、COR17又はCO2R18を示し、
R6及びR9は、同一又は異なって、水素原子又はC1-4アルキルを示し、
R7及びR8は、それぞれ同一又は異なって、水素原子、C1-4アルキル、C3-6シクロアルキルを示し、ここで、R7及びR8がC1-4アルキルであるとき、一緒になって3~6員の飽和複素環を形成してもよく、
R10は、水素原子、C1-4アルキル、C3-6シクロアルキル、又はC6-14アリールを示し、
R11及びR12は、それぞれ同一又は異なって、水素原子、C1-4アルキル、C3-6シクロアルキル又はC6-14アリールを示し、ここで、R11及びR12がC1-4アルキルであるとき、一緒になって3~6員の飽和複素環を形成してもよく、
R13は、C1-4アルキル、C3-6シクロアルキル又はC6-14アリールを示し、
R14は、ヒドロキシ、C1-4アルキル、C3-6シクロアルキル、C1-4アルコキシ、C6-14アリールオキシ又はC6-14アリールを示し、
R15及びR16は、それぞれ同一又は異なって、水素原子又はC1-4アルキルを示し、ここで、R15及びR16がC1-4アルキルであるとき、一緒になって3~6員の飽和複素環を形成してもよく、
R17は、水素原子、C1-4アルキル又はC3-6シクロアルキルを示し、
R18は、C1-4アルキル又はC3-6シクロアルキルを示す。]
で表される化合物又はその薬学上許容される塩;
但し以下の化合物を除く;
N-1-(4-メタンスルホニルフェニル)プロピル-1-メチルピペリジン-3-カルボキシアミド;
N-1-(4-ピロリジン-1-イルフェニル)エチル-1-メチルピペリジン-3-カルボキシアミド;
N-1-(2,4-ジメチルフェニル)エチル-1-メチルピペリジン-3-カルボキシアミド;
N-1-フェニルエチル-1-プロピル-3-(4-エチルフェニル)ピペリジン-5-カルボキシアミド;
[項2]
nが1又は3である、
項1又は項1-2に記載の化合物又はその薬学上許容される塩;
[項3]
nが3である、
項1又は項1-2に記載の化合物又はその薬学上許容される塩;
[項4]
R2及びR3が、それぞれ同一又は異なって、フッ素原子及びヒドロキシからなる群から選択される同一又は異なる1~5個の置換基で置換されてもよいC1-4アルキルであり、ここで、R2及びR3が一緒になって、1個の-O-又は-SO2-を含んでいてもよい3~6員の飽和環を形成してもよい、
項1~3及び項1-2のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項4-2]
R2及びR3が、以下の(1)又は(2)である、項4に記載の化合物又はその薬学上許容される塩:
(1)R2及びR3がC1-3アルキルである;
(2)R2及びR3が一緒になって、1若しくは2個のフッ素原子で置換されていてもよい、1個の-O-を含んでいてもよい3~6員の飽和環を形成する;
[項4-3]
R2及びR3がメチルである、項4に記載の化合物又はその薬学上許容される塩;
[項4-4]
R2が水素原子を表し、R3がトリフルオロメチル基を表す、項1~3及び項1-2のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項4-5]
R2及びR3が一緒になって、3~6員の飽和環、又は以下の式:
[項5]
AがC6-14アリールであり、上記C6-14アリールが、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、フッ素原子、塩素原子、臭素原子、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、シアノ、CO2R10、CONR11R12、SO2NR11R12及びNR11R12からなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよい、
項1~4、項1-2及び項4-2~項4-5のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項5-2]
Aが、フェニル又はナフチルであり、上記フェニル又はナフチルが、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、フッ素原子、塩素原子、臭素原子、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ及びC1-4アルキルチオからなる群から選択される同一又は異なる1~2個の置換基で置換されていてもよい、項5に記載の化合物又はその薬学上許容される塩;
[項5-3]
Aがフェニル又は1-ナフチルであり、上記フェニル又は1-ナフチルが、メチル基、エチル基、メトキシ基、トリフルオロメトキシ基、メチルチオ基、フッ素原子、塩素原子及び臭素原子からなる群から選択される同一又は異なる1~2個の置換基で置換されている、項5に記載の化合物又はその薬学上許容される塩;
[項5-4]
Aが1-ナフチルである、項5-3に記載の化合物又はその薬学上許容される塩;
[項5-5]
Aがフェニルであり、上記フェニルが、少なくとも1個の塩素原子又は臭素原子で置換されている、項5-3に記載の化合物又はその薬学上許容される塩;
[項6-0]
R1がC1-4アルキルである、
項1~5、項1-2、項4-2~項4-5及び項5-2~項5-5のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項6]
R1がC1-3アルキルである、
項1~5、項1-2、項4-2~項4-5及び項5-2~項5-5のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項7]
R4a及びR4bが、それぞれ同一又は異なって、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、ハロゲン、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、ヒドロキシ及びシアノからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC6-14アリール;フッ素原子、ヒドロキシ及びC1-3アルコキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル;1~5個のフッ素原子で置換されていてもよいC1-3アルコキシ;水素原子;フッ素原子;又はCO2R9であり、ここで、R4a及びR4bが置換されていてもよいC1-4アルキルであるとき、上記置換されていてもよいC1-4アルキルは一緒になって4~7員の飽和環を形成してもよく、
R4c及びR4dが、水素原子である、
項1~6、項1-2、項4-2~項4-5、項5-2~項5-5及び項6-0のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項8]
R1がC1-3アルキルであり、
R2及びR3がそれぞれ同一又は異なって、C1-4アルキルである、
項1~7、項1-2、項5-2~項5-5及び項6-0のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項9]
AがC6-14アリールであり、上記C6-14アリールは、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、フッ素原子、塩素原子、臭素原子、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ及びシアノからなる群から選択される同一又は異なる1~3個の置換基で置換されていていてもよい、
項1~8、項1-2、項4-2~項4-5及び項6-0のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項10]
nが3であるとき、
R4a及びR4bが、それぞれ同一又は異なって、ピペリジン環の2位、5位又は6位の置換基であって、ヒドロキシ及びC1-3アルコキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル又は水素原子であり、ここで、R4a及びR4bが、置換されていてもよいC1-4アルキルであるとき、上記C1-4アルキルは一緒になって4~7員の飽和環を形成してもよく、
R4c及びR4dが、水素原子であり、
ただし、R1の位置がピペリジン環の1位で、アミド基の位置がピペリジン環の3位である、
項3~9、項4-2~項4-5、項5-2~項5-5及び項6-0のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項11]
nが3であるとき、
R4aが、ピペリジン環の4位の置換基であって、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、ハロゲン、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、ヒドロキシ及びシアノからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC6-14アリール;又は水素原子であり、
R4b、R4c及びR4dが、水素原子であり、
ただし、R1の位置がピペリジン環の1位で、アミド基の位置がピペリジン環の3位である、
項3~9、項4-2~項4-5、項5-2~項5-5及び項6-0のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項11-2]
R4aが、ピペリジン環の4位の置換基であって、1~5個のフッ素原子で置換されていてもよいC1-3アルキル、ハロゲン、1~5個のフッ素原子で置換されていてもよいC1-3アルコキシ、C1-3アルキルチオ及びヒドロキシからなる群から選択される同一又は異なる1~3個の置換基で置換されていてもよいフェニル基であり、
R4b、R4c及びR4dが、水素原子である、
項11に記載の化合物又はその薬学上許容される塩;
[項12]
nが3であるとき、
R4aが、ピペリジン環の2位又は6位の置換基であって、フッ素原子、ヒドロキシ及びC1-3アルコキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル又は水素原子であり、
R4b、R4c及びR4dが、水素原子であり、
ただし、R1の位置がピペリジン環の1位で、アミド基の位置がピペリジン環の3位である、
項3~9、項4-2~項4-5、項5-2~項5-5及び項6-0のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項12-2]
R4aが、ピペリジン環の2位の置換基であって、C1-4アルキルであり、
R4b、R4c及びR4dが、水素原子である、項12に記載の化合物又はその薬学上許容される塩;
[項12-3]
R4aが、ピペリジン環の6位の置換基であって、ヒドロキシ又はC1-3アルコキシで置換されていてもよいC1-4アルキルであり、
R4b、R4c及びR4dが、水素原子である、項12に記載の化合物又はその薬学上許容される塩;
[項12-4]
R4aが、ピペリジン環の6位の置換基であって、ヒドロキシで置換されていてもよいC1-3アルキルであり、R4b、R4c及びR4dが、水素原子である、項12に記載の化合物又はその薬学上許容される塩;
[項12-5]
nが3であるとき、
R4a及びR4bがともに、ピペリジン環の6位の置換基であって、メチルであり、
R4c及びR4dが、水素原子であり、
ただし、R1の位置がピペリジン環の1位で、アミド基の位置がピペリジン環の3位である、
る、項3~9、項4-2~項4-5、項5-2~項5-5及び項6-0のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項13]
nが3であるとき、
R4aが、ピペリジン環の5位の置換基であって、フッ素原子、ヒドロキシ及びC1-3アルコキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル;1~5個のフッ素原子で置換されていてもよいC1-3アルコキシ;フッ素原子;又は水素原子であり、
R4b、R4c及びR4dが、水素原子であり、
ただし、R1の位置がピペリジン環の1位で、アミド基の位置がピペリジン環の3位である、
項3~9、項4-2~項4-5、項5-2~項5-5及び項6-0のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項13-2]
nが3であるとき、
R4aが、ピペリジン環の5位の置換基であって、C1-3アルキル、C1-3アルコキシ、フッ素原子又はヒドロキシであり、
R4b、R4c及びR4dが、水素原子であり、
ただし、R1の位置がピペリジン環の1位で、アミド基の位置がピペリジン環の3位である、項3~9、項4-2~項4-5、項5-2~項5-5及び項6-0のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項13-3]
R4aが、ピペリジン環の5位の置換基であって、メチル、メトキシ、フッ素原子又はヒドロキシであり、
R4b、R4c及びR4dが、水素原子である、項13-2に記載の化合物又はその薬学上許容される塩;
[項13-4]
nが3であるとき、
R4a及びR4bがともに、ピペリジン環の5位の置換基であって、フッ素原子又はメチルであり、
R4c及びR4dが、水素原子であり、
ただし、R1の位置がピペリジン環の1位で、アミド基の位置がピペリジン環の3位である、項3~9、項4-2~項4-5、項5-2~項5-5及び項6-0のいずれか一項に記載の化合物又はその薬学上許容される塩;
[項14]
R4a、R4b、R4c及びR4dが、水素原子である、
項1~13、項1-2、項4-2~項4-5、項5-2~項5-5及び項6-0のいずれか一項に記載の化合物又はその薬学上許容される塩;
以下の化合物から選択される、項1に記載の化合物又はその薬学上許容される塩;
(3S)-1-メチル-N-[2-(ナフタレン-1-イル)プロパン-2-イル]ピペリジン-3-カルボキシアミド(実施例2);
N-[1-(2,3-ジメチルフェニル)シクロプロピル]-1-メチルピペリジン-3-カルボキシアミド(実施例5);
N-[4-(3,5-ジクロロフェニル)テトラヒドロ-2H-ピラン-4-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例9);
(3S)-N-[2-(2,3-ジクロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例19);
(3S)-N-[2-(2,4-ジクロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例20);
(3S)-N-[2-(2,5-ジクロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例21);
(3S)-N-[2-(2,3-ジメチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例23);
(3S)-N-[2-(2-クロロ-3-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例26);
(3S)-N-[2-(3-クロロ-2-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例27);
(3S)-N-[2-(3-クロロ-5-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3―カルボキシアミド(実施例29);
(3S)-N-[2-(4-クロロ-2-メトキシフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例30);
(3S)-N-[2-(4-クロロ-2-エチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例31);
(3S)-N-[2-(2,4-ジエチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例32);
(3S)-N-[2-(2,4―ジメチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例35);
(3S)-N-[2-(2-クロロ-4-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例37);
(3S)-N-[2-(2-クロロ-5-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例38);
(3S)-N-[2-(2-クロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例40);
(3S)-N-[2-(2-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例43);
(3S)-N-[2-(3-クロロ-4-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例47);
N-[2-(4-クロロ-2-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例12);
(3S)-N-[2-(5-クロロ-2-メトキシフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例51);
(3S)-N-[2-(5-フルオロ-2-メトキシフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例54);
(3S)-N-[2-(2,6-ジクロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例55);
(3S)-N-{2-[2-(トリフルオロメトキシ)フェニル]プロパン-2-イル}-1-メチルピペリジン-3-カルボキシアミド(実施例60);
(3S)-N-{2-[2-(メチルスルファニル)フェニル]プロパン-2-イル}-1-メチルピペリジン-3-カルボキシアミド(実施例61);
(3S)-N-[2-(2-ブロモフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例67);
(3S)-N-[2-(2-クロロ-3-フルオロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例71);
(3S)-N-[2-(2-クロロ-4-フルオロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例72);
(3S)-N-[2-(2-クロロ-5-フルオロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例73);
(3S)-N-[2-(2-エチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例76);
(3S)-N-[2-(2-クロロフェニル)プロパン-2-イル]-1-エチルピペリジン-3-カルボキシアミド(実施例110);又は
(3S)-N-[2-(ナフタレン-1-イル)プロパン-2-イル]-1-(プロパン-2-イル)ピペリジン-3-カルボキシアミド(実施例115);
(3S)-N-[2-(5-クロロ-2-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド(実施例50);
項1~15、項1-2、項4-2~項4-5、項5-2~項5-5、項6-0、項11-2、項12-2~項12-5及び項13-2~項13-4のいずれか一項に記載の化合物又はその薬学上許容される塩を含有する医薬組成物;
[項17]
請求項1~15、項1-2、項4-2~項4-5、項5-2~項5-5、項6-0、項11-2、項12-2~項12-5及び項13-2~項13-4のいずれか一項に記載の化合物又はその薬学上許容される塩を含有する、ソマトスタチン受容体サブタイプ4の活性化剤;
[項18]
項1~15、項1-2、項4-2~項4-5、項5-2~項5-5、項6-0、項11-2、項12-2~項12-5及び項13-2~項13-4のいずれか一項に記載の化合物又はその薬学上許容される塩を有効成分として含有する、ソマトスタチン受容体サブタイプ4を活性化することによって治療又は予防が可能な疾患の治療剤又は予防剤;
[項19]
上記疾患が、癲癇、うつ病、行動障害、記憶障害、学習障害、注意欠陥障害、疼痛、神経変性疾患又は神経因性膀胱である、項18に記載の治療剤又は予防剤;
[項20]
上記疾患が、過増殖性障害、先端巨大症、黒色腫、乳がん、前立腺腺腫、前立腺がん、肺がん、腸がん又は皮膚がんである、項18に記載の治療剤又は予防剤;
[項21]
上記疾患が、関節炎、関節リウマチ又はリウマチ性脊椎炎である、項18に記載の治療剤又は予防剤;
[項22]
上記疾患が、乾癬、アトピー性皮膚炎又は喘息である、項18に記載の治療剤又は予防剤;
[項23]
上記疾患が、グレーブス病、炎症性腸疾患、腎症、糖尿病性血管障害、虚血性疾患又は良性前立腺肥大である、項18に記載の治療剤又は予防剤;
[項24]
上記疾患が、加齢性黄斑変性、緑内障又は糖尿病性網膜症である、項18に記載の治療剤又は予防剤;
[項25]
ソマトスタチン受容体サブタイプ4を活性化することによって治療又は予防が可能な疾患を治療又は予防するための、項1~15、項1-2、項4-2~項4-5、項5-2~項5-5、項6-0、項11-2、項12-2~項12-5及び項13-2~項13-4のいずれか一項に記載の化合物又はそれらの薬学上許容される塩の使用。
[項26]
ソマトスタチン受容体サブタイプ4を活性化することによって治療又は予防が可能な疾患の治療剤又は予防剤の製造における、項1~15、項1-2、項4-2~項4-5、項5-2~項5-5、項6-0、項11-2、項12-2~項12-5及び項13-2~項13-4のいずれか一項に記載の化合物又はその薬学上許容される塩の使用。
[項27]
項1~15、項1-2、項4-2~項4-5、項5-2~項5-5、項6-0、項11-2、項12-2~項12-5及び項13-2~項13-4のいずれか一項に記載の化合物又はその薬学上許容される塩の有効量を患者に投与することを含む、ソマトスタチン受容体サブタイプ4を活性化することによって治療又は予防が可能な疾患を治療又は予防する方法。
[項28]
ソマトスタチン受容体サブタイプ4を活性化することによって治療又は予防が可能な疾患を治療又は予防するための、項1~15、項1-2、項4-2~項4-5、項5-2~項5-5、項6-0、項11-2、項12-2~項12-5及び項13-2~項13-4のいずれか一項に記載の化合物又はその薬学上許容される塩。
[項29]
項1~15、項1-2、項4-2~項4-5、項5-2~項5-5、項6-0、項11-2、項12-2~項12-5及び項13-2~項13-4のいずれか一項に記載の化合物又はその薬学上許容される塩の有効量を投与することを含む、ソマトスタチン受容体サブタイプ4を活性化するための方法。
[項30]
ソマトスタチン受容体サブタイプ4を活性化するための、項1~15、項1-2、項4-2~項4-5、項5-2~項5-5、項6-0、項11-2、項12-2~項12-5及び項13-2~項13-4のいずれか一項に記載の化合物又はその薬学上許容される塩。
[項31]
項1~15、項1-2、項4-2~項4-5、項5-2~項5-5、項6-0、項11-2、項12-2~項12-5及び項13-2~項13-4のいずれか一項に記載の化合物又はその薬学上許容される塩を有効成分として含有する、癲癇、うつ病、行動障害、記憶障害、学習障害、注意欠陥障害、疼痛、神経変性疾患又は神経因性膀胱の治療剤又は予防剤;
[項32]
項1~15、項1-2、項4-2~項4-5、項5-2~項5-5、項6-0、項11-2、項12-2~項12-5及び項13-2~項13-4のいずれか一項に記載の化合物又はその薬学上許容される塩を有効成分として含有する、過増殖性障害、先端巨大症、黒色腫、乳がん、前立腺腺腫、前立腺がん、肺がん、腸がん又は皮膚がんの治療剤又は予防剤;
一般式(I)で表される化合物のいずれか1つ又は2つ以上の1Hを2H(D)に変換した重水素変換体も一般式(I)で表される化合物に包含される。
本発明には、式(I)で表される化合物又はその薬学上許容される塩の水和物、エタノール溶媒和物等の溶媒和物も一般式(I)で表される化合物に包含される。
R3はR2と一緒になって、3~6員の飽和環を形成していてもよい。上記飽和環は1~5個の置換基で置換されていてもよい。R2とR3とで形成される無置換の3~6員の飽和環として好ましくは、1個の-O-又は-SO2-を含んでいてもよい飽和環が挙げられ、より好ましくは1個の-O-を含んでいてもよい飽和環が挙げられ、さらに好ましくは3~6員のシクロアルキルが挙げられる。R2とR3とで形成される無置換の3~6員の飽和環としてもっとも好ましくは、シクロプロピル又はシクロへキシルが挙げられる。
[化合物A]
式(I)においてR1が、C1-3アルキルであり、
R2及びR3が、それぞれ同一又は異なって、フッ素原子及びヒドロキシからなる群から選択される同一又は異なる1~5個の置換基で置換されてもよいC1-4アルキルであり、ここで、R2及びR3が一緒になって、1個の-O-又は-SO2-を含んでいてもよい3~6員の飽和環を形成してもよく、
R4a及びR4bが、それぞれ同一又は異なって、置換可能な1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、ハロゲン、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、ヒドロキシ及びシアノからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC6-14アリール;フッ素原子、ヒドロキシ及びC1-3アルコキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル;1~5個のフッ素原子で置換されていてもよいC1-3アルコキシ;水素原子;フッ素原子;またはCO2R9であり、ここで、R4a及びR4bが置換されていてもよいC1-4アルキルであるとき、上記置換されていてもよいC1-4アルキルは一緒になって4~7員の飽和環を形成してもよく、
R4c及びR4dが、水素原子であり、
Aが、C6-14アリールであり、上記C6-14アリールが、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、フッ素原子、塩素原子、臭素原子、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、シアノ、CO2R10、CONR11R12、SO2NR11R12及びNR11R12からなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよく、
R9及びR10が、メチルであり、
R11及びR12が、それぞれ同一又は異なって、メチル又はエチルであるか、又はR11及びR12が一緒になってピロリジン環を形成し、
nが、2又は3であり、好ましくは3である、
化合物又はその薬学上許容される塩。
[化合物B]
式(I)においてR1が、C1-3アルキルであり、
R2及びR3が、それぞれ同一又は異なって、C1-4アルキルであり、
R4a及びR4bが、それぞれ同一又は異なって、フッ素原子、ヒドロキシ及びC1-3アルコキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル;1~5個のフッ素原子で置換されていてもよいC1-3アルコキシ;水素原子;又はフッ素原子であり、
R4c及びR4dが、水素原子であり、
Aが、C6-14アリールであり、上記C6-14アリールが、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、フッ素原子、塩素原子、臭素原子、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ及びシアノからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよく、
nが、3である、
化合物又はその薬学上許容される塩。
(3S)-1-メチル-N-[2-(ナフタレン-1-イル)プロパン-2-イル]ピペリジン-3-カルボキシアミド;
N-[1-(2,3-ジメチルフェニル)シクロプロピル]-1-メチルピペリジン-3-カルボキシアミド;
N-[4-(3,5-ジクロロフェニル)テトラヒドロ-2H-ピラン-4-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,3-ジクロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,4-ジクロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,5-ジクロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,3-ジメチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロ-3-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(3-クロロ-2-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(3-クロロ-5-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3―カルボキシアミド;
(3S)-N-[2-(4-クロロ-2-メトキシフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(4-クロロ-2-エチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,4-ジエチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,4―ジメチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロ-4-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロ-5-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(3-クロロ-4-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(5-クロロ-2-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(5-クロロ-2-メトキシフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(5-フルオロ-2-メトキシフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,6-ジクロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-{2-[2-(トリフルオロメトキシ)フェニル]プロパン-2-イル}-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-{2-[2-(メチルスルファニル)フェニル]プロパン-2-イル}-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-ブロモフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロ-3-フルオロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロ-4-フルオロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロ-5-フルオロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-エチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロフェニル)プロパン-2-イル]-1-エチルピペリジン-3-カルボキシアミド;及び
N-[2-(ナフタレン-1-イル)プロパン-2-イル]-1-(プロパン-2-イル)ピペリジン-3-カルボキシアミド、
からなる群から選択される化合物、それらのラセミ体若しくはそれらの光学活性体、又はそれらの薬学的に許容される塩が特に好ましい。
式(I)で表される本発明の化合物がカルボキシル基等の酸性官能基を有する場合、各種の塩基と塩を形成しうる。この場合の薬学的に許容される塩としては、ナトリウム塩及びカリウム塩等のアルカリ金属塩、カルシウム塩等のアルカリ土類金属塩、並びに、アンモニウム塩等が挙げられる。これらの塩は、式(I)で表される本発明の化合物を酸又は塩基と混合した後、再結晶等の常法によって得ることができる。
化合物a-5は、市販品として購入できるか、例えば、国際公開第2011/26917号、Tetrahedron, 2007, 63, 10486-10496、国際公開第2006/91697号、国際公開第2010/118207号、国際公開第2011/26904号、Journal of Medicinal Chemistry, 2006, 49, 942-946、国際公開第2012/36997号、Journal of American Chemical Society, 2011, 133, 2878-2880、Bioorganic and Medicinal Chemistry, 2009, 17, 5639-5647、European Journal of Medicinal Chemistry, 1999, 34, 363-380、国際公開第2004/58727号等に記載されている方法によって合成することができる。
本工程は、化合物a-1と化合物a-5との縮合反応を行うことで、化合物a-2を得る工程である。本反応は常法に従って行うことができる。例えば、この反応は化合物a-5を反応性誘導体(例えば、低級アルキルエステル、活性エステル、酸無水物、酸ハライド等)に変換し、化合物a-1と反応させることによって達成される。活性エステルの具体例としては、p-ニトロフェニルエステル、N-ヒドロキシコハク酸イミドエステル、ペンタフルオロフェニルエステル等が挙げられる。酸無水物の具体例としては、クロロ炭酸エチル、クロロ炭酸イソブチル、イソ吉草酸、ピバリン酸等との混合酸無水物が挙げられる。
本工程は、上記A-1工程で得られた化合物a-2のアミノ基の保護基P1を、脱保護することによって、化合物a-3を得る工程である。本工程はProtective Groups in Organic Synthesis(Theodora W. Greene, Peter G. M. Wuts著、John Wiley & Sons, Inc.発行、1999年)に記載されている方法等に準じて行うことができる。
本工程は、上記A-2工程で得られた化合物a-3のアミノ基を、例えば還元的アミノ化反応によってアルキル化することで、化合物a-4を得る工程である。本反応は常法に従って行うことができる。例えば、この反応は適当な溶媒中又は無溶媒下で、化合物a-3を各種ケトン又はアルデヒド等と、還元剤等を共存させて反応を行うことで達成される。還元剤等の具体例としては、水素化ホウ素ナトリウム、水素化リチウムアルミニウム、水素化トリアセトキシホウ素ナトリウム、シアノ水素化ホウ素ナトリウム等が挙げられる。溶媒の具体例としては、原料化合物の種類等に従って選択されるべきであるが、例えばジクロロメタン、クロロホルム、ジクロロエタン、THF、1,4-ジオキサン、DME、アセトニトリル、DMF、DMA、NMP、DMSO、酢酸、水、又はメタノール、エタノール、イソプロパノール及び2,2,2-トリフロオロエタノール等のアルコール類が挙げられる。上記溶媒は、単独又は混合溶媒として使用することができる。反応温度は、用いられる原料化合物及び試薬の種類等によって異なるが、通常-20℃~200℃、好ましくは0℃~100℃である。反応時間は、用いられる原料化合物の種類等によって異なるが、通常、30分~72時間、好ましくは約1時間~12時間である。
式(I)で表される本発明の化合物の中間体が、カルボキシル基を有する場合には、光学活性なアミン(例えば、1-フェニルエチルアミン等)を用いてアミドを形成させることによって、光学分割を行うこともできる。
検出機器:APIシリーズ用Agilent 1100シリーズ (applied Biosystems社製)
HPLC:API 150EX LC/MS system (applied Biosystems社製)
Column:YMC CombiScreen Hydrosphere C18 (S-5μM, 12nm, 4.6×50mm)
Solvent:A液:0.05% TFA/H2O、B液:0.05% TFA/MeOH
Gradient Condition:
0.0-6.0分;A/B=75:25~1:99(linear gradient)
Flow rate:3.5mL/分
UV:254nm
カラム温度:40℃
検出機器:Waters ACQUITY UPLC
Column:ACQUITY UPLC BEH C18 1.7μm 2.1×50mm column
Solvent:A液:0.05% HCOOH/H2O、B液:CH3CN
Gradient Condition:
0.0-1.3分;A/B=90:10~1:99(linear gradient)
1.3-1.5分;A/B=1:99
1.5-2分;A/B=90:10
Flow Rate:0.75mL/分
UV:220nm, 254nm
カラム温度:50℃
検出機器:Shimadzu LCMS-2020
Column:Phenomenex Kinetex 1.7μm C18 2.1mm×50mm
Solvent:A液:MeOH、B液:0.05% TFA/H2O
Gradient Condition:
0.0分;A/B= 30:70
0.0-1.90分;A/B=99:1
1.91-3.00分;A/B=30:70
Flow Rate:0.5mL/分
UV:220nm
カラム温度:40℃
2-(2-フルオロフェニル)プロパン-2-オール
2-(2-フルオロフェニル)プロパン-2-アミン
対応する原料化合物を用いて参考例2と同様に反応及び処理し、表1~表3に示す化合物を得た。
tert-ブチル(3S)-3-{[2-(2-フルオロフェニル)プロパン-2-イル]カルバモイル}ピペリジン-1-カルボキシレート
1-フェニル-N-(プロパン-2-イリデン)メタンアミン
N-ベンジル-2-メチルペント-4-エン-2-アミン
エチル 2-{[ベンジル(2-メチルペント-4-エン-2-イル)アミノ]メチル}プロプ-2-エノエート
エチル 1-ベンジル-6,6-ジメチル-1,2,5,6-テトラヒドロピリジン-3-カルボキシレート
1-(tert-ブトキシカルボニル)-6,6-ジメチルピペリジン-3-カルボン酸
エチル 1-ベンジル-6,6-ジメチル-1,2,5,6-テトラヒドロピリジン-3-カルボキシレート(584mg)のメタノール(20mL)溶液にマグネシウム(519mg)を加え、室温にて4時間攪拌した。反応液にマグネシウム(550mg)を追加し、さらに室温にて16時間攪拌した。その後、反応液に飽和塩化アンモニウム水溶液(100mL)を加えた。ジクロロメタン(160mL)で生成物を抽出し、得られた有機層を無水硫酸ナトリウムで乾燥し、ろ過した。得られたろ液を減圧濃縮して、エチル 1-ベンジル-6,6-ジメチルピペリジン-3-カルボキシレート(375mg)をオイルとして得た。精製は行わずにそのまま次の反応に用いた。
耐圧ガラス容器中に工程1で得られたエチル 1-ベンジル-6,6-ジメチルピペリジン-3-カルボキシレート(137mg)を加え、メタノール(5mL)に溶解した。20%水酸化パラジウム/炭素担体(68mg)を反応液に添加し、中圧水素雰囲気下(~0.40MPa)、室温にて16時間攪拌した。反応液をセライトでろ過し、ろ液を減圧濃縮して、エチル 6,6-ジメチルピペリジン-3-カルボキシレートを得た。精製は行わずにそのまま次の反応に用いた。
工程2で得られたエチル 6,6-ジメチルピペリジン-3-カルボキシレートのジクロロメタン(5mL)溶液に、トリエチルアミン(77μL)、Boc2O(120mg)を添加し、室温下5時間攪拌した。反応液を減圧濃縮して1-tert-ブチル 3-エチル 6,6-ジメチルピペリジン-1,3-ジカルボキシレートを得た。精製は行わずにそのまま次の反応に用いた。
1-tert-ブチル 3-エチル 6,6-ジメチルピペリジン-1,3-ジカルボキシレートのメタノール(2mL)溶液に、2mol/L 水酸化ナトリウム水溶液(2mL)を加えて70℃にて30分攪拌した。反応液を室温まで冷却した。その後、反応液に2mol/L 塩酸(5mL)を加えて中和し、ジクロロメタン(60mL)で生成物を抽出した。得られた有機層を無水硫酸ナトリウムで乾燥した後、ろ過及び減圧濃縮を行った。得られた残渣をシリカゲルカラムクロマトグラフィーで精製し(クロロホルム/メタノール=95/5)、1-(tert-ブトキシカルボニル)-6,6-ジメチルピペリジン-3-カルボン酸(100mg)をオイルとして得た。
1-tert-ブチル 3-メチル 4-{[トリフルオロメチル]スルフォニル}オキシ}-5,6-ジヒドロピリジン-1,3(2H)-ジカルボキシレート
1-tert-ブチル 3-メチル 4-フェニル-5,6-ジヒドロピリジン-1,3(2H)-ジカルボキシレート
トランス-1-(tert-ブトキシカルボニル)-4-フェニルピペリジン-3-カルボン酸
1-(tert-ブトキシカルボニル)-4-フェニル-1,2,5,6-テトラヒドロピリジン-3-カルボン酸
シス-1-(tert-ブトキシカルボニル)-4-フェニルピペリジン-3-カルボン酸
2-フェニルニコチン酸エチル
1-(tert-ブトキシカルボニル)-2-フェニルピペリジン-3-カルボン酸
2-フェニルニコチン酸エチル(3.41g)のエタノール溶液(30mL)にパラジウム/炭素(1.30g)、酢酸(24mL)を加え、中圧水素雰囲気下(0.40MPa)室温にて30時間攪拌した。反応液をセライトでろ過した。その後、ろ液を減圧濃縮して、エチル 2-フェニルピペリジン-3-カルボキシレートをオイルとして得た。
工程1で得られたエチル 2-フェニルピペリジン-3-カルボキシレートのテトラヒドロフラン溶液(15mL)に飽和水酸化ナトリウム水溶液(30mL)を加え、そこにBoc2O(3.60g)のテトラヒドロフラン溶液(15mL)を滴下した。反応液を室温にて2時間激しく攪拌した後に分液した。得られた有機層を飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥した。混合液をろ過後、ろ液を減圧濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィー(Rf:0.24、ヘキサン/酢酸エチル=5/95)で精製し、1-tert-ブチル 3-エチル 2-フェニルピペリジン-1,3-ジカルボキシレート(2.97g)を得た。
1-tert-ブチル 3-エチル 2-フェニルピペリジン-1,3-ジカルボキシレート(2.97g)のメタノール溶液(15mL)に2mol/L 水酸化ナトリウム水溶液(15mL)を加え70℃にて20分攪拌した。反応液を減圧濃縮後、2mol/L 塩酸(20mL)で中和した。クロロホルム(90mL)で生成物を抽出し、有機層を無水硫酸ナトリウムで乾燥し、ろ過した。その後、ろ液を減圧濃縮して、1-(tert-ブトキシカルボニル)-2-フェニルピペリジン-3-カルボン酸(2.76g)をアモルファスとして得た。
1-(tert-ブトキシカルボニル)-5-ヒドロキシピペリジン-3-カルボン酸
MS m/z 244 [M-H]
1-(tert-ブトキシカルボニル)-5-フルオロピペリジン-3-カルボン酸
1-(tert-ブトキシカルボニル)-5-ヒドロキシピペリジン-3-カルボン酸(259mg)のジクロロメタン溶液(3mL)にアルゴン雰囲気下、-78℃にてDBU(228mg)、XTalFluor-E(344mg)を攪拌下に添加した。そのまま反応液を30分攪拌した後、室温まで昇温し24時間攪拌した。反応液にジクロロメタン(30mL)を加え、飽和炭酸水素ナトリウム水溶液(50mL)及び0.2mol/L 塩酸(50mL)で洗浄した。得られた有機層を無水硫酸ナトリウムで乾燥、ろ過した。ろ液を減圧濃縮し、得られた残渣をシリカゲルカラムクロマトグラフィー(ヘキサン/酢酸エチル=97/3~76/24、Rf=0.59)で精製し、1-tert-ブチル 3-メチル 5-フルオロピペリジン-1,3-ジカルボキシレート(80mg)を得た。
1-tert-ブチル 3-メチル 5-フルオロピペリジン-1,3-ジカルボキシレート(80mg)のメタノール溶液(1mL)に2mol/L 水酸化ナトリウム水溶液(1mL)を加え、70℃にて6時間攪拌した。反応液に2mol/L 塩酸(5mL)を加えて中和後、ジクロロメタン(50mL)で生成物を抽出した。得られた有機層を無水硫酸ナトリウムで乾燥、ろ過後、ろ液を減圧濃縮して、1-(tert-ブトキシカルボニル)-5-フルオロピペリジン-3-カルボン酸(65mg)を固体として得た。
1-tert-ブチル 3-メチル 5-オキソピペリジン-1,3-ジカルボキシレート
1-tert-ブチル 3-メチル 5,5-ジフルオロピペリジン-1,3-ジカルボキシレート
1-(tert-ブトキシカルボニル)-5、5-ジフルオロピペリジン-3-カルボン酸
1-(tert-ブトキシカルボニル)-5-メトキシピペリジン-3-カルボン酸
シス-1-(tert-ブトキシカルボニル)-2-メチルピペリジン-3-カルボン酸
1-tert-ブチル 3-エチル-シス-2-メチルピペリジン-1,3-ジカルボキシレート
1-tert-ブチル 3-エチル-トランス-2-メチルピペリジン-1,3-ジカルボキシレート
トランス-1-(tert-ブトキシカルボニル)-2-メチルピペリジン-3-カルボン酸
1-(tert-ブトキシカルボニル)-5-メチルピペリジン-3-カルボン酸
1-tert-ブチル 3-メチル-シス-6-メチルピペリジン-1、3-ジカルボキシレート
2-メチルニコチン酸メチル(5.00g)のメタノール/酢酸溶液(40mL/50mL)にパラジウム/炭素(2.50g)を加え、中圧水素雰囲気下(0.35MPa)室温にて20時間攪拌した。反応液をセライトでろ過し、ろ液を減圧濃縮した。得られた残渣に飽和炭酸水素ナトリウム水溶液(150mL)、0.2mol/L 水酸化ナトリウム水溶液(50mL)を添加した。ジクロロメタン(150mL)、クロロホルム/メタノール(90mL/10mL)で生成物を抽出し、有機層を無水硫酸ナトリウムで乾燥し、ろ過した。その後、ろ液を減圧濃縮して、メチル 6-メチルピペリジン-3-カルボキシレート(3.90g)を得た。
工程1で得られたメチル 6-メチルピペリジン-3-カルボキシレート(3.90g)のジクロロメタン溶液(40mL)にトリエチルアミン(2.64g)を加え、室温攪拌下にBoc2O(5.68g)のジクロロメタン溶液(5mL)を添加した。室温にて70時間攪拌後、反応液を1mol/L 塩酸(100mL)で洗浄し、有機層を無水硫酸ナトリウムで乾燥し、ろ過した。ろ液を減圧濃縮することによって得られた残渣をシリカゲルカラムクロマトグラフィー(ヘキサン/酢酸エチル=100/0~13/87)で精製し、1-tert-ブチル 3-メチル-シス-6-メチルピペリジン-1、3-ジカルボキシレート(2.66g、低極性)、1-tert-ブチル 3-メチル-トランス-6-メチルピペリジン-1、3-ジカルボキシレート(1.39g、高極性)をそれぞれオイルとして得た。
トランス体: 1H NMR (300 MHz, CDCl3) δ1.14 (d, 3H), 1.30-1.40 (m, 1H), 1.46 (s, 9H), 1.72-1.96 (m, 2H), 1.96-2.06 (bd, 1H), 2.58 (br, 1H), 3.04-3.10 (m, 1H), 3.68 (s, 3H), 4.30-4.45 (m, 2H).
シス-1-(tert-ブトキシカルボニル)-6-メチルピペリジン-3-カルボン酸
トランス-1-(tert-ブトキシカルボニル)-6-メチルピペリジン-3-カルボン酸
6-ヒドロキシメチル-1-メチルピペリジン-3-カルボン酸メチル
6-メトキシカルボニルニコチン酸メチル(3.00g、15.4mmol)のメタノール(68mL)、THF(34mL)溶液に、塩化カルシウム(6.82g、61.5mmol)を加えた。その後、反応液を0℃まで冷却し、水素化ホウ素ナトリウム(1.46g、38.4mmol)を加え、0℃で7時間撹拌した。反応液に水(100mL)を加え、クロロホルム(100mL)で3回、生成物を抽出した。得られた有機層を水(100mL)で3回洗浄した。有機層を硫酸ナトリウムで乾燥した後に溶媒を減圧留去し、6-ヒドロキシメチルニコチン酸メチルの粗結晶(2.01g、粗収率78%)を得た。更なる精製はせずに次の反応に用いた。
6-ヒドロキシメチルニコチン酸メチル(1.16g、6.94mmol)のメタノール(16mL)、酢酸(20mL)溶液に、10%パラジウム/炭素(580mg)を加えた。その後、反応液を室温で4気圧(0.4MPa)の水素雰囲気下で12時間撹拌した。反応液をセライトでろ過し、溶媒を減圧留去することによってピペリジン誘導体を得た。更なる精製はせずに次の反応に用いた。200mLナスフラスコ中、上述の反応で得られたピペリジン誘導体のアセトニトリル(46mL)溶液に、37%ホルマリン水溶液(1.24mL)、トリアセトキシ水素化ホウ素ナトリウム(3.97g、18.7mmol)を加え、室温で30分間撹拌した。反応液に20%炭酸カリウム水溶液20mLを加え、クロロホルム/メタノール=9/1溶液(50mL)で6回生成物を抽出した。有機層を合わせて硫酸ナトリウムで乾燥した後に溶媒を減圧留去した。その後、得られた残渣をアミノシリカゲルカラムクロマトグラフィー(クロロホルム/メタノール=9/1)で精製し、結晶の6-ヒドロキシメチル-1-メチルピペリジン-3-カルボン酸メチル(1.02g、収率79%、2工程)を得た。
トランス-6-tert-ブチルジメチルシロキシメチル-1-メチルピペリジン-3-カルボン酸メチル
対応する原料のカルボン酸化合物(市販品又は参考例65~90で合成した化合物)及び原料のアミン化合物(市販品又は参考例2~63で合成した化合物)を用いて、参考例64に引き続き、実施例1で行った方法と同様に反応及び処理を行い、表4~21に示す実施例2~108の化合物を得た。
トランス-6-ヒドロキシメチル-1-メチル-N-[2-(ナフタレン-1-イル)プロパン-2-イル]ピペリジン-3-カルボキサミド
上述の反応で得られたカルボン酸誘導体のジメチルホルムアミド(0.5mL)溶液に、2-(ナフタレン-1-イル)プロパン-2-アミン塩酸塩(22.2mg、0.10mmol)、HATU(57.0mg、0.15mmol)を加え、室温で12時間撹拌した。反応液に0.1mol/L 水酸化ナトリウム水溶液(10mL)を加え、塩化メチレン(10mL)で5回生成物を抽出した。有機層を合わせて硫酸ナトリウムで乾燥した後に溶媒を減圧留去し、アミノシリカゲルカラムクロマトグラフィー(ヘキサン/酢酸エチル=1/9)で粗精製した。更なる精製は行わずそのまま次の反応に用いた。
上述の反応で得られたシリルエーテル誘導体のTHF(0.3mL)溶液に、1mol/L TBAFのTHF溶液(32μL)を加え、室温で4時間撹拌した。溶媒を減圧留去した後、アミノシリカゲルカラムクロマトグラフィー(クロロホルム/メタノール=95/5)で精製し、無色アモルファスの、トランス-6-ヒドロキシメチル-1-メチル-N-[2-(ナフタレン-1-イル)プロパン-2-イル]ピペリジン-3-カルボキサミド(15mg、収率44%、3工程)を得た。
(3S)-N-[2-(2-クロロフェニル)プロパン-2-イル]-1-エチルピペリジン-3-カルボキサアミド
(3S)-N-[2-(2-クロロフェニル)プロパン-2-イル]-ピペリジン-3-カルボキサアミド(100mg、0.36mmol)のジメチルホルムアミド(0.7mL)溶液に、炭酸カリウム(52mg、0.37mmol)、臭化エチル(78mg、0.71mmol)を加え、室温で5時間撹拌した。さらに反応液を60℃まで昇温し3時間撹拌した。反応液に水(5mL)を加え、酢酸エチル(4mL)、ヘキサン(2mL)の混合溶液で2回生成物を抽出した。有機層を合わせて硫酸ナトリウムで乾燥した後に溶媒を減圧留去した。得られた残渣をアミノシリカゲルカラムクロマトグラフィー(ヘキサン/クロロホルム=1/1)で精製し、白色結晶の(3S)-N-[2-(2-クロロフェニル)プロパン-2-イル]-1-エチルピペリジン-3-カルボキサアミド(76mg、収率69%)を得た。
対応する原料のカルボン酸化合物(市販品)及び原料のアミン化合物(市販品)を用いて、参考例64に引き続き、実施例110で行った方法と同様の反応及び処理を行い、表22~24に示す実施例111~122の化合物を得た。
以下に、本発明の代表的な化合物の薬理試験結果を示し、該化合物についての薬理作用を説明するが、本発明はこれらの試験例に限定されるものではない。
(1)ヒトSSTR4安定発現細胞
ヒトSSTR4安定発現細胞を作製し、培養に供した。具体的には、宿主細胞としてヒト腎臓由来細胞であるHEK293細胞を用いた。ヒトSSTR遺伝子を挿入したpcDNA3.1(cat. No. V79020, invitrogen, Carlsbad, CA,USA)をHEK293細胞に導入することによってヒトSSTR4安定発現細胞株を得た。選別にはG418(cat. No. 16513-84, Nacalai tesque, Japan)を用いた。
培地には10%FBS、200μg/mL G418を含むD-MEM培地(cat. No.11995,GIBCO, USA)を用い、225cm2フラスコ(cat. No. 11-006-010, Iwaki, Japan)にて培養を行った。
約80%コンフルエントな状態で、20倍希釈した0.25%Trypsin-EDTA(cat. No.35554-64, Nacalai tesque, Japan)処理にて細胞を回収した。回収した細胞は、Hanks Buffer(cat. No. 14065-056, invitrogen, Carlsbad, CA,USA)/20mM Hepes(cat. No.15630-080, invitrogen, Carlsbad, CA,USA)、及び0.1% BSA(cat. No.A7906, Sigma Aldrich, USA)からなる反応培地にて70000 cells/mLに調製した。回収した細胞にGα16,apoaequorinを一過的に導入し、約2000 cells/30μL/wellとなるように384wellプレート(cat. No.781090, Greiner, Germany)に播種した。細胞を播種した翌日に、セレンテラジンH(cat. No.S2011, Promega, USA)を終濃度0.5μmol/Lとなるように各wellに添加し(10μL/well)、プレートを遠心した。その後、4時間室温、遮光下で、プレートを静置した。
試験化合物を用いて終濃度の1000倍の濃度となるようにDMSO溶液を作製した。得られたDMSO溶液をHanks/20mmol/L Hepes/0.1% BSAにて終濃度の10倍の濃度となるように調製した。
SSTR4刺激による発光シグナルの検出にはFDSS7000(浜松ホトニクス社製、製品名)を用いた。細胞及び発光基質を添加したプレートに試験化合物の溶液を添加し、90秒間発光シグナルを測定して相対発光量(RLU)を算出した。ソマトスタチン1μmol/Lの溶液を用いたときの値を100%とし試験化合物のアゴニスト活性を評価した。評価結果を表25~27に示す。
25-35g又は27-30gのSlc:ddYマウス(雄性、日本エスエルシー)を用いたY―maze試験において、0.6mg/kgのScopolamine HBr(cat. No.S0929, Sigma Aldrich, USA)をマウスに皮下投与すると記憶障害が惹起され、自発交替行動率の低下が認められる。そこで本発明に係る化合物をマウスに経口投与することによって前処置し、記憶障害改善作用を評価した。その結果、実施例2で得られた化合物は、1又は3mg/kg(経口)において有意な記憶障害改善作用が確認された。(以下、実施例2評価時の各群における交替行動率を示す。0.5%MC投与群:69.9±3.5、Scopolamine投与群:43.9±1.9、1mg/kg投与群:59.6±3.2、3mg/kg投与群:65.0±1.8)。また、実施例21で得られた化合物においても1又は3mg/kg(経口)において有意な記憶障害改善作用が確認された。(以下、実施例21評価時の各群における交替行動率を示す。0.5%MC投与群:71.2±3.5、Scopolamine投与群:47.5±2.6、1mg/kg投与群:60.7±2.6、3mg/kg投与群:64.6±2.2)。
25-45g又は35-40gのSlc:ddYマウス(雄性、日本エスエルシー)を用いたmORTにおいて、第一試行(トレーニング)と第二試行(テスト)の間隔時間依存的に、既知物体に対する記憶低下が認められる。第一試行を行った24時間後に第二試行を行った場合、顕著な忘却が認められる。そこで本発明に係る化合物を第一試行前に投与し、第二試行における記憶増強作用を評価した。その結果、実施例2で得られた化合物は3mg/kg(経口)において記憶増強作用の傾向が確認された。(以下、実施例2評価時の認知機能の指標として識別係数を示す:0.5%MC投与群:0.050±0.048、3mg/kg投与群:0.216±0.053)また、実施例21で得られた化合物においても3mg/kg(経口)において有意な記憶増強作用が確認された。(以下、実施例21評価時の認知機能の指標として識別係数を示す:0.5%MC投与群:0.014±0.034、3mg/kg投与群:0.214±0.072)さらに、実施例21の化合物は、第1試行の後に投与した場合においても、3mg/kg(経口)において有意な記憶増強作用が確認された。(認知機能の指標として、識別係数を示す。0.5%MC投与群:0.054±0.026、3mg/kg投与群:0.245±0.066)
ヒトSSTR4を強制発現させたChem-1細胞からHepes Bufferを用いて細胞膜を調製した。調製後の細胞膜、0.1nmol/L [125I]Tyr11-Somatostatin 14、及び試験化合物からなる反応液を調製し、25℃で2時間インキュベートした。インキュベート後の細胞膜をフィルター処理し、洗浄を行った。フィルターを乾燥させた後、シンチレーターに浸し、放射活性をシンチレーションカウンターにて測定した。試験化合物非添加群と1μmol/L Somatostatin 14添加群の放射活性の差を特異的結合量とし、試験化合物を添加したときの阻害率を算出した。阻害曲線から算出した試験化合物のIC50、[125I] Tyr11-Somatostatin 14の濃度、Somatostatin 14のKdより試験化合物のKiを算出した。その結果、実施例21で得られた化合物のSSTR4のKiは21nmol/Lであった。また、各SSTR発現細胞膜を用いて、同様の方法でSSTR1、SSTR2、SSTR3、SSTR5に対する結合親和性を評価したところ、実施例21で得られた化合物のKiは以下の表28に示す値となった。
Crlj:WIラットの海馬にガイドカニューラを留置し、動物の回復後にプローブを挿入し、マイクロダイアリシスをおこなった。本発明に係る化合物を投与した後、15分間潅流液を高カリウム溶液に変更し、海馬に刺激を与えた。潅流液中のアセチルコリンの量をHPLC-ECD装置で解析した。その結果、実施例21で得られた化合物は10mg/kg(経口)において、投与後60分経過時のアセチルコリンの量を、Vehicle投与群と比較して有意に増加させた。
ヒトネプリライシン/ヒトSSTR4を安定発現したSH-SY5Y細胞を培養プレートに播種し、37℃、5%CO2インキュベーターで一晩インキュベートした。翌日、本発明に係る化合物を添加し、37℃、5%CO2インキュベーターでさらに一晩インキュベートした。翌日、4%パラホルムアルデヒドを添加し細胞を固定した。細胞を洗浄した後、3%BSA溶液でブロッキングした。その後、抗ネプリライシン抗体およびAlexa Fluor 488 donkey anti-mouse IgGで免疫染色を実施し、IN Cell Analyzerで解析を実施した。その結果、実施例21で得られた化合物は濃度依存的にネプリライシンを膜移行させ、EC50は9.3nMであった。
脳内において過剰なAβが産生されるTg2576マウスはAβに起因した認知機能低下を示す。4カ月齢のTg2576マウスに本発明に係る化合物を4カ月間混餌投与した。投与終了後、認知機能評価のためにmORT試験を実施し、その後、脳内Aβの量をELISAによって定量した。その結果、実施例21で得られた化合物は30mg/kg/dayにおいて有意な認知機能改善作用を示した。認知機能評価の指標として識別係数を示す。(Vehicle:0.064±0.049、30mg/kg/day:0.330±0.062)。また、100mg/kg/dayにおいてVehicle投与群と比較して有意な海馬Abeta42低下作用を示した。(Vehicle:283.99±27.89pmol/g、100mg/kg/day:198.11±26.32pmol/g)。
本発明の化合物をマウスに10mg/kgの用量で経口投与した後、1時間経過時、4時間経過時において血漿および脳を採取し、LC/MS/MSを用いて投与した化合物の濃度測定を実施した。同時に血漿、及び脳における蛋白結合率の測定を平衡透析法によって実施し、それぞれの非結合型の濃度を算出した。実施例7、14、15、16、17、18、20、21、27、40および50の化合物における投与後1時間経過時、4時間経過時における脳-血漿中薬物濃度比はいずれも約5であり、良好な中枢移行性を示した。また、投与後4時間経過時における脳内における非結合型の薬物濃度は、ヒトSSTR4安定発現細胞を用いたアゴニスト活性評価におけるEC50値を10倍以上も上回った。
以上の結果から、本発明の化合物は、特許文献1に記載のピロリジン誘導体と比較して優れた体内動態、中枢移行性、暴露量を有している。
Claims (25)
- 下記式(I):
R1は、1~5個のフッ素原子で置換されていてもよいC1-4アルキルを示し、
nは、1~4の整数であり、
R2は、フッ素原子及びヒドロキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル、又は、水素原子を示し、
R3は、フッ素原子及びヒドロキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキルを示し、
ここで、nが1、3又は4であるとき、R3はR2と一緒になって、1個の-O-、-NR5-、-SO-又は-SO2-を含んでいてもよい3~6員の飽和環を形成していてもよく、前記飽和環は、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、ハロゲン、ヒドロキシ、シアノ、オキソ、CO2R6、及びCONR7R8からなる群から選択される1~5個の置換基で置換されていてもよく、nが2であるとき、R2及びR3は、一緒になって前記飽和環を形成せず、
R4a、R4b、R4c及びR4dは、それぞれ同一又は異なって、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、ハロゲン、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、ヒドロキシ及びシアノからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC6-14アリール;フッ素原子、ヒドロキシ及びC1-3アルコキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル;1~5個のフッ素原子で置換されていてもよいC1-3アルコキシ;水素原子;フッ素原子;ヒドロキシ;又はCO2R9を示し、ここで、nが2であるとき、R4a、R4b、R4c及びR4dは、水素原子であり、nが1、3又は4で、R4a、R4b、R4c及びR4dのいずれか2個以上が置換されていてもよいC1-4アルキルであるとき、2個以上の前記置換されていてもよいC1-4アルキルは、一緒になって4~7員の飽和環を形成してもよく、
Aは、C6-14アリール又は5~11員のヘテロアリールを示し、前記C6-14アリール及び前記5~11員のへテロアリールは、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、ハロゲン、C6-14アリール、C6-14アリールオキシ、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、ヒドロキシ、シアノ、ニトロ、CO2R10、CONR11R12、NR10COR11、NR10CONR11R12、SOR13、SO2R14、SO2NR11R12及びNR11R12からなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよく、ここで、nが3で、R2が水素原子で、R3がtert-ブチルであるとき、Aは置換基で置換されていないフェニルではなく、
R5は、水素原子、C1-4アルキル、C3-6シクロアルキル、CONR15R16、COR17又はCO2R18を示し、
R6及びR9は、同一又は異なって、水素原子又はC1-4アルキルを示し、
R7及びR8は、それぞれ同一又は異なって、水素原子、C1-4アルキル、C3-6シクロアルキルを示し、ここで、R7及びR8がC1-4アルキルであるとき、一緒になって3~6員の飽和複素環を形成してもよく、
R10は、水素原子、C1-4アルキル、C3-6シクロアルキル、又はC6-14アリールを示し、
R11及びR12は、それぞれ同一又は異なって、水素原子、C1-4アルキル、C3-6シクロアルキル又はC6-14アリールを示し、ここで、R11及びR12がC1-4アルキルであるとき、一緒になって3~6員の飽和複素環を形成してもよく、
R13は、C1-4アルキル、C3-6シクロアルキル又はC6-14アリールを示し、
R14は、ヒドロキシ、C1-4アルキル、C3-6シクロアルキル、C1-4アルコキシ、C6-14アリールオキシ又はC6-14アリールを示し、
R15及びR16は、それぞれ同一又は異なって、水素原子又はC1-4アルキルを示し、ここで、R15及びR16がC1-4アルキルであるとき、一緒になって3~6員の飽和複素環を形成してもよく、
R17は、水素原子、C1-4アルキル又はC3-6シクロアルキルを示し、
R18は、C1-4アルキル又はC3-6シクロアルキルを示す。]
で表される化合物又はその薬学上許容される塩。 - nが1又は3である、
請求項1に記載の化合物又はその薬学上許容される塩。 - nが3である、
請求項1に記載の化合物又はその薬学上許容される塩。 - R2及びR3が、それぞれ同一又は異なって、フッ素原子及びヒドロキシからなる群から選択される同一又は異なる1~5個の置換基で置換されてもよいC1-4アルキルであり、ここで、R2及びR3が一緒になって、1個の-O-又は-SO2-を含んでいてもよい3~6員の飽和環を形成してもよい、
請求項1~3のいずれか一項に記載の化合物又はその薬学上許容される塩。 - AがC6-14アリールであり、前記C6-14アリールが、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、フッ素原子、塩素原子、臭素原子、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、シアノ、CO2R10、CONR11R12、SO2NR11R12及びNR11R12からなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよい、
請求項1~4のいずれか一項に記載の化合物又はその薬学上許容される塩。 - R1がC1-3アルキルである、
請求項1~5のいずれか一項に記載の化合物又はその薬学上許容される塩。 - R4a及びR4bが、それぞれ同一又は異なって、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、ハロゲン、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、ヒドロキシ及びシアノからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC6-14アリール;フッ素原子、ヒドロキシ及びC1-3アルコキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル;1~5個のフッ素原子で置換されていてもよいC1-3アルコキシ;水素原子;フッ素原子;又はCO2R9であり、ここで、R4a及びR4bが置換されていてもよいC1-4アルキルであるとき、前記置換されていてもよいC1-4アルキルは一緒になって4~7員の飽和環を形成してもよく、
R4c及びR4dが、水素原子である、
請求項1~6のいずれか一項に記載の化合物又はその薬学上許容される塩。 - R1がC1-3アルキルであり、
R2及びR3がそれぞれ同一又は異なって、C1-4アルキルである、
請求項1~7のいずれか一項に記載の化合物又はその薬学上許容される塩。 - AがC6-14アリールであり、前記C6-14アリールは、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、フッ素原子、塩素原子、臭素原子、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ及びシアノからなる群から選択される同一又は異なる1~3個の置換基で置換されていていてもよい、
請求項1~8のいずれか一項に記載の化合物又はその薬学上許容される塩。 - nが3であるとき、
R4a及びR4bが、それぞれ同一又は異なって、ピペリジン環の2位、5位又は6位の置換基であって、ヒドロキシ及びC1-3アルコキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル又は水素原子であり、ここで、R4a及びR4bが、置換されていてもよいC1-4アルキルであるとき、前記C1-4アルキルは一緒になって4~7員の飽和環を形成してもよく、
R4c及びR4dが、水素原子であり、
ただし、R1の位置がピペリジン環の1位で、アミド基の位置がピペリジン環の3位である、
請求項3~9のいずれか一項に記載の化合物又はその薬学上許容される塩。 - nが3であるとき、
R4aが、ピペリジン環の4位の置換基であって、1~5個のフッ素原子で置換されていてもよいC1-4アルキル、C3-6シクロアルキル、ハロゲン、1~5個のフッ素原子で置換されていてもよいC1-4アルコキシ、C1-4アルキルチオ、ヒドロキシ及びシアノからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC6-14アリール;又は水素原子であり、
R4b、R4c及びR4dが、水素原子であり、
ただし、R1の位置がピペリジン環の1位で、アミド基の位置がピペリジン環の3位である、
請求項3~9のいずれか一項に記載の化合物又はその薬学上許容される塩。 - nが3であるとき、
R4aが、ピペリジン環の2位又は6位の置換基であって、フッ素原子、ヒドロキシ及びC1-3アルコキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル又は水素原子であり、
R4b、R4c及びR4dが、水素原子であり、
ただし、R1の位置がピペリジン環の1位で、アミド基の位置がピペリジン環の3位である、
請求項3~9のいずれか一項に記載の化合物又はその薬学上許容される塩。 - nが3であるとき、
R4aが、ピペリジン環の5位の置換基であって、フッ素原子、ヒドロキシ及びC1-3アルコキシからなる群から選択される同一又は異なる1~5個の置換基で置換されていてもよいC1-4アルキル;1~5個のフッ素原子で置換されていてもよいC1-3アルコキシ;フッ素原子;又は水素原子であり、
R4b、R4c及びR4dが、水素原子であり、
ただし、R1の位置がピペリジン環の1位で、アミド基の位置がピペリジン環の3位である、
請求項3~9のいずれか一項に記載の化合物又はその薬学上許容される塩。 - R4a、R4b、R4c及びR4dが、水素原子である、
請求項1~13のいずれか一項に記載の化合物又はその薬学上許容される塩。 - 以下の化合物から選択される、請求項1に記載の化合物又はその薬学上許容される塩;
(3S)-1-メチル-N-[2-(ナフタレン-1-イル)プロパン-2-イル]ピペリジン-3-カルボキシアミド;
N-[1-(2,3-ジメチルフェニル)シクロプロピル]-1-メチルピペリジン-3-カルボキシアミド;
N-[4-(3,5-ジクロロフェニル)テトラヒドロ-2H-ピラン-4-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,3-ジクロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,4-ジクロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,5-ジクロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,3-ジメチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロ-3-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(3-クロロ-2-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(3-クロロ-5-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3―カルボキシアミド;
(3S)-N-[2-(4-クロロ-2-メトキシフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(4-クロロ-2-エチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,4-ジエチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,4―ジメチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロ-4-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロ-5-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(3-クロロ-4-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
N-[2-(4-クロロ-2-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(5-クロロ-2-メトキシフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(5-フルオロ-2-メトキシフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2,6-ジクロロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-{2-[2-(トリフルオロメトキシ)フェニル]プロパン-2-イル}-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-{2-[2-(メチルスルファニル)フェニル]プロパン-2-イル}-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-ブロモフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロ-3-フルオロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロ-4-フルオロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロ-5-フルオロフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-エチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド;
(3S)-N-[2-(2-クロロフェニル)プロパン-2-イル]-1-エチルピペリジン-3-カルボキシアミド;又は
(3S)-N-[2-(ナフタレン-1-イル)プロパン-2-イル]-1-(プロパン-2-イル)ピペリジン-3-カルボキシアミド;又は
(3S)-N-[2-(5-クロロ-2-メチルフェニル)プロパン-2-イル]-1-メチルピペリジン-3-カルボキシアミド。 - 請求項1~15のいずれか一項に記載の化合物又はその薬学上許容される塩を含有する医薬組成物。
- 請求項1~15のいずれか一項に記載の化合物又はその薬学上許容される塩を含有する、ソマトスタチン受容体サブタイプ4の活性化剤。
- 請求項1~15のいずれか一項に記載の化合物又はその薬学上許容される塩を有効成分として含有する、ソマトスタチン受容体サブタイプ4を活性化することによって治療又は予防が可能な疾患の治療剤又は予防剤。
- 前記疾患が、癲癇、うつ病、行動障害、記憶障害、学習障害、注意欠陥障害、疼痛、神経変性疾患又は神経因性膀胱である、請求項18に記載の治療剤又は予防剤。
- 前記疾患が、過増殖性障害、先端巨大症、黒色腫、乳がん、前立腺腺腫、前立腺がん、肺がん、腸がん又は皮膚がんである、請求項18に記載の治療剤又は予防剤。
- 前記疾患が、関節炎、関節リウマチ又はリウマチ性脊椎炎である、請求項18に記載の治療剤又は予防剤。
- 前記疾患が、乾癬、アトピー性皮膚炎又は喘息である、請求項18に記載の治療剤又は予防剤。
- 前記疾患が、グレーブス病、炎症性腸疾患、腎症、糖尿病性血管障害、虚血性疾患又は良性前立腺肥大である、請求項18に記載の治療剤又は予防剤。
- 前記疾患が、加齢性黄斑変性、緑内障又は糖尿病性網膜症である、請求項18に記載の治療剤又は予防剤。
- ソマトスタチン受容体サブタイプ4を活性化することによって治療又は予防が可能な疾患を治療又は予防するための、請求項1~15のいずれか一項に記載の化合物又はそれらの薬学上許容される塩の使用。
Priority Applications (6)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US15/021,231 US20160221948A1 (en) | 2013-09-12 | 2014-09-12 | Nitrogen-containing saturated heterocyclic compound |
| CN201480049801.5A CN105764887A (zh) | 2013-09-12 | 2014-09-12 | 含氮饱和杂环化合物 |
| CA2923804A CA2923804A1 (en) | 2013-09-12 | 2014-09-12 | Nitrogen-containing saturated heterocyclic compound |
| JP2015536649A JPWO2015037716A1 (ja) | 2013-09-12 | 2014-09-12 | 含窒素飽和複素環化合物 |
| EP14843405.3A EP3045448A4 (en) | 2013-09-12 | 2014-09-12 | Nitrogen-containing saturated heterocyclic compound |
| HK16112132.6A HK1223927A1 (zh) | 2013-09-12 | 2016-10-20 | 含氮飽和雜環化合物 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013189577 | 2013-09-12 | ||
| JP2013-189577 | 2013-09-12 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2015037716A1 true WO2015037716A1 (ja) | 2015-03-19 |
Family
ID=52665812
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2014/074283 WO2015037716A1 (ja) | 2013-09-12 | 2014-09-12 | 含窒素飽和複素環化合物 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20160221948A1 (ja) |
| EP (1) | EP3045448A4 (ja) |
| JP (1) | JPWO2015037716A1 (ja) |
| CN (1) | CN105764887A (ja) |
| CA (1) | CA2923804A1 (ja) |
| HK (1) | HK1223927A1 (ja) |
| WO (1) | WO2015037716A1 (ja) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IL276998B2 (en) | 2018-03-01 | 2024-02-01 | Takeda Pharmaceuticals Co | Piperidinyl-3-(aryloxy)propanamides and propanoates |
| TW202146403A (zh) * | 2020-05-21 | 2021-12-16 | 大陸商廣州費米子科技有限責任公司 | 含氮飽和雜環化合物及其製備方法、藥物組合物和應用 |
Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1997043278A1 (en) | 1996-05-14 | 1997-11-20 | Novo Nordisk A/S | Somatostatin agonists and antagonists |
| WO1999019301A1 (fr) | 1997-10-14 | 1999-04-22 | Yoshitomi Pharmaceutical Industries, Ltd. | Composes de piperazine et utilisation medicale desdits composes |
| WO2004058727A1 (en) | 2002-12-20 | 2004-07-15 | Bayer Pharmaceuticals Corporation | Substituted 3,5-dihydro-4h-imidazol-4-ones for the treatment of obesity |
| WO2006091697A1 (en) | 2005-02-23 | 2006-08-31 | Psychenomics, Inc. | Dopamine transporter inhibitors for use in treatment of movement disorders and other cns indications |
| WO2010059922A1 (en) | 2008-11-21 | 2010-05-27 | Ligand Pharmaceuticals Incorporated | Pyrrolidine carboxamide compounds |
| WO2010118207A1 (en) | 2009-04-09 | 2010-10-14 | Schering Corporation | Pyrazolo [1, 5-a] pyrimidine derivatives as mtor inhibitors |
| WO2011026904A1 (en) | 2009-09-04 | 2011-03-10 | Novartis Ag | Pyrazinylpyridines useful for the treatment of proliferative diseases |
| WO2011026917A1 (en) | 2009-09-04 | 2011-03-10 | Novartis Ag | Heteroaryl compounds as kinase inhibitors |
| WO2011047165A1 (en) | 2009-10-16 | 2011-04-21 | Southern Illinois University Edwardsville | Methods for treating memory impairment |
| WO2012036997A1 (en) | 2010-09-16 | 2012-03-22 | Schering Corporation | Fused pyrazole derivatives as novel erk inhibitors |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102010048374A1 (de) * | 2010-10-13 | 2012-04-19 | Merck Patent Gmbh | Pyrrolidinone als MetAP-2 Inhibitoren |
| DE102012006884A1 (de) * | 2012-04-04 | 2013-10-10 | Merck Patent Gmbh | Cyclische Amide als MetAP-2 Inhibitoren |
-
2014
- 2014-09-12 CA CA2923804A patent/CA2923804A1/en not_active Abandoned
- 2014-09-12 JP JP2015536649A patent/JPWO2015037716A1/ja active Pending
- 2014-09-12 US US15/021,231 patent/US20160221948A1/en not_active Abandoned
- 2014-09-12 CN CN201480049801.5A patent/CN105764887A/zh active Pending
- 2014-09-12 WO PCT/JP2014/074283 patent/WO2015037716A1/ja active Application Filing
- 2014-09-12 EP EP14843405.3A patent/EP3045448A4/en not_active Withdrawn
-
2016
- 2016-10-20 HK HK16112132.6A patent/HK1223927A1/zh unknown
Patent Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1997043278A1 (en) | 1996-05-14 | 1997-11-20 | Novo Nordisk A/S | Somatostatin agonists and antagonists |
| WO1999019301A1 (fr) | 1997-10-14 | 1999-04-22 | Yoshitomi Pharmaceutical Industries, Ltd. | Composes de piperazine et utilisation medicale desdits composes |
| WO2004058727A1 (en) | 2002-12-20 | 2004-07-15 | Bayer Pharmaceuticals Corporation | Substituted 3,5-dihydro-4h-imidazol-4-ones for the treatment of obesity |
| WO2006091697A1 (en) | 2005-02-23 | 2006-08-31 | Psychenomics, Inc. | Dopamine transporter inhibitors for use in treatment of movement disorders and other cns indications |
| WO2010059922A1 (en) | 2008-11-21 | 2010-05-27 | Ligand Pharmaceuticals Incorporated | Pyrrolidine carboxamide compounds |
| WO2010118207A1 (en) | 2009-04-09 | 2010-10-14 | Schering Corporation | Pyrazolo [1, 5-a] pyrimidine derivatives as mtor inhibitors |
| WO2011026904A1 (en) | 2009-09-04 | 2011-03-10 | Novartis Ag | Pyrazinylpyridines useful for the treatment of proliferative diseases |
| WO2011026917A1 (en) | 2009-09-04 | 2011-03-10 | Novartis Ag | Heteroaryl compounds as kinase inhibitors |
| WO2011047165A1 (en) | 2009-10-16 | 2011-04-21 | Southern Illinois University Edwardsville | Methods for treating memory impairment |
| WO2012036997A1 (en) | 2010-09-16 | 2012-03-22 | Schering Corporation | Fused pyrazole derivatives as novel erk inhibitors |
Non-Patent Citations (19)
| Title |
|---|
| "Series of Experimental Chemistry", vol. 1, MARUZEN CO., LTD. |
| BIOORGANIC AND MEDICINAL CHEMISTRY, vol. 17, 2009, pages 5639 - 5647 |
| BIOORGANIC AND MEDICINAL CHEMISTRY, vol. 19, 2011, pages 5238 - 5246 |
| COSTAKIS E. ET AL.: "Synthesis and preliminary pharmacological study of some a-phenylalkylamides and a-phenylalkylamines", ANNALES PHARMACEUTIQUES FRANCAISES, vol. 36, no. 7-8, 1978, pages 349 - 360, XP008182993 * |
| DATABASE REGISTRY [online] 18 December 2013 (2013-12-18), "3-PIPERIDINECARBOXAMIDE, N-[1-(5-AMINO-1,3,4-THIADIAZOL-2-YL)-1-METHYLETHYL]-1-(1-METHYLETHYL)- (CA INDEX NAME)", XP055328012, accession no. STN Database accession no. 1497636-62-0 * |
| DATABASE REGISTRY [online] 21 March 2010 (2010-03-21), "3-PIPERIDINECARBOXAMIDE, 1-(CYCLOPROPYLMETHYL)-5-(4-ETHYLPHENYL)-N-(1- PHENYLETHYL)- (CA INDEX NAME)", XP055327938, accession no. STN Database accession no. 1212064-14-6 * |
| DATABASE REGISTRY [online] 21 March 2010 (2010-03-21), "3-PIPERIDINECARBOXAMIDE, 5-(4-ETHYLPHENYL)-N-(1-PHENYLETHYL)-1-PROPYL- (CA INDEX NAME)", XP055327939, accession no. STN Database accession no. 1212329-68-4 * |
| DATABASE REGISTRY [online] 24 September 2010 (2010-09-24), "3-PIPERIDINECARBOXAMIDE, N-[1-(2,4-DIMETHYLPHENYL)ETHYL]-1-METHYL- (CA INDEX NAME)", XP055327942, accession no. STN Database accession no. 1242816-21-2 * |
| DATABASE REGISTRY [online] 26 September 2010 (2010-09-26), "3-PIPERIDINECARBOXAMIDE, 1-METHYL-N-[1-[4-(1-PYRROLIDINYL)PHENYL]ETHYL]- (CA INDEX NAME)", XP055327984, accession no. STN Database accession no. 1242830-57-4 * |
| DATABASE REGISTRY [online] 26 September 2010 (2010-09-26), "3-PIPERIDINECARBOXAMIDE, 1-METHYL-N-[1-[4-(METHYLSULFONYL)PHENYL]PROPYL]- (CA INDEX NAME)", XP055328000, accession no. STN Database accession no. 1242835-30-8 * |
| DATABASE REGISTRY [online] 3 January 2014 (2014-01-03), "4-THIAZOLECARBOXYLIC ACID, 2-[1-[[(1-METHYL-3- PYRROLIDINYL)CARBONYL]AMINO]ETHYL]- (CA INDEX NAME)", XP055328052, accession no. STN Database accession no. 1510323-50-8 * |
| EUROPEAN JOURNAL OF MEDICINAL CHEMISTRY, vol. 34, 1999, pages 363 - 380 |
| JOURNAL OF AMERICAN CHEMICAL SOCIETY, vol. 133, 2011, pages 2878 - 2880 |
| JOURNAL OF MEDICINAL CHEMISTRY, vol. 49, 2006, pages 942 - 946 |
| JOURNAL OF MEDICINAL CHEMISTRY, vol. 54, 2011, pages 1836 - 1846 |
| See also references of EP3045448A4 * |
| TETRAHEDRON LETTERS, vol. 28, 1987, pages 6513 - 6516 |
| TETRAHEDRON, vol. 63, 2007, pages 10486 - 10496 |
| THEODORA W. GREENE; PETER G M. WUTS: "Protective Groups in Organic Synthesis", 1999, JOHN WILEY & SONS, INC |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2923804A1 (en) | 2015-03-19 |
| EP3045448A4 (en) | 2017-01-25 |
| JPWO2015037716A1 (ja) | 2017-03-02 |
| EP3045448A1 (en) | 2016-07-20 |
| US20160221948A1 (en) | 2016-08-04 |
| CN105764887A (zh) | 2016-07-13 |
| HK1223927A1 (zh) | 2017-08-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102644889B1 (ko) | Rock 억제제로서의 스피로헵타닐 히단토인 | |
| CA3079617A1 (en) | Antagonists of the muscarinic acetylcholine receptor m4 | |
| JP4012068B2 (ja) | ムスカリンアンタゴニスト | |
| JP3447745B2 (ja) | ニューロキニンアンタゴニストとしてのピペラジノ誘導体 | |
| US20040034226A1 (en) | Imidazopyridine compounds as 5-HT4 receptor modulators | |
| US20040122043A1 (en) | Imidazopyridine compounds as 5-HT4 receptor agonists | |
| JP7015092B2 (ja) | ドーパミンd3受容体拮抗作用を有する含窒素縮環化合物 | |
| WO2012176763A1 (ja) | 新規インダゾール誘導体 | |
| WO2012133509A1 (ja) | 新規ベンズイミダゾール誘導体 | |
| JP2004500355A (ja) | ニューロンの生長及び伸長を刺激する化合物、組成物及び方法 | |
| JPWO2014054635A1 (ja) | イミダゾール誘導体 | |
| JP6088491B2 (ja) | 新規1位置換インダゾール誘導体 | |
| WO2014021273A1 (ja) | モルヒナン誘導体 | |
| WO2015037716A1 (ja) | 含窒素飽和複素環化合物 | |
| JP2014073982A (ja) | 新規ベンズイミダゾール誘導体からなる医薬 | |
| JP2015054844A (ja) | シクロアルカン誘導体 | |
| WO2019146739A1 (ja) | ドーパミンd3受容体拮抗作用を有する縮環化合物 | |
| JP2015199722A (ja) | イミダゾール誘導体からなる医薬 | |
| EP3150598B1 (en) | Substituted tropane derivatives | |
| CN113717161B (zh) | 含氮饱和杂环化合物及其制备方法、药物组合物和应用 | |
| JP2015214492A (ja) | 3−(4−ピペリジル)−インダゾール誘導体 | |
| KR20240005786A (ko) | 피페라진 폴리사이클릭 유도체를 함유하는 염, 이의 결정형, 이의 제조 방법, 및 이의 용도 | |
| JP6088476B2 (ja) | 新規1位置換インダゾール誘導体からなる医薬 | |
| JP2019127467A (ja) | ドーパミンd3受容体拮抗作用を有する含窒素縮環化合物を含有する医薬組成物 | |
| JP2017100948A (ja) | 4−アリールイミダゾール誘導体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 14843405 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2015536649 Country of ref document: JP Kind code of ref document: A |
|
| ENP | Entry into the national phase |
Ref document number: 2923804 Country of ref document: CA |
|
| REEP | Request for entry into the european phase |
Ref document number: 2014843405 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 15021231 Country of ref document: US Ref document number: 2014843405 Country of ref document: EP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |