WO2015016373A1 - テトラゾリノン化合物及びその用途 - Google Patents
テトラゾリノン化合物及びその用途 Download PDFInfo
- Publication number
- WO2015016373A1 WO2015016373A1 PCT/JP2014/070414 JP2014070414W WO2015016373A1 WO 2015016373 A1 WO2015016373 A1 WO 2015016373A1 JP 2014070414 W JP2014070414 W JP 2014070414W WO 2015016373 A1 WO2015016373 A1 WO 2015016373A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- halogen atoms
- atoms
- optionally
- atom
- Prior art date
Links
- 0 Cc(c(*)c(*)c(*)c1*)c1OC(*)(*)c(c(*)c(*)c(*)c1*)c1N1N=NN(*)C1=* Chemical compound Cc(c(*)c(*)c(*)c1*)c1OC(*)(*)c(c(*)c(*)c(*)c1*)c1N1N=NN(*)C1=* 0.000 description 15
- FLLLEDHCLWQCQA-UHFFFAOYSA-N CC(C)(C)c1cccc(-c(cc2)cc(C)c2OCc(c(OC)ccc2)c2N2N=NNC2=O)c1 Chemical compound CC(C)(C)c1cccc(-c(cc2)cc(C)c2OCc(c(OC)ccc2)c2N2N=NNC2=O)c1 FLLLEDHCLWQCQA-UHFFFAOYSA-N 0.000 description 1
- FEGYFPZRAFLBLA-UHFFFAOYSA-N CC(Nc1cccc(-c(cc2)cc(C)c2OCc(c(OC)ccc2)c2N2N=NNC2=O)c1)=O Chemical compound CC(Nc1cccc(-c(cc2)cc(C)c2OCc(c(OC)ccc2)c2N2N=NNC2=O)c1)=O FEGYFPZRAFLBLA-UHFFFAOYSA-N 0.000 description 1
- QAWMUHLAUOOZSX-UHFFFAOYSA-N CC(c(cc1)cc(C)c1OCc(c(C)ccc1)c1N1N=NN(C)C1=O)O Chemical compound CC(c(cc1)cc(C)c1OCc(c(C)ccc1)c1N1N=NN(C)C1=O)O QAWMUHLAUOOZSX-UHFFFAOYSA-N 0.000 description 1
- PPMLCQMOXVAHDK-UHFFFAOYSA-N CCCCN(C)C(c(cc1)cc(C)c1OCc(c(OC)ccc1)c1N1N=NN(C)C1=O)=O Chemical compound CCCCN(C)C(c(cc1)cc(C)c1OCc(c(OC)ccc1)c1N1N=NN(C)C1=O)=O PPMLCQMOXVAHDK-UHFFFAOYSA-N 0.000 description 1
- MJUFMRLJCKACJE-UHFFFAOYSA-N CCN(c1ccccc1)c(cc1)cc(C)c1OCc(c(C)ccc1)c1N1N=NN(C)C1=O Chemical compound CCN(c1ccccc1)c(cc1)cc(C)c1OCc(c(C)ccc1)c1N1N=NN(C)C1=O MJUFMRLJCKACJE-UHFFFAOYSA-N 0.000 description 1
- VYNIMLVMWZHBCA-UHFFFAOYSA-N CCc(cc(c(C)c1F)OCc(cccc2)c2N)c1N Chemical compound CCc(cc(c(C)c1F)OCc(cccc2)c2N)c1N VYNIMLVMWZHBCA-UHFFFAOYSA-N 0.000 description 1
- RKYGLQGWYWEXQB-UHFFFAOYSA-N CCc(cc(cc1)OCc(c(C)ccc2)c2N2N=NNC2=O)c1Br Chemical compound CCc(cc(cc1)OCc(c(C)ccc2)c2N2N=NNC2=O)c1Br RKYGLQGWYWEXQB-UHFFFAOYSA-N 0.000 description 1
- RKZHNBZDFGNLKT-UHFFFAOYSA-N CCc1cccc(N2N=NN(C)C2=O)c1CBr Chemical compound CCc1cccc(N2N=NN(C)C2=O)c1CBr RKZHNBZDFGNLKT-UHFFFAOYSA-N 0.000 description 1
- GDJHPRSIBJEAKX-UHFFFAOYSA-N CN(C1=O)N=NN1c1c(CBr)c(OC)ccc1 Chemical compound CN(C1=O)N=NN1c1c(CBr)c(OC)ccc1 GDJHPRSIBJEAKX-UHFFFAOYSA-N 0.000 description 1
- OVDOCFUCQBSZBO-UHFFFAOYSA-N Cc(c(Cl)ccc1)c1N1N=NN(C)C1=O Chemical compound Cc(c(Cl)ccc1)c1N1N=NN(C)C1=O OVDOCFUCQBSZBO-UHFFFAOYSA-N 0.000 description 1
- AVOZPEYUADPVNG-UHFFFAOYSA-N Cc(c(Cl)ccc1)c1N1N=NNC1=O Chemical compound Cc(c(Cl)ccc1)c1N1N=NNC1=O AVOZPEYUADPVNG-UHFFFAOYSA-N 0.000 description 1
- PSXWSKMUMKTPLF-UHFFFAOYSA-N Cc(c(N=C=O)ccc1)c1Br Chemical compound Cc(c(N=C=O)ccc1)c1Br PSXWSKMUMKTPLF-UHFFFAOYSA-N 0.000 description 1
- VUBZIKUZMILQCX-UHFFFAOYSA-N Cc(c(OC)ccc1)c1N1N=NNC1=O Chemical compound Cc(c(OC)ccc1)c1N1N=NNC1=O VUBZIKUZMILQCX-UHFFFAOYSA-N 0.000 description 1
- XZIJYHBFTQZPAZ-UHFFFAOYSA-N Cc(cc(cc1)-c(cc2)ccc2OC)c1OCc(c(OC)ccc1)c1N1N=NN(C)C1=O Chemical compound Cc(cc(cc1)-c(cc2)ccc2OC)c1OCc(c(OC)ccc1)c1N1N=NN(C)C1=O XZIJYHBFTQZPAZ-UHFFFAOYSA-N 0.000 description 1
- IMFKBZHGJQWYBU-UHFFFAOYSA-N Cc(cc(cc1)-c2cc(OC)ccc2)c1OCc(c(OC)ccc1)c1N(C(NNC)=O)N Chemical compound Cc(cc(cc1)-c2cc(OC)ccc2)c1OCc(c(OC)ccc1)c1N(C(NNC)=O)N IMFKBZHGJQWYBU-UHFFFAOYSA-N 0.000 description 1
- CKAODMWZEIHUCT-UHFFFAOYSA-N Cc(cc(cc1)-c2ccccc2C(F)(F)F)c1OCc(c(OC)ccc1)c1N1N(C)NNC1=O Chemical compound Cc(cc(cc1)-c2ccccc2C(F)(F)F)c1OCc(c(OC)ccc1)c1N1N(C)NNC1=O CKAODMWZEIHUCT-UHFFFAOYSA-N 0.000 description 1
- YBAMJXSWKDVISZ-UHFFFAOYSA-N Cc(cc(cc1)C(O)=O)c1OCc(c(OC)ccc1)c1N1N=NN(C)C1=O Chemical compound Cc(cc(cc1)C(O)=O)c1OCc(c(OC)ccc1)c1N1N=NN(C)C1=O YBAMJXSWKDVISZ-UHFFFAOYSA-N 0.000 description 1
- IGJTXDCPTKAAIT-UHFFFAOYSA-N Cc1cccc(-c(cc2)cc(C)c2OCc(c(OC)ccc2)c2N2NN(C)N(C)C2=O)c1 Chemical compound Cc1cccc(-c(cc2)cc(C)c2OCc(c(OC)ccc2)c2N2NN(C)N(C)C2=O)c1 IGJTXDCPTKAAIT-UHFFFAOYSA-N 0.000 description 1
- CEJRIGKATIQHAJ-UHFFFAOYSA-N Cc1cccc(N2N=NN(C)C2=O)c1COc(cc1)c(C)cc1N Chemical compound Cc1cccc(N2N=NN(C)C2=O)c1COc(cc1)c(C)cc1N CEJRIGKATIQHAJ-UHFFFAOYSA-N 0.000 description 1
- CEVDWOXLCDWEIT-UHFFFAOYSA-N Cc1cccc(N2N=NN(C)C2=O)c1COc(cc1)cc(C(F)(F)F)c1Br Chemical compound Cc1cccc(N2N=NN(C)C2=O)c1COc(cc1)cc(C(F)(F)F)c1Br CEVDWOXLCDWEIT-UHFFFAOYSA-N 0.000 description 1
- GXEMGAKMYFQVKR-UHFFFAOYSA-N Cc1cccc(N2N=NN(C)C2=O)c1COc(cc1)ccc1-c1ccccc1 Chemical compound Cc1cccc(N2N=NN(C)C2=O)c1COc(cc1)ccc1-c1ccccc1 GXEMGAKMYFQVKR-UHFFFAOYSA-N 0.000 description 1
- HPGZPXPPEZTWCD-UHFFFAOYSA-N Cc1cccc(N2N=NN(C)C2=O)c1COc1c(C)cc(C=O)cc1 Chemical compound Cc1cccc(N2N=NN(C)C2=O)c1COc1c(C)cc(C=O)cc1 HPGZPXPPEZTWCD-UHFFFAOYSA-N 0.000 description 1
- TZPVEPZIBUNOFG-UHFFFAOYSA-N Cc1cccc(N2N=NN(C)C2=O)c1COc1c(C)cc(COc2ccccc2)cc1 Chemical compound Cc1cccc(N2N=NN(C)C2=O)c1COc1c(C)cc(COc2ccccc2)cc1 TZPVEPZIBUNOFG-UHFFFAOYSA-N 0.000 description 1
- SQNMNBHENUQJFU-KEBDBYFISA-N Cc1cccc(N2N=NNC2=O)c1COc1c(C)cc(/C=N/NC)cc1 Chemical compound Cc1cccc(N2N=NNC2=O)c1COc1c(C)cc(/C=N/NC)cc1 SQNMNBHENUQJFU-KEBDBYFISA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D257/00—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms
- C07D257/02—Heterocyclic compounds containing rings having four nitrogen atoms as the only ring hetero atoms not condensed with other rings
- C07D257/04—Five-membered rings
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/713—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with four or more nitrogen atoms as the only ring hetero atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings
- C07D401/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D403/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00
- C07D403/02—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings
- C07D403/12—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, not provided for by group C07D401/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
Definitions
- the present invention relates to a tetrazolinone compound and its use.
- the present invention provides a compound having an excellent control effect against pests.
- the present inventors have found that the tetrazolinone compound represented by the following formula (1) has an excellent control effect against pests.
- the present invention has been completed. That is, the present invention is as follows [1] to [8].
- R 1 , R 2 , R 3 and R 11 are each independently a C1-C6 alkyl group optionally having one or more atoms or groups selected from group P 1 , a halogen atom, a hydrogen atom, one or more A C1-C6 alkoxy group optionally having one halogen atom, a cyano group, a nitro group, a C2-C6 alkenyl group optionally having one or more halogen atoms, and one or more halogen atoms
- a C2-C6 alkynyl group which may have one or more C1-C8 alkylamino group which may have one or more halogen atoms
- a C1-C6 alkylthio group which may have one or more halogen atoms, one or more halogen atoms
- a C1-C6 alkylsulfinyl group optionally having C1, a C1-C6 alkylsulfonyl group optionally having one
- R 10 may be a C1-C3 alkyl group optionally having one or more halogen atoms, a C2-C3 alkenyl group optionally having one or more halogen atoms, or one or more halogen atoms.
- R 12 may have one or more atoms or groups selected from group P 2 and may have one or more atoms or groups selected from group P 2.
- C 6 -C 16 may have one or more atoms or groups selected from group P 2.
- aryloxy group, one or more atoms or groups may have a C6-C16 arylthio group selected from the group P 2, which may have one or more atoms or groups selected from the group P 2 C7- C18 aralkyl group, 1 or more atoms may be C7-C18 aralkyloxy group optionally having a group selected from the group P 2, which may have one or more atoms or groups selected from the group P 2 C7 -C16 aryloxyalkyl groups, one or more atoms which may anilino group which may have a group selected from the group P 2, C2-C5 alkylthioalkyl group, one or more C1-C3 al A C1-C6 alkyl group optionally having a xyl group and / or a halogen atom, a C1-C6 alkoxy group optionally having one or more halogen atoms
- Group P 1 a halogen atom, a cyano group, a C3-C6 cycloalkyl group optionally having one or more halogen atoms, a C1-C4 alkoxy group optionally having one or more halogen atoms, or one or more The group which consists of the C1-C4 alkylthio group which may have a halogen atom.
- Group P 2 a C1-C6 alkyl group which may have one or more halogen atoms, a halogen atom, a cyano group, a hydroxy group, a C3-C6 cycloalkyl group which may have one or more halogen atoms, A C1-C6 alkoxy group which may have one or more halogen atoms, a C1-C6 alkylthio group which may have one or more halogen atoms, and a C2- which may have one or more halogen atoms.
- R 1 is a C1-C3 alkyl group optionally having one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group optionally having one or more halogen atoms, one or more halogens
- R 2 and R 3 are a hydrogen atom, a halogen atom, a C1-C4 alkyl group optionally having one or more halogen atoms, a C1-C4 alkoxy group optionally having one or more halogen atoms, or cyano.
- R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms;
- R 6 has a C1-C4 alkyl group optionally having one or more halogen atoms, a halogen atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, and one or more halogen atoms.
- R 10 is a methyl group;
- R 12 is tetrazolinone compound according to an one or more atoms a phenyl group which may have a group selected from the following group P 3 [1] or [2].
- Group P 3 a C1-C3 alkyl group optionally having one or more halogen atoms, a halogen atom, a cyano group, a C1-C3 alkoxy group optionally having one or more halogen atoms, one or more halogens
- R 12 is tetrazolinone compound according to 1 or more atoms or phenoxy groups that may also contain a group selected from the following group P 3 [1] or [2].
- Group P 3 a C1-C3 alkyl group optionally having one or more halogen atoms, a halogen atom, a cyano group, a C1-C3 alkoxy group optionally having one or more halogen atoms, one or more halogens
- R 1 is a C1-C3 alkyl group optionally having one or more halogen atoms, a hydrogen atom, or a C1-C3 alkoxy group optionally having one or more halogen atoms;
- R 2 is a hydrogen atom, a halogen atom, a C1-C4 alkyl group that may have one or more halogen atoms, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group.
- R 3 is a hydrogen atom, a halogen atom, a C1-C4 alkyl group optionally having one or more halogen atoms
- R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- R 6 has a C1-C4 alkyl group optionally having one or more halogen atoms, a halogen atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, or one or more halogen atoms.
- R 10 is a methyl group
- X is an oxygen atom
- R 12 is 1 or more atoms or one or more atoms which may phenoxy group which may have a group selected from a phenyl group or the following group P 3 have a group selected from the following group P 3
- Group P 3 a group consisting of a C1-C3 alkyl group optionally having one or more halogen atoms, a halogen atom, a cyano group, and a C1-C3 alkoxy group optionally having one or more halogen atoms.
- a method for controlling pests which comprises treating an effective amount of the tetrazolinone compound according to any one of [1] to [5] to a plant or soil.
- pests can be controlled.
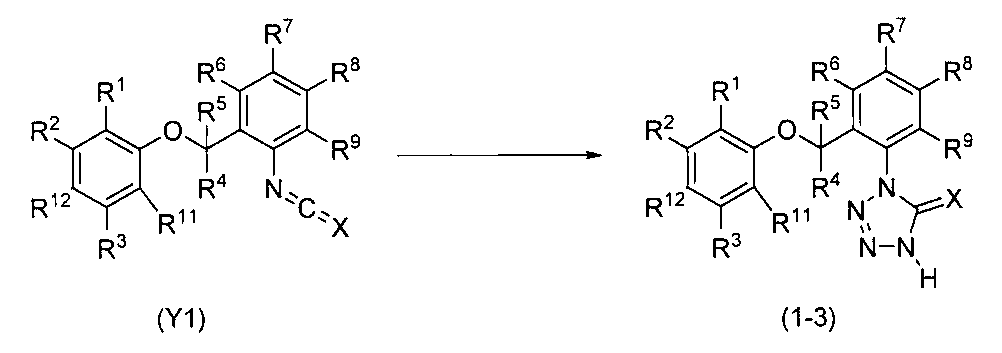
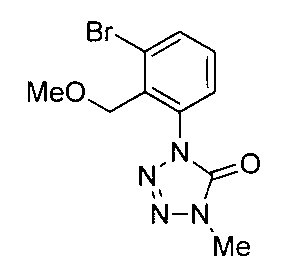
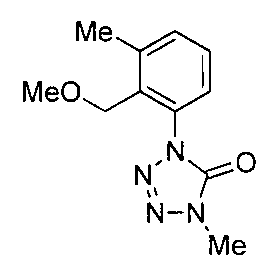
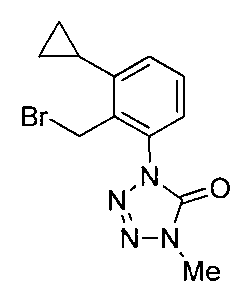
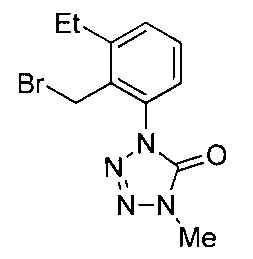
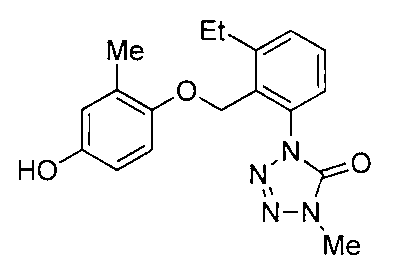
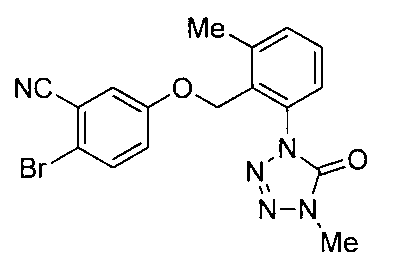
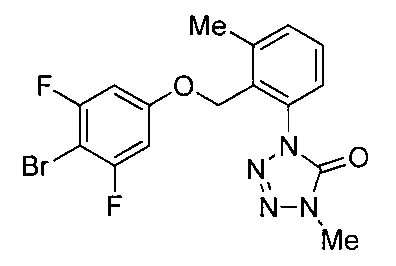
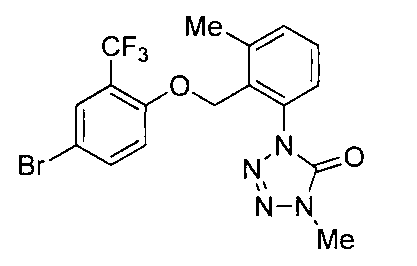
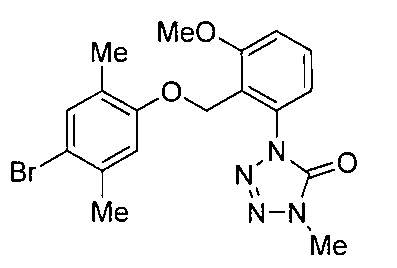
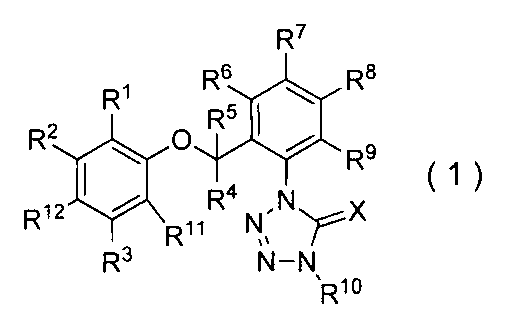
- the compound of the present invention (hereinafter referred to as the present compound) is a tetrazolinone compound represented by the formula (1).
- Formula (1) [Wherein the symbols have the same meaning as described above. ]
- halogen atom examples include a fluorine atom, a chlorine atom, a bromine atom and an iodine atom.
- the C1-C6 alkyl group optionally having one or more halogen atoms is a linear or branched alkyl group having 1-6 carbon atoms in which one or more hydrogen atoms are substituted with halogen atoms.
- Examples thereof include a fluoromethyl group, a dichlorofluoromethyl group, a chlorodifluoromethyl group and a 2,2-difluoroethyl group.
- the C1-C4 alkyl group optionally having one or more halogen atoms is a linear or branched alkyl group having 1 to 4 carbon atoms in which one or more hydrogen atoms are substituted with halogen atoms.
- the one or more atoms or C1-C6 alkyl group which may have a group selected from the group P 1, for example a methyl group, an ethyl group, a propyl group, an isopropyl group, butyl group, isobutyl group, sec- butyl group Tert-butyl group, pentyl group, hexyl group, 2,2,2, -trifluoroethyl group, 2,2,2, -trichloroethyl group, 3,3,3, -trifluoropropyl group, 2,2 -Difluoroethyl group, 1,1-difluoroethyl group, pentafluoroethyl group, heptafluoroisopropyl group, 1,1,2,2-tetrafluoroethyl group, 2,2,3,3,3-pentafluoropropyl group 2,2,3,3,3-pentafluorobutyl group, 2- (cyclopropyl)
- the one or more atoms may be C3-C6 cycloalkyl group optionally having a group selected from the group P 1, a hydrogen atom may be substituted with one or more atoms or groups selected from the group P 1 represents C3-C6 cycloalkyl, C3-C6 cycloalkyl group, and when two or more atoms or groups selected from the group P 1, also the atoms and groups selected from these groups P 1 identical to one another Or they may be different from each other.
- Examples of the C3-C6 cycloalkyl group optionally having one or more atoms or groups selected from the group P 1 include a cyclopropyl group, a 1-fluorocyclopropyl group, a 2,2-difluorocyclopropyl group, 1-chloro-2-fluorocyclopropyl group, 2,2-dichlorocyclopropyl group, 2,2-dibromocyclopropyl group, 2,2,3,3-tetrafluorocyclobutyl group, 2-chlorocyclopentyl group, 3 -Chlorocyclopentyl group, 3,3-difluorocyclopentyl group, 1-fluorocyclohexyl group, 2,2-difluorocyclohexyl group, 3,3-difluorocyclohexyl group, 4,4-difluorocyclohexyl group, 1-cyclopropylcyclopropyl group 2-cyclopropylcyclopropyl
- the C2-C6 alkenyl group which may have one or more halogen atoms is a linear or branched alkenyl group having 1 to 6 carbon atoms in which one or more hydrogen atoms are substituted with halogen atoms.
- the C2-C3 alkenyl group optionally having one or more halogen atoms is a linear or branched alkenyl group having 1 to 3 carbon atoms in which one or more hydrogen atoms are substituted with halogen atoms.
- the C2-C6 alkynyl group which may have one or more halogen atoms means that one or more hydrogen atoms of a linear or branched alkynyl group having 1 to 6 carbon atoms are substituted with halogen atoms.
- the C2-C3 alkynyl group optionally having one or more halogen atoms is a linear or branched alkynyl group having 1-3 carbon atoms in which one or more hydrogen atoms are substituted with halogen atoms.
- An ethynyl group, propargyl group, fluoroethynyl group, 3-chloro-2-propynyl group, 3-bromo-2-propynyl group, 3-iodo-2-propynyl group and 3-chloro- A 1-propynyl group is mentioned.
- the C3-C6 cycloalkyl group optionally having one or more halogen atoms is a group in which one or more hydrogen atoms of a cycloalkyl group having 3 to 6 carbon atoms may be substituted with a halogen atom.
- the C1-C6 alkoxy group which may have one or more halogen atoms is a linear or branched alkoxy group having 1 to 6 carbon atoms in which one or more hydrogen atoms are substituted with halogen atoms.
- the C1-C3 alkoxy group optionally having one or more halogen atoms is a linear or branched alkoxy group having 1 to 3 carbon atoms in which one or more hydrogen atoms are substituted with halogen atoms.
- the C1-C6 alkylthio group which may have one or more halogen atoms means that at least one hydrogen atom of a linear or branched alkylthio group having 1-6 carbon atoms is substituted with a halogen atom.
- the C3-C6 cycloalkyloxy group which may have one or more halogen atoms may be one in which one or more hydrogen atoms of a cycloalkyloxy group having 3 to 6 carbon atoms are substituted with a halogen atom.
- the C3-C6 cycloalkylthio group optionally having one or more halogen atoms is a group in which one or more hydrogen atoms of a cycloalkylthio group having 3 to 6 carbon atoms may be substituted with a halogen atom.
- Examples thereof include a cyclopropylthio group, a 2,2-difluorocyclopropylthio group, a cyclobutylthio group, a cyclopentylthio group, and a cyclohexylthio group.
- the C3-C6 alkenyloxy group optionally having one or more halogen atoms is a linear or branched alkenyloxy group having 3-6 carbon atoms, wherein one or more hydrogen atoms are halogen atoms.
- the C3-C6 alkynyloxy group optionally having one or more halogen atoms is a linear or branched alkynyloxy group having 3-6 carbon atoms, wherein one or more hydrogen atoms are halogen atoms.
- the C3-C6 alkenylthio group which may have one or more halogen atoms is a linear or branched alkenylthio group having 3 to 6 carbon atoms in which one or more hydrogen atoms are halogen atoms.
- Represents an optionally substituted group for example, 2-propenylthio group, 2-butenylthio group, 1-methyl-2-propenylthio group, 3-butenylthio group, 2-methyl-2-propenylthio group, 2-pentenyl Thio group, 3-pentenylthio group, 4-pentenylthio group, 1-methyl-3-butenylthio group, 5-hexenylthio group, 3-chloro-2-propenylthio group, 3-bromo-2-propenylthio group, 3-bromo-3,3-difluoro-1-propenylthio group, 2,3,3,3-tetrachloro-1-propenylthio group, 2-chloro-2-propenylthio group, 3,3-di Ruoro-2-propenylthio group, 2,3,3-trichloro-2-propenylthio group and 5-bromo -4,5,5- trifluoro-4-trifluoro
- the C3-C6 alkynylthio group optionally having one or more halogen atoms is a linear or branched alkynylthio group having 3 to 6 carbon atoms in which one or more hydrogen atoms are halogen atoms.
- the C2-C6 alkoxycarbonyl group represents a group in which a C1-C5 alkoxy group and a carbonyl group are bonded, and may be linear or branched, for example, a methoxycarbonyl group, an ethoxycarbonyl group, a propyl group Oxycarbonyl group, isopropyloxycarbonyl group, butyloxycarbonyl group, isobutyloxycarbonyl group, sec-butyloxycarbonyl group, tert-butyloxycarbonyl group, pentyloxycarbonyl group, isoamyloxycarbonyl group, neopentyloxycarbonyl group, 2 -Pentyloxycarbonyl group, 3-pentyloxycarbonyl group and 2-methylbutyloxycarbonyl group are mentioned.
- aminocarbonyl group which may have one or more C1-C6 alkyl groups
- 1 and / or 2 hydrogen atoms on nitrogen may be substituted with the same or different C1-C6 alkyl groups.
- Represents an aminocarbonyl group for example, aminocarbonyl group, methylaminocarbonyl group, ethylaminocarbonyl group, propylaminocarbonyl group, isopropylaminocarbonyl group, butylaminocarbonyl group, dimethylaminocarbonyl group, diethylaminocarbonyl group, dipropylaminocarbonyl Group, diisopropylaminocarbonyl group, pentylaminocarbonyl group and hexylaminocarbonyl group,
- the one or more atoms may also be C6-C16 aryl group optionally having a group selected from the group P 2, a hydrogen atom of the aryl group substituted with one or more atoms or groups selected from the group P 2 represents may also be C6-C16 aryl group, when atom or a group selected from the group P 2 is two or more, those atoms and groups may be the same or different.
- the one or more atoms or C6-C16 aryl group which may have a group selected from the group P 2, for example, a phenyl group, 2-fluorophenyl group, 3-fluorophenyl group, 4-fluorophenyl group, 2 -Chlorophenyl group, 3-chlorophenyl group, 4-chlorophenyl group, 2-bromophenyl group, 3-bromophenyl group, 4-bromophenyl group, 2-iodophenyl group, 3-iodophenyl group, 4-iodophenyl group, 4-methylphenyl group, 4-trifluoromethylphenyl group, 4-methoxyphenyl group, 4-nitrophenyl group, 4-dimethylaminophenyl group, 4-methylthiophenyl group, 2-cyanophenyl group, 3-cyanophenyl group 4-cyanophenyl group, 2,4-difluorophenyl group, 2,5-difluoropheny
- the one or more atoms a phenyl group which may have a group selected from the group P 3, hydrogen atoms of the phenyl group may be substituted with one or more atoms or groups selected from the group P 3 phenyl It represents a group, when atom or a group selected from the group P 3 is two or more, those atoms and groups may be the same or different.
- the one or more atoms a phenyl group which may have a group selected from the group P 3, for example, a phenyl group, 2-fluorophenyl group, 3-fluorophenyl group, 4-fluorophenyl group, 2-chlorophenyl group 3-chlorophenyl group, 4-chlorophenyl group, 2-bromophenyl group, 3-bromophenyl group, 4-bromophenyl group, 2-iodophenyl group, 3-iodophenyl group, 4-iodophenyl group, 4-methyl Phenyl group, 4-trifluoromethylphenyl group, 4-methoxyphenyl group, 4-methylthiophenyl group, 2-cyanophenyl group, 3-cyanophenyl group, 4-cyanophenyl group, 2,4-difluorophenyl group, 2 , 5-difluorophenyl group, 2,6-difluorophenyl group, 3,5-difluor
- Group P 3 a C1-C3 alkyl group optionally having one or more halogen atoms, a halogen atom, a cyano group, a C1-C3 alkoxy group optionally having one or more halogen atoms, one or more halogens A group consisting of a C3-C4 cycloalkyl group optionally having atoms and a C1-C3 alkylthio group optionally having one or more halogen atoms.
- Group P 4 A group consisting of a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a cyano group, a methoxy group, an ethoxy group, a trifluoromethyl group, a cyclopropyl group, and a methylthio group.
- phenyl group optionally having one or more atoms or groups selected from the group P 4 include a phenyl group, a 2-fluorophenyl group, a 3-fluorophenyl group, a 4-fluorophenyl group, and a 2-chlorophenyl group.
- the one or more atoms may also be C6-C16 aryloxy group optionally having a group selected from the group P 2, is substituted with one or more atoms or groups which the hydrogen atom of the aryloxy group is selected from the group P 2 represents not be C6-C16 aryloxy group, if atom or a group selected from the group P 2 is two or more, those atoms and groups may be the same or different.
- the one or more atoms or C6-C16 aryloxy group which may have a group selected from the group P 2, such as phenoxy group, 1-naphthyloxy group, 2-naphthyloxy group, 9-anthryl group 2-fluorophenoxy group, 3-fluorophenoxy group, 4-fluorophenoxy group, 2-chlorophenoxy group, 3-chlorophenoxy group, 4-chlorophenoxy group, 2-bromophenoxy group, 3-bromophenoxy group, 4 -Bromophenoxy group, 2-iodophenoxy group, 3-iodophenoxy group, 4-iodophenoxy group, 2,4-difluorophenoxy group, 2,5-dichlorophenoxy group, 2,4,6-trifluorophenoxy group, 2,3,4-trichlorophenoxy group, pentafluorophenoxy group, 2-bromo-4-fluoro Phenoxy group, 2-chloro-3-fluorophenoxy group, 2-fluoro
- the one or more atoms which may phenoxy group optionally having a group selected from the group P 3, hydrogen atoms of the phenoxy group may be substituted with one or more atoms or groups selected from the group P 3 phenoxy It represents a group, when atom or a group selected from the group P 3 is two or more, those atoms and groups may be the same or different.
- phenoxy group which may have one or more atoms or groups selected from the group P 3 include, for example, phenoxy group, 2-fluorophenoxy group, 3-fluorophenoxy group, 4-fluorophenoxy group, 2-chloro Phenoxy group, 3-chlorophenoxy group, 4-chlorophenoxy group, 2-bromophenoxy group, 3-bromophenoxy group, 4-bromophenoxy group, 2-iodophenoxy group, 3-iodophenoxy group, 4-iodophenoxy group 2,4-difluorophenoxy group, 2,5-dichlorophenoxy group, 2,4,6-trifluorophenoxy group, 2,3,4-trichlorophenoxy group, pentafluorophenoxy group, pentachlorophenoxy group, 2- Bromo-4-fluorophenoxy group, 2-chloro-3-fluorophenoxy group, 2-methyl Examples thereof include tilphenoxy group, 3-methylphenoxy group, 4-methylphenoxy group, 2-cyanophenoxy group, 2-
- the one or more atoms which may phenoxy group optionally having a group selected from the group P 4, a hydrogen atom of the phenoxy group may be substituted with one or more atoms or groups selected from the group P 4-phenoxy
- the atom or group selected from group P 4 is 2 or more, these atoms and groups may be the same or different.
- phenoxy group which may have one or more atoms or groups selected from group P 4 include, for example, phenoxy group, 2-fluorophenoxy group, 3-fluorophenoxy group, 4-fluorophenoxy group, 2-chloro Phenoxy group, 3-chlorophenoxy group, 4-chlorophenoxy group, 2,4-difluorophenoxy group, 2,5-dichlorophenoxy group, 2,4,6-trifluorophenoxy group, 2,3,4-trichlorophenoxy group Group, pentafluorophenoxy group, pentachlorophenoxy group, 2-chloro-3-fluorophenoxy group, 2-methylphenoxy group, 3-methylphenoxy group, 4-methylphenoxy group, 2-cyanophenoxy group, 3-cyanophenoxy group Group and 4-cyanophenoxy group.
- the one or more atoms which may have a group C6-C16 arylthio group selected from the group P 2, a hydrogen atom of the arylthio group is optionally substituted with one or more atoms or groups selected from the group P 2 represents may also be C6-C16 arylthio group, if atom or a group selected from the group P 2 is two or more, those atoms and groups may be the same or different.
- the one or more atoms or C6-C16 arylthio group which may have a group selected from the group P 2, such as phenylthio group, naphthylthio group, 2-naphthylthio group, 1-Asenafuchiruchio group, 1- Fenantori Ruthio group, 2-fluorophenylthio group, 3-fluorophenylthio group, 4-fluorophenylthio group, 2-chlorophenylthio group, 3-chlorophenylthio group, 4-chlorophenylthio group, 2-bromophenylthio group, 3 -Bromophenylthio group, 4-bromophenylthio group, 2-iodophenylthio group, 3-iodophenylthio group, 4-iodophenylthio group, 2,4-difluorophenylthio group and 1-fluoro-2-naphthylthio Group.
- the C7-C18 aralkyl group optionally having one or more atoms or groups selected from the group P 2 has 7 to 18 carbon atoms in total of the alkyl part and the aryl part, and the alkyl part and the aryl part. represents one or more atoms or optionally substituted C7-C18 aralkyl group with a group in which a hydrogen atom is selected from the group P 2 in the part, when an atom or group selected from the group P 2 is two or more, their
- the atoms and groups may be the same or different.
- the one or more atoms or C7-C18 aralkyl group which may have a group selected from the group P 2, for example benzyl, 2-phenylethyl, 3-phenylpropyl, 4-phenylbutyl group, 5 -Phenylpentyl group, 6-phenylhexyl group, 7-phenylheptyl group, 12-phenyldodecyl group, 1-methoxy-2-phenylethyl group, 1-naphthylmethyl group, 2- (1-naphthyl) ethyl group, 2 -Naphtylmethyl group, 2- (2-naphthyl) ethyl group, 2-fluorobenzyl group, 3-fluorobenzyl group, 4-fluorobenzyl group, 2-chlorobenzyl group, 3-chlorobenzyl group, 4-chlorobenzyl group 2-bromobenzyl group, 3-bromobenzyl group,
- the C7-C10 aralkyl group which may have one or more C1-C4 alkoxy groups and / or hydroxy groups has a total number of carbon atoms of the alkyl part and the aryl part of 7 to 10, Represents a C7-C18 aralkyl group in which the hydrogen atom of the aryl moiety may be substituted with one or more C1-C4 alkoxy groups and / or hydroxy groups, such as benzyl group, 2-phenylethyl group, 3-phenylpropyl group, Examples thereof include 1-hydroxy-1-phenylmethyl group, 1-methoxy-1-phenylmethyl group and 4-phenylbutyl group.
- the one or more atoms which may have a group C7-C18 aralkyloxy group selected from the group P 2, the total number of carbon atoms in the aryl moiety and the alkoxy moiety of the aralkyl from 7 to 18 alkoxy It represents a moiety and the aryl moiety of one or more atoms or aralkyloxy group optionally substituted with a group having a hydrogen atom selected from the group P 2, when atoms and groups selected from the group P 2 is two or more, they The atoms or groups may be the same or different.
- the one or more atoms may also be C7-C18 aralkyloxy group optionally having a group selected from the group P 2, for example benzyloxy, 2-phenylethyl group, 3-phenylpropyl group, 12-phenyl Dodecyloxy group, naphthylmethyloxy group, naphthylethyloxy group, 4-fluorobenzyloxy group, 2-chlorobenzyloxy group, 3-bromobenzyloxy group, 4-iodobenzyloxy group, 2-methylbenzyloxy group, 3 -Methylbenzyloxy group, 4-methylbenzyloxy group, 2-methoxybenzyloxy group, 3-methoxybenzyloxy group, 4-methoxybenzyloxy group, 2-cyanobenzyloxy group, 3-cyanobenzyloxy group, 4- Cyanobenzyloxy group, 2,4-difluorobenzyloxy group 2,5-dichlorobenzyloxy group, 3,4,5-trifluorobenz
- the C7-C10 aralkyloxy group represents an aralkyloxy group having a total of 7 to 10 carbon atoms in the aryl and alkoxy moieties.
- Examples of the C7-C10 aralkyloxy group include benzyloxy group and 2-phenyl Examples thereof include an ethyloxy group, a 3-phenylpropyloxy group, and a 4-phenylbutyloxy group.
- the C7-C10 aryloxyalkyl group represents a group in which an aryloxy group is bonded to an alkyl group, and represents a group having 7 to 10 total carbon atoms as a C7-C10 aryloxyalkyl group.
- Examples of the C7-C10 aryloxyalkyl group include a phenoxymethyl group, a phenoxyethyl group, a phenoxypropyl group, and a phenoxybutyl group.
- the one or more atoms which may have a group C7-C16 aryloxyalkyl groups selected from the group P 2, the total number of carbon atoms of the aryloxy moiety and the alkyl moiety is a 7-16 aryl represents one or more atoms or optionally substituted C7-C16 aryloxyalkyl group with a group in which a hydrogen atom of the oxy group is selected from the group P 2, atom or a group selected from the group P 2 is 2 or more In some cases, these atoms and groups may be the same or different.
- the one or more atoms may also be C7-C16 aryloxyalkyl group optionally having a group selected from the group P 2, for example, phenoxymethyl, 1-naphthyl oxymethyl group, 2-naphthyloxy methyl, 3- Examples thereof include a fluorophenoxymethyl group, a 4-fluorophenoxymethyl group, a 2-chlorophenoxymethyl group, a 3-chlorophenoxymethyl group, a 4-chlorophenoxymethyl group, a phenoxyethyl group, and a naphthyloxyethyl group.
- An anilino group optionally having one or more atoms or groups selected from group P 2 is one or more atoms or groups in which a hydrogen atom on phenyl and / or a hydrogen atom on nitrogen is selected from group P 2 in substituted represents also good anilino group, if atom or a group selected from the group P 2 is two or more, those atoms and groups may be the same or different.
- anilino group optionally having one or more atoms or groups selected from the group P 2 include an anilino group, an N-methyl-anilino group, an N-ethyl-anilino group, and an N-methyl-2-fluoroani Lino group, N-methyl-3-fluoroanilino group, N-methyl-4-fluoroanilino group, N-methyl-4-chloroanilino group, N-methyl-4-methylanilino group and N-methyl-4-cyanoanilino Group.
- the anilino group optionally having a C1-C4 alkyl group represents an anilino group in which a hydrogen atom on phenyl and / or a hydrogen atom on nitrogen may be substituted with an alkyl group.
- Examples of the anilino group optionally having a C1-C4 alkyl group include an anilino group, an N-methyl-anilino group, an N-ethyl-anilino group, and an N-methyl-4-methylanilino group.
- the C3-C6 cycloalkenyl group which may have one or more halogen atoms is a group in which one or more hydrogen atoms of a C3-C6 cycloalkenyl group may be substituted with a halogen atom.
- Examples thereof include a cyclopropenyl group, a cyclobutenyl group, a cyclopentenyl group, a cyclohexenyl group, a 4,4-difluorocyclohexenyl group, and a 4-chlorocyclohexenyl group.
- C2-C9 heteroaryloxy group (wherein the heteroaryl moiety is a 5-membered ring, a 6-membered ring, a 5-membered ring or a 5-membered ring, a 5-membered ring or a 6-membered ring or a 6-membered ring) Represents a heteroaryloxy group containing one or more atoms selected from the group consisting of a nitrogen atom, an oxygen atom and a sulfur atom as a ring constituent atom, and represents two or more atoms.
- the atoms may be the same or different and the heteroaryl moiety may be a 5-membered ring, a 6-membered ring, a 5-membered and 5-membered fused ring, a 5-membered ring and a 6-membered fused ring, or 6 It is a fused ring of member ring and six member ring.
- Examples of the C2-C9 heteroaryloxy group include 2-pyridyloxy group, 3-pyridyloxy group, 4-pyridyloxy group, 2-pyrimidyloxy group, 3-pyridyloxy group, 2-pyrazyloxy group, 2-thiazolyloxy group, Examples include 2-oxazolyloxy group, 2-benzthiazolyloxy group, 2-benzoxazolyloxy group, 2-quinolyloxy group, 3-pyrazolyloxy group, 3-furyloxy group and 3-thienyloxy group. .
- a C2-C9 heteroaryloxy group optionally having one or more atoms or groups selected from group P 2 (wherein the heteroaryl moiety is a condensed 5-membered ring, 6-membered ring, 5-membered ring and 5-membered ring) ring, 5-membered ring as a condensed ring or 6-membered ring and six-membered ring of the fused 6-membered ring), one or more atoms or groups which the hydrogen atom of the C2-C9 heteroaryl group is selected from the group P 2 in substituted represents even heteroaryl group, when atom or a group selected from the group P 2 is two or more, those atoms and groups may be the same or different.
- the one or more atoms or C2-C9 heteroaryl group that may have a group selected from the group P 2, for example, 2-pyridyloxy group, 3-pyridyloxy group, 4-pyridyloxy group, 2- Pyrimidyloxy group, 3-methyl-2-pyridyloxy group, 4-methyl-2-pyridyloxy group, 5-methyl-2-pyridyloxy group, 6-methyl-2-pyridyloxy group, 6-cyano-2-pyridyl group Oxy group, 3-pyridazyloxy group, 2-pyrazyloxy group, 2-thiazolyloxy group, 2-oxazolyloxy group, 2-benzthiazolyloxy group, 2-benzoxazolyloxy group, 2-quinolyloxy group, 2 -A pyrazolyloxy group, a 3-furyloxy group and a 3-thienyloxy group.
- the C3-C9 trialkylsilyl group represents an alkylsilyl group in which three hydrogen atoms on the silyl group are substituted with the same or different C1-C4 alkyl groups.
- a trimethylsilyl group a tert-butyldimethylsilyl group , Triethylsilyl group, isopropyldimethylsilyl group and triisopropylsilyl group.
- the C1-C6 alkylsulfonyl group which may have one or more halogen atoms is a linear or branched alkylsulfonyl group having 1-6 carbon atoms in which one or more hydrogen atoms are halogen atoms.
- Represents an optionally substituted group such as methylsulfonyl group, ethylsulfonyl group, propylsulfonyl group, isopropylsulfonyl group, butylsulfonyl group, hexylsulfonyl group, trifluoromethylsulfonyl group, pentafluoroethylsulfonyl group, and periodate.
- a hexylsulfonyl group is a linear or branched alkylsulfonyl group having 1-6 carbon atoms in which one or more hydrogen atoms are halogen atoms.
- the C1-C6 alkylsulfinyl group optionally having one or more halogen atoms is a linear or branched alkylsulfinyl group having 1-6 carbon atoms, wherein one or more hydrogen atoms are halogen atoms.
- Examples of the C1-C3 alkyl group include a methyl group, an ethyl group, a propyl group, and an isopropyl group.
- the C1-C3 alkyl group optionally having one or more halogen atoms represents a group in which one or more hydrogen atoms of the C1-C3 alkyl group may be substituted with a halogen atom, such as a methyl group, Ethyl, propyl, isopropyl, chloromethyl, dichloromethyl, fluoromethyl, difluoromethyl, chlorofluoromethyl, dichlorofluoromethyl, chlorodifluoromethyl, trifluoromethyl, trichloromethyl, tri Bromomethyl group, 2-fluoroethyl group, 2,2-difluoroethyl group, 2,2,2-trifluoroethyl group, 2-chloroethyl group, 2,2-dichloroethyl group, 2,2,2-trich
- the C3-C5 cycloalkyl group optionally having one or more halogen atoms is a group in which one or more hydrogen atoms of a cycloalkyl group having 3 to 5 carbon atoms may be substituted with a halogen atom.
- cyclopropyl group, cyclobutyl group, cyclopentyl group 2-methylcyclopropyl group, 2,2-dimethylcyclopropyl group, 2,3-dimethylcyclopropyl group, 2-fluorocyclopropyl group, 2,2-difluoro Cyclopropyl group, 2-chloro-2-fluorocyclopropyl group, 2,2-dichlorocyclopropyl group, 2,2-dibromocyclopropyl group, 2,2-difluoro-1-methylcyclopropyl group, 2,2- Dichloro-1-methylcyclopropyl group, 2,2-dibromo-1-methylcyclopropyl group, 1- (trifluoromethyl Cyclopropyl group, 2,2,3,3-tetrafluorocyclobutyl group, 2-chloro-cyclopentyl group and 3-chloro-cyclopentyl group.
- the C1-C4 alkoxy group optionally having one or more halogen atoms is a linear or branched alkoxy group having 1-4 carbon atoms in which one or more hydrogen atoms are substituted with halogen atoms.
- the C1-C8 alkylamino group optionally having one or more halogen atoms is an amino group in which 1 and / or 2 hydrogen atoms on nitrogen are substituted with the same or different C1-C8 alkyl groups.
- the aminocarbonyl group optionally having a C1-C6 alkyl group represents an aminocarbonyl group in which 1 and / or 2 hydrogen atoms on nitrogen are substituted with the same or different C1-C8 alkyl groups,
- aminocarbonyl group N-methylaminocarbonyl group, N-ethylaminocarbonyl group, N-propylaminocarbonyl group, N-isopropylaminocarbonyl group, N-butylaminocarbonyl group, N, N-dimethylaminocarbonyl group
- Examples thereof include N, N-diethylaminocarbonyl group, N, N-dipropylaminocarbonyl group, N-ethyl-N-methylaminocarbonyl group and N-propyl-N-methylaminocarbonyl group.
- the C2-C5 alkoxyalkyl group has a total number of carbon atoms of the alkoxy part and the alkyl part of 2 to 5, and may be either linear or branched, such as methoxymethyl group, ethoxymethyl Group, propyloxymethyl group, isopropyloxymethyl group, butyloxymethyl group, isobutyloxymethyl group, sec-butyloxymethyl group, 1-methoxyethyl group, 2-methoxyethyl group, 2-propyloxyethyl group, 2- Examples thereof include isopropyloxyethyl group, 3-methoxypropyl group, 3-ethoxypropyl group, 3-methoxybutyl group and 4-methoxybutyl group.
- the C2-C5 alkylthioalkyl group has a total number of carbon atoms of the alkylthio moiety and the alkyl moiety of 2 to 5, and may be linear or branched, such as methylthiomethyl group, ethylthio Methyl group, propylthiomethyl group, isopropylthiomethyl group, butylthiomethyl group, isobutylthiomethyl group, sec-butylthiomethyl group, 1-methylthioethyl group, 2-methylthioethyl group, 2-propylthioethyl group, 2 -Isopropylthioethyl group, 3-methylthiopropyl group, 3-ethylthiopropyl group, 3-methylthiobutyl group and 4-methylthiobutyl group.
- the C2-C6 alkylcarbonyl group represents a linear or branched alkylcarbonyl group having 1 to 5 carbon atoms and having 1 to 5 carbon atoms, such as a methylcarbonyl group or an ethylcarbonyl group.
- the C2-C6 alkylcarbonyloxy group represents a linear or branched alkylcarbonyl group having an alkyl group having 1 to 5 carbon atoms, such as a methylcarbonyloxy group, an ethylcarbonyloxy group, a propylcarbonyloxy group. Group, isopropylcarbonyloxy group, pivaloyloxy group, butylcarbonyloxy group, and pentylcarbonyloxy group.
- the C1-C4 alkylthio group which may have one or more halogen atoms means that one or more hydrogen atoms of a linear or branched alkylthio group having 1-4 carbon atoms are substituted with halogen atoms.
- the C1-C6 alkyl group which may have one or more C1-C3 alkoxy groups and / or halogen atoms means that one or more hydrogen atoms of a linear or branched C1-C6 alkyl group are 1
- the above-mentioned C1-C3 alkoxy group and / or a group that may be substituted with a halogen atom are represented, and examples thereof include a methoxymethyl group, an ethoxymethyl group, and a trifluoromethyl group.
- the total number of carbon atoms of the alkyl moiety and the carbonyl in the C2-C6 alkylcarbonylamino group is 2-6.
- Examples of the C2-C6 alkylcarbonylamino group include an acetylamino group, a propionylamino group, a butyrylamino group, an isobutyrylamino group, a pentanoylamino group, a 2-methylbutyrylamino group, and a hexanoylamino group.
- the total number of carbon atoms of the alkyl moiety and the carbonyl in the C2-C4 alkylcarbonylamino group is 2-4.
- Examples of the C2-C4 alkylcarbonylamino group include an acetylamino group, a propionylamino group, a butyrylamino group, and an isobutyrylamino group.
- Examples of the aspect of the compound of the present invention include compounds in which the substituent in formula (1) is as shown below.
- a compound in which R 12 is a phenyl group optionally having one or more atoms or groups selected from group P 3 ;
- R 12 may have one or more atoms or groups selected from the group P 3 (wherein the heteroaryl moiety is a 5-membered ring, a 6-membered ring, a 5-membered ring and a 5-membered ring)
- a compound in which R 2 is a hydrogen atom;
- a compound in which R 3 is a hydrogen atom;
- the compound wherein R 4 is a hydrogen atom;
- the compound wherein R 5 is a hydrogen atom;
- R 6 is a C1-C3 alkyl group optionally having one or more halogen atoms; The compound wherein R 6 is a C3-C4 cycloalkyl group; A compound in which R 6 is a halogen atom; The compound wherein R 6 is a C2-C3 alkenyl group; The compound wherein R 6 is a C2-C3 alkynyl group; A compound in which R 6 is a C1-C3 alkoxy group optionally having one or more halogen atoms; R 6 may be a C1-C3 alkyl group optionally having one or more halogen atoms, a halogen atom, a C3-C4 cycloalkyl group, a C1-C3 alkoxy group optionally having one or more halogen atoms, C2 A compound which is a -C3 alkenyl group or a C2-C3 alkynyl group; A compound in which R 6 is a methyl
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- a tetrazolinone compound which is a good phenyl group, R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are a hydrogen atom, R 10 is a methyl group, and X is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- a tetrazolinone compound which is a good phenoxy group
- R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- R 10 is a methyl group
- X is an oxygen atom
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group which may have one, a C1-C4 alkoxy group which may have one or more halogen atoms or a cyano group
- R 6 is a methyl group, an ethyl group, a cyclopropyl group, chlorine atom, a bromine atom, a methoxy group, an ethoxy group or a trifluoromethyl group, with one or more atoms or phenyl group which may have a group
- R 12 is selected from the group P 3, Ri, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a methyl group,
- X is tetrazolinone compound is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group which may have one, a C1-C4 alkoxy group which may have one or more halogen atoms or a cyano group
- R 6 is a methyl group, an ethyl group, a cyclopropyl group, chlorine atom, a bromine atom, a methoxy group, an ethoxy group, or a trifluoromethyl or a methyl group
- R 12 is selected from the group P 3
- R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom
- R 10 is a methyl group
- X is tetrazolinone compound is an oxygen atom
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group which may have one, a C1-C4 alkoxy group which may have one or more halogen atoms or a cyano group
- R 6 is a methyl group, an ethyl group, a cyclopropyl group, chlorine atom, a bromine atom, a methoxy group, an ethoxy group or a trifluoromethyl group, with one or more atoms or phenyl group which may have a group
- R 12 is selected from the group P 4, Ri, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a methyl group,
- X is tetrazolinone compound is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group which may have one, a C1-C4 alkoxy group which may have one or more halogen atoms or a cyano group
- R 6 is a methyl group, an ethyl group, a cyclopropyl group, chlorine atom, a bromine atom, a methoxy group, an ethoxy group, or a trifluoromethyl or a methyl group
- R 12 is selected from the group P 4, There, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a methyl group, X is tetrazolinone compound is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 3 is a hydrogen atom or a methyl group, and R 6 is one or more halogen atoms.
- C1-C4 alkyl group optionally having an atom, halogen atom, C1-C4 alkoxy group optionally having one or more halogen atoms, optionally having one or more halogen atoms
- a tetrazolinone compound is selected from the group P 3 R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are a hydrogen atom, R 10 is a methyl group, and X is an oxygen atom.
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 3 is a hydrogen atom or a methyl group, and R 6 is one or more halogen atoms.
- C1-C4 alkyl group optionally having an atom, halogen atom, C1-C4 alkoxy group optionally having one or more halogen atoms, optionally having one or more halogen atoms
- a tetrazolinone compound is selected from the group P 3 R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are a hydrogen atom, R 10 is a methyl group, and X is an oxygen atom.
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 3 is a hydrogen atom or a methyl group, and R 6 is one or more halogen atoms.
- C1-C4 alkyl group optionally having an atom, halogen atom, C1-C4 alkoxy group optionally having one or more halogen atoms, optionally having one or more halogen atoms
- a tetrazolinone compound
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 3 is a hydrogen atom or a methyl group, and R 6 is one or more halogen atoms.
- C1-C4 alkyl group optionally having an atom, halogen atom, C1-C4 alkoxy group optionally having one or more halogen atoms, optionally having one or more halogen atoms
- a tetrazolinone compound
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group, ethyl group, a cyclopropyl group, a chlorine atom, a bromine atom, a methoxy group, an ethoxy group or a trifluoromethyl group, has one or more atoms or groups
- R 12 is selected from the group P 3
- a phenyl group which may have, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom
- R 10 is a methyl group
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group, ethyl group, a cyclopropyl group, a chlorine atom, a bromine atom, a methoxy group, an ethoxy group or a trifluoromethyl group, has one or more atoms or groups
- R 12 is selected from the group P 3
- a good phenoxy group can have, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a methyl group, X is
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group, ethyl group, a cyclopropyl group, a chlorine atom, a bromine atom, a methoxy group, an ethoxy group or a trifluoromethyl group, has one or more atoms or groups
- R 12 is selected from the group P 4
- R 10 is a methyl group
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group, ethyl group, a cyclopropyl group, a chlorine atom, a bromine atom, a methoxy group, an ethoxy group or a trifluoromethyl group, has one or more atoms or groups
- R 12 is selected from the group P 4
- a good phenoxy group can have, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a methyl group, X
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 has a C1-C4 alkyl group optionally having one or more halogen atoms, a halogen atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, and one or more halogen atoms.
- R 12 from the group P 3 Is is one or more atoms or phenyl group which may have a group, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is methyl group A tetrazolinone compound in which X is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 has a C1-C4 alkyl group optionally having one or more halogen atoms, a halogen atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, and one or more halogen atoms.
- R 12 from the group P 3 Is is one or more atoms or phenoxy groups that may also contain a group, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is methyl group A tetrazolinone compound in which X is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 has a C1-C4 alkyl group optionally having one or more halogen atoms, a halogen atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, and one or more halogen atoms.
- R 12 from the group P 4 Is is one or more atoms or phenyl group which may have a group, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is methyl group A tetrazolinone compound in which X is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 has a C1-C4 alkyl group optionally having one or more halogen atoms, a halogen atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, and one or more halogen atoms.
- R 12 from the group P 4 Is is one or more atoms or phenoxy groups that may also contain a group, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is methyl group A tetrazolinone compound in which X is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group, an ethyl group, a cyclopropyl group, a chlorine atom, a bromine atom, a methoxy group, an ethoxy group, or a trifluoromethyl group
- R 12 represents one or more atoms or groups selected from the group P 3
- An optionally substituted phenyl group, R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are a hydrogen atom
- R 10 is a methyl group
- X is an oxygen atom Tetrazo Non compounds
- R 1 is one or more halogen atoms optionally may C1-C3 alkyl group which may have a hydrogen atom, 1 or more halogen atoms which may have a C2-C3 alkynyl group, have one or more halogen atoms An optionally substituted C3-C5 cycloalkyl group or a C1-C3 alkoxy group optionally having one or more halogen atoms,
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group, an ethyl group, a cyclopropyl group, a chlorine atom, a bromine atom, a methoxy group, an ethoxy group, or a trifluoromethyl group
- R 12 is one or more atoms or groups selected from the group P 3 A phenoxy group which may have, R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atom
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group, an ethyl group, a cyclopropyl group, a chlorine atom, a bromine atom, a methoxy group, an ethoxy group, or a trifluoromethyl group
- R 12 represents one or more atoms or groups selected from the group P 4
- An optionally substituted phenyl group, R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are a hydrogen atom
- R 10 is a methyl group
- X is an oxygen atom Tetrazo Non compounds
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group, an ethyl group, a cyclopropyl group, a chlorine atom, a bromine atom, a methoxy group, an ethoxy group, or a trifluoromethyl group
- R 12 represents one or more atoms or groups selected from the group P 4 A phenoxy group which may have, R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms, R 10 is a methyl group, and X is an oxygen atom Tetra Perinone compounds;
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 and R 3 may have a hydrogen atom, a halogen atom, or one or more halogen atoms.
- R 6 is a C1-C4 alkyl group optionally having one or more halogen atoms.
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 and R 3 may have a hydrogen atom, a halogen atom, or one or more halogen atoms.
- R 6 is a C1-C4 alkyl group optionally having one or more halogen atoms.
- R 12 is selected from the group P 3 Ri, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a methyl group, X is tetrazolinone compound is an oxygen atom;
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 and R 3 may have a hydrogen atom, a halogen atom, or one or more halogen atoms.
- R 6 is a C1-C4 alkyl group optionally having one or more halogen atoms.
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 and R 3 may have a hydrogen atom, a halogen atom, or one or more halogen atoms.
- R 6 is a C1-C4 alkyl group optionally having one or more halogen atoms.
- R 12 is selected from the group P 4 Ri, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a methyl group, X is tetrazolinone compound is an oxygen atom;
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 and R 3 may have a hydrogen atom, a halogen atom, or one or more halogen atoms.
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 and R 3 may have a hydrogen atom, a halogen atom, or one or more halogen atoms.
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 and R 3 may have a hydrogen atom, a halogen atom, or one or more halogen atoms.
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 and R 3 may have a hydrogen atom, a halogen atom, or one or more halogen atoms.
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom, a halogen atom, or a C1-C4 alkyl optionally having one or more halogen atoms A C1-C4 alkoxy group or a cyano group which may have one or more halogen atoms,
- R 3 is a hydrogen atom or a methyl group, and R 6 has one or more halogen atoms.
- a C1-C4 alkyl group, a halogen atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, a C3-C5 cycloalkyl group optionally having one or more halogen atoms, 1 or more halogen atom has optionally may C2-C4 alkenyl group or also a C2-C4 alkynyl group, having one or more atoms or groups
- R 12 are selected from the group P 3 And is also a phenyl group, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a methyl group,
- X is tetrazolinone compound is an oxygen atom;
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom, a halogen atom, or a C1-C4 alkyl optionally having one or more halogen atoms A C1-C4 alkoxy group or a cyano group which may have one or more halogen atoms,
- R 3 is a hydrogen atom or a methyl group, and R 6 has one or more halogen atoms.
- a C1-C4 alkyl group, a halogen atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, a C3-C5 cycloalkyl group optionally having one or more halogen atoms, 1 or more halogen atom has optionally may C2-C4 alkenyl group or also a C2-C4 alkynyl group, having one or more atoms or groups R 12 are selected from the group P 3 And is also good phenoxy group, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a methyl group, X is tetrazolinone compound is an oxygen atom;
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom, a halogen atom, or a C1-C4 alkyl optionally having one or more halogen atoms A C1-C4 alkoxy group or a cyano group which may have one or more halogen atoms,
- R 3 is a hydrogen atom or a methyl group, and R 6 has one or more halogen atoms.
- a C1-C4 alkyl group, a halogen atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, a C3-C5 cycloalkyl group optionally having one or more halogen atoms, 1 or more halogen atom has optionally may C2-C4 alkenyl group or also a C2-C4 alkynyl group, having one or more atoms or groups
- R 12 is selected from the group P 4 And is also a phenyl group, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a methyl group,
- X is tetrazolinone compound is an oxygen atom;
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom, a halogen atom, or a C1-C4 alkyl optionally having one or more halogen atoms A C1-C4 alkoxy group or a cyano group which may have one or more halogen atoms,
- R 3 is a hydrogen atom or a methyl group, and R 6 has one or more halogen atoms.
- a C1-C4 alkyl group, a halogen atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, a C3-C5 cycloalkyl group optionally having one or more halogen atoms, 1 or more halogen atom has optionally may C2-C4 alkenyl group or also a C2-C4 alkynyl group, having one or more atoms or groups
- R 12 is selected from the group P 4 And is also good phenoxy group, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a methyl group, X is tetrazolinone compound is an oxygen atom;
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom, a halogen atom, or a C1-C4 alkyl optionally having one or more halogen atoms A C1-C4 alkoxy group which may have one or more halogen atoms, or a cyano group
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group, an ethyl group, a cyclopropyl group, A chlorine atom, a bromine atom, a methoxy group, an ethoxy group, or a trifluoromethyl group
- R 12 is a phenyl group optionally having one or more atoms or groups selected from group P 3 , R 4 , A tetrazolinone compound in which R 5 , R 7 , R 8
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom, a halogen atom, or a C1-C4 alkyl optionally having one or more halogen atoms A C1-C4 alkoxy group which may have one or more halogen atoms, or a cyano group
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group, an ethyl group, a cyclopropyl group, A chlorine atom, a bromine atom, a methoxy group, an ethoxy group, or a trifluoromethyl group
- R 12 is a phenoxy group that may have one or more atoms or groups selected from group P 3 , R 4 , A tetrazolinone compound in which R 5 , R 7 , R 8
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom, a halogen atom, or a C1-C4 alkyl optionally having one or more halogen atoms A C1-C4 alkoxy group which may have one or more halogen atoms, or a cyano group
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group, an ethyl group, a cyclopropyl group, A chlorine atom, a bromine atom, a methoxy group, an ethoxy group, or a trifluoromethyl group
- R 12 is a phenyl group that may have one or more atoms or groups selected from group P 4 , R 4 , A tetrazolinone compound in which R 5 , R 7 , R 8
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom, a halogen atom, or a C1-C4 alkyl optionally having one or more halogen atoms A C1-C4 alkoxy group which may have one or more halogen atoms, or a cyano group
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group, an ethyl group, a cyclopropyl group, A chlorine atom, a bromine atom, a methoxy group, an ethoxy group, or a trifluoromethyl group
- R 12 is a phenoxy group that may have one or more atoms or groups selected from group P 4 , R 4 , A tetrazolinone compound in which R 5 , R 7 , R 8
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 is 1 or more A C1-C4 alkyl group optionally having one halogen atom, a halogen atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, and a C3 optionally having one or more halogen atoms -C5 cycloalkyl group, one or more halogen atoms or C2-C4 alkenyl group or have a, a C2-C4 alkynyl group, have the one or more atoms or groups
- R 12 is selected from the group P 3 a phenyl group which may have, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 is 1 or more A C1-C4 alkyl group optionally having one halogen atom, a halogen atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, and a C3 optionally having one or more halogen atoms -C5 cycloalkyl group, one or more halogen atoms or C2-C4 alkenyl group or have a, a C2-C4 alkynyl group, have the one or more atoms or groups
- R 12 is selected from the group P 3 a good phenoxy group which may, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 is 1 or more A C1-C4 alkyl group optionally having one halogen atom, a halogen atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, and a C3 optionally having one or more halogen atoms -C5 cycloalkyl group, one or more halogen atoms or C2-C4 alkenyl group or have a, a C2-C4 alkynyl group, have the one or more atoms or groups
- R 12 is selected from the group P 4 a phenyl group which may have, R 4, R 5, R 7, R 8, R 9 and R 11 is hydrogen atom, R 10 is a
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 is 1 or more C1-C4 alkyl group optionally having halogen atom, halogen atom, C1-C4 alkoxy group optionally having one or more halogen atoms, C3-C1 optionally having one or more halogen atoms
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group
- R 12 may have one or more atoms or groups selected from the group P 3 A tetrazolinone compound in which R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are a hydrogen atom, R 10 is a methyl group, and X is an oxygen atom;
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group
- R 12 may have one or more atoms or groups selected from the group P 3 A tetrazolinone compound in which R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are a hydrogen atom, R 10 is a methyl group, and X is an oxygen atom;
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group
- R 12 may have one or more atoms or groups selected from group P 4 A tetrazolinone compound in which R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are a hydrogen atom, R 10 is a methyl group, and X is an oxygen atom;
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group
- a phenoxy which is an ethyl group, a cyclopropyl group, a chlorine atom, a bromine atom, a methoxy group, an ethoxy group, or a trifluoromethyl group
- R 12 may have one or more atoms or groups selected from the group P 4 A tetrazolinone compound in which R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are a hydrogen atom, R 10 is a methyl group, and X is an oxygen atom;
- R 1 is a methyl group, an ethyl group, a fluorine atom, a chlorine atom, a bromine atom or a trifluoromethyl group:
- R 2 is a hydrogen atom
- R 3 is a hydrogen atom or a methyl group
- R 6 is a methyl group
- R 12 may have one or more atoms or groups selected from group P 4 A phenoxy group optionally having one or more atoms or groups selected from the group or group P 4 , wherein R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms;
- a tetrazolinone compound in which 10 is a methyl group and X is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- a tetrazolinone compound which is a C7-C18 aralkyl group, R 10 is a methyl group, and X is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- a tetrazolinone compound which is a C7-C18 aralkyloxy group, R 10 is a methyl group, and X is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C3 alkyl group that may have one, a C1-C3 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C3 alkyl group that may have one, a C1-C3 alkoxy group that may have one or more halogen atoms, or a cyano group, and R 6 may have one or more halogen atoms.
- a C2-C4 alkenyl group which may have one or more halogen atoms, or a C2-C4 alkynyl group, and R 12 may have one or more halogen atoms.
- a tetrazolinone compound which is a group or a C3-C6 cycloalkenyl group optionally having one or more halogen atoms, R 10 is a methyl group, and X is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group which may have one, a C1-C4 alkoxy group which may have one or more halogen atoms or a cyano group, R 6 is a methyl group, and R 12 is from group P 3
- a phenyl group which may have one or more selected atoms or groups, R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms, and R 10 is a methyl group Yes, X is Tetrazolinone compound is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group which may have one, a C1-C4 alkoxy group which may have one or more halogen atoms, or a cyano group
- R 6 is an ethyl group
- R 12 is from group P 3
- a phenyl group which may have one or more selected atoms or groups
- R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- R 10 is a methyl group Yes
- X is Tetrazolinone compound is an oxygen atom
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group which may have one, a C1-C4 alkoxy group which may have one or more halogen atoms or a cyano group, R 6 is a cyclopropyl group, and R 12 is a group P 3.
- a phenyl group which may have one or more atoms or groups selected from R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms, and R 10 is a methyl group
- X tetrazolinone compound wherein A represents an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group which may have one, a C1-C4 alkoxy group which may have one or more halogen atoms or a cyano group, R 6 is a chlorine atom, and R 12 is from group P 3
- a phenyl group which may have one or more selected atoms or groups, R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms, and R 10 is a methyl group Yes, X is Tetrazolinone compound is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group which may have one, a C1-C4 alkoxy group which may have one or more halogen atoms or a cyano group, R 6 is a bromine atom, and R 12 is from group P 3
- a phenyl group which may have one or more selected atoms or groups, R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms, and R 10 is a methyl group Yes, X is Tetrazolinone compound is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group that may have one, a C1-C4 alkoxy group that may have one or more halogen atoms, or a cyano group
- R 6 is a methoxy group
- R 12 is from group P 3
- a phenyl group which may have one or more selected atoms or groups
- R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- R 10 is a methyl group Yes
- X Tetrazolinone compound is an oxygen atom
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group which may have one, a C1-C4 alkoxy group which may have one or more halogen atoms or a cyano group, R 6 is an ethoxy group, and R 12 is from group P 3
- a phenyl group which may have one or more selected atoms or groups, R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms, and R 10 is a methyl group Yes, X Tetrazolinone compound is an oxygen atom;
- R 1 has a C1-C3 alkyl group which may have one or more halogen atoms, a hydrogen atom, a C2-C3 alkynyl group which may have one or more halogen atoms, and one or more halogen atoms.
- a C1-C4 alkyl group which may have one, a C1-C4 alkoxy group which may have one or more halogen atoms or a cyano group, R 6 is a trifluoromethyl group, and R 12 is a group P.
- 3 is a phenyl group optionally having one or more atoms or groups selected from 3 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms, and R 10 is methyl Base There, X tetrazolinone compound wherein A represents an oxygen atom;
- R 1 is a hydrogen atom, a C1-C6 alkyl group which may have one or more atoms or groups selected from group P 1 or a halogen atom
- R 2 is a hydrogen atom, one or more selected from group P 1 A C1-C6 alkyl group optionally having one or more atoms, a C1-C6 alkoxy group optionally having one or more halogen atoms, or a cyano group
- R 3 is a hydrogen atom, or group P A C1-C6 alkyl group which may have one or more atoms or groups selected from 1,
- R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- R 6 May have a C1-C6 alkyl group optionally having one or more halogen atoms, a C1-C6 alkoxy group optionally having one or more halogen atoms, or may have one or more halogen atoms.
- an R 10 is 1 or more halogen atoms C1-C3 alkyl group which may have a
- R 12 may have one or more atoms or groups selected from the group P 2 good C6-C16 aryl group, have one or more atoms or C6-C16 aryloxy group has a group
- one or more atoms or groups selected from the group P 2 is selected from the group P 2 may also be C7-C18 aralkyl group
- 1 or more atoms may be C7-C18 aralkyloxy group optionally having a group selected from the group P 2
- R 1 is a hydrogen atom, a C1-C6 alkyl group or a halogen atom
- R 2 is a hydrogen atom, a C1-C6 alkyl group, a C1-C6 alkoxy group, or a cyano group
- R 3 is a hydrogen atom, or C1- A C6 alkyl group
- R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- R 6 is a C1-C6 alkyl group, a C1-C6 alkoxy group, or a C3-C6 cycloalkyl group.
- R 10 is a C1-C3 alkyl group
- R 12 may have one or more halogen atoms, C1-C4 alkyl group, halogen atom, C1-C4 alkoxy group, C1-C4 alkylthio group 1 or more selected from the group consisting of cyano group, C1-C4 alkylcarbonyl group, C1-C4 alkylsulfonyl group and C2-C4 alkylcarbonylamino group
- a phenyl group optionally having an atom or group of A phenoxy group optionally having one or more atoms or groups selected from the group consisting of a C1-C4 alkyl group, a C1-C4 alkoxy group, a halogen atom and a cyano group
- a C7-C10 aralkyl group optionally having one or more C1-C4 alkoxy groups and / or hydroxy groups, A C7-C10 aralkyloxy group,
- C1-C6 alkyl group or C2-C9 heteroaryloxy group (wherein the heteroaryl moiety is a 5-membered ring, a 6-membered ring, a 5-membered ring, a 5-membered condensed ring, a 5-membered ring and a 6-membered condensed ring, or A tetrazolinone compound in which X is an oxygen atom [Group P 4 : methyl group, ethyl group, fluorine atom, chlorine atom, cyano group, methoxy group, ethoxy group, trifluoro group] A group consisting of a methyl group, a cyclopropyl group and a methylthio group];
- R 1 is a C1-C6 alkyl group optionally having one or more halogen atoms, a halogen atom or a hydrogen atom
- R 2 is a C1-C6 alkyl group optionally having one or more halogen atoms.
- R 3 is a hydrogen atom, a halogen atom or a C1-C6 alkyl group
- R 6 May have a C1-C6 alkyl group optionally having one or more halogen atoms, a C1-C6 alkoxy group optionally having one or more halogen atoms, or may have one or more halogen atoms.
- C3-C6 cycloalkyl group one or more atoms which may have a group C6-C16 aryl group R 12 is selected from the group P 2 (provided that the C6-C16 aryl Is a C1-C6 alkyl group optionally having one or more halogen atoms, a halogen atom, a cyano group, a C1-C6 alkoxy group optionally having one or more halogen atoms, and one or more halogen atoms.
- R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms, and R 10 is one or more halogen atoms.
- a tetrazolinone compound which is a C1-C3 alkyl group optionally having an atom, and X is an oxygen atom.
- R 1 is a C1-C6 alkyl group optionally having one or more halogen atoms, a halogen atom or a hydrogen atom
- R 2 is a C1-C6 alkyl group optionally having one or more halogen atoms.
- R 3 is a hydrogen atom, a halogen atom or a C1-C6 alkyl group
- R 6 is a C1-C6 alkyl group, a C1-C6 alkoxy group.
- a C3-C6 cycloalkyl group and R 12 is a phenyl group (provided that the phenyl group may have one or more halogen atoms, a C1-C6 alkyl group, a halogen atom, a cyano group, C1- C6-alkoxy group, C1-C6 alkylthio group, C1-C6 alkylsulfonyl group, C2-C6 alkylcarbonyl group, and C2-C6 alkylcarbo group
- Arylamino a selected from the group consisting of groups may have one or more atoms or groups.
- R 4, R 5 , R 7, R 8, R 9 and R 11 are hydrogen atoms
- R A tetrazolinone compound in which 10 is a C1-C3 alkyl group and X is an oxygen atom
- a tetrazolinone compound in which R 6 is a C1-C6 alkyl group
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 may be a C1-C6 alkyl group which may have one or more halogen atoms.
- R 12 is a phenoxy group (provided that the phenoxy group is One or more selected from the group consisting of a C1-C6 alkyl group optionally having one or more halogen atoms, a halogen atom, a cyano group, and a C1-C6 alkoxy group optionally having one or more halogen atoms
- R 2 , R 3 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms, and R 10 is 1 or more.
- R 1 is a C1-C6 alkyl group or a hydrogen atom
- R 6 is a C1-C6 alkyl group C1-C6 alkoxy group, or a C3-C6 cycloalkyl group
- R 12 is a phenoxy group (provided that the phenoxy group is , A C1-C6 alkyl group, a halogen atom, a cyano group, and a C1-C6 alkoxy group, which may have one or more atoms or groups.)
- R 2 , R 3 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- R 10 is a C1-C3 alkyl group optionally having one or more halogen atoms
- X is an oxygen atom A tetrazolinone compound
- a tetrazolinone compound in which R 6 is a C1-C6 alkyl group
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 may be a C1-C6 alkyl group which may have one or more halogen atoms, or one or more A C1-C6 alkoxy group which may have a halogen atom
- R 12 is a C2-C6 alkoxycarbonyl group
- X is an oxygen atom
- a tetrazolinone compound in which R 6 is a C1-C6 alkyl group
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 may be a C1-C6 alkyl group which may have one or more halogen atoms, or one or more A C1-C6 alkoxy group which may have a halogen atom
- R 12 represents one or more atoms or groups selected from a hydroxy group and a C1-C6 alkoxy group which may have one or more halogen atoms.
- R 6 a tetrazolinone compound in which R 6 is a C1-C6 alkyl group
- a tetrazolinone compound in which R 6 is a C1-C6 alkoxy group.
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 may be a C1-C6 alkyl group which may have one or more halogen atoms, or one or more A C1-C6 alkoxy group which may have a halogen atom
- R 12 is a C2-C6 alkenyl group which may have one or more halogen atoms
- R 2 , R 3 , R 4 , R 5 a tetrazolinone compound in which R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- R 10 is a C1-C3 alkyl group optionally having one or more halogen atoms
- X is an oxygen atom
- a tetrazolinone compound in which R 6 is a C1-C6 alkyl group
- R 1 is a C1-C6 alkyl group optionally having one or more halogen atoms, a halogen atom or a hydrogen atom
- R 6 is a C1-C6 alkyl group optionally having one or more halogen atoms
- R 12 is a C1-C6 alkyl group optionally having one or more C1-C3 alkoxy groups and / or halogen atoms
- R 2 , R 3 , R 4 , R 5 , R 7 , R 8 A tetrazolinone compound in which R 9 and R 11 are hydrogen atoms, R 10 is a C1-C3 alkyl group optionally having one or more halogen atoms, and X is an oxygen atom;
- R 6 is a C1-C6 alkyl group which may have one or more halogen atoms
- R 12 is a C1-C6 alkylsulfonyl group which may have one or more halogen atoms
- R 1 , R 2 , R 3 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- R 10 is a C1-C3 alkyl group optionally having one or more halogen atoms.
- a tetrazolinone compound wherein X is an oxygen atom;
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 is a C1-C6 alkyl group which may have one or more halogen atoms
- R 12 is an anilino group optionally having one or more C1-C6 alkyl groups
- R 2 , R 3 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms.
- a tetrazolinone compound in which R 10 is a C1-C3 alkyl group optionally having one or more halogen atoms, and X is an oxygen atom;
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 is a C1-C6 alkyl group which may have one or more halogen atoms
- R 2 , R 3 , R 4 , R 5 , R 7 , R 8 , R 9 and R which 12 may have one or more atoms or groups selected from group P 2
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 is a C1-C6 alkyl group which may have one or more halogen atoms
- R 12 1 or more atoms may be C7-C16 aryloxyalkyl group having a group selected from group P 2, R 2, R 3 , R 4, R 5, R 7, R 8, R 9 and A tetrazolinone compound in which R 11 is a hydrogen atom, R 10 is a C1-C3 alkyl group optionally having one or more halogen atoms, and X is an oxygen atom;
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 is a C1-C6 alkyl group which may have one or more halogen atoms
- R 12 is a C3-C6 cycloalkyl group optionally having one or more halogen atoms
- R 2 , R 3 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms.
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 is a C1-C6 alkyl group which may have one or more halogen atoms
- R 12 is an aminocarbonyl group optionally having a C1-C6 alkyl group
- R 2 , R 3 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- a tetrazolinone compound in which 10 is a C1-C3 alkyl group optionally having one or more halogen atoms, and X is an oxygen atom;
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 is a C1-C6 alkyl group which may have one or more halogen atoms
- R 12 is a C3-C6 cycloalkenyl group optionally having one or more halogen atoms
- R 2 , R 3 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms.
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 is a C1-C6 alkyl group which may have one or more halogen atoms
- R 12 is a C2-C6 alkylcarbonyloxy group
- R 2 , R 3 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- R 10 is one or more halogen atoms
- a tetrazolinone compound that is an optionally substituted C1-C3 alkyl group and X is an oxygen atom;
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 is a C1-C6 alkyl group which may have one or more halogen atoms
- R 12 is R 13 R 14 N—CH ⁇ N—
- R 2 , R 3 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- R 10 is 1 or more A tetrazolinone compound which is a C1-C3 alkyl group optionally having a halogen atom, and X is an oxygen atom;
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 is a C1-C6 alkyl group which may have one or more halogen atoms
- R 12 is R 13 R 14 N—N ⁇ CH—
- R 2 , R 3 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- R 10 is 1 or more A tetrazolinone compound which is a C1-C3 alkyl group optionally having a halogen atom
- X is an oxygen atom
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 6 is a C1-C6 alkyl group which may have one or more halogen atoms
- R 12 is a C2-C9 heteroaryloxy group
- R 2 , R 3 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- R 10 is one or more halogen atoms
- a tetrazolinone compound which is an optionally substituted C1-C3 alkyl group and X is an oxygen atom;
- R 1 is a C1-C6 alkyl group optionally having one or more halogen atoms
- R 2 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms
- 3 and R 10 are each a C1-C3 alkyl group optionally having one or more halogen atoms
- R 6 is a C1-C4 alkyl group optionally having one or more halogen atoms, a halogen atom, 1
- a C1-C4 alkoxy group optionally having one or more halogen atoms or a C3-C5 cycloalkyl group optionally having one or more halogen atoms
- R 12 is a phenyl group (provided that the phenyl group is One or more selected from the group consisting of a C1-C3 alkyl group optionally having one or more halogen atoms, a halogen atom, a cyano group, and a C
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 2 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms.
- R 3 and R 10 are each a C1-C3 alkyl group optionally having one or more halogen atoms
- R 6 is a C1-C6 alkyl group optionally having one or more halogen atoms, halogen An atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, or a C3-C5 cycloalkyl group optionally having one or more halogen atoms
- R 12 is a phenyl group (provided that The phenyl group is selected from the group consisting of a C1-C3 alkyl group optionally having one or more halogen atoms, a halogen atom, a cyano group, and a C1-C3 alkoxy group optionally having one or more halogen atoms. . Which may have one or more atoms or groups), and tetrazolinone compounds wherein X is an oxygen atom;
- R 1 is a C1-C6 alkyl group which may have one or more halogen atoms or a hydrogen atom
- R 2 , R 4 , R 5 , R 7 , R 8 , R 9 and R 11 are hydrogen atoms.
- R 3 and R 10 are each a C1-C3 alkyl group optionally having one or more halogen atoms
- R 6 is a C1-C6 alkyl group optionally having one or more halogen atoms, halogen An atom, a C1-C4 alkoxy group optionally having one or more halogen atoms, or a C3-C5 cycloalkyl group optionally having one or more halogen atoms
- R 12 is a phenoxy group (provided that The phenoxy group is a group consisting of a C1-C3 alkyl group which may have one or more halogen atoms, a halogen atom, a cyano group, and a C1-C3 alkoxy group which may have one or more halogen atoms. It may have one or more atoms or groups selected.), And tetrazolinone compounds wherein X is an oxygen atom.
- the structural formula of a compound may represent a certain isomer for convenience, but the present invention includes all active geometric isomers, optical isomers, stereoisomers, It includes isomers of mutated isomers and isomer mixtures, and is not limited to the description of the formula for convenience, and may be either isomer or a mixture. Therefore, it may have an asymmetric carbon atom in the molecule, and an optically active substance and a racemate may exist.
- the present invention is not particularly limited and includes any case.
- the compound of the present invention can be produced, for example, by the following production method.
- (Production method A) (Hereinafter referred to as compound (1)) is a compound represented by formula (A1) (hereinafter referred to as compound (A1)) and a compound represented by formula (A2) (hereinafter referred to as compound (A2)).
- R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R 8 , R 9 , R 10 , R 11 , R 12 and X represent the same meaning as above, Z 11 represents a leaving group such as a chlorine atom, a bromine atom, an iodine atom, a methanesulfonyloxy group, a trifluoromethanesulfonyloxy group, or a p-toluenesulfonyloxy group.
- the reaction is usually performed in a solvent.
- Examples of the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone, N-methylpyrrolidone, etc.
- hydrocarbons such as n-hexane, cyclohexane, toluene and xylene
- ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether,
- Acid amides esters such as ethyl acetate and methyl acetate, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone, nitriles such as acetonitrile, water and Mixtures of al and the like.
- the base used for the reaction include organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene, and alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- alkali metal hydrogen carbonate such as sodium hydrogen carbonate
- alkali metal hydroxide such as lithium hydroxide, sodium hydroxide, potassium hydroxide, cesium hydroxide
- alkali such as sodium fluoride, potassium fluoride, cesium fluoride
- metal halides alkali metal hydrides such as lithium hydride, sodium hydride and potassium hydride
- alkali metal alkoxides such as sodium tert-butoxide and potassium tert-butoxide.
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- sodium iodide, tetrabutylammonium iodide or the like may be added as necessary, and these compounds are usually in a ratio of 0.001 to 1.2 mol with respect to 1 mol of the compound (A1).
- the compound (1) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer.
- the isolated compound of the present invention can be further purified by chromatography, recrystallization and the like.
- a compound in which R 12 is A 1 (hereinafter referred to as compound (1-1)) is a compound represented by formula (B1) (hereinafter referred to as compound (B1)) and a formula.
- the compound represented by (B2) (hereinafter referred to as compound (B2)) can be produced by subjecting it to a coupling reaction in the presence of a base and a catalyst.
- R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R 8 , R 9 , R 10 , R 11 and X represent the same meaning as described above, and A 1 represents a group 1 or more atoms may be C6-C16 aryl group optionally having a group selected from P 2, selected one or more halogen atoms optionally may C3-C6 cycloalkenyl group bonded to a carbon atom or a group P 2 1 Represents a C7-C18 aralkyl group which may have the above atoms or groups, Z 21 represents a chlorine atom, a bromine atom or an iodine atom, and Z 31 represents B (OH) 2 , an alkoxyboranyl group or a trifluoroboron group.
- the reaction is usually performed in a solvent.
- the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone, N-methylpyrrolidone, etc.
- Acid amides esters such as ethyl acetate and methyl acetate, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone, nitriles such as acetonitrile, methanol Ethanol, propanol, alcohols such as butanol, water and mixtures thereof.
- sulfoxides such as dimethyl sulfoxide
- ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone
- nitriles such as acetonitrile
- methanol Ethanol propanol
- alcohols such as butanol, water and mixtures thereof.
- B2 a commercially available compound is usually used, or N.I. Miyaura and A.M. Suzuki, Chem. Rev. , 1995, 95, 2457, etc., can also be used.
- Compounds used in the reaction (B2) are, for example, iodine compounds (A 1 - I) or bromo compound - after reaction with (A 1 Br) with an alkyl lithium such as butyl lithium, is reacted with boric acid ester
- a boronic acid ester derivative can be produced.
- a boronic acid derivative can be manufactured by hydrolyzing the boronic acid ester derivative obtained by the above-mentioned reaction as needed.
- Molander et al. Acc. Chem. Res. , 2007, 40, 275, etc. can be used to obtain the trifluoroborate salt BF 3 ⁇ K + by fluorinating the boronic ester with potassium hydrogen fluoride or the like.
- Catalysts used in the reaction include palladium (II) acetate, dichlorobis (triphenylphosphine) palladium, tetrakistriphenylphosphinepalladium (0), palladium (II) acetate / triscyclohexylphosphine, bis (diphenylphosphaneferrocenyl) ) Palladium (II) dichloride, 1,3-bis (2,6-diisopropylphenyl) imidazol-2-ylidene (1,4-naphthoquinone) palladium dimer, allyl (chloro) (1,3-dimesityl-1,3- Dihydro-2H-imidazol-2-ylidene) palladium or palladium (II) acetate / dicyclohexyl (2 ′, 4 ′, 6′-triisopropylbiphenyl-2-yl) phos
- Examples of the base used for the reaction include organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene, and alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene
- alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- alkali metal hydrogen carbonate such as sodium hydrogen carbonate
- alkali metal hydroxide such as lithium hydroxide, sodium hydroxide, potassium hydroxide, cesium hydroxide
- alkali such as sodium fluoride, potassium fluoride, cesium fluoride
- Metal halides alkali metal hydrides such as lithium hydride, sodium hydride, potassium hydride, alkali metal phosphates such as tripotassium phosphate, sodium methoxide, sodium ethoxide, sodium tert-butoxide, potassium tert- Alkali metal alkoxides such as Tokishido like.
- compound (B2) is usually used in a proportion of 1 to 10 mol
- base is usually in a proportion of 1 to 10 mol
- catalyst is usually used in a proportion of 0.0001 to 1 mol. It is done.
- the reaction temperature is usually in the range of 0 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (1-1) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer.
- the isolated compound of the present invention can be further purified by chromatography, recrystallization and the like.
- a compound in which A is A 1 (hereinafter referred to as compound (1-2)) is a compound represented by formula (C1) (hereinafter referred to as compound (C1)) and formula ( The compound represented by C2) (hereinafter referred to as compound (C2)) can be produced by subjecting it to a coupling reaction in the presence of a base and a catalyst.
- a coupling reaction in the presence of a base and a catalyst.
- R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R 8 , R 9 , R 10 , R 11 , A 1 , Z 21 , Z 31 and X are the same as above. Represents the same meaning.
- the reaction is usually performed in a solvent.
- Examples of the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone, N-methylpyrrolidone, etc.
- hydrocarbons such as n-hexane, cyclohexane, toluene and xylene
- ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether,
- Acid amides esters such as ethyl acetate and methyl acetate, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone, nitriles such as acetonitrile, water and Mixtures of al and the like.
- the compound (C2) used in the reaction a commercially available product can be used. Specific examples include bromobenzene, iodobenzene, 1-bromo-2-methylbenzene, and the like.
- Catalysts used in the reaction include palladium (II) acetate, dichlorobis (triphenylphosphine) palladium, tetrakistriphenylphosphinepalladium (0), palladium (II) acetate / triscyclohexylphosphine, bis (diphenylphosphaneferrocenyl) ) Palladium (II) dichloride, 1,3-bis (2,6-diisopropylphenyl) imidazol-2-ylidene (1,4-naphthoquinone) palladium dimer, allyl (chloro) (1,3-dimesityl-1,3- Dihydro-2H-imidazol-2-ylidene) palladium or palladium (II) acetate / dicyclohexyl (2 ′, 4 ′, 6′-triisopropylbiphenyl-2-yl) phos
- Examples of the base used for the reaction include organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene, and alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene
- alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- alkali metal hydrogen carbonate such as sodium hydrogen carbonate
- alkali metal hydroxide such as lithium hydroxide, sodium hydroxide, potassium hydroxide, cesium hydroxide
- alkali such as sodium fluoride, potassium fluoride, cesium fluoride
- Metal halides alkali metal hydrides such as lithium hydride, sodium hydride, potassium hydride, alkali metal phosphates such as tripotassium phosphate, sodium methoxide, sodium ethoxide, sodium tert-butoxide, potassium tert- Alkali metal alkoxides such as Tokishido like.
- compound (B2) is usually used in a proportion of 1 to 10 mol
- base is usually in a proportion of 1 to 10 mol
- catalyst is usually used in a proportion of 0.0001 to 1 mol. It is done.
- the reaction temperature is usually in the range of 0 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (1-2) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer.
- the isolated compound of the present invention can be further purified by chromatography, recrystallization and the like.
- Compound (1) includes a compound represented by formula (1-3) (hereinafter referred to as compound (1-3)) and a compound represented by formula (E1) (hereinafter referred to as compound (E1)).
- compound (1-3) a compound represented by formula (1-3)
- compound (E1) a compound represented by formula (E1)
- Examples of the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone, N-methylpyrrolidone, etc.
- hydrocarbons such as n-hexane, cyclohexane, toluene and xylene
- ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether,
- Acid amides esters such as ethyl acetate and methyl acetate, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone, nitriles such as acetonitrile, water and Mixtures of al and the like.
- sulfoxides such as dimethyl sulfoxide
- ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone
- nitriles such as acetonitrile
- halogenated alkyls such as methyl bromide, ethyl bromide, n-propyl bromide, methyl iodide, ethyl iodide, n-propyl iodide, isopropyl iodide, methyl p-toluenesulfonate, Sulfonic acid esters such as ethyl p-toluenesulfonate, n-propyl p-toluenesulfonate, methyl methanesulfonate, ethyl methanesulfonate, n-propyl methanesulfonate, and dimethyl sulfate, diethyl sulfate, di-n-sulfate And sulfates such as propyl.
- Examples of the base used for the reaction include organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene, and alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene
- alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- alkali metal hydrogen carbonate such as sodium hydrogen carbonate
- alkali metal hydroxide such as lithium hydroxide, sodium hydroxide, potassium hydroxide, cesium hydroxide
- alkali such as sodium fluoride, potassium fluoride, cesium fluoride
- Metal halides alkali metal hydrides such as lithium hydride, sodium hydride and potassium hydride
- alkali metal hydrides such as lithium hydride, sodium hydride and potassium hydride, sodium tert-butoxide, potassium tert-butoxide and the like
- alkali metal alkoxides alkali metal hydrogen carbonate
- alkali metal hydroxide such as lithium hydroxide, sodium hydroxide, potassium hydroxide, cesium hydroxide
- alkali such as sodium fluoride, potassium fluoride, cesium fluoride
- Metal halides alkali metal hydrides such as lithium hydride, sodium hydride and potassium hydride
- alkali metal hydrides such as lithium
- the compound (E1) is usually used in a proportion of 1 to 10 mol, and the base is usually used in a proportion of 1 to 10 mol.
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (1) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer.
- the isolated compound of the present invention can be further purified by chromatography, recrystallization and the like.
- Examples of the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Examples thereof include halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, and chlorobenzene, nitriles such as acetonitrile, and mixtures thereof.
- hydrocarbons such as n-hexane, cyclohexane, toluene and xylene
- ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and di
- sulfurizing agent used in the reaction examples include phosphorus pentasulfide and Lawesson's reagent (2,4-bis (4-methoxyphenyl) -1,3,2,4-dithiadiphosphatane 2,4-disulphide).
- a sulfiding agent is preferably used in a proportion of 0.5 to 1.5 mol with respect to 1 mol of the compound (1-O).
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- an organic base such as pyridine or triethylamine, an inorganic base such as an alkali metal hydroxide or an alkali metal carbonate, and the like may be added. It is 0.5 to 1.5 mol with respect to.
- the compound (1-S) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer.
- the isolated compound of the present invention can be further purified by chromatography, recrystallization and the like.
- a compound represented by the formula (1-4) in which R 6 is R 71 (hereinafter referred to as a compound (1-4)) is a compound represented by the formula (G1) (hereinafter referred to as a compound (1)).
- Compound (G1)) and a compound represented by formula (G21) (hereinafter referred to as compound (G21)) can be produced by subjecting to a coupling reaction in the presence of a base and a catalyst.
- R 1 , R 2 , R 3 , R 4 , R 5 , R 7 , R 8 , R 9 , R 10 , R 11 , R 12 and Z 31 represent the same meaning as described above, and Z 41 represents Represents a chlorine atom, a bromine atom, an iodine atom or a trifluoromethanesulfonyloxy group, and R 71 may have one or more halogen atoms, a C1-C6 alkyl group, and may have one or more halogen atoms.
- a C2-C6 alkenyl group, a C2-C6 alkynyl group optionally having one or more halogen atoms, or a C3-C6 cycloalkyl group optionally having one or more halogen atoms is represented.
- the reaction can be carried out according to the reaction described in Production Method B.
- a compound represented by formula (1-5) in which R 7 is R 72 (hereinafter referred to as compound (1-5)) is a compound represented by formula (G2) (hereinafter referred to as compound (1)).
- Compound (G2)) and the compound represented by formula (G22) (hereinafter referred to as compound (G22)) can be produced by subjecting to a coupling reaction in the presence of a base and a catalyst.
- R 72 represents a C1-C4 alkyl group optionally having one or more halogen atoms or a C3-C5 cycloalkyl group optionally having one or more halogen atoms.
- compound (G3) a compound represented by formula (1-6) in which R 8 is R 72 (hereinafter referred to as compound (1-6)) is a compound represented by formula (G3) (hereinafter referred to as “compound (G3)”).
- Compound (G3)) and compound (G22) can be produced by subjecting them to a coupling reaction in the presence of a base and a catalyst. [Wherein the symbols have the same meaning as described above. ] The reaction can be carried out according to the reaction described in Production Method B.
- a compound represented by formula (1-7) in which R 9 is R 72 (hereinafter referred to as compound (1-7)) is a compound represented by formula (G4) (hereinafter referred to as compound (1)).
- Compound (G4)) and compound (G22) can be produced by subjecting them to a coupling reaction in the presence of a base and a catalyst. [Wherein the symbols have the same meaning as described above. ] The reaction can be carried out according to the reaction described in Production Method B.
- a compound in which two or more substituents selected from R 6 , R 7 , R 8 and R 9 in the compound (1) is any one of R 71 and R 72 can be produced.
- Compound (1) can also be produced by using another known coupling reaction instead of the coupling reaction of Production Method B.
- a compound represented by formula (1-8) in which R 1 is R 73 (hereinafter referred to as compound (1-8)) is a compound represented by formula (H1) (hereinafter referred to as “compound (1)”).
- Compound (H1)) and a compound represented by formula (H21) (hereinafter referred to as compound (H21)) can be produced by subjecting to a coupling reaction in the presence of a base and a catalyst.
- R 73 is 1 or more atoms C1-C6 alkyl group optionally having a group selected from the group P 1; one or more atoms or groups C3-C6 cycloalkyl group selected from the group P 1; 1 or more A C2-C6 alkenyl group optionally having a halogen atom; or a C2-C6 alkynyl group optionally having one or more halogen atoms.
- the reaction can be carried out according to the reaction described in Production Method B.
- a compound represented by the formula (1-9) in which R 2 is R 73 (hereinafter referred to as a compound (1-9)) is a compound represented by the formula (H2) (hereinafter referred to as a compound (1)).
- Compound (H2)) and compound (H21) can be produced by subjecting them to a coupling reaction in the presence of a base and a catalyst. [Wherein the symbols have the same meaning as described above. ] The reaction can be carried out according to the reaction described in Production Method B.
- a compound represented by the formula (1-10) in which R 3 is R 73 (hereinafter referred to as a compound (1-10)) is a compound represented by the formula (H3) (hereinafter referred to as a compound (1)). It can be prepared by subjecting compound (H3)) and compound (H21) to a coupling reaction in the presence of a base and a catalyst. [Wherein the symbols have the same meaning as described above. ] The reaction can be carried out according to the reaction described in Production Method B.
- a compound represented by formula (1-11) in which R 11 is R 73 (hereinafter referred to as compound (1-11)) is a compound represented by formula (H4) (hereinafter referred to as “compound”). It can be prepared by subjecting compound (H4)) and compound (H21) to a coupling reaction in the presence of a base and a catalyst. [Wherein the symbols have the same meaning as described above. ] The reaction can be carried out according to the reaction described in Production Method B.
- the compound (1) can also be produced by using another known coupling reaction instead of the coupling reaction of the production method B.
- R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R 8 , R 9 , R 10 , R 11 , Z 21 and X represent the same meaning as described above, and A 1 or more atoms may be C6-C16 aryl group optionally having a group, one or more atoms or C7-C18 aralkyl which may have a group selected from the group P 2 is selected 2 from the group P 2 have one or more atoms or groups selected from the group or the group P 2 represents a heteroaryl group.
- the reaction is usually performed in a solvent.
- Examples of the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone, N-methylpyrrolidone, etc.
- hydrocarbons such as n-hexane, cyclohexane, toluene and xylene
- ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether,
- Acid amides esters such as ethyl acetate and methyl acetate, sulfoxides such as dimethyl sulfoxide, nitriles such as acetonitrile, and mixtures thereof.
- the catalyst used in the reaction include copper (I) iodide, copper (I) bromide, copper (I) chloride, copper (I) oxide and copper (II) acetate.
- the ligand used in the reaction include ethylenediamine, 2-picolinic acid, N-butylimidazole, and dipivaloylmethane.
- Examples of the base used for the reaction include organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene, and alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene
- alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- alkali metal hydrogen carbonate such as sodium hydrogen carbonate
- alkali metal hydroxide such as lithium hydroxide, sodium hydroxide, potassium hydroxide, cesium hydroxide
- alkali such as sodium fluoride, potassium fluoride, cesium fluoride
- Metal halides alkali metal hydrides such as lithium hydride, sodium hydride, potassium hydride, alkali metal phosphates such as tripotassium phosphate, sodium methoxide, sodium ethoxide, sodium tert-butoxide, potassium tert- Alkali metal alkoxides such Tokishido like.
- compound (B2) is usually used in a proportion of 1 to 10 mol
- base is usually in a proportion of 1 to 10 mol
- catalyst is usually used in a proportion of 0.0001 to 1 mol. It is done.
- the reaction temperature is usually in the range of 0 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 72 hours.
- the compound (1-12) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer.
- the isolated compound of the present invention can be further purified by chromatography, recrystallization and the like.
- a compound in which R 12 is A 4 (hereinafter referred to as compound (1-13)) is a compound represented by formula (J1) (hereinafter referred to as compound (J1)) and a formula.
- a compound represented by (J2) (hereinafter referred to as compound (J2)) can be produced by subjecting it to a coupling reaction in the presence of a base, a catalyst and a ligand.
- a 4 may have one or more atoms or groups selected from the group P 2 C6-C16 aryloxy group, one or more atoms or groups may have a C7-C18 selected from the group P 2 aralkyloxy group may have one or more atoms or groups selected from one or more atoms or groups may have a C6-C16 arylthio group, or a group P 2 selected from the group P 2 C2- C9 heteroaryloxy group (wherein the heteroaryl moiety is a 5-membered ring, a 6-membered ring, a 5-membered ring, a 5-membered ring, a 5-membered ring or a 6-membered ring, A condensed ring).
- the reaction can be
- a compound represented by formula (XA3) (hereinafter referred to as compound (XA3)) is a compound represented by formula (XA1) (hereinafter referred to as compound (XA1)) or a compound represented by formula (XA2) ( Hereinafter, it can be produced by reacting compound (XA2)) with an azidating agent.
- R 101 represents P 11 , P 12 or P 13
- R 91 represents a C1-C12 alkyl group
- Z 101 represents a chlorine atom or a bromine atom
- a wavy line represents a binding site.
- Examples of the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone, N-methylpyrrolidone, etc.
- hydrocarbons such as n-hexane, cyclohexane, toluene and xylene
- ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether,
- Acid amides esters such as ethyl acetate and methyl acetate, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone, nitriles such as acetonitrile and the like Mixtures thereof.
- the azidating agent used in the reaction include inorganic azides such as sodium azide, barium azide or lithium azide, and organic azides such as trimethylsilyl azide and diphenylphosphoryl azide.
- the azidating agent is usually used in a ratio of 1 to 10 mol per 1 mol of the compound (XA1) or the compound (XA2).
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- a Lewis acid such as aluminum chloride or zinc chloride may be added as necessary, and these compounds are usually added in an amount of 0.05 to 5 to 1 mol of the compound (XA1) or the compound (XA2). Used in molar proportions.
- the compound (XA3) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. The isolated compound (XA3) can be further purified by chromatography, recrystallization and the like.
- Compound (XA1) can be produced by reacting a compound represented by formula (XB1) (hereinafter referred to as compound (XB1)) with an isocyanate agent. [Wherein the symbols have the same meaning as described above. ] The reaction is usually performed in a solvent.
- Examples of the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, esters such as ethyl acetate and methyl acetate, ketones such as acetone, methyl ethyl ketone, and methyl isobutyl ketone, acetonitrile, etc.
- hydrocarbons such as n-hexane, cyclohexane, toluene and xylene
- ethers such as tetrahydro
- Nitriles and mixtures thereof examples include phosgene, diphosgene, triphosgene, thiophosgene, N, N-carbodiimidazole, N, N-thiocarbodiimidazole, and the like.
- an isocyanate agent is usually used in a proportion of 0.34 to 10 mol per 1 mol of compound (XB1).
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the reaction may be carried out, if necessary, by using an organic base such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine, diazabicycloundecene, alkali metal carbonate such as lithium carbonate, sodium carbonate or potassium carbonate. Salts, alkali metal hydrogen carbonates such as sodium hydrogen carbonate and the like may be added, and these compounds are usually used at a ratio of 0.05 to 5 mol with respect to 1 mol of compound (XB1).
- the compound (XA1) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- Compound (XA2) can be produced by reacting a compound represented by the formula (XC1) (hereinafter referred to as compound (XC1)) with a halogenating agent. [Wherein the symbols have the same meaning as described above. ] The reaction is usually performed in a solvent.
- Examples of the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, esters such as ethyl acetate and methyl acetate, ketones such as acetone, methyl ethyl ketone, and methyl isobutyl ketone, acetonitrile, etc.
- hydrocarbons such as n-hexane, cyclohexane, toluene and xylene
- ethers such as tetrahydro
- Examples include oxalyl, oxalyl dibromide, triphosgene, diphosgene, phosgene, and sulfuryl chloride.
- the halogenating agent is usually used at a ratio of 1 to 10 mol per 1 mol of the compound (XC1).
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- a catalyst may be added, and N, N-dimethylformamide or the like is used.
- the amount of the catalyst used is usually 0.001 to 1 mol with respect to 1 mol of compound (XC1).
- the reaction may be carried out as necessary with an organic base such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine, diazabicycloundecene, or an alkali metal carbonate such as lithium carbonate, sodium carbonate or potassium carbonate.
- Salts, alkali metal hydrogen carbonates such as sodium hydrogen carbonate and the like may be added, and these compounds are usually used at a ratio of 0.05 to 5 mol with respect to 1 mol of compound (XC1).
- the compound (XA2) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- Compound (XA1) is obtained by reacting compound (XB1) with a carbamate agent to obtain a compound represented by formula (XD1) (hereinafter referred to as compound (XD1)), and then compound (XD1) and isocyanate. It can be produced by reacting with an agent.
- XD1 a compound represented by formula (XD1)
- R 6 , R 7 , R 8 , R 9 , R 101 and X represent the same meaning as described above, and R 111 represents a C1-C12 alkyl group or a phenyl group.
- the reaction is usually performed in a solvent.
- the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone, N-methylpyrrolidone, etc.
- Acid amides esters such as ethyl acetate and methyl acetate, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone, nitriles such as acetonitrile, water and Mixtures of al and the like.
- Carbamate agents used in the reaction include phenyl chlorocarbonate, methyl chlorocarbonate, ethyl chlorocarbonate, n-propyl chlorocarbonate, isopropyl chlorocarbonate, n-butyl chlorocarbonate, tert-butyl chlorocarbonate, di-tert dicarbonate.
- the carbamate agent is usually used at a ratio of 1 to 10 moles relative to 1 mole of the compound (XB1).
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the reaction may be carried out, if necessary, by using an organic base such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine, diazabicycloundecene, alkali metal carbonate such as lithium carbonate, sodium carbonate or potassium carbonate. Salts, alkali metal hydrogen carbonates such as sodium hydrogen carbonate and the like may be added, and these compounds are usually used at a ratio of 0.05 to 5 mol with respect to 1 mol of compound (XB1).
- the compound (XD1) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- the reaction is usually performed in a solvent.
- the solvent used in the reaction include ethers such as tetrahydrofuran, dioxane, ethylene glycol dimethyl ether and methyl tert-butyl ether, aromatic hydrocarbons such as toluene and xylene, carbon tetrachloride, chloroform or Halogenated hydrocarbons such as 1,2-dichloroethane and chlorobenzene, nitriles such as acetonitrile, acid amides such as N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone and N-methylpyrrolidone, Examples thereof include sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone, and methyl isobutyl ketone, and mixtures thereof.
- Examples of the isocyanate agent used in the reaction include phosphorus pentachloride, phosphorus oxychloride, diphosphorus pentoxide, trichlorosilane, dichlorosilane, monochlorosilane, boron trichloride, 2-chloro-1,3,2- Benzodioxaborol, diiodinated silane, methyltrichlorosilane, dimethyldichlorosilane, chlorotrimethylsilane, and the like can be used.
- the isocyanate agent is usually used at a ratio of 1 to 10 moles with respect to 1 mole of the compound (XD1).
- the reaction temperature is usually in the range of ⁇ 20 to 250 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the reaction may be carried out, if necessary, by using an organic base such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine, diazabicycloundecene, alkali metal carbonate such as lithium carbonate, sodium carbonate or potassium carbonate. Salts, alkali metal hydrogen carbonates such as sodium hydrogen carbonate and the like may be added, and these compounds are usually used at a ratio of 0.05 to 5 mol with respect to 1 mol of compound (XD1).
- the compound (XA1) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- a compound represented by formula (XE2) (hereinafter, compound (XE2) is produced by reacting a compound represented by formula (XE1) (hereinafter referred to as compound (XE1)) with hydrogen in the presence of a catalyst. can do.
- a compound represented by formula (XE1) hereinafter referred to as compound (XE1)
- R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R 8 , R 9 , R 10 , R 11 and R 12 represent the same meaning as described above, and R 181 represents represents a hydrogen atom or P 21, the wavy line represents a bond site.
- the reaction is usually performed in a solvent.
- Examples of the solvent used in the reaction include alcohols such as methanol, ethanol, propanol and butanol, esters such as ethyl acetate and butyl acetate, carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, Halogenated hydrocarbons such as chlorobenzene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, water and These mixtures are mentioned.
- alcohols such as methanol, ethanol, propanol and butanol
- esters such as ethyl acetate and butyl acetate
- carbon tetrachloride chloroform
- the catalyst As a catalyst used for the reaction, palladium carbon (Pd / C), platinum carbon (Pt / C), osmium carbon (Os / C), ruthenium carbon (Ru / C), rhodium carbon (Rh / C), Raney nickel, etc. Can give.
- the catalyst is usually used at a ratio of 0.0001 to 1 mol with respect to 1 mol of the compound (XE1).
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (XE2) can be isolated by post-treatment such as filtration of the catalyst and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- Compound (XE2) can be produced by reacting compound (XE1) with a reducing agent in the presence of an acid.
- the reaction is usually performed in a solvent.
- the solvent used in the reaction include aliphatic carboxylic acids such as acetic acid, alcohols such as methanol and ethanol, water, and mixtures thereof.
- the reducing agent used in the reaction include iron, tin, and zinc.
- the acid used in the reaction include hydrochloric acid, sulfuric acid, acetic acid, ammonium chloride aqueous solution, and the like.
- the reducing agent is usually used in a proportion of 1 to 30 mol per 1 mol of the compound (XE1).
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (XE2) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- the compound represented by the formula (XG2) (hereinafter referred to as the compound (XG2)) is obtained by combining the compound represented by the formula (XG1) (hereinafter referred to as the compound (XG1)) with the compound (E1). It can manufacture by making it react under. [Wherein R 6 , R 7 , R 8 , R 9 , R 10 and Z 11 represent the same meaning as described above, and R 191 represents P 11 or P 12 . ] The reaction can be carried out according to the reaction described in Production Method D.
- a compound represented by formula (XH2) (hereinafter referred to as compound (XH2)) is obtained by reacting a compound represented by formula (XH1) (hereinafter referred to as compound (XH1)) with a halogenating agent.
- a halogenating agent (wherein, R 4 , R 5 , R 6 , R 7 , R 8 , R 9 , R 10 , Z 21 and X represent the same meaning as described above, and R 201 represents P 51 or a nitro group. ]
- the reaction is usually performed in a solvent.
- Examples of the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Examples include halogenated hydrocarbons such as chloroform, 1,2-dichloroethane, and chlorobenzene, esters such as ethyl acetate and methyl acetate, ketones such as acetone, methyl ethyl ketone, and methyl isobutyl ketone, nitriles such as acetonitrile, and mixtures thereof.
- hydrocarbons such as n-hexane, cyclohexane, toluene and xylene
- ethers such as tetrahydrofuran, 1,4-dioxane
- halogenating agent examples include chlorination, bromination or iodination agents such as chlorine, bromine, iodine, sulfuryl chloride, N-chlorosuccinimide, N-bromosuccinimide, 1,3-dibromo-5. , 5-dimethylhydantoin, iodosuccinimide, tert-butyl hypochlorite, N-chloroglutarimide, N-bromoglutarimide, N-chloro-N-cyclohexyl-benzenesulfonimide, N-bromophthalimide, etc. Can do.
- a radical initiator can also be used for this reaction.
- the radical initiator used in the reaction includes benzoyl peroxide, azobisisobutyronitrile (AIBN), diacyl peroxide, dialkylperoxydicarbonate, tert-alkylperoxyester, monoperoxycarbonate, di (tert-alkylperoxy). ) Ketals and ketone peroxides.
- the halogenating agent is usually used in a proportion of 1 to 10 mol and the radical initiator is usually used in a proportion of 0.01 to 5 mol with respect to 1 mol of the compound (XH1).
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (XH2) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- solvent used in the reaction examples include ethers such as diethyl ether, tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, anisole, methyl tert-butyl ether, diisopropyl ether, n-hexane, cyclohexane.
- ethers such as diethyl ether, tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, anisole, methyl tert-butyl ether, diisopropyl ether, n-hexane, cyclohexane.
- Hydrocarbons such as toluene and xylene, carbon tetrachloride, chloroform, dichloromethane, halogenated hydrocarbons such as 1,2-dichloroethane, tetrachloroethane and chlorobenzene, nitriles such as acetonitrile, N, N-dimethylformamide, 1 , 3-dimethyl-2-imidazolidinone, acid amides such as N-methylpyrrolidone, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone, methyl isobutyl ketone, methanol, Ethanol, propanol, and mixtures thereof, such as butanol.
- nitriles such as acetonitrile, N, N-dimethylformamide, 1 , 3-dimethyl-2-imidazolidinone
- acid amides such as N-methylpyrrolidone
- compound (XJ1) sodium methoxide, sodium ethoxide, sodium n-propoxide, sodium n-butoxide, sodium isopropoxide, sodium sec-butoxide, sodium tert-butoxide, potassium methoxy And potassium ethoxide, potassium n-propoxide, potassium n-butoxide, potassium isopropoxide, potassium sec-butoxide, potassium tert-butoxide, sodium phenoxide and the like.
- compound (XJ1) is usually used at a ratio of 1 to 10 mol with respect to 1 mol of compound (XH2).
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (XJ2) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- a compound represented by the formula (XK1) (hereinafter referred to as compound (XK1)) can be produced by reacting compound (XH2) with water in the presence of a base. [Wherein the symbols have the same meaning as described above. ] The reaction is usually performed in water or a solvent containing water. Examples of the solvent used in the reaction include ethers such as diethyl ether, tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, anisole, methyl tert-butyl ether, diisopropyl ether, n-hexane, cyclohexane.
- ethers such as diethyl ether, tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, anisole, methyl tert-butyl ether, diisopropyl ether, n-hexane, cyclohexane.
- Hydrocarbons such as toluene and xylene, carbon tetrachloride, chloroform, dichloromethane, halogenated hydrocarbons such as 1,2-dichloroethane, tetrachloroethane and chlorobenzene, nitriles such as acetonitrile, N, N-dimethylformamide, 1 , 3-dimethyl-2-imidazolidinone, acid amides such as N-methylpyrrolidone, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone, methyl isobutyl ketone, methanol, Ethanol, propanol, and mixtures thereof, such as butanol.
- nitriles such as acetonitrile, N, N-dimethylformamide, 1 , 3-dimethyl-2-imidazolidinone
- acid amides such as N-methylpyrrolidone
- Examples of the base used in the reaction include triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine, diazabicycloundecene and other organic bases, lithium formate, lithium acetate, sodium formate, sodium acetate, formic acid.
- Metal organic acid salts such as potassium and potassium acetate, metal nitrates such as silver nitrate and sodium nitrate, alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate, alkali metal hydrogen carbonates such as sodium hydrogen carbonate, lithium hydroxide, Examples thereof include alkali metal hydroxides such as sodium hydroxide, potassium hydroxide and cesium hydroxide, sodium methoxide, sodium ethoxide, sodium tert-butoxide, and alkali metal alkoxide of potassium tert-butoxide.
- the base is usually used at a ratio of 1 to 100 mol per 1 mol of the compound (XH2).
- the reaction water is usually used in a proportion of 1 mol to large excess with respect to 1 mol of compound (XH2).
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (XK1) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- Compound (XH2) can be produced by reacting compound (XJ2) with a halogenating agent.
- a solvent examples include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, and halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane and chlorobenzene.
- Ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone, nitriles such as acetonitrile, organic acids such as formic acid, acetic acid and trifluoroacetic acid, water, and mixtures thereof.
- the halogenating agent used in the reaction include hydrochloric acid, hydrobromic acid, and hydriodic acid.
- the halogenating agent is usually used at a ratio of 1 mol or more per 1 mol of the compound (XJ2).
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (XH2) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- Compound (XH2) can be produced by reacting compound (XK1) with a halogenating agent.
- the reaction is usually performed in a solvent.
- the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, esters such as ethyl acetate and methyl acetate, ketones such as acetone, methyl ethyl ketone, and methyl isobutyl ket
- halogenating agent used in the reaction examples include bromine, chlorine, sulfuryl chloride, hydrochloric acid, hydrobromic acid, hydroiodic acid, boron tribromide, phosphorus tribromide, trimethylsilyl chloride, trimethylsilyl bromide.
- the halogenating agent is usually used at a ratio of 1 to 10 moles relative to 1 mole of the compound (XK1).
- additives depending on the halogenating agent used may be added, specifically zinc chloride for acetyl chloride, triphenylphosphine for carbon tetrabromide, dimethyl sulfide for N-bromosuccinimide.
- the compound (XH2) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- R 901 represents a C1-C6 alkyl group, a C1-C6 haloalkyl group, C6-C16 aryl group, a C6-C16 haloaryl group
- Z 801 represents a fluorine atom, a chlorine atom, a bromine atom or an iodine atom.
- the reaction is usually performed in a solvent.
- Examples of the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, nitriles such as acetonitrile, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone And acid amides such as N-methylpyrrolidone, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone, and methyl isobutyl ketone, and mixtures thereof.
- Examples of the base used for the reaction include organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene, and alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene
- alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- alkali metal hydrogen carbonates such as sodium hydrogen carbonate
- alkali metal hydroxides such as lithium hydroxide, sodium hydroxide, potassium hydroxide, cesium hydroxide
- alkalis such as lithium hydride, sodium hydride, potassium hydride
- metal hydrides sodium methoxide, sodium ethoxide, sodium tert-butoxide, alkali metal alkoxides of potassium tert-butoxide, and the like.
- compound (XK1) compound (XM2) is usually used in a proportion of 1 to 10 mol
- base is usually used in a proportion of 1 to 5 mol.
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- sodium iodide, tetrabutylammonium iodide, etc. may be added, and these compounds are usually in a ratio of 0.001 to 1.2 mol with respect to 1 mol of compound (XK1).
- the compound (XM3) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- the compound represented by the formula (XN12) (hereinafter referred to as the compound (XN12)) is obtained by converting the compound represented by the formula (XN11) (hereinafter referred to as the compound (XN11)) and the compound (G21) into a base and a catalyst. It can be produced by subjecting it to a coupling reaction in the presence.
- R 501 represents a hydrogen atom or an OR 111 group
- R 111 , R 4 , R 5 , R 7, R 8 , R 9 , R 10 , R 71 , X, Z 31 and Z 41 are the same as above. Represents meaning.
- the reaction can be carried out according to the reaction described in Production Method B.
- the compound represented by the formula (XN22) (hereinafter referred to as the compound (XN22)) is obtained by converting the compound represented by the formula (XN21) (hereinafter referred to as the compound (XN21)) and the compound (G22) into a base and a catalyst. It can be produced by subjecting it to a coupling reaction in the presence. [Wherein the symbols have the same meaning as described above. ] The reaction can be carried out according to the reaction described in Production Method B.
- the compound represented by the formula (XN32) (hereinafter referred to as the compound (XN32)) is obtained by converting the compound represented by the formula (XN31) (hereinafter referred to as the compound (XN31)) and the compound (G22) into a base and a catalyst. It can be produced by subjecting it to a coupling reaction in the presence. [Wherein the symbols have the same meaning as described above. ] The reaction can be carried out according to the reaction described in Production Method B.
- the compound represented by the formula (XN42) (hereinafter referred to as the compound (XN42)) is obtained by converting the compound represented by the formula (XN41) (hereinafter referred to as the compound (XN41)) and the compound (G22) into a base and a catalyst. It can be produced by subjecting it to a coupling reaction in the presence. [Wherein the symbols have the same meaning as described above. ] The reaction can be carried out according to the reaction described in Production Method B.
- the compound represented by the formula (XW2) (hereinafter referred to as the compound (XW2)) is the compound represented by the formula (XW1) (hereinafter referred to as the compound (XW1)) in the presence of a reaction accelerator.
- XW3 (hereinafter referred to as compound (XW3)).
- the reaction is usually performed in a solvent.
- the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone, N-methylpyrrolidone, etc.
- Acid amides esters such as ethyl acetate and methyl acetate, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone, nitriles such as acetonitrile and the like
- compound (XW3) may also be used compound (XW3) as solvent.
- the compound (XW3) that can be used in the reaction include methyl alcohol, ethyl alcohol, propyl alcohol, isopropyl alcohol, n-butyl alcohol, sec-butyl alcohol, t-butanol, and n-pentanol.
- reaction accelerator used in the reaction examples include mineral acids such as hydrochloric acid and sulfuric acid, carbodiimides such as dicyclohexylcarbodiimide, diisopropylcarbodiimide, N ′-(3-dimethylaminopropyl) -N-ethylcarbodiimide, methanesulfonic acid, and toluenesulfone.
- mineral acids such as hydrochloric acid and sulfuric acid
- carbodiimides such as dicyclohexylcarbodiimide, diisopropylcarbodiimide, N ′-(3-dimethylaminopropyl) -N-ethylcarbodiimide, methanesulfonic acid, and toluenesulfone.
- organic acids such as acids
- Mitsunobu reaction reagents such as triphenylylphosphine / diethyl azodicarboxylate, thionyl
- the reaction accelerator is usually used in a proportion of 0.01 to 10 mol per 1 mol of the compound (XW1).
- the reaction may be carried out, if necessary, by using an organic base such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine, diazabicycloundecene, alkali metal carbonate such as lithium carbonate, sodium carbonate or potassium carbonate. Salts, alkali metal hydrogen carbonates such as sodium hydrogen carbonate and the like may be added, and these compounds are usually used in a proportion of 0.001 to 5 mol with respect to 1 mol of compound (XW1).
- the reaction an excess amount of the compound (XW3) is used with respect to the compound (XW1).
- the reaction temperature is usually in the range of ⁇ 78 to 100 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (XW2) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- Compound (XW2) is obtained by reacting compound (XW1) with a halogenating agent to obtain a compound represented by formula (XV1) (hereinafter referred to as compound (XV1)), and then compound (XV1) and compound (XV1). XW3) can be reacted. [Wherein the symbols have the same meaning as described above. ]
- the method for producing compound (XV1) by reacting compound (XW1) with a halogenating agent can be carried out according to the reaction described in Reference Production Method C.
- the reaction is usually performed in a solvent.
- the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone, N-methylpyrrolidone, etc.
- Acid amides esters such as ethyl acetate and methyl acetate, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone, nitriles such as acetonitrile and the like Compound.
- compound (XW3) as solvent.
- an excess amount of the compound (XW3) is used with respect to the compound (XV1).
- the reaction temperature is usually in the range of ⁇ 78 to 100 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (XW2) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- Compound (XW2) can be produced by reacting compound (XW1) with an alkylating agent. [Wherein the symbols have the same meaning as described above. ] The reaction is usually performed in a solvent.
- the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone, N-methylpyrrolidone, etc.
- Acid amides esters such as ethyl acetate and methyl acetate, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone, nitriles such as acetonitrile, water and Mixtures of al and the like.
- alkylating agent that can be used in the reaction include alkyl halides such as methyl bromide, ethyl bromide, n-propyl bromide, methyl iodide, ethyl iodide, n-propyl iodide, and isopropyl iodide.
- Sulfonates such as methyl p-toluenesulfonate, ethyl p-toluenesulfonate, n-propyl p-toluenesulfonate, methyl methanesulfonate, ethyl methanesulfonate, n-propyl methanesulfonate, and sulfuric acid Examples thereof include sulfate esters such as dimethyl, diethyl sulfate, and di-n-propyl sulfate.
- the alkylating agent is usually used at a ratio of 1 to 10 moles relative to 1 mole of the compound (XW1).
- the reaction may be carried out as necessary with an organic base such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine, diazabicycloundecene, or an alkali metal carbonate such as lithium carbonate, sodium carbonate or potassium carbonate.
- an organic base such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine, diazabicycloundecene
- an alkali metal carbonate such as lithium carbonate, sodium carbonate or potassium carbonate.
- Salts, alkali metal hydrogen carbonates such as sodium hydrogen carbonate, quaternary ammonium salts such as tetra (n-butyl) ammonium hydroxide, and the like may be added, and these compounds are usually used relative to 1 mol of compound (XW1). , 0.001 to 5 mol.
- the reaction temperature is usually
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (XW2) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer. Further, purification may be performed by operations such as distillation, chromatography, recrystallization and the like.
- a compound represented by formula (XS2) (hereinafter referred to as compound (XS2)) is obtained by combining a compound represented by formula (XS1) (hereinafter referred to as compound (XS1)) with compound (A2). It can manufacture by making it react in presence. [Wherein the symbols have the same meaning as described above. ] This reaction can be carried out according to the reaction described in Production Method A.
- a compound represented by formula (XU2) (hereinafter referred to as compound (XU2)) is obtained by combining a compound represented by formula (XU1) (hereinafter referred to as compound (XU1)) and compound (B2) with a base and It can be produced by subjecting it to a coupling reaction in the presence of a catalyst. [Wherein the symbols have the same meaning as described above. ] The reaction can be carried out according to the reaction described in Production Method B.
- Compound (B1) can be produced by reacting a compound represented by the formula (XO1) (hereinafter referred to as compound (XO1)) with compound (XU1) in the presence of a base. [Wherein the symbols have the same meaning as described above. ] This reaction can be carried out according to the reaction described in Production Method A.
- Compound (C1) can be produced by reacting compound (B1) with a borylating reagent in the presence of a catalyst and a base.
- Z 51 represents an alkoxyboranyl group
- R 1 , R 2 , R 3 , R 4 , R 5 , R 6 , R 7 , R 8 , R 9 , R 10 , R 11 and X are Represents the same meaning as above.
- the reaction is usually performed in a solvent.
- Examples of the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone, N-methylpyrrolidone, etc.
- hydrocarbons such as n-hexane, cyclohexane, toluene and xylene
- ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether,
- Acid amides esters such as ethyl acetate and methyl acetate, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone, nitriles such as acetonitrile and the like Mixtures thereof.
- borating reagent used in the reaction include bis (pinacolato) diboron, pinacolborane, and the like.
- Catalysts used in the reaction include palladium (II) acetate, dichlorobis (triphenylphosphine) palladium, tetrakistriphenylphosphinepalladium (0), palladium (II) acetate / triscyclohexylphosphine, bis (diphenylphosphaneferrocenyl) ) Palladium (II) dichloride, 1,3-bis (2,6-diisopropylphenyl) imidazol-2-ylidene (1,4-naphthoquinone) palladium dimer, allyl (chloro) (1,3-dimesityl-1,3- Dihydro-2H-imidazol-2-ylidene) palladium or palladium (II) acetate / dicyclohexyl (2 ′, 4 ′, 6′-triisopropylbiphenyl-2-yl) phos
- Examples of the base used for the reaction include organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene, and alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene
- alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- alkali metal hydrogen carbonate such as sodium hydrogen carbonate
- alkali metal hydroxide such as lithium hydroxide, sodium hydroxide, potassium hydroxide, cesium hydroxide
- alkali such as sodium fluoride, potassium fluoride, cesium fluoride
- Metal halides alkali metal hydrides such as lithium hydride, sodium hydride, potassium hydride, alkali metal phosphates such as tripotassium phosphate, sodium methoxide, sodium ethoxide, sodium tert-butoxide, potassium tert- Alkali metal alkoxides such as Tokishido like.
- the borating reagent is usually used in a proportion of 1 to 10 mol
- the base is usually used in a proportion of 1 to 10 mol
- the catalyst is usually used in a proportion of 0.0001 to 1 mol with respect to 1 mol of the compound (B1).
- the reaction temperature is usually in the range of 0 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (C1) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer.
- the isolated compound of the present invention can be further purified by chromatography, recrystallization and the like.
- Compound (I1) can be produced by reacting compound (C1) with aqueous hydrogen peroxide in the presence of a base. [Wherein the symbols have the same meaning as described above. ] The reaction is usually performed in a solvent.
- Examples of the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone, N-methylpyrrolidone, etc.
- hydrocarbons such as n-hexane, cyclohexane, toluene and xylene
- ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether,
- concentration of hydrogen peroxide used in the reaction is usually in the range of 1 to 70%.
- Catalysts used in the reaction include palladium (II) acetate, dichlorobis (triphenylphosphine) palladium, tetrakistriphenylphosphinepalladium (0), palladium (II) acetate / triscyclohexylphosphine, bis (diphenylphosphaneferrocenyl) ) Palladium (II) dichloride, 1,3-bis (2,6-diisopropylphenyl) imidazol-2-ylidene (1,4-naphthoquinone) palladium dimer, allyl (chloro) (1,3-dimesityl-1,3- Dihydro-2H-imidazol-2-ylidene) palladium or
- Examples of the base used for the reaction include organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene, and alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- organic bases such as triethylamine, pyridine, N-methylmorpholine, 4-dimethylaminopyridine, diisopropylethylamine and diazabicycloundecene
- alkali metal carbonates such as lithium carbonate, sodium carbonate and potassium carbonate.
- alkali metal hydrogen carbonate such as sodium hydrogen carbonate
- alkali metal hydroxide such as lithium hydroxide, sodium hydroxide, potassium hydroxide, cesium hydroxide
- alkali such as sodium fluoride, potassium fluoride, cesium fluoride
- Metal halides alkali metal hydrides such as lithium hydride, sodium hydride, potassium hydride, alkali metal phosphates such as tripotassium phosphate, sodium methoxide, sodium ethoxide, sodium tert-butoxide, potassium tert- Alkali metal alkoxides such as Tokishido like.
- the reaction with respect to 1 mol of the compound (C1), hydrogen peroxide is usually used in a proportion of 1 to 10 mol, and the base is usually used in a proportion of 1 to 10 mol.
- the reaction temperature of the reaction is usually in the range of ⁇ 78 ° C. to 100 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- the compound (I1) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer.
- the isolated compound of the present invention can be further purified by chromatography, recrystallization and the like.
- Compound (1-3) can be produced by reacting a compound represented by formula (Y1) (hereinafter referred to as compound (Y1)) with an azidating agent. [Wherein the symbols have the same meaning as described above. ] The reaction is usually performed in a solvent.
- Examples of the solvent used in the reaction include hydrocarbons such as n-hexane, cyclohexane, toluene and xylene, ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether, methyl tert-butyl ether and diisopropyl ether, Halogenated hydrocarbons such as carbon tetrachloride, chloroform, dichloromethane, 1,2-dichloroethane, tetrachloroethane, chlorobenzene, N, N-dimethylformamide, 1,3-dimethyl-2-imidazolidinone, N-methylpyrrolidone, etc.
- hydrocarbons such as n-hexane, cyclohexane, toluene and xylene
- ethers such as tetrahydrofuran, 1,4-dioxane, ethylene glycol dimethyl ether,
- Acid amides esters such as ethyl acetate and methyl acetate, sulfoxides such as dimethyl sulfoxide, ketones such as acetone, methyl ethyl ketone and methyl isobutyl ketone, nitriles such as acetonitrile and the like Mixtures thereof.
- the azidating agent used in the reaction include inorganic azides such as sodium azide, barium azide or lithium azide, and organic azides such as trimethylsilyl azide and diphenylphosphoryl azide. In the reaction, the azidating agent is usually used at a ratio of 1 to 10 mol per 1 mol of the compound (Y1).
- the reaction temperature of the reaction is usually in the range of ⁇ 20 to 150 ° C.
- the reaction time is usually in the range of 0.1 to 24 hours.
- a Lewis acid such as aluminum chloride or zinc chloride may be added as necessary, and these compounds are usually used at a ratio of 0.05 to 5 mol with respect to 1 mol of compound (Y1). It is done.
- the compound (1-3) can be isolated by performing post-treatment operations such as extraction of the reaction mixture with an organic solvent, and drying and concentration of the organic layer.
- the isolated compound of the present invention can be further purified by chromatography, recrystallization and the like.
- the form of the compound of the present invention may be the compound of the present invention alone.
- the compound of the present invention is mixed with a solid carrier, a liquid carrier, a surfactant, etc., and if necessary, a fixing agent or a dispersing agent.
- Additives for preparations such as stabilizers, wettable powder, granular wettable powder, flowable powder, granules, dry flowable powder, emulsion, aqueous liquid, oil, smoke, aerosol, micro It is used in the form of capsules.
- These preparations contain the compound of the present invention in a weight ratio of usually 0.1 to 99%, preferably 0.2 to 90%.
- Examples of the solid support include clays (for example, kaolin, diatomaceous earth, synthetic hydrous silicon oxide, fusamic clay, bentonite, acidic clay), talc, and other inorganic minerals (for example, sericite, quartz powder, sulfur powder, activated carbon). , Calcium carbonate, hydrated silica) and the like.
- Examples of the liquid carrier include water, alcohols (eg, methanol, ethanol), ketones (eg, acetone).
- Methyl ethyl ketone aromatic hydrocarbons (for example, benzene, toluene, xylene, ethylbenzene, methylnaphthalene), aliphatic hydrocarbons (for example, n-hexane, cyclohexanone, kerosene), esters (for example, ethyl acetate, acetic acid) Butyl), nitriles (eg acetonitrile, isobutyronitrile), ethers (eg If, dioxane, diisopropyl d - ether), acid amides (e.g., DMF, dimethylacetamide), halogenated hydrocarbons (e.g., dichloroethane, trichlorethylene, carbon tetrachloride) and the like.
- aromatic hydrocarbons for example, benzene, toluene, xylene, ethylbenzene, methyl
- surfactant examples include alkyl sulfates, alkyl sulfonates, alkyl aryl sulfonates, alkyl aryl ethers and polyoxyethylene compounds thereof, polyoxyethylene glycol ethers, polyvalent Examples include alcohol esters and sugar alcohol derivatives.
- formulation adjuvants include, for example, fixing agents, dispersants, and stabilizers.
- casein gelatin, polysaccharides (for example, starch, arabic gum, cellulose derivatives, alginic acid), lignin derivatives, Bentonite, sugars, synthetic water-soluble polymers (for example, polyvinyl alcohol, polyvinyl pyrrolidone, polyacrylic acids), PAP (isopropyl acid phosphate), BHT (2,6-di-tert-butyl-4-methylphenol) ), BHA (mixture of 2-tert-butyl-4-methoxyphenol and 3-tert-butyl-4-methoxyphenol), vegetable oil, mineral oil, fatty acid or ester thereof, and the like.
- polysaccharides for example, starch, arabic gum, cellulose derivatives, alginic acid
- lignin derivatives Bentonite
- sugars synthetic water-soluble polymers (for example, polyvinyl alcohol, polyvinyl pyrrol
- the method of applying the compound of the present invention is not particularly limited as long as the compound of the present invention can be applied substantially, but for example, treatment of plants such as foliage spraying, cultivation of plants such as soil treatment, etc. Treatment to the seed such as treatment on the ground and seed disinfection is mentioned.
- oils such as mineral oil and vegetable oil, or surfactant.
- Oils that can be specifically mixed and used as surfactants include Nimbus (registered trademark), Assist (registered trademark), Aureo (registered trademark), Iharol (registered trademark), Silwet L-77 (registered trademark), BreakThru (registered trademark), Sundance II (registered trademark), Induce (registered trademark), Penetrator (registered trademark), AgriDex (registered trademark), Lutensol A8 (registered trademark), NP-7 (registered trademark), Triton (registered trademark) , Nufilm (registered trademark), Emulator NP7 (registered trademark), Emulad (registered trademark), TRITON X 45 (registered trademark), AGRAL 90 (registered trademark), AGROTIN (registered trademark), ARPON (registered trademark), EnSpray N ( Recorded trademark), BANOLE (registered trademark), Nimbus (registered trademark),
- the compound of the present invention can be used simultaneously with or without mixing with other fungicides, insecticides, acaricides, and nematicides.
- other bactericides include the following.
- Azol fungicides propiconazole, prothioconazole, triadimenol, prochloraz, penconazole, fluconol, teconazole Flusilazole, diniconazole, bromconazole, epoxyconazole, difenoconol, cyproconazole, diproconazole, cyproconazole, diproconazole. (Triflumizole), Tet Teconconazole, microbutanil, fenbuconazole, hexaconazole, fluquinconazole, triticol ter.
- Examples of such other insecticides include the following.
- Organophosphorus compounds acephate, aluminum phosphide, butathiofos, cadusafos, chlorethoxyphos, chlorfenvinphos, chlorpyvinphos folpyphos , Chloropyrifos-methyl, cyanophos (CYAP), diazinon, DCIP (dichrofenisopropyl ether), dichlorfenthion (ECP), dichlorvos (Dchlo-D) (Dimethoate), dimethylvinphos, disulfoton, EPN, etion, ethoprofos, etrimfos, fenthion (MPP), fenitrothion (fetiothion) (Fosthiazate), formothione (formation), hydrogen phosphide (isofenphos), isoxathion (isoxathion), malathion (malathion), mesul
- Phenylpyrazole compound Acetoprole, etiprole, fipronil, vaniliprole, pyriprole, pyrafluprole, etc .
- acaricides include, for example, acequinocyl, amitraz, benzoxymate, bifenate, phenisobromolate, quinopropyrate, (Chinomethionat), Chlorbenzilate, CPCBS (Chlorfenson), Clofentezine, Cyflumetofen, Kelsen (dicophor), Etofazol tin oxide (etoxazole) (Fenothiocarb) , Fenpyroximate, fluacrylpyrim, fluproxyfen, hexythiazox, propargite (BP), polynactin complex (pi), polynactin complex (pi) Tebufenpyrad, tetradiphon, spirodiclofen, spiromesifen, spirotetramat, amidoflumet, cienopyramet, cienopyramet yrafen), and the like.
- acequinocyl amitraz, benzoxymate, bifenate
- nematicides include, for example, DCIP, fostiazate, levamisole hydrochloride, methylisothiocyanate, and morantel tartrate. tartarate, imicyafos, fluensulfone and the like.
- Examples of such other plant growth regulators include the following. Gibberellin A (Kibberdelin A), abscisicin acid (abscisinic acid), abscisicin acid (abscisinic acid) (Benzyladine), 1,3-diphenylurea, forchlorfenuron, thidiazuron, 4-oxo-4- (2-phenylethyl) aminobutyric acid, 5- (trifluoromethyl) benzo [b] thiophene Methyl-2-carboxylate, 5- (trifluoromethyl) benzo [b] thiophene-2-carboxylic acid Etc..
- the application amount of the compound of the present invention varies depending on weather conditions, formulation form, application time, application method, application place, target disease, target crop, etc., but is usually 1 to 500 g, preferably 2 to 200 g per 1000 m 2. .
- Emulsions, wettable powders, suspensions and the like are usually diluted with water and applied.
- the concentration of the compound of the present invention after dilution is usually 0.0005 to 2% by weight, preferably 0.005 to 1.
- the powder, granules and the like are usually applied as they are without dilution.
- the amount of the compound of the present invention relative to 1 kg of seeds is usually 0.001 to 100 g, preferably 0.01 to 50 g.
- habitats for pests in the present invention include paddy fields, fields, tea gardens, orchards, non-agricultural land, houses, seedling trays and seedling boxes, seedling culture soil, and seedling mats.
- the organism or parasite that parasitizes the vertebrate is systemically or non-systemically.
- Examples of such internal administration include oral administration, anal administration, transplantation, subcutaneous, intramuscular and intravenous administration by injection.
- External administration includes transdermal administration.
- the dosage can be varied widely depending on the administration method, etc. It is desirable to administer the active ingredient (the compound of the present invention or a salt thereof) at a dose of 0.1 mg to 2000 mg, preferably 0.5 mg to 1000 mg.
- the compound of the present invention can be used as a plant disease control agent in agricultural land such as fields, paddy fields, lawns, orchards.
- the compound of the present invention can control diseases of the cultivated land in the cultivated lands where the “plants” and the like listed below are cultivated.
- Agricultural crops corn, rice, wheat, barley, rye, oats, sorghum, cotton, soybeans, peanuts, buckwheat, sugar beet, rapeseed, sunflower, sugarcane, tobacco, etc., vegetables; solanaceous vegetables (eggplants, tomatoes, peppers) , Pepper, potato, etc.), cucurbitaceae vegetables (cucumber, pumpkin, zucchini, watermelon, melon, etc.), cruciferous vegetables (radish, turnip, horseradish, cold rabi, Chinese cabbage, cabbage, mustard, broccoli, cauliflower -), Asteraceae vegetables (burdock, garlic, artichoke, lettuce, etc.), Liliaceae vegetables (leek, onion, garlic, asparagus), Aceraceae vegetables (carrots, parsley, celery, American redfish, etc.) , Red vegetables (spinach, chard, etc.), perilla vegetables (perilla, mint, basil) ), Strawberry, sweet potato, yam, taro, etc
- Trees other than fruit trees tea, mulberry, flowering trees, street trees (ash, birch, dogwood, eucalyptus, ginkgo, lilac, maple, oak, poplar, redwood, fu, sycamore, zelkova, black bean, peach tree, tsuga, rat, Pine, spruce, yew).
- plants include genetically modified crops.
- Rice blast (Magnaporthe grisea), sesame leaf blight (Cochliobolus miyabeanus), blight (Rhizoctonia solani), idiotic seedling (Gibberella fujikuroi) or yellow rot sorghum Graminis), red mold disease (Fusarium graminearum, F. avenaceum, F. culmorum, Microdochium nitrile), rust disease (Puccinia striformis), P. graminis, P. recondetic color. Nuclear disease ( yphula sp.), naked scab (Ustilago tritici), lintel scab (Tilletia caries, T.
- Leafy leaf disease Panophora graminea
- lambaria disease Roso-cygni
- Rhizoctonia solani corn rust disease
- Herpes disease Setosph aeria turcica, sesame leaf blight (Cochliobolus heterotrophus), anthracnose (Colletotrichum glaminicola), gray leaf spot disease (Cercospora zeae-maisedae), brown spot disease (Kabatiellae phaephae leaf disease)
- Cotton anthracnose Colletotrichum gossypi
- mildew Ramuraria areola
- black spot Alternaria macrospora, A.
- coffee rust Hemileia vastatrix
- Bacterial rot of rapeseed (Sclerotinia sclerotiorum), black spot disease (Alternaria brassicae), root rot (Phoma lingam); citrus black spot disease (Diaporthecitri), common scab (Elsinoetium rot) P. italicum); apple Monilia mary, rot (Valsa ceratosperma), powdery mildew (Podosphaera leucotrica), spot leaf rot (Alternaria altarapeurposis). Glomerell Cingulata); Pear black spot disease (Venturia nashichicola, V.
- Black spot disease Alternaria alternaumumumapirumirumamor disease; Gynosporangiumumamor disease; Phomopsis spoilage disease (Phomopsis sp.); Grapes black rot (Elsinoe ampelina), late rot (Glomerella gingulata), powdery mildew (Uncinula necator), rust disease (Phakopsora adiplopsis disease) nardia bidwellii), downy mildew (Plasmopara viticola); oyster anthracnose (Gloeosporium kakii), deciduous leaf disease (Cercospora kaki, Mycosphaerella nawae); , Vine blight (Didymella bryoniae), brown spot (Corynespora cassiicola), vine split disease (Fusarium oxysporum), downy mildew (Pseudoperosporum cubensis), plague
- Tomato ring disease Alternaria solani
- leaf mold Clodosporium fulvum
- Japanese scab Pseudocercospora fuligena
- plague Phytophthora infestans
- brown rot Phomopsis cerevisiae
- Disease Alternaria japonica
- white spot disease Cercosporella brassicae
- root-knot disease Plasmodiophora brassicae
- downy mildew Peronospora parasitica
- leek rust Pierinia
- Soybean purpura (Cercospora kikuchii), black pepper (Elsinoe glycines), sunspot disease (Diaporthe phaseolumum var. Sojae), rust disease (Phacopsora pachyrespiri crest) Truncatum), leaf rot (Rhizoctonia solani), brown spot (Septorya glycines), spot disease (Cercospora sojina); bean anthracnose (Colletotrichum lindemspear) ( ercospora arachidicola, white silkworm (Sclerotium olfsiii); pea powdery mildew (Erysiphepisii); potato summer plague (Alternaria solanitis, phytophthora infectious illness) V.
- Japanese radish black spot disease (Alternaria brassicicola); Dwarf spot disease (Sclerotinia homecarpa), Brown patch disease and brown patch disease (Rhizoctonia solani);
- Hemiptera small brown planthopper (Laodelphax striatellus), brown planthopper (Nilaparvata lugens), Sejirounka (Sogatella furcifera) planthoppers such as, green rice leafhopper (Nephotettix cincticeps), Taiwan green rice leafhopper (Nephotettix virescens) leafhoppers such as, cotton aphid (Aphis gossypii) , Peaches aphids (Myzus persicae), radish aphids (Brevicoryne brassicae), tulip beetle aphids (Macrosiphum euphorbiae), potato beetle aphids (Aulacorthum solani) Aphids such as wheat leaf aphid (Rhopalosiphum padi), citrus aphid (Toxoptera citriticidus), Nezara antenis wormcite (Rip
- Lepidoptera rice stem borer (Chilo suppressalis), Sankameiga (Tryporyza incertulas), leaf roller (Cnaphalocrocis medinalis), Watanomeiga (Notarcha derogata), Indian meal moth (Plodia interpunctella), the European corn borer (Ostrinia furnacalis), high Madara Roh moth (Hellula undalis), Japanese medusa such as Shibata toga (Pediasia teterrellus), Spodoptera litura, Spodoptera exigua, Ayuyotoga (Pseudaletia sepata), Atoga rassicae, Agrotis ipsilon, Tamanaginawaba (Plusia nigrisigna), Trichopulsia, Heliotis, Helicoberpa, etc.
- Thysanoptera western flower thrips (Frankliniella occidentalis), Minami thrips (Thrips palmi), yellow tea thrips (Scirtothrips dorsalis), green onion thrips (Thrips tabaci), Hirazuhanaazamiuma (Frankliniella intonsa), tobacco thrips (Frankliniella fusca) thrips, such as Etc.
- Diptera Housefly (Musca domestica), Culex (Culex pipiens pallens), gadfly (Tabanus trigonus), onion maggot (Hylemya antiqua), seedcorn maggot (Hylemya platura), Anopheles sinensis (Anopheles sinensis), rice leafminer (Agromyza oryzae), rice Hydrelia grisela, Chlorops oryzae, Dwarf cucurbitae, Ceratitis capitata, Lizari friti i ripi.
- Coleoptera beetle, Epilachna vigintioctopunctata (Epilachna vigintioctopunctata), cucurbit leaf beetle (Aulacophora femoralis), Kisujinomihamushi (Phyllotreta striolata), Inedorooimushi (Oulema oryzae), rice weevil (Echinocnemus squameus), rice water weevil (Lissorhoptrus oryzophilus), boll weevil (Anthonomus grandis), Azuki beetle (Callosobruchus chinensis), Shibahorusu weevil (Sphenophorus venatus), Japanese beetle (Popilia japonica), Douganebububu (Anomala cupre) ), Corn rootworm mate (Diabrotica spp.), Colorado potato beetle (Leptinotarsa decemlineat
- Direct insect pests Tocusama grasshopper (Locusta migratoria), Kera (Gryllotalpa africana), Oxya yezoensis, Oyana japonica, etc.
- Hymenoptera Athalia rosae, Achillyrmex spp., Fire ant (Solenopsis spp.) And the like.
- Nematodes Rice moth nematode (Aphelenchoides besseyy), Strawberry nematode (Heterodera glycines) .
- Cockroach pests German cockroaches (Blatella germanica), Black cockroaches (Periplaneta furiginosa), American cockroaches (Periplaneta americana), Japanese cockroaches (Peripraneta brunet)
- Acarina Tetranychus urticae, Pandychus citri, Odonidus spp., Acarops pelekassi, Mite, Phyphagotaris Mite, such as Typhophagus putrescentiae, Mite, Dermatophagoides falinae, Mite, Mite censis), Tsumedani such as Minami Tsumedani (Cheyletus moorei), chicken mites, and the like.
- the preparation containing the compound of the present invention or a salt thereof is used in the field of livestock disease treatment and livestock industry, and in vertebrates such as humans, cows, sheep, goats, pigs, poultry, dogs, cats and fishes. It can be used to maintain public health by combating organisms and parasites that parasitize inside and / or outside.
- the pests include ticks (Ixodes spp.) (Eg, Ixodes scapularis), bovine ticks (Boophilus spp. (Eg, Boophilus microplus), larvae ticks (Amblyomma splo. ., Rhipicephalus spp.
- Nutka (Curicodes spp), house flies (Musca spp.), Cow flies (Hypoderma spp.), Horse flies (Gasteophilus spp.), Sand flies (Haematobia spp), bubs (us) Spp. p haronis) and nematodes (eg, ciliate nematodes (eg, Nippostronylus brasiliensis), Trichostrogenylus axiei, Trichostrochylus cobrifoniformus, eg, Trichinella spp.), Trichinella sp. Ostertagia stomachworm (Ostertagia circcumcincta), Couperia (Cooperia spp. ), Hymenolepis nana] and the like.
- nematodes eg, ciliate nematodes (eg, Nippostronylus brasiliensis), Trichostrogenylus axie
- the compounds 2 to 40, 46 to 57, 113 to 148, and 151 to 156 of the present invention were synthesized using the compounds described in Reference Production Examples or commercially available compounds.
- the structural formula and its 1 H-NMR data are shown below.
- the compounds 43 to 45, 149 and 150 of the present invention were synthesized according to the reaction described in Production Example 3.
- the structural formula and its 1 H-NMR data are shown below.
- the compounds of the present invention 60 to 70 were synthesized according to the reaction described in Production Example 5.
- the structural formula and its 1 H-NMR data are shown below.
- the compounds of the present invention 75, 76, and 112 were synthesized according to the reaction described in Production Example 6.
- the structural formula and 1 H-NMR data are shown below.
- the compounds 73, 74 and 111 of the present invention were synthesized according to the reaction described in Production Example 7.
- the structural formula and 1 H-NMR data are shown below.
- the present compound 79 was synthesized according to the reaction described in Production Example 11.
- the structural formula and its 1 H-NMR data are shown below.
- 02 (2H, s), 3.70-3.68 (5H, m), 2.53 (3H, s), 2.07 (3H, s), 1.20 (3H, t, J 7. 0 Hz).
- Production Example 12 While stirring a mixture of 2.07 g of 32A described in Reference Production Example 32 and 10 mL of methanol at 0 degree, 0.76 g of sodium borohydride was added, and the mixture was stirred at room temperature for 4 hours. Water was poured into the reaction solution, and the mixture was extracted with chloroform. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Production Example 19 A mixture of 0.33 g of 38A described in Reference Production Example 38, 19 g of p-toluenesulfonic acid monohydrate and 3 mL of trimethyl orthoformate was heated and stirred at 100 degrees for 1 hour. After cooling, the mixture was concentrated under reduced pressure, 0.18 g of N-ethyl-N-methylamine and 3 mL of dimethoxyethane were added to the residue, and the mixture was stirred with heating at 80 ° C. for 1 hour.
- the compound 88 of the present invention was synthesized according to the reaction described in Production Example 19.
- the structural formula and its 1 H-NMR data are shown below.
- the compound 165 of the present invention was synthesized according to the reaction described in Production Example 20.
- the structural formula and its 1 H-NMR data are shown below.
- 1 H-NMR (CDCl 3 ) ⁇ : 7.42-7.37 (2H, m), 7.26-7.23 (1H, m), 6.73 (1H, s), 6.63 (1H , S), 4.98 (2H, s), 3.64 (3H, s), 2.50 (3H, s), 2.37 (3H, s), 2.02 (3H, s), 1 79-1.75 (1H, m), 0.88-0.82 (2H, m), 0.57-0.52 (2H, m).
- the compound 102 of the present invention was synthesized according to the reaction described in Production Example 21.
- the structural formula and its 1 H-NMR data are shown below.
- the compound 104 of the present invention was synthesized according to the reaction described in Production Example 22.
- the structural formula and its 1 H-NMR data are shown below.
- 1 H-NMR (CDCl 3 ) ⁇ : 7.45 (1H, t, J 8.2 Hz), 7.12-7.04 (4H, m), 6.82-6.79 (1H, m) , 6.00-5.97 (1H, m), 5.24 (2H, s), 3.91 (3H, s), 3.58 (3H, s), 2.36-2.32 (2H , M), 2.19-2.15 (2H, m), 1.99 (3H, s), 1.77-1.72 (2H, m), 1.66-1.61 (2H, m ).
- the present compound 109 was synthesized according to the reaction described in Production Example 26.
- the structural formula and its 1 H-NMR data are shown below.
- 1 H-NMR (CDCl 3 ) ⁇ : 7.45-7.39 (3H, m), 7.31-7.25 (2H, m), 7.23 (1H, s), 6.80 (1H , D, J 8.5 Hz), 5.04 (2H, s), 3.61 (3H, s), 2.91 (6H, s), 2.49 (3H, s), 2.08 ( 3H, s).
- Production Example 28 A mixture of 0.41 g of 19-2A described in Reference Production Example 19-2, 0.09 g of phenol, 0.019 g of copper iodide, 0.06 g of N-butylimidazole, 0.28 g of potassium carbonate, and 2 mL of toluene was 120 degrees. For 16 hours. The reaction solution was poured into water and extracted with chloroform. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- the compound 158 of the present invention was synthesized according to the reaction described in Production Example 28.
- the structural formula and 1 H-NMR data are shown below.
- Production Example 29 A mixture of 0.34 g of 57A described in Reference Production Example 57, 0.16 g of 2-bromopyridine, 0.019 g of copper iodide, 0.06 g of N-butylimidazole, 0.28 g of potassium carbonate and 2 mL of toluene at 120 degrees. Stir for 6 hours. The reaction solution was poured into water and extracted with chloroform. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- the compound 160 of the present invention was synthesized according to the reaction described in Production Example 29.
- the structural formula and 1 H-NMR data are shown below.
- Reference production example 1 Anhydrous aluminum chloride (21.9 g) was added to 250 mL of N, N-dimethylformamide under ice-cooling and stirred for 15 minutes. To this was added 10.7 g of sodium azide and stirred for 15 minutes. Then, 25.0 g of 1-chloro-3-isocyanato-2-methylbenzene was added and heated at 80 ° C. for 5 hours. After cooling, the reaction solution was added to a mixture of 35 g of sodium nitrite, 2 L of water and 500 g of ice with stirring. The mixture was acidified with 10% hydrochloric acid and extracted with ethyl acetate.
- Reference production example 2 To a mixture of 10.00 g of 1A described in Reference Production Example 1 and 100 mL of N, N-dimethylformamide, 2.30 g of 60% sodium hydride was added under ice cooling. The mixture was warmed to room temperature and stirred for 1 hour. To the reaction mixture, 3.2 mL of methyl iodide was added under ice cooling. The mixture was warmed to room temperature and stirred for 14 hours. Water was poured into the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with 10% hydrochloric acid, water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference production example 3 A mixture of 1.56 g of 2A described in Reference Production Example 2, 0.34 g of 1,1′-azobis (cyclohexane-1-carbonitrile), 1.42 g of N-bromosuccinimide and 30 mL of chlorobenzene was stirred with heating under reflux for 5 hours. did. After cooling, water was poured into the reaction solution and extracted with ethyl acetate. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference production example 5 16.0 g of anhydrous aluminum chloride was added to 180 mL of N, N-dimethylformamide under ice cooling, and the mixture was stirred for 15 minutes. Sodium azide 7.8g was added here, and after stirring for 15 minutes, 17.0g of 4A described in the reference manufacture example 4 was added, and it heated at 80 degreeC for 4.5 hours. After cooling, the reaction solution was added to a mixture of 25 g of sodium nitrite, 2 L of water and 500 g of ice with stirring. The mixture was acidified with 10% hydrochloric acid and extracted with ethyl acetate.
- Reference production example 6 To a mixture of 10.00 g of 5A described in Reference Production Example 5 and 100 mL of N, N-dimethylformamide, 2.47 g of 60% sodium hydride was added under ice cooling. The mixture was warmed to room temperature and stirred for 1 hour. To the reaction mixture, 3.5 mL of methyl iodide was added under ice cooling. The mixture was warmed to room temperature and stirred for 14 hours. Water was poured into the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with 10% hydrochloric acid, water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference production example 7 A mixture of 2.19 g of 6A described in Reference Production Example 6, 0.52 g of 1,1′-azobis (cyclohexane-1-carbonitrile), 2.16 g of N-bromosuccinimide and 40 mL of chlorobenzene was stirred with heating under reflux for 5 hours. did. After cooling, water was poured into the reaction solution and extracted with ethyl acetate. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference production example 8 A mixture of 25.0 g of 1-bromo-2-methyl-3-aminobenzene, 60.0 g of triphosgene and 400 ml of toluene was stirred with heating under reflux for 3 hours. The reaction mixture allowed to cool was concentrated under reduced pressure to obtain 30.3 g of 1-bromo-3-isocyanato-2-methylbenzene (referred to as 8A).
- Reference production example 9 19.7 g of anhydrous aluminum chloride was added to 220 mL of N, N-dimethylformamide under ice cooling and stirred for 15 minutes. To this was added 9.6 g of sodium azide and stirred for 15 minutes. Then, 30.3 g of 8A described in Reference Production Example 8 was added and heated at 80 ° C. for 5 hours. After cooling, the reaction solution was added to a mixture of 33 g of sodium nitrite, 2 L of water and 500 g of ice with stirring. The mixture was acidified with 10% hydrochloric acid and extracted with ethyl acetate.
- Reference production example 10 To a mixture of 31.4 g of 9A described in Reference Production Example 9 and 250 mL of N, N-dimethylformamide, 5.90 g of 60% sodium hydride was added under ice cooling. The mixture was warmed to room temperature and stirred for 1 hour. To the reaction mixture, 8.4 mL of methyl iodide was added under ice cooling. The mixture was warmed to room temperature and stirred for 14 hours. Water was poured into the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with 10% hydrochloric acid, water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference production example 11 A mixture of 8.47 g of 10A described in Reference Production Example 10, 1.54 g of 1,1′-azobis (cyclohexane-1-carbonitrile), 6.44 g of N-bromosuccinimide, and 125 mL of chlorobenzene was stirred with heating under reflux for 5 hours. did. After cooling, water was poured into the reaction solution and extracted with ethyl acetate. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference production example 12 A mixture of 45.0 g of 11A described in Reference Production Example 11, 37.4 g of sodium methoxide, and 600 mL of tetrahydrofuran was stirred at room temperature for 3 hours. Saturated aqueous sodium hydrogen carbonate was poured into the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated aqueous sodium hydrogen carbonate and dried over anhydrous sodium sulfate. After concentration under reduced pressure, 36.2 g of 1- (2-methoxymethyl-3-bromophenyl) -4-methyl-1,4-dihydrotetrazol-5-one (denoted as 12A) was obtained.
- Reference production example 13 36.2 g of 12A described in Reference Production Example 12, 23.2 g of methylboronic acid, 66.7 g of cesium fluoride, [1,1′-bis (diphenylphosphino) ferrocene] palladium (II) dichloride dichloromethane adduct
- a mixture of 6 g and 500 ml dioxane was stirred at 90 ° C. for 5.5 hours. After cooling, the reaction mixture was filtered, and the filtrate was concentrated under reduced pressure.
- Reference production example 14 A mixture of 132 g of 13A described in Reference Production Example 13, 50 mL of acetic acid and 50 mL of 25% hydrogen bromide-acetic acid solution was stirred at 65 ° C. for 1 hour. Saturated brine was poured into the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated aqueous sodium hydrogen carbonate and dried over anhydrous sodium sulfate. After concentration under reduced pressure, 27.9 g of 1- (2-bromomethyl-3-methylphenyl) -4-methyl-1,4-dihydrotetrazol-5-one (denoted as 14A) was obtained.
- Reference production example 15 30.1 g of 12A described in Reference Production Example 12, 12.9 g of cyclopropylboronic acid, 46.2 g of cesium fluoride, [1,1′-bis (diphenylphosphino) ferrocene] palladium (II) dichloride dichloromethane adduct
- a mixture of 8.2 g and 680 ml of dioxane was stirred at 90 ° C. for 4 hours. After cooling, the reaction mixture was filtered, and the filtrate was concentrated under reduced pressure.
- Reference Production Example 16 A mixture of 26.0 g of 15A described in Reference Production Example 15, 40 mL of acetic acid and 40 mL of 25% hydrogen bromide-acetic acid solution was stirred at 65 ° C. for 2 hours. Saturated brine was poured into the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated aqueous sodium hydrogen carbonate and dried over anhydrous sodium sulfate. After concentration under reduced pressure, 30.8 g of 1- (2-bromomethyl-3-cyclopropylphenyl) -4-methyl-1,4-dihydrotetrazol-5-one (referred to as 16A) was obtained.
- 16A 1- (2-bromomethyl-3-cyclopropylphenyl) -4-methyl-1,4-dihydrotetrazol-5-one
- Reference Production Example 17 A mixture of 29.8 g of 12A described in Reference Production Example 12, 35.2 g of tributylvinyltin, 11.6 g of tetrakistriphenylphosphine palladium and 500 mL of toluene was stirred with heating under reflux for 14 hours. After cooling, a saturated aqueous ammonium chloride solution was poured into the reaction solution, and the mixture was extracted with ethyl acetate. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 19-1 A mixture of 19.3 g of 18A described in Reference Production Example 18, 40 mL of acetic acid and 40 mL of 25% hydrogen bromide-acetic acid solution was stirred at 65 ° C. for 1.5 hours. Saturated brine was poured into the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated aqueous sodium hydrogen carbonate and dried over anhydrous sodium sulfate. After concentration under reduced pressure, 13.3 g of 1- (2-bromomethyl-3-ethylphenyl) -4-methyl-1,4-dihydrotetrazol-5-one (referred to as 19-1A) was obtained.
- 19-1A 1- (2-bromomethyl-3-ethylphenyl) -4-methyl-1,4-dihydrotetrazol-5-one
- Reference Production Example 19-2 A mixture of 9.11 g of 3A described in Reference Production Example 3, 5.61 g of 4-bromo-2-methylphenol, 8.29 g of potassium carbonate, and 120 mL of acetonitrile was heated and stirred at 80 ° C. for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 20 A mixture of 23.5 g of 14A described in Reference Production Example 14, 15.5 g of 4-bromo-2-methylphenol, 22.9 g of potassium carbonate, and 330 mL of acetonitrile was stirred at 80 ° C. for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 21 A mixture of 8.97 g of 7A described in Reference Production Example 7, 5.61 g of 4-bromo-2-methylphenol, 8.29 g of potassium carbonate, and 120 mL of acetonitrile was stirred at 80 ° C. for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 22 A mixture of 8.91 g of 19-1A described in Reference Production Example 19, 5.61 g of 4-bromo-2-methylphenol, 8.29 g of potassium carbonate, and 120 mL of acetonitrile was heated and stirred at 80 degrees for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 23 A mixture of 9.27 g of 16A described in Reference Production Example 16, 5.61 g of 4-bromo-2-methylphenol, 8.29 g of potassium carbonate, and 120 mL of acetonitrile was stirred at 80 ° C. for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 24 A mixture of 5.66 g of 14A described in Reference Production Example 14, 3.74 g of 4-bromo-3-methylphenol, 5.53 g of potassium carbonate, and 80 mL of acetonitrile was stirred at 80 ° C. for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 25 A mixture of 4.25 g of 14A described in Reference Production Example 14, 3.02 g of 4-bromo-2,5-dimethylphenol, 4.15 g of potassium carbonate, and 60 mL of acetonitrile was stirred at 80 ° C. for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure. The obtained residue was subjected to silica gel column chromatography to give 1- [2- (4-bromo-2,5-dimethylphenoxymethyl) -3-methylphenyl] -4-methyl-1,4-dihydrotetrazole-5.
- Reference Production Example 26 A mixture of 2.97 g of 19-1A described in Reference Production Example 19, 1.91 g of 4-bromo-2-fluorophenol, 2.76 g of potassium carbonate, and 40 mL of acetonitrile was heated and stirred at 80 degrees for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 27 A mixture of 2.83 g of 14A described in Reference Production Example 14, 2.03 g of 4-bromo-3-methoxyphenol, 2.76 g of potassium carbonate, and 40 mL of acetonitrile was heated and stirred at 80 degrees for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 28 4.05 g of 21A described in Reference Production Example 21, 2.79 g of bis (pinacolato) diboron, 0.25 g of [1,1′-bis (diphenylphosphino) ferrocene] palladium (II) dichloride dichloromethane adduct, potassium acetate A mixture of 2.94 g and 30 mL of dimethyl sulfoxide was stirred for 8 hours while heating at 80 degrees under a nitrogen atmosphere. Water was poured into the cooled reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 29 3.89 g of 20A described in Reference Production Example 20, 2.79 g of bis (pinacolato) diboron, 0.25 g of [1,1′-bis (diphenylphosphino) ferrocene] palladium (II) dichloride dichloromethane adduct, potassium acetate A mixture of 2.94 g and 30 mL of dimethyl sulfoxide was stirred for 8 hours while heating at 80 degrees under a nitrogen atmosphere. Water was poured into the cooled reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 30 4.03 g of 22A described in Reference Production Example 22, 2.79 g of bis (pinacolato) diboron, 0.25 g of [1,1′-bis (diphenylphosphino) ferrocene] palladium (II) dichloride dichloromethane adduct, potassium acetate A mixture of 2.94 g and 30 mL of dimethyl sulfoxide was stirred for 8 hours while heating at 80 degrees under a nitrogen atmosphere. Water was poured into the cooled reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 31 While stirring a mixture of 13.1 g of 29A described in Reference Production Example 29, 8.40 g of sodium hydroxide, 60 ml of tetrahydrofuran and 30 ml of water at 0 ° C. at 0 ° C., 17.0 ml of 30% aqueous hydrogen peroxide was added, Stir for 1 hour. After warming to room temperature and stirring for another 1 hour, a saturated aqueous sodium thiosulfate solution was added to the reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 32 A mixture of 2.83 g of 14A described in Reference Production Example 14, 2.12 g of 4-hydroxy-3-methylbenzophenone, 2.76 g of potassium carbonate, and 40 mL of acetonitrile was stirred for 2 hours while heating at 80 degrees. Water was poured into the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 33 A mixture of 2.83 g of 14A described in Reference Production Example 14, 1.36 g of 4-hydroxy-3-methyl-benzaldehyde, 2.76 g of potassium carbonate, and 40 mL of acetonitrile was stirred with heating under reflux for 4 hours. Cool to room temperature, filter the reaction mixture and concentrate the filtrate. The obtained residue was subjected to silica gel column chromatography to give 3-methyl-4- ⁇ [2-methyl-6- (4-methyl-1,4-dihydrotetrazol-5-one-1-yl) phenyl] methyl. 2.96 g of oxy ⁇ benzaldehyde (referred to as 33A) was obtained.
- Reference Production Example 34 A mixture of 5.66 g of 14A described in Reference Production Example 14 and 3.00 g of 4′-hydroxy-3′-methyl-acetophenone, 5.53 g of potassium carbonate, and 40 mL of acetonitrile was stirred with heating under reflux for 4 hours. Cool to room temperature, filter the reaction mixture and concentrate the filtrate. The obtained residue was subjected to silica gel column chromatography to give 1- ⁇ 2- (2-methyl-4-acetyl-phenoxymethyl) -3-methyl-phenyl ⁇ -4-methyl-1,4-dihydrotetrazole-5. -4.73 g of ON (denoted as 34A) was obtained.
- Reference Production Example 35 While stirring a mixture of 1.35 g of 33A described in Reference Production Example 33 and 8 mL of methanol at 0 degree, 0.30 g of sodium borohydride was added and stirred at room temperature for 4 hours. Water was poured into the reaction solution, and the mixture was extracted with chloroform. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure. The obtained residue was subjected to silica gel column chromatography, and 1- [2- ⁇ 4-hydroxymethyl-2-methylphenoxymethyl ⁇ -3-methylphenyl] -4-methyl-1,4-dihydrotetrazole-5- 1.25 g of ON (denoted 35A) was obtained.
- Reference Production Example 36 While stirring a mixture of 0.71 g of 34A described in Reference Production Example 34 and 4 mL of methanol at 0 degree, 0.15 g of sodium borohydride was added, and the mixture was stirred at room temperature for 4 hours. Water was poured into the reaction solution, and the mixture was extracted with chloroform. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 37 A mixture of 8.49 g of 14A described in Reference Production Example 14, 4.59 g of 4-nitro-2-methylphenol, 2.76 g of potassium carbonate, and 120 mL of acetonitrile was stirred at 80 ° C. for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 38 A mixture of 7.11 g of 37A described in Reference Production Example 37, 6.00 g of electrolytic iron, 80 ml of acetic acid, and 20 mL of water was stirred at 60 ° C. for 2 hours. After concentration under reduced pressure, a saturated aqueous sodium hydrogen carbonate solution was added to the residue, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 39 While stirring a mixture of 2.25 g of 30A described in Reference Production Example 30, 1.40 g of sodium hydroxide, 10 ml of tetrahydrofuran and 5 mL of water at 0 ° C. at 0 ° C., 2.83 ml of 30% hydrogen peroxide water was added. Stir for 1 hour. After raising the temperature to room temperature and stirring for 4 hours, a saturated aqueous sodium thiosulfate solution was poured into the reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 40 A mixture of 1.42 g of 14A described in Reference Production Example 14, 1.00 g of 4-bromo-2-ethylphenol, 1.38 g of potassium carbonate, and 20 mL of acetonitrile was heated and stirred at 80 degrees for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 41 A mixture of 1.42 g of 14A described in Reference Production Example 14, 1.00 g of 4-bromo-3-cyanophenol, 1.38 g of potassium carbonate, and 20 mL of acetonitrile was heated and stirred at 80 degrees for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 42 A mixture of 1.35 g of 14A described in Reference Production Example 14, 1.00 g of 4-bromo-3,5-difluorophenol, 1.32 g of potassium carbonate, and 19 mL of acetonitrile was heated and stirred at 80 degrees for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure. The resulting residue was washed with hexane and methyl-tert-butylketone to give 1- [2- (4-bromo-3,5-difluorophenoxymethyl) -3-methylphenyl] -4-methyl-1,4-dihydro.
- Reference Production Example 43 A mixture of 2.83 g of 14A described in Reference Production Example 14, 2.41 g of 4-bromo-3-trifluoromethylphenol, 2.76 g of potassium carbonate, and 40 mL of acetonitrile was heated and stirred at 80 degrees for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 44 A mixture of 2.83 g of 14A described in Reference Production Example 14, 2.41 g of 4-bromo-2-trifluoromethylphenol, 2.76 g of potassium carbonate, and 40 mL of acetonitrile was stirred at 80 ° C. for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 47 A mixture of 2.83 g of 14A described in Reference Production Example 14 and 2.01 g of 45A described in Reference Production Example 45, 2.76 g of potassium carbonate and 40 mL of acetonitrile was heated and stirred at 80 ° C. for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference production example 48 A mixture of 2.83 g of 14A described in Reference Production Example 14, 2.29 g of 46A described in Reference Production Example 46, 2.76 g of potassium carbonate, and 40 mL of acetonitrile was heated and stirred at 80 degrees for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 49 A mixture of 2.83 g of 14A described in Reference Production Example 14, 2.01 g of 4-bromo-2,3-dimethylphenol, 2.76 g of potassium carbonate, and 40 mL of acetonitrile was heated and stirred at 80 degrees for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure. The obtained residue was subjected to silica gel column chromatography to give 1- [2- (4-bromo-2,3-dimethylphenoxymethyl) -3-methylphenyl] -4-methyl-1,4-dihydrotetrazole-5.
- Reference production example 50 A mixture of 2.23 g of 19-1A described in Reference Production Example 19 and 1.51 g of 4-bromo-2,5-dimethylphenol, 2.07 g of potassium carbonate, and 30 mL of acetonitrile was stirred at 80 ° C. for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 51 A mixture of 2.24 g of 7A described in Reference Production Example 7, 1.51 g of 4-bromo-2,5-dimethylphenol, 2.07 g of potassium carbonate, and 30 mL of acetonitrile was heated and stirred at 80 degrees for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure. The obtained residue was subjected to silica gel column chromatography to give 1- [2- (4-bromo-2,5-dimethylphenoxymethyl) -3-methoxyphenyl] -4-methyl-1,4-dihydrotetrazole-5.
- Reference Production Example 53 A mixture of 2.83 g of 14A described in Reference Production Example 14, 2.09 g of 4-bromo-2,6-difluorophenol, 2.76 g of potassium carbonate, and 40 mL of acetonitrile was heated and stirred at 80 degrees for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure. The obtained residue was subjected to silica gel column chromatography to give 1- [2- (4-bromo-2,6-difluorophenoxymethyl) -3-methylphenyl] -4-methyl-1,4-dihydrotetrazole-5.
- Reference production example 54 A mixture of 2.83 g of 14A described in Reference Production Example 14, 2.45 g of 4-bromo-2,3,5,6-tetrafluorophenol, 2.76 g of potassium carbonate and 40 mL of acetonitrile was heated and stirred at 80 ° C. for 4 hours. did. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure. The obtained residue was subjected to silica gel column chromatography to give 1- [2- (4-bromo-2,3,5,6-tetrafluorophenoxymethyl) -3-methylphenyl] -4-methyl-1,4.
- Reference Production Example 55 A mixture of 2.83 g of A14 described in Reference Production Example 14, 2.05 g of 4-bromo-5-fluoro-2-methylphenol, 2.76 g of potassium carbonate, and 40 mL of acetonitrile was heated and stirred at 80 degrees for 4 hours. Water was added to the reaction mixture, and the mixture was extracted with ethyl acetate. The organic layer was washed with saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure. The obtained residue was washed with hexane and methyl-tert-butylketone to give 1- [2- (4-bromo-5-fluoro-2-methylphenoxymethyl) -3-methylphenyl] -4-methyl-1,4.
- Reference production example 56 8.06 g of 25A described in Reference Production Example 25, 5.59 g of bis (pinacolato) diboron, 0.49 g of [1,1′-bis (diphenylphosphino) ferrocene] palladium (II) dichloride dichloromethane adduct, potassium acetate A mixture of 5.89 g and 60 mL of dimethyl sulfoxide was stirred for 8 hours while heating at 80 degrees under a nitrogen atmosphere. Water was poured into the cooled reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Reference Production Example 57 While stirring a mixture of 5.40 g of 56A described in Reference Production Example 56, 3.36 g of sodium hydroxide, 24 ml of tetrahydrofuran and 12 ml of water at 0 ° C. under ice zero, 6.8 ml of 30% hydrogen peroxide water was added, Stir for 1 hour. After raising the temperature to room temperature and stirring for 4 hours, a saturated aqueous sodium thiosulfate solution was poured into the reaction mixture, and the mixture was extracted with chloroform. The organic layer was washed with water and saturated brine, dried over anhydrous magnesium sulfate, and concentrated under reduced pressure.
- Compounds Q1A-001 to Q11L-633 can be obtained according to the above method.
- Compounds Q1A-001 to Q11L-633 are each tetrazolinone compounds shown below. [Wherein Y is a substituent corresponding to each of substituent numbers 1 to 633]
- Compounds EB1A-001 to EG1N-342 can be obtained according to the above method.
- Compounds EB1A-001 to EG1N-342 are each represented by the following formula.
- Z 101 represents the same meaning as described above, and Q represents a substituent corresponding to each of substituent numbers 1 to 342. ]
- control agent of the present invention examples include the following.
- Pest control composition Pest control composition containing any one of the present compounds 1 to 166 and metconazole at a ratio of 10: 1; Any one of the present compounds 1 to 166 and Tebuconazole A pest control composition containing any one of the compounds 1 to 166 of the present invention and tebuconazole in a ratio of 1: 1; A pest control composition comprising any one of the compounds 1-166 and tebuconazole in a ratio of 10: 1; any one of the present compounds 1-166; tetraconazole; , A pest control composition containing 0.1: 1 of the ratio; a pest control composition containing any one of compounds 1 to 166 of the present invention and tetraconazole in a ratio of 1: 1; A pest control composition containing any one of the inventive compounds 1 to 166 and tetraconazole in a ratio of 10: 1; any one of the inventive compounds 1 to 166 and cyproconazole Pest control composition containing 1: 1 ratio; Pest control composition containing any one of compounds 1
- Control composition Pest control composition containing any one of the compounds 1 to 166 of the present invention and imazalil in a ratio of 10: 1; Any compound of the compounds 1 to 166 of the present invention and epoxyconazol
- Pest control composition containing in proportion: Pest control composition containing any one of compounds 1 to 166 of the present invention and triticonazole in a ratio of 10: 1; any of compounds 1 to 166 of the present invention A pest control composition containing any one compound and ipconazole at a ratio of 0.1: 1; a pest containing any one compound of the compounds 1 to 166 of the present invention and ipconazole at a ratio of 1: 1.
- Pest control composition containing any one compound of the present compounds 1 to 166 and ipconazole in a ratio of 10: 1; Any one compound of the present compounds 1 to 166 and trif A pest control composition containing misol in a ratio of 0.1: 1; a pest control composition containing any one of the compounds 1 to 166 of the present invention and triflumizole in a ratio of 1: 1 A pest control composition containing any one of the compounds 1 to 166 of the present invention and triflumizole in a ratio of 10: 1; and any one of the compounds 1 to 166 of the present invention and fenbuconazole; , A pest control composition containing 0.1: 1 ratio; a pest control composition containing any one of the compounds 1 to 166 of the present invention and fenbuconazole in a ratio of 1: 1; A pest control composition comprising any one of the inventive compounds 1 to 166 and fenbuconazole in a ratio of 10: 1; any one of the inventive compounds 1 to 166 and he
- Pest control composition containing any one compound of the present compounds 1 to 166 and dimoxystrobin in a ratio of 0.1: 1; any one compound of the present compounds 1 to 166 and dimoxist A pest control composition containing robin at a ratio of 1: 1; a pest control composition containing any one of the compounds 1 to 166 of the present invention and dimoxystrobin at a ratio of 10: 1
- Control composition Pest control composition containing any one compound of the present compounds 1 to 166 and isophetamide in a ratio of 10: 1; any one compound of the present compounds 1 to 166 and N- Pest control composition containing [2- (3,4-difluorophenyl) phenyl] -3-trifluoromethylpyrazine-2-carboxylic acid amide in a ratio of 0.1: 1; A pest control composition comprising any one compound of 166 and N- [2- (3,4-difluorophenyl) phenyl] -3-trifluoromethylpyrazine-2-carboxylic acid amide in a ratio of 1: 1.
- a pest control composition comprising: any one of the compounds 1 to 166 of the present invention and (R)-( ⁇ )-N- (1,1,3-trimethylindan-4-yl) -1-methyl- 3-Diff A pest control composition containing oromethylpyrazole-4-carboxylic acid amide in a ratio of 0.1: 1; any one of the compounds 1 to 166 of the present invention and (R)-(-)-N- Pest control composition containing (1,1,3-trimethylindan-4-yl) -1-methyl-3-difluoromethylpyrazole-4-carboxylic acid amide in a ratio of 1: 1; compound of the present invention Any one of 1 to 166 and (R)-( ⁇ )-N- (1,1,3-
- a pest control composition comprising any one of the present compounds 1 to 166 and 3-chloro-4- (2,6-difluorophenyl) -6-methyl-5-phenylpyridazine in a ratio of 1: 1.
- a pest control composition comprising any one of the compounds 1 to 166 of the present invention and 3-chloro-4- (2,6-difluorophenyl) -6-methyl-5-phenylpyridazine in a ratio of 10: 1;
- Product any one of the compounds 1 to 166 of the present invention and 3-cyano-4- (2,6-difluorophenyl) -6-methyl-5-phenylpyridazine in a ratio of 0.1: 1
- a pest control composition comprising: any one of the compounds 1 to 166 of the present invention and 3-cyano-4- (2,6-difluorophenyl) -6-methyl-5-phenylpyridazine Including ratio
- a pest control composition comprising: any one of
- Pest control composition containing any one compound of the present compounds 1-166 and metalaxyl M (mefenoxam) in a ratio of 0.1: 1; any one compound of the present compounds 1-166 and metalaxyl M A pest control composition containing (mefenoxam) in a ratio of 1: 1; a pest containing a compound of any one of the compounds 1 to 166 of the present invention and metalaxyl M (mefenoxam) in a ratio of 10: 1
- Control composition Pest control composition containing any one compound of the present compounds 1 to 166 and benalaxyl in a ratio of 0.1: 1; Any one compound of the present compounds 1 to 166 and benalaxyl; A pest control composition containing the compound of any one of the compounds 1 to 166 of the present invention and benalaxyl in a ratio of 1: 1.
- composition A pest control composition containing any one of the compounds of the present invention 1 to 166 and benalaxyl M (kiralaxil) in a ratio of 0.1: 1; any one of the compounds 1 to 166 of the present invention And benalaxyl M (kiralaxil) in a ratio of 1: 1; a compound of any one of the compounds 1 to 166 of the present invention and benalaxyl M (kiralaxyl) in a ratio of 10: 1
- a pest control composition comprising: any one of the compounds 1 to 166 of the present invention and dimethomorph in a ratio of 0.1: 1; any one compound of the present compounds 1 to 166 And dimethomorph in a ratio of 1: 1; a pest containing a compound of any one of the compounds 1 to 166 of the present invention and dimethomorph in a ratio of 10: 1
- Control composition Pest control composition containing any one compound of the present compounds 1 to 166 and iprovalicarb in
- Pest control composition containing; Pest control composition containing any one of compounds 1 to 166 of the present invention and simoxanil in a ratio of 0.1: 1; Any of compounds 1 to 166 of the present invention A pest control composition containing one compound and simoxanil in a ratio of 1: 1; a pest control composition containing any one of the compounds 1 to 166 of the present invention and simoxanil in a ratio of 10: 1 A pesticidal composition containing any one of the compounds 1 to 166 of the present invention and fluopicolide in a ratio of 0.1: 1; and any one of the compounds 1 to 166 of the present invention and fluopicolide 1 : A pest control composition containing the compound in a ratio of 1: any one of the compounds of the present invention 1 to 166 and fluopicolide in a ratio of 10: 1; A pest control composition containing any one compound and cyazofamide in a ratio of 0.1: 1; any one of the compounds 1 to 166 of the present invention and cyazofamide in
- a pest control composition containing any one of the present compounds 1 to 166 and propamocarb hydrochloride at a ratio of 0.1: 1; any one of the present compounds 1 to 166 and propamocarb hydrochloride A pest control composition containing any one of the compounds 1 to 166 of the present invention and fenpyrazamine in a ratio of 0.1: 1; A pest control composition containing any one of the compounds 1 to 166 and fenpyrazamine in a ratio of 1: 1; any one of the compounds 1 to 166 of the present invention and fenpyrazamine in a ratio of 10: 1 Pest control composition containing; Pest control composition containing any one compound of present invention compounds 1-166 and fenhexamide in a ratio of 0.1: 1; Present compound 1-1 A pest control composition containing any one of the compounds 66 and fenhexamide in a ratio of 1: 1; any one of the compounds 1 to 166 of the present invention and fenhexamide in a ratio of 10: 1 A pest control composition
- a pest control composition comprising one compound and validamycin in a ratio of 10: 1; a pest control composition comprising any one of the compounds 1 to 166 of the present invention and isoprothiolane in a ratio of 0.1: 1
- Composition Pest control composition containing any one compound of the present compounds 1 to 166 and isoprothiolane in a ratio of 1: 1; Any combination of the present compounds 1 to 166 And a isoprothiolane, 10: pesticidal composition containing in a ratio of 1;
- Pest control composition containing any one compound of the present compounds 1 to 166 and hydroxyisoxazole in a ratio of 0.1: 1; any one compound of the present compounds 1 to 166 and hydroxyisoxazole A pesticidal composition containing sol in a ratio of 1: 1; a pesticidal composition containing any one of the compounds 1 to 166 of the present invention and hydroxyisoxazole in a ratio of 10: 1
- Pest control composition to be contained any one of the compounds 1 to 166 of the present invention and 2,6-dimethyl-1H, 5H- [1,4] dithino [2,3-c: 5,6-c ′]
- a pest control composition comprising: any one of the compounds 1 to 166 of the present invention and 3- (5-fluoro-3,3,4,4-tetramethyl-3,4-dihydroisoquinolin-1-yl); A pest control composition containing quinoline in a ratio of 10: 1; any one of the compounds 1 to 166 of the present invention and 3- (4,4,5-trifluoro-3,3-dimethyl-3, Pest control composition containing 4-dihydroisoquinolin-1-yl) quinoline in a ratio of 0.1: 1; any one of compounds 1 to 166 of the present invention and 3- (4,4,5- Trifluoro-3,3-dimethyl-3,4-di Pest control composition containing hydroisoquinolin-1-yl) quinoline in a
- Containing pest control composition any one of the compounds 1 to 166 of the present invention and [3- (4-chloro-2-fluorophenyl) -5- (2,4-difluorophenyl) -1, 2-oxazole -4-yl
- a pest control composition containing (pyridin-3-yl) methanol in a ratio of 1: 1; any one of the compounds 1 to 166 of the present invention and [3- (4-chloro-2-fluorophenyl) Pest control composition containing -5- (2,4-difluorophenyl) -1,2-oxazol-4-yl] (pyridin-3-yl) methanol in a ratio of 10: 1; Any one of 1 to 166 and (S)-[3- (4-chloro-2-fluorophenyl) -5- (2,4-difluorophenyl) -1,2-oxazol-4-yl] (pyridine) -3-yl) methanol pest
- Pesticide composition containing (pyridin-3-yl) methanol in a ratio of 1: 1; any one of the compounds 1 to 166 of the present invention and (S)-[3- (4-chloro- Pest control composition containing 2-fluorophenyl) -5- (2,4-difluorophenyl) -1,2-oxazol-4-yl] (pyridin-3-yl) methanol in a ratio of 10: 1 Product; any one of the compounds 1 to 166 of the present invention and (R)-[3- (4-chloro-2-fluorophenyl) -5- (2,4-difluorophenyl) -1, 2-oxazole-4 -Yl] (pyridine-3- P) Pesticide composition containing (pyridin-3-yl) methanol in a ratio of 1: 1; any one of the compounds 1 to 166 of the present invention and (R)-[3- (4-chloro-2-fluorophenyl) -5- (2
- Decomposition composition any one of compounds 1 to 166 of the present invention and 2- ⁇ [(2R, 3R) -3- (2-chlorophenyl) -2- (2,4-difluorophenyl) oxilan-2-yl] Pest control composition containing methyl ⁇ -2,4-dihydro-3H-1,2,4-triazole-3-thione at a ratio of 10: 1; any one of compounds 1 to 166 of the present invention And 2- ⁇ [(2S, 3S) -3- (2-chlorophenyl) -2- (2,4-difluorophenyl) oxiran-2-yl] methyl ⁇ -2,4-dihydro-3H-1,2, A pest control composition comprising 4-triazole-3-thione in a ratio of 0.1: 1;
- Pest control composition to be contained any one of the compounds 1 to 166 of the present invention and 1- ⁇ [3- (2-chlorophenyl) -2- (2,4-difluorophenyl) oxiran-2-yl] methyl ⁇ -1H-1,2,4-triazole-5-thiol in a ratio of 10: 1; a pest control composition; any one of the compounds 1 to 166 of the present invention and 1- ⁇ [rel- ( 2R, 3S) -3- (2-chrome Phenyl) -2- (2,4-difluorophenyl) oxiran-2-yl] methyl ⁇ -1H-1,2,4-triazole-5-thiol in a ratio of 0.1: 1 Control composition; any one of the compounds 1 to 166 of the present invention and 1- ⁇ [rel- (2R, 3S) -3- (2-chlorophenyl) -2- (2,4-difluorophenyl) oxirane-2- Yl] methyl ⁇
- a pest control composition comprising a ratio of 1: 1; any one of the compounds 1 to 166 of the present invention and 9-fluoro-2,3-dihydro-2,2-dimethyl-5- (quinolin-3-yl) ) -1,4-benzoxazepine at a ratio of 1: 1; a pest control composition; any one of the compounds 1 to 166 of the present invention and 9-fluoro-2,3-dihydro-2, A pest control composition containing 2-dimethyl-5- (quinolin-3-yl) -1,4-benzoxazepine in a ratio of 10: 1; any one of compounds 1 to 166 of the present invention; N-cyclopropyl-3- (difluoromethyl ) -5-fluoro-
- Pest control composition any one of compounds 1 to 166 of the present invention and N-cyclopropyl-3- (difluoromethyl) -5-fluoro-N- (5-chloro-2-isopropylbenzyl) -1-methyl -1H-pyrazole-4-carboxamide in a ratio of 1: 1; a pest control composition; any one of the compounds 1 to 166 of the present invention and N-cyclopropyl-3- (difluoromethyl) -5 Harmful containing 10% of fluoro-N- (5-chloro-2-isopropylbenzyl) -l-methyl-lH-pyrazole-4-carboxamide Biocontrol composition; any one of the compounds 1 to 166 of the present invention and N- [1- (2,4-dichlorophenyl) -1-methoxypropan-2-yl] -3-difluoromethyl-1-methyl-1H A pest control composition comprising pyrazole-4-carboxamide in a ratio of 0.1: 1
- Any one of the compounds 1 to 166 of the present invention and 3-difluoromethyl-N-methoxy-1-methyl-N- [1-methyl-2- (2,4,6-trichlorophenyl) ethyl] pyrazole-4- A pest control composition containing carboxamide in a ratio of 0.1: 1; any one of the compounds 1 to 166 of the present invention and 3-difluoromethyl-N-methoxy-1-methyl-N- [1- Pest control composition containing methyl-2- (2,4,6-trichlorophenyl) ethyl] pyrazole-4-carboxamide in a ratio of 1: 1; any one of compounds 1 to 166 of the present invention; 3-difluoromethyl-N-methoxy-1-methyl-N- [1-methyl-2- (2,4,6-trichlorophenyl) ethyl] pyrazole-4-carboxamide
- a pest control composition comprising: any one of the compounds 1 to 166 of the present invention and
- Pest control composition any one of compounds 1 to 166 of the present invention and 3-butyn-1-yl N- ⁇ 6-[( ⁇ (Z)-[(1-methyl-1H-tetrazol-5-yl ) Phenylmethylene] amino Oxy) methyl] -2-pyridinyl ⁇ carbamate in a ratio of 10: 1; any one of the compounds 1 to 166 of the present invention and 5-fluoro-2-[(4-methyl) Phenyl) methoxy] -4-pyrimidinamine in a ratio of 0.1: 1; any one of the compounds 1 to 166 of the present invention and 5-fluoro-2-[(4- Pest control composition containing methylphenyl) methoxy] -4-pyrimidinamine in a ratio of 1: 1; any one of compounds 1 to 166 of the present invention and 5-fluoro-2-[(4-methyl Phenyl) methoxy] -4-pyrimidinamine in a ratio of 10: 1; any one of Compounds 1 to
- Pest control composition; Pest control composition containing any one compound of the present compounds 1 to 166 and dichlorane; Pest control composition containing any one compound of the present compounds 1 to 166 and diflumetrim A pest control composition containing any one of the compounds 1 to 166 of the present invention and dimesimol; any one of the compounds 1 to 166 of the present invention
- a pest control composition comprising a compound and a dinocap; a pest control composition comprising any one of the compounds of the present invention Compounds 1 to 166 and dithianon;
- Pest control composition containing any one compound of the present compounds 1 to 166 and flumeciclos; Pest control composition containing any one compound of the present compounds 1 to 166 and iodocarb; Pest control composition containing any one compound of the present compounds 1 to 166 and iprobenphos; Pest control composition containing any one compound of the present compounds 1 to 166 and meptyl dinocap A pest control composition containing any one of the compounds 1 to 166 of the present invention and metasulfocarb; compounds 1 to 166 of the present invention; A pest control composition containing any one compound and methylam; a pest control composition containing any one of the compounds 1 to 166 of the present invention and naphthifine; any one compound of the compounds 1 to 166 of the present invention And a pest control composition containing any one of the compounds 1 to 166 of the present invention and oxilinone; and any one compound of the present compounds 1 to 166 and pefrazoate.
- Pest control composition containing; Pest control composition containing any one compound of the present compounds 1 to 166 and phosphorous acid; Any one compound of the present compounds 1 to 166 and sodium phosphite A pesticidal composition containing a salt; a pesticidal composition containing any one of the compounds 1 to 166 of the present invention and an ammonium salt of phosphorous acid; Pesticidal compositions containing the any one compound polyoxin of Compound 1-166;
- a pest control composition containing one compound and chloretoxyphos in a ratio of 1:10; any one of the compounds 1 to 166 of the present invention and chloretoxyphos in a ratio of 1:50 A pest control composition comprising any one of the compounds 1 to 166 of the present invention and chlorfenvinphos in a ratio of 1: 1; any one of the compounds 1 to 166 of the present invention.
- a pest control composition containing the compound and chlorfenvin phos in a ratio of 1:10; any one of the compounds 1 to 166 of the present invention and chlorfenvin phos in a ratio of 1:50 A pest control composition; a pest control composition containing any one of the compounds 1 to 166 of the present invention and chlormefos in a ratio of 1: 1; a compound of any one of the compounds 1 to 166 of the present invention and chlormefos :
- a pest control composition containing any one compound of Compounds 1 to 166 and chlorpyrifos in a ratio of 1: 1; any one compound of the present compounds 1 to 166 and chlorpyrifos in a ratio of 1:10 A pest control composition comprising:
- a pest control composition containing any one compound of the present compounds 1 to 166 and chlorpyrifos in a ratio of 1:50; any one compound of the present compounds 1 to 166 and chlorpyrifos methyl are mixed 1: 1.
- a pest control composition containing any one compound of the present compounds 1-166 and etoprophos in a ratio of 1:50; any one compound of the present compounds 1-166 and fanful 1: 1 A pest control composition containing the compound of any one of the present compounds 1 to 166 and fanful in a ratio of 1:10; any of the compounds 1 to 166 of the present invention A pest control composition containing any one compound and fanful in a ratio of 1:50; pest control containing any one of the compounds 1 to 166 of the present invention and fenamiphos in a ratio of 1: 1
- Pest control composition containing; Pest control composition containing any one of compounds 1 to 166 of the present invention and betacyfluthrin in a ratio of 1:10; Any one of compounds 1 to 166 of the present invention A pest control composition containing the compound and cyhalothrin in a ratio of 0.1: 1; a pest control composition containing any one of the compounds 1 to 166 of the present invention and cyhalothrin in a ratio of 1: 1 A pest control composition containing any one of the compounds 1 to 166 of the present invention and cyhalothrin in a ratio of 1:10; and any one compound of the compounds 1 to 166 of the present invention and gamma cyhalothrin.
- a pest control composition containing any one compound and tetraniprolol in a ratio of 1:10; any one compound of the present compounds 1 to 166 and tetraniliprol in a ratio of 1:50 A pest control composition comprising: any one of the compounds 1 to 166 of the present invention and Bacillus thuringiensis Aizawai subspecies in a ratio of 1: 1;
- any of the compounds 1 to 166 of the present invention A pest control composition containing any one compound and Bacillus thuringiensis Isla Ellensis subsp. In a ratio of 1: 1; any one of the compounds 1 to 166 of the present invention and Bacillus thuringiensis larensis subtilis A pest control composition containing the seed in a ratio of 1:10; any one of the compounds 1 to 166 of the present invention and Bacillus And Yuringenshisu Isla Ellen cis subspecies, 1: pest control composition containing 50 ratio of;
Abstract
Description
すなわち、本発明は以下の〔1〕~〔8〕のとおりである。
〔1〕 式(1)
〔式中、
R1、R2、R3およびR11は各々独立して、群P1から選ばれる1以上の原子もしくは基を有していてもよいC1−C6アルキル基、ハロゲン原子、水素原子、1以上のハロゲン原子を有していてもよいC1−C6アルコキシ基、シアノ基、ニトロ基、1以上のハロゲン原子を有していてもよいC2−C6アルケニル基、1以上のハロゲン原子を有していてもよいC2−C6アルキニル基、1以上のハロゲン原子を有していてもよいC1−C8アルキルアミノ基、1以上のハロゲン原子を有していてもよいC1−C6アルキルチオ基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルフィニル基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルホニル基、ペンタフルオロスルファニル基、C3−C9トリアルキルシリル基、C2−C6アルキルカルボニル基、C2−C6アルコキシカルボニル基またはC1−C6アルキル基を有していてもよいアミノカルボニル基を表し;
R4およびR5は各々独立して、水素原子、ハロゲン原子またはC1−C3アルキル基を表し;
R6は1以上のハロゲン原子を有していてもよいC1−C6アルキル基、1以上のハロゲン原子を有していてもよいC1−C6アルコキシ基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルキル基、ハロゲン原子、1以上のハロゲン原子を有していてもよいC2−C6アルケニル基、シアノ基、1以上のハロゲン原子を有していてもよいC1−C6アルキルチオ基、1以上のハロゲン原子を有していてもよいC2−C6アルキニル基、ニトロ基、1以上のC1−C6アルキル基を有していてもよいアミノカルボニル基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルキルオキシ基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルキルチオ基、1以上のハロゲン原子を有していてもよいC3−C6アルケニルオキシ基、1以上のハロゲン原子を有していてもよいC3−C6アルキニルオキシ基、1以上のハロゲン原子を有していてもよいC3−C6アルケニルチオ基、1以上のハロゲン原子を有していてもよいC3−C6アルキニルチオ基、C2−C6アルコキシカルボニル基、ヒドロキシ基、スルファニル基、1以上のハロゲン原子を有していてもよいC1−C8アルキルアミノ基、ペンタフルオロスルファニル基、C3−C9トリアルキルシリル基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルホニル基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルフィニル基、C2−C6アルキルカルボニル基、C2−C5アルコキシアルキル基またはC2−C5アルキルチオアルキル基を表し;
R7、R8およびR9は各々独立して、水素原子、ハロゲン原子、1以上のハロゲン原子を有していてもよいC1−C3アルキル基、1以上のハロゲン原子を有していてもよいC2−C3アルケニル基、または1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基を表し;
R10は1以上のハロゲン原子を有していてもよいC1−C3アルキル基、1以上のハロゲン原子を有していてもよいC2−C3アルケニル基、1以上のハロゲン原子を有していてもよいC2−C3アルキニル基または1以上のハロゲン原子を有していてもよいC3−C5シクロアルキル基を表し;
R12は群P2から選ばれる1以上の原子もしくは基を有していてもよいC6−C16アリール基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC6−C16アリールオキシ基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC6−C16アリールチオ基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC7−C18アラルキル基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC7−C18アラルキルオキシ基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC7−C16アリールオキシアルキル基、群P2から選ばれる1以上の原子もしくは基を有していてもよいアニリノ基、C2−C5アルキルチオアルキル基、1以上のC1−C3アルコキシ基および/もしくはハロゲン原子を有していてもよいC1−C6アルキル基、1以上のハロゲン原子を有していてもよいC1−C6アルコキシ基、1以上のハロゲン原子を有していてもよいC2−C6アルケニル基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルキル基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルケニル基、1以上のハロゲン原子を有していてもよいC1−C8アルキルアミノ基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC2−C9ヘテロアリールオキシ基(但し、ヘテロアリール部分は5員環、6員環、5員環と5員環との縮合環、5員環と6員環との縮合環または6員環と6員環との縮合環を表す)、R13R14N−N=CH−、R13R14N−CH=N−、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルフィニル基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルホニル基、ペンタフルオロスルファニル基、C2−C6アルコキシカルボニル基、C2−C6アルキルカルボニルオキシ基、C1−C6アルキル基を有していてもよいアミノカルボニル基またはC3−C9トリアルキルシリル基を表し;
R13およびR14は、各々独立して水素原子またはC1−C3アルキル基を表し;
Xは酸素原子または硫黄原子を表す。
群P1:ハロゲン原子、シアノ基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルキル基、1以上のハロゲン原子を有していてもよいC1−C4アルコキシ基または1以上のハロゲン原子を有していてもよいC1−C4アルキルチオ基からなる群。
群P2:1以上のハロゲン原子を有していてもよいC1−C6アルキル基、ハロゲン原子、シアノ基、ヒドロキシ基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルキル基、1以上のハロゲン原子を有していてもよいC1−C6アルコキシ基、1以上のハロゲン原子を有していてもよいC1−C6アルキルチオ基、1以上のハロゲン原子を有していてもよいC2−C6アルケニル基、1以上のハロゲン原子を有していてもよいC2−C6アルキニル基、1以上のハロゲン原子を有していてもよいC1−C8アルキルアミノ基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルフィニル基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルホニル基、ペンタフルオロスルファニル基、C2−C6アルコキシカルボニル基、C2−C6アルキルカルボニル基、C2−C6アルキルカルボニルオキシ基、C2−C6アルキルカルボニルアミノ基、C1−C6アルキル基を有していてもよいアミノカルボニル基およびC3−C9トリアルキルシリル基からなる群。〕
で示されるテトラゾリノン化合物。
R2およびR3が、水素原子、ハロゲン原子、1以上のハロゲン原子を有していてもよいC1−C4アルキル基、1以上のハロゲン原子を有していてもよいC1−C4アルコキシ基またはシアノ基であり;
R4、R5、R7、R8、R9およびR11が、水素原子であり;
R6が、1以上のハロゲン原子を有していてもよいC1−C4アルキル基、ハロゲン原子、1以上のハロゲン原子を有していてもよいC1−C4アルコキシ基、1以上のハロゲン原子を有していてもよいC3−C5シクロアルキル基、1以上のハロゲン原子を有していてもよいC2−C4アルケニル基または、C2−C4アルキニル基であり;
R10が、メチル基であり;
Xが、酸素原子である、〔1〕に記載のテトラゾリノン化合物。
群P3:1以上のハロゲン原子を有していてもよいC1−C3アルキル基、ハロゲン原子、シアノ基、1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基、1以上のハロゲン原子を有していてもよいC3−C4シクロアルキル基および1以上のハロゲン原子を有していてもよいC1−C3アルキルチオ基からなる群。
群P3:1以上のハロゲン原子を有していてもよいC1−C3アルキル基、ハロゲン原子、シアノ基、1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基、1以上のハロゲン原子を有していてもよいC3−C4シクロアルキル基および1以上のハロゲン原子を有していてもよいC1−C3アルキルチオ基からなる群。
R2が、水素原子、ハロゲン原子、1以上のハロゲン原子を有していてもよいC1−C4アルキル基、1以上のハロゲン原子を有していてもよいC1−C4アルコキシ基またはシアノ基であり;
R3が、水素原子、ハロゲン原子、1以上のハロゲン原子を有していてもよいC1−C4アルキル基であり;
R4、R5、R7、R8、R9およびR11が、水素原子であり;
R6が、1以上のハロゲン原子を有していてもよいC1−C4アルキル基、ハロゲン原子、1以上のハロゲン原子を有していてもよいC1−C4アルコキシ基または1以上のハロゲン原子を有していてもよいC3−C5シクロアルキル基であり;
R10が、メチル基であり;
Xが、酸素原子であり;
R12が下記群P3から選ばれる1以上の原子もしくは基を有していてもよいフェニル基または下記群P3から選ばれる1以上の原子もしくは基を有していてもよいフェノキシ基である〔1〕または〔2〕に記載のテトラゾリノン化合物。
群P3:1以上のハロゲン原子を有していてもよいC1−C3アルキル基、ハロゲン原子、シアノ基および1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基からなる群。
ハロゲン原子としては、フッ素原子、塩素原子、臭素原子およびヨウ素原子があげられる。
1以上のハロゲン原子を有していてもよいC1−C6アルキル基とは、直鎖状もしくは分枝状の炭素原子数1−6のアルキル基の、1以上の水素原子がハロゲン原子で置換されていてもよい基を表し、例えばメチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、ヘキシル基、フルオロメチル基、クロロメチル基、ジクロロメチル基、ジフルオロメチル基、トリフルオロメチル基、トリクロロメチル基、トリブロモメチル基、2,2,2−トリフルオロエチル基、2,2,2−トリクロロエチル基、ペンタフルオロエチル基、クロロフルオロメチル基、ジクロロフルオロメチル基、クロロジフルオロメチル基および2,2−ジフルオロエチル基があげられる。
1以上のハロゲン原子を有していてもよいC1−C4アルキル基とは、直鎖状もしくは分枝状の炭素原子数1−4のアルキル基の、1以上の水素原子がハロゲン原子で置換されていてもよい基を表し、例えばメチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、モノフルオロメチル基、モノクロロメチル基、ジクロロメチル基、ジフルオロメチル基、トリフルオロメチル基、トリクロロメチル基、トリブロモメチル基、2,2,2−トリフルオロエチル基、2,2,2−トリクロロエチル基、ペンタフルオロエチル基、クロロフルオロメチル基、ジクロロフルオロメチル基、クロロジフルオロメチル基および、2,2−ジフルオロエチル基があげられる。
群P1から選ばれる1以上の原子もしくは基を有していてもよいC1−C6アルキル基としては、例えばメチル基、エチル基、プロピル基、イソプロピル基、ブチル基、イソブチル基、sec−ブチル基、tert−ブチル基、ペンチル基、ヘキシル基、2,2,2,−トリフルオロエチル基、2,2,2,−トリクロロエチル基、3,3,3,−トリフルオロプロピル基、2,2−ジフルオロエチル基、1,1−ジフルオロエチル基、ペンタフルオロエチル基、ヘプタフルオロイソプロピル基、1,1,2,2−テトラフルオロエチル基、2,2,3,3,3−ペンタフルオロプロピル基、2,2,3,3,3−ペンタフルオロブチル基、2−(シクロプロピル)エチル基、3−(シクロプロピル)プロピル基、4−(シクロプロピル)ブチル基、2−(シクロブチル)エチル基、3−シクロプロピル−2,2−ジフルオロプロピル基2−メトキシエチル基、2−エトキシエチル基、2−tert−ブトキシエチル基、3−メトキシプロピル基、3−エトキシプロピル基2−(トリフルオロメトキシ)エチル基、2−メチルチオエチル基、3−メチルチオプロピル基、2−エチルチオエチル基、3−エチルチオプロピル基、2−(tert−ブチルチオ)−エチル基、3−(tert−ブチルチオ)−プロピル基、2−(トリフルオロメチルチオ)エチル基、2−シアノエチル基、3−シアノプロピル基、1−シアノエチル基、2−シアノ−2−メチルエチル基、2−シアノ−2−メチルプロピル基が挙げられる。
群P1から選ばれる1以上の原子もしくは基を有していてもよいC3−C6シクロアルキル基としては、例えば、シクロプロピル基、1−フルオロシクロプロピル基、2,2−ジフルオロシクロプロピル基、1−クロロ−2−フルオロシクロプロピル基、2,2−ジクロロシクロプロピル基、2,2−ジブロモシクロプロピル基、2,2,3,3−テトラフルオロシクロブチル基、2−クロロシクロペンチル基、3−クロロシクロペンチル基、3,3−ジフルオロシクロペンチル基、1−フルオロシクロヘキシル基、2,2−ジフルオロシクロヘキシル基、3,3−ジフルオロシクロヘキシル基、4,4−ジフルオロシクロヘキシル基、1−シクロプロピルシクロプロピル基、2−シクロプロピルシクロプロピル基、1−メトキシシクロプロピル基、1−イソプロポキシシクロヘキシル基、1−(トリフルオロメトキシ)シクロプロピル基、1−エチルチオシクロプロピル基、2−メチルチオシクロプロピル基、1−(トリフルオロメチルチオ)シクロプロピル基、2−(トリフルオロメチルチオ)シクロプロピル基、1−シアノシクロプロピル基、2−シアノシクロプロピル基、および2,2−ジシアノシクロプロピル基が挙げられる。
1以上のハロゲン原子を有していてもよいC2−C3アルケニル基とは、直鎖状もしくは分枝状の炭素原子数1−3のアルケニル基の、1以上の水素原子がハロゲン原子で置換されていてもよい基を表し、例えばビニル基、1−プロペニル基、イソプロペニル基、2−プロペニル基、2−クロロビニル基、2−ブロモビニル基、2−ヨードビニル基、3−クロロ−2−プロペニル基、3−ブロモ−2−プロペニル基、1−クロロメチルビニル基、2−ブロモ−1−メチルビニル基、1−トリフルオロメチルビニル基、3,3,3−トリクロロ−1−プロペニル基、3−ブロモ−3,3−ジフルオロ−1−プロペニル基、2,3,3,3−テトラクロロ−1−プロペニル基、1−トリフルオロメチル−2,2−ジフルオロビニル基、2−クロロ−2−プロペニル基、3,3−ジフルオロ−2−プロペニル基および2,3,3−トリクロロ−2−プロペニル基があげられる。
1以上のハロゲン原子を有していてもよいC2−C3アルキニル基とは、直鎖状もしくは分枝状の炭素原子数1−3のアルキニル基の、1以上の水素原子がハロゲン原子で置換されていてもよい基を表し、例えばエチニル基、プロパルギル基、フルオロエチニル基、3−クロロ−2−プロピニル基、3−ブロモ−2−プロピニル基、3−ヨード−2−プロピニル基および3−クロロ−1−プロピニル基があげられる。
1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基とは、直鎖状もしくは分枝状の炭素原子数1−3のアルコキシ基の、1以上の水素原子がハロゲン原子で置換されていてもよい基を表し、例えばメトキシ基、エトキシ基、プロポキシ基、イソプロポキシ基、トリフルオロメトキシ基、トリクロロメトキシ基、クロロメトキシ基、ジクロロメトキシ基、フルオロメトキシ基、ジフルオロメトキシ基、クロロフルオロメトキシ基、ジクロロフルオロメトキシ基、クロロジフルオロメトキシ基、ペンタフルオロエトキシ基、ペンタクロロエトキシ基、2,2,2−トリフルオロエトキシ基、ヘプタフルオロプロポキシ基および3,3,3−トリフルオロプロポキシ基があげられる。
1以上のハロゲン原子を有していてもよいC3−C6シクロアルキルオキシ基とは、炭素原子数3−6のシクロアルキルオキシ基の、1以上の水素原子がハロゲン原子で置換されていてもよい基を表し、例えばシクロプロピルオキシ基、シクロブチルオキシ基、シクロペンチルオキシ基、シクロヘキシルオキシ基、2−フルオロシクロプロピルオキシ基、2,2−ジフルオロシクロプロピルオキシ基、2−クロロ−2−フルオロシクロプロピルオキシ基、2,2−ジクロロシクロプロピルオキシ基、2,2−ジブロモシクロプロピルオキシ基、2,2,3,3−テトラフルオロシクロブチルオキシ基、2−クロロシクロヘキシルオキシ基、4,4−ジフルオロシクロヘキシルオキシ基および4−クロロシクロヘキシルオキシ基があげられる。
1以上のハロゲン原子を有していてもよいC3−C6シクロアルキルチオ基とは、炭素原子数3−6のシクロアルキルチオ基の、1以上の水素原子がハロゲン原子で置換されていてもよい基を表し、例えばシクロプロピルチオ基、2,2−ジフルオロシクロプロピルチオ基、シクロブチルチオ基、シクロペンチルチオ基およびシクロヘキシルチオ基があげられる。
1以上のハロゲン原子を有していてもよいC3−C6アルキニルオキシ基とは、直鎖状もしくは分枝状の炭素原子数3−6のアルキニルオキシ基の、1以上の水素原子がハロゲン原子で置換されていてもよい基を表し、例えばプロパルギルオキシ基、1−ブチン−3−イルオキシ基、3−メチル−1−ブチン−3−イルオキシ基、2−ブチニルオキシ基、3−ブチニルオキシ基、2−ペンチニルオキシ基、3−ペンチニルオキシ基、4−ペンチニルオキシ基、5−ヘキシニルオキシ基、3−クロロ−2−プロピニルオキシ基、3−ブロモ−2−プロピニルオキシ基、3−ヨード−2−プロピニルオキシ基、5−クロロ−4−ペンチニルオキシ基、3−フルオロ−2−プロピニルオキシ基、ペルフルオロ−2−ブチニルオキシ基、ペルフルオロ−3−ブチニルオキシ基、ペルフルオロ−2−ペンチニルオキシ基、ペルフルオロ−3−ペンチニルオキシ基、ペルフルオロ−4−ペンチニルオキシ基およびペルフルオロ−5−ヘキシニルオキシ基があげられる。
1以上のハロゲン原子を有していてもよいC3−C6アルキニルチオ基とは、直鎖状もしくは分枝状の炭素原子数3−6のアルキニルチオ基の、1以上の水素原子がハロゲン原子で置換されていてもよい基を表し、例えばプロパルギルチオ基、1−ブチン−3−イルチオ基、3−メチル−1−ブチン−3−イルチオ基、2−ブチニルチオ基、3−ブチニルチオ基、2−ペンチニルチオ基、3−ペンチニルチオ基、4−ペンチニルチオ基、5−ヘキシニルチオ基、3−クロロ−2−プロピニルチオ基、3−ブロモ−2−プロピニルチオ基、3−ヨード−2−プロピニルチオ基、5−クロロ−4−ペンチニルチオ基、3−フルオロ−2−プロピニルチオ基、ペルフルオロ−2−ブチニルチオ基、ペルフルオロ−3−ブチニルチオ基、ペルフルオロ−2−ペンチニルチオ基、ペルフルオロ−3−ペンチニルチオ基、ペルフルオロ−4−ペンチニルチオ基およびペルフルオロ−5−ヘキシニルチオ基があげられる。
1以上のC1−C6アルキル基を有していてもよいアミノカルボニル基とは、窒素上の1および/または2の水素原子が、同一または相異なるC1−C6アルキル基で置換されていてもよいアミノカルボニル基を表し、例えば、アミノカルボニル基、メチルアミノカルボニル基、エチルアミノカルボニル基、プロピルアミノカルボニル基、イソプロピルアミノカルボニル基、ブチルアミノカルボニル基、ジメチルアミノカルボニル基、ジエチルアミノカルボニル基、ジプロピルアミノカルボニル基、ジイソプロピルアミノカルボニル基、ペンチルアミノカルボニル基およびヘキシルアミノカルボニル基があげられ、
群P3:1以上のハロゲン原子を有していてもよいC1−C3アルキル基、ハロゲン原子、シアノ基、1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基、1以上のハロゲン原子を有していてもよいC3−C4シクロアルキル基および1以上のハロゲン原子を有していてもよいC1−C3アルキルチオ基からなる群。
群P4:メチル基、エチル基、フッ素原子、塩素原子、シアノ基、メトキシ基、エトキシ基、トリフルオロメチル基、シクロプロピル基およびメチルチオ基からなる群。
群P4から選ばれる1以上の原子もしくは基を有していてもよいフェニル基としては、例えばフェニル基、2−フルオロフェニル基、3−フルオロフェニル基、4−フルオロフェニル基、2−クロロフェニル基、3−クロロフェニル基、4−クロロフェニル基、4−メチルフェニル基、4−トリフルオロメチルフェニル基、4−メトキシフェニル基、4−メチルチオフェニル基、2−シアノフェニル基、3−シアノフェニル基、4−シアノフェニル基、2,4−ジフルオロフェニル基、2,5−ジフルオロフェニル基、2,6−ジフルオロフェニル基、3,5−ジフルオロフェニル基、2,4−ジクロロフェニル基、2,5−ジクロロフェニル基、2,6−ジクロロフェニル基、3,5−ジクロロフェニル基、2,4,6−トリフルオロフェニル基、ペンタフルオロフェニル基、2−クロロ−4−フルオロフェニル基、3,4,5−トリフルオロフェニル基、2,3−ジメチルフェニル基、2,4−ジメチルフェニル基、2,5−ジメチルフェニル基、2,6−ジメチルフェニル基、3,4−ジメチルフェニル基、3,5−ジメチルフェニル基および2−フルオロ−4−メチルフェニル基があげられる。
群P2から選ばれる1以上の原子もしくは基を有していてもよいC7−C18アラルキルオキシ基としては、例えばベンジルオキシ基、2−フェニルエチルオキシ基、3−フェニルプロピルオキシ基、12−フェニルドデシルオキシ基、ナフチルメチルオキシ基、ナフチルエチルオキシ基、4−フルオロベンジルオキシ基、2−クロロベンジルオキシ基、3−ブロモベンジルオキシ基、4−ヨードベンジルオキシ基、2−メチルベンジルオキシ基、3−メチルベンジルオキシ基、4−メチルベンジルオキシ基、2−メトキシベンジルオキシ基、3−メトキシベンジルオキシ基、4−メトキシベンジルオキシ基、2−シアノベンジルオキシ基、3−シアノベンジルオキシ基、4−シアノベンジルオキシ基、2,4−ジフルオロベンジルオキシ基、2,5−ジクロロベンジルオキシ基、3,4,5−トリフルオロベンジルオキシ基、4−ブロモ−2−フルオロベンジルオキシ基、2−クロロ−3−フルオロベンジルオキシ基、2−(3−クロロフェニル)エチルオキシ基、2−(2−ブロモフェニル)エチルオキシ基、3−(4−ヨードフェニル)プロピルオキシ基、12−(4−ブロモフェニル)ドデシルオキシ基、4−フルオロ−1−ナフチルメチルオキシ基、1−クロロ−2−ナフチルメチルオキシ基およびジフルオロ(フェニル)メチルオキシ基があげられる。
C1−C4アルキル基を有していてもよいアニリノ基とは、フェニル上の水素原子および/または窒素上の水素原子がアルキル基で置換されていてもよいアニリノ基を表す。
C1−C4アルキル基を有していてもよいアニリノ基としては、例えばアニリノ基、N−メチル−アニリノ基、N−エチル−アニリノ基およびN−メチル−4−メチルアニリノ基があげられる。
群P2から選ばれる1以上の原子もしくは基を有していてもよいC2−C9ヘテロアリールオキシ基(但し、ヘテロアリール部分は5員環、6員環、5員環と5員環の縮合環、5員環と6員環の縮合環または6員環と6員環の縮合環)とは、C2−C9ヘテロアリールオキシ基の水素原子が群P2から選ばれる1以上の原子または基で置換されていてもよいヘテロアリールオキシ基を表し、群P2から選ばれる原子または基が2以上である場合、それらの原子および基は同一でも相異なっていてもよい。群P2から選ばれる1以上の原子もしくは基を有していてもよいC2−C9ヘテロアリールオキシ基としては、例えば2−ピリジルオキシ基、3−ピリジルオキシ基、4−ピリジルオキシ基、2−ピリミジルオキシ基、3−メチル−2−ピリジルオキシ基、4−メチル−2−ピリジルオキシ基、5−メチル−2−ピリジルオキシ基、6−メチル−2−ピリジルオキシ基、6−シアノ−2−ピリジルオキシ基、3−ピリダジルオキシ基、2−ピラジルオキシ基、2−チアゾリルオキシ基、2−オキサゾリルオキシ基、2−ベンズチアゾリルオキシ基、2−ベンズオキサゾリルオキシ基、2−キノリルオキシ基、2−ピラゾリルオキシ基、3−フリルオキシ基および3−チエニルオキシ基があげられる。
1以上のハロゲン原子を有していてもよいC1−C3アルキル基とは、C1−C3アルキル基の、1以上の水素原子がハロゲン原子で置換されていてもよい基を表し、例えばメチル基、エチル基、プロピル基、イソプロピル基、クロロメチル基、ジクロロメチル基、フルオロメチル基、ジフルオロメチル基、クロロフルオロメチル基、ジクロロフルオロメチル基、クロロジフルオロメチル基、トリフルオロメチル基、トリクロロメチル基、トリブロモメチル基、2−フルオロエチル基、2,2−ジフルオロエチル基、2,2,2−トリフルオロエチル基、2−クロロエチル基、2,2−ジクロロエチル基、2,2,2−トリクロロエチル基、ペンタフルオロエチル基、ペンタクロロエチル基、2−クロロ−2−フルオロエチル基、2−クロロ−2,2−ジフルオロエチル基、2−フルオロプロピル基、3−フルオロプロピル基、2,2−ジフルオロプロピル基、2,3−ジフルオロプロピル基、3,3,3−トリフルオロプロピル基、ヘプタフルオロプロピル基および1−(フルオロメチル)−2−フルオロエチル基があげられる。
C1−C6アルキル基を有していてもよいアミノカルボニル基とは、窒素上の1および/または2の水素原子が、同一もしくは相異なるC1−C8アルキル基で置換されたアミノカルボニル基を表し、例えば、アミノカルボニル基、N−メチルアミノカルボニル基、N−エチルアミノカルボニル基、N−プロピルアミノカルボニル基、N−イソプロピルアミノカルボニル基、N−ブチルアミノカルボニル基、N,N−ジメチルアミノカルボニル基、N,N−ジエチルアミノカルボニル基、N,N−ジプロピルアミノカルボニル基、N−エチル−N−メチルアミノカルボニル基およびN−プロピル−N−メチルアミノカルボニル基があげられる。
C2−C5アルキルチオアルキル基とは、アルキルチオ部分とアルキル部分との炭素原子数の合計が2~5であり、直鎖状もしくは分枝状のいずれであってもよく、例えばメチルチオメチル基、エチルチオメチル基、プロピルチオメチル基、イソプロピルチオメチル基、ブチルチオメチル基、イソブチルチオメチル基、sec−ブチルチオメチル基、1−メチルチオエチル基、2−メチルチオエチル基、2−プロピルチオエチル基、2−イソプロピルチオエチル基、3−メチルチオプロピル基、3−エチルチオプロピル基、3−メチルチオブチル基および4−メチルチオブチル基があげられる。
C2−C6アルキルカルボニルオキシ基とは、直鎖状もしくは分枝状の炭素原子数1−5のアルキル基を有するアルキルカルボニル基を表し、例えば、メチルカルボニルオキシ基、エチルカルボニルオキシ基、プロピルカルボニルオキシ基、イソプロピルカルボニルオキシ基、ピバロイルオキシ基、ブチルカルボニルオキシ基、およびペンチルカルボニルオキシ基があげられる。
C2−C4アルキルカルボニルアミノ基におけるアルキル部分とカルボニルとの合計の炭素原子数は2~4である。C2−C4アルキルカルボニルアミノ基としては、例えば、アセチルアミノ基、プロピオニルアミノ基、ブチリルアミノ基およびイソブチリルアミノ基があげられる。
R12が群P3から選ばれる1以上の原子もしくは基を有していてもよいフェノキシ基である化合物;
R12が群P3から選ばれる1以上の原子もしくは基を有していてもよいC2−C9ヘテロアリールオキシ基(但し、ヘテロアリール部分は5員環、6員環、5員環と5員環の縮合環、5員環と6員環の縮合環または6員環と6員環の縮合環)である化合物;
R2が水素原子である化合物;
R3が水素原子である化合物;
R4が水素原子である化合物;
R5が水素原子である化合物;
R7が水素原子である化合物;
R8が水素原子である化合物;
R9が水素原子である化合物;
R10が水素原子である化合物;
R11が水素原子である化合物;
R1が1以上のハロゲン原子を有していてもよいC1−C3アルキル基である化合物;
R1がC3−C4シクロアルキル基である化合物;
R1がハロゲン原子である化合物;
R1がメチル基である化合物;
R1がエチル基である化合物;
R1がシクロプロピル基である化合物;
R1がトリフルオロメチル基である化合物;
R1がフッ素原子である化合物;
R1が塩素原子である化合物;
R1が臭素原子である化合物;
R6がC3−C4シクロアルキル基である化合物;
R6がハロゲン原子である化合物;
R6がC2−C3アルケニル基である化合物;
R6がC2−C3アルキニル基である化合物;
R6が1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基である化合物;
R6が1以上のハロゲン原子を有していてもよいC1−C3アルキル基、ハロゲン原子、C3−C4シクロアルキル基、1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基、C2−C3アルケニル基またはC2−C3アルキニル基である化合物;
R6がメチル基である化合物;
R6がエチル基である化合物;
R6がプロピル基である化合物;
R6がシクロプロピル基である化合物;
R6がトリフルオロメチル基である化合物;
R6がジフルオロメチル基である化合物;
R6がビニル基である化合物;
R6が2−プロペニル基である化合物;
R6が塩素原子である化合物;
R6が臭素原子である化合物;
R6がヨウ素原子である化合物;
R6がフッ素原子である化合物;
R6がメトキシ基である化合物;
R6がエトキシ基である化合物;
R2が水素原子である化合物;
R2が水素原子、メチル基、メトキシ基またはシアノ基である化合物;
R10がメチル基である化合物;
Xが酸素原子である化合物;
Xが硫黄原子である化合物;
1以上のハロゲン原子を有していてもよいC1−C4アルキル基、ハロゲン原子、C1−C4アルコキシ基、C1−C4アルキルチオ基、シアノ基、C1−C4アルキルカルボニル基、C1−C4アルキルスルホニル基およびC2−C4アルキルカルボニルアミノ基からなる群より選ばれる1以上の原子もしくは基を有していてもよいフェニル基、
C1−C4アルキル基、C1−C4アルコキシ基、ハロゲン原子およびシアノ基からなる群より選ばれる1以上の原子もしくは基を有していてもよいフェノキシ基、
1以上のC1−C4アルコキシ基および/もしくはヒドロキシ基を有していてもよいC7−C10アラルキル基、
C7−C10アラルキルオキシ基、C7−C10アリールオキシアルキル基、C1−C4アルキル基を有していてもよいアニリノ基、C1−C3アルコキシ基および/もしくは1以上のハロゲン原子を有していてもよいC1−C6アルキル基またはC2−C9ヘテロアリールオキシ基(但し、ヘテロアリール部分は5員環、6員環、5員環と5員環の縮合環、5員環と6員環の縮合環または6員環と6員環の縮合環)であり、Xが酸素原子であるテトラゾリノン化合物
[群P4:メチル基、エチル基、フッ素原子、塩素原子、シアノ基、メトキシ基、エトキシ基、トリフルオロメチル基、シクロプロピル基およびメチルチオ基からなる群];
R1が1以上のハロゲン原子を有していてもよいC1−C6アルキル基、ハロゲン原子または水素原子であり、R2が、1以上のハロゲン原子を有していてもよいC1−C6アルキル基、ハロゲン原子、水素原子、シアノ基またはC1−C6アルコキシ基であり、R3が、水素原子、ハロゲン原子またはC1−C6アルキル基であり、R6がC1−C6アルキル基、C1−C6アルコキシ基、またはC3−C6シクロアルキル基であり、R12がフェニル基(但し、該フェニル基は、1以上のハロゲン原子を有していてもよいC1−C6アルキル基、ハロゲン原子、シアノ基、C1−C6アルコキシ基、C1−C6アルキルチオ基、C1−C6アルキルスルホニル基、C2−C6アルキルカルボニル基、およびC2−C6アルキルカルボニルアミノ基からなる群より選ばれる1以上の原子または基を有していてもよい。)であり、R4、R5、R7、R8、R9およびR11が水素原子であり、R10がC1−C3アルキル基であり、Xが酸素原子であるテトラゾリノン化合物;
[態様1]において、R6がC1−C6アルキル基であるテトラゾリノン化合物;
[態様1]において、R6がC1−C6アルコキシ基であるテトラゾリノン化合物;
[態様1]において、R6がC3−C6シクロアルキル基であるテトラゾリノン化合物。
R1がC1−C6アルキル基または水素原子であり、R6がC1−C6アルキル基C1−C6アルコキシ基、またはC3−C6シクロアルキル基であり、R12がフェノキシ基(但し、該フェノキシ基は、C1−C6アルキル基、ハロゲン原子、シアノ基、およびC1−C6アルコキシ基からなる群より選ばれる1以上の原子または基を有していてもよい。)であり、R2、R3、R4、R5、R7、R8、R9およびR11が水素原子であり、R10が1以上のハロゲン原子を有していてもよいC1−C3アルキル基であり;Xが酸素原子であるテトラゾリノン化合物;
[態様2]において、R6がC1−C6アルキル基であるテトラゾリノン化合物;
[態様2]において、R6がC1−C6アルコキシ基であるテトラゾリノン化合物;
[態様2]において、R6がC3−C6シクロアルキル基であるテトラゾリノン化合物。
R1が1以上のハロゲン原子を有していてもよいC1−C6アルキル基または水素原子であり、R6が1以上のハロゲン原子を有していてもよいC1−C6アルキル基または1以上のハロゲン原子を有していてもよいC1−C6アルコキシ基であり、R12がC2−C6アルコキシカルボニル基であり、R2、R3、R4、R5、R7、R8、R9およびR11が水素原子であり、R10が1以上のハロゲン原子を有していてもよいC1−C3アルキル基であり;Xが酸素原子であるテトラゾリノン化合物;
[態様3]において、R6がC1−C6アルキル基であるテトラゾリノン化合物;
[態様3]において、R6がC1−C6アルコキシ基であるテトラゾリノン化合物。
R1が1以上のハロゲン原子を有していてもよいC1−C6アルキル基または水素原子であり、R6が1以上のハロゲン原子を有していてもよいC1−C6アルキル基または1以上のハロゲン原子を有していてもよいC1−C6アルコキシ基であり、R12がヒドロキシ基および1以上のハロゲン原子を有していてもよいC1−C6アルコキシ基から選ばれる1以上の原子もしくは基を有していてもよいC7−C18アラルキル基であり、R2、R3、R4、R5、R7、R8、R9およびR11が水素原子であり、R10が1以上のハロゲン原子を有していてもよいC1−C3アルキル基であり、Xが酸素原子であるテトラゾリノン化合物;
[態様4]において、R6がC1−C6アルキル基であるテトラゾリノン化合物;
[態様4]において、R6がC1−C6アルコキシ基であるテトラゾリノン化合物。
R1が1以上のハロゲン原子を有していてもよいC1−C6アルキル基または水素原子であり、R6が1以上のハロゲン原子を有していてもよいC1−C6アルキル基または1以上のハロゲン原子を有していてもよいC1−C6アルコキシ基であり、R12が1以上のハロゲン原子を有していてもよいC2−C6アルケニル基であり、R2、R3、R4、R5、R7、R8、R9およびR11が水素原子であり、R10が1以上のハロゲン原子を有していてもよいC1−C3アルキル基であり、Xが酸素原子であるテトラゾリノン化合物;
[態様5]において、R6がC1−C6アルキル基であるテトラゾリノン化合物;
[態様5]において、R6がC1−C6アルコキシ基であるテトラゾリノン化合物。
本発明化合物は、例えば以下の製造法により製造することができる。
(製造法A)
(以下、化合物(1)と記す。)は、式(A1)で示される化合物(以下、化合物(A1)と記す。)と式(A2)で示される化合物(以下、化合物(A2)と記す。)とを塩基の存在下で反応させることにより製造することができる。
〔式中、R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11、R12およびXは前記と同じ意味を表し、Z11は塩素原子、臭素原子、ヨウ素原子、メタンスルホニルオキシ基、トリフルオロメタンスルホニルオキシ基またはp−トルエンスルホニルオキシ基等の脱離基を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、酢酸エチル、酢酸メチル等のエステル類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類、水およびこれらの混合物が挙げられる。
該反応に用いられる塩基としては、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、水酸化セシウム等のアルカリ金属水酸化物、フッ化ナトリウム、フッ化カリウム、フッ化セシウム等のアルカリ金属ハロゲン化物、水素化リチウム、水素化ナトリウム、水素化カリウム等のアルカリ金属水素化物、ナトリウムtert−ブトキシド、カリウムtert−ブトキシド等のアルカリ金属アルコキシドが挙げられる。
該反応には化合物(A1)1モルに対して、化合物(A2)が通常1~10モルの割合、塩基が通常0.5~5モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
該反応は、必要に応じてヨウ化ナトリウム、ヨウ化テトラブチルアンモニウムなどを加えてもよく、これらの化合物は通常、化合物(A1)1モルに対して、0.001~1.2モルの割合で用いられる。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(1)を単離することができる。単離された本発明化合物は、クロマトグラフィー、再結晶等によりさらに精製することもできる。
化合物(1)のうち、R12がA1である化合物(以下化合物(1−1)と記す。)は、式(B1)で示される化合物(以下、化合物(B1)と記す。)と式(B2)で示される化合物(以下、化合物(B2)と記す。)とを、塩基及び触媒存在下でカップリング反応に供することにより製造することができる。
〔式中、R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11およびXは前記と同じ意味を表し、A1は群P2から選ばれる1以上の原子もしくは基を有していてもよいC6−C16アリール基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルケニル基または群P2から選ばれる1以上の原子もしくは基を有していてもよいC7−C18アラルキル基を表し、Z21は塩素原子、臭素原子またはヨウ素原子を表し、Z31はB(OH)2、アルコキシボラニル基またはトリフルオロボレート塩BF3 −K+を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、酢酸エチル、酢酸メチル等のエステル類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類、メタノール、エタノール、プロパノール、ブタノール等のアルコール類、水およびこれらの混合物が挙げられる。
該反応に用いられる化合物(B2)は、通常市販のものを用いるか、N. Miyaura and A. Suzuki, Chem. Rev.,1995,95,2457等に記載された公知の方法により製造したものを用いることもできる。該反応に用いられる化合物(B2)は、例えば、ヨウ素化合物(A1 −I)またはブロモ化合物(A1 −Br)とブチルリチウムなどのアルキルリチウムとを反応させた後、ホウ酸エステルと反応させることによりボロン酸エステル誘導体を製造することができる。また、前述の反応で得られたボロン酸エステル誘導体を、必要に応じて加水分解することによりボロン酸誘導体を製造することができる。さらに、Molander et al.Acc.Chem.Res.,2007,40,275などに記載された公知の方法に従い、前記ボロン酸エステルをフッ化水素カリウム等でフッ素化することにより、トリフルオロボレート塩BF3 −K+を得ることもできる。
該反応に用いられる触媒としては、酢酸パラジウム(II)、ジクロロビス(トリフェニルホスフィン)パラジウム、テトラキストリフェニルホスフィンパラジウム(0)、パラジウム(II)アセテート/トリスシクロヘキシルホスフィン、ビス(ジフェニルホスファンフェロセニル)パラジウム(II)ジクロリド、1,3−ビス(2,6−ジイソプロピルフェニル)イミダゾール−2−イリデン(1,4−ナフトキノン)パラジウムダイマー、アリル(クロロ)(1,3−ジメシチル−1,3−ジヒドロ−2H−イミダゾール−2−イリデン)パラジウムまたはパラジウム(II)アセテート/ジシクロヘキシル(2’,4’,6’−トリイソプロピルビフェニル−2−イル)ホスフィン、トリス(ジベンジリデンアセトン)ジパラジウム等が挙げられる。
該反応に用いられる塩基としては、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、水酸化セシウム等のアルカリ金属水酸化物、フッ化ナトリウム、フッ化カリウム、フッ化セシウム等のアルカリ金属ハロゲン化物、水素化リチウム、水素化ナトリウム、水素化カリウム等のアルカリ金属水素化物、リン酸三カリウム等のアルカリ金属リン酸塩、ナトリウムメトキシド、ナトリウムエトキシド、ナトリウムtert−ブトキシド、カリウムtert−ブトキシド等のアルカリ金属アルコキシドが挙げられる。
該反応には化合物(B1)1モルに対して、化合物(B2)が通常1~10モルの割合、塩基が通常1~10モルの割合、触媒が通常0.0001~1モルの割合で用いられる。
該反応の反応温度は通常0~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(1−1)を単離することができる。単離された本発明化合物は、クロマトグラフィー、再結晶等によりさらに精製することもできる。
化合物(1)のうち、AがA1である化合物(以下化合物(1−2)と記す。)は、式(C1)で示される化合物(以下、化合物(C1)と記す。)と式(C2)で示される化合物(以下、化合物(C2)と記す。)とを、塩基及び触媒存在下でカップリング反応に供することにより製造することができる。
〔式中、R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11、A1、Z21、Z31およびXは前記と同じ意味を表す。〕
反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、酢酸エチル、酢酸メチル等のエステル類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類、水およびこれらの混合物が挙げられる。
該反応に用いられる化合物(C2)は、通常市販のものを用いることができる。具体的には、ブロモベンゼン、ヨードベンゼン、1−ブロモ−2−メチルベンゼン等を挙げることができる。
該反応に用いられる触媒としては、酢酸パラジウム(II)、ジクロロビス(トリフェニルホスフィン)パラジウム、テトラキストリフェニルホスフィンパラジウム(0)、パラジウム(II)アセテート/トリスシクロヘキシルホスフィン、ビス(ジフェニルホスファンフェロセニル)パラジウム(II)ジクロリド、1,3−ビス(2,6−ジイソプロピルフェニル)イミダゾール−2−イリデン(1,4−ナフトキノン)パラジウムダイマー、アリル(クロロ)(1,3−ジメシチル−1,3−ジヒドロ−2H−イミダゾール−2−イリデン)パラジウムまたはパラジウム(II)アセテート/ジシクロヘキシル(2’,4’,6’−トリイソプロピルビフェニル−2−イル)ホスフィン、トリス(ジベンジリデンアセトン)ジパラジウム等が挙げられる。
該反応に用いられる塩基としては、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、水酸化セシウム等のアルカリ金属水酸化物、フッ化ナトリウム、フッ化カリウム、フッ化セシウム等のアルカリ金属ハロゲン化物、水素化リチウム、水素化ナトリウム、水素化カリウム等のアルカリ金属水素化物、リン酸三カリウム等のアルカリ金属リン酸塩、ナトリウムメトキシド、ナトリウムエトキシド、ナトリウムtert−ブトキシド、カリウムtert−ブトキシド等のアルカリ金属アルコキシドが挙げられる。
該反応には化合物(B1)1モルに対して、化合物(B2)が通常1~10モルの割合、塩基が通常1~10モルの割合、触媒が通常0.0001~1モルの割合で用いられる。
該反応の反応温度は通常0~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(1−2)を単離することができる。単離された本発明化合物は、クロマトグラフィー、再結晶等によりさらに精製することもできる。
化合物(1)は、式(1−3)で示される化合物(以下、化合物(1−3)と記す。)と式(E1)で示される化合物(以下、化合物(E1)と記す。)とを、塩基の存在下で反応させることにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、酢酸エチル、酢酸メチル等のエステル類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類、水およびこれらの混合物が挙げられる。
該反応に用いられる化合物(E1)は、通常市販のものを用いることができる。具体的には、臭化メチル、臭化エチル、臭化n−プロピル、ヨウ化メチル、ヨウ化エチル、ヨウ化n−プロピル、ヨウ化イソプロピル等のハロゲン化アルキル類、p−トルエンスルホン酸メチル、p−トルエンスルホン酸エチル、p−トルエンスルホン酸n−プロピル、メタンスルホン酸メチル、メタンスルホン酸エチル、メタンスルホン酸n−プロピル等のスルホン酸エステル類、および硫酸ジメチル、硫酸ジエチル、硫酸ジn−プロピル等の硫酸エステル類が挙げられる。
該反応に用いられる塩基としては、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、水酸化セシウム等のアルカリ金属水酸化物、フッ化ナトリウム、フッ化カリウム、フッ化セシウム等のアルカリ金属ハロゲン化物、水素化リチウム、水素化ナトリウム、水素化カリウム等のアルカリ金属水素化物、水素化リチウム、水素化ナトリウム、水素化カリウム等のアルカリ金属水素化物、ナトリウムtert−ブトキシド、カリウムtert−ブトキシド等のアルカリ金属アルコキシドが挙げられる。
該反応には化合物(1−3)1モルに対して、化合物(E1)が通常1~10モルの割合、塩基が通常1~10モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(1)を単離することができる。単離された本発明化合物は、クロマトグラフィー、再結晶等によりさらに精製することもできる。
化合物(1)のうちXが硫黄原子である化合物(以下、化合物(1−S)と記す。)は、化合物(1)のうちXが酸素原子である化合物(以下、化合物(1−O)と記す。)から、公知の硫化反応により製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、アセトニトリル等のニトリル類およびこれらの混合物が挙げられる。
該反応に用いられる硫化剤としては五硫化リン、ローソン試薬(2,4−Bis(4−methoxyphenyl)−1,3,2,4−dithiadiphosphetane 2,4−disulfide)が挙げられる。
該反応には、硫化剤が、化合物(1−O)1モルに対して好ましくは0.5~1.5モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
該反応は、必要に応じてピリジンやトリエチルアミンなどの有機塩基、アルカリ金属水酸化物やアルカリ金属炭酸塩などの無機塩基などを加えてもよく、添加する塩基の使用量は化合物(1−O)に対して0.5~1.5モルである。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(1−S)を単離することができる。単離された本発明化合物は、クロマトグラフィー、再結晶等によりさらに精製することもできる。
化合物(1)のうち、R6がR71である式(1−4)で示される化合物(以下、化合物(1−4)と記す。)は、式(G1)で示される化合物(以下、化合物(G1)と記す。)と式(G21)で示される化合物(以下、化合物(G21)と記す。)とを、塩基及び触媒存在下でカップリング反応に供することにより製造することができる。
〔式中、R1、R2、R3、R4、R5、R7、R8、R9、R10、R11、R12およびZ31は前記と同じ意味を表し、Z41は塩素原子、臭素原子、ヨウ素原子またはトリフルオロメタンスルホニルオキシ基を表し、R71は1以上のハロゲン原子を有していてもよいC1−C6アルキル基、1以上のハロゲン原子を有していてもよいC2−C6アルケニル基、1以上のハロゲン原子を有していてもよいC2−C6アルキニル基または1以上のハロゲン原子を有していてもよいC3−C6シクロアルキル基を表す。〕
該反応は、製造法Bに記載の反応に準じて実施することができる。
〔式中、R1、R2、R3、R4、R5、R6、R8、R9、R10、R11、R12、Z31およびZ41は前記と同じ意味を表し、R72は1以上のハロゲン原子を有していてもよいC1−C4アルキル基または1以上のハロゲン原子を有していてもよいC3−C5シクロアルキル基を表す。〕
該反応は、製造法Bに記載の反応に準じて実施することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、製造法Bに記載の反応に準じて実施することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、製造法Bに記載の反応に準じて実施することができる。
化合物(1)のうち、R1がR73である式(1−8)で示される化合物(以下、化合物(1−8)と記す。)は、式(H1)で示される化合物(以下、化合物(H1)と記す。)と式(H21)で示される化合物(以下、化合物(H21)と記す。)とを、塩基及び触媒存在下でカップリング反応に供することにより製造することができる。
〔式中、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11、R12、Z31およびZ41は前記と同じ意味を表し、R73は群P1から選ばれる1以上の原子もしくは基を有していてもよいC1−C6アルキル基;群P1から選ばれる1以上の原子もしくは基C3−C6シクロアルキル基;1以上のハロゲン原子を有していてもよいC2−C6アルケニル基;または1以上のハロゲン原子を有していてもよいC2−C6アルキニル基を表す。〕
該反応は、製造法Bに記載の反応に準じて実施することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、製造法Bに記載の反応に準じて実施することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、製造法Bに記載の反応に準じて実施することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、製造法Bに記載の反応に準じて実施することができる。
化合物(1)のうち、R12が−O−A2である化合物(以下化合物(1−12)と記す。)は、式(I1)で示される化合物(以下、化合物(I1)と記す。)と式(I2)で示される化合物(以下、化合物(I2)と記す。)とを、塩基、触媒及び配位子存在下でカップリング反応に供することにより製造することができる。
〔式中、R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11、Z21およびXは前記と同じ意味を表し、A2は群P2から選ばれる1以上の原子もしくは基を有していてもよいC6−C16アリール基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC7−C18アラルキル基または群P2から選ばれる1以上の原子もしくは基を有していてもよいヘテロアリール基を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、酢酸エチル、酢酸メチル等のエステル類、ジメチルスルホキシド等のスルホキシド類、アセトニトリル等のニトリル類およびこれらの混合物が挙げられる。
該反応に用いられる触媒としては、ヨウ化銅(I)、臭化銅(I)、塩化銅(I)、酸化銅(I)酢酸銅(II)等が挙げられる。
該反応に用いられる配位子としては、エチレンジアミン、2−ピコリン酸、N−ブチルイミダゾール、ジピバロイルメタン等が挙げられる。
該反応に用いられる塩基としては、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、水酸化セシウム等のアルカリ金属水酸化物、フッ化ナトリウム、フッ化カリウム、フッ化セシウム等のアルカリ金属ハロゲン化物、水素化リチウム、水素化ナトリウム、水素化カリウム等のアルカリ金属水素化物、リン酸三カリウム等のアルカリ金属リン酸塩、ナトリウムメトキシド、ナトリウムエトキシド、ナトリウムtert−ブトキシド、カリウムtert−ブトキシドのアルカリ金属アルコキシド等が挙げられる。
該反応には化合物(B1)1モルに対して、化合物(B2)が通常1~10モルの割合、塩基が通常1~10モルの割合、触媒が通常0.0001~1モルの割合で用いられる。
該反応の反応温度は通常0~150℃の範囲である。該反応の反応時間は通常0.1~72時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(1−12)を単離することができる。単離された本発明化合物は、クロマトグラフィー、再結晶等によりさらに精製することもできる。
化合物(1)のうち、R12がA4である化合物(以下化合物(1−13)と記す。)は、式(J1)で示される化合物(以下、化合物(J1)と記す。)と式(J2)で示される化合物(以下、化合物(J2)と記す。)とを、塩基、触媒及び配位子存在下でカップリング反応に供することにより製造することができる。
〔式中、R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11、Z21およびXは前記と同じ意味を表し、A4は群P2から選ばれる1以上の原子もしくは基を有していてもよいC6−C16アリールオキシ基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC7−C18アラルキルオキシ基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC6−C16アリールチオ基または群P2から選ばれる1以上の原子もしくは基を有していてもよいC2−C9ヘテロアリールオキシ基(但し、ヘテロアリール部分は5員環、6員環、5員環と5員環の縮合環、5員環と6員環の縮合環または6員環と6員環の縮合環)を表す。〕
該反応は、製造法Hに記載の反応に準じて実施することができる。
式(XA3)で示される化合物(以下、化合物(XA3)と記す。)は、式(XA1)で示される化合物(以下、化合物(XA1)と記す。)または式(XA2)で示される化合物(以下、化合物(XA2)と記す。)とアジド化剤とを反応させることにより製造することができる。
〔式中、R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11、R12およびXは前記と同じ意味を表し、R101はP11、P12またはP13を表し、R91はC1−C12アルキル基を表し、Z101は塩素原子または臭素原子を表し、波線は結合部位を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、酢酸エチル、酢酸メチル等のエステル類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類およびこれらの混合物が挙げられる。
該反応に用いられるアジド化剤としては例えばアジ化ナトリウム、アジ化バリウムまたはアジ化リチウム等の無機アジド類、アジ化トリメチルシリル、アジ化ジフェニルホスホリル等の有機アジド類が挙げられる。
該反応には化合物(XA1)または化合物(XA2)1モルに対して、アジド化剤が通常1~10モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
該反応は、必要に応じて、塩化アルミニウムもしくは塩化亜鉛等のルイス酸を加えてもよく、これらの化合物は通常、化合物(XA1)または化合物(XA2)1モルに対して、0.05~5モルの割合で用いられる。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XA3)を単離することができる。単離された化合物(XA3)は、クロマトグラフィー、再結晶等によりさらに精製することもできる。
化合物(XA1)は、式(XB1)で示される化合物(以下、化合物(XB1)と記す。)とイソシアナート化剤とを反応させることにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、酢酸エチル、酢酸メチル等のエステル類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類およびこれらの混合物が挙げられる。
該反応に用いられるイソシアナート化剤としては、例えば、ホスゲン、ジホスゲン、トリホスゲン、チオホスゲン、N,N−カルボジイミダゾールおよびN,N−チオカルボジイミダゾール等が挙げられる。
該反応には化合物(XB1)1モルに対して、イソシアナート化剤が通常0.34~10モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
該反応は、必要に応じて、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩等を加えてもよく、これらの化合物は通常、化合物(XB1)1モルに対して、0.05~5モルの割合で用いられる。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XA1)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
化合物(XA2)は、式(XC1)で示される化合物(以下、化合物(XC1)と記す。)とハロゲン化剤とを反応させることにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、酢酸エチル、酢酸メチル等のエステル類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類およびこれらの混合物が挙げられる。
該反応に用いられるハロゲン化剤としては、例えば、オキシ塩化リン、三塩化リン、五塩化リン、塩化チオニル、オキシ臭化リン、三臭化リン、五臭化リン、三ヨウ化リン、二塩化オキサリル、二臭化オキサリル、トリホスゲン、ジホスゲン、ホスゲンおよび塩化スルフリル等が挙げられる。
該反応には化合物(XC1)1モルに対して、ハロゲン化剤が通常1~10モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
該反応は触媒を加えてもよく、N,N−ジメチルホルムアミド等が用いられる。触媒の使用量は、通常、化合物(XC1)1モルに対して、0.001~1モルの割合で用いられる。
該反応は、必要に応じて、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩等を加えてもよく、これらの化合物は通常、化合物(XC1)1モルに対して、0.05~5モルの割合で用いられる。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XA2)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
化合物(XA1)は、化合物(XB1)とカーバメート化剤とを反応させ、式(XD1)で示される化合物(以下、化合物(XD1)と記す。)を得たのち、化合物(XD1)とイソシアナート化剤とを反応させることにより製造することができる。
〔式中、R6、R7、R8、R9、R101およびXは前記と同じ意味を表し、R111はC1−C12アルキル基またはフェニル基を表す。〕
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、酢酸エチル、酢酸メチル等のエステル類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類、水およびこれらの混合物が挙げられる。
該反応に用いられるカーバメート化剤としては、クロロ炭酸フェニル、クロロ炭酸メチル、クロロ炭酸エチル、クロロ炭酸n−プロピル、クロロ炭酸イソプロピル、クロロ炭酸n−ブチル、クロロ炭酸tert−ブチル、二炭酸ジ−tert−ブチル、二炭酸ジメチル、二炭酸ジエチル、クロロチオぎ酸O−フェニル、クロロチオぎ酸O−メチル、クロロチオぎ酸O−エチル等が挙げられる。
該反応には化合物(XB1)1モルに対して、カーバメート化剤が通常1~10モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
該反応は、必要に応じて、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩等を加えてもよく、これらの化合物は通常、化合物(XB1)1モルに対して、0.05~5モルの割合で用いられる。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XD1)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
該反応に用いられる溶媒としては、例えば、テトラヒドロフラン、ジオキサン、エチレングリコ−ルジメチルエ−テル、メチルtert−ブチルエーテル等のエ−テル類、トルエン、キシレン等の芳香族炭化水素類、四塩化炭素、クロロホルムまたは1,2−ジクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、アセトニトリル等のニトリル類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類及びこれらの混合物が挙げられる。
該反応に用いられるイソシアナート化剤としては、例えば、五塩化リン、オキシ塩化リン、五酸化二リン、トリクロロシラン、ジクロロシラン、モノクロロシラン、三塩化ホウ素、2−クロロ−1,3,2−ベンゾジオキサボロール、二ヨウ化シラン、メチルトリクロロシラン、ジメチルジクロロシラン、クロロトリメチルシラン等を用いることができる。
該反応には化合物(XD1)1モルに対して、イソシアナート化剤が通常1~10モルの割合で用いられる。
該反応の反応温度は通常−20~250℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
該反応は、必要に応じて、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩等を加えてもよく、これらの化合物は通常、化合物(XD1)1モルに対して、0.05~5モルの割合で用いられる。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XA1)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
式(XE2)で示される化合物(以下、化合物(XE2)は、式(XE1)で示される化合物(以下、化合物(XE1)と記す。)と水素とを、触媒存在下で反応させることにより製造することができる。
〔式中、R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11およびR12は前記と同じ意味を表し、R181は水素原子またはP21を表し、波線は結合部位を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、メタノール、エタノール、プロパノール、ブタノール等のアルコール類、酢酸エチル、酢酸ブチル等のエステル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、水およびこれらの混合物が挙げられる。
該反応に用いられる触媒として、パラジウム炭素(Pd/C)、白金炭素(Pt/C)、オスミウム炭素(Os/C)、ルテニウム炭素(Ru/C)、ロジウム炭素(Rh/C)、ラネーニッケル等をあげることができる。
該反応には化合物(XE1)1モルに対して、触媒が通常0.0001~1モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、触媒を濾過後、有機層を濃縮する等の後処理操作を行うことにより、化合物(XE2)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
化合物(XE2)は、酸の存在下で化合物(XE1)と還元剤とを反応することにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、溶媒としては、酢酸等の脂肪族カルボン酸類、メタノール、エタノール等のアルコール類、水およびそれらの混合物が挙げられる。
該反応に用いられる還元剤としては、例えば、鉄、スズ、亜鉛が挙げられる。
該反応に用いられる酸としては、例えば、塩酸、硫酸、酢酸、塩化アンモニウム水溶液等が挙げられる。
該反応には化合物(XE1)1モルに対して、還元剤が通常1~30モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XE2)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
式(XG2)で示される化合物(以下、化合物(XG2)と記す。)は、式(XG1)で示される化合物(以下、化合物(XG1)と記す。)と化合物(E1)とを塩基の存在下で反応させることにより製造することができる。
〔式中、R6、R7、R8、R9、R10およびZ11は前記と同じ意味を表し、R191はP11またはP12を表す。〕
該反応は、製造法Dに記載の反応に準じて実施することができる。
式(XH2)で示される化合物(以下、化合物(XH2)と記す。)は、式(XH1)で示される化合物(以下、化合物(XH1)と記す。)とハロゲン化剤とを反応させることにより製造することができる。
〔式中、R4、R5、R6、R7、R8、R9、R10、Z21およびXは前記と同じ意味を表し、R201はP51またはニトロ基を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、クロロホルム、1,2−ジクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、酢酸エチル、酢酸メチル等のエステル類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類およびこれらの混合物が挙げられる。
該反応に用いることができるハロゲン化剤としては、塩素化、臭素化もしくはヨウ素化剤、例えば塩素、臭素、ヨウ素、塩化スルフリル、N−クロロスクシンイミド、N−ブロモスクシンイミド、1,3−ジブロモ−5,5−ジメチルヒダントイン、ヨードスクシンイミド、次亜塩素酸tert−ブチル、N−クロログルタルイミド、N−ブロモグルタルイミド、N−クロロ−N−シクロヘキシル−ベンゼンスルホンイミド、およびN−ブロモフタルイミド等を挙げることができる。
該反応にはラジカル開始剤を用いることも出来る。
該反応に用いられるラジカル開始剤としては、過酸化ベンゾイル、アゾビスイソブチロニトリル(AIBN)、ジアシルペルオキシド、ジアルキルペルオキシジカルボネート、tert−アルキルペルオキシエステル、モノペルオキシカルボネート、ジ(tert−アルキルペルオキシ)ケタールおよびケトンペルオキシド等を挙げることができる。
該反応には化合物(XH1)1モルに対して、ハロゲン化剤が通常1~10モルの割合、ラジカル開始剤は通常0.01~5モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XH2)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
式(XJ2)で示される化合物(以下、化合物(XJ2)と記す。)は、化合物(XH2)と式(XJ1)で示される化合物(以下、化合物(XJ1)と記す。)とを反応させることにより製造することができる。
〔式中、R4、R5、R6、R7、R8、R9、R111、およびZ21は前記と同じ意味を表し、Mはナトリウム、カリウム、またはリチウムを表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、ジエチルエーテル、テトラヒドロフラン、1,4−ジオキサン、エチレングリコ−ルジメチルエ−テル、アニソール、メチルtertert−ブチルエーテル、ジイソプロピルエーテル等のエ−テル類、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、アセトニトリル等のニトリル類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、メタノール、エタノール、プロパノール、ブタノール等のアルコール類およびこれらの混合物が挙げられる。
該反応に用いることができる化合物(XJ1)としては、ナトリウムメトキシド、ナトリウムエトキシド、ナトリウムn−プロポキシド、ナトリウムn−ブトキシド、ナトリウムイソプロポキシド、ナトリウムsec−ブトキシド、ナトリウムtert−ブトキシド、カリウムメトキシド、カリウムエトキシド、カリウムn−プロポキシド、カリウムn−ブトキシド、カリウムイソプロポキシド、カリウムsec−ブトキシド、カリウムtert−ブトキシド、ナトリウムフェノキシド等が挙げられる。
該反応には化合物(XH2)1モルに対して、化合物(XJ1)が通常1~10モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XJ2)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
式(XK1)で示される化合物(以下、化合物(XK1)と記す。)は、化合物(XH2)と水とを塩基の存在下で反応させることにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、通常、水中もしくは、水を含む溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、ジエチルエーテル、テトラヒドロフラン、1,4−ジオキサン、エチレングリコ−ルジメチルエ−テル、アニソール、メチルtertert−ブチルエーテル、ジイソプロピルエーテル等のエ−テル類、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、アセトニトリル等のニトリル類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、メタノール、エタノール、プロパノール、ブタノール等のアルコール類およびこれらの混合物が挙げられる。
該反応に用いられる塩基としては、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、ギ酸リチウム、酢酸リチウム、ギ酸ナトリウム、酢酸ナトリウム、ギ酸カリウム、酢酸カリウム等の金属有機酸塩、硝酸銀、硝酸ナトリウム等の金属硝酸塩、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、水酸化セシウム等のアルカリ金属水酸化物、ナトリウムメトキシド、ナトリウムエトキシド、ナトリウムtert−ブトキシド、カリウムtert−ブトキシドのアルカリ金属アルコキシド等が挙げられる。
該反応には化合物(XH2)1モルに対して、塩基が通常1~100モルの割合で用いられる。
該反応には化合物(XH2)1モルに対して、水が通常1モル~大過剰の割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XK1)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
化合物(XH2)は、化合物(XJ2)とハロゲン化剤とを反応させることにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類、ギ酸、酢酸、トリフルオロ酢酸等の有機酸類、水およびこれらの混合物が挙げられる。
該反応に用いられるハロゲン化剤としては、例えば、塩酸、臭化水素酸、ヨウ化水素酸が挙げられる。
該反応には化合物(XJ2)1モルに対して、ハロゲン化剤が通常1モル以上の割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XH2)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
化合物(XH2)は、化合物(XK1)とハロゲン化剤とを反応させることにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、酢酸エチル、酢酸メチル等のエステル類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類、ギ酸、酢酸、トリフルオロ酢酸等の有機酸類、水およびこれらの混合物が挙げられる。
該反応に用いられるハロゲン化剤としては、例えば、臭素、塩素、塩化スルフリル、塩化水素酸、臭化水素酸、ヨウ化水素酸、三臭化ホウ素、三臭化リン、塩化トリメチルシリル、臭化トリメチルシリル、ヨウ化トリメチルシリル、塩化チオニル、臭化チオニル、オキシ塩化リン、三塩化リン、五塩化リン、塩化チオニル、オキシ臭化リン、五臭化リン、三ヨウ化リン、二塩化オキサリル、二臭化オキサリル、塩化アセチル、四臭化炭素、N−ブロモスクシンイミド、塩化リチウム、ヨウ化ナトリウム、臭化アセチル等が挙げられる。
該反応には化合物(XK1)1モルに対して、ハロゲン化剤が通常1~10モルの割合で用いられる。
該反応を促進するため、使用するハロゲン化剤に応じた添加剤を加えてもよく、具体的には、塩化アセチルに対する塩化亜鉛、四臭化炭素に対するトリフェニルホスフィン、N−ブロモスクシンイミドに対するジメチルスルフィド、ヨウ化ナトリウムに対する三フッ化ホウ素ジエチルエーテル錯体、臭化アセチルに対する三フッ化ホウ素ジエチルエーテル錯体、塩化リチウムに対するトリエチルアミン及び塩化メタンスルホニル、ヨウ化ナトリウムに対する塩化アルミニウム、ヨウ化ナトリウムに対する塩化トリメチルシリル等が挙げられる。その使用量はいずれの添加剤も、通常、化合物(XK1)1モルに対して、0.01~5モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XH2)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
式(XM3)で示される化合物(以下、化合物(XM3)と記す。)は、化合物(XK1)と式(XM2)で示される化合物(以下、化合物(XM2)と記す。)とを塩基の存在下で反応させることにより製造することができる。
〔式中、R4、R5、R6、R7、R8、R9およびR201は前記と同じ意味を表し、R901はC1−C6アルキル基、C1−C6ハロアルキル基、C6−C16アリール基、C6−C16ハロアリール基を表し、Z801はフッ素原子、塩素原子、臭素原子またはヨウ素原子を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、アセトニトリル等のニトリル類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類及びこれらの混合物が挙げられる。
該反応に用いられる塩基としては、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、水酸化セシウム等のアルカリ金属水酸化物、水素化リチウム、水素化ナトリウム、水素化カリウム等のアルカリ金属水素化物、ナトリウムメトキシド、ナトリウムエトキシド、ナトリウムtert−ブトキシド、カリウムtert−ブトキシドのアルカリ金属アルコキシド等が挙げられる。
該反応には化合物(XK1)1モルに対して、化合物(XM2)が通常1~10モルの割合、塩基が通常1~5モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
該反応は、必要に応じてヨウ化ナトリウム、ヨウ化テトラブチルアンモニウムなどを加えてもよく、これらの化合物は通常、化合物(XK1)1モルに対して、0.001~1.2モルの割合で用いられる。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XM3)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
式(XN12)で示される化合物(以下、化合物(XN12)と記す。)は、式(XN11)で示される化合物(以下、化合物(XN11)と記す。)と化合物(G21)とを塩基及び触媒存在下で、カップリング反応に供することにより製造することができる。
〔式中、R501は水素原子またはOR111基を表し、R111、R4、R5、R7、R8、R9、R10、R71、X、Z31およびZ41は前記と同じ意味を表す。〕
該反応は、製造法Bに記載の反応に準じて実施することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、製造法Bに記載の反応に準じて実施することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、製造法Bに記載の反応に準じて実施することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、製造法Bに記載の反応に準じて実施することができる。
〔式中、記号は前記と同じ意味を表す。〕
で示される化合物群のうちR6、R7、R8、およびR9から選ばれる2以上の置換基がR71および/またはR72である化合物を製造することができる。
さらに、製造法Bに記載のカップリング反応に代えて、他の公知のカップリング反応を用いることもできる。
式(XW2)で示される化合物(以下、化合物(XW2)と記す。)は、式(XW1)で示される化合物(以下、化合物(XW1)と記す。)を反応促進剤の存在下、式(XW3)で示される化合物(以下、化合物(XW3)と記す。)と反応させることにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、酢酸エチル、酢酸メチル等のエステル類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類及びこれらの混合物があげられ、また、化合物(XW3)を溶媒として用いてもよい。
該反応に用いることができる化合物(XW3)としては、例えばメチルアルコール、エチルアルコール、プロピルアルコール、イソプロピルアルコール、n−ブチルアルコール、sec−ブチルアルコール、t−ブタノール、n−ペンタノール等があげられる。
該反応に用いられる反応促進剤としては、塩酸、硫酸等の鉱酸類、ジシクロヘキシルカルボジイミド、ジイソプロピルカルボジイミド、N’−(3−ジメチルアミノプロピル)−N−エチルカルボジイミド等のカルボジイミド、メタンスルホン酸、トルエンスルホン酸等の有機酸、トリフェニリルホスフィン/アゾジカルボン酸ジエチル等の光延反応試薬、塩化チオニル、ボロントリフルオリド−エチルエーテル コンプレックス等が挙げられる。
該反応には化合物(XW1)1モルに対して、反応促進剤が通常0.01~10モルの割合で用いられる。
該反応は、必要に応じて、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩等を加えてもよく、これらの化合物は通常、化合物(XW1)1モルに対して、0.001~5モルの割合で用いられる。
該反応には、化合物(XW1)に対して過剰量の化合物(XW3)を用いる。
該反応の反応温度は通常−78~100℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XW2)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
化合物(XW2)は、化合物(XW1)とハロゲン化剤とを反応させ、式(XV1)で示される化合物(以下、化合物(XV1)と記す。)を得た後、化合物(XV1)と化合物(XW3)とを反応させることにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
化合物(XW1)とハロゲン化剤とを反応させ化合物(XV1)を製造する方法は、参考製造法Cに記載の反応に準じて実施することができる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、酢酸エチル、酢酸メチル等のエステル類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類及びこれらの混合物があげられ、化合物(XW3)を溶媒として用いてもよい。
該反応には、化合物(XV1)に対して、過剰量の化合物(XW3)を用いる。
該反応の反応温度は通常−78~100℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XW2)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
化合物(XW2)は、化合物(XW1)とアルキル化剤とを反応させることにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、酢酸エチル、酢酸メチル等のエステル類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類、水およびこれらの混合物が挙げられる。
該反応に用いることができるアルキル化剤としては、例えば臭化メチル、臭化エチル、臭化n−プロピル、ヨウ化メチル、ヨウ化エチル、ヨウ化n−プロピル、ヨウ化イソプロピル等のハロゲン化アルキル類、p−トルエンスルホン酸メチル、p−トルエンスルホン酸エチル、p−トルエンスルホン酸n−プロピル、メタンスルホン酸メチル、メタンスルホン酸エチル、メタンスルホン酸n−プロピル等のスルホン酸エステル類、および硫酸ジメチル、硫酸ジエチル、硫酸ジn−プロピル等の硫酸エステル類が挙げられる。
該反応には化合物(XW1)1モルに対して、アルキル化剤が通常1~10モルの割合で用いられる。
該反応は、必要に応じて、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩、テトラ(n−ブチル)アンモニウムヒドロキシド等の4級アンモニウム塩等を加えてもよく、これらの化合物は通常、化合物(XW1)1モルに対して、0.001~5モルの割合で用いられる。
該反応の反応温度は通常−78~100℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(XW2)を単離することができる。さらに蒸留、クロマトグラフィー、再結晶等の操作で精製してもよい。
式(XS2)で示される化合物(以下、化合物(XS2)と記す。)は、式(XS1)で示される化合物(以下、化合物(XS1)と記す。)と化合物(A2)とを、塩基の存在下で反応させることにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、製造法Aに記載の反応に準じて実施することができる。
式(XU2)で示される化合物(以下、化合物(XU2)と記す。)は、式(XU1)で示される化合物(以下、化合物(XU1)と記す。)と化合物(B2)とを、塩基及び触媒存在下でカップリング反応に供することにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、製造法Bに記載の反応に準じて実施することができる。
化合物(B1)は、式(XO1)で示される化合物(以下、化合物(XO1)と記す。)と化合物(XU1)とを塩基の存在下で反応させることにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、製造法Aに記載の反応に準じて実施することができる。
化合物(C1)は、化合物(B1)とボリル化試薬とを、触媒と塩基の存在下で反応させることにより製造することができる。
〔式中、Z51はアルコシキボラニル基を表し、R1、R2、R3、R4、R5、R6、R7、R8、R9、R10、R11およびXは前記と同じ意味を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、酢酸エチル、酢酸メチル等のエステル類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類およびこれらの混合物が挙げられる。
該反応に用いられるボリル化試薬としては、ビス(ピナコラト)ジボロン、およびピナコールボラン等が挙げられる。
該反応に用いられる触媒としては、酢酸パラジウム(II)、ジクロロビス(トリフェニルホスフィン)パラジウム、テトラキストリフェニルホスフィンパラジウム(0)、パラジウム(II)アセテート/トリスシクロヘキシルホスフィン、ビス(ジフェニルホスファンフェロセニル)パラジウム(II)ジクロリド、1,3−ビス(2,6−ジイソプロピルフェニル)イミダゾール−2−イリデン(1,4−ナフトキノン)パラジウムダイマー、アリル(クロロ)(1,3−ジメシチル−1,3−ジヒドロ−2H−イミダゾール−2−イリデン)パラジウムまたはパラジウム(II)アセテート/ジシクロヘキシル(2’,4’,6’−トリイソプロピルビフェニル−2−イル)ホスフィン、トリス(ジベンジリデンアセトン)ジパラジウム等が挙げられる。
該反応に用いられる塩基としては、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、水酸化セシウム等のアルカリ金属水酸化物、フッ化ナトリウム、フッ化カリウム、フッ化セシウム等のアルカリ金属ハロゲン化物、水素化リチウム、水素化ナトリウム、水素化カリウム等のアルカリ金属水素化物、リン酸三カリウム等のアルカリ金属リン酸塩、ナトリウムメトキシド、ナトリウムエトキシド、ナトリウムtert−ブトキシド、カリウムtert−ブトキシド等のアルカリ金属アルコキシドが挙げられる。
該反応には化合物(B1)1モルに対してボリル化試薬が通常1~10モルの割合、塩基が通常1~10モルの割合、触媒が通常0.0001~1モルの割合で用いられる。
該反応の反応温度は通常0~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(C1)を単離することができる。単離された本発明化合物は、クロマトグラフィー、再結晶等によりさらに精製することもできる。
化合物(I1)は、化合物(C1)と過酸化水素水とを塩基の存在下で反応させることにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、アセトニトリル等のニトリル類、水およびこれらの混合物が挙げられる。
該反応に用いられる過酸化水素水の濃度は通常1~70%の範囲である。
該反応に用いられる触媒としては、酢酸パラジウム(II)、ジクロロビス(トリフェニルホスフィン)パラジウム、テトラキストリフェニルホスフィンパラジウム(0)、パラジウム(II)アセテート/トリスシクロヘキシルホスフィン、ビス(ジフェニルホスファンフェロセニル)パラジウム(II)ジクロリド、1,3−ビス(2,6−ジイソプロピルフェニル)イミダゾール−2−イリデン(1,4−ナフトキノン)パラジウムダイマー、アリル(クロロ)(1,3−ジメシチル−1,3−ジヒドロ−2H−イミダゾール−2−イリデン)パラジウムまたはパラジウム(II)アセテート/ジシクロヘキシル(2’,4’,6’−トリイソプロピルビフェニル−2−イル)ホスフィン、およびトリス(ジベンジリデンアセトン)ジパラジウム等が挙げられる。
該反応に用いられる塩基としては、トリエチルアミン、ピリジン、N−メチルモルホリン、4−ジメチルアミノピリジン、ジイソプロピルエチルアミン、ジアザビシクロウンデセン等の有機塩基、炭酸リチウム、炭酸ナトリウム、炭酸カリウム等のアルカリ金属炭酸塩、炭酸水素ナトリウム等のアルカリ金属炭酸水素塩、水酸化リチウム、水酸化ナトリウム、水酸化カリウム、水酸化セシウム等のアルカリ金属水酸化物、フッ化ナトリウム、フッ化カリウム、フッ化セシウム等のアルカリ金属ハロゲン化物、水素化リチウム、水素化ナトリウム、水素化カリウム等のアルカリ金属水素化物、リン酸三カリウム等のアルカリ金属リン酸塩、ナトリウムメトキシド、ナトリウムエトキシド、ナトリウムtert−ブトキシド、カリウムtert−ブトキシド等のアルカリ金属アルコキシドが挙げられる。
該反応には化合物(C1)1モルに対して、過酸化水素水が通常1~10モルの割合、塩基が通常1~10モルの割合で用いられる。
該反応の反応温度は通常−78℃~100℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(I1)を単離することができる。単離された本発明化合物は、クロマトグラフィー、再結晶等によりさらに精製することもできる。
化合物(1−3)は、式(Y1)で示される化合物(以下、化合物(Y1)と記す。)とアジド化剤とを反応させることにより製造することができる。
〔式中、記号は前記と同じ意味を表す。〕
該反応は、通常溶媒中で行われる。
該反応に用いられる溶媒としては、例えば、n−ヘキサン、シクロヘキサン、トルエン、キシレン等の炭化水素類、テトラヒドロフラン、1,4−ジオキサン、エチレングリコールジメチルエーテル、メチルtert−ブチルエーテル、ジイソプロピルエーテル等のエーテル類、四塩化炭素、クロロホルム、ジクロロメタン、1,2−ジクロロエタン、テトラクロロエタン、クロロベンゼン等のハロゲン化炭化水素類、N,N−ジメチルホルムアミド、1,3−ジメチル−2−イミダゾリジノン、N−メチルピロリドン等の酸アミド類、酢酸エチル、酢酸メチル等のエステル類、ジメチルスルホキシド等のスルホキシド類、アセトン、メチルエチルケトン、メチルイソブチルケトン等のケトン類、アセトニトリル等のニトリル類およびこれらの混合物が挙げられる。
該反応に用いられるアジド化剤としては例えばアジ化ナトリウム、アジ化バリウムまたはアジ化リチウム等の無機アジド類、アジ化トリメチルシリル、アジ化ジフェニルホスホリル等の有機アジド類が挙げられる。
該反応には化合物(Y1)1モルに対して、アジド化剤が通常1~10モルの割合で用いられる。
該反応の反応温度は通常−20~150℃の範囲である。該反応の反応時間は通常0.1~24時間の範囲である。
該反応は、必要に応じて、塩化アルミニウムもしくは塩化亜鉛等のルイス酸を加えてもよく、これらの化合物は通常、化合物(Y1)1モルに対して、0.05~5モルの割合で用いられる。
反応終了後は、反応混合物を有機溶媒で抽出し、有機層を乾燥、濃縮する等の後処理操作を行うことにより、化合物(1−3)を単離することができる。単離された本発明化合物は、クロマトグラフィー、再結晶等によりさらに精製することもできる。
かかる他の殺菌剤としては、例えば以下のものが挙げられる。
プロピコナゾ−ル(propiconazole)、プロチオコナゾ−ル(prothioconazole)、トリアジメノ−ル(triadimenol)、プロクロラズ(prochloraz)、ペンコナゾ−ル(penconazole)、テブコナゾ−ル(tebuconazole)、フルシラゾ−ル(flusilazole)、ジニコナゾ−ル(diniconazole)、ブロムコナゾ−ル(bromuconazole)、エポキシコナゾ−ル(epoxiconazole)、ジフェノコナゾ−ル(difenoconazole)、シプロコナゾ−ル(cyproconazole)、メトコナゾ−ル(metconazole)、トリフルミゾ−ル(triflumizole)、テトラコナゾ−ル(tetraconazole)、マイクロブタニル(myclobutanil)、フェンブコナゾ−ル(fenbuconazole)、ヘキサコナゾ−ル(hexaconazole)、フルキンコナゾ−ル(fluquinconazole)、トリティコナゾ−ル(triticonazole)、ビテルタノ−ル(bitertanol)、イマザリル(imazalil)、フルトリアホ−ル(flutriafol)、シメコナゾ−ル(simeconazole)、イプコナゾ−ル(ipconazole)等;
(2)アミン殺菌剤
フェンプロピモルフ(fenpropimorph)、トリデモルフ(tridemorph)、フェンプロピジン(fenpropidin)、スピロキサミン(spiroxamine)等;
(3)ベンズイミダゾ−ル殺菌剤
カルベンダジム(carbendazim)、ベノミル(benomyl)、チアベンダゾ−ル(thiabendazole)、チオファネ−トメチル(thiophanate−methyl)等;
プロシミドン(procymidone)、イプロジオン(iprodione)、ビンクロゾリン(vinclozolin)等;
(5)アニリノピリミジン殺菌剤
シプロディニル(cyprodinil)、ピリメタニル(pyrimethanil)、メパニピリム(mepanipyrim)等;
(6)フェニルピロ−ル殺菌剤
フェンピクロニル(fenpiclonil)、フルジオキソニル(fludioxonil)等;
(7)ストロビルリン殺菌剤
クレソキシムメチル(kresoxim−methyl)、アゾキシストロビン(azoxystrobin)、トリフロキシストロビン(trifloxystrobin)、フルオキサストロビン(fluoxastrobin)、ピコキシストロビン(picoxystrobin)、ピラクロストロビン(pyraclostrobin)、ジモキシストロビン(dimoxystrobin)、ピリベンカルブ(pyribencarb)、メトミノストロビン(metominostrobin)、オリサストロビン(orysastrobin)、エネストロビン(enestrobin)、ピラオキシストロビン(pyraoxystrobin)、ピラメトストロビン(pyrametostrobin)、フルフェノキシストロビン(flufenoxystrobin)、フェナミンストロビン(fenaminstrobin)、エノキサストロビン(enoxastrobin)、クモキシストロビン(coumoxystrobin)、ピリミノストロビン(pyriminostrobin)、トリクロピリカルブ(triclopyricarb)、マンデストロビン(mandestrobin)等;
(8)フェニルアマイド殺菌剤
メタラキシル(metalaxyl)、メタラキシルMまたはメフェノキサム(metalaxyl−M or mefenoxam)、ベナラキシル(benalaxyl)、ベナラキシルMまたはキララキシル(benalaxyl−M or kiralaxyl)等;
(9)カルボン酸アミド殺菌剤
ジメトモルフ(dimethomorph)、イプロバリカルブ(iprovalicarb)、ベンチアバリカルブイソプロピル(benthivalicarb−isopropyl)、マンジプロパミド(mandipropamid)、バリフェナル(valiphenal)
(10)カルボキサミド殺菌剤
カルボキシン(carboxin)、メプロニル(mepronil)、フルトラニル(flutolanil)、チフルザミド(thifluzamide)、フラメトピル(furametpyr)、ボスカリド(boscalid)、ペンチオピラド(penthiopyrad)、フルオピラム(fluopyram)、ビキサフェン(bixafen)、ペンフルフェン(penflufen)、セダキサン(sedaxane)、フルキサピロキサド(fluxapyroxad)、イソピラザム(isopyrazam)、ベンゾビンジフルピル(benzovindiflupyr)、イソフェタミド(isofetamid)、N−[2−(3,4−ジフルオロフェニル)フェニル]−3−トリフルオロメチルピラジン−2−カルボン酸アミド、N−(1,1,3−トリメチルインダン−4−イル)−1−メチル−3−ジフルオロメチルピラゾール−4−カルボン酸アミド(ラセミ体又はエナンチオマー、R体のエナンチオマーとS体のエナンチオマーの任意の割合での混合物を含む)等
ジエトフェンカルブ(diethofencarb);チウラム(thiuram);フルアジナム(fluazinam);マンコゼブ(mancozeb);クロロタロニル(chlorothalonil);キャプタン(captan);ジクロフルアニド(dichlofluanid);フォルペット(folpet);キノキシフェン(quinoxyfen);フェンヘキサミド(fenhexanid);ファモキサドン(fanoxadon);フェナミドン(fenamidon);ゾキサミド(zoxamide);エタボキサム(ethaboxam);アミスルブロム(amisulbrom);シアゾファミド(cyazofamid);メトラフェノン(metrafenone);ピリオフェノン(pyriofenone);シフルフェナミド(cyflufenamid);プロキナジド(proquinazid);フルスルファミド(flusulfamide);フルオピコリド(fluopicolide);フォセチル(fosetyl);シモキサニル(cymoxanil);ペンシクロン(pencycuron);トルクロホスメチル(tolclofos‐methyl);カルプロパミド(carpropamid);ジクロシメット(diclocymet);フェノキサニル(fenoxanil);トリシクラゾ−ル(tricyclazole);ピロキロン(pyroquilon);プロベナゾ−ル(probenazole);イソチアニル(isotianil);チアジニル(tiadinil);テブフロキン(tebufloquin);ジクロメジン(diclomezine);カスガマイシン(kasugamycin);フェリムゾン(ferimzone);フサライド(fthalide);バリダマイシン(validamycin);ヒドロキシイソキサゾ−ル(hydroxyisoxazole);イミノクタジン酢酸塩(iminoctadine acetate);イソプロチオラン(isoprothiolane);オキソリニック酸(oxolinic acid);オキシテトラサイクリン(oxytetracycline);ストレプトマイシン(streptomycin);塩基性塩化銅(copper oxychloride);水酸化第二銅(copper hydroxide);塩基性硫酸銅(copper hydroxide sulfate);有機銅(organocopper);硫黄(sulfur);アメトクトラジン(ametoctradin);フェンピラザミン(fenpyrazamine);オキサチアピプロリン(oxathiapiprolin);3−クロロ−4−(2,6−ジフルオロフェニル)−6−メチル−5−フェニルピリダジン;3−シアノ−4−(2,6−ジフルオロフェニル)−6−メチル−5−フェニルピリダジン等が挙げられる。
(1)有機リン化合物
アセフェ−ト(acephate)、りん化アルミニウム(Aluminium phosphide)、ブタチオホス(butathiofos)、キャドサホス(cadusafos)、クロルエトキシホス(chlorethoxyfos)、クロルフェンビンホス(chlorfenvinphos)、クロルピリホス(chlorpyrifos)、クロルピリホスメチル(chlorpyrifos−methyl)、シアノホス(cyanophos:CYAP)、ダイアジノン(diazinon)、DCIP(dichlorodiisopropyl ether)、ジクロフェンチオン(dichlofenthion:ECP)、ジクロルボス(dichlorvos:DDVP)、ジメトエ−ト(dimethoate)、ジメチルビンホス(dimethylvinphos)、ジスルホトン(disulfoton)、EPN、エチオン(ethion)、エトプロホス(ethoprophos)、エトリムホス(etrimfos)、フェンチオン(fenthion:MPP)、フエニトロチオン(fenitrothion:MEP)、ホスチアゼ−ト(fosthiazate)、ホルモチオン(formothion)、りん化水素(Hydrogen phosphide)、イソフェンホス(isofenphos)、イソキサチオン(isoxathion)、マラチオン(malathion)、メスルフェンホス(mesulfenfos)、メチダチオン(methidathion:DMTP)、モノクロトホス(monocrotophos)、ナレッド(naled:BRP)、オキシデプロホス(oxydeprofos:ESP)、パラチオン(parathion)、ホサロン(phosalone)、ホスメット(phosmet:PMP)、ピリミホスメチル(pirimiphos−methyl)、ピリダフェンチオン(pyridafenthion)、キナルホス(quinalphos)、フェントエ−ト(phenthoate:PAP)、プロフェノホス(profenofos)、プロパホス(propaphos)、プロチオホス(prothiofos)、ピラクロホス(pyraclorfos)、サリチオン(salithion)、スルプロホス(sulprofos)、テブピリムホス(tebupirimfos)、テメホス(temephos)、テトラクロルビンホス(tetrachlorvinphos)、テルブホス(terbufos)、チオメトン(thiometon)、トリクロルホン(trichlorphon:DEP)、バミドチオン(vamidothion)、フォレ−ト(phorate)、カズサホス(cadusafos)等;
アラニカルブ(alanycarb)、ベンダイオカルブ(bendiocarb)、ベンフラカルブ(benfuracarb)、BPMC、カルバリル(carbaryl)、カルボフラン(carbofuran)、カルボスルファン(carbosulfan)、クロエトカルブ(cloethocarb)、エチオフェンカルブ(ethiofencarb)、フェノブカルブ(fenobucarb)、フェノチオカルブ(fenothiocarb)、フェノキシカルブ(fenoxycarb)、フラチオカルブ(furathiocarb)、イソプロカルブ(isoprocarb:MIPC)、メトルカルブ(metolcarb)、メソミル(methomyl)、メチオカルブ(methiocarb)、NAC、オキサミル(oxamyl)、ピリミカ−ブ(pirimicarb)、プロポキスル(propoxur:PHC)、XMC、チオジカルブ(thiodicarb)、キシリルカルブ(xylylcarb)、アルジカルブ(aldicarb)等;
(3)合成ピレスロイド化合物
アクリナトリン(acrinathrin)、アレスリン(allethrin)、ベンフルスリン(benfluthrin)、ベ−タ−シフルトリン(beta−cyfluthrin)、ビフェントリン(bifenthrin)、シクロプロトリン(cycloprothrin)、シフルトリン(cyfluthrin)、シハロトリン(cyhalothrin)、シペルメトリン(cypermethrin)、デルタメトリン(deltamethrin)、エスフェンバレレ−ト(esfenvalerate)、エトフェンプロックス(ethofenprox)、フェンプロパトリン(fenpropathrin)、フェンバレレ−ト(fenvalerate)、フルシトリネ−ト(flucythrinate)、フルフェンプロックス(flufenoprox)、フルメスリン(flumethrin)、フルバリネ−ト(fluvalinate)、ハルフェンプロックス(halfenprox)、イミプロトリン(imiprothrin)、ペルメトリン(permethrin)、プラレトリン(prallethrin)、ピレトリン(pyrethrins)、レスメトリン(resmethrin)、シグマ−サイパ−メスリン(sigma−cypermethrin)、シラフルオフェン(silafluofen)、テフルトリン(tefluthrin)、トラロメトリン(tralomethrin)、トランスフルトリン(transfluthrin)、テトラメトリン(tetramethrin)、フェノトリン(phenothrin)、シフェノトリン(cyphenothrin)、アルファシペルメトリン(alpha−cypermethrin)、ベータシペルメトリン(beta−cypermethrin)、シータシペルメトリン(theta−cypermethrin)、ゼ−タシペルメトリン(zeta−cypermethrin)、ラムダシハロトリン(lambda−cyhalothrin)、ガンマシハロトリン(gamma−cyhalothrin)、フラメトリン(furamethrin)、タウフルバリネ−ト(tau−fluvalinate)、ハルフェンプロックス(halfenprox)、プロトリフェンビュ−ト(protrifenbute)、2,3,5,6−テトラフルオロ−4−(メトキシメチル)ベンジル(EZ)−(1RS,3RS;1RS,3SR)−2,2−ジメチル−3−プロプ−1−エニルシクロプロパンカルボキシレ−ト、2,3,5,6−テトラフルオロ−4−メチルベンジル(EZ)−(1RS,3RS;1RS,3SR)−2,2−ジメチル−3−プロプ−1−エニルシクロプロパンカルボキシレ−ト、2,3,5,6−テトラフルオロ−4−(メトキシメチル)ベンジル(1RS,3RS;1RS,3SR)−2,2−ジメチル−3−(2−メチル−1−プロペニル)シクロプロパンカルボキシレ−ト等;
カルタップ(cartap)、ベンスルタップ(bensultap)、チオシクラム(thiocyclam)、モノスルタップ(monosultap)、ビスルタップ(bisultap)等;
(5)ネオニコチノイド化合物
イミダクロプリド(imidacloprid)、ニテンピラム(nitenpyram)、アセタミプリド(acetamiprid)、チアメトキサム(thiamethoxam)、チアクロプリド(thiacloprid)、ジノテフラン(dinotefuran)、クロチアニジン(clothianidin)等;
(6)ベンゾイル尿素化合物
クロルフルアズロン(chlorfluazuron)、ビストリフルロン(bistrifluron)、ジアフェンチウロン(diafenthiuron)、ジフルベンズロン(diflubenzuron)、フルアズロン(fluazuron)、フルシクロクスロン(flucycloxuron)、フルフェノクスロン(flufenoxuron)、ヘキサフルムロン(hexaflumuron)、ルフェヌロン(lufenuron)、ノバルロン(novaluron)、ノビフルムロン(noviflumuron)、テフルベンズロン(teflubenzuron)、トリフルムロン(triflumuron)、トリアズロン等;
(7)フェニルピラゾ−ル化合物
アセトプロ−ル(acetoprole)、エチプロ−ル(ethiprole)、フィプロニル(fipronil)、バニリプロ−ル(vaniliprole)、ピリプロ−ル(pyriprole)、ピラフルプロ−ル(pyrafluprole)等;
(8)Btトキシン殺虫剤
バチルス・チュ−リンゲンシス菌由来の生芽胞および産生結晶毒素、並びにそれらの混合物;
(9)ヒドラジン化合物
クロマフェノジド(chromafenozide)、ハロフェノジド(halofenozide)、メトキシフェノジド(methoxyfenozide)、テブフェノジド(tebufenozide)等;
(10)有機塩素化合物
アルドリン(aldrin)、ディルドリン(dieldrin)、ジエノクロル(dienochlor)、エンドスルファン(endosulfan)、メトキシクロル(methoxychlor)等;
(11)天然殺虫剤
マシン油(machine oil)、硫酸ニコチン(nicotine−sulfate);
アベルメクチン(avermectin−B)、ブロモプロピレ−ト(bromopropylate)、ブプロフェジン(buprofezin)、クロルフェナピル(chlorphenapyr)、シロマジン(cyromazine)、D−D(1,3−Dichloropropene)、エマメクチンベンゾエ−ト(emamectin−benzoate)、フェナザキン(fenazaquin)、フルピラゾホス(flupyrazofos)、ハイドロプレン(hydroprene)、メトプレン(methoprene)、インドキサカルブ(indoxacarb)、メトキサジアゾン(metoxadiazone)、ミルベマイシンA(milbemycin−A)、ピメトロジン(pymetrozine)、ピリダリル(pyridalyl)、ピリプロキシフェン(pyriproxyfen)、スピノサッド(spinosad)、スルフラミド(sulfluramid)、トルフェンピラド(tolfenpyrad)、トリアゼメイト(triazamate)、フルベンジアミド(flubendiamide)、ドラメクチン(doramectin)、レピメクチン(lepimectin)、亜ひ酸(Arsenic acid)、ベンクロチアズ(benclothiaz)、石灰窒素(Calcium cyanamide)、石灰硫黄合剤(Calcium polysulfide)、クロルデン(chlordane)、DDT、DSP、フルフェネリウム(flufenerim)、フロニカミド(flonicamid)、フルリムフェン(flurimfen)、ホルメタネ−ト(formetanate)、メタム・アンモニウム(metam−ammonium)、メタム・ナトリウム(metam−sodium)、臭化メチル(Methyl bromide)、オレイン酸カリウム(Potassium oleate)、スピロメシフェン(spiromesifen)、硫黄(Sulfur)、メタフルミゾン(metaflumizone)、スピロテトラマット(spirotetramat)、ピリフルキナゾン(pyrifluquinazone)、スピネトラム(spinetoram)、クロラントラニリプロ−ル(chlorantraniliprole)、シアントラニリプロ−ル(cyantraniliprole)、シクラニリプロール(cyclaniliprole)、スルホキサフロール(sulfoxaflor)、フルピラジフロン(flupyradifurone)等。
かかる他の殺線虫剤(殺線虫活性成分)としては、例えば、DCIP、フォスチアゼ−ト(fosthiazate)、塩酸レバミゾ−ル(levamisol)、メチルイソチオシアネ−ト(methyisothiocyanate)、酒石酸モランテル(morantel tartarate)、イミシアホス(imicyafos)、フルエンスルホン(fluensulfone)等。
エテホン(ethephon)、クロルメコート(chlormequat−chloride)、メピコート(mepiquat−chloride)、ジベレリンA3(Gibberellin A3)に代表されるジベレリンA(Gibberellin A)、アブシシン酸(abscisic acid)、カイネチン(Kinetin)、ベンジルアデニン(benzyladenine)、1,3−ジフェニルウレア、ホルクロルフェヌロン(forchlorfenuron)、チジアズロン(thidiazuron)、4−オキソ−4−(2−フェニルエチル)アミノ酪酸、5−(トリフルオロメチル)ベンゾ[b]チオフェン−2−カルボン酸メチル、5−(トリフルオロメチル)ベンゾ[b]チオフェン−2−カルボン酸等。
果樹;仁果類(リンゴ、セイヨウナシ、ニホンナシ、カリン、マルメロ等)、核果類(モモ、スモモ、ネクタリン、ウメ、オウトウ、アンズ、プル−ン等)、カンキツ類(ウンシュウミカン、オレンジ、レモン、ライム、グレ−プフル−ツ等)、堅果類(クリ、クルミ、ハシバミ、ア−モンド、ピスタチオ、カシュ−ナッツ、マカダミアナッツ等)、液果類(ブル−ベリ−、クランベリ−、ブラックベリ−、ラズベリ−等)、ブドウ、カキ、オリ−ブ、ビワ、バナナ、コ−ヒ−、ナツメヤシ、ココヤシ等、
果樹以外の樹;チャ、クワ、花木、街路樹(トネリコ、カバノキ、ハナミズキ、ユ−カリ、イチョウ、ライラック、カエデ、カシ、ポプラ、ハナズオウ、フウ、プラタナス、ケヤキ、クロベ、モミノキ、ツガ、ネズ、マツ、トウヒ、イチイ)等。
アザミウマ目害虫:ミカンキイロアザミウマ(Frankliniella occidentalis)、ミナミキイロアザミウマ(Thrips palmi)、チャノキイロアザミウマ(Scirtothrips dorsalis)、ネギアザミウマ(Thrips tabaci)、ヒラズハナアザミウマ(Frankliniella intonsa)、タバコアザミウマ(Frankliniella fusca)などのアザミウマ類等。
双翅目害虫:イエバエ(Musca domestica)、アカイエカ(Culex pipiens pallens)、ウシアブ(Tabanus trigonus)、タマネギバエ(Hylemya antiqua)、タネバエ(Hylemya platura)、シナハマダラカ(Anopheles sinensis)、イネハモグリバエ(Agromyza oryzae)、イネヒメハモグリバエ(Hydrellia griseola)、イネキモグリバエ(Chlorops oryzae)、ウリミバエ(Dacus cucurbitae)、チチュウカイミバエ(Ceratitis capitata)、マメハモグリバエ(Liriomyza trifolii)等。
直翅目害虫:トノサマバッタ(Locusta migratoria)、ケラ(Gryllotalpa africana)、コバネイナゴ(Oxya yezoensis)、ハネナガイナゴ(Oxya japonica)等。
膜翅目害虫:カブラハバチ(Athalia rosae)、ハキリアリ(Acromyrmex spp.)、ファイヤーアント(Solenopsis spp.)等。
線虫類:イネシンガレセンチュウ(Aphelenchoides besseyi)、イチゴメセンチュウ(Nothotylenchus acris)、ダイズシストセンチュウ(Heterodera glycines)サツマイモネコブセンチュウ(Meloidogyne incognita)、キタネグサレセンチュウ(Pratylenchus penetrans)、ニセネコブセンチュウ(Nacobbus aberrans)等。
ゴキブリ目害虫:チャバネゴキブリ(Blattella germanica)、クロゴキブリ(Periplaneta fuliginosa)、ワモンゴキブリ(Periplaneta americana)、トビイロゴキブリ(Periplaneta brunnea)、トウヨウゴキブリ(Blatta orientalis)等。
ダニ目害虫:ナミハダニ(Tetranychus urticae)、ミカンハダニ(Panonychus citri)、オリゴニカス属等のハダニ類、ミカンサビダニ(Aculops pelekassi)等のフシダニ類、チャノホコリダニ(Polyphagotarsonemus latus)等のホコリダニ類、ヒメハダニ類、ケナガハダニ類、ケナガコナダニ(Tyrophagus putrescentiae)等のコナダニ類、コナヒョウヒダニ(Dermatophagoides farinae)、ヤケヒョウヒダニ(Dermatophagoides ptrenyssnus)等のヒョウヒダニ類、ホソツメダニ(Cheyletus eruditus)、クワガタツメダニ(Cheyletus malaccensis)、ミナミツメダニ(Cheyletus moorei)等のツメダニ類、ワクモ類等。
まず、製造例を示す。
参考製造例14に記載の14Aを0.28g、p−ヒドロキシビフェニル0.17g、炭酸カリウム0.28gおよびアセトニトリル4mLの混合物を加熱還流下4時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−フェニルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物1と記す。)0.30gを得た。
本発明化合物1
1H−NMR(CDCl3)δ:7.55−7.47(4H,m),7.42−7.37(4H,m),7.30−7.27(2H,m),6.96−6.92(2H,m),5.06(2H,s),3.58(3H,s),2.49(3H,s).
1H−NMR(CDCl3)δ:7.44−7.39(2H,m),7.32−7.26(3H,m),7.05(1H,t,J=7.4Hz),6.97−6.92(4H,m),6.87−6.83(2H,m),5.01(2H,s),3.64(3H,s),2.51(3H,s).
本発明化合物92
1H−NMR(CDCl3)δ:7.42−7.36(2H,m),7.29−7.26(1H,m),7.13(1H,d,J=1.9Hz),6.96−6.93(1H,m),6.76(1H,d,J=8.2Hz),5.11(2H,s),3.66(3H,s),2.53(3H,s),2.25(3H,s).
本発明化合物93
1H−NMR(CDCl3)δ:7.83(1H,dd,J=8.6,2.3Hz),7.77−7.74(1H,m),7.48(1H,t,J=8.2Hz),7.12−7.06(2H,m),6.90(1H,d,J=8.6Hz),5.33(2H,s),3.94(3H,s),3.86(3H,s),3.59(3H,s),2.00(3H,s).
本発明化合物94
1H−NMR(CDCl3)δ:7.53(2H,d,J=8.9Hz),7.46−7.40(2H,m),7.31−7.28(1H,m),6.94(2H,d,J=8.9Hz),5.07(2H,s),3.61(3H,s),2.49(3H,s).
本発明化合物95
1H−NMR(CDCl3)δ:7.43−7.37(2H,m),7.28−7.25(1H,m),7.06(2H,d,J=8.7Hz),6.79−6.76(2H,m),4.99(2H,s),3.61(3H,s),2.48(3H,s),2.28(3H,s).
本発明化合物96
1H−NMR(CDCl3)δ:7.86(1H,dd,J=8.5,2.4Hz),7.80(1H,s),7.46−7.40(2H,m),7.30−7.26(1H,m),6.86(1H,d,J=8.5Hz),5.10(2H,s),3.88(3H,s),3.62(3H,s),2.50(3H,s),2.11(3H,s).
本発明化合物97
1H−NMR(CDCl3)δ:7.85(2H,d,J=9.1Hz),7.47−7.39(2H,m),7.32−7.28(1H,m),7.00(2H,d,J=8.8Hz),5.09(2H,s),3.64(3H,s),3.02(3H,s),2.48(3H,s).
本発明化合物98
1H−NMR(CDCl3)δ:7.76(1H,dd,J=8.6,2.3Hz),7.72−7.69(1H,m),7.48(1H,t,J=8.2Hz),7.12−7.06(2H,m),6.91(1H,d,J=8.5Hz),5.35(2H,s),3.94(3H,s),3.59(3H,s),2.52(3H,s),2.02(3H,s).
本発明化合物99
1H−NMR(CDCl3)δ:7.45(1H,t,J=8.2Hz),7.23(1H,dd,J=8.8,2.4Hz),7.16(1H,d,J=2.4Hz),7.10−7.03(2H,m),6.99(1H,s),6.80(1H,d,J=8.7Hz),5.22(2H,s),3.92(3H,s),3.60(3H,s),2.34(2H,q,J=7.6Hz),1.98(3H,s),1.23(3H,t,J=7.6Hz).
本発明化合物162
1H−NMR(CDCl3)δ:7.44−7.38(2H,m),7.27−7.23(1H,m),6.94−6.90(2H,m),6.73(1H,d,J=8.9Hz),4.99(2H,s),3.63(3H,s),2.50(3H,s),2.24(3H,s),2.06(3H,s).
本発明化合物163
1H−NMR(CDCl3)δ:7.41−7.36(2H,m),7.28−7.23(1H,m),7.00(1H,d,J=8.2Hz),6.68(1H,s),6.62(1H,d,J=8.2Hz),4.97(2H,s),3.61(3H,s),2.48(3H,s),2.21(3H,s),2.18(3H,s).
本発明化合物164
1H−NMR(CDCl3)δ:7.43−7.37(2H,m),7.27−7.24(1H,m),6.75(1H,d,J=8.7Hz),6.70−6.67(1H,m),6.63(1H,dd,J=8.7,3.1Hz),4.97(2H,s),3.74(3H,s),3.63(3H,s),2.50(3H,s),2.07(3H,s).
参考製造例20に記載の20Aを0.39g、3,4−ジクロロフェニルボロン酸0.15g、リン酸三カリウム0.28g、水0.4ml、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン付加物0.02gおよびジオキサン4mLの混合物を加熱還流下4時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−(3,4−ジクロロフェニル)−2−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物41と記す。)0.37gを得た。
本発明化合物41
1H−NMR(CDCl3)δ:7.61(1H,d,J=2.2Hz),7.47−7.40(3H,m),7.37−7.27(4H,m),6.90(1H,d,J=8.5Hz),5.08(2H,s),3.63(3H,s),2.52(3H,s),2.15(3H,s).
以下にその構造式とその1H−NMRデータを記す。
1H−NMR(CDCl3)δ:7.52(1H,t,J=1.8Hz),7.46−7.39(3H,m),7.36−7.24(5H,m),6.91(1H,d,J=8.4Hz),5.08(2H,s),3.64(3H,s),2.53(3H,s),2.16(3H,s).
本発明化合物3
1H−NMR(CDCl3)δ:7.46−7.40(2H,m),7.31−7.27(1H,m),7.13−7.05(5H,m),6.88(1H,d,J=8.0Hz),5.07(2H,s),3.65(3H,s),2.54(3H,s),2.33(3H,s),2.17(3H,s),2.13(3H,s).
本発明化合物4
1H−NMR(CDCl3)δ:7.44−7.26(7H,m),7.20−7.10(2H,m),6.93(1H,d,J=8.5Hz),5.08(2H,s),3.64(3H,s),2.53(3H,s),2.15(3H,s).
本発明化合物5
1H−NMR(CDCl3)δ:7.46−7.40(2H,m),7.37−7.33(2H,m),7.30−7.27(1H,m),7.17−7.15(2H,m),6.96(1H,s),6.90(1H,d,J=9.2Hz),5.08(2H,s),3.63(3H,s),2.53(3H,s),2.37(6H,s),2.16(3H,s).
本発明化合物6
1H−NMR(CDCl3)δ:7.48−7.40(3H,m),7.30−7.16(5H,m),6.91(1H,d,J=8.2Hz),5.08(2H,s),3.65(3H,s),2.53(3H,s),2.14(3H,s).
本発明化合物7
1H−NMR(CDCl3)δ:7.59−7.54(2H,m),7.51(1H,t,J=8.2Hz),7.43(2H,t,J=8.2Hz),7.40−7.31(3H,m),7.13(2H,t,J=8.2Hz),6.99(1H,d,J=8.2Hz),5.34(2H,s),3.97(3H,s),3.63(3H,s),2.10(3H,s).
本発明化合物8
1H−NMR(CDCl3)δ:7.53−7.47(3H,m),7.41−7.37(2H,m),7.35−7.29(2H,m),7.12(2H,t,J=8.5Hz),6.97(1H,d,J=8.5Hz),5.34(2H,s),3.97(3H,s),3.64(3H,s),2.09(3H,s).
本発明化合物9
1H−NMR(CDCl3)δ:7.50−7.42(2H,m),7.32−7.19(4H,m),7.17−7.15(1H,m),7.09(2H,t,J=8.2Hz),6.94(1H,d,J=8.2Hz),5.30(2H,s),3.93(3H,s),3.61(3H,s),2.05(3H,s).
本発明化合物10
1H−NMR(CDCl3)δ:7.52−7.49(1H,m),7.46(1H,d,J=8.0Hz),7.41−7.38(1H,m),7.33−7.23(4H,m),7.09(2H,t,J=8.5Hz),6.94(1H,d,J=8.5Hz),5.31(2H,s),3.94(3H,s),3.60(3H,s),2.06(3H,s).
1H−NMR(CDCl3)δ:7.79(1H,t,J=1.6Hz),7.74(1H,dt,J=7.8,1.6Hz),7.55(1H,dt,J=7.6,1.4Hz),7.51−7.45(2H,m),7.33−7.27(2H,m),7.09(2H,t,J=8.5Hz),6.96(1H,d,J=8.5Hz),5.32(2H,s),3.95(3H,s),3.61(3H,s),2.06(3H,s).
本発明化合物12
1H−NMR(CDCl3)δ:7.79(1H,s),7.72(1H,d,J=7.1Hz),7.58−7.49(3H,m),7.40−7.34(2H,m),7.13(2H,t,J=8.2Hz),6.99(1H,d,J=8.2Hz),5.35(2H,s),3.98(3H,s),3.64(3H,s),2.10(3H,s).
本発明化合物13
1H−NMR(CDCl3)δ:7.63(1H,s),7.48−7.42(2H,m),7.35−7.20(5H,m),7.10−7.05(2H,m),6.92(1H,d,J=8.2Hz),5.29(2H,s),3.93(3H,s),3.59(3H,s),2.04(3H,s),2.04(3H,s).
本発明化合物14
1H−NMR(CDCl3)δ:7.52(1H,s),7.47(1H,t,J=8.2Hz),7.35−7.29(4H,m),7.27−7.25(1H,m),7.08(2H,t,J=8.4Hz),6.94(1H,d,J=8.5Hz),5.30(2H,s),3.93(3H,s),3.59(3H,s),2.07(3H,s),1.36(9H,s).
本発明化合物15
1H−NMR(CDCl3)δ:7.48(1H,t,J=8.1Hz),7.21−7.05(5H,m),6.93−6.82(3H,m),5.30(2H,s),3.94(3H,s),3.62(3H,s),2.03(6H,s),2.02(3H,s).
本発明化合物16
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.1Hz),7.35−7.26(5H,m),7.11−7.08(3H,m),6.94(1H,d,J=8.2Hz),5.30(2H,s),3.93(3H,s),3.59(3H,s),2.40(3H,s),2.06(3H,s).
本発明化合物17
1H−NMR(CDCl3)δ:7.50−7.42(3H,m),7.30−7.25(2H,m),7.10−7.06(2H,m),6.94−6.92(3H,m),5.29(2H,s),3.93(3H,s),3.84(3H,s),3.59(3H,s),2.05(3H,s).
本発明化合物18
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.2Hz),7.35−7.29(3H,m),7.12−7.05(4H,m),6.94(1H,d,J=8.2Hz),6.84(1H,dd,J=8.2,2.5Hz),5.30(2H,s),3.93(3H,s),3.85(3H,s),3.59(3H,s),2.06(3H,s).
本発明化合物19
1H−NMR(CDCl3)δ:7.48(1H,t,J=8.1Hz),7.14−7.02(7H,m),6.91(1H,d,J=8.2Hz),5.29(2H,s),3.94(3H,s),3.62(3H,s),2.33(3H,s),2.23(3H,s),2.04(3H,s).
本発明化合物20
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.2Hz),7.30−7.24(4H,m),7.10−7.06(2H,m),7.01−6.92(3H,m),5.28(2H,s),3.93(3H,s),3.81(3H,s),3.62(3H,s),2.05(3H,s).
1H−NMR(CDCl3)δ:7.73(1H,dd,J=7.8,0.9Hz),7.62−7.58(1H,m),7.52−7.44(2H,m),7.40−7.33(2H,m),7.28−7.26(1H,m),7.12−7.08(2H,m),7.00(1H,d,J=8.5Hz),5.32(2H,s),3.95(3H,s),3.63(3H,s),2.08(3H,s).
本発明化合物22
1H−NMR(CDCl3)δ:7.45(1H,t,J=8.1Hz),7.41(2H,dd,J=6.3,1.7Hz),7.33−7.27(2H,m),7.19(2H,d,J=8.0Hz),7.09−7.04(2H,m),6.92(1H,d,J=8.2Hz),5.28(2H,s),3.92(3H,s),3.58(3H,s),2.36(3H,s),2.04(3H,s).
本発明化合物23
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.2Hz),7.38(1H,td,J=7.8,1.8Hz),7.32−7.23(3H,m),7.18−7.06(4H,m),6.95(1H,d,J=8.5Hz),5.30(2H,s),3.93(3H,s),3.60(3H,s),2.05(3H,s).
本発明化合物24
1H−NMR(CDCl3)δ:7.46(1H,t,J=8.1Hz),7.35−7.17(5H,m),7.10−7.05(2H,m),6.98−6.90(2H,m),5.29(2H,s),3.92(3H,s),3.58(3H,s),2.04(3H,s).
本発明化合物25
1H−NMR(CDCl3)δ:7.53−7.45(3H,m),7.43−7.40(1H,m),7.36−7.25(5H,m),6.92(1H,d,J=8.0Hz),5.10(2H,s),3.60(3H,s),2.86(2H,q,J=7.6Hz),2.14(3H,s),1.30(3H,t,J=7.6Hz).
本発明化合物26
1H−NMR(CDCl3)δ:7.52(1H,t,J=1.7Hz),7.47−7.40(2H,m),7.36−7.25(6H,m),6.95(1H,d,J=8.2Hz),5.30(2H,s),3.62(3H,s),2.17−2.12(4H,m),1.03−0.97(2H,m),0.81−0.75(2H,m).
本発明化合物27
1H−NMR(CDCl3)δ:7.81(1H,s),7.77−7.75(1H,m),7.57(1H,d,J=7.6Hz),7.53−7.45(3H,m),7.36−7.28(3H,m),6.94(1H,d,J=8.2Hz),5.10(2H,s),3.61(3H,s),2.86(2H,q,J=7.6Hz),2.15(3H,s),1.30(3H,t,J=7.6Hz).
本発明化合物28
1H−NMR(CDCl3)δ:7.81(1H,t,J=1.5Hz),7.75(1H,dt,J=7.8,1.5Hz),7.57(1H,dt,J=7.7,1.4Hz),7.50(1H,t,J=7.7Hz),7.45(1H,t,J=7.9Hz),7.36−7.32(2H,m),7.30−7.26(2H,m),6.97(1H,d,J=8.2Hz),5.31(2H,s),3.62(3H,s),2.17−2.13(4H,m),1.03−0.98(2H,m),0.80−0.76(2H,m).
本発明化合物29
1H−NMR(CDCl3)δ:7.45−7.37(4H,m),7.34−7.26(4H,m),7.14(1H,d,J=8.2Hz),6.80−6.75(2H,m),5.04(2H,s),3.65(3H,s),2.52(3H,s),2.25(3H,s).
本発明化合物30
1H−NMR(CDCl3)δ:7.45−7.40(2H,m),7.30−7.26(1H,m),7.23−7.16(4H,m),7.13(1H,d,J=8.2Hz),6.80−6.74(2H,m),5.04(2H,s),3.65(3H,s),2.52(3H,s),2.40(3H,s),2.25(3H,s).
1H−NMR(CDCl3)δ:7.45−7.41(2H,m),7.30−7.19(4H,m),7.08(1H,d,J=6.9Hz),7.00(1H,d,J=8.2Hz),6.81−6.78(1H,m),6.75(1H,dd,J=8.2,2.5Hz),5.05(2H,s),3.65(3H,s),2.53(3H,s),2.06(3H,s),2.02(3H,s).
本発明化合物32
1H−NMR(CDCl3)δ:7.46−7.40(2H,m),7.33−7.26(4H,m),7.16(1H,dt,J=7.0,1.7Hz),6.96(1H,s),6.73(1H,s),5.05(2H,s),3.67(3H,s),2.53(3H,s),2.24(3H,s),2.08(3H,s).
本発明化合物33
1H−NMR(CDCl3)δ:7.46−7.40(2H,m),7.30−7.26(2H,m),7.15−7.07(4H,m),6.80−6.74(2H,m),5.04(2H,s),3.65(3H,s),2.52(3H,s),2.39(3H,s),2.25(3H,s).
本発明化合物34
1H−NMR(CDCl3)δ:7.45−7.25(8H,m),7.00(1H,s),6.75(1H,s),5.06(2H,s),3.67(3H,s),2.54(3H,s),2.26(3H,s),2.09(3H,s).
本発明化合物35
1H−NMR(CDCl3)δ:7.54(2H,dd,J=8.27,1.02Hz),7.46−7.35(4H,m),7.37−7.35(2H,m),7.33−7.26(2H,m),6.92(1H,d,J=8.83Hz),5.07(2H,s),3.63(3H,s),2.53(3H,s),2.16(3H,s).
本発明化合物36
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.2Hz),7.11−7.02(7H,m),6.90(1H,d,J=8.4Hz),5.29(2H,s),3.93(3H,s),3.62(3H,s),2.35(3H,s),2.24(3H,s),2.03(3H,s).
本発明化合物37
1H−NMR(CDCl3)δ:7.68−7.65(2H,m),7.62−7.59(2H,m),7.48(1H,t,J=8.2Hz),7.36−7.31(2H,m),7.12−7.06(2H,m),6.96(1H,d,J=8.6Hz),5.32(2H,s),3.94(3H,s),3.60(3H,s),2.05(3H,s).
本発明化合物38
1H−NMR(CDCl3)δ:8.11(1H,t,J=1.7Hz),7.87(1H,dt,J=7.8,1.4Hz),7.74−7.71(1H,m),7.51−7.45(2H,m),7.38−7.34(2H,m),7.09(2H,t,J=8.1Hz),6.96(1H,d,J=8.2Hz),5.32(2H,s),3.95(3H,s),3.61(3H,s),2.65(3H,s),2.07(3H,s).
本発明化合物39
1H−NMR(CDCl3)δ:7.50−7.44(3H,m),7.30−7.25(2H,m),7.12−7.05(4H,m),6.93(1H,d,J=8.2Hz),5.30(2H,s),3.94(3H,s),3.60(3H,s),2.06(3H,s).
本発明化合物40
1H−NMR(CDCl3)δ:7.98(1H,d,J=1.4Hz),7.91−7.83(3H,m),7.71(1H,dd,J=8.5,1.8Hz),7.53−7.41(6H,m),7.30(1H,dd,J=6.5,2.6Hz),6.98−6.95(1H,m),5.11(2H,s),3.64(3H,s),2.55(3H,s),2.20(3H,s).
1H−NMR(CDCl3)δ:7.94(1H,d,J=8.5Hz),7.90(1H,d,J=8.0Hz),7.83(1H,d,J=8.2Hz),7.53−7.38(6H,m),7.31−7.26(3H,m),6.97(1H,d,J=8.0Hz),5.12(2H,s),3.67(3H,s),2.57(3H,s),2.18(3H,s).
本発明化合物47
1H−NMR(CDCl3)δ:7.74(1H,dd,J=7.8,1.4Hz),7.61(1H,td,J=7.7,1.4Hz),7.49−7.37(4H,m),7.30−7.26(3H,m),7.00(1H,d,J=8.5Hz),5.31(2H,s),3.64(3H,s),2.17−2.14(4H,m),1.05−1.00(2H,m),0.81−0.76(2H,m).
本発明化合物48
1H−NMR(CDCl3)δ:7.73(1H,dd,J=7.7,0.9Hz),7.63−7.58(1H,m),7.51−7.46(3H,m),7.41−7.37(2H,m),7.31−7.27(2H,m),6.97(1H,d,J=8.4Hz),5.10(2H,s),3.62(3H,s),2.86(2H,q,J=7.6Hz),2.15(3H,s),1.30(3H,t,J=7.6Hz).
本発明化合物49
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.3Hz),7.41−7.39(1H,m),7.33−7.26(4H,m),7.17(1H,dt,J=7.1,1.8Hz),7.10−7.06(2H,m),6.94(1H,d,J=8.4Hz),5.30(2H,s),3.93(3H,s),3.60(3H,s),2.52(3H,s),2.05(3H,s).
本発明化合物50
1H−NMR(CDCl3)δ:7.52−7.45(2H,m),7.29(1H,dd,J=6.8,2.4Hz),7.12−7.03(5H,m),6.89(1H,d,J=8.0Hz),5.09(2H,s),3.62(3H,s),2.88(2H,q,J=7.6Hz),2.36(3H,s),2.26(3H,s),2.12(3H,s),1.31(3H,t,J=7.6Hz).
本発明化合物51
1H−NMR(CDCl3)δ:7.49−7.37(6H,m),7.31−7.21(3H,m),6.57(1H,dd,J=8.4,2.3Hz),6.51(1H,d,J=2.3Hz),5.06(2H,s),3.76(3H,s),3.63(3H,s),2.53(3H,s).
本発明化合物52
1H−NMR(CDCl3)δ:7.54−7.39(6H,m),7.35−7.24(4H,m),7.01(1H,t,J=8.5Hz),5.18(2H,s),3.65(3H,s),2.88(2H,q,J=7.6Hz),1.31(3H,t,J=7.6Hz).
本発明化合物53
1H−NMR(CDCl3)δ:7.46−7.36(4H,m),7.29(1H,dd,J=6.6,2.7Hz),7.22−7.19(3H,m),6.56(1H,dd,J=8.4,2.3Hz),6.51(1H,d,J=2.3Hz),5.06(2H,s),3.76(3H,s),3.63(3H,s),2.53(3H,s),2.38(3H,s).
本発明化合物54
1H−NMR(CDCl3)δ:7.46−7.42(1H,m),7.29−7.22(3H,m),7.12−7.02(4H,m),6.92(1H,d,J=8.2Hz),5.29(2H,s),3.63(3H,s),2.36(3H,s),2.26(3H,s),2.20−2.11(4H,m),1.04−0.98(2H,m),0.81−0.75(2H,m).
本発明化合物55
1H−NMR(CDCl3)δ:7.79(1H,dd,J=2.4,1.0Hz),7.75−7.71(1H,m),7.62(1H,dt,J=7.7,1.4Hz),7.55−7.44(3H,m),7.31−7.22(3H,m),7.04(1H,t,J=8.4Hz),5.20(2H,s),3.67(3H,s),2.88(2H,q,J=7.6Hz),1.32(3H,t,J=7.6Hz).
1H−NMR(CDCl3)δ:7.53−7.40(8H,m),7.31(1H,dd,J=7.3,1.8Hz),7.23(1H,d,J=2.5Hz),7.15(1H,dd,J=8.7,2.5Hz),5.08(2H,s),3.68(3H,s),2.52(3H,s).
本発明化合物57
1H−NMR(CDCl3)δ:7.48−7.42(4H,m),7.38(1H,d,J=8.7Hz),7.31(1H,dd,J=7.3,1.8Hz),7.20(1H,d,J=2.8Hz),7.12(1H,dd,J=8.7,2.7Hz),7.02−6.98(2H,m),5.06(2H,s),3.86(3H,s),3.67(3H,s),2.51(3H,s).
本発明化合物113
1H−NMR(CDCl3)δ:7.55(2H,dd,J=8.0,1.1Hz),7.44−7.37(6H,m),7.33−7.27(2H,m),6.95(1H,d,J=9.2Hz),5.06(2H,s),3.64(3H,s),2.57(2H,q,J=7.6Hz),2.53(3H,s),1.14(3H,t,J=7.6Hz).
本発明化合物114
1H−NMR(CDCl3)δ:7.74(1H,dd,J=7.8,0.9Hz),7.61(1H,td,J=7.8,1.1Hz),7.50−7.34(6H,m),7.30−7.28(1H,m),6.98(1H,d,J=8.2Hz),5.07(2H,s),3.66(3H,s),2.58(2H,q,J=7.6Hz),2.53(3H,s),1.14(3H,t,J=7.6Hz).
本発明化合物115
1H−NMR(CDCl3)δ:7.49−7.40(2H,m),7.38−7.33(2H,m),7.30(1H,dd,J=7.3,1.4Hz),7.01−6.95(2H,m),6.52(2H,d,J=9.4Hz),5.02(2H,s),3.85(3H,s),3.68(3H,s),2.51(3H,s).
本発明化合物116
1H−NMR(CDCl3)δ:7.47−7.35(7H,m),7.30(1H,dd,J=7.4,1.7Hz),6.53(2H,d,J=9.3Hz),5.02(2H,s),3.68(3H,s),2.51(3H,s).
本発明化合物117
1H−NMR(CDCl3)δ:7.47−7.36(5H,m),7.32−7.22(5H,m),7.05(1H,dd,J=8.5,2.6Hz),5.09(2H,s),3.66(3H,s),2.53(3H,s).
本発明化合物118
1H−NMR(CDCl3)δ:7.48−7.43(2H,m),7.33−7.26(2H,m),7.25−7.22(2H,m),7.21−7.16(1H,m),7.16−7.09(2H,m),7.05(1H,dd,J=8.4,2.6Hz),5.10(2H,s),3.67(3H,s),2.54(3H,s),2.04(3H,s).
本発明化合物119
1H−NMR(CDCl3)δ:7.47−7.41(2H,m),7.33−7.19(5H,m),7.03(1H,d,J=8.7Hz),6.94−6.89(2H,m),5.09(2H,s),3.85(3H,s),3.66(3H,s),2.52(3H,s).
本発明化合物120
1H−NMR(CDCl3)δ:7.46−7.40(2H,m),7.33−7.26(2H,m),7.00(1H,s),6.89−6.83(3H,m),6.74(1H,s),5.06(2H,s),3.83(3H,s),3.67(3H,s),2.54(3H,s),2.26(3H,s),2.09(3H,s).
1H−NMR(CDCl3)δ:7.45−7.39(2H,m),7.30−7.26(1H,m),7.20(2H,dd,J=6.6,2.1Hz),6.97(1H,s),6.92(2H,dd,J=6.6,2.1Hz),6.73(1H,s),5.05(2H,s),3.84(3H,s),3.66(3H,s),2.53(3H,s),2.24(3H,s),2.08(3H,s).
本発明化合物122
1H−NMR(CDCl3)δ:7.72−7.70(1H,m),7.62−7.57(1H,m),7.46−7.38(3H,m),7.35−7.31(1H,m),7.30−7.26(1H,m),6.94(1H,s),6.76(1H,s),5.06(2H,s),3.67(3H,s),2.53(3H,s),2.16(3H,s),2.08(3H,s).
本発明化合物123
1H−NMR(CDCl3)δ:7.42−7.40(2H,m),7.34−7.26(2H,m),7.12(1H,dd,J=7.5,1.8Hz),7.01−6.92(3H,m),6.74(1H,s),5.03(2H,s),3.77(3H,s),3.67(3H,s),2.53(3H,s),2.11(3H,s),2.07(3H,s).
本発明化合物124
1H−NMR(CDCl3)δ:7.32−7.22(3H,m),7.17−7.12(3H,m),7.06−7.03(1H,m),6.92−6.86(3H,m),4.90(2H,s),3.65(3H,s),3.60(3H,s),2.19(3H,s),1.30(9H,s).
本発明化合物125
1H−NMR(CDCl3)δ:7.49−7.41(2H,m),7.34−7.29(3H,m),7.26−7.23(1H,m),7.19(1H,d,J=7.3Hz),6.56−6.49(2H,m),5.03(2H,s),3.69(3H,s),2.52(3H,s),2.18(3H,s).
本発明化合物126
1H−NMR(CDCl3)δ:7.41−7.35(2H,m),7.33−7.17(7H,m),6.90−6.86(1H,m),6.75−6.72(1H,m),4.98(2H,s),3.59(3H,s),2.63(2H,q,J=7.6Hz),2.28(3H,s),1.24(3H,t,J=6.7Hz).
本発明化合物127
1H−NMR(CDCl3)δ:7.36−7.32(3H,m),7.30−7.27(1H,m),7.21−7.17(2H,m),6.89−6.86(1H,m),6.86−6.81(2H,m),6.74(1H,s),4.96(2H,s),3.82(3H,s),3.61(3H,s),2.63(2H,q,J=7.6Hz),2.32(3H,s),1.24(3H,t,J=7.6Hz).
本発明化合物128
1H−NMR(CDCl3)δ:7.39−7.26(4H,m),7.22−7.16(2H,m),7.08−7.04(1H,m),6.89−6.84(3H,m),4.95(2H,s),3.82(3H,s),3.58(3H,s),2.33(3H,s),1.29(9H,s).
本発明化合物129
1H−NMR(CDCl3)δ:7.33−7.22(3H,m),7.17−7.09(3H,m),6.92−6.84(3H,m),6.75(1H,d,J=1.4Hz),4.94(2H,s),3.64(3H,s),3.63(3H,s),2.65(2H,q,J=7.6Hz),2.20(3H,s),1.26(3H,t,J=7.6Hz).
本発明化合物130
1H−NMR(CDCl3)δ:7.44−7.17(9H,m),7.07(1H,dd,J=7.9,1.8Hz),6.88(1H,d,J=1.8Hz),4.97(2H,s),3.56(3H,s),2.30(3H,s),1.29(9H,s).
1H−NMR(CDCl3)δ:7.45−7.40(2H,m),7.35−7.27(2H,m),7.12(1H,dd,J=7.4,1.7Hz),7.09(1H,d,J=8.2Hz),7.00(1H,td,J=7.4,1.0Hz),6.95(1H,dd,J=8.2,0.7Hz),6.80−6.74(2H,m),5.03(2H,s),3.77(3H,s),3.65(3H,s),2.52(3H,s),2.11(3H,s).
本発明化合物132
1H−NMR(CDCl3)δ:7.76(1H,d,J=2.3Hz),7.67(1H,dd,J=8.5,2.3Hz),7.54−7.51(2H,m),7.47−7.39(4H,m),7.37−7.28(2H,m),7.04(1H,d,J=8.5Hz),5.19(2H,s),3.69(3H,s),2.53(3H,s).
本発明化合物133
1H−NMR(CDCl3)δ:7.71(1H,d,J=2.1Hz),7.63(1H,dd,J=8.6,2.1Hz),7.45−7.40(2H,m),7.35−7.25(3H,m),7.04−7.01(2H,m),6.98(1H,d,J=8.2Hz),5.17(2H,s),3.82(3H,s),3.69(3H,s),2.53(3H,s).
本発明化合物134
1H−NMR(CDCl3)δ:7.29−7.25(2H,m),7.16(1H,d,J=7.6Hz),7.13−7.07(2H,m),6.95−6.93(2H,m),6.91−6.85(2H,m),4.58(2H,s),3.74(3H,s),3.65(3H,s),2.25(3H,s),1.96−1.93(6H,m).
本発明化合物135
1H−NMR(CDCl3)δ:7.40−7.36(2H,m),7.31−7.25(4H,m),7.15(1H,d,J=7.3Hz),7.10(1H,d,J=7.8Hz),7.00(1H,d,J=7.8Hz),6.95(1H,d,J=7.8Hz),4.66(2H,s),3.64(3H,s),2.24(3H,s),2.10(3H,s),1.91(3H,s).
本発明化合物136
1H−NMR(CDCl3)δ:7.72(1H,dd,J=7.8,0.6Hz),7.63−7.57(1H,m),7.57−7.50(1H,m),7.50−7.39(2H,m),7.34(1H,d,J=7.8Hz),7.29(1H,dd,J=6.8,2.4Hz),6.94(1H,s),6.78(1H,s),5.08(2H,s),3.64(3H,s),2.87(2H,q,J=7.6Hz),2.17(3H,s),2.07(3H,s),1.31(3H,t,J=7.6Hz).
本発明化合物137
1H−NMR(CDCl3)δ:7.51−7.45(2H,m),7.41−7.36(2H,m),7.32−7.27(4H,m),6.99(1H,s),6.75(1H,s),5.07(2H,s),3.64(3H,s),2.88(2H,q,J=7.6Hz),2.26(3H,s),2.07(3H,s),1.30(3H,t,J=7.6Hz).
本発明化合物138
1H−NMR(CDCl3)δ:7.51−7.44(2H,m),7.34−7.26(2H,m),7.15−7.10(1H,m),7.01−6.94(3H,m),6.76(1H,s),5.06(2H,s),3.79(3H,s),3.66(3H,s),2.88(2H,q,J=7.6Hz),2.12(3H,s),2.06(3H,s),1.30(3H,t,J=7.6Hz).
本発明化合物139
1H−NMR(CDCl3)δ:7.51−7.45(2H,m),7.34−7.15(4H,m),7.14−7.08(1H,m),6.97(1H,s),6.78(1H,s),5.08(2H,s),3.64(3H,s),2.87(2H,q,J=7.6Hz),2.18(3H,s),2.07(3H,s),1.30(3H,t,J=7.6Hz).
本発明化合物140
1H−NMR(CDCl3)δ:7.71(1H,dd,J=7.8,0.6Hz),7.59(1H,td,J=7.7,1.4Hz),7.48(1H,t,J=8.1Hz),7.43−7.38(1H,m),7.32(1H,dd,J=7.7,0.6Hz),7.12−7.07(2H,m),6.90(1H,s),6.82(1H,s),5.28(2H,s),3.94(3H,s),3.63(3H,s),2.15(3H,s),1.99(3H,s).
1H−NMR(CDCl3)δ:7.52(1H,t,J=8.2Hz),7.44−7.40(2H,m),7.36−7.31(3H,m),7.17−7.10(2H,m),6.99(1H,s),6.84(1H,s),5.33(2H,s),3.99(3H,s),3.68(3H,s),2.28(3H,s),2.04(3H,s).
本発明化合物142
1H−NMR(CDCl3)δ:7.52(1H,t,J=8.2Hz),7.38−7.32(1H,m),7.16−7.10(3H,m),7.05−7.00(1H,m),6.98(1H,dd,J=8.4,0.8Hz),6.93(1H,s),6.83(1H,s),5.30(2H,s),3.98(3H,s),3.81(3H,s),3.69(3H,s),2.14(3H,s),2.02(3H,s).
本発明化合物143
1H−NMR(CDCl3)δ:7.46−7.40(2H,m),7.34−7.27(2H,m),7.23−7.19(1H,m),7.19−7.15(1H,m),7.14−7.08(1H,m),6.96(1H,s),6.76(1H,s),5.06(2H,s),3.66(3H,s),2.53(3H,s),2.17(3H,s),2.08(3H,s).
本発明化合物144
1H−NMR(CDCl3)δ:7.44−7.39(2H,m),7.30−7.16(4H,m),7.09−7.04(1H,m),6.86−6.82(1H,m),6.74−6.70(1H,m),5.05(2H,s),3.67(3H,s),2.54(3H,s),2.08−2.05(6H,m),2.02(3H,s).
本発明化合物145
1H−NMR(CDCl3)δ:7.73(1H,d,J=7.8Hz),7.56−7.50(1H,m),7.47−7.39(3H,m),7.30−7.26(1H,m),7.20(1H,d,J=7.6Hz),6.86(1H,s),6.71(1H,s),5.12−5.02(2H,m),3.65(3H,s),2.54(3H,s),2.05(3H,s),1.98(3H,s).
本発明化合物146
1H−NMR(CDCl3)δ:7.46−7.40(4H,m),7.37−7.33(2H,m),7.30−7.27(1H,m),7.24−7.20(2H,m),6.90(1H,d,J=9.2Hz),5.07(2H,s),3.63(3H,s),2.52(3H,s),2.38(3H,s),2.15(3H,s).
本発明化合物147
1H−NMR(CDCl3)δ:7.48−7.41(7H,m),7.24(1H,t,J=4.6Hz),5.29(2H,s),3.72(3H,s),2.65(3H,s).
本発明化合物148
1H−NMR(CDCl3)δ:7.51−7.47(2H,m),7.46−7.40(4H,m),7.39−7.34(1H,m),7.26−7.23(1H,m),7.07(2H,d,J=9.5Hz),5.18(2H,s),3.73(3H,s),2.64(3H,s).
本発明化合物151
1H−NMR(CDCl3)δ:7.46−7.39(2H,m),7.30−7.25(1H,m),7.20−7.14(1H,m),6.95−6.83(3H,m),6.75(1H,s),5.06(2H,s),3.66(3H,s),2.53(3H,s),2.15(3H,s),2.08(3H,s).
本発明化合物152
1H−NMR(CDCl3)δ:7.53−7.48(2H,m),7.47−7.39(4H,m),7.36−7.28(2H,m),7.17(1H,dd,J=8.9,0.5Hz),6.68(1H,d,J=12.1Hz),5.05(2H,s),3.66(3H,s),2.53(3H,s),2.09(3H,s).
1H−NMR(CDCl3)δ:7.47−7.41(2H,m),7.36−7.32(1H,m),7.29(1H,dd,J=6.9,2.3Hz),7.23(1H,d,J=6.9Hz),7.07(1H,d,J=8.5Hz),7.04−6.96(2H,m),6.68(1H,d,J=11.4Hz),5.03(2H,s),3.82(3H,s),3.68(3H,s),2.53(3H,s),2.07(3H,s).
本発明化合物154
1H−NMR(CDCl3)δ:7.47−7.39(2H,m),7.30−7.26(1H,m),6.94(1H,t,J=10.0Hz),6.88(1H,s),6.79−6.71(2H,m),5.04(2H,s),3.73(3H,s),3.68(3H,s),2.53(3H,s),2.09(3H,s),2.07(3H,s).
本発明化合物155
1H−NMR(CDCl3)δ:7.65−7.61(1H,m),7.55−7.51(2H,m),7.48(1H,t,J=8.0Hz),7.42−7.36(4H,m),7.36−7.33(1H,m),7.32−7.28(1H,m),6.92(1H,d,J=8.4Hz),5.35(2H,s),3.60(3H,s),2.09(3H,s).
本発明化合物156
1H−NMR(CDCl3)δ:7.47−7.40(2H,m),7.31−7.25(3H,m),7.15−7.07(3H,m),6.99(1H,s),6.74(1H,s),5.06(2H,s),3.67(3H,s),2.54(3H,s),2.39(3H,s),2.25(3H,s),2.09(3H,s).
参考製造例28に記載の)28Aを0.45g、4−ブロモ−o−キシレン0.19g、リン酸三カリウム0.28g、水0.40ml、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン付加物0.02gおよびジオキサン4mLの混合物を加熱還流下4時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(3,4−ジメチルフェニル)−2−メチルフェノキシメチル}−3−メトキシフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物42と記す。)0.33gを得た。
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.2Hz),7.33−7.24(3H,m),7.18−7.04(4H,m),6.92(1H,d,J=8.2Hz),5.29(2H,s),3.93(3H,s),3.59(3H,s),2.31(3H,s),2.28(3H,s),2.05(3H,s).
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.2Hz),7.34−7.29(2H,m),7.15(2H,s),7.09(2H,t,J=7.4Hz),6.95−6.91(2H,m),5.30(2H,s),3.93(3H,s),3.59(3H,s),2.36(6H,s),2.06(3H,s).
本発明化合物44
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.3Hz),7.11−6.97(6H,m),6.90(1H,d,J=8.4Hz),5.28(2H,s),3.93(3H,s),3.62(3H,s),2.26(3H,s),2.24(3H,s),2.21(3H,s),2.03(3H,s).
本発明化合物45
1H−NMR(CDCl3)δ:7.60(1H,d,J=8.0Hz),7.48(1H,t,J=8.2Hz),7.33(1H,dd,J=8.2,2.3Hz),7.26−7.24(2H,m),7.19−7.17(1H,m),7.12−7.06(2H,m),6.98(1H,d,J=8.5Hz),5.31(2H,s),3.94(3H,s),3.62(3H,s),2.43(3H,s),2.06(3H,s).
本発明化合物149
1H−NMR(CDCl3)δ:7.47−7.41(2H,m),7.31−7.21(3H,m),7.04−6.95(2H,m),5.09(2H,s),3.64(3H,s),2.53(3H,s),2.15(3H,s).
本発明化合物150
1H−NMR(CDCl3)δ:7.47−7.41(2H,m),7.31−7.16(3H,m),6.96(1H,d,J=8.5Hz),5.09(2H,s),3.64(3H,s),2.53(3H,s),2.14(3H,s).
本発明化合物49を1.18g、メタクロロ過安息香酸0.77gおよびクロロホルム10mLの混合物を室温で12時間攪拌した。水に反応液を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(3−メタンスルホニルフェニル)−2−メチルフェノキシメチル}−3−メトキシフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物58と記す。)0.80gを得た。
1H−NMR(CDCl3)δ:8.08(1H,t,J=1.7Hz),7.85−7.78(2H,m),7.58(1H,t,J=7.8Hz),7.48(1H,t,J=8.3Hz),7.38−7.33(2H,m),7.11−7.07(2H,m),6.96(1H,d,J=8.2Hz),5.32(2H,s),3.95(3H,s),3.61(3H,s),3.08(3H,s),2.06(3H,s).
参考製造例21に記載の21Aを0.41g、フェノール0.11g、ヨウ化銅0.04g、2−ピコリン酸0.02g、リン酸三カリウム0.42gおよびジメチルスルホキシド2.5mLの混合物を120度で8時間攪拌した。水に反応液を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{(2−メチル−4−フェノキシ)フェノキシメチル}−3−メトキシフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物89と記す。)0.35gを得た。
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.2Hz),7.32−7.26(2H,m),7.11−7.00(3H,m),6.95−6.91(2H,m),6.83(1H,d,J=8.5Hz),6.79−6.74(2H,m),5.24(2H,s),3.93(3H,s),3.63(3H,s),1.98(3H,s).
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.2Hz),7.24(1H,dd,J=7.4,1.7Hz),7.13−7.00(4H,m),6.80−6.76(2H,m),6.72(1H,d,J=3.0Hz),6.66(1H,dd,J=8.9,3.0Hz),5.22(2H,s),3.92(3H,s),3.63(3H,s),2.67(2H,q,J=7.6Hz),1.97(3H,s),1.22(3H,t,J=7.6Hz).
本発明化合物61
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.2Hz),7.18−7.11(1H,m),7.10−7.02(4H,m),6.97−6.92(1H,m),6.81(1H,d,J=8.9Hz),6.78−6.71(2H,m),5.22(2H,s),3.92(3H,s),3.62(3H,s),1.98(3H,s).
本発明化合物62
1H−NMR(CDCl3)δ:7.45−7.40(2H,m),7.33−7.26(3H,m),7.06−7.02(1H,m),6.96−6.93(2H,m),6.82(1H,s),6.80−6.78(2H,m),5.01(2H,s),3.65(3H,s),2.52(3H,s),2.07(3H,s).
本発明化合物63
1H−NMR(CDCl3)δ:7.44−7.39(2H,m),7.28−7.25(1H,m),7.22(1H,dd,J=7.3,0.7Hz),7.14−7.10(1H,m),7.01(1H,td,J=7.3,1.1Hz),6.80(1H,dd,J=8.0,1.1Hz),6.77−6.73(2H,m),6.70−6.66(1H,m),4.99(2H,s),3.65(3H,s),2.51(3H,s),2.27(3H,s),2.05(3H,s).
本発明化合物64
1H−NMR(CDCl3)δ:7.45−7.40(3H,m),7.29−7.25(1H,m),7.18(1H,t,J=7.7Hz),6.86−6.74(5H,m),5.02(2H,s),3.65(3H,s),2.53(3H,s),2.32(3H,s),2.07(3H,s).
本発明化合物65
1H−NMR(CDCl3)δ:7.45−7.39(3H,m),7.29−7.25(1H,m),7.14−7.08(2H,m),6.87−6.84(2H,m),6.80(1H,s),6.77(1H,s),5.01(2H,s),3.65(3H,s),2.52(3H,s),2.32(3H,s),2.06(3H,s).
本発明化合物66
1H−NMR(CDCl3)δ:7.49−7.45(2H,m),7.33−7.26(4H,m),7.07−7.03(1H,m),6.97−6.93(2H,m),6.82−6.79(2H,m),5.02(2H,s),3.62(3H,s),2.85(2H,q,J=7.6Hz),2.05(3H,s),1.28(3H,t,J=7.6Hz).
本発明化合物67
1H−NMR(CDCl3)δ:7.43(1H,t,J=7.9Hz),7.33−7.25(4H,m),7.06−7.02(1H,m),6.96−6.93(2H,m),6.84−6.79(3H,m),5.23(2H,s),3.64(3H,s),2.17−2.13(1H,m),2.06(3H,s),1.04−0.98(2H,m),0.80−0.74(2H,m).
本発明化合物68
1H−NMR(CDCl3)δ:7.44−7.38(2H,m),7.28−7.24(1H,m),7.09−7.04(1H,m),7.00−6.97(1H,m),6.90−6.83(2H,m),6.80−6.71(3H,m),4.98(2H,s),3.87(3H,s),3.64(3H,s),2.51(3H,s),2.05(3H,s).
本発明化合物69
1H−NMR(CDCl3)δ:7.45−7.40(2H,m),7.28−7.25(1H,m),7.20−7.16(1H,m),6.82(1H,s),6.80−6.78(2H,m),6.61−6.58(1H,m),6.53−6.50(2H,m),5.01(2H,s),3.77(3H,s),3.65(3H,s),2.52(3H,s),2.06(3H,s).
本発明化合物70
1H−NMR(CDCl3)δ:7.44−7.39(2H,m),7.28−7.24(1H,m),6.93−6.90(2H,m),6.87−6.84(2H,m),6.76−6.69(3H,m),4.99(2H,s),3.79(3H,s),3.65(3H,s),2.51(3H,s),2.05(3H,s).
参考製造例33に記載の31Aを0.33g、3−ブロモフルオロベンゼン0.18g、ヨウ化銅0.19g、N−ブチルイミダゾール0.06g、炭酸カリウム0.28gおよびトルエン2mLの混合物を120度で8時間攪拌した。水に反応液を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(3−フルオロフェノキシ)−2−メチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物71と記す。)0.02gを得た。
1H−NMR(CDCl3)δ:7.44−7.39(2H,m),7.29−7.26(1H,m),7.24−7.20(1H,m),7.14−7.10(1H,m),6.84−6.80(2H,m),6.75−6.70(2H,m),6.62(1H,dt,J=10.6,2.3Hz),5.02(2H,s),3.65(3H,s),2.52(3H,s),2.07(3H,s).
1H−NMR(CDCl3)δ:8.18(1H,dd,J=5.0,1.0Hz),7.68−7.63(1H,m),7.45−7.40(2H,m),7.29−7.25(1H,m),6.97−6.84(5H,m),5.01(2H,s),3.67(3H,s),2.52(3H,s),2.10(3H,s).
本発明化合物76
1H−NMR(CDCl3)δ:8.56(2H,d,J=4.8Hz),7.45−7.38(3H,m),7.29−7.26(1H,m),7.02−6.96(3H,m),5.02(2H,s),3.67(3H,s),2.51(3H,s),2.11(3H,s).
本発明化合物118
1H−NMR(CDCl3)δ:8.17(1H,dd,J=5.0,1.4Hz),7.69−7.62(1H,m),7.50−7.41(3H,m),7.29−7.26(1H,m),6.96−6.85(4H,m),5.02(2H,s),3.64(3H,s),2.85(2H,q,J=7.6Hz),2.08(3H,s),1.28(3H,t,J=7.6Hz).
参考製造例33に記載の31Aを0.33g、2−フルオロベンゾニトリル0.12g、炭酸セシウム0.65gおよびN,N−ジメチルホルムアミド2mLの混合物を120度で6時間攪拌した。水に反応液を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(4−シアノフェノキシ)−2−メチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物72と記す。)0.25gを得た。
本発明化合物72
1H−NMR(CDCl3)δ:7.59−7.55(2H,m),7.46−7.41(2H,m),7.28(1H,dd,J=7.4,3.1Hz),6.98−6.93(2H,m),6.84−6.82(3H,m),5.04(2H,s),3.66(3H,s),2.53(3H,s),2.09(3H,s).
1H−NMR(CDCl3)δ:7.44−7.40(2H,m),7.37(1H,d,J=8.2Hz),7.32−7.27(2H,m),7.21−7.17(1H,m),7.13−7.12(1H,m),6.83−6.81(3H,m),5.04(2H,s),3.66(3H,s),2.54(3H,s),2.09(3H,s).
本発明化合物74
1H−NMR(CDCl3)δ:7.63(1H,dd,J=7.7,1.5Hz),7.47−7.41(3H,m),7.30−7.26(1H,m),7.07(1H,td,J=7.6,0.9Hz),6.88−6.83(3H,m),6.82−6.79(1H,m),5.04(2H,s),3.66(3H,s),2.53(3H,s),2.09(3H,s).
本発明化合物117
1H−NMR(CDCl3)δ:7.63(1H,dd,J=7.7,1.7Hz),7.51−7.42(3H,m),7.29(1H,dd,J=7.1,2.1Hz),7.08(1H,td,J=7.7,0.8Hz),6.87−6.79(4H,m),5.05(2H,s),3.63(3H,s),2.86(2H,q,J=7.6Hz),2.07(3H,s),1.30(3H,t,J=7.6Hz).
参考製造例21に記載の21Aを0.41g、ベンジルボロン酸ピナコールエステル0.22g、リン酸三カリウム0.43g、水0.40ml、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン付加物0.08gおよびジオキサン4mLの混合物を加熱還流下4時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−ベンジル−2−メチルフェノキシメチル)−3−メトキシフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物90と記す。)0.20gを得た。
1H−NMR(CDCl3)δ:7.45(1H,t,J=8.2Hz),7.29−7.25(2H,m),7.21−7.15(3H,m),7.10−7.03(2H,m),6.91(2H,d,J=7.8Hz),6.78(1H,d,J=8.0Hz),5.22(2H,s),3.91(3H,s),3.86(2H,s),3.56(3H,s),1.96(3H,s).
参考製造例20に記載の20Aを0.39g、2−フェニルエチルボロン酸0.15g、炭酸セシウム0.65g、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン付加物0.08gおよびジメトキシエタン4mLの混合物を加熱還流下4時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(2−フェニルエチル)−2−メチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物91と記す。)0.20gを得た。
1H−NMR(CDCl3)δ:7.45−7.41(3H,m),7.35−7.20(5H,m),7.00−6.96(2H,m),6.79(1H,d,J=8.5Hz),5.03(2H,s),3.64(3H,s),2.93−2.82(4H,m),2.52(3H,s),2.10(3H,s).
参考製造例33に記載の31Aを0.33g、ベンジルブロマイド0.17g、炭酸カリウム0.28gおよびアセトニトリル4mLの混合物を加熱還流下4時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−ベンジルオキシ−2−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物77と記す。)0.20gを得た。
1H−NMR(CDCl3)δ:7.43−7.30(7H,m),7.28−7.24(1H,m),6.79−6.68(3H,m),5.00(2H,s),4.97(2H,s),3.62(3H,s),2.50(3H,s),2.07(3H,s).
参考製造例20に記載の20Aを0.39g、N−メチルアニリン0.11g、tert−ブトキシナトリウム0.29g、2−(ジ−tert−ブチルホスフィノ)ビフェニル0.12g、パラジウムジベンジリデンアセトン錯体0.18gおよびトルエン4mLの混合物を加熱還流下4時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(N−メチルアニリノ)−2−メチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物78と記す。)0.34gを得た。
1H−NMR(CDCl3)δ:7.45−7.40(2H,m),7.29−7.27(1H,m),7.23−7.17(2H,m),6.94−6.90(2H,m),6.82−6.77(4H,m),5.02(2H,s),3.67(3H,s),3.24(3H,s),2.53(3H,s),2.06(3H,s).
以下にその構造式とその1H−NMRデータを記す。
1H−NMR(CDCl3)δ:7.44−7.40(2H,m),7.28(1H,dd,J=6.4,2.7Hz),7.17(2H,t,J=7.6Hz),6.91(2H,t,J=2.7Hz),6.83−6.80(1H,m),6.75−6.72(3H,m),5.02(2H,s),3.70−3.68(5H,m),2.53(3H,s),2.07(3H,s),1.20(3H,t,J=7.0Hz).
参考製造例32に記載の32Aを2.07gおよびメタノール10mLの混合物を0度で攪拌しながら、水素化ホウ素ナトリウム0.76gを加え、室温で4時間攪拌した。反応液に水を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(ヒドロキシ(フェニル)メチル)−2−メチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物80と記す。)1.90gを得た。
1H−NMR(CDCl3)δ:7.43−7.37(4H,m),7.34(2H,dd,J=8.2,6.9Hz),7.27−7.24(2H,m),7.13−7.09(2H,m),6.78(1H,d,J=8.9Hz),5.77(1H,s),5.01(2H,s),3.60(3H,s),2.49(3H,s),2.22(1H,br s),2.05(3H,s).
水素化ナトリウム0.44gおよびテトラヒドロフラン4mlの混合物に本発明化合物80を0.42gを加え、室温で30分攪拌したのち、ヨードメタン0.14gを加え、室温で4時間攪拌した。反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(メトキシ(フェニル)メチル)−2−メチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物81と記す。)0.30gを得た。
1H−NMR(CDCl3)δ:7.43−7.38(2H,m),7.36−7.29(4H,m),7.26−7.22(2H,m),7.09−7.06(2H,m),6.77(1H,t,J=4.4Hz),5.15(1H,s),4.98(2H,s),3.58(3H,s),3.36(3H,s),2.47(3H,s),2.05(3H,s).
参考製造例35に記載の35Aを0.54gおよびトルエン4mlの混合物に塩化チオニル0.28gを加え、60度で2時間攪拌した。反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮し、1−[2−{4−クロロメチル−2−メチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物82と記す。)0.54gを得た。
1H−NMR(CDCl3)δ:7.45−7.39(2H,m),7.29−7.26(1H,m),7.18−7.14(2H,m),6.81(1H,d,J=8.0Hz),5.03(2H,s),4.53(2H,s),3.63(3H,s),2.50(3H,s),2.09(3H,s).
本発明化合物82を0.36g、フェノールを0.09g、炭酸カリウム0.28gおよびアセトニトリル4mLの混合物を加熱還流下4時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−フェノキシメチル−2−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物83と記す。)0.20gを得た。
1H−NMR(CDCl3)δ:7.45−7.39(2H,m),7.31−7.26(3H,m),7.23−7.20(2H,m),6.99−6.94(3H,m),6.85(1H,d,J=8.4Hz),5.03(2H,s),4.94(2H,s),3.62(3H,s),2.50(3H,s),2.11(3H,s).
水素化ナトリウム0.22gおよびテトラヒドロフラン2mlの混合物に参考製造例35に記載の35Aを0.17gを加え、室温で30分攪拌したのち、ブロモエタン0.55gを加え、室温で4時間攪拌した。反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−エトキシメチル−2−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物84と記す。)0.05gを得た。
1H−NMR(CDCl3)δ:7.44−7.38(2H,m),7.28−7.25(1H,m),7.13−7.08(2H,m),6.80(1H,d,J=8.8Hz),5.01(2H,s),4.39(2H,s),3.63(3H,s),3.51(2H,q,J=7.0Hz),2.49(3H,s),2.08(3H,s),1.23(3H,t,J=7.0Hz).
水素化ナトリウム0.44gおよびテトラヒドロフラン2mlの混合物に参考製造例36に記載の36Aを0.35gを加え、室温で30分攪拌したのち、ヨードメタン0.28gを加え、室温で4時間攪拌した。反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(1−メトキシエチル)−2−メチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物85と記す。)0.30gを得た。
1H−NMR(CDCl3)δ:7.44−7.38(2H,m),7.28−7.24(1H,m),7.08−7.04(2H,m),6.81(1H,d,J=9.1Hz),5.01(2H,s),4.20(1H,q,J=6.3Hz),3.63(3H,s),3.19(3H,s),2.50(3H,s),2.09(3H,s),1.40(3H,d,J=6.3Hz).
参考製造例38に記載の38Aを0.33gおよびN,N−ジメチルホルムアミドジメチルアセタール5mLの混合物を90度で4時間過熱攪拌した。冷却後、シリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(N,N−ジメチルアミノメチリデンアミノ)−2−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物86と記す。)0.10gを得た。
1H−NMR(CDCl3)δ:7.47(1H,s),7.43−7.38(2H,m),7.28−7.24(1H,m),6.77−6.70(3H,m),4.98(2H,s),3.63(3H,s),3.00(6H,s),2.50(3H,s),2.05(3H,s).
参考製造例38に記載の38Aを0.33g、p−トルエンスルホン酸・一水和物19gおよびオルトぎ酸トリメチル3mLの混合物を100度で1時間過熱攪拌した。冷却後、減圧下で濃縮し、残渣にN−エチル−N−メチルアミン0.18gおよびジメトキシエタン3mLを加え、80度で1時間過熱攪拌した。反応液を減圧下で濃縮した後、残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(N−エチル−N−メチルアミノメチリデンアミノ)−2−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物87と記す。)0.10gを得た。
1H−NMR(CDCl3)δ:7.50(1H,br s),7.43−7.38(2H,m),7.27−7.24(1H,m),6.76−6.69(3H,m),4.98(2H,s),3.63(3H,s),3.39−3.27(2H,m),2.98(3H,s),2.50(3H,s),2.06(3H,s),1.19(3H,t,J=7.2Hz).
以下にその構造式とその1H−NMRデータを記す。
本発明化合物88
1H−NMR(CDCl3)δ:7.50(1H,br s),7.41−7.37(2H,m),7.27−7.24(1H,m),6.76−6.70(3H,m),4.98(2H,s),3,63(3H,s),3.25−3.18(2H,m),2.98(3H,s),2.50(3H,s),2.06(3H,s),1.61(2H,dd,J=14.4,7.3Hz),0.91(3H,t,J=7.3Hz).
参考製造例20に記載の20Aを0.39g、シクロプロピルボロン酸0.13g、フッ化セシウム0.30g、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン付加物0.08gおよびジオキサン5mLの混合物を加熱還流下4時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−シクロプロピル−2−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物100と記す。)0.20gを得た。
1H−NMR(CDCl3)δ:7.43−7.37(2H,m),7.26−7.24(1H,m),6.87−6.82(2H,m),6.73(1H,d,J=8.0Hz),4.98(2H,s),3.63(3H,s),2.49(3H,s),2.06(3H,s),1.84−1.77(1H,m),0.90−0.84(2H,m),0.62−0.56(2H,m).
以下にその構造式とその1H−NMRデータを記す。
1H−NMR(CDCl3)δ:7.42−7.37(2H,m),7.26−7.23(1H,m),6.73(1H,s),6.63(1H,s),4.98(2H,s),3.64(3H,s),2.50(3H,s),2.37(3H,s),2.02(3H,s),1.79−1.75(1H,m),0.88−0.82(2H,m),0.57−0.52(2H,m).
参考製造例52に記載の52Aを0.50g、N,N−ジメチルホルムアミド0.01gおよびジオキサン5mLの混合物に塩化オキサリル0.18g、N,N−ジメチルホルムアミド0.01gを加え、室温で2時間攪拌した。減圧下で濃縮した後、N−エチル−N−メチルアミン0.12g、トリエチルアミン0.3mLを加えて室温で3時間攪拌した。反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、N−エチル−3,N−ジメチル−4−[2−メトキシ−6−(4−メチル−5−オキソ−4,5−ジヒドロ−テトラゾール−1−イル)−ベンジルオキシ]−ベンズアミド(以下、本発明化合物101と記す。)0.42gを得た。
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.2Hz),7.19−7.12(2H,m),7.11−7.05(2H,m),6.86(1H,d,J=8.5Hz),5.28(2H,s),3.92(3H,s),3.61(3H,s),3.57−3.27(2H,m),2.99(3H,s),1.99(3H,s),1.24−1.09(3H,m).
以下にその構造式とその1H−NMRデータを記す。
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.2Hz),7.20−7.12(2H,m),7.11−7.05(2H,m),6.86(1H,d,J=8.5Hz),5.28(2H,s),3.93(3H,s),3.61(3H,s),3.55−3.19(2H,m),3.00(3H,s),1.99(3H,s),1.61−1.12(4H,m),1.04−0.77(3H,m).
参考製造例21に記載の21Aを0.41g、2−(1−メチルエテニル)−4,4,5,5−テトラメチル−1,3,2−ジオキサボロラン0.17g、リン酸三カリウム0.28g、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン付加物0.08gおよびジオキサン4mLの混合物を加熱還流下4時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−イソプロペニル−2−メチルフェノキシメチル)−3−メトキシフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物103と記す。)0.29gを得た。
1H−NMR(CDCl3)δ:7.43−7.37(2H,m),7.26−7.24(1H,m),6.87−6.82(2H,m),6.73(1H,d,J=8.0Hz),4.98(2H,s),3.63(3H,s),2.49(3H,s),2.06(3H,s),1.84−1.77(1H,m),0.90−0.84(2H,m),0.62−0.56(2H,m).
以下にその構造式とその1H−NMRデータを記す。
1H−NMR(CDCl3)δ:7.45(1H,t,J=8.2Hz),7.12−7.04(4H,m),6.82−6.79(1H,m),6.00−5.97(1H,m),5.24(2H,s),3.91(3H,s),3.58(3H,s),2.36−2.32(2H,m),2.19−2.15(2H,m),1.99(3H,s),1.77−1.72(2H,m),1.66−1.61(2H,m).
トリフェニルプロピルホスホニウムブロミド1.16gおよびテトラヒドロフラン12mLの混合物に氷冷下でn−ブチルリチウム(1.6M)1.9mLを滴下し、0度で1時間攪拌した。参考製造例34に記載の34Aを1.06およびテトラヒドロフラン12mLの混合物を加え、室温で2時間攪拌した。反応液に水を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥した後、減圧下で濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−{2−[4−(1−メチル−1−ブテン−1−イル)−2−メチルフェノキシメチル]−3−メチルフェニル}−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物105と記す。)0.29gを得た。
1H−NMR(CDCl3)δ:7.44−7.38(2H,m),7.28−7.25(1H,m),7.15−7.12(1H,m),6.97−6.93(1H,m),6.82−6.75(1H,m),5.66(0.3H,t,J=7.1Hz),5.39(0.7H,t,J=6.6Hz),5.02(2H,s),3.63−3.62(3H,m),2.51−2.50(3H,m),2.18(0.7H,t,J=7.3Hz),2.09(3H,s),2.00(1.3H,d,J=7.6Hz),1.97(3H,s),1.26(1H,t,J=7.3Hz),0.93(2H,t,J=7.6Hz).
本発明化合物110を0.30gおよびエタノール15mLの混合物にパラジウム−フィブロイン複合体0.03gを加え、水素1気圧の雰囲気下、室温で8時間攪拌した。反応液をセライト(登録商標)でろ過した後、有機層を減圧下で濃縮し、1−{2−[4−(ペンタン−2−イル)−2−メチルフェノキシメチル]−3−メチルフェニル}−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物106と記す。)0.25gを得た。
1H−NMR(CDCl3)δ:7.44−7.38(2H,m),7.28−7.25(1H,m),6.95−6.91(2H,m),6.76(1H,d,J=8.5Hz),4.99(2H,s),3.63(3H,s),2.64−132(1H,m),2.50(3H,s),2.08(3H,s),1.53−1.46(2H,m),1.26−1.23(2H,m),1.19(3H,d,J=6.9Hz),0.86(3H,t,J=7.3Hz).
参考製造例34に記載の34Aを2.82gおよびクロロホルム16mLの混合物にメタクロロ過安息香酸0.66gを加え、室温で72時間攪拌した。反応液に飽和炭酸水素ナトリウム水溶液を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥した後、減圧下で濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−アセチルオキシ−2−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物107と記す。)1.44gを得た。
1H−NMR(CDCl3)δ:7.44−7.38(2H,m),7.27−7.24(1H,m),6.85−6.78(3H,m),4.99(2H,s),3.63(3H,s),2.49(3H,s),2.26(3H,s),2.07(3H,s).
参考製造例33に記載の33Aを0.34g、メチルヒドラジン0.05g、酢酸0.4mLおよびエタノール4mLの混合物を80度で10時間攪拌した。反応液を減圧下で濃縮した後、得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(2−メチルカルボヒドラゾノイル)−2−メチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物108と記す。)0.14gを得た。
1H−NMR(CDCl3)δ:7.50(1H,s),7.42−7.38(4H,m),7.29−7.26(1H,m),6.81(1H,d,J=8.5Hz),5.04(2H,s),3.92−3.90(1H,m),3.62(3H,s),2.95(3H,s),2.50(3H,s),2.09(3H,s).
以下にその構造式とその1H−NMRデータを記す。
1H−NMR(CDCl3)δ:7.45−7.39(3H,m),7.31−7.25(2H,m),7.23(1H,s),6.80(1H,d,J=8.5Hz),5.04(2H,s),3.61(3H,s),2.91(6H,s),2.49(3H,s),2.08(3H,s).
水素化ナトリウム0.04gおよびN,N−ジメチルホルムアミド2mlの混合物に参考製造例36に記載の36Aを0.35gを加え、0度で30分攪拌したのち、ブロモエタン0.55gを加え、室温で2時間攪拌した。反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(1−エトキシエチル)−2−メチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物110と記す。)0.30gを得た。
1H−NMR(CDCl3)δ:7.45−7.39(2H,m),7.28−7.25(1H,m),7.09−7.05(2H,m),6.81(1H,d,J=8.0Hz),5.01(2H,s),4.31(1H,q,J=6.6Hz),3.64(3H,s),3.36−3.29(2H,m),2.50(3H,s),2.09(3H,s),1.41(3H,d,J=6.6Hz),1.17(3H,t,J=7.1Hz).
参考製造例19−2に記載の19−2Aを0.41g、フェノール0.09g、ヨウ化銅0.019g、N−ブチルイミダゾール0.06g、炭酸カリウム0.28gおよびトルエン2mLの混合物を120度で16時間攪拌した。水に反応液を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−フェノキシ−2−メチルフェノキシメチル}−3−クロロフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物157と記す。)0.15gを得た。
1H−NMR(CDCl3)δ:7.64−7.60(1H,m),7.48(1H,t,J=8.0Hz),7.40(1H,dd,J=8.0,1.1Hz),7.32−7.28(2H,m),7.06−7.02(1H,m),6.95−6.93(2H,m),6.82−6.79(3H,m),5.29(2H,s),3.64(3H,s),2.02(3H,s).
以下にその構造式と1H−NMRデータを記す。
1H−NMR(CDCl3)δ:7.46−7.38(3H,m),7.29−7.23(3H,m),7.02−6.97(1H,m),6.84(1H,dd,J=8.7,1.1Hz),6.73(1H,d,J=5.3Hz),6.69(1H,s),5.00(2H,s),3.64(3H,s),2.49(3H,s),2.34(3H,s),2.02(3H,s).
参考製造例57に記載の57Aを0.34g、2−ブロモピリジン0.16g、ヨウ化銅0.019g、N−ブチルイミダゾール0.06g、炭酸カリウム0.28gおよびトルエン2mLの混合物を120度で6時間攪拌した。水に反応液を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(ピリジン−2−イル)−2,5−ジメチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物159と記す。)0.15gを得た。
1H−NMR(CDCl3)δ:8.19−8.14(1H,m),7.66−7.62(1H,m),7.46−7.39(2H,m),7.28−7.25(1H,m),6.94−6.91(1H,m),6.84(1H,d,J=8.4Hz),6.81(1H,s),6.71(1H,s),5.00(2H,s),3.68(3H,s),2.52(3H,s),2.11(3H,s),2.04(3H,s).
以下にその構造式と1H−NMRデータを記す。
1H−NMR(CDCl3)δ:1H−NMR(CDCl3)物),7.66−7.62(1H,m),7.46−7.39(2H,m),7.28−7.25(1H,m),6.94−6.91(1H,m),6.84(1H,d,J=8.4Hz),66.62(1H,dd,J=8.6,0.6Hz),5.03(2H,s),3.67(3H,s),2.53(3H,s),2.13(3H,s),2.03(3H,s).
参考製造例25に記載の)25Aを0.40g、メチルボロン酸0.12g、炭酸セシウム0.98g、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリドジクロロメタン付加物0.08gおよびジメトキシエタン4mLの混合物を加熱還流下4時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{2,4,5−トリメチルフェノキシメチル}−3−メトキシフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(以下、本発明化合物164と記す。)0.06gを得た。
1H−NMR(CDCl3)δ:7.42−7.36(2H,m),7.27−7.22(1H,m),6.86(1H,s),6.63(1H,s),4.98(2H,s),3.62(3H,s),2.49(3H,s),2.21(3H,s),2.15(3H,s),2.03(3H,s).[0306]
製造例31
本発明化合物156を0.42g、ローソン試薬(2,4−Bis(4−methoxyphenyl)−1,3,2,4−dithiadiphosphetane2,4−disulfide)0.49g、トリエチルアミン0.01gおよびトルエン10mLの混合物を加熱還流下8時間攪拌した後、減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−{2−[2,5−ジメチル−4−(3−メチルフェニル)フェノキシメチル]−3−メチルフェニル}−4−メチル−1,4−ジヒドロテトラゾール−5−チオン(以下、本発明化合物166と記す。)を0.30g得た。
1H−NMR(CDCl3)δ:7.50−7.45(2H,m),7.30−7.24(2H,m),7.14−7.05(3H,m),6.97(1H,s),6.69(1H,s),4.95(2H,s),3.94(3H,s),2.55(3H,s),2.38(3H,s),2.24(3H,s),2.08(3H,s).
参考製造例1
無水塩化アルミニウム21.9gを氷冷下、N,N−ジメチルホルムアミド250mLに加え、15分攪拌した。ここにアジ化ナトリウム10.7gを加え、15分攪拌した後、1−クロロ−3−イソシアナト−2−メチルベンゼン25.0gを加え、80℃で5時間加熱した。冷却後、反応液を亜硝酸ナトリウム35g、水2Lおよび氷500gの混合物中に攪拌しながら加えた。混合物を10%塩酸で酸性とした後、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮し、1−(2−メチル−3−クロロフェニル)−1,4−ジヒドロテトラゾール−5−オン(1Aと記す)17.0gを得た。
1H−NMR(CDCl3)δ(ppm):2.32(3H,s),7.28−7.36(2H,m),7.57(1H,dd,J=6.8,2.2Hz),13.08(1H,s).
参考製造例1に記載の1Aを10.00gおよびN,N−ジメチルホルムアミド100mLの混合物に、氷冷下、60%水素化ナトリウム2.30gを加えた。混合物を室温に昇温し、1時間攪拌した。反応混合物に氷冷下、ヨウ化メチル3.2mLを加えた。混合物を室温に昇温し、14時間攪拌した。反応混合物に水を注加し、酢酸エチルで抽出した。有機層を10%塩酸、水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−(2−メチル−3−クロロフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(2Aと記す)1.56gを得た。
1H−NMR(CDCl3)δ(ppm):2.30(3H,s),3.73(3H,s),7.27(1H,d,J=2.7Hz),7.28(1H,d,J=7.1Hz),7.52(1H,dd,J=2.7,6.8Hz).
参考製造例2に記載の2Aを1.56g、1,1’−アゾビス(シクロヘキサン−1−カルボニトリル)0.34g、N−ブロモスクシンイミド1.42gおよびクロロベンゼン30mLの混合物を加熱還流下5時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−(2−ブロモメチル−3−クロロフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(3Aと記す)1.94gを得た。
1H−NMR(CDCl3)δ(ppm):3.76(3H,s),4.69(2H,s),7.35(1H,dd,J=1.2,8.1Hz),7.43(1H,t,J=8.1Hz),7.58(1H,dd,J=1.2,8.1Hz).
3−アミノ−1−メトキシ−2−メチルベンゼン15.0g、トリホスゲン48.7gおよびトルエン350mlの混合物を加熱還流下3時間攪拌した。放冷した反応混合物を減圧下濃縮し、1−メトキシ−3−イソシアナト−2−メチルベンゼン(4Aと記す)17.0gを得た。
1H−NMR(CDCl3)δ(ppm):2.19(3H,s),3.82(3H,s),6.69(1H,d,J=8.2Hz),6.72(1H,dd,J=0.5,8.0Hz),7.09(1H,t,J=8.2Hz).
無水塩化アルミニウム16.0gを氷冷下、N,N−ジメチルホルムアミド180mLに加え、15分攪拌した。ここにアジ化ナトリウム7.8gを加え、15分攪拌した後、参考製造例4に記載の4Aを17.0g加え、80℃で4.5時間加熱した。冷却後、反応液を亜硝酸ナトリウム25g、水2Lおよび氷500gの混合物中に攪拌しながら加えた。混合物を10%塩酸で酸性とした後、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮し、1−(2−メチル−3−メトキシフェニル)−1,4−ジヒドロテトラゾール−5−オン(5Aと記す)16.2gを得た。
1H−NMR(DMSO−d6)δ(ppm):1.99(3H,s),3.87(3H,s),7.01(1H,d,J=8.1Hz),7.17(1H,d,J=8.1Hz).7.36(1H,t,J=8.3Hz),14.63(1H,s).
参考製造例5に記載の5Aを10.00gおよびN,N−ジメチルホルムアミド100mLの混合物に、氷冷下、60%水素化ナトリウム2.47gを加えた。混合物を室温に昇温し、1時間攪拌した。反応混合物に氷冷下、ヨウ化メチル3.5mLを加えた。混合物を室温に昇温し、14時間攪拌した。反応混合物に水を注加し、酢酸エチルで抽出した。有機層を10%塩酸、水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−(2−メチル−3−メトキシフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(6Aと記す)2.19gを得た。
1H−NMR(CDCl3)δ(ppm):2.11(3H,s),3.72(3H,s),3.88(3H,s),6.95(1H,d,J=8.2Hz),6.98(1H,d,J=8.5Hz),7.29(1H,t,J=8.2Hz)
参考製造例6に記載の6Aを2.19g、1,1’−アゾビス(シクロヘキサン−1−カルボニトリル)0.52g、N−ブロモスクシンイミド2.16gおよびクロロベンゼン40mLの混合物を加熱還流下5時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−(2−ブロモメチル−3−メトキシフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(7Aと記す)2.36gを得た。
1H−NMR(CDCl3)δ(ppm):3.74(3H,s),3.96(3H,s),4.93(2H,s),7.02(1H,dd,J=1.0,8.5Hz),7.04(1H,d,J=9.0Hz),7.43(1H,t,J=8.1Hz).
1−ブロモ−2−メチル−3−アミノベンゼン25.0g、トリホスゲン60.0gおよびトルエン400mlの混合物を加熱還流下3時間攪拌した。放冷した反応混合物を減圧下濃縮し、1−ブロモ−3−イソシアナト−2−メチルベンゼン(8Aと記す)30.3gを得た。
1H−NMR(CDCl3)δ(ppm):2.42(3H,s),7.00(1H,dt,J=0.5,8.0Hz),7.05(1H,dd,J=1.7,8.0Hz),7.39(1H,dd,1.5,7.7Hz).
無水塩化アルミニウム19.7gを氷冷下、N,N−ジメチルホルムアミド220mLに加え、15分攪拌した。ここにアジ化ナトリウム9.6gを加え、15分攪拌した後、参考製造例8に記載の8Aを30.3g加え、80℃で5時間加熱した。冷却後、反応液を亜硝酸ナトリウム33g、水2Lおよび氷500gの混合物中に攪拌しながら加えた。混合物を10%塩酸で酸性とした後、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮し、1−(2−メチル−3−ブロモフェニル)−1,4−ジヒドロテトラゾール−5−オン(9Aと記す)31.4gを得た。
1H−NMR(DMSO−d6)δ(ppm):2.22(3H,s),7.34(1H,t,J=7.2Hz),7.49(1H,dd,J=8.2,1.1Hz),7.82(1H,dd,J=8.0,1.0Hz),14.72(1H,s).
参考製造例9に記載の9Aを31.4gおよびN,N−ジメチルホルムアミド250mLの混合物に、氷冷下、60%水素化ナトリウム5.90gを加えた。混合物を室温に昇温し、1時間攪拌した。反応混合物に氷冷下、ヨウ化メチル8.4mLを加えた。混合物を室温に昇温し、14時間攪拌した。反応混合物に水を注加し、酢酸エチルで抽出した。有機層を10%塩酸、水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−(2−メチル−3−ブロモフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(10Aと記す)8.47gを得た。
1H−NMR(CDCl3)δ(ppm):2.33(3H,s),3.73(3H,s),7.21(1H,dt,J=0.5,7.8Hz),7.30(1H,dd,J=1.0,8.0Hz),7.71(1H,dd,J=1.2,8.3Hz).
参考製造例10に記載の10Aを8.47g、1,1’−アゾビス(シクロヘキサン−1−カルボニトリル)1.54g、N−ブロモスクシンイミド6.44gおよびクロロベンゼン125mLの混合物を加熱還流下5時間攪拌した。冷却後、反応液に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−(2−ブロモメチル−3−ブロモフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(11Aと記す)7.52gを得た。
1H−NMR(CDCl3)δ(ppm):3.76(3H,s),4.71(2H,s),7.34(1H,t,J=7.8Hz),7.38(1H,dd,J=8.0,1.7Hz),7.77(1H,dd,J=7.8,1.7Hz).
参考製造例11に記載の11Aを45.0g、ナトリウムメトキシド37.4gおよびテトラヒドロフラン600mLの混合物を室温で3時間攪拌した。反応混合物に飽和重曹水を注加し、酢酸エチルで抽出した。有機層を飽和重曹水で洗浄し、無水硫酸ナトリウムで乾燥した。減圧下に濃縮後、1−(2−メトキシメチル−3−ブロモフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(12Aと記す)36.2gを得た。
1H−NMR(CDCl3)δ(ppm):3.23(3H,s),3.72(3H,s),4.67(2H,s),7.33(1H,t,J=7.8Hz),7.38(1H,dd,J=1.2,8.1Hz),7.76(1H,dd,J=1.5,7.8Hz).
参考製造例12に記載の12Aを36.2g、メチルボロン酸23.2g、フッ化セシウム66.7g、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリド ジクロロメタン付加物10.6gおよびジオキサン500mlの混合物を90℃で5.5時間攪拌した。冷却後、反応混合物をろ過し、ろ液を減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−(2−メトキシメチル−3−メチルフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(13Aと記す)132gを得た。
1H−NMR(CDCl3)δ(ppm):2.48(3H,s),3.23(3H,s),3.72(3H,s),4.42(2H,s),7.21(1H,t,J=5.1Hz),7.35(2H,d,J=4.8Hz).
参考製造例13に記載の13Aを132g、酢酸50mL及び25%臭化水素−酢酸溶液50mLの混合物を65℃で1時間攪拌した。反応混合物に飽和食塩水を注加し、酢酸エチルで抽出した。有機層を飽和重曹水で洗浄し、無水硫酸ナトリウムで乾燥した。減圧下に濃縮後、1−(2−ブロモメチル−3−メチルフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(14Aと記す)を27.9g得た。
1H−NMR(CDCl3)δ(ppm):2.51(3H,s),3.75(3H,s),4.51(2H,s),7.22−7.24(1H,m),7.36−7.39(2H,m).
参考製造例12に記載の12Aを30.1g、シクロプロピルボロン酸12.9g、フッ化セシウム46.2g、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリド ジクロロメタン付加物8.2gおよびジオキサン680mlの混合物を90℃で4時間攪拌した。冷却後、反応混合物をろ過し、ろ液を減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−(2−メトキシメチル−3−シクロプロピルフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(15Aと記す)26.0gを得た。
1H−NMR(CDCl3)δ(ppm):7.36(1H,t,J=8.0Hz),7.20(2H,d,J=8.0Hz),4.64(2H,s),3.72(3H,s),3.24(3H,s),2.20−2.13(1H,m),1.04−1.00(2H,m),0.76−0.72(2H,m).
参考製造例15に記載の15Aを26.0g、酢酸40mLおよび25%臭化水素−酢酸溶液40mLの混合物を65℃で2時間攪拌した。反応混合物に飽和食塩水を注加し、酢酸エチルで抽出した。有機層を飽和重曹水で洗浄し、無水硫酸ナトリウムで乾燥した。減圧下に濃縮後、1−(2−ブロモメチル−3−シクロプロピルフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(16Aと記す)30.8gを得た。
1H−NMR(CDCl3)δ(ppm):7.38(1H,t,J=7.8Hz),7.26−7.22(2H,m),4.77(2H,s),3.75(3H,s),2.16−2.09(1H,m),1.10−1.06(2H,m),0.82−0.78(2H,m).
参考製造例12に記載の12Aを29.8g、トリブチルビニルスズ35.2g、テトラキストリフェニルホスフィンパラジウム11.6gおよびトルエン500mLの混合物を加熱還流下14時間攪拌した。冷却後、反応液に飽和塩化アンモニウム水溶液を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−(2−メトキシメチル−3−エテニルフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(17Aと記す)を19.7g得た。
1H−NMR(CDCl3)δ(ppm):7.67(1H,dd,J=7.8,1.3Hz),7.44(1H,t,J=7.8Hz),7.29(1H,dd,J=7.8,1.3Hz),7.11(1H,dd,J=17.4,11.1Hz),5.72(1H,dd,J=17.4,1.3Hz),5.44(1H,dd,J=11.1,1.3Hz),4.45(2H,s),3.72(3H,s),3.23(3H,s).
参考製造例17に記載の17Aを19.7g、パラジウム−フィブロイン複合体3.02gおよびメタノール1Lの混合物を水素雰囲気下、室温で11時間攪拌した。反応混合物をろ過し、ろ液を減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−(2−メトキシメチル−3−エチルフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(18Aと記す)を19.3g得た。
1H−NMR(CDCl3)δ(ppm):7.42−7.38(2H,m),7.23−7.20(1H,m),4.44(2H,s),3.72(3H,s),3.22(3H,s),2.82(2H,q,J=7.6Hz),1.27(3H,t,J=7.6Hz).
参考製造例18に記載の18Aを19.3g、酢酸40mLおよび25%臭化水素−酢酸溶液40mLの混合物を65℃で1.5時間攪拌した。反応混合物に飽和食塩水を注加し、酢酸エチルで抽出した。有機層を飽和重曹水で洗浄し、無水硫酸ナトリウムで乾燥した。減圧下に濃縮後、1−(2−ブロモメチル−3−エチルフェニル)−4−メチル−1,4−ジヒドロテトラゾール−5−オン(19−1Aと記す)を23.3g得た。
1H−NMR(CDCl3)δ(ppm):7.44−7.37(2H,m),7.23(1H,dd,J=7.1,2.0Hz),4.56(2H,s),3.75(3H,s),2.85(2H,q,J=7.6Hz),1.33(3H,t,J=7.6Hz).
参考製造例3に記載の3Aを9.11g、4−ブロモ−2−メチルフェノール5.61g、炭酸カリウム8.29gおよびアセトニトリル120mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−2−メチルフェノキシメチル)−3−クロロフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(19−2Aと記す)11.8gを得た。
1H−NMR(CDCl3)δ:7.65(1H,d,J=8.0Hz),7.51(1H,t,J=8.0Hz),7.45−7.42(1H,m),7.30−7.24(2H,m),6.75(1H,d,J=8.2Hz),5.31(2H,s),3.65(3H,s),2.03(3H,s).
参考製造例14に記載の14Aを23.5g、4−ブロモ−2−メチルフェノール15.5g、炭酸カリウム22.9gおよびアセトニトリル330mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−2−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(20Aと記す)30.1gを得た。
1H−NMR(CDCl3)δ:7.46−7.39(2H,m),7.29−7.26(1H,m),7.25−7.21(2H,m),6.70(1H,d,J=9.4Hz),5.00(2H,s),3.63(3H,s),2.49(3H,s),2.06(3H,s).
参考製造例7に記載の7Aを8.97g、4−ブロモ−2−メチルフェノール5.61g、炭酸カリウム8.29gおよびアセトニトリル120mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣を得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−ブロモ−2−メチルフェノキシメチル)−3−メトキシフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(21Aと記す)12.3gを得た。
1H−NMR(CDCl3)δ:7.46(1H,t,J=8.2Hz),7.20−7.15(2H,m),7.10−7.04(2H,m),6.73(1H,d,J=8.2Hz),5.22(2H,s),3.91(3H,s),3.59(3H,s),1.96(3H,s).
参考製造例19に記載の19−1Aを8.91g、4−ブロモ−2−メチルフェノール5.61g、炭酸カリウム8.29gおよびアセトニトリル120mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−2−メチルフェノキシメチル)−3−エチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(22Aと記す)12.2gを得た。
1H−NMR(CDCl3)δ:7.50−7.43(2H,m),7.30−7.26(1H,m),7.25−7.21(2H,m),6.71(1H,d,J=8.7Hz),5.02(2H,s),3.60(3H,s),2.83(2H,q,J=7.6Hz),2.04(3H,s),1.27(3H,t,J=7.6Hz).
参考製造例16に記載の16Aを9.27g、4−ブロモ−2−メチルフェノール5.61g、炭酸カリウム8.29gおよびアセトニトリル120mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−2−メチルフェノキシメチル)−3−シクロプロピルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(23Aと記す)12.8gを得た。
1H−NMR(CDCl3)δ:7.44(1H,t,J=7.8Hz),7.26−7.24(4H,m),6.75(1H,d,J=8.2Hz),5.23(2H,s),3.62(3H,s),2.12−2.07(1H,m),2.05(3H,s),1.02−0.96(2H,m),0.79−0.73(2H,m).
参考製造例14に記載の14Aを5.66g、4−ブロモ−3−メチルフェノール3.74g、炭酸カリウム5.53gおよびアセトニトリル80mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−3−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(24Aと記す)7.42gを得た。
1H−NMR(CDCl3)δ:7.47(1H,t,J=8.2Hz),7.21−7.17(2H,m),7.10−7.05(2H,m),6.74(1H,d,J=8.5Hz),5.23(2H,s),3.93(3H,s),3.60(3H,s),1.96(3H,s).
参考製造例14に記載の14Aを4.25g、4−ブロモ−2,5−ジメチルフェノール3.02g、炭酸カリウム4.15gおよびアセトニトリル60mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−ブロモ−2,5−ジメチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(25Aと記す)5.82gを得た。
1H−NMR(CDCl3)δ:7.45−7.37(2H,m),7.28−7.25(1H,m),7.23(1H,s),6.68(1H,s),4.99(2H,s),3.64(3H,s),2.49(3H,s),2.33(3H,s),2.01(3H,s).
参考製造例19に記載の19−1Aを2.97g、4−ブロモ−2−フルオロフェノール1.91g、炭酸カリウム2.76gおよびアセトニトリル40mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−2−フルオロフェノキシメチル)−3−エチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(26Aと記す)3.79gを得た。
1H−NMR(CDCl3)δ:7.50−7.42(2H,m),7.29(1H,dd,J=7.4,1.7Hz),7.21(1H,dd,J=10.4,2.4Hz),7.18−7.14(1H,m),6.83(1H,t,J=8.7Hz),5.12(2H,s),3.66(3H,s),2.84(2H,q,J=7.6Hz),1.29(3H,t,J=7.6Hz).
参考製造例14に記載の14Aを2.83g、4−ブロモ−3−メトキシフェノール2.03g、炭酸カリウム2.76gおよびアセトニトリル40mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−3−メトキシフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(27Aと記す)3.92gを得た。
1H−NMR(CDCl3)δ:7.44−7.39(3H,m),7.30−7.26(1H,m),6.45−6.38(2H,m),5.01(2H,s),3.84(3H,s),3.63(3H,s),2.50(3H,s).
参考製造例21に記載の21Aを4.05g、ビス(ピナコラト)ジボロン2.79g、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリド ジクロロメタン付加物0.25g、酢酸カリウム2.94gおよびジメチルスルホキシド30mLの混合物を窒素雰囲気下、80度で加熱しながら8時間攪拌した。放冷した反応混合物に水を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(4,4,5,5−テトラメチル−[1,3,2]ジオキサボロラン−2−イル)−2−メチルフェノキシメチル}−3−メトキシフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(28Aと記す)2.92gを得た。
1H−NMR(CDCl3)δ:7.58(1H,dd,J=8.2,1.4Hz),7.51(1H,s),7.45(1H,t,J=8.3Hz),7.08−7.04(2H,m),6.87(1H,d,J=8.2Hz),5.28(2H,s),3.91(3H,s),3.57(3H,s),1.97(3H,s),1.31(12H,s).
参考製造例20に記載の20Aを3.89g、ビス(ピナコラト)ジボロン2.79g、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリド ジクロロメタン付加物0.25g、酢酸カリウム2.94gおよびジメチルスルホキシド30mLの混合物を窒素雰囲気下、80度で加熱しながら8時間攪拌した。放冷した反応混合物に水を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(4,4,5,5−テトラメチル−[1,3,2]ジオキサボロラン−2−イル)−2−メチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(29Aと記す)3.44gを得た。
1H−NMR(CDCl3)δ:7.62(1H,dd,J=8.0,1.4Hz),7.57(1H,s),7.44−7.38(2H,m),7.29−7.25(1H,m),6.85(1H,d,J=8.2Hz),5.05(2H,s),3.62(3H,s),2.49(3H,s),2.08(3H,s),1.33(12H,s).
参考製造例22に記載の22Aを4.03g、ビス(ピナコラト)ジボロン2.79g、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリド ジクロロメタン付加物0.25g、酢酸カリウム2.94gおよびジメチルスルホキシド30mLの混合物を窒素雰囲気下、80度で加熱しながら8時間攪拌した。放冷した反応混合物に水を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(4,4,5,5−テトラメチル−[1,3,2]ジオキサボロラン−2−イル)−2−メチルフェノキシメチル}−3−エチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(30Aと記す)3.87gを得た。
1H−NMR(CDCl3)δ:7.63(1H,dd,J=8.1,1.3Hz),7.56(1H,s),7.49−7.43(2H,m),7.29−7.25(1H,m),6.86(1H,d,J=8.2Hz),5.07(2H,s),3.59(3H,s),2.83(2H,q,J=7.6Hz),2.07(3H,s),1.33(12H,s),1.26(3H,t,J=7.6Hz).
参考製造例29に記載の29Aを13.1g、水酸化ナトリウム8.40g、テトラヒドロフラン60mlおよび水30mLの混合物を氷零下0度で攪拌しながら、30%過酸化水素水17.0mlを加え、0度で1時間攪拌した。室温まで昇温しさらに1時間攪拌したのち、反応混合物に飽和チオ硫酸ナトリウム水溶液を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−ヒドロキシ−2−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(31Aと記す)5.92gを得た。
1H−NMR(CDCl3)δ:7.30(1H,t,J=7.9Hz),7.06(1H,d,J=7.9Hz),7.02(1H,d,J=7.8Hz),6.90(1H,d,J=8.2Hz),6.66−6.62(2H,m),4.97(2H,s),4.48(1H,br s),2.41(3H,s),2.15(3H,s),1.59(3H,s).
参考製造例14に記載の14Aを2.83g、4−ヒドロキシ−3−メチルベンゾフェノン2.12g、炭酸カリウム2.76gおよびアセトニトリル40mLの混合物を80度で過熱しながら2時間攪拌した。反応混合物に水を注加し、酢酸エチルで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−ベンゾイル−2−メチル−フェノキシメチル)−3−メチル−フェニル]−4−メチル−1,4−ジヒドロ−テトラゾール−5−オン(32Aと記す)4.08gを得た。
1H−NMR(CDCl3)δ:7.75(2H,dd,J=8.2,1.0Hz),7.68−7.63(2H,m),7.60−7.54(1H,m),7.51−7.40(4H,m),7.30(1H,dd,J=7.1,2.1Hz),6.89(1H,d,J=8.2Hz),5.13(2H,s),3.64(3H,s),2.52(3H,s),2.13(3H,s).
参考製造例14に記載の14Aを2.83g、4−ヒドロキシ−3−メチル−ベンズアルデヒド1.36g、炭酸カリウム2.76gおよびアセトニトリル40mLの混合物を加熱還流下4時間攪拌した。室温まで冷却し、反応混合物を濾過し、濾液を濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、3−メチル−4−{[2−メチル−6−(4−メチル−1,4−ジヒドロテトラゾール−5−オン−1−イル)フェニル]メチルオキシ}ベンズアルデヒド(33Aと記す)2.96gを得た。
1H−NMR(CDCl3)δ:9.86(1H,s),7.70(1H,dd,J=8.2,2.1Hz),7.68−7.66(1H,m),7.48−7.41(2H,m),7.30(1H,dd,J=7.4,1.7Hz),6.96(1H,d,J=8.2Hz),5.14(2H,s),3.63(3H,s),2.51(3H,s),2.14(3H,s).
参考製造例14に記載の14Aを5.66g、4’−ヒドロキシ−3’−メチル−アセトフェノン3.00g、炭酸カリウム5.53gおよびアセトニトリル40mLの混合物を加熱還流下4時間攪拌した。室温まで冷却し、反応混合物を濾過し、濾液を濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−{2−(2−メチル−4−アセチル−フェノキシメチル)−3−メチル−フェニル}−4−メチル−1,4−ジヒドロテトラゾール−5−オン(34Aと記す)4.73gを得た。
1H−NMR(CDCl3)δ:7.79(1H,dd,J=8.54,2.24Hz),7.75(1H,d,J=1.46Hz),7.46−7.40(2H,m),7.29(1H,dd,J=7.32,1.95Hz),6.86(1H,d,J=8.54Hz),5.11(2H,s),3.62(3H,s),2.54(3H,s),2.50(3H,s),2.12(3H,s).
参考製造例33に記載の33Aを1.35gおよびメタノール8mLの混合物を0度で攪拌しながら、水素化ホウ素ナトリウム0.30gを加え、室温で4時間攪拌した。反応液に水を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−ヒドロキシメチル−2−メチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(35Aと記す)1.25gを得た。
1H−NMR(CDCl3)δ:7.44−7.39(2H,m),7.27−7.25(1H,m),7.14−7.10(2H,m),6.83−6.79(1H,m),5.03(2H,s),4.58(2H,d,J=5.7Hz),3.63(3H,s),2.51(3H,s),2.08(3H,s).
参考製造例34に記載の34Aを0.71gおよびメタノール4mLの混合物を0度で攪拌しながら、水素化ホウ素ナトリウム0.15gを加え、室温で4時間攪拌した。反応液に水を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(1−ヒドロキシエチル)−2−メチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(36Aと記す)0.45gを得た。
1H−NMR(CDCl3)δ:7.44−7.39(2H,m),7.27−7.24(1H,m),7.14−7.12(2H,m),6.82−6.78(1H,m),5.02(2H,s),4.84−4.79(1H,m),3.64(3H,s),2.51(3H,s),2.09(3H,s),1.73(1H,d,J=3.4Hz),1.47(3H,d,J=6.4Hz).
参考製造例14に記載の14Aを8.49g、4−ニトロ−2−メチルフェノール4.59g、炭酸カリウム2.76gおよびアセトニトリル120mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ニトロ−2−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(37Aと記す)10.4gを得た。
1H−NMR(CDCl3)δ:7.47(1H,s),7.43−7.38(2H,m),7.27−7.25(1H,m),6.76−6.71(2H,m),4.98(2H,s),3.63(3H,s),2.50(3H,s),2.06(3H,s).
参考製造例37に記載の37Aを7.11g、電解鉄6.00g、酢酸80mlおよび水20mLの混合物を60度で2時間過熱攪拌した。減圧下で濃縮したのち、残渣に飽和炭酸水素ナトリウム水溶液を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−アミノ−2−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(38Aと記す)10.4gを得た。
1H−NMR(CDCl3)δ:7.42−7.36(2H,m),7.26−7.23(1H,m),6.65(1H,d,J=8.4Hz),6.49(1H,d,J=2.5Hz),6.45(1H,dd,J=8.5,2.5Hz),4.93(2H,s),3.64(3H,s),3.39(2H,br s),2.49(3H,s),2.02(3H,s).
参考製造例30に記載の30Aを2.25g、水酸化ナトリウム1.40g、テトラヒドロフラン10mlおよび水5mLの混合物を氷零下0度で攪拌しながら、30%過酸化水素水2.83mlを加え、0度で1時間攪拌した。室温まで昇温しさらに4時間攪拌したのち、反応混合物に飽和チオ硫酸ナトリウム水溶液を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−ヒドロキシ−2−メチルフェノキシメチル)−3−エチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(39Aと記す)1.47gを得た。
1H−NMR(CDCl3)δ:7.49−7.41(2H,m),7.28−7.24(1H,m),6.68(1H,d,J=8.5Hz),6.61(1H,d,J=3.0Hz),6.56(1H,dd,J=8.5,3.0Hz),4.97(2H,s),4.58(1H,br s),3.61(3H,s),2.84(2H,q,J=7.6Hz),2.03(3H,s),1.27(3H,t,J=7.6Hz).
参考製造例14に記載の14Aを1.42g、4−ブロモ−2−エチルフェノール1.00g、炭酸カリウム1.38gおよびアセトニトリル20mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えてクロロホルムで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−2−エチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(40Aと記す)1.90gを得た。
1H−NMR(CDCl3)δ:7.46−7.39(2H,m),7.30−7.22(3H,m),6.73(1H,d,J=9.4Hz),4.99(2H,s),3.64(3H,s),2.51−2.43(5H,m),1.08(3H,t,J=7.6Hz).
参考製造例14に記載の14Aを1.42g、4−ブロモ−3−シアノフェノール1.00g、炭酸カリウム1.38gおよびアセトニトリル20mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えてクロロホルムで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−3−シアノフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(41Aと記す)1.94gを得た。
1H−NMR(CDCl3)δ:7.53(1H,d,J=8.9Hz),7.46(1H,t,J=7.6Hz),7.43−7.39(1H,m),7.30(1H,dd,J=7.6,1.1Hz),7.14(1H,d,J=3.0Hz),6.97(1H,dd,J=8.9,3.0Hz),5.01(2H,s),3.67(3H,s),2.48(3H,s).
参考製造例14に記載の14Aを1.35g、4−ブロモ−3,5−ジフルオロフェノール1.00g、炭酸カリウム1.32gおよびアセトニトリル19mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えてクロロホルムで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−3,5−ジフルオロフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(42Aと記す)1.75gを得た。
1H−NMR(CDCl3)δ:7.47−7.40(2H,m),7.29(1H,dd,J=7.6,1.4Hz),6.55−6.49(2H,m),4.98(2H,s),3.67(3H,s),2.47(3H,s).
参考製造例14に記載の14Aを2.83g、4−ブロモ−3−トリフルオロメチルフェノール2.41g、炭酸カリウム2.76gおよびアセトニトリル40mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えてクロロホルムで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−3−トリフルオロメチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(43Aと記す)4.20gを得た。
1H−NMR(CDCl3)δ:7.59(1H,d,J=8.7Hz),7.50−7.42(2H,m),7.32(1H,dd,J=7.4,1.5Hz),7.21(1H,d,J=3.0Hz),6.92(1H,dd,J=8.7,3.0Hz),5.06(2H,s),3.67(3H,s),2.51(3H,s).
参考製造例14に記載の14Aを2.83g、4−ブロモ−2−トリフルオロメチルフェノール2.41g、炭酸カリウム2.76gおよびアセトニトリル40mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えてクロロホルムで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−2−トリフルオロメチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(44Aと記す)4.05gを得た。
1H−NMR(CDCl3)δ:7.67−7.64(1H,m),7.58−7.53(1H,m),7.47−7.38(2H,m),7.29(1H,dd,J=7.4,1.3Hz),6.86(1H,d,J=8.7Hz),5.13(2H,s),3.68(3H,s),2.49(3H,s).
3−エチルフェノール7.33gおよびクロロホルム600mLの混合物を氷零下0度で攪拌しながら、N−ブロモスクシンイミド10.7gを加えた。室温まで昇温しさらに2時間攪拌したのち、減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、4−ブロモ−3‐エチルフェノール(45Aと記す)7.25gを得た。
1H−NMR(CDCl3)δ:7.37(1H,d,J=8.2Hz),6.90(1H,d,J=2.1Hz),6.69(1H,dd,J=8.2,2.1Hz),5.48(1H,s),2.61(2H,q,J=7.6Hz),1.24(3H,t,J=7.6Hz).
3−tert−ブチルフェノール9.01gおよびクロロホルム600mLの混合物を氷零下0度で攪拌しながら、N−ブロモスクシンイミド10.7gを加えた。室温まで昇温しさらに2時間攪拌したのち、減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、4−ブロモ−3−tert−ブチルフェノール(46Aと記す)7.59gを得た。
1H−NMR(CDCl3)δ:7.39(1H,d,J=8.5Hz),7.09(1H,d,J=2.3Hz),6.88(1H,dd,J=8.5,2.3Hz),5.48(1H,s),1.32(9H,s).
参考製造例14に記載の14Aを2.83g、参考製造例45に記載の45Aを2.01g、炭酸カリウム2.76gおよびアセトニトリル40mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えてクロロホルムで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−3−エチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(47Aと記す)3.77gを得た。
1H−NMR(CDCl3)δ:7.44−7.36(3H,m),7.28(1H,dd,J=7.1,2.1Hz),6.70−6.66(2H,m),5.14(2H,s),3.68(3H,s),2.57(2H,q,J=7.6Hz),2.55(3H,s),1.20(3H,t,J=7.6Hz).
参考製造例14に記載の14Aを2.83g、参考製造例46に記載の46Aを2.29g、炭酸カリウム2.76gおよびアセトニトリル40mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えてクロロホルムで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−3−tert−ブチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(48Aと記す)4.00gを得た。
1H−NMR(CDCl3)δ:7.46−7.40(3H,m),7.33−7.30(1H,m),6.89(1H,dd,J=8.4,2.3Hz),6.84(1H,d,J=2.3Hz),5.20(2H,s),3.71(3H,s),2.58(3H,s),1.28(9H,s).
参考製造例14に記載の14Aを2.83g、4−ブロモ−2,3−ジメチルフェノール2.01g、炭酸カリウム2.76gおよびアセトニトリル40mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−ブロモ−2,3−ジメチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(49Aと記す)1.08gを得た。
1H−NMR(CDCl3)δ:7.41−7.38(2H,m),7.22−7.17(2H,m),6.76(1H,d,J=8.2Hz),5.09(2H,s),3.63(3H,s),2.63(3H,s),2.14(3H,s),1.86(3H,s).
参考製造例19に記載の19−1Aを2.23g、4−ブロモ−2,5−ジメチルフェノール1.51g、炭酸カリウム2.07gおよびアセトニトリル30mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−ブロモ−2,5−ジメチルフェノキシメチル)−3−エチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(50Aと記す)3.01gを得た。
1H−NMR(CDCl3)δ:7.49−7.43(2H,m),7.29−7.26(1H,m),7.23(1H,s),6.70(1H,s),5.00(2H,s),3.61(3H,s),2.83(2H,q,J=7.6Hz),2.34(3H,s),2.00(3H,s),1.27(3H,t,J=7.6Hz).
参考製造例7に記載の7Aを2.24g、4−ブロモ−2,5−ジメチルフェノール1.51g、炭酸カリウム2.07gおよびアセトニトリル30mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−ブロモ−2,5−ジメチルフェノキシメチル)−3−メトキシフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(51Aと記す)3.02gを得た。
1H−NMR(CDCl3)δ:7.46(1H,t,J=8.2Hz),7.18(1H,s),7.09−7.05(2H,m),6.74(1H,s),5.21(2H,s),3.93(3H,s),3.60(3H,s),2.31(3H,s),1.92(3H,s).
本発明化合物93を1.0g、水酸化リチウム0.19g、フッ化セシウム0.30g、テトラヒドロフラン5mL、メタノール5mLおよび水5mLの混合物を室温で8時間攪拌した。減圧下で濃縮した後、12N塩酸でpHを7以下に調整して、析出した個体を濾取し、3−メチル−4−[2−メトキシ−6−(4−メチル−5−オキソ−4,5−ジヒドロ−テトラゾール−1−イル)−ベンジルオキシ]−安息香酸(52Aと記す。)0.64gを得た。
1H−NMR(CDCl3)δ:7.90(1H,dd,J=8.6,2.3Hz),7.83−7.80(1H,m),7.48(1H,t,J=8.2Hz),7.13−7.06(2H,m),6.92(1H,d,J=8.6Hz),5.35(2H,s),3.94(3H,s),3.60(3H,s),2.02(3H,s).
参考製造例14に記載の14Aを2.83g、4−ブロモ−2,6−ジフルオロフェノール2.09g、炭酸カリウム2.76gおよびアセトニトリル40mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−ブロモ−2,6−ジフルオロフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(53Aと記す)4.26gを得た。
1H−NMR(CDCl3)δ:7.45−7.40(2H,m),7.25−7.21(1H,m),7.03(2H,d,J=7.7Hz),5.12(2H,s),3.72(3H,s),2.60(3H,s).
参考製造例14に記載の14Aを2.83g、4−ブロモ−2,3,5,6−テトラフルオロフェノール2.45g、炭酸カリウム2.76gおよびアセトニトリル40mLの混合物を80度で4時間過熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−ブロモ−2,3,5,6−テトラフルオロフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(54Aと記す)4.48gを得た。
1H−NMR(CDCl3)δ:7.47−7.41(2H,m),7.24−7.21(1H,m),5.25(2H,s),3.72(3H,s),2.62(3H,s).
参考製造例14に記載のA14を2.83g、4−ブロモ−5−フルオロ−2−メチルフェノール2.05g、炭酸カリウム2.76gおよびアセトニトリル40mLの混合物を80度で4時間加熱攪拌した。反応混合物に水を加えて酢酸エチルで抽出した。有機層を飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下に濃縮した。得られた残渣をヘキサンとメチル−tert−ブチルケトンで洗浄し、1−[2−(4−ブロモ−5−フルオロ−2−メチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(55Aと記す)3.98gを得た。
1H−NMR(CDCl3)δ:2.02(3H,s),2.49(3H,s),3.65(3H,s),4.98(2H,s),6.65(1H,d,J=10.2Hz),7.23(1H,dd,J=7.9,0.7Hz),7.29(1H,dd,J=7.5,1.7Hz),7.41(1H,dd,J=8.4,1.8Hz),7.41(1H,t,J=7.5Hz).
参考製造例25に記載の25Aを8.06g、ビス(ピナコラト)ジボロン5.59g、[1,1’−ビス(ジフェニルホスフィノ)フェロセン]パラジウム(II)ジクロリド ジクロロメタン付加物0.49g、酢酸カリウム5.89gおよびジメチルスルホキシド60mLの混合物を窒素雰囲気下、80度で加熱しながら8時間攪拌した。放冷した反応混合物に水を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−{4−(4,4,5,5−テトラメチル−[1,3,2]ジオキサボロラン−2−イル)−2,5−ジメチルフェノキシメチル}−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(56Aと記す)8.47gを得た。
1H−NMR(CDCl3)δ:7.51(1H,s),7.44−7.38(2H,m),7.29−7.25(1H,m),6.65(1H,s),5.03(2H,s),3.63(3H,s),2.51(3H,s),2.48(3H,s),2.03(3H,s),1.32(12H,s).
参考製造例56に記載の56Aを5.40g、水酸化ナトリウム3.36g、テトラヒドロフラン24mlおよび水12mLの混合物を氷零下0度で攪拌しながら、30%過酸化水素水6.8mlを加え、0度で1時間攪拌した。室温まで昇温しさらに4時間攪拌したのち、反応混合物に飽和チオ硫酸ナトリウム水溶液を注加し、クロロホルムで抽出した。有機層を水および飽和食塩水で洗浄し、無水硫酸マグネシウムで乾燥した後、減圧下濃縮した。得られた残渣をシリカゲルカラムクロマトグラフィーに付し、1−[2−(4−ヒドロキシ−2,5−ジメチルフェノキシメチル)−3−メチルフェニル]−4−メチル−1,4−ジヒドロテトラゾール−5−オン(57Aと記す)3.01gを得た。
1H−NMR(CDCl3)δ:7.44−7.37(2H,m),7.26−7.23(1H,m),6.58(1H,s),6.54(1H,s),4.95(2H,s),4.34(1H,s),3.65(3H,s),2.50(3H,s),2.19(3H,s),2.00(3H,s).
化合物Q1A−001~Q11L−633はそれぞれ、下記で示されるテトラゾリノン化合物である。
〔式中、Yは置換基番号1~633に各々対応する置換基〕
[117;2,3,5,6−テトラメチルフェニル基]、[118;2,3,4,5,6−ペンタメチルフェニル基]、[119;2−エチルフェニル基]、[120;3−エチルフェニル基]、[121;4−エチルフェニル基]、[122;2,4−ジエチルフェニル基]、[123;2,6−ジエチルフェニル基]、[124;3,5−ジエチルフェニル基]、[125;2,4,6−トリエチルフェニル基]、[126;2−n−プロピルフェニル基]、[127;3−n−プロピルフェニル基]、[128;4−n−プロピルフェニル基]、[129;2−イソプロピルフェニル基]、[130;3−イソプロピルフェニル基]、[131;4−イソプロピルフェニル基]、[132;2,4−ジイソプロピルフェニル基]、[133;2,6−ジイソプロピルフェニル基]、[134;3,5−ジイソプロピルフェニル基]、[135;2−s−ブチルフェニル基]、[136;3−s−ブチルフェニル基]、[137;4−s−ブチルフェニル基]、[138;2−t−ブチルフェニル基]、[139;3−t−ブチルフェニル基]、[140;4−t−ブチルフェニル基]、[141;4−n−ブチルフェニル基]、[142;4−n−ノニルフェニル基]、[143;2−メチル−4−t−ブチルフェニル基]、[144;2−メチル−6−t−ブチルフェニル基]、[145;2−メチル−4−イソプロピルフェニル基]
[291;4−クロロ−3−トリフルオロメトキシフェニル基]、[292;5−クロロ−3−トリフルオロメトキシフェニル基]、[293;6−クロロ−3−トリフルオロメトキシフェニル基]、[294;2−クロロ−4−トリフルオロメトキシフェニル基]、[295;3−クロロ−4−トリフルオロメトキシフェニル基]、[296;3,4−ジクロロ−2−トリフルオロメトキシフェニル基]、[297;3,5−ジクロロ−2−トリフルオロメトキシフェニル基]、[298;3,6−ジクロロ−2−トリフルオロメトキシフェニル基]、[299;4,5−ジクロロ−2−トリフルオロメトキシフェニル基]、[300;4,6−ジクロロ−2−トリフルオロメトキシフェニル基]、[301;5,6−ジクロロ−2−トリフルオロメトキシフェニル基]、[302;2,4−ジクロロ−3−トリフルオロメトキシフェニル基]、[303;2,5−ジクロロ−3−トリフルオロメトキシフェニル基]、[304;2,6−ジクロロ−3−トリフルオロメトキシフェニル基]、[305;4,5−ジクロロ−3−トリフルオロメトキシフェニル基]、[306;4,6−ジクロロ−3−トリフルオロメトキシフェニル基]、[307;5,6−ジクロロ−3−トリフルオロメトキシフェニル基]、[308;2,3−ジクロロ−4−トリフルオロメトキシフェニル基]、[309;2,5−ジクロロ−4−トリフルオロメトキシフェニル基]、[310;2,6−ジクロロ−4−トリフルオロメトキシフェニル基]、[311;3,5−ジクロロ−4−トリフルオロメトキシフェニル基]、[312;3,6−ジクロロ−4−トリフルオロメトキシフェニル基]、[313;N,N−ジメチルアミノ基]、[314;N,N−ジエチルアミノ基]、[315;N−メチル−N−エチルアミノ基]、[316;2−(N−メチルアミノカルボニル)フェニル基]、[317;3−(N−メチルアミノカルボニル)フェニル基]、[318;4−(N−メチルアミノカルボニル)フェニル基]、[319;2−(N,N−ジメチルアミノカルボニル)フェニル基]
化合物EB1A−001~EG1N−342はそれぞれ、下記式で表される化合物である。
製剤例1
本発明化合物1~166のいずれか1化合物50部、リグニンスルホン酸カルシウム3部、ラウリル硫酸マグネシウム2部及び合成含水酸化珪素45部をよく粉砕混合することにより、製剤を得る。
本発明化合物1~166いずれか1化合物20部とソルビタントリオレエ−ト1.5部とを、ポリビニルアルコ−ル2部を含む水溶液28.5部と混合し、湿式粉砕法で微粉砕した後、この中に、キサンタンガム0.05部及びアルミニウムマグネシウムシリケ−ト0.1部を含む水溶液40部を加え、さらにプロピレングリコ−ル10部を加えて攪拌混合し、製剤を得る。
本発明化合物1~166のいずれか1化合物2部、カオリンクレ−88部及びタルク10部をよく粉砕混合することにより、製剤を得る。
本発明化合物1~166のいずれか1化合物5部、ポリオキシエチレンスチリルフェニルエ−テル14部、ドデシルベンゼンスルホン酸カルシウム6部及びキシレン75部をよく混合することにより、製剤を得る。
本発明化合物1~166のいずれか1化合物2部、合成含水酸化珪素1部、リグニンスルホン酸カルシウム2部、ベントナイト30部及びカオリンクレ−65部をよく粉砕混合した後、水を加えてよく練り合せ、造粒乾燥することにより、製剤を得る。
本発明化合物1~166のいずれか1化合物10部;ポリオキシエチレンアルキルエ−テルサルフェ−トアンモニウム塩50部を含むホワイトカ−ボン35部;及び水55部を混合し、湿式粉砕法で微粉砕することにより、製剤を得る。
なお防除効果は、調査時の供試植物上の病斑の面積を目視観察し、本発明化合物を処理した植物の病斑の面積と、無処理の植物の病斑の面積とを比較することにより評価した。
プラスチックポットに土壌を詰め、そこにイネ(品種;日本晴)を播種し、温室内で20日間生育させた。その後、本発明化合物9、20、4、22、23、24、25、29、32、33、89、61、62、63、64、65、66、68、100、101、106、110、79、80、85、121,122、123、132、136、137、139、140、143、144および91のいずれか一つの化合物を、所定濃度(500ppm)含有するように調整した界面活性剤等を含む水希釈液を、上記イネの葉面に充分付着するように茎葉散布した。散布後、植物を風乾し、昼間24℃、夜間20℃多湿下で、前記散布処理をしたイネと、イネいもち病菌(Magnaporthe grisea)に罹病したイネ苗(品種;日本晴)とを接触させながら6日間置いた後、病斑面積を調査した。その結果、本発明化合物9、20、4、22、23、24、25、29、32、33、89、61、62、63、64、65、66、68、100、101、106、110、79、80、85、121,122、123、132、136、137、139、140、143、144または91を処理した植物における病斑面積はいずれも、無処理の植物における病斑面積の30%以下であった。
プラスチックポットに土壌を詰め、そこにコムギ(品種;シロガネ)を播種し、温室内で9日間生育させた。本発明化合物9、14、5、46、23、26、29、33、36、44、89、75、66、101、102、79、85、53、115、122、136、140、143、144、145および91のいずれか一つの化合物を、所定濃度(500ppm)含有するように調整した界面活性剤等を含む水希釈液を、上記コムギの葉面に充分付着するように茎葉散布した。散布後植物を風乾し、20℃、照明下で5日間栽培した後、コムギのさび病菌(Puccinia recondita)の胞子をふりかけ接種した。接種後植物を23℃、暗黒多湿下に1日間置いた後、20℃、照明下で8日間栽培し、病斑面積を調査した。その結果、本発明化合物9、14、5、46、23、26、29、33、36、44、89、75、66、101、102、79、85、53、115、122、136、140、143、144、145または91を処理した植物における病斑面積はいずれも、無処理の植物における病斑面積の30%以下であった。
プラスチックポットに土壌を詰め、そこにオオムギ(品種;ニシノホシ)を播種し、温室で7日間生育させた。本発明化合物7、8、9、10、11、12、13、14、15、16、17、18、19、20、41、2、3、4、5、40、46、6、21、22、23、24、25、26、28、29、30、31、32、33、34、36、37、38、39、44、42、43、45、59、89、60、61、62、63、64、65、75、76、66、67、68、69、70、72、73、74、100、98、99、93、94、95、101、102、103、104、105、106、90、110、96、78、77、107、79、80、85、81、83、91、97、113、115、116、117、118、120、121、122、123、126、131、132、133、136、137、138、139、140、141、142、144、145、146、147、148、149、150、151、152、153、154、156、157、158、159、160および88のいずれか一つの化合物を、所定濃度(500ppm)含有するように調整した界面活性剤等を含む水希釈液を、上記オオムギの葉面に充分付着するように茎葉散布した。散布後植物を風乾し、2日後にオオムギ網斑病菌(Pyrenophora teres)胞子の水懸濁液を噴霧接種した。接種後植物を昼間23℃、夜間20℃の温室内で多湿下に3日間置き、次に温室内で7日間栽培した後、病斑面積を調査した。その結果、本発明化合物7、8、9、10、11、12、13、14、15、16、17、18、19、20、41、2、3、4、5、40、46、6、21、22、23、24、25、26、28、29、30、31、32、33、34、36、37、38、39、44、42、43、45、59、89、60、61、62、63、64、65、75、76、66、67、68、69、70、72、73、74、100、98、99、93、94、95、101、102、103、104、105、106、90、110、96、78、77、107、79、80、85、81、83、91、97、113、115、116、117、118、120、121、122、123、126、131、132、133、136、137、138、139、140、141、142、144、145、146、147、148、149、150、151、152、153、154、156、157、158、159、160または88を処理した植物における病斑面積はいずれも、無処理の植物における病斑面積の30%以下であった。
プラスチックポットに土壌を詰め、インゲン(品種;長鶉菜豆)を播種し、温室内で8日間生育させた。本発明化合物7、8、9、10、11、12、14、15、16、17、18、19、20、2、3、4、40、46、6、21、22、23、24、29、30、32、33、34、35、1、39、44、43、89、61、62、63、64、65、75、76、68、69、92、100、93、94、95、102、103、104、105、106、90、110、78、77、80、85、91、87、122、123、131、136、140、141、143、144および88のいずれか一つの化合物を、所定濃度(500ppm)含有するように調整した界面活性剤等を含む水希釈液を、上記インゲン葉面に充分付着するように茎葉散布した。散布後植物を風乾し、インゲン菌核病菌(Sclerotinia sclerotiorum)の菌糸含有PDA培地をインゲン葉面上に置いた。接種後全てのインゲンは夜間のみ多湿下におき、接種4日後に病斑面積を調査した。その結果、本発明化合物7、8、9、10、11、12、14、15、16、17、18、19、20、2、3、4、40、46、6、21、22、23、24、29、30、32、33、34、35、1、39、44、43、89、61、62、63、64、65、75、76、68、69、92、100、93、94、95、102、103、104、105、106、90、110、78、77、80、85、91、87、122、123、131、136、140、141、143、144または88を処理した植物における病斑面積はいずれも、無処理の植物における病斑面積の30%以下であった。
プラスチックポットに土壌を詰め、そこにコムギ(品種;アポジー)を播種し、温室内で10日間生育させた。本発明化合物7、8、9、10、11、12、13、14、15、19、20、41、2、4、5、46、6、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、1、36、39、44、42、43、61、62、63、64、65、75、76、66、67、89、60、68、69、70、72、73、74、100、93、101、102、103、104、105、106、90、110、78、77、、80、85、91、87、53、54、116、121、122、123、132、136、137、138、139、140、143、144、145、149、151、152、153、154および88のいずれか一つの化合物を、所定濃度(500ppm)含有するように調整した界面活性剤等を含む水希釈液を、上記コムギの葉面に充分付着するように茎葉散布した。散布後植物を風乾し、4日後にコムギ葉枯病菌(Septoria tritici)胞子の水懸濁液を噴霧接種した。接種後植物を18℃多湿下に3日間置き、次に照明下に14日から18日間置いた後、病斑面積を調査した。その結果、本発明化合物7、8、9、10、11、12、13、14、15、19、20、41、2、4、5、46、6、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、1、36、39、44、42、43、61、62、63、64、65、75、76、66、67、89、60、68、69、70、72、73、74、100、93、101、102、103、104、105、106、90、110、78、77、80、85、91、87、53、54、116、121、122、123、132、136、137、138、139、140、143、144、145、149、151、152、153、154または88を処理した植物における病斑面積はいずれも、無処理の植物における病斑面積の30%以下であった。
プラスチックポットに土壌を詰め、そこにキュウリ(品種;相模半白)を播種し、温室内で12日間生育させた。本発明化合物7、8、9、10、11、12、13、14、15、16、17、18、19、20、41、2、3、4、5、40、46、6、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、1、36、37、39、44、43、89、60、61、62、63、64、65、75、76、66、67、68、69、70、72、73、74、92、100、93、94、95、101、103、104、105、106、90、110、78、77、80、85、91、87、47、48、49、50、51、52、54、58、56、113、116、117、118、120、121、122、123、125、127、131、132、133、136、137、138、139、140、141、142、143、144、145、146、147、148、149、150、151、152、154、156、157、158、159、160および88のいずれか一つの化合物を、所定濃度(500ppm)含有するように調整した界面活性剤等を含む水希釈液を、上記キュウリ葉面に充分付着するように茎葉散布した。散布後植物を風乾し、キュウリうどんこ病菌(Sphaerotheca fuliginea)胞子をふりかけ接種した。植物を昼間24℃、夜間20℃の温室で8日間栽培した後、病斑面積を調査した。その結果、本発明化合物7、8、9、10、11、12、13、14、15、16、17、18、19、20、41、2、3、4、5、40、46、6、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、1、36、37、39、44、43、89、60、61、62、63、64、65、75、76、66、67、68、69、70、72、73、74、92、100、93、94、95、101、103、104、105、106、90、110、78、77、80、85、91、87、47、48、49、50、51、52、54、58、56、113、116、117、118、120、121、122、123、125、127、131、132、133、136、137、138、139、140、141、142、143、144、145、146、147、148、149、150、151、152、154、156、157、158、159、160または88を処理した植物における病斑面積はいずれも、無処理の植物における病斑面積の30%以下であった。
プラスチックポットに土壌を詰め、そこにダイズ(品種;黒千石)を播種し、温室内で13日間生育させた。本発明化合物7、9、10、16、18、19、20、4、5、46、22、23、24、25、27、29、30、31、32、33、34、35、89、60、61、62、63、64、66、68、69、100、106、110、79、80、84、39、44、42、43、53、113、122、127、129、131、132、135、136、137、138、139、141および85のいずれか一つの化合物を、所定濃度(200ppm)含有するように調整した界面活性剤等を含む水希釈液を、上記ダイズの葉面に充分付着するように茎葉散布した。散布後植物を風乾し、2日後にダイズさび病菌(Phakopsora pachyrhizi)胞子の水懸濁液を噴霧接種した。接種後植物を昼間23℃、夜間20℃の温室内で多湿下に3日間置き、次に温室内で14日間栽培した後、病斑面積を調査した。その結果、本発明化合物7、9、10、16、18、19、20、4、5、46、22、23、24、25、27、29、30、31、32、33、34、35、89、60、61、62、63、64、66、68、69、100、106、110、79、80、84、39、44、42、43、53、113、122、127、129、131、132、135、136、137、138、139、141または85を処理した植物における病斑面積はいずれも、無処理の植物における病斑面積の30%以下であった。
プラスチックポットに土壌を詰め、そこにオオムギ(品種;ニシノホシ)を播種し、温室で7日間生育させた。本発明化合物7、8、9、10、11、12、13、14、15、16、17、18、19、20、41、2、3、4、5、40、46、6、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、1、36、37、89、60、61、62、63、64、65、75、76、66、67、68、69、70、71、72、73、92、100、99、93、94、101、102、103、104、106、108、109、90、110、96、78、77、79、80、84、85、81、83、39、44、42、43、47、49、50、51、52、53、54、58、56、113、116、117、118、119、120、121、122、123、126、129、131、132、133、135、136、137、139、140、141、および91のいずれか一つの化合物を、所定濃度(200ppm)含有するように調整した界面活性剤等を含む水希釈液を、上記オオムギの葉面に充分付着するように茎葉散布した。散布後植物を風乾し、2日後にオオムギ雲形病菌(Rhynchosporium secalis)胞子の水懸濁液を噴霧接種した。接種後植物を昼間23℃、夜間20℃の温室内で多湿下に3日間置き、次に温室内で7日間栽培した後、病斑面積を調査した。その結果、本発明化合物7、8、9、10、11、12、13、14、15、16、17、18、19、20、41、2、3、4、5、40、46、6、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、1、36、37、89、60、61、62、63、64、65、75、76、66、67、68、69、70、71、72、73、92、100、99、93、94、101、102、103、104、106、108、109、90、110、96、78、77、79、80、84、85、81、83、39、44、42、43、47、49、50、51、52、53、54、58、56、113、116、117、118、119、120、121、122、123、126、129、131、132、133、135、136、137、139、140、141、または91を処理した植物における病斑面積はいずれも、無処理の植物における病斑面積の30%以下であった。
プラスチックポットに土壌を詰め、そこにキュウリ(品種;相模半白)を播種し、温室内で19日間生育させた。本発明化合物7、8、9、10、12、16、17、18、19、2、3、21、23、24、25、26、27、29、89、60、61、63、64、65、75、67、100、94、95、103、104、105、106、90、110、78、77、131、132、136、138、139、140、142、143、144および145のいずれか一つの化合物を、所定濃度(200ppm)含有するように調整した界面活性剤等を含む水希釈液を、上記キュウリ葉面に充分付着するように茎葉散布した。散布後植物を風乾し、1日後にキュウリ褐斑病菌(Corynespora cassiicola)胞子の水懸濁液を噴霧接種した。接種後は昼間24℃、夜間20℃の多湿下で7日間栽培した後、病斑面積を調査した。その結果、本発明化合物7、8、9、10、12、16、17、18、19、2、3、21、23、24、25、26、27、29、89、60、61、63、64、65、75、67、100、94、95、103、104、105、106、90、110、78、77、131、132、136、138、139、140、142、143、144または145を処理した植物における病斑面積はいずれも、無処理の植物における病斑面積の30%以下であった。
プラスチックポットに土壌を詰め、そこにキュウリ(品種;相模半白)を播種し、温室内で19日間生育させた。本発明化合物7、8、9、10、14、16、17、18、19、2、3、4、5、46、6、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、39、42、43、89、61、62、63、64、65、75、66、67、68、69、70、73、74、100、93、104、105、106、90、110、96、78、77、79、80、84、81、51、53、58、56、117、120、122、123、131、133および91のいずれか一つの化合物を、所定濃度(200ppm)含有するように調整した界面活性剤等を含む水希釈液を、上記キュウリ葉面に充分付着するように茎葉散布した。散布後植物を風乾し、1日後にキュウリ炭そ病菌(Colletotrichum lagenarium)胞子の水懸濁液を噴霧接種した。接種後はじめは23℃、多湿下に1日間置き、続いて昼間24℃、夜間20℃の温室で6日間栽培した後、病斑面積を調査した。その結果、本発明化合物7、8、9、10、14、16、17、18、19、2、3、4、5、46、6、21、22、23、24、25、26、27、28、29、30、31、32、33、34、35、36、37、39、42、43、89、61、62、63、64、65、75、66、67、68、69、70、73、74、100、93、104、105、106、90、110、96、78、77、79、80、84、81、51、53、58、56、117、120、122、123、131、133または91を処理した植物における病斑面積はいずれも、無処理の植物における病斑面積の30%以下であった。
本発明化合物24、29、79、90および93のいずれか一つの化合物を、所定濃度(500ppm)含有するように調整した界面活性剤等を含む水希釈液(試験用薬液)を調製した。
ポリエチレンカップで第1本葉が展開するまで育成したキュウリ(品種;相模半白節成)葉上に、ワタアブラムシ(Aphis gossypii)30頭(成虫、幼虫を含む)を放し、翌日上記試験用薬液20mLを散布した。6日後に生存虫数を数え、次式により防除価を求めた。
防除価(%)={1−(Cb×Tai)/(Cai×Tb)}×100
なお、式中の文字は以下の意味を表す。
Cb:無処理区の薬液散布前の虫数
Cai:無処理区の生存虫数
Tb:処理区の薬液散布前の虫数
Tai:処理区の生存虫数
その結果、本発明化合物24、29、79、90および93はいずれも、防除価90%以上を示した。
本発明化合物20、29および79のいずれか一つの化合物を、所定濃度(500ppm)含有するように調整した界面活性剤等を含む水希釈液を試験用薬液とした。
上記試験用薬液0.7mLをイオン交換水100mLに加え有効成分濃度を3.5ppmに調製した。該液中にアカイエカ(Culex pipiens pallens)終令幼虫20頭を放ち、8日後に死亡虫数を数えた。
死亡率は下式により求めた。
死亡率(%)=(死亡虫数/供試虫数)×100
その結果、本発明化合物20、29および79はいずれも死亡率100%を示した。
プラスチックポットに土壌を詰め、そこにキュウリ(品種;相模半白)を播種し、温室内で12日間生育させた。1−{2−(4−メチルフェノキシメチル)フェニル}−4−メチル−1,4−ジヒドロテトラゾール−5−オンを、所定濃度(500ppm)含有するように調整した界面活性剤等を含む水希釈液を、上記キュウリ葉面に充分付着するように茎葉散布した。散布後植物を風乾し、キュウリうどんこ病菌(Sphaerotheca fuliginea)胞子をふりかけ接種した。植物を昼間24℃、夜間20℃の温室で8日間栽培した後、病斑面積を調査した。その結果、1−{2−(4−メチルフェノキシメチル)フェニル}−4−メチル−1,4−ジヒドロテトラゾール−5−オンを処理した植物における病斑面積は、無処理の植物における病斑面積の70%以上であった。
Claims (8)
- 式(1)
〔式中、
R1、R2、R3およびR11は各々独立して、群P1から選ばれる1以上の原子もしくは基を有していてもよいC1−C6アルキル基、ハロゲン原子、水素原子、1以上のハロゲン原子を有していてもよいC1−C6アルコキシ基、シアノ基、ニトロ基、1以上のハロゲン原子を有していてもよいC2−C6アルケニル基、1以上のハロゲン原子を有していてもよいC2−C6アルキニル基、1以上のハロゲン原子を有していてもよいC1−C8アルキルアミノ基、1以上のハロゲン原子を有していてもよいC1−C6アルキルチオ基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルフィニル基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルホニル基、ペンタフルオロスルファニル基、C3−C9トリアルキルシリル基、C2−C6アルキルカルボニル基、C2−C6アルコキシカルボニル基またはC1−C6アルキル基を有していてもよいアミノカルボニル基を表し;
R4およびR5は各々独立して、水素原子、ハロゲン原子またはC1−C3アルキル基を表し;
R6は1以上のハロゲン原子を有していてもよいC1−C6アルキル基、1以上のハロゲン原子を有していてもよいC1−C6アルコキシ基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルキル基、ハロゲン原子、1以上のハロゲン原子を有していてもよいC2−C6アルケニル基、シアノ基、1以上のハロゲン原子を有していてもよいC1−C6アルキルチオ基、1以上のハロゲン原子を有していてもよいC2−C6アルキニル基、ニトロ基、1以上のC1−C6アルキル基を有していてもよいアミノカルボニル基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルキルオキシ基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルキルチオ基、1以上のハロゲン原子を有していてもよいC3−C6アルケニルオキシ基、1以上のハロゲン原子を有していてもよいC3−C6アルキニルオキシ基、1以上のハロゲン原子を有していてもよいC3−C6アルケニルチオ基、1以上のハロゲン原子を有していてもよいC3−C6アルキニルチオ基、C2−C6アルコキシカルボニル基、ヒドロキシ基、スルファニル基、1以上のハロゲン原子を有していてもよいC1−C8アルキルアミノ基、ペンタフルオロスルファニル基、C3−C9トリアルキルシリル基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルホニル基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルフィニル基、C2−C6アルキルカルボニル基、C2−C5アルコキシアルキル基またはC2−C5アルキルチオアルキル基を表し;
R7、R8およびR9は各々独立して、水素原子、ハロゲン原子、1以上のハロゲン原子を有していてもよいC1−C3アルキル基、1以上のハロゲン原子を有していてもよいC2−C3アルケニル基、または1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基を表し;
R10は1以上のハロゲン原子を有していてもよいC1−C3アルキル基、1以上のハロゲン原子を有していてもよいC2−C3アルケニル基、1以上のハロゲン原子を有していてもよいC2−C3アルキニル基または1以上のハロゲン原子を有していてもよいC3−C5シクロアルキル基を表し;
R12は群P2から選ばれる1以上の原子もしくは基を有していてもよいC6−C16アリール基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC6−C16アリールオキシ基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC6−C16アリールチオ基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC7−C18アラルキル基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC7−C18アラルキルオキシ基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC7−C16アリールオキシアルキル基、群P2から選ばれる1以上の原子もしくは基を有していてもよいアニリノ基、C2−C5アルキルチオアルキル基、1以上のC1−C3アルコキシ基および/もしくはハロゲン原子を有していてもよいC1−C6アルキル基、1以上のハロゲン原子を有していてもよいC1−C6アルコキシ基、1以上のハロゲン原子を有していてもよいC2−C6アルケニル基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルキル基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルケニル基、1以上のハロゲン原子を有していてもよいC1−C8アルキルアミノ基、群P2から選ばれる1以上の原子もしくは基を有していてもよいC2−C9ヘテロアリールオキシ基(但し、ヘテロアリール部分は5員環、6員環、5員環と5員環との縮合環、5員環と6員環との縮合環または6員環と6員環との縮合環を表す)、R13R14N−N=CH−、R13R14N−CH=N−、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルフィニル基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルホニル基、ペンタフルオロスルファニル基、C2−C6アルコキシカルボニル基、C2−C6アルキルカルボニルオキシ基、C1−C6アルキル基を有していてもよいアミノカルボニル基またはC3−C9トリアルキルシリル基を表し;
R13およびR14は各々独立して、水素原子またはC1−C3アルキル基を表し;Xは酸素原子または硫黄原子を表す。
群P1:ハロゲン原子、シアノ基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルキル基、1以上のハロゲン原子を有していてもよいC1−C4アルコキシ基および1以上のハロゲン原子を有していてもよいC1−C4アルキルチオ基からなる群。
群P2:1以上のハロゲン原子を有していてもよいC1−C6アルキル基、ハロゲン原子、シアノ基、ヒドロキシ基、1以上のハロゲン原子を有していてもよいC3−C6シクロアルキル基、1以上のハロゲン原子を有していてもよいC1−C6アルコキシ基、1以上のハロゲン原子を有していてもよいC1−C6アルキルチオ基、1以上のハロゲン原子を有していてもよいC2−C6アルケニル基、1以上のハロゲン原子を有していてもよいC2−C6アルキニル基、1以上のハロゲン原子を有していてもよいC1−C8アルキルアミノ基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルフィニル基、1以上のハロゲン原子を有していてもよいC1−C6アルキルスルホニル基、ペンタフルオロスルファニル基、C2−C6アルコキシカルボニル基、C2−C6アルキルカルボニル基、C2−C6アルキルカルボニルオキシ基、C2−C6アルキルカルボニルアミノ基、C1−C6アルキル基を有していてもよいアミノカルボニル基およびC3−C9トリアルキルシリル基からなる群。〕
で示されるテトラゾリノン化合物。 - R1が、1以上のハロゲン原子を有していてもよいC1−C3アルキル基、水素原子、1以上のハロゲン原子を有していてもよいC2−C3アルキニル基、1以上のハロゲン原子を有していてもよいC3−C5シクロアルキル基または1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基であり;
R2およびR3が、水素原子、ハロゲン原子、1以上のハロゲン原子を有していてもよいC1−C4アルキル基、1以上のハロゲン原子を有していてもよいC1−C4アルコキシ基またはシアノ基であり;
R4、R5、R7、R8、R9およびR11が、水素原子であり;
R6が、1以上のハロゲン原子を有していてもよいC1−C4アルキル基、ハロゲン原子、1以上のハロゲン原子を有していてもよいC1−C4アルコキシ基、1以上のハロゲン原子を有していてもよいC3−C5シクロアルキル基、1以上のハロゲン原子を有していてもよいC2−C4アルケニル基または、C2−C4アルキニル基であり;
R10が、メチル基であり;
Xが、酸素原子である、請求の範囲1に記載のテトラゾリノン化合物。 - R12が下記群P3から選ばれる1以上の原子もしくは基を有していてもよいフェニル基である請求の範囲1または2に記載のテトラゾリノン化合物。
群P3:1以上のハロゲン原子を有していてもよいC1−C3アルキル基、ハロゲン原子、シアノ基、1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基、1以上のハロゲン原子を有していてもよいC3−C4シクロアルキル基および1以上のハロゲン原子を有していてもよいC1−C3アルキルチオ基からなる群。 - R12が下記群P3から選ばれる1以上の原子もしくは基を有していてもよいフェノキシ基である請求項1または2に記載のテトラゾリノン化合物。
群P3:1以上のハロゲン原子を有していてもよいC1−C3アルキル基、ハロゲン原子、シアノ基、1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基、1以上のハロゲン原子を有していてもよいC3−C4シクロアルキル基および1以上のハロゲン原子を有していてもよいC1−C3アルキルチオ基からなる群。 - R1が、1以上のハロゲン原子を有していてもよいC1−C3アルキル基、水素原子、または1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基であり;
R2が、水素原子、ハロゲン原子、1以上のハロゲン原子を有していてもよいC1−C4アルキル基、1以上のハロゲン原子を有していてもよいC1−C4アルコキシ基またはシアノ基であり;
R3が、水素原子、ハロゲン原子、1以上のハロゲン原子を有していてもよいC1−C4アルキル基であり;
R4、R5、R7、R8、R9およびR11が、水素原子であり;
R6が、1以上のハロゲン原子を有していてもよいC1−C4アルキル基、ハロゲン原子、1以上のハロゲン原子を有していてもよいC1−C4アルコキシ基または1以上のハロゲン原子を有していてもよいC3−C5シクロアルキル基であり;
R10が、メチル基であり;
Xが、酸素原子であり;
R12が下記群P3から選ばれる1以上の原子もしくは基を有していてもよいフェニル基または下記群P3から選ばれる1以上の原子もしくは基を有していてもよいフェノキシ基である請求の範囲1または2に記載のテトラゾリノン化合物。
群P3:1以上のハロゲン原子を有していてもよいC1−C3アルキル基、ハロゲン原子、シアノ基および1以上のハロゲン原子を有していてもよいC1−C3アルコキシ基からなる群。 - 請求の範囲1~5のいずれかに記載のテトラゾリノン化合物を含有する有害生物防除剤。
- 請求の範囲1~5のいずれかに記載のテトラゾリノン化合物の有効量を植物または土壌に処理することを含む有害生物の防除方法。
- 有害生物を防除するための請求の範囲1~5のいずれかに記載のテトラゾリノン化合物の使用。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201480040770.7A CN105392779B (zh) | 2013-07-31 | 2014-07-29 | 四唑啉酮化合物及其用途 |
| JP2015529639A JP6428618B2 (ja) | 2013-07-31 | 2014-07-29 | テトラゾリノン化合物及びその用途 |
| EP14832810.7A EP3029030B1 (en) | 2013-07-31 | 2014-07-29 | Tetrazolinone compound, and use therefor |
| BR112016002063-4A BR112016002063B1 (pt) | 2013-07-31 | 2014-07-29 | composto de tetrazolinona, seu uso do mesmo, agente e método de controle de peste |
| US14/907,699 US9512090B2 (en) | 2013-07-31 | 2014-07-29 | Tetrazolinone compound and use thereof |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2013-158726 | 2013-07-31 | ||
| JP2013158726 | 2013-07-31 | ||
| JP2013225026 | 2013-10-30 | ||
| JP2013-225026 | 2013-10-30 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2015016373A1 true WO2015016373A1 (ja) | 2015-02-05 |
Family
ID=52431892
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2014/070414 WO2015016373A1 (ja) | 2013-07-31 | 2014-07-29 | テトラゾリノン化合物及びその用途 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US9512090B2 (ja) |
| EP (1) | EP3029030B1 (ja) |
| JP (1) | JP6428618B2 (ja) |
| CN (1) | CN105392779B (ja) |
| BR (1) | BR112016002063B1 (ja) |
| WO (1) | WO2015016373A1 (ja) |
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015147332A1 (ja) * | 2014-03-28 | 2015-10-01 | 住友化学株式会社 | テトラゾリノン化合物及びその用途 |
| WO2015147337A1 (ja) * | 2014-03-28 | 2015-10-01 | 住友化学株式会社 | テトラゾリノン化合物及びその用途 |
| US20160081339A1 (en) * | 2013-04-26 | 2016-03-24 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and use of same |
| US9560850B2 (en) | 2012-12-27 | 2017-02-07 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and use thereof |
| US9675072B2 (en) | 2013-05-29 | 2017-06-13 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and application of same |
| US9730448B2 (en) | 2013-08-29 | 2017-08-15 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and use of same |
| US9888688B2 (en) | 2013-07-12 | 2018-02-13 | Sumitomo Chemical Company, Limited | Tetrazolinone compounds and applications thereof |
| US10070646B2 (en) | 2014-03-28 | 2018-09-11 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and application thereof |
| US10077254B2 (en) | 2013-10-17 | 2018-09-18 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and use thereof |
| US10091998B2 (en) | 2013-10-28 | 2018-10-09 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and use thereof |
| US11889833B2 (en) | 2022-01-14 | 2024-02-06 | Enko Chem, Inc. | Protoporphyrinogen oxidase inhibitors |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015060461A1 (ja) * | 2013-10-25 | 2015-04-30 | 住友化学株式会社 | テトラゾリノン化合物及びその用途 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1996036229A1 (en) * | 1995-05-17 | 1996-11-21 | E.I. Du Pont De Nemours And Company | Fungicidal cyclic amides |
| JPH09208565A (ja) * | 1996-02-07 | 1997-08-12 | Sumitomo Chem Co Ltd | テトラゾリノン誘導体、その用途およびその製造中間体 |
| JPH11501015A (ja) * | 1995-02-24 | 1999-01-26 | イー・アイ・デユポン・ドウ・ヌムール・アンド・カンパニー | 殺菌・殺カビ性環式アミド |
| JP2001506984A (ja) * | 1996-11-26 | 2001-05-29 | イー・アイ・デユポン・ドウ・ヌムール・アンド・カンパニー | メチル置換された殺菌・殺カビ剤および殺節足動物剤 |
| WO2014104384A1 (ja) * | 2012-12-27 | 2014-07-03 | 住友化学株式会社 | テトラゾリノン化合物及びその用途 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1241116A (zh) * | 1996-11-26 | 2000-01-12 | 纳幕尔杜邦公司 | 甲基取代的杀真菌剂和杀节肢动物剂 |
| WO1999046246A1 (de) * | 1998-03-09 | 1999-09-16 | Basf Aktiengesellschaft | Hetarylsubstituierte benzylphenylether, verfahren zu ihrer herstellung und ihre verwendung zur bekämpfung von schadpilzen und tierischen schädlingen |
| WO2013092224A1 (en) * | 2011-12-21 | 2013-06-27 | Basf Se | Use of strobilurin type compounds for combating phytopathogenic fungi resistant to qo inhibitors |
| JP6075182B2 (ja) | 2012-04-27 | 2017-02-08 | 住友化学株式会社 | テトラゾリノン化合物及びその用途 |
| JP6107377B2 (ja) | 2012-04-27 | 2017-04-05 | 住友化学株式会社 | テトラゾリノン化合物及びその用途 |
| JP6142752B2 (ja) | 2012-09-28 | 2017-06-07 | 住友化学株式会社 | テトラゾリノン化合物及びその用途 |
| US9867372B2 (en) * | 2013-04-26 | 2018-01-16 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and use of same |
| US9521848B2 (en) | 2013-07-31 | 2016-12-20 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and use therefor |
-
2014
- 2014-07-29 US US14/907,699 patent/US9512090B2/en active Active
- 2014-07-29 CN CN201480040770.7A patent/CN105392779B/zh active Active
- 2014-07-29 WO PCT/JP2014/070414 patent/WO2015016373A1/ja active Application Filing
- 2014-07-29 JP JP2015529639A patent/JP6428618B2/ja active Active
- 2014-07-29 EP EP14832810.7A patent/EP3029030B1/en active Active
- 2014-07-29 BR BR112016002063-4A patent/BR112016002063B1/pt active IP Right Grant
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH11501015A (ja) * | 1995-02-24 | 1999-01-26 | イー・アイ・デユポン・ドウ・ヌムール・アンド・カンパニー | 殺菌・殺カビ性環式アミド |
| WO1996036229A1 (en) * | 1995-05-17 | 1996-11-21 | E.I. Du Pont De Nemours And Company | Fungicidal cyclic amides |
| JPH09208565A (ja) * | 1996-02-07 | 1997-08-12 | Sumitomo Chem Co Ltd | テトラゾリノン誘導体、その用途およびその製造中間体 |
| JP2001506984A (ja) * | 1996-11-26 | 2001-05-29 | イー・アイ・デユポン・ドウ・ヌムール・アンド・カンパニー | メチル置換された殺菌・殺カビ剤および殺節足動物剤 |
| WO2014104384A1 (ja) * | 2012-12-27 | 2014-07-03 | 住友化学株式会社 | テトラゾリノン化合物及びその用途 |
Non-Patent Citations (2)
| Title |
|---|
| MOLANDER ET AL., ACC. CHEM. RES., vol. 40, 2007, pages 275 |
| N. MIYAURA; A. SUZUKI, CHEM. REV., vol. 95, 1995, pages 2457 |
Cited By (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US9560850B2 (en) | 2012-12-27 | 2017-02-07 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and use thereof |
| US20160081339A1 (en) * | 2013-04-26 | 2016-03-24 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and use of same |
| US9867372B2 (en) * | 2013-04-26 | 2018-01-16 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and use of same |
| US9675072B2 (en) | 2013-05-29 | 2017-06-13 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and application of same |
| US9888688B2 (en) | 2013-07-12 | 2018-02-13 | Sumitomo Chemical Company, Limited | Tetrazolinone compounds and applications thereof |
| US9730448B2 (en) | 2013-08-29 | 2017-08-15 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and use of same |
| US10077254B2 (en) | 2013-10-17 | 2018-09-18 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and use thereof |
| US10091998B2 (en) | 2013-10-28 | 2018-10-09 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and use thereof |
| US9822095B2 (en) | 2014-03-28 | 2017-11-21 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and application thereof |
| US9826741B2 (en) | 2014-03-28 | 2017-11-28 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and application thereof |
| CN106132938A (zh) * | 2014-03-28 | 2016-11-16 | 住友化学株式会社 | 四唑啉酮化合物及其应用 |
| WO2015147337A1 (ja) * | 2014-03-28 | 2015-10-01 | 住友化学株式会社 | テトラゾリノン化合物及びその用途 |
| US10070646B2 (en) | 2014-03-28 | 2018-09-11 | Sumitomo Chemical Company, Limited | Tetrazolinone compound and application thereof |
| WO2015147332A1 (ja) * | 2014-03-28 | 2015-10-01 | 住友化学株式会社 | テトラゾリノン化合物及びその用途 |
| CN106132938B (zh) * | 2014-03-28 | 2019-05-17 | 住友化学株式会社 | 四唑啉酮化合物及其应用 |
| US11889833B2 (en) | 2022-01-14 | 2024-02-06 | Enko Chem, Inc. | Protoporphyrinogen oxidase inhibitors |
Also Published As
| Publication number | Publication date |
|---|---|
| BR112016002063B1 (pt) | 2021-02-09 |
| JPWO2015016373A1 (ja) | 2017-03-02 |
| BR112016002063A2 (pt) | 2017-08-01 |
| US20160159755A1 (en) | 2016-06-09 |
| JP6428618B2 (ja) | 2018-11-28 |
| EP3029030A1 (en) | 2016-06-08 |
| EP3029030B1 (en) | 2019-09-04 |
| CN105392779B (zh) | 2018-01-19 |
| CN105392779A (zh) | 2016-03-09 |
| EP3029030A4 (en) | 2017-03-08 |
| US9512090B2 (en) | 2016-12-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6428618B2 (ja) | テトラゾリノン化合物及びその用途 | |
| JP6323450B2 (ja) | テトラゾリノン化合物及びその用途 | |
| JP6369466B2 (ja) | テトラゾリノン化合物及びその用途 | |
| JP6237646B2 (ja) | テトラゾリノン化合物及びその用途 | |
| JP6390617B2 (ja) | テトラゾリノン化合物及びその用途 | |
| US9781933B2 (en) | Tetrazolinone compound and use thereof | |
| BR112015012209B1 (pt) | Composto de tetrazolinona, seu uso, agente e método para o controle de pragas | |
| WO2014104268A1 (ja) | テトラゾリノン化合物及びその用途 | |
| WO2014104382A1 (ja) | テトラゾリノン化合物及びその用途 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 201480040770.7 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 14832810 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2015529639 Country of ref document: JP Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2014832810 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14907699 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| REG | Reference to national code |
Ref country code: BR Ref legal event code: B01A Ref document number: 112016002063 Country of ref document: BR |
|
| ENP | Entry into the national phase |
Ref document number: 112016002063 Country of ref document: BR Kind code of ref document: A2 Effective date: 20160129 |