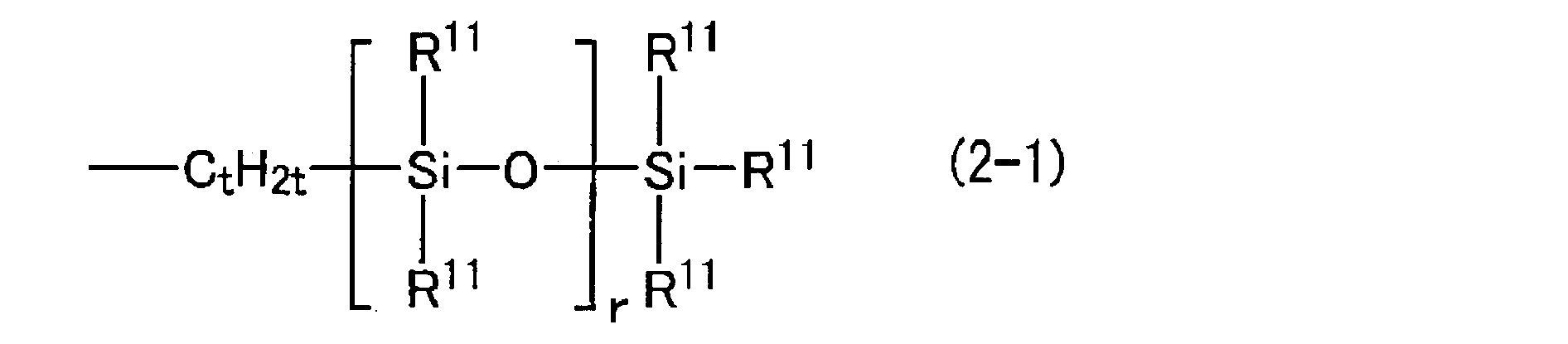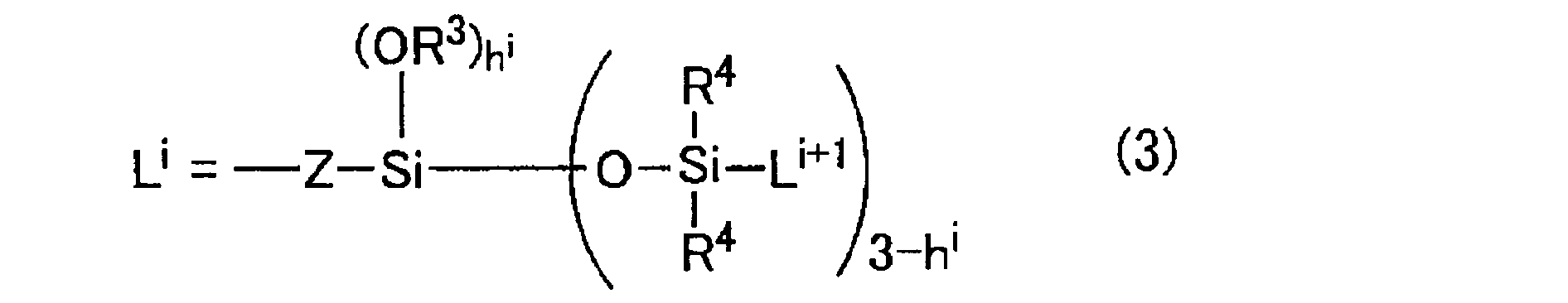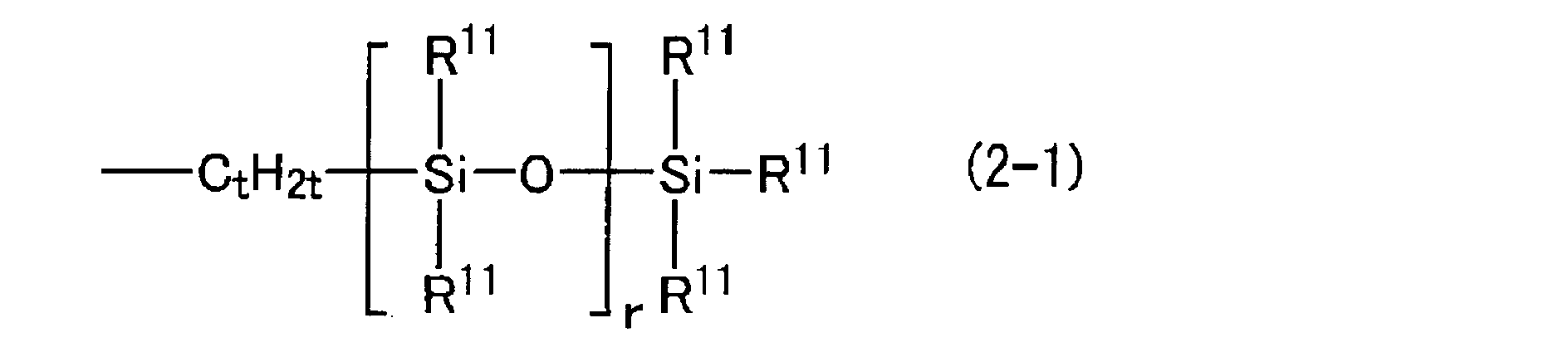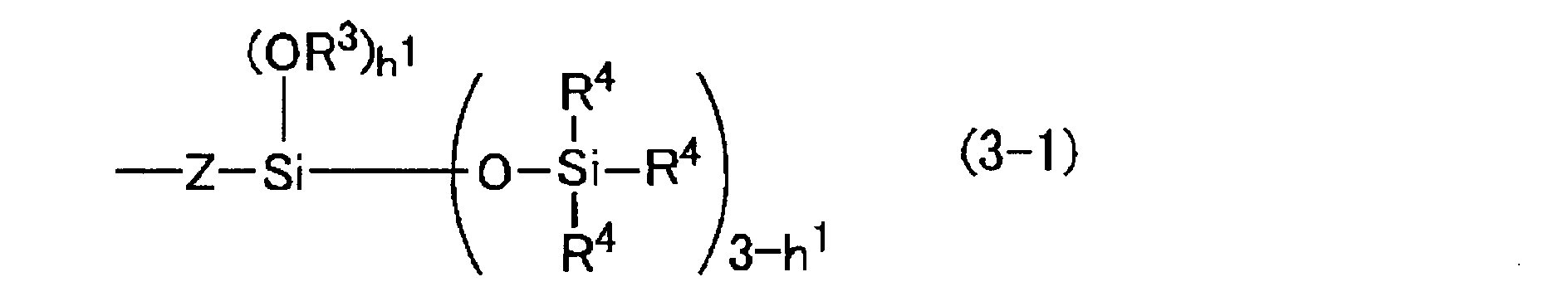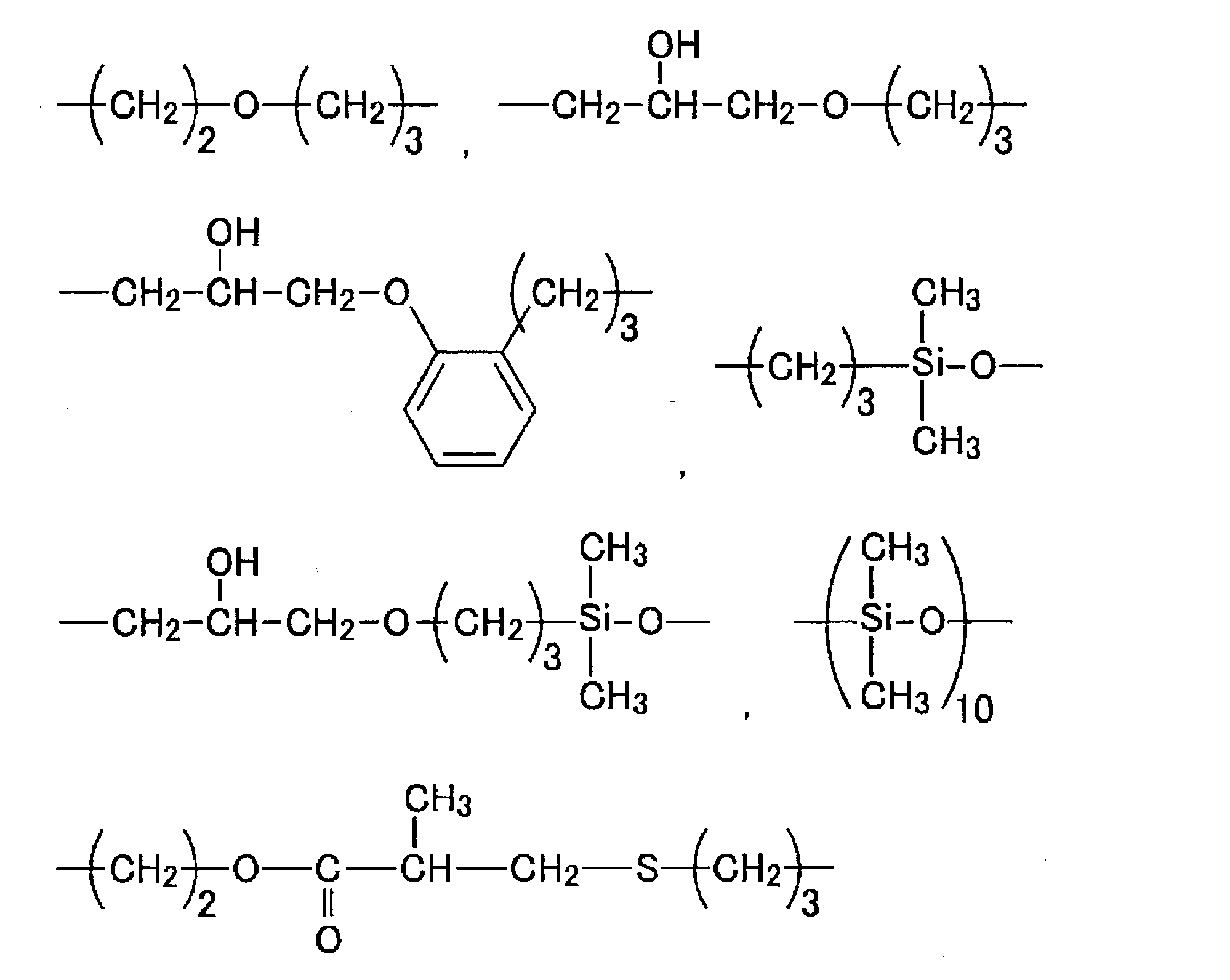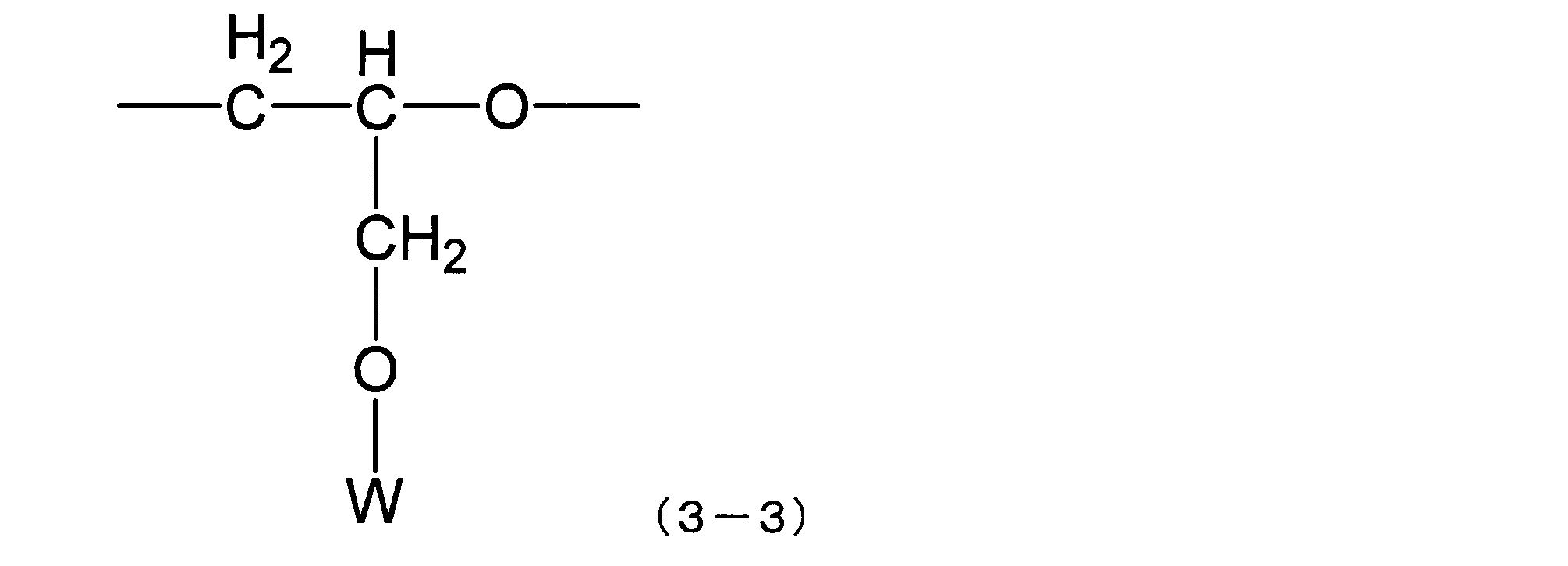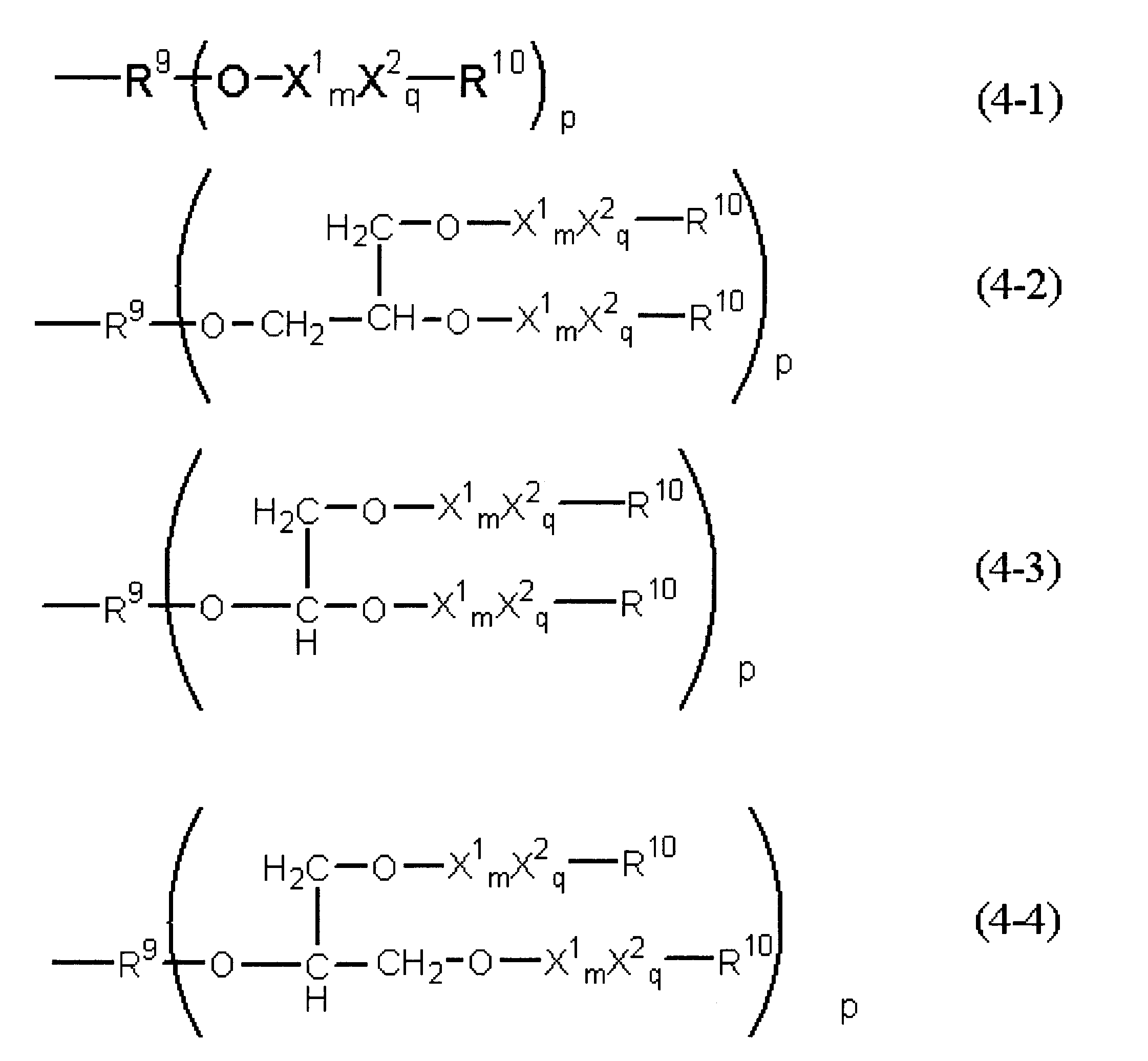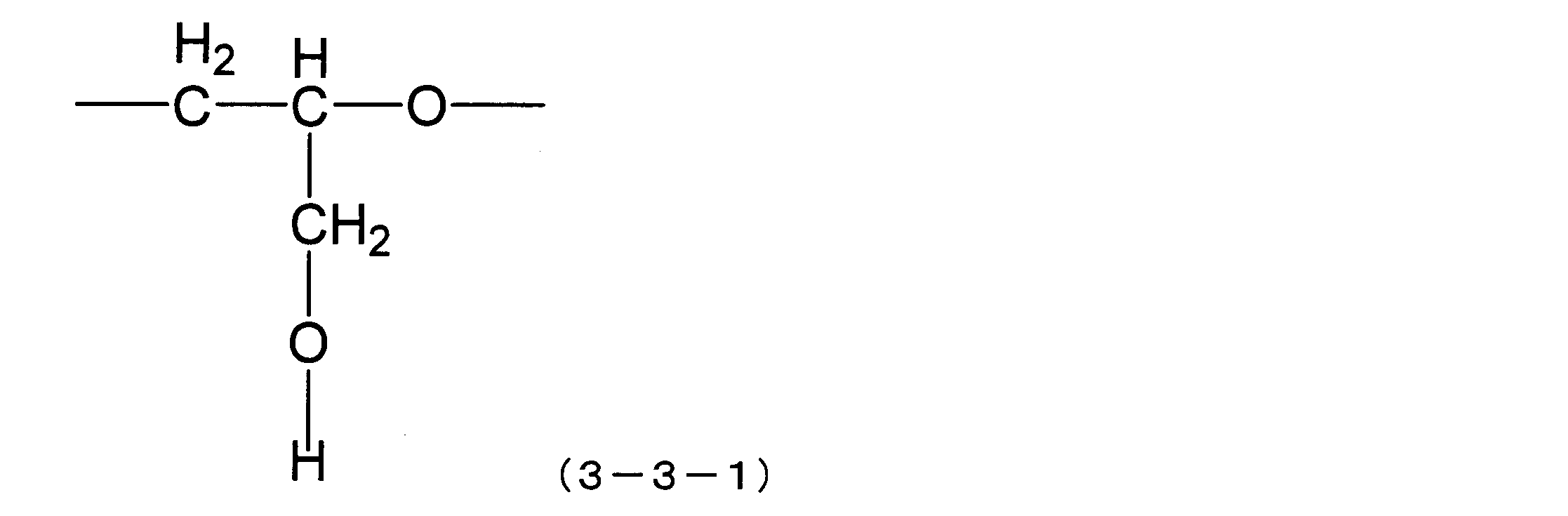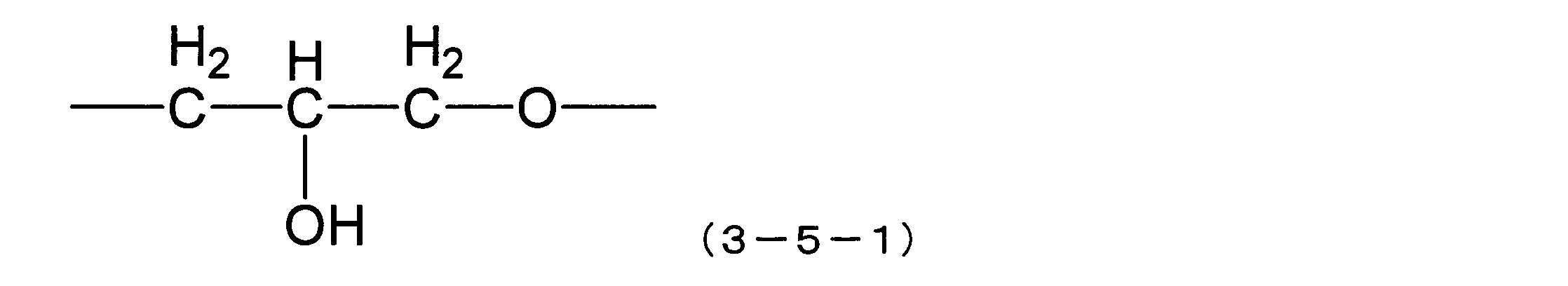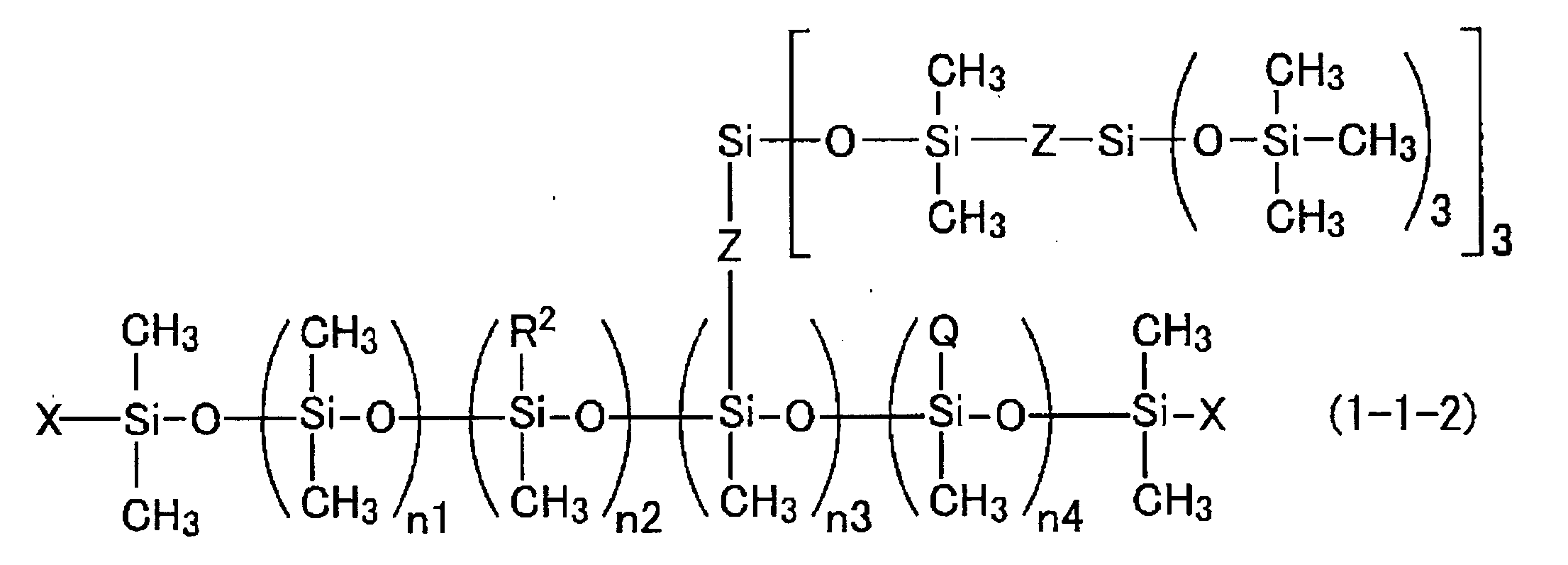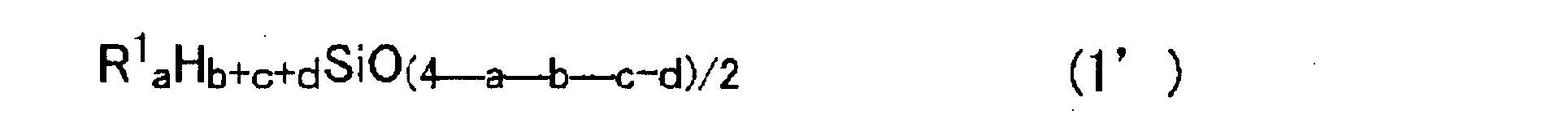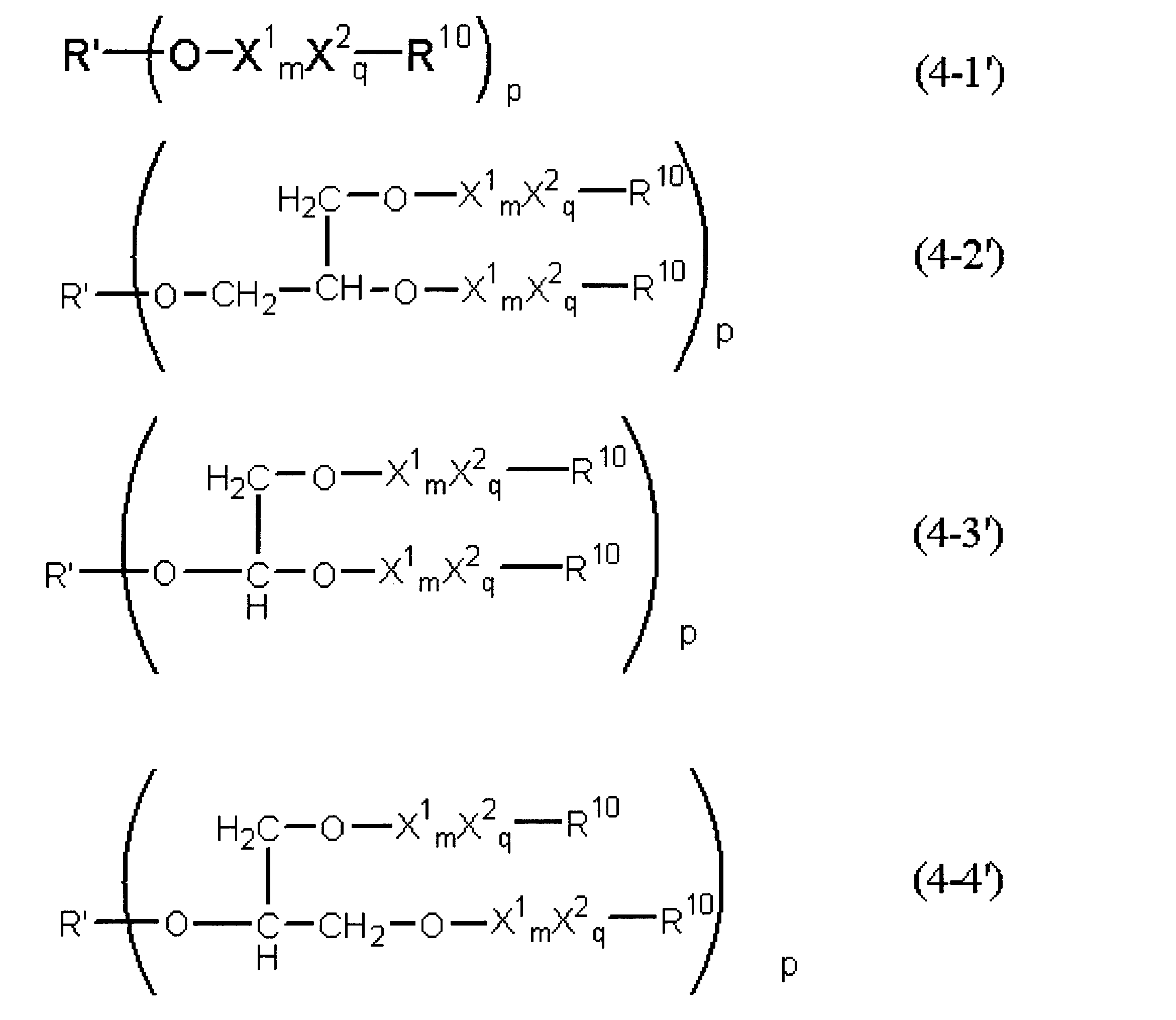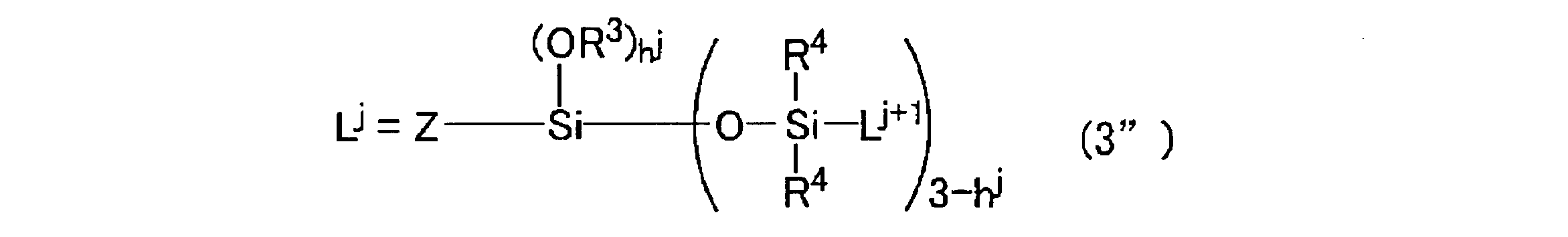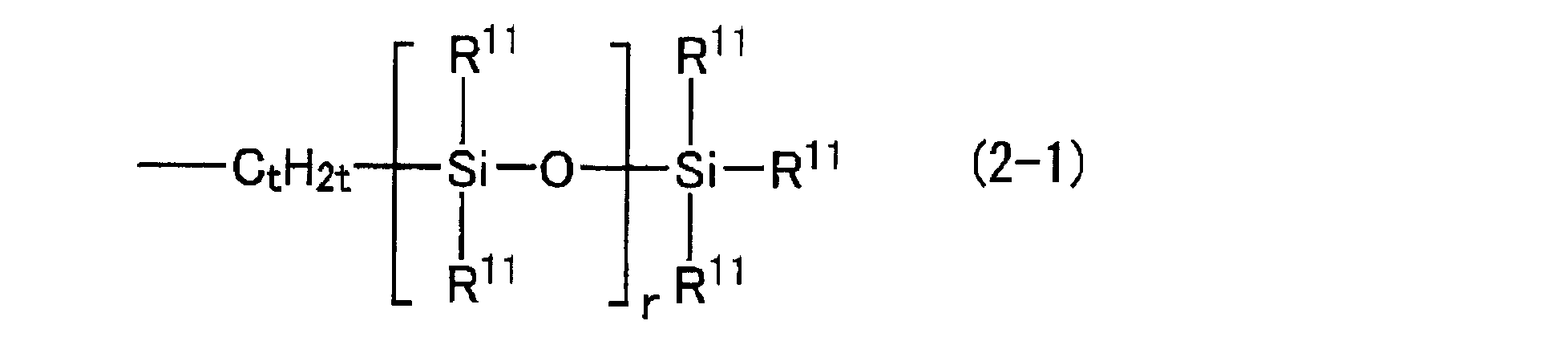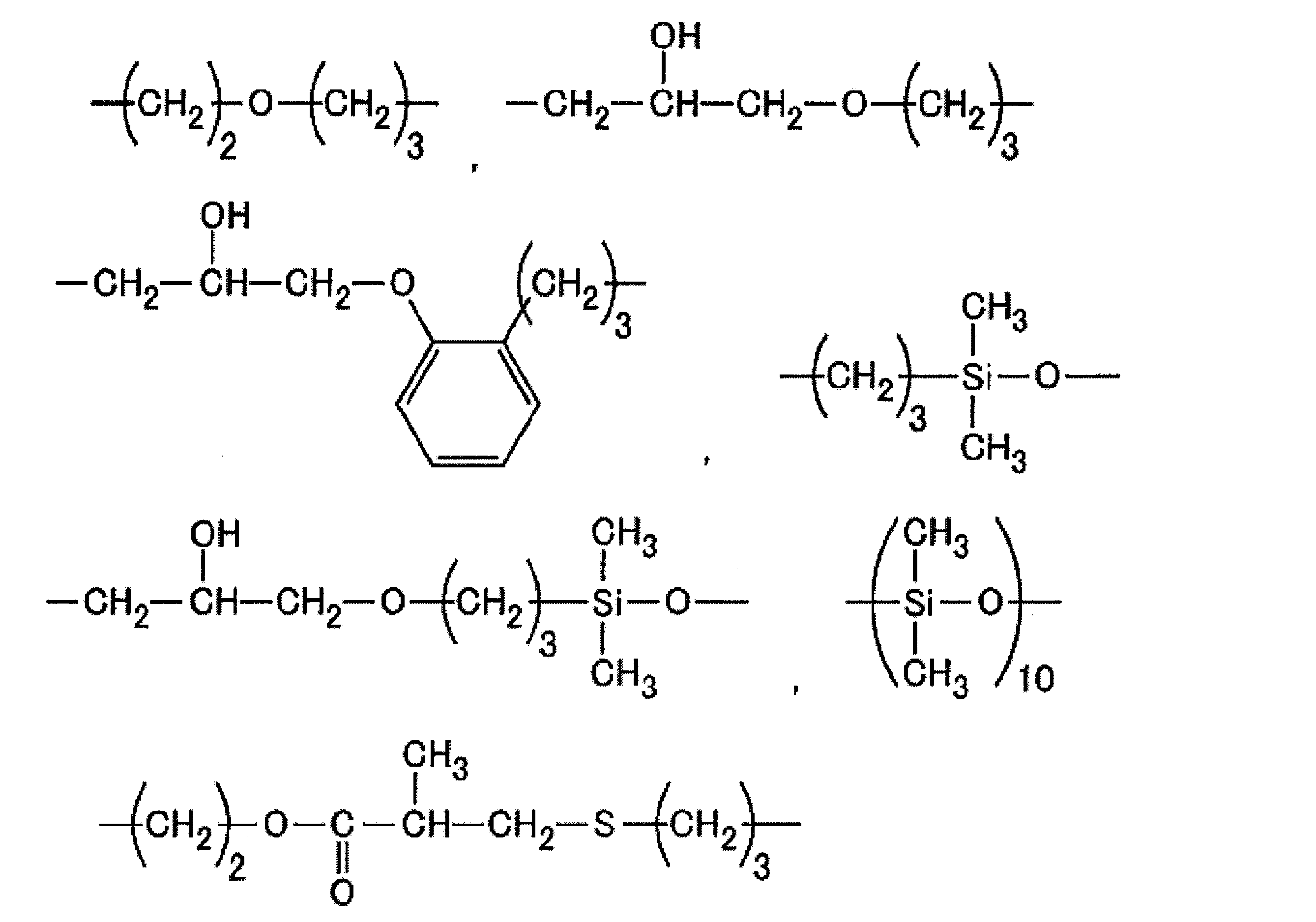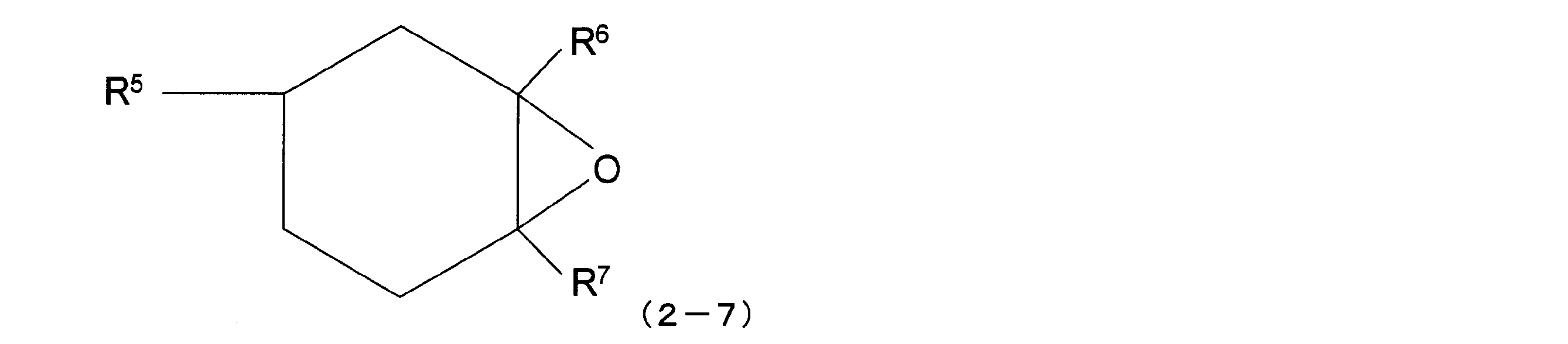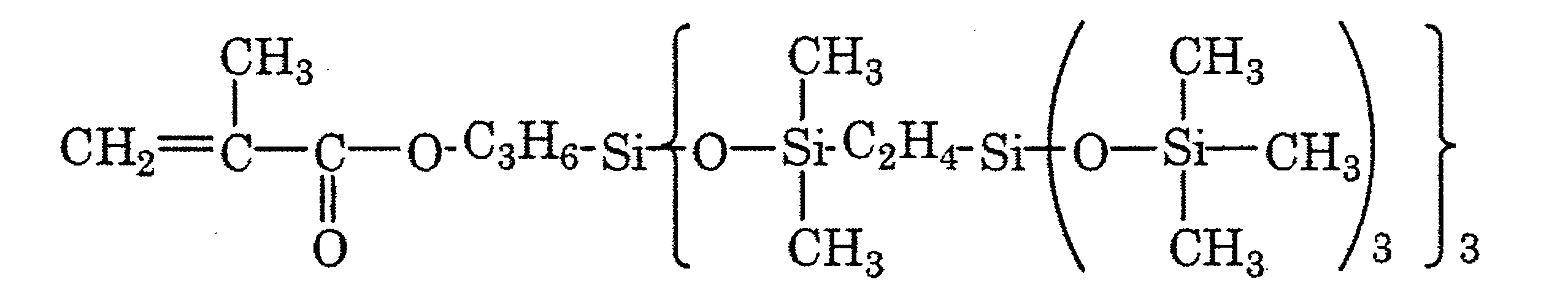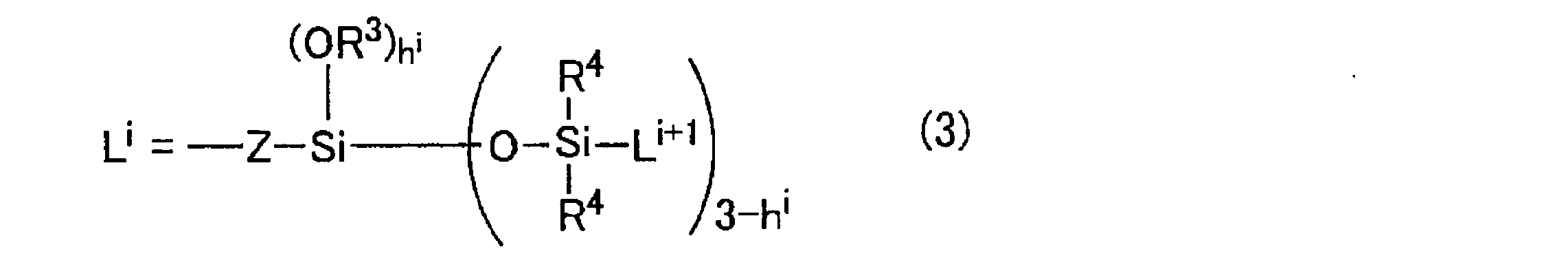WO2014104256A1 - 高純度グリセリン誘導体変性シリコーンの製造法 - Google Patents
高純度グリセリン誘導体変性シリコーンの製造法 Download PDFInfo
- Publication number
- WO2014104256A1 WO2014104256A1 PCT/JP2013/085005 JP2013085005W WO2014104256A1 WO 2014104256 A1 WO2014104256 A1 WO 2014104256A1 JP 2013085005 W JP2013085005 W JP 2013085005W WO 2014104256 A1 WO2014104256 A1 WO 2014104256A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- modified silicone
- glycerin derivative
- organic
- groups
- Prior art date
Links
- 0 C*C1CC2(*)OC2(*)CC1 Chemical compound C*C1CC2(*)OC2(*)CC1 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/32—Post-polymerisation treatment
- C08G77/34—Purification
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic System
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0834—Compounds having one or more O-Si linkage
- C07F7/0838—Compounds with one or more Si-O-Si sequences
- C07F7/0872—Preparation and treatment thereof
- C07F7/0876—Reactions involving the formation of bonds to a Si atom of a Si-O-Si sequence other than a bond of the Si-O-Si linkage
- C07F7/0878—Si-C bond
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/72—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds
- A61K8/84—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds obtained by reactions otherwise than those involving only carbon-carbon unsaturated bonds
- A61K8/89—Polysiloxanes
- A61K8/891—Polysiloxanes saturated, e.g. dimethicone, phenyl trimethicone, C24-C28 methicone or stearyl dimethicone
- A61K8/892—Polysiloxanes saturated, e.g. dimethicone, phenyl trimethicone, C24-C28 methicone or stearyl dimethicone modified by a hydroxy group, e.g. dimethiconol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/72—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds
- A61K8/84—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds obtained by reactions otherwise than those involving only carbon-carbon unsaturated bonds
- A61K8/89—Polysiloxanes
- A61K8/891—Polysiloxanes saturated, e.g. dimethicone, phenyl trimethicone, C24-C28 methicone or stearyl dimethicone
- A61K8/893—Polysiloxanes saturated, e.g. dimethicone, phenyl trimethicone, C24-C28 methicone or stearyl dimethicone modified by an alkoxy or aryloxy group, e.g. behenoxy dimethicone or stearoxy dimethicone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/72—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds
- A61K8/84—Cosmetics or similar toiletry preparations characterised by the composition containing organic macromolecular compounds obtained by reactions otherwise than those involving only carbon-carbon unsaturated bonds
- A61K8/89—Polysiloxanes
- A61K8/891—Polysiloxanes saturated, e.g. dimethicone, phenyl trimethicone, C24-C28 methicone or stearyl dimethicone
- A61K8/894—Polysiloxanes saturated, e.g. dimethicone, phenyl trimethicone, C24-C28 methicone or stearyl dimethicone modified by a polyoxyalkylene group, e.g. cetyl dimethicone copolyol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q1/00—Make-up preparations; Body powders; Preparations for removing make-up
- A61Q1/02—Preparations containing skin colorants, e.g. pigments
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q1/00—Make-up preparations; Body powders; Preparations for removing make-up
- A61Q1/02—Preparations containing skin colorants, e.g. pigments
- A61Q1/04—Preparations containing skin colorants, e.g. pigments for lips
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q1/00—Make-up preparations; Body powders; Preparations for removing make-up
- A61Q1/02—Preparations containing skin colorants, e.g. pigments
- A61Q1/08—Preparations containing skin colorants, e.g. pigments for cheeks, e.g. rouge
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q1/00—Make-up preparations; Body powders; Preparations for removing make-up
- A61Q1/02—Preparations containing skin colorants, e.g. pigments
- A61Q1/10—Preparations containing skin colorants, e.g. pigments for eyes, e.g. eyeliner, mascara
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q1/00—Make-up preparations; Body powders; Preparations for removing make-up
- A61Q1/12—Face or body powders for grooming, adorning or absorbing
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q15/00—Anti-perspirants or body deodorants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q17/00—Barrier preparations; Preparations brought into direct contact with the skin for affording protection against external influences, e.g. sunlight, X-rays or other harmful rays, corrosive materials, bacteria or insect stings
- A61Q17/04—Topical preparations for affording protection against sunlight or other radiation; Topical sun tanning preparations
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q19/00—Preparations for care of the skin
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G77/00—Macromolecular compounds obtained by reactions forming a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon in the main chain of the macromolecule
- C08G77/04—Polysiloxanes
- C08G77/38—Polysiloxanes modified by chemical after-treatment
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08L—COMPOSITIONS OF MACROMOLECULAR COMPOUNDS
- C08L83/00—Compositions of macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing silicon with or without sulfur, nitrogen, oxygen or carbon only; Compositions of derivatives of such polymers
- C08L83/04—Polysiloxanes
- C08L83/06—Polysiloxanes containing silicon bound to oxygen-containing groups
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09D—COATING COMPOSITIONS, e.g. PAINTS, VARNISHES OR LACQUERS; FILLING PASTES; CHEMICAL PAINT OR INK REMOVERS; INKS; CORRECTING FLUIDS; WOODSTAINS; PASTES OR SOLIDS FOR COLOURING OR PRINTING; USE OF MATERIALS THEREFOR
- C09D183/00—Coating compositions based on macromolecular compounds obtained by reactions forming in the main chain of the macromolecule a linkage containing silicon, with or without sulfur, nitrogen, oxygen, or carbon only; Coating compositions based on derivatives of such polymers
- C09D183/04—Polysiloxanes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2800/00—Properties of cosmetic compositions or active ingredients thereof or formulation aids used therein and process related aspects
- A61K2800/10—General cosmetic use
Definitions
- the present invention relates to a method for producing a high-purity glycerin derivative-modified silicone. Furthermore, the present invention relates to the use of the high-purity glycerin derivative-modified silicone for external preparations, cosmetics, and various industrial materials.
- an extraction (or precipitation / reprecipitation) separation method using the difference in solubility between the impurities and the main component.
- the organic modifier is a hydrophilic compound
- the extraction / separation method most of the impurities are first extracted and removed with a hydrophilic solvent (or conversely, the main component is extracted with a lipophilic solvent).
- glycerin derivative-modified silicone there are many cases where the entire system is emulsified and cannot be separated, and is not versatile.
- Patent Document 10 discloses a high-purity polypropylene glycol-modified organosiloxane polymer obtained by a precipitation / reprecipitation method. However, this method uses 10 times the amount of the organically modified silicone in total with the organic solvent and water per reprecipitation treatment, and by repeating this 3 times, high purity organically modified silicone free of impurities can be obtained. To get.
- the organic modifier is a polyethylene glycol derivative or a glycerin derivative
- the hydrophilicity and surface activity of the corresponding organic modified silicone are increased, and separation and purification are often difficult by this method.
- Patent Document 11 discloses an organosiloxane derivative having a sugar residue and containing no unreacted raw material, which is obtained by a membrane separation method using a dialysis tube.
- dialysis time of 3 days is required to obtain 10 g of high-purity organically modified silicone, and it cannot be said that it is suitable for mass production on a commercial scale in terms of efficiency.
- Patent Document 11 states that the organopolysiloxane derivative can be purified by column chromatography.
- Patent Document 4 discloses glyceryl ether-modified silicone purified by a silica gel column.
- column chromatography requires a large amount of solvent to circulate in order to obtain high purity organically modified silicone, such as device design, recovery of waste solvent, solvent removal from the collected solution, low productivity, etc. There are many challenges for production on a commercial scale.
- Another method for purifying organically modified silicone containing residual organic modifiers such as glycerin derivatives is to repeat residual microfiltration and adsorbent treatment, resulting in residual organic modification that also causes turbidity and phase separation.
- residual organic modifier is usually liquid in a temperature range where the organic modified silicone as a main component is in a liquid state
- a solid-liquid separation method using a filter aid or a cartridge filter is not rational. In fact, it is hardly effective.
- Patent Document 12 discloses a method for purifying an alkyl glyceryl polysiloxane derivative by ultrafiltration using a diafiltration method.
- ultrafiltration has a small pore size and the membrane is easily clogged in a short time, it is necessary to dilute an organically modified silicone containing an organic modifier with a volatile solvent such as hexane 10 times. Accordingly, there are problems in solvent removal from the filtrate, low productivity, worker safety, and the like.
- silicone having one or more functional groups selected from the group consisting of a hydroxy group, a carboxy group, an amino group, an imino group, a mercapto group, and an epoxy group is added in the presence of an acidic or basic catalyst
- a method for producing branched polyglycerol-modified silicone obtained by adding / grafting polymerization of 3-epoxy-1-propanol has been proposed.
- the siloxane main chain is cleaved during graft polymerization, and two or more kinds of components having different properties are easily produced as a copolymer, and there are many problems in terms of quality, purification process, etc. It is difficult to obtain a polyglycerol-modified silicone having high purity stably on a scale.
- Patent Document 13 discloses hydrogenation treatment of glycerin-modified polysiloxane and subsequent acid treatment in Example 5 as a method for purifying a modified silicone compound having a branch polymer composed of a hydrophilic group.
- this technique is a bromide-free technique that stabilizes the unsaturated group portion of the residual organic modifier, which is the cause of odor of the modified silicone composition, by hydrolysis and hydrogenation treatment, Silicone is not always obtained. In this technique, the surplus glycerin derivative continues to remain in the composition changing structure.
- Patent Document 8 a novel organopolysiloxane / glycerin derivative alternating copolymer has been proposed in Patent Document 8, and it is said that a high molecular weight polyglycerin-modified silicone can be obtained without problems such as cloudiness due to unreacted raw materials.
- this compound has a hydrophilic group incorporated in the main chain, as can be seen from its chemical structure. For this reason, the properties are completely different from conventionally used hydrophilic silicones such as polyether-modified silicones, and considerable technology is required to stably blend in delicate formulations such as cosmetics, and the field of use is limited. There is a problem.
- the present invention has been made to solve the above-mentioned problems, and can be applied regardless of the type of organic modifier, and can be easily applied to production on a commercial scale. Its purpose is to provide a method.
- the present invention stably produces a high-purity glycerin derivative-modified silicone on a commercial scale even when the boiling point of the organic modifier glycerin derivative is high or the molecular weight of the glycerin derivative is large. It is an object to provide a method for doing this.
- Another object of the present invention is to use the high-purity glycerin derivative-modified silicone produced by such a method for external preparations, cosmetics, or various industrial materials.
- An object of the present invention is a method for producing a liquid high-purity glycerin derivative-modified silicone, An organic wax having an affinity for the impurity and having a higher melting point than the glycerin derivative-modified silicone is added to the mixture containing the glycerin derivative-modified silicone and the impurity, and the melted organic mixture is heated, melted and mixed. Incorporating the impurities into the wax; The step of cooling the organic wax to obtain a solidified product of the organic wax is achieved by a production method including the step of solid-liquid separation of the solidified product of the glycerin derivative-modified silicone and the organic wax.
- the impurity is preferably an impurity derived from the glycerin derivative.
- the glycerin derivative-modified silicone is preferably a liquid at least at 100 ° C.
- the organic wax preferably has a melting point of 45 ° C to 150 ° C.
- the organic wax preferably has an average molecular weight of 900 or more.
- the organic wax preferably has a (poly) oxyethylene moiety.
- the organic wax is preferably a glycerin derivative containing a (poly) oxyethylene moiety.
- the silicon atom of the glycerin derivative-modified silicone can be bonded to a glycerin derivative group-containing organic group via a Si—C bond or a Si—O—C bond.
- the glycerin derivative-modified silicone has the following general formula (1): ⁇ Wherein R 1 represents a monovalent organic group (excluding R 2 , L and Q), a hydrogen atom or a hydroxyl group, and R 2 represents a substituted or unsubstituted linear chain having 9 to 60 carbon atoms. Or a branched monovalent hydrocarbon group, or the following general formula (2-1); Wherein R 11 is independently a substituted or unsubstituted monovalent hydrocarbon group having 1 to 30 carbon atoms, a hydroxyl group, or a hydrogen atom, and at least one of R 11 is the monovalent hydrocarbon group.
- T is a number in the range of 2 to 10
- r is a number in the range of 1 to 500
- each R 3 independently represents a substituted or unsubstituted, linear or branched monovalent hydrocarbon group having 1 to 30 carbon atoms, and each R 4 independently represents the number of carbon atoms.
- i represents 1-6 alkyl group or a phenyl group
- Z is a divalent organic radical
- i is represented of a silylalkyl group represented by L i
- the number of layers is a number of repetitions of the silylalkyl group is k
- L i + 1 is the silylalkyl group when i is less than k
- R 4 when i k
- h i represents a silylalkyl group having a siloxane dendron structure
- Q represents a glycerin derivative group-containing organic group
- a, b, c, and d are in the ranges of 1.0 ⁇ a ⁇ 2.5, 0 ⁇ b ⁇ 1.5, 0 ⁇ c ⁇ 1.5, and 0.0001 ⁇ d ⁇ 1.5, respectively.
- It can be a glycerin derivative-modified silicone represented by
- the glycerin derivative-modified silicone is (A) organohydrogenpolysiloxane, (B) a glycerin derivative group-containing organic compound having one or more reactive unsaturated groups in one molecule, and (C) (C1) an organic having an average number of reactive unsaturated groups greater than 1 in one molecule.
- the glycerin derivative-modified silicone is (D) an organopolysiloxane having a reactive functional group at both ends of the molecular chain or a derivative thereof, and (E) a reactive functional group located at both ends of the molecular chain of (D) in the molecule 2
- a linear glycerin derivative group-containing alternating copolymer obtained by reacting at least an organic compound having a reactive functional group.
- the mixture may further include a solvent for the glycerin derivative-modified silicone.
- the mixture containing the glycerin derivative-modified silicone and the impurities is treated with an acidic aqueous solution, and the odorous substance and water generated by the treatment of the acidic aqueous solution are removed by heating or decompression.
- an acidic aqueous solution Preferably it is.
- the objective of this invention is achieved also by the external preparation or cosmetics containing the high purity glycerol derivative modified silicone obtained by the manufacturing method of this invention, or an industrial material.
- the method for producing a high-purity glycerin derivative-modified silicone of the present invention can be applied regardless of the type of organic modifier, and can be easily handled for production on a commercial scale.
- the present invention provides high-purity glycerin even when the boiling point of the organic modifier (glycerin derivative) is high or the organic modifier (glycerin derivative) is a polymer compound, which is difficult to purify by distillation.
- Derivative-modified silicones can be stably produced on a commercial scale.
- the mixture contains a solvent for the glycerin derivative-modified silicone
- a high-purity glycerin derivative-modified silicone solution can be easily produced, and the production of the solution is excellent in yield and productivity, It is also suitable for commercial scale production.
- the high-purity glycerin derivative-modified silicone obtained by the production method of the present invention is substantially free of impurities, particularly impurities derived from organic modifiers. No settling of raw materials occurs. Therefore, it is chemically and physically stable.
- the high-purity glycerin derivative-modified silicone produced by the present invention or a solution containing the same can be suitably used for external preparations or cosmetics, and can be widely used for various industrial materials.
- a first aspect of the present invention is a method for producing a liquid high-purity glycerin derivative-modified silicone, An organic wax having an affinity for the impurity and having a higher melting point than the glycerin derivative-modified silicone is added to the mixture containing the glycerin derivative-modified silicone and the impurity, and the melted organic mixture is heated, melted and mixed. Incorporating the impurities into the wax; The step of cooling the organic wax to obtain a solidified product of the organic wax includes the step of solid-liquid separating the solidified product of the glycerin derivative-modified silicone and the organic wax.
- impurities particularly impurities derived from an organic modifier (glycerin derivative) are dissolved in the heated and melted organic wax, and then cooled, so that the impurities are taken into the organic wax while being taken into the organic wax.
- the glycerin derivative-modified silicone is separated from the impurities by utilizing the principle that the glycerin derivative-modified silicone is not compatible with the organic wax and has a low melting point and remains as a fluid. To do.
- Organic wax As the organic wax used in the present invention, any organic wax having affinity for impurities, particularly impurities derived from organic modifiers (glycerin derivatives), and having a higher melting point than the glycerin derivative-modified silicone is used. can do.
- the organic wax concerning this invention does not contain a silicon atom in the molecular structure.
- the melting point of the organic wax is arbitrary, but is preferably 45 ° C. or higher.
- the organic wax preferably has a melting point of 45 ° C. to 150 ° C., more preferably 50 ° C. to 120 ° C., even more preferably 60 ° C.
- the melting point of the organic wax is lower than 45 ° C., in particular, since the melting point of the solid produced by cooling after incorporating impurities derived from the organic modifier is further lowered, the glycerin derivative-modified silicone as the main component and the solid Is required to be filtered at a temperature of 40 ° C. or lower, for example.
- Filtration at such a low temperature tends to lead to an increase in filtration time when the glycerin derivative-modified silicone is a high-viscosity organic-modified silicone, which may reduce the production efficiency.
- a wax having a melting point lower than 45 ° C. generally has a low ability to take in impurities and solidify it, and the solid-liquid separation property tends to deteriorate.
- the filtration rate may be slow in low-temperature filtration.
- a solvent such as hexane
- the kind of impurity, etc. it may filter at low temperature and may precipitate a solid positively and may improve the removal effect of an impurity.
- the melting point of the organic wax is higher than 150 ° C., more energy is required to melt the wax, which is not preferable in terms of environment or efficiency.
- the glycerin derivative modified silicone itself tends to deteriorate generally at the temperature exceeding 150 degreeC, it is unpreferable.
- the organic wax when the molecular weight of the organic wax is less than 900, the organic wax is compatible not only with impurities derived from the organic modifier, but also with the main component glycerin derivative-modified silicone modified with the organic modifier. As a result, the added organic wax is dissolved in the main component, and solid-liquid separation can be difficult.
- the molecular weight of the organic wax although there is no particular upper limit for the molecular weight of the organic wax, it is usually 10 million or less.
- the high molecular weight organic wax may require a special catalyst or apparatus for production, which may cause problems in supply and cost. Therefore, it is preferable to use a molecular weight of 50,000 or less that is easily available.
- the organic wax when the glycerin derivative-modified silicone contains a (poly) oxyethylene moiety in the molecule, the organic wax preferably has a (poly) oxyethylene moiety. Even if the glycerin derivative-modified silicone does not contain a (poly) oxyethylene moiety in the molecule, the organic wax preferably has a (poly) oxyethylene moiety, and further has a glycerin derivative moiety. Is particularly preferred.
- An organic wax suitable in such a case is, for example, polyethylene glycol (PEG) or polyethylene oxide (PEO) satisfying the above-mentioned conditions concerning the melting point and molecular weight, or one or both of these terminal hydroxyl groups are blocked with an arbitrary blocking agent.
- the terminal blocking group examples include a methyl group, an ethyl group, a propyl group, a butyl group, a pentyl group, a hexyl group, a heptyl group, an octyl group, and a longer chain alkyl group; a cycloalkyl group such as a cyclopentyl group and a cyclohexyl group, and a vinyl group.
- Aryl groups such as allyl groups and butenyl groups, aryl groups such as phenyl groups and tolyl groups; monovalent hydrocarbon groups represented by aralkyl groups such as benzyl groups; acyl groups such as acetyl groups and benzoyl groups; Examples include, but are not limited to, a group in which a hydrogen atom bonded to a carbon atom of the group is substituted with an organic group containing at least a partial heteroatom; a trimethylsilyl group, and the like.
- the organic wax may contain other (poly) oxyalkylene chains and (poly) glycerin chains in addition to the (poly) oxyethylene chains within a range not impairing the effects of the present invention.
- the organic wax may be a compound in the form of addition polymerization of a large number of ethylene oxides with various polyhydric alcohols, or a compound based thereon. That is, the most suitable type of organic wax satisfies the above-mentioned conditions regarding the melting point and molecular weight, and has a polyoxyethylene chain and a glycerin unit.
- hydrophilic wax obtained by addition polymerization of many ethylene oxides to glycerin hydrophilic wax obtained by addition polymerization of many ethylene oxides to diglycerin, and addition polymerization of many ethylene oxides to triglycerin Hydrophilic waxes obtained by the treatment.
- the next preferred organic wax is polyethylene glycol (PEG) or polyethylene oxide (PEO) having a structure in which a large number of ethylene oxides are homopolymerized.
- the organic wax preferably has a structural unit in which a (poly) oxyethylene moiety and a (poly) oxypropylene moiety are connected in a block manner. These blocks may be repeated or may be an AB-type or ABA-type block copolymer without repetition.
- Suitable organic waxes in such cases include, for example, polyethylene glycol (PEG) / polypropylene glycol (PPG) copolymers and polyethylene oxide (PEO) / polypropylene glycol (PPG) copolymers that satisfy the above-mentioned conditions regarding the melting point and molecular weight.
- PEG polyethylene glycol
- PPG polypropylene glycol
- PEO polyethylene oxide
- PPG polypropylene glycol
- the organic wax contains other (poly) oxyalkylene moieties and (poly) glycerin moieties in addition to the (poly) oxyethylene moiety and the (poly) oxypropylene moiety within a range not impairing the effects of the present invention. It may be. Further, the organic wax may be a compound in the form of block addition polymerization of ethylene oxide and propylene oxide to various polyhydric alcohols, or a compound based on this.
- the organic wax is preferably used in an amount of 0.5 to 10% by weight, more preferably 1 to 5% by weight, based on the main component glycerin derivative-modified silicone. If it is less than 0.5% by weight, the effect of removing impurities is often insufficient, and the use amount exceeding 10% by weight is economically disadvantageous, and the filterability and yield are lowered, and the effect of removing impurities is also wasted. There are many cases.
- the organic wax having an affinity for impurities and having a melting point higher than that of the glycerin derivative-modified silicone is added and mixed by heating and melting.
- Mixing is preferably performed by mixing using mechanical force, and can be performed in, for example, a paddle mixer, a propeller stirrer, a reactor or a vessel equipped with stirring blades, and an emulsifier or a kneader as necessary. Available.
- the mixture should be sufficiently mixed and touched thoroughly. Is preferred.
- the treatment is performed by adding a solvent that is a good solvent for the glycerin derivative-modified silicone and a poor solvent for impurities, the system is lowered in viscosity, so that the contact between the impurities and the organic wax component occurs efficiently. Incorporation of impurities by organic wax (that is, purification of glycerin-modified silicone) can be promoted.
- mixing and stirring may be performed at 45 to 150 ° C., preferably 70 to 120 ° C. for 10 minutes to 5 hours, preferably about 30 minutes to 2 hours.
- the mixture is allowed to cool or cool, so that the impurities are incorporated into the wax and solidified (preferably solid particles), while the glycerin derivative-modified silicone as the main component in the system is It remains in a fluid state because it is not compatible with organic wax and has a low melting point.
- the stirring and mixing operation may or may not be performed. It is possible in principle to carry out the mixing operation using human power or animal power, but it is not advantageous from the viewpoint of stable production and efficiency on an industrial scale.
- the mixture composed of the glycerin derivative-modified silicone fluid and the solid particles obtained by the above treatment step can be separated into solid and liquid by, for example, a general filtration operation using filter paper using diatomaceous earth or activated carbon as a filter aid. .
- a general filtration operation using filter paper using diatomaceous earth or activated carbon as a filter aid for example, highly purified glycerin derivative modified silicone can be obtained easily.
- a solvent that is a good solvent for the glycerin derivative-modified silicone and a poor solvent for impurities is used in the treatment step
- a mixture of the glycerin derivative-modified silicone fluid, solid particles, and the solvent is used, for example, Solid-liquid separation is performed by a general filtration operation using filter paper using diatomaceous earth or activated carbon as a filter aid.
- the filtrate can be directly commercialized as a cosmetic raw material containing a high-purity glycerin derivative-modified silicone and an oil.
- a volatile solvent used as the solvent
- a high-purity glycerin derivative-modified silicone can also be obtained by removing the volatile solvent from the filtrate after solid-liquid separation by heating and depressurizing operation or the like. . Since the glycerin derivative-modified silicone generally has a high viscosity, it is more advantageous to increase the purity of the glycerin derivative-modified silicone and reduce turbidity by performing the treatment with the organic wax in the presence of the solvent.
- the glycerin derivative-modified silicone to which the present invention can be applied is a silicone compound modified with a glycerin derivative, and is a liquid, preferably at least 100 ° C. And if it satisfy
- liquid or “liquid” means that the liquid level of the organopolysiloxane in a predetermined container is leveled, the container is tilted, and after 1 hour, preferably after 30 minutes, more preferably Means that after 10 minutes the liquid level can become horizontal again.
- horizontal means forming a plane that intersects at right angles to the direction of action of gravity.
- the glycerin derivative-modified silicone is preferably a liquid at least at 100 ° C., but more preferably exhibits a liquid state in the range of 100 ° C. or lower to room temperature.
- liquid at 80 ° C. is preferably liquid at 80 ° C., more preferably liquid at 40 ° C., and even more preferably liquid at room temperature (25 ° C.).
- it is liquid at 100 ° C. or higher, but it may be heated to 100 ° C., for example, even if it is a semi-gel or soft solid that does not exhibit fluidity at temperatures below room temperature (25 ° C.).
- a liquid organosilicon compound is included within the range of a liquid organosilicon compound.
- the glycerin derivative-modified silicone has the following general formula (1): ⁇ Wherein R 1 represents a monovalent organic group (excluding R 2 , L and Q), a hydrogen atom or a hydroxyl group, and R 2 represents a substituted or unsubstituted linear chain having 9 to 60 carbon atoms. Or a branched monovalent hydrocarbon group, or the following general formula (2-1); Wherein R 11 is independently a substituted or unsubstituted monovalent hydrocarbon group having 1 to 30 carbon atoms, a hydroxyl group, or a hydrogen atom, and at least one of R 11 is the monovalent hydrocarbon group.
- T is a number in the range of 2 to 10
- r is a number in the range of 1 to 500
- each R 3 independently represents a substituted or unsubstituted, linear or branched monovalent hydrocarbon group having 1 to 30 carbon atoms, and each R 4 independently represents the number of carbon atoms.
- i represents 1-6 alkyl group or a phenyl group
- Z is a divalent organic radical
- i is represented of a silylalkyl group represented by L i
- the number of layers is a number of repetitions of the silylalkyl group is k
- L i + 1 is the silylalkyl group when i is less than k
- R 4 when i k
- h i represents a silylalkyl group having a siloxane dendron structure
- Q represents a glycerin derivative group-containing organic group
- a, b, c, and d are in the ranges of 1.0 ⁇ a ⁇ 2.5, 0 ⁇ b ⁇ 1.5, 0 ⁇ c ⁇ 1.5, and 0.0001 ⁇ d ⁇ 1.5, respectively.
- It can be a glycerin derivative-modified silicone represented by
- the glycerin derivative-modified silicone represented by the general formula (1) has a long-chain type organic group or a chain-like organosiloxane group represented by R 2 , b is a number greater than 0, 0.0001 ⁇ b ⁇ 1.5 is preferable, and 0.001 ⁇ b ⁇ 1.5 is more preferable.
- the glycerin derivative-modified silicone represented by the general formula (1) has a silylalkyl group having a siloxane dendron structure represented by L 1 above, c is a number greater than 0, and 0.0001 ⁇ c ⁇ 1.5 is preferable, and 0.001 ⁇ c ⁇ 1.5 is more preferable.
- Examples of the glycerin derivative-modified silicone include a glycerin derivative group-containing organic group that is Q, and a silylalkyl group having a long-chain organic group represented by R 2 or a chain-like organosiloxane group or a siloxane dendron structure represented by L 1. It is preferable to have. At this time, preferable values of b and c are expressed as follows depending on the essential functional group.
- the monovalent organic group represented by R 1 in the general formula (1) may be the same as or different from each other, and is not particularly limited as long as it is not a functional group corresponding to R 2 , L 1, or Q.
- R 5 represents a substituted or unsubstituted, linear or branched divalent hydrocarbon group having 3 to 5 carbon atoms
- R 6 represents a hydrogen atom, 1 to 24 carbon atoms
- n 1 To 100) (poly) oxyalkylene group, alkoxy group, water Group, preferably a hydrogen atom.
- Examples of the monovalent hydrocarbon group having 1 to 8 carbon atoms include, for example, alkyl groups such as methyl, ethyl, propyl, butyl, pentyl, hexyl, heptyl, and octyl; cyclopentyl, cyclohexyl Cycloalkyl groups such as vinyl groups, allyl groups, butenyl groups, etc .; aryl groups such as phenyl groups, tolyl groups; aralkyl groups such as benzyl groups; and hydrogen atoms bonded to carbon atoms of these groups At least partially a halogen atom such as fluorine, or a group substituted with an organic group including an epoxy group, glycidyl group, acyl group, carboxyl group, amino group, methacryl group, mercapto group, etc.
- alkyl groups such as methyl, ethyl, propyl, butyl, pentyl, hexy
- the monovalent hydrocarbon group is preferably a group other than an alkenyl group, and particularly preferably a methyl group, an ethyl group, or a phenyl group.
- the alkoxy group is a lower alkoxy group such as methoxy group, ethoxy group, isopropoxy group, butoxy group, lauryl alkoxy group, myristyl alkoxy group, palmityl alkoxy group, oleyl alkoxy group, stearyl alkoxy group, behenyl alkoxy group. Illustrative are higher alkoxy groups.
- R 1 is preferably a monovalent hydrocarbon group or monovalent fluorinated hydrocarbon group having 1 to 8 carbon atoms that does not have an aliphatic unsaturated bond.
- the monovalent hydrocarbon group having no aliphatic unsaturated bond belonging to R 1 include alkyl groups such as methyl group, ethyl group, propyl group, butyl group, pentyl group, hexyl group; phenyl group, tolyl group, xylyl group Aryl groups such as benzyl groups, etc., and monovalent fluorinated hydrocarbon groups include perfluoroalkyl groups such as trifluoropropyl groups and pentafluoroethyl groups.
- R 1 is preferably a methyl group, an ethyl group, or a phenyl group. Particularly, 90 mol% to 100 mol% of all R 1 are a methyl group, an ethyl group, or a phenyl group. Is preferably a group selected from:
- the glycerin derivative-modified silicone has a modified group other than the hydrophilic group (-Q), particularly a short-chain or medium-chain hydrocarbon-based group, introduced as R 1 or designed for the purpose of imparting further functionality.
- R 1 is a substituted monovalent hydrocarbon group
- the substituent can be appropriately selected according to the characteristics to be imparted and the application.
- amino groups, amide groups, aminoethylaminopropyl groups, carboxyl groups, etc. are monovalent hydrocarbon groups for the purpose of improving the feeling of use, feel and durability. Can be introduced as a substituent.
- the substituted or unsubstituted, linear or branched monovalent hydrocarbon group of 9 to 60 carbon atoms of R 2 in the general formula (1) is a long chain hydrocarbon group or the above general formula (2-1 )
- Or (2-2) is a chain-like organosiloxane group, and is introduced into the main chain and / or side chain of polysiloxane, so that it can be incorporated into an external preparation or cosmetic.
- the affinity to various components such as the body, emulsification and dispersibility, and the feeling of use can be further improved.
- R 2 may be the monovalent long-chain hydrocarbon group or the chain-like organopolysiloxane group, or may be both functional groups.
- part or all of R 2 is preferably a monovalent long-chain hydrocarbon group.
- the glycerin Derivative-modified silicones exhibit superior compatibility not only with silicone oils but also with non-silicone oils with a high alkyl group content, for example, emulsification with non-silicone oils with excellent thermal and temporal stability. Products and dispersions can be obtained.
- the substituted or unsubstituted, straight-chain or branched monovalent hydrocarbon groups having 9 to 60 carbon atoms and represented by R 2 in the general formula (1) may be the same as each other. Further, the structure may be selected from linear, branched, and partially branched. In the present invention, an unsubstituted and linear monovalent hydrocarbon group is particularly preferably used. Examples of the unsubstituted monovalent hydrocarbon group include an alkyl group, an aryl group, and an aralkyl group having 9 to 60 carbon atoms, preferably 9 to 30 carbon atoms, more preferably 10 to 25 carbon atoms.
- examples of the substituted monovalent hydrocarbon group include a perfluoroalkyl group having 9 to 30 carbon atoms, preferably 9 to 30 carbon atoms, more preferably 10 to 24 carbon atoms, an aminoalkyl group, and an amidoalkyl. Group and ester group. Moreover, a part of carbon atoms of the monovalent hydrocarbon group may be substituted with an alkoxy group, and examples of the alkoxy group include a methoxy group, an ethoxy group, and a propoxy group.
- Such a monovalent hydrocarbon group is particularly preferably an alkyl group having 9 to 30 carbon atoms, and has the general formula: — (CH 2 ) v —CH 3 (v is a number in the range of 8 to 29). The group represented by these is illustrated. An alkyl group having 10 to 24 carbon atoms is particularly preferred.
- the chain organosiloxane group represented by the general formula (2-1) or (2-2) has a linear polysiloxane chain structure.
- each R 11 is independently a substituted or unsubstituted monovalent hydrocarbon group having 1 to 30 carbon atoms, a hydroxyl group, or a hydrogen atom.
- the substituted or unsubstituted monovalent hydrocarbon group having 1 to 30 carbon atoms is preferably an alkyl group having 1 to 30 carbon atoms, an aryl group having 6 to 30 carbon atoms, or an aralkyl having 6 to 30 carbon atoms.
- a cycloalkyl group such as a group; an aryl group such as a phenyl group and a tolyl group is exemplified, and a hydrogen atom bonded to a carbon atom of these groups is at least partially a halogen atom such as fluorine, an epoxy group, an acyl group, It may be substituted with an organic group including a carboxyl group, an amino group, a methacryl group, a mercapto group, and the like.
- R 11 is particularly preferably a methyl group, a phenyl group or a hydroxyl group, a form in which a part of R 11 is a methyl group and a part is a long-chain alkyl group having 8 to 30 carbon atoms. Is preferred.
- t is a number in the range of 2 to 10
- r is a number in the range of 1 to 500
- r is a number in the range of 2 to 500. It is preferable.
- Such a linear organosiloxane group is hydrophobic, and from the viewpoint of compatibility with various oils, r is preferably a number in the range of 1 to 100, and a number in the range of 2 to 30. Particularly preferred.
- the silylalkyl group having a siloxane dendron structure represented by the general formula (3) is a functional group exhibiting high water repellency, including a structure in which carbosiloxane units spread in a dendrimer shape, and is a combination of a hydrophilic group and a hydrophilic group.
- the silylalkyl group having a siloxane dendron structure is a functional group that imparts an advantageous property that it can be used in combination with a wide range of components because it is chemically stable.
- Examples of the substituted or unsubstituted, linear or branched monovalent hydrocarbon group represented by R 3 in the general formula (3) include, for example, a methyl group, an ethyl group, Alkyl groups such as propyl, butyl, pentyl, hexyl, heptyl and octyl; cycloalkyl such as cyclopentyl and cyclohexyl; alkenyl such as vinyl, allyl and butenyl; phenyl and tolyl Aryl groups such as aralkyl groups; aralkyl groups such as benzyl groups; and hydrogen atoms bonded to carbon atoms of these groups are at least partially halogen atoms such as fluorine, or epoxy groups, glycidyl groups, acyl groups, carboxyl groups , Groups substituted with an organic group including an amino group, a methacryl group, a mercapto group and the like (provided that the total number
- examples of the alkyl group having 1 to 6 carbon atoms include methyl, ethyl, n-propyl, i- Examples include linear, branched or cyclic alkyl groups such as propyl, n-butyl, i-butyl, s-butyl, pentyl, neopentyl, cyclopentyl, hexyl and the like.
- the number k of layers is industrially preferably an integer of 1 to 3, more preferably 1 or 2.
- the group represented by L 1 is represented as follows.
- R 3 , R 4 and Z are the same groups as described above.
- L 1 is represented by the following general formula (3-1).
- L 1 is represented by the following general formula (3-2).
- L 1 is represented by the following general formula (3-3).
- h 1 , h 2 and h 3 are each independently a number in the range of 0 to 3. These h i are particularly preferably numbers in the range of 0 to 1, and h i is particularly preferably 0.
- each Z is independently a divalent organic group, specifically, a silicon-bonded hydrogen atom, an alkenyl group, an acryloxy group
- examples include divalent organic groups formed by addition reaction of a functional group having an unsaturated hydrocarbon group such as a methacryloxy group at the end.
- the functional group is not limited to this, and can be selected as appropriate.
- each Z independently represents the following general formula: Is a group selected from divalent organic groups represented by the formula:
- Z in L 1 is preferably a divalent organic group represented by the general formula —R 7 — introduced by the reaction of a silicon-bonded hydrogen atom and an alkenyl group.
- Z is preferably a divalent organic group represented by —R 7 —COO—R 8 — introduced by reaction of a silicon-bonded hydrogen atom with an unsaturated carboxylic ester group.
- the hierarchical number k is 2 or more, the silylalkyl group represented by a L 2 ⁇ L k L i, Z is an alkylene group or -R 7 -COO-R 8 having 2 to 10 carbon atoms - in
- the divalent organic group is preferably a group selected from an ethylene group, a propylene group, a methylethylene group, a hexylene group, and —CH 2 C (CH 3 ) COO—C 3 H 6 —. Particularly preferred.
- each R 7 independently represents a substituted or unsubstituted, linear or branched alkylene group or alkenylene group having 2 to 22 carbon atoms, or 6 to 22 carbon atoms.
- R 8 is an ethylene group
- a propylene group is preferably a group selected from methyl ethylene group or a hexylene group.
- R 8 is a group selected from divalent organic groups represented by the following formula.
- Q is a glycerin derivative group-containing organic group and constitutes a hydrophilic portion of the glycerin derivative-modified silicone.
- the structure of Q is not limited as long as it has a glycerin derivative moiety, but it is preferable that the glycerin derivative residue is bonded to a silicon atom via a divalent organic group.
- the glycerin derivative residue is a hydrophilic group having a (poly) glycerin structure, and a hydrophilic group having a polyglycerin structure of monoglycerin, diglycerin, triglycerin, tetraglycerin and pentamer or higher. Further, a part of the terminal hydroxyl group may be blocked with an alkyl group. Furthermore, the (poly) glycerin structure may be linear or branched, or may be a structure branched in a dendritic manner.
- Such a glycerin derivative group-containing organic group (Q) is bonded to a silicon atom via a divalent or higher linking group and has hydrophilicity represented by the following structural formulas (3-3) to (3-6).
- the organic group is preferably a glycerin derivative group-containing organic group containing at least one hydrophilic unit selected from the units.
- the hydrophilic unit constituting Q does not consist only of the following structural formula (3-6). (R is a number in the range of 1-6)
- W represents a hydrogen atom or an alkyl group having 1 to 20 carbon atoms, and is preferably a hydrogen atom.
- W is a hydrogen atom, it is difficult to be oxidized in the air, and it is difficult to produce aldehydes such as formaldehyde and allergenic compounds such as formates over time during storage. There is.
- the hydrophilic units represented by the structural formulas (3-3) to (3-5) include polyhydric alcohols mainly containing glycerin, polyglycerins (also referred to as polyglycerols), polyglycidyl ethers, or terminals thereof. It is a hydrophilic unit contained in a hydrophilic group derived from a hydrophilic compound selected from a compound in which a hydroxyl group is partially blocked with a hydrocarbon group.
- the glycerin derivative group-containing organic group (Q) according to the present invention further has a hydrophilic structure (for example, an oxyethylene unit or an oxypropylene unit) composed of an oxyalkylene unit represented by the structural formula (3-6). It may be a hydrophilic group optionally containing a polyether structure).
- Q may be a hydrophilic group having no branched structure such as a monoglycerin-modified group or a diglycerin-modified group, but like a polyglycerol group or a polyglycidyl ether group, A hydrophilic group having a branched structure in a part of the functional group may be used.
- Q is bonded to a silicon atom via a divalent or higher valent linking group, and is at least 1 selected from hydrophilic units represented by the structural formulas (3-3) to (3-6).
- Q is bonded to a silicon atom via a divalent or higher linking group and is at least one selected from hydrophilic units represented by the structural formulas (3-3) to (3-6). It may be a glycerin derivative group-containing organic group having 2 or more hydrophilic units and having a branch unit selected from the groups represented by the following structural formulas (3-7) to (3-9).
- the two oxygen atoms in the structural formulas (3-7) to (3-9) are each independently selected from hydrophilic units represented by the general formulas (3-3) to (3-6). At least one or more hydrophilic units are bonded.
- the hydrophilic unit may be further bonded to a branch unit selected from the groups represented by structural formulas (3-7) to (3-9), and the hydrophilic unit is branched in multiple layers.
- a dendritic polyether structure, a polyglycerol structure, or a polyglycidyl ether structure may be formed.
- the structure of a hydrophilic group Q having one branch unit represented by the structural formula (3-7) and two branch units represented by the structural formula (3-9) and branched in a dendritic manner is shown below.
- the dendritic polyglycerol structure is not limited to this.
- n is a number in the range of 0 to 50, but not all m are 0.
- the divalent or higher valent linking group is a bonding site to a silicon atom contained in the hydrophilic group Q, and the structure thereof is not particularly limited, but an ethylene group, a propylene group, a butylene group, hexylene.
- Alkylene groups such as ethylene phenylene groups, alkylene phenylene groups such as propylene phenylene groups, alkylene aralkylene groups such as ethylene benzylene groups; alkylenoxy phenylene groups such as ethylenoxy phenylene groups and propyleneoxy phenylene groups; Examples include alkylenoxy benzylene groups such as a nonoxy benzylene group, an ethylenoxy benzylene group, a propylenoxy benzylene group, and the groups shown below.
- the number of ether bonds in the divalent or higher linking group is preferably 0 to 3, more preferably 0 or 1.
- Q is more preferably a hydrophilic group represented by the following structural formulas (4-1) to (4-4), and these are generally hydrophilic groups derived from polyglycerin compounds. .
- R 9 is a (p + 1) -valent organic group, and p is a number of 1 or more and 3 or less.
- R 9 include the same groups as the divalent or higher linking group.
- each R 12 is independently a linear or branched alkylene group having 2 to 22 carbon atoms, an alkenylene group or an arylene group having 6 to 22 carbon atoms, which may have a substituent. .
- X 1 is each independently at least one hydrophilic unit selected from hydrophilic units represented by the following general formulas (3-3-1) to (3-5-1), and m is 1 It is a number in the range of ⁇ 5, particularly preferably 1 to 4.
- X 2 is any (poly) oxyethylene unit that Q may contain, and q is a number in the range of 0-100. q is preferably a number in the range of 0 to 50, and preferably 0 to 30. Incidentally, X 2 is (poly) can also together with oxyethylene units (poly) oxypropylene units and / or (poly) oxybutylene units.
- X 2 is a unit represented by the formula: — (C 2 H 4 O) t1 (C 3 H 6 O) t2 (C 4 H 8 O) t3 — (wherein t1, t2 and t3 are 0 ⁇ t1 ⁇ 100, 0 ⁇ t2 ⁇ 100, and 0 ⁇ t3 ⁇ 50, preferably 0 ⁇ t1 ⁇ 50, 0 ⁇ t2 ⁇ 50, and 0 ⁇ t3 ⁇ 30, and more Q is preferably included as a (poly) oxyalkylene unit represented by 0 ⁇ t1 ⁇ 30, 0 ⁇ t2 ⁇ 30, and 0 ⁇ t3 ⁇ 10.
- the form of the bond between X 1 and X 2 may be block or random. That is, the hydrophilic group represented by Q includes a hydrophilic segment formed by bonding hydrophilic units represented by the above general formulas (3-3-1) to (3-5-1) in a block form, and a polyoxyalkylene.
- bonds may be sufficient, and the hydrophilic group which the unit which comprises these couple
- a bond form such as- (X 2 ) m1 -X 1- (X 2 ) m2 -X 1- can be exemplified.
- R 10 is a group selected from the group consisting of a hydrogen atom, an alkyl group having 1 to 20 carbon atoms, an acyl group, and a glycidyl group.
- a suitable hydrophilic group Q is represented by the following structural formula (4 -1-1) is a hydrophilic group derived from (poly) glycerin.
- R 9 ′ is a divalent organic group, and examples thereof are the same as those described above.
- X 1 and R 10 are the same groups as described above, and m is a number in the range of 1 to 5.
- the hydrophilic group Q is a hydrophilic group derived from a (poly) glycerin-based compound, and a hydrophilic group derived from (poly) glycerin. Most preferred is a sex group.
- (poly) glycerin monoallyl ether, (poly) glyceryl eugenol, a hydrophilic group derived from a (poly) glycerin compound having a monoglycerin, diglycerin, triglycerin or tetraglycerin structure Is preferred.
- a particularly preferred hydrophilic group Q is a diglycerin derivative group-containing organic group in which the average number m of repeating glycerin units in the structural formula (4-1-1) is in the range of 1.5 to 2.4. It is.
- R 9 ′ is a divalent organic group, and examples thereof are the same as those described above.
- X 1 and R 10 are the same groups as described above.
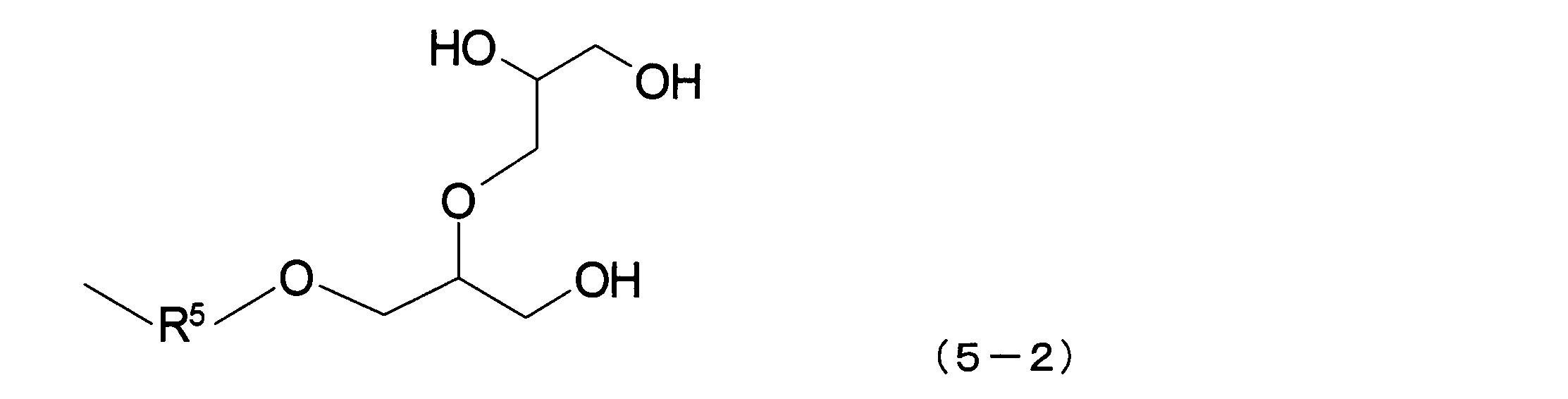
- the diglycerin derivative group-containing organic group is represented by the following general formula (5-1): (Wherein R 5 represents a divalent organic group having no oxyalkylene structure having an average number of repeating oxyalkylene units of 2 or more), or the following general formula (5-2) (Wherein R 5 is as described above), and is a diglycerin derivative group-containing organic group.
- the bonding position of the organic group (-Q) containing the glycerin derivative group may be either the side chain or the terminal of the polysiloxane main chain, and two or more glycerin derivative groups are contained in one molecule of the glycerin derivative-modified silicone.
- a structure having an organic group may also be used.
- these two or more glycerol derivative group-containing organic groups may be the same or different glycerol derivative group-containing organic groups.
- These two or more glycerin derivative group-containing organic groups may have a structure in which only the side chain of polysiloxane as the main chain, only the terminal, or the side chain and the terminal are bonded.
- the glycerin derivative-modified silicone having a glycerin derivative group-containing organic group (-Q) represented by the general formula (1) is preferably liquid at least at 100 ° C.
- the polysiloxane main chain may be any of linear, branched, and network (including micro-crosslinking and elastomer). According to the production method of the present invention, not only low-viscosity glycerin derivative-modified silicones, but also glycerin derivative-modified silicones that are solid (including gums having plasticity and poor fluidity) from high viscosity to room temperature It is possible to easily improve the opaque appearance and stabilize it to a translucent to transparent uniform liquid.
- (n1 + n2 + n3 + n4) is preferably a number in the range of 10 to 2,000, more preferably in the range of 25 to 1500, and particularly preferably in the range of 50 to 1000.
- n1 is preferably a number in the range of 10 to 2,000, more preferably in the range of 25 to 1500, and still more preferably in the range of 50 to 1000.
- n2 is preferably a number in the range of 0 to 250, and more preferably a number in the range of 0 to 150.
- n2> 1 from the viewpoint of surface activity and compatibility with oil agents other than silicone.
- n3 is preferably a number in the range of 0 to 250, particularly preferably n3> 1 and having at least one silylalkyl group (—L 1 ) having a siloxane dendron structure in the side chain portion.
- Q is preferably a glycerin derivative group-containing organic group represented by any one of the general formulas (4-1) to (4-4),
- all Qs may be one kind of glycerin derivative group-containing organic group represented by any one of the general formulas (4-1) to (4-4).
- a part of Q is an organic group containing a glycerin derivative group represented by any one of the general formulas (4-1) to (4-4), and the remaining Q is another glycerin derivative group. It may be a contained organic group.
- the glycerin derivative-modified silicone may be a mixture of one or more glycerin derivative-modified silicones represented by the general formula (1). More specifically, it may be a mixture of two or more glycerin derivative-modified silicones having different degrees of polymerization and modification rate of the siloxane main chain and different types of modifying groups.
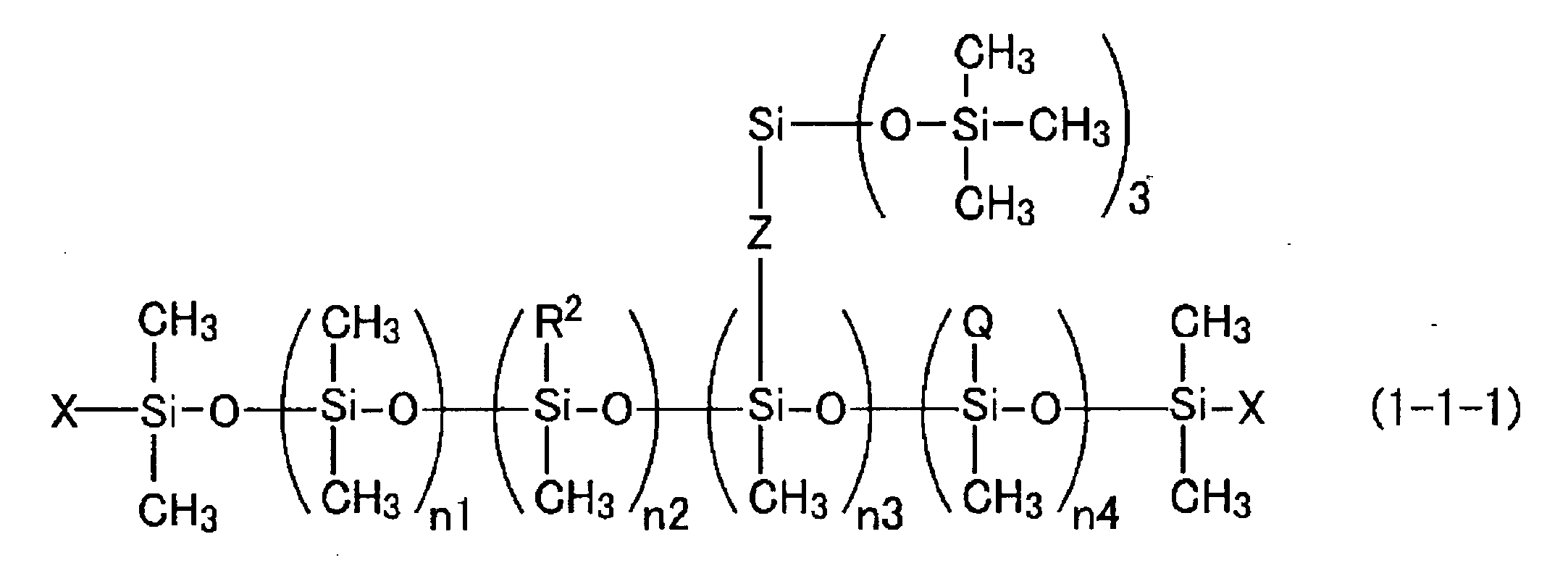
- Examples of the glycerin derivative-modified silicone include the following structural formula (1-1-1): (Where R 2 , Q, X, Z, n1, n2, n3 and n4 are as described above), or the following structural formula (1-1-2): (Where R 2 , Q, X, Z, n1, n2, n3 and n4 are as described above), and a glycerin derivative-modified silicone represented by
- the modification rate of the organopolysiloxane by the organic group containing a glycerin derivative group is preferably in the range of 0.001 to 50 mol% of all functional groups bonded to the polysiloxane as the main chain, and 0.01 to 30 The range is more preferably in the range of mol%, and still more preferably in the range of 0.1 to 10 mol%.
- Modification rate (mol%) (number of glycerol derivative group-containing organic groups bonded to silicon atoms per molecule) / ⁇ 6 + 2 ⁇ (n1 + n2 + n3 + n4) ⁇ ⁇ 100
- Modification rate (mol%) (number of glycerol derivative group-containing organic groups bonded to silicon atoms per molecule) / ⁇ 6 + 2 ⁇ (n1 + n2 + n3 + n4) ⁇ ⁇ 100
- Modification rate (mol%) (number of glycerol derivative group-containing organic groups bonded to silicon atoms per molecule) / ⁇ 6 + 2 ⁇ (n1 + n2 + n3 + n4) ⁇ ⁇ 100
- a glycerin derivative-modified silicone represented by the structural formula of MD GLY 10 M ⁇ composed of dodecylsiloxane having 10 glycerin derivative group-containing organic groups (GLY groups)
- GLY groups there are 26 silicon atom bonding functional
- the glycerin derivative-modified silicone includes, for example, (a1) a glycerin derivative having one reactive unsaturated group in one molecule in the presence of a hydrosilylation reaction catalyst, and (b1) an organopolysiloxane having a silicon atom-bonded hydrogen atom.
- the reactive unsaturated group is preferably an alkenyl group or an unsaturated fatty acid ester group which is an unsaturated functional group having a carbon-carbon double bond.
- the above -R 1 is introduced by the component (c1), the above -L 1 is introduced by the component (d1), and the above -R 2 is introduced by the component (e1).
- the glycerin derivative-modified silicone can be obtained as follows.
- the glycerin derivative-modified silicone is an organopolysiloxane having a silicon-hydrogen bond, an unsaturated organic compound having a carbon-carbon double bond at one end of the molecular chain, and a carbon-carbon double bond in the molecule. It can be obtained by addition reaction of an unsaturated ether compound of a glycerin derivative having A siloxane dendron compound having a carbon-carbon double bond at one end of the molecular chain and / or an unsaturated long-chain hydrocarbon compound having a carbon-carbon double bond at one end of the molecular chain or a piece of molecular chain A chain organopolysiloxane having a carbon-carbon double bond at the terminal may be further subjected to an addition reaction.
- the glycerin derivative-modified silicone may be the unsaturated organic compound, the unsaturated ether compound of the glycerin derivative, and optionally the siloxane dendron compound and / or the unsaturated long-chain hydrocarbon compound or It can be obtained as a hydrosilylation reaction product of a chain organopolysiloxane having a carbon-carbon double bond at one end of the molecular chain and a SiH group-containing siloxane.
- the organic group and the glycerin derivative group-containing organic group, and optionally the silylalkyl group having a siloxane dendron structure, and / or the long-chain hydrocarbon group or the chain organopolysiloxane group are converted into the glycerin derivative-modified silicone.
- the glycerin derivative-modified silicone is represented by the following general formula (1 ′) in the presence of a hydrosilylation reaction catalyst: (Where R 1 , a, b, c and d are as described above) (b2) an organohydrogensiloxane and (a2) at least a glycerol derivative having one reactive unsaturated group in one molecule It can be obtained by reaction. (D) a siloxane dendron compound having one reactive unsaturated group in one molecule, and / or (e) a hydrocarbon compound or reactive unsaturated group having one reactive unsaturated group in one molecule. It is preferable to further react the chain organopolysiloxane having one in one molecule.
- the glycerin derivative-modified silicone includes (a2) a glycerin derivative having one reactive unsaturated group in one molecule, and optionally (d) a siloxane dendron compound having one reactive unsaturated group in one molecule. And / or (e) a hydrocarbon compound having one reactive unsaturated group in one molecule or a chain organopolysiloxane having one reactive unsaturated group in one molecule,
- the component (a2), the component (d) and / or the component (e), and (b2) the organohydrogensiloxane represented by the general formula (1 ′) are reacted together or b2)
- An organohydrogensiloxane and optionally the component (d) and / or the component (e) are sequentially subjected to an addition reaction, and then the component (a2) is further subjected to an addition reaction. More, it is possible to suitably manufacture.
- the glycerin derivative-modified silicone is preferably synthesized by hydrosilylation reaction of (a) a glycerin derivative having a carbon-carbon double bond at the end of the molecular chain and (b) an organohydrogenpolysiloxane.
- the organohydrogensiloxane as the component (b) is obtained by reacting the component (d1) and / or the component (e1) with the organohydrogensiloxane by a sequential addition reaction.
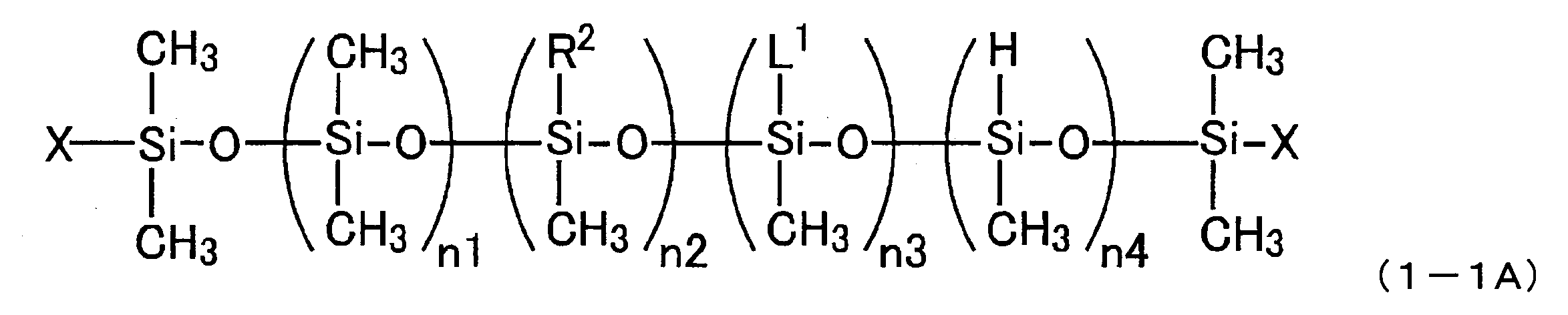
- the organohydrogensiloxane immediately before the reaction with the component (a) (after the sequential reaction with other components) is preferably represented by the following structural formula (1-1A).
- the glycerin derivative having one reactive unsaturated group in one molecule used for the synthesis of the glycerin derivative-modified silicone is preferably (a) a glycerin derivative having a carbon-carbon double bond at the end of the molecular chain. is there.
- a glycerin derivative having a carbon-carbon double bond at the end of the molecular chain. there.
- These are (poly) glycerin derivatives having a reactive functional group such as an alkenyl group at the molecular chain end, such as allyl (poly) glycerol, allyl polyglycidyl ether, and (poly) glyceryl monoallyl ether, which are synthesized by known methods. can do.
- the component (a) is (poly) glycerin monoallyl ether, (poly) glyceryl eugenol, and has a monoglycerin, diglycerin, triglycerin or tetraglycerin structure (poly). ) A glycerin compound.
- Such component (a) examples include glycerin derivatives having a carbon-carbon double bond at the end of the molecular chain represented by the following structural formulas (4-1 ′) to (4-4 ′).
- X 1 , X 2 and R 10 are the same groups as described above, and m and q are the same numbers as described above.
- R ′ is an unsaturated organic group having a carbon-carbon double bond at the terminal, and is preferably a substituted or unsubstituted, linear or branched unsaturated hydrocarbon group having 3 to 5 carbon atoms.
- the unsaturated hydrocarbon group having 3 to 5 carbon atoms include alkenyl groups such as an allyl group, a butenyl group, and a methallyl group. Preferably, it is an allyl group.
- h j is one carbon molecular chain terminal represented by ⁇ represents a silylalkyl group represented by a number ranging from 0 to 3) - preferably a compound having a siloxane dendron structure having a carbon-carbon double bond .
- (E) A hydrocarbon compound having one reactive unsaturated group in one molecule or a chain-organopolysiloxane having one reactive unsaturated group in one molecule used for the synthesis of the glycerin derivative-modified silicone according to the present invention
- siloxane the following general formula: (2 ′) Wherein R ′ is as described above, R 2 ′ represents a substituted or unsubstituted, linear or branched monovalent hydrocarbon group having 7 to 58 carbon atoms), or the following general formula (2-1); (Wherein R 11 , t and r are as defined above) or the following general formula (2-2); A monounsaturated organic compound represented by the formula (wherein R 11 and r are as described above) is preferable.
- the hydrocarbon compound having one reactive unsaturated group per molecule is preferably a monounsaturated hydrocarbon having 9 to 30 carbon atoms, more preferably 1-alkene.
- 1-alkene include 1-nonene, 1-decene, 1-undecene, 1-dodecene, 1-tridecene, 1-tetradecene, 1-hexadecene, 1-octadecene and the like.
- Examples of the chain organopolysiloxane having one reactive unsaturated group per molecule include one-end vinyl group-capped dimethylpolysiloxane and one-end vinyl group-capped methylphenyl polysiloxane.
- the hydrosilylation reaction for synthesizing the glycerin derivative-modified silicone or the composition containing the same can be performed according to a known method in the presence or absence of a solvent.
- the reaction solvent includes alcohol solvents such as ethanol and isopropyl alcohol; aromatic hydrocarbon solvents such as toluene and xylene; ether solvents such as dioxane and THF; n-hexane, cyclohexane, n-heptane, cyclohexane Examples thereof include aliphatic hydrocarbon solvents such as heptane and methylcyclohexane; chlorinated hydrocarbon organic solvents such as carbon tetrachloride.
- the hydrosilylation reaction may be performed in the absence of a catalyst, but is preferably performed in the presence of a catalyst because the reaction proceeds at a low temperature and in a short time.
- a catalyst include platinum, ruthenium, rhodium, palladium, osmium, iridium and other compounds, and platinum compounds are particularly effective because of their high catalytic activity.
- platinum compounds include: chloroplatinic acid; metal platinum; a metal platinum supported on a carrier such as alumina, silica, carbon black; platinum-vinylsiloxane complex, platinum-phosphine complex, platinum-phosphite complex And platinum complexes such as platinum alcoholate catalysts.
- the amount of the catalyst used is about 0.0001 to 0.1% by mass as metal platinum, and is preferably in the range of 0.0005 to 0.05% by mass, but is not limited thereto. .
- the reaction temperature of the hydrosilylation reaction is usually 30 to 120 ° C., and the reaction time is usually 10 minutes to 24 hours, preferably 1 to 10 hours.
- the ratio of the amount of silicon-bonded hydrogen atoms to be added] is preferably in the range of 0.8 to 1.5, and more preferably in the range of 1.0 to 1.3. That is, when synthesizing the glycerin derivative-modified silicone or the glycerin derivative-modified silicone-containing composition according to the present invention, it is more preferable to use the glycerin derivative group-containing compound slightly in excess.
- the ratio is less than 0.8, unreacted organohydrogenpolysiloxane may remain.
- the remaining organohydrogenpolysiloxane reacts with other raw materials to cause hydrogen gas generation.
- it may cause undesirable effects such as alteration of the external preparation or cosmetic preparation, the cause of fire, and the expansion of the container.
- the ratio of Si—O—C crosslinks increases and gelation occurs during production.
- the above ratio exceeds 0.8, that is, the glycerin derivative group-containing compound is reacted under more than 0.8 equivalents so that the organohydrogenpolysiloxane can be completely consumed safely.
- the glycerin derivative-modified silicone may be a liquid organic modified silicone having a glycerin derivative group-containing organic group bonded to a silicon atom and having a cross-linked structure including a carbon-silicon bond in the cross-linking portion.
- the organically modified silicone is (A) organohydrogenpolysiloxane, (B) a glycerin derivative group-containing organic compound having one or more reactive unsaturated groups in one molecule, and (C) (C1) an organic having an average number of reactive unsaturated groups greater than 1 in one molecule.
- the (A) organohydrogenpolysiloxane is not particularly limited as long as it has a silicon atom hydrogen atom, but on average more than one, preferably 1.01 to 100, more preferably Preferred are those having silicon-bonded hydrogen atoms of 1.1 to 50, more preferably 1.2 to 25, particularly preferably 1.3 to 10, and linear, branched or network organopolysiloxanes. Can be used. There is no restriction
- one type of organohydrogenpolysiloxane may be used, or two or more types of organohydrogenpolysiloxane may be used.
- component (A) examples include 1,1,3,3-tetramethyldisiloxane, 1,3,5,7-tetramethylcyclotetrasiloxane, trimethylsiloxy group-blocked methylhydrogenpolysiloxane at both ends, and both ends.
- Trimethylsiloxy-blocked dimethylsiloxane / methylhydrogensiloxane copolymer dimethylhydrogensiloxy-blocked dimethylsiloxane at both ends, dimethylhydrogensiloxy-blocked dimethylpolysiloxane at both ends, dimethylhydrogensiloxy-blocked dimethylsiloxane / methyl at both ends
- Hydrogensiloxane copolymer trimethylsiloxy group-capped methylhydrogensiloxane / diphenylsiloxane copolymer, both ends trimethylsiloxy group-capped methylhydrogensiloxane / diphenylsilo San dimethylsiloxane copolymer, (CH 3) a copolymer consisting of 2 HSiO 1/2 units and SiO 4/2 units, and (CH 3) 2 HSiO 1/2 units and SiO 4/2 units (C Examples are copolymers comprising 6 H 5 ) SiO 3/2 units.
- the component (A) is an average composition formula (1): R 1 e H f SiO (4-ef) / 2 (1) (Wherein R 1 independently represents a monovalent organic group, and 1.0 ⁇ e ⁇ 3.0 and 0.001 ⁇ f ⁇ 1.5). preferable.
- the molecular structure of the organohydrogenpolysiloxane is not limited, and examples thereof include linear, partially branched linear, branched, cyclic, and dendritic, preferably linear.
- the molecular weight is not specifically limited, From a low molecular weight body to a high molecular weight body can be used.
- the number average molecular weight is preferably in the range of 1 to 1,000,000, more preferably in the range of 300 to 500,000.
- Organohydrogenpolysiloxanes are (i) a side chain only, (ii) one end of a side chain or molecular chain, and (iii) a straight chain having silicon-bonded hydrogen atoms at both ends of the side chain or molecular chain.
- Organohydrogenpolysiloxane Organohydrogenpolysiloxane.
- the monovalent organic group is not particularly limited, but the following (D1) to (D10) (D1) a substituted or unsubstituted, linear or branched monovalent hydrocarbon group having 1 to 60 carbon atoms, (D2) —R 8 O (AO) z R 9 (wherein AO represents an oxyalkylene group having 2 to 4 carbon atoms, and R 8 is a substituted or unsubstituted straight chain having 3 to 5 carbon atoms.
- An ester group represented by the formula (1) represents a substituted or unsubstituted, linear or branched monovalent hydrocarbon group; (D6) —R 17 —OCOR 18 (wherein R 17 represents a
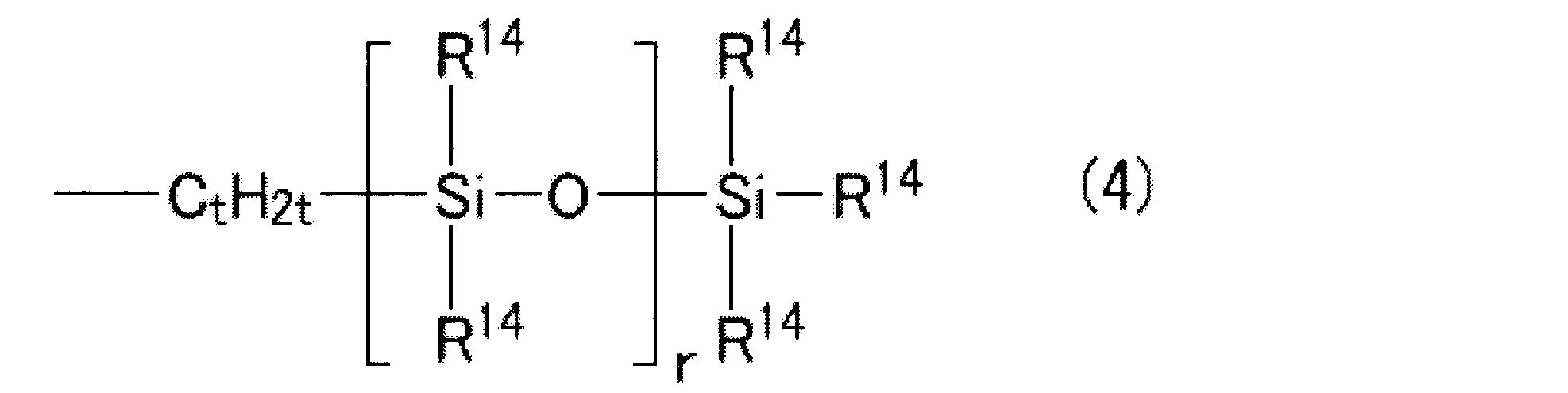
- R 14 are each independently a substituted or unsubstituted, straight or branched, monovalent hydrocarbon group having 1 to 30 carbon atoms, a hydroxyl group or a hydrogen atom, the R 14 At least one of which is the monovalent hydrocarbon group, t is a number in the range of 2 to 10, and r is a number in the range of 1 to 100).
- Alkyl groups (D9) The following general formula (5) (Wherein R 15 represents a substituted or unsubstituted, linear or branched divalent hydrocarbon group having 2 to 20 carbon atoms), (D10) The following general formula (6) (Wherein R 16 represents a substituted or unsubstituted, straight-chain or branched divalent hydrocarbon group having 2 to 20 carbon atoms, and R 6 and R 7 are each independently hydrogen. It is preferably selected from alicyclic epoxy groups represented by an atom or a substituted or unsubstituted monovalent hydrocarbon group having 1 to 30 carbon atoms.
- Examples of the substituted or unsubstituted linear or branched monovalent hydrocarbon group in (D1), (D2), (D5) to (D8) and (D10) include, for example, a methyl group, an ethyl group, Alkyl groups such as propyl, butyl, pentyl, hexyl, heptyl and octyl; cycloalkyl such as cyclopentyl and cyclohexyl; alkenyl such as vinyl, allyl and butenyl; phenyl and tolyl Aryl groups such as aralkyl groups; aralkyl groups such as benzyl groups; and hydrogen atoms bonded to carbon atoms of these groups are at least partially halogen atoms such as fluorine, or epoxy groups, glycidyl groups, acyl groups, carboxyl groups , Groups substituted with organic groups including amino group, methacryl group, mercapto group and the like.
- Examples of the substituted or unsubstituted linear or branched divalent hydrocarbon group in (D2), (D5), (D6), (D9) and (D10) include the following.
- Examples of the substituted or unsubstituted, linear or branched divalent hydrocarbon group having 1 to 30 carbon atoms include, for example, methylene group, dimethylene group, trimethylene group, tetramethylene group, pentamethylene group, hexamethylene
- a linear or branched alkylene group having 1 to 30 carbon atoms such as a group, a heptamethylene group, an octamethylene group, etc .
- a carbon atom number 2 to 2 such as a vinylene group, an arylene group, a butenylene group, a hexenylene group, an octenylene group, etc.
- the divalent hydrocarbon group is preferably an alkylene group having 1 to 30 carbon atoms, more preferably an alkylene group having 1 to 6 carbon atoms, and more preferably an alkylene group having 3 to 5 carbon atoms.
- Examples of the substituted or unsubstituted, linear or branched alkoxy group in (D3) include lower alkoxy groups such as methoxy group, ethoxy group, isopropoxy group, butoxy group, lauryl alkoxy group, myristyl alkoxy group, pal Examples include higher alkoxy groups such as a mitylalkoxy group, an oleylalkoxy group, a stearylalkoxy group, and a behenylalkoxy group.
- the alkyl group having 1 to 6 carbon atoms includes methyl, ethyl, n-propyl, i-propyl, n-butyl, i-butyl.
- Linear, branched or cyclic alkyl groups such as s-butyl, pentyl, neopentyl, cyclopentyl and hexyl.
- the number k of layers is industrially preferably an integer of 1 to 3, more preferably 1 or 2.
- the group represented by L 1 is represented as follows.
- R 12 , R 13 and Z are the same groups as described above.
- L 1 is represented by the following general formula (3-1).
- L 1 is represented by the following general formula (3-2).
- L 1 is represented by the following general formula (3-3).
- h 1 , h 2 and h 3 are each independently a number in the range of 0 to 3. These h i are particularly preferably numbers in the range of 0 to 1, and h i is particularly preferably 0.
- each Z is independently a divalent organic group, specifically, a silicon-bonded hydrogen atom, an alkenyl group, an acryloxy group
- examples include divalent organic groups formed by addition reaction of a functional group having an unsaturated hydrocarbon group such as a methacryloxy group at the end.
- the functional group is not limited to this, and can be selected as appropriate.
- each Z independently represents the following general formula: Is a group selected from divalent organic groups represented by the formula:
- Z in L 1 is preferably a divalent organic group represented by the general formula —R 19 — introduced by the reaction of a silicon-bonded hydrogen atom and an alkenyl group.
- Z is preferably a divalent organic group represented by —R 19 —COO—R 20 — introduced by reaction of a silicon-bonded hydrogen atom with an unsaturated carboxylic ester group.
- k is 2 or more
- L 2 ⁇ L in silylalkyl group represented by k a is L i
- Z is -R or an alkylene group having 2 to 10 carbon atoms 19 -COO-R 20 - in
- the divalent organic group is preferably a group selected from an ethylene group, a propylene group, a methylethylene group, a hexylene group, and —CH 2 C (CH 3 ) COO—C 3 H 6 —. Particularly preferred.
- each R 19 independently represents a substituted or unsubstituted, linear or branched alkylene group or alkenylene group having 2 to 22 carbon atoms, or 6 to 22 carbon atoms.
- R 19 is a linear alkylene group such as ethylene group, propylene group, butylene group, hexylene group; methylmethylene group, methylethylene group, 1-methylpentylene group, 1,4-dimethylbutylene group.
- R 20 is an ethylene group
- a propylene group is preferably a group selected from methyl ethylene group or a hexylene group.
- R 20 is a group selected from divalent organic groups represented by the following formula.
- the glycerol derivative group-containing organic compound having a reactive unsaturated group is not particularly limited as long as it has one or more reactive unsaturated groups and glycerol derivative group-containing organic groups in one molecule, A glycerin derivative having a carbon-carbon double bond at the end of the molecular chain is preferred, and a mono- or di- or tri- or tetra-glycerin derivative is more preferred.
- allyl monoglycerol monoglyceryl monoallyl ether
- allyl diglycerol diglycerol (diglycerin monoallyl ether)
- triglycerin monoallyl ether triglycerin monoallyl ether
- triglyceryl diallyl ether tetraglycerin monoallyl ether
- an organic compound having an average number of reactive unsaturated groups larger than 1 in one molecule is preferably more than 1.0, preferably 1.01 to 1 in one molecule. 10, more preferably 1.2 to 8, even more preferably 1.5 to 6, particularly preferably 2.0 to 4.5 reactive unsaturated groups, preferably carbon-carbon double bonds
- a linear, branched or network organic compound can be used.
- an organopolysiloxane, an unsaturated aliphatic hydrocarbon, or an unsaturated polyether compound is preferable.
- the reactive unsaturated group on the organic compound preferably organopolysiloxane or unsaturated aliphatic hydrocarbon or unsaturated polyether compound, and it is located either on the main chain or at the end. It doesn't matter. However, from the viewpoint of easy control of the crosslinking density, it is preferable to use a high-purity compound having two unsaturated groups in one molecule, for example, those positioned at both ends.
- the reactive unsaturated group is preferably present in the unsaturated aliphatic hydrocarbon group.
- the unsaturated aliphatic hydrocarbon group preferably has 2 to 30 carbon atoms, and more preferably has 2 to 20 carbon atoms.
- Examples of the monovalent unsaturated aliphatic hydrocarbon group having 2 to 30 carbon atoms include vinyl, 1-propenyl, allyl, isopropenyl, 1-butenyl, 2-butenyl, pentenyl, and hexenyl.
- a linear or branched alkenyl group such as a group; a cycloalkenyl group such as a cyclopentenyl group or a cyclohexenyl group; a cycloalkenylalkyl group such as a cyclopentenylethyl group, a cyclohexenylethyl group or a cyclohexenylpropyl group; and an ethynyl group And alkynyl groups such as propargyl group.
- Alkenyl groups are preferred, with vinyl and hexenyl groups being particularly preferred.
- the unsaturated aliphatic hydrocarbon group containing a reactive unsaturated group is preferably bonded to a silicon atom.
- the group bonded to the silicon atom other than the unsaturated aliphatic hydrocarbon has a substituted or unsubstituted monovalent hydrocarbon group or a reactive functional group. It can be a monovalent organic group.
- the substituted or unsubstituted monovalent hydrocarbon group is typically a substituted or unsubstituted, linear or branched, 1 to 30 carbon atoms, preferably 1 to 10 carbon atoms, more preferably A monovalent saturated hydrocarbon group having 1 to 4 carbon atoms and a monovalent aromatic hydrocarbon group having 6 to 30 carbon atoms, more preferably 6 to 12 carbon atoms.
- the component (C1) may have a C 1-12 alkoxy group such as a hydroxyl group, a methoxy group, an ethoxy group, a propoxy group, or a butoxy group as a monovalent organic group.
- Examples of the monovalent saturated hydrocarbon group having 1 to 30 carbon atoms include a methyl group, an ethyl group, an n-propyl group, an isopropyl group, an n-butyl group, an isobutyl group, a sec-butyl group, and a tert-butyl group.
- a linear or branched alkyl group such as a pentyl group, a hexyl group, a heptyl group, an octyl group, a nonyl group and a decyl group, and a cycloalkyl group such as a cyclopentyl group, a cyclohexyl group, a cycloheptyl group and a cyclooctyl group.
- a cycloalkyl group such as a cyclopentyl group, a cyclohexyl group, a cycloheptyl group and a cyclooctyl group.
- Examples of the monovalent aromatic hydrocarbon group having 6 to 30 carbon atoms include aryl groups such as phenyl, tolyl, xylyl, and mesityl groups.
- a phenyl group is preferred.
- the aromatic hydrocarbon group includes a group in which an aromatic hydrocarbon and an aliphatic saturated hydrocarbon are combined in addition to a group consisting of only an aromatic hydrocarbon.
- Examples of the group in which an aromatic hydrocarbon and a saturated hydrocarbon are combined include an aralkyl group such as a benzyl group or a phenethyl group.
- the hydrogen atom on the monovalent hydrocarbon group may be substituted with one or more substituents, and examples of the substituent include a halogen atom (a fluorine atom, a chlorine atom, a bromine atom and an iodine atom), a hydroxyl group , An amide group, an ester group, a carboxyl group, and an isocyanate group.
- a monovalent saturated or aromatic hydrocarbon group having at least one substituent is preferred.
- Examples of the monovalent organic group having a reactive functional group include a reactive functional group selected from the group consisting of a hydroxyl group, a mercapto group, an epoxy group, an amino group, an amide group, an ester group, a carboxyl group, and an isocyanate group. And monovalent saturated or aromatic hydrocarbon groups. There may be one or more reactive functional groups present in the monovalent organic group.
- Preferred R 1 is a monovalent saturated or aromatic hydrocarbon group having at least one reactive functional group as described above.
- the reactive functional group examples include a 3-hydroxypropyl group, a 3- (2-hydroxyethoxy) propyl group, a 3-mercaptopropyl group, a 2,3-epoxypropyl group, and a 3,4-epoxybutyl group.
- the linear component (C1) a linear or branched polysiloxane is preferable.
- the linear component (C1) is preferably a polymer containing a diorganosiloxane unit and a triorganosiloxy unit.
- the branched (C1) component is particularly preferably a polymer containing a diorganosiloxane unit, an organosilsesquioxane unit, and a triorganosiloxy unit.
- silicon-bonded organic groups in these units include alkyl groups such as methyl, ethyl, and propyl; alkenyl groups such as vinyl, allyl, butenyl, and hexenyl; and aryls such as phenyl and tolyl.
- a monovalent hydrocarbon group such as a halogenated alkyl group such as a 3,3,3-trifluoropropyl group, and may have a very small amount of a hydroxyl group, and further an alkoxy group such as a methoxy group
- the at least two silicon-bonded organic groups in the polymer must be unsaturated aliphatic hydrocarbon groups, especially alkenyl groups.
- the ratio of these units is not limited, but in this polymer, the amount of diorganosiloxane units is in the range of 80.00 to 99.65 mol%, and the organosilsesquioxane units are 0.10 to Preferably the amount is in the range of 10.00 mol% and the remaining mol% is triorganosiloxy units.
- component (C1) for example, an average composition formula (2-5): R 5 p R 6 q SiO (4-pq) / 2 (2-5)
- R 5 represents a monovalent organic group that may be independent of each other but different from R 6
- R 6 independently of each other represents a monovalent unsaturated aliphatic hydrocarbon group having 2 to 30 carbon atoms, and 1.0 ⁇ p ⁇ 2.5 and 0.001 ⁇ q ⁇ 1.5.
- the monovalent organic group as R 5 is not particularly limited, but the following (E1) to (E6): (E1) A substituted or unsubstituted, straight-chain or branched monovalent hydrocarbon group having 1 to 60 carbon atoms (however, a monovalent hydrocarbon having 2 to 20 carbon atoms having an aliphatic unsaturated group) (Excluding groups) (E2) hydroxyl (E3) -R 10 -COOR 11 (wherein, R 10 and R 11 are as defined above) an ester group (E4) -R 17 -OCOR 18 (wherein represented by, R 17 And R 18 is as described above) (E5) —R 21 —NR 22 COR 23 (wherein R 21 is a substituted or unsubstituted, straight chain having 2 to 20 carbon atoms) Represents a linear or branched divalent hydrocarbon group, R 22 represents a hydrogen atom or a substituted or unsubstituted, linear or branched monovalent hydrocarbon group, R 22 represents a
- R 25 and R 26 each independently represents a hydrogen atom or a substituted or unsubstituted linear or branched group having 1 to 20 carbon atoms.
- the definition, type, etc. of the substituted or unsubstituted linear or branched monovalent hydrocarbon group or divalent hydrocarbon group are as described above.
- the component (C1) may be an unsaturated aliphatic hydrocarbon.
- the unsaturated aliphatic hydrocarbon include those having two or more reactive unsaturated groups such as diene, diyne, and eneyne. Diene, diyne, and enyne are preferable in terms of crosslinking. Diene, diyne, and enyne are a group of compounds having a structure in which at least two reactive unsaturated groups are separated by one or more, preferably two or more single bonds in the molecule. These unsaturated aliphatic hydrocarbon groups may exist at the end of the molecular chain or may exist as a pendant group in the middle of the molecular chain.
- Examples of the unsaturated aliphatic hydrocarbon as the component (C1) include ⁇ , ⁇ -unsaturated alkenes and alkynes having 2 to 30 carbon atoms.
- Examples of the unsaturated polyether compound as the component (C1) include ⁇ , ⁇ -unsaturated polyethers.
- the component (C1) for example, the general formula (2-4): C m H 2m-1 O (C n H 2n O) y C m H 2m-1 (2-4) (Wherein 2 ⁇ m ⁇ 20, 2 ⁇ n ⁇ 4, y is the total number of repeating oxyethylene units, oxypropylene units and oxybutylene units, and 1 ⁇ y ⁇ 180)
- Bisalkenyl polyether compounds are mentioned.
- the unsaturated aliphatic hydrocarbon as the component (C1) include 1,4-pentadiene, 1,5-hexadiene, 1,6-heptadiene, 1,7-octadiene, 1,8-nonadiene, Examples include 1,9-decadiene, 1,11-dodecadiene, 1,13-tetradecadiene, 1,19-eicosadiene, 1,3-butadiene, 1,5-hexadiyne, 1-hexene-5-in and the like.
- the component (C1) can be used alone, or two or more components having different structures can be used in combination. That is, the component (C1) may be a mixture of one or more types of organopolysiloxane and one or more types of unsaturated aliphatic hydrocarbons. Therefore, “having an average number of reactive unsaturated groups greater than 1” here means that, when two or more organopolysiloxanes and / or unsaturated aliphatic hydrocarbons are used, on average Meaning having more than one reactive unsaturated group per molecule.
- (C2) Component (C2) As an organic compound having one or more reactive unsaturated groups and one or more epoxy groups in one molecule, a total of two or more, preferably 2 to 10, in one molecule There is no structural limitation as long as it has 2 to 7, more preferably 2 to 5, particularly preferably 2 to 4 reactive unsaturated groups and epoxy groups, and is linear, branched or network-like. Organic compounds can be used. As the organic compound, organopolysiloxane or unsaturated aliphatic hydrocarbon is preferable. The position of the organic compound, preferably organopolysiloxane or unsaturated aliphatic hydrocarbon, and the above reactive unsaturated group is not limited, and may be located either on the main chain or at the terminal. However, from the viewpoint of easy crosslink density control, it is preferable to use a high-purity compound in which the total of unsaturated groups and epoxy groups in one molecule is 2.
- the reactive unsaturated group is preferably present in the unsaturated aliphatic hydrocarbon group.
- examples of the unsaturated aliphatic hydrocarbon group include those described above.
- the unsaturated aliphatic hydrocarbon group containing a reactive unsaturated group and / or an epoxy group-containing organic group is preferably bonded to a silicon atom.
- the group bonded to the silicon atom other than the unsaturated aliphatic hydrocarbon or the epoxy group-containing organic group is the above-described substituted or unsubstituted monovalent hydrocarbon. Or a monovalent organic group having a reactive functional group.
- an epoxy group-containing unsaturated aliphatic hydrocarbon having at least one epoxy group is preferable.
- the unsaturated aliphatic hydrocarbon include the compounds having an unsaturated aliphatic hydrocarbon group described above. A compound having a monounsaturated aliphatic hydrocarbon group is preferred.
- Examples of the component (C2) include general formula (2-6): (In the formula, R 4 has one reactive unsaturated group, and represents a substituted or unsubstituted, linear or branched, monovalent hydrocarbon group having 2 to 20 carbon atoms)
- the definitions, types, and the like of the reactive unsaturated group and the substituted or unsubstituted linear or branched monovalent hydrocarbon group in the above general formula are as described above.
- epoxy group-containing unsaturated aliphatic hydrocarbon as the component (C2) include allyl glycidyl ether, methallyl glycidyl ether, 1-methyl-4-isopropenyl cyclohexene oxide, and 1,4-dimethylcyclohexene oxide.
- 4-vinylcyclohexene oxide, vinyl norbornene monoxide, dicyclopentadiene monooxide, butadiene monoxide, 1,2-epoxy-5-hexene, 1,2-epoxy-9-decene, 2,6-dimethyl-2, 3-epoxy-7-octene is exemplified.
- 4-vinylcyclohexene oxide is preferable.
- the component (C2) can be used alone, or two or more components having different structures can be used in combination.
- the reaction for producing the glycerin derivative-modified silicone can be performed according to a known method in the presence or absence of a reaction solvent.
- the reaction between the unsaturated group and the Si—H group is a hydrosilylation reaction.
- C2 When crosslinking is performed using an organic compound epoxide having one or more reactive unsaturated groups and one or more epoxy groups in one molecule, the reaction between the unsaturated group and the Si—H group. And the formation of an ether bond by self-ring-opening polymerization between epoxy groups (cationic polymerization reaction that occurs in the presence of a SiH group and a platinum catalyst) occurs to form a crosslink.
- irradiation with high energy rays such as ultraviolet rays or a general catalyst for cationic polymerization can be further added.
- the reaction solvent is not particularly limited as long as it is non-reactive, but alcohol solvents such as ethanol and isopropyl alcohol; aromatic hydrocarbon solvents such as toluene and xylene; ether solvents such as dioxane and THF An aliphatic hydrocarbon solvent such as n-hexane, cyclohexane, n-heptane, cycloheptane, and methylcyclohexane; and a chlorinated hydrocarbon organic solvent such as carbon tetrachloride. You may use the oil agent mentioned later as a reaction solvent.
- a composition comprising a liquid organically modified silicone having a glycerin derivative group-containing organic group bonded to a silicon atom and having a cross-linked structure containing a carbon-silicon bond in the cross-linking portion and an oil agent when an oil agent is used as a reaction solvent. Can be obtained directly.
- the hydrosilylation reaction may be performed in the absence of a catalyst, but is preferably performed in the presence of a catalyst because the reaction proceeds at a low temperature in a short time.
- the hydrosilylation reaction catalyst include compounds such as platinum, ruthenium, rhodium, palladium, osmium, iridium and the like, and platinum compounds are particularly effective because of their high catalytic activity.
- platinum compounds include: chloroplatinic acid; metal platinum; a metal platinum supported on a carrier such as alumina, silica, carbon black; platinum-vinylsiloxane complex, platinum-phosphine complex, platinum-phosphite complex And platinum complexes such as platinum alcoholate catalysts.
- the amount of the catalyst used is about 0.5 to 1000 ppm as platinum metal when using a platinum catalyst.
- the reaction temperature of the hydrosilylation reaction is usually 30 to 150 ° C., and the reaction time is usually 10 minutes to 24 hours, preferably 1 to 10 hours.
- the (A) component is crosslinked by the (C) component, and the polysiloxane chain derived from the (A) component includes a carbon-silicon bond derived from the (C) component.
- (A) component is equipped with the glycerol derivative group containing organic group derived from (B) component.
- the liquid glycerin derivative-modified silicone having a glycerin derivative group-containing organic group bonded to a silicon atom and having a cross-linked structure containing a carbon-silicon bond in the cross-linking portion according to the present invention can be obtained. .
- the liquid glycerin derivative-modified silicone having a glycerin derivative group-containing organic group bonded to a silicon atom and having a crosslinked structure containing a carbon-silicon bond in the crosslinked portion according to the present invention is essentially (C ) Having a structure connected by a cross-linked portion containing a carbon-silicon bond derived from the component, but may partially have a cross-linked portion by a Si-OC bond.
- This structure can be formed between polysiloxane chains when the components (A) to (C) have functional groups capable of condensation reaction such as silanol groups and alkoxy groups, and when the crosslinking conditions are severe, This is because the hydroxyl group in the glycerin derivative group-containing organic group derived from the component (B) may partially react with the Si—H group in (A) to be formed as a secondary.
- a liquid glycerin derivative-modified silicone having a glycerin derivative group-containing organic group bonded to a silicon atom and having a cross-linked structure containing a carbon-silicon bond in the cross-linking part according to the present invention
- the component (C) may be further reacted with the component (A), or after the reaction between the component (A) and the component (C), the component (B) is further reacted with the component (A). You may let them.
- the average value of the number of silicon atom-bonded hydrogen atoms is preferably 1.0 or more. That is, the number of silicon atom-bonded hydrogen atoms per molecule in the component (A) that constitutes a crosslinked part and reacts with the reactive unsaturated group in the component (C) is 1.0 or more on average. It is preferably in the range of 0.2 to 1.5, particularly preferably in the range of 0.6 to 1.3.
- the glycerin derivative-modified silicone is at least (D) an organopolysiloxane having a reactive functional group at both ends of the molecular chain, and (E) a reactive functional group located at both ends of the molecular chain of the (D) organopolysiloxane in the molecule 2
- It may be a glycerin derivative-modified silicone in the form of a linear glycerin derivative group-containing alternating copolymer obtained by reacting an organic compound having two reactive functional groups.
- the combination of the reactive functional groups is not particularly limited, and examples thereof include a combination of Si—H group and C ⁇ C group.
- the glycerin derivative portion is preferably contained in the molecule (E).
- examples of such a glycerin derivative group-containing alternating copolymer include those described in JP-A-2005-42097, the description of which is incorporated herein by reference.
- the high purity glycerin derivative-modified silicone obtained by the production method of the present invention is blended with an antioxidant such as phenols, hydroquinones, benzoquinones, aromatic amines, or vitamins in order to prevent oxidative degradation. , Oxidation stability can be increased.
- an antioxidant such as phenols, hydroquinones, benzoquinones, aromatic amines, or vitamins
- Oxidation stability can be increased.
- the addition of BHT (2,6-di-t-butyl-p-cresol), vitamin E, etc. further improves the stability.
- the addition amount of the antioxidant used is in the range of 10 to 1000 ppm, preferably 50 to 500 ppm, based on the weight (mass) of the high-purity glycerin derivative-modified silicone.
- Method for producing a solution containing high-purity glycerin derivative-modified silicone In the production method of the present invention, when the mixture containing the glycerin derivative-modified silicone and impurities, particularly the impurities derived from the organic modifier, contains a solvent for the glycerin derivative-modified silicone, a high-purity glycerin derivative-modified silicone is used.
- the containing solution can be manufactured.
- any solvent can be used as long as the solvent satisfies the condition of a fluid that is a good solvent for the glycerin derivative-modified silicone, and the solvent is a good solvent for the glycerin derivative-modified silicone, and It is desirable to satisfy the condition of a fluid that is a poor solvent for impurities.
- the solvent is selected from various silicone oils that are liquid at normal temperature to 100 ° C., organically modified silicone, organically modified silane compounds such as silane coupling agents, nonpolar organic compounds, or low to highly polar organic compounds.
- One or more oils and the like which may be volatile or non-volatile.
- a silicone oil agent or a silane coupling agent is optimal, but among nonpolar organic compounds and low to high polarity organic compounds, hydrocarbon oils, fatty acid ester oils, and liquid fatty acid triglycerides are preferable. Moreover, the fluid mixture of a silicone type oil agent and an organic compound may be sufficient.
- the timing of adding the solvent to a mixture containing the glycerin derivative-modified silicone as a main component and containing impurities, particularly impurities derived from an organic modifier that is a raw material of the glycerin derivative-modified silicone is the organic wax. It can be anywhere before, after, or during processing. Furthermore, the said mixture may already contain the said solvent in the step (it includes before, after, during a process) which receives the process of the acidic aqueous solution mentioned later. Regarding other points, the solution containing the high-purity glycerin derivative-modified silicone according to the present invention can be produced in the same manner as the method for producing the high-purity glycerin derivative-modified silicone according to the present invention.
- the above-mentioned antioxidant can be blended in the solution of the high purity glycerin derivative-modified silicone obtained by the production method of the present invention.
- the blending amount of the antioxidant is also as described above.
- the mixture containing the glycerin derivative-modified silicone and impurities, particularly the impurities derived from the organic modifier is treated with an acidic aqueous solution, and the odorous substance and water generated by the treatment of the acidic aqueous solution.
- an acidic aqueous solution is treated with an acidic aqueous solution, and the odorous substance and water generated by the treatment of the acidic aqueous solution.
- a glycerol derivative-modified silicone with higher purity can be obtained.
- the acidic substance contained in the acidic aqueous solution can be arbitrarily selected, but it is solid at 25 ° C. and water-soluble, and the pH at 25 ° C. of the aqueous solution when 50 g is dissolved in 1 L of ion-exchanged water. It is optimal to use one or more acidic inorganic salts characterized in that is 4 or less.
- the treatment with the acidic aqueous solution it is preferably performed before the purification treatment with the organic wax, but may be performed after or simultaneously with the purification treatment with the organic wax. .
- the treatment with the acidic aqueous solution can be most preferably carried out when the glycerin derivative-modified silicone is synthesized by a hydrosilylation reaction. Therefore, here, the case of glycerin derivative-modified silicone synthesized by hydrosilylation reaction will be described as an example of acid treatment and odor reduction method for glycerin derivative-modified silicone or a mixture containing the same.
- the acid treatment is (Ax) A glycerin derivative having a carbon-carbon double bond at the end of a molecular chain, and (bx) a hydrosilylation reaction of an organohydrogenpolysiloxane to produce a glycerin derivative-modified silicone or a reaction mixture containing the same as a main component.
- the treatment step using the acidic inorganic salt involves generation of an odor-causing substance, it may include a step of removing the odor-causing substance by heating or decompressing after the step [W]. More preferable from the viewpoint of effectiveness.
- step [V] (ax) a glycerin derivative such as (poly) glycerin monoallyl ether, (bx) a linear organohydrogenpolysiloxane represented by the structural formula (1-1A) is used.
- a glycerin derivative represented by the structural formula (1-1) A modified silicone is synthesized, and a crude product of the reaction mixture containing the glycerin derivative-modified silicone as a main component and containing the glycerin derivative-modified silicone and the unreacted component (ax) is obtained.
- the crude product is hydrolyzed using a specific acidic inorganic salt, so that the silicon-oxygen bond constituting the main chain of the polysiloxane and the carbon-oxygen bond in the side chain portion can be cleaved.
- This is a process for causing the composition to be low bromide at a high level and effectively suppressing the generation of odor over time.
- the step (W) is a step of removing odor-causing substances from the crude product of the reaction mixture containing glycerin derivative-modified silicone as a main component by hydrolysis.
- (Cx) Solid at 25 ° C. Yes, in the presence of one or more kinds of acidic inorganic salts, characterized in that the aqueous solution when dissolved in 1 L of ion-exchanged water has a pH at 25 ° C. of 4 or less when dissolved in 1 L of ion-exchanged water. It is characterized by performing.
- the pH value in the present invention is a pH value obtained by measuring a sample aqueous solution with a pH meter using a glass electrode at room temperature (25 ° C.). “HM-10P” manufactured by Denpa Kogyo Co., Ltd. was used.
- the acidic inorganic salt as the component (cx) is solid at 25 ° C., water-soluble, and the pH of the aqueous solution when 50 g is dissolved in 1 L of ion-exchanged water needs to be 4 or less. More preferably, the pH is preferably 3.5 or less, and particularly preferably 2.0 or less.
- an acidic inorganic salt for example, an acidic inorganic salt in which at least a monovalent hydrogen atom of a divalent or higher-valent inorganic acid is neutralized with a base can be used.
- the divalent or higher inorganic acid include sulfuric acid and sulfurous acid.
- the base include alkali metals and ammonia.
- the component (cx) is at least one acidic inorganic salt composed of hydrogen sulfate ion (HSO 4 ⁇ ) or hydrogen sulfite ion (HSO 3 ⁇ ) and a monovalent cation (M + ).
- the monovalent cation (M + ) include alkali metal ions and ammonium ions.
- one or more monovalent cations selected from the group consisting of sodium ion, potassium ion and ammonium ion are preferred.
- these acidic inorganic salts may be used individually by 1 type, and may be used in combination of 2 or more types.
- these acidic inorganic salts are solid at room temperature (25 ° C.), they can be easily removed by filtration after the treatment. Moreover, since it is water-soluble, it can be easily washed away with water even in a washing step after production.
- the composition after hydrolysis cannot be sufficiently brominated.
- a strong acid such as hydrochloric acid
- the hydrolysis treatment with a known solid acid such as zirconia sulfate
- Bond breakage is likely to occur.
- the acidic inorganic salt as the component (cx) include lithium hydrogen sulfate, sodium hydrogen sulfate, potassium hydrogen sulfate, rubidium hydrogen sulfate, cesium hydrogen sulfate, ammonium hydrogen sulfate, sodium hydrogen sulfite, and hydrates thereof. Illustrated.
- the pH of the aqueous solution when 50 g of the acidic inorganic salt is dissolved in 1 L of ion-exchanged water is as shown in the table below.
- one or more acidic inorganic salts selected from the group consisting of sodium hydrogen sulfate, potassium hydrogen sulfate and ammonium hydrogen sulfate are used as water-soluble acidic inorganic salts having a pH of 2.0 or less. Use is most preferred.
- the treatment in the presence of the acidic inorganic salt is performed, for example, in (1) a reaction system of a reaction mixture (for example, a reaction vessel such as a flask) containing a glycerin derivative-modified silicone synthesized by a hydrosilylation reaction as a main component.
- a reaction system of a reaction mixture for example, a reaction vessel such as a flask
- An acidic inorganic salt and water or an acidic inorganic salt and water and a hydrophilic solvent are added and stirred, and the like. It is preferable to perform the process using an acidic inorganic salt in the presence of water and / or a hydrophilic medium.
- At least an acidic inorganic salt and water are added to a reaction system containing a crude product of a reaction mixture containing a glycerin derivative-modified silicone as a main component to improve compatibility in some cases.
- Hydrolysis treatment in which another hydrophilic solvent is further added for the purpose of increasing treatment efficiency and stirring is further performed using mechanical force is preferable.
- the hydrolysis treatment can be carried out by selecting an arbitrary temperature and treatment time.
- the temperature is 0 to 200 ° C., more preferably 50 to 100 ° C., and 0.1 to 24 hours, more preferably 0.5 to
- the reaction time is preferably about 10 hours.
- the amount of the acidic inorganic salt used can be appropriately selected according to the treatment apparatus and treatment time, but is preferably in the range of 50 to 10,000 ppm, preferably 100 to 5 with respect to the reaction mixture containing glycerin derivative-modified silicone as a main component. A range of 1,000 ppm is more preferred.
- a stripping step for removing a low boiling point component (propionaldehyde or the like) that is a causative substance of odor after the acid treatment.
- the treatment in the presence of an acidic inorganic salt can be performed again to hydrolyze more propenyl ether group-containing glycerin derivatives and the like, and to remove propionaldehyde and the like that cause odor. .
- the acidic inorganic salt remains, there is no need to newly add an acidic inorganic salt, and there is an advantage that only a hydrophilic solvent represented by water needs to be added. That is, the above step [W] and the stripping step can be repeated twice or more for the purpose of increasing the degree of low bromide.
- the “low boiling point” distilled off in the stripping process includes propionaldehyde, which is the cause of odor, as well as the reaction solvent used in the hydrosilylation reaction (process [V]) and the low bromide treatment process. Used water and other hydrophilic solvents are included.
- the stripping step may be performed on the crude product of the reaction mixture containing glycerin derivative-modified silicone as a main component as the previous step of the step [W], or the step [W].
- the reaction mixture containing glycerin derivative-modified silicone as a main component may be carried out.
- it can also implement as a pre-process and post process of process [W], respectively.
- the step [W] is preferably carried out for the purpose of removing propionaldehyde which is an odor-causing substance generated by the hydrolysis reaction.
- stripping under normal pressure or reduced pressure is preferable, and it is preferable to carry out at 120 ° C. or lower.
- an inert gas injection such as nitrogen gas.
- An example of the operation of distilling off low-boiling substances is specifically shown.
- a crude product of a reaction mixture containing a glycerin derivative-modified silicone containing low-boiling substances as a main component is equipped with a reflux condenser, a nitrogen insertion port, and the like.
- the flask is charged, the inside is depressurized while supplying nitrogen gas, the temperature is raised, and the light matter is distilled off by keeping the pressure and temperature constant.
- the decompression condition is 0.1 to 10.0 KPa
- the heating temperature is 40 to 120 ° C.
- the treatment time is 10 minutes to 24 hours.
- the reaction mixture containing glycerin derivative-modified silicone as a main component may be neutralized with a basic substance.
- basic substances include inorganic bases such as sodium hydroxide, potassium hydroxide, calcium hydroxide, barium hydroxide, aqueous ammonia and sodium hydrogen carbonate, various amines, and organic bases such as basic amino acids.
- the amount of the basic substance is preferably an amount that neutralizes the reaction system containing the reaction mixture containing glycerin derivative-modified silicone as a main component, but the amount added may be adjusted so as to be weakly acidic or weakly alkaline as necessary. it can.
- an alkaline buffering agent in an amount corresponding to 100 ppm to 50000 ppm may be further added to the reaction mixture containing glycerin derivative-modified silicone as a main component obtained after the acid treatment step.
- a trace amount of acid may be locally dissolved even after a neutralization or filtration step.
- the useful alkaline buffer is not particularly limited as long as it is an alkaline buffer composed of a combination of a strong base and a weak acid, but alkaline such as trisodium phosphate, tripotassium phosphate, trisodium citrate, and sodium acetate.
- Buffering agents are exemplified. These alkaline buffering agents may be added to a glycerin derivative-modified silicone or a cosmetic raw material composed of a mixture containing the same as a main component, and other glycerin derivative-modified silicone compositions containing water and other cosmetic raw materials. Or may be added to the preparation stage of the cosmetic or the composition after blending.
- the purification treatment using the organic wax which is a feature of the present invention, is applied to the glycerin derivative-modified silicone or a mixture containing it as a main component in the presence of an acidic solution containing water as necessary. Since it is carried out after the treatment of (2), sufficient bromide-free is achieved in combination with high purification. Therefore, as long as the production method of the present invention is used, there is little need to add an alkaline buffer for the purpose of suppressing odors with time.
- the glycerin derivative-modified silicone or a mixture containing the glycerin derivative-modified silicone as a main component can be subjected to hydrogenation treatment as a pre-process or a post-process of the treatment in the presence of an acidic inorganic salt in the step [W].
- the treatment by the hydrogenation reaction may be performed after the treatment in the presence of the acidic inorganic salt according to the step [W], while the treatment by the hydrogenation reaction is performed. You may process in presence of the acidic inorganic salt concerning said process [W].
- the hydrogenation treatment generally leads to an increase in cost at the time of product manufacture.
- the high-purification treatment using the organic wax which is a feature of the present invention, is performed on the glycerin derivative-modified silicone or a mixture containing it as a main component in the presence of an acidic solution containing water as necessary. Since it is carried out after carrying out the process, non-bromide exceeding the hydrotreatment is achieved in combination with high purification. Therefore, as long as the production method of the present invention is used, there is no point in performing further hydrogenation treatment for the purpose of non-bromide.
- the second aspect of the present invention is an external preparation or cosmetic or industrial material containing the high purity glycerin derivative-modified silicone obtained by the production method of the present invention.
- the high-purity glycerin derivative-modified silicone obtained by the production method of the present invention can be suitably blended in an external preparation or cosmetic, and can constitute the external preparation or cosmetic of the present invention.
- the raw material for external preparations and cosmetics containing the high purity glycerol derivative modified silicone obtained by the manufacturing method of this invention can be manufactured, and it can also mix
- the high-purity glycerin derivative-modified silicone obtained by the production method of the present invention does not have a specific odor, and has little odor during formulation or over time.
- the silicon-oxygen bond that can constitute the main chain of the glycerin derivative-modified silicone and the carbon-oxygen bond that can constitute the side chain are hardly broken. Therefore, the high-purity glycerin derivative-modified silicone obtained by the production method of the present invention can be suitably used as an external preparation used for the human body and a raw material for cosmetics.
- the high-purity glycerin derivative-modified silicone can be diluted with an appropriate medium such as silicone oil, organic oil, alcohol, or the like, and used as a raw material for external preparations or cosmetics.
- the proportion of the high-purity glycerin derivative-modified silicone in the external preparation or cosmetic raw material is preferably 10 to 100% by weight (mass) based on the total weight (mass) of the raw material, and 20 to 100% by weight. (Mass)% is more preferred, and 30 to 100 weight (mass)% is even more preferred.
- the ratio of the raw material blended into the external preparation or cosmetic is not particularly limited, but for example, 0.1 to 40% by weight (mass)% based on the total weight (mass) of the external preparation or cosmetic. Preferably, it can be in the range of 1 to 30% by weight, more preferably 2 to 20% by weight, and even more preferably 3 to 10% by weight.
- Patent Document 14 International Patent Publication No. WO2011 / 049248
- Patent Document 15 International Patent Publication
- Co-modified organopolysiloxanes described in WO2011 / 049247) and Patent Document 17 Japanese Patent Application Laid-Open No. 2012-046507), or novel organoorganisms described in Patent Document 16 (International Patent Publication WO2011 / 049246) It is possible to apply to a common use with the polysiloxane copolymer.
- the high-purity glycerin derivative-modified silicone obtained by the production method of the present invention can be used in combination with any cosmetic raw material components, external preparations, especially cosmetic dosage forms, types and formulation examples. It can be used in the same manner as the co-modified organopolysiloxane described in Document 15 and Patent Document 17 or the novel organopolysiloxane copolymer described in Patent Document 16, and can be blended in various cosmetics.
- the cosmetics of the present invention include skin products such as skin cleanser products, skin care products, makeup products, antiperspirant products, UV protection products; hair cleanser products, hair styling products, Hair coloring products, hair nourishing products, hair rinse products, hair conditioner products, hair treatment products, etc .;
- Examples of the medicament of the present invention include, but are not limited to, hair growth agents, hair growth agents, analgesics, bactericides, anti-inflammatory agents, refreshing agents, and skin antiaging agents.
- An external preparation is applied to human skin, nails, hair, and the like.
- a pharmaceutical active ingredient can be blended and used for treatment of various diseases.
- Cosmetics are also applied to human skin, nails, hair, etc., but are used for cosmetic purposes.
- an antiperspirant, skin cleanser, skin external preparation or skin cosmetic, or a hair cleanser, hair external preparation or hair cosmetic is preferable.
- the antiperspirant, skin cleanser, skin external preparation or skin cosmetic according to the present invention contains the high-purity glycerin derivative-modified silicone obtained by the production method of the present invention, and the form thereof is not particularly limited. , Emulsion, cream, solid, semi-solid, paste, gel, powder, multilayer, mousse, water-in-oil or oil-in-water emulsion composition (emulsion composition) There may be.
- Basic cosmetics such as agents; makeup cosmetics such as foundation, makeup base, blusher, lipstick, eye shadow, eyeliner, mascara, nail enamel, etc.
- the hair cleansing agent, hair external preparation or hair cosmetic according to the present invention contains the high-purity glycerin derivative-modified silicone obtained by the production method of the present invention and can be used in various forms. For example, they may be used by dissolving or dispersing them in alcohols, hydrocarbons, volatile cyclic silicones, etc., or by dispersing them in water using an emulsifier and using them in the form of an emulsion.
- a propellant such as propane, butane, trichloromonofluoromethane, dichlorodifluoromethane, dichlorotetrafluoroethane, carbon dioxide gas or nitrogen gas can be used as a spray.
- Examples of other forms include emulsions, creams, solids, semi-solids, pastes, gels, powders, multilayers, mousses, and the like. These various forms can be used as a shampoo, rinse, conditioning, set lotion, hair spray, permanent wave, mousse, hair dye and the like.
- the external preparation or cosmetic of the present invention is a component, water, powder or colorant, alcohol, water-soluble polymer, film formation, which is used in ordinary external preparations or cosmetics as long as the effects of the present invention are not hindered.
- Agent oil agent, oil-soluble gelling agent, organically modified clay mineral, surfactant, resin, UV absorber, salt, moisturizer, preservative, antibacterial agent, fragrance, salt, antioxidant, pH adjuster, chelating agent , Refreshing agents, anti-inflammatory agents, skin beautifying agents (whitening agents, cell activators, rough skin improving agents, blood circulation promoters, skin astringents, antiseborrheic agents, etc.), vitamins, amino acids, nucleic acids, hormones, inclusions A compound or the like, a physiologically active substance, a pharmaceutically active ingredient, and a fragrance can be added, and these are not particularly limited.
- the water that can be used in the cosmetics or external preparations according to the present invention does not contain components harmful to the human body and may be clean, and examples thereof include tap water, purified water, mineral water, and deep sea water. .
- the oil agent that can be used in the cosmetic or external preparation according to the present invention is preferably one or more selected from silicone oil, nonpolar organic compound, or low polarity to high polarity organic compound that is liquid at 5 to 100 ° C.
- non-polar organic compounds and low to high polar organic compounds hydrocarbon oils, fatty acid ester oils and liquid fatty acid triglycerides are preferable. These are components that are widely used especially as base materials for cosmetics, but these oils include known vegetable oils, animal fats, higher alcohols, fatty acid triglycerides, artificial sebum, fluorine-based oils. You may use together 1 type selected from oil, or 2 or more types.
- hydrocarbon oil and / or fatty acid ester oil together with silicone oil, in addition to the refreshing feel unique to silicone oil, it retains moisture on the skin and moisturizes skin and hair in cosmetics.
- a moisturizing feeling also referred to as “moist feeling”
- a smooth feel can be imparted, and there is an advantage that the temporal stability of the cosmetic is not impaired.
- cosmetics containing hydrocarbon oils and / or fatty acid ester oils and silicone oils apply these moisturizing ingredients (hydrocarbon oils and / or fatty acid ester oils) on the skin or hair in a more stable and uniform state. Therefore, the moisturizing effect of the moisturizing component on the skin is improved.
- cosmetics containing silicone oil together with non-silicone oils can give a smoother and moist feel. There is an advantage that you can.
- fluorinated oil examples include perfluoropolyether, perfluorodecalin, and perfluorooctane.
- the powder or colorant that can be used in the cosmetic or external preparation according to the present invention is generally used as a component of cosmetics, and includes white and colored pigments and extender pigments.
- White and colored pigments are used for coloring cosmetics, while extender pigments are used for improving the feel of cosmetics.
- white and colored pigments usually used in cosmetics, and extender pigments can be used without particular limitation. In this invention, it is preferable to mix
- Powder shape (spherical, rod-like, needle-like, plate-like, irregular shape, spindle-like, bowl-like, etc.), particle size (fog-like, fine particles, pigment grade, etc.), and particle structure (porous, nonporous) Etc.) is not limited at all, but the average primary particle diameter is preferably in the range of 1 nm to 100 ⁇ m.
- these powders or colorants are blended as pigments, one or more kinds selected from inorganic pigment powders, organic pigment powders, and resin powders having an average particle diameter in the range of 1 nm to 20 ⁇ m. Is preferably blended.
- the powder examples include inorganic powders, organic powders, surfactant metal salt powders (metal soaps), colored pigments, pearl pigments, metal powder pigments, and the like, which are combined. be able to. Furthermore, what gave the water repellency process to these surfaces can be mentioned.
- the silicone elastomer powder is a crosslinked product of a linear diorganopolysiloxane mainly composed of diorganosiloxy units (D units), and an organohydrogenpolysiloxane having a silicon-bonded hydrogen atom at the side chain or terminal and a side chain or
- a diorganopolysiloxane having an unsaturated hydrocarbon group such as an alkenyl group at the terminal can be suitably obtained by a crosslinking reaction under a hydrosilylation reaction catalyst.
- Silicone elastomer powder is softer and more resilient than silicone resin powder consisting of T units and Q units, and also has excellent oil absorption, so that it absorbs fats and oils on the skin and prevents breakup of makeup. it can. And, when surface treatment is performed with the high-purity glycerin derivative-modified silicone obtained by the production method of the present invention, it is possible to perform uniform treatment with good treatment efficiency, without reducing the suede feel of the silicone elastomer powder, It is possible to impart a specific effect and feel according to the type of the high-purity glycerin derivative-modified silicone. Further, when the high-purity glycerin derivative-modified silicone is blended in the cosmetic together with the silicone elastomer powder, the dispersion stability of the powder in the entire cosmetic is improved, and a stable cosmetic over time can be obtained. .
- the silicone elastomer powder can take various shapes such as a spherical shape, a flat shape, and an indefinite shape.
- the silicone elastomer powder may be in the form of an oil dispersion.
- the cosmetic of the present invention is a silicone elastomer powder having a particle shape, and has an average primary particle diameter measured by observation using an electron microscope and / or laser diffraction / scattering method of 0.1. Silicone elastomer powder that falls within a range of ⁇ 50 ⁇ m and has a spherical primary particle shape can be suitably blended.
- the silicone elastomer constituting the silicone elastomer powder preferably has a hardness of 80 or less, more preferably 65 or less according to the type A durometer of JIS K 6253 “Testing method for hardness of vulcanized rubber and thermoplastic rubber”. .
- silicone elastomer powders the specific example of the silicone elastomer spherical powder is particularly the same as that disclosed in paragraph 0168 of Patent Document 14, and as exemplified in the paragraphs 0150 to 0152, water repellency is achieved. Silicone elastomer powder that has been subjected to various surface treatments such as the above may be used.
- the cosmetic or external preparation of the present invention can further contain other surfactants.
- These surfactants are components that function as a skin or hair washing component or an oil emulsifier, and a desired one can be selected according to the type and function of the cosmetic.
- the other surfactant is selected from the group consisting of an anionic surfactant, a cationic surfactant, a nonionic surfactant, an amphoteric surfactant, and a semipolar surfactant.
- the high-purity glycerin derivative-modified silicone obtained by the production method of the present invention has a polar group and a nonpolar group in the molecule, and thus has a function as a dispersant. For this reason, when used in combination with a nonionic surfactant, it may function as an auxiliary to improve the performance of the nonionic surfactant, and may improve the stability of the entire preparation.
- a solution containing a high-purity glycerin derivative-modified silicone or high-purity glycerin derivative-modified silicone obtained by the production method of the present invention has improved compatibility and affinity with various modified silicones.
- Polyglyceryl-modified silicone, glyceryl-modified silicone, sugar-modified silicone, sugar alcohol-modified silicone, and these silicone-based nonionic surfactants include alkyl branches, linear silicone branches, siloxane dendrimer branches, etc. Can be suitably used as well as being provided with a hydrophilic group as needed.
- one or more polyhydric alcohols and / or lower monohydric alcohols can be used depending on the purpose. These alcohols are the same as those disclosed in paragraphs 0159 and 0160 of Patent Document 14.
- one or more inorganic salts and / or organic acid salts can be used depending on the purpose. These salts are the same as those disclosed by the applicants in paragraph 0161 of Patent Document 14.
- the cosmetic or external preparation of the present invention includes a crosslinkable organopolysiloxane, organopolysiloxane elastomer spherical powder, silicone resin, acrylic silicone dendrimer copolymer, silicone raw rubber, polyamide-modified silicone, alkyl-modified silicone wax, depending on the purpose.
- silicone resin acrylic silicone dendrimer copolymer
- silicone raw rubber silicone raw rubber
- polyamide-modified silicone silicone raw rubber
- polyamide-modified silicone silicone raw rubber
- polyamide-modified silicone silicone raw rubber
- polyamide-modified silicone silicone raw rubber
- polyamide-modified silicone alkyl-modified silicone wax
- one or more water-soluble polymers can be used depending on the purpose. These water-soluble polymers are the same as those disclosed in paragraph 0201 of Patent Document 14.
- one or more ultraviolet protection components can be used depending on the purpose.
- These UV protection components are the same as the organic and inorganic UV protection components disclosed in paragraphs 0202 to 0204 of Patent Document 14, and the UV protection components that can be suitably used include finely divided titanium oxide, Fine zinc oxide, 2-ethylhexyl paramethoxycinnamate, 4-tert-butyl-4'-methoxydibenzoylmethane, hexyl diethylaminohydroxybenzoylbenzoate, benzotriazole UV absorber and 2,4,6-tris [4 -(2-Ethylhexyloxycarbonyl) anilino] 1,3,5-triazine " ⁇ INCI: octyltriazone ⁇ , 2,4-bis ⁇ [4- (2-ethyl-hexyloxy) -2-hydroxy] phenyl ⁇ -6- (4-Methoxyphenyl) -1,3,5-triazine
- UV protection components are widely used, are easily available, and have a high UV protection effect, so that they can be suitably used.
- the UV protection component is stabilized in the cosmetic while improving the overall feel and storage stability of the cosmetic. Therefore, it is possible to impart an excellent UV protection function to cosmetics.
- the cosmetics or external preparations of the present invention include oil-soluble gelling agents, organically modified clay minerals, antibacterial and antiseptics, physiologically active ingredients, skin beautifying ingredients, pH adjusters, antioxidants Various components such as a solvent, a chelating agent, a moisturizing component, and a fragrance can be used as long as the object of the present invention is not impaired.
- These cosmetic optional ingredients are the same as those disclosed in paragraphs 0207, 0208, 0220 to 0228, etc. of Patent Document 14.
- an antiperspirant active ingredient and a deodorant agent can be mix
- antiperspirant components and deodorant components are the same as those disclosed in paragraphs 0209 to 0219 of Patent Document 14.
- the cosmetic or external preparation according to the present invention is an antiperspirant composition
- the preparation and usage of various antiperspirant compositions are disclosed in paragraphs 0234 to 0275 of Patent Document 14, etc. And in common.
- the method for producing high-purity glycerin derivative-modified silicone of the present invention can be applied regardless of the type of organic modifier, is inexpensive and simple, has excellent yield or productivity, and can be easily produced on a commercial scale. It is possible. Moreover, the high-purity glycerin derivative-modified silicone obtained by the production method of the present invention is substantially free of impurities derived from organic modifiers, and thus consists of a single component. Sedimentation does not occur. In particular, the high-purity glycerin derivative-modified silicone obtained by the production method of the present invention maintains a highly transparent appearance regardless of the temperature environment to be used. Therefore, the compound is used or compounded in a cold region.
- the production process can be stabilized without inconveniences such as performance degradation and quality fluctuations due to poor compatibility between the main component and impurities.
- performance degradation and quality fluctuations due to incompatibility of the main component and impurities Since inconvenience does not occur and it is not easily affected by deterioration due to oxidation or the like, it is possible not only to stabilize the production process but also to improve the quality level of the final product. Therefore, the present invention solves a fundamental problem that has been possessed by organically modified silicones and organically modified silanes, which are difficult to purify by conventional methods.
- the high-purity glycerin derivative-modified silicone obtained by the present invention can be suitably used as a raw material for external preparations, pharmaceuticals or cosmetics, and is excellent in, for example, fiber treatment agents, heat resistance / warm resistance / electrical properties.
- Varnishes paint additives, coating agents, primers, pressure-sensitive adhesives, various polyols, foam stabilizers and modifiers for urethane and foaming agents, release agents, release agents, antifoaming agents, greases and oil compounds, insulation / Glossing / Water repellent / Heat medium / Refrigerant / Lubricating oils, Rubber / resin modifiers / additives / Surface treatment agents, Silicone modified organic resin raw materials, Silane coupling agents As a raw material for general industrial materials such as modifiers and precursors, coating / sealing materials for construction / lining, protective agents, lubricants and buffering agents for optical fibers / electric wires, and electronic / electric parts. Preferably it can be used.
- Me represents a methyl (—CH 3 ) group
- Me 3 SiO group (or Me 3 Si group) is “M”
- Me 2 SiO group is “D”
- MeHSiO group is “D H ”.
- M represents a methyl (—CH 3 ) group
- Me 3 SiO group or Me 3 Si group
- Me 2 SiO group is “D”
- MeHSiO group is “D H ”.
- M R is denoted as "M R" and "D R”.
- IPA shows isopropyl alcohol in a manufacture example.
- Step 1 215.0 g of methylhydrogenpolysiloxane represented by the average composition formula MD 47.5 DH 10.5 M in the reactor, represented by the average composition formula CH 2 ⁇ CH—Si (OSiMe 3 ) 3 16.9 g of vinyltristrimethylsiloxysilane and 0.39 g of an IPA solution of platinum-1,3-divinyl-1,1,3,3-tetramethyldisiloxane complex (Pt concentration 0.45 wt%) Heating was started with stirring under a nitrogen stream. After reacting at 30-50 ° C.
- reaction solution was collected, and an alkali decomposition gas generation method (remaining Si—H groups were decomposed with KOH ethanol / water solution, and the reaction rate was calculated from the volume of generated hydrogen gas.
- the reaction rate was as planned.
- Step 3 23.7 g of diglycerin monoallyl ether represented by the structural formula CH 2 ⁇ CH—CH 2 —O ⁇ CH 2 CH (OH) CH 2 O ⁇ 2 —H and natural vitamin E were added to the reaction solution. 0.035 g and 245 g of IPA were added, and 0.38 g of the same platinum catalyst solution as above was added. When the reaction was carried out at 45 to 65 ° C. for 1 hour and confirmed by the same method as in Step 1, the reaction rate was as planned. The amount of diglycerin monoallyl ether charged here was an excess of 1.10 moles relative to the Si—H group ( 2 DH ) to be reacted. Therefore, the excess glycerol derivative remains in the reaction solution.
- diglycerin monoallyl ether represented by the structural formula CH 2 ⁇ CH—CH 2 —O ⁇ CH 2 CH (OH) CH 2 O ⁇ 2 —H and natural vitamin E were added to the reaction solution. 0.035 g and 245 g of IPA were added, and 0.
- Step 5 The reaction solution was heated under reduced pressure and kept under conditions of 95-105 ° C. and 10 mmHg under bubbling with nitrogen gas for 1 hour to distill off low boiling components such as IPA. Thereafter, when the pressure was reduced to 75 ° C. or lower and the pressure was restored, the content liquid was a yellowish brown and transparent uniform liquid.
- Step 6 An aqueous solution prepared by dissolving 0.055 g of sodium hydrogensulfate monohydrate in 5.3 g of ion-exchanged water was charged into the reactor contents, and the mixture was stirred at 60 to 70 ° C. for 1 hour while stirring under nitrogen flow. Acid treatment was performed. Thereafter, the pressure was reduced at 66 ° C., and the pressure was restored when the distillation of water and other low-boiling components stopped (first acid treatment). Next, after 5.3 g of water was added and the treatment was performed for 10 minutes, the pressure was reduced in the same manner, and the pressure was restored when the distillation of water and other low-boiling components stopped (second acid treatment).
- R * 11, R * 21 and R * 31 are as follows.
- R * 11 -C 16 H 33
- R * 21 -C 3 H 6 O ⁇ CH 2 CH (OH) CH 2 O ⁇ 2 -H
- R * 31 -C 2 H 4 Si (OSiMe 3) 3
- Comparative Example 1 ⁇ Glycerin derivative-modified silicone No. Preparation of Comparative Composition RE-1 Containing 1> Using 340 g of the grey-brown opaque uniform liquid obtained in Production Example 1, 10 g of high flow supercell (Celite, baked product of diatomized flux) is used as a filter aid, and ADVANTEC No. Using 424 (diameter 110 mm, Toyo Roshi Kaisha, Ltd.), filtration was performed at room temperature with a pressure filter at N 2 pressure of 400 kPa. However, the turbidity was not improved at all from the beginning to the end of the filtration, and 322 g of a grayish brown opaque turbid liquid was obtained over 1 hour. ⁇ Viscosity (25 ° C.): 8400 mPa.s s ⁇ Compared with the composition obtained in Production Example 1, the appearance transparency was not improved at all.
- Comparative Example 2 ⁇ Glycerin derivative-modified silicone No. Preparation of Comparative Composition RE-2 Containing 1> Then removed gray-brown opaque turbid liquid 315g obtained in Comparative Example 1, Zeta Plus filter 30C (diameter 90 mm, 3M, zeta potential adsorption filtration filter) by, the N 2 pressure 150kPa by using a special filter Then, pressure filtration was performed. In addition, since the said filter has low pressure resistance and cannot apply a pressure exceeding 200 kPa on the property, it had to perform filtration by the pressurization state lower than the comparative example 1. FIG.
- Example 1 ⁇ High purity glycerin derivative-modified silicone No. Preparation of 1> 120 g of the grayish brown opaque uniform liquid obtained in Comparative Example 2 and 3.6 g of PEG # 20000 (polyethylene oxide with a molecular weight of 20,000, melting point: about 65 ° C.) flake product (organic wax) were charged into a flask, Heating was started with stirring. When the mixture was vigorously mixed and stirred at 80 ° C. for 40 minutes, the appearance was a uniform dispersion with white turbidity. Thereafter, the mixture was allowed to cool to 40 ° C. or lower with stirring (2 hours) to complete the treatment. The appearance of the flask contents was the same as before cooling.
- PEG # 20000 polyethylene oxide with a molecular weight of 20,000, melting point: about 65 ° C.
- flake product organic wax
- the reaction mixture was charged with 5.2 g of 3-methacryloxypropyl (tris (trimethylsiloxy) silylethyldimethylsiloxy) silane represented by the following formula: platinum-1,3-divinyl-1,1,3,3- 0.10 g of a tetramethyldisiloxane complex hexamethyldisiloxane solution (Pt concentration 0.45 wt%) was added and heating was started. After reacting at 50-60 ° C. for 2 hours, the reaction solution was collected and confirmed by an alkali decomposition gas generation method. The reaction rate was as planned.
- Step 2 In the reaction solution, 14.8 g of diglycerin monoallyl ether represented by the average composition formula CH 2 ⁇ CH—CH 2 —O (C 3 H 6 O 2 ) 2 —H, and natural vitamin E of 0. 03 g and 120 g of IPA were added, and 0.15 g of the same platinum catalyst solution as above was added.
- the reaction was carried out at 50-60 ° C. for 5.5 hours and confirmed by the same method as in Step 1.
- the reaction rate was as planned, and the average composition formula: MD 43.4 D R * 32 0.1 D R * 22 It was found that a modified silicone intermediate represented by 1.56 D R * 11 3.1 DH 2.64 M was produced.
- R * 11, R * 22, and R * 32 are as follows.
- R * 11 -C 16 H 33
- the diglycerol monoallyl ether used in Production Example 2 was synthesized by ring-opening addition of 1 mol of glycidol per 1 mol of glycerol monoallyl ether. Since glycerin monoallyl ether has two hydroxyl groups and glycidol can react with both, the diglycerin moiety here is not a single composition consisting only of a chain structure.
- Step 3 200 g of FZ-3196 (manufactured by Toray Dow Corning Co., Caprylylmethicone), which is a reaction solvent and diluent during the crosslinking reaction, is added to the reaction solution, and the pressure is reduced at 45-50 ° C. to remove IPA. went. Thereafter, the pressure was restored and 5.51 g of 1,5-hexadiene was added at 47 ° C., and an additional 0.25 g of the same platinum catalyst solution as above was further added.
- the C C / Si—H molar ratio at the time of this crosslinking reaction was 1.20. After the reaction at 50 ° C. for 8 hours, the reaction was confirmed by the same method as in Step 1. As a result, a thick cloudy liquid was obtained.
- Step 4 Reactor contents are charged with 6.0 g of 0.16% phosphoric acid aqueous solution, 80 g of IPA, and 3.0 g of ion-exchanged water, and the acid treatment is performed at 70 to 80 ° C. for 3 hours while stirring under nitrogen flow Went. Thereafter, the pressure was reduced, and from the point where distillation of low boiling point stopped, the pressure was maintained for 1.5 hours under conditions of 70 to 90 ° C. and 10 mmHg or less, and then the pressure was restored.
- the main component is a liquid organically modified silicone having a glycerin derivative group and a crosslinked part, and the crosslinked part connecting the organopolysiloxane part and the organic part by Si—C bonds, and the same amount as that.
- 395 g of a composition (reaction mixture) containing caprylyl methicone (diluent oil) as the second main component was obtained.
- This product was a grayish brown liquid having a large turbidity at 25 ° C. Viscosity (25 ° C.): 1400 mPa.s s
- Example 2 ⁇ High purity glycerin derivative-modified silicone No. Preparation of 2> 279 g of a lightly turbid pale brown viscous liquid obtained in Production Example 2 and 8.4 g of PEG # 20000 (polyethylene oxide with a molecular weight of 20,000, melting point: about 65 ° C.) flake product (organic wax) were charged into a flask, and nitrogen was added. Heating was started while stirring under circulation. When the mixture was vigorously mixed and stirred at 85 to 100 ° C. for 1 hour, the appearance was a uniform dispersion with white turbidity. Thereafter, the mixture was allowed to cool to 2.5 ° C. or less under stirring, and the treatment was completed.
- PEG # 20000 polyethylene oxide with a molecular weight of 20,000, melting point: about 65 ° C.
- organic wax organic wax
- the contents of “Comparative compositions RE-1 to RE-2 containing glycerin derivative-modified silicone No. 1 and Comparative composition RE-3 containing glycerin derivative-modified silicone No. 2” are shown in Tables 1 and 2 below. Shown in
- Odor test evaluation criteria ⁇ : Odor is not felt at all ⁇ : Aldehyde odor is not found at all, but some substrate odor is felt ⁇ : Slight aldehyde odor is observed ⁇ : Aldehyde odor with a nose is clearly recognized and uncomfortable is there
- the high-purity glycerin derivative-modified silicone obtained by the present invention can be used for various external preparations and cosmetics, for example.
- Specific examples of the formulation include silicone compounds No. 1 to No. 1 in Formulation Examples 1 to 43 of various cosmetics and external preparations described in, for example, Patent Document 14 (International Patent Publication WO2011 / 049248).
- the component corresponding to 16 and / or various polyether-modified silicones are replaced with high-purity glycerin derivative-modified silicones (high-purity glycerin derivative-modified silicone No. 1, No. 2, etc.) according to the present invention or solutions thereof. Can be mentioned.
- various components and / or various components corresponding to silicone compounds No. 1 to No. 14 in formulation examples 1 to 24 of various cosmetics and external preparations disclosed in Patent Document 15 include those obtained by replacing the polyether-modified silicone with the high-purity glycerin derivative-modified silicone (high-purity glycerin derivative-modified silicone No. 1, No. 2, etc.) or a solution thereof according to the present invention.
- silicone compounds No. 1 to No. 8 included in Formulation Examples 1 to 14 of various cosmetics and external preparations disclosed in Patent Document 17 Japanese Patent Laid-Open No. 2012-046507
- Examples include those obtained by replacing the polyether-modified silicone with the high-purity glycerin derivative-modified silicone (high-purity glycerin derivative-modified silicone No. 1, No. 2, etc.) or a solution thereof according to the present invention.
- the high-purity glycerin derivative-modified silicone of the present invention has been removed from organic modifiers that are significantly different in polarity from the silicones, and therefore, in designing prescriptions for cosmetics and external preparations, they have poor compatibility when blended with various raw materials. There are advantages that problems do not occur easily and the range of prescription design is widened. At the same time, concerns and risks related to the stability of the final product can be reduced. Compared with general organosilicon compounds with high impurity content due to high purity, there are less deterioration phenomena such as feel improvement effect, moisturizing effect, aging odor, surface active effect, emulsification performance, powder dispersion This is advantageous in terms of stability, powder surface treatment effect, or sustainability of these effects.
- the medicinal ingredients and powders are used in cosmetics and external preparations more than before due to the properties of the high-purity glycerin derivative-modified silicone obtained by the present invention.
- the original effect of the formulation is enhanced, such as improvement of makeup and color development, improvement of skin care and UV filter effect.
- the prescription which does not contain a powder it is possible to easily obtain a stable product having excellent transparency and low viscosity due to the characteristics of the high-purity glycerin derivative-modified silicone obtained by the present invention.
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Birds (AREA)
- Epidemiology (AREA)
- Dermatology (AREA)
- General Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Wood Science & Technology (AREA)
- Cosmetics (AREA)
- Silicon Polymers (AREA)
Abstract
Description
グリセリン誘導体変性シリコーン及び不純物を含有する混合物に、該不純物と親和性を有し、且つ、前記グリセリン誘導体変性シリコーンよりも高融点である有機ワックスを添加し、加熱溶融混合して、溶融した該有機ワックス内に該不純物を取り込む工程、
前記有機ワックスを冷却して有機ワックスの固化物を得る工程
前記グリセリン誘導体変性シリコーン及び前記有機ワックスの固化物を固液分離する工程
を含む製造方法によって達成される。
a 、b 、c及びdは、それぞれ、1.0≦a≦2.5、0≦b≦1.5、0≦c≦1.5、0.0001≦d≦1.5の範囲にある数である}で表される、グリセリン誘導体変性シリコーンであることができる。
(A)オルガノハイドロジェンポリシロキサン、
(B)1分子中に1以上の反応性不飽和基を有するグリセリン誘導体基含有有機化合物、並びに
(C)(C1)1分子中に平均で1より大きい数の反応性不飽和基を有する有機化合物、及び、(C2)1分子中に1以上の反応性不飽和基及び1以上のエポキシ基を有する有機化合物からなる群から選択される1種類以上の有機化合物を反応させることにより得られる{但し、前記(C)成分がグリセリン誘導体基含有有機基を含有する場合には前記(B)成分の使用は任意である}、ケイ素原子に結合したグリセリン誘導体基含有有機基を有し、且つ、架橋部にSi-C結合を含む架橋構造を有する有機変性シリコーンであることができる。
(D)分子鎖の両末端に反応性官能基を有するオルガノポリシロキサン又はその誘導体、及び
(E)分子中に前記(D)の分子鎖両末端に位置する反応性官能基と反応し得る2の反応性官能基を有する有機化合物
を少なくとも反応させて得られる直鎖状のグリセリン誘導体基含有交互共重合体であることができる。
グリセリン誘導体変性シリコーン及び不純物を含有する混合物に、該不純物と親和性を有し、且つ、前記グリセリン誘導体変性シリコーンよりも高融点である有機ワックスを添加し、加熱溶融混合して、溶融した該有機ワックス内に該不純物を取り込む工程、
前記有機ワックスを冷却して有機ワックスの固化物を得る工程
前記グリセリン誘導体変性シリコーン及び前記有機ワックスの固化物を固液分離する工程
を含む。
本発明で使用される有機ワックスとしては、不純物、特に有機変性剤(グリセリン誘導体)由来の不純物と親和性であり、且つ、前記グリセリン誘導体変性シリコーンより高融点のものである任意の有機ワックスを使用することができる。なお、本発明にかかる有機ワックスはその分子構造中にケイ素原子を含有しない。室温下で濾過等の固液分離操作を行う場合、有機ワックスの融点は任意であるが、45℃以上であることが好ましい。具体的には、前記有機ワックスは、好ましくは45℃~150℃、より好ましくは50℃~120℃以下、更により好ましくは60℃~100℃の融点を有し、また、好ましくは900以上、より好ましくは2000以上、より好ましくは5,000以上、特に好ましくは6000~50,000の数平均分子量を有する。前記有機ワックスの融点が45℃よりも低い場合、特に、有機変性剤に由来する不純物を取り込んだ後冷却により生成する固体の融点は更に低くなるため、主成分であるグリセリン誘導体変性シリコーンと当該固体とを固液分離するためには、例えば、40℃以下の温度で濾過を行う必要がある。この様な低温での濾過は、前記グリセリン誘導体変性シリコーンが高粘度の有機変性シリコーンである場合には濾過時間の増大をもたらす傾向にあり、生産効率が低下するおそれがある。また、融点が45℃よりも低いワックスは一般的に不純物を取り込んで固化させる能力が低く、固液分離性も悪くなり易い。一般に、低温濾過では濾過速度が遅くなることがあるが、ヘキサン等の溶媒で希釈して低粘度化することによって、例えば0度付近やそれ以下の低温下で濾過を行うことも可能である。なお、所望の品質、不純物の種類等に応じて、低温下で濾過を行って、積極的に固体を析出させ不純物の除去効果を高めてもよい。一方、前記有機ワックスの融点が150℃よりも高い場合には、当該ワックスを融解させるためにより多くのエネルギーを必要とするため、環境上又は効率上好ましくない。また、150℃を超える温度では、一般的にグリセリン誘導体変性シリコーン自体も劣化し易くなるため、好ましくない。
本発明を適用できるグリセリン誘導体変性シリコーンは、グリセリン誘導体で変性されたシリコーン化合物であって、液状のものであり、好ましくは少なくとも100℃で液体である。そして、この条件を満たすものであればその化学構造等に制限は無い。
a 、b 、c及びdは、それぞれ、1.0≦a≦2.5、0≦b≦1.5、0≦c≦1.5、0.0001≦d≦1.5の範囲にある数である}で表される、グリセリン誘導体変性シリコーンであることができる。
このとき、好適なb及びcの値は、必須とする官能基により以下のように表わされる。
(1)R2で表わされる基を有する場合:0.001≦b≦1.5であり、かつ0≦c≦1.5
(2)L1で表わされる基を有する場合:0≦b≦1.5であり、かつ0.001≦c≦1.5
(3)R2で表わされる基とL1で表わされる基を両方有する場合:0.001≦b≦1.5であり、かつ0.001≦c≦1.5
R2、L1及びQは、各々独立に、上記のとおりであり、
Xはメチル基、R2、L1及びQからなる群から選択される基であり、
n1、n2、n3及びn4は、それぞれ独立して、0~2,000の範囲の数であり、n1+n2+n3+n4は0~2,000の範囲の数である。但し、n4=0のとき、Xの少なくとも一方はQである)で表される直鎖状のポリシロキサン構造を有するグリセリン誘導体変性シリコーンであることが好ましい。
R2、Q、X、Z、n1、n2、n3及びn4は上記のとおりである)、又は、下記構造式(1-1-2):
R2、Q、X、Z、n1、n2、n3及びn4は上記のとおりである)で表されるグリセリン誘導体変性シリコーンがより好ましい。
変性率(モル%)=(1分子あたりの珪素原子に結合したグリセリン誘導体基含有有機基の数)/{6+2×(n1+n2+n3+n4)}×100
で示される。例えば、10個のグリセリン誘導体基含有有機基(GLY基)を有するドデシルシロキサンからなるグリセリン誘導体変性シリコーン{MDGLY 10Mの構造式で表される}の場合には、26個の珪素原子結合官能基のうち、10個がグリセリン誘導体基含有有機基により変性されているから、グリセリン誘導体基含有有機基による変性率は、38.5モル%である。
前記グリセリン誘導体変性シリコーンは、例えば、ヒドロシリル化反応触媒の存在下において、(a1)反応性不飽和基を1分子中に1つ有するグリセリン誘導体、(b1)ケイ素原子結合水素原子を有するオルガノポリシロキサン、及び、(c1)反応性不飽和基を1分子中に1つ有する有機化合物、更に必要に応じて(d1)反応性不飽和基を1分子中に1つ有するシロキサンデンドロン化合物、及び/又は(e1)反応性不飽和基を1分子中に1つ有する長鎖炭化水素化合物又は鎖状オルガノポリシロキサン化合物、を反応させることにより、得ることができる。上記の反応性不飽和基は、好適には、炭素-炭素二重結合を有する不飽和性の官能基である、アルケニル基又は不飽和脂肪酸エステル基が例示できる。成分(c1)により上記の-R1が導入され、成分(d1)により上記の-L1が導入され、成分(e1)により上記の-R2が導入される。
R1、a 、b、c及びdは上記のとおりである)で表される(b2)オルガノハイドロジェンシロキサンと、(a2)反応性不飽和基を1分子中に1つ有するグリセリン誘導体を少なくとも反応させて得ることができる。(d)反応性不飽和基を1分子中に1つ有するシロキサンデンドロン化合物、及び/又は、(e)反応性不飽和基を1分子中に1つ有する炭化水素化合物又は反応性不飽和基を1分子中に1つ有する鎖状オルガノポリシロキサンを更に反応させることが好ましい。
R1は、各々独立に、上記のとおりであり、
X’はR1又は水素原子から選択される基であり、
n1、n2、n3及びn4は上記のとおりである。但し、n2+n3+n4=0のとき、X’の少なくとも一方は水素原子である)で表されるオルガノハイドロジェンシロキサンが好ましい。
R2及びL1は、各々独立に、上記のとおりであり、
Xはメチル基、R2、L1及び水素原子(H)からなる群から選択される基であり、
n1、n2、n3及びn4は、それぞれ独立して、0~2,000の範囲の数であり、n1+n2+n3+n4は0~2,000の範囲の数である。但し、n4=0のとき、Xの少なくとも一方は水素原子である。)
R3及びR4は上記のとおりであり、RDは水素原子又はメチル基であり、
Z´は二価有機基を表し、
h1は0~3の範囲の数であり、
L´1は、R4、又は、j=1のときの下記一般式(3’’):
Zは二価有機基を表し、
jはLjで示されるシリルアルキル基の階層を表し、該シリルアルキル基の繰り返し数である階層数がk´のとき1~k´の整数であり、階層数k´は1~9の整数であり、Lj+1はjがk´未満のときは該シリルアルキル基であり、j=k´のときはR4である。
hjは0~3の範囲の数である)で表されるシリルアルキル基を表す}で表される分子鎖末端に1個の炭素-炭素二重結合を有するシロキサンデンドロン構造を有する化合物が好ましい。
R2’は炭素原子数7~58の、置換若しくは非置換の、直鎖状又は分岐状の一価炭化水素基を表す)、又は下記一般式(2-1);
前記グリセリン誘導体変性シリコーンは、ケイ素原子に結合したグリセリン誘導体基含有有機基を有し、且つ、架橋部に炭素-ケイ素結合を含む架橋構造を有する液状の有機変性シリコーンであってもよい。
(A)オルガノハイドロジェンポリシロキサン、
(B)1分子中に1以上の反応性不飽和基を有するグリセリン誘導体基含有有機化合物、並びに
(C)(C1)1分子中に平均で1より大きい数の反応性不飽和基を有する有機化合物、及び、(C2)1分子中に1以上の反応性不飽和基及び1以上のエポキシ基を有する有機化合物からなる群から選択される1種類以上の有機化合物{但し、前記(C)成分がグリセリン誘導体基含有有機基を含有する場合は前記(B)成分の使用は任意である}
を反応させることにより得ることができる。
R1 eHfSiO(4-e-f)/2 (1)
(式中、R1は、互いに独立して、一価有機基を表し、1.0≦e≦3.0、及び、0.001≦f≦1.5である)で表されるものが好ましい。
(i)R1 3SiO(R1 2SiO)v(R1SiHO)wSiR1 3
(ii)HR1 2SiO(R1 2SiO)v(R1SiHO)zSiR1 3
(iii)HR1 2SiO(R1 2SiO)v(R1SiHO)zSiR1 2H
(式中、R1は上記のとおりであり、vは0又は正の整数であり、wは正の整数であり、zは0又は正の整数である)で表されるオルガノハイドロジェンポリシロキサンが例示される。これらのオルガノハイドロジェンポリシロキサンは、(i)側鎖のみ、(ii)側鎖又は分子鎖の片末端、(iii)側鎖又は分子鎖の両末端にケイ素原子結合水素原子を有する直鎖状オルガノハイドロジェンポリシロキサンである。
(D1)炭素原子数1~60の、置換若しくは非置換の、直鎖状若しくは分岐状の一価炭化水素基、
(D2)-R8O(AO)zR9 (式中、AOは炭素原子数2~4のオキシアルキレン基を表し、R8は炭素原子数3~5の、置換若しくは非置換の、直鎖状若しくは分岐状の二価炭化水素基を表し、R9は水素原子、炭素原子数1~24の、置換若しくは非置換の、直鎖状若しくは分岐状の一価炭化水素基、又は、炭素原子数2~24の、置換若しくは非置換の、直鎖状若しくは分岐状のアシル基を表し、z=1~100である)で表されるポリオキシアルキレン基、
(D3)炭素原子数1~30の、置換若しくは非置換の、直鎖状若しくは分岐状のアルコキシ基、
(D4)水酸基、
(D5)-R10-COOR11 (式中、R10は炭素原子数2~20の、置換若しくは非置換の、直鎖状若しくは分岐状の二価炭化水素基を表し、R11は炭素原子数1~30の、置換若しくは非置換の、直鎖状若しくは分岐状の一価炭化水素基を表す)で表されるエステル基、
(D6)-R17-OCOR18 (式中、R17は炭素原子数2~20の、置換若しくは非置換の、直鎖状若しくは分岐状の二価炭化水素基を表し、R18は炭素原子数1~30の、置換若しくは非置換の、直鎖状若しくは分岐状の一価炭化水素基を表す)で表されるエステル基
(D7) L1
ここで、L1はi=1のときの下記一般式(3);
R12は、炭素原子数1~30の、置換若しくは非置換の、直鎖状若しくは分岐状の一価炭化水素基を表し、
R13は、それぞれ独立して、炭素原子数1~6のアルキル基又はフェニル基を表し、
Zは二価有機基を表し、
iはLiで示されるシリルアルキル基の階層を表し、該シリルアルキル基の繰り返し数である階層数がkのとき1~kの整数であり、階層数kは1~10の整数であり、Li+1はiがk未満のときは該シリルアルキル基であり、i=kのときはR13であり、hiは0~3の範囲の数である)で表される、シロキサンデンドロン構造を有するシリルアルキル基、
(D8)下記一般式(4)
(D9)下記一般式(5)
(D10)下記一般式(6)
から選ばれることが好ましい。
R5 pR6 qSiO(4-p-q)/2 (2-5)
(式中、R5は、互いに独立してもよいがR6とは異なる一価有機基を表し、
R6は、互いに独立して、炭素原子数2~30の一価の不飽和脂肪族炭化水素基を表し、1.0≦p≦2.5、及び、0.001≦q≦1.5である)で表される不飽和基含有シリコーン化合物が挙げられる。炭素原子数2~30の一価の不飽和脂肪族炭化水素基は既述のとおりである。
(E1)炭素原子数1~60の、置換若しくは非置換の、直鎖状若しくは分岐状の一価炭化水素基(但し、脂肪族不飽和基を有する炭素原子数2~20の一価炭化水素基を除く)
(E2)水酸基
(E3)-R10-COOR11 (式中、R10及びR11は上記の通りである)で表されるエステル基
(E4)-R17-OCOR18 (式中、R17及びR18は上記の通りである)で表されるエステル基
(E5)-R21-NR22COR23 (式中、R21は炭素原子数2~20の、置換若しくは非置換の、直鎖状若しくは分岐状の二価炭化水素基を表し、R22は水素原子又は炭素原子数1~20の置換若しくは非置換の、直鎖状若しくは分岐状の一価炭化水素基を表し、R23は炭素原子数1~30の置換若しくは非置換の、直鎖状若しくは分岐状の一価炭化水素基を表す)で表されるアミド基
(E6)-R24-CONR25R26 (式中、R24は炭素原子数2~20の、置換若しくは非置換の、直鎖状若しくは分岐状の二価炭化水素基を表し、R25及びR26は、各々独立に、水素原子又は炭素原子数1~20の置換若しくは非置換の、直鎖状若しくは分岐状の一価炭化水素基を表す)で表されるアミド基
から選ばれるものが好ましい。置換若しくは非置換の、直鎖状若しくは分岐状の一価炭化水素基又は二価炭化水素基の定義、種類等は既述のとおりである。
CH2=CH(CH2)xCH=CH2 (2-1)
(式中、1≦x≦20である)で表されるα,ω-ジエン、一般式(2-2):
CH≡C(CH2)xC≡CH (2-2)
(式中、1≦x≦20である)で表されるα,ω-ジイン、 一般式(2-3):
CH2=CH(CH2)xC≡CH (2-3)
(式中、1≦x≦20である)で表されるα,ω-エン-インが挙げられる。
CmH2m-1O(CnH2nO)yCmH2m-1 (2-4)
(式中、2≦m≦20、2≦n≦4、yはオキシエチレン単位、オキシプロピレン単位、オキシブチレン単位の繰返し数の合計値であり、1≦y≦180である)で表されるビスアルケニルポリエーテル化合物が挙げられる。
R6及びR7は、それぞれ独立して、水素原子、又は、置換若しくは非置換の炭素原子数1~30の一価炭化水素基を表す)で表される、不飽和基含有脂環式エポキシ化合物が挙げられる。上記一般式における反応性不飽和基、及び、置換若しくは非置換の、直鎖状若しくは分岐状の一価炭化水素基の定義、種類等は既述のとおりである。
前記グリセリン誘導体変性シリコーンは、少なくとも、
(D)分子鎖の両末端に反応性官能基を有するオルガノポリシロキサン、及び
(E)分子中に前記(D)オルガノポリシロキサンの分子鎖両末端に位置する反応性官能基と反応し得る2つの反応性官能基を有する有機化合物
を反応させて得られる直鎖状のグリセリン誘導体基含有交互共重合体の形式のグリセリン誘導体変性シリコーンであってもよい。反応性官能基の組み合わせは、特には限定されるものではないが、例えば、Si-H基とC=C基との組み合わせが挙げられる。この場合、グリセリン誘導体部分は前記(E)の分子中に含まれることが好適である。そのようなグリセリン誘導体基含有交互共重合体としては、例えば、特開2005-42097号公報に記載されるものが挙げられ、当該公報の記載は参照としてここに組み込まれる。
本発明の製造方法において、前記グリセリン誘導体変性シリコーン及び不純物、特に前記有機変性剤由来の不純物、を含有する混合物が、前記グリセリン誘導体変性シリコーンの溶媒を含む場合には、高純度グリセリン誘導体変性シリコーンを含有する溶液を製造することができる。
本発明の製造方法において、前記グリセリン誘導体変性シリコーン及び不純物、特に前記有機変性剤由来の不純物、を含有する混合物が、酸性水溶液によって処理されており、当該酸性水溶液の処理によって発生した臭気物質及び水が、加熱又は減圧により取り除かれている場合は、より高純度のグリセリン誘導体変性シリコーンを得ることができる。
(ax)分子鎖の末端に炭素-炭素二重結合を有するグリセリン誘導体、及び
(bx)オルガノハイドロジェンポリシロキサン
をヒドロシリル化反応させることにより、グリセリン誘導体変性シリコーン又はそれを主成分として含む反応混合物を合成する工程〔V〕;及び
上記合成工程〔V〕と共に、又は、上記合成工程〔V〕の後に、
グリセリン誘導体変性シリコーン又はそれを主成分として含む反応混合物を、
(cx)25℃で固体であり、水溶性であり、かつ、50gをイオン交換水1Lに溶解させたときの水溶液の25℃におけるpHが4以下である、1種類以上の酸性無機塩の存在下で処理する工程〔W〕
を含む。また、前記酸性無機塩を用いた処理工程は臭気原因物質の発生を伴うため、工程〔W〕の後に、加熱又は減圧することにより、臭気原因物質を除去する工程を含むことが、臭気低減の実効の観点からより好ましい。
本発明に係る化粧料又は外用剤に用いることのできる油剤は、好適には、5~100℃で液状であるシリコーンオイル、非極性有機化合物又は低極性~高極性有機化合物から選択される1以上の油剤であり、非極性有機化合物及び低極性~高極性有機化合物としては、炭化水素油及び脂肪酸エステル油及び液状脂肪酸トリグリセライドが好ましい。これらは、特に化粧料の基材として広く用いられている成分であるが、これらの油剤には、公知の植物性油脂類、動物性油脂類、高級アルコール類、脂肪酸トリグリセライド、人工皮脂、フッ素系油から選択される1種類又は2種類以上を併用しても良い。
本発明に係る化粧料又は外用剤に用いることのできる粉体又は着色剤は、化粧料の成分として一般に使用されるものであり、白色及び着色顔料、並びに、体質顔料を含む。白色及び着色顔料は化粧料の着色等に使用され、一方、体質顔料は、化粧料の感触改良等に使用される。本発明における「粉体」としては、化粧料に通常使用される白色及び着色顔料、並びに、体質顔料を特に制限なく使用することができる。本発明において、1種類又は2種類以上の粉体を配合することが好ましい。粉体の形状(球状、棒状、針状、板状、不定形状、紡錘状、繭状等)、粒子径(煙霧状、微粒子、顔料級等)、及び、粒子構造(多孔質、無孔質等)は何ら限定されるものではないが、平均一次粒子径が1nm~100μmの範囲にあることが好ましい。特に、これらの粉体又は着色剤を顔料として配合する場合、平均粒子径が1nm~20μmの範囲にある無機顔料粉体、有機顔料粉体、樹脂粉体から選択される1種類又は2種類以上を配合することが好ましい。
[光透過率]
光透過率計[島津製作所製,UV-265FW]を用いて、波長750nm、セル厚10mmにおける光透過率(%)を測定した。なお、対照としては精製水を使用した。
<グリセリン誘導体変性シリコーンNo.1の製造>
ステップ1:反応器に平均組成式 MD47.5DH 10.5M で表されるメチルハイドロジェンポリシロキサンを215.0g、平均組成式CH2=CH-Si(OSiMe3)3で表されるビニルトリストリメチルシロキシシランを16.9g、白金-1,3-ジビニル-1,1,3,3-テトラメチルジシロキサン錯体のIPA溶液(Pt濃度0.45重量%)を0.39g仕込み、窒素流通下で攪拌しながら加温を開始した。30~50℃で2時間反応を行った後、反応液を採取し、アルカリ分解ガス発生法(残存したSi-H基をKOHのエタノール/水溶液によって分解し、発生した水素ガスの体積から反応率を計算する)により確認したところ、反応率は予定通りであった。
R*11= -C16H33
R*21= -C3H6O{CH2CH(OH)CH2O}2-H
R*31= -C2H4Si(OSiMe3)3
<グリセリン誘導体変性シリコーンNo.1を含む比較用組成物RE-1の調製>
製造例1で得られた灰褐色不透明均一液体340gに対して、濾過助剤としてハイフロースーパーセル(セライト社、融剤焼成品珪藻土)10gを使用し、濾紙としてADVANTEC No.424(直径110mm、東洋濾紙社)を使用して、加圧濾過器によってN2圧400kPaにて室温で濾過を行った。しかし、濾過の最初から最後まで濁りは全く改善されず、1時間かけ灰褐色不透明濁液体322gを得た。{粘度(25℃):8400mPa.s}このものは、製造例1で得られた組成物と比較して、外観上の透明性は全く改善されていなかった。
<グリセリン誘導体変性シリコーンNo.1を含む比較用組成物RE-2の調製>
次に、比較例1で得られた灰褐色不透明濁液体315gを取り出し、ゼータプラスフィルター30C(直径90mm、スリーエム社、ゼータ電位式吸着ろ過フィルター)により、専用濾過器を用いてN2圧150kPaにて加圧濾過を行った。なお、当該フィルターはその性質上、耐圧性が低く200kPaを超える圧力をかけることができないため、比較例1よりも低い加圧状態で濾過を行わざるを得なかった。この時、室温では濾過が非常に遅かったため、40~50℃に保温して実施した。最初の濾液40g程度は透明感のある外観に改善されていたが、その後は濁りが漏れ出てきたため、最終的に得られた濾液の全量を均質になるよう混合した結果、7時間をかけて灰褐色不透明均一液体283gが得られた。{粘度(25℃):8400mPa.s}このものは、比較例1に対して外観上の透明性の改善は殆ど認められなかった。
<高純度グリセリン誘導体変性シリコーンNo.1の調製>
比較例2で得られた灰褐色不透明均一液体120gと、PEG#20000(分子量2万のポリエチレンオキサイド、融点約65℃)フレーク品(有機ワックス)の3.6gをフラスコに仕込み、窒素流通下で攪拌しながら加温を開始した。80℃で40分間激しく混合撹拌を行ったところ、外観は白濁した均一分散液であった。その後、撹拌下に40℃以下となるまで放冷(2時間)して処理を終了した。フラスコ内容物の外観は放冷前と同様であった。次いで、フラスコ内容物に対し濾過助剤としてハイフロースーパーセル(セライト社、融剤焼成品珪藻土)10gを使用し、濾紙としてADVANTEC No.424(直径110mm、東洋濾紙社)を使用して、加圧濾過器によりN2圧400kPaにて室温で1時間をかけ濾過を行った。その結果、驚いたことに最初から最後まで半透明均一な淡黄褐色の濾液が得られ、その総量は92gであった。すなわち、実施例1に示す本発明の手法によって、比較例2の不透明な反応混合物から濁りの大半を取り除くことができ、全量の半透明化を達成できた。粘度(25℃):8500mPa.s
<グリセリン誘導体変性シリコーンNo.2の製造>
ステップ1:反応器に平均組成式 MD43.4DH 7.4M で表されるメチルハイドロジェンポリシロキサンを147.5g、ヘキサデセン(αオレフィン純度=91.7%)を28.8g、下記平均組成式:
ここで、R*11及びR*22及びR*32は下記のとおりである。
R*11= -C16H33
R*22= -C3H6O-X {X=(C3H6O2)2-H (ジグリセリン部分)}
<グリセリン誘導体変性シリコーンNo.2を含む比較用組成物RE-3の調製>
製造例2で得られた濁りの大きい灰褐色液体(グリセリン誘導体変性シリコーンNo.2及びカプリリルメチコンを主成分として含む反応混合物)を、そのまま試料として用いた。
<高純度グリセリン誘導体変性シリコーンNo.2の調製>
製造例2で得られた濁りの大きい淡褐色粘稠液体279gと、PEG#20000(分子量2万のポリエチレンオキサイド、融点約65℃)フレーク品(有機ワックス)の8.4gをフラスコに仕込み、窒素流通下で攪拌しながら加温を開始した。85~100℃で1時間激しく混合撹拌を行ったところ、外観は白濁した均一分散液であった。その後、撹拌下に40℃以下となるまで放冷(2.5時間)して処理を終了した。フラスコ内容物の外観は放冷前と類似していた。次いで、フラスコ内容物に対して、濾過助剤としてハイフロースーパーセル(セライト社、融剤焼成品珪藻土)10gを使用し、濾紙としてADVANTEC No.424(直径110mm、東洋濾紙社)を使用して、加圧濾過器によってN2圧600kPaにて室温で1時間かけて濾過を行った。その結果、驚いたことに最初から最後まで半透明均一な微黄色の濾液が得られ、その総量は253gであった。{粘度(25℃):1500mPa.s}すなわち、実施例2に示す本発明の手法によっても、製造例2の不透明な反応混合物から濁りの大半を取り除くことができ、全量の半透明化を達成できた。
<シロキサンデンドロン構造を有する基:R*3>
R*31= ―C2H4Si(OSiMe3)3
R*21= -C3H6O{CH2CH(OH)CH2O}2-H
R*22= -C3H6O-X {X=(C3H6O2)2-H,本例においてはジグリセリン部分は鎖状構造だけの単一組成ではない。}
<その他の有機基:R*1>
R*11= -C16H33
実施例1、実施例2、比較例2、及び、比較例3のサンプル各40gを100mlガラス瓶に入れて密栓した。これらを室温で4ヶ月間静置した。その後、サンプル外観を記録したのち、光透過率、及び粘度の測定を行った。結果を表3に示す。
注*5)粘度の初期値からの変化率%を示す。
注*6)安定性試験後、サンプルを開封したときの臭気の程度を、嗅覚により以下の基準にしたがって評価した。
◎ : 臭気は全く感じられない
○ : アルデヒド臭は全く無いが、若干の基材臭が感じられる
△ : 少しアルデヒド臭が認められる
× : 鼻にツンとくるアルデヒド臭が明確に認められ、不快である
Claims (14)
- 液状の高純度グリセリン誘導体変性シリコーンの製造方法であって、
グリセリン誘導体変性シリコーン及び不純物を含有する混合物に、該不純物と親和性を有し、且つ、前記グリセリン誘導体変性シリコーンよりも高融点である有機ワックスを添加し、加熱溶融混合して、溶融した該有機ワックス内に該不純物を取り込む工程、
前記有機ワックスを冷却して有機ワックスの固化物を得る工程
前記グリセリン誘導体変性シリコーン及び前記有機ワックスの固化物を固液分離する工程
を含む製造方法。 - 前記不純物が前記グリセリン誘導体由来の不純物である、請求項1記載の製造方法。
- 前記グリセリン誘導体変性シリコーンが少なくとも100℃で液体である、請求項1又は2記載の製造方法。
- 前記有機ワックスが、45℃~150℃の融点を有する、請求項1乃至3のいずれかに記載の製造方法。
- 前記有機ワックスが、900以上の平均分子量を有する、請求項1乃至4のいずれかに記載の製造方法。
- 前記有機ワックスが(ポリ)オキシエチレン部位を含有する、請求項1乃至5のいずれかに記載の製造方法。
- 前記有機ワックスが、(ポリ)オキシエチレン部位を含有するグリセリン誘導体である、請求項1乃至6のいずれかに記載の製造方法。
- 前記グリセリン誘導体変性シリコーンのケイ素原子が、Si-C結合又はSi-O-C結合を介してグリセリン誘導体基含有有機基と結合している、請求項1乃至7のいずれかに記載の製造方法。
- 前記グリセリン誘導体変性シリコーンが、下記一般式(1):
a 、b 、c及びdは、それぞれ、1.0≦a≦2.5、0≦b≦1.5、0≦c≦1.5、0.0001≦d≦1.5の範囲にある数である}で表される、グリセリン誘導体変性シリコーンである、請求項1乃至8のいずれかに記載の製造方法。 - 前記グリセリン誘導体変性シリコーンが、
(A)オルガノハイドロジェンポリシロキサン、
(B)1分子中に1以上の反応性不飽和基を有するグリセリン誘導体基含有有機化合物、並びに
(C)(C1)1分子中に平均で1より大きい数の反応性不飽和基を有する有機化合物、及び、(C2)1分子中に1以上の反応性不飽和基及び1以上のエポキシ基を有する有機化合物からなる群から選択される1種類以上の有機化合物を反応させることにより得られる{但し、前記(C)成分がグリセリン誘導体基含有有機基を含有する場合には前記(B)成分の使用は任意である}、ケイ素原子に結合したグリセリン誘導体基含有有機基を有し、且つ、架橋部にSi-C結合を含む架橋構造を有する有機変性シリコーンである、請求項1乃至8のいずれかに記載の製造方法。 - 前記グリセリン誘導体変性シリコーンが、
(D)分子鎖の両末端に反応性官能基を有するオルガノポリシロキサン、及び
(E)分子中に前記(D)オルガノポリシロキサンの分子鎖両末端に位置する反応性官能基と反応し得る2つの反応性官能基を有する有機化合物
を少なくとも反応させて得られる直鎖状のグリセリン誘導体基含有交互共重合体の形式のグリセリン誘導体変性シリコーンである、請求項1乃至8のいずれかに記載の製造方法。 - 前記混合物が前記グリセリン誘導体変性シリコーンの溶媒を更に含む、請求項1乃至11のいずれかに記載の製造方法。
- 前記グリセリン誘導体変性シリコーン及び前記不純物を含有する混合物が、酸性水溶液によって処理されており、該酸性水溶液の処理によって発生した臭気物質及び水が加熱又は減圧することにより取り除かれている、請求項1乃至12のいずれかに記載の製造方法。
- 請求項1乃至13のいずれかに記載の製造方法により得られた高純度グリセリン誘導体変性シリコーンを含む、外用剤若しくは化粧料、又は、工業用材料。
Priority Applications (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2014554575A JPWO2014104256A1 (ja) | 2012-12-28 | 2013-12-26 | 高純度グリセリン誘導体変性シリコーンの製造法 |
| EP13869648.9A EP2940063A4 (en) | 2012-12-28 | 2013-12-26 | PROCESS FOR THE PREPARATION OF SILICONE MODIFIED BY A HIGH-PURITY GLYCEROL DERIVATIVE |
| US14/655,136 US20160052944A1 (en) | 2012-12-28 | 2013-12-26 | Manufacturing Method For High-Purity Glycerol Derivative-Modified Silicone |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2012-289017 | 2012-12-28 | ||
| JP2012289017 | 2012-12-28 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2014104256A1 true WO2014104256A1 (ja) | 2014-07-03 |
Family
ID=51021330
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2013/085005 WO2014104256A1 (ja) | 2012-12-28 | 2013-12-26 | 高純度グリセリン誘導体変性シリコーンの製造法 |
Country Status (4)
| Country | Link |
|---|---|
| US (1) | US20160052944A1 (ja) |
| EP (1) | EP2940063A4 (ja) |
| JP (1) | JPWO2014104256A1 (ja) |
| WO (1) | WO2014104256A1 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2014200111A1 (ja) * | 2013-06-13 | 2014-12-18 | 東レ・ダウコーニング株式会社 | 長鎖炭化水素基含有ジグリセリン誘導体変性シリコーン及びその利用 |
| US10066060B2 (en) | 2012-12-28 | 2018-09-04 | Dow Corning Toray Co., Ltd. | Production method for high-purity organosilicon compound |
| WO2022014224A1 (ja) * | 2020-07-14 | 2022-01-20 | 信越化学工業株式会社 | 親水性基変性オルガノポリシロキサン及びその製造方法 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN106414557A (zh) * | 2014-04-21 | 2017-02-15 | 道康宁东丽株式会社 | 液态高纯度多元醇衍生物改性的有机硅或其组合物的制造方法 |
Citations (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2383521A (en) * | 1942-05-18 | 1945-08-28 | Frank J Sowa | Process of separating hydrocarbons and waxes and the products so produced |
| JPS6234039A (ja) | 1985-08-07 | 1987-02-14 | Toyo Soda Mfg Co Ltd | 免疫反応測定に用いる蛍光検出装置 |
| JPS62195389A (ja) | 1986-02-24 | 1987-08-28 | Chisso Corp | ヒドロキシル基含有シロキサン化合物 |
| JPS63202629A (ja) | 1987-02-17 | 1988-08-22 | Nitto Electric Ind Co Ltd | ポリプロピレングライコ−ル変性オルガノシロキサン重合体の精製法 |
| JPH05156019A (ja) | 1991-12-03 | 1993-06-22 | Kao Corp | アルキルグリセリルポリシロキサン誘導体の精製方法 |
| JPH0689147B2 (ja) | 1990-05-15 | 1994-11-09 | 信越化学工業株式会社 | 変性シリコーン化合物及びその製造方法 |
| JP2613124B2 (ja) | 1990-08-30 | 1997-05-21 | 花王株式会社 | 新規シロキサン誘導体、その製造方法及びこれを含有する化粧料 |
| JP2844453B2 (ja) | 1996-10-02 | 1999-01-06 | 花王株式会社 | 新規シロキサン誘導体 |
| JPH11181096A (ja) * | 1997-09-29 | 1999-07-06 | Dow Corning Corp | ポリオルガノシロキサン混合物の中和方法 |
| JPH11240951A (ja) * | 1997-12-15 | 1999-09-07 | Dow Corning Corp | ポリオルガノシロキサンの中和法 |
| JP3172787B2 (ja) | 1992-01-14 | 2001-06-04 | 日本精化株式会社 | 糖残基を有するオルガノシロキサン誘導体およびその製造方法 |
| WO2002055588A1 (fr) | 2001-01-10 | 2002-07-18 | Shin-Etsu Chemical Co., Ltd. | Compose de silicone modifie inodore, preparation cosmetique renfermant ce compose et procede pour purifier un compose silicone modifie presentant un polymere ramifie a groupe hydrophile |
| JP3976226B2 (ja) | 2000-12-08 | 2007-09-12 | 信越化学工業株式会社 | 多価アルコール変性シリコーン及びそれを含有する化粧料 |
| JP4357909B2 (ja) | 2003-09-12 | 2009-11-04 | 花王株式会社 | 分岐ポリグリセロール変性シリコーンの製法 |
| JP4485134B2 (ja) | 2002-03-25 | 2010-06-16 | 花王株式会社 | 分岐ポリグリセロール変性シリコーン |
| WO2011049248A1 (ja) | 2009-10-23 | 2011-04-28 | 東レ・ダウコーニング株式会社 | 新規な共変性オルガノポリシロキサン |
| WO2011049246A1 (ja) | 2009-10-23 | 2011-04-28 | 東レ・ダウコーニング株式会社 | 新規オルガノポリシロキサン共重合体 |
| WO2011049247A1 (ja) | 2009-10-23 | 2011-04-28 | 東レ・ダウコーニング株式会社 | 油性原料の増粘剤またはゲル化剤 |
| JP2012046507A (ja) | 2010-07-30 | 2012-03-08 | Dow Corning Toray Co Ltd | 共変性オルガノポリシロキサンを含む毛髪化粧料 |
| JP5037782B2 (ja) | 2003-07-07 | 2012-10-03 | 信越化学工業株式会社 | 新規なオルガノポリシロキサン・グリセリン誘導体交互共重合体およびそれを含有する化粧料 |
-
2013
- 2013-12-26 EP EP13869648.9A patent/EP2940063A4/en not_active Withdrawn
- 2013-12-26 JP JP2014554575A patent/JPWO2014104256A1/ja active Pending
- 2013-12-26 US US14/655,136 patent/US20160052944A1/en not_active Abandoned
- 2013-12-26 WO PCT/JP2013/085005 patent/WO2014104256A1/ja active Application Filing
Patent Citations (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2383521A (en) * | 1942-05-18 | 1945-08-28 | Frank J Sowa | Process of separating hydrocarbons and waxes and the products so produced |
| JPS6234039A (ja) | 1985-08-07 | 1987-02-14 | Toyo Soda Mfg Co Ltd | 免疫反応測定に用いる蛍光検出装置 |
| JPS62195389A (ja) | 1986-02-24 | 1987-08-28 | Chisso Corp | ヒドロキシル基含有シロキサン化合物 |
| JPS63202629A (ja) | 1987-02-17 | 1988-08-22 | Nitto Electric Ind Co Ltd | ポリプロピレングライコ−ル変性オルガノシロキサン重合体の精製法 |
| JPH0689147B2 (ja) | 1990-05-15 | 1994-11-09 | 信越化学工業株式会社 | 変性シリコーン化合物及びその製造方法 |
| JP2613124B2 (ja) | 1990-08-30 | 1997-05-21 | 花王株式会社 | 新規シロキサン誘導体、その製造方法及びこれを含有する化粧料 |
| JPH05156019A (ja) | 1991-12-03 | 1993-06-22 | Kao Corp | アルキルグリセリルポリシロキサン誘導体の精製方法 |
| JP3172787B2 (ja) | 1992-01-14 | 2001-06-04 | 日本精化株式会社 | 糖残基を有するオルガノシロキサン誘導体およびその製造方法 |
| JP2844453B2 (ja) | 1996-10-02 | 1999-01-06 | 花王株式会社 | 新規シロキサン誘導体 |
| JPH11181096A (ja) * | 1997-09-29 | 1999-07-06 | Dow Corning Corp | ポリオルガノシロキサン混合物の中和方法 |
| JPH11240951A (ja) * | 1997-12-15 | 1999-09-07 | Dow Corning Corp | ポリオルガノシロキサンの中和法 |
| JP3976226B2 (ja) | 2000-12-08 | 2007-09-12 | 信越化学工業株式会社 | 多価アルコール変性シリコーン及びそれを含有する化粧料 |
| WO2002055588A1 (fr) | 2001-01-10 | 2002-07-18 | Shin-Etsu Chemical Co., Ltd. | Compose de silicone modifie inodore, preparation cosmetique renfermant ce compose et procede pour purifier un compose silicone modifie presentant un polymere ramifie a groupe hydrophile |
| JP4485134B2 (ja) | 2002-03-25 | 2010-06-16 | 花王株式会社 | 分岐ポリグリセロール変性シリコーン |
| JP5037782B2 (ja) | 2003-07-07 | 2012-10-03 | 信越化学工業株式会社 | 新規なオルガノポリシロキサン・グリセリン誘導体交互共重合体およびそれを含有する化粧料 |
| JP4357909B2 (ja) | 2003-09-12 | 2009-11-04 | 花王株式会社 | 分岐ポリグリセロール変性シリコーンの製法 |
| WO2011049248A1 (ja) | 2009-10-23 | 2011-04-28 | 東レ・ダウコーニング株式会社 | 新規な共変性オルガノポリシロキサン |
| WO2011049246A1 (ja) | 2009-10-23 | 2011-04-28 | 東レ・ダウコーニング株式会社 | 新規オルガノポリシロキサン共重合体 |
| WO2011049247A1 (ja) | 2009-10-23 | 2011-04-28 | 東レ・ダウコーニング株式会社 | 油性原料の増粘剤またはゲル化剤 |
| JP2012046507A (ja) | 2010-07-30 | 2012-03-08 | Dow Corning Toray Co Ltd | 共変性オルガノポリシロキサンを含む毛髪化粧料 |
Non-Patent Citations (1)
| Title |
|---|
| See also references of EP2940063A4 |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10066060B2 (en) | 2012-12-28 | 2018-09-04 | Dow Corning Toray Co., Ltd. | Production method for high-purity organosilicon compound |
| WO2014200111A1 (ja) * | 2013-06-13 | 2014-12-18 | 東レ・ダウコーニング株式会社 | 長鎖炭化水素基含有ジグリセリン誘導体変性シリコーン及びその利用 |
| US9783643B2 (en) | 2013-06-13 | 2017-10-10 | Dow Corning Toray Co., Ltd. | Silicone modified by long-chain hydrocarbon group-containing diglycerin derivative, and use thereof |
| WO2022014224A1 (ja) * | 2020-07-14 | 2022-01-20 | 信越化学工業株式会社 | 親水性基変性オルガノポリシロキサン及びその製造方法 |
| JP2022017749A (ja) * | 2020-07-14 | 2022-01-26 | 信越化学工業株式会社 | 親水性基変性オルガノポリシロキサン及びその製造方法 |
| CN115803367A (zh) * | 2020-07-14 | 2023-03-14 | 信越化学工业株式会社 | 亲水性基团改性有机聚硅氧烷及其制备方法 |
| JP7271478B2 (ja) | 2020-07-14 | 2023-05-11 | 信越化学工業株式会社 | 親水性基変性オルガノポリシロキサン及びその製造方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2014104256A1 (ja) | 2017-01-19 |
| US20160052944A1 (en) | 2016-02-25 |
| EP2940063A1 (en) | 2015-11-04 |
| EP2940063A4 (en) | 2016-05-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6313540B2 (ja) | ジグリセリン誘導体変性シリコーン、それを含有してなる油中水型エマルション用乳化剤、外用剤および化粧料 | |
| JP6355224B2 (ja) | 低臭性グリセリン誘導体変性シリコーンまたはそれを含む組成物の製造方法 | |
| JP6105920B2 (ja) | 共変性オルガノポリシロキサン、それを含有してなる油中水型エマルション用乳化剤、外用剤および化粧料 | |
| WO2012165237A1 (ja) | モノ-又はジ-グリセリン誘導体変性オルガノポリシロキサンエラストマー及びその利用 | |
| WO2012165233A1 (ja) | 新規液状オルガノポリシロキサン及びその利用 | |
| JP6392669B2 (ja) | 透明乃至半透明の液状のグリセリン誘導体変性シリコーン組成物の製造方法 | |
| JP6538351B2 (ja) | 高純度有機ケイ素化合物の製造方法 | |
| WO2015162906A1 (ja) | 液状の高純度多価アルコール誘導体変性シリコーン又はその組成物の製造方法 | |
| JP6243355B2 (ja) | 高純度モノアルケニル含有グリセリン誘導体及びその製造方法 | |
| WO2014104256A1 (ja) | 高純度グリセリン誘導体変性シリコーンの製造法 | |
| JP6436480B2 (ja) | 高純度有機ケイ素化合物の製造方法 | |
| WO2015162904A1 (ja) | 液状の高純度糖誘導体変性シリコーン又はその組成物の製造方法 | |
| JP6189593B2 (ja) | 透明乃至半透明の液状のグリセリン誘導体変性架橋シリコーン組成物の製造方法 | |
| JPWO2015162907A1 (ja) | 透明乃至半透明の液状の糖誘導体変性シリコーン組成物の製造方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 13869648 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2014554575 Country of ref document: JP Kind code of ref document: A |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| REEP | Request for entry into the european phase |
Ref document number: 2013869648 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2013869648 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 14655136 Country of ref document: US |