WO2009147990A1 - 新規イソオキサゾール誘導体 - Google Patents
新規イソオキサゾール誘導体 Download PDFInfo
- Publication number
- WO2009147990A1 WO2009147990A1 PCT/JP2009/059758 JP2009059758W WO2009147990A1 WO 2009147990 A1 WO2009147990 A1 WO 2009147990A1 JP 2009059758 W JP2009059758 W JP 2009059758W WO 2009147990 A1 WO2009147990 A1 WO 2009147990A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- phenyl
- isoxazol
- oxy
- atom
- Prior art date
Links
- YZEMYQZIRRDCBF-UHFFFAOYSA-N SCc1cc(cccc2)c2[o]1 Chemical compound SCc1cc(cccc2)c2[o]1 YZEMYQZIRRDCBF-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D261/00—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings
- C07D261/02—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings not condensed with other rings
- C07D261/06—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings not condensed with other rings having two or more double bonds between ring members or between ring members and non-ring members
- C07D261/10—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings not condensed with other rings having two or more double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D261/12—Oxygen atoms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/04—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings directly linked by a ring-member-to-ring-member bond
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
Definitions
- the present invention relates to an isoxazole derivative useful in the field of medicine.
- This compound acts as a GPR120 receptor (14273) function regulator and is useful as a therapeutic and / or prophylactic agent for diabetes, obesity, and hyperlipidemia.
- GPR120 which is a G protein-coupled receptor, transmits signals into cells through binding with unsaturated long-chain fatty acids such as ⁇ -linolenic acid and induces various in vivo reactions. It has been reported that in the intestinal cell line, the action of GPR120 and its ligand promotes secretion of GLP-1 (glucagon-like-peptide-1; glucagon-like peptide 1) that functions to lower blood glucose levels.
- GLP-1 is a peptide hormone released from L cells, which are enteroendocrine cells present in the ileum, large intestine, etc., and has been shown to induce insulin secretion according to blood glucose level. .
- a compound having a GLP-1 secretion promoting action can be expected as a therapeutic agent for diabetes that can avoid the risk of hypoglycemia due to overdose.
- GLP-1 has the effect of inducing proliferation of pancreatic ⁇ cells and differentiation from stem cells, it is effective in delaying apoptosis of ⁇ cells in type II diabetes and sustaining the effect of islet transplantation on type I diabetes. It is suggested that there is.
- GPR120 is also expressed in adipocytes. GPR120 has been observed to increase in expression with induction of fat differentiation. Furthermore, it has been reported that lipolysis in adipogenic cells is suppressed by the action of GPR120 and its ligand.
- GPR120 is also expressed in the pituitary gland and it has been reported that GPR120 ligand suppresses the secretion of adrenocorticotropic hormone.
- Adrenocorticotropic hormones promote secretion of glucocorticoids downstream of them, thereby promoting gluconeogenesis in the liver, inhibiting glucose uptake in muscle and peripheral tissues, lipolysis in adipose tissue, release of fatty acids and glycerol, etc. Invoke the action.
- GPR120 exerts a blood glucose lowering action and a blood lipid lowering action also in the center through an inhibitory action on the secretion of adrenocorticotropic hormone. From the above description, a compound having GPR120 agonist activity is considered to be extremely useful as a therapeutic and / or prophylactic agent for diabetes, obesity, and hyperlipidemia.
- An object of the present invention is to provide a novel isoxazole derivative having a GPR120 (14273) function regulating action.
- the present inventors have intensively studied to develop a compound having a GPR120 (14273) function regulating action, particularly an agonist action, and the compound according to the present invention is effective as a compound having a GPR120 (14273) function regulating action.
- the present invention has been found, and the present invention has been completed based on such findings.
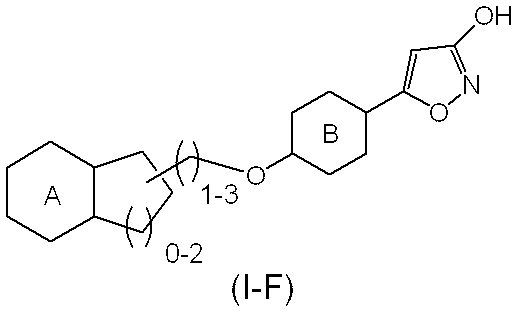
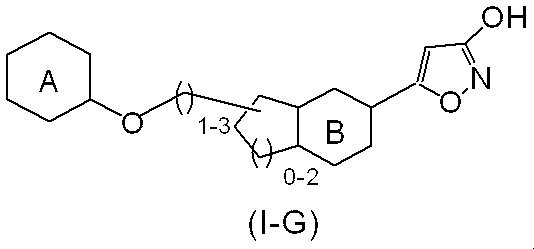
- Is a lower alkoxy group (the lower alkoxy group may be substituted by 1 to 3 halogen atoms), a lower alkoxycarbonyl group, a lower alkenyloxy group, a lower alkynyloxy group (the lower alkylthio group is a halogen atom) 1 to 3 optionally substituted), a halo lower alkyloxy group, a cycloalkyloxy group, a lower alkylthio group, a lower alkyl group (the lower alkyl group may be 1 to 3 substituted with a halogen atom), Lower alkenyl group, lower alkynyl group, cycloalkylthio group, lower alkylamino group, lower alkenylamino group, lower alkynylamino group, lower haloalkylamino group, cycloalkylamino group, nitro group, halogen atom, cyano group, lower alkylsulfonyl group , Lower al
- X is a lower alkylene group in which the main chain is composed of 2 to 4 carbon atoms, and 1 or 2 of the carbon atoms constituting the main chain may be replaced with an oxygen atom, a sulfur atom or a nitrogen atom.
- the lower alkylene group is (1) an amino group (the amino group may be substituted with a lower alkyl group, a lower alkylsulfonyl group, or a lower alkanoyl group), (2) a halogen atom, (3) a lower alkenyl group, (4) a lower alkyl group (when the same carbon atom constituting the lower alkylene group is substituted with two lower alkyl groups, these lower alkyl groups are combined to form a 3- to 7-membered
- An aliphatic ring (which may form one or two carbon atoms constituting the aliphatic ring may be replaced by a nitrogen atom, a sulfur atom or an oxygen atom)), (5) a lower alkynyl group, (6) a lower alkylidene group, (7) imino group, (8) an arylalkyl group, (9) a 5- or 6-membered heteroarylalkyl group having 1 to 4 heteroatoms in the ring selected from the group consisting of
- the lower alkyl group, lower alkynyl group, and lower alkylidene group may be substituted with 1 to 3 halogen atoms, a hydroxy group, or a lower alkoxy group;
- the imino group may be substituted with 1 to 3 lower alkyl groups, lower alkylsulfonyl groups, cyano groups, nitro groups, lower alkanoyl groups;
- the lower alkylene group may have one or two double bonds or triple bonds in the main chain, and the lower alkylene group is substituted by 1 to 3 by a lower alkoxy group, an oxo group or a hydroxy group. May be;
- 1 or 2 of carbon atoms constituting may be replaced with a nitrogen atom, a sulfur atom or an oxygen atom, and may have 1 or 2 double bonds in the ring;
- One of the carbon atoms constituting may be replaced by a nitrogen atom, a sulfur atom or an oxygen atom;
- Y is Hydrogen atom,
- a lower alkyl group (the lower alkyl group may be a lower alkoxy group, optionally substituted 1 to 3 with a halogen atom), Selected from the group consisting of a lower alkoxy group and a halogen atom], or a pharmaceutically acceptable salt thereof.
- the present invention also relates to a GPR120 function regulator comprising a compound represented by formula (I) or a pharmaceutically acceptable salt thereof as an active ingredient, and in particular, the present invention relates to a compound represented by formula (I) Or a GPR (14273) 120 agonist containing a pharmaceutically acceptable salt thereof as an active ingredient.
- the present invention also relates to a therapeutic agent for diabetes, obesity or hyperlipidemia containing the compound represented by formula (I) or a pharmaceutically acceptable salt thereof as an active ingredient.
- the present invention relates to a pharmaceutical composition
- a pharmaceutical composition comprising a compound represented by formula (I) and a pharmaceutically acceptable carrier.
- the compound (I) or a pharmaceutically acceptable salt thereof according to the present invention has a potent GPR120 (14273) function-modulating action, particularly an agonistic action, and is used for the treatment of diabetes, obesity or hyperlipidemia and Useful for prevention.
- halogen atom examples include a fluorine atom, a chlorine atom, a bromine atom, and an iodine atom.
- “Lower alkyl group” means a linear or branched alkyl group having 1 to 6 carbon atoms, for example, methyl group, ethyl group, propyl group, isopropyl group, butyl group, isobutyl group, sec-butyl group Tert-butyl group, pentyl group, isoamyl group, neopentyl group, isopentyl group, 1,1-dimethylpropyl group, 1-methylbutyl group, 2-methylbutyl group, 1,2-dimethylpropyl group, hexyl group, isohexyl group, 1-methylpentyl group, 2-methylpentyl group, 3-methylpentyl group, 1,1-dimethylbutyl group, 1,2-dimethylbutyl group, 2,2-dimethylbutyl group, 1,3-dimethylbutyl group, 2,3-dimethylbutyl group, 3,3-dimethylbutyl group, 1-ethyl
- the “lower alkoxy group” means a group in which a hydrogen atom of a hydroxy group is substituted with the lower alkyl group.
- a methoxy group, an ethoxy group, a propoxy group, an isopropoxy group, a butoxy group, a sec-butoxy group examples thereof include a tert-butoxy group, a pentyloxy group, an isopentyloxy group, a hexyloxy group, and an isohexyloxy group.
- Cycloalkyl group means a cycloalkyl group having 3 to 7 carbon atoms (C 3-7 cycloalkyl group), and specifically includes, for example, a cyclopropyl group, a cyclobutyl group, a cyclopentyl group, a cyclohexyl group, or a cycloalkyl group.
- a heptyl group is mentioned.
- the “lower alkylthio group” means a group in which a hydrogen atom of a thiol group is substituted with the lower alkyl group. Specifically, for example, a methylthio group, an ethylthio group, an n-propylthio group, an isopropylthio group, A butylthio group, an isobutylthio group, etc. are mentioned.
- Cycloalkyloxy group means a group in which a hydrogen atom of a hydroxy group is substituted with a cycloalkyl group as defined above. Specifically, for example, cyclopropyloxy, cyclobutyloxy group, cyclopentyloxy group And a cyclohexyloxy group.
- Cycloalkylthio group means a group in which a hydrogen atom of a thiol group is substituted with a cycloalkyl group as defined above. Specifically, for example, a cyclopropylthio group, a cyclobutylthio group, a cyclopentylthio group, and the like. And a cyclohexylthio group.
- the “lower alkylamino group” means a group in which 1 or 2 of the hydrogen atoms of the amino group are the same or different and substituted with the lower alkyl group as defined above.
- a methylamino group examples thereof include an ethylamino group, an n-propylamino group, an isopropylamino group, a dimethylamino group, a diethylamino group, and an ethylmethylamino group.
- Cycloalkylamino group means a group in which one or two hydrogen atoms of an amino group are the same or different and substituted with the above-defined cycloalkyl group. Specifically, for example, a cyclopropylamino group , Cyclobutylamino group, cyclopentylamino group, cyclohexylamino group and the like.
- lower alkylsulfonyl group examples include methylsulfonyl group, ethylsulfonyl group, propylsulfonyl group, isopropylsulfonyl group and the like.
- lower alkenyl group examples include a vinyl group, a propenyl group, an isopropenyl group, a 2-buten-1-yl group, and a 4-penten-1-yl group.
- Examples of the “lower alkynyl group” include 2-butyn-1-yl group and 4-pentyn-1-yl group.
- lower alkenyloxy group examples include vinyloxy group, propenyloxy group, isopropenyloxy group, 2-buten-1-yloxy group, 4-penten-1-yloxy group and the like.
- lower alkynyloxy group examples include 2-butyn-1-yloxy group, 4-pentyn-1-yloxy group and the like.
- halo lower alkyl group is a linear or branched alkyl having 1 to 6 carbon atoms in the alkyl part, and includes, for example, fluoromethyl, trifluoromethyl, chloromethyl, 2,2,2 -Trifluoroethyl, 3-chloropropyl, 3-fluoropropyl, 4-chlorobutyl, 4-fluorobutyl, 5-chloropentyl, 6-chlorohexyl, 6-fluorohexyl and the like.
- Halo lower alkyloxy group means, for example, a fluoromethoxy group, a trifluoromethoxy group, a chloromethoxy group, a 2,2,2-trifluoromethoxy group, a 3-chloropropyloxy group, a 3-fluoropropyloxy group, Examples include 4-chlorobutyloxy group, 4-fluorobutyloxy group, 5-chloropentyloxy group, 6-chlorohexyloxy group, 6-fluorohexyloxy group and the like.
- lower alkenylamino group examples include a vinylamino group, a propenylamino group, an isopropenylamino group, a 2-buten-1-ylamino group, and a 4-penten-1-ylamino group.
- lower alkynylamino group examples include 2-butyn-1-ylamino group, 4-pentyn-1-ylamino group, and the like.
- the “lower halo lower alkylamino group” means, for example, a fluoromethylamino group, a trifluoromethylamino group, a chloromethylamino group, a 2,2,2-trifluoromethylamino group, a 3-chloropropylamino group, a 3- Examples include a fluoropropylamino group, a 4-chlorobutylamino group, a 4-fluorobutylamino group, a 5-chloropentylamino group, a 6-chlorohexylamino group, and a 6-fluorohexylamino group.
- lower alkenylsulfonyl group examples include a vinylsulfonyl group, a propenylsulfonyl group, an isopropenylsulfonyl group, a 2-buten-1-ylsulfonyl group, and a 4-penten-1-ylsulfonyl group.
- lower alkynylsulfonyl group examples include 2-butyn-1-ylsulfonyl group, 4-pentyn-1-ylsulfonyl group and the like.
- lower alkylidene group refers to an alkylidene having 1 to 6 carbon atoms, and specific examples include methylidene, ethylidene, propylidene, butylidene, pentylidene, and hexylidene.
- the compound represented by these is preferable.
- the “5- or 6-membered heteroaryl group” represented by represents a 5- or 6-membered heteroaryl group having the same or different heteroatoms selected from the group consisting of a nitrogen atom, a sulfur atom and an oxygen atom, and having 1 to 4 Means.
- Examples of the 5- or 6-membered heteroaryl group include a pyridinyl group, an oxazolyl group, an isoxazolyl group, a thiazolyl group, a thiadiazolyl group, an imidazolyl group, a tetrazolyl group, and a pyrazolyl group.
- the “bicyclic group containing a phenyl ring or a 5- or 6-membered heteroaryl group” represented by, for example, isobenzofuranyl (such as 1-benzofuranyl), chromenyl (such as 2H-chromen-3-yl), benzothienyl (Such as 2-benzothienyl), indolizinyl (such as 2-indolidinyl, 3-indolidinyl), isoindolyl (such as 1-isoindolyl), 3H-indolyl (such as 3H-indol-2-yl), indolyl (such as 2-indolyl), 1H-indazolyl (such as 1H-indazol-3-yl), purinyl (such as 8-prinyl), isoquinolyl (such as 1-isoquinolyl and 3-isoquinolyl), quinolyl (such as 2-quinolyl and 3-quinolyl), phthalazyl (1- Ph
- the “lower alkoxy group” of the substituent means the same group as the “lower alkoxy group” defined above, and specifically includes, for example, a methoxy group, an ethoxy group, a propoxy group, an isopropoxy group, and the like. It is done.
- the “lower alkenyloxy group” of the substituent means the same group as the “lower alkenyloxy group” defined above.
- the “lower alkynyloxy group” of the substituent means the same group as the “lower alkynyloxy group” defined above.
- halo-lower alkoxy group of the substituent means a lower alkoxy group substituted by 1 to 3 substituents with the same or different halogen atoms. Etc.
- cycloalkyloxy group of the substituent means the same group as the “cycloalkyloxy group” defined above.
- the “lower alkylthio group” of the substituent means the same group as the “lower alkylthio group” defined above.
- the “lower alkylamino group” of the substituent means the same group as the “lower alkylamino group” defined above.
- the “lower alkenylamino group” of the substituent means the same group as the “lower alkenylamino group” defined above.
- the “lower alkynylamino group” of the substituent means the same group as the “lower alkynylamino group” defined above.
- halo-lower alkylamino group of the substituent means a lower alkylamino group substituted with the same or different 1 to 3 halogen atoms.
- cycloalkylamino group of the substituent means the same group as the “cycloalkylamino group” defined above.
- halogen atom of the substituent means the same group as the “halogen atom” defined above.
- the “lower alkylsulfonyl group” of the substituent means the same group as the “lower alkylsulfonyl group” defined above.
- the “5- or 6-membered heteroaryl group” of the substituent means a heteroaryl group having 1 to 4 heteroatoms in the ring, selected from the group consisting of a nitrogen atom, a sulfur atom and an oxygen atom.
- Specific examples include a pyridinyl group, an oxazolyl group, an isoxazolyl group, a thiazolyl group, a thiadiazolyl group, an imidazolyl group, a tetrazolyl group, and a pyrazolyl group.
- the “5- or 6-membered heteroaryloxy group” of the substituent means the heteroaryl group and oxy group having 1 to 4 heteroatoms in the ring selected from the group consisting of a nitrogen atom, a sulfur atom and an oxygen atom. And a group to which is bonded.
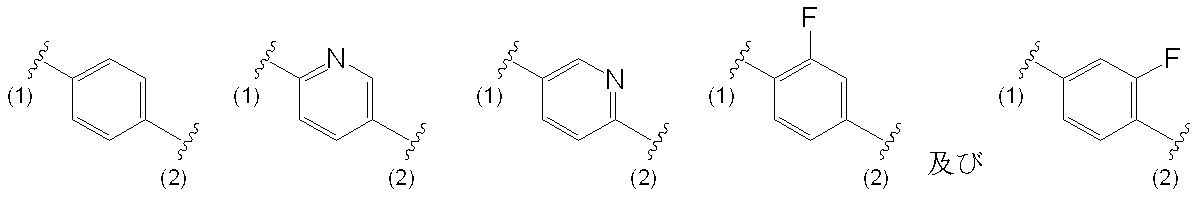
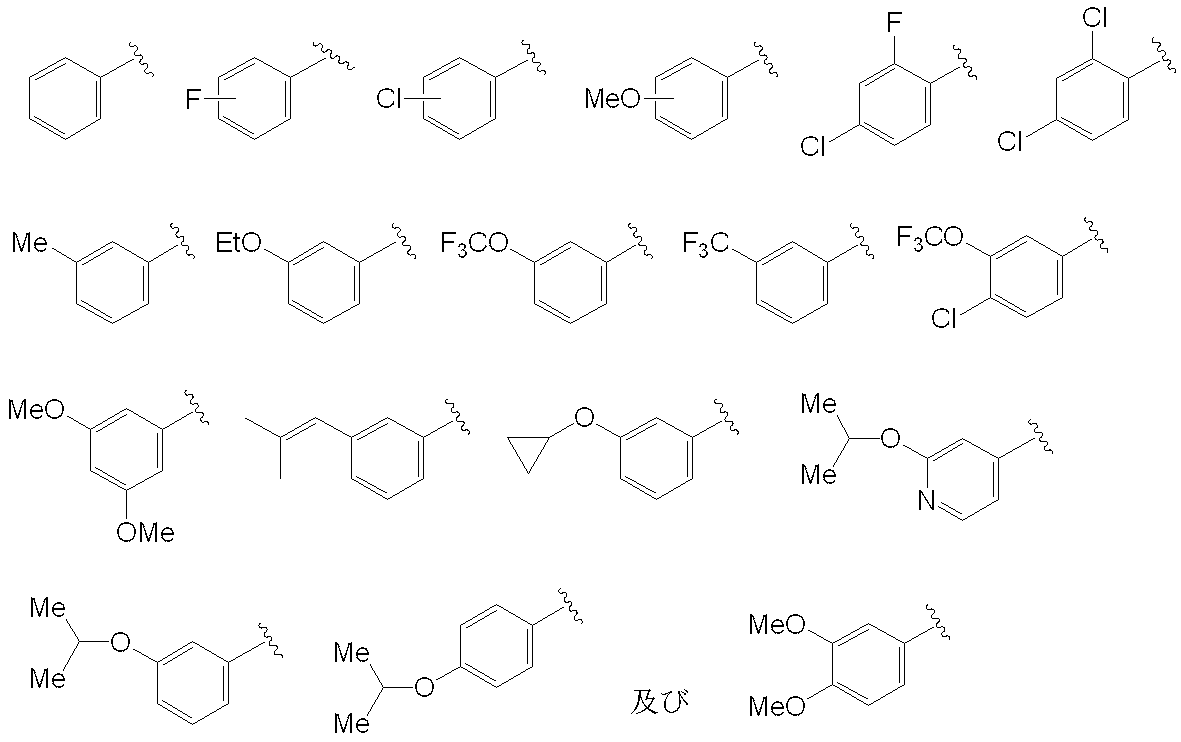
- a lower alkoxy group (the lower alkoxy group may be substituted with the same or different 1 to 3 halogen atoms), A C3-7 cycloalkyloxy group, A lower alkyl group (the lower alkyl group may be substituted with the same or different 1 to 3 halogen atoms), A lower alkenyl group and a group selected from the group consisting of halogen atoms are the same or different, and a phenyl group or a pyridinyl group substituted with 1 to 2 is preferable,
- W 1 all or a carbon atom, or 1 or 2 nitrogen atoms of the W 1, the remaining W 1 is a group consisting of a halogen atom, a lower alkyl group and a lower alkoxy group Which is a carbon atom which may be substituted by 1 to 4 by a group selected from the above.
- the binding site is shown.
- halogen atom of the substituent means the same group as the “halogen atom” defined above.
- the “lower alkyl group” of the substituent means the same group as the “lower alkyl group” defined above.
- the “lower alkoxy group” of the substituent means the same group as the “lower alkoxy group” defined above.
- a group selected from the group consisting of a halogen atom, a lower alkyl group and a lower alkoxy group which may be the same or different and may be substituted by 1 to 4 hydrogen atoms, excluding two hydrogen atoms from the benzene ring or pyridine ring
- X means lower alkylene having a main chain composed of 2 to 4 carbon atoms.
- one or two carbon atoms constituting the main chain may be replaced with a nitrogen atom, a sulfur atom or an oxygen atom.
- the X is (1) an amino group (the amino group may be substituted by 1 to 3 with a lower alkyl group, a lower alkylsulfonyl group, or a lower alkanoyl group), (2) a halogen atom, (3) a lower alkenyl group, (4) Lower alkyl group (when the same carbon atom constituting X is substituted with two lower alkyl groups, these lower alkyl groups are combined to form a 3- to 7-membered aliphatic group.
- a ring (one or two carbon atoms constituting the aliphatic ring may be replaced by a nitrogen atom, a sulfur atom or an oxygen atom)), (5) a lower alkynyl group, (6) a lower alkylidene group, (7) imino group, (8) an arylalkyl group, (9) a heteroarylalkyl group having 1 to 4 heteroatoms in the ring selected from the group consisting of a nitrogen atom, a sulfur atom and an oxygen atom; (10) a heteroaryl group having 1 to 4 heteroatoms in the ring selected from the group consisting of a nitrogen atom, a sulfur atom and an oxygen atom; (11) an arylalkyloxy group, and (12) a group consisting of a 5- or 6-membered heteroarylalkyloxy group having 1 to 4 heteroatoms in the ring selected from the group consisting of a nitrogen atom, a sulfur atom and an oxygen atom
- the groups are more or less selected and
- amino group optionally substituted by 1 to 3 with a lower alkyl group, lower alkylsulfonyl group or lower alkanoyl group include, for example, methylamino group, ethylamino group, propyl Examples include amino group, isopropylamino group, methylsulfonylamino group, ethylsulfonylamino group, propylsulfonylamino group, isopropylsulfonylamino group, acetylamino group, ethylcarbonylamino group, propylcarbonylamino group, isopropylcarbonylamino group and the like.
- halogen atom of the substituent means the same group as the “halogen atom” defined above.
- the “lower alkenyl group” of the substituent means the same group as the “lower alkenyl group” defined above.
- the “lower alkyl group” of the substituent means the same group as the “lower alkyl group” defined above.
- these lower alkyl groups may be combined to form a 3- to 7-membered aliphatic ring. Good.
- the 3- to 7-membered aliphatic ring include a cyclopropyl group, a cyclobutyl group, a cyclopentyl group, a cyclohexyl group, and a cycloheptyl group.
- One or two carbon atoms constituting the 3- to 7-membered aliphatic ring may be replaced with a nitrogen atom, a sulfur atom or an oxygen atom.
- the “lower alkynyl group” of the substituent means the same group as the “lower alkynyl group” defined above.
- the “lower alkylidene group” of the substituent means the same group as the “lower alkylidene group” defined above.
- heteroaryl group having 1 to 4 heteroatoms selected from the group consisting of a nitrogen atom, a sulfur atom and an oxygen atom” in the ring
- heteroaryl group “Means the same group.
- heteroarylalkyl group of the substituent means a group in which the “heteroaryl group” defined above and the “lower alkyl group” defined above are bonded.
- heteroarylalkyloxy group of the substituent means a group in which the “heteroaryl group” defined above and the “lower alkoxy group” defined above are bonded.
- the lower alkyl group, lower alkynyl group and lower alkylidene group of the substituent may be substituted with 1 to 3 halogen atoms, hydroxy group or lower alkoxy group.
- the imino group of the substituent may be substituted with 1 to 3 lower alkyl groups, lower alkylsulfonyl groups, cyano groups, nitro groups, or lower alkanoyl groups.
- the X may have 1 or 2 double bonds or triple bonds.
- the X may be substituted by 1 to 3 with a lower alkoxy group, an oxo group or a hydroxy group.
- 1 or 2 of carbon atoms constituting may be replaced with a nitrogen atom, a sulfur atom or an oxygen atom, and may have 1 or 2 double bonds in the ring.
- One of the carbon atoms constituting may be replaced with a nitrogen atom, a sulfur atom or an oxygen atom.
- the main chain is composed of 3 carbon atoms, and 1 or 2 of the carbon atoms constituting the main chain is a lower alkylene group in which an oxygen atom, sulfur atom or nitrogen atom is substituted, And a group selected from the group consisting of a lower alkyl group, a halogen atom and an oxo group, preferably the same or different and 1 to 3 substituted,
- the main chain is composed of 3 carbon atoms, and one of the carbon atoms constituting the main chain is a lower alkylene group in which an oxygen atom, sulfur atom or nitrogen atom is substituted, and the lower alkylene group is lower More preferably, the groups are selected from the group consisting of an alkyl group, a halogen atom and an oxo group and are the same or different and are 1 or 2 substituted.
- Y is Hydrogen atom
- a lower alkyl group (the alkyl group may be the same or different with a lower alkoxy group or a halogen atom, and may be substituted by 1 to 3), A group selected from the group consisting of a lower alkoxy group and a halogen atom is shown.
- the lower alkyl group represented by Y means the same group as the “lower alkyl group” defined above.
- the lower alkyl group may be the same or different with a lower alkoxy group or a halogen atom, and may be substituted by 1 to 3 substituents.
- the lower alkoxy group represented by Y means the same group as the “lower alkoxy group” defined above.
- halogen atom represented by Y means the same group as the “halogen atom” defined above.
- Y is a hydrogen atom or a lower alkyl group (the lower alkyl is preferably the same or different with a lower alkoxy group or a halogen atom, and is preferably 1 to 3 substituted, more preferably a hydrogen atom or a methyl group, Is more preferable.
- the compound (IA) according to the present invention can be produced, for example, by the following method.
- the alkylene group in the (1) an amino group (the amino group may be substituted with a lower alkyl group, a lower alkylsulfonyl group, or a lower alkanoyl group), (2) a halogen atom, (3) a lower alkenyl group, (4) a lower alkyl group (when the same carbon atom constituting the lower alkylene group is substituted with two lower alkyl groups, these lower alkyl groups are combined to form a 3- to 7-membered
- An aliphatic ring (which may form one or two carbon atoms constituting the aliphatic ring may be replaced by a nitrogen atom, a sulfur atom or an oxygen atom)), (5) a lower alkynyl group, (6) a lower alkylidene group, (7) imino group, (8) an arylalkyl group, (9) a 5- or 6-membered heteroarylalkyl group having 1 to 4 heteroatoms in the ring selected from the group consisting of
- the lower alkyl group, the lower alkynyl group, and the lower alkylidene group may be substituted with 1 to 3 halogen atoms, a hydroxy group, or a lower alkoxy group
- the imino group may be substituted with 1 to 3 lower alkyl groups, lower alkylsulfonyl groups, cyano groups, nitro groups, lower alkanoyl groups
- the lower alkylene group may have one or two double bonds or triple bonds in the main chain, and the lower alkylene group is substituted by 1 to 3 by a lower alkoxy group, an oxo group or a hydroxy group.
- This step is a method for producing compound (3) by reacting compound (1) with compound (2).
- the reaction between the compound (1) and the compound (2) is a so-called Mitsunobu reaction.
- a phosphine compound and an azo compound a method described in the literature (for example, “Use by Mitsunobu. O”, “Use”). Of diethyl azodicarboxylate and triphenylphosphine in synthesis and transformation of natural products. 28)), methods according to them, and these and conventional methods It can be carried out by combining seen.
- the amount of compound (1) used in this step is usually 1 to 100 equivalents, preferably 1 to 5 equivalents, relative to 1 equivalent of compound (2).
- Examples of the phosphine compound used in this step include triphenylphosphine and triethylphosphine.
- the amount of the phosphine compound used is usually 1 to 100 equivalents, preferably 1 to 5 equivalents, relative to 1 equivalent of compound (2).
- Examples of the azo compound used include ethyl azodicarboxylate, diisopropyl azodicarboxylate, and the like.
- the amount of the azo compound used is usually 1 to 100 equivalents, preferably 1 to 5 equivalents, relative to 1 equivalent of compound (2).
- the reaction time in this step is usually 0.1 to 72 hours, preferably 0.5 to 24 hours.
- the reaction temperature in this step is usually 0 to 200 ° C, preferably 0 to 50 ° C.
- the reaction solvent used in this step is not particularly limited as long as it does not hinder the reaction, and examples thereof include tetrahydrofuran, diethyl ether, and the like.
- the compound (3) thus obtained can be isolated or purified by a known separation and purification means, for example, concentration, concentration under reduced pressure, crystallization, solvent extraction, reprecipitation, chromatography, etc., or without isolation and purification. It can be attached to the next process.
- a known separation and purification means for example, concentration, concentration under reduced pressure, crystallization, solvent extraction, reprecipitation, chromatography, etc., or without isolation and purification. It can be attached to the next process.
- This step is a method for producing the compound (IA) according to the present invention by reacting the compound (3) obtained in the above step 1 with hydroxyamine in the presence of a base.
- Examples of the base used in this step include sodium hydroxide and potassium hydroxide.
- the amount of the base used is usually 1 to 100 equivalents, preferably 1 to 5 equivalents, relative to 1 equivalent of compound (3).
- the amount of hydroxyamine used is usually 1 to 100 equivalents, preferably 1 to 5 equivalents, relative to 1 equivalent of compound (3).
- the reaction time in this step is usually 0.1 to 72 hours, preferably 0.5 to 24 hours.
- the reaction temperature in this step is usually 0 to 100 ° C., preferably 0 to 40 ° C.
- the reaction solvent used in this step is not particularly limited as long as it does not hinder the reaction, and examples thereof include methanol and ethanol.
- step 1 instead of compound (2),
- the thus obtained compound (IA) according to the present invention can be isolated and purified by known separation and purification means such as concentration, concentration under reduced pressure, crystallization, solvent extraction, reprecipitation, chromatography and the like. .
- the compound (2) a commercially available product can be used, or a compound produced by the following method, for example, can also be used.
- This step is a method for producing compound (2) by reacting compound (4) with ethyl propioate in the presence of copper (II) oxide.
- the amount of ethyl propioate used is usually 1 to 100 equivalents, preferably 1 to 5 equivalents, relative to 1 equivalent of compound (4).
- Examples of the compound (4) used in this step include 4-iodophenol, 4-iodophenylmethanol, 2- (4-iodophenyl) ethanol and the like. Further, methyl propioate can be used instead of ethyl propioate used in this step.
- the amount of copper (II) oxide used in this step is usually 0.1 to 100 equivalents, preferably 1 to 5 equivalents, relative to 1 equivalent of compound (4).
- the reaction temperature in this step is usually 0 to 200 ° C, preferably 50 to 120 ° C.
- the reaction time in this step is usually 0 to 72 hours, preferably 0.5 to 24 hours.
- the reaction solvent used in this step is not particularly limited as long as it does not hinder the reaction, and examples thereof include dimethylformamide and N-methylpyrrolidone.
- the compound (2) thus obtained can be isolated and purified by known separation and purification means such as concentration, concentration under reduced pressure, crystallization, solvent extraction, reprecipitation, chromatography and the like, or without isolation and purification. It can be used for other processes.
- Compound (3) can also be produced, for example, by the following method.
- An aliphatic ring (which may form one or two carbon atoms constituting the aliphatic ring may be replaced by a nitrogen atom, a sulfur atom or an oxygen atom)), (5) a lower alkynyl group, (6) a lower alkylidene group, (7) imino group, (8) an arylalkyl group, (9) a 5- or 6-membered heteroarylalkyl group having 1 to 4 heteroatoms in the ring selected
- the lower alkyl group, the lower alkynyl group, and the lower alkylidene group may be substituted with 1 to 3 halogen atoms, a hydroxy group, or a lower alkoxy group
- the imino group may be substituted with 1 to 3 lower alkyl groups, lower alkylsulfonyl groups, cyano groups, nitro groups, lower alkanoyl groups
- the lower alkylene group may have one or two double bonds or triple bonds in the main chain, and the lower alkylene group is substituted by 1 to 3 by a lower alkoxy group, an oxo group or a hydroxy group.
- This step is a method for producing compound (5) by reacting compound (1) with methanesulfonyl chloride (MsCl) in the presence of a base.
- MsCl methanesulfonyl chloride
- Examples of the base used in this step include triethylamine, diisopropylethylamine, pyridine and the like.
- the amount of the base used in this step is usually 0.1 to 100 equivalents, preferably 1 to 5 equivalents, relative to 1 equivalent of compound (1).
- the amount of methanesulfonyl chloride used in this step is usually 1 to 100 equivalents, preferably 1 to 5 equivalents, relative to 1 equivalent of compound (1).
- the reaction time in this step is usually 0.1 to 24 hours, preferably 0.5 to 3 hours.
- the reaction temperature in this step is usually 0 to 100 ° C., preferably 0 to 30 ° C.
- the reaction solvent used in this step is not particularly limited as long as it does not hinder the reaction, and examples thereof include ethyl acetate, chloroform, and tetrahydrofuran.
- the compound (5) thus obtained can be isolated and purified by known separation and purification means such as concentration, concentration under reduced pressure, crystallization, solvent extraction, reprecipitation, chromatography and the like, or without isolation and purification. It can be attached to the next step.
- This step is a method for producing compound (6) by reacting compound (5) with compound (4) in the presence of a base.
- Examples of the base used in this step include sodium hydride and potassium carbonate.
- the amount of the base used is usually 1 to 100 equivalents, preferably 1 to 5 equivalents, relative to 1 equivalent of compound (5).
- the amount of compound (4) used in this step is usually 1 to 100 equivalents, preferably 1 to 5 equivalents, relative to 1 equivalent of compound (5).
- the reaction temperature in this step is usually 0 to 200 ° C., preferably 0 to 100 ° C.
- the reaction time in this step is usually 0.1 to 24 hours, preferably 0.5 to 5 hours.
- the reaction solvent used in this step is not particularly limited as long as it does not interfere with the reaction, and examples thereof include dimethylformamide and N-methylpyrrolidone.
- the compound (6) thus obtained can be isolated or purified by a known separation and purification means, for example, concentration, concentration under reduced pressure, reprecipitation, solvent extraction, crystallization, chromatography, etc. It can be attached to the next process.
- a known separation and purification means for example, concentration, concentration under reduced pressure, reprecipitation, solvent extraction, crystallization, chromatography, etc. It can be attached to the next process.
- Step 6 This step is a method for producing compound (3) by reacting compound (6) with ethyl propioate in the presence of copper (II) oxide.
- reaction in this step can be carried out by the same method as in Step 3, a method according to this, or a combination of these with conventional methods.
- the compound (3) thus obtained is isolated or purified by a known separation and purification means, for example, concentration, concentration under reduced pressure, reprecipitation, solvent extraction, crystallization, chromatography, etc. It can be attached to the next process.
- a known separation and purification means for example, concentration, concentration under reduced pressure, reprecipitation, solvent extraction, crystallization, chromatography, etc. It can be attached to the next process.
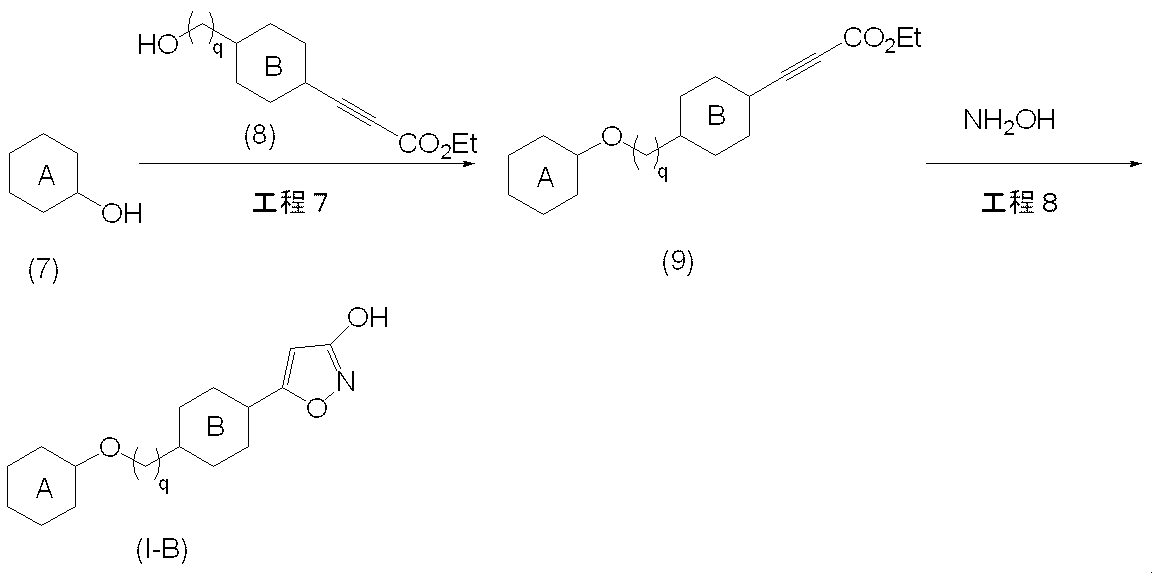
- the compound (IB) according to the present invention can be produced, for example, by the following method.
- the alkylene group in the (1) an amino group (the amino group may be substituted with a lower alkyl group, a lower alkylsulfonyl group, or a lower alkanoyl group), (2) a halogen atom, (3) a lower alkenyl group, (4) a lower alkyl group (when the same carbon atom constituting the lower alkylene group is substituted with two lower alkyl groups, these lower alkyl groups are combined to form a 3- to 7-membered
- An aliphatic ring (which may form one or two carbon atoms constituting the aliphatic ring may be replaced by a nitrogen atom, a sulfur atom or an oxygen atom)), (5) a lower alkynyl group, (6) a lower alkylidene group, (7) imino group, (8) an arylalkyl group, (9) a 5- or 6-membered heteroarylalkyl group having 1 to 4 heteroatoms in the ring selected from the group consisting of
- the lower alkyl group, the lower alkynyl group, and the lower alkylidene group may be substituted with 1 to 3 halogen atoms, a hydroxy group, or a lower alkoxy group
- the imino group may be substituted with 1 to 3 lower alkyl groups, lower alkylsulfonyl groups, cyano groups, nitro groups, lower alkanoyl groups
- the lower alkylene group may have one or two double bonds or triple bonds in the main chain, and the lower alkylene group is substituted by 1 to 3 by a lower alkoxy group, an oxo group or a hydroxy group.
- Step 7 This step is a method for producing compound (9) by reacting compound (7) with compound (8). This step is a so-called Mitsunobu reaction, and can be carried out by the same method as in Step 1, a method according to this, or a combination of these with conventional methods.
- Examples of the compound (8) used in this step include ethyl 3- (4- (hydroxymethyl) phenyl) -2-propinoate, ethyl (3- (4- (2-hydroxyethyl) phenyl) -2-propinoate Etc.
- the compound (9) thus obtained can be isolated or purified by a known separation and purification means, for example, concentration, concentration under reduced pressure, reprecipitation, solvent extraction, crystallization, chromatography, etc. It can be attached to the next process.
- a known separation and purification means for example, concentration, concentration under reduced pressure, reprecipitation, solvent extraction, crystallization, chromatography, etc. It can be attached to the next process.
- This step is a method for producing the compound (IB) according to the present invention by reacting the compound (3) obtained in the above step 1 with hydroxyamine in the presence of a base.
- the reaction in this step can be carried out by the same method as in Step 2, a method analogous thereto, or a combination of these with conventional methods.
- the compound (IB) thus obtained can be isolated and purified by known separation and purification means such as concentration, concentration under reduced pressure, crystallization, solvent extraction, reprecipitation, chromatography and the like.
- the methylene group in the (1) an amino group (the amino group may be substituted with a lower alkyl group, a lower alkylsulfonyl group, or a lower alkanoyl group), (2) a halogen atom, (3) a lower alkenyl group, (4) a lower alkyl group (when the same carbon atom constituting the lower alkylene group is substituted with two lower alkyl groups, these lower alkyl groups are combined to form a 3- to 7-membered
- An aliphatic ring (which may form one or two carbon atoms constituting the aliphatic ring may be replaced by a nitrogen atom, a sulfur atom or an oxygen atom)), (5) a lower alkynyl group, (6) a lower alkylidene group, (7) imino group, (8) an arylalkyl group, (9) a 5- or 6-membered heteroarylalkyl group having 1 to 4 heteroatoms in the ring selected from the group consisting of
- the lower alkyl group, the lower alkynyl group, and the lower alkylidene group may be substituted with 1 to 3 halogen atoms, a hydroxy group, or a lower alkoxy group
- the imino group may be substituted with 1 to 3 lower alkyl groups, lower alkylsulfonyl groups, cyano groups, nitro groups, lower alkanoyl groups
- the lower alkylene group may have one or two double bonds or triple bonds in the main chain, and the lower alkylene group is substituted by 1 to 3 by a lower alkoxy group, an oxo group or a hydroxy group.
- G represents NH, an N-lower alkyl group, a sulfur atom or an oxygen atom], for example, can be
- Step 9 This step can be carried out by the same method as in Step 4, a method according to this, or a combination of these with conventional methods.
- Step 10 This step can be carried out by the same method as in Step 5, a method according to this, or a combination of these with conventional methods.
- Step 11 This step can be carried out by the same method as in Step 6, a method according to this, or a combination of these with conventional methods.
- Step 12 This step can be carried out by the same method as in step 2, a method according to this, or a combination of these with conventional methods.
- the alkylene group in the (1) an amino group (the amino group may be substituted with a lower alkyl group, a lower alkylsulfonyl group, or a lower alkanoyl group), (2) a halogen atom, (3) a lower alkenyl group, (4) a lower alkyl group (when the same carbon atom constituting the lower alkylene group is substituted with two lower alkyl groups, these lower alkyl groups are combined to form a 3- to 7-membered
- An aliphatic ring (which may form one or two carbon atoms constituting the aliphatic ring may be replaced by a nitrogen atom, a sulfur atom or an oxygen atom)), (5) a lower alkynyl group, (6) a lower alkylidene group, (7) imino group, (8) an arylalkyl group, (9) a 5- or 6-membered heteroarylalkyl group having 1 to 4 heteroatoms in the ring selected from the group consisting of
- the lower alkyl group, the lower alkynyl group, and the lower alkylidene group may be substituted with 1 to 3 halogen atoms, a hydroxy group, or a lower alkoxy group
- the imino group may be substituted with 1 to 3 lower alkyl groups, lower alkylsulfonyl groups, cyano groups, nitro groups, lower alkanoyl groups
- the lower alkylene group may have 1 or 2 double bonds or triple bonds in the main chain, and the lower alkylene group is substituted by 1 to 3 by a lower alkoxy group, an oxo group or a hydroxy group.
- G 1 represents NH, an N-lower alkyl group, or a sulfur atom, and the other symbols are the same as
- Step 13 This step can be carried out by the same method as in Step 5, a method according to this, or a combination of these with conventional methods.
- Step 14 This step can be carried out by the same method as in Step 6, a method according to this, or a combination of these with conventional methods.
- Step 15 This step can be carried out by the same method as in step 2, a method according to this, or a combination of these with conventional methods.
- the alkylene group in the (1) an amino group (the amino group may be substituted with a lower alkyl group, a lower alkylsulfonyl group, or a lower alkanoyl group), (2) a halogen atom, (3) a lower alkenyl group, (4) a lower alkyl group (when the same carbon atom constituting the lower alkylene group is substituted with two lower alkyl groups, these lower alkyl groups are combined to form a 3- to 7-membered
- An aliphatic ring (which may form one or two carbon atoms constituting the aliphatic ring may be replaced by a nitrogen atom, a sulfur atom or an oxygen atom)), (5) a lower alkynyl group, (6) a lower alkylidene group, (7) imino group, (8) an arylalkyl group, (9) a 5- or 6-membered heteroarylalkyl group having 1 to 4 heteroatoms in the ring selected from the group consisting of
- the lower alkyl group, the lower alkynyl group, and the lower alkylidene group may be substituted with 1 to 3 halogen atoms, a hydroxy group, or a lower alkoxy group
- the imino group may be substituted with 1 to 3 lower alkyl groups, lower alkylsulfonyl groups, cyano groups, nitro groups, lower alkanoyl groups
- the lower alkylene group may have one or two double bonds or triple bonds in the main chain, and the lower alkylene group is substituted by 1 to 3 by a lower alkoxy group, an oxo group or a hydroxy group.
- the other symbols may be the same as described above], for example, and can be produced by the following method.
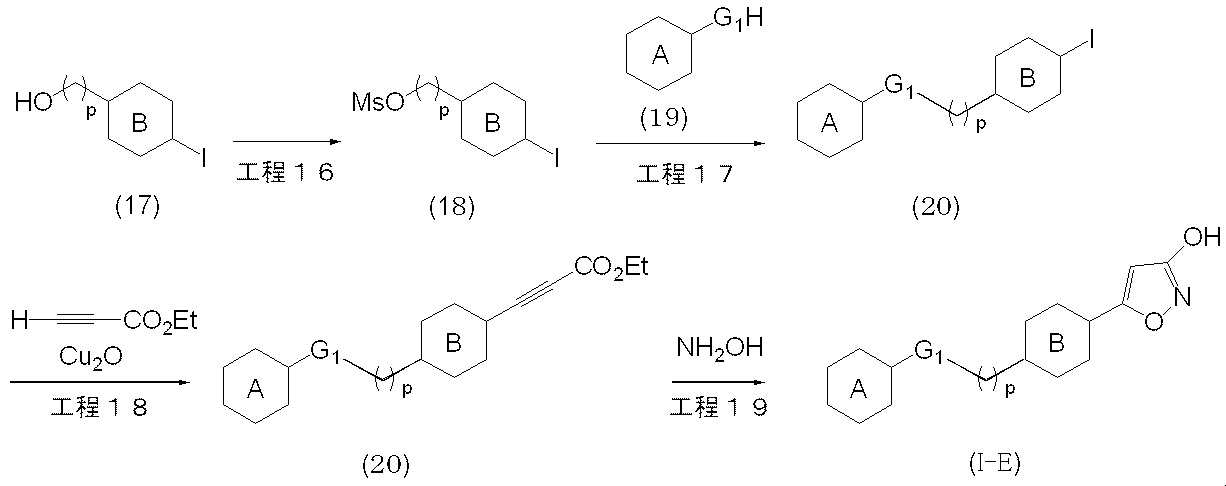
- Step 16 This step can be carried out by the same method as in Step 4, a method according to this, or a combination of these with conventional methods.
- Step 17 This step can be carried out by the same method as in Step 5, a method according to this, or a combination of these with conventional methods.
- Step 18 This step can be carried out by the same method as in Step 6, a method according to this, or a combination of these with conventional methods.
- Step 19 This step can be carried out by the same method as in step 2, a method according to this, or a combination of these with conventional methods.
- the lower alkylene group in the (1) an amino group (the amino group may be substituted with a lower alkyl group, a lower alkylsulfonyl group, or a lower alkanoyl group), (2) a halogen atom, (3) a lower alkenyl group, (4) a lower alkyl group (when the same carbon atom constituting the lower alkylene group is substituted with two lower alkyl groups, these lower alkyl groups are combined to form a 3- to 7-membered
- An aliphatic ring (which may form one or two carbon atoms constituting the aliphatic ring may be replaced by a nitrogen atom, a sulfur atom or an oxygen atom)), (5) a lower alkynyl group, (6) a lower alkylidene group, (7) imino group, (8) an arylalkyl group, (9) a 5- or 6-membered heteroarylalkyl group having 1 to 4 heteroatoms in the ring selected from the group consisting
- the lower alkyl group, the lower alkynyl group, and the lower alkylidene group may be substituted with 1 to 3 halogen atoms, a hydroxy group, or a lower alkoxy group
- the imino group may be substituted with 1 to 3 lower alkyl groups, lower alkylsulfonyl groups, cyano groups, nitro groups, lower alkanoyl groups
- the lower alkylene group may have one or two double bonds or triple bonds in the main chain, and the lower alkylene group is substituted by 1 to 3 by a lower alkoxy group, an oxo group or a hydroxy group.
- the other symbols may be the same as described above], for example, and can be produced by the following method.
- Step 20 This step can be carried out by the same method as in step 1, a method according to this, or a combination of these with conventional methods.
- Step 21 This step can be carried out by the same method as in step 2, a method according to this, or a combination of these with conventional methods.
- the lower alkylene group in the (1) an amino group (the amino group may be substituted with a lower alkyl group, a lower alkylsulfonyl group, or a lower alkanoyl group), (2) a halogen atom, (3) a lower alkenyl group, (4) a lower alkyl group (when the same carbon atom constituting the lower alkylene group is substituted with two lower alkyl groups, these lower alkyl groups are combined to form a 3- to 7-membered
- An aliphatic ring (which may form one or two carbon atoms constituting the aliphatic ring may be replaced by a nitrogen atom, a sulfur atom or an oxygen atom)), (5) a lower alkynyl group, (6) a lower alkylidene group, (7) imino group, (8) an arylalkyl group, (9) a 5- or 6-membered heteroarylalkyl group having 1 to 4 heteroatoms in the ring selected from the group consisting
- the lower alkyl group, the lower alkynyl group, and the lower alkylidene group may be substituted with 1 to 3 halogen atoms, a hydroxy group, or a lower alkoxy group
- the imino group may be substituted with 1 to 3 lower alkyl groups, lower alkylsulfonyl groups, cyano groups, nitro groups, lower alkanoyl groups
- the lower alkylene group may have one or two double bonds or triple bonds in the main chain, and the lower alkylene group is substituted by 1 to 3 by a lower alkoxy group, an oxo group or a hydroxy group.
- the other symbols may be the same as described above], for example, and can be produced by the following method.
- Step 22 This step can be carried out by the same method as in step 1, a method according to this, or a combination of these with conventional methods.
- Step 23 This step can be carried out by the same method as in step 2, a method according to this, or a combination of these with conventional methods.
- G 2 represents C (O) or S (O) 2
- R represents a hydrogen atom or a lower alkyl group, and other symbols are the same as described above
- Step 24 This step is a method for producing an amide compound or a sulfonamide compound by reacting an amino compound with a carboxylic acid compound or a sulfonic acid compound. This reaction is performed according to literature methods (for example, peptide synthesis basics and experiments, Nobuo Izumiya et al., Maruzen, 1983, Comprehensive Organic Synthesis, Vol. 6, Pergamon Press, 1991, etc.
- a normal amide or sulfonamide forming reaction may be carried out, that is, using a condensing agent well known to those skilled in the art, or It can be performed by an available ester activation method, mixed acid anhydride method, acid chloride method, carbodiimide method, or the like.
- amide-forming reagents include thionyl chloride, oxalyl chloride, N, N-dicyclohexylcarbodiimide, 1-methyl-2-bromopyridinium iodide, N, N′-carbonyldiimidazole, diphenylphosphoryl chloride.
- Examples of the base to be used include trimethylamine, triethylamine, N, N-diisopropylethylamine, N-methylmorpholine, N-methylpyrrolidine, N-methylpiperidine, N, N-dimethylaniline, 1,8-diazabicyclo [5.4. 0] tertiary aliphatic amines such as undec-7-ene (DBU), 1,5-azabicyclo [4.3.0] non-5-ene (DBN); for example, pyridine, 4-dimethylaminopyridine, picoline And aromatic amines such as lutidine, quinoline and isoquinoline. Among them, tertiary aliphatic amines are preferable, and triethylamine or N, N-diisopropylethylamine is particularly preferable.
- condensation aid to be used examples include N-hydroxybenzotriazole hydrate, N-hydroxysuccinimide, N-hydroxy-5-norbornene-2,3-dicarboximide or 3-hydroxy-3,4- Examples thereof include dihydro-4-oxo-1,2,3-benzotriazole, among which N-hydroxybenzotriazole and the like are preferable.
- the amount of amino compound used varies depending on the type of compound and solvent used and other reaction conditions, but is usually 0.1 to 10 equivalents, preferably 1 to 10 equivalents, preferably 1 equivalent of carboxylic acid or sulfonic acid or reactive derivative thereof. 0.5 to 3 equivalents.
- the amount of the amide-forming reagent used varies depending on the type of compound and solvent used and other reaction conditions, but is usually 1 to 10 equivalents relative to 1 equivalent of a carboxylic acid compound or a sulfonic acid compound or a reactive derivative thereof. Preferably 1 to 3 equivalents.
- the amount of the condensation aid used varies depending on the compound used, the type of solvent and other reaction conditions, but is usually 1 to 10 equivalents, preferably 1 equivalent to 1 equivalent of the carboxylic acid compound or sulfonic acid compound or reactive derivative thereof. 1 to 3 equivalents.
- the amount of the base used varies depending on the compound used, the type of solvent, and other reaction conditions, but is usually 1 to 10 equivalents, preferably 1 to 1 equivalent to 1 equivalent of the carboxylic acid compound or sulfonic acid compound or reactive derivative thereof. 5 equivalents.
- the reaction solvent used in this step includes, for example, an inert solvent, and is not particularly limited as long as the reaction is not hindered. Specifically, for example, methylene chloride, chloroform, 1,2-dichloroethane, N, N -Dimethylformamide, acetic acid ethyl ester, acetic acid methyl ester, acetonitrile, benzene, xylene, toluene, 1,4-dioxane, tetrahydrofuran, dimethoxyethane, or a mixed solvent thereof. From the viewpoint of securing a suitable reaction temperature, for example, Methylene chloride, chloroform, 1,2-dichloroethane, acetonitrile, N, N-dimethylformamide and the like are preferable.
- the reaction temperature in this step is usually ⁇ 78 ° C. to the boiling point of the solvent, preferably 0 to 30 ° C.
- the reaction time in this step is usually 0.5 to 96 hours, preferably 3 to 24 hours.
- the base, amide or sulfonamide forming reagent and condensation aid used in this step can be used alone or in combination.
- the amide compound or sulfonamide compound thus obtained is isolated or purified by a known separation and purification means, for example, concentration, concentration under reduced pressure, reprecipitation, solvent extraction, crystallization, chromatography, etc. It can attach to the next process, without doing.
- Step 25 This step is a method for producing the compound (IH) by removing the protective group for the hydroxy group of the isoxazole group.
- the reaction in this step is a method described in the literature (Protective Groups in Organic Synthesis), TW Green, 2nd edition, John Wiley & Sons, 1991), or a method according to this. These can be carried out in combination with a conventional method, and examples of the hydroxy-protecting group include a MOM (methoxymethoxy) group.
- the protecting group has a necessary substituent, an appropriate protecting group is introduced into these substituents as necessary, and these substituents are subsequently deprotected, thereby introducing the present invention.
- Such compounds can be produced.
- Pro means a protecting group for a hydroxy group, but a necessary protecting group can be appropriately used in each step.
- Examples of Pro include MOM (methoxymethoxy group).
- the compounds according to the invention can exist as pharmaceutically acceptable salts, (I) and (IA), (IB), (IC), (ID), (IE), (IF), (IG) included therein Or it can manufacture in accordance with a conventional method using the compound represented by (IH).
- the acid addition salt examples include hydrohalides such as hydrochloride, hydrofluoride, hydrobromide, hydroiodide; nitrate, perchlorate, sulfate, phosphate, carbonate Inorganic acid salts such as salts; lower alkyl sulfonates such as methane sulfonate, trifluoromethane sulfonate and ethane sulfonate; aryl sulfonates such as benzene sulfonate and p-toluene sulfonate; Organic acid salts such as acid salts, succinates, citrates, tartrates, oxalates and maleates; and acid addition salts which are organic acids such as amino acids such as glutamates and aspartates it can.
- hydrohalides such as hydrochloride, hydrofluoride, hydrobromide, hydroiodide
- nitrate, perchlorate, sulfate, phosphate carbonate
- the compound of the present invention when it has an acidic group in the group, for example, when it has a carboxyl group or the like, the corresponding pharmaceutically acceptable can also be obtained by treating the compound with a base.
- a base can be converted to a salt.
- the base addition salt include alkali metal salts such as sodium and potassium, alkaline earth metal salts such as calcium and magnesium, salts with organic bases such as ammonium salts, guanidine, triethylamine and dicyclohexylamine.
- the compound of the present invention may exist as any hydrate or solvate of the free compound or a salt thereof.
- the compound according to the present invention may have a stereoisomer or a tautomer such as an optical isomer, a diastereoisomer, or a geometric isomer depending on the mode of the substituent. Needless to say, all of these isomers are included in the compounds of the present invention. Furthermore, it goes without saying that any mixture of these isomers is also encompassed by the compounds according to the invention.
- the compound of formula (I) according to the present invention may be used in combination with a compound of formula (I) and a carrier. it can.
- the dosage for the prevention or treatment of the compound of formula (I) according to the present invention will of course vary depending on the nature of the condition to be treated, the particular compound selected and the route of administration.
- the daily dosage is from about 0.001 mg to about 100 mg per kg body weight, preferably from about 0.01 mg to about 50 mg per kg body weight as single or multiple doses More preferably from about 0.1 mg to 10 mg. It may be necessary to use dosages that exceed these limits.
- An example of a suitable oral dosage is at least about 0.01 mg to at most 2.0 g for a single dose or 2 to 4 multiple doses per day.
- the dosage range is from about 1.0 mg to about 200 mg, once or twice daily. More preferably, the dosage range is from about 10 mg to 100 mg once a day.
- a typical dosage range is from about 0.001 mg to about 100 mg, preferably from 0.01 mg to about 100 mg of the compound of formula (I) per kg body weight per day. 10 mg, more preferably from about 0.1 mg to 10 mg of the compound of formula (I) per kg body weight per day.
- the pharmaceutical composition comprises a compound of formula (I) and a pharmaceutically acceptable carrier.
- composition is the result of combining, combining or aggregating any two or more components, directly or indirectly, resulting from the dissociation of one or more components, or It includes active and inactive ingredients (pharmaceutically acceptable excipients) that make up the carrier, as well as those resulting from other types of actions or interactions between the ingredients.
- composition comprising an amount of a compound of formula (I) effective in combination with a pharmaceutically acceptable carrier to treat, prevent or delay the onset of type 2 diabetes or hyperlipidemia.
- Any suitable route of administration may be employed for administering an effective amount of a compound according to the present invention to mammals, particularly humans.
- mammals particularly humans.
- oral, rectal, topical, vein, eye, lung, nose and the like can be used.
- dosage forms include tablets, troches, powders, suspensions, solutions, capsules, creams, aerosols and the like, and oral tablets are preferred.
- any conventional pharmaceutical medium can be used. Examples thereof include water, glycols, oils, alcohols, fragrance additives, and storage.
- examples include suspensions, elixirs and solutions, and examples of carriers include starch, sugar, microcrystalline cellulose, Diluents, granulating agents, lubricants, binders, disintegrating agents and the like can be mentioned.
- carriers include starch, sugar, microcrystalline cellulose, Diluents, granulating agents, lubricants, binders, disintegrating agents and the like can be mentioned.
- powders, capsules, tablets and the like can be mentioned.
- a solid composition is preferred.
- tablets and capsules are the most advantageous oral dosage form. If desired, tablets can be coated by standard aqueous or nonaqueous techniques.
- compositions according to the present invention suitable for oral administration is preliminarily determined as a powder or granule, or as a water-soluble liquid, water-insoluble liquid, oil-in-water emulsion or water-in-oil emulsion. Mention may be made of capsules, cashews or tablets containing a certain amount of active ingredient. Such compositions can be prepared using any pharmacological method, but all methods also include a method of combining the active ingredient with a carrier comprising one or more necessary ingredients. .
- compositions are prepared by uniformly and intimately bringing into association the active ingredient with liquid carriers or well-separated solid carriers or both and then, if necessary, shaping the product into a suitable form.
- a tablet is prepared by compression and molding, optionally with one or more accessory ingredients.
- Compressed tablets can be mixed with binders, lubricants, inert excipients, surfactants or dispersants as appropriate, in any suitable machine, and the active ingredient can be freely formed into powders, granules, etc.
- Molded tablets are prepared by molding in a suitable machine a mixture of the powdered moist compound and an inert liquid diluent.
- each tablet contains about 1 mg to 1 g of the active ingredient and each cashew or capsule contains about 1 mg to 500 mg of the active ingredient.
- Examples of pharmaceutical dosage forms for compounds of formula (I) are as follows:
- the compound of formula (I) is combined with other drugs used in the treatment / prevention / delay of the onset of type 2 diabetes or hyperlipidemia as well as diseases or symptoms associated with type 2 diabetes or hyperlipidemia Can be used.
- the other agent can be administered simultaneously or separately with the compound of formula (I), using the route or dose normally used.
- compositions comprising the compound of formula (I) and these other drugs is preferred.
- the pharmaceutical compositions according to the invention also contain one or more other active ingredients, in addition to the compound of formula (I).
- active ingredients used in combination with a compound of formula (I) may be administered separately or in the same pharmaceutical composition, but are not limited to the following.
- A other GPR120 agonists
- glucokinase activators e.g, biguanides (eg, buformin, metformin, phenformin)
- D PPAR agonist
- E insulin
- somatostatin e.g, ⁇ -glucosidase inhibitor
- H an insulin secretagogue (e.g., acetohexamide, carbutamide, chlorpropamide, glybomlide, gliclazide, glimelpide, glipizide, glyxidine, glyoxepide, glyburide, glyhexamide, glipinamide, fenbutamide, tolazamide, tolbutamide, tolcyclamide, nateglinide, Repaglinide), and (i) insulin secretagogue (e.g., acetohexamide, carbutamide, chlorpropamide, glybomlide, gliclazide, glimelpide,
- the weight ratio of the compound of formula (I) to the PPAR agonist is generally about 1000: 1 to 1: 1000, Preferably, it is about 200: 1 to 1: 200.
- Combinations of a compound of formula (I) and other active ingredients are within the aforementioned ranges, but in each case, an effective amount of each active ingredient should be used.
- the compound according to the present invention has a GPR120 function-regulating action.
- the “GPR120 function-modulating action” means that the function of the GPR120 receptor is activated or suppressed. Included in those having a regulating action.
- Formulation Example 1 10 parts of the compound of Example 1, 15 parts of heavy magnesium oxide, and 75 parts of lactose are uniformly mixed to obtain a powdery or fine powder powder of 350 ⁇ m or less. This powder is put into a capsule container to form a capsule.
- Formulation Example 2 After uniformly mixing 45 parts of the compound of Example 1, 15 parts of starch, 16 parts of lactose, 21 parts of crystalline cellulose, 3 parts of polyvinyl alcohol and 30 parts of distilled water, the mixture was crushed and granulated and dried, and then sieved to obtain a diameter.
- Granules having a size of 1410 to 177 ⁇ m are used.
- Formulation Example 3 A granule is prepared in the same manner as in Formulation Example 2, and then 3 parts of calcium stearate is added to 96 parts of this granule and compression-molded to prepare a tablet having a diameter of 10 mm.
- Formulation Example 4 10 parts of crystalline cellulose and 3 parts of calcium stearate are added to 90 parts of the granules obtained by the method of Formulation Example 2 and compression-molded to form tablets with a diameter of 8 mm, followed by syrup gelatin and precipitated calcium carbonate Drag suspension to make dragees.
- i-Bu Isobutyl group n-Bu: n-butyl group t-Bu: tert-butyl group Boc: tert-butoxycarbonyl group Me: methyl group Et: ethyl group Ph: phenyl group i-Pr: isopropyl group n-Pr: n-propyl group CDCl 3 : Deuterated chloroform CD 3 OD: Heavy methanol DMSO-d 6 : Heavy dimethyl sulfoxide The meanings of the abbreviations in the nuclear magnetic resonance spectrum are shown below.
- reaction solution was diluted with a saturated aqueous ammonium chloride solution, extracted with ethyl acetate, and dried over anhydrous magnesium sulfate.
- the obtained residue was dissolved in 1 ml of ethanol, 0.05 ml of 50% aqueous hydroxyamine solution and 0.03 ml of 2N aqueous sodium hydroxide solution were added, and the reaction solution was stirred overnight at room temperature.
- the reaction solution was acidified with 10% aqueous citric acid solution, extracted with chloroform, and dried over anhydrous magnesium sulfate.
- the mixture was stirred at the same temperature for 30 minutes.
- the reaction mixture was poured into ice and diluted with diethyl ether and water, and the extracted organic layer was washed with saturated brine, dried over sodium sulfate, filtered and concentrated.
- the obtained reaction mixture was dissolved in 20 ml of MeOH, 5 ml of 5M aqueous sodium hydroxide solution was added, and the mixture was stirred at room temperature for 1 hour, diluted with ethyl acetate and water, and the organic layer was extracted. The organic layer was washed with saturated brine, dried over sodium sulfate, filtered and concentrated.
- the obtained crude product was purified by silica gel column chromatography to obtain 5.1 g of the title compound as a yellow oily compound.
- 5) Preparation of 5- (4- (2-phenoxypropyl) phenyl) isoxazol 3-ol
- To a solution of 5- (methoxymethoxy) -5- (4- (2-phenoxypropyl) phenyl) isoxazole (58.8 mg) in methanol (0.5 ml) was added 4M hydrochloric acid-dioxane (0.5 ml), and the reaction solution was stirred at room temperature for 24 hours. Stir for hours.
- Example 22 5- [4-( ⁇ (1R) -1-methyl-2- [3- (cyclopropyloxy) phenyl] -1-methylethyl ⁇ oxy) phenyl] isoxazol-3-ol 1) Production of (2S) -1- [3- (cyclopropyloxy) phenyl] propan-2-ol In the same manner as in Example 20, 0.37 g of the title compound was obtained as a colorless oil from 0.94 g of 1-bromo-3- (cyclopropyloxy) benzene.
- Example 28 5- ⁇ 2-Fluoro-4-[((1R) -1-methyl-2- ⁇ 3-[(1-methylethyl) oxy] phenyl ⁇ ethyl) oxy] phenyl ⁇ isoxazol-3-ol
- propan-2-ol 125 mg of the title compound was obtained as a colorless oil.
- reaction solution was quenched with saturated aqueous sodium bicarbonate solution and diluted with chloroform and water.
- the organic layer obtained by extraction was dried over sodium sulfate, filtered and concentrated, and then purified by silica gel chromatography to obtain 51 mg of the title compound as a colorless oil.
- Example 34 5- (4- (2- (3-Isopropoxyphenyl) -1-ethylethoxy) phenyl) isoxazol-3-ol
- the title compound was obtained by using the same method as in Example 4.
- Example 36 5- (4- (2,2-difluoro-2- (3-isopropoxyphenyl) ethoxy) phenyl) isoxazol 3-ol Performed by using 1- ⁇ 3-[(1-methylethyl) oxy] phenyl ⁇ ethane-1-one instead of 1- ⁇ 3-[(1-methylethyl) oxy] phenyl ⁇ propan-1-one The title compound was obtained in the same manner as in Example 30.
- Example 37 5- ⁇ 2-Fluoro-4- [2- (3-ethoxyphenyl) -1-methylethoxy] phenyl ⁇ isoxazol-3-ol
- the title compound was prepared in the same manner as in Example 4 using 2-fluoro-4- (3- (methoxymethoxy) isoxazol-5-yl) phenol and 1- (3-ethoxyphenyl) propan-2-ol. Obtained.
- the mixture was stirred at the same temperature for 30 minutes.
- the reaction mixture was poured into ice and diluted with diethyl ether and water, and the extracted organic layer was washed with saturated brine, dried over sodium sulfate, filtered and concentrated.
- the obtained reaction mixture was dissolved in MeOH (20 ml), 5M aqueous sodium hydroxide solution (5 ml) was added, and the mixture was stirred at room temperature for 1 hour, then diluted with ethyl acetate and water, and the organic layer was extracted. The organic layer was washed with saturated brine, dried over sodium sulfate, filtered and concentrated.
- the obtained crude product was purified by silica gel column chromatography to obtain 5.1 g of the title compound as a yellow oily compound.
- Reference example 4 5- [4- (2-Hydroxypropyl) phenyl] isoxazol 3-ol
- 1- (4-iodophenyl) propan-2-ol as a starting material in the same manner as in Reference Examples 1 and 2, 1.84 g of the title compound was obtained as a colorless solid.
- Reference Example 5 3-Isopropoxyphenacyl bromide Bromine (0.27 g, 1.7 mmol) CHCl 3 (1 mL) solution of 3-isopropoxyacetophenone (0.3 g, 1.7 mmol) in CHCl 3 To the (5 mL) solution was added at room temperature and the mixture was stirred at room temperature overnight. The reaction mixture was concentrated, diluted with chloroform, and washed with water.
- Reference Example 8 1- (2-((1-Methylethyl) oxy) pyridin-4-yl) propan-2-ol
- a solution of 1.51 g of 4-methyl-2-((1-methylethyl) oxy) pyridine obtained in Reference Example 1 in 20 ml of tetrahydrofuran was added 2.66 M hexane of n-butyllithium at ⁇ 78 ° C. in an argon atmosphere. After adding 4.14 ml of the solution, the temperature was raised to 0 ° C. over 30 minutes and further stirred at 0 ° C. for 20 minutes.
- Test 1 Gene cloning GenBank Accession No. NM_181745 (human), No. Primers were synthesized in the region before and after the base sequence of the known GPCR, GPR120 ORF in NM_181748 (mouse), and the gene was cloned by RT-PCR.
- the base sequences of the primers used are as follows. Restriction enzymes BamHI and EcoRI recognition sites are introduced for subcloning, respectively.
- hGPR120_F01 aggatccgccgccatgtccctgaatgcgcgcgggcag (SEQ ID NO: 1)
- hGPR120_R01 cgaattcttagccagaaataatcgacaagtcatttc (SEQ ID NO: 2)
- mGPR120_F01 aggatccgccgccatgtcccctgagtgtgcacagacgac (SEQ ID NO: 3)
- mGPR120_R01 cgaattcttagctggaaataacagacaagtcatttc (SEQ ID NO: 4)
- the human GPR120 receptor gene used was human small intestine marathon-ready cDNA (CLONTECH: current TaKaRa), and the mouse GPR120 receptor gene used was cDMA obtained by reverse transcription of mouse BAT tissue-derived RNA.
- PCR was performed using KOD_Plus (TOYOBO) for 30 cycles of 94 ° C. for 2 minutes, 94 ° C. for 15 seconds, 55 ° C. for 30 seconds, 68 ° C. for 1 minute, and after the reaction, ExTaq (TaKaRa) for 0.5 Units was added. The mixture was incubated at 72 ° C. for 10 minutes, and an addition reaction of A was performed at the end. Mouse PCR was performed for 35 cycles under conditions of a final concentration of 2% DMSO. The amplified PCR product was cloned using pCR2.1-TOPO TA cloning kit (Invitrogen). For confirmation of the base sequence, BigDye Terminator Cycle Sequencing Ready Reaction Kit ver.
- the human GPR120 gene is GenBank Accession No. It was 16 amino acids shorter than the sequence registered in NM_181745.
- the GPR120 receptor gene cloned into the pCR2.1-TOPO vector is introduced with restriction enzymes BamHI and EcoRI recognition sites, excised from the vector with the same enzyme, and the eukaryotic expression vector EF1 / V5-His B ( Subcloning into BamHI and EcoRI recognition sites of Invitrogen).
- Test 2 Preparation of expression cells Using LIPOFECTAMINE2000 (Invitrogen), GPR120 receptor cDNA was transfected into CHO / NFAT-BLA cells, drug resistant cells were isolated, and GPR120 stable expression strains were obtained.
- CHO cells expressing GPR120 were cultured in DMEM / F12 medium containing 10% fetal bovine serum, 100 units / mL penicillin, 0.1 mg / mL streptomycin sulfate, 250 ug / mL Zeocin, 500 ug / mL Geneticin 15 mM HEPES.
- Test 3 Intracellular calcium concentration measurement
- human GPR120-expressing CHO cells plated at 20,000 cells per well in a 96-well black plate (Packard, ViewPlate) in the presence of 2.5 mM Probenecid.
- 4 ⁇ M Fluo-4 AM fluorescent calcium indicator reagent was incubated for 1 hour in a CO 2 incubator and incorporated.
- a test compound diluted with an HBSS solution containing 20 mM HEPES and 2.5 mM Probenecid was added to this, and the change in intracellular calcium concentration was measured with a Fluorescence Imaging Plate Reader (FLIPR, Molecular Devices Co., Ltd.). The effect was investigated.
- FLIPR Fluorescence Imaging Plate Reader
- the GPR120 agonist action of the compound group included in the compound of the present invention was as follows.
- the compound according to the present invention has a GPR120 agonistic action and is useful for the treatment and / or prevention of diabetes, obesity and hyperlipidemia.
- the compound according to the present invention or a pharmaceutically acceptable salt thereof has a GPR120 function-regulating action, particularly a GPR120 agonist action, and is useful for the treatment and / or prevention of diabetes or hyperlipidemia.
Abstract
Description
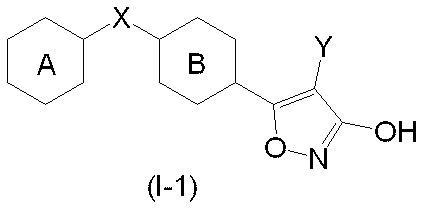
Xは、主鎖が2乃至4の炭素原子からなり、また、該主鎖を構成する炭素原子の1又は2が、酸素原子、硫黄原子又は窒素原子で置き換わっていてもよい、低級アルキレン基であって、
該低級アルキレン基は、
(1)アミノ基(該アミノ基は、低級アルキル基、低級アルキルスルホニル基、低級アルカノイル基で置換されていてもよい)、
(2)ハロゲン原子、
(3)低級アルケニル基、
(4)低級アルキル基(該低級アルキレン基を構成する同一の炭素原子が、2つの低級アルキル基で置換されている場合には、これらの低級アルキル基が一緒になって、3乃至7員の脂肪族環(該脂肪族環を構成する炭素原子の1又は2が、窒素原子、硫黄原子又は酸素原子に置き換わっていてもよい)を形成していてもよい)、
(5)低級アルキニル基、
(6)低級アルキリデン基、
(7)イミノ基、
(8)アリールアルキル基、
(9)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する、5又は6員のヘテロアリールアルキル基、
(10)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有するヘテロアリール基
(11)アリールアルキルオキシ基、及び
(12)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する5又は6員のヘテロアリールアルキルオキシ基
からなる群より選択される基で、同一又は異なって1乃至3置換されており;
ここで、低級アルキル基、低級アルキニル基、低級アルキリデン基は、1乃至3のハロゲン原子、ヒドロキシ基又は低級アルコキシ基で置換されていてもよく;
該イミノ基は、1乃至3の低級アルキル基、低級アルキルスルホニル基、シアノ基、ニトロ基、低級アルカノイル基で置換されていてもよく;
該低級アルキレン基は、主鎖中に二重結合又は三重結合を1又は2有していてもよく、さらに、該低級アルキレンは、低級アルコキシ基、オキソ基又はヒドロキシ基で1乃至3置換されていてもよく;
Yは、
水素原子、
低級アルキル基(該低級アルキル基は、低級アルコキシ基、ハロゲン原子で1乃至3置換されていてもよい)、
低級アルコキシ基、及び
ハロゲン原子
からなる群より選択される]で表される化合物又はその薬学的に許容される塩、に関する。
等が挙げられる。
低級アルコキシ基(該低級アルコキシ基は、同一又は異なる1乃至3のハロゲン原子で置換されていてもよい)、
C3-7シクロアルキルオキシ基、
低級アルキル基(該低級アルキル基は、同一又は異なる1乃至3のハロゲン原子で置換されていてもよい)、
低級アルケニル基、及び
ハロゲン原子
からなる群より選択される基で同一又は異なって、1乃至2置換されているフェニル基又はピリジニル基が好ましく、
(1)アミノ基(該アミノ基は、低級アルキル基、低級アルキルスルホニル基、低級アルカノイル基で1乃至3置換されていてもよい)、
(2)ハロゲン原子、
(3)低級アルケニル基、
(4)低級アルキル基(該Xを構成する同一の炭素原子が、2つの低級アルキル基で置換されている場合には、これらの低級アルキル基が一緒になって、3乃至7員の脂肪族環(該脂肪族環を構成する炭素原子の1又は2が、窒素原子、硫黄原子又は酸素原子で置き換わっていてもよい)を形成していてもよい)、
(5)低級アルキニル基、
(6)低級アルキリデン基、
(7)イミノ基、
(8)アリールアルキル基、
(9)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有するヘテロアリールアルキル基、
(10)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有するヘテロアリール基、
(11)アリールアルキルオキシ基、及び
(12)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する5又は6員のヘテロアリールアルキルオキシ基
からなる群より選択される基で、同一又は異なって、1乃至3置換されている。
ここで、
主鎖が3の炭素原子からなり、また、該主鎖を構成する炭素原子の1又は2が、酸素原子、硫黄原子又は窒素原子に置き換わっている低級アルキレン基であって、該低級アルキレン基が、低級アルキル基、ハロゲン原子及びオキソ基からなる群より選択される基で、同一又は異なって、1乃至3置換されている場合が好ましく、
主鎖が3の炭素原子からなり、また、該主鎖を構成する炭素原子の1つが、酸素原子、硫黄原子又は窒素原子に置き換わっている低級アルキレン基であって、該低級アルキレン基が、低級アルキル基、ハロゲン原子及びオキソ基からなる群より選択される基で、同一又は異なって、1又は2置換されている場合がより好ましく、
水素原子、
低級アルキル基(該アルキル基は、低級アルコキシ基又はハロゲン原子で同一又は異なって、1乃至3置換されていてもよい)、
低級アルコキシ基、及び
ハロゲン原子
からなる群より選択される基を示す。
(1)アミノ基(該アミノ基は、低級アルキル基、低級アルキルスルホニル基、低級アルカノイル基で置換されていてもよい)、
(2)ハロゲン原子、
(3)低級アルケニル基、
(4)低級アルキル基(該低級アルキレン基を構成する同一の炭素原子が、2つの低級アルキル基で置換されている場合には、これらの低級アルキル基が一緒になって、3乃至7員の脂肪族環(該脂肪族環を構成する炭素原子の1又は2が、窒素原子、硫黄原子又は酸素原子に置き換わっていてもよい)を形成していてもよい)、
(5)低級アルキニル基、
(6)低級アルキリデン基、
(7)イミノ基、
(8)アリールアルキル基、
(9)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する、5又は6員のヘテロアリールアルキル基、
(10)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有するヘテロアリール基
(11)アリールアルキルオキシ基、及び
(12)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する5又は6員のヘテロアリールアルキルオキシ基
からなる群より選択される基で、同一又は異なって1乃至3置換されており、
ここで、低級アルキル基、低級アルキニル基、低級アルキリデン基は、1乃至3のハロゲン原子、ヒドロキシ基又は低級アルコキシ基で置換されていてもよく、
該イミノ基は、1乃至3の低級アルキル基、低級アルキルスルホニル基、シアノ基、ニトロ基、低級アルカノイル基で置換されていてもよく、
該低級アルキレン基は、主鎖中に二重結合又は三重結合を1又は2有していてもよく、さらに、該低級アルキレンは、低級アルコキシ基、オキソ基又はヒドロキシ基で1乃至3置換されていてもよく、pは、1乃至3の整数を示す]
(工程1)
本工程は、化合物(1)と化合物(2)とを反応させることにより、化合物(3)を製造する方法である。
化合物(1)と化合物(2)との反応は、いわゆる光延反応(Mitsunobu reaction)であり、ホスフィン化合物及びアゾ化合物の存在下、文献記載の方法(例えば、ミツノブ(Mitsunobu.O)著、「ユース オブ ジエチル アゾジカルボキシレート アンド トリフェニルホスフィン イン シンセシス アンド トランスフォーメーション オブ ナチュラル プロダクツ(The use of diethyl azodicarboxylate and triphenylphosphine in synthesis and transformation of natural products)」、シンセシス(Synthesis)、第1巻、1981年、p1-28))、それに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
本工程は、塩基の存在下、前記工程1で得られた化合物(3)とヒドロキシアミンとを反応させることにより、本発明に係る化合物(I-A)を製造する方法である。
本工程は、酸化銅(II)の存在下、化合物(4)とプロピオ酸エチルとを反応させて、化合物(2)を製造する方法である。
また、本工程において用いられるプロピオ酸エチルの代わりに、プロピオ酸メチルを用いることもできる。
中のアルキレン基は、
(1)アミノ基(該アミノ基は、低級アルキル基、低級アルキルスルホニル基、低級アルカノイル基で置換されていてもよい)、
(2)ハロゲン原子、
(3)低級アルケニル基、
(4)低級アルキル基(該低級アルキレン基を構成する同一の炭素原子が、2つの低級アルキル基で置換されている場合には、これらの低級アルキル基が一緒になって、3乃至7員の脂肪族環(該脂肪族環を構成する炭素原子の1又は2が、窒素原子、硫黄原子又は酸素原子に置き換わっていてもよい)を形成していてもよい)、
(5)低級アルキニル基、
(6)低級アルキリデン基、
(7)イミノ基、
(8)アリールアルキル基、
(9)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する、5又は6員のヘテロアリールアルキル基、
(10)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有するヘテロアリール基
(11)アリールアルキルオキシ基、及び
(12)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する5又は6員のヘテロアリールアルキルオキシ基
からなる群より選択される基で、同一又は異なって1乃至3置換されており;
ここで、低級アルキル基、低級アルキニル基、低級アルキリデン基は、1乃至3のハロゲン原子、ヒドロキシ基又は低級アルコキシ基で置換されていてもよく、
該イミノ基は、1乃至3の低級アルキル基、低級アルキルスルホニル基、シアノ基、ニトロ基、低級アルカノイル基で置換されていてもよく、
該低級アルキレン基は、主鎖中に二重結合又は三重結合を1又は2有していてもよく、さらに、該低級アルキレンは、低級アルコキシ基、オキソ基又はヒドロキシ基で1乃至3置換されていてもよく、pは、1乃至3の整数を示し、他の記号は前記に同じ]
(工程4)
本工程は、塩基の存在下、化合物(1)とメタンスルホニルクロリド(MsCl)とを反応させることにより、化合物(5)を製造する方法である。
(工程5)
本工程は、塩基の存在下、化合物(5)と化合物(4)とを反応させることにより、化合物(6)を製造する方法である。
本工程は、酸化銅(II)の存在下、化合物(6)とプロピオ酸エチルとを反応させることにより、化合物(3)を製造する方法である。
(1)アミノ基(該アミノ基は、低級アルキル基、低級アルキルスルホニル基、低級アルカノイル基で置換されていてもよい)、
(2)ハロゲン原子、
(3)低級アルケニル基、
(4)低級アルキル基(該低級アルキレン基を構成する同一の炭素原子が、2つの低級アルキル基で置換されている場合には、これらの低級アルキル基が一緒になって、3乃至7員の脂肪族環(該脂肪族環を構成する炭素原子の1又は2が、窒素原子、硫黄原子又は酸素原子に置き換わっていてもよい)を形成していてもよい)、
(5)低級アルキニル基、
(6)低級アルキリデン基、
(7)イミノ基、
(8)アリールアルキル基、
(9)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する、5又は6員のヘテロアリールアルキル基、
(10)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有するヘテロアリール基
(11)アリールアルキルオキシ基、及び
(12)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する5又は6員のヘテロアリールアルキルオキシ基
からなる群より選択される基で、同一又は異なって1乃至3置換されており;
ここで、低級アルキル基、低級アルキニル基、低級アルキリデン基は、1乃至3のハロゲン原子、ヒドロキシ基又は低級アルコキシ基で置換されていてもよく、
該イミノ基は、1乃至3の低級アルキル基、低級アルキルスルホニル基、シアノ基、ニトロ基、低級アルカノイル基で置換されていてもよく、
該低級アルキレン基は、主鎖中に二重結合又は三重結合を1又は2有していてもよく、さらに、該低級アルキレンは、低級アルコキシ基、オキソ基又はヒドロキシ基で1乃至3置換されていてもよく、qは、1乃至3の整数を示し、他の記号は前記に同じ]
(工程7)
本工程は、化合物(7)と化合物(8)とを反応させることにより、化合物(9)を製造する方法である。本工程は、いわゆる光延反応(Mitsunobu reaction)であり、前記工程1と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより、行うことができる。
本工程は、塩基の存在下、前記工程1で得られた化合物(3)とヒドロキシアミンとを反応させることにより、本発明に係る化合物(I-B)を製造する方法である。
本工程における反応は、前記工程2と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
(1)アミノ基(該アミノ基は、低級アルキル基、低級アルキルスルホニル基、低級アルカノイル基で置換されていてもよい)、
(2)ハロゲン原子、
(3)低級アルケニル基、
(4)低級アルキル基(該低級アルキレン基を構成する同一の炭素原子が、2つの低級アルキル基で置換されている場合には、これらの低級アルキル基が一緒になって、3乃至7員の脂肪族環(該脂肪族環を構成する炭素原子の1又は2が、窒素原子、硫黄原子又は酸素原子に置き換わっていてもよい)を形成していてもよい)、
(5)低級アルキニル基、
(6)低級アルキリデン基、
(7)イミノ基、
(8)アリールアルキル基、
(9)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する、5又は6員のヘテロアリールアルキル基、
(10)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有するヘテロアリール基
(11)アリールアルキルオキシ基、及び
(12)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する5又は6員のヘテロアリールアルキルオキシ基
からなる群より選択される基で、同一又は異なって1乃至3置換されており、
ここで、低級アルキル基、低級アルキニル基、低級アルキリデン基は、1乃至3のハロゲン原子、ヒドロキシ基又は低級アルコキシ基で置換されていてもよく、
該イミノ基は、1乃至3の低級アルキル基、低級アルキルスルホニル基、シアノ基、ニトロ基、低級アルカノイル基で置換されていてもよく、
該低級アルキレン基は、主鎖中に二重結合又は三重結合を1又は2有していてもよく、さらに、該低級アルキレンは、低級アルコキシ基、オキソ基又はヒドロキシ基で1乃至3置換されていてもよく、GはNH、N-低級アルキル基、硫黄原子又は酸素原子を示す]で表される化合物は、例えば、以下の方法によって製造することができる。
本工程は、前記工程4と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
本工程は、前記工程5と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
本工程は、前記工程6と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
本工程は、前記工程2と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
(1)アミノ基(該アミノ基は、低級アルキル基、低級アルキルスルホニル基、低級アルカノイル基で置換されていてもよい)、
(2)ハロゲン原子、
(3)低級アルケニル基、
(4)低級アルキル基(該低級アルキレン基を構成する同一の炭素原子が、2つの低級アルキル基で置換されている場合には、これらの低級アルキル基が一緒になって、3乃至7員の脂肪族環(該脂肪族環を構成する炭素原子の1又は2が、窒素原子、硫黄原子又は酸素原子に置き換わっていてもよい)を形成していてもよい)、
(5)低級アルキニル基、
(6)低級アルキリデン基、
(7)イミノ基、
(8)アリールアルキル基、
(9)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する、5又は6員のヘテロアリールアルキル基、
(10)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有するヘテロアリール基
(11)アリールアルキルオキシ基、及び
(12)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する5又は6員のヘテロアリールアルキルオキシ基
からなる群より選択される基で、同一又は異なって1乃至3置換されており、
ここで、低級アルキル基、低級アルキニル基、低級アルキリデン基は、1乃至3のハロゲン原子、ヒドロキシ基又は低級アルコキシ基で置換されていてもよく、
該イミノ基は、1乃至3の低級アルキル基、低級アルキルスルホニル基、シアノ基、ニトロ基、低級アルカノイル基で置換されていてもよく、
該低級アルキレン基は、主鎖中に二重結合又は三重結合を1又は2有していてもよく、さらに、該低級アルキレンは、低級アルコキシ基、オキソ基又はヒドロキシ基で1乃至3置換されていてもよく、G1は、NH、N-低級アルキル基又は硫黄原子を示し、他の記号は前記に同じ]で表される化合物は、例えば、以下の方法によって製造することができる。
本工程は、前記工程5と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
本工程は、前記工程6と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
本工程は、前記工程2と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
(1)アミノ基(該アミノ基は、低級アルキル基、低級アルキルスルホニル基、低級アルカノイル基で置換されていてもよい)、
(2)ハロゲン原子、
(3)低級アルケニル基、
(4)低級アルキル基(該低級アルキレン基を構成する同一の炭素原子が、2つの低級アルキル基で置換されている場合には、これらの低級アルキル基が一緒になって、3乃至7員の脂肪族環(該脂肪族環を構成する炭素原子の1又は2が、窒素原子、硫黄原子又は酸素原子に置き換わっていてもよい)を形成していてもよい)、
(5)低級アルキニル基、
(6)低級アルキリデン基、
(7)イミノ基、
(8)アリールアルキル基、
(9)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する、5又は6員のヘテロアリールアルキル基、
(10)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有するヘテロアリール基
(11)アリールアルキルオキシ基、及び
(12)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する5又は6員のヘテロアリールアルキルオキシ基
からなる群より選択される基で、同一又は異なって1乃至3置換されており、
ここで、低級アルキル基、低級アルキニル基、低級アルキリデン基は、1乃至3のハロゲン原子、ヒドロキシ基又は低級アルコキシ基で置換されていてもよく、
該イミノ基は、1乃至3の低級アルキル基、低級アルキルスルホニル基、シアノ基、ニトロ基、低級アルカノイル基で置換されていてもよく、
該低級アルキレン基は、主鎖中に二重結合又は三重結合を1又は2有していてもよく、さらに、該低級アルキレンは、低級アルコキシ基、オキソ基又はヒドロキシ基で1乃至3置換されていてもよく、他の記号は前記に同じ]で表される化合物は、例えば、以下の方法によって製造することができる。
本工程は、前記工程4と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
本工程は、前記工程5と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
本工程は、前記工程6と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
本工程は、前記工程2と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
(1)アミノ基(該アミノ基は、低級アルキル基、低級アルキルスルホニル基、低級アルカノイル基で置換されていてもよい)、
(2)ハロゲン原子、
(3)低級アルケニル基、
(4)低級アルキル基(該低級アルキレン基を構成する同一の炭素原子が、2つの低級アルキル基で置換されている場合には、これらの低級アルキル基が一緒になって、3乃至7員の脂肪族環(該脂肪族環を構成する炭素原子の1又は2が、窒素原子、硫黄原子又は酸素原子に置き換わっていてもよい)を形成していてもよい)、
(5)低級アルキニル基、
(6)低級アルキリデン基、
(7)イミノ基、
(8)アリールアルキル基、
(9)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する、5又は6員のヘテロアリールアルキル基、
(10)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有するヘテロアリール基
(11)アリールアルキルオキシ基、及び
(12)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する5又は6員のヘテロアリールアルキルオキシ基
からなる群より選択される基で、同一又は異なって1乃至3置換されており、
ここで、低級アルキル基、低級アルキニル基、低級アルキリデン基は、1乃至3のハロゲン原子、ヒドロキシ基又は低級アルコキシ基で置換されていてもよく、
該イミノ基は、1乃至3の低級アルキル基、低級アルキルスルホニル基、シアノ基、ニトロ基、低級アルカノイル基で置換されていてもよく、
該低級アルキレン基は、主鎖中に二重結合又は三重結合を1又は2有していてもよく、さらに、該低級アルキレンは、低級アルコキシ基、オキソ基又はヒドロキシ基で1乃至3置換されていてもよく、他の記号は前記に同じ]で表される化合物は、例えば、以下の方法によって製造することができる。
本工程は、前記工程1と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
本工程は、前記工程2と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
(1)アミノ基(該アミノ基は、低級アルキル基、低級アルキルスルホニル基、低級アルカノイル基で置換されていてもよい)、
(2)ハロゲン原子、
(3)低級アルケニル基、
(4)低級アルキル基(該低級アルキレン基を構成する同一の炭素原子が、2つの低級アルキル基で置換されている場合には、これらの低級アルキル基が一緒になって、3乃至7員の脂肪族環(該脂肪族環を構成する炭素原子の1又は2が、窒素原子、硫黄原子又は酸素原子に置き換わっていてもよい)を形成していてもよい)、
(5)低級アルキニル基、
(6)低級アルキリデン基、
(7)イミノ基、
(8)アリールアルキル基、
(9)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する、5又は6員のヘテロアリールアルキル基、
(10)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有するヘテロアリール基
(11)アリールアルキルオキシ基、及び
(12)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する5又は6員のヘテロアリールアルキルオキシ基
からなる群より選択される基で、同一又は異なって1乃至3置換されており、
ここで、低級アルキル基、低級アルキニル基、低級アルキリデン基は、1乃至3のハロゲン原子、ヒドロキシ基又は低級アルコキシ基で置換されていてもよく、
該イミノ基は、1乃至3の低級アルキル基、低級アルキルスルホニル基、シアノ基、ニトロ基、低級アルカノイル基で置換されていてもよく、
該低級アルキレン基は、主鎖中に二重結合又は三重結合を1又は2有していてもよく、さらに、該低級アルキレンは、低級アルコキシ基、オキソ基又はヒドロキシ基で1乃至3置換されていてもよく、他の記号は前記に同じ]で表される化合物は、例えば、以下の方法によって製造することができる。
本工程は、前記工程1と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
本工程は、前記工程2と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより行うことができる。
本工程は、アミノ化合物とカルボン酸化合物又はスルホン酸化合物とを反応させることにより、アミド化合物又はスルホンアミド化合物を製造する方法である。本反応は、文献記載の方法(例えば、ペプチド合成の基礎と実験、泉屋信夫他、丸善、1983年、コンプリヘンシブ オーガニック シンセシス(Comprehensive Organic Synthesis)、第6巻、Pergamon Press社、1991年、等)、それに準じた方法又はこれらと常法とを組み合わせることにより、通常のアミド又はスルホンアミド形成反応を行えばよく、即ち、当業者に周知の縮合剤を用いて行うか、或いは、当業者に利用可能なエステル活性化方法、混合酸無水物法、酸クロリド法、カルボジイミド法等により行うことができる。このようなアミド形成試薬としては、例えば塩化チオニル、塩化オキザリル、N,N-ジシクロヘキシルカルボジイミド、1-メチル-2-ブロモピリジニウムアイオダイド、N,N’-カルボニルジイミダゾ-ル、ジフェニルフォスフォリルクロリド、ジフェニルフォスフォリルアジド、N,N’-ジスクシニミジルカルボネ-ト、N,N’-ジスクシニミジルオキザレ-ト、1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド塩酸塩、クロロギ酸エチル、クロロギ酸イソブチル又はベンゾトリアゾ-1-イル-オキシ-トリス(ジメチルアミノ)フォスフォニウムヘキサフルオロフォスフェイト等が挙げられ、中でも例えば塩化チオニル、1-エチル-3-(3-ジメチルアミノプロピル)カルボジイミド塩酸塩、N,N-ジシクロヘキシルカルボジイミド又はベンゾトリアゾール-1-イル-オキシ-トリス(ジメチルアミノ)フォスフォニウムヘキサフルオロフォスフェイト等が好適である。またアミド又はスルホンアミド形成反応においては、上記アミド又はスルホンアミド形成試薬と共に塩基、縮合補助剤を用いてもよい。
本工程は、イソオキサゾール基が有するヒドロキシ基の保護基を除去することにより、化合物(I-H)を製造する方法である。
-C)、(I-D)、(I-E)、(I-F)、(I-G)又は(I-H)を製造するに
あたり、X、又は
前記(I)及びそれに包含される(I-A)、(I-B)、(I-C)、(I-D)、(I-E)、(I-F)、(I-G)又は(I-H)で表される化合物を用いて、常法に従って製造することができる。
成形された錠剤は、パウダー状の湿った化合物と不活性な液体の希釈剤との混合物を適当な機械で成形することにより調製される。
好ましくは、各錠剤は、活性成分を約1mg乃至1g含み、各カシュー剤又はカプセル剤は、活性成分を約1mg乃至500mg含む。
式(I)の化合物についての医薬上の投与形態の例は、次の通りである。
(a)他のGPR120アゴニスト
(b)グルコキナーゼ活性化剤
(c)ビグアニド(例、ブホルミン、メトホルミン、フェンホルミン)
(d)PPARアゴニスト(例、トログリタゾン、ピオグリタゾン、ロシグリタゾン)
(e)インスリン
(f)ソマトスタチン
(g)α-グルコシダーゼ阻害剤(例、ボグリボース、ミグリトール、アカルボース)、
(h)インスリン分泌促進剤(例、アセトヘキサミド、カルブタミド、クロルプロパミド、グリボムリド、グリクラジド、グリメルピリド、グリピジド、グリキジン、グリソキセピド、グリブリド、グリへキサミド、グリピナミド、フェンブタミド、トラザミド、トルブタミド、トルシクラミド、ナテグリニド、レパグリニド)、及び
(i)DPP-IV(ジペプチジルペプチダーゼIV阻害剤)
2番目の活性成分に対する式(I)の化合物の重量比は、幅広い制限の範囲内で変動し、さらに、各活性成分の有効量に依存する。従って、例えば、式(I)の化合物をPPARアゴニストと組み合わせて用いる場合には、式(I)の化合物のPPARアゴニストに対する重量比は、一般的に、約1000:1乃至1:1000であり、好ましくは、約200:1乃至1:200である。式(I)の化合物と他の活性成分との組み合わせは、前述の範囲内であるが、いずれの場合にも、各活性成分の有効量が用いられるべきである。
本発明に係る化合物は、GPR120機能調節作用を有するが、ここで、「GPR120機能調節作用」とは、GPR120受容体の機能を活性化又は抑制することを意味し、例えば、GPR120アゴニストもGPR120機能調節作用を有するものに含まれる。
製剤例1
実施例1の化合物10部、重質酸化マグネシウム15部及び乳糖75部を均一に混合して、350μm以下の粉末状又は細粒状の散剤とする。この散剤をカプセル容器に入れてカプセル剤とする。
製剤例2
実施例1の化合物45部、澱粉15部、乳糖16部、結晶性セルロース21部、ポリビニルアルコール3部及び蒸留水30部を均一に混合した後、破砕造粒して乾燥し、次いで篩別して直径1410乃至177μmの大きさの顆粒剤とする。
製剤例3
製剤例2と同様の方法で顆粒剤を作製した後、この顆粒剤96部に対してステアリン酸カルシウム3部を加えて圧縮成形し直径10mmの錠剤を作製する。
製剤例4
製剤例2の方法で得られた顆粒剤90部に対して結晶性セルロース10部及びステアリン酸カルシウム3部を加えて圧縮成形し、直径8mmの錠剤とした後、これにシロップゼラチン、沈降性炭酸カルシウム混合懸濁液を加えて糖衣錠を作製する。
実施例のシリカゲルカラムクロマトグラフィーには、和光純薬社Wakogel(登録商標)C-300またはバイオタージ社製KP-Sil(登録商標)Silicaプレパックドカラムを用いた。分取用薄層クロマトグラフィーはメルク社製KieselgelTM60F254,Art.5744を用いた。塩基性シリカゲルカラムクロマトグラフィーは富士シリシア化学社製Chromatorex(登録商標)NH(100-250meshまたは200-350mesh)を用いた。
1H-NMRはVarian社製Gemini(200MHz、300MHz)、Mercury(400MHz)、Inova(400MHz)を使用し、テトラメチルシランを標準物質として用いて測定した。またマススペクトルはWaters社製micromassZQを使用しエレクトロスプレイイオン化法(ESI)又は大気圧化学イオン化法(APCI)で測定した。
i-Bu:イソブチル基
n-Bu:n-ブチル基
t-Bu:tert-ブチル基
Boc:tert-ブトキシカルボニル基
Me:メチル基
Et:エチル基
Ph:フェニル基
i-Pr:イソプロピル基
n-Pr:n-プロピル基
CDCl3:重クロロホルム
CD3OD:重メタノール
DMSO-d6:重ジメチルスルホキシド
下記に核磁気共鳴スペクトルにおける略号の意味を示す。
s :シングレット
d :ダブレット
dd:ダブルダブレット
dt:ダブルトリプレット
ddd:ダブルダブルダブレット
Sept:セプテット
t :トリプレット
m :マルチプレット
br:ブロード
brs:ブロードシングレット
q :カルテット
J :カップリング定数
Hz:ヘルツ
実施例1
5-(4-(2-(3-イソプロポキシフェニル)-1-メチルエトキシ)フェニル)イソオキサゾール3-オール
1)メチル(3-ヒドロキシフェニル)アセテートの製造
3-ヒドロキシフェニル酢酸2.0gのメタノール10ml溶液に、トシル酸・一水和物250mg及びトリメトキシメタン2.9mlを加え、反応液を5時間加熱還流した。反応液を冷却後、溶媒を減圧留去した。得られた残渣をジエチルエーテルにて希釈し、飽和炭酸水素ナトリウム水溶液にて洗浄、無水硫酸マグネシウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:酢酸エチル/ヘキサン=0/100~50/50)にて精製し、表記化合物を無色油状物質として得た。
2)メチル(3-イソプロポキシフェニル)アセテートの製造
メチル(3-ヒドロキシフェニル)アセテート200mgのテトラヒドロフラン5ml溶液に、イソプロピルアルコール0.15ml、トリフェニルホスフィン480mg及びジエチルアゾジカルボキシレート(45%トルエン溶液)0.82mlを加え、反応液を室温にて一終夜撹拌した。反応溶媒を減圧留去し、得られ残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:酢酸エチル/ヘキサン=0/100~25/75~60/40)にて精製し、表記化合物を無色油状物質として得た。
3)2-(3-イソプロポキシフェニル)エタノールの製造
メチル(3-イソプロポキシフェニル)アセテート280mgのテトラヒドロン5ml溶液に、氷冷下、水素化リチウムアルミニウ52mgを加え、反応液を同温にて25分間撹拌した。反応液に、硫酸ナトリウム10水和物を加え、室温にて2時間撹拌した。反応液を濾過した後、濾液を減圧留去した。得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:酢酸エチル/ヘキサン=0/100~50/50)にて精製し、表記化合物を無色油状物質として得た。
4)(3-イソプロポキシフェニル)アセトアルデヒドの製造
2-(3-イソプロポキシフェニル)エタノール200mgのクロロホルム7ml溶液に、Dess-Martin試薬700mgを加え、反応液を室温にて2時間撹拌した。反応液にさらにDess-Martin試薬280mgを加え、室温にて1時間撹拌した。反応液をセライトにて濾過し、濾液を飽和炭酸水素ナトリウム水溶液にて希釈、クロロホルムにて抽出し、無水硫酸マグネシウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:酢酸エチル/ヘキサン=0/100~30/70)にて精製し、表記化合物を黄色油状物質として得た。
5)1-(3-イソプロポオキシフェニル)-2-プロパノールの製造
(3-イソプロポキシフェニル)アセトアルデヒド116.6mgのテトラヒドロフラン1ml溶液に、氷冷下、メチルリチウム1.0mlを加え、反応液を同温にて1時間撹拌した。反応液を飽和塩化アンモニウム水溶液にて希釈、酢酸エチルにて抽出し、無水硫酸マグネシウムにて乾燥した。溶媒を減圧留去し、得られた残渣を分取用薄層クロマトグラフィー(KieselgelTM60F254、Art5744(メルク社製)、酢酸エチル/ヘキサン=30/70)にて精製し、表記化合物を無色油状物質として得た。
6)5-(4-(2-(3-イソプロポキシフェニル)-1-メチルエトキシ)フェニル)イソオキサゾール3-オールの製造
1-(3-イソプロポキシフェニル)-2-プロパノール87mgのテトラヒドロフラン2ml溶液に、氷冷下、参考例1で得られたエチル 3-(4-ヒドロキシフェニル)-2-プロピノエイト103mg、トリフェニルホスフィン142mg及びアゾジカルボン酸ジエチルエステル(2.2Mトルエン溶液)0.245mlを加え、反応液を室温にて1時間撹拌した。過剰量のメタノールを加えた後、溶媒を減圧留去し、得られた残渣をシリカゲルクロマトグラフィー(展開溶媒:ヘキサン/酢酸エチル=98/2~50/50)にて精製し、粗生成物を無色油状物として得た。得られた粗生成物のメタノール1mlの溶液に、塩酸ヒドロキシルアミン69mg及び5規定水酸化カリウム水溶液0.3mlを加え、反応液を室温にて一終夜撹拌した。反応液に10%クエン酸水溶液を加え、クロロホルムにて抽出した。有機層を無水硫酸ナトリウムにて乾燥した後、溶媒を減圧留去し、得られた残渣を逆相中圧液体クロマトグラフィー[ODS-AS-360-CC(YMC社製)移動相:水-アセトニトリル-0.1%トリフルオロ酢酸]にて精製した。溶媒を減圧留去し、得られた残渣をクロロホルムにて希釈、飽和食塩水にて洗浄し、有機層を無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、表記化合物を淡黄色油状物質として得た。
1HNMR(400MHz、CDCl3)δ:1.29-1.35(9H,m),2.80(1H,dd,J=13.7,6.7Hz),3.07(1H,dd,J=13.7,5.9Hz),4.47-4.58(1H,m),4.59-4.70(1H,m),6.07(1H,s),6.71-6.84(3H,m),6.94(2H,d,J=8.8Hz),7.19(1H,t,J=7.7Hz),7.63(2H,d,J=8.8Hz)
ESI-MS Found:m/z 354[M+H]+
実施例2
5-(4-(2-フルオロ-2-(3-メトキシフェニル)エトキシ)フェニル)イソオキサゾール3-オール
1)2-(4-ヨードフェノキシ)-1-(3-メトキシフェニル)エタノンの製造
2-ブロモ-1-(3-メトキシフェニル)エタノン1.0gのジメチルホルムアミド10ml溶液に、4-ヨードフェノール1.44g及び炭酸カリウム904mgを加え、反応液を80℃にて一終夜撹拌した。反応液を冷却後、1N塩酸を加え、酢酸エチルにて抽出した。有機層を合わせて、飽和食塩水にて洗浄し、無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:ヘキサン/酢酸エチル=98/2~50/50)にて精製し、表記化合物を黄色油状物質として得た。
2)1-(1-フルオロ-2-(4-ヨードフェノキシ)エチル)-3-メトキシベンゼンの製造
2-(4-ヨードフェノキシ)-1-(3-メトキシフェニル)エタノン448mgのメタノール5ml溶液に、氷冷下、水素化ホウ素ナトリウム92mgを加え、反応液を室温にて30分間撹拌した。反応液に10%クエン酸水溶液を加え、酢酸エチルにて抽出した。有機層を合わせて、飽和食塩水にて洗浄後、無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、粗生成物を無色油状物質として得た。粗生成物のクロロホルム3ml溶液に、氷冷下、デオキソ-フルオロ(ビス(2-メトキシエチル)アミノサルファートリフルオリド)0.45mlを加え、反応液を室温にて1時間撹拌した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:ヘキサン/酢酸エチル=98/2~50/50)にて精製し、表記化合物を無色油状物質として得た。
3)5-(4-(2-フルオロ-2-(3-メトキシフェニル)エトキシ)フェニル)イソオキサゾール3-オールの製造
1-(1-フルオロ-2-(4-ヨードフェノキシ)エチル)-3-メトキシベンゼン0.20gのジメチルアミドホルム2ml溶液に、プロピオール酸エチル0.15g及び酸化銅(II)0.08gを加え、反応液を110度にて15時間撹拌した。反応液を冷却後、セライト濾過し、濾液を減圧留去した。得られた残渣をエタノール1mlに溶解し、50%ヒドロキシアミン水溶液0.05ml及び2規定水酸化ナトリウム水溶液0.03mlを加え、反応液を室温にて一終夜撹拌した。反応液を10%クエン酸水溶液にて酸性にした後、クロロホルムにて抽出し、無水硫酸マグネシウムにて乾燥した。溶媒を減圧留去し、得られた残渣を分取用薄層クロマトグラフィー(KieselgelTM60F254、Art5744(メルク社製)、クロロホルム/メタノール=8/1)にて精製し、表記化合物を淡茶色固体として得た。
1H-NMR(400MHz,CDCl3)δ:3.84(3H,s),4.19-4.26(1H,m),4.31-4.40(1H,m),5.82(1H,dd,J=48.0,5.8Hz),6.10(1H,s),6.94(1H,d,J=8.4Hz),6.92-7.00(4H,m),7.35(1H,t,J=7.7Hz),7.67(2H,d,J=8.6Hz)
ESI-MS Found:m/z 330[M+H]+
実施例3
5-(4-(2、2-ジフルオロ-2-(3-メトキシフェニル)エトキシ)フェニル)イソオキサゾール3-オール
1)1-(1,1-ジフルオロ-2-(4-ヨードフェノキシ)エチル)-3-メトキシベンゼンの製造
2-(4-ヨードフェノキシ)-1-(3-メトキシフェニル)エタノン393mgのクロロホルム2ml溶液に、ビス(2-メトキシエチル)アミノサルファートリフルオリド0.394mlを加え、反応液を50℃にて24時間撹拌した。反応液にエタノール0.013mlを加え、さらに同温にて24時間撹拌した。反応液を冷却後、溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:ヘキサン/酢酸エチル=98/2~50/50)にて精製し、表記化合物を茶色油状物質として得た。
2)5-(4-(2,2-ジフルオロ-2-(3-メトキシフェニル)エトキシ)フェニル)イソオキサゾール3-オールの製造
1-(1,1-ジフルオロ-2-(4-ヨードフェノキシ)エチル)-3-メトキシベンゼンを用いて、実施例2と同様の方法、これに準じた方法又はこれらと常法とを組み合わせることにより、表記化合物を白色固体として得た。
1HNMR(400MHz,CDCl3)δ:3.86(3H,s),4.41(2H,t,J=11.9Hz),6.11(1H,s),6.97(2H,d,J=8.4Hz),7.02(1H,d,J=7.8Hz),7.12(1H,s),7.17(1H,d,J=7.8Hz),7.39(1H,t,J=7.8Hz),7.66(2H,d,J=8.4Hz)
ESI-MS Found:m/z 348[M+H]+
実施例4
5-(4-(2-(3-イソプロポキシフェニル)プロポキシ)フェニル)-イソオキサゾール3-オール
100mgの4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノールと88mgの2-(3-イソプロポキシフェニル)プロパン-1-オールをテトラヒドロフランに溶解し、237mgのトリフェニルホスフィン、183mgのジイソプロピル アゾジカルボキシレートを加え室温で撹拌した。反応液にメタノールを加え溶媒を留去して得られた残渣をシリカゲルクロマトグラフィーで精製した。生成物に1規定の塩酸/メタノールを加え室温で撹拌し、MOM基が脱保護されたことを確認して濃縮した。残渣をシリカゲルクロマトグラフィーで精製することにより、表記化合物を得た。
1H-NMR(400MHz,CDCl3)δ:7.64(2H,d,J=8.8Hz),7.26-7.22(1H,m),6.94(2H,d,J=8.8Hz),6.87-6.81(2H,m),6.78(1H,dd,J=8.2,2.2Hz),6.07(1H,s),4.56(1H,sept,J=6.1Hz),4.12(1H,dd,J=9.0,6.4Hz),3.99(1H,dd,J=9.0,7.0Hz),3.22(1H,qdd,J=6.4,6.4,7.0Hz),1.41(3H,d,J=6.4Hz),1.34(6H,d,J=6.1Hz).
ESI-MS Found:m/z 354[M+H]+
実施例5
5-(4-(2-メチル-2-(3-イソプロポキシフェニル)プロポキシ)フェニル)-イソオキサゾール3-オール
4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール及び2-メチル-2-(3-(プロパン-2-イルオキシ)フェニル)プロパン-1-オールを用いて、実施例4と同様の方法により、表記化合物を得た。
1H-NMR(400MHz,CDCl3)δ:7.63(2H,d,J=8.8Hz),7.27-7.22(1H,m),7.02-6.91(4H,m),6.76(1H,dd,J=8.4,2.0Hz),6.07(1H,s),4.55(1H,sept,J=6.2Hz),3.97(2H,s),1.46(6H,s),1.34(6H,d,J=6.2Hz)
ESI-MS Found:m/z 368[M+H]+
実施例6
5-{2-フルオロ-4-[2-(3-イソプロポキシフェニル)-1-メチルエトキシ]フェニル}イソオキサゾール3-オール
4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール及び1-フルオロ-[3-(プロパン-2-イルオキシ)フェニル]プロパン-2-オールを用いて、実施例4と同様の方法により、表記化合物を得た。
1H-NMR(400MHz,CDCl3)δ:7.75(1H,t,J=8.8Hz),7.23-7.17(1H,m),6.81-6.74(4H,m),6.67(1H,dd,J=12.7,2.4Hz),6.25(1H,d,J=3.4Hz),4.61(1H,sext,J=6.3Hz),4.53(1H,sept,J=6.3Hz),3.06(1H,dd,J=13.5,6.3Hz),2.81(1H,dd,J=13.5,6.3Hz),1.36(3H,d,J=6.3Hz),1.33(3H,d,J=6.3Hz),1.32(3H,d,J=6.3Hz).
ESI-MS Found:m/z 372[M+H]+
実施例7
5-(6-(2-(3-イソプロポキシフェニル)-1-メチルエトキシ)ピリジン-3-イル)イソオキサゾール3-オール
5-(3-(メトキシメトキシ)イソオキサゾール5-イル)ピリジン-2-オール及び1-(3-(プロパン-2-イルオキシ)フェニル)プロパン-2-オールを用いて、実施例4と同様の方法により、表記化合物を得た。
1H-NMR(400MHz,CDCl3)δ:8.53(1H,d,J=2.7Hz),7.86(1H,dd,J=8.8,2.7Hz),7.18(1H,t,J=7.8Hz),6.85-6.72(4H,m),6.13(1H,s),5.49(1H,sext,J=6.5Hz),4.53(1H,sept,J=6.2Hz),3.09(1H,dd,J=13.3,6.5Hz),2.81(1H,dd,J=13.3,6.5Hz),1.34(3H,d,J=6.2Hz),1.32(3H,d,J=6.2Hz),1.32(3H,d,J=6.2Hz).
ESI-MS Found:m/z 355[M+H]+
実施例8
5-(5-(2-(3-イソプロポキシフェニル)-1-メチルエトキシ)ピリジン-2-イル)イソオキサゾール3-オール
6-(3-(メトキシメトキシ)イソオキサゾール5-イル)ピリジン-3-オール及び1-(3-(プロパン-2-イルオキシ)フェニル)プロパン-2-オールを用いて、実施例4と同様の方法により、表記化合物を得た。
1H-NMR(400MHz,CDCl3)δ:8.33(1H,d,J=2.6Hz),7.72(1H,d,J=8.8Hz),7.26-7.17(2H,m),6.82-6.73(3H,m),6.43(1H,s),4.67(1H,sext,J=6.2Hz),4.53(1H,sept,J=6.1Hz),3.07(1H,dd,J=13.7,6.2Hz),2.84(1H,dd,J=13.7,6.2Hz),1.37(3H,d,J=6.1Hz),1.32(3H,d,J=6.1Hz),1.31(3H,d,J=6.1Hz).
ESI-MS Found:m/z 355[M+H]+
実施例9
5-(4-(((3-イソプロポキシベンジル)(メチル)アミノ)メチル)フェニル)イソオキサゾール3-オール
N-メチル-4-(3-(メトキシメトキシ)イソオキサゾール5-イル)ベンジルアミン0.10gに3-イソプロポキシベンジルクロリド0.075g、炭酸カリウム0.17gを加えジメチルホルムアミド中70℃で一晩撹拌した。反応液を冷却濃縮後、シリカゲルクロマトグラフィーで精製した。生成物をメタノールに溶解し、10%塩酸―メタノールを加えて室温で撹拌した。反応液を濃縮してクロロホルムに溶解し、炭酸水素ナトリウム水で洗浄後、乾燥、濃縮を行った。残渣をシリカゲルクロマトグラフィーで精製することで目的化合物を微黄色アモルファスとして得た。
1H-NMR(400MHz,CDCl3)δ:7.63(2H,d,J=8.8Hz),7.45-7.35(2H,m),7.26-7.18(1H,m),6.94-6.88(2H,m),6.80-6.75(1H,m),6.13(1H,s),4.55(1H,sept,J=6.1Hz),3.54-3.49(4H,brm),2.19(3H,s),1.33(6H,d,J=6.1Hz)
ESI-MS Found:m/z 353[M+H]+
実施例10
5-(4-(2-フェノキシプロピル)フェニル)イソオキサゾール3-オール
1)1-(4-ヨードフェニル)プロパン-2-オールの製造
ヨウ素3.35gの酢酸溶液25mlを100℃に加温した後、濃硫酸3ml及び1-フェニルプロパン-2-オール4.09gを順次加え、さらにヨウ素酸ナトリウム1.3g含む水溶液15mlを滴下し、同温にて30分間攪拌した。反応混合溶液を氷にあけ、ジエチルエーテル及び水で希釈後、抽出した有機層を飽和食塩水で洗浄、硫酸ナトリウムで乾燥、ろ過、濃縮した。得られた反応混合物をMeOH20mlに溶解し、5M水酸化ナトリウム水溶液5ml加え、室温にて1時間攪拌した後、酢酸エチル及び水で希釈し、有機層を抽出した。有機層を飽和食塩水で洗浄し、硫酸ナトリウムで乾燥、ろ過後、濃縮した。得られた粗生成物をシリカゲルカラムクロマトグラフィーにて精製することにより、上記表記化合物を黄色油状化合物として5.1g得た。
2)5-[4-(2-ヒドロキシプロピル)フェニル]イソオキサゾール3-オールの製造
参考例1及び2と同様にして、1-(4-ヨードフェニル)プロパン-2-オールを出発原料に用いることにより、上記表記化合物を無色固体として1.84g得た。
3)1-(4-(3-(メトキシメトキシ)イソオキサゾール5-イル)フェニル)プロパン-2-オールの製造
5-(4-(2-ヒドロキシプロピル)フェニル)イソオキサゾール3-オール1.53gのテトラヒドロフラン18ml溶液に、クロロメチルメチルエーテル0.54ml及び1,5-ジアザビシクロ(4,3,0)ノン-5-エン1.00mlを加え、反応液を0℃にて5分間撹拌した。反応液に飽和炭酸水素ナトリウム水溶液を加えたのち酢酸エチルにて抽出し、無水硫酸マグネシウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:酢酸エチル/ヘキサン=0/100~50/50)にて精製し、表記化合物を白色固体として333.2mg得た。
4)3-(メトキシメトキシ)-5-(4-(2-フェノキシプロピル)フェニル)イソオキサゾールの製造
1-(4-(3-(メトキシメトキシ)イソオキサゾール5-イル)フェニル)プロパン-2-オール50mgのトルエン1.0ml溶液に、ジイソプロピルアゾジカルボキシレート50μl、トリフェニルホスフィン75mg及びフェノール27μlを加え、反応液を室温にて12時間撹拌した。反応液をシリカゲルクロマトグラフィー(展開溶媒:酢酸エチル/ヘキサン=0/100~30/70)にて精製し、表記化合物を無色油状化合物として58.8mg得た。
5)5-(4-(2-フェノキシプロピル)フェニル)イソオキサゾール3-オールの製造
3-(メトキシメトキシ)-5-(4-(2-フェノキシプロピル)フェニル)イソオキサゾール58.8mgのメタノール0.5ml溶液に、4M塩酸-ジオキサン0.5mlを加え、反応液を室温にて24時間撹拌した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:酢酸エチル/ヘキサン=0/100~50/50)にて精製し、表記化合物を白色固体として35.6mg得た。
1HNMR(400MHz、CDCl3)δ:1.32(3H,d,J=5.6Hz),2.90(1H,dd,J=13.6,6.0Hz),3.10(1H,dd,J=13.6,6.0Hz),4.56-4.62(1H,m),6.16(1H,s),6.87-6.95(3H,m),7.24-7.28(2H,m),7.34(2H,d,J=8.0Hz),7.65(2H,d,J=8.4Hz)
ESI-MS Found:m/z 296[M+H]+
実施例11
5-(4-(2-(3-メチルフェノキシ)プロピル)フェニル)イソオキサゾール3-オール
1-(4-(3-(メトキシメトキシ)イソオキサゾール5-イル)フェニル)プロパン-2-オール50mg及びm-クレゾールを用いて、実施例10と同様の方法により、表記化合物を白色固体として38.6mg得た。
1HNMR(400MHz、CDCl3)δ:1.31(3H,d,J=6.0Hz),2.31(3H,s),2.89(1H,dd,J=13.6,5.6Hz),3.09(1H,dd,J=14.0,6.4Hz),4.56-4.61(1H,m),6.16(1H,s),6.68-6.75(3H,m),7.14(1H,t,J=7.2Hz),7.34(2H,d,J=8.0Hz),7.65(2H,d,J=8.4Hz)
ESI-MS Found:m/z 310[M+H]+
実施例12
5-(4-(2-(3-メトキシフェノキシ)プロピル)フェニル)イソオキサゾール3-オール
1-(4-(3-(メトキシメトキシ)イソオキサゾール5-イル)フェニル)プロパン-2-オール50mg及び3-メトキシフェノールを用いて、実施例10と同様の方法により、表記化合物を無色油状物質として39.4mg得た。
1HNMR(400MHz、CDCl3)δ:1.31(3H,d,J=6.0Hz),2.90(1H,dd,J=13.6,6.0Hz),3.09(1H,dd,J=13.6,6.0Hz),3.77(3H,s),4.56-4.61(1H,m),6.16(1H,s),6.44-6.51(3H,m),7.16(1H,t,J=8.0Hz),7.34(2H,d,J=8.0Hz),7.65(2H,d,J=8.4Hz)
ESI-MS Found:m/z 326[M+H]+
実施例13
5-(4-(2-(3-(トリフルオロメチル)フェノキシ)プロピル)フェニル)イソオキサゾール3-オール
1-(4-(3-(メトキシメトキシ)イソオキサゾール5-イル)フェニル)プロパン-2-オール30mg及び3-(トリフルオロメチル)フェノールを用いて、実施例10と同様の方法により、表記化合物を無色油状物質として27.3mg得た。
1HNMR(400MHz、CDCl3)δ:1.35(3H,d,J=6.0Hz),2.94(1H,dd,J=14.0,6.0Hz),3.10(1H,dd,J=13.6,6.4Hz),4.62-4.65(1H,m),6.18(1H,s),7.02(1H,d,J=8.4,2.0Hz),7.09(1H,brs),7.17(1H,d,J=7.6Hz),7.33-7.38(3H,m),7.67(2H,d,J=8.0Hz)
ESI-MS Found:m/z 364[M+H]+
実施例14
5-(4-(2-(4-メチルフェノキシ)プロピル)フェニル)イソオキサゾール3-オール
1-(4-(3-(メトキシメトキシ)イソオキサゾール5-イル)フェニル)プロパン-2-オール30mg及び4-メトキシフェノールを用いて、実施例10と同様の方法により、表記化合物を無色油状物質として24.1mg得た。
1HNMR(400MHz、CDCl3)δ:1.29(3H,d,J=6.0Hz),2.87(1H,dd,J=13.6,6.0Hz),3.08(1H,dd,J=14.0,6.8Hz),3.76(3H,s),4.43-4.48(1H,m),6.17(1H,s),6.81(4H,s),7.34(2H,d,J=8.0Hz),7.66(2H,d,J=8.4Hz)
ESI-MS Found:m/z 326[M+H]+
実施例15
5-(4-(2-(3、5-ジメトキシフェノキシ)プロピル)フェニル)イソオキサゾール3-オール
1-(4-(3-(メトキシメトキシ)イソオキサゾール5-イル)フェニル)プロパン-2-オール16mg及び3,5-ジメトキシフェノールを用いて、実施例10と同様の方法により、表記化合物を白色固体として8.9mg得た。
1HNMR(400MHz、CDCl3)δ:1.31(3H,d,J=5.6Hz),2.90(1H,dd,J=13.6,6.0Hz),3.09(1H,dd,J=13.6,6.0Hz),3.76(6H,s),4.54-4.58(1H,m),6.07(3H,s),6.17(1H,s),7.34(2H,d,J=8.0Hz),7.66(2H,d,J=8.0Hz)
ESI-MS Found:m/z 356[M+H]+
実施例16
5-(4-(2-(4-クロロフェノキシ)プロピル)フェニル)イソオキサゾール3-オール
1-(4-(3-(メトキシメトキシ)イソオキサゾール5-イル)フェニル)プロパン-2-オール16mg及び4-クロロフェノールを用いて、実施例10と同様の方法により、表記化合物を白色固体として13.4mg得た。
1HNMR(400MHz、CDCl3)δ:1.31(3H,d,J=6.4Hz),2.90(1H,dd,J=14.0,6.0Hz),3.08(1H,dd,J=14.0,6.8Hz),4.52-4.56(1H,m),6.17(1H,s),6.79(2H,d,J=8.4Hz),7.21(2H,d,J=8.8Hz),7.33(2H,d,J=8.0Hz),7.66(2H,d,J=7.6Hz)
ESI-MS Found:m/z 330[M+H]+
実施例17
5-(4-(2-(4-クロロ-2-フルオロフェノキシ)プロピル)フェニル)イソオキサゾール3-オール
1-(4-(3-(メトキシメトキシ)イソオキサゾール5-イル)フェニル)プロパン-2-オール16mg及び4-クロロ-2-フルオロフェノールを用いて、実施例10と同様の方法により、表記化合物を無色油状物質として12.3mg得た。
1HNMR(400MHz、CDCl3)δ:1.33(3H,d,J=6.4Hz),2.93(1H,dd,J=13.6,5.2Hz),3.12(1H,dd,J=14.0,6.8Hz),4.50-4.55(1H,m),6.18(1H,s),6.82(1H,t,J=8.4Hz),6.99(1H,brd,J=8.8Hz),7.08(1H,dd,J=10.4,2.0Hz),7.35(2H,d,J=8.0Hz),7.66(2H,d,J=7.6Hz)
ESI-MS Found:m/z 348[M+H]+
実施例18
5-(4-(2-(2、4-ジクロロフェノキシ)プロピル)フェニル)イソオキサゾール3-オール
1-(4-(3-(メトキシメトキシ)イソオキサゾール5-イル)フェニル)プロパン-2-オール16mg及び2,4-ジクロロフェノールを用いて、実施例10と同様の方法により、表記化合物を白色固体として10.9mg得た。
1HNMR(400MHz、CDCl3)δ:1.34(3H,d,J=6.0Hz),2.97(1H,dd,J=13.6,5.2Hz),3.13(1H,dd,J=13.6,6.4Hz),4.53-4.58(1H,m),6.18(1H,s),6.78(1H,d,J=8.8Hz),7.12(1H,dd,J=8.4,2.0Hz)7.35-7.39(3H,m),7.66(2H,d,J=7.6Hz)
ESI-MS Found:m/z 365[M+H]+
実施例19
5-(4-(2-(3((トリフルオロメチル)オキシ)フェニル)オキシ)プロピル)フェニル)イソオキサゾール3-オール
1-(4-(3-(メトキシメトキシ)イソオキサゾール5-イル)フェニル)プロパン-2-オール43mg及び3-((トリフルオロメチル)オキシ)フェノールを用いて、実施例10と同様の方法により、表記化合物を無色固体として28mg得た。
1H-NMR(CDCl3)δ:7.63(2H,d,J=8.0Hz),7.30(2H,d,J=8.0Hz),7.24-7.18(1H,m),6.78-6.73(2H,m),6.70-6.67(1H,brm),6.14(1H,s),4.59-4.51(1H,m),3.06(1H,dd,J=13.7,6.6Hz),2.88(1H,dd,J=13.7,5.7Hz),1.30(3H,d,J=5.9Hz)
ESI-MS Found:m/z 380[M+H]+
実施例20
5-{4-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール
1)(2S)-1-{3-[(1-メチルエチル)オキシ]}プロパン-2-オールの製造
1-ブロモ-3-[(1-メチル)オキシ]ベンゼン5.38gのTHF50ml溶液に2.66Mのn-ブチルリチウムヘキサン溶液10.34mlを-78℃にて加え、45分間攪拌後、(S)-(-)-プロピレンオキシド2.63ml加えた。-78℃にて30分間攪拌した後、室温まで昇温し、さらに30分間攪拌した。飽和塩化アンモニウム水溶液にてクエンチし、水にて希釈後、酢酸エチルを用いて抽出を行った。有機層を飽和食塩水にて洗浄後、硫酸ナトリウムにて乾燥、ろ過及び濃縮を行った。得られた粗生成物をシリカゲルクロマトグラフィーにて精製し、表記化合物を無色油状物として2.2g得た。
2)5-{4-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オールの製造
実施例4と同様の方法により、4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール553mg及び(2S)-1-{3-[(1-メチルエチル)オキシ]}プロパン-2-オールを用いて、上記表記化合物を無色アモルファスとして845mg得た。
1H-NMR(CDCl3)δ:7.60(2H,d,J=9.0Hz),7.16(1H,dd,J=7.8,7.8Hz),6.90(2H,d,J=9.0Hz),6.78-6.70(3H,m),6.03(1H,s),4.64-4.57(1H,m),4.52-4.46(1H,m),3.03(1H,dd,J=13.5,5.7Hz),2.76(1H,dd,J=13.5,6.6Hz),1.30-1.27(9H,m)
ESI-MS Found:m/z 354[M+H]+
実施例21
5-{4-[((1S)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール
(S)-(-)-プロピレンオキシドの代わりに(R)-(+)-プロピレンオキシドを用いて、実施例20と同様の方法により、上記表記化合物を無色アモルファスとして得た。
実施例22
5-[4-({(1R)-1-メチル-2-[3-(シクロプロピルオキシ)フェニル]-1-メチルエチル}オキシ)フェニル]イソオキサゾール3-オール
1)(2S)-1-[3-(シクロプロピルオキシ)フェニル]プロパン-2-オールの製造
実施例20と同様の方法により、1-ブロモ-3-(シクロプロピルオキシ)ベンゼン0.94gから上記表記化合物を無色油状物として0.37g得た。
2)5-[4-({(1R)-1-メチル-2-[3-(シクロプロピルオキシ)フェニル]-1-メチルエチル}オキシ)フェニル]イソオキサゾール3-オールの製造
実施例4と同様の方法により、4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール135mg及び(2S)-1-[3-(シクロプロピルオキシ)フェニル]プロパン-2-オールを用いて、上記表記化合物を無色固体として164mg得た。
1H-NMR(CDCl3)δ:7.60(2H,d,J=9.0Hz),7.18(1H,dd,J=7.8,7.8Hz),6.93-6.87(4H,m),6.81(1H,d,J=7.8Hz),6.03(1H,s),4.66-4.55(1H,m),3.69-3.64(1H,m),3.04(1H,dd,J=13.9,6.1Hz),2.79(1H,dd,J=13.9,6.1Hz),1.31(3H,d,J=5.9Hz),0.74-0.70(4H,m)
ESI-MS Found:m/z 352[M+H]+
実施例23
5-{4-[((1R)-1-メチル-2-{3-[(トリフルオロメチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール
1)(2S)-1-[3-[(トリフルオロメチル)オキシ]フェニル]プロパン-2-オールの製造
実施例20と同様の方法により、1-ブロモ-3-[(トリフルオロメチル)オキシ]ベンゼン5.0gから上記表記化合物を無色油状物として2.2g得た。
2)5-{4-[((1R)-1-メチル-2-{3-[(トリフルオロメチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オールの製造
実施例4と同様の方法により、4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール111mg及び(2S)-1-[3-[(トリフルオロメチル)オキシ]フェニル]プロパン-2-オールを用いて、上記表記化合物を無色個体として180mg得た。
1H-NMR(CDCl3)δ:7.60(2H,d,J=8.6Hz),7.28(1H,dd,J=7.8,7.8Hz),7.13(1H,d,J=7.8Hz),7.09-7.03(2H,m),6.88(2H,d,J=8.6Hz),6.03(1H,s),4.64-4.57(1H,m),3.04(1H,dd,J=13.7,6.6Hz),2.88(1H,dd,J=13.7,5.7Hz),1.31(3H,d,J=5.9Hz)
ESI-MS Found:m/z 380[M+H]+
実施例24
5-{4-[((1R)-1-メチル-2-{4-[(トリフルオロメチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール
1)(2S)-1-{4-[(1-メチルエチル)オキシ]}プロパン-2-オールの製造
実施例20と同様の方法により、1-ブロモ-4-[(トリフルオロメチル)オキシ]ベンゼン2.89gから上記表記化合物を無色油状物として1.3g得た。
2)5-{4-[((1R)-1-メチル-2-{4-[(トリフルオロメチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オールの製造
実施例4と同様の方法により、4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール111mg及び(2S)-1-[4-[(トリフルオロメチル)オキシ]フェニル]プロパン-2-オールを用いて、上記表記化合物を無色アモルファスとして175mg得た。
1H-NMR(CDCl3)δ:7.60(2H,d,J=8.6Hz),7.22(2H,d,J=8.6Hz),7.11(2H,d,J=8.6Hz),6.89(2H,d,J=8.6Hz),6.04(1H,s),4.65-4.55(1H,m),3.03(1H,dd,J=14.1,6.3Hz),2.86(1H,dd,J=14.1,5.9Hz),1.30(3H,d,J=6.3Hz)
ESI-MS Found:m/z 380[M+H]+
実施例25
5-{4-[((1R)-2-{4-クロロ-3-[(トリフルオロメチル)オキシ]フェニル}-1-メチルエチル)オキシ]フェニル}イソオキサゾール3-オール
1)(2S)-1-{4-クロロ-3-[(トリフルオロメチル)オキシ]}プロパン-2-オールの製造
実施例20と同様の方法により、4-ブロモ-1-クロロ-2-[(トリフルオロメチル)オキシ]ベンゼン3.18gから上記表記化合物を無色油状物として1.21g得た。
2)5-{4-[((1R)-2-{4-クロロ-3-[(トリフルオロメチル)オキシ]フェニル}-1-メチルエチル)オキシ]フェニル}イソオキサゾール3-オールの製造
実施例4と同様の方法により、4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール111mg及び(2S)-1-{4-クロロ-3-[(トリフルオロメチル)オキシ]}プロパン-2-オールを用いて、上記表記化合物を無色アモルファスとして204mg得た。
1H-NMR(CDCl3)δ:7.60(2H,d,J=9.0Hz),7.34(1H,d,J=8.2Hz),7.21-7.18(1H,brm),7.09(1H,dd,J=8.2,2.0Hz),6.87(2H,d,J=9.0Hz),6.04(1H,s),4.63-4.55(1H,m),2.98(1H,dd,J=14.1,7.0Hz),2.89(1H,dd,J=14.1,5.1Hz),1.31(3H,d,J=5.9Hz)
ESI-MS Found:m/z 414[M+H]+
実施例26
5-{6-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]ピリジン-3-イル}イソオキサゾール3-オール 塩酸塩
実施例4と同様の方法により、5-(3―(メトキシメトキシ)イソオキサゾール5-イル)ピリジン-2-オール111mg及び(2S)-1-{3-[(1-メチルエチル)オキシ]}プロパン-2-オールを用いて、上記表記化合物を無色個体の塩酸塩として165mg得た。
1H-NMR(DMSO-D6)δ:8.55(1H,d,J=2.3Hz),7.99(1H,dd,J=8.8,2.3Hz),7.10(1H,dd,J=8.0,8.0Hz),6.81(1H,d,J=8.8Hz),6.75-6.72(2H,m),6.69-6.65(1H,m),6.45(1H,s),5.41-5.34(1H,m),4.53-4.46(1H,m),2.92(1H,dd,J=13.5,6.6Hz),2.79(1H,dd,J=13.5,5.7Hz),1.22(3H,d,J=6.3Hz),1.17(6H,d,J=5.9Hz)
ESI-MS Found:m/z 355[M+H]+
実施例27
5-{6-[((1S)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]ピリジン-3-イル}イソオキサゾール3-オール 塩酸塩
実施例26と同様の方法により、(2S)-1-{3-[(1-メチルエチル)オキシ]}プロパン-2-オールの代わりに(2R)-1-{3-[(1-メチルエチル)オキシ]}プロパン-2-オールを用いて、上記表記化合物を無色固体として得た。
実施例28
5-{2-フルオロ-4-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール
実施例4と同様の方法により、3-フルオロ-4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール120mg及び(2S)-1-{3-[(1-メチルエチル)オキシ]}プロパン-2-オールを用いて、上記表記化合物を無色油状物として125mg得た。
1H-NMR(CDCl3)δ:7.73(1H,dd,J=8.6,8.6Hz),7.16(1H,dd,J=8.6,8.6Hz),6.77-6.70(4H,m),6.63(1H,dd,J=12.9,2.3Hz),6.23(1H,d,J=3.5Hz),5.33(2H,s),4.60-4.54(1H,m),4.52-4.45(1H,m),3.54(3H,s),3.01(1H,dd,J=13.7,5.9Hz),2.77(1H,dd,J=13.7,6.3Hz),1.31-1.27(9H,m)
ESI-MS Found:m/z 372[M+H]+
実施例29
5-{4-[(2-フルオロ-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール
1)1-{3-[(1-メチルエチル)オキシ]フェニル}-2-{[4-(3-{[(メチルオキシ)メチル]オキシ}イソオキサゾール5-イル)フェニル]オキシ}エタノンの製造
2-ブロモ-1-{3-[(1-メチルエチル)オキシ]フェニル}エタノン463mg、4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール332mg及び炭酸カリウム331mgのDMF8mlの反応液を室温下にて終夜攪拌した。飽和炭酸ナトリウム水溶液にてクエンチした後、酢酸エチル及び水で希釈した。抽出した有機層を水及び飽和食塩水で順次洗浄後、硫酸ナトリウムを用い乾燥、ろ過、濃縮した。得られた粗生成物をシリカゲルカラムクロマトグラフィーにて精製することにより、上記表記化合物を無色固体として500mg得た。
2)1-{3-[(1-メチルエチル)オキシ]フェニル}-2-{[4-(3-{[(メチルオキシ)メチル]オキシ}イソオキサゾール5-イル)フェニル]オキシ}エタノールの製造
1-{3-[(1-メチルエチル)オキシ]フェニル}-2-{[4-(3-{[(メチルオキシ)メチル]オキシ}イソオキサゾール5-イル)フェニル]オキシ}エタノン397mgのTHF4ml及びMeOH4mlの混合溶液に氷冷下にて水素化ホウ素ナトリウム57mgを加え、同温のまま30分間攪拌した。飽和塩化アンモニウム水溶液にてクエンチし、酢酸エチル及び水にて希釈後、抽出した有機層を飽和塩化ナトリウム水溶液で洗浄、硫酸ナトリウムを用いて乾燥、ろ過後、濃縮した。得られた粗生成物をシリカゲルカラムクロマトグラフィーにて精製することにより、上記表記化合物を無色固体として420mg得た。
3)5-{4-[(2-フルオロ-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}-3-{[(メチロキシ)メチル]オキシ}イソオキサゾールの製造
1-{3-[(1-メチルエチル)オキシ]フェニル}-2-{[4-(3-{[(メチルオキシ)メチル]オキシ}イソオキサゾール5-イル)フェニル]オキシ}エタノール40mgのジクロロメタン溶液2mlに氷冷下にてDEOXO-Fluor0.028mlを加え、同温にて30分間攪拌した後、直接シリカゲルクロマトグラフィーにて精製することにより、上記表記化合物を無色油状物として28mg得た。
4)5-{4-[(2-フルオロ-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オールの製造
実施例4と同様の方法により、5-{4-[(2-フルオロ-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}-3-{[(メチロキシ)メチル]オキシ}イソオキサゾール28mgから、上記表記化合物を無色固体として22mg得た。
1H-NMR(CDCl3)δ:7.63(2H,d,J=8.6Hz),7.29(1H,dd,J=8.0,8.0Hz),6.98-6.91(4H,m),6.87(1H,dd,J=8.0,2.2Hz),6.06(1H,s),5.76(1H,ddd,J=49.0,7.8,2.7Hz),4.58-4.52(1H,m),4.36-4.26(1H,m),4.17(1H,ddd,J=28.9,10.9,2.7Hz),1.32(6H,d,J=5.9Hz)
ESI-MS Found:m/z 358[M+H]+
実施例30
5-{4-[(2,2-ジフルオロ-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール
1)2-ブロモ-1-{3-[(1-メチルエチル)オキシ]フェニル}プロパン-1-オンの製造
1-{3-[(1-メチルエチル)オキシ]フェニル}プロパン-1-オン653mg及び二臭化銅1.51gの酢酸エチル10mlの反応液を過熱還流下にて8時間攪拌を行った後、セライトろ過し、濃縮後、シリカゲルクロマトグラフィーにて精製することにより、上記表記化合物を無色油状物として728mg得た。
2)1-{3-[(1-メチルエチル)オキシ]フェニル}-2-{[4-(3-{[(メチルオキシ)メチル]オキシ}イソオキサゾール5-イル)フェニル]オキシ}プロパンー1-オンの製造
実施例29と同様にして4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール332mg及び2-ブロモ-1-{3-[(1-メチルエチル)オキシ]フェニル}プロパン-1-オン488mgから上記表記化合物を無色油状物として600mg得た。
3)5-{4-[(2,2-ジフルオロ-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}-3-{[(メチロキシ)メチル]オキシ}イソオキサゾールの製造
1-{3-[(1-メチルエチル)オキシ]フェニル}-2-{[4-(3-{[(メチルオキシ)メチル]オキシ}イソオキサゾール5-イル)フェニル]オキシ}プロパンー1-オン120mgのジクロロメタン4ml溶液にDEOXO-Fluor0.80mlを加え、室温下にて3日間攪拌した。反応溶液を飽和炭酸水素ナトリウム水溶液にてクエンチし、クロロホルム及び水にて希釈した。抽出して得られた有機層を硫酸ナトリウムにより乾燥、ろ過及び濃縮後、シリカゲルクロマトグラフィーにて精製することにより、上記表記化合物を無色油状物として51mg得た。
4)5-{4-[(2,2-ジフルオロ-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オールの製造
実施例4と同様の方法により、5-{4-[(2,2-ジフルオロ-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}-3-{[(メチロキシ)メチル]オキシ}イソオキサゾール28mgから上記表記化合物を無色油状物として22mg得た。
1H-NMR(CDCl3)δ:7.59(2H,d,J=8.6Hz),7.28(1H,dd,J=8.0,8.0Hz),7.05(1H,d,J=8.0Hz),7.03-7.01(1H,brm),6.93-6.88(3H,m),6.04(1H,s),4.78-4.67(1H,brm),4.55-4.49(1H,m),1.38(3H,d,J=6.3Hz),1.29(6H,dd,J=6.3,1.6Hz)
ESI-MS Found:m/z 390[M+H]
実施例31
5-{4-[(2-フルオロ-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール
実施例30と同様にして、1-{3-[(1-メチルエチル)オキシ]フェニル}-2-{[4-(3-{[(メチルオキシ)メチル]オキシ}イソオキサゾール5-イル)フェニル]オキシ}プロパン-1-オンから還元、フッ素化、脱保護を経て、表記化合物を2種のジアステレオマーの混合物として得た。
1H-NMR(CDCl3)δ:7.64-7.59,2.0H,m),7.27-7.231.0H,m),7.01-6.79(5.0H,m),6.05-6.04(1.0H,m),5.53(0.6H,dd,J=48.0,4.0Hz),5.40(0.4H,dd,J=46.5,6.5Hz),4.75-4.60(1.0H,m),4.57-4.49(1.0H,m),1.36-1.28(7.8H,m),1.16(1.2H,d,J=6.6Hz)
ESI-MS Found:m/z 372[M+H]+
実施例32
5-{2-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]ピリミジン-5-イル}イソオキサゾール3-オール
1)5-ヨード-2-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]ピリミジンの製造
5-ヨードピリミジン-2-オール111mg、(2S)-1-{3-[(1-メチルエチル)オキシ]}プロパン-2-オール194mg及びトリフェニルホスフィン262mgのTHF5ml溶液にジイソプロピルアゾジカルボキシレート0.19ml加えた後、室温下にて30分間攪拌した。反応溶液を濃縮後、シリカゲルクロマトグラフィーにて精製することにより、上記表記化合物を無色油状物として166mg得た。
2)エチル-3-{2-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]ピリミジン-5-イル}プロピノ-2-エートの製造
参考例1と同様の方法により、5-ヨード-2-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]ピリミジン224mgを出発原料として用いて、上記表記化合物を無色油状物として113mg得た。
3)5-{2-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]ピリミジン-5-イル}イソオキサゾール3-オールの製造
エチル-3-{2-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]ピリミジン-5-イル}プロピノ-2-エート118mgのEtOH4mlとTHF1mlの反応溶液にヒドロキシルアミンの塩酸塩89mgと5M水酸化ナトリウム水溶液0.38mlの混合水溶液を氷冷下にて加え、室温下で終夜攪拌した。5M塩酸水溶液0.38mlでクエンチした後、クロロホルム及びメタノールの混合溶媒にて抽出し、硫酸ナトリウムにて乾燥、ろ過後、濃縮した。得られた粗生成物をシリカゲルクロマトグラフィーにて精製し、上記表記化合物を無色油状物として100mg得た。
1H-NMR(CDCl3) δ:8.79(2H,s),7.14(1H,dd,J=7.8,7.8Hz),6.83-6.77(2H,m),6.70(1H,dd,J=7.8,2.2Hz),6.19(1H,s),5.48-5.39(1H,m),4.53-4.47(1H,m),3.13(1H,dd,J=13.5,6.3Hz),2.80(1H,dd,J=13.5,6.8Hz),1.36(3H,d,J=6.3Hz),1.28(6H,d,J=5.9Hz)
ESI-MS Found:m/z 356[M+H]+
実施例33
5-(4-(2-(3-イソプロポキシフェニル)プロポキシ)フェニル)-イソオキサゾール3-オール
実施例4と同様の方法を用いることにより、表記化合物を得た。
1H-NMR(400MHz,CDCl3):δ7.62(2H,d,J=8.8Hz),7.22(1H,t,J=7.6Hz),6.91(2H,d,J=8.8Hz),6.75-6.82(3H,m),6.06(1H,s),4.51-4.58(1H,m),4.05-4.14(2H,m),2.89-2.96(1H,m),1.94-2.04(1H,m),1.62-1.73(1H,m),1.33(6H,d,J=6Hz),0.89(3H,t,J=7.0Hz).MS(M+H+):368.
実施例34
5-(4-(2-(3-イソプロポキシフェニル)-1-エチルエトキシ)フェニル)イソオキサゾール3-オール
実施例4と同様の方法を用いることにより、表記化合物を得た。
1H-NMR(400MHz,CDCl3):δ7.60(2H,d,J=8.6Hz),7.17(1H,t,J=7.8Hz),6.91(2H,d,J=8.6Hz),6.72-6.79(3H,m),6.06(1H,s),4.51-4.53(2H,m),2.96-3.0(1H,m),2.82-2.87(1H,m,1H),1.64-1.76(2H,m),1.30(6H,t,J=5.5Hz),0.98(3H,t,J=7.0Hz).
MS(M+H+):368.
実施例35
5-(4-(2-(3-エチルフェニル)-1-メチルエトキシ)フェニル)イソオキサゾール3-オール
実施例4と同様の方法を用いることにより、表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ7.70(1H,d,J=8.4Hz,),7.13(1H,t,J=7.6Hz),7.01(1H,d,J=2.4Hz),6.93(1H,dd,J=2.4Hz,J=8.4Hz),6.76-6.73(2H,m),6.69-6.73(1H,m),6.38(1H,s),4.75-4.78(1H,m),3.96(2H,q,J=7.2Hz),2.93-2.99(1H,m),2.80-2.86(1H,m),1.32(3H,t,J=7.2Hz),1.29(3H,d,J=6.4Hz).
ESI-MS Found:m/z 374(M+H+).
実施例36
5-(4-(2、2-ジフルオロ-2-(3-イソプロポキシフェニル)エトキシ)フェニル)イソオキサゾール3-オール
1-{3-[(1-メチルエチル)オキシ]フェニル}プロパン-1-オンの代わりに1-{3-[(1-メチルエチル)オキシ]フェニル}エタン-1-オンを用いて、実施例30と同様の方法により、表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ7.66(2H,d,J=8.0Hz),7.36(1H,t,J=8.0Hz),7.13(2H,d,J=8.0Hz),7.00-7.03(3H,m),6.17(1H,s),4.60-4.62(1H,m),4.51(2H,t,J=12.4Hz),1.30(6H,d,J=6.0Hz).
ESI-MS Found:m/z 376(M+H+).
実施例37
5-{2-フルオロ-4-[2-(3-エトキシフェニル)-1-メチルエトキシ]フェニル}イソオキサゾール3-オール
2-フルオロ-4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール及び1-(3-エトキシフェニル)プロパン-2-オールを用いて、実施例4と同様の方法により、表記化合物を得た。
1H-NMR(400MHz,CDCl3):δ7.74(1H,t,J=8.6Hz),7.20(1H,t,J=8.6Hz),6.66-6.81(5H,m),6.24(1H,d,J=3.1Hz),4.57-4.65(1H,m),3.98-4.04(2H,q,J=7.0Hz),3.03-3.08(1H,m),2.79-2.84(1H,m),1.40(3H,t,J=7.0Hz),1.32(3H,d,J=6.3Hz).
ESI-MS Found:m/z 358[M+H]+
実施例38
5-{2-フルオロ-4-[2-(3-イソプロポキシフェニル)-2-メチルプロポキシ]フェニル}イソオキサゾール3-オール
2-フルオロ-4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール及び2-メチル-2-[3-(プロパン-2-イルオキシ)フェニル]プロパン-1-オールを用いて、実施例4と同様の方法により、表記化合物を得た。
1H-NMR(400MHz,CDCl3):δ7.74(1H,t,J=8.6Hz),7.24(1H,t,J=8.6Hz),6.95-6.98(2H,m),6.75-6.77(2H,m),6.66(1H,d,J=12.5Hz),6.24(1H,d,J=3.1Hz),4.50-4.61(1H,m),3.95(2H,s),1.44(6H,s),1.33(6H,d,J=6.3Hz)
ESI-MS Found:m/z 386[M+H]+
実施例39
5-{2-フルオロ-4-[2-(3-イソプロポキシフェニル)プロポキシ]フェニル}イソオキサゾール3-オール
2-フルオロ-4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール及び2-[3-(プロパン-2-イルオキシ)フェニル]プロパン-1-オールを用いて、実施例4と同様の方法により、表記化合物を得た
1H-NMR (400MHz,CDCl3):δ7.75(1H,t,J=8.6Hz),7.23(1H,t,J=7.8Hz),6.66-6.85(5H,m),6.25(1H,d,J=3.9Hz),4.51-4.60(1H,m),4.08-4.13(1H,m),3.95-4.0(1H,m),3.16-3.25(1H,m),1.39(3H,d,J=6.3Hz),1.33(6H,d,J=6.3Hz).
ESI-MS Found:m/z 372[M+H]+
実施例40
5-(6-(2-(3-イソプロポキシフェニル)プロポキシ)ピリジン-3-イル)イソオキサゾール3-オール
5-(3-(メトキシメトキシ)イソオキサゾール5-イル)ピリジン-2-オール及び2-[3-(プロパン-2-イルオキシ)フェニル]プロパン-1-オールを用いて、実施例4と同様の方法により、表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ8.51(s,1H),7.97(d,J=8.4Hz,1H),7.17(t,J=8.4Hz,1H),6.80-6.84(m,3H),6.71-6.76(m,1H),6.26(s,1H),4.52-4.58(m,1H),4.39-4.47(m,1H),4.34-4.37(m,1H),3.24-3.34(m,1H),1.37(d,J=6.8Hz,3H),1.28(d,J=6.0Hz,6H).
ESI-MS Found:m/z 355[M+H]+
実施例41
5-(4-{[[1-(3-イソプロポキシフェニル)エチル](メチル)アミノ]メチル}フェニル)イソオキサゾール3-オール
N-メチル-4-(3-(メトキシメトキシ)イソオキサゾール-5-イル)ベンジルアミン0.10g及び1-(1-クロロエチル)-3-(プロパン-2-イルオキシ)ベンゼンを用いて、実施例9と同様の方法により、表記化合物を得た。
1H-NMR(400MHz,MeOH):δ7.85(2H,d,J=8.6Hz),7.50-7.60(2H,br),7.42(1H,t,J=7.8Hz),7.00-7.10(3H,m),6.40(1H,s),4.40-4.70(1H,m),4.0-4.10(1H,br),2.60-2.80(3H,br),1.80-1.90(3H,br),1.30(6H,d,J=6.3Hz).
ESI-MS Found:m/z 367[M+H]+
実施例42
2-[4-(3-ヒドロキシイソオキサゾール5-イル)フェノキシ]-1-(3-イソプロポキシフェニル)エタノン
実施例29―1)で得られた1-{3-[(1-メチルエチル)オキシ]フェニル}-2-{[4-(3-{[(メチルオキシ)メチル]オキシ}イソオキサゾール5-イル)フェニル]オキシ}エタノンを実施例4の方法に従い脱保護することにより、表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ7.68(2H,d,J=8.0Hz),7.61(1H,d,J=8.0Hz),7.51(1H,s),7.43(1H,t,J=8.0Hz),7.29(1H,d,J=8.0Hz),7.06(2H,d,J=8.0Hz),6.75-6.85(1H,br),5.50(2H,s),4.65-4.69(1H,m),1.29(6H,d,J=6.0Hz).
ESI-MS Found:m/z 354[M+H]+
実施例43
2-[2-(3-エトキシフェニル)-1-メチルエトキシ]-5-(3-ヒドロキシイソオキサゾール-5-イル)ピリジニウム トリフルオロアセテート
5-(3―(メトキシメトキシ)イソオキサゾール5-イル)ピリジン-2-オール及び1-(3-エトキシフェニル)プロパン-2-オールを用いて、実施例4と同様の方法により、反応混合物を得、それを逆相クロマトグラフィー(0.1%TFA含有アセトニトリルー水系)で精製することによって表記化合物を得た。
1H-NMR (400 MHz, CD3OD): δ8.51(1H,s),7.97(1H,d,J=8.4Hz,),7.13(1H,t,J=8.4Hz),6.79-6.82(3H,m),6.69-6.72(1H,m),6.26(1H,s),5.42-5.47(1H,m),3.96(2H,q,J=6.8Hz),3.01-3.06(1H,m),2.80-2.85(1H,m),1.29-1.36(6H,m).
ESI-MS Found:m/z 341[M+H]+
実施例44
5-(3-ヒドロキシイソオキサゾール-5-イル)-2-[2-(3-イソプロポキシフェニル)-2-メチルプロポキシ]ピリジニウム トリフルオロアセテート
5-(3―(メトキシメトキシ)イソオキサゾール5-イル)ピリジン-2-オール及び2-メチル-2-[3-(プロパン-2-イルオキシ)フェニル]プロパン-1-オールを用いて、実施例4と同様の方法により、表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ8.51(1H,s),7.97(1H,d,J=8.4Hz),7.18(1H,t,J=8.4Hz),6.94-6.99(2H,m),6.82(1H,d,J=8.4Hz),6.81(1H,d,J=8.4Hz),6.26(1H,s),4.52-4.58(1H,m),4.38(2H,s),1.42(6H,s),1.27(6H,d,J=6.0Hz).
ESI-MS Found:m/z 369[M+H]+
実施例45
3-{2-[4-(3-ヒドロキシイソオキサゾール-5-イル)フェノキシ]プロピル}-N,N-ジメチルアニリン 塩酸塩
4-(3―(メトキシメトキシ)イソオキサゾール5-イル)フェノール及び1-[3-(ジメチルアミノ)フェニルプロパン-2-オールを用いて、実施例4と同様の方法により、表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ7.59-7.63(3H,m),7.48-7.51(3H,m),6.95(2H,d,J=8.0Hz),6.13(1H,s),4.77-4.97(1H,m),3.23-3.33(6H,m),3.07(2H,d,J=8.0Hz),1.35(3H,d,J=8.0Hz).
ESI-MS Found:m/z 339[M+H]+
実施例46
2-[4-(3-ヒドロキシイソオキサゾール-5-イル)フェノキシ]-1-(3-イソプロポキシフェニル)プロパン-1-オン
実施例30の合成中間体1-{3-[(1-メチルエチル)オキシ]フェニル}-2-{[4-(3-{[(メチルオキシ)メチル]オキシ}イソオキサゾール-5-イル)フェニル]オキシ}プロパンー1-オンを実施例4の方法で脱保護し、表記化合物を得た。
1H-NMR (400MHz,CDCl3):δ7.48-7.55(3H,m),7.47(1H,s),7.30(1H,t,J=8.0Hz),7.03-7.06(1H,m),6.82-6.85(2H,m),5.97(1H,s),5.49-5.51(1H,q,J=8.0Hz),4.49-4.55(1H,m),1.66(3H,d,J=8.0Hz),1.27(6H,d,J=8.0Hz).
ESI-MS Found:m/z 368[M+H]+
実施例47
5-(4-{[1-(3-イソプロポキシフェニル)エトキシ]メチル}フェニル)イソオキサゾール-3-オール
3-イソプロポキシアセトフェノン(100mg)とFeCl3(3.5mg)2mlのニトロメタンに溶解し、124mgの4-(3-(メトキシメトキシ)-5-イソオキサゾリル)フェノールと61mgのトリエチルシランを氷冷下加え、攪拌した。反応液にホスフェートバッファーを加え、クロロホルムで抽出し、有機層は飽和食塩水で洗滌、無水硫酸ナトリウム上で乾燥し、濃縮した。残渣をプレパラティブTLCで精製し、5-(4-{[1-(3-イソプロポキシフェニル)エトキシ]メチル}フェニル)-3-(メトキシメトキシ)イソオキサゾールを得た。これを実施例4の方法に従い脱保護し、目的化合物を得た。
1H-NMR(400MHz,CD3OD):δ7.72(2H,d,J=8.0Hz),7.40(2H,d,J=8.0Hz),7.23(1H,t,J=8.0Hz),6.88(2H,d,J=8.0Hz),6.79(1H,t,J=8.0Hz),6.28(1H,s),4.58-4.62(1H,m),4.46-4.57(1H,m),4.39(2H,m),1.43(3H,d,J=6.4Hz),1.29(6H,d,J=6.0Hz).
ESI-MS Found:m/z 354[M+H]+
実施例48
N-{2-[4-(3-ヒドロキシイソオキサゾール-5-イル)フェニル]エチル}-3-イソプロポキシ-N-メチルアニリン トリフルオロ酢酸塩
100mgの2-[4-(3-ヒドロキシイソオキサゾール-5-イル)フェニル]エチル メタンスルホネート、56mgのN-メチル-3-イソプロポキシアニリン、5mgのヨウ化カリウム、4mlのアセトニトリルの混合物をマイクロウェーブリアクター中で110℃に20分加熱した。反応混合物を濃縮し、逆相HPLC(0.1%TFA含有アセトニトリル-水系)で精製し、表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ7.68(2H,d,J=7.8Hz),7.31(2H,d,J=7.8Hz),7.21(1H,t,J=7.8Hz),6.46-6.60(3H,m),6.26(1H,s),4.51-4.59(1H,m),3.68(2H,t,J=7.0Hz),2.99(3H,s),2.88(2H,t,J=7.0Hz),1.28(6H,d,J=6.3Hz).
ESI-MS Found:m/z 353[M+H]+
実施例49
1-[4-(3-ヒドロキシイソオキサゾール-5-イル)フェニル]-N-(3-イソプロポキシベンジル)-N-メチルエタナミン トリフルオロ酢酸塩
N-メチル-4-(3-(メトキシメトキシ)イソオキサゾール-5-イル)ベンジルアミンの代わりにN、α-ジメチル-4-(3-(メトキシメトキシ)イソオキサゾール-5-イル)ベンジルアミンを用いて、実施例9と同様の方法を用い、さらに逆相HPLC(0.1%TFA含有アセトニトリル-水系)で精製して表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ7.95(2H,d,J=8.6Hz),7.60-7.70(2H,br),7.40(1H,t,J=8.6Hz),7.05(1H,d,J=7.8Hz),6.95(2H,t,J=7.8Hz),6.42(1H,s),4.50-4.70(2H,m),4.45(2H,s),2.60-2.80(3H,m),1.80-1.90(3H,br),1.30(6H,d,J=6.3Hz).
ESI-MS Found:m/z 367[M+H]+
実施例50
5-[4-({[1-(3-イソプロポキシフェニル)エチル]チオ}メチル)フェニル]イソオキサゾール-3-オール
N-メチル-4-(3-(メトキシメトキシ)イソオキサゾール-5-イル)ベンジルアミンの代わりに4-(3-(メトキシメトキシ)イソオキサゾール-5-イル)ベンジルチオール、3-イソプロポキシベンジル クロリドの代わりに3-イソプロポキシ-α―メチルベンジル クロリドを用い、実施例9と同様の方法により、表記化合物を得た。
1H-NMR:(400MHz,CD3OD):δ7.65(2H,d,J=8.6Hz),7.30(2H,d,J=8.6Hz),7.20(1H,t,J=8.0Hz),6.70-6.90(3H,m),6.25(1H,s),4.50-4.60(1H,m),3.80(1H,q,J=7.0Hz),3.50-3.60(2H,m),1.50(3H,d,J=7.0Hz),1.30(6H,d,J=6.3Hz).
ESI-MS Found:m/z 370[M+H]+
実施例51
N-[4-(3-ヒドロキシイソオキサゾール-5-イル)ベンジル]-3-イソプロポキシ-N-メチルベンゼンスルホンアミド
100mgのN-メチル-4-(3-(メトキシメトキシ)イソオキサゾール-5-イル)ベンジルアミンのジクロロメタン(6ml)溶液に100mgの3-イソプロポキシベンゼンスルホンアミドと81mgのトリエチルアミンを加え、混合物を室温で一夜攪拌した。反応混合物は濃縮し、残渣をプレパラティブTLCで精製し3-イソプロポキシ-N-{4-[3-(メトキシメトキシ)イソオキサゾール-5-イル]ベンジル}-N-メチルベンゼンスルホンアミドを得た。生成物に1規定の塩酸/メタノールを加え室温で撹拌し、MOM基が脱保護されたことを確認して濃縮した。残渣をシリカゲルクロマトグラフィーで精製することにより、表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ7.71(2H,d,J=8.0Hz),7.49(1H,t,J=8.0Hz),7.34-7.42(3H,m),7.25(1H,d,J=4.4Hz),7.16-7.19(1H,m),6.30(1H,s),4.62-4.68(1H,m),4.18(2H,s),2.60(3H,s),1.30(6H,d,J=6.0Hz).
ESI-MS Found:m/z 381[M+H]+
実施例52
5-{4-[2-(3-イソプロポキシフェノキシ)プロピル]フェニル}イソオキサゾール-3-オール
フェノールの代わりに3-イソプロポキシフェノールを用いて、実施例10と同様の方法で、表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ7.63-7.66(2H,m),7.35(2H,d,J=8.4Hz),7.08(1H,t,J=8.0Hz),6.41-6.45(2H,m),6.33(1H,t,J=2.4Hz),6.24(1H,s),4.56-4.64(1H,m),4.44-4.50(1H,m),2.99-3.03(1H,m),2.87-2.92(1H,m),1.23-1.27(9H,m).
ESI-MS Found:m/z 354[M+H]+
実施例53
5-{4-[2-(3-イソブチルフェニル)-1-メチルエトキシ]フェニル}イソオキサゾール-3-オール
実施例4と同様の方法により、表記化合物を得た。
1H-NMR(400MHz,CDCl3):δ7.77(1H,bs),7.66(2H,d,J=8.8Hz),7.23(1H,t,J=7.6Hz),7.01-7.10(3H,m),6.96(2H,d,J=8.8Hz),6.11(1H,s),4.62-4.73(1H,m),3.07-3.15(1H,m),2.81-2.90(1H,m),2.47(2H,d,J=6.8Hz),1.79-1.95(1H,m),1.36(3H,d,J=6.0Hz),0.91(6H,d,J=7.2Hz).
ESI-MS Found:m/z 352[M+H]+
実施例54
5-{3-フルオロ-4-[2-(3-イソプロポキシフェニル)-1-メチルエトキシ]フェニル}イソオキサゾール-3-オール
実施例4と同様の方法を用いることにより、表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ7.34(1H,t,J=8.4Hz),7.17-7.21(1H,m),6.65-6.79(5H,m),6.25(1H,s),4.49-4.63(2H,m),3.02-3.07(1H,m),2.78-2.83(1H,m),1.25-1.42(9H,m).
ESI-MS Found:m/z 372[M+H]+
実施例55
5-(4-{2-[(3-イソプロポキシフェニル)チオ]プロピル}フェニル)イソオキサゾール-3-オール
実施例9と同様の方法でN-メチル-4-(3-(メトキシメトキシ)イソオキサゾール-5-イル)ベンジルアミンと3-イソプロポキシベンジルクロリドの代わりに3‐イソプロポキシチオフェノールと1-(4-(3-(メトキシメトキシ)イソオキサゾール-5-イル)フェニル)プロプ-2-イル メタンスルホネートを用い、表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ7.65(2H,d,J=7.6Hz),7.29(2H,d,J=7.6Hz),7.16(1H,t,J=7.6Hz),6.93(1H,d,J=7.6Hz),6.84-6.86(1H,m),6.73-6.76(1H,m),6.24(1H,s),4.54-4.56(1H,m),3.46-3.54(1H,m),2.93-2.99(1H,m),2.73-2.78(1H,m),1.27(6H,q,J=6.4Hz),1.24(3H,d,J=7.2Hz).
ESI-MS Found:m/z 370[M+H]+
実施例56
5-{4-[2-(3-エトキシフェニル)-1-メチルエトキシ]-3-フルオロフェニル}イソオキサゾール-3-オール
実施例4と同様の方法を用いることにより、表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ7.41-7.47(2H,m),7.06-7.15(2H,m),6.79-6.82(2H,m),6.71(1H,d,J=7.2Hz),6.19(1H,s),4.68-4.59(1H,m),3.97(2H,q,J=6.8Hz),2.97-3.02(1H,m),2.83-2.87(1H,m),1.29-1.35(6H,m).
ESI-MS Found:m/z 358[M+H]+
実施例57
5-{4-[2,2-ジフルオロ-2-(3-イソプロポキシフェニル)エトキシ]-2-フルオロフェニル}イソオキサゾール-3-オール
BAST(320mg)を5-{4-[2-オキソ-2-(3-イソプロポキシフェニル)エトキシ]-2-フルオロフェニル}-3-メトキシメトキシイソオキサゾール(200mg)のジクロロメタン(2mL)溶液に0℃で加え、混合物を一晩還流加熱した。反応混合物を放冷し、飽和食塩水を加え、ジクロロメタンで抽出した。有機層を濃縮し、残渣をプレパラティブTLC(石油エーテル:酢酸エチル=5:1)で精製して5-{4-[2,2-ジフルオロ-2-(3-イソプロポキシフェニル)エトキシ]-2-フルオロフェニル}-3-メトキシメトキシイソオキサゾールを得た。これを実施例4と同様の方法により脱保護して表記化合物を得た。
1H-NMR(400MHz,CD3OD):δ7.72(1H,t,J=8.0Hz),7.34(1H,t,J=8.0Hz),7.10(1H,d,J=8.0Hz),7.06(1H,s),6.99(1H,d,J=8.0Hz),6.83-6.87(2H,m),6.16(1H,s),4.56-4.63(1H,m),4.51(2H,t,J=12.4Hz),1.27(6H,d,J=6.4Hz).
ESI-MS Found:m/z 394[M+H]+
実施例58
5-(4-{2-[(3-イソプロポキシフェニル)(メチル)アミノ]プロピル}フェニル)イソオキサゾール-3-オール
1)N-[2-(4-ヨードフェニル)-1-メチルエチル]-3-イソプロポキシ-N-メチルアニリンの製造
N-[2-(4-ヨードフェニル)-1-メチルエチル]-3-イソプロポキシアニリン(770mg)のDMF(10ml)溶液に水素化ナトリウム(230mg)を加えた。混合物を30分室温で攪拌した後、ヨウ化メチル(830mg)をそこへ加え、50℃で一晩攪拌した。反応混合物を冷却後、水を加え、酢酸エチルで抽出した。有機層を濃縮し、750mgのN-[2-(4-ヨードフェニル)-1-メチルエチル]-3-イソプロポキシ-N-メチルアニリンを得た。
2)エチル 3-(4-{2-[(3-イソプロポキシフェニル)(メチル)アミノ]プロピル}フェニル)プロプ-2-イノエートの製造
N-[2-(4-ヨードフェニル)-1-メチルエチル]-3-イソプロポキシ-N-メチルアニリン(750mg)、HCCCO2Et(477mg)、Cu2O(278mg)、DMF(20ml)の混合物を100℃で終夜攪拌した。反応混合物をセライトで濾過し、濾液を濃縮し、プレパラティブTLC(石油エーテル/酢酸エチル=10:1)で精製して160mgの目的化合物を得た。
3)5-(4-{2-[(3-イソプロポキシフェニル)(メチル)アミノ]プロピル}フェニル)イソオキサゾール-3-オールの製造
ヒドロキシルアミン塩酸塩(0.11g)を10%NaOH水溶液(2mL)に0℃で加え、さらにMeOH(10mL)、5-(4-{2-[(3-イソプロポキシフェニル)(メチル)アミノ]プロピル}フェニル)イソオキサゾール-3-オール(150mg)を加え、混合物を室温で終夜攪拌した。反応液に10%塩酸を加えpHを2に調整し、飽和食塩水を加えて、ジクロロメタンで抽出した。有機層を濃縮し残渣をプレパラティブTLC(石油エーテル/酢酸エチル=5:1)で精製して、表記化合物を得た。
1H―NMR(400MHz,CDCl3):δ7.58(2H,d,J=8.4Hz),7.23(2H,d,J=8.4Hz),7.05(1H,t),6.30-6.28(1H,m),6.21-6.19(2H,m),6.09(1H,s),4.46-4.41(1H,m),4.11-4.06(1H,m),2.92-2.87(1H,m),2.70-2.66(1H,m),2.70(3H,s),1.29(6H,d,J=6Hz),1.11(3H,d,J=6.8Hz).
ESI-MS Found:m/z 367[M+H]+
実施例59
4-(3-ヒドロキシイソオキサゾール-5-イル)-N-[2-(3-イソプロポキシフェニル)-1-メチルエチル]アニリン トリフルオロ酢酸塩
N-[2-(3-イソプロポキシフェニル)-1-メチルエチル]-4-[3-(メトキシメトキシ)イソオキサゾール-5-イル]アニリンを実施例4と同様の方法で脱保護し、逆相HPLC(0.1%TFA含有アセトニトリル-水系)で精製し、表記化合物を得た。
1H―NMR(400MHz,CD3OD):δ7.59(2H,d,J=8.8Hz),7.14(1H,t,J=7.6Hz),6.87(2H,d,J=8.8Hz),6.68-6.76(3H,m),6.07(1H,s),4.46-4.55(1H,m),3.76-3.84(1H,m),2.88-2.93(1H,m),2.64-2.69(1H,m),1.23(6H,d,J=6.4Hz),1.15(3H,d,J=6.4Hz).
ESI-MS Found:m/z 353[M+H]+
実施例60
4-(3-ヒドロキシイソオキサゾール-5-イル)-N-[2-(3-イソプロポキシフェニル)エチル]-N-メチルアニリン トリフルオロ酢酸塩
N-[2-(3-イソプロポキシフェニル)エチル]-4-[3-(メトキシメトキシ)イソオキサゾール-5-イル]-N-メチルアニリンを実施例4と同様の方法で脱保護し逆相HPLC(0.1%TFA含有アセトニトリル-水系)で精製して表記化合物を得た。
1H―NMR(400MHz,CD3OD):δ7.53(2H,d,J=8.8Hz),7.13(1H,t,J=7.6Hz),6.68-6.76(5H,m),5.98(1H,s),4.45-4.54(1H,m),3.62(2H,t,J=7.2Hz),2.88(3H,s),2.81(2H,t,J=7.2Hz),1.23(6H,d,J=6.4Hz).
ESI-MS Found:m/z 353[M+H]+
実施例61
5-{4-[2-(3-イソプロポキシフェニル)-1-メチルエトキシ]-3-メトキシフェニル}イソオキサゾール-3-オール
実施例4と同様の方法により、表記化合物を得た。
1H―NMR(400MHz,CDCl3):δ7.09-7.28(3H,m),6.66-6.84(4H,m),6.02(1H,s),4.44-4.55(2H,m),3.84(3H,s),2.85-3.10(2H,m),1.20-1.34(9H,m).
ESI-MS Found:m/z 384[M+H]+
実施例62
5-(4-((1-メチル-2-(2-((1-メチルエチル)オキシ)ピリジン-4-イル)エチル)オキシ)フェニル)イソオキサゾール-3-オールの塩酸塩
参考例9で得られた2-((1-メチルエチル)オキシ)-4-(2-((4-(3-(((メチルオキシ)メチル)オキシ)イソオキサゾール-5-イル)フェニル)オキシ)プロピル)ピリジン16mgを10%塩酸-メタノール1mLに溶解し、室温にて2時間撹拌した。反応液を減圧留去し表記化合物の塩酸塩を淡黄色油状物質として得た。
1H-NMR(400MHz,DMSO-d6)δ:8.03(1H,d,J=5.4Hz),7.68(2H,d,J=9.0Hz),7.04(2H,d,J=9.0Hz),6.89(1H,d,J=5.4Hz),6.70(1H,s),6.37(1H,s),5.23-5.13(1H,m),4.91-4.83(1H,m),2.95(1H,dd,J=13.8,6.0Hz),2.86(1H,dd,J=13.8,6.0Hz),1.25(6H,d,J=6.0Hz),1.24(3H,d,J=6.0Hz).
ESI-MS Found:m/z 355[M+H]+
実施例63
5-(4-(((1S)-1-メチル-2-(2-((1-メチルエチル)オキシ)ピリジン-4-イル)エチル)オキシ)フェニル)イソオキサゾール-3-オールのナトリウム塩
参考例10で得られた2-((1-メチルエチル)オキシ)-4-((2S)-2-((4-(3-(((メチルオキシ)メチル)オキシ)イソオキサゾール-5-イル)フェニル)オキシ)プロピル)ピリジン84mgを10%塩酸-メタノール5mLに溶解し、室温にて2時間撹拌した。反応液を減圧留去し、シリカゲルカラムクロマトグラフィー(展開溶媒:メタノール/クロロホルム=1/99~10/90)にて精製して得られた無色油状物質を水2mLに溶解して、1N NaOH水(0.40mL)を加えた。この溶液をODSカラム(Waters社製SepPak、C18、1g、展開溶媒:メタノール/水=0/100~50/50)を用いて精製し、表記化合物のナトリウム塩を無色固体として得た。
1H-NMR(400MHz,DMSO-D6)δ:8.01(1H,dJ=5.4Hz),7.44(2H,d,J=8.8Hz),6.93(2H,d,J=8.8Hz),6.86(1H,d,J=5.4Hz),6.64(1H,s),5.54(1H,s),5.22-5.16(1H,m),4.82-4.74(1H,m),2.92(1H,dd,J=14.0,6.0Hz),2.82(1H,dd,J=14.0,6.0Hz),1.25(6H,d,J=6.0Hz),1.21(3H,d,J=6.0Hz).
ESI-MS Found:m/z 355[M+H]+
実施例64
5-(4-(((1R)-1-メチル-2-(2-((1-メチルエチル)オキシ)ピリジン-4-イル)エチル)オキシ)フェニル)イソオキサゾール-3-オールのナトリウム塩
参考例10で得られた2-((1-メチルエチル)オキシ)-4-((2R)-2-((4-(3-(((メチルオキシ)メチル)オキシ)イソオキサゾール-5-イル)フェニル)オキシ)プロピル)ピリジン80mgを出発原料に用いて、実施例2と同様の操作により表記化合物のナトリウム塩を無色固体として得た。
1H-NMR(400MHz,DMSO-D6)δ:8.01(1H,dJ=5.4Hz),7.44(2H,d,J=8.8Hz),6.93(2H,d,J=8.8Hz),6.86(1H,d,J=5.4Hz),6.64(1H,s),5.54(1H,s),5.22-5.16(1H,m),4.82-4.74(1H,m),2.92(1H,dd,J=14.0,6.0Hz),2.82(1H,dd,J=14.0,6.0Hz),1.25(6H,d,J=6.0Hz),1.21(3H,d,J=6.0Hz).
ESI-MS Found:m/z 355[M+H]+
実施例65
N-[4-(3-ヒドロキシイソオキサゾール-5-イル)ベンジル]-3-イソプロポキシ-N-メチルアニリン
N-メチル-4-[3-(メトキシメトキシ)イソオキサゾール-5-イル]ベンジルアミン(100mg)のジクロロメタン(6mL)溶液に3-イソプロポキシベンゾイル クロリド(95mg)とトリエチルアミン(81mg)を加え、混合物を終夜攪拌した。反応液を濃縮し、プレパラティブTLCで精製して、3-イソプロポキシ-N-{4-[3-(メトキシメトキシ)イソオキサゾール-5-イル]ベンジル}-N-メチルベンズアミドを得た。このものを実施例4の方法に従い脱保護し、表記化合物を得た。
1H-NMR(400MHz,DMSO-d6):δ7.75(2H,d,J=7.8Hz),7.20-7.50(3H,m),6.80-7.0(3H,m),6.50(1H,s),4.40-4.70(3H,m),2.80-2.90(3H,m),1.10-1.30(6H,m).
ESI-MS Found:m/z 367[M+H]+
参考例1
エチル 3-(4-ヒドロキシフェニル)-2-プロピノエイト
4-ヨードフェノール22.3gのジメチルホルムアミド200ml溶液に、プロピオール酸エチル19.5ml及び酸化銅(I)14.8gを加え、反応液を110度にて15時間撹拌した。反応液を冷却後、セライトにて濾過し、濾液を減圧濃縮した。得られた残渣をシリカゲルカラムクロマトフラフィー(展開溶媒:ヘキサン/酢酸エチル=4/1)にて精製した後、ヘキサン/酢酸エチルで再結晶を行い、表記化合物を無色固体として得た。
1H-NMR(400MHz、CDCl3)δ:1.36(3H,t,J=7.2Hz),4.30(2H,q,J=7.2Hz),5.86-6.25(1H,brm),6.84(2H,d,J=8.5Hz),7.46(2H,d,J=8.5Hz)
ESI-MS Found:m/z 191[M+H]+
参考例2
4-(3-(メトキシメトキシ)-5-イソキサゾリル)フェノール
1)エチル3-(4-(ベンジルオキシ)フェニル)-2-プロピノエイトの製造
参考例1にて得られたエチル3-(4-ヒドロキシフェニル)-2-プロピノエイト1.02gのアセトン25ml溶液に、炭酸カリウム3.69g及びベンジルブロミド0.64mlを加え、反応液を65℃にて4時間撹拌した。反応液を冷却後、水を加えたのちクロロホルムにて抽出し、無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:酢酸エチル/ヘキサン=10/90~50/50)にて精製し、表記化合物を白色固体として得た。
2)5-(4-(ベンジルオキシ)フェニル)イソオキサゾール3-オールの製造
エチル3-(4-(ベンジルオキシ)フェニル)-2-プロピノエイト1.46gのメタノール30ml溶液に、ヒドロキシアミン塩酸塩1.45g及び5M水酸化カリウムメタノール溶液6.25mlを加え、反応液を室温にて一終夜撹拌した。溶媒を減圧留去し、得られた残渣を水に懸濁し、2N塩酸水溶液を用いてpHを2-3に調整した。生じた固体を濾取することにより表記化合物を淡褐色固体として得た。
3)5-(4-(ベンジルオキシ)フェニル)-3-(メトキシメトキシ)イソオキサゾールの製造
5-(4-(ベンジルオキシ)フェニル)イソオキサゾール3-オール1.38gのテトラヒドロフラン30ml溶液に、トリエチルアミン2.15ml及びメトキシメチルクロリド0.51mlを加え、反応液を室温にて一終夜撹拌した。反応液に飽和塩化アンモニウム水溶液を加え、酢酸エチルにて抽出した。有機層を合わせて、飽和食塩水にて洗浄し、無水硫酸ナトリウムにて乾燥した。溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:酢酸エチル/ヘキサン=10/90~0/100)にて精製し、表記化合物を淡褐色固体として得た。
4)4-(3-(メトキシメトキシ)イソオキサゾール5-イル)フェノールの製造
5-(4-(ベンジルオキシ)フェニル)-3-(メトキシメトキシ)イソオキサゾール1.44gのメタノール15ml及びテトラヒドロフラン15mlの混合溶液に、10%パラジウム-炭素触媒を200mg加え、水素雰囲気下、反応液を一終夜撹拌した。反応液をセライトにて濾過し、溶媒を減圧留去し、得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:酢酸エチル/ヘキサン=10/90~50/50)にて精製し、表記化合物を淡黄色固体として得た。
1H-NMR(400MHz、CDCl3)δ:3.58(3H,s),5.35(2H,s),6.11(1H,s),6.40(1H,brs),6.92-6.96(2H,m),7.61-7.64(2H,m)
ESI-MS Found:m/z 222[M+H]+
参考例3
1-(4-ヨードフェニル)プロパン-2-オール
ヨウ素3.35gの酢酸溶液25mlを100℃に加温した後、濃硫酸3ml及び1-フェニルプロパン-2-オール4.09gを順次加え、さらにヨウ素酸ナトリウム1.3g含む水溶液15mlを滴下し、同温にて30分間攪拌した。反応混合溶液を氷にあけ、ジエチルエーテル及び水で希釈後、抽出した有機層を飽和食塩水で洗浄、硫酸ナトリウムで乾燥、ろ過、濃縮した。得られた反応混合物をMeOH20mlに溶解し、5M水酸化ナトリウム水溶液5ml加え、室温にて1地時間攪拌した後、酢酸エチル及び水で希釈し、有機層を抽出した。有機層を飽和食塩水で洗浄し、硫酸ナトリウムで乾燥、ろ過後、濃縮した。得られた粗生成物をシリカゲルカラムクロマトグラフィーにて精製することにより、上記表記化合物を黄色油状化合物として5.1g得た。
参考例4
5-[4-(2-ヒドロキシプロピル)フェニル]イソオキサゾール3-オール
参考例1及び2と同様の方法によって、1-(4-ヨードフェニル)プロパン-2-オールを出発原料に用いることにより、上記表記化合物を無色固体として1.84g得た。
参考例5
3-イソプロポキシフェナシルブロミド
臭素(0.27g,1.7mmol)のCHCl3(1mL)溶液を3-イソプロポキシアセトフェノン(0.3g,1.7mmol)のCHCl3(5mL)溶液に室温で加え、混合物を室温で終夜攪拌した。反応液を濃縮し、クロロホルムで薄め、水で洗浄した。有機層は濃縮し、残渣を薄層シリカゲルクロマトグラフィーで精製して100mgの目的化合物を得た。
参考例6
N-[2-(3-イソプロポキシフェニル)-1-メチルエチル]-4-[3-(メトキシメトキシ)イソオキサゾール-5-イル]アニリン
4-[3-(メトキシメトキシ)イソオキサゾール-5-イル]アニリン(50mg),1-(3-イソプロポキシフェニル)アセトン(50mg)のCl(CH2)2Cl(4mL)溶液にTi(i-PrO)4(450mg)を加え1時間後にNaBH3CN(160mg)を加え、終夜攪拌した。反応液を水でクエンチし、濾過した後、濾液を酢酸エチルで抽出した。有機層は飽和食塩水で洗滌、硫酸ナトリウム上乾燥、濃縮し、プレパラティブTLCで精製して、表記化合物を得た。
参考例7
4-メチル-2-((1-メチルエチル)オキシ)ピリジン
4-メチルピリジン-2(1H)-オン3.14gのクロロホルム30ml溶液に、2-ヨードプロパン4.03ml及び炭酸銀11.1gを加え、反応液を室温にて終夜撹拌した。反応液をセライトにて濾過し、濾液を減圧濃縮して、表記化合物を淡黄色油状物質として得た。
参考例8
1-(2-((1-メチルエチル)オキシ)ピリジン-4-イル)プロパン-2-オール
参考例1にて得られた4-メチル-2-((1-メチルエチル)オキシ)ピリジン1.51gのテトラヒドロフラン20ml溶液に、アルゴン雰囲気下、-78度にてn-ブチルリチウム2.66Mヘキサン溶液4.14mlを加えた後、30分以上かけて0度に昇温しさらに20分間0度で攪拌した。再び-78度に冷却し、アセトアルデヒド0.68mlを加え、反応液を30分以上かけて0度に昇温した。塩化アンモニウム水溶液を加え、酢酸エチルにて抽出し、飽和食塩水で洗浄後無水硫酸マグネシウムにて乾燥、ろ過後そのろ液を減圧留去した。得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:酢酸エチル/ヘキサン=10/90~50/50)にて精製し、表記化合物を無色油状物質として得た。
参考例9
2-((1-メチルエチル)オキシ)-4-(2-((4-(3-(((メチルオキシ)メチル)オキシ)イソオキサゾール-5-イル)フェニル)オキシ)プロピル)ピリジン
参考例2で得られた1-(2-((1-メチルエチル)オキシ)ピリジン-4-イル)プロパン-2-オール244mg、4-(3-(メトキシメトキシ)-5-イソキサゾリル)フェノール111mgおよびトリフェニルホスフィン393mgのテトラヒドロフラン5ml溶液に、アゾジカルボン酸ジエチルエステル2.2Mトルエン溶液0.68mlを加え、室温にて30分間撹拌した。反応液を減圧留去し得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒:酢酸エチル/ヘキサン=10/90~50/50)にて精製し、表記化合物を無色油状物質として得た。
参考例10
2-((1-メチルエチル)オキシ)-4-((2S)-2-((4-(3-(((メチルオキシ)メチル)オキシ)イソオキサゾール-5-イル)フェニル)オキシ)プロピル)ピリジンおよび2-((1-メチルエチル)オキシ)-4-((2R)-2-((4-(3-(((メチルオキシ)メチル)オキシ)イソオキサゾール-5-イル)フェニル)オキシ)プロピル)ピリジン
参考例3で得られた2-((1-メチルエチル)オキシ)-4-(2-((4-(3-(((メチルオキシ)メチル)オキシ)イソオキサゾール-5-イル)フェニル)オキシ)プロピル)ピリジン194mgをHPLC(ダイセル社製キラルパックAD-H、展開溶媒:ヘキサン/エタノール=70/30、0.1%ジエチルアミン)を用いて光学分割を行い、表記化合物を無色油状物質として得た。
試験1:遺伝子のクローニング
GenBank Accesion No. NM_181745(ヒト)、No. NM_181748(マウス)における既知のGPCR、GPR120のORFの塩基配列前後の領域でプライマーを合成し、RT-PCRにより遺伝子のクローニングを行った。使用したプライマーの塩基配列は下記の通りである。サブクローニング用にそれぞれ制限酵素BamHI、EcoRI認識部位を導入している。
hGPR120_F01: aggatccgccgccatgtcccctgaatgcgcgcgggcag (配列番号:1)
hGPR120_R01: cgaattcttagccagaaataatcgacaagtcatttc (配列番号:2)
mGPR120_F01: aggatccgccgccatgtcccctgagtgtgcacagacgac (配列番号:3)
mGPR120_R01: cgaattcttagctggaaataacagacaagtcatttc (配列番号:4)
ヒトGPR120受容体遺伝子は、Human small intestine Marathon-ready cDNA(CLONTECH社:現TaKaRa社)、マウスGPR120受容体遺伝子は、マウスBAT組織由来RNAを逆転写したcDMAをPCRの試料として用いた。
PCRは、KOD_Plus(TOYOBO社)を用い、94℃2分の後、94℃15秒、55℃30秒、68℃1分を30サイクル行い、反応後にExTaq(TaKaRa社)0.5Unitsを加えさらに72℃10分間インキュベートし、末端にAの付加反応を行った。マウスのPCRには、終濃度2% DMSOの条件で35サイクル行った。
増幅されたPCR産物は、pCR2.1-TOPO TA cloning kit(Invitrogen社)を用いてクローニングした。塩基配列の確認にはBigDye Terminator Cycle Sequencing Ready Reaction Kit ver.3.0 、DNAシークエンサー377(Applied Biosystems社)で電気泳動し塩基配列を決定した。ヒトGPR120遺伝子は、GenBank Accesion No. NM_181745に登録されている配列より16アミノ酸短いものであった。
pCR2.1-TOPOベクターにクロ-ニングされたGPR120受容体遺伝子は、制限酵素BamHI、EcoRI認識部位が導入されており、同酵素によりベクターより切り出し、真核生物発現ベクターEF1/V5-His B(Invitrogen社)のBamHI、EcoRI認識部位にサブクローニングした。
試験2:発現細胞の作製
LIPOFECTAMINE2000(Invitrogen社製)を使用して、GPR120受容体のcDNAをCHO/NFAT-BLA細胞にトランスフェクトし、薬剤耐性細胞を単離し、GPR120安定発現株を得た。GPR120を発現させたCHO細胞は、10%牛胎児血清、100units/mL penicillin、0.1mg/mL streptomycin sulfate、250ug/mL Zeocin、500ug/mL Geneticin 15mM HEPESを含むDMEM/F12培地で培養した。
試験3:細胞内カルシウム濃度測定
測定前日に96ウェルブラックプレート(パッカード社、ViewPlate)1ウェルにつき20,000細胞でプレーティングされたヒトGPR120発現CHO細胞に、2.5mM Probenecid 存在下で、4μM Fluo-4 AM(蛍光カルシウム指示試薬)をCO2インキュベーターで1時間インキュベートし、取り込ませた。これに、20mM HEPES、2.5mM Probenecidを含んだHBSS溶液にて希釈した被検化合物を加え、Fluorescence Imagin Plate Reader(FLIPR、モレキュラー・デバイス社)にて細胞内カルシウム濃度の変化を測定してアゴニスト作用を調べた。
Claims (14)
- 式(I)
Xは、主鎖が2乃至4の炭素原子からなり、また、該主鎖を構成する炭素原子の1又は2が、酸素原子、硫黄原子又は窒素原子に置き換わっていてもよい、低級アルキレン基であって;
該低級アルキレン基は、
(1)アミノ基(該アミノ基は、低級アルキル基、低級アルキルスルホニル基、低級アルカノイル基で置換されていてもよい)、
(2)ハロゲン原子、
(3)低級アルケニル基、
(4)低級アルキル基(該低級アルキレン基を構成する同一の炭素原子が、2つの低級アルキル基で置換されている場合には、これらの低級アルキル基が一緒になって、3乃至7員の脂肪族環(該脂肪族環を構成する炭素原子の1又は2が、窒素原子、硫黄原子又は酸素原子に置き換わっていてもよい)を形成していてもよい)、
(5)低級アルキニル基、
(6)低級アルキリデン基、
(7)イミノ基、
(8)アリールアルキル基、
(9)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する、5又は6員のヘテロアリールアルキル基、
(10)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有するヘテロアリール基
(11)アリールアルキルオキシ基、及び
(12)窒素原子、硫黄原子及び酸素原子からなる群より選択されるヘテロ原子を環内に1乃至4有する5又は6員のヘテロアリールアルキルオキシ基
からなる群より選択される基で、同一又は異なって1乃至3置換されており;
該低級アルキル基、低級アルキニル基、低級アルキリデン基は、1乃至3のハロゲン原子、ヒドロキシ基又は低級アルコキシ基で置換されていてもよく;
該イミノ基は、1乃至3の低級アルキル基、低級アルキルスルホニル基、シアノ基、ニトロ基、低級アルカノイル基で置換されていてもよく;
該低級アルキレン基は、主鎖中に、二重結合又は三重結合を1又は2有していてもよく;
さらに、該低級アルキレン基は、低級アルコキシ基、オキソ基又はヒドロキシ基で1乃至3置換されていてもよく;
Xと
Yは、
水素原子、
低級アルキル基(該低級アルキル基は、低級アルコキシ基、ハロゲン原子で同一又は異なって1乃至3置換されていてもよい)、
低級アルコキシ基、又は
ハロゲン原子を示す]で表される化合物又はその薬学的に許容される塩。 - Xが、主鎖が3の炭素原子からなり、また、該主鎖を構成する炭素原子の1又は2が、酸素原子、硫黄原子又は窒素原子に置き換わっている低級アルキレン基であって;
該低級アルキレン基が、低級アルキル基、ハロゲン原子及びオキソ基からなる群より選択される基で同一又は異なって、1乃至3置換されている請求項2記載の化合物又はその薬学的に許容される塩。 - Xが、主鎖が3の炭素原子からなり、また、該主鎖を構成する炭素原子の1又は2が、酸素原子、硫黄原子又は窒素原子に置き換わっている低級アルキレン基であって;
該低級アルキレン基が、低級アルキル基、ハロゲン原子及びオキソ基からなる群より選択される基で同一又は異なって、1乃至3置換されており;
低級アルコキシ基(該低級アルコキシ基は、同一又は異なるハロゲン原子で1乃至3置換されていてもよい)、
C3-7シクロアルキルオキシ基、
低級アルキル基(該低級アルキル基は、同一又は異なる1乃至3のハロゲン原子で1乃至3置換されていてもよい)、
低級アルケニル基、及び
ハロゲン原子
からなる群より選択される基で、同一又は異なって1乃至2置換されていてもよいフェニル基若しくはピリジニル基である請求項2記載の化合物又はその薬学的に許容される塩。 - Xが、主鎖が3の炭素原子からなり、また、該主鎖を構成する炭素原子の1又は2が、酸素原子、硫黄原子又は窒素原子に置き換わっている低級アルキレン基であって;
該低級アルキレン基が、低級アルキル基、ハロゲン原子及びオキソ基からなる群より選択される基で同一又は異なって、1乃至3置換されており;
低級アルコキシ基(該低級アルコキシ基は、同一又は異なるハロゲン原子で1乃至3置換されていてもよい)、
C3-7シクロアルキルオキシ基、
低級アルキル基(該低級アルキル基は、同一又は異なる1乃至3のハロゲン原子で1乃至3置換されていてもよい)、
低級アルケニル基、及び
ハロゲン原子
からなる群より選択される基で、同一又は異なって1乃至2置換されていてもよいフェニル基若しくはピリジニル基であり;
- Xが、主鎖が3の炭素原子からなり、また、該主鎖を構成する炭素原子の1が、酸素原子、硫黄原子又は窒素原子に置き換わっている低級アルキレン基であって;
該低級アルキレン基が、低級アルキル基、ハロゲン原子及びオキソ基からなる群より選択される基で同一又は異なって、1又は2置換されている請求1乃至7のいずれか1項に記載の化合物又はその薬学的に許容される塩。 - 式(I)で表される化合物が、
5-(4-(2-(3-イソプロポキシフェニル)-1-メチルエトキシ)フェニル)イソオキサゾール3-オール、
5-(4-(2-フルオロ-2-(3-メトキシフェニル)エトキシ)フェニル)イソオキサゾール3-オール、
5-(4-(2、2-ジフルオロ-2-(3-メトキシフェニル)エトキシ)フェニル)イソオキサゾール3-オール、
5-(4-(2-(3-イソプロポキシフェニル)プロポキシ)フェニル)-イソオキサゾール3-オール、
5-(4-(2-メチル-2-(3-イソプロポキシフェニル)プロポキシ)フェニル)-イソオキサゾール3-オール、
5-{2-フルオロ-4-[2-(3-イソプロポキシフェニル)-1-メチルエトキシ]フェニル}イソオキサゾール3-オール、
5-(6-(2-(3-イソプロポキシフェニル)-1-メチルエトキシ)ピリジン-3-イル)イソオキサゾール3-オール、
5-(5-(2-(3-イソプロポキシフェニル)-1-メチルエトキシ)ピリジン-2-イル)イソオキサゾール3-オール、
5-(4-(((3-イソプロポキシベンジル)(メチル)アミノ)メチル)フェニル)イソオキサゾール3-オール、
5-(4-(2-フェノキシプロピル)フェニル)イソオキサゾール3-オール、
5-(4-(2-(3-メチルフェノキシ)プロピル)フェニル)イソオキサゾール3-オール、
5-(4-(2-(3-メトキシフェノキシ)プロピル)フェニル)イソオキサゾール3-オール、
5-(4-(2-(3-(トリフルオロメチル)フェノキシ)プロピル)フェニル)イソオキサゾール3-オール、
5-(4-(2-(4-メチルフェノキシ)プロピル)フェニル)イソオキサゾール3-オール、
5-(4-(2-(3、5-ジメトキシフェノキシ)プロピル)フェニル)イソオキサゾール3-オール、
5-(4-(2-(4-クロロフェノキシ)プロピル)フェニル)イソオキサゾール3-オール、
5-(4-(2-(4-クロロ-2-フルオロフェノキシ)プロピル)フェニル)イソオキサゾール3-オール、
5-(4-(2-(2、4-ジクロロフェノキシ)プロピル)フェニル)イソオキサゾール3-オール、
5-(4-(2-(3((トリフルオロメチル)オキシ)フェニル)オキシ)プロピル)フェニル)イソオキサゾール3-オール、
5-{4-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール、
5-{4-[((1S)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール、
5-[4-({(1R)-1-メチル-2-[3-(シクロプロピルオキシ)フェニル]-1-メチルエチル}オキシ)フェニル]イソオキサゾール3-オール、
5-{4-[((1R)-1-メチル-2-{3-[(トリフルオロメチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール、
5-{4-[((1R)-1-メチル-2-{4-[(トリフルオロメチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール、
5-{4-[((1R)-2-{4-クロロ-3-[(トリフルオロメチル)オキシ]フェニル}-1-メチルエチル)オキシ]フェニル}イソオキサゾール3-オール、
5-{6-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]ピリジン-3-イル}イソオキサゾール3-オール 塩酸塩、
5-{6-[((1S)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]ピリジン-3-イル}イソオキサゾール3-オール 塩酸塩、
5-{2-フルオロ-4-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール、
5-{4-[(2-フルオロ-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール、
5-{4-[(2,2-ジフルオロ-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール、
5-{4-[(2-フルオロ-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]フェニル}イソオキサゾール3-オール、
5-{2-[((1R)-1-メチル-2-{3-[(1-メチルエチル)オキシ]フェニル}エチル)オキシ]ピリミジン-5-イル}イソオキサゾール3-オール、
5-(4-(2-(3-イソプロポキシフェニル)プロポキシ)フェニル)-イソオキサゾール3-オール、
5-(4-(2-(3-イソプロポキシフェニル)-1-エチルエトキシ)フェニル)イソオキサゾール3-オール、
5-(4-(2-(3-エチルフェニル)-1-メチルエトキシ)フェニル)イソオキサゾール3-オール、
5-(4-(2、2-ジフルオロ-2-(3-イソプロポキシフェニル)エトキシ)フェニル)イソオキサゾール3-オール、
5-{2-フルオロ-4-[2-(3-エトキシフェニル)-1-メチルエトキシ]フェニル}イソオキサゾール3-オール、
5-{2-フルオロ-4-[2-(3-イソプロポキシフェニル)-2-メチルプロポキシ]フェニル}イソオキサゾール3-オール、
5-{2-フルオロ-4-[2-(3-イソプロポキシフェニル)プロポキシ]フェニル}イソオキサゾール3-オール、
5-(6-(2-(3-イソプロポキシフェニル)プロポキシ)ピリジン-3-イル)イソオキサゾール3-オール、
5-(4-{[[1-(3-イソプロポキシフェニル)エチル](メチル)アミノ]メチル}フェニル)イソオキサゾール3-オール、
2-[4-(3-ヒドロキシイソオキサゾール5-イル)フェノキシ]-1-(3-イソプロポキシフェニル)エタノン、
2-[2-(3-エトキシフェニル)-1-メチルエトキシ]-5-(3-ヒドロキシイソオキサゾール-5-イル)ピリジニウム トリフルオロアセテート、
5-(3-ヒドロキシイソオキサゾール-5-イル)-2-[2-(3-イソプロポキシフェニル)-2-メチルプロポキシ]ピリジニウム トリフルオロアセテート、
3-{2-[4-(3-ヒドロキシイソオキサゾール-5-イル)フェノキシ]プロピル}-N,N-ジメチルアニリン 塩酸塩、
2-[4-(3-ヒドロキシイソオキサゾール-5-イル)フェノキシ]-1-(3-イソプロポキシフェニル)プロパン-1-オン、
5-(4-{[1-(3-イソプロポキシフェニル)エトキシ]メチル}フェニル)イソオキサゾール-3-オール、
N-{2-[4-(3-ヒドロキシイソオキサゾール-5-イル)フェニル]エチル}-3-イソプロポキシ-N-メチルアニリン トリフルオロ酢酸塩、
1-[4-(3-ヒドロキシイソオキサゾール-5-イル)フェニル]-N-(3-イソプロポキシベンジル)-N-メチルエタナミン トリフルオロ酢酸塩、
5-[4-({[1-(3-イソプロポキシフェニル)エチル]チオ}メチル)フェニル]イソオキサゾール-3-オール、
N-[4-(3-ヒドロキシイソオキサゾール-5-イル)ベンジル]-3-イソプロポキシ-N-メチルベンゼンスルホンアミド、
5-{4-[2-(3-イソプロポキシフェノキシ)プロピル]フェニル}イソオキサゾール-3-オール、
5-{4-[2-(3-イソブチルフェニル)-1-メチルエトキシ]フェニル}イソオキサゾール-3-オール、
5-{3-フルオロ-4-[2-(3-イソプロポキシフェニル)-1-メチルエトキシ]フェニル}イソオキサゾール-3-オール、
5-(4-{2-[(3-イソプロポキシフェニル)チオ]プロピル}フェニル)イソオキサゾール-3-オール、
5-{4-[2-(3-エトキシフェニル)-1-メチルエトキシ]-3-フルオロフェニル}イソオキサゾール-3-オール、
5-{4-[2,2-ジフルオロ-2-(3-イソプロポキシフェニル)エトキシ]-2-フルオロフェニル}イソオキサゾール-3-オール、
5-(4-{2-[(3-イソプロポキシフェニル)(メチル)アミノ]プロピル}フェニル)イソオキサゾール-3-オール、
4-(3-ヒドロキシイソオキサゾール-5-イル)-N-[2-(3-イソプロポキシフェニル)-1-メチルエチル]アニリン トリフルオロ酢酸塩、
4-(3-ヒドロキシイソオキサゾール-5-イル)-N-[2-(3-イソプロポキシフェニル)エチル]-N-メチルアニリン トリフルオロ酢酸塩、
5-{4-[2-(3-イソプロポキシフェニル)-1-メチルエトキシ]-3-メトキシフェニル}イソオキサゾール-3-オール、
5-(4-((1-メチル-2-(2-((1-メチルエチル)オキシ)ピリジン-4-イル)エチル)オキシ)フェニル)イソオキサゾール-3-オール 塩酸塩、
5-(4-(((1S)-1-メチル-2-(2-((1-メチルエチル)オキシ)ピリジン-4-イル)エチル)オキシ)フェニル)イソオキサゾール-3-オール ナトリウム塩、
5-(4-(((1R)-1-メチル-2-(2-((1-メチルエチル)オキシ)ピリジン-4-イル)エチル)オキシ)フェニル)イソオキサゾール-3-オール ナトリウム塩、又は
N-[4-(3-ヒドロキシイソオキサゾール-5-イル)ベンジル]-3-イソプロポキシ-N-メチルアニリンである請求項1記載の化合物又はその薬学的に許容される塩。 - 請求項1乃至10のいずれか1項に記載の化合物又はその薬学的に許容される塩を有効成分とするGPR120機能調節剤。
- 請求項1乃至10のいずれか1項に記載の化合物又はその薬学的に許容される塩を有効成分とするGPR120アゴニスト。
- 請求項1乃至10のいずれか1項に記載の化合物と薬学的に許容される担体とを含む医薬組成物。
- 請求項1乃至10のいずれか1項に記載の化合物を有効成分として含有する、糖尿病、肥満又は高脂血症の治療剤。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CA2725316A CA2725316A1 (en) | 2008-06-02 | 2009-05-28 | Novel isoxazole derivative |
| EP09758257A EP2298750A4 (en) | 2008-06-02 | 2009-05-28 | NOVEL ISOXAZOLE DERIVATIVE |
| US12/992,387 US20110065739A1 (en) | 2008-06-02 | 2009-05-28 | Novel isoxazole drivative |
| JP2010515846A JPWO2009147990A1 (ja) | 2008-06-02 | 2009-05-28 | 新規イソオキサゾール誘導体 |
| AU2009255183A AU2009255183A1 (en) | 2008-06-02 | 2009-05-28 | Novel isoxazole derivative |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008-144851 | 2008-06-02 | ||
| JP2008144851 | 2008-06-02 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2009147990A1 true WO2009147990A1 (ja) | 2009-12-10 |
Family
ID=41398067
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2009/059758 WO2009147990A1 (ja) | 2008-06-02 | 2009-05-28 | 新規イソオキサゾール誘導体 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US20110065739A1 (ja) |
| EP (1) | EP2298750A4 (ja) |
| JP (1) | JPWO2009147990A1 (ja) |
| AU (1) | AU2009255183A1 (ja) |
| CA (1) | CA2725316A1 (ja) |
| WO (1) | WO2009147990A1 (ja) |
Cited By (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010104195A1 (en) * | 2009-03-11 | 2010-09-16 | Banyu Pharmaceutical Co.,Ltd. | Novel isoindolin-1-one derivative |
| WO2011052756A1 (ja) | 2009-10-30 | 2011-05-05 | 持田製薬株式会社 | 新規3-ヒドロキシ-5-アリールイソキサゾール誘導体 |
| WO2011078371A1 (ja) | 2009-12-25 | 2011-06-30 | 持田製薬株式会社 | 新規3-ヒドロキシ-5-アリールイソチアゾール誘導体 |
| WO2011161030A1 (de) | 2010-06-21 | 2011-12-29 | Sanofi | Heterocyclisch substituierte methoxyphenylderivate mit oxogruppe, verfahren zu ihrer herstellung und ihre verwendung als gpr40 rezeptor modulatoren |
| WO2012004269A1 (de) | 2010-07-05 | 2012-01-12 | Sanofi | ( 2 -aryloxy -acetylamino) - phenyl - propionsäurederivate, verfahren zu ihrer herstellung und ihre verwendung als arzneimittel |
| WO2012004270A1 (de) | 2010-07-05 | 2012-01-12 | Sanofi | Spirocyclisch substituierte 1,3-propandioxidderivate, verfahren zu ihrer herstellung und ihre verwendung als arzneimittel |
| WO2012010413A1 (de) | 2010-07-05 | 2012-01-26 | Sanofi | Aryloxy-alkylen-substituierte hydroxy-phenyl-hexinsäuren, verfahren zu ihrer herstellung und ihre verwendung als arzneimittel |
| WO2012046869A1 (ja) | 2010-10-08 | 2012-04-12 | 持田製薬株式会社 | 環状アミド誘導体 |
| WO2012147516A1 (ja) | 2011-04-28 | 2012-11-01 | 持田製薬株式会社 | 環状アミド誘導体 |
| WO2012147518A1 (ja) * | 2011-04-27 | 2012-11-01 | 持田製薬株式会社 | 新規3-ヒドロキシイソチアゾール 1-オキシド誘導体 |
| WO2013037390A1 (en) | 2011-09-12 | 2013-03-21 | Sanofi | 6-(4-hydroxy-phenyl)-3-styryl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| WO2013045413A1 (en) | 2011-09-27 | 2013-04-04 | Sanofi | 6-(4-hydroxy-phenyl)-3-alkyl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| WO2014011926A1 (en) | 2012-07-11 | 2014-01-16 | Elcelyx Therapeutics, Inc. | Compositions comprising statins, biguanides and further agents for reducing cardiometabolic risk |
| WO2014069963A1 (en) | 2012-11-05 | 2014-05-08 | Lg Life Sciences Ltd. | Thioaryl derivatives as gpr120 agonists |
| JP2015510493A (ja) * | 2011-11-23 | 2015-04-09 | ザ ボード オブ リージェンツ オブ ザ ユニバーシティー オブ テキサス システム | 糖尿病に対するイソオキサゾール処置 |
| WO2018049324A1 (en) | 2016-09-12 | 2018-03-15 | Numerate, Inc. | Monocyclic compounds useful as gpr120 modulators |
| WO2018111734A1 (en) | 2016-12-15 | 2018-06-21 | Merck Sharp & Dohme Corp. | Hydroxy isoxazole compounds useful as gpr120 agonists |
| US10221138B2 (en) | 2013-06-27 | 2019-03-05 | Lg Chem, Ltd. | Biaryl derivatives as GPR120 agonists |
| CN109516914A (zh) * | 2017-09-20 | 2019-03-26 | 华东师范大学 | 苯丙炔酸类小分子有机化合物及其合成方法和用途 |
| JP2020515636A (ja) * | 2017-03-24 | 2020-05-28 | カルダン セラピューティクス リミテッドCaldan Therapeutics Limited | 医薬化合物 |
Families Citing this family (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN102076670B (zh) * | 2008-06-24 | 2013-05-22 | Irm责任有限公司 | 调节g蛋白偶联受体的化合物和方法 |
| AR074760A1 (es) | 2008-12-18 | 2011-02-09 | Metabolex Inc | Agonistas del receptor gpr120 y usos de los mismos en medicamentos para el tratamiento de diabetes y el sindrome metabolico. |
| US8299117B2 (en) | 2010-06-16 | 2012-10-30 | Metabolex Inc. | GPR120 receptor agonists and uses thereof |
| SI3459942T1 (sl) | 2012-04-24 | 2021-05-31 | Vertex Pharmaceuticals Incorporated | Inhibitorji DNA-PK |
| CN107200749B (zh) | 2013-03-12 | 2019-09-03 | 沃泰克斯药物股份有限公司 | Dna-pk抑制剂 |
| RS60426B1 (sr) | 2013-10-17 | 2020-07-31 | Vertex Pharma | Kokristali (s)-n-metil-8-(1-((2'-metil-[4,5'-bipirimidin]-6-il)amino)propan-2-il)hinolin-4-karboksamida i njihovi deuterisani derivati kao inhibitori dnk-pk |
| US10227360B2 (en) | 2014-02-19 | 2019-03-12 | Piramal Enterprises Limited | Compounds for use as GPR120 agonists |
| CA2955919A1 (en) | 2014-07-25 | 2016-01-28 | Piramal Enterprises Limited | Substituted phenyl alkanoic acid compounds as gpr120 agonists and uses thereof |
| AU2015313829B2 (en) | 2014-09-11 | 2020-07-23 | Piramal Enterprises Limited | Fused heterocyclic compounds as GPR120 agonists |
| CA3038657A1 (en) | 2016-09-27 | 2018-04-05 | Vertex Pharmaceuticals Incorporated | Method for treating cancer using a combination of dna-damaging agents and dna-pk inhibitors |
Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3536809A (en) | 1969-02-17 | 1970-10-27 | Alza Corp | Medication method |
| US3598123A (en) | 1969-04-01 | 1971-08-10 | Alza Corp | Bandage for administering drugs |
| US3630200A (en) | 1969-06-09 | 1971-12-28 | Alza Corp | Ocular insert |
| US3845770A (en) | 1972-06-05 | 1974-11-05 | Alza Corp | Osmatic dispensing device for releasing beneficial agent |
| US3916899A (en) | 1973-04-25 | 1975-11-04 | Alza Corp | Osmotic dispensing device with maximum and minimum sizes for the passageway |
| US4008719A (en) | 1976-02-02 | 1977-02-22 | Alza Corporation | Osmotic system having laminar arrangement for programming delivery of active agent |
| JPS62175458A (ja) | 1985-11-21 | 1987-08-01 | ビ−チヤム・グル−プ・ピ−エルシ− | 新規化合物、その製法及びそれを含む医薬組成物 |
| WO2004058265A1 (en) * | 2002-12-24 | 2004-07-15 | Biofocus Plc | Compound libraries of 2,3-substituted pyrazine derivatives capable of binding to g-protein coupled receptors |
| JP2004522773A (ja) * | 2001-02-20 | 2004-07-29 | 中外製薬株式会社 | 代謝調節剤として有用なマロニル−CoA脱炭酸酵素阻害剤としてのアゾール |
| WO2005051373A1 (ja) * | 2003-11-26 | 2005-06-09 | Takeda Pharmaceutical Company Limited | 受容体機能調節剤 |
| WO2008066131A1 (fr) * | 2006-12-01 | 2008-06-05 | Banyu Pharmaceutical Co., Ltd. | Nouveau dérivé de phényl-isoxazol-3-ol |
-
2009
- 2009-05-28 AU AU2009255183A patent/AU2009255183A1/en not_active Abandoned
- 2009-05-28 WO PCT/JP2009/059758 patent/WO2009147990A1/ja active Application Filing
- 2009-05-28 JP JP2010515846A patent/JPWO2009147990A1/ja active Pending
- 2009-05-28 CA CA2725316A patent/CA2725316A1/en not_active Abandoned
- 2009-05-28 US US12/992,387 patent/US20110065739A1/en not_active Abandoned
- 2009-05-28 EP EP09758257A patent/EP2298750A4/en not_active Withdrawn
Patent Citations (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3536809A (en) | 1969-02-17 | 1970-10-27 | Alza Corp | Medication method |
| US3598123A (en) | 1969-04-01 | 1971-08-10 | Alza Corp | Bandage for administering drugs |
| US3630200A (en) | 1969-06-09 | 1971-12-28 | Alza Corp | Ocular insert |
| US3845770A (en) | 1972-06-05 | 1974-11-05 | Alza Corp | Osmatic dispensing device for releasing beneficial agent |
| US3916899A (en) | 1973-04-25 | 1975-11-04 | Alza Corp | Osmotic dispensing device with maximum and minimum sizes for the passageway |
| US4008719A (en) | 1976-02-02 | 1977-02-22 | Alza Corporation | Osmotic system having laminar arrangement for programming delivery of active agent |
| JPS62175458A (ja) | 1985-11-21 | 1987-08-01 | ビ−チヤム・グル−プ・ピ−エルシ− | 新規化合物、その製法及びそれを含む医薬組成物 |
| JP2004522773A (ja) * | 2001-02-20 | 2004-07-29 | 中外製薬株式会社 | 代謝調節剤として有用なマロニル−CoA脱炭酸酵素阻害剤としてのアゾール |
| WO2004058265A1 (en) * | 2002-12-24 | 2004-07-15 | Biofocus Plc | Compound libraries of 2,3-substituted pyrazine derivatives capable of binding to g-protein coupled receptors |
| WO2005051373A1 (ja) * | 2003-11-26 | 2005-06-09 | Takeda Pharmaceutical Company Limited | 受容体機能調節剤 |
| WO2008066131A1 (fr) * | 2006-12-01 | 2008-06-05 | Banyu Pharmaceutical Co., Ltd. | Nouveau dérivé de phényl-isoxazol-3-ol |
Non-Patent Citations (7)
| Title |
|---|
| "Comprehensive Organic Synthesis", vol. 6, 1991, PERGAMON PRESS |
| DATABASE GENBANK accession no. M181745 |
| MITSUNOBU, 0.: "The Use of Diethyl Azodicarboxylate and Triphenylphosphine in Synthesis and Transformation of Natural Products", SYNTHESIS, vol. 1, 1981, pages 1 - 28 |
| NATURE MEDICINE, vol. 11, no. 1, 2005, pages 90 - 941 |
| NOBUO IZUMIYA ET AL.: "Peptide Gosei no Kiso to Jikken", 1983, MARUZEN |
| See also references of EP2298750A4 |
| T.W. GREEN: "Protective Groups in Organic Synthesis, Second Edition,", 1991, JOHN WILEY & SONS |
Cited By (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8362052B2 (en) | 2009-03-11 | 2013-01-29 | Msd K.K. | Isoindolin-1-one derivative |
| WO2010104195A1 (en) * | 2009-03-11 | 2010-09-16 | Banyu Pharmaceutical Co.,Ltd. | Novel isoindolin-1-one derivative |
| JP2012520240A (ja) * | 2009-03-11 | 2012-09-06 | Msd株式会社 | 新規イソインドリン−1−オン誘導体 |
| WO2011052756A1 (ja) | 2009-10-30 | 2011-05-05 | 持田製薬株式会社 | 新規3-ヒドロキシ-5-アリールイソキサゾール誘導体 |
| US8455500B2 (en) | 2009-10-30 | 2013-06-04 | Mochida Pharmaceutical Co., Ltd. | 3-hydroxy-5-arylisoxazole derivative |
| JP5002077B2 (ja) * | 2009-12-25 | 2012-08-15 | 持田製薬株式会社 | 新規3−ヒドロキシ−5−アリールイソチアゾール誘導体 |
| WO2011078371A1 (ja) | 2009-12-25 | 2011-06-30 | 持田製薬株式会社 | 新規3-ヒドロキシ-5-アリールイソチアゾール誘導体 |
| US8476287B2 (en) | 2009-12-25 | 2013-07-02 | Mochida Pharmaceutical Co., Ltd. | 3-hydroxy-5-arylisothiazole derivative |
| WO2011161030A1 (de) | 2010-06-21 | 2011-12-29 | Sanofi | Heterocyclisch substituierte methoxyphenylderivate mit oxogruppe, verfahren zu ihrer herstellung und ihre verwendung als gpr40 rezeptor modulatoren |
| WO2012010413A1 (de) | 2010-07-05 | 2012-01-26 | Sanofi | Aryloxy-alkylen-substituierte hydroxy-phenyl-hexinsäuren, verfahren zu ihrer herstellung und ihre verwendung als arzneimittel |
| WO2012004270A1 (de) | 2010-07-05 | 2012-01-12 | Sanofi | Spirocyclisch substituierte 1,3-propandioxidderivate, verfahren zu ihrer herstellung und ihre verwendung als arzneimittel |
| WO2012004269A1 (de) | 2010-07-05 | 2012-01-12 | Sanofi | ( 2 -aryloxy -acetylamino) - phenyl - propionsäurederivate, verfahren zu ihrer herstellung und ihre verwendung als arzneimittel |
| WO2012046869A1 (ja) | 2010-10-08 | 2012-04-12 | 持田製薬株式会社 | 環状アミド誘導体 |
| US9040525B2 (en) | 2010-10-08 | 2015-05-26 | Mochida Pharmaceutical Co., Ltd. | Cyclic amide derivative |
| JP5420796B2 (ja) * | 2011-04-27 | 2014-02-19 | 持田製薬株式会社 | 新規3−ヒドロキシイソチアゾール1−オキシド誘導体 |
| CN103517898B (zh) * | 2011-04-27 | 2015-09-30 | 持田制药株式会社 | 新的3-羟基异噻唑 1-氧化物衍生物 |
| JP2014122211A (ja) * | 2011-04-27 | 2014-07-03 | Mochida Pharmaceut Co Ltd | 新規3−ヒドロキシイソチアゾール1−オキシド誘導体 |
| US8557766B2 (en) | 2011-04-27 | 2013-10-15 | Mochida Pharmaceutical Co., Ltd. | 3-hydroxyisothiazole 1-oxide derivatives |
| US8629102B2 (en) | 2011-04-27 | 2014-01-14 | Mochida Pharmaceutical Co., Ltd. | 3-hydroxyisothiazole 1-oxide derivatives |
| CN103517898A (zh) * | 2011-04-27 | 2014-01-15 | 持田制药株式会社 | 新的3-羟基异噻唑 1-氧化物衍生物 |
| WO2012147518A1 (ja) * | 2011-04-27 | 2012-11-01 | 持田製薬株式会社 | 新規3-ヒドロキシイソチアゾール 1-オキシド誘導体 |
| US8765752B2 (en) | 2011-04-27 | 2014-07-01 | Mochida Pharmaceutical Co., Ltd. | 3-hydroxyisothiazole 1-oxide derivatives |
| CN105153146A (zh) * | 2011-04-27 | 2015-12-16 | 持田制药株式会社 | 新的3-羟基异噻唑1-氧化物衍生物 |
| WO2012147516A1 (ja) | 2011-04-28 | 2012-11-01 | 持田製薬株式会社 | 環状アミド誘導体 |
| US9072758B2 (en) | 2011-04-28 | 2015-07-07 | Mochida Pharmaceutical Co., Ltd. | Cyclic amide derivative |
| WO2013037390A1 (en) | 2011-09-12 | 2013-03-21 | Sanofi | 6-(4-hydroxy-phenyl)-3-styryl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| WO2013045413A1 (en) | 2011-09-27 | 2013-04-04 | Sanofi | 6-(4-hydroxy-phenyl)-3-alkyl-1h-pyrazolo[3,4-b]pyridine-4-carboxylic acid amide derivatives as kinase inhibitors |
| JP2015510493A (ja) * | 2011-11-23 | 2015-04-09 | ザ ボード オブ リージェンツ オブ ザ ユニバーシティー オブ テキサス システム | 糖尿病に対するイソオキサゾール処置 |
| WO2014011926A1 (en) | 2012-07-11 | 2014-01-16 | Elcelyx Therapeutics, Inc. | Compositions comprising statins, biguanides and further agents for reducing cardiometabolic risk |
| WO2014069963A1 (en) | 2012-11-05 | 2014-05-08 | Lg Life Sciences Ltd. | Thioaryl derivatives as gpr120 agonists |
| US9447044B2 (en) | 2012-11-05 | 2016-09-20 | Lg Life Sciences Ltd. | Thioaryl derivatives as GPR120 agonists |
| US10221138B2 (en) | 2013-06-27 | 2019-03-05 | Lg Chem, Ltd. | Biaryl derivatives as GPR120 agonists |
| EP3628661A1 (en) | 2013-06-27 | 2020-04-01 | Lg Chem, Ltd. | Biaryl derivatives as gpr120 agonists |
| WO2018049324A1 (en) | 2016-09-12 | 2018-03-15 | Numerate, Inc. | Monocyclic compounds useful as gpr120 modulators |
| JP2019530674A (ja) * | 2016-09-12 | 2019-10-24 | ニュメレイト, インコーポレイテッド | Gpr120モジュレーターとして有用な単環式化合物 |
| JP7086942B2 (ja) | 2016-09-12 | 2022-06-20 | インテグラル ヘルス, インコーポレイテッド | Gpr120モジュレーターとして有用な単環式化合物 |
| WO2018111734A1 (en) | 2016-12-15 | 2018-06-21 | Merck Sharp & Dohme Corp. | Hydroxy isoxazole compounds useful as gpr120 agonists |
| US10864211B2 (en) | 2016-12-15 | 2020-12-15 | Merck Sharp & Dohme Corp. | Hydroxy isoxazole compounds useful as GPR120 agonists |
| JP2020515636A (ja) * | 2017-03-24 | 2020-05-28 | カルダン セラピューティクス リミテッドCaldan Therapeutics Limited | 医薬化合物 |
| JP7099672B2 (ja) | 2017-03-24 | 2022-07-12 | カルダン セラピューティクス リミテッド | 医薬化合物 |
| CN109516914A (zh) * | 2017-09-20 | 2019-03-26 | 华东师范大学 | 苯丙炔酸类小分子有机化合物及其合成方法和用途 |
Also Published As
| Publication number | Publication date |
|---|---|
| AU2009255183A1 (en) | 2009-12-10 |
| EP2298750A1 (en) | 2011-03-23 |
| JPWO2009147990A1 (ja) | 2011-10-27 |
| US20110065739A1 (en) | 2011-03-17 |
| EP2298750A4 (en) | 2012-04-25 |
| CA2725316A1 (en) | 2009-12-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2009147990A1 (ja) | 新規イソオキサゾール誘導体 | |
| JP5405120B2 (ja) | 新規フェニル−イソキサゾール−3−オール誘導体 | |
| KR102588982B1 (ko) | 파네소이드 x 수용체 효능제 및 이의 용도 | |
| RU2627703C2 (ru) | Агонисты gpr40 | |
| ES2315912T3 (es) | Derivados de eter sustituido por hexafluorisopropanol. | |
| JP5580834B2 (ja) | 新規イソインドリン−1−オン誘導体 | |
| JP7412424B2 (ja) | Lpaアンタゴニストとしてのオキサビシクロ酸 | |
| US20080249093A1 (en) | (3,4-Disubstituted)Propanoic Carboxylates as Sip (Edg) Receptor Agonists | |
| CN112955448B (zh) | 芳环或芳杂环类化合物及其制备方法和医药用途 | |
| CN112041316A (zh) | 作为lpa拮抗剂的异噁唑o-连接的氨基甲酰基环己基酸 | |
| JP7429224B2 (ja) | Lpaアンタゴニストとしてのシクロヘプチル酸 | |
| WO2008038768A1 (fr) | Composé ayant une structure de pyrimidine bicyclique et composition pharmaceutique comprenant le composé | |
| KR20120097490A (ko) | 리소포스파티드산 수용체 길항제로서의 폴리시클릭 화합물 | |
| JPWO2009054423A1 (ja) | オキサジアゾリジンジオン化合物 | |
| CN113056265A (zh) | 法尼醇x受体激动剂及其用途 | |
| JP2015500872A (ja) | アザアダマンタン誘導体およびその使用 | |
| WO1994001433A1 (en) | Novel thiazolidinedione compound and use thereof | |
| ES2324674T3 (es) | Derivados de fenilpirazol como activadores de ppar. | |
| US9475805B2 (en) | Tricyclic compound | |
| US11597702B2 (en) | Substituted pyrazoles FFA4/GPR120 receptor agonists | |
| CN115666521A (zh) | 法尼醇x受体激动剂的结晶形式 | |
| JPWO2009041475A1 (ja) | ピラゾール−3−イル−ベンズアミド誘導体の製造方法 | |
| US20070208021A1 (en) | Phenoxyacetic Acid Derivatives and Drug Comprising The Same | |
| WO2006013939A1 (ja) | ピラゾール誘導体 | |
| EP1515960A1 (en) | 2-thioxothiazole derivative, method for preparing the same, and pharmaceutical composition containing the same |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 09758257 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12992387 Country of ref document: US |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2009255183 Country of ref document: AU |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2725316 Country of ref document: CA |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2010515846 Country of ref document: JP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2009758257 Country of ref document: EP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2009255183 Country of ref document: AU Date of ref document: 20090528 Kind code of ref document: A |