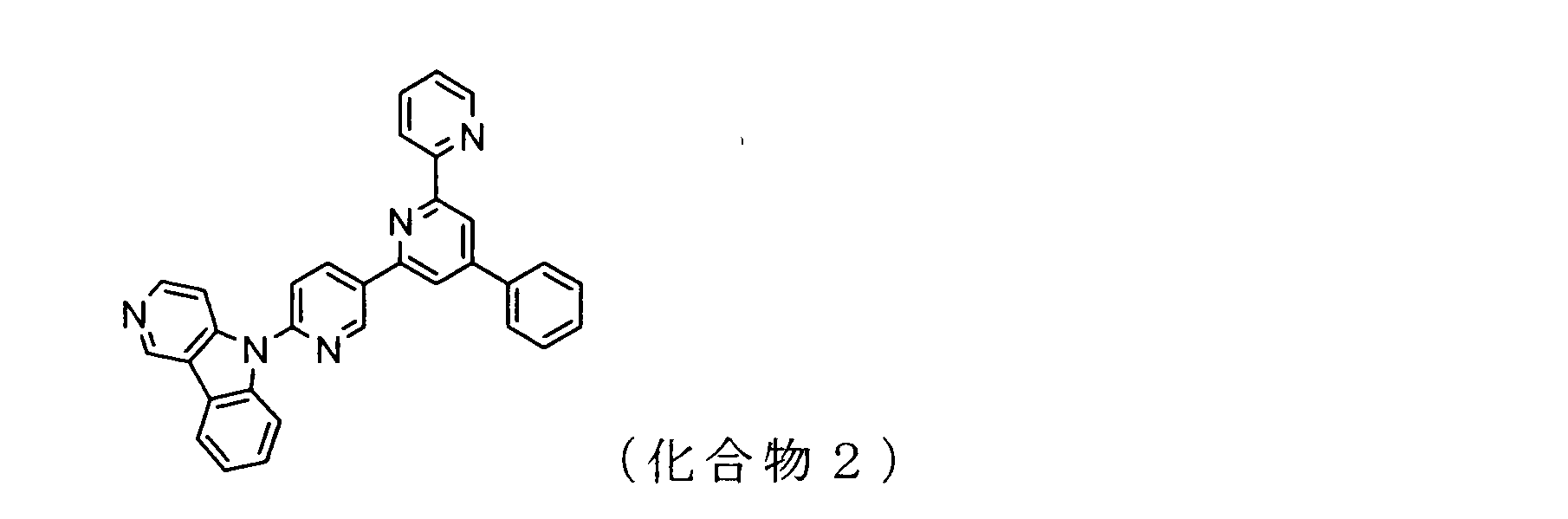
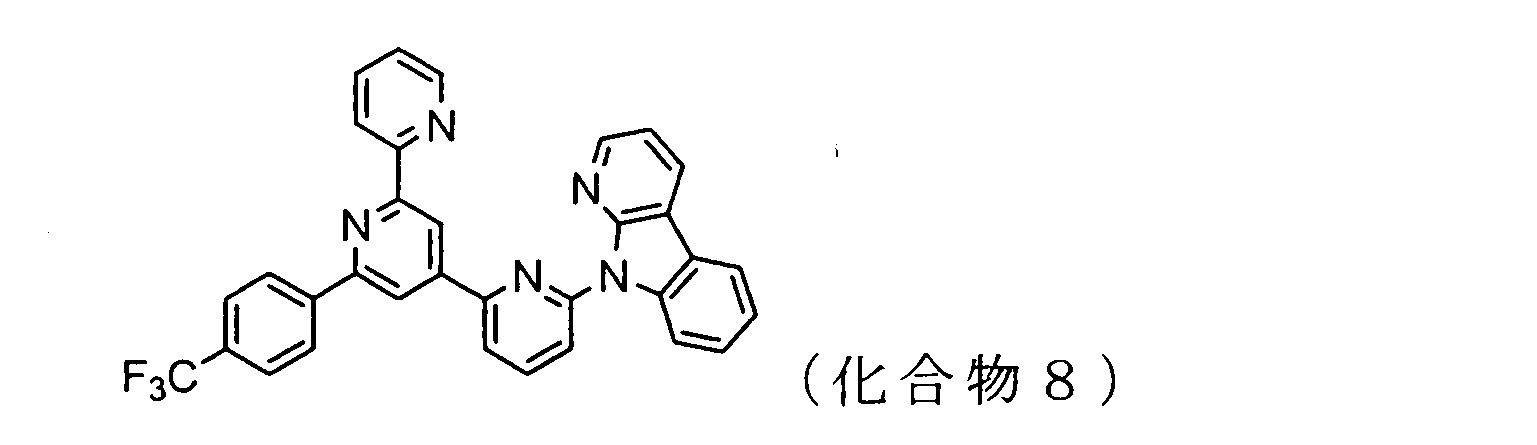
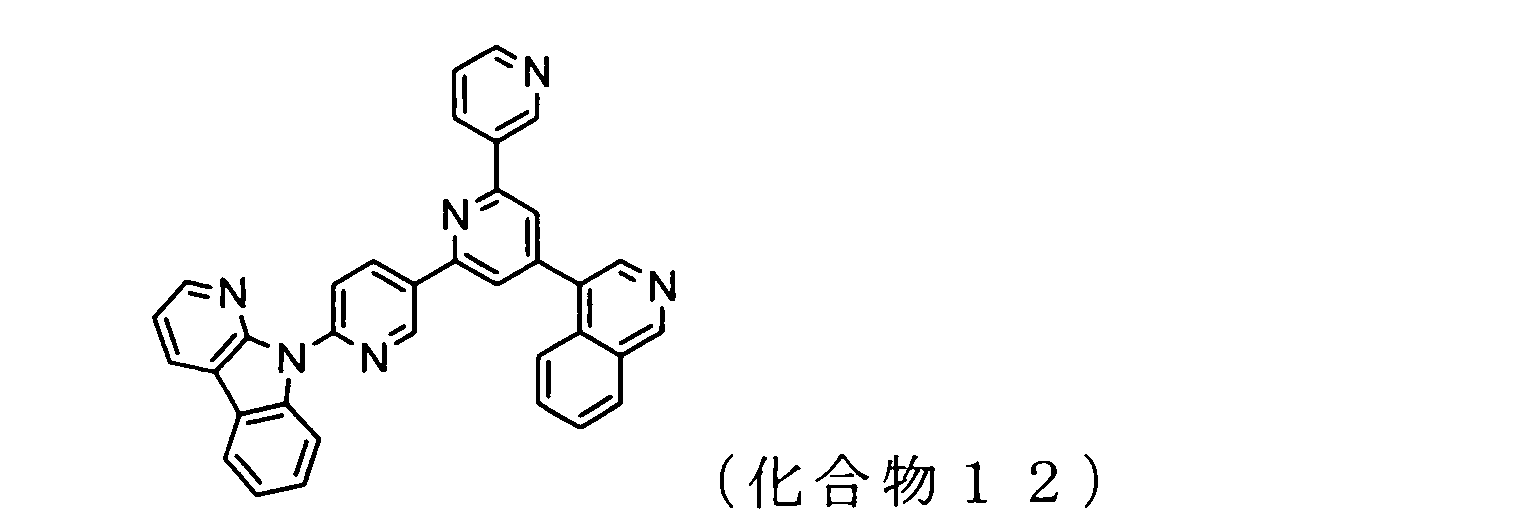
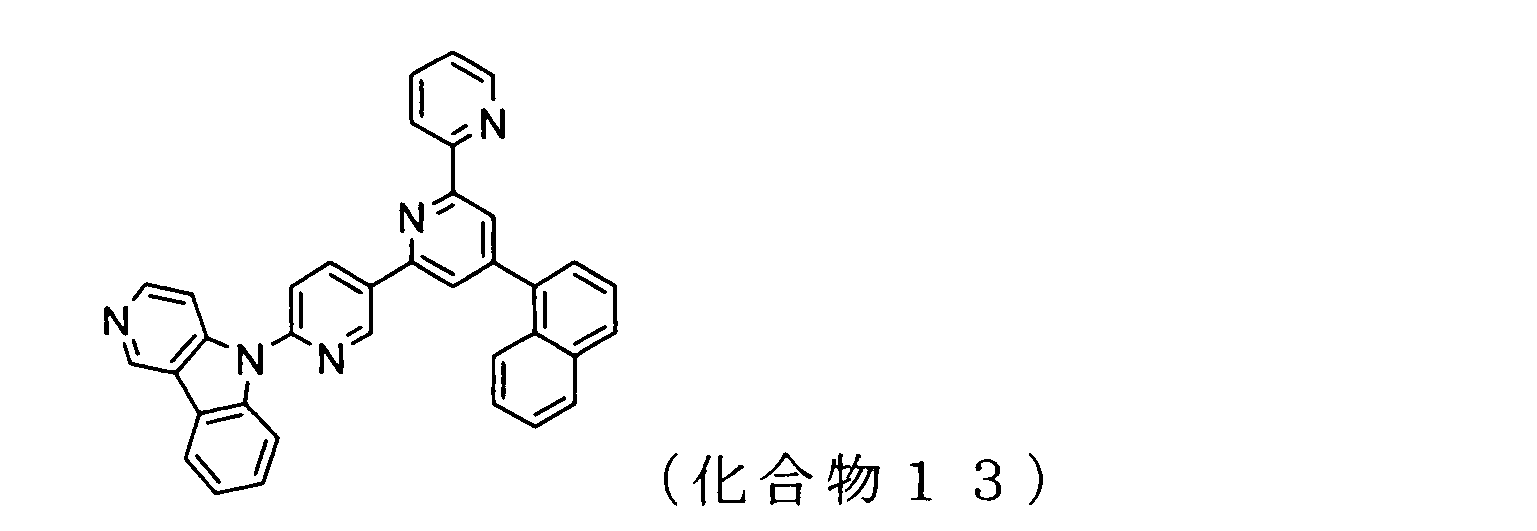
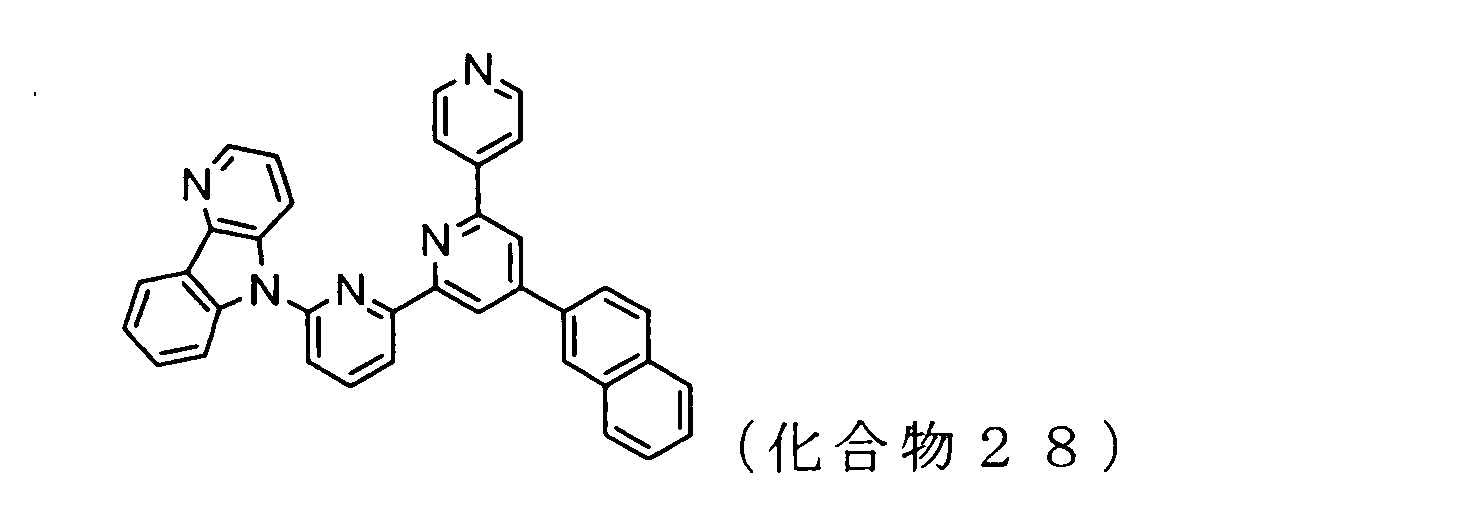
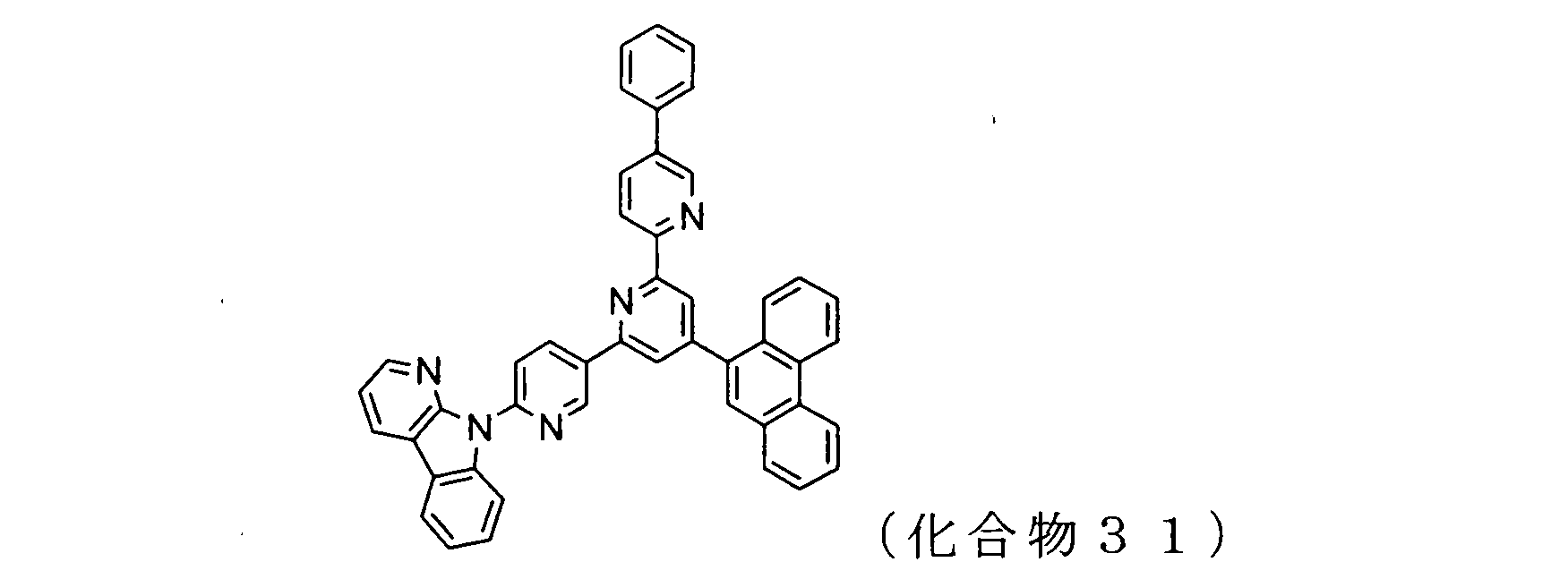
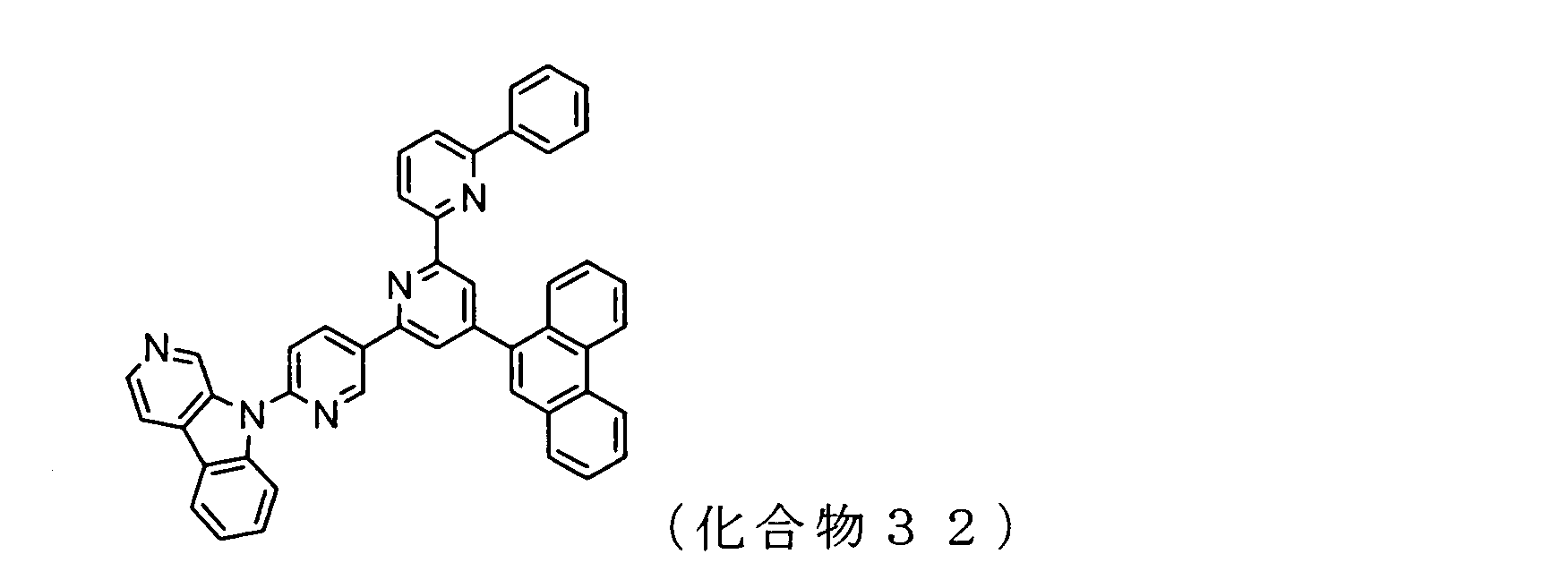
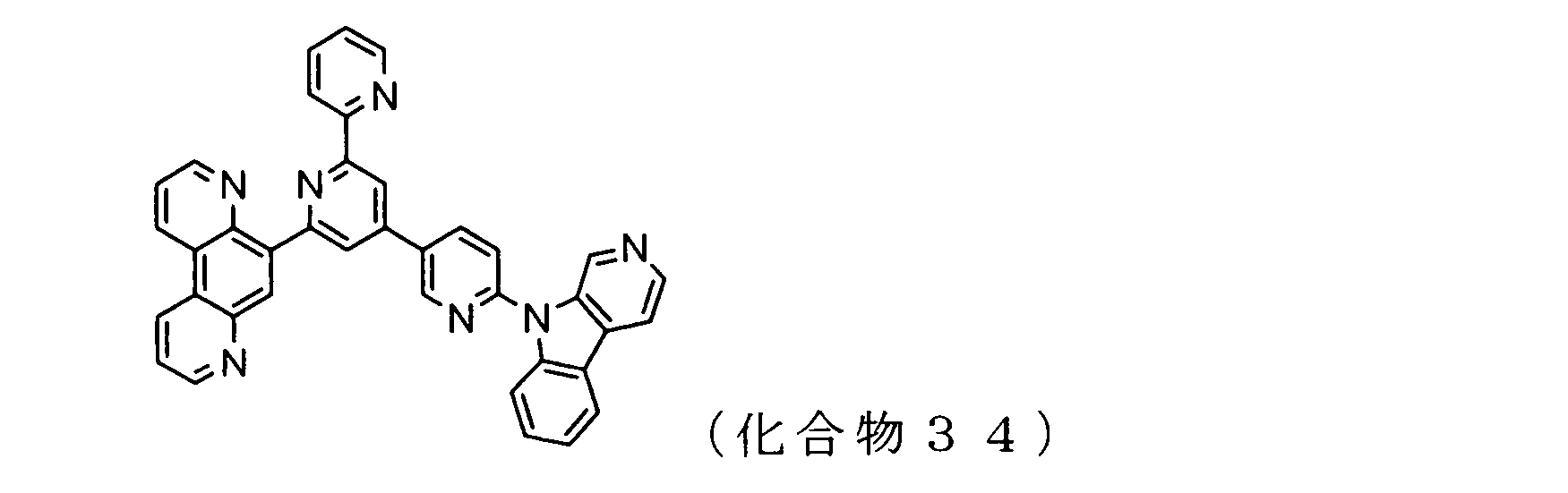
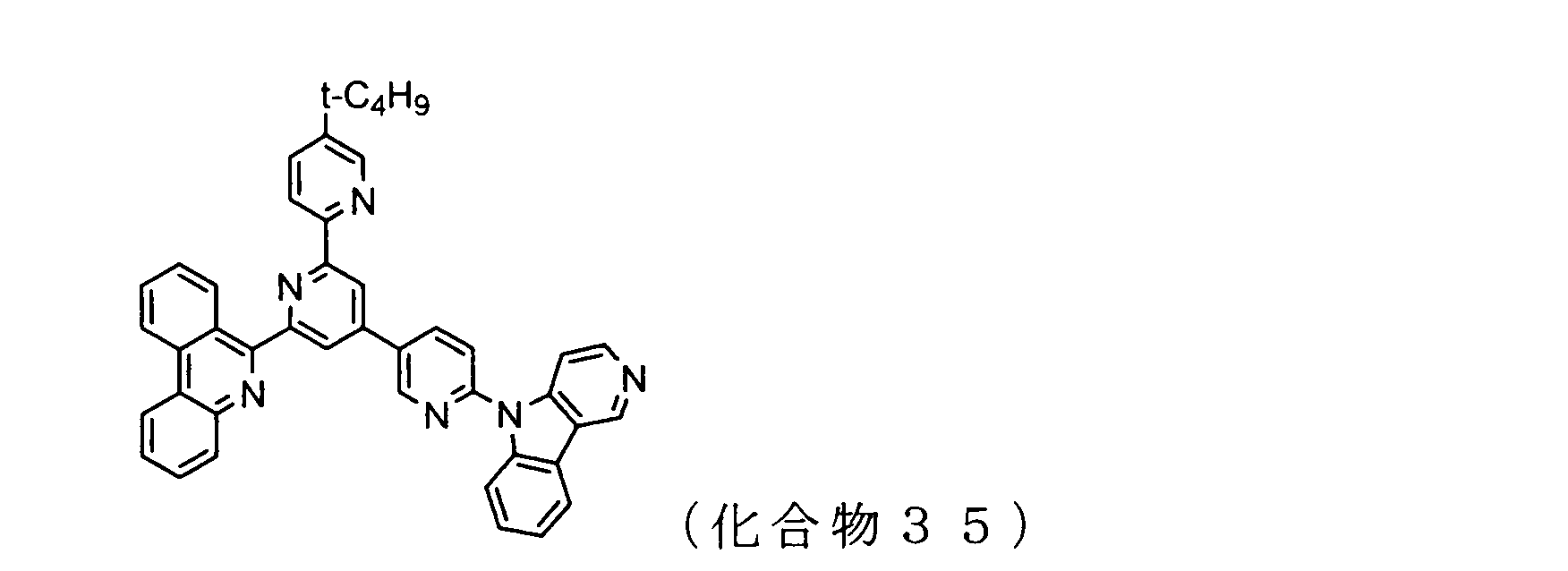
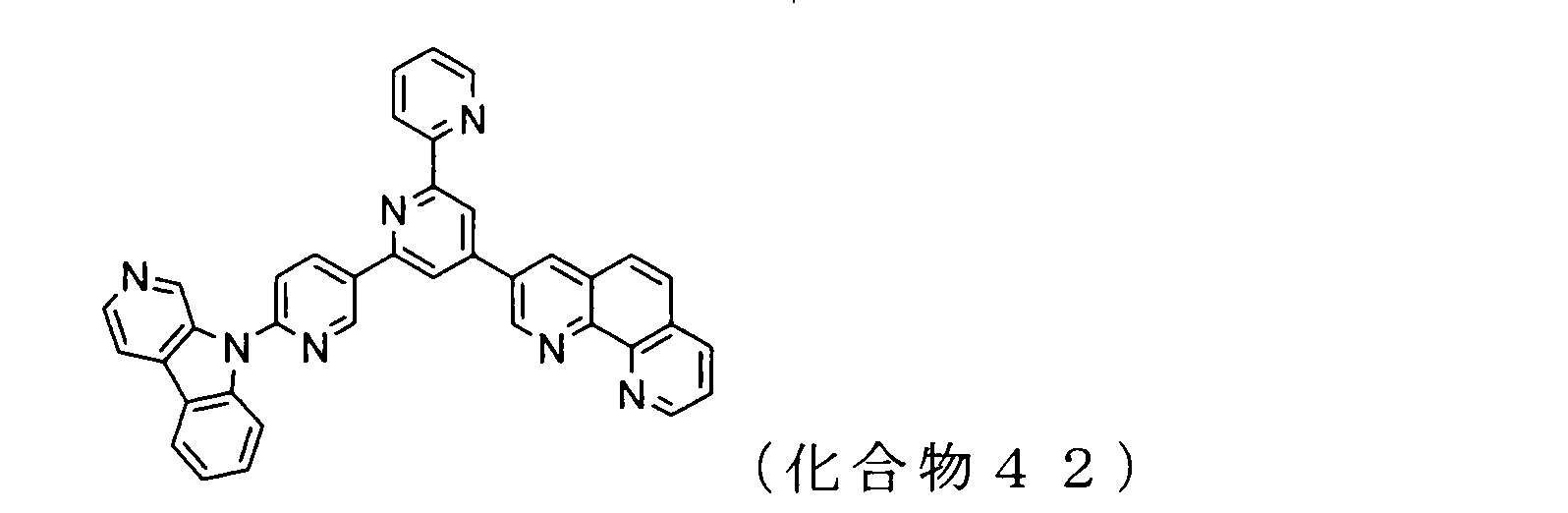
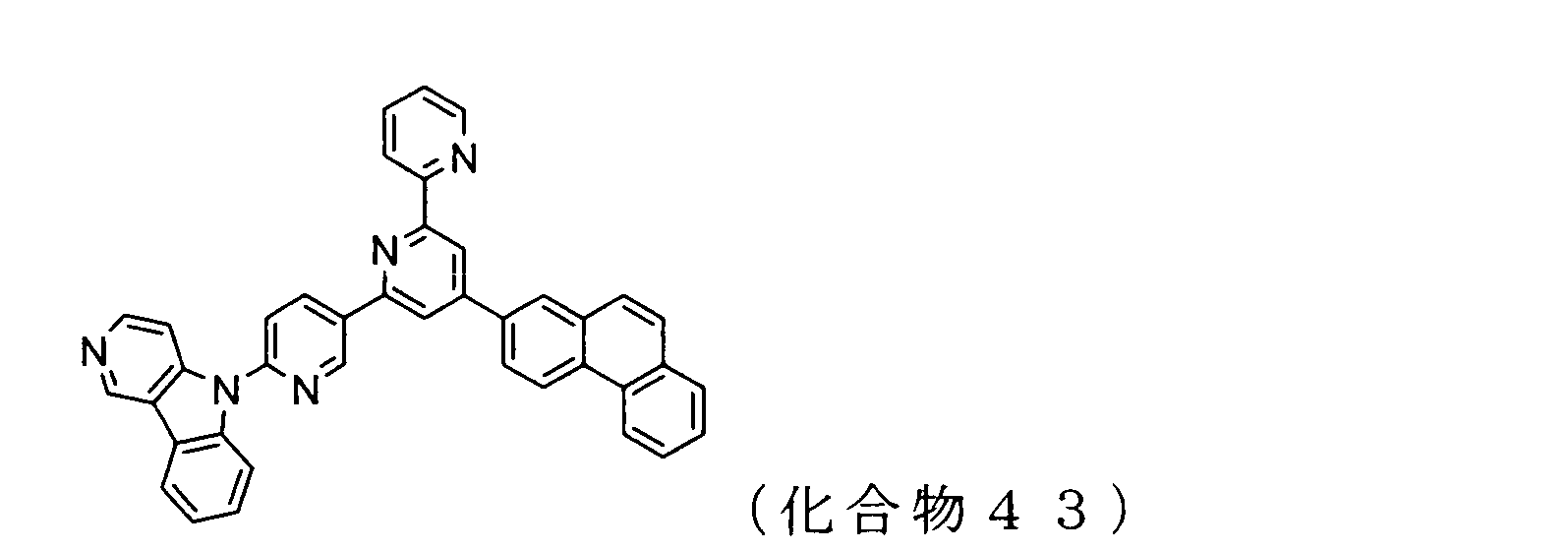
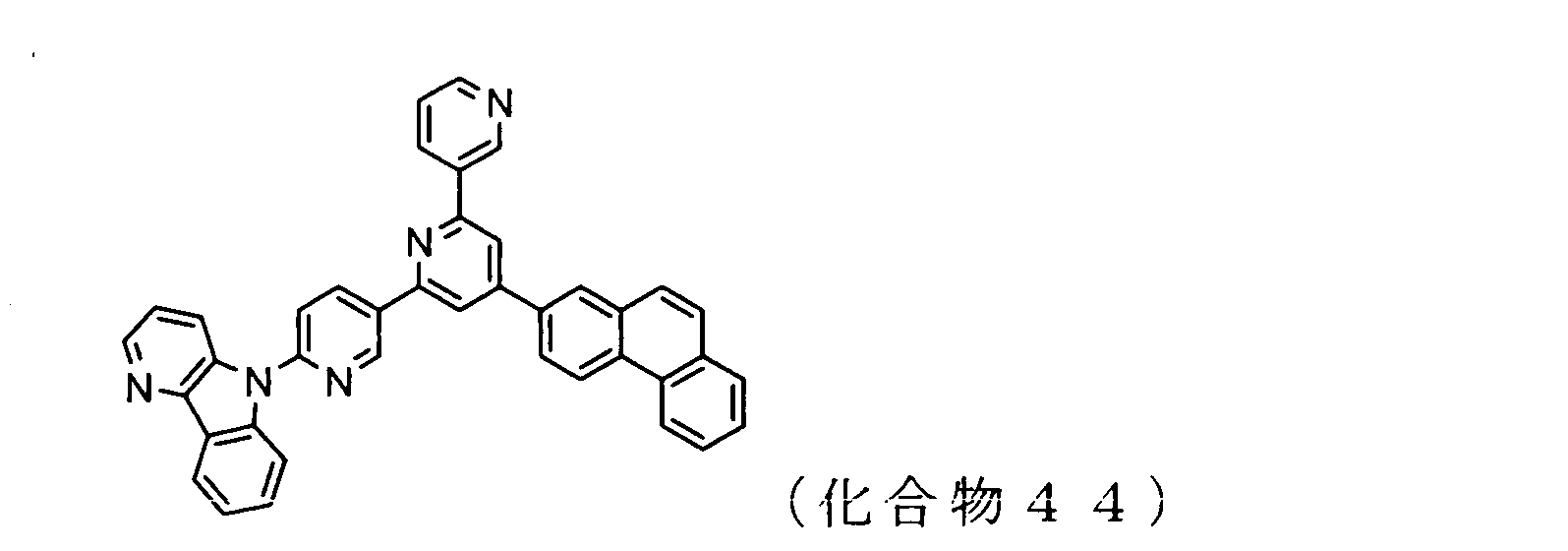
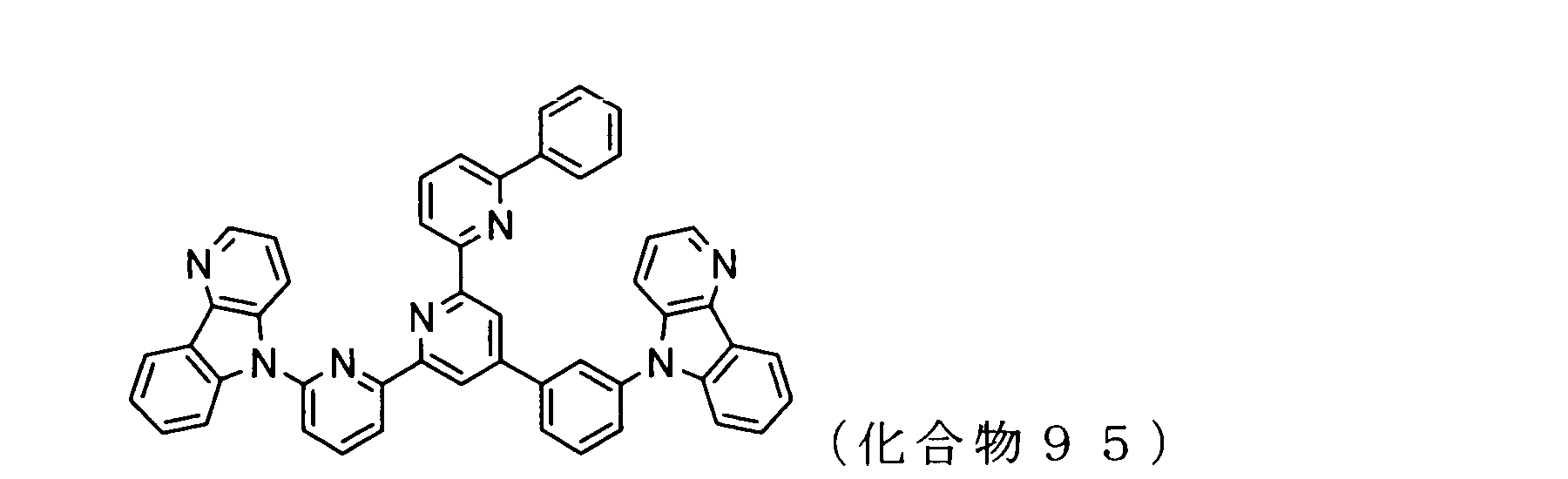
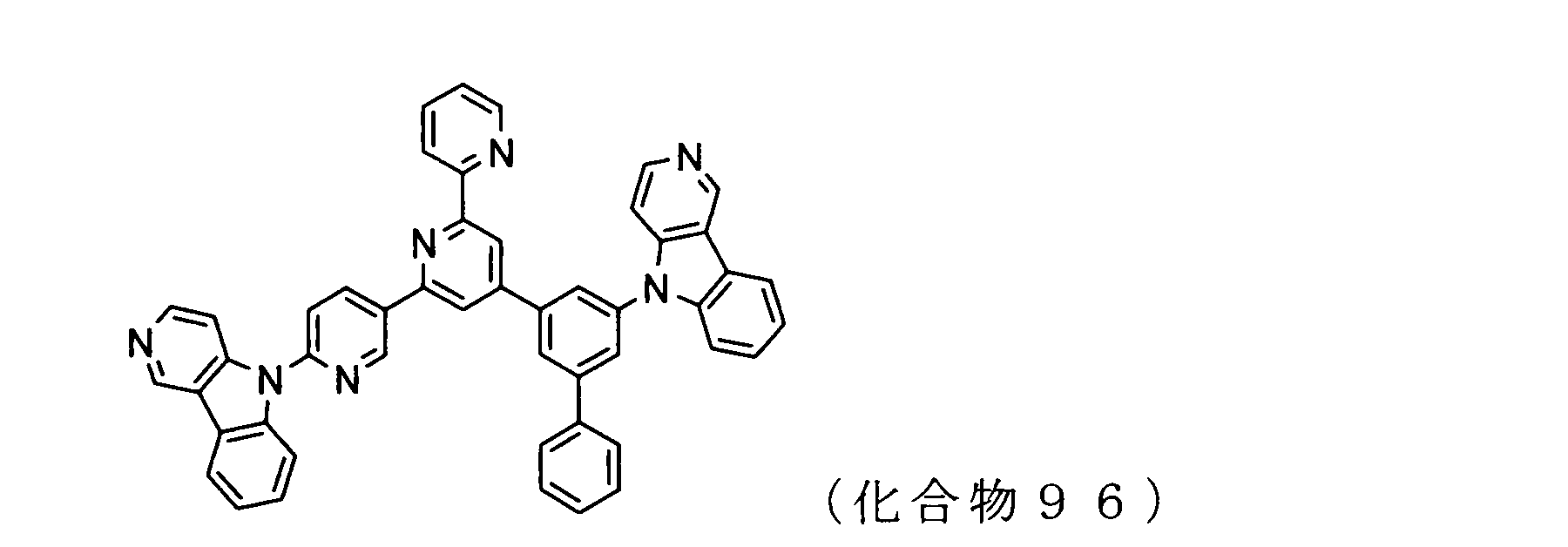
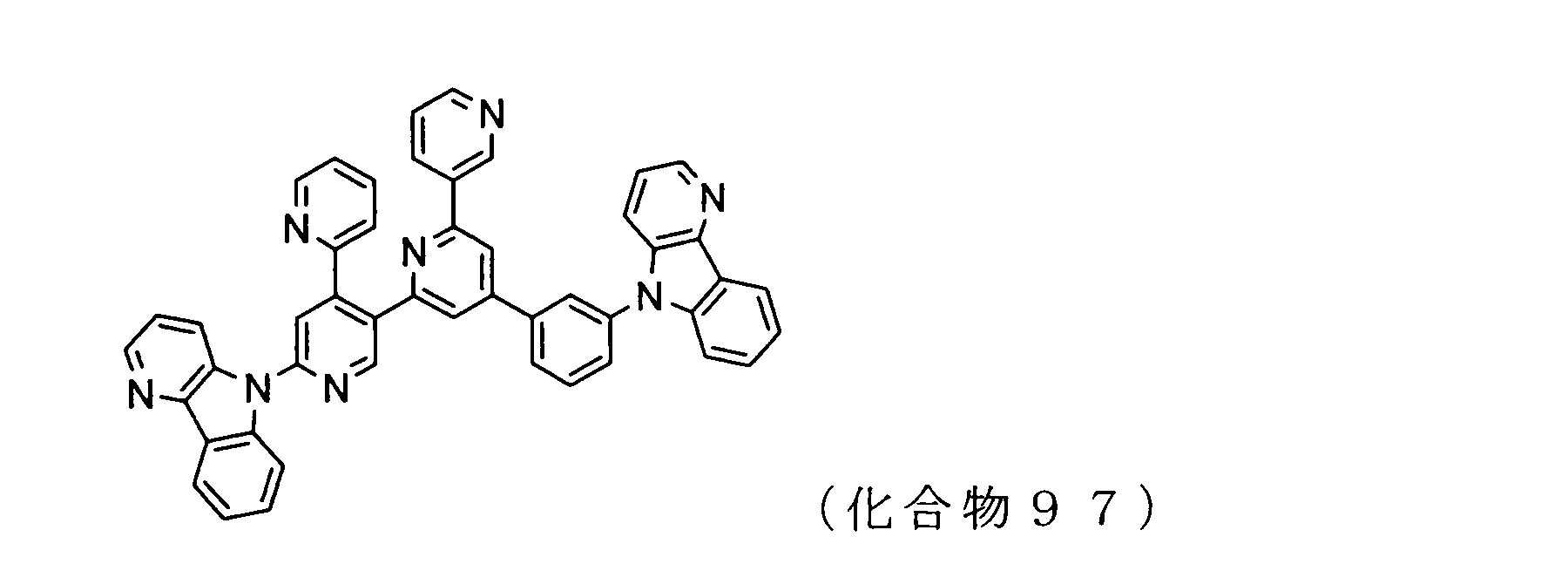
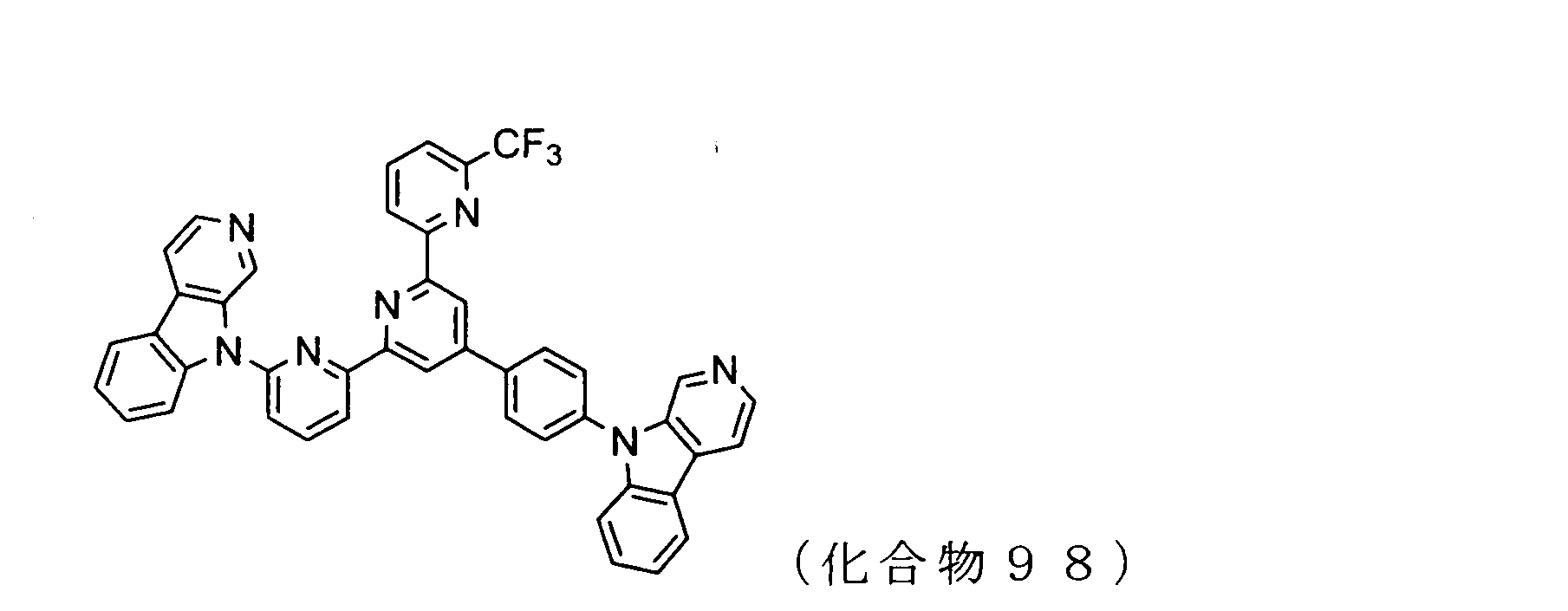
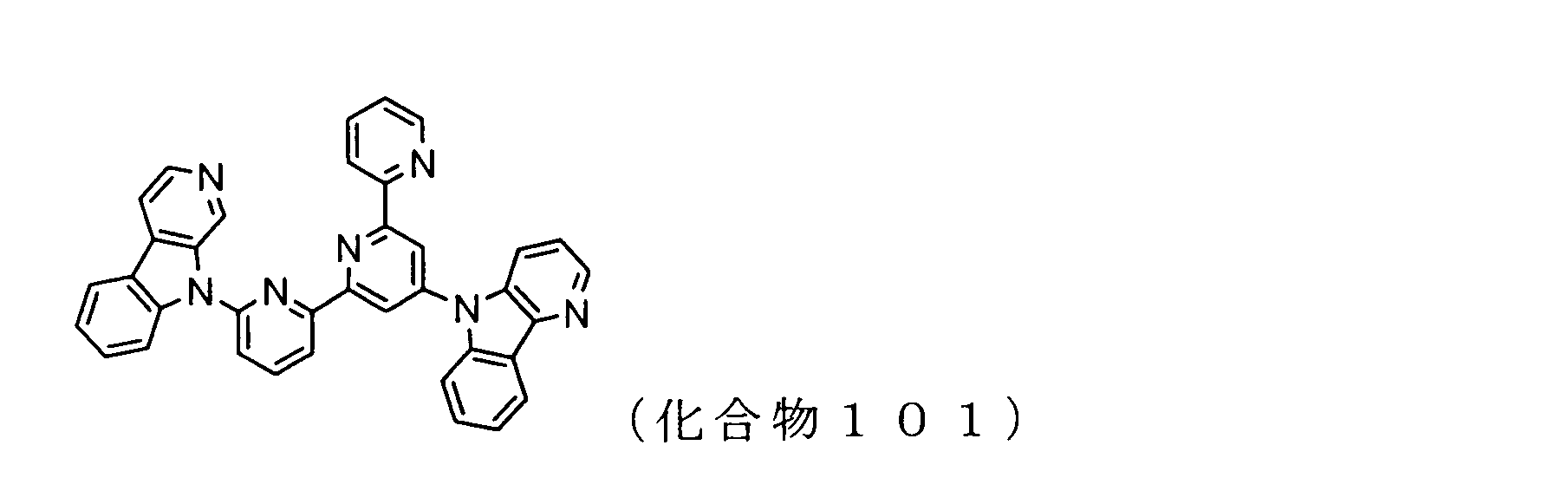
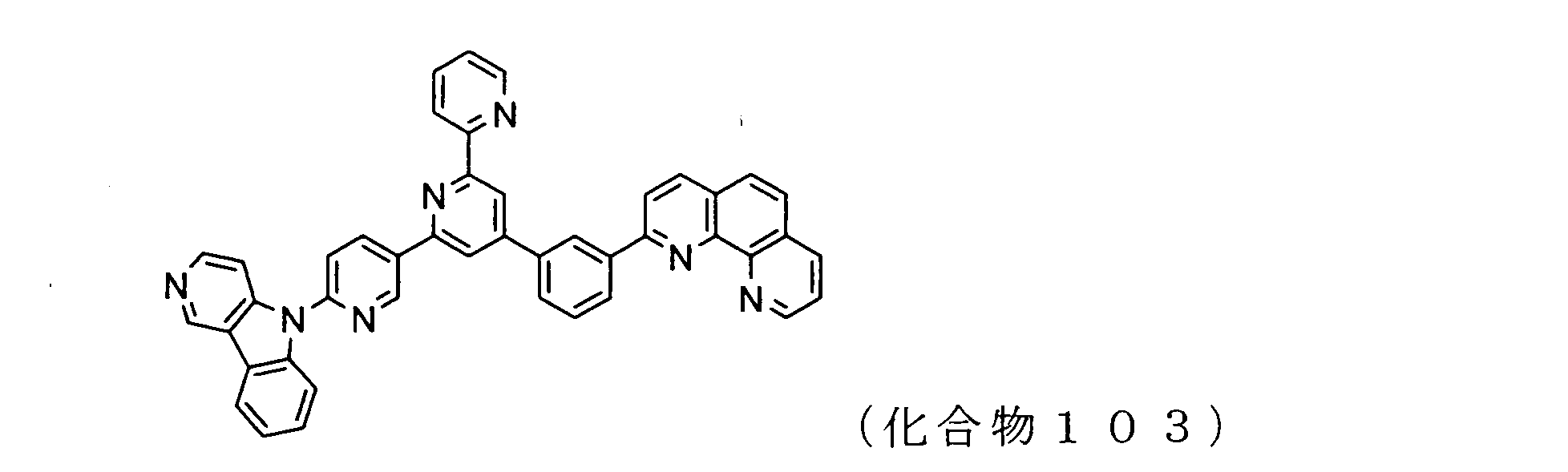
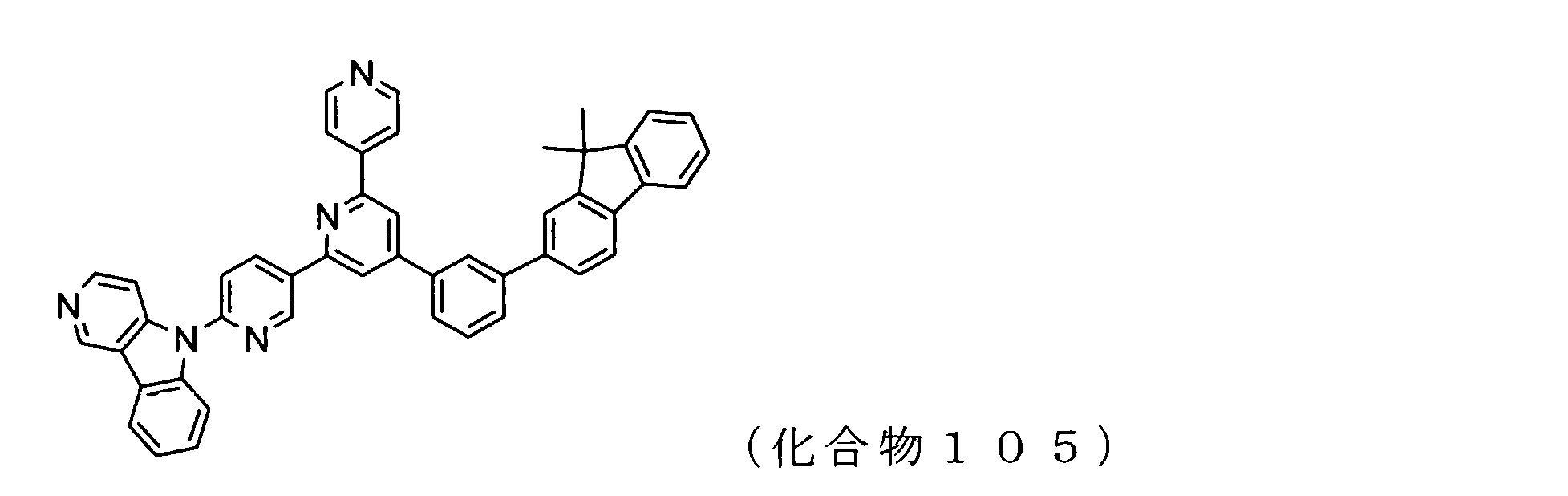
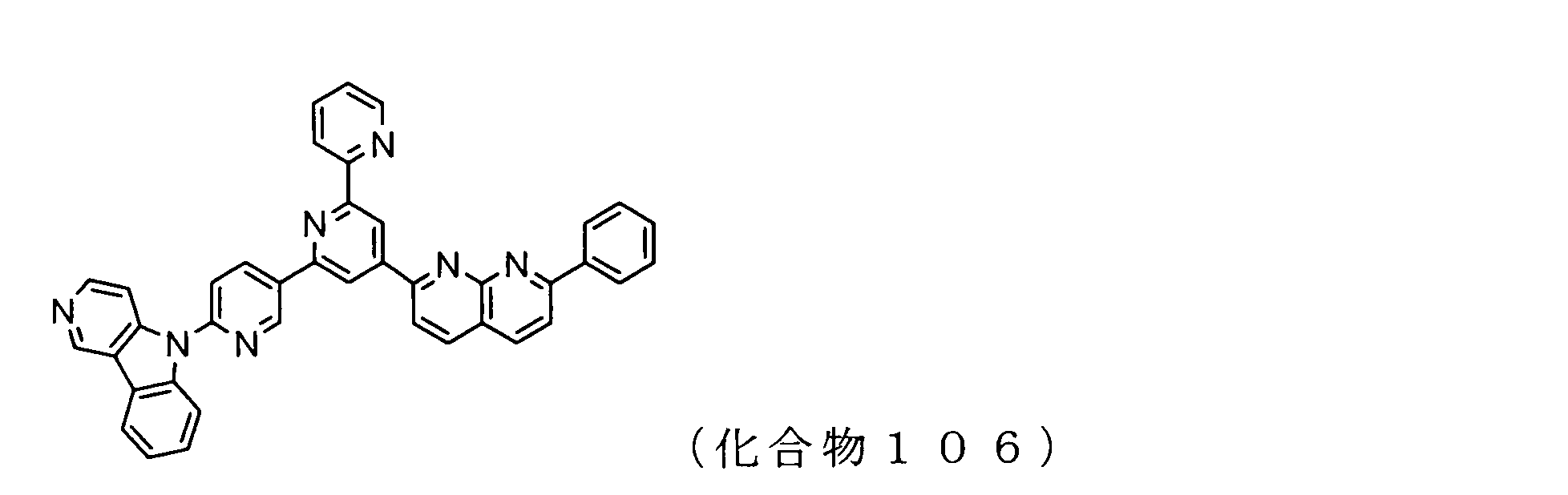
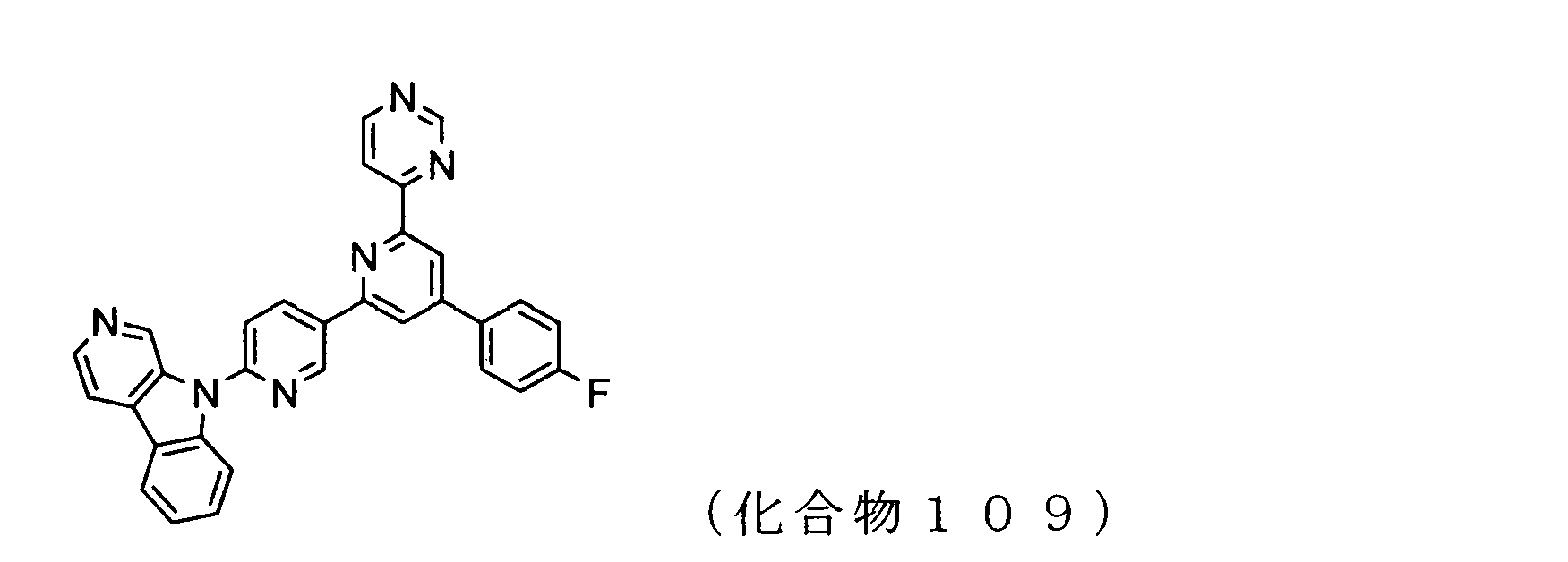
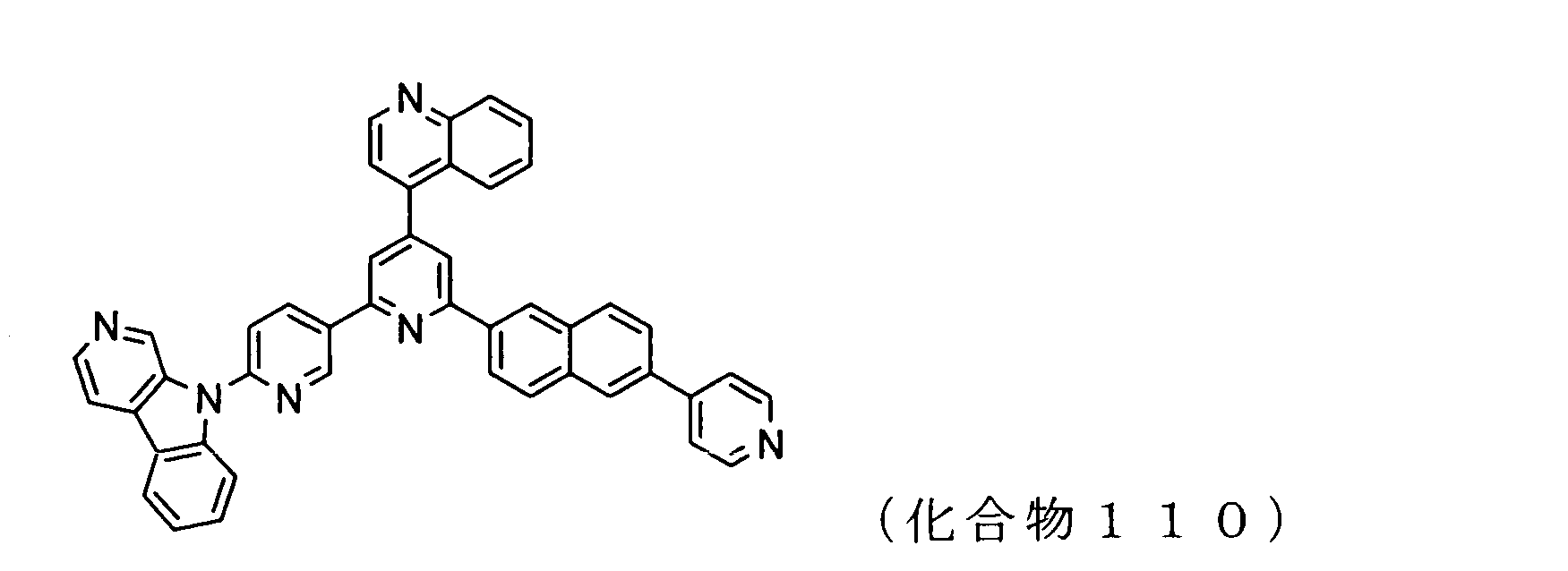
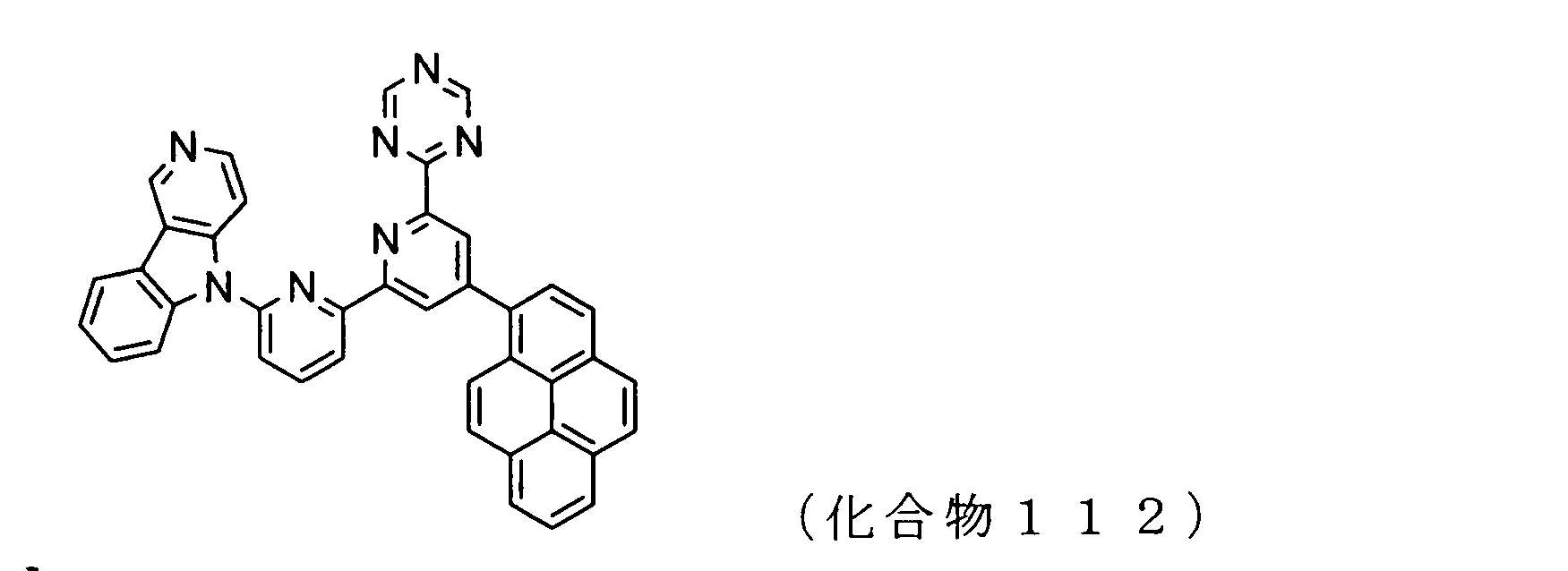
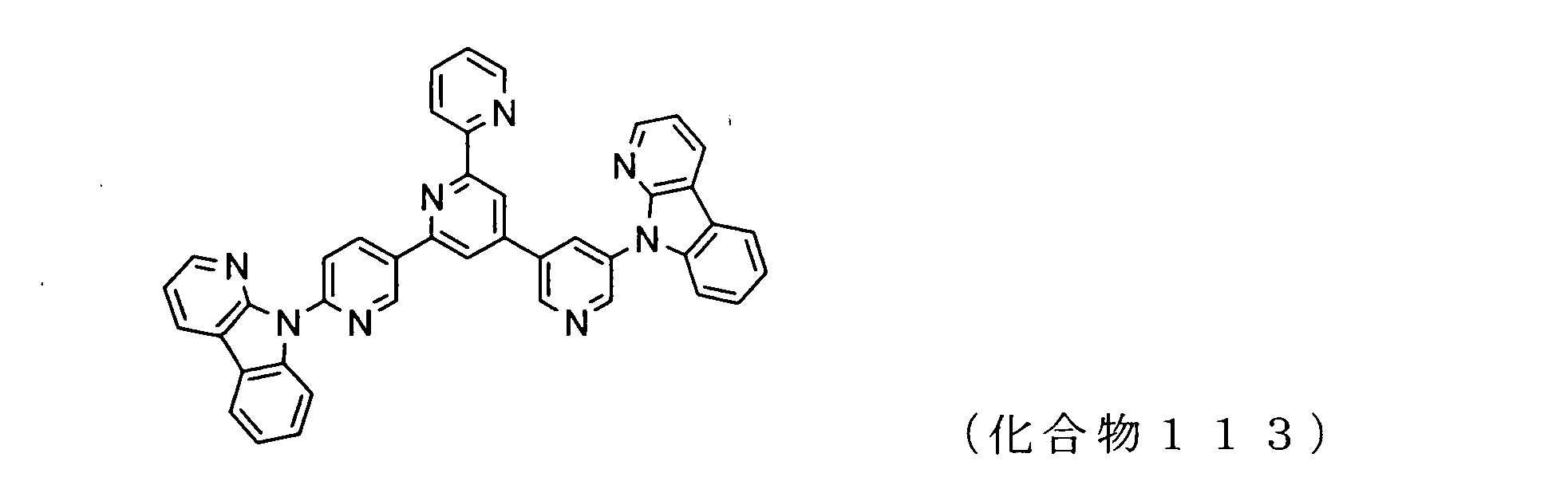
WO2009102016A1 - 置換されたピリジル基が連結したピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 - Google Patents
置換されたピリジル基が連結したピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 Download PDFInfo
- Publication number
- WO2009102016A1 WO2009102016A1 PCT/JP2009/052408 JP2009052408W WO2009102016A1 WO 2009102016 A1 WO2009102016 A1 WO 2009102016A1 JP 2009052408 W JP2009052408 W JP 2009052408W WO 2009102016 A1 WO2009102016 A1 WO 2009102016A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- compound
- substituted
- general formula
- organic
- Prior art date
Links
- HFQDJUFNTIMCNN-UHFFFAOYSA-N N#Cc(cc1c2c3nccc2)ccc1[n]3-c(nc1)ccc1-c1cc(-c2c(ccc3cccc(cc4)c33)c3c4cc2)nc(-c2cccnc2)c1 Chemical compound N#Cc(cc1c2c3nccc2)ccc1[n]3-c(nc1)ccc1-c1cc(-c2c(ccc3cccc(cc4)c33)c3c4cc2)nc(-c2cccnc2)c1 HFQDJUFNTIMCNN-UHFFFAOYSA-N 0.000 description 2
- JUEAHFWRNTWFBK-UHFFFAOYSA-N C(C(c1ccccn1)NC(c1c(ccc2c3c(cc4)ccc2)c3c4cc1)=C1)=C1c1nc(-[n]2c(ccnc3)c3c3ccccc23)ccc1 Chemical compound C(C(c1ccccn1)NC(c1c(ccc2c3c(cc4)ccc2)c3c4cc1)=C1)=C1c1nc(-[n]2c(ccnc3)c3c3ccccc23)ccc1 JUEAHFWRNTWFBK-UHFFFAOYSA-N 0.000 description 1
- PZSOYIKXPMNOLJ-UHFFFAOYSA-N Cc(cc1)c(cccc2)c2c1-c1cc(-c2cccnc2)nc(-c(cc2)cnc2-[n]2c3cccnc3c3c2cccc3)c1 Chemical compound Cc(cc1)c(cccc2)c2c1-c1cc(-c2cccnc2)nc(-c(cc2)cnc2-[n]2c3cccnc3c3c2cccc3)c1 PZSOYIKXPMNOLJ-UHFFFAOYSA-N 0.000 description 1
- AUCUUMLCFFYINB-UHFFFAOYSA-N Clc(cc1c2c3cncc2)ccc1[n]3-c(cc1)ccc1-c1cc(-c2ccncc2)nc(-c(cc2)cnc2-[n]2c3cnccc3c3c2ccc(Cl)c3)c1 Chemical compound Clc(cc1c2c3cncc2)ccc1[n]3-c(cc1)ccc1-c1cc(-c2ccncc2)nc(-c(cc2)cnc2-[n]2c3cnccc3c3c2ccc(Cl)c3)c1 AUCUUMLCFFYINB-UHFFFAOYSA-N 0.000 description 1
- QNCYTBQHCUBVPN-UHFFFAOYSA-N Fc(cc1)ccc1-c1cc(-c2ccncn2)nc(-c(cc2)cnc2-[n]2c3cnccc3c3ccccc23)c1 Chemical compound Fc(cc1)ccc1-c1cc(-c2ccncn2)nc(-c(cc2)cnc2-[n]2c3cnccc3c3ccccc23)c1 QNCYTBQHCUBVPN-UHFFFAOYSA-N 0.000 description 1
- GZJGHNSFVAINFW-UHFFFAOYSA-N c(cc1)cc(c2c3nccc2)c1[n]3-c(cc1)ccc1-c1cc(-c(cc2)cnc2-[n]2c3ncccc3c3c2cccc3)nc(-c2ccccn2)c1 Chemical compound c(cc1)cc(c2c3nccc2)c1[n]3-c(cc1)ccc1-c1cc(-c(cc2)cnc2-[n]2c3ncccc3c3c2cccc3)nc(-c2ccccn2)c1 GZJGHNSFVAINFW-UHFFFAOYSA-N 0.000 description 1
- OYVLHRMBOOXKMP-UHFFFAOYSA-N c(cc1)ccc1-c(cc1)ccc1-c(cc1)ccc1-c1cc(-c(cc2)cnc2-[n](c2c3cccc2)c2c3nccc2)nc(-c2ccncc2)c1 Chemical compound c(cc1)ccc1-c(cc1)ccc1-c(cc1)ccc1-c1cc(-c(cc2)cnc2-[n](c2c3cccc2)c2c3nccc2)nc(-c2ccncc2)c1 OYVLHRMBOOXKMP-UHFFFAOYSA-N 0.000 description 1
- FOTRGSOTFWQBSJ-UHFFFAOYSA-N c(cc1)ccc1-c(cccc1)c1-c1cc(-c2nc(-[n]3c(ccnc4)c4c4c3cccc4)ccc2)nc(-c2ccccn2)c1 Chemical compound c(cc1)ccc1-c(cccc1)c1-c1cc(-c2nc(-[n]3c(ccnc4)c4c4c3cccc4)ccc2)nc(-c2ccccn2)c1 FOTRGSOTFWQBSJ-UHFFFAOYSA-N 0.000 description 1
- OXTKWBCCUWVDAX-UHFFFAOYSA-N c(cc1)ccc1-c1nccc2c1c(cccc1)c1[n]2-c(nc1)ccc1-c1cc(-c2cc3ccccc3cc2)nc(-c2ncccc2)c1 Chemical compound c(cc1)ccc1-c1nccc2c1c(cccc1)c1[n]2-c(nc1)ccc1-c1cc(-c2cc3ccccc3cc2)nc(-c2ncccc2)c1 OXTKWBCCUWVDAX-UHFFFAOYSA-N 0.000 description 1
- AUVONXZMAMVGNQ-UHFFFAOYSA-N c(cc1c2c3ccnc2)ccc1[n]3-c1cc(-c(cc2)ccc2-c2cc(-[n]3c(ccnc4)c4c4ccccc34)cc(-[n]3c(ccnc4)c4c4ccccc34)n2)nc(-[n]2c(ccnc3)c3c3c2cccc3)c1 Chemical compound c(cc1c2c3ccnc2)ccc1[n]3-c1cc(-c(cc2)ccc2-c2cc(-[n]3c(ccnc4)c4c4ccccc34)cc(-[n]3c(ccnc4)c4c4ccccc34)n2)nc(-[n]2c(ccnc3)c3c3c2cccc3)c1 AUVONXZMAMVGNQ-UHFFFAOYSA-N 0.000 description 1
- CVGUWGRZSNOLFG-UHFFFAOYSA-N c(cc1c2c3cncc2)ccc1[n]3-c1nc(-c2cc(-c3nc(-[n]4c5cnccc5c5c4cccc5)cc(-c4ncccc4)c3)cc(-c3nc(-[n]4c(cncc5)c5c5c4cccc5)cc(-c4ncccc4)c3)c2)cc(-c2ncccc2)c1 Chemical compound c(cc1c2c3cncc2)ccc1[n]3-c1nc(-c2cc(-c3nc(-[n]4c5cnccc5c5c4cccc5)cc(-c4ncccc4)c3)cc(-c3nc(-[n]4c(cncc5)c5c5c4cccc5)cc(-c4ncccc4)c3)c2)cc(-c2ncccc2)c1 CVGUWGRZSNOLFG-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional radiating surfaces
- H05B33/20—Light sources with substantially two-dimensional radiating surfaces characterised by the chemical or physical composition or the arrangement of the material in which the electroluminescent material is embedded
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/17—Carrier injection layers
- H10K50/171—Electron injection layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/631—Amine compounds having at least two aryl rest on at least one amine-nitrogen atom, e.g. triphenylamine
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Optics & Photonics (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Electroluminescent Light Sources (AREA)
- Pyridine Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Plural Heterocyclic Compounds (AREA)
Abstract
Description
2 透明陽極
3 正孔注入層
4 正孔輸送層
5 発光層
6 正孔阻止層
7 電子輸送層
8 電子注入層
9 陰極
反応容器に2-アセチル-6-ブロモピリジン11.0g、ヨウ素14.0g、ピリジン45mlを加えて加熱し、100℃で5時間攪拌を行った。室温まで冷却した後、水100mlを加え、再結晶による精製を行った。70℃、12時間減圧乾燥して、[2-(6-ブロモピリジン-2-イル)オキソエチル]ピリジニウムヨウ化物13.8g(収率62%)の褐色粉体を得た。
前記実施例1と同様に、2-ナフトアルデヒドと3-アセチルピリジンから3-(ナフタレン-2-イル)-1-(ピリジン-3-イル)-プロペノンを合成し、さらに[2-(6-ブロモピリジン-2-イル)オキソエチル]ピリジニウムヨウ化物と反応させることによって、6-ブロモ-4’-(ナフタレン-2-イル)-[2,2’;6’,3’’]ターピリジンを合成した。得られた6-ブロモ-4’-(ナフタレン-2-イル)-[2,2’;6’,3’’]ターピリジン4.4g、5H-ピリド[4,3-b]インドール1.7g、銅粉0.3g、炭酸カリウム4.2g、ジメチルスルホキシド0.3ml、オルトジクロロベンゼン20mlを加えて加熱し、140℃で3時間攪拌した。室温まで冷却し、クロロホルム50mlを加えて不溶物をろ過によって除き、ろ液を減圧下濃縮して粗製物を得た。粗製物をクロロホルムに溶解し、NHシリカゲルによる吸着精製を行った後、オルトジクロロベンゼンを用いて再結晶を行うことによって、4’-(ナフタレン-2-イル)-6-(5H-ピリド[4,3-b]インドール-5-イル)-[2,2’;6’,3’’]ターピリジン(化合物131)2.9g(収率55%)の白色粉体を得た。
前記実施例1と同様に、2-ナフトアルデヒドと4-アセチルピリジンから3-(ナフタレン-2-イル)-1-(ピリジン-4-イル)-プロペノンを合成し、さらに[2-(6-ブロモピリジン-2-イル)オキソエチル]ピリジニウムヨウ化物と反応させることによって、6-ブロモ-4’-(ナフタレン-2-イル)- [2,2’;6’,4’’]ターピリジンを合成した。得られた6-ブロモ-4’-(ナフタレン-2-イル)-[2,2’;6’,3’’]ターピリジン5.0g、5H-ピリド[4,3-b]インドール1.9g、銅粉0.4g、炭酸カリウム4.7g、ジメチルスルホキシド0.4ml、オルトジクロロベンゼン22mlを加えて加熱し、140℃で5.5時間攪拌した。室温まで冷却し、クロロホルム800mlを加えて不溶物をろ過によって除き、ろ液を減圧下濃縮して粗製物を得た。粗製物をクロロホルムに溶解し、NHシリカゲルによる吸着精製を行った後、オルトジクロロベンゼンを用いて再結晶を行うことによって、4’-(ナフタレン-2-イル)-6-(5H-ピリド[4,3-b]インドール-5-イル)-[2,2’;6’,4’’]ターピリジン(化合物132)5.1g(収率85%)の白色粉体を得た。
前記実施例1と同様に、4-ブロモベンズアルデヒドと2-アセチルピリジンから3-(4-ブロモフェニル)-1-(ピリジン-2-イル)-プロペノンを合成し、さらに[2-(6-ブロモピリジン-2-イル)オキソエチル]ピリジニウムヨウ化物と反応させることによって、6-ブロモ-4’-(4-ブロモフェニル)-[2,2’;6’,2’’]ターピリジンを合成した。得られた6-ブロモ-4’-(4-ブロモフェニル)-[2,2’;6’,2’’]ターピリジン15.3g、5H-ピリド[4,3-b]インドール5.6g、銅粉1.0g、炭酸カリウム6.8g、ジメチルスルホキシド1.0ml、オルトジクロロベンゼン80mlを加えて加熱し、120℃で7時間攪拌した。室温まで冷却し、クロロホルム200mlを加えて不溶物をろ過によって除き、ろ液を減圧下濃縮して濃縮物を得た。濃縮物にトルエン2Lを加えて不溶物をろ過によって除き、ろ液にNHシリカゲルを加えて吸着精製を行った後、ろ液を減圧下濃縮して粗製物を得た。得られた粗製物をメタノールで洗浄することによって、4’-(4-ブロモフェニル)-6-(5H-ピリド[4,3-b]インドール-5-イル)-[2,2’;6’,2’’]ターピリジン11.3g(収率62%)の褐色粉体を得た。
前記実施例4で得られた4’-(4-ブロモフェニル)-6-(5H-ピリド[4,3-b]インドール-5-イル)-[2,2’;6’,2’’]ターピリジン4.6g、2-ナフタレンボロン酸1.4g、テトラキス(トリフェニルホスフィン)パラジウム0.5g、2M炭酸カリウム水溶液21ml、トルエン72ml、エタノール18mlを加え、攪拌しながら6時間加熱還流した。室温まで冷却し、ろ過によって析出物を採取した。析出物にオルトジクロロベンゼン200mlを加えて不溶物をろ過によって除き、ろ液を減圧下濃縮して濃縮物を得た。濃縮物をクロロホルムに溶解し、NHシリカゲルによる吸着精製を行った後、ろ液を減圧下濃縮して粗製物を得た。粗製物を酢酸エチルで洗浄することによって、4’-(4-ナフタレン-2-イル-フェニル)-6-(5H-ピリド[4,3-b]インドール-5-イル)-[2,2’;6’,2’’]ターピリジン(化合物134)3.5g(収率69%)の白色粉体を得た。
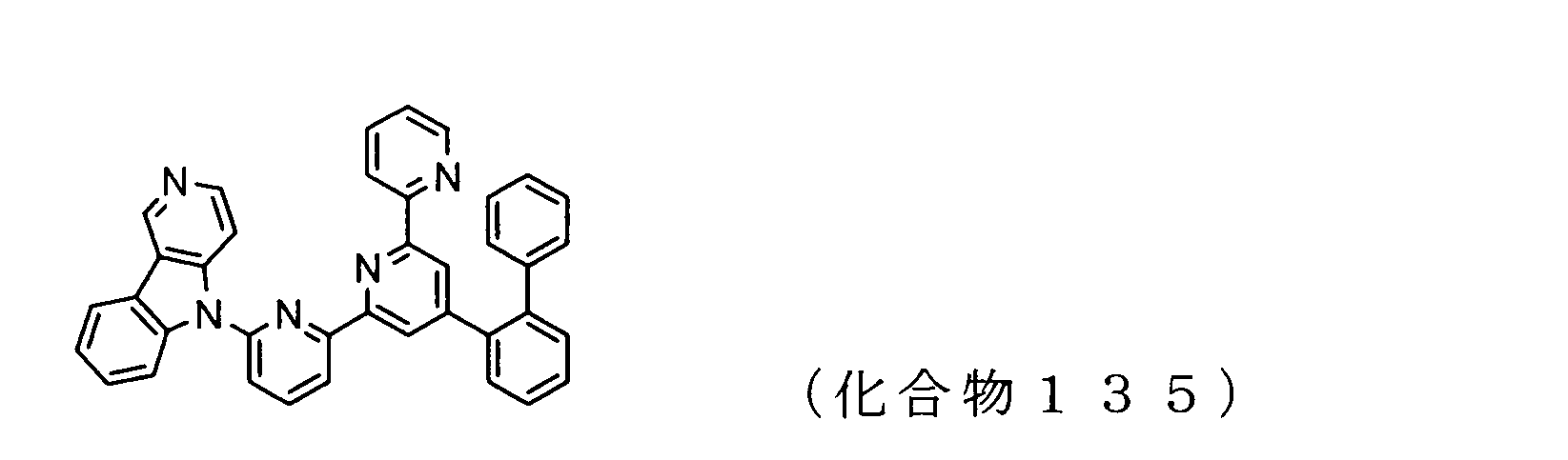
前記実施例1と同様に、2-ビフェニルカルボキシアルデヒドと2-アセチルピリジンから3-(ビフェニル-2-イル)-1-(ピリジン-2-イル)-プロペノンを合成し、さらに[2-(6-ブロモピリジン-2-イル)オキソエチル]ピリジニウムヨウ化物と反応させることによって、4’-(ビフェニル-2-イル)-6-ブロモ-[2,2’;6’,2’’]ターピリジンを合成した。得られた4’-(ビフェニル-2-イル)-6-ブロモ-[2,2’;6’,2’’]ターピリジン4.6g、5H-ピリド[4,3-b]インドール1.7g、銅粉0.3g、炭酸カリウム4.2g、ジメチルスルホキシド0.3ml、オルトジクロロベンゼン20mlを加えて加熱し、140℃で5時間攪拌した。室温まで冷却し、クロロホルム60mlを加えて不溶物をろ過によって除き、ろ液を減圧下濃縮して濃縮物を得た。濃縮物をクロロホルムに溶解し、NHシリカゲルによる吸着精製を行った後、減圧下濃縮して粗製物を得た。粗製物をメタノールで洗浄し、さらに酢酸エチルで洗浄することによって、4’-(ビフェニル-2-イル)-6-(5H-ピリド[4,3-b]インドール-5-イル)- [2,2’;6’,2’’]ターピリジン(化合物135)2.6g(収率46%)の白色粉体を得た。
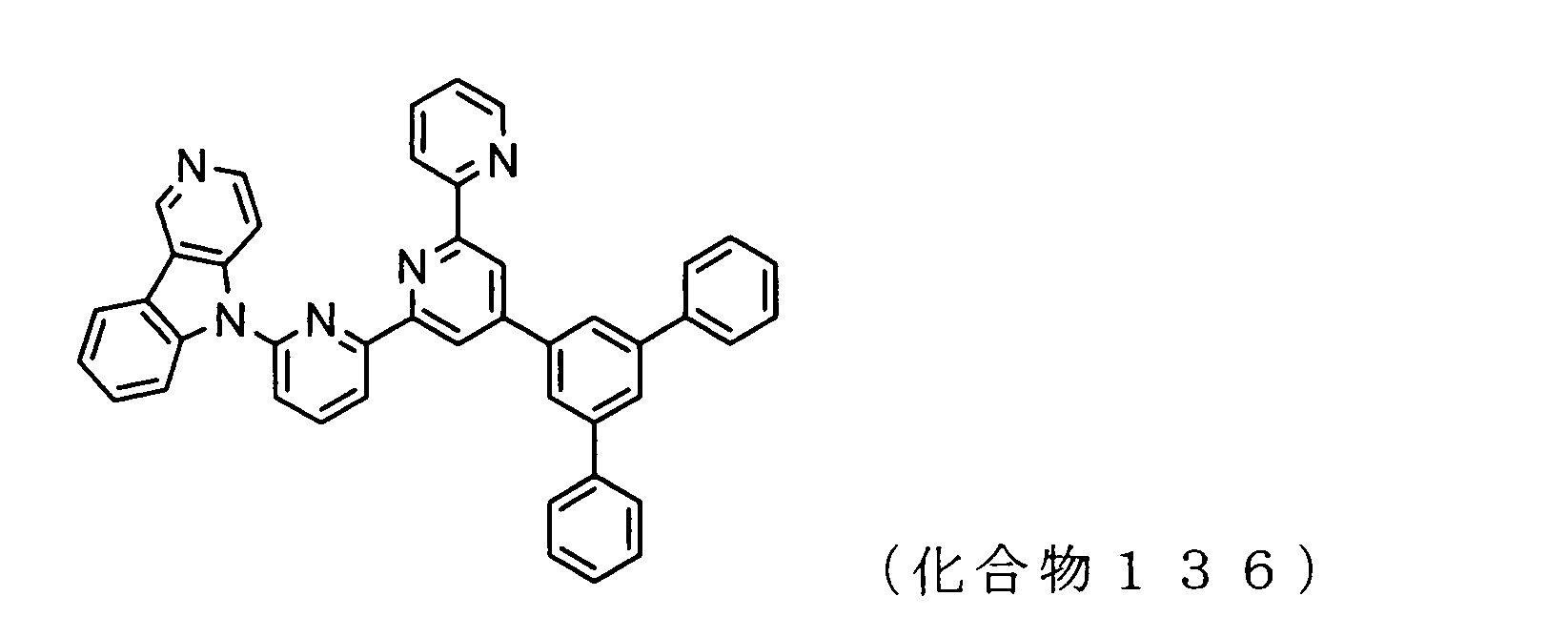
前記実施例4と同様に、3,5-ジブロモベンズアルデヒドと2-アセチルピリジンから3-(3,5-ジブロモフェニル)-1-(ピリジン-2-イル)-プロペノンを合成し、さらに[2-(6-ブロモピリジン-2-イル)オキソエチル]ピリジニウムヨウ化物と反応させることによって、6-ブロモ-4’-(3,5-ジブロモフェニル)-[2,2’;6’,2’’]ターピリジンを合成した。さらに、5H-ピリド[4,3-b]インドールと反応させることによって、4’-(3,5-ジブロモフェニル)-6-(5H-ピリド[4,3-b]インドール-5-イル)-[2,2’;6’,2’’]ターピリジンを合成した。得られた4’-(3,5-ジブロモフェニル)-6-(5H-ピリド[4,3-b]インドール-5-イル)-[2,2’;6’,2’’]ターピリジン5.1g、フェニルボロン酸2.1g、テトラキス(トリフェニルホスフィン)パラジウム0.5g、2M炭酸カリウム水溶液20ml、トルエン72ml、エタノール18mlを加え、攪拌しながら12時間加熱還流した。室温まで冷却し、ろ過によって析出物を採取した。析出物にクロロホルム80mlを加えて不溶物をろ過によって除き、ろ液を減圧下濃縮して粗製物を得た。粗製物をカラムクロマトグラフ(担体:NHシリカゲル、溶離液:トルエン)によって精製した後、オルトジクロロベンゼンを用いて再結晶を行うことによって、6-(5H-ピリド[4,3-b]インドール-5-イル)-4’-[1,1’;3’,1’’]ターフェニル-5’-イル-[2,2’;6’,2’’]ターピリジン(化合物136)2.1g(収率41%)の白色粉体を得た。
融点 ガラス転移点
本発明実施例1の化合物 281℃ 103℃
本発明実施例2の化合物 280℃ なし
本発明実施例3の化合物 301℃ 110℃
本発明実施例4の化合物 215℃ 112℃
本発明実施例5の化合物 154℃ 122℃
本発明実施例6の化合物 135℃ 108℃
本発明実施例7の化合物 247℃ 124℃
仕事関数
本発明実施例1の化合物 6.27eV
本発明実施例2の化合物 6.20eV
本発明実施例3の化合物 6.22eV
本発明実施例4の化合物 6.33eV
本発明実施例5の化合物 6.26eV
本発明実施例6の化合物 6.35eV
本発明実施例7の化合物 6.31eV
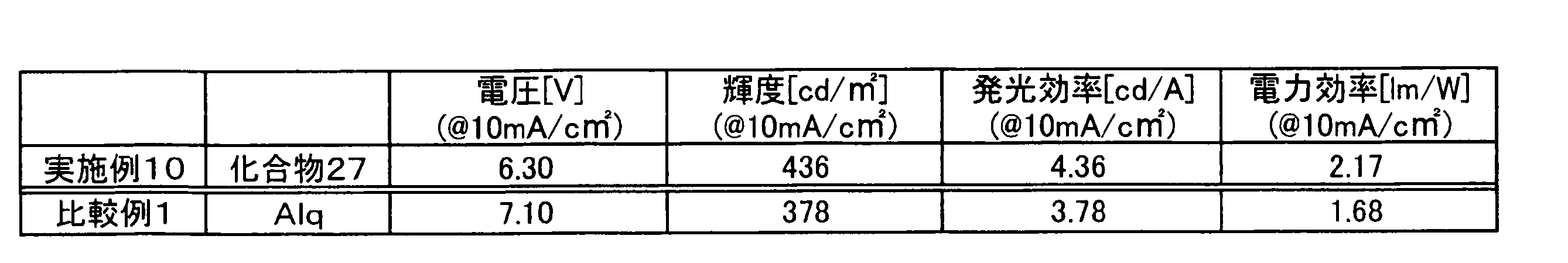
比較のために、電子輸送層7の材料をAlq3に代えて、実施例10と同様の条件で有機EL素子を作製してその特性を調べた。すなわち正孔阻止層兼電子輸送層6および7としてAlq3を蒸着速度3.6nm/minで約20nm形成した。作製した有機EL素子に電流密度10mA/cm2の電流を流したときの発光特性の測定結果は表1にまとめて示した。
[比較例2]
本出願は、2008年2月14日出願の日本特許出願2008-032672に基づくものであり、その内容はここに参照として取り込まれる。
Claims (12)
- 下記一般式(1)で表される置換されたピリジル基が連結したピリドインドール環構造を有する化合物。
- 前記一般式(1)においてn=1である、請求項1記載のピリドインドール環構造を有する化合物。
- 前記一般式(1)においてm=1、n=2である、請求項1記載のピリドインドール環構造を有する化合物。
- 前記一般式(1)においてm=1、n=3である、請求項1記載のピリドインドール環構造を有する化合物。
- 一対の電極とその間に挟まれた少なくとも一層の有機層を有する有機エレクトロルミネッセンス素子であって、前記少なくとも一層の有機層が請求項1記載のピリドインドール環構造を有する化合物を含有する有機エレクトロルミネッセンス素子。
- 前記一般式(1)においてn=1である、請求項5記載の有機エレクトロルミネッセンス素子。
- 前記一般式(1)においてm=1、n=2である、請求項5記載の有機エレクトロルミネッセンス素子。
- 前記一般式(1)においてm=1、n=3である、請求項5記載の有機エレクトロルミネッセンス素子。
- 前記少なくとも一層の有機層が電子輸送層を含み、前記一般式(1)で表される化合物が該電子輸送層中に存在する、請求項5記載の有機エレクトロルミネッセンス素子。
- 前記少なくとも一層の有機層が正孔阻止層を含み、前記一般式(1)で表される化合物が該正孔阻止層中に存在する、請求項5記載の有機エレクトロルミネッセンス素子。
- 前記少なくとも一層の有機層が発光層を含み、前記一般式(1)で表される化合物が該発光層中に存在する、請求項5記載の有機エレクトロルミネッセンス素子。
- 前記少なくとも一層の有機層が電子注入層を含み、前記一般式(1)で表される化合物が該電子注入層中に存在する、請求項5記載の有機エレクトロルミネッセンス素子。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US12/867,556 US8624228B2 (en) | 2008-02-14 | 2009-02-13 | Compound having pyridoindole ring structure bonded with substituted pyridyl group, and organic electroluminescent device |
| EP20090711282 EP2246351B1 (en) | 2008-02-14 | 2009-02-13 | Compound having pyridoindole ring structure bonded with substituted pyridyl group, and organic electroluminescent device |
| JP2009553460A JP5467873B2 (ja) | 2008-02-14 | 2009-02-13 | 置換されたピリジル基が連結したピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| CN200980104982.6A CN102015703B (zh) | 2008-02-14 | 2009-02-13 | 具有与取代的吡啶基键合的吡啶并吲哚环结构的化合物,及有机电致发光器件 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008-032672 | 2008-02-14 | ||
| JP2008032672 | 2008-02-14 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2009102016A1 true WO2009102016A1 (ja) | 2009-08-20 |
Family
ID=40957047
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2009/052408 WO2009102016A1 (ja) | 2008-02-14 | 2009-02-13 | 置換されたピリジル基が連結したピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US8624228B2 (ja) |
| EP (1) | EP2246351B1 (ja) |
| JP (2) | JP5467873B2 (ja) |
| KR (1) | KR101609397B1 (ja) |
| CN (1) | CN102015703B (ja) |
| TW (1) | TWI429647B (ja) |
| WO (1) | WO2009102016A1 (ja) |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010235575A (ja) * | 2009-03-09 | 2010-10-21 | Konica Minolta Holdings Inc | 含窒素縮合複素環化合物の製造方法 |
| WO2011016202A1 (ja) * | 2009-08-05 | 2011-02-10 | 保土谷化学工業株式会社 | 置換されたアントラセン環構造とピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| JP2011148751A (ja) * | 2010-01-25 | 2011-08-04 | Konica Minolta Holdings Inc | 含窒素縮合複素環化合物の製造方法 |
| WO2013175789A1 (ja) * | 2012-05-24 | 2013-11-28 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子用材料、及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP2014198696A (ja) * | 2013-03-29 | 2014-10-23 | 出光興産株式会社 | 含窒素芳香族複素環誘導体、有機エレクトロルミネッセンス素子用材料、及び有機エレクトロルミネッセンス素子 |
| CN111718341A (zh) * | 2020-07-10 | 2020-09-29 | 北京燕化集联光电技术有限公司 | 一种含有咔唑环的化合物及其在有机电致发光器件中的应用 |
Families Citing this family (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2008020611A1 (fr) * | 2006-08-18 | 2008-02-21 | Hodogaya Chemical Co., Ltd. | Composé à structure cyclique pyrido-indole sur laquelle est fixé un groupe pyridyle substitué et élément organique électroluminescent |
| WO2009102016A1 (ja) * | 2008-02-14 | 2009-08-20 | Hodogaya Chemical Co., Ltd. | 置換されたピリジル基が連結したピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| WO2011086941A1 (ja) | 2010-01-15 | 2011-07-21 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子 |
| US8883323B2 (en) | 2010-11-22 | 2014-11-11 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| US9324950B2 (en) | 2010-11-22 | 2016-04-26 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device |
| KR102256401B1 (ko) * | 2019-09-06 | 2021-05-27 | 엘티소재주식회사 | 헤테로고리 화합물 및 이를 포함하는 유기 발광 소자 |
| CN111718342B (zh) * | 2020-07-10 | 2021-08-17 | 北京燕化集联光电技术有限公司 | 一种新型有机材料及其应用 |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH0848656A (ja) | 1994-02-08 | 1996-02-20 | Tdk Corp | 有機el素子用化合物および有機el素子 |
| JP2734341B2 (ja) | 1993-03-26 | 1998-03-30 | 住友電気工業株式会社 | 有機エレクトロルミネッセンス素子 |
| JP3194657B2 (ja) | 1993-11-01 | 2001-07-30 | 松下電器産業株式会社 | 電界発光素子 |
| WO2004053019A1 (ja) * | 2002-12-12 | 2004-06-24 | Idemitsu Kosan Co., Ltd. | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP2006156445A (ja) * | 2004-11-25 | 2006-06-15 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| JP2007080657A (ja) * | 2005-09-14 | 2007-03-29 | Konica Minolta Holdings Inc | 非水分散液、有機エレクトロルミネッセンス素子、有機エレクトロルミネッセンス素子の製造方法、表示装置及び照明装置 |
| JP2007180147A (ja) * | 2005-12-27 | 2007-07-12 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
Family Cites Families (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH03194657A (ja) | 1989-12-22 | 1991-08-26 | Mitsubishi Electric Corp | 図形処理装置 |
| US20060251918A1 (en) * | 2003-12-11 | 2006-11-09 | Toshihiro Iwakuma | Organic electroluminescent device material and organic electroluminescent device using same |
| JP4626613B2 (ja) * | 2004-08-04 | 2011-02-09 | コニカミノルタホールディングス株式会社 | 有機エレクトロルミネッセンス素子 |
| US8053092B2 (en) * | 2005-12-12 | 2011-11-08 | Hodogaya Chemical Co., Ltd. | m-carbazolylphenyl compounds |
| CN101473464B (zh) * | 2006-06-22 | 2014-04-23 | 出光兴产株式会社 | 应用含有杂环的芳胺衍生物的有机电致发光元件 |
| WO2008020611A1 (fr) | 2006-08-18 | 2008-02-21 | Hodogaya Chemical Co., Ltd. | Composé à structure cyclique pyrido-indole sur laquelle est fixé un groupe pyridyle substitué et élément organique électroluminescent |
| WO2009102016A1 (ja) * | 2008-02-14 | 2009-08-20 | Hodogaya Chemical Co., Ltd. | 置換されたピリジル基が連結したピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| US8771841B2 (en) * | 2008-05-16 | 2014-07-08 | Hodogaya Chemical Co., Ltd. | Organic electroluminescent device |
-
2009
- 2009-02-13 WO PCT/JP2009/052408 patent/WO2009102016A1/ja active Application Filing
- 2009-02-13 US US12/867,556 patent/US8624228B2/en not_active Expired - Fee Related
- 2009-02-13 JP JP2009553460A patent/JP5467873B2/ja active Active
- 2009-02-13 TW TW098104631A patent/TWI429647B/zh not_active IP Right Cessation
- 2009-02-13 EP EP20090711282 patent/EP2246351B1/en not_active Not-in-force
- 2009-02-13 CN CN200980104982.6A patent/CN102015703B/zh not_active Expired - Fee Related
- 2009-02-13 KR KR1020107017979A patent/KR101609397B1/ko active IP Right Grant
-
2013
- 2013-12-09 JP JP2013253743A patent/JP5751727B2/ja active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2734341B2 (ja) | 1993-03-26 | 1998-03-30 | 住友電気工業株式会社 | 有機エレクトロルミネッセンス素子 |
| JP3194657B2 (ja) | 1993-11-01 | 2001-07-30 | 松下電器産業株式会社 | 電界発光素子 |
| JPH0848656A (ja) | 1994-02-08 | 1996-02-20 | Tdk Corp | 有機el素子用化合物および有機el素子 |
| WO2004053019A1 (ja) * | 2002-12-12 | 2004-06-24 | Idemitsu Kosan Co., Ltd. | 有機エレクトロルミネッセンス素子用材料及びそれを用いた有機エレクトロルミネッセンス素子 |
| JP2006156445A (ja) * | 2004-11-25 | 2006-06-15 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| JP2007080657A (ja) * | 2005-09-14 | 2007-03-29 | Konica Minolta Holdings Inc | 非水分散液、有機エレクトロルミネッセンス素子、有機エレクトロルミネッセンス素子の製造方法、表示装置及び照明装置 |
| JP2007180147A (ja) * | 2005-12-27 | 2007-07-12 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
Non-Patent Citations (5)
| Title |
|---|
| "28p-A-6 Lecture Preprint", FIFTIETH MEETING OF JAPAN SOCIETY OF APPLIED PHYSICS AND RELATED SOCIETIES,, 2003, pages 1413 |
| "Japan Society of Applied Physics Ninth Workshop Preprint", 2001, pages 55 - 61 |
| "Japan Society of Applied Physics Ninth Workshop Preprint,", 2001, pages 23 - 31 |
| JAPAN SOCIETY OF APPLIED PHYSICS, JOURNAL OF ORGANIC MOLECULES/BIOELECTRONICS SECTION, vol. 11, no. 1, 2000, pages 13 - 19 |
| See also references of EP2246351A4 |
Cited By (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010235575A (ja) * | 2009-03-09 | 2010-10-21 | Konica Minolta Holdings Inc | 含窒素縮合複素環化合物の製造方法 |
| WO2011016202A1 (ja) * | 2009-08-05 | 2011-02-10 | 保土谷化学工業株式会社 | 置換されたアントラセン環構造とピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| JP5636368B2 (ja) * | 2009-08-05 | 2014-12-03 | 保土谷化学工業株式会社 | 置換されたアントラセン環構造とピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| US8927119B2 (en) | 2009-08-05 | 2015-01-06 | Hodogaya Chemical Co., Ltd. | Compound having substituted anthracene ring structure and pyridoindole ring structure, and organic electroluminescent device |
| US9755152B2 (en) | 2009-08-05 | 2017-09-05 | Hodogaya Chemical Co., Ltd. | Compound having substituted anthracene ring structure and pyridoindole ring structure, and organic electroluminescent device |
| JP2011148751A (ja) * | 2010-01-25 | 2011-08-04 | Konica Minolta Holdings Inc | 含窒素縮合複素環化合物の製造方法 |
| WO2013175789A1 (ja) * | 2012-05-24 | 2013-11-28 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子用材料、及びそれを用いた有機エレクトロルミネッセンス素子 |
| JPWO2013175789A1 (ja) * | 2012-05-24 | 2016-01-12 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子用材料、及びそれを用いた有機エレクトロルミネッセンス素子 |
| US9318709B2 (en) | 2012-05-24 | 2016-04-19 | Idemitsu Kosan Co., Ltd. | Material for organic electroluminescence device, and organic electroluminescence device using the same |
| JP2014198696A (ja) * | 2013-03-29 | 2014-10-23 | 出光興産株式会社 | 含窒素芳香族複素環誘導体、有機エレクトロルミネッセンス素子用材料、及び有機エレクトロルミネッセンス素子 |
| CN111718341A (zh) * | 2020-07-10 | 2020-09-29 | 北京燕化集联光电技术有限公司 | 一种含有咔唑环的化合物及其在有机电致发光器件中的应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2246351A1 (en) | 2010-11-03 |
| JP5467873B2 (ja) | 2014-04-09 |
| US8624228B2 (en) | 2014-01-07 |
| EP2246351B1 (en) | 2015-05-06 |
| TW200946527A (en) | 2009-11-16 |
| CN102015703B (zh) | 2015-03-04 |
| JPWO2009102016A1 (ja) | 2011-06-16 |
| EP2246351A4 (en) | 2012-06-13 |
| KR101609397B1 (ko) | 2016-04-05 |
| CN102015703A (zh) | 2011-04-13 |
| TWI429647B (zh) | 2014-03-11 |
| JP5751727B2 (ja) | 2015-07-22 |
| KR20100115763A (ko) | 2010-10-28 |
| JP2014114287A (ja) | 2014-06-26 |
| US20100308322A1 (en) | 2010-12-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5751727B2 (ja) | 置換されたピリジル基が連結したピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 | |
| JP5352447B2 (ja) | 置換されたビピリジル基とピリドインドール環構造がフェニレン基を介して連結した化合物および有機エレクトロルミネッセンス素子 | |
| JP5291463B2 (ja) | 置換されたピリジル基が連結したピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 | |
| WO2011105373A1 (ja) | 置換されたピリジル化合物および有機エレクトロルミネッセンス素子 | |
| WO2010035723A1 (ja) | 置換されたアントラセン環構造とピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 | |
| WO2009096549A1 (ja) | 置換されたピリジル基とピリドインドール環構造がフェニレン基を介して連結した化合物および有機エレクトロルミネッセンス素子 | |
| JPWO2008023628A1 (ja) | ピリジル基で置換されたトリアジン環構造を有する化合物および有機エレクトロルミネッセンス素子 | |
| JP5979873B2 (ja) | ベンゾトリアゾール環構造を有する化合物および有機エレクトロルミネッセンス素子 | |
| EP2463287B1 (en) | Compound having substituted anthracene ring structure and pyridoindole ring structure and organic electroluminescence device | |
| WO2009107651A1 (ja) | 置換されたビピリジル化合物および有機エレクトロルミネッセンス素子 | |
| JP5955228B2 (ja) | 置換されたビピリジル基とピリドインドール環構造を有する化合物および有機エレクトロルミネッセンス素子 | |
| JP2015071619A (ja) | ベンゾピリドインドール誘導体および有機エレクトロルミネッセンス素子 | |
| JP5291340B2 (ja) | 芳香族複素環が結合したオキサジアゾール環構造を有する化合物および有機エレクトロルミネッセンス素子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 200980104982.6 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 09711282 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2009553460 Country of ref document: JP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2009711282 Country of ref document: EP |
|
| ENP | Entry into the national phase |
Ref document number: 20107017979 Country of ref document: KR Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12867556 Country of ref document: US |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |