明 細 書
含窒素複素環化合物
技術分野
[0001] 本発明は、ァセチルー CoAカルボキシラーゼ (本明細書中、 ACCと略記することが ある)阻害作用を有し、肥満症、糖尿病、高血圧症、高脂血症、心不全、糖尿病性合 併症、メタボリックシンドローム、筋肉減少症などの予防 ·治療に有用な含窒素複素 環化合物に関する。
発明の背景
[0002] ACCは、ァセチルー CoAをマロ-ルー CoAに変換する酵素であり、脂肪酸代謝で の律速反応を触媒する。 ACC触媒反応の産物であるマロ-ルー CoAは、カルニチ ンパルミトイルトランスフェラーゼ一 1 (CPT— 1)のフィードバック阻害により、ミトコンド リアの脂肪酸酸化を阻害する。従って、 ACCは肝臓と骨格筋での炭水化物と脂肪酸 利用のノ《ランスを制御するのに、また、肝臓、骨格筋、脂肪組織でのインスリン感受 性を制御するのに鍵となる役割を演ずる。
[0003] ACC阻害によるマロ-ルー CoAレベルの低下は、脂肪酸利用の増加、肝臓による トリダリセライド (TG)豊富なリポ蛋白質 (VLDL)の分泌低下、脾臓によるインスリン分 泌の制御、さら〖こは肝臓、骨格筋、脂肪組織でのインスリン感受性の改善を促し得る
[0004] また、脂肪酸利用を促進し、脂肪酸のデノボ合成を抑制することによって、 ACC阻 害作用を有する化合物の慢性投与は、低脂肪食事を消費する肥満被験体において 、肝臓と脂肪組織の TG含量を激減させ、身体脂肪を選択的に減少させ得る。
[0005] 従って、 ACC阻害作用を有する化合物は、メタボリックシンドローム、肥満症、高血 圧症、糖尿病、ァテローム性動脈硬化と関連する心臓血管系疾患などの予防および 治療に極めて有用である。
[0006] 一方、含窒素複素環化合物としては以下の化合物が報告されて 、る。
ACC阻害作用を有し、メタボリックシンドローム、動脈硬化、糖尿病、肥満などの治 療剤として有用な、式:
[0007] [化 1]
[0008] [式中、 A—:^¾N— CH、 CH—i^^;KJ¾ (CH ) (rは 2— 4の整数を示す。)を; mお
2 r
よび nはそれぞれ 1—3の整数を; Dは CO、 SOを; Eは置換されていてもよい 2— 4環
2
性環などを; Gは CO、 SO、 CR7R8 (R7および R8はそれぞれ水素原子などを示す。 )
2
を; Jは OR
1, NR
2R
3、 CR
4R
5R
6
R
2、 R
5および R
6はそれぞれ水素原子 などを示す。)を示す。]
で表される化合物 (特許文献 1参照)。
特許文献 1:国際公開 03Z072197号パンフレット
[0009] し力しながら、本発明の化合物につ!、ての報告はな!/、。
発明の開示
発明が解決しょうとする課題
[0010] ACC阻害作用を有し、肥満症、糖尿病、高血圧症、高脂血症、心不全、糖尿病性 合併症、メタボリックシンドローム、筋肉減少症などの予防 '治療に有用であり、かつ 薬効、作用時間、特異性、低毒性などの点で優れた性質を有する化合物の開発が 望まれている。
課題を解決するための手段
[0011] 本発明者らは、下記の式
環 Mは、 5または 6員芳香環を;
Wは、 Cまたは Nを;
Kは、置換されて!、てもよ 、メチレン基または置換されて 、てもよ 、イミノ基を;
Rは、水素原子、置換されていてもよい炭化水素基、置換されていてもよいヒドロキシ 基または置換されて ヽてもよ ヽ複素環基を示し;
Tおよび Uは、独立して、水素原子または置換基を示すか、あるいは、 Tおよび Uは、 環 Mとともに、置換されていてもよい二環性環を形成し;
Dおよび Gは、独立してカルボ-ル基またはスルホ -ル基を;
環 Pは、置換されて 、てもよ 、ピペリジンまたは置換されて 、てもよ 、ピペラジンを;
Bは、 CHまたは Nを;
環 Qは、置換されていてもよい単環性環を;
Aは、 C、 CHまたは Nを;
Jは、置換されていてもよい炭化水素基、置換されていてもよい複素環基または置換 されて!/ヽてもよ!/ヽァミノ基を示す。
但し、環 Mの W部分が =N—または— N =である場合、 Uは存在しない。 ]で表され る化合物またはその塩 [以下、化合物 (I)と称することがある。 ]が、優れた ACC阻害 作用を有し、肥満症、糖尿病、高血圧症、高脂血症、心不全、糖尿病性合併症、メタ ボリックシンドローム、筋肉減少症などの予防 '治療に有用であることを初めて見出し た。
この知見に基づいて、本発明者らは、鋭意研究を行い、本発明を完成するに至つ た。即ち、本発明は、
〔1〕上記化合物 (I) ;
〔2〕環 Mが、チォフェン、チアゾールまたはピリジンである、上記化合物 (I); 〔3〕Kが、イミノ基である、上記化合物 (I);
〔4〕Rが、水素原子または置換されていてもよい炭化水素基である、上記化合物 (I); 〔5〕Tが、置換されていてもよいフエ-ル基であり、かつ Uが水素原子である、上記化 合物 (I);
〔6〕Τおよび Uが、環 Μとともに、置換されていてもよい二環性環を形成する、上記化 合物 (I);
〔7〕Dが、カルボニル基である、上記化合物(I);
〔8〕Gが、カルボニル基である、上記化合物(I);
〔9〕環 Pが、ピぺリジンである、上記化合物 (I);
〔10〕環 Q力 それぞれ置換されていてもよい、ピぺリジン、ピぺラジン、モルホリンま たはベンゼンである、上記化合物 (I);
〔11〕 Aが、 Cまたは Nである、上記化合物 (I);
〔 12〕 Jが、置換されて!、てもよ 、複素環基または置換されて 、てもよ 、ァミノ基である 、上記化合物 (I) ;
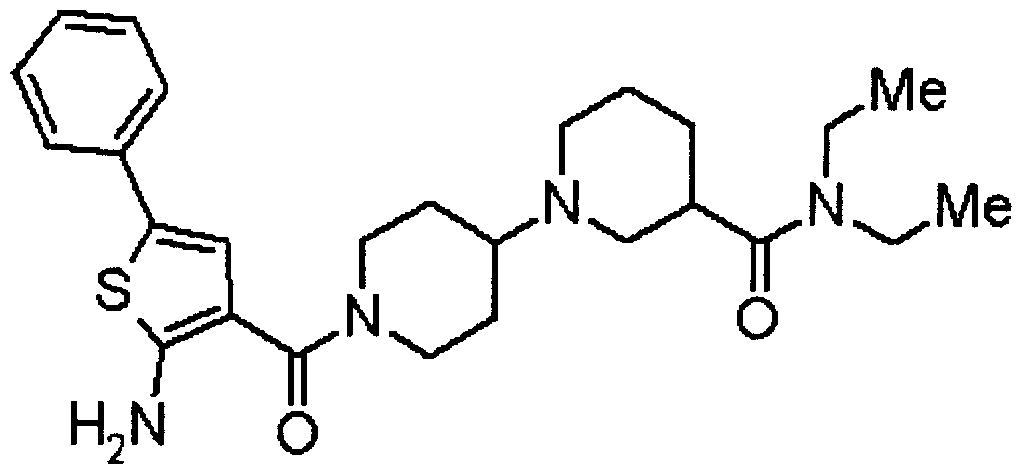
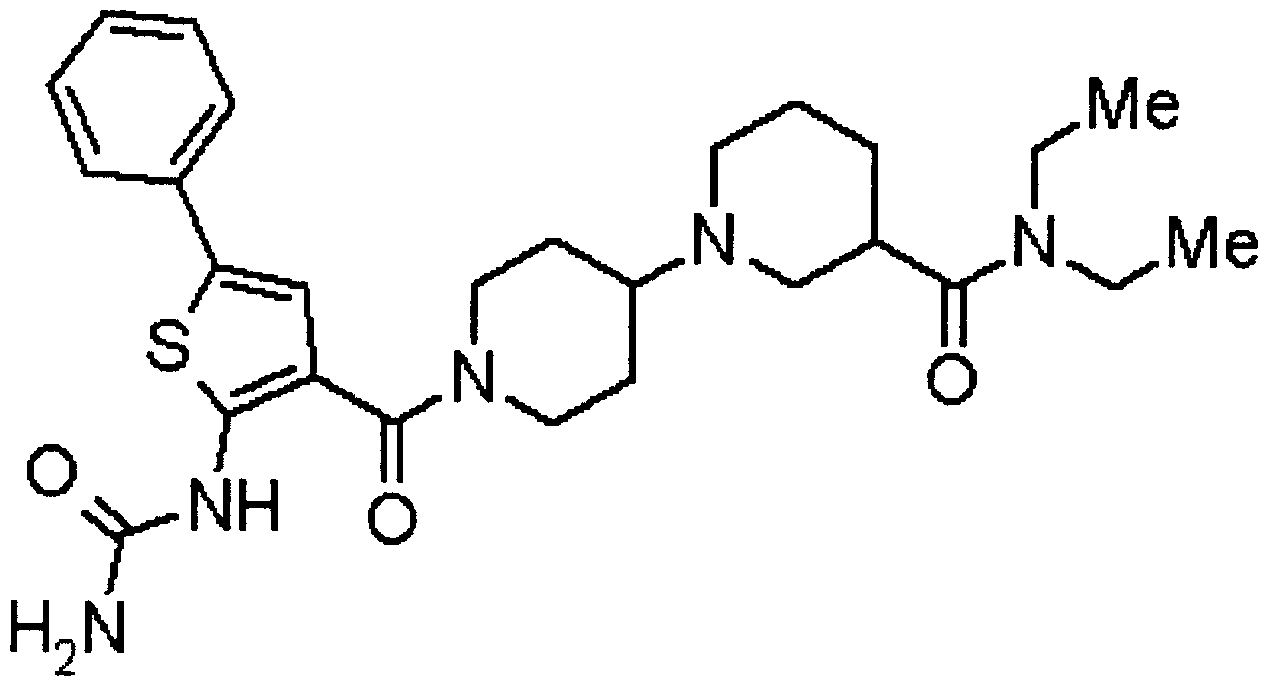
〔13〕 Ν,Ν-ジェチル -1し[(2-{[(ェチルァミノ)カルボ-ル]アミノト 1-ベンゾチォフェン- 3 -ィル)カルボ二ル]- 1 ,4'-ビピペリジン- 3-カルボキサミド;
Ν-ェチル -Ν'- (4- {[3- (モルホリン- 4-ィルカルボ-ル)- 1,4'-ビピペリジン- 1しィル]力 ルポ-ル}-2-フエ-ル- 1 ,3-チアゾール -5-ィル)尿素;
Ν-ェチル -Νし {3- {[(3R)- 3- (モルホリン- 4-ィルカルボ-ル)- 1,4'-ビピペリジン- 1しィ ル]カルボ-ル}-5-[4- (トリフルォロメチル)フエ-ル]- 2-チェ-ル}尿素;
Ν-ェチル -Ν'- (7-メトキシ- 3- {[3- (ピペリジン- 1-ィルカルボ-ル)- 1,4'-ビピペリジン- 1 '-ィル]カルボ-ル}-1-ベンゾチェン- 2-ィル)尿素;または
Ν-ェチル -1'-[(2-{ [(ェチルァミノ)カルボ-ル]アミノト 6-メチルチエノ [2,3-b]ピリジン- 3-ィル)カルボ二ル]- N-イソプロピル- 1 ,4'-ビピペリジン- 3-カルボキサミド; あるいはその塩である、上記化合物 (I);
〔14〕上記化合物 (I)のプロドラッグ;
〔15〕上記化合物(I)またはそのプロドラッグを含有してなるァセチルー CoAカルボキ シラーゼ阻害剤;
〔16〕上記化合物 (I)またはそのプロドラッグを含有してなる医薬;
〔17〕肥満症、糖尿病、高血圧症、高脂血症、心不全、糖尿病性合併症、メタボリック シンドロームまたは筋肉減少症の予防.治療剤である上記〔16〕の医薬;
〔18〕ァセチルー CoAカルボキシラーゼ阻害剤を製造するための、上記化合物 (I)ま たはそのプロドラッグの使用;
〔19〕肥満症、糖尿病、高血圧症、高脂血症、心不全、糖尿病性合併症、メタボリック シンドロームまたは筋肉減少症の予防 ·治療剤を製造するための、上記化合物 (I)ま たはそのプロドラッグの使用;
〔20〕上記化合物 (I)またはそのプロドラッグを哺乳動物に投与することを特徴とする
、該哺乳動物におけるァセチルー CoAカルボキシラーゼの阻害方法;
〔21〕上記化合物 (I)またはそのプロドラッグを哺乳動物に投与することを特徴とする
、該哺乳動物における肥満症、糖尿病、高血圧症、高脂血症、心不全、糖尿病性合 併症、メタボリックシンドロームまたは筋肉減少症の予防または治療方法、 などに関する。
[0014] 以下、式 (I)中の各記号の定義につ!、て詳述する。
なお、本明細書中、「ハロゲン原子」は、特に断りのない限り、フッ素、塩素、臭素お よびヨウ素を意味する。
Jで示される「置換されて 、てもよ 、炭化水素基」の「炭化水素基」としては、例えば 、C アルキル基、 C アルケニル基、 C アルキニル基、 C シクロアルキル
1-10 2- 10 2-10 3-10
基、 C シクロアルケニル基、 c シクロアルカジエニル基、 c 芳香族炭化水
3-10 4-10 6-14 素基、 C ァラルキル基、 C 芳香族炭化水素アルケニル基、 C シクロアルキ
7-13 8-13 3- 10
ルー C アルキル基などが挙げられる。
1 -6
[0015] ここで、 C アルキル基としては、例えば、メチル、ェチル、プロピル、イソプロピル
1- 10
、ブチル、イソブチル、 sec ブチル、 tert ブチル、ペンチル、イソペンチル、ネオ ペンチル、 1 ェチルプロピル、へキシル、イソへキシル、 1, 1ージメチルブチル、 2, 2 ジメチルブチル、 3, 3 ジメチルブチル、 2 ェチルブチル、ヘプチル、ォクチル
、ノニル、デシルなどが挙げられる。
C ァルケ-ル基としては、例えば、ェテュル、 1—プロべ-ル、 2—プロべ-ル、
2-10
2—メチルー 1 プロぺニル、 1ーブテニル、 2 ブテニル、 3 ブテニル、 3 メチル 2 ブテニノレ、 1 ペンテ二ノレ、 2 ペンテ二ノレ、 3 ペンテ二ノレ、 4 ペンテ二ノレ、 4—メチノレ一 3 ペンテ-ノレ、 1—へキセ-ノレ、 3 へキセ-ノレ、 5 へキセ-ノレ、 1— ヘプテニル、 1—オタテュルなどが挙げられる。
C アルキ-ル基としては、例えば、ェチュル、 1 プロビュル、 2—プロビュル、 1
2- 10
ブチニノレ、 2 ブチニル、 3 ブチニル、 1 ペンチニル、 2 ペンチニル、 3 ぺ ンチュル、 4 ペンチ-ル、 1—へキシュル、 2 へキシュル、 3 へキシュル、 4 へ キシニル、 5 へキシュル、 1一へプチ-ル、 1ーォクチ-ルなどが挙げられる。
C シクロアルキル基としては、例えば、シクロプロピル、シクロブチル、シクロペン
3- 10
チル、シクロへキシル、シクロへプチル、シクロォクチル、ビシクロ [2. 2. 1]ヘプチル 、ビシクロ [2. 2. 2]ォクチル、ビシクロ [3. 2. 1]ォクチル、ビシクロ [3. 2. 2]ノエル、 ビシクロ [3. 3. 1]ノ-ル、ビシクロ [4. 2. 1]ノ-ル、ビシクロ [4. 3. 1]デシル、ァダ マンチルなどが挙げられる。
C シクロアルケ-ル基としては、例えば、 2 シクロペンテン一 1—ィル、 3 シク
3- 10
口ペンテン一 1—ィル、 2 シクロへキセン一 1—ィル、 3 シクロへキセン一 1—ィル などが挙げられる。
C シクロアルカジエ-ル基としては、例えば、 2, 4ーシクロペンタジェンー 1ーィ
4- 10
ル、 2, 4 シクロへキサジェン 1 ィル、 2, 5 シクロへキサジェン 1ーィルなど が挙げられる。
C 芳香族炭化水素基としては、例えば、フエニル、ナフチル、アントリル、フエナ
6- 14
ントリル、ァセナフチレ-ル、ビフエ-リルなどが挙げられる。なかでもフエ-ル、 1—ナ フチル、 2—ナフチルなどが好ましい。
C ァラルキル基としては、例えば、ベンジル、フエネチル、ナフチルメチル、ビフ
7- 13
ェ-リルメチルなどが挙げられる。
C 芳香族炭化水素アルケニル基としては、例えば、スチリルなどが挙げられる。
8- 13
C シクロアルキル—C アルキル基としては、例えば、シクロへキシルメチルな
どが挙げられる。
上記した C アルキル基、 C ァルケ-ル基および C アルキ-ル基は、置換
1 - 10 2- 10 2- 10
可能な位置に 1な 、し 3個の置換基を有して 、てもよ 、。
このような置換基としては、例えば、
( 1) C シクロアルキル基(例、シクロプロピル、シクロへキシル);
3- 10
(2) 1〜3個のハロゲン原子で置換されていてもよい C アルキル基(例、メチル、ェ
1 -6
チル)、ヒドロキシ基、 C アルコキシ基 (例、メトキシ、エトキシ)、カルボキシル基およ
1 -6
びハロゲン原子から選ばれる 1な 、し 3個の置換基で置換されて!/、てもよ!/、C 芳
6- 14 香族炭化水素基 (例、フエ-ル、ナフチル);
(3) 1〜3個のハロゲン原子で置換されていてもよい C アルキル基(例、メチル、ェ
1 -6
チル)、ヒドロキシ基、 C アルコキシ基 (例、メトキシ、エトキシ)、カルボキシル基およ
1 -6
びハロゲン原子力も選ばれる 1な 、し 3個の置換基で置換されて 、てもよ 、芳香族複 素環基 (例、チェニル、フリル、ピリジル、ォキサゾリル、チアゾリル、テトラゾリル、ォキ サジァゾリル、ピラジニル、キノリル、インドリル);
(4) 1〜3個のハロゲン原子で置換されていてもよい C アルキル基(例、メチル、ェ
1 -6
チル)、ヒドロキシ基、 C アルコキシ基 (例、メトキシ、エトキシ)、ォキソ基、カルボキ
1 -6
シル基およびノヽロゲン原子力も選ばれる 1な 、し 3個の置換基で置換されて 、てもよ い非芳香族複素環基 (例、テトラヒドロフリル、モルホリニル、チオモルホリニル、ピペリ ジニル、ピロリジニル、ピぺラジュル、ジォキソリル、ジォキソラニル、 1, 3 ジヒドロー 2—ベンゾフラニル、チアゾリジェニル);
(5) C アルキル基(例、メチル、ェチル)、 C アルキル カルボ-ル基(例、ァセ
1 -6 1 -6
チル、イソブタノィル、イソペンタノィル)、 C アルコキシ カルボ-ル基(例、メトキ
1 -6
シカノレボニノレ、エトキシカルボニル、プロポキシカノレボニノレ、 tert ブトキシカルボ二 ル)および C アルキル基でモノまたはジ置換されて!、てもよ!/、力ルバモイル基(例、
1 -6
メチルカルバモイル、ェチルカルバモイル)力 選ばれる置換基でモノまたはジ置換 されていてもよいアミノ基;
(6) C アルキルスルホ -ルァミノ基(例、メチルスルホ -ルァミノ);
1 -6
(7)アミジノ基;
(8) 1〜3個のハロゲン原子で置換されていてもよい C アルキル カルボ-ル基(
1 -6
例、ァセチノレ、イソブタノイノレ、イソペンタノィノレ);
(9) 1〜3個のハロゲン原子で置換されていてもよい C アルコキシ カルボ-ル基
1 -6
(例、メトキシカルボ-ル、エトキシカルボ-ル、プロポキシカルボ-ル、 tert—ブトキ シカルボ-ル);
(10) 1〜3個のハロゲン原子で置換されて!ヽてもよい C アルキルスルホニル基(例
1 -6
ゝメチノレスノレホ-ノレ);
(11) 1〜3個のハロゲン原子で置換されて! 、てもよ 、c アルキル基(例、メチル、
1 -6
ェチル)でモノまたはジ置換されて!、てもよ!/ヽカルバモイル基;
(12) 1〜3個のハロゲン原子で置換されて! 、てもよ 、c アルキル基(例、メチル、
1 -6
ェチル)でモノまたはジ置換されて!、てもよ!/ヽチォ力ルバモイル基;
(13) 1〜3個のハロゲン原子で置換されて! 、てもよ 、c アルキル基(例、メチル、
1 -6
ェチル)でモノまたはジ置換されて!、てもよ!/ヽスルファモイル基;
(14)カルボキシル基;
(15)ヒドロキシ基;
(16) 1〜3個のハロゲン原子で置換されて! 、てもよ 、c アルコキシ基 (例、メトキシ
1 -6
、エトキシ);
(17) 1〜3個のハロゲン原子で置換されて! 、てもよ!/ヽ C アルケニルォキシ基(例、 エテュノレ才キシ);
(18) C シクロアルキルォキシ基(例、シクロへキシルォキシ);
3- 10
( 19) C ァラルキルォキシ基(例、ベンジルォキシ);
7- 13
(20) C 芳香族炭化水素ォキシ基 (例、フエ-ルォキシ、ナフチルォキシ);
6- 14
(21) C アルキル カルボ-ルォキシ基(例、ァセチルォキシ、 tert ブチルカル
1 -6
ボニノレ才キシ);
(22)チオール基;
(23) 1〜3個のハロゲン原子で置換されていてもよい C アルキルチオ基(例、メチ
1 -6
ノレチォ、ェチノレチォ);
(24) C ァラルキルチオ基 (例、ベンジルチオ);
(25) C 芳香族炭化水素チォ基 (例、フエ-ルチオ、ナフチルチオ);
6-14
(26)スルホ基;
(27)シァノ基;
(28)アジド基;
(29)ニトロ基;
(30)二トロソ基;
(31)ハロゲン原子;
( 32) C アルキルスルフィエル基(例、メチルスルフィ -ル);
1-6
(33)ォキソ基;
などが挙げられる。
[0018] また、上記「炭化水素基」として例示した、 C シクロアルキル基、 C シクロアル
3-10 3-10 ケ-ル基、 C シクロアルカジエ-ル基、 C 芳香族炭化水素基、 C ァラルキ
4- 10 6-14 7-13 ル基、 c 芳香族炭化水素アルケニル基および C シクロアルキル C アルキ
8-13 3-10 1-6 ル基は、置換可能な位置に 1な 、し 3個の置換基を有して 、てもよ 、。
このような置換基としては、例えば、
(1)上記した C アルキル基等における置換基として例示した置換基;
1-10
(2)ハロゲン原子、カルボキシル基、 C アルコキシ カルボ-ル基(例、メトキシカ
1-6
ルポ-ル、エトキシカルボ-ル)および力ルバモイル基から選ばれる 1ないし 3個の置 換基で置換されて 、てもよ 、C アルキル基(例、メチル、ェチル);
1- 6
(3)ハロゲン原子、カルボキシル基、 C アルコキシ カルボ-ル基(例、メトキシカ
1-6
ルポ-ル、エトキシカルボ-ル)および力ルバモイル基から選ばれる 1ないし 3個の置 換基で置換されて 、てもよ ヽ C ァルケ-ル基(例、ェテュル、 1—プロべ-ル);
2- 6
(4) 1〜3個のハロゲン原子で置換されていてもよい C アルキル基、ヒドロキシ基、
1 -6
C アルコキシ基およびノヽロゲン原子力 選ばれる 1ないし 3個の置換基で置換され
1 -6
ていてもよい C ァラルキル基(例、ベンジル);
7-13
などが挙げられる。
[0019] Jで示される「置換されて 、てもよ 、複素環基」における「複素環基」としては、「芳香 族複素環基」および「非芳香族複素環基」が挙げられる。
該芳香族複素環基としては、例えば、環構成原子として炭素原子以外に酸素原子
、硫黄原子および窒素原子力 選ばれるヘテロ原子を 1な 、し 4個含有する 5〜7員 の単環式芳香族複素環基および縮合芳香族複素環基が挙げられる。該縮合芳香族 複素環基としては、例えば、これら 5〜7員の単環式芳香族複素環基と、 1ないし 2個 の窒素原子を含む 5または 6員の芳香族複素環 (例、ピロール、イミダゾール、ピラゾ ール、ピラジン、ピリジン、ピリミジン)、 1個の硫黄原子を含む 5員の芳香族複素環( 例、チォフェン)およびベンゼン環力 選ばれる 1または 2個が縮合した環力 誘導さ れる基等が挙げられる。
芳香族複素環基の好適な例としては、
フリル(例、 2 フリル、 3 フリル)、チェ-ル(例、 2 チェ-ル、 3 チェ-ル)、ピリ ジル(例、 2 ピリジル、 3 ピリジル、 4 ピリジル)、ピリミジ-ル(例、 2 ピリミジ -ル 、 4 ピリミジ -ル、 5—ピリミジ -ル、 6—ピリミジ -ル)、ピリダジ-ル(例、 3—ピリダジ -ル、 4 ピリダジ-ル)、ビラジ-ル(例、 2 ピラジ -ル)、ピロリル(例、 1 ピロリル 、 2 ピロリル、 3 ピロリル)、イミダゾリル(例、 1 イミダゾリル、 2 イミダゾリル、 4— イミダゾリル、 5—イミダゾリル)、ピラゾリル(例、 1—ピラゾリル、 3 ピラゾリル、 4 ピ ラゾリル)、チアゾリル(例、 2 チアゾリル、 4 チアゾリル、 5 チアゾリル)、イソチア ゾリル(例、 4 イソチアゾリル)、ォキサゾリル(例、 2—ォキサゾリル、 4 ォキサゾリ ル、 5—ォキサゾリル)、イソォキサゾリル、ォキサジァゾリル(例、 1, 2, 4ーォキサジ ァゾールー 5 ィル、 1, 3, 4 ォキサジァゾ一ルー 2 ィル)、チアジアゾリル(例、 1 , 3, 4 チアジアゾール—2—ィル)、トリァゾリル(例、 1, 2, 4 トリァゾール— 1—ィ ル、 1, 2, 4 卜リアゾール—3—ィル、 1, 2, 3 卜リアゾール—1—ィル、 1, 2, 3 卜 リアゾールー 2 ィル、 1, 2, 3 トリァゾール— 4—ィル)、テトラゾリル(例、テトラゾ ール— 1—ィル、テトラゾール— 5—ィル)、トリアジ-ル(例、 1, 2, 4 トリァゾール—
1—ィル、 1, 2, 4 トリァゾール— 3—ィル)などの単環式芳香族複素環基; キノリル(例、 2 キノリル、 3 キノリル、 4 キノリル、 6 キノリル)、イソキノリル(例、 3 イソキノリル)、キナゾリル(例、 2 キナゾリル、 4 キナゾリル)、キノキサリル(例、
2 キノキサリル、 6 キノキサリル)、ベンゾフリル(例、 2 べンゾフリル、 3 べンゾ フリル)、ベンゾチェ-ル(例、 2 べンゾチェ-ル、 3 べンゾチェ-ル)、ベンゾォキ
サゾリル(例、 2—べンゾォキサゾリル)、ベンズイソォキサゾリル(例、 7—べンズイソォ キサゾリル)、ベンゾチアゾリル(例、 2—べンゾチアゾリル)、ベンズイミダゾリル(例、 ベンズイミダゾールー 1 ィル、ベンズイミダゾールー 2—ィル、ベンズイミダゾールー 5—ィル)、ベンゾトリァゾリル(例、 1H— 1 , 2, 3 ベンゾトリアゾール—5—ィル)、ィ ンドリル(例、インドールー 1 ィル、インドールー 2 ィル、インドールー 3 ィル、ィ ンドール 5 ィル)、インダゾリル(例、 1H—インダゾールー 3 ィル)、ピロロビラジ -ル(例、 1H ピロ口 [2, 3— b]ピラジン一 2—ィル、 1H ピロ口 [2, 3— b]ピラジン 6 ィル)、イミダゾピリジ-ル(例、 1H—イミダゾ [4, 5—b]ピリジンー2 ィル、 1H —イミダゾ [4, 5— c]ピリジン一 2—ィル、 2H—イミダゾ [ 1 , 2— a]ピリジン一 3—ィル )、イミダゾピラジュル(例、 1H—イミダゾ [4, 5—b]ピラジンー2 ィル)、ビラゾロピリ ジ-ル(例、 1H ピラゾ口 [4, 3— c]ピリジン 3 ィル)、ビラゾロチェ-ル(例、 2H —ビラゾロ [3, 4— b]チォフェン一 2—ィル)、ビラゾロトリアジ-ル(例、ピラゾ口 [5, 1 — c] [ l , 2, 4]トリァジン一 3—ィル)、チェノビリジ-ル(例、チエノ [2, 3— b]ピリジン 3—ィル)などの縮合芳香族複素環基;などが挙げられる。
該非芳香族複素環基としては、例えば、環構成原子として炭素原子以外に酸素原 子、硫黄原子および窒素原子力 選ばれるヘテロ原子を 1な 、し 4個含有する 5〜7 員の単環式非芳香族複素環基および縮合非芳香族複素環基が挙げられる。該縮合 非芳香族複素環基としては、例えば、これら 5〜7員の単環式非芳香族複素環基と、 1ないし 2個の窒素原子を含む 5または 6員の芳香族複素環 (例、ピロール、イミダゾ ール、ピラゾール、ピラジン、ピリジン、ピリミジン)、 1個の硫黄原子を含む 5員の芳香 族複素環 (例、チォフェン)およびベンゼン環力 選ばれる 1または 2個の環が縮合し た環から誘導される基、ならびに該基の部分飽和により得られる基等が挙げられる。 非芳香族複素環基の好適な例としては、ピロリジ -ル (例、 1 ピロリジニル)、ピぺ リジ-ル(例、ピペリジノ)、モルホリニル(例、モルホリノ)、チオモルホリニル(例、チォ モルホリノ)、ピペラジ-ル(例、 1ーピペラジ-ル)、へキサメチレンイミ-ル(例、へキ サメチレンイミンー 1ーィル)、ォキサゾリジ-ル(例、ォキサゾリジン 3 ィル)、チア ゾリジ-ル(例、チアゾリジン ィル)、イミダゾリジ-ル(例、イミダゾリジン 3ーィ ル)、ジォキソリル(例、 1 , 3 ジォキソールー 4 ィル)、ジォキソラ-ル(例、 1 , 3—
ジォキソランー4 ィル)、ジヒドロォキサジァゾリル(例、 4, 5 ジヒドロー 1, 2, 4 ォキサジァゾ一ルー 3 ィル)、 2 チォキソー 1, 3 ォキサゾリジン 5 ィル、テト ラヒドロビラニル (例、 4—テトラヒドロビラ-ル)などの単環式非芳香族複素環基; ジヒドロイソインドリル(例、 1, 3 ジヒドロ一 2H—イソインドール一 2—ィル)、 4, 5, 6 , 7—テトラヒドロ一 1—ベンゾフラ-ル(例、 4, 5, 6, 7—テトラヒドロ一 1—ベンゾフラ ン— 3—ィル)、4, 5, 6, 7—テトラヒドロ 1—ベンゾチェ-ル(例、 4, 5, 6, 7—テト ラヒドロ一 1—ベンゾチォフェン一 3—ィル)、インダ-ル(例、インダン一 5—ィル)、ク ロメ-ル(例、 4H クロメン一 2—ィル、 2H クロメン一 3—ィル)、ジヒドロイソキノリニ ル(例、 1, 2 ジヒドロイソキノリン一 4—ィル)、テトラヒドロイソキノリニル(例、 1, 2, 3 , 4—テトラヒドロイソキノリン一 4—ィル)、ジヒドロフタラジュル(例、 1, 4 ジヒドロフタ ラジン 4 ィル)、ビラゾリジ-ル(例、ビラゾリジン 1 ィル)、テトラヒドロキノリニ ル (例、 1, 2, 3, 4—テトラヒドロキノリン— 4—ィル)などの縮合非芳香族複素環基; などが挙げられる。
Jで示される「置換されて 、てもよ 、複素環基」における「複素環基」は、置換可能な 位置に 1ないし 3個の置換基を有していてもよい。このような置換基としては、例えば、 上言 6Jで示される「置換されて 、てもよ 、炭化水素基」の「炭化水素基」として例示した C シクロアルキル基が有して 、てもよ 、置換基として例示したものが挙げられる。
3- 10
Jで示される「置換されて 、てもよ 、複素環基」としては、 1〜3個のハロゲン原子で 置換されていてもよい C アルキル基および C シクロアルキル基力 選ばれる 1
1 -6 3- 10
または 2個の置換基で置換されて 、てもよ 、含窒素非芳香族複素環基 (例、ピロリジ -ル、イミダゾリジ -ル、ビラゾリジ-ル、ピベリジ-ル、ピぺラジュル、モルホリニル、 チオモルホリニル、テトラヒドロキノリニル、テトラヒドロイソキノリニル)などが好ましい。 Jで示される「置換されていてもよいアミノ基」としては、例えば、それぞれ置換されて いてもよい、 C アルキル基、 C ァルケ-ル基、 C シクロアルキル基、 C
1— 10 2— 10 3— 10 3— 10 シクロアルケニル基、 c 芳香族炭化水素基、 C ァラルキル基および C 芳
6 - 14 7- 13 8- 13 香族炭化水素ァルケ-ル基など力 選ばれる 1または 2個の置換基で置換されてい てもよ 、ァミノ基が挙げられる。
ここで、 C アルキル基、 C ァルケ-ル基、 C シクロアルキル基、 C シク
ロアルケニル基、 C 芳香族炭化水素基、 C ァラルキル基および C 芳香族
6- 14 7- 13 8- 13 炭化水素ァルケ-ル基としては、それぞれ上言 ejで示される「置換されて 、てもよ 、炭 化水素基」における「炭化水素基」として例示したものが挙げられる。
[0022] これらの C アルキル基、 C アルケニル基、 C シクロアルキル基、 C シ
1 - 10 2- 10 3- 10 3- 10 クロアルケニル基、 c 芳香族炭化水素基、 C ァラルキル基および C 芳香
6- 14 7- 13 8- 13 族炭化水素ァルケ-ル基は、それぞれ置換可能な位置に 1な 、し 3個の置換基を有 していてもよい。このような置換基としては、例えば、
ハロゲン原子;
C アルコキシ カルボ-ル基(例、メトキシカルボ-ル、エトキシカルボ-ル、 tert
1 -6
ブトキシカルボニル);
C アルキル カルボ-ル基;
1 -6
シァノ基;
C アルキル基(例、メチル、ェチル、プロピル、イソプロピル、ネオペンチル)でモ
1 - 10
ノまたはジ置換されて 、てもよ 、力ルバモイル基;
ヒドロキシ基;
カルボキシル基;
等が挙げられる。
[0023] Jで示される「置換されていてもよいアミノ基」は、好ましくは、 1〜3個のハロゲン原子 で置換されて 、てもよ 、C アルキル基(例、メチル、ェチル、プロピル、イソプロピ
1 -6
ル)および C シクロアルキル基(例、シクロペンチル、シクロへキシル、ァダマンチ
3- 10
ル)力も選ばれる置換基でモノまたはジ置換されて 、てもよ 、ァミノ基などである。
[0024] Jとしては、「置換されて 、てもよ 、ァミノ基」および「置換されて 、てもよ 、複素環基 」が好ましぐさらに、
1)それぞれ 1〜3個のハロゲン原子で置換されていてもよい C アルキル基および
1 -6
C シクロアルキル基力 選ばれる置換基でモノまたはジ置換されて!、てもよ!/、アミ
3- 10
ノ基;
2)それぞれ 1〜3個のハロゲン原子で置換されて!、てもよ!/、C アルキル基および
1 -6
C シクロアルキル基力 選ばれる 1または 2個の置換基で置換されていてもよい含
窒素非芳香族複素環基 (例、ピロリジニル、イミダゾリジニル、ビラゾリジ -ル、ピベリジ ニル、ピペラジニル、モルホリニル、チォモルホリニル、テトラヒドロキノリニル、テトラヒ ドロイソキノリニル)などが好まし 、。
[0025] 環 Mで示される「5または 6員芳香環」としては、例えば、 5または 6員の芳香族炭化 水素、 5または 6員の芳香族複素環などが挙げられる。ここで、 5または 6員の芳香族 炭化水素としては、例えば、 Jで示される「置換されて 、てもよ 、炭化水素基」の「炭化 水素基」として例示した C 芳香族炭化水素基に対応する C 芳香族炭化水素
6-14 6- 14
のうち 5または 6員のもの(例、ベンゼン環)などが好ましい。 5または 6員の芳香族複 素環としては、例えば、上言 6Jで示される「置換されていてもよい複素環基」における「 複素環基」として例示した「芳香族複素環基」に対応する芳香族複素環のうち 5また は 6員環であるものが挙げられ、なかでも、フラン、チォフェン、チアゾール、ォキサゾ ール、イミダゾール、トリァゾール、ピラゾール、ピリミジン、ピリジンなどが好ましぐチ オフヱン、チアゾール、ピリジンなどが好ましぐチォフェンが最も好ましい。
[0026] Kで表される「置換されて!、てもよ!/、メチレン基または置換されて 、てもよ 、ィミノ基
」が有していてもよい「置換基」としては、例えば、前言 ejで示される「置換されていても よいアミノ基」における置換基として例示した、「それぞれ置換されていてもよい、 c アルキル基、 c ァルケ-ル基、 c シクロアルキル基、 c シクロアルケ-ル
0 2-10 3-10 3-10
基、 C 芳香族炭化水素基、 C ァラルキル基および C 芳香族炭化水素アル
6-14 7-13 8- 13
ケニル基」が挙げられる。
Kは、好ましくはィミノ基(— NH— )である。
[0027] Rで表される「置換されて 、てもよ 、炭化水素基」および「置換されて 、てもよ!/、複 素環基」としては、例えば、上言 ejで示される「置換されていてもよい炭化水素基」およ び「置換されていてもよい複素環基」として例示したものがそれぞれ挙げられる。
Rで表される「置換されて 、てもよ 、ヒドロキシ基」が有して 、てもよ 、「置換基」とし ては、例えば、前言 ejで示される「置換されていてもよいアミノ基」における置換基とし て例示した、「それぞれ置換されていてもよい、 c アルキル基、 アルケニル
1-10 c 2-10
基、 C シクロアルキル基、 C シクロアルケニル基、 C 芳香族炭化水素基、 C
3-10 3-10 6-14
ァラルキル基および C 芳香族炭化水素アルケニル基」が挙げられる。
Rは好ましくは水素原子、置換されて ヽてもよ ヽ炭化水素基 (好ましくはじ アルキ
1-6 ル)などである。
[0028] Tおよび Uで表される「置換基」としては、例えば、上言 6Jで示される「置換されて!、て もよ 、炭化水素基」の「炭化水素基」として例示した c シクロアルキル基が有して
3-10
いてもよい置換基として例示したものがそれぞれ挙げられる。該置換基は、好ましくは
(1) 1〜3個のハロゲン原子で置換されていてもよい C アルキル基、ヒドロキシ基、
1 -6
C アルコキシ基、カルボキシル基、ハロゲン原子および C アルキルスルホニル
1 -6 1-6
基力も選ばれる 1な 、し 3個の置換基で置換されて 、てもよ 、C 芳香族炭化水素
6-14
基 (好ましくはフエ二ル);
(2) 1〜3個のハロゲン原子で置換されていてもよい C アルキル基、ヒドロキシ基、
1 -6
C アルコキシ基、カルボキシル基およびハロゲン原子から選ばれる 1ないし 3個の
1 -6
置換基で置換されて 、てもよ 、芳香族複素環基 (好ましくはピリジル);
(3)ハロゲン原子、カルボキシル基、 C アルコキシ カルボ-ル基およびカルバモ
1-6
ィル基力も選ばれる 1な 、し 3個の置換基で置換されて!、てもよ!/、C アルキル基;
1-6
(4) 1〜3個のハロゲン原子で置換されていてもよい C アルキル カルボ-ル基;
1 -6
などである。
[0029] Tおよび Uが環 Mとともに形成する「置換されて 、てもよ 、二環性環」の「二環性環」 としては、例えば、 ω上言 ejで示される「置換されていてもよい複素環基」における「複 素環基」として例示した「縮合芳香族複素環基」に対応する環のうち、 5または 6員芳 香環を含む二環性環であるもの、(ii)上言 ejで示される「置換されて 、てもよ ヽ複素環 基」における「複素環基」として例示した「非芳香族複素環基」に対応する環のうち、 5 または 6員芳香環を含む二環性環であるもの、 (iii)上言 ejで示される「置換されて 、て もよい炭化水素基」として挙げた C シクロアルキル基、 C シクロアルケニル基、
3-10 3-10
C シクロアルカジエ-ル基および C 芳香族炭化水素基から選ばれる 1つの基
4-10 6-14
に対応する環と、 1つの 5または 6員芳香環とが縮合して形成する二環性環などが挙 げられる。ここで、「5または 6員芳香環」としては、前記環 Mとして例示したものが挙げ られる。
該「二環性環」としては、例えば、キノリン、イソキノリン、キナゾリン、キノキサリン、ベ ンゾフラン、ベンゾチォフェン、ベンズォキサゾール、ベンズイソォキサゾール、ベン ゾチアゾール、ベンズイミダゾール、ベンゾトリアゾール(例、 1H—1, 2, 3—べンゾト リアゾール)、インドール、インダゾール、ピロロビラジン(例、 1H—ピロ口 [2, 3—b]ピ ラジン、 1H—ピロ口 [2, 3— b]ピラジン)、イミダゾピリジン(例、 1H—イミダゾ [4, 5— b]ピリジン、 1H—イミダゾ [4, 5— c]ピリジン、 2H—イミダゾ [1, 2— a]ピリジン)、イミ ダゾピラジン(例、 1H—イミダゾ [4, 5— b]ピラジン)、ピラゾ口ピリジン(例、 1H—ビラ ゾロ [4, 3— c]ピリジン)、チェノビリジン(例、チエノ [2, 3— b]ピリジン)、ビラゾロチ 才フェン 列、 2H—ピラゾ口 [3, 4—b]チ才フェン)、ピラゾロトリアジン(f列、ピラゾ口 [
5. 1 - c] [l, 2, 4]トリアジン)、 4, 5, 6, 7—テトラヒドロ— 1—ベンゾフラン、 4, 5, 6 , 7—テトラヒドロ一 1—ベンゾチォフェン、インダン、クロメン、ジヒドロイソキノリン(例、
1. 2—ジヒドロイソキノリン)、テトラヒドロイソキノリン (例、 1, 2, 3, 4ーテトラヒドロイソ キノリン)、ジヒドロフタラジン(例、 1, 4ージヒドロフタラジン)、ビラゾリジン、テトラヒドロ キノリン (例、 1, 2, 3, 4—テトラヒドロキノリン)、ナフタレン、インデンなどが挙げられ、 好ましくはベンゾチォフェン、 4, 5, 6, 7—テトラヒドロベンゾチォフェン、チェノビリジ ンなどである。
上記「置換されて 、てもよ 、二環性環」が有して!/、てもよ 、「置換基」としては、例え ば、上言 6Jで示される「置換されて 、てもよ 、炭化水素基」における「炭化水素基」とし て例示した C シクロアルキル基が有して 、てもよ 、置換基として例示したものが挙
3- 10
げられる。
該置換基は、好ましくはォキソ、 C アルキル基、 C アルコキシ基などである。
1 -6 1 -6
好ましくは、 Tおよび Uは、独立して、
(1)水素原子;
(2)置換基 (好ましくは、 1〜3個のハロゲン原子で置換されていてもよい C アルキ
1 - 6 ル基、ヒドロキシ基、 C アルコキシ基、カルボキシル基、ハロゲン原子および C ァ
1 -6 1 -6 ルキルスルホニル基から選ばれる 1な!/、し 3個の置換基)で置換されて!/、てもよ!/、C
6- 芳香族炭化水素基 (好ましくはフ ニル);
14
(3)置換基 (好ましくは、 1〜3個のハロゲン原子で置換されていてもよい C アルキ
ル基、ヒドロキシ基、 C アルコキシ基、カルボキシル基およびノヽロゲン原子力 選
1 -6
ばれる 1な 、し 3個の置換基)で置換されて 、てもよ 、芳香族複素環基 (好ましくはピ リジル);または
(4)置換基 (好ましくは、ハロゲン原子、カルボキシル基、 C アルコキシ カルボ-
1 -6
ル基および力ルバモイル基カも選ばれる 1な 、し 3個の置換基)で置換されて ヽても よい C アルキル基;
1 -6
を示すか、
あるいは、 Tおよび Uは、環 Mとともに、置換基 (好ましくは、ォキソ、 C アルキル基
1 -6
および C アルコキシ基力も選ばれる 1な!、し 3個の置換基)で置換されて!、てもよ
1 -6
い二環性環(好ましくはベンゾチォフェン、 4, 5, 6, 7—テトラヒドロベンゾチォフェン 、チェノビリジン)を形成する。
Tおよび Uの好適な組み合わせとしては、
1) Tが、置換基 (好ましくは、 1〜3個のハロゲン原子で置換されていてもよい C 了
1 -6 ルキル基、ヒドロキシ基、 C アルコキシ基、カルボキシル基、ハロゲン原子および C
1 -6
アルキルスルホニル基から選ばれる 1な!/、し 3個の置換基)で置換されて!/、てもよ
1 -6
いじ 芳香族炭化水素基 (好ましくはフ ニル)であり、かつ、 uが、水素原子ある
6- 14
いは C アルキル (好ましくは、水素原子)である場合;
1 -6
2) Τおよび Uが、環 Μとともに、置換基 (好ましくは、ォキソ、 C アルキル基および C
1 -6
アルコキシ基力も選ばれる 1な 、し 3個の置換基)で置換されて 、てもよ 、二環性
1 -6
環(好ましくは、ベンゾチォフェン、 4, 5, 6, 7—テトラヒドロベンゾチォフェン、チエノ ピリジン)を形成する場合;
などが挙げられる。
但し、環 Μの W部分が =Ν—または— Ν =である場合(例えば、環 Μが、 1, 3 チ ァゾールの場合)、 Uは存在しない。
[0031] Dおよび Gは、好ましくはそれぞれカルボ-ル基である。
[0032] 環 Ρで表される「置換されて 、てもよ 、ピペリジンまたは置換されて 、てもよ 、ピペラ ジン」における「ピペリジン」または「ピペラジン」は、 D基および Q環基で置換されて!ヽ るのにカ卩えて、置換可能な位置に 1ないし 3個の置換基をさらに有していてもよい。こ
のような「置換基」としては、例えば、上言 ejで示される「置換されていてもよい炭化水 素基」における「炭化水素基」として例示した c シクロアルキル基が有して 、てもよ
3-10
、置換基として例示したものが挙げられる。
環 Pは、好ましくはピペリジンである。
[0033] Bは、好ましくは CHである。
[0034] 環 Qで表される「置換されて 、てもよ 、単環性環」の「単環性環」としては、例えば、 上言 ejで示される「置換されて ヽてもよ ヽ炭化水素基」として例示した c シクロアル
3-10 キル基、 C シクロアルケニル基、 C シクロアルカジエニル基および C 芳香
3-10 4-10 6-14 族炭化水素基に対応する環のうち単環式のもの、ならびに上言 ejで示される「置換さ れて!、てもよ!/、複素環基」として例示した単環式芳香族複素環基および単環式非芳 香族複素環基に対応する環などが挙げられる。
該「単環性環」は、好ましくはピペリジン、ピぺラジン、モルホリン、ベンゼンなどであ る。
環 Qで表される「置換されて!ヽてもよ!/ヽ単環性環」の「単環性環」は、 P環基および G 基で置換されているのに加えて、置換可能な位置に 1ないし 3個の置換基をさらに有 していてもよい。このような「置換基」としては、例えば、上言 ejで示される「置換されて
V、てもよ 、炭化水素基」の「炭化水素基」として例示した c シクロアルキル基が有
3-10
していてもよい置換基として例示したもの(例、 1〜3個のハロゲン原子で置換されて
V、てもよ 、C アルキル カルボ-ル基、 C アルキル基)が挙げられる。該置換基
1-6 1-6
の数は、例えば 1ないし 3個である。
環 Qは、好ましくは、置換基 (例、 1〜3個のハロゲン原子で置換されていてもよい C アルキル カルボ-ル基、および C アルキル基から選ばれる 1ないし 3個の置
1 -6 1-6
換基)でそれぞれ置換されていてもよい、ピぺリジン、ピぺラジン、モルホリン、または ベンゼンである。
[0035] Aは、好ましくは Cまたは Nであり、さらに好ましくは Nである。
[0036] 化合物 (I)の好ましい例には、例えば、以下が挙げられる:
(化合物 A)
環 Mが、チォフェン、チアゾール等であり;
K力 イミノ基であり;
Rが、水素原子または置換されて 、てもよ 、炭化水素基 (例、 C アルキル)であり;
1 -6
Τが、 C 芳香族炭化水素基 (好ましくはフ ニル)であり、かつ、 Uが、水素原子ま
6- 14
たは C アルキルであるか、
1 -6
あるいは Τおよび Uは、環 Μとともに、置換基 (例、ォキソ)で置換されていてもよい二 環性環(例、ベンゾチォフェン、 4, 5, 6, 7—テトラヒドロベンゾチォフェン)を形成す る;
Dが、カルボニル基であり;
G力 カルボニル基であり;
環 Ρが、ピぺリジンであり;
Βが、 CHであり;
環 Qが、 1〜3個のハロゲン原子で置換されていてもよい C アルキル カルボ-ル
1 -6
基でそれぞれ置換されていてもよい、ピぺリジン、ピぺラジン、モルホリン、またはベン ゼンであり;
Α力 Cまたは Nであり、かつ
Jが、置換されていてもよい複素環基 (例、モルホリノ)または置換されていてもよいアミ ノ基 (例、 C アルキル基でモノまたはジ置換されて 、てもよ 、ァミノ基)
1 -6
である、化合物 (1)。
(化合物 B)
環 Mが、チォフェン、チアゾール、ピリジンであり;
K力 イミノ基であり;
Rが、水素原子または置換されて 、てもよ 、炭化水素基 (例、 C アルキル)であり;
1 -6
T力 置換基(例、 1〜3個のハロゲン原子で置換されていてもよい C アルキル基、
1 -6
ヒドロキシ基、 C アルコキシ基、カルボキシル基、ハロゲン原子および C アルキ
1 -6 1 - 6 ルスルホ-ル基カも選ばれる 1な 、し 3個の置換基)で置換されて!、てもよ!/、フエ-ル 基であり、かつ Uが水素原子である;
Dが、カルボニル基であり;
G力 カルボニル基であり;
環 Pが、ピぺリジンであり;
Bが、 CHであり;
環 Qが、置換基(例、 1〜3個のハロゲン原子で置換されていてもよい C アルキル
1 -6
—カルボ-ル基、および C アルキル基力も選ばれる 1な!、し 3個の置換基)でそれ
1 -6
ぞれ置換されていてもよい、ピぺリジン、ピぺラジン、モルホリン、またはベンゼンであ り;
A力 Cまたは Nであり、かつ
Jが、置換されていてもよい複素環基 (例、それぞれ 1〜3個のハロゲン原子で置換さ れていてもよい C アルキル基、および C シクロアルキル基力 選ばれる 1または
1 - 6 3- 10
2個の置換基で置換されて 、てもよ 、含窒素非芳香族複素環基 (例、ピロリジニル、 イミダゾリジニル、ビラゾリジニル、ピベリジニル、ピぺラジュル、モルホリニル、チォモ ルホリニル、テトラヒドロキノリニル、テトラヒドロイソキノリニル))、または置換されてい てもよぃァミノ基(例、 1〜3個のハロゲン原子で置換されていてもよい C アルキル
1 - 6 基および C シクロアルキル基力 選ばれる置換基でモノまたはジ置換されて 、て
3- 10
ちょいアミノ基)
である、化合物 (1)。
(化合物 C)
環 Mが、チオフ ンであり;
K力 イミノ基であり;
Rが、水素原子または置換されて 、てもよ 、炭化水素基 (例、 C アルキル)であり;
1 -6
Tおよび Uが、環 Mととも〖こ、置換基(例、ォキソ、 C アルキル基および C アルコ
1 - 6 1 -6 キシ基力も選ばれる 1な 、し 3個の置換基)で置換されて 、てもよ 、二環性環 (例、ベ ンゾチォフェン、 4, 5, 6, 7—テトラヒドロベンゾチォフェン、チェノビリジン)を形成す る;
Dが、カルボニル基であり;
G力 カルボニル基であり;
環 Pが、ピぺリジンであり;
Bが、 CHであり;
環 Qが、置換基(例、 1〜3個のハロゲン原子で置換されていてもよい C アルキル
1 -6
—カルボ-ル基、および C アルキル基力も選ばれる 1な!、し 3個の置換基)でそれ
1 -6
ぞれ置換されていてもよい、ピぺリジン、ピぺラジン、モルホリン、またはベンゼンであ り;
A力 Cまたは Nであり、かつ
Jが、置換されていてもよい複素環基 (例、それぞれ 1〜3個のハロゲン原子で置換さ れていてもよい C アルキル基、および C シクロアルキル基力 選ばれる 1または
1 - 6 3- 10
2個の置換基で置換されて 、てもよ 、含窒素非芳香族複素環基 (例、ピロリジニル、 イミダゾリジニル、ビラゾリジニル、ピベリジニル、ピぺラジュル、モルホリニル、チォモ ルホリニル、テトラヒドロキノリニル、テトラヒドロイソキノリニル))、または置換されてい てもよぃァミノ基(例、 1〜3個のハロゲン原子で置換されていてもよい C アルキル
1 - 6 基および C シクロアルキル基力 選ばれる置換基でモノまたはジ置換されて 、て
3- 10
ちょいアミノ基)
である、化合物 (1)。
(化合物 D)
Ν,Ν-ジェチル -1'-[(2-{[(ェチルァミノ)カルボ-ル]アミノト 1-ベンゾチォフェン- 3-ィル )カルボ二ル]- 1 ,4'-ビピペリジン- 3-カルボキサミド;
Ν-ェチル -Ν'- (4- {[3- (モルホリン- 4-ィルカルボ-ル)- 1,4'-ビピペリジン- 1しィル]力 ルポ-ル}-2-フエ-ル- 1 ,3-チアゾール -5-ィル)尿素;
Ν-ェチル -Νし {3- {[(3R)- 3- (モルホリン- 4-ィルカルボ-ル)- 1,4'-ビピペリジン- 1しィ ル]カルボ-ル}-5-[4- (トリフルォロメチル)フエ-ル]- 2-チェ-ル}尿素;
Ν-ェチル -Ν'- (7-メトキシ- 3- {[3- (ピペリジン- 1-ィルカルボ-ル)- 1,4'-ビピペリジン- 1 '-ィル]カルボ-ル}-1-ベンゾチェン- 2-ィル)尿素;または
Ν-ェチル -1'-[(2-{ [(ェチルァミノ)カルボ-ル]アミノト 6-メチルチエノ [2,3-b]ピリジン- 3-ィル)カルボ二ル]- N-イソプロピル- 1 ,4'-ビピペリジン- 3-カルボキサミド; あるいはその塩。
式 (I)で表される化合物の塩としては、薬理学的に許容される塩が好ましぐこのよう な塩としては、例えば、無機塩基との塩、有機塩基との塩、無機酸との塩、有機酸と
の塩、塩基性または酸性アミノ酸との塩が挙げられる。
無機塩基との塩の好適な例としては、ナトリウム塩、カリウム塩などのアルカリ金属塩 ;カルシウム塩、マグネシウム塩などのアルカリ土類金属塩;アルミニウム塩;アンモニ ゥム塩が挙げられる。
有機塩基との塩の好適な例としては、トリメチルァミン、トリェチルァミン、ピリジン、ピ コリン、エタノールァミン、ジエタノールァミン、トリエタノールァミン、トロメタミン [トリス( ヒドロキシメチル)メチルァミン]、 tert ブチルァミン、シクロへキシルァミン、ベンジル ァミン、ジシクロへキシルァミン、 N, N ジベンジルエチレンジァミンとの塩が挙げら れる。
無機酸との塩の好適な例としては、塩酸、臭化水素酸、硝酸、硫酸、リン酸との塩が 挙げられる。
有機酸との塩の好適な例としては、ギ酸、酢酸、トリフルォロ酢酸、フタル酸、フマル 酸、シユウ酸、酒石酸、マレイン酸、クェン酸、コハク酸、リンゴ酸、メタンスルホン酸、 ベンゼンスルホン酸、 p—トルエンスルホン酸との塩が挙げられる。
塩基性アミノ酸との塩の好適な例としては、アルギニン、リジン、オル-チンとの塩が 挙げられる。
酸性アミノ酸との塩の好適な例としては、ァスパラギン酸、グルタミン酸との塩が挙げ られる。
上記した塩の中でも無機酸との塩および有機酸との塩が好ましぐさらに塩酸塩、ト リフルォロ酢酸塩、フマル酸塩などが好ましい。
化合物 (I)のプロドラッグは、生体内における生理条件下で酵素や胃酸等による反 応により化合物 (I)に変換する化合物、すなわち酵素的に酸化、還元、加水分解等 を起こして化合物 (I)に変化する化合物、胃酸等により加水分解などを起こして化合 物 (I)に変化する化合物である。化合物 (I)のプロドラッグとしては、化合物 (I)のアミ ノ基がァシル化、アルキル化、リン酸化された化合物(例、化合物 (I)のァミノ基がエイ コサノィル化、ァラ-ル化、ペンチルァミノカルボ-ル化、(5—メチル—2 ォキソ— 1, 3 ジォキソレンー4 ィル)メトキシカルボ-ル化、テトラヒドロフラ-ル化、ピロリ ジルメチル化、ビバロイルォキシメチル化、 tert ブチル化された化合物);化合物(I
)の水酸基がァシル化、アルキル化、リン酸化、ホウ酸化された化合物(例、化合物 (I )の水酸基がァセチル化、パルミトイル化、プロパノィル化、ビバロイル化、サクシ-ル ィ匕、フマリル化、ァラニル化、ジメチルァミノメチルカルボ二ルイ匕された化合物);ィ匕合 物(I)のカルボキシル基がエステル化、アミド化されたィ匕合物(例、化合物(I)のカル ボキシル基がェチルエステル化、フエ-ルエステル化、カルボキシメチルエステル化 、ジメチルァミノメチルエステル化、ビバロイルォキシメチルエステル化、エトキシカル ボ-ルォキシェチルエステル化、フタリジルエステル化、(5—メチルー 2 ォキソ 1 , 3—ジォキソレン— 4—ィル)メチルエステル化、シクロへキシルォキシカルボニルェ チルエステル化、メチルアミド化された化合物など)等が挙げられる。これらの化合物 は自体公知の方法によって化合物 (I)カゝら製造することができる。
また、化合物 (I)のプロドラッグは、広川書店 1990年刊「医薬品の開発」第 7卷分子 設計 163頁から 198頁に記載されているような、生理的条件で化合物 (I)に変化する ものであってもよい。
また、化合物 (I)は、同位元素 (例、 3H、 "C、 35S、 1251)などで標識されていてもよい さらに、化合物(I)は、無水物であっても、水和物であってもよい。
[0039] 化合物 (I)またはそのプロドラッグ (以下、単に本発明化合物と略記することがある) は、毒性が低ぐそのまま、または薬理学的に許容し得る担体などと混合して医薬組 成物とすることにより、哺乳動物(例、ヒト、マウス、ラット、ゥサギ、ィヌ、ネコ、ゥシ、ゥ マ、ブタ、サル)に対して、後述する各種疾患の予防または治療剤として用いることが できる。
ここにおいて、薬理学的に許容し得る担体としては、製剤素材として慣用の各種有 機あるいは無機担体物質が用いられ、固形製剤における賦形剤、滑沢剤、結合剤、 崩壊剤;液状製剤における溶剤、溶解補助剤、懸濁化剤、等張化剤、緩衝剤、無痛 ィ匕剤などとして配合される。また必要に応じて、防腐剤、抗酸化剤、着色剤、甘味剤 などの製剤添加物を用いることもできる。
[0040] 賦形剤の好適な例としては、乳糖、白糖、 D—マン-トール、 D—ソルビトール、デ ンプン、 α化デンプン、デキストリン、結晶セルロース、低置換度ヒドロキシプロピルセ
ルロース、カルボキシメチルセルロースナトリウム、アラビアゴム、プルラン、軽質無水 ケィ酸、合成ケィ酸アルミニウム、メタケイ酸アルミン酸マグネシウムが挙げられる。 滑沢剤の好適な例としては、ステアリン酸マグネシウム、ステアリン酸カルシウム、タ ルク、コロイドシリカ力 S挙げられる。
結合剤の好適な例としては、 α化デンプン、ショ糖、ゼラチン、アラビアゴム、メチル セルロース、カルボキシメチルセルロース、カルボキシメチルセルロースナトリウム、結 晶セルロース、白糖、 D—マン-トール、トレハロース、デキストリン、プルラン、ヒドロキ シプロピルセルロース、ヒドロキシプロピルメチルセルロース、ポリビュルピロリドンが挙 げられる。
崩壊剤の好適な例としては、乳糖、白糖、デンプン、カルボキシメチルセルロース、 カルボキシメチルセルロースカルシウム、クロスカルメロースナトリウム、カルボキシメ チルスターチナトリウム、軽質無水ケィ酸、低置換度ヒドロキシプロピルセルロースな どが挙げられる。
[0041] 溶剤の好適な例としては、注射用水、生理的食塩水、リンゲル液、アルコール、プロ ピレンダリコール、ポリエチレングリコール、ゴマ油、トウモロコシ油、ォリーブ油、綿実 油が挙げられる。
溶解補助剤の好適な例としては、ポリエチレングリコール、プロピレングリコール、 D —マンニトール、トレハロース、安息香酸ベンジル、エタノール、トリスァミノメタン、コレ ステロール、トリエタノールァミン、炭酸ナトリウム、クェン酸ナトリウム、サリチル酸ナト リウム、酢酸ナトリウムが挙げられる。
懸濁化剤の好適な例としては、ステアリルトリエタノールァミン、ラウリル硫酸ナトリウ ム、ラウリルアミノプロピオン酸、レシチン、塩化ベンザルコ-ゥム、塩化べンゼトニゥム 、モノステアリン酸グリセリンなどの界面活性剤;ポリビュルアルコール、ポリビュルピロ リドン、カルボキシメチルセルロースナトリウム、メチルセルロース、ヒドロキシメチルセ ルロース、ヒドロキシェチルセルロース、ヒドロキシプロピルセルロースなどの親水性高 分子;ポリソルベート類、ポリオキシエチレン硬化ヒマシ油が挙げられる。
[0042] 等張化剤の好適な例としては、塩ィ匕ナトリウム、グリセリン、 D—マン-トール、 D—ソ ルビトール、ブドウ糖が挙げられる。
緩衝剤の好適な例としては、リン酸塩、酢酸塩、炭酸塩、クェン酸塩の緩衝液が挙 げられる。
無痛化剤の好適な例としては、ベンジルアルコールが挙げられる。
防腐剤の好適な例としては、ノ ラオキシ安息香酸エステル類、クロロブタノール、ベ ンジルアルコール、フエネチルアルコール、デヒドロ酢酸、ソルビン酸が挙げられる。 抗酸化剤の好適な例としては、亜硫酸塩、ァスコルビン酸塩が挙げられる。
着色剤の好適な例としては、水溶性食用タール色素(例、食用赤色 2号および 3号
、食用黄色 4号および 5号、食用青色 1号および 2号の食用色素)、水不溶性レーキ 色素(例、上記水溶性食用タール色素のアルミニウム塩)、天然色素(例、 j8—カロチ ン、クロロフィル、ベンガラ)が挙げられる。
甘味剤の好適な例としては、サッカリンナトリウム、グリチルリチン酸二カリウム、ァス パルテーム、ステビアが挙げられる。
[0043] 上記医薬組成物の剤形としては、例えば、錠剤 (糖衣錠、フィルムコーティング錠、 舌下錠、 口腔内崩壊錠を含む)、カプセル剤(ソフトカプセル、マイクロカプセルを含 む)、顆粒剤、散剤、トローチ剤、シロップ剤、乳剤、懸濁剤、フィルム剤(例、口腔内 崩壊フィルム)などの経口剤;および注射剤 (例、皮下注射剤、静脈内注射剤、筋肉 内注射剤、腹腔内注射剤、点滴剤)、外用剤 (例、経皮製剤、軟膏剤)、坐剤 (例、直 腸坐剤、膣坐剤)、ペレット、経鼻剤、経肺剤(吸入剤)、点眼剤等の非経口剤が挙げ られる。これらはそれぞれ経口的あるいは非経口的(例、局所、直腸、静脈投与)に 安全に投与できる。
これらの製剤は、速放性製剤または徐放性製剤などの放出制御製剤 (例、徐放性 マイクロカプセル)であってもよ 、。
医薬組成物は、製剤技術分野において慣用の方法、例えば、 日本薬局方に記載 の方法等により製造することができる。以下に、製剤の具体的な製造法について詳 述する。
なお、医薬組成物中の本発明化合物の含量は、剤形、本発明化合物の投与量な どにより異なるが、例えば、約 0. 1〜: LOO重量%である。
[0044] 経口剤を製造する際には、必要により、味のマスキング、腸溶性あるいは持続性を
目的として、コーティングを行ってもよい。
コーティングに用いられるコーティング基剤としては、例えば、糖衣基剤、水溶性フ イルムコーティング基剤、腸溶性フィルムコーティング基剤、徐放性フィルムコーティ ング基剤などが挙げられる。
[0045] 糖衣基剤としては、白糖が用いられ、さらに、タルク、沈降炭酸カルシウム、ゼラチン 、アラビアゴム、プルラン、カルナパロウなど力も選ばれる 1種または 2種以上を併用し てもよい。
水溶性フィルムコーティング基剤としては、例えば、ヒドロキシプロピルセルロース、 ヒドロキシプロピノレメチノレセノレロース、ヒドロキシェチノレセノレロース、メチノレヒドロキシェ チルセルロースなどのセルロース系高分子;ポリビュルァセタールジェチルアミノアセ テート、アミノアルキルメタアタリレートコポリマー E〔オイドラギット E (商品名)、ローム フアルマ社〕、ポリビニルピロリドンなどの合成高分子;プルランなどの多糖類が挙げら れる。
腸溶性フィルムコーティング基剤としては、例えば、ヒドロキシプロピルメチルセル口 ース フタレート、ヒドロキシプロピルメチルセルロース アセテート サクシネート、力 ルボキシメチルェチルセルロース、酢酸フタル酸セルロースなどのセルロース系高分 子;メタアクリル酸コポリマー L〔オイドラギット L (商品名)、ロームフアルマ社〕、メタァク リル酸コポリマー LD〔オイドラギット L— 30D55 (商品名)、ロームフアルマ社〕、メタァ クリル酸コポリマー S〔オイドラギット S (商品名)、ロームフアルマ社〕などのアクリル酸 系高分子;セラックなどの天然物が挙げられる。
徐放性フィルムコーティング基剤としては、例えば、ェチルセルロースなどのセル口 ース系高分子;アミノアルキルメタアタリレートコポリマー RS〔オイドラギット RS (商品名 )、ロームフアルマ社〕、アクリル酸ェチルーメタクリル酸メチル共重合体懸濁液〔ォイド ラギット NE (商品名)、ロームフアルマ社〕などのアクリル酸系高分子が挙げられる。 上記したコーティング基剤は、その 2種以上を適宜の割合で混合して用いてもょ ヽ 。また、コーティングの際に、例えば、酸化チタン、三二酸化鉄等のような遮光剤を用 いてもよい。
[0046] 本発明化合物は、毒性 (例、急性毒性、慢性毒性、遺伝毒性、生殖毒性、心毒性、
癌原性)が低ぐ副作用も少なぐ哺乳動物 (例えば、ヒト、ゥシ、ゥマ、ィヌ、ネコ、サ ル、マウス、ラット等、特にヒト)に対し、各種疾患の予防または治療剤、または診断薬 として用いることができる。
本発明化合物は、優れた ACC (ァセチルー CoAカルボキシラーゼ)阻害作用を有 する。ここで、 ACCとしては、肝臓、脂肪組織、脾臓特異的ァイソザィム (ACC1);筋 肉特異的ァイソザィム (ACC2);などが挙げられる。本発明化合物は、とりわけ、 AC C2に対して選択的な阻害作用を有する。
[0047] 本発明化合物は、肥満症、糖尿病 (例、 1型糖尿病、 2型糖尿病、妊娠糖尿病、肥 満型糖尿病)、高脂血症 (例、高トリグリセリド血症、高コレステロール血症、低 HDL 血症、食後高脂血症)、高血圧症、心不全、糖尿病性合併症 [例、神経障害、腎症、 網膜症、白内障、大血管障害、骨減少症、糖尿病性高浸透圧昏睡、感染症 (例、呼 吸器感染症、尿路感染症、消化器感染症、皮膚軟部組織感染症、下肢感染症)、糖 尿病性壊疽、口腔乾燥症、聴覚の低下、脳血管障害、末梢血行障害]、メタボリック シンドローム(高トリグリセライド (TG)血症、低 HDLコレステロール(HDL— C)血症、 高血圧、腹部肥満および耐糖能異常から選ばれる 3つ以上を保有する病態)、筋肉 減少症などの予防 ·治療剤として用いることができる。
[0048] 糖尿病の判定基準については、日本糖尿病学会から新たな判定基準が報告され ている。
この報告によれば、糖尿病とは、空腹時血糖値 (静脈血漿におけるグルコース濃度 )が 126mg/dl以上、 75g経ロブドウ糖負荷試験(75gOGTT) 2時間値 (静脈血漿 におけるグルコース濃度)が 200mgZdl以上、随時血糖値 (静脈血漿におけるダル コース濃度)が 200mgZdl以上のいずれかを示す状態である。また、上記糖尿病に 該当せず、かつ、「空腹時血糖値 (静脈血漿におけるグルコース濃度)が llOmgZd 1未満または 75g経口ブドウ糖負荷試験(75gOGTT) 2時間値 (静脈血漿におけるグ ルコース濃度)が 140mgZdl未満を示す状態」(正常型)でない状態を、「境界型」と 呼ぶ。
[0049] また、糖尿病の判定基準については、 ADA (米国糖尿病学会)および WHOから、 新たな判定基準が報告されて 、る。
これらの報告によれば、糖尿病とは、空腹時血糖値 (静脈血漿におけるグルコース 濃度)が 126mgZdl以上であり、かつ、 75g経ロブドウ糖負荷試験 2時間値 (静脈血 漿におけるグルコース濃度)が 200mgZdl以上を示す状態である。
[0050] また、 ADAおよび WHOの上記報告によれば、耐糖能不全とは、 75g経口ブドウ糖 負荷試験 2時間値 (静脈血漿におけるグルコース濃度)が 140mgZdl以上 200mg Zdl未満を示す状態である。さらに、 ADAの報告によれば、空腹時血糖値 (静脈血 漿におけるグルコース濃度)が lOOmgZdl以上 126mgZdl未満の状態を IFG (Imp aired Fasting Glucoseノと呼ふ。一方、 WHOは、 亥 IFG (Impaired Fasting ulucos e)を空腹時血糖値 (静脈血漿におけるグルコース濃度)が llOmgZdl以上 126mg Zdl未満の状態とし、 IFG (Impaired Fasting Glycemia)と呼ぶ。
[0051] 本発明化合物は、上記した新たな判定基準により決定される糖尿病、境界型、耐 糖會小全、 IFG (Impaired Fasting ulucose)およひ、IFG (Impaired Fasting ulycem ia)の予防 '治療剤としても用いられる。さらに、本発明化合物は、境界型、耐糖能不 王、 IFG (Impaired Fasting Glucose)または丄 FG (Impaired Fasting Glycemia)力ら 糖尿病への進展を防止することもできる。
[0052] 本発明化合物は、例えば、糖尿病性合併症、骨粗鬆症、悪液質 (例、癌性悪液質 、結核性悪液質、糖尿病性悪液質、血液疾患性悪液質、内分泌疾患性悪液質、感 染症性悪液質または後天性免疫不全症候群による悪液質)、脂肪肝、多嚢胞性卵 巣症候群、腎臓疾患 (例、糖尿病性ネフ口パシー、糸球体腎炎、糸球体硬化症、ネ フローゼ症候群、高血圧性腎硬化症、末期腎臓疾患)、筋ジストロフィー、心筋梗塞 、狭心症、脳血管障害 (例、脳梗塞、脳卒中)、アルツハイマー病、パーキンソン病、 不安症、痴呆症、インスリン抵抗性症候群、シンドローム X、高インスリン血症、高イン スリン血症における知覚障害、腫瘍 (例、白血病、乳癌、前立腺癌、皮膚癌)、過敏性 腸症候群、急性または慢性下痢、炎症性疾患 (例、動脈硬化症 (例、ァテローム性動 脈硬化症)、慢性関節リウマチ、変形性脊椎炎、変形性関節炎、腰痛、痛風、手術ま たは外傷後の炎症、腫脹、神経痛、咽喉頭炎、膀胱炎、肝炎 (非アルコール性脂肪 性肝炎を含む)、肺炎、脾炎、腸炎、炎症性腸疾患 (炎症性大腸疾患を含む)、潰瘍 性大腸炎、胃粘膜損傷 (アスピリンにより引き起こされた胃粘膜損傷を含む))、小腸
粘膜損傷、吸収不良、精巣機能障害、内臓肥満症候群、筋肉減少症などの予防,治 療剤としても用 、ることができる。
本発明化合物は、上記した各種疾患 (例、心筋梗塞などの心血管イベント)の 2次 予防および進展抑制にも用いられる。
[0053] 本発明化合物の投与量は、投与対象、投与ルート、対象疾患、症状などによっても 異なるが、例えば、成人の糖尿病患者に経口投与する場合、通常 1回量として約 0. 01〜: LOOmgZkg体重、好ましくは 0. 05〜30mgZkg体重、さらに好ましくは 0. 1 〜10mgZkg体重であり、この量を 1日 1回〜 3回投与するのが望ましい。
[0054] 本発明化合物は、該化合物の作用の増強または該化合物の投与量の低減などを 目的として、糖尿病治療剤、糖尿病性合併症治療剤、抗高脂血症剤、降圧剤、抗肥 満剤、利尿剤、抗血栓剤などの薬剤 (以下、併用薬剤と略記する)と組み合わせて用 いることができる。この際、本発明化合物と併用薬剤の投与時期は限定されず、これ らを投与対象に対し、同時に投与してもよいし、時間差をおいて投与してもよい。さら に、本発明化合物と併用薬剤とは、それぞれの活性成分を含む 2種類の製剤として 投与されてもょ ヽし、両方の活性成分を含む単一の製剤として投与されてもょ 、。 併用薬剤の投与量は、臨床上用いられている用量を基準として適宜選択すること ができる。また、本発明化合物と併用薬剤の配合比は、投与対象、投与ルート、対象 疾患、症状、組み合わせなどにより適宜選択することができる。例えば、投与対象がヒ トである場合、本発明化合物 1重量部に対し、併用薬剤を 0. 01〜: L00重量部用い ればよい。
[0055] なお、糖尿病治療剤としては、インスリン製剤 (例、ゥシ、ブタの脾臓カゝら抽出された 動物インスリン製剤;大腸菌、イーストを用い遺伝子工学的に合成したヒトインスリン製 剤;インスリン亜翁;プロタミンインスリン亜翁 ;インスリンのフラグメントまたは誘導体 ( 例、 INS - 1)、経口インスリン製剤)、インスリン抵抗性改善剤(例、ピオグリタゾンま たはその塩 (好ましくは、塩酸塩)、ロシグリタゾンまたはその塩 (好ましくは、マレイン 酸塩)、テサグリタザール(Tesaglitazar)、ラガグリタザール(Ragaglitazar)、ムラグリタ ザール(Muraglitazar)、ェダグリタゾン (Edaglitazone)、メタグリダセン (Metaglidasen)、 ナベグリタザール(Naveglitazar)、 AMG- 131、 THR-0921)、 a—ダルコシダーゼ阻害
剤(例、ボグリボース、ァカルボース、ミグリトール、エミダリテート)、ビグアナイド剤(例 、メトホルミン、ブホルミンまたはそれらの塩(例、塩酸塩、フマル酸塩、コハク酸塩))、 インスリン分泌促進剤 [スルホ-ルゥレア剤(例、トルプタミド、ダリベンクラミド、ダリクラ ジド、クロルプロパミド、トラザミド、ァセトへキサミド、グリクロビラミド、グリメピリド、グリピ ザイド、ダリブゾール)、レパグリニド、ナテグリニド、ミチグリニドまたはそのカルシウム 塩水和物]、ジぺプチジルぺプチダーゼ IV阻害剤(例、ヴィルダグリプチン (Vildaglipt in)、シタグリブチン (Sitagliptin)、サクサグリプチン (Saxagliptin)、 T-6666、 TS-021)、 β 3ァゴ-スト(例、 AJ- 9677)、 GPR40ァゴ-スト、 GLP— 1受容体ァゴ-スト [例、 GLP -1、 GLP- 1MR剤、 ΝΝ- 2211、 AC- 2993(exendin- 4)、 BIM- 51077、 Aib(8,35)hGLP- 1(7 ,37)NH、 CJC- 1131]、アミリンァゴニスト(例、プラムリンチド)、ホスホチロシンホスファ
2
ターゼ阻害剤 (例、バナジン酸ナトリウム)、糖新生阻害剤 (例、グリコーゲンホスホリラ ーゼ阻害剤、グルコースー6—ホスファターゼ阻害剤、グルカゴン拮抗剤)、 SGLUT (sodium-glucose cotransporter)阻害剤(例、 T- 1095)、 11 βーヒドロキシステロイドデ ヒドロゲナーゼ阻害薬(例、 BVT-3498)、アジポネクチンまたはその作動薬、 ΙΚΚ阻 害薬 (例、 AS-2868)、レブチン抵抗性改善薬、ソマトスタチン受容体作動薬、ダルコ キナーゼ活性化薬(例、 Ro- 28- 1675)、 GIP (Glucose- dependent insulinotropic pepti de)等が挙げられる。
糖尿病性合併症治療剤としては、例えばアルドース還元酵素阻害剤(例、トルレス タツト、ェパノレレスタツト、ゼナレスタツト、ゾポノレレスタツト、ミナノレレスタツト、フィダレス タツト、 CT— 112)、神経栄養因子およびその増加薬(例、 NGF、 NT— 3、 BDNF、 WO01Z14372に記載の-ユーロトロフィン産生 '分泌促進剤(例えば、 4— (4 ク ロロフエ-ル) - 2- (2—メチル 1—イミダゾリル) 5— [3— (2—メチルフエノキシ) プロピル]ォキサゾール))、神経再生促進薬 (例、 Y— 128)、 PKC阻害剤(例、ルポ キシスタウリン メシレート (ruboxistaurin mesylate))、 AGE阻害剤(例、 ALT946、ピマ ゲジン、ピラトキサチン、 N-フエナシルチアゾリゥム ブロマイド (ALT766)、 ALT-711, EXO-226,ピリドリン (Pyridorin)、ピリドキサミン)、活性酸素消去薬 (例、チォタト酸)、 脳血管拡張剤 (例、チアプリド、メキシレチン)、ソマトスタチン受容体作動薬 (例、 BIM 23190)、アポトーシスシグナルレギユレ一ティングキナーゼ -1 (ASK- 1)阻害薬が挙げ
られる。
抗高脂血症剤としては、例えばスタチン系化合物(例、プラバスタチン、シンパスタ チン、口パスタチン、アトノレパスタチン、フルパスタチン、ロスパスタチン、ピタバスタチ ンまたはそれらの塩 (例、ナトリウム塩、カルシウム塩))、スクアレン合成酵素阻害剤( 例、 WO97Z10224に記載の化合物、例えば、 N— [ [(3R,5S)- 1- (3-ァセトキシ- 2,2 -ジメチルプロピル)- 7-クロ口- 5-(2,3-ジメトキシフエ二ル)- 2-ォキソ -1,2,3, 5-テトラヒド 口- 4,1-ベンゾォキサゼピン- 3-ィル]ァセチル]ピぺリジン- 4-酢酸)、フイブラート系化 合物(例、ベザフイブラート、クロフイブラート、シムフイブラート、クリノフイブラート)、 A CAT阻害剤(例、アバシマイブ (Avasimibe)、エフルシマイブ(Eflucim¾e) )、陰ィォ ン交換樹脂(例、コレスチラミン)、プロブコール、ニコチン酸系薬剤(例、ニコモール( nicomol)、 -セリトロール (niceritrol))、ィコサペント酸ェチル、植物ステロール(例、ソ イステロ一ノレ (soysterol)、ガンマオリザノーノレ(γ—oryzanol))が挙げられる。
降圧剤としては、例えばアンジォテンシン変換酵素阻害剤(例、カプトプリル、ェナ ラプリル、デラプリル)、アンジォテンシン II拮抗剤(例、カンデサルタン シレキセチル 、口サルタン、ェプロサルタン、バルサルタン、テルミサルタン、ィルベサルタン、タソ サルタン、 1-[[2'-(2,5-ジヒドロ- 5-ォキソ -4H-1,2,4-ォキサジァゾール -3-ィル)ビフエ -ル -4-ィル]メチル ]-2-エトキシ -1H-ベンズイミダゾール- 7-カルボン酸)、カルシゥ ム拮抗剤(例、マ-ジピン、 -フエジピン、アムロジピン、エホ-ジピン、 -カルジピン) 、カリウムチャンネル開口薬(例、レブクロマカリム、 L- 27152、 AL 0671、 NIP- 121)、 クロ-ジンが挙げられる。
抗肥満剤としては、例えば中枢性抗肥満薬 (例、デキスフェンフルラミン、フェンフ ルラミン、フェンテルミン、シブトラミン、アンフエプラモン、デキサンフエタミン、マジン ドール、フエ-ルプロパノールァミン、クロべンゾレックス; MCH受容体拮抗薬(例、 SB -568849 ;SNAP-7941; WO01/82925および WO01/87834に含まれる化合物);ニュー 口ペプチド Ύ拮抗薬 (例、 CP-422935);カンナピノイド受容体拮抗薬 (例、 SR-141716 、 SR-14778);グレリン拮抗薬; 11 βーヒドロキシステロイドデヒドロゲナーゼ阻害薬 (例 、 BVT- 3498) )、脾リパーゼ阻害薬 (例、オルリスタツト、セティリスタツト)、 β 3ァゴニス ト(例、 AJ-9677、 AZ40140)、ペプチド性食欲抑制薬(例、レプチン、 CNTF (毛様体
神経栄養因子))、コレシストキュンァゴ-スト (例、リンチトリブト、 FPL-15849)、摂食 抑制薬 (例、 P-57)が挙げられる。
[0058] 利尿剤としては、例えば、キサンチン誘導体 (例、サリチル酸ナトリウムテオプロミン 、サリチル酸カルシウムテオプロミン)、チアジド系製剤(例、ェチアジド、シクロペンチ アジド、トリクロルメチアジド、ヒドロクロ口チアジド、ヒドロフルメチアジド、ベンチルヒド 口クロ口チアジド、ペンフルチジド、ポリチアジド、メチクロチアジド)、抗アルドステロン 製剤 (例、スピロノラタトン、トリアムテレン)、炭酸脱水酵素阻害剤 (例、ァセタゾラミド) 、クロルベンゼンスルホンアミド系製剤(例、クロルタリドン、メフルシド、インダパミド)、 ァゾセミド、イソソルビド、エタクリン酸、ピレタ -ド、ブメタ-ド、フロセミドが挙げられる
[0059] 抗血栓剤としては、例えば、へパリン (例、へパリンナトリウム、へパリンカルシウム、 ダルテパリンナトリウム (dalteparin sodium))、ヮルフアリン(例、ヮルフアリンカリウムな ど)、抗トロンビン薬(例、アルガトロバン (aragatroban))、血栓溶解薬(例、ゥロキナー ゼ (urokinase)、チソキナーゼ (tisokinase)、ァノレテプラーゼ (alteplase)、ナテプラーゼ (n ateplase)、モンテプラーゼ (monteplase)、ノヽミテプラーゼ (jmmiteplase))、血小板凝集 抑制薬(例、塩酸チクロピジン (ticlopidine hydrochloride)、シロスタゾール (cilostazol) 、ィコサペント酸ェチル、ベラプロストナトリウム (beraprost sodium),塩酸サルポグレラ ~~ト、 sarpogrelate hydrochloride)) けられる。
[0060] 以下、化合物 (I)の製造法について説明する。化合物 (I)は、例えば、以下に詳述 する [製造法]、あるいはこれらに準ずる方法によって製造することができる。
なお、下記の [製造法]において、原料ィ匕合物として用いられる化合物は、それぞ れ塩として用いてもよい。このような塩としては、式 (I)で表される化合物の塩として例 示したものが用いられる。
下記の各製造法において、アルキル化反応、加水分解反応、アミノ化反応、エステ ル化反応、アミド化反応、エステル化反応、エーテル化反応、酸化反応、還元反応な どを行う場合、これらの反応は、自体公知の方法に従って行われる。このような方法と しては、例えばオーガニック ファンクショナル グループ プレパレーシヨンズ(ORG ANIC FUNCTIONAL GROUP PREPARATIONS)第 2版、アカデミックプ
レス社 (ACADEMIC PRESS, INC. ) 1989年刊;コンプリヘンシブ.オーガ-ッ ク 'トフンスフォ ~~メ ~~シヨン (Comprehensive Organic Transformations) V CH Publishers Inc. , 1989年刊などに記載の方法などが挙げられる。
[0061] [製造法]
化合物 (I)は、例えば、以下の反応式 1および 2によって製造される。
<反応式 1 >
[0062] [化 3]
[0063] [式中の記号は前記と同意義を示す]
本反応は、下記の「脱水縮合剤を用いる方法」および「カルボン酸な 、しスルホン酸 の反応性誘導体を用いる方法」などによって行われる。
[0064] i)脱水縮合剤を用いる方法
化合物 (ΠΙ)、 1ないし 5当量の化合物 (Π)、および 1ないし 2当量の脱水縮合剤を、 不活性溶媒中で反応させる。必要に応じ、 1ないし 1. 5当量の 1—ヒドロキシベンゾト リアゾール (HOBt)、触媒量ないし 5当量の塩基などの共存下に反応を行ってもよい
上記「脱水縮合剤」としては、例えば、ジシクロへキシルカルポジイミド (DCC)、 1 - ェチル 3—(3 ジメチルァミノプロピル)カルボジイミド塩酸塩 (EDC · HC1)などが 挙げられる。これらのなかでも、 EDC'HClが好ましい。
上記「不活性溶媒」としては、例えば、二トリル系溶媒、アミド系溶媒、ハロゲン化炭 化水素系溶媒、エーテル系溶媒などが挙げられる。これらは、二種以上を適宜の割 合で混合して用いてもよい。
ここで、二トリル系溶媒としては、例えば、ァセトニトリル、プロピオ-トリルが用いられ る。なかでも、ァセトニトリルが好ましい。
アミド系溶媒としては、例えば、 N, N ジメチルホルムアミド(DMF)、 N, N ジメ チルァセトアミド、 N—メチルピロリドンが用いられる。なかでも、 DMFが好ましい。 ハロゲン化炭化水素系溶媒としては、例えば、ジクロロメタン、クロ口ホルム、 1, 2— ジクロロエタン、四塩ィ匕炭素が用いられる。なかでも、ジクロロメタンが好ましい。
エーテル系溶媒としては、例えば、ジェチルエーテル、テトラヒドロフラン (THF)、 1 , 4 ジォキサン、 1, 2 ジメトキシェタンが用いられる。なかでも、 THFが好ましい。 上記「塩基」としては、
1)例えば、アルカリ金属またはアルカリ土類金属の水素化物(例、水素化リチウム、 水素化ナトリウム、水素化カリウム、水素化カルシウム)、アルカリ金属またはアルカリ 土類金属のアミド類 (例、リチウムアミド、ナトリウムアミド、リチウムジイソプロピルアミド 、リチウムジシクロへキシルアミド、リチウムへキサメチルジシラジド、ナトリウムへキサメ チルジシラジド、カリウムへキサメチルジシラジド)、アルカリ金属またはアルカリ土類 金属の低級 (C )アルコキシド (例、ナトリウムメトキシド、ナトリウムエトキシド、力リウ
1-6
ム tert ブトキシド)などの強塩基;
2)例えば、アルカリ金属またはアルカリ土類金属の水酸ィ匕物(例、水酸ィ匕ナトリウム 、水酸ィ匕カリウム、水酸化リチウム、水酸化バリウム)、アルカリ金属またはアルカリ土 類金属の炭酸塩 (例、炭酸ナトリウム、炭酸カリウム、炭酸セシウム)、アルカリ金属の 炭酸水素塩 (例、炭酸水素ナトリウム、炭酸水素カリウム)などの無機塩基;および
3)例えば、トリエチルァミン、ジイソプロピルェチルァミン、 N—メチルモルホリンなど
のァミン類;例えば、ピリジン、 4 ジメチルァミノピリジン、 DBU (1, 8 ジァザビシク 口〔5. 4. 0〕ゥンデスー7 ェン)、 DBN (1, 5 ジァザビシクロ〔4. 3. 0〕ノンー5— ェン)、イミダゾール、 2, 6—ルチジンなどの塩基性複素環化合物などの有機塩基な どが挙げられる。
これらの塩基のなかでも、トリェチルァミン、 4—ジメチルァミノピリジンなどが好まし い。
反応温度は、通常、室温 (本明細書中、室温とは 1ないし 30°Cの温度を意味する) である。反応時間は、例えば、 1ないし 24時間である。
ii)カルボン酸な 、しスルホン酸の反応性誘導体を用いる方法
化合物 (Π)の反応性誘導体と 1な!、し 5当量 (好ましくは 1な!、し 3当量)の化合物 (I Π)とを、不活性溶媒中で反応させる。必要に応じ、 1ないし 10当量、好ましくは 1ない し 3当量の塩基の共存下に反応を行ってもよい。
化合物 (II)の「反応性誘導体」としては、例えば、酸ハライド (例、酸クロリド、酸ブロミ ド)、混合酸無水物 (例、 C アルキル一力ルボン酸、 C ァリール一力ルボン酸ま
1 -6 6- 10
たは C アルキル炭酸との酸無水物)、活性エステル (例、置換基を有して!/ヽてもよ!/ヽ
1 -6
フエノール、 HOBtまたは N ヒドロキシスクシンイミドとのエステル)
などが挙げられる。
上記「置換基を有していてもよいフエノール」における「置換基」としては、例えば、 ハロゲン原子、ニトロ基、ハロゲン化されて!/、てもよ 、C アルキル基、ハロゲン化さ
1 - 6
れていてもよい C アルコキシ基が挙げられる。置換基の数は、例えば 1ないし 5個
1 - 6
である。
ここで、「ハロゲン化されていてもよい C アルキル基」としては、例えば、 1ないし 5
1 -6
個、好ましくは 1ないし 3個のハロゲン原子を有していてもよい C アルキル基 (例、メ
1 -6
チル、ェチル、プロピル、イソプロピル、ブチル、イソブチル、 sec ブチル、 tert ブ チル、ペンチル、へキシル)が挙げられる。具体例としては、メチル、クロロメチル、ジ フルォロメチル、トリクロロメチル、トリフルォロメチル、ェチル、 2—ブロモェチル、 2, 2 , 2 トリフルォロェチル、ペンタフルォロェチル、プロピル、 3, 3, 3 トリフルォロプ 口ピル、イソプロピル、ブチル、 4, 4, 4 トリフルォロブチル、イソブチル、 sec ブチ
ル、 tert ブチル、ペンチノレ、イソペンチル、ネオペンチル、 5, 5, 5—トリフルォロぺ ンチル、へキシル、 6, 6, 6—トリフルォ口へキシルが挙げられる。
また「ノヽロゲン化されていてもよい C アルコキシ基」としては、例えば、 1ないし 5個
1 -6
、好ましくは 1ないし 3個のハロゲン原子を有していてもよい C アルコキシ基 (例、メト
1 -6
キシ、エトキシ、プロポキシ、ブトキシ、ペンチルォキシ、へキシルォキシ)が挙げられ る。具体例としては、メトキシ、ジフルォロメトキシ、トリフルォロメトキシ、エトキシ、 2, 2 , 2 トリフルォロエトキシ、プロポキシ、イソプロポキシ、ブトキシ、 4, 4, 4 トリフルォ ロブトキシ、イソブトキシ、 sec ブトキシ、ペンチルォキシ、イソペンチルォキシ、へキ シルォキシが挙げられる。
また、「置換基を有していてもよいフエノール」の具体例としては、フエノール、ペンタ クロ口フエノール、ペンタフルオロフェノール、 p 二トロフエノールが挙げられる。 反応性誘導体は、好ましくは酸ノ、ライドである。
上記「不活性溶媒」としては、例えば、エーテル系溶媒、ハロゲンィ匕炭化水素系溶 媒、芳香族系溶媒、脂肪族炭化水素系溶媒、二トリル系溶媒、アミド系溶媒、ケトン系 溶媒、スルホキシド系溶媒、水が挙げられる。これらは、二種以上を適宜の割合で混 合して用いてもよい。なかでも、ァセトニトリル、 THF、ジクロロメタン、クロ口ホルムな どが好ましい。
ここで、エーテル系溶媒、ハロゲン化炭化水素系溶媒、二トリル系溶媒およびアミド 系溶媒としては、前述の「脱水縮合剤を用いる方法」において例示したものが用いら れる。
芳香族系溶媒としては、例えば、ベンゼン、トルエン、キシレン、ピリジンが用いられ る。
脂肪族炭化水素系溶媒としては、例えば、へキサン、ペンタン、シクロへキサンが用 いられる。
ケトン系溶媒としては、例えば、アセトン、メチルェチルケトンが用いられる。
スルホキシド系溶媒としては、例えば、ジメチルスルホキシド(DMSO)が用いられる 上記「塩基」としては、前述の「脱水縮合剤を用いる方法」と同様のものが用いられ、
好ましくは、水素化ナトリウム、炭酸カリウム、炭酸ナトリウム、水酸化ナトリウム、水酸 化カリウム、炭酸水素ナトリウム、炭酸水素カリウム、トリェチルァミン、ピリジンなどで ある。
反応温度は、通常、 20°Cないし 50°C、好ましくは室温である。
反応時間は、通常、 5分間ないし 40時間、好ましくは 30分間ないし 18時間である。 上記製造法において、原料ィ匕合物として用いられる化合物 (ΠΙ)は、 自体公知の方 法、例えば、 WO03Z72197号パンフレットに記載の方法あるいはこれに準ずる方 法により製造することができる。また、化合物 (Π)は、自体公知の方法により製造する ことができる。
[0066] <反応式 2>
[0067] [化 4]
[式中の記号は前記と同意義を示す]
化合物 (V)は、前記反応式 1と同様の方法を用いて、化合物 (IV)と化合物 (III)か ら製造することがでさる。
ここで、原料ィ匕合物として用いられる化合物 (IV)は、自体公知の方法により製造す ることがでさる。
化合物 (I)のうち Kが置換されて 、てもよ 、イミノ基を示す化合物は、化合物 (V)と イソシアン酸エステルとを、所望により塩基の存在下、反応させることにより製造するこ とちでさる。
イソシアン酸エステルの使用量は、化合物(V) 1モルに対し、約 1ないし約 5モル、 好ましくは約 1ないし約 2モルである。
「塩基」としては、例えば前記反応式 1において例示した強塩基、無機塩基、塩基 性複素環化合物が挙げられる。塩基の使用量は、化合物 ) 1モルに対し、約 1ない し約 5モル、好ましくは約 1ないし約 3モルである。
本反応は無溶媒または反応に不活性な溶媒を用いて行うのが有利である。このよう な溶媒としては、反応が進行する限り特に限定されないが、例えばエーテル系溶媒、 脂肪族炭化水素系溶媒、アミド系溶媒、ハロゲン化炭化水素系溶媒、二トリル系溶媒 、ケトン系溶媒、スルホキシド系溶媒、芳香族系溶媒、水などの溶媒またはこれら二 種以上の混合物などが好ま 、。
ここで、エーテル系溶媒、脂肪族炭化水素系溶媒、アミド系溶媒、ハロゲンィ匕炭化 水素系溶媒、二トリル系溶媒、ケトン系溶媒、スルホキシド系溶媒および芳香族系溶 媒としては、前記反応式 1にお 、て例示したものが用いられる。
反応温度は約— 20°Cないし約 200°C、好ましくは約 0°Cないし約 150°Cである。反 応時間は通常約 5分ないし約 48時間、好ましくは約 10分ないし約 24時間である。 化合物 (I)のうち Kが置換されて 、てもよ 、イミノ基を示す化合物は、化合物 (V)と、 式 RNHで示されるァミンおよび活性カルボ二ルイ匕合物〔例、ホスゲン、炭酸ビス(トリ
2
クロロメチル)、 N, N,一カルボ-ルジイミダゾール、クロ口炭酸イソブチル〕とを縮合さ せること〖こより製造することちでさる。
式 RNHで示されるァミンの使用量は、化合物(V) 1モルに対し、約 1ないし約 3モ
2
ル、好ましくは約 1ないし約 2モルである。
活性カルボニル化合物の使用量は、化合物 (V) 1モルに対し、約 1ないし約 10モ ル、好ましくは約 1ないし約 5モルである。
本反応は、所望により塩基の存在下で行うことができる。「塩基」としては、例えば前 記反応式 1において例示した強塩基、無機塩基、塩基性複素環化合物が挙げられる 。塩基の使用量は、化合物 (V) 1モルに対し、約 1ないし約 10モル、好ましくは約 1な いし約 5モルである。
本反応は無溶媒または反応に不活性な溶媒を用いて行うのが有利である。このよう
な溶媒としては、反応が進行する限り特に限定されないが、例えばエーテル系溶媒、 脂肪族炭化水素系溶媒、アミド系溶媒、ハロゲン化炭化水素系溶媒、二トリル系溶媒 、ケトン系溶媒、スルホキシド系溶媒、芳香族系溶媒などの溶媒またはこれら二種以 上の混合物などが好まし 、。
ここで、エーテル系溶媒、脂肪族炭化水素系溶媒、アミド系溶媒、ハロゲンィ匕炭化 水素系溶媒、二トリル系溶媒、ケトン系溶媒、スルホキシド系溶媒および芳香族系溶 媒としては、前記反応式 1にお 、て例示したものが用いられる。
反応温度は約— 20°Cないし約 200°C、好ましくは約— 10°Cないし約 100°Cである 。反応時間は通常約 5分ないし約 48時間、好ましくは約 10分ないし約 24時間である
[0070] このようにして得られたィ匕合物 (I)にお 、て、分子内の官能基は、 自体公知の化学 反応を組み合わせることにより目的の官能基に変換することもできる。ここで、化学反 応の例としては、酸化反応、還元反応、アルキル化反応、加水分解反応、アミノ化反 応、エステルイ匕反応、ァリールカップリング反応、脱保護反応などが挙げられる。
[0071] 上記製造法にお!、て、原料ィ匕合物が置換基としてアミノ基、カルボキシ基、ヒドロキ シ基、カルボ二ル基を有する場合、これらの基にペプチドィ匕学などで一般的に用いら れるような保護基が導入されていてもよぐ反応後に必要に応じて保護基を除去する ことにより目的ィ匕合物を得ることができる。
ァミノ基の保護基としては、例えば、ホルミル基、 C アルキル カルボニル基 (例、
1 -6
ァセチル、プロピオ-ル)、 c アルコキシ カルボ-ル基 (例、メトキシカルボ-ル、
1 -6
エトキシカルボ-ル、 tert ブトキシカルボ-ル)、ベンゾィル基、 C ァラルキル
7- 10
カルボ-ル基 (例、ベンジルカルボニル)、 C ァラルキルォキシ カルボ-ル基 (例
7- 14
、ベンジルォキシカルボニル、 9 フルォレニルメトキシカルボ二ル)、トリチル基、フタ ロイル基、 Ν,Ν ジメチルアミノメチレン基、置換シリル基 (例、トリメチルシリル、トリエ チルシリル、ジメチルフヱニルシリル、 tert ブチルジメチルシリル、 tert ブチルジェ チルシリル)、 C アルケニル基 (例、 1ーァリル)などが挙げられる。これらの基は、ノヽ
2-6
ロゲン原子、 C アルコキシ基 (例、メトキシ、エトキシ、プロポキシ)およびニトロ基から
1 -6
選ばれる 1な!/、し 3個の置換基で置換されて!/、てもよ!/、。
カルボキシ基の保護基としては、例えば、 C アルキル基 (例、メチル、ェチル、プ
1 - 6
口ピル、イソプロピル、ブチル、 tert ブチル)、 C ァラルキル基 (例、ベンジル)、フ
7- 11
ェ-ル基、トリチル基、置換シリル基 (例、トリメチルシリル、トリェチルシリル、ジメチル フエニルシリル、 tert ブチルジメチルシリル、 tert ブチルジェチルシリル)、 C ァ
2-6 ルケニル基 (例、 1ーァリル)などが挙げられる。これらの基は、ハロゲン原子、 C 了
1 -6 ルコキシ基 (例、メトキシ、エトキシ、プロポキシ)および-トロ基力も選ばれる 1ないし 3 個の置換基で置換されて 、てもよ 、。
ヒドロキシ基の保護基としては、例えば、 C アルキル基 (例、メチル、ェチル、プロ
1 -6
ピル、イソプロピル、ブチル、 tert ブチル)、フエニル基、トリチル基、 C ァラルキ
7- 10 ル基 (例、ベンジル)、ホルミル基、 C アルキル カルボニル基 (例、ァセチル、プロ
1 - 6
ピオ二ル)、ベンゾィル基、 c ァラルキル カルボニル基 (例、ベンジルカルボニル
7- 10
), 2—テトラヒドロビラ-ル基、 2—テトラヒドロフラ-ル基、置換シリル (例、トリメチルシ リル、トリェチルシリル、ジメチルフヱニルシリル、 tert ブチルジメチルシリル、 tert— ブチルジェチルシリル)、 C アルケニル基 (例、 1ーァリル)などが挙げられる。これら
2- 6
の基は、ハロゲン原子、 C アルキル基 (例、メチル、ェチル、 n—プロピル)、 C ァ
1 -6 1 -6 ルコキシ基 (例、メトキシ、エトキシ、プロポキシ)および-トロ基力も選ばれる 1ないし 3 個の置換基で置換されて 、てもよ 、。
カルボニル基の保護基としては、例えば、環状ァセタール (例、 1, 3 ジォキサン)、 非環状ァセタール (例、ジー C アルキルァセタール)などが挙げられる。
1 -6
上記した保護基の除去方法は、自体公知の方法、例えば、プロテクティブグルー プスインォー刀ニックシンセシス (Protective Groups in Organic Synthesis)、 John Wiley and Sons刊(1980)に記載の方法などに準じて行うことができる。具体的には、 酸、塩基、紫外光、ヒドラジン、フエ-ルヒドラジン、 N メチルジチォ力ルバミン酸ナト リウム、テトラプチルアンモ -ゥムフルオリド、酢酸パラジウム、トリアルキルシリルハラ イド (例えば、トリメチルシリルョージド、トリメチルシリルプロミドなど)などを使用する方 法、還元法などが用いられる。
上記製造法により得られた化合物 (I)は、公知の手段、例えば、溶媒抽出、液性変 換、転溶、晶出、再結晶、クロマトグラフィーなどによって単離精製することができる。
[0073] 化合物 (I)が、光学異性体、立体異性体、位置異性体、回転異性体を含有する場 合には、これらも化合物 (I)として含有されるとともに、自体公知の合成手法、分離手 法によりそれぞれを単品として得ることができる。例えば、化合物 (I)に光学異性体が 存在する場合には、該化合物から分割された光学異性体も化合物 (I)に包含される ここで、光学異性体は自体公知の方法により製造することができる。
[0074] 化合物 (I)は、結晶であってもよ 、。
化合物 (I)の結晶(以下、本発明の結晶と略記することがある)は、化合物 (I)に自 体公知の結晶化法を適用して、結晶化することによって製造することができる。
[0075] 本明細書中、融点は、例えば、微量融点測定器 (ャナコ、 MP— 500D型または Bu chi、 B— 545型)または DSC (示差走査熱量分析)装置(SEIKO、 EXSTAR6000 )等を用いて測定される融点を意味する。
一般に、融点は、測定機器、測定条件などによって変動する場合がある。本明細書 中の結晶は、通常の誤差範囲内であれば、本明細書に記載の融点と異なる値を示 す結晶であってもよい。
本発明の結晶は、物理ィ匕学的性質 (例、融点、溶解度、安定性など)および生物学 的性質 (例、体内動態 (吸収性、分布、代謝、排泄)、薬効発現など)に優れ、医薬と して極めて有用である。
実施例
[0076] 本発明は、以下の参考例、実施例、実験例および製剤例によって、さらに詳しく説 明されるが、これらは本発明を限定するものではなぐまた本発明の範囲を逸脱しな V、範囲で変化させてもよ!、。
なお、参考例および実施例中の略号は次の意味を有する。
s :シングレット、
d:ダブレット、
t :トリプレット、
q :クワルテット、
m:マルチプレット、
br:ブロード、
J :カップリング定数、
HOBt: 1-ヒドロキシ- 1H-ベンゾトリァゾール、
DMF: Ν,Ν-ジメチルホルムアミド、
EDC -HC1: 1-ェチル -3- (3-ジメチルァミノプロピル)カルボジイミド 塩酸塩、
AcOEt:酢酸ェチル、
THF:テトラヒドロフラン。
また、参考例および実施例中、%は特記しない限り重量%を示す。
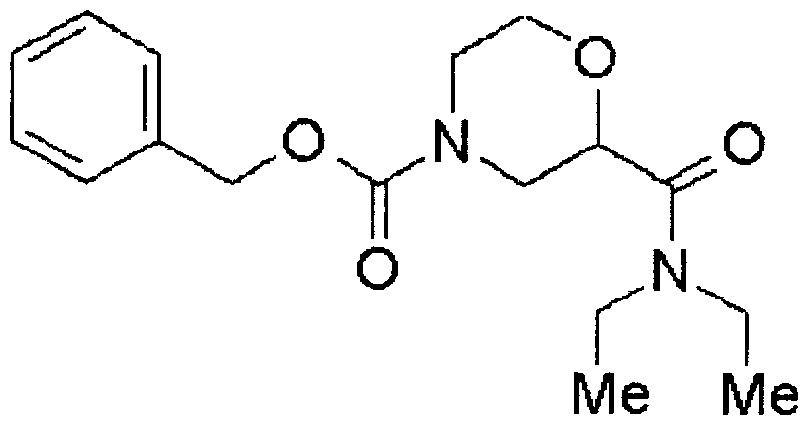
[0077] 参考例 1 1-ベンジル 4-tert-ブチル 2- (モルホリン- 4-ィルカルボ-ル)ピぺラジン- 1
4-ジカルボキシレート
[0078] [化 5]
[0079] 1- [(ベンジルォキシ)カルボ-ル]- 4-(tert-ブトキシカルボ-ル)ピぺラジン- 2-カルボ ン酸(2.95 g, 8.10 mmol)、モルホリン(0.847 ml, 9.71 mmoi;^HOBt (1.24 g, 8.10 mmol)の DMF (10 ml)溶液に、 EDC 'HC1 (1.55 g, 8.10 mmol)を氷冷下加え、室温で 16時間攪拌した。反応液を酢酸ェチルに溶かし、 0.5N塩酸、炭酸カリウム水溶液と 飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥した。溶媒を減圧下留去し、得られ た残渣を NH-シリカゲルカラムクロマトグラフィー(展開溶媒;酢酸ェチル)に通し、表 題ィ匕合物 3.51 g (定量的)を油状物として得た。これ以上精製することなく参考例 2に 進んだ。
[0080] 参考例 2 ベンジル 2- (モルホリン- 4-ィルカルボ-ル)ピぺラジン- 1-カルボキシレー 卜
ヽ
[0082] 参考例 1で得られた 1-ベンジル 4-tert-ブチル 2- (モルホリン- 4-ィルカルボ-ル)ピ ペラジン- 1,4-ジカルボキシレート(3.51 g, 8.10 mmol)に 4N HCFAcOEt (40 ml)をカロ え、 2時間後に溶媒を減圧下留去した。残渣を水に溶かし、炭酸カリウムを加え塩基 性とした後、酢酸ェチルで抽出した。抽出液を飽和食塩水で洗浄後、無水硫酸ナトリ ゥムで乾燥した。溶媒を減圧下留去し、表題ィ匕合物 2.51 g (収率 92.9%)を油状物とし て得た。これ以上精製することなく参考例 3に進んだ。
[0083] 参考例 3 ベンジル 4-[l-(tert-ブトキシカルボ-ル)ピぺリジン- 4-ィル] -2- (モルホリ ン -4-ィルカルボニル)ピぺラジン- 1-カルボキシレート
[0084] [化 7]
[0085] 参考例 2で得られたベンジル 2- (モルホリン- 4-ィルカルボ-ル)ピぺラジン- 1-カル ボキシレート(2.51 g, 7.53 mmol)、 tert-ブチル 4-ォキソピペリジン- 1-カルボキシレ ート(1.53 g, 7.53 mmol)と酢酸(0.431 ml, 7.53 mmol)の THF (30 ml)溶液にトリァセト キシ水素化ホウ素ナトリウム (2.39 g, 11.3 mmol)をカ卩え、室温で 16時間攪拌した後、 溶媒を減圧下留去した。残渣に酢酸ェチルを加え、炭酸カリウム水溶液と飽和食塩 水で洗浄後、無水硫酸ナトリウムで乾燥した。溶媒を減圧下留去し、得られた残渣を シリカゲルカラムクロマトグラフィー(展開溶媒;へキサン-酢酸ェチル = 1: 1から酢酸
ェチル)で精製し、表題ィ匕合物 1.73 g (収率 44.5%)を油状物として得た。
EI(pos) 517.2 [M+H]+
[0086] 参考例 4 tert-ブチル 4-[3- (モルホリン- 4-ィルカルボ-ル)ピぺラジン- 1-ィル]ピぺ リジン- 1-力ノレボキシレート
[0087] [化 8]
[0088] 参考例 3で得られたベンジノレ 4-[l-(tert-ブトキシカルボ-ル)ピぺリジン- 4-ィル] -2 -(モルホリン- 4-ィルカルボ-ル)ピぺラジン- 1-カルボキシレート(1.72 g, 3.32 mmol) と 10%パラジウム炭素(1 g)に THF (20 ml)をカ卩え、水素雰囲気下に室温で 16時間攪 拌した。反応液をセライトろ過し、溶媒を減圧下留去することにより表題化合物 1.27 g (定量的)を油状物として得た。これ以上精製することなく参考例 5に進んだ。
[0089] 参考例 5 tert-ブチル 4-[3- (モルホリン- 4-ィルカルボ-ル) -4- (トリフルォロアセチ ル)ピぺラジン- 1-ィル]ピぺリジン- 1-カルボキシレート
[0090] [化 9]
参考例 4で得られた tert-ブチル 4-[3- (モルホリン- 4-ィルカルボ-ル)ピぺラジン- 1 -ィル]ピぺリジン- 1-カルボキシレート(1.27 g, 3.32 mmol)を THF (20 ml)に溶かし、 氷冷下でトリェチルァミン(0.693 ml, 4.98 mmol)とトリフルォロ酢酸無水物(0.563 ml,
3.99 mmol)を加え、室温で 3時間攪拌した後、溶媒を減圧下留去した。残渣に酢酸 ェチルを加え、炭酸水素ナトリウム水溶液と飽和食塩水で洗浄後、無水硫酸ナトリウ ムで乾燥した。溶媒を減圧下留去し、表題ィ匕合物 1.31 g (収率 82.4%)を油状物として 得た。
EI(pos) 479.2 [M+H]+
[0092] 参考例 6 4-{[4- (ピペリジン- 4-ィル) -1- (トリフルォロアセチル)ピぺラジン- 2-ィル]力 ルボニル}モルホリン二塩酸塩
[0093] [化 10]
[0094] 参考例 5で得られた tert-ブチル 4-[3- (モルホリン- 4-ィルカルボ-ル) -4- (トリフル ォロアセチル)ピぺラジン- 1-ィル]ピぺリジン- 1-カルボキシレート(1.31 g, 2.74 mmol) に 4N塩ィ匕水素-酢酸ェチル(15 ml)を加えた。反応液を 2時間攪拌した後、溶媒を減 圧下留去して、油状物 1.22 g (収率 98.2%)を得た。
[0095] 参考例 7 3-({4- [3- (モルホリン- 4-ィルカルボ-ル) -4- (トリフルォロアセチル)ピペラ ジン- 1-ィル]ピぺリジン- 1-ィル }カルボ二ル)- 1-ベンゾチォフェン- 2-ァミン
[0096] [化 11]
[0097] 参考例 6で得られた 4-{[4- (ピペリジン- 4-ィル) -1- (トリフルォロアセチル)ピぺラジン -2-ィル]カルボ-ル}モルホリン二塩酸塩(500 mg, 1.11 mmol)と 2-ァミノ- 1-ベンゾ チォフェン- 3-カルボン酸(214 mg, 1.11 mmol)を用いて、参考例 1と同様の操作を行 うことにより、表題ィ匕合物 407 mg (収率 66.5%)を得た。
EI(pos) 554.1 [M+H]+
[0098] 参考例 8 ベンジル 2- [(ジェチルァミノ)カルボ-ル]モルホリン- 4-カルボキシレート [0099] [化 12]
[0100] 4- [(ベンジルォキシ)カルボ-ル]モルホリン- 2-カルボン酸(4.35 g, 16.4 mmol)とジ ェチルァミン(1.87 ml, 18.0 mmol)を用いて、参考例 1と同様の操作を行い、ジィソプ 口ピルエーテルで粉末にすることにより、表題ィ匕合物 4.68 g (収率 89.2%)を得た。これ 以上精製することなく参考例 9に進んだ。
[0101] 参考例 9 Ν,Ν-ジェチルモルホリン- 2-カルボキサミド
[0102] [化 13]
Me Me
[0103] 参考例 8で得られたベンジル 2- [(ジェチルァミノ)カルボ-ル]モルホリン- 4-カルボ キシレート(4.68 g, 14.6 mmol)を用いて、参考例 4と同様の操作を行うことにより、表 題ィ匕合物 2.39 g (収率 87.9%)を得た。これ以上精製することなく参考例 10に進んだ。
[0104] 参考例 10 ベンジル 4-{2- [(ジェチルァミノ)カルボ-ル]モルホリン- 4-ィル }ピベリジ ン -1-カルボキシレート塩酸塩
[0105] [化 14]
[0106] 参考例 9で得られた Ν,Ν-ジェチルモルホリン- 2-カルボキサミド(2.39 g, 12.8 mmol) とべンジル 4-ォキソピペリジン- 1-カルボキシレート(3.29 g, 14.1 mmol)を用いて、 参考例 3と同様の操作を行い、得られた油状物に 4N塩ィ匕水素-酢酸ェチル (3.2 ml) を加え、ジイソプロピルエーテルで粉末にすることにより、表題ィ匕合物 5.65 g (定量的 )を得た。
[0107] 参考例 11 Ν,Ν-ジェチル -4- (ピペリジン- 4-ィル)モルホリン- 2-カルボキサミド塩酸 塩
[0108] [化 15]
Me Me
[0109] 参考例 10で得られたベンジル 4-{2- [(ジェチルァミノ)カルボ-ル]モルホリン- 4-ィ ル}ピペリジン- 1-カルボキシレート塩酸塩(5.50 g, 12.5 mmol)を用いて、参考例 4と 同様の操作を行うことにより、表題ィ匕合物 3.32 g (収率 87.0%)を得た。これ以上精製 することなく参考例 12に進んだ。
[0110] 参考例 12 4-{1-[(2-ァミノ- 1-ベンゾチォフェン- 3-ィル)カルボ-ル]ピぺリジン- 4-ィ
}-N,N-ジェチルモルホリン- 2-カルボキサミド
[0111] [化 16]
[0112] 参考例 11で得られた Ν,Ν-ジェチル -4- (ピペリジン- 4-ィル)モルホリン- 2-カルボキ サミド塩酸塩(480 mg, 1.57 mmol)と 2-ァミノ- 1-ベンゾチォフェン- 3-カルボン酸(30 3 mg, 1.57 mmol)を用いて、参考例 1と同様の操作を行うことにより、表題化合物 393 mg (収率 56.3%)を得た。
EI(pos) 445.1 [M+H]+
[0113] 参考例 13 Ν,Ν-ジェチル- 3- (ピリジン- 4-ィル)ベンズアミド
[0114] [化 17]
[0115] 3-ブロモ -Ν,Ν-ジェチルベンズアミド(3.00 g, 11.7 mmol)、ピリジン- 4-ィルボロン酸 (2.88 g, 23.4 mmol)、 2規定炭酸ナトリウム水溶液(11.7 ml)のテトラヒドロフラン(120 ml)溶液に窒素雰囲気下でテトラキストリフエ-ルホスフィンパラジウム(406 mg, 0.351 mmol)を加え、 1日間加熱還流した。室温まで冷却した後、酢酸ェチルをカ卩え、水層 を分離し、無水硫酸ナトリウムで乾燥した。溶媒を減圧下留去し、得られた残渣をシリ 力ゲルカラムクロマトグラフィー(展開溶媒;へキサン-酢酸ェチル = 1: 1から酢酸ェチ ル)で精製し、表題ィ匕合物 2.05 g (収率 68.8%)を油状物として得た。
EI(pos) 255.2 [M+H]+
[0116] 参考例 14 tert-ブチル 4-{3- [(ジェチルァミノ)カルボ-ル]フエ-ル}ピペリジン- 1- カルボキシレート
[0117] [化 18]
[0118] 参考例 13で得られた Ν,Ν-ジェチル -3- (ピリジン- 4-ィル)ベンズアミド(1.73 g, 6.80 mmol)とロジウム炭素(700 mg)の酢酸(40 ml)懸濁液を 0.5 MPaの水素雰囲気下に 8 0°Cで 5時間攪拌した。反応終了後、ロジウム炭素をろ過で除き、ろ液を減圧下濃縮 した。得られた残渣、炭酸カリウム(2.82 g, 20.4 mmol)のテトラヒドロフラン (50 ml)と 水(50 ml)溶液に、二炭酸ジ tert-ブチル(1.56 ml, 6.80 mmol)をカ卩ぇ 16時間攪拌し た。酢酸ェチルをカ卩え、水層を分離後、 0.5N塩酸、炭酸カリウム水溶液と飽和食塩 水で洗浄後、無水硫酸ナトリウムで乾燥した。溶媒を減圧下留去し、得られた残渣を シリカゲルカラムクロマトグラフィー(展開溶媒;へキサン:酢酸ェチル = 3: 1から 1: 1) に通し、表題ィ匕合物 1.23 g (収率 50.2%)を油状物として得た。
EI(pos) 361.0 [M+H]+
[0119] 参考例 15 Ν,Ν-ジェチル- 3- (ピペリジン- 4-ィル)ベンズアミド塩酸塩
[0120] [化 19]
[0121] 参考例 14で得られた tert-ブチル 4-{3- [(ジェチルァミノ)カルボ-ル]フエ-ル}ピぺ リジン- 1-カルボキシレート(1.23 g, 3.41 mmol)を用いて、参考例 6と同様の操作を行 うことにより、表題化合物 906 mg (収率 89.7%)を得た。これ以上精製することなく参考 例 16に進んだ。
[0122] 参考例 16 3-{1-[(2-ァミノ- 1-ベンゾチォフェン- 3-ィル)カルボ-ル]ピぺリジン- 4-ィ ル}- Ν,Ν-ジェチルベンズアミド
[0123]
[0124] 参考例 15で得られた Ν,Ν-ジェチル -3- (ピペリジン- 4-ィル)ベンズアミド塩酸塩(20 6 mg, 0.694 mmol)と 2-ァミノ- 1-ベンゾチォフェン- 3-カルボン酸(134 mg, 0.694 mm ol)を用いて、参考例 1と同様の操作を行うことにより、表題化合物 230 mg (収率 76.2% )を得た。
EI(pos) 436.0 [M+H]+
[0125] 参考例 17 1 '-[(2-ァミノ- 1-ベンゾチォフェン- 3-ィル)カルボ-ル]- Ν,Ν-ジェチル -1 ,4'-ビピペリジン- 3-カルボキサミド
[0126] [化 21]
[0127] Ν,Ν-ジェチル- 1,4'-ビピペリジン- 3-カルボキサミド 2塩酸塩(220 mg, 0.646 mmol )と 2-ァミノ- 1-ベンゾチォフェン- 3-カルボン酸(124 mg, 0.646 mmol)を用いて、参考 例 1と同様の操作を行うことにより、表題化合物 198 mg (収率 69.1%)を得た。
EI(pos) 443.0 [M+H]+
[0128] 参考例 18 3-{[3- (モルホリン- 4-ィルカルボ-ル) -1 ,4'-ビピペリジン- 1しィル]カルボ 二ル}-1-ベンゾチォフェン- 2-ァミン
[0129] [化 22]
[0130] 3- (モルホリン- 4-ィルカルボ-ル)- 1,4'-ビピペリジン 2塩酸塩(600 mg, 1.69 mmol) と 2-ァミノ- 1-ベンゾチォフェン- 3-カルボン酸(327 mg, 1.69 mmol)を用いて、参考例 1と同様の操作を行うことにより、表題化合物 533 mg (収率 65.0%)を得た。本化合物は 、これ以上精製することなく次の反応に用いた。
[0131] 参考例 19 2-ァミノ- 7-ォキソ -4,5,6,7-テトラヒドロ- 1-ベンゾチォフェン- 3-カルボン 酸
[0132] [化 23]
H
[0133] ェチル 2-ァミノ- 7-ォキソ - 4,5,6,7-テトラヒドロ- 1-ベンゾチォフェン- 3-カルボキレ ート(885 mg, 3.70 mmol)にエタノール(9 mL)と 2規定水酸化ナトリウム水溶液(3.70 mL, 7.40 mmol)をカ卩え、 80°Cで 3時間加熱した。溶媒を減圧下留去し、残渣を水に溶 かし、 1規定塩酸を加え、酢酸ェチルで抽出した。抽出液を飽和食塩水で洗浄後、 無水硫酸ナトリウムで乾燥した。溶媒を減圧下留去し、得られた残渣をシリカゲルカラ ムクロマトグラフィー(展開溶媒;酢酸ェチル)で精製し、ジイソプロピルエーテルで粉 末にすることにより、表題化合物 233 mg (収率 29.8%)を得た。
1H NMR (DMSO-d ) δ 1.98 (2Η, m), 2.37 (2H, t, J = 6.3 Hz), 2.93 (2H, t, J = 6.0 H
6
z), 8.24 (2H, s), 12.53 (1H, s).
[0134] 参考例 20 2-ァミノ- 3- {[3- (モルホリン- 4-ィルカルボ-ル)- 1,4'-ビピペリジン- 1しィ ル]カルボ-ル}-5,6-ジヒドロ- 1-ベンゾチォフェン- 7(4H)_オン
[0135] [化 24]
3- (モルホリン- 4-ィルカルボ-ル)- 1,4'-ビピペリジン 2塩酸塩(200 mg, 0.564 mmol )と参考例 19で得られた 2-ァミノ- 7-ォキソ -4,5,6,7-テトラヒドロ- 1-ベンゾチォフェン- 3-カルボン酸(119 mg, 0.564 mmol)を用いて、参考例 1と同様の操作を行うことにより 、表題化合物 20 mg (収率 7.5%)を得た。
EI(pos) 475.1 [M+H]+
[0137] 参考例 21 2-[(tert-ブトキシカルボ-ル)ァミノ] -5-フエ-ルチオフェン- 3-カルボン 酸メチル
[0138] [化 25]
[0139] 2-ァミノ- 5-フエ-ルチオフェン- 3-カルボン酸メチル(10.3 g, 44.2 mmol)のテトラヒ ドロフラン- tert-ブタノール(50 ml-200 ml)混合溶媒中に二炭酸ジ- tert-ブチル(12. 2 ml, 53.0 mmol)と 4-ジメチルァミノピリジン(270 mg, 2.21 mmol)を加え、室温で 14時 間撹拌した。反応液を減圧下濃縮し、得られた白色固体を酢酸ェチルで洗浄して、 表題ィ匕合物 9.18 g (収率 62.3%)を得た。
JH NMR (CDC1 ) δ 1.55 (9Η, s), 3.89 (3H, s), 7.23-7.28 (1H, m), 7.33-7.38 (3H, m
3
), 7.55-7.58 (2H, m), 10.06 (1H, brs).
[0140] 参考例 22 2-[(tert-ブトキシカルボ-ル)ァミノ] -5-フエ-ルチオフェン- 3-カルボン 酸
[0141] [化 26]
参考例 21で得られた 2-[(tert-ブトキシカルボ-ル)ァミノ] -5-フエ-ルチオフェン- 3- カルボン酸メチル(2.00 g, 6.00 mmol)を用いて、参考例 19と同様の操作を行うことに
より、表題ィ匕合物 1.73 g (収率 90.0%)を得た。
1H NMR (CDC1 ) δ 1.58 (9Η, s), 7.27-7.30 (IH, m), 7.35-7.40 (2H, m), 7.43 (IH, d
3
, J = 0.8 Hz), 7.56-7.59 (2H, m), 9.88 (IH, brs).
[0143] 参考例 23 tert-ブチル [3- ({3- [(ジェチルァミノ)カルボ-ル]- 1,4'-ビピペリジン- 1'- ィル }カルボ二ル)- 5-フエニル- 2-チェニル]力ルバメート
[0144] [化 27]
[0145] Ν,Ν-ジェチル- 1,4'-ビピペリジン- 3-カルボキサミド 2塩酸塩(218 mg, 0.641 mmol )と参考例 22で得られた 2-[(tert-ブトキシカルボ-ル)ァミノ] -5-フエ-ルチオフェン- 3-カルボン酸(205 mg, 0.641 mmol)を用いて、参考例 1と同様の操作を行うことにより 、表題化合物 295 mg (収率 80.9%)を得た。
EI(pos) 569.1 [M+H]+
[0146] 参考例 24 1'- [(2-ァミノ- 5-フエ-ル- 3-チェ-ル)カルボ-ル]- Ν,Ν-ジェチル- 1,4'- ビピペリジン- 3-カルボキサミド
[0147] [化 28]
[0148] 参考例 23で得られた tert-ブチル [3-({3- [(ジェチルァミノ)カルボ-ル] -1 ,4'-ビピ
ペリジン- 1'-ィル }カルボ二ル)- 5-フエニル- 2-チェニル]力ルバメート(284 mg, 0.499 mmol)をトリフルォロ酢酸 (2.5 mL)に溶かし、 1時間後に減圧下濃縮した。残渣を酢 酸ェチルに溶かし、炭酸カリウム水溶液と飽和食塩水で洗浄した。溶媒を減圧下留 去し、 NH-シリカゲルカラムクロマトグラフィー(展開溶媒;酢酸ェチル)で精製し、表 題化合物 221 mg (収率 94.4%)を油状物として得た。
EI(pos) 469.0 [M+H]+
[0149] 参考例 25 tert-ブチル(3-{[3- (モルホリン- 4-ィルカルボ-ル) -1,4'-ビピペリジン- 1
-ィル]カルボ二ル}-5-フエニル- 2-チェニル)力ルバメート
[0150] [化 29]
[0151] 3- (モルホリン- 4-ィルカルボ-ル)- 1,4'-ビピペリジン 2塩酸塩(500 mg, 1.41 mmol) と参考例 22で得られた 2-[(tert-ブトキシカルボ-ル)ァミノ] -5-フエ-ルチオフェン- 3 -カルボン酸 (451 mg, 1.41 mmol)を用いて、参考例 1と同様の操作を行うことにより、 表題化合物 698 mg (収率 84.9%)を得た。
EI(pos) 583.1 [M+H]+
[0152] 参考例 26 3-{[3- (モルホリン- 4-ィルカルボ-ル) -1 ,4'-ビピペリジン- 1しィル]カルボ
-ル }-5-フエ-ルチオフェン- 2-ァミン
[0153] [化 30]
[0154] 参考例 25で得られた tert-ブチル(3-{[3- (モルホリン- 4-ィルカルボ-ル) -1 ,4'-ビピ ペリジン- 1'-ィル]カルボ-ル}- 5-フエ-ル- 2-チェ-ル)力ルバメート(697 mg, 1.20 m mol)を用いて、後述の実施例 13と同様の操作を行うことにより、表題ィ匕合物 491 mg ( 収率 85.2%)を得た。
EI(pos) 483.0 [M+H]+
[0155] 参考例 27 5-ァミノ- 2-フエ-ル- 1,3-チアゾール -4-カルボン酸
[0156] [化 31]
[0157] ェチル 5-ァミノ- 2-フエ-ル- 1,3-チアゾール -4-カルボキシレート(480 mg, 1.93 m mol)を用いて、参考例 19と同様の操作を行うことにより、表題化合物 338 mg (収率 79 .3%)を得た。
1H NMR (DMSO-d ) δ 7.35-7.46 (3Η, m), 7.50 (2H, s), 7.73 (2H, m), 12.17 (1H, s)
[0158] 参考例 28 4-{[3- (モルホリン- 4-ィルカルボ-ル) -1 ,4'-ビピペリジン- 1しィル]カルボ
-ル }- 2-フエ-ル- 1 ,3-チアゾール -5-ァミン
[0159] [化 32]
[0160] 3- (モルホリン- 4-ィルカルボ-ル)- 1,4'-ビピペリジン 2塩酸塩(331 mg, 0.935 mmol )と参考例 27で得られた 5-ァミノ- 2-フエ-ル- 1,3-チアゾール -4-カルボン酸(206 mg ,0.935 mmol)を用いて、参考例 1と同様の操作を行うことにより、表題化合物 340 mg( 収率 75.2%)を得た。
EI(pos) 484.0 [M+H]+
[0161] 参考例 29 ェチル 2- (ァセチルァミノ)- 6-ブロモ -7-ォキソ -4,5,6,7-テトラヒドロ- 1-ベ ンゾチォフェン- 3-カルボキシレート
[0162] [化 33]
[0163] ェチル 2- (ァセチルァミノ)- 7-ォキソ -4,5,6,7-テトラヒドロ- 1-ベンゾチォフェン- 3-力 ルボキシレート(8.00 g, 28.4 mmol)のクロ口ホルム(80 mL)溶液に、臭素(1.5 mL, 29 .8 mmol)のクロ口ホルム(15 mL)溶液を加熱還流下で 20分間かけて滴下し、同温度 で 1.5時間撹拌した。この溶液を飽和食塩水で 3回洗浄後、無水硫酸マグネシウムで 乾燥した。溶媒を減圧下留去し、得られた残渣をシリカゲルカラムクロマトグラフィー( 展開溶媒;酢酸ェチル:へキサン = 1 : 1から 1 : 0)で精製して、表題化合物 9.07 g (収 率 89%)を油状物として得た。
[0164] 参考例 30ェチル 2- (ァセチルァミノ) -7-ヒドロキシ- 1-ベンゾチォフェン- 3-カルボキ シレート
[0165] [化 34]
[0166] 参考例 29で得られたェチル 2- (ァセチルァミノ) -6-ブロモ -7-ォキソ -4,5,6,7-テトラ ヒドロ- 1-ベンゾチォフェン- 3-カルボキシレート(8.11 g, 22.6 mmol)の DMF (50 mL) 溶液に炭酸リチウム (2.50 g, 33.8 mmol)をカ卩えて 90°Cで 5時間撹拌した。さらに炭酸 リチウム(2.50 g, 33.8 mmol)を加えて 90°Cで 3時間撹拌した。反応液を酢酸ェチルで 希釈し、飽和食塩水で 3回洗浄した後、無水硫酸マグネシウムで乾燥した。溶媒を減 圧下留去して、得られた固体をろ取し、へキサン 酢酸ェチルで洗浄することにより 表題ィ匕合物 2.63 g (収率 41%)を得た。
1H NMR (DMSO-d ) δ 1.51 (3Η, t, J = 7.2 Hz), 2.36 (3H, s), 4.48 (2H, q, J = 7.2 H
6
z), 5.35 (IH, s), 6.72 (IH, d, J = 8.5 Hz), 7.30 (IH, m), 7.89 (IH, d, J = 8.1 Hz), 11 .77 (IH, br).
[0167] 参考例 31ェチル 2- (ァセチルァミノ) -7-メトキシ- 1-ベンゾチォフェン- 3-カルボキシ レート
[0168] [化 35]
[0169] 参考例 30で得られたェチル 2- (ァセチルァミノ) -7-ヒドロキシ- 1-ベンゾチォフェン- 3-カルボキシレート(10.0 g, 35.8 mmol)と炭酸カリウム(7.42 g, 53.7 mmol)の DMF(9 0 mL)懸濁液にヨウ化メチル (2.67 mL, 43.0 mmol)をカ卩え、室温で 5時間撹拌した。 反応液を酢酸ェチルで希釈後、水と飽和食塩水で洗浄し、無水硫酸ナトリウムで乾 燥した。この液を塩基性シリカゲルに通し、得られた残渣を酢酸ェチルから再結晶す ることにより、表題ィ匕合物 8.10 g (収率 77%)を固体として得た。
JH NMR (DMSO-d ) δ 1.42 (3Η, t, J = 7.2 Hz), 2.32 (3H, s), 3.95 (3H, s), 4.42 (2H
6
, q, J = 7.2 Hz), 6.92 (IH, d, J = 7.5 Hz), 7.39 (IH, dd, J = 7.5, 8.1 Hz), 7.82 (IH, d, J = 8.1 Hz), 11.37 (IH, s).
[0170] 参考例 32 2-ァミノ- 7-メトキシ- 1-ベンゾチォフェン- 3-カルボン酸
[0171] [化 36]
参考例 31で得られたェチル 2- (ァセチルァミノ) -7-メトキシ- 1-ベンゾチォフェン- 3 カルボキシレート(2.03 g, 6.92 mmol)のエタノール(35 mL)溶液に 8N水酸化ナトリウ
ム水溶液 (8.65 mL, 69.2 mmol)をカ卩え、 90°Cで 1時間撹拌した。反応液を減圧下濃 縮後、水で希釈し、 1N塩酸 (70 mL)を加え、酢酸ェチルで抽出した。抽出液を水と飽 和食塩水で洗浄し、無水硫酸ナトリウムで乾燥した。得られた残渣をジイソプロピルェ 一テルで粉末にすることにより、表題ィ匕合物 1.27 g (収率 82%)を固体として得た。 1H NMR (DMSO-d ) δ 3.87 (3Η, s), 6.69 (1H, d, J = 7.5 Hz), 7.17-7.22 (1H, m), 7.
6
60 (1H, d, J = 8.1 Hz), 7.92 (2H, br), 12.23 (1H, br).
[0173] 参考例 33 5-ブロモ -2-[(tert-ブトキシカルボ-ル)ァミノ]チォフェン- 3-カルボン酸 [0174] [化 37]
[0175] 5-ブロモ -2-[(tert-ブトキシカルボ-ル)ァミノ]チォフェン- 3-カルボン酸メチル(2.00 g, 5.95 mmol)を用いて、参考例 19と同様の操作を行うことにより、表題ィ匕合物 1.05 g (収率 55%)を黄色固体として得た。
JH NMR (DMSO-d ) δ 1.50 (9Η, s), 7.20 (1Η, s), 10.20 (1H, br).
6
[0176] 参考例 34 tert-ブチル(5-ブロモ -3-{[(3R)-3- (モルホリン- 4-ィルカルボ-ル) -1,4'- ビピペリジン- 1'-ィル]カルボ二ル}-2-チェニル)力ルバメート
[0177] [化 38]
[0178] (3R)-3- (モルホリン- 4-ィルカルボ-ル) -1,4'-ビピペリジン 2塩酸塩(1.70 g, 4.80 m mol)と参考例 33で得られた 5-ブロモ -2-[(tert-ブトキシカルボ-ル)ァミノ]チォフェン -3-カルボン酸(1.55 g, 4.80 mmol)を用いて、参考例 1と同様の操作を行うことにより 、表題ィ匕合物 2.76 g (収率 98.3%)を得た。
EI(pos) 586.9 [M+H]+
[0179] 参考例 35 tert-ブチル {3-{[(3R)-3- (モルホリン- 4-ィルカルボ-ル) -1,4'-ビピベリジ ン- 1しィル]カルボ-ル}-5-[4- (トリフルォロメチル)フエ-ル]- 2-チェ-ル}カルバメー 卜
[0180] [化 39]
参考例 34で得られた tert-ブチル(5-ブロモ _3-{[(3R)-3- (モルホリン- 4_ィルカルボ -ル) -1,4'-ビピペリジン- 1しィル]カルボ-ル}- 2-チェ-ル)力ルバメート(400 mg, 0.6
83 mmol)、 [4- (トリフルォロメチル)フエ-ル]ボロン酸(259 mg, 1.37 mmol)および 2規 定炭酸ナトリウム水溶液(0.683 mL)の Ν,Ν-ジメチルホルムアミド(3 mL)溶液に 1,1'-
mg, 0.034 mmol)をカ卩 え、 90°Cで窒素雰囲気下に 16時間撹拌した。反応終了後、酢酸ェチルで希釈し、 飽和食塩水で 3回洗浄した後、無水硫酸ナトリウムで乾燥した。溶媒を減圧下留去し て、得られた残渣をシリカゲルカラムクロマトグラフィー(展開溶媒;酢酸ェチル:メタノ 一ル= 1 : 0から 4 : 1)と塩基性シリカゲルカラムクロマトグラフィー(展開溶媒;へキサ ン:酢酸ェチル = 3 : 1から 0 : 1)で 2回精製して、表題化合物 137 mg (収率 31%)を得 た。
EI(pos) 651.1 [M+H]+
[0182] 参考例 36 3-{[(3R)-3- (モルホリン- 4-ィルカルボ-ル) -1,4しビピペリジン- 1しィル]力 ルポ-ル}-5-[4- (トリフルォロメチル)フエ-ル]チォフェン- 2-ァミン
[0183] [化 40]
[0184] 参考例 35で得られた tert-ブチル {3-{[(3R)-3- (モルホリン- 4-ィルカルボ-ル) -1,4' -ビピペリジン- 1'-ィル]カルボ-ル}- 5- [4- (トリフルォロメチル)フエ-ル]- 2-チェ-ル} 力ルバメート(136 mg, 0.209 mmol)を用いて、参考例 24と同様の操作を行うことによ り、表題化合物 94.6 mg (収率 82.3%)を得た。
EI(pos) 551.1 [M+H]+
[0185] 参考例 37 tert-ブチル(6-クロ口- 4-{[3- (モルホリン- 4-ィルカルボ-ル) -1,4'-ビピぺ リジン- 1'-ィル]カルボ二ル}ピリジン- 3-ィル)力ルバメート
[0186] [化 41]
[0187] 5-[(tert-ブトキシカルボ-ル)ァミノ] -2-クロ口イソニコチン酸(569 mg, 2.09 mmol)と 3- (モルホリン- 4-ィルカルボ-ル)- 1,4'-ビピペリジン 2塩酸塩(704 mg, 1.99 mmol) を用い、参考例 1と同様の操作を行い、ジイソプロピルエーテルとへキサンで粉末に することにより、表題化合物 685 mg (収率 64%)を得た。
EI(pos) 536.1 [M+H]+
[0188] 参考例 38 tert-ブチル(6- [4- (メチルスルホ -ル)フエ-ル]- 4- {[3- (モルホリン- 4-ィ ルカルボニル) -1,4'-ビピペリジン- 1 '-ィル]カルボ二ル}ピリジン- 3-ィル)力ルバメート [0189] [化 42]
参考例 37で得られた tert-ブチル(6-クロ口- 4-{[3- (モルホリン- 4-ィルカルボ-ル) - 1,4'-ビピペリジン- 1しィル]カルボ二ル}ピリジン- 3-ィル)力ルバメート(200 mg, 0.373 mmol)と [4- (メチルスルホ -ル)フエ-ル]ボロン酸(149 mg, 0.746 mmol)を用い、参考 例 13と同様の操作を行い、ジイソプロピルエーテルで粉末にすることにより、表題ィ匕
合物 182 mg (収率 74%)を得た。
EI(pos) 656.3 [M+H]+
[0191] 参考例 39 6- [4- (メチルスルホ -ル)フエ-ル]- 4- {[3- (モルホリン- 4-ィルカルボ-ル) -
1 ,4'-ビピペリジン- 1しィル]カルボ二ル}ピリジン- 3-ァミン
[0192] [化 43]
[0193] 参考例 38で得られた tert-ブチル(6- [4- (メチルスルホ -ル)フエ-ル]- 4- {[3- (モル ホリン- 4-ィルカルボニル) -1,4しビピペリジン- 1'-ィル]カルボ二ル}ピリジン- 3-ィル)力 ルバメート(178 mg, 0.271 mmol)を用い、参考例 24と同様の操作を行い、ジイソプロ ピルエーテルで粉末にすることにより、表題化合物 121 mg (収率 80%)を得た。
EI(pos) 556.0 [M+H]+
[0194] 参考例 40 1'-ベンジル- 1,4'-ビピペリジン- 3-カルボン酸 2塩酸塩
[0195] [化 44]
ェチル 1'-ベンジル- 1,4'-ビピペリジン- 3-カルボキシレート(71.1 g, 0.215 mol)を 濃塩酸 (500 mL)に溶かし、還流下に 16時間撹拌した。反応終了後、減圧下に濃縮 し、テトラヒドロフランで粉末にした。得られた沈殿物を集め、ジイソプロピルエーテル で洗浄することにより、表題化合物 76.7 mg (収率 95%)を粉末として得た。これ以上精 製することなく参考例 41に進んだ。
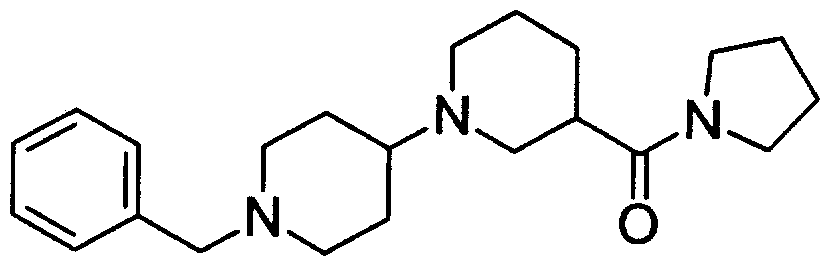
[0197] 参考例 41 1'-ベンジル- 3- (ピロリジン- 1-ィルカルボ-ル)- 1,4'-ビピペリジン
[0198] [化 45]
[0199] 参考例 40で得られた 1'-ベンジル- 1,4'-ビピペリジン- 3-カルボン酸 2塩酸塩(2.00 g, 5.33 mmol)とピロリジン(0.677 mL, 7.99 mmol)を用い、参考例 1と同様の操作を行 うことにより、表題ィ匕合物 1.69 g (収率 90%)を得た。これ以上精製することなく参考例 4 2に進んだ。
[0200] 参考例 42 3- (ピロリジン- 1-ィルカルボ-ル) -1,4しビピペリジン 2塩酸塩
[0201] [化 46]
[0202] 参考例 41で得られた 1'-ベンジル- 3- (ピロリジン- 1-ィルカルボ-ル)- 1,4'-ビピペリ ジン(1.69 g, 4.75 mmol)、 4規定塩化水素 酢酸ェチル(3.57 mL, 14.3 mmol)と 10% ノラジウム炭素(1 g)にメタノール (25 mL)を加え、水素雰囲気下、室温で 16時間攪 拌した。反応液をセライトろ過し、溶媒を減圧下留去することにより表題ィ匕合物 1.61 g (定量的)を油状物として得た。これ以上精製することなく参考例 43に進んだ。
[0203] 参考例 43 3-{[3- (ピロリジン- 1-ィルカルボ-ル) -1 ,4しビピペリジン- 1しィル]カルボ- ル}- 1-ベンゾチォフェン- 2-ァミン
[0204] [化 47]
[0205] 参考例 42で得られた 3- (ピロリジン- 1-ィルカルボ-ル) -1 ,4'-ビピペリジン 2塩酸塩 (554 mg, 1.64 mmol)と 2-ァミノ- 1-ベンゾチォフェン- 3-カルボン酸(288 mg, 1.49 m mol)を用いて、参考例 1と同様の操作を行い、ジイソプロピルエーテルで粉末にする ことにより、表題化合物 357 mg (収率 54%)を得た。
EI(pos) 441.0 [M+H]+
[0206] 参考例 44 1 '-ベンジル- 3- (ピペリジン- 1-ィルカルボ-ル)- 1 ,4'-ビピペリジン
[0207] [化 48]
[0208] 参考例 40で得られた 1'-ベンジル- 1,4'-ビピペリジン- 3-カルボン酸 2塩酸塩(2.00 g, 5.33 mmol)とピペリジン(0.79 mL, 7.99 mmol)を用い、参考例 1と同様の操作を行 うことにより、表題ィ匕合物 1.97 g (定量的)を得た。これ以上精製することなく参考例 45 に進んだ。
[0209] 参考例 45 3- (ピペリジン- 1-ィルカルボ-ル) -1,4しビピペリジン 2塩酸塩
[0210] [化 49]
[0211] 参考例 44で得られた 1'-ベンジル- 3- (ピペリジン- 1-ィルカルボ-ル)- 1,4'-ビピペリ ジン(1.97 g, 5.33 mmol)、 4規定塩化水素 酢酸ェチル(4.0 mL, 16.0 mmol)と 10% パラジウム炭素(1 g)にメタノール (27 mL)をカ卩え、水素雰囲気下に室温で 16時間攪 拌した。反応液をセライトろ過し、溶媒を減圧下留去することにより表題ィ匕合物 1.88 g (定量的)を油状物として得た。これ以上精製することなく参考例 46に進んだ。
[0212] 参考例 46 3-{[3- (ピペリジン- 1-ィルカルボ-ル) -1,4'-ビピペリジン- 1しィル]カルボ 二ル}-1-ベンゾチォフェン- 2-ァミン
[0213] [化 50]
[0214] 参考例 45で得られた 3- (ピペリジン- 1-ィルカルボ-ル) -1,4'-ビピペリジン 2塩酸塩
(575 mg, 1.63 mmol)と 2-ァミノ- 1-ベンゾチォフェン- 3-カルボン酸(287 mg, 1.48 m mol)を用いて、参考例 1と同様の操作を行い、ジイソプロピルエーテルで粉末にする ことにより、表題化合物 316 mg (収率 47%)を得た。
EI(pos) 455.1 [M+H]+
[0215] 参考例 47 7-メトキシ -3-{[3- (ピペリジン- 1-ィルカルボ-ル) -1,4'-ビピペリジン- 1しィ ル]カルボ二ル}-1-ベンゾチォフェン- 2-ァミン
[0216] [化 51]
[0217] 参考例 45で得られた 3- (ピペリジン- 1-ィルカルボ-ル) -1,4'-ビピペリジン 2塩酸塩
(418 mg, 1.19 mmol)と参考例 32で得られた 2-ァミノ- 7-メトキシ- 1-ベンゾチォフェン -3-カルボン酸(265 mg, 1.19 mmol)を用いて、参考例 1と同様の操作を行い、ジイソ プロピルエーテルとへキサンで粉末にすることにより、表題化合物 341 mg (収率 59%) を得た。
EI(pos) 485.1 [M+H]+
[0218] 参考例 48ベンジル 3-{ [ェチル (イソプロピル)ァミノ]カルボ-ル}ピペリジン- 1-カルボ キシレート
[0219] [化 52]
[0220] 1- [(ベンジルォキシ)カルボ-ル]ピぺリジン- 3-カルボン酸(3.00 g, 11.4 mmol)と D MF (2滴)の THF (60 mL)溶液に、氷冷下で塩化ォキザリル(1.47 mL, 17.1 mmol)を 加え、 1時間後、減圧下濃縮した。得られた残渣を THF (60 mL)に溶かし、ェチルイソ プロピルアミン (4.14 mL, 34.2 mmol)を氷冷下でカ卩え、 30分間撹拌した。溶媒を減圧 下留去し、残渣に酢酸ェチルをカ卩え、これを 1N塩酸、 10%炭酸カリウム、飽和食塩水 で洗浄後、無水硫酸ナトリウムで乾燥した。この溶液を塩基性シリカゲルに通すことに より、表題ィ匕合物 3.79 g (定量的)を得た。これ以上精製することなく参考例 49に進ん だ。
[0221] 参考例 49 tert-ブチル 3-{ [ェチル (イソプロピル)ァミノ]カルボ-ル}-1,4'-ビピベリジ ン- 1'-カルボキシレート
[0222] [化 53]
[0223] 参考例 48で得られたベンジル 3-{ [ェチル (イソプロピル)ァミノ]カルボ-ル}ピベリジ ン- 1-カルボキシレート(3.79 g, 11.4 mmol)と 10%パラジウム炭素(2 g)の THF (60 mL )懸濁液を水素雰囲気下に、 16時間撹拌した。触媒をろ過し、ろ液を減圧下濃縮した 。得られた油状物と tert-ブチル 4-ォキソピペリジン- 1-カルボキシレート(2.27 g, 11. 4 mmol)の THF (60 mL)溶液にトリァセトキシ水素化ホウ素ナトリウム(3.62 g, 17.1 m mol)を加え、室温で 16時間撹拌した。溶媒を減圧下留去し、残渣に酢酸ェチルを加 え、これを 10%炭酸カリウムと飽和食塩水で洗浄後、無水硫酸ナトリウムで乾燥した。 この溶液を塩基性シリカゲルに通した後、シリカゲルカラムクロマトグラフィー(展開溶 媒;酢酸ェチル:メタノール = 1 : 0から 9 : 1)で精製することにより、表題ィ匕合物 1.71 g
(収率 39.2%)を得た。
EI(pos) 382.2 [M+H]+
[0224] 参考例 50 N-ェチル -N-イソプロピル- 1,4'-ビピペリジン- 3-カルボキサミド 2塩酸塩 [0225] [化 54]
参考例 49で得られた tert-ブチル 3-{ [ェチル (イソプロピル)ァミノ]カルボ-ル}-1,4'- ビピペリジン- 1'-カルボキシレート(1.70 g, 4.46 mmol)に 4N塩化水素-酢酸ェチル(2 0 mL)を加え、 1時間後減圧下濃縮することにより、表題ィ匕合物 1.58 g (定量的)を得 た。これ以上精製することなく参考例 51に進んだ。
[0226] 参考例 51 1 '-[(2-ァミノ- 7-メトキシ- 1-ベンゾチェン- 3-ィル)カルボ-ル]- N-ェチル- N-イソプロピル- 1,4'-ビピペリジン- 3-カルボキサミド
[0227] [化 55]
[0228] 参考例 50で得られた N-ェチル -N-イソプロピル- 1,4しビピペリジン- 3-カルボキサミ ド 2塩酸塩(381 mg, 1.08 mmol)と参考例 32で得られた 2-ァミノ- 7-メトキシ- 1-ベン ゾチォフェン- 3-カルボン酸(240 mg, 1.08 mmol)を用いて、参考例 1と同様の操作を 行い、ジイソプロピルエーテルとへキサンで粉末にすることにより、表題化合物 381 m g (収率 73%)を得た。
EI(pos) 487.5 [M+H]+
[0229] 参考例 52
3-ァミノ- 6-メチルチエノ [2 , 3-b]ピリジン- 2-カルボン酸ェチル
[0230] [化 56]
[0231] 2-クロ口- 6-メチルニコチノ-トリル(44.0 g, 0.289 mol)とチォグリコール酸ェチル(3 5.0 mL, 0.318 mol)の DMF(500 mL)溶液にナトリウムエトキシド(21.7 g, 0.318 mol) を加えて、室温で 30分間撹拌した。さらに、ナトリウムエトキシド(5.00 g, 73.5 mmol)を 加えて室温で 30分間撹拌した。反応液に水を加えて析出した固体をろ取し、水洗、 乾燥して表題化合物 66.4 g (収率 97%)を黄色固体として得た。
JH NMR (CDC1 ) δ 1.39 (3Η, t, J = 7.2 Hz), 2.68 (3H, s), 4.36 (2H, q, J = 7.2 Hz),
3
5.89 (2H, br), 7.16 (1H, d, J = 8.3 Hz), 7.81 (1H, d, J = 8.3 Hz).
[0232] 参考例 53
3-ブロモ -6-メチルチエノ [2,3-b]ピリジン- 2-カルボン酸ェチル
[0233] [化 57]
[0234] 参考例 52で得られた 3-ァミノ- 6-メチルチエノ [2,3-b]ピリジン- 2-カルボン酸ェチル
(36.1 g, 0.153 mol)を臭化銅(II) (37.5 g, 0.168 mol)と亜硝酸 tert-ブチル(23.6 mL, 0.199 mol)のァセトニトリル(350 mL)混合液に水冷下で 2時間かけて加え、混合物 を 1時間撹拌した。反応液に 1規定塩酸 (700 mL)をゆっくりと加え、生じた沈殿物を ろ取した後、水洗した。この固体を THFに溶かし、酢酸ェチルで希釈した。この溶液 を 1規定塩酸と飽和食塩水で洗浄した後、無水硫酸ナトリウムで乾燥した (溶液 A)。 先のろ液を酢酸ェチルで抽出し、抽出液を飽和食塩水で洗浄し、無水硫酸ナトリウ ムで乾燥した。残渣を塩基性シリカゲルカラムクロマトグラフィー(展開溶媒;酢酸ェチ ル)に付し、粗生成物約 5 gを得た。これを溶液 Aと合わせ、再び塩基性シリカゲル力
ラムクロマトグラフィー(酢酸ェチル)に付した後、へキサン力 結晶化させ、表題化合 物 30.5 g (収率 66%)を淡黄色固体として得た。
1H NMR (CDC1 ) δ 1.35 (3Η, t, J = 7.1 Hz), 2.67 (3H, s), 4.39 (2H, q, J = 7.1 Hz),
3
7.54 (IH, d, J = 8.3 Hz), 8.20 (IH, d, J = 8.3 Hz).
[0235] 参考例 54 3-ブロモ -6-メチルチエノ [2,3-b]ピリジン- 2-カルボン酸
[0236] [化 58]
[0237] 参考例 53で得られた 3-ブロモ -6-メチルチエノ [2,3-b]ピリジン- 2-カルボン酸ェチ ル(79.2 g, 0.264 mol)のエタノール(250 mL)溶液に、 2規定水酸化ナトリウム水溶液 (264 mL, 0.527 mol)をカ卩えて、室温で 16時間撹拌した。反応液を水(1 L)で希釈し 、 1規定塩酸 (530 mL)で pH 5〜6に調製した後、析出した固体を集めて、水で洗浄し た。得られた固体をアセトンに懸濁し、ろ取した後、アセトンとジイソプロピルエーテル で順次洗浄して、表題化合物 68.5 g (収率 95%)を得た。
1H NMR (CDC1 ) δ 2.66 (3Η, s), 7.52 (IH, d, J = 8.5 Hz), 8.18 (IH, d, J = 8.3 Hz),
3
14.06 (IH, br).
[0238] 参考例 55 (3-ブロモ -6-メチルチエノ [2,3- b]ピリジン- 2-ィル)力ルバミン酸 tert-ブチ ル
[0239] [化 59]
Me
参考例 54で得られた 3-ブロモ -6-メチルチエノ [2 ,3-b]ピリジン- 2-カルボン酸( 15.0 g, 55.2 mmol)、アジ化ジフエ-ルホスホリル(13.1 mL, 60.6 mmol)、トリェチルアミン( 11.6 mL, 82.8 mmol)の tert-ブタノール(100 mL)溶液を 90°Cで 15時間加熱した。反
応液を酢酸ェチルで希釈した後、この溶液を飽和炭酸水素ナトリウム水溶液と飽和 食塩水で順次洗浄した。無水硫酸マグネシウムで乾燥した後、溶媒を減圧下留去し
、得られた残渣をシリカゲルカラムクロマトグラフィー(酢酸ェチル:へキサン = 1: 19 力も 3 : 7)で精製して、表題ィ匕合物 16.3 g (収率 86%)を白色固体として得た。
1H NMR (DMSO-d ) δ 1.51 (9Η, s), 2.58 (3H, s), 7.32 (IH, d, J = 8.4 Hz), 7.78 (IH
6
, d, J = 8.4 Hz), 10.12 (IH, s).
[0241] 参考例 56 2-[(tert-ブトキシカルボ-ル)ァミノ] -6-メチルチエノ [2,3-b]ピリジン- 3-力 ルボン酸
[0242] [化 60]
[0243] 参考例 55で得られた (3-ブロモ -6-メチルチエノ [2,3-b]ピリジン- 2-ィル)カルノ ミン 酸 tert-ブチル(9.07 g, 26.4 mmol)の無水 THF (88 mL)溶液に 1.6 M n-ブチルリチウ ムへキサン溶液(38 mL, 60.7 mmol)を窒素雰囲気下、 - 78°Cで滴下し、その後同温 度で 1時間撹拌した。ドライアイスカゝら気化させた乾燥炭酸ガスを 0-10°Cでパブリング させた。反応液を水と酢酸ェチルで希釈し、 1規定塩酸を加えた後、析出した固体を ろ取した。得られた固体を水、ァセトニトリル/ジェチルエーテル(1:1)で、順次懸濁ろ 取を繰り返すことにより精製を行い、表題ィ匕合物 6.51 g (収率 80%)を白色結晶として 得た。
融点 162-163°C
EI(pos) 309 [M+H]+
JH NMR (DMSO-d ) δ 1.53 (9H, s), 2.50 (3H, s), 7.29 (IH, d, J = 8.3 Hz), 8.37 (IH
6
, d, J = 8.3 Hz), 11.26 (IH, br).
[0244] 参考例 57 tert-ブチル {3-[(3-{ [ェチル (イソプロピル)ァミノ]カルボ-ル}-1,4'-ビピぺ リジン- 1'-ィル)カルボ-ル] -6-メチルチエノ [2,3-b]ピリジン- 2-ィル }力ルバメート [0245] [化 61]
[0246] 参考例 50で得られた N-ェチル -N-イソプロピル- 1,4'-ビピペリジン- 3-カルボキサミ ド 2塩酸塩(335 mg, 0.945 mmol)と参考例 56で得られた 2-[(tert-ブトキシカルボ- ル)ァミノ] -6-メチルチエノ [2,3-b]ピリジン- 3-カルボン酸(292 mg, 0.945 mmol)を用 いて、参考例 1と同様の操作を行うことにより、表題ィ匕合物 192 mg (収率 36%)を油状 物として得た。
EI(pos) 572.1 [M+H]+
[0247] 参考例 58 1 '-[(2-ァミノ- 6-メチルチエノ [2,3-b]ピリジン- 3-ィル)カルボ-ル]- N-ェチ ル- N-イソプロピル- 1,4'-ビピペリジン- 3-カルボキサミド
[0248] [化 62]
[0249] 参考例 57で得られたtert-ブチル{3-[(3-{[ェチル(ィソプロピル)ァミノ]カルボ-ル}- l,4'-ビピぺリジン-l'-ィル)カルボ-ル]-6-メチルチェノ[2,3-b]ピリジン-2-ィル}カル ノメート(192 mg, 0.336 mmol)を用いて、参考例 24と同様の操作を行うことにより、表 題化合物 158 mg (収率 99%)を油状物として得た。
EI(pos) 472.1 [M+H]+
[0250] 参考例 59 tert-ブチル 3-{[(2R,6S)-2,6-ジメチルビペリジン- 1-ィル]カルボ-ル}-1,4
'-ビピぺリジン- 1'-カルボキシレート
[0251] [化 63]
[0252] 1- [(ベンジルォキシ)カルボ-ル]ピぺリジン- 3-カルボン酸(3.00 g, 11.4 mmol)を用 いて、参考例 48および 49と同様の操作を行うことにより、表題ィ匕合物 3.12 g (収率 67 %)を得た。
EI(pos) 408.2 [M+H]+
[0253] 参考例 60 3-{[(2R,6S)-2,6-ジメチルビペリジン- 1-ィル]カルボ-ル}-1,4'-ビピベリジ ン 2塩酸塩
[0254] [化 64]
[0255] 参考例 59で得られた tert-ブチル 3-{[(2R,6S)-2,6-ジメチルビペリジン- 1-ィル]カル ボ-ル }- 1,4'-ビピペリジン- 1'-カルボキシレート(3.12 g, 7.65 mmol)を用いて、参考 例 50と同様の操作を行うことにより、表題ィ匕合物 2.91 g (定量的)を得た。これ以上精 製することなく次工程に進んだ。
[0256] 参考例 61 3- [(3- {[(2R,6S)- 2,6-ジメチルビペリジン- 1-ィル]カルボ-ル}- 1,4'-ビピぺ リジン- 1しィル)カルボ二ル]- 1-ベンゾチォフェン- 2-ァミン
[0258] 参考例 60で得られた 3-{[(2R,6S)-2,6-ジメチルビペリジン- 1-ィル]カルボ-ル}-1,4' -ビピペリジン 2塩酸塩(260 mg, 0.683 mmol)と 2-ァミノ- 1-ベンゾチォフェン- 3-カル ボン酸(132 mg, 0.683 mmol)を用いて、参考例 1と同様の操作を行い、ジイソプロピ ルエーテルとへキサンで粉末にすることにより、表題化合物 253 mg (収率 77%)を得た
EI(pos) 483.1 [M+H]+
[0259] 参考例 62 l-(tert-ブトキシカルボ-ル) -3-メチルビペリジン- 3-カルボン酸
[0260] [化 66]
[0261] 1-tert-ブチル 3-ェチル 3-メチルビペリジン- 1,3-ジカルボキシレート(4.56 g, 16.8 mmol)を用いて、参考例 19と同様の操作を行い、へキサンで結晶化させることにより 、表題ィ匕合物 3.69 mg (収率 90%)を得た。これ以上精製することなく参考例 62に進ん だ。
[0262] 参考例 62 tert-ブチル 3- [(ジェチルァミノ)カルボ-ル] -3-メチルビペリジン- 1-カル ボキシレート
[0263] [化 67]
[0264] 参考例 61で得られた l-(tert-ブトキシカルボ-ル) -3-メチルビペリジン- 3-カルボン
酸(2.00 g, 8.22 mmol)とジェチルァミン(1.28 mL, 12.3 mmol)を用いて、参考例 1と 同様の操作を行うことにより、表題ィ匕合物 1.63 g (収率 67%)を油状物として得た。 EI(pos) 199.2 [M-Boc+H]+
[0265] 参考例 63 Ν,Ν-ジェチル -3-メチルビペリジン- 3-カルボキサミド塩酸塩
[0266] [化 68]
[0267] 参考例 62で得られた tert-ブチル 3_ [(ジェチルァミノ)カルボ-ル] _3_メチルビペリ ジン- 1-カルボキシレート(1.63 g, 5.46 mmol)を用いて、参考例 6と同様の操作を行う ことにより、表題ィ匕合物 1.28 g (定量的)を油状物として得た。これ以上精製することな く参考例 64に進んだ。
[0268] 参考例 64 tert-ブチル 3- [(ジェチルァミノ)カルボ-ル] -3-メチル -1,4'-ビピペリジン
-1'-カルボキシレート
[0269] [化 69]
[0270] 参考例 63で得られた Ν,Ν-ジェチル -3-メチルビペリジン- 3-カルボキサミド塩酸塩
(1.28 g, 5.45 mmol)、 tert-ブチル 4-ォキソピペリジン- 1-カルボキシレート(1.19 g, 6 .00 mmol) ,トリェチルァミン(0.76 mL, 5.45 mmol)と酢酸(2 ml)の THF(20 ml)溶液 にトリァセトキシ水素化ホウ素ナトリウム(1.73 g, 8.18 mmol)をカ卩え、室温で 3日間攪 拌した。反応液に酢酸ェチルを加え、炭酸カリウム水溶液と飽和食塩水で洗浄後、 無水硫酸ナトリウムで乾燥した。溶媒を減圧下留去し、得られた残渣をシリカゲルカラ ムクロマトグラフィー(展開溶媒;へキサン-酢酸ェチル = 9: 1から 3: 1)で精製し、表
題ィ匕合物 1.37 g (収率 66%)を油状物として得た。
EI(pos) 382.2 [M+H]+
[0271] 参考例 65 Ν,Ν-ジェチル -3-メチル -1,4'-ビピペリジン- 3-カルボキサミド 2塩酸塩 [0272] [化 70]
[0273] 参考例 64で得られた tert-ブチル 3- [(ジェチルァミノ)カルボ-ル] -3-メチル -1 ,4'- ビピペリジン- 1'-カルボキシレート(1.37 g, 3.59 mmol)を用いて、参考例 6と同様の操 作を行うことにより、表題ィ匕合物 1.27 g (定量的)を油状物として得た。これ以上精製 することなく参考例 66に進んだ。
[0274] 参考例 66 1 '-[(2-ァミノ- 1-ベンゾチェン- 3-ィル)カルボ-ル]- Ν,Ν-ジェチル -3-メチ ル- 1 ,4'-ビピペリジン- 3-カルボキサミド
[0275] [化 71]
[0276] 参考例 65で得られた Ν,Ν-ジェチル -3-メチル -1,4'-ビピペリジン- 3-カルボキサミド 2塩酸塩(700 mg, 1.98 mmol)と 2-ァミノ- 1-ベンゾチォフェン- 3-カルボン酸(382 mg, 1.98 mmol)を用いて、参考例 1と同様の操作を行うことにより、表題化合物 295 mg( 収率 33%)を油状物として得た。
EI(pos) 457.1 [M+H]+
[0277] 実施例 1 N-ェチル -Ν'- [3- ({4- [3- (モルホリン- 4-ィルカルボ-ル)- 4- (トリフルォロア セチル)ピぺラジン- 1-ィル]ピぺリジン- 1-ィル }カルボ二ル)- 1-ベンゾチォフェン- 2-ィ ル]尿素
[0278] [化 72]
[0279] 参考例 7で得られた 3-({4- [3- (モルホリン- 4-ィルカルボ-ル) -4- (トリフルォロアセチ ル)ピぺラジン- 1-ィル]ピぺリジン- 1-ィル }カルボ二ル)- 1-ベンゾチォフェン- 2-アミン( 200 mg, 0.361 mmol)をピリジン(1 mL)に溶力し、イソチアン酸ェチル(0.057 mL, 0.7 23 mmol)をカ卩え、 60°Cで 16時間攪拌した。溶媒を減圧下留去し、 NH-シリカゲルカラ ムクロマトグラフィー(展開溶媒;へキサン-酢酸ェチル = 1: 1から酢酸ェチル)で精製 し、ジイソプロピルエーテルで粉末にすることにより、表題化合物 181 mg (収率 80.1%) を得た。
EI(pos) 625.0 [M+H]+
[0280] 実施例 2 N-ェチル - N'-[3-({4- [3- (モルホリン- 4-ィルカルボ-ル)ピぺラジン- 1-ィル
]ピペリジン- 1-ィル }カルボ-ル)- 1-ベンゾチォフェン- 2-ィル]尿素
[0281] [化 73]
[0282] 実施例 1で得られた N-ェチル -Ν'- [3- ({4- [3- (モルホリン- 4-ィルカルボ二ル)- 4- (トリ
フルォロアセチル)ピぺラジン- 1-ィル]ピぺリジン- 1-ィル }カルボ二ル)- 1-ベンゾチォ フェン- 2-ィル]尿素(178 mg, 0.285 mmol)をメタノール(1.5 mL)に溶力し、炭酸力リウ ム(118 mg, 0.855 mmol)の水溶液(0.5 mL)をカ卩え、室温で 16時間攪拌した。酢酸ェ チルで希釈後、飽和食塩水で洗浄し、無水硫酸ナトリウムで乾燥した。溶媒を減圧下 留去し、得られた残渣を NH-シリカゲルカラムクロマトグラフィー(展開溶媒;酢酸ェチ ルから酢酸ェチル:メタノール = 10 : 1)で精製し、ジイソプロピルエーテルで粉末に することにより、表題化合物 121 mg (収率 80.3%)を得た。
EI(pos) 529.0 [M+H]+
[0283] 実施例 3 N-[3-({4- [3- (モルホリン- 4-ィルカルボ-ル)ピぺラジン- 1-ィル]ピぺリジン
-1-ィル }カルボ-ル)- 1-ベンゾチォフェン- 2-ィル]尿素
[0284] [化 74]
Ηつ Ν
[0285] 実施例 1で得られた N-ェチル -Ν'- [3- ({4- [3- (モルホリン- 4-ィルカルボ二ル)- 4- (トリ フルォロアセチル)ピぺラジン- 1-ィル]ピぺリジン- 1-ィル }カルボ二ル)- 1-ベンゾチォ フェン- 2-ィル]尿素(200 mg, 0.361 mmol)をテトラヒドロフラン(1 mL)に溶力し、トリク ロロァセチルイソシァネート(0.086 mL, 0.723 mmol)を氷冷下でカ卩え、 1時間攪拌し た後、 7規定アンモニア—メタノール(1 mL)を加え、室温で 16時間攪拌した。溶媒を 減圧下留去し、得られた残渣を NH-シリカゲルカラムクロマトグラフィー(展開溶媒;酢 酸ェチルから酢酸ェチル:メタノール =4 : 1)で精製し、ジイソプロピルエーテルで粉 末にすることにより、表題ィ匕合物 115 mg (収率 63.4%)を得た。
EI(pos) 501.0 [M+H]+
[0286] 実施例 4 Ν,Ν-ジェチル- 4- {1- [(2- {[(ェチルァミノ)カルボニル]アミノト 1-ベンゾチォ フェン- 3-ィル)カルボニル]ピぺリジン- 4-ィル }モルホリン- 2-カルボキサミド
[0287] [化 75]
[0288] 参考例 12で得られた 4-{1-[(2-ァミノ- 1-ベンゾチォフェン- 3-ィル)カルボニル]ピぺ リジン- 4-ィル) -Ν,Ν-ジェチルモルホリン- 2-カルボキサミド(150 mg, 0.337 mmol)を 用いて、実施例 1と同様の操作を行うことにより、表題化合物 137 mg (収率 79.0%)を得 た。
EI(pos) 516.0 [M+H]+
[0289] 実施例 5 4-[1-({2- [(ァミノカルボ-ル)ァミノ] -1-ベンゾチォフェン- 3-ィル }カルボ二 ル)ピぺリジン- 4-ィル] -N,N-ジェチルモルホリン- 2-カルボキサミド
[0290] [化 76]
参考例 12で得られた 4-{1-[(2-ァミノ- 1-ベンゾチォフェン- 3-ィル)カルボ-ル]ピぺ リジン- 4-ィル }-N,N-ジェチルモルホリン- 2-カルボキサミド(232 mg, 0.522 mmol)を 用いて、実施例 3と同様の操作を行うことにより、表題化合物 28.6 mg (収率 11.3%)を 得た。
EI(pos) 488.0 [ +H]+
[0292] 実施例 6 Ν,Ν-ジェチル -3-{l-[(2-{[(ェチルァミノ)カルボ-ル]アミノト 1-ベンゾチォ フェン- 3-ィル)カルボニル]ピぺリジン- 4-ィル }ベンズァミド
[0293] [化 77]
[0294] 参考例 16で得られた 3-{1-[(2-ァミノ- 1-ベンゾチォフェン- 3-ィル)カルボ-ル]ピぺ リジン- 4-ィル }-N,N-ジェチルベンズアミド(100 mg, 0.230 mmol)を用いて、実施例 1 と同様の操作を行うことにより、表題ィ匕合物 102 mg (収率 88.3%)を得た。
EI(pos) 507.0 [M+H]+
[0295] 実施例 7 Ν,Ν-ジェチル -1 '-[(2-{ [(ェチルァミノ)カルボ-ル]アミノ}- 1-ベンゾチオフ ェン -3-ィル)カルボニル] -1,4'-ビピペリジン- 3-カルボキサミド
[0296] [化 78]
[0297] 参考例 17で得られた 1 '-[(2-ァミノ- 1-ベンゾチォフェン- 3-ィル)カルボ-ル]- Ν,Ν- ジェチル -1,4'-ビピペリジン- 3-カルボキサミド(172 mg, 0.389 mmol)を用いて、実施 例 3と同様の操作を行うことにより、表題化合物 124 mg (収率 62.1%)を得た。
EI(pos) 514.1 [M+H]
[0298] 実施例 8 Ν,Ν-ジェチル -1 '-[(2-{ [(ェチルァミノ)カルボニル]アミノ}- 5-フエニル- 3-チ ェニル)カルボ二ル]- 1,4'-ビピペリジン- 3-カルボキサミド
[0299] [化 79]
[0300] 参考例 24で得られた 1'- [(2-ァミノ- 5-フエ-ル- 3-チェ-ル)カルボ-ル]- Ν,Ν-ジェ チル -1,4'-ビピペリジン- 3-カルボキサミド(55.0 mg, 0.117 mmol)を用いて、実施例 1 と同様の操作を行うことにより、表題化合物 22.4 mg (収率 35.4%)を得た。
EI(pos) 540.1 [M+H]+
[0301] 実施例 9 1 '-({2- [(アミノカルボニル)ァミノ]- 5-フエニル- 3-チェ二ル}カルボ二ル)- N,
N-ジェチル- 1,4'-ビピペリジン- 3-カルボキサミド
[0302] [化 80]
[0303] 参考例 24で得られた 1'- [(2-ァミノ- 5-フエ-ル- 3-チェ-ル)カルボ-ル]- Ν,Ν-ジェ
チル -1,4'-ビピペリジン- 3-カルボキサミド(165 mg, 0.352 mmol)を用いて、実施例 3 と同様の操作を行うことにより、表題化合物 85.6 mg (収率 47.6%)を得た。
EI(pos) 512.0 [M+H]+
[0304] 実施例 10 N-ェチル -Ν'- (3- {[3- (モルホリン- 4-ィルカルボ-ル)- 1,4'-ビピペリジン-
1 '-ィル]カルボ-ル}-1-ベンゾチォフェン- 2-ィル)尿素塩酸塩
[0305] [化 81]
[0306] 参考例 18で得られた 3- {[3- (モルホリン- 4-ィルカルボ-ル)- 1 ,4'-ビピペリジン- 1 '- ィル]カルボ-ル}-1-ベンゾチォフェン- 2-ァミン(0.50 g, 1.10 mmol)を用いて、実施 例 1と同様の操作を行うことにより、表題化合物の遊離塩基を得た。これを 4M塩ィ匕水 素酢酸ェチル溶液を用いて塩酸塩にした後、エタノール Z酢酸ェチルカ 再結晶し 、表題化合物 0.28 g (収率 45.1%)を得た。
EI(pos) 528.2 [遊離塩基の M+H]+
[0307] 実施例 11 N-(3-{[3- (モルホリン- 4-ィルカルボ-ル) -1,4'-ビピペリジン- 1しィル]力 ルポ-ル}-1-ベンゾチォフェン- 2-ィル)尿素
[0308] [化 82]
H2N
[0309] 参考例 18で得られた 3- {[3- (モルホリン- 4-ィルカルボ-ル)- 1 ,4'-ビピペリジン- 1 '- ィル]カルボ-ル }-1-ベンゾチォフェン- 2-ァミン(250 mg, 0.548 mmol)を用いて、実 施例 3と同様の操作を行うことにより、表題化合物 102 mg (収率 37.2%)を得た。
EI(pos) 500.0 [M+H]+
[0310] 実施例 12 N-ェチル -Ν'- (3- {[3- (モルホリン- 4-ィルカルボ-ル)- 1 ,4'-ビピペリジン- 1しィル]カルボ-ル}-7-ォキソ -4,5,6,7-テトラヒドロ- 1-ベンゾチォフェン- 2-ィル)尿素 [0311] [化 83]
[0312] 参考例 20で得られた 2-ァミノ- 3-{[3- (モルホリン- 4-ィルカルボ-ル) -1,4'-ビピペリ ジン- 1しィル]カルボ二ル}-5,6-ジヒドロ- 1-ベンゾチォフェン- 7(4Η)-オン(20 mg, 0.0 42 mmol)を用いて、実施例 1と同様の操作を行うことにより、表題化合物 10 mg (収率 43.5%)を得た。
EI(pos) 546.1 [M+H]+
[0313] 実施例 13 N-ェチル -Ν'- (3- {[3- (モルホリン- 4-ィルカルボ二ル)- 1,4'-ビピペリジン-
1 '-ィル]カルボ-ル}-5-フエ-ル- 2-チェ-ル)尿素
[0314] [化 84]
[0315] 参考例 26で得られた 3- {[3- (モルホリン- 4-ィルカルボ-ル)- 1,4'-ビピペリジン- 1'- ィル]カルボ-ル}- 5-フエ-ルチオフェン- 2-ァミン(163 mg, 0.338 mmol)を用いて、 実施例 1と同様の操作を行うことにより、表題化合物 151 mg (収率 81.0%)を得た。 EI(pos) 554.2 [M+H]+
[0316] 実施例 14 N- (3- {[3- (モルホリン- 4-ィルカルボ-ル)- 1 ,4'-ビピペリジン- 1しィル]力 ルポ-ル}-5-フエ-ル- 2-チェ-ル)尿素
[0317] [化 85]
参考例 26で得られた 3-{[3- (モルホリン- 4-ィルカルボ-ル) -1,4'-ビピペリジン- 1' ィル]カルボ-ル}- 5-フエ-ルチオフェン- 2-ァミン(289 mg, 0.599 mmol)を用いて、 実施例 3と同様の操作を行うことにより、表題化合物 160 mg (収率 50.9%)を得た。
EI(pos) 526.1 [M+H]
[0319] 実施例 15 N-ェチル -Ν'- (4- {[3- (モルホリン- 4-ィルカルボ-ル)- 1 ,4'-ビピペリジン-
1 '-ィル]カルボ-ル}-2-フエ-ル- 1 ,3-チアゾール -5-ィル)尿素
[0320] [化 86]
[0321] 参考例 28で得られた 4- {[3- (モルホリン- 4-ィルカルボ-ル)- 1,4'-ビピペリジン- 1'- ィル]カルボ-ル}- 2-フエ-ル- 1,3-チアゾール -5-ァミン(150 mg, 0.310 mmol)を用 いて、実施例 1と同様の操作を行うことにより、表題ィ匕合物 149 mg (収率 86.7%)を得た
EI(pos) 555.2 [M+H]+
[0322] 実施例 16 N- (4- {[3- (モルホリン- 4-ィルカルボ-ル)- 1 ,4'-ビピペリジン- 1しィル]力 ルポ-ル}-2-フエ-ル- 1 ,3-チアゾール -5-ィル)尿素
[0323] [化 87]
[0324] 参考例 28で得られた 4- {[3- (モルホリン- 4-ィルカルボ-ル)- 1 ,4'-ビピペリジン- 1 '-
ィル]カルボ-ル}- 2-フエ-ル- 1,3-チアゾール -5-ァミン(184 mg, 0.380 mmol)を用 いて、実施例 3と同様の操作を行うことにより、表題化合物 129 mg (収率 64.6%)を得た
EI(pos) 527.2 LM+H]
[0325] 実施例 17 N-ェチル -Nし {3- {[(3R)- 3- (モルホリン- 4-ィルカルボ二ル)- 1 ,4'-ビピペリ ジン- 1'-ィル]カルボ-ル}- 5- [4- (トリフルォロメチル)フエ-ル]- 2-チェ-ル}尿素 [0326] [化 88]
[0327] 参考例 36で得られた 3-{[(3R)-3- (モルホリン- 4-ィルカルボ-ル) -1,4'-ビピペリジン -1'-ィル]カルボ-ル}- 5- [4- (トリフルォロメチル)フエ-ル]チォフェン- 2-ァミン(94.6 mg, 0.172 mmol)を用いて、実施例 1と同様の操作を行うことにより、表題化合物 66.3 mg (収率 62.0%)を得た。
EI(pos) 622.2 [M+H]+
[0328] 実施例 18 N-ェチル -Ν'- (6- [4- (メチルスルホニル)フエ二ル]- 4- {[3- (モルホリン- 4-ィ ルカルボ-ル) -1 ,4しビピペリジン- 1 '-ィル]カルボ-ル}ピリジン- 3-ィル)尿素
[0329] [化 89]
[0330] 参考例 39で得られた 6- [4- (メチルスルホ -ル)フエニル] -4- {[3- (モルホリン- 4-ィル カルボ二ル)- 1,4しビピペリジン- -ィル]カルボ-ル}ピリジン- 3-ァミン(113 mg, 0.203 mmol)を用いて、実施例 1と同様の操作を行うことにより、表題化合物 36.9 mg (収率 2 9.1%)を得た。
EI(pos) 627.1 [M+H]+
[0331] 実施例 19 N-ェチル -Ν'- (3- {[3- (ピロリジン- 1-ィルカルボ二ル)- 1,4しビピペリジン- 1'
-ィル]カルボ-ル}-1-ベンゾチェン- 2-ィル)尿素
[0332] [化 90]
参考例 43で得られた 3-{[3- (ピロリジン- 1-ィルカルボニル) -1,4'-ビピペリジン- 1'-ィ ノレ]カルボ-ル}-1-ベンゾチォフェン- 2-ァミン(100 mg, 0.227 mmol)を用いて、実施 例 1と同様の操作を行うことにより、表題化合物 76.1 mg (収率 65.6%)を得た。
EI(pos) 512.1 [M+H]+
[0334] 実施例 20 N-ェチル -Ν'- (3- {[3- (ピペリジン- 1-ィルカルボ-ル)- 1 ,4'-ビピペリジン- 1
'-ィル]カルボ-ル}-1-ベンゾチェン- 2-ィル)尿素
[0335] [化 91]
[0336] 参考例 46で得られた 3- {[3- (ピペリジン- 1-ィルカルボ-ル)- 1 ,4'-ビピペリジン- 1 '- ィル]カルボ-ル}-1-ベンゾチォフェン- 2-ァミン(100 mg, 0.220 mmol)を用いて、実 施例 1と同様の操作を行うことにより、表題化合物 70.7 mg (収率 60.9%)を得た。
EI(pos) 526.1 [M+H]+
[0337] 実施例 21 N- (7-メトキシ -3-{[3- (ピペリジン- 1-ィルカルボ-ル) -1,4しビピペリジン- 1'
-ィル]カルボ-ル}-1-ベンゾチェン- 2-ィル) -Ν'-メチル尿素
[0338] [化 92]
[0339] 参考例 47で得られた 7-メトキシ -3-{[3- (ピペリジン- 1-ィルカルボ-ル) -1,4'-ビピぺ リジン- 1しィル]カルボ-ル}-1-ベンゾチォフェン- 2-ァミン(115 mg, 0.237 mmol)を用 いて、実施例 1と同様の操作を行うことにより、表題化合物 94.8 mg (収率 74%)を得た
EI(pos) 542.5 [M+H]+
[0340] 実施例 22 N-ェチル -Ν'- (7-メトキシ- 3- {[3- (ピペリジン- 1-ィルカルボ-ル)- 1 ,4'-ビ
ピぺリジン- 1'-ィル]カルボ-ル}-1-ベンゾチェン- 2-ィル)尿素
[0341] [化 93]
[0342] 参考例 47で得られた 7-メトキシ -3-{[3- (ピペリジン- 1-ィルカルボ-ル) -1,4'-ビピぺ リジン- 1'-ィル]カルボ-ル}-1-ベンゾチォフェン- 2-ァミン(200 mg, 0.413 mmol)を用 いて、実施例 1と同様の操作を行うことにより、表題化合物 200 mg (収率 87%)を得た。 EI(pos) 556.1 [M+H]+
[0343] 実施例 23 N-ェチル - N-イソプロピル- 1し[(7-メトキシ -2-{[(メチルァミノ)カルボ-ル] アミノ}-1-ベンゾチェン- 3-ィル)カルボニル] -1,4しビピペリジン- 3-カルボキサミド [0344] [化 94]
[0345] 参考例 51で得られた 1 '-[(2-ァミノ- 7-メトキシ- 1-ベンゾチェン- 3-ィル)カルボ-ル] -N-ェチル -N-イソプロピル- 1,4'-ビピペリジン- 3-カルボキサミド(186 mg, 0.382 mm ol)を用いて、実施例 1と同様の操作を行うことにより、表題化合物 128 mg (収率 62%) を得た。
EI(pos) 544.5 [M+H]+
[0346] 実施例 24 N-ェチル -1 '-[(2- { [(ェチルァミノ)カルボ-ル]アミノト 7-メトキシ- 1-ベンゾ
チェン- 3-ィル)カルボ二ル]- N-イソプロピル- 1,4'-ビピペリジン- 3-カルボキサミド
[0347] [化 95]
[0348] 参考例 51で得られた 1 '-[(2-ァミノ- 7-メトキシ- 1-ベンゾチェン- 3-ィル)カルボ-ル] -N-ェチル -N-イソプロピル- 1,4'-ビピペリジン- 3-カルボキサミド(117 mg, 0.240 mm ol)を用いて、実施例 1と同様の操作を行うことにより、表題化合物 76.3 mg (収率 57%) を得た。
EI(pos) 558.5 [M+H]+
[0349] 実施例 25 N-ェチル -1'-[(2-{ [(ェチルァミノ)カルボ-ル]アミノ}-6-メチルチエノ [2,3- b]ピリジン- 3-ィル)カルボ-ル]- N-イソプロピル- 1,4しビピペリジン- 3-カルボキサミド [0350] [化 96]
[0351] 参考例 58で得られた 1'-[(2-ァミノ- 6-メチルチエノ [2,3-b]ピリジン- 3-ィル)カルボ- ル]- N-ェチル -N-イソプロピル- 1,4'-ビピペリジン- 3-カルボキサミド(158 mg, 0.335 mmol)を用いて、実施例 1と同様の操作を行うことにより、表題化合物 139 mg (収率 77 %)を得た。
EI(pos) 543.1 [M+H]
[0352] 実施例 26 N- {3- [(3- {[(2R,6S)- 2,6-ジメチルビペリジン- 1-ィル]カルボ-ル}- 1,4'-ビ ピぺリジン- 1しィル)カルボ二ル]- 1-ベンゾチェン- 2-ィル }尿素
[0353] [化 97]
[0354] 参考例 61で得られた 3-[(3-{[(2R,6S)-2,6-ジメチルビペリジン- 1-ィル]カルボ-ル} - 1,4'-ビピペリジン- 1しィル)カルボ二ル]- 1-ベンゾチォフェン- 2-ァミン(400 mg, 0.829 mmol)を用いて、実施例 3と同様の操作を行うことにより、表題化合物 222 mg (収率 5 1%)を得た。
EI(pos) 526.2 [M+H]+
[0355] 実施例 27 N- {3- [(3- {[(2R,6S)- 2,6-ジメチルビペリジン- 1-ィル]カルボ-ル}- 1,4'-ビ ピぺリジン- 1しィル)カルボ-ル]- 1-ベンゾチェン- 2-ィル }-Ν'-メチル尿素
[0356] [化 98]
[0357] 参考例 61で得られた 3-[(3-{[(2R,6S)-2,6-ジメチルビペリジン- 1-ィル]カルボ-ル} - 1,4'-ビピペリジン- 1しィル)カルボ二ル]- 1-ベンゾチォフェン- 2-ァミン(120 mg, 0.249 mmol)を用いて、実施例 1と同様の操作を行うことにより、表題化合物 88.8 mg (収率 6 6%)を得た。
EI(pos) 540.4 [M+H]+
[0358] 実施例 28 Ν,Ν-ジェチル -3-メチル -l'-[(2-{ [(メチルァミノ)カルボ-ル]アミノト 1-ベン ゾチェン- 3-ィル)カルボニル] -1,4'-ビピペリジン- 3-カルボキサミド
[0359] [化 99]
[0360] 参考例 66で得られた 1'-[(2-ァミノ- 1-ベンゾチェン- 3-ィル)カルボ-ル]- Ν,Ν-ジェ チル -3-メチル -1,4'-ビピペリジン- 3-カルボキサミド(147 mg, 0.32 mmol)を用いて、 実施例 1と同様の操作を行うことにより、表題化合物 38.1 mg (収率 23%)を得た。
EI(pos) 514.1 [M+H]+
[0361] 実施例 29 1'- ({2- [(アミノカルボ-ル)ァミノ]- 1-ベンゾチェン- 3-ィル }カルボ-ル)- N,
N-ジェチル -3-メチル -1,4'-ビピペリジン- 3-カルボキサミド
[0362] [化 100]
[0363] 参考例 66で得られた 1'-[(2-ァミノ- 1-ベンゾチェン- 3-ィル)カルボ-ル]- Ν,Ν-ジェ チル -3-メチル -1,4'-ビピペリジン- 3-カルボキサミド(147 mg, 0.32 mmol)を用いて、 実施例 3と同様の操作を行うことにより、表題ィ匕合物 17.3 mg (収率 11%)を得た。
EI(pos) 500.1 [M+H]+
[0364] 実験例 1
以下の方法により、本発明化合物の ACC1阻害作用を評価した。
(1)ヒト ACC1遺伝子のクローユングと組換えバキュロウィルスの調製
ヒト ACCl遺伝子は、ヒト肝臓 cDNAライブラリー(Clontech社)を铸型とし、以下に示 す Primer 1および Primer 2を用いた PCRによりクローユングした。 Primer 1および Prime r2は、ヒト ACCl遺伝子の塩基配列(Genbank Accession U19822)情報より、 Sail, Notl 制限酵素認識配列を加えて作製した。 列番号 1)
Primer 2 5, AAAAGCGGCCGCCTACGTAGAAGGGGAGTCCATAGTG (配列番 号 2)
PCRは Pyrobest DNA polymerase (タカラバイオ株式会社)を用いて実施した。得ら れた PCR産物を pT7 Blue vector(Novagen社)にクローニングし、塩基配列を確認後、 制限酵素 Sall、 Notlで消化した。得られる DNA断片を、制限酵素 Sall、 Notlで消化した pFAST- BacHTc (インビトロジェン社)へ挿入し、発現プラスミド ACCl/pFAST-BacHTc を作製した。
該発現プラスミドおよび BAC- TO- BAC Baculovirus Expression System (インビトロ ジェン社)を用いて、組換えバキュロウィルスのウィルスストック BAC— ACC1を調製 した。
(2)ACC1タンパクの調製
SF-9細胞 (インビトロジェン社)を昆虫細胞用培地(10%ゥシ胎児血清(トレース社) 、 50mg/L Gentamicin (インビトロジェン社)、 0.1% Pluronic F- 68 (インビトロジェン 社)を含む Sf- 900IISFM培地(インビトロジェン社) ) 1Lに 1 X 106 cells/mLとなるよう に播種し、 2L容マイヤーを用いて 27°C、 lOOrpmで振盪培養した。
培養 24時間後に組換えバキュロウィルス BAC- ACC1を 10mL添カロし、さらに 3日間 の培養を行った。培養液を 1000 X gで 5分間遠心分離し、ウィルス感染細胞を得た。 該細胞をリン酸生理緩衝液 (インビトロジェン社)で洗浄して同条件で遠心分離後、 得られる細胞を- 80°Cで凍結保存した。
凍結保存した細胞を氷中で融解後、 Complete Protease Inhibitor (ベーリンガー社) を添カ卩した 10% Glycerol, 0.13M NaCl、 ImM EDTA、 25mM Sodium β -Glycerophos phateゝ ImM Sodium Orthovanadateを含む 25mM HEPES緩衝液 (pH7.5)100 mLに
懸濁した。得られる懸濁液をポリトロンホモジナイザー(キネマティ力社)を用いて 20,0 00 rpm, 30秒の条件で 3回ホモジナイズした。得られる細胞破砕液を 185700 X g, 50 分間の遠心分離により清澄化後、 0.45 mフィルターを用いたろ過を行った。ろ過液 を N卜 NTA Super Flow Gel (キアゲン社) 12mLを詰めたカラムに流速約 5 mL/minで 通した。カラムを緩衝液 A(0.3M NaClを含む 50mM HEPES (pH7.5) )で洗浄し、更に 2 OmM Imidazoleを含む緩衝液 Aで洗浄した後、 lOOmM Imidazoleを含む緩衝液 Aで溶 出した。溶出液を分画分子量 30Kのビバスピン 20 (ビバサイエンス社)で濃縮した。得 られる濃縮液を 10mM MgCl、 2mM DithiothreitoU lOmM Tripotassium Citrate, 0.3
2
M NaClを含む 50mM HEPES(pH7.5)で平衡化した SephadexG- 25(アマシャムバイオ サイエンス社) 358mLを用いて透析した。透析内液を分画分子量 30Kのビバスピン 20 ( ビバサイエンス社)で濃縮した後、濃縮液を 0.22 mフィルターでろ過し、 ACC1を得 た。得られた ACC1は- 80°Cで凍結保存した。
[0366] (3)ACC1阻害活性の測定
上記(2)で得られた ACCl (0.93mg/ml)を酵素反応用緩衝液(50mM HEPES (pH7 .5), 10mM MgCl , lOmM Tripottasium Citrate, 2mM Dithiothreitol, 0.75mg/ml Fatty
2
acid free BSA)で 8 μ g/mlの濃度に希釈後、 384 well assay plate(Nunc 265196)の各 ゥエルに 10 μ 1ずつ添カ卩した。
以後、後述の実験例 2— (3)と同様にして、 ACC1阻害率 (%)を求め、 IC 値を算
50 出した。
その結果、実施例 4、 7〜15、 17、 19〜27の化合物は、 以下の IC 値を示し
50 た。
[0367] 実験例 2
以下の方法により、本発明化合物の ACC2阻害作用を評価した。
(1)ヒト ACC2遺伝子のクローユングと組換えバキュロウィルスの調製
ヒト ACC2遺伝子は、ヒト骨格筋 cDNAライブラリー(Clontech社)を铸型とし、以下に 示す Primer 1および Primer 2を用いた PCRによりクローユングした。 Primerlおよび Pri mer 2は、ヒト ACC2遺伝子の塩基配列(Genbank Accession U89344)情報より、 Sail, Xbal制限酵素認識配列を加えて作製した。
Primer 1 5
列番号 3)
Primer 2 5, TTTTTCTAGATCAGGTAGAGGCCGGGCTGTCCATG (配列番号 4) PCRは Pyrobest DNA polymerase (タカラバイオ株式会社)を用いて実施した。得ら れた PCR産物を pT7 Blue vector(Novagen社)にクローニングし、塩基配列を確認後、 制限酵素 Sall、 Xbalで消化した。得られる DNA断片を、制限酵素 Sall、 Xbalで消化し た pFAST- BacHTa (インビトロジェン社)へ挿入し、発現プラスミド ACC2/pFAST-BacH Taを作製した。
該発現プラスミドを铸型とし、以下に示す Primer 3および Primer 4を用いた PCRによ り、ミトコンドリア移行配列を除去した ACC2を発現させるためのプラスミドを作製した。
Primer 3 5, CCAGGTCGACCCGCCAACGGGACTGGGACACAAGG (配列番号 5
)
Primer 4 5,CGCACTCTCAGTTTCCCGGATTCCC (配列番号 6)
PCRは Pyrobest-DNA polymerase (タカラバイオ株式会社)を用いて実施した。得ら れた PCR産物を pT7Blue vector(Novagen)にクローニングし、塩基配列を確認後、制 限酵素 Sall、 Aflllで消化した。得られる DNA断片を、制限酵素 Sall、 Aflllで消化した pF AST- BacHTa (インビトロジェン社)へ挿入し、発現プラスミド ACC2mito7/pFAST-Bac HTaを作製した。
該発現プラスミドおよび BAC- TO- BAC Baculovirus Expression System (インビトロ ジェン社)を用いて、組換えバキュロウィルスのウィルスストック BAC— ACC2 (N term inal deletion (以下 Nd))を調製した。
(2)ACC2(Nd)タンパクの調製
SF-9細胞 (インビトロジェン社)を昆虫細胞用培地(10%ゥシ胎児血清(トレース社) 、 50mg/L Gentamicin (インビトロジェン社)、 0.1% Pluronic F- 68 (インビトロジェン社) を含む Sf- 900IISFM培地(インビトロジェン社) ) 2Lに 0.5 X 106 cells/mLとなるように播 種し、 Waveバイオリアクター (Wave社)を用いて 27°C、 20rpm、揺動角度 6度、酸素濃 度 30%で振盪培養した。
培養 4日目に 3Lの昆虫細胞用培地を加え揺動角度を 8度にし、さらに培養を行った
。培養 5日目に組換えバキュロウィルス BAC- ACC2 (Nd)を lOOmL添カロし、さらに昆虫 細胞用培地 5Lを加え、揺動角度を 11度として 3日間の培養を行った。培養液を 1000 X gで 10分間遠心分離し、ウィルス感染細胞を得た。該細胞をリン酸生理緩衝液 (ィ ンビトロジヱン社)で洗浄して同条件で遠心分離後、得られる細胞を- 80°Cで凍結保 存した。
凍結保存した細胞を氷中で融解後、 Complete Protease Inhibitor (ベーリンガー社) を添カ卩した 10% Glycerol, 0.13M NaCl、 ImM EDTA、 25mM Sodium β -Glycerophos phateゝ ImM Sodium Orthovanadateを含む 25mM HEPES緩衝液 (pH7.5)900 mLに 懸濁した。得られる懸濁液をポリトロンホモジナイザー(キネマティ力社)を用いて 20,0 00 rpm, 30秒の条件で 3回ホモジナイズした。得られる細胞破砕液を 31000 X g, 60分 間の遠心分離により清澄化後、 0.45 /z mフィルターを用いたろ過を行った。ろ過液を Ni-NTA Super Flow Gel (キアゲン社) 60mLを詰めたカラムに流速約 5 mL/minで通 した。カラムを緩衝液 A(0.3M NaClを含む 50mM HEPES (pH7.5) )で洗浄し、更に 20 mM Imidazoleを含む緩衝液 Aで洗浄した後、 lOOmM Imidazoleを含む緩衝液 Aで溶 出した。溶出液を分画分子量 30Kのビバスピン 20 (ビバサイエンス社)で濃縮した。得 られた濃縮液を 10mM MgCl、 2mM DithiothreitoU lOmM Tripotassium Citrateゝ 0.3
2
M NaClを含む 50mM HEPES(pH7.5)に対して透析した。透析内液を 0.22 μ mフィルタ 一でろ過し、 ACC2 (Nd)を得た。得られた ACC2 (Nd)は- 80°Cで凍結保存した。 (3)ACC2阻害活性の測定
上記(2)で得られた ACC2 (Nd) (l.lmg/ml)を酵素反応用緩衝液 (50mM HEPES( pH7.5), 10mM MgCl , lOmM Tripottasium Citrate, 2mM Dithiothreitol , 0.75mg/ml
2
Fatty acid free BSA)で 6.4 g/mlの濃度に希釈後、 384 well assay plate(Nunc 26519 6)の各ゥエルに 10 ずつ添カ卩した。ついで、各ゥエルに、ジメチルスルホキシド (DMS 0)に溶解した試験化合物を酵素反応用緩衝液で希釈した溶液 5 1ずつを添加し、 3 0°Cで 60分間インキュベーションした。ついで、各ゥエルに、基質溶液(50mM KHCO
3
, 200uM ATP, 200uM Acetyl-CoA) 5 ,u 1ずつを添カ卩し、 30°Cで 20分間反応させた(試 験化合物添加群)。
また、試験化合物を添加しない以外、上記と同様の反応を行った (試験化合物非
添加群)。さらに、試験化合物および Acety卜 CoAを添カ卩しない以外、上記と同様の反 応を行った(コントロール群)。
このようにして得られる各反応液にマラカイトグリーン液 5 μ 1ずつを添加し攪拌する ことにより反応を停止させた。得られる反応液を室温で 20分間放置した後、 wallacl42 0(Perkin Elmer社)を用いて吸光度 (620nm)を測定した。なお、前記マラカイトグリーン 液は、 A液 (0.12%マラカイトグリーン溶液。 5N H SOで調製、遮光し 4°Cで保存)、 B液
2 4
(7.5%アンモ-ゥムモリブデート水溶液。用時調製)および C液(11% Tween 20水溶液 。室温保存)を、 A液: B液: C液 = 100: 25: 2の割合 (容積比)で混合することにより調 製した。
ついで、 ACC2阻害率 (%)を計算式:
(1 (試験化合物添加群の吸光度 コントロール群の吸光度) ÷ (試験化合物非添カロ 群の吸光度 コントロール群の吸光度)) X 100
により求め、 IC 値を算出した。
50
その結果、実施例 4、 7〜15、 17、 19〜27の化合物は、 100 nM以下の IC 値を示
50 した。
[0370] [表 1] 製剤例 1 (カプセルの製造)
1 ) 雄例 1の化合物 3 0 mg
2 ) 微粉末セルロース 1 0 mg
3 ) 1 9 mg
4 ) ステアリン酸マグネシウム 1
計 6 0 mg
[0371] 1)、 2)、 3)および 4)を混合して、ゼラチンカプセルに充填する。
[0372] [表 2]
製剤例 2 (錠剤の製造)
1) 実施例 1の化合物 30 g
2) 乳糖 50 g
3) トウモロコシデンプン 15 g
4) カルボキシメチノ Mrルロースカルシウム 44 g
5) ステアリン酸マグネシウム 1 g
1000錠 計 140 g
[0373] 1)、 2)、 3)の全量および 30gの 4)を水で練合し、真空乾燥後、整粒を行う。
この整粒末に 14gの 4)および lgの 5)を混合し、打錠機により打錠する。このように して、 1錠あたり実施例 1の化合物 30mgを含有する錠剤 1000錠を得る。
産業上の利用可能性
[0374] 本発明化合物は、 ACC (ァセチルー Co Aカルボキシラーゼ)阻害作用を有し、肥 満症、糖尿病、高血圧症、高脂血症、心不全、糖尿病性合併症、メタボリックシンドロ ーム、筋肉減少症などの予防,治療に有用である。
本出願は日本で出願された特願 2006— 112769を基礎としており、その内容は本 明細書にすべて包含される。また、本明細書で引用した特許文献および非特許文献 は、引用したことによってその内容の全てが開示されたと同程度に本明細書中に組 み込まれるものである。