WO2007101811A1 - Verfahren zum abbau von cellulose in lösung - Google Patents
Verfahren zum abbau von cellulose in lösung Download PDFInfo
- Publication number
- WO2007101811A1 WO2007101811A1 PCT/EP2007/051870 EP2007051870W WO2007101811A1 WO 2007101811 A1 WO2007101811 A1 WO 2007101811A1 EP 2007051870 W EP2007051870 W EP 2007051870W WO 2007101811 A1 WO2007101811 A1 WO 2007101811A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- acid
- methyl
- cellulose
- general formula
- Prior art date
Links
- 0 *C1(*)C(*)(*)[N+](*)=NC1(*)* Chemical compound *C1(*)C(*)(*)[N+](*)=NC1(*)* 0.000 description 2
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08B—POLYSACCHARIDES; DERIVATIVES THEREOF
- C08B15/00—Preparation of other cellulose derivatives or modified cellulose, e.g. complexes
- C08B15/02—Oxycellulose; Hydrocellulose; Cellulosehydrate, e.g. microcrystalline cellulose
Definitions
- the present invention describes a process for the degradation of cellulose by dissolving the cellulose in an ionic liquid and treating it with an acid, optionally with the addition of water.
- Cellulose is the most important renewable raw material and represents an important starting material for, for example, the textile, paper and nonwoven industries. It also serves as a raw material for derivatives and modifications of cellulose, to which cellulose ethers, such as, for example, Methylcellulose and carboxymethylcellulose, cellulose esters based on organic acids, e.g. Cellulose acetate, cellulose butyrate, and cellulose esters based on inorganic acids, e.g. Cellulose nitrate, and others count. These derivatives and modifications find a variety of applications, for example in the food, construction and paint industries.
- cellulose ethers such as, for example, Methylcellulose and carboxymethylcellulose
- cellulose esters based on organic acids e.g. Cellulose acetate, cellulose butyrate
- inorganic acids e.g. Cellulose nitrate
- Cellulose is characterized by insolubility, especially in common solvents of organic chemistry.
- N-methyl-morpholine-N-oxide, anhydrous hydrazine, binary mixtures such as methylamine / dimethyl sulfoxide, or ternary mixtures such as ethylenediamine / SO 2 / dimethyl sulfoxide are used as solvent today.
- saline systems e.g. LiCl / dimethylacetamide, LiCl / N-methylpyrrolidone, potassium thiocyanate / dimethyl sulfoxide, etc.
- cellulose is characterized by the average degree of polymerization (DP).
- DP average degree of polymerization
- the DP of cellulose depends on its origin; so the DP of raw cotton can be up to 12,000.
- cotton linters have a DP of 800 to 1800 and in wood pulp it is in the range of 600 to 1200.
- the DP reduces the cellulose only to a small extent becomes.
- An uncontrolled degradation takes place in the thermal treatment and also the cellulose is modified, in particular dehydrocelluloses can be formed.
- cellulose can be treated with high-energy radiation, such as X-radiation.
- high-energy radiation such as X-radiation.
- chemical modification of the cellulose also occurs by forming a high number of carboxylic acid or keto functions.
- less energy-rich radiation such as UV / visible light, it is necessary to use photosensitizers.
- the cellulose is suspended in dilute mineral acid and treated at elevated temperature.
- LOPD level-off DP
- the LODP appears to be related to the size of the crystalline regions of the cellulose employed. It depends on the cellulose used, but also on the reaction medium, if, for example, solvents, such as dimethyl sulfoxide, water, alcohols or methyl ethyl ketone are additionally added.
- solvents such as dimethyl sulfoxide, water, alcohols or methyl ethyl ketone are additionally added.
- the yield of degraded cellulose is low, because the amorphous regions or the accessible regions of the cellulose are completely hydrolyzed.
- cellulose in a homogeneous system to an acidic degradation.
- cellulose is dissolved, for example, in a mixture of LiCl / dimethylformamide and treated with an acid.
- the preparation of the solution is very complicated, the work-up complicated and low the yield of degraded cellulose.
- the oxidative degradation of cellulose is usually carried out with oxygen. As a preliminary step, it usually involves the formation of individual anhydroglucose units, which react further to form unstable intermediates and ultimately lead to a chain break. The control of this reaction is usually difficult.
- the abovementioned methods therefore have various disadvantages and there is therefore a need for a method for the targeted degradation of cellulose, which takes place without modification of the polymer and in high yields.
- a process has now been found for the controlled degradation of cellulose by dissolving cellulose in an ionic liquid and treating it with an acid, optionally with the addition of water.
- n 1, 2, 3 or 4
- [A] + is a quaternary ammonium cation
- the ionic liquids have a melting point of less than 180 ° C. More preferably, the melting point is in a range of -50 ° C to 150 ° C, more preferably in the range of -20 ° C to 120 ° C, and most preferably below 100 ° C.
- Such compounds may contain oxygen, phosphorus, sulfur or in particular nitrogen atoms, for example at least one nitrogen atom, preferably 1 to 10 nitrogen atoms, more preferably 1 to 5, most preferably 1 to 3 and especially 1 to 2 nitrogen atoms.
- nitrogen atom is a suitable carrier of the positive charge in the cation of the ionic liquid, of which then, in equilibrium, a proton or an alkyl group can be transferred to the anion to form an electrically neutral molecule.
- a cation in the synthesis of the ionic liquids a cation can first be generated by quaternization on the nitrogen atom of, for example, an amine or nitrogen heterocycle.
- the quaternization can be carried out by alkylation of the nitrogen atom.
- salts with different anions are obtained.
- this can be done in a further synthesis step.
- the halide can be reacted with a Lewis acid to form a complex anion from halide and Lewis acid.
- replacement of a halide ion with the desired anion is possible. This can be done by adding a metal salt with precipitation of the metal halide formed, via an ion exchanger or by displacement of the halide ion by a strong acid (with liberation of the hydrohalic acid). Suitable methods are, for example, in Angew. Chem. 2000, 12, pp. 3926-3945 and the literature cited therein.
- Suitable alkyl radicals with which the nitrogen atom in the amines or nitrogen heterocycles may be quaternized are C 1 -C 6 -alkyl, preferably C 1 -C 10 -alkyl, particularly preferably C 1 -C 6 -alkyl and very particularly preferably methyl.
- the alkyl group may be unsubstituted or have one or more identical or different substituents.
- aromatic heterocycles are particularly preferred.
- Particularly preferred compounds are those which have a molecular weight below 1000 g / mol, very particularly preferably below 500 g / mol and in particular below 350 g / mol.
- radical R is hydrogen, a carbon-containing organic, saturated or unsaturated, acyclic or cyclic, aliphatic, aromatic or araliphatic, unsubstituted or interrupted by 1 to 5 heteroatoms or functional groups radical having 1 to 20 carbon atoms;
- radicals R 1 to R 9 independently of one another represent hydrogen, a sulfo
- radicals R 1 to R 9 which in the abovementioned formulas (III) to a carbon atom (and not to a heteroatom) may additionally be also halogen or a functional group; or
- the carbon-containing group contains heteroatoms, oxygen, nitrogen, sulfur, phosphorus and silicon are preferable.
- the radicals R 1 to R 9 are, in the cases in which these are attached in the above formulas (III) to a carbon atom (and not to a heteroatom), also be bound directly via the heteroatom.
- Functional groups and heteroatoms may also be directly adjacent so that combinations of several adjacent atoms, such as -O- (ether), -S- (thioether), -COO- (ester), -CONH- (secondary amide ) or -CONR'- (tertiary amide), are included, for example, di (Ci-C4-alkyl) amino, Ci-C4-alkyloxycarbonyl or Ci-C4-alkyloxy.
- the radicals R ' are the remainder of the carbon-containing radical.
- Halogens are fluorine, chlorine, bromine and iodine.
- the radical R preferably stands for
- N, N-di-Ci-C ⁇ -alkyl-amino such as N, N-dimethylamino and N 1 N-diethylamino.
- the radical R particularly preferably represents unbranched and unsubstituted C 1 -C 6 -alkyl, such as, for example, methyl, ethyl, 1-propyl, 1-butyl, 1-pentyl, 1-hexyl, 1-heptyl, 1-octyl, 1-decyl, 1-dodecyl, 1-tetradecyl, 1-hexadecyl, 1-octadecyl, 1-propen-3-yl especially methyl, ethyl, 1-butyl and 1-octyl, and for CH3O- (CH2 CH2 ⁇ ) m -CH 2 CH 2 and CH 3 CH 2 O- (CH 2 CH 2 O) m -CH 2 CH 2 - with m equal to 0 to 3.
- C 1 -C 6 -alkyl such as, for example, methyl, ethyl, 1-propyl, 1-butyl, 1-pentyl, 1-hexyl, 1-
- radicals R 1 to R 9 are preferably each independently
- aryl, alkyl, aryloxy, alkyloxy, halogen, heteroatoms and / or heterocycles substituted and / or interrupted by one or more oxygen and / or sulfur atoms and / or one or more substituted or unsubstituted imino groups cis-alkyl;
- aryl, alkyl, aryloxy, alkyloxy, halogen, heteroatoms and / or heterocycles substituted and / or interrupted by one or more oxygen and / or sulfur atoms and / or one or more substituted or unsubstituted imino groups cis alkenyl;
- aryl optionally substituted by functional groups, aryl, alkyl, aryloxy, alkyloxy, halogen, heteroatoms and / or heterocycles substituted C6-Ci2-aryl;
- aryl optionally substituted by functional groups, aryl, alkyl, aryloxy, alkyloxy, halogen, heteroatoms and / or heterocycles substituted C5-Ci2-cycloalkyl;
- C5-C12-cycloalkenyl substituted by functional groups, aryl, alkyl, aryloxy, alkyloxy, halo, heteroatoms and / or heterocycles; or
- aryl, alkyl, aryloxy, alkyloxy, halogen, heteroatoms and / or heterocycles d-cis-alkyl is preferably methyl, ethyl, 1-propyl, 2-propyl, 1-butyl, 2- Butyl, 2-methyl-1-propyl (isobutyl), 2-methyl-2-propyl (tert-butyl), 1-pentyl, 2-pentyl, 3-pentyl, 2-methyl-1-butyl, 3-methyl 1-butyl, 2-methyl-2-butyl, 3-methyl-2-butyl, 2,2-dimethyl-1-propyl, 1-hexyl, 2-hexyl, 3-hexyl, 2-methyl-1-pentyl , 3-methyl-1-pentyl, 4-methyl-1-pentyl, 2-methyl-2-pentyl, 3-methyl-2-pentyl, 4-methyl-2-pentyl, 2-methyl-3-pentyl, 3 -
- aryl, alkyl, aryloxy, alkyloxy, halogen, heteroatoms and / or heterocycles is preferably phenyl, ToIyI, XyIyI, ⁇ -naphthyl, ß-naphthyl, 4-diphenylyl, Chlorophenyl, dichlorophenyl, trichlorophenyl, difluorophenyl, methylphenyl, dimethylphenyl, trimethylphenyl, ethylphenyl, diethylphenyl, isopropylphenyl, tert-butylphenyl, dodecylphenyl, methoxyphenyl, dimethoxyphenyl, ethoxyphenyl, hexyloxyphenyl, methylnaphthyl, isopropylnaphthyl, chloronaphth
- C 5 -C 12 -cycloalkyl optionally substituted by functional groups, aryl, alkyl, aryloxy, alkyloxy, halo, heteroatoms and / or heterocycles is preferably cyclopentyl, cyclohexyl, cyclooctyl, cyclododecyl, methylcyclopentyl, dimethylcyclopentyl, methylcyclohexyl, Dimethylcyclohexyl, diethylcyclohexyl, butylcyclohexyl, methoxycyclohexyl, dimethoxycyclohexyl, diethoxycyclohexyl, butylthiocyclohexyl, chlorocyclohexyl, dichlorocyclohexyl, dichlorocyclopentyl, C m F 2 ( m -a) - (ib) H 2a-b with im ⁇ 30, 0 ⁇ a ⁇ m and
- An optionally substituted by functional groups, aryl, alkyl, aryloxy, alkyloxy, halogen, heteroatoms and / or heterocycles substituted five to six-membered, oxygen, nitrogen and / or sulfur atoms containing heterocycle is preferably furyl, thiophenyl, Pyrryl, pyridyl, indolyl, benzoxazolyl, dioxolyl, dioxo, benzimidazolyl, benzothiazolyl, dimethylpyridyl, methylquinolyl, dimethylpyrryl, methoxyfuryl, dimethoxypyridyl or difluoropyridyl.
- Two adjacent radicals together form an unsaturated, saturated or aromatic, optionally substituted by functional groups, aryl, alkyl, aryloxy, alkyloxy, halogen, heteroatoms and / or heterocycles and optionally substituted by one or more oxygen and / or sulfur atoms and / or one or more several substituted or unsubstituted imino groups interrupted ring, it is preferably 1, 3-propylene, 1, 4-butylene, 1, 5-pentylene, 2-oxa-1, 3-propylene, 1-oxa-1, 3- propylene, 2-oxa-1, 3-propylene, 1-oxa-1, 3-propenylene, 3-oxa 1, 5-pentylene, 1-aza-1, 3-propenylene, 1-C 1 -C 4 -alkyl-1-aza-1, 3-propenylene, 1, 4-buta-1, 3-dienylene, 1-Aza 1, 4-buta-1, 3-dienylene or 2-aza-1,4-buta-1,3-dienylene.
- radicals contain oxygen and / or sulfur atoms and / or substituted or unsubstituted imino groups
- the number of oxygen and / or sulfur atoms and / or imino groups is not restricted. As a rule, it is not more than 5 in the radical, preferably not more than 4, and very particularly preferably not more than 3.
- radicals contain heteroatoms, then between two heteroatoms there are generally at least one carbon atom, preferably at least two carbon atoms.
- radicals R 1 to R 9 are each independently
- C 1 -C 20 -alkyl which is unsubstituted or branched, unsubstituted or monosubstituted to hydroxyl, halogen, phenyl, cyano, C 1 -C 6 -alkoxycarbonyl and / or SO 3 H and has a total of 1 to 20 carbon atoms, such as, for example, methyl, ethyl, 1 Propyl, 2-propyl, 1-butyl, 2-butyl, 2-methyl-1-propyl, 2-methyl-2-propyl, 1-pentyl, 2-pentyl, 3-pentyl, 2-methyl-1-butyl , 3-methyl-1-butyl, 2-methyl-2-butyl, 3-methyl-2-butyl, 2,2-dimethyl-1-propyl, 1-hexyl, 2-hexyl, 3-hexyl, 2-methyl 1-pentyl, 3-hexyl, 2-methyl 1-pentyl, 3-methyl-1-pentyl, 4-methyl
- Glycols, butylene glycols and their oligomers having 1 to 100 units and a hydrogen or a C 1 to C 1 alkyl as end group, such as R A O- (CHR B -CH 2 -O) m -CHR B -CH 2 - or
- R A O- (CH 2 CH 2 CH 2 CH 2 ⁇ ) m -CH 2 CH 2 CH 2 CH 2 - with R A and R B preferably hydrogen, methyl or ethyl and n preferably 0 to 3, in particular 3-oxabutyl, 3-oxapentyl, 3,6-dioxaheptyl, 3,6 Dioxaoctyl, 3,6,9-trioxadecyl, 3,6,9-trioxa-undecyl, 3,6,9,12-tetraoxatridecyl and 3,6,9,12-tetraoxatetradecyl; • vinyl;
- N 1 N-di-Ci-C ⁇ alkyl-amino such as N, N-dimethylamino and N 1 N-diethylamino.
- radicals R 1 to R 9 are independently hydrogen or Ci-Ci8-alkyl, such as methyl, ethyl, 1-butyl, 1-pentyl, 1-hexyl, 1-heptyl, 1-octyl, phenyl , for 2-hydroxyethyl, for 2-cyanoethyl, for
- radicals R 1 to R 5 are methyl, ethyl or chlorine and the remaining radicals R 1 to R 5 are hydrogen;
- R 3 is dimethylamino and the remaining radicals R 1 , R 2 , R 4 and R 5 are hydrogen;
- R 2 is carboxy or carboxamide and the remaining radicals R 1 , R 2 , R 4 and R 5 are hydrogen; or
- R 1 and R 2 or R 2 and R 3 is 1, 4-buta-1,3-dienylene and the remaining radicals R 1 , R 2 , R 4 and R 5 are hydrogen;
- R 1 to R 5 are hydrogen
- radicals R 1 to R 5 are methyl or ethyl and the remaining radicals R 1 to R 5 are hydrogen.
- pyridinium ions (IIIa) which may be mentioned are 1-methylpyridinium, 1-ethylpyridinium, 1- (1-butyl) pyridinium, 1- (1-hexyl) pyridinium, 1- (1-octyl) -pyridinium, 1 (1-Hexyl) pyridinium, 1- (1-octyl) pyridinium, 1- (1-dodecyl) pyridinium, 1- (1-tetradecyl) pyridinium, 1- (1-hexadecyl) pyridinium, 1, 2-dimethylpyridinium, 1-ethyl-2-methylpyridinium, 1- (1-butyl) -2-methylpyridinium, 1- (1-hexyl) -2-methylpyridinium, 1- (1-octyl) -2-methylpyridinium, 1- (1 Dodecyl) -2-methylpyridinium, 1- (1-tetradec
- MIb very particularly preferred pyridazinium ions
- R 1 to R 4 are hydrogen
- radicals R 1 to R 4 are methyl or ethyl and the remaining radicals R 1 to R 4 are hydrogen.
- MIc very particularly preferred pyrimidinium ions
- R 1 is hydrogen, methyl or ethyl and R 2 to R 4 are independently hydrogen or methyl; or
- R 1 is hydrogen, methyl or ethyl
- R 2 and R 4 are methyl and R 3 is hydrogen.
- MId very particularly preferred pyrazinium ions
- R 1 is hydrogen, methyl or ethyl and R 2 to R 4 are independently hydrogen or methyl;
- R 1 is hydrogen, methyl or ethyl, R 2 and R 4 are methyl and R 3 is hydrogen;
- R 1 to R 4 are methyl
- R 1 to R 4 are methyl hydrogen.
- Very particularly preferred as Imidazoliumionen (Never) are those in which
- R 1 is hydrogen, methyl, ethyl, 1-propyl, 1-butyl, 1-pentyl, 1-hexyl, 1-octyl, 1-propen-3-yl, 2-hydroxyethyl or 2-cyanoethyl and R 2 to R 4 independently of one another are hydrogen, methyl or ethyl.
- MIe very particularly preferred imidazolium ions
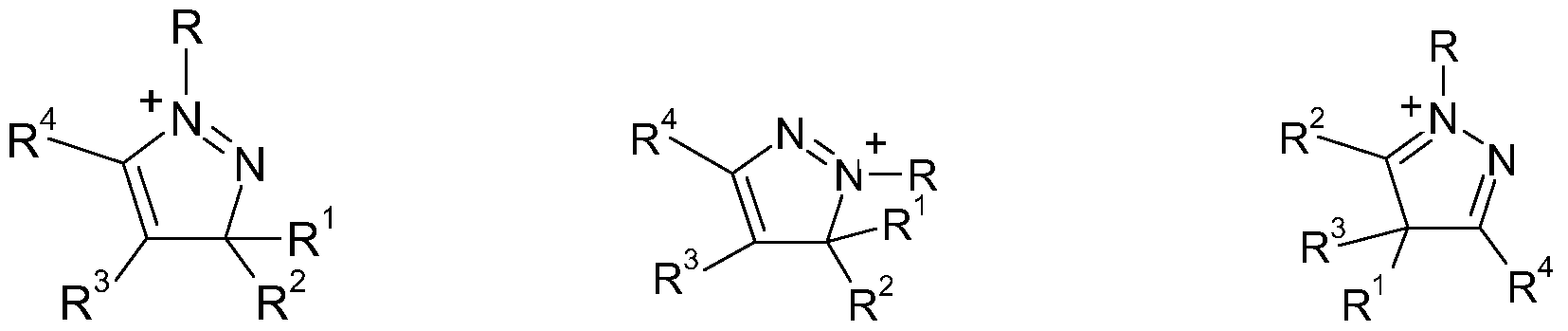
- MIf very particularly preferred pyrazolium ions
- R 1 is hydrogen, methyl or ethyl and R 2 to R 4 are independently hydrogen or methyl.
- R 1 to R 4 are independently hydrogen or methyl.
- R 1 is hydrogen, methyl, ethyl or phenyl and R 2 to R 6 are independently hydrogen or methyl.
- MIk 3-pyrazolinium ions
- IMk ' 3-pyrazolinium ions
- R 1 and R 2 are independently hydrogen, methyl, ethyl or phenyl and R 3 to R 6 are independently hydrogen or methyl.
- IUI imidazolinium ions
- R 1 and R 2 are independently hydrogen, methyl, ethyl, 1-butyl or phenyl, R 3 and R 4 are independently hydrogen, methyl or ethyl, and R 5 and R 6 are independently hydrogen or methyl.
- Imidazoliniumionen (Ulm) or (MIm ') are those in which
- R 1 and R 2 are independently hydrogen, methyl or ethyl and R 3 to R 6 are independently hydrogen or methyl.
- R 1 to R 3 are independently hydrogen, methyl or ethyl and R 4 to R 6 are independently hydrogen or methyl.
- MIo thiazolium ions
- MIo ' thiazolium ions
- MIp oxazolium ions
- R 1 is hydrogen, methyl, ethyl or phenyl and R 2 and R 3 are independently hydrogen or methyl.
- MIq 1,2,4-triazolium ions
- MIq ' 1,2,4-triazolium ions
- MIq ' 1,2,4-triazolium ions
- R 1 is hydrogen, methyl or ethyl and R 2 and R 3 are independently hydrogen or methyl, or R 2 and R 3 together are 1, 4-buta-1, 3-dienylene.
- MIs very particularly preferred pyrrolidinium ions
- R 1 is hydrogen, methyl, ethyl or phenyl and R 2 to R 9 are independently of one another hydrogen or methyl.
- R 1 and R 4 are independently hydrogen, methyl, ethyl or phenyl and R 2 and R 3 and R 5 to R 8 are independently hydrogen or methyl.
- ammonium ions (MIu) used are those in which
- R 1 to R 3 are independently of each other Ci-Cis-alkyl
- R 1 and R 2 together are 1, 5-pentylene or 3-oxa-1, 5-pentylene and R 3 is Ci-Cis-alkyl, 2-hydroxyethyl or 2-cyanoethyl.
- ammonium ions may be mentioned methyl tri (1-butyl) -ammonium, N, N-dimethylpiperidinium and N, N-dimethylmorpholinium.
- tertiary amines from which the quaternary ammonium ions of the general formula (IMu) are derived by quaternization with the abovementioned radicals R are diethyl-n-butylamine, diethyl-tert-butylamine, diethyl-n-pentylamine, diethylhexylamine, Diethyloctylamine, diethyl (2-ethylhexyl) amine, di-n-propylbutylamine, di-n-propyl-n-pentylamine, di-n-propylhexylamine, di-n-propyloctylamine, di-n-propyl (2-ethylhexyl ) -amine, di-isopropylethylamine, di-isopropyl-n-propylamine, di-isopropyl-butylamine, di-isopropylpentylamine, di
- Preferred tertiary amines are di-iso-propylethylamine, diethyl-tert-butylamine, di-iso-propylbutylamine, di-n-butyl-n-pentylamine, N, N-di-n-butylcyclohexylamine and tertiary amines of pentyl isomers.
- tertiary amines are di-n-butyl-n-pentylamine and tertiary amines of pentyl isomers.
- Another preferred tertiary amine having three identical residues is triallylamine.
- MIv guanidinium ions
- R 1 to R 5 are methyl.
- guanidinium ion N, N, N ', N', N ", N" - hexamethylguanidinium.
- MIw cholinium ions
- R 1 and R 2 are independently methyl, ethyl, 1-butyl or 1-octyl and R 3 is hydrogen, methyl, ethyl, acetyl, -SO 2 OH or -PO (OH) 2 ;
- R 1 is methyl, ethyl, 1-butyl or 1-octyl
- R 2 is a -CH 2 -CH 2 -OR 4 group and R 3 and R 4 are independently hydrogen, methyl, ethyl, acetyl, -SO 2 OH or -PO (OH) 2 ; or
- R 1 is a -CH 2 -CH 2 -OR 4 group
- R 2 is a -CH 2 -CH 2 -OR 5 group
- R 3 to R 5 are independently hydrogen, methyl, ethyl, acetyl, -SO 2 OH or -PO (OH) 2 are.
- Particularly preferred cholinium ions are those in which R 3 is selected from hydrogen, methyl, ethyl, acetyl, 5-methoxy-3-oxa-pentyl, 8-methoxy-3,6- dioxo-octyl, 1-methoxy-3,6,9-trioxa-undecyl, 7-methoxy-4-oxa-heptyl, 1-methoxy-4,8-dioxa-undecyl, 15-methoxy-4,8, 12-trioxa-pentadecyl, 9-methoxy-5-oxa-nonyl, 14-methoxy-5,10-oxa-tetradecyl, 5-ethoxy-3-oxa-pentyl, 8-ethoxy-3,6-dioxa-octyl, 11-ethoxy-3,6,9-trioxa-undecyl, 7-ethoxy-4-oxa
- phosphonium ions are those in which
- R 1 to R 3 are independently C 1 -C 6 -alkyl, in particular butyl, isobutyl, 1-hexyl or 1-octyl.
- the pyridinium ions, pyrazolinium, pyrazolium ions and the imidazolinium and imidazolium ions are preferred.
- ammonium ions are preferred.
- the anion [Y] n - the ionic liquid is for example selected from
- silicates and silicic acid esters of the general formula: SiO 4 4 -, HSiO 4 3 -, H 2 SiO 4 2 -, H 3 SiO 4 -, R 3 SiO 4 3 " , R 3 R b Si0 4 2" , R 3 R b R 1 SiO 4 " , HR 3 SiO 4 2” , H 2 R 3 SiO 4 " , HR 3 R b SiO 4 -
- R a, R b, R c and R d are each independently hydrogen, Ci- C3o-alkyl, optionally substituted by one or more nonadjacent oxygen and / or sulfur atoms and / or one or more substituted or the unsubstituted imino groups te interrupted C2-Ci8-alkyl, C6-Ci4-aryl, C5-Ci2-cycloalkyl or a five- to six-membered, oxygen, nitrogen and / or sulfur-containing heterocycle, wherein two of them together an unsaturated, saturated or aromatic, optionally can form a ring interrupted by one or more oxygen and / or sulfur atoms and / or one or more unsubstituted or substituted imino groups, where the radicals mentioned are each additionally denoted by functional groups, aryl, alkyl, aryloxy, alkyloxy, halogen, heteroatoms and / or heterocycles may be substituted.
- Ci-cis-alkyl for example methyl, ethyl, propyl, isopropyl, n-butyl, sec-butyl, tert.
- C2-Ci8-alkyl for example, 5-hydroxy-3-oxapentyl, 8-hydroxy-3,6- dioxaoctyl, 11-hydroxy-3,6,9-trioxaundecyl, 7-hydroxy-4-oxaheptyl, 1-hydroxy-4,8-dioxaundecyl, 15-hydroxy-4,8,12-trioxapentadecyl, 9-hydroxy-5 oxa-nonyl, 14-hydroxy-5,10-oxatetradecyl, 5-methoxy-3-oxapentyl, 8-methoxy-3,6-dioxa-octyl, 1-methoxy-3,6,9-trioxaundecyl, 7- Methoxy-4-oxaheptyl, 11-meth
- radicals can be taken together, for example, as fused building block 1, 3-propylene, 1,4-butylene, 2-oxa-1,3-propylene, 1-oxa-1,3-propylene, 2-oxa -1, 3-propenylene, 1-aza-1, 3-propenylene, 1-C 1 -C 4 -alkyl-1-aza-1, 3-propenylene, 1, 4-buta-1, 3-dienylene, 1-aza -1, 4-buta-1, 3-dienylene or 2-aza-1,4-buta-1,3-dienylene.
- the number of non-adjacent oxygen and / or sulfur atoms and / or imino groups is basically not limited, or is automatically limited by the size of the remainder or of the ring building block. As a rule, it is not more than 5 in the respective radical, preferably not more than 4 or very particularly preferably not more than 3. Furthermore, at least one, preferably at least two, carbon atoms (e) are generally present between two heteroatoms.
- Substituted and unsubstituted imino groups may be, for example, imino, methylimino, iso-propylimino, n-butylimino or tert-butylimino.
- the term "functional groups” is to be understood as meaning, for example, the following: carboxy, carboxamide, hydroxy, di- (C 1 -C 4 -alkyl) -amino, C 1 -C 4 -alkyloxy- carbonyl, cyano or CrC 4 -alkoxy.
- Ci to C4-alkyl is methyl, ethyl, propyl, isopropyl, n-butyl, sec-butyl or tert-butyl.
- C6-C4-aryl substituted by functional groups are, for example, phenyl, ToIyI, XyIyI, ⁇ -naphthyl, ⁇ -naphthyl, 4-diphenylyl, chlorophenyl, dichlorophenyl nyl, trichlorophenyl, difluorophenyl, methylphenyl, dimethylphenyl, trimethylphenyl, ethylphenyl, diethylphenyl, iso-propylphenyl, tert-butylphenyl, dodecylphenyl, methoxyphenyl, dimethoxyphenyl, ethoxyphenyl, hexyloxyphenyl, methylnaphthyl, isopropylnaphthyl, chlor
- C5-C12-cycloalkyl which is substituted by functional groups, aryl, alkyl, aryloxy, halogen, heteroatoms and / or heterocycles are, for example, cyclopentyl, cyclohexyl, cyclooctyl, cyclododecyl, methylcyclopentyl, dimethylcyclopentyl, methylcyclohexyl, dimethylcyclohexyl, diethylcyclohexyl, butylcyclohexyl, methoxycyclohexyl, Dimethoxycyclohexyl, diethoxycyclohexyl, butylthiocyclohexyl, chlorocyclohexyl, dichlorocyclohexyl, dichlorocyclopentyl and a saturated or unsaturated bicyclic system such as norbornyl or norbornenyl.
- a five- to six-membered, oxygen, nitrogen and / or sulfur-containing heterocycle is, for example, furyl, thiophenyl, pyrryl, pyridyl, indolyl, benzoxazolyl, dioxolyl, dioxy, benzimidazolyl, benzthiazolyl, dimethylpyridyl, methylquinolyl, dimethylpyrryl, methoxyfuryl, dimethoxypyridyl , Difluoropyridyl, methylthiophenyl, isopropylthiophenyl or tert-butylthiophenyl.
- Preferred anions are selected from the group of halides and halogen-containing compounds, the group of carboxylic acids, the group of sulfates, sulfites and sulfonates and the group of phosphates, in particular from the group of halides and halogen-containing compounds, the group of carboxylic acids, the Group containing SO 4 2 " , SO 3 2" , R 3 OSO 3 " and R 3 SO 3 -, and the group containing PO 4 3" and R 3 R b PO 4 -.
- Preferred anions are chloride, bromide, iodide, SCN, OCN, CN, acetate, CrC 4 alkyl sulfates, R 3 -C00 " , R 3 SO 3 -, R 3 R b PO 4 -, methanesulfonate, tosylate or CrC 4 - Dialkyl phosphates.
- Particularly preferred anions are Ch, CH 3 COO, C 2 H 5 COO, C 6 H 5 COO, CH 3 SO 3 -, (CH 3 O) 2 PO 2 - or (C 2 H 5 O) 2 PO 2 -
- an ionic liquid of the formula I is used or a mixture of ionic liquids of the formula I, preferably an ionic liquid of the formula I is used.
- the acids used are inorganic acids, organic acids or mixtures thereof.
- inorganic acids are hydrohalic acids, such as HF, HCl, HBr or Hl, perhalogenic acids, such as HCIO 4 , halogen acids, such as HCIO3, sulfur-containing acids, such as H2SO4, polysulfuric acid or H2SO3, nitrogen-containing acids, such as HNO3, or phosphorus-containing Acids, such as H3PO4, polyphosphoric acid or H3PO3
- hydrohalic acids such as HF, HCl, HBr or Hl
- perhalogenic acids such as HCIO 4
- halogen acids such as HCIO3, sulfur-containing acids, such as H2SO4, polysulfuric acid or H2SO3, nitrogen-containing acids, such as HNO3, or phosphorus-containing Acids, such as H3PO4, polyphosphoric acid or H3PO3
- hydrogen halide acids such as HCl or HBr, H2SO4, HN ⁇ 3 ⁇ der H3PO4 used, in particular HCl, H 2 SO 4 or H 3
- organic acids examples include carboxylic acids, such as
- C 1 -C 6 -alkanecarboxylic acids for example acetic acid, propionic acid, n-butanecarboxylic acid or pivalic acid,
- Polycarboxylic acids for example succinic acid, maleic acid or fumaric acid,
- Hydroxycarboxylic acids for example hydroxyacetic acid, lactic acid, malic acid or citric acid,
- Halogenated carboxylic acids for example Ci-C ⁇ -haloalkanecarboxylic acids, e.g. Fluoroacetic acid, chloroacetic acid, bromoacetic acid, difluoroacetic acid, dichloroacetic acid, chlorofluoroacetic acid, trifluoroacetic acid, trichloroacetic acid,
- Aromatic carboxylic acids for example arylcarboxylic acids, such as benzoic acid;
- C 1 -C 6 -alkanesulfonic acids for example methanesulfonic acid or ethanesulfonic acid,
- Halogenated sulfonic acids for example C 1 -C 8 -haloalkanesulfonic acids, such as trifluoromethanesulfonic acid,
- Aromatic sulfonic acids for example arylsulfonic acids, such as benzenesulfonic acid or 4-methylphenylsulfonic acid.
- C 1 -C 6 -alkanecarboxylic acids preference is given to C 1 -C 6 -alkanecarboxylic acids, for example acetic acid or propionic acid, halogenated carboxylic acids, for example C 6 -haloalkanecarboxylic acids, for example fluoroacetic acid, chloroacetic acid, difluoroacetic acid, dichloroacetic acid, chlorofluoroacetic acid, trifluoroacetic acid, trichloroacetic acid or perfluoropropionic acid, or sulfonic acids, such as C 1 -C 6 -alkanesulfonic acids, for example methanesulfonic acid or ethanesulfonic acid, halogenated sulfonic acids, for example C 1 -C 6 -haloalkanesulfonic acids, such as trifluoromethanesulfonic acid, or arylsulfonic acids, such as benzenesulfonic
- acetic acid chlorofluoroacetic acid, trifluoroacetic acid, perfluoropropionic acid, methanesulfonic acid, trifluoromethanesulfonic acid or 4-methyl-phenylsulfonic acid are used.
- the acid sulfuric acid in a particular embodiment of the invention are used as the acid sulfuric acid, acetic acid, trifluoroacetic acid, methanesulfonic acid or 4-methylphenyl sulfonic acid. If 4-methylphenylsulfonic acid monohydrate is used, there is already one equivalent of water present.
- ionic liquids and acids are used whose anions are identical.
- these anions are acetate, trifluoroacetate, chloride or bromide.
- ionic liquids and acids are used whose anions are not identical.
- celluloses from a wide variety of sources can be used, e.g. cotton, flax, ramie, straw, bacteria etc., or wood or bagasse, in the cellulose-enriched form.
- the process according to the invention can be used not only for the degradation of cellulose but generally for the cleavage or degradation of poly-, oligo- and disaccharides, as well as derivatives thereof.
- polysaccharides in addition to cellulose and hemicellulose, starch, glycogen, dextran and tunicin may be mentioned.
- these include the polycondensates of D-fructose, such as inulin, and u.a. Chitin, and alginic acid.
- Sucrose is an example of a disaccharide.
- cellulose derivatives i.a. Cellulose ethers, such as methylcellulose and carboxymethylcellulose, cellulose esters, such as cellulose acetate, cellulose butyrate and cellulose senitrate.
- cellulose derivatives i.a. Cellulose ethers, such as methylcellulose and carboxymethylcellulose
- cellulose esters such as cellulose acetate, cellulose butyrate and cellulose senitrate.
- a solution of cellulose in ionic liquid is prepared.
- concentration of cellulose can be varied within a wide range. It is usually in the range from 0.1 to 50% by weight, based on the total weight of the solution, preferably from 0.2 to 40% by weight, in particular It is preferably from 0.3 to 30% by weight, and more preferably from 0.5 to 20% by weight.
- This dissolution process can be carried out at room temperature or with heating, but above the melting or softening temperature of the ionic liquid, usually at a temperature of 0 to 200 ° C., preferably at 20 to 180 ° C., particularly preferably at 50 to 150 ° C.
- it is also possible to accelerate the dissolution process by intensive stirring or mixing as well as by introduction of microwave or ultrasonic energy or by a combination thereof.
- the acid and optionally water is added.
- the addition of water may be necessary if the water adhering to the cellulose used is insufficient to reach the desired degree of degradation.
- the proportion of water in conventional cellulose in the range of 5 to 10 wt .-%, based on the total weight of the cellulose used (cellulose per se + adherent water).
- the ionic liquid, acid and possibly water are premixed and the cellulose is dissolved in this mixture.
- Suitable solvents are those which do not adversely affect the solubility of the cellulose, such as aprotic-dipolar solvents, for example dimethyl sulfoxide, dimethylformamide, dimethylacetamide or sulfolane.
- the reaction mixture contains less than 5 wt .-%, preferably less than 2 wt .-%, in particular less than 0.1 wt .-% of other solvents, based on the total weight of the reaction mixture.
- the hydrolysis is usually carried out at a temperature from the melting point of the ionic liquid to 200 ° C., preferably from 20 to 180 ° C., in particular from 50 to 150 ° C., depending on the ionic liquid used and the acid used.
- the reaction is carried out at ambient pressure.
- it may also be advantageous on a case-by-case basis to work at overpressure, especially when volatile acids are used.
- the reaction is carried out in air. But it is also possible under inert gas, so for example under N2, to work a noble gas, CO2 or a mixture thereof.
- reaction time is in a range of 1 to 24 hours.
- the amount of acid used, the water to be added if necessary, in each case in relation to the cellulose used, the reaction time and optionally the reaction temperature is set.
- the acid can be used here in catalytic amounts, preferably in the range from 1 to 50 mol% based on x. However, it is also possible to increase the proportion of acid up to the stoichiometric ratio (with respect to x) or in excess.
- n-anhydroglucose units / n s acid> 1 the amounts of water used and acid used are usually adjusted accordingly (n-anhydroglucose units / n s acid> 1).
- the hydrolysis reaction when the desired degree of degradation is achieved by separating the cellulose from the reaction mixture. This can be done, for example, by cooling the reaction mixture and then adding an excess of water or other suitable solvent in which the degraded cellulose is insoluble, such as a lower alcohol such as methanol, ethanol, propanol or butanol, or with a ketone, for example Acetone, etc., or mixtures thereof. Preferably, an excess of water or methanol is used. It is also possible to stop the hydrolysis reaction when the desired degree of degradation is achieved by precipitating the cellulose from the reaction mixture without first cooling the reaction mixture.
- reaction mixture is dissolved in water or another suitable solvent in which the degraded cellulose is insoluble, e.g. a lower alcohol, such as methanol, ethanol, propanol or butanol, or a ketone, for example acetone, etc., or mixtures thereof, initiate and, depending on the embodiment, for example, fibers, films, etc. obtained from degraded cellulose.
- a suitable solvent e.g. a lower alcohol, such as methanol, ethanol, propanol or butanol, or a ketone, for example acetone, etc., or mixtures thereof, initiate and, depending on the embodiment, for example, fibers, films, etc. obtained from degraded cellulose.
- the filtrate is worked up as described above.
- Suitable bases include both inorganic bases, e.g. Alkali hydroxides, carbonates, hydrogen carbonates, but also organic bases such as e.g. Amines which are used in stoichiometric ratio to the acid or in excess.
- a hydroxide can be used as the base, which is characterized in that its cation corresponds to that of the ionic liquid used.
- the workup of the reaction mixture is usually carried out by the cellulose is precipitated as described above and the cellulose is filtered off. From the filtrate, the ionic liquid can be recovered by conventional methods by dissolving the volatile components, e.g. the precipitating agent, any added water and if volatile acids such as e.g. Organic acids were used, these, or possibly further solvent are distilled off. The remaining ionic liquid can be reused in the process according to the invention.
- the acid can also, if it is worked up without neutralization, remain after removal of the solvent in the ionic liquid and the mixture (if necessary after addition of water) can be used again for the cellulose degradation.
- the ionic liquid to be regenerated contains only a small amount of glucose or its oligomers. Any existing amounts of these compounds can be separated by extraction with a solvent or by adding a precipitant from the ionic liquid.
- the corresponding glucose can be separated by conventional methods, such as precipitation with ethanol from the ionic liquid.
- the ionic liquid may contain up to 15% by weight, preferably up to 10% by weight, in particular up to 5% by weight of precipitant (s) as described above , contain.
- the process can be carried out batchwise, semicontinuously or continuously.
- Cotton linters hereafter Linters
- Avicel PH 101 microcrystalline cellulose
- the ionic liquids were dried overnight at 120 ° C and 0.05 mbar with stirring.
- the ionic liquids then contain about 200 ppm of water.
- the average degree of polymerization DP of the (used as far as necessary) and of the degraded cellulose was determined by measuring the viscosity in each case.
- Example 8 Complete degradation of cellulose in EMIM Cl by trifluoroacetic acid at 120 ° C.
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Materials Engineering (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Compositions Of Macromolecular Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
Description
Claims
Priority Applications (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2008557720A JP2009531024A (ja) | 2006-03-08 | 2007-02-28 | 溶液中のセルロースの分解方法 |
| EP07712359A EP1994059A1 (de) | 2006-03-08 | 2007-02-28 | Verfahren zum abbau von cellulose in lösung |
| US12/281,786 US20090062524A1 (en) | 2006-03-08 | 2007-02-28 | Method for breaking down cellulose in solution |
| BRPI0708590-7A BRPI0708590A2 (pt) | 2006-03-08 | 2007-02-28 | processo para a degradação de polissacarìdeos, oligossacarìdeos ou dissacarìdeos ou derivados dos mesmos |
| CA002642863A CA2642863A1 (en) | 2006-03-08 | 2007-02-28 | Method for breaking down cellulose in solution |
| AU2007222455A AU2007222455B2 (en) | 2006-03-08 | 2007-02-28 | Method for breaking down cellulose in solution |
| US13/350,051 US20120116068A1 (en) | 2006-03-08 | 2012-01-13 | Method for breaking down cellulose in solution |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102006011075A DE102006011075A1 (de) | 2006-03-08 | 2006-03-08 | Verfahren zum Abbau von Cellulose in Lösung |
| DE102006011075.7 | 2006-03-08 |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| US13/350,051 Continuation US20120116068A1 (en) | 2006-03-08 | 2012-01-13 | Method for breaking down cellulose in solution |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2007101811A1 true WO2007101811A1 (de) | 2007-09-13 |
Family
ID=37963943
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2007/051870 WO2007101811A1 (de) | 2006-03-08 | 2007-02-28 | Verfahren zum abbau von cellulose in lösung |
Country Status (11)
| Country | Link |
|---|---|
| US (2) | US20090062524A1 (de) |
| EP (1) | EP1994059A1 (de) |
| JP (1) | JP2009531024A (de) |
| KR (1) | KR20080104053A (de) |
| CN (1) | CN101395184A (de) |
| AU (1) | AU2007222455B2 (de) |
| BR (1) | BRPI0708590A2 (de) |
| CA (1) | CA2642863A1 (de) |
| DE (1) | DE102006011075A1 (de) |
| WO (1) | WO2007101811A1 (de) |
| ZA (1) | ZA200808486B (de) |
Cited By (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2033973A1 (de) * | 2007-09-06 | 2009-03-11 | The Queen's University of Belfast | Konversionsverfahren |
| EP2033974A1 (de) * | 2007-09-06 | 2009-03-11 | The Queens University of Belfast | Konversionsverfahren |
| DE102007058394A1 (de) | 2007-12-03 | 2009-06-04 | Bayer Technology Services Gmbh | Verfahren zur Herstellung von Kraftstoffen aus Biomasse |
| WO2009115075A1 (de) * | 2008-03-18 | 2009-09-24 | Studiengesellschaft Kohle Mbh | Verfahren zur depolymerisation von cellulose |
| JP2010083850A (ja) * | 2008-10-02 | 2010-04-15 | Kri Inc | リグノセルロースの糖化及びエタノール発酵方法 |
| ITMI20082251A1 (it) * | 2008-12-18 | 2010-06-19 | Eni Spa | Procedimento per la produzione di zuccheri da biomassa |
| JP2010189324A (ja) * | 2009-02-18 | 2010-09-02 | Kanagawa Prefecture | アルコールの製造方法 |
| CN101250285B (zh) * | 2007-10-10 | 2011-04-20 | 中国科学院过程工程研究所 | 一种降解聚对苯二甲酸乙二醇酯的方法 |
| CN101402658B (zh) * | 2008-07-16 | 2011-07-06 | 大连工业大学 | 一种离子液体溶剂催化热降解纤维素的方法 |
| WO2011086082A1 (en) | 2010-01-15 | 2011-07-21 | Basf Se | Method of chlorinating polysaccharides or oligosaccharides |
| CN102134615A (zh) * | 2010-12-30 | 2011-07-27 | 浙江师范大学 | 一种水解甲壳素和壳聚糖的方法 |
| JP2012531892A (ja) * | 2009-07-01 | 2012-12-13 | ウイスコンシン アラムナイ リサーチ ファウンデーシヨン | バイオマス加水分解 |
| WO2013053630A1 (en) | 2011-10-14 | 2013-04-18 | Basf Se | Preparation of oligosaccharides containing amine groups |
| US8884003B2 (en) | 2010-01-15 | 2014-11-11 | Basf Se | Method of chlorinating polysaccharides or oligosaccharides |
| EP2899214A1 (de) | 2014-01-27 | 2015-07-29 | Basf Se | Ethylenisch ungesättigte Polysaccharide, Verfahren zu deren Herstellung und deren Verwendung |
| EP2899213A1 (de) | 2014-01-27 | 2015-07-29 | Basf Se | Modifizierte Polysaccharide, Verfahren zu deren Herstellung und deren Verwendung |
Families Citing this family (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2674941A1 (en) * | 2007-01-23 | 2008-07-31 | Basf Se | Method for producing glucose by enzymatic hydrolysis of cellulose that can be pretreated with an ionic liquid containing a polyatomic anion |
| US8153782B2 (en) | 2007-02-14 | 2012-04-10 | Eastman Chemical Company | Reformation of ionic liquids |
| US9834516B2 (en) * | 2007-02-14 | 2017-12-05 | Eastman Chemical Company | Regioselectively substituted cellulose esters produced in a carboxylated ionic liquid process and products produced therefrom |
| US10174129B2 (en) | 2007-02-14 | 2019-01-08 | Eastman Chemical Company | Regioselectively substituted cellulose esters produced in a carboxylated ionic liquid process and products produced therefrom |
| US7674608B2 (en) | 2007-02-23 | 2010-03-09 | The University Of Toledo | Saccharifying cellulose |
| CA2680790C (en) * | 2007-03-14 | 2018-09-11 | The University Of Toledo | Biomass pretreatment |
| US20100297532A1 (en) * | 2008-01-09 | 2010-11-25 | Basf Se | Process for working up ionic liquids |
| US9777074B2 (en) | 2008-02-13 | 2017-10-03 | Eastman Chemical Company | Regioselectively substituted cellulose esters produced in a halogenated ionic liquid process and products produced therefrom |
| US8188267B2 (en) | 2008-02-13 | 2012-05-29 | Eastman Chemical Company | Treatment of cellulose esters |
| US8158777B2 (en) * | 2008-02-13 | 2012-04-17 | Eastman Chemical Company | Cellulose esters and their production in halogenated ionic liquids |
| US8354525B2 (en) * | 2008-02-13 | 2013-01-15 | Eastman Chemical Company | Regioselectively substituted cellulose esters produced in a halogenated ionic liquid process and products produced therefrom |
| CA2726126C (en) | 2008-06-17 | 2018-07-17 | Wisconsin Alumni Research Foundation | Chemical transformation of lignocellulosic biomass into fuels and chemicals |
| US7999355B2 (en) * | 2008-07-11 | 2011-08-16 | Air Products And Chemicals, Inc. | Aminosilanes for shallow trench isolation films |
| US8067488B2 (en) * | 2009-04-15 | 2011-11-29 | Eastman Chemical Company | Cellulose solutions comprising tetraalkylammonium alkylphosphate and products produced therefrom |
| JP2011184420A (ja) * | 2010-03-11 | 2011-09-22 | Univ Of Tokyo | 単糖類の製造方法 |
| US8980050B2 (en) | 2012-08-20 | 2015-03-17 | Celanese International Corporation | Methods for removing hemicellulose |
| CN102559943B (zh) * | 2010-12-31 | 2014-02-12 | 北京化工大学 | 一种分离葡萄糖与离子液体的工艺方法 |
| US9096691B2 (en) | 2011-04-13 | 2015-08-04 | Eastman Chemical Company | Cellulose ester optical films |
| AU2012275265B2 (en) * | 2011-06-29 | 2017-05-04 | Covidien Lp | Dissolution of oxidized cellulose |
| US8986501B2 (en) | 2012-08-20 | 2015-03-24 | Celanese International Corporation | Methods for removing hemicellulose |
| JP2016527330A (ja) * | 2013-05-24 | 2016-09-08 | メッツァ ファイバー オサケユキチュアMetsa Fibre Oy | ポリマーを修飾する方法 |
| ES2528394B1 (es) * | 2013-07-08 | 2015-11-18 | Consejo Superior De Investigaciones Científicas (Csic) | Procedimiento de hidrólisis de biomasa lignocelulósica |
| ITMI20132069A1 (it) * | 2013-12-11 | 2015-06-12 | Versalis Spa | Procedimento per la produzione di zuccheri da biomassa |
| CN106632528A (zh) * | 2016-12-27 | 2017-05-10 | 温县兴发生物科技有限公司 | 一种百香果低聚糖的制备方法 |
| JP2019122262A (ja) * | 2018-01-11 | 2019-07-25 | 株式会社ダイセル | グルコースの製造方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005066374A1 (en) * | 2004-01-05 | 2005-07-21 | Kemira Oyj | Depolymerization method |
| WO2006000197A1 (de) * | 2004-06-26 | 2006-01-05 | Thüringisches Institut für Textil- und Kunststoff-Forschung e.V. | Verfahren und vorrichtung zur herstellung von formkörpern aus cellulose |
| WO2006108861A2 (de) * | 2005-04-15 | 2006-10-19 | Basf Aktiengesellschaft | Löslichkeit von cellulose in ionischen flüssigkeiten unter zugabe von aminbase |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4174976A (en) * | 1978-03-08 | 1979-11-20 | Purdue Research Foundation | Acid hydrolysis of cellulose to yield glucose |
| DE4003172A1 (de) * | 1990-02-03 | 1991-08-08 | Basf Ag | Pfropfcopolymerisate von monosacchariden, oligosacchariden, polysacchariden und modifizierten polysacchariden, verfahren zu ihrer herstellung und ihre verwendung |
| AR038161A1 (es) * | 2002-01-24 | 2004-12-29 | Basf Ag | Procedimiento para separar acidos de mezclas de reaccion quimicas con la ayuda de liquidos ionicos |
-
2006
- 2006-03-08 DE DE102006011075A patent/DE102006011075A1/de not_active Withdrawn
-
2007
- 2007-02-28 CN CNA2007800081191A patent/CN101395184A/zh active Pending
- 2007-02-28 AU AU2007222455A patent/AU2007222455B2/en not_active Ceased
- 2007-02-28 US US12/281,786 patent/US20090062524A1/en not_active Abandoned
- 2007-02-28 EP EP07712359A patent/EP1994059A1/de not_active Withdrawn
- 2007-02-28 WO PCT/EP2007/051870 patent/WO2007101811A1/de active Application Filing
- 2007-02-28 BR BRPI0708590-7A patent/BRPI0708590A2/pt not_active IP Right Cessation
- 2007-02-28 JP JP2008557720A patent/JP2009531024A/ja active Pending
- 2007-02-28 CA CA002642863A patent/CA2642863A1/en not_active Abandoned
- 2007-02-28 KR KR1020087024461A patent/KR20080104053A/ko not_active Application Discontinuation
-
2008
- 2008-10-06 ZA ZA200808486A patent/ZA200808486B/xx unknown
-
2012
- 2012-01-13 US US13/350,051 patent/US20120116068A1/en not_active Abandoned
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005066374A1 (en) * | 2004-01-05 | 2005-07-21 | Kemira Oyj | Depolymerization method |
| WO2006000197A1 (de) * | 2004-06-26 | 2006-01-05 | Thüringisches Institut für Textil- und Kunststoff-Forschung e.V. | Verfahren und vorrichtung zur herstellung von formkörpern aus cellulose |
| WO2006108861A2 (de) * | 2005-04-15 | 2006-10-19 | Basf Aktiengesellschaft | Löslichkeit von cellulose in ionischen flüssigkeiten unter zugabe von aminbase |
Non-Patent Citations (2)
| Title |
|---|
| HUSEMAN E ET AL: "N-AETHYL-PYRIDINIUM-CHLORID ALS LOESUNGSMITTEL UND REAKTIONSMEDIUM FUER CELLULOSE", MAKROMOLEKULARE CHEMIE, HUETHIG UND WEPF, BASEL, CH, vol. 128, no. 1, 17 October 1969 (1969-10-17), pages 288 - 291, XP009073037, ISSN: 0025-116X * |
| T. HEINZE ET AL.: "Ionic Liquids as Reaction Medium in Cellulose Functionalization", MACROMOLECULAR BISOSCIENCE, 2005, pages 520 - 525, XP002432049 * |
Cited By (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2033974A1 (de) * | 2007-09-06 | 2009-03-11 | The Queens University of Belfast | Konversionsverfahren |
| WO2009030950A1 (en) * | 2007-09-06 | 2009-03-12 | The Queen's University Of Belfast | Conversion method |
| WO2009030949A1 (en) * | 2007-09-06 | 2009-03-12 | The Queen's University Of Belfast | Conversion method |
| AU2008294513B2 (en) * | 2007-09-06 | 2013-05-30 | Petroliam Nasional Berhad (Petronas) | Conversion method |
| US8574368B2 (en) | 2007-09-06 | 2013-11-05 | Petroliam Nasional Berhard (Petronas) | Conversion method |
| EP2033973A1 (de) * | 2007-09-06 | 2009-03-11 | The Queen's University of Belfast | Konversionsverfahren |
| US8721795B2 (en) | 2007-09-06 | 2014-05-13 | Petroliam Nasional Berhad (Petronas) | Conversion method |
| EA019759B1 (ru) * | 2007-09-06 | 2014-06-30 | Дзе Куин'С Юнивёсити Оф Белфаст | Способ получения водорастворимых продуктов гидролиза целлюлозы |
| EA022504B1 (ru) * | 2007-09-06 | 2016-01-29 | Петролиам Назионал Берхад (Петронас) | Способ получения растворимых в воде продуктов гидролиза целлюлозы |
| JP2010537662A (ja) * | 2007-09-06 | 2010-12-09 | ザ クイーンズ ユニバーシティ オブ ベルファスト | 転化方法 |
| JP2010537661A (ja) * | 2007-09-06 | 2010-12-09 | ザ クイーンズ ユニバーシティ オブ ベルファスト | 転化方法 |
| CN101250285B (zh) * | 2007-10-10 | 2011-04-20 | 中国科学院过程工程研究所 | 一种降解聚对苯二甲酸乙二醇酯的方法 |
| DE102007058394A1 (de) | 2007-12-03 | 2009-06-04 | Bayer Technology Services Gmbh | Verfahren zur Herstellung von Kraftstoffen aus Biomasse |
| WO2009115075A1 (de) * | 2008-03-18 | 2009-09-24 | Studiengesellschaft Kohle Mbh | Verfahren zur depolymerisation von cellulose |
| CN101402658B (zh) * | 2008-07-16 | 2011-07-06 | 大连工业大学 | 一种离子液体溶剂催化热降解纤维素的方法 |
| JP2010083850A (ja) * | 2008-10-02 | 2010-04-15 | Kri Inc | リグノセルロースの糖化及びエタノール発酵方法 |
| WO2010069583A1 (en) * | 2008-12-18 | 2010-06-24 | Eni S.P.A. | Process for the production of sugars from biomass |
| ITMI20082251A1 (it) * | 2008-12-18 | 2010-06-19 | Eni Spa | Procedimento per la produzione di zuccheri da biomassa |
| JP2010189324A (ja) * | 2009-02-18 | 2010-09-02 | Kanagawa Prefecture | アルコールの製造方法 |
| US8722878B2 (en) | 2009-07-01 | 2014-05-13 | Wisconsin Alumni Research Foundation | Biomass hydrolysis |
| JP2012531892A (ja) * | 2009-07-01 | 2012-12-13 | ウイスコンシン アラムナイ リサーチ ファウンデーシヨン | バイオマス加水分解 |
| JP2015213507A (ja) * | 2009-07-01 | 2015-12-03 | ウイスコンシン アラムナイ リサーチ ファウンデーシヨンWisconsin Alumni Research Foundation | バイオマス加水分解 |
| US8884003B2 (en) | 2010-01-15 | 2014-11-11 | Basf Se | Method of chlorinating polysaccharides or oligosaccharides |
| WO2011086082A1 (en) | 2010-01-15 | 2011-07-21 | Basf Se | Method of chlorinating polysaccharides or oligosaccharides |
| CN102134615B (zh) * | 2010-12-30 | 2013-04-17 | 浙江师范大学 | 一种水解甲壳素和壳聚糖的方法 |
| CN102134615A (zh) * | 2010-12-30 | 2011-07-27 | 浙江师范大学 | 一种水解甲壳素和壳聚糖的方法 |
| WO2013053630A1 (en) | 2011-10-14 | 2013-04-18 | Basf Se | Preparation of oligosaccharides containing amine groups |
| EP2899214A1 (de) | 2014-01-27 | 2015-07-29 | Basf Se | Ethylenisch ungesättigte Polysaccharide, Verfahren zu deren Herstellung und deren Verwendung |
| EP2899213A1 (de) | 2014-01-27 | 2015-07-29 | Basf Se | Modifizierte Polysaccharide, Verfahren zu deren Herstellung und deren Verwendung |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20080104053A (ko) | 2008-11-28 |
| JP2009531024A (ja) | 2009-09-03 |
| CN101395184A (zh) | 2009-03-25 |
| CA2642863A1 (en) | 2007-09-13 |
| AU2007222455B2 (en) | 2012-06-07 |
| EP1994059A1 (de) | 2008-11-26 |
| ZA200808486B (en) | 2009-12-30 |
| BRPI0708590A2 (pt) | 2011-06-07 |
| US20090062524A1 (en) | 2009-03-05 |
| AU2007222455A1 (en) | 2007-09-13 |
| DE102006011075A1 (de) | 2007-09-13 |
| US20120116068A1 (en) | 2012-05-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2007101811A1 (de) | Verfahren zum abbau von cellulose in lösung | |
| EP1994060A1 (de) | Verfahren zum abbau von cellulose | |
| EP1994058A1 (de) | Verfahren zum abbau von cellulose mit nucleophilen | |
| WO2008000666A1 (de) | Verfahren zur acylierung von cellulose mit gezieltem durchschnittlichen polymerisationsgrad | |
| EP2035458A1 (de) | Verfahren zur acylierung von cellulose | |
| EP1893651B1 (de) | Löslichkeit von cellulose in ionischen flüssigkeiten unter zugabe von aminbase | |
| EP1881994B1 (de) | Lösungen von cellulose in ionischen flüssigkeiten | |
| EP2041183A1 (de) | Verfahren zur darstellung von celluloseacetalen | |
| EP1966284B1 (de) | Lösungssystem auf der basis geschmolzener ionischer flüssigkeiten, dessen herstellung sowie verwendung zur herstellung regenerierter kohlenhydrate | |
| EP2035460A1 (de) | Verfahren zur silylierung von cellulose | |
| DE102005062608A1 (de) | Lösungssystem auf der Basis geschmolzener ionischer Flüssigkeiten ein Verfahren zu dessen Herstellung sowie zur Herstellung regenerierter Kohlenydrate | |
| DE102006011076A1 (de) | Verfahren zum Abbau von Cellulose | |
| DE102006035830A9 (de) | Lösungssystem auf der Basis geschmolzener ionischer Flüssigkeiten, dessen Herstellung sowie Verwendung zur Herstellung regenerierter Kohlenhydrate | |
| DE102006029306A1 (de) | Verfahren zur Silylierung von Cellulose | |
| DE102006031810A1 (de) | Verfahren zur Darstellung von Celluloseacetalen | |
| DE102006042892A1 (de) | Verfahren zur Acylierung von Cellulose mit gezieltem durchschnittlichen Polymerisationsgrad | |
| DE102006042891A1 (de) | Verfahren zum Abbau von Cellulose | |
| DE102006030696A1 (de) | Verfahren zur Acylierung von Cellulose mit gezieltem durchschnittlichen Polymerisationsgrad | |
| DE102006054213A1 (de) | Verfahren zur Darstellung von Celluloseacetalen | |
| DE102006042890A1 (de) | Verfahren zur Silylierung von Cellulose | |
| DE102006032569A1 (de) | Verfahren zur Silylierung von Cellulose | |
| DE102006054233A1 (de) | Verfahren zur Silylierung von Cellulose |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application | ||
| WWE | Wipo information: entry into national phase |
Ref document number: 2642863 Country of ref document: CA |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2007712359 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12281786 Country of ref document: US |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2007222455 Country of ref document: AU Ref document number: 2008557720 Country of ref document: JP Ref document number: 200780008119.1 Country of ref document: CN |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| ENP | Entry into the national phase |
Ref document number: 2007222455 Country of ref document: AU Date of ref document: 20070228 Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 5380/CHENP/2008 Country of ref document: IN Ref document number: 1020087024461 Country of ref document: KR |
|
| ENP | Entry into the national phase |
Ref document number: PI0708590 Country of ref document: BR Kind code of ref document: A2 Effective date: 20080905 |