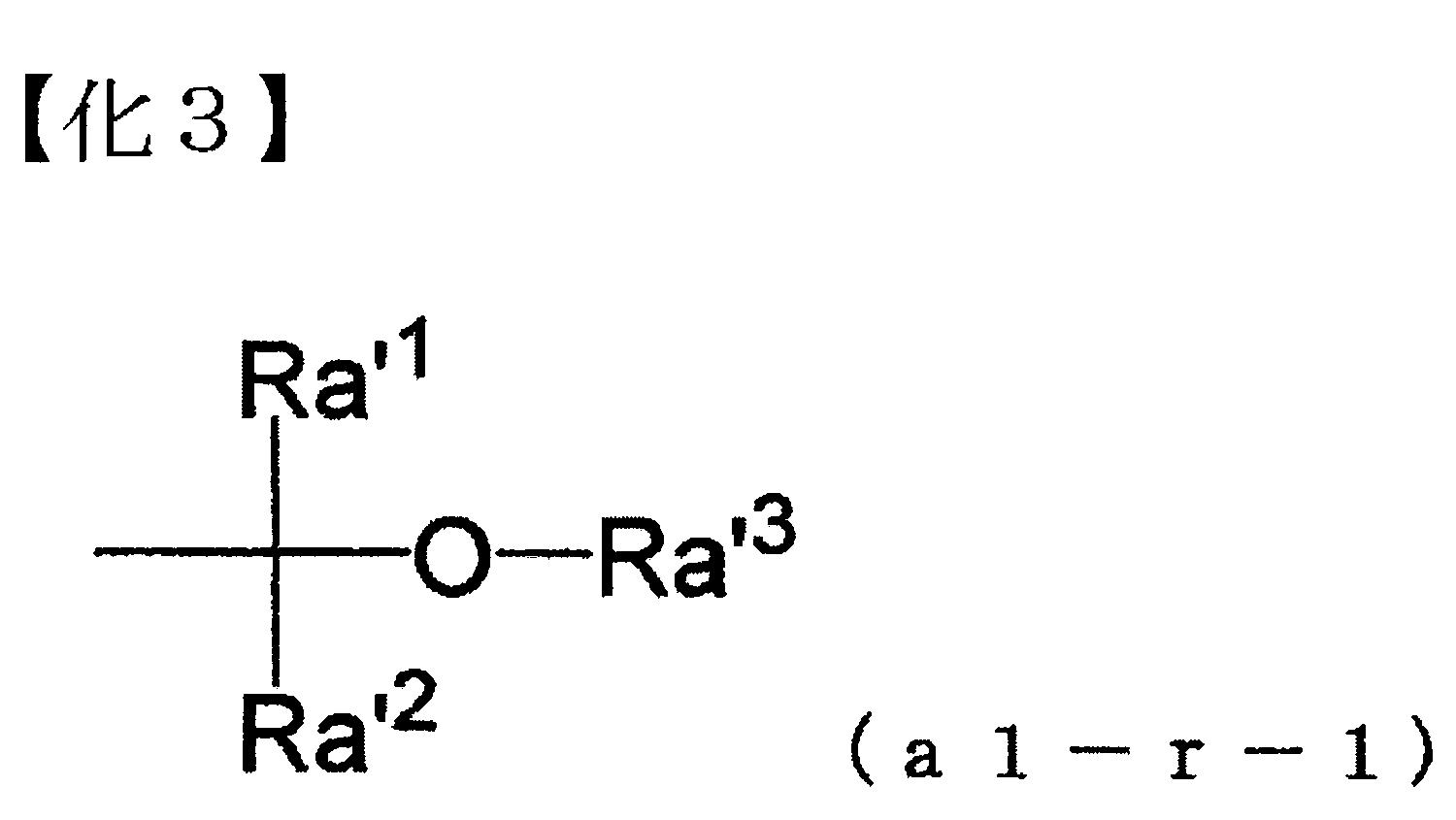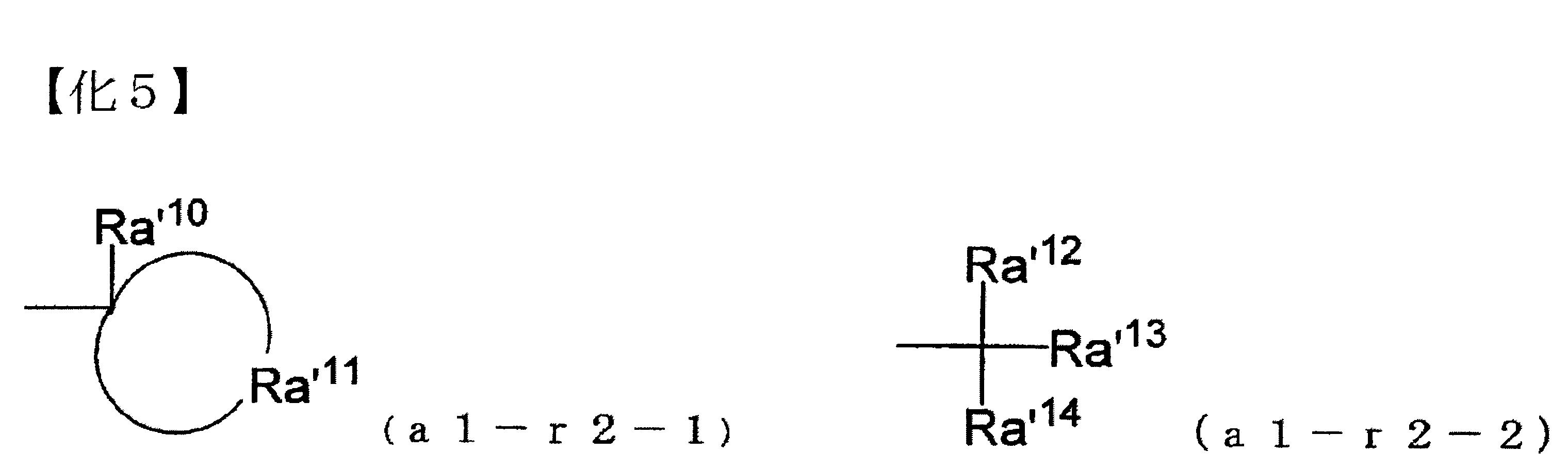TWI761475B - 阻劑組成物及阻劑圖型形成方法,與化合物及酸擴散控制劑 - Google Patents
阻劑組成物及阻劑圖型形成方法,與化合物及酸擴散控制劑 Download PDFInfo
- Publication number
- TWI761475B TWI761475B TW107110436A TW107110436A TWI761475B TW I761475 B TWI761475 B TW I761475B TW 107110436 A TW107110436 A TW 107110436A TW 107110436 A TW107110436 A TW 107110436A TW I761475 B TWI761475 B TW I761475B
- Authority
- TW
- Taiwan
- Prior art keywords
- group
- acid
- substituent
- component
- atom
- Prior art date
Links
Classifications
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/0045—Photosensitive materials with organic non-macromolecular light-sensitive compounds not otherwise provided for, e.g. dissolution inhibitors
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D285/00—Heterocyclic compounds containing rings having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by groups C07D275/00 - C07D283/00
- C07D285/01—Five-membered rings
- C07D285/02—Thiadiazoles; Hydrogenated thiadiazoles
- C07D285/04—Thiadiazoles; Hydrogenated thiadiazoles not condensed with other rings
- C07D285/10—1,2,5-Thiadiazoles; Hydrogenated 1,2,5-thiadiazoles
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D285/00—Heterocyclic compounds containing rings having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by groups C07D275/00 - C07D283/00
- C07D285/01—Five-membered rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D285/00—Heterocyclic compounds containing rings having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by groups C07D275/00 - C07D283/00
- C07D285/01—Five-membered rings
- C07D285/02—Thiadiazoles; Hydrogenated thiadiazoles
- C07D285/04—Thiadiazoles; Hydrogenated thiadiazoles not condensed with other rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D285/00—Heterocyclic compounds containing rings having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by groups C07D275/00 - C07D283/00
- C07D285/01—Five-membered rings
- C07D285/02—Thiadiazoles; Hydrogenated thiadiazoles
- C07D285/14—Thiadiazoles; Hydrogenated thiadiazoles condensed with carbocyclic rings or ring systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D513/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00
- C07D513/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00 in which the condensed system contains two hetero rings
- C07D513/04—Ortho-condensed systems
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/038—Macromolecular compounds which are rendered insoluble or differentially wettable
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/039—Macromolecular compounds which are photodegradable, e.g. positive electron resists
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/039—Macromolecular compounds which are photodegradable, e.g. positive electron resists
- G03F7/0392—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition
- G03F7/0397—Macromolecular compounds which are photodegradable, e.g. positive electron resists the macromolecular compound being present in a chemically amplified positive photoresist composition the macromolecular compound having an alicyclic moiety in a side chain
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/004—Photosensitive materials
- G03F7/09—Photosensitive materials characterised by structural details, e.g. supports, auxiliary layers
- G03F7/091—Photosensitive materials characterised by structural details, e.g. supports, auxiliary layers characterised by antireflection means or light filtering or absorbing means, e.g. anti-halation, contrast enhancement
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/20—Exposure; Apparatus therefor
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/26—Processing photosensitive materials; Apparatus therefor
-
- G—PHYSICS
- G03—PHOTOGRAPHY; CINEMATOGRAPHY; ANALOGOUS TECHNIQUES USING WAVES OTHER THAN OPTICAL WAVES; ELECTROGRAPHY; HOLOGRAPHY
- G03F—PHOTOMECHANICAL PRODUCTION OF TEXTURED OR PATTERNED SURFACES, e.g. FOR PRINTING, FOR PROCESSING OF SEMICONDUCTOR DEVICES; MATERIALS THEREFOR; ORIGINALS THEREFOR; APPARATUS SPECIALLY ADAPTED THEREFOR
- G03F7/00—Photomechanical, e.g. photolithographic, production of textured or patterned surfaces, e.g. printing surfaces; Materials therefor, e.g. comprising photoresists; Apparatus specially adapted therefor
- G03F7/70—Microphotolithographic exposure; Apparatus therefor
- G03F7/70008—Production of exposure light, i.e. light sources
- G03F7/70025—Production of exposure light, i.e. light sources by lasers
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01L—SEMICONDUCTOR DEVICES NOT COVERED BY CLASS H10
- H01L21/00—Processes or apparatus adapted for the manufacture or treatment of semiconductor or solid state devices or of parts thereof
- H01L21/02—Manufacture or treatment of semiconductor devices or of parts thereof
- H01L21/027—Making masks on semiconductor bodies for further photolithographic processing not provided for in group H01L21/18 or H01L21/34
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Engineering & Computer Science (AREA)
- Architecture (AREA)
- Plasma & Fusion (AREA)
- Optics & Photonics (AREA)
- Structural Engineering (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- Manufacturing & Machinery (AREA)
- Computer Hardware Design (AREA)
- Microelectronics & Electronic Packaging (AREA)
- Power Engineering (AREA)
- Materials For Photolithography (AREA)
- Exposure And Positioning Against Photoresist Photosensitive Materials (AREA)
- Nitrogen- Or Sulfur-Containing Heterocyclic Ring Compounds With Rings Of Six Or More Members (AREA)
Abstract
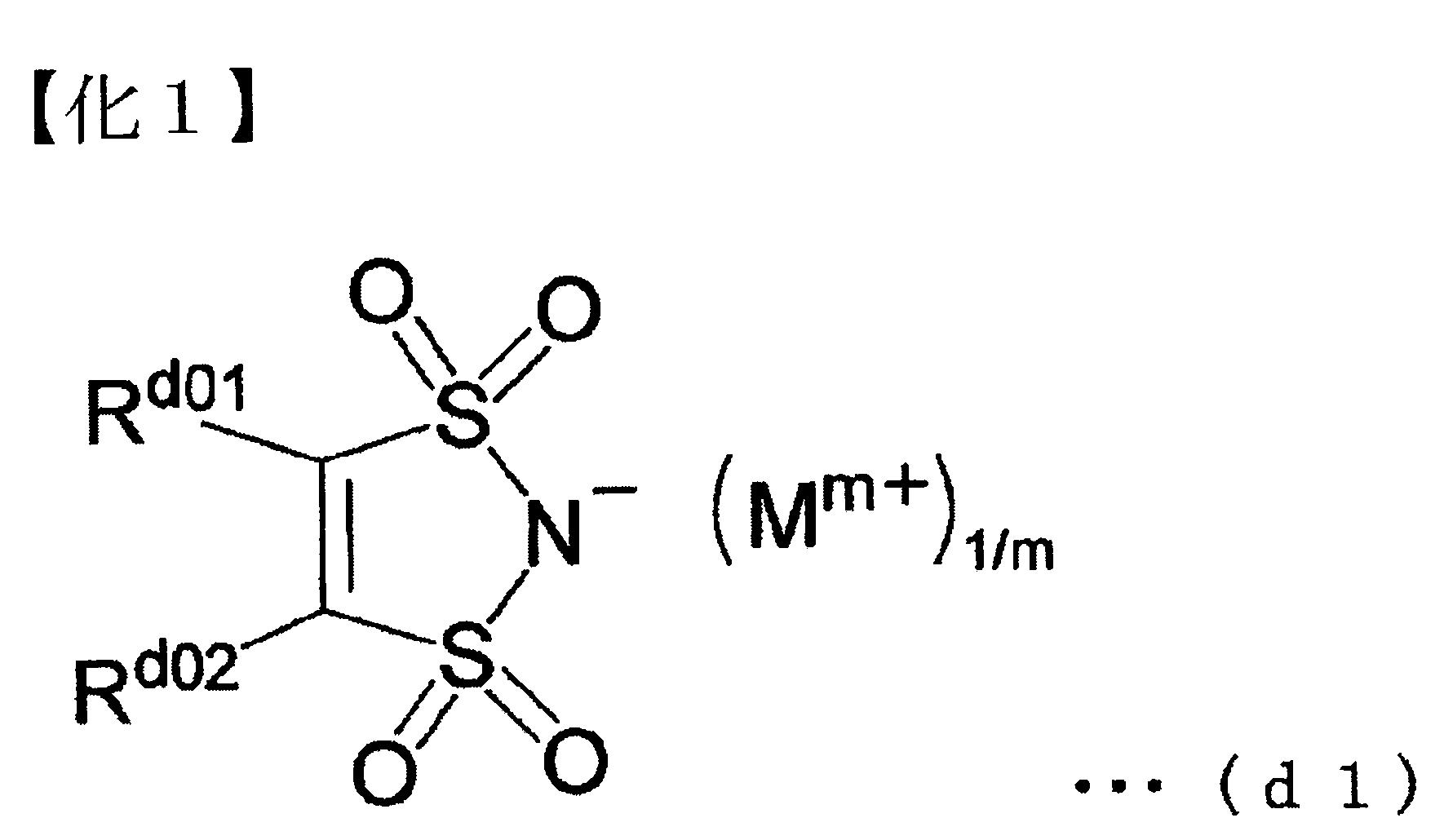
一種阻劑組成物,其為經由曝光而產生酸,且,經由酸的作用而對顯影液之溶解性產生變化的阻劑組成物,其特徵為含有: 經由酸的作用而對顯影液之溶解性產生變化的基材成份(A),與通式(d1)所表示之化合物(D1)。 通式(d1)中,Rd01
及Rd02
各自獨立為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基;或,Rd01
與Rd02
可相互鍵結,形成縮合環;m為1以上之整數,又,Mm +
表示m價之有機陽離子。
Description
本發明為有關阻劑組成物及阻劑圖型形成方法,與化合物及酸擴散控制劑。 本案為以2017年3月31日於日本申請之特願2017-073070號為基礎主張優先權,該內容係援用於本案。
微影蝕刻技術中,多使用例如於基板上形成由阻劑材料所形成之阻劑膜,對該阻劑膜進行選擇性曝光,以實施顯影處理之方式,而於前述阻劑膜形成特定形狀的阻劑圖型等步驟進行。阻劑膜的曝光部改變為可溶解於顯影液之特性的阻劑材料稱為正型、阻劑膜的曝光部改變為不溶解於顯影液之特性的阻劑材料稱為負型。 近年來,於半導體元件或液晶顯示元件之製造中,因微影蝕刻技術之進步而急速地使圖型進入微細化。微細化之方法,一般為將曝光光源施以短波長化(高能量化)之方式進行。具體而言,以往為使用以g線、i線為代表的紫外線,但現在則開始使用KrF準分子雷射,或ArF準分子雷射進行半導體元件之量產。又,對於較該些準分子雷射更短波長(高能量)的EUV(極紫外線),或EB(電子線)、X線等,亦已開始進行研究。
阻劑材料中,則尋求對於該些曝光光源之感度、可重現微細尺寸圖型的解析度等的微影蝕刻特性。 可滿足該些需求的阻劑材料,以往為使用含有經由酸的作用而對顯影液之溶解性產生變化的基材成份,與經由曝光而產生酸的酸產生劑成份的化學增強型阻劑組成物。 例如上述顯影液為鹼顯影液(鹼顯影製程)時,正型化學增強型阻劑組成物,一般為使用含有經由酸之作用而增大對鹼顯影液之溶解性的樹脂成份(基底樹脂),與酸產生劑成份者。使用該阻劑組成物所形成的阻劑膜,於阻劑圖型形成過程中,進行選擇性曝光時,於曝光部中,會由酸產生劑成份產生酸,經由該酸之作用而增大基底樹脂之極性,使阻劑膜的曝光部相對於鹼顯影液為可溶。因此,經由鹼顯影處理,可使阻劑膜的未曝光部以圖型方式殘留,而形成正型圖型。 另一方面,該些化學增強型阻劑組成物於使用於含有有機溶劑的顯影液(有機系顯影液)之溶劑顯影製程時,因基底樹脂極性之增大,相對地會降低對有機系顯影液之溶解性,故阻劑膜的未曝光部經有機系顯影液而被溶解、去除,使阻劑膜的曝光部以圖型方式殘留,而形成負型阻劑圖型。依此方式形成負型阻劑圖型的溶劑顯影製程亦稱為負型顯影製程(例如專利文獻1內容說明)。
化學增強型阻劑組成物中,所使用的基底樹脂,一般而言,就提高微影蝕刻特性等的目的,多具有複數的結構單位。 例如,為經由酸之作用而增大對鹼顯影液之溶解性的樹脂成份時,為併用經由酸產生劑等所發生的酸之作用而分解,而增大極性的含有酸分解性基的結構單位,其他亦有併用含有含內酯之環式基的結構單位、含有羥基等的極性基的結構單位等。
又,於阻劑圖型的形成中,經由曝光而由酸產生劑成份產生之酸的機制,為對微影蝕刻特性產生極大影響的要素之一。 對於此點,已有與酸產生劑成份同時,合併使用可控制經由曝光而由該酸產生劑成份產生的酸之擴散的酸擴散控制劑之化學增強型阻劑組成物的提案。 例如專利文獻2中,揭示一種含有:經由酸的作用而對顯影液之溶解性產生變化的樹脂成份,與酸產生劑成份,與作為酸擴散控制劑的具有特定構造的陽離子部之光反應性抑制劑的阻劑組成物。該光反應性抑制劑作為,可與由酸產生劑成份所產生的酸發生離子交換反應而發揮出抑制效果之成份,經由添加該光反應性抑制劑時,可控制由酸產生劑成份產生酸之阻劑膜的曝光部向未曝光部擴散,而可提高微影蝕刻特性。 [先前技術文獻] [專利文獻]
[專利文獻1] 特開2009-025723號公報 [專利文獻2] 特開2014-115386號公報
[發明所欲解決之問題]
近來,伴隨微影蝕刻技術的更進步、應用領域的擴大等,而急速地進行圖型微細化。又伴隨此點,於製造半導體元件等之際,則尋求一種可以良好形狀形成圖型寬度尺寸低於100nm的微細圖型之技術。 但,於基板上形成使用以往之阻劑組成物的前述微細圖型(例如微細的線路與空間圖型)時,多會發生圖型倒塌等的解析度之問題。此外,即使改善該解析度後之成品,例如圖型中之空間寬度的均勻性(低粗糙度)之部份,仍未能達到充份的要求。
本發明,即是鑑於上述情事而提出者,而以提供一種可以提高解析度,且更低圖型粗糙度的良好形狀,形成更微細圖型的阻劑組成物為目的。 [解決問題之方法]
解決上述問題的本發明之第1態樣為,一種阻劑組成物,其為含有經由曝光而產生酸,且,經由酸的作用而對顯影液之溶解性產生變化的阻劑組成物,其特徵為含有:經由酸的作用而對顯影液之溶解性產生變化的基材成份(A),與下述通式(d1)所表示之化合物(D1)。
[式中,Rd01
及Rd02
各自獨立為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基;或,Rd01
與Rd02
可相互鍵結,形成縮合環;m為1以上之整數,又,Mm+
表示m價之有機陽離子]。
本發明之第2態樣為,一種阻劑圖型形成方法,其特徵為具有:於支撐體上,使用前述第1態樣之阻劑組成物形成阻劑膜之步驟、使前述阻劑膜曝光之步驟,及使前述曝光後的阻劑膜進行顯影,形成阻劑圖型之步驟。
本發明之第3態樣為,一種化合物,其特徵為,由下述通式(d1)所表示者。
[式中,Rd01
及Rd02
各自獨立為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基;或,Rd01
與Rd02
可相互鍵結,形成縮合環;m為1以上之整數,又,Mm+
表示m價之有機陽離子]。
本發明之第4態樣為,一種酸擴散控制劑,其特徵為,由前述第3態樣的化合物所形成者。 [發明之效果]
使用本發明之阻劑組成物時,可以更高解析度,且圖型的粗糙度更低的良好形狀,形成更微細的圖型。 此外,本發明之阻劑組成物時,亦具有良好的焦點景深寬度(DOF)特性、製程寬容度更大,且所形成之阻劑圖型具有優良的微影蝕刻特性之良好形狀。
又,本發明可提供一種使用前述阻劑組成物的阻劑圖型形成方法,及適合使用於該阻劑組成物的化合物及酸擴散控制劑。 [實施發明之形態]
本說明書及本專利申請專利範圍中,「脂肪族」對芳香族為相對性之概念,定義為不具有芳香族性之基、化合物等之意。 「烷基」,於無特別限定下,為包含直鏈狀、支鏈狀及環狀的1價飽合烴基者。烷氧基中之烷基亦為相同意義。 「伸烷基」,於無特別限定下,為包含直鏈狀、支鏈狀及環狀的2價飽合烴基者。 「鹵化烷基」為,烷基的氫原子中之一部份或全部被鹵素原子所取代之基,該鹵素原子可列舉如,氟原子、氯原子、溴原子、碘原子。 「氟化烷基」或「氟化伸烷基」係指,烷基或伸烷基的氫原子中之一部份或全部被氟原子所取代之基之意。 「結構單位」係指,構成高分子化合物(樹脂、聚合物、共聚物)的單體單位(monomer unit)之意。 記載為「可具有取代基」時,為包含氫原子(-H)被1價之基所取代之際,與伸甲基(-CH2
-)被2價之基所取代之時等二者之情況。 「曝光」為包含所有輻射線照射的概念。
「丙烯酸酯所衍生的結構單位」係指,丙烯酸酯的乙烯性雙鍵經開裂所構成的結構單位之意。 「丙烯酸酯」係指,丙烯酸(CH2
=CH-COOH)的羧基末端之氫原子被有機基所取代之化合物。 丙烯酸酯中,α位的碳原子所鍵結之氫原子可被取代基所取代。取代該α位的碳原子所鍵結之氫原子的取代基(Rα0
)為,氫原子以外的原子或基,例如碳數1~5之烷基、碳數1~5之鹵化烷基等。又,取代基(Rα0
)亦包含:被包含酯鍵結的取代基所取代的依康酸二酯,或取代基(Rα0
)被羥烷基或其羥基經修飾後之基所取代的α羥基丙烯酸酯。又,丙烯酸酯的α位之碳原子,於無特別限定下,係指丙烯酸的羰基所鍵結的碳原子之意。 以下,α位的碳原子所鍵結之氫原子被取代基所取代的丙烯酸酯亦稱為α取代丙烯酸酯。又,包括丙烯酸酯與α取代丙烯酸酯亦統稱為「(α取代)丙烯酸酯」。
「丙烯醯胺所衍生的結構單位」係指,丙烯醯胺的乙烯性雙鍵經開裂而構成的結構單位之意。 丙烯醯胺中,α位的碳原子所鍵結之氫原子可被取代基所取代,或丙烯醯胺的胺基中之氫原子的一者或二者可被取代基所取代皆可。又,丙烯醯胺之α位的碳原子,於無特別限定下,係指丙烯醯胺的羰基所鍵結的碳原子之意。 取代丙烯醯胺之α位的碳原子所鍵結之氫原子的取代基,可列舉如,與前述α取代丙烯酸酯中,α位的取代基所列舉者(取代基(Rα0
))為相同之內容等。
「羥苯乙烯或羥苯乙烯衍生物所衍生的結構單位」係指,羥苯乙烯或羥苯乙烯衍生物的乙烯性雙鍵經開裂而構成的結構單位之意。 「羥苯乙烯衍生物」係指,羥苯乙烯之α位的氫原子被烷基、鹵化烷基等其他取代基所取代者,及包含該些衍生物之概念。該些衍生物,可列舉如,α位的氫原子可被取代基所取代的羥苯乙烯的羥基中之氫原子被有機基所取代者;α位的氫原子可被取代基所取代的羥苯乙烯之苯環上,鍵結羥基以外的取代基者等。又,α位(α位的碳原子),於無特別限定下,係指苯環所鍵結的碳原子之意。 取代羥苯乙烯之α位的氫原子之取代基,可列舉如,與前述α取代丙烯酸酯中,α位的取代基所列舉者為相同之內容等。
「乙烯基安息香酸或乙烯基安息香酸衍生物所衍生的結構單位」係指,乙烯基安息香酸或乙烯基安息香酸衍生物的乙烯性雙鍵經開裂而構成的結構單位之意。 「乙烯基安息香酸衍生物」係指,乙烯基安息香酸之α位的氫原子被烷基、鹵化烷基等其他取代基所取代者,及包含該些衍生物之概念。該些衍生物,可列舉如,α位的氫原子可被取代基所取代的乙烯基安息香酸的羧基中之氫原子被有機基所取代者;α位的氫原子可被取代基所取代的乙烯基安息香酸的苯環上,鍵結羥基及羧基以外的取代基者等。又,α位(α位的碳原子),於無特別限定下,係指苯環所鍵結的碳原子之意。
「苯乙烯」係指,包含苯乙烯及苯乙烯之α位的氫原子被烷基、鹵化烷基等其他取代基所取代者之概念。 「苯乙烯衍生物」係指,苯乙烯之α位的氫原子被烷基、鹵化烷基等其他取代基所取代者,及包含該些衍生物之概念。該些衍生物,可列舉如,α位的氫原子可被取代基所取代的羥苯乙烯的苯環上鍵結取代基者等。又,α位(α位的碳原子),於無特別限定下,係指苯環所鍵結的碳原子之意。 「苯乙烯所衍生的結構單位」、「苯乙烯衍生物所衍生的結構單位」係指,苯乙烯或苯乙烯衍生物的乙烯性雙鍵經開裂而構成的結構單位之意。
上述α位的取代基之烷基,以直鏈狀或支鏈狀烷基為佳,具體而言,可列舉如,碳數1~5之烷基(甲基、乙基、丙基、異丙基、n-丁基、異丁基、tert-丁基、戊基、異戊基、新戊基)等。 又,α位的取代基之鹵化烷基,具體而言,可列舉如,上述「α位的取代基之烷基」的氫原子中之一部份或全部被鹵素原子所取代之基等。該鹵素原子,可列舉如,氟原子、氯原子、溴原子、碘原子等,特別是以氟原子為佳。 又,α位的取代基之羥烷基,具體而言,可列舉如,上述「α位的取代基之烷基」中之氫原子的一部份或全部,被羥基所取代之基等。該羥烷基中之羥基的數目,以1~5為佳,以1為最佳。
(阻劑組成物) 本發明之第1態樣的阻劑組成物,為經由曝光而產生酸,且,經由酸的作用而對顯影液之溶解性產生變化的阻劑組成物,其含有:經由酸的作用而對顯影液之溶解性產生變化的基材成份(A)(以下,亦稱為「(A)成份」),與通式(d1)所表示之化合物(D1)(以下,亦稱為「(D1)成份」)。
使用該阻劑組成物形成阻劑膜,並對該阻劑膜進行選擇性曝光時,該阻劑膜的曝光部會產生酸,經由該酸之作用而使(A)成份對顯影液之溶解性發生變化的同時,因該阻劑膜的未曝光部中之(A)成份對顯影液之溶解性並未發生變化,使曝光部與未曝光部之間產生對顯影液之溶解性的差異。因此,該阻劑膜進行顯影時,於該阻劑組成物為正型時,阻劑膜的曝光部被溶解去除而形成正型之阻劑圖型,該阻劑組成物為負型時,該阻劑膜的未曝光部將被溶解去除而形成負型的阻劑圖型。 本說明書中,阻劑膜的曝光部被溶解去除而形成正型阻劑圖型的阻劑組成物稱為正型阻劑組成物,阻劑膜的未曝光部被溶解去除而形成負型阻劑圖型的阻劑組成物稱為負型阻劑組成物。 本態樣的阻劑組成物,可為正型阻劑組成物亦可、負型阻劑組成物亦可。 又,本態樣的阻劑組成物,可使用於形成阻劑圖型時的顯影處理為使用鹼顯影液之鹼顯影製程用亦可、使用於該顯影處理為使用包含有機溶劑的顯影液(有機系顯影液)之溶劑顯影製程用亦可。
本態樣的阻劑組成物,為具有經由曝光而產生酸的酸發生能力者,其中,(A)成份可經由曝光而產生酸亦可、添加與(A)成份相異的其他添加劑成份經由曝光而產生酸者亦可。 本態樣的阻劑組成物,具體而言為:(1)可為含有經由曝光而產生酸的酸產生劑成份(B)(以下,亦稱為「(B)成份」)者、(2)(A)成份為經由曝光而產生酸的成份亦可、(3)(A)成份為經由曝光而產生酸的成份,且,尚含有(B)成份者亦可。 即,為上述(2)及(3)之時,(A)成份為「經由曝光而產生酸,且,經由酸的作用而對顯影液之溶解性產生變化的基材成份」。(A)成份為經由曝光而產生酸,且,經由酸的作用而對顯影液之溶解性產生變化的基材成份時,後述之(A1)成份,以經由曝光而產生酸,且,經由酸的作用而對顯影液之溶解性產生變化的高分子化合物為佳。該些高分子化合物,可列舉如,可使用具有經由曝光而產生酸的結構單位之樹脂。經由曝光而產生酸的結構單位,可使用公知之成份。
該阻劑組成物,於上述之中,又以為上述(1)時者,即,含有(A)成份與(D1)成份,再含有(B)成份(又,前述(D1)成份除外)的實施形態為特佳。
<(A)成份> (A)成份為,經由酸的作用而對顯影液之溶解性產生變化的基材成份。 本發明中之「基材成份」,係指具有膜形成能力的有機化合物,較佳為使用分子量為500以上的有機化合物。該有機化合物的分子量為500以上時,可提高膜形成能力,此外,也容易形成奈米程度的阻劑圖型。 作為基材成份使用的有機化合物,可大致區分為非聚合物與聚合物。 非聚合物,通常為使用分子量為500以上、未達4000者。以下,稱為「低分子化合物」時,係指分子量為500以上、未達4000的非聚合物。 聚合物,通常為使用分子量為1000以上者。以下,稱為「樹脂」或「高分子化合物」時,係指分子量為1000以上的聚合物。 聚合物之分子量,為使用GPC(凝膠滲透色層分析)之聚苯乙烯換算的質量平均分子量。
本實施形態之阻劑組成物,於鹼顯影製程中,為形成負型阻劑圖型之「鹼顯影製程用負型阻劑組成物」時,或,溶劑顯影製程中,為形成正型阻劑圖型之「溶劑顯影製程用正型阻劑組成物」時,(A)成份較佳為使用對鹼顯影液為可溶性的基材成份(A-2)(以下,亦稱為「(A-2)成份」),再添加交聯劑成份。該阻劑組成物,例如,經由曝光而由(B)成份產生酸時,經由該酸之作用而使該(A-2)成份與交聯劑成份之間引起交聯,其結果,將會降低對鹼顯影液之溶解性(增大對有機系顯影之溶解性)。 因此,於阻劑圖型之形成中,對於將該阻劑組成物塗佈於支撐體上所得的阻劑膜進行選擇性曝光時,可使阻劑膜的曝光部轉變為對鹼顯影液為難溶性(對有機系顯影為可溶性)的同時,因阻劑膜的未曝光部對鹼顯影液仍為可溶性(對有機系顯影液為難溶性)而未有變化之狀態,故使用鹼顯影液進行顯影時,即可形成負型阻劑圖型。又,此時使用有機系顯影液進行顯影時,即可形成正型之阻劑圖型。 (A-2)成份中,較佳者為使用對鹼顯影液為可溶性之樹脂(以下,亦稱為「鹼可溶性樹脂」)。 鹼可溶性樹脂,例如特開2000-206694號公報所揭示之具有由α-(羥烷基)丙烯酸,或α-(羥烷基)丙烯酸之烷酯(較佳為碳數1~5之烷酯)所選出之至少一個所衍生的結構單位的樹脂;美國專利6949325號公報所揭示之具有碸醯胺基的α位的碳原子所鍵結的氫原子可被取代基所取代的丙烯酸樹脂或多環烯烴樹脂;美國專利6949325號公報、特開2005-336452號公報、特開2006-317803號公報所揭示之含有氟化醇,且α位的碳原子所鍵結的氫原子可被取代基所取代的丙烯酸樹脂;特開2006-259582號公報所揭示之具有氟化醇的多環烯烴樹脂等,以期可形成膨潤較少的良好阻劑圖型而為較佳。 又,前述α-(羥烷基)丙烯酸中,α位的碳原子所鍵結之氫原子可被取代基所取代丙烯酸,為表示羧基所鍵結的α位的碳原子上鍵結氫原子的丙烯酸,該α位的碳原子鍵結羥烷基(較佳為碳數1~5之羥烷基)的α-羥烷基丙烯酸之一者或二者之意。 交聯劑成份,例如,就可形成膨潤較少的良好阻劑圖型之觀點,以使用具有羥甲基或烷氧甲基的乙炔脲等之胺基系交聯劑,或三聚氰胺系交聯劑等為佳。交聯劑成份之添加量,相對於鹼可溶性樹脂100質量份,以1~50質量份為佳。
本實施形態之阻劑組成物,為於鹼顯影製程中形成正型阻劑圖型的「鹼顯影製程用正型阻劑組成物」時,或,於溶劑顯影製程中形成負型阻劑圖型的「溶劑顯影製程用負型阻劑組成物」時,(A)成份較佳為作為經由酸之作用而增大極性的基材成份(A-1)(以下,亦稱為「(A-1)成份」)使用。使用(A-1)成份時,因曝光前後的基材成份之極性會產生變化,故不僅鹼顯影製程,於溶劑顯影製程中,亦可得到良好的顯影對比。 使用於鹼顯影製程時,該(A-1)成份於曝光前對鹼顯影液為難溶性,例如,經由曝光而由(B)成份產生酸時,經由該酸之作用,而使極性增大而增大對鹼顯影液之溶解性。因此,於阻劑圖型之形成中,對於將該阻劑組成物塗佈於支撐體上而得的阻劑膜進行選擇性曝光時,於阻劑膜的曝光部對鹼顯影液由難溶性轉變為可溶性的同時,阻劑膜的未曝光部則仍為鹼難溶性而未有變化,故經由鹼顯影而可形成正型阻劑圖型。 另一方面,使用於溶劑顯影製程時,該(A-1)成份於曝光前對於有機系顯影液具有高度溶解性,經由曝光產生酸時,經由該酸之作用,使極性提高,而降低對有機系顯影液之溶解性。因此,於阻劑圖型之形成中,對於將該阻劑組成物塗佈於支撐體上而得之阻劑膜進行選擇性曝光時,阻劑膜的曝光部由對有機系顯影為可溶性轉變為難溶性的同時,阻劑膜的未曝光部仍為可溶性而未有變化,故經由有機系顯影液進行顯影時,於曝光部與未曝光部之間會產生明顯對比,而形成負型阻劑圖型。
本實施形態之阻劑組成物中,(A)成份以前述(A-1)成份為佳。即,本實施形態之阻劑組成物以於鹼顯影製程中形成正型阻劑圖型之「鹼顯影製程用正型阻劑組成物」,或,溶劑顯影製程中形成負型阻劑圖型之「溶劑顯影製程用負型阻劑組成物」為佳。 (A)成份中,為使用高分子化合物及/或低分子化合物。
(A)成份為(A-1)成份時,(A-1)成份以含有高分子化合物者為佳,以含有具有含經由酸之作用而增大極性的酸分解性基的結構單位(a1)的高分子化合物(A1)(以下,亦稱為「(A1)成份」)者為較佳。 (A1)成份,除結構單位(a1)以外,又以使用具有含內酯之環式基、含-SO2
-之環式基或含碳酸酯之環式基的結構單位(a2)之高分子化合物為佳。 又,(A1)成份,除結構單位(a1)以外,或結構單位(a1)及結構單位(a2)以外,再使用具有含有含極性基之脂肪族烴基的結構單位(a3)(又,相當於結構單位(a1)或結構單位(a2)者除外)之高分子化合物亦佳。 又,(A1)成份,除結構單位(a1)~(a3)以外,可再具有含非酸解離性之脂肪族環式基的結構單位(a4)、經由曝光而產生酸的結構單位等。
≪結構單位(a1)≫ 結構單位(a1),為含有經由酸之作用而增大極性的酸分解性基的結構單位。 「酸分解性基」係指,可經由酸之作用,使該酸分解性基的構造中之至少一部份鍵結產生開裂之具有酸分解性之基。 經由酸之作用而增大極性的酸分解性基,例如,經由酸之作用而分解生成極性基之基等。 極性基,例如羧基、羥基、胺基、磺酸基(-SO3
H)等。該些之中,又以構造中含有-OH的極性基(以下,亦稱為「含有OH之極性基」)為佳,以羧基或羥基為較佳,以羧基為特佳。 酸分解性基,更具體而言,例如,前述極性基被酸解離性基所保護之基(例如含有OH之極性基的氫原子被酸解離性基所保護之基)等。 此處,「酸解離性基」係指:(i)經由酸之作用,使該酸解離性基與該酸解離性基鄰接的原子之間的鍵結產生開裂之具有酸解離性之基,或,(ii)經由酸之作用而使一部份鍵結產生開裂之後,再生成去碳酸反應,使該酸解離性基與該酸解離性基鄰接的原子之間的鍵結產生開裂之基,等二者。 構成酸分解性基之酸解離性基,必須為極性較經該酸解離性基解離而生成的極性基為更低之基,如此,經由酸之作用使該酸解離性基解離之際,可生成較該酸解離性基具有更高極性的極性基,而增大極性。其結果,而增大(A1)成份全體之極性。經由極性之增大,相對的會使對顯影液之溶解性產生變化,於顯影液為鹼顯影液時會增大溶解性,顯影液為有機系顯影液時會降低溶解性。
酸解離性基,例如,目前為止被提案作為化學增強型阻劑組成物用的基底樹脂之酸解離性基者。 被提案作為化學增強型阻劑組成物用的基底樹脂之酸解離性基者,具體而言,例如,以下說明之「縮醛型酸解離性基」、「三級烷酯型酸解離性基」、「三級烷氧羰酸解離性基」等。
・縮醛型酸解離性基: 前述極性基中,保護羧基或羥基的酸解離性基,例如,下述通式(a1-r-1)所表示之酸解離性基(以下,亦稱為「縮醛型酸解離性基」)等。
式(a1-r-1)中,Ra’1
及Ra’2
之中,以至少一者為氫原子為佳,以二者皆為氫原子為較佳。 Ra’1
或Ra’2
為烷基時,該烷基,例如,與上述α取代丙烯酸酯的說明中,可與α位的碳原子鍵結的取代基中所列舉的烷基為相同之內容,又以碳數1~5之烷基為佳。具體而言,以直鏈狀或支鏈狀烷基為較佳之例示。更具體而言,例如,甲基、乙基、丙基、異丙基、n-丁基、異丁基、tert-丁基、戊基、異戊基、新戊基等,又以甲基或乙基為較佳,以甲基為特佳。
式(a1-r-1)中,Ra’3
之烴基,例如,直鏈狀或支鏈狀烷基、環狀之烴基等。 該直鏈狀烷基,以碳數1~5為佳,以1~4為較佳,以1或2為更佳。具體而言,例如,甲基、乙基、n-丙基、n-丁基、n-戊基等。該些之中,又以甲基、乙基或n-丁基為佳,以甲基或乙基為較佳。
該支鏈狀烷基,以碳數3~10為佳,3~5為較佳。具體而言,例如,異丙基、異丁基、tert-丁基、異戊基、新戊基、1,1-二乙基丙基、2,2-二甲基丁基等,又以異丙基為佳。
Ra’3
為環狀之烴基時,該烴基可為脂肪族烴基亦可、芳香族烴基亦可,又,亦可為多環式基或單環式基。 單環式基之脂肪族烴基,以由單環鏈烷去除1個氫原子而得之基為佳。該單環鏈烷,以碳數3~6者為佳,具體而言,例如,環戊烷、環己烷等。 多環式基之脂肪族烴基,以由多環鏈烷去除1個氫原子而得之基為佳,該多環鏈烷,以碳數7~12者為佳,具體而言,例如,金剛烷、降莰烷、異莰烷、三環癸烷、四環十二烷等。
Ra’3
之環狀之烴基為芳香族烴基時,該芳香族烴基,為至少具有1個芳香環之烴基。 該芳香環,只要為具有4n+2個的π電子之環狀共軛系時,並未有特別之限定,其可為單環式亦可、多環式亦可。芳香環之碳數以5~30為佳,以5~20為較佳,6~15為較佳,以6~12為特佳。 芳香環,具體而言,例如,苯、萘、蒽、菲等之芳香族烴環;構成前述芳香族烴環中的一部份碳原子被雜原子所取代之芳香族雜環等。芳香族雜環中之雜原子,例如,氧原子、硫原子、氮原子等。芳香族雜環,具體而言,例如,吡啶環、噻吩環等。 Ra’3
中之芳香族烴基,具體而言,例如,前述芳香族烴環或芳香族雜環去除1個氫原子而得之基(芳基或雜芳基);由含有2個以上之芳香環的芳香族化合物(例如聯苯、茀等)去除1個氫原子而得之基;前述芳香族烴環或芳香族雜環中之1個氫原子被伸烷基所取代之基(例如,苄基、苯乙基、1-萘甲基、2-萘甲基、1-萘乙基、2-萘乙基等的芳烷基等)等。前述芳香族烴環或芳香族雜環所鍵結的伸烷基之碳數,以1~4為佳,以1~2為較佳,以1為特佳。
Ra’3
與Ra’1
、Ra’2
之任一者鍵結形成環時,該環式基,例如,以4~7員環為佳,以4~6員環為較佳。該環式基之具體例如,四氫吡喃基、四氫呋喃基等。
・三級烷酯型酸解離性基: 上述極性基中,保護羧基的酸解離性基,例如,下述通式(a1-r-2)所表示之酸解離性基等。 又,下述式(a1-r-2)所表示之酸解離性基中,由烷基所構成者,以下於簡便上亦稱為「三級烷酯型酸解離性基」。
Ra’4
~Ra’6
之烴基,例如,與前述Ra’3
為相同之內容等。 Ra’4
以碳數1~5之烷基為佳。Ra’5
與Ra’6
互相鍵結形成環時,例如,下述通式(a1-r2-1)所表示之基等。另一方面,Ra’4
~Ra’6
未互相鍵結,而為獨立之烴基時,例如,下述通式(a1-r2-2)所表示之基等。
式(a1-r2-1)中,Ra’10
之碳數1~10之烷基,以式(a1-r-1)中之Ra’3
之直鏈狀或支鏈狀烷基所列舉的基為佳。式(a1-r2-1)中,Ra’11
與Ra’10
鍵結的碳原子共同形成之脂肪族環式基,以式(a1-r-1)中之Ra’3
的單環式基或多環式基之脂肪族烴基所列舉的基為佳。
式(a1-r2-2)中,Ra’12
及Ra’14
各自獨立以碳數1~10之烷基為佳,該烷基以式(a1-r-1)中之Ra’3
之直鏈狀或支鏈狀烷基所列舉的基為較佳,以碳數1~5之直鏈狀烷基為較佳,以甲基或乙基為特佳。 式(a1-r2-2)中,Ra’13
以式(a1-r-1)中之Ra’3
的烴基所例示之直鏈狀或支鏈狀烷基、單環式基或多環式基之脂肪族烴基為佳。該些之中,又以Ra’3
之單環式基或多環式基之脂肪族烴基所列舉的基為較佳。
前述式(a1-r2-1)所表示之基之具體例,係如以下所列舉之內容。*表示鍵結鍵(以下,於本說明書中皆為相同意義)。
前述式(a1-r2-2)所表示之基之具體例,係如以下所列舉之內容。
・三級烷氧羰酸解離性基: 保護前述極性基中之羥基的酸解離性基,例如,下述通式(a1-r-3)所表示之酸解離性基(以下,於簡便上,亦稱為「三級烷氧羰酸解離性基」)。
式(a1-r-3)中,Ra’7
~Ra’9
以各自為碳數1~5之烷基為佳,以1~3為較佳。 又,各烷基之合計碳數,以3~7為佳,以3~5為較佳,以3~4為最佳。
結構單位(a1),例如,α位的碳原子所鍵結之氫原子可被取代基所取代的丙烯酸酯所衍生的結構單位、丙烯醯胺所衍生的結構單位、羥苯乙烯或羥苯乙烯衍生物所衍生的結構單位的羥基中之氫原子的至少一部份被酸解離性基所保護的結構單位、乙烯基安息香酸或乙烯基安息香酸衍生物所衍生的結構單位之-C(=O)-OH中之氫原子的至少一部份被酸解離性基所保護的結構單位等。
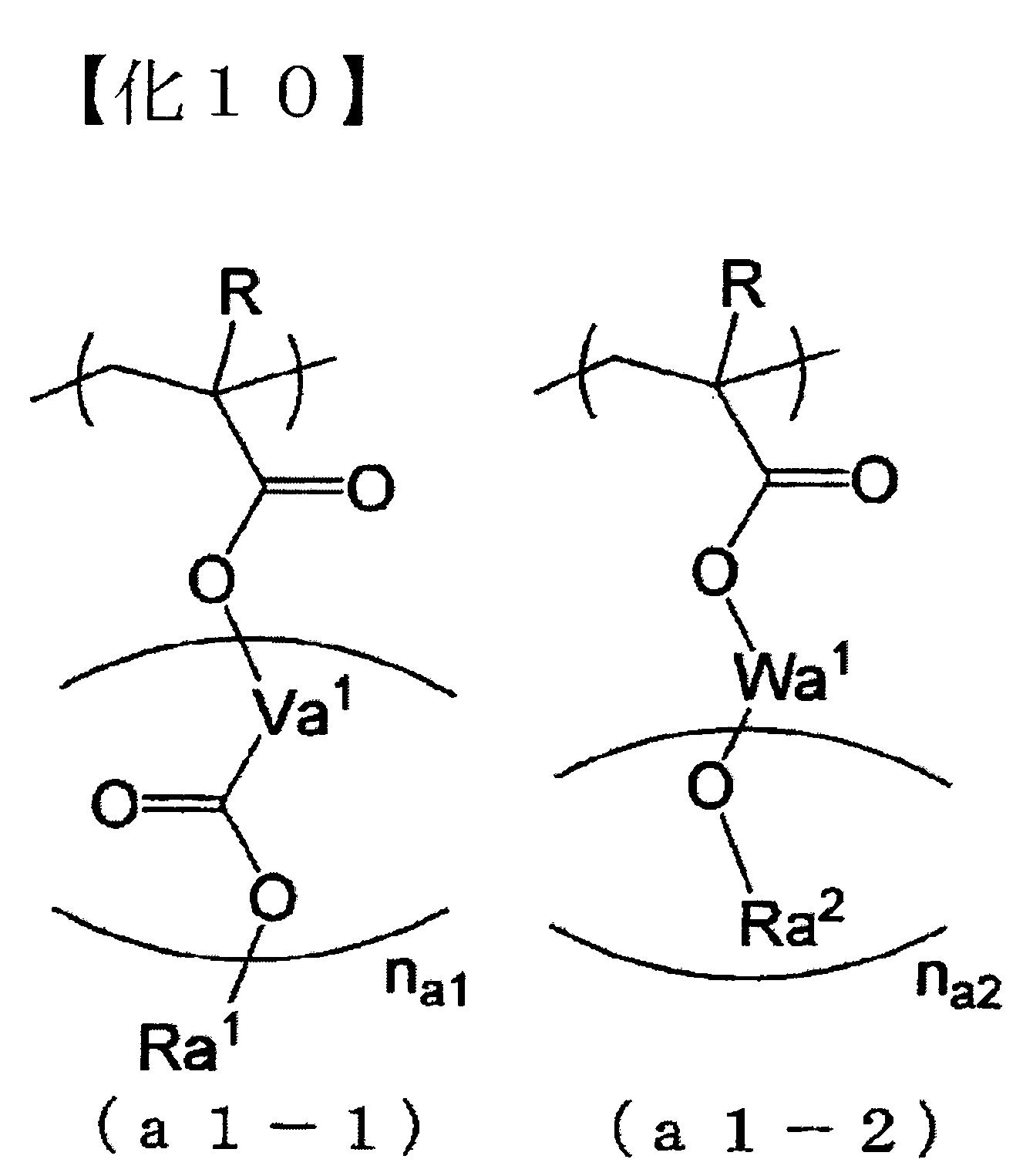
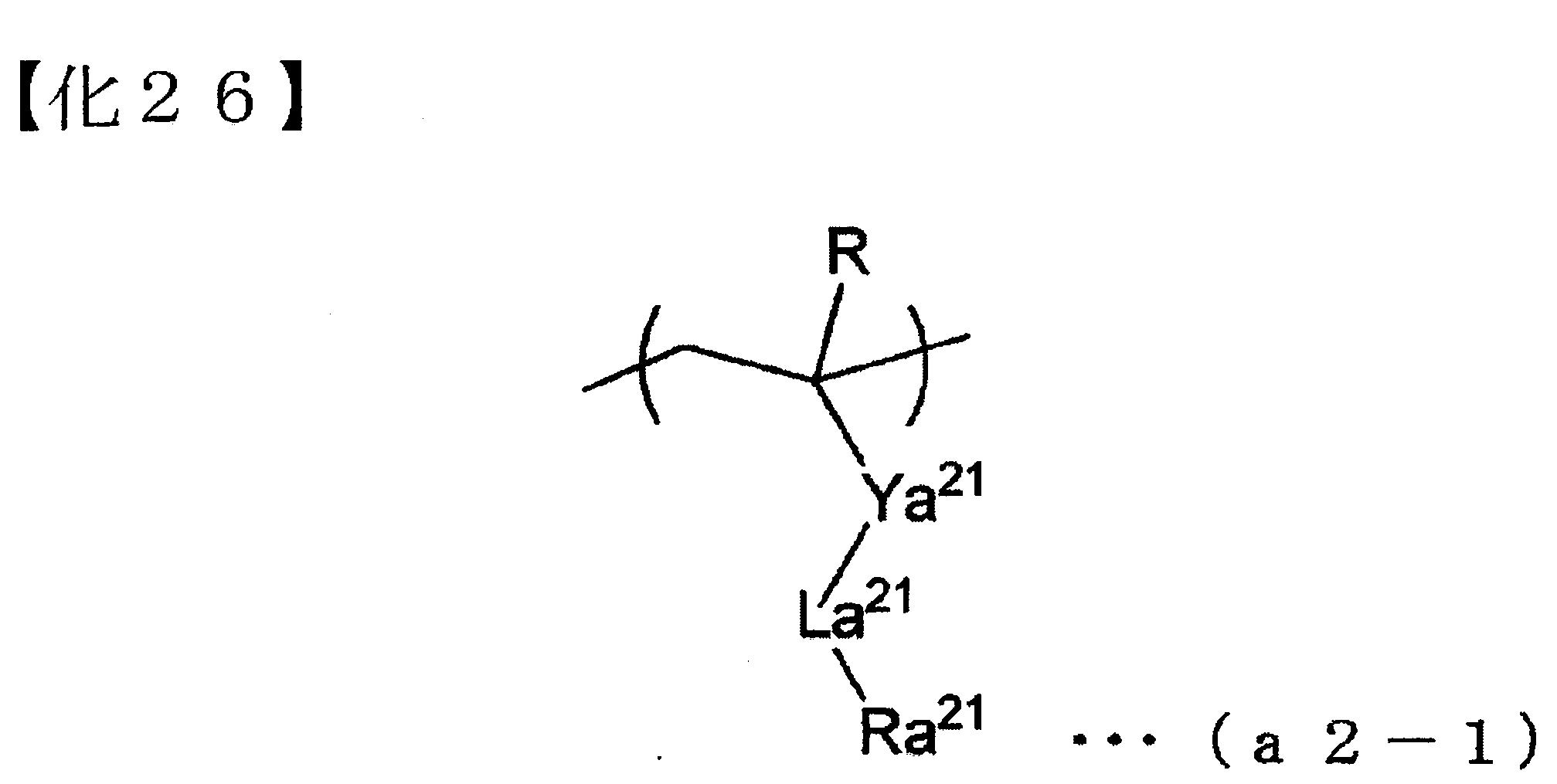
結構單位(a1),於上述之中,又以α位的碳原子所鍵結的氫原子可被取代基所取代的丙烯酸酯所衍生的結構單位為佳。 該結構單位(a1)的較佳具體例,例如,下述通式(a1-1)或(a1-2)所表示的結構單位等。
[式中,R為氫原子、碳數1~5之烷基或碳數1~5之鹵化烷基;Va1
為可具有醚鍵結之2價烴基,na1
為0~2,Ra1
為上述式(a1-r-1)或(a1-r-2)所表示之酸解離性基;Wa1
為na2
+1價之烴基,na2
為1~3,Ra2
為上述式(a1-r-1)或(a1-r-3)所表示之酸解離性基]。
前述式(a1-1)中,R之碳數1~5之烷基,以碳數1~5之直鏈狀或支鏈狀烷基為佳,具體而言,例如,甲基、乙基、丙基、異丙基、n-丁基、異丁基、tert-丁基、戊基、異戊基、新戊基等。碳數1~5之鹵化烷基,為前述碳數1~5之烷基中的氫原子之一部份或全部被鹵素原子所取代之基。該鹵素原子,可列舉如,氟原子、氯原子、溴原子、碘原子等,特別是以氟原子為佳。 R,以氫原子、碳數1~5之烷基或碳數1~5之氟化烷基為佳,就工業上取得之容易度,以氫原子或甲基為最佳。
前述式(a1-1)中,Va1
中之2價烴基,可為脂肪族烴基亦可、芳香族烴基亦可。
Va1
中作為2價之烴基的脂肪族烴基,可為飽合者亦可、不飽合者亦可,通常以飽合者為佳。 該脂肪族烴基,更具體而言,例如,直鏈狀或支鏈狀之脂肪族烴基,或,構造中含有環之脂肪族烴基等。
前述直鏈狀或支鏈狀之脂肪族烴基,以碳數1~10為佳,以1~6為較佳,以1~4為較佳,以1~3為最佳。 直鏈狀之脂肪族烴基,以直鏈狀之伸烷基為佳,具體而言,例如,伸甲基[-CH2
-]、伸乙基[-(CH2
)2
-]、伸三甲基[-(CH2
)3
-]、伸四甲基[-(CH2
)4
-]、伸五甲基[-(CH2
)5
-]等。 支鏈狀之脂肪族烴基,以支鏈狀之伸烷基為佳,具體而言,例如,-CH(CH3
)-、-CH(CH2
CH3
)-、-C(CH3
)2
-、 -C(CH3
)(CH2
CH3
)-、-C(CH3
)(CH2
CH2
CH3
)-、-C(CH2
CH3
)2
-等之烷基伸甲基;-CH(CH3
)CH2
-、-CH(CH3
)CH(CH3
)-、 -C(CH3
)2
CH2
-、-CH(CH2
CH3
)CH2
-、-C(CH2
CH3
)2
-CH2
-等之烷基伸乙基;-CH(CH3
)CH2
CH2
-、-CH2
CH(CH3
)CH2
-等之烷基伸三甲基;-CH(CH3
)CH2
CH2
CH2
-、 -CH2
CH(CH3
)CH2
CH2
-等之烷基伸四甲基等之烷基伸烷基等。烷基伸烷基中之烷基,以碳數1~5之直鏈狀烷基為佳。
前述構造中含有環之脂肪族烴基,例如,脂環式烴基(由脂肪族烴環去除2個氫原子而得之基)、脂環式烴基鍵結於直鏈狀或支鏈狀脂肪族烴基的末端之基、脂環式烴基介於直鏈狀或支鏈狀脂肪族烴基的中間之基等。前述直鏈狀或支鏈狀之脂肪族烴基,例如,前述直鏈狀之脂肪族烴基或前述支鏈狀之脂肪族烴基為相同之內容等。 前述脂環式烴基,以碳數3~20為佳,以3~12為較佳。 前述脂環式烴基,可為多環式亦可、單環式亦可。單環式之脂環式烴基,以由單環鏈烷去除2個氫原子而得之基為佳。該單環鏈烷以碳數3~6者為佳,具體而言,例如,環戊烷、環己烷等。多環式之脂環式烴基,以由多環鏈烷去除2個氫原子而得之基為佳,該多環鏈烷以碳數7~12者為佳,具體而言,例如,金剛烷、降莰烷、異莰烷、三環癸烷、四環十二烷等。
Va1
中作為2價之烴基的芳香族烴基,為具有芳香環之烴基。 該芳香族烴基,以碳數3~30為佳,以5~30為較佳,5~20為較佳,以6~15為特佳,以6~10為最佳。其中,該碳數為不包含取代基中之碳數者。 芳香族烴基所具有的芳香環,具體而言,例如,苯、聯苯、茀、萘、蒽、菲等之芳香族烴環;構成前述芳香族烴環中的一部份碳原子被雜原子所取代之芳香族雜環等。芳香族雜環中之雜原子,例如,氧原子、硫原子、氮原子等。 該芳香族烴基,具體而言,例如,由前述芳香族烴環去除2個氫原子而得之基(伸芳基);前述芳香族烴環去除1個氫原子而得之基(芳基)中之1個氫原子被伸烷基所取代之基(例如,由苄基、苯乙基、1-萘甲基、2-萘甲基、1-萘乙基、2-萘乙基等的芳烷基中之芳基再去除1個氫原子而得之基)等。前述伸烷基(芳烷基中之烷鏈)之碳數,以1~4為佳,以1~2為較佳,以1為特佳。
前述式(a1-2)中,Wa1
中之na2
+1價之烴基,可為脂肪族烴基亦可、芳香族烴基亦可。該脂肪族烴基為不具有芳香族性的烴基之意,其可為飽合亦可、不飽合亦可,通常以飽合為佳。前述脂肪族烴基,例如,直鏈狀或支鏈狀之脂肪族烴基、構造中含有環之脂肪族烴基,或直鏈狀或支鏈狀之脂肪族烴基與構造中含有環之脂肪族烴基組合而得之基等。 前述na2
+1價,以2~4價為佳,以2或3價為較佳。
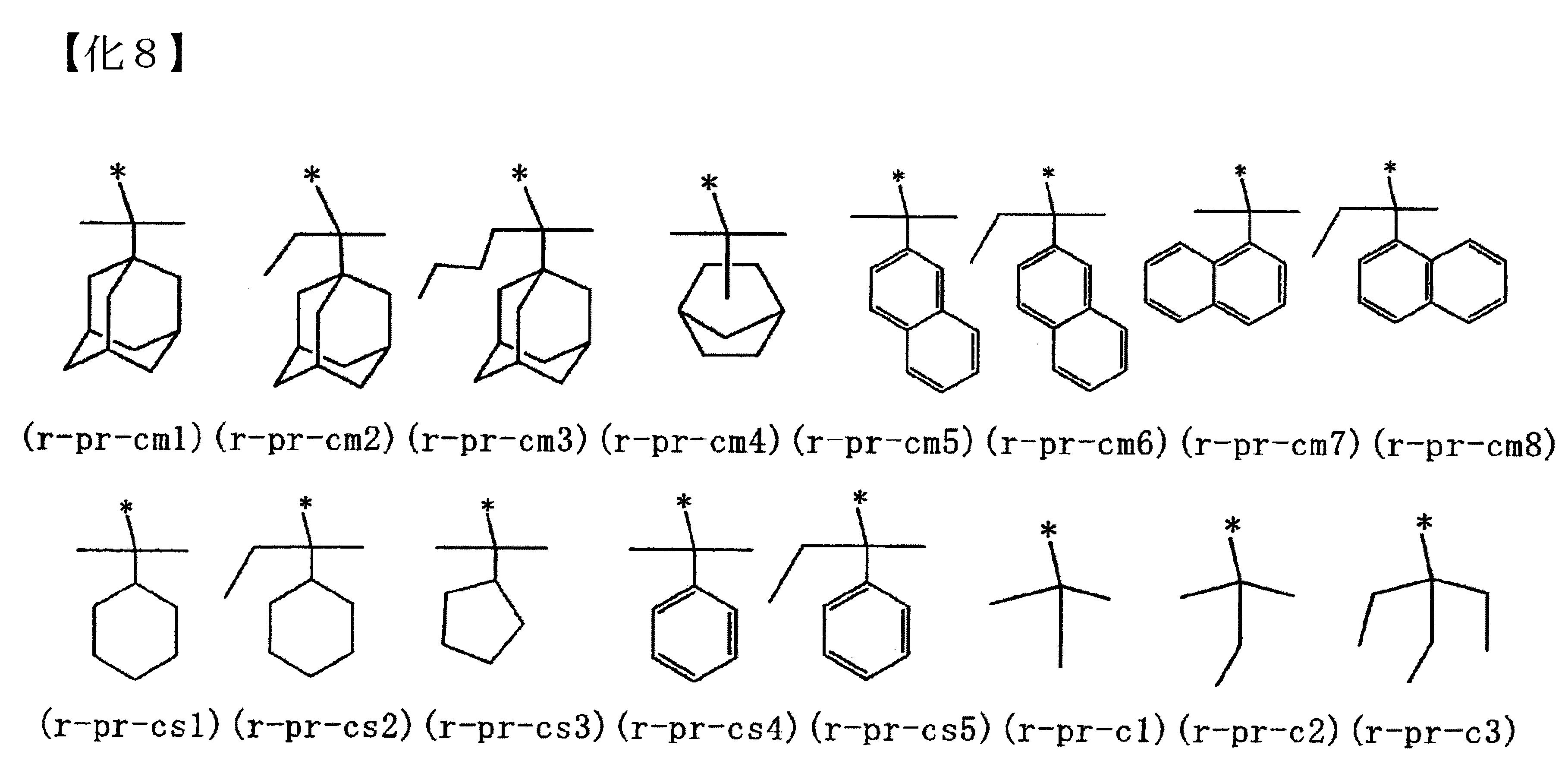
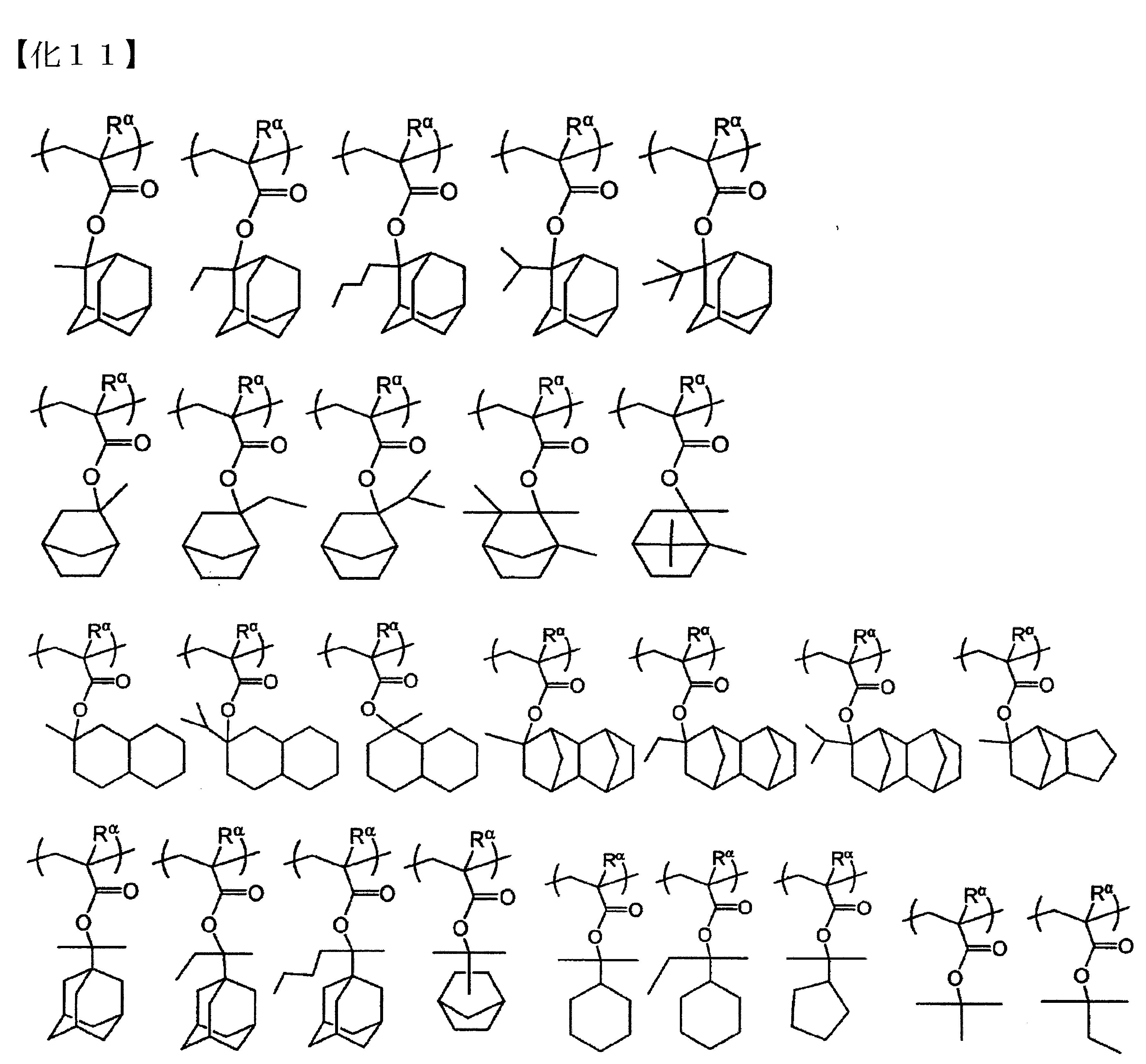
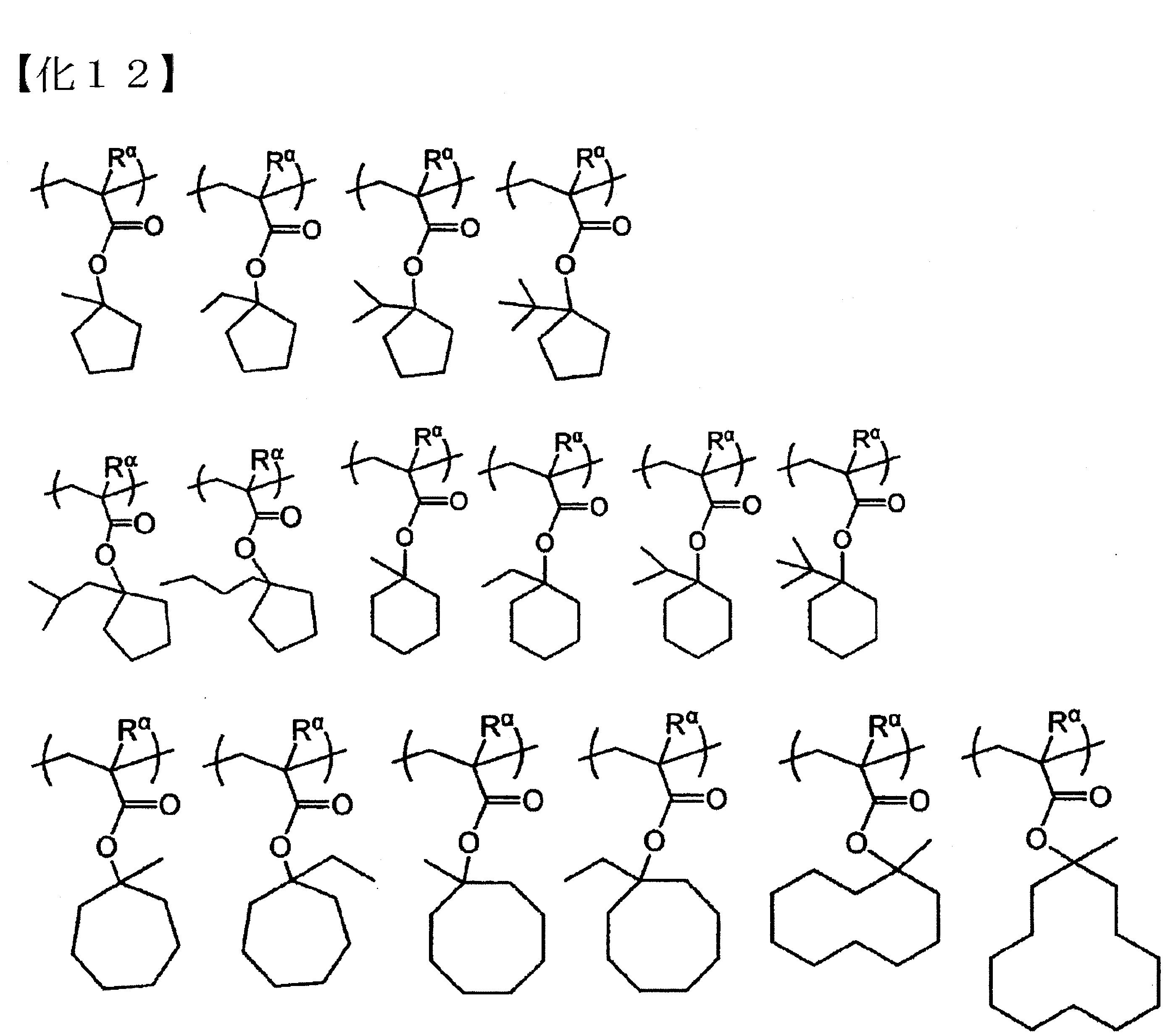
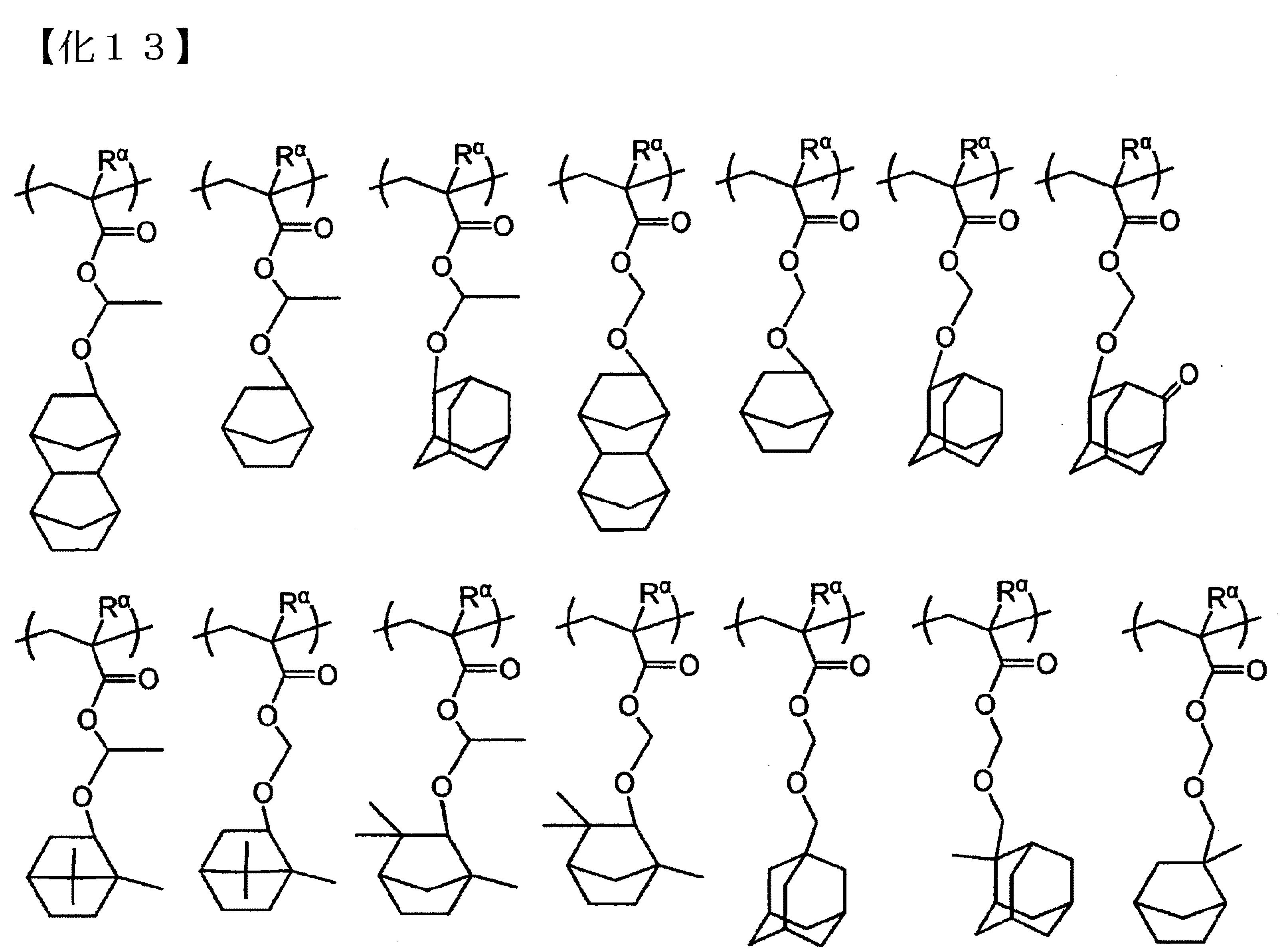
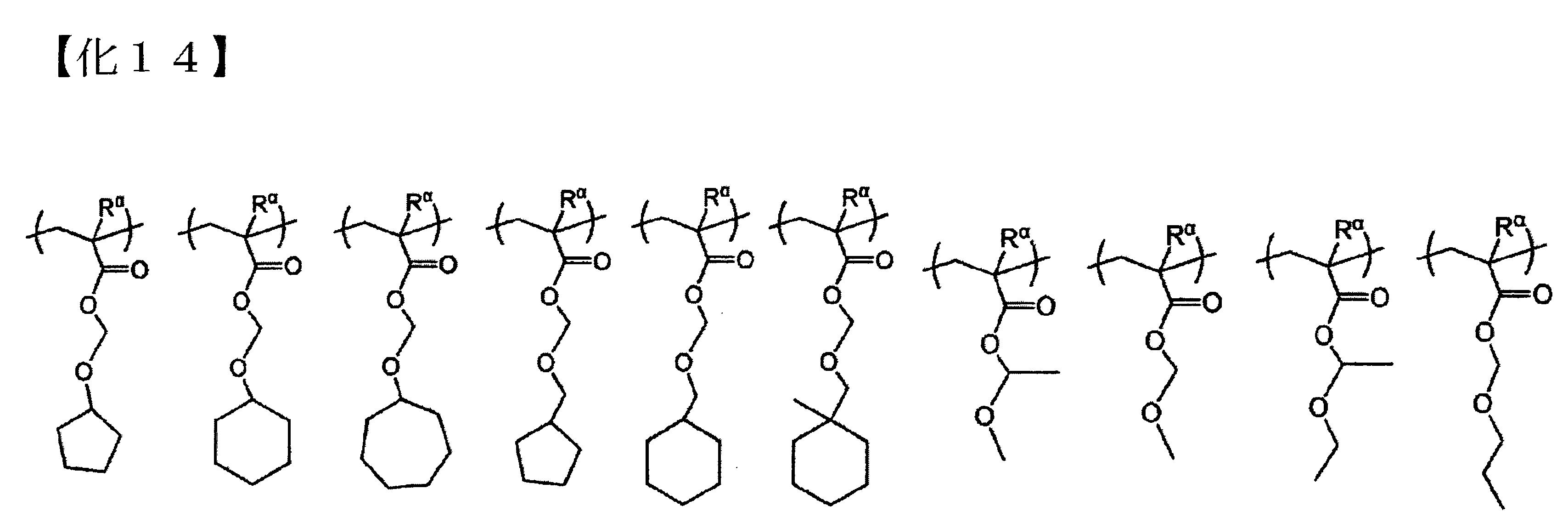
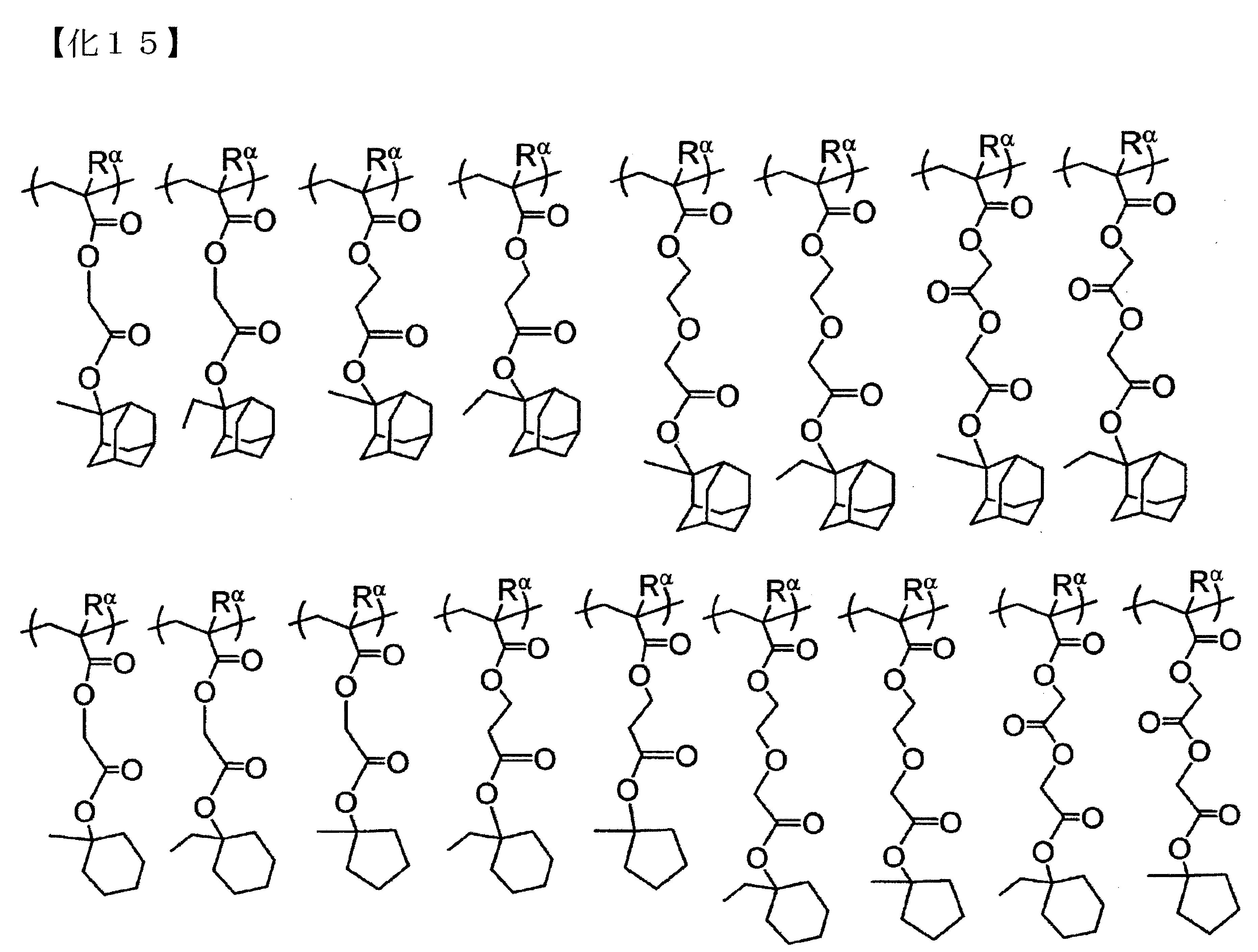
以下為前述式(a1-1)所表示的結構單位的具體例示。以下各式中,Rα
表示氫原子、甲基或三氟甲基。
以下為前述式(a1-2)所表示的結構單位的具體例示。
(A1)成份所具有的結構單位(a1),可為1種或2種以上皆可。 (A1)成份中的結構單位(a1)之比例,相對於構成(A1)成份的全結構單位之合計,以5~60莫耳%為佳,以10~55莫耳%為較佳,20~50莫耳%為更佳。 結構單位(a1)的比例為下限值以上時,容易製得阻劑圖型,且可提高感度、解析度、邊緣粗糙度之改善或EL寬容度等的微影蝕刻特性。又,為上限值以下時,可取得與其他結構單位之平衡。
≪結構單位(a2)≫ 結構單位(a2)為含有含內酯之環式基、含-SO2
-之環式基或含碳酸酯之環式基之結構單位(又,相當於結構單位(a1)者除外)。 結構單位(a2)之含內酯之環式基、含-SO2
-之環式基或含碳酸酯之環式基,於(A1)成份使用於形成阻劑膜時,就提高阻劑膜對基板的密著性之觀點為有效者。又,具有結構單位(a2)時,於鹼顯影製程中,於顯影時,可提高阻劑膜對鹼顯影液之溶解性。
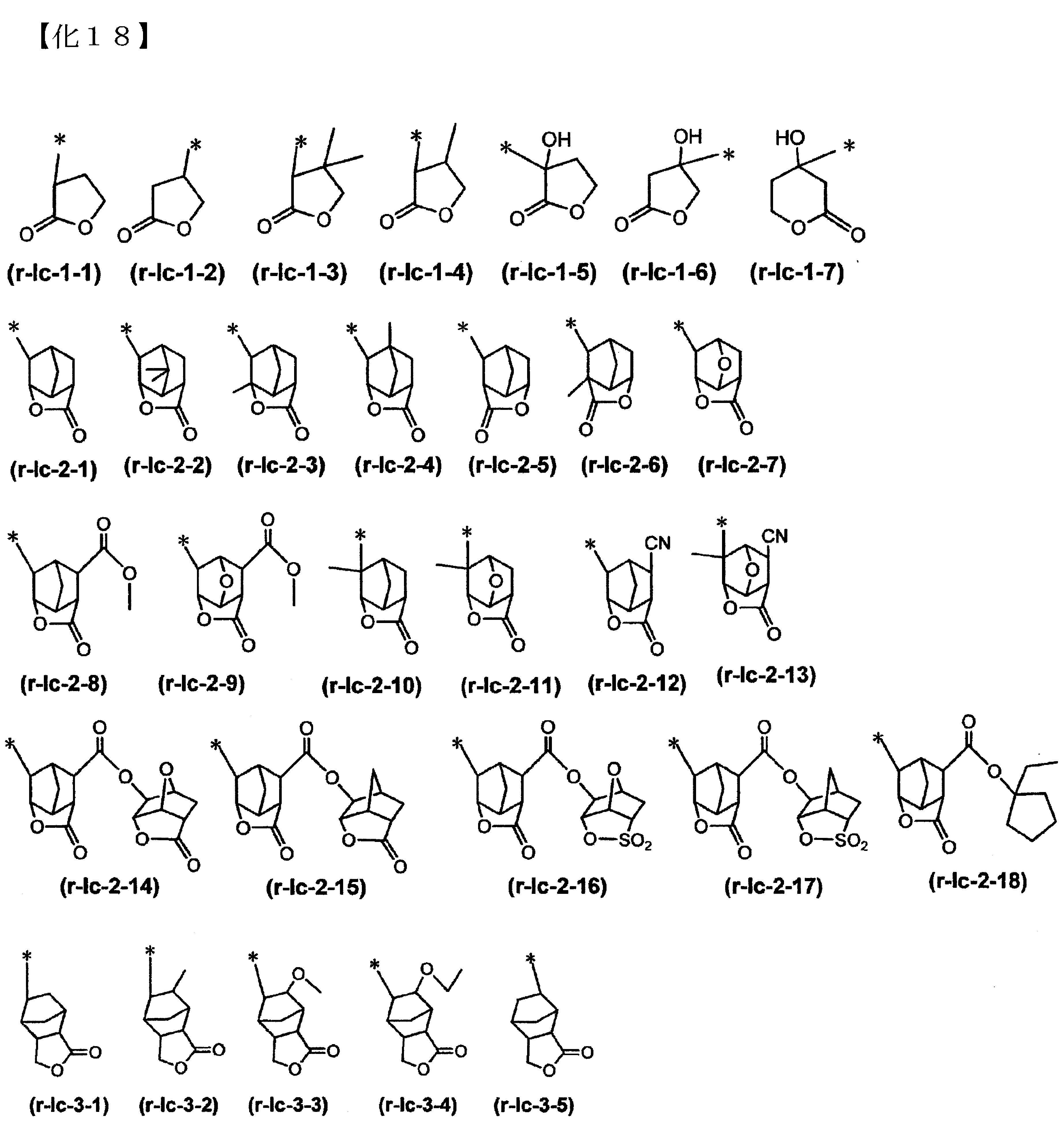
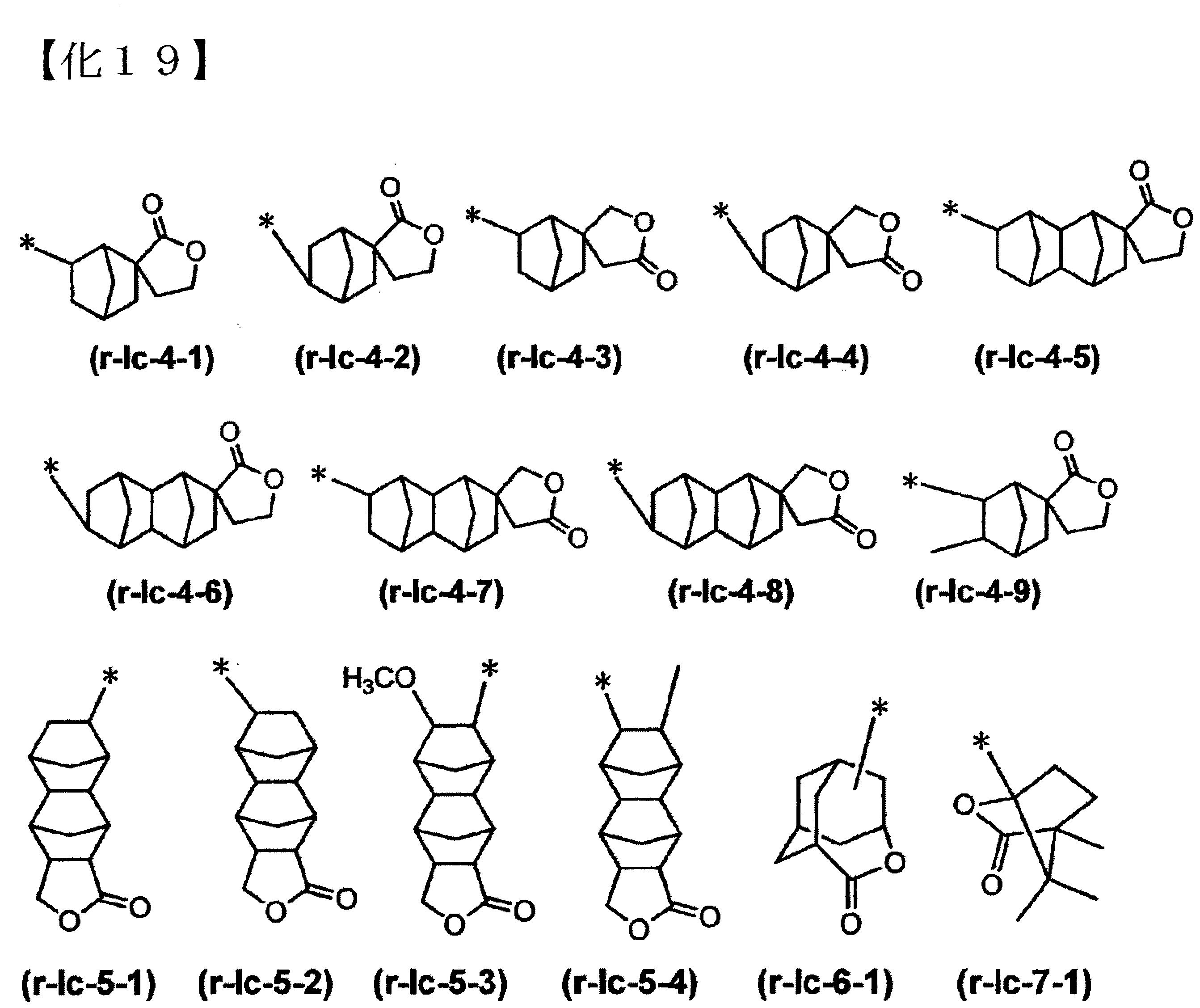
「含內酯之環式基」係指,其環骨架中含有含-O-C(=O)-之環(內酯環)的環式基。將內酯環以一個環之方式計數,僅為內酯環時稱為單環式基,尚具有其他環構造時,無論其構造為何,皆稱為多環式基。含內酯之環式基,可為單環式基亦可、多環式基亦可。 結構單位(a2)中之含內酯之環式基,並未有特別限定,而可使用任意的成份。具體而言,為下述通式(a2-r-1)~(a2-r-7)所各別表示的基等。
[式中,Ra’21
各自獨立為氫原子、烷基、烷氧基、鹵素原子、鹵化烷基、羥基、-COOR”、-OC(=O)R”、羥烷基或氰基;R”為氫原子、烷基、含內酯之環式基、含碳酸酯之環式基,或含-SO2
-之環式基;A”為可含有氧原子(-O-)或硫原子(-S-)的碳數1~5之伸烷基、氧原子或硫原子,n’為0~2之整數,m’為0或1]。
前述通式(a2-r-1)~(a2-r-7)中,Ra’21
中之烷基,以碳數1~6之烷基為佳。該烷基以直鏈狀或支鏈狀為佳。具體而言,例如,甲基、乙基、丙基、異丙基、n-丁基、異丁基、tert-丁基、戊基、異戊基、新戊基、己基等。該些之中,又以甲基或乙基為佳,以甲基為特佳。 Ra’21
中之烷氧基,以碳數1~6之烷氧基為佳。 該烷氧基以直鏈狀或支鏈狀為佳。具體而言,例如,前述Ra’21
中之烷基所列舉的烷基與氧原子(-O-)連結之基等。 Ra’21
中之鹵素原子,可列舉如,氟原子、氯原子、溴原子、碘原子等,又以氟原子為佳。 Ra’21
中之鹵化烷基,例如,前述Ra’21
中之烷基中的氫原子之一部份或全部被前述鹵素原子所取代之基等。該鹵化烷基,以氟化烷基為佳,特別是以全氟烷基為佳。
Ra’21
中之-COOR”、-OC(=O)R”中,R”之任一者皆為氫原子、烷基、含內酯之環式基、含碳酸酯之環式基,或含-SO2
-含有環式基。 R”中之烷基,可為直鏈狀、支鏈狀、環狀之任一者,其碳數以1~15為佳。 R”為直鏈狀或支鏈狀烷基時,以碳數1~10為佳,以碳數1~5為較佳,以甲基或乙基為特佳。 R”為環狀之烷基時,以碳數3~15為佳,以碳數4~12為更佳,以碳數5~10為最佳。具體而言,例如,由可被氟原子或氟化烷基所取代,或未被取代的單環鏈烷去除1個以上的氫原子而得之基;由雙環鏈烷、三環鏈烷、四環鏈烷等由多環鏈烷去除1個以上的氫原子而得之基等例示。更具體而言,例如,由環戊烷、環己烷等的單環鏈烷去除1個以上的氫原子而得之基;由金剛烷、降莰烷、異莰烷、三環癸烷、四環十二烷等由多環鏈烷去除1個以上的氫原子而得之基等。 R”中之含內酯之環式基,例如,與前述通式(a2-r-1)~(a2-r-7)所各別表示的基為相同之內容等。 R”中之含碳酸酯之環式基,例如,與後述含碳酸酯之環式基為相同之內容,具體而言,例如,通式(ax3-r-1)~(ax3-r-3)所各別表示的基等。 R”中之含-SO2
-之環式基,例如,與後述之含-SO2
-之環式基為相同之內容,具體而言,例如,通式(a5-r-1)~(a5-r-4)所各別表示的基等。 Ra’21
中之羥烷基,以碳數1~6者為佳,具體而言,例如,前述Ra’21
中之的烷基中之至少1個氫原子被羥基所取代之基等。
前述通式(a2-r-2)、(a2-r-3)、(a2-r-5)中,A”中之碳數1~5之伸烷基,以直鏈狀或支鏈狀之伸烷基為佳,例如,伸甲基、伸乙基、n-伸丙基、伸異丙基等。該伸烷基含有氧原子或硫原子時,其具體例如,前述伸烷基的末端或碳原子間介有-O-或-S-之基等,例如-O-CH2
-、 -CH2
-O-CH2
-、-S-CH2
-、-CH2
-S-CH2
-等。A”,以碳數1~5之伸烷基或-O-為佳,以碳數1~5之伸烷基為較佳,以伸甲基為最佳。
下述為通式(a2-r-1)~(a2-r-7)所各別表示的基之具體例。
「含-SO2
-之環式基」係指,其環骨架中含有含-SO2
-之環的環式基之意,具體而言,例如,-SO2
-中之硫原子(S)形成為環式基之環骨架的一部份之環式基;其環骨架中以含-SO2
-之環作為一個環之方式計數,僅為該環時,稱為單環式基,尚具有其他環構造時,無論其構造為何,皆稱為多環式基。含-SO2
-之環式基,可為單環式基亦可、多環式基亦可。 含-SO2
-之環式基,特別是其環骨架中含有含-O-SO2
-之環式基,即以-O-SO2
-中的-O-S-形成環骨架的一部份之含有磺內酯(sultone)環之環式基為佳。 含-SO2
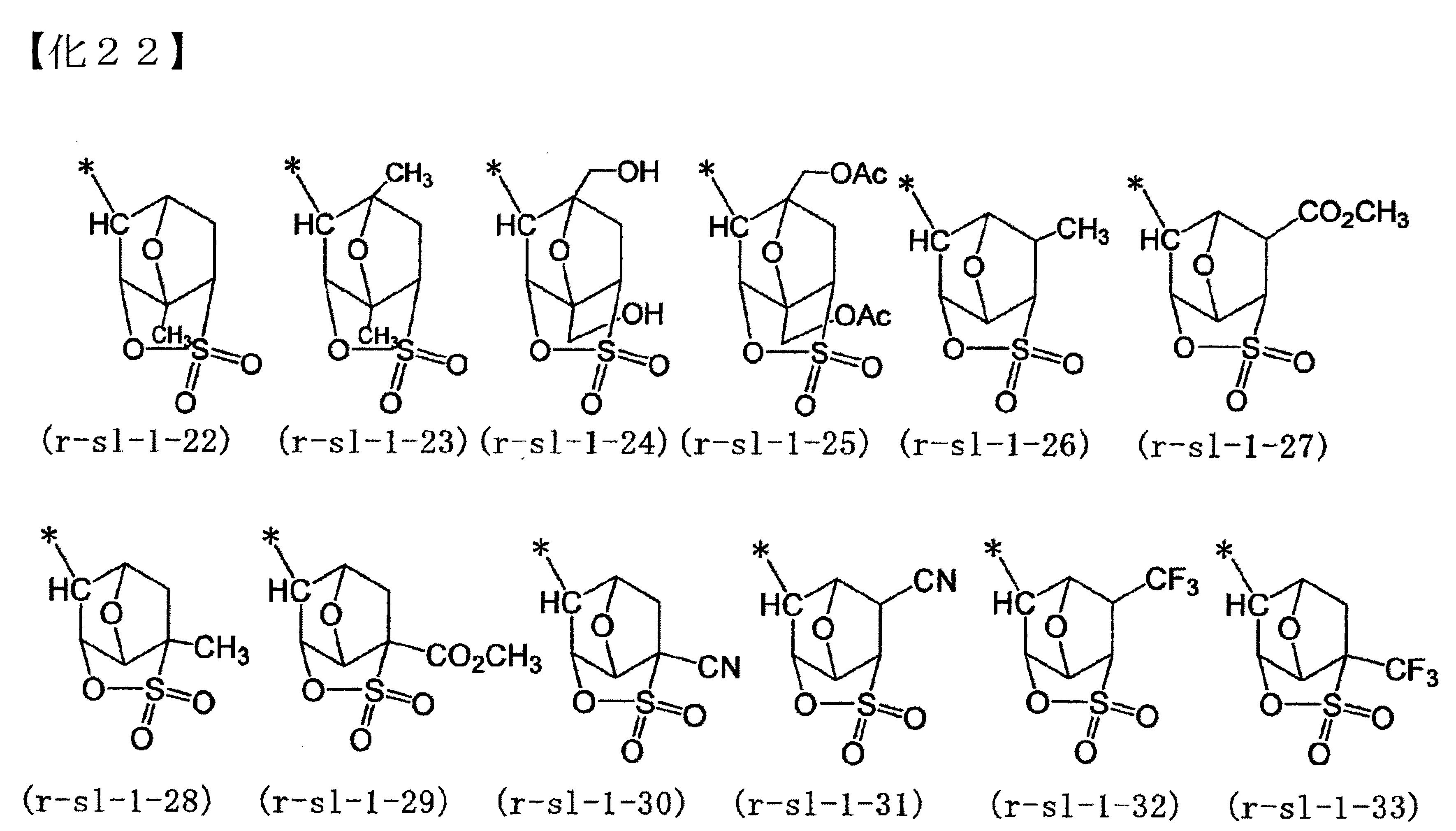
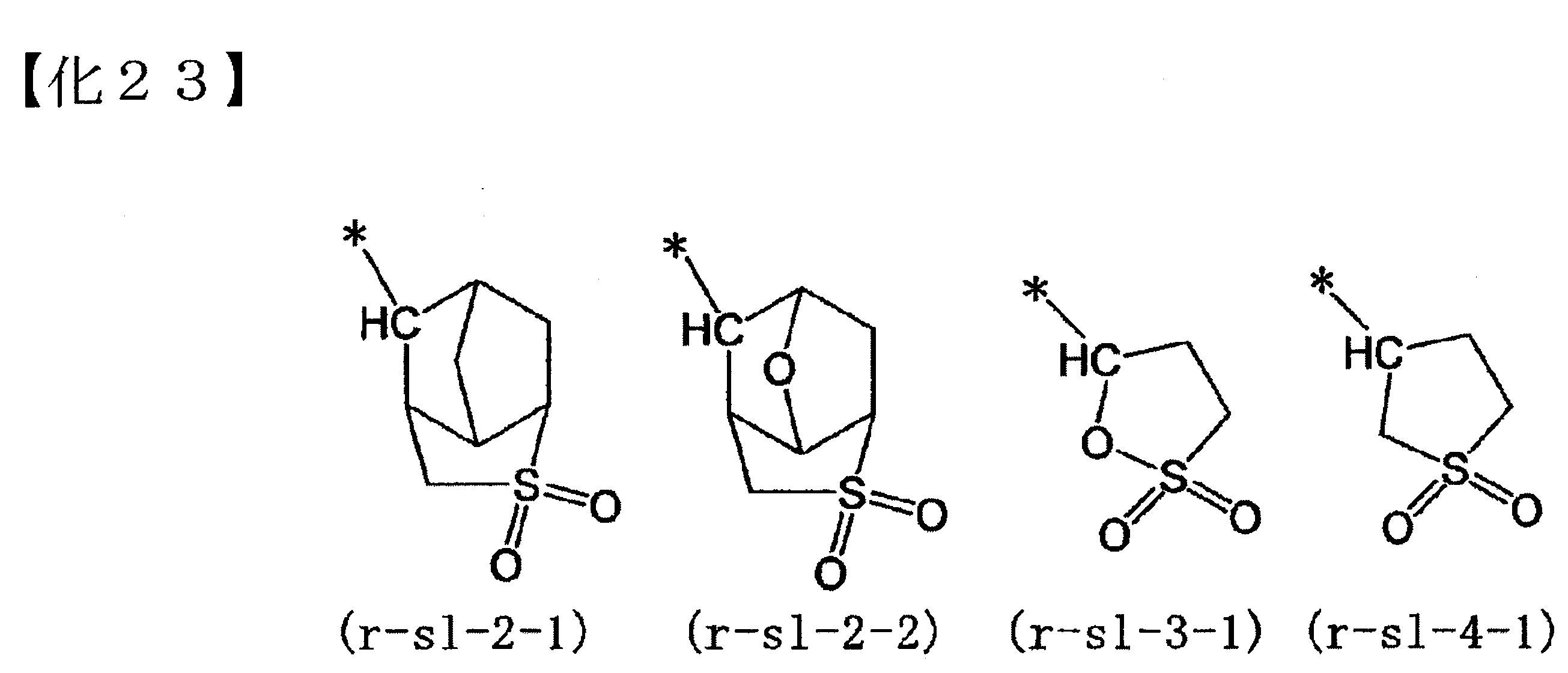
-之環式基,更具體而言,為下述通式(a5-r-1)~(a5-r-4)所各別表示的基等。
[式中,Ra’51
各自獨立為氫原子、烷基、烷氧基、鹵素原子、鹵化烷基、羥基、-COOR”、-OC(=O)R”、羥烷基或氰基;R”為氫原子、烷基、含內酯之環式基、含碳酸酯之環式基,或含-SO2
-之環式基;A”為可含有氧原子或硫原子的碳數1~5之伸烷基、氧原子或硫原子,n’為0~2之整數]。
前述通式(a5-r-1)~(a5-r-2)中,A”與前述通式(a2-r-2)、(a2-r-3)、(a2-r-5)中之A”為相同之內容。 Ra’51
中之烷基、烷氧基、鹵素原子、鹵化烷基、-COOR”、-OC(=O)R”、羥烷基,分別與前述通式(a2-r-1)~(a2-r-7)中之Ra’21
的說明中所列舉者為相同之內容。 下述為通式(a5-r-1)~(a5-r-4)所各別表示的基之具體例。式中之「Ac」為表示乙醯基。
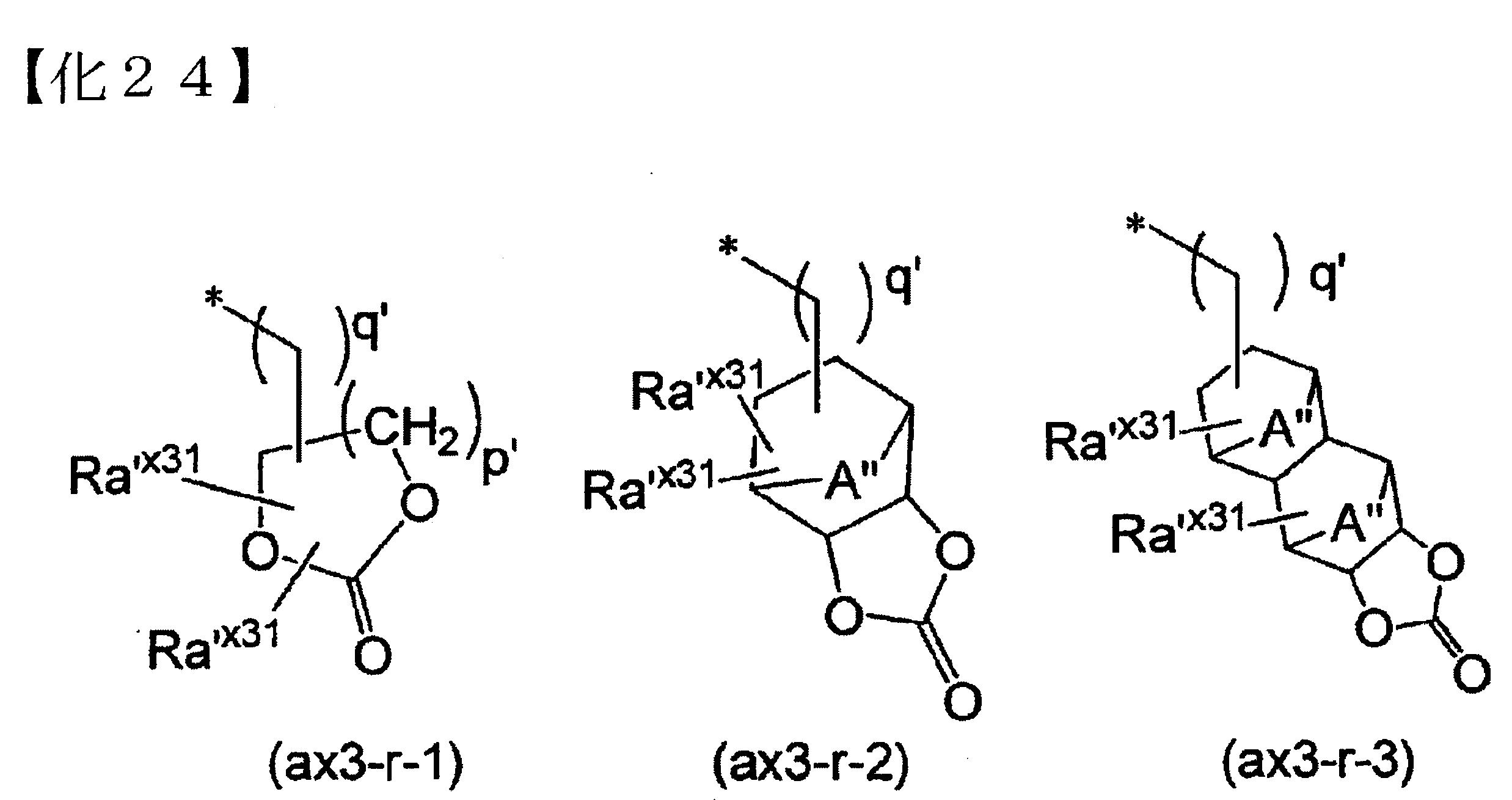
「含碳酸酯之環式基」係指,其環骨架中含有含-O-C(=O)-O-之環(碳酸酯環)的環式基。將碳酸酯環以一個環之方式計數,僅為碳酸酯環時稱為單環式基,尚具有其他環構造時,無論其構造為何,皆稱為多環式基。含碳酸酯之環式基,可為單環式基亦可、多環式基亦可。 含碳酸酯環之環式基,並未有特別限定,而可使用任意的成份。具體而言,為下述通式(ax3-r-1)~(ax3-r-3)所各別表示的基等。
[式中,Ra’x31
各自獨立為氫原子、烷基、烷氧基、鹵素原子、鹵化烷基、羥基、-COOR”、-OC(=O)R”、羥烷基或氰基;R”為氫原子、烷基、含內酯之環式基、含碳酸酯之環式基,或含-SO2
-之環式基;A”為可含有氧原子或硫原子的碳數1~5之伸烷基、氧原子或硫原子,p’為0~3之整數,q’為0或1]。
前述通式(ax3-r-2)~(ax3-r-3)中,A”與前述通式(a2-r-2)、(a2-r-3)、(a2-r-5)中之A”為相同之內容。 Ra’31
中之烷基、烷氧基、鹵素原子、鹵化烷基、 -COOR”、-OC(=O)R”、羥烷基,分別與前述通式(a2-r-1)~ (a2-r-7)中之Ra’21
的說明中所列舉者為相同之內容。 下述為通式(ax3-r-1)~(ax3-r-3)所各別表示的基之具體例。
結構單位(a2),又以由α位的碳原子所鍵結的氫原子可被取代基所取代的丙烯酸酯所衍生的結構單位為佳。 該結構單位(a2),以下述通式(a2-1)所表示的結構單位為佳。
[式中,R為氫原子、碳數1~5之烷基或碳數1~5之鹵化烷基;Ya21
為單鍵或2價之連結基;La21
為-O-、-COO-、 -CON(R’)-、-OCO-、-CONHCO-或-CONHCS-;R’表示氫原子或甲基;但,La21
為-O-之時,Ya21
不為-CO-。Ra21
為含內酯之環式基、含碳酸酯之環式基,或含-SO2
-之環式基]。
前述式(a2-1)中,R與前述為相同之內容。 Ya21
的2價之連結基,一般並未有特別之限定,又以可具有取代基之2價之烴基、含雜原子的2價之連結基等為較佳之例示。
・可具有取代基之2價之烴基: Ya21
為可具有取代基之2價之烴基時,該烴基,可為脂肪族烴基亦可、芳香族烴基亦可。
・・Ya21
中之脂肪族烴基 該脂肪族烴基,係指不具有芳香族性之烴基之意。該脂肪族烴基,可為飽合者亦可、不飽合者亦可,通常以飽合者為佳。 前述脂肪族烴基,例如,直鏈狀或支鏈狀之脂肪族烴基,或構造中含有環之脂肪族烴基等。
・・・直鏈狀或支鏈狀之脂肪族烴基 該直鏈狀或支鏈狀之脂肪族烴基,以碳數1~10為佳,以1~6為較佳,以1~4為較佳,以1~3為最佳。 直鏈狀之脂肪族烴基,以直鏈狀之伸烷基為佳,具體而言,例如,伸甲基[-CH2
-]、伸乙基[-(CH2
)2
-]、伸三甲基[-(CH2
)3
-]、伸四甲基[-(CH2
)4
-]、伸五甲基[-(CH2
)5
-]等。 支鏈狀之脂肪族烴基,以支鏈狀之伸烷基為佳,具體而言,例如,-CH(CH3
)-、-CH(CH2
CH3
)-、-C(CH3
)2
-、 -C(CH3
)(CH2
CH3
)-、-C(CH3
)(CH2
CH2
CH3
)-、-C(CH2
CH3
)2
-等之烷基伸甲基;-CH(CH3
)CH2
-、-CH(CH3
)CH(CH3
)-、 -C(CH3
)2
CH2
-、-CH(CH2
CH3
)CH2
-、-C(CH2
CH3
)2
-CH2
-等之烷基伸乙基;-CH(CH3
)CH2
CH2
-、-CH2
CH(CH3
)CH2
-等之烷基伸三甲基;-CH(CH3
)CH2
CH2
CH2
-、 -CH2
CH(CH3
)CH2
CH2
-等之烷基伸四甲基等之烷基伸烷基等。烷基伸烷基中之烷基,以碳數1~5之直鏈狀烷基為佳。
前述直鏈狀或支鏈狀之脂肪族烴基,可具有取代基亦可、不具有取代基亦可。該取代基,例如,氟原子、被氟原子所取代之碳數1~5之氟化烷基、羰基等。
・・・構造中含有環之脂肪族烴基 該構造中含有環之脂肪族烴基,例如,環構造中可含有含雜原子的取代基的環狀之脂肪族烴基(由脂肪族烴環去除2個氫原子而得之基)、前述環狀之脂肪族烴基鍵結於直鏈狀或支鏈狀脂肪族烴基的末端之基、前述環狀之脂肪族烴基介於直鏈狀或支鏈狀脂肪族烴基的中間之基等。前述直鏈狀或支鏈狀之脂肪族烴基,例如與前述為相同之內容。 環狀之脂肪族烴基,以碳數3~20為佳,以3~12為較佳。 環狀之脂肪族烴基,可為多環式基亦可、單環式基亦可。單環式之脂環式烴基,以由單環鏈烷去除2個氫原子而得之基為佳。該單環鏈烷以碳數3~6者為佳,具體而言,例如,環戊烷、環己烷等。多環式之脂環式烴基,以由多環鏈烷去除2個氫原子而得之基為佳,該多環鏈烷以碳數7~12者為佳,具體而言,例如,金剛烷、降莰烷、異莰烷、三環癸烷、四環十二烷等。
環狀之脂肪族烴基,可具有取代基亦可、不具有取代基亦可。該取代基,例如,烷基、烷氧基、鹵素原子、鹵化烷基、羥基、羰基等。 前述作為取代基之烷基,以碳數1~5之烷基為佳,以甲基、乙基、丙基、n-丁基、tert-丁基為最佳。 前述作為取代基之烷氧基,以碳數1~5之烷氧基為佳,以甲氧基、乙氧基、n-丙氧基、iso-丙氧基、n-丁氧基、tert-丁氧基為佳,甲氧基、乙氧基為最佳。 前述作為取代基之鹵素原子,可列舉如,氟原子、氯原子、溴原子、碘原子等,又以氟原子為佳。 前述取代基之鹵化烷基,例如,前述烷基中的氫原子之一部份或全部被前述鹵素原子所取代之基等。 環狀之脂肪族烴基中,構成該環構造的碳原子中之一部份可被含雜原子的取代基所取代。該含雜原子的取代基,例如,以-O-、-C(=O)-O-、-S-、-S(=O)2
-、 -S(=O)2
-O-為佳。
・・Ya21
中之芳香族烴基 該芳香族烴基,為至少具有1個芳香環之烴基。 該芳香環,只要為具有4n+2個的π電子之環狀共軛系時,並未有特別之限定,其可為單環式亦可、多環式亦可。芳香環之碳數以5~30為佳,以5~20為較佳,以6~15為更佳,以6~12為特佳。其中,該碳數為不包含取代基中之碳數者。芳香環,具體而言,例如,苯、萘、蒽、菲等之芳香族烴環;構成前述芳香族烴環中的一部份碳原子被雜原子所取代之芳香族雜環等。芳香族雜環中之雜原子,例如,氧原子、硫原子、氮原子等。 芳香族雜環,具體而言,例如,吡啶環、噻吩環等。 芳香族烴基,具體而言,例如,由前述芳香族烴環或芳香族雜環去除2個氫原子而得之基(伸芳基或雜伸芳基);由含有2個以上的芳香環之芳香族化合物(例如聯苯、茀等)去除2個氫原子而得之基;由前述芳香族烴環或芳香族雜環去除1個氫原子而得之基(芳基或雜芳基)中的1個氫原子被伸烷基所取代之基(例如,由苄基、苯乙基、1-萘甲基、2-萘甲基、1-萘乙基、2-萘乙基等的芳烷基中之芳基再去除1個氫原子而得之基)等。前述芳基或雜芳基所鍵結的伸烷基之碳數,以1~4為佳,以1~2為較佳,以1為特佳。
前述芳香族烴基中,該芳香族烴基所具有的氫原子亦可被取代基所取代。例如該芳香族烴基中的芳香環所鍵結的氫原子亦可被取代基所取代。該取代基,例如,烷基、烷氧基、鹵素原子、鹵化烷基、羥基等。 前述作為取代基之烷基,以碳數1~5之烷基為佳,以甲基、乙基、丙基、n-丁基、tert-丁基為最佳。 前述取代基之烷氧基、鹵素原子及鹵化烷基,例如,取代前述環狀之脂肪族烴基所具有的氫原子之取代基所例示之內容。
・含雜原子的2價之連結基: Ya21
為含雜原子的2價之連結基時,該連結基中,較佳者例如,-O-、-C(=O)-O-、-C(=O)-、-O-C(=O)-O-、 -C(=O)-NH-、-NH-、-NH-C(=NH)-(H可被烷基、醯基等取代基所取代)、-S-、-S(=O)2
-、-S(=O)2
-O-、通式 -Y21
-O-Y22
-、-Y21
-O-、-Y21
-C(=O)-O-、-C(=O)-O-Y21
-、 -[Y21
-C(=O)-O]m”
-Y22
-、-Y21
-O-C(=O)-Y22
-或 -Y21
-S(=O)2
-O-Y22
-所表示之基[式中,Y21
及Y22
各自獨立表示可具有取代基之2價之烴基,O為氧原子,m”為0~3之整數]等。 前述含有雜原子的2價之連結基為-C(=O)-NH-、 -C(=O)-NH-C(=O)-、-NH-、-NH-C(=NH)-時,該H可被烷基、醯基等的取代基所取代。該取代基(烷基、醯基等),以碳數為1~10者為佳,以1~8為較佳,以1~5為特佳。 通式-Y21
-O-Y22
-、-Y21
-O-、-Y21
-C(=O)-O-、 -C(=O)-O-Y21
-、-[Y21
-C(=O)-O]m”
-Y22
-、 -Y21
-O-C(=O)-Y22
-或-Y21
-S(=O)2
-O-Y22
-中,Y21
及Y22
,各自獨立表示可具有取代基之2價之烴基。該2價之烴基,例如,與前述2價之連結基的說明中所列舉的(可具有取代基之2價之烴基)為相同之內容等。 Y21
,以直鏈狀之脂肪族烴基為佳,以直鏈狀之伸烷基為較佳,以碳數1~5之直鏈狀之伸烷基為較佳,以伸甲基或伸乙基為特佳。 Y22
,以直鏈狀或支鏈狀之脂肪族烴基為佳,以伸甲基、伸乙基或烷基伸甲基為較佳。該烷基伸甲基中之烷基,以碳數1~5之直鏈狀烷基為佳,以碳數1~3之直鏈狀烷基為較佳,以甲基為最佳。 式-[Y21
-C(=O)-O]m”
-Y22
-所表示之基中,m”為0~3之整數,又以0~2之整數為佳,以0或1為較佳,以1為特佳。其中,又以式-[Y21
-C(=O)-O]m”
-Y22
-所表示之基為佳,以式 -Y21
-C(=O)-O-Y22
-所表示之基為特佳。其中,又以式 -(CH2
)a’
-C(=O)-O-(CH2
)b’
-所表示之基為佳。該式中,a’為1~10之整數,又以1~8之整數為佳,以1~5之整數為較佳,以1或2為更佳,以1為最佳。b’為1~10之整數,又以1~8之整數為佳,以1~5之整數為較佳,以1或2為更佳,以1為最佳。
Ya21
,以單鍵、酯鍵結[-C(=O)-O-]、醚鍵結(-O-)、直鏈狀或支鏈狀之伸烷基,或該些之組合為佳。
前述式(a2-1)中,Ra21
為含內酯之環式基、含-SO2
-之環式基或含碳酸酯之環式基。 Ra21
中之含內酯之環式基、含-SO2
-之環式基、含碳酸酯之環式基,分別以前述通式(a2-r-1)~(a2-r-7)所各別表示的基、通式(a5-r-1)~(a5-r-4)所各別表示的基、通式(ax3-r-1)~(ax3-r-3)所各別表示的基為較佳之例示。 其中,又以含內酯之環式基或含-SO2
-之環式基為佳,以前述通式(a2-r-1)、(a2-r-2)、(a2-r-6)或(a5-r-1)所各別表示的基為較佳。具體而言,以前述化學式(r-lc-1-1)~(r-lc-1-7)、(r-lc-2-1)~(r-lc-2-18)、(r-lc-6-1)、(r-sl-1-1)、(r-sl-1-18)所各別表示的任一之基為較佳。
(A1)成份所具有的結構單位(a2),可為1種或2種以上皆可。 (A1)成份具有結構單位(a2)時,結構單位(a2)之比例,相對於構成該(A1)成份的全結構單位之合計,以1~80莫耳%為佳,以10~70莫耳%為較佳,以10~65莫耳%為較佳,以10~60莫耳%為特佳。 結構單位(a2)之比例為較佳下限值以上時,含有結構單位(a2)可得到充份之效果,另一方面,為較佳上限值以下時,可取得與其他結構單位之平衡,而可使各種微影蝕刻特性及圖型形狀良好。
≪結構單位(a3)≫ 結構單位(a3)為,含有含極性基之脂肪族烴基的結構單位(又,相當於結構單位(a1)或結構單位(a2)者除外)。 (A1)成份具有結構單位(a3)時,可提高(A)成份之親水性、提升解析度。
極性基,例如,羥基、氰基、羧基、烷基的氫原子中之一部份被氟原子所取代之羥烷基等,特別是以羥基為佳。 脂肪族烴基,例如,碳數1~10之直鏈狀或支鏈狀之烴基(較佳為伸烷基),或環狀之脂肪族烴基(環式基)等。該環式基,可為單環式基亦可、多環式基亦可,例如可由ArF準分子雷射用阻劑組成物用的樹脂中,被多數提案之內容中適當地選擇使用。該環式基以多環式基為佳,以碳數7~30為較佳。 其中又以由含有含羥基、氰基、羧基,或烷基的氫原子中之一部份被氟原子所取代之羥烷基的脂肪族多環式基之丙烯酸酯所衍生的結構單位為較佳。該多環式基,例如,由雙環鏈烷、三環鏈烷、四環鏈烷等去除2個以上的氫原子而得之基等。具體而言,例如,由金剛烷、降莰烷、異莰烷、三環癸烷、四環十二烷等的多環鏈烷去除2個以上的氫原子而得之基等。該些多環式基之中,又以由金剛烷去除2個以上的氫原子而得之基、由降莰烷去除2個以上的氫原子而得之基、由四環十二烷去除2個以上的氫原子而得之基,就工業上而言為較佳。
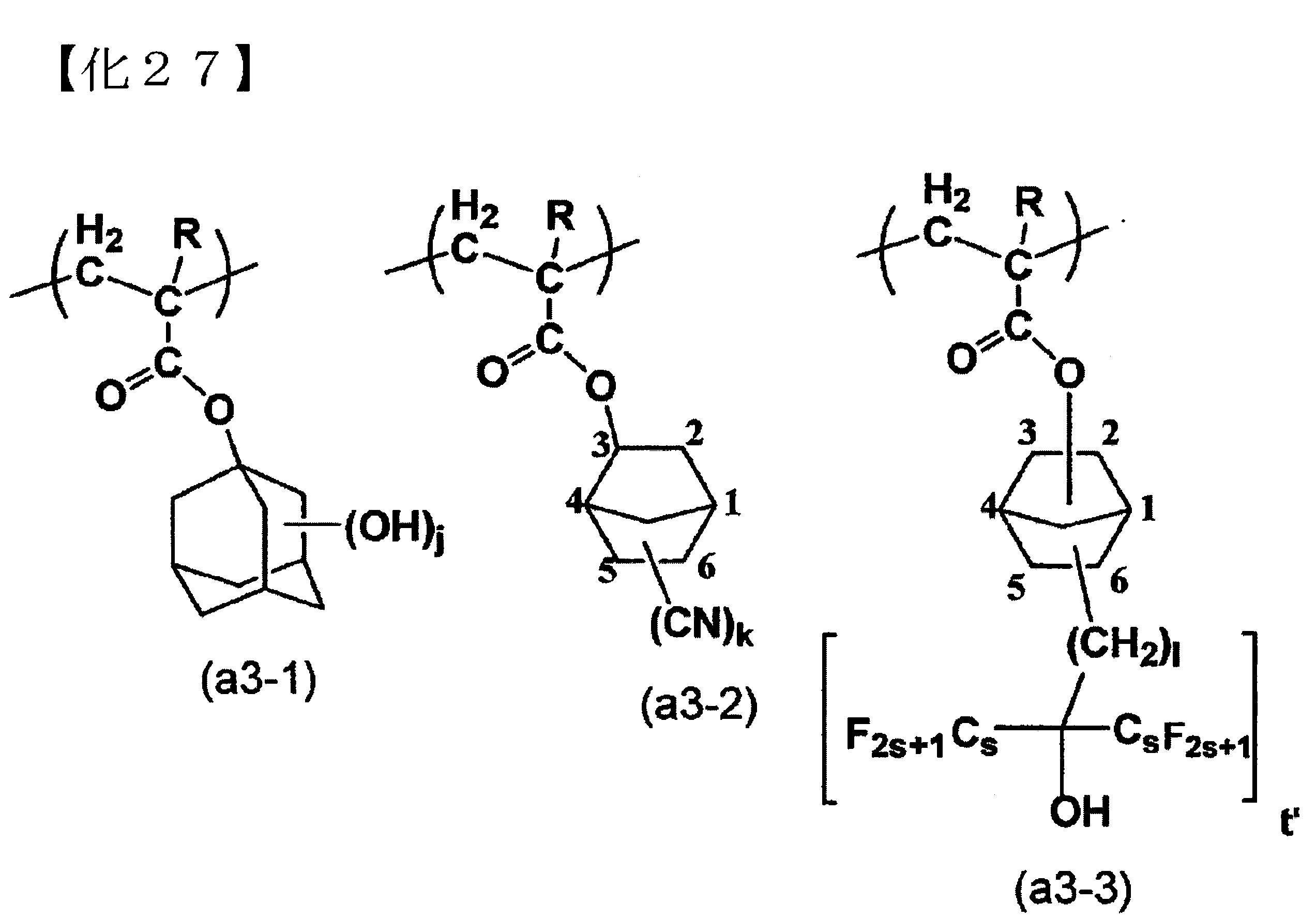
結構單位(a3),只要為含有含極性基之脂肪族烴基者時,並未有特別之限定,而可使用任意的成份。 結構單位(a3)中,以α位的碳原子所鍵結之氫原子可被取代基所取代的丙烯酸酯所衍生之結構單的含有含極性基之脂肪族烴基的結構單位為佳。 結構單位(a3),於含極性基之脂肪族烴基中之烴基為碳數1~10之直鏈狀或支鏈狀之烴基時,以由丙烯酸之羥乙酯所衍生的結構單位為佳,該烴基為多環式基時,又以下述式(a3-1)所表示的結構單位、式(a3-2)所表示的結構單位、式(a3-3)所表示的結構單位為較佳之例示。
式(a3-1)中,j以1或2為佳,以1為更佳。j為2時,羥基以鍵結於金剛烷基之3位與5位者為佳。j為1時,羥基以鍵結於金剛烷基之3位者為佳。 j以1為佳,羥基以鍵結於金剛烷基之3位者為特佳。
式(a3-2)中,k以1為佳。氰基以鍵結於降莰基的5位或6位者為佳。
式(a3-3)中,t’以1為佳。l以1為佳。s以1為佳。該些之中,又以丙烯酸的羧基之末端,鍵結2-降莰基或3-降莰基者為佳。氟化烷醇以鍵結於降莰基的5或6位者為佳。
(A1)成份所具有的結構單位(a3),可為1種或2種以上皆可。 (A1)成份具有結構單位(a3)時,結構單位(a3)之比例,相對於構成該(A1)成份的全結構單位之合計,以5~50莫耳%為佳,以5~40莫耳%為較佳,以5~35莫耳%為更佳。 結構單位(a3)之比例為較佳下限值以上時,含有結構單位(a3)可得到充份的效果,另一方面,為較佳上限值以下時,可容易取得與其他結構單位之平衡。
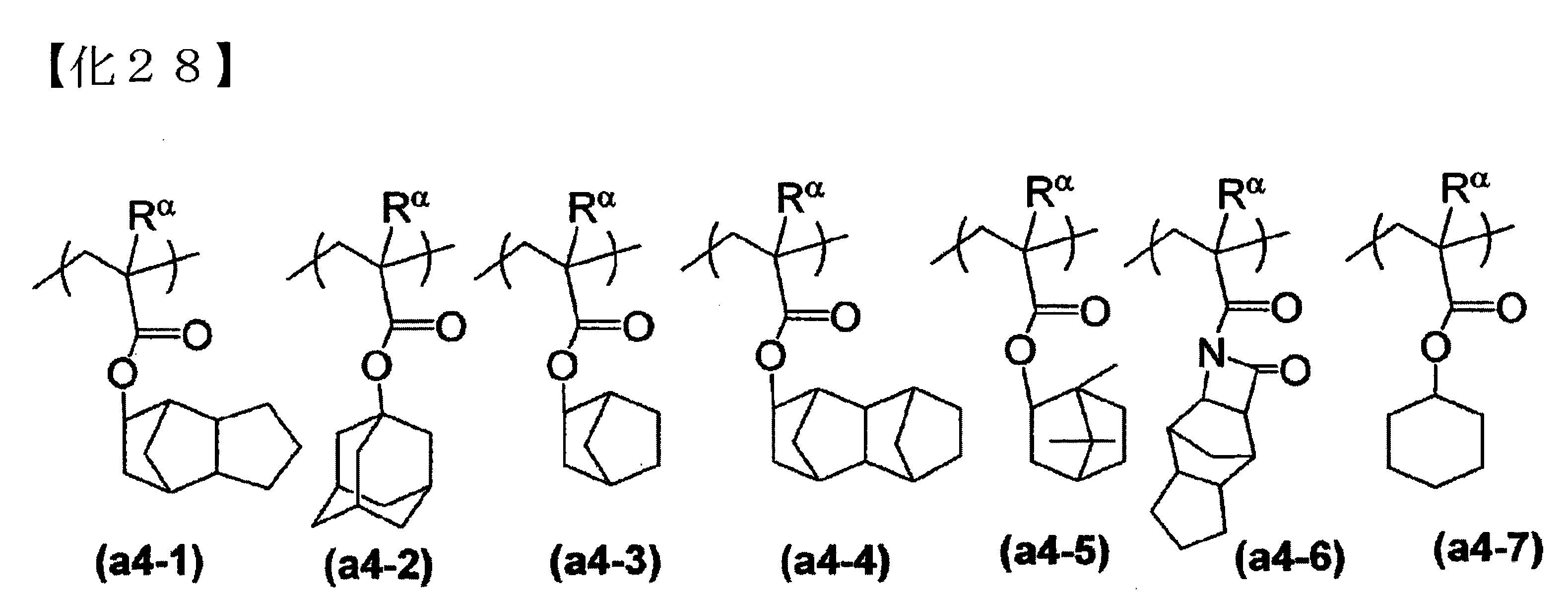
≪結構單位(a4)≫ 結構單位(a4)為含非酸解離性之脂肪族環式基的結構單位。 (A1)成份具有結構單位(a4)時,可提高所形成的阻劑圖型之乾蝕刻耐性。又,可提升(A)成份之疏水性。疏水性之提升,特別是於溶劑顯影製程時,可提高解析度、阻劑圖型形狀等。 結構單位(a4)中之「非酸解離性環式基」,於經由曝光而於該阻劑組成物中產生酸之際(例如,由後述的(B)成份產生酸之際),即使受到該酸之作用也不會解離,而以原貌殘留於該結構單位中之環式基。 結構單位(a4),例如以由含非酸解離性之脂肪族環式基之丙烯酸酯所衍生的結構單位等為佳。該環式基,可使用ArF準分子雷射用、KrF準分子雷射用(較佳為ArF準分子雷射用)等的阻劑組成物之樹脂成份所使用的以往已知的多數成份。 特別是由三環癸基、金剛烷基、四環十二烷基、異莰基、降莰基所選出之至少1種,就工業上容易取得之觀點為較佳。該些多環式基,可具有作為取代基之碳數1~5之直鏈狀或支鏈狀烷基。 結構單位(a4),具體而言,可列舉如,下述通式(a4-1)~(a4-7)所各別表示的結構單位等例示。
(A1)成份所具有的結構單位(a4),可為1種或2種以上皆可。 (A1)成份具有結構單位(a4)時,結構單位(a4)之比例,相對於構成該(A1)成份的全結構單位之合計,以1~30莫耳%為佳,以3~20莫耳%為較佳。 結構單位(a4)之比例為較佳下限值以上時,含有結構單位(a4)時,可得到充份的效果,另一方面,為較佳上限值以下時,可容易取得與其他結構單位之平衡。
本實施形態之阻劑組成物中,(A)成份以含有具有結構單位(a1)之高分子化合物(A1)者為佳。 該(A1)成份,具體而言,例如,由結構單位(a1)與結構單位(a2)之重複構造所形成的高分子化合物、結構單位(a1)與結構單位(a3)之重複構造所形成的高分子化合物、結構單位(a1)與結構單位(a2)與結構單位(a3)之重複構造所形成的高分子化合物等例示。
(A1)成份之質量平均分子量(Mw)(依凝膠滲透色層分析(GPC)之聚苯乙烯換算基準),並未有特別之限定,又以1000~500000左右為佳,以3000~50000左右為較佳。 (A1)成份之Mw於該範圍的較佳上限值以下時,作為阻劑使用時,對於阻劑溶劑具有充份的溶解性,於該範圍的較佳下限值以上時,可使耐乾蝕刻性或阻劑圖型斷面形狀良好。 (A1)成份之分散度(Mw/Mn),並未有特別之限定,又以1.0~4.0左右為佳,以1.0~3.0左右為較佳,以1.5~2.5程度為特佳。又,Mn表示數平均分子量。
(A1)成份,可單獨使用1種亦可、將2種以上合併使用亦可。 (A)成份中的(A1)成份之比例,相對於(A)成份之總質量,以25質量%以上為佳,以50質量%以上為較佳,以75質量%以上為較佳,亦可為100質量%。該比例為25質量%以上時,可容易形成高感度化,或具有改善邊緣粗糙度等各種微影蝕刻特性的優良阻劑圖型。
(A1)成份之製造方法: (A1)成份,可將衍生各結構單位的單體溶解於聚合溶劑中,再將例如偶氮二異丁腈(AIBN)、二甲基2,2’-偶氮二異丁酸酯(例如V-601等)等的自由基聚合起始劑加入其中,進行聚合反應之方式製得。又,聚合之際,例如可併用HS-CH2
-CH2
-CH2
-C(CF3
)2
-OH等鏈移轉劑使用之方式,於末端導入-C(CF3
)2
-OH基。依此方式,導入該於烷基的氫原子中之一部份被氟原子所取代的羥烷基之共聚物,可有效地降低顯影缺陷或降低LER(線路邊緣粗糙度:線路側壁的不均勻凹凸)。
本實施形態之阻劑組成物中,(A)成份,可單獨使用1種亦可、將2種以上合併使用亦可。 本實施形態之阻劑組成物中,(A)成份之含量,可配合所欲形成的阻劑膜厚等進行調整即可。
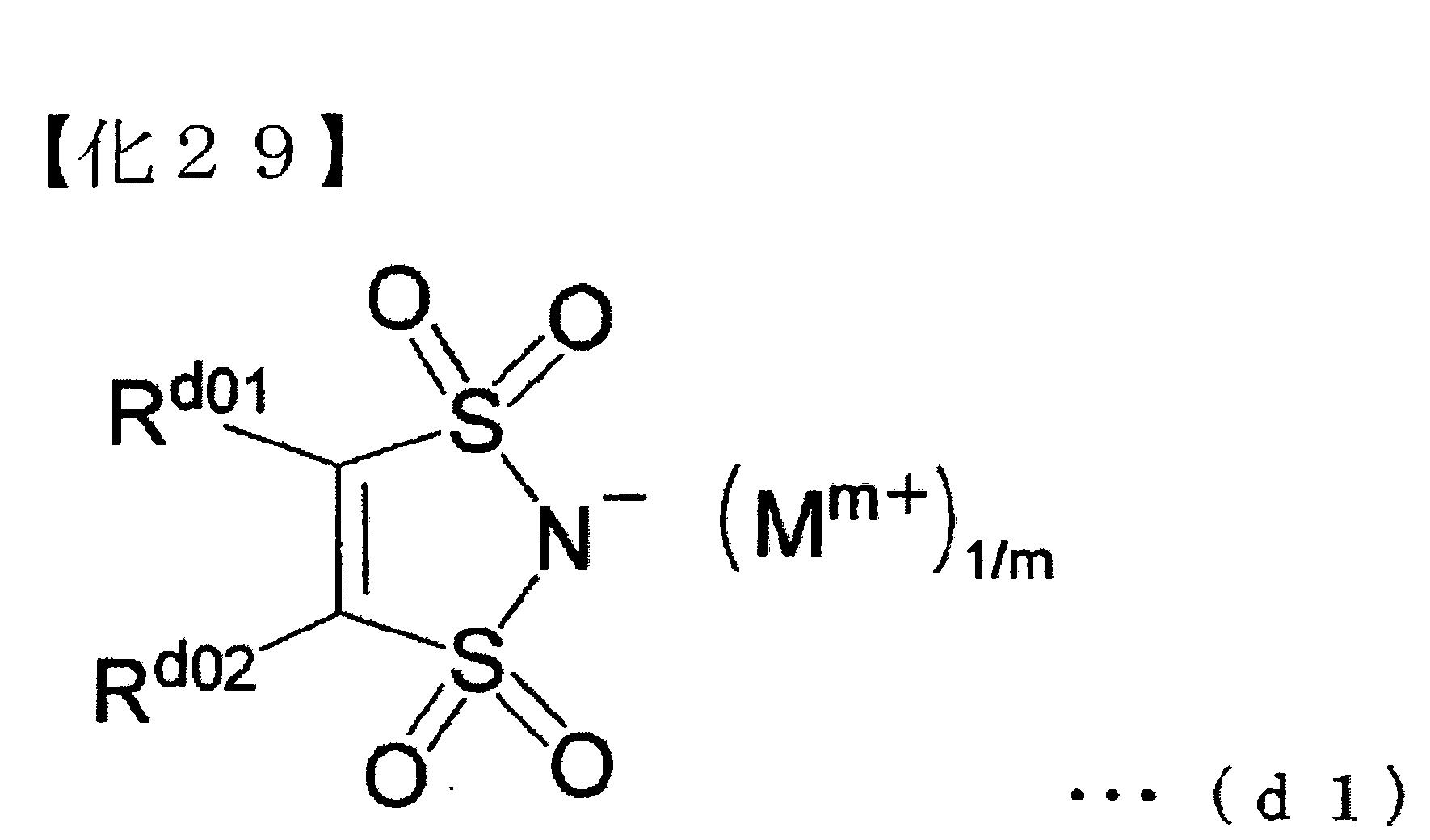
<(D1)成份> (D1)成份為下述通式(d1)所表示之化合物。 本實施形態之阻劑組成物中,因含有(D1)成份,故可提高解析度,且以更低圖型粗糙度的良好形狀,形成更微細的圖型。此外,因含有(D1)成份,故於形成阻劑圖型之際,可提高焦點景深寬度(DOF)等特性,擴大製程寬容度。
[式中,Rd01
及Rd02
各自獨立為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基;或,Rd01
與Rd02
可相互鍵結,形成縮合環;m為1以上之整數,又,Mm+
表示m價之有機陽離子]。
≪陰離子部≫ (D1)成份中之陰離子部,為具有含二碸醯亞胺(-SO2
N-
SO2
-)基的5員環構造者。 前述式(d1)中,Rd01
及Rd02
各自獨立為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基;或,Rd01
與Rd02
可相互鍵結,形成縮合環。
可具有取代基之環式基: 該環式基,以環狀之烴基為佳,該環狀之烴基,可為芳香族烴基亦可、脂肪族烴基亦可。脂肪族烴基,係指不具有芳香族性之烴基之意。又,脂肪族烴基,可為飽合者亦可、不飽合者亦可,通常以飽合者為佳。
Rd01
及Rd02
中之芳香族烴基,為具有芳香環之烴基;該芳香族烴基之碳數以3~30為佳,以5~30為較佳,以5~20為更佳,以6~15為特佳,以6~10為最佳。又,該碳數為不包含取代基中之碳數者。 Rd01
及Rd02
中之芳香族烴基所具有的芳香環,具體而言,例如,苯、茀、萘、蒽、菲、聯苯,或構成該些芳香環的碳原子中之一部份被雜原子所取代之芳香族雜環等。芳香族雜環中之雜原子,例如,氧原子、硫原子、氮原子等。 Rd01
及Rd02
中之芳香族烴基,具體而言,例如,由前述芳香環去除1個氫原子而得之基(芳基:例如,苯基、萘基等)、前述芳香環中之1個氫原子被伸烷基所取代之基(例如,苄基、苯乙基、1-萘甲基、2-萘甲基、1-萘乙基、2-萘乙基等的芳烷基等)等。前述伸烷基(芳烷基中之烷鏈)之碳數,以1~4為佳,以1~2為較佳,以1為特佳。
Rd01
及Rd02
中之環狀之脂肪族烴基,例如,構造中含有環之脂肪族烴基。 該構造中含有環之脂肪族烴基,例如,脂環式烴基(脂肪族烴環去除1個氫原子而得之基)、脂環式烴基鍵結於直鏈狀或支鏈狀脂肪族烴基的末端之基、脂環式烴基介於直鏈狀或支鏈狀脂肪族烴基的中間之基等。 前述脂環式烴基,以碳數3~20為佳,以3~12為較佳。 前述脂環式烴基,可為多環式基亦可、單環式基亦可。單環式之脂環式烴基,以由單環鏈烷去除1個以上的氫原子而得之基為佳。該單環鏈烷,以碳數3~8者為佳,具體而言,例如,環戊烷、環己烷、環庚烷、環辛烷等。多環式之脂環式烴基,又以由多環鏈烷去除1個以上的氫原子而得之基為佳,該多環鏈烷,以碳數7~30者為佳。其中,該多環鏈烷,又以金剛烷、降莰烷、異莰烷、三環癸烷、四環十二烷等的具有交聯環系的多環式骨架之多環鏈烷;具有膽固醇骨架的環式基等的具有縮合環系的多環式骨架之多環鏈烷為較佳。
其中,Rd01
及Rd02
中之環狀之脂肪族烴基,以由單環鏈烷或多環鏈烷去除1個以上的氫原子而得之基為佳,以由多環鏈烷去除1個氫原子而得之基為較佳,以金剛烷基、降莰基為特佳,以金剛烷基為最佳。
可與脂環式烴基鍵結之直鏈狀或支鏈狀之脂肪族烴基,以碳數1~10為佳,以1~6為較佳,以1~4為較佳,以1~3為最佳。 直鏈狀之脂肪族烴基,以直鏈狀之伸烷基為佳,具體而言,例如,伸甲基[-CH2
-]、伸乙基[-(CH2
)2
-]、伸三甲基[-(CH2
)3
-]、伸四甲基[-(CH2
)4
-]、伸五甲基[-(CH2
)5
-]等。 支鏈狀之脂肪族烴基,以支鏈狀之伸烷基為佳,具體而言,例如,-CH(CH3
)-、-CH(CH2
CH3
)-、-C(CH3
)2
-、 -C(CH3
)(CH2
CH3
)-、-C(CH3
)(CH2
CH2
CH3
)-、-C(CH2
CH3
)2
-等之烷基伸甲基;-CH(CH3
)CH2
-、-CH(CH3
)CH(CH3
)-、 -C(CH3
)2
CH2
-、-CH(CH2
CH3
)CH2
-、-C(CH2
CH3
)2
-CH2
-等之烷基伸乙基;-CH(CH3
)CH2
CH2
-、-CH2
CH(CH3
)CH2
-等之烷基伸三甲基;-CH(CH3
)CH2
CH2
CH2
-、 -CH2
CH(CH3
)CH2
CH2
-等之烷基伸四甲基等之烷基伸烷基等。烷基伸烷基中之烷基,以碳數1~5之直鏈狀烷基為佳。
又,Rd01
及Rd02
中之環狀之烴基,可含有雜環等的雜原子。具體而言,例如,前述通式(a2-r-1)~(a2-r-7)所各別表示的含內酯之環式基、前述通式(a5-r-1)~(a5-r-4)所各別表示的含-SO2
-之環式基、其他下述化學式(r-hr-1)~(r-hr-16)所各別表示的雜環式基等。
Rd01
及Rd02
之環式基中之取代基,例如,烷基、烷氧基、鹵素原子、鹵化烷基、羥基、羰基、硝基等。 作為取代基之烷基,以碳數1~5之烷基為佳,以甲基、乙基、丙基、n-丁基、tert-丁基為最佳。 作為取代基之烷氧基,以碳數1~5之烷氧基為佳,以甲氧基、乙氧基、n-丙氧基、iso-丙氧基、n-丁氧基、tert-丁氧基為較佳,以甲氧基、乙氧基為最佳。 作為取代基之鹵素原子,可列舉如,氟原子、氯原子、溴原子、碘原子等,又以氟原子為佳。 作為取代基之鹵化烷基,例如,碳數1~5之烷基,例如甲基、乙基、丙基、n-丁基、tert-丁基等中的氫原子之一部份或全部被前述鹵素原子所取代之基等。 作為取代基之羰基,為取代構成環狀烴基的伸甲基(-CH2
-)之基。
可具有取代基之鏈狀烷基: Rd01
及Rd02
之鏈狀烷基,可為直鏈狀或支鏈狀之任一者。 直鏈狀烷基,以碳數1~20為佳,以1~15為較佳,以1~10為最佳。具體而言,例如,甲基、乙基、丙基、丁基、戊基、己基、庚基、辛基、壬基、癸基、十一烷基、十二烷基、十三烷基、異十三烷基、十四烷基、十五烷基、十六烷基、異十六烷基、十七烷基、十八烷基、十九烷基、二十烷基、二十一烷基、二十二烷基等。 支鏈狀烷基,以碳數3~20為佳,以3~15為較佳,以3~10為最佳。具體而言,例如,1-甲乙基、1-甲基丙基、2-甲基丙基、1-甲基丁基、2-甲基丁基、3-甲基丁基、1-乙基丁基、2-乙基丁基、1-甲基戊基、2-甲基戊基、3-甲基戊基、4-甲基戊基、1,1-二甲乙基、1,1-二甲基丙基等。
可具有取代基之鏈狀烯基: Rd01
及Rd02
之鏈狀烯基,可為直鏈狀或支鏈狀之任一者,又以碳數2~10為佳,以2~5為較佳,以2~4為更佳,以3為特佳。直鏈狀烯基,例如,乙烯基、丙烯基(烯丙基)、丁烯基等。支鏈狀烯基,例如,1-甲基乙烯基、2-甲基乙烯基、1-甲基丙烯基、2-甲基丙烯基等。 鏈狀烯基,於上述之中,以直鏈狀烯基為佳,以乙烯基、丙烯基為較佳,以乙烯基為特佳。
Rd01
及Rd02
之鏈狀烷基或烯基中之取代基,例如,烷氧基、鹵素原子、鹵化烷基、羥基、羰基、硝基、胺基、上述Rd01
及Rd02
中之環式基等。
上述之中,Rd01
及Rd02
以可具有取代基之環式基為佳,以可具有取代基之環狀之烴基為較佳。
前述式(d1)中,陰離子部亦可為Rd01
與Rd02
相互鍵結,形成縮合環者。Rd01
與Rd02
形成縮合環時,該縮合環構造,為含有含二碸醯亞胺(-SO2
N-
SO2
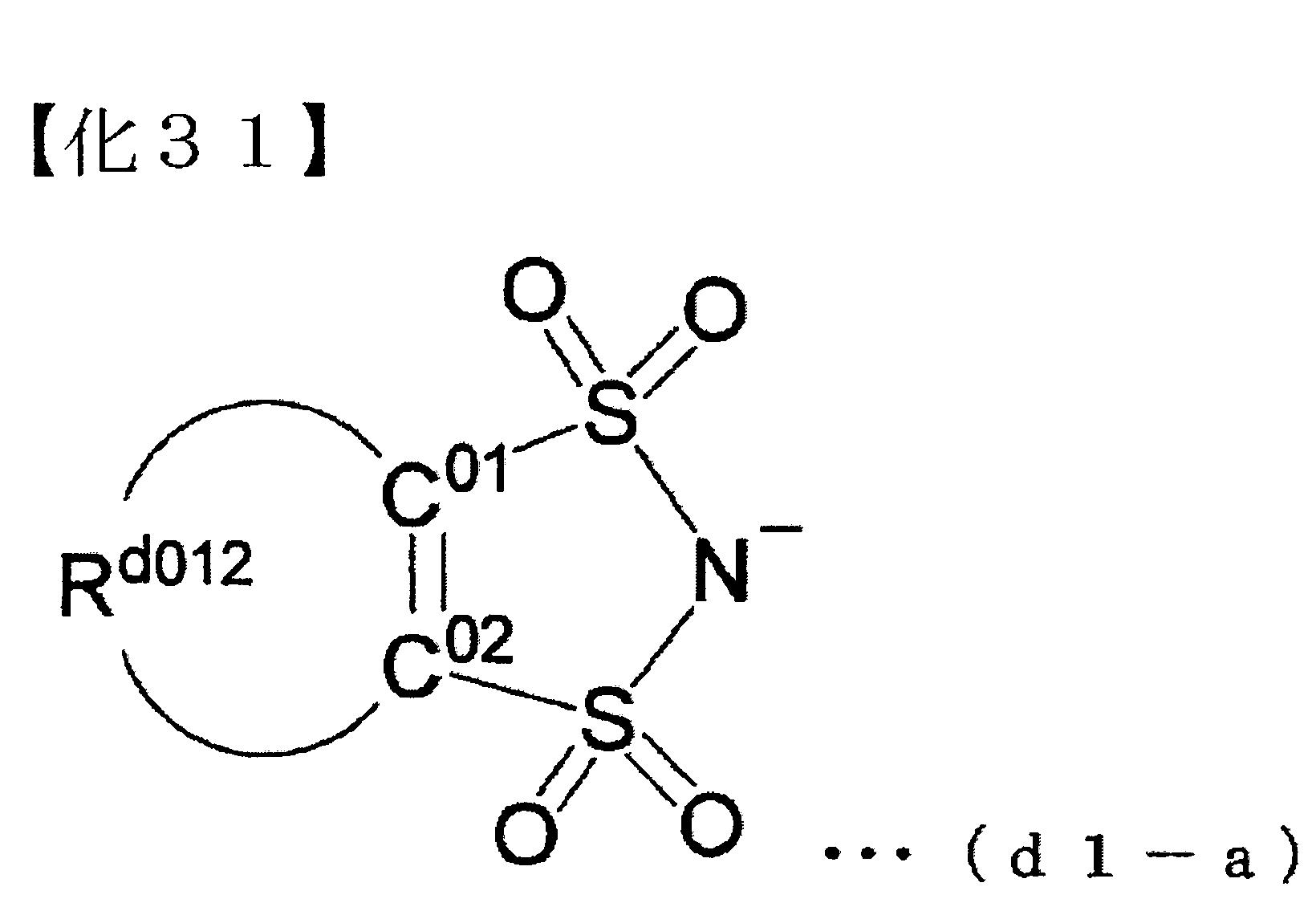
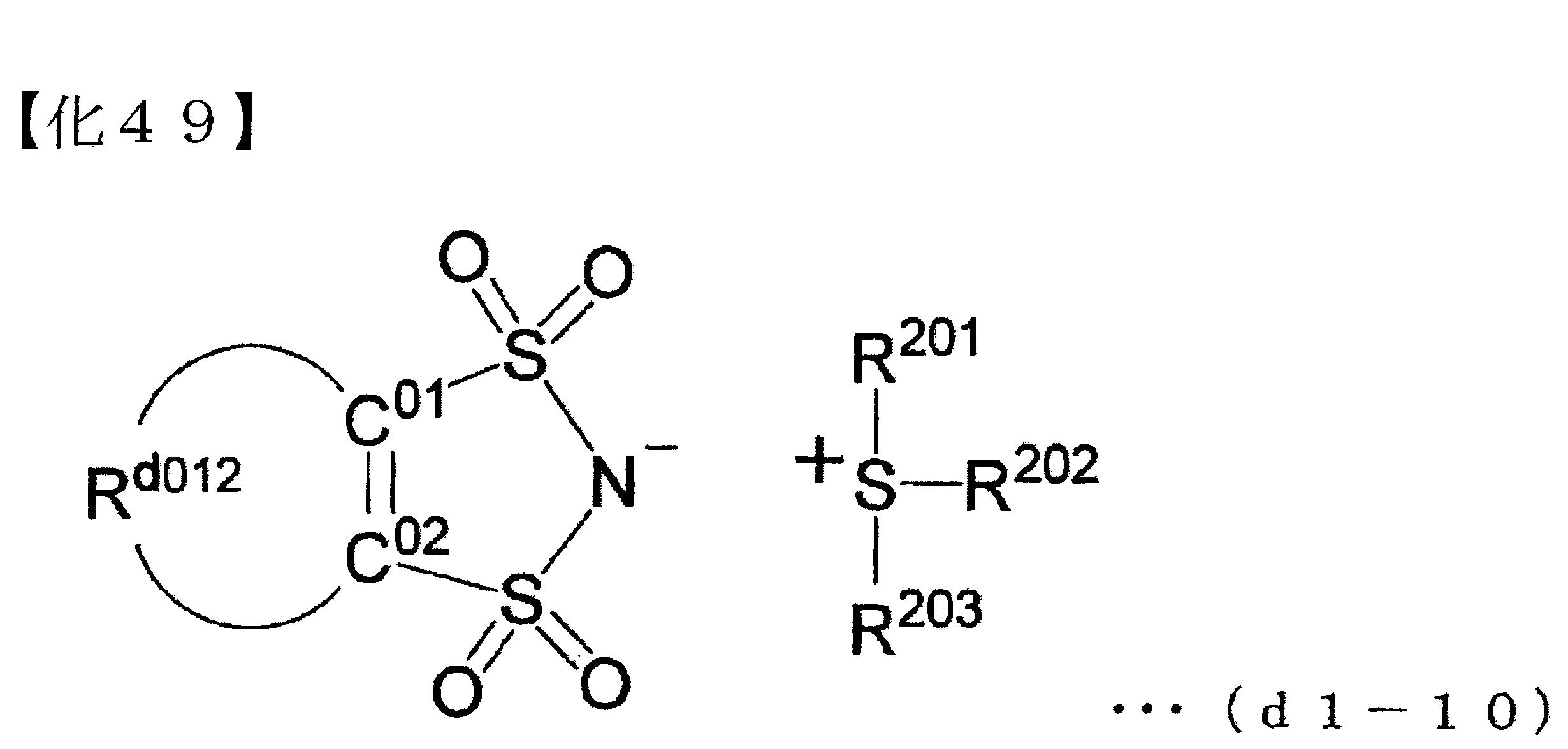
-)基之5員環者。 形成該縮合環時之陰離子部,例如,以下述通式(d1-a)所表示之陰離子等。
前述式(d1-a)中,Rd012
,與C01
與C02
形成之環構造(即,縮合環之一部份),可為單環亦可、多環亦可。又,該構成環構造之碳原子的一部份可被雜原子所取代。該環中之雜原子,例如,氧原子、硫原子、氮原子等。
該Rd012
與C01
與C02
所形成的環構造,較佳為可具有取代基之芳香環等,該芳香環可為單環亦可、多環亦可。 該芳香環之碳數(包含C01
與C02
之碳數),以5~30為佳,以5~20為較佳,6~15為較佳,以6~12為特佳。 該芳香環,具體而言,例如,苯、萘、蒽、菲等之芳香族烴環;構成該芳香族烴環的碳原子之一部份被雜原子所取代之芳香族雜環;芳香環與脂肪族環之縮合環等。芳香族雜環中之雜原子,例如,氧原子、硫原子、氮原子等。芳香族雜環,具體而言,例如,吡啶環、噻吩環等。
該些之中,由Rd012
與C01
與C02
所形成之環構造,就更提高本發明效果之觀點,以可具有取代基之芳香族環(芳香環)為佳,以可具有取代基之芳香族烴環為較佳,以可具有取代基之苯環、可具有取代基之萘環為更佳,以可具有取代基之苯環為特佳。
Rd012
與C01
與C02
所形成的環構造所可具有的取代基,例如烷基、烷氧基、鹵素原子、鹵化烷基等。 作為前述取代基之烷基,以碳數1~5之烷基為佳,以甲基、乙基、丙基、n-丁基、tert-丁基為佳,以甲基、乙基為較佳。 作為前述取代基之烷氧基,以碳數1~5之烷氧基為佳,以甲氧基、乙氧基、n-丙氧基、iso-丙氧基、n-丁氧基、tert-丁氧基為佳,以甲氧基、乙氧基為較佳。 前述取代基之鹵素原子,例如,氟原子、氯原子、溴原子、碘原子等,又以氟原子為佳。 作為前述取代基之鹵化烷基,為前述烷基中的氫原子之一部份或全部被前述鹵素原子所取代之基等。
此外,由Rd012
與C01
與C02
所形成的環構造中所可具有的取代基,又例如,單環或多環之脂環式基、醯基、羧基、烷氧羰基、氰基、硝基、烷基磺醯基(例如甲基磺醯基等)、可具有取代基之芳香族烴基。
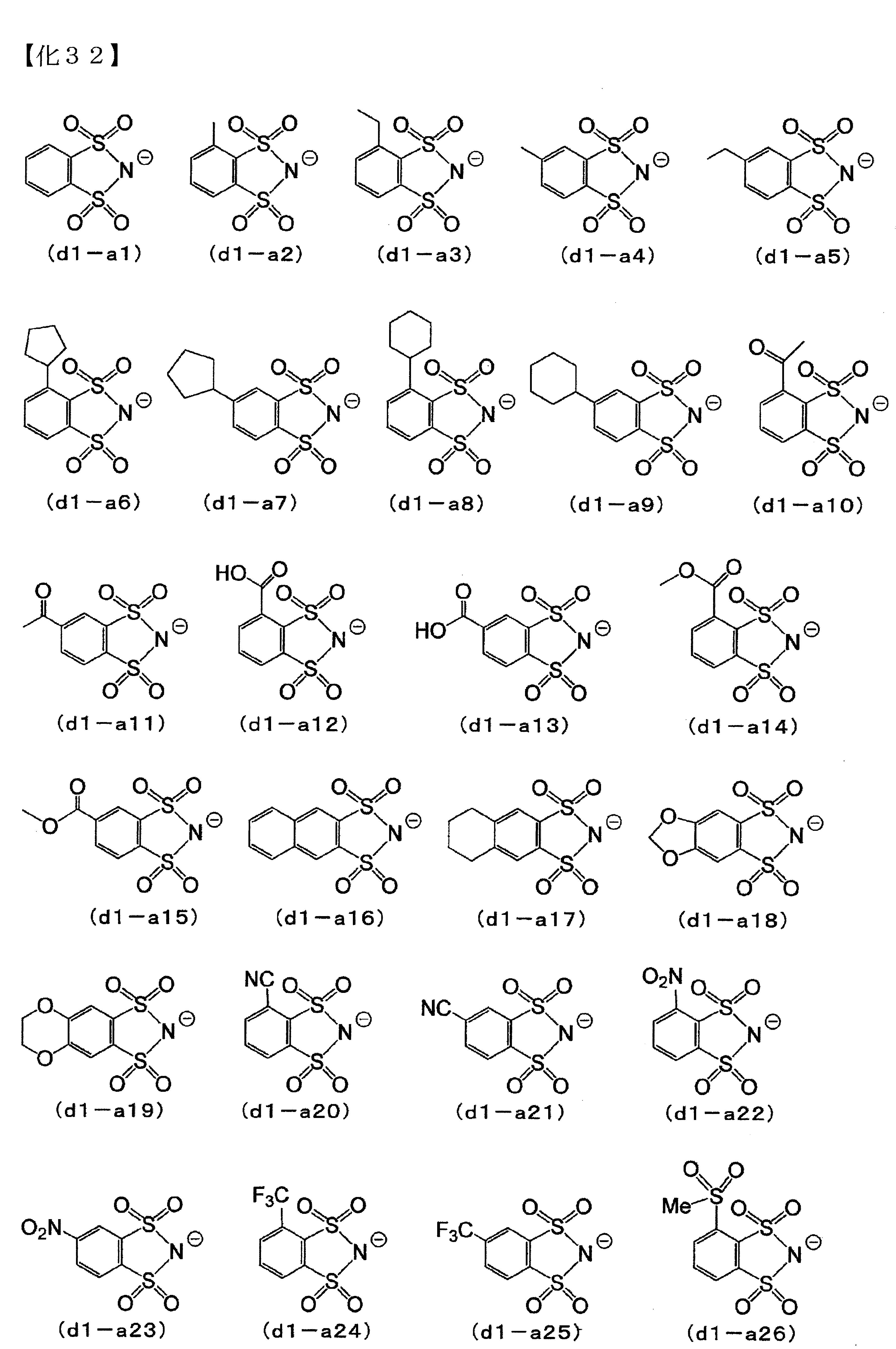
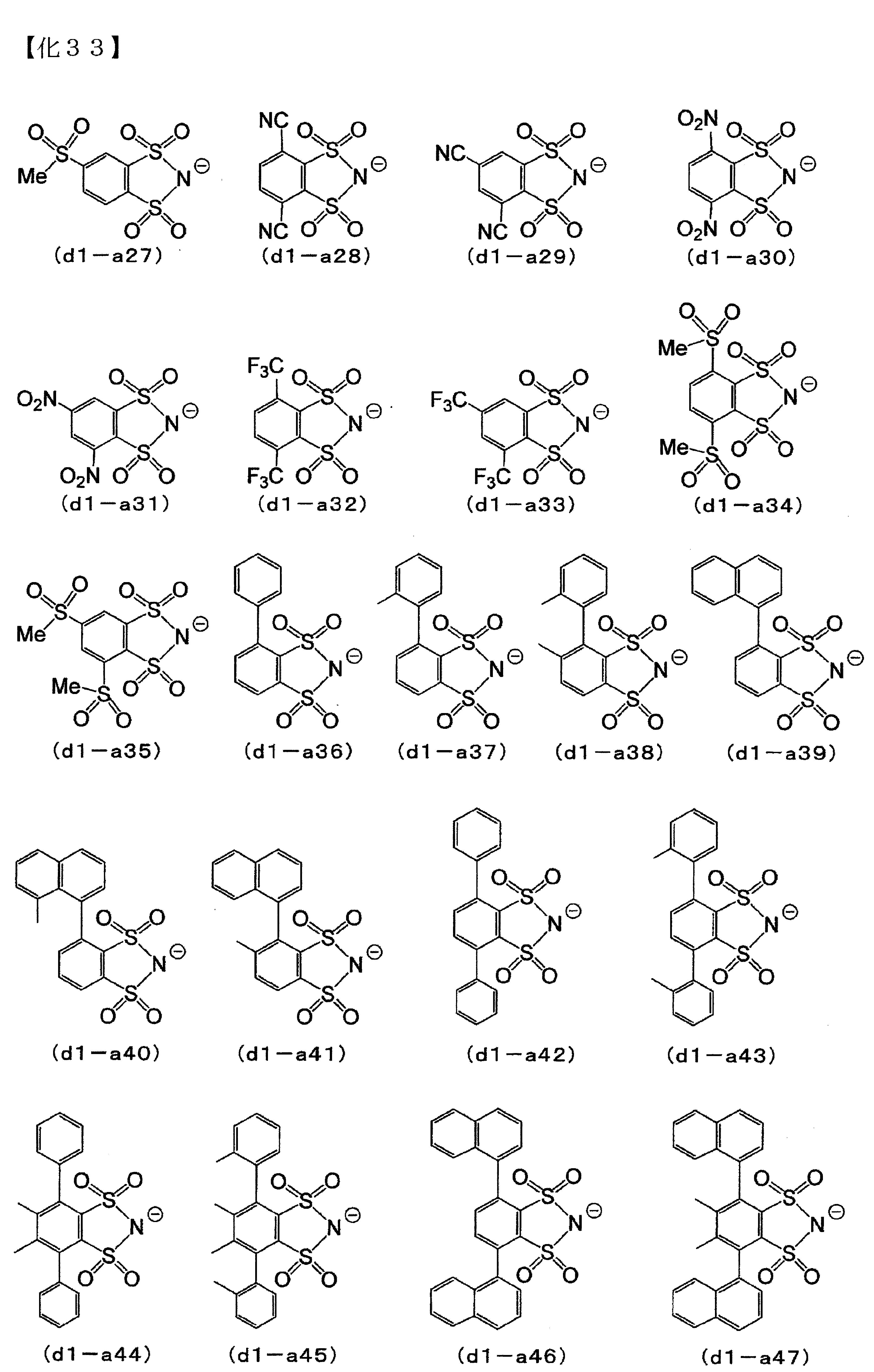
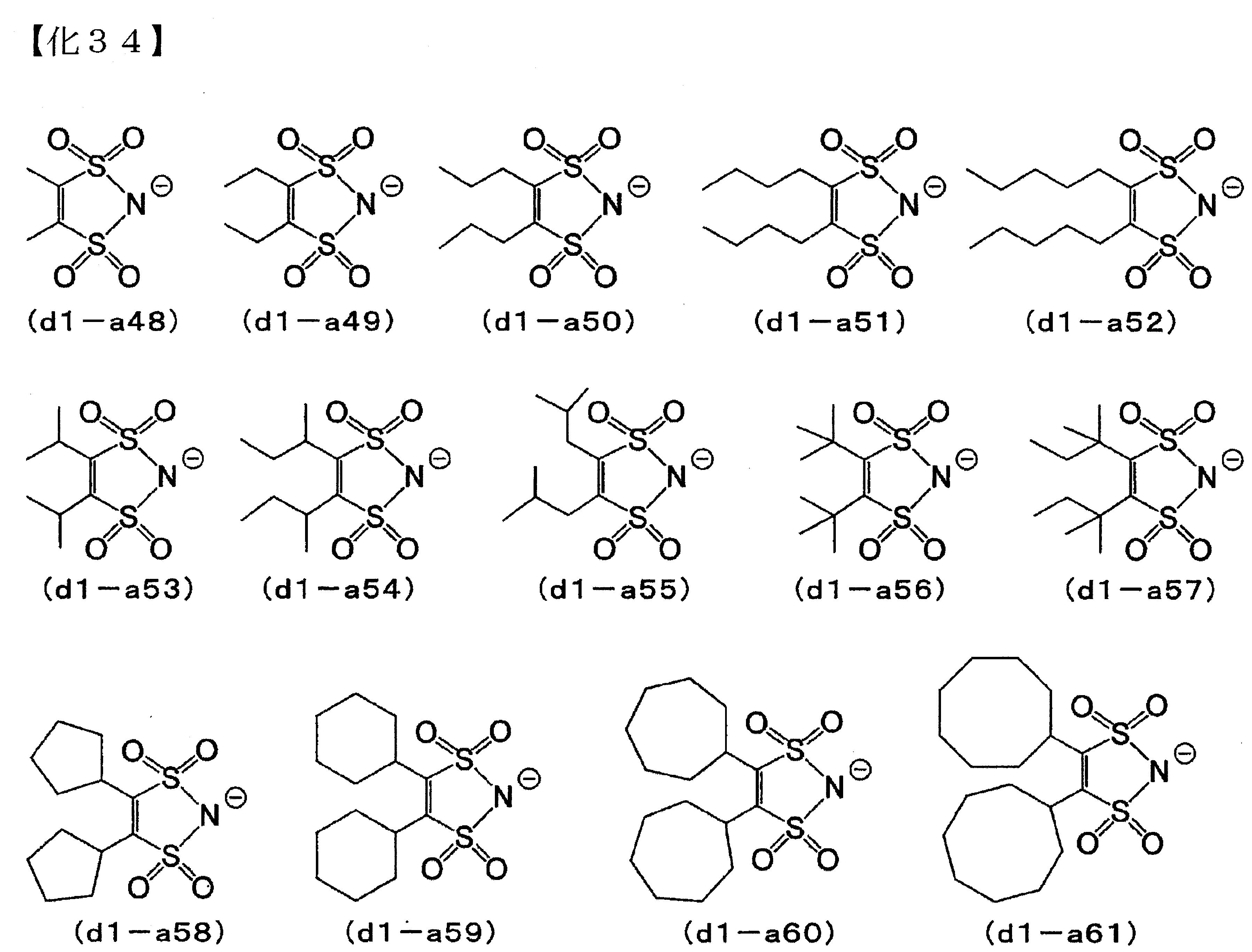
較佳的陰離子部,為由Rd01
與Rd02
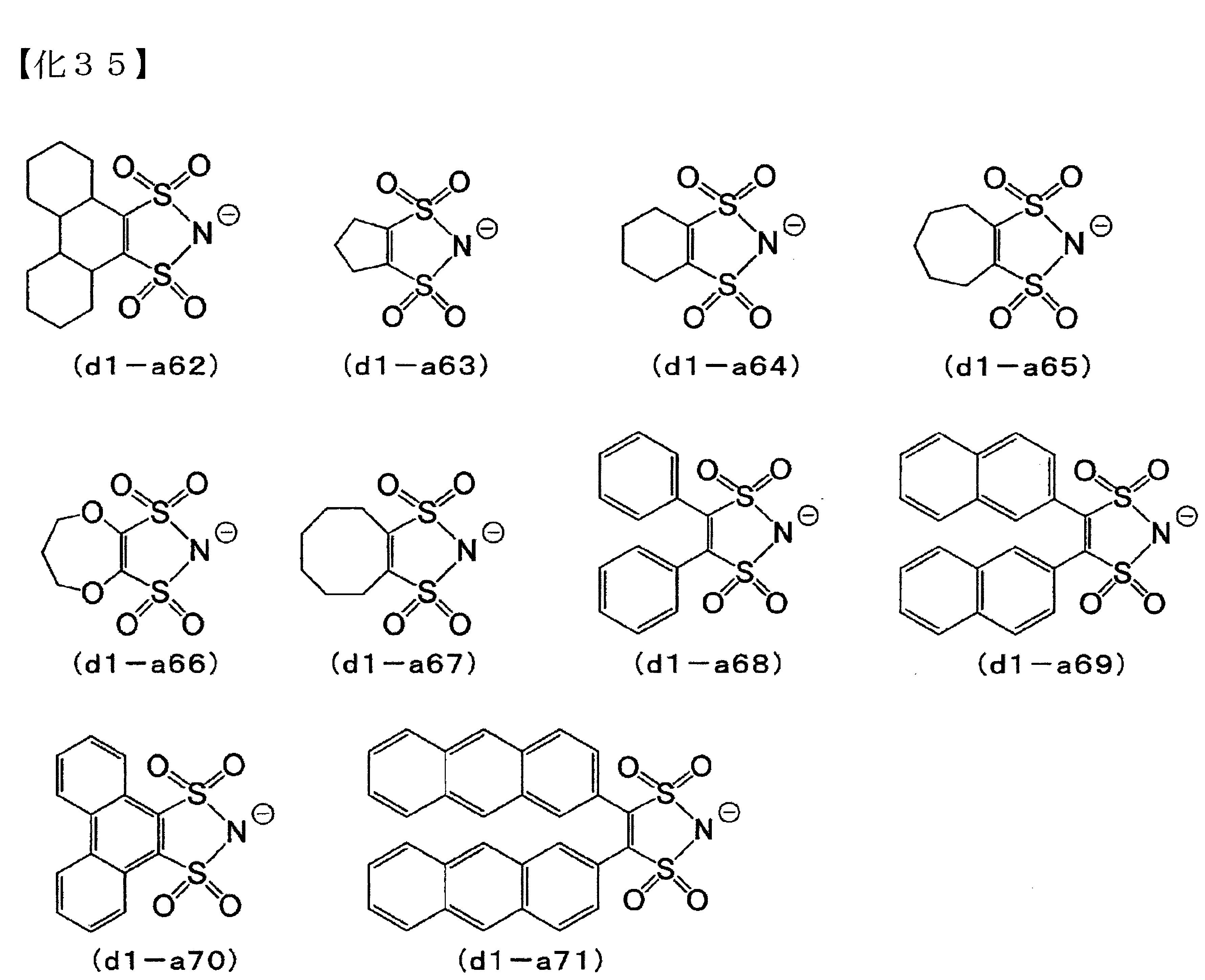
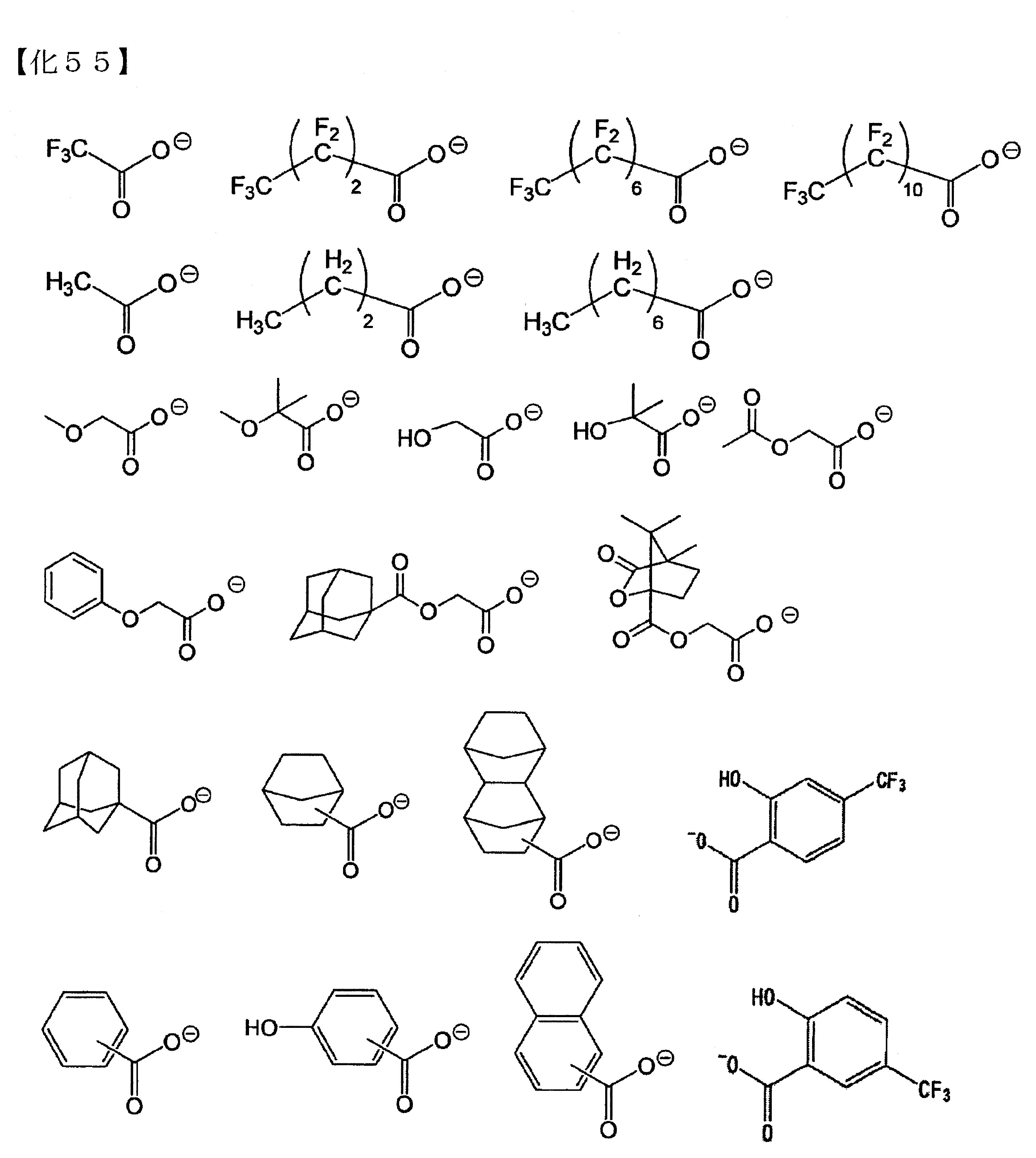
相互鍵結形成縮合環者,具體而言,例如,前述通式(d1-a)所表示之陰離子。 (D1)成份中的陰離子部之具體例,係如以下所列舉之內容。
≪(Mm+
)1/m
:陽離子部≫ 前述式(d1)中,Mm+
表示m價之有機陽離子。 Mm+
中之有機陽離子,以鎓陽離子為佳,以鋶陽離子、錪陽離子為較佳。m為1以上之整數。
較佳的(Mm+
)1/m
(陽離子部),例如,下述通式(ca-1)~(ca-4)所各別表示的有機陽離子等。
[式中,R201
~R207
,及R211
~R212
,各自獨立表示可具有取代基之芳基、烷基或烯基;R201
~R203
、R206
~R207
、R211
~R212
,可相互鍵結並與式中的硫原子共同形成環;R208
~R209
各自獨立表示氫原子或碳數1~5之烷基;R210
表示可具有取代基之芳基、可具有取代基之烷基、可具有取代基之烯基,或可具有取代基之含-SO2
-之環式基;L201
表示-C(=O)-或-C(=O)-O-;Y201
各自獨立表示伸芳基、伸烷基或伸烯基;x為1或2;W201
表示(x+1)價之連結基]。
R201
~R207
,及R211
~R212
中之芳基,例如碳數6~20之無取代的芳基,又以苯基、萘基為佳。 R201
~R207
,及R211
~R212
中之烷基,例如為鏈狀或環狀之烷基,且碳數以1~30者為佳。 R201
~R207
,及R211
~R212
中之烯基,以碳數2~10為佳。 R201
~R207
,及R210
~R212
所可具有的取代基,例如,烷基、鹵素原子、鹵化烷基、羰基、氰基、胺基、芳基、烷基磺醯基、下述通式(ca-r-1)~(ca-r-7)所各別表示的基等。
R’201
之可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基,除與後述式(b-1)中之R101
為相同之內容以外,又例如,可具有取代基之環式基或可具有取代基之鏈狀烷基,亦例如與上述式(a1-r-2)所表示之酸解離性基為相同之內容。
R201
~R203
、R206
~R207
、R211
~R212
,於相互鍵結並與式中的硫原子共同形成環時,亦可介由硫原子、氧原子、氮原子等的雜原子,或羰基、-SO-、-SO2
-、 -SO3
-、-COO-、-CONH-或-N(RN
)-(該RN
為碳數1~5之烷基)等的官能基予以鍵結。所形成之環中,式中的硫原子包含於該環骨架中的1個之環,包含硫原子,以3~10員環為佳,以5~7員環為特佳。所形成之環的具體例,例如噻吩環、噻唑環、苯併噻吩環、噻蒽環、苯併噻吩環、二苯併噻吩環、9H-硫
環、9-氧硫
環、噻蒽環、啡噁噻環、四氫噻吩鎓環、四氫硫代吡喃鎓環等。
R208
~R209
各自獨立表示氫原子或碳數1~5之烷基,又以氫原子或碳數1~3之烷基為佳,為烷基時,其可相互鍵結形成環。
R210
,例如,可具有取代基芳基、可具有取代基之烷基、可具有取代基之烯基,或可具有取代基之含-SO2
-之環式基。 R210
中之芳基,例如碳數6~20之無取代的芳基,又以苯基、萘基為佳。 R210
中之烷基,例如為鏈狀或環狀之烷基,且碳數以1~30者為佳。 R210
中之烯基,以碳數2~10為佳。 R210
中之可具有取代基之含-SO2
-之環式基,例如,以「含-SO2
-之多環式基」為佳,又以上述通式(a5-r-1)所表示之基為較佳。
Y201
各自獨立表示伸芳基、伸烷基或伸烯基。 Y201
中之伸芳基,例如,由後述式(b-1)中之R101
中之芳香族烴基所例示的芳基去除1個氫原子而得之基等。 Y201
中之伸烷基、伸烯基,例如,由後述式(b-1)中之R101
中之鏈狀烷基、鏈狀烯基所例示之基去除1個氫原子而得之基等。
前述式(ca-4)中,x為1或2。 W201
為(x+1)價,即2價或3價之連結基。 W201
中的2價之連結基,以可具有取代基之2價之烴基為佳,例如,與上述之通式(a2-1)中之Ya21
相同的可具有取代基之2價之烴基等。W201
中的2價之連結基,可為直鏈狀、支鏈狀、環狀之任一者皆可,又以環狀為佳。其中又以伸芳基的兩端組合2個羰基而得之基為佳。伸芳基,例如,伸苯基、伸萘基等,又以伸苯基為特佳。 W201
中的3價之連結基,例如,由前述W201
中的2價之連結基去除1個氫原子而得之基、前述2價之連結基再鍵結前述2價之連結基而得之基等。W201
中的3價之連結基,例如,以伸芳基鍵結2個羰基而得之基為佳。
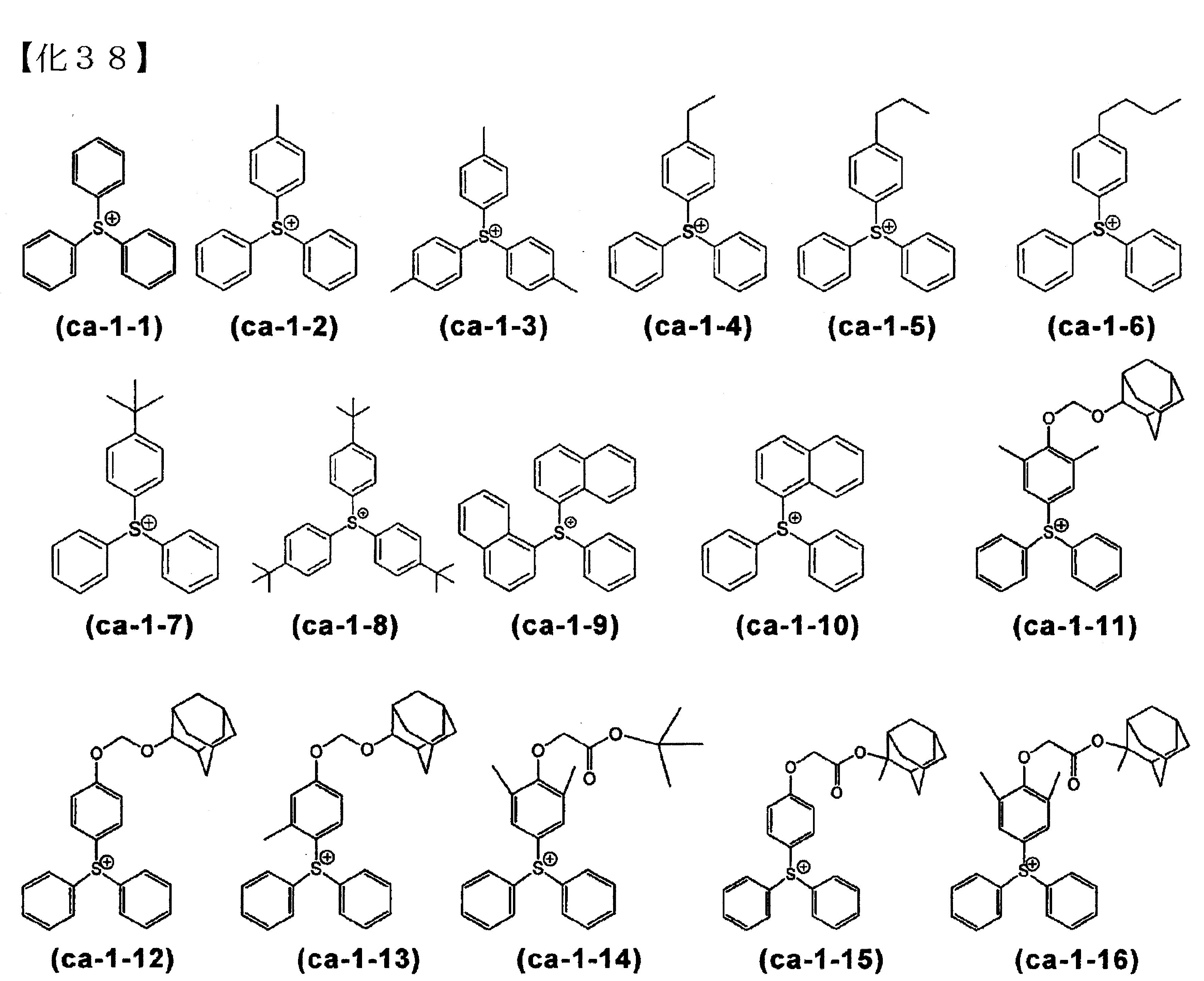
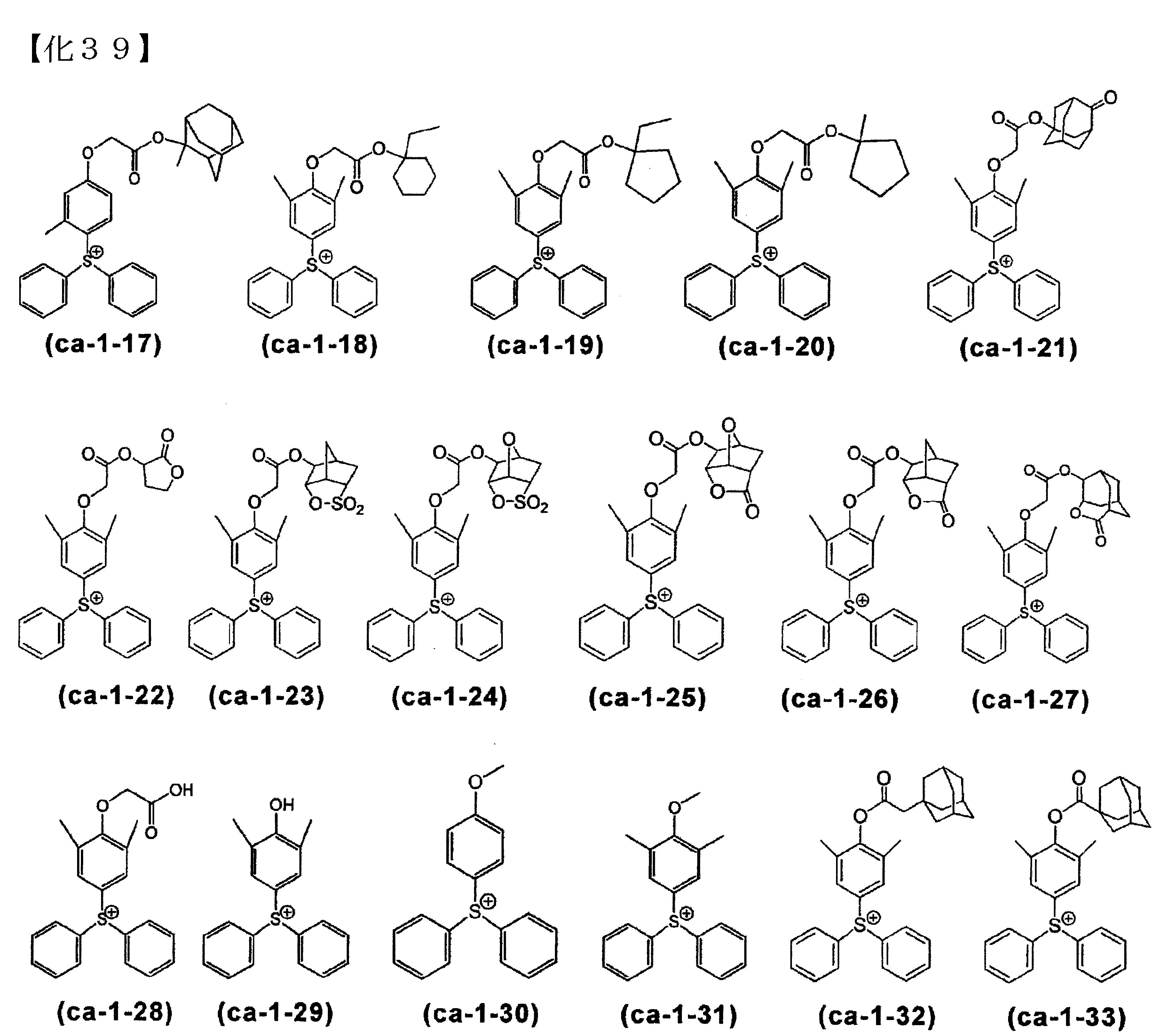
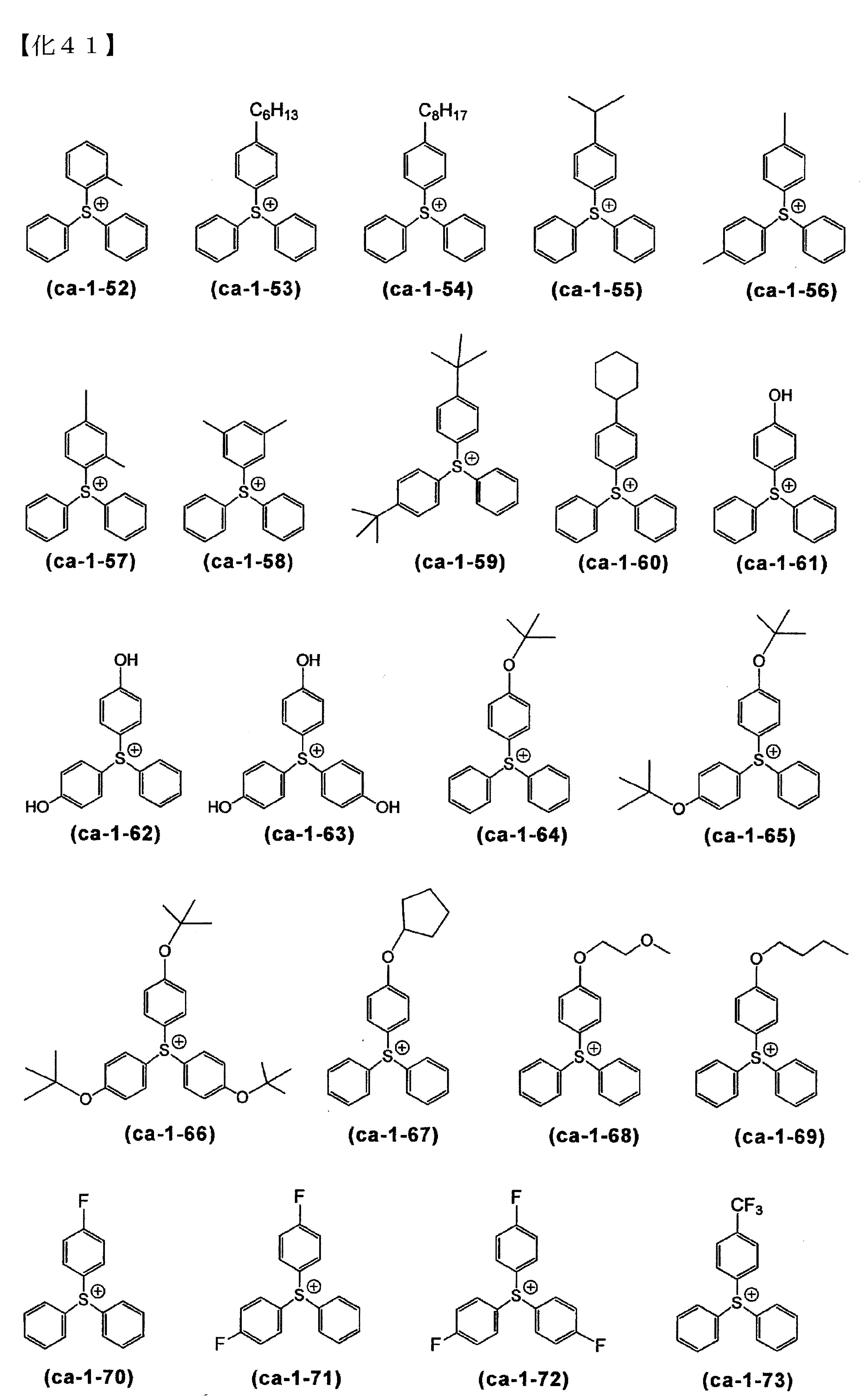
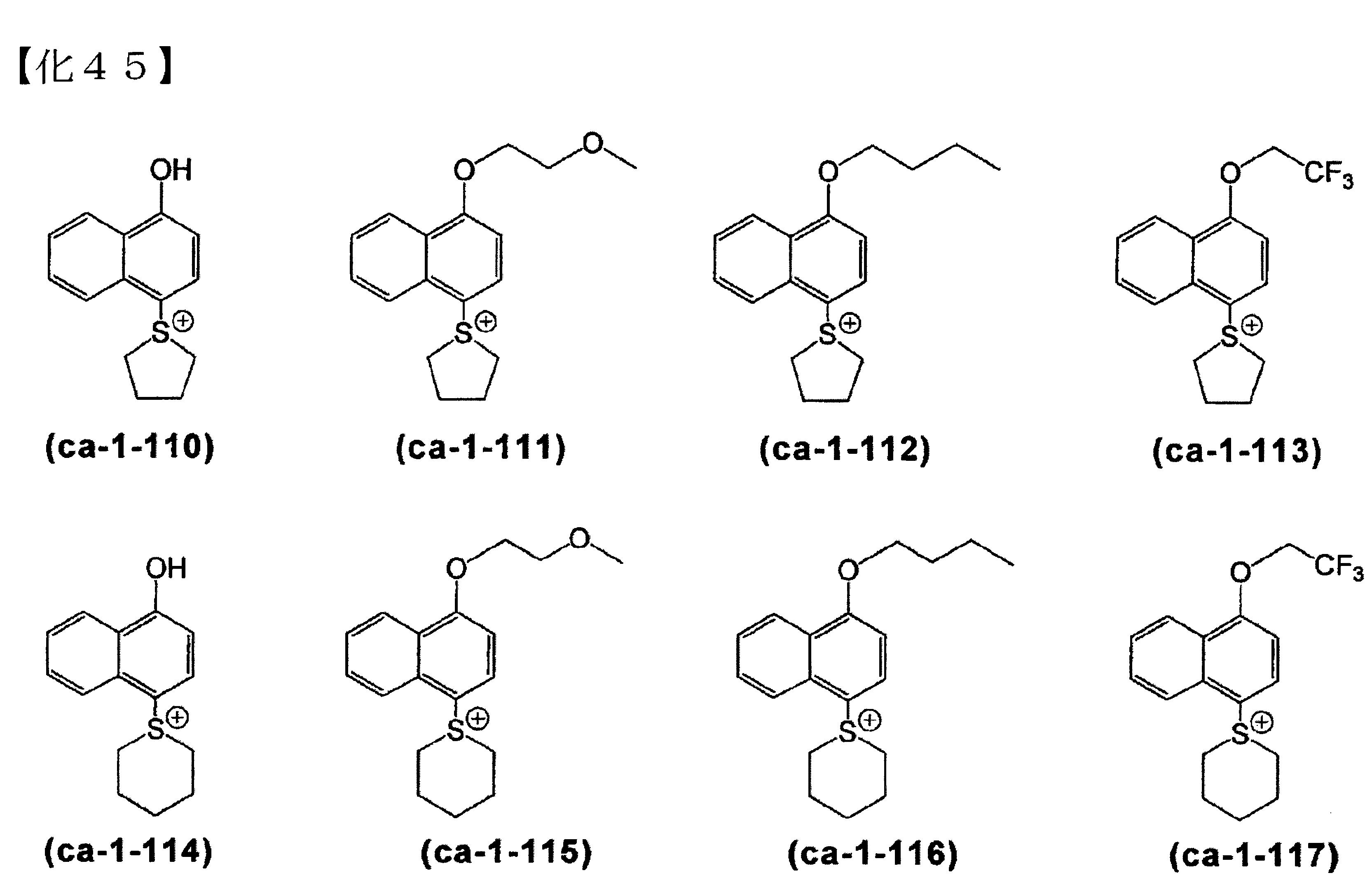
前述式(ca-1)所表示之較佳的陽離子,具體而言,例如下述式(ca-1-1)~(ca-1-127)所各別表示的陽離子等。
前述式(ca-2)所表示之較佳的陽離子,具體而言,例如,二苯基錪陽離子、雙(4-tert-丁苯基)錪陽離子等。
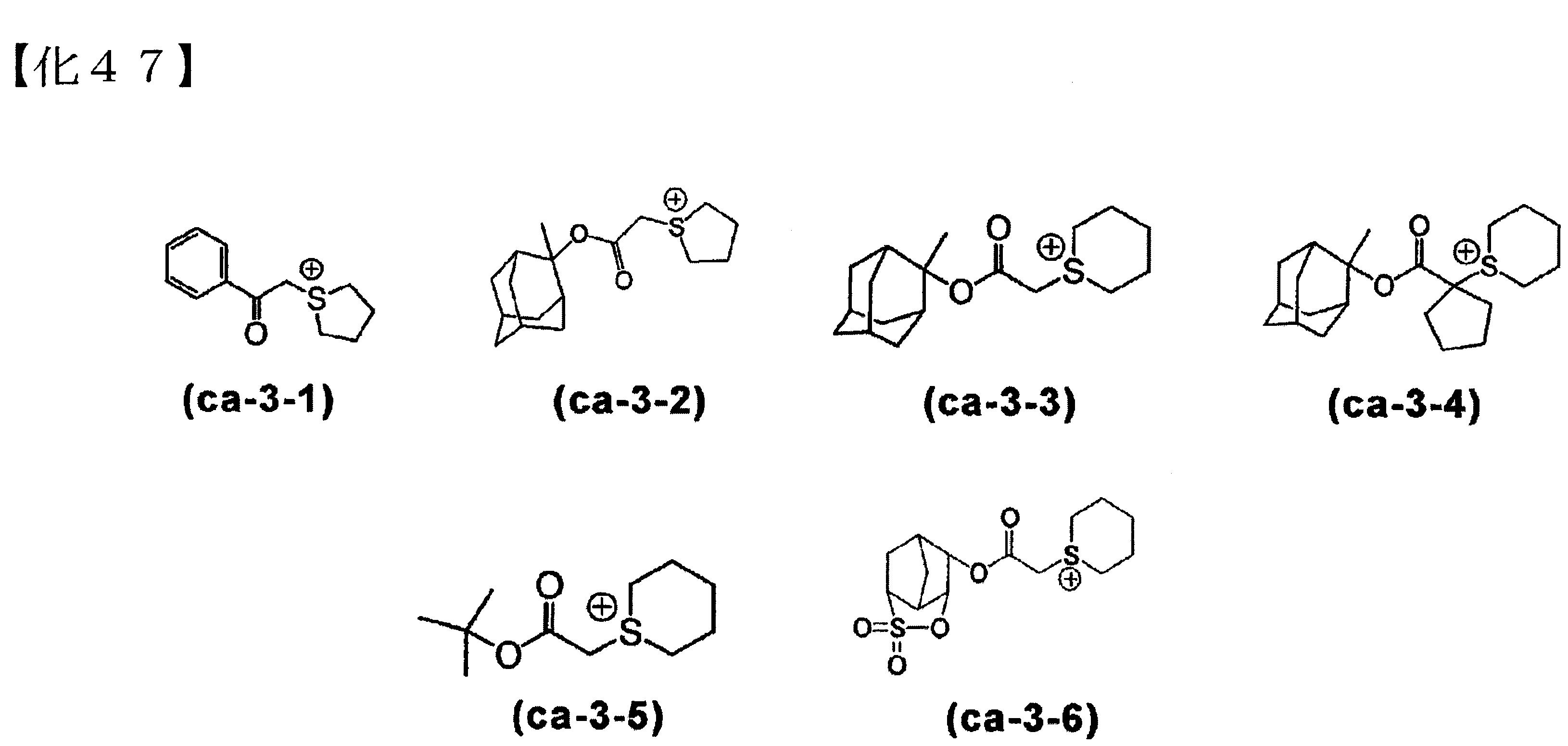
前述式(ca-3)所表示之較佳的陽離子,具體而言,例如下述式(ca-3-1)~(ca-3-6)所各別表示的陽離子等。
前述式(ca-4)所表示之較佳的陽離子,具體而言,例如下述式(ca-4-1)~(ca-4-2)所各別表示的陽離子等。
上述之中,(Mm+
)1/m
(陽離子部)又以通式(ca-1)所表示之陽離子為佳,以式(ca-1-1)~(ca-1-127)所各別表示的陽離子為較佳。
(D1)成份之共軛酸的酸解離常數(pKa),以1.10以下為佳,更佳為pKa為-2.0~1.0,特佳為pKa為-1.5~-0.5。 (D1)成份之共軛酸的pKa,於前述較佳範圍內時,可使本發明之效果更向上提升。
特別是,就更容易提升解析度及抑制圖型倒塌之效果的觀點,(D1)成份之共軛酸的pKa,以1.10以下為佳,更佳為pKa為1.0以下,特佳為pKa為-0.5以下。 又,就更容易改善圖型形狀及降低粗糙度之效果的觀點,(D1)成份之共軛酸的pKa,以1.10以下為佳,更佳為pKa為0.5以下,特佳為pKa為0以下。
本發明中,「酸解離常數(pKa)」為表示對象物質的酸強度之一般常用之指標。 該(D1)成份之共軛酸的pKa,可依通常方法進行測定而求得。又,亦可使用「ACD/Labs」(商品名、Advanced Chemistry Development公司製)等的公知軟體而得之計算值。
又,(D1)成份之辛醇/水分配係數(logPow
),以-0.90以上、2.00以下為佳,更佳為logPow
為-0.5~1.5,特佳為logPow
為0~0.5。 (D1)成份之logPow
為前述較佳範圍的下限值以上時,可使制圖型之倒塌受到更大抑制,而可使解析度再向上提升。另一方面,(D1)成份之logPow
為前述較佳範圍的上限值以下時,可使圖型的粗糙度更為降低,而容易形成良好形狀之阻劑圖型。
特別是就更加改善圖型形狀之觀點,(D1)成份之logPow
以-0.90以上為佳,更佳為logPow
為-0.5以上,特佳為logPow
為0以上,最佳為logPow
為0~1.5。
本發明中之「logPow
」,係為辛醇/水分配係數(Pow
)之對數值。「logPow
」,對於廣範圍之化合物,為可有效標記其親水性/疏水性特徴的參數。一般而言,為不經由實驗而由計算所求得之分配係數,於本發明中,為使用CS ChemDraw Ultra Ver.8.0 software package (Crippen’s fragmentation method)計算而得之值。 logPow
之值於包含0的正值側的數值越大時其疏水性越高,於負值側的絕對值越大時表示其水溶性越高之意。logPow
與有機化合物的水溶性形成負相關,而被廣泛地使用作為判斷有機化合物的親疏水性之參數。
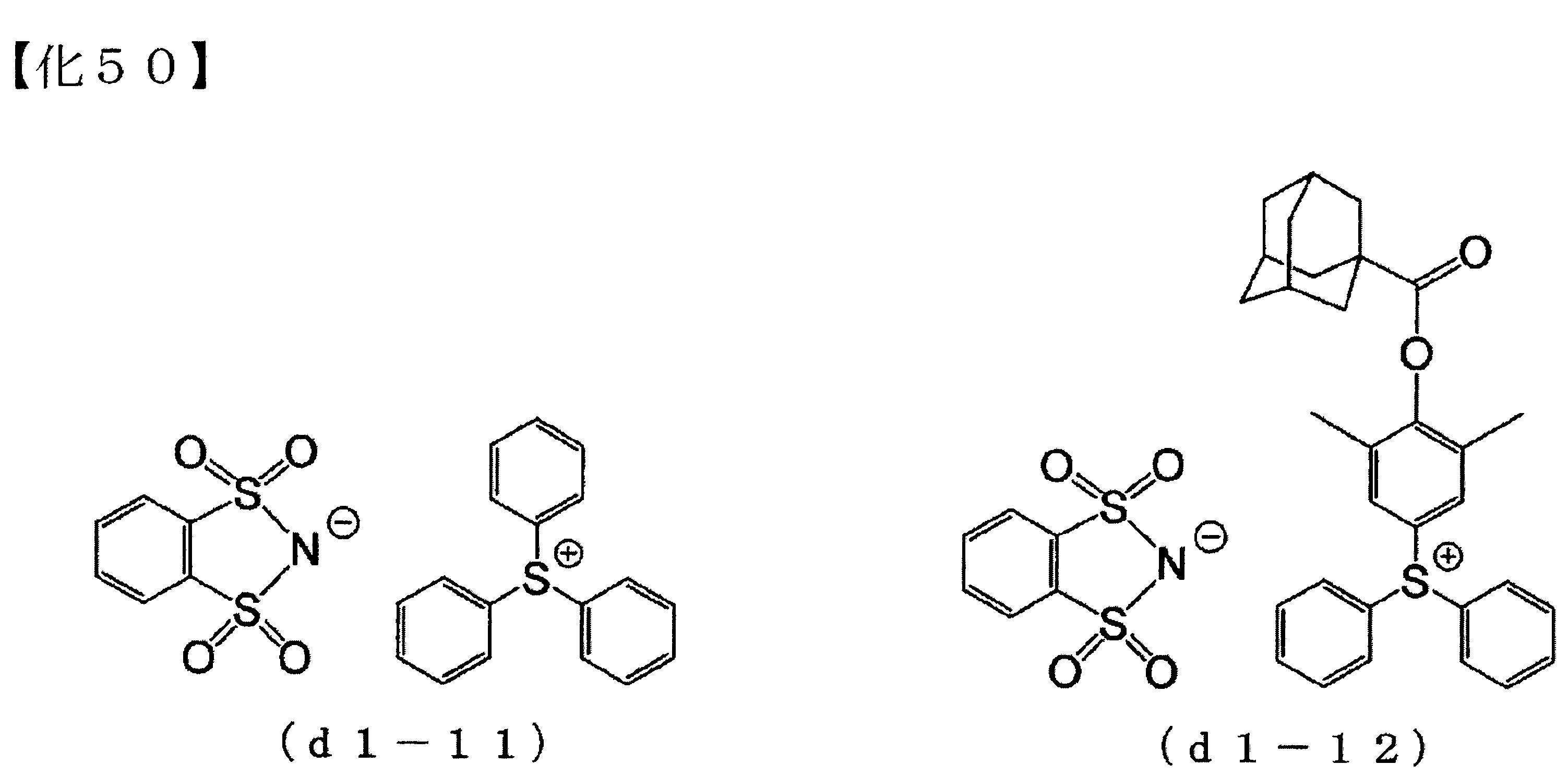
較佳的(D1)成份,例如,下述通式(d1-10)所表示之化合物等。
[式中,C01
及C02
分別表示碳原子。Rd012
為分別與C01
與C02
鍵結形成環構造之基,其與前述式(d1-a)中之C01
、C02
及Rd012
為相同之內容。R201
~R203
與前述式(ca-1)中之R201
~R203
為相同之內容]。
以下為較佳(D1)成份之具體例。 又,與具體例同時標記之pKa為使用「Software V11.02(1994-2013 ACD/Labs)」(商品名、Advanced Chemistry Development公司製)的計算值。logPow
為表示依上述方式而得之計算值。
本實施形態之阻劑組成物中,(D1)成份,可單獨使用1種亦可、將2種以上合併使用亦可。 本實施形態之阻劑組成物中,(D1)成份之含量,相對於(A)成份100質量份,以0.5~10質量份為佳,以0.5~8質量份為較佳,以1~8質量份為更佳。 (D1)成份之含量,為前述較佳範圍之下限值以上時,特別是可得到良好的解析度、低粗糙度、DOF特性等微影蝕刻特性及良好的阻劑圖型形狀。又,於前述較佳範圍的上限值以下時,可維持良好的感度,亦具有優良的產率。
<(B)成份> (B)成份為經由曝光而產生酸的酸產生劑成份(又,前述(D1)成份除外)。 (B)成份,並未有特別之限定,其可使用目前為止被提案作為化學增強型阻劑組成物用之酸產生劑者。 該些酸產生劑,可列舉如,錪鹽或鋶鹽等之鎓鹽系酸產生劑、肟磺酸酯系酸產生劑;雙烷基或雙芳基磺醯基重氮甲烷類、聚(雙磺醯基)重氮甲烷類等之重氮甲烷系酸產生劑;硝基苄基磺酸酯系酸產生劑、亞胺基磺酸酯系酸產生劑、二碸系酸產生劑等多種成份。該些之中,又以使用鎓鹽系酸產生劑為佳。
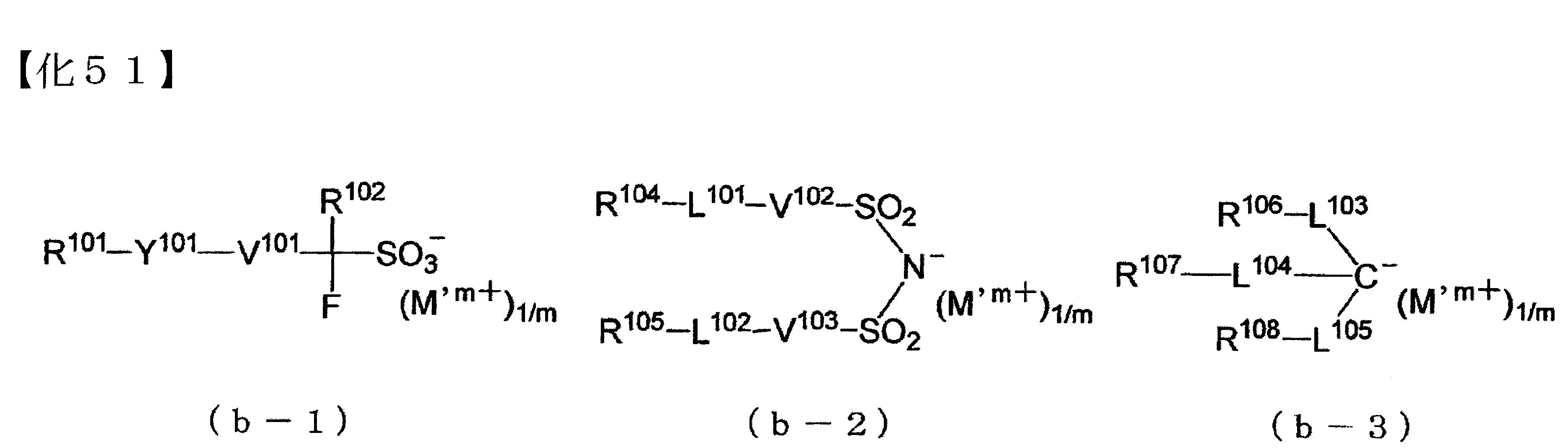
鎓鹽系酸產生劑,例如,下述通式(b-1)所表示之化合物(以下,亦稱為「(b-1)成份」)、通式(b-2)所表示之化合物(以下,亦稱為「(b-2)成份」)或通式(b-3)所表示之化合物(以下,亦稱為「(b-3)成份」)等。
[式中,R101
、R104
~R108
各自獨立為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基;R104
、R105
可相互鍵結形成環。 R102
為氟原子或碳數1~5之氟化烷基;Y101
為單鍵或含有氧原子的2價之連結基;V101
~V103
各自獨立為單鍵、伸烷基或氟化伸烷基;L101
~L102
各自獨立為單鍵或氧原子。L103
~L105
各自獨立為單鍵、-CO-或-SO2
-。m為1以上之整數,又,M’m+
為m價之鎓陽離子]。
{陰離子部} ・(b-1)成份之陰離子部 式(b-1)中,R101
為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基。
可具有取代基之環式基: 該環式基,以環狀之烴基為佳,該環狀之烴基,可為芳香族烴基亦可、脂肪族烴基亦可。脂肪族烴基,係指不具有芳香族性之烴基之意。又,脂肪族烴基,可為飽合者亦可、不飽合者亦可,通常以飽合者為佳。
R101
中之芳香族烴基,為具有芳香環之烴基;該芳香族烴基之碳數以3~30為佳,以5~30為較佳,5~20為較佳,以6~15為特佳,以6~10為最佳。又,該碳數為不包含取代基中之碳數者。 R101
中之芳香族烴基所具有的芳香環,具體而言,例如,苯、茀、萘、蒽、菲、聯苯,或構成該些芳香環的碳原子中之一部份被雜原子所取代之芳香族雜環等。芳香族雜環中之雜原子,例如,氧原子、硫原子、氮原子等。 R101
中之芳香族烴基,具體而言,例如,由前述芳香環去除1個氫原子而得之基(芳基:例如,苯基、萘基等)、前述芳香環中之1個氫原子被伸烷基所取代之基(例如,苄基、苯乙基、1-萘甲基、2-萘甲基、1-萘乙基、2-萘乙基等的芳烷基等)等。前述伸烷基(芳烷基中之烷鏈)之碳數,以1~4為佳,以1~2為較佳,以1為特佳。
R101
中之環狀之脂肪族烴基,例如,構造中含有環之脂肪族烴基。 該構造中含有環之脂肪族烴基,例如,脂環式烴基(脂肪族烴環去除1個氫原子而得之基)、脂環式烴基鍵結於直鏈狀或支鏈狀脂肪族烴基的末端之基、脂環式烴基介於直鏈狀或支鏈狀脂肪族烴基的中間之基等。 前述脂環式烴基,以碳數3~20為佳,以3~12為較佳。 前述脂環式烴基,可為多環式基亦可、單環式基亦可。單環式之脂環式烴基,以由單環鏈烷去除1個以上的氫原子而得之基為佳。該單環鏈烷,以碳數3~6者為佳,具體而言,例如,環戊烷、環己烷等。多環式之脂環式烴基,又以由多環鏈烷去除1個以上的氫原子而得之基為佳,該多環鏈烷,以碳數7~30者為佳。其中,該多環鏈烷,又以金剛烷、降莰烷、異莰烷、三環癸烷、四環十二烷等的具有交聯環系的多環式骨架之多環鏈烷;具有膽固醇骨架的環式基等的具有縮合環系的多環式骨架之多環鏈烷為較佳。
其中,R101
中之環狀之脂肪族烴基,以由單環鏈烷或多環鏈烷去除1個以上的氫原子而得之基為佳,以由多環鏈烷去除1個氫原子而得之基為較佳,以金剛烷基、降莰基為特佳,以金剛烷基為最佳。
可與脂環式烴基鍵結之直鏈狀或支鏈狀之脂肪族烴基,以碳數1~10為佳,以1~6為較佳,以1~4為較佳,以1~3為最佳。 直鏈狀之脂肪族烴基,以直鏈狀之伸烷基為佳,具體而言,例如,伸甲基[-CH2
-]、伸乙基[-(CH2
)2
-]、伸三甲基[-(CH2
)3
-]、伸四甲基[-(CH2
)4
-]、伸五甲基[-(CH2
)5
-]等。 支鏈狀之脂肪族烴基,以支鏈狀之伸烷基為佳,具體而言,例如,-CH(CH3
)-、-CH(CH2
CH3
)-、-C(CH3
)2
-、 -C(CH3
)(CH2
CH3
)-、-C(CH3
)(CH2
CH2
CH3
)-、-C(CH2
CH3
)2
-等之烷基伸甲基;-CH(CH3
)CH2
-、-CH(CH3
)CH(CH3
)-、 -C(CH3
)2
CH2
-、-CH(CH2
CH3
)CH2
-、-C(CH2
CH3
)2
-CH2
-等之烷基伸乙基;-CH(CH3
)CH2
CH2
-、-CH2
CH(CH3
)CH2
-等之烷基伸三甲基;-CH(CH3
)CH2
CH2
CH2
-、 -CH2
CH(CH3
)CH2
CH2
-等之烷基伸四甲基等之烷基伸烷基等。烷基伸烷基中之烷基,以碳數1~5之直鏈狀烷基為佳。
又,R101
中之環狀之烴基,可含有雜環等的雜原子。具體而言,例如,前述通式(a2-r-1)~(a2-r-7)所各別表示的含內酯之環式基、前述通式(a5-r-1)~(a5-r-4)所各別表示的含-SO2
-之環式基、其他上述之化學式(r-hr-1)~(r-hr-16)所各別表示的雜環式基等。
R101
之環式基中之取代基,例如,烷基、烷氧基、鹵素原子、鹵化烷基、羥基、羰基、硝基等。 作為取代基之烷基,例如,碳數1~12之烷基為佳,甲基、乙基、丙基、n-丁基、tert-丁基為最佳。 作為取代基之烷氧基,以碳數1~5之烷氧基為佳,以甲氧基、乙氧基、n-丙氧基、iso-丙氧基、n-丁氧基、tert-丁氧基為較佳,以甲氧基、乙氧基為最佳。 作為取代基之鹵素原子,可列舉如,氟原子、氯原子、溴原子、碘原子等,又以氟原子為佳。 作為取代基之鹵化烷基,例如,碳數1~5之烷基,例如甲基、乙基、丙基、n-丁基、tert-丁基等中的氫原子之一部份或全部被前述鹵素原子所取代之基等。 作為取代基之羰基,為取代構成環狀烴基的伸甲基 (-CH2
-)之基。
可具有取代基之鏈狀烷基: R101
之鏈狀烷基,可為直鏈狀或支鏈狀之任一者。 直鏈狀烷基,例如,以碳數1~20為佳,以1~15為較佳,以1~10為最佳。具體而言,例如,甲基、乙基、丙基、丁基、戊基、己基、庚基、辛基、壬基、癸基、十一烷基、十二烷基、十三烷基、異十三烷基、十四烷基、十五烷基、十六烷基、異十六烷基、十七烷基、十八烷基、十九烷基、二十烷基、二十一烷基、二十二烷基等。 支鏈狀烷基,以碳數3~20為佳,以3~15為較佳,以3~10為最佳。具體而言,例如,1-甲乙基、1-甲基丙基、2-甲基丙基、1-甲基丁基、2-甲基丁基、3-甲基丁基、1-乙基丁基、2-乙基丁基、1-甲基戊基、2-甲基戊基、3-甲基戊基、4-甲基戊基等。
可具有取代基之鏈狀烯基: R101
之鏈狀烯基,例如,可為直鏈狀或支鏈狀之任一者,又以碳數2~10為佳,以2~5為較佳,以2~4為較佳,以3為特佳。直鏈狀烯基,例如,乙烯基、丙烯基(烯丙基)、丁烯基等。支鏈狀烯基,例如,1-甲基乙烯基、2-甲基乙烯基、1-甲基丙烯基、2-甲基丙烯基等。 鏈狀烯基,於上述之中,以直鏈狀烯基為佳,以乙烯基、丙烯基為較佳,以乙烯基為特佳。
R101
之鏈狀烷基或烯基中之取代基,例如,烷氧基、鹵素原子、鹵化烷基、羥基、羰基、硝基、胺基、上述R101
中之環式基等。
上述之中,R101
又以可具有取代基之環式基為佳,以可具有取代基之環狀之烴基為較佳。更具體而言,例如,以苯基、萘基、由多環鏈烷去除1個以上的氫原子而得之基;前述通式(a2-r-1)~(a2-r-7)所各別表示的含內酯之環式基;前述通式(a5-r-1)~(a5-r-4)所各別表示的含-SO2
-之環式基等為佳。
式(b-1)中,Y101
為單鍵或含有氧原子的2價之連結基。 Y101
為含有氧原子的2價連結基時,該Y101
可含有氧原子以外之原子。氧原子以外之原子,例如碳原子、氫原子、硫原子、氮原子等。 含有氧原子的2價之連結基,例如,氧原子(醚鍵結:-O-)、酯鍵結(-C(=O)-O-)、氧羰基(-O-C(=O)-)、醯胺鍵結(-C(=O)-NH-)、羰基(-C(=O)-)、碳酸酯鍵結(-O-C(=O)-O-)等的含非烴系的氧原子之連結基;該含非烴系的氧原子之連結基與伸烷基之組合等。該組合中,可再連結磺醯基(-SO2
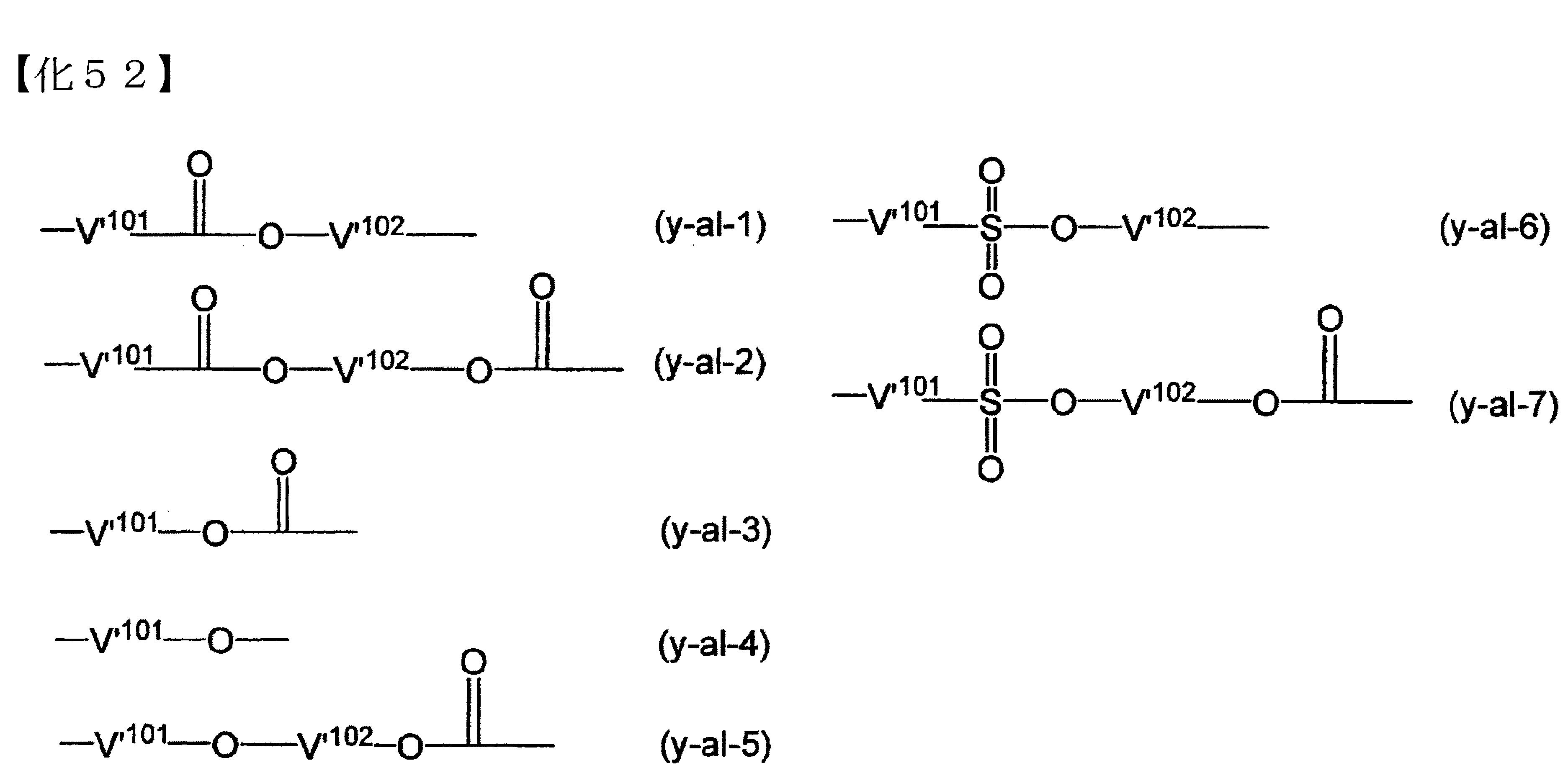
-)。該含有氧原子的2價之連結基,例如下述通式(y-al-1)~(y-al-7)所各別表示的連結基等。
V’102
中的2價之飽合烴基,以碳數1~30之伸烷基為佳,以碳數1~10之伸烷基為較佳,以碳數1~5之伸烷基為更佳。
V’101
及V’102
中之伸烷基,可為直鏈狀之伸烷基亦可、支鏈狀之伸烷基亦可,又以直鏈狀之伸烷基為佳。 V’101
及V’102
中之伸烷基,具體而言,例如,伸甲基 [-CH2
-];-CH(CH3
)-、-CH(CH2
CH3
)-、-C(CH3
)2
-、 -C(CH3
)(CH2
CH3
)-、-C(CH3
)(CH2
CH2
CH3
)-、-C(CH2
CH3
)2
-等之烷基伸甲基;伸乙基[-CH2
CH2
-];-CH(CH3
)CH2
-、 -CH(CH3
)CH(CH3
)-、-C(CH3
)2
CH2
-、-CH(CH2
CH3
)CH2
-等之烷基伸乙基;伸三甲基(n-伸丙基)[-CH2
CH2
CH2
-]; -CH(CH3
)CH2
CH2
-、-CH2
CH(CH3
)CH2
-等之烷基伸三甲基;伸四甲基[-CH2
CH2
CH2
CH2
-]; -CH(CH3
)CH2
CH2
CH2
-、-CH2
CH(CH3
)CH2
CH2
-等之烷基伸四甲基;伸五甲基[-CH2
CH2
CH2
CH2
CH2
-]等。 又,V’101
或V’102
中,前述伸烷基中之一部份的伸甲基,可被碳數5~10的2價之脂肪族環式基所取代。該脂肪族環式基,以由前述式(a1-r-1)中之Ra’3
之環狀之脂肪族烴基(單環式之脂肪族烴基、多環式之脂肪族烴基)再去除1個氫原子而得的2價之基為佳,以伸環己基、1,5-伸金剛烷基或2,6-伸金剛烷基為較佳。
Y101
,以含有酯鍵結的2價之連結基,或含有醚鍵結的2價之連結基為佳,以上述式(y-al-1)~(y-al-5)所各別表示的連結基為較佳。
式(b-1)中,V101
為單鍵、伸烷基或氟化伸烷基;V101
中之伸烷基、氟化伸烷基,以碳數1~4者為佳。V101
中之氟化伸烷基,例如,V101
中之伸烷基的氫原子之一部份或全部被氟原子所取代之基等。其中,V101
又以單鍵,或碳數1~4之氟化伸烷基為佳。
式(b-1)中,R102
為氟原子或碳數1~5之氟化烷基;R102
以氟原子或碳數1~5之全氟烷基為佳,以氟原子為較佳。
(b-1)成份之陰離子部之具體例,例如,Y101
為單鍵時,例如,三氟甲烷磺酸酯陰離子或全氟丁烷磺酸酯陰離子等之氟化烷基磺酸酯陰離子等;Y101
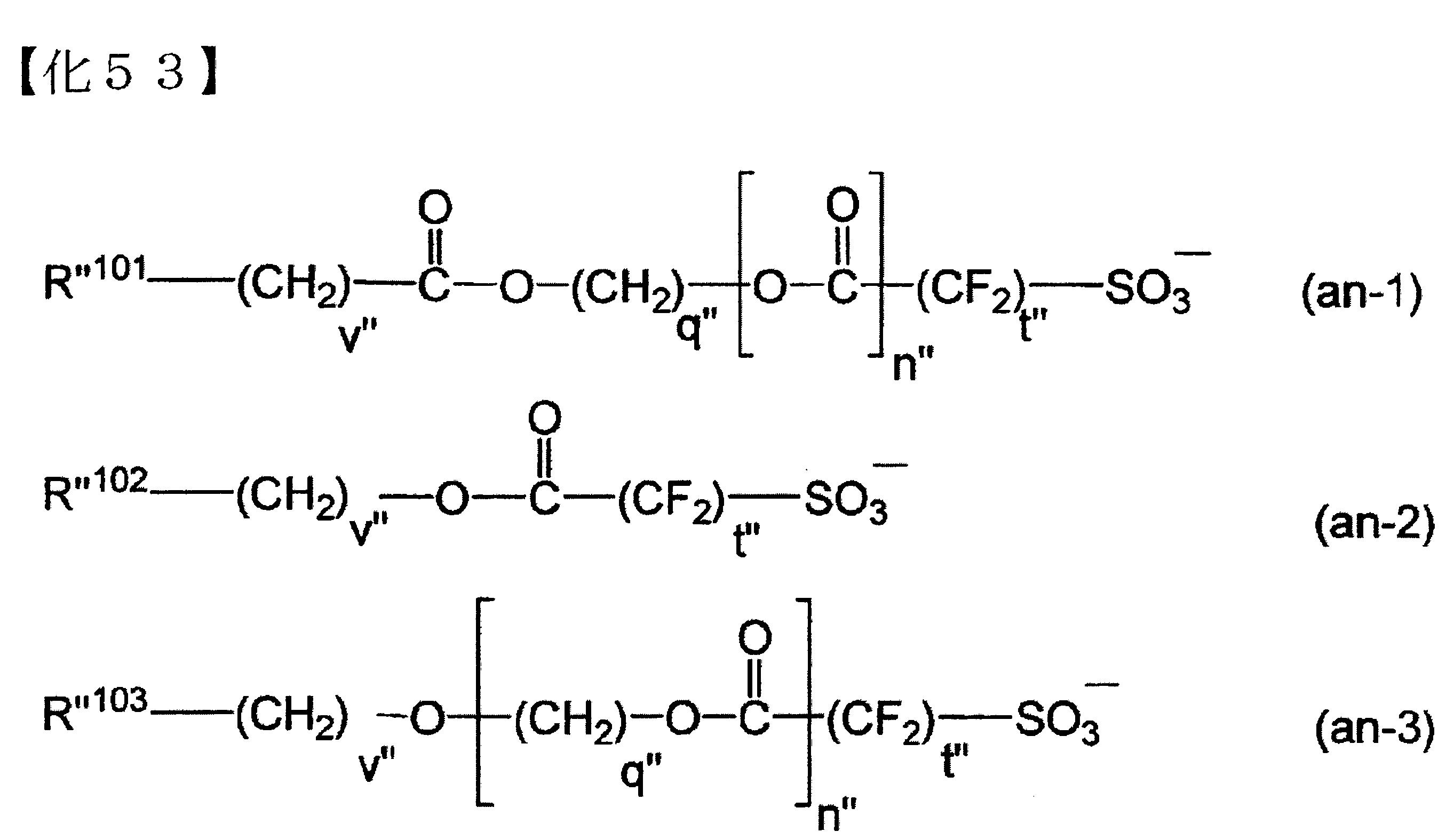
為含有氧原子的2價連結基時,例如,下述式(an-1)~(an-3)之任一者所表示之陰離子等。
[式中,R”101
為可具有取代基脂肪族環式基、前述式(r-hr-1)~(r-hr-6)所各別表示的基,或可具有取代基之鏈狀烷基;R”102
為可具有取代基脂肪族環式基、前述通式(a2-r-1)~(a2-r-7)所各別表示的含內酯之環式基,或前述通式(a5-r-1)~(a5-r-4)所各別表示的含-SO2
-之環式基;R”103
為可具有取代基芳香族環式基、可具有取代基之脂肪族環式基,或可具有取代基之鏈狀烯基;v”各自獨立為0~3之整數,q”各自獨立為1~20之整數,t”為1~3之整數,n”為0或1]。
R”101
、R”102
及R”103
的可具有取代基之脂肪族環式基,以前述R101
中之環狀之脂肪族烴基所例示之基為佳。前述取代基,例如,與可取代R101
中之環狀之脂肪族烴基的取代基為相同之內容等。
R”103
中之可具有取代基之芳香族環式基,以前述R101
中之環狀之烴基中之芳香族烴基所例示之基為佳。前述取代基,例如,與可取代R101
中之該芳香族烴基的取代基為相同之內容等。
R”101
中之可具有取代基之鏈狀烷基,以前述R101
中之鏈狀烷基所例示之基為佳。R”103
中之可具有取代基之鏈狀烯基,以前述R101
中之鏈狀烯基所例示之基為佳。
・(b-2)成份之陰離子部 式(b-2)中,R104
、R105
各自獨立為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基,其分別與式(b-1)中之R101
為相同之內容等。其中,R104
、R105
可相互鍵結形成環。 R104
、R105
,以可具有取代基鏈狀烷基為佳,以直鏈狀或支鏈狀烷基,或直鏈狀或支鏈狀之氟化烷基為較佳。 該鏈狀烷基之碳數,以1~10為佳,更佳為碳數1~7,特佳為碳數1~3。R104
、R105
之鏈狀烷基之碳數,於上述碳數之範圍內,基於對阻劑用溶劑具有良好溶解性等的理由,以越小越好。又,R104
、R105
之鏈狀烷基中,被氟原子取代的氫原子數越多時,其酸的強度越強,又,就可提高對於200nm以下的高能量光或電子線的透明性之觀點為較佳。 前述鏈狀烷基中的氟原子之比例,即氟化率,較佳為70~100%,特佳為90~100%,最佳為全部的氫原子被氟原子取代而得的全氟烷基。 式(b-2)中,V102
、V103
各自獨立為單鍵、伸烷基,或氟化伸烷基,其分別與式(b-1)中之V101
為相同之內容等。 式(b-2)中,L101
、L102
,各自獨立為單鍵或氧原子。
・(b-3)成份之陰離子部 式(b-3)中,R106
~R108
各自獨立為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基,其分別與式(b-1)中之R101
為相同之內容等。 L103
~L105
各自獨立為單鍵、-CO-或-SO2
-。
{陽離子部} 式(b-1)、(b-2)及(b-3)中,m為1以上之整數,又,M’m+
為m價之鎓陽離子,又以鋶陽離子、錪陽離子為較佳之例示,例如上述之通式(ca-1)~(ca-4)所各別表示的有機陽離子等。
上述式(ca-1)所表示之較佳的陽離子,具體而言,可列舉如,上述式(ca-1-1)~(ca-1-127)所各別表示的陽離子。
上述式(ca-2)所表示之較佳的陽離子,具體而言,可列舉如,二苯基錪陽離子、雙(4-tert-丁苯基)錪陽離子等。
上述式(ca-3)所表示之較佳的陽離子,具體而言,可列舉如,上述式(ca-3-1)~(ca-3-6)所各別表示的陽離子。
上述式(ca-4)所表示之較佳的陽離子,具體而言,可列舉如,上述式(ca-4-1)~(ca-4-2)所各別表示的陽離子。
上述之中,陽離子部[(M’m+
)1/m
],以通式(ca-1)所表示之陽離子為佳,以式(ca-1-1)~(ca-1-127)所各別表示的陽離子為較佳。
本實施形態之阻劑組成物中,(B)成份,可單獨使用1種亦可、將2種以上合併使用亦可。 本實施形態之阻劑組成物中,(B)成份之含量相對於(A)成份100質量份,以0.5~60質量份為佳,以1~50質量份為較佳,以1~40質量份為更佳。 (B)成份之含量於上述範圍時,可充份進行圖型之形成。又,阻劑組成物之各成份於溶解於有機溶劑之際,可容易得到均勻的溶液,作為阻劑組成物時具有良好的保存穩定性等,而為較佳。
<任意成份> 本實施形態之阻劑組成物,可再含有上述(A)成份、(D1)成份及(B)成份以外的成份(任意成份)。 該任意成份,例如,以下所示之(D2)成份、(E)成份、(F)成份、(S)成份等。
≪(D2)成份:酸擴散控制劑成份≫ 本實施形態之阻劑組成物,於無損本發明效果之範圍,可含有(D1)成份以外的酸擴散控制劑成份(以下,亦稱為「(D2)成份」)。 (D2)成份,於阻劑組成物中,為具有作為捕集因曝光而產生之酸的抑制劑之作用者。 (D2)成份,可為經由曝光而分解而喪失酸擴散控制性的光崩壞性鹼(D21)(以下,亦稱為「(D21)成份」)、不相當於該(D21)成份之含氮有機化合物(D22)(以下,亦稱為「(D22)成份」)亦可。
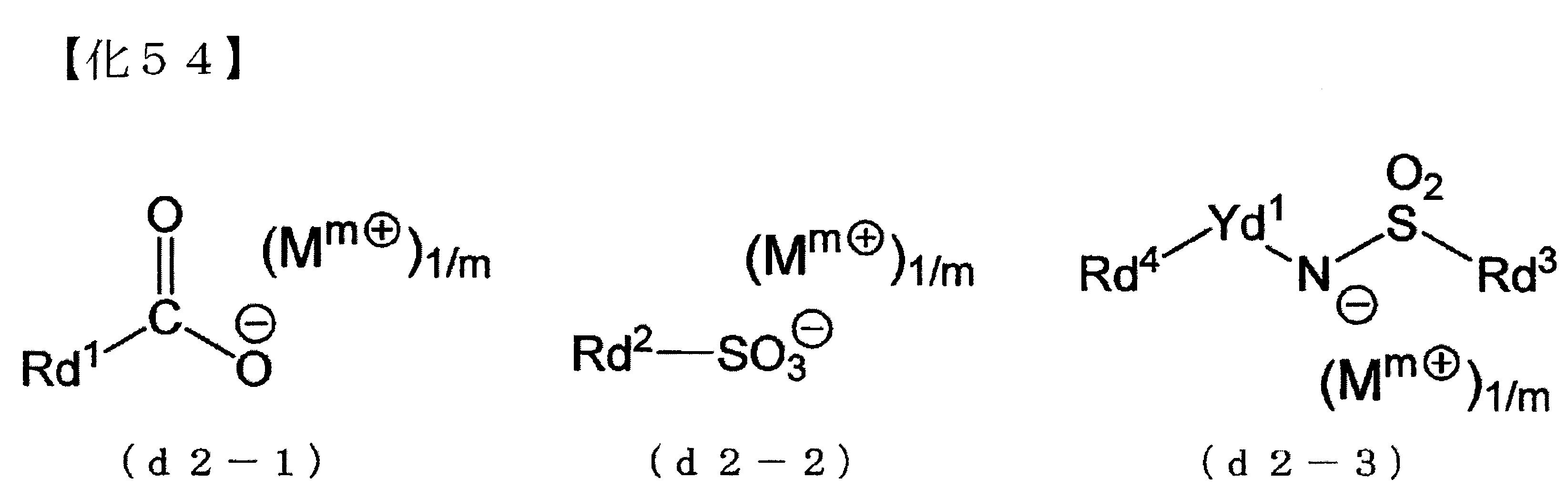
・(D21)成份 (D21)成份,以由下述通式(d2-1)所表示之化合物(以下,亦稱為「(d2-1)成份」)、下述通式(d2-2)所表示之化合物(以下,亦稱為「(d2-2)成份」)及下述通式(d2-3)所表示之化合物(以下,亦稱為「(d2-3)成份」)所成之群所選出的1種以上之化合物為佳。 (d2-1)~(d2-3)成份,於阻劑膜的曝光部中,不具有會因分解而喪失酸擴散控制性(鹼性)的抑制劑之作用,於未曝光部中則具有作為抑制劑之作用。
[式中,Rd1
~Rd4
為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基;又,式(d2-2)中之Rd2
中,S原子鄰接的碳原子為不鍵結氟原子者。Yd1
為單鍵或2價之連結基;m為1以上之整數,又,Mm+
各自獨立為m價之有機陽離子]。
{(d2-1)成份} ・・陰離子部 式(d2-1)中,Rd1
為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基,其分別與前述式(b-1)中之R101
為相同之內容等。 該些之中,Rd1
又以可具有取代基芳香族烴基、可具有取代基之脂肪族環式基,或可具有取代基之鏈狀烷基為佳。該些之基所可具有的取代基,例如,羥基、側氧基、烷基、芳基、氟原子、氟化烷基、上述通式(a2-r-1)~(a2-r-7)所各別表示的含內酯之環式基、醚鍵結、酯鍵結,或該些之組合等。含有作為取代基之醚鍵結或酯鍵結時,其間可介有伸烷基,此時之取代基,以上述式(y-al-1)~(y-al-5)所各別表示的連結基為佳。 前述芳香族烴基,以苯基或萘基為較佳。 前述脂肪族環式基,以由金剛烷、降莰烷、異莰烷、三環癸烷、四環十二烷等的多環鏈烷去除1個以上的氫原子而得之基為較佳。 前述鏈狀烷基,以碳數1~10為佳,具體而言,例如,甲基、乙基、丙基、丁基、戊基、己基、庚基、辛基、壬基、癸基等的直鏈狀烷基;1-甲乙基、1-甲基丙基、2-甲基丙基、1-甲基丁基、2-甲基丁基、3-甲基丁基、1-乙基丁基、2-乙基丁基、1-甲基戊基、2-甲基戊基、3-甲基戊基、4-甲基戊基等的支鏈狀烷基等。
前述鏈狀烷基為具有作為取代基的氟原子或氟化烷基之氟化烷基時,氟化烷基之碳數,以1~11為佳,以1~8為較佳,以1~4為更佳。該氟化烷基可含有氟原子以外的原子。氟原子以外的原子,例如氧原子、硫原子、氮原子等。 Rd1
,以構成直鏈狀烷基的一部份或全部的氫原子被氟原子所取代的氟化烷基為佳,以構成直鏈狀烷基的全部氫原子被氟原子所取代的氟化烷基(直鏈狀之全氟烷基)為特佳。
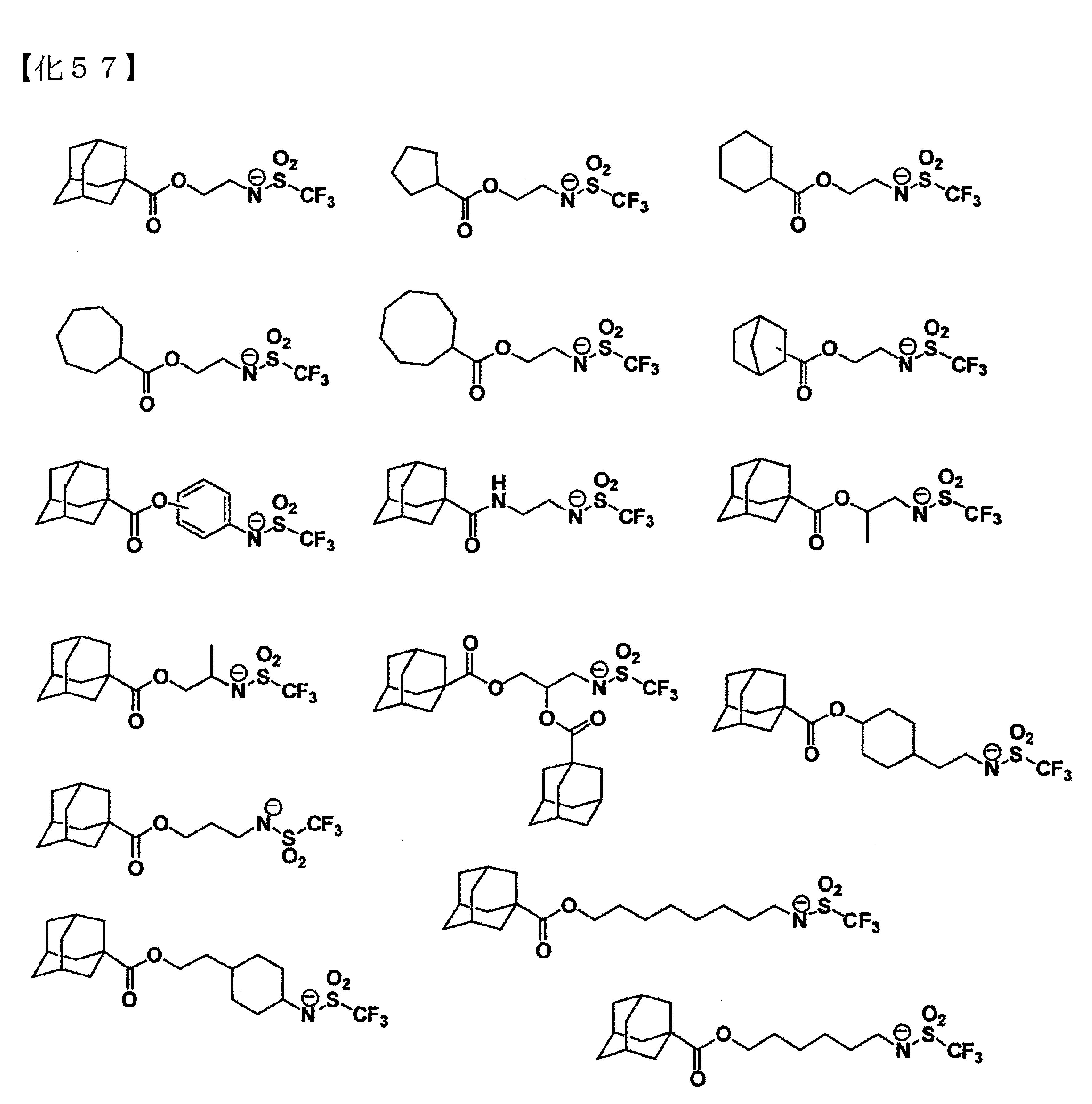
以下為(d2-1)成份之陰離子部的較佳具體例示。
・・陽離子部 式(d2-1)中,Mm+
為m價之有機陽離子。 Mm+
之有機陽離子,例如與前述通式(ca-1)~(ca-4)所各別表示的陽離子為相同之內容為佳,以前述通式(ca-1)所表示之陽離子為較佳,以前述式(ca-1-1)~(ca-1-127)所各別表示的陽離子為更佳。 (d2-1)成份,可單獨使用1種,或將2種以上組合使用皆可。
{(d2-2)成份} ・・陰離子部 式(d2-2)中,Rd2
為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基,例如與前述式(b-1)中之R101
為相同之內容等。 其中,Rd2
中,S原子鄰接的碳原子為不鍵結氟原子(未被氟所取代)者。如此,(d2-2)成份之陰離子將形成適度的弱酸陰離子,而可提高(D2)成份之抑制能力。 Rd2
以可具有取代基鏈狀烷基,或可具有取代基之脂肪族環式基為佳。鏈狀烷基,以碳數1~10為佳,以3~10為較佳。脂肪族環式基,例如,由金剛烷、降莰烷、異莰烷、三環癸烷、四環十二烷等去除1個以上的氫原子而得之基(可具有取代基);又以由莰烷等去除1個以上的氫原子而得之基為較佳。 Rd2
之烴基可具有取代基,該取代基,例如,與前述式(d2-1)的Rd1
中之烴基(芳香族烴基、脂肪族環式基、鏈狀烷基)所可具有的取代基為相同之內容等。
以下為(d2-2)成份之陰離子部的較佳具體例示。
・・陽離子部 式(d2-2)中,Mm+
為m價之有機陽離子,其與前述式(d2-1)中之Mm+
為相同之內容。 (d2-2)成份,可單獨使用1種,或將2種以上組合使用皆可。
{(d2-3)成份} ・・陰離子部 式(d2-3)中,Rd3
為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基,例如與前述式(b-1)中之R101
為相同之內容,又以含有氟原子的環式基、鏈狀烷基,或鏈狀烯基為佳。其中,又以氟化烷基為佳,以與前述Rd1
之氟化烷基為相同之內容為較佳。
式(d2-3)中,Rd4
為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基,例如與前述式(b-1)中之R101
為相同之內容等。 其中,又以可具有取代基之烷基、烷氧基、烯基、環式基為佳。 Rd4
中之烷基,以碳數1~5之直鏈狀或支鏈狀烷基為佳,具體而言,例如,甲基、乙基、丙基、異丙基、n-丁基、異丁基、tert-丁基、戊基、異戊基、新戊基等。Rd4
之烷基的氫原子中之一部份可被羥基、氰基等所取代。 Rd4
中之烷氧基,以碳數1~5之烷氧基為佳,碳數1~5之烷氧基,具體而言,例如,甲氧基、乙氧基、n-丙氧基、iso-丙氧基、n-丁氧基、tert-丁氧基等。其中,又以甲氧基、乙氧基為佳。
Rd4
中之烯基,與上述式(b-1)中之R101
為相同之內容,又以乙烯基、丙烯基(烯丙基)、1-甲基丙烯基、2-甲基丙烯基為佳。該些之基再具有取代基時,可具有碳數1~5之烷基或碳數1~5之鹵化烷基。
Rd4
中之環式基,例如與上述式(b-1)中之R101
為相同之內容,又以由環戊烷、環己烷、金剛烷、降莰烷、異莰烷、三環癸烷、四環十二烷等的環鏈烷去除1個以上的氫原子而得之脂環式基,或,苯基、萘基等之芳香族基為佳。Rd4
為脂環式基時,因阻劑組成物可良好地溶解於有機溶劑中,故可使微影蝕刻特性良好。又,Rd4
為芳香族基時,於使用EUV等作為曝光光源的微影蝕刻中,該阻劑組成物具有優良的光吸收效率,而可使感度或微影蝕刻特性良好。
式(d2-3)中,Yd1
為單鍵或2價之連結基。 Yd1
中的2價之連結基,並未有特別之限定,例如,可具有取代基之2價之烴基(脂肪族烴基、芳香族烴基)、含雜原子的2價之連結基等。該些分別與上述式(a2-1)中之Ya21
中的2價之連結基的說明中所列舉的可具有取代基之2價之烴基、含雜原子的2價之連結基為相同之內容等。 Yd1
,以羰基、酯鍵結、醯胺鍵結、伸烷基或該些之組合為佳。伸烷基,以直鏈狀或支鏈狀之伸烷基為較佳,以伸甲基或伸乙基為更佳。
以下為(d2-3)成份之陰離子部的較佳具體例示。
・・陽離子部 式(d2-3)中,Mm+
為m價之有機陽離子,其與前述式(d2-1)中之Mm+
為相同之內容。 (d2-3)成份,可單獨使用1種,或將2種以上組合使用皆可。
本實施形態之阻劑組成物中,(D21)成份,可僅使用上述(d2-1)~(d2-3)成份之任一種,亦可將2種以上組合使用。 阻劑組成物含有(D21)成份時,(D21)成份之含量,相對於(A)成份100質量份,以0.5~10質量份為佳,以0.5~8質量份為較佳,以1~8質量份為更佳。 (D21)成份之含量為較佳下限值以上時,特別是容易得到良好的微影蝕刻特性及阻劑圖型之形狀。另一方面,於上限值以下時,可維持良好的感度,亦具有優良的產率。
(D21)成份之製造方法: 前述(d2-1)成份、(d2-2)成份之製造方法,並未有特別之限定,其可使用公知的方法予以製造。 又,(d2-3)成份之製造方法,並未有特別之限定,例如可使用與US2012-0149916號公報所記載之相同方法製得。
・(D22)成份 (D22)成份,只要為具有作為酸擴散控制劑之作用,且,不相當(D1)成份及(D21)成份者之時,並未有特別之限定,其可任意地使用公知的成份。其中,又以脂肪族胺為佳,該些之中,特別是以二級脂肪族胺或三級脂肪族胺為較佳。 脂肪族胺,為具有1個以上之脂肪族基之胺,該脂肪族基以碳數為1~12為佳。 脂肪族胺,例如,氨NH3
的氫原子中之至少1個,被碳數12以下之烷基或羥烷基取代之胺(烷胺或烷醇胺)或環式胺等。 烷胺及烷醇胺之具體例,例如,n-己胺、n-庚胺、n-辛胺、n-壬胺、n-癸胺等的單烷基胺;二乙胺、二-n-丙胺、二-n-庚胺、二-n-辛胺、二環己胺等的二烷基胺;三甲胺、三乙胺、三-n-丙胺、三-n-丁胺、三-n-戊胺、三-n-己胺、三-n-庚胺、三-n-辛胺、三-n-壬胺、三-n-癸胺、三-n-十二烷基胺等的三烷基胺;二乙醇胺、三乙醇胺、二異丙醇胺、三異丙醇胺、二-n-辛醇胺、三-n-辛醇胺等之烷醇胺等。該些之中,又以碳數5~10的三烷基胺為較佳,以三-n-戊胺或三-n-辛胺為特佳。
環式胺,例如,含有作為雜原子的氮原子之雜環化合物。該雜環化合物,可為單環式者(脂肪族單環式胺),或多環式者(脂肪族多環式胺)皆可。 脂肪族單環式胺,具體而言,例如,哌啶、哌嗪等。 脂肪族多環式胺,以碳數6~10者為佳,具體而言,例如,1,5-二氮雜雙環[4.3.0]-5-壬烯、1,8-二氮雜雙環[5.4.0]-7-十一烯、伸六甲基四胺、1,4-二氮雜雙環[2.2.2]辛烷等。
其他之脂肪族胺,例如,三(2-甲氧基甲氧乙基)胺、三{2-(2-甲氧基乙氧基)乙基}胺、三{2-(2-甲氧基乙氧基甲氧基)乙基}胺、三{2-(1-甲氧基乙氧基)乙基}胺、三{2-(1-乙氧基乙氧基)乙基}胺、三{2-(1-乙氧基丙氧基)乙基}胺、三[2-{2-(2-羥基乙氧基)乙氧基}乙基]胺、三乙醇胺三乙酸酯等,又以三乙醇胺三乙酸酯為佳。
又,(D22)成份,可使用芳香族胺。 芳香族胺,例如,4-二甲胺基吡啶、吡咯、吲哚、吡唑、咪唑或該些之衍生物、三苄胺、2,6-二異丙苯胺、N-tert-丁氧基羰基吡咯啶等。
本實施形態之阻劑組成物中,(D22)成份,可單獨使用1種、亦可將2種以上組合使用。 阻劑組成物含有(D22)成份時,(D22)成份之含量,相對於(A)成份100質量份,通常為使用0.01~5質量份之範圍。於上述範圍時,可提高阻劑圖型形狀、延遲烘烤(Post Exposure Delay)的放置穩定性( temporal stability)等。
≪(E)成份:由有機羧酸及磷的含氧酸及其衍生物所成之群所選出之至少1種之化合物≫ 本實施形態之阻劑組成物中,就防止感度劣化,或提高阻劑圖型形狀、延遲烘烤的放置穩定性等目的,可再含有作為任意成份之由有機羧酸及磷的含氧酸及其衍生物所成之群所選出之至少1種的化合物(E)(以下,亦稱為「(E)成份」)。 有機羧酸,例如,以乙酸、丙二酸、枸椽酸、蘋果酸、琥珀酸、安息香酸、水楊酸等為佳。 磷的含氧酸,例如,磷酸、膦酸(phosphonic acid)、次膦酸(phosphine acid)等,該些之中,特別是以膦酸為佳。 磷的含氧酸之衍生物,例如,上述含氧酸的氫原子被烴基取代而得之酯等,前述烴基,例如,碳數1~5之烷基、碳數6~15之芳基等。 磷酸之衍生物,例如,磷酸二-n-丁酯、磷酸二苯酯等的磷酸酯等。 膦酸衍生物,例如,膦酸二甲酯、膦酸-二-n-丁酯、膦酸苯酯、膦酸二苯酯、膦酸二苄酯等的膦酸酯等。 次膦酸之衍生物,例如,次膦酸酯或次膦酸苯酯等。 本實施形態之阻劑組成物中,(E)成份,可單獨使用1種亦可、將2種以上合併使用亦可。 阻劑組成物含有(E)成份時,(E)成份之含量,相對於(A)成份100質量份,通常為使用0.01~5質量份之範圍。
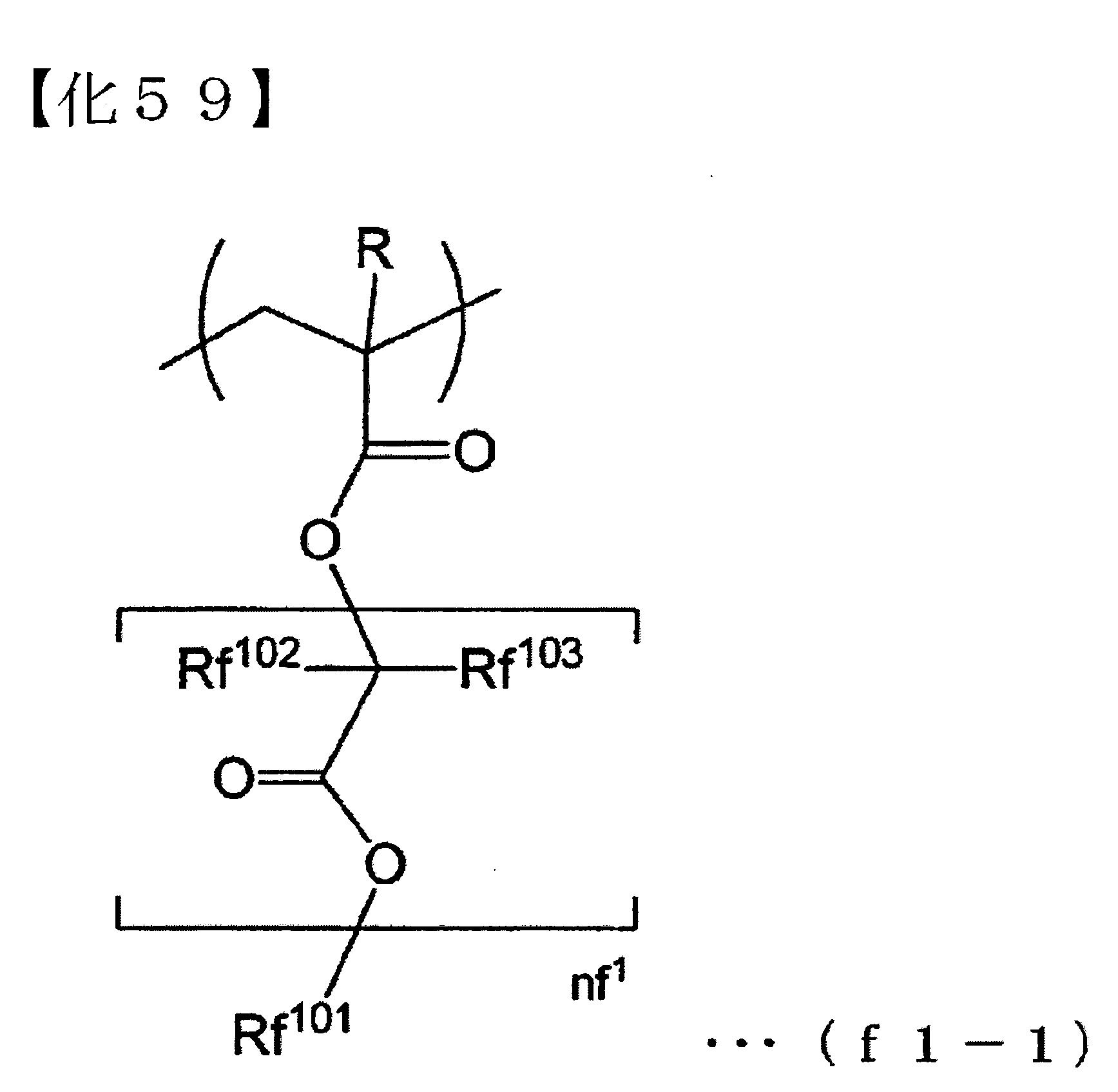
≪(F)成份:氟添加劑成份≫ 本實施形態之阻劑組成物中,為賦予阻劑膜撥水性之目的,亦可含有氟添加劑成份(以下,亦稱為「(F)成份」)。 (F)成份,例如,可使用特開2010-002870號公報、特開2010-032994號公報、特開2010-277043號公報、特開2011-13569號公報、特開2011-128226號公報所記載的含氟高分子化合物。 (F)成份,更具體而言,例如,具有下述式(f1-1)所表示的結構單位(f1)的聚合物。前述聚合物,以僅由下述式(f1-1)所表示的結構單位(f1)所形成之聚合物(均聚物);該結構單位(f1)與前述結構單位(a1)之共聚物;該結構單位(f1),與丙烯酸或甲基丙烯酸所衍生的結構單位,與前述結構單位(a1)之共聚物為佳。其中,可與該結構單位(f1)共聚之前述結構單位(a1),以由1-乙基-1-(甲基)丙烯酸環辛酯所衍生的結構單位、1-甲基-1-(甲基)丙烯酸金剛烷酯所衍生的結構單位為佳。
[式中,R與前述為相同之內容,Rf102
及Rf103
各自獨立表示氫原子、鹵素原子、碳數1~5之烷基或碳數1~5之鹵化烷基;Rf102
及Rf103
可為相同或相異皆可;nf1
為0~5之整數,Rf101
為含有氟原子之有機基]。
式(f1-1)中,α位的碳原子所鍵結的R,與前述為相同之內容。R以氫原子或甲基為佳。 式(f1-1)中,Rf102
及Rf103
之鹵素原子,可列舉如,氟原子、氯原子、溴原子、碘原子等,特別是以氟原子為佳。Rf102
及Rf103
之碳數1~5之烷基,與上述R之碳數1~5之烷基為相同之內容,又以甲基或乙基為佳。Rf102
及Rf103
之碳數1~5之鹵化烷基,具體而言,可列舉如,碳數1~5之烷基的氫原子中之一部份或全部,被鹵素原子所取代之基等。 該鹵素原子,可列舉如,氟原子、氯原子、溴原子、碘原子等,特別是以氟原子為佳。其中,Rf102
及Rf103
,又以氫原子、氟原子,或碳數1~5之烷基為佳,以氫原子、氟原子、甲基,或乙基為佳。 式(f1-1)中,nf1
為0~5之整數,以0~3之整數為佳,以0~2之整數為較佳,以0或1為更佳。
式(f1-1)中,Rf101
為含氟原子之有機基,又以含有氟原子之烴基為佳。 含有氟原子之烴基,可為直鏈狀、支鏈狀或環狀之任一者,又以碳數1~20為佳,以碳數1~15為較佳,以碳數1~10為特佳。 又,含有氟原子之烴基,以該烴基中的氫原子中之25%以上被氟化者為佳,以50%以上被氟化者為較佳,而60%以上被氟化者,於浸潤曝光時可提高阻劑膜的疏水性,而為特佳。 其中,Rf101
又以碳數1~6之氟化烴基為較佳,以三氟甲基、-CH2
-CF3
、-CH2
-CF2
-CF3
、-CH(CF3
)2
、-CH2
-CH2
-CF3
、-CH2
-CH2
-CF2
-CF2
-CF2
-CF3
為特佳。
(F)成份之質量平均分子量(Mw)(凝膠滲透色層分析之聚苯乙烯換算基準),以1000~50000為佳,以5000~40000為較佳,以10000~30000為最佳。於該範圍的上限值以下時,作為阻劑使用時,對阻劑用溶劑具有充份的溶解性,於該範圍的下限值以上時,可使耐乾蝕刻性或阻劑圖型斷面形狀良好。 (F)成份之分散度(Mw/Mn),以1.0~5.0為佳,以1.0~ 3.0為較佳,以1.2~2.5為最佳。
本實施形態之阻劑組成物中,(F)成份,可單獨使用1種亦可、將2種以上合併使用亦可。 阻劑組成物中,含有(F)成份時,(F)成份之含量,相對於(A)成份100質量份,通常為使用0.5~10質量份之比例。
≪(S)成份:有機溶劑成份≫ 本實施形態之阻劑組成物,可將阻劑材料溶解於有機溶劑成份(以下,亦稱為「(S)成份」)之方式而製得。 (S)成份,只要為可溶解所使用的各成份,形成均勻溶液者即可,其可適當選擇使用以往作為化學增強型阻劑組成物的溶劑使用的公知成份中的任意成份。 (S)成份,例如,以γ-丁內酯等的內酯類;丙酮、甲基乙酮、環己酮、甲基-n-戊酮、甲基異戊酮、2-庚酮等之酮類;乙二醇、二乙二醇、丙二醇、二丙二醇等之多元醇類;乙二醇單乙酸酯、二乙二醇單乙酸酯、丙二醇單乙酸酯,或二丙二醇單乙酸酯等的具有酯鍵結之化合物、前述多元醇類或前述具有酯鍵結之化合物的單甲醚、單乙醚、單丙醚、單丁醚等的單烷醚或單苯醚等的具有醚鍵結之化合物等的多元醇類之衍生物[該些之中,以丙二醇單甲醚乙酸酯(PGMEA)、丙二醇單甲醚(PGME)為佳];二噁烷般的環式醚類,或乳酸甲酯、乳酸乙酯(EL)、乙酸甲酯、乙酸乙酯、乙酸丁酯、丙酮酸甲酯、丙酮酸乙酯、甲氧基丙酸甲酯、乙氧基丙酸乙酯等之酯類;苯甲醚、乙基苄醚、甲苯酚甲醚、二苯醚、二苄醚、苯乙醚、丁苯醚、乙苯、二乙苯、戊苯、異丙苯、甲苯、二甲苯、異丙基甲苯、三甲苯等之芳香族系有機溶劑、二甲基亞碸(DMSO)等。 本實施形態之阻劑組成物中,(S)成份,可單獨使用1種亦可,以2種以上之混合溶劑方式使用亦可。 其中,又以PGMEA、PGME、γ-丁內酯、EL、環己酮為佳。 又,亦可使用PGMEA與極性溶劑混合而得之混合溶劑。其添加比(質量比),可於考量PGMEA與極性溶劑之相溶性等,再作適當適當決定即可,較佳為1:9~9:1,更佳為以2:8~8:2之範圍內為佳。 更具體而言,例如,添加作為極性溶劑之EL或環己酮時,PGMEA:EL或環己酮之質量比,較佳為1:9~9:1,更佳為2:8~8:2。又,添加作為極性溶劑之PGME時,PGMEA:PGME之質量比,較佳為1:9~9:1,更佳為2:8~8:2,特佳為3:7~7:3。又,亦可使用PGMEA與PGME與環己酮之混合溶劑。 又,(S)成份,其他亦可使用由PGMEA及EL之中所選出之至少1種,與γ-丁內酯之混合溶劑。此時,混合比例依前者與後者之質量比,較佳為70:30~95:5。 (S)成份之使用量,並未有特別之限定,其可於塗佈於基板等的可能濃度,配合塗佈膜厚度等,作適當之設定。一般而言,為使阻劑組成物之固形成份濃度為1~20質量%,較佳為2~15質量%之範圍內使用(S)成份。
本實施形態之阻劑組成物中,可再配合目的,適當地添加含有混合性的添加劑,例如改良阻劑膜性能所附加的樹脂、溶解抑制劑、可塑劑、安定劑、著色劑、抗暈劑、染料等。
如以上說明般,本實施形態之阻劑組成物,為含有陰離子部具有「具有二碸醯亞胺(-SO2
N-
SO2
-)基之環構造」的(D1)成份。 該阻劑組成物中,於形成阻劑圖型之際,該(D1)成份經由鹼交換,而具有作為捕集阻劑組成物中因曝光而產生的酸之抑制劑(酸擴散控制劑)的作用。因此,可將顯影前之阻劑膜中的酸性或鹼性的強度調整至適當程度,而可提高阻劑膜的曝光部與未曝光部的抑制性的對比。如此,可提高解析度,且亦可提高DOF特性。 又,該(D1)成份為具有適度的高極性。因此,於阻劑組成物中,更可適度地縮短因曝光所產生之酸於阻劑膜中的擴散長度。因此,可容易地得到低粗糙度之效果。 因具有該些之作用效果,故本實施形態之阻劑組成物,可以提高解析度,且以更低的圖型粗糙度之良好形狀,形成更微細的圖型。此外,本實施形態之阻劑組成物,亦具有良好的焦點景深寬度(DOF)特性,故推測可擴大製程寬容度,形成具有優良微影蝕刻特性的良好形狀之阻劑圖型。
(阻劑圖型形成方法) 本發明之第2態樣的阻劑圖型形成方法為具有:於支撐體上,使用上述第1態樣之阻劑組成物形成阻劑膜之步驟、使前述阻劑膜曝光之步驟,及使前述曝光後的阻劑膜進行顯影,形成阻劑圖型之步驟。 該阻劑圖型形成方法,例如依以下所示方式進行之實施形態。
本實施形態之阻劑圖型形成方法為,首先,將上述第1態樣的阻劑組成物使用旋轉塗佈器等塗佈於支撐體上,例如80~150℃之溫度條件下,實施40~120秒鐘、較佳為60~90秒鐘之燒焙(曝前燒焙(Post Apply Bake) (PAB))處理,而形成阻劑膜。 其次,例如使用ArF曝光裝置、電子線描畫裝置、EUV曝光裝置等的曝光裝置,介由形成特定圖型的遮罩(遮罩圖型)對該阻劑膜進行曝光或不介由遮罩圖型而以電子線直接照射進行描畫等方式進行選擇性曝光後,例如於80~150℃之溫度條件下,實施40~120秒鐘、較佳為60~90秒鐘之燒焙(曝後燒焙(Post Exposure Bake)(PEB))處理。 其次,對前述阻劑膜進行顯影處理。顯影處理為,於鹼顯影製程時,使用鹼顯影液,於溶劑顯影製程時,使用含有有機溶劑之顯影液(有機系顯影液)進行。 顯影處理後,較佳為進行洗滌處理。洗滌處理,於鹼顯影製程時,以使用純水的水洗滌為佳,於溶劑顯影製程時,以使用含有有機溶劑的洗滌液為佳。 溶劑顯影製程時,可於前述顯影處理或洗滌處理之後,使用超臨界流體進行去除附著於圖型上的顯影液或洗滌液之處理。 於顯影處理後或洗滌處理後,進行乾燥。又,依情況之不同,亦可於上述顯影處理後進行燒焙處理(後燒焙處理)。 依前述方式,即可形成阻劑圖型。
支撐體,並未有特別之限定,其可使用以往公知之物,例如,電子零件用之基板,或於其上形成特定配線圖型者等。更具體而言,例如,矽晶圓、銅、鉻、鐵、鋁等的金屬製之基板,或玻璃基板等。配線圖型之材料,例如可使用銅、鋁、鎳、金等。 又,支撐體,亦可為於上述般之基板上,設有無機系及/或有機系之膜者。無機系之膜,例如,無機抗反射膜(無機BARC)。有機系之膜,例如,有機抗反射膜(有機BARC),或多層阻劑法中之下層有機膜等的有機膜。 其中,多層阻劑法係指,於基板上,設置至少一層的有機膜(下層有機膜),與至少一層的阻劑膜(上層阻劑膜),並使用上層阻劑膜所形成的阻劑圖型作為遮罩,對下層有機膜進行圖型形成(Patterning)之方法,其可形成高長徑比之圖型。即,依多層阻劑法,因可確保下層有機膜所需要的厚度,故可使阻劑膜薄膜化,而可形成高長徑比的微細圖型。 多層阻劑法,基本上可分為上層阻劑膜,與下層有機膜等的二層構造之方法(2層阻劑法),與上層阻劑膜與下層有機膜之間,設有一層以上的中間層(金屬薄膜等)的三層以上的多層構造之方法(3層阻劑法)。
曝光所使用的波長,並未有特別之限定,其可使用ArF準分子雷射、KrF準分子雷射、F2
準分子雷射、EUV(極紫外線)、VUV(真空紫外線)、EB(電子線)、X線、軟X線等的輻射線進行曝光。前述阻劑組成物,對KrF準分子雷射、ArF準分子雷射、EB或EUV用具有高度有用性,對於ArF準分子雷射、EB或EUV用特別有用。
阻劑膜之曝光方法,可為於空氣或氮氣等的惰性氣體中進行的通常曝光(乾式曝光)亦可、浸潤式曝光(Liquid Immersion Lithography)亦可。 浸潤式曝光為,預先於阻劑膜與曝光裝置的最下位置之透鏡間,充滿具有折射率大於空氣的折射率之溶劑(浸潤媒體),並於該狀態下進行曝光(浸潤式曝光)之方法。 浸潤媒體,以具有較空氣的折射率為更大,且,較被曝光的阻劑膜之折射率為更小折射率的溶劑為佳。該溶劑的折射率,只要於前述範圍內時,並未有特別之限制。 具有較空氣的折射率為更大,且,較前述阻劑膜之折射率為更小折射率的溶劑,例如,以水、氟系惰性液體、矽系溶劑、烴系溶劑等。 氟系惰性液體之具體例如,C3
HCl2
F5
、C4
F9
OCH3
、C4
F9
OC2
H5
、C5
H3
F7
等的氟系化合物為主成份之液體等,又以沸點為70~180℃者為佳,以80~160℃者為較佳。氟系惰性液體具有上述範圍之沸點者時,於曝光結束後,可使用簡便方法去除浸潤所使用的媒體,而為較佳。 氟系惰性液體,特別是以烷基的全部氫原子被氟原子取代而得之全氟烷基化合物為佳。全氟烷基化合物,具體而言,例如,全氟烷醚化合物、全氟烷胺化合物等。 又,具體而言,前述全氟烷醚化合物,可列舉如全氟(2-丁基-四氫呋喃)(沸點102℃),前述全氟烷胺化合物可列舉如全氟三丁胺(沸點174℃)。 浸潤媒體,就費用、安全性、環境問題、廣用性等觀點,以使用水為佳。
鹼顯影製程中之顯影處理所使用的鹼顯影液,例如0.1~10質量%氫氧化四甲基銨(TMAH)水溶液等。 溶劑顯影製程中之顯影處理所使用的含有有機系顯影液的有機溶劑,只要可溶解(A)成份(曝光前的(A)成份)者即可,其可由公知的有機溶劑中適當地選擇。具體而言,例如,酮系溶劑、酯系溶劑、醇系溶劑、腈系溶劑、醯胺系溶劑、醚系溶劑等的極性溶劑、烴系溶劑等。 酮系溶劑,為構造中含有C-C(=O)-C之有機溶劑。酯系溶劑,為構造中含有C-C(=O)-O-C之有機溶劑。醇系溶劑,為構造中含有醇性羥基之有機溶劑。「醇性羥基」係指,脂肪族烴基的碳原子所鍵結的羥基之意。腈系溶劑,為構造中含有腈基之有機溶劑。醯胺系溶劑,為構造中含有醯胺基之有機溶劑。醚系溶劑,為構造中含有C-O-C之有機溶劑。 有機溶劑中,其構造中亦存在多數種含有具有上述各溶劑特徴的官能基之有機溶劑,此時,亦相當於該有機溶劑所具有的含任一官能基的溶劑種類者。例如,二乙二醇單甲醚,則相當於上述分類中之醇系溶劑、醚系溶劑中之任一者。 烴系溶劑為,由可被鹵化的烴所形成,為不具有鹵素原子以外的取代基之烴溶劑。鹵素原子,可列舉如,氟原子、氯原子、溴原子、碘原子等,又以氟原子為佳。 有機系顯影液所含有的有機溶劑,於上述之中,又以極性溶劑為佳,以酮系溶劑、酯系溶劑、腈系溶劑等為佳。
酮系溶劑,例如,1-辛酮、2-辛酮、1-壬酮、2-壬酮、丙酮、4-庚酮、1-己酮、2-己酮、二異丁酮、環己酮、甲基環己酮、苯基丙酮、甲基乙酮、甲基異丁酮、乙醯基丙酮、丙酮基丙酮、紫羅蘭酮、二丙酮醇、乙醯基卡必醇(carbinol)、苯乙酮、甲基萘酮、異佛爾酮、丙烯碳酸酯、γ-丁內酯、甲基戊酮(2-庚酮)等。該些之中,酮系溶劑,又以甲基戊酮(2-庚酮)為佳。
酯系溶劑,例如,乙酸甲酯、乙酸丁酯、乙酸乙酯、乙酸異丙酯、乙酸戊酯、乙酸異戊酯、甲氧基乙酸乙酯、乙氧基乙酸乙酯、丙二醇單甲醚乙酸酯、乙二醇單乙醚乙酸酯、乙二醇單丙醚乙酸酯、乙二醇單丁醚乙酸酯、乙二醇單苯醚乙酸酯、二乙二醇單甲醚乙酸酯、二乙二醇單丙醚乙酸酯、二乙二醇單乙醚乙酸酯、二乙二醇單苯醚乙酸酯、二乙二醇單丁醚乙酸酯、二乙二醇單乙醚乙酸酯、2-甲氧基丁基乙酸酯、3-甲氧基丁基乙酸酯、4-甲氧基丁基乙酸酯、3-甲基-3-甲氧基丁基乙酸酯、3-乙基-3-甲氧基丁基乙酸酯、丙二醇單甲醚乙酸酯、丙二醇單乙醚乙酸酯、丙二醇單丙醚乙酸酯、2-乙氧基丁基乙酸酯、4-乙氧基丁基乙酸酯、4-丙氧基丁基乙酸酯、2-甲氧基戊基乙酸酯、3-甲氧基戊基乙酸酯、4-甲氧基戊基乙酸酯、2-甲基-3-甲氧基戊基乙酸酯、3-甲基-3-甲氧基戊基乙酸酯、3-甲基-4-甲氧基戊基乙酸酯、4-甲基-4-甲氧基戊基乙酸酯、丙二醇二乙酸酯、甲酸甲酯、甲酸乙酯、甲酸丁酯、甲酸丙酯、乳酸乙酯、乳酸丁酯、乳酸丙酯、碳酸乙酯、碳酸丙酯、碳酸丁酯、丙酮酸甲酯、丙酮酸乙酯、丙酮酸丙酯、丙酮酸丁酯、乙醯乙酸甲酯、乙醯乙酸乙酯、丙酸甲酯、丙酸乙酯、丙酸丙酯、丙酸異丙酯、2-羥基丙酸甲酯、2-羥基丙酸乙酯、甲基-3-甲氧基丙酸酯、乙基-3-甲氧基丙酸酯、乙基-3-乙氧基丙酸酯、丙基-3-甲氧基丙酸酯等。該些之中,酯系溶劑,又以乙酸丁酯為佳。
腈系溶劑,例如,乙腈、丙腈、戊腈、丁腈等。
有機系顯影液中,必要時,可添加公知的添加劑。該添加劑,例如,界面活性劑等。界面活性劑,並未有特別之限定,例如可使用離子性或非離子性的氟系及/或矽系界面活性劑等。 界面活性劑,以非離子性的界面活性劑為佳,以非離子性的氟系界面活性劑,或非離子性的矽系界面活性劑為較佳。 添加界面活性劑時,其添加量,相對於有機系顯影液之全量,通常為0.001~5質量%,又以0.005~2質量%為佳,以0.01~0.5質量%為較佳。
顯影處理,可使用公知的顯影方法實施,例如將支撐體浸漬於顯影液中維持一定時間之方法(浸漬法)、使顯影液以表面張力覆蓋支撐體表面並靜止一定時間之方法(攪練(puddle)法)、將顯影液對支撐體表面進行噴霧之方法(噴霧法)、於依一定速度迴轉的支撐體上,將依一定速度塗出顯影液的塗出噴嘴於掃描中持續塗出顯影液之方法(Dynamicdispense法)等。
溶劑顯影製程中,於顯影處理後的洗滌處理所使用的洗滌液所含有的有機溶劑,例如可使用由前述有機系顯影液所使用的有機溶劑中列舉的有機溶劑中,適當地選擇不易溶解阻劑圖型者。通常為使用由烴系溶劑、酮系溶劑、酯系溶劑、醇系溶劑、醯胺系溶劑及醚系溶劑所選出的至少1種之溶劑。該些之中,又以由烴系溶劑、酮系溶劑、酯系溶劑、醇系溶劑及醯胺系溶劑所選出之至少1種為佳,以由醇系溶劑及酯系溶劑所選出之至少1種為較佳,以醇系溶劑為特佳。 洗滌液所使用的醇系溶劑,以碳數6~8的1價醇為佳,該1價醇可為直鏈狀、分支狀或環狀之任一者。具體而言,例如,1-己醇、1-庚醇、1-辛醇、2-己醇、2-庚醇、2-辛醇、3-己醇、3-庚醇、3-辛醇、4-辛醇、苄醇等。該些之中,以1-己醇、2-庚醇、2-己醇為佳,以1-己醇、2-己醇為較佳。 該些之有機溶劑中,任何1種皆可單獨使用,或將2種以上合併使用亦可。又,亦可與上述以外的有機溶劑或水混合使用。但,於考慮顯影特性時,洗滌液中之水的添加量,相對於洗滌液之全量,以30質量%以下為佳,以10質量%以下為較佳,以5質量%以下為更佳,以3質量%以下為特佳。 洗滌液中,必要時,可添加公知的添加劑。該添加劑,例如,界面活性劑等。界面活性劑,例如與前述為相同之內容,又以非離子性之界面活性劑為佳,以非離子性之氟系界面活性劑,或非離子性之矽系界面活性劑為較佳。 添加界面活性劑時,其添加量,相對於洗滌液之全量,通常為0.001~5質量%,又以0.005~2質量%為佳,以0.01~0.5質量%為較佳。
使用洗滌液之洗滌處理(洗淨處理),可使用公知的洗滌方法實施。該洗滌處理之方法,例如,於依一定速度迴轉的支撐體上,使洗滌液持續塗出之方法(迴轉塗佈法)、將支撐體浸漬於洗滌液中維持一定時間之方法(浸漬法)、將洗滌液對支撐體表面進行噴霧之方法(噴霧法)等。
以上說明的本實施形態之阻劑圖型形成方法,因使用上述第1態樣的阻劑組成物,故可以提高解析度,且使圖型的粗糙度更低的良好形狀之方式,形成更微細的圖型。
(化合物) 本發明之第3態樣的化合物,為下述通式(d1)所表示者。
[式中,Rd01
及Rd02
各自獨立為可具有取代基之環式基、可具有取代基之鏈狀烷基,或可具有取代基之鏈狀烯基;或,Rd01
與Rd02
可相互鍵結,形成縮合環;m為1以上之整數,又,Mm+
表示m價之有機陽離子]。
該第3態樣的化合物,與上述第1態樣的阻劑組成物中之說明中的(D1)成份為相同之化合物。前述式(d1)中之Rd01
及Rd02
及Mm+
,亦與上述為相同之內容。
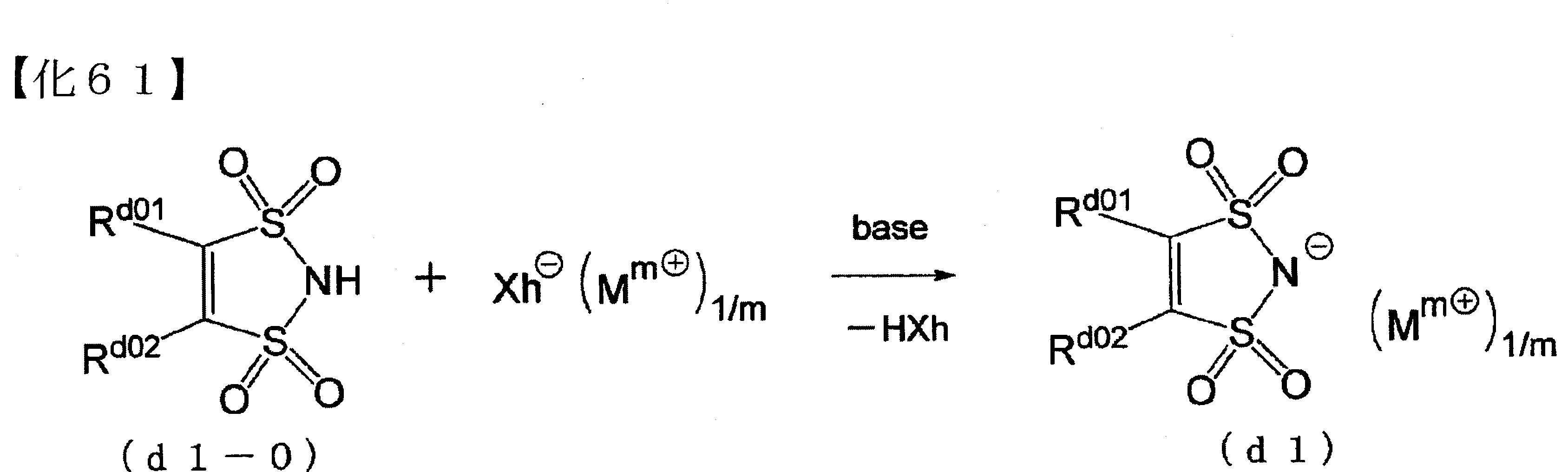
[化合物((D1)成份)之製造方法] (D1)成份,例如可依以下方式製造。即,於適當的鹼存在下,使下述通式(d1-0)所表示之化合物(d1-0),與下述化學式所表示之鹼交換用化合物(Xh-
(Mm+
)1/m
),經由鹼交換反應,而可製得作為(D1)成份之下述通式(d1)所表示之化合物。
[式中,Rd01
及Rd02
分別與上述通式(d1)中之Rd01
及Rd02
為相同之內容。Xh-
表示鹵素離子或烷基磺酸離子。Mm+
為m價之有機陽離子,其與上述通式(d1)中之Mm+
為相同之內容]。
前述式中,構成Xh-
之鹵素離子的鹵素原子例如,氟原子、氯原子、溴原子、碘原子等,該些之中,又以氟原子為佳。 烷基磺酸離子中之烷基,可為直鏈狀、支鏈狀或環狀之任一者。前述直鏈狀或支鏈狀烷基,以碳數1~10為佳,以碳數1~8為較佳,以碳數1~4為更佳,以甲基或乙基為特佳。前述環狀之烷基,以碳數4~15為佳,以碳數4~10為較佳,以碳數6~10為更佳。 鹼,例如,三乙胺、4-二甲胺基吡啶(DMAP)、吡啶等的有機鹼;氫化鈉、K2
CO3
、Cs2
CO3
等的無機鹼等。 化合物(d1-0)與有機陽離子(Mm+
)之鹼交換,可依與以往公知的鹼取代方法為相同之方法實施。例如,將化合物(d1-0)與鹼交換用化合物(Xh-
(Mm+
)1/m
),於水、二氯甲烷、乙腈、氯仿等的溶劑下,經由攪拌等方式使其進行反應方式實施。 反應溫度,以0~100℃左右為佳,以0~50℃左右為較佳。 反應時間,依化合物(d1-0)與鹼交換用化合物之反應性或反應溫度等而有所不同,通常以10分鐘以上、24小時以下為佳,以10分鐘以上、12小時以下為較佳。
鹼交換反應結束之後,可將反應液中之化合物單離、純化。單離、純化之方法,可使用以往公知之方法,例如,可將濃縮、溶劑萃取、蒸餾、結晶化、再結晶、色層分析等方法適當地組合使用。 依上述方法所製得之化合物的構造,可使用1
H-核磁共振(NMR)圖譜法、13
C-NMR圖譜法、19
F-NMR圖譜法、紅外線吸收(IR)圖譜法、質量分析(MS)法、元素分析法、X線結晶繞射法等的一般的有機分析法鑑別。
(酸擴散控制劑) 本發明之第4態樣的酸擴散控制劑,為由上述第3態樣的化合物所形成者。 該酸擴散控制劑,適合作為化學增強型阻劑組成物用之抑制劑,例如適合作為上述第1態樣的阻劑組成物之抑制劑。該酸擴散控制劑使用於化學增強型阻劑組成物時,可提高解析度,且使更低圖型粗糙度的良好形狀之方式,容易形成更微細的圖型。
[實施例]
以下,將使用實施例對本發明作更詳細之說明,但本發明並不受該些例示所限定。 本實施例中,化學式(1)所表示之化合物將標記為「化合物(1)」,其他化學式所表示之化合物將進行相同的標記。
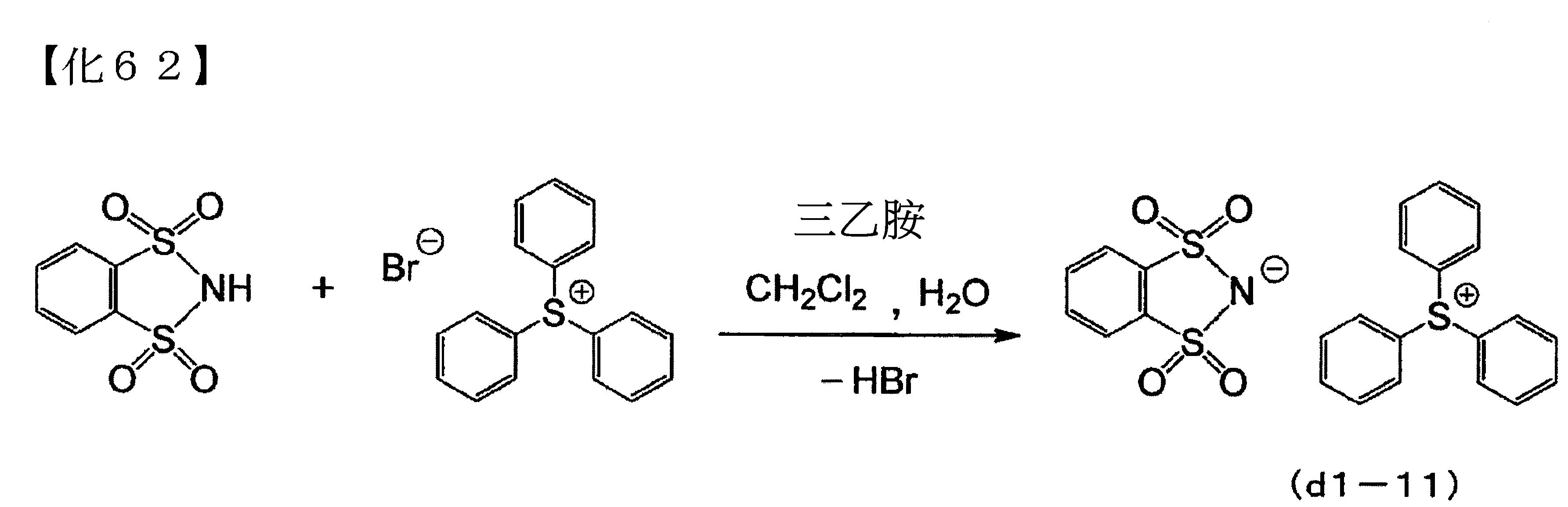
<化合物的製造例> (實施例1) 將1,2-苯二磺酸醯亞胺(3g),與三苯基鋶溴化物(4.7g),與三乙胺(1.4g),與二氯甲烷(60g),與離子交換水(70g)混合,於室溫下攪拌30分鐘。 隨後,分取有機相,於回收的有機相中,加入離子交換水(70g),於室溫下攪拌30分鐘後,分取有機相。重複10次該水洗操作。 隨後,將所得有機層濃縮,而製得式(d1-11)所表示之化合物(3.9g)。
對所得化合物(d1-11)進行NMR測定,基於以下之測定結果,鑑別其構造。1
H NMR(DMSO-d6
)δ(ppm)=7.88-7.73(m,17H),7.72-7.68(m,2H)。
所得化合物(d1-11)之共軛酸的pKa為-1.10、化合物(d1-11)之logPow
為0.27。
(實施例2) 將1,2-苯二磺酸醯亞胺(15g),與式(d0)所表示之鹽(38.6g),與三乙胺(6.8g),與二氯甲烷(420g),與離子交換水(480g)混合,於室溫下攪拌30分鐘。 隨後,分取有機相,於回收的有機相中,加入離子交換水(480g),於室溫下攪拌30分鐘後,分取有機相。重複10次該水洗操作。 隨後,將所得有機層濃縮,製得式(d1-12)所表示之化合物(45.5g)。
對所得化合物(d1-12)進行NMR測定,基於以下之測定結果,鑑別該構造。1
H NMR(DMSO-d6
)δ(ppm)=7.93-7.72(m,12H),7.72-7.61(m,4H),2.13(s,6H),2.04(s,9H),1.73(s,6H)。
所得化合物(d1-12)之共軛酸的pKa為-1.10、化合物(d1-12)之logPow
為0.27。
<阻劑組成物之製造> (實施例3~4、比較例1~2) 將表1所示各成份混合、溶解,分別製得各例之阻劑組成物(固形成份濃度3.0質量%)。
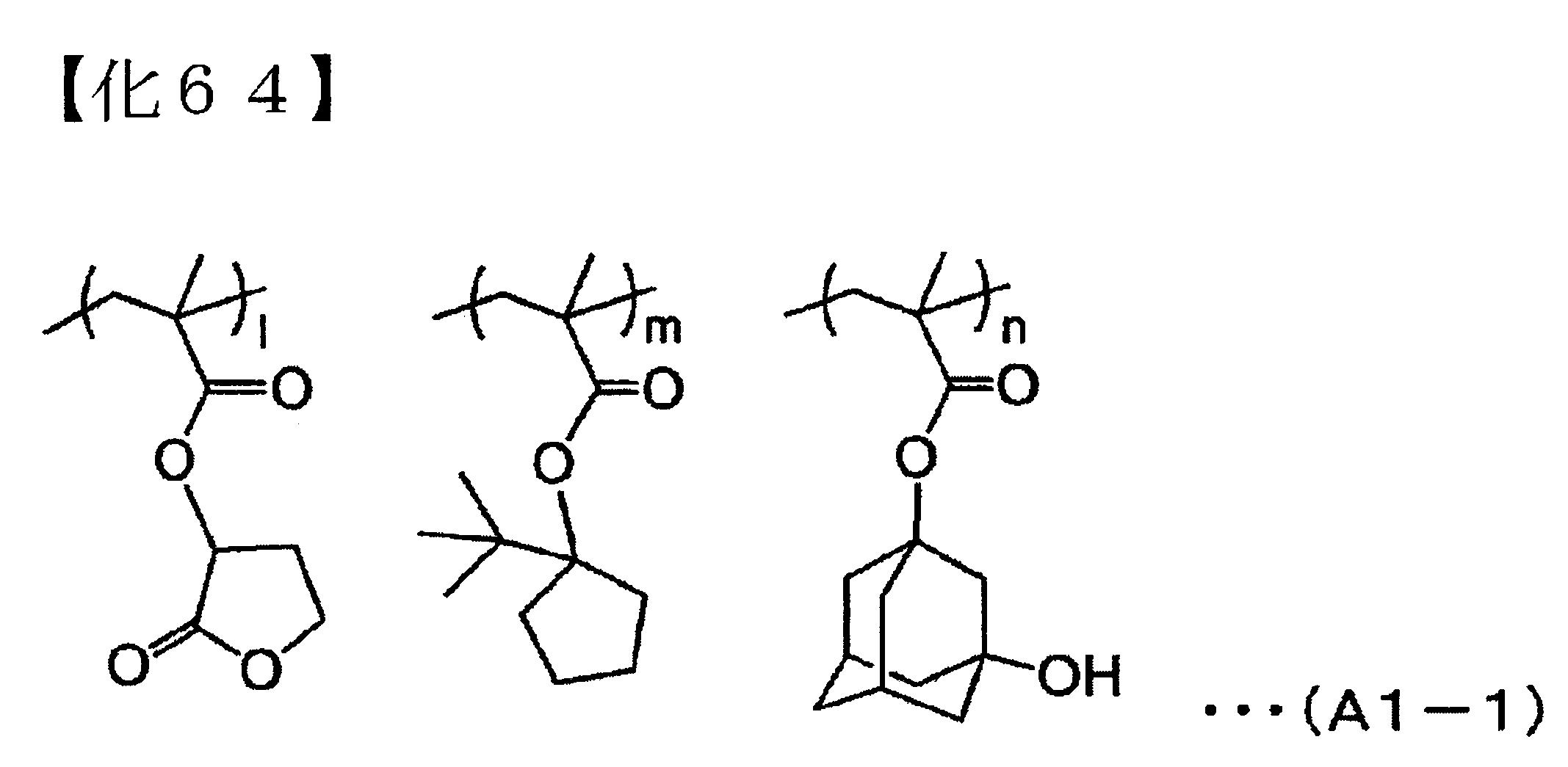
表1中,各簡稱分別具有以下之意義。[ ]內之數值為添加量(質量份)。 (A)-1:下述化學式(A1-1)所表示之高分子化合物。GPC測定所求得的標準聚苯乙烯換算的質量平均分子量(Mw)為9000、分子量分散度(Mw/Mn)為1.81。13
C-NMR所求得的共聚組成比(構造式中之各結構單位之比例(莫耳比))為l/m/n=40/50/10。
(D1)-1:上述化學式(d1-11)所表示之化合物所形成的酸擴散控制劑。 (D1)-2:上述化學式(d1-12)所表示之化合物所形成的酸擴散控制劑。
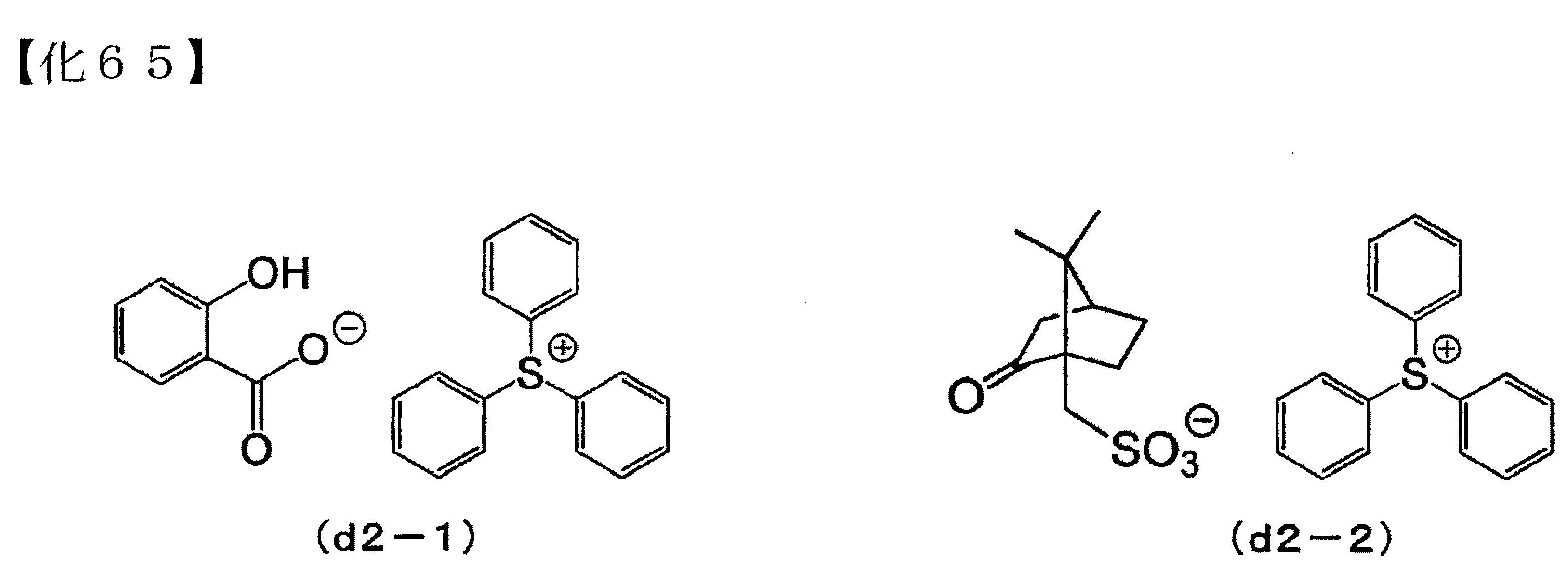
(D2)-1:下述化學式(d2-1)所表示之化合物所形成的酸擴散控制劑。該化合物(d2-1)之共軛酸的pKa為3.01、化合物(d2-1)之logPow
為2.01。 (D2)-2:下述化學式(d2-2)所表示之化合物所形成的酸擴散控制劑。該化合物(d2-2)之共軛酸的pKa為1.17、化合物(d2-2)之logPow
為-0.94。
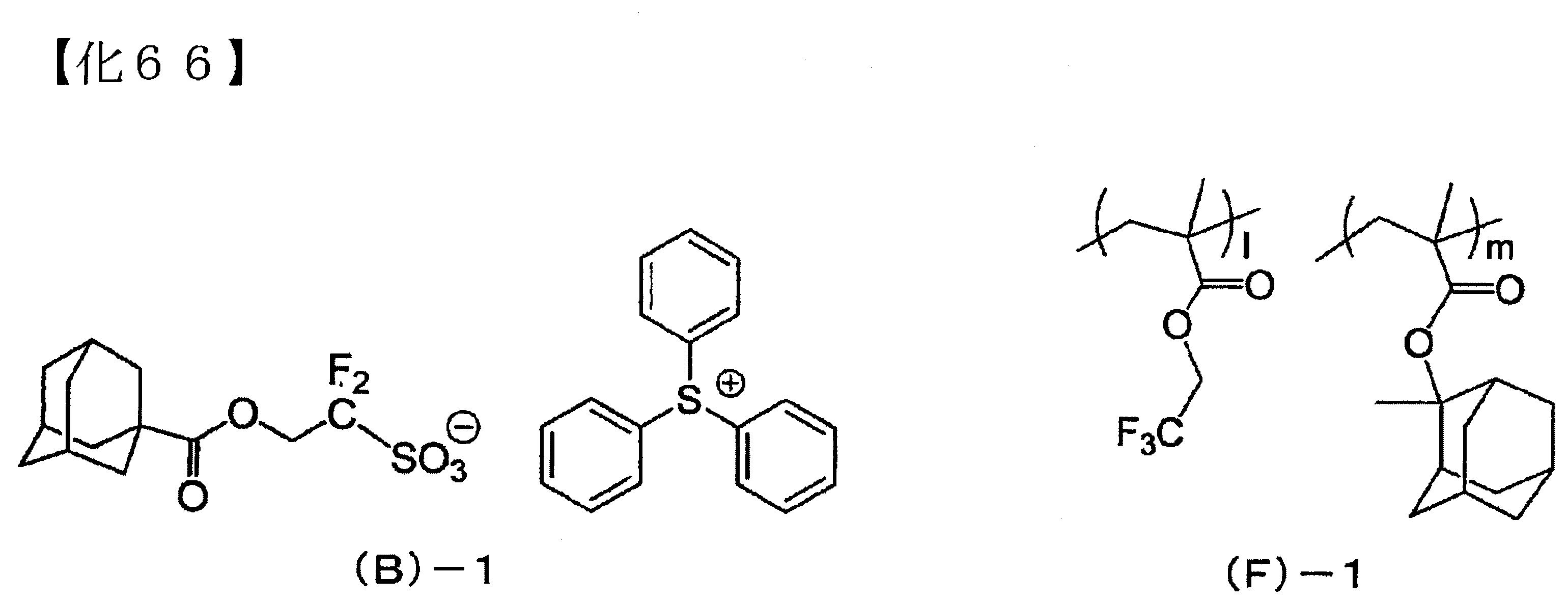
(B)-1:下述化學式(B)-1所表示之化合物所形成的酸產生劑。 (F)-1:下述化學式(F)-1所表示之含氟高分子化合物。GPC測定所求得的標準聚苯乙烯換算的質量平均分子量(Mw)為15500、分子量分散度(Mw/Mn)為1.67。13
C-NMR所求得的共聚組成比(構造式中之各結構單位之比例(莫耳比))為l/m=50/50。 (S)-1:γ-丁內酯。 (S)-2:PGMEA/PGME/環己酮(質量比45/30/25)之混合溶劑。
<阻劑組成物之評估> 使用所得阻劑組成物形成阻劑圖型,並分別依以下方式評估感度(Eop)、線路寬度粗糙度(LWR)、解析度、焦點景深寬度(DOF)特性。
[阻劑圖型之形成] 將實施例3~4及比較例1~2之各阻劑組成物分別塗佈於12英吋之矽晶圓上,於加熱板上,進行90℃、60秒鐘之曝前燒焙(PAB)處理,經乾燥處理,形成膜厚90nm之阻劑膜。 其次,使用浸潤用ArF曝光裝置NSR-S610C[尼康公司製;NA1.30,Cross pole,0.85/0.67,浸潤媒體:水],介由LS用遮罩,以ArF準分子雷射(193nm)對該阻劑膜進行選擇性照射。 隨後,進行80℃、60秒鐘之曝後燒焙(PEB)處理。 其次,於23℃下,使用乙酸丁酯進行30秒鐘的溶劑顯影後,進行振動乾燥。其結果,無論任一個實施例中,皆形成有空間寬度45nm/間距102nm之線路與空間圖型(SL圖型)。
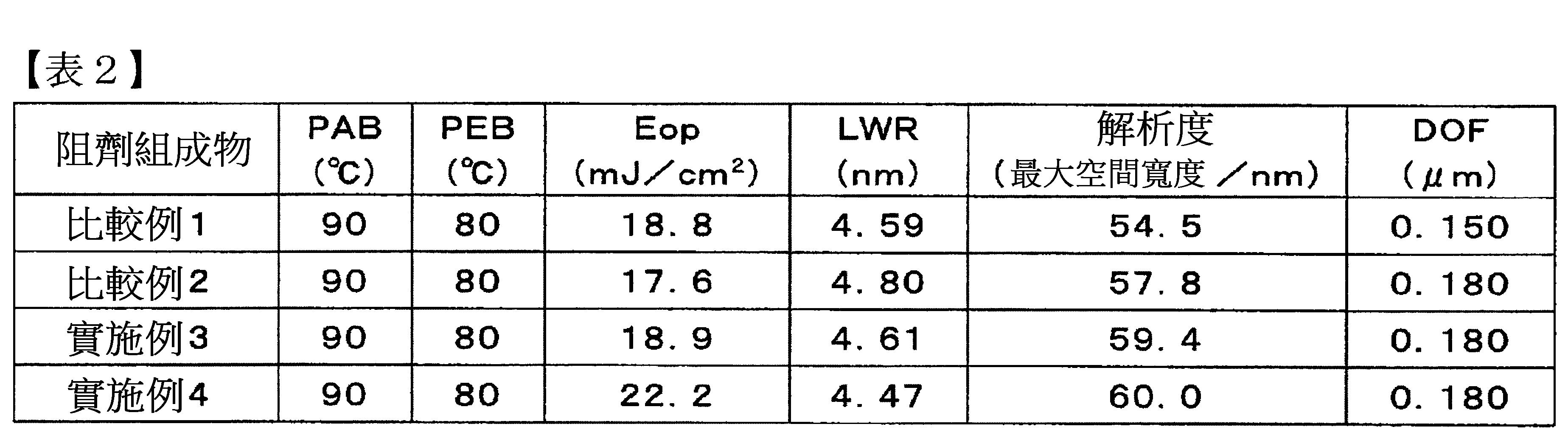
[感度(Eop)之評估] 於上述之阻劑圖型之形成中,求取形成標靶尺寸的SL圖型之最佳曝光量(mJ/cm2
)。該結果以「Eop(mJ/cm2
)」標記如表2所示。
[線路寬度粗糙度(LWR)之評估] 對依上述之阻劑圖型之形成而形成的SL圖型,求取標示LWR尺度之3σ。將其以「LWR(nm)」標記如表2所示。 「3σ」為,使用掃瞄型電子顯微鏡(加速電壓800V、商品名:S-9380、日立高科技公司製),測定線路長度方向的400處之線路位置,由該測定結果所求得的標準偏差(σ)之3倍值(3σ)(單位:nm)之意。 該3σ之值越小時,表示線路側壁的粗糙度越小,而可得到更均勻寬度的SL圖型之意。
[解析度之評估] 上述Eop中之臨界解析度,即,由最佳曝光量Eop逐漸少許增大曝光量形成SL圖型之際,使用掃瞄型電子顯微鏡(加速電壓800V、商品名:S-9380、日立高科技公司製)測定未倒塌而可解析的圖型之最大空間寬度。隨後,依將該圖型的最大空間寬度作為指標的下述之評估基準,評估該解析度。其結果以「解析度(最大空間寬度/nm)」標記如表2所示。 評估基準 A:未倒塌而可解析的圖型之最大空間寬度為58nm以上。 B:前述最大空間寬度為55nm以上、未達58nm。 C:前述最大空間寬度為未達55nm。
[焦點景深寬度(DOF)特性之評估] 上述之於阻劑圖型的形成中,於上述Eop中,將焦點適度地上下移動,依與形成上述阻劑圖型之相同方法形成阻劑圖型。此時,求取形成於空間部份的範圍之焦點景深寬度(DOF、單位:μm)。其結果以「DOF(μm)」標記如表2所示。 「DOF」係指,於同一曝光量下,將焦點上下移動進行曝光之際,可形成特定形狀之阻劑圖型的焦點深度之範圍,即可忠實地得到遮罩圖型之阻劑圖型之範圍之意。該範圍越廣(數值越大)時,表示製程寬容度越大之意。
由表2所示結果得知,使用本發明的實施例3~4之阻劑組成物,與比較例1~2之阻劑組成物相比較時,得知可以提高解析度,且以更低圖型粗糙度的良好形狀之方式,形成更微細的圖型。 此外,得知實施例3~4之阻劑組成物,亦具有良好的焦點景深寬度(DOF)特性,且亦具有較大的製程寬容度。 如上所述,即使欲形成空間寬度50nm以下的微細空間圖型時,確認使用本發明,即可以提高解析度,且,以更低圖型粗糙度的良好形狀之方式,形成更微細的圖型。
Claims (7)
- 如請求項1之阻劑組成物,其中,前述化合物(D1)之共軛酸的酸解離常數(pKa)為1.10以下。
- 如請求項1之阻劑組成物,其中,前述化合物(D1)之辛醇/水分配係數(logPow)為-0.90以上、2.00以下。
- 如請求項1之阻劑組成物,其尚含有經由曝光而產生 酸的酸產生劑成份(B)(又,前述化合物(D1)除外)。
- 如請求項1之阻劑組成物,其中,前述基材成份(A)為含有高分子化合物(A1),該高分子化合物(A1)為具有:含有經由酸之作用而增大極性的酸分解性基的結構單位(a1)。
- 一種阻劑圖型形成方法,其特徵為具有:於支撐體上,使用請求項1~5中任一項之阻劑組成物形成阻劑膜之步驟、使前述阻劑膜曝光之步驟,及使前述曝光後的阻劑膜進行顯影,形成阻劑圖型之步驟。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2017-073070 | 2017-03-31 | ||
| JP2017073070A JP6890454B2 (ja) | 2017-03-31 | 2017-03-31 | レジスト組成物及びレジストパターン形成方法、並びに、化合物及び酸拡散制御剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| TW201902883A TW201902883A (zh) | 2019-01-16 |
| TWI761475B true TWI761475B (zh) | 2022-04-21 |
Family
ID=63668807
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW107110436A TWI761475B (zh) | 2017-03-31 | 2018-03-27 | 阻劑組成物及阻劑圖型形成方法,與化合物及酸擴散控制劑 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US10514600B2 (zh) |
| JP (1) | JP6890454B2 (zh) |
| KR (1) | KR102483029B1 (zh) |
| CN (1) | CN108693711B (zh) |
| TW (1) | TWI761475B (zh) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20230092100A (ko) * | 2021-12-16 | 2023-06-26 | 주식회사 동진쎄미켐 | 염 화합물 및 이를 포함하는 산확산 억제제, 포토레지스트 조성물 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998039312A1 (en) * | 1997-03-04 | 1998-09-11 | Consiglio Nazionale Delle Ricerche | Stable arenediazonium salts, a process for the preparation thereof and the uses thereof |
| US20040161694A1 (en) * | 2002-08-23 | 2004-08-19 | Fuji Photo Film Co., Ltd. | Heat-sensitive recording material |
| TW200740737A (en) * | 2006-03-16 | 2007-11-01 | Toyo Gosei Co Ltd | Sulfonium salts |
| TW201426169A (zh) * | 2012-12-07 | 2014-07-01 | Tokyo Ohka Kogyo Co Ltd | 光阻組成物及光阻圖型之形成方法 |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4387222A (en) * | 1981-01-30 | 1983-06-07 | Minnesota Mining And Manufacturing Company | Cyclic perfluoroaliphaticdisulfonimides |
| JP2005172949A (ja) * | 2003-12-08 | 2005-06-30 | Tokyo Ohka Kogyo Co Ltd | ホトレジスト組成物およびレジストパターン形成方法 |
| JP2005173468A (ja) * | 2003-12-15 | 2005-06-30 | Tokyo Ohka Kogyo Co Ltd | ポジ型レジスト組成物およびレジストパターン形成方法 |
| JP2009025723A (ja) | 2007-07-23 | 2009-02-05 | Fujifilm Corp | ネガ型現像用レジスト組成物及びこれを用いたパターン形成方法 |
| TWI391781B (zh) * | 2007-11-19 | 2013-04-01 | Tokyo Ohka Kogyo Co Ltd | 光阻組成物,光阻圖型之形成方法,新穎化合物及酸產生劑 |
| US8455176B2 (en) * | 2008-11-12 | 2013-06-04 | Az Electronic Materials Usa Corp. | Coating composition |
| KR20100121427A (ko) * | 2009-05-07 | 2010-11-17 | 제이에스알 가부시끼가이샤 | 감방사선성 수지 조성물 |
| JP5310656B2 (ja) * | 2010-06-18 | 2013-10-09 | 信越化学工業株式会社 | シルフェニレン含有光硬化性組成物、それを用いたパターン形成方法およびその方法により得られる光半導体素子 |
| JP5856809B2 (ja) * | 2011-01-26 | 2016-02-10 | 東京応化工業株式会社 | レジスト組成物、レジストパターン形成方法 |
| JP5789396B2 (ja) * | 2011-04-05 | 2015-10-07 | 東京応化工業株式会社 | レジストパターン形成方法 |
| JP6252292B2 (ja) * | 2013-04-15 | 2017-12-27 | 住友化学株式会社 | 塩、レジスト組成物及びレジストパターンの製造方法 |
| KR101702510B1 (ko) * | 2013-09-06 | 2017-02-03 | 제일모직 주식회사 | 감광성 수지막의 제조 방법, 및 그 제조 방법에 의해 제조된 감광성 수지막 |
| EP3590975B1 (en) * | 2017-02-28 | 2022-05-04 | FUJIFILM Corporation | Curable composition, lithographic printing plate precursor, method for preparing lithographic printing plate, and compound |
-
2017
- 2017-03-31 JP JP2017073070A patent/JP6890454B2/ja active Active
-
2018
- 2018-03-23 US US15/934,378 patent/US10514600B2/en active Active
- 2018-03-27 TW TW107110436A patent/TWI761475B/zh active
- 2018-03-27 KR KR1020180035426A patent/KR102483029B1/ko active IP Right Grant
- 2018-03-29 CN CN201810271130.7A patent/CN108693711B/zh active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1998039312A1 (en) * | 1997-03-04 | 1998-09-11 | Consiglio Nazionale Delle Ricerche | Stable arenediazonium salts, a process for the preparation thereof and the uses thereof |
| US20040161694A1 (en) * | 2002-08-23 | 2004-08-19 | Fuji Photo Film Co., Ltd. | Heat-sensitive recording material |
| TW200740737A (en) * | 2006-03-16 | 2007-11-01 | Toyo Gosei Co Ltd | Sulfonium salts |
| TW201426169A (zh) * | 2012-12-07 | 2014-07-01 | Tokyo Ohka Kogyo Co Ltd | 光阻組成物及光阻圖型之形成方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| JP2018173606A (ja) | 2018-11-08 |
| TW201902883A (zh) | 2019-01-16 |
| CN108693711B (zh) | 2023-06-06 |
| US20180284610A1 (en) | 2018-10-04 |
| KR102483029B1 (ko) | 2022-12-29 |
| US10514600B2 (en) | 2019-12-24 |
| JP6890454B2 (ja) | 2021-06-18 |
| KR20180111596A (ko) | 2018-10-11 |
| CN108693711A (zh) | 2018-10-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TWI699353B (zh) | 阻劑組成物及阻劑圖型形成方法、與化合物及酸擴散控制劑 | |
| TWI612381B (zh) | 光阻組成物、光阻圖型之形成方法、高分子化合物、化合物 | |
| JP7042551B2 (ja) | レジスト組成物及びレジストパターン形成方法 | |
| TWI795498B (zh) | 阻劑組成物、阻劑圖型形成方法,與化合物及酸擴散控制劑 | |
| TWI534541B (zh) | 光阻組成物及光阻圖型之形成方法 | |
| TW201937278A (zh) | 阻劑組成物及阻劑圖型形成方法 | |
| TW202030550A (zh) | 阻劑組成物及阻劑圖型形成方法 | |
| TW201805721A (zh) | 光阻組成物及光阻圖型形成方法 | |
| JP7101541B2 (ja) | レジスト組成物及びレジストパターン形成方法 | |
| TWI756346B (zh) | 阻劑組成物及阻劑圖型之形成方法 | |
| TW201936664A (zh) | 阻劑組成物及阻劑圖型形成方法 | |
| JP2022075817A (ja) | 化合物 | |
| TWI814949B (zh) | 阻劑組成物、阻劑圖型形成方法及化合物 | |
| TWI756395B (zh) | 阻劑組成物、阻劑圖型形成方法、含氟高分子化合物,及化合物 | |
| TW202001423A (zh) | 阻劑組成物及阻劑圖型形成方法 | |
| TWI631420B (zh) | 光阻組成物、光阻圖型之形成方法及高分子化合物 | |
| TWI758447B (zh) | 阻劑組成物及阻劑圖型形成方法 | |
| TWI762606B (zh) | 阻劑組成物及阻劑圖型形成方法 | |
| TW201439670A (zh) | 光阻組成物,光阻圖型之形成方法 | |
| TWI761475B (zh) | 阻劑組成物及阻劑圖型形成方法,與化合物及酸擴散控制劑 | |
| TW201937276A (zh) | 阻劑組成物及阻劑圖型形成方法 | |
| TWI597570B (zh) | 光阻組成物及光阻圖型之形成方法 | |
| TW202036157A (zh) | 阻劑組成物、阻劑圖型形成方法,及高分子化合物 | |
| KR20140067911A (ko) | 레지스트 조성물, 레지스트 패턴 형성 방법 | |
| TWI620986B (zh) | 光阻圖型之形成方法及光阻組成物 |