RU2716025C1 - ЛЕКАРСТВЕННАЯ ФОРМА С УЛУЧШЕННЫМИ ХАРАКТЕРИСТИКАМИ pH-ЗАВИСИМОГО ВЫСВОБОЖДЕНИЯ ПРЕПАРАТА, СОДЕРЖАЩАЯ ЭЗОМЕПРАЗОЛ ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМУЮ СОЛЬ - Google Patents
ЛЕКАРСТВЕННАЯ ФОРМА С УЛУЧШЕННЫМИ ХАРАКТЕРИСТИКАМИ pH-ЗАВИСИМОГО ВЫСВОБОЖДЕНИЯ ПРЕПАРАТА, СОДЕРЖАЩАЯ ЭЗОМЕПРАЗОЛ ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМУЮ СОЛЬ Download PDFInfo
- Publication number
- RU2716025C1 RU2716025C1 RU2019105024A RU2019105024A RU2716025C1 RU 2716025 C1 RU2716025 C1 RU 2716025C1 RU 2019105024 A RU2019105024 A RU 2019105024A RU 2019105024 A RU2019105024 A RU 2019105024A RU 2716025 C1 RU2716025 C1 RU 2716025C1
- Authority
- RU
- Russia
- Prior art keywords
- methacrylic acid
- weight
- coating
- esomeprazole
- release
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0002—Galenical forms characterised by the drug release technique; Application systems commanded by energy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2072—Pills, tablets, discs, rods characterised by shape, structure or size; Tablets with holes, special break lines or identification marks; Partially coated tablets; Disintegrating flat shaped forms
- A61K9/2077—Tablets comprising drug-containing microparticles in a substantial amount of supporting matrix; Multiparticulate tablets
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2833—Organic macromolecular compounds
- A61K9/284—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2833—Organic macromolecular compounds
- A61K9/284—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone
- A61K9/2846—Poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2833—Organic macromolecular compounds
- A61K9/286—Polysaccharides, e.g. gums; Cyclodextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2806—Coating materials
- A61K9/2833—Organic macromolecular compounds
- A61K9/286—Polysaccharides, e.g. gums; Cyclodextrin
- A61K9/2866—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2886—Dragees; Coated pills or tablets, e.g. with film or compression coating having two or more different drug-free coatings; Tablets of the type inert core-drug layer-inactive layer
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
- A61K9/2893—Tablet coating processes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5005—Wall or coating material
- A61K9/5021—Organic macromolecular compounds
- A61K9/5026—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5073—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals having two or more different coatings optionally including drug-containing subcoatings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5084—Mixtures of one or more drugs in different galenical forms, at least one of which being granules, microcapsules or (coated) microparticles according to A61K9/16 or A61K9/50, e.g. for obtaining a specific release pattern or for combining different drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
Abstract
Представлена лекарственная форма, содержащая эзомепразол или его фармацевтически приемлемую соль для лечения желудочных и рефлюксных заболеваний пищевода. Лекарственная форма содержит ядро, содержащее эзомепразол, слой эндотелиального покрытия, сформированный на ядре, и слой контролирующего высвобождение покрытия, сформированный на слое эндотелиального покрытия. Слой эндотелиального покрытия содержит по меньшей мере одно вещество, выбранное из гидроксипропилметилцеллюлозы, поливинилпирролидона, низкозамещенной гидроксипропилцеллюлозы, крахмала и желатина. Слой контролирующего высвобождение покрытия содержит полимер, в котором сополимер S метакриловой кислоты и сополимер L метакриловой кислоты смешаны в весовом соотношении от 1,5:1 до 3,5:1 в качестве материала основы контролирующего высвобождение покрытия, где сополимер S метакриловой кислоты представляет собой анионный сополимер, содержащий метакриловую кислоту и метилметакрилат в соотношении 1:2, а сополимер L метакриловой кислоты – анионный сополимер, содержащий метакриловую кислоту и метилметакрилат в соотношении 1:1. Вес сополимера S метакриловой кислоты и сополимера L метакриловой кислоты в качестве материалов основы контролирующего высвобождение покрытия составляет от 15 до 40% относительно веса таблетки с эндотелиальным покрытием. Лекарственная форма при испытании на высвобождение через 2 часа элюирует 5% или меньше эзомепразола или его фармацевтически приемлемой соли, а через 6 часов элюируется по меньшей мере 90% эзомепразола или его фармацевтически приемлемой соли. Также описан способ получения лекарственной формы эзомепразола. Лекарственная форма по изобретению характеризуется улучшенными характеристиками pH-зависимого высвобождения препарата, начинает высвобождать эзомепразол или его фармацевтически приемлемую соль после заданного времени задержки при пероральном введении, продолжает высвобождение в течение заданного времени и заканчивает высвобождение через заранее определенное время, обеспечивая тем самым отменное удобство для пациента и превосходные терапевтические эффекты по сравнению с другими стандартными формами. 3 н. и 5 з.п. ф-лы, 2 ил., 10 табл., 4 пр.
Description
Область техники, к которой относится изобретение
Настоящее изобретение касается новой лекарственной формы с улучшенными характеристиками pH-зависимого высвобождения препарата, содержащей эзомепразол или его фармацевтически приемлемую соль, а также способа её получения.
Уровень техники
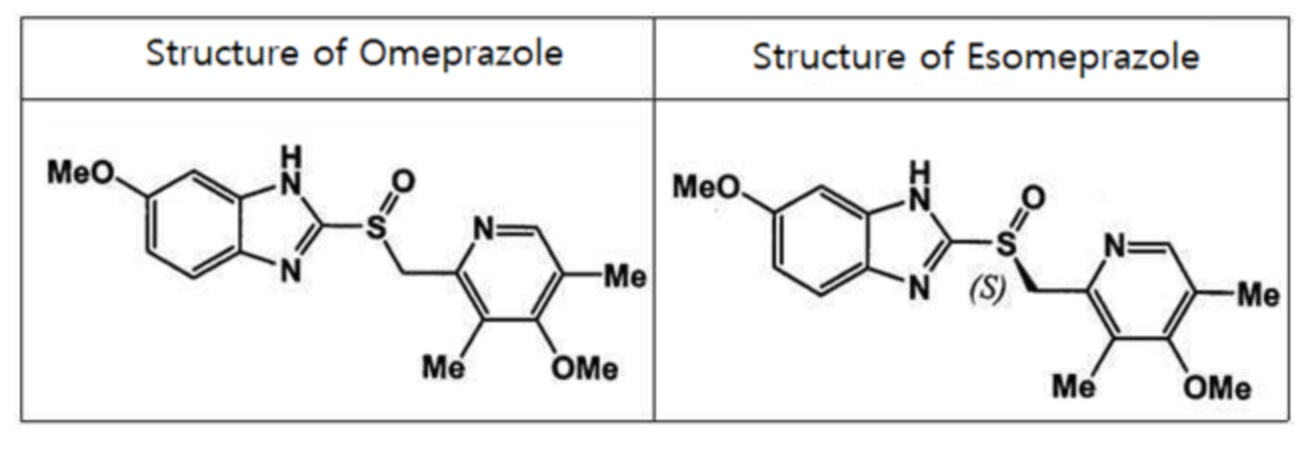
Эзомепразол [(S)-5-метокси-2-[(4-метокси-3,5-диметилпиридин-2-ил)метилсульфинил]-3H-бензимидазол)] является одним из ингибиторов протонного насоса (PPI) со структурой, представленной формулой 2 в виде (S)-энантиомера, среди двух оптических изомеров омепразола со структурой, представленной формулой 1. Из двух оптических изомеров омепразола (R)-энантиомер быстрее метаболизируется в неактивный метаболит (не обладающий активностью) и имеет большое отличие в скорости метаболизма между ними по сравнению с (S)-энантиомером. Таким образом, (R)-энантиомер проявляет больше побочных эффектов, более слабые эффекты лечения и менее равномерные показатели лечения, чем (S)-энантиомер, тогда как (S)-энантиомер, то есть эзомепразол, имеет преимущество в меньшем воздействии на метаболизм в печени по сравнению с (R)-энантиомером, а также с рацематом омепразола.
Таблица 1. Структуры омепразола и эзомепразола
Ингибиторы протонного насоса, к которым принадлежит эзомепразол, обладают свойством ингибирования секреции желудочной кислоты у млекопитающих, включая человека, путем регуляции секреции желудочной кислоты на последней стадии пути секреции кислоты. Таким образом, ингибиторы протонного насоса можно использовать для профилактики и лечения желудочных и рефлюксных заболеваний пищевода типа рефлюкс-эзофагита и заболеваний, связанных с гиперпролиферацией желудка, включая гастрит, дуоденит, язвы желудка, язвы двенадцатиперстной кишки и пептические язвы.
С другой стороны, эзомепразол легко разлагается или трансформируется в кислых условиях. Поэтому пероральные препараты, содержащие эзомепразол, не должны контактировать с кислым желудочным соком и должны доставляться в область желудочно-кишечного тракта, где рН почти нейтрален и может происходить быстрое всасывание. По этой причине активно разрабатывались лекарственные формы с использованием такого способа, как формирование энтеросолюбильных покрытий.
Однако исследования лекарственных форм эзомепразола до настоящего времени были сосредоточены только на разработке энтеросолюбильных покрытий для всасывания в кишечнике при одновременном предотвращении воздействия желудочной кислоты в желудке. Разработка таких форм, которые начинают высвобождаться после заданного времени задержки после перорального введения, продолжают высвобождаться в течение требуемого периода времени и заканчивают высвобождение через определенное время, исходя из исследования характеристик рН-зависимого высвобождения, была недостаточной и неудовлетворительной. В этом контексте существует безотлагательная и все возрастающая потребность в новых формах, содержащих эзомепразол и его фармацевтически приемлемые соли, с такими улучшенными характеристиками рН-зависимого высвобождения.
На этом техническом фоне авторы настоящего изобретения обнаружили, что характеристики рН-зависимого высвобождения эзомепразола или его фармацевтически приемлемой соли можно значительно улучшить, если на ядрах, содержащих эзомепразол или его фармацевтически приемлемую соль, формируется слой эндотелиального покрытия, на котором находится слой контролирующего высвобождение покрытия, содержащий полимер, состоящий из сополимера метакриловой кислоты S и сополимера метакриловой кислоты L, смешанных в определенном соотношении, причем сополимер метакриловой кислоты S и сополимер метакриловой кислоты L, содержащиеся в слое контролирующего высвобождение покрытия, присутствуют в определенном соотношении по отношению к весу таблетки с эндотелиальным покрытием или слоя эндотелиального покрытия, и тем самым совершили настоящее изобретение.
Раскрытие изобретения
Итак, объектом настоящего изобретения является получение новой лекарственной формы с улучшенными характеристиками рН-зависимого высвобождения препарата, содержащего эзомепразол или его фармацевтически приемлемую соль, а также способ её получения.
В соответствии с настоящим изобретением, вышеуказанные и другие цели могут быть достигнуты путем получения лекарственной формы, включающей: (a) ядро, содержащее эзомепразол или его фармацевтически приемлемую соль в качестве активного ингредиента, (b) слой эндотелиального покрытия, сформированный на ядре, и (c) слой контролирующего высвобождение покрытия, сформированный на слое эндотелиального покрытия, причем материал эндотелиального покрытия, содержащийся в слое эндотелиального покрытия, и сополимер метакриловой кислоты S и сополимер метакриловой кислоты L, содержащиеся в качестве материала основы контролирующего высвобождение покрытия в слое контролирующего высвобождение покрытия, присутствуют в определенном соотношении.
Лекарственная форма может быть выбрана из группы, состоящей из гранул, минитаблеток (MUST), таблеток, смеси гранул и минитаблеток и капсул, но настоящее изобретение не ограничивается этим. Гранулы и/или минитаблетки могут быть заключены в капсулы.
В соответствии с другим аспектом настоящего изобретения, предусмотрен способ получения лекарственной формы, содержащей эзомепразол или его фармацевтически приемлемую соль, включающий: (a) смешивание эзомепразола или его фармацевтически приемлемой соли с разбавителем, (b) добавление в смесь из стадии (a) разрыхлителя, связующего и смазывающего вещества с последующим смешиванием, (c) гранулирование смеси из стадии (b) и затем таблетированиe с получением минитаблеток (MUST) или таблеток, (d) нанесение на таблетированные минитаблетки или таблетки, полученные на стадии (c), эндотелиального покрытия с помощью сушилки с псевдоожиженным слоем (FBG) и устройства для нанесения покрытия, и (e) формирование у минитаблеток или таблеток с эндотелиальным покрытием, полученных на стадии (d), слоя контролирующего высвобождение покрытия с использованием смеси, содержащей сополимер метакриловой кислоты S и сополимер метакриловой кислоты L.
Краткое описание фигур
Вышеуказанные и другие цели, признаки и другие преимущества настоящего изобретения станут более понятными из следующего подробного описания в сочетании с прилагаемыми чертежами.
На фиг. 1 представлены результаты испытания на характеристики высвобождения в отношении лекарственной формы по настоящему изобретению, в которой соотношение в смеси между сополимером S метакриловой кислоты и сополимером L метакриловой кислоты, присутствующими в качестве материала основы контролирующего высвобождение покрытия в слое контролирующего высвобождение покрытия, составляет от 2:1 до 3:1 (вес/вес), а вес сополимера S метакриловой кислоты и сополимера L метакриловой кислоты, присутствующих в качестве материала основы контролирующего высвобождение покрытия в слое контролирующего высвобождение покрытия, составляет от 20 до 35% (вес/вес) относительно веса таблетки с эндотелиальным покрытием.
На фиг. 2 представлены результаты испытания на характеристики высвобождения в отношении сравнительной лекарственной формы, в которой соотношение в смеси между сополимером S метакриловой кислоты и сополимером L метакриловой кислоты, присутствующими в качестве материала основы контролирующего высвобождение покрытия в слое контролирующего высвобождение покрытия, составляет 6:1 (вес/вес), а вес сополимера S метакриловой кислоты и сополимера L метакриловой кислоты, присутствующих в качестве материала основы контролирующего высвобождение покрытия в слое контролирующего высвобождение покрытия, составляет от 10 до 40% (вес/вес) относительно веса таблетки с эндотелиальным покрытием.
Осуществление изобретения
Если не указано иначе, все используемые здесь технические и научные термины имеют те же значения, которые известны специалистам в той области, к которой относится настоящее изобретение. В общем, используемая здесь номенклатура хорошо известна в данной области, она же обычно и применяется.
В одном аспекте настоящего изобретения предусмотрены фармацевтические композиции, содержащие эзомепразол или его фармацевтически приемлемую соль, которые включают:
(a) ядро, содержащее эзомепразол или его фармацевтически приемлемую соль в качестве активного ингредиента;
(b) слой эндотелиального покрытия, сформированный на ядре; и
(c) слой контролирующего высвобождение покрытия, сформированный на слое эндотелиального покрытия и содержащий полимер, состоящий из сополимера метакриловой кислоты S и сополимера метакриловой кислоты L, смешанных в определенном соотношении;
причем слой эндотелиального покрытия содержит по меньшей мере одно, выбранное из группы, состоящей из гидроксипропилметилцеллюлозы (HPMC), поливинилпирролидона (PVP), низкозамещенной гидроксипропилцеллюлозы (HPC-L), крахмала, желатина и этилцеллюлозы (ЕС),
слой контролирующего высвобождение покрытия содержит смесь из сополимера S метакриловой кислоты и сополимера L метакриловой кислоты в соотношении от 1,5:1 до 3,5:1 (вес/вес), предпочтительно от 2:1 до 3:1, а
вес сополимера S метакриловой кислоты и сополимера L метакриловой кислоты в качестве материала основы контролирующего высвобождение покрытия составляет от 15 до 40% (вес/вес), предпочтительно от 20 до 35% (вес/вес) относительно веса таблетки с эндотелиальным покрытием.
Лекарственная форма по настоящему изобретению предпочтительно представлена в виде гранул, минитаблеток (MUST), таблеток, смеси гранул и минитаблеток или капсул, но настоящее изобретение не ограничивается этим, а данные гранулы или минитаблетки могут быть заключены в капсулы.
Лекарственная форма по настоящему изобретению практически не разлагается в желудке и начинает выделять эзомепразол или его фармацевтически приемлемую соль в желудочно-кишечном тракте в диапазоне рН от 6,5 до 7,0. В частности, лекарственная форма начинает выделять эзомепразол или его фармацевтически приемлемую соль при рН от 6,7 до 6,9 после задержки в 2 часа, а заканчивает выделять через 6 часов, что дает преимущества большого удобства для пациента и получения отличного терапевтического эффекта.
В лекарственных формах по настоящему изобретению можно использовать любые фармацевтически приемлемые соли эзомепразола без ограничений, если только они обычно применяются в данной области, а предпочтительные примеры фармацевтически приемлемых солей эзомепразола включают, без ограничения, соли металлов типа магниевых солей (Mg), стронциевых солей (Sr), литиевых солей, натриевых солей, калиевых солей или кальциевых солей эзомепразола и аммониевые соли эзомепразола. Наиболее предпочтительно используются магниевые соли или стронциевые соли эзомепразола.
Кроме того, в лекарственных формах по настоящему изобретению можно использовать эзомепразол или его фармацевтически приемлемую соль в виде ангидрида или гидрата.
У лекарственной формы по настоящему изобретению ядро, содержащее эзомепразол или его фармацевтически приемлемую соль, также может содержать надлежащее количество обычных приемлемых эксципиентов, наряду с эзомепразолом или его фармацевтически приемлемой солью в качестве активного ингредиента. Предпочтительно ядро может содержать один или несколько эксципиентов из числа разбавителей, связующих веществ, разрыхлителей, смазывающих веществ, поверхностно-активных веществ, антиоксидантов, консервантов и стабилизаторов, без ограничения.
Разбавитель, который может содержаться в ядрах лекарственной формы по настоящему изобретению, может включать по меньшей мере одно, выбранное из группы, состоящей из маннита, микрокристаллической целлюлозы, лактозы, целлюлозы и их производных, двухосновного или трехосновного фосфата кальция, эритрита, низкозамещенной гидроксипропилцеллюлозы, желатинизированного крахмала, сорбита и ксилита. Однако предпочтительно используется маннит и/или микрокристаллическая целлюлоза.
Связующее может быть выбрано из группы, состоящей из гидроксипропилцеллюлозы (HPC), соповидона (сополимера винилпирролидона с другими винильными производными), гидроксипропилметилцеллюлозы (HPMC), поливинилпирролидона (повидона), желатинизированного крахмала и низкозамещенной гидроксипропилцеллюлозы (HPC-L), но не ограничивается этим. Предпочтительно используется гидроксипропилцеллюлоза.
Разрыхлитель может включать по меньшей мере одно, выбранное из группы, состоящей из натриевой кроскармеллозы, кукурузного крахмала, кросповидона, низкозамещенной гидроксипропилцеллюлозы (HPC-L) или желатинизированного крахмала, но не ограничивается этим. Предпочтительно используется натриевая кроскармеллоза.
Смазывающее вещество может включать по меньшей мере одно, выбранное из группы, состоящей из стеарилфумарата натрия, стеарата магния, талька, полиэтиленгликоля, бегената кальция, стеарата кальция и гидрогенизированного касторового масла, но не ограничивается этим. Предпочтительно используется стеарилфумарат натрия.
У лекарственной формы по настоящему изобретению слой эндотелиального покрытия, сформированный на ядре, содержащем эзомепразол или его фармацевтически приемлемую соль, включает по меньшей мере одно вещество, выбранное из группы, состоящей из гидроксипропилметилцеллюлозы (HPMC), поливинилпирролидона (PVP), низкозамещенной гидроксипропилцеллюлозы (HPC-L), крахмала, желатина и этилцеллюлозы (EC). Предпочтительно используется гидроксипропилметилцеллюлоза (HPMC).
В настоящем изобретении термин “таблетки с эндотелиальным покрытием” означает минитаблетки (MUST), содержащие слой эндотелиального покрытия, сформированный на ядре, содержащем эзомепразол или его фармацевтически приемлемую соль в качестве активного ингредиента.
По меньшей мере одно вещество, выбранное из группы, состоящей из гидроксипропилметилцеллюлозы (HPMC), поливинилпирролидона (PVP), низкозамещенной гидроксипропилцеллюлозы (HPC-L), крахмала, желатина и этилцеллюлозы (EC), которое содержится в слое эндотелиального покрытия, предпочтительно присутствует в количестве от 4,4 до 5,2% (вес/вес), предпочтительно от 4,7 до 4,9% (вес/вес) относительно веса таблетки с эндотелиальным покрытием.
У лекарственной формы по настоящему изобретению слой контролирующего высвобождение покрытия, сформированный на слое эндотелиального покрытия (которое здесь может использоваться взаимозаменяемо со “слоем энтеросолюбильного покрытия”), содержит смесь сополимера S метакриловой кислоты и сополимера L метакриловой кислоты в качестве материала основы контролирующего высвобождение покрытия в соотношении от 1,5:1 до 3,5:1 (вес/вес), предпочтительно от 2:1 до 3:1 (вес/вес).
Сополимер S метакриловой кислоты представляет собой анионный сополимер, содержащий метакриловую кислоту и метилметакрилат в соотношении примерно 1:2, который продается под торговым названием “Eudragit S-100”, а сополимер L метакриловой кислоты – анионный сополимер, содержащий метакриловую кислоту и метилметакрилат в соотношении около 1:1, который продается под торговым названием “Eudragit L-100”.
В настоящем изобретении термин “таблетки с контролирующим высвобождение покрытием” означает минитаблетки (MUST) или таблетки, содержащие слой контролирующего высвобождение покрытия, сформированный на слое эндотелиального покрытия.
У лекарственной формы по настоящему изобретению материалы основы контролирующего высвобождение покрытия, содержащиеся в слое контролирующего высвобождение покрытия, а именно сополимер S метакриловой кислоты и сополимер L метакриловой кислоты, присутствуют в количестве от 15 до 40% (вес/вес), предпочтительно от 20 до 35% (вес/вес) относительно веса таблетки с эндотелиальным покрытием.
Содержание по меньшей мере одного вещества, выбранного из группы, состоящей из гидроксипропилметилцеллюлозы (HPMC), поливинилпирролидона (PVP), низкозамещенной гидроксипропилцеллюлозы (HPC-L), крахмала, желатина и этилцеллюлозы (EC), которое содержится в слое эндотелиального покрытия, относительно веса сополимера S метакриловой кислоты и сополимера L метакриловой кислоты составляет от 3,5 до 8,0 (вес/вес), предпочтительно от 4,2 до 7,4 (вес/вес).
Кроме того, лекарственная форма по настоящему изобретению отличается тем,
что при испытании на высвобождение (растворение) с использованием искусственной кишечной жидкости (среды) со значением рН от 6,7 до 6,9 при 75 об/мин и 37°C в соответствии с лопастным методом USP через 2 часа элюируется 5% или меньше, предпочтительно 2% или меньше эзомепразола или его фармацевтически приемлемой соли, а через 6 часов элюируется 90% или больше, предпочтительно 98% или больше эзомепразола или его фармацевтически приемлемой соли.
что при испытании на высвобождение (растворение) с использованием искусственной кишечной жидкости (среды) со значением рН от 6,7 до 6,9 при 75 об/мин и 37°C в соответствии с лопастным методом USP через 2 часа элюируется 5% или меньше, предпочтительно 2% или меньше эзомепразола или его фармацевтически приемлемой соли, а через 6 часов элюируется 90% или больше, предпочтительно 98% или больше эзомепразола или его фармацевтически приемлемой соли.
Если содержание по меньшей мере одного вещества, выбранного из группы, состоящей из гидроксипропилметилцеллюлозы (HPMC), поливинилпирролидона (PVP), низкозамещенной гидроксипропилцеллюлозы (HPC-L), крахмала, желатина и этилцеллюлозы (EC), которое содержится в слое эндотелиального покрытия, относительно веса сополимера S метакриловой кислоты и сополимера L метакриловой кислоты в качестве материала основы контролирующего высвобождение покрытия по настоящему изобретению составляет менее 3,5 (вес/вес) или более 8,0 (вес/вес), то эзомепразол или его фармацевтически приемлемая соль начинает элюироваться еще до требуемого времени задержки по настоящему изобретению либо эзомепразол или его фармацевтически приемлемая соль не элюируется в достаточной степени по достижении требуемого времени растворения.
Если содержание по меньшей мере одного вещества, выбранного из группы, состоящей из гидроксипропилметилцеллюлозы (HPMC), поливинилпирролидона (PVP), низкозамещенной гидроксипропилцеллюлозы (HPC-L), крахмала, желатина и этилцеллюлозы (EC), относительно веса таблетки с эндотелиальным покрытием составляет менее 4,4 (вес/вес) или более 5,2 (вес/вес), то эзомепразол или его фармацевтически приемлемая соль начинает элюироваться еще до требуемого времени задержки по настоящему изобретению либо эзомепразол или его фармацевтически приемлемая соль не элюируется в достаточной степени по достижении требуемого времени растворения.
В другом аспекте настоящего изобретения предусмотрен способ получения лекарственной формы, содержащей эзомепразол или его фармацевтически приемлемую соль в качестве активного ингредиента.
В частности, способ получения лекарственной формы, содержащей эзомепразол или его фармацевтически приемлемую соль в качестве активного ингредиента, будет описан в виде примера, в котором форма представляет собой минитаблетки (MUST) или таблетки. В частности, лекарственная форма может быть получена способом, включающим, без ограничения:
(a) смешивание эзомепразола или его фармацевтически приемлемой соли с разбавителем;
(b) добавление разрыхлителя, связующего и смазывающего вещества в смесь из стадии (a) с последующим перемешиванием;
(c) сухое гранулирование смеси из стадии (b), а затем таблетирование с получением минитаблеток или таблеток;
(d) нанесение эндотелиального покрытия на таблетированные минитаблетки или таблетки, полученные на стадии (c), с помощью сушилки с псевдоожиженным слоем (FBG) и устройства для нанесения покрытия; и
(e) формирование у минитаблеток или таблеток с эндотелиальным покрытием, полученных на стадии (d), слоя контролирующего высвобождение покрытия, используя смесь, содержащую сополимер S метакриловой кислоты и сополимер L метакриловой кислоты.
В следующем аспекте настоящего изобретения предусмотрено применение лекарственной формы, содержащей эзомепразол или его фармацевтически приемлемую соль в качестве активного ингредиента, для профилактики и лечения желудочных и рефлюксных заболеваний пищевода типа рефлюкс-эзофагита и заболеваний, связанных с гиперпролиферацией желудка, включая гастрит, дуоденит, язвы желудка, язвы двенадцатиперстной кишки и пептические язвы, а также способ профилактики и лечения с помощью лекарственной формы, содержащей эзомепразол или его фармацевтически приемлемую соль в качестве активного ингредиента, для профилактики и лечения желудочных и рефлюксных заболеваний пищевода типа рефлюкс-эзофагита и заболеваний, связанных с гиперпролиферацией желудка, включая гастрит, дуоденит, язвы желудка, язвы двенадцатиперстной кишки и пептические язвы, который включает введение лекарственной формы по настоящему изобретению нуждающимся в лечении пациентам.
Примеры
Далее настоящее изобретение будет описано более подробно со ссылкой на примеры. Однако специалистам в данной области должно быть ясно, что эти примеры приводятся только для иллюстрации настоящего изобретения и не должны рассматриваться как ограничивающие объем настоящего изобретения.
Примеры 1-4. Получение таблеток, содержащих магниевую соль эзомепразола
Смешивали магниевую соль эзомепразола и маннит и гранулировали через кольцевое сито на 30 меш. Полученную смесь смешивали с микрокристаллической целлюлозой, натриевой кроскармеллозой, гидроксипропилцеллюлозой и стеарилфумаратом натрия в пустом блендере в течение 15 мин, получая конечную смесь. Конечную смесь подвергали сухой грануляции в роликовом уплотнителе, а полученные гранулы гранулировали через кольцевое сито на 20 меш.
Затем получали минитаблетки (MUST) с твердостью от 1 до 2 кПа и заданным весом в 7,5 мг путем таблетирования с пуансоном MUST диаметром 2,0 мм в таблеточной машине.
Состав конечного ядра, содержащего магниевую соль эзомепразола, представлен в табл. 2.
Таблица 2. Состав ядра, содержащего магниевую соль эзомепразола
| Ингредиент | Вес (мг на 10 таблеток) |
Вес (%) |
|
| Ядро | Эзомепразол, магниевая соль | 21,7 | 28,9 |
| Микрокристаллическая целлюлоза | 15,0 | 20,0 | |
| Маннитол | 30,5 | 40,7 | |
| Кроскармеллоза натриевая | 2,4 | 3,2 | |
| Гидроксипропилцеллюлоза | 2,4 | 3,2 | |
| Стеарилфумарат натрия | 3,0 | 4,0 | |
| Итого | 75,0 | 100,0 |
Затем наносили покрытие в соответствии с составом из табл. 3 в устройстве для нанесения покрытий с псевдоожиженным слоем, получая таблетки с эндотелиальным покрытием весом 7,88 мг.
В таблетках с эндотелиальным покрытием присутствовал HPMC в соотношении 4,82 (вес/вес) относительно веса таблетки с эндотелиальным покрытием.
Таблица 3. Состав таблеток с эндотелиальным покрытием
| Ингредиент | Вес (мг на 10 таблеток) |
Вес (%) |
|
| Таблетка с эндотелиальным покрытием | Гидроксипропилметилцеллюлоза | 3,8 | 100,0 |
| Очищенная вода | надлежащее количество | - | |
| Итого | 78,8 | 100,0 |
После этого на вышеприведенные таблетки с эндотелиальным покрытием наносили покрытие в соответствии с составом из табл. 4 в устройстве для нанесения покрытий с псевдоожиженным слоем, получая таблетки, покрытые (таблетки с контролирующим высвобождение покрытием) слоями контролирующего высвобождение покрытия (слоями энтеросолюбильного покрытия), как показано в Примерах 1-4.
Таблица 4. Состав слоя контролирующего высвобождение покрытия в соответствии с примерами из настоящего изобретения
| Вес (мг на 10 таблеток) | |||||
| Ингредиент | Eudragit S/L=2:1 | Eudragit S/L=3:1 | |||
| Пример 1 | Пример 2 | Пример 3 | Пример 4 | ||
| Слой контролирующего высвобождение покрытия |
Eudragit S-100 | 13,3 | 18,6 | 12,0 | 18,0 |
| Eudragit L-100 | 6,7 | 9,4 | 4,0 | 6,0 | |
| Триэтилцитрат | 2,0 | 2,8 | 1,6 | 2,4 | |
| Тальк | 10,0 | 14,0 | 8,0 | 12,0 | |
| Этанол | надлежащее количество | надлежащее количество | надлежащее количество | надлежащее количество | |
| Дистиллированная вода | надлежащее количество | надлежащее количество | надлежащее количество | надлежащее количество | |
| Итого | 110,8 | 123,6 | 104,4 | 117,2 | |
В примерах 1 и 2 из табл. 4 представлены таблетки, в которых Eudragit S-100 и L-100 в качестве материалов основы контролирующего высвобождение покрытия смешаны в соотношении 2:1, а слой контролирующего высвобождение покрытия составляет от 25 до 35% (вес/вес) относительно веса таблетки с эндотелиальным покрытием. В примерах 3 и 4 представлены таблетки, в которых Eudragit S-100 и L-100 в качестве материалов основы контролирующего высвобождение покрытия смешаны в соотношении 3:1, а слой контролирующего высвобождение покрытия составляет от 20 до 30% (вес/вес) относительно веса таблетки с эндотелиальным покрытием. Кроме того, соотношение между содержанием HPMC в слое эндотелиального покрытия и общим весом материалов основы контролирующего высвобождение покрытия, то есть сополимера S метакриловой кислоты и сополимера L метакриловой кислоты, содержащихся в слое контролирующего высвобождение покрытия, составляет от 4,21 до 7,37 (вес/вес).
В общем, в табл. 5 приведено содержание и соотношения соответствующих ингредиентов у лекарственных форм в соответствии с примерами из настоящего изобретения.
Таблица 5. Составы и соотношения у лекарственных форм в соответствии с примерами из настоящего изобретения
| Вес (мг на 10 таблеток) | ||||
| Ингредиент | Eudragit S/L=2:1 | Eudragit S/L=3:1 | ||
| Пример 1 | Пример 2 | Пример 3 | Пример 4 | |
| Вес материала основы контролирующего высвобождение покрытия | 20 | 28 | 16 | 24 |
| Вес HPMC | 3,8 | 3,8 | 3,8 | 3,8 |
| Вес таблетки с эндотелиальным покрытием | 78,8 | 78,8 | 78,8 | 78,8 |
| Вес таблетки с контролирующим высвобождение покрытием | 110,8 | 123,6 | 104,4 | 117,2 |
| Вес материала основы контролирующего высвобождение покрытия/вес HPMC | 5,26 | 7,37 | 4,21 | 6,32 |
| Вес материала основы контролирующего высвобождение покрытия/вес таблетки с эндотелиальным покрытием | 25,38% | 35,53% | 20,30% | 30,46% |
| Вес материала основы контролирующего высвобождение покрытия/вес таблетки с контролирующим высвобождение покрытием | 18,05% | 22,65% | 15,33% | 20,48% |
| Вес HPMC/вес таблетки с эндотелиальным покрытием | 4,82% | 4,82% | 4,82% | 4,82% |
| Вес HPMC/вес таблетки с контролирующим высвобождение покрытием | 3,43% | 3,07% | 3,64% | 3,24% |
Сравнительные примеры 1-6. Получение таблеток с магниевой солью эзомепразола
В сравнительных примерах 1-6 получали таблетки, у которых минитаблетки с эндотелиальным покрытием в соответствии со способами получения из примеров 1-4 снабжены слоем контролирующего высвобождение покрытия, сформированным в соответствии с составами из табл. 6.
В сравнительных примерах 1 и 2 из табл. 6 представлены композиции, в которых Eudragit S-100 и Eudragit L-100 смешаны в соотношении 2:1, а материал основы контролирующего высвобождение покрытия составляет от 10 до 40% (вес/вес) относительно веса таблетки с эндотелиальным покрытием. Кроме того, в сравнительных примерах 3 и 4 представлены таблетки, в которых Eudragit S-100 и Eudragit L-100 смешаны в соотношении 3:1, а материал основы контролирующего высвобождение покрытия составляет от 10 до 40% (вес/вес) относительно веса таблетки с эндотелиальным покрытием.
В сравнительных примерах 5 и 6 представлены таблетки, в которых Eudragit S-100 и Eudragit L-100 смешаны в соотношении 6:1, а материал основы контролирующего высвобождение покрытия составляет от 10 до 20% (вес/вес) относительно веса таблетки с эндотелиальным покрытием.
Таблица 6. Состав слоя контролирующего высвобождение покрытия в соответствии со сравнительными примерами из настоящего изобретения
| Вес (мг на 10 таблеток) | |||||||
| Ингредиент | Eudragit S/L=2:1 | Eudragit S/L=3:1 | Eudragit S/L=6:1 | ||||
| Пример 1 | Пример 2 | Пример 3 | Пример 4 | Пример 5 | Пример 6 | ||
| Энтеросолюбильное покрытие | Eudragit S-100 | 5,3 | 21,2 | 6,0 | 24,0 | 6,86 | 13,7 |
| Eudragit L-100 | 2,7 | 10,8 | 2,0 | 8,0 | 1,14 | 2,3 | |
| Триэтилцитрат | 0,8 | 3,2 | 0,8 | 3,2 | 0,8 | 1,6 | |
| Тальк | 4,0 | 16,0 | 4,0 | 16,0 | 4,0 | 8,0 | |
| Этанол | надлеж. количество | надлеж. количество | надлеж. количество | надлеж. количество | надлеж. количество | надлеж. количество | |
| Дистиллированная вода | надлеж. количество | надлеж. количество | надлеж. количество | надлеж. количество | надлеж. количество | надлеж. количество | |
| Итого | 91,6 | 130,0 | 91,6 | 130,0 | 91,6 | 104,4 | |
В общем, содержание и соотношения соответствующих ингредиентов у лекарственных форм в соответствии с примерами из настоящего изобретения приведены в табл. 7.
Таблица 7. Составы и соотношения у лекарственных форм в соответствии со сравнительными примерами из настоящего изобретения
| Вес (мг на 10 таблеток) | ||||||
| Ингредиент | Eudragit S/L=2:1 | Eudragit S/L=3:1 | Eudragit S/L=6:1 | |||
| Сравнит. пример 1 | Сравнит. пример 2 | Сравнит. пример 3 | Сравнит. пример 4 | Сравнит. пример 5 | Сравнит. пример 6 | |
| Вес материала основы контролирующего высвобождение покрытия | 8 | 32 | 8 | 32 | 8 | 16 |
| Вес HPMC | 3,8 | 3,8 | 3,8 | 3,8 | 3,8 | 3,8 |
| Вес таблетки с эндотелиальным покрытием | 78,8 | 78,8 | 78,8 | 78,8 | 78,8 | 78,8 |
| Вес таблетки с контролирующим высвобождение покрытием | 91,6 | 130 | 91,6 | 130 | 91,6 | 140,4 |
| Вес материала основы контролирующего высвобождение покрытия/вес HPMC | 2,11 | 8,42 | 2,11 | 8,42 | 2,11 | 4,21 |
| Вес материала основы контролирующего высвобождение покрытия/вес таблетки с эндотелиальным покрытием | 10,15% | 40,61% | 10,15% | 40,61% | 10,15% | 20,30% |
| Вес материала основы контролирующего высвобождение покрытия/вес таблетки с контролирующим высвобождение покрытием | 8,73% | 24,62% | 8,73% | 24,62% | 8,73% | 15,33% |
| Вес HPMC/вес таблетки с эндотелиальным покрытием | 4,82% | 4,82% | 4,82% | 4,82% | 4,82% | 4,82% |
| Вес HPMC/вес таблетки с контролирующим высвобождение покрытием | 4,15% | 2,92% | 4,15% | 2,92% | 4,15% | 3,64% |
Тест-пример 1.
Измеряли скорость растворения магниевой соли эзомепразола по времени в условиях, приведенных в табл. 8, используя лекарственные формы из примеров 1-4 и из сравнительных примеров 1-6.
Таблица 8. Условия при измерении скорости растворения магниевых солей эзомепразола
| Условия при растворении | |
| Растворяющая жидкость | искусственная кишечная жидкость, 900 мл (рН 6,8) |
| Устройство | лопастной метод USP, 75 об/мин |
| Температура | 37°С |
| Время растворения | анализ через 30, 60, 90, 120, 180, 240, 300, 360 минут |
| Условия при анализе | |
| Аналитический прибор | HPLC (Hitachi 5000 series, Japan) |
| Детектор | УФ-спектрофотометр (длина волны измерения: 320 нм) |
| Колонка | колонка с трубкой из нержавеющей стали (внутренний диаметр 4,0 мм, длина 10 см), заполненной силикагелем для жидкостной хроматографии (диаметр частиц: 5 мкм) |
| Подвижная фаза | натрий-фосфатный буфер (pH 7,3): ацетонитрил: дистиллированная вода = 50:35:15 |
| Скорость потока | 1,0 мл/мин |
| Температура | 30°С |
Результаты измерения скорости растворения представлены в табл. 9 и 10 и на фиг. 1 и 2. Как видно из табл. 9 и фиг. 1, в примерах 1-4 возможна задержка высвобождения препарата на 2 часа или больше в искусственной кишечной жидкости, а высвобождение ускоряется после начала высвобождения.
А именно, видно, что, когда слой контролирующего высвобождение покрытия содержит полимер, состоящий из сополимера S метакриловой кислоты и сополимера L метакриловой кислоты, смешанных в качестве материалов основы контролирующего высвобождение покрытия в соотношении от 1,5:1 до 3,5:1 (вес/вес), предпочтительно от 2:1 до 3:1 (вес/вес), а вес материала основы контролирующего высвобождение покрытия составляет от 15 до 40% (вес/вес), предпочтительно от 20 до 35% (вес/вес) относительно веса таблетки, содержащей слой эндотелиального покрытия, и соотношение между весом материала основы контролирующего высвобождение покрытия и HPMC в слое эндотелиального покрытия составляет от 3,5 до 8,0 (вес/вес), предпочтительно от 4,2 до 7,4 (вес/вес), а вес HPMC в слое эндотелиального покрытия составляет от 4,4 до 5,2% (вес/вес), предпочтительно от 4,7 до 4,9% (вес/вес) относительно веса таблетки с эндотелиальным покрытием, то магниевая соль эзомепразола почти не высвобождается в течение 2 часов и начинает быстро высвобождаться через 2 часа, а через 6 часов высвобождается 99% её или больше, что означает отличные характеристики высвобождения.
При сравнении примера 1 и примера 3 видно, что при повышении доли Eudragit
S-100, который сравнительно нерастворим в искусственной кишечной жидкости, возможна достаточная задержка высвобождения препарата, несмотря на использование сравнительно небольшого количества материала основы контролирующего высвобождение покрытия.
S-100, который сравнительно нерастворим в искусственной кишечной жидкости, возможна достаточная задержка высвобождения препарата, несмотря на использование сравнительно небольшого количества материала основы контролирующего высвобождение покрытия.
С другой стороны, как видно из сравнительного примера 1 и сравнительного примера 3, при использовании меньшего количества вещества контролирующего высвобождение покрытия, чем в примерах (при этом материал основы контролирующего высвобождение покрытия составлял 10% или меньше относительно таблетки с эндотелиальным покрытием ядра), эффект замедления высвобождения препарата в искусственной кишечной жидкости был слабым, а из сравнительного примера 2 и сравнительного примера 4 видно, что при использовании большего количества вещества контролирующего высвобождение покрытия, чем в примерах (при этом материал основы контролирующего высвобождение покрытия составлял 40% или больше относительно таблетки с эндотелиальным покрытием ядра), затрудняется быстрое высвобождение препарата, которое не завершается даже через 6 часов, так что препарат может подвергаться экскреции еще до всасывания in vivo.
Кроме того, учитывая сравнительный пример 5 и сравнительный пример 6 с высокой долей сравнительно нерастворимого Eudragit S-100 в искусственной кишечной жидкости, при использовании материала основы контролирующего высвобождение покрытия в количестве 10% или меньше относительно таблетки с эндотелиальным покрытием ядра эффект замедления высвобождения был слабым, а при использовании материала основы контролирующего высвобождение покрытия в количестве 20% или больше препарат высвобождался медленно в течение длительного времени после задержки высвобождения, что неблагоприятно, причем конечная степень растворения тоже была ниже 100%.
Таблица 9. Скорость растворения магниевой соли эзомепразола (в примерах)
| Степень растворения (%) | ||||||||
| Пример 1 | Пример 2 | Пример 3 | Пример 4 | |||||
| Время (мин) | Среднее | Станд. отклонение | Среднее | Станд. отклонение | Среднее | Станд. отклонение | Среднее | Станд. отклонение |
| 0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 |
| 60 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 |
| 90 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 |
| 120 | 0,0 | 0,0 | 0,0 | 0,0 | 1,8 | 3,1 | 0,0 | 0,0 |
| 180 | 64,6 | 2,1 | 0,0 | 0,0 | 65,5 | 2,6 | 0,9 | 1,5 |
| 240 | 94,4 | 0,2 | 76,4 | 7,7 | 83,2 | 6,6 | 31,1 | 9,7 |
| 300 | 101,2 | 2,1 | 93,8 | 2,0 | 93,2 | 9,7 | 91,7 | 11,1 |
| 360 | 102,1 | 1,2 | 100,2 | 1,0 | 99,4 | 7,7 | 99,5 | 10,2 |
Таблица 10. Скорость растворения магниевой соли эзомепразола (в сравнительных примерах)
| Степень растворения (%) | ||||||||||||
| Сравнит. пример 1 | Сравнит. пример 2 | Сравнит. пример 3 | Сравнит. пример 4 | Сравнит. пример 5 | Сравнит. пример 6 | |||||||
| Время (мин) | Среднее | Станд. отклон. | Среднее | Станд. отклон. | Среднее | Станд. отклон. | Среднее | Станд. отклон. | Среднее | Станд. отклон. | Среднее | Станд. отклон. |
| 0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 | 0,0 |
| 60 | 13,8 | 3,0 | 0,0 | 0,0 | 0,5 | 0,3 | 0,0 | 0,0 | 1,4 | 2,4 | 0,0 | 0,0 |
| 90 | 62,9 | 6,5 | 0,0 | 0,0 | 25,9 | 2,6 | 0,0 | 0,0 | 17,7 | 3,1 | 0,0 | 0,0 |
| 120 | 76,5 | 10,6 | 0,0 | 0,0 | 65,9 | 13,8 | 0,0 | 0,0 | 44,5 | 4,0 | 0,0 | 0,0 |
| 180 | 93,6 | 7,0 | 0,0 | 0,0 | 82,6 | 4,8 | 0,0 | 0,0 | 63,6 | 4,2 | 3,0 | 5,1 |
| 240 | 99,0 | 1,1 | 0,0 | 0,0 | 96,8 | 10,1 | 0,0 | 0,0 | 88,8 | 8,2 | 44,5 | 8,0 |
| 300 | 91,5 | 0,8 | 56,4 | 7,7 | 100,4 | 3,9 | 0,0 | 0,0 | 98,8 | 9,3 | 61,2 | 6,2 |
| 360 | 86,5 | 0,8 | 73,8 | 2,0 | 98,8 | 5,3 | 32,3 | 16,9 | 95,7 | 7,9 | 72,9 | 5,6 |
Настоящее изобретение было описано на основе его предпочтительных воплощений. Специалистам в той области техники, к которой относится настоящее изобретение, должно быть ясно, что настоящее изобретение может быть реализовано в модифицированном виде без отклонения от сущности и объема изобретения.
Итак, воплощения, раскрытые выше, следует рассматривать в иллюстративном, а не в ограничительном смысле. Объем настоящего изобретения определяется прилагаемой формулой изобретения, а не предшествующим изложением, а все отличия, которые попадают в сферу его эквивалентов, должны рассматриваться как включенные в настоящее изобретение.
Промышленная применимость
Настоящее изобретение касается лекарственной формы, содержащей эзомепразол или его фармацевтически приемлемую соль. Лекарственная форма по настоящему изобретению, исходя из значительно улучшенных характеристик pH-зависимого высвобождения препарата, начинает высвобождать эзомепразол или его фармацевтически приемлемую соль после заданного времени задержки при пероральном введении, продолжает высвобождение в течение заданного времени и заканчивает высвобождение через заранее определенное время, обеспечивая тем самым большое удобство для пациента и превосходные терапевтические эффекты по сравнению с другими обычными формами.
Хотя конкретные конфигурации настоящего изобретения были описаны подробно, однако специалистам в данной области должно быть ясно, что это описание приводится
в качестве предпочтительных воплощений для иллюстративных целей и не должно рассматриваться как ограничивающее объем настоящего изобретения. Таким образом, существенный объем настоящего изобретения определяется прилагаемой формулой изобретения и её эквивалентами.
в качестве предпочтительных воплощений для иллюстративных целей и не должно рассматриваться как ограничивающее объем настоящего изобретения. Таким образом, существенный объем настоящего изобретения определяется прилагаемой формулой изобретения и её эквивалентами.
Claims (22)
1. Лекарственная форма для профилактики и лечения желудочных и рефлюксных заболеваний пищевода типа рефлюкс-эзофагита и заболеваний, связанных с гиперпролиферацией желудка, включая гастрит, дуоденит, язвы желудка, язвы двенадцатиперстной кишки и пептические язвы, включающая:
(a) ядро, содержащее эзомепразол или его фармацевтически приемлемую соль в качестве активного ингредиента;
(b) слой эндотелиального покрытия, сформированный на ядре; и
(c) слой контролирующего высвобождение покрытия, сформированный на слое эндотелиального покрытия,
причем слой эндотелиального покрытия содержит по меньшей мере одно вещество, выбранное из группы, состоящей из гидроксипропилметилцеллюлозы (HPMC), поливинилпирролидона (PVP), низкозамещенной гидроксипропилцеллюлозы (HPC-L), крахмала и желатина,
слой контролирующего высвобождение покрытия содержит полимер, в котором сополимер S метакриловой кислоты и сополимер L метакриловой кислоты смешаны в соотношении от 1,5:1 до 3,5:1 (вес/вес) в качестве материала основы контролирующего высвобождение покрытия, а
вес сополимера S метакриловой кислоты и сополимера L метакриловой кислоты в качестве материалов основы контролирующего высвобождение покрытия составляет от 15 до 40% (вес/вес) относительно веса таблетки с эндотелиальным покрытием,
где при испытании на высвобождение (растворение) с использованием искусственной кишечной жидкости (среды) со значением рН от 6,7 до 6,9 при 75 об/мин и 37°C в соответствии с лопастным методом USP через 2 часа элюируется 5% или меньше эзомепразола или его фармацевтически приемлемой соли, а через 6 часов элюируется по меньшей мере 90% эзомепразола или его фармацевтически приемлемой соли, и
где сополимер S метакриловой кислоты представляет собой анионный сополимер, содержащий метакриловую кислоту и метилметакрилат в соотношении 1:2, а сополимер L метакриловой кислоты - анионный сополимер, содержащий метакриловую кислоту и метилметакрилат в соотношении 1:1.
2. Лекарственная форма по п. 1, в которой содержание по меньшей мере одного вещества, выбранного из группы, состоящей из гидроксипропилметилцеллюлозы (HPMC), поливинилпирролидона (PVP), низкозамещенной гидроксипропилцеллюлозы (HPC-L), крахмала и желатина, которое содержится в слое эндотелиального покрытия, относительно веса сополимера S метакриловой кислоты и сополимера L метакриловой кислоты в качестве материалов основы контролирующего высвобождение покрытия составляет от 3,5 до 8,0 (вес/вес), а
содержание по меньшей мере одного вещества, выбранного из группы, состоящей из гидроксипропилметилцеллюлозы (HPMC), поливинилпирролидона (PVP), низкозамещенной гидроксипропилцеллюлозы (HPC-L), крахмала и желатина, которое содержится в слое эндотелиального покрытия, составляет от 4,4 до 5,2% (вес/вес) относительно веса таблетки с эндотелиальным покрытием.
3. Лекарственная форма по п. 1, в которой эзомепразол или его фармацевтически приемлемая соль представляет собой магниевую соль эзомепразола или стронциевую соль эзомепразола.
4. Лекарственная форма по п. 1, в которой эзомепразол или его фармацевтически приемлемая соль представляет собой гидрат.
5. Лекарственная форма по п. 1, в которой ядро, содержащее эзомепразол или его фармацевтически приемлемую соль, дополнительно содержит по меньшей мере один эксципиент из числа разбавителей, связующих веществ, разрыхлителей, смазывающих веществ, поверхностно-активных веществ, антиоксидантов, консервантов и стабилизаторов.
6. Лекарственная форма по п. 1, которая выбрана из группы, состоящей из гранул, мини-таблеток (MUST), таблеток, смеси гранул и мини-таблеток и капсул.
7. Применение лекарственной формы по любому из пп. 1-6 для профилактики и лечения желудочных и рефлюксных заболеваний пищевода типа рефлюкс-эзофагита и заболеваний, связанных с гиперпролиферацией желудка, включая гастрит, дуоденит, язвы желудка, язвы двенадцатиперстной кишки и пептические язвы.
8. Способ получения лекарственной формы, содержащей эзомепразол или его фармацевтически приемлемую соль согласно любому из пп. 1-6, включающий:
(a) смешивание эзомепразола или его фармацевтически приемлемой соли с разбавителем;
(b) добавление в смесь из стадии (a) разрыхлителя, связующего и смазывающего вещества с последующим смешиванием;
(c) получение мини-таблеток (MUST) или таблеток путем сухого гранулирования смеси из стадии (b), а затем таблетирования;
(d) нанесение на таблетированные мини-таблетки или таблетки, полученные на стадии (c), эндотелиального покрытия с помощью сушилки с псевдоожиженным слоем (FBG) и устройства для нанесения покрытия; и
(e) формирование у мини-таблеток или таблеток с эндотелиальным покрытием, полученных на стадии (d), слоя контролирующего высвобождение покрытия с использованием смеси, содержащей сополимер S метакриловой кислоты и сополимер L метакриловой кислоты.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020160094238A KR101907116B1 (ko) | 2016-07-25 | 2016-07-25 | 에스오메프라졸, 또는 약학적으로 허용 가능한 그의 염을 포함하는, pH-의존성 약물 방출 특성이 개선된 제형 |
| KR10-2016-0094238 | 2016-07-25 | ||
| PCT/KR2017/007933 WO2018021772A1 (ko) | 2016-07-25 | 2017-07-24 | 에스오메프라졸, 또는 약학적으로 허용 가능한 그의 염을 포함하는, pH-의존성 약물 방출 특성이 개선된 제형 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2716025C1 true RU2716025C1 (ru) | 2020-03-05 |
Family
ID=61017504
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2019105024A RU2716025C1 (ru) | 2016-07-25 | 2017-07-24 | ЛЕКАРСТВЕННАЯ ФОРМА С УЛУЧШЕННЫМИ ХАРАКТЕРИСТИКАМИ pH-ЗАВИСИМОГО ВЫСВОБОЖДЕНИЯ ПРЕПАРАТА, СОДЕРЖАЩАЯ ЭЗОМЕПРАЗОЛ ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМУЮ СОЛЬ |
Country Status (11)
| Country | Link |
|---|---|
| US (2) | US10946003B2 (ru) |
| EP (1) | EP3488845A4 (ru) |
| JP (1) | JP2019523258A (ru) |
| KR (1) | KR101907116B1 (ru) |
| CN (1) | CN109789102A (ru) |
| AU (1) | AU2017304029B2 (ru) |
| BR (1) | BR112019001423A2 (ru) |
| MX (1) | MX2019001032A (ru) |
| PH (1) | PH12019500154A1 (ru) |
| RU (1) | RU2716025C1 (ru) |
| WO (1) | WO2018021772A1 (ru) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2018341729A1 (en) * | 2017-09-28 | 2020-02-06 | Hanmi Pharm. Co., Ltd. | Pharmaceutical composition including multi-unit spheroidal tablet containing esomeprazole and spheroidal pharmaceutically acceptable salt thereof, and method of preparing the pharmaceutical composition |
| KR102080023B1 (ko) | 2018-01-29 | 2020-02-21 | 주식회사 종근당 | 에스오메프라졸 및 탄산수소나트륨을 포함하는 안정한 약제학적 조성물 |
| KR102006777B1 (ko) | 2018-01-29 | 2019-10-08 | 주식회사 종근당 | 에스오메프라졸 및 탄산수소나트륨을 포함하는 약제학적 제제 |
| MX2021011795A (es) * | 2019-04-02 | 2022-01-18 | Hanmi Pharm Ind Co Ltd | Composición farmaceutica que comprende esomeprazol 0 sal farmaceuticamente aceptable del mismo y que tiene un perfil de liberación doble. |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005051362A2 (en) * | 2003-11-28 | 2005-06-09 | Ranbaxy Laboratories Limited | Oral benzimidazole compositions comprising an active core, an optional separating layer and an enteric coating |
| KR20100078462A (ko) * | 2008-12-30 | 2010-07-08 | 한미약품 주식회사 | 에스오메프라졸의 과립 및 그 장용성 과립의 제조방법 |
| KR20120104991A (ko) * | 2009-11-07 | 2012-09-24 | 라보라토리오스 델 드라. 에스테브.에스.에이. | 약학적 고체 제형 |
| KR20140076998A (ko) * | 2012-12-13 | 2014-06-23 | 한미약품 주식회사 | 에스오메프라졸 유리염기 또는 그의 알칼리염을 포함하는 고미가 차폐된 약학 제제 및 이의 제조방법 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MY148805A (en) * | 2002-10-16 | 2013-05-31 | Takeda Pharmaceutical | Controlled release preparation |
| BRPI0412697A (pt) | 2003-07-17 | 2006-10-03 | Reddys Lab Inc Dr | composições farmacêuticas que apresentam um revestimento expansìvel |
| US7411804B2 (en) * | 2005-06-30 | 2008-08-12 | Seiko Epson Corporation | Integrated circuit device and electronic instrument |
| US20070026071A1 (en) | 2005-07-28 | 2007-02-01 | Qpharma, Llc | Magnesium salt proton pump inhibitor dosage forms |
| RU2412694C2 (ru) | 2005-07-29 | 2011-02-27 | Стихтинг Гронинген Сентр фор Драг Рисерч | pH-КОНТРОЛИРУЕМЫЕ СИСТЕМЫ ИМПУЛЬСНОЙ ДОСТАВКИ, МЕТОДЫ ПОЛУЧЕНИЯ И ИХ ИСПОЛЬЗОВАНИЯ |
| US20110172249A1 (en) * | 2008-09-03 | 2011-07-14 | Takeda Pharmaceutical Company Limted | Method for improving absorbability of preparation, and preparation having improved absorbability |
-
2016
- 2016-07-25 KR KR1020160094238A patent/KR101907116B1/ko active IP Right Grant
-
2017
- 2017-07-24 JP JP2019503533A patent/JP2019523258A/ja active Pending
- 2017-07-24 CN CN201780052180.XA patent/CN109789102A/zh active Pending
- 2017-07-24 US US16/319,161 patent/US10946003B2/en active Active
- 2017-07-24 RU RU2019105024A patent/RU2716025C1/ru active
- 2017-07-24 WO PCT/KR2017/007933 patent/WO2018021772A1/ko unknown
- 2017-07-24 MX MX2019001032A patent/MX2019001032A/es unknown
- 2017-07-24 BR BR112019001423-3A patent/BR112019001423A2/pt active Search and Examination
- 2017-07-24 AU AU2017304029A patent/AU2017304029B2/en not_active Ceased
- 2017-07-24 EP EP17834714.2A patent/EP3488845A4/en not_active Withdrawn
-
2019
- 2019-01-21 PH PH12019500154A patent/PH12019500154A1/en unknown
-
2021
- 2021-02-04 US US17/167,802 patent/US20210154180A1/en not_active Abandoned
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005051362A2 (en) * | 2003-11-28 | 2005-06-09 | Ranbaxy Laboratories Limited | Oral benzimidazole compositions comprising an active core, an optional separating layer and an enteric coating |
| KR20100078462A (ko) * | 2008-12-30 | 2010-07-08 | 한미약품 주식회사 | 에스오메프라졸의 과립 및 그 장용성 과립의 제조방법 |
| KR20120104991A (ko) * | 2009-11-07 | 2012-09-24 | 라보라토리오스 델 드라. 에스테브.에스.에이. | 약학적 고체 제형 |
| KR20140076998A (ko) * | 2012-12-13 | 2014-06-23 | 한미약품 주식회사 | 에스오메프라졸 유리염기 또는 그의 알칼리염을 포함하는 고미가 차폐된 약학 제제 및 이의 제조방법 |
Non-Patent Citations (4)
| Title |
|---|
| Malic D. et al. Formulation and evaluation of press coated tablets of esomeprazole for colonic delivery. Asian Journal of Pharmaceuticals, 2012, vol. 6, pages 252-258; page 253, Table 2, F4. * |
| Malic D. et al. Formulation and evaluation of press coated tablets of esomeprazole for colonic delivery. Asian Journal of Pharmaceuticals, 2012, vol. 6, pages 252-258; page 253, Table 2, F4. Инструкция по медицинскому применению ПРЕПАРАТА Дульколакс, таблетки, покрытые кишечнорастворимой оболочкой 5 мг фирмы Берингер Ингельхайм Интернешнл ГмбХ, Регистрационный номер: П N015358/01 от 21.04.2010 с изменениями от 06.06.2012. * |
| Инструкция по медицинскому применению лекарственного препарата для медицинского применения ЭЗОМЕПРАЗОЛ КАНОН, Регистрационный номер ЛП-003017 от 02.06.2015. * |
| Инструкция по медицинскому применению ПРЕПАРАТА Дульколакс, таблетки, покрытые кишечнорастворимой оболочкой 5 мг фирмы Берингер Ингельхайм Интернешнл ГмбХ, Регистрационный номер: П N015358/01 от 21.04.2010 с изменениями от 06.06.2012. * |
Also Published As
| Publication number | Publication date |
|---|---|
| US20190240209A1 (en) | 2019-08-08 |
| JP2019523258A (ja) | 2019-08-22 |
| MX2019001032A (es) | 2019-09-10 |
| WO2018021772A1 (ko) | 2018-02-01 |
| KR101907116B1 (ko) | 2018-10-11 |
| AU2017304029A1 (en) | 2019-02-21 |
| PH12019500154A1 (en) | 2019-10-14 |
| EP3488845A4 (en) | 2020-04-08 |
| AU2017304029B2 (en) | 2019-10-10 |
| KR20180011624A (ko) | 2018-02-02 |
| EP3488845A1 (en) | 2019-05-29 |
| BR112019001423A2 (pt) | 2019-05-07 |
| US20210154180A1 (en) | 2021-05-27 |
| US10946003B2 (en) | 2021-03-16 |
| CN109789102A (zh) | 2019-05-21 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101378973B1 (ko) | 구형에 가까운 형태의 다중 투여 단위 정제를 포함하는 경질 캡슐 복합 제형 및 이의 제조방법 | |
| RU2716025C1 (ru) | ЛЕКАРСТВЕННАЯ ФОРМА С УЛУЧШЕННЫМИ ХАРАКТЕРИСТИКАМИ pH-ЗАВИСИМОГО ВЫСВОБОЖДЕНИЯ ПРЕПАРАТА, СОДЕРЖАЩАЯ ЭЗОМЕПРАЗОЛ ИЛИ ЕГО ФАРМАЦЕВТИЧЕСКИ ПРИЕМЛЕМУЮ СОЛЬ | |
| KR102146395B1 (ko) | 에스오메프라졸 및 탄산수소나트륨을 포함하는 우수한 방출특성을 갖는 약제학적 제제 | |
| JP2017501201A (ja) | Azd9291を含む医薬組成物 | |
| JPWO2005092336A1 (ja) | 溶出制御製剤とその製造方法 | |
| KR20070083956A (ko) | 양성자 펌프 억제제를 위한 신규 변형 방출 정제 제형 | |
| RU2672573C2 (ru) | Фармацевтический комбинированный состав капсулы, содержащий тадалафил и тамсулозин | |
| KR20090015890A (ko) | 저 홍조 니아신 제형 | |
| KR20110011643A (ko) | 변형 방출 니아신 배합물 | |
| CN109890372B (zh) | 含埃索美拉唑的复合胶囊及其制备方法 | |
| US20200368219A1 (en) | Pharmaceutical composition including multi-unit spheroidal tablet containing esomeprazole and spheroidal pharmaceutically acceptable salt thereof, and method of preparing the pharmaceutical composition | |
| JP2023510140A (ja) | シベンゾリンまたはその塩を含む薬学剤形 | |
| KR20210012881A (ko) | 에스오메프라졸 및 탄산수소나트륨을 포함하는 우수한 방출특성을 갖는 약제학적 제제 | |
| CN107224585B (zh) | 一种包含非甾体抗炎药和质子泵抑制剂的组合物 | |
| JP2015503555A (ja) | ボセンタン制御放出性経口製剤 | |
| RU2734970C1 (ru) | Система доставки 2-этил-6-метил-3-гидроксипиридина сукцината для перорального применения в форме гастроретентивной таблетки | |
| EA044361B1 (ru) | Составная капсула, содержащая эзомепразол, и способ ее получения | |
| EA042314B1 (ru) | Фармацевтическая композиция, включающая многокомпонентную таблетку сфероидной формы, содержащую эзомепразол и его фармацевтически приемлемую соль, и способ приготовления такой фармацевтической композиции | |
| KR20210130663A (ko) | 안전성과 안정성이 개선된 피르페니돈을 포함하는 장용성 제제 및 이의 제조방법 | |
| KR20200034293A (ko) | 제어 방출용 바레니클린 제제 | |
| Mahesh | Formulation and Evaluation of Bilayer Tablet Containg Pseudoephedrine HCL SR and Loratadine Ir. | |
| KR20150057263A (ko) | 레베티라세탐 또는 이의 약제학적으로 허용되는 염을 함유하는 서방성 제제 및 이의 제조방법 | |
| WO2010134938A1 (en) | Modified release niacin pharmaceutical formulations |