RU2671209C2 - Lactobacillus rhamnosus rht-3201, конъюгированные с полисахаридным полимерным связующим и их применение для профилактики или лечения атопических заболеваний - Google Patents
Lactobacillus rhamnosus rht-3201, конъюгированные с полисахаридным полимерным связующим и их применение для профилактики или лечения атопических заболеваний Download PDFInfo
- Publication number
- RU2671209C2 RU2671209C2 RU2016147690A RU2016147690A RU2671209C2 RU 2671209 C2 RU2671209 C2 RU 2671209C2 RU 2016147690 A RU2016147690 A RU 2016147690A RU 2016147690 A RU2016147690 A RU 2016147690A RU 2671209 C2 RU2671209 C2 RU 2671209C2
- Authority
- RU
- Russia
- Prior art keywords
- lactobacillus rhamnosus
- rht
- heat
- conjugated
- inactivated
- Prior art date
Links
- 241000218588 Lactobacillus rhamnosus Species 0.000 title claims abstract description 113
- 229920001282 polysaccharide Polymers 0.000 title claims abstract description 94
- 239000005017 polysaccharide Substances 0.000 title claims abstract description 94
- 208000012657 Atopic disease Diseases 0.000 title claims abstract description 41
- 238000011282 treatment Methods 0.000 title claims abstract description 29
- 229920005596 polymer binder Polymers 0.000 title claims abstract description 10
- 239000002491 polymer binding agent Substances 0.000 title claims abstract description 10
- 150000004676 glycans Chemical class 0.000 title claims abstract 21
- 230000002265 prevention Effects 0.000 title description 17
- 238000000034 method Methods 0.000 claims abstract description 76
- 206010012438 Dermatitis atopic Diseases 0.000 claims abstract description 64
- 201000008937 atopic dermatitis Diseases 0.000 claims abstract description 64
- 239000000203 mixture Substances 0.000 claims abstract description 40
- 239000004480 active ingredient Substances 0.000 claims abstract description 20
- 230000001603 reducing effect Effects 0.000 claims abstract description 19
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 12
- 239000003795 chemical substances by application Substances 0.000 claims abstract description 6
- 206010003645 Atopy Diseases 0.000 claims abstract description 5
- 241000894006 Bacteria Species 0.000 claims description 129
- 239000011230 binding agent Substances 0.000 claims description 100
- 229920000642 polymer Polymers 0.000 claims description 65
- 229920002674 hyaluronan Polymers 0.000 claims description 32
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 claims description 31
- 229960003160 hyaluronic acid Drugs 0.000 claims description 31
- 238000000855 fermentation Methods 0.000 claims description 28
- 230000004151 fermentation Effects 0.000 claims description 28
- 239000000706 filtrate Substances 0.000 claims description 26
- 230000002779 inactivation Effects 0.000 claims description 26
- 235000013305 food Nutrition 0.000 claims description 23
- 238000010438 heat treatment Methods 0.000 claims description 21
- 239000001963 growth medium Substances 0.000 claims description 13
- 239000000047 product Substances 0.000 claims description 12
- 235000010443 alginic acid Nutrition 0.000 claims description 8
- 229920000615 alginic acid Polymers 0.000 claims description 8
- 238000002156 mixing Methods 0.000 claims description 8
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 claims description 7
- 229920001661 Chitosan Polymers 0.000 claims description 7
- 229920002774 Maltodextrin Polymers 0.000 claims description 7
- 239000005913 Maltodextrin Substances 0.000 claims description 7
- 229940072056 alginate Drugs 0.000 claims description 7
- 229940045110 chitosan Drugs 0.000 claims description 7
- 229940035034 maltodextrin Drugs 0.000 claims description 7
- 230000001268 conjugating effect Effects 0.000 claims description 4
- 235000015140 cultured milk Nutrition 0.000 claims description 4
- 238000012258 culturing Methods 0.000 claims description 4
- 235000005911 diet Nutrition 0.000 claims description 4
- 230000000378 dietary effect Effects 0.000 claims description 4
- 235000015872 dietary supplement Nutrition 0.000 claims description 3
- 235000020124 milk-based beverage Nutrition 0.000 claims description 2
- 235000013618 yogurt Nutrition 0.000 claims description 2
- 230000000694 effects Effects 0.000 abstract description 24
- 238000004519 manufacturing process Methods 0.000 abstract description 21
- 230000001225 therapeutic effect Effects 0.000 abstract description 10
- 239000000126 substance Substances 0.000 abstract description 6
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 75
- 150000004804 polysaccharides Chemical class 0.000 description 73
- 208000037851 severe atopic dermatitis Diseases 0.000 description 54
- 239000006041 probiotic Substances 0.000 description 51
- 235000018291 probiotics Nutrition 0.000 description 51
- 238000012360 testing method Methods 0.000 description 37
- 239000004310 lactic acid Substances 0.000 description 36
- 235000014655 lactic acid Nutrition 0.000 description 36
- 230000000529 probiotic effect Effects 0.000 description 34
- 210000004027 cell Anatomy 0.000 description 27
- 239000000463 material Substances 0.000 description 27
- 241000699670 Mus sp. Species 0.000 description 25
- 210000003491 skin Anatomy 0.000 description 25
- 102000004127 Cytokines Human genes 0.000 description 22
- 108090000695 Cytokines Proteins 0.000 description 22
- 102000013462 Interleukin-12 Human genes 0.000 description 20
- 108010065805 Interleukin-12 Proteins 0.000 description 20
- 102000004388 Interleukin-4 Human genes 0.000 description 20
- 108090000978 Interleukin-4 Proteins 0.000 description 20
- 239000000523 sample Substances 0.000 description 20
- 239000000428 dust Substances 0.000 description 19
- 238000002360 preparation method Methods 0.000 description 19
- 210000004347 intestinal mucosa Anatomy 0.000 description 18
- 230000008569 process Effects 0.000 description 16
- OGQHCUYSWDOIMP-UHFFFAOYSA-N 7-(diethylamino)-n-[2-[(2-iodoacetyl)amino]ethyl]-2-oxochromene-3-carboxamide Chemical compound C1=C(C(=O)NCCNC(=O)CI)C(=O)OC2=CC(N(CC)CC)=CC=C21 OGQHCUYSWDOIMP-UHFFFAOYSA-N 0.000 description 15
- 239000003814 drug Substances 0.000 description 14
- 239000002609 medium Substances 0.000 description 14
- 108010074328 Interferon-gamma Proteins 0.000 description 13
- 108090000174 Interleukin-10 Proteins 0.000 description 13
- 241000699666 Mus <mouse, genus> Species 0.000 description 13
- 229940079593 drug Drugs 0.000 description 13
- 210000001035 gastrointestinal tract Anatomy 0.000 description 13
- 208000024891 symptom Diseases 0.000 description 13
- 102100037850 Interferon gamma Human genes 0.000 description 12
- 239000000284 extract Substances 0.000 description 12
- 210000001165 lymph node Anatomy 0.000 description 12
- 230000002829 reductive effect Effects 0.000 description 12
- 210000000447 Th1 cell Anatomy 0.000 description 11
- 210000004241 Th2 cell Anatomy 0.000 description 11
- 210000003630 histaminocyte Anatomy 0.000 description 11
- 210000004989 spleen cell Anatomy 0.000 description 11
- 210000001519 tissue Anatomy 0.000 description 11
- 239000000427 antigen Substances 0.000 description 10
- 108091007433 antigens Proteins 0.000 description 10
- 102000036639 antigens Human genes 0.000 description 10
- 230000019734 interleukin-12 production Effects 0.000 description 10
- 230000017307 interleukin-4 production Effects 0.000 description 10
- 230000009467 reduction Effects 0.000 description 10
- 241001465754 Metazoa Species 0.000 description 9
- 239000002253 acid Substances 0.000 description 9
- 230000008859 change Effects 0.000 description 9
- 238000006243 chemical reaction Methods 0.000 description 9
- 230000000052 comparative effect Effects 0.000 description 9
- 239000007788 liquid Substances 0.000 description 9
- 239000000843 powder Substances 0.000 description 9
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 8
- 230000001464 adherent effect Effects 0.000 description 8
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 8
- 229960003957 dexamethasone Drugs 0.000 description 8
- 150000003431 steroids Chemical class 0.000 description 8
- 239000003613 bile acid Substances 0.000 description 7
- 230000037396 body weight Effects 0.000 description 7
- 239000012531 culture fluid Substances 0.000 description 7
- 208000003251 Pruritus Diseases 0.000 description 6
- 210000001744 T-lymphocyte Anatomy 0.000 description 6
- 238000001035 drying Methods 0.000 description 6
- 230000003832 immune regulation Effects 0.000 description 6
- 239000002674 ointment Substances 0.000 description 6
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 5
- 210000002421 cell wall Anatomy 0.000 description 5
- 238000005119 centrifugation Methods 0.000 description 5
- 230000002860 competitive effect Effects 0.000 description 5
- 210000004443 dendritic cell Anatomy 0.000 description 5
- 230000004957 immunoregulator effect Effects 0.000 description 5
- 229910052500 inorganic mineral Inorganic materials 0.000 description 5
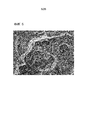
- 238000001000 micrograph Methods 0.000 description 5
- 239000011707 mineral Substances 0.000 description 5
- 235000010755 mineral Nutrition 0.000 description 5
- 239000002994 raw material Substances 0.000 description 5
- 239000000725 suspension Substances 0.000 description 5
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 4
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 4
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 4
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 4
- 201000004624 Dermatitis Diseases 0.000 description 4
- 206010020751 Hypersensitivity Diseases 0.000 description 4
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 4
- 229920002472 Starch Polymers 0.000 description 4
- 102000008228 Toll-like receptor 2 Human genes 0.000 description 4
- 108010060888 Toll-like receptor 2 Proteins 0.000 description 4
- 210000000941 bile Anatomy 0.000 description 4
- 229910052799 carbon Inorganic materials 0.000 description 4
- 238000001816 cooling Methods 0.000 description 4
- 239000003937 drug carrier Substances 0.000 description 4
- 239000012091 fetal bovine serum Substances 0.000 description 4
- 210000002865 immune cell Anatomy 0.000 description 4
- 230000036039 immunity Effects 0.000 description 4
- 230000006698 induction Effects 0.000 description 4
- 230000001939 inductive effect Effects 0.000 description 4
- 230000002401 inhibitory effect Effects 0.000 description 4
- 230000007803 itching Effects 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- 230000010534 mechanism of action Effects 0.000 description 4
- 239000006872 mrs medium Substances 0.000 description 4
- 229910052757 nitrogen Inorganic materials 0.000 description 4
- 239000008363 phosphate buffer Substances 0.000 description 4
- 239000008055 phosphate buffer solution Substances 0.000 description 4
- 239000013641 positive control Substances 0.000 description 4
- 102000005962 receptors Human genes 0.000 description 4
- 108020003175 receptors Proteins 0.000 description 4
- 230000001105 regulatory effect Effects 0.000 description 4
- 238000006748 scratching Methods 0.000 description 4
- 230000002393 scratching effect Effects 0.000 description 4
- 210000002966 serum Anatomy 0.000 description 4
- 235000020183 skimmed milk Nutrition 0.000 description 4
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 4
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- MSFSPUZXLOGKHJ-UHFFFAOYSA-N Muraminsaeure Natural products OC(=O)C(C)OC1C(N)C(O)OC(CO)C1O MSFSPUZXLOGKHJ-UHFFFAOYSA-N 0.000 description 3
- 108010013639 Peptidoglycan Proteins 0.000 description 3
- 239000002202 Polyethylene glycol Substances 0.000 description 3
- 206010039085 Rhinitis allergic Diseases 0.000 description 3
- 239000005862 Whey Substances 0.000 description 3
- 102000007544 Whey Proteins Human genes 0.000 description 3
- 108010046377 Whey Proteins Proteins 0.000 description 3
- 230000009471 action Effects 0.000 description 3
- 208000026935 allergic disease Diseases 0.000 description 3
- 201000010105 allergic rhinitis Diseases 0.000 description 3
- 235000019270 ammonium chloride Nutrition 0.000 description 3
- 208000006673 asthma Diseases 0.000 description 3
- 208000010668 atopic eczema Diseases 0.000 description 3
- 210000001520 comb Anatomy 0.000 description 3
- 201000010099 disease Diseases 0.000 description 3
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 3
- 210000002615 epidermis Anatomy 0.000 description 3
- 238000011156 evaluation Methods 0.000 description 3
- 239000000945 filler Substances 0.000 description 3
- 238000004108 freeze drying Methods 0.000 description 3
- 230000036541 health Effects 0.000 description 3
- 230000001900 immune effect Effects 0.000 description 3
- 210000000987 immune system Anatomy 0.000 description 3
- 230000008595 infiltration Effects 0.000 description 3
- 238000001764 infiltration Methods 0.000 description 3
- 239000004615 ingredient Substances 0.000 description 3
- 230000000968 intestinal effect Effects 0.000 description 3
- 210000000936 intestine Anatomy 0.000 description 3
- 208000037852 mild atopic dermatitis Diseases 0.000 description 3
- 229940062713 mite extract Drugs 0.000 description 3
- 239000002245 particle Substances 0.000 description 3
- 229920001223 polyethylene glycol Polymers 0.000 description 3
- 230000004044 response Effects 0.000 description 3
- 210000000813 small intestine Anatomy 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- 210000000952 spleen Anatomy 0.000 description 3
- 238000013112 stability test Methods 0.000 description 3
- 238000010186 staining Methods 0.000 description 3
- 235000019698 starch Nutrition 0.000 description 3
- 238000003860 storage Methods 0.000 description 3
- 239000000758 substrate Substances 0.000 description 3
- 229950003937 tolonium Drugs 0.000 description 3
- HNONEKILPDHFOL-UHFFFAOYSA-M tolonium chloride Chemical compound [Cl-].C1=C(C)C(N)=CC2=[S+]C3=CC(N(C)C)=CC=C3N=C21 HNONEKILPDHFOL-UHFFFAOYSA-M 0.000 description 3
- 230000004580 weight loss Effects 0.000 description 3
- 229920001817 Agar Polymers 0.000 description 2
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 2
- SRBFZHDQGSBBOR-IOVATXLUSA-N D-xylopyranose Chemical compound O[C@@H]1COC(O)[C@H](O)[C@H]1O SRBFZHDQGSBBOR-IOVATXLUSA-N 0.000 description 2
- 206010013786 Dry skin Diseases 0.000 description 2
- 238000008157 ELISA kit Methods 0.000 description 2
- 206010015150 Erythema Diseases 0.000 description 2
- 241000588724 Escherichia coli Species 0.000 description 2
- 208000010201 Exanthema Diseases 0.000 description 2
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 244000068988 Glycine max Species 0.000 description 2
- 235000010469 Glycine max Nutrition 0.000 description 2
- WZUVPPKBWHMQCE-UHFFFAOYSA-N Haematoxylin Chemical compound C12=CC(O)=C(O)C=C2CC2(O)C1C1=CC=C(O)C(O)=C1OC2 WZUVPPKBWHMQCE-UHFFFAOYSA-N 0.000 description 2
- 239000012981 Hank's balanced salt solution Substances 0.000 description 2
- NTYJJOPFIAHURM-UHFFFAOYSA-N Histamine Chemical compound NCCC1=CN=CN1 NTYJJOPFIAHURM-UHFFFAOYSA-N 0.000 description 2
- 108060003951 Immunoglobulin Proteins 0.000 description 2
- 108010002616 Interleukin-5 Proteins 0.000 description 2
- 241000186660 Lactobacillus Species 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 206010024438 Lichenification Diseases 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 108010058846 Ovalbumin Proteins 0.000 description 2
- DBMJMQXJHONAFJ-UHFFFAOYSA-M Sodium laurylsulphate Chemical compound [Na+].CCCCCCCCCCCCOS([O-])(=O)=O DBMJMQXJHONAFJ-UHFFFAOYSA-M 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 244000269722 Thea sinensis Species 0.000 description 2
- 239000000853 adhesive Substances 0.000 description 2
- 230000001070 adhesive effect Effects 0.000 description 2
- 239000008272 agar Substances 0.000 description 2
- 235000010419 agar Nutrition 0.000 description 2
- PYMYPHUHKUWMLA-UHFFFAOYSA-N arabinose Natural products OCC(O)C(O)C(O)C=O PYMYPHUHKUWMLA-UHFFFAOYSA-N 0.000 description 2
- 210000003719 b-lymphocyte Anatomy 0.000 description 2
- 235000015278 beef Nutrition 0.000 description 2
- SRBFZHDQGSBBOR-UHFFFAOYSA-N beta-D-Pyranose-Lyxose Natural products OC1COC(O)C(O)C1O SRBFZHDQGSBBOR-UHFFFAOYSA-N 0.000 description 2
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 2
- 210000004369 blood Anatomy 0.000 description 2
- 239000008280 blood Substances 0.000 description 2
- 210000004204 blood vessel Anatomy 0.000 description 2
- 229910000019 calcium carbonate Inorganic materials 0.000 description 2
- 235000013574 canned fruits Nutrition 0.000 description 2
- 239000006285 cell suspension Substances 0.000 description 2
- 230000007969 cellular immunity Effects 0.000 description 2
- 230000001684 chronic effect Effects 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 230000021615 conjugation Effects 0.000 description 2
- 230000016396 cytokine production Effects 0.000 description 2
- 235000013365 dairy product Nutrition 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 210000004207 dermis Anatomy 0.000 description 2
- ZPWVASYFFYYZEW-UHFFFAOYSA-L dipotassium hydrogen phosphate Chemical compound [K+].[K+].OP([O-])([O-])=O ZPWVASYFFYYZEW-UHFFFAOYSA-L 0.000 description 2
- 229910000396 dipotassium phosphate Inorganic materials 0.000 description 2
- 235000019797 dipotassium phosphate Nutrition 0.000 description 2
- 239000012153 distilled water Substances 0.000 description 2
- 239000008298 dragée Substances 0.000 description 2
- 235000021271 drinking Nutrition 0.000 description 2
- 230000035622 drinking Effects 0.000 description 2
- 230000037336 dry skin Effects 0.000 description 2
- 235000013399 edible fruits Nutrition 0.000 description 2
- 231100000321 erythema Toxicity 0.000 description 2
- 201000005884 exanthem Diseases 0.000 description 2
- 238000000445 field-emission scanning electron microscopy Methods 0.000 description 2
- 235000013373 food additive Nutrition 0.000 description 2
- 239000002778 food additive Substances 0.000 description 2
- 235000011389 fruit/vegetable juice Nutrition 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 235000013376 functional food Nutrition 0.000 description 2
- 210000004211 gastric acid Anatomy 0.000 description 2
- 230000004727 humoral immunity Effects 0.000 description 2
- 230000028993 immune response Effects 0.000 description 2
- 102000018358 immunoglobulin Human genes 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 210000004969 inflammatory cell Anatomy 0.000 description 2
- 229940039696 lactobacillus Drugs 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 230000003902 lesion Effects 0.000 description 2
- 210000004185 liver Anatomy 0.000 description 2
- 210000002540 macrophage Anatomy 0.000 description 2
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 2
- 235000019341 magnesium sulphate Nutrition 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 244000005700 microbiome Species 0.000 description 2
- 210000004400 mucous membrane Anatomy 0.000 description 2
- 235000012149 noodles Nutrition 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 2
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 2
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 230000001737 promoting effect Effects 0.000 description 2
- 238000011321 prophylaxis Methods 0.000 description 2
- 206010037844 rash Diseases 0.000 description 2
- 230000000306 recurrent effect Effects 0.000 description 2
- 235000015067 sauces Nutrition 0.000 description 2
- 150000004666 short chain fatty acids Chemical class 0.000 description 2
- 239000002356 single layer Substances 0.000 description 2
- 238000005507 spraying Methods 0.000 description 2
- 239000008107 starch Substances 0.000 description 2
- 238000003756 stirring Methods 0.000 description 2
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 2
- 238000012916 structural analysis Methods 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 239000007940 sugar coated tablet Substances 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- 230000008961 swelling Effects 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 230000008719 thickening Effects 0.000 description 2
- 238000000108 ultra-filtration Methods 0.000 description 2
- OMDQUFIYNPYJFM-XKDAHURESA-N (2r,3r,4s,5r,6s)-2-(hydroxymethyl)-6-[[(2r,3s,4r,5s,6r)-4,5,6-trihydroxy-3-[(2s,3s,4s,5s,6r)-3,4,5-trihydroxy-6-(hydroxymethyl)oxan-2-yl]oxyoxan-2-yl]methoxy]oxane-3,4,5-triol Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@@H]1OC[C@@H]1[C@@H](O[C@H]2[C@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)O)[C@H](O)[C@H](O)[C@H](O)O1 OMDQUFIYNPYJFM-XKDAHURESA-N 0.000 description 1
- LNAZSHAWQACDHT-XIYTZBAFSA-N (2r,3r,4s,5r,6s)-4,5-dimethoxy-2-(methoxymethyl)-3-[(2s,3r,4s,5r,6r)-3,4,5-trimethoxy-6-(methoxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6r)-4,5,6-trimethoxy-2-(methoxymethyl)oxan-3-yl]oxyoxane Chemical compound CO[C@@H]1[C@@H](OC)[C@H](OC)[C@@H](COC)O[C@H]1O[C@H]1[C@H](OC)[C@@H](OC)[C@H](O[C@H]2[C@@H]([C@@H](OC)[C@H](OC)O[C@@H]2COC)OC)O[C@@H]1COC LNAZSHAWQACDHT-XIYTZBAFSA-N 0.000 description 1
- LUEWUZLMQUOBSB-FSKGGBMCSA-N (2s,3s,4s,5s,6r)-2-[(2r,3s,4r,5r,6s)-6-[(2r,3s,4r,5s,6s)-4,5-dihydroxy-2-(hydroxymethyl)-6-[(2r,4r,5s,6r)-4,5,6-trihydroxy-2-(hydroxymethyl)oxan-3-yl]oxyoxan-3-yl]oxy-4,5-dihydroxy-2-(hydroxymethyl)oxan-3-yl]oxy-6-(hydroxymethyl)oxane-3,4,5-triol Chemical compound O[C@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@@H](O[C@@H]2[C@H](O[C@@H](OC3[C@H](O[C@@H](O)[C@@H](O)[C@H]3O)CO)[C@@H](O)[C@H]2O)CO)[C@H](O)[C@H]1O LUEWUZLMQUOBSB-FSKGGBMCSA-N 0.000 description 1
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 1
- OWEGMIWEEQEYGQ-UHFFFAOYSA-N 100676-05-9 Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC2C(OC(O)C(O)C2O)CO)O1 OWEGMIWEEQEYGQ-UHFFFAOYSA-N 0.000 description 1
- NHBKXEKEPDILRR-UHFFFAOYSA-N 2,3-bis(butanoylsulfanyl)propyl butanoate Chemical compound CCCC(=O)OCC(SC(=O)CCC)CSC(=O)CCC NHBKXEKEPDILRR-UHFFFAOYSA-N 0.000 description 1
- 241000251468 Actinopterygii Species 0.000 description 1
- 235000001674 Agaricus brunnescens Nutrition 0.000 description 1
- 229920002101 Chitin Polymers 0.000 description 1
- 206010010356 Congenital anomaly Diseases 0.000 description 1
- 206010010744 Conjunctivitis allergic Diseases 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 241000238710 Dermatophagoides Species 0.000 description 1
- 229920002307 Dextran Polymers 0.000 description 1
- 108010082495 Dietary Plant Proteins Proteins 0.000 description 1
- 208000030453 Drug-Related Side Effects and Adverse reaction Diseases 0.000 description 1
- 239000004278 EU approved seasoning Substances 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 241000305071 Enterobacterales Species 0.000 description 1
- 241000194033 Enterococcus Species 0.000 description 1
- 239000004386 Erythritol Substances 0.000 description 1
- UNXHWFMMPAWVPI-UHFFFAOYSA-N Erythritol Natural products OCC(O)C(O)CO UNXHWFMMPAWVPI-UHFFFAOYSA-N 0.000 description 1
- 240000008620 Fagopyrum esculentum Species 0.000 description 1
- 235000009419 Fagopyrum esculentum Nutrition 0.000 description 1
- 229930091371 Fructose Natural products 0.000 description 1
- 239000005715 Fructose Substances 0.000 description 1
- RFSUNEUAIZKAJO-ARQDHWQXSA-N Fructose Chemical compound OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-ARQDHWQXSA-N 0.000 description 1
- 229920000855 Fucoidan Polymers 0.000 description 1
- 229920000926 Galactomannan Polymers 0.000 description 1
- IAJILQKETJEXLJ-UHFFFAOYSA-N Galacturonsaeure Natural products O=CC(O)C(O)C(O)C(O)C(O)=O IAJILQKETJEXLJ-UHFFFAOYSA-N 0.000 description 1
- 241000173371 Garcinia indica Species 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 229920002581 Glucomannan Polymers 0.000 description 1
- 206010018910 Haemolysis Diseases 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 102000012214 Immunoproteins Human genes 0.000 description 1
- 108010036650 Immunoproteins Proteins 0.000 description 1
- 206010061218 Inflammation Diseases 0.000 description 1
- 241000194036 Lactococcus Species 0.000 description 1
- GUBGYTABKSRVRQ-PICCSMPSSA-N Maltose Natural products O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-PICCSMPSSA-N 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- OVRNDRQMDRJTHS-UHFFFAOYSA-N N-acelyl-D-glucosamine Natural products CC(=O)NC1C(O)OC(CO)C(O)C1O OVRNDRQMDRJTHS-UHFFFAOYSA-N 0.000 description 1
- OVRNDRQMDRJTHS-FMDGEEDCSA-N N-acetyl-beta-D-glucosamine Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O OVRNDRQMDRJTHS-FMDGEEDCSA-N 0.000 description 1
- MBLBDJOUHNCFQT-LXGUWJNJSA-N N-acetylglucosamine Natural products CC(=O)N[C@@H](C=O)[C@@H](O)[C@H](O)[C@H](O)CO MBLBDJOUHNCFQT-LXGUWJNJSA-N 0.000 description 1
- 206010030113 Oedema Diseases 0.000 description 1
- 241000192001 Pediococcus Species 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 239000001888 Peptone Substances 0.000 description 1
- 108010080698 Peptones Proteins 0.000 description 1
- 229920001715 Porphyran Polymers 0.000 description 1
- 206010037660 Pyrexia Diseases 0.000 description 1
- 239000012980 RPMI-1640 medium Substances 0.000 description 1
- 241000607142 Salmonella Species 0.000 description 1
- 208000031709 Skin Manifestations Diseases 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 241000194017 Streptococcus Species 0.000 description 1
- 206010042674 Swelling Diseases 0.000 description 1
- 102000002689 Toll-like receptor Human genes 0.000 description 1
- 108020000411 Toll-like receptor Proteins 0.000 description 1
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 1
- 240000008042 Zea mays Species 0.000 description 1
- 235000005824 Zea mays ssp. parviglumis Nutrition 0.000 description 1
- 235000002017 Zea mays subsp mays Nutrition 0.000 description 1
- 241000212749 Zesius chrysomallus Species 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 229940023476 agar Drugs 0.000 description 1
- 235000013334 alcoholic beverage Nutrition 0.000 description 1
- IAJILQKETJEXLJ-QTBDOELSSA-N aldehydo-D-glucuronic acid Chemical compound O=C[C@H](O)[C@@H](O)[C@H](O)[C@H](O)C(O)=O IAJILQKETJEXLJ-QTBDOELSSA-N 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 208000002205 allergic conjunctivitis Diseases 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- 208000030961 allergic reaction Diseases 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- WQZGKKKJIJFFOK-PHYPRBDBSA-N alpha-D-galactose Chemical compound OC[C@H]1O[C@H](O)[C@H](O)[C@@H](O)[C@H]1O WQZGKKKJIJFFOK-PHYPRBDBSA-N 0.000 description 1
- WNROFYMDJYEPJX-UHFFFAOYSA-K aluminium hydroxide Chemical compound [OH-].[OH-].[OH-].[Al+3] WNROFYMDJYEPJX-UHFFFAOYSA-K 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 210000004102 animal cell Anatomy 0.000 description 1
- 230000003266 anti-allergic effect Effects 0.000 description 1
- 239000000043 antiallergic agent Substances 0.000 description 1
- 239000003146 anticoagulant agent Substances 0.000 description 1
- 229940127219 anticoagulant drug Drugs 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 229940125715 antihistaminic agent Drugs 0.000 description 1
- 239000000739 antihistaminic agent Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- PYMYPHUHKUWMLA-WDCZJNDASA-N arabinose Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)C=O PYMYPHUHKUWMLA-WDCZJNDASA-N 0.000 description 1
- 208000024998 atopic conjunctivitis Diseases 0.000 description 1
- 244000052616 bacterial pathogen Species 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- GUBGYTABKSRVRQ-QUYVBRFLSA-N beta-maltose Chemical compound OC[C@H]1O[C@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@@H]1O GUBGYTABKSRVRQ-QUYVBRFLSA-N 0.000 description 1
- 235000013361 beverage Nutrition 0.000 description 1
- 210000003445 biliary tract Anatomy 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 229940041514 candida albicans extract Drugs 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 230000000747 cardiac effect Effects 0.000 description 1
- 235000010418 carrageenan Nutrition 0.000 description 1
- 239000000679 carrageenan Substances 0.000 description 1
- 229920001525 carrageenan Polymers 0.000 description 1
- 229940113118 carrageenan Drugs 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000009134 cell regulation Effects 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 235000013351 cheese Nutrition 0.000 description 1
- 239000012141 concentrate Substances 0.000 description 1
- 235000008504 concentrate Nutrition 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- 235000014510 cooky Nutrition 0.000 description 1
- 235000005822 corn Nutrition 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 229940099112 cornstarch Drugs 0.000 description 1
- 238000005520 cutting process Methods 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000013872 defecation Effects 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 208000002173 dizziness Diseases 0.000 description 1
- 238000002651 drug therapy Methods 0.000 description 1
- 230000002500 effect on skin Effects 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 238000002149 energy-dispersive X-ray emission spectroscopy Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- YQGOJNYOYNNSMM-UHFFFAOYSA-N eosin Chemical compound [Na+].OC(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C(O)=C(Br)C=C21 YQGOJNYOYNNSMM-UHFFFAOYSA-N 0.000 description 1
- UNXHWFMMPAWVPI-ZXZARUISSA-N erythritol Chemical compound OC[C@H](O)[C@H](O)CO UNXHWFMMPAWVPI-ZXZARUISSA-N 0.000 description 1
- 235000019414 erythritol Nutrition 0.000 description 1
- 229940009714 erythritol Drugs 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- 238000001704 evaporation Methods 0.000 description 1
- 230000008020 evaporation Effects 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 239000012894 fetal calf serum Substances 0.000 description 1
- 235000011194 food seasoning agent Nutrition 0.000 description 1
- 235000013611 frozen food Nutrition 0.000 description 1
- 235000015203 fruit juice Nutrition 0.000 description 1
- 229930182830 galactose Natural products 0.000 description 1
- 210000004051 gastric juice Anatomy 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 229960002518 gentamicin Drugs 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 229940046240 glucomannan Drugs 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 229940097043 glucuronic acid Drugs 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 235000009569 green tea Nutrition 0.000 description 1
- 230000008588 hemolysis Effects 0.000 description 1
- 229960001340 histamine Drugs 0.000 description 1
- 238000007602 hot air drying Methods 0.000 description 1
- 239000003906 humectant Substances 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 1
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 1
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 1
- 210000003405 ileum Anatomy 0.000 description 1
- 230000005965 immune activity Effects 0.000 description 1
- 208000026278 immune system disease Diseases 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 230000003308 immunostimulating effect Effects 0.000 description 1
- 230000001506 immunosuppresive effect Effects 0.000 description 1
- 230000001976 improved effect Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000010874 in vitro model Methods 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 239000000411 inducer Substances 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 208000030603 inherited susceptibility to asthma Diseases 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 238000011081 inoculation Methods 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 230000031261 interleukin-10 production Effects 0.000 description 1
- 239000007928 intraperitoneal injection Substances 0.000 description 1
- FZWBNHMXJMCXLU-BLAUPYHCSA-N isomaltotriose Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1OC[C@@H]1[C@@H](O)[C@H](O)[C@@H](O)[C@@H](OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C=O)O1 FZWBNHMXJMCXLU-BLAUPYHCSA-N 0.000 description 1
- 239000010410 layer Substances 0.000 description 1
- 238000009630 liquid culture Methods 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 210000003141 lower extremity Anatomy 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 239000000845 maltitol Substances 0.000 description 1
- 235000010449 maltitol Nutrition 0.000 description 1
- VQHSOMBJVWLPSR-WUJBLJFYSA-N maltitol Chemical compound OC[C@H](O)[C@@H](O)[C@@H]([C@H](O)CO)O[C@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O VQHSOMBJVWLPSR-WUJBLJFYSA-N 0.000 description 1
- 229940035436 maltitol Drugs 0.000 description 1
- SQQMAOCOWKFBNP-UHFFFAOYSA-L manganese(II) sulfate Chemical compound [Mn+2].[O-]S([O-])(=O)=O SQQMAOCOWKFBNP-UHFFFAOYSA-L 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 235000013310 margarine Nutrition 0.000 description 1
- 239000003264 margarine Substances 0.000 description 1
- 235000013372 meat Nutrition 0.000 description 1
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 1
- 201000005299 metal allergy Diseases 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 229950006780 n-acetylglucosamine Drugs 0.000 description 1
- 239000013642 negative control Substances 0.000 description 1
- 231100000957 no side effect Toxicity 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 235000015097 nutrients Nutrition 0.000 description 1
- 235000016709 nutrition Nutrition 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 125000001477 organic nitrogen group Chemical group 0.000 description 1
- 238000004806 packaging method and process Methods 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 235000015927 pasta Nutrition 0.000 description 1
- 235000014594 pastries Nutrition 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 235000019319 peptone Nutrition 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 229920002492 poly(sulfone) Polymers 0.000 description 1
- 239000002861 polymer material Substances 0.000 description 1
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 229920000053 polysorbate 80 Polymers 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 229940116317 potato starch Drugs 0.000 description 1
- 230000001376 precipitating effect Effects 0.000 description 1
- 238000001556 precipitation Methods 0.000 description 1
- 238000004321 preservation Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 230000000644 propagated effect Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 230000009257 reactivity Effects 0.000 description 1
- 235000021067 refined food Nutrition 0.000 description 1
- 230000024833 regulation of cytokine production Effects 0.000 description 1
- 210000003289 regulatory T cell Anatomy 0.000 description 1
- 210000002345 respiratory system Anatomy 0.000 description 1
- 238000001223 reverse osmosis Methods 0.000 description 1
- 229940100486 rice starch Drugs 0.000 description 1
- 235000013580 sausages Nutrition 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 210000002955 secretory cell Anatomy 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- 208000017520 skin disease Diseases 0.000 description 1
- 206010040882 skin lesion Diseases 0.000 description 1
- 231100000444 skin lesion Toxicity 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- 235000010413 sodium alginate Nutrition 0.000 description 1
- 239000000661 sodium alginate Substances 0.000 description 1
- 229940005550 sodium alginate Drugs 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000012439 solid excipient Substances 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- -1 soytone Substances 0.000 description 1
- 238000001694 spray drying Methods 0.000 description 1
- 238000013097 stability assessment Methods 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 229960005322 streptomycin Drugs 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000008163 sugars Chemical class 0.000 description 1
- 230000008093 supporting effect Effects 0.000 description 1
- 230000002195 synergetic effect Effects 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 235000013616 tea Nutrition 0.000 description 1
- 229940124597 therapeutic agent Drugs 0.000 description 1
- 239000005028 tinplate Substances 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 239000012137 tryptone Substances 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- 229940100445 wheat starch Drugs 0.000 description 1
- 239000000811 xylitol Substances 0.000 description 1
- 235000010447 xylitol Nutrition 0.000 description 1
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 1
- 229960002675 xylitol Drugs 0.000 description 1
- 239000012138 yeast extract Substances 0.000 description 1
- 235000008924 yoghurt drink Nutrition 0.000 description 1
- UHVMMEOXYDMDKI-JKYCWFKZSA-L zinc;1-(5-cyanopyridin-2-yl)-3-[(1s,2s)-2-(6-fluoro-2-hydroxy-3-propanoylphenyl)cyclopropyl]urea;diacetate Chemical compound [Zn+2].CC([O-])=O.CC([O-])=O.CCC(=O)C1=CC=C(F)C([C@H]2[C@H](C2)NC(=O)NC=2N=CC(=CC=2)C#N)=C1O UHVMMEOXYDMDKI-JKYCWFKZSA-L 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/135—Bacteria or derivatives thereof, e.g. probiotics
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms, e.g. protozoa; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L2/00—Non-alcoholic beverages; Dry compositions or concentrates therefor; Their preparation
- A23L2/52—Adding ingredients
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS, OR NON-ALCOHOLIC BEVERAGES, NOT COVERED BY SUBCLASSES A21D OR A23B-A23J; THEIR PREPARATION OR TREATMENT, e.g. COOKING, MODIFICATION OF NUTRITIVE QUALITIES, PHYSICAL TREATMENT; PRESERVATION OF FOODS OR FOODSTUFFS, IN GENERAL
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/74—Bacteria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2400/00—Lactic or propionic acid bacteria
- A23V2400/11—Lactobacillus
- A23V2400/175—Rhamnosus
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Mycology (AREA)
- Food Science & Technology (AREA)
- Polymers & Plastics (AREA)
- Nutrition Science (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Microbiology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Molecular Biology (AREA)
- Epidemiology (AREA)
- Wood Science & Technology (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Genetics & Genomics (AREA)
- General Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Biochemistry (AREA)
- Virology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Dermatology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicinal Preparation (AREA)
- Coloring Foods And Improving Nutritive Qualities (AREA)
Abstract
Настоящее изобретение относится к фармацевтической промышленности, а именно к инактивированным нагреванием Lactobacillus rhamnosus, конъюгированным с полисахаридным полимерным связующим. Способ получения инактивированных нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), конъюгированных с полимерным полисахаридным связующим. Инактивированные нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), конъюгированные с полимерным полисахаридным связующим. Фармацевтическая композиция для лечения атопических заболеваний, где композиция содержит в качестве активного ингредиента инактивированные нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), конъюгированные с полимерным полисахаридным связующим. Применение инактивированных нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), конъюгированных с полимерным полисахаридным связующим, для получения агента для лечения атопического дерматита. Способ лечения атопии. Композиция продукта для снижения выраженности атопического дерматита. Применение инактивированных нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), конъюгированных с полимерным полисахаридным связующим, для получения продукта для снижения выраженности атопического дерматита. Способ лечения или снижения выраженности атопического заболевания. Вышеописанные средства обладают повышенным терапевтическим эффектом при атопических заболеваниях. 8 н. и 7 з.п. ф-лы, 26 ил., 13 табл.
Description
Для данной заявки испрашивается приоритет по корейской патентной заявке № 10-2014-0054237, поданной 7 мая 2014, которая включена в данное описание посредством ссылки в полном объеме.
Настоящее изобретение относится к инактивированным нагреванием Lactobacillus rhamnosus, конъюгированным с полимерным полисахаридным связующим, способу их получения и их применению и, в частности, к способу получения инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, инактивированным нагреванием Lactobacillus rhamnosus, конъюгированным с полимерным полисахаридным связующим, полученным этим способом, и фармацевтической композиции и композиции пищевого продукта для профилактики и лечения атопических заболеваний, содержащей инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, в качестве активного ингредиента.
УРОВЕНЬ ТЕХНИКИ
Атопический дерматит (AD) относится к хроническому и рецидивному воспалительному кожному проявлению, сопровождающемуся кожным зудом, и главным образом, наблюдающемуся у детей младшего и среднего возраста. Атопическое заболевание является самым типичным аллергическим заболеванием вместе с аллергическими ринитами и бронхиальной астмой, при этом известный показатель распространенности атопических заболеваний составляет 10-30% у детей и 1-3% у взрослых.
Атопический дерматит проявляется из-за гиперчувствительной реакции иммунной системы на антигены, такие как частицы пылевого клеща, попавшие на тело человека. Макрофаги представляют антигены T клеткам, при и этом T клетки дифференцируются на Th1 или Th2 клетки согласно типу антигенов или рецепторов, с которыми они реагируют. Th2 клетки активируют гуморальный иммунитет через цитокины, такие как IL-4, IL-5, и IL-10, и активируют B клетки, приводя к повышению продуцирования IgE и, таким образом, вызывая атопический дерматит. В то время как Th1 клетки активируют клеточный иммунитет через IL-12 и IFN-γ, и IFN-γ, ингибируя продуцирование IgE. Следовательно, для облегчения симптомов атопических заболеваний поддерживается баланс иммунной регуляции Th1 клеток и Th2 клеток.
Несмотря на то, что до сих пор отсутствует основной эффективный метод лечения атопического дерматита, для этого используют противоаллергические лекарственные средства, антигистаминные лекарственные средства, стероиды и другие медикаменты. Наиболее часто назначаемыми из них для лечения атопического дерматита являются стероиды в форме мази, которые снижают иммунологическую реактивность, снижая воспаление, при этом сообщается о возникновении различных типов побочных эффектов при их длительном применение.
В тоже время на рынке в качестве пищевых материалов представлены многие молочнокислые бактерии или молочные продукты, содержащие молочно-кислые бактерии, которые обладают иммунорегулирующим действием. Примеры молочнокислых бактерий могут включать род Lactobacillus, род Lactococcus, род Streptococcus, род Pediococcus, род Enterococcus и аналогичное им, также известно, что эти молочнокислые бактерии обладают иммуностимулирующим или противоаллергическим действием. Авторы настоящего изобретения получили патентные права на Lactobacillus rhamnosus IDCC 3201, обладающие сбалансированной иммунорегулирующей функцией Th1 и Th2 клеток, которые являются новым штаммовым материалом, не имеющим побочных эффектов при использовании в течение длительного периода времени и позволяющим по существу проводить лечение атопического дерматита (зарегистрированный в Корее патент № 1007429000000 (Korean Patent Registration No. 1007429000000)).
Однако в качестве резидентной флоры в кишечнике человека живут 100 триллионов или более энтеробактерий, относящихся к около 500 различным типам, при этом вредные бактерии, такие как E. coli, и полезные бактерии, такие как молочнокислые бактерии, сбалансированы. Следовательно, введенные пробиотические молочнокислые бактерии имеют ограниченную способность конкурентной адгезии к слизистой кишечника и, следовательно, их влияние варьируется в зависимости от скорости их адгезии. Дополнительно, определенное количество пробиотических молочнокислых бактерий погибает при прохождении желудочно-кишечного тракта или выходит из конкурентной адгезии при дефекации. Следовательно, пробиотические молочнокислые бактерии ограничены в своем вкладе в лечение тяжелых атопических заболеваний.
Дополнительно, пробиотики необходимо вводить в избыточном количестве по сравнению с их стандартным количеством для улучшения эффективности их адгезии к слизистой кишечника, поскольку во время прохождения желудочно-кишечного тракта им приходится преодолевать множество препятствий до момента достижения кишечника. Следовательно, трудно прогнозировать потребленное количество микроорганизмов и эффективность лечения атопического заболевания. В виду этих проблем существует несколько молочнокислых бактерий, которые демонстрируют тот же уровень или эффективность лечения, как и лекарственные средства на основе стероидов. Несмотря на усилия по улучшению эффективности пробиотиков в составе формулы, продолжают существовать проблемы, состоящие в невозможности установления нормализованного уровня влияния пробиотиков из-за гибели штаммов пробиотических бактерий, в норме происходящей во время их хранения.
В виду произошедшего в последнее время прогресса в исследованиях иммунной системы слизистой оболочки кишечника человека сообщается о взаимодействии и прочности адгезии между иммунными клетками слизистой оболочки кишечника человека, являющегося хозяином, и компонентами клеточных стенок молочнокислых бактерий. Из них toll-подобный рецептор-2 (TLR-2) дендритных клеток (DC) связывается с липотейхоевой кислотой и пептидогликаном, находящимся в клеточных стенках указанных бактерий, для доставки иммунных сигналов.
Дополнительно, молочнокислые бактерии с иммунорегулирующими функциями позволяют внеклеточное продуцирование короткоцепочечной жирной кислоты (SCFA) и иммунопротеинов при ферментации в специфических и различных средах, способствуя, таким образом, секреции IFN-γ и IL-12 из Th1 клеток и, таким образом, приводя к снижению выраженности атопического дерматита. Однако хотя большинство продуктов ферментации молочнокислыми бактериями не приводят к снижению выраженности атопического дерматита, только некоторые селективные молочнокислые бактерии продуцируют такие вещества и, следовательно, значение разработки таких бактерий очень высоко.
Такие предпосылки привели к разработке композиции, требуемой для использования при лечении атопического дерматита по существу с преодолением побочных эффектов лекарственных средств на основе стероидов, используемых для лечения атопического дерматита, и ограничения пробиотических молочнокислых бактерий при лечении атопического дерматита из-за их скорости адгезии.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ТЕХНИЧЕСКАЯ ПРОБЛЕМА
Авторы настоящего изобретения во время исследования по разработке материала для лечения атопического дерматита без побочных эффектов с высоким уровнем эффективности, эквивалетным таковому у лекарственных средств на основе стероидов, подтвердили, что конъюгат инактивированных нагреванием Lactobacillus rhamnosus и связующего, полученный смешиванием полимерного полисахарида с культуральным фильтратом, имеет превосходную способность к адгезии с иммунными клетками слизистой кишечника и терапевтически эффективен при тяжелом атопическом дерматите без побочных эффектов, и достигается настоящим изобретением. Следовательно, в одном аспекте настоящее изобретение относится к способу получения инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, способ включает: (a) разделение ферментационной культуральной среды, полученной культивированием Lactobacillus rhamnosus, на бактерии и ферментационный фильтрат; (b) смешивание ферментационного фильтрата со стадии (a) и полимерного полисахарида с получением полимерного полисахаридного связующего; (c) инактивацию нагреванием бактерий, отделенных на стадии (a); и (d) конъюгирование инактивированных нагреванием бактерий на стадии (c) со связующим, полученным на стадии (b).
В другом аспекте настоящее изобретение относится к инактивированным нагреванием Lactobacillus rhamnosus, конъюгированным с полимерным полисахаридным связующим, полученным указанным выше способом.
В другом аспекте настоящее изобретение относится к фармацевтической композиции для профилактики и лечения атопических заболеваний, где композиция содержит в качестве активного ингредиента инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим.
В другом аспекте настоящее изобретение относится к применению инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, для получения агента для лечения атопического дерматита.
В другом аспекте настоящее изобретение относится к способу профилактики или лечения атопического заболевания, где способ включает введение эффективного количества инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, субъекту, нуждающемуся в профилактике или лечение атопического заболевания.
В другом аспекте настоящее изобретение относится к композиции пищевого продукта для профилактики и снижения выраженности атопического дерматита, где композиция содержит в качестве активного ингредиента инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим.
В другом аспекте настоящее изобретение относится к применению инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, для получения пищевого продукта для профилактики и снижения выраженности атопического дерматита.
В другом аспекте настоящее изобретение относится к способу профилактики или снижения выраженности атопического заболевания, где способ включает употребление в пищу пищевого продукта, содержащего в качестве активного ингредиента эффективное количество инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, субъекту, нуждающемуся в профилактике или снижение выраженности атопического заболевания.
РЕШЕНИЕ ТЕХНИЧЕСКОЙ ПРОБЛЕМЫ
Согласно одному из аспектов настоящее изобретение относится к способу получения инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, где способ включает: (a) разделение ферментационной культуральной среды, полученной культивированием Lactobacillus rhamnosus, на бактерии и ферментационный фильтрат; (b) смешивание ферментационного фильтрата со стадии (a) и полимерного полисахарида с получением полимерного полисахаридного связующего; (c) инактивацию нагреванием бактерий, отделенных на стадии (a); и (d) конъюгирование инактивированных нагреванием бактерий на стадии (c) со связующим, полученным на стадии (b).
Согласно другому аспекту настоящее изобретение относится к инактивированным нагреванием Lactobacillus rhamnosus, конъюгированным с полимерным полисахаридным связующим, полученных указанным выше способом.
Согласно другому аспекту настоящее изобретение относится к фармацевтической композиции для профилактики и лечения атопических заболеваний, где композиция содержит в качестве активного ингредиента инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим.
Согласно другому аспекту настоящее изобретение относится к применениям инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, для получения агента для лечения атопического дерматита.
Согласно другому аспекту настоящее изобретение относится к способу профилактики или лечения атопического заболевания, где способ включает введение эффективного количества инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, субъекту, нуждающемуся в профилактике или лечении атопического заболевания.
Согласно другому аспекту настоящее изобретение относится к композиции пищевого продукта для профилактики или снижения выраженности атопического дерматита, где композиция содержит в качестве активного ингредиента инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим.
Согласно другому аспекту настоящее изобретение относится к применению инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, для получения пищевого продукта для профилактики и снижения выраженности атопического дерматита.
Согласно другому аспекту настоящее изобретение относится к способу профилактики или снижения выраженности атопического заболевания, где способ включает употребление в пищу пищевого продукта, содержащего в качестве активного ингредиента эффективное количество инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, субъекту, нуждающемуся в профилактике или снижении выраженности атопического заболевания.
Далее настоящее изобретение будет описано более подробно.
Настоящее изобретение относится к способу получения инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, где способ включает:
(a) разделение ферментационной культуральной среды, полученной культивированием Lactobacillus rhamnosus, на бактерии и ферментационный фильтрат;
(b) смешивание ферментационного фильтрата со стадии (a) и полимерного полисахарида с получением полимерного полисахаридного связующего;
(c) инактивацию нагреванием бактерий, отделенных на стадии (a); и
(d) конъюгирование инактивированных нагреванием бактерий на стадии (c) со связующим, полученным на стадии (b).
Стадия (a) представляет процесс разделения ферментационной культуральной среды, которая представляет продукт культивирования Lactobacillus rhamnosus, на бактерии и ферментационный фильтрат.
Молочнокислые бактерии Lactobacillus rhamnosus по настоящему изобретению включают все штаммы Lactobacillus rhamnosus и могут предпочтительно представлять Lactobacillus rhamnosus KCTC 10833 BP.
Lactobacillus rhamnosus KCTC 10833 BP назван как «Lactobacillus rhamnosus IDCC 3201» в более ранней корейской патентной заявке (No. 10-2006-0038066), поданной заявителем настоящей патентной заявки, и в описании настоящей патентной заявки названия могут быть взаимозаменяемы.
Используемый в описании настоящей патентной заявки термин «культивирование» включает в объем понятия ферментацию. Указанное культивирование может быть проведено при использовании известных способов культивирования молочнокислых бактерий. Примеры культивирования могут включать без ограничения способ, в котором бактерии инокулируют в культуральную среду или культуральный субстрат и затем оставляют на определенный период времени, поддерживая при этом заранее заданную температуру роста при аэробных или анаэробных условиях.
Используемый в описании настоящей патентной заявки термин «культуральная среда» относится к твердому или жидкому культуральному субстрату, содержащему нутриенты, необходимые для роста животных клеток, растительных клеток или микроорганизмов. Указанная культуральная среда может включать известную культуральную среду для молочнокислых бактерий. Примеры культуральной среды могут включать без ограничения жидкую среду deMan Rogosa Sharpe (MRS), многоцелевую среду с Tween (APT) и бульонную среду с сердечно-мозговым экстрактом (BHI), и предпочтительно может представлять жидкую среду MRS. Среда может быть использована в форме модифицированной среды (например, модифицированная MRS среда) селективным регулированием композиции материалов, составляющих среду, согласно требованиям специалиста в области техники, к которой относится настоящее изобретение.
Культуральная среда по настоящему изобретению содержит в качестве культуральных субстратов источники углерода, источники азота, минеральные вещества и ростовые элементы, необходимые для роста молочнокислых бактерий. Типы источников углерода, источников азота, минеральных веществ и ростовые элементы не ограничиваются при условии, что эти материалы стимулируют синергетическое действие на рост молочнокислых бактерий, при этом эти материалы являются известными из области техники, к которой относится настоящее изобретение. Например, в качестве источника углерода могут быть использованы различные углеводы. Источник углерода предпочтительно может представлять глюкозу, сахарозу, мальтозу, фруктозу, лактозу, ксилозу, галактозу или арабинозу. Дополнительно, в качестве источника азота могут быть использованы различные органические источники азота. Источник азота предпочтительно может представлять дрожжевой экстракт, сойтон (soytone), пептон, экстракт говядины, триптон или казитон. Тип источника минеральных веществ не ограничен при условии, что источник минеральных веществ известен из области техники, к которой относится настоящее изобретение, для выращивания молочнокислых бактерий. Примеры источников минеральных веществ могут включать сульфат магния (MgSO4), сульфат марганца (MnSO4), вторичный кислый фосфат калия (K2HPO4), хлорид аммония (NH4Cl), карбонат кальция (CaCO3), и ацетат натрия (CH3COONa). Дополнительно, различные порошкообразные сырьевые пищевые материалы или экстракты могут быть добавлены в культуральную среду согласно требованиям специалиста в области техники, к которой относится настоящее изобретение, при этом их примеры могут включать без ограничения порошкообразную кукурузу или экстракт, сухую сыворотку или экстракт, сухое обезжиренное молоко или экстракт, порошкообразный зеленый чай или экстракт, или порошкообразные грибы или экстракт.
В процессе культивирования температура может быть изменена в зависимости от типа молочнокислых бактерий специалистом в области техники, к которой относится настоящее изобретение. Например, температура может составлять 30-45° без ограничения. Предпочтительно температура может составлять 33-40°, и наиболее предпочтительно 35-39°.
В процессе культивирования время культивирования может быть изменено в зависимости от заданной производительности специалистом в области техники, к которой относится настоящее изобретение. Например, оно может составлять 12-96 часов без ограничения.
Используемый в описании настоящей патентной заявки термин «ферментационная культуральная среда» относится к таковой, полученной инокулированием и ферментацией (или культивированием) штамма в жидкой среде, при этом термин «ферментационный фильтрат» относится к культуральному фильтрату, полученному удалением штамма из ферментированной культуральной жидкости.
Отделение бактерий и ферментационного фильтрата может быть проведено при использовании известных способов отделения бактерий (например, центрифугирование или ультрафильтрация) без ограничения.
Стадия (b) представляет процесс смешивания ферментационного фильтрата, отделенного на стадии (a), с полимерным полисахаридным материалом с получением полимерного полисахаридного связующего.
Используемый в описании настоящей патентной заявки термин «полимерное полисахаридное связующее» относится к смеси из ферментационного фильтрата и полимерного полисахаридного материала или концентрата смеси. В зависимости от композиции и процедуры получения связующего, способность к адгезии со слизистой кишечника и способность продуцирования различных цитокинов в иммунных клетках может регулироваться.
Тип полимерного полисахаридного материала на стадии (b) не ограничивается при условии, что полимерный полисахаридный материал известен в области техники, к которой относится настоящее изобретение. Примеры полимерного полисахаридного материала могут включать гиалуроновую кислоту, альгинат, мальтодекстрин, хитозан, каррагенан, галактоманнан, глюкоманнан, декстран, фукоидан, агар, порфиран, хитин и аналогичное им. Полимерный полисахарид по настоящему изобретению предпочтительно может представлять гиалуроновую кислоту, альгинат, мальтодекстрин или хитозан.
Процент добавленного полимерного полисахаридного материала может быть селективно изменен в зависимости от требуемой вязкости или прочности адгезии, заданной специалистом в области техники, к которой относится настоящее изобретение. Например, полимерный полисахаридный материал может быть добавлен в ферментационный фильтрат в соотношении 0,0001-10%(масса/объем), без ограничения.
В предпочтительном варианте воплощения настоящего изобретения стадия (b) может включать добавление гиалуроновой кислоты в качестве полимерного полисахаридного материала в ферментационный фильтрат в соотношении 0,0001-10%(масса/объем), и наиболее предпочтительно добавление гиалуроновой кислоты в ферментационный фильтрат в соотношении 0,0001-0,01%(масса/объем).
Гиалуроновая кислота представляет один из комплексных полисахаридов, состоящий из аминокислот и уроновых кислот, и представляет полимерное соединение, состоящее из N-ацетилглюкозамина и глюкуроновой кислоты. Молекулярная масса гиалуроновой кислоты по настоящему изобретению не ограничена. Например, гиалуроновая кислота включает гиалуроновые кислоты с молекулярной массой 1,000,000, 2,000,000, 3,000,000, 4,000,000, и 4,500,000, предпочтительна гиалуроновая кислота с молекулярной массой 1,000,000 или 2,000,000, и наиболее предпочтительна гиалуроновая кислота с молекулярной массой 1,000,000.
Стадия (b) дополнительно может включать процесс концентрирования с получением высоко концентрированного полимерного полисахаридного связующего.
Указанное концентрирование может быть проведено при использовании устройств для концентрирования или способов, известных из области техники, к которой относится настоящее изобретение. Примеры концентрирования могут включать без ограничения концентрирование осаждением, концентрирование выпариванием, концентрирование при пониженном давлении, ультрафильтрацию, обратный осмос и центрифугирование, предпочтительно концентрирование при пониженном давлении.
Стадия (c) представляет процесс инактивации нагреванием бактерий, отделенных на стадии (a).
Используемый в описании настоящей патентной заявки термин «инактивация нагреванием» относится к инактивации пробиотических бактерий термической обработкой в течение заданного периода времени, при этом инактивация нагреванием влияет на композицию активных ингредиентов, содержащихся в бактериях, структуру бактерий и способность к адгезии в кишечнике в зависимости от условий инактивации нагреванием. Самой важной целью инактивации нагреванием пробиотических бактерий является формирование структуры, которая способствует адгезии с иммунными клетками слизистой кишечника индуцированием липотейхоевой кислотой и пептидогликаном, которые являются типичными ингредиентами, содержащимися в клеточной структуре Lactobacillus rhamnosus. То есть, липотейхоевая кислота и пептидогликан, образующие клеточную структуру, скомбинированы с TRL-2 дендритных клеток слизистой кишечника для способствования продуцирования иммунных цитокинов и, следовательно, очень важно, чтобы структура была получена в такой форме, чтобы иметь самую благоприятную эффективность адгезии.
Температура инактивации нагреванием в настоящем изобретении не ограничена при условии, что она находится в температурных пределах, в которых функциональные ингредиенты бактерий не денатурируют. Температура может составлять, например, 60-100°, предпочтительно 70-90° и наиболее предпочтительно 75-85°.
Время инактивации нагреванием не ограничивается при условии, что оно находится во временных пределах, в которых функциональные ингредиенты бактерий не денатурируют. Время может составлять, например, 10-120 минут, предпочтительно 30-90 минут и наиболее предпочтительно 50-70 минут.
После процесса инактивации нагреванием необязательно может быть добавлен процесс охлаждения согласно требованиям специалиста в области техники, к которой относится настоящее изобретение. Процесс охлаждения может быть проведен при использовании известных способов, и температура охлаждения может быть селективно изменена согласно требованиям специалиста в области техники, к которой относится настоящее изобретение. Процесс охлаждения может быть проведен при температурных пределах, например, 10-40° и предпочтительно 25-35°.
Стадия (d) представляет процесс конъюгирования инактивированных нагреванием бактерий со стадии (c) со связующим, полученным на стадии (b).
Используемый в описании настоящей патентной заявки термин «конъюгирование» относится к образованию единого блока соединением двух или более материалов. На стадии (d) связующее и инактивированные нагреванием бактерии конъюгируют проведением серий реакций, индуцированных проникновением инактивированных нагреванием бактерий стадии (c) в связующее, полученное на стадии (b), или смешиванием инактивированных нагреванием бактерий и связующего.
Способ получения, включающий стадии (a) - (d), может необязательно дополнительно включать процесс добавления наполнителя, процесс сушки и процесс распыления для облегчения транспортной обработки, хранения и аналогичного им в процессе получения инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, согласно требованиям специалиста в области техники, к которой относится настоящее изобретение.
Тип наполнителя не ограничивается при условии, что он представляет таковой, известный из области техники, к которой относится настоящее изобретение. Примеры наполнителя могут включать крахмал.
Процесс сушки может быть проведен при использовании известных способов сушки. Примеры процессов сушки могут включать лиофильную сушку, распылительную сушку и сушку горячим воздухом без ограничения.
Настоящее изобретение относится к инактивированным нагреванием Lactobacillus rhamnosus, конъюгированным с полимерным полисахаридным связующим, полученным указанным выше способом.
Инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, по настоящему изобретению характеризуются получением способом, включающим стадии (a) - (d). Инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, названные «RHT-3201» авторами настоящего изобретения, и используемые в описании настоящей патентной заявки термины могут быть взаимозаменяемы.
Инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, по настоящему изобретению продемонстрировали превосходный терапевтический эффект в лечении атопических заболеваний вместе со значительно улучшенной конкурентной адгезией к слизистой кишечника по сравнению с существующими препаратами молочнокислых бактерий (смотрите, Пример 6), и эффекты профилактики, снижения выраженности или лечения атопического дерматита при эквивалентном уровне для существующих лекарственных средств на основе стероидов (например, дексаметазон) (смотрите, Примеры 9 и 10).
Дополнительно, относительно стабильности в среде желудочно-кишечного тракта, что является проблемой при оральном потреблении молочнокислых пробиотиков, инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, по настоящему изобретению сохраняют свои функциональные свойства (эффективность) на более высоком уровне, чем у традиционных молочнокислых пробиотиков. В частности, несмотря на воздействие искусственного желудочного сока (желудочные кислоты) и искусственного кишечного сока (желчные кислоты), инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, по настоящему изобретению сохраняют эффективность адгезии к слизистой кишечника на высоком уровне (смотрите, Пример 7), при этом также подтверждена стабильности при хранении при различных температурах (смотрите, Пример 8).
Используемый в описании настоящей патентной заявки термин «атопическое заболевание» относится к сериям аллергических симптомов, проявленных на коже, слизистой дыхательных путей, слизистой глаз, слизистой кишечника или аналогичного им у индивидуумов со склонностью к атопическим заболеваниям, и такая склонность к атопическим заболеваниям (предрасположенность) передается по наследству, демонстрируя семейный характер. Аллергические заболевания, вызываемые склонностью к атопическим заболеваниям, могут включать атопические дерматиты, аллергические риниты, астму, аллергические конъюктивиты, атопические высыпания и аналогичное им, и эти заболевания могут протекать, как таковые по отдельности или несколько вместе одновременно. Атопический дерматит, который является одним из типичных кожных заболеваний, проявленных у персон с атопическими аллергиями, часто называемый врожденной лихорадкой (congenital fever). При атопическом дерматите кожа сухая и основным симптомом является кожный зуд, хотя в некоторых случаях он сопровождается другими аллергическими заболеваниями (такими как высыпания, аллергия на металл, астма и аллергический ринит) через свои иммунологические характеристики и семейную склонность.
Используемый в описании настоящей патентной заявки термин «атопический дерматит (AD)» относится к хроническому и рецидивирующему воспалительному кожному заболеванию с кожным зудом, и демонстрирует реакцию гиперчувствительности иммунной системы на антигены, такие как частицы пылевого клеща, попавшие на тело человека. Проникшие в тело антигены макрофаги представляют T клеткам, при и этом T клетки дифференцируются на Th1 или Th2 клетки согласно типу антигенов или рецепторов, с которыми они реагируют. Затем Th2 клетки активируют гуморальный иммунитет через цитокины, такие как IL-4, IL-5 и IL-10, и активируют B клетки, приводя к повышению продуцирования IgE и, таким образом, вызывая атопический дерматит. То есть, из-за иммунного нарушения при атопическом дерматите, в то время как иммуноглобулин IgE адгезируется на поверхности тучных клеток вокруг кровеносных сосудов в теле или в коже, антигены снова проникают в тело человека, связываясь с иммуноглобулинами для активации тучных клеток, позволяя, таким образом, тучным клеткам секретировать такие химические вещества, как гистамин. Эти химические вещества стимулируют кровеносные сосуды и клетки, вызывая на коже красные пятна, отечность и кожный зуд, в свою очередь таким образом вызывая или осложняя атопический дерматит.
В противоположность Th1 клетки активируют клеточный иммунитет через IL-12 и IFN-γ, и IFN-γ ингибирует продуцирование IgE.
Следовательно, считается, что сбалансированная иммунная регуляция Th1 клеток и Th2 клеток является основным ключом в профилактике или лечению симптомов атопических заболеваний, было обнаружено, что инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, по настоящему изобретению превосходно балансируют иммунную регуляцию Th1 и Th2 клеток, по существу достигая сбалансированной иммунной регуляции между Th1 типом цитокинов и Th2 типом цитокинов через различные иммунорегулирующие механизмы согласно тяжести атопического дерматита (смотрите, Примеры 9 и 10). То есть в случае легкого атопического дерматита, инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, по настоящему изобретению регулируют и поддерживают иммунологический баланс Th1 и Th2 клеток, в то время как в случае тяжелого атопического дерматита они ингибируют активность Th1 и Th2 клеток через стимуляцию регулировки T клеток, таким образом осуществляя терапию и снижая выраженность тяжелого атопического дерматита.
Следовательно, настоящее изобретение относится к фармацевтической композиции для профилактики и лечения атопических заболеваний, где композиция содержит в качестве активного ингредиента инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим. Дополнительно, настоящее изобретение относится к: применению инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, для получения агента для лечения атопического дерматита; и способу лечения или профилактики атопического заболевания, где способ включает введение эффективного количества инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, субъекту, нуждающемуся в лечении или профилактике атопического заболевания.
Указанный в описании настоящей патентной заявки атопический дерматит классифицируется на легкий, средний и тяжелый типы в зависимости от прогрессирования симптомов заболевания. Атопический дерматит по настоящему изобретению предпочтительно может представлять тяжелый атопический дерматит.
Используемый в описании настоящей патентной заявки термин «субъект» может относится к животному, предпочтительно млекопитающему и, в частности, животному, представляющему человека.
Сообщается о множестве шкал для оценки клинических курсов и терапевтической эффективности относительно атопического дерматита. В качестве эталонной шкалы оценки известны: индекс распространенности и тяжести экземы (Eczema Area and Severity Index) (EASI), Шкала оценки атопического дерматита (SCORing Atopic dermatitis) (SCORAD), пациент-ориентированное измерение экземы (Patient Oriented Eczema Measure) (POEM), и три степени тяжести (Three Item Severity) (TIS). Предпочтительно тяжесть атопического дерматита по настоящему изобретению классифицируется согласно шкале оценки атопического дерматита (SCORAD).
Фармацевтическая композиция по настоящему изобретению может содержать фармацевтически эффективное количество инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, как таковых или может дополнительно содержать по меньшей мере один фармацевтически приемлемый носитель. Фармацевтическая композиция по настоящему изобретению может быть введена пациенту, как однократная доза или может вводиться, как многократная доза при дробном протоколе лечения в течение длительного периода времени. Используемый в описании настоящей патентной заявки термин «фармацевтически эффективное количество» относится к количеству, требуемому для демонстрации более выраженного ответа по сравнению с отрицательным контролем, и предпочтительно количество достаточно для лечения или профилактики атопического дерматита. Эффективное количество инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, по настоящему изобретению может составлять 0,001-1000 мг/кг массы тела/день, и предпочтительно 0,055-16,65 мг/кг массы тела/день, без ограничения. Однако, фармацевтически эффективное количество может подходящим образом варьировать в зависимости от различных факторов, таких как тип заболевания и его тяжесть, возраст, масса тела, физическое состояние и пол пациента, способ введения и период лечения.
Композиция по настоящему изобретению может быть по разному составлена вместе с фармацевтически приемлемым носителем в зависимости от способа введения при использовании способов, известных из области техники, к которой относится настоящее изобретение. Используемый в описании настоящей патентной заявки термин «фармацевтически приемлемая» композиция относится к нетоксичной композиции, которая физиологически приемлема, не ингибирует действие активного ингредиента при введении людям и, как правило, не индуцирует аллергическую реакцию или аналогичные реакции, такие как проблемы с желудочно-кишечным трактом и головокружение. Композиция по настоящему изобретению может быть по разному составлена вместе с фармацевтически приемлемым носителем в зависимости от способа введения при использовании способов, известных из области техники, к которой относится настоящее изобретение. Способ введения может представлять без ограничения оральный или парентеральный и предпочтительным является оральный способ введения.
Фармацевтическая композиция по настоящему изобретению для орального введения может быть составлена вместе с подходящим носителем для орального введения в форме порошка, гранул, таблеток, пилюль, таблеток, покрытых сахарной оболочкой, капсул, жидкости, геля, сиропа, суспензии, воды или аналогичного им при использовании способов, известных из области техники, к которой относится настоящее изобретение. Например, таблетки или таблетки, покрытые сахарной оболочкой, для орального введения могут быть получены смешиванием активного ингредиента с твердым наполнителем, распылением смеси, добавлением в нее подходящего адъюванта и последующей технологической обработкой смеси в смесь в виде гранул. Примеры подходящего наполнителя могут включать: сахара, включая лактозу, декстрозу, сахарозу, сорбит, маннит, ксилит, эритрит и мальтит; крахмалы, включая кукурузный крахмал, пшеничный крахмал, рисовый крахмал и картофельный крахмал; целлюлозу, включая метилцеллюлозу, карбоксиметилцеллюлозу натрия и гидроксипропилметилцеллюлозу; и наполнитель, такой как желатин или поливинилпирролидон. В некоторых случаях в качестве разрыхлителя может быть добавлен перекрестно сшитый поливинилпирролидон, агар, альгиновая кислота или альгинат натрия. Дополнительно, фармацевтическая композиция по настоящему изобретению может дополнительно содержать антикоагулянт, лубрикант, увлажнитель, эмульгатор и консервант.
Дополнительно, для парентерального введения фармацевтическая композиция по настоящему изобретению вместе с подходящим носителем для парентерального введения может быть составлена при использовании способов, известных из области техники, к которой относится настоящее изобретение. Другими фармацевтически приемлемый носители являются, таковые описанные в следующем литературном источнике (Remington's Pharmaceutical Sciences, 19th ed., 1995, Mack Publishing Company, Easton, PA).
Дополнительно фармацевтическая композиция по настоящему изобретению может быть введена вместе с соединениями, известными, как эффективные для профилактики и лечения атопических заболеваний или атопического дерматита.
Дополнительно, настоящее изобретение относится к композиции пищевого продукта для профилактики и снижения выраженности атопического дерматита, где композиция содержит в качестве активного ингредиента инактивированные Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим. Дополнительно, настоящее изобретение относится к: применению инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, для получения пищевого продукта для профилактики и снижения выраженности атопического дерматита; и способу профилактики или снижения выраженности атопического заболевания употреблением в пищу пищевого продукта, содержащего в качестве активного ингредиента инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, субъекту, нуждающемуся в профилактике или снижении выраженности атопического заболевания
Используемый в описании настоящей патентной заявки термин «субъект» может относится к животному, предпочтительно млекопитающему и в частности, животному, представляющему человека.
Композиция пищевого продукта по настоящему изобретению включает все типы, включая функциональный пищевой продукт, нутритивные пищевые добавки, диетический пищевой продукт, пищевую добавку, питьевое и ферментированное молоко. Указанные выше типы композиций пищевых продуктов могут быть получены в различных формах при использовании способов, известных из области техники, к которой относится настоящее изобретение. Предпочтительно пищевой продукт по настоящему изобретению может представлять ферментированное молоко, йогурт, напиток, молочный напиток, пищевую добавку и диетический функциональный пищевой продукт.
Например, для диетического пищевого продукта инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, по настоящему изобретению могут быть получены для питья в форме питьевого йогурта, ферментированного молока, чая, сока, и напитка, и могут быть гранулированы, капсулированы или находиться в порошкообразной форме для потребления. Дополнительно, инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, по настоящему изобретению могут быть смешаны с известным материалом или активным ингредиентом, который известен, как эффективный для снижения выраженности атопического заболевания (в частности, атопического дерматита), получают в форме композиции.
Также для функционального пищевого продукта инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, по настоящему изобретению могут быть добавлены в напитки (включая алкогольные напитки), фрукты и прошедшие технологическую обработку продукты из них (например, консервированные в жестяной таре фрукты, консервированные в стеклянной таре фрукты, джемы, мармелады), рыба, мясо и прошедшие технологическую обработку продукты из них (например, ветчина, сосиски, консервированная говядина), кондитерские изделия и лапша (например, удон, гречневая лапша, рамен, спагетти, макароны), фруктовый сок, напитки, печенье, ирис, молочные продукты (например, сливочное масло, сыр), растительные масла, маргарин, растительные белки, пищевые продукты в реторт-упаковке, замороженные пищевые продукты, различные приправы (например, соевая паста, соевый соус, соус) или аналогичное им.
В композиции пищевого продукта по настоящему изобретению, содержание инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, предпочтительно составляет 0,001-50 масс.% готового прошедшего технологическую обработку пищевого продукта без ограничения.
Дополнительно, для применения инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, в форме пищевой добавки, инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, по настоящему изобретению могут быть получены в форме порошка или концентрированной жидкости.
В фармацевтических и композициях пищевого продукта по настоящему изобретению количество смешанного активного ингредиента может быть подходящим образом определено согласно целей их использования (профилактика, поддержание состояния здоровья или снижение выраженности симптомов), и, например, инактивированные нагреванием Lactobacillus rhamnosus, конъюгированным с полимерным полисахаридным связующим, могут содержаться в концентрации 108-1010 КОЕ/г. Эффективная доза инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим, по настоящему изобретению может быть определена согласно указанным выше пределам концентрации, но может составлять менее указанных выше пределов для целей поддержания состояния здоровья и гигиены или для долгосрочного потребления для контроля состояния здоровья. Активный ингредиент безопасен и, следовательно, может быть использован в избыточном количестве, превышающем таковые указанные выше пределы.
ПОЛЕЗНЫЙ ЭФФЕКТ
Инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, по настоящему изобретению являются превосходными для лечения атопического заболевания, значительно улучшая конкурентную адгезию со слизистой кишечника по сравнению с существующими препаратами молочнокислых бактерий и демонстрируя эффект профилактики, снижения выраженности или лечения атопического дерматита при эквивалентном уровне для существующих лекарственных средств на основе стероидов. Дополнительно, инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, по настоящему изобретению превосходно балансируют иммунную регуляцию Th1 и Th2 клеток, и по существу достигают сбалансированной иммунной регуляции между Th1 типом цитокинов и Th2 типом цитокинов через различные иммунорегулирующие механизмы согласно тяжести атопического дерматита.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
ФИГ. 1 - изображение под электронным микроскопом, демонстрирующее структуру гиалуроновой кислоты.
ФИГ. 2 - изображение под электронным микроскопом, демонстрирующее структуру гиалуроновой кислоты концентрированного связующего.
ФИГ. 3 - изображение под электронным микроскопом, демонстрирующее структуру Lactobacillus rhamnosus IDCC 3201 перед проведением инактивации нагреванием.
ФИГ. 4 - изображение под электронным микроскопом, демонстрирующее структуру Lactobacillus rhamnosus IDCC 3201 после проведения инактивации нагреванием.
ФИГ. 5 - изображение под электронным микроскопом, демонстрирующее структуру RHT-3201.
ФИГ. 6 - индекс шкалы оценки SCORAD терапевтического эффекта RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 7 - результаты наблюдения не вооруженным глазом эффекта лечения RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 8 - изменение в расчесывании при введении RHT-3201 по настоящему изобретению.
ФИГ. 9 - изменение массы тела при введении RHT-3201 по настоящему изобретению.
ФИГ. 10 - изменение уровня IgE в крови при введении RHT-3201 по настоящему изобретению.
ФИГ. 11 - результаты наблюдения не вооруженным глазом изменения в лимфатических узлах мышей при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 12 -изменение размера лимфатических узлов мышей при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 13 - изменение массы лимфатических узлов мышей при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 14 - изменение продуцирования IFN-γ при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 15 - изменение продуцирования IL-12 при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 16 - изменение продуцирования IL-4 при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 17 - изменение продуцирования IL-10 при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 18 - соотношение IL-4/ IFN-γ при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 19 - соотношение IFN-γ/IL-10 при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 20 - соотношение IL-4/IL-10 при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 21 - соотношение IL-12/IL-10 при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 22 - результаты наблюдения не вооруженным глазом патологических характеристик кожных тканей спинки при введении RHT-3201 по настоящему изобретению (верх) и результаты наблюдения под микроскопом кожных тканей, окрашенных H&E (низ) у моделей с тяжелым атопическим дерматитом.
ФИГ. 23 - толщина эпидермиса кожных тканей спинки при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 24 - толщина дермы кожных тканей спинки при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 25 - результаты наблюдения инфильтрации тучных клеток в кожных тканях спинки при окрашивании толуидиновым синим при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
ФИГ. 26 - изменение числа тучных клеток в кожных тканях спинки при введении RHT-3201 по настоящему изобретению у моделей с тяжелым атопическим дерматитом.
СПОСОБ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Далее настоящее изобретение будет описано более подробно.
Однако следующие примеры приведены только для иллюстрации настоящего изобретения и не ограничивают объем притязаний настоящего изобретения.
<Пример 1>
Оценка влияния типа связующего
<1-1> Получение образцов различных типов связующих
Lactobacillus rhamnosus IDCC 3201 (KCTC 10833BP) культивировали в MRS среде, содержащей 0,1-1% сухой сыворотки при температуре 37° в течение 24 часов. После культивирования бактерии и культуральный фильтрат разделили проведением центрифугирования. Затем в культуральный фильтрат добавили гиалуроновую кислоту, альгинат, мальтодекстрин, хитозан и полиэтиленгликоль в концентрации 0,1%(масса/объем) с последующим перемешиванием в течение 1 часа и коцентрированием после этого, с получением таким образом связующих, которые затем подвергли лиофильной сушке. Каждый образец развели раствором фосфатного буфера с получением конечного образца 1 мкг/мл. В качестве контроля использовали обезжиренное сухое молоко.
<1-2> Получение клеток селезенки
5-недельных самцов мышей BALB/c стимулировали 2 мг гидроксида алюминия и 1 мг яичного альбумина проведением интраперитонеальной инъекции и стимулировали второй раз аналогичным образом по прошествии шести дней. На 13 день провели сбор селезенок у каждой мыши, клетки селезенки экстрагировали с получением, таким образом, жидких клеток селезенки.
Предпочтительно клетки селезенки получили при использовании следующего способа.
Провели асептический сбор селезенок мышей и капельно добавили 10 μл сбалансированного солевого раствора Ненкса (HBSS). Провели разрыв при использовании пинцета над ситом с размером ячеек 60-mesh для сбора клеточной суспензии и затем сверху добавили 2,5 μл фетальной бычьей сыворотки, с последующим окрашиванием в течение 10 минут, с осаждением, таким образом, больших масс. Большие массы суспендировали в растворе NH4Cl (pH 7,0) в течение 3-4 минут с достижением гемолиза красных кровяных клеток. затем суспензию смешали с 2,5 μл фетальной бычьей сыворотки с последующим центрифугированием при 1,500 оборотах в минуту в течение 5 минут. Осадок промыли дважды HBSS и затем диспергировали в DMEM среде, содержащей 10% фетальной бычьей сыворотки и 1 мг/мл яичного альбумина в концентрации 5×106 клетки/мл, с получением, таким образом, клеток селезенки.
<1-3> Культивирование клеток селезенки и измерение цитокинов
200 μл суспензии клеток селезенки (5×106 клетки/мл) и 10 μл (1 μг/μл) каждого жидкого образца, полученного по Примеру <1-1>, добавили в каждую лунку 96-лунучного планшета с последующим культивированием в 5% CO2 инкубаторе в течение 7 дней. По окончанию культивирования в культуральной жидкости измерили уровни IL-4 и IL-12 при использовании набора Cytoset (Biosource). Уровни продуцирования IL-4 и IL-12 каждого образца выразили как показатель роста по сравнению с контролем, как приведено в Таблице 1.
[Таблица 1]
Определение связующих
| Тип связующего | Увеличение (%) по сравнению с контролем | Соотношение IL-4/IL-12 | |
| IL-4 | IL-12 | ||
| Гиалуроновая кислота | 5 | 52 | 0,09 |
| Альгинат | 15 | 29 | 0,51 |
| Мальтодекстрин | 9 | 36 | 0,25 |
| Хитозан | 17 | 38 | 0,44 |
| Полиэтиленгликоль | 13 | 22 | 0,59 |
По результатам теста связующее из гиалуроновой кислоты показало 5% увеличение продуцирования IL-4 и 52% увеличение продуцирования IL-12. Связующее из альгината показало 15% увеличение продуцирования IL-4 и 29% увеличение продуцирования IL-12. Связующее из мальтодекстрина показало 9% увеличение продуцирования IL-4 и 36% увеличение продуцирования IL-12. Связующее из хитозана показало 17% увеличение продуцирования IL-4 и 38% увеличение продуцирования IL-12. Связующее из полиэтиленгликоля показало 13% увеличение продуцирования IL-4 и 22% увеличение продуцирования IL-12. Следовательно, когда связующее получено при использовании полимерного полисахарида, показатель увеличения IL-12 был относительно высок, при этом показатель увеличения IL-4 был относительно низок. Из них гиалуроновая кислота показала самый высокий показатель увеличения IL-12 и относительно низкий показатель увеличения IL-4. После гиалуроновой кислоты хорошие результаты показали: мальтодекстрин, хитозан и альгинат.
<Пример 2>
Оценка влияния концентрации связующего
<2-1> Получение образцов концентрированием
Провели оценку влияния концентрации связующего, при этом среди полимерных полисахаридных материалов гиалуроновую кислоту, как показавшую наилучший эффект в Пример 1, использовали в качестве типичного материала. Гиалуроновую кислоту добавили в количестве 0,0001-1%(масса/объем) в культуральный фильтрат с последующим перемешиванием в течение 1 часа, и затем смесь концентрировали при пониженном давлении, с получением, таким образом, связующих из гиалуроновой кислоты с различными концентрациями, соответственно, и эти связующие подвергли лиофильной сушке. Каждый образец развели фосфатным буфером с получением конечного образца 1 μг/μл. В качестве контроля использовали сухое обезжиренное молоко.
<2-2> Тест на продуцирование цитокина
Показатель продуцирования цитокинов в клетках селезенки измерили для образцов связующих, полученных в Примере <2-1>, при использовании способа по Примеру <1-3>. Результаты приведены в Таблице 2 ниже.
[Таблица 2]
Определение концентрации добавленной гиалуроновой кислоты
| Концентрация гиалуроновой кислоты (масса/объем) | Увеличение (%) по сравнению с контролем | Соотношение IL-4/IL-12 | |
| IL-4 | IL-12 | ||
| 0,0001 | 9 | 46 | 0,19 |
| 0,001 | 7 | 52 | 0,13 |
| 0,01 | 10 | 37 | 0,27 |
| 0,1 | 12 | 33 | 0,36 |
| 1 | 15 | 25 | 0,60 |
По результатам теста, как показано в Таблице 2 выше, оптимальная концентрация гиалуроновой кислоты для получения связующего из гиалуроновой кислоты составила 0,001% (масса/объем), продуцирование IL-4 было снижено по сравнению с таковым контроля, и продуцирование IL-12 было повышено по сравнению с таковым в контроле.
<Пример 3>
Оценка влияния условий инактивации нагреванием на бактерии
Для определения оптимальных условий инактивации бактерий нагреванием оптимизировали условия инактивации нагреванием по температуре и времени и оценили адгезионную способность Caco-2 клеток, выбирая, таким образом, оптимальные условия. Далее приведено более подробное описание теста.
<3-1> Получение образцов инактивированных нагреванием бактерий
Бактерии Lactobacillus rhamnosus инактивировали нагреванием при температуре 60-120℃ в течение 10, 20, 30, 40, 50 и 60 минут (Heater, EYELA OSB-2100, China) и охладили до температуры 30℃ перед использованием их в качестве тестируемого образца. Каждый образец промыли дважды раствором фосфатного буфера, ресуспендировали в 1 μл того же раствора буфера и развели до 1×108 клеток/мл в свободной от сыворотки среде DMEM, перед использованием его в тесте.
<3-2> Оценка адгезивной способности к слизистой кишечника
Монослой клеток Caco-2 получили инокулированием Caco-2 клеток (Корейский банк линий клеток (Korean Cell Line Bank)) в концентрации 1,2×105 клеток/мл в модифицированной по способу Дульбекко среде Игл (DMEM, Hyclone, USA), обогащенной 10%(объем/объем) фетальной телячьей сыворотки и 20 мкл /мл гентамицина, диспергировали 1 мкл полученной в результате среды в каждую лунку 6-луночного планшета для культивирования тканей, культивирование клеток провели в течение 7 дней и дважды промыли раствором фосфатного буфера.
1 мкл жидкого образца, полученного по Примеру <3-1>, поместили в каждую лунку, в которой сформировался монослой клеток Caco-2, с последующим проведением реакции в течение 90 минут. В качестве контроля использовали 1 μл DMEM вместо инактивированных нагреванием молочнокислых бактерий. После проведения реакции удалили супернатант и добавили 1 μл 0,04%(масса/объем) Tween 80 для извлечения инактивированных нагреванием молочнокислых бактерий, адгезировавшихся на Caco-2 клетках, и провели подсчет количества бактерий при использовании гемоцитометра. Эффективность адгезии рассчитали, как показатель адгезировавшегося числа бактерий по сравнению с начальным числом бактерий (смотрите, Таблицу 3).
[Таблица 3]
Показатель адгезии бактерий по условиям инактивации бактерий нагреванием
| Показатель адгезии (%) с клетками Caco-2 | |||||
| Время инактивации нагреванием (минуты) | 60 | 70 | 80 | 90 | |
| 10 | 44 | 50 | 56 | 45 | |
| 20 | 48 | 53 | 68 | 49 | |
| 30 | 56 | 63 | 71 | 54 | |
| 40 | 60 | 66 | 76 | 42 | |
| 50 | 62 | 71 | 80 | 35 | |
| 60 | 63 | 72 | 85 | 32 | |
Как показано в Таблице 3, эффективность адгезии была самой хорошей, когда примененные условия инактивации нагреванием были следующими: 80 и 60 минут. Составляющие элементы, такие как липотейхоевая кислота, присутствующие на клеточных стенках молочнокислых бактерий, ингибируют адгезию болезнетворных бактерий, таких как E. coli и Salmonella, к поверхности слизистой кишечника, и связываются с TLR-2, который является одним из рецепторов дендритных клеток среди клеток слизистой кишечника, вовлеченных в активацию иммунитета желудочно-кишечного тракта человека. Следовательно, предполагается, что оптимальные условия инактивации бактерий нагреванием созданы для облегчения выхода сопряженных факторов, присутствующих на клеточной стенке, таким образом, инактивированные нагреванием молочнокислые бактерии адгезируются в желудочно-кишечном тракте, при этом конкурируя с резидентной флорой желудочно-кишечного тракта, и таким образом, в итоге активируя иммунитет желудочно-кишечного тракта.
<Пример 4>
Получение инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим
Бактерии, инактивированные нагреванием при температуре 80℃ в течение 60 минут в Примере 3, смешали с 0,001% связующего из гиалуроновой кислоты, полученным в Примере 2, в котором культуральный фильтрат Lactobacillus rhamnosus концентрировали после проведения реакции. В качестве носителя использовали такой носитель, как крахмал, который смешали с полученным в результате реакции материалом, с последующим проведением процесса сушки, с получением, таким образом, инактивированных нагреванием Lactobacillus rhamnosus, конъюгированных с полимерным полисахаридным связующим (указанные в описании настоящей патентной заявки, как «RHT-3201»). Был сопоставлен эффект промотирования иммунитета RHT-3201, полученного, как указано выше, и Lactobacillus rhamnosus IDCC 3201 в качестве пробиотика, при использовании способа по Примеру <1-3> (смотрите, Таблицу 4).
[Таблица 4]
Сравнение эффекта промотирования иммунитета традиционных пробиотических бактерий и RHT-3201 по настоящему изобретению
| RHT-3201 | Пробиотический препарат |
|
| Увеличение IL-4 (%) по сравнению с контролем | 3 | 20 |
| Увеличение IL-12 (%) по сравнению с контролем | 67 | 29 |
| Соотношение IL-4/IL-12 | 0,04 | 0,68 |
Как показано в Таблице 4, был подтвержден регулирующий эффект цитокинов, вовлеченных в Th1/Th2, и был в 17 раз выше у молочнокислых бактерий RHT-3201 по настоящему изобретению, по сравнению с существующими пробиотиками. Предполагается, что RHT-3201 был получен в процессе получения в такой форме, которая способствует связыванию с соответствующим рецептором слизистой кишечника, таким как TLR-2.
<Пример 5>
Структурный анализ при использовании электронного микроскопа (FE-SEM)
Структурный анализ фазы RHT-3201, полученной в Примере 4, провели фотографированием при использовании электронного микроскопа (FE-SEM, Model: LEO SUPRA 55, GENESIS 2000 (Carl Zeiss, EDAX)) согласно каждому способу получения. Результаты анализа, полученного при использовании электронного микроскопа согласно стадиям получения RHT-3201, приведены на Фигурах 1-5.
Как показано на Фигурах 1 и 2, видно, что в процессе получения связующего культуральный фильтрат Lactobacillus rhamnosus IDCC 3201 смешали с гиалуроновой кислотой, с последующим концентрированием, таким образом, частицы гиалуроновой кислоты становятся плотнее, формируя структуру связующего (смотрите, ФИГ. 2). Как показано на Фигурах 3 и 4, клеточные стенки молочнокислых бактерий не фрагментированы инактивацией нагреванием бактерий при специфических условиях, но подвергшаяся воздействию структура позволяет легко адгезироваться на слизистой кишечника (смотрите, ФИГ. 4). Наконец, инактивированные нагреванием бактерии были смешаны со связующим из гиалуроновой кислоты для облегчения адгезии со слизистой кишечника (смотрите, ФИГ. 5).
<Пример 6>
Получение массы из RHT-3201
Для исследования воспроизводимости при получении массы RHT-3201 способом по Примеру 4 выше показатель адгезии в желудочно-кишечном тракте сравнили с пробиотиками и полученной массой RHT-3201 (смотрите, Таблицу 5).
В частности, Lactobacillus rhamnosus IDCC культивировали при температуре 37℃ в течение ночи в ферментационном танке с получением 1 тонны. Культуральный фильтрат и бактерии разделили проведением центрифугирования и добавили в культуральный фильтрат культуральную жидкость с объемом гиалуроновой кислоты 0,001% (масса/объем), затем провели концентрирование при пониженном давлении при температуре 50°, с получением, таким образом, связующего, которое конъюгируется с поверхностью инактивированных нагреванием бактерий. Бактерии подвергли термической обработке при температуре 80° в течение 60 минут, с получением, таким образом, инактивированных нагреванием бактерий. Дополнительно, связующее и инактивированные нагреванием бактерии смешали, гомогенизировали и высушили с получением, таким образом, RHT-3201. В качестве контроля использовали пробиотики Lactobacillus rhamnosus IDCC 3201, полученные согласно традиционному способу получения пробиотических сырьевых материалов. В частности, бактерии, полученные из той же самой культуральной жидкости, суспендированные в 20 мкл раствора фосфатного буфера, и прошедшие лиофильную сушку, с получением, таким образом, бактерий в порошкообразной форме.
[Таблица 5]
Сравнение показателей адгезии традиционного пробиотического препарата и RHT-3201 по настоящему изобретению
| RHT-3201 | Пробиотический препарат | |
| Показатель адгезии (%) | 85 | 54 |
Как видно из Таблицы 5, было подтверждено, что показатель адгезии RHT-3201 показал 57% улучшение по сравнению с пробиотическим препаратом Lactobacillus rhamnosus.
<Пример 7>
Оценка стабильности при потреблении <7-1>
Стабильность при воздействии кислоты
Препарат молочнокислых бактерий подвергли воздействию желудочных кислот, которые воздействуют при прохождении через желудок и пищеварительный тракт. Провели сравнение стабильности при воздействии кислоты между пробиотическими бактериями и RHT-3201 по настоящему изобретению в среде, воспроизведенной in vitro. В частности, 10% HCl капельно добавили в MRS среду для регулирования pH до 2,3 и 2,5, и затем MRS стерилизовали для использования. 1 г пробиотиков и образцы RHT-3201, соответственно, поместили в pH-отрегулированную среду, затем провели реакцию в течение 0, 1 и 2 часов. Показатель адгезии проанализировали измерением числа бактерий, адгезировавшихся на клетки Caco-2 при использовании способа по Примеру <3-2>. Использовавшиеся в тесте молочнокислые бактерии представляли Lactobacillus rhamnosus IDCC 3201. Также в тесте использовали RHT-3201, полученные способом получения по Примеру 6, и пробитики.
[Таблица 6]
Результаты измерения стабильности при воздействии кислоты на RHT-3201 по настоящему изобретению
| Тести-руемый образец | pH 2,3(x108КОЕ/мл) | Пока-затель адгезии (%) | pH 2,5(x108КОЕ/мл) | Пока-затель адгезии (%) | ||||
| 0 | 1 ч | 2 ч | 0 | 1 ч | 2 ч | |||
| Пробио-тические бактерии | 1 | 0,1 | 0,04 | 4 | 1 | 0,19 | 0,07 | 7 |
| RHT-3201 | 1 | 0,7 | 0,34 | 34 | 1 | 0,83 | 0,48 | 48 |
Как видно из Таблицы 6, подтверждено, что по сравнению с пробиотическими бактериями эффективность адгезии RHT-3201 по настоящему изобретению остается стабильной даже при 2 часовом воздействии кислоты.
<7-2> Стабильность при воздействии желчи
Кишечно-печеночная рециркуляция желчных кислот достигается таким образом, что желчные кислоты, продуцированные в печени, выходят через желчевыводящие пути, поступают в тонкий кишечник, затем 95% абсорбируется в подвздошной кишке, которая является конечным участком тонкой кишки, и снова поступают в печень. Желчные кислоты оказывают влияние на способность к адгезии молочнокислых бактерий, поселившиеся в тонкой кишке. Следовательно, различия в показателях адгезии, полученные при проведении сравнения между пробиотическими бактериями и RHT-3201 по настоящему изобретению, вызваны воздействием желчи. В частности, после стерилизации добавили MRS среду с и без 0,3% желчных кислот. Затем 1 г пробиотических бактерий и RHT-3201 по настоящему изобретению инокулировали в среде, соответственно, с последующим проведением реакции в течение 2 часов. Затем провели анализ показателей адгезии измерением числа бактерий, адгезировавшихся на клетки Caco-2, при использовании способа по Примеру <3-2>.
Использовавшиеся в тесте молочнокислые бактерии представляли Lactobacillus rhamnosus IDCC 3201. Также в тесте использовали RHT-3201, полученные способом получения по Примеру 6, и пробитики.
[Таблица 7]
Результаты стабильности при воздействии желчи на RHT-3201 по настоящему изобретению
| Тестируемый образец | MRS (x108КОЕ/ml) | MRS+0,3% bile(x108КОЕ/ml) | Показатель адгезии (%) |
| Пробиотические бактерии | 1 | 0,23 | 23 |
| RHT-3201 | 1 | 0,57 | 57 |
Как видно из Таблицы 7, подтверждено, что при воздействии желчных кислот в течение 2 часов эффективность адгезии RHT-3201 сохраняется при значении 57%, что в около 2,5 раза выше, чем таковой у пробиотических бактерий.
<Пример 8>
Оценка стабильности при воздействии температуры с течением времени
<8-1> Сравнительный тест на стабильность в течение времени при температуре 4° между RHT-3201 и пробиотическими бактериями
RHT-3201 по настоящему изобретению, полученные по Примеру 6 выше, и пробиотические бактерии хранили в холодильнике при температуре 4° в течение 365 дней, и затем провели измерение по времени числа адгезировавшихся бактерий на 1 г сырьевого материала. Результаты приведены в Таблице 8. Число адгезировавшихся бактерий измерили при использовании способа по Примеру <3-2>. Провели анализ показателя адгезии измерением числа бактерий, адгезировавшихся на клетки Caco-2.
[ТАБЛИЦА 8]
Сравнительный тест на стабильность в течение времени при температуре 4° между RHT-3201 по настоящему изобретению и пробиотическими бактериями
| Тестируемый образец | Стабильность с течением временим при температуре 4° | Показатель остаточной адгезии (%) | |||
| 0 дней | 60 дней | 180 дней | 365 дней | ||
| Пробиотические бактерии | 65% | 52% | 34% | 19% | 29,2 |
| RHT-3201 | 82% | 71% | 52% | 45% | 54,8 |
<8-2> Сравнительный тест на стабильность при температуре 15℃ с течением времени между RHT-3201 и пробиотиками
RHT-3201 по настоящему изобретению, полученные по Примеру 6 выше, и пробиотики хранили в холодильнике при температуре 15°С в течение 365 дней, и затем провели измерение по времени числа адгезировавшихся бактерий на 1 г сырьевого материала. Результаты приведены в Таблице 9. Число адгезировавшихся бактерий измерили при использовании способа по Примеру <3-2>. Провели анализ показателя адгезии измерением числа бактерий, адгезировавшихся на клетки Caco-2.
[Таблица 9]
Сравнительный тест на стабильность в течение времени при температуре 15° между RHT-3201 по настоящему изобретению и пробиотическими бактериями
| Тестируемый образец | Стабильность с течением временим при температуре 15° | Показатель остаточной адгезии (%) | |||
| 0 дней | 60 дней | 180 дней | 365 дней | ||
| Пробиотические бактерии | 65% | 46% | 29% | 15% | 23,1 |
| RHT-3201 | 82% | 66% | 59% | 38% | 46,3 |
<8-3> Сравнительный тест на стабильность при температуре 25° с течением времени между RHT-3201 и пробиотиками
RHT-3201 по настоящему изобретению, полученные по Примеру 6 выше, и пробиотики хранили в холодильнике при температуре 25℃ в течение 365 дней, и затем провели измерение по времени числа адгезировавшихся бактерий на 1 г сырьевого материала. Результаты приведены в Таблице 10. Число адгезировавшихся бактерий измерили при использовании способа по Примеру <3-2>. Провели анализ показателя адгезии измерением числа бактерий, адгезировавшихся на клетки Caco-2.
[Таблица 10]
Сравнительный тест на стабильность в течение времени при температуре 25℃ между RHT-3201 по настоящему изобретению и пробиотическими бактериями
| Тестируемый образец | Стабильность с течением временим при температуре 4° | Показатель остаточной адгезии (%) | |||
| 0 дней | 60 дней | 180 дней | 365 дней | ||
| Пробиотические бактерии | 65% | 39% | 25% | 12% | 18,4 |
| RHT-3201 | 82% | 56% | 49% | 35% | 42,6 |
<8-4> Сравнительный тест на стабильности при температуре 37° с течением времени между RHT-3201 и пробиотиками
RHT-3201 по настоящему изобретению, полученные по Примеру 6 выше, и пробиотики хранили в холодильнике при температуре 7℃ в течение 365 дней, и затем провели измерение по времени числа адгезировавшихся бактерий на 1 г сырьевого материала. Результаты приведены в Таблице 11. Число адгезировавшихся бактерий измерили при использовании способа по Примеру <3-2>. Провели анализ показателя адгезии измерением числа бактерий, адгезировавшихся на клетки Caco-2.
[Таблица 11]
Сравнительный тест на стабильность в течение времени при температуре 37℃ между RHT-3201 по настоящему изобретению и пробиотическими бактериями
| Тестируемый образец | Стабильность с течением временим при температуре 37° | Показатель остаточной адгезии (%) | |||
| 0 дней | 60 дней | 180 дней | 365 дней | ||
| Пробиотические бактерии | 65% | 29% | 15% | 8% | 12,3 |
| RHT-3201 | 82% | 46% | 44% | 32% | 39,0 |
<Пример 9>
Регуляция продуцирования цитокинов RHT-3201 у in vitro моделей с индуцированным легким атопическим дерматитом
Провели оценку влияния RHT-3201 по настоящему изобретению, пробиотиков и препарата инактивированных бактерий, полученных из одних и тех же молочнокислых бактерий, на мышиные модели с индуцированным легким атопическим дерматитом при использовании следующего специфического способа тестирования.
<9-1> Получение образцов
RHT-3201 по настоящему изобретению и пробиотический препарат получили при использовании способа по Примеру 6 выше, при использовании культуральной жидкости, полученной культивированием Lactobacillus rhamnosus IDCC 3201 в MRS среде, содержащей 0,1-1% сухой сыворотки при температуре 37° в течение 24 часов.
Для инактивированных бактерий бактерии, полученные из культуральной жидкости, суспендировали в 500 мкл раствора фоосфатного буфера и подвергли сушке проведением лиофильной сушки. Сухие бактерии взвесили и суспендировали в стерильном фосфатном буфере до получения 300 мг/мл. Суспензию подвергли инактивации нагреванием при температуре 100°С в течение 30 минут, с получением, таким образом инактивированных бактерий. Три типа образцов развели раствором фосфатного буфера с получением 1 мкг/мл конечных образцов, соответственно. В качестве контроля использовали сухое обезжиренное молоко.
<9-2> Культура клеток селезенки и измерение цитокинов
Клетки селезенки получили при использовании способа по Примеру <1-2>. 200 μл суспензии клеток селезенки (5×106 клеток/мл) и 10 мкл (1 мкг/мл) каждого жидкого образца, полученного по Примеру <9-1>, добавили в каждую лунку 96-лунучного планшета, с последующим культивированием в 5% CO2 инкубаторе в течение 7 дней. По окончанию культивирования в культуральной жидкости измерили уровни IL-4 и IL-12 при использовании набора Cytoset (Biosource). Уровни продуцирования IL-4 и IL-12 каждого образца выразили, как показатель роста по сравнению с контролем, как приведено в Таблице 12.
[Таблица 12]
Увеличение показателя цитокинов в клетках селезенки при добавлении образца молочнокислых бактерий
| образец | Увеличение (%) по сравнению с контролем | Соотношение IL-4/IL-12 | |
| IL-4 | IL-12 | ||
| Lactobacillus rhamnosus IDCC 3201 (пробиотические бактерии) | 20 | 29 | 0,68 |
| Lactobacillus rhamnosus IDCC 3201 (инактиви-рованные бактерии) | 12 | 34 | 0,35 |
| RHT-3201 | 3 | 67 | 0,04 |
По результатам теста наблюдалось 20% увеличение продуцирования IL-4 и 29% увеличение продуцирования IL-12 у пробиотических бактерий Lactobacillus rhamnosus IDCC 3201. Инактивированные бактерии показали 12% увеличение продуцирования IL-4 и 34% увеличение продуцирования IL-12. RHT-3201 показали 3% увеличение продуцирования IL-4 и 67% увеличение продуцирования IL-12. Следовательно, подтверждается, что RHT-3201 по настоящему изобретению, которые показали значительное увеличение продуцирования IL-12 и относительно небольшое увеличение продуцирования IL-4, имеют самый наилучший эффект регулирования продуцирования цитокинов.
<Пример 10>
Терапевтический эффект RHT-3201 по настоящему изобретению у in vivo моделей с индуцированным тяжелым атопическим дерматитом
<10-1> Получение тестируемого материала и индуцирующего антигена
В качестве тестируемого материала использовали RHT-3201 по настоящему изобретению, при этом дексаметазон на основе стероида (Sigma Co. Ltd), который используют в качестве основного терапевтического агента при тяжелом атопическом дерматите, использовали в качестве положительного контроля. Экстракт Dermatophagoides farina, который является основным видом домашнего пылевого клеща, использовали в качестве материала, индуцирующего атопическое заболевание. Экстракт был приобретен в в форме мази у Central Lab. Animal Inc.
Дексаметазон получили растворением в этаноле в концентрации 0,1% (масса/объем), и RHT-3201 по настоящему изобретению получили растворением в дистиллированной воде с дозировкой 1×108 КОЕ/0,5 мл/мышь, 1×109 КОЕ/0,5 мл/мышь, и 1×1010 КОЕ/0,5 мл/мышь, соответственно. Все образцы были получены в день тестирования. Дексаметазон нанесли на кожу тестируемого субъекта в концентрации 100 μл для каждого субъекта дважды в неделю, при этом RHT-3201 по настоящему изобретению вводили орально в концентрации 0,5 μл для каждого субъекта при использовании зонда для мышей один раз в день. Дистиллированную воду вводили нормальной группе и контрольной группе с атопическим заболеванием. Введение проводили в течение 8 недель во всех тестируемых группах.
<10-2> Получение и размножение участвующих в тесте животных
Самок мышей NC/Nga (6 недельного возраста) приобрели у Central Lab. Animal Inc., и акклиматизировали в течение 1 недели перед использованием. Среда для размножения была следующей: поддерживали постоянную температуру (22±2 ℃) и постоянную влажность (50-60%), при этом цикл света (08:00~20:00) и темноты (20:00~08:00) контролировали с 12 часовым интервалом. В каждую полисульфоновую клетку поместили по три животных и провели их размножение, корм, представляющий рацион для теста, и вода находились в свободном доступе в течение 24 часов.
<10-3> Индуцирование тяжелого атопического дерматита
Полностью побрили верхнюю часть ушных раковин в областях нанесения 7 недельных мышей Th7 NC/Nga, и затем распылили на побритые участки 150 μл водного раствора 4% натрий додецилсульфата (SDS). После полного высыхания побритые места равномерно покрыли 100 мг мази с домашним пылевым клещом (экстракт домашнего пылевого клеща). Мазь с домашним пылевым клещом (экстракт домашнего пылевого клеща) наносили дважды в неделю в течении трех недель, всего шесть раз для индуцирования среднего или тяжелого дерматита. Далее мазь наносили один раз в неделю в течение периода введения тестируемым группам (8 недель), поддерживая, таким образом, тяжелый атопический дерматит.
[Таблица 13]
Оценка индуцированного тяжелого атопического дерматита у каждой модели перед обработкой тестируемыми материалами
| Оценка тяжелого атопического дерматита Среднее ± SE (n=6) |
||
| Нормальная группа | 0 | |
| Контроль - атопическое заболевание (Носитель) | 11,0 ± 0,4 | |
| Дексаметазон (Положительный контроль) | 10,8 ± 0,4 | |
| RHT-3201 | 1×108КОЕ/мышь | 10,8 ± 0,4 |
| 1×109КОЕ/мышь | 10,7 ± 0,3 | |
| 1×1010КОЕ/мышь | 10,7 ± 0,3 | |
Как видно из Таблицы 13, результат индуцирования тяжелого атопического дерматита нанесением мази с домашним пылевым клещом (экстракт домашнего пылевого клеща) NC/Nga мышам в течение трех недель, средняя оценка каждой группы составила 10 или выше, таким образом, были получены NC/Nga мыши с тяжелым атопическим дерматитом.
<10-4> Оценка атопического дерматита
В настоящей оценке тяжесть атопического дерматита выразили, как общее оценок пяти признаков, при использовании SCORAD Шкалы оценки атопического дерматита (SCORing Atopic dermatitis), которую, как правило, используют в качестве метода оценки при клинических исследованиях с проведением оценки не вооруженным глазом. Признаками для оценки были: эритема, сухая кожа, отек, расчесы и лихенификация. Оценки пяти признаков (отсутствие симптомов (оценка 0), слабовыраженные симптомы (оценка 1), умеренно выраженные симптомы (оценка 2), сильно выраженные симптомы (оценка 3) для каждого признака) сложили вместе, при этом оценочные значения детерминировали от самой низкой оценки 0 (состояние, при котором симптомы отсутствуют) до самой высокой оценки 15 (состояние, при котором симптомы всех пяти признаков - тяжелые). Тяжесть поражения кожного покрова мышей оценивали каждую неделю (смотрите, ФИГ. 6).
На ФИГ. 6, носитель - результаты групп мышей с тяжелым, индуцированным домашним пылевым клещом атопическим дерматитом, и дексаметазон - результаты групп мышей, на кожный покров которых наносили лекарственное средство с использованием дексаметазон, в качестве положительного контроля в течение 8 недель. RHT-3201 108, RHT-3201 109, и RHT-3201 1010 - результаты групп мышей с тяжелым, индуцированным домашним пылевым клещом атопическим дерматитом, которым вводили RHT-3201 по настоящему изобретению в различных концентрациях: RHT-3201 108 - результаты группы получавших терапию мышей с оральным введением 1×108 КОЕ/мышь в течение 8 недель; RHT-3201 109 -результаты группы получавших терапию мышей с оральным введением 1×109 КОЕ/мышь в течение 8 недель; и RHT-3201 1010 - результаты группы получавших терапию мышей с оральным введением 1×1010 КОЕ/мышь в течение 8 недель.
Результат исследования эффекта снижения выраженности тяжелого атопического дерматита после 8 недельной экспериментальной терапии подтвердил, как показано на ФИГ. 6, что оценка тяжелого атопического дерматита у группы с носителем без какой-либо терапии лекарственным средством имела среднее, равное 8,0, указывая на сохранение начального тяжелого состояния. При сравнении с группой мышей с тяжелым, индуцированным домашним пылевым клещом атопическим дерматитом (группа носителя) оценка тяжести поражения кожного покрова мышей была значительно ниже во всех группах, получавших терапию RHT-3201 108, RHT-3201 109, и RHT-3201 1010, соответственно. В частности, группа, которой вводили RHT-3201 108, показала оценку тяжелого атопического дерматита, равную 4,2, что в результате указывает на эффективность снижения выраженности тяжелого атопического дерматита на 47,5%. Группа, которой вводили RHT-3201 109, показала оценку тяжелого атопического дерматита, равную 2,3, что в результате указывает на эффективность снижения выраженности тяжелого атопического дерматита на 71,25%. Группа, которой вводили RHT-3201 1010, показала оценку тяжелого атопического дерматита, равную 2,7, что в результате указывает на эффективность снижения выраженности тяжелого атопического дерматита на 66,25%.
Общеизвестно, что препараты молочнокислых бактерий необходимо потреблять в больших количествах, отсутствуют данные об оптимальных концентрациях таких препаратов для достижения эффекта снижения выраженности тяжелого атопического дерматита. Причина состоит в том, что, как и молочнокислые пробиотики, молочнокислые бактерии погибают в больших количествах в желудочно-кишечном тракте под воздействием желчных кислот, проходя через желудочно-кишечный тракт, что вызывает снижение эффективности адгезии к слизистой кишечника, способной демонстрировать иммунную активность, и таким образом выводятся из тела. В отличие от этого, RHT-3201 по настоящему изобретению ясно показал обладание терапевтическим эффектом в различных концентрациях. Потребление x109 и x1010 единиц показало сходство в диапазоне значения ошибок относительно эффективности и снижения выраженности тяжелого атопического дерматита. Причина состоит в том, что комбинация с toll-подобным рецептором, расположенным в дендритных клетках слизистой кишечника, имеет порог насыщения.
ФИГ. 7 - результаты наблюдения не вооруженным глазом терапевтического эффекта Lactobacillus RHT-3201 при оральном введении при тяжелом атопическом дерматите. В очагах поражения кожного покрова группы носителя ясно наблюдалась сухая кожа, эритема, отек, лихенификация и расчесы, вызванные кожным зудом, индуцированным постоянным расчесыванием. При исследовании не вооруженным глазом было установлено, что тяжесть атопического дерматита снизилась в группах, получавших RHT-3201 во всех концентрациях.
<10-5> Расчесывание и измерение массы тела
Проводили подсчет числа расчесываний за 15 минут один раз в неделю с 1 недели введения тестируемого лекарственного средства. Проводили подсчет только расчесываний, производившихся задней конечностью, во избежание подсчета расчесываний, вызванных другими причинами помимо расчесываний из-за кожного зуда. При этом имеет место тенденция потери массы тела из-за побочных эффектов лекарственных средств и стресса во время индуцирования тяжелого атопического дерматита. Для исследования существования наличия потери массы тела, вызванного тестируемыми материалами, по настоящему изобретению проводили взвешивание участвовавших в тестах животных в течение периода введения.
Как показано на ФИГ. 8, измеренное число расчесов составило 100/час или менее во всех группах, получавших тестируемые материалы, в течение восьми недель, при этом наблюдалась тенденция снижения числа расчесов каждую неделю по сравнению с группой носителя. На 3, 6 и 8 неделях наблюдались значительные статистически значимые улучшения в группах, получавших RHT-3201 во всех концентрациях, по сравнению с группой носителя.
Дополнительно, как показано на ФИГ. 9, трансдермальное введение дексаметазона в качестве положительного контроля во время восьми недель вызвало потерю массы тела в течение 4 недель, в то время как введение RHT-3201 по настоящему изобретению показало прирост массы тела, также как и в нормальной группе; не было вызвано побочного эффекта потери массы тела, и таким образом была подтверждена безопасность RHT-3201 по настоящему изобретению.
<10-6> Измерение уровня IgE в сыворотке
После введения тестируемых лекарственных средств в течение восьми недель провели забор крови через ретро-орбитальное венозное сплетение и центрифугировали при 12,000 оборотах в минуту в течение 10 минут для отделения сыворотки. Уровень IgE в сыворотке измерили при использовании набора ELISA (SHIBAYAGI, Japan).
Как показано на ФИГ. 10 касательно IgE, в частности, известно, что во время индуцирования тяжелого атопического дерматита его уровень повышается, в группах, получавших RHT-3201, по настоящему изобретению наблюдались значительные ингибирующие эффекты, при этом, в частности, при сравнительной оценке различных концентраций, потребление x 109 единиц показало наивысший ингибирующий эффект.
<10-7> Способность продуцировать цитокины клетками лимфатического узла
После окончания введения тестируемых материалов каждую мышь NC/Nga с индуцированным тяжелым атопическим дерматитом умертвили. Провели измерение размера и массы подмышечных лимфатических узлов. Дополнительно, клеточные суспензии, полученные из подмышечных лимфатических узлов, диспергировали в RPMI-1640 среде (содержащей 10% FBS, 1% пенициллина и 1% стрептомицина) до концентрации 5×106 клеток/мл. Добавили экстракт домашнего пылевого клеща (D. farina) до получения конечной концентрации 10 мкг/мл, и культивировали в течение 48 часов в инкубаторе с 5% CO2 при температуре 370C. Собрали супернатант для измерения уровней продуцирования IFN- γ, IL-4, IL-10 и IL-12 при использовании набора ELISA (производитель IFN- γ & IL-4: R&D SYSTEMS, USA; и производитель IL-10 & IL-12: SIGMA ALDRICH, USA).
Как показано на ФИГ. 11, подмышечные лимфатические узлы участвуют в иммунном ответе кожного покрова спинки мыши NC/Nga, в то время как лимфатические узлы группы носителя были увеличены из-за воздействия антигена домашнего пылевого клеща (экстракт домашнего пылевого клеща). Как показано на Фигурах 12 и 13, показатели измерения объема и массы лимфатических узлов составили 70 мм3 и 35 мг, соответственно, что было в 5 или 7 раз больше по сравнению с нормальной группой. При этом размер подмышечных лимфатических узлов у мышей NC/Nga с тяжелым индуцированным атопическим дерматитом был значительно уменьшен в группах, получавших RHT-3201.
Для подтверждения способности продуцировать цитокины при введении RHT-3201 подмышечный лимфатический узел у мышей NC/Nga с индуцированным тяжелым атопическим дерматитом подвергли воздействию антигена домашнего пылевого клеща и затем измерили уровень цитокинов, вовлеченных в иммунный ответ. Результаты приведены на Фигурах 14-21. Было подтверждено, что введение RHT-3201 по настоящему изобретению значительно снизило цитокин IFN-γ типа Th1 (смотрите, ФИГ. 14) и его индуктор, IL-12 (смотрите, ФИГ. 15), по сравнению с носителем. Также было подтверждено, что введение RHT-3201 по настоящему изобретению значительно снизило цитокин IL-4 типа Th2 (смотрите, ФИГ. 16), по сравнению с носителем. Основные секреторные клетки IL-10 в лимфатических узлах, то есть, регуляторные T клетки, оказали иммуносупрессивное действие, ингибирующее Th1 и Th2 реакцию. Также было подтверждено, что введение RHT-3201 значительно снизило IL-10 (смотрите, ФИГ. 17) по сравнению с носителем.
Для сравнения механизма действия RHT-3201 на тяжелый атопический дерматит было показано соотношение цитокин типа Th1/цитокин типа Th2 для уровней цитокинов, экспрессировавшихся в каждой группе введения. Из приведенного на ФИГ. 18 результата видно, что соотношение IL-4/IFN-γ в группах, получавших RHT-3201, не отличалось по сравнению с группой носителя. Эти результаты отличаются от регуляторной реакции цитокин типа Th1/ цитокин типа Th2 при введении RHT-3201 по настоящему изобретению при среднем атопическом дерматите в Примере 9, указывая на то, что RHT-3201 по настоящему изобретению имеет отличающийся механизм действия на тяжелый атопический дерматит. То есть, было подтверждено, что механизм действия RHT-3201 по настоящему изобретению варьирует в зависимости от тяжести атопического дерматита.
Для подтверждения того, что цитокин IL-10 является фактором действия, вовлеченным в ингибирование регулировки T клеток (Treg) в качестве другого механизма действия на тяжелый атопический дерматит при приеме RHT-3201 по настоящему изобретению, сравнили и проанализировали соотношение IFN-γ/IL-10 (смотрите, ФИГ. 19), соотношение IL-4/IL-10 (смотрите, ФИГ. 20), и соотношение IL-12/IL-10 (смотрите, ФИГ. 21). В результате было подтверждено, что показатели соотношений были значительно снижены у групп, получавших RHT-3201 по настоящему изобретению. Следовательно, было показано, IL-10 является фактором действия, вовлеченным в лечение тяжелого атопического дерматита, и цитокин повышает активность Treg, таким образом, демонстрируя терапевтический эффект при тяжелом атопическом дерматите.
<10-8> Гистопатологическое исследование
Провели сбор кожного покрова спинок мышей NC/Nga, зафиксировали в 10% формалине и залили парафином, провели тонкую нарезку толщиной 4 мм, с получением, таким образом, препарата. Затем провели окрашивание гематоксилином & эозином (H&E) для исследования изменений толщины эпидермиса, при этом тучные клетки были подтверждены окрашиванием толуидином синим. Толщину кожного покрова и число тучных клеток рассчитали при использовании оптического микроскопа с увеличением 100 и 400.
В результате исследования окрашенных H&E кожных тканей спинки мышей NC/Nga, как показано на ФИГ. 22, группа носителя с атопическим дерматитом, индуцированным воздействием домашнего пылевого клеща, показала, что полученные гистопатологические результаты повышенного утолщения вызваны утолщением эпидермального слоя относительно дермального слоя по сравнению с нормальной группой и повышенной инфильтрацией воспалительных клеток. При микроскопическом исследовании группы, получавшие RHT-3201, по настоящему изобретению показали пониженную инфильтрацию воспалительных клеток; значительное ингибирование увеличения толщины эпидермиса (смотрите, ФИГ. 23) и повышение толщины дермы (смотрите, ФИГ. 24), что наблюдалось при индуцировании атопического дерматита по сравнению с группой носителя.
В результате исследования окрашенных толуидином синим кожных тканей спинки мышей NC/Nga было подтверждено, что тучные клетки дополнительно проникли в кожные ткани группы носителя с атопическим дерматитом, индуцированным воздействием домашнего пылевого клеща, который представляет антигенный материал, индуцирующий атопический дерматит, по сравнению с нормальной группой (смотрите, ФИГ. 25). При тяжелом атопическом дерматите число тучных клеток, как правило, возрастает в соответствии с его периодом. Как показано на ФИГ. 26, было подтверждено, что число тучных клеток повысилось в кожных тканях мышей (носитель), подвергшихся воздействию домашнего пылевого клеща, в течение 11 недель, при этом число тучных клеток у мышей с индуцированным тяжелом атопическим дерматитом было значительно снижено в группах, получавших RHT-3201, в течение восьми недель. Следовательно, RHT-3201 по настоящему изобретению оказывает значительное воздействие по снижению выраженности тяжелого атопического дерматита.
Промышленная применимость
Как указано выше, настоящее изобретение относится к инактивированные нагреванием Lactobacillus rhamnosus, конъюгированным с полимерным полисахаридным связующим, способу их получения, и их применению. Инактивированные нагреванием Lactobacillus rhamnosus, конъюгированные с полимерным полисахаридным связующим, по настоящему изобретению обладают превосходным терапевтическим эффектом при атопических заболеваниях, по существу значительно улучшают конкурентную адгезию к слизистой кишечника препаратов из традиционных молочнокислых бактерий и демонстрируют профилактический, снижающий выраженность или терапевтический эффект при атопическом дерматите на уровне, эквивалентном таковому у лекарственного средства на основе стероидов. Следовательно, настоящее изобретение имеет высокую промышленную применимость.
Claims (19)
1. Способ получения инактивированных нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), конъюгированных с полимерным полисахаридным связующим, где способ включает:
(a) разделение ферментационной культуральной среды, полученной культивированием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), на бактерии и ферментационный фильтрат;
(b) смешивание ферментационного фильтрата со стадии (a) и полимерного полисахарида с получением полимерного полисахаридного связующего, где полимерный полисахарид представляет собой по меньшей мере один, выбранный из группы, состоящей из гиалуроновой кислоты, альгината, мальтодекстрина и хитозана;
(c) инактивацию нагреванием бактерий, отделенных на стадии (a); и
(d) конъюгирование инактивированных нагреванием бактерий стадии (c) со связующим, полученным на стадии (b).
2. Способ по п. 1, где полимерный полисахарид со стадии (b) представляет гиалуроновую кислоту.
3. Способ по п. 2, где гиалуроновую кислоту смешивают с ферментационным фильтратом в соотношении 0,0001-1% (масса/объем).
4. Способ по п. 1, где инактивацию нагреванием на стадии (c) проводят при температуре в пределах 60-100°С.
5. Способ по п. 1, где инактивацию нагреванием на стадии (c) проводят в течение 10-120 минут.
6. Инактивированные нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), конъюгированные с полимерным полисахаридным связующим, полученные способом по п. 1.
7. Фармацевтическая композиция для лечения атопических заболеваний, где композиция содержит в качестве активного ингредиента инактивированные нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), конъюгированные с полимерным полисахаридным связующим по п. 6.
8. Композиция по п. 7, где композиция содержит инактивированные нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), конъюгированные с полимерным полисахаридным связующим, в концентрации 108-1010 КОЕ/г.
9. Применение инактивированных нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), конъюгированных с полимерным полисахаридным связующим, полученным согласно п. 1, для получения агента для лечения атопического дерматита.
10. Способ лечения атопии, где способ включает введение эффективного количества инактивированных нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), конъюгированных с полимерным полисахаридным связующим, полученным согласно п. 1, субъекту, нуждающемуся в лечении атопии.
11. Композиция продукта для снижения выраженности атопического дерматита, где композиция содержит в качестве активного ингредиента инактивированные нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), конъюгированные с полимерным полисахаридным связующим, по п. 6.
12. Композиция по п. 11, где композиция выбрана из группы, состоящей из ферментированного молока, йогурта, напитков, молочных напитков, пищевых добавок и диетического функционального продукта питания.
13. Композиция по п. 11, где композиция содержит инактивированные нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP), конъюгированные с полимерным полисахаридным связующим, в концентрации 108-1010 КОЕ/г.
14. Применение инактивированных нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP) по п. 6, конъюгированных с полимерным полисахаридным связующим, для получения продукта для снижения выраженности атопического дерматита.
15. Способ лечения или снижения выраженности атопического заболевания, где способ включает потребление продукта, содержащего в качестве активного ингредиента эффективное количество инактивированных нагреванием Lactobacillus rhamnosus RHT-3201 (Lactobacillus rhamnosus KCTC 10833BP) по п. 6, конъюгированных с полимерным полисахаридным связующим, субъекту, нуждающемуся в лечении или снижении выраженности атопического заболевания.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020140054237A KR101640744B1 (ko) | 2014-05-07 | 2014-05-07 | 고분자 다당 바인더에 컨쥬게이트된 락토바실러스 람노서스 rht-3201, 및 이의 아토피 예방 및 치료 용도 |
| KR10-2014-0054237 | 2014-05-07 | ||
| PCT/KR2015/003914 WO2015170839A1 (ko) | 2014-05-07 | 2015-04-20 | 고분자 다당 바인더에 컨쥬게이트된 락토바실러스 람노서스 rht-3201, 및 이의 아토피 예방 및 치료 용도 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| RU2016147690A3 RU2016147690A3 (ru) | 2018-06-08 |
| RU2016147690A RU2016147690A (ru) | 2018-06-08 |
| RU2671209C2 true RU2671209C2 (ru) | 2018-10-30 |
Family
ID=54392661
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2016147690A RU2671209C2 (ru) | 2014-05-07 | 2015-04-20 | Lactobacillus rhamnosus rht-3201, конъюгированные с полисахаридным полимерным связующим и их применение для профилактики или лечения атопических заболеваний |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US10443033B2 (ru) |
| EP (1) | EP3141254B1 (ru) |
| JP (1) | JP6408694B2 (ru) |
| KR (1) | KR101640744B1 (ru) |
| CN (1) | CN106413724B (ru) |
| BR (1) | BR112016025892B1 (ru) |
| CA (1) | CA2948312C (ru) |
| ES (1) | ES2716973T3 (ru) |
| RU (1) | RU2671209C2 (ru) |
| WO (1) | WO2015170839A1 (ru) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102061387B1 (ko) * | 2016-03-25 | 2019-12-31 | 건국대학교 산학협력단 | 락토바실러스 람노서스 배양액 및 공액리놀레산을 유효성분으로 함유하는 아토피 피부염 개선용 화장료 조성물 |
| DE102017103850A1 (de) | 2016-08-24 | 2018-03-01 | Georg Fritzmeier Gmbh & Co. Kg | Hautpflegezusammensetzung |
| PT3658160T (pt) * | 2017-07-28 | 2021-08-26 | Isdin Sa | Utilização de ramnose e seus derivados como agentes antifúngicos |
| JP2019195283A (ja) * | 2018-05-08 | 2019-11-14 | 花王株式会社 | 殺菌処理の情報取得方法 |
| CN108498549B (zh) * | 2018-05-22 | 2020-06-26 | 浙江海正药业股份有限公司 | 用于改善免疫功能的组合物及其应用 |
| KR102149102B1 (ko) * | 2019-07-05 | 2020-08-27 | 에스케이바이오랜드 주식회사 | 피부보습 및 피부재생 기능이 있는 더모바이오틱스 블록 조성물의 제조방법 |
| KR102344701B1 (ko) * | 2019-09-30 | 2021-12-30 | 에이앤펩주식회사 | 고 기능성 천연 발효물이 포함된 화장료 조성물 |
| CN116396884A (zh) * | 2022-08-15 | 2023-07-07 | 江苏华熙益能生物科技有限公司 | 鼠李糖乳杆菌和一种抑制幽门螺杆菌的组合物 |
| KR102502109B1 (ko) * | 2022-08-25 | 2023-02-23 | 일동바이오사이언스(주) | 비타민 b1 생성능이 우수한 락티카제이바실러스 람노서스 idcc 3201을 포함하는 조성물 및 건강기능식품 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050196480A1 (en) * | 2004-03-04 | 2005-09-08 | Michael Sullivan | Skin treatment method with lactobacillus extract |
| KR101166798B1 (ko) * | 2011-12-19 | 2012-07-26 | 김대현 | 락토바실러스 애시도필러스 엘비의 사균을 포함하는 알레르기 질환의 치료 또는 예방용 의약 조성물 |
| KR20120125359A (ko) * | 2010-03-19 | 2012-11-14 | 가부시키가이샤 키티 | 항알레르기용 조성물 |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5733568A (en) | 1993-12-03 | 1998-03-31 | Lafor Laboratories Limited | Micro-encapsulated lactobacilli for medical applications |
| KR100993562B1 (ko) | 2002-03-21 | 2010-11-11 | 비포단 에이/에스 | 락토바실러스 균주 |
| US20040208863A1 (en) * | 2003-01-30 | 2004-10-21 | James Versalovic | Anti-inflammatory activity from lactic acid bacteria |
| WO2005087241A1 (ja) | 2004-03-16 | 2005-09-22 | Combi Co. | 家畜・家禽類又は魚介類の感染防除剤 |
| EP1634948A1 (en) * | 2004-09-10 | 2006-03-15 | Basf Aktiengesellschaft | Means and methods for preventing and/or treating caries |
| JP2006225380A (ja) * | 2005-01-19 | 2006-08-31 | Rohto Pharmaceut Co Ltd | 免疫バランス調整剤 |
| KR100742900B1 (ko) | 2006-04-27 | 2007-07-25 | 일동제약주식회사 | 면역조절기능이 있는 락토바실루스 람노서스 아이디씨씨3201의 이용 |
| JP5457675B2 (ja) * | 2006-10-17 | 2014-04-02 | 株式会社ヒアルロン酸研究所 | アトピー性皮膚炎の治療薬又は予防薬 |
| MX2011005527A (es) * | 2008-11-28 | 2011-09-28 | Univ Otago | Uso de la bacteria de acido lactico para tratar o prevenir el eczema. |
| EP2251022A1 (en) | 2009-05-11 | 2010-11-17 | Nestec S.A. | Non-replicating micro-organisms and their immune boosting effect |
| US20110070334A1 (en) * | 2009-09-20 | 2011-03-24 | Nagendra Rangavajla | Probiotic Stabilization |
| CN101897731A (zh) | 2010-07-21 | 2010-12-01 | 朱立良 | 一种复合生物酸外用喷剂 |
| AU2011320994B2 (en) | 2010-10-27 | 2016-08-25 | Nestec S.A. | Methods and compositions suitable for promoting healthy skin |
| WO2012060579A2 (ko) | 2010-11-04 | 2012-05-10 | 주식회사 쎌바이오텍 | 항균용 유산균 사균체 및 이의 제조방법 |
| BE1019142A3 (fr) * | 2011-01-21 | 2012-03-06 | Vesale Pharma S A | Substance probiotique microencapsulee. |
| CA2833937C (en) * | 2011-05-16 | 2022-04-05 | Organobalance Medical Ag | Lactobacillus strains, compositions containing them and use of the strains to prevent or treat conditions caused by streptococcus pyogenes |
-
2014
- 2014-05-07 KR KR1020140054237A patent/KR101640744B1/ko active IP Right Grant
-
2015
- 2015-04-20 CN CN201580023814.XA patent/CN106413724B/zh active Active
- 2015-04-20 EP EP15788586.4A patent/EP3141254B1/en active Active
- 2015-04-20 JP JP2017511126A patent/JP6408694B2/ja active Active
- 2015-04-20 WO PCT/KR2015/003914 patent/WO2015170839A1/ko active Application Filing
- 2015-04-20 BR BR112016025892-4A patent/BR112016025892B1/pt active IP Right Grant
- 2015-04-20 CA CA2948312A patent/CA2948312C/en active Active
- 2015-04-20 RU RU2016147690A patent/RU2671209C2/ru active
- 2015-04-20 ES ES15788586T patent/ES2716973T3/es active Active
-
2016
- 2016-11-07 US US15/344,958 patent/US10443033B2/en active Active
-
2019
- 2019-09-09 US US16/564,793 patent/US11268064B2/en active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050196480A1 (en) * | 2004-03-04 | 2005-09-08 | Michael Sullivan | Skin treatment method with lactobacillus extract |
| KR20120125359A (ko) * | 2010-03-19 | 2012-11-14 | 가부시키가이샤 키티 | 항알레르기용 조성물 |
| KR101166798B1 (ko) * | 2011-12-19 | 2012-07-26 | 김대현 | 락토바실러스 애시도필러스 엘비의 사균을 포함하는 알레르기 질환의 치료 또는 예방용 의약 조성물 |
Non-Patent Citations (1)
| Title |
|---|
| NEGAR FOOLAD BA et all. Effect of nutrient supplementation on atopic dermatitis in children //JAMA Dermatol., 2013, 149(3): 350-355. * |
Also Published As
| Publication number | Publication date |
|---|---|
| BR112016025892B1 (pt) | 2022-03-22 |
| JP2017514922A (ja) | 2017-06-08 |
| US20190390159A1 (en) | 2019-12-26 |
| CA2948312C (en) | 2023-04-11 |
| US20170051247A1 (en) | 2017-02-23 |
| US11268064B2 (en) | 2022-03-08 |
| US10443033B2 (en) | 2019-10-15 |
| BR112016025892A2 (ru) | 2017-08-15 |
| EP3141254A1 (en) | 2017-03-15 |
| JP6408694B2 (ja) | 2018-10-17 |
| RU2016147690A3 (ru) | 2018-06-08 |
| KR20150127436A (ko) | 2015-11-17 |
| CA2948312A1 (en) | 2015-11-12 |
| WO2015170839A1 (ko) | 2015-11-12 |
| EP3141254B1 (en) | 2018-12-19 |
| ES2716973T3 (es) | 2019-06-18 |
| KR101640744B1 (ko) | 2016-07-19 |
| RU2016147690A (ru) | 2018-06-08 |
| CN106413724A (zh) | 2017-02-15 |
| EP3141254A4 (en) | 2017-12-06 |
| CN106413724B (zh) | 2020-02-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2671209C2 (ru) | Lactobacillus rhamnosus rht-3201, конъюгированные с полисахаридным полимерным связующим и их применение для профилактики или лечения атопических заболеваний | |
| JP5718917B2 (ja) | 新規なラクトバチルス・プランタラム及びこれを含む組成物 | |
| JP6329125B2 (ja) | ストレス軽減剤 | |
| JP5558475B2 (ja) | ニワトコ抽出物とl.パラカゼイ、l.カゼイ、l.ブルガリクスまたはs.サーモフィルスの菌株との組合せを含む組成物 | |
| JPWO2009066681A1 (ja) | 乳酸菌含有製剤 | |
| JP2009142266A (ja) | 新規乳酸菌 | |
| US20210353697A1 (en) | Composition comprising molokhia extract as active ingredient for improving gut microbiome or for alleviating, preventing, or treating intestinal inflammation, leaky gut syndrome, obesity, or metabolic disease | |
| US20240293488A1 (en) | Physiologically acceptable yeast compositions and uses thereof | |
| JP2014166972A (ja) | 腸炎抑制剤及び飲食品 | |
| WO2011099875A1 (en) | Use of lactic acid bacteria to treat or prevent rhinitis | |
| KR102244732B1 (ko) | 프로바이오틱 초산균인 아세토박터 파스테리아누스 mglv 및 이의 면역조절 효과 | |
| JP2007054081A (ja) | ハスの破砕物および/または抽出物と、乳酸菌とを含む抗アレルギー用食品 | |
| US20240316131A1 (en) | Physiologically acceptable yeast compositions and uses thereof | |
| JP2018174772A (ja) | 乳酸菌の製造方法、及び免疫調節用組成物 | |
| JP6487106B1 (ja) | 免疫機能向上用食品組成物 | |
| KR101823634B1 (ko) | 공액리놀레산을 생산하는 락토바실러스 헬베티커스 cbg-c23 균주 및 이의 용도 | |
| CN118541038A (zh) | 生理学上可接受的酵母菌组合物及其用途 |