RU2520134C1 - Замещенные (r)-3-(4-метилкарбамоил-3-фторфениламино)-тетрагидро-фуран-3-енкарбоновые кислоты и их эфиры, способ их получения и применения - Google Patents
Замещенные (r)-3-(4-метилкарбамоил-3-фторфениламино)-тетрагидро-фуран-3-енкарбоновые кислоты и их эфиры, способ их получения и применения Download PDFInfo
- Publication number
- RU2520134C1 RU2520134C1 RU2013108672/04A RU2013108672A RU2520134C1 RU 2520134 C1 RU2520134 C1 RU 2520134C1 RU 2013108672/04 A RU2013108672/04 A RU 2013108672/04A RU 2013108672 A RU2013108672 A RU 2013108672A RU 2520134 C1 RU2520134 C1 RU 2520134C1
- Authority
- RU
- Russia
- Prior art keywords
- compounds
- alkyl
- general formula
- fluorophenylamino
- methylcarbamoyl
- Prior art date
Links
- 0 CC(C)(C(N(C1=S)c(cc2)cc(*)c2C#N)=O)N1c(cc1)cc(*)c1C(NC)=O Chemical compound CC(C)(C(N(C1=S)c(cc2)cc(*)c2C#N)=O)N1c(cc1)cc(*)c1C(NC)=O 0.000 description 4
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D307/00—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom
- C07D307/02—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings
- C07D307/04—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having no double bonds between ring members or between ring members and non-ring members
- C07D307/18—Heterocyclic compounds containing five-membered rings having one oxygen atom as the only ring hetero atom not condensed with other rings having no double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D307/24—Carbon atoms having three bonds to hetero atoms with at the most one bond to halogen
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/10—Spiro-condensed systems
- C07D491/107—Spiro-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic System
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/081—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te
- C07F7/0812—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring
Abstract
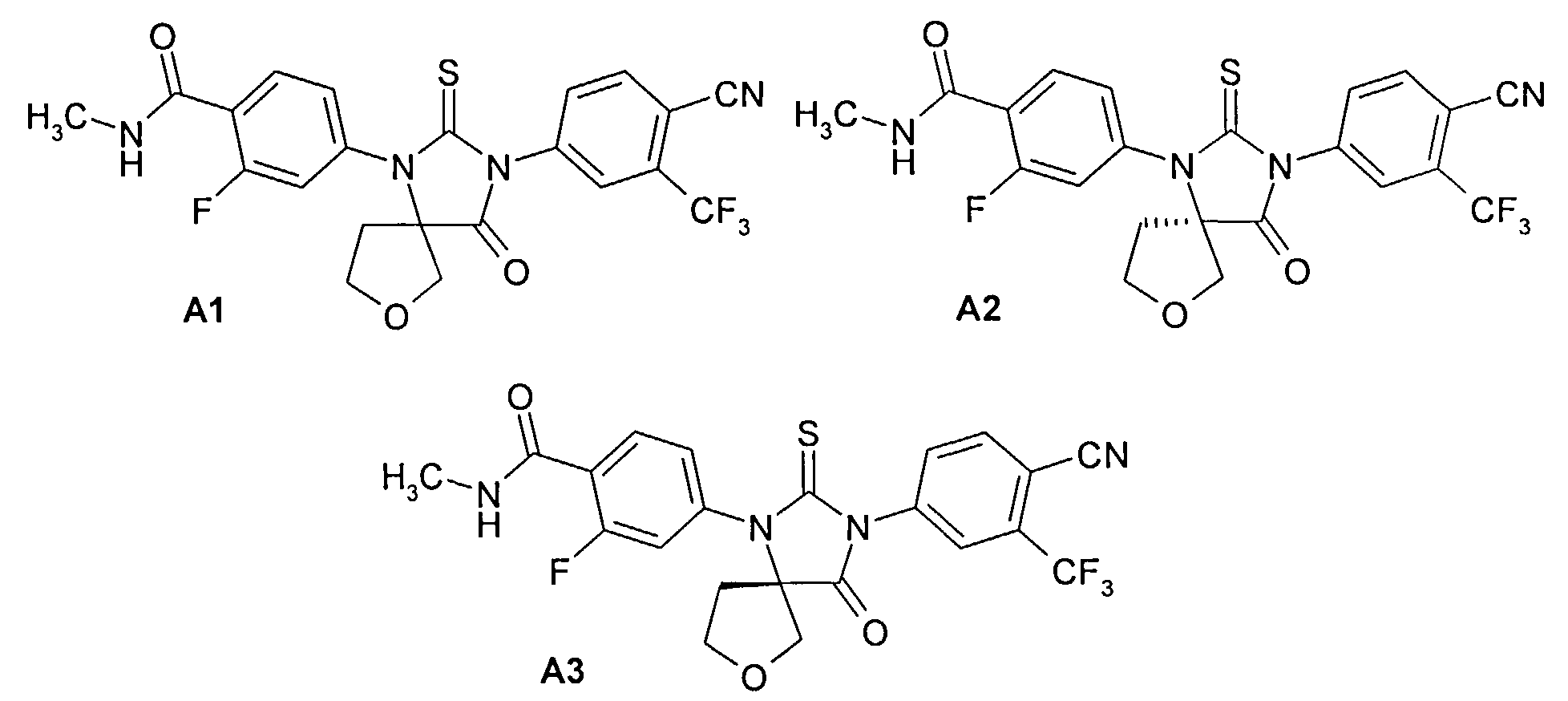
Изобретение относится к новым замещенным 3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновой кислоты или их эфирам общей формулы 1 и их стереоизомерам. Соединения формулы 1 являются полупродуктами синтеза ингибиторов андрогеновых рецепторов формулы А1, А2, А3,представляющих интерес в качестве противораковых препаратов. Изобретение также относится к способам получения соединений формулы 1 и соединений формул А1, А2, А3. В общей формуле 1
R1=Н, С1-С4алкил; R2=Н, CH2OCH2CH2Si(CH3)3.Способ получения соединений формулы (1)заключается во взаимодействии соединений общей формулы 2 с соединениями 3(1) или 3(2) в ДМФА, К2СО3 с одновременным добавлением в реакционную массу йодида меди, воды и триэтиламина.
При взаимодействии соединений формулы 1, полученных по вышеуказанному способу, с 4-изотиоцианато-2-трифторметилбензонитрилом в смеси диметилсульфоксида и этилацетата в соотношении 1:2 и повышенной температуре получают соответственно соединения А1, А2, А3, структура которых указана в формуле изобретения. Использование новых промежуточных продуктов позволяет увеличить выход и стереоселективность способа получения соединений А1, А2, А3. 3 н. и 1 з.п. ф-лы, 6 пр.
Description
Настоящее изобретение относится к новым химическим соединениям - полупродуктам синтеза ингибиторов андрогеновых рецепторов, представляющих интерес в качестве противораковых препаратов. Предметом изобретения являются также способы получения новых соединений - ингибиторов андрогеновых рецепторов.
Известны ингибиторы андрогеновых рецепторов, в том числе Enzalutamide, известный ранее как MDV3100, который в конце 2012 вышел на рынок как Xtandi и предназначен для лечения рака простаты [WO 2011/106570 А1], и ARN-509, успешно проходящий фазу II клинических исследований в качестве препарата для лечения рака простаты [WO 2008/119015 А2]
Ниже приведены определения терминов, которые использованы в описании данного изобретения.
«Алкил» означает алифатическую углеводородную линейную или разветвленную группу с 1-12 атомами углерода в цепи. Разветвленная означает, что алкильная цепь имеет один или несколько «заместителей алкила». Алкил может иметь один или несколько одинаковых или различных заместителей («алкильных заместителей»), включая галоген, алкенилокси, циклоалкил, арил, гетероарил, гетероциклил, ароил, циано, гидрокси, алкокси, карбокси, алкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероарилтио, аралкилтио, арилсульфонил, алкилсульфонилгетероаралкилокси, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-, Rk aRk+1 aNC(=S)-, Rk aRk+1 aNSO2-, где Rk a и Rk+1 a независимо друг от друга представляют собой «заместители аминогруппы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или Rk a и Rk+1 a вместе с атомом N, с которым они связаны, образуют через Rk a и Rk+1 a 4-7-членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, этоксикарбонилметил, бензилоксикарбонилметил, метокси-карбонилметил и пиридилметилоксикарбонилметил. Предпочтительными «алкильными заместителями» являются циклоалкил, арил, гетероарил, гетероциклил, гидрокси, алкокси, алкоксикарбонил, аралкокси, арилокси, алкилтио, гетероарилтио, аралкилтио, алкилсульфонил, арилсульфонил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-, аннелированный арилгетероцикленил, аннелированный арилгетероциклил.
«Алкокси» или «алкилокси» означает алкил-О- группу, в которой алкил определен в данном разделе. Предпочтительными алкилоксигруппами являются метокси, этокси, н-пропокси, изо-пропокси и н-бутокси, триметилэтилокси.
«Алкоксикарбонил» или «алкилоксикарбонил» означает алкил-O-С(=O)- группу, в которой алкил определен в данном разделе. Предпочтительными алкоксикарбонильными группами являются метоксикарбонил, этоксикарбонил, пропоксикарбонил, изопропоксикарбонил, бутилоксикарбонил и трет-бутилоксикарбонил.
«Алкоксикарбонилалкил» или «алкилоксикарбонилалкил» означает алкил-O-С(=O)-алкил- группу, в которой алкил определен в данном разделе. Предпочтительными алкоксикарбонилалкильными группами являются: метоксикарбонилметил, этоксикарбонилметил, пропоксикарбонилметил, изопропоксикарбонилметил, бутилоксикарбонилметил и трет-бутилоксикарбонилметил.
«Аминогруппа» означает Rk aRk+1 aN - группу замещенную или незамещенную «заместителем аминогруппы» Rk a и Rk+1 a, значение которых определено в данном разделе, например амино (H2N-), метиламино, диметиламино, N-(триметилсилилэтоксиметил)метиламино, диэтиламино, пирролидин, морфолин, бензиламино или фенетиламино.
«Аминокарбонил» означает C(=O)N Rk aRk+1 a - группу, замещенную или незамещенную необязательно одинаковыми «заместителями карбамоильными» Rk a и Rk+1 a, включая водород, алкенил, алкил, арил, гетероарил, гетероциклил, значение которых определено в данном разделе.
«Арил» означает ароматическую моноциклическую или полициклическую систему, включающую от 6 до 14 атомов углерода, преимущественно от 6 до 10 атомов углерода. Арил может содержать один или более «заместителей циклической системы», которые могут быть одинаковыми или разными. Представителями арильных групп являются фенил или нафтил, замещенный фенил или замещенный нафтил. Арил может быть аннелирован с неароматической циклической системой или гетероциклом. «Ацил» означает Н-С(=O)- или алкил-С(=O)-, циклоалкил-С(=O)-, гетероциклил-С(=O)-, гетероциклилалкил-С(=O)-, арил-С(=O)- арилалкил-С(=O)-, гетероарил-С(=O)- или гетероарилалкил-С(=O)- группу, в которых алкил-, циклоалкил-, гетероциклил-, гетероциклилалкил, арил-, арилалкил, гетероарил-, гетероарилалкил- определены в данном разделе.
«Ациламино» означает ацил-NH- группу, в которой значение ацил определено в данном разделе.
«Галоген» означает фтор, хлор, бром и йод. Предпочтительными являются фтор, хлор и бром.
«Гетероарил» означает ароматическую моноциклическую или полициклическую систему, включающую от 5 до 14 атомов углерода, предпочтительно от 5 до 10, в которой один или больше атомов углерода замещены гетероатомом или гетероатомами, такими как азот, сера или кислород. Приставка «аза», «окса» или «тиа» перед «гетероарил» означает наличие в циклической системе атома азота, атома кислорода или атома серы соответственно. Атом азота, находящийся в гетероариле, может быть окисленным до N-оксида. Гетероарил может иметь один или несколько «заместителей циклической системы», которые могут быть одинаковыми или разными. Представителями гетероарилов являются тетрагидрофуранил, пирролил, фуранил, тиенил, пиридил, пиразинил, пиримидинил, изооксазолил, изотиазолил, тетразолил, охазолил, тиазолил, пиразолил, фуразанил, триазолил, 1,2,4-тиадиазолил, пиридазинил, хиноксалинил, фталазинил, имидазо[1,2-а]пиридинил, имидазо[2,1-b]тиазолил, бензофуразанил, индолил, азаиндолил, бензимидазолил, бензотиазенил, хинолинил, имидазолил, тиенопиридил, хиназолинил, тиенопиримидинил, пирролопиридин, имидазопиридил, изохинолинил, бензоазаиндолил, 1,2,4-триазинил, тиенопирролил, фуропирролил, и др.
«Гетероциклил» означает ароматическую или неароматическую насыщенную моноциклическую или полициклическую систему, включающую от 3 до 10 атомов углерода, преимущественно от 5 до 6 атомов углерода, в которой один или несколько атомов углерода заменены на гетероатом, такой как азот, кислород, сера. Приставка «аза», «окса» или «тиа» перед гетероциклилом означает наличие в циклической системе атома азота, атома кислорода или атома серы соответственно. Гетероциклил может иметь один или несколько «заместителей циклической системы», которые могут быть одинаковыми или разными. Атомы азота и серы, находящиеся в гетероциклиле, могут быть окислены до N-оксида, S-оксида или S-диоксида. Представителями гетероциклилов являются тетрагидрофуран, пиперидин, пирролидин, пиперазин, морфолин, тиоморфолин, тиазолидин, 1,4-диоксан, тетрагидротиофен и др.
«Заместитель» означает химический радикал, который присоединяется к скэффолду (фрагменту), например «заместитель алкильный», «заместитель аминогруппы», «заместитель гидроксигруппы», «заместитель карбамоильный», «заместитель циклической системы», значения которых определен в данном разделе. «Заместитель алкильный» означает заместитель, присоединенный к алкилу, алкенилу, значение которых определены в данном разделе. Заместитель алкильный представляет собой водород, алкил, галоген, алкенилокси, циклоалкил, арил, гетероарил, гетероциклил, ароил, циано, гидрокси, алкокси, карбокси, алкинилокси, аралкокси, арилокси, арилоксикарбонил, алкилтио, гетероарилтио, аралкилтио, арилсульфонил, алкилсульфонилгетероаралкилокси, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонил, аралкоксикарбонил, гетероаралкилоксикарбонил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-, Rk aRk+1 aNSO2-, где Rk a и Rk+1 a независимо друг от друга представляют собой «заместители аминогруппы», значение которых определено в данном разделе, например атом водорода, алкил, арил, аралкил, гетероаралкил, гетероциклил или гетероарил, или Rk a и Rk+1 a вместе с атомом N, с которым они связаны, образуют через Rk a и Rk+1 a 4-7-членный гетероциклил или гетероцикленил. Предпочтительными алкильными группами являются метил, трифторметил, триметилсилил, циклопропилметил, циклопентилметил, этил, н-пропил, изо-пропил, н-бутил, трет-бутил, н-пентил, 3-пентил, метоксиэтил, карбоксиметил, метоксикарбонилметил, этоксикарбонилметил, бензилоксикарбонилметил, метоксикарбонилметил и пиридилметилоксикарбонилметил. Предпочтительными «алкильными заместителями» являются триметилсилил, циклоалкил, арил, гетероарил, гетероциклил, гидрокси, алкокси, алкоксикарбонил, аралкокси, арилокси, алкилтио, гетероарилтио, аралкилтио, алкилсульфонил, арилсульфонил, алкоксикарбонил, аралкоксикарбонил, гетероаралкил-оксикарбонил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-, аннелированный арилгетероцикленил, аннелированный арилгетероциклил. Значение «заместителей алкильных» определено в данном разделе.
«Заместитель аминогруппы» означает заместитель, присоединенный к аминогруппе. Заместитель аминогруппы представляет собой водород, алкил, циклоалкил, арил, гетероарил, гетероциклил, ацил, ароил, алкилсульфонил, арилсульфонил, гетероарилсульфонил, алкиламинокарбонил, ариламинокарбонил, гетероариламинокарбонил, гетероциклиламинокарбонил, алкиламинотиокарбонил, ариламинотиокарбонил, гетероариламинотиокарбонил, гетероциклиламинотиокарбонил, аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил, алкоксикарбонилалкил, аралкоксикарбонилалкил, гетероаралкилоксикарбонилалкил. Предпочтительно заместители выбираются из группы: водород, триметилсилилэтоксиметил, метил, замещенный фторфенил, замещенный алкил.
«Заместитель гидроксигруппы» означает заместитель, присоединенный к гидроксигруппе, включая алкил, арил, гетероарил, аралкил, гетероаралкил, гидроксиалкил, ацил, ароил, алкилоксиалкил, арилоксиалкил, гетероциклилоксиалкил и т.п. Предпочтительными заместителями являются водород, метил, этил, пропил, изопропил, бутил, третбутил, триметилсилилэтил.
«Заместитель карбамоильный» означает заместитель, присоединенный к карбамоильной группе, значение которой определено в данном разделе. Заместитель карбамоильный представляет собой водород, алкил, циклоалкил, арил, гетероарил, гетероциклил, алкоксикарбонилалкил, аралкоксикарбонилалкил, гетероаралкилоксикарбонилалкил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-алкил аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил. Предпочтительными «заместителями карбамоильными» являются алкил, циклоалкил, арил, гетероарил, гетероциклил, алкоксикарбонилалкил, аралкоксикарбонилалкил, гетероаралкилоксикарбонилалкил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-алкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил.
«Заместитель карбоксильный» означает заместитель, присоединенный к кислороду карбоксильной группы, значение которой определено в данном разделе. Заместитель карбоксильный представляет собой алкил, циклоалкил, арил, гетероарил, гетероциклил, алкоксикарбонилалкил, аралкоксикарбонилалкил, гетероаралкилоксикарбонилалкил или Rk aRk+1 aN-, Rk aRk+1 aNC(=O)-aлкил аннелированный гетероарилциклоалкенил, аннелированный гетероарилциклоалкил, аннелированный гетероарилгетероцикленил, аннелированный гетероарилгетероциклил, аннелированный арилциклоалкенил, аннелированный арилциклоалкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил. Предпочтительными «заместителями карбоксильными» являются алкил, циклоалкил, арил, гетероарил, гетероциклил, алкоксикарбонилалкил, аралкоксикарбонилалкил, гетероаралкилоксикарбонилалкил или Rk aRk+1 aN- алкил, Rk aRk+1 aNC(=O)-алкил, аннелированный арилгетероцикленил, аннелированный арилгетероциклил. Предпочтительно С1-С4алкил (метил, этил, пропил, изопропил, бутил, третбутил и проч.).
«Заместитель циклической системы» означает заместитель, присоединенный к ароматической или неароматической циклической системе, включая водород, алкил, алкенил, алкинил, арил, гетероарил, аралкил, гетероаралкил, гидрокси, гидроксиалкил, амино, аминоалкил, алкокси, арилокси, ацил, ароил, галоген (фтор, хлор, бром), нитро, циано, карбокси, алкоксикарбонил, арилоксикарбонил, аралкоксикарбонил, алкилоксиалкил, арилоксиалкил, гетероциклилоксиалкил, арилалкилоксиалкил, гетероциклилалкилоксиалкил, алкилсульфонил, арилсульфонил, гетероциклилсульфонил, алкилсульфинил, арилсульфинил, гетероциклилсульфинил, алкилтио, арилтио, гетероциклилтио, алкилсульфонилалкил, арилсульфонилалкил, гетероциклилсульфонилалкил, алкилсульфинилалкил, арилсульфинилалкил, гетероциклилсульфинилалкил, алкилтиоалкил, арилтиоалкил, гетероциклилтиоалкил, арилалкилсульфонилалкил, гетероциклилалкилсульфонилалкил, арилалкилтиоалкил, гетероциклилалкилтиоалкил, циклоалкил, циклоалкенил, гетероциклил, гетероцикленил, амидино, Rk aRk+1 aN-, Rk aN=, Rk aRk+1 aN-алкил-, Rk aRk+1 aNC(=O)- или Rk aRk+1 aNSO2-, где Rk a и Rk+1 a представляют собой независимо друг от друга «заместители аминогруппы», значение которых определено в данном разделе, например водород, замещенный алкил (замещенный амином, каброксигруппой, карбонильной группой), необязательно замещенный арил, необязательно замещенный аралкил, или необязательно замещенный гетероаралкил, или заместитель Rk aRk+1 aN-, в котором Rk a может быть ацил или ароил, а значение Rk+1 a определено выше, или «заместителями циклической системы» являются Rk aRk+1 aNC(=O)- или Rk aRk+1 aNSO2-, в которых Rk a и Rk+1 a вместе с атомом азота, с которым они связаны, образуют через Rk a и Rk+1 a 4-7-членный гетероциклил или гетероцикленил.
«Карбамоил» означает C(=O)N Rk aRk+1 a - группу. Карбамоил может иметь один или несколько одинаковых или различных «заместителей карбамоильных» Rk a и Rk+1 a, включая водород, алкенил, алкил, арил, гетероарил, гетероциклил, значение которых определено в данном разделе.
«Карбоксил» означает HOC(=O)-(карбоксильную) группу.
Недавно были получены эффективные ингибиторы андрогеновых рецепторов, представляющие собой 4-[3-(3-трифторметил-4-цианофенил)-4-оксо-2-тиокео-7-окса-1,3-диазаспиро[4.4]нон-1-ил]-2-фтор-N-метилбензамид А1 и его (R)- А2 и (S)- A3 стереоизомеры [патент RU 2434851, опубл. 27.11.2011; WO 2012/011840, опубл. 26.01.2012]
Синтез 4-[3-(3 -трифторметил-4-цианофенил)-4-оксо-2-тиоксо-7-окса-1,3-диаза-спиро[4.4]нон-1-ил]-2-фтор-К-метилбензамида А1 был осуществлен взаимодействием в микроволновой печи 4-тиоизоцианата-2-(трифторметил)бензонитрила Б1 с 4-(3-циано-тетрагидрофуран-3-иламино)-2-фтор-М-метилбензаминдом Б2 в диметилформамиде при 100°C в течение 12 часов по схеме 1. Продукт реакции А1 был выделен из реакционной смеси с использованием жидкостной хроматографии высокого давления и разделен на стереоизомеры А2 и A3 с помощью жидкостной хроматографии высокого давления на Chiralpak HD-H 25×1 см (Chiral Technologies Inc., USA).
Схема 1
Выделение целевого продукта А1 и его оптических изомеров А2 и A3 с помощью жидкостной хроматографии высокого давления, в том числе с использованием хиральных хроматографических колонок, усложняет и удорожает процесс их получения. В этой связи поиск новых полупродуктов для синтеза ингибиторов андрогеновых рецепторов A1, А2 и A3 является актуальной задачей.
Предметом данного изобретения являются неизвестные ранее соединения 3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновые кислоты, их эфиры общей формулы 1 и их стереоизомеры,
где R1=Н, С1-С4алкил; R2=Н,CH2OCH2CH2Si(CH3)3.
Более предпочтительными соединениями общей формулы 1 являются (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновая кислота 1(1), метил (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоксилат 1(2) или бутил (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоксилат 1(3)
Предметом данного изобретения является способ получения соединения общей формулы 1 и его стереоизомеров 1(1)-1(3) взаимодействием 4-бром-2-фтор-N-метилбензамида общей формулы 2 с 3-аминотетрагидрофуран-3-карбоновой кислотой 3.1, ее эфиром общей формулы 3.2 или их стереоизомерами
Лучшие результаты были достигнуты при взаимодействии реагентов 2 с 3.1 или 3.2 в среде водного диметилформамида в присутствии йодида меди (I), поташа, триэтиламина и 2-ацетилциклогексанона.
Предметом данного изобретения являются также полупродукты синтеза 4-[3-(3-трифторметил-4-цианофенил)-4-оксо-2-тиоксо-7-окса-1,3-диазаспиро[4.4]нон-1-ил]-2-фтор-N-метилбензамидов A1, А2 и A3, представляющие собой соединения общей формулы 1 или его стереоизомеры
Более предпочтительными полупродуктами являются (11)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновая кислота 1(1), метил (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоксилат 1(2), бутил (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоксилат 1(3).
Предметом данного изобретения является также способ получения 4-[3-(3-трифторметил-4-цианофенил)-4-оксо-2-тиоксо-7-окса-1,3-диазаспиро[4.4]нон-1-ил]-2-фтор-N-метилбензамидов A1, А2 и A3, заключающийся во взаимодействии соединения общей формулы 1 или его стереоизомера с 4-изотиоцианато-2-трифторметилбензонитрилом Б1 в смеси диметилсульфоксида и этилацетата при повышенной температуре по схеме 2.
Схема 2
Лучшие результаты были достигнуты при проведении реакции в эквивалентном соотношении 1:2 диметилсульфоксида и этилацетата соответственно под аргоном.
Использование данного изобретения позволяет упростить процесс получения ингибиторов андрогеновых рецепторов A1, А2 и A3, повысить их выход до 70% и отказаться от использования хиральной хроматографии.
Изобретение иллюстрируется, но не ограничивается, представленными ниже примерами.
Пример 1. Общий способ получения замещенной 3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновой кислоты, ее эфира общей формулы 1 и их стереоизомера
В круглодонную колбу, снабженную магнитной мешалкой, обратным холодильником и масляной баней с терморегулятором, вносили 1,2 экв. кислоты 3.1 или ее эфира общей формулы 3.2, 1 экв. 4-бром-2-фтор-N-метилбензамида общей формулы 2, 0,35 г (0,15 экв.) йодида меди (I), 6,76 г (4 экв.) поташа, 6 мл воды, 27,5 мл диметилформамида и 0,2 мл триэтиламина. Включали перемешивание и через 10 минут добавляли 0,35 г (0,2 экв.) 2-ацетилциклогексанона. Смесь выдерживали при перемешивании и 100°C в течение 2 суток. Растворители по окончании реакции отгоняли в вакууме. Получали эфир общей формулы 1, в котором R1=С1-С4алкил, который смешивали с водой и подкисляли соляной кислотой (конц.) до pH среды, равной 2-3. При перемешивании через 20-30 минут образовался осадок, который отфильтровали, промыли водой, высушили. После чего промыли эфиром. Получили кислоту общей формулы 1, в которой R1=Н. Выход более 80%.
(R)-3-{4-[Метил-(2-триметилсилилэтоксиметил)карбамоил]-3-фторфениламино}тетрагидрофуран-3-карбоновая кислота 1 [R1=Н, R2=CH2OCH2CHSi(CH3)3]. LC MS m/e 413 (М+1); 1Н ЯМР (DMSO, 400 МГц) δ 12.85 (ус, 1Н), 7.05 (т, 1H), 6.97 (ус, 1Н), 6.30 (м, 1Н), 6.15 (д, 1H), 4.84 (с, 1Н), 4.60 (с, 1Н), 4.09 (д, 1Н), 3.88 (т, 3Н), 3.50 (ус, 1Н), 3.32 (ус, 1Н), 2.90 (м, 3Н), 2.56 (м, 1H), 2.16 (м, 1Н), 0.87 (ус, 1H), 0.76 (ус, 1Н), 0.00 (м, 9Н).
(R)-3-(4-Метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновая кислота 1(1), LC MS m/e 283 (М+1); 1Н ЯМР (DMSO, 400 МГц) δ 13.01 (ус, 1H), 7.68 (с, 1H), 7.46 (т, 1Н), 7.13 (с, 1Н), 6.31 (д, 1H), 6.11 (д, 1Н), 4.09 (д, 1H), 3.86 (м, 3Н), 2.71 (м, 4Н), 2.14 (м, 1Н).
Пример 2. Способ получения метил (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоксилата 1(2)
Способ А. Смешивали 500 мг (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновой кислоты 1(1) и 294 мг (1.2 экв.) поташа в 4 мл ДМФА. Смесь нагревали до температуры 30°C и вносили 1.2 экв. метила йодистого. Повышали температуру до 40°C и выдерживали в течение часа. Затем добавляли 40 мл воды и смесь нагревали до 60°C. Отфильтровывали, водный слой экстрагировали хлороформом (дважды по 50 мл). Объединенные органические слои промывали насыщенным водным раствором хлорида натрия, растворитель отгоняли в вакууме. Продукт затирали в эфире. Получили 372 мг (70%) продукта 1(2).
Способ Б. Растворяли 10 г (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновой кислоты 1(1) в ацетонитриле, добавляли 6,89 г (1.2 экв.) карбодиимида. Смесь перемешивали при 60°C в течение 1 часа и вносили 20 мл метанола. Оставляли перемешиваться в течение 2-3 часов. Затем отгоняли растворители в вакууме, к остатку добавляли воду. Выпавший осадок отфильтровали, высушили. Выход эфира 1(2) 7,5 г (71%).
Способ В. Растворяли 15,5 г (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновой кислоты 1(1) в 150 мл метанола. Колбу охлаждали льдом с водой и в течение 10 минут, прикапали избыток (1.2 экв.) хлористого тионила. Затем реакционную массу доводили до кипения и кипятили 4 часа. После чего отгоняли растворитель и избыток тионила в вакууме. Остаток растворяли в 200 мл хлороформа, промывали насыщенным раствором гидрокарбоната натрия (50 мл), затем насыщенным раствором рассола хлорида натрия (50 мл). Хлороформ отгоняли в вакууме, к остатку добавляли эфир и отфильтровывали продукт. Выход эфира 1(2) 12,5 г (77%).
Метил (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоксилат 1(2), LC MS m/e 297 (M+1); 1H ЯМР (CDCl3, 400 МГц) δ 7.94 (т, 1H). 6.59 (ус, 1H), 6.38 (д, 1H), 6.20 (д, 1H), 4.80 (ус, 1H), 4.19 (д, 1H), 4.05 (м, 3H), 3.76 (с, 3H), 3.01 (д, 3H), 2.51 (м, 1H), 2.19 (м, 1H).
Пример 3. Способ получения бутил (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоксилата 1(3)
Смешивали 0,55 г бутил (R)-3-аминотетрагидрофуран-3-карбоксилата 3.2(1), 0,68 г (1 экв.) 4-бром-2-фтор-N-метил-N-{[2-(триметилсилил)этокси]метил}бензамида 2.1, 0,27 г (0,1 экв.) Pd*DBA, 0,37 г (0,2 экв.) BINAP в 10 мл диоксана. Смесь кипятили 2 суток под аргоном. Реакционную массу выливали в воду, экстрагировали хлороформом, экстракт промывали насыщенным раствором хлорида натрия. Хлороформ отгоняли в вакууме, а остаток хроматографировали на силикагеле. Получали бутил (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоксилата 1(3), LC MS m/e 339 (M+1) с выходом ~10%.
Пример 4. Способы получения 4-[3-(3-трифторметил-4-цианофенил)-4-оксо-2-тиоксо-7-окса-1,3-диазаспиро[4.4]нон-1-ил]-2-фтор-N-метилбензамида A1, 4-[(R)-3-(3-трифторметил-4-цианофенил)-4-оксо-2-тиоксо-7-окса-1,3-диазаспиро[4.4]нон-1-ил]-2-фтор-N-метилбензамида A2, 4-[(S)-3-(3-трифторметил-4-цианофенил)-4-оксо-2-тиоксо-7-окса-1,3-диазаспиро[4.4]нон-1-ил]-2-фтор-N-метилбензамида A3, 4-[(R)-3-(3-трифторметил-4-цианофенил)-4-оксо-2-тиоксо-7-окса-1,3-диазаспиро[4.4|нон-1-ил]-2-фтор-N-метил-N-(2-триметилсилилэтоксиметил)бензамида A4.а
Способ A. В круглодонную колбу емкостью 250 мл, снабженную магнитной мешалкой, обратным холодильником, хлоркальцевой трубкой и масляной баней с терморегулятором IKAR- ETS-D4, помещали 10.7 г (R)-3-{4-[метил-(2-триметилсилилэтоксиметил)карбамоил]-3-фторфениламино}тетрагидрофуран-3-карбоновой кислоты 1 [R1=H, R2=CH2OCH2CH2Si(CH3)3] и 1.5 экв. 4-тиозоцианата-2-(трифторметил)бензонитрила Б1 в 100 мл пиридина. Перемешивали при 80°C 48 часов. По окончании реакции (отсутствие исходных продуктов по данным LCMS) отгоняли большую часть пиридина в вакууме. Остаток растворяли в этилацетате и отфильтровывали через слой силикагеля, растворитель отгоняли в вакууме, а к остатку добавляли этанол. Выпавший осадок отфильтровывали и сушили. Получали 4.84 г 4-[(R)-3-(3-трифторметил-4-цианофенил)-4-оксо-2-тиоксо-7-окса-1,3-диазаспиро[4.4]нон-1-ил]-2-фтор-N-метил-N-(2-триметилсилилэтоксиметил)бензамида А4, LC MS m/e 623 (M+1); 1H ЯМР (CDCl3, 400 МГц) δ 8.01 (д, 1H), 7.98 (с, 1H), 7.85 (д, 1H), 7.57 (м, 1H), 7.22 (м, 2H), 4.97 (с, 1H), 4.55 (с, 1H), 4.32 (д, 1H), 4.06 (д, 1H), 3.86 (кв. 1H), 3.66 (м, 1H), 3.57 (т, 1H), 3.26 (т, 1H), 3.10 (с, 2H), 2.89 (с, 1H), 2.64 (м, 1H), 2.41 (м, 2H), 0.91 (т, 1H). 0.77 (т, 1H), 0.06 (с, 3H), 0.00 (с, 6H).
Перемешивали при комнатной температуре в течение 2-3 часов 4.8 г 4-[(R)-3-(3-трифторметил-4-цианофенил)-4-оксо-2-тиоксо-7-окса-1,3-диазаспиро[4.4]нон-1-ил]-2-фтор-N-метил-N-(2-триметилсилилэтоксиметил)бензамида А4 и 15 мл трифторуксусной кислоты в 30 мл хлористого метилена. После завершения реакции (отсутствие исходного соединения А4 по данным LCMS), реакционную массу упаривали в вакууме, а остаток подвергали хроматографической очистке на силикагеле. В качестве элюента использовали систему хлороформ - метанол (60:1). Собирали фракцию с длиной Rf=0,4. Получали с выходом 78% 4-[(R)-3-(3-трифторметил-4-цианофснил)-4-оксо-2-тиоксо-7-окса-1,3-диазаспиро[4.4]нон-1-ил]-2-фтор-N-метилбензамид А2, LC MS m/e 493 (M+1); 1H ЯМР (CDCl3, 400 МГц) δ 8.30 (т, 1H), 8.06 (д, 1H), 7.96 (с, 1H), 7.83 (д, 1H), 7.32 (д, 1H), 7.23 (д, 1H), 6.71 (м, 1H), 4.93 (д, 1H), 4.16 (д, 1H), 3.95 (кв, 1H), 3.42 (кв. 1H), 3.08 (д, 3H), 2.73 (м, 1H), 2.47 (м, 1H).
Способ Б. Перемешивали 48 часов при 80°C 5.09 г (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновой кислоты 1(1) и 1.5 экв. 4-тиоизоцианата-2-(трифторметил)бензонитрила Б1 в 50 мл пиридина. По окончании реакции (отсутствие исходных по данным LCMS) отгоняли большую часть пиридина в вакууме. Остаток подвергали хроматографированию на силикагеле. В качестве элюента использовали систему хлористый метилен - метанол (60:1). Собирали фракцию с Rf=0.6. В результате получали 630 мг (выход 7,6%) продукта A2 с чистотой 99.2%, LC MS m/e 493 (M+1); 1H ЯМР (CDCl3, 400 МГц) δ 8.30 (т, 1H), 8.06 (д, 1H), 7.96 (с, 1H), 7.83 (д. 1H), 7.32 (д, 1H), 7.23 (д, 1H), 6.71 (м, 1H), 4.93 (д, 1H), 4.16 (д, 1H), 3.95 (кв, 1H), 3.42 (кв, 1H), 3.08 (д, 3H), 2.73 (м, 1H), 2.47 (м, 1H).
Примечание. Проведение этой реакции: в микроволновом реакторе в пиридине (70°C, 3 ч) давало выход 10% целевого продукта A2; в ацетонитриле в присутствии K2CO3 (60°C, 12 ч) давало выход 8% целевого продукта A2; в ацетонитриле в присутствии (C2H5)3N под аргоном (75°C, 3 ч) давало выход 28% целевого продукта A2.
Способ В. Перемешивали 48 часов при 85°C под аргоном 1.05 г метил (R)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоксилата 1(2) и 1,62 г (2.0 экв.) 4-тиоизоцианата-2-(трифторметил)бензонитрила Б1 в смеси из 252 мкл (1 экв.) ДМСО и 692 мкл (2 экв.) этилацетата. По окончании реакции (контроль по LCMS и ТСХ) отгоняли растворители в вакууме. Остаток подвергали флеш-хроматографии на силикагеле. В качестве элюента использовали хлороформ. Собирали фракцию с Rf=0.6 (ТСХ в системе 60:1 хлороформ - метанол), растворитель отгоняли в вакууме, а остаток кристаллизовали из этанола. Получали продукт A2 с выходом 60-70%, содержащий 99,5% основного вещества, LC MS m/e 493 (M+1); 1H ЯМР (CDCl3, 400 МГц) δ 8.30 (т, 1H), 8.06 (д, 1H), 7.96 (с, 1H), 7.83 (д, 1H), 7.32 (д, 1H), 7.23 (д, 1H), 6.71 (м, 1H), 4.93 (д. 1H), 4.16 (д, 1H), 3.95 (кв, 1H), 3.42 (кв, 1H), 3.08 (д, 3H), 2.73 (м, 1H). 2.47 (м, 1H). Аналогично получают 4-[(S)-3-(3-трифторметил-4-цианофенил)-4-оксо-2-тиоксо-7-окса-1,3-диазаспиро[4.4]нон-1-ил]-2-фтор-N-метилбензамид A3 из соответствующей (S)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновой кислоты формулы 1, выход 60-65%, LC MS m/e 493 (M+1).
Аналогично получают 4-[3-(3-трифторметил-4-цианофенил)-4-оксо-2-тиоксо-7-окса-1,3-диазаспиро[4.4]нон-1-ил]-2-фтор-N-метилбензамид A1 из соответствующей 3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновой кислоты формулы 1, выход 60-65%, LC MS m/e 493 (M+1).
Claims (4)
3.Способ получения соединений общей формулы 1.1 или их стереоизомеров одновременным взаимодействием раствора 4-бром-2-фтор-N-метилбензамида общей формулы 2 в ДМФА, К2CO3, 3-аминотетрагидрофуран-3-карбоновой кислоты 3.1 или ее эфира общей формулы 3.2, или их стереоизомеров, отличающийся тем, что в реакционную смесь одновременно добавляют йодид меди(I), воду и триэтиламин
где R1=H, C1-C4алкил; R2=H, CH2OCH2CH2Si(CH3)3;
1(1): R1=H, R2=H.
где R1=H, C1-C4алкил; R2=H, CH2OCH2CH2Si(CH3)3;
1(1): R1=H, R2=H.
4. Способ получения 4-[3-(3-трифторметил-4-цианофенил)-4-оксо-2-тиоксо-7-окса-1,3-диазаспиро[4.4]нон-1-ил]-2-фтор-N-метилбензамидов A1, A2 и A3,
заключающийся во взаимодействии соединения общей формулы 1.1, или его эфира, или стереоизомера, полученного способом по п.3, с 4-изотиоцианато-2-трифторметилбензонитрилом Б1, отличающийся тем, что реагенты перемешивают в смеси диметилсульфоксида и этилацетата в соотношении 1:2 при повышенной температуре.
заключающийся во взаимодействии соединения общей формулы 1.1, или его эфира, или стереоизомера, полученного способом по п.3, с 4-изотиоцианато-2-трифторметилбензонитрилом Б1, отличающийся тем, что реагенты перемешивают в смеси диметилсульфоксида и этилацетата в соотношении 1:2 при повышенной температуре.
Priority Applications (12)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2013108672/04A RU2520134C1 (ru) | 2013-02-27 | 2013-02-27 | Замещенные (r)-3-(4-метилкарбамоил-3-фторфениламино)-тетрагидро-фуран-3-енкарбоновые кислоты и их эфиры, способ их получения и применения |
| US14/828,540 US20160016925A1 (en) | 2013-02-27 | 2014-02-26 | Substituted (R)-3-(4-methylcarbamoyl-3-fluorophenylamino)tetrahydrofuran-3-encarboxylic acid (variants) and ester thereof, method for preparation and use |
| AU2014221468A AU2014221468B2 (en) | 2013-02-27 | 2014-02-26 | Substituted (R)-3-(4-methylcarbamoyl-3-fluorophenylamino)tetrahydrofuran-3-enecarboxylic acid (variants) and ester thereof, method for producing and using same |
| CA2901107A CA2901107C (en) | 2013-02-27 | 2014-02-26 | Substituted (r)-3-(4-methylcarbamoyl-3-fluorophenylamino)tetrahydrofuran-3-encarboxylic acid (variants) and ester thereof, method for preparation and use. |
| CN201910962530.7A CN110669027B (zh) | 2013-02-27 | 2014-02-26 | 化合物和其酯、其制备方法和用途 |
| EP14756865.3A EP2963026B1 (en) | 2013-02-27 | 2014-02-26 | Substituted (r)-3-(4-methylcarbamoyl-3-fluorophenylamino)tetrahydrofuran-3-enecarboxylic acid (variants) and ester thereof, method for producing and using same |
| EA201500754A EA027369B1 (ru) | 2013-02-27 | 2014-02-26 | Замещенная (r)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновая кислота и ее эфир в качестве полупродуктов для синтеза ингибиторов андрогенных рецепторов |
| JP2015560137A JP6341939B2 (ja) | 2013-02-27 | 2014-02-26 | 置換された(r)−3−(4−メチルカルバモイル−3−フルオロフェニルアミノ)テトラヒドロフラン−3−エンカルボン酸(変種)及びそのエステル、調製のための方法並びに使用 |
| PCT/RU2014/000122 WO2014133416A2 (ru) | 2013-02-27 | 2014-02-26 | Замещенная (r)-3-(4-метилкарбамоил-3-фторфениламино)тетрагидрофуран-3-енкарбоновая кислота (варианты) и ее эфир, способ получения и применения |
| CN201480010767.0A CN105008340A (zh) | 2013-02-27 | 2014-02-26 | 取代的(r)-3-(4-甲基氨基甲酰基-3-氟苯基氨基)四氢呋喃-3-甲酸(变体)和其酯,其制备方法和用途 |
| KR1020157026287A KR102204267B1 (ko) | 2013-02-27 | 2014-02-26 | 대체된 (r)-3-(4-메틸카바모일-3-플루오로페닐아미노)테트라하이드로퓨란-3-엔카르복실산(변이체) 및 이의 에스테르, 제조 방법 및 용도 |
| HK16103440.2A HK1215436A1 (zh) | 2013-02-27 | 2016-03-23 | 取代的 -甲基氨基甲酰基- -氟苯基氨基 四氫呋喃- -甲酸 變體 和其酯,其製備方法和用途 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| RU2013108672/04A RU2520134C1 (ru) | 2013-02-27 | 2013-02-27 | Замещенные (r)-3-(4-метилкарбамоил-3-фторфениламино)-тетрагидро-фуран-3-енкарбоновые кислоты и их эфиры, способ их получения и применения |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| RU2520134C1 true RU2520134C1 (ru) | 2014-06-20 |
Family
ID=51216931
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2013108672/04A RU2520134C1 (ru) | 2013-02-27 | 2013-02-27 | Замещенные (r)-3-(4-метилкарбамоил-3-фторфениламино)-тетрагидро-фуран-3-енкарбоновые кислоты и их эфиры, способ их получения и применения |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US20160016925A1 (ru) |
| EP (1) | EP2963026B1 (ru) |
| JP (1) | JP6341939B2 (ru) |
| KR (1) | KR102204267B1 (ru) |
| CN (2) | CN110669027B (ru) |
| AU (1) | AU2014221468B2 (ru) |
| CA (1) | CA2901107C (ru) |
| EA (1) | EA027369B1 (ru) |
| HK (1) | HK1215436A1 (ru) |
| RU (1) | RU2520134C1 (ru) |
| WO (1) | WO2014133416A2 (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2557235C1 (ru) * | 2014-07-08 | 2015-07-20 | Александр Васильевич Иващенко | Замещенные 2-тиоксо-имидазолидин-4-оны и их спироаналоги, противораковый активный компонент, фармацевтическая композиция, лекарственный препарат, способ лечения рака простаты |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2434851C1 (ru) * | 2010-07-22 | 2011-11-27 | Александр Васильевич Иващенко | Циклические n, n'-диарилтиомочевины или n, n'-диарилмочевины - антагонисты андрогенных рецепторов, противораковое средство, способ получения и применения |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PL1893196T5 (pl) * | 2005-05-13 | 2015-12-31 | Univ California | Związek diarylohydantoinowy |
| WO2007127010A2 (en) * | 2006-03-29 | 2007-11-08 | The Regents Of The University Of California | Diarylthiohydantoin compounds |
| PE20081834A1 (es) * | 2006-12-31 | 2009-01-16 | Boehringer Ingelheim Int | Proceso para la sintesis de derivados de acido 3-amino-tetrahidrofuran-3-carboxilico y uso de los mismos como medicamentos |
| WO2008119015A2 (en) * | 2007-03-27 | 2008-10-02 | Sloan-Kettering Institute For Cancer Research | Synthesis of thiohydantoins |
| US8710086B2 (en) * | 2009-04-09 | 2014-04-29 | Medivation Technologies, Inc. | Substituted di-arylhydantoin and di-arylthiohydantoin compounds and methods of use thereof |
| SI3329775T1 (sl) | 2010-02-24 | 2021-09-30 | Medivation Prostate Therapeutics Llc | Procesi za sintezo spojin diariltiohidantoina in diarilhidantoina |
-
2013
- 2013-02-27 RU RU2013108672/04A patent/RU2520134C1/ru active IP Right Revival
-
2014
- 2014-02-26 KR KR1020157026287A patent/KR102204267B1/ko active IP Right Grant
- 2014-02-26 CA CA2901107A patent/CA2901107C/en active Active
- 2014-02-26 US US14/828,540 patent/US20160016925A1/en not_active Abandoned
- 2014-02-26 WO PCT/RU2014/000122 patent/WO2014133416A2/ru active Application Filing
- 2014-02-26 CN CN201910962530.7A patent/CN110669027B/zh active Active
- 2014-02-26 JP JP2015560137A patent/JP6341939B2/ja active Active
- 2014-02-26 AU AU2014221468A patent/AU2014221468B2/en active Active
- 2014-02-26 EP EP14756865.3A patent/EP2963026B1/en active Active
- 2014-02-26 EA EA201500754A patent/EA027369B1/ru unknown
- 2014-02-26 CN CN201480010767.0A patent/CN105008340A/zh active Pending
-
2016
- 2016-03-23 HK HK16103440.2A patent/HK1215436A1/zh unknown
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2434851C1 (ru) * | 2010-07-22 | 2011-11-27 | Александр Васильевич Иващенко | Циклические n, n'-диарилтиомочевины или n, n'-диарилмочевины - антагонисты андрогенных рецепторов, противораковое средство, способ получения и применения |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2557235C1 (ru) * | 2014-07-08 | 2015-07-20 | Александр Васильевич Иващенко | Замещенные 2-тиоксо-имидазолидин-4-оны и их спироаналоги, противораковый активный компонент, фармацевтическая композиция, лекарственный препарат, способ лечения рака простаты |
| WO2016007046A1 (ru) * | 2014-07-08 | 2016-01-14 | Александр Васильевич ИВАЩЕНКО | Замещенные 2-тиоксо-имидазолидин-4-оны и их спироаналоги, противораковый активный компонент, фармацевтическая композиция, лекарственный препарат, способ лечения рака простаты |
| KR20170023184A (ko) * | 2014-07-08 | 2017-03-02 | 알-팜 오버씨즈, 인코포레이티드 | 치환된 2-티옥소-이미다졸리딘-4-온 및 이의 스피로 유사체, 전립선암 치료용 항암 활성 성분, 약학적 조성물, 약제 제조 방법 및 치료 방법 |
| US10450278B2 (en) | 2014-07-08 | 2019-10-22 | R-Pharm Overseas Inc. | Substituted 2-thioxo-imidazolidin-4-ones and spiro analogues thereof, active anticancer ingredient, pharmaceutical composition, medicinal preparation, method for treating prostate cancer |
| KR102171120B1 (ko) | 2014-07-08 | 2020-10-29 | 알-팜 오버씨즈, 인코포레이티드 | 치환된 2-티옥소-이미다졸리딘-4-온 및 이의 스피로 유사체, 전립선암 치료용 항암 활성 성분, 약학적 조성물, 약제 제조 방법 및 치료 방법 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20150130327A (ko) | 2015-11-23 |
| US20160016925A1 (en) | 2016-01-21 |
| HK1215436A1 (zh) | 2016-08-26 |
| EA027369B1 (ru) | 2017-07-31 |
| CN105008340A (zh) | 2015-10-28 |
| JP6341939B2 (ja) | 2018-06-13 |
| KR102204267B1 (ko) | 2021-01-18 |
| JP2016510025A (ja) | 2016-04-04 |
| EP2963026B1 (en) | 2020-04-29 |
| AU2014221468B2 (en) | 2018-05-17 |
| AU2014221468A1 (en) | 2015-09-24 |
| CA2901107C (en) | 2020-10-27 |
| EP2963026A4 (en) | 2016-08-03 |
| EA201500754A1 (ru) | 2016-01-29 |
| EP2963026A2 (en) | 2016-01-06 |
| WO2014133416A3 (ru) | 2014-12-18 |
| CA2901107A1 (en) | 2014-09-04 |
| CN110669027B (zh) | 2021-07-06 |
| WO2014133416A2 (ru) | 2014-09-04 |
| WO2014133416A8 (ru) | 2015-09-11 |
| CN110669027A (zh) | 2020-01-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2014128655A1 (en) | Substituted imidazo[4,5-c]quinoline derivatives as bromodomain inhibitors | |
| AU2012342547C1 (en) | Method for producing substituted 5-fluoro-1H-pyrazolopyridines | |
| Grosse et al. | New imidazo [1, 2-b] pyrazoles as anticancer agents: synthesis, biological evaluation and structure activity relationship analysis | |
| CA2870062A1 (en) | Pyrrolopyrazone inhibitors of tankyrase | |
| Jin et al. | Synthesis and biological evaluation of 1-substituted-3 (5)-(6-methylpyridin-2-yl)-4-(quinoxalin-6-yl) pyrazoles as transforming growth factor-β type 1 receptor kinase inhibitors | |
| CA3143105A1 (en) | Substituted pyrazolo-pyrazines and their use as glun2b receptor modulators | |
| AU2015323702B2 (en) | Novel chiral synthesis of N-acyl-(3-substituted)-(8-substituted)-5,6-dihydro-[1,2,4]triazolo[4,3-a]pyrazines | |
| Lopes et al. | Diels–Alder reactions of 3-(1H-tetrazol-5-yl)-nitrosoalkenes: Synthesis of functionalized 5-(substituted)-1H-tetrazoles | |
| Pin et al. | Intramolecular N-aza-amidoalkylation in association with Witkop–Winterfeldt oxidation as the key step to synthesize Luotonin-A analogues | |
| EP3658552B1 (en) | Process for preparing n-(5-((4-(4-((dimethylamino)methyl)-3-phenyl-1h-pyrazol-1-yl)pyrimidin-2-yl)amino)-4-methoxy-2-morpholinophenyl)acrylamide by reacting the corresponding amine with a 3-halo-propionyl chloride | |
| WO2002026745A1 (fr) | Composes de thienopyrimidine et leurs sels et procede de preparation | |
| CN117769556A (zh) | 嘧啶并环类衍生物及其制备方法和用途 | |
| Borsini et al. | Enantiopure 2-piperidylacetaldehyde as a useful building block in the diversity-oriented synthesis of polycyclic piperidine derivatives | |
| RU2520134C1 (ru) | Замещенные (r)-3-(4-метилкарбамоил-3-фторфениламино)-тетрагидро-фуран-3-енкарбоновые кислоты и их эфиры, способ их получения и применения | |
| DK2462126T3 (en) | Process for stereoselective synthesis of bicyclic heterocyclic compounds. | |
| ITUB20151204A1 (it) | Procedimento per la preparazione di enzalutamide | |
| CN109384784B (zh) | 磺酰胺类衍生物、其制备方法及其在医药上的用途 | |
| BR112020008640A2 (pt) | novos análogos como moduladores do receptor de androgênio e receptor de glicocorticoide | |
| CN104262340B (zh) | 一种他达拉非的制备方法 | |
| Vincze et al. | Synthesis and cyclizations of 1-azapolyene derivatives | |
| Foeldesi et al. | Synthesis of a new tetracyclic ring system: pyrrolotriazepinoquinazolinone derivatives | |
| RU2490271C1 (ru) | СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ 1,2-ДИГИДРОПИРРОЛО[1,2-a]ПИРАЗИН-3(4Н)-ОНА | |
| CN101106989A (zh) | 作为β-分泌酶有效抑制剂用于治疗阿尔茨海默氏病的、具有取代的杂环的叔碳胺 | |
| EA030947B1 (ru) | Способ крупномасштабного производства 1-изопропил-3-{5-[1-(3-метоксипропил)пиперидин-4-ил]-[1,3,4]оксадиазол-2-ил}-1h-индазола оксалата | |
| RU2577537C1 (ru) | Способ получения 4-оксоалкан-1,1,2,2-тетракарбонитрилов |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| MM4A | The patent is invalid due to non-payment of fees |
Effective date: 20160228 |
|
| NF4A | Reinstatement of patent |
Effective date: 20170119 |
|
| PD4A | Correction of name of patent owner | ||
| PC41 | Official registration of the transfer of exclusive right |
Effective date: 20190218 |