RU2410081C2 - Офтальмические композиции и способы лечения глаз - Google Patents
Офтальмические композиции и способы лечения глаз Download PDFInfo
- Publication number
- RU2410081C2 RU2410081C2 RU2007117637/15A RU2007117637A RU2410081C2 RU 2410081 C2 RU2410081 C2 RU 2410081C2 RU 2007117637/15 A RU2007117637/15 A RU 2007117637/15A RU 2007117637 A RU2007117637 A RU 2007117637A RU 2410081 C2 RU2410081 C2 RU 2410081C2
- Authority
- RU
- Russia
- Prior art keywords
- eye
- composition
- compositions
- compatible
- component
- Prior art date
Links
- 239000000203 mixture Substances 0.000 title claims abstract description 246
- 238000000034 method Methods 0.000 title claims abstract description 36
- 210000001508 eye Anatomy 0.000 title description 82
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 claims abstract description 75
- 239000000126 substance Substances 0.000 claims abstract description 75
- 235000011187 glycerol Nutrition 0.000 claims abstract description 30
- 229920002134 Carboxymethyl cellulose Polymers 0.000 claims abstract description 24
- 239000003755 preservative agent Substances 0.000 claims abstract description 23
- UNXHWFMMPAWVPI-ZXZARUISSA-N erythritol Chemical compound OC[C@H](O)[C@H](O)CO UNXHWFMMPAWVPI-ZXZARUISSA-N 0.000 claims abstract description 22
- 206010023332 keratitis Diseases 0.000 claims abstract description 22
- 229960004203 carnitine Drugs 0.000 claims abstract description 18
- 239000001768 carboxy methyl cellulose Substances 0.000 claims abstract description 12
- 235000010948 carboxy methyl cellulose Nutrition 0.000 claims abstract description 12
- 239000008112 carboxymethyl-cellulose Substances 0.000 claims abstract description 11
- 238000004519 manufacturing process Methods 0.000 claims abstract description 7
- 230000035882 stress Effects 0.000 claims abstract description 6
- PHIQHXFUZVPYII-ZCFIWIBFSA-O (R)-carnitinium Chemical compound C[N+](C)(C)C[C@H](O)CC(O)=O PHIQHXFUZVPYII-ZCFIWIBFSA-O 0.000 claims abstract 4
- 230000008723 osmotic stress Effects 0.000 claims abstract 2
- OSVXSBDYLRYLIG-UHFFFAOYSA-N dioxidochlorine(.) Chemical compound O=Cl=O OSVXSBDYLRYLIG-UHFFFAOYSA-N 0.000 claims description 49
- 239000004155 Chlorine dioxide Substances 0.000 claims description 24
- 235000019398 chlorine dioxide Nutrition 0.000 claims description 24
- 239000004386 Erythritol Substances 0.000 claims description 20
- UNXHWFMMPAWVPI-UHFFFAOYSA-N Erythritol Natural products OCC(O)C(O)CO UNXHWFMMPAWVPI-UHFFFAOYSA-N 0.000 claims description 20
- 235000019414 erythritol Nutrition 0.000 claims description 20
- 229940009714 erythritol Drugs 0.000 claims description 20
- 230000002335 preservative effect Effects 0.000 claims description 17
- 239000008365 aqueous carrier Substances 0.000 claims description 3
- 229940126601 medicinal product Drugs 0.000 claims 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 abstract description 26
- 230000000694 effects Effects 0.000 abstract description 25
- 230000002411 adverse Effects 0.000 abstract description 11
- 239000003814 drug Substances 0.000 abstract description 10
- 230000004224 protection Effects 0.000 abstract description 10
- 229940079593 drug Drugs 0.000 abstract description 9
- 239000004615 ingredient Substances 0.000 abstract description 8
- 230000008569 process Effects 0.000 abstract description 5
- 150000001767 cationic compounds Chemical class 0.000 abstract description 4
- 238000011477 surgical intervention Methods 0.000 abstract description 2
- 208000003556 Dry Eye Syndromes Diseases 0.000 abstract 1
- 206010013774 Dry eye Diseases 0.000 abstract 1
- 241000360590 Erythrites Species 0.000 abstract 1
- 210000004027 cell Anatomy 0.000 description 56
- 150000001875 compounds Chemical class 0.000 description 47
- KWIUHFFTVRNATP-UHFFFAOYSA-N glycine betaine Chemical compound C[N+](C)(C)CC([O-])=O KWIUHFFTVRNATP-UHFFFAOYSA-N 0.000 description 36
- 238000001356 surgical procedure Methods 0.000 description 28
- 239000003795 chemical substances by application Substances 0.000 description 26
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 24
- 239000000243 solution Substances 0.000 description 24
- PHIQHXFUZVPYII-ZCFIWIBFSA-N (R)-carnitine Chemical class C[N+](C)(C)C[C@H](O)CC([O-])=O PHIQHXFUZVPYII-ZCFIWIBFSA-N 0.000 description 21
- 150000001413 amino acids Chemical class 0.000 description 18
- 241001465754 Metazoa Species 0.000 description 17
- 108090000765 processed proteins & peptides Proteins 0.000 description 17
- 102000004169 proteins and genes Human genes 0.000 description 17
- 108090000623 proteins and genes Proteins 0.000 description 17
- 235000002639 sodium chloride Nutrition 0.000 description 17
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 16
- 206010020772 Hypertension Diseases 0.000 description 16
- 229960003237 betaine Drugs 0.000 description 16
- 239000003792 electrolyte Substances 0.000 description 16
- 102000004196 processed proteins & peptides Human genes 0.000 description 16
- 235000001014 amino acid Nutrition 0.000 description 15
- 235000018102 proteins Nutrition 0.000 description 15
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 14
- 239000000607 artificial tear Substances 0.000 description 14
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 14
- 229910052751 metal Inorganic materials 0.000 description 14
- 239000002184 metal Substances 0.000 description 14
- 235000010447 xylitol Nutrition 0.000 description 14
- 239000000811 xylitol Substances 0.000 description 14
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 14
- 229960002675 xylitol Drugs 0.000 description 14
- -1 but not limited to Chemical class 0.000 description 13
- 239000008213 purified water Substances 0.000 description 13
- 230000001256 tonic effect Effects 0.000 description 13
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 12
- 229920001184 polypeptide Polymers 0.000 description 12
- 238000011282 treatment Methods 0.000 description 12
- 150000005846 sugar alcohols Polymers 0.000 description 11
- 125000000129 anionic group Chemical group 0.000 description 10
- 150000003839 salts Chemical class 0.000 description 10
- 230000001954 sterilising effect Effects 0.000 description 10
- 238000004659 sterilization and disinfection Methods 0.000 description 10
- XOAAWQZATWQOTB-UHFFFAOYSA-N taurine Chemical compound NCCS(O)(=O)=O XOAAWQZATWQOTB-UHFFFAOYSA-N 0.000 description 10
- XQFRJNBWHJMXHO-RRKCRQDMSA-N IDUR Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(I)=C1 XQFRJNBWHJMXHO-RRKCRQDMSA-N 0.000 description 9
- 239000000872 buffer Substances 0.000 description 9
- 230000019522 cellular metabolic process Effects 0.000 description 9
- 229960004716 idoxuridine Drugs 0.000 description 9
- 230000003204 osmotic effect Effects 0.000 description 9
- 102000007665 Extracellular Signal-Regulated MAP Kinases Human genes 0.000 description 8
- 108010007457 Extracellular Signal-Regulated MAP Kinases Proteins 0.000 description 8
- KGBXLFKZBHKPEV-UHFFFAOYSA-N boric acid Chemical compound OB(O)O KGBXLFKZBHKPEV-UHFFFAOYSA-N 0.000 description 8
- 239000004327 boric acid Substances 0.000 description 8
- 239000003889 eye drop Substances 0.000 description 8
- 229940012356 eye drops Drugs 0.000 description 8
- 230000001631 hypertensive effect Effects 0.000 description 8
- 239000002243 precursor Substances 0.000 description 8
- 108010055717 JNK Mitogen-Activated Protein Kinases Proteins 0.000 description 7
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 7
- 125000002091 cationic group Chemical group 0.000 description 7
- 230000006378 damage Effects 0.000 description 7
- 239000012530 fluid Substances 0.000 description 7
- 230000001965 increasing effect Effects 0.000 description 7
- CDAISMWEOUEBRE-GPIVLXJGSA-N inositol Chemical compound O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](O)[C@@H]1O CDAISMWEOUEBRE-GPIVLXJGSA-N 0.000 description 7
- 229960000367 inositol Drugs 0.000 description 7
- 230000007246 mechanism Effects 0.000 description 7
- 210000004379 membrane Anatomy 0.000 description 7
- 239000012528 membrane Substances 0.000 description 7
- 230000008092 positive effect Effects 0.000 description 7
- CDAISMWEOUEBRE-UHFFFAOYSA-N scyllo-inosotol Natural products OC1C(O)C(O)C(O)C(O)C1O CDAISMWEOUEBRE-UHFFFAOYSA-N 0.000 description 7
- 238000012360 testing method Methods 0.000 description 7
- 206010015946 Eye irritation Diseases 0.000 description 6
- 102000019145 JUN kinase activity proteins Human genes 0.000 description 6
- 102000043136 MAP kinase family Human genes 0.000 description 6
- 108091054455 MAP kinase family Proteins 0.000 description 6
- 241000283973 Oryctolagus cuniculus Species 0.000 description 6
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 6
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 6
- 239000002585 base Substances 0.000 description 6
- 239000011324 bead Substances 0.000 description 6
- LLSDKQJKOVVTOJ-UHFFFAOYSA-L calcium chloride dihydrate Chemical compound O.O.[Cl-].[Cl-].[Ca+2] LLSDKQJKOVVTOJ-UHFFFAOYSA-L 0.000 description 6
- 229940052299 calcium chloride dihydrate Drugs 0.000 description 6
- CDMADVZSLOHIFP-UHFFFAOYSA-N disodium;3,7-dioxido-2,4,6,8,9-pentaoxa-1,3,5,7-tetraborabicyclo[3.3.1]nonane;decahydrate Chemical compound O.O.O.O.O.O.O.O.O.O.[Na+].[Na+].O1B([O-])OB2OB([O-])OB1O2 CDMADVZSLOHIFP-UHFFFAOYSA-N 0.000 description 6
- 239000006196 drop Substances 0.000 description 6
- 231100000013 eye irritation Toxicity 0.000 description 6
- 230000006870 function Effects 0.000 description 6
- 229940050906 magnesium chloride hexahydrate Drugs 0.000 description 6
- DHRRIBDTHFBPNG-UHFFFAOYSA-L magnesium dichloride hexahydrate Chemical compound O.O.O.O.O.O.[Mg+2].[Cl-].[Cl-] DHRRIBDTHFBPNG-UHFFFAOYSA-L 0.000 description 6
- 239000002609 medium Substances 0.000 description 6
- 102000002574 p38 Mitogen-Activated Protein Kinases Human genes 0.000 description 6
- 108010068338 p38 Mitogen-Activated Protein Kinases Proteins 0.000 description 6
- 229920005862 polyol Polymers 0.000 description 6
- 238000011084 recovery Methods 0.000 description 6
- 210000001519 tissue Anatomy 0.000 description 6
- 238000009825 accumulation Methods 0.000 description 5
- 230000005754 cellular signaling Effects 0.000 description 5
- 230000036571 hydration Effects 0.000 description 5
- 238000006703 hydration reaction Methods 0.000 description 5
- 238000002156 mixing Methods 0.000 description 5
- 150000003077 polyols Chemical class 0.000 description 5
- 239000011780 sodium chloride Substances 0.000 description 5
- 229960003080 taurine Drugs 0.000 description 5
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 4
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 4
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical compound [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 4
- 238000010521 absorption reaction Methods 0.000 description 4
- 230000009286 beneficial effect Effects 0.000 description 4
- 229910052799 carbon Inorganic materials 0.000 description 4
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 4
- 210000002919 epithelial cell Anatomy 0.000 description 4
- 238000005461 lubrication Methods 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- 230000001033 osmoprotective effect Effects 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 230000004044 response Effects 0.000 description 4
- 235000000346 sugar Nutrition 0.000 description 4
- 150000008163 sugars Chemical class 0.000 description 4
- 230000032258 transport Effects 0.000 description 4
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 3
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 3
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 3
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 3
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 3
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 3
- 239000012594 Earle’s Balanced Salt Solution Substances 0.000 description 3
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 3
- 101000950669 Homo sapiens Mitogen-activated protein kinase 9 Proteins 0.000 description 3
- 206010020751 Hypersensitivity Diseases 0.000 description 3
- ONIBWKKTOPOVIA-BYPYZUCNSA-N L-Proline Chemical compound OC(=O)[C@@H]1CCCN1 ONIBWKKTOPOVIA-BYPYZUCNSA-N 0.000 description 3
- 229930195725 Mannitol Natural products 0.000 description 3
- 102100037809 Mitogen-activated protein kinase 9 Human genes 0.000 description 3
- ONIBWKKTOPOVIA-UHFFFAOYSA-N Proline Natural products OC(=O)C1CCCN1 ONIBWKKTOPOVIA-UHFFFAOYSA-N 0.000 description 3
- 239000002253 acid Substances 0.000 description 3
- 230000007815 allergy Effects 0.000 description 3
- 238000004458 analytical method Methods 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 230000003139 buffering effect Effects 0.000 description 3
- 230000001684 chronic effect Effects 0.000 description 3
- 210000004087 cornea Anatomy 0.000 description 3
- 230000000875 corresponding effect Effects 0.000 description 3
- 230000002349 favourable effect Effects 0.000 description 3
- 239000012091 fetal bovine serum Substances 0.000 description 3
- 239000000499 gel Substances 0.000 description 3
- 229960005150 glycerol Drugs 0.000 description 3
- 229920002674 hyaluronan Polymers 0.000 description 3
- 229960003160 hyaluronic acid Drugs 0.000 description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 3
- 230000006872 improvement Effects 0.000 description 3
- 230000007794 irritation Effects 0.000 description 3
- 239000000314 lubricant Substances 0.000 description 3
- 235000010355 mannitol Nutrition 0.000 description 3
- 239000000594 mannitol Substances 0.000 description 3
- 230000004060 metabolic process Effects 0.000 description 3
- 239000002997 ophthalmic solution Substances 0.000 description 3
- 229920000642 polymer Polymers 0.000 description 3
- 239000001103 potassium chloride Substances 0.000 description 3
- 235000011164 potassium chloride Nutrition 0.000 description 3
- 238000002360 preparation method Methods 0.000 description 3
- 239000000600 sorbitol Substances 0.000 description 3
- 235000010356 sorbitol Nutrition 0.000 description 3
- 230000004083 survival effect Effects 0.000 description 3
- 208000024891 symptom Diseases 0.000 description 3
- 230000000699 topical effect Effects 0.000 description 3
- 238000001262 western blot Methods 0.000 description 3
- XHZPRMZZQOIPDS-UHFFFAOYSA-N 2-Methyl-2-[(1-oxo-2-propenyl)amino]-1-propanesulfonic acid Chemical class OS(=O)(=O)CC(C)(C)NC(=O)C=C XHZPRMZZQOIPDS-UHFFFAOYSA-N 0.000 description 2
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 2
- MAGFQRLKWCCTQJ-UHFFFAOYSA-N 4-ethenylbenzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=C(C=C)C=C1 MAGFQRLKWCCTQJ-UHFFFAOYSA-N 0.000 description 2
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 2
- 241000283707 Capra Species 0.000 description 2
- 102000000541 Defensins Human genes 0.000 description 2
- 108010002069 Defensins Proteins 0.000 description 2
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 2
- 229930182566 Gentamicin Natural products 0.000 description 2
- 239000004471 Glycine Substances 0.000 description 2
- SQUHHTBVTRBESD-UHFFFAOYSA-N Hexa-Ac-myo-Inositol Natural products CC(=O)OC1C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C(OC(C)=O)C1OC(C)=O SQUHHTBVTRBESD-UHFFFAOYSA-N 0.000 description 2
- 101000950695 Homo sapiens Mitogen-activated protein kinase 8 Proteins 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- 206010061218 Inflammation Diseases 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 102100037808 Mitogen-activated protein kinase 8 Human genes 0.000 description 2
- 108091000080 Phosphotransferase Proteins 0.000 description 2
- 102000001253 Protein Kinase Human genes 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- 239000006180 TBST buffer Substances 0.000 description 2
- 235000010443 alginic acid Nutrition 0.000 description 2
- 229920000615 alginic acid Polymers 0.000 description 2
- 239000003513 alkali Substances 0.000 description 2
- 150000001342 alkaline earth metals Chemical class 0.000 description 2
- 208000026935 allergic disease Diseases 0.000 description 2
- 230000000172 allergic effect Effects 0.000 description 2
- 125000000539 amino acid group Chemical group 0.000 description 2
- 229920006321 anionic cellulose Polymers 0.000 description 2
- 230000006907 apoptotic process Effects 0.000 description 2
- 238000003556 assay Methods 0.000 description 2
- 208000010668 atopic eczema Diseases 0.000 description 2
- 239000001110 calcium chloride Substances 0.000 description 2
- 229960002713 calcium chloride Drugs 0.000 description 2
- 229910001628 calcium chloride Inorganic materials 0.000 description 2
- 125000004432 carbon atom Chemical group C* 0.000 description 2
- 229910021386 carbon form Inorganic materials 0.000 description 2
- 125000002057 carboxymethyl group Chemical group [H]OC(=O)C([H])([H])[*] 0.000 description 2
- 230000024245 cell differentiation Effects 0.000 description 2
- 230000010261 cell growth Effects 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- OSASVXMJTNOKOY-UHFFFAOYSA-N chlorobutanol Chemical compound CC(C)(O)C(Cl)(Cl)Cl OSASVXMJTNOKOY-UHFFFAOYSA-N 0.000 description 2
- 235000014113 dietary fatty acids Nutrition 0.000 description 2
- 201000010099 disease Diseases 0.000 description 2
- 208000035475 disorder Diseases 0.000 description 2
- 230000007613 environmental effect Effects 0.000 description 2
- 210000003979 eosinophil Anatomy 0.000 description 2
- 208000002854 epidermolysis bullosa simplex superficialis Diseases 0.000 description 2
- 238000001704 evaporation Methods 0.000 description 2
- 230000008020 evaporation Effects 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 239000000194 fatty acid Substances 0.000 description 2
- 229930195729 fatty acid Natural products 0.000 description 2
- 150000004665 fatty acids Chemical class 0.000 description 2
- 239000012634 fragment Substances 0.000 description 2
- 229960002518 gentamicin Drugs 0.000 description 2
- 210000004907 gland Anatomy 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 210000003630 histaminocyte Anatomy 0.000 description 2
- 239000012456 homogeneous solution Substances 0.000 description 2
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 2
- 239000000819 hypertonic solution Substances 0.000 description 2
- 238000011065 in-situ storage Methods 0.000 description 2
- 230000004054 inflammatory process Effects 0.000 description 2
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 230000003834 intracellular effect Effects 0.000 description 2
- 230000002045 lasting effect Effects 0.000 description 2
- 229960002337 magnesium chloride Drugs 0.000 description 2
- 229910001629 magnesium chloride Inorganic materials 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 150000002739 metals Chemical class 0.000 description 2
- 239000003226 mitogen Substances 0.000 description 2
- 239000000820 nonprescription drug Substances 0.000 description 2
- 229940054534 ophthalmic solution Drugs 0.000 description 2
- 239000002357 osmotic agent Substances 0.000 description 2
- 102000020233 phosphotransferase Human genes 0.000 description 2
- 229920000447 polyanionic polymer Chemical class 0.000 description 2
- 238000004321 preservation Methods 0.000 description 2
- 230000001681 protective effect Effects 0.000 description 2
- 108060006633 protein kinase Proteins 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 230000000717 retained effect Effects 0.000 description 2
- FSYKKLYZXJSNPZ-UHFFFAOYSA-N sarcosine Chemical compound C[NH2+]CC([O-])=O FSYKKLYZXJSNPZ-UHFFFAOYSA-N 0.000 description 2
- 239000001509 sodium citrate Substances 0.000 description 2
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 description 2
- YWIVKILSMZOHHF-QJZPQSOGSA-N sodium;(2s,3s,4s,5r,6r)-6-[(2s,3r,4r,5s,6r)-3-acetamido-2-[(2s,3s,4r,5r,6r)-6-[(2r,3r,4r,5s,6r)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2- Chemical compound [Na+].CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 YWIVKILSMZOHHF-QJZPQSOGSA-N 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 238000003786 synthesis reaction Methods 0.000 description 2
- 238000012546 transfer Methods 0.000 description 2
- BSVBQGMMJUBVOD-UHFFFAOYSA-N trisodium borate Chemical compound [Na+].[Na+].[Na+].[O-]B([O-])[O-] BSVBQGMMJUBVOD-UHFFFAOYSA-N 0.000 description 2
- NLVXSWCKKBEXTG-UHFFFAOYSA-N vinylsulfonic acid Chemical compound OS(=O)(=O)C=C NLVXSWCKKBEXTG-UHFFFAOYSA-N 0.000 description 2
- GHKCSRZBNZQHKW-UHFFFAOYSA-N 1-sulfanylethanol Chemical compound CC(O)S GHKCSRZBNZQHKW-UHFFFAOYSA-N 0.000 description 1
- SMZOUWXMTYCWNB-UHFFFAOYSA-N 2-(2-methoxy-5-methylphenyl)ethanamine Chemical compound COC1=CC=C(C)C=C1CCN SMZOUWXMTYCWNB-UHFFFAOYSA-N 0.000 description 1
- AVVURERHJAFJNK-UHFFFAOYSA-N 2-(2-methylprop-2-enoylperoxy)ethanesulfonic acid Chemical class CC(=C)C(=O)OOCCS(O)(=O)=O AVVURERHJAFJNK-UHFFFAOYSA-N 0.000 description 1
- 229920000536 2-Acrylamido-2-methylpropane sulfonic acid Polymers 0.000 description 1
- SQDAZGGFXASXDW-UHFFFAOYSA-N 5-bromo-2-(trifluoromethoxy)pyridine Chemical compound FC(F)(F)OC1=CC=C(Br)C=N1 SQDAZGGFXASXDW-UHFFFAOYSA-N 0.000 description 1
- APKFDSVGJQXUKY-KKGHZKTASA-N Amphotericin-B Natural products O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1C=CC=CC=CC=CC=CC=CC=C[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-KKGHZKTASA-N 0.000 description 1
- 238000009020 BCA Protein Assay Kit Methods 0.000 description 1
- 241000894006 Bacteria Species 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical compound OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 102000014914 Carrier Proteins Human genes 0.000 description 1
- 108010078791 Carrier Proteins Proteins 0.000 description 1
- 102000009016 Cholera Toxin Human genes 0.000 description 1
- 108010049048 Cholera Toxin Proteins 0.000 description 1
- 229920001287 Chondroitin sulfate Polymers 0.000 description 1
- 206010010744 Conjunctivitis allergic Diseases 0.000 description 1
- 208000028006 Corneal injury Diseases 0.000 description 1
- 244000303965 Cyamopsis psoralioides Species 0.000 description 1
- 229920000045 Dermatan sulfate Polymers 0.000 description 1
- 241001269524 Dura Species 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- 241000206602 Eukaryota Species 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- 229920001612 Hydroxyethyl starch Polymers 0.000 description 1
- 206010020852 Hypertonia Diseases 0.000 description 1
- 208000001953 Hypotension Diseases 0.000 description 1
- 102000004877 Insulin Human genes 0.000 description 1
- 108090001061 Insulin Proteins 0.000 description 1
- 102000011782 Keratins Human genes 0.000 description 1
- 108010076876 Keratins Proteins 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- 206010023644 Lacrimation increased Diseases 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 1
- 239000004909 Moisturizer Substances 0.000 description 1
- 102000005431 Molecular Chaperones Human genes 0.000 description 1
- 108010006519 Molecular Chaperones Proteins 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 241000282320 Panthera leo Species 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 101710093543 Probable non-specific lipid-transfer protein Proteins 0.000 description 1
- 108010077895 Sarcosine Proteins 0.000 description 1
- 229920002385 Sodium hyaluronate Polymers 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 102000004338 Transferrin Human genes 0.000 description 1
- 108090000901 Transferrin Proteins 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 208000025865 Ulcer Diseases 0.000 description 1
- 206010047513 Vision blurred Diseases 0.000 description 1
- 230000001133 acceleration Effects 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- 150000001252 acrylic acid derivatives Chemical class 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 208000002205 allergic conjunctivitis Diseases 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 229940024606 amino acid Drugs 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- APKFDSVGJQXUKY-INPOYWNPSA-N amphotericin B Chemical compound O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1/C=C/C=C/C=C/C=C/C=C/C=C/C=C/[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-INPOYWNPSA-N 0.000 description 1
- 229960003942 amphotericin b Drugs 0.000 description 1
- 229920006318 anionic polymer Polymers 0.000 description 1
- 230000000890 antigenic effect Effects 0.000 description 1
- 230000007503 antigenic stimulation Effects 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 208000024998 atopic conjunctivitis Diseases 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 229960003403 betaine hydrochloride Drugs 0.000 description 1
- 150000001642 boronic acid derivatives Chemical class 0.000 description 1
- 239000000337 buffer salt Substances 0.000 description 1
- 239000007975 buffered saline Substances 0.000 description 1
- 239000006172 buffering agent Substances 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- 150000001720 carbohydrates Chemical class 0.000 description 1
- 235000014633 carbohydrates Nutrition 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- 229920003090 carboxymethyl hydroxyethyl cellulose Polymers 0.000 description 1
- HOPSCVCBEOCPJZ-UHFFFAOYSA-N carboxymethyl(trimethyl)azanium;chloride Chemical compound [Cl-].C[N+](C)(C)CC(O)=O HOPSCVCBEOCPJZ-UHFFFAOYSA-N 0.000 description 1
- 230000005779 cell damage Effects 0.000 description 1
- 230000030833 cell death Effects 0.000 description 1
- 208000037887 cell injury Diseases 0.000 description 1
- 239000013592 cell lysate Substances 0.000 description 1
- 210000000170 cell membrane Anatomy 0.000 description 1
- 230000004656 cell transport Effects 0.000 description 1
- 230000033077 cellular process Effects 0.000 description 1
- 230000006364 cellular survival Effects 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 229960004926 chlorobutanol Drugs 0.000 description 1
- QBWCMBCROVPCKQ-UHFFFAOYSA-N chlorous acid Chemical class OCl=O QBWCMBCROVPCKQ-UHFFFAOYSA-N 0.000 description 1
- 229940059329 chondroitin sulfate Drugs 0.000 description 1
- 150000001860 citric acid derivatives Chemical class 0.000 description 1
- 230000007012 clinical effect Effects 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 230000001447 compensatory effect Effects 0.000 description 1
- 210000000795 conjunctiva Anatomy 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 231100000433 cytotoxic Toxicity 0.000 description 1
- 230000001472 cytotoxic effect Effects 0.000 description 1
- 230000000254 damaging effect Effects 0.000 description 1
- 230000004040 defense response to microbe Effects 0.000 description 1
- 230000007850 degeneration Effects 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- AVJBPWGFOQAPRH-FWMKGIEWSA-L dermatan sulfate Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@H](OS([O-])(=O)=O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O)[C@H](C([O-])=O)O1 AVJBPWGFOQAPRH-FWMKGIEWSA-L 0.000 description 1
- 229940051593 dermatan sulfate Drugs 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 229940042399 direct acting antivirals protease inhibitors Drugs 0.000 description 1
- BVTBRVFYZUCAKH-UHFFFAOYSA-L disodium selenite Chemical compound [Na+].[Na+].[O-][Se]([O-])=O BVTBRVFYZUCAKH-UHFFFAOYSA-L 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- WQXNXVUDBPYKBA-YFKPBYRVSA-N ectoine Chemical compound CC1=[NH+][C@H](C([O-])=O)CCN1 WQXNXVUDBPYKBA-YFKPBYRVSA-N 0.000 description 1
- 239000003974 emollient agent Substances 0.000 description 1
- 210000003038 endothelium Anatomy 0.000 description 1
- 230000037149 energy metabolism Effects 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- 230000002255 enzymatic effect Effects 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- 210000003722 extracellular fluid Anatomy 0.000 description 1
- 208000030533 eye disease Diseases 0.000 description 1
- 210000000744 eyelid Anatomy 0.000 description 1
- 230000001605 fetal effect Effects 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 230000037406 food intake Effects 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- 239000011544 gradient gel Substances 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 229920000669 heparin Polymers 0.000 description 1
- 229960002897 heparin Drugs 0.000 description 1
- 229920001519 homopolymer Polymers 0.000 description 1
- 229960000890 hydrocortisone Drugs 0.000 description 1
- 229940021223 hypertonic solution Drugs 0.000 description 1
- 230000036543 hypotension Effects 0.000 description 1
- 238000003125 immunofluorescent labeling Methods 0.000 description 1
- 238000010324 immunological assay Methods 0.000 description 1
- 230000001976 improved effect Effects 0.000 description 1
- 230000002779 inactivation Effects 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 229940125396 insulin Drugs 0.000 description 1
- 210000000554 iris Anatomy 0.000 description 1
- 239000000644 isotonic solution Substances 0.000 description 1
- 210000003292 kidney cell Anatomy 0.000 description 1
- 210000004561 lacrimal apparatus Anatomy 0.000 description 1
- 230000004317 lacrimation Effects 0.000 description 1
- 150000003893 lactate salts Chemical class 0.000 description 1
- 230000002197 limbic effect Effects 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 210000005229 liver cell Anatomy 0.000 description 1
- 238000011068 loading method Methods 0.000 description 1
- 229920001684 low density polyethylene Polymers 0.000 description 1
- 239000004702 low-density polyethylene Substances 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- 229960001855 mannitol Drugs 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 150000002734 metacrylic acid derivatives Chemical class 0.000 description 1
- 230000000116 mitigating effect Effects 0.000 description 1
- 239000011259 mixed solution Substances 0.000 description 1
- 230000001333 moisturizer Effects 0.000 description 1
- 230000003020 moisturizing effect Effects 0.000 description 1
- NJTGANWAUPEOAX-UHFFFAOYSA-N molport-023-220-454 Chemical compound OCC(O)CO.OCC(O)CO NJTGANWAUPEOAX-UHFFFAOYSA-N 0.000 description 1
- 210000004400 mucous membrane Anatomy 0.000 description 1
- 210000000663 muscle cell Anatomy 0.000 description 1
- 230000007372 neural signaling Effects 0.000 description 1
- 230000004112 neuroprotection Effects 0.000 description 1
- 230000000508 neurotrophic effect Effects 0.000 description 1
- 235000016709 nutrition Nutrition 0.000 description 1
- 230000035764 nutrition Effects 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 230000001151 other effect Effects 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 1
- 150000002978 peroxides Chemical class 0.000 description 1
- 239000008194 pharmaceutical composition Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- 235000021317 phosphate Nutrition 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 231100000614 poison Toxicity 0.000 description 1
- 239000002574 poison Substances 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920000058 polyacrylate Polymers 0.000 description 1
- 229920002239 polyacrylonitrile Polymers 0.000 description 1
- 239000002861 polymer material Substances 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 229960002429 proline Drugs 0.000 description 1
- UIIIBRHUICCMAI-UHFFFAOYSA-N prop-2-ene-1-sulfonic acid Chemical compound OS(=O)(=O)CC=C UIIIBRHUICCMAI-UHFFFAOYSA-N 0.000 description 1
- 229960004063 propylene glycol Drugs 0.000 description 1
- 235000013772 propylene glycol Nutrition 0.000 description 1
- 229940124272 protein stabilizer Drugs 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 230000011514 reflex Effects 0.000 description 1
- 230000003938 response to stress Effects 0.000 description 1
- 239000012266 salt solution Substances 0.000 description 1
- 229940043230 sarcosine Drugs 0.000 description 1
- 210000003786 sclera Anatomy 0.000 description 1
- 230000001932 seasonal effect Effects 0.000 description 1
- 229940125723 sedative agent Drugs 0.000 description 1
- 239000000932 sedative agent Substances 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- 235000020183 skimmed milk Nutrition 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- UKLNMMHNWFDKNT-UHFFFAOYSA-M sodium chlorite Chemical compound [Na+].[O-]Cl=O UKLNMMHNWFDKNT-UHFFFAOYSA-M 0.000 description 1
- 229960002218 sodium chlorite Drugs 0.000 description 1
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 1
- 229940010747 sodium hyaluronate Drugs 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000011781 sodium selenite Substances 0.000 description 1
- 229960001471 sodium selenite Drugs 0.000 description 1
- 235000015921 sodium selenite Nutrition 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 229960002920 sorbitol Drugs 0.000 description 1
- 238000001179 sorption measurement Methods 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- 238000012876 topography Methods 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 239000012581 transferrin Substances 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 238000013519 translation Methods 0.000 description 1
- 230000032895 transmembrane transport Effects 0.000 description 1
- 230000007723 transport mechanism Effects 0.000 description 1
- 230000008733 trauma Effects 0.000 description 1
- 230000001960 triggered effect Effects 0.000 description 1
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical class CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 231100000397 ulcer Toxicity 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 230000029663 wound healing Effects 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/205—Amine addition salts of organic acids; Inner quaternary ammonium salts, e.g. betaine, carnitine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
- A61K31/047—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates having two or more hydroxy groups, e.g. sorbitol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/14—Quaternary ammonium compounds, e.g. edrophonium, choline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/716—Glucans
- A61K31/717—Celluloses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/726—Glycosaminoglycans, i.e. mucopolysaccharides
- A61K31/728—Hyaluronic acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/1703—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
- A61K38/1709—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates from mammals
- A61K38/1732—Lectins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/02—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/26—Carbohydrates, e.g. sugar alcohols, amino sugars, nucleic acids, mono-, di- or oligo-saccharides; Derivatives thereof, e.g. polysorbates, sorbitan fatty acid esters or glycyrrhizin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/38—Cellulose; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0048—Eye, e.g. artificial tears
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/08—Solutions
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
- A61P27/04—Artificial tears; Irrigation solutions
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Ophthalmology & Optometry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Inorganic Chemistry (AREA)
- Dermatology (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Biochemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Marine Sciences & Fisheries (AREA)
- Zoology (AREA)
- Gastroenterology & Hepatology (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Medicinal Preparation (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Изобретение относится к области медицины. Офтальмическая композиция содержит водный компонент-носитель и эффективное количество как минимум одного совместимого растворимого вещества для защиты глазной поверхности от гиперосмотического стресса, где совместимое растворимое вещество выбрано из группы, состоящей из карнитина и эритрита. Офтальмическая композиция имеет осмолярность в диапазоне от 200 до 1000 мОсмоль/кг. Офтальмическая композиция дополнительно может включать глицерин и карбоксиметилцеллюлозу, консервант. Офтальмическая композиция доставляет совместимые растворимые вещества к клеткам глазной поверхности для того, чтобы уравновесить осмотический стресс на глазной поверхности. Применяют композицию для изготовления лекарственного средства для защиты глазной поверхности от гиперосмотического стресса. Способ лечения сухого кератита глаза человека включает введение указанной композиции. Изобретение обеспечивает защиту глаз при неблагоприятных воздействиях катионных соединений на поверхность глаза и/или облегчение процесса восстановления глаза после хирургического вмешательства. 3 н. и 10 з.п. ф-лы, 7 табл., 8 ил.
Description
Область изобретения
Настоящее изобретение относится к офтальмическим композициям и способам, пригодным для лечения глаз. В частности, данное изобретение относится к офтальмическим композициям, включающим смеси компонентов, которые эффективно обеспечивают желаемую защиту поверхности глаза человека или животных, а также к способам лечения глаз человека или животных с применением офтальмических композиций, например данных офтальмических композиций.
Глаза млекопитающих, таких как человек или другие млекопитающие (животные), преимущественно имеют соответствующую смазку, обеспечивающую комфорт и создающую условия для хорошего и четкого зрения. Обычно такая смазка создается естественным образом за счет слезной пленки, которая образуется на наружной, открытой поверхности глаза. Эта слезная пленка представляет собой сложную жидкость, которая постоянно восполняется естественным образом благодаря слезным, мейбомиевым и другим железам и в норме обеспечивает необходимое увлажнение и питание поверхности глаза. Кроме покрытия и защиты нежной поверхности глаза, зона контакта слезной пленки с воздухом также выполняет функцию поверхности первичного преломления. Однако во многих случаях эта слезная пленка может быть представлена в недостаточном количестве, и тогда возникает состояние, известное как «сухой кератит».
Для лечения сухого кератита было предложено довольно большое количество лекарств. Применяли, например, искусственные слезы, которые представляют собой химические композиции, функциональные свойства которых воспроизводят или имеют сходство с функциональными свойствами естественных слез. Во многих случаях такие искусственные слезы приходится применять очень часто, так как они быстро исчезают с поверхности глаза. Более того, несмотря на то что искусственные слезы увлажняют глаза, они не обеспечивают достаточной смазки глазной поверхности. Были предложены композиции, содержащие специальные смазывающие вещества. Например, для обработки глаз применяли различные композиции, содержащие соединения карбоксиметилцеллюлозы (КМЦ).
В норме поверхность глаза человека и животного омывается слезами нормальной осмотической силы, в основном изотоническими. Если осмотическая сила возрастает, клетки глазной поверхности оказываются в гиперосмотической или гипертонической среде, что вызывает неблагоприятное уменьшение объема клеток вследствие трансэпителиальной потери воды, а также другие нежелательные последствия. Компенсаторные механизмы ограничены во многих отношениях, что приводит к нарушениям глазной поверхности и вызывает дискомфорт. Например, клетки могут пытаться уравновесить осмотическое давление за счет увеличения внутриклеточной концентрации электролитов. Однако при высокой концентрации электролитов метаболизм клетки во многом меняется, включая снижение активности ферментов и повреждение мембраны. К тому же, было показано, что гипертоническая среда способствует воспалению глазной поверхности.
Клетки различных форм жизни способны компенсировать гипертоническое воздействие за счет естественной аккумуляции или синтеза так называемых «совместимых растворимых веществ», которые выполняют функции электролитов, уравновешивая осмотическое давление, и при этом не влияют, в отличие от электролитов, на клеточный метаболизм. Совместимые растворимые вещества или совместимые растворимые агенты обычно не заряженные и могут удерживаться в живой клетке, например в клетке глаза, имеют сравнительно небольшую молекулярную массу и совместимы с клеточным метаболизмом в других отношениях. Совместимые растворимые вещества также считаются осмопротекторами, так как они могут обеспечивать протекание клеточного метаболизма и/или способствовать выживанию клеток в гиперосмотических условиях, жизнь которых в противном случае была бы ограничена.
К примеру, существует группа организмов, называемых галофилами, которые населяют гипергалинные среды, такие как соленые озера, глубокие морские бассейны и искусственно созданные испарительные бассейны. Эти организмы могут быть как про-, так и эукариотами и могут обладать механизмами синтеза и/или аккумуляции множества совместимых растворимых агентов, включая многоатомные спирты, сахара, аминокислоты и их производные, такие как глицин, бетаин, пролин, эктоин и т.п.
Глицерин (глицерол) является широко применяемым осмотическим агентом, в отношении которого показано, что он является совместимым растворимым веществом во множестве типов клеток большого количества видов. Также о нем известно, что он является увлажнителем и глазной смазкой. В США глицерин наносят местно на поверхность глаза для снятия раздражения в концентрации вплоть до 1%, а также его применяли в более высоких концентрациях для создания осмотического давления в безрецептурных препаратах. Учитывая его маленький размер и биологическое происхождение, глицерин должен легко проходить через клеточные мембраны, а в некоторых типах клеток были недавно найдены транспортные каналы, облегчающие транспорт глицерина.
Хотя глицерин может сам по себе выступать в качестве совместимого растворимого вещества, он может быть излишне подвижным, то есть он может проходить сквозь мембраны слишком свободно, в большей степени, чем это нужно для того, чтобы обеспечить длительный положительный эффект в конкретных системах. Например, естественная слезная пленка глаза человека содержит очень небольшое количество глицерина. В случае местного введения препарата проникновение в клетки происходит, вероятно, весьма быстро. Однако так как его концентрация в слезной жидкости падает, возможно, глицерин теряется клетками и выходит в слезную жидкость, что ограничивает продолжительность положительного эффекта.
Другой важный класс соединений, обладающих осмопротекторными свойствами во множестве тканей - это определенные аминокислоты. В частности, было показано, что бетаин (триметилглицин) активно сорбируется клетками почек в ответ на изменения осмотического давления, а таурин накапливается в клетках глаза в условиях гипертонии.
Существует необходимость создания офтальмической композиции, например искусственных слез, глазных капель и т.п., совместимой с поверхностью глаза человека или животного и способствующей эффективному перенесению глазной поверхностью гипертонических условий.
Гипотонические композиции применяли при лечении глаз в качестве способа борьбы с эффектами гипертонических условий. Такие композиции эффективно смачивают глазную поверхность водой, которая быстро проникает в клетки, когда ее вводят в виде гипотонической искусственной слезы. Однако вследствие высокой подвижности воды в клетках и вне клеток такой эффект будет весьма кратковременным. Кроме того, было показано, что при перенесении клеток из гипертонических условий в изотонические или гипотонические угнетаются транспортные механизмы клетки, направленные на аккумуляцию совместимых растворенных веществ. Таким образом, прменение гипотонических искусственных слез снижает способность клетки противостоять гипертонии, которая снова наступает вскоре после применения капель.
Данные клинических наблюдений, что такие агенты, как натриевая карбоксиметилцеллюлоза (КМЦ) и гиалуронат натрия (ГН), пригодны для лечения симптомов сухого кератита или глазных заболеваний, являются общепризнанными. Также было показано, что два этих полианионных агента особенно пригодны в тех условиях, когда происходит повреждение роговицы (КМЦ при хирургической процедуре LASIK (laser assisted in situ ceratomileusis - лазерный кератомилез in situ) и аллергическом инсульте роговицы (ГН и язвы при аллергии)).
Кроме того, предполагается, что слезная пленка здорового глаза человека или животного может иметь повышенный (детектируемый) уровень главного белка со свойствами основания (ГБО), в то время как ранее предполагали, что данный белок экспрессируется только в условиях аллергии, сопровождающейся вовлечением в реакцию эозинофилов (поздняя фаза аллергии). В настоящее время известно, что ГБО вырабатывается тучными клетками (ТК), а также эозинофилами, которые обычно ассоциированы с тканями слизистой глаза и дегранулируют с высвобождением ГБО и других катионных соединений в случае антигенной стимуляции, механических повреждений и прочих воздействий.
Другая группа катионных белков, функционирующих на поверхности глаза, представляет собой один или несколько дефенсинов, которые являются составной частью естественной системы антимикробной защиты организма. В слезной пленке пациентов с сухим кератитом обнаруживается повышенный уровень дефенсинов, которые оказывают неблагоприятное воздействие на состояние глазной поверхности непосредственно или в результате взаимодействия с другими соединениями.
Существуют признанные виды лечения, разработанные с целью снижения вероятности дегенерации тучных клеток, причем большинство этих видов лечения применяют в отношении поверхности глаза в сочетании с лечением сезонного или хронического аллергического конъюнктивита. Однако для случая, когда дегрануляция уже произошла, не существует известных способов сорбции, очищения и инактивации высвобожденных катионных медиаторов, включая ГБО. Увлажнение с помощью солевых растворов способно снизить концентрацию таких агентов, но в большинстве случаев является нецелесообразным. Также недавние данные свидетельствуют в пользу того, что ГБО присутствует на глазной поверхности в детектируемой концентрации даже в случае, когда аллергия не наблюдается, а это значит, что избыток ГБО и возможное незначительное повреждение глазной поверхности могут произойти у индивидов в любой конкретный момент.
Было бы выгодно разработать офтальмические композиции, эффективно предотвращающие или снижающие неблагоприятное воздействие катионных, например поликатионных, веществ на поверхность глаза человека или животного.
Краткое описание изобретения
Были открыты новые офтальмические композиции для лечения глаз, а также способы лечения глаз. Настоящие композиции очень эффективно лечат глаза, например глаза, подверженные или восприимчивые к таким заболеваниям/условиям, как, не ограничиваясь этими примерами, сухой кератит, среда с пониженной влажностью, стресс/травма, например, вследствие хирургических процедур и т.д. В частности, такие композиции могут быть эффективны для смягчения повреждающих эффектов гипертонической слезной пленки независимо от причин. Данные композиции относительно эффективны, их изготовление несложно и недорого, а их применение, например местное применение на глазной поверхности, очень удобно.
В одном широком аспекте изобретения предложены фармацевтические композиции, содержащие компонент-носитель, предпочтительно водный носитель, и эффективное количество тонического компонента, включая вещество, выбранное из совместимых растворимых компонентов, например один или более конкретных совместимых растворимых агентов, и их смесь. В одном особенно предпочтительном воплощении тонический компонент включает вещество, выбранное из группы соединений эритрита и их смеси. В одном дополнительном воплощении тонический компонент содержит соединения, выбранные из комбинаций как минимум двух различных совместимых растворимых агентов.
В другом широком аспекте изобретения предложены офтальмические композиции, содержащие вещество-носитель, например, на водной основе и эффективное количество вещества, выбранного из таких компонентов, как инозит, ксилол и их смесь. Осмолярность таких соединений обычно выше или больше изотонической, например в диапазоне от минимум 310 до приблизительно 600 или до приблизительно 1000 мОсмоль/кг.
В другом широком аспекте изобретения предложены офтальмические композиции, содержащие вещество-носитель, например, на водной основе и эффективное количество вещества, выбранного из соединений карнитина и их смеси. В особенно предпочтительно воплощении композиция имеет неизотоническую осмолярность.
В дополнительном аспекте настоящего изобретения предложены офтальмические композиции, содержащие вещество-носитель, например, на водной основе и эффективное количество тонического компонента, содержащего вещество, выбранное из смеси или комбинации совместимых агентов, например, выбранных из смесей одного или более компонентов, представляющих собой многоатомные спирты, и/или одного или более компонентов, представляющих собой аминокислоты.
В каждом из упомянутых выше аспектов изобретения данные композиции предпочтительно имеют такой химический состав, чтобы вещество или смесь органических совместимых растворимых веществ, входящих в состав тонического компонента, была эффективной при применении композиции для лечения глаз, позволяя глазной поверхности переносить гипертонические условия на поверхности глаза более эффективно по сравнению с аналогичными композициями, не содержащими такое вещество или смесь органических совместимых растворимых агентов.
В еще одном широком аспекте изобретения предложены офтальмические композиции, содержащие компонент-носитель, компонент, придающий тоничность, и полианионный компонент. Тонический компонент присутствует в количестве, достаточном для придания композиции желаемой осмолярности, и содержит совместимый растворимый компонент. Полианионный компонент в случае, когда композицию применяют для лечения глаз человека или животного, присутствует в количестве, достаточном для уменьшения как минимум одного неблагоприятного эффекта, оказываемого на поверхность глаза человека или животного катионным, например поликатионным, соединением, по сравнению с аналогичными композициями, не содержащими полианионного компонента. Катионные соединения могут иметь различное происхождение, например, могут быть эндогенными, привнесенными из окружающей среды или появиться как нежелательное последствие применения в глазу какого-либо агента, например раствора для хранения или другого продукта для ухода за контактными линзами. В одном особенно предпочтительном воплощении гиалуроновая кислота не является единственным полианионным компонентом. Другие полианионные компоненты больше подходят для использования в составе данной композиции, например больше подходят для местного применения на глазной поверхности человека или животного, чем гиалуроновая кислота или ее соли. В другом воплощении данного изобретения композиция имеет осмолярность в пределах от приблизительно 300 до приблизительно 600 или приблизительно 1000 мОсмоль/кг.
В другом аспекте изобретения предложены офтальмические композиции, содержащие компонент-носитель и полианионный компонент, выбранный из полианионных пептидов, аналогов полианионных пептидов, фрагментов аналогов полианионных пептидов, карбоксиметил замещенных полимерных сахаров, включая, но не ограничиваясь этим примером, глюкозу и ей подобные сахара, а также их смеси. Такие полианионные компоненты в случае, когда композицию применяют для лечения глаз человека или животного, присутствуют в количестве, достаточном для снижения как минимум одного неблагоприятного эффекта, оказываемого на поверхность глаза человека или животного катионным, например поликатионным, соединением/веществом, по сравнению с аналогичными композициями, не содержащими полианионного компонента.
Также предложены способы лечения глаз человека или животных. Такие способы включают введение композиции, например композиции, соответствующей данному изобретению, в глаз человека или животного с целью достижения не менее одного положительного эффекта для глаз.
Любой и все описываемые признаки, а также комбинации этих признаков включены в область данного изобретения при условии, что признаки любой такой комбинации не являются взаимоисключающими.
Эти и другие аспекты данного изобретения детально описаны в последующем подробном описании, сопровождаемом чертежами, примерами и формулой изобретения.
Краткое описание чертежей
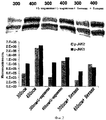
Фиг.1 представляет собой графическое отображение интенсивности по отношению к фосфорилированым c-jun N-концевым киназам (p-JNK1 и p-JNK2, JNK - jun N-terminus kinase, N-концевая киназа jun) для конкретных офтальмических композиций.
Фиг.2 представляет собой графическое отображение интенсивности по отношению к p-JNK1 и p-JNK2 для других конкретных офтальмических композиций.
Фиг.3 представляет собой графическое отображение отношения фосфорилированной JNK к общему количеству JNK для конкретных офтальмических композиций, определенного с помощью способа Биадлита (Beadlyte).
Фиг.4 представляет собой графическое отображение отношения фосфорилированной р38 MAP киназы (MAP - mitogen activated protein, активируемый митогенами белок) к общему количеству р38 MAP киназы для конкретных офтальмических композиций, определенного с помощью способа Beadlyte.
Фиг.5 представляет собой графическое отображение отношения фосфорилированной ERK MAP киназы к общему количеству ERK MAP киназы для конкретных офтальмических композиций, определенного с помощью способа Beadlyte.
Фиг.6 представляет собой графическое отображение суммы зависимых от концентрации воздействий на трансэпителиальную электрическую резистентность (ТЭЭР) для различных офтальмических композиций.
Фиг.7 представляет собой графическое отображение влияния на ТЭЭР других различных офтальмических композиций, включая композиции, содержащие комбинации совместимых растворимых агентов.
Фиг.8 представляет собой графическое отображение влияния на ТЭЭР других различных офтальмических композиций, включая композиции, содержащие комбинации совместимых растворимых агентов.
Подробное описание изобретения
Настоящее изобретение имеет отношение к офтальмическим композициям, пригодным для лечения глаз человека или животных. Как отмечалось выше, в одном аспекте изобретения предложены композиции, содержащие компонент-носитель, например, на водной основе или водный компонент-носитель, а также компонент, придающий тоничность, который включает вещество, выбранное из минимум одного совместимого растворимого вещества, например органического совместимого растворимого вещества. Такие композиции преимущественно содержат эффективное количество вещества, достаточное для того, чтобы при введении композиции в глаз вещество эффективно обеспечивало глазной поверхности возможность лучше переносить гипертонические условия, по сравнению с идентичной композицией, не содержащей такого вещества.
Хотя такие композиции могут иметь любую требуемую тоничность или осмолярность, например гипотоническую осмолярность, по существу изотоническую осмолярность или же гипертоническую осмолярность, особенно предпочтительные композиции имеют осмолярность, отличную от изотонической, например большую, чем изотоническая. В одном воплощении такие композиции имеют осмолярность в диапазоне от не менее приблизительно 300-310 до приблизительно 600-1000 мОсмоль/кг.
Многоатомные спирты, такие как компоненты, представляющие собой эритрит, ксилит, инозит, и аналогичные вещества, а также их смеси являются эффективными тоническими/осмотическими агентами и могут входить сами по себе или в сочетании с глицерином и/или другими совместимыми растворимыми агентами в состав данных композиций. Без ограничения объема изобретения каким-либо определенным принципом полагается, что поскольку многоатомные спирты имеют больший по сравнению с молекулой глицерина размер, такие компоненты - многоатомные спирты - при местном применении для лечения глаз накапливаются в клетках медленнее, чем глицерин, однако остаются внутри клеток в течение более длительного срока по сравнению с глицерином.
В одном особенно предпочтительном воплощении смеси двух или нескольких различных совместимых растворимых компонентов, например глицерина, и/или одного или нескольких компонентов - многоатомных спиртов, и/или одного или нескольких других совместимых растворимых компонентов, например одного или нескольких незаряженных или цвиттер-ионных аминокислотных компонентов и подобных им соединений, можно успешно применять вместе, обеспечивая один или несколько положительных эффектов, которые не достигаются при применении композиций, включающих только один совместимый растворимый компонент.
Термин «компонент», используемый здесь по отношении к конкретному соединению, относится к самому этому соединению, его изомерам и стереоизомерам, если таковые имеют место, к его приемлемым солям, производным соединениям и тому подобному, а также к их смесям.
Термин «производное», используемый здесь, если он относится к конкретному соединению, относится к соединению, имеющему химическое строение или структуру, достаточно схожую с данным соединением таким образом, что оно может функционировать очень сходным или таким же образом, что и данное соединение, в настоящих композициях и/или способах.
При разработке составов данных композиций можно учитывать комфорт и переносимость. Количество органических совместимых растворимых компонентов, используемых в настоящих композициях, должно эффективно обеспечивать минимум один положительный эффект для глаз пациента, не оказывая при этом на пациента нежелательного неблагоприятного воздействия, например не вызывая дискомфорта, рефлекторного слезотечения и подобных неблагоприятных эффектов.
Разработчик рецептур, являющийся специалистом в данной области, способен разработать густые жидкости и гели, которые остаются на глазной поверхности в течение более длительного периода, чем менее густые жидкости, однако при этом часто вызывают в качестве побочного эффекта временное помутнение зрения. Густые жидкости и гели, тем не менее, имеют то преимущество, что для доставки нужного количества вещества их можно наносить менее часто.
В случае использования только ксилита или эритрита может потребоваться более продолжительное время контакта для обеспечения их эффективности в качестве совместимых растворимых компонентов, например, в зависимости времени, необходимого для поглощения их клетками. Однако при попадании на место, например в клетки поверхности глаза, положительный эффект от уравновешивания гипертонических условий будет благоприятно более длительным, чем при применении эквивалентного количества глицерина, который быстро проникает в клетки и из клеток. Такой продолжительный положительный эффект в сочетании с менее частым применением препарата может быть достигнут без затуманивания зрения.
В одном воплощении настоящие композиции включают комбинацию или смесь совместимых растворимых агентов, причем все агенты относятся предпочтительно к различным типам химических веществ и/или имеют различный молекулярный размер и/или подвижность. Маленькие и подвижные агенты дают быстрый, но кратковременный эффект, например защиту от гипертонического инсульта, в то время как большие и менее подвижные агенты обеспечивают замедленное, однако более продолжительное защитное действие.
И ксилит, и эритрит, и глицерин имеют высокую концентрацию гидроксильных групп: одна группа на атом углерода. Гидроксильные группы обеспечивают лучшее связывание воды и увеличивают растворимость соединения. Для композиций, применяемых при лечении сухого кератита, высокая концентрация гидроксильных групп может увеличивать эффективность композиции за счет предотвращения потери воды тканями.
Среди многоатомных спиртов для глазного использования предпочтительны 5-углеродный ксилит, 4-углеродный эритрит и 3-углеродный глицерин. 2-Углеродная форма (этиленгликоль) является хорошо известным ядом и непригодна для использования. 6-Углеродные формы (маннит, сорбит и соответствующие деоксисоединения) можно использовать в сочетании с более мелкими молекулами. В одном воплощении данного изобретения можно использовать комбинации многоатомных спиртов, имеющих в составе 3-6 атомов углерода, деоксипроизводные 1 или 2 атомов углерода, включая, без ограничения этими примерами, изомеры, стереоизомеры и им подобные, в зависимости от того, что является пригодным.
В соответствии с настоящим изобретением в качестве органических совместимых растворимых компонентов можно использовать незаряженные или цвиттер-ионные аминокислоты.
Соединения карнитина, например сам карнитин, его изомеры/стереоизомеры, соли, производные и аналогичные вещества и их смеси, являются совместимыми растворимыми компонентами, в высокой степени пригодными для применения в данных офтальмических композициях. Карнитин широко известен как соединение, необходимое на различных этапах метаболизма жирных кислот, таким образом, он играет существенную роль в метаболизме печени и мышечных клеток. Карнитин может служить источником энергии для множества типов клеток, включая клетки глаза. Карнитиновые компоненты могут иметь уникальные свойства и обладать большим количеством функций, например выступать в качестве осмопротекторов, участвовать в метаболизме жирных кислот, выступать в качестве антиоксидантов, способствовать заживлению раны, выступать в качестве шаперонов, а также участвовать в нейропротекции.
Органический совместимый растворимый компонент в настоящих композициях предпочтительно может быть получен при использовании комбинации агентов или веществ, имеющих различные размеры, подвижность и механизмы действия. Подвижные агенты небольшого размера, такие как небольшие многоатомные спирты, должны обеспечивать быструю, но непродолжительную осмопротекцию. Некоторые аминокислоты и родственные им соединения могут функционировать как продолжительно действующие внутриклеточные совместимые растворимые вещества и стабилизаторы белков. Согласно настоящему изобретению карнитиновые компоненты можно использовать сами по себе или в сочетании с одним или более аминоорганическим совместимыми растворимыми компонентами и/или многоатомными спиртами, например, такими как описанные здесь.
Аминосодержащие органические совместимые растворимые компоненты и/или компоненты, которые можно использовать, включают, но не ограничиваются указанным, бетаин, таурин, карнитин, саркозин, пролин, триметиламины в целом, другие цвиттер-ионные аминокислоты и подобные им соединения или их смеси. Многоатомные спирты, которые можно применять в комбинации с карнитином и/или одним из ряда других аминосодержащих органических совместимых растворимых компонентов, включают, но не ограничиваются указанным, глицерин, пропилен гликоль, эритрит, ксилит, мио-инозит, манит, сорбит и им подобные вещества и их смеси.
Количество совместимых растворимых компонентов, входящих в состав данных композиций, может быть любой подходящей величиной. Однако предпочтительно такое количество эффективно обеспечивает положительный эффект при лечении глаз при введении композиции, содержащей совместимый растворимый компонент. Следует избегать появления избытка совместимых растворимых компонентов, поскольку это может доставить пациенту дискомфорт и/или причинить вред глазу во время лечения. Совместимый растворимый компонент преимущественно присутствует в количестве, достаточном для обеспечения желаемой осмолярности композиции.
Конкретное количество используемого совместимого растворимого компонента может варьироваться в широком диапазоне в зависимости от, например, общего химического состава и планируемого применения композиции, от требуемой осмолярности композиции, от использования специфического совместимого растворимого агента или комбинации таких агентов и от подобных других факторов. В одном воплощении общее количество совместимого растворимого компонента, содержащегося в данных композициях, может колебаться в пределах от приблизительно 0,01% (вес/объем) или приблизительно 0,05% (вес/объем) до приблизительно 1% (вес/объем), или приблизительно 2% (вес/объем), или приблизительно 3% (вес/объем) и более.
Клетки поверхности роговицы отвечают на осмотические изменения путем регуляции транспорта воды и солей с целью поддержания постоянного клеточного объема. В условиях хронической гипертонии, например в таких, которые наблюдаются при сухом кератите, активизируются транспортные механизмы, направленные на поглощение совместимых растворимых веществ, включая различные аминокислоты и многоатомные спирты. В одном воплощении настоящего изобретения офтальмические композиции, например искусственные слезы, содержащие совместимые растворимые компоненты, составлены таким образом, что они имеют тоничность выше или сверх изотонической и преимущественно имеют осмолярность в пределах от приблизительно 300 или приблизительно 310 до приблизительно 600 или приблизительно 1000 мОсмоль/кг. Не желая ограничивать изобретение каким-либо определенным принципом выполнения, мы предполагаем, что при таких условиях в клетках запускаются механизмы аккумуляции совместимых растворимых веществ как немедленного, так и продолжительного действия, что обеспечивает их усиленное поглощение и удержание клеткой по сравнению с изотоническими или гипотоническими условиями. Как только в клетке накапливается совместимый растворимый компонент, клетка получает усиленную защиту от возможного гипертонического инсульта, например, вызванного сухим кератитом и/или одним или другими состояниями/заболеваниями. Результатами такой усиленной защиты являются улучшение клеточного метаболизма и выживание клетки в течение часов или дней после применения офтальмической композиции по изобретению.
В нормальной слезной системе выработка слез, отток слезной жидкости и ее испарение сбалансированы, что обеспечивает увлажнение и смазку глазной поверхности. Типичные показатели осмолярности слез варьируются в пределах от 290 до 310 мОсмоль/кг у здоровых индивидуумов, и этот показатель может меняться в течение дня в ответ на изменения условий среды. У здорового индивида нервная обратная связь между глазной поверхностью и слезными железами контролирует выработку слез, что поддерживает стабильный ток жидкости на поверхности глаза. Было выдвинуто предположение, что тоничность слезной пленки является одним из основных стимулов в этой регуляторной петле обратной связи. При сухом кератите дисфункция аппарата, осуществляющего выработку (различные железы), системы оттока, нейрональных механизмов сигналинга или самой глазной поверхности приводят к неполноценности слезной пленки, повреждению глазной поверхности и дискомфорту.
На клеточном уровне сухой кератит, как правило, характеризуется хронической гипретоничностью внеклеточной среды (слезной пленки). Опубликованные данные об осмолярности слезной пленки у пациентов с сухим кератитом приводят диапазон от 300 до 500 мОсмоль/кг, при этом большинство значений лежит между 320 и 500 мОсмоль/кг. В таких условиях клетки будут терять воду и/или накапливать соли, может произойти изменение объема клеток. Было показано, что гипертония изменяет процессы клеточного метаболизма, угнетает ферментативные процессы и приводит к апоптозу и клеточной гибели.
Было показано, что в целях защиты против гипертонических изменений клетки роговицы глаза активизируют механизмы транспорта неионогенных растворимых веществ, таких как аминокислоты и полиолы, и накапливают растворенные вещества внутри клеток с целью поддержания объема клеток при неизменном балансе электролитов. В таких условиях клеточный метаболизм нарушается в меньшей степени, чем в случае изменения объема или концентрации электролитов, и такие соединения относятся к совместимым растворимым веществам. Совместимые растворимые вещества включают, но не ограничиваются, аминокислоты бетаин (триметилглицин), таурин, глицин и пролин, а также полиолы глицерин, эритрит, ксилит, сорбит и маннит. Совместимые растворимые вещества также считаются осмопротекторами, так как они поддерживают метаболизм клетки и способствуют клеточному выживанию в таких условиях гипертонии, которые сами по себе приводят к ограничению жизнедеятельности клеток.
Клетки накапливают определенные совместимые растворимые вещества путем биосинтеза внутри клетки, а другие - путем усиленного трансмембранного транспорта из внеклеточной жидкости (в данном случае из слезной пленки). В обоих случаях в процесс вовлекаются специфические синтетические белки или транспортные белки. Экспериментальные данные показывают, что эти белки активируются в условиях гипертонии, а также процессы транскрипции и трансляции данных белков стимулируются гипертонией.
Напротив, экспериментальные данные показывают, что клетки роговицы и другие клетки будут терять совместимые растворимые вещества в условиях гипотонии или при переходе от гипертонических условий к изотоническим.
При сухом кератите клетки поверхности роговицы находятся в гипертонических условиях и стимулируются к аккумулированию веществ-осмопротекторов, если таковые доступны. Добавление к глазной поверхности изо- или гипотонических искусственных слез снимает симптомы благодаря усиленному увлажнению, однако угнетает механизмы накопления осмопротекторов в этих клетках. Это может в дальнейшем спровоцировать осмотический инсульт спустя минуты или часы после употребления капель, когда слезная пленка снова станет гипертонической и подсушенной.
Согласно современным предписаниям FDA «глазной раствор должен быть осмотически эквивалентным раствору с концентрацией хлорида натрия от 0.8 до 1.0 процентов для того, чтобы соответствовать названию «изотонический раствор». Это соответствует диапазону от 274 до 342 мОсм/кг. Далее FDA постулирует, что «глазные растворы от 2 до 5% натрия хлорида являются гипертоническими и могут быть лекарствами безрецептурного отпуска в том случае, если имеют маркировку «гипертонические растворы». Этот диапазон соответствует интервалу от 684 до 1711 мОсм/кг. Согласно целям данного изобретения «супратонический» раствор должен иметь осмолярность в пределах между этими двумя интервалами, или приблизительно от 300 или 310 до приблизительно 600, или приблизительно 800, или приблизительно 1000 мОсмоль/кг, что соответствует раствору хлорида натрия с процентной концентрацией от приблизительно 0.9 до приблизительно 1.8 (1.8% - это максимальная концентрация, которую может иметь офтальмический раствор для местного применения, не маркированный как «гипертонический», согласно предписаниям FDA).
Данное изобретение принимает эти предписания к сведению при составлении супратонических искусственных слез, более совместимых с гипертоническим состоянием глаз при сухом кератите. Помимо того что данные композиции составлены как гипертонические (имеют общую осмолярность в пределах от приблизительно 300 или приблизительно 310 до приблизительно 600 или приблизительно 1000 мОсмоль/кг), они также содержат одно или несколько органических совместимых растворимых агентов согласно приведенному описанию. Супратоничность в сочетании с включением одного или нескольких совместимых растворимых веществ служит в данных композициях как для стимуляции или поддержания поглощения этих защитных веществ клетками поверхности роговицы, так и для обеспечения надежного источника таких веществ или соединений.
Помимо достаточных количеств совместимых растворимых веществ в супратонической среде, данные композиции также могут содержать соответствующее количество успокоительных и смягчающих агентов, которые обеспечат комфорт и достаточную смазку, а также преимущественно могут обеспечивать более эффективное удержание органической совместимой растворимой композиции на поверхности глаза в течение достаточного времени с целью усиления его поглощения клетками поверхности роговицы.
Следует отметить, что в предписаниях FDA четко оговаривается, что итоговая осмолярность раствора может определяться как его неионогенными, так и ионными компонентами. Таким образом, состав может содержать значительные количества глицерина и других совместимых растворимых веществ и не содержать существенных количеств каких-либо ионных тонических веществ, таких как натриевые соли. В одном воплощении данные смеси практически не содержат ионных тонических агентов.
Преимущественно данные композиции содержат комбинацию различных органических совместимых растворимых агентов, эффективно поглощаемых клетками роговицы в течение периода обработки в процессе использования капель, например от приблизительно 5 до приблизительно 30 минут в зависимости от их вязкости, после применения и удерживаемых внутри клеток в течение временного интервала длиной в несколько часов между применениями капель.
Благодаря усиленной защите от осмотического инсульта, обеспечиваемой данной композицией, продолжительность клинического эффекта, вызываемого каждой дозировкой или применением препарата, увеличена. С помощью регулярного применения данных композиций обеспечивается благоприятное состояние клеток поверхности глаза, так, в меньшей степени нарушается клеточный метаболизм и стимулируется выживание клеток.
В соответствии с другим аспектом данного изобретения разработаны композиции, содержащие компонент-носитель и полианионный компонент. Такие композиции, содержащие полианионный компонент, преимущественно, хотя и необязательно в случае некоторых воплощений, включают органические совместимые растворимые компоненты согласно приведенному описанию.
В одном воплощении разработаны композиции, содержащие компонент-носитель и полианионный компонент в количестве, достаточном для лечения глазной поверхности в условиях повышенного содержания катионных элементов, например, но не ограничиваясь этим примером, повышенного содержания Главного Основного Белка (ГОБ), и/или пониженной концентрации полианионных соединений на глазной поверхности. В одном воплощении данные офтальмические композиции содержат полианионные соединения в количестве, которое эффективно снижает как минимум одно неблагоприятное воздействие катионных, например поликатионных, соединений на глазную поверхность по сравнению с аналогичными композициями, не содержащими полианионного компонента, при введении композиций в глаз человека или животных.
В одном из воплощений композиции, содержащие полианионные компоненты, например включающие или нет совместимые растворимые компоненты, могут быть эффективно использованы перед, во время и/или после проведения хирургических процедур, включая, но не ограничиваясь, хирургические процедуры, в процессе которых глаз подвергается воздействию лазера, например при лечении пятен, сухости и других осложнений поверхности глаза после процедуры LASIK. Этиология нарушений глазной поверхности после процедуры LASIK может быть многофакторной, включая, но не ограничиваясь, вызванную хирургическим вмешательством нейротрофическую гипертензию и кератит, повреждение лимбических клеток, нарушение смыкания век вследствие изменения топографии роговицы, химические повреждения глазной поверхности лекарствами местного применения, консервантами и аналогичными веществами.
Введение композиций, содержащих полианионные компоненты, в соответствии с данным изобретением на глазную поверхность и слезную пленку может быть эффективным при лечении одного из, а возможно, больше чем одного или даже всех упомянутых выше нарушений, вызывающих повреждения глазной поверхности после процедуры LASIK.
В одном из воплощений в состав данных композиций входят полианионные компоненты, своей активностью, например антигенной и/или цитотоксической, имитирующие продомен ГОБ, который, как было показано, является полипептидом, состоящим из 90 остатков. Используемые агенты могут содержать один или более полипептидных аналогов этой последовательности или частей этой последовательности.
Согласно данному документу термин «имитирующие» означает, что полианионные компоненты, например полипептидные аналоги, имеют активность в пределах (плюс или минус) от приблизительно 5% до приблизительно 10%, или приблизительно 15%, или приблизительно 20% от соответствующей активности продомена ГОБ.
Продомен ГОБ имеет аминокислотную последовательность, представленную ниже SEQ ID NO:1
Полипептидный аналог последовательности продомена Главного Основного Белка или части последовательности продомена Главного Основного Белка означает пептид, имеющий аминокислотную последовательность, идентичную как минимум на приблизительно 75%, или приблизительно на 80%, или приблизительно на 85%, или приблизительно на 90%, или приблизительно на 95%, или приблизительно на 99%, или более гомологичной последовательности аминокислот, представленной SEQ ID NO:1, или ее части.
Карбоксиметилзамещенные полимеры сахаров, например, но не ограничиваясь, глюкоза и аналогичные сахара, могут быть использованы как полианионные компоненты в соответствии с данным изобретением.
Далее используемые дополнительно полианионные компоненты включают, но не ограничиваются, модифицированные углеводы, другие полианионные полимеры, например, но не ограничиваясь, полимеры, уже доступные для использования в фармпрепаратах и их смесях. Можно использовать смеси одного или более таких описанных выше полипептидных аналогов и одного или более упомянутых выше полианионных компонентов.
Данные композиции преимущественно являются офтальмически приемлемыми, содержат офтальмически приемлемый компонент-носитель, совместимый растворимый компонент и/или полианионный компонент.
Композиция, компонент-носитель или другой компонент или соединение считаются «офтальмически приемлемыми» в случае, если они совместимы с тканями глаза, а это означает, что они не вызывают заметные или чрезмерно нежелательные эффекты при контакте с тканями глаза. Предпочтительно, офтальмически приемлемый компонент или соединение является также совместимым с другими компонентами данного изобретения.
Используемый в тексте термин «полианионный компонент» относится к химическому объекту, например, ионного, заряженного типа, такому как несущий ионный заряженный полимерный материал, который несет более чем один дискретный анионный заряд, то есть многократный дискретный анионный заряд. Предпочтительно, полианионный компонент выбирают из группы, состоящей из полимерных материалов с многократными анионными зарядами и их смесей.
Полианионный компонент может иметь по существу постоянный или неизменный молекулярный вес или может быть образован двумя или несколькими полианионными фрагментами с различными молекулярными весами. Офтальмические композиции, содержащие полианионные компоненты, включающие два или несколько фрагментов разного молекулярного веса, описываются в U.S. Patent Application Serial No. 10/017,817 от 14 декабря 2001, описание которого в общем виде включено в данный текст в виде ссылок.
Предпочтительно, композиция имеет повышенную способность приставать к поверхности глаза при введении композиции в глаз по сравнению с практически идентичной композицией, которая не содержит полианионного компонента. Учитывая упомянутое выше хорошо выраженное свойство приставать к поверхности глаза, данные композиции предпочтительно эффективно обеспечивают наличие хорошей смазки, так что не возникает необходимости повторного применения препарата в течение более длительного периода времени по сравнению с практически идентичной композицией, которая не содержит полианионного компонента.
В соответствии с настоящим изобретением можно использовать любой подходящий полианионный компонент при условии, что он функционирует так, как описано данным документом, и не оказывает существенного неблагоприятного воздействия на композицию в целом или на глаз, куда вводится эта композиция. Полианионный компонент является предпочтительно офтальмически приемлемым в тех концентрациях, в которых он используется. Полианионный компонент предпочтительно несет три (3) или более анионных (или отрицательных) заряда. В том случае, когда полианионный компонент является полимерным материалом, предпочтительно, чтобы множество повторяющихся единиц, составляющих этот полимерный материал, несли дискретный анионный заряд. Особенно практичными анионными компонентами являются те, что растворимы в воде, например растворимые в концентрациях, используемых в данном изобретении при комнатной температуре.
Примерами подходящих полианионных компонентов, которые могут быть использованы в данных композициях, могут быть, не ограничиваясь этими примерами, анионные производные целлюлозы, анионные кислотосодержащие полимеры акрила, анионные кислотосодержащие полимеры метакрилина, анионные полимеры, содержащие аминокислоты, а также их смеси. Анионные производные целлюлозы можно легко использовать в данном изобретении.
К особенно благоприятному для использования классу полианионных компонентов относятся один или несколько видов полимерных материалов, несущих множество анионных зарядов. Примеры включают, но не ограничиваются:
металкарбоксиметилцеллюлозы
металкарбоксиметилгидроксиэтилцеллюлозы
металкарбоксиметилкрахмалы
металкарбоксиметилгидроксиэтилкрахмалы
металкарбоксиметилпропилгуары
гидролизованные полиакриламиды и полиакрилонитрилы
гепарин
глюкозамингиканы
гиалуроновая кислота
хондроитин сульфат
дерматан сульфат
пептиды и полипептиды
альгиновая кислота
альгинаты металлов
гомополимеры и сополимеры одного или нескольких веществ из следующего списка:
акриловая и метакриловая кислоты
акрилаты и метакрилаты металлов
винилсульфоновая кислота
винилсульфонаты металлов
аминокислоты, такие как аспарагиновая кислота, глютаминовая кислота и подобные соединения
металлические соли аминокислот
п-стиролсульфоновая кислота
п-стиролсульфонаты металлов
2-метакрилолооксиэтилсульфоновые кислоты
2-метакрилолооксиэтилсульфонаты металлов
3-метакрилолоокси-2-гидроксипропилсульфоновые кислоты
2-акриламидо-2-метилпропансульфоновые кислоты
2-акриламидо-2-метилпропансульфонаты металлов
аллилсульфоновая кислота
аллилсульфонаты металлов и похожие соединения.
Отличные результаты были получены при использовании полианионных компонентов, выбранных из карбоксиметилцеллюлоз и их смесей, например соединений метилцеллюлоз со щелочными и/или щелочноземельными металлами.
Данные композиции предпочтительно являются растворами, хотя могут быть использованы и другие формы, такие как мази, гели и аналогичные варианты.
Компонент-носитель является фармацевтически приемлемым и может содержать один или несколько компонентов, которые обеспечивают такую офтальмическую приемлемость, и/или улучшают характеристики композиции, и/или оказывают положительный эффект на глаз, куда вводят композицию, и/или оказывают благоприятное воздействие на пациента, глаз которого лечат.
Преимущественно компонент-носитель имеет водную основу, например содержит большое количество, то есть минимум 50% по массе, воды. Другие компоненты, которые могут быть включены в состав компонента-носителя, содержат, не ограничиваясь этим примером, буферные компоненты, компоненты-консерванты, регуляторы рН, компоненты, традиционно входящие в состав искусственных слез, и тому подобное, а также и их смеси.
Данные композиции предпочтительно обладают вязкостью, соответствующей вязкости воды. В одном воплощении вязкость данных композиций равна минимум приблизительно 10 сП (сантипуаз), более предпочтительно находится в пределах от приблизительно 10 сП до приблизительно 500 сП или приблизительно 1000 сП. Преимущественно вязкость данной композиции находится в пределах от приблизительно 15 сП, или приблизительно 30 сП, или приблизительно 70 сП до приблизительно 150 сП, или приблизительно 200 сП, или приблизительно 300 сП, или приблизительно 500 сП. Вязкость данной композиции можно измерить любым подходящим способом, например стандартным. Стандартный вискозиметр Брукфилда (Brookfield) используется для такого рода измерений вязкости.
В одном из воплощений полианионный компонент присутствует в количестве от приблизительно 0.1% до приблизительно 5%, предпочтительно от приблизительно 0.2% до приблизительно 2.5%, более предпочтительно от приблизительно 0.2% до приблизительно 1.8%, особенно предпочтительно от приблизительно 0.4% до приблизительно 1.3% (масса/объем) от композиции.
Другие компоненты, входящие в состав компонентов-носителей, включают, но не ограничиваются этим списком, буферные компоненты, тонические компоненты, консерванты, регуляторы рН, компоненты, традиционно входящие в состав искусственных слез, такие как один или несколько электролитов, подобные им вещества и их смесей. В одном из воплощений компонент-носитель содержит как минимум одно вещество из следующих: эффективное количество буферного компонента, эффективное количество тонического компонента, эффективное количество компонента-консерванта и воду.
Эти дополнительные компоненты являются предпочтительно офтальмически приемлемыми и могут быть выбраны из ряда соединений, традиционно входящих в состав офтальмических композиций, например композиций, используемых для лечения глаз, пораженных сухим кератитом, искусственных слез и подобных составов. Приемлемые эффективные концентрации таких дополнительных компонентов в композициях по изобретению уже ясны для квалифицированного практикующего фармацевта.
Компонент-носитель предпочтительно содержит эффективное количество компонента, регулирующего тоничность, для придания композиции необходимой тоничности. Компонент-носитель предпочтительно содержит буферный компонент в количестве, достаточном для поддержания рН композиции в желаемом диапазоне. Среди подходящих тонических компонентов можно использовать традиционно входящие в состав офтальмических композиций, такие как одна или несколько различных неорганических солей и похожих соединений. Хлорид натрия, хлорид калия, манит, декстроза, глицерин, пропиленгликоль и похожие соединения, а также их смеси являются очень адекватными компонентами для придания необходимой тоничности.
Среди подходящих буферных компонентов или буферных агентов, которые можно использовать, присутствуют компоненты, традиционно используемые при изготовлении офтальмических композиций. Буферные соли включают щелочные металлы, щелочноземельные металлы и/или соли аммония, а также цитраты, фосфаты, бораты, лактаты и похожие соли, а также их смеси. Можно использовать подходящие органические буферные соединения, такие как буфер Гуда (Goode) и тому подобное.
В состав данных композиций может быть включен любой подходящий компонент-консервант при условии, что он эффективен как консервант в присутствии полианионного компонента. Так, важно, чтобы на компонент-консервант не действовал существенно полианионный компонент. Безусловно, выбор компонента-консерванта зависит от многих факторов, например от наличия специфического полианионного компонента, других компонентов, входящих в состав композиции и т.д. Примерами подходящих компонентов-консервантов могут быть, не ограничиваясь этим списком, персоли, такие как пербораты, перкарбонаты и подобные соединения; пероксиды в очень низкой концентрации, например от приблизительно 50 до приблизительно 200 ppm (масса/объем) перекиси водорода и т.п.; спирты, такие как бензиловый спирт, хлорбутанол и подобные соединения; сорбиновая кислота, ее офтальмически приемлемые соли и их смеси.
Количество компонента-консерванта, входящего в состав данной композиции, содержащей такой компонент, варьируется в достаточно широком диапазоне в зависимости от, например, специфичности используемого компонента-консерванта. Количество такого компонента предпочтительно находится в пределах от приблизительно 0.000001% до приблизительно 0.05% или более (масса/объем) в данной композиции.
Одним особенно полезным для использования классом компонентов-консервантов являются предшественники диоксида хлора. В особых случаях предшественники диоксида хлора включают стабилизированный диоксид хлора (СДХ), хлориты металлов, такие как хлориты щелочных и щелочноземельных металлов, подобные соединения и их смеси. Технический хлорит натрия является очень подходящим к применению предшественником диоксида хлора.
Комплексы, содержащие диоксиды хлора, такие как комплексы диоксида хлора с карбонатом, диоксида хлора с бикарбонатом и их смеси, также можно включить в состав смеси в качестве предшественников диоксида хлора. Точный состав химической композиции, состоящей из разных предшественников диоксида хлора, например СДХ и комплексов диоксида хлора, еще окончательно не понятен. Изготовление или получение определенных предшественников диоксида хлора описано МакНиколасом (McNicholas) в патенте US 3,278,447, включенном в полном объеме в данный текст в виде ссылки. Специфические примеры соединений СДХ, пригодные для использования, включают вещества, продающиеся под торговой маркой Purite7 компанией Allergan, Inc., продающиеся под торговой маркой Dura Klor компанией Rio Linda Chemical Company, Inc., и продающиеся под торговой маркой Anthium Dioxide компанией International Dioxide, Inc.
Предшественники диоксида хлора входят в состав данных композиций для обеспечения возможности надежного сохранения композиции. Концентрации, обеспечивающие надежное сохранение, находятся предпочтительно в диапазоне от приблизительно 0.0002 или приблизительно 0.002 до приблизительно 0.02% (масса/объем) и выше.
В случае когда предшественники диоксида хлора используются в качестве компонентов-консервантов, композиции предпочтительно имеют осмолярность, равную как минимум приблизительно 200 мОсмоль/кг, и содержат буферы, поддерживающие рН на приемлемом физиологическом уровне, например на уровне от приблизительно 6 до приблизительно 8 или приблизительно 10.
Данные композиции предпочтительно содержат эффективное количество компонента-электролита, то есть одного или нескольких электролитов, например, подобных тем, что присутствуют в настоящих или искусственных слезах. Примеры таких электролитов, особенно подходящих для использования в данных композициях, включают соли щелочноземельных металлов, такие как неорганические соли щелочноземельных металлов и их смеси, например соли кальция, соли магния и их смеси, но не ограничиваются ими.
Очень хорошие результаты получают при использовании электролитического компонента, выбранного из группы, состоящей из хлорида кальция, хлорида магния и их смесей.
Объем или концентрация такого компонента-электролита в данной композиции может широко варьироваться и зависит от множества факторов, например от применяемого специфического компонента-электролита, специфической композиции, в состав которой должен войти электролит, и подобных факторов. В одном воплощении количество используемого компонента-электролита подбирается таким образом, чтобы оно как минимум частично соответствовало или практически полностью воспроизводило концентрацию электролитов в настоящих слезах человека. Предпочтительно, концентрация компонента-электролита находится в диапазоне от приблизительно 0.01 до приблизительно 0.5 или приблизительно 1% в данной композиции.
Данные композиции можно получить, используя традиционные процедуры и техники. Например, данные композиции можно получить, смешивая компоненты, например, одновременно в одной партии.
Для иллюстрации, в одном воплощении порции полианионного компонента смешивают с очищенной водой и дают им раствориться в очищенной воде, например, смешивая и/или встряхивая. Другие компоненты, такие как буферный компонент, тонический компонент, электролитический компонент, компонент-консервант и подобные компоненты, последовательно вводят в состав смеси. Полученный раствор стерилизуют, например, паровой стерилизацией при температурах не менее около 100°С, например в диапазоне от приблизительно 120°С до приблизительно 130°С, в течение как минимум приблизительно 15 минут или минимум приблизительно 30 минут, например в течение периода длиной от приблизительно 45 до приблизительно 60 минут. В одном воплощении компонент-консервант предпочтительно добавляется к смеси после стерилизации. Конечный продукт предпочтительно фильтруют, например, через 20-микронный стерильный картриджный фильтр, например 20-микронный картриджный фильтр, например, такой, который выпускается Pall под торговым названием HDC II, для получения чистого, гомогенного раствора, который затем асептически упаковывают в контейнеры, например в контейнеры из полиэтилена низкой плотности.
Иначе, каждую порцию полианионного компонента можно смешать с очищенной водой для получения отдельных порций растворов полианионного компонента. Смешивая отдельные порции растворов полианионных компонентов, можно легко получить раствор, содержащий необходимое и строго определенное количество частей отдельных полианионных компонентов. Смешанный раствор потом можно дополнить другими компонентами, стерилизовать, фильтровать и упаковать в контейнеры, как было описано выше.
В одном воплощении делают раствор порций полианионного компонента в очищенной воде так, как описано выше. Раствор стерилизуют, например, так, как описано выше. Другие компоненты, которые планируют включить в состав конечной композиции, по отдельности растворяют в очищенной воде. Этот раствор фильтруют через стерильный фильтр, например через 0.2-микронный стерильный фильтр, например, такой, который продается Pall под торговым названием Suporflow, в содержащий полианионный компонент раствор для получения конечного раствора. Конечный раствор фильтруют, например, так, как описано выше, для получения чистого, гомогенного раствора, который затем асептически упаковывают в контейнеры, как описано выше.
Данные композиции можно эффективно применять в соответствии с необходимостью способами, которые включают введение эффективного количества композиции для глаз в случае возникновения потребности в увлажнении, например в случае, если глаз подвержен сухому кератиту или имеется предрасположенность к возникновению сухого кератита. При необходимости введение препарата можно повторить несколько раз для обеспечения эффективного увлажнения глаза. Способ введения данной композиции зависит от формы композиции. Например, если композиция представляет собой раствор, ее можно закапать в глаз в виде капель, например, из обычной глазной пипетки. В общем случае данные композиции можно применять абсолютно такими же способами, как и обычно используемые офтальмические композиции. Такое введение описанных композиций обеспечивает значительные и неожиданные преимущества, что описывается данным документом.
Последующие примеры иллюстрируют определенные аспекты данного изобретения, не подразумевая при этом ограничений.
Пример 1
В данном эксперименте клетки эпителия роговицы глаза кролика изолировали и культивировали в условиях, приводящих к дифференцировке в многослойную «эрлифт» культуру, включающую базальные, многоугольные и сквамозные клетки. В результате роста и дифференцировки клеток между клетками появляются плотные контакты, которые являются необходимой основой для возникновения трансэпителиальной электрической устойчивости (ТЭЭУ) клеточных пластов между апикальной и базальной поверхностью. Величина ТЭЭУ является чувствительной мерой клеточного роста, дифференцировки и здоровья.
После 5 дней культивирования, в течение которых формируется слоистая структура, различные чашки с культурами помещались в гипертоническую жидкость (400 мОсмоль/кг) с или без добавления одного из 6 потенциальных совместимых растворимых веществ в низких концентрациях (2 мМ). После 22 часов обработки измеряли ТЭЭУ. Уровень ТЭЭУ выражали в процентах от величины ТЭЭУ такой же культуры в изотонических условиях (300 мОсмоль/кг). Результаты теста представлены в таблице 1.
| Таблица 1 | |
| Результаты теста | |
| Совместимое растворимое вещество | ТЭЭУ (% от изотонического контроля) через 22 часа |
| Изотонический контроль | 100% |
| Гипертонический контроль | 23.3 |
| 2 мМ Таурин | 39.8 |
| 2 мМ Бетаин | 53.3 |
| 2 мМ Карнитин | 118.9 |
| 2 мМ Эритрит | 107.4 |
| 2 мМ Мио-Инозит | 74.8 |
| 2 мМ Ксилит | 94.1 |
Эти результаты показывают, что все протестированные вещества-кандидаты имеют некоторые осмопротекторные свойства и увеличивают ТЭЭУ по сравнению с гипертоническим контролем. Неожиданно из всех протестированных агентов карнитин оказался самым эффективным. Не желая ограничивать изобретение определенной теорией или операцией, мы предполагаем, что хорошие результаты, полученные при использовании карнитина, могут быть обусловлены выполнением карнитином множества ролей в энергетическом метаболизме и других клеточных процессах, а также его осмопротекторными свойствами.
Далее также неожиданно эритрит показал лучшие результаты среди протестированных полиолов. Ксилит и мио-инозит показали хорошие результаты.
Эти результаты показывают, что каждое из 6 соединений-кандидатов, предпочтительно карнитин, эритрит, ксилит и мио-инозит, можно использовать в офатальмических композициях, например, для преодоления гипертонических условий на поверхности глаза человека или животного.
Кроме того, не желая ограничивать изобретение какой-либо определенной теорией или операцией, мы предполагаем, что благодаря тому что эти соединения выполняют различные роли, сочетание двух или более соединений может оказаться удачным, например, сочетание как минимум одного полиола и минимум одной аминокислоты, возможно, обеспечит более надежную защиту клеток поверхности роговицы от инсульта, развившегося, например, в результате иссушения и гиперосмолярности, как при сухом кератите.
Пример 2
Фосфорилированная JNK (активированная форма ассоциированной со стрессом протеин киназы, SAPK) играет ключевую роль в индукции воспаления и апоптоза в ответ на стресс, в том числе при гиперосмолярности.
От доноров в возрасте 16-59 лет из Техасского Lions Eye Bank (Хьюстон, Техас) были получены ткани склеры и роговицы человека. Из лимбальных эксплантов выращивали клетки эпителия роговицы. Вкратце, после осторожного удаления клеток роговицы, большей части конъюнктивы, ириса и эндотелия роговицы лимбальное кольцо разрезалось на 12 равных частей (размером приблизительно 2 на 2 мм каждый). По два таких кусочка помещали в каждую чашку 6-чашечных культуральных планшетов эпителиальной стороной вверх и каждый эксплант покрывали каплей фетальной коровьей сыворотки (FBS) на ночь. Затем экспланты культивировали в среде SHEM, которая представляла собой смесь 1:1 Dulbecco модифицированной Eagle среды (DMEM) и Ham F-12 среды, содержащей 5 нг/мл ЭФР (EGF), 5 µг/мл инсулина, 5 µг/мл трансферрина, 5 нг/мл селенита натрия, 0.5 µг/мл гидрокортизона, 30 нг/мг холерного токсина А, 0.5% DMSO, 50 µг/мл гентамицина, 1.25 µг/мл амфотерицина В и 5% FBS, при 37°С в 5% СО2 и влажности 95%. Среду меняли каждые 2-3 дня. Эпителиальный фенотип данных культур был подтвержден характерной морфологией и иммунофлуоресцентным окрашиванием антителами на цитокератин (АЕ-1/АЕ-3).
Культуральные чашки, планшеты, центрифужные пробирки и другие пластиковые предметы были получены от Becton Dickinson (Линкольн Парк, Нью Джерси).
Использовались Dulbecco модифицированная Eagle среда (DMEM), Ham F-12 среда, Фунгизон и гентамицин производства Invitrogen-GIBCO BRL (Гранд Айланд, Нью Джерси). Использовалась фетальная коровья сыворотка (РВЗ) производства Hyclone (Логан, Юта).
Серия первичных субконфлюэнтных культур эпителиальных клеток роговицы (выращиваемых в течение 12-14 дней, приблизительно 4-5×105 клеток на чашку) трижды промывали сохраняющим буферным солевым раствором (РВ8)и переводили в сбалансированный солевой раствор Earle (Earle's Balanced Salt Solution, EBSS, 300 мОсмоль/кг) на 24 часа перед обработкой. Клетки эпителия роговицы культивировали в течение 1 часа в равном объеме (2.0 мл на чашку) среды EBSS или среды осмолярностью 400 м0 смоль/кг, полученной путем добавления 53 мМ Nad или сахарозы, с примесью либо внутренней соли L-карнитина, либо гидрохлорида бетаина, либо эритрита, либо ксилита (все в концентрации 2 мМ), добавленных за 60 минут до внесения NaCl или сахарозы. Также были приготовлены и протестированы образцы, не содержащие этих осмопротекторов.
Прикрепленные клетки лизировали в буфере Beadlyte® Buffer В (входящем в состав Beadlyte® Cell Signaling buffer kit. Upstate Biotechnology, Лейк Пласид, Нью-Йорк) с добавлением не содержащей EDTA таблетки - смеси ингибиторов протеаз (Roche Applied Science, Индианаполис, Индиана), в течение 15 минут. Клеточные экстракты центрифугировали при ускорении 12,000×g в течение 15 минут при комнатной температуре, супернатанты хранили при -80°С все время перед анализом способом Вестерн блота. Тотальную концентрацию белка в клеточных экстрактах определяли с помощью Micro BCA protein assay kit (Pierce, Рокфолд, Иллинойс).
Уровень JNK1 и JNK2 определялся для каждой композиции способом Вестерн блота со специфическими антителами на фосфорилированные формы каждой киназы.
Анализ способом Вестерн блота проводили следующим образом. Образцы белка (50 µg на полосу) смешивали с 6×SDS буфером и кипятили в течение 5 минут перед загрузкой. Белки разделяли способом электрофореза в SDS полиакриламидном геле (4-15% Tris-HCl, градиентный гель производства Bio-Rad, Hercules, Калифорния) и электронным образом переносили на поливинилидиндифторидные мембраны (РУВР) производства Millipore, Бедфорд, Массачусетс). Мембраны блокировали 5% обезжиренным молоком в TTBS (50 мМ Tris, pH 7.5, 0.9% NaCl и 0.1% Tween-20) в течение одного часа при комнатной температуре (RT), a затем инкубировали в течение 2 часов при RT в растворе 1:1000 кроличьих антител на фосфо-р38 МАРК (Cell Signaling, Беверли, Массачусетс), 1:100 кроличьих антител на фосфо-JNK или 1:500 растворе моноклональных антител на фосфо-р44/42 ERK (Santa Cruz Biotechnology, Санта Круз, Калифорния).
После трех промываний в TTBS мембраны инкубировали в течение одного часа при RT в растворе вторых антител (козьи антитела IgG на кролика), конъюгированных с пероксидазой хрена (1:2000 раствор, Cell Signaling, Беверли, Массачусетс), или козьих антител IgG на мышь (1:5000 раствор, Pierce, Рокфолд, Иллинойс). После четырехкратной промывки мембраны сигнал детектировался с помощью ECL хемифлуоресцентного реагента (Amersham, Пискатавэй, Нью-Джерси), а изображения были получены с помощью Kodak image station 2000R (Eastman Kodak, Нью Хевен, Коннектикут). Проводили стриппинг мембран в 62,5 мМ Tris HCl, pH 6.8, содержащем 2% SDS и 100 мМ α-меркаптноэтанола, при 60°С в течение 30 минут, затем на них снова проводились пробы с помощью 1:100 раствора кроличьих антител на JNK (Santa Cruz Biotechnology) HnH 1:1000 раствора кроличьих антител на ERK или р38 МАРК (Cell Signaling). Эти три разновидности антител способны определять как фосфорилированную, так и нефосфорилированную формы, что дает представление об общем уровне данных МАР-киназ. Сигналы детектировали и фиксировали так же, как было описано выше.
Оценка интенсивности производилась путем анализа картины итоговых бэндов.
Результаты теста представлены на Фиг.1 и 2.
Что касается Фиг.1, ни эритрит, ни ксилит не оказывали влияния на активацию JNK. Однако в отношении Фиг.2 можно сказать, что заметно существенное снижение уровней JNK1 и JNK2 в культурах с L-карнитином и бетаином по сравнению со средой 400 мОсмоль/кг без добавок. В культурах на среде 300 мОсмоль/кг эффект был не таким выраженным.
Пример 3
В другой серии экспериментов использовали анализ Beadlyte® Cell Signaling Assay. Этот анализ представляет собой иммунологический анализ с использованием флуоресцентных, связанных с бусинами, образующих «бутерброд» антител. Например, каждый образец (10 µπ/25 µπ) пипетировали в лунку 96-луночного планшета и инкубировали в 25 µπ разведенных 5-кратно бусин (beads), связанных с антителами, специфически захватывающими белки, в течение ночи. Такие антитела могут специфически захватывать белки, такие как JNK, р38 или ERK. Инкубация в течение ночи применялась для осуществления реакции взаимодействия захватывающих бусин (beads) с белками клеточных лизатов.
Бусины отмывали и смешивали со специфическими биотинилированными репортерными антителами на фосфо-МАРК или тотальную МАРК, а затем стрептавидином-фикоэритрином. Уровень тотальной или фосфорилироавнной МАРК определяли с помощью системы Luminex 100™ system (Luminex, Остин, Техас). Читалось 50 событий на бусину, и данные, полученные с помощью программного обеспечения Bio-Plex Manager, были перенесены в Microsoft Excel® для дальнейшего анализа. Результаты были представлены как процентное отношение фосфорилированной МАРК к тотальной МАРК.
Результаты этих тестов представлены на Фиг.3, 4 и 5.
На Фиг.3 показано отношение фосфорилированной JNK к тотальной JNK. На Фиг.4 показано отношение фосфорилированной р38 к тотальной р38. На Фиг.5 показано отношение фосфорилированной ERK к тотальной ERK.
Как показано на Фиг.3, все соединения-кандидаты, то есть и эритрит, и ксилит, и L-карнитин, и бетаин, уменьшали отношение фосфо-JNK к тотальной по сравнению с гипертоническим контролем.
Что касается Фиг.4, все соединения-кандидаты, за исключением бетаина, уменьшали отношение фосфо-р38 к тотальной по сравнению с гипертоническим контролем.
Как показано на Фиг.5, соединения-кандидаты полиолы, то есть эритрит и ксилит, снижали количество ERK относительно гипертонического контроля. Аминокислоты, бетаин и карнитин, такого эффекта не вызывали.
Пример 4
Был повторен Пример 1 за тем исключением, что были использованы различные концентрации каждого использованного соединения-кандидата, а ТЭЭУ измерялось несколько раз в интервале от 0 до 24 часов.
Результаты этих тестов представлены на Фиг.6. Так же, как и в примере 1, показатель ТЭЭУ выражается как процентное отношение ТЭЭУ к изотоническому контролю.
Данные результаты показывают, что дозозависимый отклик наблюдался при использовании L-карнитина, бетаина и эритрита.
Композицию, содержащую бетаин и стабилизированный диоксид хлора в качестве консерванта, исследовали на совместимость компонентов. Было обнаружено, что бетаин не является оптимально совместимым с данной композицией. Таким образом, бетаин не пригоден для использования в сочетании с определенными консервантами, например со стабилизированным диоксидом хлора. Однако бетаин можно успешно применять в качестве совместимого растворимого вещества в офтальмических композициях, использующих другие способы консервации или не содержащих консервантов, например, в случае одиночного или однодозового применения.
Пример 5
Был воспроизведен Пример 4 за тем исключением, что использовались композиции, содержащие комбинации совместимых растворимых веществ. Также были протестированы композиции, содержащие в качестве совместимого растворимого вещества исключительно глицерин.
Результаты теста представлены на Фиг.7 и 8.
Данные этих тестов показывают, что сочетание различных совместимых растворимых веществ потенциально может обеспечить дополнительные преимущества.
Пример 6
Было показано, что продомен Главного Основного Белка (МВР) является полипептидом, состоящим из 90 аминокислотных остатков.
В результате применения хорошо известных и поставленных методик был получен полипептидный аналог данной полипептидной цепи из 90 аминокислотных остатков.
Офтальмическая композиция была получена в результате смешивания следующих компонентов:
| Вышеупомянутый полипетидный | Концентрация % (масса/объем) |
| аналог | 0.5% |
| Глицерин | 1.0% |
| Эритрит | 0.5% |
| Борная кислота | 0.65 |
| Борат Натрия | 0.25 |
| Цитрат Натрия | 0.1 |
| Хлорид Калия | 0.01 |
| Purite®(1) | 0.01 |
| Гидроксид Натрия 1N | до уровня рН 7.2 |
| Соляная кислота 1N | до уровня рН 7.2 |
| Очищенная вода | необходимое количество |
(1) Purite® является зарегистрированной торговой маркой Allergan, Inc., стабилизированного диоксида хлора. Это соединение добавляется в смесь после термической стерилизации.
Пример 7
Композиция, описанная в примере 6, в форме глазных капель закапывалась в глаз человеку, которому предстояло перенести процедуру, в ходе которой глаз подвергается воздействию лазерной энергии, в частности хирургическую процедуру LASIK.
После хирургической процедуры пациент в меньшей степени страдал от боли, и/или дискомфорта, и/или раздражения глаз, и/или происходило ускоренное восстановление после хирургического вмешательства по сравнению с периодом после аналогичной хирургической процедуры с использованием той же композиции, не содержащей полипептидного аналога.
Пример 8
Композиция, описанная в примере 6, в форме глазных капель закапывалась в глаз человеку, проходящему процедуру, в ходе которой глаз подвергается воздействию лазерной энергии, в частности хирургическую процедуру LASIK.
После хирургической процедуры пациент в меньшей степени страдал от боли, и/или дискомфорта, и/или раздражения глаз, и/или происходило ускоренное восстановление после хирургического вмешательства по сравнению с периодом после аналогичной хирургической процедуры с использованием той же композиции, не содержащей полипептидного аналога.
Пример 9
Композиция, описанная в примере 6, в форме глазных капель закапывалась в глаз человеку, непосредственно после процедуры, в ходе которой глаз подвергался воздействию лазерной энергии, в частности хирургическую процедуру LASIK.
После хирургической процедуры пациент в меньшей степени страдал от боли, и/или дискомфорта, и/или раздражения глаз, и/или происходило ускоренное восстановление после хирургического вмешательства по сравнению с периодом после аналогичной хирургической процедуры с использованием той же композиции, не содержащей полипептидного аналога.
Пример 10
Путем смешивания различных компонентов (представленных в нижеследующей таблице) была получена серия из четырех офтальмических препаратов, соответствующих данному изобретению.
| Ингредиент | Концентрация % (масса/объем) | |||
| А | В | С | D | |
| Карбоксиметилцеллюлоза (КМЦ) | 1.0 | - | - | 0.5 |
| Глицерин | 0.5 | 0.5 | - | 0.5 |
| Эритрит | 0.25 | 0.25 | 0.75 | 0.75 |
| Борная кислота | 0.60 | 0.60 | 0.60 | 0.60 |
| Декагидрат Бората Натрия | 0.045 | 0.045 | 0.045 | 0.045 |
| Дигидрат Хлорида Кальция | 0.006 | 0.006 | 0.006 | 0.006 |
| Гексагидрат Хлорида Магния | 0.006 | 0.006 | 0.006 | 0.006 |
| Purite ®(1) | 0.0075 | 0.0075 | 0.075 | 0.075 |
| Гидроксид Натрия 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Соляная кислота 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Очищенная вода | необходимое количество | необходимое количество | необходимое количество | необходимое количество |
| (1) Purite® является зарегистрированной торговой маркой Allergan, Inc., стабилизированного диоксида хлора. Это соединение добавляется в смесь после термической стерилизации. | ||||
Пример 11
Для получения следующих композиций была воспроизведена описанная Примером 10 процедура.
| Ингредиент | Концентрация % (масса/объем) | |||
| А | В | С | D | |
| Карбоксиметилцеллюлоза (КМЦ) | 1.0 | - | - | 0.5 |
| Глицерин | 0.5 | 0.5 | - | 0.5 |
| Ксилит | 0.25 | 0.25 | 0.75 | 0.75 |
| Борная кислота | 0.60 | 0.60 | 0.60 | 0.60 |
| Декагидрат Бората Натрия | 0.045 | 0.045 | 0.045 | 0.045 |
| Дигидрат Хлорида Кальция | 0.006 | 0.006 | 0.006 | 0.006 |
| Гексагидрат Хлорида Магния | 0.006 | 0.006 | 0.006 | 0.006 |
| Purite®(1) | 0.0075 | 0.0075 | 0.075 | 0.075 |
| Гидроксид Натрия 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Соляная кислота 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Очищенная вода | необходимое количество | необходимое количество | необходимое количество | необходимое количество |
| (1) Purite® является зарегистрированной торговой маркой от Allergan, Inc., стабилизированного диоксида хлора. Это соединение добавляется в смесь после термической стерилизации. | ||||
Пример 12
Для получения следующих композиций была воспроизведена описанная Примером 10 процедура.
| Ингредиент | Концентрация % (масса/объем) | |||
| А | В | С | D | |
| Карбоксиметилцеллюлоза (КМЦ) | 1.0 | - | - | 0.5 |
| Глицерин | 0.5 | 0.5 | - | 0.5 |
| Мио-инозит | 0.25 | 0.25 | 0.75 | 0.75 |
| Борная кислота | 0.60 | 0.60 | 0.60 | 0.60 |
| Декагидрат Бората Натрия | 0.045 | 0.045 | 0.045 | 0.045 |
| Дигидрат Хлорида Кальция | 0.006 | 0.006 | 0.006 | 0.006 |
| Гексагидрат Хлорида Магния | 0.006 | 0.006 | 0.006 | 0.006 |
| Purite®(1) | 0.0075 | 0.0075 | 0.075 | 0.075 |
| Гидроксид Натрия 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Соляная кислота 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Очищенная вода | необходимое количество | необходимое количество | необходимое количество | необходимое количество |
| (1) Purite® является зарегистрированной торговой маркой от Allergan, Inc., стабилизированного диоксида хлора. Это соединение добавляется в смесь после термической стерилизации. | ||||
Пример 13
Для получения следующих композиций была воспроизведена описанная Примером 10 процедура.
| Ингредиент | Концентрация % (масса/объем) | |||
| А | В | С | D | |
| Карбоксиметилцеллюлоза (КМЦ) | 1.0 | - | - | 0.5 |
| Глицерин | 0.5 | 0.5 | - | 0.5 |
| Карнитин | 0.25 | 0.25 | 0.75 | 0.75 |
| Борная кислота | 0.60 | 0.60 | 0.60 | 0.60 |
| Декагидрат Бората Натрия | 0.045 | 0.045 | 0.045 | 0.045 |
| Дигидрат Хлорида Кальция | 0.006 | 0.006 | 0.006 | 0.006 |
| Гексагидрат Хлорида Магния | 0.006 | 0.006 | 0.006 | 0.006 |
| Purite®(1) | 0.0075 | 0.0075 | 0.075 | 0.075 |
| Гидроксид Натрия 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Соляная кислота 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Очищенная вода | необходимое количество | необходимое количество | необходимое количество | необходимое количество |
| (1) Purite® является зарегистрированной торговой маркой от Allergan, Inc., стабилизированного диоксида хлора. Это соединение добавляется в смесь после термической стерилизации. | ||||
Пример 14
Для получения следующих композиций была воспроизведена описанная Примером 10 процедура.
| Ингредиент | Концентрация % (масса/объем) | |||
| А | В | С | D | |
| Карбоксиметилцеллюлоза (КМЦ) | 1.0 | - | - | 0.5 |
| Глицерин | 0.5 | 0.5 | - | 0.5 |
| Таурин | 0.25 | 0.25 | 0.75 | 0.75 |
| Борная кислота | 0.60 | 0.60 | 0.60 | 0.60 |
| Декагидрат Бората Натрия | 0.045 | 0.045 | 0.045 | 0.045 |
| Дигидрат Хлорида Кальция | 0.006 | 0.006 | 0.006 | 0.006 |
| Гексагидрат Хлорида Магния | 0.006 | 0.006 | 0.006 | 0.006 |
| Purite®(1) | 0.0075 | 0.0075 | 0.075 | 0.075 |
| Гидроксид Натрия 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Соляная кислота 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Очищенная вода | необходимое количество | необходимое количество | необходимое количество | необходимое количество |
| (1) Purite® является зарегистрированной торговой маркой от Allergan, Inc., стабилизированного диоксида хлора. Это соединение добавляется в смесь после термической стерилизации. | ||||
Пример 15
Для получения следующих композиций была воспроизведена описанная Примером 10 процедура.
| Ингредиент | Концентрация % (масса/объем) | |||
| А | В | С | D | |
| Карбоксиметилцеллюлоза (КМЦ) | 1.0 | - | - | 0.5 |
| Глицерин | 0.5 | 0.5 | - | 0.5 |
| Бетаин(2) | 0.25 | 0.25 | 0.75 | 0.75 |
| Борная кислота | 0.60 | 0.60 | 0.60 | 0.60 |
| Декагидрат Бората Натрия | 0.045 | 0.045 | 0.045 | 0.045 |
| Дигидрат Хлорида Кальция | 0.006 | 0.006 | 0.006 | 0.006 |
| Гексагидрат Хлорида Магния | 0.006 | 0.006 | 0.006 | 0.006 |
| Purite®(1) | 0.0075 | 0.0075 | 0.075 | 0.075 |
| Гидроксид Натрия 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Соляная кислота 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Очищенная вода | необходимое количество | необходимое количество | необходимое количество | необходимое количество |
| (1)Purite® является зарегистрированной торговой маркой от Allergan, Inc., стабилизированного диоксида хлора. Это соединение добавляется в смесь после термической стерилизации. | ||||
| (2) Было показано, что Бетаин несовместим с консервантом Purite®. Таким образом, консерванты не использовались. Данные композиции могут применяться в форме одной дозы. | ||||
Пример 16
Для получения следующих композиций была воспроизведена описанная Примером 10 процедура.
| Ингредиент | Концентрация % (масса/объем) | |||
| А | В | С | D | |
| Карбоксиметилцеллюлоза (КМЦ) | 0.5 | - | 0.5(3) | - |
| Глицерин | 0.9 | 0.9 | 0.9 | 0.9 |
| Эритрит | 0.5 | 0.5 | 0.25 | 0.25 |
| Карнитин НСl | 0.1 | 0.25 | 0.1 | 0.25 |
| Борная кислота | 0.45 | 0.45 | 0.45 | 0.45 |
| Борат Натрия | 0.46 | 0.46 | 0.46 | 0.46 |
| Цитрат Натрия | 0.1 | 0.1 | 0.1 | 0.1 |
| Хлорид Калия | 0.14 | 0.14 | 0.14 | 0.14 |
| Хлорид Кальция | 0.006 | 0.006 | 0.006 | 0.006 |
| Хлорид Магния | 0.006 | 0.006 | 0.006 | 0.006 |
| Purite®(1) | 0.01 | 0.01 | 0.01 | 0.01 |
| Гидроксид Натрия 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Соляная кислота 1N | до рН 7.2 | до рН 7.2 | до рН 7.2 | до рН 7.2 |
| Очищенная вода | необходимое количество | необходимое количество | необходимое количество | необходимое количество |
| (1) Purite® является зарегистрированной торговой маркой от Allergan, Inc., стабилизированного диоксида хлора. Это соединение добавляется в смесь после термической стерилизации. | ||||
| (3) Смесь 10% по весу карбоксиметилцеллюлозы высокого молекулярного веса, имеющей средневесовой молекулярный вес порядка 700,000, и 90% по весу карбоксиметилцеллюлозы среднего молекулярного веса, имеющей средневесовой молекулярный вес порядка 250,000. | ||||
Пример 17
Каждая из композиций, полученных согласно Примерам с 10 по 16, вводилась в форме глазных капель один раз в сутки или чаще для лечения глаз пациентов, страдающих сухим кератитом. Применение может производиться как в ответ, так и перед неблагоприятными воздействиями среды, например сухого воздуха или ветра, низкой влажности, интенсивного использования компьютера и подобных воздействий. Такое применение очень похоже на применение обычно используемых искусственных слез.
У всех пациентов после одной недели такого лечения было заметно существенное улучшение состояния, например уменьшение боли, и/или уменьшение раздражения, и/или улучшение зрения, и/или улучшение внешнего вида глаз, что касается проявлений или симптомов сухого кератита. Кроме того, у пациентов, которым вводили композиции, содержащие карбоксиметилцеллюлозу (КМЦ), наблюдался благоприятный эффект благодаря анионному характеру КМЦ и относительно высокой вязкости таких композиций. Этот дополнительный благоприятный эффект выражается, не ограничиваясь приведенным списком, в уменьшении раздраженности в течение более продолжительного периода после употребления препарата, и/или более интенсивном увлажнении глаза, и/или усиленной защите от неблагоприятного воздействия катионных соединений, имеющихся на поверхности глаза пациента.
Пример 18
Каждая из содержащих карбоксиметилцеллюлозу (КМЦ) композиций, полученных согласно Примерам с 10 по 16, в форме глазных капель закапывалась в глаза различных людей, которым предстояла хирургическая процедура LASIK.
После хирургической процедуры каждый из пациентов в меньшей степени страдал от боли, и/или дискомфорта, и/или раздражения глаз, и/или происходило ускоренное восстановление после хирургического вмешательства по сравнению с периодом после аналогичной хирургической процедуры с использованием той же композиции, не содержащей карбокисметилцеллюлозы.
Пример 19
Каждая из содержащих карбоксиметилцеллюлозу (КМЦ) композиций, полученных согласно Примерам с 10 по 16, в форме глазных капель закапывалась в глаза различных людей, проходящих хирургическую процедуру LASIK.
После хирургической процедуры пациенты все в меньшей степени страдали от боли, и/или дискомфорта, и/или раздражения глаз, и/или происходило ускоренное восстановление после хирургического вмешательства по сравнению с периодом после аналогичной хирургической процедуры с использованием той же композиции, не содержащей карбокисметилцеллюлозы.
Пример 20
Каждая из содержащих карбоксиметилцеллюлозу (КМЦ) композиций, полученных согласно Примерам с 10 по 16, в форме глазных капель закапывалась в глаза различных людей, главным образом, непосредственно после хирургической процедуры LASIK.
После хирургической процедуры все в меньшей степени страдали от боли, и/или дискомфорта, и/или раздражения глаз, и/или происходило ускоренное восстановление после хирургического вмешательства по сравнению с периодом после аналогичной хирургической процедуры с использованием той же композиции, не содержащей карбокисметилцеллюлозы.
Так как данное изобретение было описано посредством различных специфических примеров и воплощений, следует отметить, что изобретение ими не ограничивается и может по-разному применяться в соответствии с нижеприведенной формулой.
Claims (13)
1. Офтальмическая композиция, содержащая
водный компонент-носитель и
эффективное количество как минимум одного совместимого растворимого вещества для защиты глазной поверхности от гиперосмотического стресса, где совместимое растворимое вещество выбрано из группы, состоящей из карнитина и эритрита, при этом композиция имеет осмолярность в диапазоне от 300 до 1000 мОсмоль/кг.
водный компонент-носитель и
эффективное количество как минимум одного совместимого растворимого вещества для защиты глазной поверхности от гиперосмотического стресса, где совместимое растворимое вещество выбрано из группы, состоящей из карнитина и эритрита, при этом композиция имеет осмолярность в диапазоне от 300 до 1000 мОсмоль/кг.
2. Офтальмическая композиция по п.1, имеющая осмолярность в диапазоне от 300 до 600 мОсмоль/кг.
3. Офтальмическая композиция по п.1, в которой совместимое растворимое вещество представляет собой карнитин и присутствует в композиции в количестве от 0,01% (вес/объем) до 1,0% (вес/объем).
4. Офтальмическая композиция по п.3, дополнительно включающая глицерин и карбоксиметилцеллюлозу.
5. Офтальмическая композиция по п.1, в которой совместимое растворимое вещество представляет собой эритрит и присутствует в композиции в количестве от 0,01% (вес/объем) до 1,0% (вес/объем).
6. Офтальмическая композиция по п.3, в которой карнитин присутствует в количестве 0,25% (вес/объем).
7. Офтальмическая композиция по п.5, в которой эритрит присутствует в количестве 0,25% (вес/объем).
8. Офтальмическая композиция по п.4, которая доставляет совместимые растворимые вещества к клеткам глазной поверхности для того, чтобы уравновесить осмотический стресс на глазной поверхности.
9. Офтальмическая композиция по п.1, которая дополнительно содержит консервант стабилизированный диоксид хлора.
10. Применение композиции по п.1, для изготовления лекарственного средства для защиты глазной поверхности от гиперосмотического стресса.
11. Применение композиции по п.10, где в композиции присутствует глицерин в количестве от 0,01% до 3% (вес/объем).
12. Применение композиции по п.10, где композиция дополнительно включает консервант стабилизированный диоксид хлора.
13. Способ лечения сухого кератита глаза человека, включающий введение композиции по п.1.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US10/990,811 | 2004-11-16 | ||
| US10/990,811 US8569367B2 (en) | 2004-11-16 | 2004-11-16 | Ophthalmic compositions and methods for treating eyes |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| RU2007117637A RU2007117637A (ru) | 2008-12-27 |
| RU2410081C2 true RU2410081C2 (ru) | 2011-01-27 |
Family
ID=36218032
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| RU2007117637/15A RU2410081C2 (ru) | 2004-11-16 | 2005-11-14 | Офтальмические композиции и способы лечения глаз |
Country Status (24)
| Country | Link |
|---|---|
| US (10) | US8569367B2 (ru) |
| EP (4) | EP2952178B1 (ru) |
| JP (1) | JP5179880B2 (ru) |
| KR (1) | KR101344602B1 (ru) |
| CN (1) | CN101056618B (ru) |
| AR (1) | AR052031A1 (ru) |
| AU (2) | AU2005306721B2 (ru) |
| BR (2) | BR122019023144B8 (ru) |
| CA (1) | CA2588044C (ru) |
| CY (2) | CY1116545T1 (ru) |
| DK (3) | DK1811959T4 (ru) |
| ES (3) | ES2550616T5 (ru) |
| HK (2) | HK1107027A1 (ru) |
| HU (2) | HUE025116T2 (ru) |
| IL (1) | IL182532A (ru) |
| NO (3) | NO346214B1 (ru) |
| NZ (2) | NZ583757A (ru) |
| PL (3) | PL1811959T3 (ru) |
| PT (2) | PT2422765E (ru) |
| RU (1) | RU2410081C2 (ru) |
| SI (2) | SI2422765T1 (ru) |
| TW (1) | TWI369996B (ru) |
| WO (1) | WO2006055454A2 (ru) |
| ZA (1) | ZA200702917B (ru) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2625301C2 (ru) * | 2011-12-23 | 2017-07-13 | Юниверсити Ов Уэстерн Сидни | Офтальмологическая композиция |
Families Citing this family (41)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20050147584A1 (en) * | 2004-01-05 | 2005-07-07 | Allergan, Inc. | Compositions and methods comprising memantine and polyanionic polymers |
| US7220422B2 (en) * | 2003-05-20 | 2007-05-22 | Allergan, Inc. | Methods and compositions for treating eye disorders |
| US8569367B2 (en) * | 2004-11-16 | 2013-10-29 | Allergan, Inc. | Ophthalmic compositions and methods for treating eyes |
| TW200722109A (en) * | 2005-03-31 | 2007-06-16 | Bausch & Lomb | Polysaccharide and polyol composition for treating dry eye and related methods of manufacture and methods of use |
| TWI393567B (zh) * | 2005-03-31 | 2013-04-21 | Bausch & Lomb | 治療乾眼之組合物及相關之製造方法及使用方法 |
| CA2611909C (en) * | 2005-07-01 | 2014-01-07 | Sigma-Tau Industrie Farmaceutiche Riunite S.P.A. | Composition for treatment of corneal disease |
| US20070004672A1 (en) * | 2005-07-01 | 2007-01-04 | Dharmendra Jani | Long lasting alginate dry eye, related methods of manufacture and methods of use |
| CN1939534B (zh) * | 2005-09-27 | 2010-12-01 | 长春金赛药业股份有限公司 | 含有人生长激素或人粒细胞巨噬细胞刺激因子的用于治疗损伤和溃疡的外用制剂 |
| DE102005055275A1 (de) * | 2005-11-17 | 2007-05-24 | Ursapharm Arzneimittel Gmbh & Co. Kg | Phosphatfreie pharmazeutische Zusammensetzung sowie deren Verwendung |
| US20080057022A1 (en) * | 2006-08-30 | 2008-03-06 | Erning Xia | Ophthalmic Pharmaceutical Compositions and Uses Thereof |
| US8138156B2 (en) | 2006-10-18 | 2012-03-20 | Bausch & Lomb Incorporated | Ophthalmic compositions containing diglycine |
| US20080095754A1 (en) * | 2006-10-18 | 2008-04-24 | Burke Susan E | Ophthalmic compositions comprising diglycine |
| JP5384362B2 (ja) * | 2006-12-11 | 2014-01-08 | シグマ−タウ・インドゥストリエ・ファルマチェウチケ・リウニテ・ソシエタ・ペル・アチオニ | 角膜疾患を処置するための点眼剤の形態の医薬の調製におけるl−カルニチンの使用 |
| DE102006060953A1 (de) * | 2006-12-12 | 2008-08-07 | Farco-Pharma Gmbh | Pharmazeutische Zubereitung für die Behandlung entzündlicher Erkrankungen des Urogenitaltraktes |
| EP2101725A1 (en) * | 2006-12-14 | 2009-09-23 | SIGMA-TAU Industrie Farmaceutiche Riunite S.p.A. | Use of l-carnitine or of alkanoyl l-carnitines for the preparation of a physiological supplement or medicament for ophthalmic use in the form of eye drops |
| US20080148689A1 (en) * | 2006-12-20 | 2008-06-26 | Bausch & Lomb Incorporated | Packaging solutions |
| US8629099B2 (en) | 2008-03-25 | 2014-01-14 | Bausch & Lomb Incorporated | Ophthalmic compositions comprising a dipeptide |
| EP2349232A1 (en) * | 2008-10-20 | 2011-08-03 | Allergan, Inc. | Ophthalmic compositions useful for improving visual acuity |
| NO2437762T3 (ru) | 2009-06-05 | 2018-01-06 | ||
| ITMI20100319A1 (it) * | 2010-02-26 | 2011-08-27 | Lo Li Pharma Srl | Composizioni comprendenti mioinositolo e il loro uso nel trattamento delle malattie respiratorie. |
| US9636355B2 (en) | 2011-09-22 | 2017-05-02 | Theo Holdings, Llc | Hypertonic dextran solution and methods of treating and preventing recurrent corneal erosion |
| US8957048B2 (en) * | 2011-10-06 | 2015-02-17 | Allergan, Inc. | Compositions for the treatment of dry eye |
| ES2896336T3 (es) | 2011-12-07 | 2022-02-24 | Allergan Inc | Suministro eficiente de lípidos a película lagrimal humana usando un sistema de emulsión sensible a sales |
| US9907826B2 (en) | 2011-12-07 | 2018-03-06 | Allergan, Inc. | Efficient lipid delivery to human tear film using a salt-sensitive emulsion system |
| US8324171B1 (en) | 2012-02-06 | 2012-12-04 | Bausch & Lomb Incorporated | Ophthalmic compositions containing diglycine |
| US8664180B2 (en) | 2012-02-06 | 2014-03-04 | Bausch & Lomb Incorporated | Ophthalmic compositions containing diglycine |
| US10085960B2 (en) | 2012-03-30 | 2018-10-02 | Brien Holden Vision Institute | Methods and compositions for reducing ocular discomfort |
| HUE044555T2 (hu) * | 2013-02-01 | 2019-11-28 | Allergan Inc | Nátrium-hialuronátot és karboximetil-cellulózt tartalmazó mûkönny |
| US9394355B2 (en) | 2014-08-20 | 2016-07-19 | Silk Technologies, Ltd. | Fibroin-derived protein composition |
| KR102487299B1 (ko) | 2014-11-25 | 2023-01-10 | 알러간, 인코포레이티드 | 안정화된 오메가-3 안과용 조성물 |
| ITUB20153104A1 (it) * | 2015-08-13 | 2017-02-13 | Sooft Italia S P A Contrada Molino 17 68333 Montegiorgio Fm | Composizione ed uso di collirio a base di inositolo per migliorare l'accomodazione visiva dei pazienti |
| JP2018534979A (ja) | 2015-10-23 | 2018-11-29 | ザ・トラスティーズ・オブ・コロンビア・ユニバーシティ・イン・ザ・シティ・オブ・ニューヨーク | 組織内のレーザ誘導によるコラーゲン架橋結合 |
| KR20190008210A (ko) | 2016-04-08 | 2019-01-23 | 코넬 유니버시티 | 실크 유래 단백질을 이용한 상처 치료를 증가시키는 방법 |
| WO2017214604A1 (en) | 2016-06-10 | 2017-12-14 | The Trustees Of Columbia University In The City Of New York | Devices, methods, and systems for detection of collagen tissue features |
| RU2623205C1 (ru) * | 2016-07-13 | 2017-06-22 | Станислав Анатольевич Кедик | Офтальмологический гель таурина |
| US11242367B2 (en) | 2016-08-12 | 2022-02-08 | Silk Technologies, Ltd. | Silk-derived protein for treating inflammation |
| US11666481B1 (en) | 2017-12-01 | 2023-06-06 | The Trustees Of Columbia University In The City Of New York | Diagnosis and treatment of collagen-containing tissues |
| CN111467349B (zh) * | 2020-05-14 | 2021-06-01 | 华熙生物科技股份有限公司 | 人工泪液及其制备方法 |
| CN116940662A (zh) * | 2021-03-10 | 2023-10-24 | 博士伦爱尔兰有限公司 | 不含防腐剂的隐形眼镜处理溶液 |
| US12012238B2 (en) * | 2021-05-26 | 2024-06-18 | Bausch + Lomb Ireland Limited | Packaging solutions |
| CA3223191A1 (en) * | 2021-09-03 | 2023-03-09 | University Of Utah Research Foundation | Compositions and methods for diagnosing, detecting and treating eosinophil-related diseases |
Family Cites Families (47)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US1781701A (en) | 1928-05-16 | 1930-11-18 | Phillips Morris Godfrey Philip | Machine for removing flags and other adhering leaf from the stalks of tobacco leaves |
| US3278447A (en) | 1963-12-02 | 1966-10-11 | Cloro Bac Products Inc | Process for stabilizing chlorine dioxide solution |
| US4201706A (en) * | 1978-09-22 | 1980-05-06 | Burton, Parsons & Company, Inc. | Treatment of corneal edema |
| ATE6466T1 (de) | 1979-10-26 | 1984-03-15 | Smith And Nephew Associated Companies P.L.C. | Autoklavierbare emulsionen. |
| WO1984004681A1 (en) * | 1983-05-25 | 1984-12-06 | Alcon Lab Inc | Ophthalmic solution |
| JPS6436255A (en) * | 1987-07-31 | 1989-02-07 | Fujitsu Ltd | Feeding circuit |
| US5192535A (en) * | 1988-02-08 | 1993-03-09 | Insite Vision Incorporated | Ophthalmic suspensions |
| IT1235153B (it) | 1988-11-15 | 1992-06-22 | Sigma Tau Ind Farmaceuti | Uso dell'acetil l-carnitina nel trattamento terapeutico della cataratta e composizioni farmaceutiche utili in tale trattamento |
| IT1224795B (it) | 1988-12-01 | 1990-10-24 | Sigma Tau Ind Farmaceuti | Uso dell'acetil d-carnitina nel trattamento terapeutico del glaucoma e composizioni farmaceutiche utili in tale trattamento |
| WO1991001718A1 (fr) | 1989-08-03 | 1991-02-21 | Eisai Co., Ltd. | Procede de photostabilisation pour collyre liquide et collyre liquide photostabilise |
| US5681555A (en) * | 1991-04-22 | 1997-10-28 | Gleich; Gerald J. | Method for the treatment of bronchial asthma by parenteral administration of anionic polymers |
| DE4229494A1 (de) † | 1992-09-04 | 1994-03-10 | Basotherm Gmbh | Arzneimittel zur topischen Anwendung am Auge zur Behandlung des erhöhten intraokularen Drucks |
| JP3431216B2 (ja) | 1993-06-18 | 2003-07-28 | 千代田化工建設株式会社 | 触媒層支持構造 |
| EP0778021A4 (en) | 1994-09-14 | 1998-06-03 | Taisho Pharmaceutical Co Ltd | DROPS TO CARE FOR THE CORNEA |
| US5980865A (en) * | 1995-08-18 | 1999-11-09 | Baker Norton Pharmaceuticals, Inc. | Method for treating late phase allergic reactions and inflammatory diseases |
| US5847294A (en) * | 1996-04-09 | 1998-12-08 | Amherst Process Instruments, Inc. | Apparatus for determining powder flowability |
| JPH1036255A (ja) * | 1996-07-24 | 1998-02-10 | Nikken Chem Co Ltd | 眼圧降下用点眼剤 |
| IT1288399B1 (it) | 1996-12-03 | 1998-09-22 | Sigma Tau Ind Farmaceuti | Medicamento per il trattamento terapeutico della maculopatia legata all'eta', della maculopatia non legata all'eta' e per la profilassi |
| FI106923B (fi) | 1997-01-03 | 2001-05-15 | Cultor Ltd Finnsugar Bioproduc | Trimetyyliglysiinin käyttö kehon limakalvojen hygieniaan ja hoitoon tarkoitetuissa valmisteissa |
| AR002194A1 (es) | 1997-03-17 | 1998-01-07 | Sanchez Reynaldo Alemany | Instrumento computarizado para el analisis del movimiento. |
| US6770675B2 (en) * | 1997-03-17 | 2004-08-03 | Novartis Ag | Compositions and methods for reducing ocular hypertension |
| DK1021204T3 (da) | 1997-09-26 | 2006-05-08 | Noven Pharma | Bioadhæsive præparater og fremgangsmåder til topisk administration af aktive midler |
| US6274725B1 (en) | 1998-06-02 | 2001-08-14 | Isis Pharmaceuticals, Inc. | Activators for oligonucleotide synthesis |
| IT1302307B1 (it) * | 1998-09-01 | 2000-09-05 | Sigma Tau Healthscience Spa | Composizione ad attivita' antiossidante ed atta a migliorarel'utilizzazione metabolica del glucosio, comprendente acetil |
| AU1295200A (en) * | 1998-11-13 | 2000-06-05 | Continental Projects Limited | Complexes of hyaluronic acid/carnitines and pharmaceutical and cosmetic compositions |
| US6228392B1 (en) * | 1999-04-29 | 2001-05-08 | Gene Tools, Llc | Osmotic delivery composition, solution, and method |
| KR100354606B1 (ko) | 2000-02-01 | 2002-09-30 | 주식회사 중외제약 | 다목적 콘택트 렌즈 관리 용액 조성물 |
| EP2153819B1 (en) * | 2000-07-14 | 2012-09-05 | Allergan, Inc. | Use of a solubility enhancing component in an aqueous composition comprising brimonidine tartrate |
| CA2355814C (en) * | 2000-09-14 | 2010-06-29 | Kabushiki Kaisha Hayashibara Seibutsu Kagaku Kenkyujo | Pharmaceutical composition for ophthalmic use |
| US8557868B2 (en) | 2000-11-04 | 2013-10-15 | Fxs Ventures, Llc | Ophthalmic and contact lens solutions using low molecular weight amines |
| DK1339418T3 (da) | 2000-11-08 | 2009-12-14 | Fxs Ventures Llc | Forbedret ophthalmiske og kontaktlinseoplösninger indeholdende simple saccharider som konserverende forstærkere |
| US20030069410A1 (en) | 2001-06-14 | 2003-04-10 | Isis Pharmaceuticals, Inc. | Methods for preparing oligonucleotides having chiral phosphorothioate linkages |
| AR036122A1 (es) | 2001-07-03 | 2004-08-11 | Avecia Biotechnology Inc | Un complejo de sal que comprende un n-alquilimidazol y una 1,1-dioxo-1,2-dihidro-1l6-benzo [d]-isotiazol-3-ona y un metodo para sintetizar oligonucleotidos utilizando la quimica de fosforamidita |
| US6936589B2 (en) | 2001-09-28 | 2005-08-30 | Albert T. Naito | Parenteral delivery systems |
| US7045121B2 (en) * | 2001-12-14 | 2006-05-16 | Allergan, Inc. | Ophthalmic compositions for lubricating eyes and methods for making and using same |
| US6858614B2 (en) * | 2002-02-19 | 2005-02-22 | Parion Sciences, Inc. | Phenolic guanidine sodium channel blockers |
| AU2003259145A1 (en) | 2002-07-17 | 2004-02-02 | Spencer P. Thornton | Treatment for dry eye syndrome |
| EP1551399A4 (en) * | 2002-09-30 | 2011-01-05 | Mark A Babizhayev | METHOD FOR THE TOPICAL TREATMENT OF EYE DISEASES AND COMPOSITION AND DEVICE FOR THIS TREATMENT |
| ITRM20020492A1 (it) | 2002-10-01 | 2004-04-02 | Sigma Tau Ind Farmaceuti | Uso della propionil l-carnitina per la preparazione di un medicamento per il trattamento del glaucoma. |
| US20040137079A1 (en) | 2003-01-08 | 2004-07-15 | Cook James N. | Contact lens and eye drop rewetter compositions and methods |
| EP1611883A1 (en) * | 2003-03-26 | 2006-01-04 | Menicon Co., Ltd. | Composition for ophthalmic use |
| US20050009836A1 (en) * | 2003-06-26 | 2005-01-13 | Laskar Paul A. | Ophthalmic composition containing quinolones and method of use |
| US8569367B2 (en) * | 2004-11-16 | 2013-10-29 | Allergan, Inc. | Ophthalmic compositions and methods for treating eyes |
| BRPI0808410A2 (pt) | 2007-02-28 | 2015-06-23 | Aciex Therapeutics Inc | Métodos e composições para normalizar secreções da glândula meibomiana |
| JP4929245B2 (ja) | 2008-07-31 | 2012-05-09 | 株式会社ベッセル工業 | 工具類のグリップ |
| NO2437762T3 (ru) | 2009-06-05 | 2018-01-06 | ||
| US9907826B2 (en) * | 2011-12-07 | 2018-03-06 | Allergan, Inc. | Efficient lipid delivery to human tear film using a salt-sensitive emulsion system |
-
2004
- 2004-11-16 US US10/990,811 patent/US8569367B2/en active Active
-
2005
- 2005-11-10 TW TW094139485A patent/TWI369996B/zh active
- 2005-11-14 EP EP15176046.9A patent/EP2952178B1/en active Active
- 2005-11-14 PL PL05821259T patent/PL1811959T3/pl unknown
- 2005-11-14 CN CN200580038995.XA patent/CN101056618B/zh active Active
- 2005-11-14 EP EP05821259.8A patent/EP1811959B2/en active Active
- 2005-11-14 BR BR122019023144A patent/BR122019023144B8/pt active IP Right Grant
- 2005-11-14 DK DK05821259.8T patent/DK1811959T4/da active
- 2005-11-14 EP EP20100185764 patent/EP2422765B1/en active Active
- 2005-11-14 NZ NZ583757A patent/NZ583757A/en unknown
- 2005-11-14 BR BRPI0518173A patent/BRPI0518173B8/pt active IP Right Grant
- 2005-11-14 DK DK10185764.7T patent/DK2422765T3/en active
- 2005-11-14 WO PCT/US2005/041064 patent/WO2006055454A2/en active Application Filing
- 2005-11-14 NO NO20072170A patent/NO346214B1/no unknown
- 2005-11-14 KR KR1020077011097A patent/KR101344602B1/ko active IP Right Grant
- 2005-11-14 HU HUE10185764A patent/HUE025116T2/en unknown
- 2005-11-14 SI SI200531991T patent/SI2422765T1/sl unknown
- 2005-11-14 PL PL10185764T patent/PL2422765T3/pl unknown
- 2005-11-14 PT PT101857647T patent/PT2422765E/pt unknown
- 2005-11-14 ES ES05821259T patent/ES2550616T5/es active Active
- 2005-11-14 PL PL383268A patent/PL218364B1/pl unknown
- 2005-11-14 RU RU2007117637/15A patent/RU2410081C2/ru active
- 2005-11-14 HU HUE05821259A patent/HUE026575T2/en unknown
- 2005-11-14 NO NO20220060A patent/NO347855B1/no unknown
- 2005-11-14 DK DK15176046.9T patent/DK2952178T3/da active
- 2005-11-14 PT PT58212598T patent/PT1811959E/pt unknown
- 2005-11-14 JP JP2007543142A patent/JP5179880B2/ja active Active
- 2005-11-14 NZ NZ597106A patent/NZ597106A/xx unknown
- 2005-11-14 AU AU2005306721A patent/AU2005306721B2/en active Active
- 2005-11-14 ES ES15176046T patent/ES2842226T3/es active Active
- 2005-11-14 EP EP20193341.3A patent/EP3777836A1/en active Pending
- 2005-11-14 ES ES10185764.7T patent/ES2543974T3/es active Active
- 2005-11-14 SI SI200532012T patent/SI1811959T2/sl unknown
- 2005-11-14 CA CA2588044A patent/CA2588044C/en active Active
- 2005-11-15 AR ARP050104802A patent/AR052031A1/es not_active Application Discontinuation
-
2007
- 2007-04-10 ZA ZA200702917A patent/ZA200702917B/xx unknown
- 2007-04-12 IL IL182532A patent/IL182532A/en active IP Right Grant
-
2008
- 2008-01-24 HK HK08100909.2A patent/HK1107027A1/zh unknown
-
2012
- 2012-06-08 AU AU2012203398A patent/AU2012203398B2/en active Active
-
2013
- 2013-03-15 US US13/842,555 patent/US8569370B2/en active Active
- 2013-09-11 US US14/024,332 patent/US8729125B2/en active Active
- 2013-09-11 US US14/024,404 patent/US20140045773A1/en not_active Abandoned
-
2014
- 2014-04-08 US US14/248,227 patent/US9254324B2/en active Active
-
2015
- 2015-07-29 CY CY20151100661T patent/CY1116545T1/el unknown
- 2015-11-10 CY CY20151101009T patent/CY1116936T1/el unknown
-
2016
- 2016-01-04 US US14/987,333 patent/US9668997B2/en active Active
- 2016-06-08 HK HK16106605.6A patent/HK1218620A1/zh unknown
-
2017
- 2017-05-03 US US15/585,888 patent/US10213405B2/en active Active
-
2019
- 2019-01-15 US US16/248,268 patent/US20190365692A1/en not_active Abandoned
-
2021
- 2021-05-11 US US17/317,078 patent/US20210401789A1/en not_active Abandoned
-
2023
- 2023-03-21 US US18/187,165 patent/US20230404961A1/en active Pending
-
2024
- 2024-02-13 NO NO20240132A patent/NO20240132A1/no unknown
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| RU2625301C2 (ru) * | 2011-12-23 | 2017-07-13 | Юниверсити Ов Уэстерн Сидни | Офтальмологическая композиция |
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| RU2410081C2 (ru) | Офтальмические композиции и способы лечения глаз | |
| JP2008520671A5 (ru) | ||
| EP2349232A1 (en) | Ophthalmic compositions useful for improving visual acuity | |
| MX2007005463A (en) | Ophthalmic compositions and methods for treating eyes |