KR900008692B1 - 친수성 다공질 막, 그의 제조방법 및 친수성 다공질 막을 이용한 혈장분리 장치 - Google Patents
친수성 다공질 막, 그의 제조방법 및 친수성 다공질 막을 이용한 혈장분리 장치 Download PDFInfo
- Publication number
- KR900008692B1 KR900008692B1 KR1019870004476A KR870004476A KR900008692B1 KR 900008692 B1 KR900008692 B1 KR 900008692B1 KR 1019870004476 A KR1019870004476 A KR 1019870004476A KR 870004476 A KR870004476 A KR 870004476A KR 900008692 B1 KR900008692 B1 KR 900008692B1
- Authority
- KR
- South Korea
- Prior art keywords
- porous membrane
- membrane
- hydrophilic
- hydrophobic
- plasma
- Prior art date
Links
- 239000012528 membrane Substances 0.000 title claims description 327
- 238000004519 manufacturing process Methods 0.000 title claims description 16
- 210000002381 plasma Anatomy 0.000 claims description 116
- 230000002209 hydrophobic effect Effects 0.000 claims description 93
- 238000000926 separation method Methods 0.000 claims description 68
- 239000000178 monomer Substances 0.000 claims description 65
- 238000000034 method Methods 0.000 claims description 42
- 230000008961 swelling Effects 0.000 claims description 25
- -1 polypropylene Polymers 0.000 claims description 23
- 229920000098 polyolefin Polymers 0.000 claims description 22
- 239000004743 Polypropylene Substances 0.000 claims description 19
- 229920001155 polypropylene Polymers 0.000 claims description 19
- 238000010559 graft polymerization reaction Methods 0.000 claims description 17
- 229940088644 n,n-dimethylacrylamide Drugs 0.000 claims description 15
- YLGYACDQVQQZSW-UHFFFAOYSA-N n,n-dimethylprop-2-enamide Chemical group CN(C)C(=O)C=C YLGYACDQVQQZSW-UHFFFAOYSA-N 0.000 claims description 15
- 239000002033 PVDF binder Substances 0.000 claims description 10
- 229920002981 polyvinylidene fluoride Polymers 0.000 claims description 10
- 238000006116 polymerization reaction Methods 0.000 claims description 8
- 229910052757 nitrogen Inorganic materials 0.000 claims description 6
- WOBHKFSMXKNTIM-UHFFFAOYSA-N Hydroxyethyl methacrylate Chemical group CC(=C)C(=O)OCCO WOBHKFSMXKNTIM-UHFFFAOYSA-N 0.000 claims description 4
- 230000001678 irradiating effect Effects 0.000 claims description 4
- 238000002834 transmittance Methods 0.000 claims description 4
- 239000006260 foam Substances 0.000 claims description 2
- 210000000170 cell membrane Anatomy 0.000 claims 1
- 229920002620 polyvinyl fluoride Polymers 0.000 claims 1
- 238000002360 preparation method Methods 0.000 claims 1
- 238000004017 vitrification Methods 0.000 claims 1
- 239000011148 porous material Substances 0.000 description 36
- 238000006243 chemical reaction Methods 0.000 description 17
- 238000011282 treatment Methods 0.000 description 16
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 15
- 210000004369 blood Anatomy 0.000 description 14
- 239000008280 blood Substances 0.000 description 14
- 238000001914 filtration Methods 0.000 description 14
- 239000000463 material Substances 0.000 description 12
- 230000035699 permeability Effects 0.000 description 10
- 239000007789 gas Substances 0.000 description 8
- 239000000758 substrate Substances 0.000 description 8
- 229920001600 hydrophobic polymer Polymers 0.000 description 7
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 239000000706 filtrate Substances 0.000 description 6
- 238000009832 plasma treatment Methods 0.000 description 6
- 229920000642 polymer Polymers 0.000 description 6
- 230000008569 process Effects 0.000 description 6
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 5
- 150000003926 acrylamides Chemical class 0.000 description 5
- 239000002585 base Substances 0.000 description 5
- 229920002678 cellulose Polymers 0.000 description 5
- 239000001913 cellulose Substances 0.000 description 5
- 229920002301 cellulose acetate Polymers 0.000 description 5
- 230000005465 channeling Effects 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- 235000018102 proteins Nutrition 0.000 description 5
- 102000004169 proteins and genes Human genes 0.000 description 5
- 108090000623 proteins and genes Proteins 0.000 description 5
- 239000000243 solution Substances 0.000 description 5
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 4
- 239000007864 aqueous solution Substances 0.000 description 4
- 230000005540 biological transmission Effects 0.000 description 4
- 230000017531 blood circulation Effects 0.000 description 4
- 230000007423 decrease Effects 0.000 description 4
- 230000005855 radiation Effects 0.000 description 4
- 210000002966 serum Anatomy 0.000 description 4
- 238000009987 spinning Methods 0.000 description 4
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 238000000502 dialysis Methods 0.000 description 3
- 230000001939 inductive effect Effects 0.000 description 3
- 150000002978 peroxides Chemical class 0.000 description 3
- 230000000704 physical effect Effects 0.000 description 3
- 239000002861 polymer material Substances 0.000 description 3
- 235000004252 protein component Nutrition 0.000 description 3
- 239000002904 solvent Substances 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 2
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 102000004506 Blood Proteins Human genes 0.000 description 2
- 108010017384 Blood Proteins Proteins 0.000 description 2
- 241000283690 Bos taurus Species 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 239000003513 alkali Substances 0.000 description 2
- 229910052786 argon Inorganic materials 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 210000000601 blood cell Anatomy 0.000 description 2
- 239000011248 coating agent Substances 0.000 description 2
- 238000000576 coating method Methods 0.000 description 2
- 230000008878 coupling Effects 0.000 description 2
- 238000010168 coupling process Methods 0.000 description 2
- 238000005859 coupling reaction Methods 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 238000000635 electron micrograph Methods 0.000 description 2
- 238000005187 foaming Methods 0.000 description 2
- 230000005660 hydrophilic surface Effects 0.000 description 2
- 230000001965 increasing effect Effects 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 229940057995 liquid paraffin Drugs 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 239000000203 mixture Substances 0.000 description 2
- 239000003921 oil Substances 0.000 description 2
- 239000003960 organic solvent Substances 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 238000012856 packing Methods 0.000 description 2
- 230000000379 polymerizing effect Effects 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 230000000153 supplemental effect Effects 0.000 description 2
- DZSVIVLGBJKQAP-UHFFFAOYSA-N 1-(2-methyl-5-propan-2-ylcyclohex-2-en-1-yl)propan-1-one Chemical compound CCC(=O)C1CC(C(C)C)CC=C1C DZSVIVLGBJKQAP-UHFFFAOYSA-N 0.000 description 1
- PRAMZQXXPOLCIY-UHFFFAOYSA-N 2-(2-methylprop-2-enoyloxy)ethanesulfonic acid Chemical compound CC(=C)C(=O)OCCS(O)(=O)=O PRAMZQXXPOLCIY-UHFFFAOYSA-N 0.000 description 1
- SQVSEQUIWOQWAH-UHFFFAOYSA-N 2-hydroxy-3-(2-methylprop-2-enoyloxy)propane-1-sulfonic acid Chemical compound CC(=C)C(=O)OCC(O)CS(O)(=O)=O SQVSEQUIWOQWAH-UHFFFAOYSA-N 0.000 description 1
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 1
- XEEYSDHEOQHCDA-UHFFFAOYSA-N 2-methylprop-2-ene-1-sulfonic acid Chemical compound CC(=C)CS(O)(=O)=O XEEYSDHEOQHCDA-UHFFFAOYSA-N 0.000 description 1
- MAGFQRLKWCCTQJ-UHFFFAOYSA-N 4-ethenylbenzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=C(C=C)C=C1 MAGFQRLKWCCTQJ-UHFFFAOYSA-N 0.000 description 1
- 206010018910 Haemolysis Diseases 0.000 description 1
- CERQOIWHTDAKMF-UHFFFAOYSA-N Methacrylic acid Chemical compound CC(=C)C(O)=O CERQOIWHTDAKMF-UHFFFAOYSA-N 0.000 description 1
- WHNWPMSKXPGLAX-UHFFFAOYSA-N N-Vinyl-2-pyrrolidone Chemical compound C=CN1CCCC1=O WHNWPMSKXPGLAX-UHFFFAOYSA-N 0.000 description 1
- 229920002292 Nylon 6 Polymers 0.000 description 1
- 239000004952 Polyamide Substances 0.000 description 1
- 239000004698 Polyethylene Substances 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 241000473945 Theria <moth genus> Species 0.000 description 1
- 150000007513 acids Chemical class 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 150000001408 amides Chemical class 0.000 description 1
- 239000012736 aqueous medium Substances 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000000740 bleeding effect Effects 0.000 description 1
- 210000001124 body fluid Anatomy 0.000 description 1
- 239000010839 body fluid Substances 0.000 description 1
- 230000005587 bubbling Effects 0.000 description 1
- 150000001875 compounds Chemical class 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 229920001577 copolymer Polymers 0.000 description 1
- 238000011026 diafiltration Methods 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- 150000001993 dienes Chemical class 0.000 description 1
- 201000010099 disease Diseases 0.000 description 1
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 238000010894 electron beam technology Methods 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 239000007792 gaseous phase Substances 0.000 description 1
- 229920000578 graft copolymer Polymers 0.000 description 1
- 230000008588 hemolysis Effects 0.000 description 1
- 229920001519 homopolymer Polymers 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 125000004435 hydrogen atom Chemical class [H]* 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 125000005395 methacrylic acid group Chemical group 0.000 description 1
- 238000001471 micro-filtration Methods 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 238000002715 modification method Methods 0.000 description 1
- 239000002808 molecular sieve Substances 0.000 description 1
- 230000036651 mood Effects 0.000 description 1
- 229920000620 organic polymer Polymers 0.000 description 1
- 239000003973 paint Substances 0.000 description 1
- 230000000149 penetrating effect Effects 0.000 description 1
- 229920002239 polyacrylonitrile Polymers 0.000 description 1
- 229920002647 polyamide Polymers 0.000 description 1
- 229920000515 polycarbonate Polymers 0.000 description 1
- 239000004417 polycarbonate Substances 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920000573 polyethylene Polymers 0.000 description 1
- 229920000139 polyethylene terephthalate Polymers 0.000 description 1
- 239000005020 polyethylene terephthalate Substances 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 238000003825 pressing Methods 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 238000010526 radical polymerization reaction Methods 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 230000035484 reaction time Effects 0.000 description 1
- 238000001223 reverse osmosis Methods 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 239000004094 surface-active agent Substances 0.000 description 1
- 238000012360 testing method Methods 0.000 description 1
- 230000000930 thermomechanical effect Effects 0.000 description 1
- 150000005671 trienes Chemical class 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- NLVXSWCKKBEXTG-UHFFFAOYSA-N vinylsulfonic acid Chemical compound OS(=O)(=O)C=C NLVXSWCKKBEXTG-UHFFFAOYSA-N 0.000 description 1
- 229920003169 water-soluble polymer Polymers 0.000 description 1
- 238000009736 wetting Methods 0.000 description 1
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D67/00—Processes specially adapted for manufacturing semi-permeable membranes for separation processes or apparatus
- B01D67/0081—After-treatment of organic or inorganic membranes
- B01D67/0093—Chemical modification
- B01D67/00931—Chemical modification by introduction of specific groups after membrane formation, e.g. by grafting
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D67/00—Processes specially adapted for manufacturing semi-permeable membranes for separation processes or apparatus
- B01D67/0081—After-treatment of organic or inorganic membranes
- B01D67/009—After-treatment of organic or inorganic membranes with wave-energy, particle-radiation or plasma
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D69/00—Semi-permeable membranes for separation processes or apparatus characterised by their form, structure or properties; Manufacturing processes specially adapted therefor
- B01D69/02—Semi-permeable membranes for separation processes or apparatus characterised by their form, structure or properties; Manufacturing processes specially adapted therefor characterised by their properties
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D71/00—Semi-permeable membranes for separation processes or apparatus characterised by the material; Manufacturing processes specially adapted therefor
- B01D71/06—Organic material
- B01D71/26—Polyalkenes
- B01D71/262—Polypropylene
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D71/00—Semi-permeable membranes for separation processes or apparatus characterised by the material; Manufacturing processes specially adapted therefor
- B01D71/06—Organic material
- B01D71/30—Polyalkenyl halides
- B01D71/32—Polyalkenyl halides containing fluorine atoms
- B01D71/34—Polyvinylidene fluoride
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J5/00—Manufacture of articles or shaped materials containing macromolecular substances
- C08J5/20—Manufacture of shaped structures of ion-exchange resins
- C08J5/22—Films, membranes or diaphragms
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2323/00—Details relating to membrane preparation
- B01D2323/02—Hydrophilization
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2323/00—Details relating to membrane preparation
- B01D2323/38—Graft polymerization
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2325/00—Details relating to properties of membranes
- B01D2325/04—Characteristic thickness
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01D—SEPARATION
- B01D2325/00—Details relating to properties of membranes
- B01D2325/38—Hydrophobic membranes
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10S—TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10S521/00—Synthetic resins or natural rubbers -- part of the class 520 series
- Y10S521/905—Hydrophilic or hydrophobic cellular product
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T428/00—Stock material or miscellaneous articles
- Y10T428/249921—Web or sheet containing structurally defined element or component
- Y10T428/249953—Composite having voids in a component [e.g., porous, cellular, etc.]
- Y10T428/249978—Voids specified as micro
- Y10T428/249979—Specified thickness of void-containing component [absolute or relative] or numerical cell dimension
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Health & Medical Sciences (AREA)
- Inorganic Chemistry (AREA)
- Transplantation (AREA)
- Plasma & Fusion (AREA)
- Physics & Mathematics (AREA)
- Materials Engineering (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Separation Using Semi-Permeable Membranes (AREA)
- Manufacture Of Porous Articles, And Recovery And Treatment Of Waste Products (AREA)
- External Artificial Organs (AREA)
- Treatments For Attaching Organic Compounds To Fibrous Goods (AREA)
Abstract
내용 없음.
Description
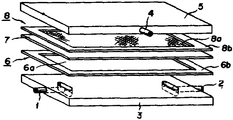
제1도는 본 발명의 혈장분리 장치의 일례를 나타낸다.
제2도는 본 발명의 친수성 다공질 막에서 수득된 그라프트 비(graft ratio)와 포점(bubble point)사이의 관계를 나타내는 그래프이다.
제3도∼제6도는 본 발명의 친수성 다공질 막의 구조를 나타내는 전자 광현미경 사진이다.
제7도∼제10도는 기질로서 사용된 소수성 다공질 막의 구조를 나타내는 전자 광현미경 사진이다.
제11도∼제12도는 비교용 다공질 막의 구조를 나타내는 전자 광현미경 사진이다.
제13도는 TMA 측정결과 수득된 데이터를 나타내는 도표이다.
본 발명은 친수성 다공질 막, 그의 제조방법 및 친수성 다공질 막을 이용한 혈장분리 장치에 관한 것이다. 보다 구체적으로는, 사용시 우수한 치수 안정성 및 강도를 나타내고 막 성질의 분해가 거의 없는 친수성 다공질 막, 막의 제조방법 및 친수성 다공질 막을 이용한 혈장분리 장치에 관한 것이다.
여과 또는 고분자의 다공질 막을 이용한 투석에 의한 물질의 분리가 실시가능성 및 경제적인 면에서 이점이 있기 때문에 여러 적용시 유용하는 것을 발견하였다. 일반적으로 수용액 및 혈액과 같은 수용성 매질의 분리에 있어서, 친수성 다공질 막이 사용되거나 또는 친수성 획득을 위한 처리를 받은 소수성 다공질 막이 사용된다.
친수성 다공질 막으로는, 높은 물 투과성을 갖는 셀룰로오스 유도체의 다공질 막, 특히 셀룰로오스 아세테이트가 널리 알려져 있다. 그러나, 상기의 셀룰로오스 유도체는 산, 알칼리 및 유기 용매에 대한 저항성이 불충분하며 또한 열과 압력에 의해서 쉽게 변형되는 결점을 지니고 있다. 따라서, 상기의 셀룰로오스 유도체는 매우 제한된 상황하에서만 사용된다. 또한 셀롤로오스 유도체는 물과 접촉시, 팽윤한다. 상기에 기술한 셀룰로오스 유도체로 이루어진 다공질 막을 장치에 끼워 사용할 때, 팽윤 현상으로 인해 다공질 막이 자체 변형하여 장치내에 형성된 유로(flow paths)를 방해하고, 채널링(channeling) 현상을 일으키며, 막이 그 작용을 하는 것을 충분히 방해할 정도까지 가능할 만큼 막의 표면에 주름이 생긴다. 셀룰로오스 아세테이트로 이루어진 다공질 막을 혈장 분리용으로 생의학적인 분야에서 사용할 때, 상기의 막은 체액내의 보충요소를 활성화시키며 생체 적응성의 관점에서 조차도 어려움을 수반한다.
대조적으로, 소수성 다공질 막은 일반적으로 높은 강도, 우수한 화학적 저항성 및 막을 형성하는 소수성 고분자 본래의 다른 우수한 바람직한 성질을 가지며 물내에서 팽윤하지 않으므로, 상기에 언급한 난점들을 수반하지 않는다. 그러나, 널리 실시되는 여과의 조건(에를들어, 1㎏/㎠ 이하의 여과 압력)하에서, 다공질 막은 연결소공을 통한 물의 통과를 허용치 않는다. 따라서, 상기의 막은 소공이 친수성 표면을 갖도록 처리되어야 한다. 친수성 표면을 제조하기 위한 처리법으로는 소수성 다공질 막을 유기용매(예, 에탄올 또는 다른 알코올)_에 침지시킨 후 물로 막내에 함유되어 있는 유기알콜을 친환함으로써 친수성 표면을 제조하는 유기용매-물 치환법과 소수성 막을 계면활성제 또는 글리세롤 또는 폴리비닐 알코올 또는 친수성 중합체로 피복시킴으로써 표면을 제조하는 피복법이 잘 공지되어 있다. 불행하게도, 상기의 방법들로는, 막에 영구적인 친수성을 부가하는 것을 불가능하다.
따라서, 막이 이같은 친수성을 상실할 때마다 친수성을 다시 갖도록 처리하여야만 한다. 이와같은 불가피한 반복 처리는 상기의 막을 사용하는 것을 복잡하게 한다. 특이하게도, 전자의 방법으로 처리한 막은 건조후에 친수성을 상실하고 후자의 방법으로 처리한 막은 피복시키는 화합물이 막 외부로 흘러나간 후에 친수성을 상실한다. 소수성 다공질 막에 반영구적인 친수성을 부여하는 여러 시도가 진행되고 있다. 그러나, 소수성 다공질 막은 본래 다공질이기 때문에 많은 문제점을 갖는다. 반영구적인 친수성을 완전하게 부여할 수 있는 방법은 아직까지 없다. 알칼리(예, 수산화나트륨 또는 수산화칼륨)수용액을 사용하는 처리에 의해 막의 표면에 친수성기를 부여하는 방법(일본국 특허공보 SHO 58(1983-93,734)은 알칼리의 작용으로 막의 강도를 상실한 가능성이 있으며 처리 조건을 조절하는데 어려운 문제를 수반한다. 소수성 다공질 막을 알콜내에 침지시킨 후, 수용서 중합체 수용액이 막으로 스며들게 하여, 처리된 막을 건조시키고, 그다음 열 도는 방사선으로 막을 처리하여 막상에 남아있는 수용성 중합체를 불용화시키는 방법(일본국 특허 공보 SHO 54(1978)-17,978, 일본국 특허 공개 SHo 56(1981)-38,333 등)은, 중합체 수용액으로 치환하는 과정을 거쳐 알콜내에 침지시키는 과정에서 많은 시간이 소비되며, 불용화처리시 열 도는 방사선의 영향으로 막의 강도가 떨어지고, 및 막내의 소공의 지경에 변화가 일어날 가능성이 크다. 또한, 상기의 방법은 장치, 안정성 및 비용에 관해 해결해얌할 문제점이 있다.
플라즈마 변형법은 플라즈마를 소수성 고분자 막의 표면에 조사함으로써 친수성을 부여한다. 이와같은 처리에 의한 친수성은 시간이 지남에 따라 점차적으로 감소되기 때문에(이까다교수, 교오또 대학교 "고교 자이료" : vol.31, No.7, p.62-69, 상기의 방법은 지속적인 친수성을 부여하는 것이 불가능하다는 중대한 결점을 갖는다.
또한 소수성 고분자 표면상에 활성점을 제조하여 고분자상에 친수성 단량체를 그리고 중합화시킴으로써 친수성을 부여하는 것은 허용되는 것으로 나타났다. 그라프트 중합화를 높은 투과력을 갖는 전자선 또는 γ선과 같은 방사선을 사용하여 실행할 때, 상기의 방법은 기본 물질의 강도를 상실하며 장치, 안전성 및 비용에 관해 어려운 문제를 수반한다. 또한,그라프트 중합화는, 그라프트 중합화를 할 것을 갖지 않는 유기고분자가 그라프트화되지 않은 단일 중합체를 형성하도록 한다. 따라서, 상기의 방법에는 효과 및 효능에 관해서 요구되는 것들이 많다. 현재, 고분자의 기본 물지르이 표면을 변형시키는 데에 가격이 저렴한 플라즈마를 이용한 그라프트 중합법의 개발이 연구중에 있다. 플라즈마의 투과력이 방사선의 투과력에 비해 약하기 때문에, 일반적인 플라즈마를 이용한 방법에 의해서, 다공질 막내부의 소공과 같은 미세한 구멍의 표면은 효과적으로 쉽게 처리되지는 않는다.
플라즈마를 이용한 처리가 목적하는 효과를 나타내는, 고분자 물질의 외부 표면으로부터의 깊이는 기껏해야 단 수 마이크론이라는 것(일본국 특허 공개 SHO 56(1981)-38, 38,333 p.11-13 및 고교 자이료, vol.31, No.7, p.62-69)이 알려졌다.
생각컨대, 다공질 물질의 내부에 깊이 친수성을 부여하는 것은 그라프트의 양을 충분히 증가시켜줌으로써 수득될 수도 있다. 그러나 그라프트의 양이 증가될 때, 다공질 막내의 소공이 매우 심하게 막혀 있어서 막이 물을 충분한 통과를 제공하는 것을 방해하거나 소공의 직경이 매우 심하게 변화하여서 막이 분자체(분리막)의 작용을 행하는 것을 방해한다. 또한 습한 조건하에서 막은 매우 많은 팽윤하므로, 장치내에 끼워 사용한 막은, 막이 상기에 기술한 채널링 현상을 일으킬 중대한 결점을 수반한다. 최근에, 소수성 막에 친수성을 부여하는 데에 플라즈마를 적용시키는 경우가 보고되었다(일본국 특허 공개 SHO 59(1984)-160, 504). 플라즈마 존재하에 기체상태의 단량체의 반응을 유발시키는 것을 목적으로 하는 종래의 플라즈마 처리와는 달리 상기의 방법은 주어진 기본 불질에 플라즈마를 조사하여 기본 물질의 표면상에 라디칼과 같은 활성점을 형성시킨후 플라즈마의 부재하에 단량체의 수용액내에서 기본 물질을 중합화시키는 소위 플라즈마 그라프트 중합화를 이용한다. 상기의 방법은 그라프트 중합비를 목적하는 대로 조절하는 것이 요구된다. 그러나, 상기의 방법은, 앞에 언급한 결점을 없애는데 충분한 비교적 낮은 그라프트비로 다공질 막 내의 소공의 표면에 완전한 친수성을 부여하는 것이 가능한 것으로는 알려져 있지 않다. 그라프트 중합이 명세서내에 열거한 임의의 친수성 불포화 단량체를 사용하여 수행될 때, 그라프트 층은 불포화 단량체가 기분 물질을 형성하는 소수성 고분자에 대한 친화성이 낮기 때문에 기본 물질로서 다공질 막상의 외부쪽에 형성된다. 단량체는 용액의 형태로 충분히 공급되므로, 그라프트 체인의 성장이 활발하게 진행되어 플라즈마 조사로 생성된 활성점이 비교적 널리 분포된 다공질 막의 외부표면 근처의 그라프트 층의 전개는 막 내부의 깊은 그라프트층의 전개와 비교해 볼 때 매우 빨리 일어난다.
완전한 친수성의 부여가 다공질 막 내부의 소공 표면에 완전히 진행하기 전에, 다공질 막의외부표면 근처에 충분히 전개된 그라프트 층이 다공질 막 내부의 소공을 막을것이라는 것은 당연하다. 상업적인 면에서 조차, 상기의 방법은 단량체가 많이 소비되고 반응이 액상내에서 일어나기 때문에 실기가능성도 낮다는 결점을 갖는다. 플라즈마에 의해 개시된 중합화의 동일 기구를 N, N-디메틸 아크릴아미드의 기질과 폴리프로필렌의 다공질 막 사이의 상호 높은 친화성 조합에 적용시킬 때, 그라프트 층이 기질 내부에 깊이 전개된다는 것을 발명자들에 의해 밝혀졌다. 그러나 단량체는 반응에 용액의 형태로 공급되기 때문에, 그라프트 층은 매우 많이 전개하여 기질의 강도를 낮춘 가능성도 있다. 상기의 방법은 여과 또는 투석에 사용할 목적인 소수성 다공질 막에 친수성을 부여하기 위한 목적에는 적합하다고 할 수가 없다.
본 발명은 신규 친수성 다공질 막, 그를 제조하는 방법, 및 친수성 다공질 막을 이용한 혈장 분리를 제공하는 것을 목적으로 한다. 또한 본 발명은 사용시 우수한 치수 안정성 및 강도를 나타내며 막 성질의 분해가 거의 없는 친수성 다공질 막, 그의 제조방법, 및 친수성 다공질 막을 이용한 혈장분리 장치를 제공하는 것을 목적으로 한다. 또한 본 발명은 소수성 다공질 막 본래의 매우 바람직한 물리적 성질의 파괴없이 막에 지속적인 친수성을 부여하여 우수한 물 투과성을 갖는 친수성 다공질 막, 그의 제조방법, 및 친수성 다공질막을 이용한 혈장분리 장치를 제공하는 것을 목적으로 한다. 또한, 본 발명은 장치, 안정성 및 비용면에서 큰 이점을 갖는 친수성 다공질 막, 그의 제조방법, 및 친수성 다공질 막을 이용한 혈장분리 장치를 제공하는 것을 목적으로 한다.
상기에 기술한 목적은 소수성 다공질 막의 표면상에 친수성 단량제의 그라프트 체인을 형성하여 표면에 완전한 친수성을 부여하고, 제조된 막이 젖을 경우, 1% 이하의 팽윤비과 0.5-8㎏/㎠범위내에서 포점을 나타내는 제조방법이 특징적인 친수성 다공질 막을 사용하여 완성된다.
또한 본 발명은 친수성 단량체의 그라프트 체인이, 변형되지 않은 상태에서 다공질 막의 외부 표면에 플라즈마를 조사하여 기체 상태로 공급된 친수성 단량제를 외부 표면사에 그라프트 중합화시킴으로서 소수성 다공질 막의 표면상에 형성되는, 친수성 다공질 막을 나타낸다. 또한 본 발명은 소수성 다공질 막이 풀리올레핀 또는 부분적으로 플로르화되거나 플루오르화된 플리올레핀으로 이루어진 친수성 다공질 막을 나타낸다. 또한 본 발명은 소수성 다공질 막이 폴리비닐리덴 플루오라이드로 이루어진 친수성 다공질 막을 나타낸다. 또한 본 발명은 20-250㎛의 범위내에서 벽 두께를 갖는 친수성 다공질 막임을 나타낸다. 또한, 본 발명은 소수성 다공질 막이 그의 외부 표면부위상에 피층을 갖지않는 친수성 다공질 막임을 나타낸다. 본 발명은 또한 친수성 단량체가 N, N-디메틸 아크릴아미드인 친수성 다공질 막임을 나타낸다. 본 발명은 또한 젖었을 때 0-0.5% 범위내의 팽윤비와 0.8-2㎏/㎠ 범위내의 포점을 갖는 친수성 다공질 막임을 나타낸다.
상기에 기술한 목적들은, 친수성 다공질 막의 제조방법에 의해서, 즉 변형되지 않는 상태에서 소수성 다공질 막의 외부표면에 플라즈마를 조사한 후, 기체 상태의 친수성 단량체를 공급해 줌으로써 친수성 단량체를 다공질 막의 표면상에 그라프트 중합화시키는 것이 가능한 공정에 의해 완성된다.
본 발명은 소수성 다공질 막이 20-250㎛ 내의 벽 두께를 갖는 친수성 다공질 막의 제조방법을 나타낸다. 본 발명은 또한 소수성 다공질 막이 0.05-1.0㎛ 범위내의 평균 소공 직경을 갖는 친수성 다공질 막의 제조방법을 나타낸다.
본 발명은 소수성 다공질 막이 폴리올레핀 또는 부분적으로 클로르화도거나 플루오르화된 폴리올레핀으로 이루어진 친수성 다공질 막의 제조방법을 나타낸다. 본 발명은 또한 소수성 다공질 막이 폴리프로필렌으로 이루어진 친수성 다공질 막의 제조방법을 나타낸다. 또한, 본 발명은 소수성 다공질 막이 폴리비닐리덴 플루오라이드로 이루어진 친수성 다공질 막의 제조방법을 나타낸다. 본 발명은 친수성 단량체가 N, N-디메틸 아크릴아미드인 친수성 다공질 막의 제조방법을 나타낸다. 또한 본 발명은 그라프트 비가 2-30% 범위로 낮춰지는 조건하에서 중합화가 수행되는 친수성 다공질 막의 제조방법을 나타낸다.
상기에 기술한 목적들은 또한 혈장 분리막으로서, 소수성 다공질 막의 표면상에 친수성 단량체의 그라프트 체인을 형성하여 표면에 완전한 친수성을 부여하고, 제조된 막이 젖었을 때 팽윤비가 1% 이하이며, 0.5-8㎏/㎠ 범위내에서 포점을 나타내는 제조방법으로 측정짖는 친수성 다공질 막을 갖는 혈장분리 장치에 의해 완성된다.
본 발명은 혈장 분리막이 혈장의 총 단백질의 90% 이상의 투과율을 갖는 혈장분리 장치를 나타낸다. 상기의 발명은 또한 변형되지 않은 상태에서 소수성 다공질 막의 외부 표면에 플라즈마를 조사하고 이어 기체상태의 친수성 단량체를 공급하여 소수성 다공질 막의 표면상에 그라프트 중합화시키고 소수성 다공질 막의 표면상에 결과적으로 형성된 그라프트 체인이 친수성 다공질 막에 완전한 친수성을 부여하는 것으로 구성된 방법에 의해서 제조된 친수성 다공질 막이 혈장분리 막인 혈장분리 장치를 나타낸다. 상기의 발명은 또한 소수성 다공질 막이 폴리올레핀 또는 부분적으로 클로르화되거나 플로오르화된 폴리올레핀으로 이루어진 혈장분리 장치를 나타낸다.
또한 본 발명은 소수성 다공질 막이 폴리프로필렌으로 이루어진 혈장분리 장치를 나타낸다. 본 발명은 또한 소수성 다공질 막이 폴리비닐리덴 플루오라이드로 이루어진 혈장분리 장치를 나타냈다. 나아가, 본 발명은 친수성 단량체가 2-히드록시 에틸 메타크릴레이트 또는 N, N-디메틸 아크릴아미드인 혈장분리 장치를 나타낸다. 본 발명은 20-250㎛ 범위내에서 벽두께를 갖는 혈장분리 장치를 나타낸다. 나아가, 본 발명은 친수성 다공질 막이 젖었을 때 0-0.5% 범위내에 팽윤비가 0.8-2㎏/㎠ 범위내의 포점을 나타내는 혈장분리 장치를 나타낸다.
본 명세서 내에서 사용된 다공질 막의 "표면"이란 다공질 막의 단순한 외부 표면을 의미하는 것이 아니고 보다 넓게 막 내부에 분포되어 있는 소공의 표면을 포함한 다공질 막의 표면을 의미한다. 따라서, 소수성 다공질 막의 표면이 완전하게 친수성으로 된다는 것은, 완전한 친수성이 소수성 다공질 막의 표면 뿐만 아니라 막내부에 분포된 소공의 표면에도 부여됨을 나타낸다.
이하에 실시예를 들어 본 발명을 보다 상세히 설명한다.
본 발명의 친수성 다공질 막은 소수성 다공질 막의 표면상에 친수성 단량체의 그라프트 체인을 형성하여 소수성 다공질 막의 표면에 완전한 친수성을 부여함으로써 수득된 생성물이다. 이러한 친수성 다공질 막은, 젖었을 때 1% 이하의 팽윤비, 바람직하게는 0-0.5% 범위내의 팽윤비, 및 0.5-8㎏/㎠ 범위내의 포점, 바람직하게는 0.8-2㎏/㎠의 포점을 나타낸다. 상기의 성질에서 보듯이 친수성을 완전하게 부여하는데 사용되는 친수성 단량체의 그라프트 체인은 소수성 막의 외부 표면 뿐만 아니라 막 내부에 분포된 소공의 표면을 덮는데, 이러한 사실에도 불구하고 그라프트 체인은 소수성 다공질 막 본래의 소공 특성에 영향을 미칠 정도까지 충분하게 전개되지는 않고 표면에 부착된 매우 얇은 층내에 전개된다. 포점은, 일반적으로 주어진 다공질 막의 최대 소공 직경에 의한 크기를 나타낸다. 상기에 기술한 성질들을 갖는 본 발명의 친수성 다공질 막은, 플라즈마 처리로 친수성 다공질 막의 표면을 활성화시키고 활성화된 표면에 핀수성 단량체를 그라프트 중합화시킴으로써 수득된다. 본 발명에서 사용된 "플라즈마"는 종래으 방법에 의해 얻을 수 있는 저온 저압 기체 플라즈마이다.
일반적으로, 전기에너지를 사용하여 기체를 여기시킴으로써 생성된다. 따라서 전기 에너지는 직류로부터 마이크로파까지의 여기 범위내에서 효과적으로 사용된다. 본 전기 에너지의 공급은 어느 것이 좀더 상황에 적합하느냐에 따라서 용량 결합 또는 유도성 결합에 의해 실행될 수 있다. 그렇지 않으면 내부 전극법 또는 외부 전극법에 의해서 실행될 수 있다. 일반적으로 플라즈마는 10-3~10Torrs 범위내의 압력하에서 질소, 수소, 이르곤, 또는 공기와 같은 기체를 도입하고, 그 기체에 고주파 발생기를 사용하여 0.1-300W 범위내의 전력을 걸어줌으로써 생성된다.
첫째로, 상기와 같이 생성된 플라즈마를 소수성 다공질 막의 표면을 활성화시키기 위해서 일반적으로 약 1-60초동안 소수성 다공질 막상에 방사시킨다. 상기의 클라즈마 처리에 적합한 조건은 쉽게 한정할 수가 없는데, 그 이유는 반응 용기의 용량, 처리에 사용된 시료의 크기, 및 사용 장치의 종류에 따라서 조건이 변화하기 때문이다. 플라즈마 처리가 친수성 다공질 막의 외부표면 부위 뿐만아니라 소수성 다공질 막의 외부표면, 막 내부에 분포된 소공의 표면상에, 플라즈마를 조사하는 동안 균일하게 활성 점이 형성되도록 하는 것은 변형되지 않은 상태에서, 즉 소수성 다공질 막이 반응 용기의 벽 표면과 접촉하지 않거나 소수성 다공지 막이 지지대상에 표장되지 않은 상황하에서 유지된다는 것이 설명된다. 플라즈마 처리가 소수성 다공질 막 상에서 수행될대 다공질 막의 한쪽면 상의 외부 표면이 반응 용기의 벽 표면에 부착되어 있는데, 예를들면 친수성 단량제의 그라프트 층은 주로 플라즈마 또는 플라즈마로부터 생긴 고에너지선에 직접 노출되어 있는 외부 표면 부분에서만 주로 형성된다. 따라서, 친수성의 완전한 부여는 소수성 다공질 막의 표면상에서는 수득될 수가 없다.
상기 언급한 플라즈마 처리를 받은 소수성 다공질 막의 표면상에는 활성 시이드(seed)가 형성된다. 다공질 막이 폴리올레핀계 물질로 이루어지면, 예들 들어 반응성이 높은 알칼라디칼이 기질상에 주로 형성된다. 이러한 라디칼은 산소와 접촉시 과산화물로 빠르게 전환된다. 친수성 단량체가 플라즈마의 부재하에 기체상태로 상기에 언급한 플라즈마 처리를 받은 다공질 막에 공급될 때, 다공질 막의 표면상의 활성 시이드가 단량체를 소비하기 시작하며 소위 그라프트 중합화가 진행된다. 그라프트 중합화는 산소에 대한 노출 대신 알킬 라디칼을 사용하여 진행시킬 수가 있다. 활성 시이드가 과산화물로 전환된 후에 과산화물은 열로 인해 분열되거나 금속 이온과 함께 라디칼의 생성을 유도하여 그라프트 중합화를 촉진시킨다.
그라프트 중합화에 있어서, 친수성 단량체는 그라프트 중합화가 부적당할 정도로 격렬하게 진행하여 그라프트 층의 전재가 결국 다공질 막의 외부 표면 부위와 친수성 단량체가 용액의 형태로 공급된 막 내부에 분포된 소공의 표면 사이에서 진행할 수 없으므로 기체 상태로 공급된다. 플라즈마를 사용하여 중합화를 개시하느 기구에 있어, 플라즈마에 노출시킨 후에 단량체의 체인 중합화 반응을 액상 또는 고형의 상태에서 수행하는 것이 일반적으로 통상적인 방법이다. 놀랍게도, 체인 중량화 반응은 단량체가 기체 상태 또는 기체상으로 공급될 때 조차도 충분하면서도 이롭게 진행된다는 것이 증명된다.
그라프트 중합화는 0℃~80℃, 바람직하게는 2℃~60℃ 범위내의 온도에서 10-2~104Torrs, 바람직하게는 1~103Torrs 범위내의 압력하게 수행하는 것이 일반적이다. 그라프트 반응은 10초~60분내에 완결된다. 그라프트 중합체의 양은 그라프트 중합체의 양은 그라프트 중합화의 조건(예, 온도, 단량체 농도 및 반응시간) 및 플라즈마 조사의 조건에 의해 조절할 수가 있다. 그라프트 비는 2-30%, 바람직하게는 5-15% 범위내로 낮출 것이 요구된다. 그라프트 비가 2% 이하이면, 소수성 다공질 막에 친수성을 충분하게 부여치 못할 가능성이 있다. 그라프트 비가 30%를 초과하게 되면, 소수성 다공질 막 본래의 소공 직경이 소공 및 막을 막을 정도까지 작아지며, 젖었을 때 팽창되어 변형될 가능성이 있다.
본 발명에서 기질로써 사용되는 소수성 다공질 막은 소수성 고분자 물질로 형성되어 물을 함유할 수 없는 소공을 갖는 다공질 막 계이다. 본 발명은 원료 물질의 종류에 의해서 소수성 다공질 막을 구별하지는 않는다.
그러나, 소수성 막의 물질은 우수한 물리적 및 화학적 특징을 나타낼 것이 요구된다. 물질의 대표적인 예를 들면, 폴리에틸렌 및 폴리프로필렌 같은 폴리올레핀류, 나일론 6 및 나일로 6, 6와 같은 에티렌디클로로디플루오로에틸렌 공중합체 폴리아미드류와 같은 부분적으로 클로르화되거나 플루오르화된 폴리올레핀유, 폴리에틸렌테레프탈레이트와 같은 포화 폴리에스테르류 및 폴리아크릴로니트릴 및 폴리비닐리덴 폴루오라이드를 들 수 있다.
상기에 기재한 다른 유용한 물질들 가운데서, 폴리올레핀류, 부분적으로 클로르화거나 플루오르화된 폴리올레핀유 및 폴리비닐리덴 플루오라이드가 바람직한 것으로 증명된다. 그들중 가장 바람직한 것은 포리프로필렌이다. 소수성 다공질 막은 활성 시이드가 낮은 플라즈마로 처리한 다공질 막의 내부에 있는 소공의 표면상에 충분하게 생성될 수 있을 정도일 것이 요구된다. 막은 20-250㎛ 범위내의 두께를 갖을 것이 요구된다.
막의 벽 두께가 250㎛를 초과하면, 플라즈마로 처리하여 친수성을 부여하는 것이 막 내부의 소공의 표면상에 조차 도달될 수 없게될 가능성이 있다. 다공질 막 내부에 있는 소공은 0.05-1.0㎛, 바람직하게는 0.2-0.5㎛ 범위내의 직경을 갖을 것이 요구된다.
그라프트 체인의 형성에 사용되는 친수성 단량체는 불포화 비닐 또는 알릴기를 갖고, 친수성을 나타내며, 및 정상적인 라디칼 중합화를 하도록 요구되는 단량체이다. 상기의 목적에 부합되는 단량체로는 아크릴계, 메타크릴계, 불포화 아미드계, 디엔계 및 트리엔계 단량체가 있다. 상기의 단량체의 대표적인 에를들면, (메트)아크릴아미드류, N-메틸(메트)아크릴아미드류, N.N-디메틸(메트)아크릴아미드류, N,N-메틸에틸(매트)아크릴아미드류, N,N-디에틸(메트)N,N-메틸에틸(매트)아크릴아미드류, (메트)아크릴산류, 2-히드록시에틸(메트)아크릴아미드류, N,N-디에틸아미노에틸(매트)아크릴아미드류, N-비닐 피롤리돈, p-스티렌 슬폰산, 비닐 슬폰산, 2-메타크로릴로일 옥시에틸 슬폰산, 3-메타크릴로일 옥시-2-히드록시프로필 슬폰ㅅ산, 알릴 슬폰산, 메타크릴 슬폰산, 및 2-아크릴아미드-2-메킬프로판 슬폰산이 있다. 상기에 언급한 친수성 단량체 가운데, 소수성 다공질 막용 소수성 고분자 물질에 대한 친화성을 갖고 높은 중합화 속도를 나타내는 단량제 가운데, 소수성 다공질 막용 소수성 고분자 물질에 대한 친화성을 갖고 높은 중량화 속도를 나타내는 단량체가 특히 바람직하다. 소수성 다공성 막이 폴리프로필렌으로 이루어진 경우, 예를들어 N, N-디메틸 아크릴아미드가 단량체들 가운데서 가장 바람직한 것으로 증명된다. 최종적으로 제조된 친수성 다공질 막이 생의학적인 분야에서 혈장분리 장치에 이용되도록 고안된 경우, 예를들어 친수성 단량체로부터 제조된 중합체는 생체-적용성에서 우수해야 할 것이 요구된다.
이러한 관점에서 볼 때, 친수성 단량체가 2-히드록시 메타크릴레이트일 것이 특히 요구된다.
위에서 열거한 친수성 단량체는 독립적으로 사용되도록 항상 요구되는 것은 아니다. 임의로, 상기의 친수성 단량체를 둘 또는 그 이상의 혼합물 형태로 사용하기도 한다. 친수성 단량체는, 배합된 불포화 단량체가 친수성 부여의 목적을 어렵게 하지 않을 정도로 소수성 불포화 단량체를 부분적으로 배합하기도 한다.
상기에 기술한 수득된 본 발명의 친수성 다공질 막은 얇고 균일한 그라프트 층이 표면을 완전하게 덮기 위해 소수성 다공질 막의 표면에 결합되는 배우를 갖는다. 따라서, 친수성 다공질 막은 기질로서 사용되는 소수성 다공질 막 본래의 우수한 물리적 및 화학적 성질을 갖을 수 있는 동시에, 그의 표면 상에 형성된 그라프트 층에 기인한 완전한 친수성을 획득한다.
또한, 그라프트 층은 얇고 균일하기 때문에, 소수성 다공질 막 본래의 소공 특성이 저하되지는 않는다. 따라서, 생성된 친수성 소공 막은 0.5-8㎏/㎠ 범위내에 포점을 갖는다. 포점이 8㎏/㎠을 초과하면, 친수성 다공질 소공 막은 충분히 높은 물 투과성을 갖기가 어렵다. 막은 1% 이하의 팽윤비를 갖는다. 상기의 다공질 막을 장치내에 끼워서 사용할 때, 처리시 유로를 통한 액체의 완만한 흐름을 방해할 정도로 심하게 표면상에 함께 주름이 생길 수는 없다.
본 발명의 친수성 다공질 막은 다양한 수용성 매질내에서 정밀 여과막, 한의여과막, 역 삼투막, 또는 투석막으로서 또는 고속 장치용 물질로서 그의 소공 특성에 따라 광범위하게 사용할 수 있다. 혈장분리 막은 본 발명의 친수성 다공질 막으로 발견된 특히 바람직한 용도를 갖는 .
제1도는 혈장분리 막으로서 본 발명의 친수성 다공질 막을 갖는 혈장분리 장치의 일례를 나타낸 다이아그램이다. 혈액 유입부분 1과 여과 잔류물 유출 부분 2로 구성된 측면판 3 및 여액 유출 부문 4로 구성된 측면판 5, 직사각형 틀의 패킹부분 6b 내에 빈 공간을 갖는 판 6을 형성하는 유로, 혈장분리 막 7, 및 망상의 여액 유로 부분 8a 주위가 패킹 8b로 구성된 판 8을 구성하는 여액 유로 및 상기에 언급한 것들을 물이 새지 않게 눌러 완전하게 고정시켜 놓음으로써 혈장분리 장치를 얻는다. 혈장분리 막 7과 같이, 상기에 기재한 바와같이 제조된 본 발명의 친수성 다공질 막이 사용된다. 혈장분리 막 7로서 사용되는 친수성 다공질 막은 소수성 다공지 막의 표면상에 친수성 단량체의 그라프트 체인을 형성하여, 제조된 막이 젖었을 때 1% 이하의 팽윤비와 0.6-2㎏/㎠ 범위내의 포점을 나타내는 정도로 표면에 완전한 친수서을 부여하여 수득된다.바람직하게는 본 발명의 막은 혈장 총 단백질의 95% 이상의 투과율을 갖는다. 본 분리 장치에서 혈액 유입 부분 1을 통해 내부로 흐르는 혈액이 빈 공간 6a를 통해 흘러혈장분리 막 7을 통해서 여과된다. 혈액의 혈구 부분을 여파잔류물 유출 부분 2를 통해 방출하여 여액으로서 생성된 혈장을 흐름 부분 8a를 통해 통과시키고 여액 유출 부분 4를 통해 방출한다.
여과의 수행이라는 면에서, 상기에 기재한 혈장분리 장치는 다음과 같은 특징을 갖는다. 혈장분리 막은 획득한 완전한 친수성을 갖고 0.6-2㎏/㎠ 범위내의 포점을 나타내기 때문에, 혈장의 여과에 필요한 매우 큰 용량을 제공하고 임의의 혈장 단백질 성분의 분리없이 안전하게 여과를 시킨다.
상기 종류의 혈장분리 장치에서, 여과막의 벽 전단속도가 증가하고 여과력이 혈액 유로의 두께가 감소함에 비례하여 증가된다. 제1도에 나타난 분리장치에서 혈액의 허용 흐름에 필요한 빈 공간 6a로 구성된 유로의 두께는 판 6을 형성하는 유로의 두께를 감소시킴으로써 감소될 수가 있다.
예를들어 셀롤로오스 아세테이트로 이루어진 다공질 막과 같은 종래으 혈장분리 막의 경우에, 상기의 막은 높은 팽윤비를 갖고 젖었을때 변형하는 경향이 있기 때문에 혈액의 통과시 필요한 빈 공간 6a에 의해 형성된 유로는 판 6을 형성하는 유로의 두께에 의해 결정된 그의 두께를 유지하지 못하며 유로의 두께는 채널링 현상을 유도하는 정도까지 심하게 변화된다. 대조적으로 본 발명의 혈장분리 장치에서는, 혈장분리 막은 막이 젖었을 때 1% 이하의 팽윤비를 나타내는 정도까지 바람직한 높은 치수 안정성을 갖는다. 유로는 여과에 필요한 용량을 제공할 정도로 얇은 두께일 때 조차도, 유로는 균일한 두께를 갖으며 채널링 현상을 유도할 가능성은 없다. 따라서 제1도에서 나타낸 매우 단순한 구조의 기구는 바람직한 높은 여과력을 갖는다.
또한 분리 장치내에 사용되는 혈장분리 막에 있어, 소수성 다공질 막의 표면상에 놓인 그라프트 층이 예를들어 2-히드록시에틸 메타크릴레이트와 같은 높은 혈액 적응성을 갖는 친수성 단량체로 형성될 때, 처리시 그라프트 층이 혈액의 보조성분을 활성화시킬 가능성은 거의 없다.
제1도는 본 발명의 혈장분리 장치의 일례로서 가장 기본적인 배위를 갖는 혈장분리 장치를 나타낸다. 본 발명은 그의 형식, 방식 등에 의해 혈장분리 장치를 구별하지는 않으며, 단 본 분리장치는 최소한 그의 혈장분리 막으로서 상기에 기술한 친수성 다공질 막을 갖을 것이 요구된다. 물론 본 분리장치는 혈장분리 막을 복수로 이용해도 좋다.
이하에, 실시예를 들어 본 발명을 보다 상세하게 설명한다.
이하의 실시예 및 대조예를 나타낸 수치는 다음의 각각의 정의를 근거로 하여 결정된 것이다.
[그라프트 비]
그라프트된 막을 약 50시간 동안 적당한 용매로 세척하고, 진공 건조시켜 무게를 잰다(Wg), 그라프트된 막의 무제, Wg와 그라프트 전의 막의 무게 Wo 사이의 차이를 근거로 그라프트 비를 결정하며, 이하와 같다.
[팽윤비]
열 기게적 분석기(세이고 렌시 고교 k.k. 제품, 상품명 "TMA")에, 길이가 150㎜이고 폭이 5㎜인 축정용 시료를 놓고, 증류수에 침지시켜 3분동안 5g의 물체 아래에 놓고, 젖은 길이, 1w를 측정한다. 길이, Lw와 젖기 전의 길이, lo 사이의 차리를 근거로 팽윤비를 결정하며, 아래와 같다.
[포점]
본 성질은 ASTM F 316에 의해 정의된 방법에 따라서, 이소프로필 알코올을 사용하여 결정한다.
[혈장내의 총 단백질 투과성]
제조된 막을 100㎜Hg이하의 여과압하에서 소의 혈액을 여과시험하여 막이 혈장 총 단백질의 90% 이상의 투과율을 안정하게 나타내는가의 여부를 결정한다.
식중, Cin 은 혈액 유로 상의 농도를 의미하여 Cf는 여액상의 농도를 의미한다.
이와같은 경우에 있어 농도는 뷰렛법으로 측정한다.
[실시예 1]
폴리프로필렌, 액체 파라핀 및 첨가물들을 합하여 막 생성용 도우프를 제조하고, T 다이를 통해 압출시킨 다음, 액체 파라핀의 배출용 용매내에 용해시킨 후, 이어서 열적으로 고정시킨다. 결과적으로 0.45㎛의 평균 소공 직경 및 80-120㎛의 벽두께를 갖는 소수서 다공질 막이 수득된다. 상기 다공질 막에서 직격 47㎜의 원을 뚫고 그 자리의 내부에 내부 직경 30㎜의 반응 용기를 관의 벽과 닿지 않도록 위치시킨다. 0.1Torr의 아르곤 기체하에서, 13,56㎒의 고주파 발생기와 연결시킨 유도코일에 의해 발생되는 100W의 전력을 걸어주어 플ㄹ라즈마를 생성시킨 다음, 10초동안 막에 방사한다. 플라즈마를 방사한 후, N, N-디메틸 아클리아미드 기체를 반응 용기내에 도입하고, 1Torr하의 20℃ 온도에서 10분동안 그라프트 반응을 진행시킨다. 결과적으로 수득된 막을 속슬레(soxhlet)추출기내에서 메탄올을 사용하여 50시간 동안 세정하고, 시료로서 사용하기 위한 목적으로 진공 건조시킨다. 상기 시료는 13.25%의 그라프트비를 나타내었으며, 막의 내부 깊숙이까지 친수성을 갖도록 하는 것으로 나타났다. 0.7㎏/㎠의 압력하에서 2.2㎖/분.㎠의 투과율을 나타났다. 생성된 친수성 다공질 막은 그의 포점이 1.32㎏/㎠이고 및 팽윤비는 0.2% 이하로서 고도로 만족스러운 치수 안정성을 나타내었다.
[실시예 2~8 및 대조예 1]
실시예 1에서 사용한 것과 동일한 폴리프로필렌의 다공짊 가에 대하여 이하의 표 1에 나타내는 조건들하에 실시예 1에서와 동일한 친수성 부여처리를 수행한다. 결과적으로 수득된 모든 친수성 다공질 막은 모두 일정하게 그들 내부 깊숙이까지 친수성을 획득하는 것으로 나타났다. 비교하기 위한 목적(대조액)으로 친수성을 부여 처리이전의 폴리프로필렌의 다공질 막의 픔질도 또한 표1에 나타낸다. 제2도는 친수성 다공질 막 직각에서의 포점과 그라프트비 사이의 관계를 나타낸다.
15.4%의 그라프트비를 갖는 실시예 4의 시료의 막구조 및 친수성 부여 처리를 실시하지 않은 대조예 1의 시료의 막구조를 전자 현미경하에서 조사하였다.
제3도는 실시예 4의 시료의 외부표면의 전자 광현미경 사진(×500)이고 제4도는 실시예 4의 시료 단면의 전자 광현미경 사진(×500)이며, 제5~6도는 실시예 4의 시료 단면의 전자 광현미경 사진이고, 제7도는 대조에 1의 시료의 외부표면의 전자 광현미경 사진(×500)이며, 제8도는 대조에 1의 시료 단면의 전자 광현미경 사진(×500)이고, 및 제9~10도는 대조예 1의 시료단면의 전자 광현미경 사진(×2000)이다. 이들전자 광현미경 사진들로부터 병백히 알 수 있는 바와같이, 막 구조는 그라프트 처리전과 후에 실질적으로 전혀 변화가 없는 것으로 나타났다
또한, 제13도는 실시에 4의 시료의 팽윤비(0.18%)의 TMA측정결과 수득된 데이터를 나타낸다.
[표 1]
[대조 예2]
실시예 1에서 사용한 것가 동일한 폴리프로필렌의 다공질 막에 대하여, 폴라즈마를 방사하고자 하는 막을 반응 용기내에 그의 외부표면이 반응 용기의 벽과 접촉하도록 위치시키는 것을 제외하고는, 실시예 1의 방법에 따라 친수성 부여처리를 수행한다. 결과적으로 수득된 시료는 막의 외부 측면에만 친수성을 획득하는 것으로 나타났다. 막 내부에 존재하는 소공들의 표면은 물에 대한 막의 친수성이 0으로서 전혀 친수성을 획득하지 못했다.
[대조예 3]
실시예 1에서 사용한 것과 동일한 폴리프로필렌의 다공질 막에 대조예 2의 방법에 다라 플라자마를 방사한다. 플라즈마 방사 후, 다공질 막을 N, N-디메틸 아크릴아미드 용액내에 위치시키고, 40℃에서 20분 동안 그 안에 방치하여 그라프트 반응을 진행시킨다.
수득된 시료는 67.5%의 그라프트비를 나타냈다. 친수성이 막내부에까지 부여되지는 않았다. 따라서, 막은 물에 재하여 0의 투과율을 나타냈다. 표면(×500)을 나타내는 제11도 및 단면(×500)을 나타내는 제12도의 전자 광현미경 사진으로부터 알 수 있는 바와같이, 외부 표면상에 존재하는 소공들은 그라프트화된 N, N-디메틸 아크릴아미드로 충전되어 있고, 외부 표면 가까이 위치하는 다공성 기질 부분은 그라프트 층에 의해 외형이 손실되었다.
[실시예 9]
폴리프로필렌의 다공질 막 대신에, 소수성 다공질 막으로서의 폴리비닐리덴 플로오라이드의 AS 다공질막(소공 직경 : 0.45㎛, 벽 두께 : 130㎛)에 대하여 실시예 1의 공정에 따라 친수성 부여처리를 실시한다. 결과로서, N, N-디메틸 아크릴아미드가 다공질 막에 그라프트화되어 12.4%의 그라프트비를 갖는 친수성 다공질 막이 생성되었다. 상기 막은 1.54㎏/㎠의 포점, 0.17%의 팽윤비 및 압력 0.7㎏/㎠하에서 투과율 2.1㎖분 ㎝를 나타냈다.
[실시예 10]
실시예 1의 방법으로 평균 소공직경 0.45㎛ 및 벽 두께 160㎛를 갖는 소수성 다공질 막을 수록하였다. 상기 다공질 막으로부터 6×7㎝의 사각형을 절단하고, 상기 부위의 내부에 내부 직경 30㎜의 반응용기를 , 반응용기의 벽과 닿지 않도록 위치시킨다. 0.1Torr의 아르곤 기체하에서 13.56㎒의 고주파 발생기와 연길시킨 유도코일에 의해 발생된 10WE의 전력을 걸어주어 플라즈마를 생성시킨 후, 막이 3초 동안 방사한다. 플라즈마 방사 후, N, N-디메틸 아크릴아미드 기체를 반응관내에 도입하고, 1Torr하의 20℃온도에서 30분 동안 방치하여 그라프트 중합을 진행시킨다. 결과적으로 수득된 막을 속슬래 추출기내에서 용매로서 메탄올을 사용하여 50분 동안 세정한 후, 진공 건조시킨다. 결과로서, 7.6%의 그라프트비를 갖는 것으로 나타났다. 팽윤비를 0.2% 이하로 나타났다. 전자현미경하에서 관찰한 결과, 그라프트 전과 후에 있어서 막구조는 실질적으로 변화하지 않은 것으로 나타났다.
수득된 다공질 막을, 두이은 친수성 부여처리를 수행하지 않은채로, 제1도에 예시한 바와 같이 구조된, 혈류 통로 두께가 0.035㎝인 혈장분리 장치내에 위치시켰다. 소의 혈액을 도입율을 변경시키면서 단일-패스 방법으로 막에 통과시켜 혈장의 단백질 성분에 대한 막의 투과율을 측정하였다. 이하의 표2에 나타낸 결과들로부터 알 수 있는 바와같이, 막은 90% 이상의 안정한 투과율을 나타냈다. 시험 기간 중에, 막은 용혈 현상을 유발하지 않았으며, 극히 바람직스러운 혈장 투과기능을 발휘하였다.
셀룰로오스 아세테이트로 만들어졌으며 평균 소공직경 0.45㎛ 및 벽 두께 160㎛를 갖는 시판(도료 로시 가부시끼가이샤) 혈장분리 막은 1.44+0.98%(m=10)의 팽윤비를 갖는 것으로 나타났다. 대표적인 일련의 TMA 데이터를 제13도내에 점섬으로 나타낸다. 상기 혈장분리 장치를 실시예 10에서 사용하여 이용할 경우, 혈장분리 막이 수분에 의해 지나치게 팽윤 및 증대되어 혈류 통로를 차단하여 채널링을 유발한다.
[대조예 5]
그라프트 중합을 수행하지 않으면서 실시에 10의 방법을 실시하여 제조한 폴리프로필렌의 다공질 막을 실시예 10에서와 동일한 장치내에서 사용한다. 결과로서, 혈장여과용 기능을 전혀 갖고 있지 않으며 혈장의 총단백질에 투과율은 0으로 나타났다.
[표 2]
[실시예 11 및 대조예 6~7]
제1도에 나타낸 바와같이 구조되어져 있으며 폴리카르보네이트 하우징(housing)을 설비한 혈장분리 장치내에 실시예 1에서와 동일한 방법으로 그 위에 중합된 N,N-디메틸 아크릴아미드 그라프트(그라프트 비 9.915)의 폴리프로필렌다공질 막(실시예 11), 친수성 부여 처리를 실시하지 않은 폴리프로필렌의 다공질 막(대조예 6) 및 대조예 4의 막과 유사한 셀룰로오스 아세테이트의 다공질 막(대조에 7) 각각을 37℃에서 1시간 동안 혈청과, 막의 접촉면적을 혈청 단위 ㎖당 약 25㎠로 고정시킨 상태에서 접촉시킨다. 혈청에 대하여 RIA법을 이용하여 C3a농도를 시험하였다. 결과는 이하의 표3에 나타낸다.
[표 3]
상술한 바와같이 본 발명은 소수성 다공질 막의 표면상에 친수성 단랴체의 그라프트 체인을 형성시킴으로서 상기 표면에 완전한 친수성을 제공하여 생성된 막이 젖었을 때 1% 이하의 팽윤비 및 0.5-8㎏/㎠ 범위이내의 포점을 나타내도록 하는 제조방법을 특징으로 하는 친수성 다공질 막에 관한 것이다. 따라서, 친수성 다공질 막의 사용시의 치수 안정성 및 강도와 같은 물리적 특성면에 있어서 우수하고, 막 품질의 붕괴에 대하여 강한 내성을 지니며, 광범위한 용도의 실용성을 갖는다. 나아가, 본 발명의 친수성 다공질 막내에서 다공질 단량체의 그라프트 체인이 상술한 바와같이 다공질 막의 외부표면은 그대로 변형되지 않은 상태로 유지시키면서 소수성 다공질 막에 플라즈마를 방사하고 이어서 기체 상태의 친수성 단량체를 그라프트 중합시킴으로써 다공질 막의 표면에 형성된 것일 겨우, 이를 그라프트 체인은 상술한 다공질 막에 의해 부여된 친수성에 기인하여 안정하게 유지되며 유용한 기능을 발휘하게 된다. 또한, 본 발명의 친수성 다공질 막은 그라프트비가 2-30% 범위 이내이고, 소수성 다공질 막이 폴리올레핀 도는 부분 염소화 또는 불소화된 폴리올레핀, 바람직하기로는 폴리프로필렌 또는 폴ㄹ리비닐리덴 플루오라이드로 이루어져 있으며, 막의 두께가 20-250㎛ 범위이내이고, 친수성 단량체가 N, N-디메틸 아크릴아미드이며, 팽윤비가 0-0.5% 범위이내이고 및 젖었을때의 포점이 0.8-2.0㎏/㎠ 범위이내일 경우보다 바람직한 물리적 특성을 및 보다 만족스러운 소공 특성을 갖는다.
본 발명은 또한 소수성 다공질 막의 외부 표면에 변형되지 않은 상태에서 플라즈마를 방사하고, 이어서 기체 상태의 친수성 단량체를 도입하여 친수성 단량체를 다공질 막의 표면상에 그라프트 중합시키는 단계들로 구성되는 소수성 다공질 막의 제조방법과도 관련된 것이다. 따라서, 본 발명은 대규모의 설비를 필요로 하지 않으면서 안전하고 저렴하게 상술한 바와같은 탁월한 특성들을 소유하는 친수성 다공질 막을 제공할 수 있다. 이와같은 방법으로, 소수성 다공질 막의 두께가 20-250㎛ 범위내이고, 소수성 다공질 막이 그외 외부 부위상에 피층을 갖지 않으며, 소수성 다공질 막이 0.05-1.0㎛ 범위이내의 평균 소공직경을 갖고, 소수성 다공질 막이 폴리올레핀 또는 부분염소화 또는 불소화 폴리올레핀, 바람직하기로는 폴리프로필렌 또는 폴리비닐리덴 플루오라이드로 이루어진 것이며, 및 친수성 단량체가 N, N-디메틸 아크릴아미드일 경우 보다 확실하게 보다 바람직한 특성들을 갖는 소수성 다공질 막을 제조할 수 있다.
나아가, 본 발명은 소수성 다공질 막의 표면상에 친수성 단량체의 그라프트 체인을 형성시킴으로써 상기 표면에, 생성된 막이 젖었을 때 1% 이하의 팽윤비 및 0.6-2.0㎏/㎠ 범위 이내의 포점을 나타내도록 할 정도의 완전한 친수성을 부여하는 제조방법으로 제조된 소수성 다공질 막을 혈장분리 막으로 갖음을 특징으로 하는 혈장분리 장치와도 관련되어 있다. 이러한 혈장분리 장치는 고도의 혈장 여과 기능 및 혈장의 총단백질에 대한 높은 투과성을 갖으며, 친수성을 부여하기 위한 임의의 또다른 처리를 필요로 함이 없이 혈액을 혈액구 성분과 혈장 성분으로 완전히 분리하므로, 따라서 질병의 치료용으로서 및 수혈시 유용하게 이용할 수 있다. 상기 장치에 있어서 혈장의 총 단백질 성분에 대한 투과율이 90%를 초과할 정도로 높을 경우보다 바람직한 성능을 발휘한다. 친수성 단량체가 2-히드록시에틸 메타크릴레이트 또는 N, N-디메틸 아크릴아미드일 겨우에 처리시 혈액의 보충 성분을 활성화시키는 장치의 기능이 저하된다.
Claims (27)
- 소수성 다공질 막의 표면상에 소수성 단량체의 그라프트 체인을 형성하여 상기의 표면에 완전한 친수성을 부여함으로써 제조된 막이 젖었을 때 1% 이하의 팽윤비와 0.5-8㎏/㎠ 범위내의 포점을 나타내도록 하는 제조방법을 특징으로 하는 친수성 다공질 막.
- 제1항에 있어서, 상기의 소수성 단량체의 그라프트 체인이, 변형되지 않은 상태에서 상기의 다공질 막의 외부표면에 플라즈마를 조사하여 기체상태의 상기의 친수성 단량체를 도입하여 상기의 외부 표면상에 그라프트 중합시킴으로써 상기의 친수성 다공질 막의 표면상에 형성하는 친수성 다공질 막.
- 제1항에 있어서, 그라프트 비가 2-30% 범위내인 친수성 다공질 막.
- 제1항에 있어서, 상기의 소수성 다공질 막이 폴리올레핀 또는 부분적으로 클로르화되거나 플루오르화된 폴리올레핀으로 이루어진 친수성 다공질 막.
- 제4항에 있어서, 상기의 소수성 다공질 막이 플로프로필렌으로 이루어진 친수성 다공질 막.
- 제1항에 있어서, 상기의 소수성 다공질 막이 폴리비닐리덴 플루오라이드로 이루어진 친수성 다공질 막.
- 제1항에 있어서, 상기 막의 두께가 20-250㎛ 범위내인 친수성 다공질 막.
- 제1항에 있어서, 상기의 소수성 다공질 막이 그의 외부 표면 부위상에 피층을 갖지 않는 친수성 다공질 막.
- 제1항에 있어서, 상기의 친수성 단량체가 N, N-디메틸 아크릴아미드인 친수성 다공질 막.
- 제2항에 있어서, 상기의 막이 젖었을 때 0-0.5% 범위내의 팽윤비와 0.8-2㎏/㎠의 범위내의 포점을 나타내는 친수성 다공질 막.
- 변형되지 않은 상태에서 소수성 다공질 막의 외부표면에 플라즈마를 조사한 후, 기체 상태의 친수성 단량체를 도입하여 상기의 친수성 단량체를 상기의 다공질 막이 표면상에 그라프트 중합시킬 수 있게 하는 단계에 의한 친수성 다공질 막의 제조방법.
- 제11항에 있어서, 상기의 소수성 다공질 막이 20-250㎛ 범위내의 벽 두께를 갖는 친수성 다공질 막.
- 제11항에 있어서, 상기의 소수성 다공질 막이 폴리올레핀 또는 부분적으로 클로로화되거나 플로오르화된 폴리올레핀으로 이루어진 친수성 다공질 막의제조방법.
- 제11항에 있어서, 상기의 소수성 다공질 막이 폴리올레핀 또는 부분적으로 클로로화되거나 플로오르호된 폴리올레핀으로 이루어진 친수성 다공질 막의 제조방법.
- 제14항에 있어서, 상기의 소수성 다공질 막이 폴리프로필렌으로 이루엊니 친수성 다공질 막의 제조방법.
- 제11항에 있어서 상기의 소수성 다공질 막이 폴리비닐리덴 플루오라이드로 이루어진 친수성 다공질 막의 제조방법.
- 제11항에 있어서, 상기의 친수성 단량체가 N,N-디메틸 아클리아미드신 c친수성 다공질 막의 제조방법.
- 제11항에 있어서, 상기의 그라프트 중합을 그라프트 비가 2-30% 범위내인 조건하에서 수행하는 친수성 다공질 막의 제조방법.
- 소수성 다공질 막의 표면상에 친수성 단량체의 그라프트 체인을 형성하여 상기의 표면에 완전한 친수성을 부여함으로써, 제조된 막이 젖었을 때 1% 이하의 팽윤비와 0.5-8㎏/㎠ 범위내의 포점을 갖는 친수성 다공질 막을 혈장분리 막(7)으로 갖는 것을 특징으로 하는 혈장분리 장치.
- 제19항에 있어서, 상기의 혈장분리 막(7)이 혈액 혈장의 총 단백질 서분으 90% 이상의 투과율을 갖는 혈장분리 장치.
- 제19항에 있어서, 상기의 혈액 혈장분리 막(7)이, 변형되지 않은 상태에서 소수성 다공질 막의 외부표면에 플라즈마를 조사한 후, 기체형태의 친수성 단량체를 도입하여 상기의 소수성 다공질 막의 표면상에 그라프트 중합시켜 상기의 소수성 다공질 막의 표면상에 결과적으로 형성된 그라프트 체인이 상기의 친수성 다공질 막에 완전한 친수성을 부여하기 위해서 상기의 소수성 다공질 막에 완전한 친수성을 부여한 친수성 다공질 막인 혈장분리 장치.
- 제19항에 있어사, 상기의 소수성 다공질 막이 폴리올레핀 또는 부분적으로 클로르화되거나 플루오르호된 폴리올레핀으로 이루어진 혈장분리 장치.
- 제22항에 있어서, 상기 소수성 다공질 막이 플리프로필렌으로 이루어진 혈장분리 장치.
- 제19항에 있어서, 상기의 소수성 다공질 막이 폴리비닐플루오라이드로 이루어진 혈장분리 장치.
- 제19항에 있어서, 상기의 친수성 단량체가 2-히드록시에틸메타크릴레이트 또는 N, N-디메틸 아크릴아미드인 혈장분리 장치.
- 제19항에 있어서, 상기의 막이 20-250㎛ 범위내의 벽 두께를 갖는 혈장분리 장치.
- 제19항에 있어서, 상기의 친수성 다공질 막이 젖었을 때 0.-05% 범위내에 팽윤비와 0.8-2㎏/㎠ 범위내의 포점을 나타내는 혈장분리 장치.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP103,011 | 1986-05-07 | ||
| JP61103011A JPS62262705A (ja) | 1986-05-07 | 1986-05-07 | 親水性多孔質膜、その製造方法およびこの親水性多孔質膜を用いた血漿分離装置 |
| JP103011 | 1999-03-08 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR870010887A KR870010887A (ko) | 1987-12-18 |
| KR900008692B1 true KR900008692B1 (ko) | 1990-11-27 |
Family
ID=14342700
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1019870004476A KR900008692B1 (ko) | 1986-05-07 | 1987-05-07 | 친수성 다공질 막, 그의 제조방법 및 친수성 다공질 막을 이용한 혈장분리 장치 |
Country Status (6)
| Country | Link |
|---|---|
| US (1) | US4845132A (ko) |
| EP (1) | EP0249513B1 (ko) |
| JP (1) | JPS62262705A (ko) |
| KR (1) | KR900008692B1 (ko) |
| CA (1) | CA1313441C (ko) |
| DE (1) | DE3769011D1 (ko) |
Families Citing this family (87)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4906374A (en) * | 1986-12-23 | 1990-03-06 | Pall Corporation | Filtration media with low protein adsorbability |
| DE3886405T2 (de) * | 1987-08-06 | 1994-05-05 | Terumo Corp | Hydrophile, poröse membran, verfahren zu deren herstellung und plasmatrennungsgerät. |
| WO1989002303A1 (en) * | 1987-09-11 | 1989-03-23 | Japan As Represented By Director General, Agency O | Hydrophilic polypropylene porous membrane, process for its production, and apparatus for separating blood plasma |
| US5186835A (en) * | 1987-09-11 | 1993-02-16 | Agency Of Industrial Science And Technology | Porous hydrophilic polypropylene membrane, method for production thereof, and blood plasma separation apparatus |
| IL88081A0 (en) * | 1987-10-20 | 1989-06-30 | Pall Corp | Device and method for depletion of the leucocyte content of blood and blood components |
| CA1329559C (en) * | 1988-03-03 | 1994-05-17 | Keiji Naoi | Leukocyte separator and method of making the same |
| US5423989A (en) * | 1988-05-19 | 1995-06-13 | Chemtrack, Inc. | Plasma forming device |
| CA1314666C (en) * | 1988-06-13 | 1993-03-23 | Kazuo Toyomoto | Selectively ion-adsorptive, porous membrane |
| JPH064713B2 (ja) * | 1988-07-22 | 1994-01-19 | テルモ株式会社 | 生体適合性材料 |
| JPH0257270A (ja) * | 1988-08-24 | 1990-02-27 | Terumo Corp | 多孔質膜からの有機化合物の溶出抑制方法 |
| US4959150A (en) * | 1988-09-26 | 1990-09-25 | Pall Corporation | Fluid treatment system having low affinity for proteinaceous materials |
| US5202025A (en) * | 1989-04-12 | 1993-04-13 | Terumo Kabushiki Kaisha | Porous membrane and method for preparing the same |
| US5061751A (en) * | 1989-06-02 | 1991-10-29 | Exxon Chemical Patents Inc. | Vinylpyrrolidone grafted polyolefins in polymer blends and composites |
| US5180492A (en) * | 1989-07-21 | 1993-01-19 | Terumo Kabushiki Kaisha | Hydrophilic porous material sterilizable with gamma-ray |
| JP2898665B2 (ja) * | 1989-09-28 | 1999-06-02 | テルモ株式会社 | 血漿分離膜およびそれを用いた血漿分離器 |
| US5244578A (en) * | 1989-09-28 | 1993-09-14 | Terumo Kabushiki Kaisha | Blood plasma-separating membrane and blood plasma separator using the membrane |
| US6022902A (en) * | 1989-10-31 | 2000-02-08 | The United States Of America As Represented By The Administrator Of The National Aeronautics And Space Administration | Porous article with surface functionality and method for preparing same |
| US5158721A (en) * | 1989-11-30 | 1992-10-27 | Millipore Corporation | Porous membrane formed from interpenetrating polymer network having hydrophilic surface |
| US5079272A (en) * | 1989-11-30 | 1992-01-07 | Millipore Corporation | Porous membrane formed from interpenetrating polymer network having hydrophilic surface |
| AU7034791A (en) * | 1989-12-29 | 1991-07-24 | University Technologies International Inc. | Methods for modelling tertiary structures of biologically active ligands including agonists and antagonists thereto and novel synthetic antagonists based on angiotensin |
| US5258127A (en) * | 1990-07-27 | 1993-11-02 | Pall Corporation | Leucocyte depleting filter device and method of use |
| US5104729A (en) * | 1990-08-20 | 1992-04-14 | Monsanto Company | Process for surface modifying a support membrane and product produced |
| DE69119688T2 (de) * | 1990-10-10 | 1997-01-16 | Minnesota Mining & Mfg | Pfropfcopolymere und Pfropfcopolymer-/Protein- Zusammensetzungen |
| FR2668077B1 (fr) * | 1990-10-22 | 1992-12-04 | Commissariat Energie Atomique | Membrane d'osmose inverse ou de nanofiltration et son procede de fabrication. |
| US5217627A (en) * | 1990-11-06 | 1993-06-08 | Pall Corporation | System and method for processing biological fluid |
| US5198505A (en) * | 1991-04-11 | 1993-03-30 | Pall Corporation | Uniform polyvinylidene difluoride membranes |
| US5443743A (en) * | 1991-09-11 | 1995-08-22 | Pall Corporation | Gas plasma treated porous medium and method of separation using same |
| CA2074671A1 (en) * | 1991-11-04 | 1993-05-05 | Thomas Bormann | Device and method for separating plasma from a biological fluid |
| US5275738A (en) * | 1992-06-10 | 1994-01-04 | Pall Corporation | Filter device for acids and process for filtering inorganic acids |
| DE4223151C2 (de) * | 1992-07-14 | 1994-11-10 | Loesche Gmbh | Verfahren zur Mahlung von Rohbraunkohle |
| GB9311988D0 (en) * | 1993-06-10 | 1993-07-28 | Pall Corp | Device and method for separating plasma from a blood product |
| US5433745A (en) * | 1993-10-13 | 1995-07-18 | Allergan, Inc. | Corneal implants and methods for producing same |
| US5632773A (en) * | 1994-05-03 | 1997-05-27 | Allergan, Inc. | Biostable corneal implants |
| US5630946A (en) * | 1995-02-15 | 1997-05-20 | Pall Corporation | Method for processing a biological fluid including leukocyte removal in an extracorporeal circuit |
| US5843789A (en) * | 1995-05-16 | 1998-12-01 | Neomecs Incorporated | Method of analysis of genomic biopolymer and porous materials for genomic analyses |
| US6241886B1 (en) * | 1995-06-09 | 2001-06-05 | Toyo Boseki Kabushiki Kaisha | Plasma separation filter |
| EP0748636B1 (en) * | 1995-06-14 | 2003-08-27 | Hisamitsu Pharmaceutical Co., Inc. | Interface for iontophoresis |
| US5837365A (en) * | 1996-04-08 | 1998-11-17 | The Penn State Research Foundation | Hydrophilic polypropylene membranes |
| DE19643566C2 (de) * | 1996-10-22 | 2001-06-07 | Geesthacht Gkss Forschung | Verfahren und Vorrichtung zur Membranmodifizierung |
| US6083393A (en) * | 1997-10-27 | 2000-07-04 | Pall Corporation | Hydrophilic membrane |
| US6187391B1 (en) * | 1997-12-26 | 2001-02-13 | Agency Of Industrial Science & Technology | Method for modifying one surface of textile fabric or nonwoven fabric |
| US6036659A (en) | 1998-10-09 | 2000-03-14 | Flexsite Diagnostics, Inc. | Collection device for biological samples and methods of use |
| WO2000032294A1 (en) * | 1998-12-02 | 2000-06-08 | Lg Chemical Ltd. | Methods for reforming polymer surface for improved wettability |
| TW581709B (en) | 1999-10-22 | 2004-04-01 | Asahi Kasei Corp | Heat-resistant microporous film |
| AU2005211551B2 (en) * | 1999-10-23 | 2008-08-07 | Corning Incorporated | Binding surface |
| GB9925016D0 (en) * | 1999-10-23 | 1999-12-22 | Univ Sheffield | Binding surface |
| EP1110524A1 (en) * | 1999-12-23 | 2001-06-27 | The Procter & Gamble Company | Liquid handling member with a membrane assembly comprising a membrane wetting region |
| AU2001237000A1 (en) | 2000-02-15 | 2001-08-27 | Hollingsworth And Vose Company | Melt blown composite hepa filter media and vacuum bag |
| US6451386B1 (en) * | 2000-08-30 | 2002-09-17 | Pti Advanced Filtration, Inc. | Modified polymer having improved properties and process for manufacturing same |
| WO2002043940A1 (en) * | 2000-11-29 | 2002-06-06 | Exigent | A method of altering and preserving the surface properties of a polishing pad and specific applications therefor |
| US6579604B2 (en) | 2000-11-29 | 2003-06-17 | Psiloquest Inc. | Method of altering and preserving the surface properties of a polishing pad and specific applications therefor |
| US7059946B1 (en) | 2000-11-29 | 2006-06-13 | Psiloquest Inc. | Compacted polishing pads for improved chemical mechanical polishing longevity |
| EP1385597A1 (en) * | 2001-05-02 | 2004-02-04 | HOLLINGSWORTH & VOSE COMPANY | Filter media with enhanced stiffness and increased dust holding capacity |
| KR100805977B1 (ko) * | 2001-08-01 | 2008-02-25 | 아사히 가세이 메디컬 가부시키가이샤 | 다층 미다공막 |
| US7456025B2 (en) * | 2001-08-28 | 2008-11-25 | Porex Corporation | Sintered polymer membrane for analyte detection device |
| KR100409028B1 (ko) * | 2001-10-29 | 2003-12-06 | 전흥재 | 면역인자흡수체가 그라프트된 백혈구 제거필터 제조방법및 이에 의해 제조된 필터 |
| AU2002359432A1 (en) * | 2001-11-21 | 2003-06-10 | Porex Corporation | Discrete hydrophilic-hydrophobic porous materials and methods for making the same |
| US20030203696A1 (en) * | 2002-04-30 | 2003-10-30 | Healey David Thomas | High efficiency ashrae filter media |
| KR100529209B1 (ko) * | 2002-08-28 | 2005-11-17 | 한국과학기술연구원 | 세포 친화성이 향상된 생분해성의 조직 공학용 다공성고분자 지지체의 제조방법 |
| AU2003301399B2 (en) * | 2002-10-18 | 2006-07-06 | Asahi Kasei Medical Co., Ltd. | Microporous hydrophilic membrane |
| AU2003289072A1 (en) * | 2002-12-12 | 2004-06-30 | Asahi Kasei Kabushiki Kaisha | Virus-removing bag and virus-removing method using the same |
| KR100682346B1 (ko) * | 2003-05-15 | 2007-02-15 | 충남대학교산학협력단 | 대기압 플라즈마 연속 표면 처리 공정으로 개질한 거대다공성 고분자 이온 교환체, 이의 제조방법 및 용도 |
| US20050055885A1 (en) * | 2003-09-15 | 2005-03-17 | Psiloquest | Polishing pad for chemical mechanical polishing |
| CN101039744B (zh) * | 2004-08-13 | 2010-05-05 | 麦克马斯特大学 | 包含非交联的胶凝聚合物的复合材料 |
| DE602005024991D1 (de) | 2004-09-30 | 2011-01-05 | Univ Mcmaster | Verbundwerkstoff mit übereinandergelagerten hydrophilen beschichtungen |
| SI22048A (sl) * | 2005-06-02 | 2006-12-31 | Institut "Jozef Stefan" | Metoda in naprava za lokalno funkcionalizacijo polimernih materialov |
| US20070059473A1 (en) * | 2005-08-19 | 2007-03-15 | Sun Medical Technology Research Corp. | Sheet-like covering member used for implant medical device |
| KR101312217B1 (ko) * | 2006-12-28 | 2013-09-27 | 주식회사 효성 | 친수화된 분리막의 제조방법 |
| US8288118B2 (en) | 2007-09-19 | 2012-10-16 | Becton, Dickinson And Company | Method of analyzing various surface chemistries for culturing a given cell line |
| WO2009067087A1 (en) * | 2007-11-23 | 2009-05-28 | Hyflux Membrane Manufacturing (S) Pte Ltd | Hydrophilization of permeable hydrophobic polymer membranes |
| DE102008015386B4 (de) * | 2008-03-20 | 2015-10-01 | Sartorius Stedim Biotech Gmbh | Bioreaktor |
| FR2931081B1 (fr) * | 2008-05-14 | 2010-06-25 | Direction Et Pirorites | Dispositif de filtration d'un liquide complexe tel que du sang, notamment applicable a un autotransfuseur |
| JP2011523965A (ja) * | 2008-05-30 | 2011-08-25 | スリーエム イノベイティブ プロパティズ カンパニー | リガンド官能化基材 |
| US20100212272A1 (en) * | 2009-02-24 | 2010-08-26 | Hollingsworth & Vose Company | Filter media suitable for ashrae applications |
| US8377672B2 (en) * | 2010-02-18 | 2013-02-19 | 3M Innovative Properties Company | Ligand functionalized polymers |
| EP2889625B1 (en) * | 2010-03-03 | 2016-09-14 | 3M Innovative Properties Company | Ligand guanidinyl functionalized polymers |
| US20140083628A1 (en) | 2012-09-27 | 2014-03-27 | Velico Medical, Inc. | Spray drier assembly for automated spray drying |
| AU2012327218C1 (en) * | 2011-11-30 | 2015-12-24 | Wellstat Diagnostics, Llc. | Filtration Module |
| CN102512990B (zh) * | 2012-01-10 | 2014-05-14 | 苏州汇龙膜技术发展有限公司 | 内支撑聚偏氟乙烯中空纤维膜的制备方法 |
| US10239021B2 (en) | 2012-06-14 | 2019-03-26 | Teledyne Scientific & Imaging, Llc | Fouling resistant coating for filtration membranes and methods of producing and using same |
| CN103861465B (zh) * | 2014-03-21 | 2015-12-30 | 东华大学 | 一种疏水性分离膜材料表面超亲水改性的方法 |
| US9561184B2 (en) | 2014-09-19 | 2017-02-07 | Velico Medical, Inc. | Methods and systems for multi-stage drying of plasma |
| US20190247805A1 (en) * | 2016-11-04 | 2019-08-15 | Asahi Kasei Medical Co., Ltd. | Porous membrane and method for manufacturing porous membrane |
| US11998861B2 (en) | 2022-09-15 | 2024-06-04 | Velico Medical, Inc. | Usability of a disposable for a spray drying plasma system |
| US11975274B2 (en) | 2022-09-15 | 2024-05-07 | Velico Medical, Inc. | Blood plasma product |
| US11841189B1 (en) | 2022-09-15 | 2023-12-12 | Velico Medical, Inc. | Disposable for a spray drying system |
| US12083447B2 (en) | 2022-09-15 | 2024-09-10 | Velico Medical, Inc. | Alignment of a disposable for a spray drying plasma system |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| BE604952A (ko) * | 1960-06-15 | 1961-12-13 | ||
| JPS5644098B2 (ko) * | 1973-12-28 | 1981-10-17 | ||
| US4353799A (en) * | 1976-05-19 | 1982-10-12 | Baxter Travenol Laboratories, Inc. | Hydrophobic diffusion membranes for blood having wettable surfaces |
| JPS52148564A (en) * | 1976-06-04 | 1977-12-09 | Kansai Paint Co Ltd | Method of surface treatment of base material of hydrophobic high polymer for hydrophilization |
| JPS53134876A (en) * | 1977-04-30 | 1978-11-24 | Sumitomo Electric Ind Ltd | Production of hydrophilic composite construction |
| JPS5417978A (en) * | 1977-07-11 | 1979-02-09 | Sumitomo Electric Ind Ltd | Hydrophilic and porous composite structure and its production |
| JPS55106239A (en) * | 1979-02-05 | 1980-08-14 | Japan Atom Energy Res Inst | Preparation of hydrophilic membrane based on polyethylene membrane |
| JPS5923566B2 (ja) * | 1979-08-01 | 1984-06-02 | 東レ株式会社 | 放電グラフト重合法 |
| DE3032380A1 (de) * | 1979-09-04 | 1981-03-19 | Celanese Corp., 10036 New York, N.Y. | Verfahren zur herstellung hydrophiler mikroporoeser folien |
| DE3147579A1 (de) * | 1980-12-02 | 1982-08-05 | Sumitomo Chemical Co., Ltd., Osaka | "hohlfasermembran zur trennung von gasen und verfahren zu ihrer herstellung" |
| US4331719A (en) * | 1980-12-23 | 1982-05-25 | Desoto, Inc. | Low temperature curing thermosetting coatings for solvent-sensitive moldings |
| JPS5893734A (ja) * | 1981-11-30 | 1983-06-03 | Asahi Chem Ind Co Ltd | 親水性ポリフツ化ビニリデン樹脂多孔膜の製造方法 |
| JPS59152913A (ja) * | 1983-02-21 | 1984-08-31 | Yoshito Ikada | 高分子材料表面改質法 |
| JPS59160504A (ja) * | 1983-03-03 | 1984-09-11 | Kanebo Ltd | 親水化分離膜及びその製造方法 |
| JPS6086132A (ja) * | 1983-10-19 | 1985-05-15 | Mitsubishi Rayon Co Ltd | 多孔質膜の親水化処理法 |
| US4618533A (en) * | 1984-11-30 | 1986-10-21 | Millipore Corporation | Porous membrane having hydrophilic surface and process |
| US4695592A (en) * | 1986-01-07 | 1987-09-22 | Mitsubishi Rayon Co., Ltd. | Hydrophilized porous membrane and production process thereof |
| JPH06104753B2 (ja) * | 1986-02-04 | 1994-12-21 | 旭化成工業株式会社 | 非吸着性親水性中空糸状多孔膜 |
-
1986
- 1986-05-07 JP JP61103011A patent/JPS62262705A/ja active Granted
-
1987
- 1987-05-05 CA CA 536428 patent/CA1313441C/en not_active Expired - Lifetime
- 1987-05-06 US US07/046,449 patent/US4845132A/en not_active Expired - Lifetime
- 1987-05-07 DE DE8787401053T patent/DE3769011D1/de not_active Expired - Lifetime
- 1987-05-07 KR KR1019870004476A patent/KR900008692B1/ko not_active IP Right Cessation
- 1987-05-07 EP EP19870401053 patent/EP0249513B1/en not_active Expired - Lifetime
Also Published As
| Publication number | Publication date |
|---|---|
| DE3769011D1 (de) | 1991-05-08 |
| EP0249513B1 (en) | 1991-04-03 |
| JPH0570493B2 (ko) | 1993-10-05 |
| JPS62262705A (ja) | 1987-11-14 |
| KR870010887A (ko) | 1987-12-18 |
| CA1313441C (en) | 1993-02-09 |
| EP0249513A2 (en) | 1987-12-16 |
| US4845132A (en) | 1989-07-04 |
| EP0249513A3 (en) | 1988-01-07 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR900008692B1 (ko) | 친수성 다공질 막, 그의 제조방법 및 친수성 다공질 막을 이용한 혈장분리 장치 | |
| EP0352199B1 (en) | Hydrophilic material and method of manufacturing the same | |
| US5202025A (en) | Porous membrane and method for preparing the same | |
| US5049275A (en) | Modified microporous structures | |
| US4743258A (en) | Polymer materials for vascular prostheses | |
| EP0257997B1 (en) | Plugged microporous film | |
| US4501785A (en) | Hydrophilized membrane of porous hydrophobic material and process of producing same | |
| CA1333236C (en) | Hydrophilic microporous membrane and process for preparing same | |
| EP0640007A4 (en) | MICROPOROUS AND HYDROPHILIC POLYOLEFIN MEMBRANE. | |
| WO2010096429A1 (en) | Hydrophilic porous substrates | |
| JP2725094B2 (ja) | 分離膜、その製造方法及び分離方法 | |
| EP1016425B1 (en) | Process for producing hydrophilized polyolefins and leukocyte-removing material thereof | |
| AU5613700A (en) | Polyvinylidene difluoride membranes and methods for making such membranes | |
| EP0566754B1 (en) | Heat-resisting porous membrane, hydrophilized heat-resisting porous membrane and production processes thereof | |
| CA2287157C (en) | Introducing functional groups to a polymer | |
| JPH0427891B2 (ko) | ||
| JPH0774289B2 (ja) | 親水性四弗化エチレン樹脂多孔質膜の製造方法 | |
| EP0164468A2 (en) | Porous membrane | |
| JP2004154613A (ja) | 機能性多孔膜の製造方法 | |
| JP3313176B2 (ja) | 分離膜、その製造方法及び分離方法 | |
| WO2009067087A1 (en) | Hydrophilization of permeable hydrophobic polymer membranes | |
| JPS6142303A (ja) | 多孔質膜 | |
| Thomes | The influence on protein adsorption of surface chemistry and surface roughness produced via the pulsed plasma technique | |
| Woerly et al. | Poly (Glyceryl Methacrylate) Hydrogels-Effect of Composition and Crosslinking Density on Structure and Release of Dextran as a Model Macromolecule | |
| JPS6383111A (ja) | 吸水性材料 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| G160 | Decision to publish patent application | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant | ||
| FPAY | Annual fee payment |
Payment date: 19941101 Year of fee payment: 5 |
|
| LAPS | Lapse due to unpaid annual fee |