KR870001237B1 - 요소 합성법 - Google Patents
요소 합성법 Download PDFInfo
- Publication number
- KR870001237B1 KR870001237B1 KR8205292A KR820005292A KR870001237B1 KR 870001237 B1 KR870001237 B1 KR 870001237B1 KR 8205292 A KR8205292 A KR 8205292A KR 820005292 A KR820005292 A KR 820005292A KR 870001237 B1 KR870001237 B1 KR 870001237B1
- Authority
- KR
- South Korea
- Prior art keywords
- ammonia
- carbon dioxide
- urea
- urea synthesis
- liquid
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C273/00—Preparation of urea or its derivatives, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups
- C07C273/02—Preparation of urea or its derivatives, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups of urea, its salts, complexes or addition compounds
- C07C273/04—Preparation of urea or its derivatives, i.e. compounds containing any of the groups, the nitrogen atoms not being part of nitro or nitroso groups of urea, its salts, complexes or addition compounds from carbon dioxide and ammonia
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
내용 없음.
Description
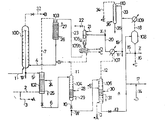
제1도는 본 발명의 방법의 실시에 적합한 시스템의 일예를 나타낸 도면이고,
제2도는 본 발명의 실시태양을 설명하기 위한 도면이다.
* 도면의 주요부분에 대한 부호의 설명
100 : 요소합성관 107 : 저압흡수기
102 : 스트립퍼 108 : 진공농축기
104 : 중앙 분해컬럼 109 : 응축기
106 : 저압 분해컬럼 110 : 정류컬럼
본 발명은 우레아 합성 공정에서 우레아 합성 유출액의 조성을 조절하기 위한 방법에 관한 것으로, 더 구체적으로는 본 발명은 우레아 합성관으로부터의 온도와 고압에서 방출되는 유출액을 정기적으로 자동으로 샘플링하여 유출액 중 암모니아 함량과 암모늄 카바메이트 함량을 정량적으로 분석한 다음 이 결과 수득된 분석 데이터에 따라서 공정을 조정하므로서 요소 합성의 조작을 원하는 조작 상태로 유지시킴을 특징으로 하는 순환식 요소 합성 방법에 관한 것이다.
요소 합성은 공업적으로는 출발 물질로 암모니아와 이산화탄소를 사용하여 고온 고압하에 수행된다. 합성관에 송입되는 암모니아, 이산화탄소의 비율은 각각 암모늄 카바메이트 요소 등의 화합물 형태이든 그 자체이든 간에 모두 암모니아, 이산화탄소로 환산하여 몰비로 2.5/1.0 내지 5.5/1.0으로 되어 있다. 즉 암모니아는 이산화탄소에 대하여 당량(몰비=2/1)이상 합성관으로 송입된다. 하기 반응과 같이 2몰의 암모니아를 1몰의 이산화탄소와 결합시켜 요소를 제조하는 것은 공지이다.
이 몰비는 요소의 합성률을 결정하는 가장 중요한 인자의 하나로서 이 비율의 고저에 따라서 각각 다른 특징을 갖는 공정이 나타나게 된다. 그런데 이 중요한 암모니아, 이산화탄소의 몰비의 검출은 종래의 공정에 따라서 각양 각색으로 수행할 수 있다. 예를들면 비교적 낮은 이산화탄소에 대한 암모니아의 몰비를 사용하는 스트리핑 공정으로서는 일본 특공소 제25253/1974호에 기재되어 있는 바와같이 고압 카바메이트 응축기에서의 가스축의 암모니아, 이산화탄소 비를 가스 크로마토그라피에 의하여 검출하고 이에 의하여 가스축에 대한 액측에서의 비율을 추정하고 그리하여 합성관 중에서의 비율을 간접적으로 추정하는 방법이다.
또한 몰비가 약 4.0/1.0인 높은 비의 공정에서는 합성관에의순환액의 량과 분석된 조성, 이에 적용되는 암모니아, 이산화탄소의 량에 의하여 합성관에서의 이산화탄소에 대한 암모니아의 몰비를 추정하는 방법이 채용되고 있다. 합성관 중의 이산화탄소에 대한 암모니아의 몰비는 공지의 방법으로 직접 결정되므로, 샘플을 채취하여 결과를 수득하는데 장시간이 요구된다. 그러므로 합성관 중의 몰비를 원하는 값까지 연속적으로 따르지 않는다.
상기 언급한 이산화탄소에 대한 암모니아의 몰비를 결정하는 시간 소비과정은 정확하고 빠르게 원하는 값의 몰비를 얻지 못하므로 조작자는 원하는 값과 다소 차이있는 비를 얻는다. 그러나 산업상 고 정확조절에 대한 욕망으로서, 이 욕망은 요소 합성법의 개량으로 인한 것으로 신속한 분석과 응답조작에 의하여 상술한 문제를 해결할 필요가 있다.
본 발명의 목적은 요소합성관 내에서 제조한 조 요소합성액 중의 이산화탄소에 대한 암모니아의 몰비를 신속히 조정하여 원하는 값까지 유지시키게 할 수 있게 한다.
본 발명은 요소합성의 특정에 기기분석의 자동화를 교묘하게 결합시켜서 공정상의 중요 부분, 예를들면 요소합성관 출구액 중의 미반응의 과잉 암모니아 및 암모늄 카바메이트 함유율을 검출하고 이에 응답하여 합성 및/또는 그 주변의 조작을 관리함으로써 그 용액중의 암모니아, 이산화탄소 몰비를 소망의 값으로 조절하는 것을 발견하였다.
따라서, 본 발명은 하기의 순환식 요소 합성법을 제공한다. 본 발명의 순환식 요소 합성법은 상기 주어진 요소합성 반응식에 따라 통상적인 요소합성 압력과 온도에서 요소합성관 중의 당량 또는 과잉량의 암모니아와 이산화탄소를 반응시켜 미반응 이산화탄소와 암모니아를 포함하는 조 요소합성액을 수득하여 이 요소 합성액을 가열 및/또는 요소 합성액을 이산화탄소 또는 1단계 이상의 가압 단계에서 불활성 가스로 스트립핑시켜 우레아 합성액으로부터 미반응 이산화탄소와 암모니아를 포함하는 조 요소 합성액을 수득하므로서 요소 합성액으로부터 요소 수용액을 회수하여 잔류 NH3와 암모늄 카바메이트를 포함하는 액인 흡수액으로 각 압력단계에서 분리된 최소한 미반응 이산화탄소와 암모니아의 부분을 흡수하며, 이 액은 CO2와 NH3흡수 단계보다도 더 낮은 압력에서 행한 선행 흡수 단계에서 제조한 것이고 최종 흡수액을 요소 합성관에 순환시키고, 임의로는 액체 암모니아로서 과잉 암모니아를 회수하여 이를 요소 합성용으로 순환, 재 이용함을 포함한다. 본 발명의 개량법은 상기 언급한 요소 합성법의 필요한 단위조작 단계에서 순환반응 스팀을 규칙적으로 샘플링하는 것을 포함하는데, 여기서 이 스팀을 분석하여 원하는 단위조작단계를 조정하고 스팀 중의 포함된 암모니아와 암모늄 카바메이트의 양을 분석할 수 있는 지침 또는 신호를 수득할 수가 있어 필요할 때 이 수득된 데이터를 단위조작 단계에 원하는 상태로 유지하며 수득할 수 있도록 유효한 조작변형을 이용할 수 있다.
본 발명은 이후 더 상세히 서술된다.
요소의 합성 수율은 요소 합성관의 여러 조작 조건으로 결정된다. 경험에 따르면 합성관 속에 충진된 이산화탄소에 대한 물의 몰비와 온도는 각각 0.3 내지 약 0.7이고 175°내지 205℃이다. 상기 범위에서, 다른 조건이 변화되지 않는 한 요소합성 수율의 어떤 특별한 변화는 없다. 비록 이산화탄소에 대한 물의 몰비도 중요하지만 이산화탄소에 대한 암모니아의 몰비가 더 중요하여 만족한 합성을 수득할 수 있다. 이산화탄소에 대한 암모니아의 몰비로서 전자는 이 비에 의하여 부차적으로 결정되며 압력은 온도와 이산화탄소에 대한 암모니아의 몰비에 의하여 거의 결정된다. 따라서, 합성관 출구액의 조성은 이산화탄소에 대한 암모니아의 몰비에 의하여 거의 결정된다고 할 수 있다.
종래 요소 및 뷰레트를 함유하는 암모니아-암모늄 카바메이트-수개의 용액의 분석에서 요소 및 뷰레트는 각각의 표준 분석법에 의하여, 암모니아 및 암모늄 카바메이트 형태의 질소는 암모니아로서 분석하며, 암모늄 카바메이트 형태의 탄소는 이산화탄소로서 분석하여 이들의 값으로부터 전 이산화탄소에 대한 전 암모니아의 몰비를 구하였다. 특히 합성관 출구액에 대하여는 샘플링 자체가 위험을 수반하기 때문에 일상적으로는 행해지지 않으며 다른 류의 유량, 분석값등으로부터 간접적으로 추정하였다.
그런데 합성관 출구액의 조성은 송입전 이산화탄소에 대한 전 암모니아 몰비에 의하여 거의 결정된다고 설명하였는데 더 이 조성을 상세히 조사한 결과 다음과 같은 결과를 발견하여 본 발명에 이르렀다. 즉, 전 이산화탄소에 대한 전 암모니아 비에 의하여 요소합성률이 결정됨은 미반응의 과잉 암모니아 및 암모늄 카바메이트의 각 비율도 결정됨을 뜻한다. 엄밀하게는 다른 조건도 영향이 있지만 중요하지 않다. 더우기 (2) 암모늄 카바메이트 형태의 이산화탄소에 대한 (1) 암모늄 카바메이트 형태의 암모니아에 과잉의 암모니아를 합한 값에 대한 값의 비 R1은 전 이산화탄소에 대한 전 암모니아 비 R2에 비교하여 큰 값이 된다. 예를들면 어떤 합성 조건에서는 R1의 변화에 대하여 R2는 다음과 같이 된다.
R14.4 8.2 13.2
R23.0 4.0 5.0
R1/R21.47 2.05 2.64
필요하다면, R1및 R2의 실험치로부터 본 분야에 숙련된 사람들은 주어진 일련의 분석 조건하에서 또는 실험치 R1및 R2로부터 주어진 R2에 대한 R1의 값을 측정할 수 있는 수학적 수식을 유도하여 그라프 보간법에 의해 R2값을 구할 수 있다.
이는 R2의 약간의 변화의 영향이 확대되어서 R1이 되어서 나타남을 뜻하며 이는 공정 조정상 대단히 바람직하다. 또 R1의 측정에 허용되는 오차는 R2의 오차에 대한 것보다 많아도 된다. 즉 합성관 출구액 중의 과잉 암모니아 및 암모늄 카바메이트를 분석하여 상술의 R1을 알면 전 이산화탄소에 대한 전 암모니아를 알 수 있게 된다. 따라서, 샘플링을 포함한 자동분석계를 이용함으로써 신속한 응답조작이 가능하게 된다.
즉, 구체적으로는 다음과 같이 하여 목적이 달성된다. 조정의 대상으로 하는 공정류 예로서 합성관에서는 출구액의 극히 일부를 샘플링용으로 분기한다. 그 양은 물론 분석용에는 충분하며 그리고 분기에 의한 문제가 일어나지 않을 정도의 적은 양이다. 예를들면 합성관 출구액의 경우는 분석용에는 충분하지만 분기 후 방냉에 의한 폐색이 있어서는 안된다. 분기류에 곧 희석용의 순수를 주입한다. 그 량은 분석정도를 저하시키지 않을 정도로 충분한 통상 샘플 용량으로 10∼1000의 범위이다. 희석된 분기 샘플류는 약 0∼1㎏/㎠(게이지)로 감압하여 잘 혼합시킨다. 필요하다면 기화하지 않도록 냉각한다. 혼합후의 희석액 중 분석에 불필요한 대부분의 양은 플랜트의 적당한 개소에 보내진다. 분석에 필요한 0.5∼50㎖가 자동분석계에 인도된다.
이 분석계는 예를들면 다음과 같이 하여 분석을 실시한다. 즉 과잉 암모니아 및 암모늄 카바메이트 형태의 암모니아A는 암모늄 이온으로서, 암모늄 카바메이트 형태의 이산화탄소B는 탄산 또는 중탄산이온으로서 취급되어 분석된다. 즉 희석된 상술의 샘플에 대하여A는 산에 의한 PH 적정에 의하여 정량된다.B는 이 적정의 도중에서의 pH의 급격한 변화가 있으면 소위 2단계법에 의하여도 정량할 수 있다. 또는 다른 샘플에 의하여 탄산가스용 이온전극을 사용하여 직접 측정하는 방법,A의 측정 전에 샘플액의 전도도를 측정하는 등의 방법에 의하여도 정량된다. 물론A의 정량을 이온전극법에 의하여 행하여도 무방하다. 합성관의 온도, 압력이 일정하다면 합성액 중의 전 이산화탄소에 대한 전 암모니아 비 R2는 얻어진A/B인 R1의 함수이므로 이로부터 R2를 계산할 수 있다.
또 요소는 비색법, 예를들면 p-디메틸아미노벤즈알데히드의 염산 산성하에서 발색시키는 방법에 의하여 정량할 수 있으므로 소망한다면 이도 실행하면 전 이산화탄소에 대한 전 암모니아 비 R2, 따라서 합성률도 구할 수가 있다. 따라서, 이와같이 하면 나머지는 물로서의 분석값도 얻어진다. 요소의 분석을 하지 않으면 이들 분석계에 의하여 1회의 분석은 거의 5∼10분으로 실시할 수 있다. 그리고 분석계로서는 상기의 것에 한정되지 않음은 더 말할 나위 없다.
이상으로부터 대상 공정류의 조성을 거의 연속적으로 알 수 있으므로 이에 응답하여 필요한 조작을 변화시키면 소망의 조성이 빨리 안정한 상태로 얻어지게 된다. 물론 자동 분석계로부터 얻어지는 조성을 제어기에의 입력으로 하여 필요한 조작 변화량을 출력으로 하는 자동 제어방법도 가능하다.
상기에서, 본 발명은 요소 합성관에 적용된 것으로 설명될 수 있다. 본 발명은 예로서 제1도의 분해 및 미반응 물질용 회수시스템 또는 정제 시스템과 같은 기타 요소 합성관에 동일하게 적용될 수 있다. 제1도를 참조하면 라인(1)을 통하는 액체 암모니아 및 라인(4)을 통하는 암모니아, 이산화탄소 및 물의 가스-액체 혼합물을 요소 합성관(100) 속에 충진시킨다. 요소 합성관(100)은 160∼200㎏/㎠G와 170∼200℃의 온도에서 작동된다. 요소, 암모니아, 이산화탄소 및 물로 구성된 요소 합성액을 수득한다. 다시 말해서, 불활성 가스를 포함하는 가스성 혼합물을 라인(32)을 통해 요소 합성관(100)의 상단에서 제거하고 중간 압력 흡수기의 냉각기(105b)까지 보낸다. 상기 요소 합성액을 라인(5)을 통해서 동일한 압력의 스트립퍼(102)내에 여러단의 시이브 트레이가 있는 정류대역의 상단에 도입한다. 요소 합성액을 정류대역을 통해 하강시키면서 암모니아, 이산화탄소 및 물을 포함하는 가스성 혼합물의 상류와 상호적으로 접촉시켜 요소합성액 중의 과잉 암모니아를 가스혼합물 중의 이산화탄소와 교환시키고 요소 합성액내의 이산화탄소에 대한 암모니아 비를 정류대역 하부의 스트립 가능범위의 값까지 조정한다. 이후 요소 합성액을 적하필름 가열관을 통해 하향시키면서, 미반응 물질을 라인(24)을 통해 공급되는 고압 스팀으로 가열시켜 요소 합성액으로부터 스트립핑시켜 라인(25)을 통해 방출시키고, 라인(2)을 통해 가압 이산화탄소를 충진시킨다. 스트립퍼(102)의 하부로부터 요소, 암모니아, 이산화탄소, 고온의 물로 구성된 용액을 수득한다.
상기 용액을 즉시 감압시켜 라인(6)을 통해 10∼25㎏/㎠ 게이지의 압력에서 분출시켜 이를 중간 압력 분해컬럼(104) 속에 도입시킨다. 중간압력 분해컬럼(104)을 여러 시이브 트레이단으로 형성하고 가열대역을 시이브 트레이 하부에 위치시킨다.
이것은 라인(28)을 통해 공급된 고압스팀에 의해 가열되어 라인(29)을 통하여 미리 미반응 물질까지 방출된다. 미반응 물질의 분리후 용액을 요소, 물 및 소량의 미반응 암모니아 및 미반응 이산화탄소로 구성한다. 이 용액을 라인(10)을 통해 1∼5㎏/㎠G의 압력까지 가압시켜 저압 분해컬럼(106) 속으로 도입된다. 저압 분해컬럼(106)은 여러 시이브 트레이단으로 형성시켜 가열대역을 시이브 트레이 하부에 위치시키고 스트립핑 대역은 가열대역 하부에 위치시킨다. 스팀은 라인(30)을 통해 가열대역에 공급시켜 라인(31)을 통해 방출시킨다. 이산화탄소를 라인(3)을 통해 스트립핑 대역속에 도입시킨다. 저압력 분해컬럼(106)내에 우레아 용액 중에 잔존하는 미반응 암모니아와 미반응 이산화탄소를 실질적으로 분리시킨다.
저압 분해컬럼(106)으로부터 방출되는 요소용액을 감압시켜 진공농축기(108) 속에 주입시켜 요소슬러리 형태로 농축한다. 회수라인(15)은 라인(16)으로부터 라인(13) 속에 인도된다.
소량의 암모니아, 이산화탄소 및 요소를 함유하는 수증기는 라인(18)을 통해 진공농축기(108)로 방출되어 응축기(109)내에서 응축되어 암모늄 카바메이트와 요소의 회수용액을 형성한다. 이 용액을 일부는 라인(33)을 통해 정류컬럼(110) 속에 주입되어 라인(34)으로부터 방출되는 암모니아, 이산화탄소, 물, 수증기의 가스성 혼합물로 분리되어 여기의 물은 라인(35)으로부터 방출된다. 가열용 스팀은 라인(36)을 통해 컬럼(110)의 하부에 주입된다.
암모늄 카바메이트와 요소의 회수용액의 잔존부분은 라인(19)을 통하여 저압흡수기(107) 속에 주입된다. 한편으로는 라인(12)을 통해 저압 분해컬럼(106)으로부터 방출되는 가스성 혼합물은 회수용액 속에 흡수 되어 저압 흡수액을 형성한다.
저압 흡수액은 라인(20)을 통해 중간 압력 흡수기의 흡수컬럼(105a)의 상부 부분으로 도입된다. 중간압 분해컬럼(104) 중에 분리된 암모니아, 이산화탄소 및 수증기의 가스성 혼합물과 요소합성관(100)의 상단 내에 분리된 불활성 가스를 라인(11)과 라인(32)을 각각 통해 중간압 흡수기의 냉각기(105b) 속에 주입시킨다. 냉각기(105b) 속에서 주입가스 속에 포함된 이산화탄소와 암모니아의 대부분을 흡수컬럼(105a)으로부터 용액속에 흡수시킨다. 냉각기(105b)내에서 발생되는 흡수열을 진공농축기(108)으로부터 라인(16)을 통해 주입된 요소 슬러리에 의해 제거시켜 약 100℃의 온도를 유지시킨다.
라인(14)내의 가열요소 슬러리 중에서, 요소생성물에 상응하는 량을 라인 (17)을 통해 최종단계에 전달한다. 잔류물을 진공농축기(108)에 되돌리고 이의 물의 량을 증발시킨다.
냉각기(105b) 속에 존재하는 소량의 비흡수 가스를 흡수관(105a)의 충진층을 통해 상승시킨다. 상승시키는 과정에서, 미흡수된 가스는 저압흡수기(107)로부터 라인(20)을 통해 도입된 저압흡수액과 라인(21)을 통해 도입된 물 속에 흡수시켜 냉각기(105b) 속에 적가시킨다. 이 결과 불활성 가스만을 라인(22)을 통해 컬럼(105a)의 상단으로부터 제거시킨다. 냉각기(105b)로부터 중간-압력 흡수액을 수득한다.
이 중간 압력 흡수액을 가압시킨 다음 라인(23)을 통해 카바메이트 응축 기(103)에 주입시킨다. 스트립퍼(102)내에 분리된 가스성 혼합물을 카바메이트 응축기(103)에 주입시키고 여기의 가스혼합물의 일부를 응축시켜 흡수하여 요소합성관(100)으로부터의 요소 합성액이 예비 결정온도를 갖도록 한다. 흡수에 의해 발생되는 열은 라인(27)으로부터 저압스팀으로 회수된다(공급수는 라인(26)을 통해 도입된다). 이 결과 수득된 흡수액은 가스혼합물과 같은 비흡수가스와 함께 라인(4)을 통해 요소합성관(100)까지 재순환된다. 카바메이트 응축기(103)내에 회수된 저압스팀은 저압 분해컬럼(106) 및 최종 단계뿐 아니라 정류컬럼(110)내에서 사용된다.
제1도에 나타낸 샘플링라인, 샘플, 성분분석 및 분석 목적을 하기 표에 나타내었다.
여러 요소 합성법 중에서, 본 발명의 방법은 특히 스트립핑 공정에 적합하다. 즉 스트립핑 공정에서는 과잉 암모니아는 직접 개량 가능한 상태에서는 순환하고 있지 않으므로 일본 특공소 제25253/1974호에도 기재되어 있는 바와같이 간접적인 방법이 종래 채용되어 왔으나 본 발명을 적용하면 직접적이 되므로 이로부터 얻어지는 이익은 크다. 본 발명의 방법에 의하여 예를들면 소망의 이산화탄소에 대한 암모니아 몰비가 4에 대하여 분석 결과로부터 환산하여 3.8로 산출된 경우에는 차 0.2에 다른 양에 의하여 암모니아 공급량을 증가하든가, 이산화탄소의 공급량을 감소함으로써 분석값과 조작량을 곧 대응시켜서 소망의 이산화탄소에 대한 암모니아 몰비에 빠른 시간에 수족시킬 수가 있다. 또한 본 발명은 신속성에 의하여 프랜트의 출발시에는 특히 유효하며 종래보다도 짧은 시간에 소망 조성의 합성관 출구액을 얻을 수가 있다.
실시예
요소생산량 : 100t/일
제2도를 참조하여, 합성간(201)에는 라인(211)으로부터 예열된 액체 암모니아가 라인(221)으로부터는 고압 카바메이트 콘덴서(203)로부터의 암모늄 카바메이트 용액 및 암모니아, 이산화탄소, 물의 혼합가스가 가스액 혼상으로 함께 순환되었다. 합성관(1)에서는 그 정부가 190℃로 유지되고 합성관(201) 정부에서의 합성액의 소망 조성값은 전 이산화탄소에 대한 전 암모니아 몰비가 4.0이었다. 합성관(201) 정부에서는 방식공기를 포함하는 불활성 가스가 합성액으로부터 합성 압력 180㎏/㎠(게이지)의 상태에서 분리되어서 라인(225)을 거쳐서 중압계에 감압, 배출되었다. 불활성 가스로부터 분리된 요소 합성액은 하강관(213)을 통하여 합성관(1)으로부터 거의 동압의 스트립퍼(202)의 정부에 공급되었다.
합성액은 합성관과 실질 동일압에 의하여 조작되는 스트립퍼(202)의 튜브내를 박막으로 되어서 유하하는 사이에 밑에서부터 상승하는 원료용 이산화탄소 가스와 도관(223a)을 통해 공급되어 도관(223b)을 통해 방출되는 고압 [20㎏/㎠(게이지)] 수증기의 가열에 의하여 과잉 암모니아의 97%와 미반응 암모늄 카바메이트의 50%가 스트립핑된다. 스트립퍼는 합성관(201)과 동일한 압력으로 조작된다. 스트립퍼(202)의 저부로부터는 190℃의 잔류 암모늄 카바메이트와 잔류 과잉 암모니아를 함유하는 요소 합성액이 라인(214)으로부터 17㎏/㎠(게이지)로 조작되는 중압분해계(도시하지 않음)로 배출된다. 이후 요소 수용액을 통상의 처리를 거쳐서 최종 제품 요소가 얻어졌다. 중압단계 이후의 각 단계로부터 회수된 미반응물에 의하여 형성된 수용액은 라인(222)으로부터 합성관과 실질 동일 압력에 의하여 조작되는 고압 카바메이트 콘덴서(203)에 공급되며 스트립퍼(202)로부터 분리된 암모니아와 암모늄 카바메이트를 함유하는 혼합가스(라인(20))를 흡수하여 라인(220)을 통해 고압 카바메이트 응축기(203)에 공급시켰다. 그 발열은 합성관(201)의 정부의 온도가 190℃로 유지되도록 라인(224)을 통한 수증기의 발생(라인(224))에 의하여 조절시켰다. 고압 카바메이트 콘덴서(203)의 저부로부터는 응축된 암모늄 카바메이트와 미흡수 가스 혼합물을 포함하는 2상 기-액류를 라인(221)을 통해 합성관(201)의 저부에 순환시킨다.
합성관(201) 저부와 스트립퍼(202) 입구 사이의A점으로부터 방열에 의해 분리 라인(215)의 폐쇄를 일으키지 않을 정도의 속도로 요소 합성액의 소량을 끊임없이 분기 도관(215) 속에 주입시킨다. 여기에 분석계의 감도 및 정도가 충분히 유지되는 정도의 양의 순수물이 도관(216)을 통해 도관(215)으로 희석용으로 끊임없이 주입되었다. 이 분기 합성액량에 대하여 희석수량의 비는 통상 10-1000:1정도이다.
약 1㎏/㎠(게이지)로 감압 후 희석된 합성용액은 혼합조(204)에서 잘 교반시켜서 이중 일부 25㎖가 암모니아와 이산화탄소 전자동 분석계(205)에 간헐적으로, 예를들면 15분 간격으로 완전히 자동화된 암모니아와 이산화탄소 분석계(205)에 라인(217)을 통해 공급되었다. 다른 대부분은 대기압 이하의 압력에 의하여 조작되는 응축기(도시하지 않음)에 라인(218)을 통해 감압 도입되었다.
사용된 분석계(205)는 “Digi Chem 3000”(일본국 유아사아이오닉스사제, 상품명)이다. 분석계에서는 수용액 샘플중의 과잉 암모니아 및 암모늄 카바메이트 형태의 질소는 암모니아로서 또 암모늄 카바메이트 형태의 탄소는 중탄산으로서 적정된다. 이 결과로부터 이산화탄소에 대한 소위 유리 암모니아 몰비 R1이 얻어지며 또한 합성액의 전 이산화탄소에 대한 전 질소 몰비로 환산되었다. 이 값은 어떤 때에 3.85이었다. 소망값 4보다 0.15 낮으므로 곧 액체 암모니아의 공급량을 2.94tons /hr 증가하였다. 50분 후의 분석 값은 거의 소망값의 4를 나타냈으므로 암모니아의 공급량을 조금씩 감소하여 경과를 보았다. 8시간 후에도 분석값은 4를 나타냈으므로 정상값에 달했다고 판단되었다.
이 실시예에서는 과잉 암모니아는 모든 스트립퍼로부터 고압 응축기를 경유하여 합성관으로 순환하므로 정상시에 암모니아 펌프로부터 공급되는 것은 요소 형성에 소비되는 암모니아를 보충하는데 필요한 암모니아 뿐이다.
그리고 정상상태에 도달한 다음 갖은 분석계에 의하여 요소도 전술의 비색법에 의하여 때때로 분석하여 이 탄소의 값과 적정으로부터의 이산화탄소와의 합계 값 즉, 전 탄소로부터 요소 합성률을 산출하였다. 이 데이타는 요소 수율을 최대로 하기 위한 합성관의 조작상태의 조절에 유효하게 기여하였다.
본 발명의 사상으로부터 이탈됨이 없이 본 발명은 본 분야에 숙련된 사람들에 의해 변형되고 수정될 수 있음은 자명한 사실이다.
Claims (6)
- 이산화탄소와 화학량론적으로 동일한 또는 과잉의 암모니아를 요소 합성압력 및 요소 합성온도로 요소합성관 내에서 반응시켜서 미반응의 이산화탄소 및 암모니아를 함유하는 조요소 합성액을 수득한 다음 이 조 요소액으로부터 미반응 이산화탄소와 암모니아를 분리시켜 조 요소 합성액을 요소 수용액으로 전환시킨 후, 흡수액을 사용하여 분리된 미반응 이산화탄소와 암모니아의 적어도 일부분을 흡수시키고 이어서 상기 흡수액을 요소 합성관에 재순환시키는 단계를 포함하는 순환식 요소 합성법에 있어서, 상기 1단계에서 순환하는 류의 소량부분을 샘플로서 주기적으로 회수하고 ; 상기 샘플중의 암모니아 함량과 암모늄 카바메이트 함량을 양적으로 분석하고 ; 상기 단계의 하나 이상의 조작인자를 상기 암모니아와 암모늄 카바메이트 함량으로 측정한 값에 따라 조정하여 상기 단계의 조작을 원하는 상태로 유지시킴을 특징으로 하는 순환식 요소 합성법.
- 제1항에 있어서, 상기 샘플은 요소 합성관으로부터 회수한 조 요소액의 소량 부분이고, 상기 샘플을 정량 분석하여 상기 조 요소액내에 존재하는 암모니아 함량과 암모늄 카바메이트 함량을 결정하며, 상기 관에 공급한 새로운 암모니아와 이산화탄소의 량을 수득한 상기 샘플중의 암모니아와 암모늄 카바메이트의 함량에 근거로 하여 계산한 상기 관중에 존재하는 총 이산화탄소에 대한 총 암모니아의 몰비에 따라 조절하여 상기 관 중에 존재하는 총 이산화탄소에 대한 총 암모니아의 몰비를 예비 결정범위로 유지시키는 상기 순환식 요소합성법.
- 제1항에 있어서, 상기 조 요소 합성액으로부터 미반응 이산화탄소와 암모니아를 분리하는 단계를 상기 요소 합성액을 가열시켜 수행하는 상기 방법.
- 제1항에 있어서, 상기 조 요소 합성액으로부터 미반응 이산화탄소와 암모니아를 분리하는 단계를 이산화탄소 또는 불활성 가스로 상기 조 요소액을 1회 이상 스트립핑시켜 수행하는 상기 방법.
- 제1항에 있어서, 상기 흡수액에 의해 흡수되지 않은 과잉의 암모니아를 회수하여 이들로부터 액체 암모니아를 얻어 이 액체 암모니아를 상기 요소 합성관에 재순환시키는 단계를 더 포함하는 상기 방법.
- 제2항에 있어서, 요소 합성관으로부터 회수한 상기 조 요소 합성액은 고압 스트립핑 컬럼에 직접 제1라인을 통해 이송하고, 상기 조 요소 합성액으로부터 미반응 이산화탄소와 암모니아의 분리단계를 수행하고, 상기 조 요소 수용액의 샘플은 제1라인에 연결된 제2지선 타인을 통해 회수하고, 물을 사용하여 상기 샘플을 샘플 부피의 10 내지 1000배 량으로 희석한 후, 상기 샘플을 완전히 혼합시키면서 0내지 1㎏/㎠ 게이지 압으로 한 다음, 상기 샘플의 잔여분을 상기 반응스팀에 재순환시키면서 상기 샘플 0.5내지 50㎖를 포함하는 소부분을 분석기에 의해 분석하며, 상기 분석기는 상기 샘플에 존재하는 암모니아와 상기 샘플에 존재하는 암모늄 카바메이트와 결합한 암모니아의 합인 비 R1을 결정하며, 상기 요소 합성관에 공급된 이산화탄소에 대한 암모니아 비를 원하는 값 R1에 멀어진 상기 비 R1의 차이에 따라 변화시키는 단계를 포함하는 상기 방법.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP56187775A JPS5890544A (ja) | 1981-11-25 | 1981-11-25 | 尿素合成法 |
| JP187775/81 | 1981-11-25 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR840002348A KR840002348A (ko) | 1984-06-25 |
| KR870001237B1 true KR870001237B1 (ko) | 1987-06-26 |
Family
ID=16211989
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR8205292A KR870001237B1 (ko) | 1981-11-25 | 1982-11-24 | 요소 합성법 |
Country Status (9)
| Country | Link |
|---|---|
| JP (1) | JPS5890544A (ko) |
| KR (1) | KR870001237B1 (ko) |
| BR (1) | BR8206811A (ko) |
| DE (1) | DE3243356A1 (ko) |
| FR (1) | FR2516918A1 (ko) |
| GB (1) | GB2110675B (ko) |
| IN (1) | IN159630B (ko) |
| IT (1) | IT1155070B (ko) |
| NL (1) | NL8204495A (ko) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP4928740B2 (ja) * | 2005-05-31 | 2012-05-09 | 東洋エンジニアリング株式会社 | 尿素合成方法および装置 |
| JP5564497B2 (ja) | 2009-05-28 | 2014-07-30 | 東洋エンジニアリング株式会社 | カルバミン酸アンモニウム水溶液の分析方法および未反応ガス吸収槽の運転方法 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3758572A (en) * | 1971-04-26 | 1973-09-11 | Dow Chemical Co | Process for recovering urea from pyrolysis systems |
-
1981
- 1981-11-25 JP JP56187775A patent/JPS5890544A/ja active Granted
-
1982
- 1982-11-15 GB GB08232566A patent/GB2110675B/en not_active Expired
- 1982-11-15 IN IN1331/CAL/82A patent/IN159630B/en unknown
- 1982-11-19 NL NL8204495A patent/NL8204495A/nl not_active Application Discontinuation
- 1982-11-24 BR BR8206811A patent/BR8206811A/pt unknown
- 1982-11-24 KR KR8205292A patent/KR870001237B1/ko active
- 1982-11-24 FR FR8219689A patent/FR2516918A1/fr not_active Withdrawn
- 1982-11-24 DE DE19823243356 patent/DE3243356A1/de not_active Withdrawn
- 1982-11-24 IT IT24430/82A patent/IT1155070B/it active
Also Published As
| Publication number | Publication date |
|---|---|
| BR8206811A (pt) | 1983-10-04 |
| IT8224430A0 (it) | 1982-11-24 |
| IT1155070B (it) | 1987-01-21 |
| IN159630B (ko) | 1987-05-30 |
| GB2110675B (en) | 1985-07-24 |
| GB2110675A (en) | 1983-06-22 |
| FR2516918A1 (fr) | 1983-05-27 |
| JPS5890544A (ja) | 1983-05-30 |
| IT8224430A1 (it) | 1984-05-24 |
| DE3243356A1 (de) | 1983-06-01 |
| NL8204495A (nl) | 1983-06-16 |
| JPS6239152B2 (ko) | 1987-08-21 |
| KR840002348A (ko) | 1984-06-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US4225516A (en) | Process for the manufacture of beta-methylthiopropionaldehyde | |
| KR101433989B1 (ko) | 산화 에틸렌 및 에틸렌 글리콜의 제조방법 | |
| RU2183623C2 (ru) | Способ водно-эмульсионного окисления кумола | |
| US3826815A (en) | Recovery of residual ammonia from weak aqueous solutions thereof | |
| AU2009317550B2 (en) | Method and plant for obtaining NH3 from a mixture comprising NH3 and acidic gases | |
| EP3050866A1 (en) | Method for preparing butadiene through oxidative dehydrogenation | |
| US4208347A (en) | Process for the synthesis of urea | |
| EP1215169B1 (en) | Method and apparatus for the production of nitrogen trifluoride | |
| US3404072A (en) | Ammonia recovery from an acid gas in a plural stage, controlled distillation system | |
| US3383173A (en) | Ammonia purification | |
| KR870001237B1 (ko) | 요소 합성법 | |
| EP3594197A1 (en) | Acetic acid production method | |
| US3600283A (en) | Ammonia stripper overhead control method | |
| EP3597633B1 (en) | Method for granulating urea | |
| US3981684A (en) | Apparatus for controlling urea system | |
| EP0039556B1 (en) | Water removal in a process for continuous nitration of a nitratable aromatic compound | |
| SU1058503A3 (ru) | Способ выделени аммиака и двуокиси углерода | |
| JP3270700B2 (ja) | 尿素の合成方法 | |
| JPS5823658A (ja) | 尿素合成法 | |
| US4420645A (en) | Process for the nitration of halobenzenes | |
| US1973892A (en) | Manufacture of ammonium sulphate | |
| EP3604266B1 (en) | Acetic acid production method | |
| JPH06184085A (ja) | カルバミン酸アンモニウム溶液の分析法およびそれを用いた尿素プラントの制御方法 | |
| JPS61219853A (ja) | アンモニア濃度自動測定方法 | |
| SU606858A1 (ru) | Способ получени мочевины |