KR20220075383A - 암 치료용 다중 특이적 결합 단백질 - Google Patents
암 치료용 다중 특이적 결합 단백질 Download PDFInfo
- Publication number
- KR20220075383A KR20220075383A KR1020227014608A KR20227014608A KR20220075383A KR 20220075383 A KR20220075383 A KR 20220075383A KR 1020227014608 A KR1020227014608 A KR 1020227014608A KR 20227014608 A KR20227014608 A KR 20227014608A KR 20220075383 A KR20220075383 A KR 20220075383A
- Authority
- KR
- South Korea
- Prior art keywords
- seq
- amino acid
- acid sequence
- cdr1
- cdr2
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2827—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against B7 molecules, e.g. CD80, CD86
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2809—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against the T-cell receptor (TcR)-CD3 complex
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/80—Vaccine for a specifically defined cancer
- A61K2039/82—Colon
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/24—Immunoglobulins specific features characterized by taxonomic origin containing regions, domains or residues from different species, e.g. chimeric, humanized or veneered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/31—Immunoglobulins specific features characterized by aspects of specificity or valency multispecific
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/33—Crossreactivity, e.g. for species or epitope, or lack of said crossreactivity
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/30—Immunoglobulins specific features characterized by aspects of specificity or valency
- C07K2317/35—Valency
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/52—Constant or Fc region; Isotype
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/55—Fab or Fab'
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
- C07K2317/565—Complementarity determining region [CDR]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/74—Inducing cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
Abstract
본 발명은 신규 B7H6/CD3 결합 단백질에 관한 것이다. 본 발명은 또한 상기 단백질을 암호화하는 핵산; 상기 단백질을 제조하는 방법; 상기 단백질을 발현하거나 발현할 수 있는 숙주 세포; 상기 단백질을 포함하는 조성물; 및 특히 암 질환 분야에서 치료 목적을 위한 상기 단백질 또는 상기 조성물의 용도에 관한 것이다.
Description
본 발명은 B7H6 (본원에서 "B7-H6"이라고도 함)에 특이적인 제1 항원 결합 단위 및 CD3에 특이적인 제2 항원 결합 단위를 포함하는 다중 특이적 결합 단백질에 관한 것이다. 본 발명은 또한 이러한 결합 단백질을 암호화하는 핵산, 이러한 결합 단백질을 제조하는 방법; 이러한 결합 단백질을 발현하거나 발현할 수 있는 숙주 세포, 이러한 결합 단백질을 포함하는 조성물, 및 특히 암 질환 분야에서 치료 목적을 위한 이러한 결합 단백질 또는 이러한 조성물의 용도에 관한 것이다.
B7H6은 표적 세포에 대한 선천적 면역을 유도하는 것으로 기술되어 있는 종양 선택성 B7 패밀리 구성원이고, 세포외 도메인에 2개의 Ig-유사 도메인, N-말단 IgV-유사 도메인 및 C-말단 IgCl-유사 도메인을 갖는 다른 B7 패밀리 구성원과 유사한 기능을 공유한다. B7H6은 인간 자연 살해 (NK) 세포의 NKp30 매개 활성화를 촉발시켜 탈과립 및 IFNγ 분비를 유도한다. (Brandt et al., J. Exp. Med. 2009 206(7); 1495-1503). 현재 이용가능한 데이터는 감염성 상태에 대한 염증 반응뿐만 아니라 고형 종양에서 B7H6의 역할을 제안한다.
B7H6은 이러한 급성 질환 상태에서 염증 과정의 결과로서 패혈증 환자의 말초 혈액으로부터 단리된 CD14+CD16+ 세포 상에서 발현되는 것으로 밝혀졌다. 이러한 발견은 IL-Iβ 및 TNFα에 의한 자극시 CD14+CD16+ 전염증성 단핵구 및 호중구의 세포 표면 상에서의 B7H6의 상향조절의 시험관내 분석에 의해 확인되어 (Matta et al., Blood 2013 122(3)) 패혈증 상태에 대한 염증 반응에서 B7H6의 역할을 제시한다.
전술한 패혈증 상태를 제외하고, B7H6는 종양 세포에서 선택적으로 발현되고 정상 상태의 정상 인간 조직에서는 검출될 수 없다. 예를 들어, B7H6의 발현은 T 세포 림프종, 골수성 백혈병, 결장 암종, 유방암 및 난소 암종 세포주 (Brandt et al., J. Exp. Med. 2009 206(7): 1495-1503; Li et al., J. Exp.Med.2011 208(4); Greaves et al., Blood 2013 121(5); Zhang et al. Oncology Letters 2018 16:91-96), 비-소세포 폐암 조직 (Zhang et al., Int J clin Exp Pathol 2014;7(10):6936-6942), 위장 종양 조직 (Chen et al., Pathol. Oncol. Res.2014 20:203-207; Zhao et al., Cell Proliferation 2018; e12468), 난소 암종 조직 (Zhou et al., Int clin Exp Pathol 2015 8(8)), 경구 편평 암종 조직 (Wang et al., J Oral Pathol Med. 2017;46:766-772), 및 간세포 암종 조직 (Li et al., Int. J. Mol. Sci. 2019, 20, 156)에 대해 기술되었지만, 종양에서의 B7H6의 기능은 완전히 이해되지 않고 있다.
ADCC/CDC 경로에 관여하는 항-B7H6 항체 또는 항-B7H6 항체-약물 접합체를 사용한 암의 치료를 포함하는 치료적 적용이 W02009/046407 A2 및 WO2011/07044 A2에 기재되어 있다.
그러나, ADCC/CDC 활성에 기초한 B7H6 표적화 요법은 B7H6의 낮은 세포 표면 발현 및 고형 종양에서 ADCC/CDC 활성을 갖는 종래 항체를 사용한 낮은 성공률 때문에 최적의 작용 방식이 아니다.
B7H6-특이적 항체 약물 접합체 (ADC)에 기초한 표적화된 치료법은 또한, 대부분의 환자가 화학요법 치료 후 재발하고 세포 표면에서의 B7H6의 낮은 발현으로 인해 한계를 가질 수 있다. 또한, ADC 접근법은 종종 링커 불안정성 또는 분해의 결과로 자유 약물에 의해 야기되는 오프-타겟 독성을 갖는다.
CAR-T-세포 및 T 세포 결합 항체는 B7H6-발현 고형 종양의 표적화된 치료를 위한 추가의 접근법이다 (Wu et al., Gene 2015 22, 675-684; Hua et al. Protein Engineering, Design & Selection 201730(10), 713-721; WO2017/181001). 예를 들어, 우 등 (Wu et al.) (J Immunol. 2015 Jun 1; 194 (11):5305-11)은 2개의 단일쇄 가변 단편 (scFv)으로 이루어진 약 55 Kda 융합 단백질인 이중 특이적 T 세포 인게이저를 위해 존재하는 BiTE인 B7H6-특이적-BiTE로의 전임상 데이터를 기술한다. 이 경우, B7H6-특이적-BiTE는 OKT3-CD3-결합제 및 이전에 공개된 B7H6 항체에 기초하여 조작되었다 (Zhang et al., J Immunol. 2012 Sep 1;189(5):2290-9; WO 2013/169691). 그러나, OKT3 항체는 사이노몰거스 원숭이 CD3과 교차-반응성이 없으며, 따라서 임상 시험 준비를 위한 바람직한 시험 종인 사이노몰거스 원숭이에서 전임상 독성학적 시험을 허용하지 않는다 (Chatenoud et al., The Rev Diabet Stud 2012;9(4):372-381). 추가적인 도전은 상대적으로 작고 쉽게 분해되는 BiTE 분자의 짧은 반감기이며, 이는 임상에서 연속적인 정맥내 투약을 필요로 한다. 따라서, 이러한 접근 방식이 성공할지는 미지수다. 현재까지, B7-H6-발현 종양에 대한 어떠한 표적화된 치료법도 이용가능하지 않고, 현재의 접근법에 의해 다루어지지 않은 충족되지 않은 요구가 남아 있다.
예를 들어, 결장직장암 (CRC)은 B7-H6의 높은 유병률 및 예측 가능한 발현을 나타낸다. 이것은 전세계적으로 암 이환율과 사망률의 주요 원인 중 하나이다. 초기 과잉 전이와 전이성 질환이 있는 CRC 환자의 약 25%가 새로 진단된 환자의 40-50%에서 발생한다. 비록 화학요법 및 표적화된 요법에서의 최근의 개선이 전이성 CRC의 생존 기간을 연장시켰지만, 대부분의 환자는 그들의 질병에 굴복할 것이다.
진행 질환 암 환자들의 좋지 않은 전망을 고려하여, 더 효과적인 요법, 특히 내약성이 향상된 효과적인 요법을 동정할 필요가 있다.
따라서, 본 발명의 목적은 현재 사용되고/거나 당업계에 공지된 제제, 조성물 및/또는 방법과 비교하여 특정 이점을 제공하는 약리학적 활성제, 조성물 및/또는 치료 방법을 제공하는 것이다. 이러한 이점은, 특히 당업계에 이미 공지된 후보 약물과 비교하여, 개선된 치료 및 약리학적 특성, 예컨대 생체내 효능, 덜한 부작용, 감소된 면역원성, 개선된 치료 창, 감소된 투여 (예를 들어, 주입) 시간, 더 낮은 투약, 덜 빈번한 투약을 가능하게 하는 연장된 반감기, 및 개선된 제조 용이성, 안정성, 통상적인 항체 과정과의 상용성 또는 물품의 감소된 비용과 같은 다른 유리한 특성을 포함한다.
발명의 개요
본 발명은 T 세포 상에서 발현되는 CD3에 대한 결합 아암 (arm) 및 종양 세포의 세포 표면 상에서 발현되는 B7H6에 대한 결합 암을 갖는 다중 특이적 결합 단백질을 이용하는 이중 특이적 T 세포 결합 (engaging) 접근법에 기초한다. T 세포 및 종양 세포에의 동시 결합을 통해, 본 발명의 T 세포 인게이저 (T cell engager)는 두 세포 사이에 세포용해 시냅스의 형성을 강제하고, 이에 의해 T 세포 활성을 선택적으로 표적화된 종양 세포로 재지향시킨다.
한 측면에서, 본 발명은 B7H6에 특이적으로 결합하는 제1 항원 결합 단위 및 CD3에 특이적으로 결합하는 제2 항원 결합 단위를 포함하는 다중 특이적 결합 단백질을 제공하고, 여기서 B7H6에 특이적으로 결합하는 상기 제1 항원 결합 단위는 하기 i) 내지 xxiv)로 이루어진 군으로부터 선택된다:
i) 서열 번호 1 (CDR1), 서열 번호 2 (CDR2) 및 서열 번호 3 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 4 (CDR1), 서열 번호 5 (CDR2) 및 서열 번호 6 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
ii) 서열 번호 7 (CDR1), 서열 번호 8 (CDR2) 및 서열 번호 9 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 10 (CDR1), 서열 번호 11 (CDR2) 및 서열 번호 12 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
iii) 서열 번호 13 (CDR1), 서열 번호 14 (CDR2) 및 서열 번호 15 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 16 (CDR1), 서열 번호 17 (CDR2) 및 서열 번호 18 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
iv) 서열 번호 19 (CDR1), 서열 번호 20 (CDR2) 및 서열 번호 21 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 22 (CDR1), 서열 번호 23 (CDR2) 및 서열 번호 24 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
v) 서열 번호 25 (CDR1), 서열 번호 26 (CDR2) 및 서열 번호 27 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 28 (CDR1), 서열 번호 29 (CDR2) 및 서열 번호 30 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
vi) 서열 번호 31 (CDR1), 서열 번호 32 (CDR2) 및 서열 번호 33 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 34 (CDR1), 서열 번호 35 (CDR2) 및 서열 번호 36 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
vii) 서열 번호 37 (CDR1), 서열 번호 38 (CDR2) 및 서열 번호 39 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 40 (CDR1), 서열 번호 41 (CDR2) 및 서열 번호 42 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
viii) 서열 번호 43 (CDR1), 서열 번호 44 (CDR2) 및 서열 번호 45 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 46 (CDR1), 서열 번호 47 (CDR2) 및 서열 번호 48 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
ix) 서열 번호 49 (CDR1), 서열 번호 50 (CDR2) 및 서열 번호 51 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 52 (CDR1), 서열 번호 53 (CDR2) 및 서열 번호 54 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
x) 서열 번호 55 (CDR1), 서열 번호 56 (CDR2) 및 서열 번호 57 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 58 (CDR1), 서열 번호 59 (CDR2) 및 서열 번호 60 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xi) 서열 번호 61 (CDR1), 서열 번호 62 (CDR2) 및 서열 번호 63 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 64 (CDR1), 서열 번호 65 (CDR2) 및 서열 번호 66 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xii) 서열 번호 67 (CDR1), 서열 번호 68 (CDR2) 및 서열 번호 69 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 70 (CDR1), 서열 번호 71 (CDR2) 및 서열 번호 72 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xiii) 서열 번호 73 (CDR1), 서열 번호 74 (CDR2) 및 서열 번호 75 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 76 (CDR1), 서열 번호 77 (CDR2) 및 서열 번호 78 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xiv) 서열 번호 79 (CDR1), 서열 번호 80 (CDR2) 및 서열 번호 81 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 82 (CDR1), 서열 번호 83 (CDR2) 및 서열 번호 84 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xv) 서열 번호 85 (CDR1), 서열 번호 86 (CDR2) 및 서열 번호 87 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 88 (CDR1), 서열 번호 89 (CDR2) 및 서열 번호 90 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xvi) 서열 번호 91 (CDR1), 서열 번호 92 (CDR2) 및 서열 번호 93 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 94 (CDR1), 서열 번호 95 (CDR2) 및 서열 번호 96 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xvii) 서열 번호 97 (CDR1), 서열 번호 98(CDR2) 및 서열 번호 99 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 100 (CDR1), 서열 번호 101 (CDR2) 및 서열 번호 102 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xviii) 서열 번호 103 (CDR1), 서열 번호 104 (CDR2) 및 서열 번호 105 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 106 (CDR1), 서열 번호 107 (CDR2) 및 서열 번호 108 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xix) 서열 번호 109 (CDR1), 서열 번호 110 (CDR2) 및 서열 번호 111 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 112 (CDR1), 서열 번호 113 (CDR2) 및 서열 번호 114 (CDR3)의 아미노산 서열을 포함하는 중쇄 CD을 포함하는 항원 결합 단위;
xx) 서열 번호 115 (CDR1), 서열 번호 116 (CDR2) 및 서열 번호 117 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 118 (CDR1), 서열 번호 119 (CDR2) 및 서열 번호 120 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xxi) 서열 번호 121 (CDR1), 서열 번호 122 (CDR2) 및 서열 번호 123 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 124 (CDR1), 서열 번호 125 (CDR2) 및 서열 번호 126 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xxii) 서열 번호 127 (CDR1), 서열 번호 128 (CDR2) 및 서열 번호 129 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 130 (CDR1), 서열 번호 131 (CDR2) 및 서열 번호 132 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xxiii) 서열 번호 133 (CDR1), 서열 번호 134 (CDR2) 및 서열 번호 135 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 136 (CDR1), 서열 번호 137 (CDR2) 및 서열 번호 138 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위; 및
xxiv) 서열 번호 139 (CDR1), 서열 번호 140 (CDR2) 및 서열 번호 141 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 142 (CDR1), 서열 번호 143 (CDR2) 및 서열 번호 144 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위.
본 발명의 결합 단백질의 일부 실시양태에서, B7H6에 특이적으로 결합하는 제1 항원 결합 단위는 하기 i) 내지 xxiv)로 이루어진 군으로부터 선택된다:
i) 서열 번호 145의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 146의 아미노산 서열을 포함하는 중쇄 가변 도메인;
ii) 서열 번호 147의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 148의 아미노산 서열을 포함하는 중쇄 가변 도메인;
iii) 서열 번호 149의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 150의 아미노산 서열을 포함하는 중쇄 가변 도메인;
iv) 서열 번호 151의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 152의 아미노산 서열을 포함하는 중쇄 가변 도메인;
v) 서열 번호 153의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 154의 아미노산 서열을 포함하는 중쇄 가변 도메인;
vi) 서열 번호 155의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 156의 아미노산 서열을 포함하는 중쇄 가변 도메인;
vii) 서열 번호 157의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 158의 아미노산 서열을 포함하는 중쇄 가변 도메인;
viii) 서열 번호 159의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 160의 아미노산 서열을 포함하는 중쇄 가변 도메인;
ix) 서열 번호 161의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 162의 아미노산 서열을 포함하는 중쇄 가변 도메인;
x) 서열 번호 163의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 164의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xi) 서열 번호 165의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 166의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xii) 서열 번호 167의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 168의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xiii) 서열 번호 169의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 170의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xiv) 서열 번호 171의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 172의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xv) 서열 번호 173의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 174의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xvi) 서열 번호 175의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 176의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xvii) 서열 번호 177의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 178의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xviii) 서열 번호 179의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 180의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xix) 서열 번호 181의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 182의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xx) 서열 번호 183의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 184의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xxi) 서열 번호 185의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 186의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xxii) 서열 번호 187의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 188의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xxiii) 서열 번호 189의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 190의 아미노산 서열을 포함하는 중쇄 가변 도메인; 및
xxiv) 서열 번호 191의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 192의 아미노산 서열을 포함하는 중쇄 가변 도메인.
본 발명의 결합 단백질의 일부 실시양태에서, CD3에 특이적으로 결합하는 제2 항원 결합 단위는 하기 i) 내지 vi)로 이루어진 군으로부터 선택된다:
i) 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
ii) 서열 번호 263 (CDR1), 서열 번호 264 (CDR2) 및 서열 번호 265 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 266 (CDR1), 서열 번호 267 (CDR2) 및 서열 번호 268 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
iii) 서열 번호 269 (CDR1), 서열 번호 270 (CDR2) 및 서열 번호 271 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 272 (CDR1), 서열 번호 273 (CDR2) 및 서열 번호 274 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
iv) 서열 번호 275 (CDR1), 서열 번호 276 (CDR2) 및 서열 번호 277 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 278 (CDR1), 서열 번호 279 (CDR2) 및 서열 번호 280 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
v) 서열 번호 281 (CDR1), 서열 번호 282 (CDR2) 및 서열 번호 283 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 284 (CDR1), 서열 번호 285 (CDR2) 및 서열 번호 286 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위; 및
vi) 서열 번호 287 (CDR1), 서열 번호 288 (CDR2) 및 서열 번호 289 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 290 (CDR1), 서열 번호 291 (CDR2) 및 서열 번호 292 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위.
본 발명의 결합 단백질의 일부 실시양태에서, CD3에 특이적으로 결합하는 제2 항원 결합 단위는 하기 i) 내지 vi)로 이루어진 군으로부터 선택된다:
i) 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인;
ii) 서열 번호 295의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 296의 아미노산 서열을 포함하는 중쇄 가변 도메인;
iii) 서열 번호 297의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 298의 아미노산 서열을 포함하는 중쇄 가변 도메인;
iv) 서열 번호 299의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 300의 아미노산 서열을 포함하는 중쇄 가변 도메인;
v) 서열 번호 301의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 302의 아미노산 서열을 포함하는 중쇄 가변 도메인; 및
vi) 서열 번호 303의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 304의 아미노산 서열을 포함하는 중쇄 가변 도메인.
본 발명의 결합 단백질의 일부 실시양태에서, B7H6에 특이적으로 결합하는 제1 항원 결합 단위는 그의 N-말단에서 C-말단으로 제1 경쇄 가변 도메인, 제1 경쇄 불변 도메인, 제1 펩티드 링커, 제1 중쇄 가변 도메인 및 제1 중쇄 불변 CH1 도메인을 포함하고; CD3에 특이적으로 결합하는 제2 항원 결합 단위는 그의 N-말단에서 C-말단으로 제2 경쇄 가변 도메인, 제2 경쇄 불변 도메인, 제2 펩티드 링커, 제2 중쇄 가변 도메인 및 제2 중쇄 불변 CH1 도메인을 포함한다. 본 발명의 결합 단백질의 일부 실시양태에서, 제1 및/또는 제2 펩티드 링커는 26 내지 42개의 아미노산, 바람직하게는 30 내지 40개의 아미노산, 34 내지 40개의 아미노산, 또는 36 내지 39개의 아미노산 중 어느 하나, 보다 바람직하게는 38개의 아미노산을 포함한다. 본 발명의 일부 실시양태에서, 제1 링커 및/또는 제2 링커는 바람직하게는 서열 번호 250의 아미노산 서열을 포함하는 Gly-Ser 링커이고, 보다 바람직하게는 상기 제1 및 제2 펩티드 링커는 동일한 서열 (예: 서열 번호 250)을 포함한다. 본 발명의 일부 실시양태에서, 제1 경쇄 불변 도메인 및 제2 경쇄 불변 도메인은 독립적으로 인간 카파 또는 람다 도메인을 포함한다.
일부 실시양태에서, 본 발명의 결합 단백질의 B7H6에 특이적인 제1 항원 결합 단위는 서열 번호 193, 서열 번호 194, 서열 번호 195, 서열 번호 196 서열 번호 197 서열 번호 198 서열 번호 199 서열 번호 200 서열 번호 201 서열 번호 202 서열 번호 203 서열 번호 204 서열 번호 205, 서열 번호 206, 서열 번호 207, 서열 번호 208, 서열 번호 209, 서열 번호 210, 서열 번호 211, 서열 번호 212, 서열 번호 213, 서열 번호 214, 서열 번호 215, 및 서열 번호 216으로 이루어진 군으로부터 선택된 아미노산 서열을 포함하고, CD3에 특이적인 제2 항원 결합 단위는 서열 번호 305, 서열 번호 306, 서열 번호 307, 서열 번호 308, 서열 번호 309, 및 서열 번호 310, 바람직하게는 서열 번호 305로 이루어진 군으로부터 선택된 아미노산 서열을 포함한다.
일부 실시양태에서, 본 발명의 결합 단백질은 제1 및 제2 Fc 도메인을 추가로 포함하고, 여기서 상기 제1 Fc 도메인은 상기 제1 항원 결합 단위, 바람직하게는 상기 제1 항원 결합 단위의 C-말단에 공유적으로 연결되고, 상기 제2 Fc 도메인은 상기 제2 항원 결합 단위, 바람직하게는 상기 제2 항원 결합 단위의 C-말단에 공유적으로 연결된다.
본 발명의 일부 실시양태에서,
i) 제1 Fc 도메인은 위치 366에 티로신 (Y) [T366Y]을 포함하고, 제2 Fc 도메인은 위치 407에 트레오닌 (T) [Y407T]을 포함하거나, 또는
ii) 제1 Fc 도메인은 위치 366에 트립토판 (W) [T366W]을 포함하고, 제2 Fc 도메인은 위치 366에 세린 (S) [T366S], 위치 368에 알라닌 (A) [L368A] 및 위치 407에서 발린 (V) [Y407V]을 포함하거나, 또는
iii) 제2 Fc 도메인은 위치 366에 티로신 (Y) [T366Y]을 포함하고, 제1 Fc 도메인은 위치 407에 트레오닌 (T) [Y407T]을 포함하거나, 또는
iv) 제2 Fc 도메인은 위치 366에 트립토판 (W) [T366W]을 포함하고, 제1 Fc 도메인은 위치 366에 세린 (S) [T366S], 위치 368에 알라닌 (A) [L368A] 및 위치 407에서 발린 (V) [Y407V]을 포함하고,
바람직하게는 제1 또는 제2 Fc 도메인은 위치 435에 아르기닌 [H435R] 및 위치 436에 페닐알라닌 [Y436F]을 추가로 포함한다. 일부 실시양태에서, 제1 및/또는 제2 Fc 도메인은 위치 234 [L234A] 및 위치 235 [L235A]에 알라닌을 포함한다.
일부 실시양태에서, 본 발명의 결합 단백질은 서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 서열 번호 221, 서열 번호 222, 서열 번호 223, 서열 번호 224, 서열 번호 225, 서열 번호 226, 서열 번호 227, 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 및 서열 번호 240으로 이루어진 군으로부터 선택된 아미노산 서열을 포함하는 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 및 서열 번호 311, 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 및 서열 번호 316, 바람직하게는 서열 번호 311로 이루어진 군으로부터 선택된 아미노산 서열을 포함하는 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄를 포함한다.
추가 측면에서, 본 발명은 i) 본 발명의 결합 단백질의 제1 항원 결합 단위 및/또는 제2 항원 결합 단위를 암호화하고, 선택적으로 제1 및/또는 제2 Fc 도메인을 추가로 암호화하거나, 또는 ii) 본 발명의 결합 단백질의 제1 및/또는 제2 폴리펩티드 쇄를 암호화하는 단리된 핵산 분자를 제공한다. 추가 측면에서 본 발명의 핵산 분자를 포함하는 발현 벡터, 이러한 발현 벡터로 형질감염된 숙주 세포, 및 본 발명의 단백질을 제조하는 방법이 본원에서 제공된다.
본 발명의 추가 측면에서, B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 및 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄를 포함하는 다중-특이적 결합 단백질이 제공되며, 여기서 제1 폴리펩티드 쇄는 제1 경쇄, 제1 링커 및 제1 중쇄를 포함하고, 제2 폴리펩티드 쇄는 제2 경쇄, 제2 링커 및 제2 중쇄를 포함하며, 바람직하게는 상기 제1 경쇄의 C-말단은 제1 펩티드 링커를 통해 제1 중쇄의 N-말단에 공유 결합되며, 제2 경쇄의 C-말단은 제2 펩티드 링커를 통해 상기 제2 중쇄의 N-말단에 공유 결합된다. 당업자는 본원에서 "경쇄" 또는 "중쇄"에 대한 임의의 언급이 각각 항체 경쇄 또는 항체 중쇄를 지칭한다는 것을 이해할 것이다.
본 발명의 단백질의 일부 실시양태에서, B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄는 본원에 설명된 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23 및 B7H6#24의 항원 결합 단위에 대해 정의된 바와 같은 CDR 서열, VH/VL 서열 및/또는 단일쇄 Fab 서열을 포함하는 경쇄 가변 및 중쇄 가변 도메인을 포함한다. 일부 실시양태에서, CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄는 본원에 기재된 바와 같이 CD3#1의 항원 결합 단위에 대해 정의된 바와 같은 CDR 서열, VH/VL 서열 및/또는 scFab 서열을 포함하는 경쇄 가변 및 중쇄 가변 도메인을 포함한다.
본 발명의 결합 단백질을 포함하는 추가 측면, 실시양태, 용도 및 방법은 본 발명의 하기 상세한 설명 및 이어지는 청구범위로부터 명백해질 것이다.
본 발명은 (전이성) 결장직장암 ((m)CRC), 비소세포 폐암 (NSCLC) 또는 두경부 편평세포암 (HNSCC)과 같은 B7H6 발현 암의 보다 효율적인 치료를 가능하게 하는 신규 결합 단백질을 제공한다.
도 1: 본 발명의 이중 특이성 결합 단백질의 개략도.
도 2: CHO-K1 세포의 세포 표면에서 발현되는 세포외 B7H6 단백질의 개략도.
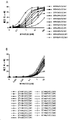
도 3: 재조합 인간 B7H6 세포외 단백질에 대한 34개의 예시적인 B7H6/CD3 결합 단백질의 결합.
도 4: 재조합 인간 알라닌-돌연변이화 B7H6 세포외 단백질에 대한 34개의 예시적인 B7H6/CD3 결합 단백질의 결합.
도 5: 내인성 인간 B7H6을 발현하는 HCT-15 세포에 대한 34개의 예시적인 B7H6/CD3 결합 단백질의 결합.
도 6: 사이노몰거스 원숭이 B7H6을 발현하는 재조합 CHO-K1 세포에 대한 23개의 예시적인 B7H6/CD3 결합 단백질의 결합.
도 7: CD3을 발현하는 인간 T-세포에 대한 23개의 예시적인 B7H6/CD3 결합 단백질의 결합.
도 8: B7H6-음성 CHO-K1 세포에 대한 23개의 예시적인 B7H6/CD3 결합 단백질의 결합.
도 9: NK-92MI 세포에 의한 B7H6-의존성 IFNγ 분비의 17개의 예시적인 B7H6/CD3 결합 단백질의 억제 활성.
도 10: 자극되지 않은 T-세포를 인간 HCT-15 세포로 재지향시키는 11개의 예시적인 B7H6/CD3 결합 단백질의 표적 세포를 용해시키는 효능.
도 11: 자극되지 않은 T-세포를 인간 HCT-15 세포로 재지향시키는 23개의 예시적인 B7H6/CD3 결합 단백질의 표적 세포를 용해시키는 효능.
도 12: 다양한 이펙터 대 표적 (E:T) 세포 비율에서 예시적인 B7H6/CD3 결합 단백질의 표적 세포를 용해시키는 효능.
도 13: 자극되지 않은 T-세포를 B7-H6 및 Cho wt 세포로 형질감염된 재조합 CHO 세포로 재지향시키는 23개의 예시적인 B7H6/CD3 결합 단백질의 용해 세포에서의 효능.
도 14: 6개의 예시적인 B7H6/CD3 결합 단백질의 HCT-15 세포의 존재하에 T-세포에서 CD25 발현의 상향조절 효능.
도 15: 6개의 예시적인 B7H6/CD3 결합 단백질의 HCT-15 세포의 존재하에 T-세포에서 세포내 퍼포린 발현의 상향조절 효능.
도 16: 6개의 예시적인 B7H6/CD3 결합 단백질의 HCT-15 세포의 존재하에 T-세포에서 세포내 그랜자임 B 발현의 상향조절 효능.
도 17: 6개의 예시적인 B7H6/CD3 결합 단백질의 HCT-15 세포의 존재하에 T-세포의 증식 효능.
도 18: 5개의 예시적인 B7H6/CD3 결합 단백질의 HCT-15 세포의 존재하에 T-세포에 의한 IFNγ 분비 효능.
도 19: 하나의 예시적인 B7H6/CD3 결합 단백질의 약동학적 프로파일.
도 20: T-세포 이식된 마우스 이종이식 모델에서 하나의 예시적인 B7H6/CD3 결합 단백질의 항종양 활성.
도 21: 예시적인 B7H6/CD3 결합 단백질을 갖는 NCI-H716 이종이식 종양 조직에서의 T 세포 침윤.
도 22: 4개의 예시적인 B7H6 결합 단백질의 약동학적 프로파일.
도 23: T-세포 이식된 마우스 이종이식 모델에서 4개의 예시적인 B7H6/CD3 결합 단백질의 항종양 활성.
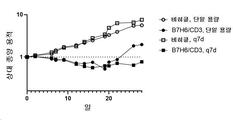
도 24: q7d 또는 1회 단일 용량으로 투여된 T-세포 이식된 마우스 이종이식 모델에서 예시적인 B7H6/CD3 결합 단백질의 항종양 활성.
도 2: CHO-K1 세포의 세포 표면에서 발현되는 세포외 B7H6 단백질의 개략도.
도 3: 재조합 인간 B7H6 세포외 단백질에 대한 34개의 예시적인 B7H6/CD3 결합 단백질의 결합.
도 4: 재조합 인간 알라닌-돌연변이화 B7H6 세포외 단백질에 대한 34개의 예시적인 B7H6/CD3 결합 단백질의 결합.
도 5: 내인성 인간 B7H6을 발현하는 HCT-15 세포에 대한 34개의 예시적인 B7H6/CD3 결합 단백질의 결합.
도 6: 사이노몰거스 원숭이 B7H6을 발현하는 재조합 CHO-K1 세포에 대한 23개의 예시적인 B7H6/CD3 결합 단백질의 결합.
도 7: CD3을 발현하는 인간 T-세포에 대한 23개의 예시적인 B7H6/CD3 결합 단백질의 결합.
도 8: B7H6-음성 CHO-K1 세포에 대한 23개의 예시적인 B7H6/CD3 결합 단백질의 결합.
도 9: NK-92MI 세포에 의한 B7H6-의존성 IFNγ 분비의 17개의 예시적인 B7H6/CD3 결합 단백질의 억제 활성.
도 10: 자극되지 않은 T-세포를 인간 HCT-15 세포로 재지향시키는 11개의 예시적인 B7H6/CD3 결합 단백질의 표적 세포를 용해시키는 효능.
도 11: 자극되지 않은 T-세포를 인간 HCT-15 세포로 재지향시키는 23개의 예시적인 B7H6/CD3 결합 단백질의 표적 세포를 용해시키는 효능.
도 12: 다양한 이펙터 대 표적 (E:T) 세포 비율에서 예시적인 B7H6/CD3 결합 단백질의 표적 세포를 용해시키는 효능.
도 13: 자극되지 않은 T-세포를 B7-H6 및 Cho wt 세포로 형질감염된 재조합 CHO 세포로 재지향시키는 23개의 예시적인 B7H6/CD3 결합 단백질의 용해 세포에서의 효능.
도 14: 6개의 예시적인 B7H6/CD3 결합 단백질의 HCT-15 세포의 존재하에 T-세포에서 CD25 발현의 상향조절 효능.
도 15: 6개의 예시적인 B7H6/CD3 결합 단백질의 HCT-15 세포의 존재하에 T-세포에서 세포내 퍼포린 발현의 상향조절 효능.
도 16: 6개의 예시적인 B7H6/CD3 결합 단백질의 HCT-15 세포의 존재하에 T-세포에서 세포내 그랜자임 B 발현의 상향조절 효능.
도 17: 6개의 예시적인 B7H6/CD3 결합 단백질의 HCT-15 세포의 존재하에 T-세포의 증식 효능.
도 18: 5개의 예시적인 B7H6/CD3 결합 단백질의 HCT-15 세포의 존재하에 T-세포에 의한 IFNγ 분비 효능.
도 19: 하나의 예시적인 B7H6/CD3 결합 단백질의 약동학적 프로파일.
도 20: T-세포 이식된 마우스 이종이식 모델에서 하나의 예시적인 B7H6/CD3 결합 단백질의 항종양 활성.
도 21: 예시적인 B7H6/CD3 결합 단백질을 갖는 NCI-H716 이종이식 종양 조직에서의 T 세포 침윤.
도 22: 4개의 예시적인 B7H6 결합 단백질의 약동학적 프로파일.
도 23: T-세포 이식된 마우스 이종이식 모델에서 4개의 예시적인 B7H6/CD3 결합 단백질의 항종양 활성.
도 24: q7d 또는 1회 단일 용량으로 투여된 T-세포 이식된 마우스 이종이식 모델에서 예시적인 B7H6/CD3 결합 단백질의 항종양 활성.
발명의 상세한 설명
사용된 용어 및 정의
본 발명의 상기 및 다른 측면 및 실시양태들이 본원의 추가 설명으로부터 명백해질 것이다.
지시되지 않거나 달리 정의되지 않는 한, 사용된 모든 용어는 당해 기술 분야에서 당업자에게 명백한 통상의 의미를 가질 것이다. 표준 핸드북, 예컨대 [Sambrook et al, "Molecular Cloning: A Laboratory Manual" (2nd Ed.), VoIs. 1-3, Cold Spring Harbor Laboratory Press (1989); Lewin, "Genes IV", Oxford University Press, New York, (1990), 및 Roitt et al., "Immunology" (2nd Ed.), Gower Medical Publishing, London, New York (1989)], 뿐만 아니라 여기에 인용된 일반적인 배경기술이 참조될 수 있다. 또한, 달리 언급하지 않는 한, 상세하게 구체적으로 기술되지 않은 모든 방법, 단계, 기술 및 조작은 당업자에게 명백한 바와 같이 그 자체로 공지된 방식으로 수행될 수 있고 또한 수행되었다. 예를 들어, 표준 핸드북, 위에서 언급한 일반적인 배경기술 및 그 안에 인용된 다른 참고 문헌을 다시 참조할 수 있다.
본원에서 사용되는 경우 용어 "포함하는" 및 "포함한다" 및 "포함하다"와 같은 그의 변형은 용어 "함유하는" 또는 "가지는" 또는 "갖는"으로 대체될 수 있다.
본원에 사용된 용어 "서열" (예를 들어 "중/경쇄 서열", "항체 서열", "가변 도메인 서열", "불변 도메인 서열" 또는 "단백질 서열"과 같은 용어)은 일반적으로 문맥상 더 제한적인 해석을 요구하지 않는 한, 관련된 아미노산 서열뿐만 아니라 이를 암호화하는 핵산 서열 또는 뉴클레오티드 서열을 모두 포함하는 것으로 이해하여야 한다.
본원에 사용된 용어 "항원 결합 단위"는 특정 표적 또는 항원에 대한 결합을 허용하는 항체로부터 유래된 최소 구조적 요건 (즉, 항체에 전형적으로 존재하는 최소 구조적 요건)을 포함한다. 따라서, 항원 결합 단위는 적어도 3개의 경쇄 및 3개의 중쇄 CDR 서열을 포함하고; 바람직하게는 적어도 경쇄 가변 도메인 및 중쇄 가변 도메인을 포함한다.
항체 또는 면역글로불린의 일반화된 구조는 당업자에게 잘 알려져 있다. 이들 분자는 전형적으로 2개의 동일한 경쇄 (L) 및 2개의 동일한 중쇄 (H)로 구성된 약 150,000 달톤의 이종사량체 당단백질이며, 일반적으로 전장 항체라고 한다. 각 경쇄는 하나의 이황화 결합에 의해 중쇄에 공유적으로 연결되어 이종이량체를 형성하고, 이종사량체 분자는 이종이량체의 2개의 동일한 중쇄 사이의 공유 이황화 결합을 통해 형성된다. 경쇄와 중쇄가 하나의 이황화 결합에 의해 함께 연결되어 있지만, 두 중쇄 사이의 이황화 결합의 수는 면역글로불린 동형에 따라 다르다. 각 중쇄 및 경쇄는 또한 규칙적으로 이격된 쇄 내 이황화 다리를 가지고 있다. 각 중쇄는 N-말단에 가변 도메인 (VH), 이어서 3개 또는 4개 (IgE의 경우)의 불변 도메인 (CH1, CH2, CH3 및 CH4)과 CH1과 CH2 사이에 힌지 영역을 가지고 있다. 각 경쇄에는 N-말단 가변 도메인 (VL) 및 C-말단 불변 도메인 (CL)의 두 도메인이 있다. VL 도메인은 VH 도메인과 비공유적으로 결합하는 반면, CL 도메인은 일반적으로 이황화 결합을 통해 CH1 도메인에 공유적으로 연결된다. 특정 아미노산 잔기는 경쇄 가변 도메인과 중쇄 가변 도메인 사이에 인터페이스를 형성하는 것으로 여겨진다 (Chothia et al, 1985, J. Mol. Biol. 186: 651-663). 가변 도메인은 또한 본원에서 가변 영역 또는 Fv로 지칭되며 항원 결합 부위를 보유함으로써 항원에 대한 항체에 특이성을 부여하는 부분을 나타낸다.
본원에 사용된 "경쇄 가변 도메인" (또는 "경쇄 가변 영역") 및 "중쇄 가변 도메인" (또는 "중쇄 가변 영역")은 동일한 일반 구조를 가지며 각 도메인은 본질적으로 그의 서열이 광범위하게 보존된 4개의 프레임워크 (FR) 영역으로 이루어져 있으며, 이는 당업계 및 이하 본원에서 "프레임워크 영역 1" 또는 "FR1"; "프레임워크 영역 2" 또는 "FR2"; "프레임워크 영역 3" 또는 "FR3"; 및 "프레임워크 영역 4" 또는 "FR4"로 각각 지칭되며; 프레임워크 영역은 3개의 초가변 영역, HVR (또는 CDR)에 의해 중단되며, 이는 당업계 및 이하에서 "상보성 결정 영역 1" 또는 "CDR1"; "상보성 결정 영역 2" 또는 "CDR2" 및 "상보성 결정 영역 3" 또는 "CDR3"으로 각각 지칭된다. 따라서, 면역글로불린 가변 도메인의 일반적인 구조 또는 서열은 다음과 같이 표시될 수 있다: FR1-CDR1-FR2-CDR2-FR3-CDR3-FR4. 프레임워크 영역은 베타 시트 형태를 채용하고, CDR은 베타 시트 구조를 연결하는 루프를 형성할 수 있다. 각 쇄의 CDR은 프레임워크 영역에 의해 3차원 구조로 유지되고 다른 쇄로부터의 CDR과 함께 항원 결합 부위를 형성한다.
CDR의 다양한 정의가 당업계에 공지되어 있으며, 예를 들면 IMGT라고도 지칭되는 CCG에 기반한 정의 (Lefranc MP, Pommie C, Ruiz M, Giudicelli V, Foulquier E, Truong L, Thouvenin-Contet V, Lefranc G. "IMGT unique numbering for immunoglobulin and T cell receptor variable domains and Ig superfamily V-like domains." Dev Comp Immunol. 2003 Jan;27(1):55-77; Giudicelli V, Brochet X, Lefranc MP. "IMGT/V-QUEST: IMGT standardized analysis of the immunoglobulin (IG) and T cell receptor (TR) nucleotide sequences". Cold Spring Harb Protoc. 2011;2011(6):695-715)) 또는 Kabat (E.A. Kabat, T.T. Wu, H. Bilofsky, M. Reid-Miller 및 H. Perry, Sequence of Proteins of Immunological Interest, National Institutes of Health, Bethesda (1983))와 함께 Chothia에 기반한 정의 (Chothia and Lesk, J. Mol. Biol. 1987, 196: 901-917)가 있다. 본 발명의 맥락 내에서, CDR에 대한 언급은 CCG (IMGT)의 정의에 기반한다.
본 출원에서 사용되는 용어 "불변 도메인" 또는 "불변 영역"은 가변 영역 이외의 총 항체 도메인을 의미한다. 이러한 불변 도메인 및 영역은 당업계의 기술 수준에서 잘 알려져 있으며, Kabat 등에 의해 기술되었다 ("Sequence of proteins of immunological interest", US Public Health Services, NIH Bethesda, MD, Publication No. 91-3242 (1991)). 그의 중쇄 불변 영역의 아미노산 서열에 따라, 항체 또는 면역글로불린은 IgA, IgD, IgE, IgG 및 IgM 클래스로 분류된다. 중쇄 불변 영역에 따라, 면역글로불린의 상이한 부류는 각각 α, δ, ε, γ 및 μ로 불린다. 이들 중 몇 개는 하위 클래스 (동형), 예를 들어 IgG1, IgG2, IgG3 및 IgG4, IgA1 및 IgA2로 더 분류될 수 있다.
항체의 "Fc 부분" 또는 "Fc 도메인"은 항원에 대한 항체의 결합에 직접적으로 관여하지 않지만, 다양한 이펙터 기능을 나타낸다. "항체의 Fc 부분/도메인"은 당업자에게 잘 알려진 용어이며 항체의 파파인 절단에 기초하여 정의된다. 항체의 Fc 부분은 보체 활성화, C1q 결합 및 Fc 수용체 결합에 기초하여 ADCC (항체 의존성 세포 매개 세포 독성) 및 CDC (보체 의존성 세포 독성)에 직접 관여한다. 보체 활성화 (CDC)는 대부분의 IgG 항체 하위 클래스의 Fc 부분에 보체 인자 C1q를 결합시킴으로써 개시된다. 보체 시스템에 대한 항체의 영향은 특정 조건에 의존적이지만, Clq에 대한 결합은 Fc 부분의 한정된 결합 부위에 의해 야기된다. 이러한 결합 부위는 예를 들어 L234, L235, D270, N297, E318, K320, K322, P331 및 P329 (Eu 넘버링에 따른 번호 매김, Edelman et al, Proc Natl Acad Sci U S A. 1969 May;63(1):78-85 참조)이다. IgG1에서 C1q 및 Fcγ 수용체 결합을 매개하는 이들 잔기 중에서 가장 중요한 것은 L234 및 L235이다 (Hezareh et al., J. Virology 75 (2001) 12161- 12168, Shields et al (2001) JBC, 276 (9): 6591-6604). 하위 클래스 IgG1 및 IgG3의 항체는 보체 활성화 및 C1q 및 C3 결합을 보인 반면, IgG2 및 IgG4는 보체 시스템을 활성화시키지 않으며 C1q 및 C3에 결합하지 않는다.
용어 "항체" 또는 "항체 분자" (본원에서 동의어로 사용됨)는 모노클로날 항체, 폴리클로날 항체, 인간 항체, 인간화 항체, 서열 최적화 항체, 키메라 항체, 다중 특이적 항체 (예를 들어 이중 특이적 항체), 항체의 단편, 특히 Fv, Fab, Fab' 또는 F(ab')2 단편, 단일쇄 항체, 특히 단일쇄 가변 단편 (scFv), 단일쇄 Fab 단편 (scFab), 소형 모듈 면역약제 (SMIP), 도메인 항체, 나노바디®, 디아바디 (diabody)를 포함한다. 항체는 항체의 Fc 부분에 의해 통상 매개되는 ADCC 또는 CDC와 같은 이펙터 기능을 가질 수 있거나 또는 예를 들어 Fc 부분을 갖지 않거나 차단, 마스킹된 Fc 부분, 본질적으로 면역 세포 또는 보체 시스템과 같은 면역계 성분에 의해 인식되지 않거나 불충분하게 인식되는 Fc 부분을 가짐으로써 이펙터 기능을 갖지 않을 수 있다.
모노클로날 항체 (mAb)는 아미노산 서열이 동일한 단일 특이성 항체이다. 그들은 특이적 항체 생성 B 세포와 골수종 (B 세포 암) 세포의 융합 클론을 나타내는 하이브리드 세포주 (하이브리도마 (hybridoma)라 칭함)로부터 하이브리도마 기술에 의해 생성될 수 있다 (Kohler G, Milstein C. Continuous cultures of fused cells secreting antibody of predefined specificity. Nature 1975;256:495-7). 대안적으로, 모노클로날 항체는 숙주 세포에서 재조합 발현에 의해 생성될 수 있다 (Norderhaug L, Olafsen T, Michaelsen TE, Sandlie I. (May 1997). "Versatile vectors for transient and stable expression of recombinant antibody molecules in mammalian cells." J Immunol Methods 204 (1): 77-87; 또한 하기 참조). "재조합 항체" 또는 "재조합 결합 분자"는 재조합적으로 조작된 숙주 세포에 의해 생성된 항체 또는 결합 분자이다. 이는 선택적으로 단리되거나 정제된다.
본 발명에 따른 항체 분자는 또한 Fab, Fab', 또는 F(ab')2 단편과 같은 항원 결합 특성을 유지하는 면역글로불린의 단편을 포함한다. 이러한 단편은 예를 들어 면역글로불린의 단편화, 예를 들어 단백질 분해 또는 이러한 단편의 재조합 발현에 의해 얻을 수 있다. 예를 들어, 면역글로불린 소화는 일상적인 기술, 예를 들어 파파인 또는 펩신 사용 (WO 94/29348)으로 이룰 수 있다. 항체의 파파인 소화는 전형적으로 두개의 동일한 항원 결합 단편 (Fab)을 생성한다. Fab 단편은 중쇄 및 경쇄 각각의 하나의 불변 및 하나의 가변 도메인으로 구성된다. 펩신 처리는 F (ab')2를 산출한다. Fab 단편에서, 가변 도메인은 각각 바람직하게는 인간 기원의 면역글로불린 불변 도메인에 융합된다. 따라서, 중쇄 가변 도메인은 CH1 도메인 (소위 Fd 단편)에 융합되고, 경쇄 가변 도메인은 CL 도메인에 융합된다. Fab 단편은 숙주 세포에서 각각의 핵산의 재조합 발현에 의해 생성될 수 있다 (아래 참조).
상이한 분자 맥락에서 면역글로불린의 가변 도메인, 또는 이러한 가변 도메인으로부터 유래된 분자를 배치하기 위한 다수의 기술이 개발되어 왔다. 이들 또한 본 발명에 따른 "항체" 또는 "항체 분자"로 간주되어야 한다. 일반적으로, 이러한 항체 분자는 면역글로불린에 비해 크기가 더 작으며, 단일 아미노산 쇄 또는 여러 아미노산 쇄를 포함할 수 있다. 예를 들어, "단일쇄 가변 단편 (scFv)"은 일반적으로 세린 (S) 또는 글리신 (G)과 같은 짧은 링커와 함께 연결된 면역글로불린의 중쇄 및 경쇄 가변 영역의 융합이다 (WO 88/01649; WO 91/17271; Huston et al; International Reviews of Immunology, Volume 10, 1993, 195 - 217). "단일 도메인 항체" 또는 "나노바디®"는 단일 Ig-유사 도메인에 항원 결합 부위를 보유한다 (WO 94/04678; WO 03/050531, Ward et al., Nature. 1989 Oct 12;341(6242):544-6; Revets et al., Expert Opin Biol Ther. 5(1):111-24, 2005). 동일하거나 상이한 항원에 대한 결합 특이성을 갖는 하나 이상의 단일 도메인 항체가 함께 연결될 수 있다. "디아바디"는 2개의 가변 도메인을 포함하는 2개의 아미노산 쇄로 이루어진 2가 항체 분자이다 (WO 94/13804, Holliger et al., Proc Natl Acad Sci U S A. 1993 Jul 15;90(14):6444-8). 항체-유사 분자의 다른 예는 "면역글로불린 슈퍼패밀리 항체" (IgSF; Srinivasan and Roeske, Current Protein Pept. Sci. 2005, 6(2): 185-96)이다. 다른 개념은 불변 도메인 CH1이 없는 단일쇄 힌지 및 이펙터 도메인에 연결된 Fv 도메인을 포함하는 소위 "소형 모듈형 면역약제 (SMIP)"로 이어진다 (WO 02/056910). "단일쇄 Fab" 또는 "scFab"는 경쇄 Fab 도메인 (즉, 하나의 경쇄 불변 도메인 (CL)에 연결된 경쇄 가변 도메인 (VL))과 중쇄 Fab 도메인 (즉, 하나의 중쇄 불변 도메인 (CH1)에 연결된 중쇄 가변 도메인 (VH))의 융합이다. 단일쇄 Fab는 항원을 인식하고 결합할 수 있다. scFab는 또한 CL과 VH 도메인 사이에 위치한 링커 (예: 펩티드 링커)를 선택적으로 포함할 수 있다 (Hust et al. BMC Biotechnology2007, 7:14).
인간에서의 적용을 위해, 기원적으로 마우스와 같은 다른 종에서 유래된 치료 분자, 예컨대 본원에 기술된 바와 같이 항원 결합 단위를 포함하는 항체 또는 결합 단백질의 면역원성을 감소시키는 것이 종종 바람직하다. 이것은 키메라 항체/결합 단백질의 작제 또는 "인간화"로 불리는 과정에 의해 이루어질 수 있다. 이 문맥에서, "키메라 항체"; 또는 "키메라 항원 결합 단위"는 상이한 종 (예를 들어 인간)으로부터 유래된 서열 부분 (예를 들어, 불변 도메인)에 융합된 하나의 종 (예를 들어 마우스)으로부터 유래된 서열 부분 (예를 들어 가변 도메인)을 포함하는 항체 또는 항원 결합 단위로 이해된다. 이 문맥에서, "인간화 항체", "인간화 항원 결합 단위" 또는 "인간화 VL/VH 도메인"은 기원적으로 비인간 종에서 유래된 가변 도메인을 포함하는 항체, 항원 결합 단위 또는 VL/VH 도메인이며, 여기서 특정 아미노산은 그 가변 도메인의 전체 서열을 인간 가변 도메인의 서열에 보다 가깝게 만들기 위해 돌연변이되어 있다. 항체의 인간화 방법은 당해 기술 분야에 잘 알려져 있다 (Billetta R, Lobuglio AF. "Chimeric antibodies". Int Rev Immunol. 1993;10(2-3):165-76; Riechmann L, Clark M, Waldmann H, Winter G (1988). "Reshaping human antibodies for therapy". Nature: 332:323).
본원에 사용된 용어 "인간 항체", "인간 항원 결합 단위" 또는 "인간 VH/VL 도메인"은 인간 생식계열 면역글로불린 서열로부터 유래된 가변 (및 적용 가능한 경우 불변) 영역을 갖는 항체, 항원 결합 단위 또는 VH/VL 도메인을 포함한다. 본원에 사용된 용어 "인간 항체", "인간 항원 결합 단위" 또는 "인간 VH/VL 도메인"은 마우스, 래트 또는 토끼와 같은 다른 (포유류) 종의 생식계열로부터 유래된 CDR 서열이 인간 프레임워크 서열에 이식되어 있는 항체를 포함하도록 의도되지 않는다. 따라서, 본원에 사용된 용어 "인간 항체", "인간 항원 결합 단위", 또는 "인간 VH/VL 도메인"은 단백질의 모든 부분 (예를 들어, CDR, 프레임워크, CL, CH 도메인 (예를 들어, CH1, CH2, CH3), 힌지, VL, VH)이 인간에서 실질적으로 비면역원성이며, 하기 본원에서 추가로 기술되는 바와 같이 단지 약간의 서열 변화 또는 변이를 갖는 항체, 항원 결합 단위 또는 VH/VL 도메인을 지칭한다.
이러한 "인간 항체", "인간 항원 결합 단위", 또는 "인간 VH/VL 도메인"을 생성하기 위한 기술이 기재되어 있으며, 파지 디스플레이 또는 형질전환 동물의 사용을 제한없이 포함한다 (WWW. Ablexis.com/technology-alivamab.php; WO 90/05144; D. Marks, H.R. Hoogenboom, T.P. Bonnert, J. McCafferty, A.D. Griffiths and G. Winter (1991) "By-passing immunisation. human antibodies from V-gene libraries displayed on phage." J.Mol.Biol., 222, 581-597; Knappik et al., J. Mol. Biol. 296: 57-86, 2000; S. Carmen and L. Jermutus, "Concepts in antibody phage display". Briefings in Functional Genomics and Proteomics 2002 1(2):189-203; Lonberg N, Huszar D. "Human antibodies from transgenic mice". Int Rev Immunol. 1995;13(1):65-93.; Brueggemann M, Taussig MJ. "Production of human antibody repertoires in transgenic mice". Curr Opin Biotechnol. 1997 Aug;8(4):455-8.).
따라서, 인간 항체, 인간 항원 결합 단위 또는 인간 VH/VL 도메인은 예를 들어 키메라 또는 인간화 항체와 구별된다. 인간 항체, 인간 항원 결합 단위 또는 인간 VH/VL 도메인은 기능적으로 재배열된 인간 면역글로불린 (예를 들어, 중쇄 및/또는 경쇄) 유전자를 발현할 수 있는 비-인간 동물 또는 원핵 또는 진핵 세포에 의해 생성될 수 있음이 언급된다.
본 발명의 키메라, 인간화 또는 인간 항체, 항원 결합 단위, 또는 VH/VL 도메인은 추가로 최적화될 수 있고; 본원에서 "최적화된" 또는 "서열 최적화된" 항체, 항원 결합 단위 또는 VH/VL 도메인으로도 지칭된다. 이러한 최적화는 예를 들어 인간에서 면역원성을 감소시키거나 탈아미드화, 바람직하지 않은 전하 또는 친유성 또는 비특이적 결합을 피하기 위해 바람직하지 않은 아미노산의 제거 또는 교환을 제한 없이 포함한다. 바람직하지 않은 아미노산의 이러한 제거 또는 교환은 예를 들어 시험관내 무작위 또는 부위-특이적 돌연변이유발에 의해 또는 생체내 체세포 돌연변이에 의해 도입될 수 있다. 더욱이, 키메라 또는 인간화 항체, 항원 결합 단위 또는 VH/VL 도메인과 관련하여, 특정 마우스 FR 잔기가 최적화된 항체, 항원 결합 단위 및 VH/VL 도메인의 기능에 중요할 수 있음이 이해될 것이다. 따라서 이러한 중요한 아미노산 잔기는 최적화된 항체, 항원 결합 단위 및 VH/VL 도메인에 유지될 수 있다.
용어 "단량체"는 본원에 기재된 항체 또는 다중 특이적 단백질의 균질한 형태를 지칭한다. 예를 들어, 전장 항체의 경우 단량체는 2개의 동일한 중쇄와 2개의 동일한 경쇄를 갖는 단량체 항체를 의미한다. 본 발명의 맥락에서, 단량체는 본원에 기술된 바와 같이 B7H6에 특이적인 단일 항원 결합 단위 및 CD3에 특이적인 단일 항원 결합 단위를 갖는 본 발명의 단백질을 의미한다. 예를 들어, 본원에 기재된 결합 단백질의 단량체는 2개의 폴리펩티드 쇄, 즉 B7H6에 특이적인 단일쇄 Fab 및 제1 Fc 도메인을 포함하는 제1 폴리펩티드 쇄 및 CD3에 특이적인 단일쇄 Fab 및 제2 Fc 도메인을 포함하는 제2 폴리펩티드 쇄를 가질 수 있다.
에피토프는 항체 또는 항원 결합 모이어티 (예를 들어, 본원에 기재된 단백질의 항원 결합 단위)에 의해 결합되는 항원의 영역이다. 용어 "에피토프"는 항체 또는 항원 결합 모이어티에 특이적으로 결합할 수 있는 임의의 폴리펩티드 결정인자를 포함한다. 특정 실시양태에서, 에피토프 결정인자는 아미노산, 글리칸 측쇄, 포스포릴 또는 설포닐과 같은 분자의 화학적 활성 표면 그룹을 포함하고, 특정 실시양태에서 특정 3차원 구조적 특성 및/또는 특정 전하 특성을 가질 수 있다. 구조적 및 비구조적 에피토프는 변성 용매의 존재하에서 전자에 대한 결합이 손실되지 않고 후자에서는 그렇치 않다는 점에서 구별된다.
특정 에피토프, 항원 또는 단백질 (또는 그의 적어도 하나의 부분, 단편 또는 에피토프에 대해) "과 결합할 수 있다", "에 결합할 수 있다" 또는 "와 특이적으로 결합할 수 있다", "과 결합한다" 또는 "와 특이적으로 결합한다", "에 대해 친화성을 가진다, "에 대해 특이적이다" 및/또는 "에 대해 특이성을 가진다"는 항원 결합 분자/단백질 (예를 들어, 면역글로불린, 항체, 항원 결합 단위 또는 이러한 항원 결합 분자/단백질의 단편)은 상기 에피토프, 항원 또는 단백질 "에 대한", "에 대해 지향된"이라고 하거나, 또는 이러한 에피토프, 항원 또는 단백질에 대한 "결합 "분자/단백질이다. 이러한 용어는 본원에서 상호 교환 가능하게 사용된다.
본원에 사용된 용어 "결합" 및 "특이적 결합"은 정제된 야생형 항원을 사용한 시험관내 분석, 바람직하게는 플라즈몬 공명 분석 (Malmqvist M., "Surface plasmon resonance for detection and measurement of antibody-antigen affinity and kinetics.", Curr Opin Immunol. 1993 Apr;5(2):282-6.)에서 항원의 에피토프에 대한 항원 결합 분자/단백질 (예를 들어, 면역글로불린, 항체, 항원 결합 단위 또는 이러한 항원 결합 분자/단백질의 단편)의 결합을 지칭한다. 항체 친화성은 또한 키네틱 배제 분석 (kinetic exclusion assay (KinExA)) 기술을 사용하여 측정할 수 있다 (Darling, R.J., and Brault P-A., "Kinetic exclusion assay technology: Characterization of Molecular Interactions." ASSAY and Drug Development Technologies. 2004, Dec 2(6): 647-657). 예를 들어, 본 발명의 결합 단백질 또는 단백질은 그의 제1 항원 결합 단위/제1 폴리펩티드 쇄를 갖는 B7H6의 에피토프 및 그의 제2 항원 결합 단위/제2 폴리펩티드 쇄를 갖는 CD3의 에피토프에 결합한다.
일반적으로, 용어 "특이성"은 특정 항원 결합 분자/단백질 (예컨대 면역글로불린, 항체, 항원 결합 단위, 또는 항원 결합 분자/단백질의 단편)이 결합할 수 있는 상이한 타입의 항원 또는 에피토프의 수를 지칭한다. B7H6에 대한 결합 특이성은 본 발명의 항원 결합 단백질/분자 (예를 들어, 이러한 결합 단백질의 제1 항원 결합 단위)가 구조적으로 관련이 없는 분자보다 B7H6에 대해 상당히 더 높은 결합 친화성을 갖는다는 것을 의미한다. CD3에 대한 결합 특이성은 본 발명의 항원 결합 단백질/분자 (예를 들어, 이러한 결합 단백질의 제2 항원 결합 단위)가 구조적으로 관련이 없는 분자보다 CD3에 대해 상당히 더 높은 결합 친화도를 갖는다는 것을 의미한다. 항원-결합 분자/단백질의 특이성은 그의 친화력 및/또는 결합력에 기초하여 결정될 수 있다. 항원과 항원 결합 단백질의 해리에 대한 평형 상수 (KD)로 표시되는 친화력은 항원 결합 분자/단백질상의 항원 결합 부위와 에피토프 사이의 결합 강도를 측정하기 위한 척도이다; KD 값이 작을수록 에피토프와 항원-결합 부위 사이의 결합 강도가 강해진다 (대안적으로, 친화력은 또한 1/KD인 친화력 상수 (KA)로서 표시될 수 있다). 당업자에게 명백한 바와 같이 (예를 들어, 본원에서의 추가적인 개시에 기초하여), 친화도는 관심있는 특정 항원에 따라 그 자체로 공지된 방식으로 결정될 수 있다. 결합도는 항원-결합 분자/단백질 (면역글로불린, 항체, 항원 결합 단위 또는 이러한 항원 결합 분자/단백질의 단편과 같은)와 관련 항원 사이의 결합 강도의 척도이다. 결합도는 항원 결합 분자/단백질상의 에피토프와 그것의 항원 결합 부위 사이의 친화력 및 항원 결합 분자/단백질 상에 존재하는 관련 결합 부위의 수 모두와 관련된다.
항원 결합 단위/항원, 리간드/수용체, 또는 다른 결합 쌍을 언급할 때, 용어 "특이적으로 결합한다" 또는 "선택적으로 결합한다"는 단백질 및 다른 생물학적 제제의 이종 집단에서 단백질의 존재를 결정하는 결합 반응을 나타낸다. 따라서, 지정된 조건에서 특정 항원 결합 단위는 특정 항원에 결합하고 샘플에 존재하는 다른 단백질에는 상당한 양으로 결합하지 않는다. 항원 결합 단위는 비관련 항원과의 친화성보다 지정된 조건에서 적어도 2배, 바람직하게는 적어도 10배, 보다 바람직하게는 적어도 20배, 가장 바람직하게는 적어도 100배의 친화도로 항원에 결합한다.
본원에 사용된 용어 "단리된 (isolated)"은 원래 또는 자연 환경 (예를 들어, 자연 발생인 경우 천연 환경)으로부터 제거되는 물질을 지칭한다. 예를 들어, 살아있는 동물에 존재하는 자연 발생 폴리뉴클레오티드 또는 폴리펩티드는 단리된 것이 아니지만, 인간이 개입하여 자연계에서 공존하는 물질의 일부 또는 전부로부터 분리된 동일한 폴리뉴클레오티드 또는 폴리펩티드는 단리된 것이다. 그러한 폴리뉴클레오티드는 벡터의 일부일 수 있고/있거나 그러한 폴리뉴클레오티드 또는 폴리펩티드는 조성물의 일부일 수 있고, 그러한 벡터 또는 조성물은 자연계에서 발견되는 환경의 일부가 아니라는 점에서 여전히 단리된 것일 수 있다. 예를 들어, 그의 천연 생물학적 공급원 및/또는 그로부터 얻은 반응 배지 또는 배양 배지와 비교할 때 다른 핵산, 다른 단백질/폴리펩티드, 다른 생물학적 성분 또는 거대 분자 또는 적어도 하나의 오염물, 불순물 또는 미량 성분과 같이 일반적으로 상기 공급원 또는 배지에서 결합되는 적어도 하나의 다른 성분으로부터 분리된 경우 이 핵산, 단백질/폴리펩티드 분자는 "본질적으로 단리된 (형태)"로 간주된다. 특히, 핵산 또는 단백질/폴리펩티드 분자는 적어도 2배, 특히 적어도 10배, 더욱 특히 적어도 100배, 최대 1000배까지 정제되었을 때 "본질적으로 단리된" 것으로 간주된다. "본질적으로 단리된 형태"인 핵산 또는 단백질/폴리펩티드 분자는 적합한 크로마토그래피 기술, 예를 들어 폴리아크릴 아미드-겔 전기영동과 같은 적합한 기술을 사용하여 결정된 바, 바람직하게는 본질적으로 균질하다.
본원에서 사용된 것으로 2 이상의 핵산 또는 폴리펩티드 서열의 문맥에서 "동일" 또는 "퍼센트 동일성"이란 용어는 동일하거나, 또는 비교하고 최대한 대응되도록 정렬되었을 때 동일한 특정 퍼센트의 뉴클레오티드 또는 아미노산 잔기를 가지는 2 이상의 서열 또는 부분 서열들을 지칭한다. 퍼센트 동일성을 결정하기 위해, 서열은 최적의 비교 목적을 위해 정렬된다 (예를 들어, 제2 아미노 또는 핵산 서열과의 최적의 정렬을 위해 제1 아미노산의 서열 또는 핵산 서열에 갭이 도입될 수 있다). 이어서, 상응하는 아미노산 위치 또는 뉴클레오티드 위치의 아미노산 잔기 또는 뉴클레오티드를 비교한다. 제1 서열의 위치가 제2 서열의 상응하는 위치와 동일한 아미노산 잔기 또는 뉴클레오티드에 의해 점유된 경우, 분자는 그 위치에서 동일하다. 두 서열 간의 퍼센트 동일성은 서열에 의해 공유되는 동일한 위치의 수의 함수이다 (즉, % 동일성 = 동일한 위치의 수/전체 위치의 수 (예를 들어, 중첩 위치)×100). 일부 실시양태에서, 비교되는 2개의 서열은 적합하다면 갭이 서열 내에 도입된 후 동일한 길이이다 (예를 들어, 비교되는 서열을 넘어서 연장되는 추가 서열을 배제한다). 예를 들어, 가변 영역 서열이 비교될 때, 선도 (신호 펩티드) 및/또는 불변 도메인 서열은 고려되지 않는다. 두 서열 간의 서열 비교를 위해, "상응하는" CDR은 양 서열에서 동일한 위치에 있는 CDR을 의미한다 (예를 들어, 각 서열의 CDR-H1).
두 서열 간의 % 동일성 또는 % 유사성의 결정은 수학적 알고리즘을 사용하여 수행할 수 있다. 두 서열의 비교에 이용되는 수학적 알고리즘의 바람직한 비제한적인 예는 [Karlin and Altschul, 1990, Proc. Natl. Acad. Sci. USA 87:2264-2268, modified as in Karlin and Altschul, 1993, Proc. Natl. Acad. Sci. USA 90:5873-5877]의 알고리즘이다. 이러한 알고리즘은 [Altschul et al., 1990, J. Mol. Biol. 215:403-410]의 NBLAST 및 XBLAST 프로그램에 통합되어 있다. 관심있는 단백질을 암호화하는 핵산에 상동성인 뉴클레오티드 서열을 얻기 위해 NBLAST 프로그램, score = 100, wordlength = 12로 BLAST 뉴클레오티드 검색을 수행할 수 있다. 관심있는 단백질과 상동성인 아미노산 서열을 얻기 위해 XBLAST 프로그램, score = 50, wordlength = 3으로 BLAST 단백질 검색을 수행할 수 있다. 비교 목적을 위한 갭 정렬을 얻기 위해, Gapped BLAST를 [Altschul et al., 1997, Nucleic Acids Res. 25:3389-3402]에 기재된 바와 같이 이용할 수 있다. 대안적으로, PSI-Blast를 사용하여 분자 간의 거리 관계를 검출하는 반복 검색을 수행할 수 있다 (상동). BLAST, Gapped BLAST 및 PSI-Blast 프로그램을 사용하는 경우, 각 프로그램 (예를 들어, XBLAST 및 NBLAST)의 디폴트 매개변수가 이용될 수 있다. 서열의 비교에 이용되는 수학적 알고리즘의 또 다른 바람직한 비제한적 예는 Myers and Miller, CABIOS (1989)의 알고리즘이다. 이러한 알고리즘은 GCG 서열 정렬 소프트웨어 패키지의 일부인 ALIGN 프로그램 (버전 2.0)에 통합된다. 아미노산 서열을 비교하기 위한 ALIGN 프로그램을 이용하는 경우, PAM120 중량 잔기 표, 갭 길이 패널티 12 및 갭 패널티 4가 사용될 수 있다. 서열 분석을 위한 추가적인 알고리즘은 당업계에 공지되었으며 [Torellis and Robotti, 1994, Comput. Appl. Biosci. 10:3-5]에 기술된 바와 같은 ADVANCE 및 ADAM; 및 [Pearson and Lipman, 1988, Proc. Natl. Acad. Sci. USA 85:2444-8]에 기술된 바와 같은 FASTA를 포함한다. FASTA 내에서, ktup은 검색의 민감도와 속도를 설정하는 제어 옵션이다. ktup=2인 경우, 비교되는 두 서열의 유사한 영역은 정렬된 잔기의 쌍을 관찰함으로써 발견된다; ktup=1이면 단일 정렬된 아미노산을 조사한다. ktup은 단백질 서열의 경우 2 또는 1로, DNA 서열의 경우 1에서 6까지 설정할 수 있다. ktup을 지정하지 않으면 디폴트값은 단백질의 경우 2이고 DNA의 경우 6이다. 대안적으로, 단백질 서열 정렬은 [Higgins et al., 1996, Methods Enzymol. 266:383-402]에 기술된 바와 같은 CLUSTAL W 알고리즘을 사용하여 수행할 수 있다.
본원에 사용된 용어 "공유 연결" 또는 "공유 결합"은 잔기 사이의 직접 공유 결합, 또는 2개의 잔기가 직접 결합되지 않고 둘 다 중간 분자 또는 도메인, 예를 들어 면역글로불린의 중간 도메인 또는 링커에 공유 결합되는 간접 연결/결합을 의미한다.
본 발명의 다중-특이적 결합 단백질
본 발명은 B7H6에 특이적으로 결합하는 적어도 하나의 항원 결합 단위 (제1 항원 결합 단위) 및 CD3에 특이적으로 결합하는 적어도 하나의 항원 결합 단위 (제2 항원 결합 단위)를 포함하는 다중 특이적 결합 단백질을 제공한다. T 세포 상의 종양 세포 항원 및 CD3에 대한 동시 결합을 통해, 결합 단백질은 T 세포 활성화 단백질로서 작용하고 본원에서 T 세포 인게이저로도 지칭된다. 용어 "(다중 특이적) 결합 단백질"은 본원에서 용어 "(다중 특이적) 결합 분자"와 상호교환적으로 사용된다. 본 발명의 다중 특이적 결합 단백질을 지칭하기 위해 본원에 사용된 추가 용어는 "본 발명의 단백질", "본 발명의 결합 단백질", "항원-결합 단백질" 및 "다중 특이적 단백질"이다.
본 발명자들은 놀랍게도 본 발명의 다중 특이적 결합 단백질이 T 세포의 존재하에 B7H6-양성 결장직장암 세포주의 강력하고 선택적인 용해를 유도하고 표적 세포에 대한 낮은 이펙터 비에서 이미 활성임을 발견하였다. 중요하게는, 본 발명의 결합 단백질은 B7H6-음성 세포를 용해하지 않고 B7H6-양성 세포의 부재하에 T 세포 활성화, T 세포 증식 및 사이토카인 분비를 일으키지 않는다. 특히, 시험관내 NKp30을 통한 B7H6 의존성 NK 세포 활성화를 억제하지 않는 본 발명의 단백질은 B7H6-양성 종양 세포를 용해시키는 데 더 강력하다. 이 활성은 예를 들어 실시예 11의 시험관내 분석에서 설명된다.
의심의 여지를 피하기 위해, 본원에 사용된 B7H6은 UniProt Q68D85의 인간 B7H6 및 그 단백질을 암호화하는 핵산 서열을 지칭한다. 본원에서 CD3는 인간 CD3엡실론 (UniProt P07766) 및 CD3 감마 (Uniprot: P09693) 복합체 (인간 CD3εγ 복합체)를 의미한다. 당업자는 B7H6 및 B7-H6이라는 용어가 본 명세서에서 상호교환가능하게 사용됨을 이해할 것이다.
일 측면에서, 본 발명의 다중 특이적 결합 단백질은 B7H6에 특이적으로 결합하는 제1 항원 결합 단위 및 CD3에 특이적으로 결합하는 제2 항원 결합 단위를 포함하고, 여기서 상기 제1 결합 단위는 하기 i) 내지 xxiv)로 이루어진 군으로부터 선택된다:
i) 서열 번호 1 (CDR1), 서열 번호 2 (CDR2) 및 서열 번호 3 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 4 (CDR1), 서열 번호 5 (CDR2) 및 서열 번호 6 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#1);
ii) 서열 번호 7 (CDR1), 서열 번호 8 (CDR2) 및 서열 번호 9 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 10 (CDR1), 서열 번호 11 (CDR2) 및 서열 번호 12 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#2);
iii) 서열 번호 13 (CDR1), 서열 번호 14 (CDR2) 및 서열 번호 15 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 16 (CDR1), 서열 번호 17 (CDR2) 및 서열 번호 18 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#3);
iv) 서열 번호 19 (CDR1), 서열 번호 20 (CDR2) 및 서열 번호 21 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 22 (CDR1), 서열 번호 23 (CDR2) 및 서열 번호 24 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#4);
v) 서열 번호 25 (CDR1), 서열 번호 26 (CDR2) 및 서열 번호 27 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 28 (CDR1), 서열 번호 29 (CDR2) 및 서열 번호 30 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#5);
vi) 서열 번호 31 (CDR1), 서열 번호 32 (CDR2) 및 서열 번호 33 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 34 (CDR1), 서열 번호 35 (CDR2) 및 서열 번호 36 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#6);
vii) 서열 번호 37 (CDR1), 서열 번호 38 (CDR2) 및 서열 번호 39 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 40 (CDR1), 서열 번호 41 (CDR2) 및 서열 번호 42 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#7);
viii) 서열 번호 43 (CDR1), 서열 번호 44 (CDR2) 및 서열 번호 45 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 46 (CDR1), 서열 번호 47 (CDR2) 및 서열 번호 48 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#8);
ix) 서열 번호 49 (CDR1), 서열 번호 50 (CDR2) 및 서열 번호 51 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 52 (CDR1), 서열 번호 53 (CDR2) 및 서열 번호 54 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#9);
x) 서열 번호 55 (CDR1), 서열 번호 56 (CDR2) 및 서열 번호 57 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 58 (CDR1), 서열 번호 59 (CDR2) 및 서열 번호 60 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#10);
xi) 서열 번호 61 (CDR1), 서열 번호 62 (CDR2) 및 서열 번호 63 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 64 (CDR1), 서열 번호 65 (CDR2) 및 서열 번호 66 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#11);
xii) 서열 번호 67 (CDR1), 서열 번호 68 (CDR2) 및 서열 번호 69 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 70 (CDR1), 서열 번호 71 (CDR2) 및 서열 번호 72 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#12));
xiii) 서열 번호 73 (CDR1), 서열 번호 74 (CDR2) 및 서열 번호 75 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 76 (CDR1), 서열 번호 77 (CDR2) 및 서열 번호 78 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#13);
xiv) 서열 번호 79 (CDR1), 서열 번호 80 (CDR2) 및 서열 번호 81 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 82 (CDR1), 서열 번호 83 (CDR2) 및 서열 번호 84 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#14);
xv) 서열 번호 85 (CDR1), 서열 번호 86 (CDR2) 및 서열 번호 87 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 88 (CDR1), 서열 번호 89 (CDR2) 및 서열 번호 90 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#15);
xvi) 서열 번호 91 (CDR1), 서열 번호 92 (CDR2) 및 서열 번호 93 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 94 (CDR1), 서열 번호 95 (CDR2) 및 서열 번호 96 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#16);
xvii) 서열 번호 97 (CDR1), 서열 번호 98(CDR2) 및 서열 번호 99 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 100 (CDR1), 서열 번호 101 (CDR2) 및 서열 번호 102 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#17);
xviii) 서열 번호 103 (CDR1), 서열 번호 104 (CDR2) 및 서열 번호 105 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 106 (CDR1), 서열 번호 107 (CDR2) 및 서열 번호 108 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#18);
xix) 서열 번호 109 (CDR1), 서열 번호 110 (CDR2) 및 서열 번호 111 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 112 (CDR1), 서열 번호 113 (CDR2) 및 서열 번호 114 (CDR3)의 아미노산 서열을 포함하는 중쇄 CD을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#19);
xx) 서열 번호 115 (CDR1), 서열 번호 116 (CDR2) 및 서열 번호 117 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 118 (CDR1), 서열 번호 119 (CDR2) 및 서열 번호 120 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#20);
xxi) 서열 번호 121 (CDR1), 서열 번호 122 (CDR2) 및 서열 번호 123 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 124 (CDR1), 서열 번호 125 (CDR2) 및 서열 번호 126 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#21);
xxii) 서열 번호 127 (CDR1), 서열 번호 128 (CDR2) 및 서열 번호 129 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 130 (CDR1), 서열 번호 131 (CDR2) 및 서열 번호 132 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#22);
xxiii) 서열 번호 133 (CDR1), 서열 번호 134 (CDR2) 및 서열 번호 135 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 136 (CDR1), 서열 번호 137 (CDR2) 및 서열 번호 138 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#23); 및
xxiv) 서열 번호 139 (CDR1), 서열 번호 140 (CDR2) 및 서열 번호 141 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 142 (CDR1), 서열 번호 143 (CDR2) 및 서열 번호 144 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 B7H6#24).
본 발명의 결합 단백질의 일부 실시양태에서, CD3에 특이적으로 결합하는 상기 제2 항원 결합 단위는 하기 i) 내지 vi)로 이루어진 군으로부터 선택된다:
i) 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 CD3#1);
ii) 서열 번호 263 (CDR1), 서열 번호 264 (CDR2) 및 서열 번호 265 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 266 (CDR1), 서열 번호 267 (CDR2) 및 서열 번호 268 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 CD3#2);
iii) 서열 번호 269 (CDR1), 서열 번호 270 (CDR2) 및 서열 번호 271 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 272 (CDR1), 서열 번호 273 (CDR2) 및 서열 번호 274 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 CD3#3);
iv) 서열 번호 275 (CDR1), 서열 번호 276 (CDR2) 및 서열 번호 277 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 278 (CDR1), 서열 번호 279 (CDR2) 및 서열 번호 280 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 CD3#4);
v) 서열 번호 281 (CDR1), 서열 번호 282 (CDR2) 및 서열 번호 283 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 284 (CDR1), 서열 번호 285 (CDR2) 및 서열 번호 286 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 CD3#5); 및
vi) 서열 번호 287 (CDR1), 서열 번호 288 (CDR2) 및 서열 번호 289 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 290 (CDR1), 서열 번호 291 (CDR2) 및 서열 번호 292 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위 (항원 결합 단위 CD3#6).
상기 설명된 바와 같은 제1 항원 결합 단위 i) 내지 xxiv)는 각각 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 및 B7H6#2로 지칭되고, 상기 설명된 바와 같은 제2 항원 결합 단위 i) 내지 vi)는 각각 CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 및 CD3#6으로 지칭된다. 본원에서는 본 발명의 특정 항원 결합 단위 및 전장 결합 단백질에 대한 개별 아미노산 서열의 식별 용이성을 위해 서열 표를 제공한다. 이것은 실시예 2의 표 1에 요약되었다.
일반적으로 본원에서 사용되는 항원 결합 단위에 관한 용어 "제1" 및 "제2"는 이들 단위가 (다른 표적 항원에 결합하기 때문에) 2개의 상이한 단위임을 나타내기 위한 것이다. 따라서, 이들 용어는 본 발명의 결합 단백질 내의 단위의 정확한 순서 또는 서열을 나타내는 것으로 이해되어서는 안된다.
일부 실시양태에서, 본 발명의 결합 단백질은 표 1에 나타낸 각각의 CDR 서열에 의해 정의된 바와 같은 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 및 B7H6#24로 이루어진 군으로부터 선택된 제1 항원 결합 단위 및 표 1에 나타낸 각각의 CDR 서열에 의해 정의된 바와 같은 CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 및 CD3#6으로 이루어진 군으로부터 선택된 제2 항원 결합 단위를 포함한다.
일부 실시양태에서, 본 발명의 결합 단백질은 표 1에 나타낸 각각의 CDR 서열에 의해 정의된 바와 같은 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 및 B7H6#24로 이루어진 군으로부터 선택된 제1 항원 결합 단위 및 표 1에 나타낸 각각의 CDR 서열에 의해 정의된 바와 같은 CD3#1의 제2 항원 결합 단위를 포함한다. 바람직한 실시양태에서, 본 발명의 결합 단백질은 표 1에 나타낸 각각의 CDR 서열에 의해 정의된 바와 같은 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 및 B7H6#24로 이루어진 군으로부터 선택된 제1 항원 결합 단위 및 표 1에 나타낸 각각의 CDR 서열에 의해 정의된 바와 같은 CD3#1의 제2 항원 결합 단위를 포함한다. 바람직한 실시양태에서, 본 발명의 결합 단백질은 표 1에 나타낸 각각의 CDR 서열에 의해 정의된 바와 같은 B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 및 B7H6#24로 이루어진 군으로부터 선택된 제1 항원 결합 단위 및 표 1에 나타낸 각각의 CDR 서열에 의해 정의된 바와 같은 CD3#1의 제2 항원 결합 단위를 포함한다. 바람직한 실시양태에서, 본 발명의 결합 단백질은 표 1에 나타낸 각각의 CDR 서열에 의해 정의된 바와 같은 B7H6#12, B7H6#14, B7H6#15, B7H6#16, 및 B7H6#23으로 이루어진 군으로부터 선택된 제1 항원 결합 단위 및 표 1에 나타낸 각각의 CDR 서열에 의해 정의된 바와 같은 CD3#1의 제2 항원 결합 단위를 포함한다.
본원에 기재된 CDR 서열 외에, 본 발명의 결합 단백질의 항원 결합 단위는 면역글로불린 프레임워크 영역 (FR) 서열을 포함한다. 이들 서열은 바람직하게는 인간에서 면역원성이 아니며, 따라서 바람직하게는 인간, 인간화 또는 최적화된 FR 서열이다. 적합한 인간, 인간화 또는 최적화된 FR 서열은 당업계에 공지되어 있다. 특히 바람직한 FR 서열은 완전한 항원 결합 단위 및 그에 따른 CDR 서열 및 FR 서열을 개시하는 본원에 제시된 실시양태로부터 취해질 수 있다. 바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 67 (CDR1), 서열 번호 68 (CDR2) 및 서열 번호 69 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 70 (CDR1), 서열 번호 71 (CDR2) 및 서열 번호 72 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 B7H6에 특이적으로 결합하는 제1 항원 결합 단위와 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 CD3에 특이적으로 결합하는 제2 항원 결합 단위를 포함한다. 이러한 항원 결합 단백질은 본원에서 B7H6#14/CD3#1로 지칭된다. 특히 바람직한 실시양태에서, 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위는 각각 VL/VH 도메인 내, 예를 들어 서열 최적화된 VL/VH 도메인 내에 상기 정의된 바와 같은 CDR(B7H6#12/CD3#1)을 포함한다. 특히 바람직한 실시양태에서, 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위 (B7H6#12/CD3#1)는 각각 scFab에 의해 형성되고 선택적으로 각각 Fc 도메인에 연결된다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 79 (CDR1), 서열 번호 80 (CDR2) 및 서열 번호 81 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 82 (CDR1), 서열 번호 83 (CDR2) 및 서열 번호 84 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 B7H6에 특이적으로 결합하는 제1 항원 결합 단위와 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 CD3에 특이적으로 결합하는 제2 항원 결합 단위를 포함한다. 이러한 항원 결합 단백질은 본원에서 B7H6#14/CD3#1로 지칭된다. 특히 바람직한 실시양태에서, 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위는 각각 VL/VH 도메인, 예를 들어, 서열 최적화된 VL/VH 도메인 내에 상기 정의된 바와 같은 CDR (B7H6#14/CD#1)을 포함한다. 특히 바람직한 실시양태에서, 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위 (B7H6#14/CD3#1)는 각각 scFab에 의해 형성되고 선택적으로 각각 Fc 도메인에 연결된다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 85 (CDR1), 서열 번호 86 (CDR2) 및 서열 번호 87 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 88 (CDR1), 서열 번호 89 (CDR2) 및 서열 번호 90 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 B7H6에 특이적으로 결합하는 제1 항원 결합 단위와 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 CD3에 특이적으로 결합하는 제2 항원 결합 단위를 포함한다. 이러한 항원 결합 단백질은 본원에서 B7H6#15/CD3#1로 지칭된다. 특히 바람직한 실시양태에서, 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위는 VL/VH 도메인, 예를 들어 서열 최적화된 VL/VH 도메인 내에 각각 상기 정의된 바와 같은 CDR (B7H6#15/CD3#1)을 포함한다. 특히 바람직한 실시양태에서, 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위 (B7H6#15/CD3#1)는 각각 scFab에 의해 형성되고 선택적으로 각각 Fc 도메인에 연결된다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 91 (CDR1), 서열 번호 92 (CDR2) 및 서열 번호 93 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 94 (CDR1), 서열 번호 95 (CDR2) 및 서열 번호 96 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 B7H6에 특이적으로 결합하는 제1 항원 결합 단위와 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 CD3에 특이적으로 결합하는 제2 항원 결합 단위를 포함한다. 이러한 항원 결합 단백질은 본원에서 B7H6#16/CD3#1로 지칭된다. 특히 바람직한 실시양태에서, 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위는 VL/VH 도메인, 예를 들어 서열 최적화된 VL/VH 도메인 내에 각각 상기 정의된 바와 같은 CDR (B7H6#16/CD3#1)을 포함한다. 특히 바람직한 실시양태에서, 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위 (B7H6#16/CD3#1)는 각각 scFab에 의해 형성되고 선택적으로 각각 Fc 도메인에 연결된다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 133 (CDR1), 서열 번호 134 (CDR2) 및 서열 번호 135 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 136 (CDR1), 서열 번호 137 (CDR2) 및 서열 번호 138 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 B7H6에 특이적으로 결합하는 제1 항원 결합 단위와 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 CD3에 특이적으로 결합하는 제2 항원 결합 단위를 포함한다. 이러한 항원 결합 단백질은 본원에서 B7H6#14/CD3#1로 지칭된다. 특히 바람직한 실시양태에서, 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위는 각각 VL/VH 도메인, 예를 들어 서열 최적화된 VL/VH 도메인 내에 각각 상기 정의된 바와 같은 CDR (B7H6#23/CD3#1) 을 포함한다. 특히 바람직한 실시양태에서, 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위 (B7H6#23/CD3#1)는 각각 scFab에 의해 형성되고 선택적으로 각각 Fc 도메인에 연결된다.
본 발명의 결합 단백질의 바람직한 실시양태에서, 제1 및 제2 결합 단위는 각각 경쇄 가변 도메인 및 중쇄 가변 도메인을 포함하고, 상기 경쇄/중쇄 가변 도메인은 제1 항원 결합 단위에 대한 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 또는 B7H6#24 중 어느 하나의 CDR 서열에 의해 정의된 바와 같고, 상기 경쇄/중쇄 가변 도메인은 제2 항원 결합 단위에 대한 CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 또는 CD3#6 중 어느 하나의 CDR 서열에 의해 정의된 바와 같다. 본 발명의 결합 단백질의 일부 실시양태에서, B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, B7H6#24, CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 또는 CD3#6 중 어느 하나의 항원 결합 단위의 VH 및/또는 VL 도메인은 인간, 인간화 또는 최적화된 VH 및/또는 VL 도메인이다.
본 발명의 결합 단백질의 바람직한 실시양태에서, B7H6에 특이적으로 결합하는 제1 항원 결합 단위의 경쇄/중쇄 가변 도메인은 하기와 같이 추가로 정의된다:
i) 서열 번호 145의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 146의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#1); 또는
ii) 서열 번호 147의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 148의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#2); 또는
iii) 서열 번호 149의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 150의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#3); 또는
iv) 서열 번호 151의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 152의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#4); 또는
v) 서열 번호 153의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 154의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#5); 또는
vi) 서열 번호 155의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 156의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#6); 또는
vii) 서열 번호 157의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 158의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#7); 또는
viii) 서열 번호 159의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 160의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#8); 또는
ix) 서열 번호 161의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 162의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#9); 또는
x) 서열 번호 163의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 164의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#10); 또는
xi) 서열 번호 165의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 166의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#11); 또는
xii) 서열 번호 167의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 168의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#12); 또는
xiii) 서열 번호 169의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 170의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#13); 또는
xiv) 서열 번호 171의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 172의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#14); 또는
xv) 서열 번호 173의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 174의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#15); 또는
xvi) 서열 번호 175의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 176의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#16); 또는
xvii) 서열 번호 177의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 178의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#17); 또는
xviii) 서열 번호 179의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 180의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#18); 또는
xix) 서열 번호 181의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 182의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#19); 또는
xx) 서열 번호 183의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 184의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#20); 또는
xxi) 서열 번호 185의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 186의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#21); 또는
xxii) 서열 번호 187의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 188의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#22); 또는
xxiii) 서열 번호 189의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 190의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#23); 또는
xxiv) 서열 번호 191의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 192의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 B7H6#24).
본 발명의 결합 단백질의 바람직한 실시양태에서, CD3에 특이적으로 결합하는 제2 항원 결합 단위의 경쇄/중쇄 가변 도메인은 하기와 같이 추가로 정의된다:
i) 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 CD3#1); 또는
ii) 서열 번호 295의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 296의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 CD3#2); 또는
iii) 서열 번호 297의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 298의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 CD3#3); 또는
iv) 서열 번호 299의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 300의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 CD3#4); 또는
v) 서열 번호 301의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 302의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 CD3#5); 또는
vi) 서열 번호 303의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 304의 아미노산 서열을 포함하는 중쇄 가변 도메인 (항원 결합 단위 CD3#6).
바람직한 실시양태에서, 본 발명의 결합 단백질은 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#6/CD3#1, B7H6#7/CD3#1, B7H6#8/CD3#1, B7H6#9/CD3#1, B7H6#10/CD3#1, B7H6#11/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, 및 B7H6#24/CD3#1로 이루어진 군으로부터 선택된 제1 및 제2 항원 결합 단위의 조합을 포함하고, 제1 및 제2 항원 결합 단위는 표 1에 나타낸 항원 결합 단위의 CDR 및/또는 VH 및 VL 서열에 의해 정의된다.
바람직한 실시양태에서, 본 발명의 결합 단백질은 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, 및 B7H6#24/CD3#1로 이루어진 군으로부터 선택된 제1 및 제2 항원 결합 단위의 조합을 포함하고, 제1 및 제2 항원 결합 단위는 표 1에 나타낸 항원 결합 단위의 CDR 및/또는 VH 및 VL 서열에 의해 정의된다.
바람직한 실시양태에서, 본 발명의 결합 단백질은 B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1로 이루어진 군으로부터 선택된 제1 및 제2 항원 결합 단위의 조합을 포함하고, 제1 및 제2 항원 결합 단위는 표 1에 나타낸 항원 결합 단위의 CDR 및/또는 VH 및 VL 서열에 의해 정의된다.
바람직한 실시양태에서, 본 발명의 결합 단백질은 B7H6#12/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, 및 B7H6#23/CD3#1로 이루어진 군으로부터 선택된 제1 및 제2 항원 결합 단위의 조합을 포함하고, 제1 및 제2 항원 결합 단위는 표 1에 나타낸 항원 결합 단위의 CDR 및/또는 VH 및 VL 서열에 의해 정의된다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 (i) 서열 번호 167의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 168의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 항원 결합 단위 및 (ii) 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 항원 결합 단위를 포함한다. 이러한 결합 단백질은 본원에서 B7H6#12/CD3#1로 지칭된다. 특히 바람직한 실시양태에서, 상기 정의된 바와 같은 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위 (B7H6#12/CD3#1)는 Fc 도메인에 선택적으로 공유 연결된 scFab에 의해 각각 형성된다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 (i) 서열 번호 171의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 172의 서열 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 항원 결합 단위 및 (ii) 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 항원 결합 단위를 포함한다. 이러한 결합 단백질은 본원에서 B7H6#14/CD3#1로 지칭된다. 특히 바람직한 실시양태에서, 상기 정의된 바와 같이 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위 (B7H6#14/CD3#1)는 선택적으로 Fc 도메인에 공유 연결된 scFab에 의해 각각 형성된다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 (i) 서열 번호 173의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 174의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 항원 결합 단위 및 (ii) 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 항원 결합 단위를 포함한다. 이러한 결합 단백질은 본원에서 B7H6#15/CD3#1로 지칭된다. 특히 바람직한 실시양태에서, 상기 정의된 바와 같이 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위 (B7H6#15/CD3#1)는 선택적으로 Fc 도메인에 공유 연결된 scFab에 의해 각각 형성된다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 (i) 서열 번호 175의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 176의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 항원 결합 단위 및 (ii) 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 항원 결합 단위를 포함한다. 이러한 결합 단백질은 본원에서 B7H6#16/CD3#1로 지칭된다. 특히 바람직한 실시양태에서, 상기 정의된 바와 같은 각각 B7H6 및 CD3에 특이적으로 결합하는 항원 결합 단위 (B7H6#16/CD3#1)는 선택적으로 Fc 도메인에 공유 연결된 scFab에 의해 각각 형성된다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 (i) 서열 번호 189의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 190의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 항원 결합 단위 및 (ii) 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 항원 결합 단위를 포함한다. 이러한 결합 단백질은 본원에서 B7H6#23/CD3#1로 지칭된다. 특히 바람직한 실시양태에서, 상기 정의된 바와 같은 B7H6 및 CD3에 각각 특이적으로 결합하는 항원 결합 단위 (B7H6#23/CD3#1)는 Fc 도메인에 선택적으로 공유 연결된 scFab에 의해 각각 형성된다.
일부 실시양태에서, 본 발명의 결합 단백질은 i) 제1 펩티드 링커로 제1 중쇄 가변 도메인에 공유 연결된 제1 경쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 항원 결합 단위 (예를 들어, 각각 표 1에 나타낸 각각의 CDR 또는 VH/VL 서열에 의해 정의된 바와 같은 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18 B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, B7H6#24 중 어느 하나) 및/또는 ii) 제2 펩티드 링커로 제2 중쇄 가변 도메인에 공유적으로 연결된 제2 경쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 항원 결합 단위 (예를 들어, 표 1에 나타낸 각각의 CDR 또는 VH/VL 서열에 의해 정의된 바와 같은 CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 또는 CD3#6 중 어느 하나)를 포함한다. 선택적으로, 제1 및 제2 항원 결합 단위는 펩티드 링커로 서로 공유 연결된다.
본 발명의 결합 단백질의 일부 실시양태에서, 제1 및/또는 제2 항원 결합 단위는 통상적인 항체 분자의 경/중 Fab 단편에서와 같이 CL 및 CH1 도메인을 추가로 포함하고, 따라서 상기 제1 결합 단위는 a) 제1 CL 도메인에 공유 연결 (바람직하게는 직접 결합)된 VL 도메인 (예를 들어, 경쇄 CDR (LCCDR) 또는 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 또는 B7H6#24 중 어느 하나의 VL 서열에 의해 정의됨) 및 b) 제1 CH1 도메인에 공유 결합 (바람직하게는 직접 결합)된 VH 도메인 (예를 들어, 중쇄 CDR (HCCDR) 또는 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6 B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 또는 B7H6#24 중 어느 하나의 VH 서열에 의해 정의됨)을 포함하고/거나, 상기 제2 항원 결합 단위는 a) 제2 CL 도메인에 공유 연결 (바람직하게는 직접 결합)된 VL 도메인 (예를 들어, LCCDR 또는 CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 또는 CD3#6 중 어느 하나의 VL 서열에 의해 정의됨) 및 b) 제2 CH1 도메인에 공유 결합 (바람직하게는 직접 결합)된 VH 도메인 (예를 들어, HCCDR 또는 CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 또는 CD3#6 중 어느 하나의 VH 서열에 의해 정의됨)을 포함한다.
본 발명의 맥락에서, CL 도메인은 항체 경쇄, 예를 들어 카파 (κ) 또는 람다 (λ) 경쇄의 불변 도메인이다. 카파 경쇄의 불변 영역의 예는 서열 번호 247에 제시되어 있다. 람다 경쇄의 불변 영역의 예는 서열 번호 248에 제시되어 있다. 일부 실시양태에서, 제1 및 제2 CL 도메인은 동일하고, 예를 들어 제1 및 제2 CL 도메인은 둘 다 카파 경쇄 불변 도메인이거나, 제1 및 제2 CL 도메인은 둘 다 람다 경쇄 불변 도메인이다. 바람직한 실시양태에서, 제1 및 제2 CL 도메인은 상이하며, 예를 들어, 제1 CL 도메인은 불변 카파 도메인이고 제2 CL 도메인은 불변 람다 도메인이거나, 또는 그 반대이다.
본 발명의 맥락에서, CH1 도메인은 항체 중쇄의 제1 불변 도메인이다. 불변 CH1 도메인의 예는 서열 번호 249에 제시되었다.
본 발명의 결합 단백질의 바람직한 실시양태에서, B7H6에 특이적인 제1 항원 결합 단위 (예를 들어, 표 1에 나타낸 CDR 및/또는 VH/VL 서열에 의해 정의된 바와 같은 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6 B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 또는 B7H6#24 중 어느 하나)는 N-말단에서 C-말단으로: 제1 경쇄 가변 도메인, 제1 CL 도메인, 제1 링커 펩티드, 제1 VH 도메인 및 제1 CH1 도메인을 포함하고/거나, 본 발명의 결합 단백질의 제2 결합 단위 (예를 들어, 표 1에 나타낸 CDR 및/또는 VH/VL 서열에 의해 정의된 바와 같은 CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 또는 CD3#6 중 어느 하나)는 N-말단에서 C-말단으로: 제2 경쇄 가변 도메인, 제2 CL 도메인, 제2 링커 펩티드, 제2 VH 도메인 및 제2 CH1 도메인을 포함한다. 이들 실시양태에서, 제1 및/또는 제2 결합 단위는 단일쇄 Fab의 구조를 갖는다. 제1 및/또는 제2 항원 결합 단위 둘 다에 대해, 단일쇄 Fab를 형성할 때, 항원 결합 단위가 N-말단에서 C-말단으로 VH-CH1-[링커 펩티드]-VL-CL을 포함하도록 순서가 역전될 수 있다. 본 발명의 단백질의 일부 실시양태에서, 제1 및/또는 제2 항원 결합 단위가 Fab 또는 단일쇄 Fab를 포함하는 경우, 불변 도메인은 동일한 유형 (예를 들어, 두 CL 도메인은 모두 카파 또는 람다 경쇄 불변 도메인임) 또는 상이한 유형 (제1 CL 도메인은 카파이고 제2 CL 도메인은 람다 경쇄 불변 도메인이거나 그 반대임)일 수 있으며, 바람직하게는 제1 및/또는 제2 CL 도메인은 상이한 유형이다. 바람직한 실시양태에서, 제1 항원 결합 단위는 B7H6에 특이적인 제1 단일쇄 Fab (바람직하게는 표 1에 나타낸 CDR 및 VH/VL 서열에 의해 정의된 바와 같은 B7H6#12, B7H6#14, B7H6#15, B7H6#16 또는 B7H6#23 중 어느 하나)로 이루어지고, 제2 항원 결합 단위는 CD3에 특이적인 제2 단일쇄 Fab (예를 들어, 표 1에 나타낸 CDR 및/또는 VH/VL 서열에 의해 정의된 바와 같은 CD3#1)로 이루어진다.
B7H6/CD3 결합 단백질 (예를 들어, 상기 기재된 B7H6/CD3 scFab)의 링커 서열은 자연 발생 서열 또는 비-자연 발생 서열일 수 있다. 치료 목적으로 사용되는 경우, 링커는 바람직하게는 본 발명의 결합 단백질이 투여되는 대상체에서 비-면역원성이다. 바람직하게는, 링커는 26 내지 42개의 아미노산, 예를 들어 30 내지 40개의 아미노산을 포함한다. 추가 측면에서, 본 발명의 단백질에 사용되는 링커는 34 내지 40개의 아미노산, 예를 들어 36 내지 39개의 아미노산, 예를 들어 38개의 아미노산을 포함한다.
링커 서열의 하나의 유용한 그룹은 WO1996/34103 및 WO1994/04678에 기재된 바와 같은 중쇄 항체의 힌지 영역으로부터 유래된 링커이다. 다른 예는 Ala-Ala-Ala와 같은 폴리-알라닌 링커 서열이다.
링커 서열의 추가의 바람직한 예는 예를 들어, (gly4ser)3, (gly4ser)5, (gly4ser)7, (gly3ser)3, (gly3ser)5, (gly3ser)7, (gly3ser2)3, (gly3ser2)5, 및 (gly3ser2)7을 포함하는 (glyxsery)z 링커와 같은 상이한 길이의 Gly/Ser 링커 또는 서열 번호 250, 251, 252, 253, 254, 255 또는 256 중 어느 하나, 바람직하게는 서열 번호 250의 링커이다.
본 발명의 결합 단백질의 일부 실시양태에서, 제1 항원 결합 단위의 VL 도메인 (예를 들어, 표 1에 나타낸 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18 B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, B7H6#24 중 어느 하나의 경쇄 CDR (LCCDR) 또는 VL 서열에 의해 정의됨)은 제1 Gly/Ser 링커 (예를 들어, 26 내지 42개의 아미노산, 30 내지 40개의 아미노산, 34 내지 40개의 아미노산, 또는 36 내지 39개의 아미노산 중 어느 하나, 바람직하게는 38개의 아미노산의 Gly/Ser 링커)를 통해 제1 항원 결합 단위의 VH 도메인 (예를 들어, 표 1에 나타낸 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18 B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, B7H6#24 중 어느 하나의 중쇄 CDR (HCCDR) 또는 VH 서열에 의해 정의됨)에 공유 연결되고; 제2 항원 결합 단위의 VL 도메인 (예를 들어, 표 1에 나타낸 CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 또는 CD3#6 중 어느 하나의 경쇄 CDR (LCCDR) 또는 VL 서열에 의해 정의됨)은 제2 Gly/Ser 링커 (예를 들어, 26 내지 42개 아미노산, 30 내지 40개 아미노산, 34 내지 40개 아미노산, 또는 36 내지 40개 아미노산 중 어느 하나의 Gly/Ser 링커)를 통해 제2 항원 결합 단위의 VH 도메인 (예를 들어, 표 1에 나타낸 CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 또는 CD3#6 중 어느 하나의 중쇄 CDR (HCCDR) 또는 VH 서열에 의해 정의됨)에 공유 연결된다. 보다 바람직하게는, 제1 및 제2 링커는 동일하다. 보다 더 바람직하게는, 제1 및 제2 링커는 각각 서열 번호 250의 아미노산 서열을 포함한다.
본 발명의 결합 단백질의 바람직한 실시양태에서, B7H6에 특이적으로 결합하는 제1 항원 결합 단위는 N에서 C-말단으로 i) VL 도메인 (예를 들어, 표 1에 나타낸 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18 B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, B7H6#24 중 어느 하나의 경쇄 CDR (LCCDR) 또는 VL 서열에 의해 정의됨), ii) 제1 CL 도메인, iii) 제1 Gly/Ser 링커 (예를 들어, 26 내지 42개 아미노산, 30 내지 40개 아미노산, 34 내지 40개 아미노산, 또는 36 내지 39개 아미노산, 바람직하게는 38개 아미노산 중 어느 하나의 Gly/Ser 링커)를 통해, iv) VH 도메인 (예를 들어, 표 1에 나타낸 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18 B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, B7H6#24 중 어느 하나의 중쇄 CDR (HCCDR) 또는 VH 서열에 의해 정의됨) 및 v) 제1 CH1 도메인을 포함하고/거나, CD3에 특이적으로 결합하는 제2 항원 결합 단위는 N에서 C 말단으로 i) VL 도메인 (예를 들어, 표 1에 나타낸 CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 또는 CD3 중 어느 하나의 경쇄 CDR (LCCDR) 또는 VL 서열에 의해 정의됨), ii) 제2 CL 도메인, iii) 제2 Gly/Ser 링커 (예를 들어, 26 내지 42개 아미노산, 30 내지 40개 아미노산, 34 내지 40개 아미노산, 또는 36 내지 39개 아미노산, 바람직하게는 38개 아미노산 중 어느 하나의 Gly/Ser 링커), iv) 제2 항원 결합 단위의 VH 도메인 단위 (예를 들어, 표 1에 나타낸 CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 또는 CD3 중 어느 하나의 중쇄 CDR (HCCDR) 또는 VH 서열에 의해 정의됨) 및 v) 제2 CH1 도메인을 포함한다. 바람직하게는, i) 내지 v)는 각각 직접 공유 결합을 통해 항원 결합 단위의 N에서 C 말단으로 i) 내지 v)의 순서로 연결된다 (각 항원 결합 단위는 scFab의 구조를 가짐). 보다 바람직하게는, 제1 및 제2 링커는 동일하다. 보다 더 바람직하게는, 제1 및 제2 링커는 각각 서열 번호 250의 아미노산 서열을 포함한다.
바람직한 실시양태에서, 본 발명의 결합 단백질은 B7H6에 특이적인 제1 항원 결합 단위를 형성하고 서열 번호 193, 서열 번호 194, 서열 번호 195, 서열 번호 196, 서열 번호 197, 서열 번호 198 서열 번호 199, 서열 번호 200, 서열 번호 201, 서열 번호 202, 서열 번호 203, 서열 번호 204, 서열 번호 205, 서열 번호 206, 서열 번호 207, 서열 번호 208, 서열 번호 209, 서열 번호 210, 서열 번호 211, 서열 번호 212, 서열 번호 213, 서열 번호 214, 서열 번호 215 및 서열 번호 216으로 이루어진 군으로부터 선택된 서열을 포함하는 제1 단일쇄 Fab, 및 CD3에 특이적인 제2 항원 결합 단위를 형성하고 서열 번호 305의 서열을 포함하는 제2 단일쇄 Fab를 포함한다.
바람직한 실시양태에서, 본 발명의 결합 단백질은 B7H6에 특이적인 제1 항원 결합 단위를 형성하고 서열 번호 193, 서열 번호 194, 서열 번호 195, 서열 번호 196, 서열 번호 197, 서열 번호 204, 서열 번호 205, 서열 번호 206, 서열 번호 207, 서열 번호 208, 서열 번호 209, 서열 번호 210, 서열 번호 211, 서열 번호 212, 서열 번호 213, 서열 번호 214, 서열 번호 215 및 서열 번호 216으로 이루어진 군으로부터 선택된 서열을 포함하는 제1 단일쇄 Fab, 및 CD3에 특이적인 제2 항원 결합 단위를 형성하고 서열 번호 305의 서열을 포함하는 제2 단일쇄 Fab를 포함한다.
바람직한 실시양태에서, 본 발명의 결합 단백질은 B7H6에 특이적인 제1 항원 결합 단위를 형성하고 서열 번호 204, 서열 번호 205, 서열 번호 206, 서열 번호 207, 서열 번호 208, 서열 번호 209, 서열 번호 210, 서열 번호 211, 서열 번호 212, 서열 번호 213, 서열 번호 214, 서열 번호 215 및 서열 번호 216으로 이루어진 군으로부터 선택된 서열을 포함하는 제1 단일쇄 Fab, 및 CD3에 특이적인 제2 항원 결합 단위를 형성하고 서열 번호 305의 서열을 포함하는 제2 단일쇄 Fab를 포함한다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 204의 서열을 포함하는 제1 단일쇄 Fab 및 서열 번호 305의 서열을 포함하는 제2 단일쇄 Fab를 포함하고, 선택적으로 각각의 단일쇄 Fab는 Fc 도메인에 추가 연결되어 제1 폴리펩티드 쇄 ("B7H6 쇄") 및 제2 폴리펩티드 쇄 ("CD3 쇄")를 형성한다. 바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 206의 서열을 포함하는 제1 단일쇄 Fab 및 서열 번호 305의 서열을 포함하는 제2 단일쇄 Fab를 포함하고, 선택적으로 각각의 단일쇄 Fab는 Fc 도메인에 추가 연결되어 제1 폴리펩티드 쇄 (B7H6 쇄) 및 제2 폴리펩티드 쇄 (CD3 쇄)를 형성한다. 바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 207의 서열을 포함하는 제1 단일쇄 Fab 및 서열 번호 305의 서열을 포함하는 제2 단일쇄 Fab를 포함하고, 선택적으로 각각의 단일쇄 Fab는 Fc 도메인에 추가 연결되어 제1 폴리펩티드 쇄 (B7H6 쇄) 및 제2 폴리펩티드 쇄 (CD3 쇄)를 형성한다. 바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 208의 서열을 포함하는 제1 단일쇄 Fab 및 서열 번호 305의 서열을 포함하는 제2 단일쇄 Fab를 포함하고, 선택적으로 각각의 단일쇄 Fab는 Fc 도메인에 추가로 연결되어 제1 폴리펩티드 쇄 (B7H6 쇄) 및 제2 폴리펩티드 쇄 (CD3 쇄)를 형성한다. 바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 215의 서열을 포함하는 제1 단일쇄 Fab 및 서열 번호 305의 서열을 포함하는 제2 단일쇄 Fab를 포함하고, 선택적으로 각각의 단일쇄 Fab는 Fc 도메인에 추가로 연결되어 제1 폴리펩티드 쇄 (B7H6 쇄) 및 제2 폴리펩티드 쇄 (CD3 쇄)를 형성한다.
일부 실시양태에서, 제1 항원 결합 단위 (예를 들어, 표 1에 나타낸 CDR 및/또는 VH/VL 서열에 의해 정의된 바와 같은 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18 B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 또는 B7H6#24 중 어느 하나) 및/또는 제2 항원 결합 단위 (예를 들어, 예를 들어, 표 1에 나타낸 CDR 및/또는 VH/VL 서열에 의해 정의된 바와 같은 CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 또는 CD3#6 중 어느 하나)은 CL 도메인에 공유 결합 (바람직하게는 직접 결합된)된 VL 도메인 및 CH1 도메인에 연결된 VH 도메인을 포함하고 (함께 Fab 단편 형성), 상기 CH1 도메인은 Fc 도메인에 추가로 공유 연결 (예를 들어, 직접 결합)되어 하나의 경쇄 및 하나의 중쇄를 갖는 통상적인 Y-형 항체 분자의 아암을 형성한다. 일부 실시양태에서, 제1 및 제2 항원 결합 단위는 각각 Fab 단편, 즉 제1 및 제2 Fab 단편을 형성하고, 이는 각각 제1 및 제2 Fc 도메인에 각각 공유 결합 (바람직하게는 직접 결합)되어 기존의 이종사량체 이중 특이성 및 이가 (각각 B7H6 및 CD3에 대해 1가) 항체 분자를 형성한다.
바람직한 실시양태에서, 본 발명의 결합 단백질은 (i) 펩티드 링커 (예를 들어, 26 내지 42개 아미노산, 30 내지 40개 아미노산, 34 내지 40개 아미노산, 또는 36 내지 39개 아미노산, 바람직하게는 38개 아미노산 중 어느 하나의 Gly/Ser 링커, 보다 더 바람직하게는 서열 번호 250의 링커)를 통해 B7H6에 특이적으로 결합하는 제1 단일쇄 Fab, 즉, 중쇄의 VH-CH1 도메인에 공유적으로 연결된 항체 경쇄 (VL-CL) (표 1에 나타낸 CDR 및/또는 VH/VL 서열에 의해 정의된 바와 같은 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18 B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 또는 B7H6#24 중 어느 하나의 VL 및 VH 도메인)를 포함하는 제1 항원 결합 단위 - 여기서, 제1 항원 결합 단위는 제1 Fc 도메인에 공유 연결됨 (예를 들어, 직접 결합됨) - 및 (ii) CD3에 특이적으로 결합하는 제2 단일쇄 Fab를 포함하는 제2 항원 결합 단위, 즉, 중쇄의 VH-CH1 도메인에 공유적으로 연결된 항체 경쇄 (VL-CL) (표 1에 나타낸 CDR 및/또는 VH/VL 서열에 의해 정의된 바와 같은 CD3#1 CD3#2, CD3#3, CD3#4, CD3#5, CD3#6 중 어느 하나의 VL 및 VH 도메인)를 포함하는 제2 항원 결합 단위 - 여기서, 제2 항원 결합 단위는 제2 Fc 도메인에 공유 연결됨 (예를 들어, 직접 결합됨) -를 포함한다. 따라서, 바람직한 실시양태에서, 본 발명의 결합 단백질은 (i) (a) B7H6에 특이적인 제1 항원 결합 단위 - 상기 제1 항원 결합 단위는 B7H6에 특이적인 제1 단일쇄 Fab (바람직하게는 표 1에 나타낸 CDR 및/또는 VH/VL 서열에 의해 정의된 바와 같은 B7H6#12, B7H6#14, B7H6#15, B7H6#16 또는 B7H6#23 중 어느 하나)를 포함함 - 및 (b) 제1 Fc 도메인을 포함하는 제1 폴리펩티드 쇄 (이 제1 폴리펩티드 쇄는 본원에서 "B7H6 쇄"로도 지칭됨) 및 (ii) (a) CD3에 특이적인 제2 단일쇄 Fab를 포함하는 제2 항원 결합 단위 (바람직하게는 표 1에 나타낸 CDR 및/또는 VL/VH 서열에 의해 정의된 바와 같은 CD3#1) 및 (b) 제2 Fc 도메인을 포함하는 CD3에 특이적인 제2 폴리펩티드 쇄 (이 제2 폴리펩티드 쇄는 본원에서 "CD3 쇄"로도 지칭됨)를 포함한다. 따라서, 본원에 사용된 용어 "폴리펩티드 쇄"는 적어도 scFab 및 Fc 도메인을 포함한다. 일부 실시양태에서, 제1 및 제2 Fc 도메인은 동일하다. 바람직한 실시양태에서, 제1 및 제2 Fc 도메인은 상이하다. 본 발명의 생성된 결합 단백질은 완전한 Fc를 갖고 2개의 독립적인 결합 부위를 갖는 2개의 상이한 폴리펩티드 쇄, B7H6에 특이적인 제1 scFab에 의해 형성된 제1 항원 결합 단위 및 CD3에 특이적인 제2 scFab에 의해 형성된 제2 결합 단위를 포함한다.
바람직한 실시양태에서, 본 발명의 결합 단백질은 각각 Fc 도메인에 공유적으로 연결된 상이한 특이성을 갖는 scFab에 의해 형성된 항원 결합 단위를 포함하는 2개의 상이한 폴리펩티드 쇄를 포함하고, 폴리펩티드 쇄는 이황화 결합 또는 잠재적으로 펩티드 링커를 통해 서로 공유적으로 연결된다. 바람직한 실시양태에서, 본 발명의 결합 단백질은 2개의 폴리펩티드 쇄를 포함하는 이중 특이성, 2가 (각각 B7H6 및 CD3에 대해 1가) 이종이량체성 단백질이며, 하나의 폴리펩티드 쇄 (제1 폴리펩티드 쇄 또는 B7H6 쇄)는 B7H6에 특이적으로 결합하는 scFab에 의해 형성된 항원 결합 단위 (예를 들어, 표 1에 나타낸 CDR 및/또는 VH/VL 서열에 의해 정의된 바와 같은 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18 B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 또는 B7H6#24 중 어느 하나) 및 Fc 도메인 (바람직하게는 서열 번호 242의 Fc 도메인)을 포함하고, 또 다른 폴리펩티드 쇄 (제2 폴리펩티드 쇄 또는 CD3 쇄)는 CD3에 특이적으로 결합하는 scFab에 의해 형성된 항원 결합 단위 (예를 들어, CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 또는 CD3#6 중 어느 하나) 및 Fc 도메인 (바람직하게는 서열 번호 243의 Fc 도메인)을 포함한다. 일부 실시양태에서, 제1 항원 결합 단위는 제1 단일쇄 Fab로 이루어지고 제2 항원 결합 단위는 제2 단일쇄 Fab로 이루어진다. 결합 단백질의 일부 실시양태에서, B7H6에 특이적인 제1 폴리펩티드 쇄 (B7H6 쇄)는 a) scFab로 이루어진 제1 항원 결합 단위 (바람직하게는 표 1에 나타낸 CDR, VH/VL 및/또는 scFab 서열에 의해 정의된 바와 같은 B7H6#12, B7H6#14, B7H6#15, B7H6#16 또는 B7H6#23 중 어느 하나)로 이루어지고, b) CD3에 특이적인 제1 Fc 도메인 및 제2 폴리펩티드 쇄 (CD3 쇄)는 a) scFab로 이루어진 제2 항원 결합 단위 (바람직하게는 표 1에 나타낸 CDR, VH/VL 및/또는 scFab 서열에 의해 정의된 바와 같은 CD3#1) 및 b) 제2 Fc 도메인으로 이루어진다. 바람직하게는, scFab의 C-말단은 직접 공유 결합을 통해 Fc 도메인의 N-말단에 연결된다. 바람직하게는, 제1 및 제2 폴리펩티드 쇄는 이황화 결합을 통해 서로 공유 연결되어 있으며, 기존의 Y-형 항체 분자와 유사한 항체 유사 구조 (도 1)를 형성한다.
본 발명의 맥락에서, Fc 도메인은 예를 들어 IgG의 중쇄, 예를 들어 IgG1, IgG2 또는 IgG4로부터 유래된다. 예를 들어, 본 발명의 Fc 도메인은 IgG1 또는 IgG4 중쇄의 Fc 도메인이며 힌지 영역과 2개의 불변 도메인 (CH2 및 CH3)을 포함한다. Fc 도메인 (힌지 영역 포함)의 예는 서열 번호 241 및 244에 제시되어 있다.
본 발명의 단백질의 아미노산 쇄에서 아미노산의 넘버링은 달리 명시되지 않는 한 Eu 넘버링 시스템 (Edelman et al, PNAS USA 1969 May, 63(1):78-85;, Cunningham et al. PNAS USA 1969, Nov, 64(3):997-1003)에 따른다. 이는 본원에 표시된 아미노산 번호가 달리 명시되지 않는 한 Eu 넘버링 시스템에 따라 해당 하위 유형의 중쇄 (예를 들어, IgG1 또는 IgG4)의 위치에 해당함을 의미한다.
일부 실시양태에서, 본 발명의 단백질의 제1 Fc 도메인 및 제2 Fc 도메인은 각각 제1 및 제2 폴리펩티드 쇄의 이종이량체 대신에 제1 또는 제2 폴리펩티드 쇄의 동종이량체의 형성을 감소시키는 하나 이상의 아미노산 변화를 포함한다. 이러한 변화를 통해, 중쇄 중 하나의 인터페이스로부터 하나 이상의 작은 아미노산 측쇄를 더 큰 측쇄 (예를 들어, 티로신 또는 트립토판)로 대체함으로써 Fc 도메인 중 하나에서 "돌출부"가 생성된다. 큰 아미노산 측쇄를 더 작은 측쇄 (예를 들어, 알라닌 또는 트레오닌)로 대체하여 동일하거나 유사한 크기의 보상 "공동"이 다른 Fc 도메인의 인터페이스에 생성된다. 이것은 동종이량체, 특히 "돌출부"를 갖는 Fc 도메인의 동종이량체와 같은 다른 원치 않는 최종 생성물에 비해 이종이량체의 수율을 증가시키는 메커니즘을 제공한다 (예를 들어 Ridgway et al. Protein Eng, 1996. 9(7): p. 617-21; Atwell et al, JMB, 1997, 270, 26-35 참조). 일부 실시양태에서, 이러한 아미노산 변화는 제1 Fc 도메인의 위치 366에서의 티로신 (Y) [T366Y] 및 제2 Fc 도메인의 위치 407에서의 트레오닌 (T) [Y407T]이다. 일부 실시양태에서, 제1 Fc 도메인은 위치 366에 세린 (S) [T366S]을 포함하고 제2 Fc 도메인은 위치 366에 트립토판 (W) [T366W], 위치 368에 알라닌 (A) [L368A] 및 위치 407에 발린 (V) [Y407V]을 포함한다. 바람직한 실시양태에서, 제1 Fc 도메인은 위치 366에 트립토판 (W) [T366W]을 포함하고 제2 Fc 도메인은 위치 366에 세린 (S) [T366S], 위치 368에 알라닌 (A) [L368A] 및 위치 407에 발린 (V) [Y407V]을 포함한다. 예를 들어, 서열 번호 241의 인간 IgG1 Fc 서열에서 아미노산 위치 146에 해당하는 Eu 넘버링에 따른 Fc 도메인의 위치 366은 서열 번호 241의 위치 146에서의 T에서 서열 번호 242의 위치 146에서의 W로 변경되고; 서열 번호 241의 아미노산 위치 146, 148 및 187에 각각 상응하는 Eu 넘버링에 따른 위치 366, 368 및 407은 서열 번호 241의 이들 위치에서 T, L 및 Y로부터 서열 번호 243의 이들 위치에서 S, A 및 V로 변경된다. 이들 실시양태 중 어느 하나에서, 제1 Fc 도메인에 대해 기재된 아미노산 변화는 제2 Fc 도메인에 위치할 수 있고, 제2 Fc 도메인에 대한 각각의 아미노산 변화는 제1 Fc 도메인에 위치할 수 있다. 즉, 용어 "제1" 및 "제2"는 이들 실시양태예에서 교환될 수 있다. 일부 실시양태에서, 이러한 Fc 도메인은 IgG1 또는 IgG4의 중쇄로부터 유래된 Fc 도메인이다.
일부 실시양태에서, 제1 Fc 도메인은 위치 366에 트립토판 (W) [T366W] 외에 위치 354에 시스테인 (C) [S354C]을 포함하고, 제2 Fc 도메인은 위치 366에 세린 (S) [T366S], 위치 368에 알라닌 (A) [L368A] 및 위치 407에 발린 (V) [Y407V] 외에, 위치 349에 시스테인 (C) [Y349C]을 포함한다. 한 측면에서, 이러한 Fc 도메인은 IgG4의 중쇄에서 유래된 Fc 도메인이다.
일부 실시양태에서, 본 발명의 결합 단백질에서 제1 Fc 도메인 또는 제2 Fc 도메인은 단백질 A에 대한 Fc 도메인의 결합을 감소시키는 하나 이상의 아미노산 변화를 추가로 포함한다. 일부 실시양태에서, 이러한 아미노산 변화는 Fc 도메인 중 하나의 위치 435에 아르기닌 [H435R] 및 위치 436에 페닐알라닌 [Y436F]이다. 두 가지 변화 모두 인간 IgG3의 서열에서 유래된다 (IgG3 서열은 단백질 A에 결합하지 않음). 이들 2개의 돌연변이는 CH3 도메인에 위치하고 Fc 도메인 중 하나에 통합되어 단백질 A에 대한 결합을 감소시킨다 (예를 들어 Jendeberg et al. J Immunol Methods, 1997. 201 (1): p. 25-34 참조). 이러한 두 가지 변화는 단백질 정제 동안 이러한 변화를 포함하는 중쇄의 동종이량체의 제거를 용이하게 한다.
일부 실시양태에서, 본 발명의 결합 단백질에서, 위치 407에 트레오닌 (T) [Y407T]을 포함하는 Fc 도메인은 위치 435에 아르기닌 [H435R] 및 위치 436에 페닐알라닌 [Y436F]을 추가로 포함한다. 이 경우, 다른 중쇄는 위치 366에 티로신 (Y) [T366Y]을 포함하지만 위치 435 및 436에서 두 가지 변화를 포함하지 않는다. 대안적으로, 일부 실시양태에서, 본 발명의 단백질에서 위치 366에 세린 (S) [T366S], 위치 368에 알라닌 (A) [L368A] 및 위치 407에 발린 (V) [Y407V]을 포함하는 Fc 도메인은 위치 435에 아르기닌 [H435R] 및 위치 436에 페닐알라닌 [Y436F]을 추가로 포함한다. 이 경우, 다른 Fc 도메인은 위치 366에 트립토판 (W) [T366W]을 포함하지만 위치 435 및 436에 2개의 변화를 포함하지 않는다. 따라서, 전술한 바와 같이 "공동"을 초래하는 아미노산 변화를 포함하는 Fc 도메인은 또한 단백질 A에 대한 결합을 감소시키는 아미노산 변화를 포함한다. 이 Fc 도메인을 포함하는 동종이량체는 단백질 A에 대한 결합 감소를 통해 제거된다. "돌출부"를 포함하는 다른 Fc 도메인의 동종이량체의 생성이 "돌출부"의 존재에 의해 감소된다.
일부 실시양태에서, 본 발명의 단백질의 Fc 도메인은 YTE 돌연변이 (M252Y/S254T/T256E, Eu 넘버링 (Dall'Acqua et al. J. Biol. Chem.2006, 281(33):23514-24))를 추가로 포함하거나 포함하지 않을 수 있다. 이들 돌연변이는 pH 6.0에서 신생아 FcRn 수용체에 대한 결합 친화성의 우선적 향상을 통해 Fc 도메인의 약동학적 특성을 개선하는 것으로 나타났다.
일부 실시양태에서, IgG1로부터 유래된 본 발명의 제1 및/또는 제2 Fc 도메인은 또한 "KO" 돌연변이 (L234A, L235A)를 포함한다 (Xu et al, Cellular Immunology 2000 Feb 25, 200(1):16-26). 추가 측면에서, IgG4로부터 유래된 본 발명의 제1 및/또는 제2 Fc 도메인은 또한 Pro 힌지 돌연변이 (S228P)를 포함한다 (Angal et al, Molecular Immunology 1993, 30(1):105-108; Labrijn et al, Nature Biotechnology 2009, 27:767-771).
본 발명의 결합 단백질의 바람직한 실시양태에서, 제1 Fc 도메인은 서열 번호 242의 아미노산 서열을 포함하고 제2 Fc 도메인은 서열 번호 243의 아미노산 서열을 포함한다.
본 발명의 바람직한 실시양태에서, 결합 단백질은 i) 서열 번호 217의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#1/CD3#1), 또는 ii) 서열 번호 218의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#2/CD3#1), 또는 iii) 서열 번호 219의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#3/CD3#1), 또는 iv) 서열 번호 220의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#4/CD3#1), 또는 v) 서열 번호 221의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#5/CD3#1), 또는 vi) 서열 번호 222의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#6/CD3#1); 또는 vii) 서열 번호 223의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#7/CD3#1); 또는 viii) 서열 번호 224의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#8/CD3#1); 또는 ix) 서열 번호 225의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#9/CD3#1); 또는 x) 서열 번호 226의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#10/CD3#1); 또는 xi) 서열 번호 227의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#11/CD3#1); 또는 xii) 서열 번호 228의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#12/CD3#1); 또는 xiii) 서열 번호 229의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#13/CD3#1); 또는 xiv) 서열 번호 230의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#14/CD3#1); 또는 xv) 서열 번호 231의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#15/CD3#1); 또는 xvi) 서열 번호 232의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#16/CD3#1); 또는 xvii) 서열 번호 233의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#17/CD3#1); 또는 xviii) 서열 번호 234의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#18/CD3#1); 또는 xix) 서열 번호 235의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#19/CD3#1); 또는 xx) 서열 번호 236의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#20/CD3#1); 또는 xxi) 서열 번호 237의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#21/CD3#1); 또는 xxii) 서열 번호 238의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#22/CD3#1); 또는 xxiii) 서열 번호 239의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#23/CD3#1); 또는 xxiv) 서열 번호 240의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#24/CD3#1)를 포함한다. 바람직하게는, 제1 및 제2 폴리펩티드 쇄는 하나 이상의 이황화 결합을 통해 연결되고 통상적인 Y-형 항체 분자와 유사한 항체 유사 구조 (도 1)를 형성한다.
바람직한 실시양태에서, 제1 폴리펩티드 쇄는 서열 번호 217, 218, 219, 220, 221, 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 및 240 중 어느 하나로 이루어진 군으로부터의 아미노산 서열을 포함하고, 제2 폴리펩티드 쇄는 서열 번호 311의 아미노산 서열을 포함한다. 보다 더 바람직하게는, 제1 폴리펩티드 쇄는 228, 229, 230, 231, 232, 233, 234, 235, 236, 237, 238, 239, 및 240 중 어느 하나의 아미노산 서열을 포함하고, 제2 폴리펩티드 쇄는 서열 번호 311의 아미노산 서열을 포함하며, 제1 및 제2 폴리펩티드 쇄는 하나 이상의 이황화 결합을 통해 연결되고 기존의 Y-형 항체 분자와 유사한 항체 유사 구조 (도 1)를 형성한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 228의 아미노산 서열을 포함하는 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 230의 아미노산 서열을 포함하는 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 231의 아미노산 서열을 포함하는 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 232의 아미노산 서열을 포함하는 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 239의 아미노산 서열을 포함하는 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다.
본원에 기재된 모든 실시양태에 대해, "포함하는"이라는 용어를 사용함으로써, 각각의 단백질, 분자, 항원 결합 단위 또는 폴리펩티드 쇄가 제시되는 바와 같은 아미노산으로 "이루어진" 실시양태도 포함하는 것으로 이해되어야 한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 228의 아미노산 서열로 이루어진 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열로 이루어진 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다. 바람직하게는, 제1 및 제2 폴리펩티드 쇄는 하나 이상의 이황화 결합을 통해 연결되고 기존의 Y-형 항체 분자와 유사한 항체 유사 구조 (도 1)를 형성한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 230의 아미노산 서열로 이루어진 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열로 이루어진 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다. 바람직하게는, 제1 및 제2 폴리펩티드 쇄는 하나 이상의 이황화 결합을 통해 연결되고 기존의 Y-형 항체 분자와 유사한 항체 유사 구조 (도 1)를 형성한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 231의 아미노산 서열로 이루어진 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열로 이루어진 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다. 바람직하게는, 제1 및 제2 폴리펩티드 쇄는 하나 이상의 이황화 결합을 통해 연결되고 기존의 Y-형 항체 분자와 유사한 항체 유사 구조 (도 1)를 형성한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 232의 아미노산 서열로 이루어진 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열로 이루어진 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다. 바람직하게는, 제1 및 제2 폴리펩티드 쇄는 하나 이상의 이황화 결합을 통해 연결되고 기존의 Y-형 항체 분자와 유사한 항체 유사 구조 (도 1)를 형성한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 239의 아미노산 서열로 이루어진 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열로 이루어진 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다. 바람직하게는, 제1 및 제2 폴리펩티드 쇄는 하나 이상의 이황화 결합을 통해 연결되고 기존의 Y-형 항체 분자와 유사한 항체 유사 구조 (도 1)를 형성한다.
추가 측면에서, 본 발명은 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 (B7H6 쇄) 및 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄 (CD3 쇄)를 포함하는 결합 단백질을 제공하며, 여기서 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄는 제1 링커에 공유 연결된 (바람직하게는 직접 결합된) 제1 경쇄를 포함하고, 이는 그 자체가 제1 중쇄에 공유 연결되고 (예를 들어, 직접 결합됨), 여기서 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄는 제2 링커에 공유 연결된 (바람직하게는 직접 결합된) 제2 경쇄를 포함하고, 이는 그 자체가 제2 중쇄에 공유 연결된다 (예를 들어, 직접 결합됨).
구체적으로 언급된 항원-결합 단위를 갖는 본 발명의 결합 단백질과 관련하여 상기 본원에 제공된 모든 정의 및 바람직한 실시양태는 본원에 달리 정의되지 않는 한 제1 및 제2 폴리펩티드 쇄를 포함하는 본 발명의 결합 단백질에도 준용하여 적용된다.
일부 실시양태에서, 그의 N-말단으로부터 출발하는 제1 폴리펩티드 쇄 (본원에서 B7H6 쇄로도 지칭됨)는 B7H6에 특이적으로 결합하는 제1 경쇄 가변 도메인, 제1 경쇄 불변 도메인, 제1 링커, B7H6에 특이적인 제1 중쇄 가변 도메인 및 제1 중쇄 불변 영역을 포함한다. 일부 실시양태에서, 그의 N-말단으로부터 출발하는 제2 폴리펩티드 쇄 (본원에서 CD3 쇄로도 지칭됨)는 CD3에 특이적으로 결합하는 제2 경쇄 가변 도메인, 제2 경쇄 불변 도메인, 제2 링커, CD3에 특이적인 제2 중쇄 가변 도메인 및 제2 중쇄 불변 도메인을 포함한다.
생성된 단백질은 완전한 Fc를 갖고, IgG보다 크고 (경쇄와 중쇄 사이에 링커가 있기 때문에) 2개의 독립적인 결합 부위 (예를 들어, 각 결합 부위는 각 항원에 대해 1가임), B7H6에 대한 제1 결합 부위 및 CD3에 대한 제2 결합 부위를 가진다. 바람직하게는, 제1 및 제2 폴리펩티드 쇄는 하나 이상의 이황화 결합을 통해 연결된다. 이와 같이, 본 발명의 단백질은 각각 scFab 및 Fc 도메인을 포함하는 2개의 폴리펩티드 쇄를 포함하는, 통상적인 전장 항체의 Y-형 구조 (도 1 참조)를 갖는 항체-유사 구조이다. 바람직한 실시양태에서, 본 발명의 단백질은 (i) B7H6에 특이적인 제1 scFab 및 제1 Fc 도메인으로 이루어진 B7H6에 특이적인 제1 폴리펩티드 쇄 (B7H6 쇄) 및 (ii) CD3에 특이적인 제2 단일쇄 Fab 및 제2 Fc 도메인으로 이루어진 CD3에 특이적인 제2 폴리펩티드 쇄 (CD3 쇄)를 포함한다.
바람직하게는, 제1 scFab는 직접 공유 결합을 통해 제1 Fc 도메인에 연결되고 제2 scFab는 직접 공유 결합을 통해 제2 Fc 도메인에 연결된다. 이 이중 특이성 형식은 원치 않는 면역원성 반응을 생성할 가능성이 적은 구조 내에서 결합 모이어티의 기능적 특성을 유지하면서 발현 및 정제 후 이질성을 크게 감소시킨다 (예를 들어, 서로 다른 결합 특이성을 갖는 가볍고 무거운 가변 도메인의 잘못된 쌍을 피함으로써). 이것은 또한 예를 들어 포유동물 세포에서 이종이량체 단백질의 우수한 발현을 가능하게 한다.
본 발명의 단백질의 바람직한 실시양태에서, B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 (B7H6 쇄)는 하기 i) 내지 xxiv)로 이루어진 군으로부터 선택되는 CDR 서열을 포함하는, 제1 경쇄 가변 도메인 및 제1 중쇄 가변 도메인을 포함한다:
i) 서열 번호 1 (CDR1), 서열 번호 2 (CDR2) 및 서열 번호 3 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 4 (CDR1), 서열 번호 5 (CDR2) 및 서열 번호 6 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
ii) 서열 번호 7 (CDR1), 서열 번호 8 (CDR2) 및 서열 번호 9 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 10 (CDR1), 서열 번호 11 (CDR2) 및 서열 번호 12 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
iii) 서열 번호 13 (CDR1), 서열 번호 14 (CDR2) 및 서열 번호 15 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 16 (CDR1), 서열 번호 17 (CDR2) 및 서열 번호 18 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
iv) 서열 번호 19 (CDR1), 서열 번호 20 (CDR2) 및 서열 번호 21 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 22 (CDR1), 서열 번호 23 (CDR2) 및 서열 번호 24 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
v) 서열 번호 25 (CDR1), 서열 번호 26 (CDR2) 및 서열 번호 27 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 28 (CDR1), 서열 번호 29 (CDR2) 및 서열 번호 30 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
vi) 서열 번호 31 (CDR1), 서열 번호 32 (CDR2) 및 서열 번호 33 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 34 (CDR1), 서열 번호 35 (CDR2) 및 서열 번호 36 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
vii) 서열 번호 37 (CDR1), 서열 번호 38 (CDR2) 및 서열 번호 39 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 40 (CDR1), 서열 번호 41 (CDR2) 및 서열 번호 42 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
viii) 서열 번호 43 (CDR1), 서열 번호 44 (CDR2) 및 서열 번호 45 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 46 (CDR1), 서열 번호 47 (CDR2) 및 서열 번호 48 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
ix) 서열 번호 49 (CDR1), 서열 번호 50 (CDR2) 및 서열 번호 51 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 52 (CDR1), 서열 번호 53 (CDR2) 및 서열 번호 54 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
x) 서열 번호 55 (CDR1), 서열 번호 56 (CDR2) 및 서열 번호 57 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 58 (CDR1), 서열 번호 59 (CDR2) 및 서열 번호 60 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xi) 서열 번호 61 (CDR1), 서열 번호 62 (CDR2) 및 서열 번호 63 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 64 (CDR1), 서열 번호 65 (CDR2) 및 서열 번호 66 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xii) 서열 번호 67 (CDR1), 서열 번호 68 (CDR2) 및 서열 번호 69 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 70 (CDR1), 서열 번호 71 (CDR2) 및 서열 번호 72 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xiii) 서열 번호 73 (CDR1), 서열 번호 74 (CDR2) 및 서열 번호 75 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 76 (CDR1), 서열 번호 77 (CDR2) 및 서열 번호 78 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xiv) 서열 번호 79 (CDR1), 서열 번호 80 (CDR2) 및 서열 번호 81 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 82 (CDR1), 서열 번호 83 (CDR2) 및 서열 번호 84 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xv) 서열 번호 85 (CDR1), 서열 번호 86 (CDR2) 및 서열 번호 87 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 88 (CDR1), 서열 번호 89 (CDR2) 및 서열 번호 90 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xvi) 서열 번호 91 (CDR1), 서열 번호 92 (CDR2) 및 서열 번호 93 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 94 (CDR1), 서열 번호 95 (CDR2) 및 서열 번호 96 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xvii) 서열 번호 97 (CDR1), 서열 번호 98(CDR2) 및 서열 번호 99 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 100 (CDR1), 서열 번호 101 (CDR2) 및 서열 번호 102 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xviii) 서열 번호 103 (CDR1), 서열 번호 104 (CDR2) 및 서열 번호 105 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 106 (CDR1), 서열 번호 107 (CDR2) 및 서열 번호 108 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xix) 서열 번호 109 (CDR1), 서열 번호 110 (CDR2) 및 서열 번호 111 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 112 (CDR1), 서열 번호 113 (CDR2) 및 서열 번호 114 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xx) 서열 번호 115 (CDR1), 서열 번호 116 (CDR2) 및 서열 번호 117 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 118 (CDR1), 서열 번호 119 (CDR2) 및 서열 번호 120 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xxi) 서열 번호 121 (CDR1), 서열 번호 122 (CDR2) 및 서열 번호 123 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 124 (CDR1), 서열 번호 125 (CDR2) 및 서열 번호 126 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xxii) 서열 번호 127 (CDR1), 서열 번호 128 (CDR2) 및 서열 번호 129 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 130 (CDR1), 서열 번호 131 (CDR2) 및 서열 번호 132 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xxiii) 서열 번호 133 (CDR1), 서열 번호 134 (CDR2) 및 서열 번호 135 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 136 (CDR1), 서열 번호 137 (CDR2) 및 서열 번호 138 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 및
xxiv) 서열 번호 139 (CDR1), 서열 번호 140 (CDR2) 및 서열 번호 141 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 142 (CDR1), 서열 번호 143 (CDR2) 및 서열 번호 144 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR.
이들 CDR 서열에 의해 정의된 각각의 경쇄/중쇄 가변 도메인은 각각 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23 및 B7H6#24로 칭해진다.
본 발명의 결합 단백질의 바람직한 실시양태에서, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄 (CD3 쇄)는 하기로 이루어진 군으로부터 선택된 CDR 서열을 포함하는, 제2 경쇄 가변 도메인 및 제2 중쇄 가변 도메인을 포함한다:
i) 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
ii) 서열 번호 263 (CDR1), 서열 번호 264 (CDR2) 및 서열 번호 265 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 266 (CDR1), 서열 번호 267 (CDR2) 및 서열 번호 268 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
iii) 서열 번호 269 (CDR1), 서열 번호 270 (CDR2) 및 서열 번호 271 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 272 (CDR1), 서열 번호 273 (CDR2) 및 서열 번호 274 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
iv) 서열 번호 275 (CDR1), 서열 번호 276 (CDR2) 및 서열 번호 277 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 278 (CDR1), 서열 번호 279 (CDR2) 및 서열 번호 280 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
v) 서열 번호 281 (CDR1), 서열 번호 282 (CDR2) 및 서열 번호 283 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 284 (CDR1), 서열 번호 285 (CDR2) 및 서열 번호 286 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 및
vi) 서열 번호 287 (CDR1), 서열 번호 288 (CDR2) 및 서열 번호 289 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 290 (CDR1), 서열 번호 291 (CDR2) 및 서열 번호 292 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR.
이들 CDR 서열에 의해 정의된 각각의 경쇄/중쇄 가변 도메인은 각각 CD3#1, CD3#2, CD3#3, CD3#4, CD3#5 및 CD3#6으로 칭해진다.
바람직하게는, 경쇄 및 중쇄 CDR 서열은 상기 정의한 바와 같은 B7H6#1, B7H6#2, B7H6#, B7H6#4, B7H6#5, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23 및 B7H6#24로 이루어진 군으로부터 선택된다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 67 (CDR1), 서열 번호 68 (CDR2) 및 서열 번호 69 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR을 가지는 제1 경쇄 가변 도메인 및 서열 번호 70 (CDR1), 서열 번호 71 (CDR2) 및 서열 번호 72 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 가지는 제1 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 (B7H6 쇄) 및 (ii) 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR을 가지는 제2 경쇄 가변 도메인 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 가지는 제2 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄를 포함한다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 79 (CDR1), 서열 번호 80 (CDR2) 및 서열 번호 81 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR을 가지는 제1 경쇄 가변 도메인 및 서열 번호 82 (CDR1), 서열 번호 83 (CDR2) 및 서열 번호 84 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 가지는 제1 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 (B7H6 쇄) 및 (ii) 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR을 가지는 제2 경쇄 가변 도메인 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 가지는 제2 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄를 포함한다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 85 (CDR1), 서열 번호 86 (CDR2) 및 서열 번호 87 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR을 가지는 제1 경쇄 가변 도메인 및 서열 번호 88 (CDR1), 서열 번호 89 (CDR2) 및 서열 번호 90 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 가지는 제1 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 (B7H6 쇄) 및 (ii) 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR을 가지는 제2 경쇄 가변 도메인 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 가지는 제2 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄를 포함한다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 91 (CDR1), 서열 번호 92 (CDR2) 및 서열 번호 93 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR을 가지는 제1 경쇄 가변 도메인 및 서열 번호 94 (CDR1), 서열 번호 95 (CDR2) 및 서열 번호 96 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 가지는 제1 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 (B7H6 쇄) 및 (ii) 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의의 아미노산 서열을 포함하는 경쇄 CDR을 가지는 제2 경쇄 가변 도메인 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 가지는 제2 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄를 포함한다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 서열 번호 133 (CDR1), 서열 번호 134 (CDR2) 및 서열 번호 135 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR을 가지는 제1 경쇄 가변 도메인 및 서열 번호 136 (CDR1), 서열 번호 137 (CDR2) 및 서열 번호 138 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 가지는 제1 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 (B7H6 쇄) 및 (ii) 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR을 가지는 제2 경쇄 가변 도메인 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 가지는 제2 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄를 포함한다.
본 발명의 단백질의 바람직한 실시양태에서, B7H6에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄 (B7H6 쇄)는 하기 i) 내지 xiv)로 이루어진 군으로부터 선택되는 경쇄 가변 도메인 (제1 경쇄 가변 도메인) 및 중쇄 가변 도메인 (제1 중쇄 가변 도메인)을 포함한다:
i) 서열 번호 145의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 146의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#1);
ii) 서열 번호 147의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 148의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#2);
iii) 서열 번호 149의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 150의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#3);
iv) 서열 번호 151의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 152의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#4);
v) 서열 번호 153의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 154의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#5);
vi) 서열 번호 155의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 156의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#6);
vii) 서열 번호 157의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 158의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#7);
viii) 서열 번호 159의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 160의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#8);
ix) 서열 번호 161의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 162의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#9);
x) 서열 번호 163의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 164의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#10);
xi) 서열 번호 165의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 166의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#11);
xii) 서열 번호 167의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 168의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#12);
xiii) 서열 번호 169의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 170의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#13);
xiv) 서열 번호 171의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 172의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#14);
xv) 서열 번호 173의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 174의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#15);
xvi) 서열 번호 175의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 176의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#16);
xvii) 서열 번호 177의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 178의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#17);
xviii) 서열 번호 179의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 180의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#18);
xix) 서열 번호 181의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 182의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#19);
xx) 서열 번호 183의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 184의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#20);
xxi) 서열 번호 185의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 186의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#21);
xxii) 서열 번호 187의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 188의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#22);
xxiii) 서열 번호 189의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 190의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#23); 및
xxiv) 서열 번호 191의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 192의 아미노산 서열을 포함하는 중쇄 가변 도메인 (B7H6#24).
바람직하게는, 경쇄 가변 및 중쇄 가변 도메인 서열은 상기에서 정의한 바와 같은 B7H6#1, B7H6#2, B7H6#, B7H6#4, B7H6#5, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23 및 B7H6#24로 이루어진 군에서 선택된다.
본 발명의 단백질의 바람직한 실시양태에서, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄 (CD3 쇄)는 다음으로 이루어진 군에서 선택되는 경쇄 가변 도메인 (제2 경쇄 가변 도메인) 및 중쇄 가변 도메인 (제2 중쇄 가변 도메인)을 포함한다:
i) 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인 (CD3#1);
ii) 서열 번호 295의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 296의 아미노산 서열을 포함하는 중쇄 가변 도메인 (CD3#2);
iii) 서열 번호 297의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 298의 아미노산 서열을 포함하는 중쇄 가변 도메인 (CD3#3)
iv) 서열 번호 299의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 300의 아미노산 서열을 포함하는 중쇄 가변 도메인 (CD3#4)
v) 서열 번호 301의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 302의 아미노산 서열을 포함하는 중쇄 가변 도메인 (CD3#5)
vi) 서열 번호 303의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 304의 아미노산 서열을 포함하는 중쇄 가변 도메인 (CD3#6).
일부 실시양태에서, 본 발명의 결합 단백질은 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#6/CD3#1, B7H6#7/CD3#1, B7H6#8/CD3#1, B7H6#9/CD3#1, B7H6#10/CD3#1, B7H6#11/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1로 이루어진 목록으로부터 선택된 경쇄/중쇄 가변 도메인의 CDR 및/또는 VH 및 VL 서열을 포함하는 제1 및 제2 폴리펩티드 쇄를 포함한다. 바람직한 실시양태에서, 본 발명의 결합 단백질은 B7H6#12/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#23/CD3#1로 이루어진 목록에서 선택된 경쇄/중쇄 가변 도메인의 CDR 및/또는 VH 및 VL 서열을 포함하는 제1 및 제2 폴리펩티드 쇄를 포함한다. 보다 더 바람직하게는, 제1 폴리펩티드 쇄는 서열 번호 242의 아미노산 서열을 포함하는 Fc 도메인을 포함하고, 상기 제2 폴리펩티드 쇄는 서열 번호 243의 아미노산 서열을 포함하는 Fc 도메인을 포함한다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 (i) 서열 번호 167의 경쇄 가변 도메인 및 서열 번호 168의 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 (B7H6 쇄); 및 (ii) 서열 번호 293의 경쇄 가변 도메인 및 서열 번호 294의 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄 (CD3 쇄)를 포함한다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 (i) 서열 번호 171의 경쇄 가변 도메인 및 서열 번호 172의 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 (B7H6 쇄); 및 (ii) 서열 번호 293의 경쇄 가변 도메인 및 서열 번호 294의 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄 (CD3 쇄)를 포함한다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 (i) 서열 번호 173의 경쇄 가변 도메인 및 서열 번호 174의 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 (B7H6 쇄); 및 (ii) 서열 번호 293의 경쇄 가변 도메인 및 서열 번호 294의 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄 (CD3 쇄)를 포함한다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 (i) 서열 번호 175의 경쇄 가변 도메인 및 서열 번호 176의 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 (B7H6 쇄); 및 (ii) 서열 번호 293의 경쇄 가변 도메인 및 서열 번호 294의 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄 (CD3 쇄)를 포함한다.
바람직한 일 실시양태에서, 본 발명의 결합 단백질은 (i) 서열 번호 189의 경쇄 가변 도메인 및 서열 번호 190의 중쇄 가변 도메인을 포함하는 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 (B7H6 쇄); 및 (ii) 서열 번호 293의 경쇄 가변 도메인 및 서열 번호 294의 중쇄 가변 도메인을 포함하는 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄 (CD3 쇄)를 포함한다.
바람직한 실시양태에서, B7H6에 특이적인 제1 폴리펩티드 쇄는 서열 번호 193, 서열 번호 194, 서열 번호 195, 서열 번호 196, 서열 번호 197, 서열 번호 198, 서열 번호 199, 서열 번호 200, 서열 번호 201, 서열 번호 202, 서열 번호 203, 서열 번호 204, 서열 번호 205, 서열 번호 206, 서열 번호 207, 서열 번호 208, 서열 번호 209, 서열 번호 210, 서열 번호 211, 서열 번호 212, 서열 번호 213, 서열 번호 214, 서열 번호 215 또는 서열 번호 216 중 어느 하나의 아미노산 서열을 갖는 단일쇄 Fab를 포함하고 CD3에 특이적인 제2 폴리펩티드 쇄는 서열 번호 305의 아미노산 서열을 갖는 단일쇄 Fab를 포함한다.
바람직하게는, 제1 폴리펩티드 쇄는 서열 번호 193, 서열 번호 194, 서열 번호 195, 서열 번호 196, 서열 번호 197, 서열 번호 204, 서열 번호 205, 서열 번호 206, 서열 번호 207, 서열 번호 208, 서열 번호 209, 서열 번호 210, 서열 번호 211, 서열 번호 212, 서열 번호 213, 서열 번호 214, 서열 번호 215 및 서열 번호 216으로 이루어진 군으로부터 선택된 아미노산 서열, 보다 바람직하게는 서열 번호 204, 서열 번호 205, 서열 번호 206, 서열 번호 207, 서열 번호 208, 서열 번호 209, 서열 번호 210, 서열 번호 211, 서열 번호 212, 서열 번호 213, 서열 번호 214, 서열 번호 215 및 서열 번호 216으로 이루어진 군으로부터 선택된 아미노산 서열을 포함하는 단일쇄 Fab를 포함하고, 제2 폴리펩티드 쇄는 서열 번호 305의 아미노산 서열을 포함하는 단일쇄 Fab를 포함한다.
바람직한 일 실시양태에서, B7H6에 특이적인 제1 폴리펩티드 쇄 (B7H6 쇄)는 서열 번호 204의 아미노산 서열을 포함하는 단일쇄 Fab를 포함하고, CD3에 특이적인 제2 폴리펩티드 쇄 (CD3 쇄)는 서열 번호 305의 아미노산 서열을 포함하는 단일쇄 Fab를 포함한다.
바람직한 일 실시양태에서, B7H6에 특이적인 제1 폴리펩티드 쇄 (B7H6 쇄)는 서열 번호 206의 아미노산 서열을 포함하는 단일쇄 Fab를 포함하고, CD3에 특이적인 제2 폴리펩티드 쇄 (CD3 쇄)는 서열 번호 305의 아미노산 서열을 포함하는 단일쇄 Fab를 포함한다.
바람직한 일 실시양태에서, B7H6에 특이적인 제1 폴리펩티드 쇄 (B7H6 쇄)는 서열 번호 207의 아미노산 서열을 포함하는 단일쇄 Fab를 포함하고, CD3에 특이적인 제2 폴리펩티드 쇄 (CD3 쇄)는 서열 번호 305의 아미노산 서열을 포함하는 단일쇄 Fab를 포함한다.
바람직한 일 실시양태에서, B7H6에 특이적인 제1 폴리펩티드 쇄 (B7H6 쇄)는 서열 번호 208의 아미노산 서열을 포함하는 단일쇄 Fab를 포함하고, CD3에 특이적인 제2 폴리펩티드 쇄 (CD3 쇄)는 서열 번호 305의 아미노산 서열을 포함하는 단일쇄 Fab를 포함한다.
바람직한 일 실시양태에서, B7H6에 특이적인 제1 폴리펩티드 쇄 (B7H6 쇄)는 서열 번호 215의 아미노산 서열을 포함하는 단일쇄 Fab를 포함하고, CD3에 특이적인 제2 폴리펩티드 쇄 (CD3 쇄)는 서열 번호 305의 아미노산 서열을 포함하는 단일쇄 Fab를 포함한다.
또한 scFab에 대한 이러한 특정 실시양태와 관련하여, 용어 "포함하는"은 보다 일반적인 용어로 상기 본원에 정의된 바와 같은 아미노산 서열로 "이루어진" 것도 포함하는 것으로 의도된다.
본 발명의 결합 단백질의 일부 실시양태에서, 제1 및 제2 폴리펩티드 쇄는 IgG, 예를 들어 IgG1, IgG2 또는 IgG4의 중쇄로부터 유래된 Fc 도메인을 포함한다. 예를 들어, 본 발명의 Fc 도메인은 IgG1 또는 IgG4 중쇄의 Fc 도메인이며 힌지 영역과 2개의 불변 도메인 (CH2 및 CH3)을 포함한다. 인간 IgG의 Fc 도메인의 예는 서열 번호 241 및 244에 제시되어 있다.
본 발명의 결합 단백질의 일부 실시양태에서, 중쇄는 하나 이상의 아미노산 변화를 포함한다. 예를 들어, 이러한 아미노산 변화는 제1 중쇄의 위치 366에서의 티로신 (Y) [T366Y] 및 제2 중쇄의 위치 407에서의 트레오닌 (T) [Y407T]이다. 일부 실시양태에서, 제1 중쇄는 위치 366에 세린 (S) [T366S]을 포함하고 제2 중쇄는 위치 366에 트립토판 (W) [T366W], 위치 368에 알라닌 (A) [L368A] 및 위치 407에 발린 (V) [Y407V]을 포함한다. 바람직한 실시양태에서, 제1 중쇄는 위치 366에 트립토판 (W) [T366W]을 포함하고 제2 중쇄는 위치 366에 세린 (S) [T366S], 위치 368에 알라닌 (A) [L368A] 및 위치 407에 발린 (V) [Y407V]을 포함한다. 예를 들어, 서열 번호 241의 인간 IgG1 Fc 서열에서 아미노산 위치 146에 상응하는 Eu 넘버링에 따른 Fc 도메인의 위치 366은 서열 번호 241에 위치 146의 T로부터 서열 번호 242에 위치 146의 W로 변경되고; 서열 번호 241의 아미노산 위치 146, 148 및 187에 각각 상응하는 Eu 넘버링에 따른 위치 366, 368 및 407은 서열 번호 241에 이들 위치에서의 T, L 및 Y로부터 서열 번호 243에 이들 위치에서의 S, A 및 V로 변경된다. 이들 임의의 실시양태에서, 제1 중쇄에 대해 기재된 아미노산 변화는 제2 중쇄에 위치할 수 있고 제2 중쇄에 대한 각각의 아미노산 변화는 제1 중쇄에 위치할 수 있다. 즉, 용어 "제1" 및 "제2"는 이러한 실시양태에서 교환될 수 있다. 일부 실시양태에서, 중쇄는 IgG1 또는 IgG4의 중쇄로부터 유래된다.
일부 실시양태에서, 본 발명의 단백질의 제1 중쇄 또는 제2 중쇄는 단백질 A에 대한 중쇄의 결합을 감소시키는 하나 이상의 아미노산 변화를 추가로 포함한다. 일부 실시양태에서, 이러한 아미노산 변화는 한 중쇄의 위치 435에서 아르기닌 [H435R] 및 위치 436에서 페닐알라닌 [Y436F]이다.
일부 실시양태에서, 본 발명의 단백질에서 위치 407에 트레오닌 (T) [Y407T]을 포함하는 중쇄는 위치 435에 아르기닌 [H435R] 및 위치 436에 페닐알라닌 [Y436F]을 추가로 포함한다. 이 경우, 다른 중쇄는 위치 366에서 티로신 (Y) [T366Y]을 포함하지만 위치 435 및 436에서 두 가지 변화를 포함하지 않는다. 대안적으로, 일부 실시양태에서, 본 발명의 단백질에서, 중쇄는 위치 366에 세린 (S) [T366S], 위치 368에 알라닌 (A) [L368A] 및 위치 407에 발린 (V) [Y407V]을 포함하며, 위치 435에 아르기닌 [H435R] 및 위치 436에 페닐알라닌 [Y436F]을 추가로 포함한다. 이 경우, 다른 중쇄는 위치 366에 트립토판 (W) [T366W]을 포함하지만, 위치 435 및 436에서의 두 가지 변화는 포함하지 않는다. 따라서, 아미노산을 포함하는 중쇄 위에서 설명한 "공동"을 초래하는 산 변화는 또한 단백질 A에 대한 결합을 감소시키는 아미노산 변화를 포함한다. 이들 중쇄를 포함하는 동종이량체는 단백질 A에 대한 결합 감소를 통해 제거된다. "돌출부"를 포함하는 다른 중쇄의 동종이량체의 생성은 "돌출부"의 존재에 의해 감소된다.
일부 실시양태에서, 본 발명의 단백질의 중쇄는 YTE 돌연변이 (M252Y/S254T/T256E, Eu 넘버링 (Dall'Acqua et al., J. Biol. Chem.2006, 281(33):23514-24))를 추가로 포함하거나 포함하지 않을 수 있다. 이러한 돌연변이는 pH 6.0에서 신생아 FcRn 수용체에 대한 결합 친화도의 우선적 향상을 통해 중쇄의 약동학적 특성을 개선하는 것으로 나타났다.
일부 실시양태에서, IgG1으로부터 유래된 본 발명의 제1 및/또는 제2 중쇄는 또한 "KO" 돌연변이 (L234A, L235A)를 포함한다 (Xu et al, Cellular Immunology 2000 Feb 25, 200(1):16-26). 추가 측면에서, IgG4로부터 유래된 본 발명의 제1 및/또는 제2 중쇄는 또한 Pro 힌지 돌연변이 (S228P)를 포함한다 (Angal et al, Molecular Immunology 1993, 30(1):105-108; Labrijn et al, Nature Biotechnology 2009, 27:767-771).
본 발명의 결합 단백질의 바람직한 실시양태에서, 제1 폴리펩티드 쇄는 서열 번호 242의 아미노산 서열을 포함하는 Fc 도메인을 포함하고 제2 폴리펩티드 쇄는 서열 번호 243의 아미노산 서열을 포함하는 Fc 도메인을 포함한다.
본 발명의 바람직한 실시양태에서, 결합 단백질은 i) 서열 번호 217의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#1/CD3#1), 또는 ii) 서열 번호 218의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#2/CD3#1), 또는 iii) 서열 번호 219의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#3/CD3#1), 또는 iv) 서열 번호 220의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 제2 폴리펩티드 서열 번호 311의 아미노산 서열을 포함하는 쇄 (B7H6#4/CD3#1), 또는 v) 서열 번호 221의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#5/CD3#1), 또는 vi) 서열 번호 222의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#6/CD3#1); 또는 vii) 서열 번호 223의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#7/CD3#1); 또는 viii) 서열 번호 224의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#8/CD3#1); 또는 ix) 서열 번호 225의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#9/CD3#1); 또는 x) 서열 번호 226의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#10/CD3#1); 또는 xi) 서열 번호 227의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#11/CD3#1); 또는 xii) 서열 번호 228의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#12/CD3#1); 또는 xiii) 서열 번호 229의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#13/CD3#1); 또는 xiv) 서열 번호 230의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#14/CD3#1); 또는 xv) 서열 번호 231의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#15/CD3#1); 또는 xvi) 서열 번호 232의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#16/CD3#1); 또는 xvii) 서열 번호 233의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#17/CD3#1); 또는 xviii) 서열 번호 234의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#18/CD3#1); 또는 xix) 서열 번호 235의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#19/CD3#1); 또는 xx) 서열 번호 236의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#20/CD3#1); 또는 xxi) 서열 번호 237의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#21/CD3#1); 또는 xxii) 서열 번호 238의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#22/CD3#1); 또는 xxiii) 서열 번호 239의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#23/CD3#1); 또는 xxiv) 서열 번호 240의 아미노산 서열을 포함하는 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 제2 폴리펩티드 쇄 (B7H6#24/CD3#1)를 포함한다. 바람직하게는, 제1 및 제2 폴리펩티드 쇄는 하나 이상의 이황화 결합을 통해 연결되고 통상적인 Y-형 항체 분자와 유사한 항체 유사 구조 (도 1)를 형성한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 228의 아미노산 서열을 포함하는 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다. 바람직하게는, 제1 및 제2 폴리펩티드 쇄는 하나 이상의 이황화 결합을 통해 연결되고 기존의 Y-형 항체 분자와 유사한 항체 유사 구조 (도 1)를 형성한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 230의 아미노산 서열을 포함하는 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다. 바람직하게는, 제1 및 제2 폴리펩티드 쇄는 하나 이상의 이황화 결합을 통해 연결되고 기존의 Y-형 항체 분자와 유사한 항체 유사 구조 (도 1)를 형성한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 231의 아미노산 서열을 포함하는 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다. 바람직하게는, 제1 및 제2 폴리펩티드 쇄는 하나 이상의 이황화 결합을 통해 연결되고 기존의 Y-형 항체 분자와 유사한 항체 유사 구조 (도 1)를 형성한다.
바람직한 일 실시양태에서, 결합 단백질은 서열 번호 232의 아미노산 서열을 포함하는 B7H6에 특이적인 제1 폴리펩티드 쇄 및 서열 번호 311의 아미노산 서열을 포함하는 CD3에 특이적인 제2 폴리펩티드 쇄를 포함한다. 바람직하게는, 제1 및 제2 폴리펩티드는 쇄는 하나 이상의 이황화 결합을 통해 연결되고 기존의 Y-형 항체 분자와 유사한 항체 유사 구조 (도 1)를 형성한다.
추가 측면에서, 본 발명의 단백질은 인간 및 사이노몰거스 원숭이 B7H6에 대해 바람직하게는 ≤ 10 nM, 보다 바람직하게는 ≤ 1 nM, 보다 더 바람직하게는 ≤ 0.1 nM의 친화도로 B7H6에 특이적인 제1 항원 결합 단위 또는 폴리펩티드 쇄를 포함한다. 친화도는, 예를 들어, 실시예 또는 당업자에게 잘 알려진 다른 방법에 기술된 바와 같이 재조합 B7H6-단백질을 사용하여 SPR (BIAcore® SPR 시스템 (GE Healthcare Life Sciences)) 분석에서 측정할 수 있다. 단백질은 인간 및 사이노몰거스 원숭이 CD3εγ 복합체에 대해 바람직하게는 ≤ 500 nM, 보다 바람직하게는 ≤ 100 nM, 보다 더 바람직하게는 ≤ 10 nM의 친화도를 갖는 제2 항원 결합 단위 또는 폴리펩티드 쇄를 포함한다.
추가 측면에서, 본 발명의 B7H6/CD3 결합 단백질은 B7H6-음성 세포에 결합하지 않고 B7H1과 교차 반응하지 않는다 (예를 들어, 각각 실시예 10 및 실시예 4 참조).
바람직한 실시양태에서, 본 발명의 B7H6/CD3 결합 단백질 (예를 들어, B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)은 자연 살해 세포의 활성화를 억제하지 않는다. 특히, 시험관내에서 자연 살해 세포의 활성화를 억제하지 않는 본 발명의 B7H6/CD3 결합 단백질은 NKp30 상호작용 부위가 알라닌으로 치환된 B7H6에 결합한다.
세포 표면 상의 B7H6은 NK 세포의 세포 표면 상의 NKp30에 결합하여 NK 세포의 NKp30 매개 활성화, NK 세포 세포독성 및 사이토카인 분비를 촉발한다 (Brandt et al, J.Exp. Med.2009, 206(7):1495-503). 이 상황은 CD25 또는 CD69와 같은 활성화 마커 또는 NK 세포에 의한 사이토카인 분비의 상향 조절에 대한 후속 분석과 함께 재조합 B7H6 세포외 도메인 단백질로 코팅된 플레이트에서 NK 세포주 (예: NK92MI) 또는 1차 NK 세포를 배양함으로써 시험관내에서 모방될 수 있다. 이 분석 설정을 사용하여 우리의 B7H6/CD3 결합 단백질이 B7H6과 NKp30의 상호작용을 억제하여 IFNγ 분비를 억제하는지 여부를 평가하였다 (실시예 11).
재조합 Ala 돌연변이 B7H6 세포외 단백질 사용; NKp30 상호작용 부위가 알라닌으로 치환된 경우, 두 그룹의 결합 단백질이 있음을 알 수 있었다: 1) 야생형 B7H6에는 강력하게 결합하지만 재조합 Ala-돌연변이 B7H6 세포외 단백질에는 결합하지 않거나 약하게만 결합하는 결합 단백질 단백질은 시험관내에서 NK 세포에 의한 IFNγ의 B7H6 의존적 분비를 억제하고 ("B7H6 의존성 NK 세포 활성화의 억제제"), 2) 야생형 B7H6에 강력하게 결합하고 재조합 Ala-돌연변이된 B7H6 세포외 단백질에도 결합하는 능력을 유지하는 결합 단백질은 NK 세포의 B7H6 의존적 활성화 및 관련 IFNγ 분비를 시험관내에서 억제하지 않는 ("B7H6 의존적 NK 세포 활성화의 비억제제") 것으로 밝혀졌다 (실시예 6 및 11, 도 4 및 9 참조). 놀랍게도, B7H6 의존성 NK 세포 활성화의 비억제제인 본 발명의 결합 단백질은 B7H6 발현 종양 세포의 T 세포 재지향 용해에서 더 강력하다 (실시예 12, 도 10 및 11 참조). 이론에 얽매이지 않고, B7H6 의존성 NK 세포 활성화의 비억제제는 선천성 면역을 매개하는데 B7H6의 자연적 역할에 영향을 미치지 않으면서 B7H6 NKp30 상호작용을 허용할 가능성이 있다.
추가 측면에서, 본 발명의 B7H6/CD3 결합 단백질은 NK 세포 활성과 무관하게 종양 세포에 대한 T 세포 재지향 세포독성을 매개할 수 있다 (NK 세포가 존재하지 않는 마우스 이종이식 모델에 나타난 바와 같음, 실시예 19 참조, 도 20 및 23 참조, 및 NK 세포의 부재하에 세포 용해 분석에서 입증됨, 실시예 12, 도 10 및 11 참조).
본 발명의 B7H6/CD3 결합 단백질에 의해 매개되는 세포 독성을 측정하기 위해 다양한 방법이 사용될 수 있다. 예를 들어, 세포 독성은 실시예 12에 기재된 방법을 사용하여 측정될 수 있다. 이펙터 세포는 예를 들어 자극되거나 자극되지 않은 (인간 또는 사이노몰거스 원숭이) T 세포 또는 이들의 서브세트 (예를 들어, CD4, CD8) 또는 자극되지 않은 (인간 또는 사이노몰거스 원숭이) 말초 혈액 단핵 세포 (PBMC)일 수 있다. 표적 세포는 적어도 (인간 또는 사이노몰거스 원숭이) B7H6의 세포 외 도메인을 발현해야 하며 인간 소세포 폐암종 세포주 SHP77, NCI-H82와 같은 내인성 (천연) B7H6 발현을 갖는 세포, 또는 전장 B7H6 또는 B7H6의 세포 외 도메인을 발현하는 재조합 세포일 수 있다. 이펙터 대 표적 세포 비율 (E:T)은 보통 약 10:1이지만 상이할 수 있다. B7H6/CD3 결합 분자의 세포 독성 활성은 예를 들어 48 또는 72 시간의 인큐베이션 후 LDH-방출 분석으로 결정될 수 있다. 인큐베이션 시간 및 세포 독성의 결정에 사용되는 판독의 변경이 가능하며 당업자에게 알려져 있다. 세포 독성에 대한 판독 시스템은 MTT/MTS 분석, ATP 기반 분석법, FACS 기반 분석법, 51-크롬 방출 분석, 설포로다민 B (SRB) 분석, 비색 (WST) 분석, 클론 생성 분석, ECIS 기술 및 생물 발광 분석을 포함할 수 있다.
본 발명의 B7H6/CD3 결합 단백질에 의해 매개되는 세포 독성 활성은 바람직하게는 세포 기반 세포 독성 분석에서 측정된다. 세포 독성은 세포 독성 분석에서 측정된 EC90 값으로 표시된다. 당업자는 정제된 T 세포가 이펙터 세포로 사용되는 경우 PBMC와 비교하여 EC90이 더 낮을 것으로 예상될 수 있음을 알고 있으며, 또한 당업자는 자극된 T 세포가 사용되는 경우 EC90이 훨씬 더 낮을 수 있음을 알고 있다. 또한 표적 세포가 세포 표면에서 적은 수의 B7H6 분자를 발현하는 세포에 비해 세포 표면에서 많은 수의 B7H6을 발현하는 경우 EC90 값이 더 낮을 것으로 예상할 수 있다. B7H6/CD3 결합 단백질의 EC90은 바람직하게는 ≤10 nM, 더 바람직하게는 ≤5 nM, 보다 더 바람직하게는 ≤1 nM이다.
바람직하게는, 본 발명의 다중 특이적 결합 단백질은 B7H6 음성 세포의 용해를 유도/매개하지 않는다. B7H6-음성 세포의 "용해를 유도/매개하지 않는다"라는 용어는 B7H6/CD3 결합 분자가 B7H6-음성 세포의 용해를 30% 이상으로 유도하거나 매개하지 않고, 바람직하게는 20% 이하, 더 바람직하게는 10% 이하, 특히 5% 이하로 용해 또는 B7H6-음성 세포를 유도하거나 매개하는 것을 의미하며, 반면에, B7H6-양성 직장결장암 세포주의 용해는 100%로 설정된다. 이것은 보통 최대 1000 nM의 결합 단백질 농도에 적용된다.
또한, 본 발명의 B7H6/CD3 결합 단백질은 2 단계 정제 공정에서 95% 초과의 단량체 함량에 도달하고 (실시예 20 참조), 유리한 약동학적 특성 및 양호한 다운스트림 제조가능성을 가지며, 추가로 양호한 생체 분포 (예를 들어, 실시예 18 참조)를 갖는 것으로 나타났다. 또한, 본 발명의 단백질은 유리한 면역원성 프로파일 (실시예 22 참조)을 갖고 시험관내 및 생체내에서 우수한 안정성을 갖는 것 (예를 들어, 실시예 21 및 18 참조)으로 나타났다. 또한, 본 발명의 B7H6/CD3 결합 단백질은 인간화 생체내 이종이식 마우스 모델에서 유리한 효능을 나타낸다. B7H6/CD3 결합 단백질은 B7H6/CD3 결합 단백질의 제1 용량 이후 이미 시작하여 강력한 종양 퇴행을 유도하였다 (예를 들어, 실시예 19 참조). 또한, 본 발명의 B7H6/CD3 결합 단백질은 매주 1회 (q7d) 투여되는 0.05 mg/kg의 매우 낮은 투여량에서 종양 퇴행을 유도하여 그의 치료적 적용성을 추가로 뒷받침한다. 특히, 본 발명의 B7H6/CD3 결합 단백질은 B7H6-음성 표적 세포의 존재하에 있지 않고 B7H6-양성 표적의 존재하에서만 선택적 T 세포 증식, T 세포 활성화, T 세포 탈과립화 및 사이토카인 분비를 유도하고 (각각 실시예 16, 14, 15, 17 참조). 종양 조직으로의 T 세포 침윤을 더욱 현저하게 증가시킨다 (실시예 24 참조).
본 발명의 추가 측면은 본 발명의 다중 특이적 결합 단백질의 제1 및/또는 제2 항원 결합 단위 (각각 표 1에 나타낸 CDR, VH/VL 또는 scFab 서열에 의해 정의된 바와 같은 항원 결합 단위 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 및 B7H6#24 중 어느 하나 및/또는 항원 결합 단위 CD3#1, CD3#2, CD3#3, CD3 중 어느 하나)를 암호화하는 단리된 핵산 분자를 제공한다. 일부 실시양태에서, 핵산 분자는 본원에 기재된 바와 같은 제1 및/또는 제2 Fc 도메인을 추가로 암호화하고, 제1 및/또는 제2 Fc 도메인은 각각 제1 및/또는 제2 항원 결합 단위를 암호화하는 핵산 분자의 3' 말단에 연결된다. 일부 실시양태에서, 핵산 분자는 i) B7H6에 특이적인 제1 단일쇄 Fab를 포함하는 제1 폴리펩티드 쇄 (예를 들어, B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 및 B7H6#24 중 어느 하나) 및 제1 Fc 도메인을 포함하는 제1 폴리펩티드 쇄 및/또는 ii) CD3에 특이적인 제2 단일쇄 Fab 및 제2 Fc 도메인을 포함하는 제2 폴리펩티드 쇄 (예를 들어, CD3#1, CD3#2, CD3#3, CD3#4, CD3#5, 및 CD3#6 중 어느 하나, 바람직하게는 CD3#1)를 포함한다.
바람직하게는, 핵산 분자는 서열 번호 193, 서열 번호 194, 서열 번호 195, 서열 번호 196, 서열 번호 197, 서열 번호 198, 서열 번호 199, 서열 번호 200, 서열 번호 201, 서열 번호 202, 서열 번호 203, 서열 번호 204, 서열 번호 205, 서열 번호 206, 서열 번호 207, 서열 번호 208, 서열 번호 209, 서열 번호 210, 서열 번호 211, 서열 번호 212, 서열 번호 213, 서열 번호 214, 서열 번호 215 또는 서열 번호 216 중 어느 하나의 B7H6에 특이적인 제1 단일쇄 Fab 및/또는 서열 번호 305의 제2 단일쇄 Fab를 암호화하는 뉴클레오티드 서열을 포함한다. 바람직한 실시양태에서, 핵산 분자는 서열 번호 204, 서열 번호 206, 서열 번호 207, 서열 번호 208, 또는 서열 번호 215 중 어느 하나의 B7H6에 특이적인 제1 scFab를 암호화하는 뉴클레오티드 서열 및/또는 서열 번호 305의 아미노산 서열을 포함하는 CD3에 특이적인 제2 scFab를 암호화하는 뉴클레오티드 서열을 포함한다.
본 발명의 추가 측면은 제1 및/또는 제2 항원 결합 도메인 (예를 들어, 본 발명의 제1 및/또는 제2 단일쇄 Fab)을 암호화하는 뉴클레오티드 서열을 포함하는 DNA 분자를 함유하는 발현 벡터를 제공한다. 바람직하게는 발현 벡터는 추가로 제1 및/또는 제2 항원 결합 도메인 (예를 들어, 각각 제1 및/또는 제2 단일쇄 Fab)을 암호화하는 핵산 분자, 바람직하게는 DNA 분자에 연결된 제1 및/또는 제2 Fc 도메인을 암호화하는 핵산 분자, 바람직하게는 DNA 분자를 포함한다. 이와 같이, 발현 벡터는 제1 Fc 도메인에 연결된 제1 단일쇄 Fab를 포함하는 폴리펩티드 쇄를 암호화하는 뉴클레오티드 서열 및/또는 제2 Fc 도메인에 연결된 제2 단일쇄 Fab를 포함하는 폴리펩티드 쇄를 암호화하는 뉴클레오티드 서열을 포함한다.
바람직한 실시양태에서, 발현 벡터는 본 발명의 B7H6에 특이적인 제1 폴리펩티드 쇄 및/또는 CD3에 특이적인 제2 폴리펩티드 쇄를 암호화하는 뉴클레오티드 서열을 포함하는 DNA 분자를 함유한다. 바람직한 실시양태에서, 발현 벡터는 서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 서열 번호 221, 서열 번호 222, 서열 번호 223, 서열 번호 224, 서열 번호 225, 서열 번호 226, 서열 번호 227, 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239 또는 서열 번호 240 중 어느 하나의 제1 폴리펩티드 쇄를 암호화하는 뉴클레오티드 서열 및/또는 서열 번호 311을 포함하는 제2 폴리펩티드 쇄를 암호화하는 뉴클레오티드 서열을 포함한다.
추가의 바람직한 실시양태에서, 발현 벡터는 서열 번호 228, 서열 번호 230, 서열 번호 231, 서열 번호 232, 및 서열 번호 239 중 어느 하나의 제1 폴리펩티드 쇄를 암호화하는 뉴클레오티드 서열 및/또는 서열 번호 311을 포함하는 제2 폴리펩티드 쇄를 암호화하는 뉴클레오티드 서열을 포함한다.
특히 바람직한 실시양태에서, 2개의 발현 벡터가 사용될 수 있는데, 이 중 하나는 B7H6에 특이적인 제1 폴리펩티드 쇄의 발현을 위해, 다른 하나는 CD3에 특이적인 제2 폴리펩티드 쇄의 발현을 위해 사용될 수 있고, 두 발현 벡터는 모두 재조합 단백질 발현을 위해 숙주 세포로 형질감염될 수 있다.
바람직하게는, 발현 벡터는 적어도 하나의 조절 서열에 작동 가능하게 연결된 상기 핵산 분자 또는 분자를 포함하는 벡터일 것이며, 여기서 이러한 조절 서열은 프로모터, 인핸서 또는 종결자 서열, 가장 바람직하게는 이종 프로모터, 인핸서, 또는 종결자 서열일 수 있다.
또 다른 측면에서, 본 발명은 본 발명의 B7H6에 특이적인 제1 폴리펩티드 쇄를 암호화하는 발현 벡터 및 본 발명의 CD3에 특이적인 제2 폴리펩티드 쇄를 암호화하는 발현 벡터를 갖는 숙주 세포에 관한 것이다.
특히 바람직한 실시양태에 따르면, 상기 숙주 세포는 포유동물 세포와 같은 진핵 세포이다. 또 다른 실시양태에서, 이러한 숙주 세포는 박테리아 세포이다. 다른 유용한 세포는 효모 세포 또는 기타 진균 세포이다.
적합한 포유동물 세포에는 예를 들어 CHO 세포, BHK 세포, HeLa 세포, COS 세포 등이 포함된다. 그러나, 양서류 세포, 곤충 세포, 식물 세포 및 이종 단백질의 발현을 위해 당업계에서 사용되는 다른 세포도 사용될 수 있다.
항-B7H6 항체
본 발명의 추가 측면은 다음을 포함하는 항-B7H6 항체 분자를 제공한다:
i) 서열 번호 1 (CDR1), 서열 번호 2 (CDR2) 및 서열 번호 3 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 4 (CDR1), 서열 번호 5 (CDR2) 및 서열 번호 6 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
ii) 서열 번호 7 (CDR1), 서열 번호 8 (CDR2) 및 서열 번호 9 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 10 (CDR1), 서열 번호 11 (CDR2) 및 서열 번호 12 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
iii) 서열 번호 13 (CDR1), 서열 번호 14 (CDR2) 및 서열 번호 15 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 16 (CDR1), 서열 번호 17 (CDR2) 및 서열 번호 18 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
iv) 서열 번호 19 (CDR1), 서열 번호 20 (CDR2) 및 서열 번호 21 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 22 (CDR1), 서열 번호 23 (CDR2) 및 서열 번호 24 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
v) 서열 번호 25 (CDR1), 서열 번호 26 (CDR2) 및 서열 번호 27 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 28 (CDR1), 서열 번호 29 (CDR2) 및 서열 번호 30 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
vi) 서열 번호 31 (CDR1), 서열 번호 32 (CDR2) 및 서열 번호 33 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 34 (CDR1), 서열 번호 35 (CDR2) 및 서열 번호 36 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
vii) 서열 번호 37 (CDR1), 서열 번호 38 (CDR2) 및 서열 번호 39 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 40 (CDR1), 서열 번호 41 (CDR2) 및 서열 번호 42 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
viii) 서열 번호 43 (CDR1), 서열 번호 44 (CDR2) 및 서열 번호 45 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 46 (CDR1), 서열 번호 47 (CDR2) 및 서열 번호 48 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
ix) 서열 번호 49 (CDR1), 서열 번호 50 (CDR2) 및 서열 번호 51 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 52 (CDR1), 서열 번호 53 (CDR2) 및 서열 번호 54 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
x) 서열 번호 55 (CDR1), 서열 번호 56 (CDR2) 및 서열 번호 57 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 58 (CDR1), 서열 번호 59 (CDR2) 및 서열 번호 60 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xi) 서열 번호 61 (CDR1), 서열 번호 62 (CDR2) 및 서열 번호 63 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 64 (CDR1), 서열 번호 65 (CDR2) 및 서열 번호 66 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xii) 서열 번호 67 (CDR1), 서열 번호 68 (CDR2) 및 서열 번호 69 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 70 (CDR1), 서열 번호 71 (CDR2) 및 서열 번호 72 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xiii) 서열 번호 73 (CDR1), 서열 번호 74 (CDR2) 및 서열 번호 75 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 76 (CDR1), 서열 번호 77 (CDR2) 및 서열 번호 78 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xiv) 서열 번호 79 (CDR1), 서열 번호 80 (CDR2) 및 서열 번호 81 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 82 (CDR1), 서열 번호 83 (CDR2) 및 서열 번호 84 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xv) 서열 번호 85 (CDR1), 서열 번호 86 (CDR2) 및 서열 번호 87 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 88 (CDR1), 서열 번호 89 (CDR2) 및 서열 번호 90 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xvi) 서열 번호 91 (CDR1), 서열 번호 92 (CDR2) 및 서열 번호 93 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 94 (CDR1), 서열 번호 95 (CDR2) 및 서열 번호 96 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xvii) 서열 번호 97 (CDR1), 서열 번호 98 (CDR2) 및 서열 번호 99 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 100 (CDR1), 서열 번호 101 (CDR2) 및 서열 번호 102 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xviii) 서열 번호 103 (CDR1), 서열 번호 104 (CDR2) 및 서열 번호 105 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 106 (CDR1), 서열 번호 107 (CDR2) 및 서열 번호 108 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xix) 서열 번호 109 (CDR1), 서열 번호 110 (CDR2) 및 서열 번호 111 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 112 (CDR1), 서열 번호 113 (CDR2) 및 서열 번호 114 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xx) 서열 번호 115 (CDR1), 서열 번호 116 (CDR2) 및 서열 번호 117 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 118 (CDR1), 서열 번호 119 (CDR2) 및 서열 번호 120 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xxi) 서열 번호 121 (CDR1), 서열 번호 122 (CDR2) 및 서열 번호 123 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 124 (CDR1), 서열 번호 125 (CDR2) 및 서열 번호 126 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xxii) 서열 번호 127 (CDR1), 서열 번호 128 (CDR2) 및 서열 번호 129 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 130 (CDR1), 서열 번호 131 (CDR2) 및 서열 번호 132 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xxiii) 서열 번호 133 (CDR1), 서열 번호 134 (CDR2) 및 서열 번호 135 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 136 (CDR1), 서열 번호 137 (CDR2) 및 서열 번호 138 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xxiv) 서열 번호 139 (CDR1), 서열 번호 140 (CDR2) 및 서열 번호 141 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 142 (CDR1), 서열 번호 143 (CDR2) 및 서열 번호 144 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR.
상기 설명된 바와 같은 항체 i) 내지 xxiv)는 각각 B7H6#1, B7H6#2, B7H6#3, B7H6#4, B7H6#5, B7H6#6, B7H6#7, B7H6#8, B7H6#9, B7H6#10, B7H6#11, B7H6#12, B7H6#13, B7H6#14, B7H6#15, B7H6#16, B7H6#17, B7H6#18, B7H6#19, B7H6#20, B7H6#21, B7H6#22, B7H6#23, 및 B7H6#24로 칭해진다. 본 발명의 특정 항체에 대한 개별 아미노산 서열의 식별이 용이하도록 서열표가 본원에 제공된다.
일부 실시양태에서, 본 발명의 항-B7H6 항체는 키메라, 인간화, 인간 또는 최적화된 항체 분자이다. 일부 실시양태에서, 항체 분자는 모노클로날 항체 Fab, F (ab)2, Fv 또는 scFv이다. 일부 실시양태에서, 본 발명의 항-B7H6 항체 분자는 IgG1, IgG2, IgG3, IgG4, IgM, IgA 및 IgE 불변 영역으로 이루어진 군으로부터 선택된 중쇄 불변 영역을 포함한다. 일부 실시양태에서, 본 발명의 항-B7H6 항체 분자의 경쇄 불변 영역은 카파 또는 람다이다.
일부 실시양태에서, 본 발명의 항-B7H6 항체는 서열 번호 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190, 및 192 중 어느 하나와 적어도 85% 동일한 아미노산 서열을 포함하는 중쇄 가변 도메인을 갖는다. 바람직하게는, 항체 분자는 서열 번호 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190 또는 192의 아미노산을 포함하는 중쇄 가변 도메인을 갖는다.
일부 실시양태에서, 항-B7H6 항체 분자는 서열 번호 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 및 191 중 어느 하나와 적어도 85% 동일한 아미노산 서열을 포함하는 경쇄 가변 도메인을 갖는다. 바람직하게는, 항체 분자는 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 및 191의 아미노산 서열을 포함하는 경쇄 가변 도메인을 갖는다.
아미노산 서열 동일성을 계산하는 방법은 당업계에 잘 알려져 있으며 본 명세서의 정의 섹션에 자세히 논의되었다.
일부 실시양태에서, 항-B7H6 항체 분자는 i) 서열 번호 146의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 145의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#1); 또는 ii) 서열 번호 148의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 147의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#2); 또는 iii) 서열 번호 150의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 149의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#3); 또는 iv) 서열 번호 152의 아미노산을 포함하는 중쇄 가변 도메인 및 서열 번호 151의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#4); 또는 v) 서열 번호 154의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 153의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#5); 또는 vi) 서열 번호 156의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 155의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#6); 또는 vii) 서열 번호 158의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 157의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#7); 또는 viii) 서열 번호 160의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 159의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#8); 또는 ix) 서열 번호 162의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 161의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#9); 또는 x) 서열 번호 164의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 163의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#10); 또는 xi) 서열 번호 166의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 165의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#11); 또는 xii) 서열 번호 168의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 167의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#12); 또는 xiii) 서열 번호 170의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 169의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#13); 또는 xiv) 서열 번호 172의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 171의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#14); 또는 xv) 서열 번호 174의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 173의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#15); 또는 xvi) 서열 번호 176의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 175의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#16); 또는 xvii) 서열 번호 178의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 177의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#17); 또는 xviii) 서열 번호 180의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 179의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#18); 또는 xix) 서열 번호 182의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 181의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#19); 또는 xx) 서열 번호 184의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 183의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#20); 또는 xxi) 서열 번호 186의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 185의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#21); 또는 xxii) 서열 번호 188의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 187의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#22); 또는 xxiii) 서열 번호 190의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 189의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#23); 또는 xxiv) 서열 번호 192의 아미노산 서열을 포함하는 중쇄 가변 도메인 및 서열 번호 191의 아미노산 서열을 포함하는 경쇄 가변 도메인 (B7H6#24)을 가진다.
일부 실시양태에서, 본 발명의 항-B7H6 항체는 마우스 모노클로날 항체이다. 본 발명의 맥락에서, 마우스 모노클로날 항체는 인간 B7H6 단백질로 마우스를 면역화하고, 인간 B7H6에 대해 특정 친화도로 결합하는 적합한 VH 및 VL 서열을 후속 선택한 후, 상기 VH 및 VL 서열을 재조합 기술에 의해 마우스 (예를 들어, 마우스 IgG2a로부터)로부터 유래되고; 숙주 세포에서 재조합 발현에 의해 생성된 불변 도메인에 추가 연결하여 VH 및 VL이 수득된 항체를 포함한다. 예를 들어 상이한 종으로부터의 가변 및 불변 영역을 포함하는 키메라 항체가 본 발명에 추가로 포함된다. 일부 실시양태에서, 본 발명의 항체 분자는 상기 기재된 바와 같이 마우스로부터 유래된 VH 및 VL 도메인을 포함하고 인간, 토끼, 래트, 염소, 당나귀와 같은 다른 종으로부터 유래된 불변 도메인을 추가로 포함하는 키메라 항체이다. 일부 실시양태에서, 키메라 항체는 마우스로부터 유래된 VH 및 VL 도메인을 포함하고 추가로 인간화되거나 상기 정의된 바와 같이 최적화된 서열을 포함하고 다른 종으로부터 유래된 불변 도메인을 추가로 포함한다. 일부 실시양태에서, 키메라 항체는 인간 IgG 서열을 포함하는 유전자이식 동물 (예를 들어, 마우스)로부터 유래된 VH 및 VL 도메인을 포함하고, 따라서 인간 VH 및 VL 서열을 포함하고, 다른 종으로부터 유래된 불변 도메인을 추가로 포함한다. 상술된 키메라 항체의 임의의 실시양태에서, 중쇄 불변 영역은 마우스, 인간, 토끼, 래트, 염소 또는 당나귀 중쇄 영역이다.
일부 실시양태에서, 본 발명의 항-B7H6 항체 분자는 IgG1, IgG2, IgG3, IgG4, IgM, IgA 및 IgE 불변 도메인으로 이루어진 군으로부터 선택된 불변 도메인을 갖는다. 바람직한 실시양태에서, 항-B7H6 항체는 IgG2a의 불변 도메인을 갖는다. 일부 실시양태에서, 항-B7H6 항체 분자는 카파 또는 람다인 경쇄 불변 도메인을 갖고, 바람직하게는 경쇄 불변 도메인은 바람직하게는 서열 번호 247의 서열을 포함하는 카파 경쇄 불변 도메인이다.
본원에 제공된 B7H6 특이적 항체는 염료, 약물 또는 상이한 항원에 대한 결합 특이성을 갖는 다른 분자를 부착함으로써 B7H6을 발현하는 세포를 표지화, 국소화, 식별 또는 표적화하는 데 (예를 들어 ELISA 분석, FACS 분석, 면역조직학 등에서) 사용될 수 있다.
본 발명의 또 다른 측면은 본 발명의 항-B7H6 항체 분자의 중쇄 가변 도메인 및/또는 경쇄 가변 도메인을 암호화하는 단리된 핵산 분자를 제공한다.
바람직하게는 핵산 분자는 서열 번호 146, 148, 150, 152, 154, 156, 158, 160, 162, 164, 166, 168, 170, 172, 174, 176, 178, 180, 182, 184, 186, 188, 190, 또는 192 중 어느 하나의 중쇄 가변 도메인을 암호화하는 뉴클레오티드 서열을 포함한다. 바람직하게는 핵산 분자는 서열 번호 145, 147, 149, 151, 153, 155, 157, 159, 161, 163, 165, 167, 169, 171, 173, 175, 177, 179, 181, 183, 185, 187, 189, 또는 191 중 어느 하나의 경쇄 가변 도메인을 암호화하는 뉴클레오티드 서열을 포함한다.
본 발명의 추가 측면은 본 발명의 항-B7H6 항체 분자의 중쇄 가변 도메인 및/또는 경쇄 가변 도메인을 암호화하는 뉴클레오티드 서열을 포함하는 DNA 분자를 함유하는 발현 벡터를 제공한다.
바람직하게는 발현 벡터는 추가로 각각 중쇄 불변 도메인 및/또는 경쇄 불변 도메인을 암호화하는 핵산 분자, 바람직하게는 DNA 분자에 연결된 중쇄의 불변 도메인 및/또는 경쇄의 불변 도메인을 각각 암호화하는 핵산 분자, 바람직하게는 DNA 분자를 포함한다.
특히 바람직한 실시양태에서, 2개의 발현 벡터가 사용될 수 있는데, 그 중 하나는 중쇄의 발현을 위한 것이고 다른 하나는 경쇄의 발현을 위한 것이며, 두 발현 벡터는 모두 재조합 단백질 발현을 위해 숙주 세포로 형질감염될 수 있다.
바람직하게는, 발현 벡터는 적어도 하나의 조절 서열에 작동 가능하게 연결된 상기 핵산 분자 또는 분자들을 포함하는 벡터일 것이며, 여기서 이러한 조절 서열은 프로모터, 인핸서 또는 종결자 서열, 가장 바람직하게는 이종 프로모터, 인핸서, 또는 종결자 서열일 수 있다.
또 다른 측면에서, 본 발명은 본 발명의 항-B7H6 항체 분자의 중쇄를 암호화하는 발현 벡터 및 본 발명의 항-B7H6 항체 분자의 경쇄를 암호화하는 발현 벡터를 갖는 숙주 세포에 관한 것이다.
특히 바람직한 실시양태에 따르면, 상기 숙주 세포는 포유동물 세포와 같은 진핵 세포이다. 또 다른 실시양태에서, 이러한 숙주 세포는 박테리아 세포이다. 다른 유용한 세포는 효모 세포 또는 기타 진균 세포이다.
적합한 포유동물 세포는 예를 들어 CHO 세포, BHK 세포, HeFa 세포, COS 세포 등을 포함한다. 그러나, 양서류 세포, 곤충 세포, 식물 세포 및 이종 단백질의 발현을 위해 당업계에서 사용되는 다른 세포도 사용될 수 있다.
제조 및 정제 방법
본 발명은 본 발명의 다중-특이적 결합 단백질을 제조하는 방법을 추가로 제공하며, 이 방법은 일반적으로 다음 단계를 포함한다:
- 본 발명의 결합 단백질의 형성을 허용하는 조건 하에서 본 발명의 결합 단백질을 암호화하는 핵산을 포함하는 발현 벡터를 포함하는 숙주 세포를 배양하는 단계;
- 배양물로부터 숙주 세포에 의해 발현된 결합 단백질을 회수하는 단계; 및
- 임의로 본 발명의 결합 단백질을 추가로 정제 및/또는 변형 및/또는 제형화하는 단계.
본 발명은 본 발명의 항-B7H6 항체를 제조하는 방법을 추가로 제공하며, 이 방법은 일반적으로 다음 단계를 포함한다:
- 항체 분자의 형성을 허용하는 조건 하에서 본 발명의 항체 분자를 암호화하는 핵산을 포함하는 발현 벡터를 포함하는 숙주 세포를 배양하는 단계;
- 배양물로부터 숙주 세포에 의해 발현된 항체 분자를 회수하는 단계; 및
- 임의로 본 발명의 항체 분자를 추가로 정제 및/또는 변형 및/또는 제형화하는 단계.
본 발명의 핵산은 예를 들어 암호화 서열뿐만 아니라 조절 서열 및 임의로 천연 또는 인공 인트론을 포함하는 DNA 분자이거나 cDNA 분자일 수 있다. 그것은 원래의 코돈을 가질 수 있거나 의도된 숙주 세포 또는 숙주 유기체에서의 발현을 위해 특이적으로 조정된 최적화된 코돈 사용을 가질 수 있다. 본 발명의 일 실시양태에 따르면, 본 발명의 핵산은 상기 정의된 바와 같이 본질적으로 단리된 형태이다.
본 발명의 핵산은 본원에 제공된 본 발명의 단백질에 대한 아미노산 서열에 대한 정보에 기초하여 그 자체로 공지된 방식 (예를 들어, 자동화된 DNA 합성 및/또는 재조합 DNA 기술에 의해)으로 제조되거나 수득될 수 있다.
본 발명의 핵산은 전형적으로 발현 벡터, 즉 적합한 숙주 세포 또는 다른 발현 시스템으로 형질감염되는 경우 단백질의 발현을 제공할 수 있는 벡터에 통합될 것이다.
본 발명의 결합 단백질 또는 항체를 제조하기 위해, 숙련된 기술자는 당업계에 널리 공지된 매우 다양한 발현 시스템, 예를 들어 Kipriyanow and Le Gall, 2004에서 검토된 것을 선택할 수 있다.
발현 벡터는 플라스미드, 레트로바이러스, 코스미드, EBV 유래 에피솜 등을 포함한다. 발현 벡터 및 발현 조절 서열은 숙주 세포와 양립할 수 있도록 선택된다. 제1 항원 결합 단위 (예를 들어, 본 발명의 결합 단백질의 B7H6 특이적 단일쇄 Fab 또는 전장 B7H6 쇄)를 암호화하는 뉴클레오티드 서열 및 B7H6/CD3 결합 단백질의 제2 항원 결합 단위를 암호화하는 뉴클레오티드 서열 (예를 들어, 본 발명의 결합 단백질의 CD3 특이적 단일쇄 Fab 또는 전장 CD3 쇄)은 별도의 벡터에 삽입될 수 있다. 특정 실시양태에서, 양 DNA 서열은 동일한 발현 벡터에 삽입된다. B7H6 항체의 경쇄를 암호화하는 뉴클레오티드 서열 및 B7H6 항체의 중쇄를 암호화하는 뉴클레오티드 서열은 별도의 벡터에 삽입될 수 있다. 특정 실시양태에서, 양 DNA 서열은 동일한 발현 벡터에 삽입된다.
편리한 벡터는 상술된 바와 같이 단일쇄 Fab 서열 또는 임의의 중쇄/경쇄 가변 도메인과 같은 임의의 항원 결합 단위가 쉽게 삽입 및 발현될 수 있도록 조작된 적절한 제한 부위와 함께 기능적으로 완전한 인간 CH (불변 중쇄) 면역글로불린 서열을 암호화하는 벡터이다. 항체 중쇄의 경우, 이는 제한없이 임의의 IgG 동형 (IgG1, IgG2, IgG3, IgG4) 또는 대립 유전자 변이체를 포함한 기타 면역글로불린일 수 있다.
재조합 발현 벡터는 또한 숙주 세포로부터 전장 CD3 또는 B7H6 쇄 또는 항-B7H6 항체의 경쇄/중쇄의 분비를 촉진하는 신호 펩티드를 암호화할 수 있다. 단백질 쇄를 암호화하는 DNA는 신호 펩티드가 성숙한 전장 쇄 DNA의 아미노 말단에 프레임 내로 연결되도록 벡터에 클로닝될 수 있다. 신호 펩티드는 면역글로불린 신호 펩티드 또는 비면역글로불린 단백질로부터의 이종 펩티드일 수 있다. 대안적으로, 본 발명의 단백질의 전장 쇄를 암호화하는 DNA 서열은 이미 신호 펩티드 서열을 포함하고 있을 수 있다.
DNA 서열을 암호화하는 B7H6/CD3 쇄 또는 DNA 서열을 암호화하는 B7H6 항체의 중쇄/경쇄에 추가하여, 재조합 발현 벡터는 전형적으로 프로모터, 인핸서, 종결 및 폴리아데닐화 신호 및 숙주 세포에서 항체 쇄의 발현을 조절하는 다른 발현 조절 요소를 포함하는 조절 서열, 임의로 이종 조절 서열을 가진다. (포유동물 세포에서의 발현을 위해 예시된) 프로모터 서열의 예로는 CMV 유래의 프로모터 및/또는 인핸서 (예컨대, CMV 유인원바이러스 40 (SV40) 프로모터/인핸서), 아데노바이러스 (예를 들어, 아데노바이러스 주요 후기 프로모터 (AdMLP)), 폴리오마 및 천연 면역글로불린 및 액틴 프로모터와 같은 강력한 포유동물 프로모터가 있다. 폴리아데닐화 신호의 예로서 BGH polyA, SV40 후기 또는 초기 polyA; 또는, 면역글로불린 유전자의 3'UTR 등이 사용될 수 있다.
재조합 발현 벡터는 또한 숙주 세포에서 벡터의 복제 (예를 들어, 복제 기원) 및 선별 마커 유전자를 조절하는 서열을 보유할 수 있다. 제1 항원 결합 단위 (단일쇄 Fab 및 Fc 도메인) 또는 그의 항원 결합 부분을 갖는 전장 쇄 및/또는 제2 항원 결합 단위 (단일쇄 Fab 및 Fc 도메인) 또는 그의 항원 결합 부분을 갖는 전장 쇄를 암호화하는 핵산 분자 및 이들 DNA 분자를 포함하는 벡터는 리포좀-매개 형질감염, 폴리양이온-매개 형질감염, 원형질체 융합, 마이크로주입, 인산칼슘 침전법, 전기천공 또는 바이러스 벡터에 의한 전달을 비롯한 당업계에 공지된 형질감염 방법에 따라 숙주 세포, 예를 들어 박테리아 세포 또는 고등 진핵 세포, 예를 들면, 포유동물 세포 내로 도입될 수 있다.
바람직하게는, 본 발명의 단백질의 B7H6 및 CD3 쇄를 암호화하는 DNA 분자는 숙주 세포, 바람직하게는 포유동물 세포로 공동-형질감염되는 2개의 발현 벡터에 존재한다.
발현을 위한 숙주로서 이용가능한 포유동물 세포주는 당업계에 잘 알려져 있으며, 특히 중국 햄스터 난소 (CHO) 세포, NS0, SP2/0 세포, HeLa 세포, 베이비 햄스터 신장 (BHK) 세포, 원숭이 신장 세포 (COS), 인간 암종 세포 (예를 들어, Hep G2 및 A-549 세포), 3T3 세포 또는 임의의 그러한 세포주의 유도체/자손을 포함한다. 인간, 마우스, 래트, 원숭이 및 설치류 세포주를 예로 들 수 있으나 이에 한정되지 않는 다른 포유동물 세포, 또는 효모, 곤충 및 식물 세포를 예로 들 수 있으나 이에 한정되지 않는 다른 진핵 세포 또는 박테리아와 같은 원핵 세포가 사용될 수 있다.
본 발명의 단백질은 숙주 세포에서 단백질의 발현을 허용하기에 충분한 시간 동안 숙주 세포를 배양함으로써 생성된다. 단백질 분자는 바람직하게는 분비된 폴리펩티드로서 배양 배지로부터 회수되거나, 예를 들어 분비 신호없이 발현되는 경우 숙주 세포 용해물로부터 회수될 수 있다. 단백질의 실질적으로 균질한 제제가 얻어지는 방식으로 재조합 단백질 및 숙주 세포 단백질에 사용되는 표준 단백질 정제 방법을 사용하여 단백질 분자를 정제하는 것이 필요하다. 예를 들어, 본 발명의 단백질 분자를 얻는 데 유용한 최첨단 정제 방법은 제1 단계로서 배양 배지 또는 용해물로부터 세포 및/또는 미립자 세포 파편을 제거하는 단계를 포함한다. 이어서 단백질이 예를 들어 면역 친화성 또는 이온 교환 컬럼, 에탄올 침전, 역상 HPLC, Sephadex 크로마토그래피, 실리카상의 크로마토그래피 또는 양이온 교환 수지상에서의 분획화에 의해 오염 가용성 단백질, 폴리펩티드 및 핵산으로부터 정제된다. 단백질 분자 제제를 수득하기 위한 공정의 최종 단계로서, 정제된 결합 분자 또는 항체는 치료적 적용을 위해 하기 기술된 바와 같이, 건조, 예를 들면 동결 건조될 수 있다.
본 발명은 적어도 2개의 상이한 표적에 대해 결합 특이성을 갖는 결합 단백질에 관한 것이다. 본 발명과 관련하여, 결합 분자는 항체로부터 유래된다. 결합 분자를 제조하는 기술에는 상이한 특이성을 갖는 2개의 면역글로불린 쇄 쌍의 재조합 공동 발현 (Milstein and Cuello, Nature 305: 537 (1983)), WO 93/08829, 및 Traunecker et al., EMBO J. 10: 3655 (1991) 참조), 및 "노브-인-홀 (knob-in-hole)" 공학 (예를 들어, 미국 특허 제5,731,168호 참조; Atwell et al, JMB, 1997, 270, 26-35 참조)이 있으나 이에 한정되지 않는다. 본 발명의 결합 분자는 또한 항체 Fc-헤테로이량체 분자를 제조하기 위한 정전기적 조종 효과 (electrostatic steering effect)의 조작 (WO 2009/089004A1); 2개 이상의 항체 또는 단편의 교차 연결 (예를 들어, 미국 특허 제4,676,980호 및 Brennan et al., Science, 229: 81 (1985) 참조); 이중 특이적 항체를 제조하기 위한 류신 지퍼 이용 (예를 들어, Kostelny et al., Immunol., 148(5): 1547-1553 (1992) 참조); 이중 특이적 단편을 제조하기 위한 "디아바디" 기술 이용 (예를 들어, Hollinger et al., Proc. Natl. Acad. Sci. USA, 90:6444-6448 (1993) 참조); 및 단일쇄 Fv (sFv) 이량체 사용 (예를 들어, Gruber et al., Immunol., 152:5368 (1994) 참조); 및 예를 들어 문헌 [Tutt et al. Immunol. 147: 60 (1991)]에 기재되어 있는 삼중 특이성 항체 제조에 의해 제조될 수 있다.
본원에 개시된 조성물 (예를 들어, 다중-특이적 결합 단백질 및 항-B7H6 항체) 및 방법은 명시된 서열, 또는 이와 실질적으로 동일하거나 유사한 서열, 예를 들어, 명시된 서열과 적어도 85%, 90%, 95% 동일한 서열을 갖는 폴리펩티드 및 핵산을 포함한다. 아미노산 서열과 관련하여, 용어 "실질적으로 동일한"은 제1 및 제2 아미노산 서열이 공통 구조 도메인 및/또는 공통 기능 활성을 가질 수 있도록 제2 아미노산 서열에서 정렬된 아미노산 잔기와 i) 동일하거나, ii) 보존적 치환인 충분한 또는 최소 수의 아미노산 잔기를 함유하는 제1 아미노산 서열을 지칭하기 위해 본원에서 사용된다. 예를 들어, 공통 구조 도메인을 함유하는 아미노산 서열은 참조 서열, 예를 들어 본원에 제공된 서열과 적어도 약 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% 또는 99%의 동일성을 갖는다. 뉴클레오티드 서열과 관련하여, 용어 "실질적으로 동일한"은 제1 및 제2 뉴클레오티드 서열이 공통 기능적 활성을 갖는 폴리펩티드를 암호화하거나, 공통 구조적 폴리펩티드 도메인 또는 공통 기능적 폴리펩티드 활성을 암호화하도록 제2 핵산 서열에서 정렬된 뉴클레오티드와 동일한 충분한 또는 최소 수의 뉴클레오티드를 포함하는 제1 핵산 서열을 지칭하기 위해 본원에서 사용되며, 예를 들어 뉴클레오티드 서열은 참조 서열과 적어도 약 85%, 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% 또는 99% 동일성을 갖는다.
본 발명의 핵산 분자는 서열 목록에 제시된 폴리펩티드 서열을 암호화하는 DNA 분자를 포함하지만, 이에 한정되는 것은 아니다. 또한, 본 발명은 WO 2007/042309에 정의된 바와 같이 매우 엄격한 결합 및 세척 조건하에 서열 목록에 제시된 폴리펩티드 서열을 암호화하는 DNA 분자에 하이브리드화하는 핵산 분자에 관한 것이다. 바람직한 분자 (mRNA 관점에서)는 본원에 기재된 DNA 분자 중 하나와 적어도 75% 또는 80% (바람직하게는 적어도 85%, 보다 바람직하게는 적어도 90%, 가장 바람직하게는 적어도 95%)의 상동성 또는 서열 동일성을 갖는 것이다. 예를 들어, 진핵 세포에서 항체를 발현한다는 관점에서, 서열 목록에 제시된 DNA 서열은 진핵 세포에서의 코돈 용법과 일치하도록 설계되었다. 대장균에서 항체를 발현하는 것이 바람직하다면, 이 서열을 대장균 코돈 용법에 맞추기 위해 변경할 수 있다. 본 발명의 DNA 분자의 변이체는 다수의 상이한 방법으로, 예를 들어 WO 2007/042309에 기재된 바와 같이 작제될 수 있다.
본 발명의 단백질은 특정 발현 시스템 (예컨대 특정 벡터 또는 숙주 세포)을 사용하여 발현되거나, 봉입체 또는 가용성 형태로 발현되거나, 배지 또는 주변 세포질 공간으로 분비되거나, 세포 내에 포함되거나, 더 균질한 산물을 생성하도록 분자를 최적화하기 위해, 변형된 N-말단 서열, 예를 들어 하나 이상의 N-말단 아미노산의 결실, 또는 예를 들어 제1 N-말단 아미노산의 교환 (예를 들어, 글루타메이트에서 알라닌으로)을 가질 수 있다. 본 발명의 폴리펩티드는 예를 들어, 이러한 폴리펩티드의 안정성을 더욱 향상시키거나 면역원성을 감소시키기 위해, 예를 들어 WO2012/175741호, WO2011/075861호 또는 W02013/024059호에서 설명된 바와 같이, 추가 알라닌과 같은 변형된 C-말단 서열, 및/또는 C-말단 부분 또는 임의의 프레임워크 영역 내의 다른 정의된 위치에 추가 아미노산 교환을 가질 수 있다.
의심의 여지를 없애기 위해, 단독으로 또는 추가 치료제와의 조합 (아래에 더 자세히 명시됨)으로 본원에 기재된 임의의 다중 특이적 결합 단백질에 대해 본원에 기재된 바와 같은 약학적 조성물, 키트, 치료 방법, 의학적 용도, 조합, 투여 방법 및 용법에 관한 모든 실시양태가 고려된다.
약학적 조성물, 투여 방법, 투여량
본 발명은 또한 본 발명의 적어도 하나의 다중 특이적 결합 단백질을 포함하는, 질환 치료를 위한 약학적 조성물에 관한 것이다. 본 발명은 추가로 본 발명의 적어도 하나의 다중-특이적 단백질 또는 하기 제시된 바와 같은 약학적 조성물을 사용하여 질환을 치료하는 방법 (아래에 보다 상세히 명시됨)을 포함하고, 본 발명의 이러한 결합 단백질 또는 약학적 조성물을 사용하여 이러한 질환을 치료하기 위한 약제의 제조를 추가로 포함한다.
본 발명의 결합 단백질 (예를 들어, 표 1에 나타낸 서열에 의해 정의된 바와 같은 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#6/CD3#1, B7H6#7/CD3#1, B7H6#8/CD3#1, B7H6#9/CD3#1, B7H6#10/CD3#1, B7H6#11/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나) 및/또는 이를 포함하는 조성물은 사용되는 특정 약학적 제형 또는 조성물에 따라 임의의 적절한 방식으로 이를 필요로 하는 환자에게 투여된다. 따라서, 본 발명의 결합 단백질 및/또는 이를 포함하는 조성물은 유효량 또는 용량으로 예를 들어 정맥내 (iv), 피하 (sc), 근육내 (im), 복강 내 (ip), 경피, 경구, 설하 (예를 들어, 설하 정제의 형태, 혀 아래에 배치되고 점막을 통해 혀 아래의 모세관 네트워크로 흡수되는 스프레이 또는 드롭 형태), 비강 (내) (예를 들어, 비강 스프레이 및/또는 에어로졸 형태), 국소, 좌약, 흡입, 또는 임의의 다른 적절한 방식으로 투여될 수 있다. 결합 단백질은 주입, 볼루스 또는 주사로 투여할 수 있다. 바람직한 실시양태에서, 투여는 정맥내 주입 또는 피하 주사이다.
본 발명의 결합 단백질 및/또는 이를 포함하는 조성물은 치료 또는 완화될 질환, 장애 또는 상태를 치료 및/또는 완화시키는 데 적합한 치료 요법에 따라 투여된다. 임상의는 일반적으로 치료 또는 완화될 질환, 장애 또는 상태, 질환의 중증도, 질환 증상의 중증도, 사용되는 본 발명의 특이적 결합 단백질, 사용되는 특정 투여 경로 및 사용되는 약학 제형 또는 조성물, 환자의 연령, 성별, 체중, 식이, 일반적인 상태 및 임상의에게 잘 알려진 유사 요인과 같은 인자에 따라 적합한 치료 요법을 결정할 수 있을 것이다. 일반적으로, 치료 요법은 본 발명의 하나 이상의 결합 단백질, 또는 이를 포함하는 하나 이상의 조성물을 치료적 유효량 또는 용량으로 투여하는 것을 포함할 것이다.
일반적으로, 본원에 언급된 질환, 장애 및 상태의 치료 및/또는 완화를 위해 그리고 치료할 특정 질환, 장애 또는 상태, 사용될 본 발명의 특이적 결합 단백질의 효능, 특정 투여 경로 및 사용된 특정 약학 제형 또는 조성물에 따라, 본 발명의 결합 단백질은 일반적으로 체중kg 및 용량 당 0.005 내지 20.0 mg, 바람직하게는 0.05 내지 10.0 mg/kg/용량으로 연속적으로 (예를 들어 주입에 의해) 또는 더 바람직하게는 단일 용량 (예를 들어, 1주에 2회, 매주, 2주 또는 3주에 1회 또는 월간 용량; 하기 참조)으로 투여될 것이나, 특히 상기 언급된 매개변수에 따라 상당히 다를 수 있다. 따라서 어떤 경우에는 위에 주어진 최소 용량보다 적게 사용하는 것으로 충분할 수 있지만 다른 경우에는 상한을 초과해야 할 수도 있다. 다량을 투여할 때는 일정 기간에 걸쳐, 예를 들면 2일 이상에 걸쳐 여러 번 작은 용량으로 나누는 것이 좋다.
본 발명의 특이적 결합 단백질 및 이의 특이적 약동학 및 기타 특성에 따라, 매일, 2일, 3일, 4일, 5일 또는 6일마다, 매주, 2주 또는 3주마다 1회, 매월 등으로 투여될 수 있다. 투여 요법은 장기 치료를 포함할 수 있다. "장기"는 적어도 2주, 바람직하게는 수개월 또는 수년의 기간을 의미한다.
본 발명의 다중 특이적 결합 단백질 및 이를 포함하는 조성물의 효능은 관련된 특정 질환에 따라 임의의 적합한 시험관내 분석, 세포 기반 분석법, 생체 내 분석 및/또는 그 자체로 알려진 동물 모델, 또는 이들의 임의 조합을 사용하여 시험될 수 있다. 적합한 분석 및 동물 모델은 당업자에게 명확할 것이며, 예를 들어 아래 실시예에서 사용되는 분석 및 동물 모델을 포함한다.
제형
약학적 용도를 위해, 본 발명의 결합 단백질은 (i) 본 발명의 적어도 하나의 결합 단백질 (예를 들어, B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#6/CD3#1, B7H6#7/CD3#1, B7H6#8/CD3#1, B7H6#9/CD3#1, B7H6#10/CD3#1, B7H6#11/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나) 및 (ii) 적어도 하나의 약학적으로 허용되는 담체, 희석제, 부형제, 보조제 및/또는 안정화제, 및 (iii) 임의로 하나 이상의 추가 약리학적 활성 폴리펩티드 및/또는 또는 화합물을 포함하는 약학 제제로 제형될 수 있다.
"약학적으로 허용되는"은 각각의 물질이 개인에게 투여될 때 어떠한 생물학적 또는 다르게는 바람직하지 않은 효과를 나타내지 않으며, 함유된 약학적 조성물의 임의의 다른 성분 (예를 들어, 약학적 활성 성분)과 유해한 방식으로 상호작용하지 않음을 의미한다. 특정 예제는 표준 핸드북, 예를 들어 Remington's Pharmaceutical Sciences, 18th Ed., Mack Publishing Company, USA (1990)에서 찾을 수 있다. 예를 들어, 본 발명의 결합 단백질은 통상적인 항체 및 항체 단편 및 다른 약학 활성 단백질에 대해 그 자체로 알려진 임의의 방식으로 제형화되고 투여될 수 있다. 따라서, 추가 실시양태에 따르면, 본 발명은 본 발명의 적어도 하나의 결합 단백질 및 적어도 하나의 약학적으로 허용되는 담체, 희석제, 부형제, 보조제 및/또는 안정화제, 및 임의로 하나 이상의 추가의 약리학적 활성 물질을 함유하는 동결 건조 또는 다르게 건조된 제형 또는 수성 또는 비수성 용액 또는 현탁액 형태의 약학적 조성물 또는 제제에 관한 것이다.
정맥내, 근육내, 피하 주사 또는 정맥내 주입과 같은 비경구 투여용 약학적 제제는 예를 들어, 활성 성분을 포함하며 임의로 추가의 용해 또는 희석 단계 후에 주입 또는 주사에 적합한 멸균 용액, 현탁액, 분산액, 유제 또는 분말일 수 있다. 이러한 제제를 위한 적합한 담체 또는 희석제는 예를 들어 멸균수 및 생리 학적 인산염 완충 염수, 링거액, 덱스트로스 용액 및 행크 용액과 같은 약학적으로 허용가능한 수성 완충액 및 용액; 물 오일; 글리세롤; 에탄올; 글리콜, 예컨대 프로필렌 글리콜뿐만 아니라 미네랄 오일, 동물성 오일 및 식물성 오일, 예를 들어 땅콩유, 대두유 및 이들의 적합한 혼합물을 제한없이 포함한다.
본 발명의 결합 단백질의 용액은 또한 항균 및 항진균제, 예를 들어, p-하이드록시벤조에이트, 파라벤, 클로로부탄올, 페놀, 소르브산, 티오메살, 에틸렌디아민 테트라아세트산 (의 알칼리 금속 염) 등과 같은 미생물의 증식을 방지하기 위한 방부제를 함유할 수 있다. 많은 경우에, 당, 완충액 또는 염화나트륨과 같은 등장제를 포함하는 것이 바람직할 것이다. 임의로, 유화제 및/또는 분산제가 사용될 수 있다. 적절한 유동성은 예를 들어, 리포좀의 형성, 분산액의 경우에 필요한 입자 크기의 유지 또는 계면활성제의 사용에 의해 유지될 수 있다. 흡수를 지연시키는 다른 제제, 예를 들면, 알루미늄 모노스테아레이트 및 젤라틴이 또한 첨가될 수 있다. 용액은 주사 바이알, 앰풀, 주입 병 등에 채울 수 있다.
모든 경우에 있어서 최종 투여 형태는 제조 및 저장 조건하에서 무균, 유동성 및 안정해야 한다. 멸균 주사 용액은 활성 화합물을 필요에 따라 상기 열거한 여러 가지 다른 성분과 적절한 용매에 도입한 다음 필터 멸균하여 제조한다. 멸균 주사 용액의 제조를 위한 멸균 분말의 경우, 바람직한 제조 방법은 사전 멸균 여과된 용액에 존재하는 활성 성분과 임의의 추가의 원하는 성분의 분말을 생성하는 진공 건조 및 동결 건조 기술이다.
보통, 수용액 또는 현탁액이 바람직할 것이다. 일반적으로, 본 발명의 결합 단백질과 같은 치료 단백질에 적합한 제형은 완충된 단백질 용액, 예컨대 적절한 농도 (예를 들어, 0.001 내지 400 mg/ml, 바람직하게는 0.005 내지 200 mg/ml, 보다 바람직하게는 0.01 내지 200 mg/ml, 보다 바람직하게는 1.0 내지 100 mg/ml, 예컨대 1.0 mg/ml (iv 투여) 또는 100 mg/ml (sc 투여)의 단백질을 포함하는 용액 및 다음과 같은 수성 완충액:
- 포스페이트 완충 염수, pH 7.4,
- 다른 인산염 완충액, pH 6.2 내지 8.2,
- 아세트산염 완충액, pH 3.2 내지 7.5, 바람직하게는 pH 4.8 내지 5.5
- 히스티딘 완충액, pH 5.5 내지 7.0,
- 숙신산염 완충액, pH 3.2 내지 6.6,
- 시트르산염 완충액, pH 2.1 내지 6.2,
및 임의로 용액의 등장성을 제공하기 위한 염 (예, NaCl) 및/또는 당 (예컨대, 수크로스 및 트레할로스) 및/또는 다른 폴리알콜 (예를 들어, 만니톨 및 글리세롤)을 포함하는 용액이다.
또한, 다른 제제, 예를 들면, 세제, 예를 들어, 0.02% TWEENTM 20 또는 TWEENTM-80이 이러한 용액에 포함될 수 있다. 피하 적용을 위한 제형은 본 발명의 항체를 상당히 더 높은 농도로, 예컨대 최대 100 mg/ml 또는 심지어 100 mg/ml 초과로 포함할 수 있다. 그러나, 상기 주어진 성분 및 그 양은 오로지 하나의 바람직한 옵션을 나타내고자 한다는 것이 당업자에게는 명백할 것이다. 이들의 대안 및 변형은 당업자에게 아주 분명할 것이거나, 상기 개시 내용으로부터 출발하여 용이하게 구상될 수 있다. 상기 기재된 제형은 용액, 예를 들어, 주사용수 (WFI)에서 재구성될 동결 건조된 제형으로서 선택적으로 제공될 수 있다.
본 발명의 추가 측면에 따르면, 본 발명의 결합 단백질은 주사기, 주입기 펜, 마이크로펌프 또는 다른 장치와 같이 단백질의 투여에 유용한 장치와 조합하여 사용될 수 있다.
치료 방법
본 발명의 추가 측면은 본 발명의 결합 단백질의 치료적 유효량을 이를 필요로 하는 환자에게 투여하는 것을 포함하는 암 치료 방법을 제공한다.
본 발명의 추가 측면은 암 치료 방법에 사용하기 위한 본 발명의 결합 단백질을 제공한다.
본 발명의 추가 측면은 암 치료용 약학적 조성물을 제조하기 위한 본 발명의 결합 단백질의 용도이다.
의심의 여지를 없애기 위해, 본 발명의 의학적 사용 측면은 상기 기재된 바와 같은 본 발명의 특이적 결합 단백질 중 임의의 것 (예를 들어, B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#6/CD3#1, B7H6#7/CD3#1, B7H6#8/CD3#1, B7H6#9/CD3#1, B7H6#10/CD3#1, B7H6#11/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)을 포함할 수 있다.
본원에 사용된 용어 "암"은 조직병리학적 유형 또는 침범 단계와 무관하게 모든 유형의 암성 증식 또는 발암 과정, 전이 조직 또는 악성으로 형질전환된 세포, 조직 또는 기관을 포함하는 것을 의미한다.
본원에 기재된 다중 특이적 결합 단백질을 사용하여 성장이 억제될 수 있는 예시적인 암은 임의의 B7H6 발현 종양, 바람직하게는 결장직장암 (예: 전이성 결장직장암, mCRC), 비-소세포 폐암 (NSCLC), 두경부 편평 세포 암종이다 (HNSCC).
본원에 기재된 다중 특이적 결합 단백질을 사용하여 성장이 억제될 수 있는 암은 T 세포 림프종, 골수성 백혈병, 유방암; 난소암, 구강 편평상피암 및 위장관암을 포함하나 이에 제한되지 않는 임의의 B7H6 발현 종양이다. 위장관암은 식도암 (예: 위식도 접합부암), 위 (위장)암, 간세포암종, 담도암 (예: 담관암), 담낭암, 췌장암 또는 결장직장암 (CRC)을 포함하나 이에만 제한되지 않는다.
일부 실시양태에서, 하기 암, 종양 및 기타 증식성 질환이 본 발명의 다중 특이적 결합 단백질로 치료될 수 있다: 두경부암, 바람직하게는 HNSCC; 폐암; 바람직하게는 NSCLC; 유방암; 갑상선암; 자궁 경부암; 난소암; 자궁내막암; 간암 (간모세포종 또는 간세포 암종); 췌장암; 전립선암; 위 육종; 위장관 기질 종양, 식도암; 대장암; 결장직장암; 신장암; 피부암; 뇌종양; 교모세포종; 비호지킨 림프종 (T 또는 B 세포 림프종); 백혈병 (만성 또는 급성 골수성 백혈병, 비림프구성 백혈병) 또는 다발성 골수종.
본 발명의 바람직한 실시양태에서 암은 mCRC이다.
신체의 특정 위치/기원을 특징으로 하는 상기 언급된 모든 암, 종양, 신생물 등은 원발성 종양 및 그로부터 유래된 전이성 종양을 모두 포함하도록 의도된다.
환자가 B7H6의 높은 발현을 특징으로 하는 암을 앓고 있는 경우, 환자는 본 발명의 결합 단백질 (본원에 기술된 바와 같음)을 사용한 치료에 더 반응할 가능성이 높다. 따라서, 일부 실시양태에서, 본 발명의 결합 단백질로 치료될 암은 B7H6의 높은 발현을 갖는 암이고, 예를 들어 B7H6 발현은 동일한 유형의 B7H6 발현 암을 앓고 있는 환자 집단의 암세포에서의 평균 발현보다 더 높다.
본 발명의 결합 단백질은 제1 선, 제2 선, 또는 임의의 추가 선 치료 및 유지 치료와 관련하여 치료 요법에 사용될 수 있다.
본 발명의 결합 단백질은 임의로 또한 방사선 요법, 하나 이상의 추가 치료제 및/또는 수술과 결합하여 상기 언급된 질환의 예방, 단기 또는 장기 치료에 사용될 수 있다.
바람직한 실시양태에서, 본 발명의 단백질은 항-PD-1 항체 또는 항-PDL-1 항체와 같은 PD-1 길항제와 조합하여 암 치료에 사용된다. 바람직하게는 상기 항-PD-1 항체는 본원 (하기 표 A에 서열에 의해 정의됨) 및 WO2017/198741 (본원에 참고로 포함됨)에 기재된 바와 같이 펨브롤리주맙, 니볼루맙, 피딜리주맙, PD1-1, PD1-2, PD1-3, PD1-4 및 PD1-5로 이루어진 군으로부터 선택된다. 바람직하게는 상기 항-PDL-1 항체는 아테졸리주맙, 아벨루맙 및 두르발루맙으로 이루어진 군으로부터 선택된다. 특히 바람직한 실시양태에서, 본 발명의 결합 단백질 (바람직하게는 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)은 PD1-1과 조합하여 암 치료에 사용된다. 특히 바람직한 실시양태에서, 본 발명의 결합 단백질 (바람직하게는 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)은 PD1-2와 조합하여 암 치료에 사용된다. 특히 바람직한 실시양태에서, 본 발명의 결합 단백질 (바람직하게는 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)은 PD1-3과 조합하여 암 치료에 사용된다. 특히 바람직한 실시양태에서, 본 발명의 결합 단백질 (바람직하게는 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)은 PD1-4와 조합하여 암 치료에 사용된다. 특히 바람직한 실시양태에서, 본 발명의 결합 단백질 (바람직하게는 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)은 PD1-5와 조합하여 암 치료에 사용된다.
이들 바람직한 실시양태 및 본 발명의 임의의 다른 측면에 따르면, 항체 PD1-1, PD1-2, PD1-3, PD1-4 및 PD1-5는 WO2017/198741호에 개시된 항체 분자이고, 상기 표 A에 기재된 서열에 의해 정의된다.
따라서, PD1-1은 서열 번호 331의 아미노산 서열을 포함하는 중쇄 및 서열 번호 332의 아미노산 서열을 포함하는 경쇄를 갖고;
PD1-2는 서열 번호 333의 아미노산 서열을 포함하는 중쇄 및 서열 번호 334의 아미노산 서열을 포함하는 경쇄를 갖고;
PD1-3은 서열 번호 335의 아미노산 서열을 포함하는 중쇄 및 서열 번호 336의 아미노산 서열을 포함하는 경쇄를 갖고;
PD1-4는 서열 번호 337의 아미노산 서열을 포함하는 중쇄 및 서열 번호 338의 아미노산 서열을 포함하는 경쇄를 갖고;
PD1-5는 서열 번호 339의 아미노산 서열을 포함하는 중쇄 및 서열 번호 340의 아미노산 서열을 포함하는 경쇄를 갖는다.
상기는 또한 이를 필요로 하는 환자에게 치료적 유효량을 투여함으로써 상기 질환을 치료하는 다양한 방법에서 본 발명의 결합 단백질의 용도뿐만 아니라 상기 질환 치료용 약제 제조를 위한 이들 결합 단백질의 용도, 본 발명의 이러한 결합 단백질을 포함하는 약학적 조성물, 본 발명의 이러한 결합 단백질을 포함하는 약제의 제제 및/또는 제조 등을 포함한다.
다른 활성 물질 또는 치료제와의 조합
본 발명의 결합 단백질 (예를 들어, B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#6/CD3#1, B7H6#7/CD3#1, B7H6#8/CD3#1, B7H6#9/CD3#1, B7H6#10/CD3#1, B7H6#11/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)은 단독으로 또는 다른 암 치료법, 예를 들어, 수술, 방사선 요법, 화학 요법, 표적 요법, 면역 요법 또는 이들의 조합과 함께 사용할 수 있다. 예를 들어, 본 발명의 결합 단백질은 하나 이상의 추가 치료제, 특히 세포독성 또는 세포증식억제 화학요법제, 혈관신생을 억제하는 치료 활성 화합물, 신호 전달 경로 억제제, 예를 들어, EGFR 억제제, 면역 조절제, 면역 체크포인트 억제제, 유사 분열 체크포인트 억제제 또는 호르몬 치료제와 같은 화학요법제와 조합하여 사용될 수 있다.
추가 치료제는 임의로 동일한 약학 제제의 성분으로서 B7H6/CD3 결합 단백질의 투여와 동시, 전 또는 후에 투여될 수 있다.
본 발명의 결합 분자와 조합하여 투여될 수 있는 세포 증식 억제 및/또는 세포 독성 활성 물질은, 호르몬, 호르몬 유사체 및 항호르몬, 아로마타제 억제제, LHRH 작용제 및 길항제, 성장 인자 (예를 들어, 혈소판 유래 성장 인자 (PDGF), 섬유아세포 성장 인자 (FGF), 혈관 내피 성장 인자 (VEGF), 상피 성장 인자 (EGF), 인슐린-유사 성장 인자 (IGF), 인간 상피 성장 인자 (HER, 예를 들어, HER2, HER3, HER4) 및 간세포 성장 인자 (HGF)와 같은 성장 인자)의 억제제를 포함하지만 이들에 한정되지 않으며, 억제제는, 예를 들어, (항-)성장 인자 항체, (항-)성장 인자 수용체 항체 및 티로신 키나제 억제제, 예를 들어, 세툭시맙, 게피티닙, 아파티닙, 닌테다닙, 이마티닙, 라파티닙, 보수티닙 및 트라스투주맙; 항대사물질 (예를 들어, 메토트렉세이트, 랄티트렉세드와 같은 항엽산제, 5-플루오로우라실 (5-FU)과 같은 피리미딘 유사체, FOLFOX (폴린산, 5-FU 및 옥살리플라틴의 조합 요법), FOLFIRI (엽산, 5-FU 및 이리노테칸의 조합), 겜시타빈, 이리노테칸, 독소루비신, TAS-102, 카페시타빈 및 겜시타빈, 머캅토퓨린, 티오구아닌, 클라드리빈 및 펜토스타틴과 같은 퓨린 및 아데노신 유사체, 시타라빈 (ara C), 플루다라빈); 항종양 항생제 (예를 들어, 안트라사이클린); 백금 유도체 (예를 들어, 시스플라틴, 옥살리플라틴, 카보플라틴); 알킬화제 (예를 들어, 에스트라무스틴, 메클로레타민, 멜팔란, 클로람부실, 부술판, 다카바진, 사이클로포스파미드, 이포스파미드, 테모졸로미드, 니트로소우레아, 예를 들어, 카르무스틴 및 로무스틴, 티오테파); 항유사분열제 (예를 들어, 빈블라스틴, 빈데신, 비노렐빈 및 빈크리스틴과 같은 빈카 알칼로이드; 및 파클리탁셀, 도세탁셀과 같은 탁산); 혈관형성 억제제 (베바시주맙, 라무시루맙 및 아플리베르셉 포함), 튜블린 억제제; DNA 합성 억제제, PARP 억제제, 토포아이소머라제 억제제 (예를 들어, 에피포도필로톡신, 예컨대 에토포시드 및 에토포포스, 테니포시드, 암사크린, 토포테칸, 이리노테칸, 미톡산트론), 세린/트레오닌 키나제 억제제 (예를 들어, PDK1 억제제, Raf 억제제, A-Raf 억제제, B-Raf 억제제, C-Raf 억제제, mTOR 억제제, mTORC1/2 억제제, PI3K 억제제, PI3Kα 억제제, 이중 mTOR/PI3K 억제제, STK33 억제제, AKT 억제제, PLK1 억제제 (예를 들어, 볼라세르팁), CDK 억제제 (CDK9 억제제 포함), 오로라 키나제 억제제), 티로신 키나제 억제제 (예를 들어, PTK2/FAK 억제제), 단백질 단백질 상호작용 억제제, MEK 억제제, ERK 억제제, FLT3 억제제, BRD4 억제제, IGF-1R 억제제, Bcl-xL 억제제, Bcl-2 억제제, Bcl-2/Bcl-xL 억제제, ErbB 수용체 억제제, BCR-ABL 억제제, ABL 억제제, Src 억제제, 라파마이신 유사체 (예를 들어, 에베롤리무스, 템시롤리무스, 리다포롤리무스, 시롤리무스), 안드로겐 합성 억제제, 안드로겐 수용체 억제제, DNMT 억제제, HDAC 억제제, ANG1/2 억제제, CYP17 억제제, 방사성 의약품, 면역치료제, 예를 들어, 면역 체크포인트 억제제 (예를 들어, CTLA4, PD1, PD-L1, LAG3 및 TIM3 결합 분자/면역글로불린, 예를 들어, 이필리무맙, 니볼루맙, 펨브롤리주맙) 및 각종 화학요법제, 예를 들어, 아미포스틴, 아나그렐리드, 클로드로나트, 필그라스틴, 인터페론, 인터페론 알파, 류코보린, 리툭시맙, 프로카바진, 레바미솔, 메스나, 미토탄, 파미드로네이트 및 포르피머; 프로테아좀 억제제 (예를 들어, 보르테조밉); Smac 및 BH3 모방체; mdm2-p53 길항제를 비롯한 p53 기능을 회복시키는 약제; Wnt/베타 카테닌 신호전달 경로의 억제제; 및/또는 사이클린 의존성 키나제 9 억제제이다.
특히 바람직한 것은 항-PD-1 및 항-PD-L1 제제 및 항 LAG3 제제를 포함하는 하나 이상의 면역치료제와 조합하여 본 발명의 결합 분자를 사용한 치료이다: 예시적인 항-PD1 제제는 항-PD1 항체 PDR-001, 펨브롤리주맙, 니볼루맙, 피딜리주맙 및 본원 (표 A) 및 WO2017/198741호에 기재된 바와 같은 PD1-1, PD1-2, PD1-3, PD1-4 및 PD1-5를 포함하나 이에 제한되지는 않는다. 예시적인 항-PDL-1 제제는 아테졸리주맙, 아벨루맙 및 두르발루맙을 포함하지만 이에 제한되지 않는다. 바람직한 실시양태에서, 본 발명의 결합 분자 (바람직하게는 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)은 PD1-1과 결합된다. 바람직한 실시양태에서, 본 발명의 결합 분자 (바람직하게는 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)은 PD1-2와 결합된다. 바람직한 실시양태에서, 본 발명의 결합 분자 (바람직하게는 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)은 PD1-3과 결합된다. 바람직한 실시양태에서, 본 발명의 결합 분자 (바람직하게는 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)은 PD1-4와 결합된다. 바람직한 실시양태에서, 본 발명의 결합 분자 (바람직하게는 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)은 PD1-5와 결합된다.
특정 실시양태에서, 추가 치료제는 TIM-1, TIM-3, TIM-4, PD-L2, LAG3, CTLA-4, 갈렉틴 9, 갈렉틴-1, CD69, CD113, GPR56, CD48, GARP, CAECAM-1, BTLA, TIGIT, CD160, LAIR1, 2B4, CEACAM, CD39, TGFβ, IL-10, Fas 리간드, ICOS, B7 패밀리 (B7-1, B7-2, B7-H1 (PDL-1), B7-DC (PD-L2), B7-H2 (ICOS-L), B7-H3, B7-H4, B7-H5 (VISTA)), gp49B, PIR-B, KIR 패밀리 수용체, SIRPalpha (CD47), ILT-2, ILT-4, IDO, CD39, 아르기나제, CD73 HHLA2, 부티로필린 또는 A2aR의 조절제와 같은 추가 면역치료제일 수 있다.
일부 실시양태에서, 추가의 면역치료제는 CD40 및 CD40L, OX-40, OX-40L, CD70, CD27L, CD30, CD30L, 4-lBBL, CD137, CD137/FAP, GITR, TRAIL/Apo2-L, TRAILR1/DR4, TRAILR2/DR5, TRAILR3, TRAILR4, OPG, RANK, RANKL, TWEAKR/Fn14, TWEAK, BAFFR, EDAR, XEDAR, TACI, APRIL, BCMA, LIGHT, DcR3, HVEM, VEGI/TLlA, TRAMP/DR3, EDAR, EDAl, XEDAR, EDA2, TNFRl, 림프독소 α/TNFβ, TNFR2, TNFα, LTβR, 림프독소 α1β2, FAS, FASL, RELT, DR6, NGFR를 포함하는 동족 TNF 수용체 패밀리 구성원에 결합하는 TNF 패밀리 분자의 구성원이다. 바람직하게는, 추가 면역치료제는 CD137/FAP이다.
일부 실시양태에서, 추가 면역치료제는 (i) T 세포 활성화를 억제하는 사이토카인의 길항제 (예를 들어, IL-6, IL-10, TGF-B, VEGF; "면역억제 사이토카인") 및/또는 (ii) 면역 반응을 자극하여 예를 들어 암과 같은 증식성 질환을 치료하기 위한 T 세포 활성화 및/또는 IL2와 같은 사이토카인을 자극하는 사이토카인의 작용제로부터 선택된다.
일부 실시양태에서, 추가 면역치료제는 T 세포 활성화를 자극하는 단백질의 작용제, 예컨대 CD28, GITRL, OX40L, CD27, 및 CD28H 또는 STING 작용제이다.
일부 실시양태에서, 추가 치료제는 박시니아바이러스, 아데노바이러스, (AdV), 단순 포진바이러스 (HSV1 또는 HSV2), 레오바이러스, 점액종 바이러스 (MYXV), 폴리오바이러스, 수포성 구내염 바이러스 (VSV), 마라바 바이러스, 수두바이러스, 홍역 바이러스 (MV) 또는 뉴캐슬병 바이러스 (NDV)로부터 유래된 종양 용해성 바이러스를 포함하나 이에 제한되지 않는 종양 용해성 바이러스이다.
키트
본 발명은 또한 본 발명의 다중-특이적 결합 단백질 (예를 들어, BB7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#6/CD3#1, B7H6#7/CD3#1, B7H6#8/CD3#1, B7H6#9/CD3#1, B7H6#10/CD3#1, B7H6#11/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나) 및 임의로 상기 기재된 바와 같은 질환 및 장애의 치료에 사용되는 다른 약물로 이루어진 군으로부터 선택된 하나 이상의 다른 성분을 포함하는 키트를 포함한다.
일 실시양태에서, 키트는 단위 투여 형태의 유효량의 본 발명의 결합 단백질을 함유하는 조성물을 포함한다.
본 발명은 또한 적어도 본 발명의 다중-특이적 결합 단백질, 및 상기 기재된 바와 같은 질환 및 장애의 치료에 사용되는 다른 약물로 구성된 군으로부터 선택된 하나 이상의 다른 성분을 포함하는 키트를 포함한다.
일 실시양태에서, 키트는 단위 투여 형태의 유효량의 본 발명의 다중-특이적 결합 단백질 (바람직하게는 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)을 함유하는 조성물을 포함한다. 추가 실시양태에서 키트는 유효량의 단위 투여 형태의 본 발명의 다중-특이적 결합 단백질 (바람직하게는 B7H6#1/CD3#1, B7H6#2/CD3#1, B7H6#3/CD3#1, B7H6#4/CD3#1, B7H6#5/CD3#1, B7H6#12/CD3#1, B7H6#13/CD3#1, B7H6#14/CD3#1, B7H6#15/CD3#1, B7H6#16/CD3#1, B7H6#17/CD3#1, B7H6#18/CD3#1, B7H6#19/CD3#1, B7H6#20/CD3#1, B7H6#21/CD3#1, B7H6#22/CD3#1, B7H6#23/CD3#1, B7H6#24/CD3#1 중 어느 하나)을 함유하는 조성물 및 단위 투여 형태의 유효량의 PD-1 길항제, 예컨대 항 PD-1 항체, 가장 바람직하게는 본원 (예를 들어 표 A) 및 WO2017/198741호에 기술된 바와 같은 PD1-1, PD1-2, PD1-3, PD1-4 및 PD1-5을 함유하는 조성물을 모두 포함한다.
일부 실시양태에서, 키트는 이러한 조성물을 함유하는 멸균 용기를 포함한다; 이러한 용기는 상자, 앰플, 병, 바이알, 튜브, 백, 파우치, 블리스터 팩, 또는 당업계에 공지된 다른 적합한 용기 형태일 수 있다. 상기 용기는 플라스틱, 유리, 적층지, 금속 호일 또는 의약품 보관에 적합한 기타 재료로 만들어질 수 있다. 추가로, 키트는 동결 건조된 형태의 본 발명의 결합 단백질이 들어 있는 제1 용기 및 주사를 위한 약학적으로 허용되는 희석제 (예를 들어, 멸균수)가 있는 제2 용기에 약학적 조성물을 포함할 수 있다. 약학적으로 허용되는 희석제는 결합 단백질의 재구성 또는 희석에 사용될 수 있다.
필요한 경우, 본 발명의 다중-특이적 결합 단백질은 다중-특이적 결합 단백질을 암에 걸린 대상체에 투여하기 위한 설명서와 함께 제공된다. 설명서에는 일반적으로 암 치료 또는 예방을 위한 조성물의 사용에 대한 정보가 포함된다. 다른 실시양태에서, 설명서는 다음 중 적어도 하나를 포함한다: 치료제에 대한 설명; 암 또는 그의 증상의 치료 또는 예방을 위한 투약 일정 및 투여; 예방 조치; 경고; 징후; 대항 징후; 및 과복용 정보; 이상 반응; 동물 약리학; 임상 연구; 및/또는 문의. 설명서는 (있는 경우)에 용기 위에 직접 인쇄되거나, 용기에 부착된 표지로, 또는 용기에 또는 함께 제공된 별도의 시트, 팜플렛, 카드 또는 폴더로 인쇄될 수 있다.
허용할 수 있는 바와 같이, 이러한 제안된 키트 구성 요소는 당업자가 사용하기 위해 통상적인 방식으로 포장될 수 있다. 예를 들어, 이러한 제안된 키트 구성 요소는 용액 또는 액체 분산액 등으로 제공될 수 있다.
실시예
다음 실시예는 본 발명을 설명한다. 이들 실시예는 본 발명의 범위를 제한하는 것으로 해석되어서는 안된다.
실시예 1: B7H6/CD3 결합 단백질의 설계 및 작제
본 발명자들은 B7H6 및 CD3에 결합하고 T-세포 활성화를 유도하여 B7H6-발현 종양 세포의 용해를 유도하는 다중-특이적 결합 단백질을 개발하였다. 사용된 분자 설계는 IgG 항체 스캐폴드 및 IgG 유사 구조를 가지고 있다. 이는 노브 및 홀 아암의 이종-이량체화를 위해 Fc에서 노브-인-홀 (knod-in-hole) 기술을 특징으로 한다. 또한, 결합 단백질은 각 아암에서 경쇄와 대응 중쇄 사이에 유연한 펩티드 서열을 가지고 있다. 따라서, 결합 단백질은 하나는 CD3에 결합하고 다른 하나는 B7H6에 결합하는 두개의 아암을 포함하고, 각 아암은 단일쇄 Fab 및 Fc 영역을 포함한다 (도 1 참조).
바람직하게는 결합 분자는 이중 특이적이고 2가 (두 표적 각각에 대해 1 가)이다.
하이브리도마 및 배양된 단일 B 세포로부터 고 처리량 V 유전자 회수를 사용하여 B7H6 및 CD3를 인식하는 결합 도메인의 제조.
항-B7H6 결합제를 수득하기 위해, B7H6 면역화 야생형 및 ALIVAMABTM 인간화 마우스 (Ablexis, San Francisco, CA, USA: ALIVAMABMOUSETM transgenic mouse platform with human immunoglobulin loci)로부터 유래된 하이브리도마 또는 단일 B 세포를 시험관내에서 배양하였다. 상청액을 ALPHALISA® Immunoassay kit (PerkinElmer, Waltham, MA, USA)에 의해 인간 B7H6을 발현하는 재조합 인간 B7H6에 대한 결합에 대해, 유세포 분석법에 의해 인간 CHO 세포 상에서 재조합적으로 발현된 사이노몰거스 B7-H6에 대한 결합에 대해 스크리닝하였다.
이어 면역글로불린 (Ig) VH 및 VL 유전자를 식별된 양성 클론에서 증폭시켰다. 하이브리도마에서 RNA를 단리하기 위해, 모노클로날로부터 약 2×106개의 세포를 펠렛화하여 원료 물질로 사용하였다. 단일 B 세포의 경우, 단일 단리된 B 세포에서 확장된 100 내지 500개의 세포를 원료 물질로 사용하였다. RNeasy® Plus 미니 RNA 추출 키트 (Qiagen, Hilden, Germany)를 사용하여 RNA를 단리하였다. 이어 SMARTer® cDNA 합성 키트 (Clontech, Mountain View, CA)를 제조업체의 지침에 따라 사용하여 cDNA를 합성하였다. cDNA 합성을 촉진하기 위해, oligodT를 사용하여 모든 메신저 RNA의 역전사를 프라임하고 SMARTer IIA 올리고뉴클레오티드로 "5' 캡핑"을 수행하였다. SMARTer IIA 캡을 표적으로 하는 5' 프라이머 및 CH1에서 공통 영역을 표적으로 하는 3' 프라이머를 사용한 2 단계 PCR 증폭을 사용하여 VH 및 VL 단편의 후속 증폭을 수행하였다. 요약하면, 각 50 ㎕ PCR 반응은 20 μM의 정방향 및 역방향 프라이머 믹스, 25 ㎕의 PrimeSTAR® Max DNA 중합효소 프리믹스 (Clontech), 2 ㎕의 비정제 cDNA 및 21 ㎕의 이중 증류 H20로 이루어졌다. 사이클링 프로그램을 94 ℃에서 3 분으로 시작하여 35 사이클 (94 ℃에서 30 초, 50 ℃에서 1 분, 68 ℃에서 1 분)을 진행한 후, 72 ℃에서 7 분으로 종료하였다. 각각의 pTT5 모 벡터 (VH 및 VL)에서 각각의 영역에 "겹치는" 15bp 상보성 확장을 포함하는 VL 및 VH 제2 라운드 프라이머로 제2 라운드 PCR을 수행하였다. 제2 라운드 PCR을 동일한 사이클링 프로그램으로 수행하였다.
In-Fusion® HD Cloning Kit (Clontech, U.S.A.)를 사용하여 VL 유전자를 pTT5 huIgK 벡터로, VH 유전자를 pTT5 huIgGlKO 벡터로 지향 클로닝하였다. In-Fusion® HD 클로닝을 용이하게 하기 위해, In-Fusion HD 클로닝 전에 PCR 산물을 정제하고 클로닝 인핸서 (Cloning Enhancer)로 처리하였다. 클로닝 및 변환을 제조업체의 프로토콜 (Clontech, U.S.A.)에 따라 수행하였다. Mini-prep DNA를 Sanger 시퀀싱에 적용하여 완전한 V-유전자 단편이 얻어졌는지 확인하였다.
이 방법론을 사용하여 B7H6에 대한 특이성을 갖는 결합 도메인을 암호화하는 Ig VH 및 VL 유전자 쌍을 준비하였다. 상응하는 중쇄 및 경쇄 암호화 플라스미드로 CHO-E37 세포를 일시 형질감염시켜 재조합 항체를 생성하였다.
추가적인 항-CD3 결합제를 얻기 위해, huCD3ε 펩티델-27 작제물을 사용하여 WT 마우스의 면역화를 수행하였다. 하이브리도마 상청액을 재조합 huCD3E+G-Fc 단백질 및 재조합 cyCD3E+G-Fc 단백질에 대한 결합, 및 huCD3-양성 및 cyCD3-양성 세포에 대한 결합에 대해 스크리닝하였다. 양성 클론의 가변 영역을 회수하고, 추가 평가를 위해 IgG 또는 IgG-유사 이중 특이적 작제물로서 클로닝하였다.
B7H6 및 CD3 결합제의 인간화/최적화
상기 기재된 바와 같은 B7H6 또는 CD3 결합제 및 문헌에 기술된 CD3 결합제의 서열 (Pessano et al., EMBO J. 1985 Feb; 4 (2): 337-44; Salmeron A et al, J Immunol. 1991 Nov l; l47) (9): 3047-52)을 인간화 및/또는 최적화하였다. 항체의 서열 최적화/인간화는 인간에서 생성된 항체와 유사한 치료제로 사용하기 위해 (특정 항원/에피토프에 대해) 비인간 종에서 생성된 항체를 조작하여 특이성을 유지하면서 면역원성과 같은 잠재적인 부작용을 제거하는 방법이다. 여기에 사용된 서열 최적화/인간화 접근 방식은 Singh et al, 2015 (Singh S et al., mAbs 2015: 7 (4): 778-9l)에 의해 설명되었다. 요약하면, 밀접하게 일치하는 인간 생식세포 계열을 인 실리코 (in silico)로 식별하고 파지 스크리닝 방법을 사용하여 최적화/인간화 변이체를 평가하였다. 결합, 인간 점수 퍼센트 및 EpiVax® (잠재적 면역원성에 대한 인 실리코 예측 도구) 점수를 기반으로 최종 선도 후보 서열을 선택하였다.
B7H6 및 CD3에 결합하는 이중 특이적 단백질의 작제
B7H6 및 CD3 결합제의 가변 영역을 일반적인 분자 생물학 기술을 사용하여 발현 벡터 pTT5 (캐나다 국립 연구 위원회)에 클로닝하여 Fc 영역 및 B7H6에 대한 단일쇄 Fab 결합을 포함하는 하나의 B7H6 특이적 결합 아암 (이러한 결합 단위는 본원에서 "B7H6 아암" 또는 "B7H6 쇄"라고도 함)와 Fc 영역 및 및 CD3에 결합하는 단일쇄 Fab를 포함하는 CD3 특이적 결합 아암 (이러한 결합 단위는 본원에서 "CD3 아암" 또는"CD3 쇄"라고도 함)를 가지는 이중 특이적 결합 단백질을 형성하였다. B7H6 및 CD3 아암의 Fc 영역은 "W" 또는 "SAV" 돌연변이 (Atwell et al, JMB, 1997, 270, 26-35)를 포함하고 각각의 쇄는 W" 또는 SAV 쇄로 지칭된다. 다중 단편 DNA 어셈블리의 경우, Gibson 어셈블리 및 NEBuilder® HiFi DNA 어셈블리 접근법을 제조업체의 프로토콜 (New England Biolabs, Ipswich, MA, USA)에 따라 사용하였다. DNA 미니 프렙 (mini-prep)을 시퀀싱하였다.
각 발현 벡터는 쇄 암호화 유전자 (B7H6 또는 CD3 아암/쇄), 즉 신호 서열과 경쇄 및 중쇄를 암호화하는 유전자에 대한 진핵 프로모터 요소, 암피실린과 같은 원핵 선별 마커 유전자에 대한 발현 카세트, 및 복제 기원을 함유한다. 이들 DNA 플라스미드를 암피실린 내성 대장균 콜로니 및 배양물에서 증식시키고 정제하였다.
실시예 2: B7H6 및 CD3에 결합하는 이중 특이적 결합 단백질의 발현 및 정제
B7H6/CD3-쇄-암호화 유전자 (하나의 쇄는 W 쇄이고 다른 하나의 쇄는 SAV 쇄임)를 가지는 pTT5 벡터로 CHO-E 세포를 일시적으로 형질감염시켜 B7H6 및 CD3에 결합하는 이중 특이적 분자를 생성하였다. 요약하면, 무혈청 배지에서 현탁액 중에서 성장하는 형질감염된 CHO-E 세포를 140 rpm, 37℃ 및 5% CO2에서 교반하에 진탕 플라스크에서 배양하고, 지수 성장 조건에서 유지시켰다. 형질감염 당일에, 세포를 Mirus Bio TransIT Pro® 형질감염 시약을 사용하여 1:3 질량비로 W-쇄 플라스미드 및 SAV-쇄 플라스미드로 화학적으로 형질감염시켰다. 이어서, 세포를 1 L의 Gibco® FreeStyleTM CHO 발현 배지 (LifeTechnologies, NY, US)에 1 내지 2x106 세포/ml로 시딩하였다. 이어서, 세포를 200 ml의 상업적 공급 용액과 함께 7일에 1회 공급하여 10일 동안 궤도 진탕하에 인큐베이션하여 단백질의 발현을 최적화하였다. 세포 배양 상청액 중의 항체 역가를 Octet® 기기 (Pall ForteBio, CA, US) 및 protA 바이오센서 팁을 제조업체의 지시에 따라 사용하여 결정하였다.
GE Healthcare Life Sciences AKTATM 순수 단백질 정제 시스템을 이용하여 배양 상층액으로부터 재조합 B7H6/CD3 결합 단백질을 2 단계 공정으로 정제하였다. 먼저, Mab SelectTM 컬럼 (GE Healthcare)을 이용하여 Protein-A 친화성 크로마토그래피를 이용하여 수확한 세포 배양액으로부터 샘플을 포획하였다. 단백질을 중성 pH에서 단백질 A에 결합시키고, 고염 (1M NaCl)으로 세척하여 세포 배양 배지 성분 및 단백질 A에 비특이적으로 결합한 모든 단백질 또는 성분을 제거하였다. 항체 또는 항체-유사 적제물 샘플을 30 mM 아세트산나트륨, pH 3.5를 사용하여 등용매 방식으로 용출시켰다. 용출된 샘플을 3M 아세트산나트륨, pH 9.0의 1% 용액을 사용하여 pH 5.0으로 중화시켰다. 중화된 단백질을 0.22 μm 여과 시스템으로 멸균 여과하였다. 농도를 나노드롭 8000 분광광도계에 의해 UV280에서 측정하였다. 제2 정제에서는, POROSTM 50 HS 양이온 교환 수지 컬럼 (Applied Biosystems, Carlsbad, CA, USA)을 사용한 양이온 교환 크로마토그래피 또는 HiLoad® 26/600 Superdex® 200 pg 컬럼 (GE Healthcare)를 사용한 크기-배제 크로마토그래피를 적용하였다. 2 단계 정제된 물질을 50 mM 아세트산나트륨 및 10 mM NaCl, pH 5.0의 최종 완충액에 저장하고, 샘플의 순도 및 불균질도를 분석적 크기 배제 크로마토그래피, 질량 분광법 및 분석적 초원심분리에 의해 평가하였다. 기능성 시험을 위해 진행된 샘플은 약 95 내지 99%의 단량체 함량을 갖는 2 단계 정제된 물질을 포함하였다.
실시예 3: 재조합 단백질 생성
· 인간 B7H6-His
Lenti-XTM 렌티바이러스 시스템 (Clontech)을 사용한 일시적 형질감염에 의해 pTT 벡터 (인간 B7H6-His를 암호화, 서열 번호 317)를 사용하여 His6-태그로 인간 B7H6의 전체 세포외 도메인을 발현시켰다. HEK 293F 세포 (Thermo Fisher)를 GibcoTM FreestyleTM F17 발현 배지 (Thermo Fisher Scientific)에서 형질감염 시 1.6 x 106 세포/ml로 사용하였다. 1:3 비율의 DNA:PEI 복합체 및 1 mg/L의 DNA를 5분 동안 예비 인큐베이션하고, 여과하고, 실온에서 추가로 15분 동안 예비 인큐베이션한 후, 세포에 첨가하였다. 세포를 37℃, 5% CO2에서 140 rpm으로 진탕하에 인큐베이션하였다. 트립톤 N1을 0.5%의 최종 농도로 형질감염 24시간 후에 세포에 첨가하였다. 세포를 2 mM 글루타민 및 2 g/L 글루코스로 형질감염시킨 후 48시간에 다시 공급하였다. 동시에, 온도를 33℃로 낮추었다. 2 mM 글루타민 및 1 g/L 글루코스로 형질감염시킨 후 120시간에 최종 공급물을 첨가하였다. 6000 rpm에서 15분 동안 원심분리하여 형질감염 후 144시간에 세포를 수확하였다. 상청액을 G4 필터를 사용하여 정화시켰다.
단백질 정제를 2 단계로 수행하였다. 제1 단계에서, Ni-NTA 컬럼을 10 CV에 대해 세척 완충액 1x PBS, pH 7.2 + 10 mM 이미다졸을 사용한 다음, 10 CV에 대해 세척 완충액 1x PBS, pH 7.2 + 20 mM 이미다졸을 사용하고 0.5 M 이미다졸이 보충된 1x PBS, pH 7.2의 용리 구배 4-60%를 사용하는 친화성 크로마토그래피에 사용하였다. 분획을 수집하고, 풀링 및 농축 전에 SDS-PAGE에 의해 분석하였다. 제2 단계에서, Superdex® 200, 16/600, 120 ml 컬럼을 겔 여과 크로마토그래피 (GE Healthcare Life Sciences)에 사용하였다. 친화성 크로마토그래피 후 농축된 풀, 5 ml를 0.5 ml/분의 유속으로 컬럼에 로딩하였다. 제형 완충액은 20 mM HEPES, 100 mM NaCl, 5% 수크로스, pH 7.4였다. 분획을 수집하고, 풀링 전에 SDS-PAGE로 분석한 후, 0.2 um 필터를 사용하여 멸균하였다.
· Cyno B7H6-His
Cyno-B7H6의 전체 세포외 도메인을 Lenti-XTM 렌티바이러스 시스템 (Clontech)을 이용한 일시적 형질감염에 의해 pTT 벡터 (cyno B7H6-His 암호화, 서열 번호 320)를 사용하여 His6-태그로 발현시켰다. HEK 293F 세포 (Thermo Fisher)를 GibcoTM FreestyleTM F17 발현 배지 (Thermo Fisher Scientific)에서 형질감염 시 1.6 x 106 세포/ml로 사용하였다. 1:3 비율의 DNA:PEI 복합체 및 1 mg/L의 DNA를 5분 동안 예비 인큐베이션하고, 여과하고, 실온에서 추가로 15분 동안 예비 인큐베이션한 후, 세포에 첨가하였다. 세포를 37℃, 5% CO2에서 140 rpm으로 진탕하에 인큐베이션하였다. 트립톤 N1을 0.5%의 최종 농도로 형질감염 24시간 후에 세포에 첨가하였다. 세포를 2 mM 글루타민 및 2 g/L 글루코스로 형질감염시킨 후 48시간에 다시 공급하였다. 동시에, 온도를 33℃로 낮추었다. 2 mM 글루타민 및 1 g/L 글루코스로 형질감염시킨 후 120시간에 최종 공급물을 첨가하였다. 6000 rpm에서 15분 동안 원심분리하여 형질감염 후 144시간에 세포를 수확하였다. 상청액을 G4 필터를 사용하여 정화시켰다.
단백질 정제를 2 단계로 수행하였다. 제1 단계에서, Ni-NTA 컬럼을 10 CV에 대해 세척 완충액 1x PBS, 0.2 M 수크로스, 0.01% CHAPS, 5% 글리세롤, pH 7.2, + 10 mM 이미다졸, 이어서 10 CV에 대해 세척 완충액 1x PBS, pH 7.2 + 20 mM 이미다졸을 사용하고, 0.5 M 이미다졸이 보충된 4-60%의 1x PBS, 0.2 M 수크로스, 0.01% CHAPS, 5% 글리세롤, pH 7.2를 사용한 용출 구배를 사용한 친화성 크로마토그래피에 사용하였다. 분획을 수집하고, 풀링 및 농축 전에 SDS-PAGE에 의해 분석하였다. 제2 단계에서, Superdex® 200, 16/600을 겔 여과 크로마토그래피 (GE Healthcare Life Sciences)에 사용하였다. 친화성 크로마토그래피 후 농축된 풀, 10 ml를 1.0 ml/분의 유속으로 컬럼에 로딩하였다. 제형 완충액은 IX PBS, 0.2M 수크로스, 0.01% CHAPS, 5% 글리세롤, pH 7.2였다. 분획을 수집하고, 풀링 전에 SDS-PAGE로 분석한 후, 0.2 um 필터를 사용하여 멸균하였다.
· 인간 CD3 E+G HuFc-6xHis (E+G는 εγ 서브유닛을 나타냄)
HEK-293 세포 (Thermo Fisher), Lenti-XTM 렌티바이러스 시스템 (Clontech), 및 인간 CD3 E+G HuFc-6xHis를 암호화하는 플라스미드 (인간 CD3E 수탁 번호: P07766; 인간 CD3E+G-HuFc-His: 서열 번호 322)를 사용하여 인간 CD3 E+G HuFc-6xHis를 생산하는 세포주를 생성하였다. 발현을 위해, 세포를 FreestyleTM 293 배지 (Thermo Fisher Scientific)에서 37℃에서, 가습 8% C02 환경에서 135 rpm으로 진탕하면서 배양하고 확장시켰다. 조건화된 배양 상청액을 제6일에 9300xg으로 30분 동안 원심분리하여 수확하였다. 발현을 SDS-PAGE 및 웨스턴 블롯팅으로 모니터링하였다. 조건화된 배양 상청액을 0.2M 수크로스, 5% 글리세롤, 0.01% CHAPS, 및 1O mM 이미다졸로 조정하였다. 이어서, pH를 7.2로 조정하였다. 정제를 2 단계 공정으로 수행하였다: Ni/NTA 수지를 이용한 친화성 정제 (4℃에서 밤새 인큐베이션, 및 250 mM 이미다졸을 이용하여 용출); 이어서 0.2M 수크로스, 5% 글리세롤, 0.01% CHAPS, I mM TCEP, pH7.2를 갖는 목적 완충액 PBS 중의 Superdex® 200 200 컬럼 (GE Healthcare Life Sciences)에서 크기-배제 크로마토그래피. 풀링 물질을 최종 분석 및 저장 전에 10K MWCO PES 막 Vivacell® 100 원심분리 장치를 사용하여 농축하였다. 정제된 물질을 질량 분광법 및 분석적 초원심분리에 의해 정량화하였다.
· Cyno CD3 E+G HuFc-6xHis (E+G는 εγ 서브유닛을 나타냄)
HEK-293 세포 (Thermo Fisher), Lenti-XTM 렌티바이러스 시스템 (Clontech), 및 Cyno CD3 E+GHuFc-6xHis를 암호화하는 플라스미드 (Cynomolgus CD3E 수탁 번호: Q95LI5<, cyno CD3 E+GhuFc-His: 서열 번호 323)를 사용하여 Cyno CD3 E+G HuFc-6xHis를 생산하는 세포주를 생성하였다. 발현을 위해, 세포를 FreestyleTM 293 배지 (Thermo Fisher Scientific)에서 37℃에서, 가습 8% C02 환경에서 135 rpm으로 진탕하면서 배양하고 확장시켰다. 조건화된 배양 상청액을 제6일에 9300xg으로 30분 동안 원심분리하여 수확하였다. 발현을 SDS-PAGE 및 웨스턴 블롯팅으로 모니터링하였다. 조건화된 배양 상청액을 0.2M 수크로스, 5% 글리세롤, 0.01% CHAPS, 및 1O mM 이미다졸로 조정하였다. 이어서, pH를 7.2로 조정하였다. 정제를 2 단계 공정으로 수행하였다: Ni/NTA 수지를 이용한 친화성 정제 (4℃에서 밤새 인큐베이션, 및 250 mM 이미다졸을 이용한 용출); 이어서 0.2M 수크로스, 5% 글리세롤, 0.01% CHAPS, ImM TCEP, pH7.2를 갖는 목적 완충액 PBS 중의 Superdex® 200 200 컬럼 (GE Healthcare Life Sciences)에서 크기-배제 크로마토그래피. 풀링 물질을 최종 분석 및 저장 전에 10K MWCO PES 막 Vivacell® 100 원심분리 장치를 사용하여 농축하였다. 정제된 물질을 질량 분광법 및 분석적 초원심분리에 의해 정량화하였다.
· Fc-His-태그된 인간 B7H6 ECD
이 작제물에서, huB7H6 ECD에 이어 GS 링커가 후속되고, huIgGl-Fc 도메인 및 C-말단 His6 태그 (서열 번호 318)가 뒤따른다. HEK293-6E 세포를 이용한 일시적 형질감염에 의해, 1:3의 DNA:PEI 비율 및 L 배양물 당 1 mg DNA로 작제물을 발현시켰다. PEI 시약은 선형 PEI MAX [Mw 40,000] (Polysciences: Cat# 24765-2)이었다. 형질감염된 세포를 37℃ 및 5% CO2에서 130 rpm 하에 인큐베이션하였다. 형질감염 24시간 후, 트립톤 N1 (Organotechnie; Cat# 19553) 및 글루코스를 각각 0.5% 및 1 g/L의 최종 농도로 첨가하였다. 세포를 5일 후 수확하였다. 원심분리 후, 상층액을 0.2 ㎛ 멤브레인 필터로 여과하였다. huB7H6-ECD-Fc-His 단백질을 2 단계 정제로 정제하였다: 먼저 Ni NTA 아가로스 매트릭스 상의 친화성에 의해, 이차로 Superdex® 200, 26/600 컬럼 (GE Healthcare Life Sciences)을 사용한 겔 여과에 의해. 풀링 분획을 여과하고, 1x PBS, 0.2 M 수크로스, 5% 글리세롤, 0.01% CHAPS, pH-7.2 제형 완충액에 저장하였다.
· Fc-His-태그된 인간 Ala-돌연변이화 B7H6 ECD (Ala로 치환된 NKp30 상호작용 부위 aa35-38 및 aal02-105).
이 작제물 (서열 번호 319)은 위치 35-38 및 102-105에서 Ala 치환을 갖는 huB7H6을 가지므로, NKp30에 결합하지 않는다. huB7H6-Ala-ECD에 이어 GS 링커, 이어 huIgGIFc 도메인 및 C-말단 His6 태그가 뒤따른다. 이 작제물을 일시적 형질감염에 의해 HEK293-6E 세포에서 발현시키고, 2 단계 정제 공정으로 정제하고, Fc-His-태깅된 huB7H6-ECD 작제물에 대해 상기 기재된 바와 같이 저장하였다.
· 인간 B7H1-Fc
이 작제물 (서열 번호 324)은 cMyc 태그, 트롬빈 절단 부위 및 huFc 도메인을 갖는 huB7Hl을 함유한다. 작제물을 HEK293f 세포, 1:1.5의 DNA:PEI 비율 및 L 배양물 당 1 mg의 DNA를 사용하여 일시적 형질감염에 의해 발현시켰다. 플라스크를 37℃ 및 가습된 8% CO2 환경에서 135 rpm으로 진탕하에 인큐베이션하였다. 3일 후에 세포를 수확하였다. 세포를 원심분리한 후, 상청액으로부터 단백질을 정제하였다. 일차로, nProtein A Sepharose® 4 Fast Flow 배지 (GE Healthcare, #17-5280-03)를 사용하여 친화성 정제를 수행하고, 용출액을 20 mM Tris, 100 mM NaCl, 10% 글리세롤, 1 mM TCEP, 3 mM CaCl2, pH 8.0에서 투석하였다. 이차로, 샘플을 Thrombin CleanCleaveTM 수지 (1 mL, Sigma)와 함께 인큐베이션하였다. 삼차로, 이전 단계로부터의 풀을 다시 nProtein A Sepharose® 4 Fast Flow 배지에 결합시켰다. 비결합 물질을 제외하고, PBS, 1 mM TCEP, pH 7.2 완충액에서 평형화된 Superdex® 75 (GE Healthcare) 컬럼 상에서 겔 여과에 의해 추가로 연마하고, 농축시켰다.
실시예 4: 재조합 B7H6 및 CD3εγ 서브유닛에 대한 친화성 및 종간 교차-반응성의 SPR 기반 결정.
인간 및 cyno B7H6 및 인간 B7H1의 B7H6/CD3 결합 단백질에 대한 친화성을 측정하기 위하여, BiacoreTM 8K 기기 (GE Healthcare Life Sciences)에서 실험을 수행하였다. 요약하면, B7H6/CD3 결합 단백질을 단백질 A/G를 통해 포획하였다. 이 실험을 위한 러닝 완충액 및 모든 연속 희석물을 HBS-EP+에서 제조하였다. CM5 센서 칩을 10 μL/분의 유속으로 420초 동안 양 유동 세포에 걸쳐 EDC/NHS의 동일한 혼합물로 활성화시키고, 10 μL/분의 유속으로 420초 동안 모든 유동 세포에 걸쳐 재조합 단백질 A/G (10 mM NaOAc 중의 50 μg/ml, pH 4.5)로 고정시켜 표면 상에 약 2500 RU의 단백질 A/G를 생성하였다. 센서 칩을 10 μL/분의 유속으로 420초 동안 모든 유동 세포에 걸쳐 1M 에탄올아민-HCl로 비활성화시켰다.
B7H6/CD3 결합 단백질 약 700 RU를 단백질 A/G 표면의 플로우 셀 2에서 60초 동안 10 μL/분의 유속으로 포획하였다. 분석물 HuB7H6, CyB7H6 및 HuB7Hl을 1200초의 해리와 함께 30 μL/분의 유속으로 300초 동안 포획된 B7H6/CD3 결합 단백질 상에서 양 유동 세포에 걸쳐 주입하였다. HuB7H6 및 CyB7H6의 농도는 0 nM, 6.25 nM, 12.5 nM, 25 nM, 50 nM 및 100 nM이었다. HuB7Hl의 농도는 0 nM 및 1 μM이었다. 양 유동 세포에 걸쳐 30 μL/분의 유속으로 20초 동안 10 mM 글리신-HCl, pH 1.5를 주입하여 표면을 재생시켰다.
기준 유동 셀 1 (센서 표면과 상호작용) 및 블랭크 (HBS-EP+ 또는 0 nM 분석물)를 미가공 데이터에서 제하였다. BiacoreTM 8K Evaluation Software를 사용하여, 센서그램을 1:1 Langmuir 결합에 전역적으로 피팅하여 결합율 상수 (ka), 해리율 상수 (kd) 및 평형 해리상수 (KD) 값을 제공하였다.
B7H6/CD3 결합 단백질의 인간 및 사이노 CD3E+G-hFc에 대한 친화성을 측정하기 위해, Bio-Rad ProteOnTM XPR36 기기 상에서 실험을 수행하였다. 요약하면, HuCD3E+G-hFc 및 CyCD3E+G를 ProteOnTM GLM 센서 칩 (Bio-Rad) 상에서 아민-커플링시키고, B7H6/CD3 결합 단백질을 고정화된 표면 위로 흘려보냈다. 이 실험을 위한 러닝 완충액 및 모든 연속 희석물을 HBS-EP+에서 제조하였다. GLM 센서 칩을 Bio-Rad의 권장에 따라 정규화하였다. 센서 칩을 수평 방향으로 EDC/s-NHS의 동일한 혼합물로 300초 동안 30 μL/분의 유속으로 활성화시켰다. HuCD3E+G-hFc를 수직 방향으로 10 mM 아세테이트 pH 4.5 중 0.4 μg/mL, 0.2 μg/mL 및 0.1 μg/mL로 각각 L1, L2 및 L3에 300초 동안 30 μL/분의 유속으로 고정시켜 약 100 RU의 HuCD3E+G-hFc를 LI 상에, 40 RU의 HuCD3E+G-hFc를 L2 상에, 0 RU의 HuCD3E+G-hFc를 L3 상에 생성하였다. CyCD3E+G-hFc를 수직 방향으로 10 mM 아세테이트 pH 4.5 중 0.4 μg/mL, 0.2 μg/mL 및 0.1 μg/mL로 각각 L4, L5 및 L6에 300초 동안 30 μL/분의 유속으로 고정시켜 약 385 RU의 HuCD3E+G-hFc를 L4 상에, 170 RU의 CyCD3E+G-hFc를 L5 상에, 50 RU의 CyCD3E+G-hFc를 L6 상에 생성하였다, 센서 칩을 수평 방향으로 1M 에탄올아민-HCl로 30 μL/분의 유속으로 300초 동안 비활성화시켰다. 센서 칩을 100 μL/분 유속의 0.85% 인산으로 18초 동안 수평으로 2회, 수직으로 2회 재생하였다.
B7H6/CD3 결합 단백질 분석물을 600초의 해리와 함께 30 μL/분의 유속으로 300초 동안 고정화된 표면에 수평으로 주입하였다. 사용된 B7H6/CD3 결합 단백질의 농도는 0 nM, 1.2 nM, 3.7 nM, 11.1 nM, 33.3 nM 및 100 nM이었다. 0.85% 인산을 18초 동안 100 μL/분의 유속으로 수평으로 2회 주입하여 표면을 재생하였다.
미가공 데이터에서 인터스팟 (센서 표면과 상호작용) 및 블랭크 (HBS-EP+ 또는 0 nM 분석물)를 제하였다. Bio-Rad ProteOnTM Manager 소프트웨어를 사용하여, 센서그램을 1:1 Langmuir 결합에 전역적으로 피팅하여 결합 속도 상수 (ka), 해리 속도 상수 (kd) 및 평형 해리 상수 (KD) 값을 제공하였다.
상기 기재된 바와 같이 결정된 친화도를 표 2에 예시적인 B7H6/CD3 결합 단백질 (각각 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6 쇄 및 서열 번호 311의 CD3 쇄를 포함하는 B7H6/CD3 결합 단백질, 및 서열 번호 230 또는 서열 번호 239의 B7H6 쇄 및 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3 쇄를 포함하는 B7H6 결합 단백질)에 대해 나타내었다.
|
B7H6
결합제 |
CD3
결합제 |
huB7-H6 [nM] | cyB7-H6 [nM] | cy/hu B7-H6 |
huCD3
[nM] |
cyCD3
[nM] |
cy/hu CD3 | huB7-H1 |
| B7H6#12 | CD3#1 | 1.1 | 2.3 | 2.1 | 3.6 | 2.5 | 0.7 | nb at1μM |
| B7H6#13 | CD3#1 | 3.0 | 4.6 | 1.5 | 4.1 | 2.8 | 0.7 | nb at1μM |
| B7H6#14 | CD3#1 | 0.1 | 0.6 | 5.9 | 4.2 | 2.7 | 0.6 | nb at1μM |
| B7H6#15 | CD3#1 | 0.8 | 2.2 | 2.8 | 3.8 | 2.6 | 0.7 | nb at1μM |
| B7H6#16 | CD3#1 | 3.1 | 7.2 | 2.3 | 3.7 | 2.6 | 0.7 | nb at1μM |
| B7H6#17 | CD3#1 | 8.7 | 8.4 | 1.0 | 13.5 | 3.7 | 0.3 | nb at1μM |
| B7H6#18 | CD3#1 | 1.4 | 3.3 | 2.3 | 3.9 | 2.8 | 0.7 | nb at1μM |
| B7H6#19 | CD3#1 | 1.6 | 5.1 | 3.1 | 4.0 | 2.4 | 0.6 | nb at1μM |
| B7H6#20 | CD3#1 | 1.1 | 4.9 | 4.6 | 4.0 | 2.6 | 0.7 | nb at1μM |
| B7H6#21 | CD3#1 | 3.3 | 1.4 | 0.4 | 4.4 | 2.7 | 0.6 | nb at1μM |
| B7H6#22 | CD3#1 | 1.5 | 1.4 | 1.0 | 5.1 | 2.8 | 0.5 | nb at1μM |
| B7H6#23 | CD3#1 | 1.3 | 1.2 | 0.9 | 5.5 | 2.7 | 0.5 | nb at1μM |
| B7H6#24 | CD3#1 | 1.8 | 3.1 | 1.7 | 7.8 | 3.3 | 0.4 | nb at1μM |
| B7H6#14 | CD3#2 | 1.2 | 1.0 | 0.9 | 16.9 | 17.7 | 1.0 | nb at1μM |
| B7H6#14 | CD3#3 | 1.1 | 1.1 | 0.9 | 4.8 | 7.1 | 1.5 | nb at1μM |
| B7H6#14 | CD3#4 | 1.3 | 1.1 | 0.8 | 7.6 | 8.5 | 1.1 | nb at1μM |
| B7H6#14 | CD3#5 | 0.9 | 1.0 | 1.1 | 4.3 | 5.2 | 1.2 | nb at1μM |
| B7H6#14 | CD3#6 | 0.4 | 0.9 | 2.1 | 4.1 | 5.7 | 1.4 | nb at1μM |
| B7H6#23 | CD3#2 | 1.9 | 2.0 | 1.1 | 10.4 | 10.0 | 1.0 | nb at1μM |
| B7H6#23 | CD3#3 | 2.2 | 1.9 | 0.9 | 13.8 | 11.9 | 0.9 | nb at1μM |
| B7H6#23 | CD3#4 | 1.7 | 1.7 | 1.0 | 3.8 | 3.6 | 0.9 | nb at1μM |
| B7H6#23 | CD3#5 | 2.2 | 1.9 | 0.9 | 2.8 | 3.7 | 1.3 | nb at1μM |
| B7H6#23 | CD3#6 | 1.9 | 2.0 | 1.1 | 3.4 | 3.9 | 1.2 | nb at1μM |
nb: 결합 없음
실시예 5: 세포 표면 상에 사이노몰거스 원숭이 B7H6 세포외 도메인을 발현하는 재조합 CHO-K1 세포주의 생성
세포 표면 상에 사이노몰거스 원숭이 B7H6의 세포외 도메인 (NCBI: XP 005578557)을 발현하는 안정한 CHO-K1 세포를 생성하기 위해, 각각의 암호화 서열 (XP_005578557.1의 aa 25 내지 262)을 pcDNA3.1 (Thermo Fisher Scientific)에 클로닝하였다. 상기 작제물은 N-말단 마우스 IgG Vk-리딩 서열에 이어서 6-His-myc-tag 및 사이노몰거스 원숭이 B7H6 세포외 도메인 (NCBI XP 005578557.1의 aa25-262)을 함유한다. B7H6 세포외 도메인의 세포 표면 국재화를 보장하기 위해, 작제물에 링커, 및 EpCAM (Uniprot P16422)의 막관통 및 세포내 도메인이 이어졌다. 세포 표면에서의 B7H6 도메인의 발현을 마우스 모노클로날 항-myc 항체 (AbD Serotec)를 이용하여 유세포 분석으로 검증하였다. 사용된 서열은 표 3에 열거되어 있고, 작제물의 개략도는 도 2에 도시되어 있다.
| 명칭 | 서열 |
| Vk 리더 | METDTLLLWVLLLWVPGSTGD (서열 번호 325) |
| 6-His-myc 태그 | HHHHHHEQKLISEEDL (서열 번호 326) |
| 사이노몰거스 B7-H6 세포외 도메인 (NCBI XP_005578557.1, aa25-262) |
DLKVEMMARGIQATRLNDSVTISCKVIYSQPLNITSMGITWFRKSLTLDKEVKVFEFFGDHQKAFRPGANVSLWRLKSGDASLKLPGVQLEEAGEYRCEVVVTPLKAQGTVQLKVVASPTSRLFQDQAVVKENEGKYMCESSRFYPKDINITWEKWTQKSPHHVVISENVITGPTIKNMDGTFNITSYLKLNSSQEDPGTVYRCVIRHESLHTPVSIDFILTAPQQSLSEPEKTDIFS (서열 번호 327) |
| 링커 | SGGGGS (서열 번호 328) |
| 인간 EpCAM 막관통 도메인 (Uniprot P16422, aa266-288) |
AGVIAVIVVVVIAVVAGIVVLVI (서열 번호 329) |
| 인간 EpCAM 세포내 도메인 (Uniprot P16422, aa289-314) |
SRKKRMAKYEKAEIKEMGEMHRELNA (서열 번호 330) |
실시예 6: 재조합 인간 B7H6 세포외 도메인 단백질에 대한 예시적인 B7H6 결합 단백질의 결합.
실시예 3에 기재된 바와 같은 재조합 인간 Fc-His 태그 B7H6 ECD 및 인간 Fc-His-태그 Ala-돌연변이화 B7H6 세포외 단백질에 대한 B7H6/CD3 결합 단백질의 결합을 평가하기 위해, MediSorpTM 플레이트 (Nunc, 467320)를 4℃에서 밤새 2 μl/ml 재조합 단백질로 코팅하였다. 다음 날, 플레이트를 실온 (RT)에서 1시간 동안 인산 완충 식염수(PBS) 중 0.5% 소 혈청 알부민(BSA)으로 차단하였다. 이어서, 플레이트를 0.05% TWEEN®20 점성 액체를 함유하는 OBS로 세척하고, B7H6/CD3 결합 단백질을 0.00001 내지 10 μg/ml 범위의 농도로 인큐베이션하였다. 추가 세척 단계 후, 결합된 B7H6/CD3 결합 단백질을 퍼옥시다제 접합된 염소 항-인간 IgG F(ab')2-특이적 이차 항체 (Jackson Immunoresearch)에 의해 검출하고, TMB 기질 용액 (Bender Med Systems)으로 가시화하였다. 도 3A+B 및 4A+B는 재조합 인간 B7H6 ECD (도 3A+B) 및 인간 Ala-돌연변이화 B7H6 ECD (도 4A+B) 단백질에 대한 예시적인 B7H6/CD3 결합 단백질 (각각 서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 서열 번호 221, 서열 번호 222, 서열 번호 223, 서열 번호 224, 서열 번호 225, 서열 번호 226, 서열 번호 227, 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6 쇄 및 서열 번호 311의 CD3쇄를 포함하는 B7H6/CD3 결합 단백질, 및 서열 번호 230 또는 서열 번호 239의 B7H6쇄 및 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3쇄를 포함하는 B7H6 결합 단백질)의 결합을 나타낸다.
시험된 모든 예시적인 B7H6/CD3 결합 단백질은 재조합 인간 B7H6 ECD에 필적하는 결합을 나타내는 반면 (도 3A+B), 서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 서열 번호 221, 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6 쇄 및 서열 번호 311의 CD3 쇄를 포함하는 B7H6 결합 단백질, 및 서열 번호 230 또는 서열 번호 239의 B7H6 쇄 및 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3 쇄를 포함하는 B7H6 결합 단백질은 각각 인간 Fc-His-표지된 Ala-돌연변이화 B7H6 세포외 단백질에 강한 결합을 나타내었으며, 여기서 NKp30 결합 부위는 알라닌으로 돌연변이되었다. 서열 번호 222, 서열 번호 223, 서열 번호 224, 서열 번호 225, 서열 번호 226, 또는 서열 번호 227의 B7H6 쇄 및 서열 번호 311의 CD3 쇄를 포함하는 B7H6/CD3 결합 단백질은 고농도에서 Fc-His-태그된 Ala-돌연변이화 B7H6 세포외 단백질에 약한 결합만을 나타내거나 결합을 나타내지 않는다.
실시예 7: B7H6-양성 HCT 세포에 결합.
인간 (결장직장암) CRC 세포주인 HCT-15에 대한 B7H6/CD3 결합 단백질의 결합을 유세포 분석법으로 시험하였다. 이전 실험에서, HCT-15 세포는 RNA 수준뿐만 아니라 세포 표면 상에 약 8,000개의 B7-H6 수용체를 갖는 단백질 수준에서도 B7-H6을 발현하는 것으로 확인되었다 (데이터는 나타내지 않음). B7H6/CD3 결합 단백질을 실시예 2에 기재된 바와 같이 제조하였다. FACS 완충액 (PBS/0.5%BSA/0.05% 아지드화나트륨)에서 2 단계 정제된 B7H6/CD3 결합 단백질의 농도를 증가시키면서 HCT-15 세포를 염색하였다. 결합된 분자를 PE-접합된 항-인간 2차 항체 (Sigma-Aldrich, #P8047)로 검출하였다. 도 5A+B는 인간 HCT-15 세포에 대한 예시적인 B7H6/CD3 결합 단백질 (각각 서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 서열 번호 221, 서열 번호 222, 서열 번호 223, 서열 번호 224, 서열 번호 225, 서열 번호 226, 서열 번호 227, 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6 쇄 및 서열 번호 311의 CD3쇄를 포함하는 B7H6/CD3 결합 단백질 및 서열 번호 230 또는 서열 번호 239의 B7H6 쇄 및 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3쇄를 포함하는 B7H6/CD3 결합 단백질)의 결합을 보여준다.
실시예 8: 사이노몰거스 원숭이 B7H6에 대한 교차 반응성
사이노몰거스 B7H6를 발현하는 재조합 CHO-K1 세포에 대한 B7H6/CD3 결합 단백질의 결합을 유세포 분석법으로 시험하였다. B7H6/CD3 결합 단백질을 실시예 2에 기재된 바와 같이 제조하였다. 재조합 사이노몰거스 B7H6-발현 세포주를 실시예 5에 기재된 바와 같이 생성하였다. 세포를 FACS 완충액 (PBS/0.5%BSA/0.05% 아지드화나트륨)에서 2 단계 정제된 B7H6/CD3 결합 단백질의 농도를 증가시키면서 염색하였다. 결합된 분자를 PE-접합된 항-인간 이차 항체 (Sigma-Aldrich, #P8047)로 검출하였다. 도 6은 재조합 사이노몰거스 원숭이 B7H6 발현 세포에 대한 예시적인 B7H6/CD3 결합 단백질 (각각 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6 쇄 및 서열 번호 311의 CD3 쇄를 포함하는 B7H6/CD3 결합 단백질 및 서열 번호 230 또는 서열 번호 239의 B7H6 쇄 및 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3 쇄를 포함하는 B7H6 결합 단백질)의 결합을 나타낸다.
실시예 9: 인간 T-세포에의 결합
정제된 인간 T-세포에 대한 B7H6/CD3 결합 단백질의 결합을 유세포 분석법으로 시험하였다. B7H6/CD3 결합 단백질을 실시예 2에 기재된 바와 같이 제조하였다. T-세포를 오스트리아 적십자사로부터 얻은 버피 코트에서 단리하였다. 헬싱키 선언에 따르고 오스트리아의 선택 윤리위원회의 승인에 따라 모든 버피 코트에 대해 사전 동의를 얻었다.
인간 말초 혈액 단핵 세포 (PBMC)를 Ficoll® Paque 밀도 구배 배지 (GE Healthcare Lifesciences)를 사용하여 제조한 후 원심분리하였다. 인간 말초 혈액 단핵 세포 (PBMC)는 수혈을 위해 혈액을 수집하는 혈액 뱅크의 부산물인 농축 림프구 제제 (버피 코트)에서 유래된 것이다. 따라서, 단핵 세포를 Ficoll® 밀도 구배 원심분리 (1400 rpm에서 브레이크 없이 35분)에 의해 단리하고, PBS로 철저히 세척하였다. 남은 적혈구를 ACK 용해 완충액 (Thermo Fisher Scientific, A1049201)에서 3분 동안 인큐베이션한 후, PBS에서 세척하여 제거하고, RPMI 1640 GlutaMAXTM 보충제 (Gibco #61870-010), 5% 인간 AB 혈청 AB (Gemini, GemCell cat # 100-512 LOT#H56500I) + 1% MEM-NEAA (Gibco #11140-035), 1O mM HEPES (Affymetrix #7365-49-9), 10 μM 베타-머캅토에탄올 (Gibco #21985-023) 및 피루브산나트륨 (Gibco #11360-039)을 포함하는 분석 배지에 현탁시켰다.
Pan T Cell Isolation Kit II (Miltenyi Biotec #130-091-156)를 사용하여 음성 선별에 의해 T-세포를 단리하였다. 요약하면, 세포를 10 Mio 세포 당 40 ㎕ 완충액 PBS/0.5% BSA (Gibco ref#041-94553 M)/2 mM EDTA (Invitrogen ref# 15575-038)에 재현탁시키고, 10 Mio 세포 당 10 ㎕의 비오틴-항체 칵테일과 함께 4℃에서 5분 동안 인큐베이션하였다. 이어서, 30 ㎕ 완충액 및 20 ㎕ 항-비오틴 MACS® MicroBeds/천만 세포를 첨가하고, 4℃에서 10분 동안 인큐베이션하였다. 이어서, 혼합물을 적합한 MACS® 마이크로비드 분리기 (Miltenyi Biotec)의 자기장 하에 사전-세정된 25LS 칼럼 (Miltenyi Biotec #130-042-401)에 위치시켰다. 통과물을 수집하고 분석 배지에서 세척하였다.
T-세포를 FACS 완충액 (PBS/0.5%BSA/0.05% 아지드화나트륨)에서 2 단계 정제된 B7H6/CD3 결합 단백질의 농도를 증가시키면서 염색하였다. 결합된 분자를 PE-접합된 항-인간 2차 항체 (Sigma-Aldrich, #P8047)로 검출하였다. 도 7은 인간 T-세포에대한 예시적인 B7H6/CD3 결합 단백질 (각각 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6 쇄 및 서열 번호 311의 CD3를 포함하는 B7H6/CD3 결합 단백질 및 서열 번호 230 또는 서열 번호 239의 B7H6 쇄 및 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3쇄를 포함하는 B7H6 결합 단백질)의 결합을 나타낸다.
실시예 10: 결합 선택성
B7H6- 및 CD3-음성 CHO-K1 세포에 대한 B7H6/CD3 결합 단백질의 결합을 유세포 분석으로 시험하였다. B7H6/CD3 결합 단백질을 실시예 2에 기재된 바와 같이 제조하였다. CHO-K1 세포를 FACS 완충액 (PBS/0.5%BSA/0.05% 아지드화나트륨)에서 2 단계 정제된 B7H6/CD3 결합 단백질의 농도를 증가시키면서 염색하였다. 결합된 분자를 PE-접합된 항-인간 2차 항체 (Sigma-Aldrich, #P8047)로 검출하였다. 도 8은 CHO-K1 세포에 대한 예시적인 B7H6/CD3 결합 단백질 (각각 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6 쇄 및 서열 번호 311의 CD3 쇄를 포함하는 B7H6/CD3 결합 단백질, 및 서열 번호 230 또는 서열 번호 239의 B7H6 쇄 및 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3 쇄를 포함하는 B7H6 결합 단백질)의 결합을 보여준다.
실시예 11: B7H6-의존성 NK 세포 활성의 억제
세포 표면에 발현된 B7H6은 NK 세포 상의 NKp30에 결합하여 NK 세포의 NKp30-매개 활성화 및 NK 세포 세포독성 및 사이토카인 분비를 촉발시킨다 (Brandt et al, J.Exp. Med. 2009;206(7):1495-1503). NK 세포의 B7H6 의존성 활성화를 평가하기 위해, 96-웰 평탄 바닥 세포 배양 플레이트에 100 nM 재조합 인간 B7H6 단백질 (R&DSsystems#7144-B7-050)을 4℃에서 밤새 코팅하였다. 다음날, 플레이트를 PBS로 세척한 후, B7H6/CD3 결합 단백질 또는 재조합 NKp30 단백질 (R&DSsystems#1849-NK-025)을 농도를 증가시키면서 첨가하고, 실온에서 1시간 동안 인큐베이션하였다. B7H6/CD3 결합 단백질을 실시예 2에 기재된 바와 같이 제조하였다. 추가 세척 단계 후, 웰당 100 ㎕ 배지 (12.5% 소태아 혈청, 12.5% 말 혈청, 0.2 mM D-Myo-이노시톨, 0.02 mM 엽산 및 0.1 mM β-머캅토에탄올을 함유하는 MEM 알파) 중의 100,000 NK92MI (ATCC) 세포를 첨가하고 24시간 동안 인큐베이션하였다. 다음날, V-PLEX 인간 IFN-γ Kit (Meso Scal Discovery)를 사용하여 IFNγ 농도를 정량하였다. 도 9A+B는 B7H6/CD3 결합 단백질 (서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 서열 번호 221, 서열 번호 222, 서열 번호 223, 서열 번호 224, 서열 번호 225, 서열 번호 226, 서열 번호 227, 서열 번호 228, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 235, 서열 번호 236의 B7H6 쇄, 및 서열 번호 311의 CD3 쇄를 포함하는 B7H6/CD3 결합 단백질)이 NK-92MI에 의한 IFNγ 분비의 B7-H6-의존적 유도를 억제하는 능력을 보여준다.
NKp30 상호작용 부위가 알라닌으로 치환된 Ala-돌연변이화 B7H6 세포외 단백질에 결합하지 않거나 약하게만 결합하는 B7H6 결합 단백질 (서열 번호 222, 서열 번호 223, 서열 번호 224, 서열 번호 225, 서열 번호 226, 서열 번호 227의 B7H6쇄 및 서열 번호 311의 CD3 쇄를 포함하는 B7-H6/CD3 결합 단백질) (도 4, 실시예 6에 나타냄)은 NK-92MI 세포에 의한 IFNγ 분비의 B7-H6-의존적 유도를 억제하는 반면, 야생형 단백질에 필적하는 Ala-돌연변이화 B7H6 세포외 단백질에 대해 강한 결합을 나타내는 결합 단백질 (서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 서열 번호 221, 서열 번호 228, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 235, 서열 번호 236의 B7H6쇄 및 서열 번호 311의 CD3 쇄를 포함하는 B7-H6/CD3 결합 단백질) (도 4, 실시예 6에 나타냄)은 NK-92MI 세포에 의한 IFNγ 분비의 B7-H6-의존적 유도에 영향을 미치지 않는다.
실시예 12: T-세포 지향 (T-cell redirected) 용해 인간 HCT-15 세포의 효능.
HCT-15 세포에 대한 비-자극된 T-세포의 효능을 세포 용해에 대한 판독으로서 락테이트-데하이드로게나제 (LDH) 방출을 사용하여 결정하였다. 이 분석에서는, B7H6-양성 CRC 세포주 HCT-15를 이펙터 세포로서 인간 T-세포와 B7H6/CD3 결합 단백질의 농도를 증가시키면서 10:1의 이펙터 대 표적 세포 비로 72시간 동안 공동-배양하였다. B7H6/CD3 결합 단백질을 실시예 2에 기재된 바와 같이 제조하였다. 정제된 T-세포를 실시예 9에 기재된 바와 같이 단리하였다. 이어서, HCT-15 세포와 T-세포를 1:10의 비율로 B7H6/CD3 결합 단백질과 0.00001 nM 내지 10 nM의 농도로 72시간 동안 인큐베이션하였다.
Cytototoxicity Detection KitPLUS (Roche)를 제조업체의 지침에 따라 사용하여 세포 독성 활성을 결정하였다. 요약하면, 이 방법은 사멸 또는 원형질막 손상 세포로부터 LDH 방출 용법을 기반으로 한다. 세포 배양 상청액을 키트로부터의 반응 혼합물과 함께 30분 동안 인큐베이션하고, LDH 활성의 결과인 포르마잔의 형성을 세포 용해 대용물로서 500 nm에서 분광광도계로 측정하였다. 최대 용해 대조군에 대한 세포 독성의 백분율을 다음 공식에 따라 계산하였다:
세포 독성 (대조군 대비) = 측정값 - 배경 / 최대 용해 - 최소 용해
배경: 표적 세포 + 이펙터 세포
최대 용해: 표적 세포 + 5% Triton X-100
최소 용해: 표적 세포
GraphPad®Prism® 5.0 소프트웨어 (GraphPad Sofware, Inc)를 사용하여, 최대 용해 대조군에 대한 세포독성의 백분율을 상응하는 B7H6/CD3 결합 단백질 농도에 대해 플롯팅하였다. S자형 용량 반응 곡선의 평가를 위해 4 매개변수 로지스틱 방정식 모델로 용량 반응 곡선을 분석하고 EC50 값을 계산하였다.
도 10A+B 및 11A+B는 예시적인 B7H6/CD3 결합 단백질 (각각 서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 서열 번호 221, 서열 번호 222, 서열 번호 223, 서열 번호 224, 서열 번호 225, 서열 번호 226, 서열 번호 227, 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6 쇄 및 서열 번호 311 CD3 쇄를 포함하는 B7H6/CD3 결합 단백질, 및 서열 번호 230 또는 서열 번호 239의 B7H6 쇄 및 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3 쇄를 포함하는 B7H6 결합 단백질)에 의해 매개되는 HCT-15 세포의 T-세포 지향 용해 효능의 예를 나타낸다.
도 10 및 11은 wt 단백질과 비교할만한 정도로 NKp30 상호작용 부위가 알라닌으로 치환된 재조합 Ala-돌연변이화 B7H6 세포외 단백질에 결합하고, NK92MI 세포에 의한 IFNγ의 B7-H6-의존적 분비를 억제하지 않는 B7H6 결합 단백질 (각각 서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 서열 번호 221, 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6 쇄 및 서열 번호 311의 CD3 쇄를 포함하는 B7H6/CD3 결합 단백질, 및 서열 번호 230 또는 서열 번호 239의 B7H6 쇄 및 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3쇄를 포함하는 B7H6 결합 단백질) (실시예 6, 11에 나타냄)이 재조합 Ala-돌연변이화 B7H6 세포외 단백질에는 결합하지 않거나 약하게만 결합하고 NK92MI 세포에 의한 IFNγ의 B7-H6-의존적 분비를 억제하는 B7H6/CD3 결합 단백질 (서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 또는 서열 번호 221 및 서열 번호 CD3#l의 CD3 쇄를 포함하는 B7-H6/CD3 결합 단백질) (실시예 6, 11에 나타냄)보다 더 낮은 EC50 값 (표 4A+B)을 나타낸다. 따라서, B7H6 의존적 NK 세포 활성화를 억제하지 않는 결합 단백질은 놀랍게도 B7H6 의존적 NK 세포 활성화를 억제하는 결합 단백질과 비교하여 상당히 더 높은 T-세포 매개 종양 세포 용해를 나타낸다.
예시적인 B7H6/CD3 결합 단백질에 대해 도 12에 나타낸 바와 같이, 활성은 낮은 이펙터 대 표적 세포 비율만을 필요로 한다.
실시예 13: T-세포 지향 용해의 교차-반응성 및 선택성
HCT-15 세포에 대한 비-자극 T-세포의 효능을 실시예 12에 기재된 바와 같이 세포 용해에 대한 판독으로서 락테이트-데하이드로게나제 (LDH) 방출을 사용하여 결정하였다. B7H6/CD3 결합 단백질을 실시예 2에 기재된 바와 같이 제조하였다. 재조합 사이노몰거스 B7H6-발현 세포주를 실시예 5에 기재된 바와 같이 생성하였다.
도 13은 각각 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6 쇄 및 서열 번호 311의 CD3 쇄를 포함하는 예시적인 B7H6/CD3 결합 단백질, 및 서열 번호 230 또는 서열 번호 239의 B7H6 쇄 및 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3 쇄를 포함하는 B7H6 결합 단백질에 의해 매개되는 B7H6 발현 세포 (도 13A) 및 B7H6-음성 모 CHO-K1 세포 (도 13B)의 T-세포 지향 용해의 효능의 예를 나타낸다.
실시예 14: T 세포의 활성화 선택성
T-세포의 활성화를 결정하기 위해, 표적 세포로서 B7H6-양성 HCT-15 세포 및 비자극된 T-세포를 이용한 세포독성 분석을 실시예 12에 기재된 바와 같이 설정하였다. B7H6/CD3 결합 단백질을 실시예 2에 기재된 바와 같이 제조하였다. T 세포 활성화를 결정하기 위해, 세포를 원심분리하고, CD4 (BD #550630), CD8 (BD #557834), 및 CD25 (BD#340907)에 대한 항체로 염색하고, 유세포 분석법에 의해 측정하였다. 도 14는 서열 번호 228, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 235, 또는 서열 번호 236의 B7H6 쇄와 서열 번호 311의 CD3 쇄를 포함하는 예시적인 B7H6/CD3 결합 단백질에 의해 매개되는 B7H6-양성 HCT-15 세포의 존재 및 부재하에 CD4+ (도 14A) 및 CD8+ (도 14B) 세포의 활성화 효능의 예를 나타낸다.
실시예 15 T 세포의 탈과립 선택성
퍼포린 및 그랜자임 B의 세포내 발현을 통해 T-세포의 탈과립을 결정하기 위해, 표적 세포로서 B7H6-양성 HCT-15 세포 및 비자극된 T-세포를 사용하는 세포독성 분석을 실시예 12에 기재된 바와 같이 설정하였다. B7H6/CD3 결합 단백질을 실시예 2에 기재된 바와 같이 제조하였다. 그랜자임 B 및 퍼포린의 세포내 수준을 측정하기 위해, 세포를 원심분리하고, CD4 (BD #550630), CD8 (BD #557834)에 대한 항체로 염색한 후, 고정/투과 용액 (BD #554714)을 사용하여 세포를 투과하고, 퍼포린 (BioLegend #308120) 및 그랜자임 B (BD #560221)에 대한 항체로 염색하고, 유세포 분석법으로 측정하였다. 도 15는 CD4+ (도 15A) 및 CD8+ (도 15B) 세포에서의 세포내 퍼포린 발현의 상향조절 효능의 예를 나타내고, 도 16은 서열 번호 228, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 235 또는 서열 번호 236의 B7H6 쇄 및 서열 번호 311의 CD3 쇄를 포함하는 예시적인 B7H6/CD3 결합 단백질에 의해 매개되는 B7H6-양성 HCT-15 세포의 존재 및 부재하에 CD4+ (도 16A) 및 CD8+ (도 16B) 세포에서의 세포내 그랜자임 B 발현의 상향조절을 나타낸다.
실시예 16: T-세포 증식 유도
표적 세포로서 B7H6-양성 HCT-15 세포 I 비자극된 T-세포를 이용한 세포독성 분석을 실시예 12에 기재된 바와 같이 설정하였다. B7H6/CD3 결합 단백질을 실시예 2에 기재된 바와 같이 제조하였다. T 세포의 증식을 측정하기 위해, PBMC를 5 μM Cell TraceTM CFSE (Invitrogen, C34554)으로 표지하고, 항-CD3 항체 (BioLegend cat#: 317336)로 염색하였다. 이어서, 표지된 PBMC를 HCT-15 세포와 10:1의 비율로 B7H6/CD3 결합 단백질의 농도를 증가시키면서 6일 동안 인큐베이션하였다. 도 17은 B7H6-양성 HCT-15 세포의 존재하에 서열 번호 228, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 235 또는 서열 번호 236의 B7H6 쇄 및 서열 번호 311의 CD3 쇄를 포함하는 예시적인 B7H6/CD3 결합 단백질에 의한 B7H6-결합 단백질에 의한 T-세포 증식의 용량 의존적 유도를 나타낸다.
실시예 17: IFNγ 분비의 선택성
표적 세포로서 B7H6-양성 HCT-15 세포 및 비자극된 T-세포를 이용한 세포독성 분석을 실시예 12에 기재된 바와 같이 설정하였다. B7H6/CD3 결합 단백질을 실시예 2에 기재된 바와 같이 제조하였다. 상청액 중의 사이토카인 수준을 V-Plex 인간 IFN-γ 키트 (MSD, CAT: K151QOD-4)로 측정하였다. 도 18은 서열 번호 228, 서열 번호 230, 서열 번호 231, 서열 번호 235 또는 서열 번호 236의 B7H6 쇄 및 서열 번호 311의 CD3 쇄를 포함하는 5개의 예시적인 B7H6/CD3 결합 단백질에 의해 유도된 IFNγ의 분비를 나타낸다.
실시예 18: 마우스 PK
B7H6/CD3 결합 단백질을 실시예 2에 기재된 바와 같이 제조하였다.
C57BL/6 마우스에서 단일 1 mg/kg i.v. 용량 후 B7H6/CD3 결합 단백질의 PK를 평가하였다. B7H6 포획/CD3 검출 분석을 사용하여 B7H6/CD3 결합 단백질의 혈청 농도를 결정하였다.
요약하면, 수컷 C57BL/6 마우스에 단일 1 mg/kg 정맥내 (IV) 용량 (분자 당 n = 3)을 투여하였다. 투여 전 및 투여 후 0.25, 2, 6, 24, 48, 96, 168, 240 및 336 시간에 혈액 샘플을 수집하였다. 비오티닐화된 B7H6을 포획 시약으로 사용하고 설포 태그된 CD3ε를 검출 시약으로 사용하여 MSD 기반 리간드 결합 분석으로 혈청 약물 수준을 측정하였다. 비구획 분석을 사용하여 혈청 농도 시간 프로파일로부터 약동학 (PK) 매개변수를 계산하였다. 다음 PK 매개변수가 평가되었다: AUCtlast (시간 0에서 마지막 정량화 가능한 시점까지 혈청 농도-시간 곡선 아래 면적), AUCinf (무한대로 외삽된 혈청 농도 시간 곡선 아래 면적), CL (전신 청소율), Vss (정상 상태 부피 분포) 및 T1/2 (종말 반감기).
예시적인 B7H6/CD3 결합 단백질에 대한 평균 (SD) 혈청 농도 시간-프로파일을 도 19에 요약하였다. 이러한 예시적인 BH6/CD3 결합 단백질에 대한 평균 (SD) PK 매개변수는 표 5에 요약되어 있다.
|
용량
(mg/kg) |
C
max
(ng/mL) |
AUC
tlast
(ng·hr/mL) |
AUC
inf
*
(ng·hr/mL) |
CL
(mL/d/kg) |
V
ss
(mL/kg) |
T
1/2
(일) |
MRT
(일) |
| 1 | 20500 (458) |
1200000 (78100) |
1840000 (112000) |
13.1 (0.8) |
173 (30) |
10.2 (2.2) |
13.3 (3.0) |
| *20% 초과 외삽된 AUC | |||||||
실시예 18A: 마우스 PK
B7H6/CD3 결합 단백질의 PK를 실시예 18에 기재된 바와 같이 평가하였다. 서열 번호 228, 서열 번호 230, 서열 번호 231, 또는 서열 번호 232의 B7H6 쇄, 및 서열 번호 311의 CD3 쇄를 포함하는 4개의 예시적인 B7H6/CD3 결합 단백질에 대한 평균 (SD) 혈청 농도 시간-프로파일을 도 22에 요약하였다.
실시예 19: 생체내 효능
인간 T 세포로 재구성된 인간 이종이식 마우스 모델을 사용하여 효능 연구를 수행하였다. 구체적으로, 치사 이하량으로 조사된 (2 Gy, -1일) 암컷 NOD.Cg-Prkdc scid Il2rg tm1Sug /JicTac 마우스의 우측 등쪽 옆구리에 인간 NCI-H716 결장직장암 세포 (2.5 x 107)를 피하 주사 (s.c.)하였다 (-16일). 이와 병행하여, 인간 CD3 양성 T 세포 (건강한 인간 혈액 공여자로부터 단리됨)를 시험관내에서 증식시켰다.
인간 말초 혈액 단핵 세포 (PBMC)를 실시예 9에 기재된 바와 같이 제조하였다.
Pan T 세포 단리 키트 II (Miltenyi Biotec #130-096-535)를 사용하여 음성 선택에 의해 T-세포를 단리하였다. 요약하면, 세포를 10x106 세포 당 40 ㎕ 완충액 PBS/0.5% BSA (Gibco ref# 041-94553 M)/2 mM EDTA (Invitrogen ref# 15575-038)에 재현탁시키고, 4 ℃에서 5 분 동안 10 x106 세포 당 10 ㎕의 비오틴-항체 칵테일과 인큐베이션하였다. 그 후 30 ㎕ 완충액 및 20 ㎕ 항-비오틴 MACS® MicroBeads/10 x106개의 세포를 첨가하고 4 ℃에서 10 분 동안 인큐베이션하였다. 이어서 혼합물을 적합한 MACS® 마이크로비드 분리기 (Miltenyi Biotec)의 자기장에서 미리 헹구어낸 25LS 컬럼 (Miltenyi Biotec#130-042-401)에 위치시켰다. 통과물을 수집하고 분석 배지에서 세척하였다.
이어서, T 세포 활성화/확장 키트 인간 (Miltenyi Biotec Cat#130-091-441)을 사용하여 17일 동안 T 세포를 확장시켰다. 요약하면, 항-비오틴 MACSiBeadTM 입자에 CD2-, CD3-, CD28 비오틴을 적재하고 입자 당 2개 세포의 비율로 정제된 T 세포로 전달한 후, 20 단위 재조합 IL-2 (R&D #202-IL-050/CF)의 존재하에 0.5-106 세포/ml의 밀도로 14일 동안 인큐베이션하였다. 세포에 3 일마다 20 단위의 신선한 IL-2를 보충하였다. 동물에 주입하기 3 일 전에 T 세포를 CD2-, CD3-, CD28 비오틴을 4개 세포 당 1개의 비드 비율로 적재한 항-비오틴 MACSiBeadTM 입자로 추가 3일 동안 재자극하였다. 마지막으로, MACSiMAGTM 분리기 (Miltenyi Biotec)로 비드를 제거하고 T 세포를 PBS에서 세척하였다.
-2일째에, 동물을 종양 용적에 기초하여 처리 그룹으로 무작위화하고, 2 x 107 인간 T 세포를 복강내 (i.p.) 주사하였다. B7H6/CD3 결합 단백질을 실시예 2에 기재된 바와 같이 제조하였다. 1일째에 치료를 시작하였고, B7H6/CD3 결합 단백질 또는 비히클 완충액 (50 mM NaOAc, 1O0 mM NaCl, pH 5.0)을 측면 꼬리 정맥에 정맥내 (i.v.) 볼루스 주사에 의해 q7d 투여 요법으로 투여하였다. 종양 성장을 외부 캘리퍼스 측정에 의해 모니터링하고, 종양 용적을 표준 반타원체 공식을 사용하여 계산하였다. 희생 기준에 도달한 동물들은 윤리적인 이유로 연구 중에 조기에 안락사시켰다. 종양 보유 마우스를 B7H6/CD3 결합 단백질로 주 1회 0.05 mg/kg로 i.v. 처리하여 상당한 종양 퇴행을 유도하였다 (도 20).
실시예 19A: 생체내 효능
실시예 19에 기재된 바와 같이 인간 CD3+ T 세포로 재구성된 인간 NCI-H716 이종이식 마우스 모델을 사용하여 효능 연구를 수행하였다. 종양 보유 마우스를 서열 번호 228, 서열 번호 230, 서열 번호 231, 또는 서열 번호 232의 B7H6 쇄, 및 서열 번호 311의 CD3 쇄를 포함하는 B7H6/CD3 결합 단백질로 주 1회 0.05 mg/kg으로 i.v. 투여하여 상당한 종양 퇴행을 유도하였다 (도 23).
실시예 19B: 생체내 효능
실시예 19에 기재된 바와 같이 인간 CD3+ T 세포로 재구성된 인간 NCI-H716 이종이식 마우스 모델을 사용하여 효능 연구를 수행하였다. 종양 보유 마우스를 B7H6/CD3 결합 단백질로 주 1회 또는 단일 용량으로 0.05 mg/kg으로 i.v. 투여하여 상당한 종양 퇴행을 유도하였다 (도 24).
실시예 20: B7H6/CD3 결합 단백질의 단량체 함량 퍼센트
B7H6/CD3 결합 단백질 (서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 서열 번호 221, 서열 번호 222, 서열 번호 223, 서열 번호 224, 서열 번호 225, 서열 번호 225, 서열 번호 227, 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6쇄, 또는 서열 번호 240 및 서열 번호 311의 CD3쇄를 포함하는 B7H6/CD3 결합 단백질, 및 서열 번호 230 또는 서열 번호 239의 B7H6 쇄 및 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3쇄를 포함하는 B7H6 결합 단백질)에 대한 단량체 퍼센트를 분석적 크기 배제 크로마토그래피 (aSEC)에 의해 결정하였다 (표 6에 나타냄). 단백질 BEH SEC 컬럼 200Å, 1.7 μm, 4.6x150 mm (Cat# 186005225)을 사용하여 Waters® Acquity UPLC® 시스템 상에서 SEC를 수행하였다. 전개 조건은 다음과 같다: 이동상: 50 mM 인산나트륨, 200 mM 아르기닌 및 0.05% 아지드화나트륨; 유속: 0.5 ml/분; 런타임: 5분; 샘플 로딩량: 10 μg; 피크 검출: A280 nm; 크로마토그램의 자동화 처리 방법.
|
B7H6
결합제 |
CD3
결합제 |
제1 단계 후
단량체 퍼센트 |
제2 단계 후
단량체 퍼센트 |
| B7H6#1 | CD3#1 | 70.5 | 98.5 |
| B7H6#2 | CD3#1 | 38.7 | 95.1 |
| B7H6#3 | CD3#1 | 50.1 | 96.6 |
| B7H6#4 | CD3#1 | 56.0 | 99.9 |
| B7H6#5 | CD3#1 | 66.5 | 99.3 |
| B7H6#6 | CD3#1 | 63.7 | 99.1 |
| B7H6#7 | CD3#1 | 43.4 | 97.7 |
| B7H6#8 | CD3#1 | 68.3 | 96.8 |
| B7H6#9 | CD3#1 | 61.3 | 95.7 |
| B7H6#10 | CD3#1 | 66.3 | 97.7 |
| B7H6#11 | CD3#1 | 38.2 | 95.3 |
| B7H6#12 | CD3#1 | 67.4 | 99.9 |
| B7H6#13 | CD3#1 | 61.9 | 99.9 |
| B7H6#14 | CD3#1 | 64.6 | 99.9 |
| B7H6#15 | CD3#1 | 53.8 | 99.9 |
| B7H6#16 | CD3#1 | 52.4 | 99.7 |
| B7H6#17 | CD3#1 | 46.8 | 99.9 |
| B7H6#18 | CD3#1 | 50.1 | 99.8 |
| B7H6#19 | CD3#1 | 64.1 | 99.9 |
| B7H6#20 | CD3#1 | 62.3 | 99.9 |
| B7H6#21 | CD3#1 | 60.4 | 99.9 |
| B7H6#22 | CD3#1 | 57.5 | 99.9 |
| B7H6#23 | CD3#1 | 59.5 | 99.8 |
| B7H6#24 | CD3#1 | 51.7 | 99.9 |
| B7H6#14 | CD3#2 | 71.9 | 99.9 |
| B7H6#14 | CD3#3 | 68.2 | 99.9 |
| B7H6#14 | CD3#4 | 62.2 | 99.6 |
| B7H6#14 | CD3#5 | 76.5 | 99.9 |
| B7H6#14 | CD3#6 | 70.5 | 99.9 |
| B7H6#23 | CD3#2 | 69.8 | 99.8 |
| B7H6#23 | CD3#3 | 67.3 | 99.6 |
| B7H6#23 | CD3#4 | 62.2 | 99.7 |
| B7H6#23 | CD3#5 | 75 | 99.9 |
| B7H6#23 | CD3#6 | 69.6 | 99.9 |
실시예 21: 열안정성.
열안정성을 TSA (Thermal Shift Analysis)에 의해 측정하고, B7H6/CD3 결합 단백질 (서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6 쇄 및 서열 번호 311의 CD3 쇄를 포함하는 B7H6/CD3 결합 단백질, 및 서열 번호 230 또는 서열 번호 239의 B7H6 쇄 및 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3쇄를 포함하는 B7H6 결합 단백질)의 제1 용융 전이 (Tm1)의 결과를 표 7에 나타내었다. 외인성 형광단으로서 SYPRO® 오렌지 단백질 겔 염색 (Invitrogen, Carlsbad, CA)을 갖는 QuantStudioTM 6 Flex 실시간 PCR 시스템 (Applied Biosystems, Waltham, MA)을 사용하여 온도 함수로서의 형광 강도 프로파일을 획득하였다. 샘플을 40 mM 염화나트륨 및 0.02% 아지드화나트륨을 사용하여 10 mM 히스티딘, pH 6.0에서 0.4 mg/ml로 희석하였다. 용융 곡선을 25℃에서부터 95℃까지 2℃/분의 속도의 가열 램프로 생성하고, 데이터를 'ROX' 필터 세트 (Ex: 580±10 nm, Em: 623±14 nm)를 통해 대략 0.4℃마다 수집하였다. 데이터를 Protein Thermal ShiftTM Software Version vl.3 (ThermoFisher Scientific, Waltham, MA)을 사용하여 분석하였다.
| B7H6 결합제 | CD3 결합제 | Tm1 (℃) |
| B7H6#12 | CD3#1 | 65.3 |
| B7H6#13 | CD3#1 | 65.2 |
| B7H6#14 | CD3#1 | 65.7 |
| B7H6#15 | CD3#1 | 65.4 |
| B7H6#16 | CD3#1 | 65.4 |
| B7H6#17 | CD3#1 | 65.4 |
| B7H6#18 | CD3#1 | 65.0 |
| B7H6#19 | CD3#1 | 64.0 |
| B7H6#20 | CD3#1 | 62.5 |
| B7H6#21 | CD3#1 | 64.9 |
| B7H6#22 | CD3#1 | 58.7 |
| B7H6#23 | CD3#1 | 64.7 |
| B7H6#24 | CD3#1 | 65.3 |
| B7H6#14 | CD3#2 | 61.7 |
| B7H6#14 | CD3#3 | 60.4 |
| B7H6#14 | CD3#4 | 60.3 |
| B7H6#14 | CD3#5 | 61.4 |
| B7H6#14 | CD3#6 | 61.4 |
| B7H6#23 | CD3#2 | 60.1 |
| B7H6#23 | CD3#3 | 64.9 |
| B7H6#23 | CD3#4 | 58.0 |
| B7H6#23 | CD3#5 | 57.9 |
| B7H6#23 | CD3#6 | 57.5 |
실시예 22: Epivax에 의한 인 실리코 (
in silico
) 예측 면역원성 점수.
서열의 면역원성을 수학적 알고리즘으로 인 실리코로 평가하였다. 구체적으로, 면역원성 스코어의 척도로서 EpiMatrix® Treg-조정된 스코어 (EpiVax Inc., Providence RI)를 B7H6 쇄 (서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 서열 번호 221, 서열 번호 222, 서열 번호 223, 서열 번호 224, 서열 번호 225, 서열 번호 225, 서열 번호 227, 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6 쇄) 및 CD3 쇄 (서열 번호 311, 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3 쇄)에 대해 측정하고, 다양한 Fc 서열의 스코어와 비교하였다. 이들 스코어는 T-세포 에피토프와 Treg 에피토프를 고려하고 있다. 면역원성 스코어가 낮을수록 면역원성이 될 가능성이 더 적다. 일반적으로, 음의 스코어는 낮은 면역원성의 위험으로 간주되는 반면, 높은 양의 스코어는 잠재적인 면역원성에 대한 지표로서 간주된다. 하기 표 8 및 9에 나타낸 바와 같이, 본원에 기재된 예시적인 B7H6/CD3 결합 단백질은 면역원성 점수가 매우 낮으며, 이는 이들 결합 단백질에 대해 면역원성 위험이 낮음을 나타낸다.
|
B7H6 또는 CD3
결합 단백질 |
VH | VL | 전체 폴리펩티드 쇄 (VL-CL-링커-VH-CH1-힌자-CH2-CH3) |
| B7H6#1 B7H6 쇄 | -9.94 | 17.52 | -29.07 |
| B7H6#2 B7H6 쇄 | 17.12 | 1.78 | -27.07 |
| B7H6#3 B7H6 쇄 | 67.70 | 32.77 | -11.61 |
| B7H6#4 B7H6 쇄 | -20.24 | -6.54 | -34.34 |
| B7H6#5 B7H6 쇄 | -58.29 | -29.64 | -43.99 |
| B7H6#6 B7H6 쇄 | 4.77 | -9.90 | -30.99 |
| B7H6#7 B7H6 쇄 | 16.81 | -13.51 | -28.20 |
| B7H6#8 B7H6 쇄 | -31.42 | 35.40 | -29.91 |
| B7H6#9 B7H6 쇄 | -4.61 | -4.44 | -31.45 |
| B7H6#10 B7H6 쇄 | 10.78 | 3.40 | -26.72 |
| B7H6#11 B7H6 쇄 | 4.49 | 47.21 | -22.15 |
| B7H6#12 B7H6 쇄 | -24.63 | -48.50 | -39.76 |
| B7H6#13 B7H6 쇄 | -19.87 | -48.50 | -39.00 |
| B7H6#14 B7H6 쇄 | -23.93 | -48.50 | -39.65 |
| B7H6#15 B7H6 쇄 | -19.71 | -48.50 | -38.98 |
| B7H6#16 B7H6 쇄 | -17.72 | -48.50 | -38.66 |
| B7H6#17 B7H6 쇄 | -19.71 | -48.50 | -38.98 |
| B7H6#18 B7H6 쇄 | -19.71 | -50.41 | -39.25 |
| B7H6#19 B7H6 쇄 | -22.64 | -48.50 | -39.44 |
| B7H6#20 B7H6 쇄 | -24.63 | -50.41 | -40.03 |
| B7H6#21 B7H6 쇄 | -21.94 | -48.50 | -39.33 |
| B7H6#22 B7H6 쇄 | -23.93 | -50.41 | -39.92 |
| B7H6#23 B7H6 쇄 | -21.94 | -50.41 | -39.61 |
| B7H6#24 B7H6 쇄 | -19.71 | -50.41 | -39.25 |
| CD3#1 CD3 쇄 | -9.68 | -50.52 | -35.25 |
| CD3#2 CD3 쇄 | -40.29 | -8.95 | -33.62 |
| CD3#3 CD3 쇄 | -41.48 | -4.54 | -33.15 |
| CD3#4 CD3 쇄 | -39.06 | -4.54 | -32.77 |
| CD3#5 CD3 쇄 | -55.51 | -14.24 | -36.83 |
| CD3#6 CD3 쇄 | -41.48 | -14.24 | -34.60 |
| Fc 단백질 쇄 | 조정된 Epivax 스코어 |
| Fc-IgG1-WT | -25.64 |
| Fc-IgG1-LALA | -29.83 |
| Fc-IgG1-LALA-KNOB | -31.76 |
| Fc-IgG1-LALA-HOLE | -18.01 |
실시예 23: 표면에 대한 비특이적 결합
본 발명의 B7H6/CD3 결합 단백질의 특이성을 고하전된 단백질을 이용한 표면 플라즈몬 공명 (SPR) 기반 분석으로 추가로 시험하였다. 결합 단백질이 비관련 하전 단백질에 유의적인 결합을 갖는지를 결정하기 위해 바이오센서 기술을 사용하여 비특이적 결합 분석을 개발하였다. 이 분석에서는, B7H6/CD3 결합 단백질을 2개의 SPR 표면 위에 통과시켰는데, 하나는 음으로 하전된 단백질 (트립신 억제제)로 코팅되었고, 다른 하나는 양으로 하전된 단백질 (리소자임)로 코팅되었다. 단백질이 이러한 표면에 상당한 비특이적 결합을 보이는 경우 결합의 원인은 후보에 양전하 또는 음전하를 띤 표면 패치의 존재일 가능성이 높다. 단백질의 비특이적 결합은 약동학 (PK) 및 생체 분포 불량으로 해석될 수 있으며 다운스트림 제조 가능성에 영향을 미칠 수도 있다.
실험을 Biacore® T200 SPR 시스템 (GE Healthcare Life Sciences)에서 수행하였다. 10X HBS-EP로부터 제조된 IX HBS-EP 완충액에서 25℃에서 희석, 표면 제조 및 결합 실험을 수행하였다. 고정화 프로토콜 및 결합 실험 둘 다에 대한 유속은 5 μL/분이었다.
비특이적 결합 실험을 위한 표면을 제조하기 위해, 난백 리소자임 및 글리신 맥스 대두 유래 트립신 억제제를 제조 지침에 따라 아민 커플링 키트를 사용하여 3000-5000 RU의 표면 밀도로 Biacore® series S CM5 센서 칩 (GE Healthcare sciences)에 수동으로 커플링시켰다. 샘플을 1X HBS-EP 완충액에서 1 μM로 준비하였다. 샘플을 10 분 회합 및 10 분 해리로 활성화된 표면 위에 주입하였다. Biacore® T200 Control Software version 2.0.1을 사용하여 데이터를 수집하고, Biacore® T200 Evaluation Software version 3.0 (GE Healthcare Life Sciences)을 사용하여 분석하였다.
표 10은 예시적인 B7H6/CD3 결합 단백질 (각각 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 또는 서열 번호 240의 B7H6 쇄 및 서열 번호 311의 CD3 쇄를 포함하는 B7H6 결합 단백질, 및 서열 번호 230 또는 서열 번호 239의 B7H6 쇄 및 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 또는 서열 번호 316의 CD3 쇄를 포함하는 B7H6 결합 단백질)이 고하전된 두 단백질, 트립신 억제제 및 리소자임에 결합하지 않거나 매우 적게 결합함을 나타낸다.
| B7H6 결합제 | CD3 결합제 | 비특이적 결합(RU), 리소자임(양성) | 비특이적 결합(RU), Tryp 억제제(음성) |
| B7H6#12 | CD3#1 | 9.2 | 35.4 |
| B7H6#13 | CD3#1 | 7.2 | 30.6 |
| B7H6#14 | CD3#1 | 8.1 | 32.7 |
| B7H6#15 | CD3#1 | 7.2 | 32.8 |
| B7H6#16 | CD3#1 | 8.2 | 42.6 |
| B7H6#17 | CD3#1 | 15.3 | 88.4 |
| B7H6#18 | CD3#1 | 6.6 | 32.8 |
| B7H6#19 | CD3#1 | 8.2 | 40.3 |
| B7H6#20 | CD3#1 | 9.8 | 48.4 |
| B7H6#21 | CD3#1 | 8.1 | 42 |
| B7H6#22 | CD3#1 | 7.8 | 39.5 |
| B7H6#23 | CD3#1 | 8.1 | 45.7 |
| B7H6#24 | CD3#1 | 7.9 | 43.5 |
| B7H6#14 | CD3#2 | 11.2 | 12.2 |
| B7H6#14 | CD3#3 | 12.4 | 26.4 |
| B7H6#14 | CD3#4 | 8.8 | 22.6 |
| B7H6#14 | CD3#5 | 16.2 | 109.6 |
| B7H6#14 | CD3#6 | 15.7 | 34 |
| B7H6#23 | CD3#2 | 37.8 | 47.8 |
| B7H6#23 | CD3#3 | 18.9 | 38.7 |
| B7H6#23 | CD3#4 | 6.8 | 20.7 |
| B7H6#23 | CD3#5 | 15 | 114.7 |
| B7H6#23 | CD3#6 | 57.2 | 96.5 |
실시예 24: SHP77 이종이식 종양 조직에서 예시적인 B7H6/CD3 결합 단백질의 T 세포 침윤
실시예 19에 기재된 연구에서 마우스로부터의 나머지 종양 조직을 준비하여 포르말린에 고정시키고, 파라핀에 포매하였다. 이어서, 조직 절편을 제조하고, T 세포 상의 CD3 발현을 위해 염색하였다 (항-CD3 (2GV6), Ventana Medical Systems). NCI-H716 이종이식 종양 조직에서 예시적인 B7H6/CD3 결합 단백질의 T 세포 침윤을 도 21에 나타내었다. 표 11의 스코어링을 사용하여 이종이식 종양 조직에서의 CD3 발현을 정량화하였다.
| 스코어 | 설명 |
| 0 | HPF당 < 5 CD3-양성 T-세포 (고배율 시야) |
| 1 | HPF당 5-99 CD3-양성 T-세포 (고배율 시야) |
| 2 | HPF당 100-200 CD3-양성 T-세포 (고배율 시야) |
| 3 | HPF당 > 300 CD3 양성 T 세포 (고배율 시야) |
실시예 25: i.v 투여용 약학적 제형
본 발명의 상기 임의의 결합 단백질/분자가 i.v. 적용 약학적 제형의 제조를 위해 선택될 수 있다. 본 발명의 항체에 적합한 약학적 제형의 예는 다음과 같다.
10 mL 바이알이 히스티딘, 트레할로스, 폴리소르베이트 20 및 주사용수를 포함하는 완충액 중에 본 발명의 B7H6/CD3 결합 분자/단백질을 10 mg/mL로 함유한다.
SEQUENCE LISTING
<110> Boehringer Ingelheim International GmbH
<120> Multi-specific binding proteins for cancer treatment
<130> 12-0442-WO-1
<160> 340
<170> BiSSAP 1.3.6
<210> 1
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#1 LCCDR1
<400> 1
Lys Ser Ser Gln Ser Leu Phe Tyr Ser Ser Asn Gln Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 2
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#1 LCCDR2
<400> 2
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 3
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#1 LCCDR3
<400> 3
Gln Gln Tyr Tyr Asn Tyr Pro Arg Thr
1 5
<210> 4
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#1 HCCDR1
<400> 4
Gly Tyr Thr Phe Thr Asp Tyr Tyr Met Asn
1 5 10
<210> 5
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#1 HCCDR2
<400> 5
Tyr Ile Tyr Pro Lys Thr Gly Gly Asn Gly Tyr Asn Gln Lys Phe Lys
1 5 10 15
Asp
<210> 6
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#1 HCCDR3
<400> 6
Glu Asn Trp Asp Gly Tyr Thr Met Ala Tyr
1 5 10
<210> 7
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#2 LCCDR1
<400> 7
Arg Ala Thr Ser Ser Leu Tyr Ser Met His
1 5 10
<210> 8
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#2 LCCDR2
<400> 8
Ala Thr Phe Asn Leu Ala Ser
1 5
<210> 9
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#2 LCCDR3
<400> 9
Gln Gln Trp Ser Thr Asn Pro Pro Lys Leu Thr
1 5 10
<210> 10
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#2 HCCDR1
<400> 10
Gly Phe Asn Ile Lys Asn Thr Phe Ile His
1 5 10
<210> 11
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#2 HCCDR2
<400> 11
Arg Ile Asp Pro Ala Asn Gly Asn Thr Ile Tyr Ala Ser Lys Phe Gln
1 5 10 15
Gly
<210> 12
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#2 HCCDR3
<400> 12
Thr Tyr Gly Gly Thr Asn Tyr Phe Asp Tyr
1 5 10
<210> 13
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#3 LCCDR1
<400> 13
Lys Ala Ser His Asn Val Gly Val Tyr Val Ala
1 5 10
<210> 14
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#3 LCCDR2
<400> 14
Ser Ala Ser Asn Arg Tyr Ser
1 5
<210> 15
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#3 LCCDR3
<400> 15
Gln Gln Tyr Asn Ser Tyr Pro Leu Thr
1 5
<210> 16
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#3 HCCDR1
<400> 16
Gly Phe Thr Phe Ser Asp Tyr Tyr Met Thr
1 5 10
<210> 17
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#3 HCCDR2
<400> 17
Asn Ile Asp Tyr Asp Gly Ser Arg Ile Tyr Tyr Leu Asp Ser Leu Lys
1 5 10 15
Ser
<210> 18
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#3 HCCDR3
<400> 18
Asp Asp Pro Ala Trp Leu Ala Tyr
1 5
<210> 19
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#4 LCCDR1
<400> 19
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 20
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#4 LCCDR2
<400> 20
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 21
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#4 LCCDR3
<400> 21
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 22
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#4 HCCDR1
<400> 22
Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn
1 5 10
<210> 23
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#4 HCCDR2
<400> 23
Gly Ile Tyr Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 24
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#4 HCCDR3
<400> 24
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 25
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#5 LCCDR1
<400> 25
Arg Ala Ser Gln Asp Ile Arg Asn Asp Leu Gly
1 5 10
<210> 26
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#5 LCCDR2
<400> 26
Ala Ala Ser Ser Leu Glu Ser
1 5
<210> 27
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#5 LCCDR3
<400> 27
Leu Gln Tyr Tyr Asn His Pro Leu Thr
1 5
<210> 28
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#5 HCCDR1
<400> 28
Gly Tyr Thr Phe Thr Gly Tyr Tyr Ile His
1 5 10
<210> 29
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#5 HCCDR2
<400> 29
Trp Ile Asn Pro His Ser Gly Ala Thr Asn Tyr Ala Gln Asn Phe Gln
1 5 10 15
Gly
<210> 30
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#5 HCCDR3
<400> 30
Glu Arg Trp Gly Ser Gly Thr Phe Asn Ile
1 5 10
<210> 31
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#6 LCCDR1
<400> 31
Lys Ala Ser Gln Ser Val Ser Asn Asp Val Val
1 5 10
<210> 32
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#6 LCCDR2
<400> 32
Ser Thr Ser Asn Arg Tyr Ile
1 5
<210> 33
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#6 LCCDR3
<400> 33
Gln Gln Asp Tyr Ser Ser Pro Tyr Thr
1 5
<210> 34
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#6 HCCDR1
<400> 34
Gly Tyr Thr Phe Thr Asp Tyr Thr Met His
1 5 10
<210> 35
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#6 HCCDR2
<400> 35
Gly Ile Asn Pro Asn Tyr Asp Asn Thr Gly Tyr Ser Glu Lys Phe Lys
1 5 10 15
Asp
<210> 36
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#6 HCCDR3
<400> 36
Ser Gly Ser Arg Arg Ser Phe Tyr Phe Asp Tyr
1 5 10
<210> 37
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#7 LCCDR1
<400> 37
Arg Ala Ser Gln Gly Ile Ser Ser Trp Leu Ala
1 5 10
<210> 38
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#7 LCCDR2
<400> 38
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 39
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#7 LCCDR3
<400> 39
Gln Gln Ala Asn Ser Phe Pro Arg Thr
1 5
<210> 40
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#7 HCCDR1
<400> 40
Gly Gly Ser Ile Ser Tyr Asn Tyr Trp Ser
1 5 10
<210> 41
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#7 HCCDR2
<400> 41
His Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 42
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#7 HCCDR3
<400> 42
Val Gly Thr Trp Gly Ser Phe Asp Asp
1 5
<210> 43
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#8 LCCDR1
<400> 43
Arg Ser Ser Gln Ser Leu Leu Tyr Asn Asn Arg Tyr Asn Tyr Leu Asp
1 5 10 15
<210> 44
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#8 LCCDR2
<400> 44
Leu Gly Ser Asn Arg Ala Ser
1 5
<210> 45
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#8 LCCDR3
<400> 45
Met Gln Thr Leu Gln Ile Pro Ile Thr
1 5
<210> 46
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#8 HCCDR1
<400> 46
Gly Asp Thr Leu Asn Ser Tyr Gly Ile Ser
1 5 10
<210> 47
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#8 HCCDR2
<400> 47
Gly Ile Ile Pro Ile Phe Asp Thr Thr Lys Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 48
<211> 18
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#8 HCCDR3
<400> 48
Glu Arg Gly Tyr Arg Phe Ser Glu Asp Tyr Tyr Phe Tyr Tyr Gly Met
1 5 10 15
Asp Val
<210> 49
<211> 15
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#9 LCCDR1
<400> 49
Arg Ala Ser Glu Ser Val Asp Asn Phe Gly Val Ser Phe Met Asn
1 5 10 15
<210> 50
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#9 LCCDR2
<400> 50
Ala Ala Ser Asn Gln Gly Ser
1 5
<210> 51
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#9 LCCDR3
<400> 51
Gln Gln Ser Lys Glu Val Pro Trp Thr
1 5
<210> 52
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#9 HCCDR1
<400> 52
Asp Tyr Thr Phe Thr His Tyr Trp Ile His
1 5 10
<210> 53
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#9 HCCDR2
<400> 53
Ile Ile Gly Pro Ser Asp Asn Glu Ile His Tyr Asn Gln Asp Phe Lys
1 5 10 15
Asp
<210> 54
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#9 HCCDR3
<400> 54
Gln Ile Ile Ser Met Val Val Gly Thr Glu Tyr Phe Asp Val
1 5 10
<210> 55
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#10 LCCDR1
<400> 55
Arg Ala Ser Gln Gly Ile Ser Ser Trp Leu Ala
1 5 10
<210> 56
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#10 LCCDR2
<400> 56
Val Ala Ser Ser Leu Gln Arg
1 5
<210> 57
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#10 LCCDR3
<400> 57
Gln Gln Ala Asn Ser Phe Pro Arg Thr
1 5
<210> 58
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#10 HCCDR1
<400> 58
Gly Asp Ser Ile Ser Ser Tyr Tyr Trp Ser
1 5 10
<210> 59
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#10 HCCDR2
<400> 59
His Ile Tyr Thr Ser Glu Lys Asn Asn Tyr Asn Pro Ser Leu Lys Ser
1 5 10 15
<210> 60
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#10 HCCDR3
<400> 60
Val Gly Asn Trp Gly Ser His Asp Ala
1 5
<210> 61
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#11 LCCDR1
<400> 61
Arg Ser Ser Gln Ser Leu Leu His Ser Asn Gly Tyr Asn Tyr Leu Asp
1 5 10 15
<210> 62
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#11 LCCDR2
<400> 62
Leu Gly Ser Asn Arg Ala Ser
1 5
<210> 63
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#11 LCCDR3
<400> 63
Met Gln Ala Leu Gln Thr Pro Leu Thr
1 5
<210> 64
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#11 HCCDR1
<400> 64
Gly Ile Thr Phe Ser Tyr Tyr Thr Met Asn
1 5 10
<210> 65
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#11 HCCDR2
<400> 65
Ser Ile Ser Ser Arg Ser Ser Tyr Ile Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 66
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#11 HCCDR3
<400> 66
Asp Lys Gly Asp Tyr Ser Lys Asp Ile Tyr Tyr Tyr Tyr Gly Met Asp
1 5 10 15
Val
<210> 67
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#12 LCCDR1
<400> 67
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 68
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#12 LCCDR2
<400> 68
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 69
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#12 LCCDR3
<400> 69
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 70
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#12 HCCDR1
<400> 70
Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn
1 5 10
<210> 71
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#12 HCCDR2
<400> 71
Gly Ile Tyr Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 72
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#12 HCCDR3
<400> 72
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 73
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#13 LCCDR1
<400> 73
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 74
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#13 LCCDR2
<400> 74
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 75
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#13 LCCDR3
<400> 75
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 76
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#13 HCCDR1
<400> 76
Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn
1 5 10
<210> 77
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#13 HCCDR2
<400> 77
Gly Ile Tyr Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 78
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#13 HCCDR3
<400> 78
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 79
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#14 LCCDR1
<400> 79
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 80
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#14 LCCDR2
<400> 80
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 81
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#14 LCCDR3
<400> 81
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 82
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#14 HCCDR1
<400> 82
Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn
1 5 10
<210> 83
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#14 HCCDR2
<400> 83
Gly Ile Tyr Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 84
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#14 HCCDR3
<400> 84
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 85
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#15 LCCDR1
<400> 85
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 86
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#15 LCCDR2
<400> 86
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 87
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#15 LCCDR3
<400> 87
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 88
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#15 HCCDR1
<400> 88
Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn
1 5 10
<210> 89
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#15 HCCDR2
<400> 89
Gly Ile Tyr Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 90
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#15 HCCDR3
<400> 90
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 91
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#16 LCCDR1
<400> 91
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 92
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#16 LCCDR2
<400> 92
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 93
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#16 LCCDR3
<400> 93
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 94
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#16 HCCDR1
<400> 94
Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn
1 5 10
<210> 95
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#16 HCCDR2
<400> 95
Gly Ile Tyr Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 96
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#16 HCCDR3
<400> 96
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 97
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#17 LCCDR1
<400> 97
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 98
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#17 LCCDR2
<400> 98
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 99
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#17 LCCDR3
<400> 99
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 100
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#17 HCCDR1
<400> 100
Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn
1 5 10
<210> 101
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#17 HCCDR2
<400> 101
Gly Ile Tyr Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 102
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#17 HCCDR3
<400> 102
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 103
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#18 LCCDR1
<400> 103
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 104
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#18 LCCDR2
<400> 104
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 105
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#18 LCCDR3
<400> 105
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 106
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#18 HCCDR1
<400> 106
Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn
1 5 10
<210> 107
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#18 HCCDR2
<400> 107
Gly Ile Tyr Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 108
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#18 HCCDR3
<400> 108
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 109
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#19 LCCDR1
<400> 109
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 110
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#19 LCCDR2
<400> 110
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 111
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#19 LCCDR3
<400> 111
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 112
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#19 HCCDR1
<400> 112
Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn
1 5 10
<210> 113
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#19 HCCDR2
<400> 113
Gly Ile Tyr Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 114
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#19 HCCDR3
<400> 114
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 115
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#20 LCCDR1
<400> 115
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 116
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#20 LCCDR2
<400> 116
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 117
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#20 LCCDR3
<400> 117
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 118
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#20 HCCDR1
<400> 118
Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn
1 5 10
<210> 119
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#20 HCCDR2
<400> 119
Gly Ile Tyr Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 120
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#20 HCCDR3
<400> 120
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 121
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#21 LCCDR1
<400> 121
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 122
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#21 LCCDR2
<400> 122
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 123
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#21 LCCDR3
<400> 123
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 124
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#21 HCCDR1
<400> 124
Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn
1 5 10
<210> 125
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#21 HCCDR2
<400> 125
Gly Ile Tyr Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 126
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#21 HCCDR3
<400> 126
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 127
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#22 LCCDR1
<400> 127
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 128
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#22 LCCDR2
<400> 128
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 129
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#22 LCCDR3
<400> 129
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 130
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#22 HCCDR1
<400> 130
Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn
1 5 10
<210> 131
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#22 HCCDR2
<400> 131
Gly Ile Tyr Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 132
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#22 HCCDR3
<400> 132
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 133
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#23 LCCDR1
<400> 133
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 134
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#23 LCCDR2
<400> 134
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 135
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#23 LCCDR3
<400> 135
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 136
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#23 HCCDR1
<400> 136
Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn
1 5 10
<210> 137
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#23 HCCDR2
<400> 137
Gly Ile Tyr Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 138
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#23 HCCDR3
<400> 138
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 139
<211> 11
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#24 LCCDR1
<400> 139
Lys Ala Ser Gln Asn Val Gly Lys Tyr Val Ala
1 5 10
<210> 140
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#24 LCCDR2
<400> 140
Ser Ala Ser Asn Arg Tyr Asp
1 5
<210> 141
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#24 LCCDR3
<400> 141
Gln Gln Tyr Ile Ser Tyr Pro Leu Thr
1 5
<210> 142
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#24 HCCDR1
<400> 142
Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn
1 5 10
<210> 143
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#24 HCCDR2
<400> 143
Gly Ile Tyr Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys
1 5 10 15
Gly
<210> 144
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#24 HCCDR3
<400> 144
Arg Gly Asp Tyr Phe Gly Asp Phe
1 5
<210> 145
<211> 113
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#1 VL
<400> 145
Asp Ile Val Met Ser Gln Ser Pro Ser Ser Leu Ala Val Ser Val Gly
1 5 10 15
Glu Lys Val Thr Met Asn Cys Lys Ser Ser Gln Ser Leu Phe Tyr Ser
20 25 30
Ser Asn Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Lys Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Asn Tyr Pro Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys
<210> 146
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#1 VH
<400> 146
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro Gly Thr
1 5 10 15
Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Tyr Met Asn Trp Val Lys Gln Ser Gln Gly Lys Asn Leu Glu Trp Ile
35 40 45
Ala Tyr Ile Tyr Pro Lys Thr Gly Gly Asn Gly Tyr Asn Gln Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Asn Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Gly Arg Glu Asn Trp Asp Gly Tyr Thr Met Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Ser Val Thr Val Ser Ser
115
<210> 147
<211> 108
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#2 VL
<400> 147
Glu Ile Val Leu Thr Gln Ser Pro Asp Phe Leu Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Thr Ser Ser Leu Tyr Ser Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Pro Trp Ile Tyr
35 40 45
Ala Thr Phe Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Thr Arg Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Thr Asn Pro Pro Lys
85 90 95
Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 148
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#2 VH
<400> 148
Glu Val Gln Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Thr Ala Ser Gly Phe Asn Ile Lys Asn Thr
20 25 30
Phe Ile His Trp Val Asn Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile
35 40 45
Gly Arg Ile Asp Pro Ala Asn Gly Asn Thr Ile Tyr Ala Ser Lys Phe
50 55 60
Gln Gly Arg Ala Thr Ile Thr Thr Asp Thr Ser Ser Asn Thr Ala Tyr
65 70 75 80
Met His Leu Ser Ser Leu Thr Ser Gly Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Thr Tyr Gly Gly Thr Asn Tyr Phe Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Leu Thr Val Ser Ser
115
<210> 149
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#3 VL
<400> 149
Asp Ile Val Met Thr Gln Ser Gln Lys Leu Leu Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Ile Ser Val Thr Cys Lys Ala Ser His Asn Val Gly Val Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly His Ser Pro Lys Ala Leu Ile
35 40 45
His Ser Ala Ser Asn Arg Tyr Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Asn Val Gln Ser
65 70 75 80
Glu Asp Leu Ala Glu Tyr Phe Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Ile
100 105
<210> 150
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#3 VH
<400> 150
Glu Val Lys Leu Val Glu Ser Glu Gly Gly Leu Val Gln Pro Gly Ser
1 5 10 15
Ser Met Lys Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Asp Tyr
20 25 30
Tyr Met Thr Trp Val Arg Gln Val Pro Glu Lys Gly Leu Glu Trp Val
35 40 45
Gly Asn Ile Asp Tyr Asp Gly Ser Arg Ile Tyr Tyr Leu Asp Ser Leu
50 55 60
Lys Ser Arg Phe Ile Ile Ser Arg Asp Asn Ala Lys Asn Ile Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Ser Glu Asp Thr Ala Thr Tyr Tyr Cys
85 90 95
Ala Arg Asp Asp Pro Ala Trp Leu Ala Tyr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 151
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#4 VL
<400> 151
Asp Ile Val Met Thr Gln Ser Gln Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Val Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Ala Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Asn Val Gln Ser
65 70 75 80
Glu Asp Leu Thr Glu Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys
100 105
<210> 152
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#4 VH
<400> 152
Gln Val Gln Leu Gln Gln Pro Gly Ser Val Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Arg Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met Asn Trp Met Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile Tyr Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Leu Thr Val Asp Thr Ser Ser Ser Thr Thr Tyr
65 70 75 80
Met Asp Leu Ser Ser Leu Thr Tyr Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Thr Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Thr
100 105 110
Leu Thr Val Ser Ser
115
<210> 153
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#5 VL
<400> 153
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn Asp
20 25 30
Leu Gly Trp Phe Gln Gln Arg Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Arg Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Tyr Asn His Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105
<210> 154
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#5 VH
<400> 154
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Ile His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Asn Pro His Ser Gly Ala Thr Asn Tyr Ala Gln Asn Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Ser Arg Leu Arg Ser Asp Asp Ala Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Arg Trp Gly Ser Gly Thr Phe Asn Ile Trp Gly Gln Gly
100 105 110
Thr Met Val Thr Val Ser Ser
115
<210> 155
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#6 VL
<400> 155
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Pro Val Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Ser Asn Asp
20 25 30
Val Val Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Met
35 40 45
Tyr Ser Thr Ser Asn Arg Tyr Ile Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Ser Thr Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Phe Cys Gln Gln Asp Tyr Ser Ser Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 156
<211> 120
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#6 VH
<400> 156
Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Leu Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Ile Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Asp Tyr
20 25 30
Thr Met His Trp Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile
35 40 45
Gly Gly Ile Asn Pro Asn Tyr Asp Asn Thr Gly Tyr Ser Glu Lys Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Glu Leu Arg Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Ser Gly Ser Arg Arg Ser Phe Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Thr Leu Thr Val Ser Ser
115 120
<210> 157
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#7 VL
<400> 157
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 158
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#7 VH
<400> 158
Gln Val Gln Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Tyr Thr Val Ser Gly Gly Ser Ile Ser Tyr Asn
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Pro Glu Lys Gly Leu Glu Trp Ile
35 40 45
Gly His Ile Tyr Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Thr Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Lys Leu Asn Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Val Gly Thr Trp Gly Ser Phe Asp Asp Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 159
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#8 VL
<400> 159
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu Tyr Asn
20 25 30
Asn Arg Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Glu Val Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Phe Gly Val Tyr Tyr Cys Met Gln Thr
85 90 95
Leu Gln Ile Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105 110
<210> 160
<211> 127
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#8 VH
<400> 160
Gln Val Gln Val Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ser
1 5 10 15
Ser Val Lys Val Ser Cys Lys Gly Ser Gly Asp Thr Leu Asn Ser Tyr
20 25 30
Gly Ile Ser Trp Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Ile Pro Ile Phe Asp Thr Thr Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Thr Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Phe Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Glu Arg Gly Tyr Arg Phe Ser Glu Asp Tyr Tyr Phe Tyr Tyr
100 105 110
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 161
<211> 111
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#9 VL
<400> 161
Asp Ile Val Leu Thr Gln Ser Pro Val Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Asn Phe
20 25 30
Gly Val Ser Phe Met Asn Trp Phe Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Gln Gly Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ser Leu Asn Ile His
65 70 75 80
Pro Leu Glu Glu Asp Asp Thr Ala Met Tyr Phe Cys Gln Gln Ser Lys
85 90 95
Glu Val Pro Trp Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys
100 105 110
<210> 162
<211> 123
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#9 VH
<400> 162
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Met Val Arg Pro Gly Ser
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Asp Tyr Thr Phe Thr His Tyr
20 25 30
Trp Ile His Trp Val Lys Gln Arg Pro Leu Glu Gly Leu Glu Trp Ile
35 40 45
Gly Ile Ile Gly Pro Ser Asp Asn Glu Ile His Tyr Asn Gln Asp Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Asn Thr Ala Tyr
65 70 75 80
Leu His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Gln Ile Ile Ser Met Val Val Gly Thr Glu Tyr Phe Asp Val
100 105 110
Trp Gly Thr Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 163
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#10 VL
<400> 163
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Val Ala Ser Ser Leu Gln Arg Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Asn Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 164
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#10 VH
<400> 164
Gln Val His Leu Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu
1 5 10 15
Thr Leu Ser Leu Thr Cys Thr Val Ser Gly Asp Ser Ile Ser Ser Tyr
20 25 30
Tyr Trp Ser Trp Ile Arg Gln Pro Ala Gly Lys Gly Leu Glu Trp Ile
35 40 45
Gly His Ile Tyr Thr Ser Glu Lys Asn Asn Tyr Asn Pro Ser Leu Lys
50 55 60
Ser Arg Val Ile Met Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu
65 70 75 80
Asn Leu Ser Ser Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala
85 90 95
Arg Val Gly Asn Trp Gly Ser His Asp Ala Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 165
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#11 VL
<400> 165
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Val Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
<210> 166
<211> 126
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#11 VH
<400> 166
Glu Leu Gln Leu Val Asn Ser Gly Gly Gly Leu Val Lys Ser Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Thr Phe Ser Tyr Tyr
20 25 30
Thr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ser Ile Ser Ser Arg Ser Ser Tyr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Glu Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Lys Gly Asp Tyr Ser Lys Asp Ile Tyr Tyr Tyr Tyr Gly
100 105 110
Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 167
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#12 VL
<400> 167
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 168
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#12 VH
<400> 168
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 169
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#13 VL
<400> 169
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 170
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#13 VH
<400> 170
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 171
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#14 VL
<400> 171
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 172
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#14 VH
<400> 172
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met Asn Trp Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile Tyr Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Val Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 173
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#15 VL
<400> 173
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 174
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#15 VH
<400> 174
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met Asn Trp Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 175
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#16 VL
<400> 175
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 176
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#16 VH
<400> 176
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 177
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#17 VL
<400> 177
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 178
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#17 VH
<400> 178
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 179
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#18 VL
<400> 179
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 180
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#18 VH
<400> 180
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 181
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#19 VL
<400> 181
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 182
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#19 VH
<400> 182
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 183
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#20 VL
<400> 183
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 184
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#20 VH
<400> 184
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Ala Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 185
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#21 VL
<400> 185
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 186
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#21 VH
<400> 186
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile Tyr Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Val Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 187
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#22 VL
<400> 187
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 188
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#22 VH
<400> 188
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile Tyr Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Val Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 189
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#23 VL
<400> 189
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 190
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#23 VH
<400> 190
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Met Asn Trp Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Gly Ile Tyr Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Lys Val Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 191
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#24 VL
<400> 191
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 192
<211> 117
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#24 VH
<400> 192
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr
20 25 30
Trp Met Asn Trp Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Gly Ile Tyr Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe
50 55 60
Lys Gly Arg Val Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Arg Gly Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 193
<211> 480
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#1 scFab
<400> 193
Asp Ile Val Met Ser Gln Ser Pro Ser Ser Leu Ala Val Ser Val Gly
1 5 10 15
Glu Lys Val Thr Met Asn Cys Lys Ser Ser Gln Ser Leu Phe Tyr Ser
20 25 30
Ser Asn Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Lys Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Asn Tyr Pro Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly
210 215 220
Ser Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu
225 230 235 240
Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly
245 250 255
Gly Ser Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro
260 265 270
Gly Thr Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr
275 280 285
Asp Tyr Tyr Met Asn Trp Val Lys Gln Ser Gln Gly Lys Asn Leu Glu
290 295 300
Trp Ile Ala Tyr Ile Tyr Pro Lys Thr Gly Gly Asn Gly Tyr Asn Gln
305 310 315 320
Lys Phe Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Asn Thr
325 330 335
Ala Tyr Met Glu Leu Arg Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr
340 345 350
Tyr Cys Gly Arg Glu Asn Trp Asp Gly Tyr Thr Met Ala Tyr Trp Gly
355 360 365
Gln Gly Thr Ser Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
370 375 380
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
385 390 395 400
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
405 410 415
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
420 425 430
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
435 440 445
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
450 455 460
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
465 470 475 480
<210> 194
<211> 475
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#2 scFab
<400> 194
Glu Ile Val Leu Thr Gln Ser Pro Asp Phe Leu Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Thr Ser Ser Leu Tyr Ser Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Pro Trp Ile Tyr
35 40 45
Ala Thr Phe Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Thr Arg Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Thr Asn Pro Pro Lys
85 90 95
Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser
210 215 220
Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly
225 230 235 240
Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Glu Val Gln
245 250 255
Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala Ser Val Lys
260 265 270
Leu Ser Cys Thr Ala Ser Gly Phe Asn Ile Lys Asn Thr Phe Ile His
275 280 285
Trp Val Asn Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile Gly Arg Ile
290 295 300
Asp Pro Ala Asn Gly Asn Thr Ile Tyr Ala Ser Lys Phe Gln Gly Arg
305 310 315 320
Ala Thr Ile Thr Thr Asp Thr Ser Ser Asn Thr Ala Tyr Met His Leu
325 330 335
Ser Ser Leu Thr Ser Gly Asp Thr Ala Val Tyr Tyr Cys Ala Arg Thr
340 345 350
Tyr Gly Gly Thr Asn Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Thr Leu
355 360 365
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
370 375 380
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
385 390 395 400
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
405 410 415
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
420 425 430
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
435 440 445
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
450 455 460
Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
465 470 475
<210> 195
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#3 scFab
<400> 195
Asp Ile Val Met Thr Gln Ser Gln Lys Leu Leu Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Ile Ser Val Thr Cys Lys Ala Ser His Asn Val Gly Val Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly His Ser Pro Lys Ala Leu Ile
35 40 45
His Ser Ala Ser Asn Arg Tyr Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Asn Val Gln Ser
65 70 75 80
Glu Asp Leu Ala Glu Tyr Phe Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Ile Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Glu Val Lys Leu
245 250 255
Val Glu Ser Glu Gly Gly Leu Val Gln Pro Gly Ser Ser Met Lys Leu
260 265 270
Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Asp Tyr Tyr Met Thr Trp
275 280 285
Val Arg Gln Val Pro Glu Lys Gly Leu Glu Trp Val Gly Asn Ile Asp
290 295 300
Tyr Asp Gly Ser Arg Ile Tyr Tyr Leu Asp Ser Leu Lys Ser Arg Phe
305 310 315 320
Ile Ile Ser Arg Asp Asn Ala Lys Asn Ile Leu Tyr Leu Gln Met Asn
325 330 335
Ser Leu Lys Ser Glu Asp Thr Ala Thr Tyr Tyr Cys Ala Arg Asp Asp
340 345 350
Pro Ala Trp Leu Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 196
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#4 scFab
<400> 196
Asp Ile Val Met Thr Gln Ser Gln Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Val Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Ala Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Asn Val Gln Ser
65 70 75 80
Glu Asp Leu Thr Glu Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Gln Gln Pro Gly Ser Val Leu Val Arg Pro Gly Ala Ser Val Arg Leu
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn Trp
275 280 285
Met Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile Gly Gly Ile Tyr
290 295 300
Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Ala
305 310 315 320
Thr Leu Thr Val Asp Thr Ser Ser Ser Thr Thr Tyr Met Asp Leu Ser
325 330 335
Ser Leu Thr Tyr Glu Asp Ser Ala Val Tyr Tyr Cys Thr Thr Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 197
<211> 474
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#5 scFab
<400> 197
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn Asp
20 25 30
Leu Gly Trp Phe Gln Gln Arg Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Arg Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Tyr Asn His Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Ile His Trp
275 280 285
Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn
290 295 300
Pro His Ser Gly Ala Thr Asn Tyr Ala Gln Asn Phe Gln Gly Arg Val
305 310 315 320
Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr Met Glu Leu Ser
325 330 335
Arg Leu Arg Ser Asp Asp Ala Ala Val Tyr Tyr Cys Ala Arg Glu Arg
340 345 350
Trp Gly Ser Gly Thr Phe Asn Ile Trp Gly Gln Gly Thr Met Val Thr
355 360 365
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
370 375 380
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
385 390 395 400
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
405 410 415
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
420 425 430
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
435 440 445
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
450 455 460
Val Asp Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 198
<211> 475
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#6 scFab
<400> 198
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Pro Val Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Ser Asn Asp
20 25 30
Val Val Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Met
35 40 45
Tyr Ser Thr Ser Asn Arg Tyr Ile Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Ser Thr Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Phe Cys Gln Gln Asp Tyr Ser Ser Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Glu Val Gln Leu
245 250 255
Gln Gln Ser Gly Pro Glu Leu Leu Lys Pro Gly Ala Ser Val Lys Ile
260 265 270
Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Asp Tyr Thr Met His Trp
275 280 285
Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile Gly Gly Ile Asn
290 295 300
Pro Asn Tyr Asp Asn Thr Gly Tyr Ser Glu Lys Phe Lys Asp Lys Ala
305 310 315 320
Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr Met Glu Leu Arg
325 330 335
Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Thr Arg Ser Gly
340 345 350
Ser Arg Arg Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Thr Leu
355 360 365
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
370 375 380
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
385 390 395 400
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
405 410 415
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
420 425 430
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
435 440 445
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
450 455 460
Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
465 470 475
<210> 199
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#7 scFab
<400> 199
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu
260 265 270
Thr Tyr Thr Val Ser Gly Gly Ser Ile Ser Tyr Asn Tyr Trp Ser Trp
275 280 285
Ile Arg Gln Pro Pro Glu Lys Gly Leu Glu Trp Ile Gly His Ile Tyr
290 295 300
Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr
305 310 315 320
Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Asn Ser
325 330 335
Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Val Gly Thr
340 345 350
Trp Gly Ser Phe Asp Asp Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 200
<211> 487
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#8 scFab
<400> 200
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu Tyr Asn
20 25 30
Asn Arg Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Glu Val Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Phe Gly Val Tyr Tyr Cys Met Gln Thr
85 90 95
Leu Gln Ile Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Gln Val Gln Val Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
260 265 270
Ser Ser Val Lys Val Ser Cys Lys Gly Ser Gly Asp Thr Leu Asn Ser
275 280 285
Tyr Gly Ile Ser Trp Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
290 295 300
Met Gly Gly Ile Ile Pro Ile Phe Asp Thr Thr Lys Tyr Ala Gln Lys
305 310 315 320
Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Thr Thr Val
325 330 335
Tyr Met Glu Leu Ser Ser Leu Arg Phe Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Glu Arg Gly Tyr Arg Phe Ser Glu Asp Tyr Tyr Phe Tyr
355 360 365
Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
370 375 380
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
385 390 395 400
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
405 410 415
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
420 425 430
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
435 440 445
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
450 455 460
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
465 470 475 480
Arg Val Glu Pro Lys Ser Cys
485
<210> 201
<211> 482
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#9 scFab
<400> 201
Asp Ile Val Leu Thr Gln Ser Pro Val Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Asn Phe
20 25 30
Gly Val Ser Phe Met Asn Trp Phe Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Gln Gly Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ser Leu Asn Ile His
65 70 75 80
Pro Leu Glu Glu Asp Asp Thr Ala Met Tyr Phe Cys Gln Gln Ser Lys
85 90 95
Glu Val Pro Trp Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu
210 215 220
Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys
225 230 235 240
Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser
245 250 255
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Met Val Arg Pro Gly Ser
260 265 270
Ser Val Lys Leu Ser Cys Lys Ala Ser Asp Tyr Thr Phe Thr His Tyr
275 280 285
Trp Ile His Trp Val Lys Gln Arg Pro Leu Glu Gly Leu Glu Trp Ile
290 295 300
Gly Ile Ile Gly Pro Ser Asp Asn Glu Ile His Tyr Asn Gln Asp Phe
305 310 315 320
Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Asn Thr Ala Tyr
325 330 335
Leu His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
340 345 350
Ala Arg Gln Ile Ile Ser Met Val Val Gly Thr Glu Tyr Phe Asp Val
355 360 365
Trp Gly Thr Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly
370 375 380
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
385 390 395 400
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
405 410 415
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
420 425 430
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
435 440 445
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
450 455 460
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
465 470 475 480
Ser Cys
<210> 202
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#10 scFab
<400> 202
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Val Ala Ser Ser Leu Gln Arg Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Asn Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val His Leu
245 250 255
Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu
260 265 270
Thr Cys Thr Val Ser Gly Asp Ser Ile Ser Ser Tyr Tyr Trp Ser Trp
275 280 285
Ile Arg Gln Pro Ala Gly Lys Gly Leu Glu Trp Ile Gly His Ile Tyr
290 295 300
Thr Ser Glu Lys Asn Asn Tyr Asn Pro Ser Leu Lys Ser Arg Val Ile
305 310 315 320
Met Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Asn Leu Ser Ser
325 330 335
Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Val Gly Asn
340 345 350
Trp Gly Ser His Asp Ala Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 203
<211> 486
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#11 scFab
<400> 203
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Val Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Glu Leu Gln Leu Val Asn Ser Gly Gly Gly Leu Val Lys Ser Gly
260 265 270
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Thr Phe Ser Tyr
275 280 285
Tyr Thr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
290 295 300
Val Ser Ser Ile Ser Ser Arg Ser Ser Tyr Ile Tyr Tyr Ala Asp Ser
305 310 315 320
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Glu Asn Ser Leu
325 330 335
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asp Lys Gly Asp Tyr Ser Lys Asp Ile Tyr Tyr Tyr Tyr
355 360 365
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala
370 375 380
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
385 390 395 400
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
405 410 415
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
420 425 430
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
435 440 445
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
450 455 460
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
465 470 475 480
Val Glu Pro Lys Ser Cys
485
<210> 204
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#12 scFab
<400> 204
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn Trp
275 280 285
Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Ala
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 205
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#13 scFab
<400> 205
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Arg Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 206
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#14 scFab
<400> 206
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn Trp
275 280 285
Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile Gly Gly Ile Tyr
290 295 300
Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 207
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#15 scFab
<400> 207
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn Trp
275 280 285
Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Arg Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 208
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#16 scFab
<400> 208
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Arg Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 209
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#17 scFab
<400> 209
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Arg Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 210
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#18 scFab
<400> 210
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Arg Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 211
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#19 scFab
<400> 211
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Ala
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 212
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#20 scFab
<400> 212
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Ala
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 213
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#21 scFab
<400> 213
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 214
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#22 scFab
<400> 214
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 215
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#23 scFab
<400> 215
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 216
<211> 472
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#24 scFab
<400> 216
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn Trp
275 280 285
Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Arg Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys
465 470
<210> 217
<211> 706
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#1 chain
<400> 217
Asp Ile Val Met Ser Gln Ser Pro Ser Ser Leu Ala Val Ser Val Gly
1 5 10 15
Glu Lys Val Thr Met Asn Cys Lys Ser Ser Gln Ser Leu Phe Tyr Ser
20 25 30
Ser Asn Gln Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Ser Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Thr Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Val Lys Ala Glu Asp Leu Ala Val Tyr Tyr Cys Gln Gln
85 90 95
Tyr Tyr Asn Tyr Pro Arg Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile
100 105 110
Lys Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp
115 120 125
Glu Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn
130 135 140
Phe Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu
145 150 155 160
Gln Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp
165 170 175
Ser Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr
180 185 190
Glu Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser
195 200 205
Ser Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly
210 215 220
Ser Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu
225 230 235 240
Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly
245 250 255
Gly Ser Glu Val Gln Leu Gln Gln Ser Gly Pro Glu Leu Val Lys Pro
260 265 270
Gly Thr Ser Val Lys Met Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr
275 280 285
Asp Tyr Tyr Met Asn Trp Val Lys Gln Ser Gln Gly Lys Asn Leu Glu
290 295 300
Trp Ile Ala Tyr Ile Tyr Pro Lys Thr Gly Gly Asn Gly Tyr Asn Gln
305 310 315 320
Lys Phe Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Asn Thr
325 330 335
Ala Tyr Met Glu Leu Arg Ser Leu Thr Ser Asp Asp Ser Ala Val Tyr
340 345 350
Tyr Cys Gly Arg Glu Asn Trp Asp Gly Tyr Thr Met Ala Tyr Trp Gly
355 360 365
Gln Gly Thr Ser Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser
370 375 380
Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala
385 390 395 400
Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val
405 410 415
Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala
420 425 430
Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val
435 440 445
Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His
450 455 460
Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
465 470 475 480
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
485 490 495
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
500 505 510
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
515 520 525
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
530 535 540
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
545 550 555 560
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
565 570 575
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
580 585 590
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
595 600 605
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
610 615 620
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
625 630 635 640
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
645 650 655
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
660 665 670
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
675 680 685
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
690 695 700
Pro Gly
705
<210> 218
<211> 701
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#2 chain
<400> 218
Glu Ile Val Leu Thr Gln Ser Pro Asp Phe Leu Ser Ala Ser Pro Gly
1 5 10 15
Glu Lys Val Thr Met Thr Cys Arg Ala Thr Ser Ser Leu Tyr Ser Met
20 25 30
His Trp Tyr Gln Gln Lys Pro Gly Ser Ser Pro Lys Pro Trp Ile Tyr
35 40 45
Ala Thr Phe Asn Leu Ala Ser Gly Val Pro Ala Arg Phe Ser Gly Ser
50 55 60
Gly Ser Gly Thr Ser Tyr Ser Leu Thr Ile Thr Arg Val Glu Ala Glu
65 70 75 80
Asp Ala Ala Thr Tyr Tyr Cys Gln Gln Trp Ser Thr Asn Pro Pro Lys
85 90 95
Leu Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala
100 105 110
Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser
115 120 125
Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu
130 135 140
Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser
145 150 155 160
Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu
165 170 175
Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val
180 185 190
Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys
195 200 205
Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser
210 215 220
Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly
225 230 235 240
Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Glu Val Gln
245 250 255
Leu Gln Gln Ser Gly Ala Glu Leu Val Arg Pro Gly Ala Ser Val Lys
260 265 270
Leu Ser Cys Thr Ala Ser Gly Phe Asn Ile Lys Asn Thr Phe Ile His
275 280 285
Trp Val Asn Gln Arg Pro Glu Gln Gly Leu Glu Trp Ile Gly Arg Ile
290 295 300
Asp Pro Ala Asn Gly Asn Thr Ile Tyr Ala Ser Lys Phe Gln Gly Arg
305 310 315 320
Ala Thr Ile Thr Thr Asp Thr Ser Ser Asn Thr Ala Tyr Met His Leu
325 330 335
Ser Ser Leu Thr Ser Gly Asp Thr Ala Val Tyr Tyr Cys Ala Arg Thr
340 345 350
Tyr Gly Gly Thr Asn Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Thr Leu
355 360 365
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
370 375 380
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
385 390 395 400
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
405 410 415
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
420 425 430
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
435 440 445
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
450 455 460
Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
465 470 475 480
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
485 490 495
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
500 505 510
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
515 520 525
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
530 535 540
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
545 550 555 560
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
565 570 575
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
580 585 590
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
595 600 605
Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
610 615 620
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
625 630 635 640
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
645 650 655
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
660 665 670
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
675 680 685
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695 700
<210> 219
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#3 chain
<400> 219
Asp Ile Val Met Thr Gln Ser Gln Lys Leu Leu Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Ile Ser Val Thr Cys Lys Ala Ser His Asn Val Gly Val Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly His Ser Pro Lys Ala Leu Ile
35 40 45
His Ser Ala Ser Asn Arg Tyr Ser Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Asn Val Gln Ser
65 70 75 80
Glu Asp Leu Ala Glu Tyr Phe Cys Gln Gln Tyr Asn Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Ile Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Glu Val Lys Leu
245 250 255
Val Glu Ser Glu Gly Gly Leu Val Gln Pro Gly Ser Ser Met Lys Leu
260 265 270
Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Asp Tyr Tyr Met Thr Trp
275 280 285
Val Arg Gln Val Pro Glu Lys Gly Leu Glu Trp Val Gly Asn Ile Asp
290 295 300
Tyr Asp Gly Ser Arg Ile Tyr Tyr Leu Asp Ser Leu Lys Ser Arg Phe
305 310 315 320
Ile Ile Ser Arg Asp Asn Ala Lys Asn Ile Leu Tyr Leu Gln Met Asn
325 330 335
Ser Leu Lys Ser Glu Asp Thr Ala Thr Tyr Tyr Cys Ala Arg Asp Asp
340 345 350
Pro Ala Trp Leu Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 220
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#4 chain
<400> 220
Asp Ile Val Met Thr Gln Ser Gln Lys Phe Met Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Ser Val Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Ala Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Thr Asn Val Gln Ser
65 70 75 80
Glu Asp Leu Thr Glu Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Leu Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Gln Gln Pro Gly Ser Val Leu Val Arg Pro Gly Ala Ser Val Arg Leu
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn Trp
275 280 285
Met Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile Gly Gly Ile Tyr
290 295 300
Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Ala
305 310 315 320
Thr Leu Thr Val Asp Thr Ser Ser Ser Thr Thr Tyr Met Asp Leu Ser
325 330 335
Ser Leu Thr Tyr Glu Asp Ser Ala Val Tyr Tyr Cys Thr Thr Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Thr Leu Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 221
<211> 700
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#5 chain
<400> 221
Ala Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Asp Ile Arg Asn Asp
20 25 30
Leu Gly Trp Phe Gln Gln Arg Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Arg Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Leu Gln Tyr Tyr Asn His Pro Leu
85 90 95
Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr Tyr Ile His Trp
275 280 285
Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Trp Ile Asn
290 295 300
Pro His Ser Gly Ala Thr Asn Tyr Ala Gln Asn Phe Gln Gly Arg Val
305 310 315 320
Thr Met Thr Arg Asp Thr Ser Ile Ser Thr Ala Tyr Met Glu Leu Ser
325 330 335
Arg Leu Arg Ser Asp Asp Ala Ala Val Tyr Tyr Cys Ala Arg Glu Arg
340 345 350
Trp Gly Ser Gly Thr Phe Asn Ile Trp Gly Gln Gly Thr Met Val Thr
355 360 365
Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro
370 375 380
Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val
385 390 395 400
Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala
405 410 415
Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly
420 425 430
Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly
435 440 445
Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys
450 455 460
Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
465 470 475 480
Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu
485 490 495
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
500 505 510
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
515 520 525
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
530 535 540
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
545 550 555 560
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
565 570 575
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
580 585 590
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
595 600 605
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys
610 615 620
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
625 630 635 640
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
645 650 655
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
660 665 670
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
675 680 685
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695 700
<210> 222
<211> 701
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#6 chain
<400> 222
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Pro Val Ser Ala Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Ser Val Ser Asn Asp
20 25 30
Val Val Trp Tyr Gln Gln Lys Pro Gly Gln Ser Pro Lys Leu Leu Met
35 40 45
Tyr Ser Thr Ser Asn Arg Tyr Ile Gly Val Pro Asp Arg Phe Thr Gly
50 55 60
Ser Gly Tyr Gly Thr Asp Phe Thr Phe Thr Ile Ser Thr Val Gln Ala
65 70 75 80
Glu Asp Leu Ala Val Tyr Phe Cys Gln Gln Asp Tyr Ser Ser Pro Tyr
85 90 95
Thr Phe Gly Gly Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Glu Val Gln Leu
245 250 255
Gln Gln Ser Gly Pro Glu Leu Leu Lys Pro Gly Ala Ser Val Lys Ile
260 265 270
Ser Cys Lys Thr Ser Gly Tyr Thr Phe Thr Asp Tyr Thr Met His Trp
275 280 285
Val Lys Gln Ser His Gly Lys Ser Leu Glu Trp Ile Gly Gly Ile Asn
290 295 300
Pro Asn Tyr Asp Asn Thr Gly Tyr Ser Glu Lys Phe Lys Asp Lys Ala
305 310 315 320
Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr Met Glu Leu Arg
325 330 335
Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys Thr Arg Ser Gly
340 345 350
Ser Arg Arg Ser Phe Tyr Phe Asp Tyr Trp Gly Gln Gly Thr Thr Leu
355 360 365
Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala
370 375 380
Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu
385 390 395 400
Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly
405 410 415
Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser
420 425 430
Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu
435 440 445
Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr
450 455 460
Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr
465 470 475 480
Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe
485 490 495
Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro
500 505 510
Glu Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val
515 520 525
Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr
530 535 540
Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val
545 550 555 560
Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys
565 570 575
Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser
580 585 590
Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro
595 600 605
Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val
610 615 620
Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly
625 630 635 640
Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp
645 650 655
Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp
660 665 670
Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His
675 680 685
Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695 700
<210> 223
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#7 chain
<400> 223
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu
260 265 270
Thr Tyr Thr Val Ser Gly Gly Ser Ile Ser Tyr Asn Tyr Trp Ser Trp
275 280 285
Ile Arg Gln Pro Pro Glu Lys Gly Leu Glu Trp Ile Gly His Ile Tyr
290 295 300
Tyr Ser Gly Ser Thr Asn Tyr Asn Pro Ser Leu Lys Ser Arg Val Thr
305 310 315 320
Ile Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Lys Leu Asn Ser
325 330 335
Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Val Gly Thr
340 345 350
Trp Gly Ser Phe Asp Asp Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 224
<211> 713
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#8 chain
<400> 224
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu Tyr Asn
20 25 30
Asn Arg Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Glu Val Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Phe Gly Val Tyr Tyr Cys Met Gln Thr
85 90 95
Leu Gln Ile Pro Ile Thr Phe Gly Gln Gly Thr Arg Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Gln Val Gln Val Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
260 265 270
Ser Ser Val Lys Val Ser Cys Lys Gly Ser Gly Asp Thr Leu Asn Ser
275 280 285
Tyr Gly Ile Ser Trp Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
290 295 300
Met Gly Gly Ile Ile Pro Ile Phe Asp Thr Thr Lys Tyr Ala Gln Lys
305 310 315 320
Phe Gln Gly Arg Val Thr Ile Thr Ala Asp Lys Ser Thr Thr Thr Val
325 330 335
Tyr Met Glu Leu Ser Ser Leu Arg Phe Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Glu Arg Gly Tyr Arg Phe Ser Glu Asp Tyr Tyr Phe Tyr
355 360 365
Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
370 375 380
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
385 390 395 400
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
405 410 415
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
420 425 430
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
435 440 445
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
450 455 460
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
465 470 475 480
Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
485 490 495
Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
500 505 510
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
515 520 525
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
530 535 540
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
545 550 555 560
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
565 570 575
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
580 585 590
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
595 600 605
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu
610 615 620
Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr
625 630 635 640
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
645 650 655
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
660 665 670
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
675 680 685
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
690 695 700
Gln Lys Ser Leu Ser Leu Ser Pro Gly
705 710
<210> 225
<211> 708
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#9 chain
<400> 225
Asp Ile Val Leu Thr Gln Ser Pro Val Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Gln Arg Ala Thr Ile Ser Cys Arg Ala Ser Glu Ser Val Asp Asn Phe
20 25 30
Gly Val Ser Phe Met Asn Trp Phe Gln Gln Lys Pro Gly Gln Pro Pro
35 40 45
Lys Leu Leu Ile Tyr Ala Ala Ser Asn Gln Gly Ser Gly Val Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Ser Leu Asn Ile His
65 70 75 80
Pro Leu Glu Glu Asp Asp Thr Ala Met Tyr Phe Cys Gln Gln Ser Lys
85 90 95
Glu Val Pro Trp Thr Phe Gly Gly Gly Thr Arg Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu
210 215 220
Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys
225 230 235 240
Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser
245 250 255
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Met Val Arg Pro Gly Ser
260 265 270
Ser Val Lys Leu Ser Cys Lys Ala Ser Asp Tyr Thr Phe Thr His Tyr
275 280 285
Trp Ile His Trp Val Lys Gln Arg Pro Leu Glu Gly Leu Glu Trp Ile
290 295 300
Gly Ile Ile Gly Pro Ser Asp Asn Glu Ile His Tyr Asn Gln Asp Phe
305 310 315 320
Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Asn Thr Ala Tyr
325 330 335
Leu His Leu Asn Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
340 345 350
Ala Arg Gln Ile Ile Ser Met Val Val Gly Thr Glu Tyr Phe Asp Val
355 360 365
Trp Gly Thr Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly
370 375 380
Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly
385 390 395 400
Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val
405 410 415
Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe
420 425 430
Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val
435 440 445
Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val
450 455 460
Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys
465 470 475 480
Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala
485 490 495
Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
500 505 510
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
515 520 525
Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val
530 535 540
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser
545 550 555 560
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
565 570 575
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala
580 585 590
Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
595 600 605
Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln
610 615 620
Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
625 630 635 640
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
645 650 655
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu
660 665 670
Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser
675 680 685
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
690 695 700
Leu Ser Pro Gly
705
<210> 226
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#10 chain
<400> 226
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Val Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Val Ala Ser Ser Leu Gln Arg Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Asn Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ala Asn Ser Phe Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val His Leu
245 250 255
Gln Glu Ser Gly Pro Gly Leu Val Lys Pro Ser Glu Thr Leu Ser Leu
260 265 270
Thr Cys Thr Val Ser Gly Asp Ser Ile Ser Ser Tyr Tyr Trp Ser Trp
275 280 285
Ile Arg Gln Pro Ala Gly Lys Gly Leu Glu Trp Ile Gly His Ile Tyr
290 295 300
Thr Ser Glu Lys Asn Asn Tyr Asn Pro Ser Leu Lys Ser Arg Val Ile
305 310 315 320
Met Ser Val Asp Thr Ser Lys Asn Gln Phe Ser Leu Asn Leu Ser Ser
325 330 335
Val Thr Ala Ala Asp Thr Ala Val Tyr Tyr Cys Ala Arg Val Gly Asn
340 345 350
Trp Gly Ser His Asp Ala Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 227
<211> 712
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#11 chain
<400> 227
Asp Ile Val Met Thr Gln Ser Pro Leu Ser Leu Pro Val Thr Pro Gly
1 5 10 15
Glu Pro Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Leu Leu His Ser
20 25 30
Asn Gly Tyr Asn Tyr Leu Asp Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Gln Val Leu Ile Tyr Leu Gly Ser Asn Arg Ala Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Val Gly Val Tyr Tyr Cys Met Gln Ala
85 90 95
Leu Gln Thr Pro Leu Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Glu Leu Gln Leu Val Asn Ser Gly Gly Gly Leu Val Lys Ser Gly
260 265 270
Gly Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Ile Thr Phe Ser Tyr
275 280 285
Tyr Thr Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp
290 295 300
Val Ser Ser Ile Ser Ser Arg Ser Ser Tyr Ile Tyr Tyr Ala Asp Ser
305 310 315 320
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Glu Asn Ser Leu
325 330 335
Tyr Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asp Lys Gly Asp Tyr Ser Lys Asp Ile Tyr Tyr Tyr Tyr
355 360 365
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala
370 375 380
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser
385 390 395 400
Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
405 410 415
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
420 425 430
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
435 440 445
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr
450 455 460
Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
465 470 475 480
Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro
485 490 495
Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys
500 505 510
Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val
515 520 525
Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr
530 535 540
Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu
545 550 555 560
Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His
565 570 575
Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys
580 585 590
Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln
595 600 605
Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met
610 615 620
Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro
625 630 635 640
Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn
645 650 655
Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu
660 665 670
Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val
675 680 685
Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln
690 695 700
Lys Ser Leu Ser Leu Ser Pro Gly
705 710
<210> 228
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#12 chain
<400> 228
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn Trp
275 280 285
Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Ala
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 229
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#13 chain
<400> 229
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Arg Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 230
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#14 chain
<400> 230
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn Trp
275 280 285
Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile Gly Gly Ile Tyr
290 295 300
Leu Asn Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 231
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#15 chain
<400> 231
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn Trp
275 280 285
Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Arg Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 232
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#16 chain
<400> 232
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Arg Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 233
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#17 chain
<400> 233
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Arg Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 234
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#18 chain
<400> 234
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Arg Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 235
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#19 chain
<400> 235
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Ala
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 236
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#20 chain
<400> 236
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Val Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Ala
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 237
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#21 chain
<400> 237
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 238
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#22 chain
<400> 238
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 239
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#23 chain
<400> 239
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Phe Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr Trp Met Asn Trp
275 280 285
Met Lys Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Glu Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Lys Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 240
<211> 698
<212> PRT
<213> Artificial Sequence
<220>
<223> B7H6#24 chain
<400> 240
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Lys Ala Ser Gln Asn Val Gly Lys Tyr
20 25 30
Val Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ser Ala Ser Asn Arg Tyr Asp Ala Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Thr Thr Tyr Tyr Cys Gln Gln Tyr Ile Ser Tyr Pro Leu
85 90 95
Thr Phe Gly Ala Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser
210 215 220
Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser
225 230 235 240
Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Gln Val Gln Leu
245 250 255
Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala Ser Val Lys Val
260 265 270
Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Asn Tyr Trp Met Asn Trp
275 280 285
Met Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met Gly Gly Ile Tyr
290 295 300
Leu Ser Gly Asp Ser Thr Asp Tyr Asn Glu Lys Phe Lys Gly Arg Val
305 310 315 320
Thr Met Thr Val Asp Thr Ser Thr Ser Thr Val Tyr Met Glu Leu Ser
325 330 335
Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys Thr Arg Arg Gly
340 345 350
Asp Tyr Phe Gly Asp Phe Trp Gly Gln Gly Thr Leu Val Thr Val Ser
355 360 365
Ser Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser
370 375 380
Lys Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp
385 390 395 400
Tyr Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr
405 410 415
Ser Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr
420 425 430
Ser Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln
435 440 445
Thr Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp
450 455 460
Lys Arg Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro
465 470 475 480
Cys Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro
485 490 495
Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr
500 505 510
Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn
515 520 525
Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg
530 535 540
Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val
545 550 555 560
Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser
565 570 575
Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys
580 585 590
Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Glu
595 600 605
Glu Met Thr Lys Asn Gln Val Ser Leu Trp Cys Leu Val Lys Gly Phe
610 615 620
Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu
625 630 635 640
Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe
645 650 655
Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly
660 665 670
Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr
675 680 685
Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly
690 695
<210> 241
<211> 226
<212> PRT
<213> Artificial Sequence
<220>
<223> Fc domain* (IgG1)
<400> 241
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
1 5 10 15
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
20 25 30
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
35 40 45
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
50 55 60
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
65 70 75 80
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
85 90 95
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
100 105 110
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
115 120 125
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
130 135 140
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
145 150 155 160
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
165 170 175
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
180 185 190
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
195 200 205
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
210 215 220
Pro Gly
225
<210> 242
<211> 226
<212> PRT
<213> Artificial Sequence
<220>
<223> Fc W domain (IgG1, LALA)
<400> 242
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
1 5 10 15
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
20 25 30
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
35 40 45
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
50 55 60
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
65 70 75 80
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
85 90 95
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
100 105 110
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
115 120 125
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
130 135 140
Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
145 150 155 160
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
165 170 175
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
180 185 190
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
195 200 205
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
210 215 220
Pro Gly
225
<210> 243
<211> 226
<212> PRT
<213> Artificial Sequence
<220>
<223> Fc, SAV domain (IgG1, RF/LALA)
<400> 243
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly
1 5 10 15
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
20 25 30
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
35 40 45
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
50 55 60
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
65 70 75 80
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
85 90 95
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
100 105 110
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
115 120 125
Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser
130 135 140
Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
145 150 155 160
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
165 170 175
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val
180 185 190
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
195 200 205
His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser
210 215 220
Pro Gly
225
<210> 244
<211> 228
<212> PRT
<213> Artificial Sequence
<220>
<223> Fc domain (IgG4Pro)
<400> 244
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
1 5 10 15
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
20 25 30
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
35 40 45
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
50 55 60
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
65 70 75 80
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
85 90 95
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
100 105 110
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
115 120 125
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
130 135 140
Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
145 150 155 160
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
165 170 175
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
180 185 190
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
195 200 205
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
210 215 220
Leu Ser Leu Gly
225
<210> 245
<211> 228
<212> PRT
<213> Artificial Sequence
<220>
<223> Fc W domain (IgG4Pro)
<400> 245
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
1 5 10 15
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
20 25 30
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
35 40 45
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
50 55 60
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
65 70 75 80
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
85 90 95
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
100 105 110
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
115 120 125
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
130 135 140
Val Ser Leu Trp Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
145 150 155 160
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
165 170 175
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu
180 185 190
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
195 200 205
Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser
210 215 220
Leu Ser Leu Gly
225
<210> 246
<211> 228
<212> PRT
<213> Artificial Sequence
<220>
<223> Fc SAV domain (IgG4Pro, RF)
<400> 246
Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe
1 5 10 15
Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr
20 25 30
Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val
35 40 45
Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly Val
50 55 60
Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser
65 70 75 80
Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu
85 90 95
Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro Ser
100 105 110
Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro
115 120 125
Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn Gln
130 135 140
Val Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala
145 150 155 160
Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr
165 170 175
Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Arg Leu
180 185 190
Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys Ser
195 200 205
Val Met His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser
210 215 220
Leu Ser Leu Gly
225
<210> 247
<211> 107
<212> PRT
<213> Artificial Sequence
<220>
<223> constant region of a kappa light chain
<400> 247
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 248
<211> 106
<212> PRT
<213> Artificial Sequence
<220>
<223> constant region of a lambda light chain
<400> 248
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Lys Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Asn Thr Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Ala Glu Cys Ser
100 105
<210> 249
<211> 103
<212> PRT
<213> Artificial Sequence
<220>
<223> Constant region of heavy chain CH1
<400> 249
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Pro Lys Ser Cys
100
<210> 250
<211> 38
<212> PRT
<213> Artificial Sequence
<220>
<223> Linker
<400> 250
Gly Gly Gly Gly Ser Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser
1 5 10 15
Lys Ser Thr Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser
20 25 30
Thr Gly Gly Gly Gly Ser
35
<210> 251
<211> 22
<212> PRT
<213> Artificial Sequence
<220>
<223> Linker
<400> 251
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Ser Gly Gly Ser
1 5 10 15
Gly Gly Gly Gly Gly Ser
20
<210> 252
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> Linker
<400> 252
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly
1 5 10 15
Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser
20 25
<210> 253
<211> 30
<212> PRT
<213> Artificial Sequence
<220>
<223> Linker
<400> 253
Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Gly Ser Gly Gly Gly Gly
1 5 10 15
Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly Ser
20 25 30
<210> 254
<211> 34
<212> PRT
<213> Artificial Sequence
<220>
<223> Linker
<400> 254
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly
1 5 10 15
Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly
20 25 30
Gly Ser
<210> 255
<211> 38
<212> PRT
<213> Artificial Sequence
<220>
<223> Linker
<400> 255
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly
1 5 10 15
Gly Ser Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser
20 25 30
Gly Gly Gly Gly Gly Ser
35
<210> 256
<211> 42
<212> PRT
<213> Artificial Sequence
<220>
<223> Linker
<400> 256
Gly Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly
1 5 10 15
Gly Ser Gly Gly Gly Ser Gly Gly Gly Gly Ser Gly Gly Gly Gly Gly
20 25 30
Ser Gly Gly Gly Ser Gly Gly Gly Gly Ser
35 40
<210> 257
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#1 LCCDR1
<400> 257
Arg Ser Ser Thr Gly Ala Val Thr Thr Ser Asn Tyr Ala Asn
1 5 10
<210> 258
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#1 LCCDR2
<400> 258
Gly Thr Asn Lys Arg Ala Pro
1 5
<210> 259
<211> 9
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#1 LCCDR3
<400> 259
Ala Leu Trp Tyr Ser Asn Leu Trp Val
1 5
<210> 260
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#1 HCCDR1
<400> 260
Gly Phe Thr Phe Asn Thr Tyr Ala Met Asn
1 5 10
<210> 261
<211> 19
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#1 HCCDR2
<400> 261
Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser
1 5 10 15
Val Lys Asp
<210> 262
<211> 14
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#1 HCCDR3
<400> 262
His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr
1 5 10
<210> 263
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#2 LCCDR1
<400> 263
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Asn Tyr Leu
1 5 10 15
Ala
<210> 264
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#2 LCCDR2
<400> 264
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 265
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#2 LCCDR3
<400> 265
Lys Gln Ser Phe Ile Leu Arg Thr
1 5
<210> 266
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#2 HCCDR1
<400> 266
Gly Tyr Ser Phe Thr Asp Tyr Tyr Val His
1 5 10
<210> 267
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#2 HCCDR2
<400> 267
Trp Ile Tyr Pro Gly Asn Gly Asn Ile Lys Tyr Asn Glu Arg Phe Arg
1 5 10 15
Gly
<210> 268
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#2 HCCDR3
<400> 268
Asp Asn Tyr Ser Ala Tyr Tyr Phe Ala Tyr
1 5 10
<210> 269
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#3 LCCDR1
<400> 269
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Val Tyr Leu
1 5 10 15
Ala
<210> 270
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#3 LCCDR2
<400> 270
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 271
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#3 LCCDR3
<400> 271
Lys Gln Ser Phe Ile Leu Arg Thr
1 5
<210> 272
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#3 HCCDR1
<400> 272
Gly Tyr Thr Phe Thr Ser Tyr Tyr Val His
1 5 10
<210> 273
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#3 HCCDR2
<400> 273
Trp Ile Tyr Pro Gly Gly Gly Asn Ile Lys Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 274
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#3 HCCDR3
<400> 274
Asp Gln Tyr Ser Ala Tyr Tyr Phe Ala Tyr
1 5 10
<210> 275
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#4 LCCDR1
<400> 275
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Val Tyr Leu
1 5 10 15
Ala
<210> 276
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#4 LCCDR2
<400> 276
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 277
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#4 LCCDR3
<400> 277
Lys Gln Ser Phe Ile Leu Arg Thr
1 5
<210> 278
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#4 HCCDR1
<400> 278
Gly Tyr Ser Phe Thr Ser Tyr Tyr Val His
1 5 10
<210> 279
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#4 HCCDR2
<400> 279
Trp Ile Tyr Pro Gly Gly Gly Asn Ile Lys Tyr Asn Gln Lys Phe Gln
1 5 10 15
Gly
<210> 280
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#4 HCCDR3
<400> 280
Asp His Tyr Ser Ala Tyr Tyr Phe Ala Tyr
1 5 10
<210> 281
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#5 LCCDR1
<400> 281
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Thr Tyr Leu
1 5 10 15
Ala
<210> 282
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#5 LCCDR2
<400> 282
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 283
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#5 LCCDR3
<400> 283
Lys Gln Ser Phe Ile Leu Arg Thr
1 5
<210> 284
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#5 HCCDR1
<400> 284
Gly Tyr Thr Phe Thr Gly Tyr Tyr Val His
1 5 10
<210> 285
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#5 HCCDR2
<400> 285
Trp Ile Tyr Pro Gly Gly Gly Ser Thr Lys Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 286
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#5 HCCDR3
<400> 286
Asp Gln Tyr Ser Ala Tyr Tyr Phe Ala Tyr
1 5 10
<210> 287
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#6 LCCDR1
<400> 287
Lys Ser Ser Gln Ser Leu Leu Asn Ser Arg Thr Arg Lys Thr Tyr Leu
1 5 10 15
Ala
<210> 288
<211> 7
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#6 LCCDR2
<400> 288
Trp Ala Ser Thr Arg Glu Ser
1 5
<210> 289
<211> 8
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#6 LCCDR3
<400> 289
Lys Gln Ser Phe Ile Leu Arg Thr
1 5
<210> 290
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#6 HCCDR1
<400> 290
Gly Tyr Thr Phe Thr Ser Tyr Tyr Val His
1 5 10
<210> 291
<211> 17
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#6 HCCDR2
<400> 291
Trp Ile Tyr Pro Gly Gly Gly Asn Ile Lys Tyr Ala Gln Lys Phe Gln
1 5 10 15
Gly
<210> 292
<211> 10
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#6 HCCDR3
<400> 292
Asp Gln Tyr Ser Ala Tyr Tyr Phe Ala Tyr
1 5 10
<210> 293
<211> 109
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#1 VL
<400> 293
Glu Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Gly Gln Leu Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Val Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Phe Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu
100 105
<210> 294
<211> 125
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#1 VH
<400> 294
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Lys Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Arg Ile Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp
50 55 60
Ser Val Lys Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Ala Tyr Leu Gln Met Asn Asn Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Val Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe
100 105 110
Ala Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ala
115 120 125
<210> 295
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#2 VL
<400> 295
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 296
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#2 VH
<400> 296
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Asp Tyr
20 25 30
Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Tyr Pro Gly Asn Gly Asn Ile Lys Tyr Asn Glu Arg Phe
50 55 60
Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Asn Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 297
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#3 VL
<400> 297
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Val Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 298
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#3 VH
<400> 298
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Trp Ile Tyr Pro Gly Gly Gly Asn Ile Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gln Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 299
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#4 VL
<400> 299
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Val Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 300
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#4 VH
<400> 300
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Ser Tyr
20 25 30
Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Trp Ile Tyr Pro Gly Gly Gly Asn Ile Lys Tyr Asn Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp His Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 301
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#5 VL
<400> 301
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 302
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#5 VH
<400> 302
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly Tyr
20 25 30
Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Met
35 40 45
Gly Trp Ile Tyr Pro Gly Gly Gly Ser Thr Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gln Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 303
<211> 112
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#6 VL
<400> 303
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
<210> 304
<211> 119
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#6 VH
<400> 304
Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly Ala
1 5 10 15
Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Trp Ile Tyr Pro Gly Gly Gly Asn Ile Lys Tyr Ala Gln Lys Phe
50 55 60
Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val Tyr
65 70 75 80
Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Gln Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln Gly
100 105 110
Thr Thr Val Thr Val Ser Ser
115
<210> 305
<211> 481
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#1 scFab
<400> 305
Glu Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Gly Gln Leu Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Val Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Phe Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gln Pro
100 105 110
Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu Glu Leu
115 120 125
Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr Pro
130 135 140
Gly Ala Val Lys Val Ala Trp Lys Ala Asp Gly Ser Pro Val Asn Thr
145 150 155 160
Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys Tyr Ala
165 170 175
Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His Arg
180 185 190
Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys Thr
195 200 205
Val Ala Pro Ala Glu Cys Ser Gly Gly Gly Gly Ser Glu Gly Lys Ser
210 215 220
Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly
225 230 235 240
Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Glu Val Gln
245 250 255
Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys
260 265 270
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr Ala Met Asn
275 280 285
Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile
290 295 300
Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
305 310 315 320
Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Ala Tyr Leu
325 330 335
Gln Met Asn Asn Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Val
340 345 350
Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr Trp
355 360 365
Gly Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro
370 375 380
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
385 390 395 400
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
405 410 415
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
420 425 430
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
435 440 445
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
450 455 460
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser
465 470 475 480
Cys
<210> 306
<211> 479
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#2 scFab
<400> 306
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
260 265 270
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Asp
275 280 285
Tyr Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
290 295 300
Met Gly Trp Ile Tyr Pro Gly Asn Gly Asn Ile Lys Tyr Asn Glu Arg
305 310 315 320
Phe Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val
325 330 335
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asp Asn Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln
355 360 365
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
465 470 475
<210> 307
<211> 479
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#3 scFab
<400> 307
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Val Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
260 265 270
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser
275 280 285
Tyr Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
290 295 300
Ile Gly Trp Ile Tyr Pro Gly Gly Gly Asn Ile Lys Tyr Ala Gln Lys
305 310 315 320
Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val
325 330 335
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asp Gln Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln
355 360 365
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
465 470 475
<210> 308
<211> 479
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#4 scFab
<400> 308
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Val Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
260 265 270
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Ser
275 280 285
Tyr Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
290 295 300
Ile Gly Trp Ile Tyr Pro Gly Gly Gly Asn Ile Lys Tyr Asn Gln Lys
305 310 315 320
Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val
325 330 335
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asp His Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln
355 360 365
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
465 470 475
<210> 309
<211> 479
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#5 scFab
<400> 309
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
260 265 270
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly
275 280 285
Tyr Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
290 295 300
Met Gly Trp Ile Tyr Pro Gly Gly Gly Ser Thr Lys Tyr Ala Gln Lys
305 310 315 320
Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val
325 330 335
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asp Gln Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln
355 360 365
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
465 470 475
<210> 310
<211> 479
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#6 scFab
<400> 310
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
260 265 270
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser
275 280 285
Tyr Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
290 295 300
Ile Gly Trp Ile Tyr Pro Gly Gly Gly Asn Ile Lys Tyr Ala Gln Lys
305 310 315 320
Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val
325 330 335
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asp Gln Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln
355 360 365
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys
465 470 475
<210> 311
<211> 707
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#1 chain
<400> 311
Glu Ala Val Val Thr Gln Glu Pro Ser Leu Thr Val Ser Pro Gly Gly
1 5 10 15
Thr Val Thr Leu Thr Cys Arg Ser Ser Thr Gly Ala Val Thr Thr Ser
20 25 30
Asn Tyr Ala Asn Trp Val Gln Glu Lys Pro Gly Gln Leu Pro Arg Gly
35 40 45
Leu Ile Gly Gly Thr Asn Lys Arg Ala Pro Trp Val Pro Ala Arg Phe
50 55 60
Ser Gly Ser Leu Leu Gly Gly Lys Ala Ala Leu Thr Leu Ser Gly Ala
65 70 75 80
Gln Pro Glu Asp Glu Ala Glu Tyr Phe Cys Ala Leu Trp Tyr Ser Asn
85 90 95
Leu Trp Val Phe Gly Gly Gly Thr Lys Leu Thr Val Leu Gly Gln Pro
100 105 110
Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu Glu Leu
115 120 125
Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr Pro
130 135 140
Gly Ala Val Lys Val Ala Trp Lys Ala Asp Gly Ser Pro Val Asn Thr
145 150 155 160
Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys Tyr Ala
165 170 175
Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His Arg
180 185 190
Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys Thr
195 200 205
Val Ala Pro Ala Glu Cys Ser Gly Gly Gly Gly Ser Glu Gly Lys Ser
210 215 220
Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly Lys Ser Ser Gly
225 230 235 240
Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly Ser Glu Val Gln
245 250 255
Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly Ser Leu Lys
260 265 270
Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Thr Tyr Ala Met Asn
275 280 285
Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val Ala Arg Ile
290 295 300
Arg Ser Lys Tyr Asn Asn Tyr Ala Thr Tyr Tyr Ala Asp Ser Val Lys
305 310 315 320
Asp Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr Ala Tyr Leu
325 330 335
Gln Met Asn Asn Leu Lys Thr Glu Asp Thr Ala Val Tyr Tyr Cys Val
340 345 350
Arg His Gly Asn Phe Gly Asn Ser Tyr Val Ser Trp Phe Ala Tyr Trp
355 360 365
Gly Gln Gly Thr Leu Val Thr Val Ser Ala Ala Ser Thr Lys Gly Pro
370 375 380
Ser Val Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr
385 390 395 400
Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr
405 410 415
Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro
420 425 430
Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr
435 440 445
Val Pro Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn
450 455 460
His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser
465 470 475 480
Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala
485 490 495
Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu
500 505 510
Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser
515 520 525
His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu
530 535 540
Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr
545 550 555 560
Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn
565 570 575
Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro
580 585 590
Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln
595 600 605
Val Tyr Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val
610 615 620
Ser Leu Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val
625 630 635 640
Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro
645 650 655
Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr
660 665 670
Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val
675 680 685
Met His Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu
690 695 700
Ser Pro Gly
705
<210> 312
<211> 705
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#2 chain
<400> 312
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Asn Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
260 265 270
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Asp
275 280 285
Tyr Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
290 295 300
Met Gly Trp Ile Tyr Pro Gly Asn Gly Asn Ile Lys Tyr Asn Glu Arg
305 310 315 320
Phe Arg Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val
325 330 335
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asp Asn Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln
355 360 365
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
610 615 620
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
660 665 670
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly
705
<210> 313
<211> 705
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#3 chain
<400> 313
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Val Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
260 265 270
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser
275 280 285
Tyr Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
290 295 300
Ile Gly Trp Ile Tyr Pro Gly Gly Gly Asn Ile Lys Tyr Ala Gln Lys
305 310 315 320
Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val
325 330 335
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asp Gln Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln
355 360 365
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
610 615 620
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
660 665 670
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly
705
<210> 314
<211> 705
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#4 chain
<400> 314
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Asn Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Val Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
260 265 270
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Ser
275 280 285
Tyr Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
290 295 300
Ile Gly Trp Ile Tyr Pro Gly Gly Gly Asn Ile Lys Tyr Asn Gln Lys
305 310 315 320
Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val
325 330 335
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asp His Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln
355 360 365
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
610 615 620
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
660 665 670
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly
705
<210> 315
<211> 705
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#5 chain
<400> 315
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
260 265 270
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Gly
275 280 285
Tyr Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
290 295 300
Met Gly Trp Ile Tyr Pro Gly Gly Gly Ser Thr Lys Tyr Ala Gln Lys
305 310 315 320
Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val
325 330 335
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asp Gln Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln
355 360 365
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
610 615 620
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
660 665 670
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly
705
<210> 316
<211> 705
<212> PRT
<213> Artificial Sequence
<220>
<223> CD3#6 chain
<400> 316
Asp Ile Val Met Thr Gln Ser Pro Asp Ser Leu Ala Val Ser Leu Gly
1 5 10 15
Glu Arg Ala Thr Ile Ser Cys Lys Ser Ser Gln Ser Leu Leu Asn Ser
20 25 30
Arg Thr Arg Lys Thr Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln
35 40 45
Pro Pro Lys Leu Leu Ile Tyr Trp Ala Ser Thr Arg Glu Ser Gly Val
50 55 60
Pro Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr
65 70 75 80
Ile Ser Ser Leu Gln Ala Glu Asp Val Ala Val Tyr Tyr Cys Lys Gln
85 90 95
Ser Phe Ile Leu Arg Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105 110
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
115 120 125
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
130 135 140
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
145 150 155 160
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
165 170 175
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
180 185 190
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
195 200 205
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys Gly Gly Gly Gly Ser
210 215 220
Glu Gly Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Glu Gly
225 230 235 240
Lys Ser Ser Gly Ser Gly Ser Glu Ser Lys Ser Thr Gly Gly Gly Gly
245 250 255
Ser Gln Val Gln Leu Val Gln Ser Gly Ala Glu Val Lys Lys Pro Gly
260 265 270
Ala Ser Val Lys Val Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser
275 280 285
Tyr Tyr Val His Trp Val Arg Gln Ala Pro Gly Gln Gly Leu Glu Trp
290 295 300
Ile Gly Trp Ile Tyr Pro Gly Gly Gly Asn Ile Lys Tyr Ala Gln Lys
305 310 315 320
Phe Gln Gly Arg Val Thr Met Thr Arg Asp Thr Ser Thr Ser Thr Val
325 330 335
Tyr Met Glu Leu Ser Ser Leu Arg Ser Glu Asp Thr Ala Val Tyr Tyr
340 345 350
Cys Ala Arg Asp Gln Tyr Ser Ala Tyr Tyr Phe Ala Tyr Trp Gly Gln
355 360 365
Gly Thr Thr Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
370 375 380
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
385 390 395 400
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
405 410 415
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
420 425 430
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
435 440 445
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
450 455 460
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Pro Lys Ser Cys Asp
465 470 475 480
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Ala Ala Gly Gly
485 490 495
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
500 505 510
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
515 520 525
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
530 535 540
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
545 550 555 560
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
565 570 575
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
580 585 590
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
595 600 605
Thr Leu Pro Pro Ser Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu
610 615 620
Ser Cys Ala Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
625 630 635 640
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
645 650 655
Leu Asp Ser Asp Gly Ser Phe Phe Leu Val Ser Lys Leu Thr Val Asp
660 665 670
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
675 680 685
Glu Ala Leu His Asn Arg Phe Thr Gln Lys Ser Leu Ser Leu Ser Pro
690 695 700
Gly
705
<210> 317
<211> 248
<212> PRT
<213> Artificial Sequence
<220>
<223> His-tagged human B7H6 ECD ECD
<400> 317
Asp Leu Lys Val Glu Met Met Ala Gly Gly Thr Gln Ile Thr Pro Leu
1 5 10 15
Asn Asp Asn Val Thr Ile Phe Cys Asn Ile Phe Tyr Ser Gln Pro Leu
20 25 30
Asn Ile Thr Ser Met Gly Ile Thr Trp Phe Trp Lys Ser Leu Thr Phe
35 40 45
Asp Lys Glu Val Lys Val Phe Glu Phe Phe Gly Asp His Gln Glu Ala
50 55 60
Phe Arg Pro Gly Ala Ile Val Ser Pro Trp Arg Leu Lys Ser Gly Asp
65 70 75 80
Ala Ser Leu Arg Leu Pro Gly Ile Gln Leu Glu Glu Ala Gly Glu Tyr
85 90 95
Arg Cys Glu Val Val Val Thr Pro Leu Lys Ala Gln Gly Thr Val Gln
100 105 110
Leu Glu Val Val Ala Ser Pro Ala Ser Arg Leu Leu Leu Asp Gln Val
115 120 125
Gly Met Lys Glu Asn Glu Asp Lys Tyr Met Cys Glu Ser Ser Gly Phe
130 135 140
Tyr Pro Glu Ala Ile Asn Ile Thr Trp Glu Lys Gln Thr Gln Lys Phe
145 150 155 160
Pro His Pro Ile Glu Ile Ser Glu Asp Val Ile Thr Gly Pro Thr Ile
165 170 175
Lys Asn Met Asp Gly Thr Phe Asn Val Thr Ser Cys Leu Lys Leu Asn
180 185 190
Ser Ser Gln Glu Asp Pro Gly Thr Val Tyr Gln Cys Val Val Arg His
195 200 205
Ala Ser Leu His Thr Pro Leu Arg Ser Asn Phe Thr Leu Thr Ala Ala
210 215 220
Arg His Ser Leu Ser Glu Thr Glu Lys Thr Asp Asn Phe Ser Ala Gly
225 230 235 240
Ser Gly His His His His His His
245
<210> 318
<211> 500
<212> PRT
<213> Artificial Sequence
<220>
<223> Fc-His-tagged human B7H6 ECD
<400> 318
Asp Leu Lys Val Glu Met Met Ala Gly Gly Thr Gln Ile Thr Pro Leu
1 5 10 15
Asn Asp Asn Val Thr Ile Phe Cys Asn Ile Phe Tyr Ser Gln Pro Leu
20 25 30
Asn Ile Thr Ser Met Gly Ile Thr Trp Phe Trp Lys Ser Leu Thr Phe
35 40 45
Asp Lys Glu Val Lys Val Phe Glu Phe Phe Gly Asp His Gln Glu Ala
50 55 60
Phe Arg Pro Gly Ala Ile Val Ser Pro Trp Arg Leu Lys Ser Gly Asp
65 70 75 80
Ala Ser Leu Arg Leu Pro Gly Ile Gln Leu Glu Glu Ala Gly Glu Tyr
85 90 95
Arg Cys Glu Val Val Val Thr Pro Leu Lys Ala Gln Gly Thr Val Gln
100 105 110
Leu Glu Val Val Ala Ser Pro Ala Ser Arg Leu Leu Leu Asp Gln Val
115 120 125
Gly Met Lys Glu Asn Glu Asp Lys Tyr Met Cys Glu Ser Ser Gly Phe
130 135 140
Tyr Pro Glu Ala Ile Asn Ile Thr Trp Glu Lys Gln Thr Gln Lys Phe
145 150 155 160
Pro His Pro Ile Glu Ile Ser Glu Asp Val Ile Thr Gly Pro Thr Ile
165 170 175
Lys Asn Met Asp Gly Thr Phe Asn Val Thr Ser Cys Leu Lys Leu Asn
180 185 190
Ser Ser Gln Glu Asp Pro Gly Thr Val Tyr Gln Cys Val Val Arg His
195 200 205
Ala Ser Leu His Thr Pro Leu Arg Ser Asn Phe Thr Leu Thr Ala Ala
210 215 220
Arg His Ser Leu Ser Glu Thr Glu Lys Thr Asp Asn Phe Ser Gly Gly
225 230 235 240
Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser
245 250 255
Gly Gly Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
260 265 270
Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
275 280 285
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
290 295 300
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
305 310 315 320
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
325 330 335
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
340 345 350
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
355 360 365
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
370 375 380
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
385 390 395 400
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
405 410 415
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
420 425 430
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
435 440 445
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
450 455 460
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
465 470 475 480
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ala Gly Ser Gly His His
485 490 495
His His His His
500
<210> 319
<211> 500
<212> PRT
<213> Artificial Sequence
<220>
<223> Fc-His-tagged human Ala-mutated B7H6 ECD (NKp30 interaction sites
aa35-38 and aa102-105 substituted by Ala)
<400> 319
Asp Leu Lys Val Glu Met Met Ala Gly Gly Thr Gln Ile Thr Pro Leu
1 5 10 15
Asn Asp Asn Val Thr Ile Phe Cys Asn Ile Phe Tyr Ser Gln Pro Leu
20 25 30
Asn Ile Ala Ala Ala Ala Ile Thr Trp Phe Trp Lys Ser Leu Thr Phe
35 40 45
Asp Lys Glu Val Lys Val Phe Glu Phe Phe Gly Asp His Gln Glu Ala
50 55 60
Phe Arg Pro Gly Ala Ile Val Ser Pro Trp Arg Leu Lys Ser Gly Asp
65 70 75 80
Ala Ser Leu Arg Leu Pro Gly Ile Gln Leu Glu Glu Ala Gly Glu Tyr
85 90 95
Arg Cys Glu Val Val Val Ala Ala Ala Ala Ala Gln Gly Thr Val Gln
100 105 110
Leu Glu Val Val Ala Ser Pro Ala Ser Arg Leu Leu Leu Asp Gln Val
115 120 125
Gly Met Lys Glu Asn Glu Asp Lys Tyr Met Cys Glu Ser Ser Gly Phe
130 135 140
Tyr Pro Glu Ala Ile Asn Ile Thr Trp Glu Lys Gln Thr Gln Lys Phe
145 150 155 160
Pro His Pro Ile Glu Ile Ser Glu Asp Val Ile Thr Gly Pro Thr Ile
165 170 175
Lys Asn Met Asp Gly Thr Phe Asn Val Thr Ser Cys Leu Lys Leu Asn
180 185 190
Ser Ser Gln Glu Asp Pro Gly Thr Val Tyr Gln Cys Val Val Arg His
195 200 205
Ala Ser Leu His Thr Pro Leu Arg Ser Asn Phe Thr Leu Thr Ala Ala
210 215 220
Arg His Ser Leu Ser Glu Thr Glu Lys Thr Asp Asn Phe Ser Gly Gly
225 230 235 240
Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser
245 250 255
Gly Gly Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
260 265 270
Pro Ala Pro Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro
275 280 285
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
290 295 300
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
305 310 315 320
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
325 330 335
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
340 345 350
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
355 360 365
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
370 375 380
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
385 390 395 400
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
405 410 415
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
420 425 430
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
435 440 445
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
450 455 460
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
465 470 475 480
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ala Gly Ser Gly His His
485 490 495
His His His His
500
<210> 320
<211> 245
<212> PRT
<213> Artificial Sequence
<220>
<223> His-tagged cyno B7H6 ECD
<400> 320
Asp Leu Lys Val Glu Met Met Ala Arg Gly Ile Gln Ala Thr Arg Leu
1 5 10 15
Asn Asp Ser Val Thr Ile Ser Cys Lys Val Ile Tyr Ser Gln Pro Leu
20 25 30
Asn Ile Thr Ser Met Gly Ile Thr Trp Phe Arg Lys Ser Leu Thr Leu
35 40 45
Asp Lys Glu Val Lys Val Phe Glu Phe Phe Gly Asp His Gln Lys Ala
50 55 60
Phe Arg Pro Gly Ala Asn Val Ser Leu Trp Arg Leu Lys Ser Gly Asp
65 70 75 80
Ala Ser Leu Lys Leu Pro Gly Val Gln Leu Glu Glu Ala Gly Glu Tyr
85 90 95
Arg Cys Glu Val Val Val Thr Pro Leu Lys Ala Gln Gly Thr Val Gln
100 105 110
Leu Lys Val Val Ala Ser Pro Thr Ser Arg Leu Phe Gln Asp Gln Ala
115 120 125
Val Val Lys Glu Asn Glu Gly Lys Tyr Met Cys Glu Ser Ser Arg Phe
130 135 140
Tyr Pro Lys Asp Ile Asn Ile Thr Trp Glu Lys Trp Thr Gln Lys Ser
145 150 155 160
Pro His His Val Val Ile Ser Glu Asn Val Ile Thr Gly Pro Thr Ile
165 170 175
Lys Asn Met Asp Gly Thr Phe Asn Ile Thr Ser Tyr Leu Lys Leu Asn
180 185 190
Ser Ser Gln Glu Asp Pro Gly Thr Val Tyr Arg Cys Val Ile Arg His
195 200 205
Glu Ser Leu His Thr Pro Val Ser Ile Asp Phe Ile Leu Thr Ala Pro
210 215 220
Gln Gln Ser Leu Ser Glu Pro Glu Lys Thr Asp Ala Gly Ser Gly His
225 230 235 240
His His His His His
245
<210> 321
<211> 497
<212> PRT
<213> Artificial Sequence
<220>
<223> Fc-His-tagged cyno B7H6 ECD
<400> 321
Asp Leu Lys Val Glu Met Met Ala Arg Gly Ile Gln Ala Thr Arg Leu
1 5 10 15
Asn Asp Ser Val Thr Ile Ser Cys Lys Val Ile Tyr Ser Gln Pro Leu
20 25 30
Asn Ile Thr Ser Met Gly Ile Thr Trp Phe Arg Lys Ser Leu Thr Leu
35 40 45
Asp Lys Glu Val Lys Val Phe Glu Phe Phe Gly Asp His Gln Lys Ala
50 55 60
Phe Arg Pro Gly Ala Asn Val Ser Leu Trp Arg Leu Lys Ser Gly Asp
65 70 75 80
Ala Ser Leu Lys Leu Pro Gly Val Gln Leu Glu Glu Ala Gly Glu Tyr
85 90 95
Arg Cys Glu Val Val Val Thr Pro Leu Lys Ala Gln Gly Thr Val Gln
100 105 110
Leu Lys Val Val Ala Ser Pro Thr Ser Arg Leu Phe Gln Asp Gln Ala
115 120 125
Val Val Lys Glu Asn Glu Gly Lys Tyr Met Cys Glu Ser Ser Arg Phe
130 135 140
Tyr Pro Lys Asp Ile Asn Ile Thr Trp Glu Lys Trp Thr Gln Lys Ser
145 150 155 160
Pro His His Val Val Ile Ser Glu Asn Val Ile Thr Gly Pro Thr Ile
165 170 175
Lys Asn Met Asp Gly Thr Phe Asn Ile Thr Ser Tyr Leu Lys Leu Asn
180 185 190
Ser Ser Gln Glu Asp Pro Gly Thr Val Tyr Arg Cys Val Ile Arg His
195 200 205
Glu Ser Leu His Thr Pro Val Ser Ile Asp Phe Ile Leu Thr Ala Pro
210 215 220
Gln Gln Ser Leu Ser Glu Pro Glu Lys Thr Asp Gly Gly Ser Gly Gly
225 230 235 240
Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Glu
245 250 255
Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro
260 265 270
Glu Ala Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
275 280 285
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
290 295 300
Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp
305 310 315 320
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr
325 330 335
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
340 345 350
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu
355 360 365
Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
370 375 380
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys
385 390 395 400
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
405 410 415
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
420 425 430
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
435 440 445
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser
450 455 460
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
465 470 475 480
Leu Ser Leu Ser Pro Gly Lys Ala Gly Ser Gly His His His His His
485 490 495
His
<210> 322
<211> 487
<212> PRT
<213> Artificial Sequence
<220>
<223> Human CD3E+G-HuFc-His
<400> 322
Gln Asp Gly Asn Glu Glu Met Gly Gly Ile Thr Gln Thr Pro Tyr Lys
1 5 10 15
Val Ser Ile Ser Gly Thr Thr Val Ile Leu Thr Cys Pro Gln Tyr Pro
20 25 30
Gly Ser Glu Ile Leu Trp Gln His Asn Asp Lys Asn Ile Gly Gly Asp
35 40 45
Glu Asp Asp Lys Asn Ile Gly Ser Asp Glu Asp His Leu Ser Leu Lys
50 55 60
Glu Phe Ser Glu Leu Glu Gln Ser Gly Tyr Tyr Val Cys Tyr Pro Arg
65 70 75 80
Gly Ser Lys Pro Glu Asp Ala Asn Phe Tyr Leu Tyr Leu Arg Ala Arg
85 90 95
Val Cys Glu Asn Cys Met Glu Met Asp Gly Gly Gly Ser Gly Gly Gly
100 105 110
Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly
115 120 125
Ser Gly Gly Gln Ser Ile Lys Gly Asn His Leu Val Lys Val Tyr Asp
130 135 140
Tyr Gln Glu Asp Gly Ser Val Leu Leu Thr Cys Asp Ala Glu Ala Lys
145 150 155 160
Asn Ile Thr Trp Phe Lys Asp Gly Lys Met Ile Gly Phe Leu Thr Glu
165 170 175
Asp Lys Lys Lys Trp Asn Leu Gly Ser Asn Ala Lys Asp Pro Arg Gly
180 185 190
Met Tyr Gln Cys Lys Gly Ser Gln Asn Lys Ser Lys Pro Leu Gln Val
195 200 205
Tyr Tyr Arg Met Cys Gln Asn Cys Ile Glu Leu Asn Ala Ala Thr Ile
210 215 220
Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Ser
225 230 235 240
Gly Gly Ser Gly Gly Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
245 250 255
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
260 265 270
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
275 280 285
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
290 295 300
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
305 310 315 320
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
325 330 335
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
340 345 350
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
355 360 365
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
370 375 380
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
385 390 395 400
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
405 410 415
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
420 425 430
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
435 440 445
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
450 455 460
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys Ala Gly Ser
465 470 475 480
Ala His His His His His His
485
<210> 323
<211> 477
<212> PRT
<213> Artificial Sequence
<220>
<223> cyno CD3 E+G huFc-His
<400> 323
Gln Asp Gly Asn Glu Glu Met Gly Ser Ile Thr Gln Thr Pro Tyr Gln
1 5 10 15
Val Ser Ile Ser Gly Thr Thr Val Ile Leu Thr Cys Ser Gln His Leu
20 25 30
Gly Ser Glu Ala Gln Trp Gln His Asn Gly Lys Asn Lys Gly Asp Ser
35 40 45
Gly Asp Gln Leu Phe Leu Pro Glu Phe Ser Glu Met Glu Gln Ser Gly
50 55 60
Tyr Tyr Val Cys Tyr Pro Arg Gly Ser Asn Pro Glu Asp Ala Ser His
65 70 75 80
His Leu Tyr Leu Lys Ala Arg Val Cys Glu Asn Cys Met Glu Met Asp
85 90 95
Val Met Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly
100 105 110
Gly Ser Gly Gly Gly Ser Gly Gly Gly Ser Gly Gly Gln Ser Phe Glu
115 120 125
Glu Asn Arg Lys Leu Asn Val Tyr Asn Gln Glu Asp Gly Ser Val Leu
130 135 140
Leu Thr Cys His Val Lys Asn Thr Asn Ile Thr Trp Phe Lys Glu Gly
145 150 155 160
Lys Met Ile Asp Ile Leu Thr Ala His Lys Asn Lys Trp Asn Leu Gly
165 170 175
Ser Asn Thr Lys Asp Pro Arg Gly Val Tyr Gln Cys Lys Gly Ser Lys
180 185 190
Asp Lys Ser Lys Thr Leu Gln Val Tyr Tyr Arg Met Cys Gln Asn Cys
195 200 205
Ile Glu Leu Asn Ala Ala Thr Gly Gly Ser Gly Gly Ser Gly Gly Ser
210 215 220
Gly Gly Ser Gly Gly Ser Gly Gly Ser Gly Gly Glu Pro Lys Ser Cys
225 230 235 240
Asp Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly
245 250 255
Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met
260 265 270
Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His
275 280 285
Glu Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val
290 295 300
His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr
305 310 315 320
Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly
325 330 335
Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile
340 345 350
Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val
355 360 365
Tyr Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser
370 375 380
Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu
385 390 395 400
Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro
405 410 415
Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val
420 425 430
Asp Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met
435 440 445
His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser
450 455 460
Pro Gly Lys Ala Gly Ser Ala His His His His His His
465 470 475
<210> 324
<211> 461
<212> PRT
<213> Artificial Sequence
<220>
<223> Human B7H1-Fc
<400> 324
Thr Val Thr Val Pro Lys Asp Leu Tyr Val Val Glu Tyr Gly Ser Asn
1 5 10 15
Met Thr Ile Glu Cys Lys Phe Pro Val Glu Lys Gln Leu Asp Leu Ala
20 25 30
Ala Leu Ile Val Tyr Trp Glu Met Glu Asp Lys Asn Ile Ile Gln Phe
35 40 45
Val His Gly Glu Glu Asp Leu Lys Val Gln His Ser Ser Tyr Arg Gln
50 55 60
Arg Ala Arg Leu Leu Lys Asp Gln Leu Ser Leu Gly Asn Ala Ala Leu
65 70 75 80
Gln Ile Thr Asp Val Lys Leu Gln Asp Ala Gly Val Tyr Arg Cys Met
85 90 95
Ile Ser Tyr Gly Gly Ala Asp Tyr Lys Arg Ile Thr Val Lys Val Asn
100 105 110
Ala Pro Tyr Asn Lys Ile Asn Gln Arg Ile Leu Val Val Asp Pro Val
115 120 125
Thr Ser Glu His Glu Leu Thr Cys Gln Ala Glu Gly Tyr Pro Lys Ala
130 135 140
Glu Val Ile Trp Thr Ser Ser Asp His Gln Val Leu Ser Gly Lys Thr
145 150 155 160
Thr Thr Thr Asn Ser Lys Arg Glu Glu Lys Leu Phe Asn Val Thr Ser
165 170 175
Thr Leu Arg Ile Asn Thr Thr Thr Asn Glu Ile Phe Tyr Cys Thr Phe
180 185 190
Arg Arg Leu Asp Pro Glu Glu Asn His Thr Ala Glu Leu Val Ile Pro
195 200 205
Glu Leu Pro Leu Ala His Pro Pro Asn Glu Arg Thr Glu Gln Lys Leu
210 215 220
Ile Ser Glu Glu Asp Leu Leu Val Pro Arg Gly Ser Arg Ser Val Glu
225 230 235 240
Cys Pro Pro Cys Pro Ala Pro Pro Val Ala Gly Pro Ser Val Phe Leu
245 250 255
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
260 265 270
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
275 280 285
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
290 295 300
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
305 310 315 320
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
325 330 335
Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys
340 345 350
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
355 360 365
Arg Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
370 375 380
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
385 390 395 400
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
405 410 415
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
420 425 430
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Gly Leu His Asn
435 440 445
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
450 455 460
<210> 325
<211> 21
<212> PRT
<213> Artificial Sequence
<220>
<223> Vk leader
<400> 325
Met Glu Thr Asp Thr Leu Leu Leu Trp Val Leu Leu Leu Trp Val Pro
1 5 10 15
Gly Ser Thr Gly Asp
20
<210> 326
<211> 16
<212> PRT
<213> Artificial Sequence
<220>
<223> 6-His-myc tag
<400> 326
His His His His His His Glu Gln Lys Leu Ile Ser Glu Glu Asp Leu
1 5 10 15
<210> 327
<211> 238
<212> PRT
<213> Artificial Sequence
<220>
<223> Cynomolgus B7-H6 extracellular domain (NCBI XP_005578557.1,
aa25-262)
<400> 327
Asp Leu Lys Val Glu Met Met Ala Arg Gly Ile Gln Ala Thr Arg Leu
1 5 10 15
Asn Asp Ser Val Thr Ile Ser Cys Lys Val Ile Tyr Ser Gln Pro Leu
20 25 30
Asn Ile Thr Ser Met Gly Ile Thr Trp Phe Arg Lys Ser Leu Thr Leu
35 40 45
Asp Lys Glu Val Lys Val Phe Glu Phe Phe Gly Asp His Gln Lys Ala
50 55 60
Phe Arg Pro Gly Ala Asn Val Ser Leu Trp Arg Leu Lys Ser Gly Asp
65 70 75 80
Ala Ser Leu Lys Leu Pro Gly Val Gln Leu Glu Glu Ala Gly Glu Tyr
85 90 95
Arg Cys Glu Val Val Val Thr Pro Leu Lys Ala Gln Gly Thr Val Gln
100 105 110
Leu Lys Val Val Ala Ser Pro Thr Ser Arg Leu Phe Gln Asp Gln Ala
115 120 125
Val Val Lys Glu Asn Glu Gly Lys Tyr Met Cys Glu Ser Ser Arg Phe
130 135 140
Tyr Pro Lys Asp Ile Asn Ile Thr Trp Glu Lys Trp Thr Gln Lys Ser
145 150 155 160
Pro His His Val Val Ile Ser Glu Asn Val Ile Thr Gly Pro Thr Ile
165 170 175
Lys Asn Met Asp Gly Thr Phe Asn Ile Thr Ser Tyr Leu Lys Leu Asn
180 185 190
Ser Ser Gln Glu Asp Pro Gly Thr Val Tyr Arg Cys Val Ile Arg His
195 200 205
Glu Ser Leu His Thr Pro Val Ser Ile Asp Phe Ile Leu Thr Ala Pro
210 215 220
Gln Gln Ser Leu Ser Glu Pro Glu Lys Thr Asp Ile Phe Ser
225 230 235
<210> 328
<211> 6
<212> PRT
<213> Artificial Sequence
<220>
<223> Linker
<400> 328
Ser Gly Gly Gly Gly Ser
1 5
<210> 329
<211> 23
<212> PRT
<213> Artificial Sequence
<220>
<223> Human EpCAM transmembrane domain (Uniprot P16422, aa266-288)
<400> 329
Ala Gly Val Ile Ala Val Ile Val Val Val Val Ile Ala Val Val Ala
1 5 10 15
Gly Ile Val Val Leu Val Ile
20
<210> 330
<211> 26
<212> PRT
<213> Artificial Sequence
<220>
<223> Human EpCAM intracellular domain (Uniprot P16422, aa289-314)
<400> 330
Ser Arg Lys Lys Arg Met Ala Lys Tyr Glu Lys Ala Glu Ile Lys Glu
1 5 10 15
Met Gly Glu Met His Arg Glu Leu Asn Ala
20 25
<210> 331
<211> 446
<212> PRT
<213> Artificial Sequence
<220>
<223> PD1-1 HC
<400> 331
Glu Val Met Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Ala Ser
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Tyr Ile Ser Gly Gly Gly Gly Asp Thr Tyr Tyr Ser Ser Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Ser Asn Val Asn Tyr Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 332
<211> 218
<212> PRT
<213> Artificial Sequence
<220>
<223> PD1-1 LC
<400> 332
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Met Ser Cys Arg Ala Ser Glu Asn Ile Asp Thr Ser
20 25 30
Gly Ile Ser Phe Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Val Ala Ser Asn Gln Gly Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Val Pro Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 333
<211> 446
<212> PRT
<213> Artificial Sequence
<220>
<223> PD1-2 HC
<400> 333
Glu Val Met Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Ala Ser
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Tyr Ile Ser Gly Gly Gly Gly Asp Thr Tyr Tyr Ser Ser Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Ser Asn Pro Asn Tyr Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 334
<211> 218
<212> PRT
<213> Artificial Sequence
<220>
<223> PD1-2 LC
<400> 334
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Met Ser Cys Arg Ala Ser Glu Asn Ile Asp Thr Ser
20 25 30
Gly Ile Ser Phe Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Val Ala Ser Asn Gln Gly Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Val Pro Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 335
<211> 446
<212> PRT
<213> Artificial Sequence
<220>
<223> PD1-3 HC
<400> 335
Glu Val Met Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Lys Ser
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Tyr Ile Ser Gly Gly Gly Gly Asp Thr Tyr Tyr Ser Ser Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Ser Asn Val Asn Tyr Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 336
<211> 218
<212> PRT
<213> Artificial Sequence
<220>
<223> PD1-3 LC
<400> 336
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Met Ser Cys Arg Ala Ser Glu Asn Ile Asp Val Ser
20 25 30
Gly Ile Ser Phe Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Val Ala Ser Asn Gln Gly Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Val Pro Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 337
<211> 446
<212> PRT
<213> Artificial Sequence
<220>
<223> PD1-4 HC
<400> 337
Glu Val Met Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Lys Ser
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Tyr Ile Ser Gly Gly Gly Gly Asp Thr Tyr Tyr Ser Ser Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Ser Asn Val Asn Tyr Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 338
<211> 218
<212> PRT
<213> Artificial Sequence
<220>
<223> PD1-4 LC
<400> 338
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Met Ser Cys Arg Ala Ser Glu Asn Ile Asp Val Ser
20 25 30
Gly Ile Ser Phe Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Val Ala Ser Asn Gln Gly Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Val Pro Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
<210> 339
<211> 446
<212> PRT
<213> Artificial Sequence
<220>
<223> PD1-5 HC
<400> 339
Glu Val Met Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Thr Ala Ser Gly Phe Thr Phe Ser Lys Ser
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Tyr Ile Ser Gly Gly Gly Gly Asp Thr Tyr Tyr Ser Ser Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg His Ser Asn Val Asn Tyr Tyr Ala Met Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Cys Ser Arg Ser Thr Ser Glu Ser Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Lys Thr Tyr Thr Cys Asn Val Asp His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Arg Val Glu Ser Lys Tyr Gly Pro
210 215 220
Pro Cys Pro Pro Cys Pro Ala Pro Glu Phe Leu Gly Gly Pro Ser Val
225 230 235 240
Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr
245 250 255
Pro Glu Val Thr Cys Val Val Val Asp Val Ser Gln Glu Asp Pro Glu
260 265 270
Val Gln Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys
275 280 285
Thr Lys Pro Arg Glu Glu Gln Phe Asn Ser Thr Tyr Arg Val Val Ser
290 295 300
Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys
305 310 315 320
Cys Lys Val Ser Asn Lys Gly Leu Pro Ser Ser Ile Glu Lys Thr Ile
325 330 335
Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro
340 345 350
Pro Ser Gln Glu Glu Met Thr Lys Asn Gln Val Ser Leu Thr Cys Leu
355 360 365
Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn
370 375 380
Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser
385 390 395 400
Asp Gly Ser Phe Phe Leu Tyr Ser Arg Leu Thr Val Asp Lys Ser Arg
405 410 415
Trp Gln Glu Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu
420 425 430
His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Leu Gly
435 440 445
<210> 340
<211> 218
<212> PRT
<213> Artificial Sequence
<220>
<223> PD1-5 LC
<400> 340
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Met Ser Cys Arg Ala Ser Glu Asn Ile Asp Val Ser
20 25 30
Gly Ile Ser Phe Met Asn Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro
35 40 45
Lys Leu Leu Ile Tyr Val Ala Ser Asn Gln Gly Ser Gly Ile Pro Ala
50 55 60
Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser
65 70 75 80
Arg Leu Glu Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Ser Lys
85 90 95
Glu Val Pro Trp Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg
100 105 110
Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln
115 120 125
Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr
130 135 140
Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser
145 150 155 160
Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr
165 170 175
Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys
180 185 190
His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro
195 200 205
Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
210 215
Claims (53)
- B7H6에 특이적으로 결합하는 제1 항원 결합 단위 및 CD3에 특이적으로 결합하는 제2 항원 결합 단위를 포함하는 단백질로서, 여기서 B7H6에 특이적으로 결합하는 상기 제1 항원 결합 단위는 하기 i) 내지 xxiv)로 이루어진 군으로부터 선택되는 단백질:
i) 서열 번호 1 (CDR1), 서열 번호 2 (CDR2) 및 서열 번호 3 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 4 (CDR1), 서열 번호 5 (CDR2) 및 서열 번호 6 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
ii) 서열 번호 7 (CDR1), 서열 번호 8 (CDR2) 및 서열 번호 9 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 10 (CDR1), 서열 번호 11 (CDR2) 및 서열 번호 12 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
iii) 서열 번호 13 (CDR1), 서열 번호 14 (CDR2) 및 서열 번호 15 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 16 (CDR1), 서열 번호 17 (CDR2) 및 서열 번호 18 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
iv) 서열 번호 19 (CDR1), 서열 번호 20 (CDR2) 및 서열 번호 21 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 22 (CDR1), 서열 번호 23 (CDR2) 및 서열 번호 24 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
v) 서열 번호 25 (CDR1), 서열 번호 26 (CDR2) 및 서열 번호 27 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 28 (CDR1), 서열 번호 29 (CDR2) 및 서열 번호 30 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
vi) 서열 번호 31 (CDR1), 서열 번호 32 (CDR2) 및 서열 번호 33 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 34 (CDR1), 서열 번호 35 (CDR2) 및 서열 번호 36 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
vii) 서열 번호 37 (CDR1), 서열 번호 38 (CDR2) 및 서열 번호 39 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 40 (CDR1), 서열 번호 41 (CDR2) 및 서열 번호 42 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
viii) 서열 번호 43 (CDR1), 서열 번호 44 (CDR2) 및 서열 번호 45 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 46 (CDR1), 서열 번호 47 (CDR2) 및 서열 번호 48 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
ix) 서열 번호 49 (CDR1), 서열 번호 50 (CDR2) 및 서열 번호 51 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 52 (CDR1), 서열 번호 53 (CDR2) 및 서열 번호 54 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
x) 서열 번호 55 (CDR1), 서열 번호 56 (CDR2) 및 서열 번호 57 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 58 (CDR1), 서열 번호 59 (CDR2) 및 서열 번호 60 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xi) 서열 번호 61 (CDR1), 서열 번호 62 (CDR2) 및 서열 번호 63 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 64 (CDR1), 서열 번호 65 (CDR2) 및 서열 번호 66 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xii) 서열 번호 67 (CDR1), 서열 번호 68 (CDR2) 및 서열 번호 69 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 70 (CDR1), 서열 번호 71 (CDR2) 및 서열 번호 72 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xiii) 서열 번호 73 (CDR1), 서열 번호 74 (CDR2) 및 서열 번호 75 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 76 (CDR1), 서열 번호 77 (CDR2) 및 서열 번호 78 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xiv) 서열 번호 79 (CDR1), 서열 번호 80 (CDR2) 및 서열 번호 81 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 82 (CDR1), 서열 번호 83 (CDR2) 및 서열 번호 84 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xv) 서열 번호 85 (CDR1), 서열 번호 86 (CDR2) 및 서열 번호 87 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 88 (CDR1), 서열 번호 89 (CDR2) 및 서열 번호 90 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xvi) 서열 번호 91 (CDR1), 서열 번호 92 (CDR2) 및 서열 번호 93 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 94 (CDR1), 서열 번호 95 (CDR2) 및 서열 번호 96 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xvii) 서열 번호 97 (CDR1), 서열 번호 98(CDR2) 및 서열 번호 99 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 100 (CDR1), 서열 번호 101 (CDR2) 및 서열 번호 102 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xviii) 서열 번호 103 (CDR1), 서열 번호 104 (CDR2) 및 서열 번호 105 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 106 (CDR1), 서열 번호 107 (CDR2) 및 서열 번호 108 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xix) 서열 번호 109 (CDR1), 서열 번호 110 (CDR2) 및 서열 번호 111 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 112 (CDR1), 서열 번호 113 (CDR2) 및 서열 번호 114 (CDR3)의 아미노산 서열을 포함하는 중쇄 CD을 포함하는 항원 결합 단위;
xx) 서열 번호 115 (CDR1), 서열 번호 116 (CDR2) 및 서열 번호 117 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 118 (CDR1), 서열 번호 119 (CDR2) 및 서열 번호 120 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xxi) 서열 번호 121 (CDR1), 서열 번호 122 (CDR2) 및 서열 번호 123 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 124 (CDR1), 서열 번호 125 (CDR2) 및 서열 번호 126 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xxii) 서열 번호 127 (CDR1), 서열 번호 128 (CDR2) 및 서열 번호 129 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 130 (CDR1), 서열 번호 131 (CDR2) 및 서열 번호 132 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
xxiii) 서열 번호 133 (CDR1), 서열 번호 134 (CDR2) 및 서열 번호 135 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 136 (CDR1), 서열 번호 137 (CDR2) 및 서열 번호 138 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위; 및
xxiv) 서열 번호 139 (CDR1), 서열 번호 140 (CDR2) 및 서열 번호 141 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 142 (CDR1), 서열 번호 143 (CDR2) 및 서열 번호 144 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위. - 제1항에 있어서, B7H6에 특이적으로 결합하는 상기 제1 항원 결합 단위는 하기 i) 내지 xxiv)로 이루어진 군으로부터 선택되는 단백질:
i) 서열 번호 145의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 146의 아미노산 서열을 포함하는 중쇄 가변 도메인;
ii) 서열 번호 147의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 148의 아미노산 서열을 포함하는 중쇄 가변 도메인;
iii) 서열 번호 149의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 150의 아미노산 서열을 포함하는 중쇄 가변 도메인;
iv) 서열 번호 151의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 152의 아미노산 서열을 포함하는 중쇄 가변 도메인;
v) 서열 번호 153의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 154의 아미노산 서열을 포함하는 중쇄 가변 도메인;
vi) 서열 번호 155의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 156의 아미노산 서열을 포함하는 중쇄 가변 도메인;
vii) 서열 번호 157의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 158의 아미노산 서열을 포함하는 중쇄 가변 도메인;
viii) 서열 번호 159의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 160의 아미노산 서열을 포함하는 중쇄 가변 도메인;
ix) 서열 번호 161의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 162의 아미노산 서열을 포함하는 중쇄 가변 도메인;
x) 서열 번호 163의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 164의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xi) 서열 번호 165의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 166의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xii) 서열 번호 167의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 168의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xiii) 서열 번호 169의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 170의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xiv) 서열 번호 171의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 172의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xv) 서열 번호 173의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 174의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xvi) 서열 번호 175의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 176의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xvii) 서열 번호 177의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 178의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xviii) 서열 번호 179의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 180의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xix) 서열 번호 181의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 182의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xx) 서열 번호 183의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 184의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xxi) 서열 번호 185의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 186의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xxii) 서열 번호 187의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 188의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xxiii) 서열 번호 189의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 190의 아미노산 서열을 포함하는 중쇄 가변 도메인; 및
xxiv) 서열 번호 191의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 192의 아미노산 서열을 포함하는 중쇄 가변 도메인. - 제1항 또는 제2항에 있어서, CD3에 특이적으로 결합하는 상기 제2 항원 결합 단위는 하기 i) 내지 vi)로 이루어진 군으로부터 선택되는 단백질:
i) 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
ii) 서열 번호 263 (CDR1), 서열 번호 264 (CDR2) 및 서열 번호 265 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 266 (CDR1), 서열 번호 267 (CDR2) 및 서열 번호 268 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
iii) 서열 번호 269 (CDR1), 서열 번호 270 (CDR2) 및 서열 번호 271 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 272 (CDR1), 서열 번호 273 (CDR2) 및 서열 번호 274 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
iv) 서열 번호 275 (CDR1), 서열 번호 276 (CDR2) 및 서열 번호 277 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 278 (CDR1), 서열 번호 279 (CDR2) 및 서열 번호 280 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위;
v) 서열 번호 281 (CDR1), 서열 번호 282 (CDR2) 및 서열 번호 283 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 284 (CDR1), 서열 번호 285 (CDR2) 및 서열 번호 286 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위; 및
vi) 서열 번호 287 (CDR1), 서열 번호 288 (CDR2) 및 서열 번호 289 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 290 (CDR1), 서열 번호 291 (CDR2) 및 서열 번호 292 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는 항원 결합 단위. - 제1항 내지 제3항 중 어느 한 항에 있어서, CD3에 특이적으로 결합하는 상기 제2 항원 결합 단위는 하기 i) 내지 vi)로 이루어진 군으로부터 선택되는 단백질:
i) 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인;
ii) 서열 번호 295의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 296의 아미노산 서열을 포함하는 중쇄 가변 도메인;
iii) 서열 번호 297의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 298의 아미노산 서열을 포함하는 중쇄 가변 도메인;
iv) 서열 번호 299의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 300의 아미노산 서열을 포함하는 중쇄 가변 도메인;
v) 서열 번호 301의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 302의 아미노산 서열을 포함하는 중쇄 가변 도메인; 및
vi) 서열 번호 303의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 304의 아미노산 서열을 포함하는 중쇄 가변 도메인. - 제1항 내지 제4항 중 어느 한 항에 있어서,
i) B7H6에 특이적으로 결합하는 상기 제1 항원 결합 단위는 그의 N-에서 C-말단으로 제1 경쇄 가변 도메인, 제1 경쇄 불변 도메인, 제1 펩티드 링커, 제1 중쇄 가변 도메인 및 제1 중쇄 불변 CH1 도메인을 포함하고;
ii) CD3에 특이적으로 결합하는 상기 제2 항원 결합 단위는 그의 N-말단에서 C-말단으로 제2 경쇄 가변 도메인, 제2 경쇄 불변 도메인, 제2 펩티드 링커, 제2 중쇄 가변 도메인 및 제2 중쇄 불변 CH1 도메인을 포함하는,
단백질. - 제5항에 있어서,
i) 상기 제1 항원 결합 단위는 서열 번호 67 (CDR1), 서열 번호 68 (CDR2) 및 서열 번호 69 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 70 (CDR1), 서열 번호 71 (CDR2) 및 서열 번호 72 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하고, 상기 제2 항원 결합 단위는 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하거나;
ii) 상기 제1 항원 결합 단위는 서열 번호 79 (CDR1), 서열 번호 80 (CDR2) 및 서열 번호 81 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 82 (CDR1), 서열 번호 83 (CDR2) 및 서열 번호 84 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하고, 상기 제2 항원 결합 단위는 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하거나;
iii) 상기 제1 항원 결합 단위는 서열 번호 85 (CDR1), 서열 번호 86 (CDR2) 및 서열 번호 87 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 88 (CDR1), 서열 번호 89 (CDR2) 및 서열 번호 90 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하고, 상기 제2 항원 결합 단위는 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하거나; 또는
iv) 상기 제1 항원 결합 단위는 서열 번호 91 (CDR1), 서열 번호 92 (CDR2) 및 서열 번호 93 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 94 (CDR1), 서열 번호 95 (CDR2) 및 서열 번호 96 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하고, 상기 제2 항원 결합 단위는 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는,
단백질. - 제5항 또는 제6항에 있어서,
i) 상기 제1 항원 결합 단위는 서열 번호 167의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 168의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하고, 상기 제2 항원 결합 단위는 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하거나;
ii) 상기 제1 항원 결합 단위는 서열 번호 171의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 172의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하고, 상기 제2 항원 결합 단위는 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하거나;
iii) 상기 제1 항원 결합 단위는 서열 번호 173의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 174의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하고, 상기 제2 항원 결합 단위는 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하거나; 또는
상기 제1 항원 결합 단위는 서열 번호 175의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 176의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하고, 상기 제2 항원 결합 단위는 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하는,
단백질. - 제5항 내지 제7항 중 어느 한 항에 있어서, 상기 제1 및/또는 제2 펩티드 링커는 26 내지 42개의 아미노산, 바람직하게는 30 내지 40개의 아미노산, 34 내지 40개의 아미노산, 또는 36 내지 39개의 아미노산 중 어느 하나, 보다 바람직하게는 38개의 아미노산을 포함하는 단백질.
- 제5항 내지 제8항 중 어느 한 항에 있어서, 상기 제1 링커 및/또는 제2 링커는 바람직하게는 서열 번호 250의 아미노산 서열을 포함하는 Gly-Ser 링커이고, 보다 바람직하게는 상기 제1 및 제2 펩티드 링커는 동일한 서열 (예: 서열 번호 250)을 포함하는 단백질.
- 제5항 내지 제9항 중 어느 한 항에 있어서, 제1 경쇄 불변 도메인 및 제2 경쇄 불변 도메인은 인간 카파 또는 람다 도메인을 포함하는 단백질.
- 제5항 내지 제10항 중 어느 한 항에 있어서, B7H6에 특이적인 상기 제1 항원 결합 단위는 서열 번호 193, 서열 번호 194, 서열 번호 195, 서열 번호 196 서열 번호 197 서열 번호 198 서열 번호 199 서열 번호 200 서열 번호 201 서열 번호 202 서열 번호 203 서열 번호 204 서열 번호 205, 서열 번호 206, 서열 번호 207, 서열 번호 208, 서열 번호 209, 서열 번호 210, 서열 번호 211, 서열 번호 212, 서열 번호 213, 서열 번호 214, 서열 번호 215, 및 서열 번호 216으로 이루어진 군으로부터 선택되는 아미노산 서열을 포함하고, CD3에 특이적인 상기 제2 항원 결합 단위는 서열 번호 305, 서열 번호 306, 서열 번호 307, 서열 번호 308, 서열 번호 309, 및 서열 번호 310으로 이루어진 군으로부터 선택된 아미노산 서열을 포함하는 단백질.
- 제11항에 있어서,
(i) B7H6에 특이적인 상기 제1 항원 결합 단위는 서열 번호 204의 아미노산 서열을 포함하고, CD3에 특이적인 상기 제2 항원 결합 단위는 서열 번호 305의 아미노산 서열을 포함하거나;
(ii) B7H6에 특이적인 상기 제1 항원 결합 단위는 서열 번호 206의 아미노산 서열을 포함하고, CD3에 특이적인 상기 제2 항원 결합 단위는 서열 번호 305의 아미노산 서열을 포함하거나;
(iii) B7H6에 특이적인 상기 제1 항원 결합 단위는 서열 번호 207의 아미노산 서열을 포함하고, CD3에 특이적인 상기 제2 항원 결합 단위는 서열 번호 305의 아미노산 서열을 포함하거나; 또는
(iv) B7H6에 특이적인 상기 제1 항원 결합 단위는 서열 번호 208의 아미노산 서열을 포함하고, CD3에 특이적인 상기 제2 항원 결합 단위는 서열 번호 305의 아미노산 서열을 포함하는,
단백질. - 제5항 내지 제12항 중 어느 한 항에 있어서, 제1 및 제2 Fc 도메인을 추가로 포함하고, 상기 제1 Fc 도메인은 상기 제1 항원 결합 단위, 바람직하게는 상기 제1 항원 결합 단위의 C-말단에 공유적으로 연결되고, 상기 제2 Fc 도메인은 상기 제2 항원 결합 단위, 바람직하게는 상기 제2 항원 결합 단위의 C-말단에 공유적으로 연결된 단백질.
- 제13항에 있어서,
i) 상기 제1 Fc 도메인은 위치 366에 티로신 (Y) [T366Y]을 포함하고, 상기 제2 Fc 도메인은 위치 407에 트레오닌 (T) [Y407T]을 포함하거나,
ii) 상기 제1 Fc 도메인은 위치 366에 트립토판 (W) [T366W]을 포함하고, 상기 제2 Fc 도메인은 위치 366에 세린 (S) [T366S], 위치 368에 알라닌 (A) [L368A] 및 위치 407에 발린 (V) [Y407V]을 포함하거나,
iii) 상기 제2 Fc 도메인은 위치 366에 티로신 (Y) [T366Y]을 포함하고, 상기 제1 Fc 도메인은 위치 407에 트레오닌 (T) [Y407T]을 포함하거나, 또는
iv) 상기 제2 Fc 도메인은 위치 366에 트립토판 (W) [T366W]을 포함하고, 상기 제1 Fc 도메인은 위치 366에 세린 (S) [T366S], 위치 368에 알라닌 (A) [L368A] 및 위치 407에 발린 (V) [Y407V]을 포함하고,
바람직하게는 상기 제1 또는 상기 제2 Fc 도메인은 위치 435에 아르기닌 [H435R] 및 위치 436에 페닐알라닌 [Y436F]을 추가로 포함하는,
단백질. - 제13항 또는 제14항에 있어서, 상기 제1 및/또는 상기 제2 Fc 도메인은 위치 234 [L234A] 및 위치 235 [L235A]에 알라닌을 포함하고, 바람직하게는 상기 제1 Fc 도메인은 서열 번호 242의 아미노산 서열을 포함하고, 상기 제2 Fc 도메인은 서열 번호 243의 아미노산 서열을 포함하는 단백질.
- 제5항 내지 제15항 중 어느 한 항에 있어서, 서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 서열 번호 221, 서열 번호 222, 서열 번호 223, 서열 번호 224, 서열 번호 225, 서열 번호 226, 서열 번호 227, 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 및 서열 번호 240으로 이루어진 군으로부터 선택된 아미노산 서열을 포함하는 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 및 서열 번호 311, 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 및 서열 번호 316으로 이루어진 군으로부터 선택된 아미노산 서열을 포함하는 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄를 포함하는 단백질.
- 제16항에 있어서,
(i) B7H6에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 서열 번호 228의 아미노산 서열을 포함하고, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 서열 번호 311의 아미노산 서열을 포함하거나;
(ii) B7H6에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 서열 번호 230의 아미노산 서열을 포함하고, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 서열 번호 311의 아미노산 서열을 포함하거나,
(iii) B7H6에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 서열 번호 231의 아미노산 서열을 포함하고, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 서열 번호 311의 아미노산 서열을 포함하거나; 또는
(iv) B7H6에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 서열 번호 232의 아미노산 서열을 포함하고, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 서열 번호 311의 아미노산 서열을 포함하는,
단백질. - 제16항 내지 제17항 중 어느 한 항에 있어서, 상기 제1 및 상기 제2 폴리펩티드 쇄는 이황화 결합을 통해 연결되어 이중 특이성, 이가 및 이종이량체성 단백질을 형성하는 단백질.
- 제1항 내지 제12항 중 어느 한 항의 단백질의 제1 항원 결합 단위 및/또는 제2 항원 결합 단위를 암호화하고, 선택적으로 제1 및/또는 제2 Fc 도메인을 추가로 암호화하는 단리된 핵산 분자.
- 제16항 또는 제17항의 제1 및/또는 제2 폴리펩티드 쇄를 암호화하는 단리된 핵산 분자.
- 제19항 또는 제20항의 핵산 분자를 포함하는 발현 벡터.
- 제21항의 발현 벡터로 형질감염된 숙주 세포.
- i) 제22항의 숙주 세포를 제1항 내지 제18항 중 어느 한 항의 단백질을 발현할 수 있는 조건하에서 배양하는 단계; 및,
ii) 단백질을 회수하는 단계; 및 선택적으로
iii) 단백질을 추가로 정제 및/또는 변형 및/또는 제형화하는 단계를 포함하는,
제1항 내지 제18항 중 어느 한 항의 단백질을 제조하는 방법. - B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 (B7H6 쇄) 및 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄 (CD3 쇄)를 포함하는 단백질로서, 여기서 상기 제1 폴리펩티드 쇄는 제1 경쇄, 제1 링커 및 제1 중쇄를 포함하고 상기 제2 폴리펩티드 쇄는 제2 경쇄, 제2 링커, 및 제2 중쇄를 포함하며, 바람직하게는 상기 제1 경쇄의 C-말단은 상기 12 펩티드 링커를 통해 상기 제1 중쇄의 N-말단에 공유적으로 연결되고, 상기 제2 경쇄의 C-말단은 상기 제2 펩티드 링커를 통해 상기 제2 중쇄의 N-말단에 공유적으로 연결된, 단백질.
- 제20항에 있어서, 상기 제1 및 상기 제2 폴리펩티드 쇄는 이황화 결합을 통해 연결되어 이중 특이성, 이가 및 이종이량체성 단백질을 형성하는 단백질.
- 제24항에 있어서, B7H6에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 하기 i) 내지 xxiv)로 이루어진 군으로부터 선택된 CDR 서열을 포함하는 경쇄 가변 도메인 및 중쇄 가변 도메인을 포함하는 단백질:
i) 서열 번호 1 (CDR1), 서열 번호 2 (CDR2) 및 서열 번호 3 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 4 (CDR1), 서열 번호 5 (CDR2) 및 서열 번호 6 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
ii) 서열 번호 7 (CDR1), 서열 번호 8 (CDR2) 및 서열 번호 9 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 10 (CDR1), 서열 번호 11 (CDR2) 및 서열 번호 12 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
iii) 서열 번호 13 (CDR1), 서열 번호 14 (CDR2) 및 서열 번호 15 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 16 (CDR1), 서열 번호 17 (CDR2) 및 서열 번호 18 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
iv) 서열 번호 19 (CDR1), 서열 번호 20 (CDR2) 및 서열 번호 21 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 22 (CDR1), 서열 번호 23 (CDR2) 및 서열 번호 24 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
v) 서열 번호 25 (CDR1), 서열 번호 26 (CDR2) 및 서열 번호 27 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 28 (CDR1), 서열 번호 29 (CDR2) 및 서열 번호 30 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
vi) 서열 번호 31 (CDR1), 서열 번호 32 (CDR2) 및 서열 번호 33 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 34 (CDR1), 서열 번호 35 (CDR2) 및 서열 번호 36 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
vii) 서열 번호 37 (CDR1), 서열 번호 38 (CDR2) 및 서열 번호 39 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 40 (CDR1), 서열 번호 41 (CDR2) 및 서열 번호 42 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
viii) 서열 번호 43 (CDR1), 서열 번호 44 (CDR2) 및 서열 번호 45 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 46 (CDR1), 서열 번호 47 (CDR2) 및 서열 번호 48 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
ix) 서열 번호 49 (CDR1), 서열 번호 50 (CDR2) 및 서열 번호 51 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 52 (CDR1), 서열 번호 53 (CDR2) 및 서열 번호 54 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
x) 서열 번호 55 (CDR1), 서열 번호 56 (CDR2) 및 서열 번호 57 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 58 (CDR1), 서열 번호 59 (CDR2) 및 서열 번호 60 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xi) 서열 번호 61 (CDR1), 서열 번호 62 (CDR2) 및 서열 번호 63 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 64 (CDR1), 서열 번호 65 (CDR2) 및 서열 번호 66 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xii) 서열 번호 67 (CDR1), 서열 번호 68 (CDR2) 및 서열 번호 69 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 70 (CDR1), 서열 번호 71 (CDR2) 및 서열 번호 72 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xiii) 서열 번호 73 (CDR1), 서열 번호 74 (CDR2) 및 서열 번호 75 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 76 (CDR1), 서열 번호 77 (CDR2) 및 서열 번호 78 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xiv) 서열 번호 79 (CDR1), 서열 번호 80 (CDR2) 및 서열 번호 81 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 82 (CDR1), 서열 번호 83 (CDR2) 및 서열 번호 84 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xv) 서열 번호 85 (CDR1), 서열 번호 86 (CDR2) 및 서열 번호 87 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 88 (CDR1), 서열 번호 89 (CDR2) 및 서열 번호 90 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xvi) 서열 번호 91 (CDR1), 서열 번호 92 (CDR2) 및 서열 번호 93 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 94 (CDR1), 서열 번호 95 (CDR2) 및 서열 번호 96 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xvii) 서열 번호 97 (CDR1), 서열 번호 98(CDR2) 및 서열 번호 99 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 100 (CDR1), 서열 번호 101 (CDR2) 및 서열 번호 102 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xviii) 서열 번호 103 (CDR1), 서열 번호 104 (CDR2) 및 서열 번호 105 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 106 (CDR1), 서열 번호 107 (CDR2) 및 서열 번호 108 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xix) 서열 번호 109 (CDR1), 서열 번호 110 (CDR2) 및 서열 번호 111 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 112 (CDR1), 서열 번호 113 (CDR2) 및 서열 번호 114 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xx) 서열 번호 115 (CDR1), 서열 번호 116 (CDR2) 및 서열 번호 117 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 118 (CDR1), 서열 번호 119 (CDR2) 및 서열 번호 120 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xxi) 서열 번호 121 (CDR1), 서열 번호 122 (CDR2) 및 서열 번호 123 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 124 (CDR1), 서열 번호 125 (CDR2) 및 서열 번호 126 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xxii) 서열 번호 127 (CDR1), 서열 번호 128 (CDR2) 및 서열 번호 129 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 130 (CDR1), 서열 번호 131 (CDR2) 및 서열 번호 132 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
xxiii) 서열 번호 133 (CDR1), 서열 번호 134 (CDR2) 및 서열 번호 135 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 136 (CDR1), 서열 번호 137 (CDR2) 및 서열 번호 138 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 및
xxiv) 서열 번호 139 (CDR1), 서열 번호 140 (CDR2) 및 서열 번호 141 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 142 (CDR1), 서열 번호 143 (CDR2) 및 서열 번호 144 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR. - 제24항 또는 제26항에 있어서, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 하기 i) 내지 vi)로 이루어진 군으로부터 선택된 CDR 서열을 포함하는 경쇄 가변 도메인 및 중쇄 가변 도메인을 포함하는 단백질:
i) 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
ii) 서열 번호 263 (CDR1), 서열 번호 264 (CDR2) 및 서열 번호 265 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 266 (CDR1), 서열 번호 267 (CDR2) 및 서열 번호 268 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
iii) 서열 번호 269 (CDR1), 서열 번호 270 (CDR2) 및 서열 번호 271 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 272 (CDR1), 서열 번호 273 (CDR2) 및 서열 번호 274 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
iv) 서열 번호 275 (CDR1), 서열 번호 276 (CDR2) 및 서열 번호 277 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 278 (CDR1), 서열 번호 279 (CDR2) 및 서열 번호 280 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR;
v) 서열 번호 281 (CDR1), 서열 번호 282 (CDR2) 및 서열 번호 283 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 284 (CDR1), 서열 번호 285 (CDR2) 및 서열 번호 286 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 및
vi) 서열 번호 287 (CDR1), 서열 번호 288 (CDR2) 및 서열 번호 289 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 290 (CDR1), 서열 번호 291 (CDR2) 및 서열 번호 292 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR. - 제24항 내지 제27항 중 어느 한 항에 있어서,
i) B7H6 경쇄에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 서열 번호 67 (CDR1), 서열 번호 68 (CDR2) 및 서열 번호 69 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 70 (CDR1), 서열 번호 71 (CDR2) 및 서열 번호 72 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하고; CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하거나;
ii) B7H6 경쇄에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 서열 번호 79 (CDR1), 서열 번호 80 (CDR2) 및 서열 번호 81 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 82 (CDR1), 서열 번호 83 (CDR2) 및 서열 번호 84 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하고, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하거나;
iii) B7H6 경쇄에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 서열 번호 85 (CDR1), 서열 번호 86 (CDR2) 및 서열 번호 87 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 88 (CDR1), 서열 번호 89 (CDR2) 및 서열 번호 90 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하고, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하거나; 또는
iv) B7H6 경쇄에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 서열 번호 91 (CDR1), 서열 번호 92 (CDR2) 및 서열 번호 93 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 94 (CDR1), 서열 번호 95 (CDR2) 및 서열 번호 96 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하고, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 서열 번호 257 (CDR1), 서열 번호 258 (CDR2) 및 서열 번호 259 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 260 (CDR1), 서열 번호 261 (CDR2) 및 서열 번호 262 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR을 포함하는,
단백질. - 제24항 내지 제27항 중 어느 한 항에 있어서, B7H6에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 하기 i) 내지 xxiv)로 이루어진 군으로부터 선택된 경쇄 가변 도메인 및 중쇄 가변 도메인을 포함하는 단백질:
i) 서열 번호 145의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 146의 아미노산 서열을 포함하는 중쇄 가변 도메인;
ii) 서열 번호 147의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 148의 아미노산 서열을 포함하는 중쇄 가변 도메인;
iii) 서열 번호 149의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 150의 아미노산 서열을 포함하는 중쇄 가변 도메인;
iv) 서열 번호 151의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 152의 아미노산 서열을 포함하는 중쇄 가변 도메인;
v) 서열 번호 153의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 154의 아미노산 서열을 포함하는 중쇄 가변 도메인;
vi) 서열 번호 155의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 156의 아미노산 서열을 포함하는 중쇄 가변 도메인;
vii) 서열 번호 157의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 158의 아미노산 서열을 포함하는 중쇄 가변 도메인;
viii) 서열 번호 159의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 160의 아미노산 서열을 포함하는 중쇄 가변 도메인;
ix) 서열 번호 161의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 162의 아미노산 서열을 포함하는 중쇄 가변 도메인;
x) 서열 번호 163의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 164의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xi) 서열 번호 165의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 166의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xii) 서열 번호 167의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 168의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xiii) 서열 번호 169의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 170의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xiv) 서열 번호 171의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 172의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xv) 서열 번호 173의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 174의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xvi) 서열 번호 175의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 176의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xvii) 서열 번호 177의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 178의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xviii) 서열 번호 179의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 180의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xix) 서열 번호 181의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 182의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xx) 서열 번호 183의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 184의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xxi) 서열 번호 185의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 186의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xxii) 서열 번호 187의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 188의 아미노산 서열을 포함하는 중쇄 가변 도메인;
xxiii) 서열 번호 189의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 190의 아미노산 서열을 포함하는 중쇄 가변 도메인; 및
xxiv) 서열 번호 191의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 192의 아미노산 서열을 포함하는 중쇄 가변 도메인. - 제24항 내지 제29항 중 어느 한 항에 있어서, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 하기 i) 내지 vi)로 이루어진 군으로부터 선택된 경쇄 가변 도메인 및 중쇄 가변 도메인을 포함하는 단백질:
i) 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인;
ii) 서열 번호 295의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 296의 아미노산 서열을 포함하는 중쇄 가변 도메인;
iii) 서열 번호 297의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 298의 아미노산 서열을 포함하는 중쇄 가변 도메인;
iv) 서열 번호 299의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 300의 아미노산 서열을 포함하는 중쇄 가변 도메인;
v) 서열 번호 301의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 302의 아미노산 서열을 포함하는 중쇄 가변 도메인; 및
vi) 서열 번호 303의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 304의 아미노산 서열을 포함하는 중쇄 가변 도메인. - 제24항 내지 제30항 중 어느 한 항에 있어서,
i) B7H6에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 서열 번호 167의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 168의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하고, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하거나;
ii) B7H6에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 서열 번호 171의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 172의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하고, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하거나;
iii) B7H6에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 서열 번호 173의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 174의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하고, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하거나;
iv) B7H6에 특이적으로 결합하는 상기 제1 폴리펩티드 쇄는 서열 번호 175의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 176의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하고, CD3에 특이적으로 결합하는 상기 제2 폴리펩티드 쇄는 서열 번호 293의 아미노산 서열을 포함하는 경쇄 가변 도메인 및 서열 번호 294의 아미노산 서열을 포함하는 중쇄 가변 도메인을 포함하는,
단백질. - 제24항 내지 제31항 중 어느 한 항에 있어서, 상기 제1 및/또는 제2 펩티드 링커는 26 내지 42개의 아미노산, 바람직하게는 30 내지 40개의 아미노산, 34 내지 40개의 아미노산, 또는 36 내지 39개의 아미노산 중 어느 하나, 보다 바람직하게는 38개의 아미노산을 포함하는 단백질.
- 제32항에 있어서, 상기 제1 링커 및/또는 제2 링커는 바람직하게는 서열 번호 250의 아미노산 서열을 포함하는 Gly-Ser 링커이고, 보다 바람직하게는 상기 제1 및 제2 펩티드 링커는 동일한 서열 (예를 들어, 서열 번호 250)을 포함하는 단백질.
- 제24항 내지 제33항 중 어느 한 항에 있어서, 상기 제1 경쇄 및 상기 제2 경쇄는 독립적으로 인간 카파 또는 람다 도메인을 포함하는 단백질.
- 제24항 내지 제34항 중 어느 한 항에 있어서, 상기 제1 폴리펩티드 쇄는 서열 번호 193, 서열 번호 194, 서열 번호 195, 서열 번호 196 서열 번호 197 서열 번호 198 서열 번호 199 서열 번호 200 서열 번호 201 서열 번호 202 서열 번호 203 서열 번호 204 서열 번호 205, 서열 번호 206, 서열 번호 207, 서열 번호 208, 서열 번호 209, 서열 번호 210, 서열 번호 211, 서열 번호 212, 서열 번호 213, 서열 번호 214, 서열 번호 215, 및 서열 번호 216으로 이루어진 군으로부터 선택된 아미노산 서열을 포함하는 B7H6에 결합하는 scFab를 포함하고, 상기 제2 폴리펩티드 쇄는 서열 번호 305, 서열 번호 306, 서열 번호 307, 서열 번호 308, 서열 번호 309, 및 서열 번호 310으로 이루어진 군으로부터 선택된 아미노산 서열을 포함하는 CD3에 결합하는 scFab를 포함하는 단백질.
- 제35항에 있어서,
i) 상기 제1 폴리펩티드 쇄는 서열 번호 204의 아미노산 서열을 포함하는 B7H6에 결합하는 scFab를 포함하고, 상기 제2 폴리펩티드 쇄는 서열 번호 305의 아미노산 서열을 포함하는 CD3에 결합하는 scFab를 포함하거나;
ii) 상기 제1 폴리펩티드 쇄는 서열 번호 206의 아미노산 서열을 포함하는 B7H6에 결합하는 scFab를 포함하고, 상기 제2 폴리펩티드 쇄는 서열 번호 305의 아미노산 서열을 포함하는 CD3에 결합하는 scFab를 포함하거나;
iii) 상기 제1 폴리펩티드 쇄는 서열 번호 207의 아미노산 서열을 포함하는 B7H6에 결합하는 scFab를 포함하고, 상기 제2 폴리펩티드 쇄는 서열 번호 305의 아미노산 서열을 포함하는 CD3에 결합하는 scFab를 포함하거나; 또는
iv) 상기 제1 폴리펩티드 쇄는 서열 번호 208의 아미노산 서열을 포함하는 B7H6에 결합하는 scFab를 포함하고, 상기 제2 폴리펩티드 쇄는 서열 번호 305의 아미노산 서열을 포함하는 CD3에 결합하는 scFab를 포함하는,
단백질. - 제24항 내지 제36항 중 어느 한 항에 있어서,
i) 상기 제1 중쇄는 위치 366에 티로신 (Y) [T366Y]을 포함하고, 상기 제2 중쇄는 위치 407에 트레오닌 (T) [Y407T]을 포함하거나,
ii) 상기 제1 중쇄는 위치 366에 트립토판 (W) [T366W]을 포함하고, 상기 제2 중쇄는 위치 366에 세린 (S) [T366S], 위치 368에 알라닌 (A) [L368A] 및 위치 407에 발린 (V) [Y407V]을 포함하거나,
iii) 상기 제2 중쇄는 위치 366에 티로신 (Y) [T366Y]을 포함하고, 상기 제1 중쇄는 위치 407에 트레오닌 (T) [Y407T]을 포함하거나, 또는
iv) 상기 제2 중쇄는 위치 366에 트립토판 (W) [T366W]을 포함하고, 상기 제1 중쇄는 위치 366에 세린 (S) [T366S], 위치 368에 알라닌 (A) [L368A] 및 위치 407에서 발린 (V) [Y407V]을 포함하고,
바람직하게는 상기 제1 또는 상기 제2 중쇄는 위치 435에 아르기닌 [H435R] 및 위치 436에 페닐알라닌 [Y436F]을 추가로 포함하는,
단백질. - 제24항 내지 제37항 중 어느 한 항에 있어서, 상기 제1 중쇄 및/또는 상기 제2 중쇄는 위치 234 [L234A] 및 위치 235 [L235A]에 알라닌을 포함하고, 바람직하게는 상기 제1 중쇄는 서열 번호 242의 아미노산 서열을 갖는 Fc 도메인을 포함하고, 상기 제2 중쇄 도메인은 서열 번호 243의 아미노산 서열을 갖는 Fc 도메인을 포함하는 단백질.
- 제24항 내지 제38항 중 어느 한 항에 있어서, 서열 번호 217, 서열 번호 218, 서열 번호 219, 서열 번호 220, 서열 번호 221, 서열 번호 222, 서열 번호 223, 서열 번호 224, 서열 번호 225, 서열 번호 226, 서열 번호 227, 서열 번호 228, 서열 번호 229, 서열 번호 230, 서열 번호 231, 서열 번호 232, 서열 번호 233, 서열 번호 234, 서열 번호 235, 서열 번호 236, 서열 번호 237, 서열 번호 238, 서열 번호 239, 및 서열 번호 240으로 이루어진 군으로부터 선택되는 아미노산 서열을 포함하는 B7H6에 특이적으로 결합하는 제1 폴리펩티드 쇄 및 서열 번호 311, 서열 번호 312, 서열 번호 313, 서열 번호 314, 서열 번호 315, 및 서열 번호 316으로 이루어진 군으로부터 선택되는 아미노산 서열을 포함하는 CD3에 특이적으로 결합하는 제2 폴리펩티드 쇄를 포함하는 단백질.
- 제38항에 있어서,
i) 상기 제1 폴리펩티드 쇄는 서열 번호 228의 아미노산 서열을 포함하고, 상기 제2 폴리펩티드 쇄는 서열 번호 311의 아미노산 서열을 포함하거나;
ii) 상기 제1 폴리펩티드 쇄는 서열 번호 230의 아미노산 서열을 포함하고, 상기 제2 폴리펩티드 쇄는 서열 번호 311의 아미노산 서열을 포함하거나;
iii) 상기 제1 폴리펩티드 쇄는 서열 번호 231의 아미노산 서열을 포함하고, 상기 제2 폴리펩티드 쇄는 서열 번호 311의 아미노산 서열을 포함하거나; 또는
iv) 상기 제1 폴리펩티드 쇄는 서열 번호 232의 아미노산 서열을 포함하고 상기 제2 폴리펩티드 쇄는 서열 번호 311의 아미노산 서열을 포함하는,
단백질. - 제24항 내지 제40항 중 어느 한 항의 제1 및/또는 제2 폴리펩티드 쇄를 암호화하는 단리된 핵산 분자.
- 제41항의 핵산 분자를 포함하는 발현 벡터.
- 제42항의 발현 벡터로 형질감염된 숙주 세포.
- 제1항 내지 제18항 또는 제24항 내지 제40항 중 어느 한 항에 있어서, 의약에 사용하기 위한 단백질.
- 제1항 내지 제18항 또는 제24항 내지 제40항 중 어느 한 항의 단백질 및 약학적으로 허용되는 담체를 포함하는 약학적 조성물.
- 제1항 내지 제18항 또는 제24항 내지 제40항 중 어느 한 항의 단백질의 치료적 유효량을 이를 필요로 하는 환자에게 투여하는 것을 포함하는, 암을 치료하는 방법.
- 암 치료용 약학적 조성물을 제조하기 위한 제1항 내지 제18항 또는 제24항 내지 제40항 중 어느 한 항의 단백질의 용도.
- 제1항 내지 제18항 또는 제24항 내지 제40항 중 어느 한 항에 있어서, 암을 치료하는 방법에 사용하기 위한 단백질.
- 제46항의 방법, 제47항의 용도 또는 제48항의 사용을 위한 단백질에 있어서, 암은 B7H6 발현 종양이고, 바람직하게는 암은 (전이성) 결장직장암 ((m)CRC), 비소세포 폐암 (NSCLC) 또는 두경부 편평 세포 암종 (HNSCC)인 방법, 용도 또는 단백질.
- 제46항 또는 제49항의 방법, 제47항 또는 제49항의 용도, 또는 제48항 또는 제49항의 사용을 위한 단백질에 있어서, 상기 단백질은 세포독성 또는 세포증식억제 화학요법제, 혈관신생을 억제하는 치료적 활성 화합물, 신호 전달 경로 억제제 (예: EGFR 억제제), 면역 조절제, 면역 체크포인트 억제제, 유사분열 체크포인트 억제제 또는 호르몬 요법제인 방법, 용도 또는 단백질.
- 제50항에 있어서, 상기 단백질은 면역 체크포인트 억제제, 바람직하게는 항-PD-1 항체 또는 항-PD-L1 항체와 조합되어 사용되는 방법, 용도 또는 단백질.
- 제51항에 있어서, 항-PD-1 항체는 PD1-1, PD1-2, PD1-3, PD1-4, 및 PD1-5로 이루어진 군으로부터 선택되는 방법, 용도 또는 단백질.
- 다음을 포함하는 항-B7H6 항체 분자:
i) 서열 번호 1 (CDR1), 서열 번호 2 (CDR2) 및 서열 번호 3 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 4 (CDR1), 서열 번호 5 (CDR2) 및 서열 번호 6 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
ii) 서열 번호 7 (CDR1), 서열 번호 8 (CDR2) 및 서열 번호 9 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 10 (CDR1), 서열 번호 11 (CDR2) 및 서열 번호 12 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
iii) 서열 번호 13 (CDR1), 서열 번호 14 (CDR2) 및 서열 번호 15 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 16 (CDR1), 서열 번호 17 (CDR2) 및 서열 번호 18 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
iv) 서열 번호 19 (CDR1), 서열 번호 20 (CDR2) 및 서열 번호 21 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 22 (CDR1), 서열 번호 23 (CDR2) 및 서열 번호 24 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
v) 서열 번호 25 (CDR1), 서열 번호 26 (CDR2) 및 서열 번호 27 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 28 (CDR1), 서열 번호 29 (CDR2) 및 서열 번호 30 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
vi) 서열 번호 31 (CDR1), 서열 번호 32 (CDR2) 및 서열 번호 33 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 34 (CDR1), 서열 번호 35 (CDR2) 및 서열 번호 36 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
vii) 서열 번호 37 (CDR1), 서열 번호 38 (CDR2) 및 서열 번호 39 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 40 (CDR1), 서열 번호 41 (CDR2) 및 서열 번호 42 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
viii) 서열 번호 43 (CDR1), 서열 번호 44 (CDR2) 및 서열 번호 45 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 46 (CDR1), 서열 번호 47 (CDR2) 및 서열 번호 48 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
ix) 서열 번호 49 (CDR1), 서열 번호 50 (CDR2) 및 서열 번호 51 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 52 (CDR1), 서열 번호 53 (CDR2) 및 서열 번호 54 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
x) 서열 번호 55 (CDR1), 서열 번호 56 (CDR2) 및 서열 번호 57 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 58 (CDR1), 서열 번호 59 (CDR2) 및 서열 번호 60 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xi) 서열 번호 61 (CDR1), 서열 번호 62 (CDR2) 및 서열 번호 63 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 64 (CDR1), 서열 번호 65 (CDR2) 및 서열 번호 66 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xii) 서열 번호 67 (CDR1), 서열 번호 68 (CDR2) 및 서열 번호 69 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 70 (CDR1), 서열 번호 71 (CDR2) 및 서열 번호 72 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xiii) 서열 번호 73 (CDR1), 서열 번호 74 (CDR2) 및 서열 번호 75 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 76 (CDR1), 서열 번호 77 (CDR2) 및 서열 번호 78 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xiv) 서열 번호 79 (CDR1), 서열 번호 80 (CDR2) 및 서열 번호 81 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 82 (CDR1), 서열 번호 83 (CDR2) 및 서열 번호 84 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xv) 서열 번호 85 (CDR1), 서열 번호 86 (CDR2) 및 서열 번호 87 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 88 (CDR1), 서열 번호 89 (CDR2) 및 서열 번호 90 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xvi) 서열 번호 91 (CDR1), 서열 번호 92 (CDR2) 및 서열 번호 93 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 94 (CDR1), 서열 번호 95 (CDR2) 및 서열 번호 96 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xvii) 서열 번호 97 (CDR1), 서열 번호 98 (CDR2) 및 서열 번호 99 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 100 (CDR1), 서열 번호 101 (CDR2) 및 서열 번호 102 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xviii) 서열 번호 103 (CDR1), 서열 번호 104 (CDR2) 및 서열 번호 105 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 106 (CDR1), 서열 번호 107 (CDR2) 및 서열 번호 108 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xix) 서열 번호 109 (CDR1), 서열 번호 110 (CDR2) 및 서열 번호 111 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 112 (CDR1), 서열 번호 113 (CDR2) 및 서열 번호 114 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xx) 서열 번호 115 (CDR1), 서열 번호 116 (CDR2) 및 서열 번호 117 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 118 (CDR1), 서열 번호 119 (CDR2) 및 서열 번호 120 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xxi) 서열 번호 121 (CDR1), 서열 번호 122 (CDR2) 및 서열 번호 123 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 124 (CDR1), 서열 번호 125 (CDR2) 및 서열 번호 126 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xxii) 서열 번호 127 (CDR1), 서열 번호 128 (CDR2) 및 서열 번호 129 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 130 (CDR1), 서열 번호 131 (CDR2) 및 서열 번호 132 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xxiii) 서열 번호 133 (CDR1), 서열 번호 134 (CDR2) 및 서열 번호 135 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 136 (CDR1), 서열 번호 137 (CDR2) 및 서열 번호 138 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR; 또는
xxiv) 서열 번호 139 (CDR1), 서열 번호 140 (CDR2) 및 서열 번호 141 (CDR3)의 아미노산 서열을 포함하는 경쇄 CDR 및 서열 번호 142 (CDR1), 서열 번호 143 (CDR2) 및 서열 번호 144 (CDR3)의 아미노산 서열을 포함하는 중쇄 CDR.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP19201200 | 2019-10-02 | ||
| EP19201200.3 | 2019-10-02 | ||
| PCT/EP2020/077586 WO2021064137A2 (en) | 2019-10-02 | 2020-10-01 | Multi-specific binding proteins for cancer treatment |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20220075383A true KR20220075383A (ko) | 2022-06-08 |
Family
ID=68136317
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227014608A KR20220075383A (ko) | 2019-10-02 | 2020-10-01 | 암 치료용 다중 특이적 결합 단백질 |
Country Status (19)
| Country | Link |
|---|---|
| US (2) | US11732045B2 (ko) |
| EP (1) | EP4038100A2 (ko) |
| JP (2) | JP7387885B2 (ko) |
| KR (1) | KR20220075383A (ko) |
| CN (1) | CN114641496A (ko) |
| AR (1) | AR120138A1 (ko) |
| AU (1) | AU2020358893A1 (ko) |
| BR (1) | BR112022004047A2 (ko) |
| CA (1) | CA3153372A1 (ko) |
| CL (1) | CL2022000664A1 (ko) |
| CO (1) | CO2022003552A2 (ko) |
| CR (1) | CR20220136A (ko) |
| EC (1) | ECSP22019193A (ko) |
| IL (1) | IL291817A (ko) |
| JO (1) | JOP20220079A1 (ko) |
| MX (1) | MX2022004042A (ko) |
| PE (1) | PE20221412A1 (ko) |
| TW (1) | TW202128756A (ko) |
| WO (1) | WO2021064137A2 (ko) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20230162013A (ko) | 2021-03-26 | 2023-11-28 | 이나뜨 파르마 에스.에이. | Nk 세포 관여를 위해 사이토카인에 융합된 nkp46-결합 부위, 암 항원 결합 부위를 포함하는 다중특이적 단백질 |
| US20220388986A1 (en) | 2021-04-29 | 2022-12-08 | Boehringer Ingelheim International Gmbh | Heterocyclic compounds capable of activating sting |
| WO2022258691A1 (en) | 2021-06-09 | 2022-12-15 | Innate Pharma | Multispecific proteins binding to nkg2d, a cytokine receptor, a tumour antigen and cd16a |
| WO2022258678A1 (en) | 2021-06-09 | 2022-12-15 | Innate Pharma | Multispecific proteins binding to nkp30, a cytokine receptor, a tumour antigen and cd16a |
| WO2022258662A1 (en) | 2021-06-09 | 2022-12-15 | Innate Pharma | Multispecific proteins binding to nkp46, a cytokine receptor, a tumour antigen and cd16a |
| CN114395043B (zh) * | 2021-12-07 | 2023-07-11 | 合肥天港免疫药物有限公司 | Ncr3lg1抗体及其应用 |
| CN114395047B (zh) * | 2021-12-07 | 2023-11-07 | 合肥天港免疫药物有限公司 | 双特异性抗体及其应用 |
| CN114395045B (zh) * | 2021-12-07 | 2023-06-09 | 合肥天港免疫药物有限公司 | B7h6抗体及其应用 |
Family Cites Families (31)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US168A (en) | 1837-04-17 | Improvement in fire-arms | ||
| US5731A (en) | 1848-08-22 | Elisha k | ||
| US4676980A (en) | 1985-09-23 | 1987-06-30 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Target specific cross-linked heteroantibodies |
| WO1988001649A1 (en) | 1986-09-02 | 1988-03-10 | Genex Corporation | Single polypeptide chain binding molecules |
| ES2052027T5 (es) | 1988-11-11 | 2005-04-16 | Medical Research Council | Clonacion de secuencias de dominio variable de inmunoglobulina. |
| US5427908A (en) | 1990-05-01 | 1995-06-27 | Affymax Technologies N.V. | Recombinant library screening methods |
| WO1993008829A1 (en) | 1991-11-04 | 1993-05-13 | The Regents Of The University Of California | Compositions that mediate killing of hiv-infected cells |
| EP0658230B1 (en) | 1992-08-10 | 1996-09-25 | Alcan Aluminium Uk Limited | Fence |
| PT1498427E (pt) | 1992-08-21 | 2010-03-22 | Univ Bruxelles | Imunoglobulinas desprovidas de cadeias leves |
| CA2150262C (en) | 1992-12-04 | 2008-07-08 | Kaspar-Philipp Holliger | Multivalent and multispecific binding proteins, their manufacture and use |
| ES2108460T3 (es) | 1993-06-03 | 1997-12-16 | Therapeutic Antibodies Inc | Fragmentos de anticuerpos en terapeutica. |
| EP0739981A1 (en) | 1995-04-25 | 1996-10-30 | Vrije Universiteit Brussel | Variable fragments of immunoglobulins - use for therapeutic or veterinary purposes |
| EP2706116A1 (en) | 2001-01-17 | 2014-03-12 | Emergent Product Development Seattle, LLC | Binding domain-immunoglobulin fusion proteins |
| WO2003050531A2 (en) | 2001-12-11 | 2003-06-19 | Algonomics N.V. | Method for displaying loops from immunoglobulin domains in different contexts |
| NL1019562C2 (nl) | 2001-12-13 | 2003-06-17 | Heineken Tech Services | Klepsamenstel voor gebruik bij drankafgifte. |
| US8764654B2 (en) | 2008-03-19 | 2014-07-01 | Zin Technologies, Inc. | Data acquisition for modular biometric monitoring system |
| ME02886B (me) | 2005-10-12 | 2018-04-20 | Morphosys Ag | Proizvodnja i karakterizacija potpuno humanih terapeutskih antitela dobijenih HuCAL GOLD tehnologijom, specifičnih za humani CD38 |
| JP5496897B2 (ja) | 2007-10-04 | 2014-05-21 | ザイモジェネティクス, インコーポレイテッド | B7ファミリーメンバーのzB7H6ならびに関連する組成物および方法 |
| PL2235064T3 (pl) | 2008-01-07 | 2016-06-30 | Amgen Inc | Sposób otrzymywania cząsteczek przeciwciał z heterodimerycznymi fc z zastosowaniem kierujących efektów elektrostatycznych |
| FI20090280A (fi) | 2009-07-17 | 2011-01-18 | Kone Corp | Hissijärjestely ja menetelmä hissikorin liikuttamiseksi hissikuilussa |
| WO2011075861A1 (en) | 2009-12-23 | 2011-06-30 | Esbatech, An Alcon Biomedical Research Unit Llc | Method for decreasing immunogenicity |
| MX369220B (es) | 2011-05-21 | 2019-10-31 | Macrogenics Inc | Moleculas que enlazan cd3 capaces de enlazar a cd3 humano y no humano. |
| MX350074B (es) | 2011-06-23 | 2017-08-25 | Ablynx Nv | Tecnicas para predecir, detectar, y reducir la interferencia de proteinas no especificas en ensayos que implican dominios variables individuales de inmunoglobulina. |
| EP2987806A3 (en) | 2011-08-17 | 2016-07-13 | Glaxo Group Limited | Modified single variable domain antibodies with reduced binding to anti-drug-antibodies |
| DK2766392T3 (da) * | 2011-10-10 | 2019-10-07 | Xencor Inc | Fremgangsmåde til oprensning af antistoffer |
| EP2847223B1 (en) | 2012-05-07 | 2019-03-27 | Trustees of Dartmouth College | Anti-b7-h6 antibody, fusion proteins, and methods of using the same |
| WO2014018572A2 (en) * | 2012-07-23 | 2014-01-30 | Zymeworks Inc. | Immunoglobulin constructs comprising selective pairing of the light and heavy chains |
| JP7082604B2 (ja) * | 2016-03-21 | 2022-06-08 | マレンゴ・セラピューティクス,インコーポレーテッド | 多重特異性および多機能性分子ならびにその使用 |
| EP3442576A4 (en) * | 2016-04-15 | 2020-05-13 | Trustees of Dartmouth College | HIGH AFFINITY B7-H6 ANTIBODIES AND ANTIBODY FRAGMENTS |
| KR20220103806A (ko) | 2016-05-18 | 2022-07-22 | 베링거 인겔하임 인터내셔날 게엠베하 | 암 치료용 항-pd1 및 항-lag3 항체 |
| TW202016151A (zh) * | 2018-06-09 | 2020-05-01 | 德商百靈佳殷格翰國際股份有限公司 | 針對癌症治療之多特異性結合蛋白 |
-
2020
- 2020-09-30 TW TW109134076A patent/TW202128756A/zh unknown
- 2020-10-01 JP JP2022520371A patent/JP7387885B2/ja active Active
- 2020-10-01 MX MX2022004042A patent/MX2022004042A/es unknown
- 2020-10-01 WO PCT/EP2020/077586 patent/WO2021064137A2/en active Application Filing
- 2020-10-01 US US17/060,111 patent/US11732045B2/en active Active
- 2020-10-01 EP EP20789508.7A patent/EP4038100A2/en active Pending
- 2020-10-01 CA CA3153372A patent/CA3153372A1/en active Pending
- 2020-10-01 AU AU2020358893A patent/AU2020358893A1/en active Pending
- 2020-10-01 JO JOP/2022/0079A patent/JOP20220079A1/ar unknown
- 2020-10-01 CN CN202080068909.4A patent/CN114641496A/zh active Pending
- 2020-10-01 IL IL291817A patent/IL291817A/en unknown
- 2020-10-01 KR KR1020227014608A patent/KR20220075383A/ko unknown
- 2020-10-01 AR ARP200102733A patent/AR120138A1/es unknown
- 2020-10-01 BR BR112022004047A patent/BR112022004047A2/pt unknown
- 2020-10-01 CR CR20220136A patent/CR20220136A/es unknown
- 2020-10-01 PE PE2022000468A patent/PE20221412A1/es unknown
-
2022
- 2022-03-14 EC ECSENADI202219193A patent/ECSP22019193A/es unknown
- 2022-03-18 CL CL2022000664A patent/CL2022000664A1/es unknown
- 2022-03-25 CO CONC2022/0003552A patent/CO2022003552A2/es unknown
-
2023
- 2023-06-20 US US18/337,693 patent/US20230340130A1/en active Pending
- 2023-11-15 JP JP2023194494A patent/JP2024020414A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| AU2020358893A1 (en) | 2022-03-31 |
| MX2022004042A (es) | 2022-05-02 |
| JP7387885B2 (ja) | 2023-11-28 |
| EP4038100A2 (en) | 2022-08-10 |
| CA3153372A1 (en) | 2021-04-08 |
| US20210107983A1 (en) | 2021-04-15 |
| CR20220136A (es) | 2022-05-27 |
| TW202128756A (zh) | 2021-08-01 |
| WO2021064137A3 (en) | 2021-05-14 |
| BR112022004047A2 (pt) | 2022-05-24 |
| JP2022551081A (ja) | 2022-12-07 |
| IL291817A (en) | 2022-06-01 |
| ECSP22019193A (es) | 2022-04-29 |
| US20230340130A1 (en) | 2023-10-26 |
| CL2022000664A1 (es) | 2023-01-06 |
| JOP20220079A1 (ar) | 2023-01-30 |
| AR120138A1 (es) | 2022-02-02 |
| CN114641496A (zh) | 2022-06-17 |
| CO2022003552A2 (es) | 2022-04-19 |
| WO2021064137A2 (en) | 2021-04-08 |
| US11732045B2 (en) | 2023-08-22 |
| JP2024020414A (ja) | 2024-02-14 |
| PE20221412A1 (es) | 2022-09-20 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20230295337A1 (en) | Multi-specific binding proteins for cancer treatment | |
| TWI821202B (zh) | 抗cd38抗體及其使用方法 | |
| JP7387885B2 (ja) | 癌処置のための多重特異性結合タンパク質 | |
| JP6703520B2 (ja) | Cd3イプシロンおよびbcmaに対する二特異性抗体 | |
| US11377477B2 (en) | PD-1 targeted IL-15/IL-15RALPHA fc fusion proteins and uses in combination therapies thereof | |
| US20240043566A1 (en) | Bi-functional molecules | |
| KR20230104222A (ko) | B 세포 악성종양 치료를 위한 항-cd19 작용제 및 b 세포 표적화제 병용 요법 | |
| US20220411533A1 (en) | Novel Tri-specific Binding Molecules | |
| WO2023086897A1 (en) | Siglec-6 antibodies, derivative compounds and related uses | |
| NZ769422A (en) | Dll3-cd3 bispecific antibodies |