KR20220042359A - 니켈 코발트 복합 산화물의 제조 방법, 니켈 코발트 복합 산화물, 정극 활물질, 전고체 리튬 이온 이차 전지용 정극 및 전고체 리튬 이온 이차 전지 - Google Patents
니켈 코발트 복합 산화물의 제조 방법, 니켈 코발트 복합 산화물, 정극 활물질, 전고체 리튬 이온 이차 전지용 정극 및 전고체 리튬 이온 이차 전지 Download PDFInfo
- Publication number
- KR20220042359A KR20220042359A KR1020227003165A KR20227003165A KR20220042359A KR 20220042359 A KR20220042359 A KR 20220042359A KR 1020227003165 A KR1020227003165 A KR 1020227003165A KR 20227003165 A KR20227003165 A KR 20227003165A KR 20220042359 A KR20220042359 A KR 20220042359A
- Authority
- KR
- South Korea
- Prior art keywords
- nickel
- positive electrode
- composite oxide
- less
- solution
- Prior art date
Links
Images
Classifications
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/52—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron
- H01M4/525—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of nickel, cobalt or iron of mixed oxides or hydroxides containing iron, cobalt or nickel for inserting or intercalating light metals, e.g. LiNiO2, LiCoO2 or LiCoOxFy
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G53/00—Compounds of nickel
- C01G53/006—Compounds containing, besides nickel, two or more other elements, with the exception of oxygen or hydrogen
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G53/00—Compounds of nickel
- C01G53/40—Nickelates
- C01G53/42—Nickelates containing alkali metals, e.g. LiNiO2
- C01G53/44—Nickelates containing alkali metals, e.g. LiNiO2 containing manganese
- C01G53/50—Nickelates containing alkali metals, e.g. LiNiO2 containing manganese of the type [MnO2]n-, e.g. Li(NixMn1-x)O2, Li(MyNixMn1-x-y)O2
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
- H01M10/0525—Rocking-chair batteries, i.e. batteries with lithium insertion or intercalation in both electrodes; Lithium-ion batteries
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0561—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of inorganic materials only
- H01M10/0562—Solid materials
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/48—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides
- H01M4/50—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese
- H01M4/505—Selection of substances as active materials, active masses, active liquids of inorganic oxides or hydroxides of manganese of mixed oxides or hydroxides containing manganese for inserting or intercalating light metals, e.g. LiMn2O4 or LiMn2OxFy
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/62—Selection of inactive substances as ingredients for active masses, e.g. binders, fillers
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/01—Particle morphology depicted by an image
- C01P2004/03—Particle morphology depicted by an image obtained by SEM
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/30—Particle morphology extending in three dimensions
- C01P2004/45—Aggregated particles or particles with an intergrown morphology
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/51—Particles with a specific particle size distribution
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2004/00—Particle morphology
- C01P2004/60—Particles characterised by their size
- C01P2004/61—Micrometer sized, i.e. from 1-100 micrometer
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/11—Powder tap density
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/12—Surface area
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/40—Electric properties
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M2004/021—Physical characteristics, e.g. porosity, surface area
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M2004/026—Electrodes composed of, or comprising, active material characterised by the polarity
- H01M2004/028—Positive electrodes
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Inorganic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Electrochemistry (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Physics & Mathematics (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- General Physics & Mathematics (AREA)
- Materials Engineering (AREA)
- Battery Electrode And Active Subsutance (AREA)
- Secondary Cells (AREA)
Abstract
전고체 리튬 이온 이차 전지의 내부 저항을 저감 가능한 전고체 리튬 이온 이차 전지용 정극이 제공된다. 정극은, 정극 활물질 및 고체 전해질 재료를 포함하는 활물질층을 구비한다. 정극 활물질은, 리튬 전이금속 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함한다. 이차 입자의 평활도는 0.73보다 크고, 이차 입자의 원형도는 0.83보다 크다.
Description
본 개시는 니켈 코발트 복합 산화물의 제조 방법, 니켈 코발트 복합 산화물, 정극 활물질, 전고체 리튬 이온 이차 전지용 정극 및 전고체 리튬 이온 이차 전지에 관한 것이다.
안전성 등의 관점에서, 가연성의 비수 전해액 대신에 무기의 고체 전해질을 사용하는 전고체 리튬 이온 이차 전지가 검토되고 있다. 전고체 리튬 이온 이차 전지에서는, 출력 특성의 향상이 요구되고 있다. 예를 들면, 국제 공개 제2007/004590호에는, 정극 활물질의 표면에 리튬 이온 전도성 산화물층을 형성하는 기술이 제안되어, 고출력 특성이 우수한 것으로 되어 있다.
한편, 정극 활물질로서, 일차 입자가 응집하여 대략 구상(球狀)으로 형성된 이차 입자의 입도 분포를 좁게 하는 기술이 제안되어, 전지의 고용량화가 가능하게 되고 있다(예를 들면, 국제 공개 제2013/183711호 참조). 나아가, 공침(共沈)법에 의해 구형 수산화 니켈 코발트 알루미늄 전구체 재료를 제조하는 기술이 제안되어, 사이클 특성이 향상되는 것으로 되어 있다(예를 들면, 국제 공개 제2016/180288호 참조).
리튬 이온 이차 전지에는 한층 더 전지 특성의 향상이 요구되고 있다. 또한, 거기에 사용되는 정극 활물질이나 그 전구체의 특성의 향상이 요구되고 있다.
제1 양태는 니켈 코발트 복합 산화물의 제조 방법이다. 제조 방법은, 니켈 이온 및 코발트 이온을 포함하는 제1 용액을 준비하는 것과, 착이온 형성 인자를 포함하는 제2 용액을 준비하는 것과, pH가 10 이상 13.5 이하의 범위에 있는 액매체를 준비하는 것과, 액매체에, 제1 용액 및 제2 용액을 따로따로 또한 동시에 공급하면서, (메타)아크릴산에서 유래하는 구성 단위를 포함하는 중합체를 공급하여, pH가 10 이상 13.5 이하의 범위로 유지되는 반응 용액을 얻는 것과, 반응 용액으로부터 니켈 및 코발트를 포함하는 복합 수산화물을 얻는 것과, 얻어지는 복합 수산화물을 열 처리하여, 니켈 및 코발트를 포함하는 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 얻는 것을 포함한다. 니켈 코발트 복합 산화물을 구성하는 이차 입자의 평활도는 0.74보다 크면 좋다.
제2 양태는, 니켈 및 코발트를 포함하는 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함하는 니켈 코발트 복합 산화물이다. 니켈 코발트 복합 산화물을 구성하는 이차 입자의 평활도는 0.74보다 크다.
제3 양태는, 층상 구조를 가지며, 리튬, 니켈 및 코발트를 포함하는 리튬 전이금속 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함하는 정극 활물질이다. 정극 활물질을 구성하는 이차 입자의 평활도는 0.73보다 크고, 이차 입자의 원형도는 0.83보다 크다.
제4 양태는, 정극 활물질 및 고체 전해질 재료를 포함하는 활물질층을 구비하는 전고체 리튬 이온 이차 전지용 정극이다. 정극 활물질은, 리튬 전이금속 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함한다. 이차 입자는, 평활도가 0.73보다 크고, 원형도가 0.83보다 크다.
제5 양태는, 상기 정극과, 부극과, 고체 전해질층을 구비하는 전고체 리튬 이온 이차 전지이다.
본 개시에 따른 일 양태에 의하면, 전고체 리튬 이온 이차 전지의 내부 저항을 저감 가능한 정극을 제공할 수 있다.
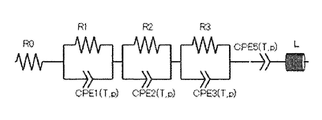
도 1은 전고체 이차 전지의 등가 회로도이다.
도 2a는 실시예 3에 따른 니켈 코발트 복합 산화물의 주사 전자 현미경(SEM) 화상의 일례이다.
도 2b는 도 2a를 더욱 확대한 SEM 화상이다.
도 3a는 실시예 7에 따른 니켈 코발트 복합 산화물의 SEM 화상의 일례이다.
도 3b는 도 3a를 더욱 확대한 SEM 화상이다.
도 4a는 비교예 2에 따른 니켈 코발트 복합 산화물의 SEM 화상의 일례이다.
도 4b는 도 4a를 더욱 확대한 SEM 화상이다.
도 2a는 실시예 3에 따른 니켈 코발트 복합 산화물의 주사 전자 현미경(SEM) 화상의 일례이다.
도 2b는 도 2a를 더욱 확대한 SEM 화상이다.
도 3a는 실시예 7에 따른 니켈 코발트 복합 산화물의 SEM 화상의 일례이다.
도 3b는 도 3a를 더욱 확대한 SEM 화상이다.
도 4a는 비교예 2에 따른 니켈 코발트 복합 산화물의 SEM 화상의 일례이다.
도 4b는 도 4a를 더욱 확대한 SEM 화상이다.
본 명세서에 있어서 「공정」이라는 단어는, 독립된 공정뿐만 아니라, 다른 공정과 명확히 구별할 수 없는 경우라 하더라도 그 공정의 소기의 목적이 달성되면, 본 용어에 포함된다. 또한, 조성물 중의 각 성분의 함유량은, 조성물 중에 각 성분에 해당하는 물질이 복수 존재하는 경우, 달리 특정되지 않는 한, 조성물 중에 존재하는 해당 복수의 물질의 합계량을 의미한다. 이하, 본 개시의 실시형태를 상세하게 설명한다. 다만, 이하에 나타내는 실시형태는, 본 개시의 기술 사상을 구체화하기 위한, 니켈 코발트 복합 금속 산화물의 제조 방법, 니켈 코발트 복합 산화물 및, 정극 활물질, 전고체 리튬 이온 이차 전지용 정극 및 전고체 리튬 이온 이차 전지를 예시하는 것으로서, 본 개시는, 이하에 나타내는 전고체 리튬 이온 이차 전지용 정극 활물질, 정극 및 전고체 리튬 이온 이차 전지에 한정되지 않는다.
<전고체 리튬 이온 이차 전지용 정극>
전고체 리튬 이온 이차 전지용 정극(이하, 단순히 정극이라고도 말함)은, 정극 활물질 및 고체 전해질 재료를 포함하는 활물질층을 구비한다. 활물질층에 포함되는 정극 활물질은, 리튬 전이금속 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함하여 구성된다. 정극 활물질을 구성하는 이차 입자는, 평활도가 0.73보다 크고, 원형도가 0.83보다 크다.
정극 활물질을 구성하는 이차 입자가, 평활도 및 원형도로 특정되는 특정 형상을 가지고 있음으로써, 예를 들면, 이차 입자와 고체 전해질 재료가 접촉하는 면적이 커지므로, 이차 입자와 고체 전해질의 계면에서의 저항이 저감된다고 생각된다. 또한, 사이클 특성의 개선을 목적으로 하여, 이차 입자 표면에 특정 원소를 포함하는 부착물을 부착시키는 경우에도, 부착시킬 화합물이 고르게 부착하기 쉬워져, 저항 성분을 저감할 수 있다. 나아가, 정극 형성시의 가압 성형에 의한 이차 입자의 깨어짐을 저감할 수 있다. 이것은, 예를 들면, 가압 성형의 압력이 입자 전체에 균일하게 가해지기 때문이라고 생각할 수 있다.
<정극 활물질>
정극 활물질은, 리튬 전이금속 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함하여 구성된다. 정극 활물질을 구성하는 이차 입자의 평활도는 0.73보다 크면 좋고, 또한 이차 입자의 원형도는 0.83보다 크면 좋다. 이차 입자는, 예를 들면 50개 이상의 일차 입자가 집합하여 형성된다. 정극 활물질은, 후술하는 정극 활물질의 제조 방법으로 제조되는 것이어도 된다.
이차 입자의 평활도는, 예를 들면 0.73보다 크고, 바람직하게는 0.80 이상, 보다 바람직하게는 0.83 이상이다. 한편, 평활도의 상한은 1이다. 평활도는, 이차 입자의 윤곽 형상에 있어서의 요철의 정도를 나타내는 지수이며, 평활한 형상일수록 1에 근접하고, 요철의 정도가 클수록 0에 근접한다. 한편, 상기 평활도는 이하와 같이 하여 구해진다. 대상의 이차 입자의 윤곽 형상에 대해 화상 처리 소프트웨어의 피팅 기능을 사용하여, 대상의 이차 입자의 윤곽 형상과 면적이 동등한 근사 타원을 구한다. 그 근사 타원의 긴 직경(a) 및 짧은 직경(b)으로부터, Gauss-Kummer 공식을 사용하여 근사 타원의 전체 둘레 길이(L)가 산출된다. 이차 입자의 윤곽 형상의 전체 둘레 길이를 Lop라고 하고, 근사한 타원의 전체 둘레 길이를 L로 하면, 평활도는, 입자 화상의 윤곽의 전체 둘레 길이(Lop)에 대한, 근사 타원의 전체 둘레 길이(L)의 비(L/Lop)가 된다. 이차 입자의 평활도의 산출에 사용되는 화상의 확대 배율은, 이차 입자의 입경에 따라 적절히 선택하면 된다. 확대 배율은, 예를 들면 1000배 이상 10000배 이하이면 좋고, 바람직하게는 1000배 이상 6000배 이하이며, 보다 바람직하게는 2000배 이상 6000배 이하이다.
구체적으로는, 주사 전자 현미경(SEM)을 사용하여 반사 전자상(배율; 4000배)을 촬영하고, 윤곽을 확인할 수 있는 20 내지 40개의 이차 입자에 대하여, 각각 근사 타원을 구하여 긴 직경(a) 및 짧은 직경(b)을 얻는다. 또한, 윤곽 형상의 전체 둘레 길이(Lop)를 측정한다. 긴 직경(a) 및 짧은 직경(b)으로부터 하기의 근사식에 기초하여 근사한 타원의 전체 둘레 길이(L)를 산출하여 개개의 이차 입자에 대해 비(L/Lop)를 구하고, 그들의 산술 평균값으로서 이차 입자의 평활도가 산출된다. 한편, 이차 입자의 윤곽을 확인할 수 있다는 것은, 화상 상에서 이차 입자의 윤곽 전체를 트레이스할 수 있다는 것을 의미한다.
이차 입자의 원형도는, 예를 들면 0.83보다 크고, 바람직하게는 0.86 이상, 보다 바람직하게는 0.90 이상이다. 한편, 원형도의 상한은 1이다. 원형도는, 이차 입자의 윤곽 형상의 원다움을 나타내는 지수이며, 원에 가까울수록 1에 근접한다. 원형도는, 이차 입자의 윤곽 형상에 있어서의 입자 화상 면적과 동일한 면적을 갖는 원의 직경을 원상당 직경으로 하는 경우에, 이차 입자의 윤곽 형상의 전체 둘레 길이(L0)에 대한 원상당 직경으로부터 산출되는 원주 길이(L1)의 비(L1/L0)로 정의된다.
구체적으로는, 건식 입자 화상 분석 장치(Morphologi G3S: Malvern사; 렌즈 배율 20배)를 사용하여, 약 10000개의 입자에 대해 개개의 비(L1/L0)를 산출하고, 그들의 산술 평균값으로서 이차 입자의 원형도를 구하였다.
이차 입자의 입도 분포는, 예를 들면 0.61보다 작고, 바람직하게는 0.60 이하, 보다 바람직하게는 0.58 이하, 더욱 바람직하게는 0.54 이하, 특히 바람직하게는 0.50 이하이다. 입도 분포는, 이차 입자군에 있어서의 개개의 이차 입자가 갖는 입경의 편차를 나타내는 지수이며, 값이 작을수록 입경의 편차가 작은 것을 나타낸다. 이차 입자의 입도 분포가 상기 범위 내이면, 이차 입자 표면에 다른 원소를 부착시키는 경우에, 부착물이 균일하게 부착하기 쉬워진다. 본 명세서에 있어서 입도 분포는, 이하와 같이 정의된다. 체적 기준의 누적 입도 분포에 있어서의 소경측으로부터의 누적 10%, 50% 및 90%에 대응하는 입경을 각각 10%입경(D10), 50%입경(D50) 및 90%입경(D90)으로 하는 경우에, D90과 D10의 차를 D50으로 나눈 값을 본 명세서에 있어서의 입도 분포로 한다. 즉, 이차 입자의 입도 분포는 아래 식으로 정의된다.
입도 분포 = (D90-D10)/D50
여기서 체적 기준의 누적 입도 분포는, 레이저 회절식 입경 분포 측정 장치를 사용하여 습식 조건에서 측정된다.
이차 입자의 체적 평균 입경은, 예를 들면 1㎛ 이상 30㎛ 이하이며, 바람직하게는 2㎛ 이상, 보다 바람직하게는 3㎛ 이상이며, 또한 바람직하게는 12㎛ 이하, 보다 바람직하게는 8㎛ 이하이다. 이차 입자의 체적 평균 입경이 상기 범위 내이면, 유동성이 좋고, 이차 전지를 구성할 때에 출력이 보다 향상되는 경우가 있다. 여기서 체적 평균 입경은, 체적 기준의 누적 입도 분포에 있어서의 소경측으로부터의 누적 50%에 대응하는 50%입경(D50)이다.
이차 입자는 복수의 일차 입자가 집합하여 형성된다. 일차 입자의 전자 현미경 관찰에 기초한 평균 입경(DSEM)은, 예를 들면 0.1㎛ 이상 1.5㎛ 이하이며, 바람직하게는 0.12㎛ 이상, 보다 바람직하게는 0.15㎛ 이상이다. 또한, 일차 입자의 전자 현미경 관찰에 기초한 평균 입경(DSEM)은, 바람직하게는 1.2㎛ 이하, 보다 바람직하게는 1.0㎛ 이하이다. 일차 입자의 전자 현미경 관찰에 기초한 평균 입경이 상기 범위 내이면 전지를 구성할 때에 출력이 향상되는 경우가 있다. 여기서 일차 입자의 전자 현미경 관찰에 기초한 평균 입경은, 이하와 같이 하여 측정된다. 주사 전자 현미경(SEM)을 사용하여, 입경에 따라 1000배 내지 15000배의 범위의 배율로, 이차 입자를 구성하는 일차 입자를 관찰한다. 윤곽을 확인할 수 있는 일차 입자를 50개 선택하고, 선택된 일차 입자의 윤곽으로부터 화상 처리 소프트웨어를 사용하여 구환산 직경을 산출하고, 얻어진 구환산 직경의 산술 평균값으로서 일차 입자의 전자 현미경 관찰에 기초한 평균 입경이 구해진다. 일 양태에 있어서, 일차 입자는, 그 표면에 일차 입자보다 작은 평균 입경을 갖는 입자가 부착되어 있어도 된다. 또한, 일 양태에 있어서, 일차 입자는, 일차 입자보다 작은 평균 입경을 갖는 입자의 집합체이어도 된다. 전술한 일차 입자보다 작은 평균 입경을 갖는 입자의 평균 입경은, 상기와 마찬가지로 전자 현미경 관찰에 기초하여 측정되어도 된다. 일차 입자의 윤곽을 확인할 수 있다는 것은, 화상 상에서 일차 입자의 윤곽 전체를 트레이스할 수 있다는 것을 의미한다.
이차 입자는, 체적 기준에 의한 누적 입도 분포에 있어서의 50%입경(D50)의 전자 현미경 관찰에 기초한 평균 입경(DSEM)에 대한 비 D50/DSEM이, 예를 들면, 2.5 이상이면 좋다. 비 D50/DSEM은, 예를 들면 2.5 이상 150 이하이며, 바람직하게는 5 이상, 보다 바람직하게는 10 이상이다. 또한, 비 D50/DSEM은, 바람직하게는 100 이하, 보다 바람직하게는 50 이하이다.
이차 입자를 구성하는 일차 입자에 포함되는 리튬 전이금속 복합 산화물은, 예를 들면, 조성에 니켈을 포함하고, 층상 구조를 가지고 있어도 된다. 리튬 전이금속 복합 산화물은, 적어도 리튬(Li)과 니켈(Ni) 등의 전이금속을 포함하고 있어도 되고, 알루미늄(Al), 코발트(Co) 및 망간(Mn)으로 이루어지는 군으로부터 선택되는 적어도 1종의 제1 금속 원소를 더 포함하고 있어도 된다. 리튬 전이금속 복합 산화물은, 리튬(Li), 니켈(Ni) 및 코발트(Co)을 포함하고, 알루미늄(Al) 및 망간(Mn) 중 적어도 일방을 더 포함하고 있어도 된다. 또한, 리튬 전이금속 복합 산화물은, 이들에 더하여, 마그네슘(Mg), 칼슘(Ca), 티탄(Ti), 지르코늄(Zr), 니오브(Nb), 탄탈(Ta), 크롬(Cr), 몰리브덴(Mo), 텅스텐(W), 철(Fe), 구리(Cu), 규소(Si), 주석(Sn), 비스무트(Bi), 갈륨(Ga), 이트륨(Y), 사마륨(Sm), 에르븀(Er), 세륨(Ce), 네오디뮴(Nd), 란탄(La), 카드뮴(Cd) 및 루테튬(Lu)으로 이루어지는 군으로부터 선택되는 적어도 1종의 제2 금속 원소를 더 포함하고 있어도 된다. 제2 금속 원소는, 지르코늄(Zr), 티탄(Ti), 마그네슘(Mg), 탄탈(Ta), 니오브(Nb), 몰리브덴(Mo) 및 텅스텐(W)으로 이루어지는 군으로부터 선택되는 적어도 1종이어도 된다.
리튬 전이금속 복합 산화물이 니켈을 포함하는 경우, 리튬 이외의 금속 원소의 총 몰수에 대한 니켈의 몰수의 비는, 예를 들면, 0보다 크고, 바람직하게는 0.33 이상이다. 리튬 이외의 금속 원소의 총 몰수에 대한 니켈의 몰수의 비는, 0.4 이상 또는 0.55 이상이면 좋다. 또한, 리튬 이외의 금속 원소의 총 몰수에 대한 니켈의 몰수의 비는, 예를 들면, 1 미만이며, 바람직하게는 0.95 이하, 보다 바람직하게는 0.8 이하이다. 니켈의 몰수의 비가 전술한 범위이면, 전고체 리튬 이온 이차 전지(이하, 단순히 전고체 이차 전지라고도 말함)에 있어서, 고전압시의 충방전 용량과 사이클 특성의 양립을 달성할 수 있다.
리튬 전이금속 복합 산화물이 코발트를 포함하는 경우, 리튬 이외의 금속 원소의 총 몰수에 대한 코발트의 몰수의 비는, 예를 들면, 0보다 크고, 바람직하게는 0.02 이상이며, 보다 바람직하게는 0.05 이상, 더욱 바람직하게는 0.1 이상, 특히 바람직하게는 0.15 이상이다. 또한, 리튬 이외의 금속 원소의 총 몰수에 대한 코발트의 몰수의 비는, 예를 들면, 1 미만이며, 바람직하게는 0.6 이하, 보다 바람직하게는 0.35 이하이다. 또한, 리튬 이외의 금속 원소의 총 몰수에 대한 코발트의 몰수의 비는, 0.33 이하, 0.3 이하, 또는 0.25 이하이어도 된다. 코발트의 몰수의 비가 전술한 범위이면, 전고체 이차 전지에 있어서, 고전압시에 있어서의 충분한 충방전 용량을 달성할 수 있다.
리튬 전이금속 복합 산화물이 망간 및 알루미늄 중 적어도 일방을 포함하는 경우, 리튬 이외의 금속 원소의 총 몰수에 대한 망간 및 알루미늄의 총 몰수의 비는, 예를 들면, 0보다 크고, 바람직하게는 0.01 이상, 보다 바람직하게는 0.05 이상, 더욱 바람직하게는 0.1 이상, 특히 바람직하게는 0.15 이상이다. 또한, 리튬 이외의 금속 원소의 총 몰수에 대한 망간 및 알루미늄의 총 몰수의 비는, 예를 들면, 0.6 이하, 바람직하게는 0.35 이하이다. 또한, 리튬 이외의 금속 원소의 총 몰수에 대한 망간 및 알루미늄의 총 몰수의 비는, 0.33 이하, 0.3 이하, 또는 0.25 이하이어도 된다. 망간 및 알루미늄의 총 몰수의 비가 전술한 범위 내이면, 전고체 이차 전지에 있어서, 충방전 용량과 안전성의 양립을 달성할 수 있다.
리튬 전이금속 복합 산화물에 있어서의, 리튬 이외의 금속의 총 몰수에 대한 리튬의 몰수의 비는, 예를 들면, 0.95 이상, 바람직하게는 1.0 이상이며, 보다 바람직하게는 1.03 이상, 더욱 바람직하게는 1.05 이상이다. 또한, 리튬 이외의 금속의 총 몰수에 대한 리튬의 몰수의 비는, 예를 들면, 1.5 이하이며, 바람직하게는 1.3 이하, 보다 바람직하게는 1.25 이하, 더욱 바람직하게는 1.2 이하이다. 리튬의 몰수의 비가 0.95 이상이면, 얻어지는 리튬 전이금속 복합 산화물을 포함하는 정극 활물질을 사용한 전고체 이차 전지에 있어서의 정극 표면과 고체 전해질의 계면에서 발생하는 계면 저항이 억제되기 때문에, 전고체 이차 전지의 출력이 향상되는 경향이 있다. 한편, 리튬의 몰수의 비가 1.5 이하이면, 정극 활물질을 전고체 이차 전지의 정극에 사용하는 경우의 초기 방전 용량이 향상되는 경향이 있다.
리튬 전이금속 복합 산화물이 니켈에 더하여, 코발트 및 망간을 포함하는 경우, 니켈, 코발트 및 망간의 몰수의 비는, 예를 들면, 니켈:코발트:망간=(0.33 내지 0.95):(0.02 내지 0.35):(0.01 내지 0.35)이며, 바람직하게는 (0.33 내지 0.8):(0.05 내지 0.35):(0.05 내지 0.35)이다. 리튬 전이금속 복합 산화물이 니켈에 더하여, 코발트 및 망간 및 알루미늄을 포함하는 경우, 니켈, 코발트 및 (망간+알루미늄)의 몰수의 비는, 예를 들면, 니켈:코발트:(망간+알루미늄)=(0.33 내지 0.95):(0.02 내지 0.35):(0.01 내지 0.35)이며, 바람직하게는 (0.33 내지 0.8):(0.05 내지 0.35):(0.05 내지 0.35)이다.
리튬 전이금속 복합 산화물이 적어도 1종의 제2 금속 원소를 포함하는 경우, 리튬 이외의 금속 원소의 총 몰수에 대한 제2 금속 원소의 총 몰수의 비는, 예를 들면, 0보다 크고, 바람직하게는 0.001 이상이며, 보다 바람직하게는 0.003 이상이다. 또한, 리튬 이외의 금속 원소의 총 몰수에 대한 제2 금속 원소의 총 몰수의 비는, 예를 들면, 0.02 이하이며, 바람직하게는 0.015 이하, 보다 바람직하게는 0.01 이하이다.
리튬 전이금속 복합 산화물을 조성으로서 나타내면, 예를 들면 하기 식(2)로 표현되는 리튬 전이금속 복합 산화물을 들 수 있다. 리튬 전이금속 복합 산화물은, 층상 구조를 가지고 있어도 되고, 육방정계의 결정 구조를 갖는 것이어도 된다.
LipNixCoyM1 zM2 wO2 + β
(2)
여기서, p, x, y, z, w 및 β는, 1.0≤p≤1.3, 0≤x≤1, 0≤y≤1, 0≤z≤1, 0≤w≤0.02, x+y+z+w=1, -0.1≤β≤0.1을 만족한다. x, y, z 및 w는, 0<x<1, 0≤y≤0.6, 0≤z≤0.6, 0≤w≤0.015를 만족해도 되고, 0.33≤x≤0.95, 0.01≤y≤0.35, 0≤z≤0.35, 0≤w≤0.01을 만족해도 되고, 0.33≤x≤0.95, 0.02≤y≤0.35, 0.05≤z≤0.35, 0≤w≤0.01을 만족해도 된다.
M1은 Mn 및 Al 중 적어도 일방을 나타내어도 된다. M2는 Mg, Ca, Ti, Zr, Nb, Ta, Cr, Mo, W, Fe, Cu, Si, Sn, Bi, Ga, Y, Sm, Er, Ce, Nd, La, Cd 및 Lu로 이루어지는 군으로부터 선택되는 적어도 1종을 나타내어도 되고, Zr, Ti, Mg, Ta, Nb, Mo 및 W로 이루어지는 군으로부터 선택되는 적어도 1종을 나타내어도 된다.
정극 활물질을 구성하는 이차 입자는, 그 표면에 니오브를 포함하는 부착물을 가지고 있어도 된다. 니오브를 포함하는 부착물은, 이차 입자의 표면에 부착되어 있어도 되고, 이차 입자의 입계(粒界)에 부착되어 있어도 된다. 또한, 니오브를 포함하는 부착물은 이차 입자를 구성하는 일차 입자의 표면에 부착되어 있어도 되고, 적어도 일부의 일차 입자에 고용(固溶)되어 있어도 된다. 또한, 정극 활물질을 구성하는 이차 입자는, 니오브를 포함하는 부착물 외에, 붕소, 규소, 티탄 등을 포함하는 이온 도전성을 갖는 화합물을 포함하는 부착물을 가지고 있어도 된다.
정극 활물질에 있어서의 니오브를 포함하는 부착물의 부착량은, 리튬 전이금속 복합 산화물에 대해 니오브 환산으로, 예를 들면, 0.1몰% 이상 10몰% 이하이며, 바람직하게는 0.2몰% 이상 8몰% 이하이다. 니오브의 부착량이 상기 범위이면, 양호한 사이클 특성을 유지하면서, 저항 성분을 저감할 수 있다.
니오브를 포함하는 부착물로서는, 예를 들면, 니오브산 리튬 등의 니오브 함유 화합물을 들 수 있다. 니오브를 포함하는 부착물은, 니오브 화합물의 용액 또는 분산액 또는 고체상의 니오브 화합물과, 이차 입자를 혼합하여 얻어져도 되고, 필요에 따라 혼합물을 열 처리하여 얻어져도 된다.
정극 활물질층에 있어서의 정극 활물질의 함유율은, 예를 들면 60질량% 이상이며, 바람직하게는 70질량% 이상이다. 또한, 정극 활물질의 함유율은, 예를 들면 95질량% 이하이며, 바람직하게는 90질량% 이하이다. 정극 활물질의 함유율이 60질량% 이상이면, 충분한 전지 용량이 얻어진다. 또한, 정극 활물질의 함유율이 95질량% 이하이면, 저항의 상승을 억제할 수 있다.
<고체 전해질 재료>
정극에 적용되는 고체 전해질 재료는, 리튬 이온 전도성을 갖는 재료이면 되고, 예를 들면, 황화물 고체 전해질 재료, 산화물 고체 전해질 재료, 질화물 고체 전해질 재료, 할로겐화물 고체 전해질 재료 등의 무기 고체 전해질 재료를 들 수 있다.
황화물 고체 전해질 재료로서는, 예를 들면, Li2S-P2S5, Li2S-P2S5-LiI, Li2S-P2S5-LiCl, Li2S-P2S5-LiBr, Li2S-P2S5-Li2O, Li2S-P2S5-Li2O-LiI, Li2S-SiS2, Li2S-SiS2-LiI, Li2S-SiS2-LiBr, Li2S-SiS2-LiCl, Li2S-SiS2-B2S3-LiI, Li2S-SiS2-P2S5-LiI, Li2S-B2S3, Li2S-P2S5-ZmSn(단, m, n은 양수이다. Z는 Ge, Zn 및 Ga로 이루어지는 군으로부터 선택되는 적어도 1종임), Li2S-GeS2, Li2S-SiS2-Li3PO4, Li2S-SiS2-LixMOy(단, x, y는 양수이다. M은 P, Si, Ge, B, Al, Ga 및 In으로 이루어지는 군으로부터 선택되는 적어도 1종임), Li10GeP2S12 등을 들 수 있다.
특히, 황화물 고체 전해질 재료는, Li, A(A는 P, Si, Ge, Al 및 B로 이루어지는 군으로부터 선택되는 적어도 1종임) 및 S를 함유하는 이온 전도체를 구비하는 것이 바람직하다. 나아가, 이온 전도체는, 오르토 조성의 음이온 구조(예를 들면, PS4 3- 구조, SiS4 4 - 구조, GeS4 4 - 구조, AlS3 3 - 구조, BS3 3- 구조)를 음이온의 주성분으로서 갖는 것이 바람직하다. 이에 의해, 화학 안정성이 높은 황화물 고체 전해질 재료로 할 수 있다. 오르토 조성의 음이온 구조의 비율은, 이온 전도체에 있어서의 전체 음이온 구조에 대하여, 70mol% 이상인 것이 바람직하고, 90mol% 이상인 것이 보다 바람직하다. 오르토 조성의 음이온 구조의 비율은 라만 분광법, NMR, XPS 등에 의해 결정할 수 있다.
황화물 고체 전해질 재료는, 이온 전도체에 더하여, LiI, LiBr 및 LiCl로 이루어지는 군으로부터 선택되는 적어도 1종을 함유하는 것이 바람직하다. LiI, LiBr 및 LiCl의 적어도 일부는, 통상, 각각, LiI 성분, LiBr 성분 및 LiCl 성분으로서 이온 전도체의 구조 중에 받아들여진 상태로 존재한다고 생각된다. 또한, 황화물 고체 전해질 재료는, X선 회절 측정에 있어서, LiI의 피크를 가지고 있어도 되지만, LiI의 피크를 갖지 않는 것이 바람직하다. 이에 의해, Li 이온 전도성이 보다 높아진다. 이 점에 대해서는, LiBr 및 LiCl에 대해서도 마찬가지이다. 황화물 고체 전해질 재료에 있어서의 LiX(X=I, Cl, Br)의 함유율은, 예를 들면 10mol% 이상 30mol% 이하의 범위 내이며, 15mol% 이상 25mol% 이하의 범위 내인 것이 바람직하다. 여기서, LiX의 비율이란, 황화물 고체 전해질 재료에 포함되는 LiX의 합계의 비율을 말한다.
산화물 고체 전해질 재료로서는, 예를 들면, Li2O-B2O3-P2O5, Li2O-SiO2, Li-La-Ta-O(예를 들면, Li5La3Ta2O12), Li-La-Zr-O(예를 들면, Li7La3Zr2O12), Li-Ba-La-Ta-O(예를 들면, Li6BaLa2Ta2O12), Li1 + xSixP1 - xO4(0≤x<1, 예를 들면 Li3 . 6Si0 .6P0. 4O4), Li1+xAlxGe2-x(PO4)3(0≤x≤2), Li1 + xAlxTi2 -x(PO4)3(0≤x≤2), Li3PO(4-3/2x)Nx(0≤x<1) 등을 들 수 있다. 또한, 질화물 고체 전해질 재료로서는, 예를 들면 Li3N 등을 들 수 있고, 할로겐화물 고체 전해질 재료로서는, 예를 들면 LiI 등을 들 수 있다.
고체 전해질 재료는 결정성 재료이어도 되고, 비정질 재료이어도 된다. 또한, 고체 전해질 재료는 글래스이어도 되고, 결정화 글래스(글래스 세라믹스)이어도 된다. 글래스의 제작 방법으로서는, 예를 들면, 원료 조성물에 비정질화 처리를 행하는 방법을 들 수 있다. 비정질화 처리로서는, 예를 들면, 용융 급냉법, 기계적 밀링법 등을 들 수 있다. 결정화 글래스의 제작 방법으로서는, 예를 들면, 글래스를 결정화 온도 이상의 온도로 가열하는 방법을 들 수 있다. 또한, 결정성 재료의 제작 방법으로서는, 예를 들면, 원료 조성물을 고체 그대로 가열하는 방법(고상법)을 들 수 있다.
고체 전해질 재료의 형상은, 특별히 한정되지 않지만, 예를 들면 대략 구 형상을 들 수 있다. 고체 전해질 재료의 체적 평균 입경(D50)은, 예를 들면, 0.1㎛ 이상이며, 0.5㎛ 이상이어도 된다. 한편, 고체 전해질 재료의 체적 평균 입경(D50)은, 예를 들면, 50㎛ 이하이며, 10㎛ 이하이어도 된다. 또한, 고체 전해질 재료의 Li 이온 전도도는, 25℃에서, 예를 들면, 1×10-5S/cm 이상이며, 1×10-4S/cm 이상인 것이 바람직하고, 1×10-3S/cm 이상인 것이 보다 바람직하다.
정극 활물질층에 있어서의 고체 전해질 재료의 함유율은, 예를 들면, 1질량% 이상이며, 바람직하게는 5질량% 이상, 보다 바람직하게는 10질량% 이상인 것이 바람직하다. 고체 전해질 재료의 함유율이 1질량% 이상이면, 정극 활물질층의 Li 이온 전도성이 충분히 향상된다. 한편, 정극 활물질층에 있어서의 고체 전해질 재료의 함유율은, 예를 들면, 60질량% 이하이며, 바람직하게는 50질량% 이하, 보다 바람직하게는 40질량% 이하, 더욱 바람직하게는 30질량% 이하이다. 고체 전해질 재료의 함유율이 60질량% 이하이면, 상대적으로 정극 활물질의 함유율이 너무 낮아지지 않아, 충분한 전지 용량이 얻어진다. 또한, 정극 활물질층에 있어서, 고체 전해질 재료의 함유율은, 정극 활물질의 함유율보다 낮은 것이 바람직하다.
나아가, 정극 활물질층에 있어서의 정극 활물질의 함유량에 대한 고체 전해질 재료의 함유량의 비(고체 전해질 재료/정극 활물질)는, 예를 들면, 0.01 이상이며, 바람직하게는 0.1 이상이어도 된다. 또한, 정극 활물질의 함유량에 대한 고체 전해질 재료의 함유량의 비는, 예를 들면 1.5 이하이며, 바람직하게는 1 이하이다.
정극은, 정극 활물질 및 고체 전해질 재료에 더하여, 도전 보조재를 활물질층에 함유하고 있어도 된다. 도전 보조재를 더 포함함으로서, 정극 활물질층에 있어서의 전자 전도성을 보다 향상시킬 수 있다. 도전 보조재로서는, 예를 들면, 아세틸렌 블랙(AB), 케첸 블랙(Ketjen black, KB), 기상 성장 탄소 섬유(VGCF), 카본 나노튜브(CNT), 카본 나노 파이버(CNF) 등의 탄소 재료를 들 수 있다.
정극 활물질층이 도전 보조재를 포함하는 경우, 정극 활물질층에 있어서의 도전 보조재의 함유율은, 예를 들면, 1질량% 이상이며, 바람직하게는 2질량% 이상이어도 된다. 또한, 정극 활물질층에 있어서의 도전 보조재의 함유율은, 예를 들면, 10질량% 이하이며, 바람직하게는 5질량% 이하이어도 된다.
정극은, 결착재를 활물질층에 더 함유하고 있어도 된다. 결착재를 포함함으로써, 정극 활물질층의 성형성을 보다 향상시킬 수 있다. 결착재로서는, 예를 들면, 폴리불화비닐리덴(PVDF), 부틸렌 고무(BR), 스티렌 부타디엔 고무(SBR) 등을 들 수 있다. 정극은, 증점재를 활물질층에 더 함유하고 있어도 된다.
정극의 형태로서는, 집전체와 집전체 상에 배치되는 정극 활물질층을 갖는 형태이어도 되고, 원하는 형상으로 성형되는 정극 활물질층만으로 이루어지는 형태이어도 된다.
정극의 제조 방법으로서는, 정극 활물질 및 고체 전해질 재료를 적어도 함유하는 정극 합재를 준비하는 준비 공정과, 준비한 정극 합재를 원하는 형상으로 성형하는 성형 공정을 포함하고 있어도 된다. 성형 공정은, 필요에 따라, 집전체 상에 정극 합재를 부여하는 것과, 부여한 정극 합재를 성형하는 것을 포함하고 있어도 된다.
정극 합재의 제조 방법으로서는, 예를 들면, 정극 활물질 및 고체 전해질 재료를 혼합하는 것을 포함하고, 필요에 따라 도전 보조재를 함께 혼합하는 것을 포함하는 방법을 들 수 있다. 혼합은, 예를 들면, 건식 혼합으로 할 수 있고, 믹서 등을 사용하여 행할 수 있다. 또한, 제조 방법으로서, 정극 활물질 및 고체 전해질 재료의 혼합물에 분산매를 첨가하여 슬러리를 형성하는 것과, 슬러리에 분산 촉진 처리를 행하는 것과, 슬러리로부터 분산매를 제거하는 것을 포함하는 방법을 들 수도 있다. 분산 촉진 처리로서는, 예를 들면, 초음파 처리, 진동 처리 등을 들 수 있다.
정극 합재의 성형 방법으로서는, 예를 들면, 압축 성형을 들 수 있다. 압축 성형의 압력으로서는, 예를 들면 50MPa 이상이며, 50MPa 이상 500MPa 이하, 또는 100MPa 이상 350MPa 이하로 할 수 있다. 정극 활물질층이 압축 성형으로 형성됨으로써, 정극 활물질과 고체 전해질 재료가 밀착하여, 계면 저항을 저하시킬 수 있다.
<전고체 리튬 이온 이차 전지>
전고체 리튬 이온 이차 전지는, 정극 활물질 및 고체 전해질 재료를 함유하는 정극 활물질층을 포함하는 정극과, 부극 활물질을 함유하는 부극 활물질층을 포함하는 부극과, 정극 활물질층 및 부극 활물질층의 사이에 배치되는 고체 전해질층을 포함한다. 정극 활물질을 구성하는 이차 입자가 전술한 특정 구성을 가짐으로써, 내부 저항이 저감되는 전고체 리튬 이온 이차 전지를 구성할 수 있다.
<정극>
정극은, 전술한 정극 활물질 및 고체 전해질 재료를 함유하는 정극 합재로 구성되는 형태를 포함한다. 정극에 있어서는, 필요에 따라, 정극 활물질층이 집전을 행하는 정극 집전체와 일체로 형성되어 있어도 된다. 정극 활물질은, 리튬 전이금속 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함하여 구성된다. 이차 입자의 평활도 및 원형도에 대해서는 이미 서술한 바와 같고, 바람직한 양태도 마찬가지이다. 정극 활물질층의 두께는, 예를 들면, 0.1㎛ 이상 1000㎛ 이하의 범위 내이며, 바람직하게는 0.1㎛ 이상 300㎛ 이하의 범위 내이다.
<부극>
부극은, 적어도 부극 활물질을 함유하는 부극 활물질층을 포함한다. 부극에 있어서는, 필요에 따라, 부극 활물질층이 집전을 행하는 부극 집전체와 일체로 형성되어 있어도 된다. 부극 활물질층은, 필요에 따라, 고체 전해질 재료, 도전 보조재 및 결착재 중 적어도 1종을 더 함유하고 있어도 된다. 고체 전해질 재료, 도전 보조재 및 결착재에 대해서는, 이미 서술한 바와 같다.
부극 활물질로서는, 예를 들면, 카본 활물질, 금속 활물질 및 산화물 활물질 등을 들 수 있다. 카본 활물질로서는, 예를 들면, 그래파이트, 하드 카본, 소프트 카본 등을 들 수 있다. 금속 활물질로서는, 예를 들면, In, Al, Si, Sn, 및, 이들을 적어도 포함하는 합금 등을 들 수 있다. 산화물 활물질로서는, 예를 들면, 산화니오브(예를 들면, Nb2O5), 티탄산 리튬(예를 들면, Li4Ti5O12), 산화규소(예를 들면, SiO) 등을 들 수 있다. 부극 활물질층의 두께는, 예를 들면, 0.1㎛ 이상 1000㎛ 이하의 범위 내이며, 바람직하게는 0.1㎛ 이상 300㎛ 이하의 범위 내이다.
<고체 전해질층>
고체 전해질층은, 정극 활물질층 및 부극 활물질층의 사이에 배치되는 층이다. 고체 전해질층은, 적어도 고체 전해질 재료를 함유하는 층이며, 필요에 따라, 결착재 등을 더 함유하고 있어도 된다. 고체 전해질 재료 및 결착재에 대해서는, 이미 서술한 바와 같다.
고체 전해질층에 포함되는 고체 전해질 재료의 함유율은, 예를 들면, 10질량% 이상 100질량% 이하의 범위 내이며, 바람직하게는 50질량% 이상 100질량% 이하의 범위 내이다. 고체 전해질층의 두께는, 예를 들면, 0.1㎛ 이상 1000㎛ 이하의 범위 내이며, 바람직하게는 0.1㎛ 이상 300㎛ 이하의 범위 내이다. 또한, 고체 전해질층의 형성 방법으로서는, 예를 들면, 고체 전해질 재료를 압축 성형하는 방법 등을 들 수 있다.
<그 밖의 구성>
전고체 리튬 이온 이차 전지는, 전술한 정극, 부극 및 고체 전해질층을 적어도 갖는다. 나아가, 정극 활물질층의 집전을 행하는 정극 집전체, 및 부극 활물질층의 집전을 행하는 부극 집전체를 가지고 있어도 된다. 정극 집전체의 재료로서는, 예를 들면, 스테인리스강(SUS), Ni, Cr, Au, Pt, Al, Fe, Ti, Zn 등을 들 수 있다. 부극 집전체의 재료로서는, 예를 들면, 스테인리스강(SUS), Cu, Ni, Fe, Ti, Co, Zn 등을 들 수 있다. 또한, 전고체 리튬 이온 이차 전지는, 예를 들면 SUS제 전지 케이스 등이 임의의 전지 케이스를 구비하고 있어도 된다. 전고체 리튬 이온 이차 전지의 형상으로서는, 예를 들면, 코인형, 라미네이트형, 원통형 및 각형(角型) 등을 들 수 있다.
<비수 전해질 이차 전지>
본 개시의 일 양태에 의해 얻어지는 정극 활물질은, 비수 전해질을 사용한 비수 전해질 이차 전지(이하, 비수 전해액 이차 전지)용의 정극에 사용할 수도 있다. 비수 전해질 이차 전지에 사용하는 경우에도, 정극 형성시의 가압 성형에 의한 이차 입자의 깨어짐을 저감할 수 있다. 비수 전해질 이차 전지는, 전술한 정극에 더하여, 비수 전해질 이차 전지용 부극, 비수 전해질, 세퍼레이터 등을 구비하여 구성된다. 비수 전해질 이차 전지에 있어서의, 부극, 비수 전해질, 세퍼레이터 등에 대해서는, 예를 들면, 일본특허공개 제2002-075367호 공보, 일본특허공개 제2011-146390호 공보, 일본특허공개 제2006-12433호 공보(이들은, 그 개시 내용 전체가 참조에 의해 본 명세서에 통합됨) 등에 기재된, 비수 전해질 이차 전지용을 위한 것을 적절히 사용할 수 있다.
<정극 활물질의 제조 방법>
정극 활물질의 제조 방법은, 예를 들면, 니켈 및 코발트를 포함하는 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함하며, 이차 입자의 평활도가 0.74보다 큰 니켈 코발트 복합 산화물을 준비하는 복합 산화물 준비 공정과, 니켈 코발트 복합 산화물과 리튬 화합물을 혼합하여, 리튬 혼합물을 얻는 리튬 혼합 공정과, 리튬 혼합물을 열 처리하여, 니켈 및 코발트를 포함하며 층상 구조를 갖는 리튬 전이금속 복합 산화물을 얻는 합성 공정을 포함하고 있어도 된다. 제조되는 정극 활물질은, 리튬 전이금속 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함한다. 이차 입자의 평활도는 0.73보다 크면 좋다. 이차 입자의 원형도는 0.83보다 크면 좋다. 정극 활물질의 제조 방법은, 리튬 전이금속 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함하는 정극 활물질로서, 이차 입자의 평활도가 0.73보다 크고, 이차 입자의 원형도가 0.83보다 큰 정극 활물질의 제조 방법이어도 된다.
<복합 산화물 준비 공정>
복합 산화물 준비 공정에서는, 니켈 및 코발트를 포함하는 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함하는 니켈 코발트 복합 산화물을 준비한다. 니켈 코발트 복합 산화물을 구성하는 이차 입자의 평활도는 0.74보다 크면 좋다. 니켈 코발트 복합 산화물은, 시판품으로부터 적절히 선택하여 준비해도 되고, 후술하는 니켈 코발트 복합 산화물의 제조 방법에 의해, 제조하여 준비해도 된다. 준비되는 니켈 코발트 복합 산화물의 상세에 대해서는 후술한다.
<리튬 혼합 공정>
리튬 혼합 공정에서는, 준비되는 니켈 코발트 복합 산화물과 리튬 화합물을 혼합하여 리튬 혼합물을 얻는다. 혼합 방법으로서는, 예를 들면, 니켈 코발트 복합 산화물과 리튬 화합물을 교반 혼합기 등에서 건식 혼합하는 방법, 니켈 코발트 복합 산화물의 슬러리를 조제하고, 볼 밀 등의 혼합기에서 습식 혼합하는 방법을 들 수 있다. 리튬 화합물로서는, 예를 들면, 수산화리튬, 질산 리튬, 탄산 리튬, 이들의 혼합물을 들 수 있다.
리튬 혼합물에 있어서의 리튬 이외의 금속 원소의 총 몰수에 대한 리튬의 몰수의 비(리튬비라고도 말함)은, 예를 들면 0.90 이상 1.30 이하이어도 되고, 바람직하게는 1.0 이상 1.20 이하이다. 리튬비가 0.90 이상이면 부생성물의 생성이 억제되는 경향이 있다. 또한, 리튬비가 1.30 이하이면 리튬 혼합물의 표면에 존재하는 알칼리 성분량의 증가가 억제되고, 알칼리 성분의 조해성(潮解性)에 의한 수분 흡착이 억제되어, 핸들링성이 향상되는 경향이 있다.
<합성 공정>
합성 공정에서는, 리튬 혼합물을 열 처리하여, 니켈 및 코발트를 포함하며 층상 구조를 갖는 리튬 전이금속 복합 산화물을 얻는다. 리튬 전이금속 복합 산화물은 일차 입자에 포함되고, 일차 입자가 복수 집합하여 이루어지는 이차 입자가 정극 활물질에 포함된다. 합성 공정에서는, 리튬 화합물에 포함되는 리튬이 니켈 코발트 복합 산화물 중에 확산함으로써, 리튬 전이금속 복합 산화물이 얻어져도 된다.
열 처리 온도는, 예를 들면 650℃ 이상 990℃ 이하이어도 되고, 바람직하게는 700℃ 이상 960℃ 이하이다. 열 처리 온도가 650℃ 이상이면 미반응 리튬분의 증가가 억제되는 경향이 있다. 열 처리 온도가 990℃ 이하이면 생성하는 리튬 전이금속 복합 산화물의 분해가 억제되는 경향이 있다. 열 처리 시간은 최고 온도를 보유하는 시간으로서, 예를 들면 10시간 이상이어도 된다. 열 처리의 분위기는, 산소 존재 하이어도 되고, 바람직하게는 10체적% 이상 100체적% 이하의 산소를 함유하는 분위기이다.
정극 활물질의 제조 방법에 있어서는, 합성 공정 후, 필요에 따라 얻어지는 열 처리물을 조쇄(粗碎), 분쇄, 건식 체질 등의 처리를 행해도 된다.
<니켈 코발트 복합 산화물의 제조 방법>
니켈 코발트 복합 산화물의 제조 방법은, 예를 들면, 니켈 이온 및 코발트 이온을 포함하는 제1 용액을 준비하는 제1 용액 준비 공정과, 착이온 형성 인자를 포함하는 제2 용액을 준비하는 제2 용액 준비 공정과, pH가 10 이상 13.5 이하의 범위에 있는 액매체를 준비하는 액매체 준비 공정과, 액매체에, 제1 용액 및 제2 용액을 따로따로 또한 동시에 공급하면서, (메타)아크릴산에서 유래하는 구성 단위를 포함하는 중합체를 공급하여, pH가 10 이상 13.5 이하의 범위로 유지되는 반응 용액을 얻는 정석(晶析) 공정과, 반응 용액으로부터 니켈 및 코발트를 포함하는 복합 수산화물을 얻는 복합 수산화물 회수 공정과, 얻어지는 복합 수산화물을 열 처리하여, 니켈 및 코발트를 포함하는 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 얻는 복합 수산화물 열 처리 공정을 포함한다. 제조되는 니켈 코발트 복합 산화물을 포함하는 이차 입자의 평활도는 0.74보다 크다. 니켈 코발트 복합 산화물의 제조 방법은, 니켈 및 코발트를 포함하는 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함하는 니켈 코발트 복합 산화물로서, 이차 입자의 평활도가 0.74보다 큰 니켈 코발트 복합 산화물의 제조 방법이어도 된다.
<제1 용액 준비 공정>
제1 용액 준비 공정에서는, 니켈 이온 및 코발트 이온을 포함하는 제1 용액을 준비한다. 제1 용액은, 목적으로 하는 니켈 코발트 복합 산화물의 조성에 따라, 각 금속 원소를 포함하는 염의 소정량을 물에 용해하여 조제된다. 염의 종류로서는, 질산염, 황산염, 염산염 등을 들 수 있다. 또한, 제1 용액을 조제할 때에, 물에 산성 물질(예를 들면, 황산 수용액)을 첨가해도 된다. 이에 의해, 각 금속 원소를 포함하는 염이 용해하기 쉬워지는 경우가 있다. 제1 용액의 조제에 있어서는, 염기성 물질을 더 첨가하여 pH 조정을 행해도 된다. 또한, 제1 용액에 있어서의 니켈, 코발트 등의 금속 원소의 합계 몰수는, 목적으로 하는 니켈 코발트 복합 산화물의 평균 입경에 따라 적절히 설정해도 된다. 여기서 금속 원소의 합계 몰수는, 제1 용액이, 니켈 및 코발트를 포함하는 경우에는 니켈 및 코발트의 합계 몰수이며, 니켈, 코발트 및 망간을 포함하는 경우에는 니켈, 코발트 및 망간의 합계 몰수를 의미한다.
제1 용액은, 니켈 이온 및 코발트 이온에 더하여, 알루미늄 이온 및 망간 이온 중 적어도 일방을 더 포함하고 있어도 된다. 또한, 제1 용액은, 이들에 더하여, 마그네슘, 칼슘, 티탄, 지르코늄, 니오브, 탄탈, 크롬, 몰리브덴, 텅스텐, 철, 구리, 규소, 주석, 비스무트, 갈륨, 이트륨, 사마륨, 에르븀, 세륨, 네오디뮴, 란탄, 카드뮴 및 루테튬으로 이루어지는 군으로부터 선택되는 적어도 1종의 제2 금속 원소의 이온을 더 포함하고 있어도 된다. 제2 금속 원소는, 지르코늄, 티탄, 마그네슘, 탄탈, 니오브, 몰리브덴 및 텅스텐으로 이루어지는 군으로부터 선택되는 적어도 1종이어도 된다.
제1 용액의 니켈, 코발트 등의 금속 이온의 농도는, 각 금속 이온의 합계로, 예를 들면 1.0mol/L 이상 2.6mol/L 이하이어도 되고, 바람직하게는 1.5mol/L 이상 2.2mol/L 이하이다. 제1 용액의 금속 이온 농도가 1.0mol/L 이상이면, 반응조당 정석 물량이 충분히 얻어지기 때문에 생산성이 향상된다. 한편, 제1 용액의 금속 이온 농도가 2.6mol/L 이하이면, 상온에서의 금속염의 포화 농도를 초과하는 것이 억제되어, 금속염 결정의 석출에 의한 용액 중의 금속 이온 농도의 감소가 억제된다.
<제2 용액 준비 공정>
제2 용액 준비 공정에서는, 착이온 형성 인자를 포함하는 제2 용액을 준비한다. 제2 용액은, 제1 용액에 포함되는 금속 이온과 착이온을 형성할 수 있는 착이온 형성 인자를 포함하는 것이다. 예를 들면, 착이온 형성 인자가 암모니아인 경우, 제2 용액으로서는 암모니아 수용액을 사용할 수 있다. 암모니아 수용액 중에 포함되는 암모니아의 함유량은, 예를 들면 5질량% 이상 25질량% 이하이어도 되고, 바람직하게는 10질량% 이상 20질량% 이하이다.
<액매체 준비 공정>
액매체 준비 공정에서는, pH가 10 이상 13.5 이하의 범위에 있는 액매체를 준비한다. 액매체는, 예를 들면 반응 용기에 소정량의 물과 수산화나트륨 수용액 등의 염기성 용액을 사용하여 pH 10 이상 13.5 이하의 용액으로서 조정된다. 용액의 pH를 10 이상 13.5 이하로 조정함으로써, 반응 초기에 있어서의 반응 용액의 pH 변동을 억제할 수 있다.
<정석 공정>
정석 공정에서는, 형성되는 반응 용액의 pH를 10 이상 13.5 이하의 범위로 유지하면서, 액매체에 제1 용액 및 제2 용액을 따로따로 또한 동시에 공급한다. 또한, 아울러 (메타)아크릴산에서 유래하는 구성 단위를 포함하는 중합체를 액매체에 공급한다. 이에 의해, 반응 용액으로부터 니켈 및 코발트를 포함하는 복합 수산화물 입자를 얻을 수 있다. 액매체에는, 제1 용액 및 제2 용액에 더하여, 염기성 용액을 동시에 공급해도 된다. 이에 의해, 반응 용액의 pH를 10 이상 13.5 이하의 범위에 용이하게 유지할 수 있다.
정석 공정에서는, 반응 용액의 pH가 10 이상 13.5 이하의 범위를 유지하도록 각 용액을 공급하는 것이 바람직하다. 예를 들면, 제1 용액의 공급량에 따라, 제2 용액의 공급량을 조정함으로써 반응 용액의 pH를 10 이상 13.5 이하의 범위로 유지할 수 있다. 반응 용액의 pH가 10보다 낮은 경우에는, 얻어지는 복합 수산화물에 포함되는 불순물(예를 들면, 혼합 용액에 포함되는 금속 이외의 황산분이나 질산분)의 양이 많아지고, 최종 생산물인 이차 전지의 용량 저하를 초래하는 경우가 있다. 또한, pH가 13.5보다 높은 경우에는, 미소한 이차 입자가 많이 생성되어, 얻어지는 복합 수산화물의 핸들링성이 나빠지는 경우가 있다. 또한, 반응 용액의 온도는, 예를 들면 25℃ 이상 80℃ 이하의 범위가 되도록 제어해도 된다.
정석 공정에서는, 반응 용액 중의 니켈 이온의 농도를, 예를 들면 10ppm 이상 1000ppm 이하의 범위가 되도록 유지해도 되고, 바람직하게는 10ppm 이상 100ppm 이하의 범위가 되도록 유지한다. 니켈 이온의 농도가 10ppm 이상이면, 복합 수산화물이 충분히 석출된다. 니켈 이온의 농도가 1000ppm 이하이면, 용출하는 니켈량이 적기 때문에, 목적으로 하는 조성으로부터 벗어나는 것이 억제된다. 니켈 이온 농도는, 예를 들면 착이온 형성 용액에 암모니아 수용액을 사용한 경우, 반응 용액 중의 암모늄 이온 농도가, 1000ppm 이상 15000ppm 이하가 되도록, 착이온 형성 용액을 공급함으로써, 조정할 수 있다.
제1 용액을 공급하는 시간은, 예를 들면 6시간 이상 60시간 이하이어도 되고, 바람직하게는 8시간 이상 60시간 이하이어도 되고, 보다 바람직하게는 10시간 이상 42시간 이하이다. 6시간 이상이면, 복합 수산화물의 석출 속도가 늦어지기 때문에, 보다 평활도가 높은 니켈 코발트 복합 산화물이 얻어지는 경향이 있다. 또한, 60시간 이하이면, 생산성을 보다 향상시킬 수 있다.
정석 공정 전체를 통해서 공급되는 제1 용액의 니켈, 코발트 등의 합계 몰수를 분모로 하고, 한시간당 공급되는 제1 용액의 니켈, 코발트 등의 합계 몰수를 분자로 한 값은, 예를 들면 0.015 이상 0.125 이하이어도 되고, 바람직하게는 0.020 이상 0.10 이하이다. 0.015 이상이면, 생산성을 보다 향상시킬 수 있다. 또한, 0.125 이하이면, 보다 평활도가 높은 니켈 코발트 복합 산화물이 얻어지는 경향이 있다.
액매체에 공급되는 (메타)아크릴산에서 유래하는 구성 단위를 포함하는 중합체는, 예를 들면, 계면활성제, 분산제 등으로서 기능할 수 있는 카르복시기를 갖는 음이온계 중합체이어도 된다. 중합체가 (메타)아크릴산에서 유래하는 구성 단위를 포함함으로써, 반응 용액의 기포가 억제되어, 얻어지는 복합 수산화물의 평활도 및 원형도 중 적어도 일방이 향상된다. 예를 들면, 분산제로서 일반적인 비이온계 분산제에서는, 반응 용액에 기포가 발생하여 입경 제어가 곤란해지는 경우가 있다.
중합체를 구성하는 (메타)아크릴산에서 유래하는 구성 단위에는, 아크릴산에서 유래하는 구성 단위, 메타크릴산에서 유래하는 구성 단위, 아크릴산 에스테르에서 유래하는 구성 단위, 메타크릴산 에스테르에서 유래하는 구성 단위, 아크릴산 아미드에서 유래하는 구성 단위, 메타크릴산 아미드에서 유래하는 구성 단위 등이 포함된다. 중합체는 (메타)아크릴산에서 유래하는 구성 단위에 더하여, 다른 구성 단위를 더 포함하고 있어도 된다. 다른 구성 단위로서는, 예를 들면, 불포화 이염기산 또는 그의 산무수물에서 유래하는 구성 단위를 들 수 있다.
중합체의 중량 평균 분자량은, 예를 들면 50000 이하이어도 되고, 바람직하게는 40000 이하, 30000 이하, 또는 20000 이하이다. 중합체의 중량 평균 분자량의 하한은, 예를 들면 1000 이상이어도 되고, 바람직하게는 3000 이상, 보다 바람직하게는 6000 이상이다. 중합체의 중량 평균 분자량이 상기 범위 내이면, 이차 입자의 입경 제어가 보다 용이해지며, 평활도가 보다 높아지는 경향이 있다.
중합체는, 나트륨 이온 등의 알칼리 금속 이온, 유기 암모늄 이온, 암모늄 이온 등의 중화 염기에 의해, 카르복시기의 적어도 일부가 중화된 알칼리 금속염, 유기 아민염, 암모늄염 등으로서 액매체에 공급되어도 된다. 또한, 중합체는 1종을 단독으로 사용해도 되고, 2종 이상을 조합하여 사용해도 된다. 2종 이상의 중합체를 사용하는 경우, 조성이 다른 조합, 중량 평균 분자량이 다른 조합, 중화 염기가 다른 조합, 또는 이들의 조합의 어느 것이어도 된다.
액매체에 공급되는 중합체에는, (메타)아크릴산에서 유래하는 구성 단위를 포함하는 중합체 이외의 그 밖의 계면활성제를 병용해도 된다. 그 밖의 계면활성제로서는, 인산기, 술폰산기 등을 갖는 음이온계 계면활성제, 4급 암모늄기 등을 갖는 양이온계 계면활성제, 비이온계 계면활성제 등을 들 수 있다. 그 밖의 계면활성제의 공급량은, 예를 들면 (메타)아크릴산에서 유래하는 구성 단위를 포함하는 중합체의 공급량에 대해 10질량% 이하이어도 되고, 바람직하게는 1질량% 이하이다.
중합체의 액매체에의 공급량은, 생성하는 복합 수산화물의 총 질량에 대하여, 예를 들면 0.5질량% 이상 5질량% 이하이어도 되고, 바람직하게는 1질량% 이상 3질량% 이하이다. 중합체의 공급량이 생성하는 복합 수산화물의 총 질량에 대해 0.5질량% 이상이면, 얻어지는 복합 수산화물의 평활도 및 원형도 중 적어도 일방이 향상되는 경향이 있다. 또한, 공급량이 5질량% 이하이면, 정석 공정에서의 이차 입자의 응집을 억제하며, 얻어지는 복합 수산화물의 평활도 및 원형도 중 적어도 일방이 보다 향상되는 경향이 있다.
액매체에의 중합체의 공급은, 중합체를 포함하는 중합체 용액을 제1 용액 및 제2 용액과는 독립시켜 공급해도 되고, 제1 용액 및 제2 용액 중 적어도 일방과 함께 공급해도 된다. 제1 용액 및 제2 용액 중 적어도 일방과 함께 공급하는 경우, 제1 용액 및 제2 용액 중 적어도 일방이 중합체를 포함하고 있어도 되고, 제1 용액 및 제2 용액 중 적어도 일방과 중합체 용액을 혼합하고 나서 액매체에 공급해도 된다. 액매체에의 중합체의 공급에 사용되는 용액에 있어서의 중합체의 함유량은, 용액의 질량에 대하여, 예를 들면 0.05질량% 이상 3.1질량% 이하이어도 되고, 바람직하게는 0.1질량% 이상 0.8질량% 이하이다.
정석 공정은, 제1 용액 및 제2 용액을 따로따로 또한 동시에 액매체에 공급하는 것과, 제1 용액 및 제2 용액과는 별도로 또한 동시에 중합체를 공급하거나, 또는 제1 용액 및 제2 용액 중 적어도 일방과 함께 중합체를 공급하는 것을 이 순서로 포함하고 있어도 된다. 바꾸어 말하면, 중합체의 공급에 앞서, 제1 용액 및 제2 용액의 일부를 따로따로 또한 동시에 액매체에 공급해도 된다. 제1 용액과 제2 용액을 액매체에 공급함으로써, 액매체 중에 생성하는 니켈 및 코발트를 포함하는 복합 수산화물의 입경을 원하는 크기로 제어할 수 있다. 여기서 복합 수산화물은, 예를 들면 시드 결정으로서 생성되어도 된다. 중합체의 공급에 앞서, 액매체 중에 원하는 입경을 갖는 복합 수산화물을 생성시킴으로써, 일차 입자의 응집을 억제하며, 이차 입자로서 생성하는 복합 수산화물의 평활도 및 원형도 중 적어도 일방이 보다 향상되는 경향이 있다.
정석 공정에 있어서, 중합체의 공급에 앞서, 제1 용액 및 제2 용액을 따로따로 또한 동시에 액매체에 공급하는 것을 포함하는 경우, 중합체의 공급보다 앞서는 제1 용액 및 제2 용액의 공급 시간은, 전체 공급 시간의 2% 이상 95% 이하이어도 된다. 바람직하게는 3% 이상 40% 이하이며, 보다 바람직하게는 5% 이상 20% 이하이다. 중합체의 공급보다 앞서는 제1 용액 및 제2 용액의 공급 시간을 이 범위로 함으로써, 전술한 바와 같이, 액매체 중에 원하는 입경을 갖는 복합 수산화물을 생성시킬 수 있어, 일차 입자의 응집을 억제하며, 평활도 및 원형도 중 적어도 일방이 보다 향상된다.
니켈 코발트 복합 산화물의 제조 방법은, 정석 공정에 앞서 시드 결정 생성 공정을 포함하고 있어도 된다. 시드 결정 생성 공정에서는, 예를 들면 준비한 제1 용액의 일부를 액매체에 공급함으로써, 액매체 중에 니켈 및 코발트를 포함하는 복합 수산화물을, 예를 들면 시드 결정으로서 생성시킨다. 즉, 정석 공정에 제공되는 액매체는, 복합 수산화물을 포함하는 시드 용액이어도 된다.
정석 공정에 앞서, 액매체 중에 미리 복합 수산화물 입자를 생성해 두면, 미리 생성한 복합 수산화물의 입자 1개가, 정석 공정 후에 얻어지는 복합 수산화물의 입자 1개를 구성하는 시드 결정이 된다. 이에 의해, 미리 생성시킨 복합 수산화물 입자의 수에 의해, 정석 공정 후에 얻어지는 복합 수산화물의 이차 입자의 총 수를 제어할 수 있다. 예를 들면, 미리 제1 용액을 많이 공급하면 생성하는 복합 수산화물 입자의 수가 많아지므로, 정석 공정 후의 복합 수산화물의 이차 입자의 평균 입경이 작아지는 경향이 있다. 또한, 예를 들면, 당초의 액매체의 pH를, 얻어지는 반응 용액의 pH보다 높게 하는 경우, 복합 수산화물 입자의 성장보다도, 복합 수산화물 입자의 생성이 우선된다. 이에 의해, 보다 균질한 입경을 갖는 복합 수산화물 입자가 생성되어, 입도 분포가 보다 좁은 복합 수산화물 입자를 얻을 수 있다.
정석 공정에 있어서, 제1 용액, 제2 용액 및 중합체 용액은, 각각 연속적으로 액매체에 공급되어도 되고, 단속적으로 공급되어도 된다. 원형도 및 평활도 향상의 관점에서, 제1 용액은, 정석 공정에 있어서의 제1 용액의 공급 시간 전체에 걸쳐, 연속적으로 공급되고 있는 것이 바람직하다. 여기서, 「공급 시간 전체에 걸쳐, 연속적으로」란, 공급 시간 전체를 통하여, 공급되지 않는 시간이 거의 존재하지 않는 것을 의미한다. 또한, 공급 시간이 거의 존재하지 않는다는 것은, 전체 공급 시간에 대하여 공급되지 않는 시간이 1% 미만인 것을 의미한다.
<복합 수산화물 회수 공정>
복합 수산화물 회수 공정에서는, 반응 용액으로부터 니켈 및 코발트를 포함하는 복합 수산화물을 분리하여 회수한다. 반응 용액으로부터의 복합 수산화물의 회수는, 예를 들면, 생성하는 침전물을 여별(濾別), 원심분리 등의 통상 사용되는 분리 수단으로 행할 수 있다. 얻어지는 침전물에는, 물세정, 여과, 건조 등의 처리를 행해도 된다. 복합 수산화물에 있어서의 금속 원소의 조성비는, 이들을 원료로 하여 얻어지는 리튬 전이금속 복합 산화물의 금속 원소의 조성비와 거의 일치해도 된다.
얻어지는 복합 수산화물은, 복합 수산화물에 포함되는 금속 원소의 총 몰수에 대한 니켈의 몰수의 비가, 예를 들면 0보다 크고 1 미만이어도 된다. 금속 원소의 총 몰수에 대한 니켈의 몰수의 비는, 바람직하게는 0.33 이상이다. 또한, 금속 원소의 총 몰수에 대한 니켈의 몰수의 비는, 0.4 이상, 또는 0.55 이상이어도 된다. 또한, 금속 원소의 총 몰수에 대한 니켈의 몰수의 비는, 바람직하게는 0.95 이하, 또는 0.8 이하이다.
얻어지는 복합 수산화물은, 복합 수산화물에 포함되는 금속 원소의 총 몰수에 대한 코발트의 몰수의 비가 0보다 크고 0.6 이하이어도 된다. 금속 원소의 총 몰수에 대한 코발트의 몰수의 비는, 바람직하게는 0.02 이상, 0.05 이상, 0.1 이상, 또는 0.15 이상이다. 또한, 금속 원소의 총 몰수에 대한 코발트의 몰수의 비는, 바람직하게는 0.35 이하이다. 금속 원소의 총 몰수에 대한 코발트의 몰수의 비는, 0.3 이하, 또는 0.25 이하이어도 된다.
복합 수산화물은, 그 조성에 망간 및 알루미늄 중 적어도 일방을 포함하고 있어도 된다. 복합 수산화물이, 그 조성에 망간 및 알루미늄 중 적어도 일방을 포함하는 경우, 금속 원소의 총 몰수에 대한 망간 및 알루미늄의 총 몰수의 비는, 예를 들면, 0보다 크고, 바람직하게는 0.01 이상, 보다 바람직하게는 0.05 이상, 더욱 바람직하게는 0.1 이상, 특히 바람직하게는 0.15 이상이다. 또한, 금속 원소의 총 몰수에 대한 망간 및 알루미늄의 총 몰수의 비는, 예를 들면, 0.6 이하이며, 바람직하게는 0.35 이하이다. 금속 원소의 총 몰수에 대한 망간 및 알루미늄의 총 몰수의 비는 0.33 이하, 0.3 이하, 또는 0.25 이하이어도 된다.
복합 수산화물은, 그 조성에 적어도 1종의 제2 금속 원소를 포함하고 있어도 된다. 복합 수산화물은, 그 조성에 적어도 1종의 제2 금속 원소를 포함하는 경우, 금속 원소의 총 몰수에 대한 제2 금속 원소의 총 몰수의 비는, 예를 들면, 0보다 크고, 바람직하게는 0.001 이상이며, 보다 바람직하게는 0.003 이상이다. 또한, 금속 원소의 총 몰수에 대한 제2 금속 원소의 총 몰수의 비는, 예를 들면, 0.02 이하이며, 바람직하게는 0.015 이하, 보다 바람직하게는 0.01 이하이다.
복합 수산화물은, 예를 들면 하기 식(3)으로 표현되는 조성을 가지고 있어도 된다.
NijCokM1 mM2 n(OH)2 + γ
(3)
식(3) 중, M1은 Mn 및 Al 중 적어도 일방을 나타낸다. M2는 Ca, Zr, Ti, Mg, Ta, Nb, Cr, Mo, W, Fe, Cu, Si, Sn, Bi, Ga, Y, Sm, Er, Ce, Nd, La, Cd 및 Lu로 이루어지는 군으로부터 선택되는 적어도 1종을 나타낸다. j, k, m, n 및 γ은, 0<j<1, 0<k≤0.6, 0≤m≤0.6, 0≤n≤0.02, 0≤γ≤2를 만족한다. 바람직하게는, 0.33≤j≤0.95, 0.02≤k≤0.35, 0.01≤m≤0.35, 0≤n≤0.015, 0≤γ≤1이다. 또한, 바람직하게는, M2는 Zr, Ti, Mg, Ta, Nb, Mo 및 W으로 이루어지는 군으로부터 선택되는 적어도 1종이다.
<복합 수산화물 열 처리 공정>
복합 수산화물 열 처리 공정에서는, 얻어지는 복합 수산화물을 열 처리하여, 니켈 및 코발트를 포함하는 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함하는 니켈 코발트 복합 산화물을 얻는다. 열 처리함으로써, 복합 수산화물이 탈수되어 니켈 코발트 복합 산화물이 생성된다. 니켈 코발트 복합 산화물은 리튬 전이금속 복합 산화물의 전구체이어도 되고, 정극 활물질 전구체이어도 된다.
열 처리의 온도는, 예를 들면 105℃ 이상 900℃ 이하이어도 되고, 바람직하게는 300℃ 이상 500℃ 이하이다. 열 처리의 시간은, 예를 들면 5시간 이상 30시간 이하이어도 되고, 바람직하게는 10시간 이상 20시간 이하이다. 열 처리의 분위기는, 산소를 포함하는 분위기 하이어도 되고, 대기 분위기이어도 된다.
얻어지는 니켈 코발트 복합 산화물을 포함하는 이차 입자의 평활도는, 예를 들면 0.74보다 크면 좋고, 바람직하게는 0.80 이상, 또는 0.85 이상이다. 니켈 코발트 복합 산화물을 구성하는 이차 입자의 원형도는, 예를 들면 0.80 이상이며, 바람직하게는 0.85 이상, 또는 0.87 이상이다. 여기서, 니켈 코발트 복합 산화물을 포함하는 이차 입자의 평활도 및 원형도는, 정극 활물질을 구성하는 이차 입자에 있어서의 그들과 마찬가지로 하여 측정된다. 또한, 이차 입자의 평활도 및 원형도의 상한은 1 이하이며, 1 미만이어도 된다.
니켈 코발트 복합 산화물을 포함하는 이차 입자의 입도 분포는, 체적 기준의 누적 입도 분포에 있어서의 90%입경(D90)과 10%입경(D10)의 차를 50%입경(D50)으로 나눈 값((D90-D10)/D50)로서, 예를 들면 0.8보다 작고, 바람직하게는 0.7 이하, 0.6 이하, 또는 0.5 이하이다.
니켈 코발트 복합 산화물을 포함하는 이차 입자의 체적 평균 입경은, 예를 들면 1㎛ 이상 30㎛ 이하이며, 바람직하게는 1.5㎛ 이상, 보다 바람직하게는 2㎛ 이상, 더욱 바람직하게는 3㎛ 이상이며, 또한 바람직하게는 18㎛ 이하, 보다 바람직하게는 12㎛ 이하이며, 더욱 바람직하게는 8㎛ 이하이다. 이차 입자의 체적 평균 입경이 상기 범위 내이면, 유동성이 좋고, 이차 전지를 구성할 때에 출력이 보다 향상되는 경우가 있다. 여기서 체적 평균 입경은, 체적 기준의 누적 입도 분포에 있어서의 소경측으로부터의 누적 50%에 대응하는 50%입경(D50)이다.
니켈 코발트 복합 산화물을 포함하는 이차 입자는 복수의 일차 입자가 집합하여 형성된다. 일차 입자의 전자 현미경 관찰에 기초한 평균 입경(DSEM)은, 예를 들면 0.1㎛ 이상 1.5㎛ 이하이며, 바람직하게는 0.12㎛ 이상, 보다 바람직하게는 0.15㎛ 이상이다. 또한, 일차 입자의 전자 현미경 관찰에 기초한 평균 입경(DSEM)은, 바람직하게는 1.2㎛ 이하, 보다 바람직하게는 1.0㎛ 이하이다. 일차 입자의 전자 현미경 관찰에 기초한 평균 입경이 상기 범위 내이면 전지를 구성할 때에 출력이 향상되는 경우가 있다. 여기서 일차 입자의 전자 현미경 관찰에 기초한 평균 입경은, 정극 활물질에 있어서의 평균 입경과 같은 의미이다.
니켈 코발트 복합 산화물을 포함하는 이차 입자는, 체적 기준에 의한 누적 입도 분포에 있어서의 50%입경(D50)의 전자 현미경 관찰에 기초한 평균 입경(DSEM)에 대한 비 D50/DSEM이 예를 들면, 2.5 이상이어도 된다. 비 D50/DSEM은, 예를 들면 2.5 이상 150 이하이며, 바람직하게는 5 이상, 보다 바람직하게는 10 이상이다. 또한, 비D50/DSEM은, 바람직하게는 100 이하, 보다 바람직하게는 50 이하이다.
니켈 코발트 복합 산화물은, 니켈 코발트 복합 산화물에 포함되는 금속 원소의 총 몰수에 대한 니켈의 몰수의 비가, 예를 들면, 0보다 크고 1 미만이어도 된다. 금속 원소의 총 몰수에 대한 니켈의 몰수의 비는, 바람직하게는 0.33 이상이다. 금속 원소의 총 몰수에 대한 니켈의 몰수의 비는, 0.4 이상, 또는 0.55 이상이어도 된다. 또한, 금속 원소의 총 몰수에 대한 니켈의 몰수의 비는, 바람직하게는 0.95 이하, 또는 0.8 이하이다.
니켈 코발트 복합 산화물은, 니켈 코발트 복합 산화물에 포함되는 금속 원소의 총 몰수에 대한 코발트의 몰수의 비가 0보다 크고 0.6 이하이어도 된다. 금속 원소의 총 몰수에 대한 코발트의 몰수의 비는, 바람직하게는 0.02 이상, 0.05 이상, 0.1 이상, 또는 0.15 이상이다. 또한, 금속 원소의 총 몰수에 대한 코발트의 몰수의 비는, 바람직하게는 0.35 이하이다. 금속 원소의 총 몰수에 대한 코발트의 몰수의 비는, 0.3 이하, 또는 0.25 이하이어도 된다.
니켈 코발트 복합 산화물은, 그 조성에 망간 및 알루미늄 중 적어도 일방을 포함하고 있어도 된다. 니켈 코발트 복합 산화물이, 그 조성에 망간 및 알루미늄 중 적어도 일방을 포함하는 경우, 금속 원소의 총 몰수에 대한 망간 및 알루미늄의 총 몰수의 비는, 예를 들면, 0보다 크고, 바람직하게는 0.01 이상, 보다 바람직하게는 0.05 이상, 더욱 바람직하게는 0.1 이상, 특히 바람직하게는 0.15 이상이다. 또한, 금속 원소의 총 몰수에 대한 망간 및 알루미늄의 총 몰수의 비는, 예를 들면 0.6 이하이며, 바람직하게는 0.35 이하이다. 금속 원소의 총 몰수에 대한 망간 및 알루미늄의 총 몰수의 비는, 0.33 이하, 0.3 이하, 또는 0.25 이하이어도 된다.
니켈 코발트 복합 산화물은, 그 조성에 적어도 1종의 제2 금속 원소를 포함하고 있어도 된다. 니켈 코발트 복합 산화물은, 그 조성에 적어도 1종의 제2 금속 원소를 포함하는 경우, 금속 원소의 총 몰수에 대한 제2 금속 원소의 총 몰수의 비는, 예를 들면, 0보다 크고, 바람직하게는 0.001 이상이며, 보다 바람직하게는 0.003 이상이다. 또한, 금속 원소의 총 몰수에 대한 제2 금속 원소의 총 몰수의 비는, 예를 들면, 0.02 이하이며, 바람직하게는 0.015 이하, 보다 바람직하게는 0.01 이하이다.
니켈 코발트 복합 산화물은, 예를 들면 하기 식(1)로 표현되는 조성을 가지고 있어도 된다.
NiqCorM1 sM2 tO2 + α
(1)
식(1) 중, M1은 Mn 및 Al 중 적어도 일방을 나타낸다. M2는 Ca, Zr, Ti, Mg, Ta, Nb, Cr, Mo, W, Fe, Cu, Si, Sn, Bi, Ga, Y, Sm, Er, Ce, Nd, La, Cd 및 Lu로 이루어지는 군으로부터 선택되는 적어도 1종을 나타낸다. q, r, s, t 및 α는, 0<q<1, 0<r≤0.6, 0≤s≤0.6, 0≤t≤0.02, -0.1≤α≤1.1, q+r+s+t=1을 만족한다. 바람직하게는, 0.33≤q≤0.95, 0.02≤r≤0.35, 0.01≤s≤0.35, 0.01≤t≤0.015이다. 또한, 바람직하게는, M2는 Zr, Ti, Mg, Ta, Nb, Mo 및 W로 이루어지는 군으로부터 선택되는 적어도 1종이다.
한편, 본 개시는 상기 실시형태에 한정되는 것이 아니다. 상기 실시형태는 예시이며, 본 개시의 청구범위에 기재된 기술적 사상과 실질적으로 동일한 구성을 가지며, 마찬가지의 작용 효과를 나타내는 것은, 어떠한 것이라 하더라도 본 개시의 기술적 범위에 포함된다는 것은 말할 필요도 없다.
실시예
이하, 본 개시를 실시예에 의해 구체적으로 설명하지만, 본 개시는 이들 실시예에 한정되는 것이 아니다.
일차 입자 사이즈, 즉 일차 입자의 전자 현미경 관찰에 기초한 평균 입경은, 이하와 같이 하여 측정하였다. 주사 전자 현미경(SEM)을 사용하여, 입경에 따라 1000배 내지 15000배의 범위의 배율로, 이차 입자를 구성하는 일차 입자를 관찰하였다. 입자의 윤곽을 확인할 수 있는 일차 입자를 50개 선택하고, 선택된 일차 입자의 윤곽으로부터 화상 처리 소프트웨어를 사용하여 구환산 직경을 산출하고, 얻어진 구환산 직경의 산술 평균값으로서 일차 입자의 전자 현미경 관찰에 기초한 평균 입경을 구하였다.
체적 기준의 누적 입도 분포에 있어서의 10%입경(D10), 50%입경(D50) 및 90%입경(D90)은, 레이저 회절식 입경 분포 측정 장치((주) 시마즈 제작소제 SALD-3100)를 사용하여, 체적 기준의 누적 입도 분포를 습식 조건으로 측정하고, 소경측으로부터의 누적 10%, 50% 및 90%에 대응하는 입경으로서 구하였다. 또한, 입도 분포는, D90과 D10의 차를 D50으로 나누어서 산출하였다. 즉, 이차 입자의 입도 분포는 아래 식으로 구하였다.
입도 분포=(D90-D10)/D50
평활도는, 이하와 같이 하여 측정하였다. 정극 활물질을 에폭시에 충전하여 경화한 후, 단면 가공을 행하여 단면 샘플을 제작하였다. 주사 전자 현미경(히타치 하이 테크놀로지스 SU8230; 가속 전압 3kV)을 사용하여, 반사 전자상(배율; 4000배)을 촬영하였다. 얻어진 반사 전자상에 대하여, 입자의 윤곽을 확인할 수 있는 이차 입자를 20 내지 40개 선택하고, 각각의 입자에 대해 화상 처리 소프트웨어(ImageJ)를 사용하여, 전체 둘레 길이(Lop)를 측정하였다. 또한, 선택된 입자의 윤곽에 대해 화상 처리 소프트웨어(ImageJ)를 사용하여, 가장 잘 맞는(근사하는) 타원형을 구하고, 각각의 입자에 대해 근사 타원의 긴 직경(a) 및 짧은 직경(b)을 얻었다. 얻어진 긴 직경(a) 및 짧은 직경(b)으로부터 Gauss-Kummer 공식의 근사식을 사용하여 근사 타원의 전체 둘레 길이(L)를 구하였다. 입자 화상의 윤곽의 전체 둘레 길이(Lop)에 대한, 근사한 타원의 전체 둘레 길이(L)의 비(L/Lop)로서 평활도를 구하였다. 개개의 입자의 평활도의 산술 평균으로서 이차 입자의 평활도를 산출하였다.
원형도는, 이차 입자의 윤곽 형상에 있어서의 입자 화상 면적과 동일한 면적을 갖는 원의 직경을 원상당 직경으로 하는 경우에, 이차 입자의 윤곽 형상의 전체 둘레 길이(L0)에 대한 원상당 직경으로부터 산출되는 원주 길이(L1)의 비(L1/L0)로서 구하였다. 구체적으로는, 건식 입자 화상 분석 장치(Morphologi G3S: Malvern사; 렌즈 배율 20배)를 사용하여, 약10000개의 입자에 대해 각각의 원형도를 측정하고, 그들의 산술 평균값으로서 이차 입자의 원형도를 구하였다.
탭 밀도는 이하와 같이 하여 측정하였다. 시료 20g을 20mL의 메스실린더에 투입하고, 6.5cm의 높이로부터 150회 탭핑한 후에, 체적을 측정하여, 구해진 밀도를 탭 밀도로 하였다. 부피 밀도는 이하와 같이 하여 측정하였다. 용량 30mL의 용기에 체(체눈의 크기 0.5mm)를 통과시킨 시료를 수북이 담아질 때까지 투입하고, 주걱을 사용하여 시료의 산 부분을 깍아내었다. 용기에 남은 시료 중량을 측정하여 부피 밀도를 구하였다.
비표면적은, BET 비표면적 측정 장치((주) 마운테크제 Macsorb Model-1201)를 사용하여, 질소 가스 흡착법(1점법)에 의해 측정하였다.
(실시예 1)
[고체 전해질의 제작]
아르곤 분위기 하에서 황화리튬 및 오황화인을, 그 물질량비가 7:3이 되도록 측량하였다. 측량물을 마노 막자사발에서 분쇄 혼합하여, 황화물 글래스를 얻었다. 이것을 고체 전해질로서 사용하였다.
[정극의 제작]
일차 입자 사이즈가 0.42㎛, 50%입경(D50)이 6.0㎛, 평활도가 0.84, 원형도가 0.88, 탭 밀도가 2.48g/㎤, 비표면적(BET값)이 0.43㎡/g, 부피 밀도가 1.45g/㎤, 입도 분포가 0.52인 정극 활물질을 준비하였다.
준비한 정극 활물질 70질량부, 고체 전해질 27질량부 및 VGCF(기상법 탄소 섬유) 3질량부를 혼합하여, 정극 합재를 얻었다.
[평가용 전지의 조립]
내경 11mm의 원통 형상 외형(外型)에 외경 11mm의 원기둥 형상 하형(下型)을, 외형 하부로부터 삽입하였다. 하형의 상단은 외형의 중간 위치에 고정하였다. 이 상태에서 외형의 상부로부터 하형의 상단에 고체 전해질 100mg를 투입하였다. 투입 후, 외형 11mm의 원기둥 형상 상형(上型)을 외형의 상부로부터 삽입하였다. 삽입 후, 상형의 상방으로부터 100MPa의 압력을 가하여, 고체 전해질을 성형하여 고체 전해질층으로 하였다. 성형 후, 상형을 외형의 상부로부터 빼내고, 외형의 상부로부터 고체 전해질층의 상부에 정극 합재 20mg를 투입하였다. 투입 후, 다시 상형을 삽입하고, 이번에는 100MPa의 압력을 가하여 정극 합재를 성형하여 정극 활물질층으로 하였다. 성형 후, 상형을 고정하고, 하형의 고정을 해제하여 외형의 하부로부터 빼내고, 하형의 하부로부터 고체 전해질층의 하부에 부극 활물질인 LiAl 합금을 투입하였다. 투입 후, 다시 하형을 삽입하고, 하형의 하방으로부터 350MPa의 압력을 가하여 부극 활물질을 성형하여 부극 활물질층으로 하였다. 압력을 가한 상태에서 하형을 고정하고, 상형에 정극 단자, 하형에 부극 단자를 부착하여, 평가용의 전고체 이차 전지를 얻었다.
(실시예 2)
일차 입자 사이즈가 0.41㎛, 50%입경(D50)이 6.3㎛, 평활도가 0.87, 원형도가 0.91, 탭 밀도가 2.55g/㎤, 비표면적이 0.37㎡/g, 부피 밀도가 1.67g/㎤, 입도 분포가 0.43인 정극 활물질을 사용한 것 이외에는, 실시예 1과 마찬가지로 하여, 평가용의 전고체 이차 전지를 제작하였다.
(비교예 1)
일차 입자 사이즈가 0.66㎛, 50%입경(D50)이 6.4㎛, 평활도가 0.73, 원형도가 0.83, 탭 밀도가 2.09g/㎤, 비표면적이 0.51㎡/g, 부피 밀도가 1.07g/㎤, 입도 분포가 0.61인 정극 활물질을 사용한 것 이외에는, 실시예 1과 마찬가지로 하여, 평가용의 전고체 이차 전지를 제작하였다.
[임피던스 측정]
평가용의 전고체 이차 전지를 충전하여, 충전율(SOC) 50%의 상태로 설정하였다. 25℃에서 교류 전원에 접속하여, 교류 임피던스법에 의한 저항 측정을 행하였다. 교류 전원의 주파수는 1MHz로부터 0.1Hz까지 대수적으로 변화시켰다. 등가 회로를 도 1과 같이 가정하여, 최소 제곱법에 의한 피팅에 의해 1000Hz 이상 5000Hz 이하의 주파수 범위에 나타나는 원호의 직경을 정극 활물질 유래의 저항(정극/전해질 계면의 임피던스에 있어서의 저항 성분)으로 하였다. 결과를 표 1에 나타낸다.
표 1에 나타내는 바와 같이, 실시예 1 및 실시예 2의 임피던스의 측정값은 비교예 1에 비해, 크게 감소하여 있었다. 이와 같이, 정극 활물질을 구성하는 이차 입자의 평활도를 0.73보다 크게 하고, 원형도를 0.83보다 크게 함으로써, 전고체 이차 전지의 내부 저항을 저감할 수 있다.
(실시예 3)
<각 용액의 준비>
황산 니켈 용액과, 황산 코발트 용액과, 황산 망간 용액을 각각 금속 원소의 몰비로 1:1:1이 되도록 혼합한 혼합 용액(니켈, 코발트 및 망간을 합친 농도로 1.7몰/L; 제1 용액)을 준비하였다. 혼합 용액 중의 금속 원소의 총 몰수를 474몰로 하였다. 염기성 수용액으로서, 25질량%의 수산화나트륨 수용액을 준비하였다. 착이온 형성 용액으로서, 12.5질량%의 암모니아 수용액(제2 용액)을 준비하였다. 중합체 용액으로서, 계면활성제인 아론 A-30SL(토아합성사제; 폴리아크릴산 암모늄 40질량% 수용액, 중량 평균 분자량=6000)과 아론 A-210(토아합성사제; 폴리아크릴산 나트륨 43질량% 수용액, 중량 평균 분자량=3000)을 질량비 1:1로 배합한 것을 준비하였다.
<액매체의 준비>
반응 용기에 물 30리터를 준비하고, 수산화나트륨 용액을 pH가 12.5가 되도록 첨가하였다. 질소 가스를 투입하여 반응 용기 내를 질소로 치환하여 액매체를 준비하였다.
<시드 결정 생성 공정>
액매체를 교반하면서, 액매체에 대하여 제1 용액을 금속 원소의 총 몰수로서 2몰분 첨가하여, 니켈, 코발트 및 망간을 포함하는 복합 수산화물을 석출시켰다.
<정석 공정>
준비한 복합 수산화물을 포함하는 액매체를 교반하면서, 나머지 제1 용액 472몰분과, 수산화나트륨 수용액과, 암모니아 수용액(제2 용액)을, 염기성(pH 11.3)을 유지하면서, 각각을 따로따로 또한 동시에 공급하였다. 중합체 용액은, 제1 용액, 제2 용액 및 수산화나트륨 수용액의 공급을 개시하고 나서 3시간 후부터 공급을 개시하고, 니켈, 코발트 및 망간을 포함하는 복합 수산화물을 석출시켰다. 중합체 용액의 공급량은, 생성한 복합 수산화물의 이론 수량에 대한 중합체의 공급량으로서 1질량%가 되는 공급량이었다. 또한, 제1 용액의 공급은 18시간에 걸쳐 연속적으로 공급되었다. 한편, 정석 공정에 있어서 액매체의 온도는 50℃ 정도가 되도록 제어하였다.
석출물을 회수하고, 계속해서 물세정, 여과, 건조를 행하여 니켈, 코발트, 망간을 포함하는 복합 수산화물(이하, 니켈 코발트 복합 수산화물이라고도 말함)을 얻었다.
<니켈 코발트 복합 산화물의 제조>
니켈 코발트 복합 수산화물에 대하여, 대기 분위기 하에서, 320℃에서 16시간의 열 처리를 행하여, 니켈, 코발트, 망간을 포함하는 전이금속 복합 산화물(이하, 니켈 코발트 복합 산화물이라고도 말함)로서 회수하였다.
얻어진 니켈 코발트 전이금속 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Ni0 . 338Co0 . 331Mn0 . 331O2이었다. 얻어진 니켈 코발트 복합 산화물에 대하여, 상기와 마찬가지로 하여 물성을 측정하였더니, 50%입경(D50)이 5.8㎛, 원형도가 0.91, 평활도가 0.80이었다.
(실시예 4)
시드 결정 생성 공정에서 공급한 제1 용액량을 실시예 1보다 늘리고, 그것에 맞추어 정석 공정에서 공급한 제1 용액량을 실시예 1보다 줄인 것과, 중합체의 공급량이 생성한 복합 수산화물의 이론 수량에 대하여 1.4질량%가 되도록 중합체 용액의 공급량을 변경한 것 이외에는 실시예 3과 마찬가지의 조건에서 실시하였다.
얻어진 니켈 코발트 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Ni0 . 335Co0 . 333Mn0 . 332O2이었다. 또한, 얻어진 니켈 코발트 복합 산화물은, 50%입경(D50)이 3.5㎛, 원형도가 0.85, 평활도가 0.84이었다.
(실시예 5)
시드 결정 생성 공정에서 공급한 제1 용액량을 실시예 3보다 줄이고, 그것에 맞추어 정석 공정에서 공급한 제1 용액량을 실시예 1보다 늘린 것 이외에는 실시예 3과 마찬가지의 조건에서 실시하였다.
얻어진 니켈 코발트 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Ni0 . 335Co0 . 333Mn0 . 332O2이었다. 또한, 얻어진 니켈 코발트 복합 산화물은, 50%입경(D50)이 7.9㎛, 원형도가 0.85, 평활도가 0.89이었다.
(실시예 6)
중합체의 공급량이 생성한 복합 수산화물의 이론 수량에 대하여 2질량%가 되도록 중합체 용액의 공급량을 변경한 것 이외에는 실시예 3과 마찬가지의 조건에서 실시하였다.
얻어진 니켈 코발트 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은, Ni0 . 339Co0 . 331Mn0 . 330O2이었다. 또한, 얻어진 니켈 코발트 복합 산화물은, 50%입경(D50)이 6.1㎛, 원형도가 0.89, 평활도가 0.91이었다.
(실시예 7)
중합체 용액을 계면활성제인 플로스퍼스 5000(SNF사제; 폴리아크릴산 나트륨 44% 수용액, 중량 평균 분자량=6500 내지 10000)으로 변경한 것 이외에는 실시예 3과 마찬가지의 조건에서 실시하였다.
얻어진 니켈 코발트 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Ni0 . 340Co0 . 333Mn0 . 328O2이었다. 또한, 얻어진 니켈 코발트 복합 산화물은, 50%입경(D50)이 5.9㎛, 원형도가 0.87, 평활도가 0.89이었다.
(실시예 8)
중합체 용액을 계면활성제인 플로스퍼스 9000(SNF사제; 폴리아크릴산 나트륨 40% 수용액, 중량 평균 분자량=10000 내지 17000)으로 변경한 것 이외에는 실시예 3과 마찬가지의 조건에서 실시하였다.
얻어진 니켈 코발트 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Ni0 . 338Co0 . 333Mn0 . 330O2이었다. 또한, 얻어진 니켈 코발트 복합 산화물은, 50%입경(D50)이 5.3㎛, 원형도가 0.88, 평활도가 0.85이었다.
(실시예 9)
중합체 용액을 계면활성제인 플로스퍼스 10000(SNF사제; 폴리아크릴산 나트륨 30% 수용액, 중량 평균 분자량=50000 내지 70000)으로 변경한 것 이외에는 실시예 3과 마찬가지의 조건에서 실시하였다.
얻어진 니켈 코발트 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Ni0 . 341Co0 . 331Mn0 . 328O2이었다. 또한, 얻어진 니켈 코발트 복합 산화물은, 50%입경(D50)이 8.0㎛, 원형도가 0.87, 평활도가 0.88이었다.
(실시예 10)
중합체 용액을 계면활성제인 플로스퍼스 15000(SNF사제; 폴리아크릴산 나트륨 30% 수용액, 중량 평균 분자량=100000 내지 170000)로 변경한 것 이외에는 실시예 3과 마찬가지의 조건에서 실시하였다.
얻어진 니켈 코발트 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Ni0 . 339Co0 . 331Mn0 . 329O2이었다. 또한, 얻어진 니켈 코발트 복합 산화물은, 50%입경(D50)이 8.5㎛, 원형도가 0.87, 평활도가 0.85이었다.
(실시예 11)
제1 용액의 니켈, 코발트 및 망간의 몰비를 9.2:0.4:0.4로 변경한 것 이외에는 실시예 3과 마찬가지의 조건에서 실시하였다.
얻어진 니켈 코발트 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Ni0 . 921Co0 . 040Mn0 . 039O2이었다. 또한, 얻어진 니켈 코발트 복합 산화물은, 50%입경(D50)이 5.8㎛, 원형도가 0.89, 평활도가 0.76이었다.
(비교예 2)
중합체 용액을 공급하지 않은 것 이외에는 실시예 3과 마찬가지의 조건에서 실시하였다.
얻어진 니켈 코발트 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Ni0 . 340Co0 . 330Mn0 . 329O2이었다. 또한, 얻어진 니켈 코발트 복합 산화물은, 50%입경(D50)이 6.2㎛, 원형도가 0.86, 평활도가 0.56이었다.
(비교예 3)
중합체 용액을 공급하지 않은 것 이외에는 실시예 11과 마찬가지의 조건에서 실시하였다.
얻어진 니켈 코발트 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Ni0 . 920Co0 . 040Mn0 . 040O2이었다. 또한, 얻어진 니켈 코발트 복합 산화물은, 50%입경(D50)이 5.8㎛, 원형도가 0.86, 평활도가 0.67이었다.
(비교예 4)
중합체 용액 대신에 40질량%의 구연산 용액을 공급한 것 이외에는 실시예 3과 마찬가지의 조건에서 실시하였다.
얻어진 니켈 코발트 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Ni0 . 336Co0 . 333Mn0 . 331O2이었다. 또한, 얻어진 니켈 코발트 복합 산화물은, 50%입경(D50)이 6.5㎛, 원형도가 0.88, 평활도가 0.45이었다.
(비교예 5)
중합체 용액을 공급하지 않은 것 이외에는 실시예 4과 마찬가지의 조건에서 실시하였다.
얻어진 니켈 코발트 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Ni0 . 335Co0 . 334Mn0 . 331O2이었다. 또한, 얻어진 니켈 코발트 복합 산화물은, 50%입경(D50)이 3.2㎛, 원형도가 0.83, 평활도가 0.58이었다.
(비교예 6)
중합체 용액을 공급하지 않은 것 이외에는 실시예 5과 마찬가지의 조건에서 실시하였다.
얻어진 니켈 코발트 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Ni0 . 328Co0 . 338Mn0 . 335O2이었다. 또한, 얻어진 니켈 코발트 복합 산화물은, 50%입경(D50)이 8.2㎛, 원형도가 0.82, 평활도가 0.74이었다.
(실시예 12)
실시예 3에서 얻어진 니켈 코발트 복합 산화물에 대한 탄산 리튬의 몰비가 1.15배가 되도록 양자를 건식 혼합하여 리튬 혼합물을 얻었다. 얻어진 리튬 혼합물을 대기 분위기 중 890℃에서 10시간 열 처리하였다. 그 후, 분산 처리하여 리튬 전이금속 복합 산화물을 얻었다. 얻어진 리튬 전이금속 복합 산화물 900g에 대하여, 니오브원으로서 농도가 4.2질량%인 다키화학 주식회사제의 Nb2O5졸을 사용하여, 믹서에서 리튬 전이금속 복합 산화물을 교반하면서 졸을 136g 적하함으로써, 니오브 부착물을 얻었다. 그 후, 대기 중 350℃에서 9시간 열 처리를 실시하였다. 얻어진 열 처리물을 수지제 볼 밀에서 합성 공정 후의 모재와 동일한 체적 평균 입경이 되도록 분산 처리를 행하고, 건식 체로 걸러서, Nb 처리를 실시한 리튬 전이금속 복합 산화물로서 정극 활물질을 얻었다.
얻어진 리튬 전이금속 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Li1 . 15Ni0 . 338Co0 . 331Mn0 . 331O2이었다. 평가 결과를 표 3에 나타낸다.
(실시예 13)
실시예 4에서 얻어진 니켈 코발트 복합 산화물을 사용한 것 이외에는, 실시예 13과 마찬가지로 하여 리튬 전이금속 복합 산화물을 얻었다.
얻어진 리튬 전이금속 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Li1 . 15Ni0 . 335Co0 . 333Mn0 . 332O2이었다. 평가 결과를 표 3에 나타낸다.
(비교예 7)
비교예 5에서 얻어진 니켈 코발트 복합 산화물을 사용한 것 이외에는, 실시예 12와 마찬가지로 하여 리튬 전이금속 복합 산화물을 얻었다.
얻어진 리튬 전이금속 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Li1 . 15Ni0 . 335Co0 . 334Mn0 . 331O2이었다. 평가 결과를 표 3에 나타낸다.
(실시예 14)
실시예 5에서 얻어진 니켈 코발트 복합 산화물을 사용한 것 이외에는, 실시예 12와 마찬가지로 하여 리튬 전이금속 복합 산화물을 얻었다.
얻어진 리튬 전이금속 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Li1 . 15Ni0 . 335Co0 . 333Mn0 . 332O2이었다. 평가 결과를 표 3에 나타낸다.
(비교예 8)
비교예 6에서 얻어진 니켈 코발트 복합 산화물을 사용한 것 이외에는, 실시예 12와 마찬가지로 하여 리튬 전이금속 복합 산화물을 얻었다.
얻어진 리튬 전이금속 복합 산화물을 무기산에 용해한 후, ICP 발광 분광법에 의해 화학 분석을 행하였더니, 그 조성은 Li1 . 15Ni0 . 335Co0 . 334Mn0 . 331O2이었다. 임피던스에 대해서는, 조성에 염소를 더 포함하며 결정성인 고체 전해질을 사용한 것 이외에는, 실시예 1과 동일한 방법으로 측정하였다. 이 방법에 의해 얻어진 비교예 1의 임피던스값을 1로 하였을 때의, 상대값을 상대 임피던스로서 산출하였다. 평가 결과를 표 3에 나타낸다.
실시예 3, 실시예 7, 및 비교예 2에서 얻어진 니켈 코발트 복합 산화물 입자를, 전술한 주사 전자 현미경(히타치 하이 테크놀로지스 SU8230)을 사용하여, 가속 전압 1.5kV에서 관찰을 행하였다. 도 2a, 도 2b는 실시예 3에서 얻어진 니켈 코발트 복합 산화물 입자를 관찰한 SEM 화상의 일례이며, 도 3a, 도 3b는 실시예 7에서 얻어진 니켈 코발트 복합 산화물 입자를 관찰한 SEM 화상의 일례이며, 도 4a, 도 4b는 비교예 2에서 얻어진 니켈 코발트 복합 산화물 입자를 관찰한 SEM 화상의 일례이다. 또한, 도 2a, 도 3a, 도 4a는 15000배의 배율, 도 2b, 도 3b, 도 4b는 50000배의 배율로 관찰한 SEM 화상이다. 도 2b, 도 3b, 도 4b에 나타내는 바와 같이 중합체 용액을 사용하지 않은 비교예 2와 비교하여, 중합체 용액을 사용하여 제작된 실시예 3은 일차 입자의 성장이 억제되어, 치밀한 이차 입자를 형성하여 있는 것을 알 수 있다.
표 3과 같이, 얻어진 실시예는, 평활도, 원형도 모두 비교예보다 향상되어 있는 것이 확인되고, 저항의 저감이 확인되었다. 비교예 8에 대한 실시예 14의 상대 임피던스의 비율에 비해, 비교예 1에 대한 실시예 12의 상대 임피던스의 비율이 작고, 비교예 7에 대한 실시예 13의 상대 임피던스의 비율이 보다 작게 되어 있었다. 즉, 입경이 작아질수록, 상대 임피던스의 개선 효과가 큰 것이 확인되었다.
일본특허출원 제2019-141366호(출원일: 2019년 7월 31일)의 개시는 그 전체가 참조에 의해 본 명세서에 받아들여진다. 본 명세서에 기재된 모든 문헌, 특허출원, 및 기술 규격은, 개개의 문헌, 특허출원, 및 기술 규격이 참조에 의해 받아들여진다는 것이 구체적이며 개별적으로 기록된 경우와 같은 정도로, 본 명세서에 참조에 의해 받아들여진다.
Claims (18)
- 니켈 이온 및 코발트 이온을 포함하는 제1 용액을 준비하는 단계와,
착이온 형성 인자를 포함하는 제2 용액을 준비하는 단계와,
pH가 10 이상 13.5 이하의 범위에 있는 액매체를 준비하는 단계와,
상기 액매체에, 상기 제1 용액 및 제2 용액을 따로따로 동시에 공급하면서, (메타)아크릴산에서 유래하는 구성 단위를 포함하는 중합체를 공급하여, pH가 10 이상 13.5 이하의 범위로 유지되는 반응 용액을 얻는 단계와,
상기 반응 용액으로부터 니켈 및 코발트를 포함하는 복합 수산화물을 얻는 단계와,
상기 복합 수산화물을 열 처리하여, 니켈 및 코발트를 포함하는 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 얻는 단계를 포함하고,
상기 이차 입자의 평활도가 0.74보다 큰, 니켈 코발트 복합 산화물의 제조 방법. - 제1항에 있어서,
상기 반응 용액은,
상기 제1 용액 및 상기 제2 용액을 따로따로 동시에 공급하는 단계와,
상기 제1 용액 및 상기 제2 용액과는 별도로 동시에 상기 중합체를 공급하거나, 또는 상기 제1 용액 및 상기 제2 용액 중 적어도 일방과 함께 상기 중합체를 공급하는 단계를 이 순서로 포함하는 방법에 의해 얻어지는, 니켈 코발트 복합 산화물의 제조 방법. - 제1항 또는 제2항에 있어서,
상기 액매체는, 니켈 및 코발트를 포함하는 복합 수산화물을 포함하는, 니켈 코발트 복합 산화물의 제조 방법. - 제1항 내지 제3항 중 어느 한 항에 있어서,
상기 반응 용액 중의 니켈 이온 농도가 10ppm 이상 1000ppm 이하로 유지되는, 니켈 코발트 복합 산화물의 제조 방법. - 제1항 내지 제4항 중 어느 한 항에 있어서,
상기 제1 용액을 공급하는 시간이 6시간 이상 60시간 이하인, 니켈 코발트 복합 산화물의 제조 방법. - 니켈 및 코발트를 포함하는 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함하고,
상기 이차 입자의 평활도가 0.74보다 큰, 니켈 코발트 복합 산화물. - 제6항에 있어서,
금속 원소의 총 몰수에 대한 니켈의 몰수의 비가 0보다 크고 1 미만이며,
상기 금속 원소의 총 몰수에 대한 코발트의 몰수의 비가 0보다 크고 0.6 이하인 조성을 갖는, 니켈 코발트 복합 산화물. - 제6항 또는 제7항에 있어서,
하기 식(1)로 표현되는 조성을 갖는, 니켈 코발트 복합 산화물.
NiqCorM1 sM2 tO2 + α (1)
(식(1) 중, M1은 Mn 및 Al 중 적어도 일방을 나타낸다. M2는 Ca, Zr, Ti, Mg, Ta, Nb, Cr, Mo, W, Fe, Cu, Si, Sn, Bi, Ga, Y, Sm, Er, Ce, Nd, La, Cd 및 Lu로 이루어지는 군으로부터 선택되는 적어도 1종을 나타낸다. q, r, s, t 및 α는, 0<q<1, 0<r≤0.6, 0≤s≤0.6, 0≤t≤0.02, -0.1≤α≤1.1, q+r+s+t=1을 만족한다.) - 층상 구조를 가지며, 리튬, 니켈 및 코발트를 포함하는 리튬 전이금속 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함하고,
상기 이차 입자의 평활도가 0.73보다 크고, 상기 이차 입자의 원형도가 0.83보다 큰, 정극 활물질. - 제9항에 있어서,
상기 이차 입자의 체적 평균 입경이 1㎛ 이상 30㎛ 이하인, 정극 활물질. - 제9항 또는 제10항에 있어서,
체적 기준의 누적 입도 분포에 있어서의 90%입경(D90)과 10%입경(D10)의 차분을 50%입경인 D50으로 나눈 값이 0.6 이하인, 정극 활물질. - 제9항 내지 제11항 중 어느 한 항에 있어서,
상기 리튬 전이금속 복합 산화물은, 리튬 이외의 금속 원소의 총 몰수에 대한 니켈의 몰수의 비가 0보다 크고 1 미만이며,
리튬 이외의 금속 원소의 총 몰수에 대한 코발트의 몰수의 비가 0보다 크고 0.6 이하인 조성을 갖는, 정극 활물질. - 제9항 내지 제12항 중 어느 한 항에 있어서,
상기 리튬 전이금속 복합 산화물은 하기 식(2)로 표현되는 조성을 갖는, 정극 활물질.
LipNixCoyM1 zM2 wO2+β (2)
(여기서, p, x, y, z, w 및 β는, 1.0≤p≤1.3, 0<x<1, 0<y≤0.6, 0≤z≤0.6, 0≤w≤0.02, x+y+z+w=1, -0.1≤β≤0.1을 만족한다. M1은 Mn 및 Al 중 적어도 일방을 나타낸다. M2는 Ca, Zr, Ti, Mg, Ta, Nb, Cr, Mo, W, Fe, Cu, Si, Sn, Bi, Ga, Y, Sm, Er, Ce, Nd, La, Cd 및 Lu로 이루어지는 군으로부터 선택되는 적어도 1종을 나타낸다.) - 제9항 내지 제13항 중 어느 한 항에 있어서,
상기 이차 입자는, 니오브를 포함하는 부착물을 그 표면에 갖는, 정극 활물질. - 정극 활물질 및 고체 전해질 재료를 포함하는 활물질층을 구비하고,
상기 정극 활물질은, 리튬 전이금속 복합 산화물을 포함하는 일차 입자가 복수 집합하여 이루어지는 이차 입자를 포함하고,
상기 이차 입자의 평활도가 0.73보다 크고,
상기 이차 입자의 원형도가 0.83보다 큰, 전고체 리튬 이온 이차 전지용 정극. - 제15항에 있어서,
상기 이차 입자의 체적 평균 입경이 1㎛ 이상 30㎛ 이하인, 정극. - 제15항 또는 제16항에 있어서,
상기 이차 입자는, 니오브를 포함하는 부착물을 그 표면에 갖는, 정극. - 제15항 내지 제17항 중 어느 한 항에 기재된 정극과, 부극과, 고체 전해질층을 구비하는, 전고체 리튬 이온 이차 전지.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019141366 | 2019-07-31 | ||
| JPJP-P-2019-141366 | 2019-07-31 | ||
| PCT/JP2020/029327 WO2021020531A1 (ja) | 2019-07-31 | 2020-07-30 | ニッケルコバルト複合酸化物の製造方法、ニッケルコバルト複合酸化物、正極活物質、全固体リチウムイオン二次電池用正極および全固体リチウムイオン二次電池 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20220042359A true KR20220042359A (ko) | 2022-04-05 |
Family
ID=74228883
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227003165A KR20220042359A (ko) | 2019-07-31 | 2020-07-30 | 니켈 코발트 복합 산화물의 제조 방법, 니켈 코발트 복합 산화물, 정극 활물질, 전고체 리튬 이온 이차 전지용 정극 및 전고체 리튬 이온 이차 전지 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20220259066A1 (ko) |
| EP (1) | EP4007014A1 (ko) |
| JP (1) | JPWO2021020531A1 (ko) |
| KR (1) | KR20220042359A (ko) |
| WO (1) | WO2021020531A1 (ko) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN113644272B (zh) * | 2021-08-12 | 2023-01-24 | 巴斯夫杉杉电池材料有限公司 | 一种铈铋复合氧化物掺杂锂离子电池正极材料及其制备方法 |
| WO2024004937A1 (ja) * | 2022-06-30 | 2024-01-04 | 日亜化学工業株式会社 | 二次電池用正極活物質及びその製造方法並びにそれを用いた二次電池用正極及び二次電池 |
| CN115084508B (zh) * | 2022-08-23 | 2023-01-31 | 欣旺达电动汽车电池有限公司 | 正极活性材料、电池及其制备方法 |
Family Cites Families (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002075367A (ja) | 2000-09-04 | 2002-03-15 | Mitsui Chemicals Inc | リチウム電池用正極活物質、その製法およびそれを用いた二次電池 |
| JP2006012433A (ja) | 2004-06-22 | 2006-01-12 | Nichia Chem Ind Ltd | 非水電解質二次電池用正極活物質および非水電解質二次電池 |
| US7993782B2 (en) | 2005-07-01 | 2011-08-09 | National Institute For Materials Science | All-solid lithium battery |
| WO2012096059A1 (ja) * | 2011-01-13 | 2012-07-19 | 株式会社村田製作所 | 蓄電デバイス用セパレータおよび蓄電デバイス |
| JP5382025B2 (ja) | 2011-02-16 | 2014-01-08 | 日亜化学工業株式会社 | 非水電解質二次電池、非水電解質二次電池用正極活物質および非水電解質二次電池用正極合剤 |
| WO2013183711A1 (ja) | 2012-06-06 | 2013-12-12 | 住友金属鉱山株式会社 | ニッケル複合水酸化物、非水系電解質二次電池用正極活物質、非水系電解質二次電池、およびこれらの製造方法 |
| JP6278727B2 (ja) * | 2014-02-04 | 2018-02-14 | 住友化学株式会社 | 共沈物の製造方法およびリチウム含有複合酸化物の製造方法 |
| JP6164332B2 (ja) * | 2015-04-28 | 2017-07-19 | 日亜化学工業株式会社 | ニッケルコバルト複合水酸化物粒子とその製造方法、非水系電解質二次電池用正極活物質とその製造方法、ならびに、非水系電解質二次電池 |
| CN104934595B (zh) | 2015-05-08 | 2017-08-08 | 广州锂宝新材料有限公司 | 制备具有铝元素梯度分布的镍钴铝前驱材料和正极材料的方法 |
| JP6841779B2 (ja) | 2018-02-21 | 2021-03-10 | 株式会社三共 | 遊技機 |
-
2020
- 2020-07-30 EP EP20847957.6A patent/EP4007014A1/en active Pending
- 2020-07-30 WO PCT/JP2020/029327 patent/WO2021020531A1/ja unknown
- 2020-07-30 US US17/631,317 patent/US20220259066A1/en active Pending
- 2020-07-30 KR KR1020227003165A patent/KR20220042359A/ko unknown
- 2020-07-30 JP JP2021535438A patent/JPWO2021020531A1/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| WO2021020531A1 (ja) | 2021-02-04 |
| JPWO2021020531A1 (ko) | 2021-02-04 |
| EP4007014A1 (en) | 2022-06-01 |
| US20220259066A1 (en) | 2022-08-18 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6063503B2 (ja) | 純粋相リン酸リチウムアルミニウムチタンおよびその製造方法ならびにその使用 | |
| KR20220042359A (ko) | 니켈 코발트 복합 산화물의 제조 방법, 니켈 코발트 복합 산화물, 정극 활물질, 전고체 리튬 이온 이차 전지용 정극 및 전고체 리튬 이온 이차 전지 | |
| JP5590337B2 (ja) | マンガン複合水酸化物粒子、非水系電解質二次電池用正極活物質、および非水系電解質二次電池と、それらの製造方法 | |
| KR101149638B1 (ko) | 리튬 망간 니켈 복합 산화물의 제조 방법 | |
| US20120258369A1 (en) | Lithium secondary battery and cathode active material therefor | |
| KR20140047044A (ko) | 비수계 이차 전지용 정극 활물질 및 그의 제조 방법, 및 그 정극 활물질을 이용한 비수계 전해질 이차 전지 | |
| US20120256337A1 (en) | Cathode active material precursor particle, method for producing thereof and method for producing cathode active material for lithium secondary battery | |
| JP2016026981A (ja) | リチウム含有複合酸化物およびその製造方法 | |
| KR20140008445A (ko) | 비수계 전해질 2차 전지용 정극 활물질의 전구체가 되는 전이 금속 복합 수산화물과 그 제조방법, 그 비수계 전해질 2차 전지용 정극 활물질과 그 제조방법, 및 상기 정극 활물질을 이용한 비수계 전해질 2차 전지 | |
| US20120258365A1 (en) | Cathode active material precursor particle, cathode active material particle for lithium secondary battery and lithium secondary battery | |
| JP2013507317A (ja) | 純粋相リチウムアルミニウムチタニウムホスフェートおよびそれの製造方法ならびにその使用 | |
| WO2018097137A1 (ja) | 遷移金属含有複合水酸化物とその製造方法、非水電解質二次電池用正極活物質とその製造方法、および非水電解質二次電池 | |
| WO2014030298A1 (ja) | 全固体リチウムイオン電池及び正極合材 | |
| KR20090012162A (ko) | 리튬 철 인계 복합 산화물 탄소 복합체의 제조 방법 및리튬, 철 및 인을 포함하는 공침체의 제조 방법 | |
| JP7056598B2 (ja) | 負極層および全固体電池 | |
| KR20090012187A (ko) | 리튬 철 인계 복합 산화물 탄소 복합체의 제조 방법 및리튬, 철 및 인을 포함하는 공침체의 제조 방법 | |
| KR102316442B1 (ko) | 세라믹 분말 재료, 세라믹 분말 재료의 제조 방법 및 전지 | |
| JP6443489B2 (ja) | ニッケルコバルト複合水酸化物の製造方法及び非水系電解質二次電池用正極活物質の製造方法 | |
| JP2018125305A (ja) | 非水系電解質二次電池用正極活物質の製造方法 | |
| KR20220084363A (ko) | 리튬 전지 양극 활물질 전구체, 이의 제조 방법 및 용도 | |
| KR20160018717A (ko) | 복합 입자 및 그 제조 방법과 전극 및 비수 전해질 이차 전지 | |
| JP6935601B1 (ja) | ニッケル含有水酸化物、ニッケル含有水酸化物を前駆体とした正極活物質の製造方法及びニッケル含有水酸化物の製造方法 | |
| JP7351736B2 (ja) | 固体電解質用リチウムランタンジルコニウム酸化物結晶粒子集合体の製造方法 | |
| JP7473828B2 (ja) | 非水電解質二次電池用正極及びその製造方法 | |
| JP2020066560A (ja) | 金属複合水酸化物とその製造方法、リチウムイオン二次電池用正極活物質とその製造方法、及び、それを用いたリチウムイオン二次電池 |