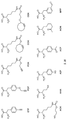KR20200085807A - 항체 약물 접합제용 친수성 링커 - Google Patents
항체 약물 접합제용 친수성 링커 Download PDFInfo
- Publication number
- KR20200085807A KR20200085807A KR1020207015856A KR20207015856A KR20200085807A KR 20200085807 A KR20200085807 A KR 20200085807A KR 1020207015856 A KR1020207015856 A KR 1020207015856A KR 20207015856 A KR20207015856 A KR 20207015856A KR 20200085807 A KR20200085807 A KR 20200085807A
- Authority
- KR
- South Korea
- Prior art keywords
- formula
- compound
- group
- subscript
- payload
- Prior art date
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/68—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an antibody, an immunoglobulin or a fragment thereof, e.g. an Fc-fragment
- A61K47/6889—Conjugates wherein the antibody being the modifying agent and wherein the linker, binder or spacer confers particular properties to the conjugates, e.g. peptidic enzyme-labile linkers or acid-labile linkers, providing for an acid-labile immuno conjugate wherein the drug may be released from its antibody conjugated part in an acidic, e.g. tumoural or environment
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/549—Sugars, nucleosides, nucleotides or nucleic acids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/50—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates
- A61K47/51—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent
- A61K47/54—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound
- A61K47/554—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient the non-active ingredient being chemically bound to the active ingredient, e.g. polymer-drug conjugates the non-active ingredient being a modifying agent the modifying agent being an organic compound the modifying agent being a steroid plant sterol, glycyrrhetic acid, enoxolone or bile acid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
Abstract
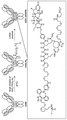
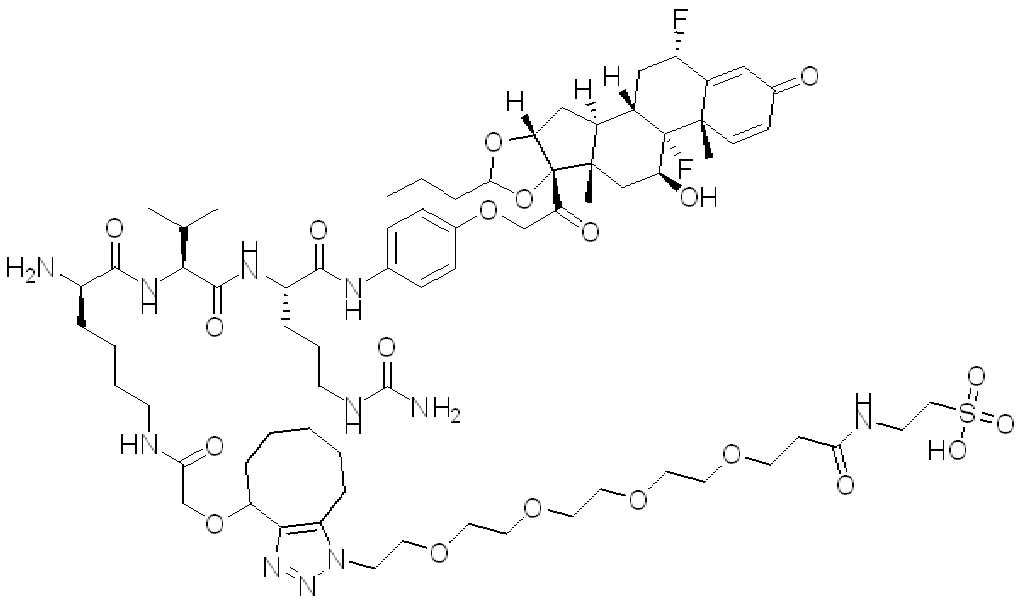
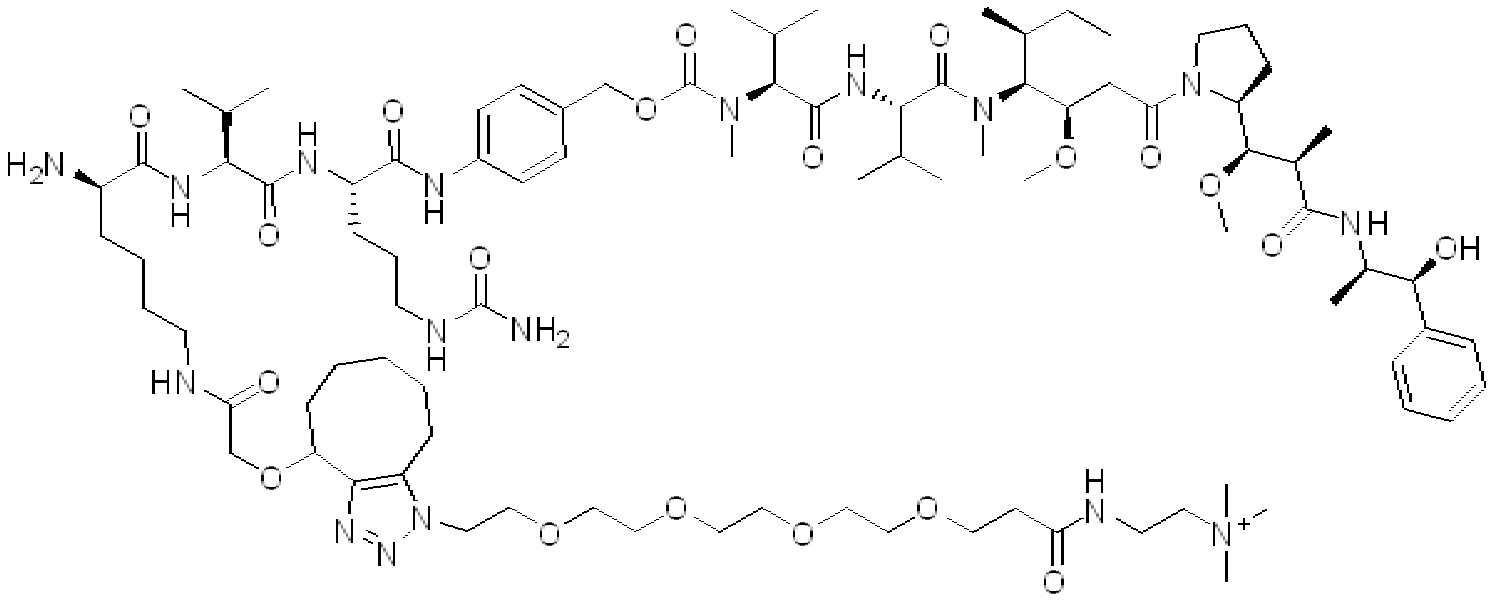
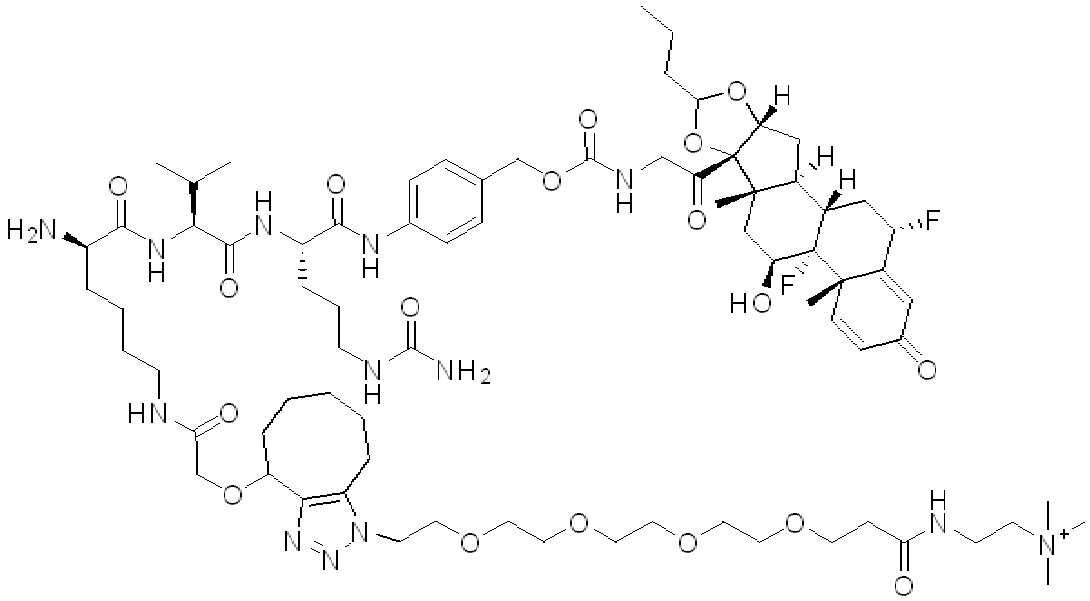
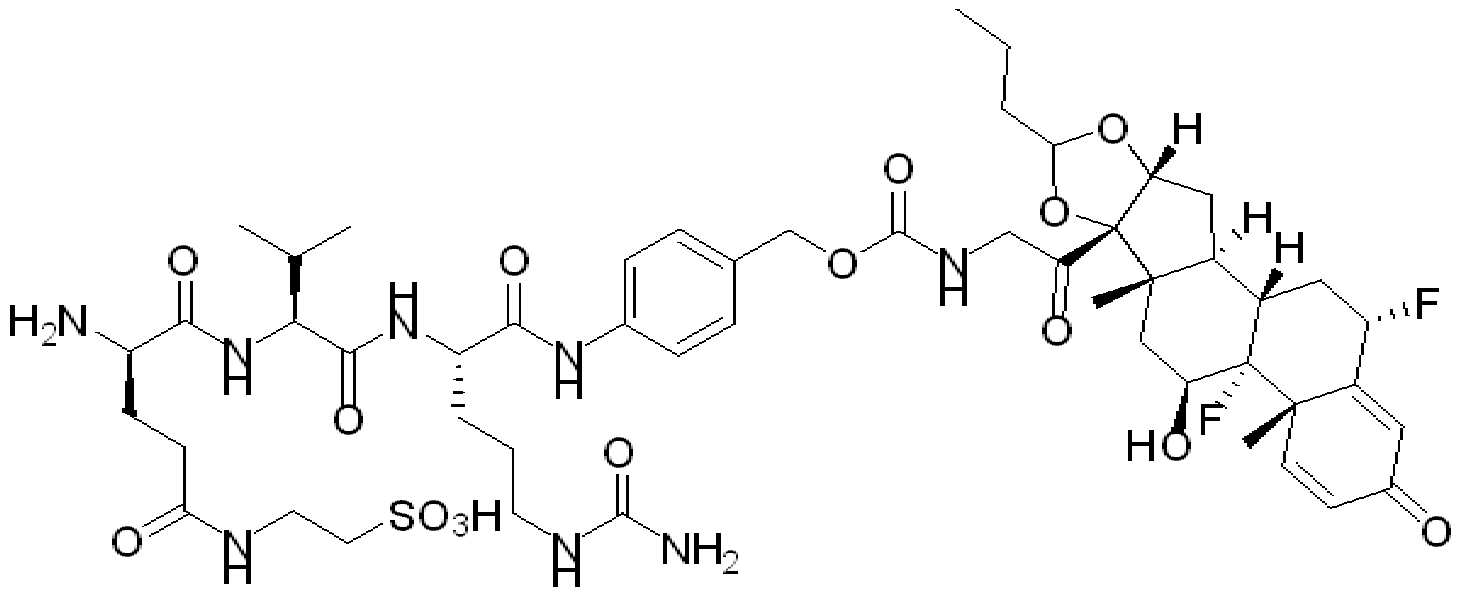
예를 들어, 약물을 세포로 표적-특이적으로 전달하는데 유용한 단백질 약물 접합제 및 이의 조성물이 본원에 기재되어 있다. 본원에 기재된 바와 같은 이들 화합물, 조성물 및 접합제를 특정 표적 세포에 투여함으로써, 비특이적 결합현상으로 인한 부작용, 예를 들어 비표적 세포에 대한 부작용이 감소된다. 특정 실시양태에서, 링커-페이로드 내의 친수성 잔기 및 이의 단백질 접합제를 포함하는 화합물, 조성물 및 접합제가 제공된다.
Description
본원에 신규 단백질, 예를 들어, 항체, 친수성 가용화 그룹을 포함하는 약물 접착체, 및/또는 친수성 가용화 그룹을 포함하는 링커, 및 친수성 가용화 그룹 및/또는 그의 링커를 포함하는 단백질 약물 접착제를 투여하는 것을 포함하는 질환, 장애 및 상태를 치료하는 방법이 제공된다.
본 PCT 국제 출원은 2018년 5월 9일에 출원된 미국 가출원 제62/669,034호; 2017년 11월 7일에 출원된 PCT국제출원 PCT/US17/60434(WO2018/089373으로 공개됨);및 2017년 11월 7일에 출원된 미국 정규 특허 출원 제 15/806,197호( US 2018/0155389로 공개됨);에 대해 우선권을 주장하고; 모든 상기 출원의 내용은 모든 목적을 위해 그 전문이 본원에 참조로 포함된다.
항체-약물 접합제(ADCs)는 생물학적 활성 소분자에 접합된 항체이다. ADC는 표적발현 세포에 강력한 약물을 선택적으로 전달하여 표적외 부작용 및/또는 독성의 잠재적 감소 및 개선된 치료 지수를 유도한다.
많은 페이로드(예를 들어, 약물)의 친유성 성질은 페이로드가 효율적으로 표적 세포로 전달되지 않는 정도로 ADC의 특성에 악영향을 줄 수 있다. 친유성 페이로드의 낮은 생체 이용률은 ADC 치료를 위한 치료 창을 좁힐 수 있다. 또한, 페이로드의 소수성 특성은 수성 조건에서 수행되는 반응인 항체와의 접합제에 대한 과제를 제시할 수 있다.
따라서, 단백질 접합제, 예를 들어, ADC와 같은 친수성 링커의 개발이 계속 요구되고 있다. 이는 친유성 페이로드 접합 가능성, 생물학적 표적의 개선된 조절, 개선된 생체 이용률 및 개선된 치료기간을 가능하게 한다.
본 발명은 예를 들어, 대사 질환, 증식성 성질환, 및 기타 질환 및 상태를 포함하지만 이에 제한되지 않는 질환, 상태 및 장애의 치료에 유용한 화합물을 제공한다.
본원에 제시된 일 실시양태에서, 하기를 포함하는 화합물 또는 그의 제약상 허용되는 염은: 하나 이상의 페이로드 부분에 연결되고 공유 링커를 통해 하나 이상의 친수성 부분에 연결되는 단백질 결합제로서, 상기 공유 링커는 각각의 결합제, 페이로드 부분 및 친수성 부분에 직접 또는 간접적으로 결합 된다.
본원에 제시된 다른 살시양태에는 다음을 포함하는 화합물이다: 하나 이상의 페이로드 부분에 연결되고 공유 링커를 통해 하나 이상의 친수성 부분에 연결된 반응성 그룹, 여기서 상기 공유 링커는 각각의 반응성 그룹, 페이로드 부분, 및 친수성 부분에 직접 또는 간접적으로 결합된다.
다른 실시양태에서, 본 원에는 항체 또는 그의 항원 결합 단편에 결합된 본원에 기재되어 있는 화합물을 갖는 항체-약물 접합제가 제시되어 있다.
다른 실시양태에서, 본 원에 제시된 화합물을 환자에게 투여하는 것을 포함하여, 이를 필요로하는 환자에서 질환, 상태 또는 장애를 치료하는 방법이 본원에 제시된다. 본 원에 제시된 질환, 상태 또는 장애를 치료하기 위한 본원에 제시된 화합물의 용도가 또한 제공된다. 본원에 제시된 질환, 상태 또는 장애를 치료하기 위한 의약의 제조를 위한 본원에 제시된 화합물의 용도가 추가로 제공된다. 일부 실시양태에서, 화합물은 항체-약물 접합제다.
또 다른 실시양태에서, 결합제와 링커-페이로드 화합물 사이의 결합을 형성하기에 적합한 조건하에 결합제를 본원에 기재된 링커-페이로드 화합물과 접촉시키는 단계를 포함하는 항체-약물 접합제의 제조 방법이 본 원에 기재되어 있다.
대상체에서 예를 들어 이상지질 혈증, 대사성 질환, 염증 또는 신경 퇴행성 질환을 치료하는데 유용한 화합물, 조성물 및 방법이 본 원에 제공된다.
본 발명을 설명하기 전에, 본 발명은 설명된 특정 방법 및 실험조건에 제한되지 않으며, 그러한 방법 및 조건은 달라질 수 있음을 이해해야 한다. 또한, 본 명세서에서 사용된 용어는 특정 실시예들을 설명하기 위한 목적을 위한 것이며, 본 발명의 범위가 첨부된 청구 범위에 의해서만 제한될 것이기 때문에 제한하려는 것이 아님을 이해해야 한다.
달리 정의되지 않는 한, 본 원에 사용된 모든 기술 및 과학 용어는 본 발명이 속하는 기술 분야의 통상의 기술자에 의해 일반적으로 이해되는 것과 동일한 의미를 갖는다. 본 원에 사용된 용어 "약"은 특정 인용 수치를 언급할 때 인용 수치와 1% 이하 차이가 날 수 있음을 의미한다. 예를 들어, 본 원에 사용된 표현 "약 100"은 99 내지 101 및 사이의 모든 값(예를 들어, 99.1, 33.2, 99.3, 99.4등)을 포함한다.
본 원에 기술된 것과 유사하거나 동등한 임의의 방법 및 재료가 본 발명의 실시 또는 시험에 사용될 수 있지만, 바람직한 방법 및 재료가 이제 설명된다. 본 명세서에 언급된 모든 특허, 출원 및 비 특허 문헌은 그 전문이 본 원에 참조로 포함한다.
정의
본 원에 제공된 화합물을 언급할 때, 하기 용어는 달리 지시되지 않는 한 다음의 의미를 갖는다. 달리 정의되지 않는 한, 본 명세서에서 사용된 모든 기술 및 과학 용어는 당업자가 일반적으로 이해하는 것과 동일한 의미를 갖는다. 본 원에 제공된 용어에 대해 복수의 정의가 있는 경우, 달리 정의되지 않는 한, 이들 정의가 우선한다.
본 원에 사용된 "알킬(alkyl)"은 1가 및 포화 탄화수소 라디칼 부분을 지칭한다. 알킬은 선택적으로 치환되고 선형, 분지형 또는 환형, 즉 시클로알킬일 수 있다. 알킬은 1-20 개의 탄소 원자를 갖는 라디칼, 즉 C1-20 알킬; 1-12 개의 탄소 원자를 갖는 라디칼, 즉 C1-12 알킬; 1-8 개의 탄소 원자를 갖는 라디칼, 즉 C1-8 알킬; 및1-3 개의 탄소 원자를 갖는 라디칼, 즉 C1-3 알킬을 포함하나, 이에 제한되지는 않는다. 알킬 잔기의 예는 메틸, 에틸, n-프로필, i-프로필, n-부틸, s-부틸, t-부틸, i-부틸, 펜틸 잔기, 헥실 잔기, 시클로 프로필, 시클로 부틸, 시클로 펜틸 및 시클로 헥실을 포함하나, 이에 제한되지는 않는다. 펜틸부분은 비제한적으로 n-펜틸 및 i-펜틸을 포함한다. 헥실 잔기는 n-헥실을 포함하나, 이에 제한되지는 않는다.
본 원에 사용된 "알킬렌(alkylene)"은 2가 알킬기를 지칭한다. 달리 명시되지 않는 한, 알킬렌은 1-20개의 탄소 원자를 포함하나 이에 제한되지는 않는다. 알킬렌기는 알킬에 대해 본원에 기재된 바와 같이 선택적으로 치환된다. 일부 실시양태에서, 알킬렌은 비치환 된다.
입체화학을 명시하지 않은 아미노산 또는 아미노산 잔기의 명칭은 L형태의 아미노산, D형태의 아미노산 또는 그의 라세미 혼합물을 포함하는 것으로 의도된다.
본 원에 사용된 "할로알킬(haloalkyl)"은 상기 정의된 바와 같은 알킬을 지칭하며, 여기서 알킬은 할로겐, 예를 들어, 불소(F), 염소(Cl), 브롬(Br), 또는 요오드(I)로부터 선택된 하나 이상의 치환기를 포함한다. 할로알킬의 예는 -CF3, -CH2CF3, -CCl2F, 및 -CCl3을 포함하지만 이에 제한되지는 않는다.
본 원에서 사용된 "알케닐(alkenyl)"은 2개 이상의 탄소 원자 및 하나 이상의 비방향족 탄소-탄소 이중결합을 함유하는 1가 탄화수소 라디칼 부분을 지칭한다. 알케닐은 선택적으로 치환되고 선형, 분지형 또는 환형일 수 있다. 알케닐은 2-20개의 탄소원자를 갖는 라디칼, 즉 C2-20알케닐; 2-12개의 탄소원자를 갖는 라디칼, 즉 C2-12알케닐; 2-8개의 탄소원자를 갖는 라디칼, 즉 C2-8알케닐; 2-6개의 탄소원자를 갖는 라디칼, 즉 C2-6알케닐; 2-4개의 탄소원자를 갖는 라디칼, 즉 C2-4알케닐을 포함하나, 이에 제한되지 않는다. 알케닐 잔기의 예는 비닐(vinyl), 프로페닐(propenyl), 부테닐(butenyl), 및 시클로헥시닐(cyclohexenyl)을 포함하지만 이에 제한되지 않는다.
본 원에 사용된 "알키닐(alkynyl)"은 2개 이상의 탄소 원자 및 1개 이상의 탄소-탄소 삼중결합을 함유하는 1가 탄화수소 라디칼 부분을 지칭한다. 알키닐은 선택적으로 치환되고 선형, 분지형 또는 환형일 수 있다. 알키닐은 2-20개의 탄소원자를 갖는 라디칼, 즉 C2-20알키닐; 2-12개의 탄소원자를 갖는 라디칼, 즉 C2-12알키닐; 2-8개의 탄소원자를 갖는 라디칼, 즉 C2-8알키닐; 2-6개의 탄소원자를 갖는 라디칼, 즉 C2-6알키닐; 2-4개의 탄소원자를 갖는 라디칼, 즉 C2-4알키닐을 포함하나, 이에 제한되지 않는다. 알키닐 잔기의 예는 에티닐(ethynyl), 프로피닐(propynyl), 및 부티닐(butynyl)을 포함하나, 이에 제한되지 않는다.
본 원에 사용된 "알콕시(akoxy)"는 탄화수소가 산소 원자에 대한 단일 결합을 포함하고 라디칼이 산소 원자에 국한된 1가 및 포화 탄화수소 라디칼 잔기를 의미하며, 예를 들어 에톡시의 경우 CH3CH2-O·이다. 알콕시 치환기는 알콕시 치환기의 이 산소원자를 통해 치환하는 화합물에 결합한다. 알콕시는 선택적으로 치환되고 선형, 분지형 또는 환형, 즉 시클로 알콕시일 수 있다. 알콕시는 2-20개의 탄소원자를 갖는 라디칼, 즉 C2-20알콕시; 2-12개의 탄소원자를 갖는 라디칼, 즉 C2-12알콕시; 2-8개의 탄소원자를 갖는 라디칼, 즉 C2-8알콕시; 2-6개의 탄소원자를 갖는 라디칼, 즉 C2-6알콕시; 2-4개의 탄소원자를 갖는 라디칼, 즉 C2-4알콕시를 포함하나, 이에 제한되지 않는다. 알콕시닐 잔기의 예는 메톡시(methoxy), 에톡시(ethoxy), n-프로폭시(n-propoxy), i-프로폭시(i-propoxy), n-부톡시(n-butoxy), s-부톡시(s-butoxy), t-부톡시(tbutoxy), i-부톡시(i-butoxy), 펜톡시잔기(a pentoxy moiety), 헥속시잔기(a hexoxy moiety), 시클로프로폭시(cyclopropoxy), 시클로부톡시(cyclobutoxy), 시클로펜톡시(cyclopentoxy), 및 시클로헥속시(cyclohexoxy)를 포함하나, 이에 제한되지 않는다.
본 원에 사용된 "할로알콕시(haloalkoxy)"는 상기 정의된 바와 같은 알콕시를 나타내며, 여기서 알콕시는 할로겐, 예를 들어 F, Cl, Br 또는 I로부터 선택된 하나 이상의 치환기를 포함한다.
본 원에 사용된 "아릴(aryl)"은 고리 원자가 탄소 원자인 방향족 화합물의 라디칼인 1가 잔기를 지칭한다. 아릴은 선택적으로 치환되고, 단환식 또는 다환식, 예를 들어 이환식 또는 삼환식일 수 있다. 아릴 잔기의 예는 6-20개의 고리탄소원자를 갖는 것, 즉 C6-20아릴, 6-15개의 고리탄소원자, 즉 C6-15아릴, 및 6-10개의 고리탄소원자를, 즉 C6-10아릴을 포함하나, 이에 제한되지 않는다. 아릴잔기의 예는 페닐(phenyl), 나프틸(naphthyl), 플루오레닐(fluorenyl), 아줄레닐(azulenyl), 안트릴(anthryl), 페난트릴(phenanthryl), 및 피레닐(pyrenyl)을 포함하지만, 이에 제한되지 않는다.
본 원에 사용된 "아릴알킬(arylalkyl)"은 알킬화합물의 라디칼인 1가 잔기를 지칭하며, 여기서 알킬화합물은 방향족 치환기로 치환되고 즉 방향족 화합물은 방향족 치환기로 치환되고, 즉 방향족 화합물은 알킬기에 대한 단일 결합을 포함하고, 여기서 라디칼은 알킬그룹 상에 위치한다. 아릴알킬기는 알킬기를 통해 예시된 화학 구조에 결합된다.
여기서 B는 방향족 잔기, 예를 들어 페닐이다. 아릴 알킬은 선택적으로 치환된 즉 아릴기 및/또는 알킬기는 본원에 개시된 바와 같이 치환될 수 있다. 아릴알킬의 예에는 벤질이 포함되나, 이에 제한되지 않는다.
본 원에 사용된 "알킬아릴(alkylaryl)"은 알킬화합물의 라디칼인 1가 잔기를 지칭하며, 여기서 아릴화합물은 알킬 치환기로 치환되며, 즉 아릴 화합물은 알킬기에 대한 단일 결합을 포함하고, 여기서 라디칼은 알릴기에 국한된다. 알킬아릴기는기는 알릴기를 통해 예시된 화학 구조에 결합된다.
여기서 B는 방향족 잔기, 예를 들어 페닐이다. 알킬아릴은 선택적으로 치환된, 즉 아릴기 및/또는 알킬기는 본원에 개시된 바와 같이 치환될 수 있다. 알킬아릴의 예는 톨루일을 포함하지만, 이에 제한되지 않는다.
본 원에 사용된 "아릴옥시(aryloxy)"는 고리원자가 탄소원자이고 고리가 산소 라디칼로 치환된 방향족 화합물의 라디칼인 1가 잔기를 말하며, 즉 방향족 화합물은 단일 결합을 포함한다 산소 원자에 라디칼이 존재하며, 여기서 라디칼은 산소원자 상에 국한되며, 예를 들어 페녹시의 경우 이다. 아릴옥시 치환기는 이 산소 원자를 통해 치환하는 화합물에 결합한다. 아릴옥시는 선택적으로 치환된다. 아릴옥시는 6 내지 20개의 고리탄소원자를 갖는 라디칼, 즉 C6-20아릴옥시, 6-15개의 고리탄소원자, 즉 C6-15아릴옥시, 및 6-10개의 고리탄소원자, 즉 C6-10아릴옥시을 포함하나, 이에 제한되지 않는다. 아릴옥시 잔기의 예는 페녹시, 나프톡시 및 안트록시를 포함하지만 이에 제한되지 않는다.
본 원에 사용된 "RaRbN-아릴옥시(aryloxy)"는 고리 원자가 탄소원자이고 고리가 하나 이상인 RaRbN - 치환기 및 하나 이상의 산소로 치환된 방향족 화합물의 라디칼인 1가 잔기를 지칭한다. 라디칼, 즉 방향족 화합물은 RaRbN - 치환기에 대한 단일 결합 및 산소원자에 대한 단일 결합을 포함하고, 라디칼은 산소원자 상에 국한되며, 예를 들어 이다.
RaRbN-아릴옥시(aryloxy) 치환기는 이 산소 원자를 통해 이들이 치환하는 화합물에 결합한다.
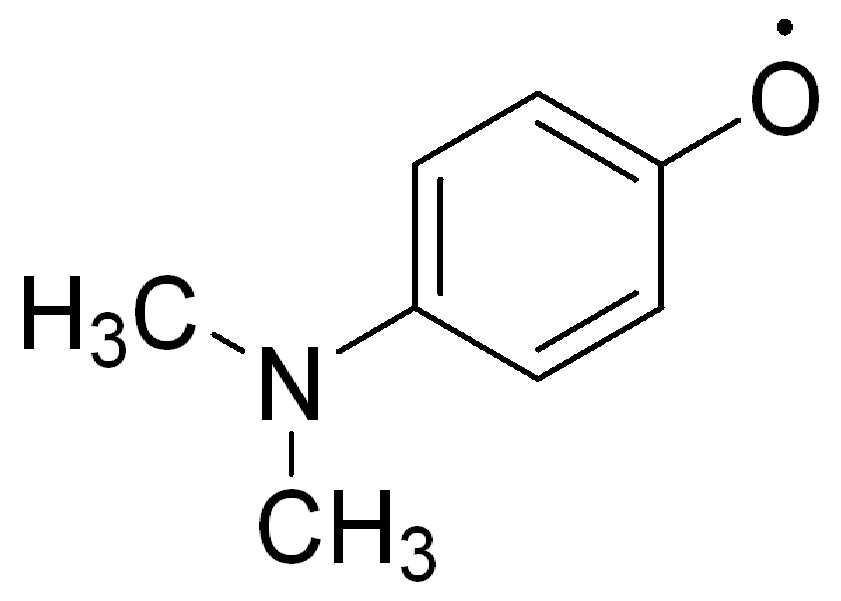
RaRbN-아릴옥시(aryloxy)는 선택적으로 치환된다. RaRbN-아릴옥시는 6 내지 20개의 고리탄소원자를 갖는 라디칼, 즉 C6-20(RaRbN)n-아릴옥시, 6-15개의 고리탄소원자, 즉 C6-15(RaRbN)n-아릴옥시, 및 6-10개의 고리탄소원자를, 즉 C6-10(RaRbN)n-아릴옥시를 포함하나, 이에 제한되지 않는다. 여기서 n은 RaRbN-치환기의 수를 나타낸다. RaRbN-아릴옥시 잔기의 예는 이에 제한되지 않지만 4-(디메틸아미노)-페녹시, 를 포함한다.
본 원에 사용된 "아릴렌(arylene)"은 고리원자가 단지 탄소원자인 방향족 화합물의 2가 잔기를 지칭한다. 아릴렌은 선택적으로 치환되고, 단환식 또는 다환식 예를 들어 이환식 도는 삼환식일 수 있다. 아릴렌 잔기의 예는 6 내지 20개의 고리탄소원자, 즉 C6-20아릴렌, 6-15개의 고리탄소원자, 즉 C6-15아릴렌, 및 6-10개의 고리탄소원자, 즉 C6-10아릴렌을 포함하나, 이에 제한되지 않는다.
본 원에 사용된 "헤테로알킬(heteroalkyl)"은 하나 이상의 탄소원자가 헤테로 원자로 대체된 알킬을 지칭한다. 본 원에 사용된 "헤테로알케닐(heteroalkenyl)"은 하나 이상의 탄소 원자가 헤테로 원자로 대체된 알케닐을 지칭한다. 본 원에 사용된 "헤테로알키닐(heteroalkynyl)"은 하나 이상의 탄소원자가 헤테로원자로 대체된 알키닐을 지칭한다. 적합한 헤테로원자는 질소, 산소 및 황 원자를 포함하지만 이에 제한되지 않는다. 헤테로 알킬은 선택적으로 치환된다. 헤테로 알킬 잔기의 예는 아미노알킬(aminoalkyl), 설포닐알킬(sulfonylalkyl) 및 설피닐알킬(sulfinylalkyl)을 포함하지만, 이에 제한되지 않는다. 헤테로 알킬 잔기의 예는 또한 메틸아미노(methylamino), 메틸술포닐(methylsulfonyl) 및 메틸술피닐(methylsulfinyl)을 포함하지만, 이에 제한되지 않는다.
본 원에 사용된 "헤테로아릴(heteroaryl)"은 고리 원자가 탄소 원자 및 하나 이상의 산소, 황, 질소 또는 인 원자를 함유하는 방향족 화합물의 라디칼인 1가 잔기를 지칭한다. 헤테로 아릴 잔기의 예는 5 내지 20개의 고리원자를 갖는 것들; 5 내지 15개의 고리원자; 및 내지 10개의 고리원자. 헤테로아릴은 선택적으로 치환된다.
본 원에 사용된 "헤테로아릴렌(heteroarylene)"은 방향족 고리의 하나 이상의 고리 원자가 산소, 황, 질소 또는 인 원자로 대체된 아릴렌을 지칭한다. 헤테로 아릴렌은 선택적으로 치환된다.
본 원에 사용된 "헤테로시클로알킬(heterocycloalkyl)"은 하나 이상의 탄소 원자가 헤테로 워나로 대체된 시클로-알킬을 지칭한다. 적합한 헤테로원자는 질소, 산소, 및 황 원자를 포함하지만 이에 제한되지는 않는다. 헤테로 시클로 알킬은 선택적으로 치환된다. 헤테로 시클로 알킬 잔기의 예는 모르폴리닐(morpholinyl), 피페리디닐(piperidinyl),테트라히드로피라닐( tetrahydropyranyl), 피롤리디닐(pyrrolidinyl), 이미다졸리디닐(imidazolidinyl), 옥사졸라디닐(oxazolidinyl), 티아졸리디닐(thiazolidinyl), 디옥소라닐(dioxolanyl), 디티올라닐(dithiolanyl), 옥사닐(oxanyl), 또는 티아닐(thianyl)을 포함하나, 이에 제한되지 않는다.
본 원에 사용된 "N-함유 헤테로시클로알킬(N-containing heterocycloalkyl)"은 하나 이상의 탄소 원자가 헤테로 원자로 대체되고 하나 이상의 헤테로 원자가 질소 원자인 시클로 알킬을 지칭한다. 질소 이외에 적합한 헤테로 원자는 산소 및 황 원자를 포함하지만 이에 제한되지 않는다. "N-함유 헤테로시클로알킬(N-containing heterocycloalkyl)"은 하나 이상의 탄소 원자가 헤테로 원자로 대체되고 하나 이상의 헤테로 원자가 질소 원자인 시클로 알킬을 지칭한다. 질소 이외에 적합한 헤테로 원자는 산소 및 황 원자를 포함하지만 이에 제한되지 않는다. N-함유 헤테로시클로알킬은 선택적으로 치환된다. N-함유 헤테로시클로알킬 잔기의 예는 모르폴리닐(morpholinyl), 피페리디닐(piperidinyl), 피롤리디닐(pyrrolidinyl), 이미다졸디닐(imidazolidinyl), 옥사졸리디닐(oxazolidinyl), 또는 티아졸리디닐(thiazolidinyl)을 포함하지만 이에 제한되지 않는다.
본 원에 사용된 바와 같이, 라디칼 잔기, 예를 들어 선택적으로 치환된 알킬을 기술하기 우해 사용될 때 "선택적으로 치환된(optionally substituted)"은 이러한 잔기가 하나 이상의 치환기에 임의로 결합됨을 의미한다. 이러한 치환의 예로는 할로(halo), 시아노(cyano), 니트로(nitro), 임의로치환된 할로알킬(optionally substituted haloalkyl), 아지도(azido), 에폭시(epoxy), 선택적으로 치환된 헤테로아릴(optionally substituted heteroaryl), 선택적으로 치환된 헤테로시클로알킬(optionally substituted heterocycloalkyl), , , , , , , , , , , , , , 또는 를 포함하지만, 이에 제한되지 않는다. 여기서, RA, RB, 및 RC 는 각각 독립적으로 수소 원자, 알킬(alkyl), 알케닐(alkenyl), 알키닐(alkynyl), 아릴(aryl), 알킬아릴(alkylaryl), 아릴알킬(arylalkyl), 헤테로알킬(heteroalkyl), 헤테로아릴(heteroaryl), 또는 헤테로시클로알킬(heterocycloalkyl)이거나, RA 및 RB 는 이들이 존재하는 원자와 함께 결합되어 포화 또는 불포화 카르보시클릭 고리를 형성하며, 여기서 고리는 선택적으로 치환되고, 하나 이상의 고리원자는 헤테로 원자로 선택적으로 치환된다. 특정 실시양태에서, 라디칼 부분이 선택적으로 치환된 헤테로 아릴, 선택적으로 치환된 헤테로시클로알킬 또는 선택적으로 치환된 포화 또는 불포화 카르보시클릭 고리로 임의로 헤테로 시클로 알킬상의 치환기 또는 선택적으로 치환된 포화 또는 불포화 카르보시클릭고리, 이들이 치환된다면, 추가 치환기로 선택적으로 치환된 치환기로 치환되지 않는다. 일부 실시양태에서, 본 원에 기술된 기가 선택적으로 치환될 때, 달리 명시되지 않는 한, 기에 결합된 치환기는 비치환된다.
본 원에 사용된 "결합제(binding agent)"는 주어진 결합 파트너, 예를 들어 항원에 특이적으로 결합할 수 있는 임의의 분자, 예를 들어 단백질을 지칭한다.
본 원에 사용된 "링커(linker)"는 본 원에 기재된 하나 이상의 화합물, 예를 들어 페이로드 화합물 및 친수성기에 결합제를 공유 결합시키는 2가, 3가 또는 다가 잔기를 지칭한다.
본 원에 사용된 "아미드 합성 조건(amide synthesis conditions)"은 예를 들어 카르복실산, 활성화된 카르복실산 또는 아실할라이드와 아민의 반응에 의해 아미드의 형성에 영향을 주기에 적합한 반응 조건을 지칭한다. 이들 예 중 일부에서, 카르복실산은 활성화된 카르복실산이 아민과 반응하여 아미드를 형성하기 전에 먼저 활성화된 카르복실산으로 전환된다. 아미드의 형성에 영향을 미치는 적합한 조건은 디시클로헥실카르보디이미드(dicyclohexylcarbodiimide (DCC)), 디이소프로필카르보디이미드(diisopropylcarbodiimide (DIC)), (벤조트리아졸-1-일옥시)트리스(디메틸아미노 포스포늄헥사플루오로포스페이트)((benzotriazol-1-yloxy)tris(dimethylamino)phosphonium hexafluorophosphate (BOP)), (벤조트라이아졸-1-일옥시)트리피롤리디노포스포늄헥사플루오로포스페이트((benzotriazol-1-yloxy)tripyrrolidinophosphonium hexafluorophosphate (PyBOP)), (7-아자벤조트리아졸-1-일옥시)트리피롤리디노포스포늄헥사플루오로포스페이트((7-azabenzotriazol-1-yloxy)tripyrrolidinophosphonium hexafluorophosphate (PyAOP)), 브로모트리피롤리디노포스포늄헥사플루오로포스페이트(bromotripyrrolidinophosphonium hexafluorophosphate (PyBrOP)), O-(벤조트리아졸-1-일)-N,N,N',N'-테트라메틸우로늄헥사플루오로포스페이트(O-(benzotriazol-1-yl)-N,N,N',N′-tetramethyluronium hexafluorophosphate (HBTU)), O-(벤조트리아졸-1-일)-N,N,N',N'-테트라메틸우로늄테트라플루오로보레이트(O-(benzotriazol-1-yl)-N,N,N',N′-tetramethyluronium tetrafluoroborate (TBTU)), 1-[비스(디메틸아미노)메틸렌]-1H-1,2,3-트리아졸로[4,5-b]피리디늄3-산화헥사플루오로포스페이트(1-[Bis(dimethylamino)methylene]-1H-1,2,3-triazolo[4,5-b]pyridinium 3-oxid hexafluorophosphate (HATU)), N-에톡시카르보닐-2-에톡시-1,2-디히드로퀴놀린(N-ethoxycarbonyl-2-ethoxy-1,2-dihydroquinoline (EEDQ)), N-에틸-N'-(3-디메틸아미노프로필)카르보디이미드(N-ethyl-N'-(3-dimethylaminopropyl)carbodiimide(EDC)), 2-클로로-1,2-디메틸이미다졸리디늄헥사플루오로포스페이트( 2-chloro-1,3-dimethylimidazolidinium hexafluorophosphate (CIP)), 2-클로로-4,6-디메톡시-1,3,5-트리아진(2-chloro-4,6-dimethoxy-1,3,5-triazine (CDMT)), 및 카르보닐디이미다졸(carbonyldiimidazole (CDI))을 포함하나 이에 제한되지 않고, 카르복실산과 아민사이의 반응을 일으키는 시약을 이용하는 조건을 포함하지만 이에 제한되지는 않는다.
일부 예에서, 카르복실산은 먼저 활성화된 카르복실산에 스테르를 아민으로 처리하여 아미드 결합을 형성하기 전에 활성화된 카르복실산 에스테르로 전환된다. 특정 실시양태에서, 카르복실산은 시약으로 처리된다. 시약은 카르복실산을 탈 양성자화 시킨 다음 탈 양성자화된 카르복실산에 의한 친 핵성 공격의 결과로 양성자화된 시약상에 카르복실산을 탈 양성화시킨 후 탈 양성자화된 카르복실산과 생성물 복합체를 형성함으로써 카르복실산을 활성화시킨다.
특정 카르복실산에 대한 활성화된 카르복실산 에스테르는 카르복실산이 활성화 되기 전보다 아민에 의한 친 핵성 공격에 더 민감하다. 이는 아미드 결합형성을 초래한다. 이와 같이, 카르복실산은 활성화된 것으로 기술되어 있다. 예를 들어 시약은 DCC 및 DIC를 포함한다.
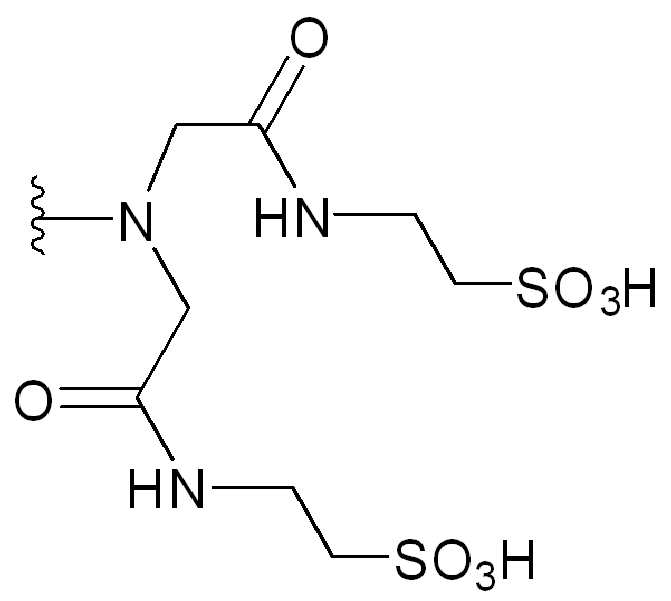
본 원에 사용된 "타우린(taurine)"은 시약 또는 를 나타내고, 여기서 는 타우린이 화학식의 인접기에 결합되는 원자를 나타낸다. 본 원에 사용된 "듀얼타우린(dualtaurine)"은 를 지칭하고, 여기서 는 이중 타우린이 화학식의 인접기에 결합되는 원자를 나타낸다.
본 원에 사용된 "입체 이성질체 형태(stereoisomeric form)"는 화합물에서 상이한 기의 상대 공간 배향을 지칭한다. 입체 이성질체 형태는 거울상 이성질체, 부분 이성질체 및/또는 이들의 혼합물을 포함한다.
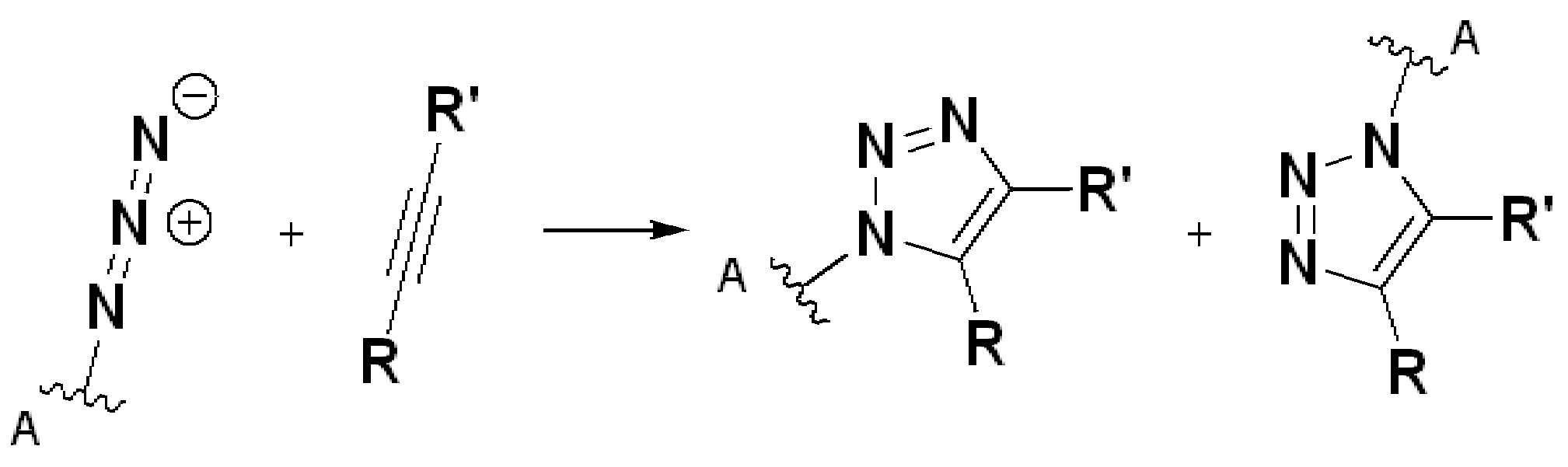
본 원에 사용된 "위치 이성질체(regioisomer)", "위치 이성질체들(regioisomers)" 또는 "위치 이성질체의 혼합물(mixture of regioisomers)"은 1,3-시클로(1,3-cycloadditions) 부가 또는 변형촉진알킨-아지드시클로첨가(strain-promoted alkyne-azide cycloadditions (SPAACs)의 생성물(들)을 지칭하며, 알킨으로 처리된 적합한 아지드(예를 들어, -N3, 또는 PEG-N3 유도체화된 항체)로부터 유도되는 클릭반응으로 공지되어 있다.
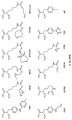
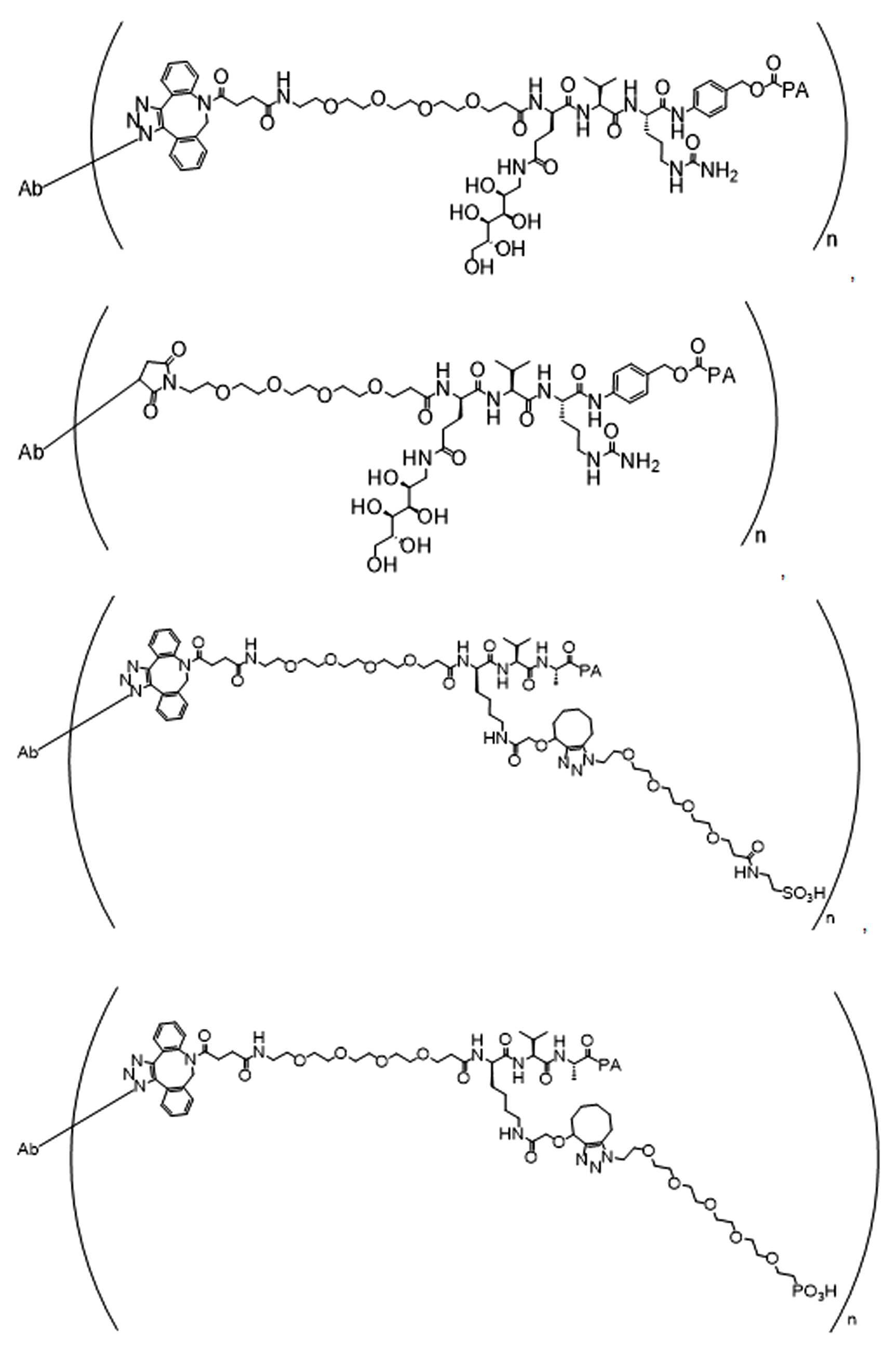
특정 실시양태에서, 예를 들어, 위치 이성질체 및 위치이성질체의 혼합물은 하기에 나타낸 클릭 반응 생성물을 특징으로 한다:
단지 예로서, 화합물 A1', 즉 화합물 A2', A3', A4'의 위치 이성질체가 하기에 나타나 있으며, 여기서 각각은 결합제에 대한 결합이고; 각각은 페이로드에 대한 결합이다.
화합물 A2'
화합물A3'
화합물 A4'
특정 실시양태에서, 하나 이상의 적합한 아지드 및 하나 이상의 적합한 알킨이 합성 공정 내에서 생성물로 전달 될 수 있으며, 여기서 각 아지드-알킨(azide-alkyne)쌍은 위치 이성질체성 클릭반응 생성물의 혼합물을 생성하기 위해 하나 이상의 독립적인 클릭 반응에 참여할 수 있다. 예를 들어, 당업자는 제1적합한 아지드가 제 1적합한 알킨과 독립적으로 반응할 수 있고, 제2 적합한 아지드는 독립적으로 생성물로 가는 제2적합한 알킨과 독립적으로 반응하여, 본 명세서에 기재된 ADC의 샘플에서 4개의 가능한 클릭반응 위치 이성질체 또는 4개의 가능한 클릭반응 위치 이성질체 혼합물의 생성을 초래할 수 있음을 인식할 것이다. 예를 들어, 당업자는 제1적합한 아지드가 생성물로가는 도중에 제1적합한 알킨과 독립적으로 반응하여 2개의 가능한 클릭반응 위치 이성질체 또는 본원에 기술된 링커-페이로드의 샘플에서 2개의 가능한 클릭 반응 위치 이성질체의 혼합물을 생성할 수 있음을 인식할 것이다.
본 원에 사용된 용어 "잔류물(residue)"은 화학 반응 후에 잔류하는 화합물 내의 화학 잔기를 지칭한다. 예를 들어, 용어 "아미노산 잔기(amino acid residue)" 또는 "N-알킬 아미노산 잔기(N-alkyl amino acid residue)"는 아미노산 또는 N-알킬 아미노산와 적합한 커플링 파트너의 아미드 커플링 또는 펩타이드 커플링 산물을 지칭하고; 예를 들어, 아미노산 또는 N-알킬 아미노산의 아미도 또는 펩티드 커플링 후에 물 분자가 방출되어 아미노산 잔기 또는 N-알킬 아미노산 잔기가 혼입된 생성물이 생성된다.
본 원에 사용된 "치료 유효량(therapeutically effective amount)"은 질환 또는 장애의 치료 또는 관리에서 환자에게 치료적 이점을 제공하거나, 질환 또는 장애와 관련된 하나 이상의 증상을 지연시키거나 최소화하기에 충분한 양(예를 들어, 화합물의)을 지칭한다.
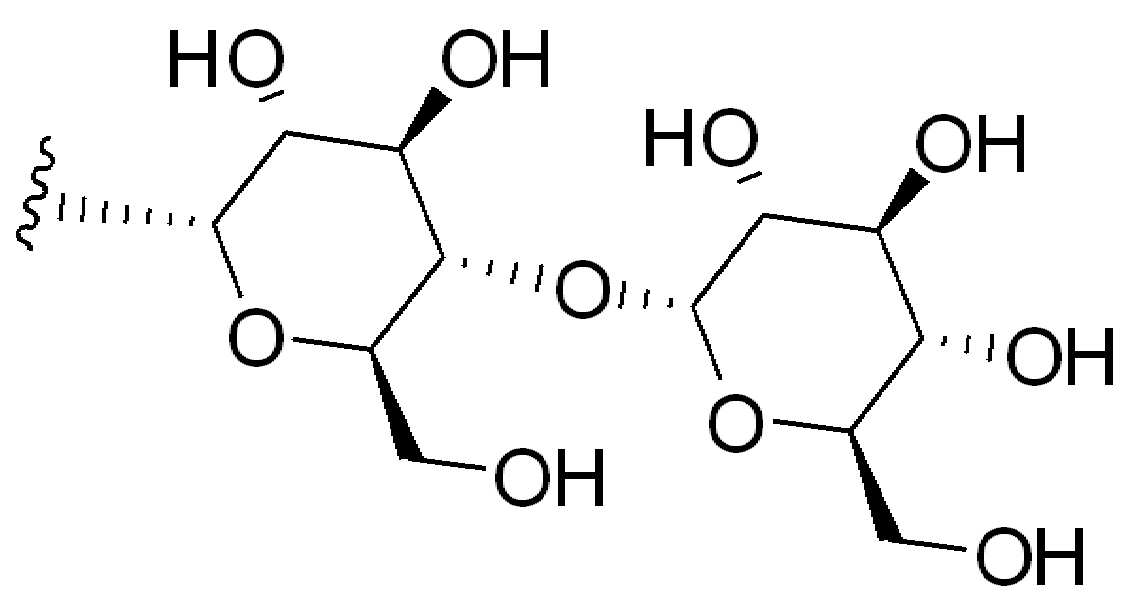
본 원에 사용된 "당(sugar)" 또는 "당 그룹(sugar group)" 또는 "당 잔기(sugar residue)"는 3-탄소(트리오스)단위, 4-탄소(테트라오스) 단위, 5-탄소(펜토스)를 포함할 수 있는 탄수화물 부분을 지칭한다. 단위, 6-탄소(헥소오스)단위, 7-탄소(헵토스) 단위 또는 이들의 조합일 수 있으며, 단당류, 이당류, 삼당류, 사당류, 오당류, 올리고당류 임의의 다른 다당류일 수 있다.
일부 경우에, "당" 또는 "당그룹" 또는 "당 잔기"는 푸라노제(예를 들어, 리보푸라노스, 프럭토푸라노스)또는 피라노제(예를 들어, 글루코피라노스, 갈락토피라노오스)또는 이들의 조합을 포함한다. 일부 경우에, "당" 또는 "당그룹" 또는 "당 잔기"는 알도오스 또는 케토스 또는 이들의 조합을 포함한다. 단당류의 비제한적인 예는 리보스, 데옥시리보스, 자일로스, 아라비노스, 포도당, 만노스, 갈락토스 및 과당을 포함한다.
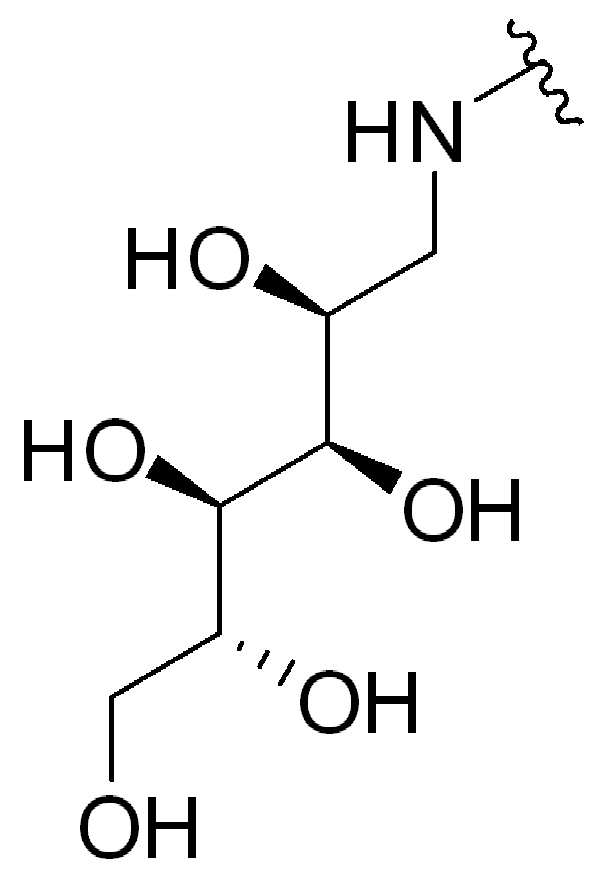
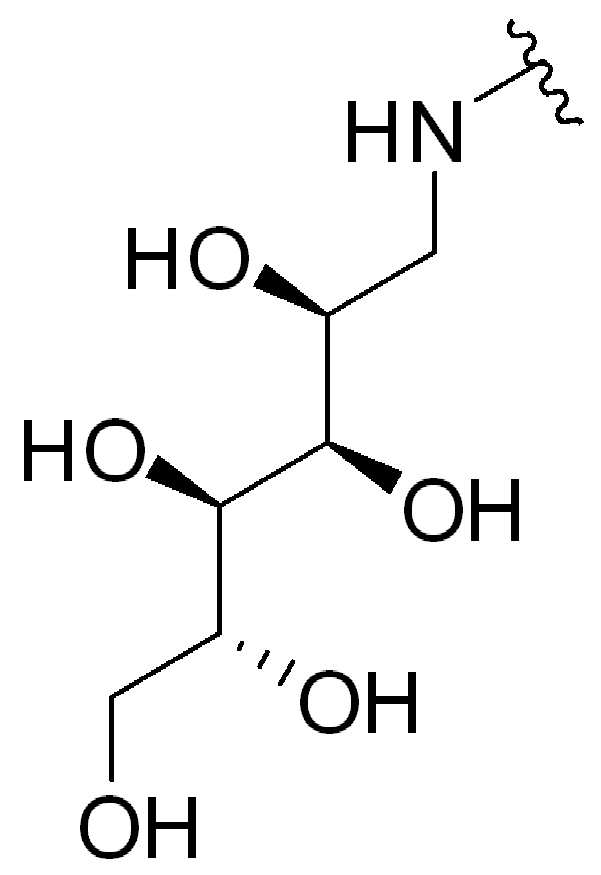
이당류의 비제한적인 예는 슈크로스, 말토오스, 락토오스, 락툴로스 및 트레할로스를 포함한다. 다른 "당" 또는 "당 그룹" 또는 "당 잔기"는 아밀로오스, 아밀로펙틴, 글리코겐, 이눌린 및 셀룰로오스를 포함하지만 이에 제한되지 않는 다당류 및/또는 올리고당을 포함한다. 일부 경우에, "당" 또는 "당 그룹" 또는 "단 잔기"는 아미노-당(amino-sugar)이다. 일부 경우에 "당" 또는 "당 그룹" 또는 "단 잔기"는 분자의 나머지(즉, 글루카마이드)와 아미드 연결을 형성하기 위해 분자의 나머지와 그것의 아미노 그룹을 통해 연결된 글루 카민 잔기(1-아미노-1-데옥시-D-글루시톨)다.
특정 기(groups), 부분(moieties), 치환기(substituents) 및 원자(atoms)는 기, 부분, 치환기, 원자가 결합되는 원자를 나타내기 위해 결합 또는 결합과 교차하는 휘글선으로 도시되어있다. 예를 들어, 다음으로 표시된 프로필 그룹으로 치환된 페닐 그룹은:
다음과 같은 구조를 가지고 있다:
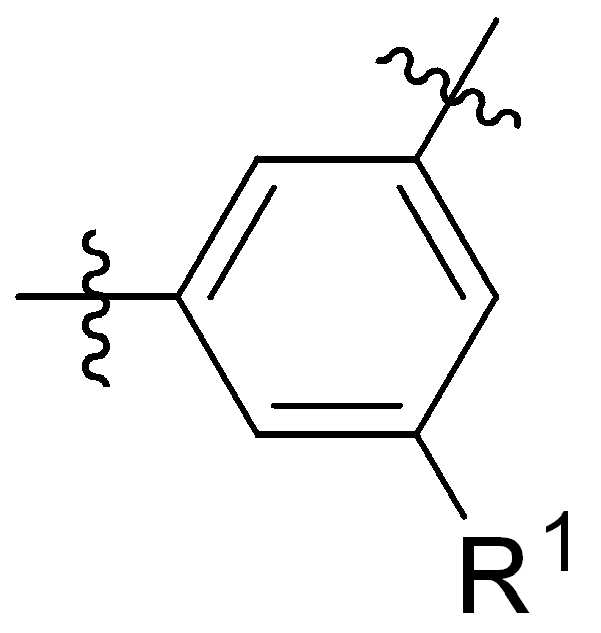
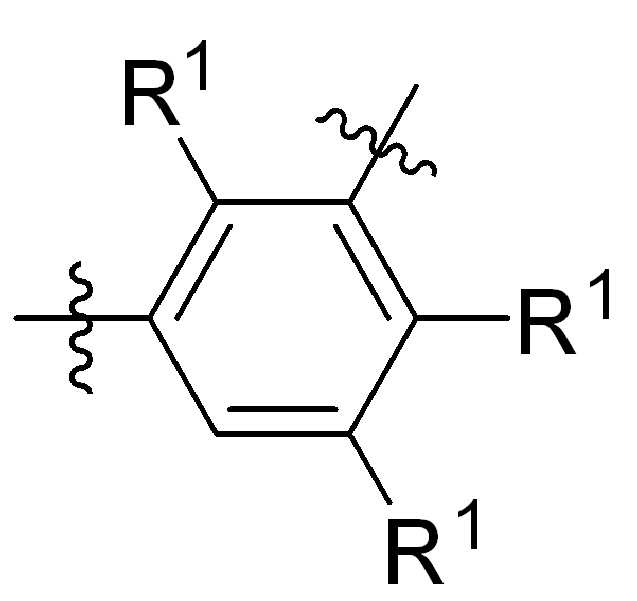
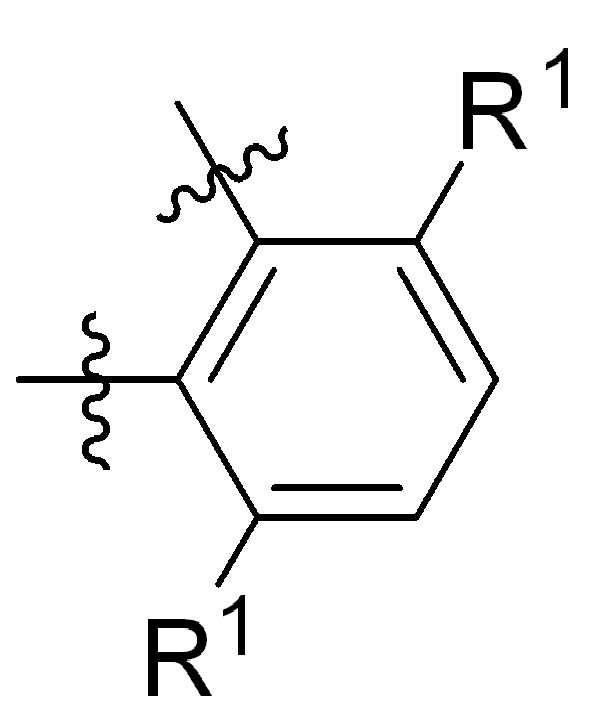
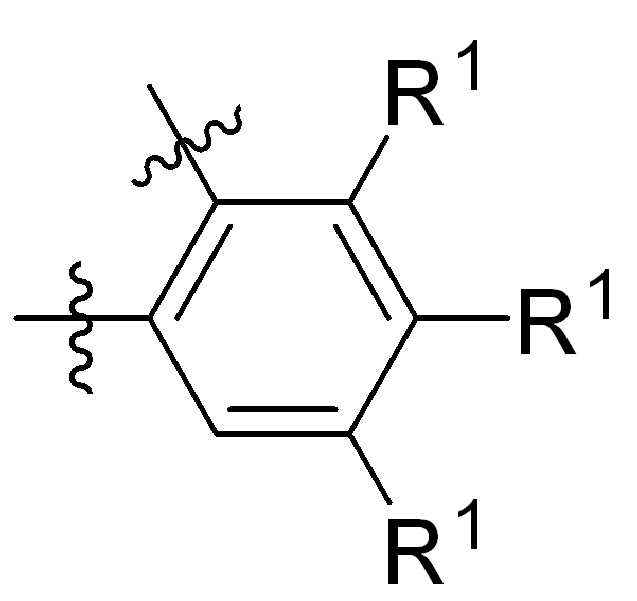
본 원에 사용된 바와 같이, 고리 원자 사이의 결합을 통해 고리형 기(예를 들어, 방향족, 헤테로 방향족, 축합고리, 및 포화 또는 불포화 시클로 알킬 또는 헤테로 시클로알킬)에 결합된 치환기를 나타내는 그림은 달리 명시되지 않는 한 고리형 기가 본 원에 기술되거나 본 개시 내용이 속하는 분야에 공지된 기술에 따라, 사이클릭그룹의 임의의 고리 위치 또는 융합된 고리 그룹의 임의의 고리상가 치환기로 치환될 수 있음을 지칭한다. 예를 들어, 첨자 q는 0 내지 4의 정수이고, 치환기 R1의 위치는 일반적으로, 즉 결합선 구조의 임의의 꼭지점, 즉 특정 고리에 직접적으로 부착되지 않는 그룹인 또는 기 탄소원자는 치환기 R1이 특정 고리탄소 원자에 결합된 기의 하기 비제한 예를 포함한다:
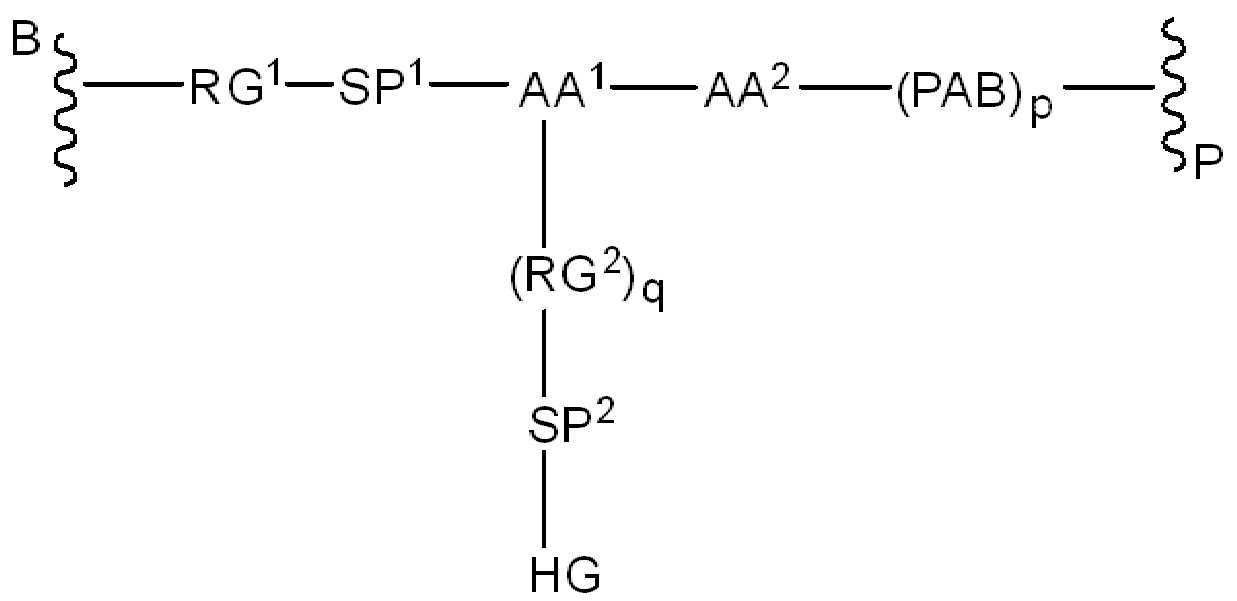
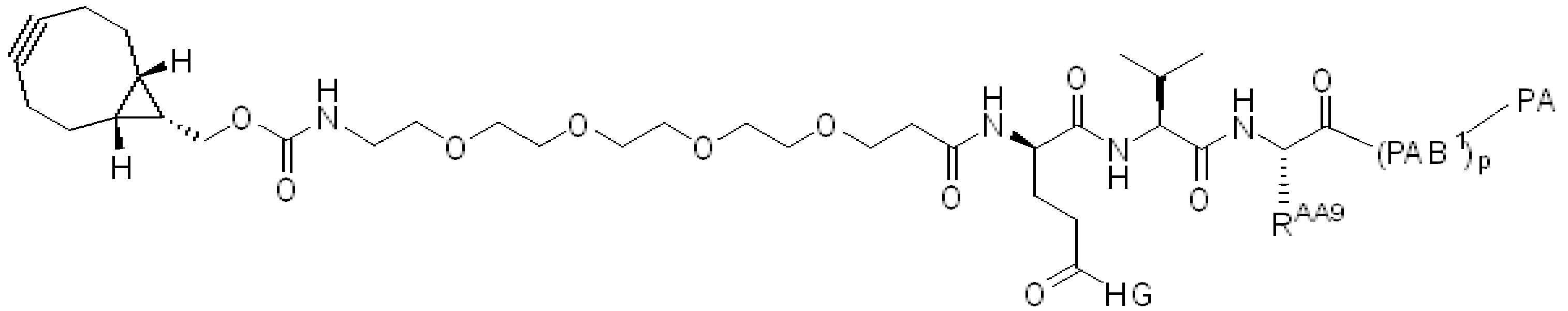
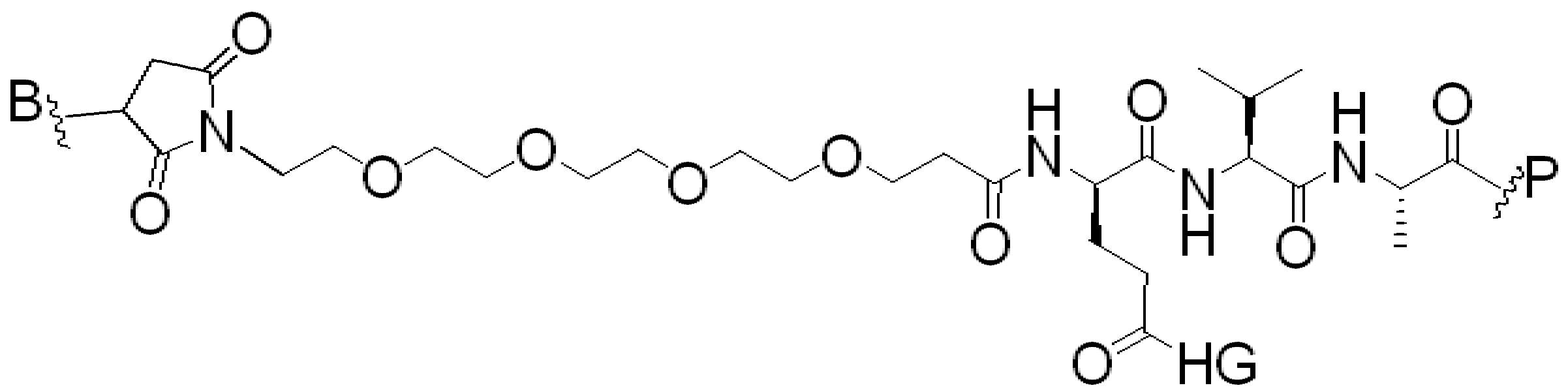
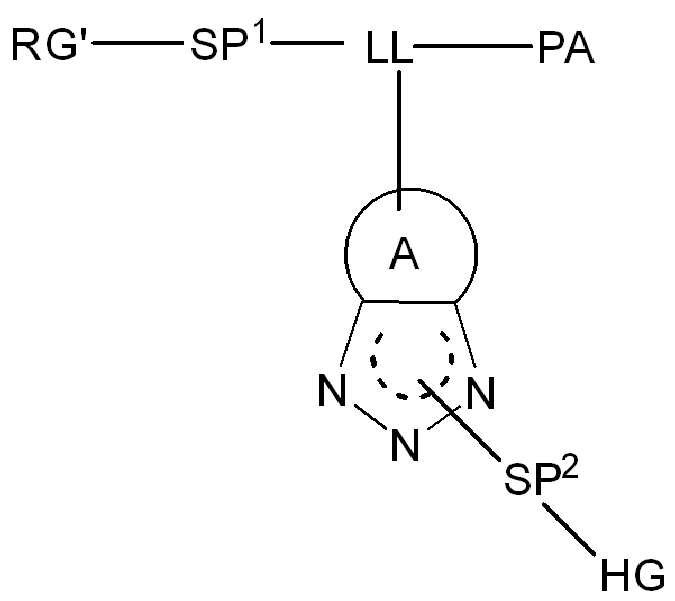
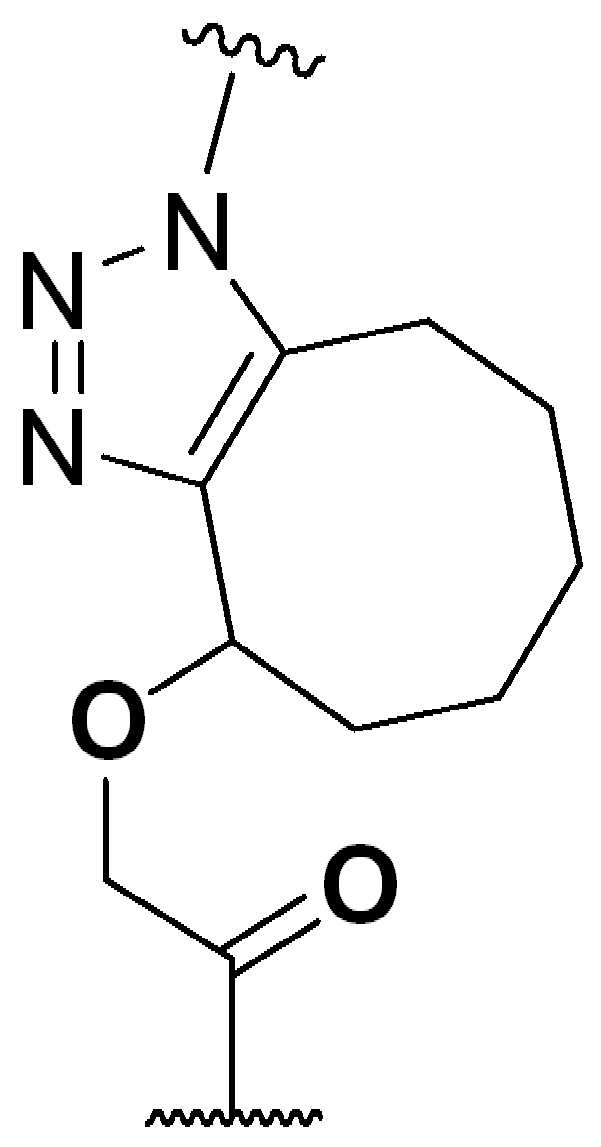
,, ,,, , ,,,, ,,,, ,,, ,,,,,,,,,,,, 및 . 본 원에 사용된 어구 "친수성 링커(HL)"는 본원에 정의된 친수성 그룹(HG) 및 본원에 정의된 스페이서 SP2를 포함하는 부분을 지칭한다.
본 원에 사용된 어구 "반응성 링커(reactive linker)"는 예를 들어, RG'가 반응성 그룹이고 SP1이 스페이서 기인, 예를 들어, 로 묘사되는, 반응성 그룹 및 스페이서기를 포함하는 1가기를 지칭한다. 본 원에 기술된 바와 같이, 반응성 링커는 하나 초과의 반응성그룹 및 하나 이상의 스페이서기를 포함할 수 있다. 스페이서 그룹은 반응성 그룹을 페이로드 또는 결합제와 같은 다른 그룹에 연결하는 임의의 2가 또는 3가 부분이다. 반응성 링커(L, LL)는 이들이 결합되는 페이로드와 함께 본원에 기술된 항체 접합제의 제조를 위한 합성 전구체로서 유용한 중간체("링커-페이로드")를 제공한다. 반응성 링커는 하나 이상의 반응성 그룹 RG(RG1, RG2 또는 RG')를 함유하며, 이는 다른 기의 반응성 부분, 예를 들어 본원에 기재된 바와 같은 항체, 변형된 항체, 또는 항원 결합 단편 또는 친수성기의 반응성 부분과 반응할 수 있는 작용기 또는 부분이다. 항체, 변형된 항체 또는 이의 항원결합 단편과 반응성 그룹의 반응으로 생성된 부분은 본원에 기재된 접합제의 "결합제 링커(binding agent linker)"("BL")부분을 포함한다.
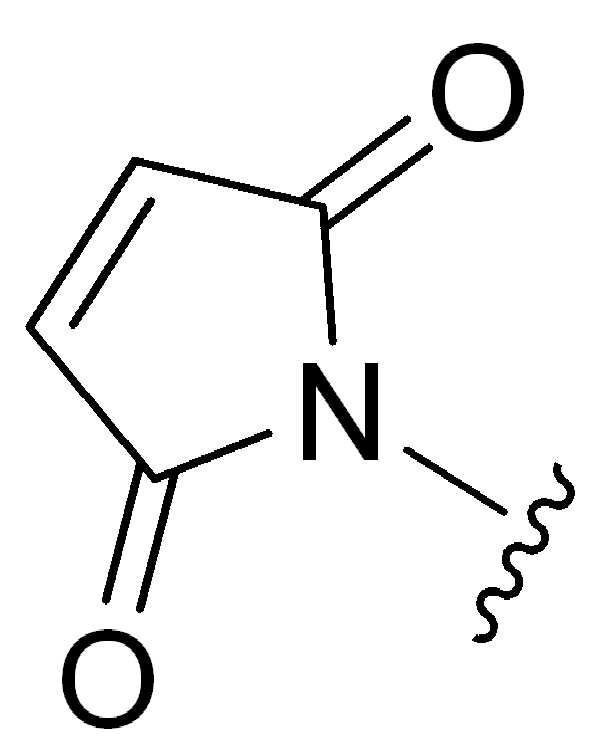
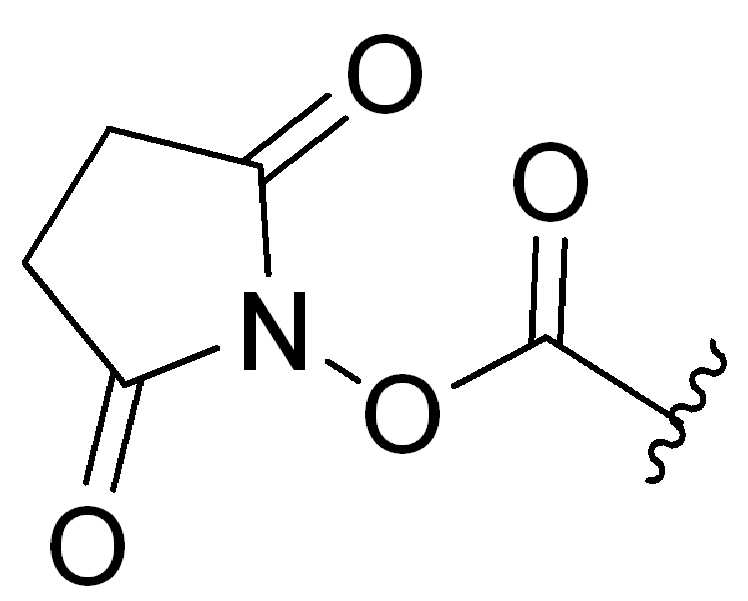
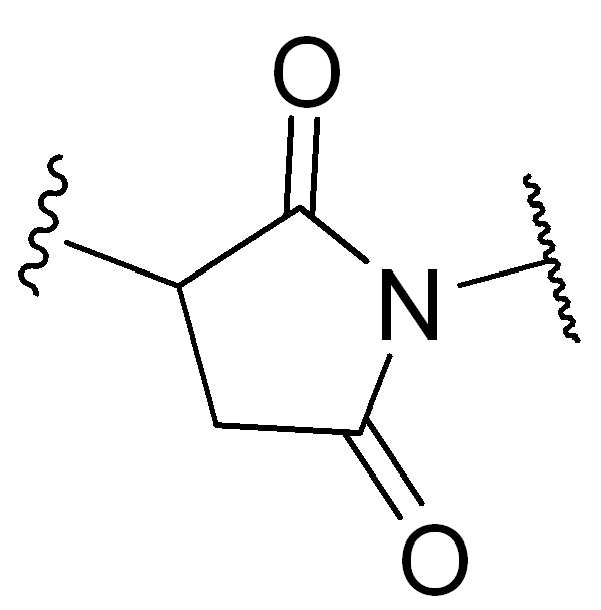
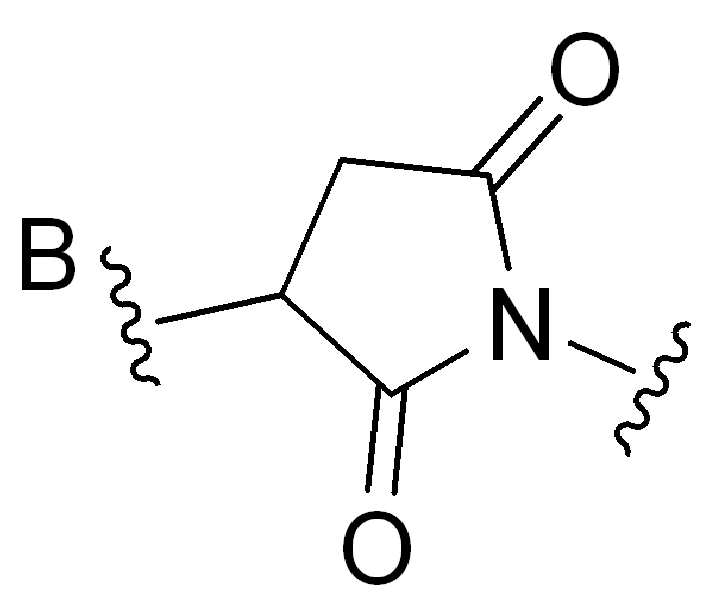
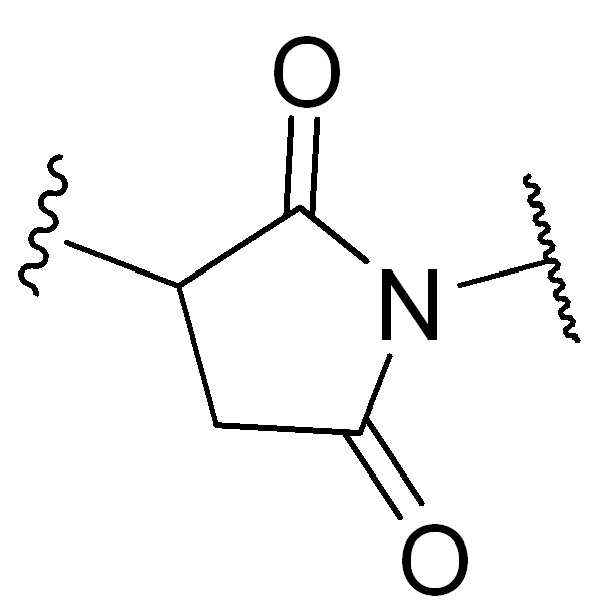
특정실시양태에서, "반응성 그룹"은 항체 또는 그의 항원-결합단편의 시스테인 또는 리신 잔기와 반응하는 작용기 또는 부분(예를 들어, 말레이 미드 또는N-히드록시숙신이미드(NHS)에스테르)이다.
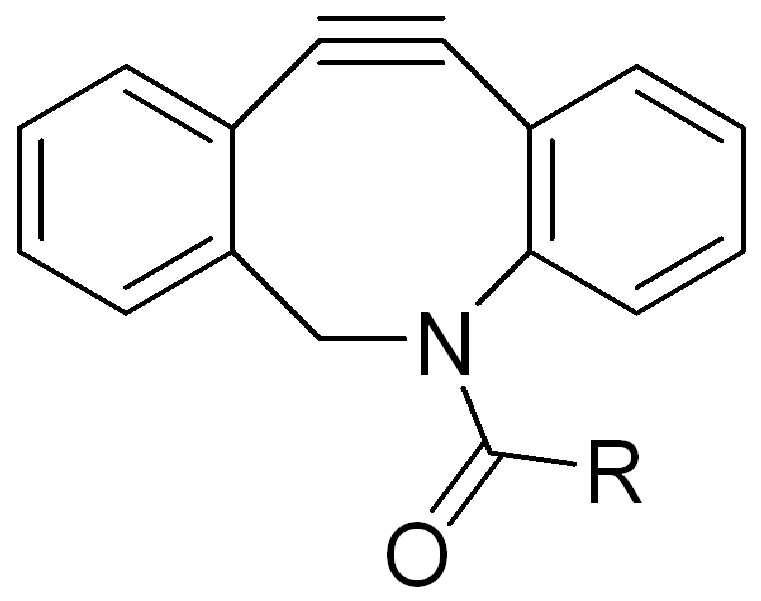
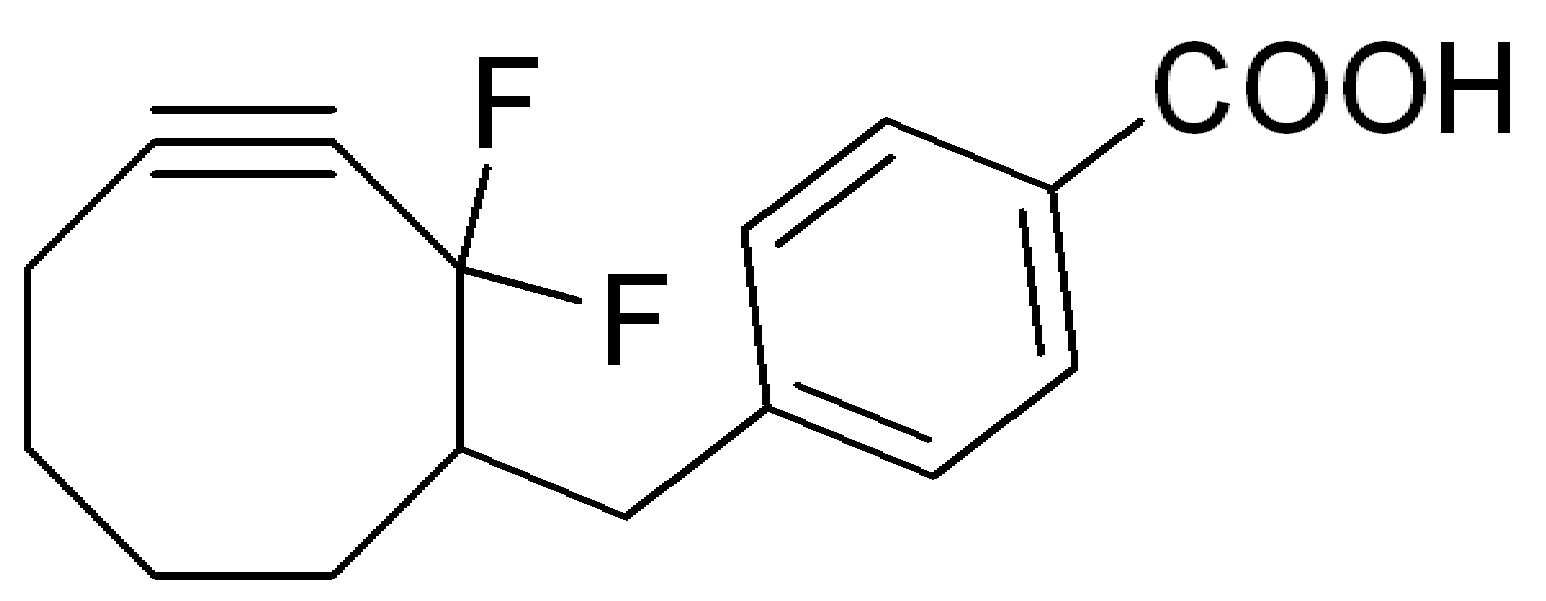
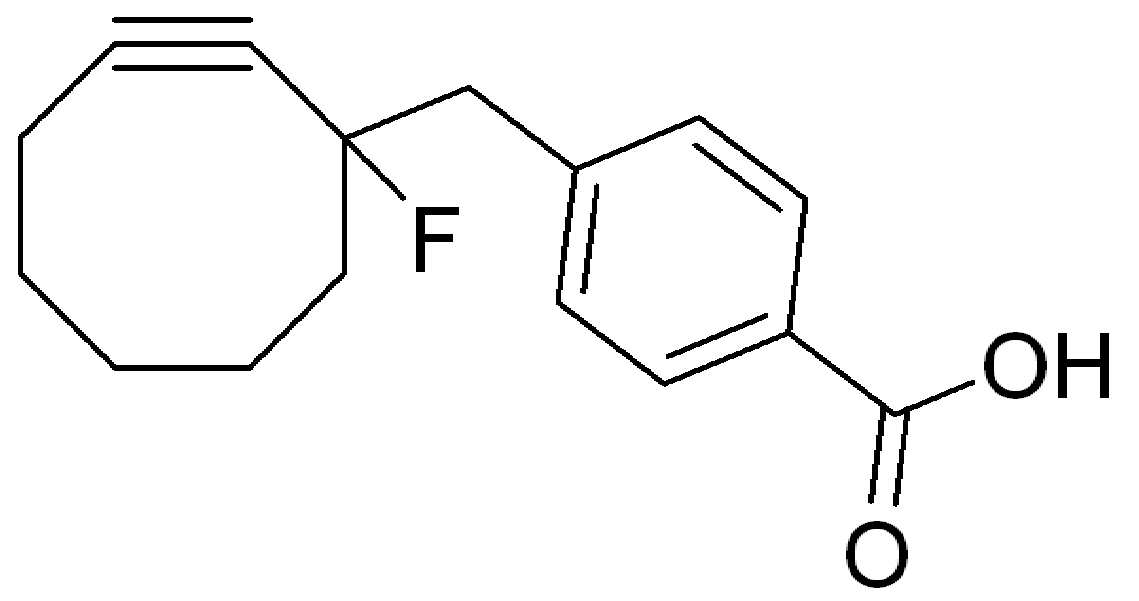
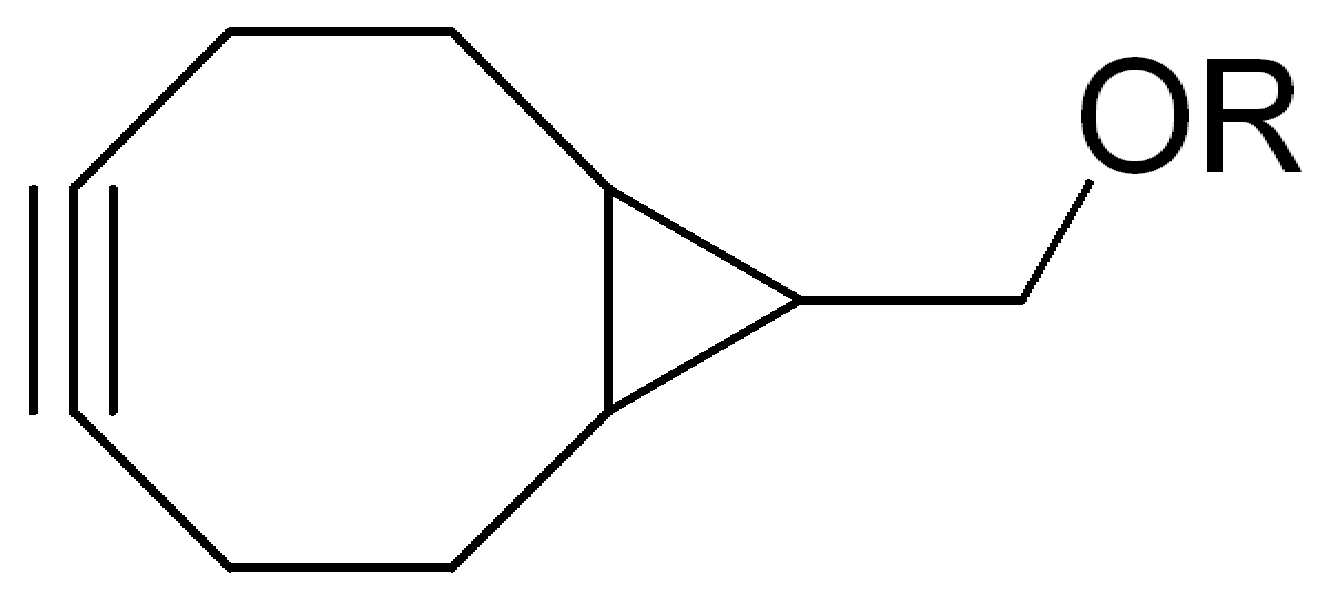
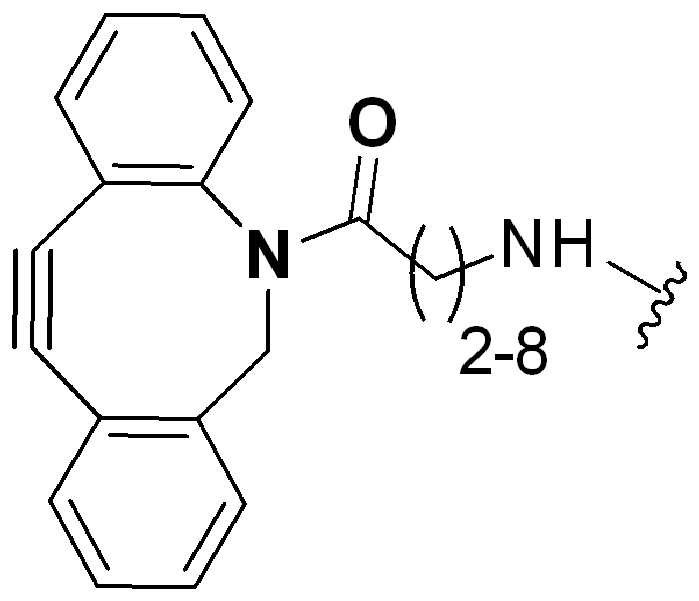
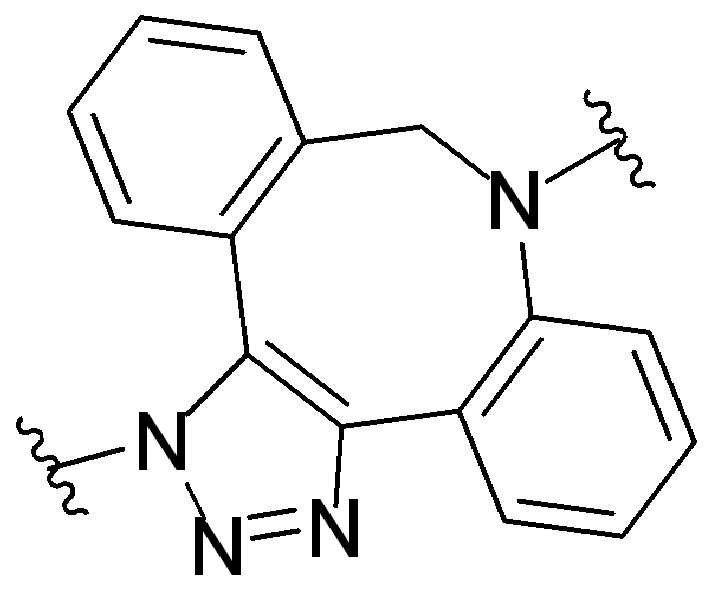
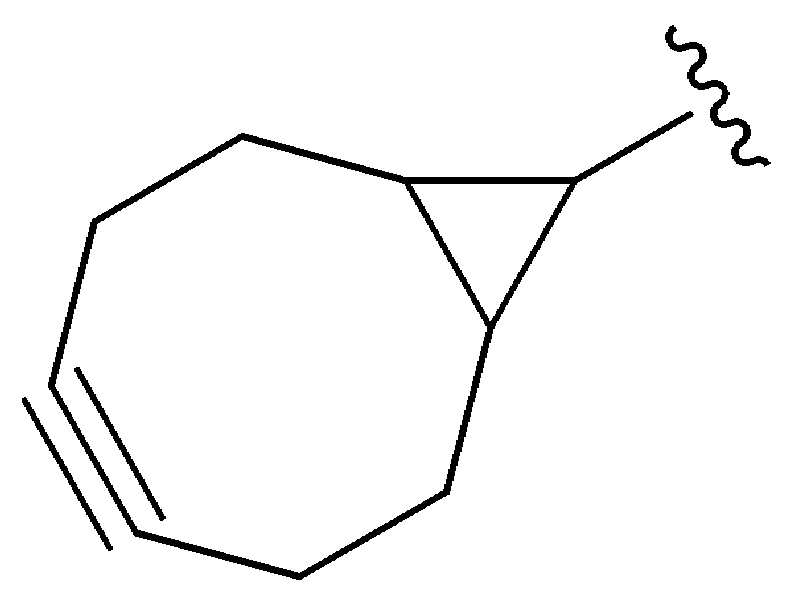
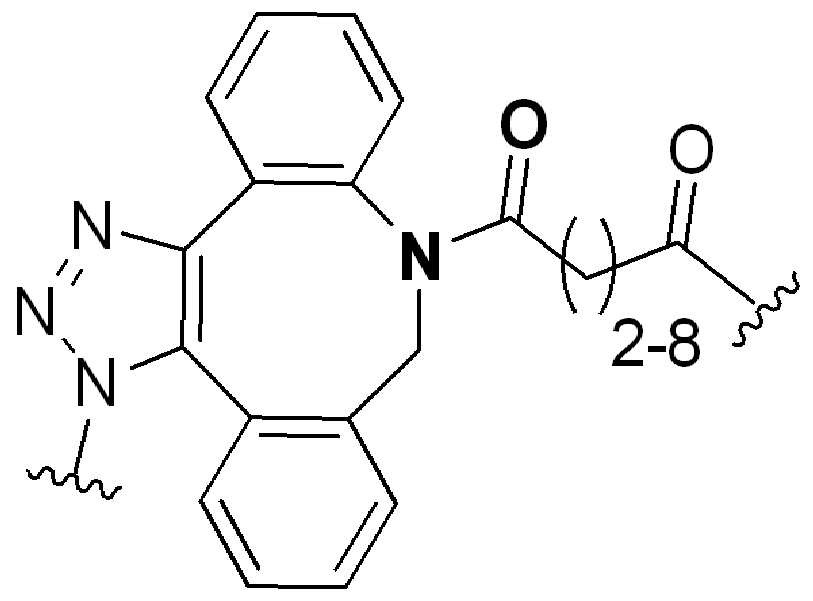
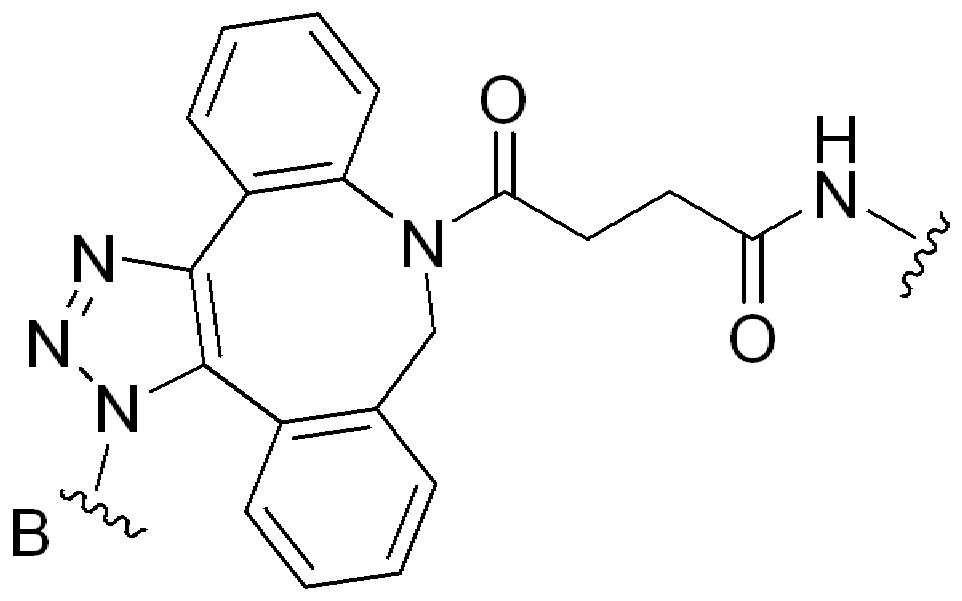
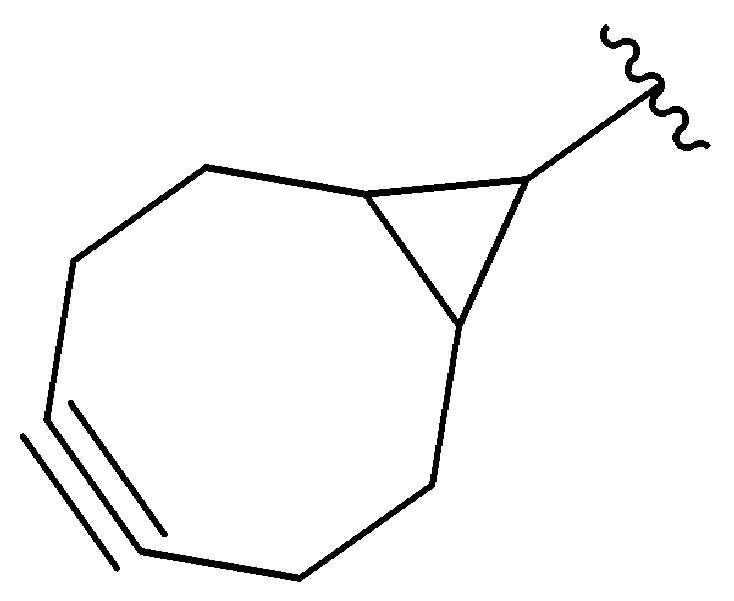
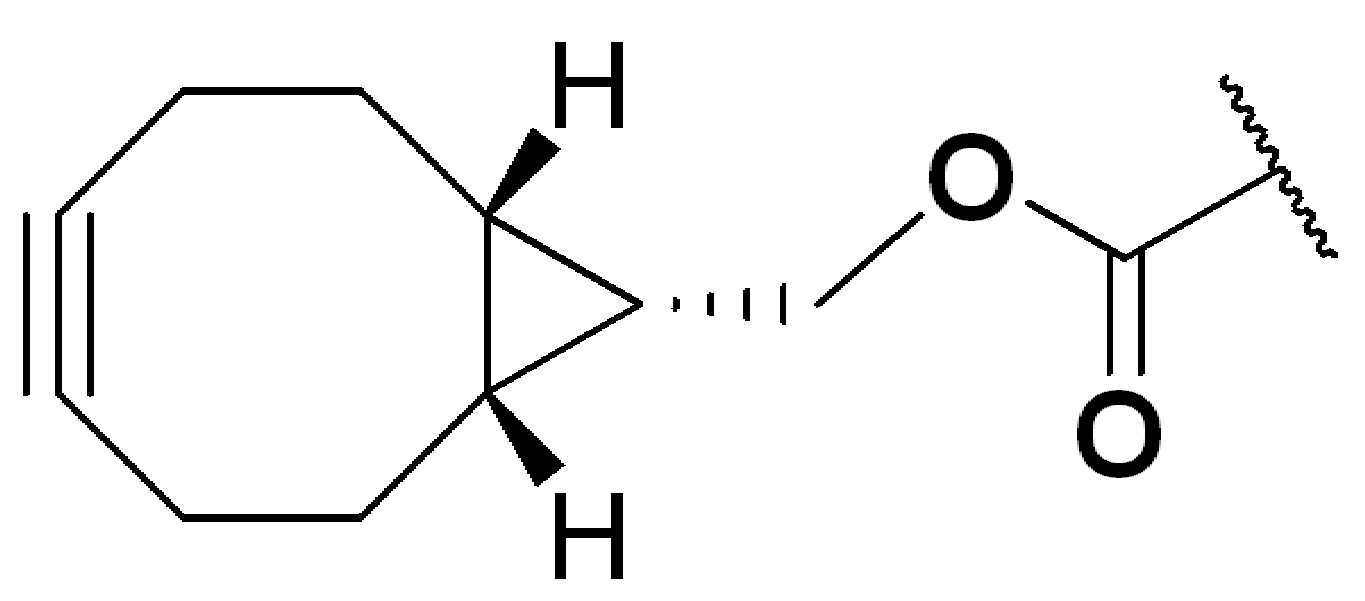
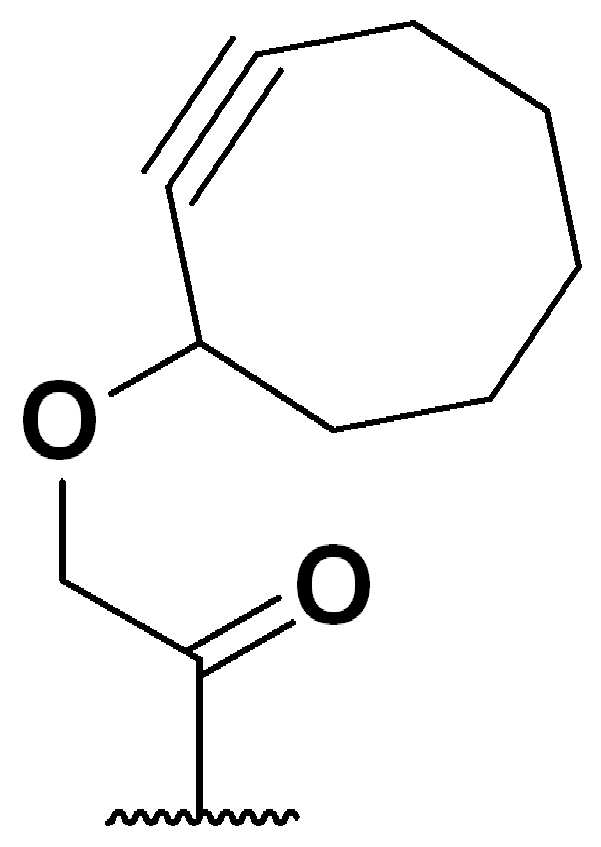
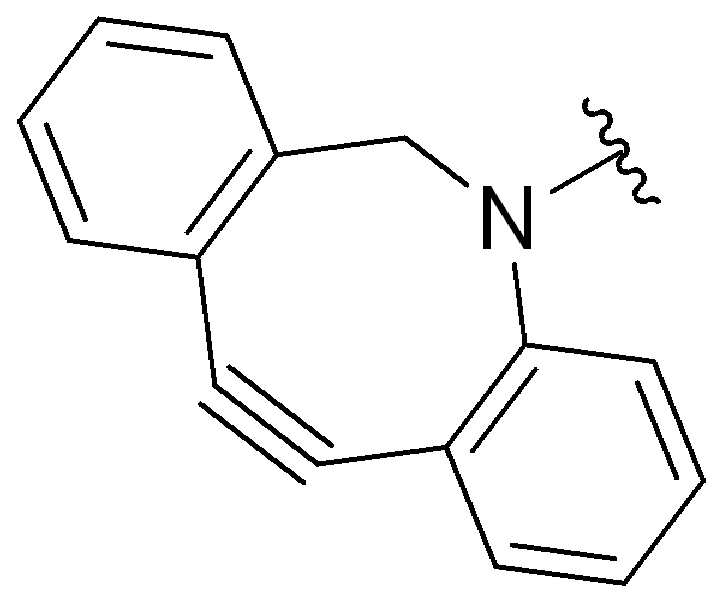
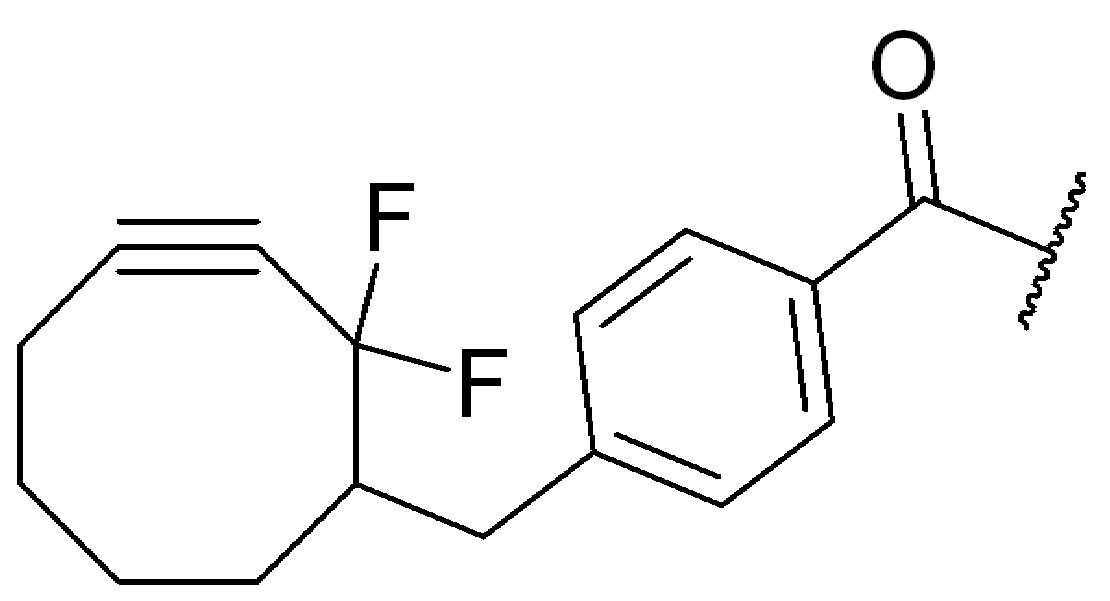
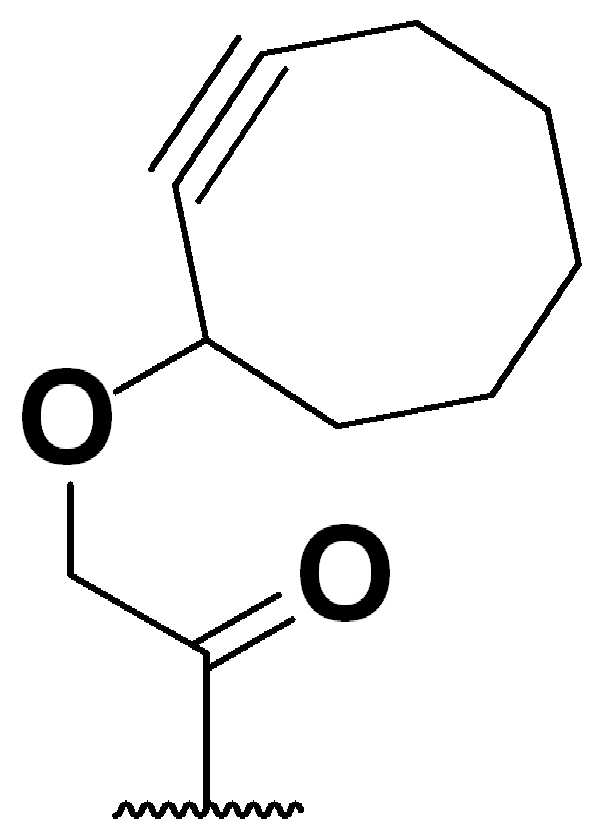
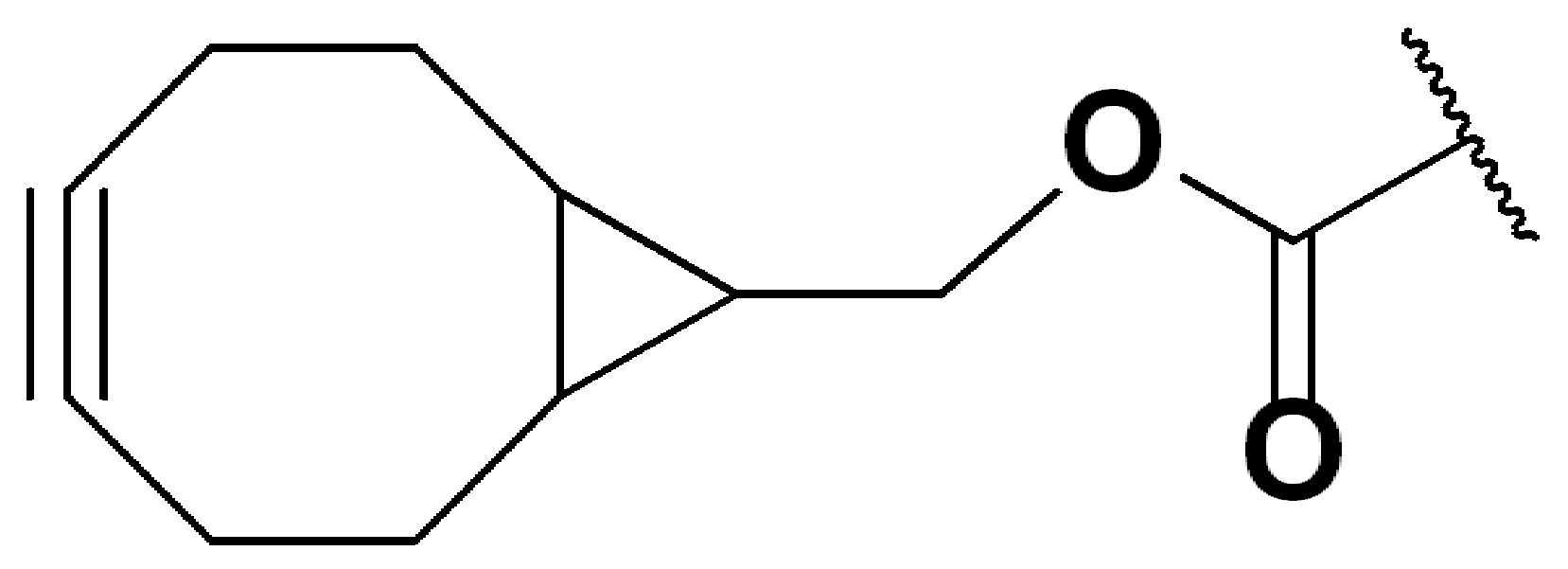
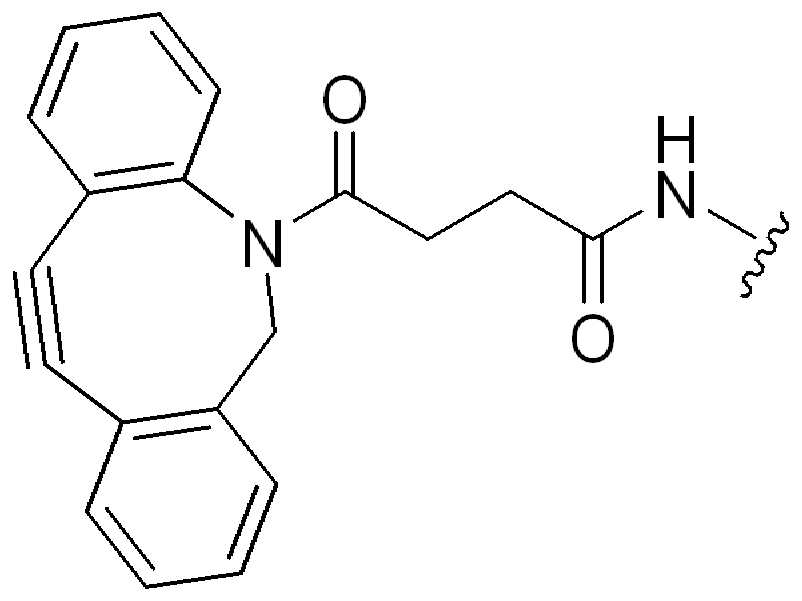
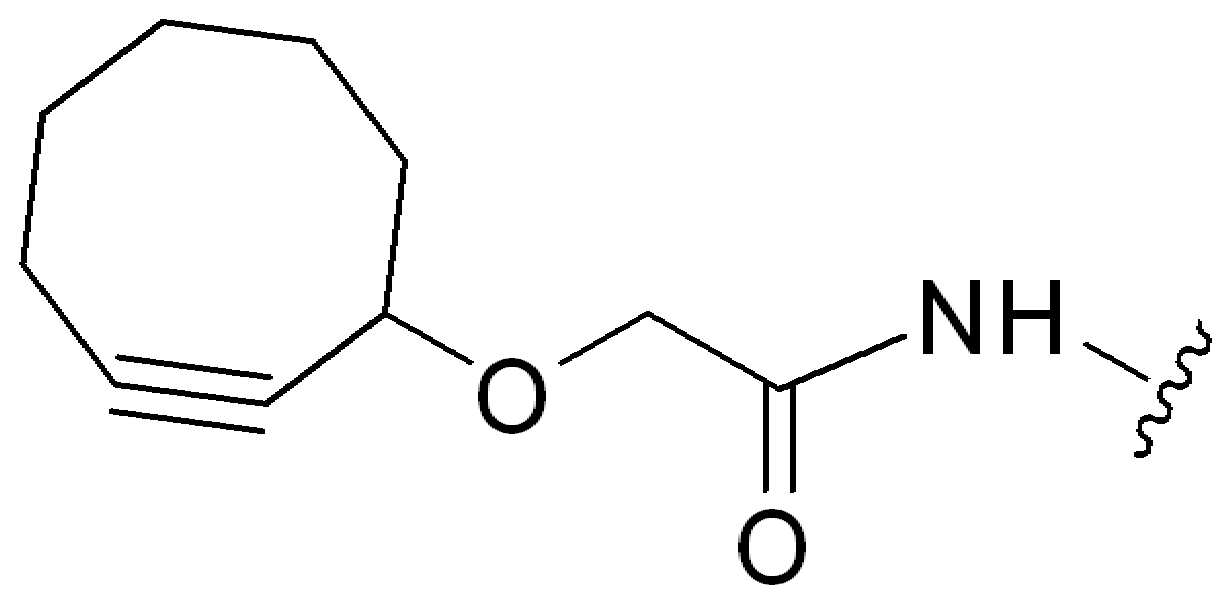
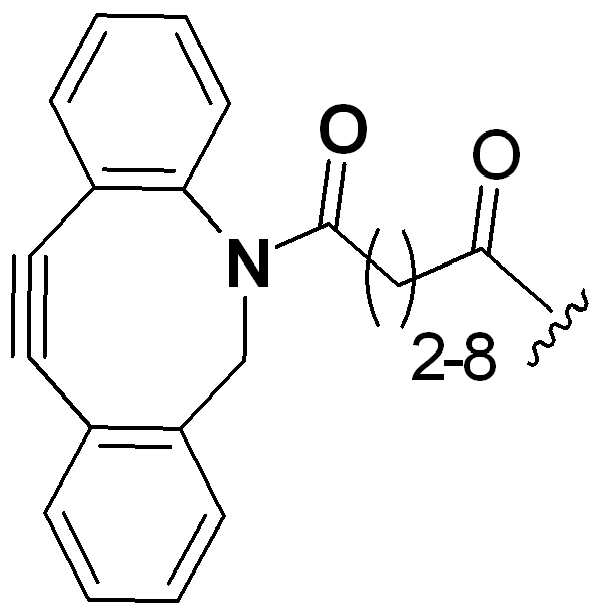
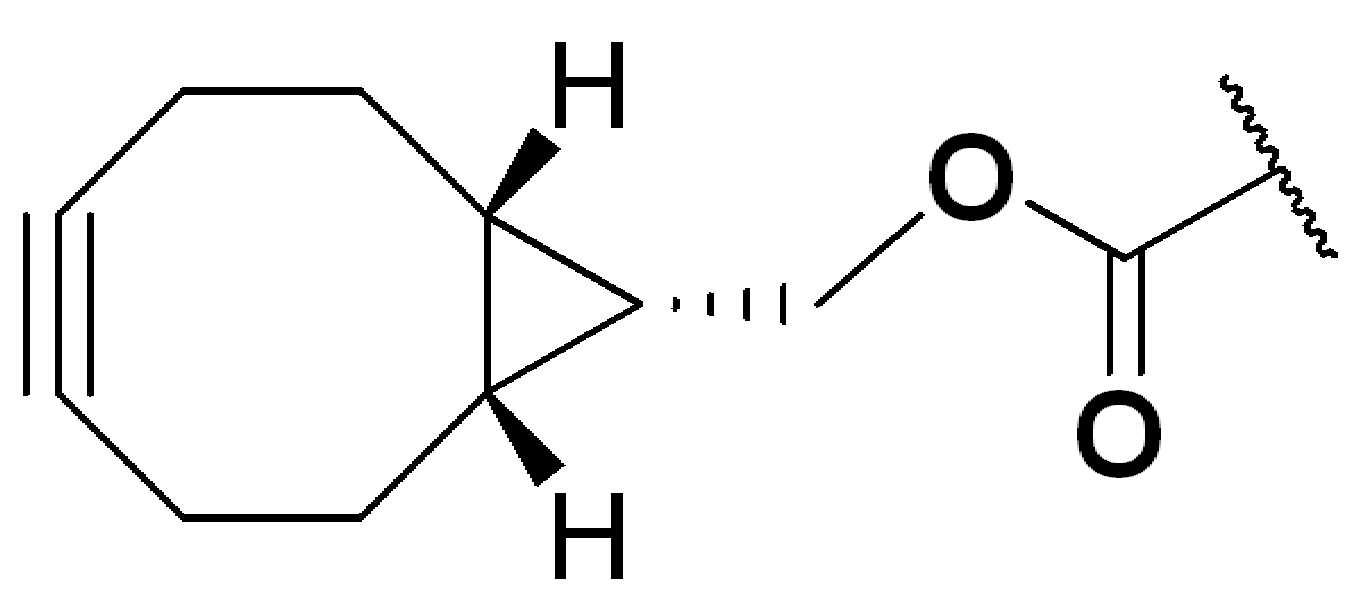
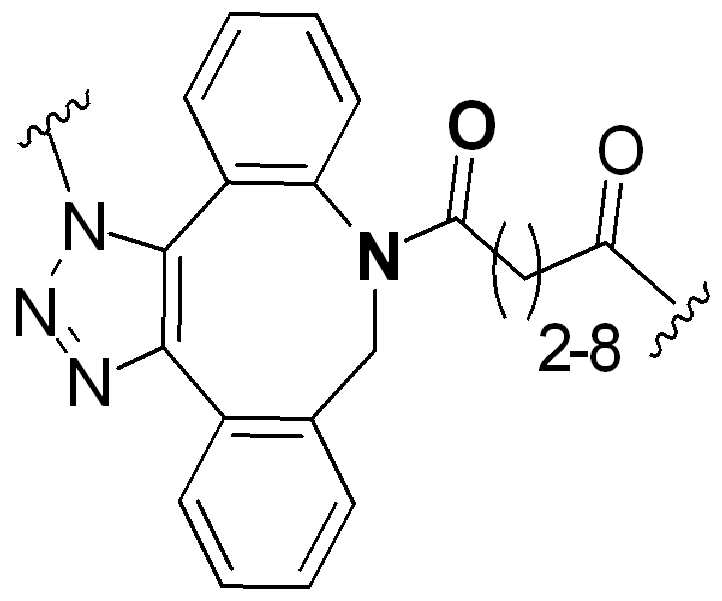
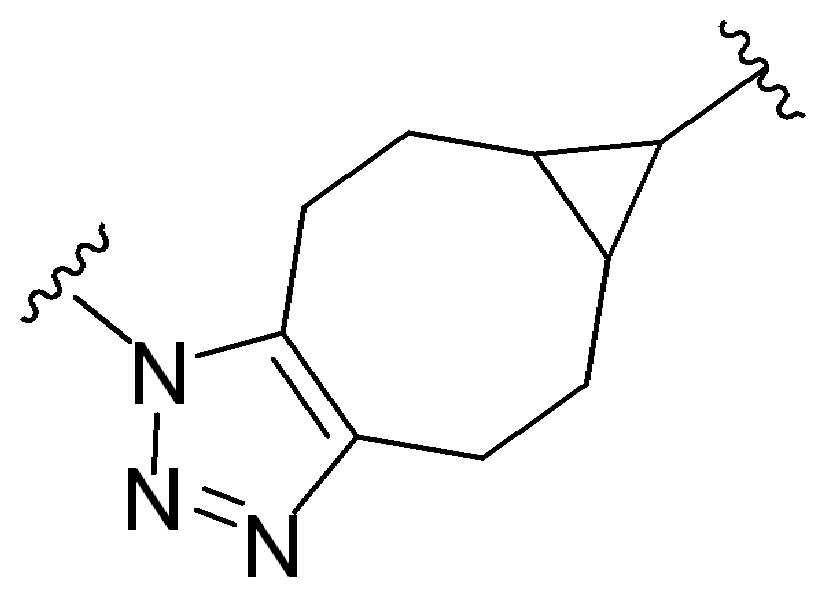
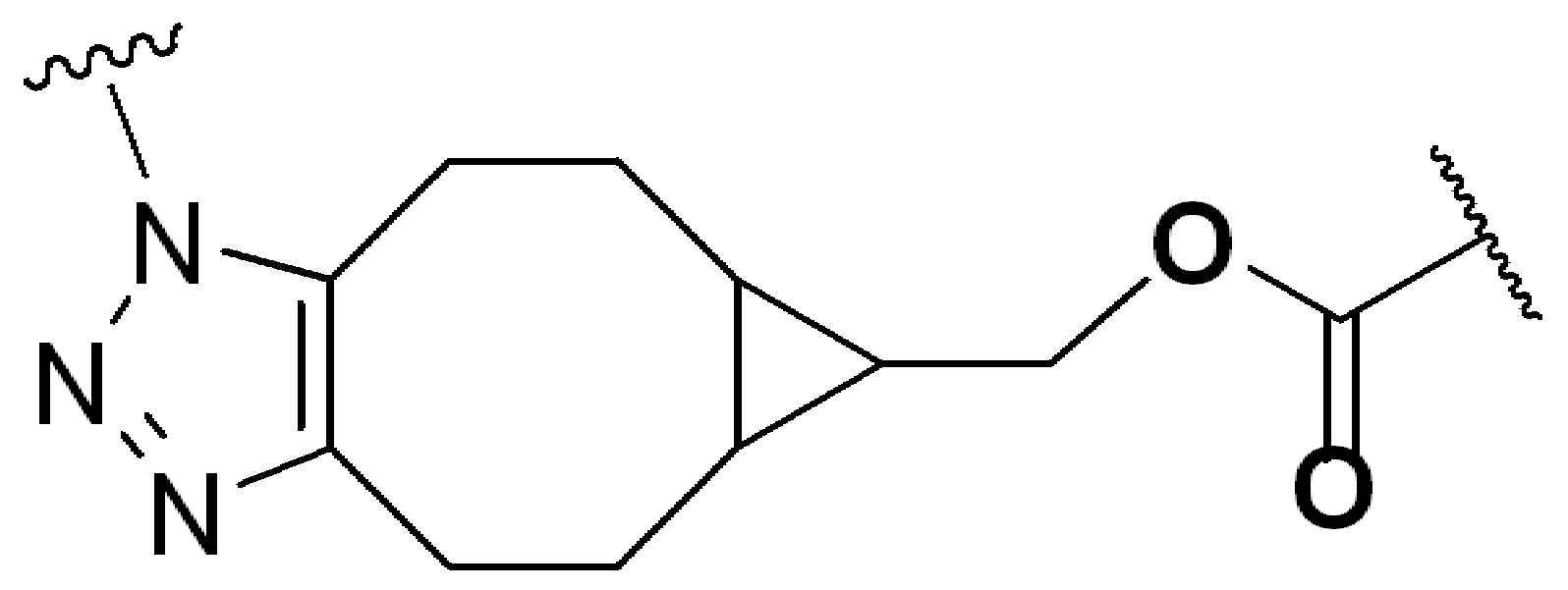
특정 실시양태에서, "반응성 기(reactive group)"는 클릭 화학반응을 겪을 수 있는 작용기 또는 부분이다(예를 들어, 클릭 화학, Huisgen Proc. Chem. Soc. 1961, Wang et al. J. Am. Chem. Soc. 2003, 및 Agard et al. J. Am. Chem. Soc. 2004). 상기 클릭 화학 반응의 일부 실시양태에서, 반응성 그룹은 아지드와 1,3-시클로 부가 반응을 겪을 수 있는 알킨이다. 아지드와 1,3-시클로 부가 반응을 겪을 수 있는 알킨은 본 명세서에서 "클릭 화학 잔기(click chemistry residue)"로도 지칭된다. 이러한 적합한 반응성 그룹은 변형된 알킨, 예를 들어 변형 촉진 알킨-아지드 시클로 부가(SPAAC), 시클로알킨, 예를 들어 시클로 옥킨, 벤질화딘 알킨 및 1,3-시클로첨가를 겪을 수 있는 알킨을 포함하지만, 이에 제한되지 않는다. 구리촉매가 없는 상태에서 알킨과의 반응. 적합한 알킨은 또한 디벤조아자시클로옥틴 또는 (DIBAC), 예를 들어, , 디벤조시클로옥틴(dibenzocyclooctyne) 또는 (DIBO), 예를 들어, , 바이아릴아자시클로옥토논(biarylazacyclooctynone) 또는 (BARAC), 예를 들어, , 다이플루오르화시클로옥틴(difluorinated cyclooctyne) 또는 (DIFO), 또는 (DIFO2), 또는 (DIFO3), (DIMAC), (ALO), (NOFO), (OCT), 및 (MOFO), 예를 들어 플루오르화 알킨, 아자-시클로 알킨, 자전거[6.1.0] 노닌(nonyne) 또는 (BCN), 여기서 R은 알킬(alkyl), 알콕시(alkoxy), 또는 아실(acyl), 및 그의 유도체, 예를 들어, 이다. 특히 유용한 알킨은 및 를 포함한다. 추가의 알킨(alkynes)에는 및 를 포함한다.
이러한 반응성 그룹을 포함하는 링커-페이로드는 아지도기로 기능화된 항체를 접합시키는데 유용하다. 이러한 기능화된 항체는 아지도-폴리에틸렌글리콜 그룹으로 기능화된 항체를 포함한다. 특정 실시양태에서, 이러한 기능화된 항체는 효소 트랜스 글루타미나제 존재 하에 아미노기 및 아지드기를 갖는 화합물로 하나 이상의 글루타민 잔기, 예를 들어 중쇄 Gln295를 갖는 항체를 처리함으로써 유도된다.
특정 실시양태에서, 항체 또는 글루타미닐-개질된 항체 또는 항원 결합 분자는 하나 이상의 폴리펩티드 사슬서열에서 하나 이상의 글루타민 잔기를 포함한다. 특정 실시양태에서, 항체 또는 글루타미닐-개질된 항체 또는 항원 결합 분자는 각각 하나의 Gln295 잔기를 갖는 2개의 중쇄 폴리펩티드를 포함한다. 추가의 실시양태에서, 항체 또는 글루타미닐-개질된 항체 또는 항원 결합 분자는 중쇄 Gln295 이외의 부위에서 하나 이상의 글루타민 잔기를 포함한다. 본 원에 기재된 N297Q 돌연변이(들)를 보유하는 항체가 본 원에 포함된다. 간략하게, 일부 실시양태에서, 글루타민 잔기를 포함하는 항체는 효소 트랜스 글루타미나아제의 존재 하에보다 상세히 후술되는 1차 아민화합물로 처리된다. 일부실시양태에서, Asn297Gln (N297Q) 잔기를 포함하는 항체는 효소 트랜스 글루타미나제 존재 하에 보다 상세히 후술되는 1차 아민 화합물로 처리된다. 일부 실시양태에서, Gln295(Q295) 잔기를 포함하는 항체는 효소 트랜스 글루타미나아제의 존재 하에 보단 상세히 후술되는 1차 아민 화합물로 처리된다.
예를 들어, 일부 실시양태에서, 이러한 항체는 서열을 제거 또는 비활성화하거나 임의의 간섭 구조와는 다른 부위에 글루타민 잔기를 삽입하기 위해 부위 지향적 돌연변이 유발에 의해 제조될 수 있다. 이러한 하에는 또한 천연 또는 인공 공급원으로부터 단리될 수 있다.
항체의 아미노산 서열은 Kabat et al., ("Kabat" numbering scheme) Al-Lazikani et al., 1997, J. Mol. Biol., 273:927-948 ("Chothia" numbering scheme); MacCallum et al., 1996, J. Mol. Biol. 262:732-745 ("Contact" numbering scheme); Lefranc et al., Dev. Comp. Immunol., 2003, 27:55-77 ("IMGT" numbering scheme); and Honegge and Plckthun, J. Mol. Biol., 2001, 309:657-70 ("AHo" numbering scheme) 에 의해 묘사된 것들을 포함하는, 임의의 알려진 넘버링 체계를 사용해 넘버링될 수 있다. 달리 명시되지 않는 한, 본 원에 사용된 넘버링 체계는 카바트 넘버링 체계이다. 그러나, 넘버링 체계(numbering scheme)는 이들이 존재하지 않는 서열의 차이를 의미하는 것으로 의도되지 않으며, 당업자는 하나 이상의 항체의 아미노산 서열을 조사함으로써 서열 위치를 요이하게 확인할 수 있다. 달리 언급되지 않는 한, "EU넘버링 체계(EU numbering scheme)"는 일반적으로 항체 중쇄 불변 영역에서 잔기를 언급할 때 사용된다(예를 들어, 상기문헌(Kabat et al.)에 보고 됨).
용어"당화 항체(aglycosylated antibody)"는 트랜스 글루타미네이션 반응을 방해 할 수 있는 글리코 실화 서열을 포함하지 않은 항체, 예를 들어 하나 이상의 중쇄 상의 N297에 당류 그룹을 갖지 않는 항체를 지칭한다. 특정 실시양태에서, 항체 중쇄는 N297돌연변이를 갖는다. 다시 말해서, 항체는 Kabat et al.에 의해 개시된 EU넘버링 시스템에 따라 위치 297에서 아스파라긴 잔기를 더 이상 갖지 않도록 돌연변이된다. 특정 실시양태에서, 항체 중쇄는 N297Q 또는 N297D돌연변이를 갖는다. 이러한 항체는 글리코실화 서열을 제거 또는 비활성화 하기 위해 부위 지향적 돌연변이 유발에 의해 또는 임의의 간섭 글리코실화 부위 도는 임의의 다른 간섭 구조로부터 분리된 부위에 글루타민 잔기를 삽입하기 위해 부위 지향적 돌연변이 유발에 의해 제조될 수 있다. 이러한 항체는 또한 천연 또는 인공 공급원으로부터 분리될 수 있다.
용어"디글리오실화된 항체 deglyosylated antibody"는 N297에서 사카라이드 그룹이 제거되어 Q295를 트랜스 글루 타미네이션(transglutamination)으로 전개하는 항체를 지칭한다. 특정 실시양태에서, 항체, 예를 들어 N297항체를 탈당화 시키는 추가 단계를 포함하는 방법이 본원에 제공된다.
일부 실시예에서, 생체 접합 반응에 사용된 알킨은 Cu(I)클릭-화학 결합 반응에 유용하다. 일부예에서, 접합 반응에 사용된 알킨은 2-시아노벤조티아졸(2- Cyanobenzothiazole, CBT)반응에서 1,2아미노티올과 반응한다. 일부예에서, 사용된 알킨은 역 전자 요구 딜스알더반응에서 BCN, BCN의 유도체 또는 트랜스 사이콜로 옥텐(trans-cyclooctene, TCO)이다. 예를 들어, Wang et al., J. Am. Chem. Soc.; (Article), 2012, 134 (6), 2950-2953에서 볼 수 있다.
일부 예에서, 그룹은 변형된 항체 또는 이의 항원결합 단편상에서 아지드와 반응한다.
일부 예에서, 반응성 기는 작용기, 예를 들어 , 항체 또는 이의 항원 결합 단편에서 시스테인 잔기와 반응하여 결합을 형성하는 것, 예를 들어, , 여기서 Ab는 항체 또는 이의 항원 결합 단편을 나타내고, S는 작용기가 Ab에 결합하는 시스테인 잔기상의 S원자를 나타낸다. 일부 예에서, 반응성 기는 작용기, 예를 들어, , 항체 또는 이의 항원 결합 단편상의 라이신 잔기와 반응하여 이에 결합을 형성하는, 예를 들어, , 여기서 Ab는 항체 또는 이의 항원 결합 단편을 나타내고 NH는 작용기가 Ab에 결합하는 라이신 측쇄 잔기상의 NH원자를 나타낸다.
본 원에 사용된 어구 "결합제 링커(binding agent linker)" 또는 "BL"은 여기에 제시된 페이로드 화합물 (예: MMAE, 비스-옥타 하이드로 페난 트렌카르복스아미드, 스테로이드) 및, 선택적으로 하나 이상의 측쇄 화합물과 결합제(예: 항체 또는 이의 항원 결합 단편)를 이음(links), 연결(connects) 또는 결합(bonds)시키는 임의의 2가, 3가 또는 다가 그룹 또는 부분을 지칭한다. 일반적으로, 본 원에 기술된 항체 접합제에 적합한 결합제 링커는 항체의 순환 반감기를 이용하기에 충분히 안정하고, 동시에 때때로 접합제의 항원-매개 내재화 후 페이로드를 방출할 수 있는 것들이다. 링커는 절단 가능하거나 절단 불가능할 수 있다. 절단 가능한 링커는 내재화 후 세포 내 대사, 예를 들어 가수분해, 환원 또는 효소 반응을 통한 절단에 의해 절단되는 링커이다. 비절단성 링커는 내재화 후 항체의 리소좀 분해를 통해 부착된 페이로드를 방출하는 링커다. 적합한 링커는 산-불안정성 링커, 가수분해-불안정성 링커, 효소적으로 절단 가능한 링커, 환원 불안정성 링커, 자가 침투성 링커 및 비절단성 링커를 포함하지만, 이에 제한되지는 않는다.
적합한 링커는 또한 펩티드(peptides), 글루쿠로니드(glucuronides), 숙신이미드-티오에테르(succinimide-thioethers), 폴리에틸렌글리콜(polyethylene glycol (PEG) units), 히드라존(hydrazones), 말-카프로일 단위(mal-caproyl units), 디펩티드 단위(dipeptide units), 발린-시트룰린 단위(valine-citrulline units), 및 파라-아미노벤질 단위(para-aminobenzyl (PAB) units) 를 포함하지만, 이에 제한되지는 않는다. 일부 실시 양태에서, 결합제 링커 (BL)는 반응성 링커(RL)의 반응성 그룹(RG)와 결합제의 반응성 부분, 예를 들어, 항체, 변형된 항체의 반응에 의해 형성된 부분 또는 이의 항원 결합 단편이다.
일부 예에서, 본원은 하기를 포함하는 화합물 또는 그의 제약상 허용되는 염이다: 하나 이상의 페이로드 부분에 연결되고 공유 링커를 통해 하나 이상의 친수성 부분에 연결된 결합제, 상기 공유 링커는 각각의 결합제, 페이로드 부분 및 친수성 부분에 직접 또는 간접적으로 연결됨.
일부 다른 실시 예에서, 본 원은 하기를 포함하는 화합물 또는 그의 제약상 허용되는 염이다:
하나 이상의 페이로드 부분에 연결되고 공유 링커를 통해 하나 이상의 친수성 부분에 연결된 단백질로서, 상기 공유 링커는 단백질, 페이로드 부분 및 친수성 부분 각각에 직접 또는 간접적으로 결합되는 단백질. 일부 실시양태에서, 단백질은 항체 또는 이의 항원 결합단편이다.
본 원에 예시된 바와 같이, 일부 예에서, 결합제는 리신 아미노산과 같은 공유 링커에 직접 결합한다. 이는 결합제가 리신 아미노산 공유 링커로부터 하나의 결합 위치라는 것을 의미한다. 이들 예 중 일부에서, 공유 링커는 또한 페이로드 부분에 직접 결합된다. 이는 공유 링커가 메이탄신노이드, MMAE, MMAF, 스테로이드, LXR 조절제 또는 본원에 제시된 임의의 페이로드와 같은 페이로드로부터 떨어져있는 하나의 결합 위치임을 의미한다. 이들 예 중 일부에서, 공유 링커는 또한 친수성 부분에 직접 결합된다. 이는 공유 링커가 친수성 잔기, 예컨대 본원에 제시된 친수성 잔기로부터 떨어진 하나의 결합 위치임을 의미한다. 이들 예 중 일부에서, 공유 링커는 리신 아미노산 또는 이의 유도체이다.
다른 예에서, 결합제는 공유 링커에 간접적으로 결합된다. 이는 결합제가 공유 링커로부터 하나의 결합 위치 이상 떨어져 있다는 것을 의미한다. 이는 또한 결합제가 다른 부분을 통해 공유 링커에 결합됨을 의미한다. 예를 들어, 결합제는 공유 링커에 결합된 폴리에틸렌글리콜기에 결합된 말레이미드기에 결합될 수 있다. 이들 예 중 일부에서, 공유 링커는 또한 페이로드 부분에 간접적으로 결합된다. 이는 공유 링커가 MMAE, 스테로이드, LXR조절제, 또는 본 원에 제시된 임의의 페이로드와 같은 페이로드로부터 하나의 결합 위치 이상 떨어져 있음을 의미한다.
이것은 또한 공유 링커가 다른 부분을 통해 페이로드에 결합됨을 의미한다. 예를 들어, 공유 링커는 페이로드에 결합될 수 있는 PAB에 결합 될 수 있는 Val-Ala 또는 Val-Cit와 같은 그러나 이에 제한되지 않는 다이펩타이드에 결합될 수 있다. 이들 예 중 일부에서, 공유 링커는 또한 친수성 부분에 간접적으로 결합된다. 이는 공유 링커가 친수성 잔기, 예를 들어 본 원에 기재된 친수성 잔기로부터 하나의 결합 위치 이상 떨어져 있음을 의미한다. 이는 또한 공유 링커가 다른 부분을 통해 친수성 부분에 결합됨을 의미한다. 예를 들어, 공유 링커는 친수성 잔기에 결합될 수 있는 반응성 그룹에 결합될수 있는 폴리에틸렌글리콜기에 결합될 수 있다. 이들 예 중 일부에서, 공유 링커는 리신 아미노산 또는 이의 유도체이다.
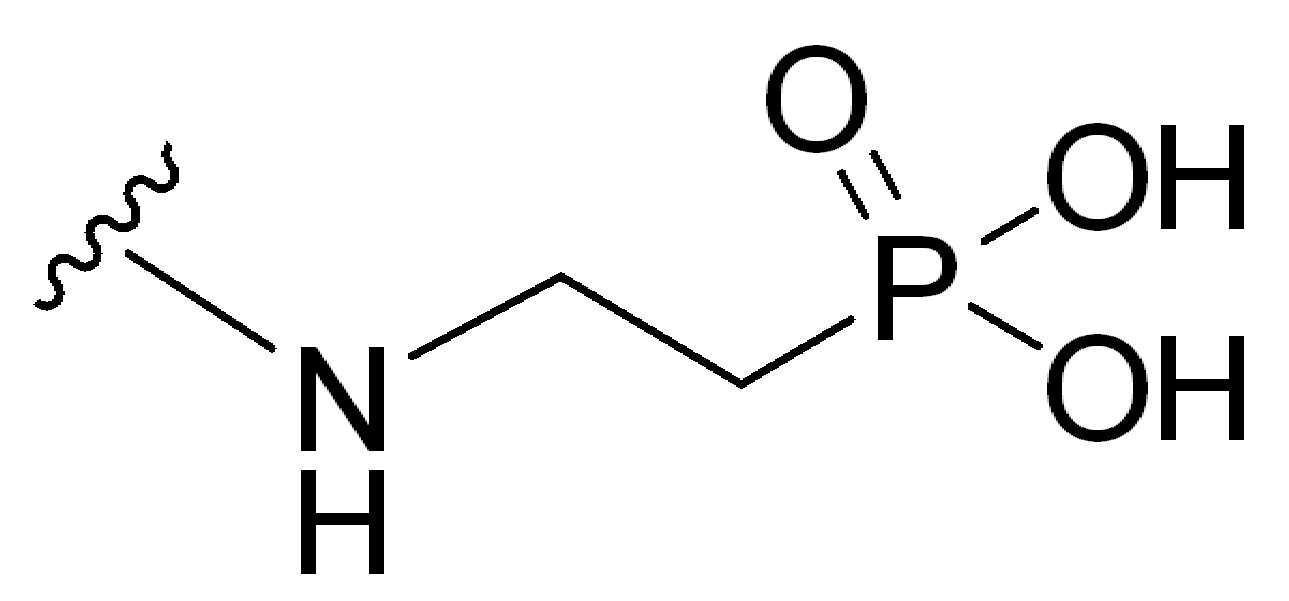
특정 경우에, 친수성 잔기는 말단 친수성기를 포함한다. 일부 경우에, 친수성 잔기는 하나 이상의 타우린기를 포함한다. 일부 경우에, 친수성 잔기는 설폰산기를 포함한다. 일부 경우에, 친수성 잔류물은 말단 설폰산기를 포함한다. 추가의 예에서, 친수성 잔기는 하나 이상의 설폰산기를 포함한다. 일부 경우에 친수성 잔류물은 하나 이상의말단 설폰산기를 포함한다.
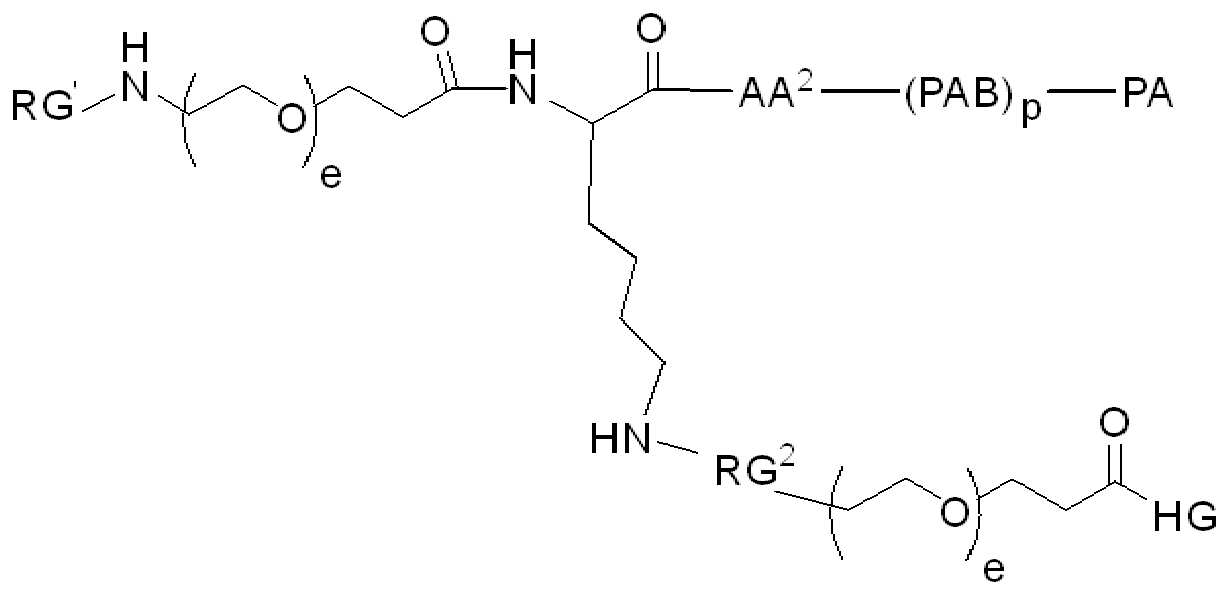
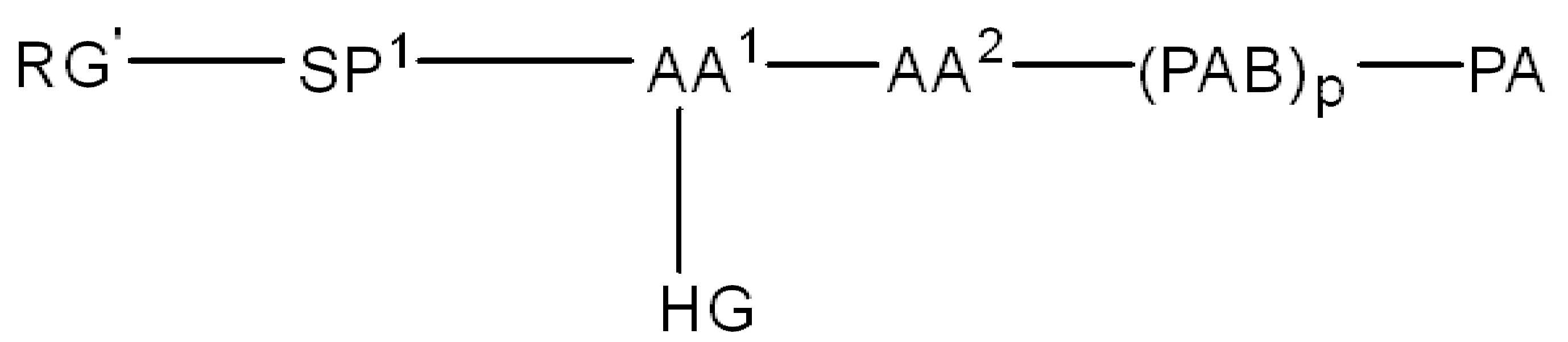
화학식 (I)에 따른 화합물이 본원에 기술된다:
(I)
또는 약제학적으로 허용되는 염, 용매화물, 입체이성질체 또는 그의 유도체, 화학식 (I)에서,
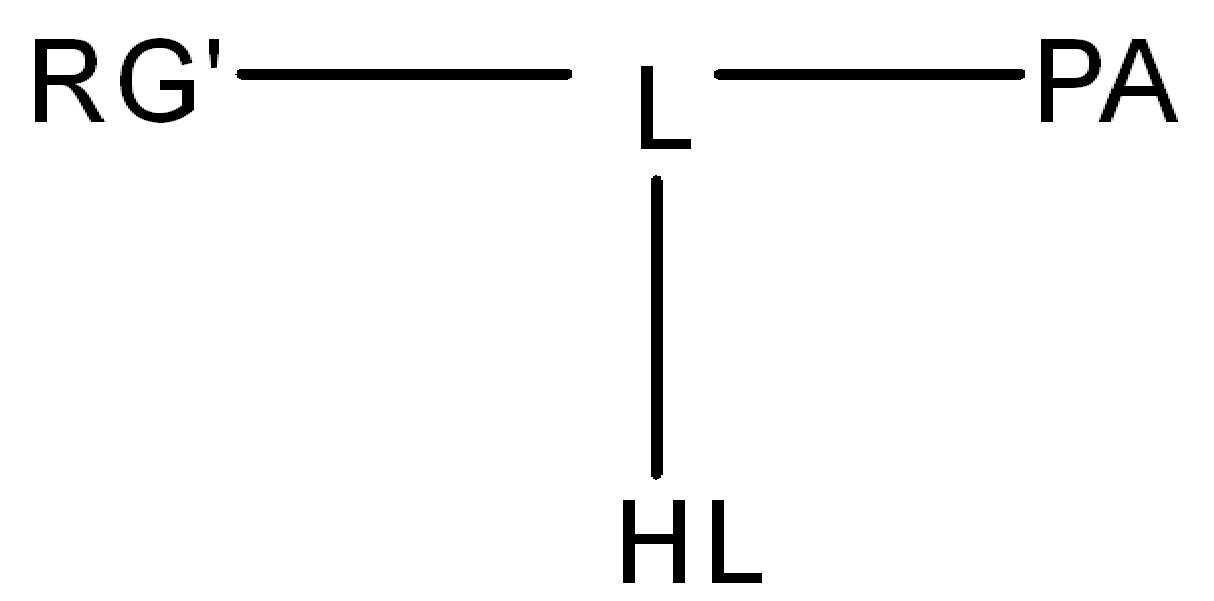
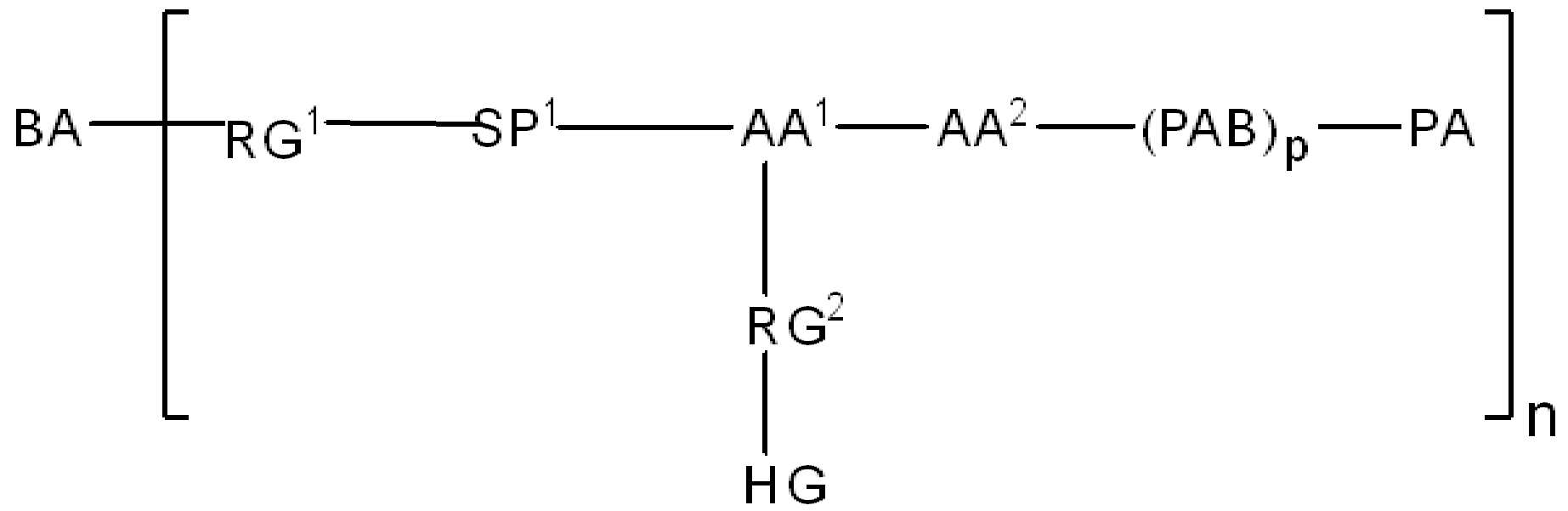
BA는 결합제이고; L은 3가 링커이고; HL은 친수성 잔기이고; PA는 페이로드 잔기이며; 및 아래 첨자 n은 1 내지 30의 정수이다. 일부 경우에, 하나 이상의 3가 링커 L이 존재할 수 있다. 일부 경우에, n은 1 내지 4의 정수이다. 일부 경우에, n은 1이다. 일부 경우에, n이 2이다. 일부 경우에 n이 3이다. 일부 경우에는 n이 4이다.
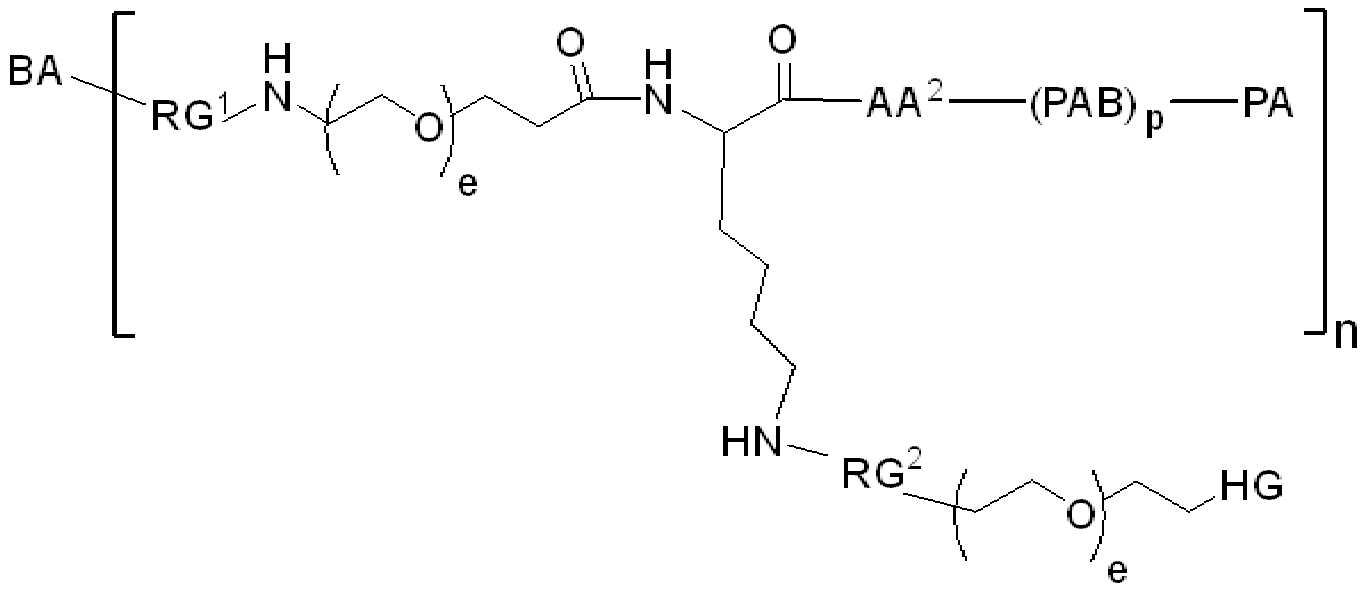
일 예에서, 화학식 (I)의 화합물은 화학식 (II)에 따른다:
(II)
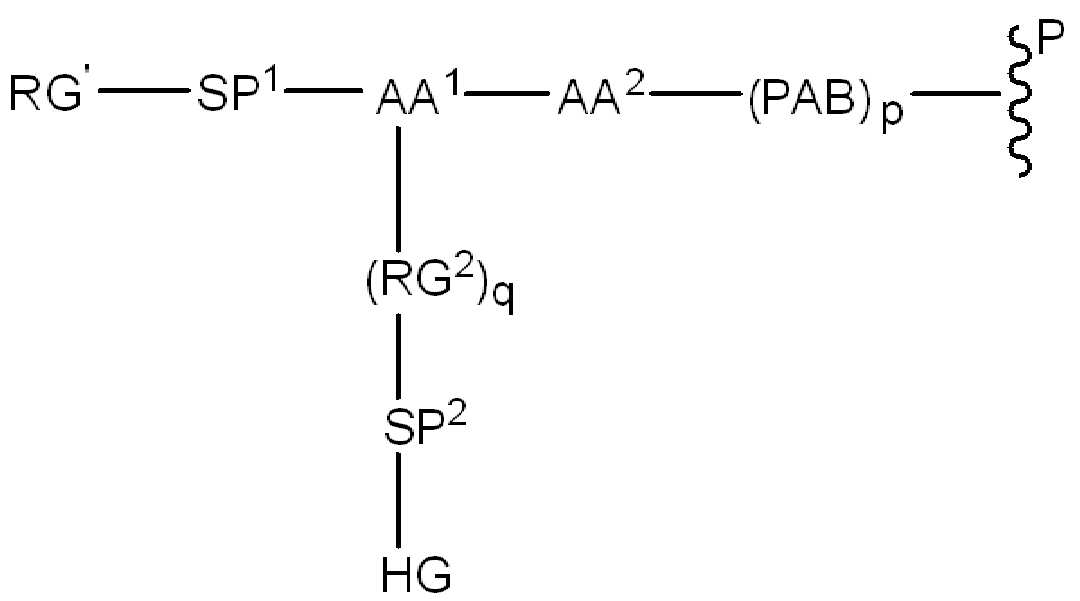
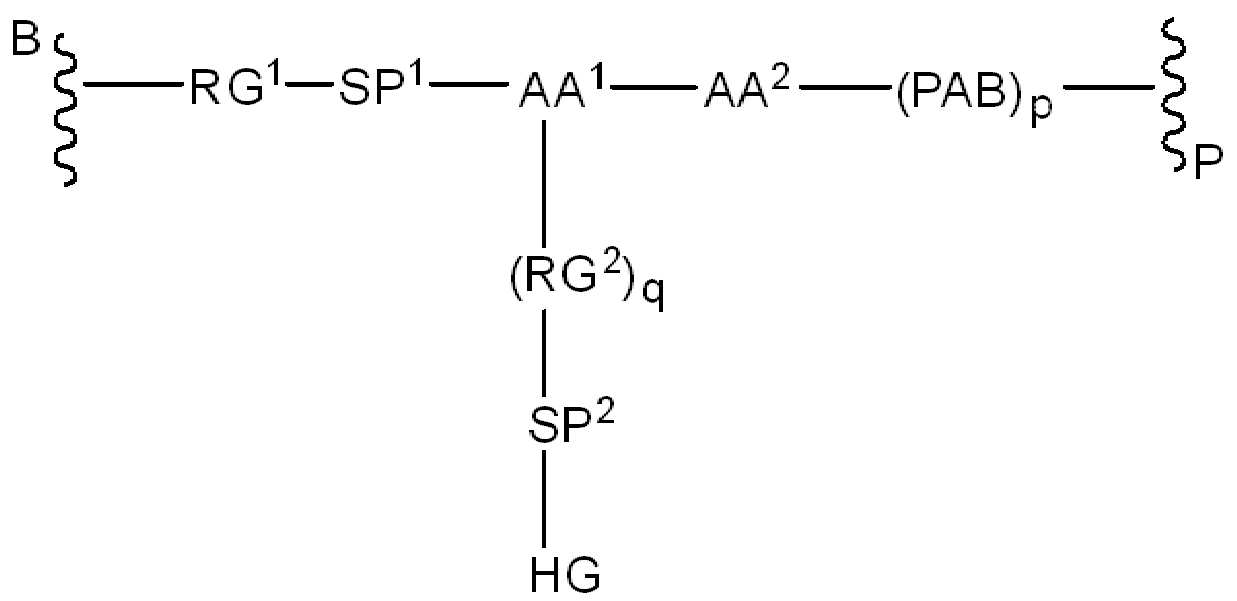
화학식 (II)에서, BA는 결합제이고; LL은 3가 링커(linker)이고; RG1 및 RG2는 반응성 그룹 잔기이고; SP1 및 SP2는 각각 독립적으로, 각 경우에, 존재하지 않거나, 또는 스페이서기 잔기이고; HG은 친수성 잔기이고; PA는 페이로드 잔기이며; 아래첨자아래 첨자 n은 1내지 30의 정수이며; 및 아래첨자아래 첨자 q는 0 또는 1이다.
일부 경우에, 하나 이상의 3가 링커(LL)가 존재할 수 있다. 일부 경우에, n은 1 내지 4의 정수이다. 일부 경우에, n은 1이다. 일부 경우에, n은 2이다. 일부 경우에, n은 3이다. 일부 경우에, n은 4이다. 일부 경우에, HG는 말단친수성기 이다. 일부 경우에, HG는 하나의 말단설폰산기(SO3H) 또는 그의 염을 포함한다. 다른경우에, HG는 하나 이상의 말단 선폰산기 또는 그의 염을 포함한다. 일부 경우에, HG는 하나의 말단타우린기 또는 그의 염을 포함한다. 다른 경우에, HG는 하나 이상의 말단타우린기 또는 이의 염을 포함한다. 일부 경우에, HG는 하나의 말단포스폰산기(PO3H) 또는 그의 염을 포함한다. 다른 경우에, HG는 하나 이상의 말단포스폰산기 또는 그의 염을 포함한다. 일부 경우에, HG는 하나의 말단 아민기 또는 그의 염을 포함한다. 다른 경우에, HG는 하나 이상의 말단아민기 또는 그의 염을 포함한다. 추가의 예에서, HG는 하나의 말단 4급 아민기 또는 그의 염을 포함한다. 추가의 예에서, HG는 하나 이상의 말단 4급 아민기 또는 기의 염을 포함한다. 일부 경우에, HG는 하나의 말단 당기(sugar group) 또는 그의 염을 포함한다. 다른 경우에, HG는 하나 이상의 말단 당기 또는 그의 염을 포함한다.
일부 경우에, 화학식 (I) 또는 화학식(II)의 화합물은 아래 첨자 n 이 1, 2, 3 또는 4인 화합물의 혼합물을 포함한다. 일부 경우에, 화학식 (I) 또는 화학식(II)의 화합물은 아래 첨자 n이 2인 화합물의 혼합물을 포함한다. 일부 경우에, 화학식 (I) 또는 화학식 (II)의 화합물은 아래 첨자 n이 4인 화합물의 혼합물을 포함한다.
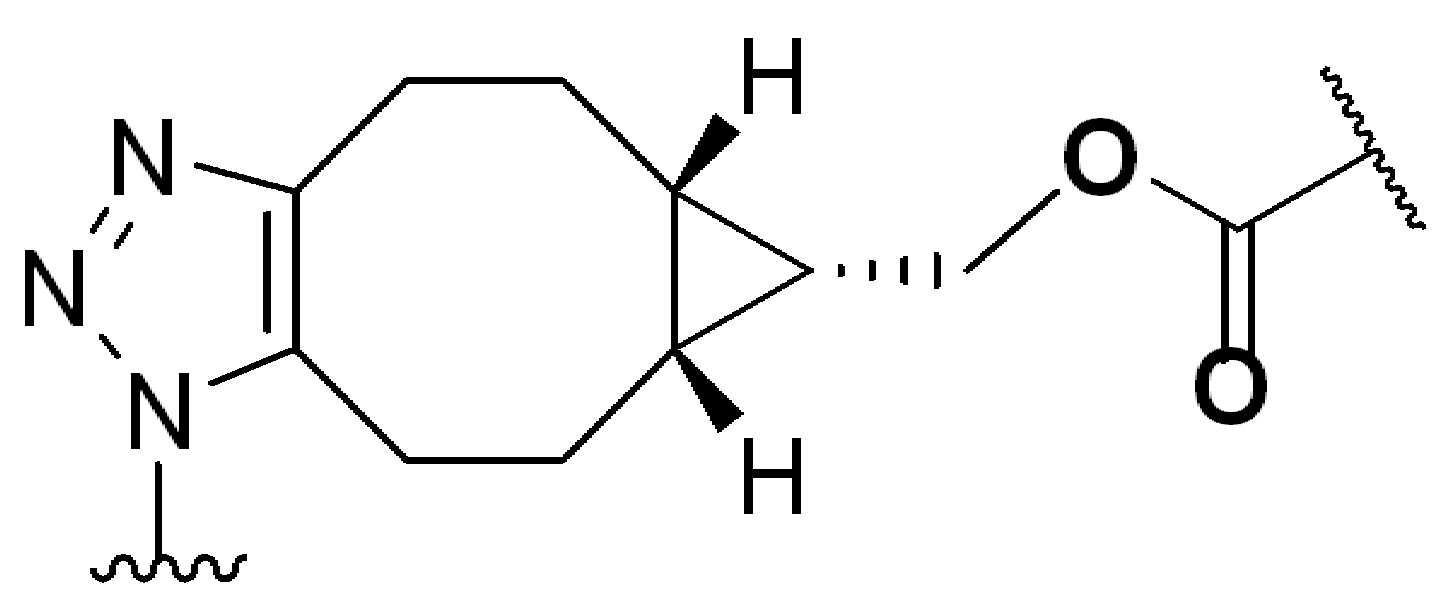
일 예에서, 화학식 (I)의 화합물은 하기 화학식 (III)에 따른다:
여기서
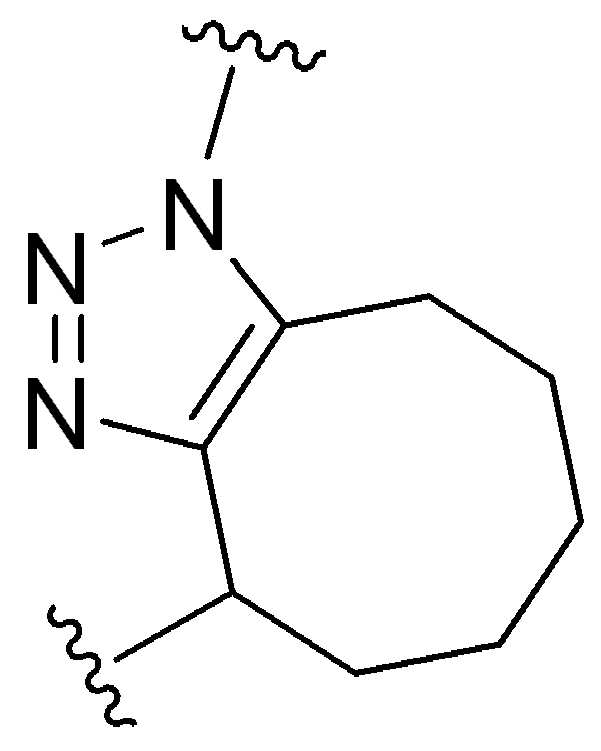
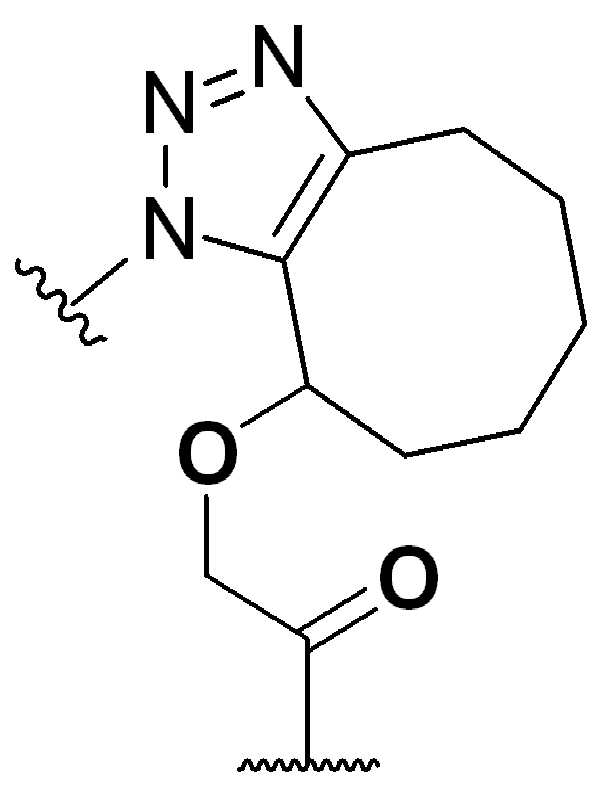
고리A는 트리아졸에 융합되고 시클로알킬(cycloalkyl), 시클로알케닐(cycloalkenyl), 헤테로시클로알킬(heterocycloalkyl), 및 헤테로시클로알케닐(heterocycloalkenyl)로 이루어진 군으로부터 선택되고;
여기서 시클로알킬(cycloalkyl), 시클로알케닐(cycloalkenyl), 헤테로시클로알킬(heterocycloalkyl), 및 헤테로시클로알케닐(heterocycloalkenyl)은 알킬, -OH, 또는 -NRaRb로 선택적으로 치환되며, 여기서 Ra 및 Rb는 각각 알킬 또는 H이다.
다른 예에서, 화학식 (I)의 화합물은 하기 화학식 (IV)에 따른다:
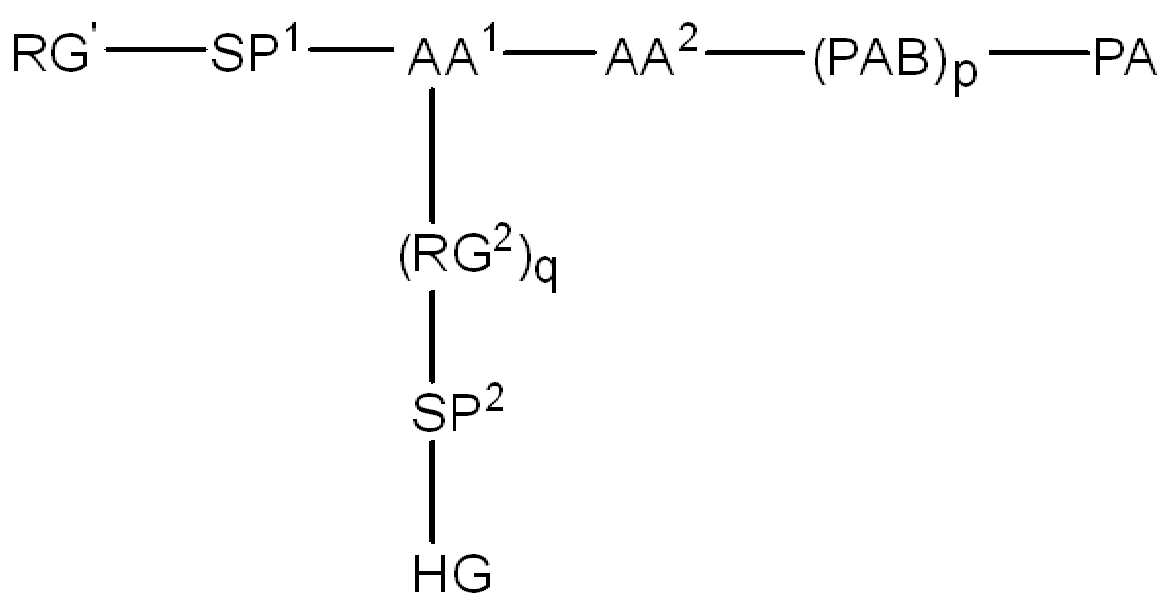
(IV).
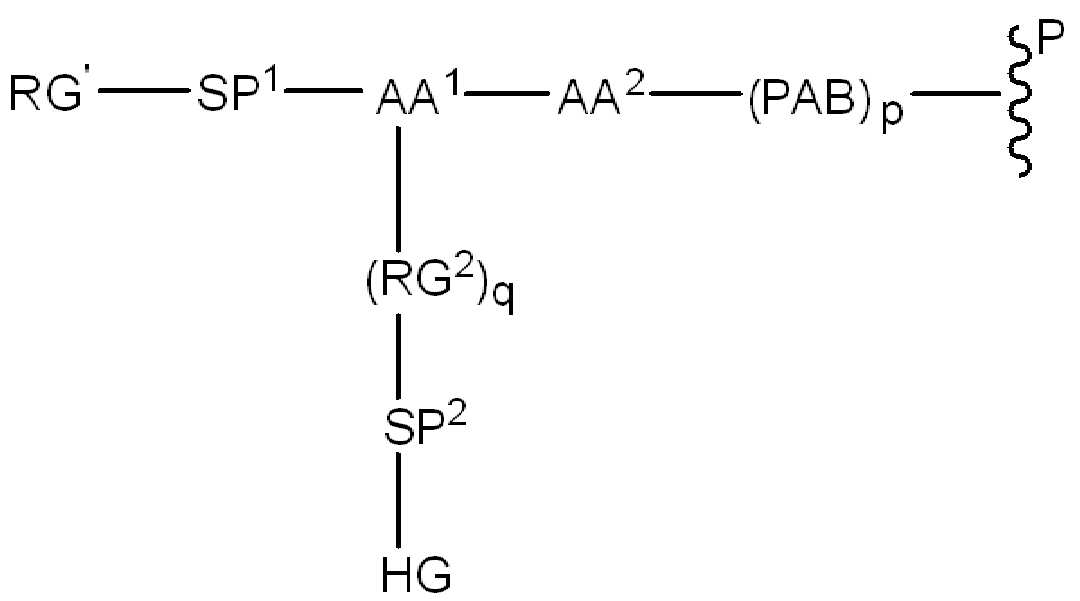
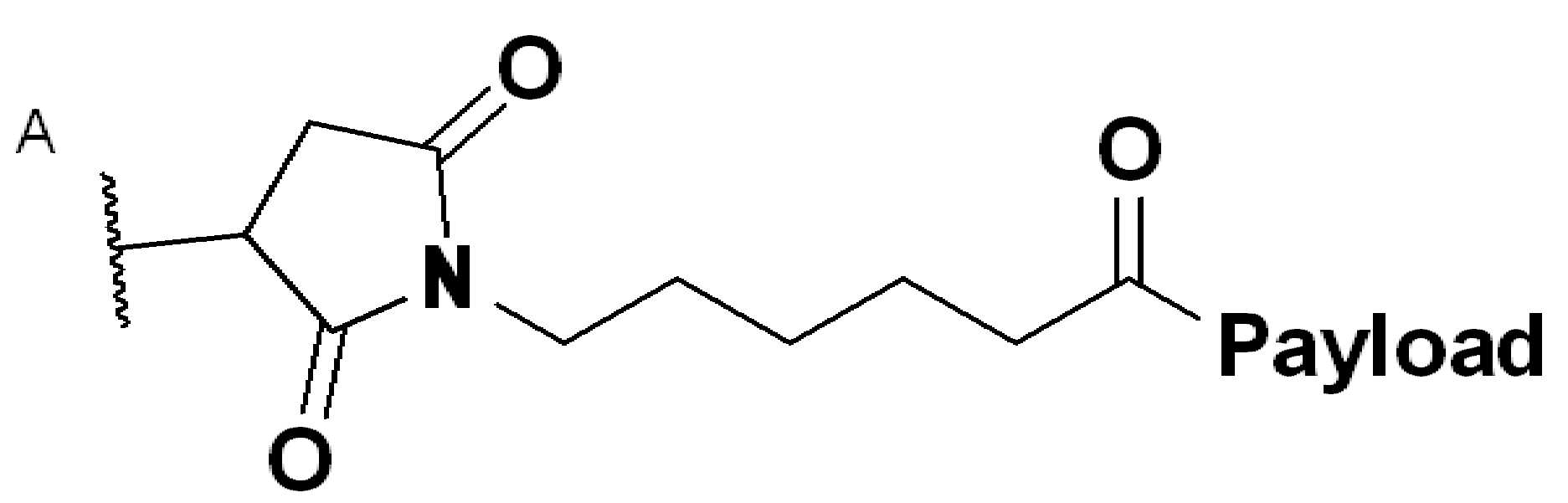
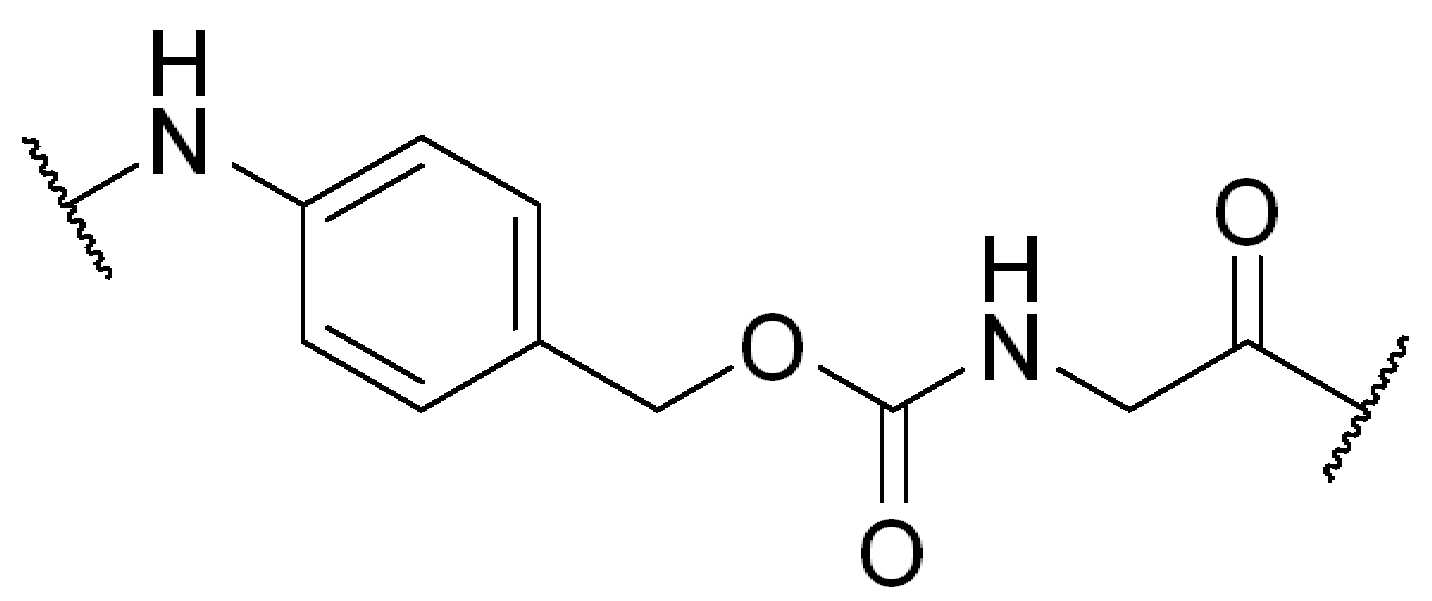
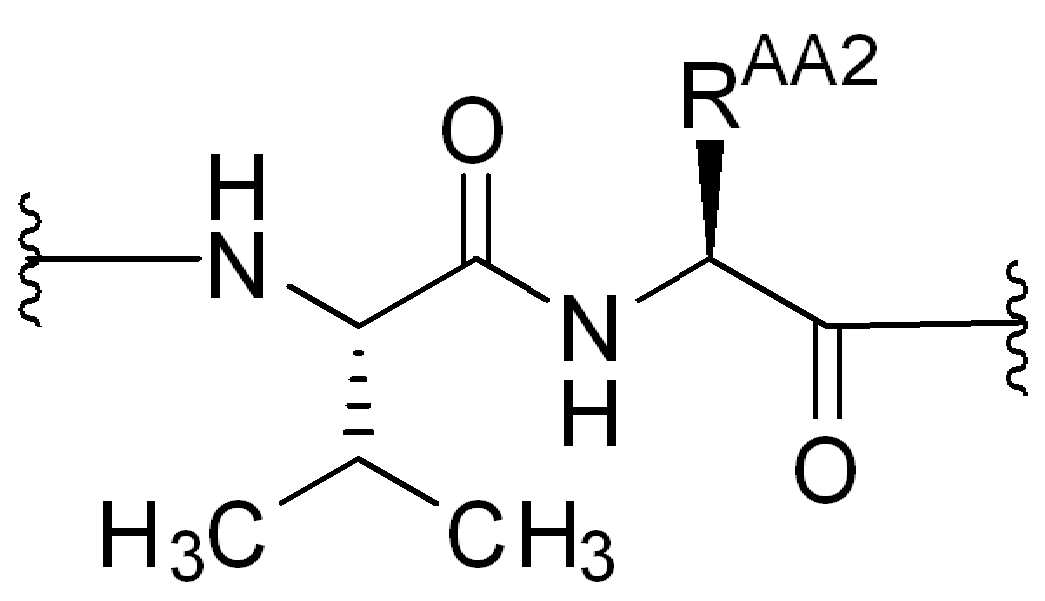
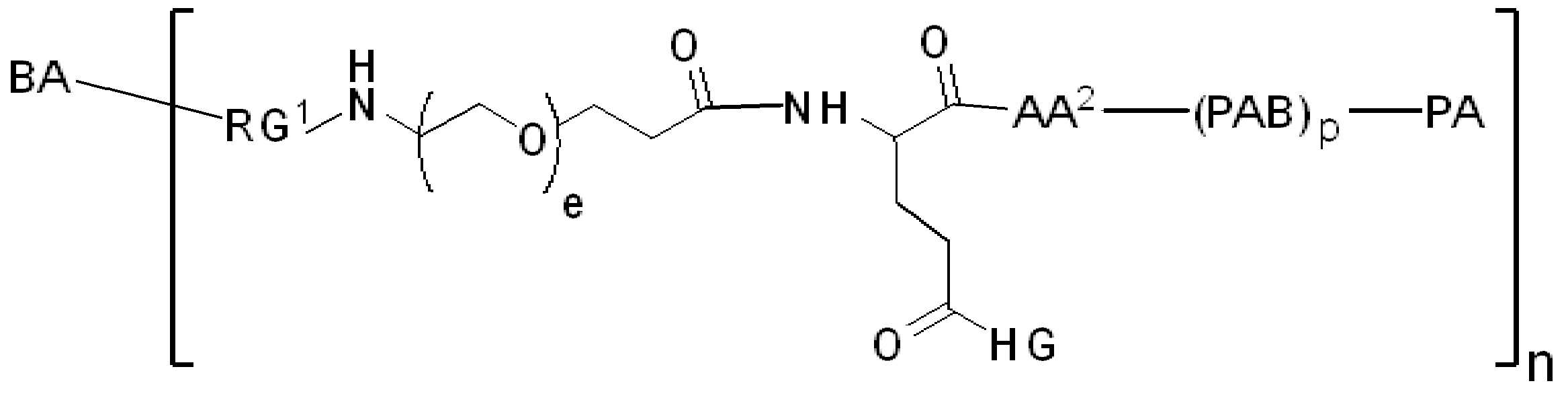
화학식 (IV)에서, BA, RG1, SP1, RG2, SP2, 및 HG는 상기 정의된 바와 같고, AA1은 아미노산 잔기를 포함하는 3가 링커이고, 항체, 페이로드 및 친수성기에 직접 또는 간접적으로 연결되어 있다; AA2는 디펩티드, AA2는 디펩티드(dipeptide), 트리펩티드(tripeptide), 또는 테트라펩티드잔기(tetrapeptide residue)이고; 및 PAB는 이고, 여기서 는 PAB가 화학식에서 인접기에 결합되는 원자를 나타내고; 아래 첨자 p는 0 또는 1이며; 아래 첨자 q는 0 또는 1이다.
일부 예에서, 아래첨자 p는 0이고 아래 첨자 q는 0이다. 어떤 경우에는, 아래 첨자 p는 1이며; 아래첨자 q는 0이다. 어떤 경우에는, 아래 첨자 p는 0이며; 아래 첨자 q는 1이다. 어떤 경우에는, 아래 첨자 p는 1이며, 아래 첨자 q는 1이다. 일부 경우에 SP1 은 0-5폴리에틸렌글리콜(PEG)잔기를 포함한다. 일부 경우에 SP2는 0 내지 5개의 PEG잔기를 포함한다. 일부 예에서, SP2는 0 내지 5개의 PEG잔기를 포함한다. 일부 예에서, SP1은 독립적으로, 각 경우에, C1-6알킬렌, -NH-, -C(O)-, (-CH2-CH2-O)e, -NH-CH2-CH2-(-O-CH2-CH2)e-C(O)-, -C(O)-(CH2)u-C(O)-, -C(O)-NH-(CH2)v-, 폴리글리신(polyglycine) (예를 들어, ((글리신)4-세린)f(((glycine)4-serine) f )으로 이루어진 군으로부터 선택되고, 여기서 아래 첨자 f는 1 내지 6의 정수이고, 아래 첨자 e는 0 내지 4의 정수이고, 아래 첨자 u는 1 내지 8의 정수이고, 첨자 v는 1 내지 8의 정수이다. 일부 예에서, 일부 예에서, SP2는 각각의 경우에 독립적으로 C1-6 알킬렌, NH-, -C(O)-, (-CH2-CH2-O)e, -NH-CH2-CH2-(-O-CH2-CH2)e-C(O)-, -C(O)-(CH2)u-C(O)-, -C(O)-NH-(CH2)v-, 폴리글리신(polyglycine) (예를 들어, ((글리신)4-세린)f(((glycine)4-serine) f )로 이루어진 군으로부터 선택되고, 여기서 아래첨자 e는 0 내지 4정수 이고, NH-, -C(O)-, (-CH2-CH2-O)e, -NH-CH2-CH2-(-O-CH2-CH2)e-C(O)-, -C(O)-(CH2)u-C(O)-, -C(O)-NH-(CH2)v-, 폴리글리신(polyglycine) (예를 들어, ((글리신)4-세린)f(((glycine)4-serine) f ) 으로 이루어진 군으로부터 선택되고, 아래 첨자 f는 1 내지 6의 정수이며, 이들의 조합이고, 여기서 아래 첨자 e는 0 내지 4의 정수이고, 아래 첨자 u는 1 내지 8의 정수이고, 아래 첨자 v는 1 내지 8의 정수이다.
일부 예에서, AA1 또는 AA2 중 어느 하나는 각각의 경우 독립적으로 알라닌, 발린, 류신, 이소류신, 메티오닌, 트립토판, 페닐알라닌, 프롤린, 세린, 트레오닌, 시스테인, 티로닌, 아스파라긴, 글루타민, 아스파르트 산, 글루탐산, 리신, 아르기닌, 히스티딘 또는 시트룰린, 이의 유도체 또는 이들의 조합이다.
특정 실시양태에서, AA1은 알라닌, 발린, 류신, 이소류신, 메티오닌, 트립토판, 페닐알라닌, 프롤린, 글리신, 세린, 트레오닌, 시스테인, 티로신, 아스파라긴, 글루타민, 아스파르트산, 글루탐산, 리신, 아르기닌, 히스티딘 또는 시트룰린, 이의 유도체 또는 이들의 조합으로부터 선택된 아미노산이다.
특정 실시양태에서, AA1은 페이로드, 결합제(예를 들어, 항체 또는 항원 결합 단편), 및 친수성기를 포함하는 링커, 예를 들어 리신, 아스파르긴, 글루탐산, 아스파르트산, 글루타민, 시스테인, 트레오닌, 세린 또는 티로신에 연결하기 위한 3개의 작용기를 갖는 아미노산이다.
특정 실시 양태에서, AA 1 는 리신 또는 리신의 유도체이다. 특정 실시 양태에서, AA 1 은 L-리신이다. 특정 실시 양태에서, AA 1 은 D-리신이다. 특정 실시 양태에서, AA 1 은 글루타민이다. 특정 실시 양태에서, AA 1 은 글루탐산이다. 특정 실시 양태에서, AA 1 은 아스파르트산이다. 특정 실시 양태에서, AA 2 은 발린-시트룰린이다. 일부 구체예에서, AA 2 은 시트룰린-발린이다. 일부 구체예에서, AA 2 는 발린-알라닌이다. 일부 구체예에서, AA 2 는 알라닌-발린이다. 일부 구체예에서, AA 2 는 발린-글리신이다. 일부 구체예에서, AA 2 는 글리신-발린이다. 일부 구체예에서, AA 1 -AA 2 는 글루타민-발린-시트룰린이다. 일부 구체예에서, AA 1 -AA 2 는 리신-발린-시트룰린이다. 일부 구체예에서, AA 1 -AA 2 는 리신-발린-알라닌이다. 일부 구체예에서, AA 1 -AA 2 는 글루타민-발린-알라닌이다. 특정 실시 양태에서, ((글리신)4-세린) f 은 (글리신)4-세린이다.
일부 예에서, 화학식 (I) 또는 화학식 (II) 또는 화학식(III) 또는 화학식 (IV)의 화합물은 하기 화학식 (IVa), 화학식 (IVb), 화학식 (IVc)에 따른다:
화학식 (IVa), 화학식 (IVb), 및 화학식 (IVc)에서, BA, RG 1 , SP 1 , RG 2 , SP 2 , HG 및 아래 첨자 p는 상기 정의된 바와 같고, AA1은 아미노산 잔기를 포함하고 항체, 페이로드 및 친수성기에 직접 또는 간접적으로 연결된 3가 링커이고; AA2는 디펩티드, 트리펩티드, 또는 테트라 펩티드 잔기이고; PAB는 이고, 여기서 는 PAB가 화학식에서 인접한기에 결합되는 원자를 나타낸다. 어떤 경우에, 아래 첨자 p는 0이다.
어떤 경우에, 아래첨자 p는 1이다. 일부 경우에 SP1은 0-5폴리에틸렌 글리콜(PEG)잔기를 포함한다. 일부 경우에 SP2는 0내지 5개의 PEG잔기를 포함한다. 일부 예에서, SP1은 독립적으로, 각 경우에, C1-6 알킬렌(alkylene), -NH-, -C(O)-, (-CH2-CH2-O)e, -NH-CH2-CH2-(-O-CH2-CH2)e-C(O)-, -C(O)-(CH2)u-C(O)-, -C(O)-NH-(CH2)v-, 폴리글리신(polyglycine) (예를 들어, ((글리신)4-세린)f(((glycine)4-serine) f )으로 이루어진 군으로부터 선택되고, 여기서 아래 첨자 f는 1 내지 6의 정수이고, 아래 첨자 e는 0 내지 4의 정수이고, 아래 첨자 u는 1 내지 8의 정수이고, 아래 첨자 v는 1 내지 8의 정수이다. 일부 예에서, SP2는 독립적으로, 각 경우에, C1-6 알킬렌(alkylene), -NH-, -C(O)-, (-CH2-CH2-O)e, -NH-CH2-CH2-(-O-CH2-CH2)e-C(O)-, -C(O)-(CH2)u-C(O)-, -C(O)-NH-(CH2)v-, 폴리글리신(polyglycine) (예를 들어, ((글리신)4-세린)f(((glycine)4-serine) f )으로 이루어진 군으로부터 선택되고, 여기서 아래 첨자 f는 1 내지 6의 정수이고, 아래 첨자 e는 0 내지 4의 정수이고, 아래 첨자 u는 1 내지 8의 정수이고, 아래 첨자 v는 1 내지 8의 정수이다.
일부 예에서, AA1 또는 AA2중 어느 하나는 각각의 경우 독립적으로 알라닌, 발린, 류신, 이소류신, 메티오닌, 트립토판, 페닐알라닌, 프롤린, 세린, 트레오닌, 시스테인, 티로신, 아스파라긴, 글루타민, 아스파라트산, 글루탐산, 리신, 아르기닌, 히스티딘 또는 시트룰린, 이의 유도체 또는 이들의 조합이다. 특정 실시양태에서, AA1은 알라닌, 발린, 류신, 이소류신, 메티오닌, 트립토판, 페닐알라닌, 프롤린, 글리신, 세린, 트레오닌, 시스테인, 티로신, 아스파라긴, 글루타민, 아스파르트산, 글루탐산, 리신, 아르기닌, 히스티딘 또는 시트룰린, 이의유도체 또는 이들의 조합으로부터 선택된 아미노산이다. 특정 실시양태에서 AA1은 리신이다. 특정 실시양태에서 AA1은 페이로드, 결합제(예를 들어, 항체 또는 항원 결합 단편), 및 친수성기, 예를 들어 리신, 아스파르긴, 글루탐산, 아스파르트산, 글루타민, 시스테인, 트레오닌, 세린 또는 티로신을 포함하는 링커에 연결하기 위한 3개의 작용기를 갖는 아미노산이다. 특정 실시양태에서, AA1은 리신 또는 리신의 유도체이다. 특정 실시양태에서, AA1은 L-리신이다. 특정 실시양태에서, AA1은 D-리신이다. 특정 실시양태에서, AA1은 글루타민이다. 특정 실시양태에서, AA1은 글루탐산이다. 특정 실시양태에서, AA1은 아스파르트산이다. 특정 실시양태에서, AA2는 발린-시트룰린이다. 일부 실시양태에서, AA2는 시트룰린-발린이다. 일부 실시양태에서, AA2는 발린-알라닌이다. 일부 실시양태에서, AA2는 알라닌-발린이다. 일부 실시양태에서, AA2는 발린-글리신이다. 일부 실시양태에서, AA2는 글리신-발린이다. 일부 실시양태에서, AA1-AA2는 글루타민-발린-시트룰린이다. AA1-AA2는 리신-발린-시트룰린이다. AA1-AA2는 리신-발린-알라닌이다. 특정 실시양태에서, ((글리신)4-세린)f는 (글리신)4-세린이다.
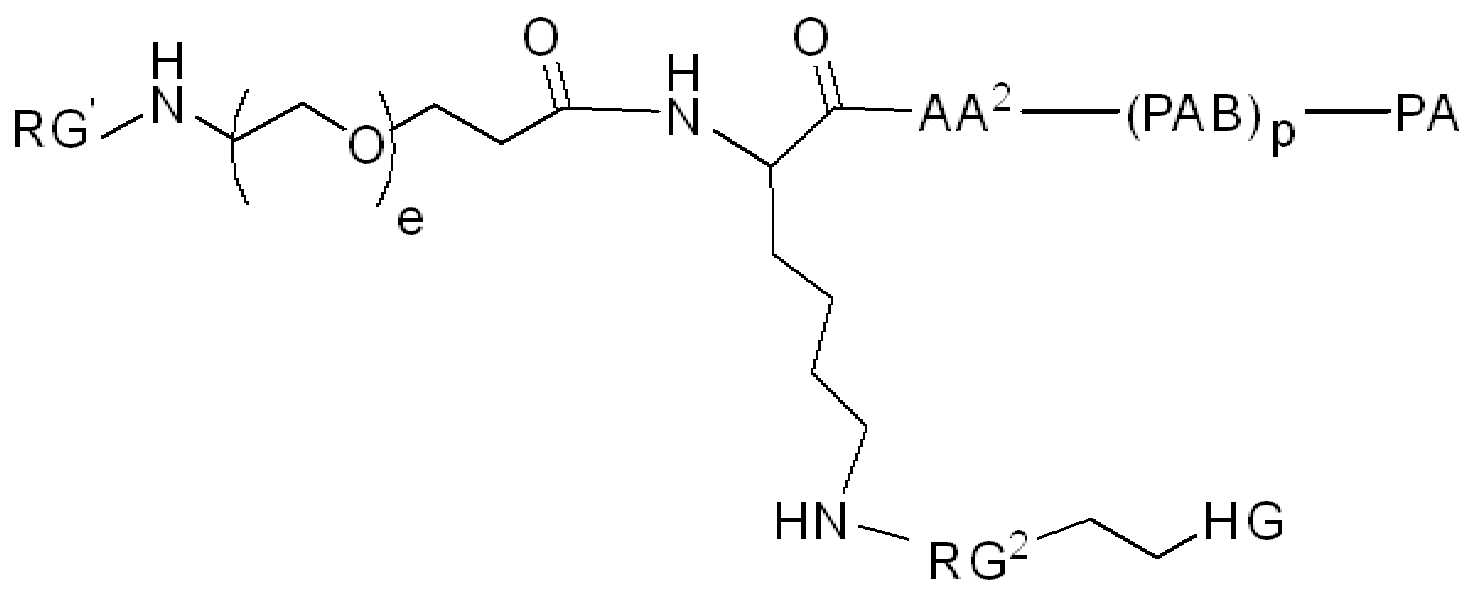
일부 예에서, 화학식(I), 또는 화학식 (II) 또는 화학식 (III) 또는 화학식 (IV)의 화합물은 각각 화학식 (Va), (Vb), (Vc) 또는 (Vd)에 따른다:
화학식 (Va), (Vb), (Vc), 및 (Vd)에서, BA, RG 1 , SP 1 , RG 2 , SP 2 , 및 HG는 상기 정의된 바와 같고, AA2는 디펩타이드, 트리 펩타이드 또는 테트라펩타이드잔기이고; PAB는 이고, 여기서 는 PAB가 화학식에서 인접기에 결합되는 원자를 나타내고; 아래 첨자 p는 0 또는 1이며, 아래 첨자 e는 각각의 경우에 독립적으로 0 내지 6의 정수, 또는 0 내지 5의 정수이다. 일부 경우에는 아래 첨자 p는 0이다. 일부 경우에는 아래 첨자 p는 1이다. 이들 예 중 임의의 것에서, 아래 첨자 e는 1, 2, 3 또는 4이다. 일부 예에서, 아래 첨자 e는 1이다. 일부 예에서, 첨자 e는 2이다. 일부 예에서, 첨자 e는 3이다. 일부 예에서, 첨자 e는 4이다. 일부 예에서, 첨자 e는 5이다. 일부 예에서, 첨자 e는 6이다.
일부 예에서, SP1은 독립적으로, 각 경우에, C1-6 알킬렌(alkylene), -NH-, -C(O)-, (-CH2-CH2-O)e, -NH-CH2-CH2-(-O-CH2-CH2)e-C(O)-, -C(O)-(CH2)u-C(O)-, -C(O)-NH-(CH2)v-, 폴리글리신(polyglycine) (예를 들어, ((글리신)4-세린)f(((glycine)4-serine) f )으로 이루어진 군으로부터 선택되고, 여기서 아래 첨자 f는 1 내지 6의 정수이고, 아래 첨자 e는 0 내지 4의 정수이고, 아래 첨자 u는 1 내지 8의 정수이고, 아래 첨자 v는 1 내지 8의 정수이다. 일부 예에서, SP2는 독립적으로, 각 경우에, C1-6 알킬렌(alkylene), -NH-, -C(O)-, (-CH2-CH2-O)e, -NH-CH2-CH2-(-O-CH2-CH2)e-C(O)-, -C(O)-(CH2)u-C(O)-, -C(O)-NH-(CH2)v-, 폴리글리신(polyglycine) (예를 들어, ((글리신)4-세린)f(((glycine)4-serine) f )으로 이루어진 군으로부터 선택되고, 여기서 아래 첨자 f는 1 내지 6의 정수이고, 아래 첨자 e는 0 내지 4의 정수이고, 아래 첨자 u는 1 내지 8의 정수이고, 아래 첨자 v는 1 내지 8의 정수이다.
일부 예에서, 임의의 AA2는 각각의 경우 독립적으로 알라닌, 발린, 류신, 이소류신, 메티오닌, 트립토판, 페닐알라닌, 프롤린, 세린, 트레오닌, 시스테인, 티로신, 아스파라긴, 글루타민, 아스파르트산, 글루탐산, 리신, 아르기닌, 히스티딘 또는 시트룰린, 이의유도체 또는 이들의 조합으로부터 선택된 아미노산이다. 특정 실시양태에서 AA2는 발린-시트룰린이다. 일부 실시양태에서, AA2는 시트룰린-발린이다. 일부 실시양태에서, AA2는 발린-알라닌이다. 일부 실시양태에서, AA2는 알라닌-발린이다. 일부 실시양태에서, AA2는 발린-글리신이다. 일부 실시양태에서, AA2는 길리신-발린이다. 특정 실시양태에서, ((글리신)4-세린)f는 (글리신)4-세린이다.
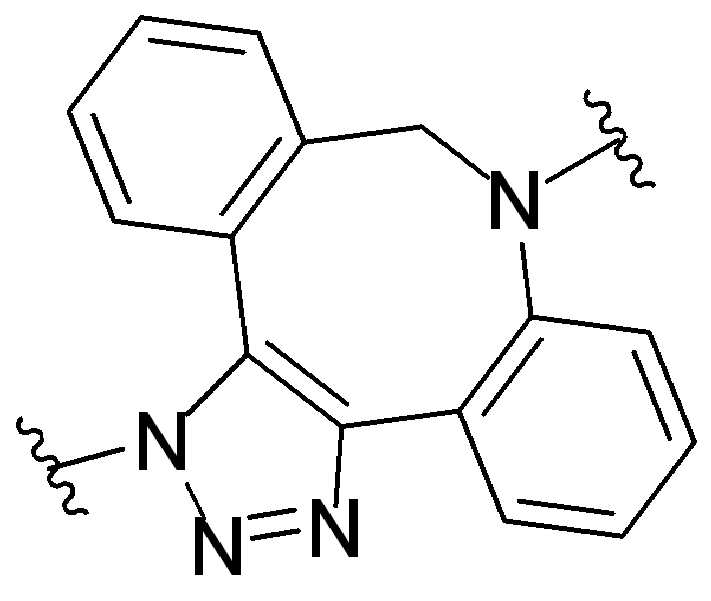
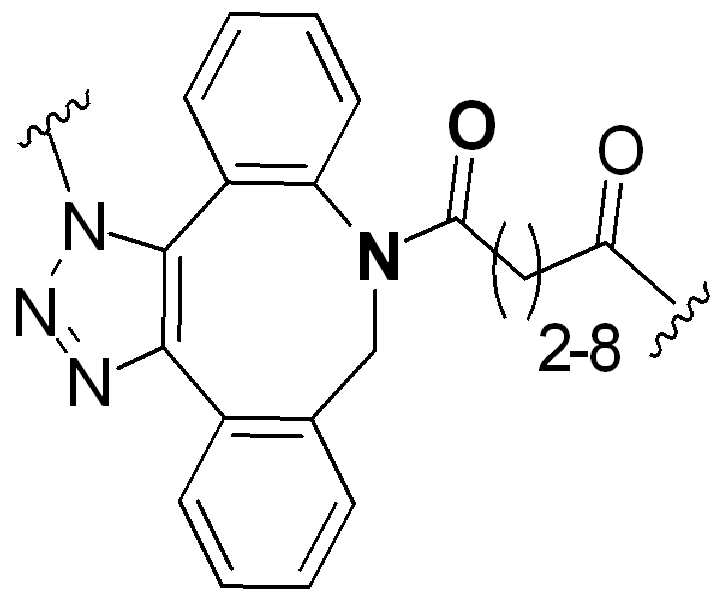
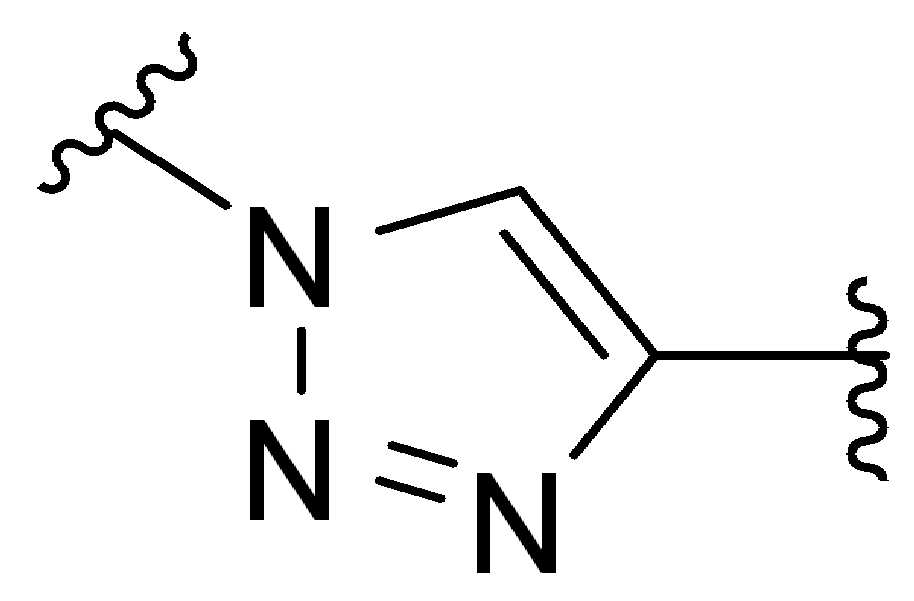
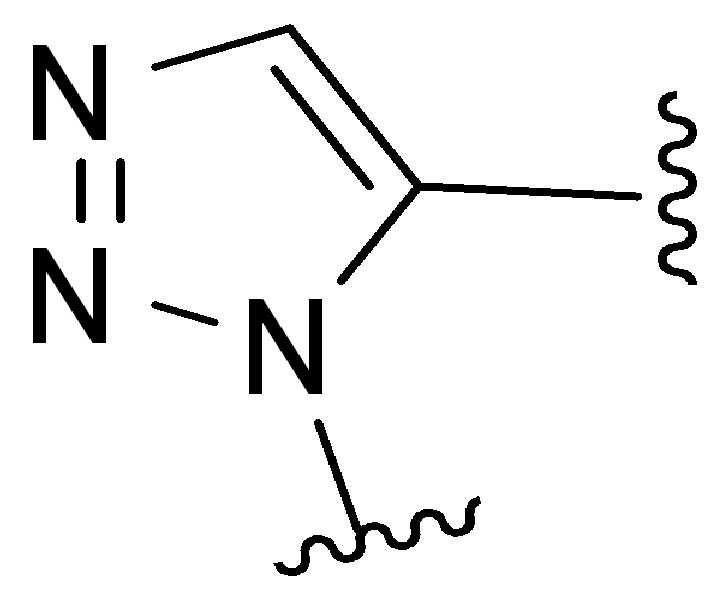
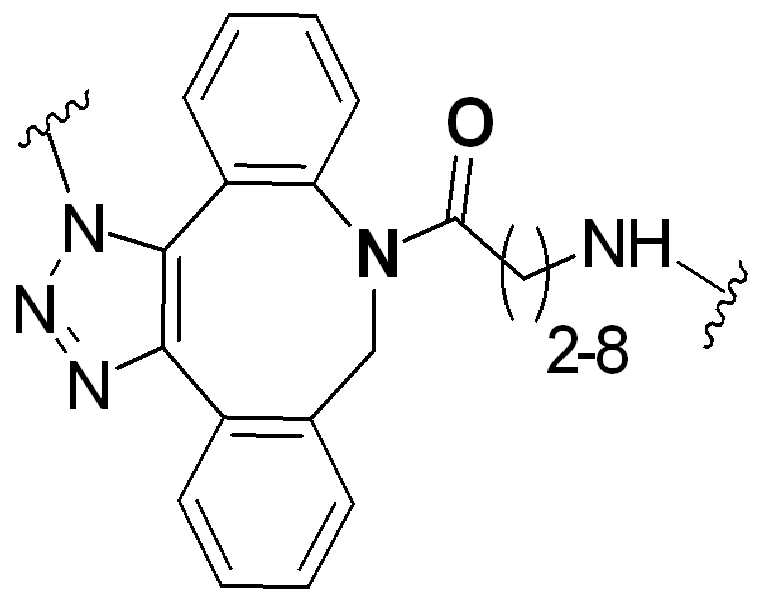
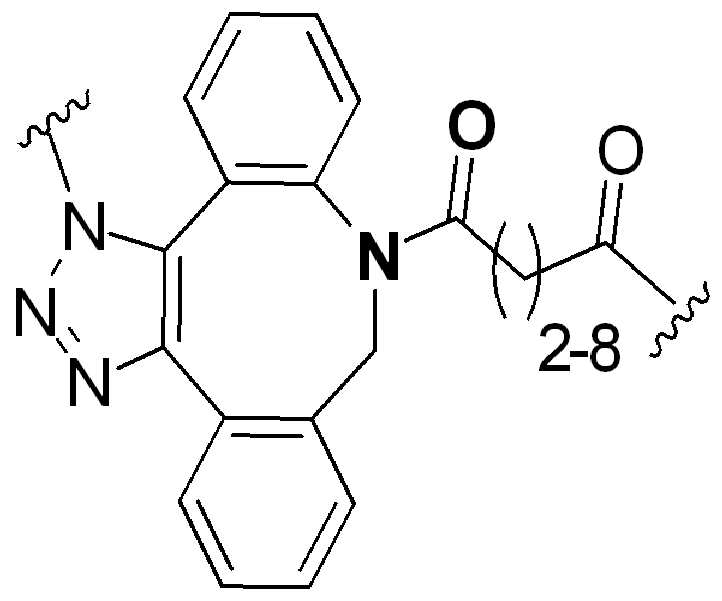
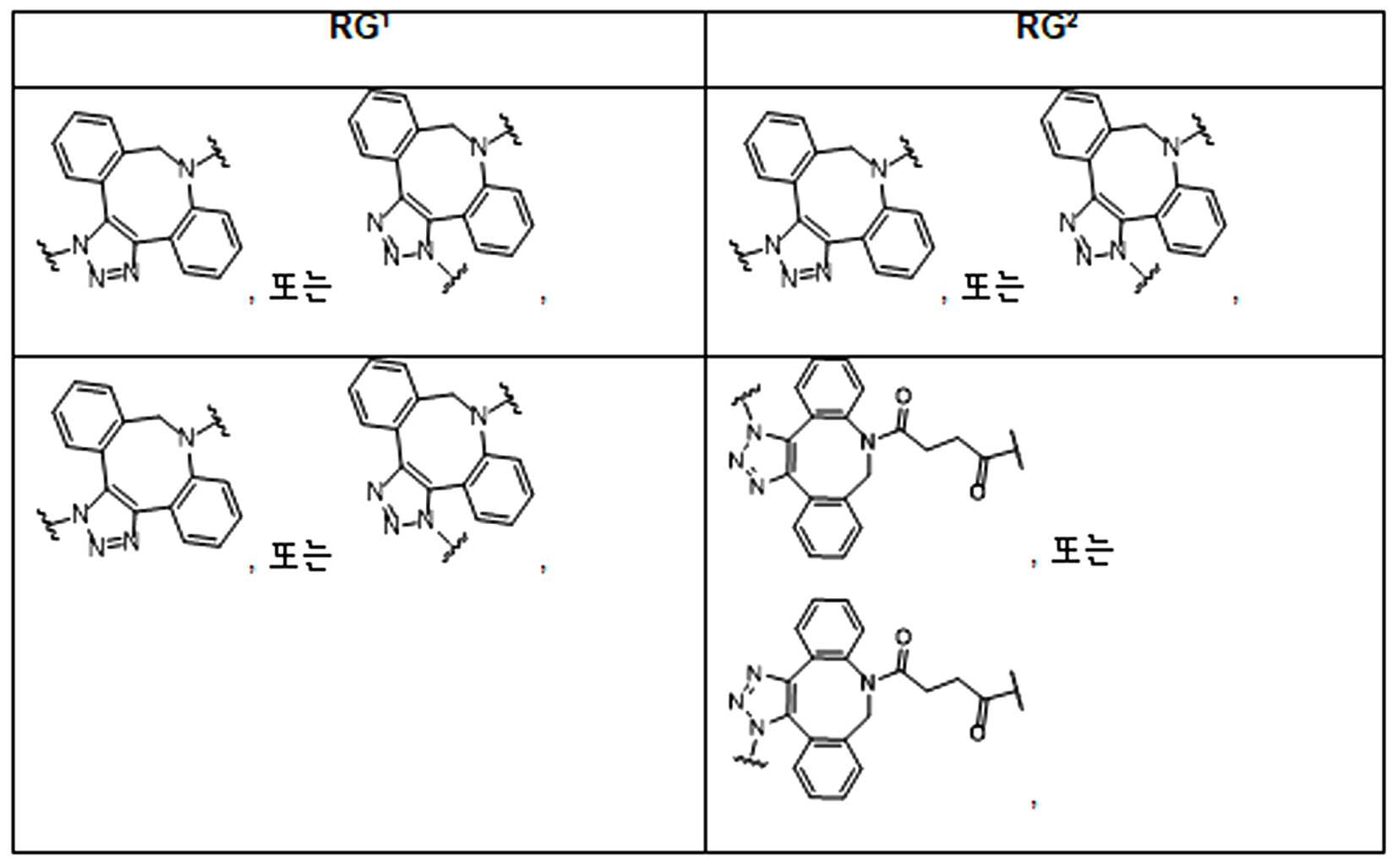
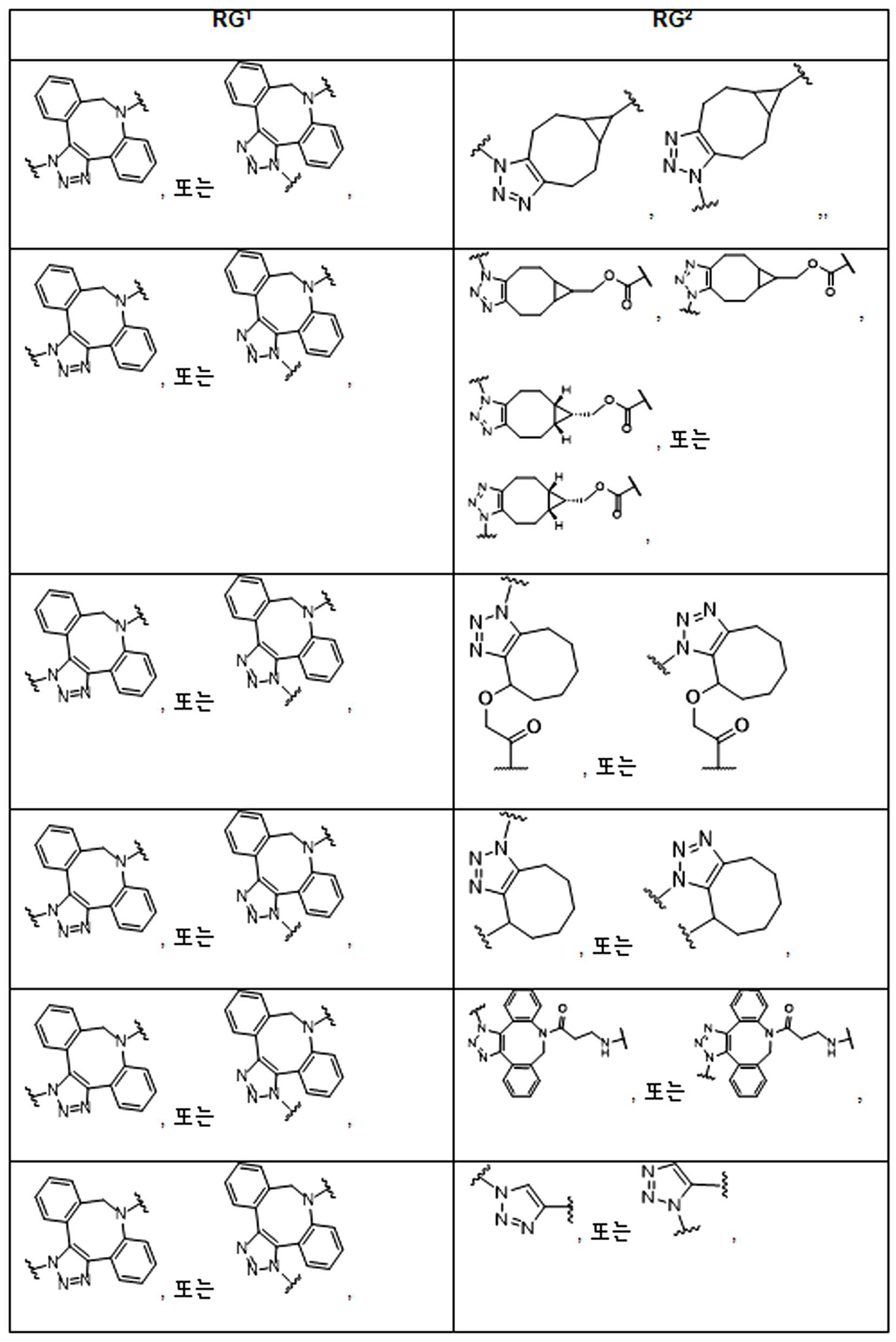
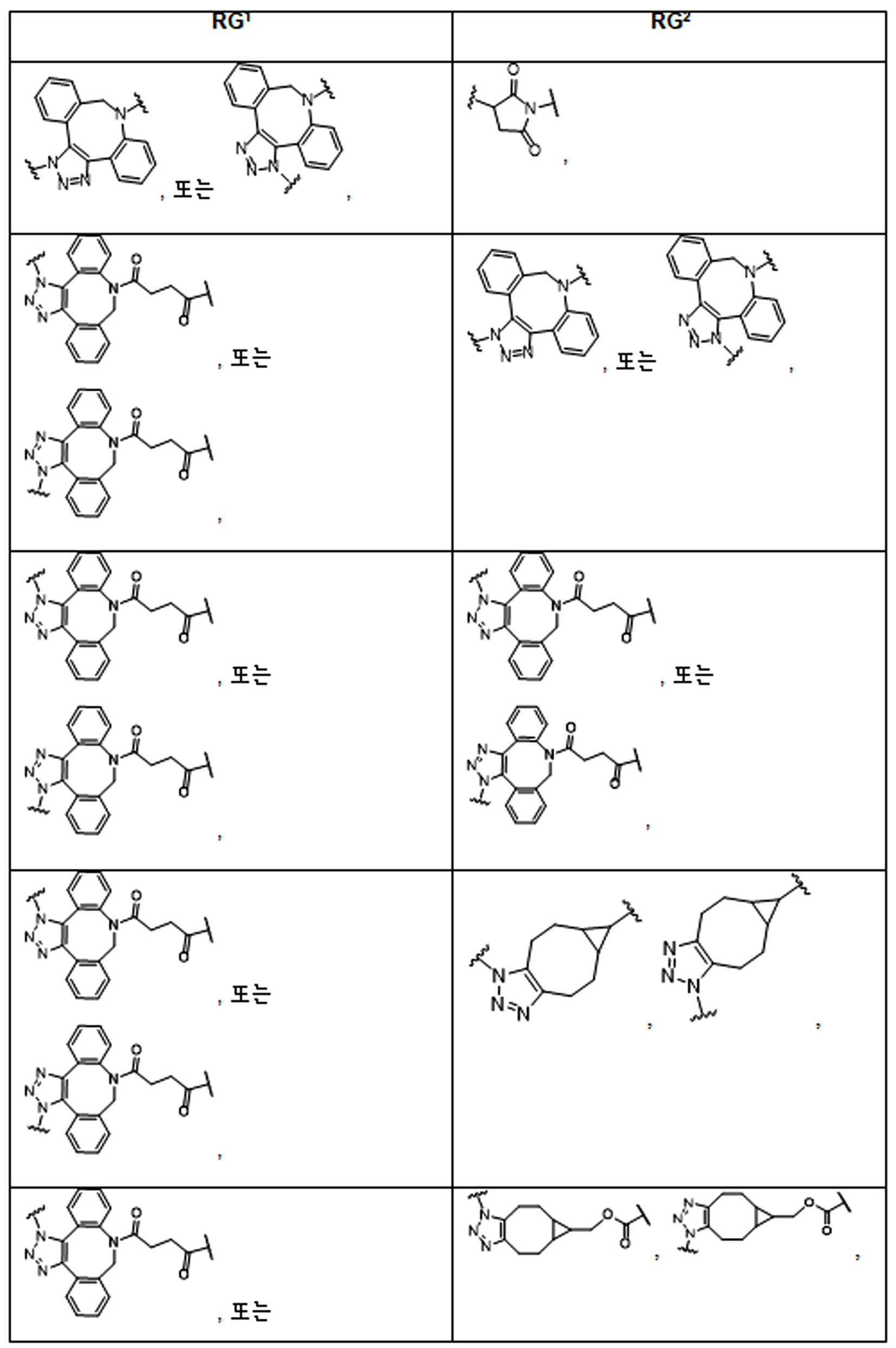
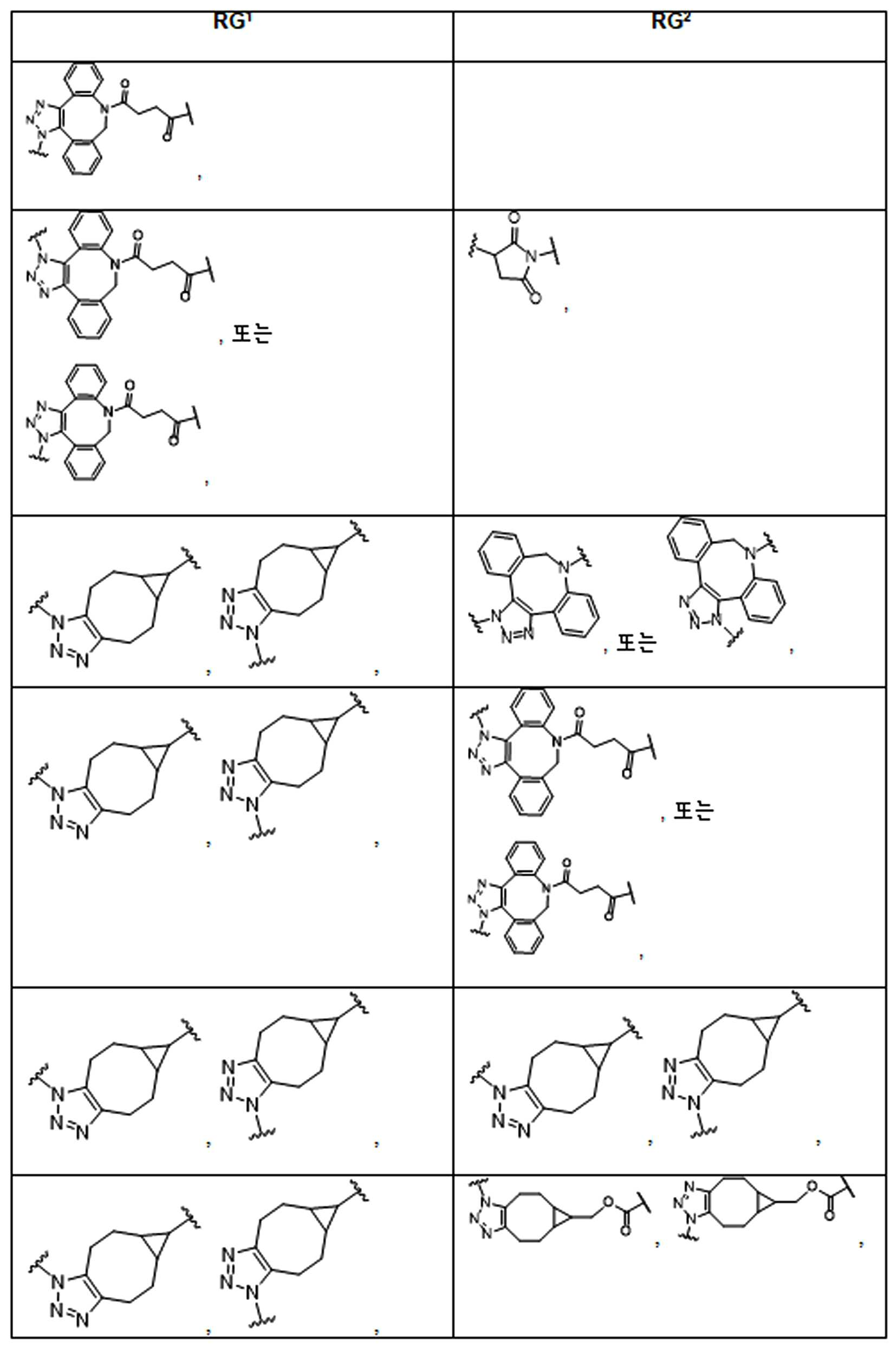
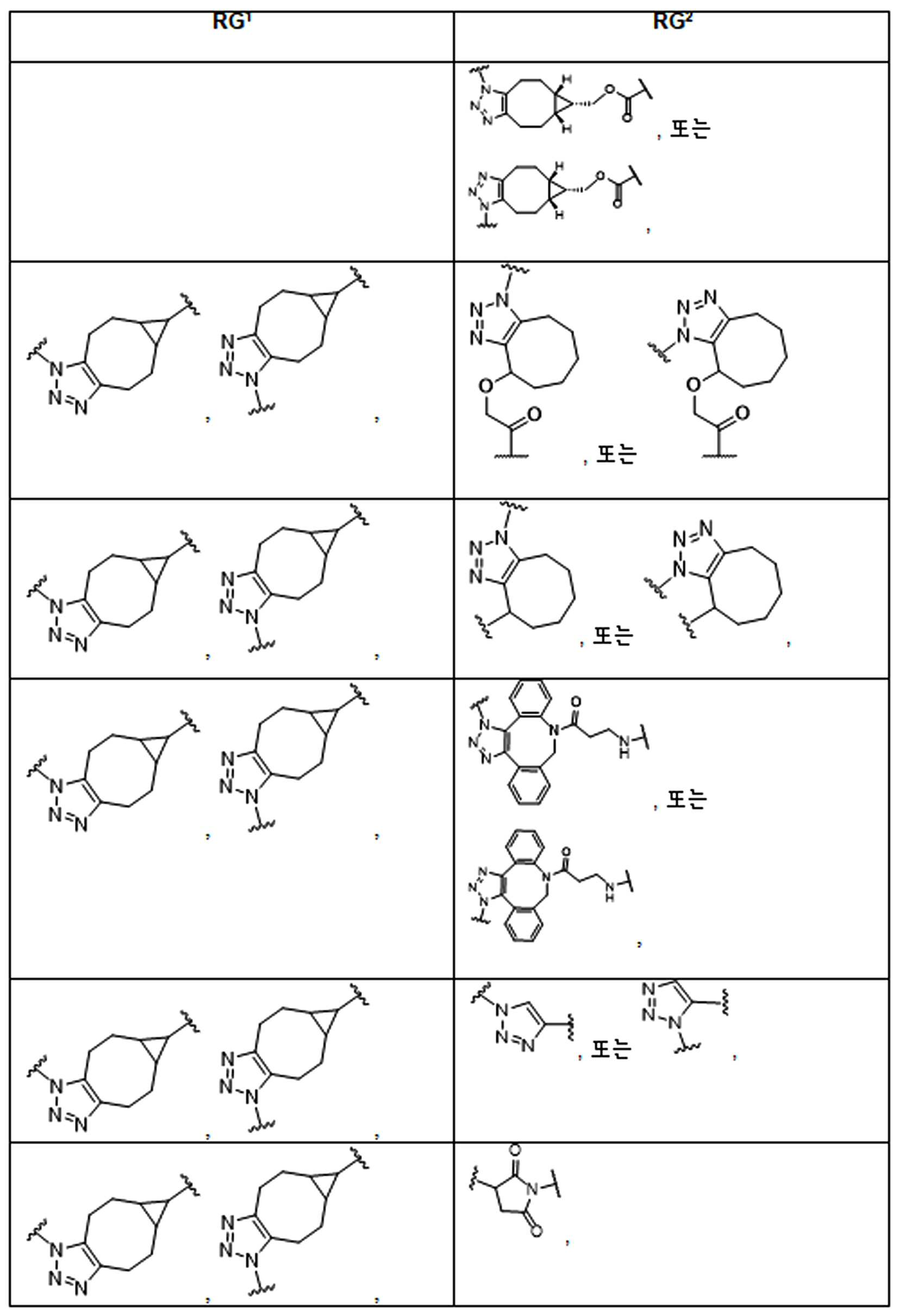
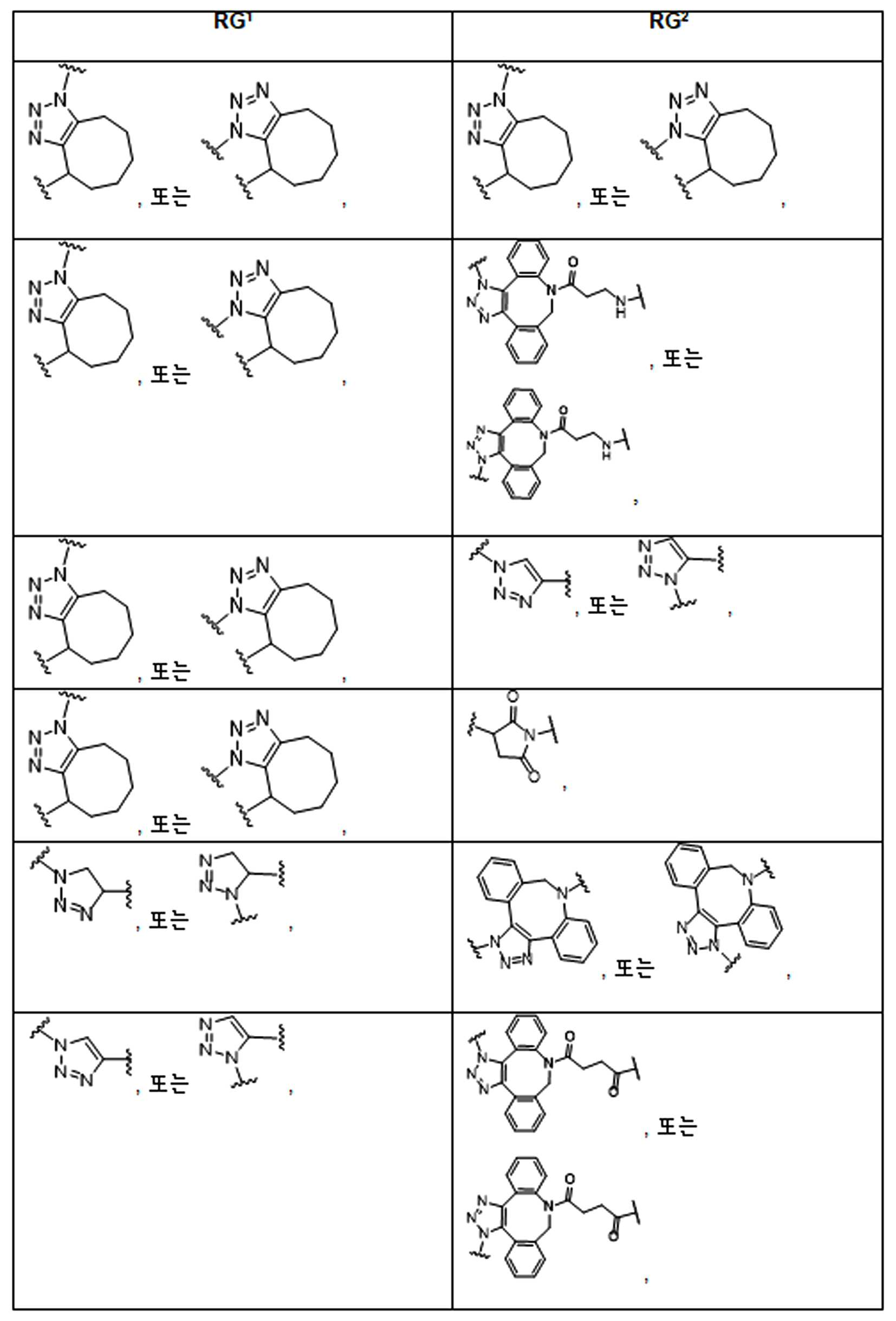
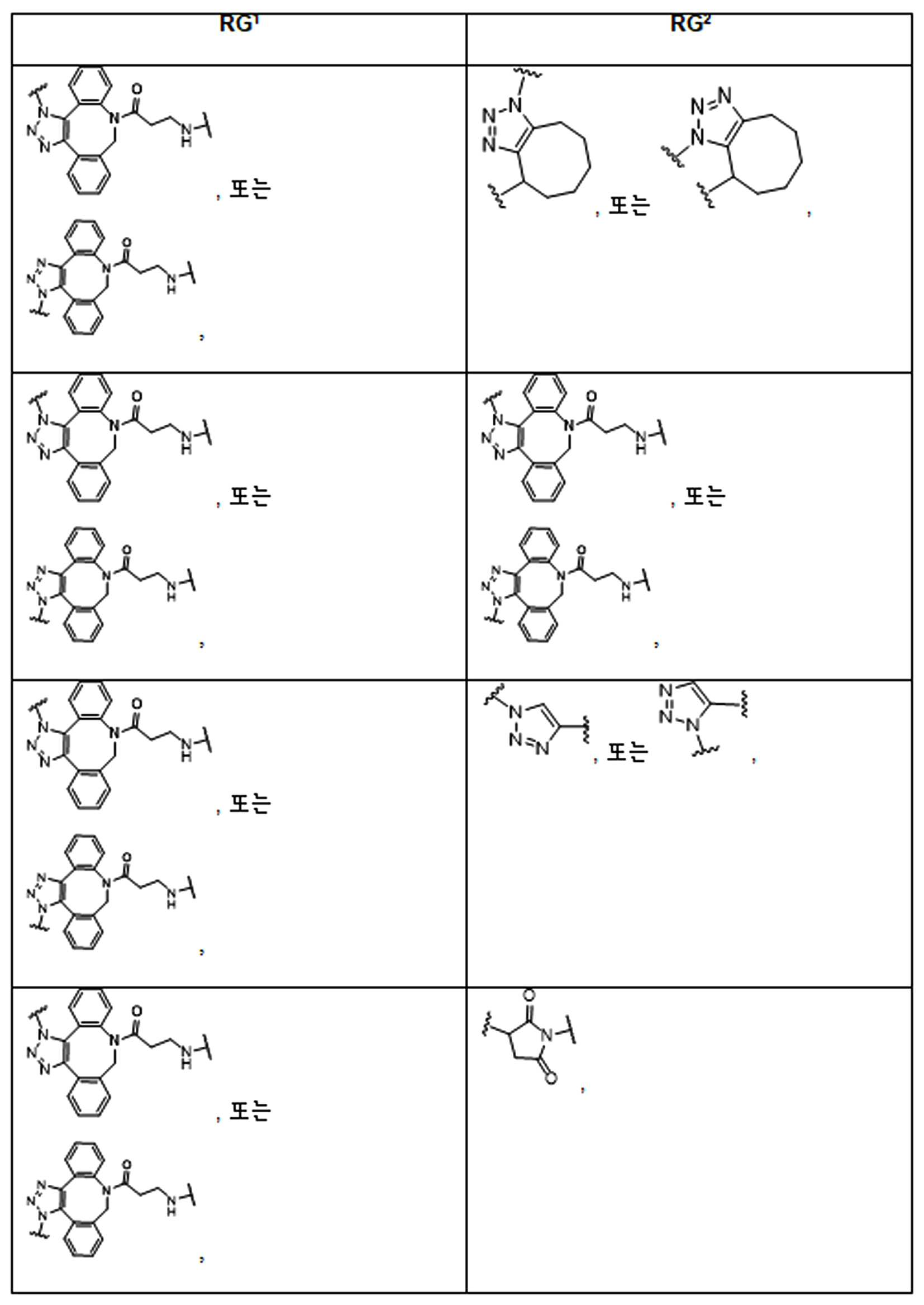
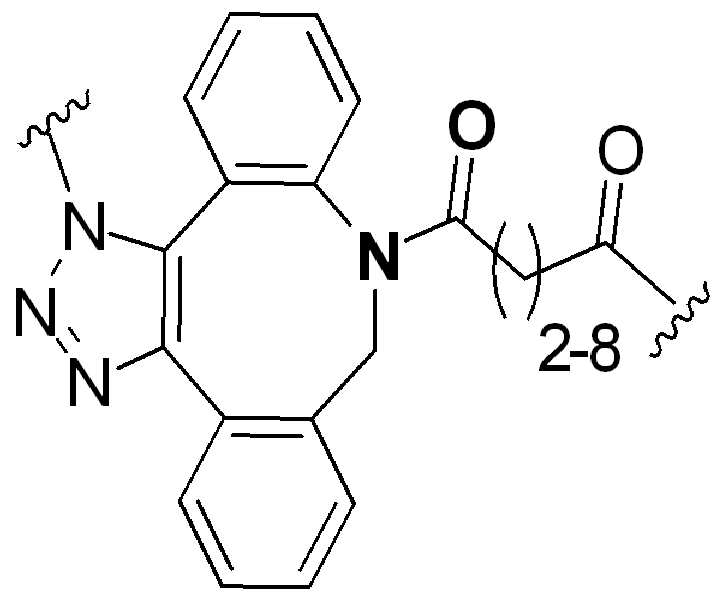
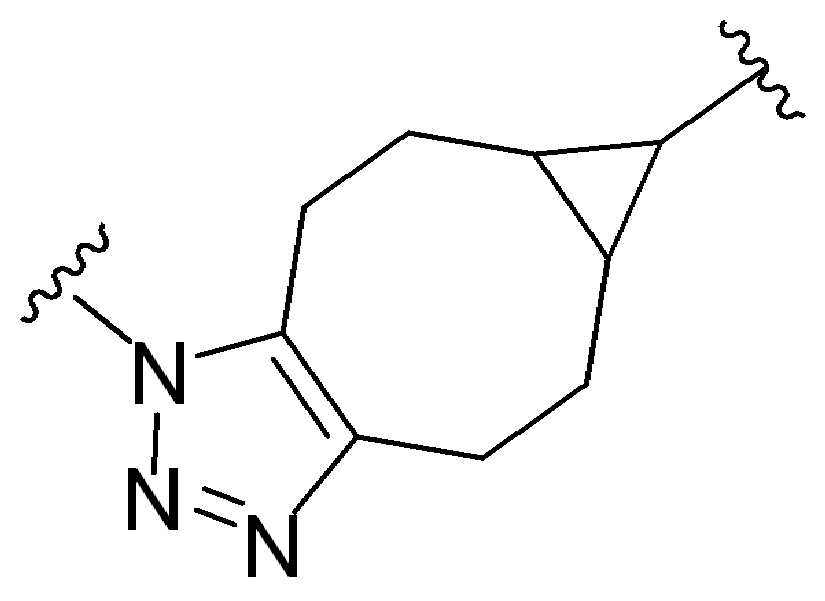
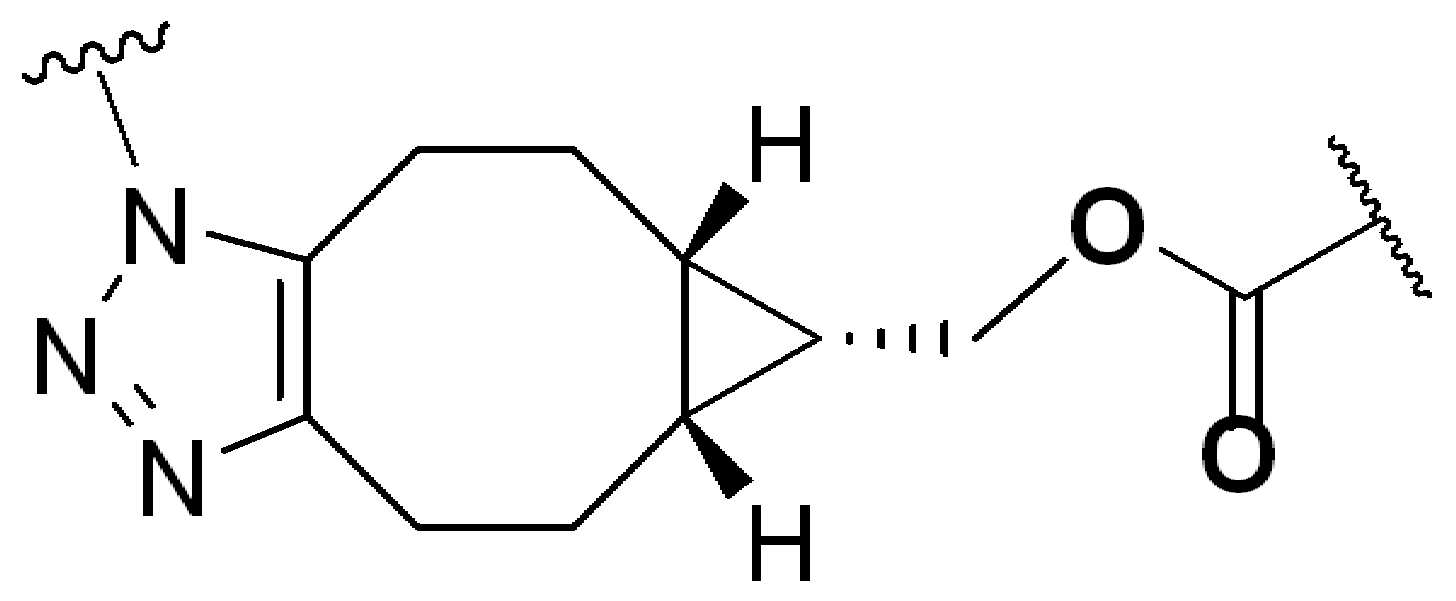
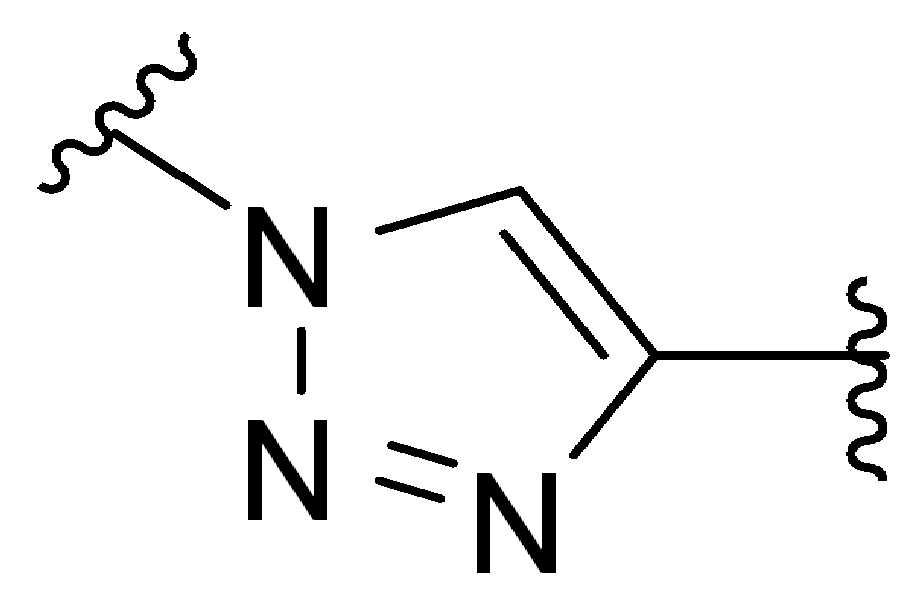
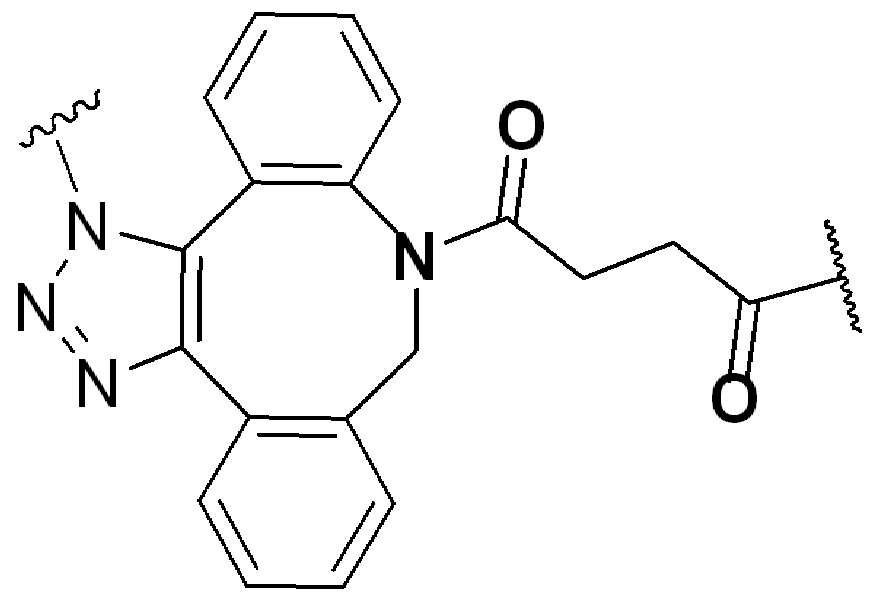
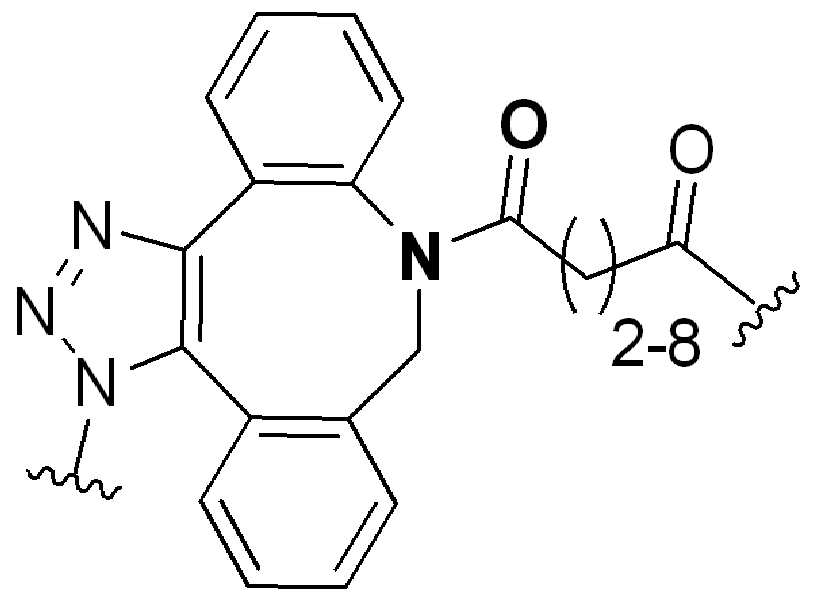
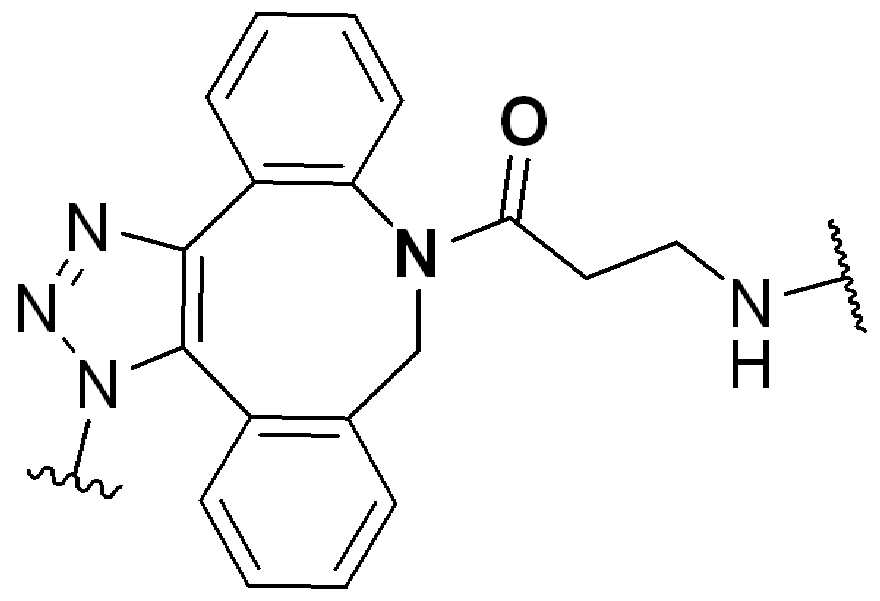
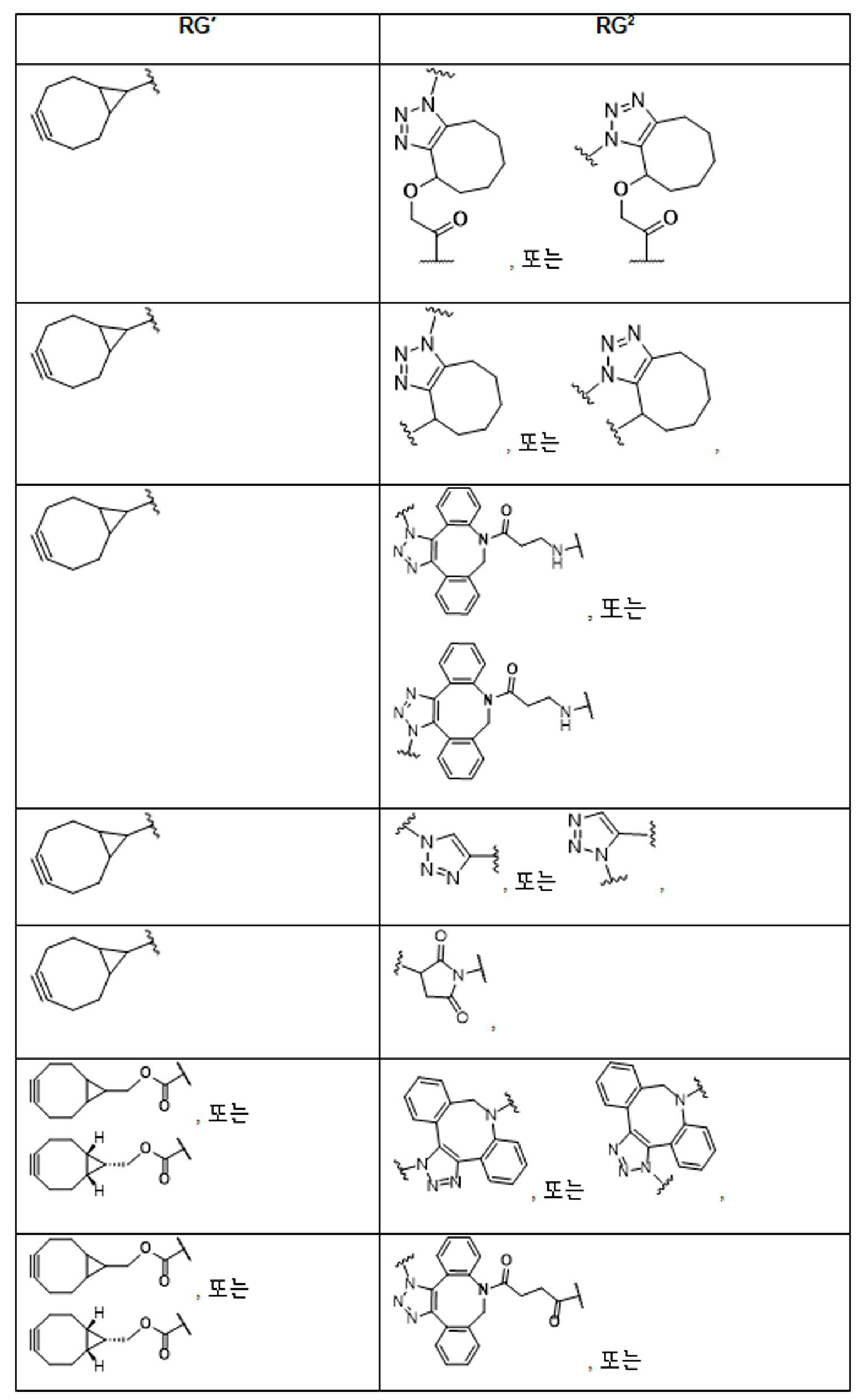
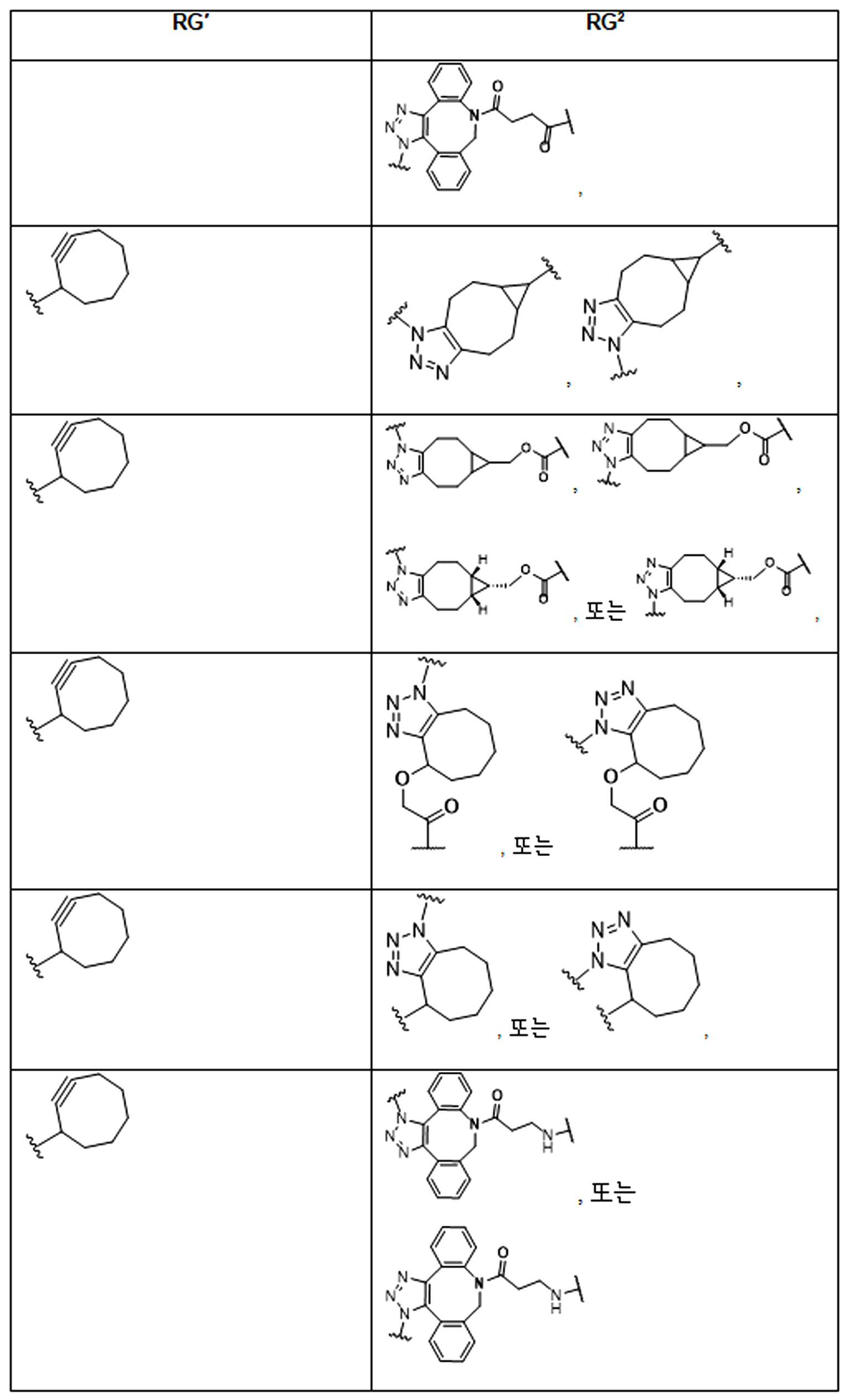
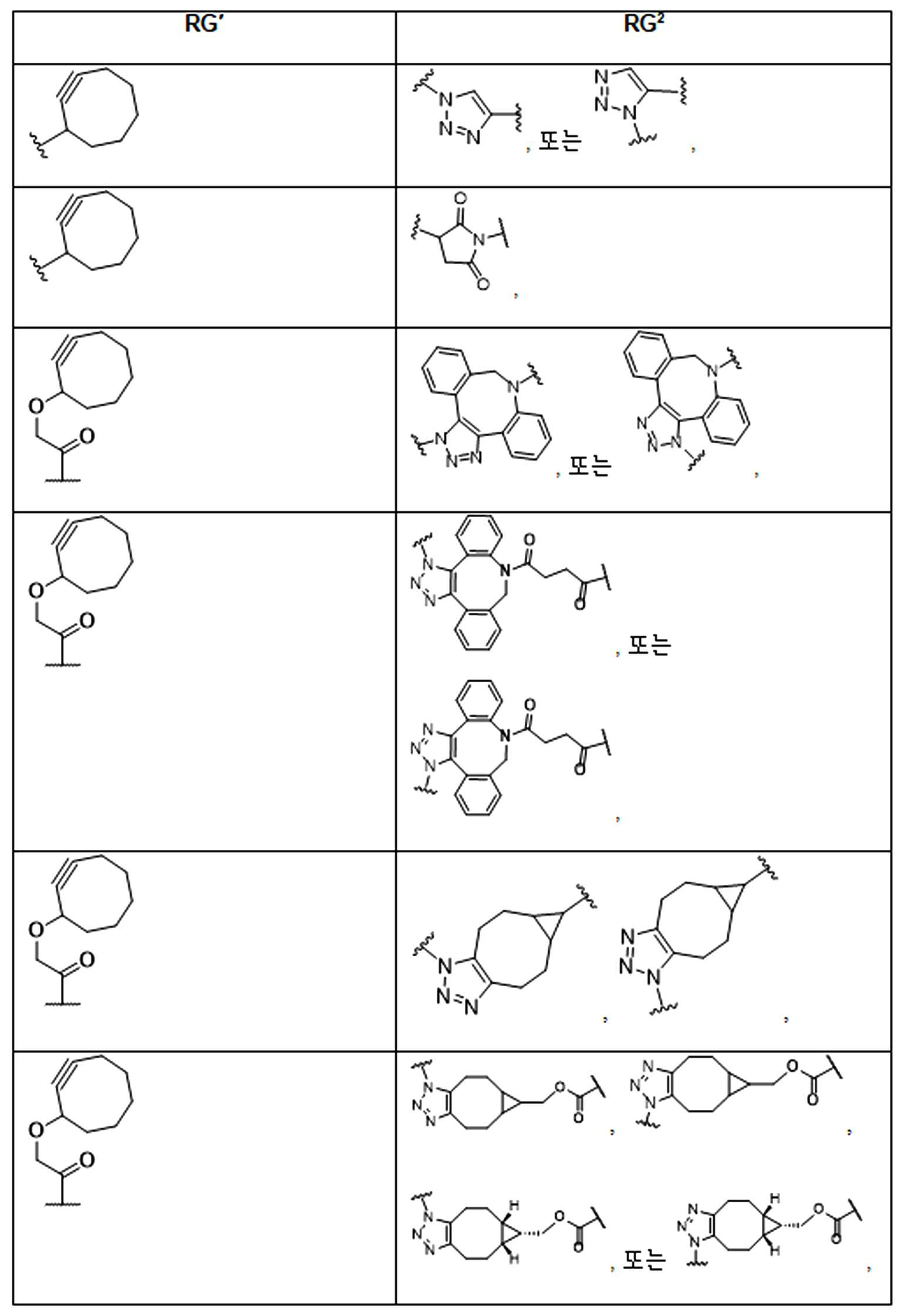
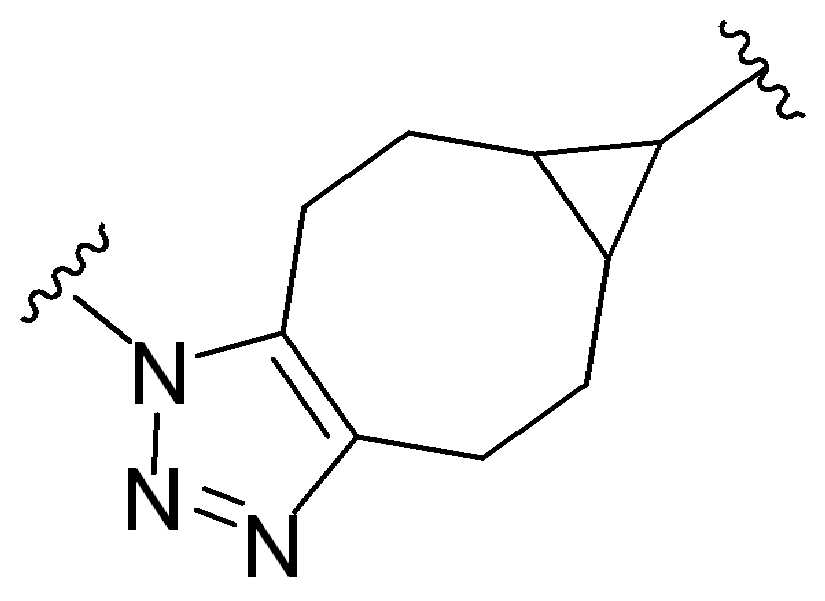
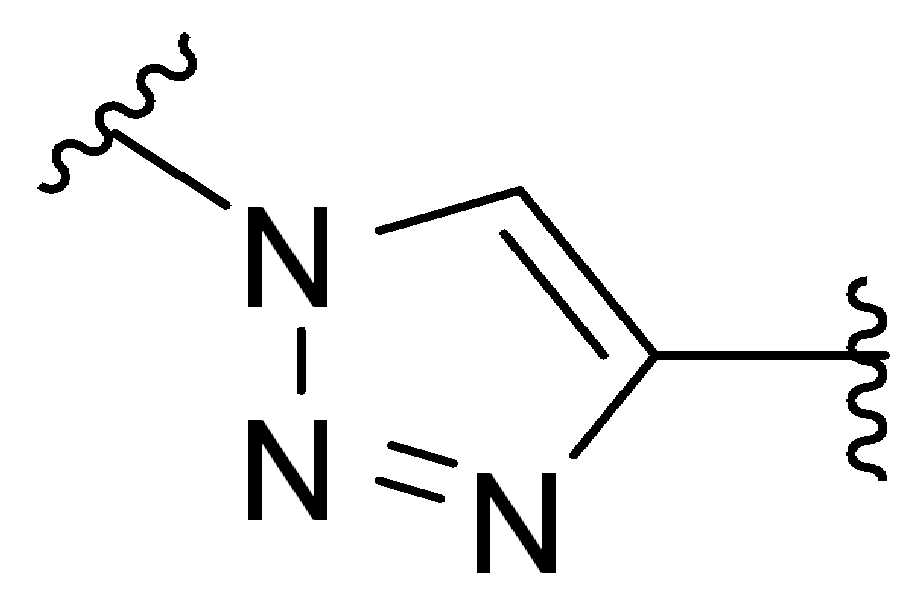
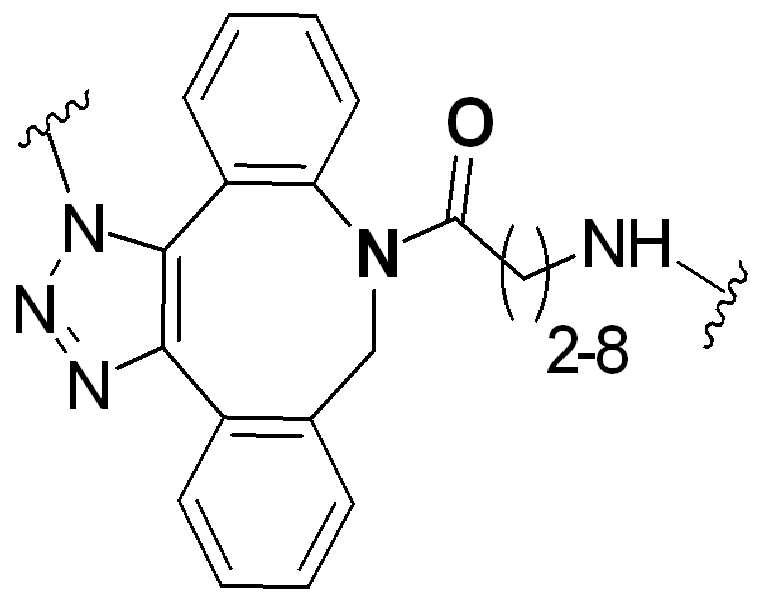
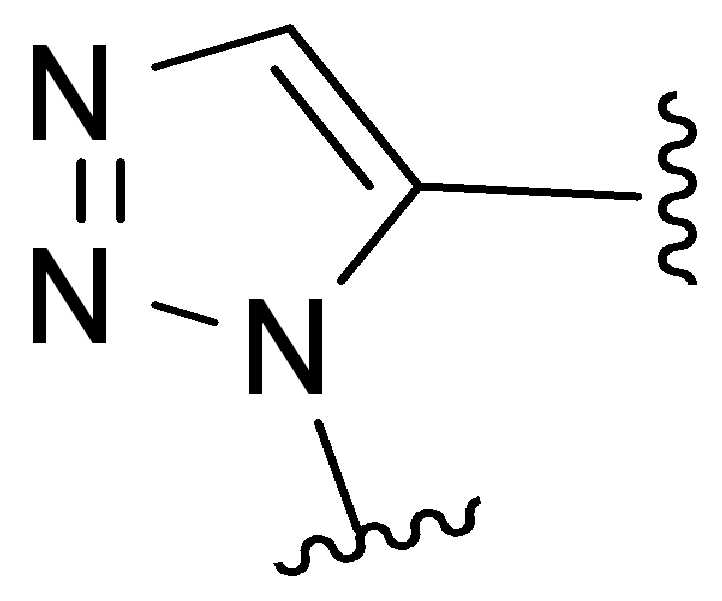
화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb) 화학식 (Vc) 화학식 (Vd)의 임의의 화합물에서, RG 1 또는 RG 2 는 각각 독립적으로 클릭 화학 잔류물이다. 일부 예에서, RG 1 및 RG 2 가 각각의 경우에 독립적으로 트리아자올 또는 융합된 트리아졸을 포함한다. 일부 경우에, RG 1 및 RG 2 는 각각의 경우에 독립적으로 ,, ,, , , , , , , , , ,, , , , , 및 로 이루어진 군으로부터 선택되고 상기 식에서 는, RG 1 또는 RG 2 가 화학식에 인접기에 결합되는 원자를 나타낸다.
어떤 경우에는, RG 1 및 RG 2 는 각각의 경우에 표 R에 나타낸 바와 같이 독립적이다.
표 R
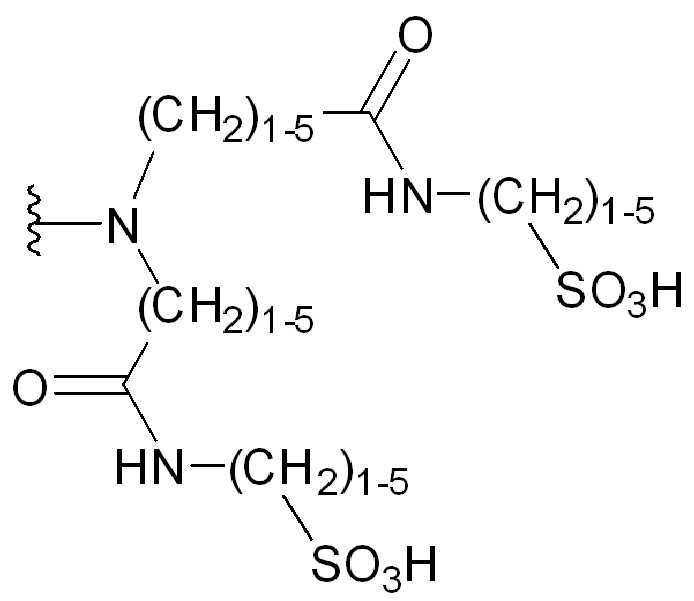
일부 경우에, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, HG는 -(CH2)1-5SO3H,
-(CH2)n-NH-(CH2)1-5SO3H, -(CH2)n-C(O)NH-(CH2)1-5SO3H,
-(CH2CH2O)m-C(O)NH-(CH2)1-5SO3H, -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5SO3H)2,
-(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5SO3H)2, 또는
-(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5SO3H)2 이고, n은 1, 2, 3, 4 또는 5이다. 한 실시양태에서, HG 는 -(CH2)1-5SO3H이다. 다른 실시양태에서, HG 는 -(CH2)n-NH-(CH2)1-5SO3H이고, 여기서 n은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG는 -(CH2)n-C(O)NH-(CH2)1-5SO3H이고, 여기서 n은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는
-(CH2CH2O)m-C(O)NH-(CH2)1-5SO3H이고, 여기서 m은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG는 -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5SO3H)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5SO3H)2이고, 여기서 n은 1, 2, 3, 4, 또는 5. 다른 실시양태에서, HG는 -(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5SO3H)2이고, 여기서 m은 1, 2, 3, 4, 또는 5이다.
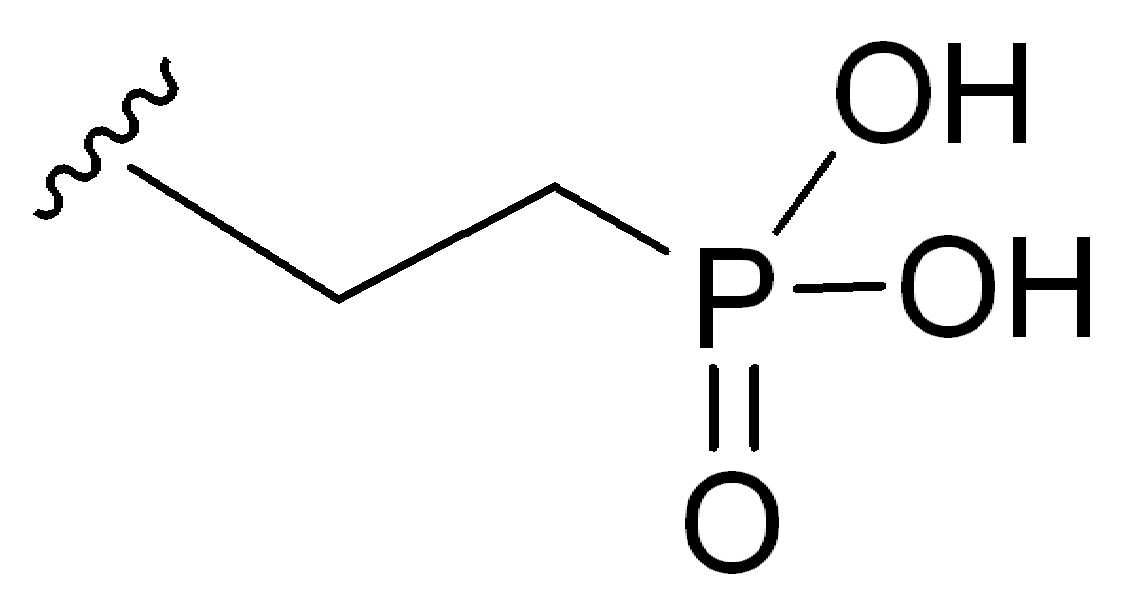
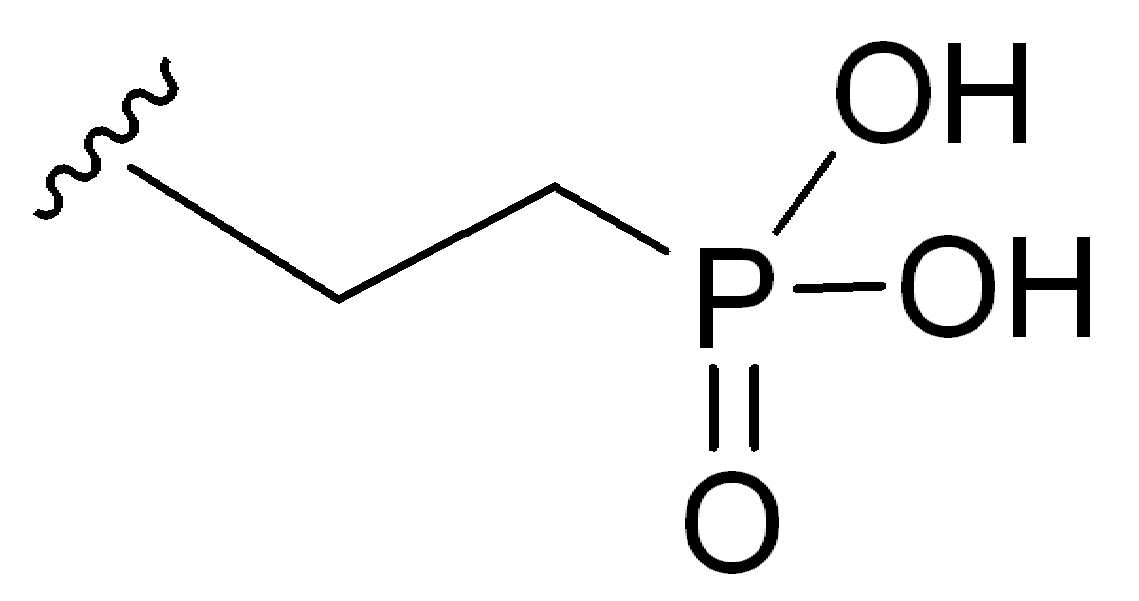
일부 경우에, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, HG 는 -(CH2)1-5PO3H, -(CH2)n-NH-(CH2)1-5PO3H, -(CH2)n-C(O)NH-(CH2)1-5PO3H,
-(CH2CH2O)m-C(O)NH-(CH2)1-5PO3H, -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5PO3H)2,
-(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5PO3H)2, 또는
-(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5PO3H)2이고,
여기서 n 은 1, 2, 3, 4, 또는 5, 및 m은 1, 2, 3, 4, 또는 5이다. 한 실시양태에서, HG는 -(CH2)1-5PO3H이다. 다른 실시양태에서, HG는 -(CH2)n-NH-(CH2)1-5PO3H이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG는 -(CH2)n-C(O)NH-(CH2)1-5PO3H이고, 여기서 n 은 1, 2, 3, 4, 또는 5. 다른 실시양태에서, HG는
-(CH2CH2O)m-C(O)NH-(CH2)1-5PO3H, 여기서 m 은 1, 2, 3, 4, 또는 5. 다른 실시양태에서, HG 는 -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5PO3H)2, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5PO3H)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG는 -(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5PO3H)2이고, 여기서 m은 1, 2, 3, 4, 또는 5이다.
일부 경우에, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, HG 는 -(CH2)1-5PO3H, -(CH2)n-NH-(CH2)1-5PO3H, -(CH2)n-C(O)NH-(CH2)1-5PO3H,
-(CH2CH2O)m-C(O)NH-(CH2)1-5PO3H, -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5PO3H)2,
-(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5PO3H)2, 또는
-(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5PO3H)2이고,
여기서 n 은 1, 2, 3, 4, 또는 5, 및 m은 1, 2, 3, 4, 또는 5이다. 한 실시양태에서, HG는 -(CH2)1-5PO3H이다. 다른 실시양태에서, HG는 -(CH2)n-NH-(CH2)1-5PO3H이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG는 -(CH2)n-C(O)NH-(CH2)1-5PO3H이고, 여기서 n 은 1, 2, 3, 4, 또는 5. 다른 실시양태에서, HG는
-(CH2CH2O)m-C(O)NH-(CH2)1-5PO3H, 여기서 m 은 1, 2, 3, 4, 또는 5. 다른 실시양태에서, HG 는 -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5PO3H)2, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5PO3H)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG는 -(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5PO3H)2이고, 여기서 m은 1, 2, 3, 4, 또는 5이다.
화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, HG 는 -(CH2)1-5N+(R M )3,
-(CH2)n-NH-(CH2)1-5N+(R M )3, -(CH2)n-C(O)NH-(CH2)1-5N+(R M )3,
-(CH2CH2O)m-C(O)NH-(CH2)1-5N+(R M )3, -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5N+(R M )3)2,
-(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+(R M )3)2, 또는
-(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+(R M )3)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이고, m 은 1, 2, 3, 4, 또는 5이고, 및 R M 은독립적으로 각 경우에, H, C1-6알킬, C3-7시클로알킬 또는 C1-6알킬-C3-7시클로알킬, 또는, 2개의 R M 은 이들이 부착되어 있는 질소 원자와 함께 3내지 7원 헤테로 시클로 알킬 고리를 형성한다. 한 실시양태에서, HG 는 -(CH2)1-5N+(R M )3이다. 다른 실시양태에서, HG 는 -(CH2)n-NH-(CH2)1-5N+(R M )3이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-C(O)NH-(CH2)1-5N+(R M )3, 여기서 n 는 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는
-(CH2CH2O)m-C(O)NH-(CH2)1-5N+(R M )3이고, 여기서 m 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5N+(R M )3)2이고, 여기서 n 은1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 은 -(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+(R M )3)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+(R M )3)2이고, 여기서 m 은 1, 2, 3, 4, 또는 5이다.
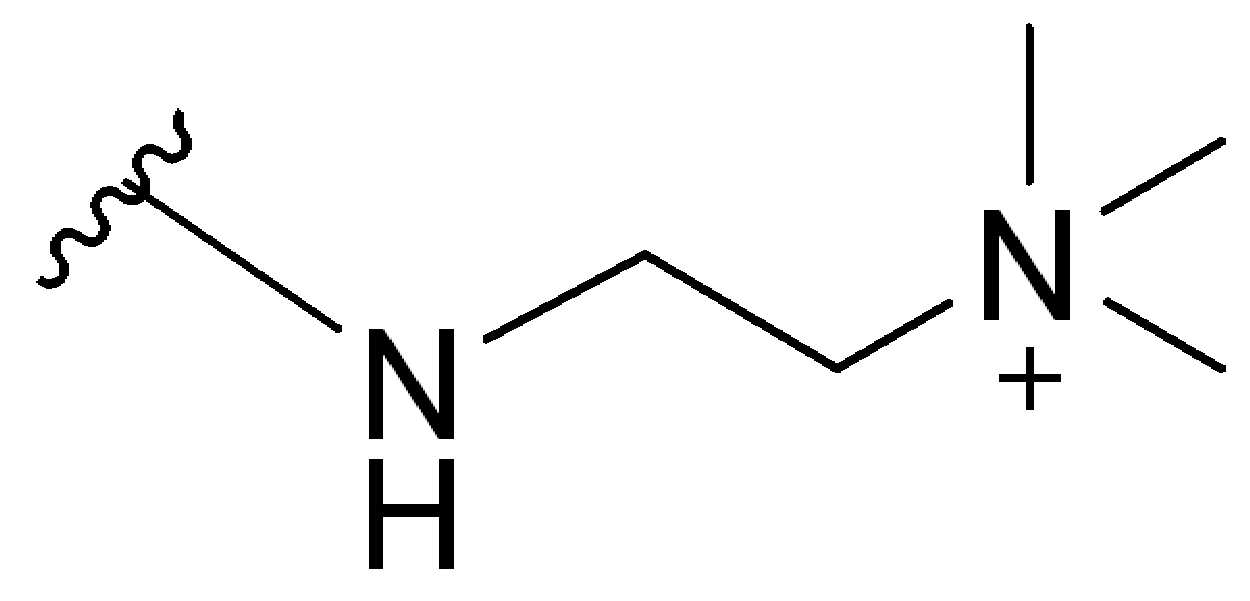
화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd) 의 임의의 화합물에 대해, HG 는-(CH2)1-5N+Me3,
-(CH2)n-NH-(CH2)1-5N+Me3, -(CH2)n-C(O)NH-(CH2)1-5N+Me3,
-(CH2CH2O)m-C(O)NH-(CH2)1-5N+Me3, -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5N+Me3)2,
-(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+Me3)2, 또는
-(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+Me3)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이고, 및 m은 1, 2, 3, 4, 또는 5이다. 한 실시양태에서, HG는 -(CH2)1-5N+Me3이다. 다른 실시양태에서, HG은 -(CH2)n-NH-(CH2)1-5N+Me3이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 은 -(CH2)n-C(O)NH-(CH2)1-5N+Me3이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는
-(CH2CH2O)m-C(O)NH-(CH2)1-5N+Me3이고, 여기서 m 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 은 -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5N+Me3)2이고, 여기서 n 는 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+Me3)2이고, 여기서 n 는 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+Me3)2이고, 여기서 m 은 1, 2, 3, 4, 또는 5이다.
일부 경우에, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, HG는
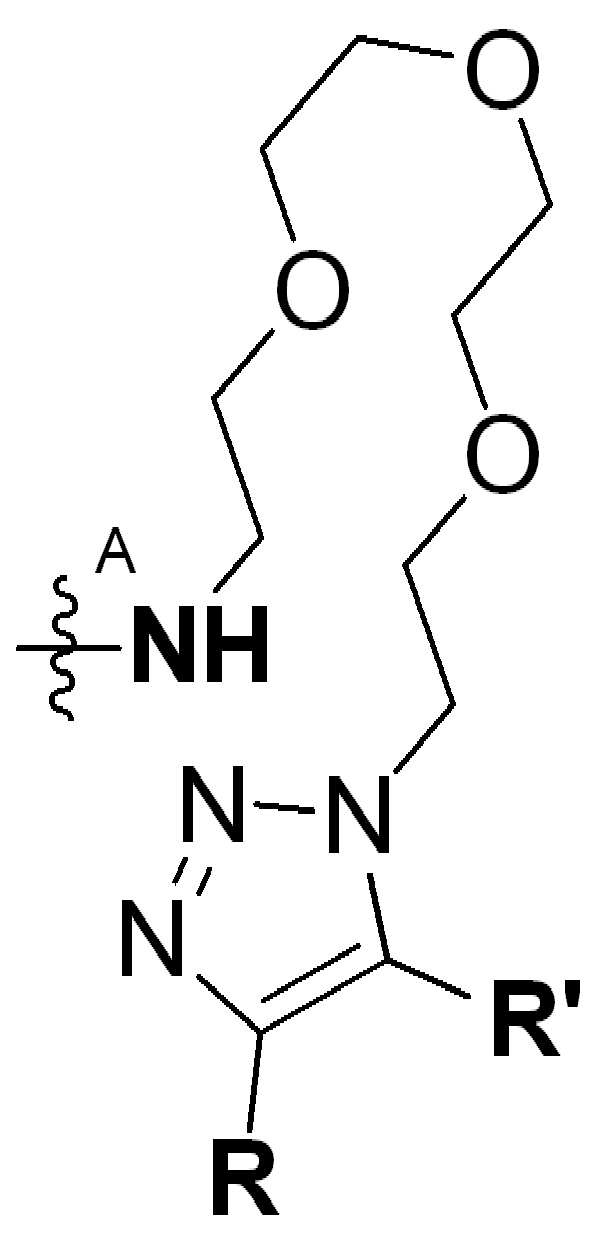
여기서 는 화학식에서HG가 인접기에 결합되는 원자를 나타낸다. 하나의 예에는, HG는 , 또는 이의 염이다. 다른 경우에는, HG는 , 또는 그의염이다. 다른 경우에는 HG는 , 또는 이의 염이다. 다른 경우에는, HG는 , 또는 이의 염이다.
화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)에서, HG는아민 또는 이의 염이고, 예를 들어, 4가 아민, 예를 들어, 이고, 여기서 는 화학식에서 HG가 인접기에 결합되는 원자를 나타낸다.
다른 예에서, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, HG는 포스폰산, 또는 이의 염, 예를 들어, 이고, 여기서 는 화학식에서 HG가 인접기에 결합되는 원자를 나타낸다. 다른 예에서, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, HG는 포스폰산, 또는 이의 염, 예를 들어이고, 여기서 는 HG가 인접기에 결합되는 원자를 나타낸다.
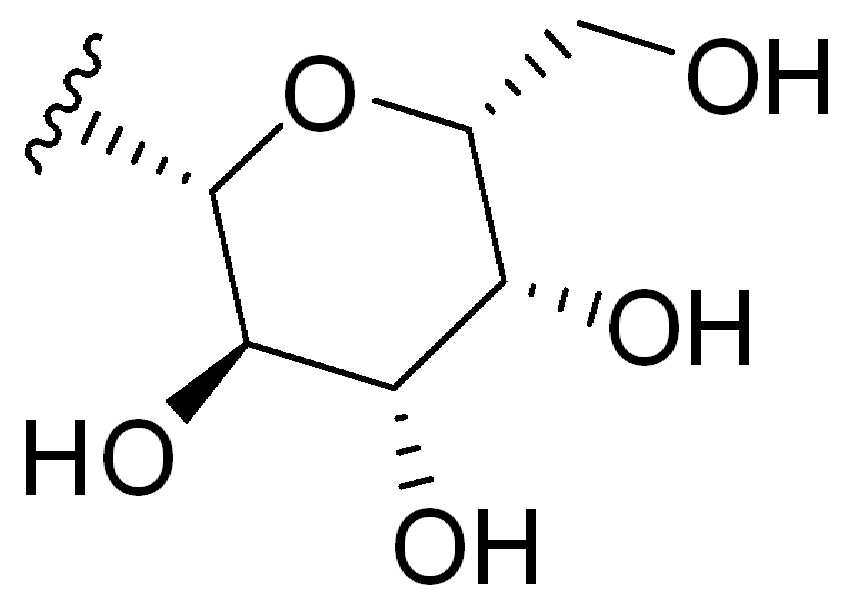
또 다른 예에서, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에서, HG는 당 잔기, 예를 들어, (갈락토오스), (클루카민), 또는 (말토오스)이며, 여기서 는 화학식에서 HG가 인접기에 결합되는 원자를 나타낸다.
일부 경우에, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, SP 1 및 SP 2 는 독립적으로, 각 경우에, 부재하거나, 또는 C1-6 알킬렌, -NH-, -C(O)-, (-CH2-CH2-O)e, -NH-CH2-CH2-(-O-CH2-CH2)e-C(O)-, -C(O)-(CH2)u-C(O)-, -C(O)-NH-(CH2)v-, 폴리글리신(예를들어, ((글리신)4-세린) f 여기서 아래 첨자 f 는 1 내지 6의 정수이고,) 으로 이루어진 군으로부터 선택되고, 아래 첨자 e는 0 내지 4의 정수이고, 첨자 u 는 1 내지 8의 정수이고, 첨자 v는 1 내지 8의 정수이다. 일부 경우에, SP 1 및 SP 2 는 독립적으로, 각 경우에, 표 S에 도시된 바와 같다.
표 S
표 R의 행 및 표 R의 행의 임의의 조합은 본 원에 기술된 화학식 (I)의 화학물에 존재할 수 있다.
일부 예에서, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해,
또는 이의 입체이성질체 형태, 또는 이의 위치 이성질체, 또는 이의 위치 이성질체의 혼합물이고,
일부 예에서, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해,
일부 예에서, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, 구조에서, 구조에서
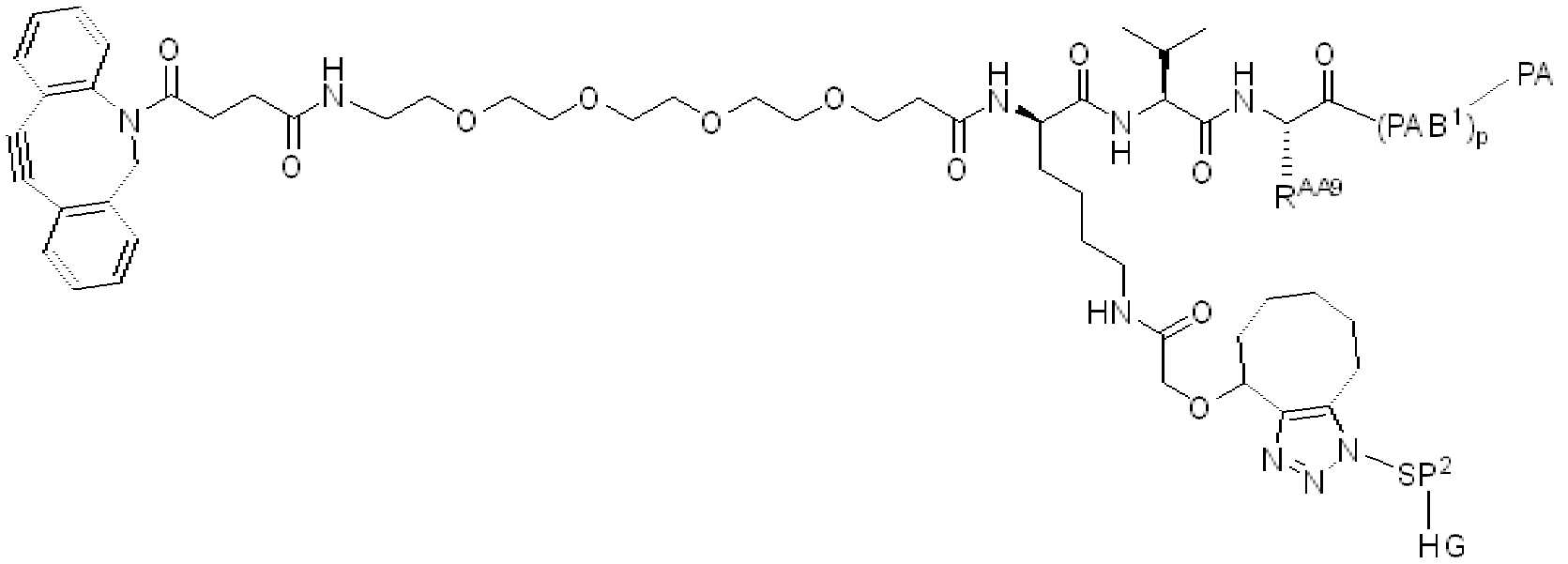
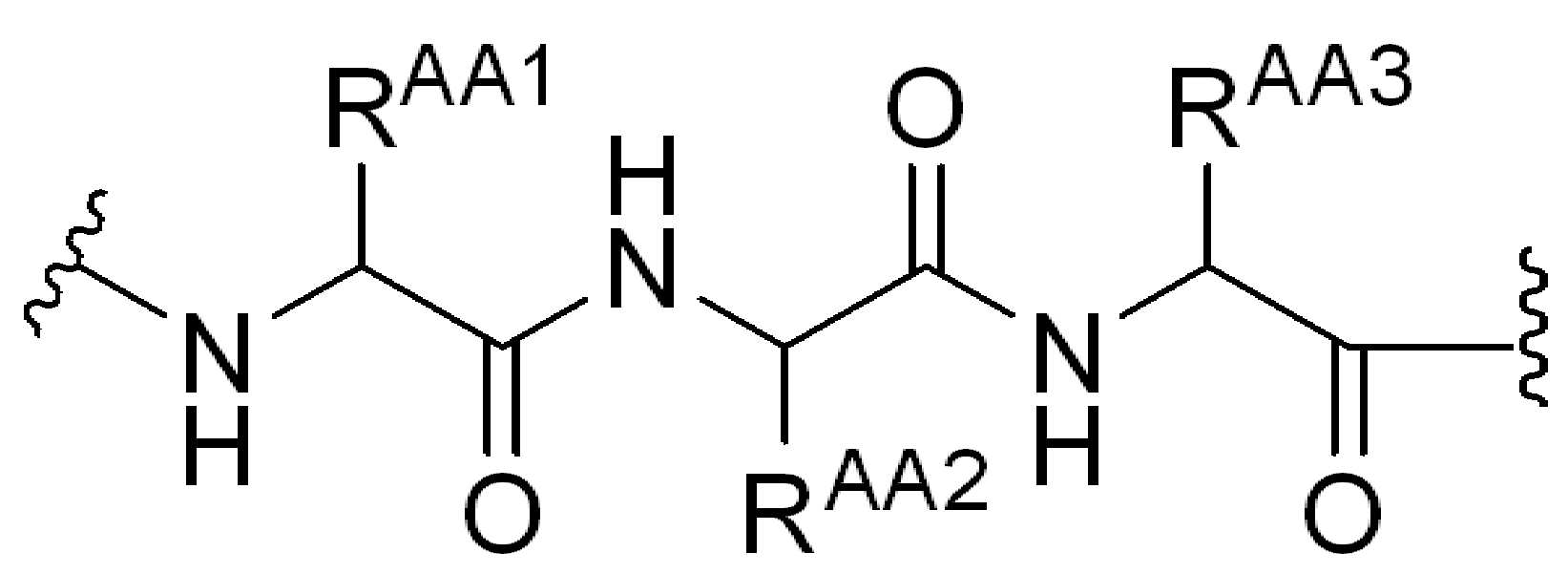
일부 예에서, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, LL은 화학식 (LL1)에 따른다:
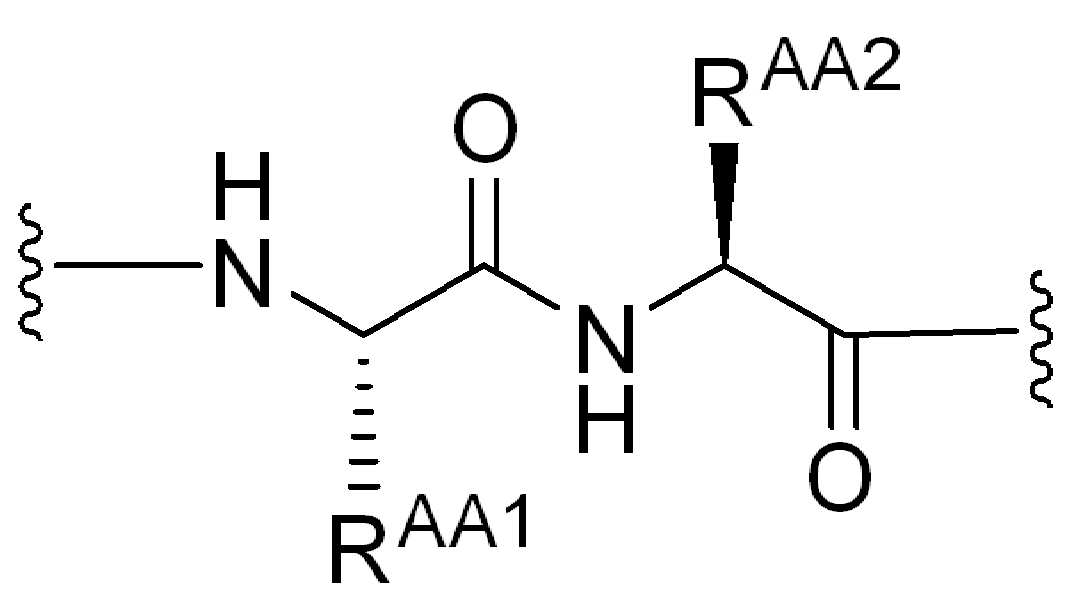
여기서 R AA1 , R AA2 , 및 R AA3 는 각각, 독립적으로, 아미노산 측쇄이며, 이들 중 적어도 하나는 -(RG 2 ) q -SP 2 -HG 에 직접 또는 간접적으로 결합함.
일부 경우에, 화학식 LL1의 경우, R AA1 이 HG에 직접 또는 간접적으로 결합된 리신, 글루타민, 글루탐산, 아스파르트산 측쇄이고, 및 R AA2 및 R AA3 는각각 발린 및 알라닌 또는 발린 및 시트룰린 측쇄이다.
경우에 따라, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, AA 2 는
여기서 R AA2 , R AA3 , R AA4 , 및 R AA5 는 각각, 독립적으로, 아미노산 측쇄이며, 이들 중 적어도 하나는-(RG 2 ) q -SP 2 -HG 에 직접 또는 간접적으로 결합하고, 상기 식에서, 는 AA 2 가 화학식의 인접기에 결합되는 원자를 나타낸다. 일부 예에서, R AA2 , R AA3 , R AA4 , 및 R AA5 ,는 독립적으로, 각 경우에, 알라닌, 발린, 류신, 이소류신, 메티오닌, 트립토판, 페닐알라닌, 프로린, 세린, 트레오닌, 시스테인, 티로신, 아스파라긴, 글루타민, 아스파르트산, 글루탐산, 리신, 아르기닌, 히스티딘 또는 시트룰린의 측쇄, 이의 유도체 또는 이들의 조합으로부터 선택된 아미노산 측쇄이다.
일부 경우에, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, AA 2 는
일부 경우에, 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물의 경우, 아래 첨자 e 는 4이다. 일부 경우에, 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물의 경우, 아래 첨자 e는 5이다.
일부 실시양태에서, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, 결합제(BA)는 항체 또는 이의 항원 결합 단편이다.
일부 경우에, 항체 또는 이의 항원-결합 단편은 종양-발현 항원에 결합한다. 일부 경우에, 항체 또는 이의 항원-결합 단편은 대식세포발현 항원에 결합한다. 일부 경우에, 결합제(BA)는 AXL, BAFFR, BCMA, BCR-목록 구성 요소, BDCA2, BDCA4, BTLA, BTNL2, BTNL3, BTNL8, BTNL9, C10 또는 f54, CCR1, CCR3, CCR4, CCR5, CCR6, CCR7, CCR9, CCR10, CD11c, CD137, CD138, CD14, CD168, CD177, CD19, CD20, CD209, CD209L, CD22, CD226, CD248, CD25, CD27, CD274, CD276, CD28, CD30, CD300A, CD33, CD37, CD38, CD4, CD40, CD44, CD45, CD46, CD48, CD5, CD52, CD55, CD56, CD59, CD62E, CD68, CD69, CD70, CD74, CD79a, CD79b, CD8, CD80, CD86, CD90.2, CD96, CLEC12A, CLEC12B, CLEC7A, CLEC9A, CR1, CR3, CRTAM, CSF1R, CTLA4, CXCR1/2, CXCR4, CXCR5, DDR1, DDR2, DEC-205, DLL4, DR6, FAP, EGFR, EGFRVIII, FCamR, FCMR, FcR's, Fire, GITR, HHLA2, HLA class II, HVEM, ICOSLG, IFNLR1, IL10R1, IL10R2, IL12R, IL13RA1, IL13RA2, IL15R, IL17RA, IL17RB, IL17RC, IL17RE, IL20R1, IL20R2, IL21R, IL22R1, IL22RA, IL23R, IL27R, IL29R, IL2Rg, IL31R, IL36R, IL3RA, IL4R, IL6R, IL5R, IL7R, IL9R, Integrins, LAG3, LIFR, MAG/Siglec-4, MET, MMR, MSR1, NCR3LG1, NKG2D, NKp30, NKp46, PDCD1, PRLR, PROKR1, PVR, PVRIG, PVRL2, PVRL3, RELT, SIGIRR, Siglec-1, Siglec-10, Siglec-5, Siglec-6, Siglec-7, Siglec-8, Siglec-9, SIRPA, SLAMF7, TACI, TCR-목록 구성요소/assoc, PTCRA, TCRb, CD3z, CD3, TEK, TGFBR1, TGFBR2, TGFBR3, TIGIT, TLR2, TLR4, TROY, TSLPR, TYRO, VLDLR, VSIG4, 및 VTCN1로 이루어진 군으로부터 선택된 항원에 대해 선택적인 항체 또는 이의 항원-결합 단편이다.
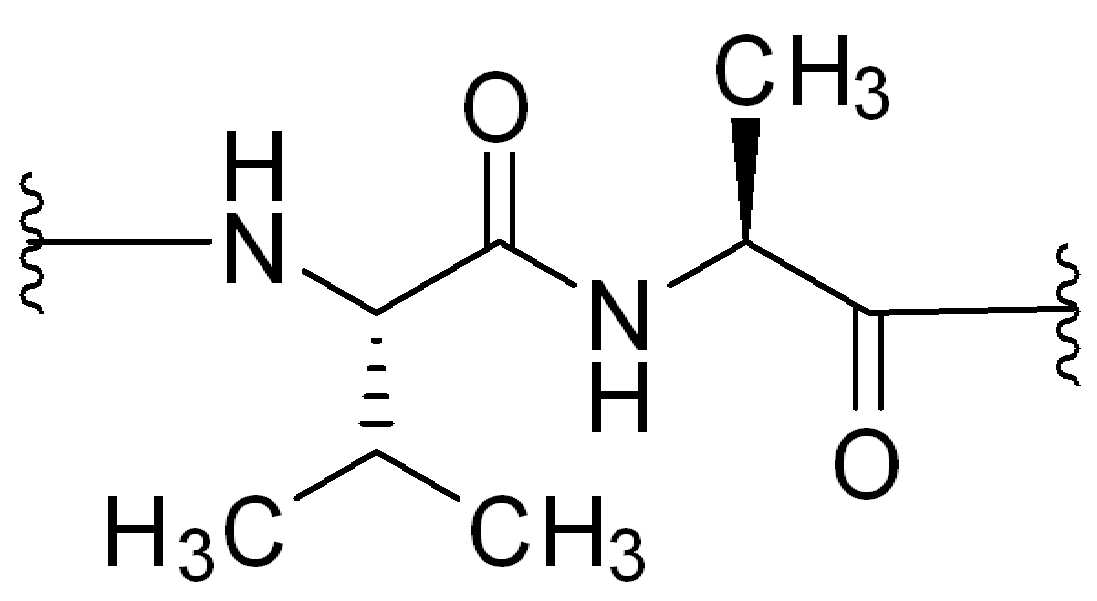
일부 경우에, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 임의의 화합물에 대해, PA는 돌라스타린(a dolastatin), 아우리스타틴(an auristatin), 메이탄시노이드(a maytansinoid), 식물 알칼로이드(a plant alkaloid), 탁산(a taxane), 빈카 알칼로이드(a vinca alkaloid), 스테로이드(a steroid), 및 간 X수용체 (a liver X receptor (LXR)) 조절제로 이루어진 군으로부터 선택된 그룹의 잔기이다.
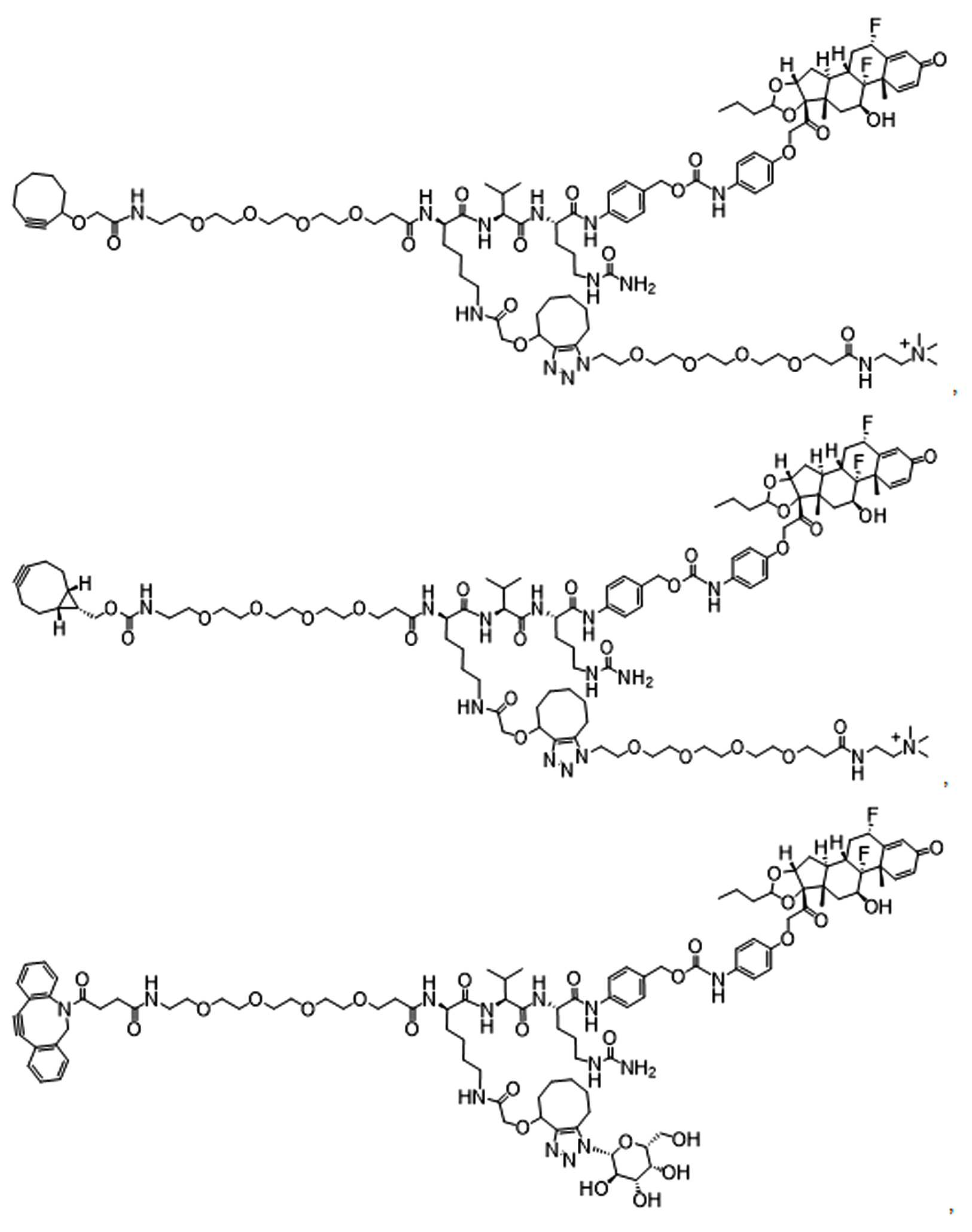
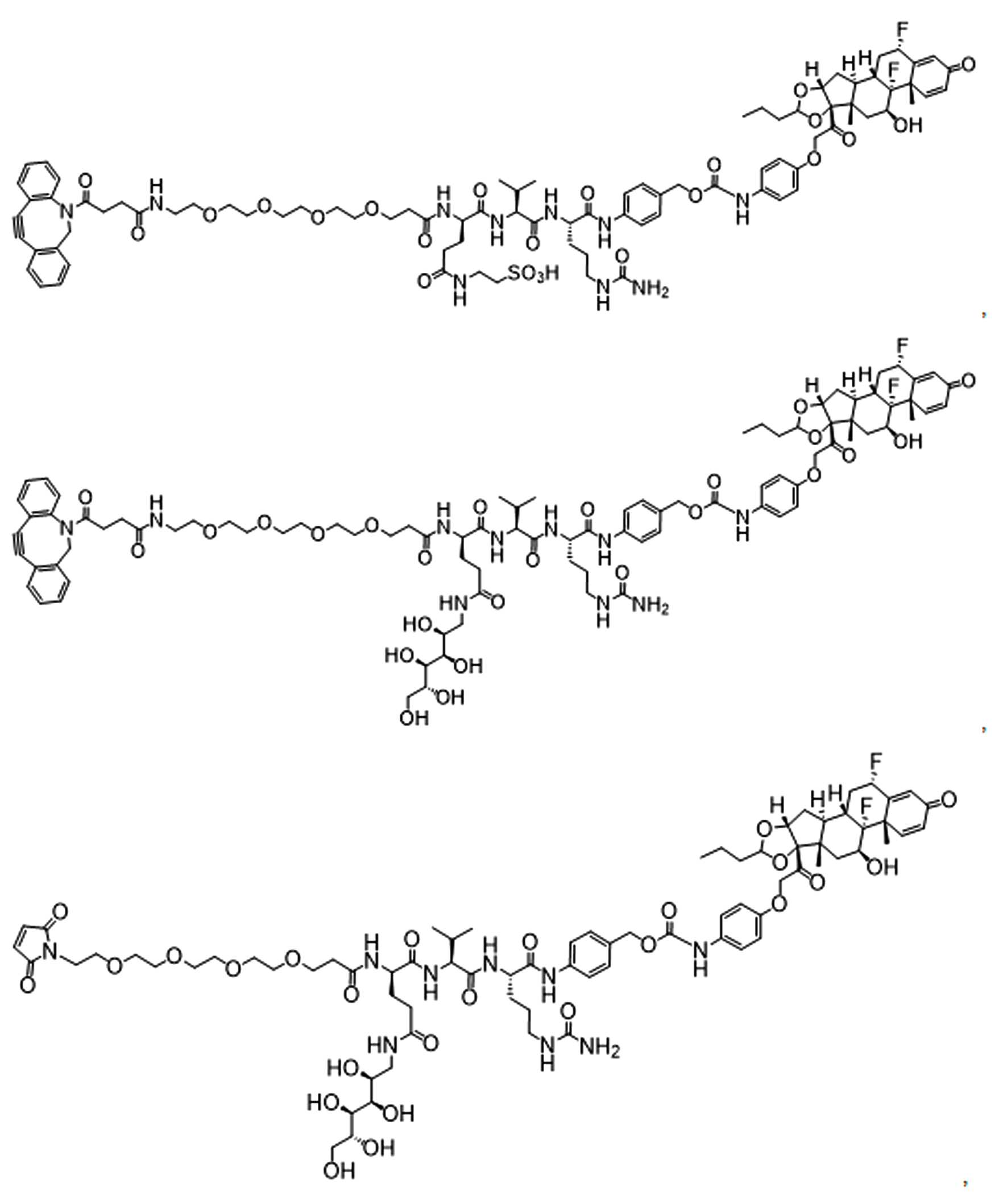
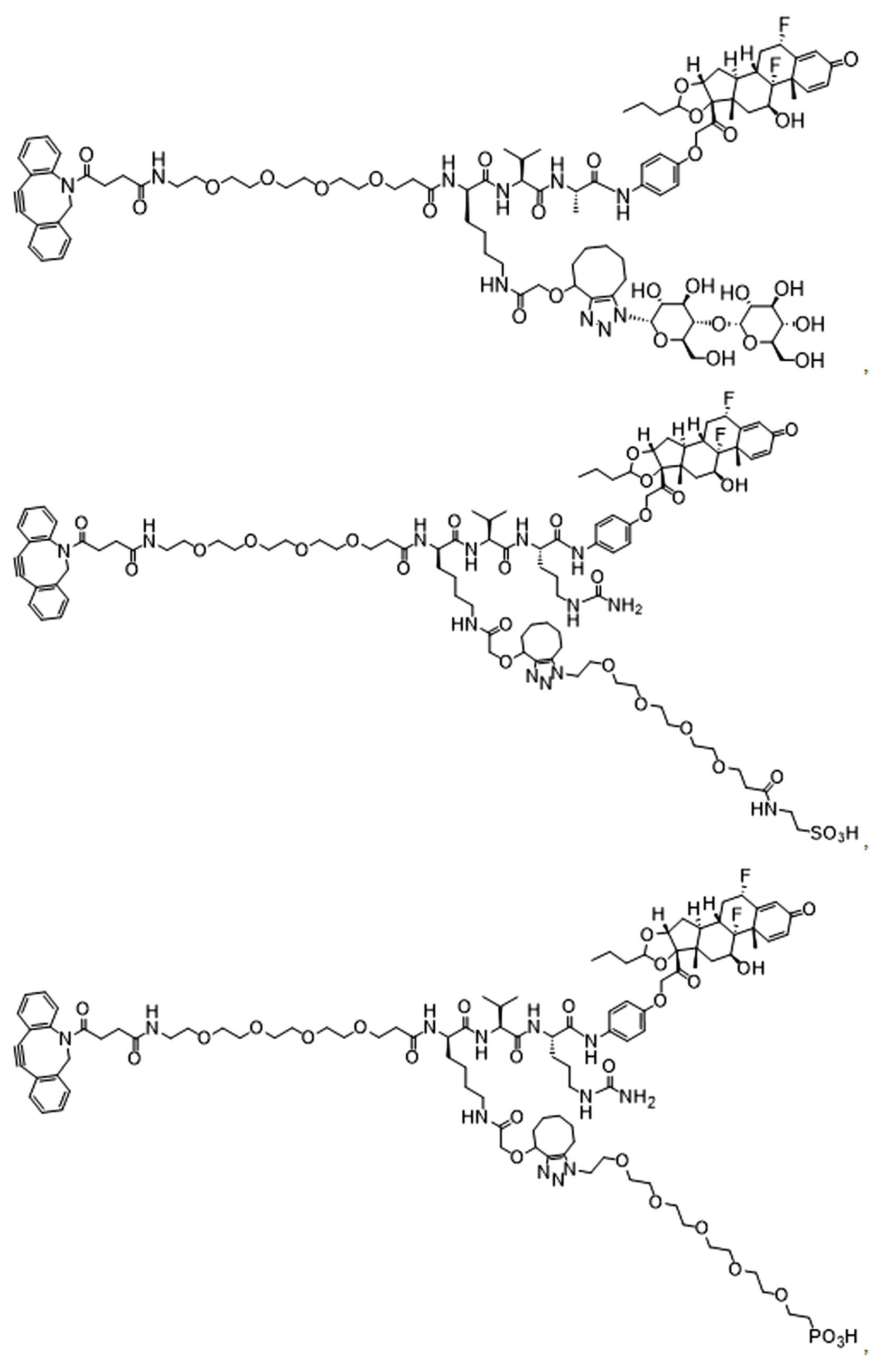
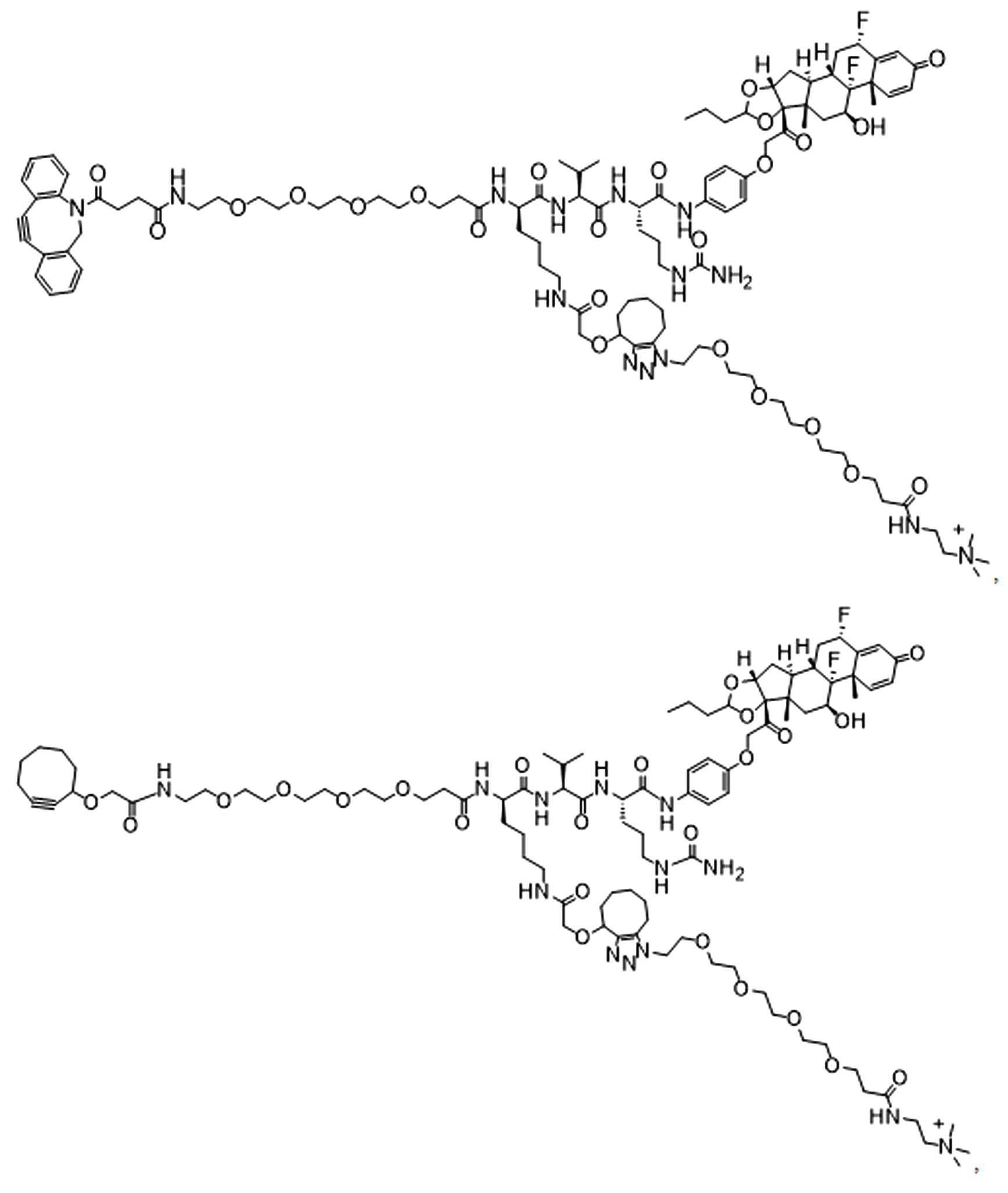
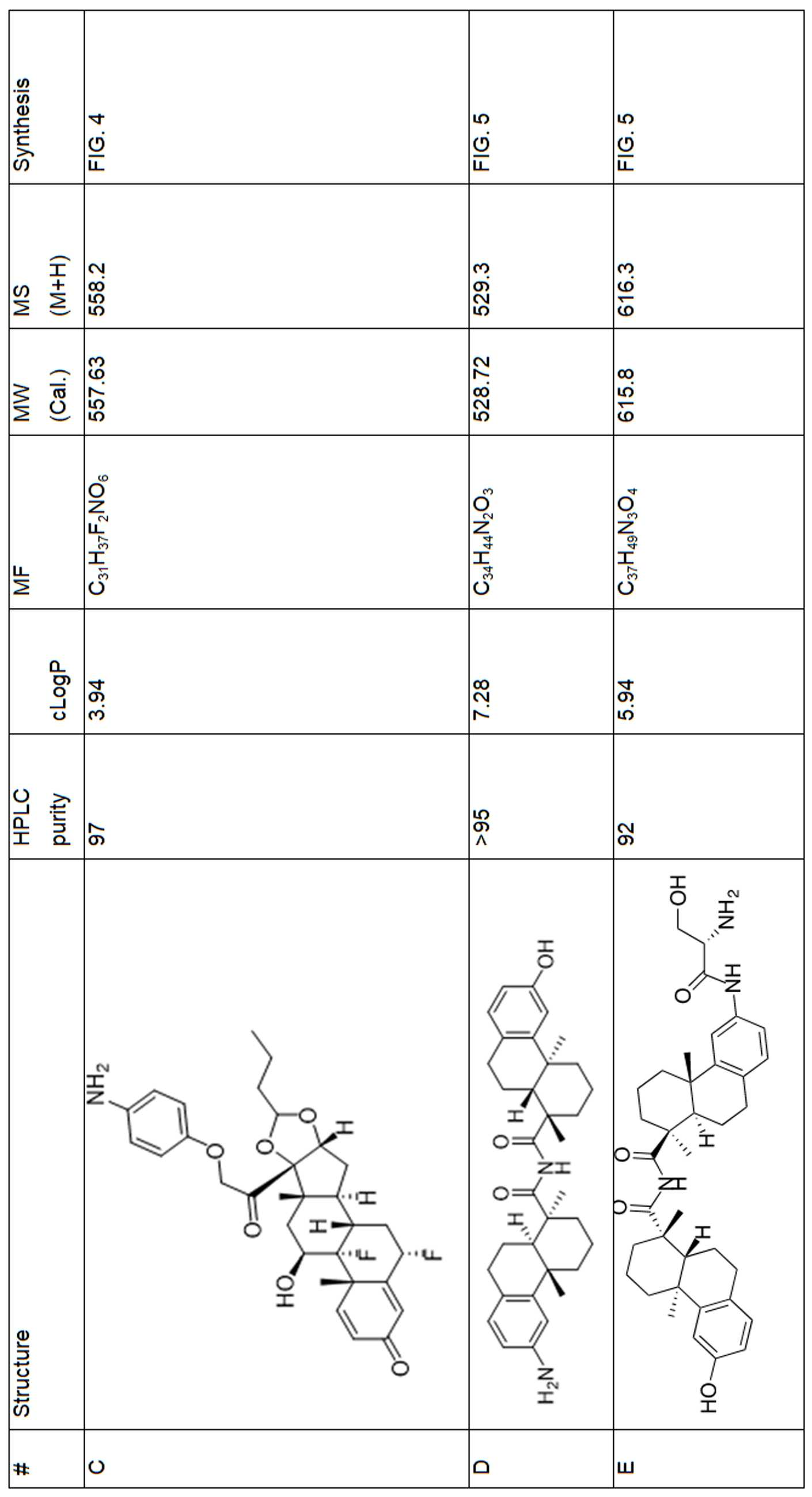
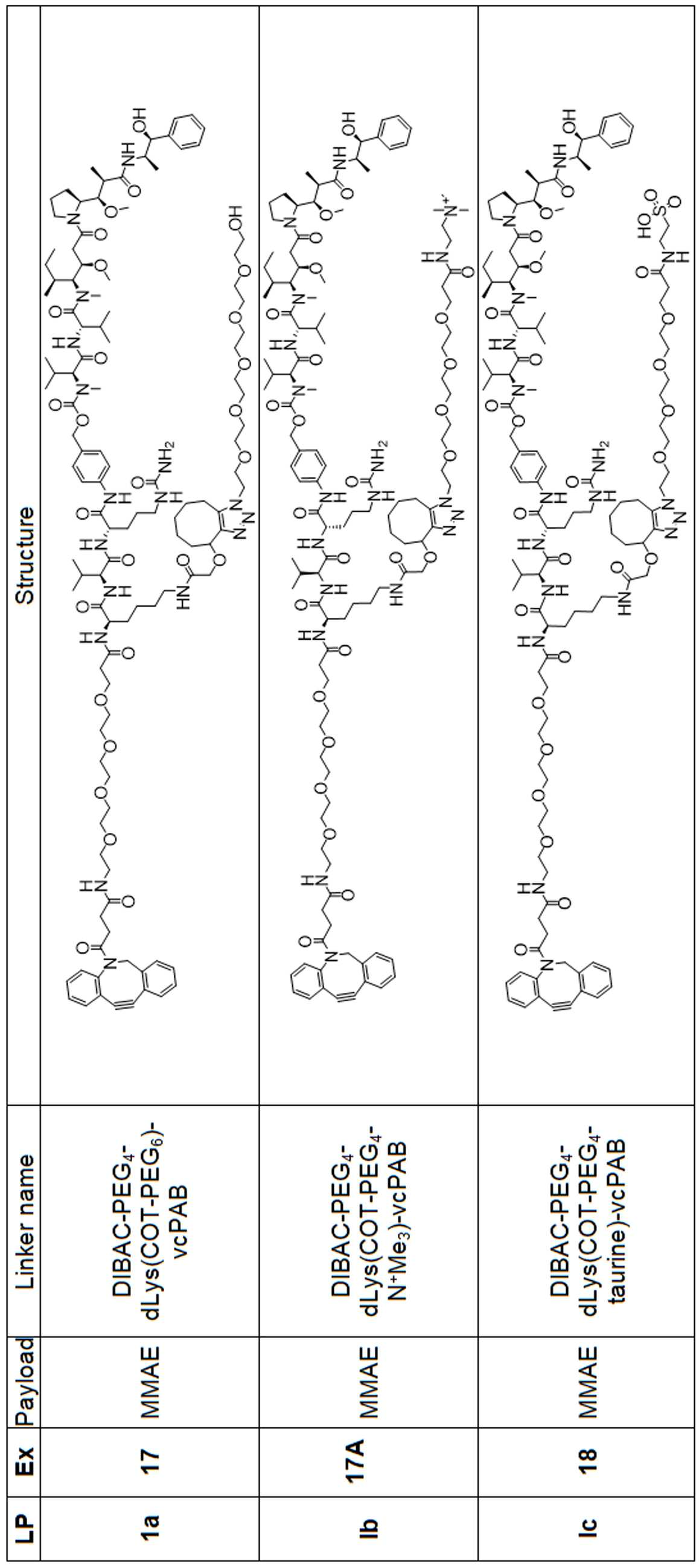
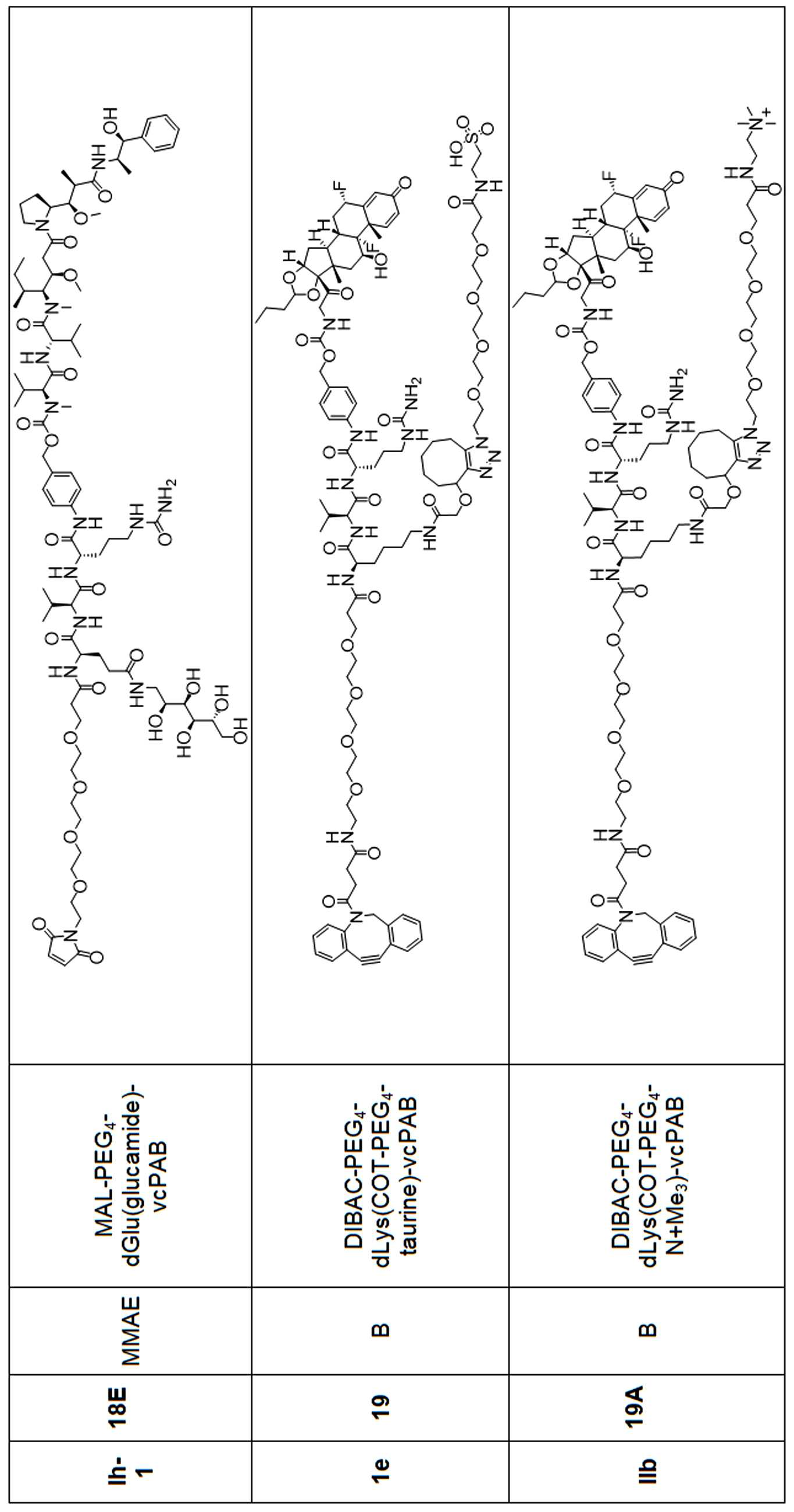
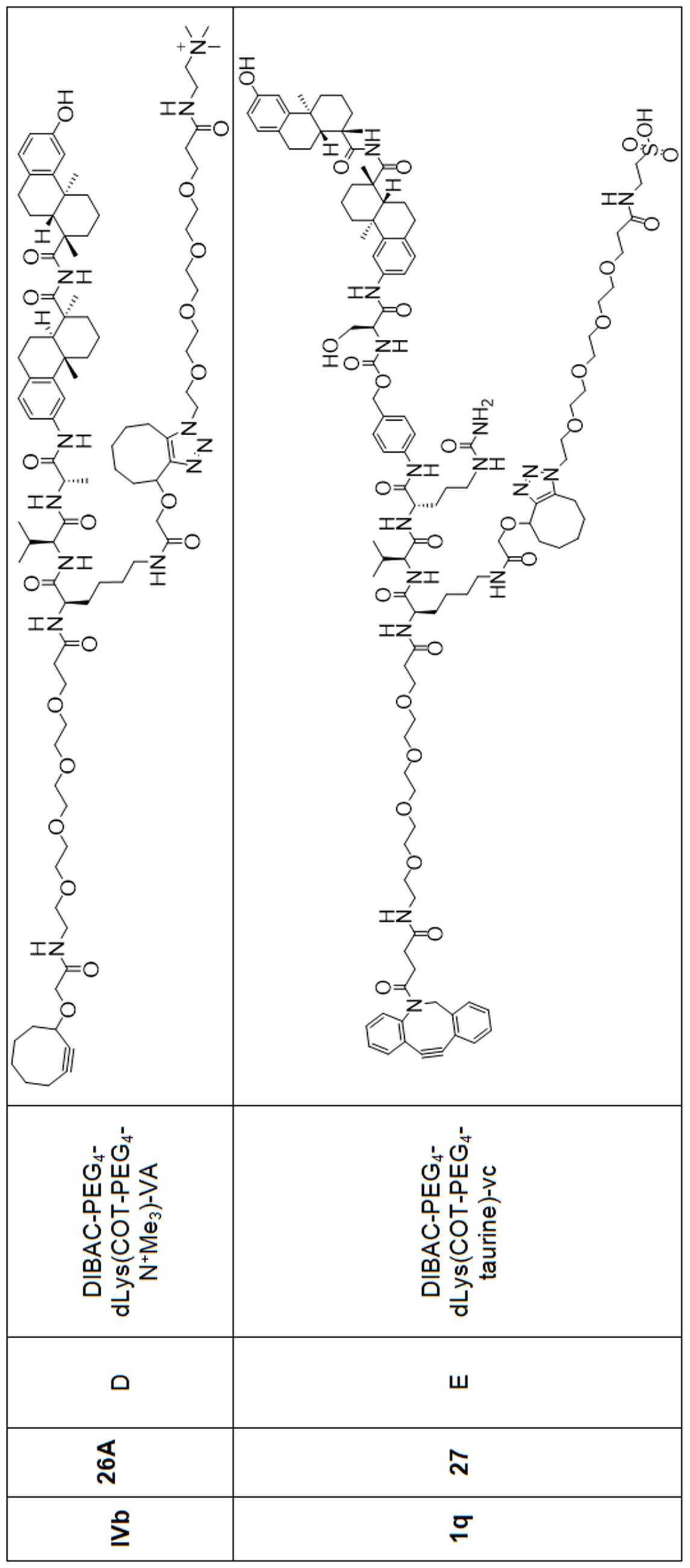
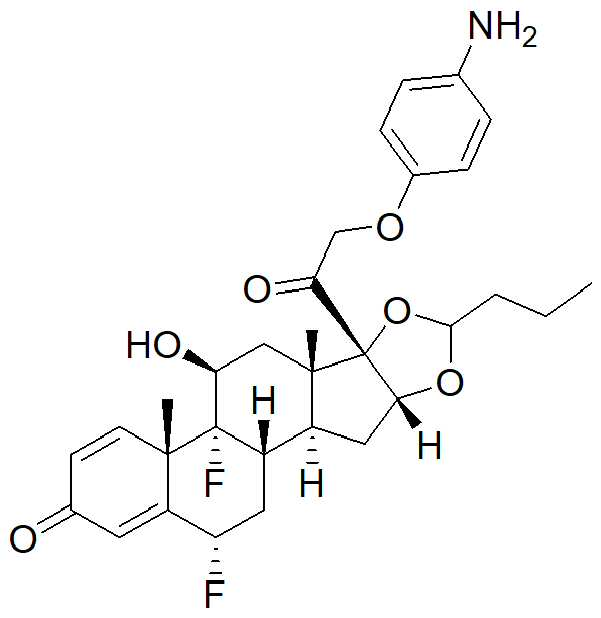
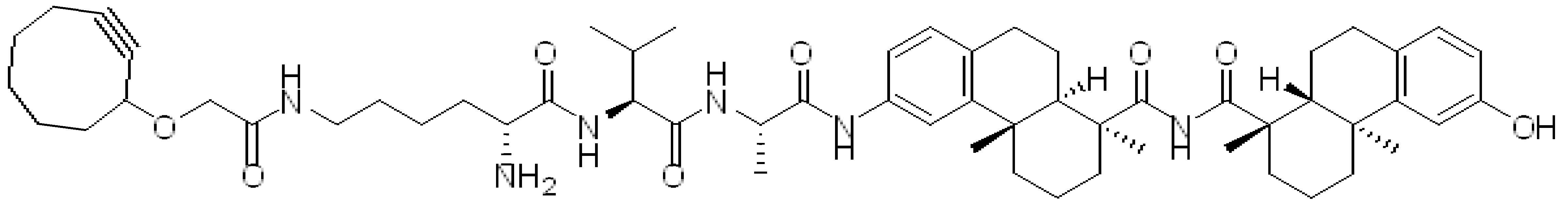
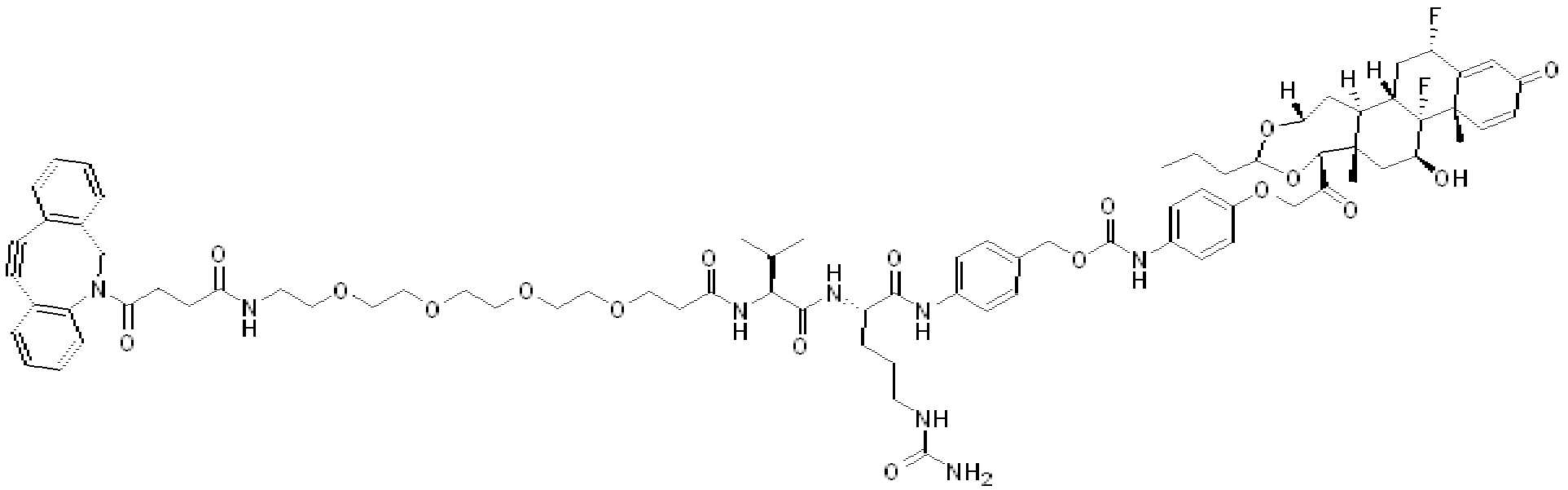
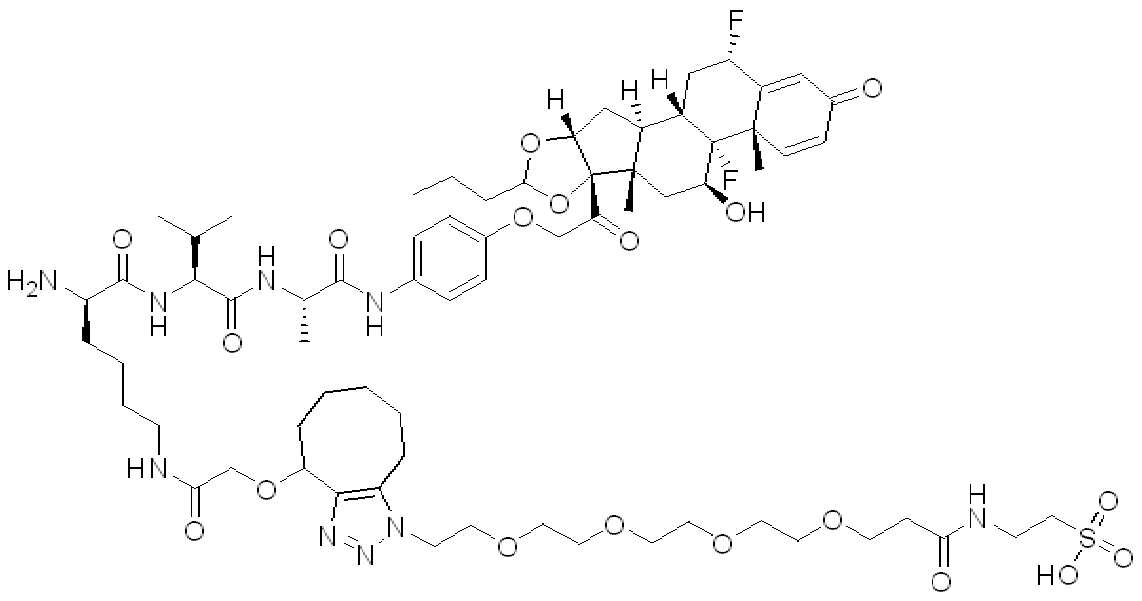
일부 경우에, PA는 돌라스타린이다. 일부 경우에, PA는 아우린스타틴이다. 일부 경우에, PA는 메이탄시노이드이다. 일부 경우에, PA는 메이탄시노이드이다. 일부 경우에, PA는 식물 알칼로이드이다. 일부 경우에, PA는 탁산이다. 일부 경우에, 빈카 알칼로이드 이다. 일부 경우에, PA는 스테로이드(a steroid)이다. 일부 경우에, PA는 LXR조절제(modulator) 이다. 일부 경우에, LXR조절제는 LXR작용제이다. 일부 실시양태에서, LXR 조절제는 LXR 길항제이다. 일부 예에서, PA는 도 1에 제시된 임의의 화합물이다. 일부 경우에, PA는 스테로이드, 예를 들어 글루코코르티코이드이다.
다른 적합한 페이로드는 고도로 소수성인 것, 예를 들어 친수성 성질로 인해 Ab 접합조건에 견딜 수 없는 것, 예를 들어 피롤리벤조디아제핀(PBD), SN38 (7-에틸-10-하이드록시-캄프토테신), 등 이다.
특정 실시양태에서, PA가 소수성 페이로드 부분인 본원의 임의의 화학식에 따른 항체-약물 접합제가 본 원에 제공된다.
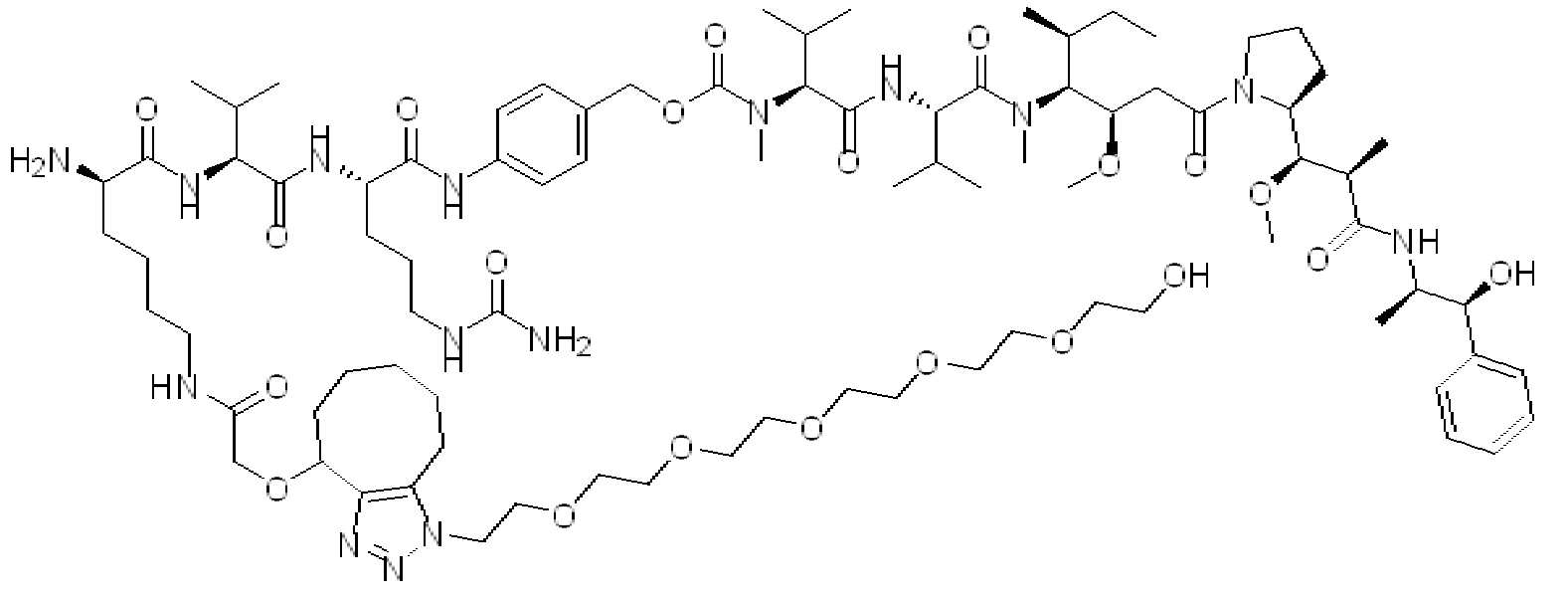
일부 실시양태에서, 화학식 (I)의 페이로드는 돌라스타틴 또는 이의 합성 유사체이다.
특정 실시양태에서, 화학식 (I)의 화합물은 페이로드는 모노페틸아우리스타틴 D(MMAD), (MMAE 모노메틸아우리스타틴 E(MMAE), 또는 모노메틸아우리스타틴F(MMAF), 또는 이의 입체 이성질체를 갖는 아우리스타틴이다.
특정 측면에서, 본 원에 기재된 화학식 (I)의 화합물은 항원-결합 단백질, 예를 들어 항체, 아우리스타틴페이로드 및 친수성 부분을 포함하는 단백질-약물 접합제, 예를 들어, 항체-약물 접합제다.
특정 실시양태에서, 화학식 (I)의 화합물의 페이로드는 메이탄시노이드이다. 미국에서 공개된 메이탄시노이드 페이로드 2016년 3월 25일 제출된 미국 정규 특허 출원번호 15/081,759제목:" MAYTANSINOID DERIVATIVES, CONJUGATES THEREOF, AND METHODS OF USE", 미국 특허 출원 공개 제 2016/0375147호로 공개된, 및 2017년 1월 24일에 출원 된 미국 임시 특허번호 15/414,537, 제목:" MAYTANSINOID DERIVATIVES, CONJUGATES THEREOF, AND METHODS OF USE". 특허번호 9,950,076은 본원에 참고로 포함된다. 특정 실시양태에서 PA는 DM1, DM3 또는 DM4이다. 특정 실시양태에서, PA는 이다. 특정 실시양태에서, PA는 이고, 여기서 A는 선택적으로 치환된 아릴렌 또는 헤테로 아릴렌이다. 특정 실시양태에서, PA는 이다.
특정 실시양태에서 물결선은 LL에 대한 결합을 나타낸다.
특정 측면에서, 본 원에 기재된 화학식 (I)의 화합물은 항원-결합 단백질, 예를 들어 항체, 메이탄시노이드 페이로드 및 친수성 부분을 포함하는 단백질-약물 접합제, 예를 들어, 항체- 약물 접합제 이다.
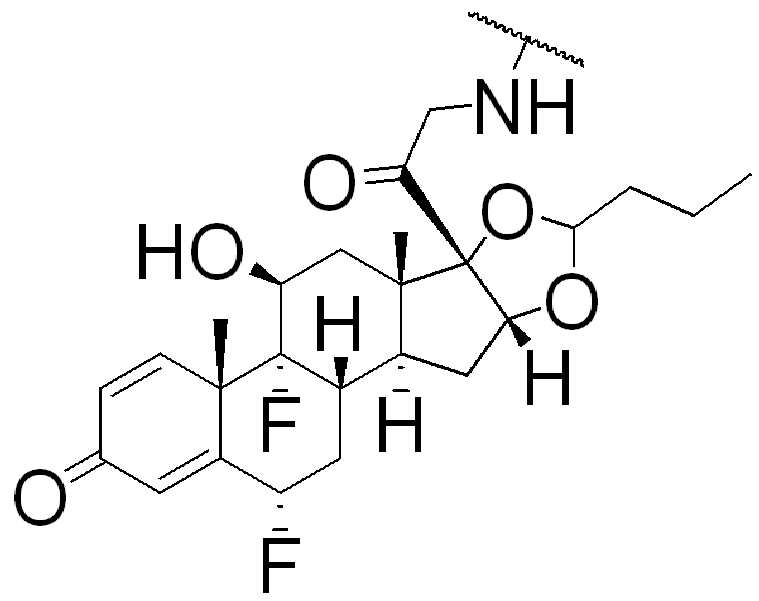
특정 실시양태에서, 화학식 (I)의 화합물의 페이로드는 화학식 (A)에 따른 글루코코르티코이드이다:
(A)
여기서
여기서 R 4 는 알킬, 아릴, 아릴알킬, 또는 N-함유 헤테로시클로알킬(an N-containing hetero cycloalkyl)이고,
여기서 알킬, 아릴, 아릴알킬, 및 N-함유 헤테로시클로알킬(an N-containing hetero cycloalkyl)은, 독립적으로 각 경우에, -NR Aa R Ab ;로 선택적으로 치환되고;
R 3 는 -OH, R Z -C(O)-X-, 헤테로알킬, 피페리디닐, -NR Aa R Ab , -옥시아릴-NR Aa R Ab 또는 -Z-A'R P ) t이고;
R Z 는 알킬;
X 는 O 또는 NR Aa 이고;
Z 는 S, S(O), S(O)2, SO2NR Aa , O, C(O)NR Aa , C(O), 또는 NR Aa 이고;
A' 는 아릴, 아릴알킬, 또는 헤테로아릴이고;
R P 는, 독립적으로 각 경우에, 할로, 선택적으로 치환된 알킬, -OH, 또는 -NR Aa R Ab 이고;
R Aa 및 R Ab 는, 독립적으로 각 경우에, -H, 선택적으로 치환된 알킬, 또는 선택적으로 치환된 아릴;
아래 첨자 a 는 0-19의 정수이며; 및
t 는 1-3의 정수이다;
단:
및
R 5A 및 R 5B 는 각각, 독립적으로, 할로 또는 수소원자이다.
특정 실시양태에서, PA는
또는 그의 제약상 허용되는 염, 용매화물 또는 입체 이성질체이다.
화학식 1110-1140 중 임의의 화학식에 따른 특정 실시양태에서, R 3 는 -O-아릴, -NR Aa R Ab , -알킬렌-NR Aa R Ab , -X-아릴렌-Y-NR Aa R Ab , -X-헤테로아릴렌-Y-NR Aa R Ab , 또는N-함유 헤테로시클로알킬; 여기서 X 는 존재하지 않거나, -N-, -CH2-, 또는 -O-이고; 여기서 Y 는 존재하지 않거나 또는 -CH2-이고; 및 R 4 는 알킬, 아릴, 알킬아릴, 또는 아릴알킬. 특정 실시양태에서, R 3 는 -O-아릴렌-NR Aa R Ab , -O-헤테로아릴렌-NR Aa R Ab 이고; 여기서 아릴 또는 헤테로아릴 은 선택적으로 치환된 할로겐, 중수소, 히드록실, 또는 메톡실로 선택적으로 치환한다. 특정 실시양태에서, R 3 는 -O-페닐-NR Aa R Ab , -O-헤테로아릴렌-NR Aa R Ab 이고; 여기서 페닐 또는 헤테로아릴은 선택적으로 치환된 할로겐 또는 중수소이다. 특정 실시양태에서, R 4 는n-프로필이다. 특정 실시양태에서, R Aa 및 R Ab 는 각각 독립적으로 수소 또는 알킬이다. , 특정 실시양태에서, R Aa 및 R Ab 중 하나는 LL에 대란 결합으로 치환된다. 특정 실시양태에서, PA 는
또는 그의 제약상 허용되는 염, 용매화물 또는 입체 이성질체. 특정 실시양태에서, PA 는 , 또는 그의 제양상 허용되는 염, 용매화물 또는 입체 이성질체이다. 특정 실시양태에서, PA 는 , 또는 그의 제양상 허용되는 염, 용매화물 또는 입체 이성질체이다. 특정 실시양태에서, PA 는 , 또는 그의 제양상 허용되는 염,
용매화물 또는 입체 이성질체이다. 특정 실시양태에서, PA 는 , 또는 그의 제양상 허용되는 염, 용매화물 또는 입체 이성질체이다. 특정 실시양태에서, PA 는이며, 또는 그의 제양상 허용되는 염, 용매화물 또는 입체 이성질체이다 . 이러한 실시예에서, 물결선은 LL에 대한 결합을 나타낸다.
일부 실시양태에서, PA는 이하로 이루어진 군으로부터 선택된다:
또는 PA는 R 3 기를 통해 잔기로서 연결되어 있으며, 예를 들어, 접합제는 페이로드 1차 또는 2차 아민의 잔기에 대한 결합을 통해 링커에 연결된 상기 기재된 페이로드를 포함한다.
특정 측면에서, 본 원에 기재된 화학식 (I)의 화합물은 항원-결합 단백질, 예를 들어 항체, 화학식 A의 페이로드, 및 친수성 부분 부분을 포함하는 단백질-약물 접합체, 예를 들어, 항체-약물 접합체이다.
2018년 1월 8일자로 출원된 미국 가출원 제 62/614,905호에 개시된 "STEROIDS AND ANTIBODY CONJUGATES THEREOF"및 2017년 11월 7일에 출원된 미국 특허 출원 제 15/806,197호에 개시된 스테로이드 페이로드, 제목 "STEROIDS AND PROTEIN-CONJUGATES THEREOF"는 본 원에 참조로 포함된다.
특정 실시양태에서, 화학식 (I)의 페이로드는 화학식 (B)에 따른 구조를 갖는 LXR 조절제 이다:
화학식 (B)
또는 그 제약상 허용되는 입체 이성질체 형태, 여기서
W 는 -CH2-, -N(H)-, 또는 -O-이고;
R B1 는 -H, -OH, -NH2, 알킬, 또는 -OP(O)(OR 6 )(OH)-OP(O)(OR 6 )2이고;
R B2 는 -H, -OH, -CH2NH2, R B3 , R B4 , R B5 , 또는 -O-R B5 , 여기서 R B1 및 R B2 는 동시에 -H가 아니며;
R B3 는 -N(R 6 )2이고,
R B4 는 -X-Y-Z 이고,
X 는 -O- 및 -N(H)-로 구성된 그룹에서 선택되고;
Y 는 알킬렌, 치환된 알킬렌 (제한적으로 옥소 치환(예를 들어, =O)을 포함하는), 헤테로알킬렌, 및 치환된 헤테로알킬렌 (제한적으로 옥소 치환 (예를 들어,=O)을 포함 함)으로 이루어진 군으로부터 선택되고;
Z 는 -OH 및 -NH2로 이루어진 군에서 선택되고;
R B5 는 알킬, 헤테로시클로알킬, 또는 치환된 헤테로시클로알킬, 여기서 각각의 헤테로시클로알킬 또는 치환된 헤테로시클로알킬은 질소 및 산소 원자를 포함하고, 하나 이상의 -OH 및 -CH2OH 치환기, 또는 하나 이상의 1차 또는 2차 질소를 포함한다, 예를 들어, O-글루코스 이고;
각각의 R 6 는 각 경우에, -H, 아미노산 잔기, N-알킬 아미노산 잔기, 펩티드, 또는 알킬; 및
각 R 7 는, 독립적으로, 할로, C1-6 알킬, C1-6 알콕시, -CN, O-글루코스, O-아미노산 잔기, 및 O-PEGb, 여기서 각 아래 첨자 b 는 0내지3의 정수이다.
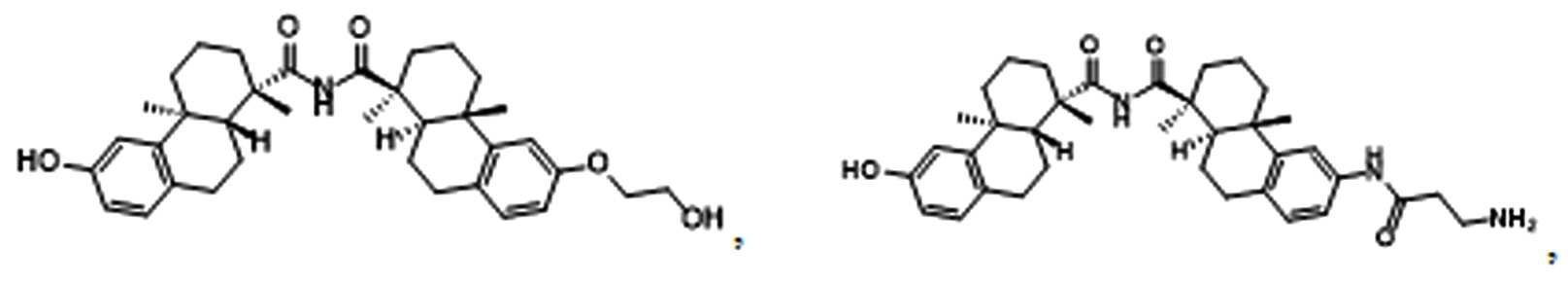
특정 실시양태에서, R B1 또는 R B2 는 치환된 LL에 결합으로 치환된다. 특정 실시양태에서, PA 는 하기로부터 선택된다:
특정 실시양태에서, 물결선은 LL에 대한 결합을 나타낸다.
특정 실시양태에서, PA는 다음으로 이루어진 군으로부터 선택된다:
또는 그의 제약상 허용되는 입체 이성질체 형태, 여기서 PA는 RB1 또는 RB2기를 통해 잔기로 연결되며, 예를 들어, 접합제는 페이로드의 1차 또는 2차 아민의 잔기에 대한 결합을 통해 링커에 연결된 상기 기재된 페이로드를 포함한다.
특정 측면에서, 본 원에 기재된 화학식 (I)의 화합물은 단백질-약물 접합제, 예를 들어, 항원-결합 단백질, 예를 들어, 항체, 화학식 (B)의 페이로드, 및 친수성 부분을 포함하는 항체-약물 접합제, 예를 들어, 항체-약물 접합제다.
2017년 5월 18일자로 출원된 제목" BIS-OCTAHYDROPHENANTHRENE CARBOXAMIDES AND PROTEIN CONJUGATES THEREOF"인 미국 가출원 제 62/508,327호에 개시된 LXR 변조기 페이로드는 본 명세서에 참조로 포함된다.
본 명세서에 제시된 실시예의 범위 내에서 미국에 개시된 페이로드가 고려된다.
2015년 9월 14일에 출원된 미국의 비 특허 출원원번호 14/776,668호에 개시된 제목이" BIOLOGICALLY ACTIVE MOLECULES, CONJUGATES THEREOF, AND THERAPEUTIC USES"이며, 미국으로 공개되었다. 2016년 2월 23일에 출원된 미국 특허 출원 공개번호 2016/0030591 및 미국 비 잠정 출원번호 14/913,965는 제목이" PHARMACEUTICAL COMPOSITIONS COMPRISING MACROLIDE DIASTEREOMERS, METHODS OF THEIR SYNTHESIS AND THERAPEUTIC USES"이며, 미국으로 공개되었다. 특허 출원공개 번호 2016/0354482에서, 상기 페이로드의 개시는 여기에 참조로 포함된다.
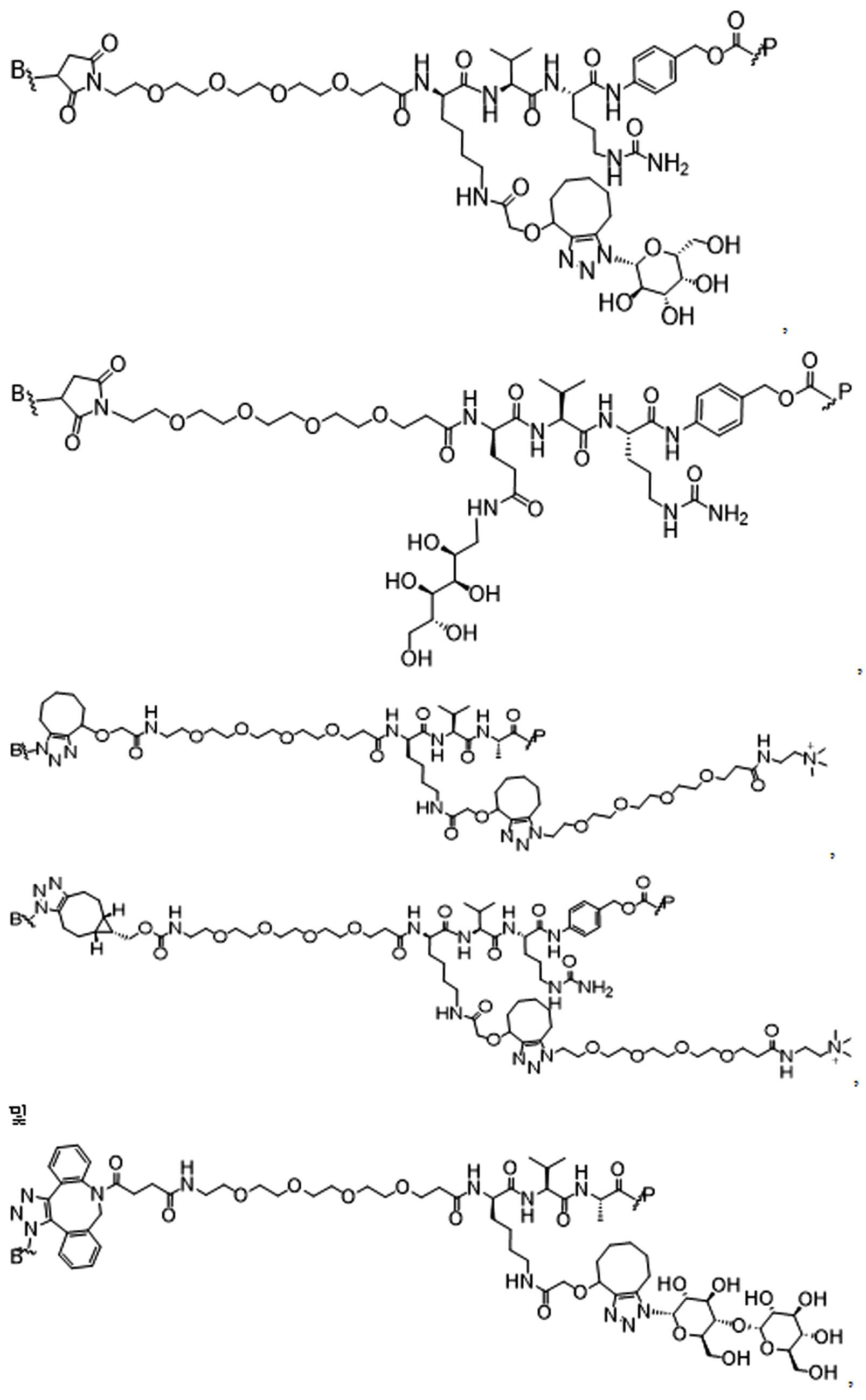
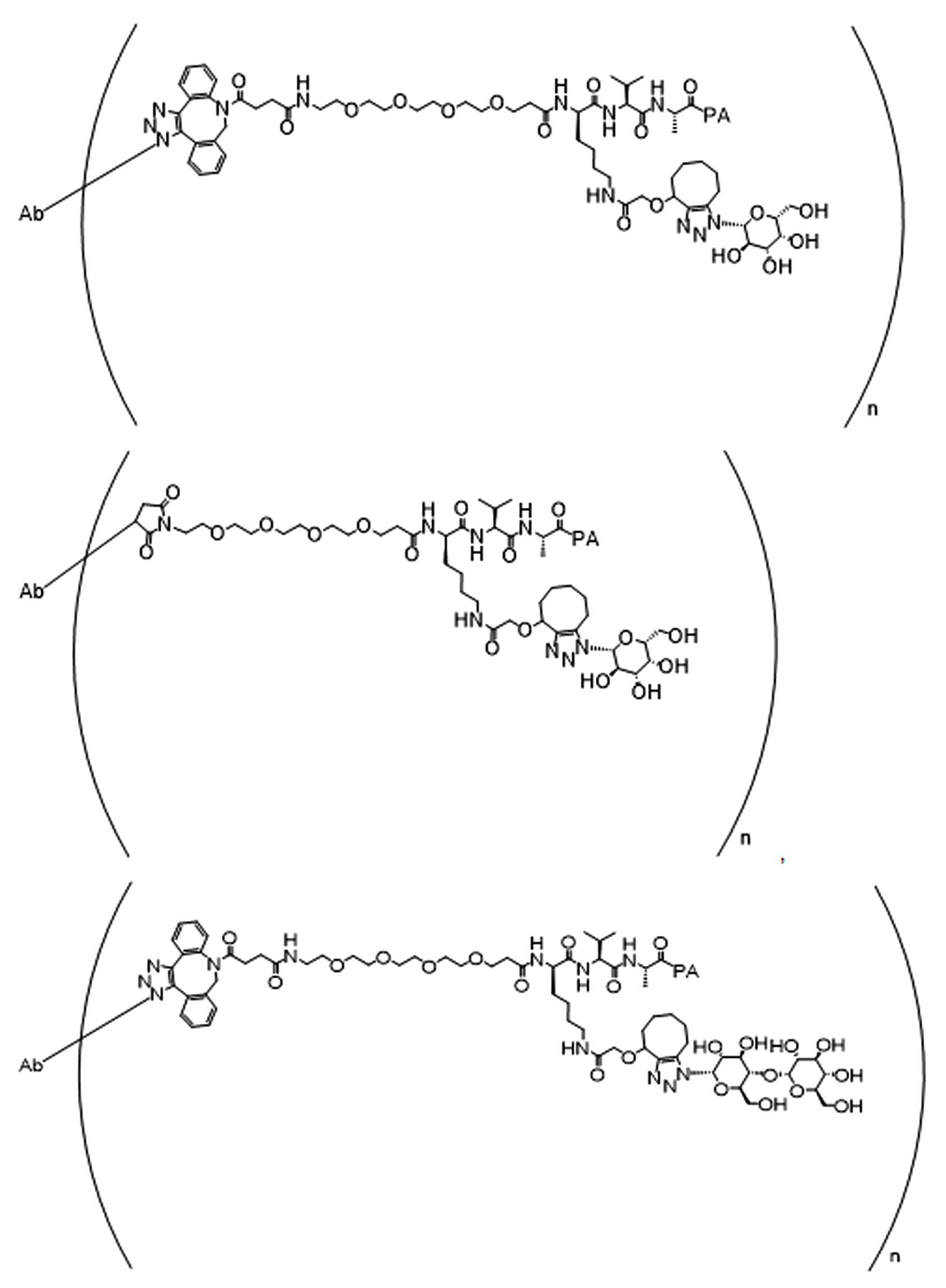
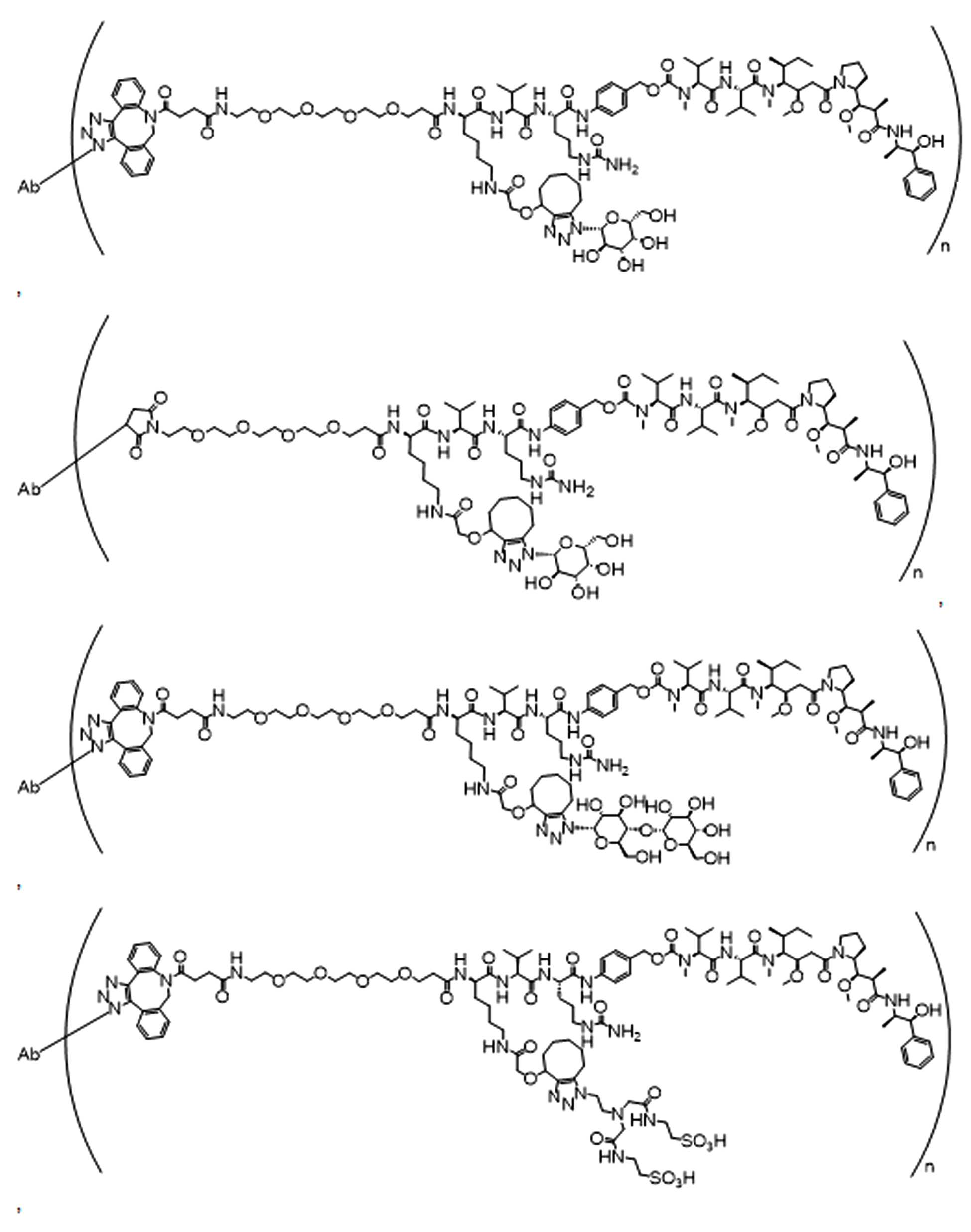
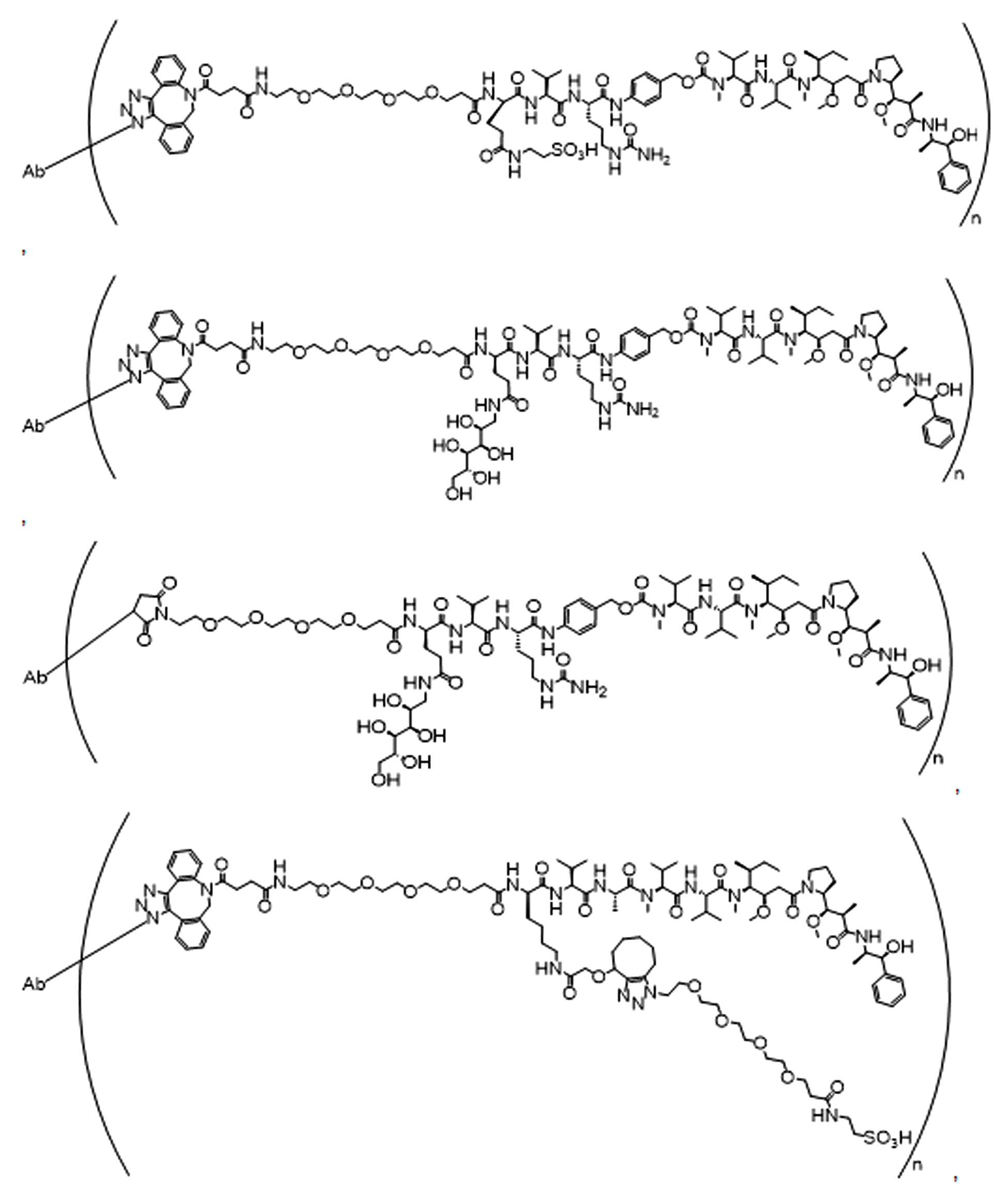
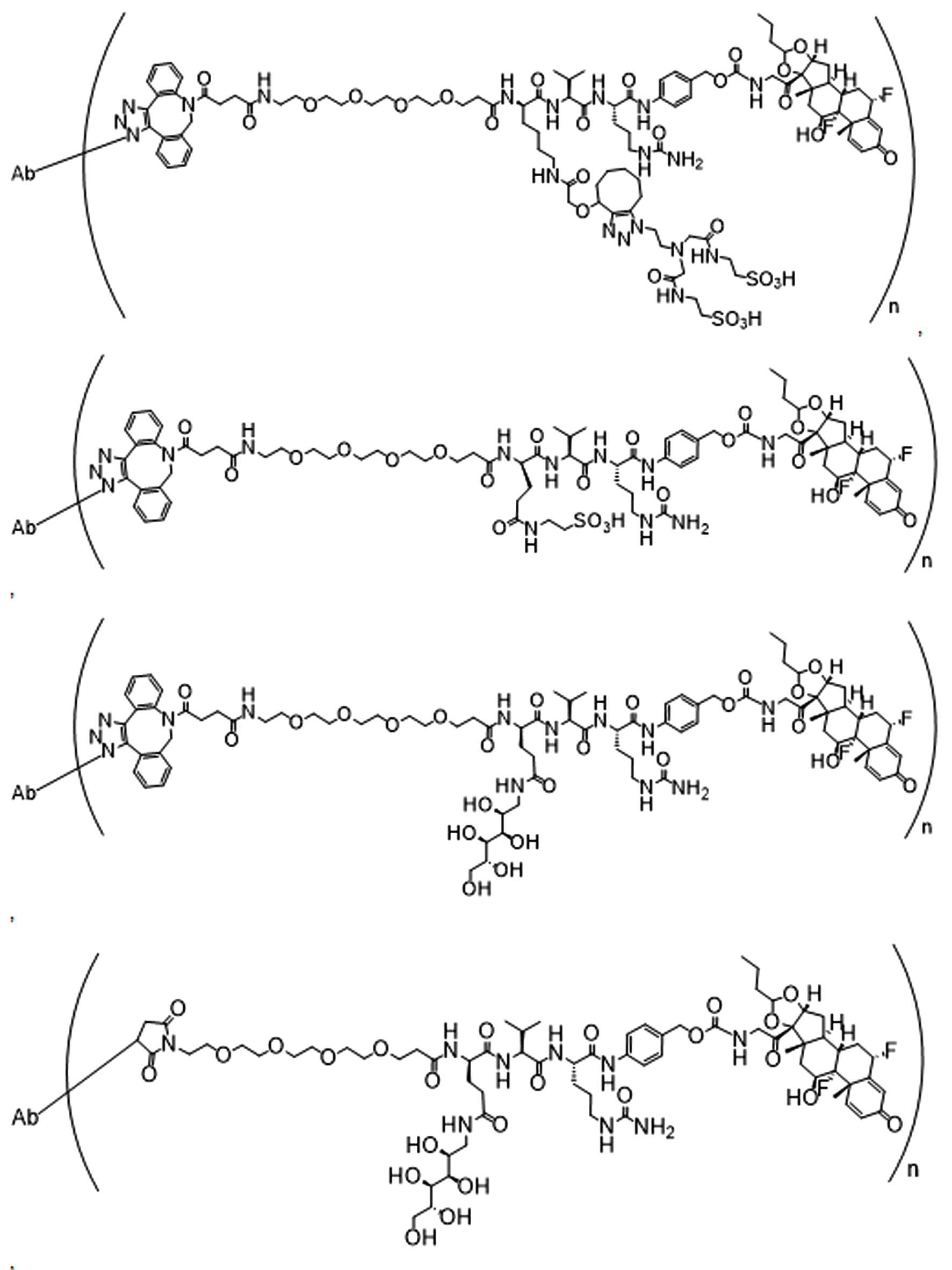
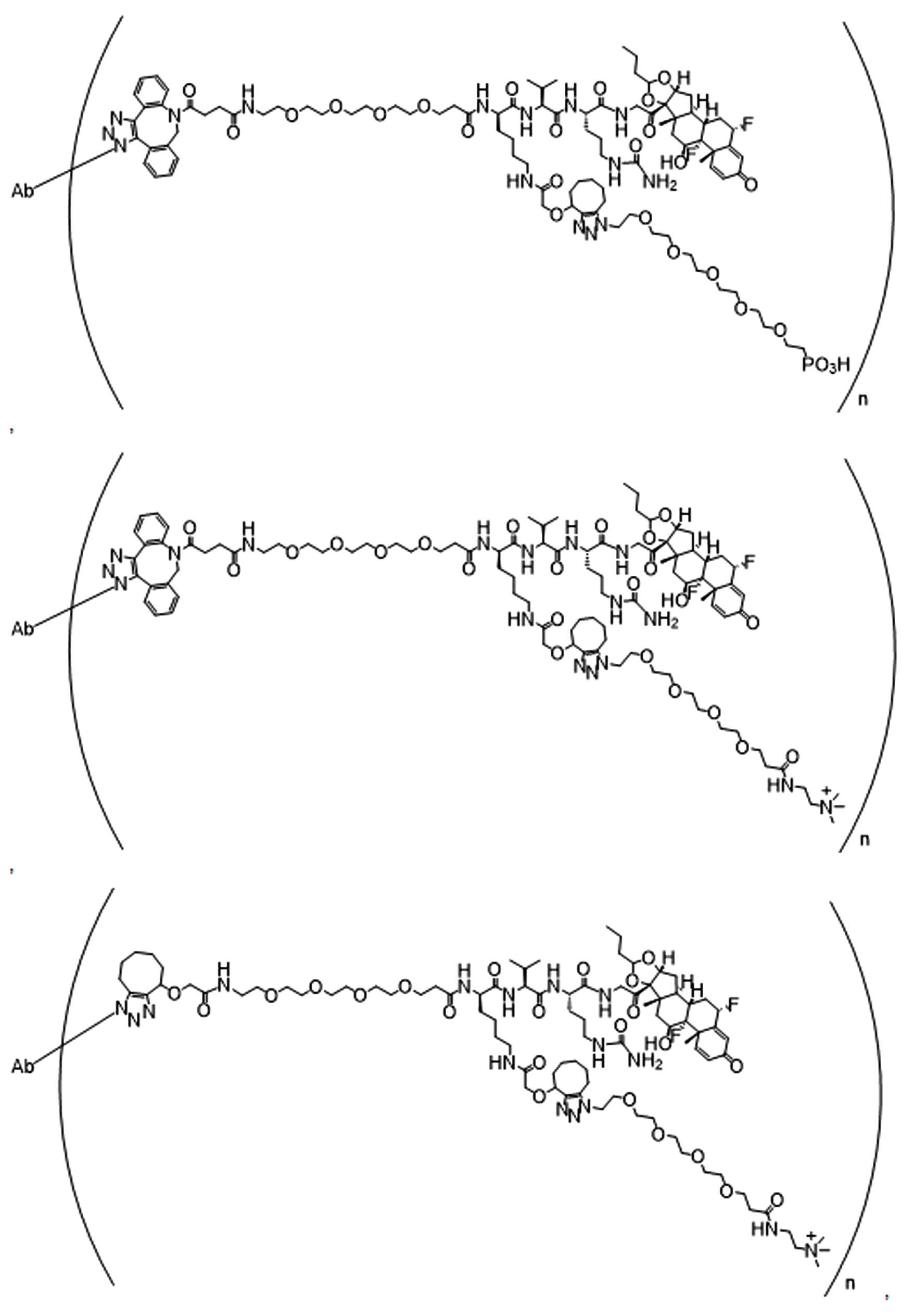
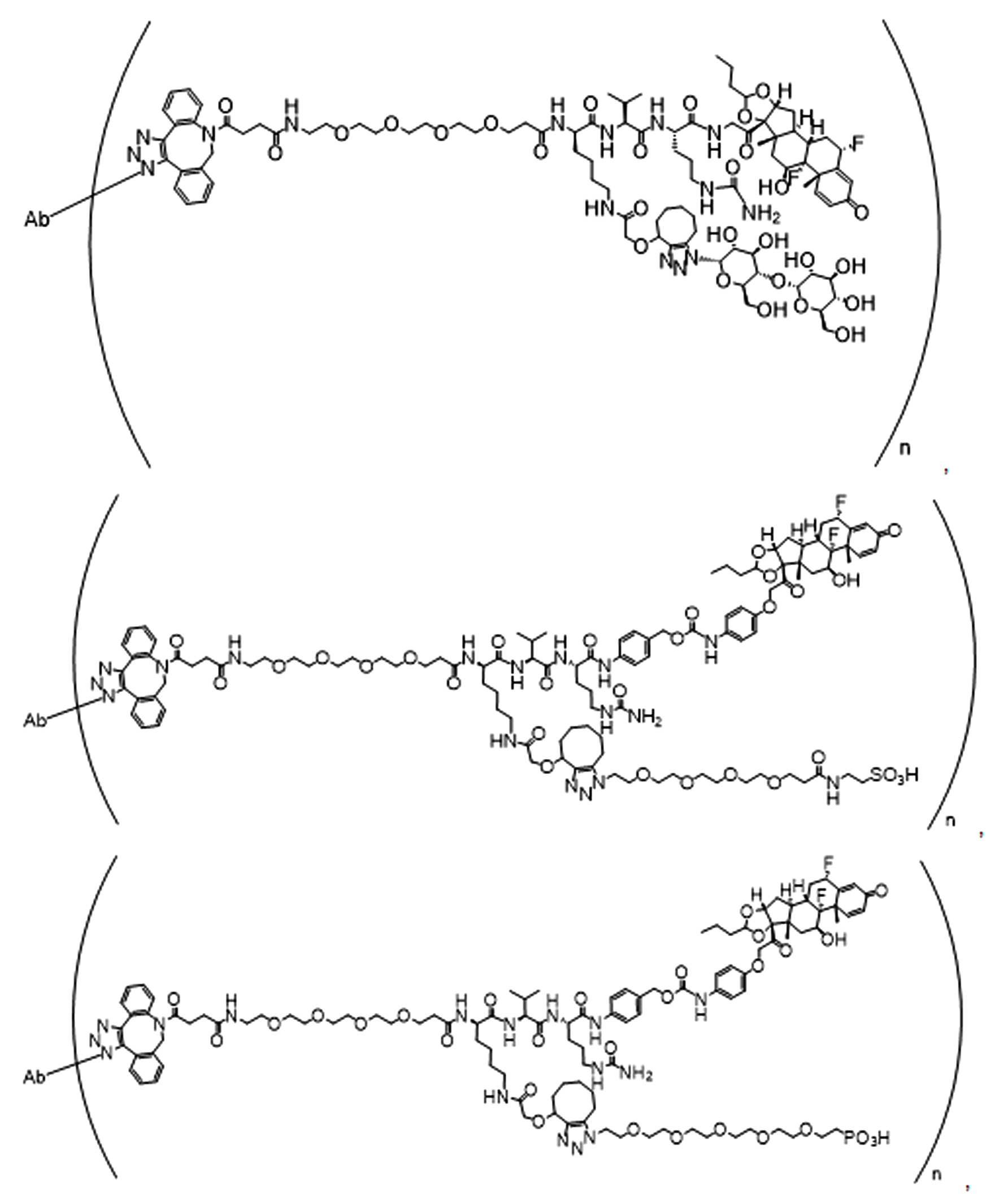
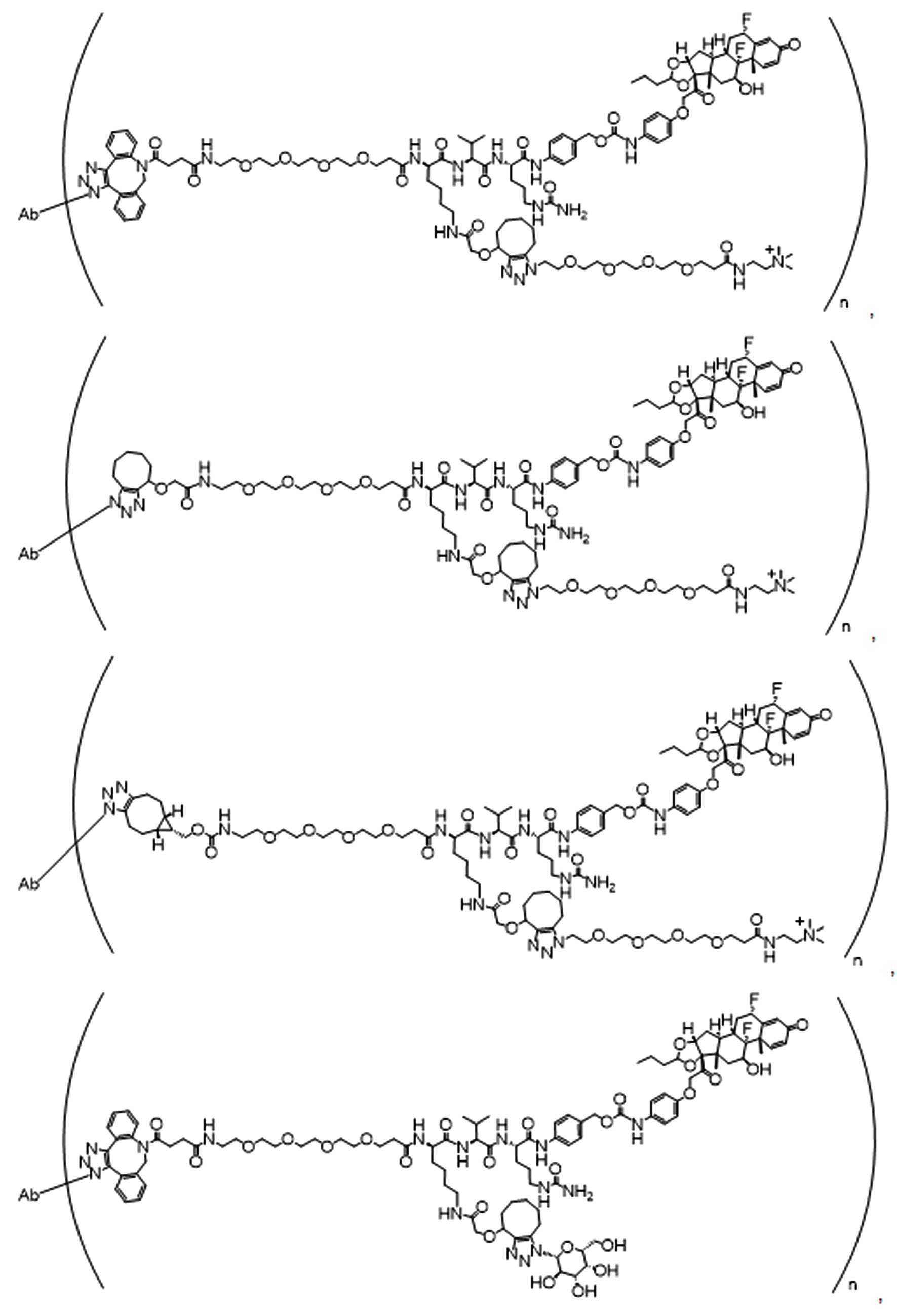
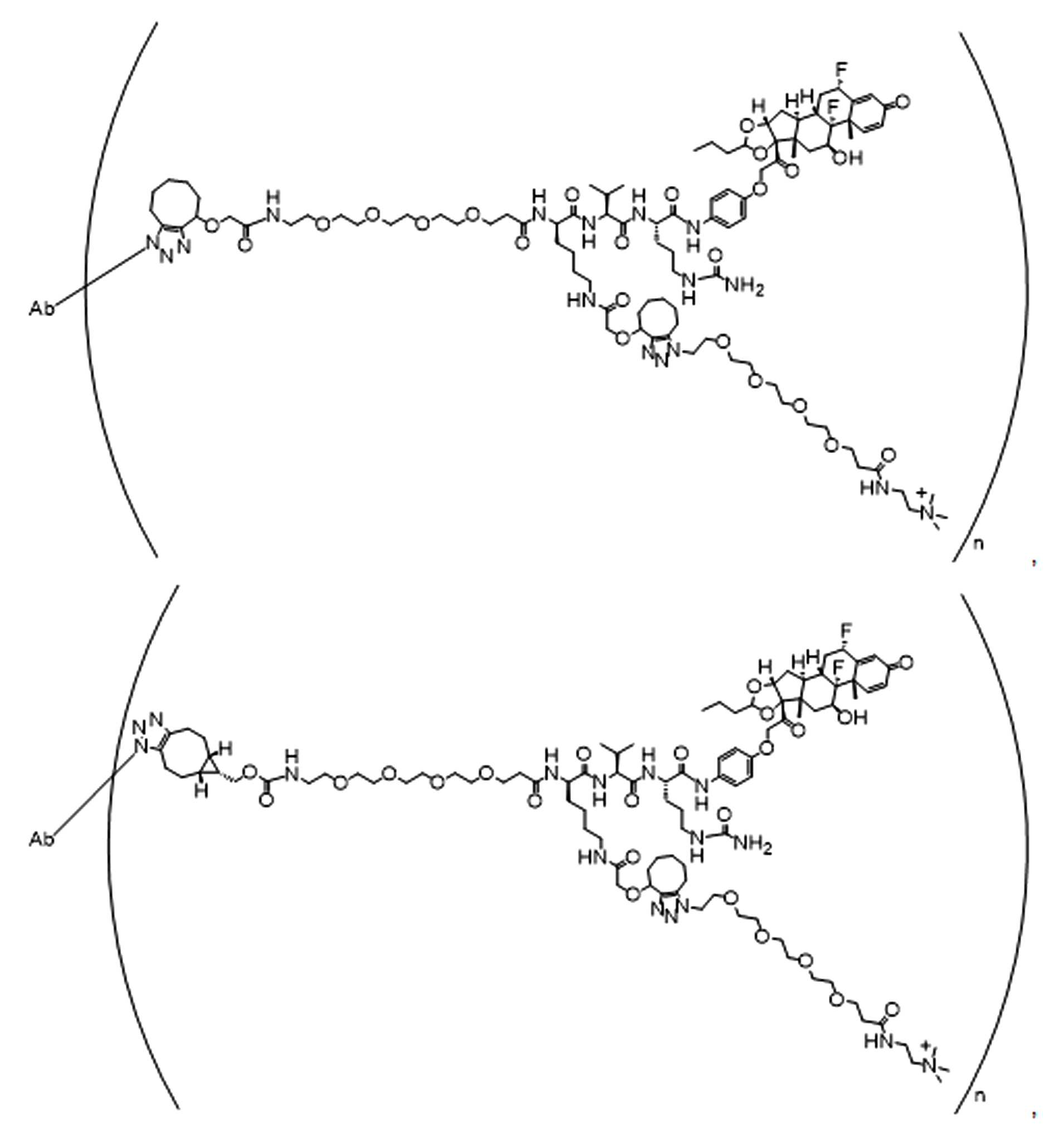
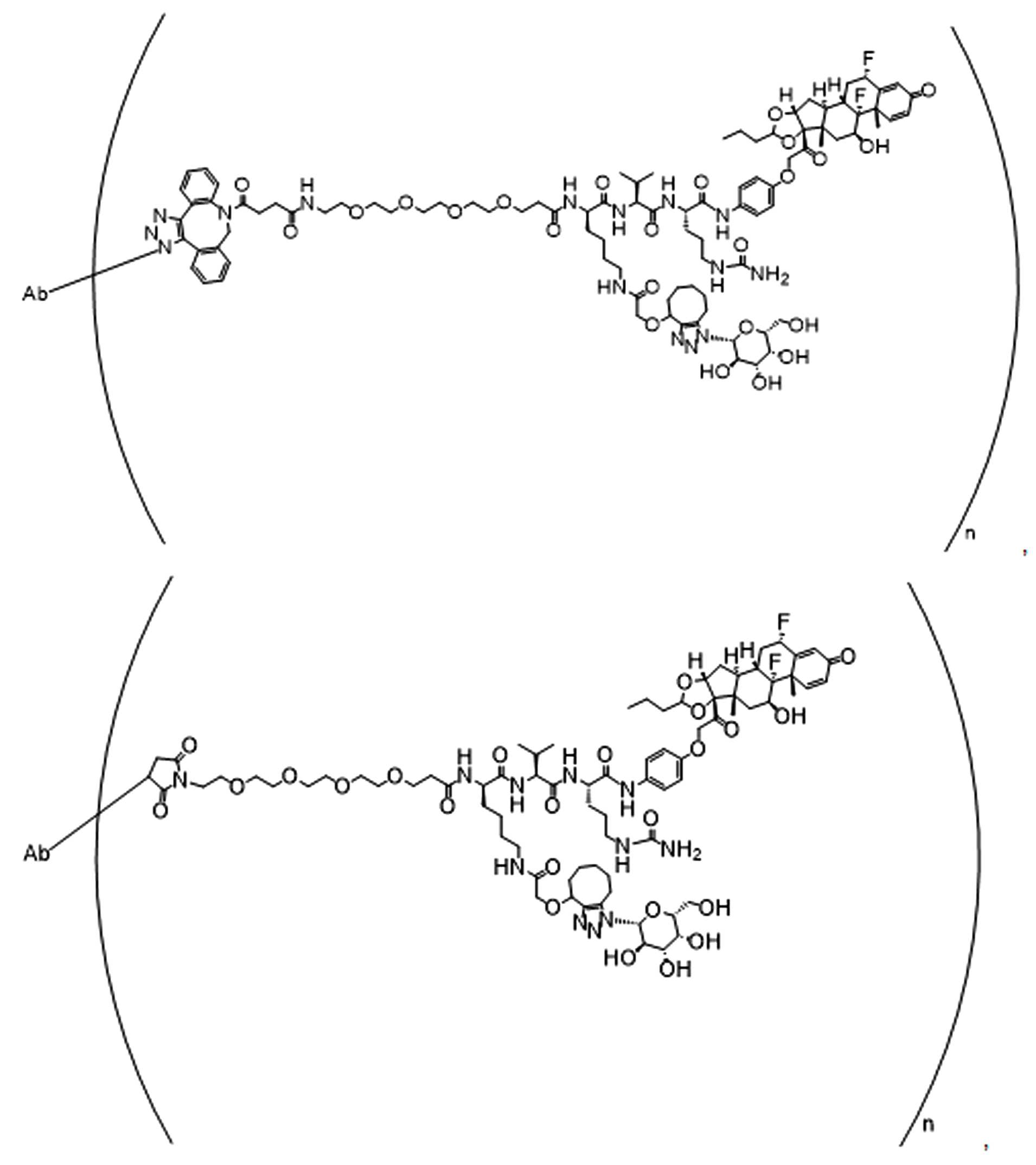
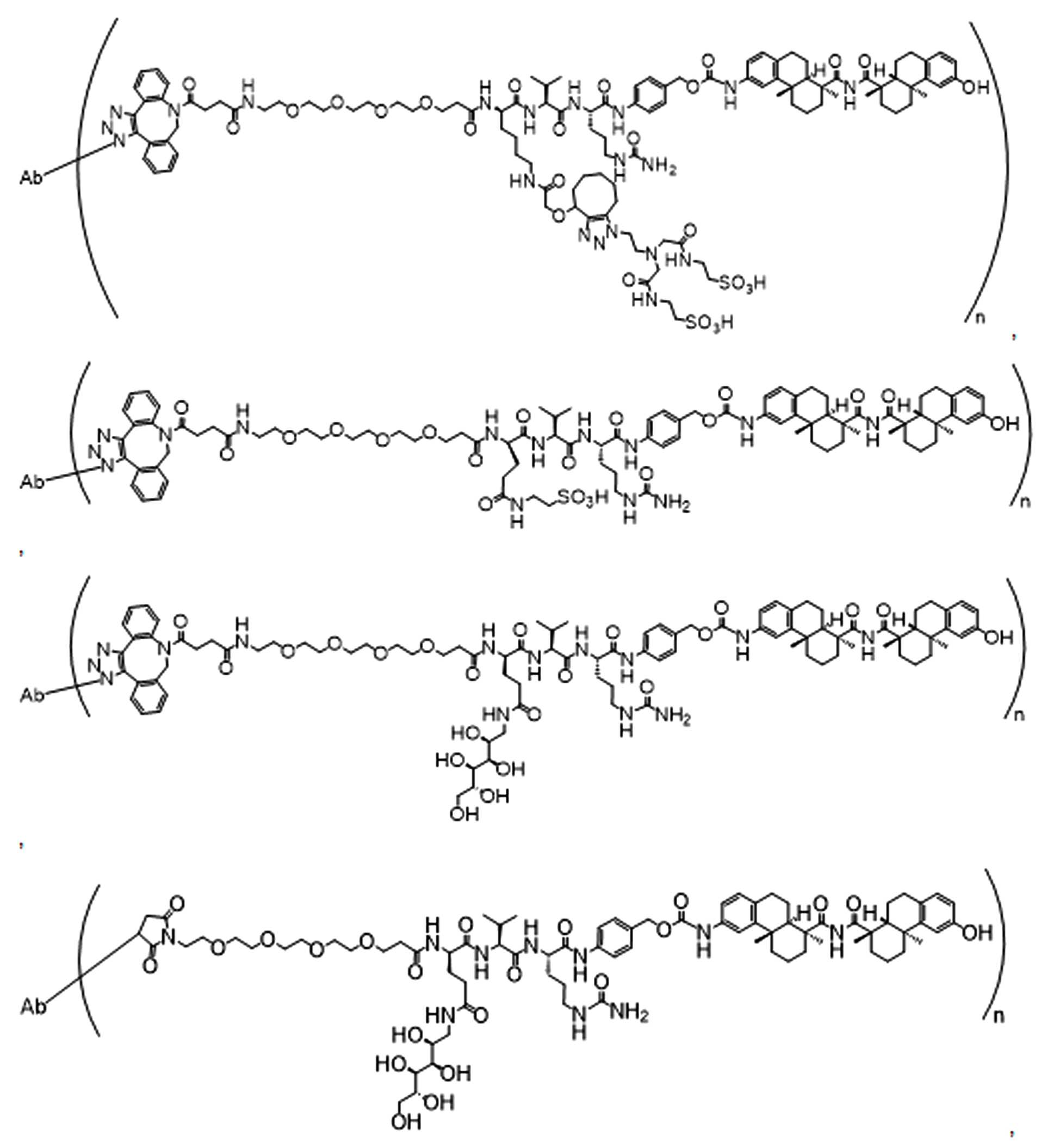
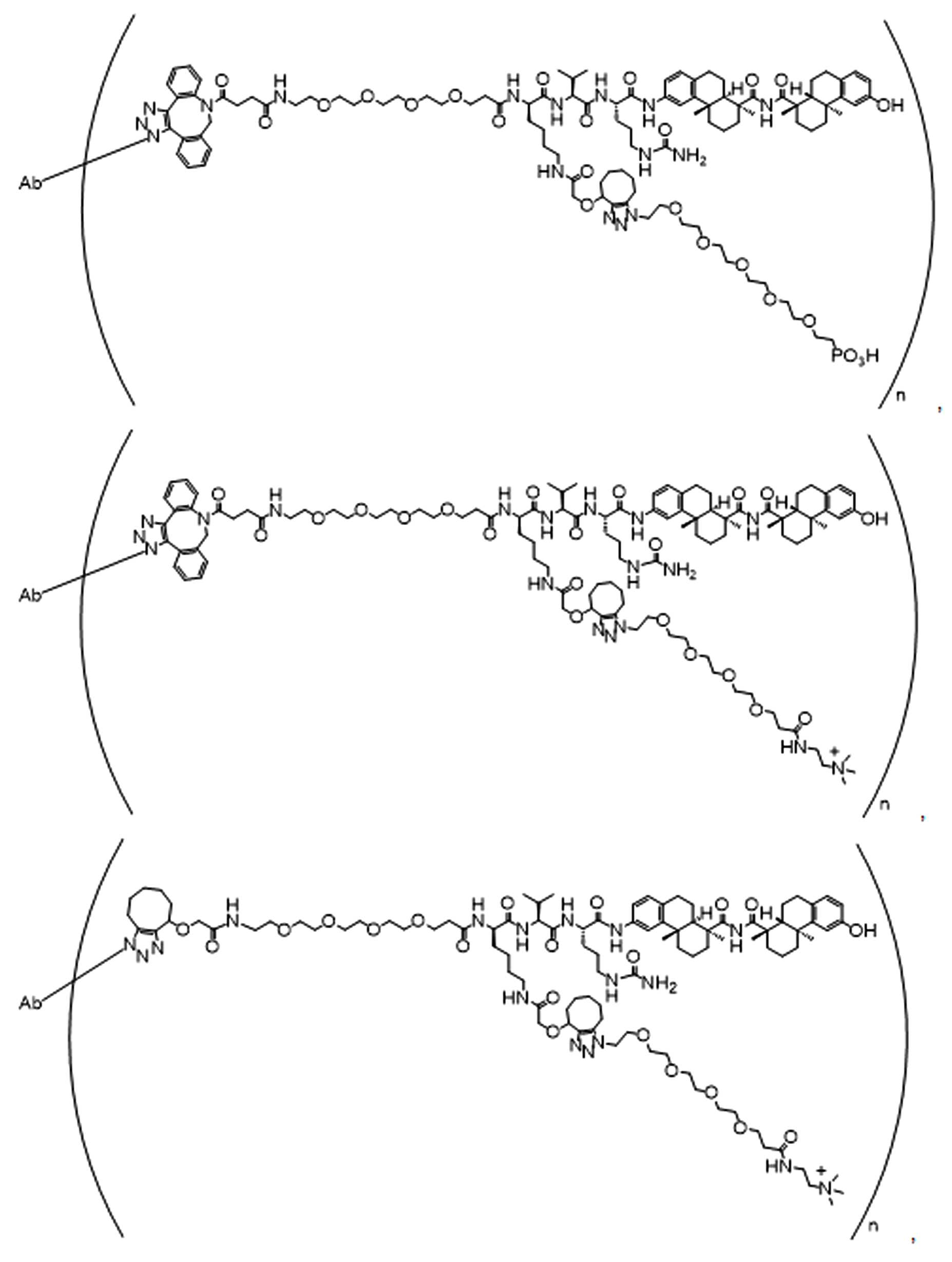
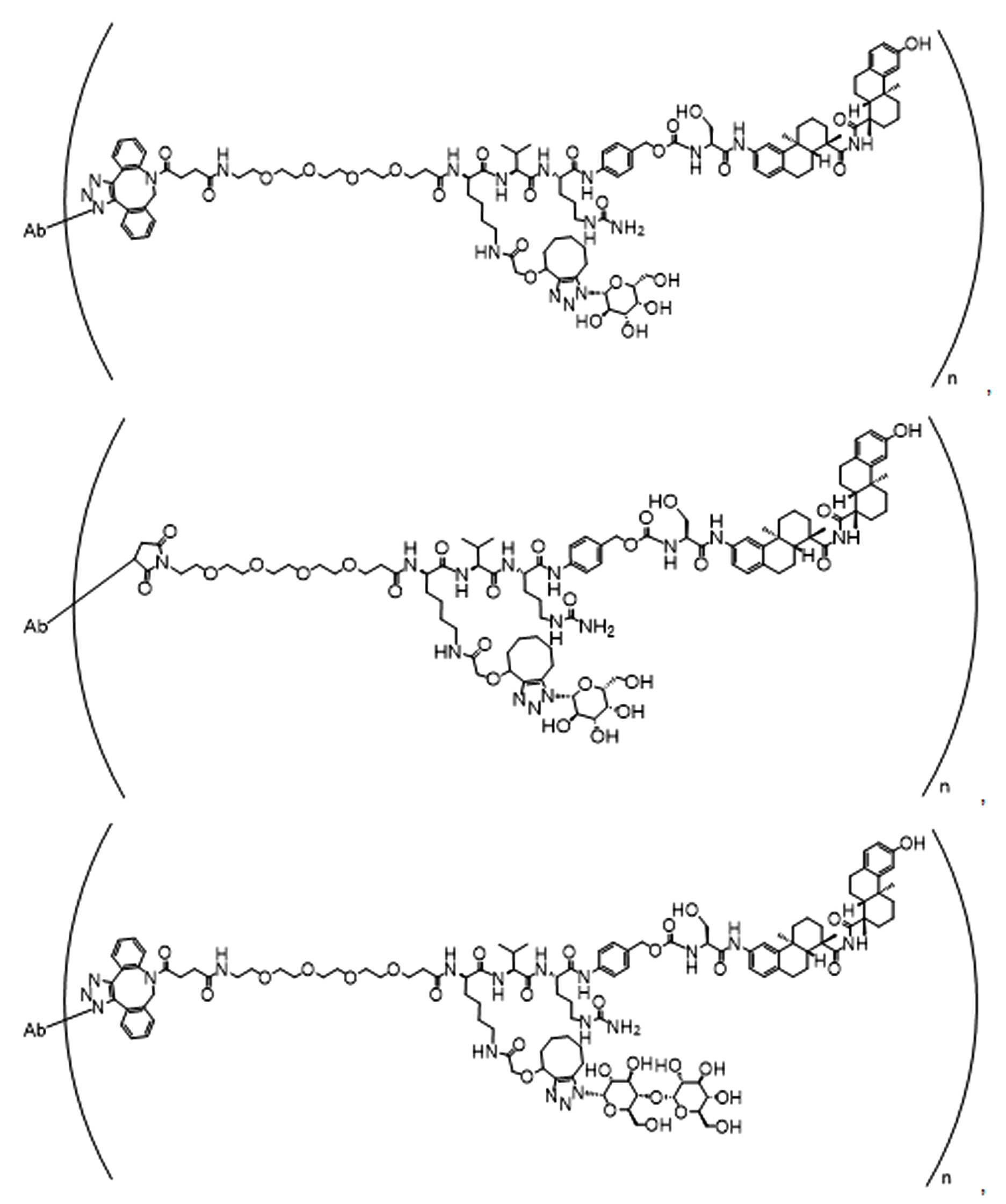
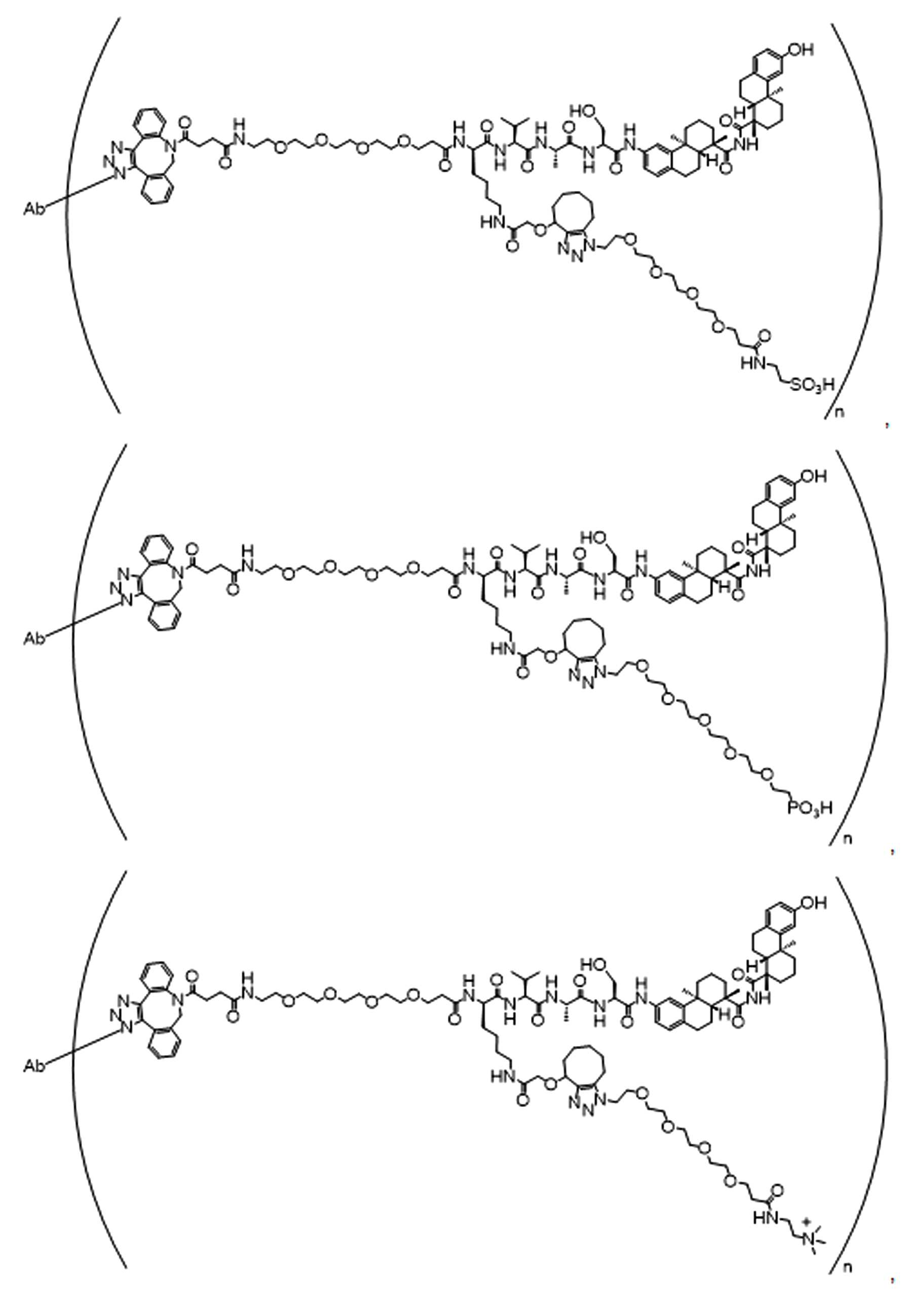
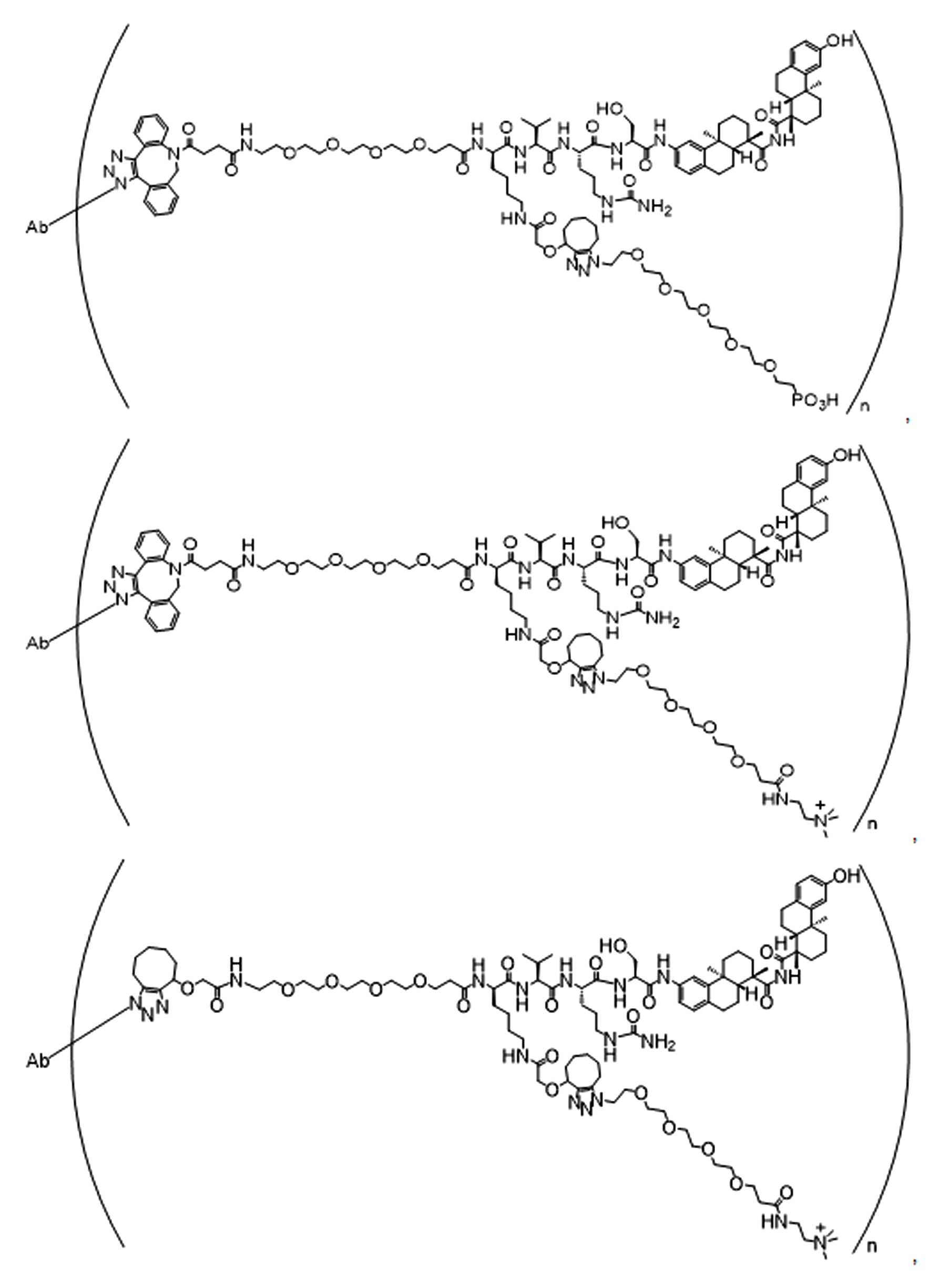
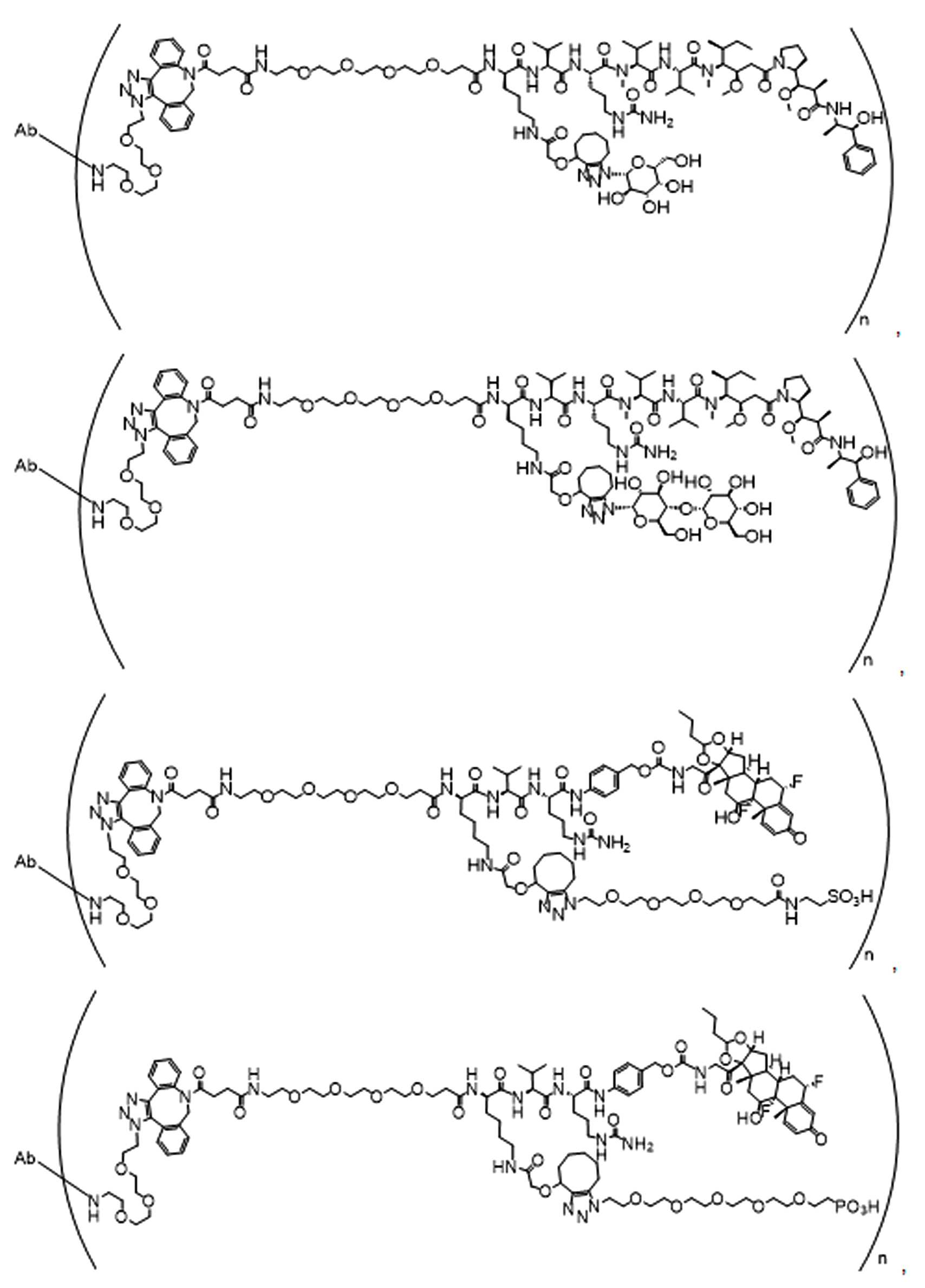
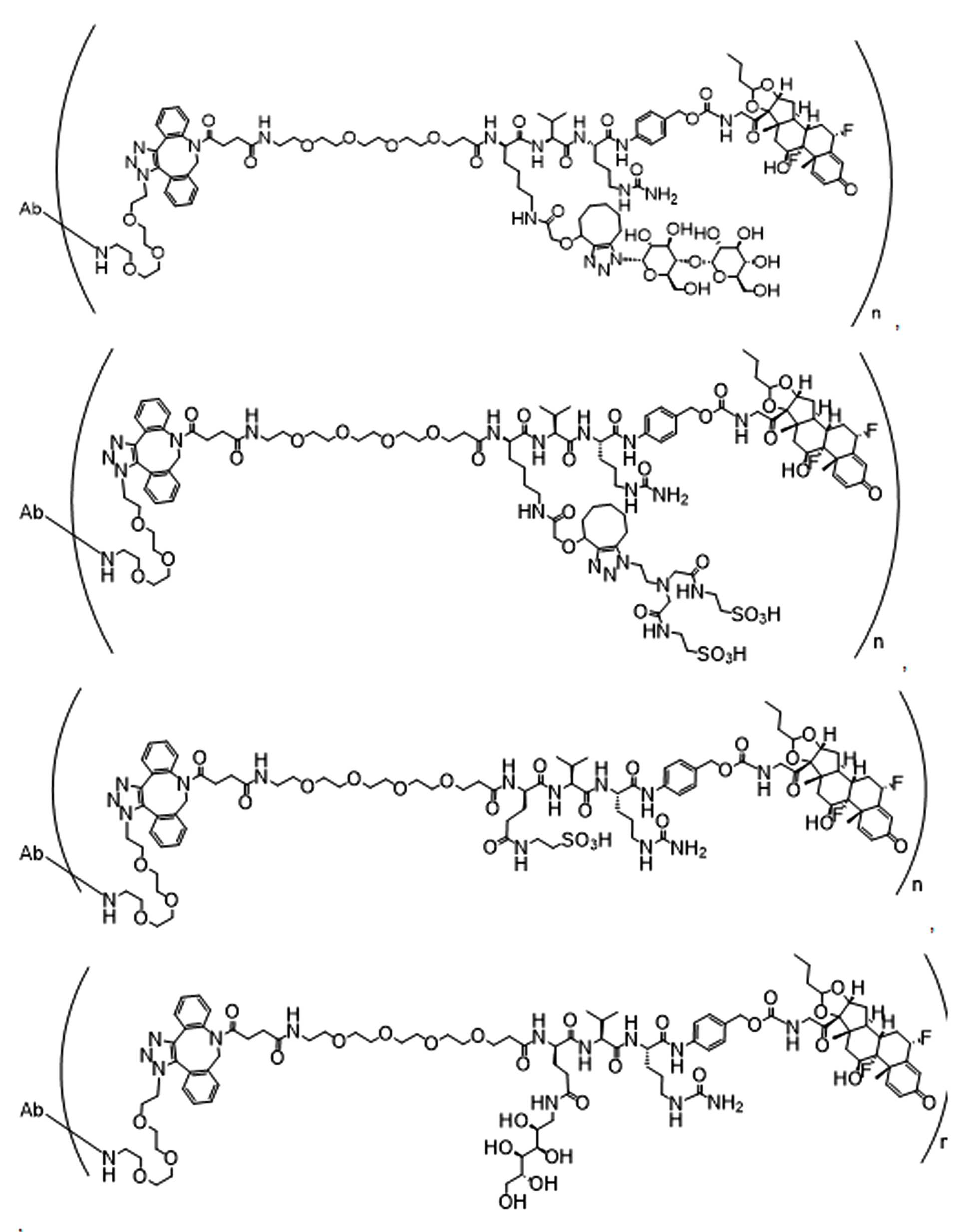
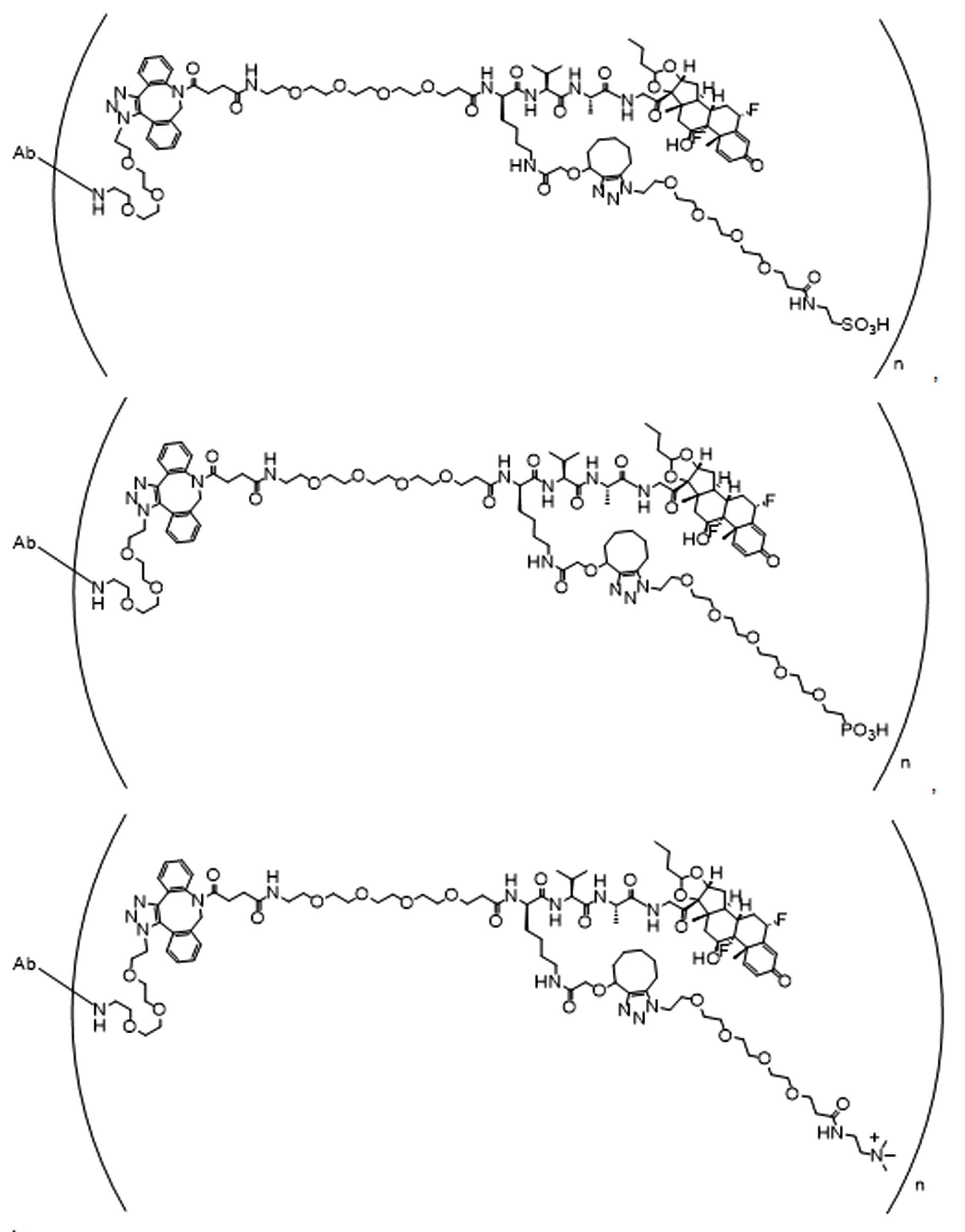
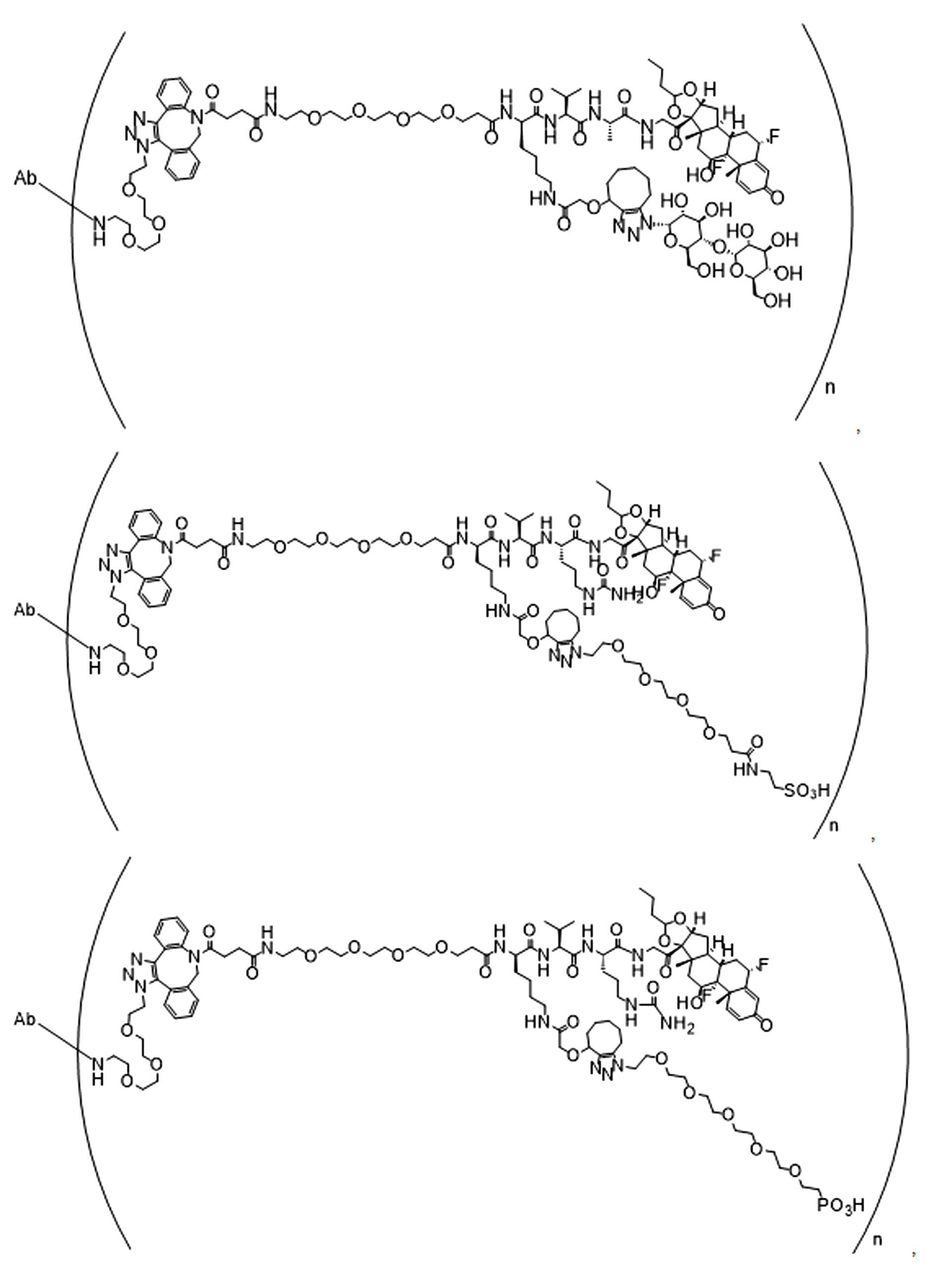
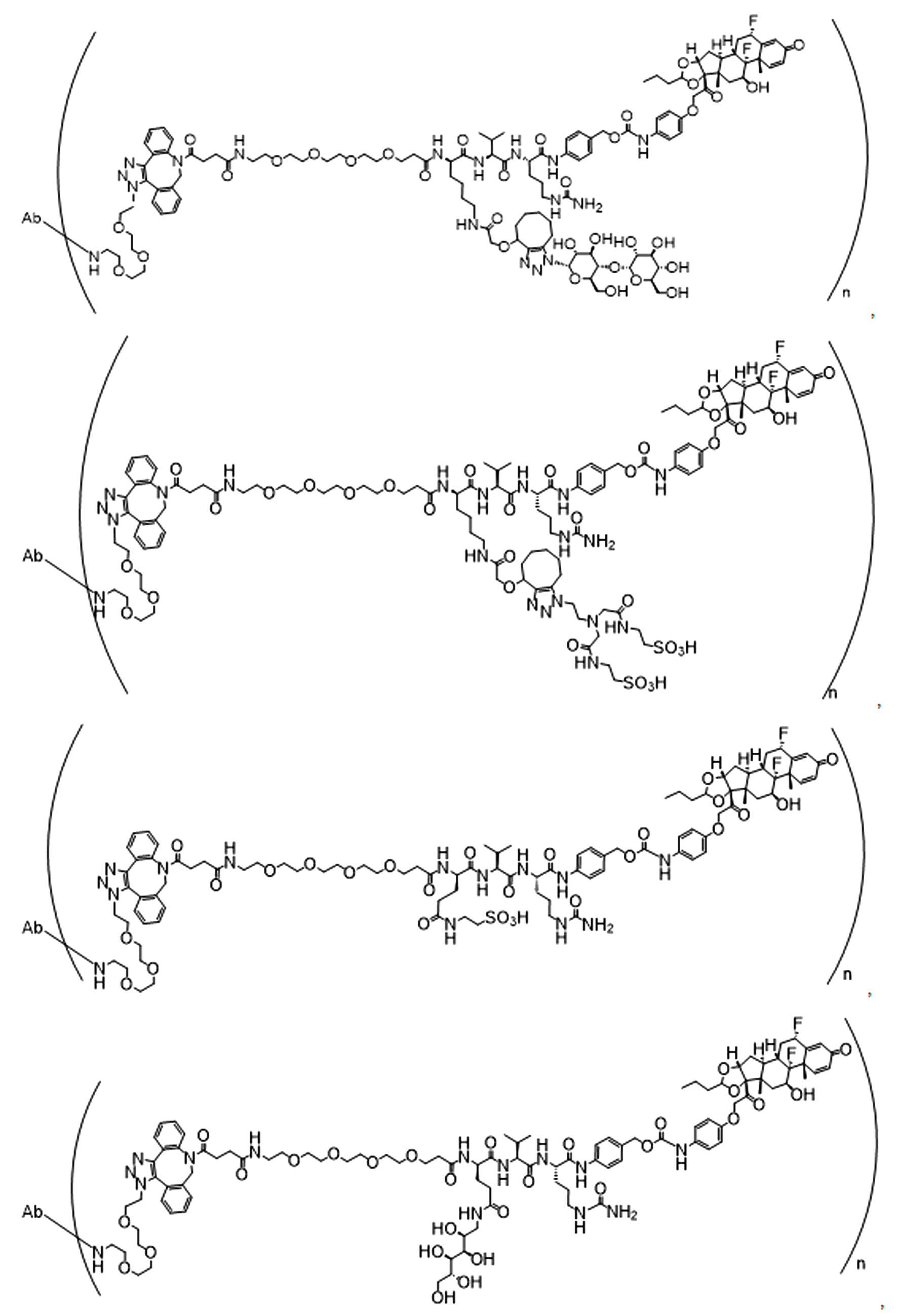
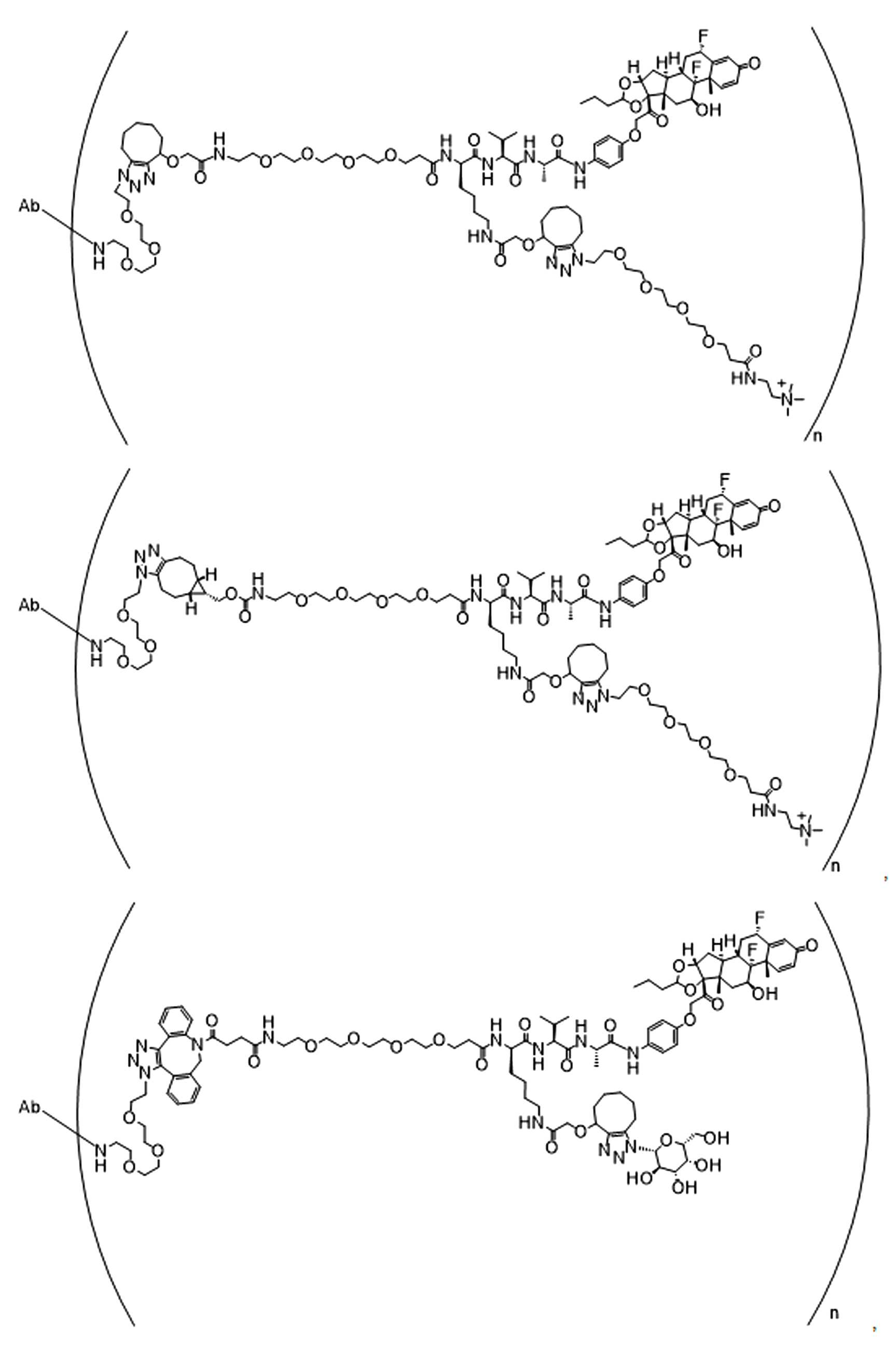
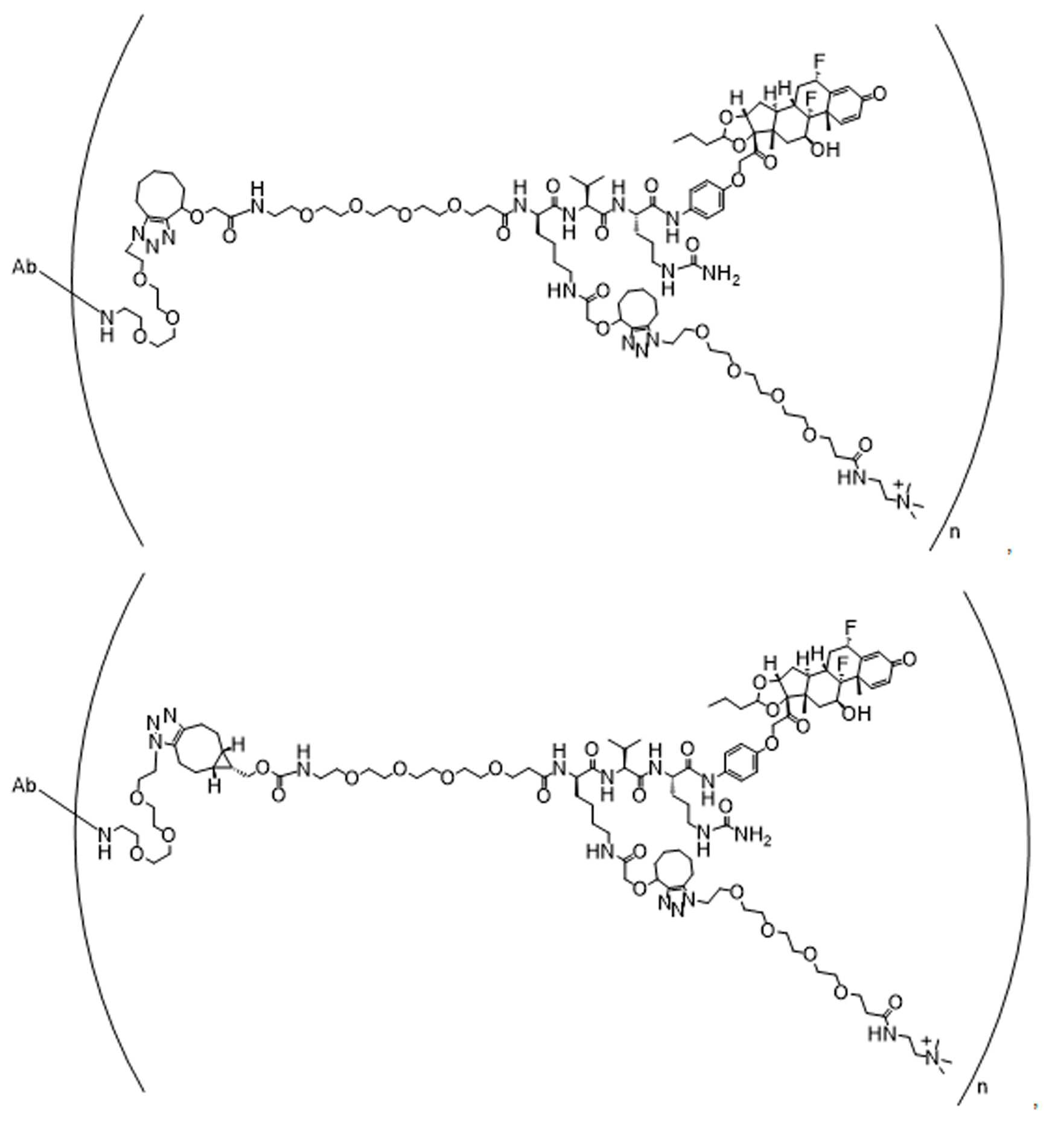
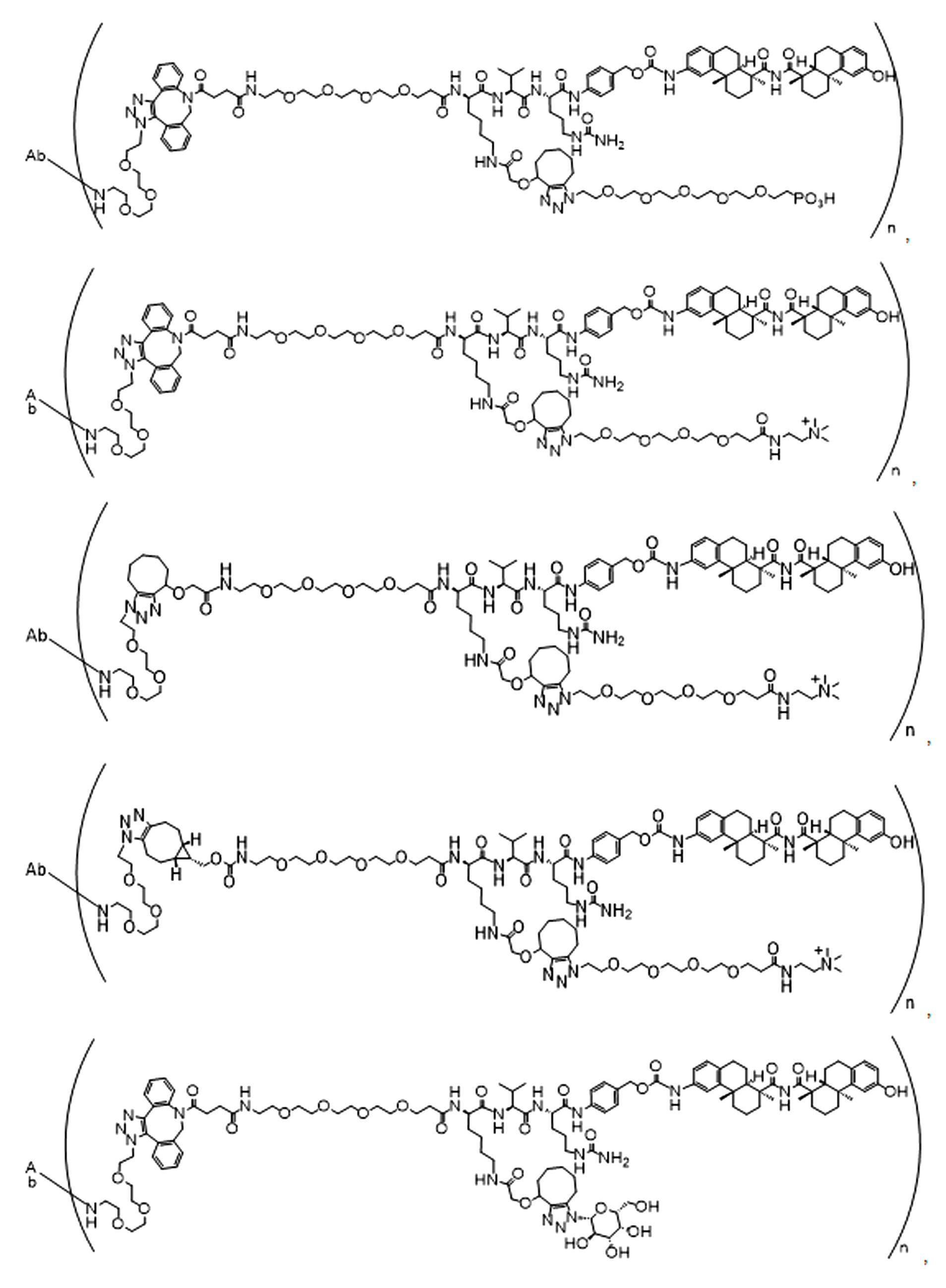
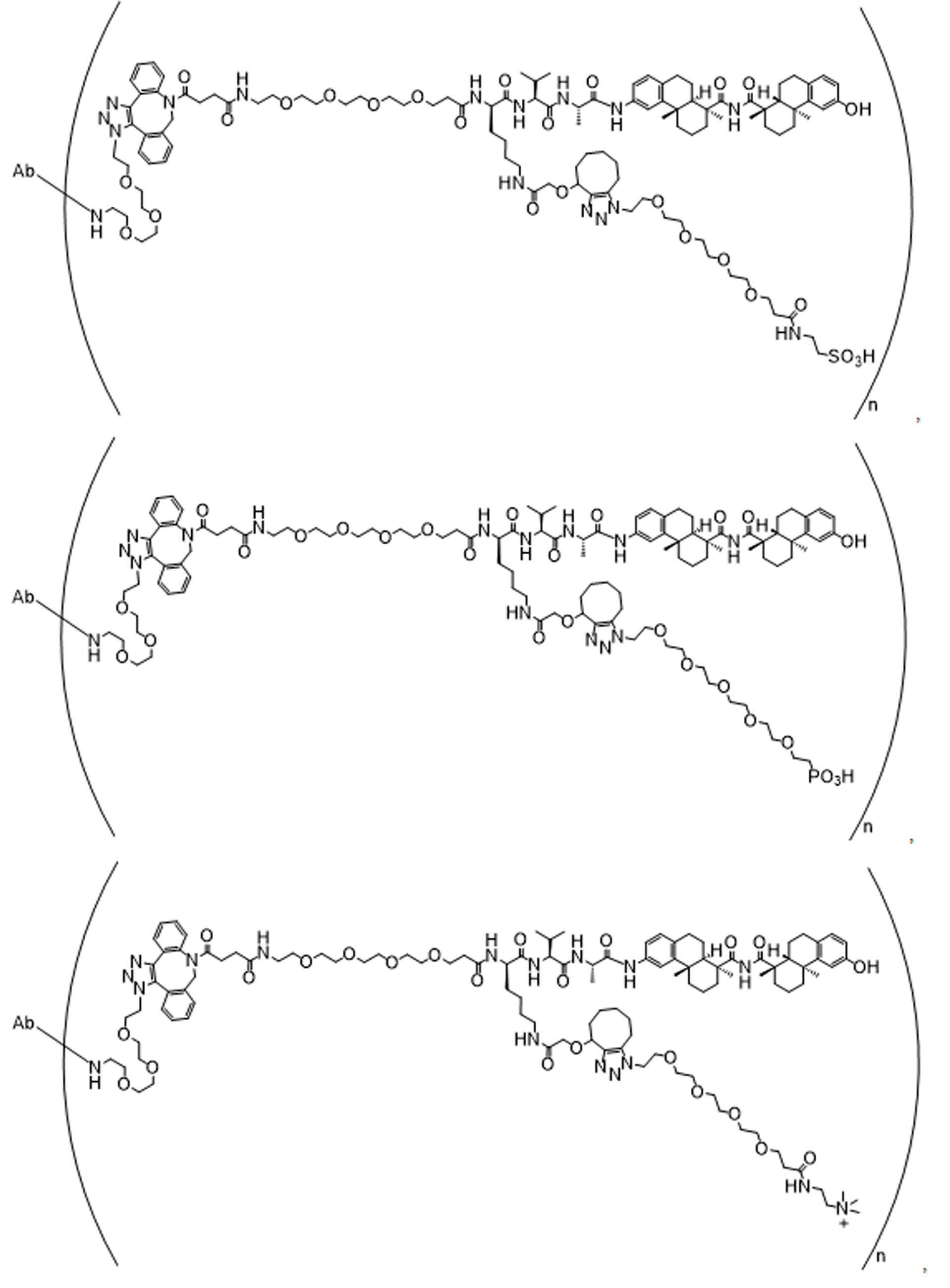
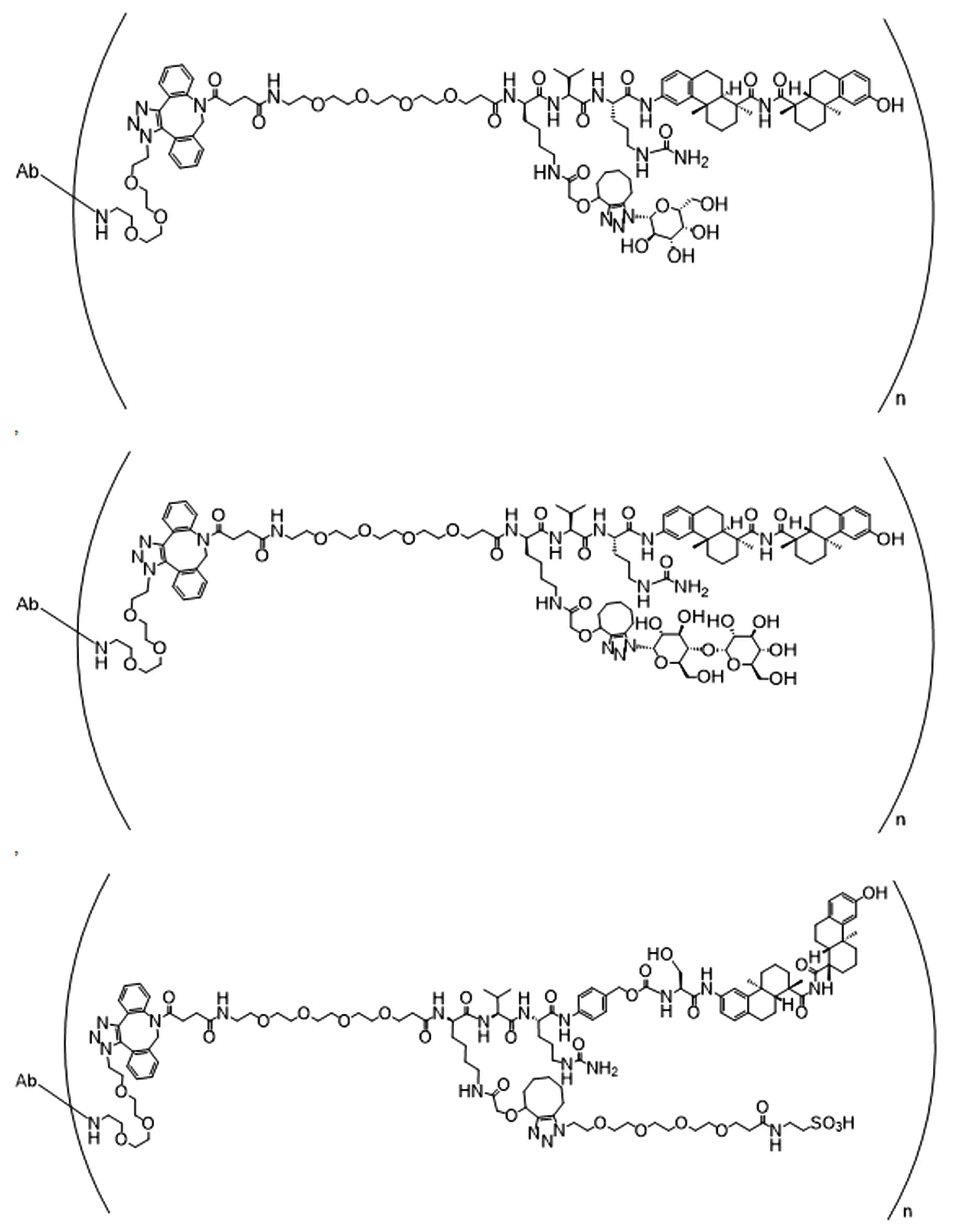
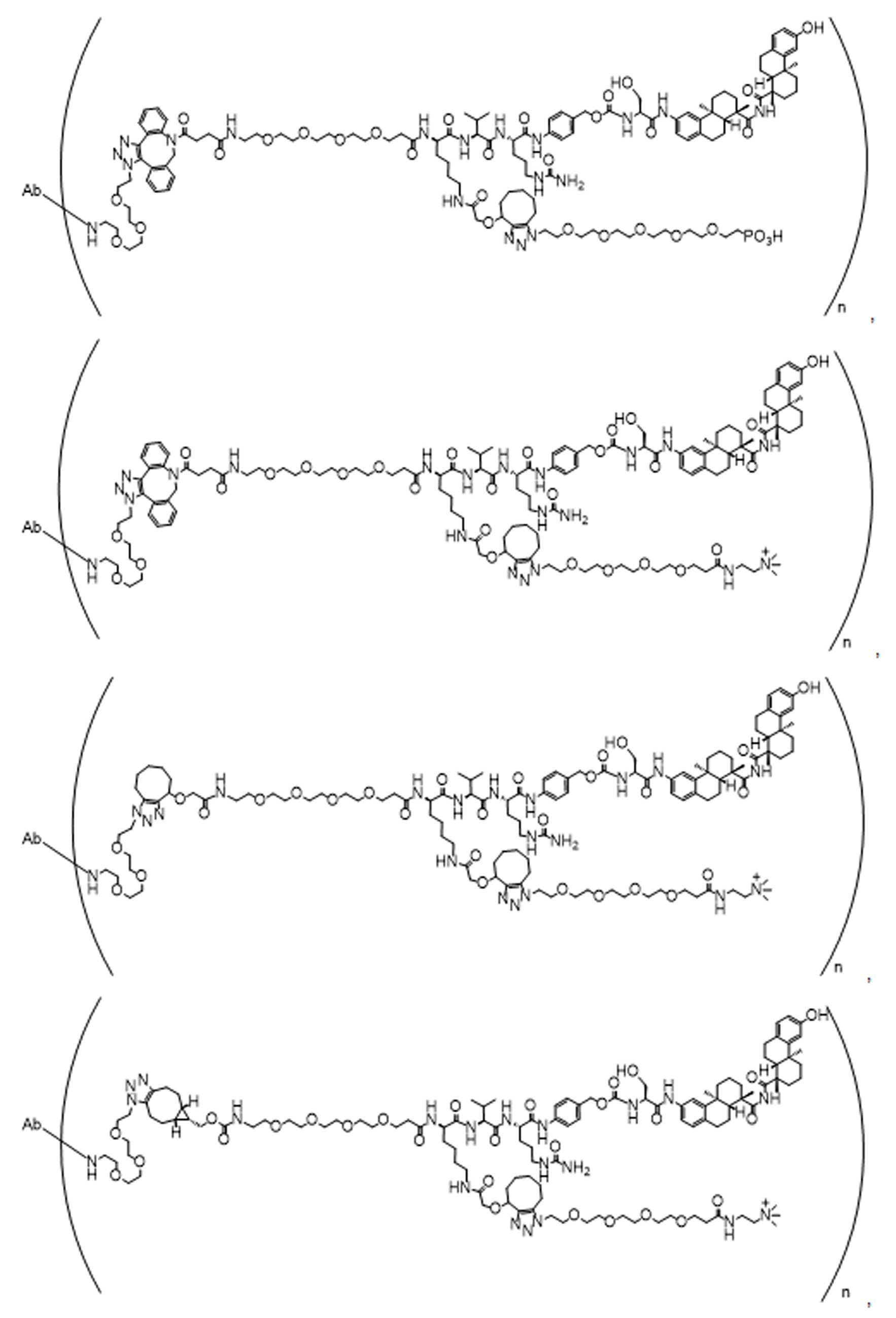
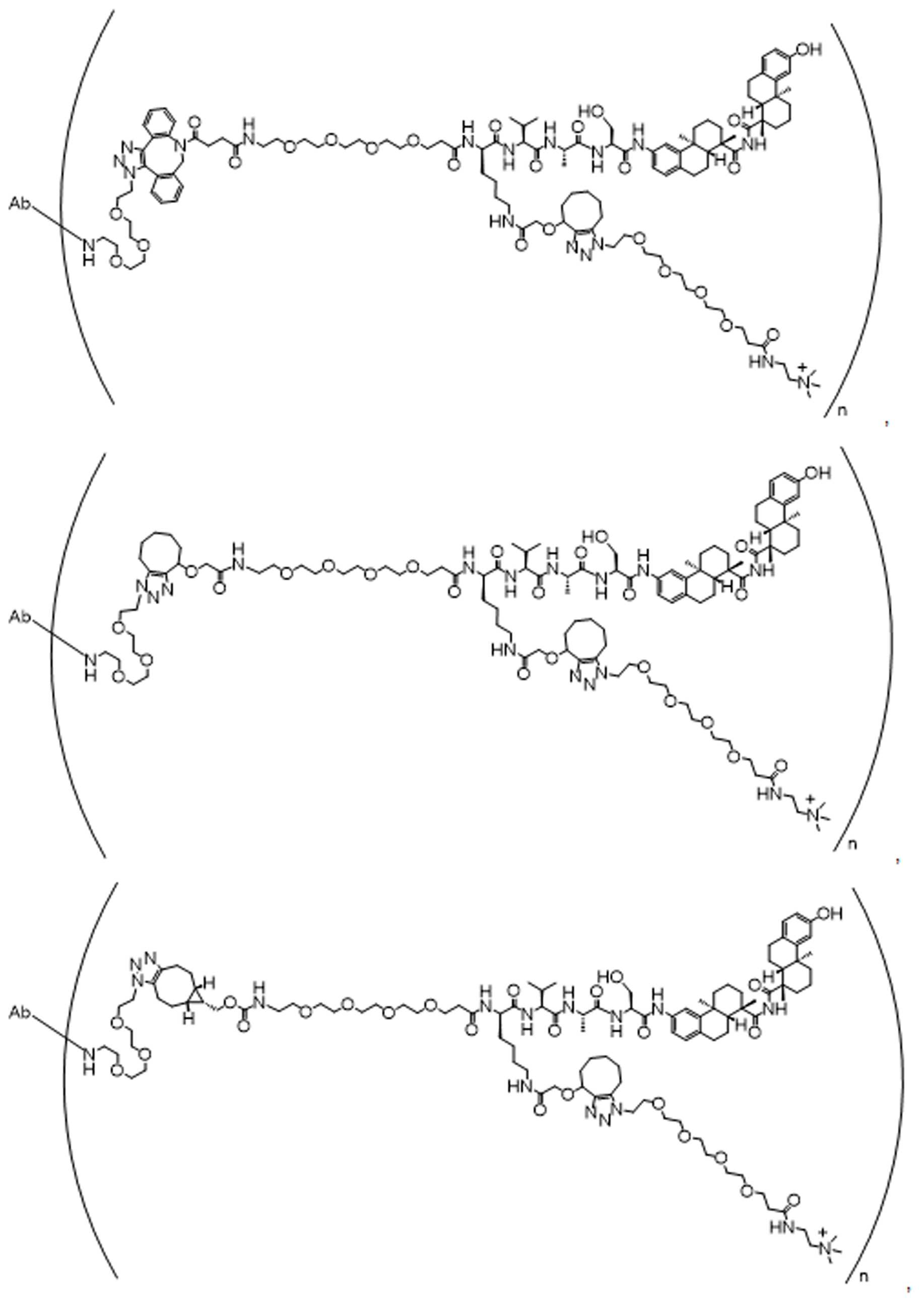
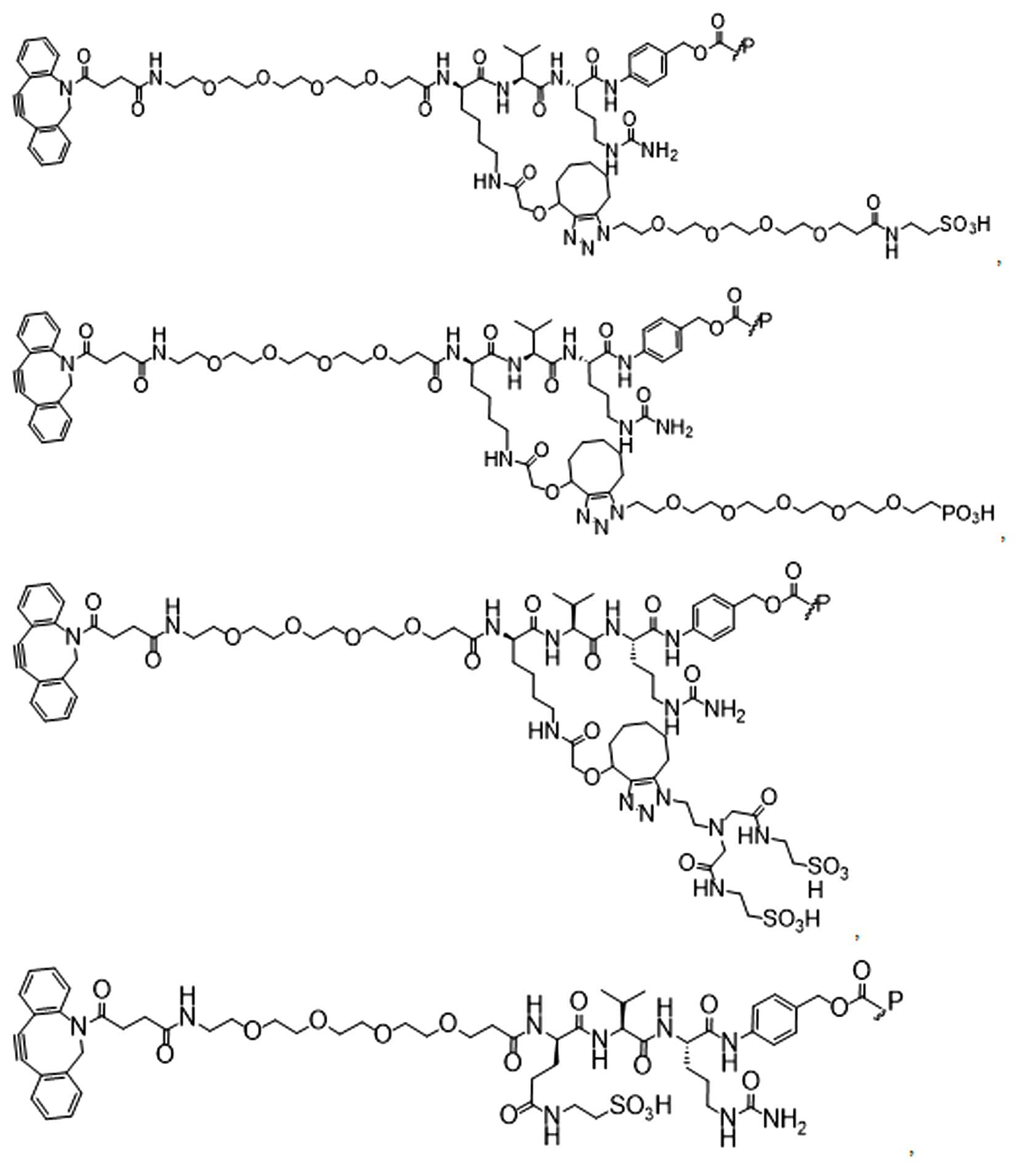
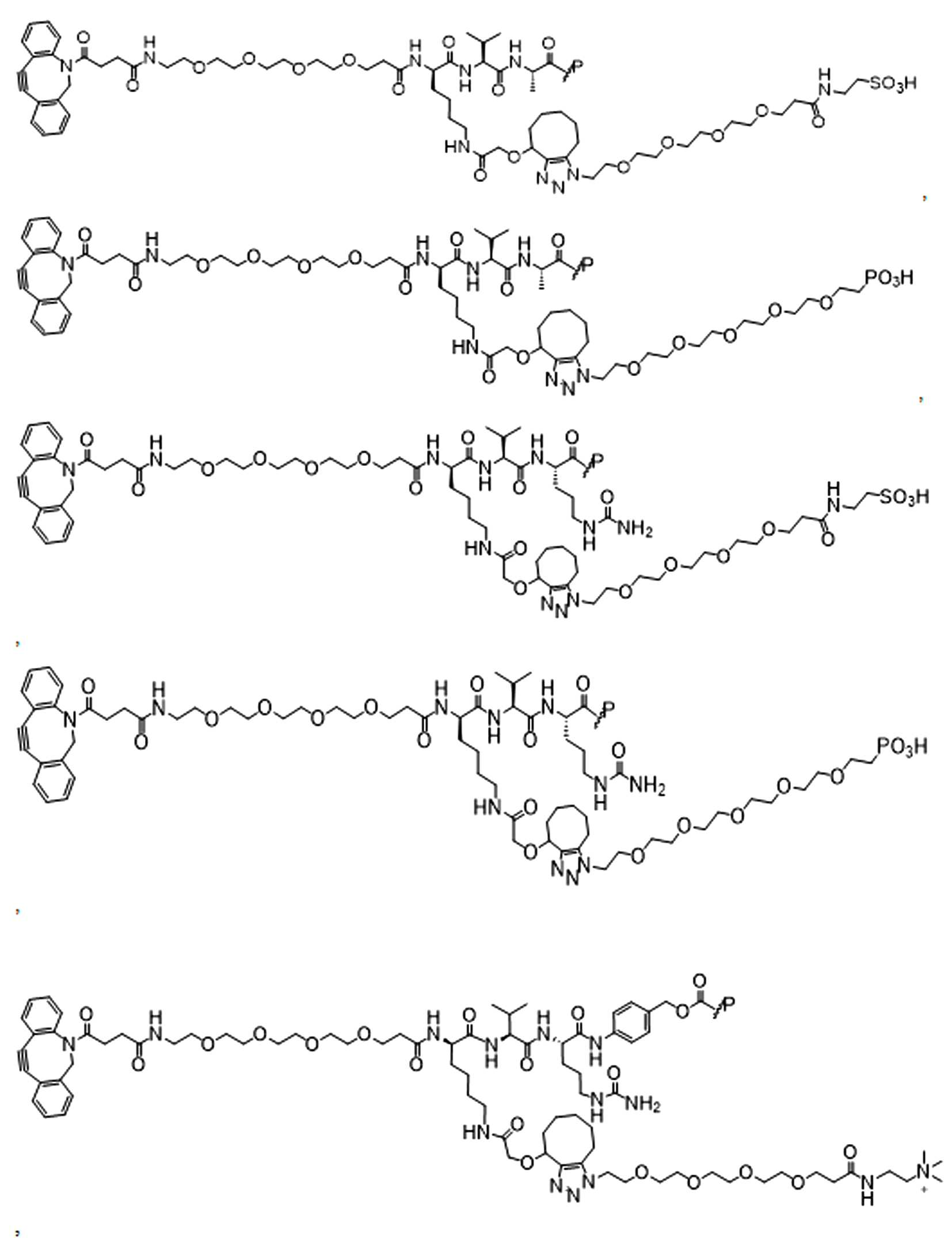
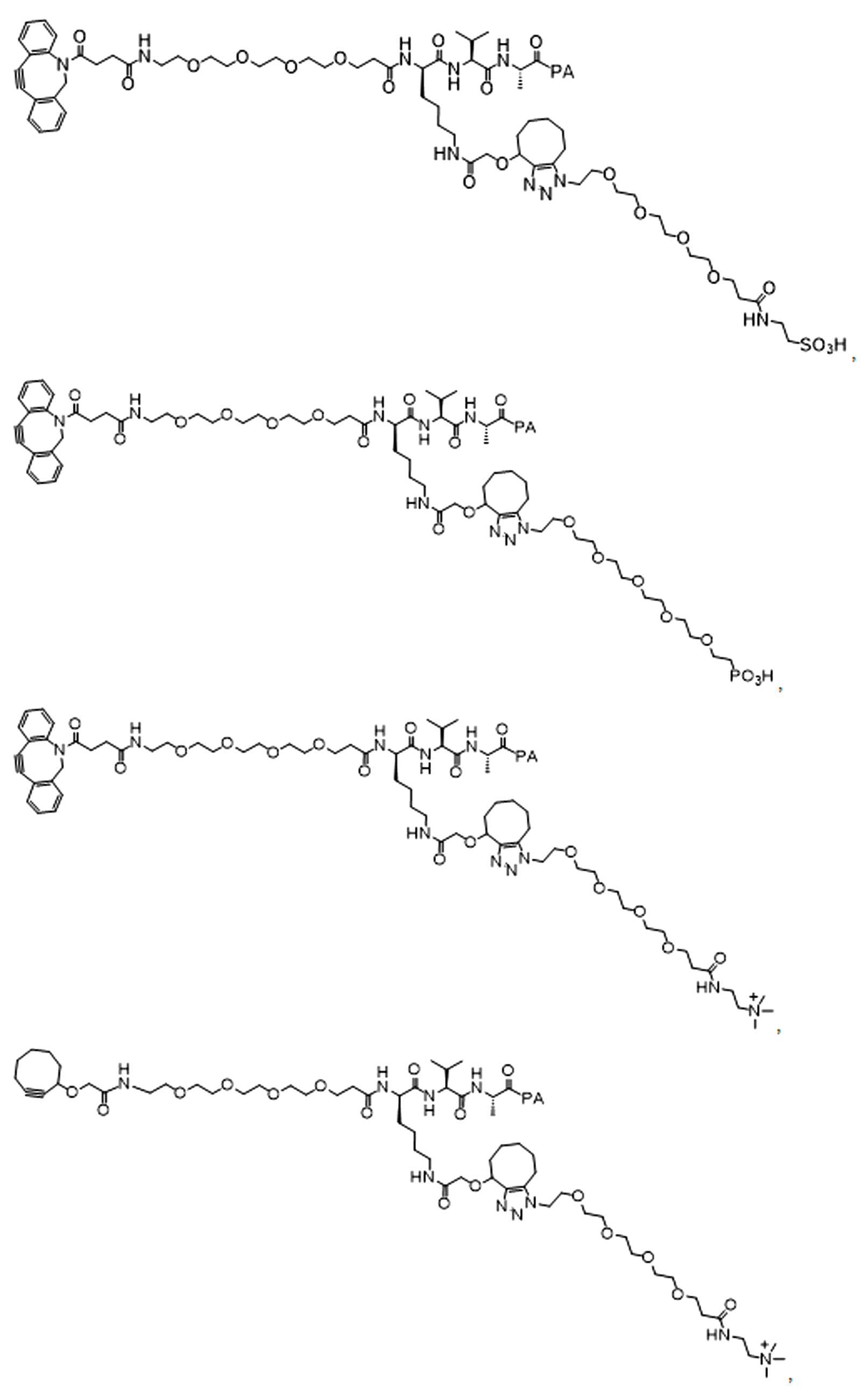
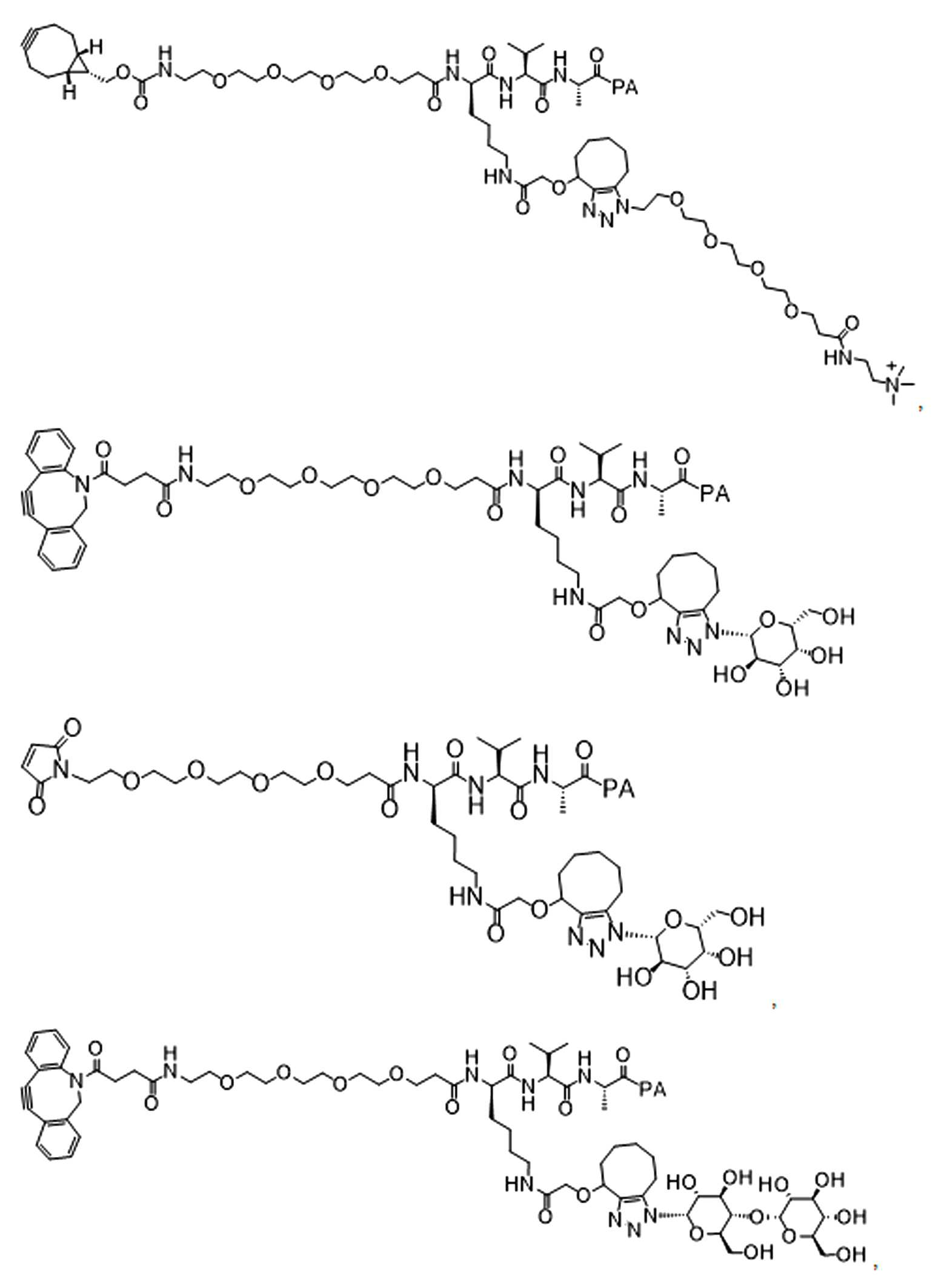
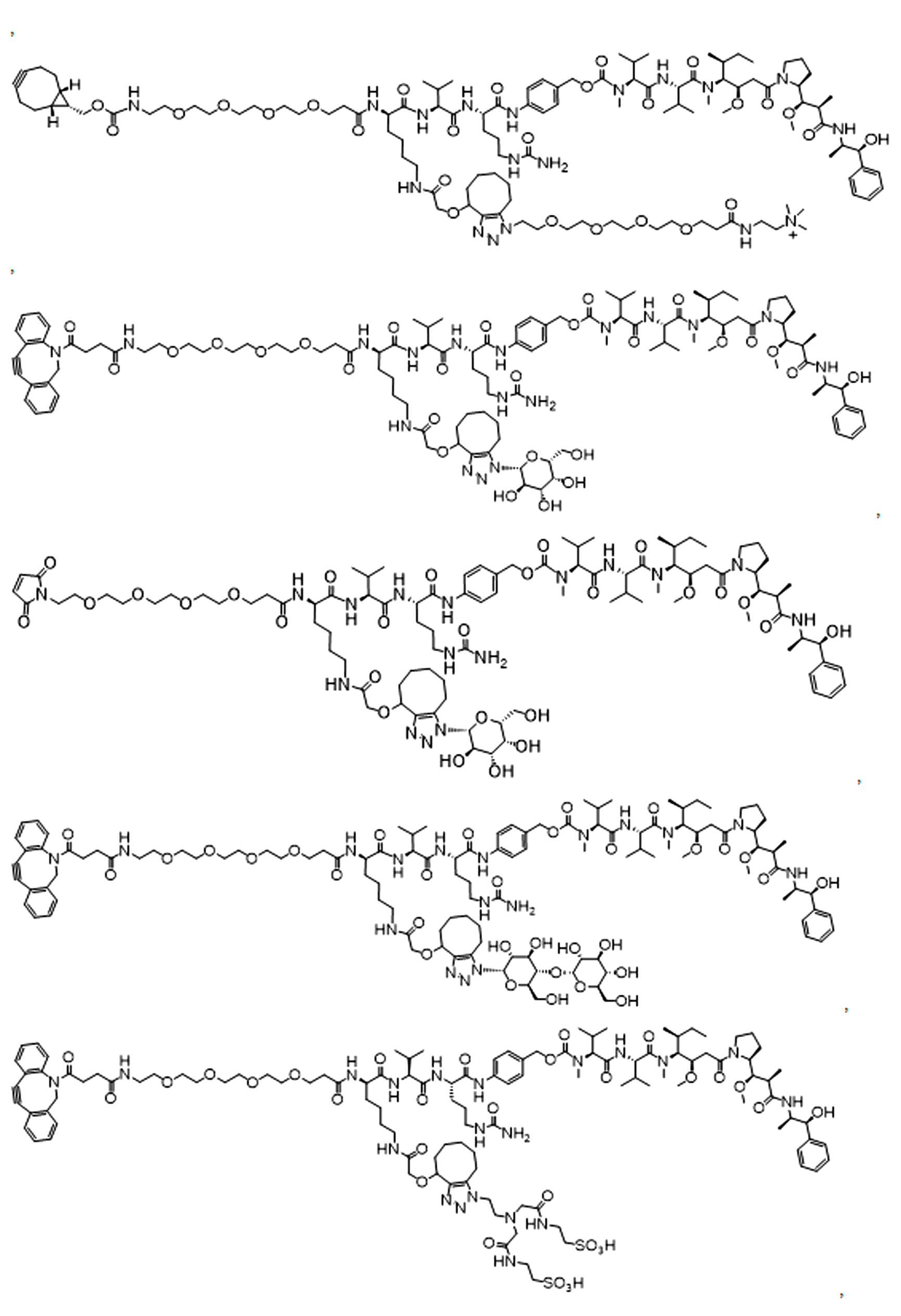
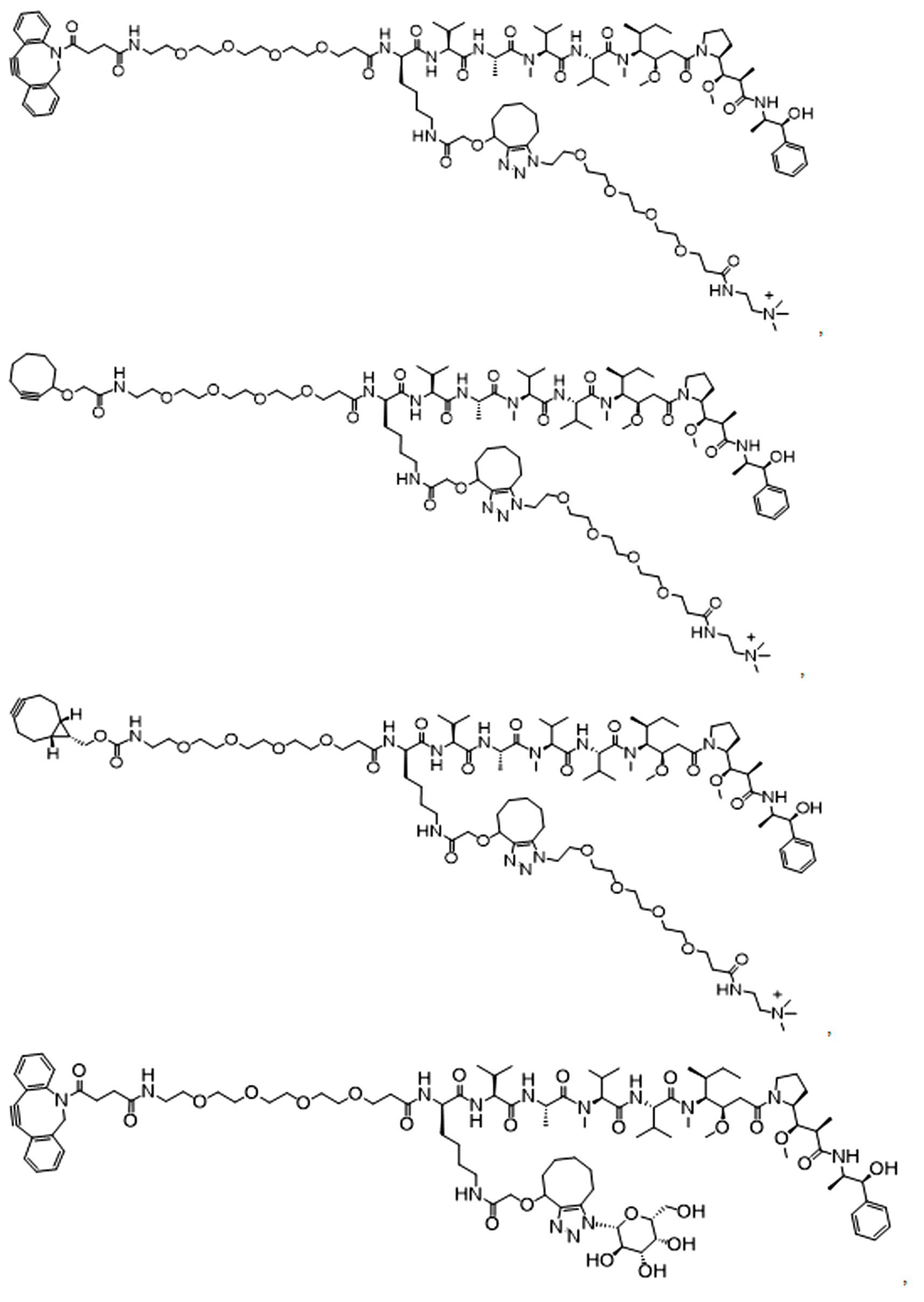
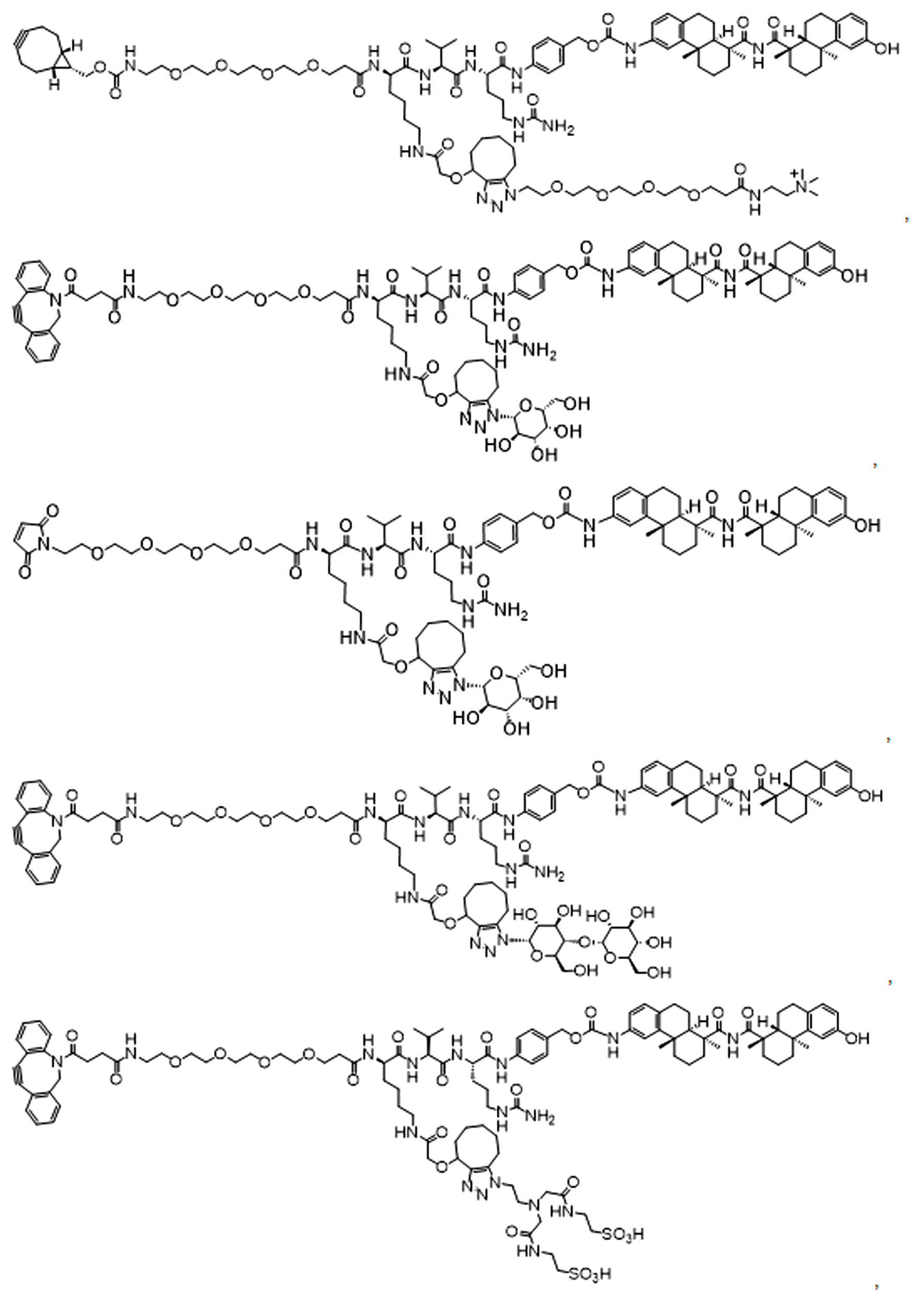
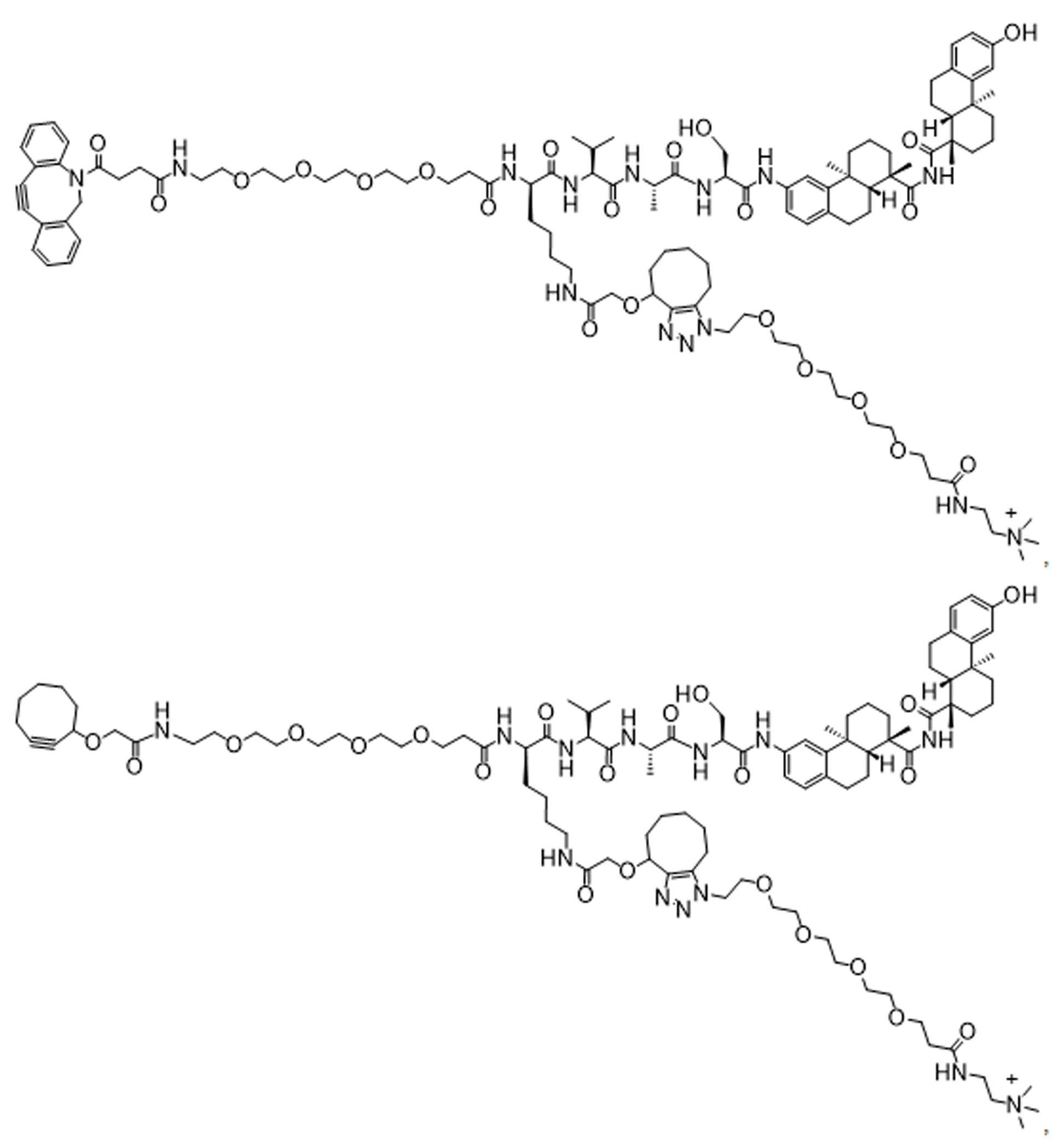
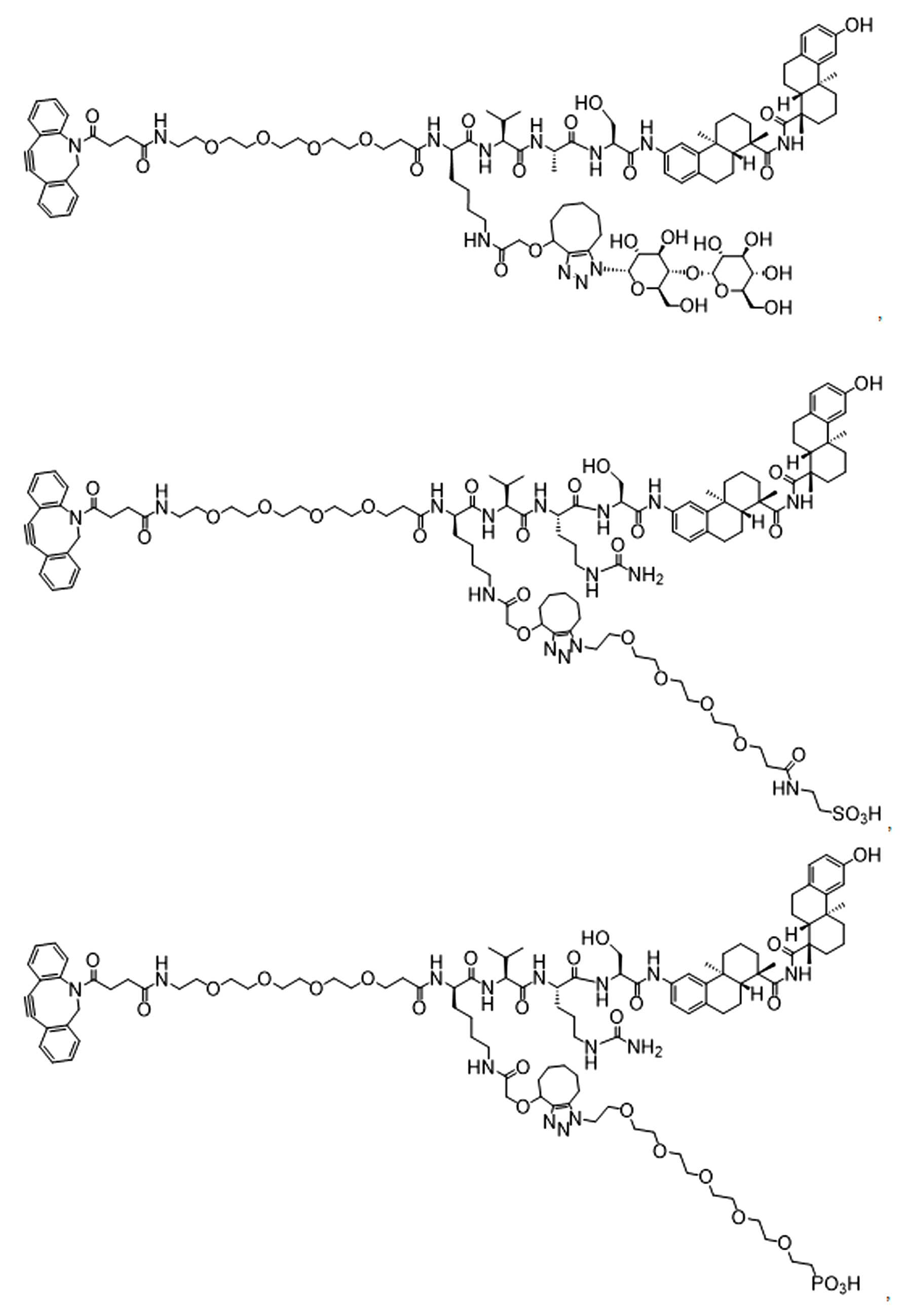
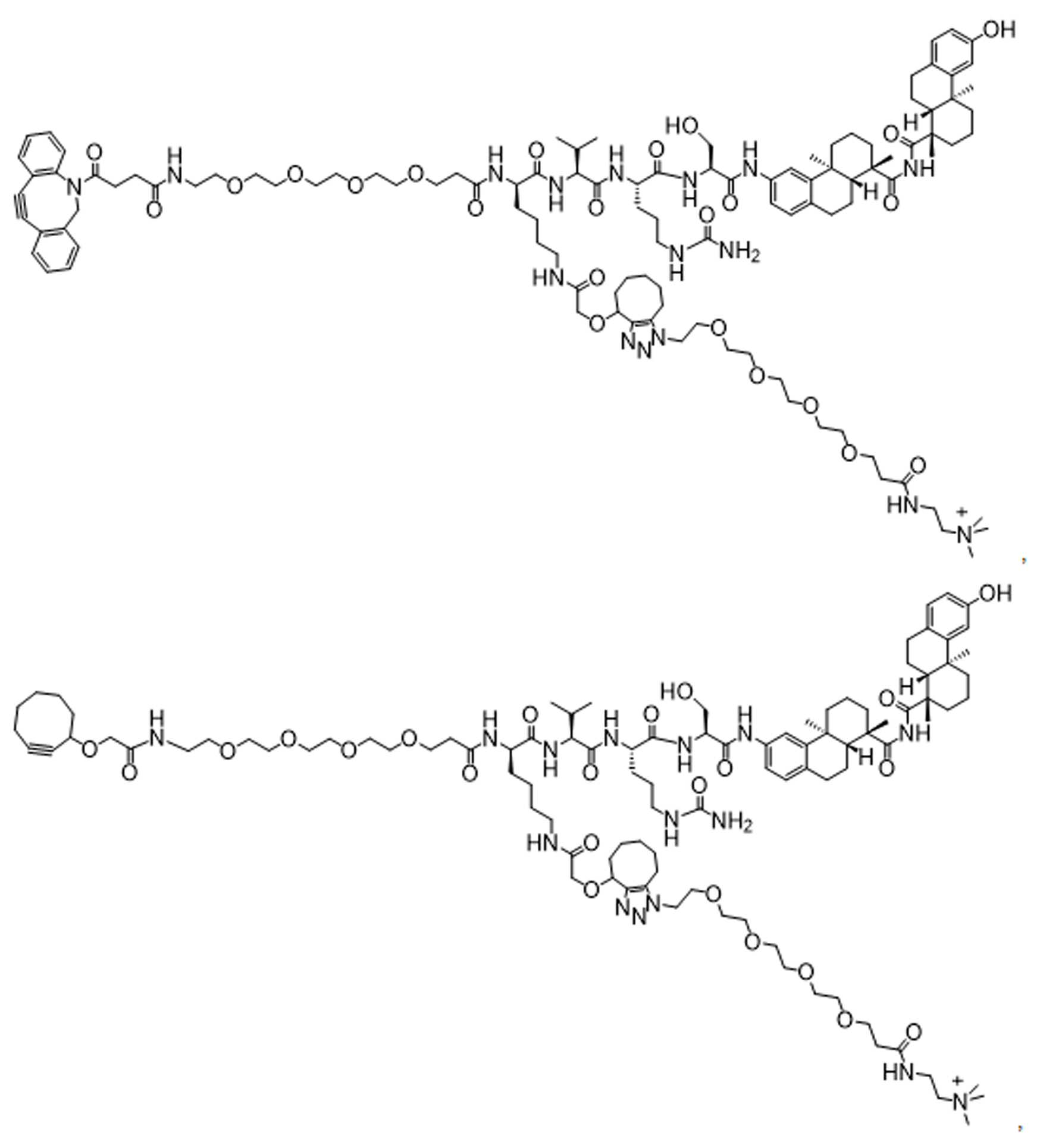
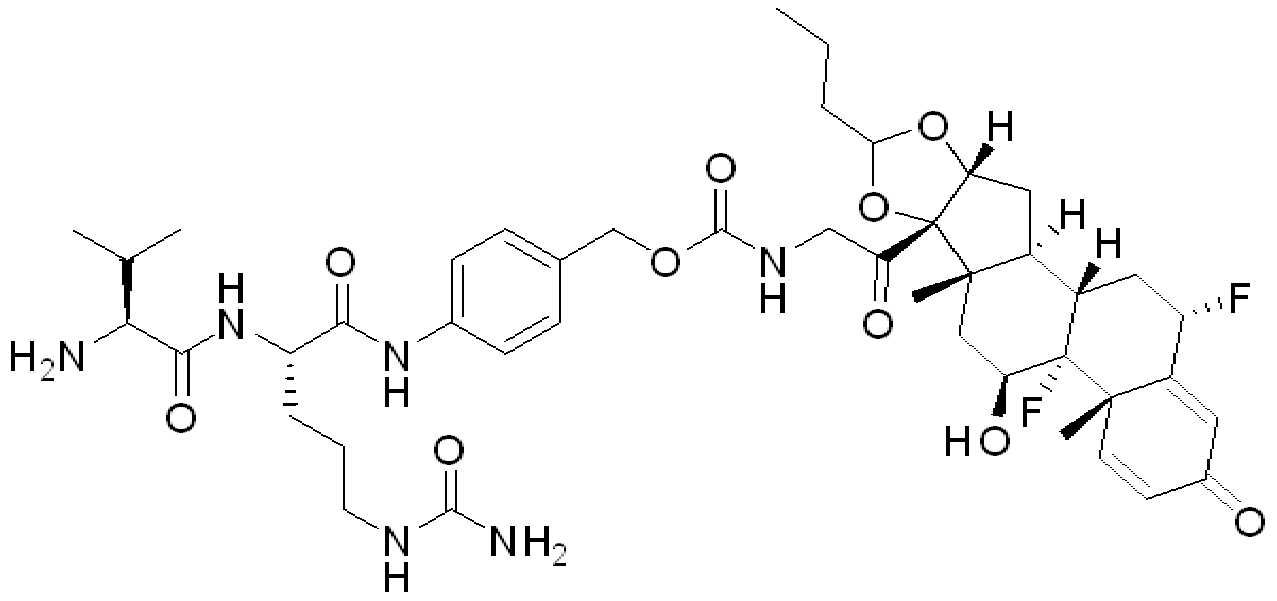
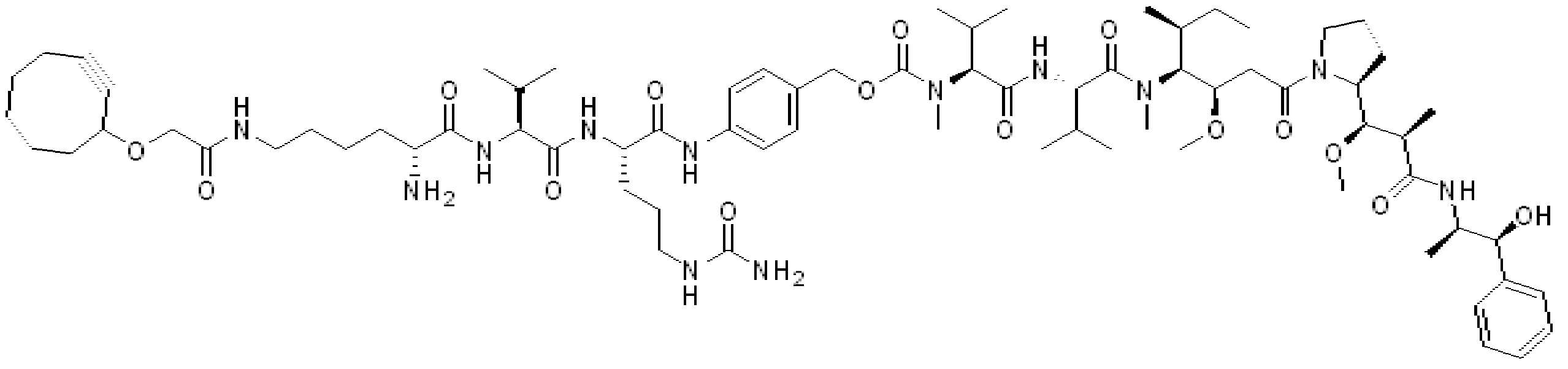
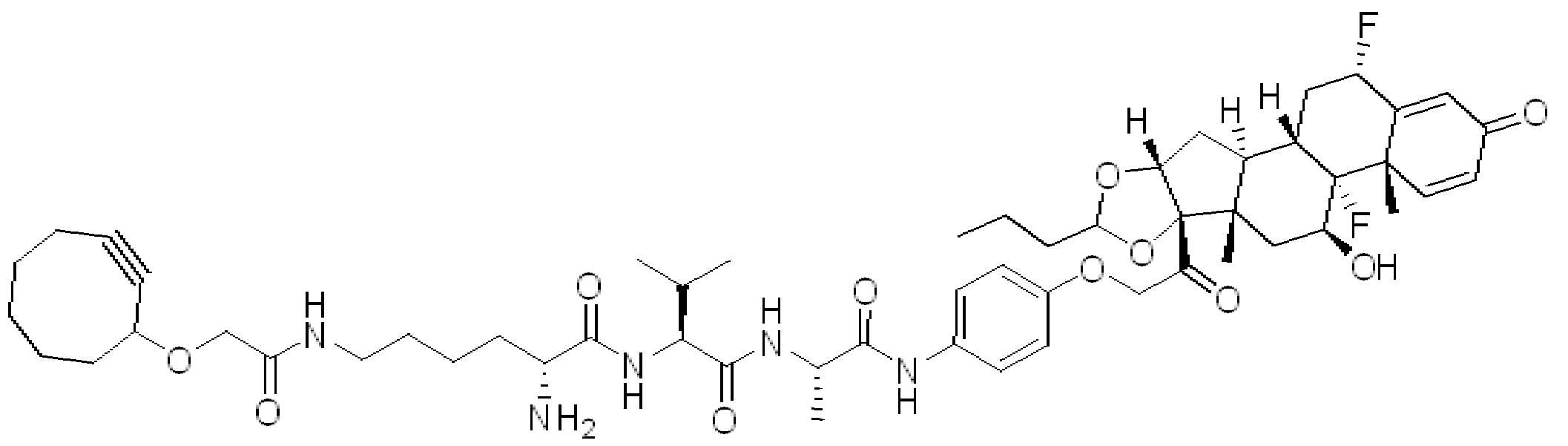
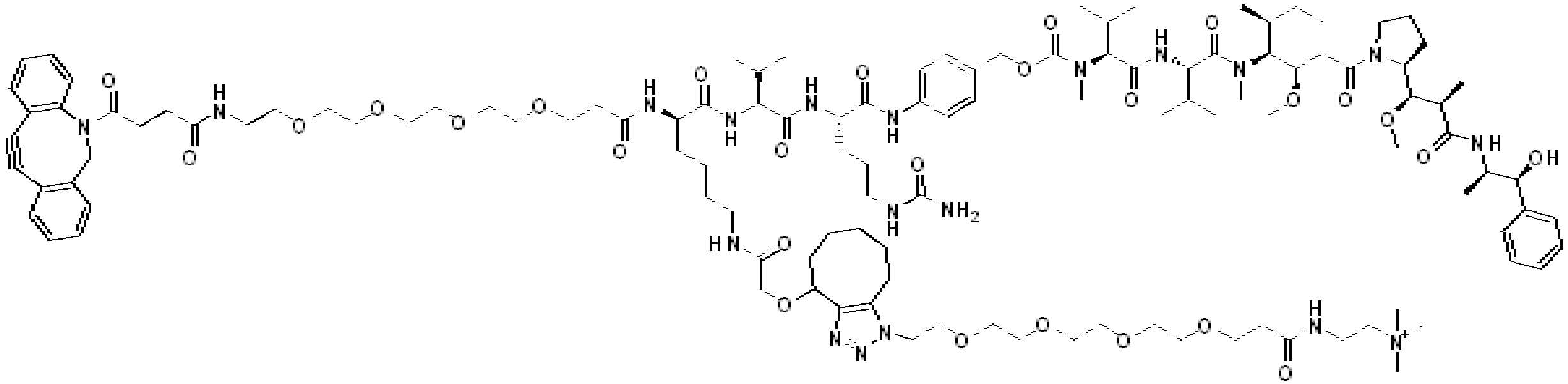
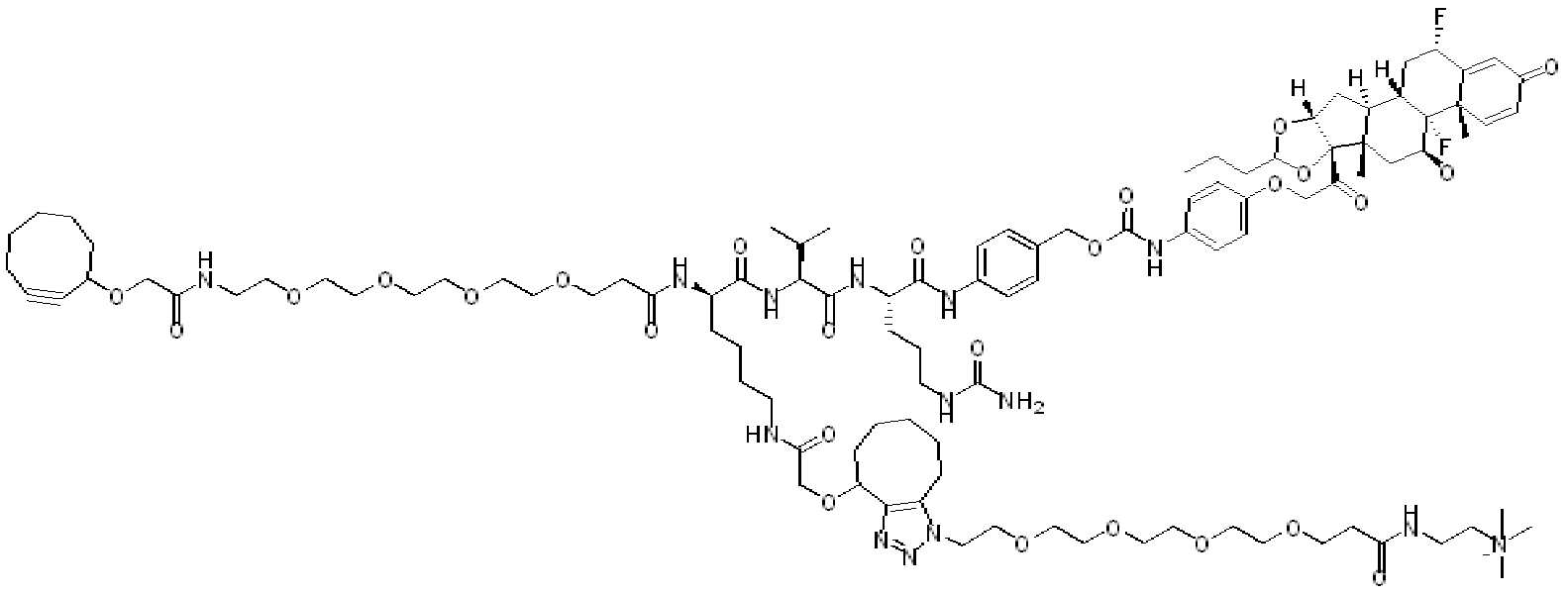
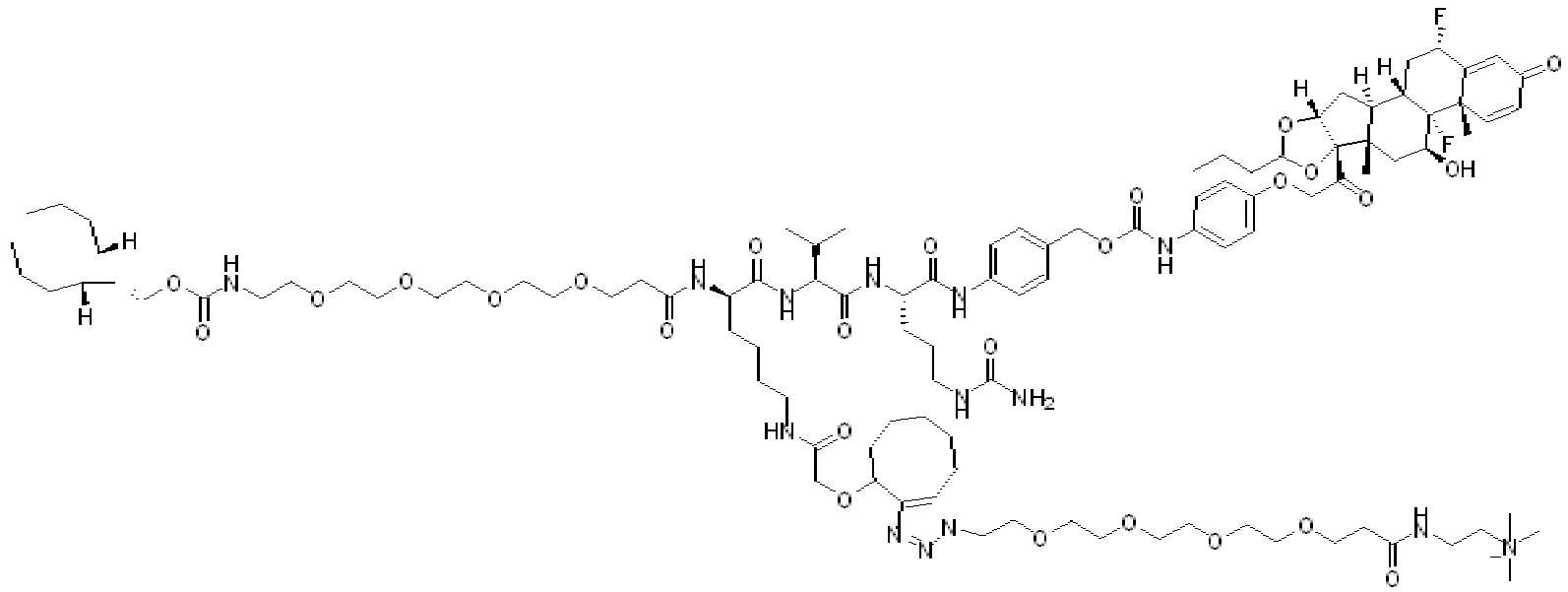
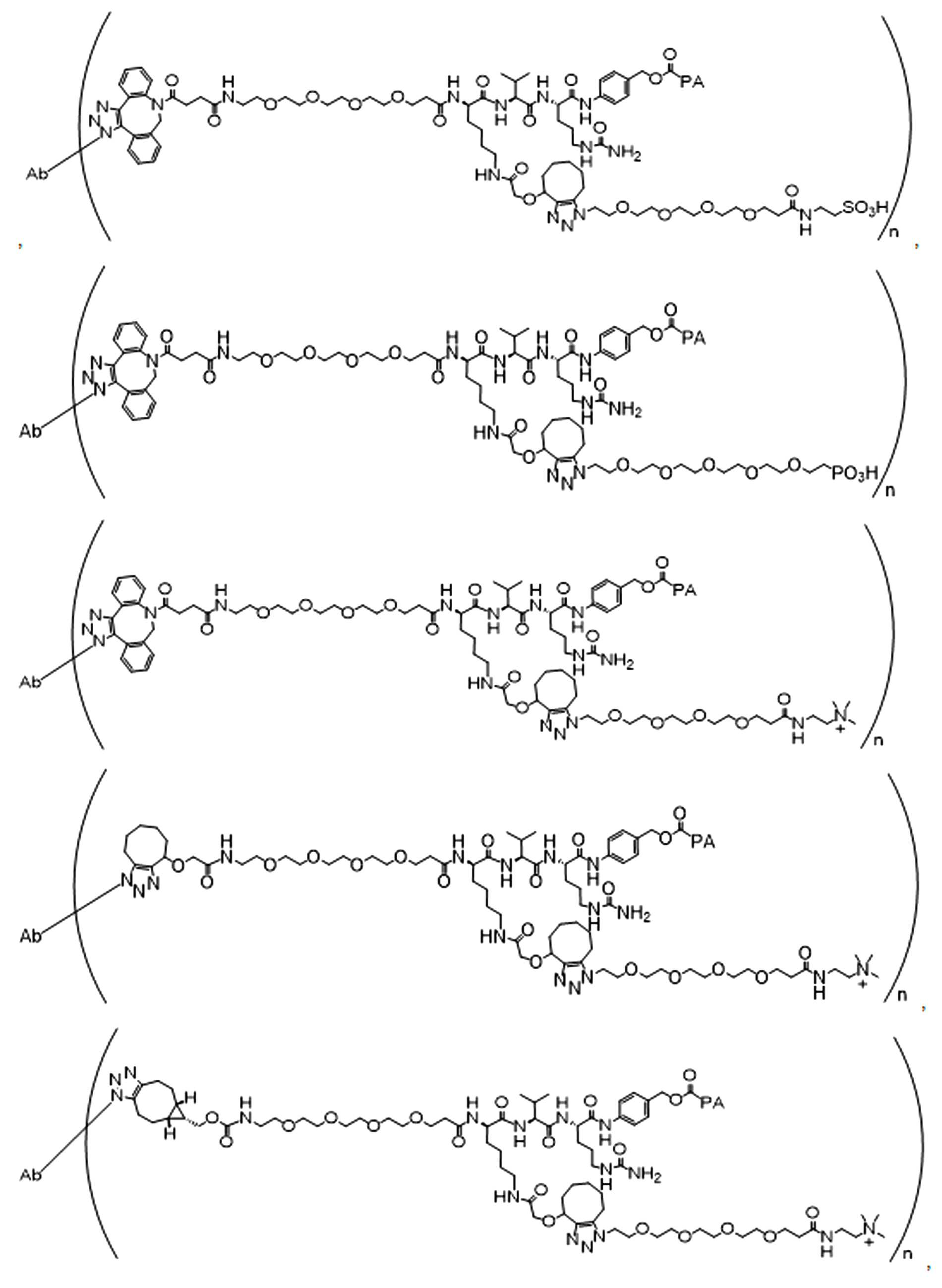
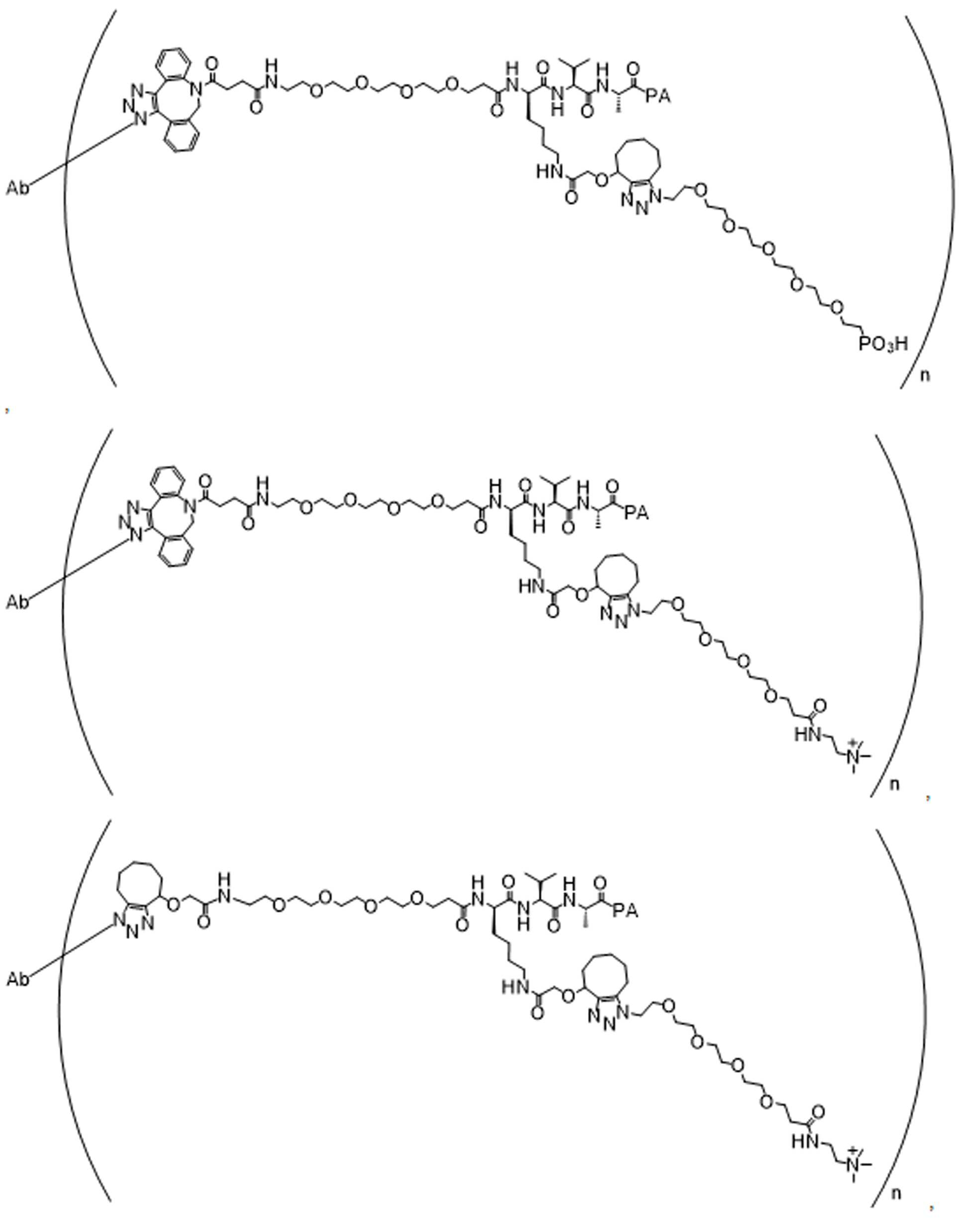
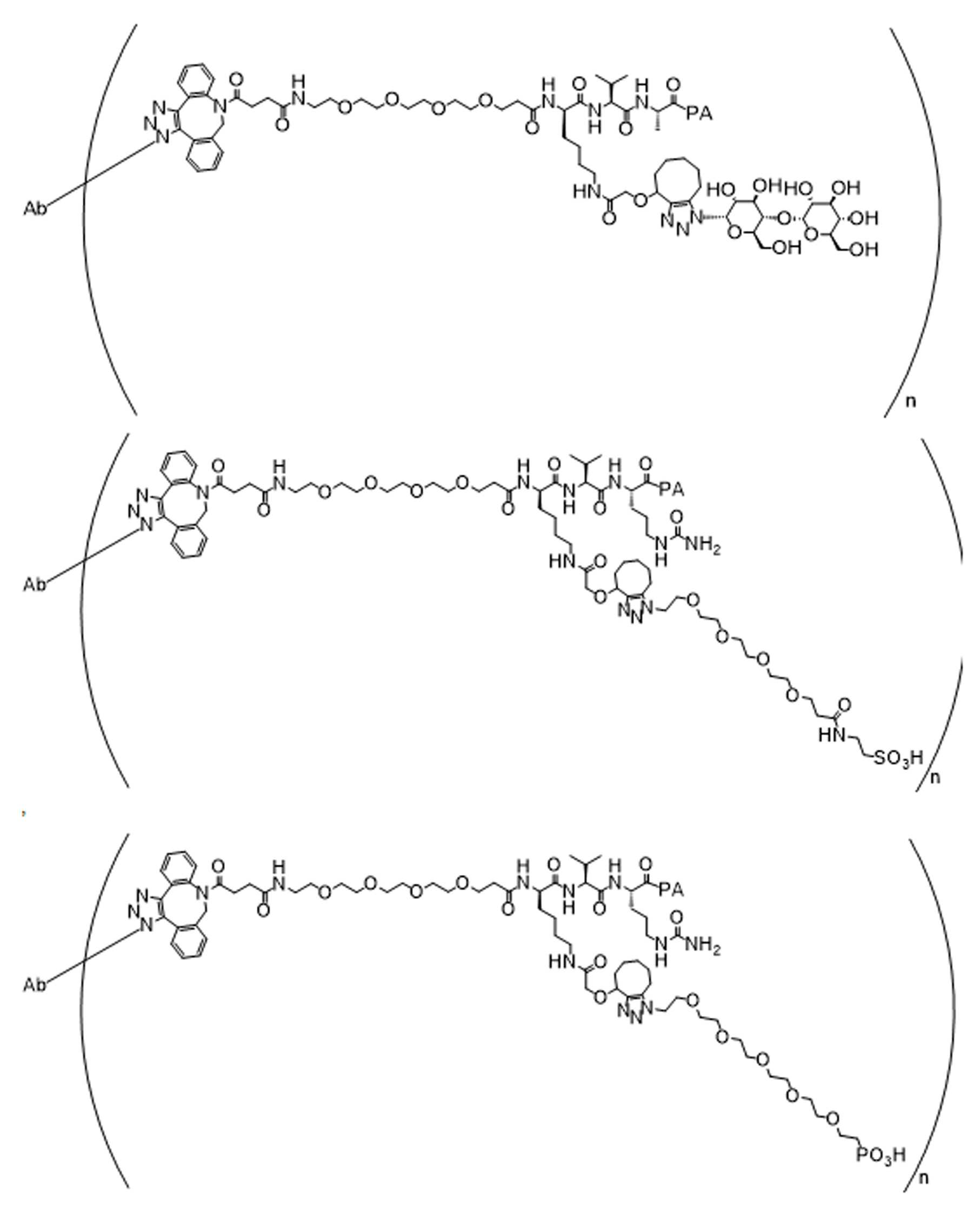
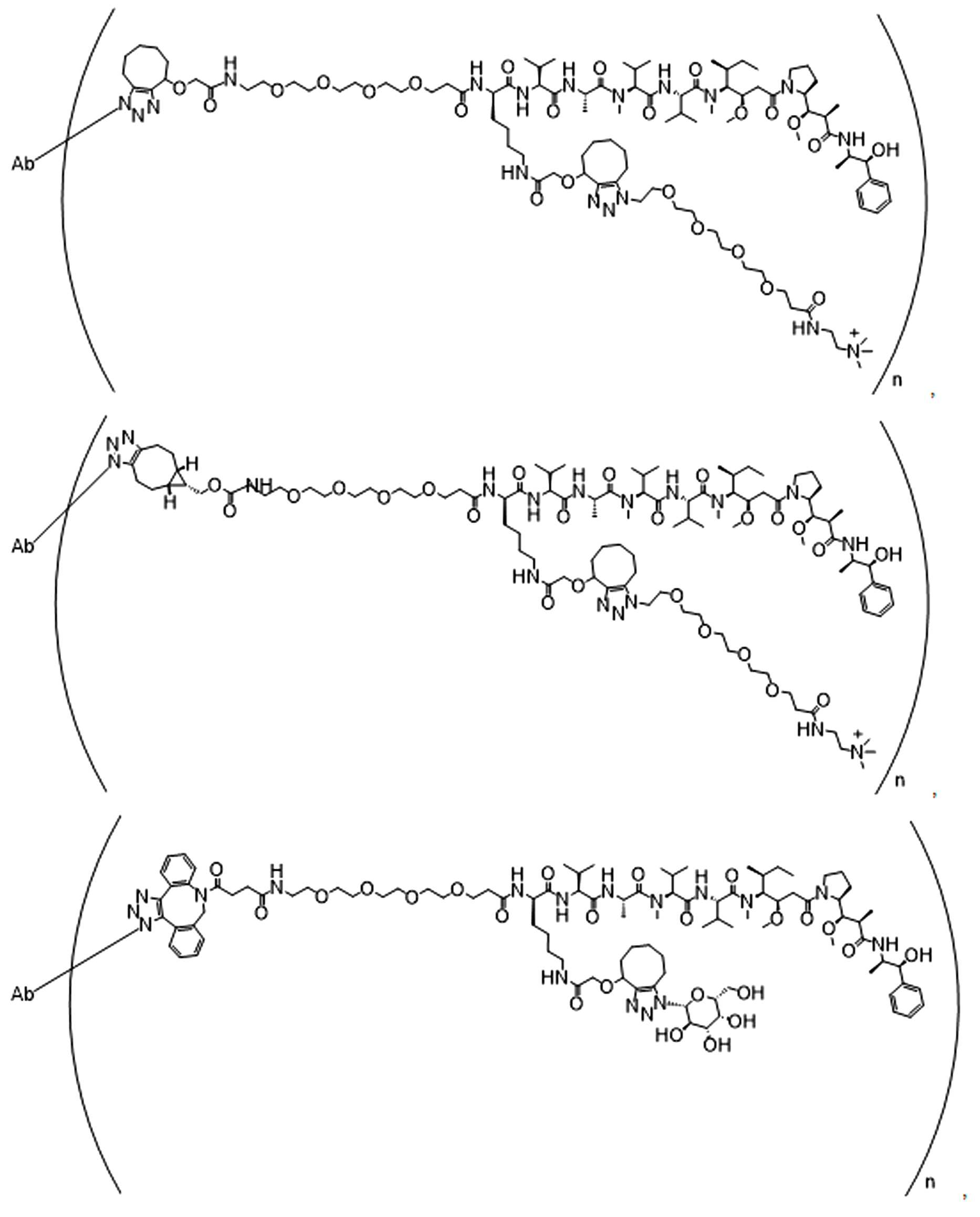
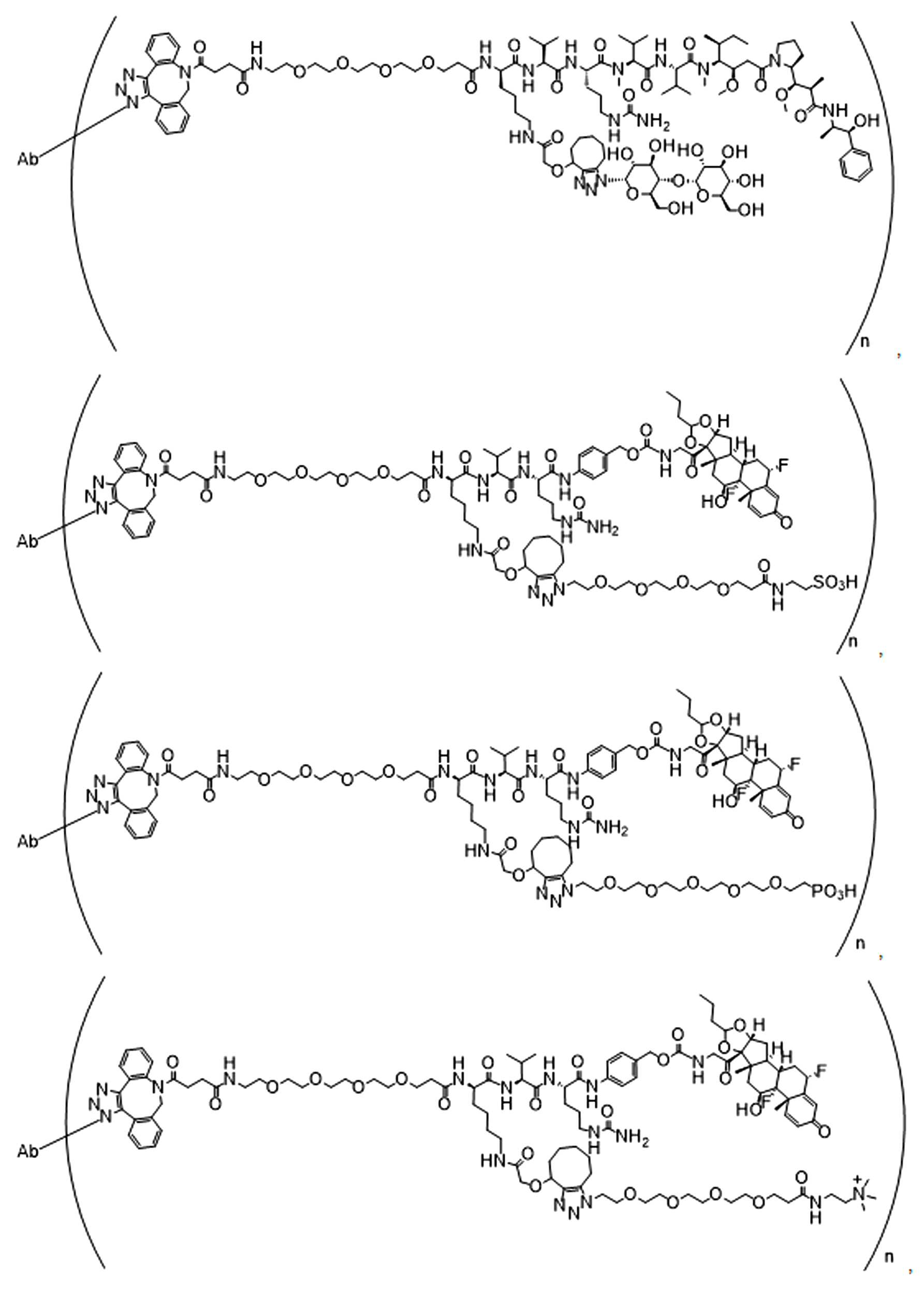
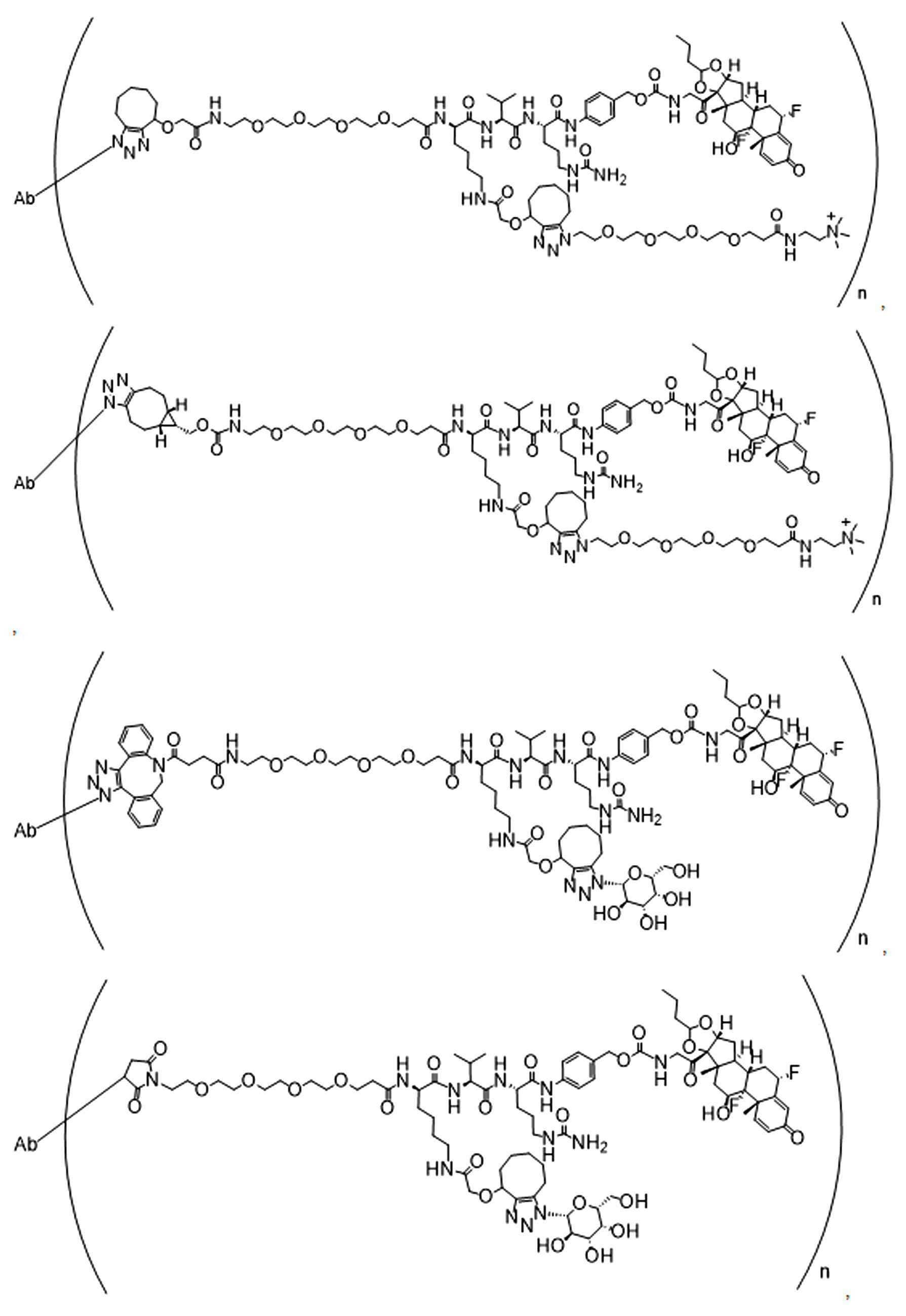
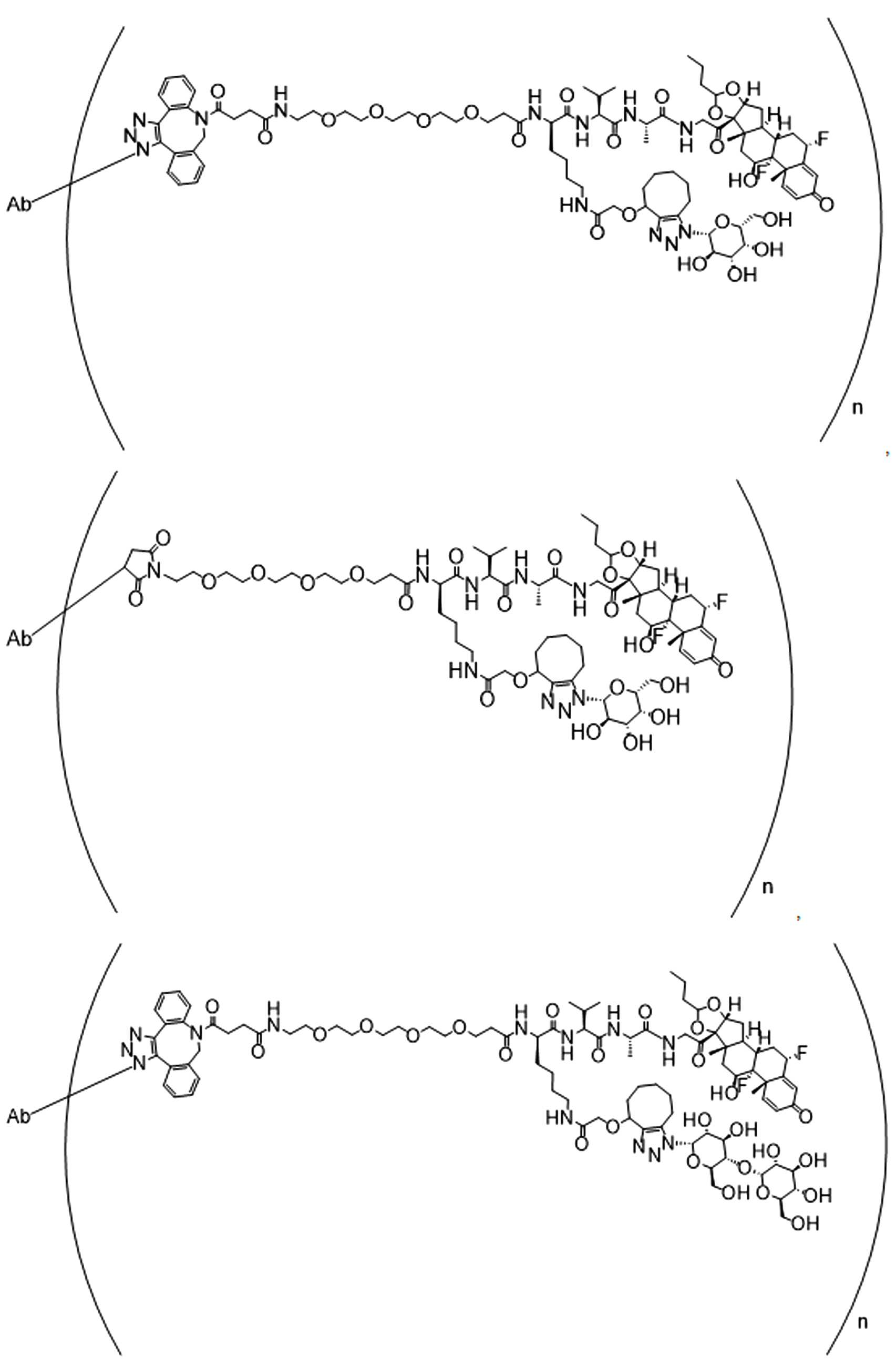
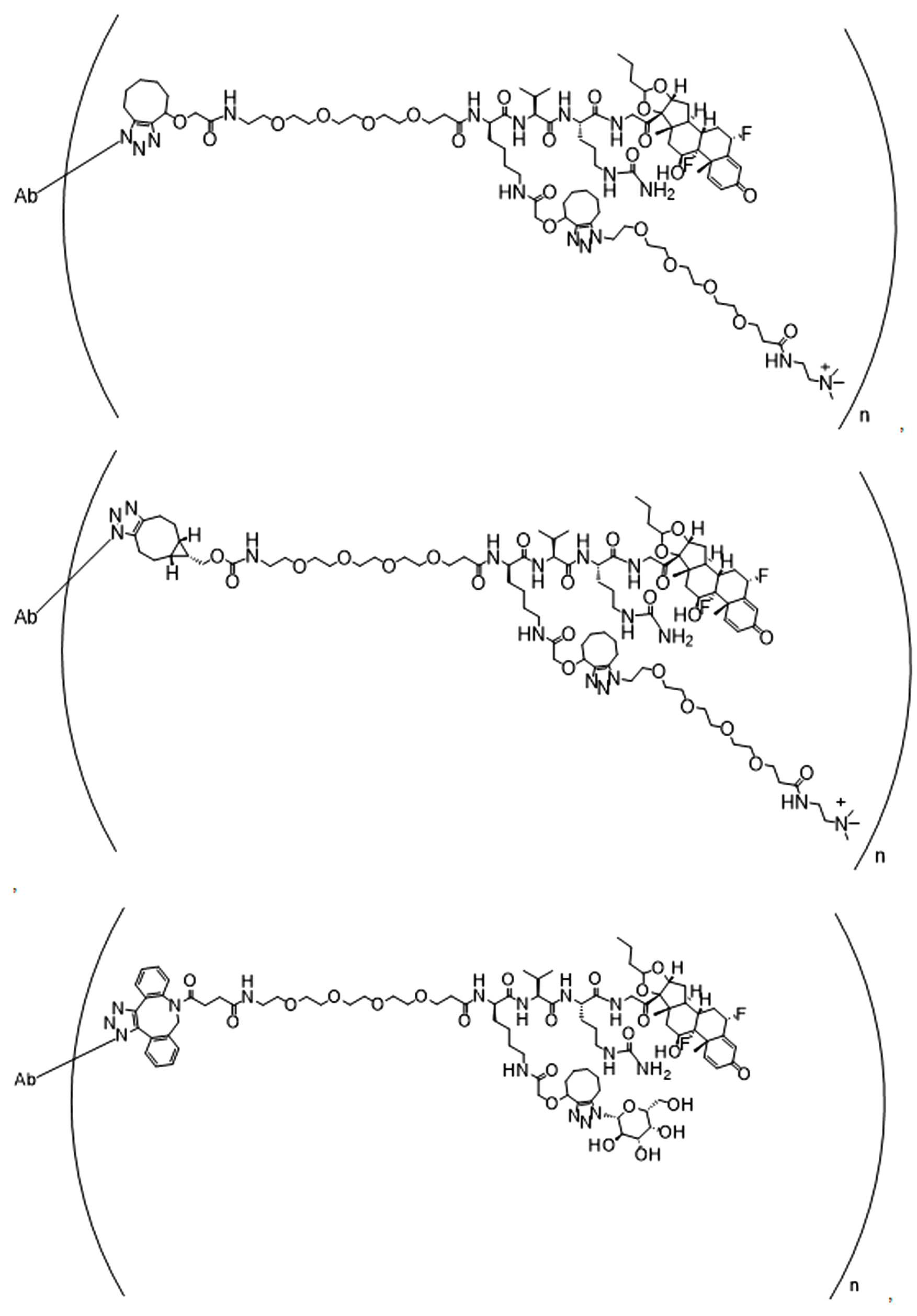
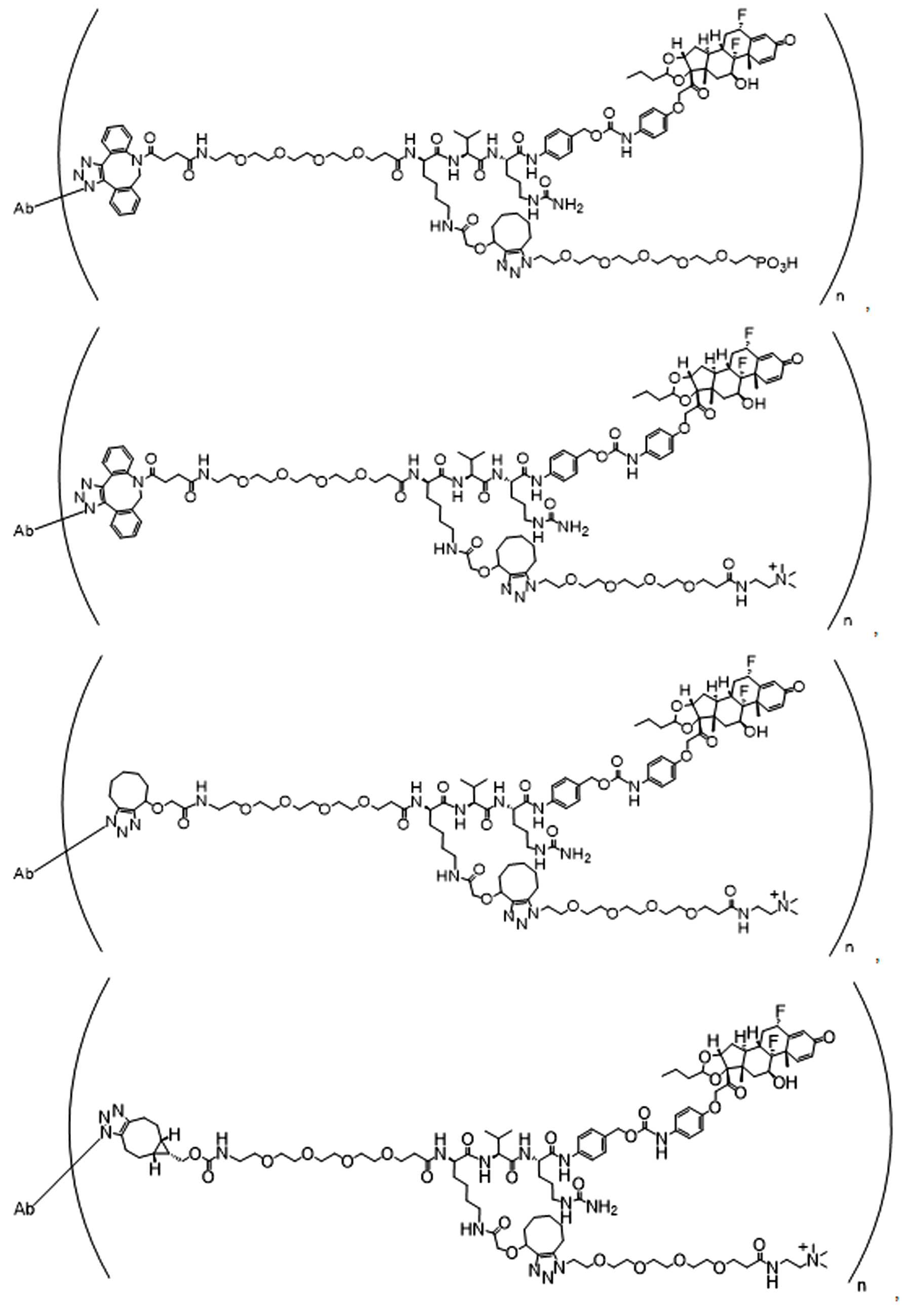
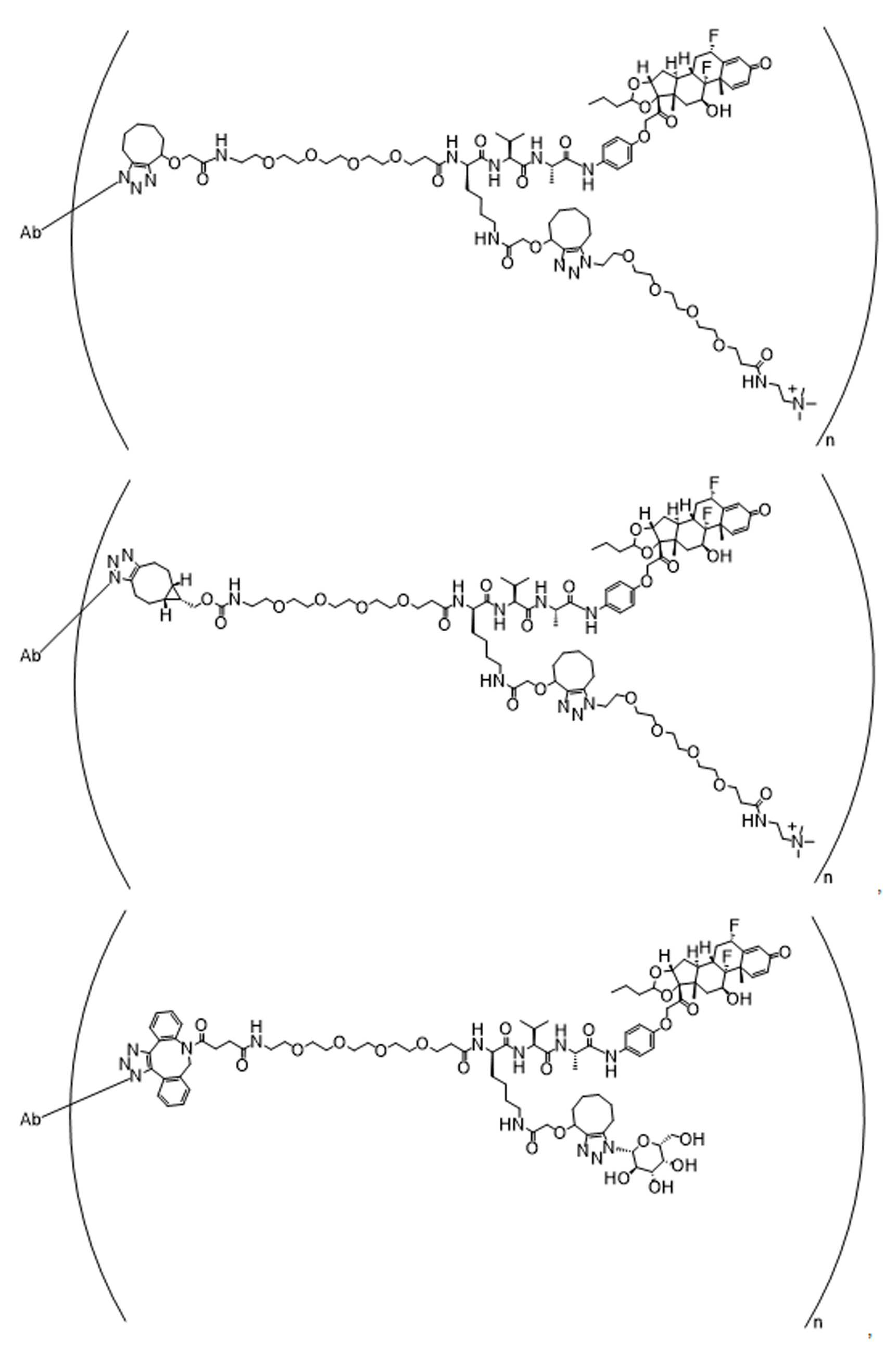
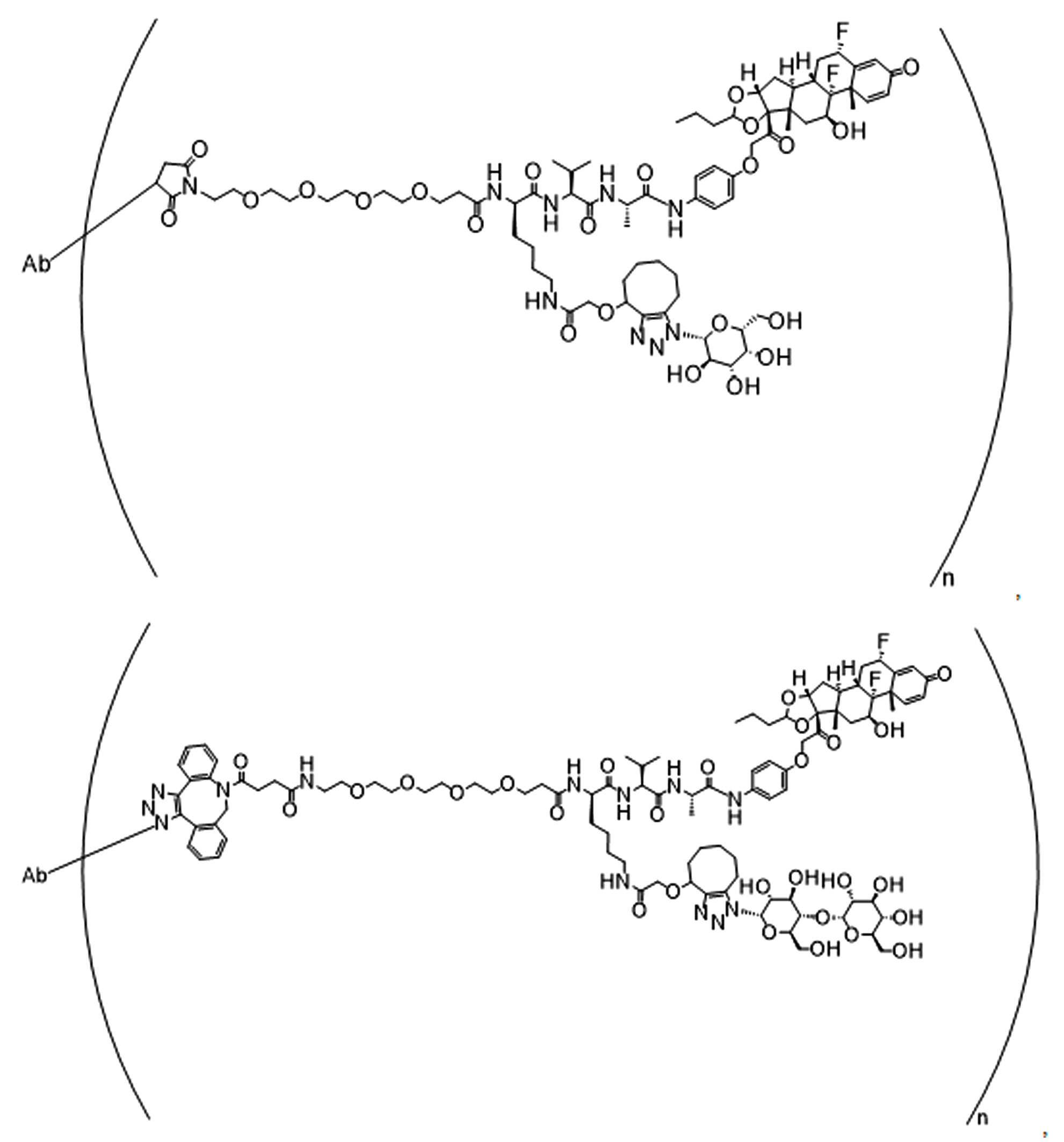
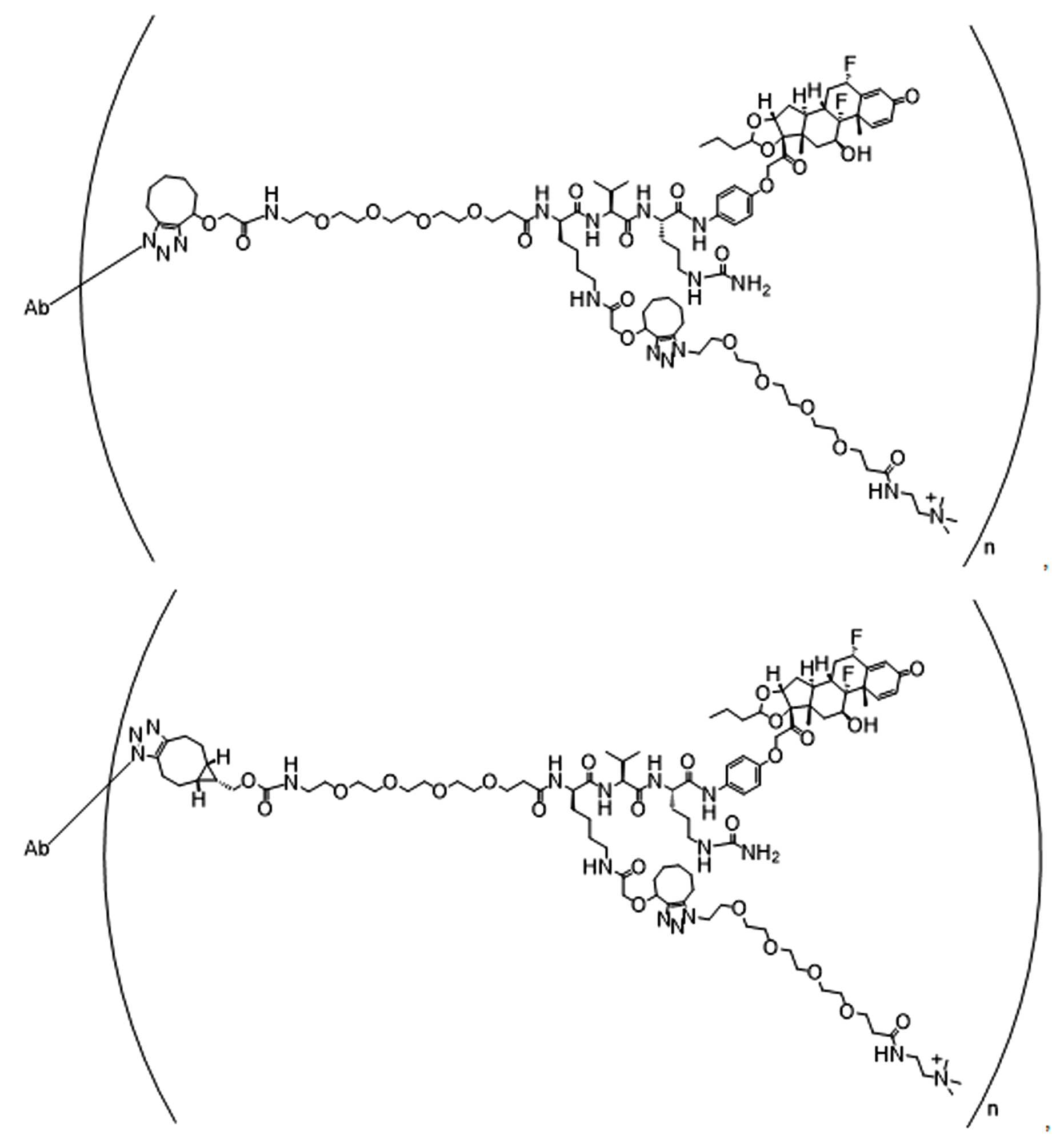
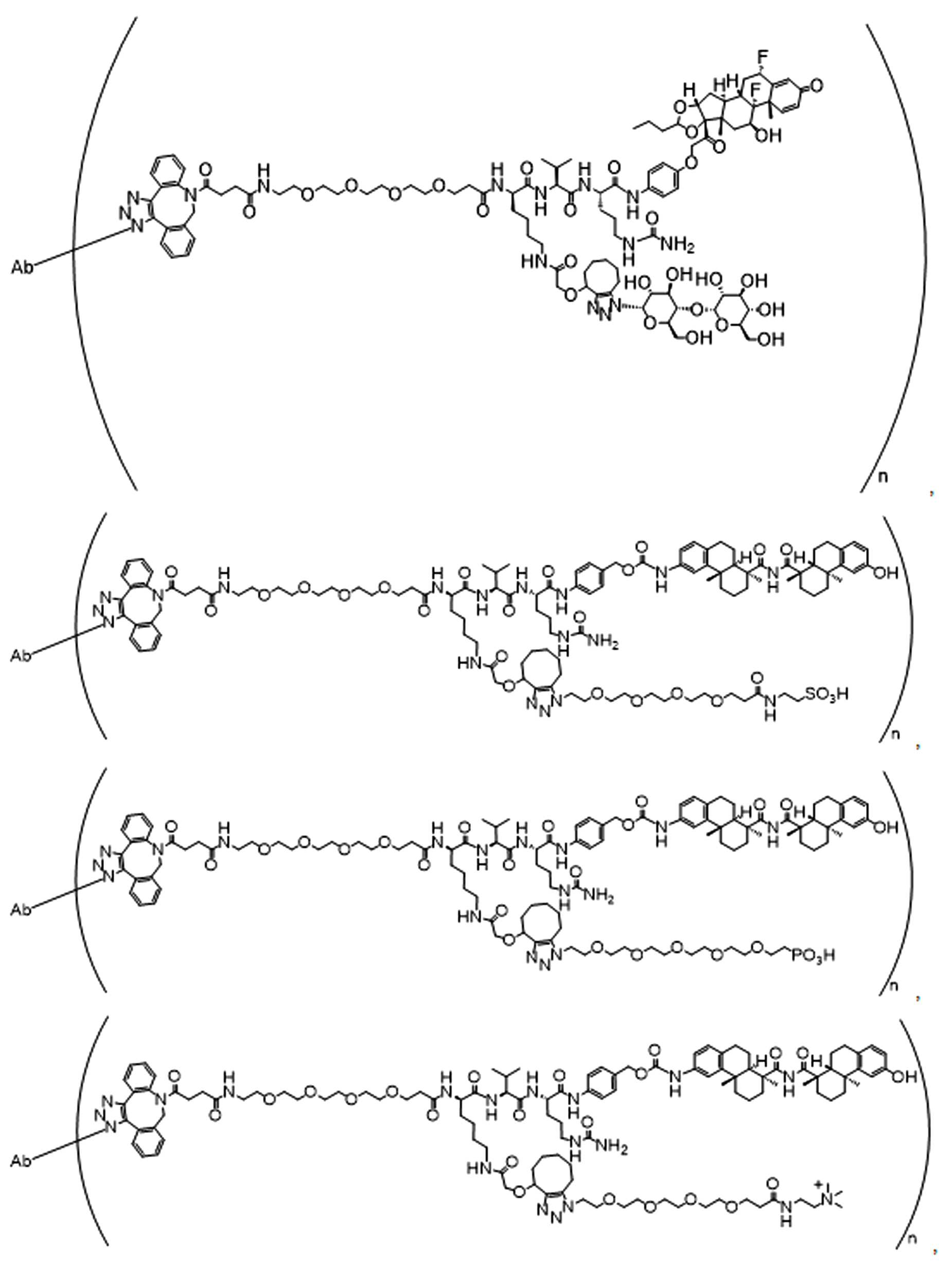
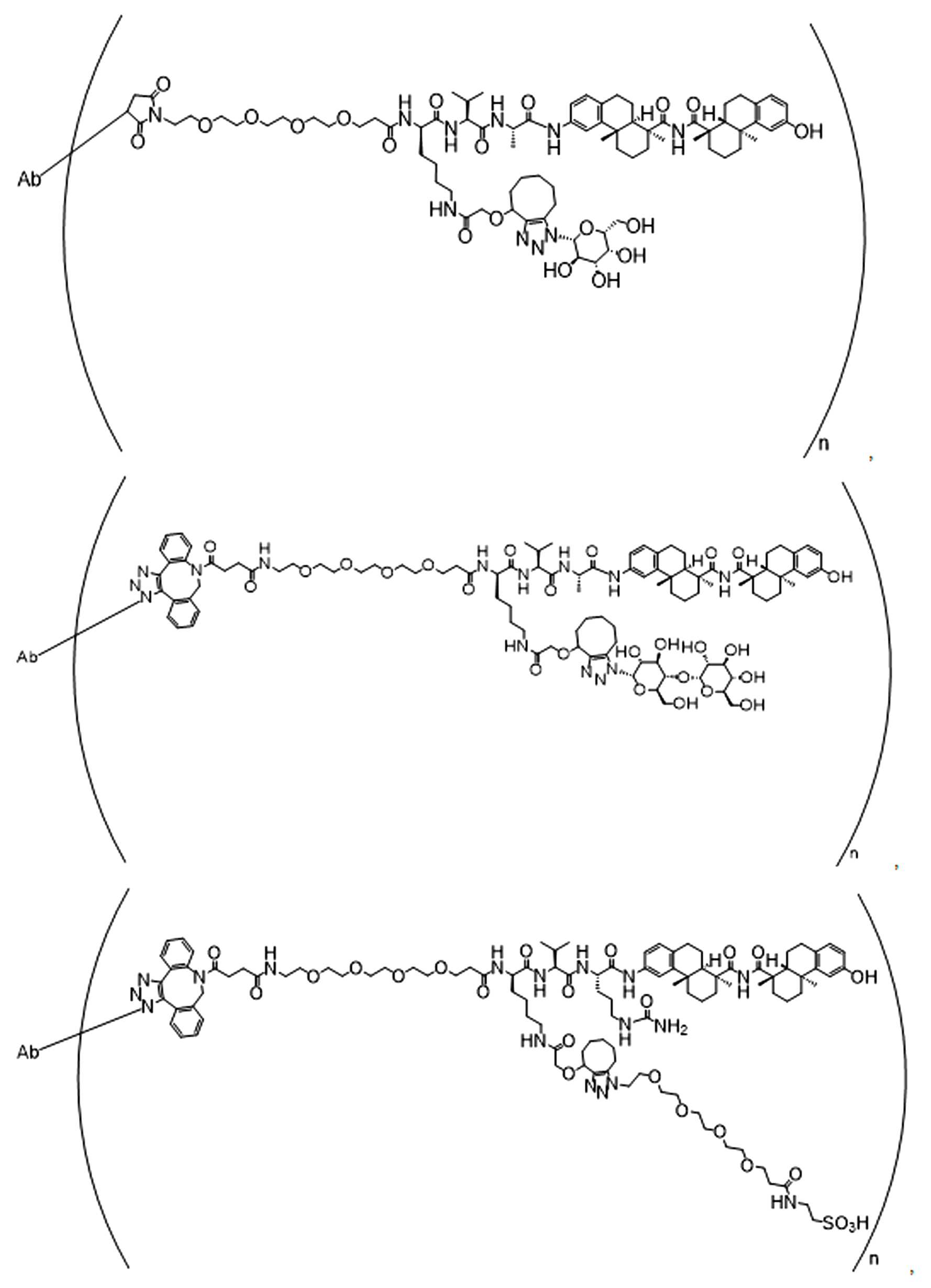
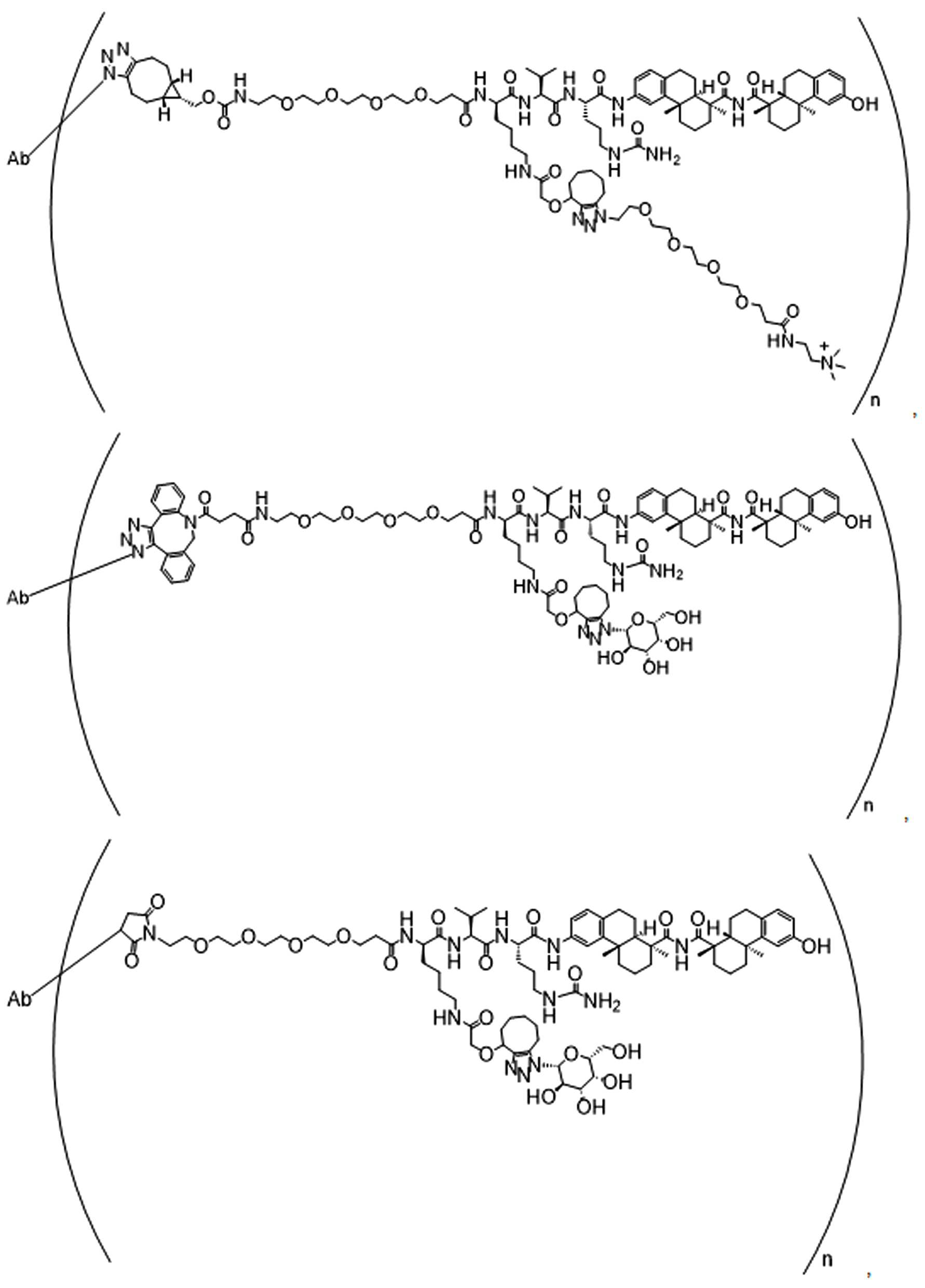
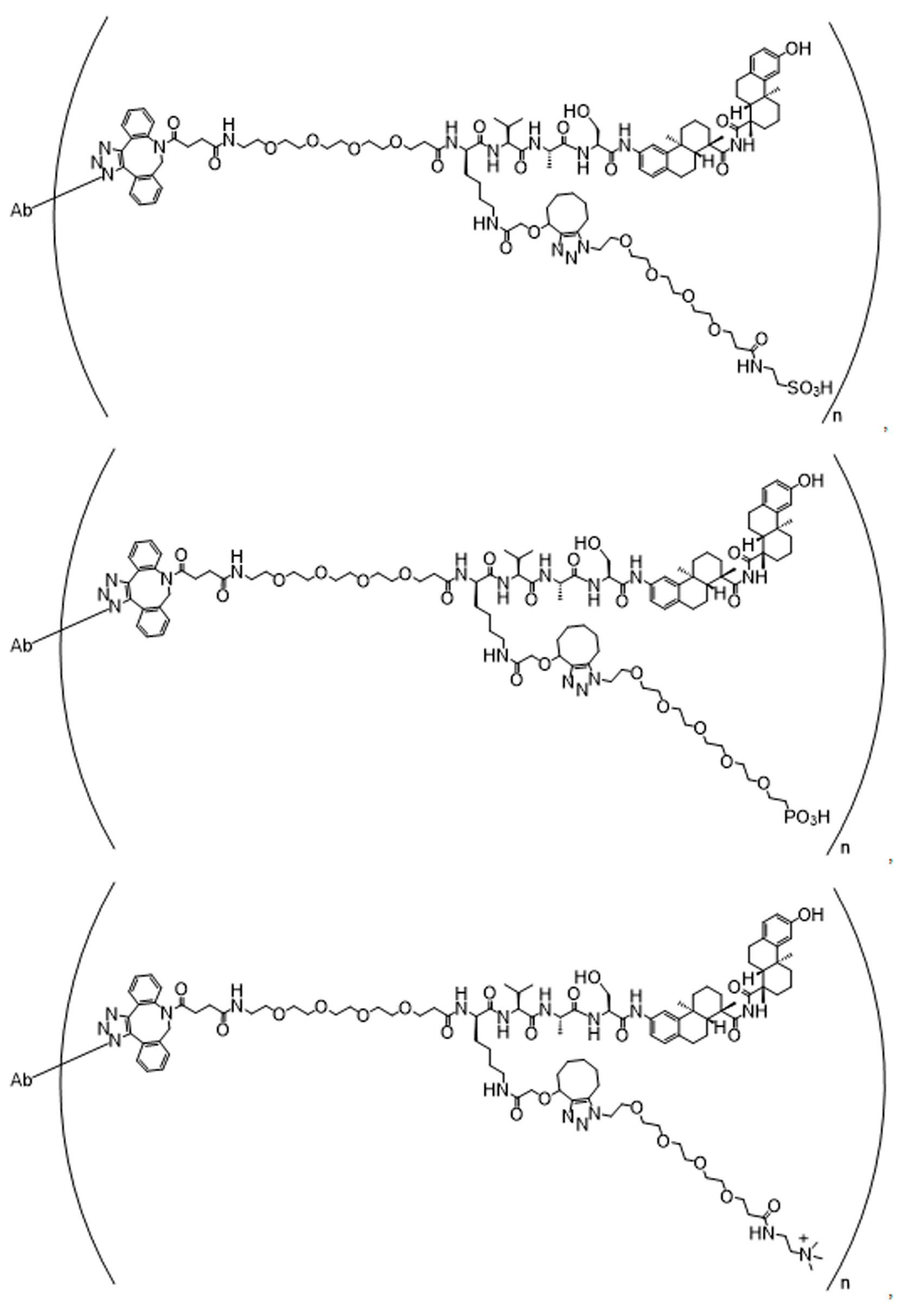
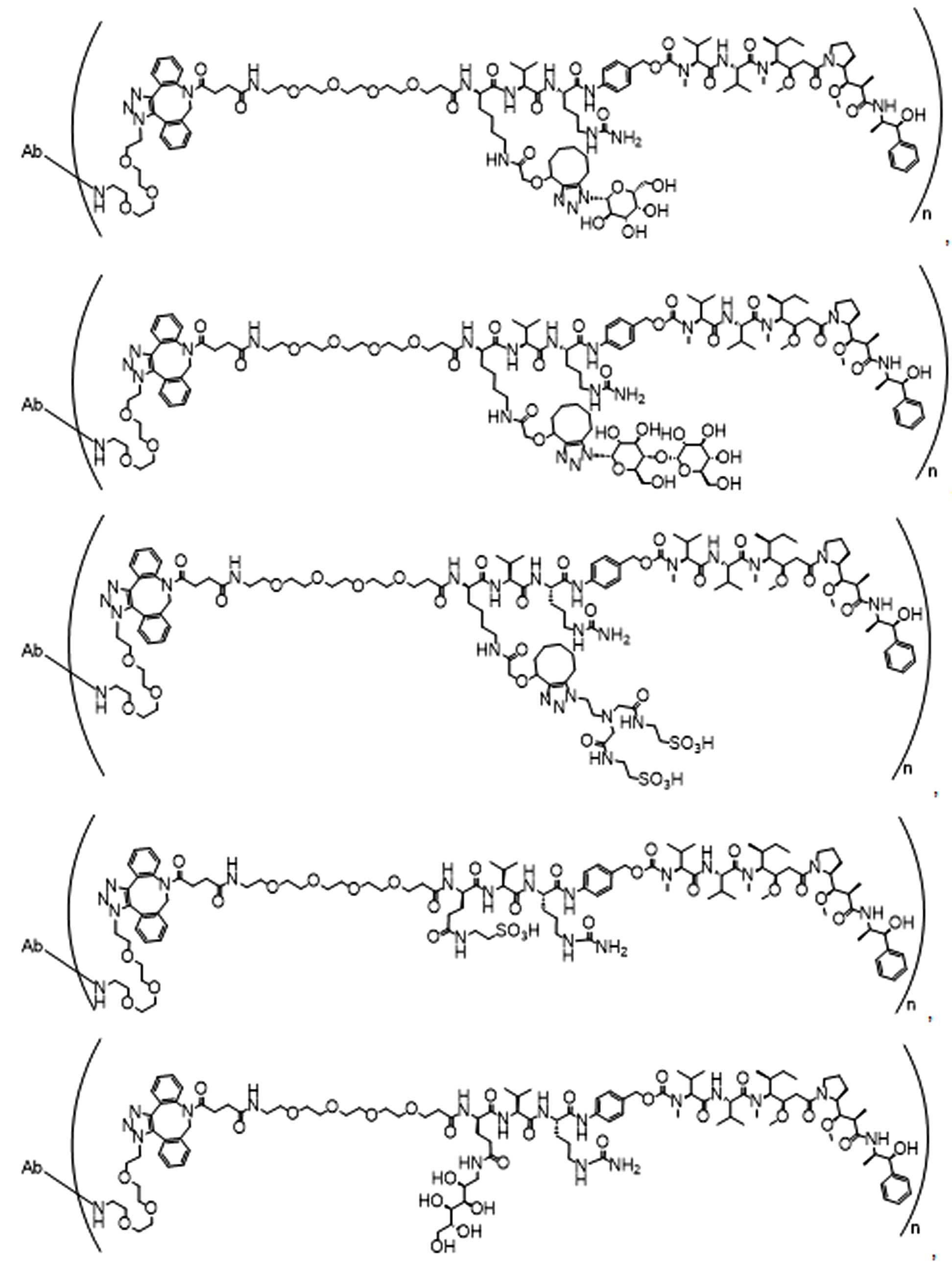
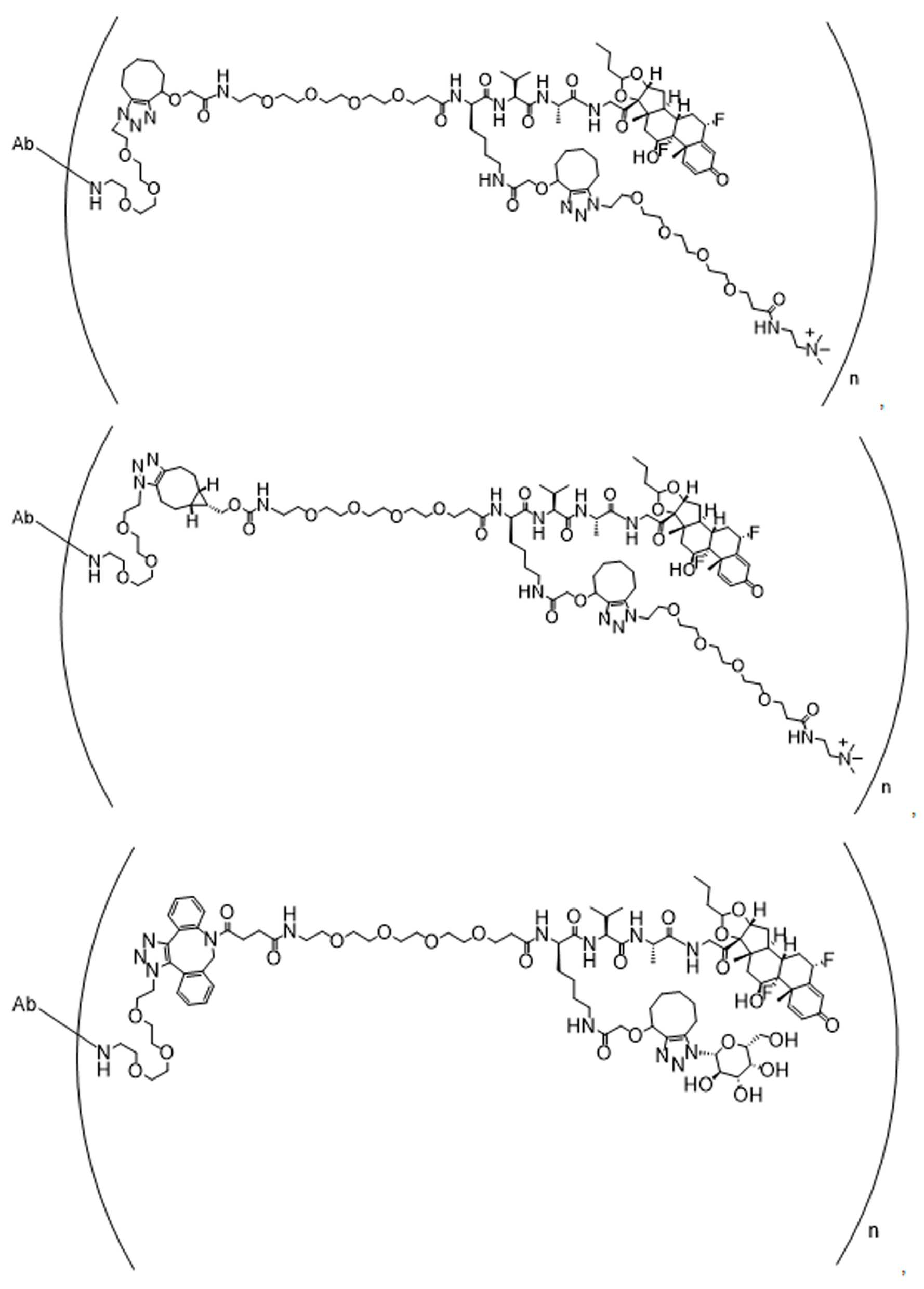
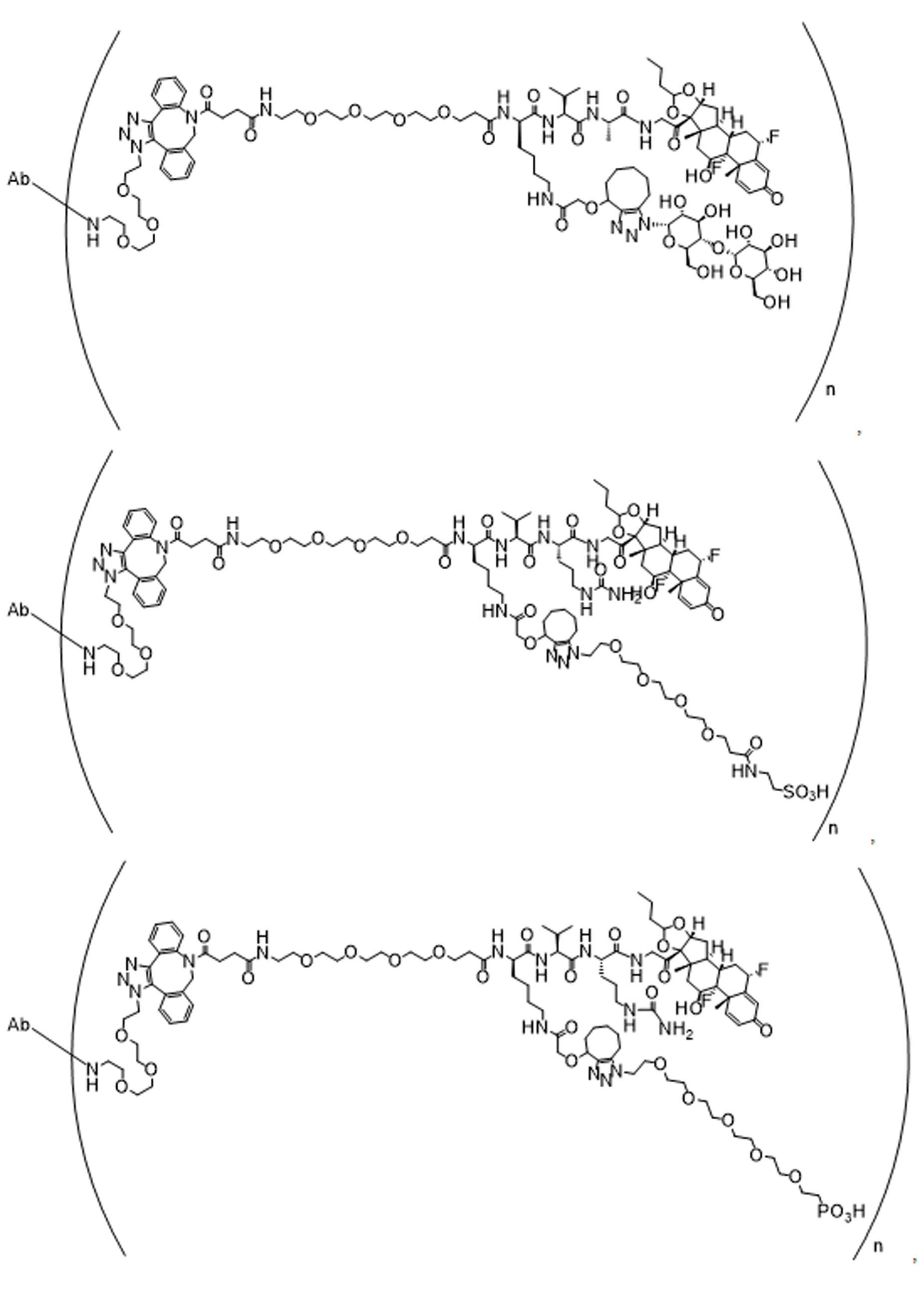
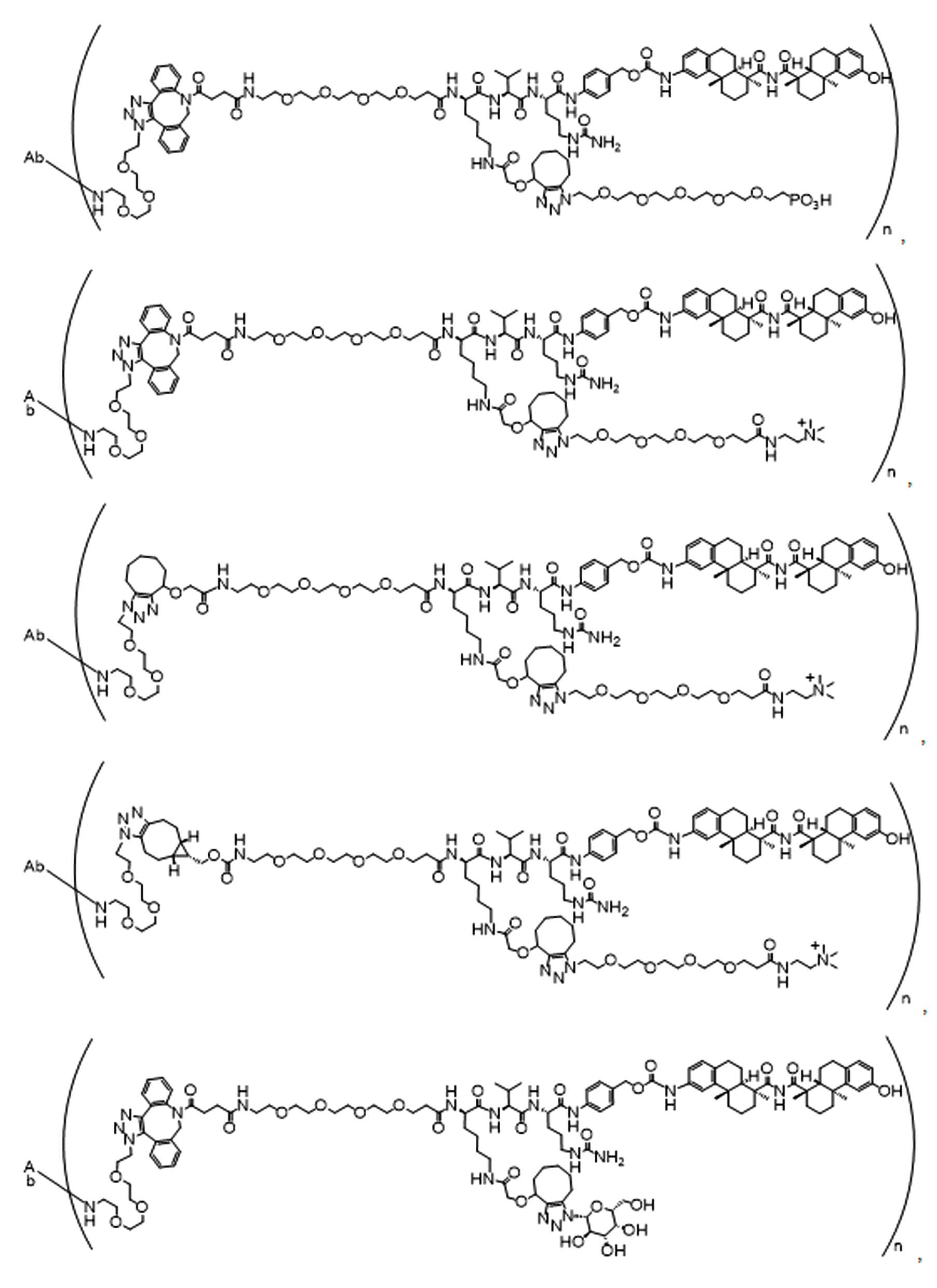
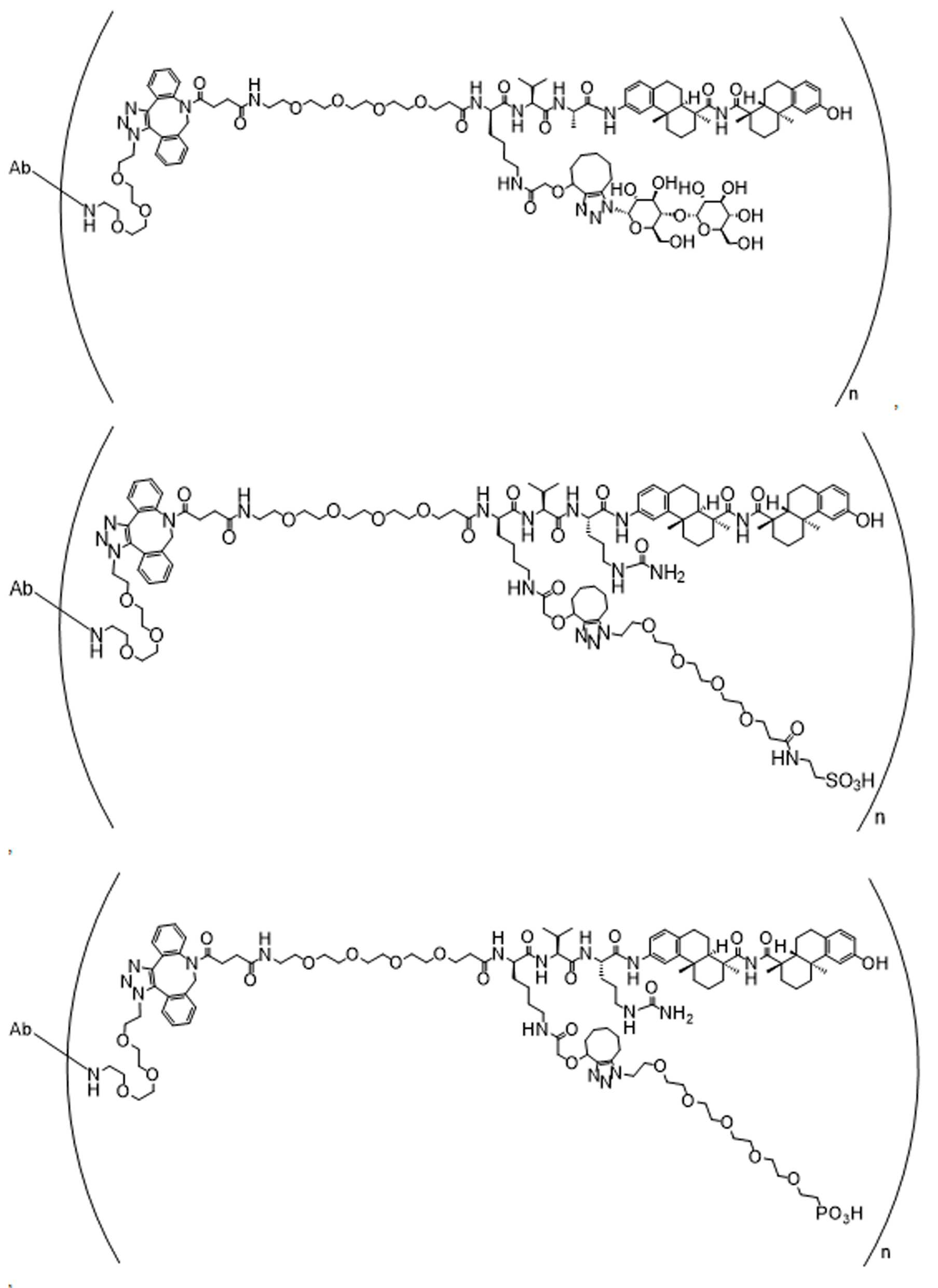
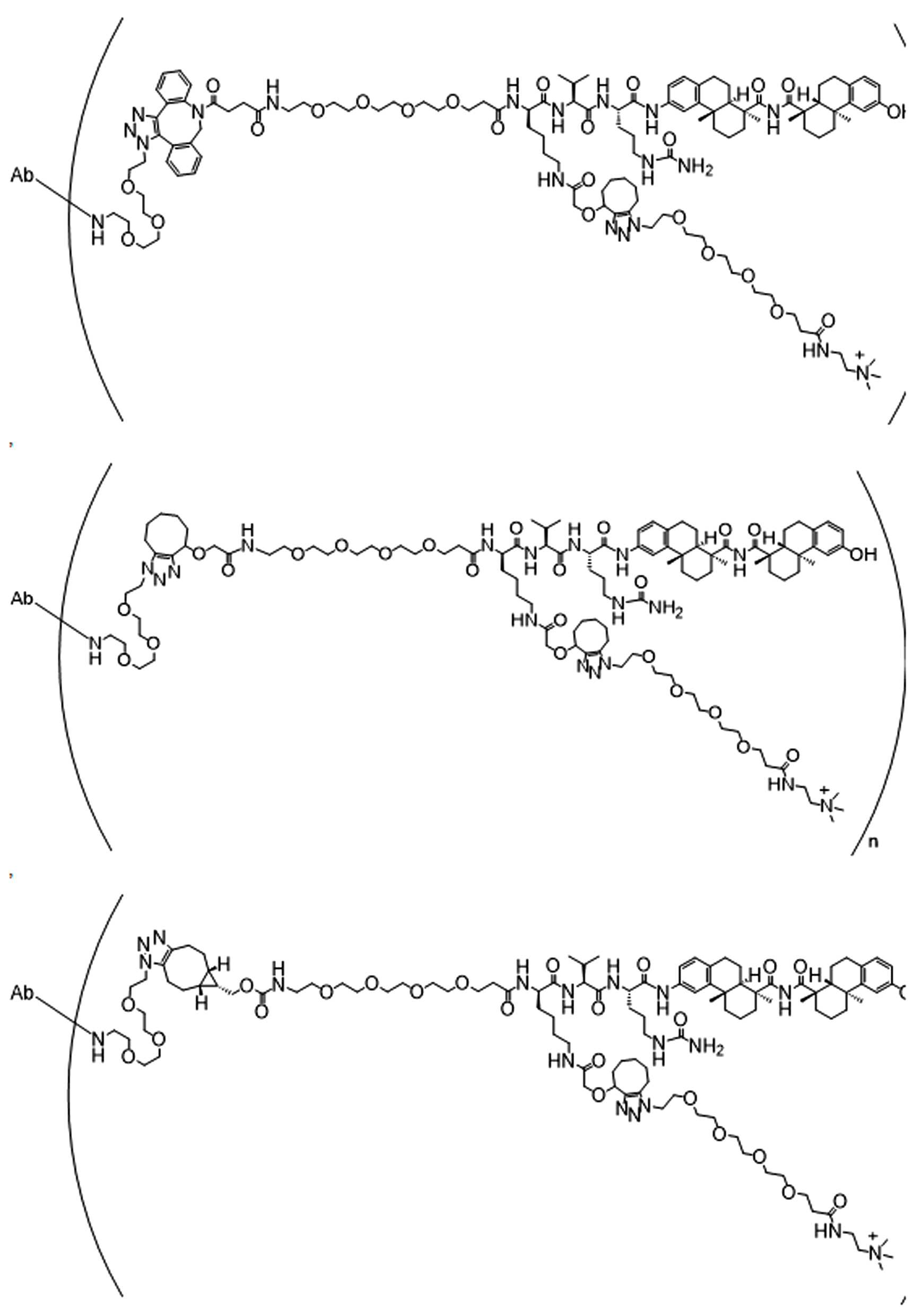
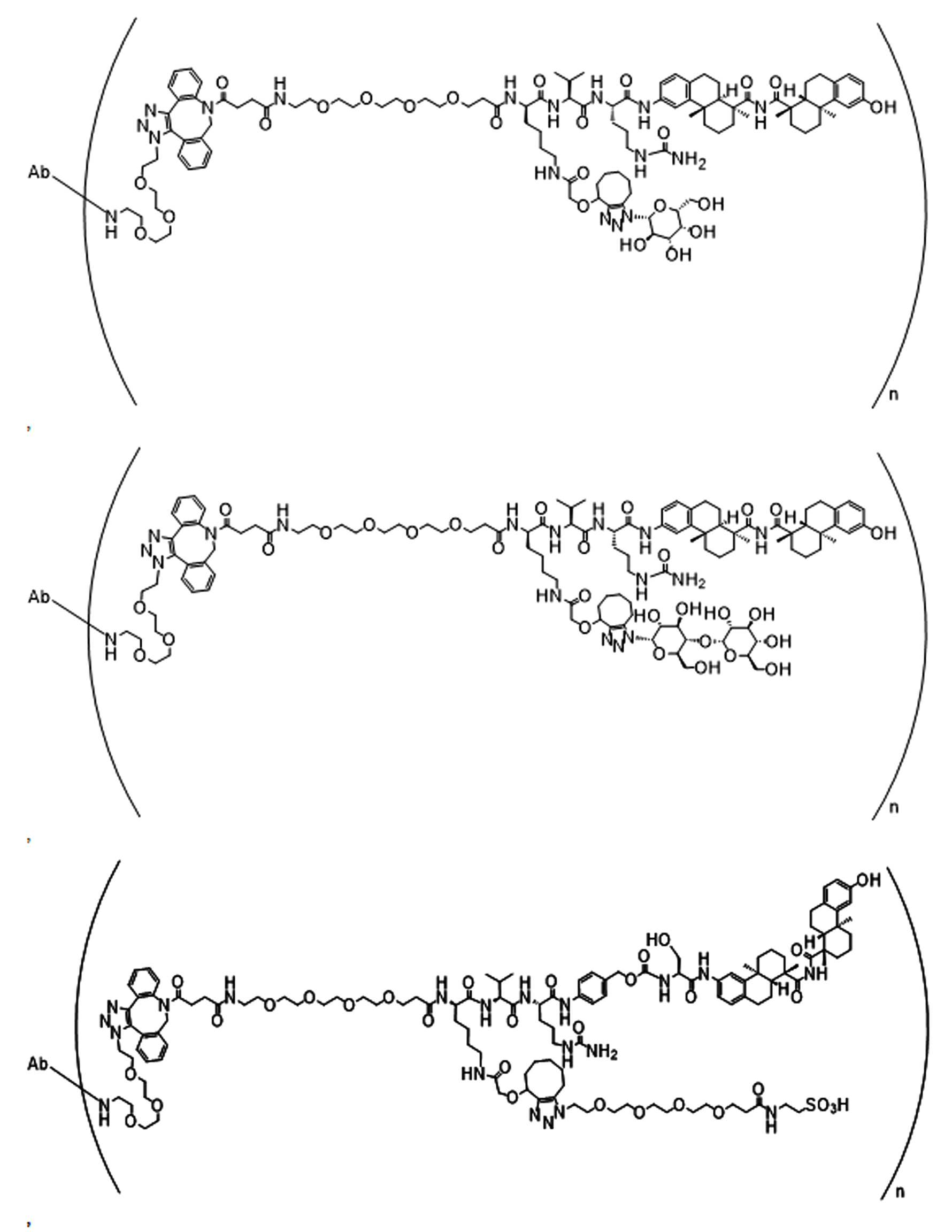
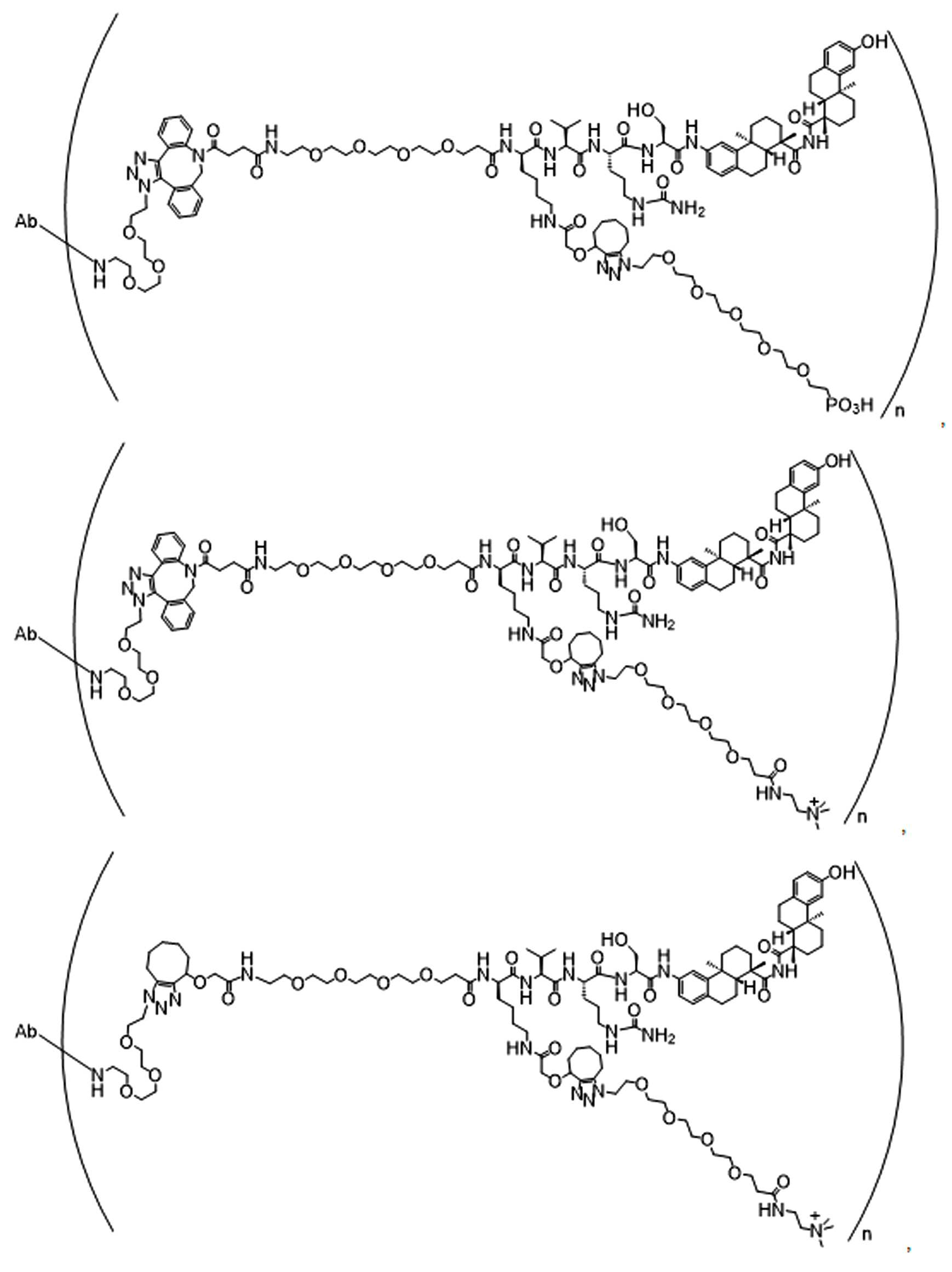
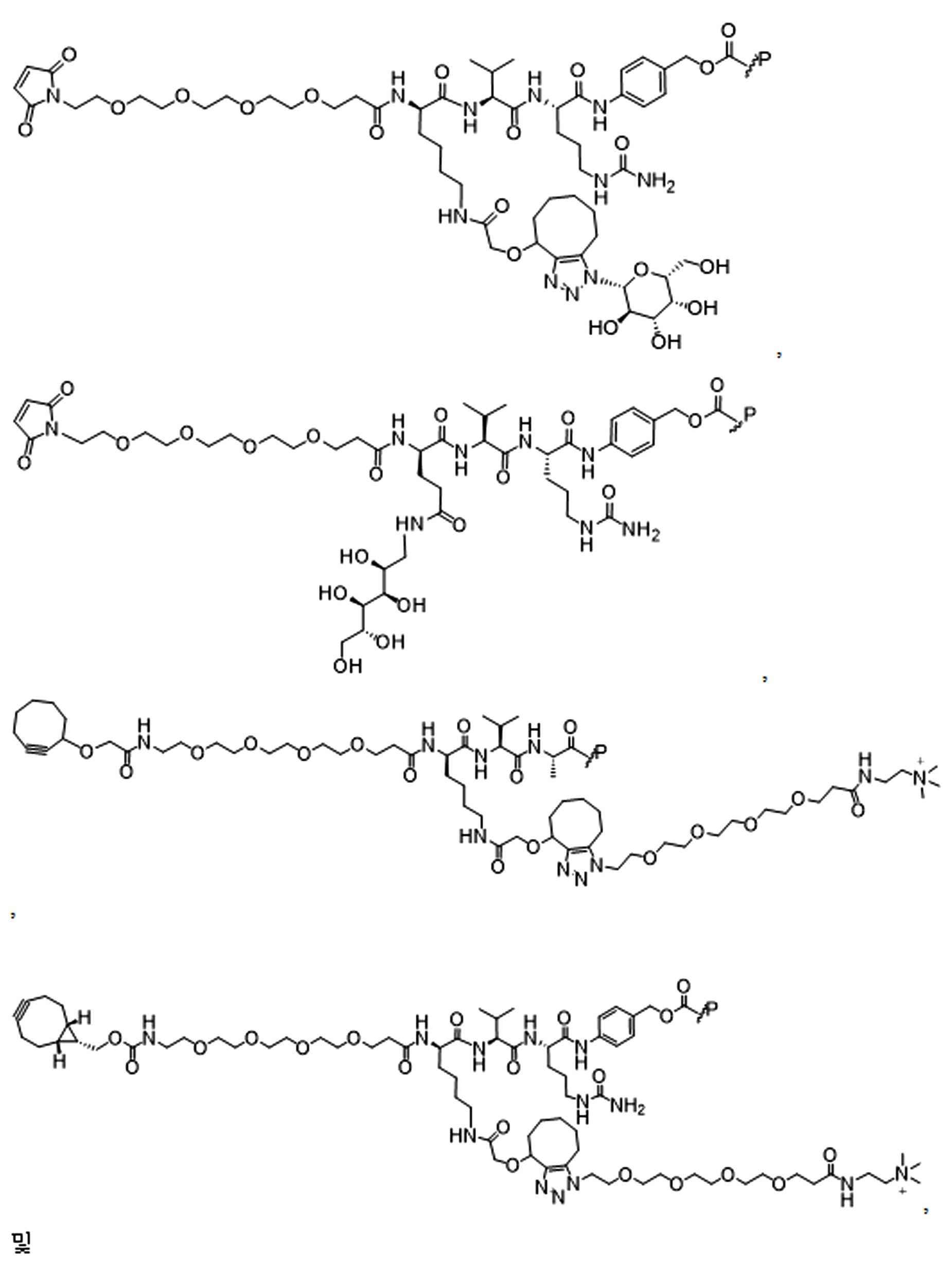
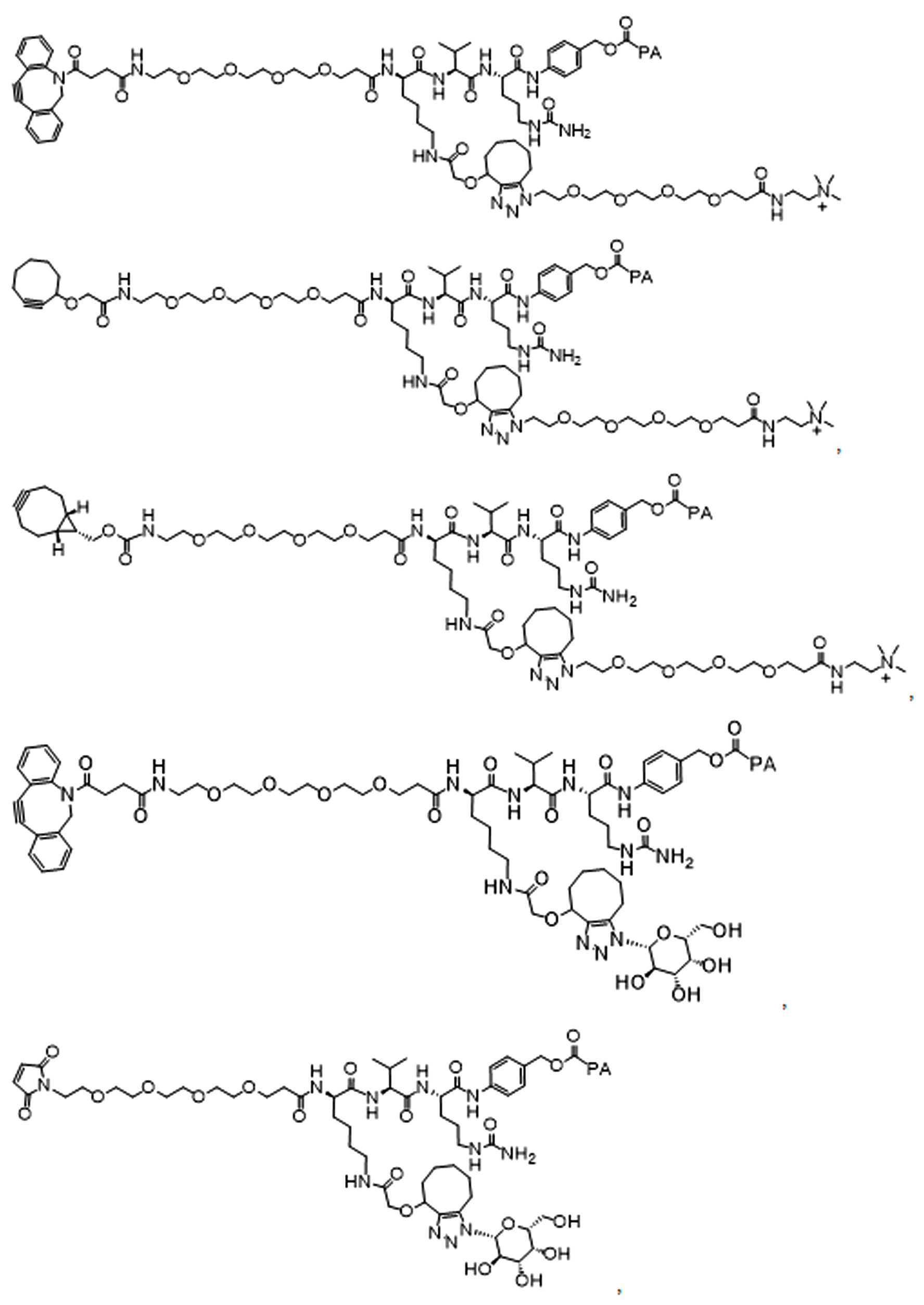
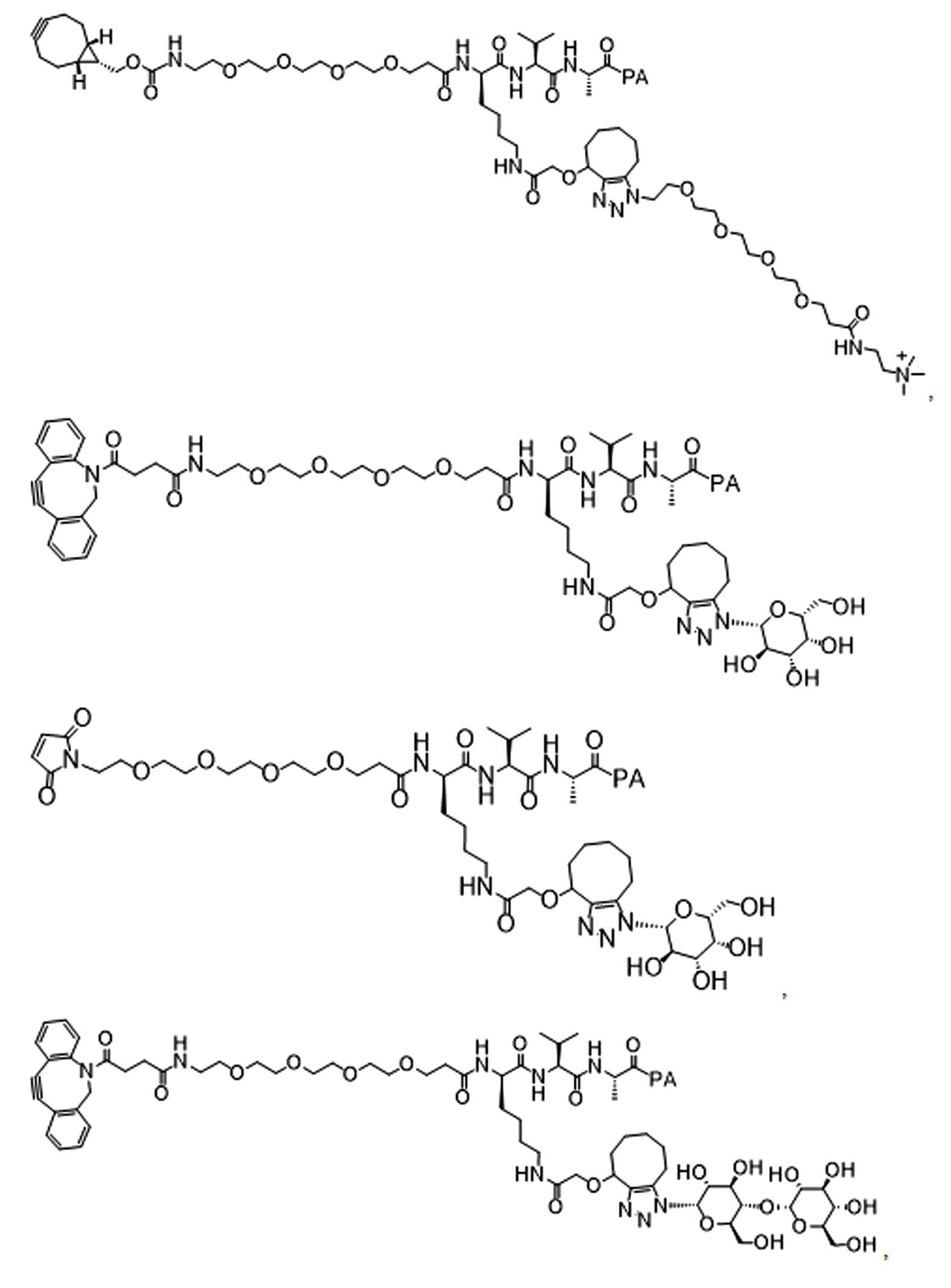
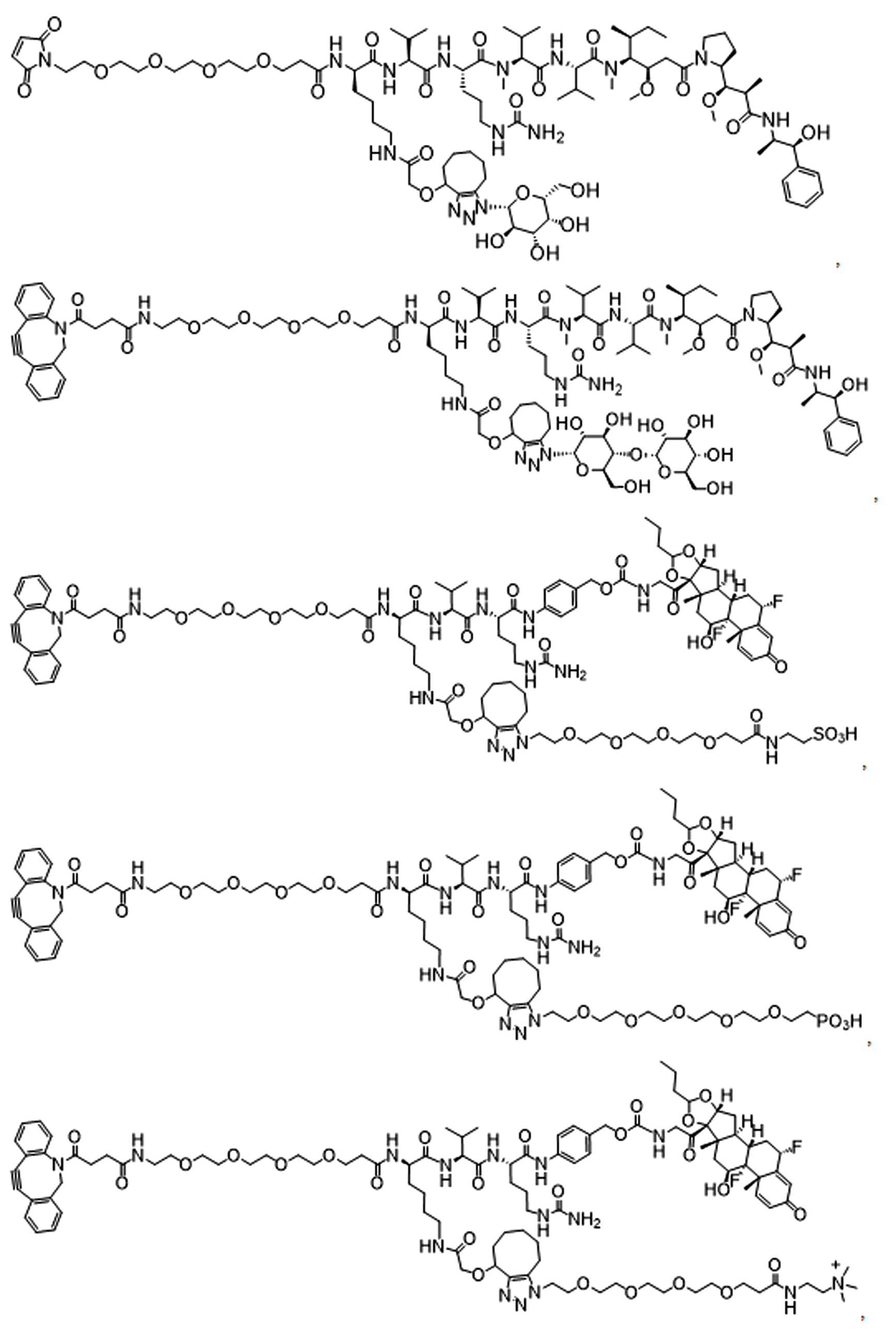
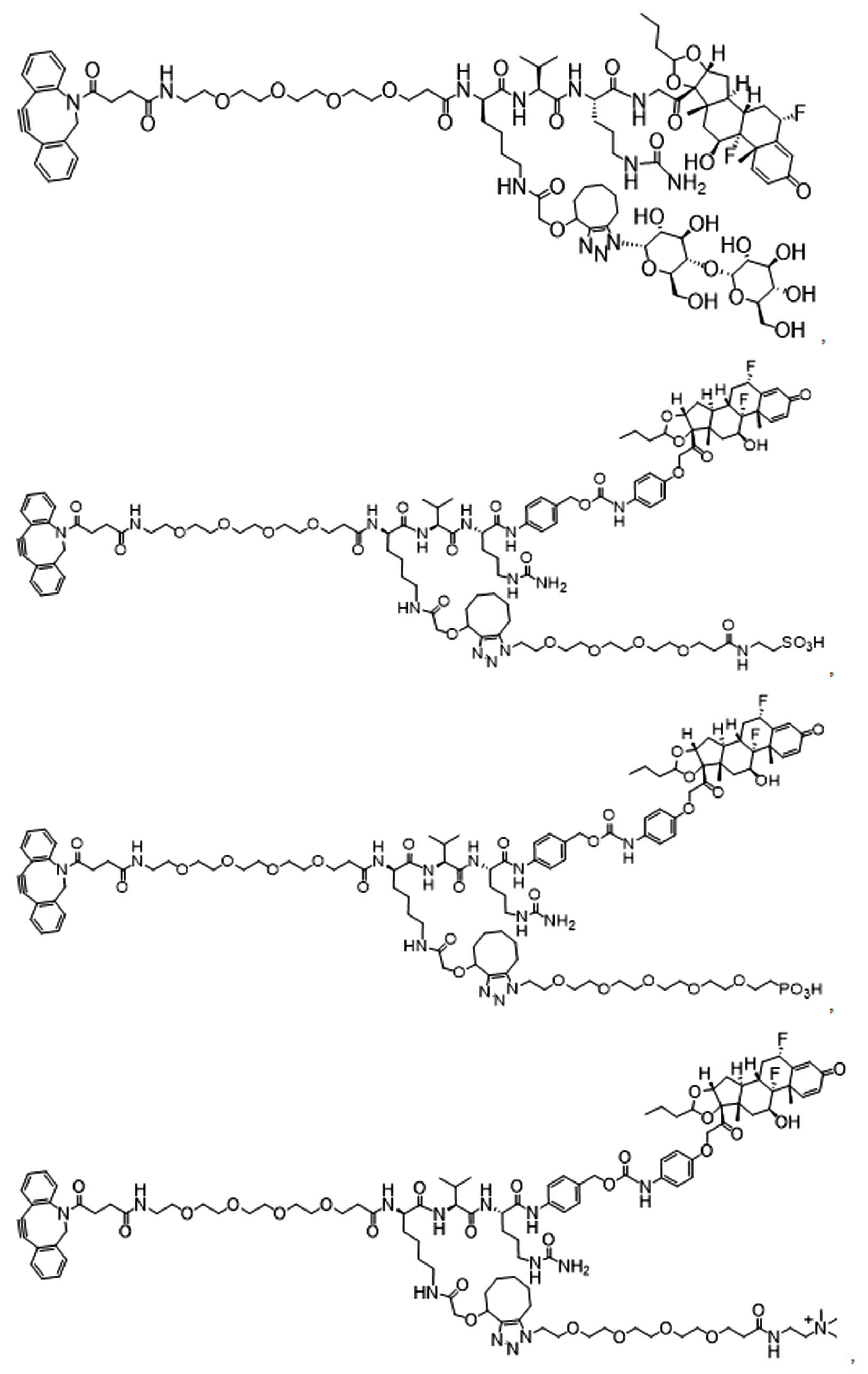
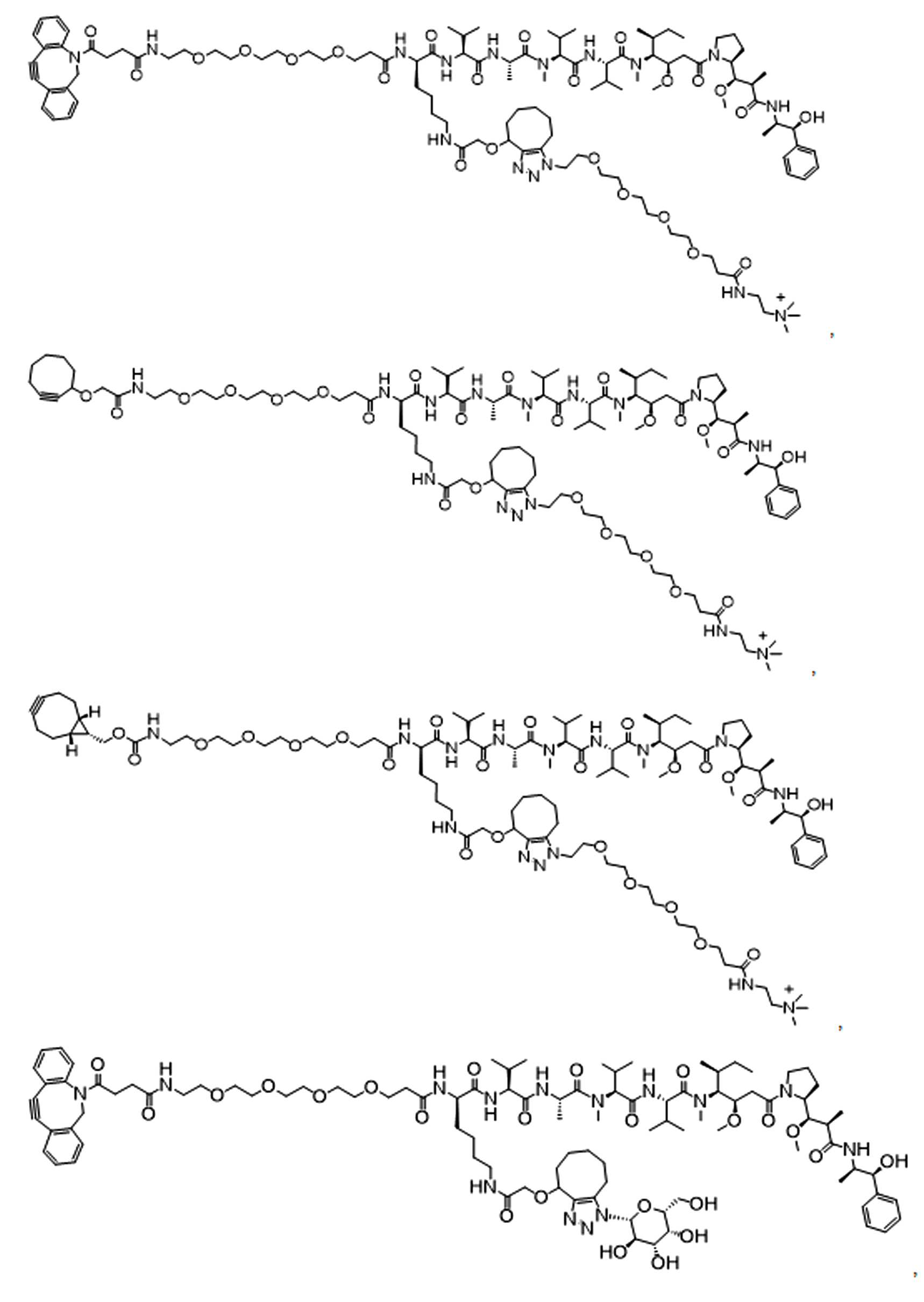
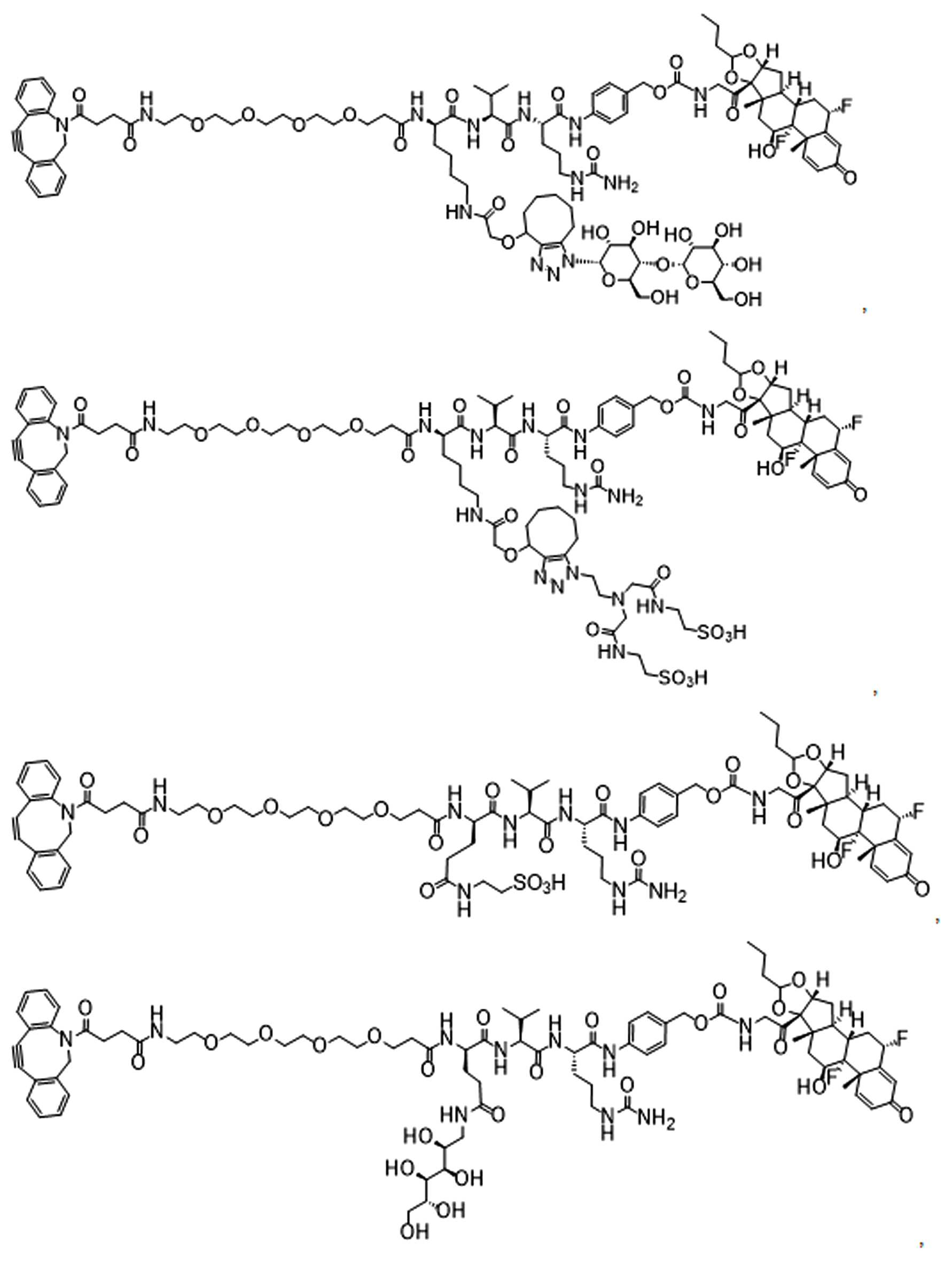
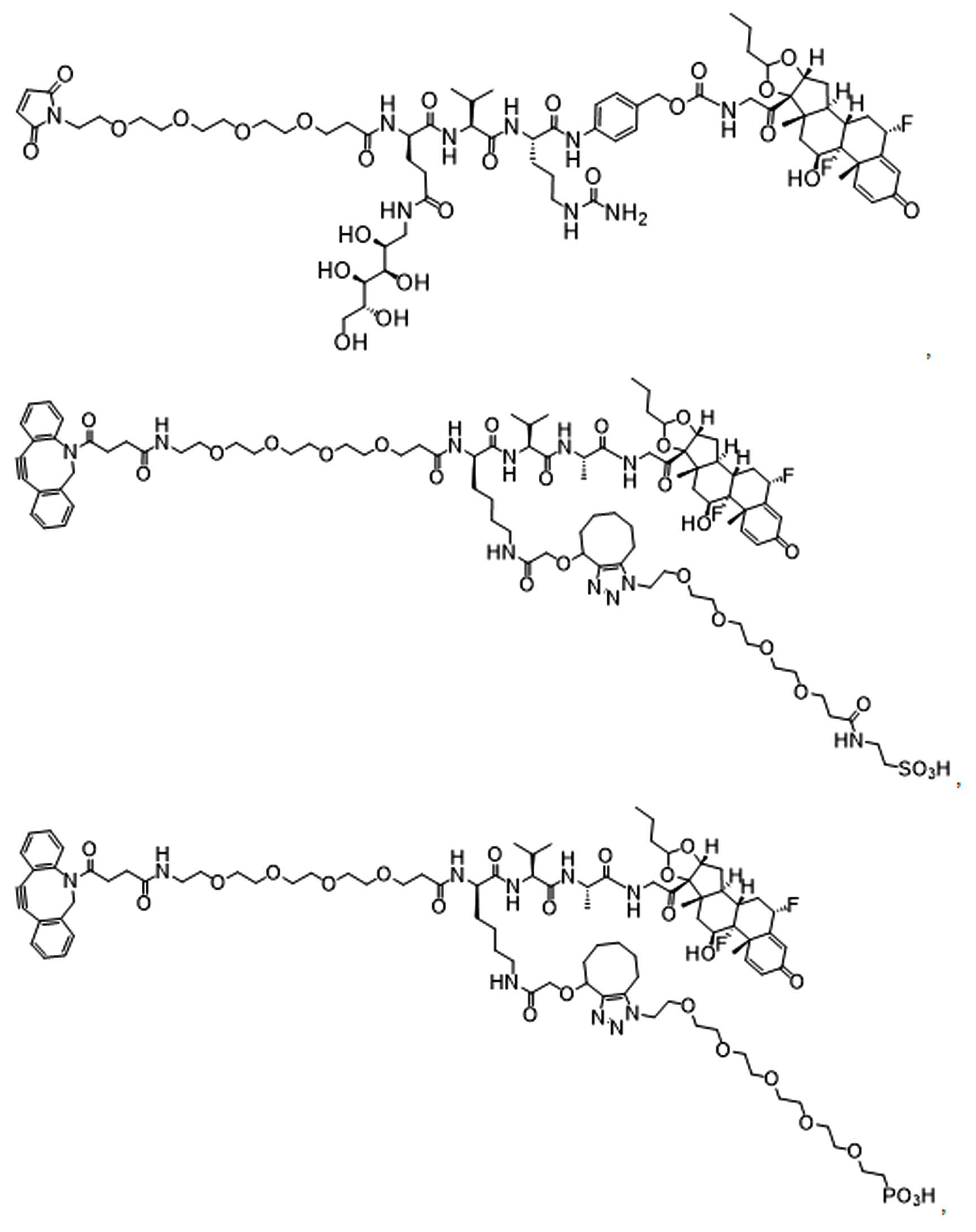
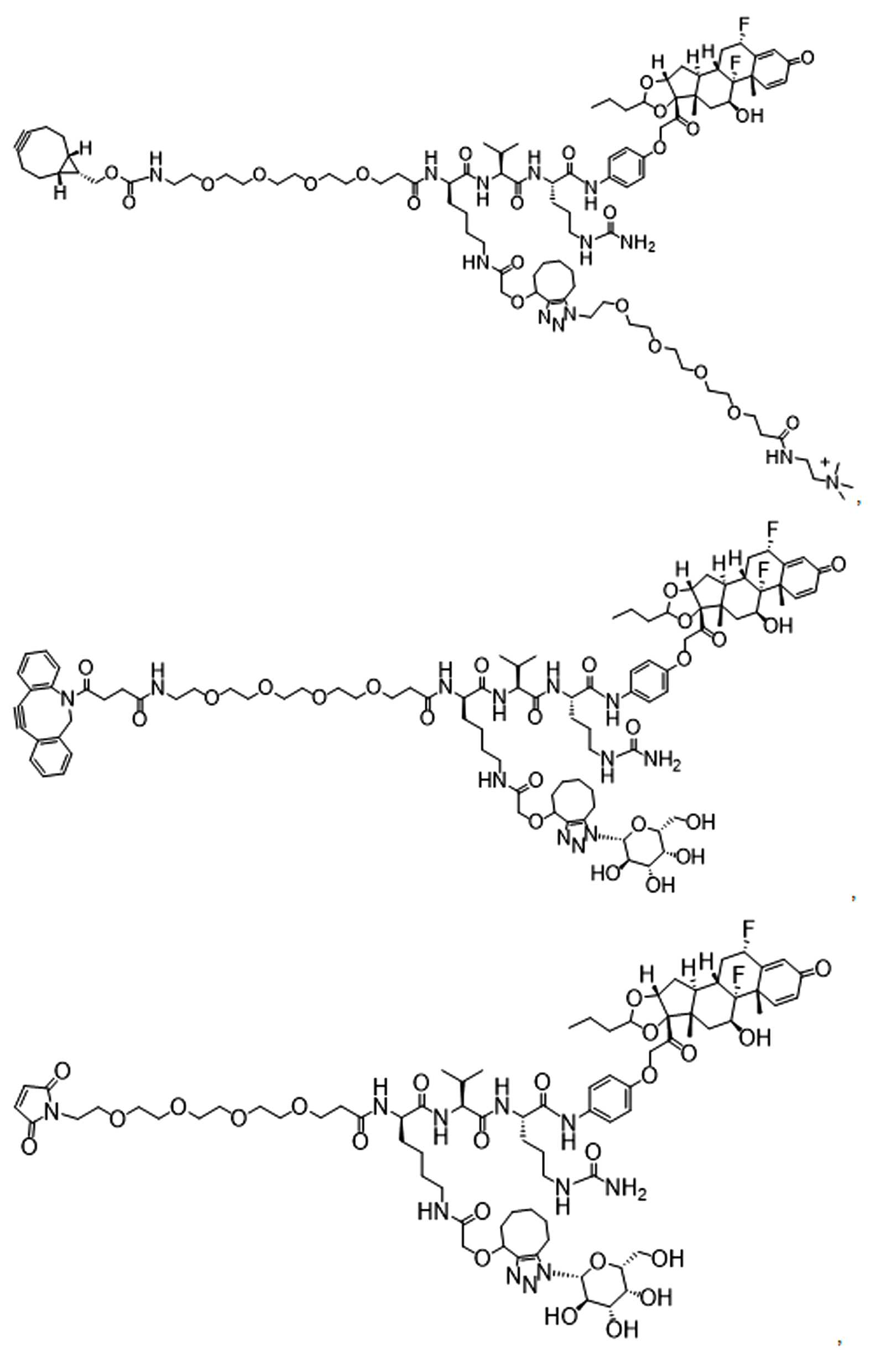
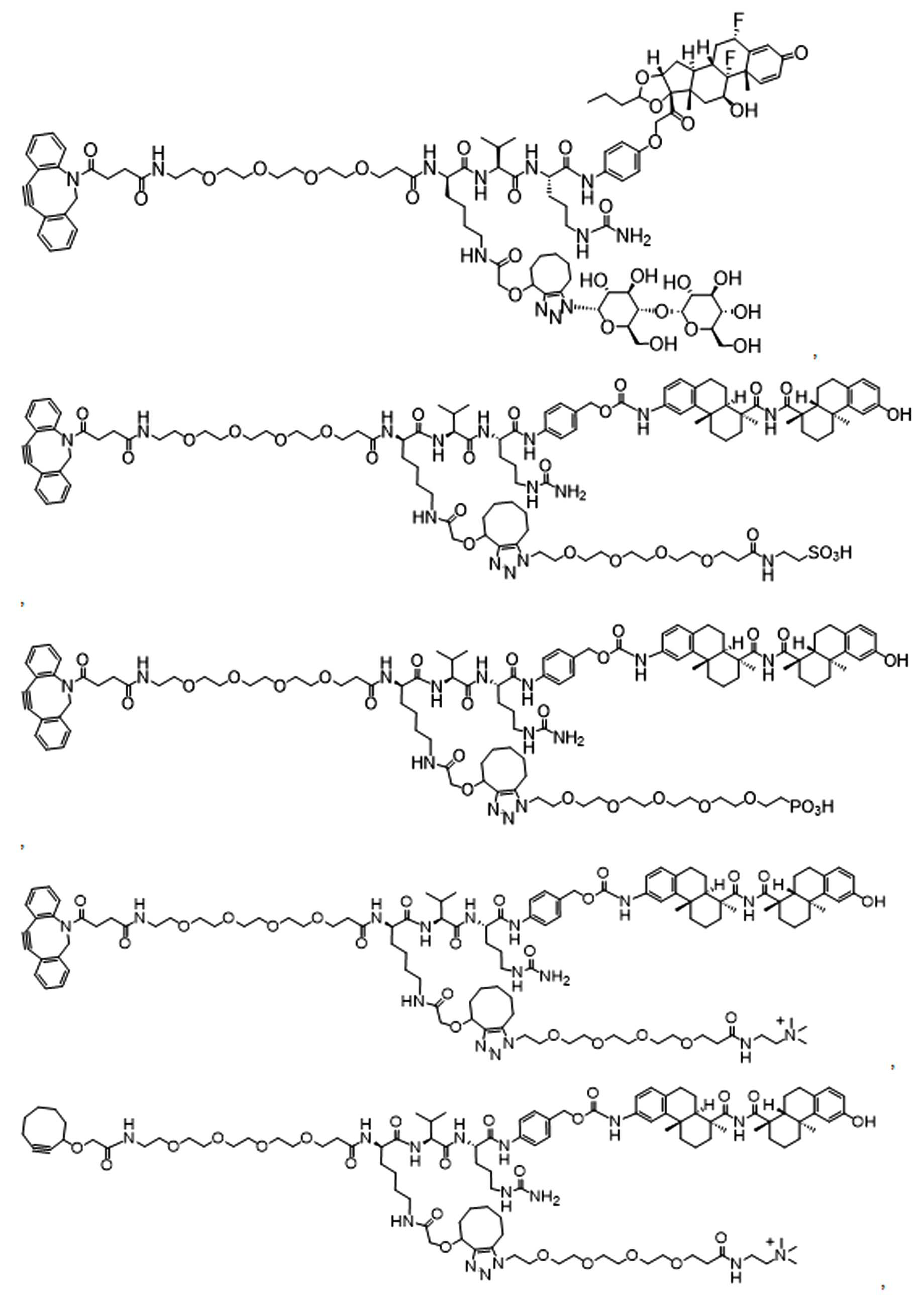
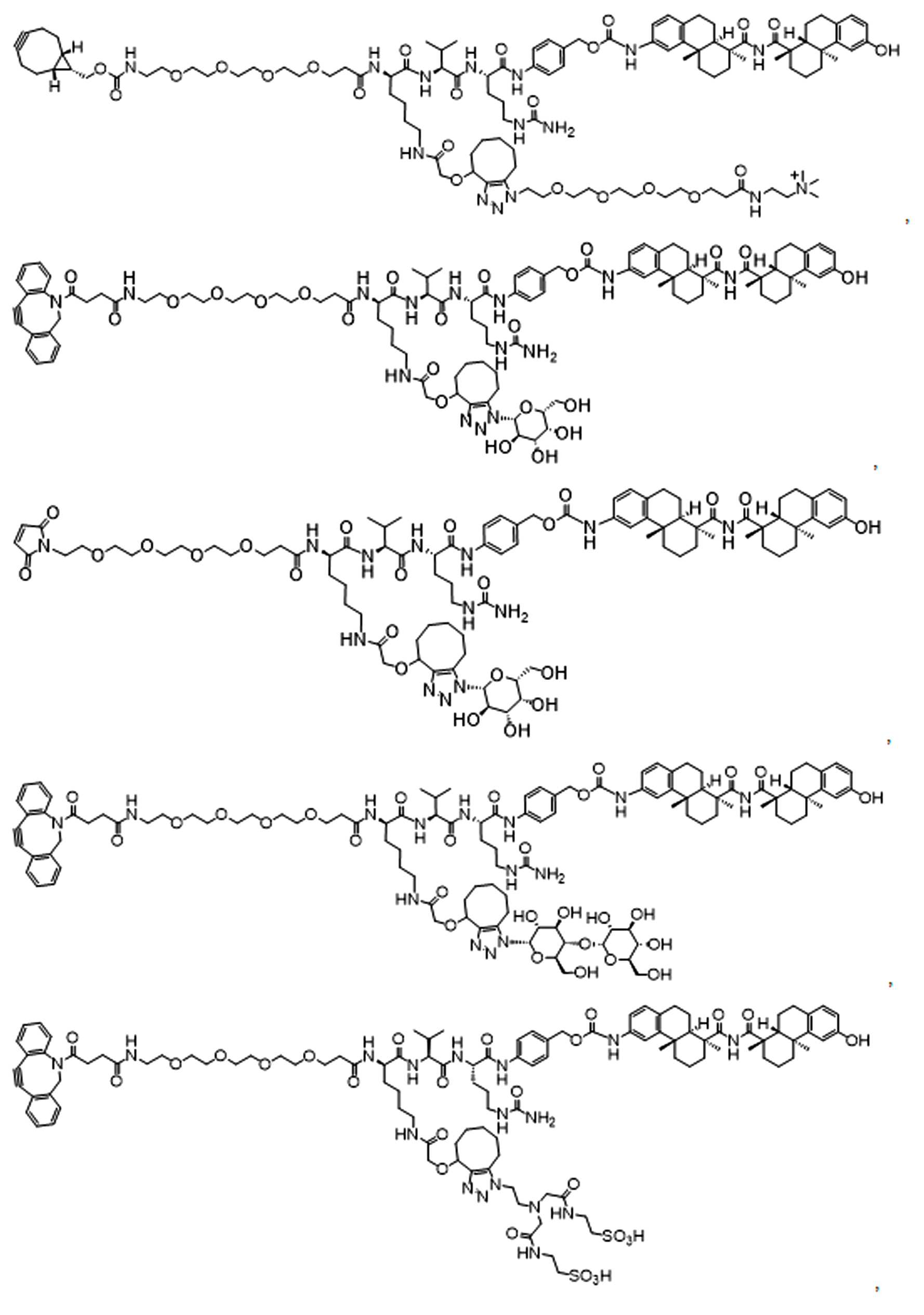
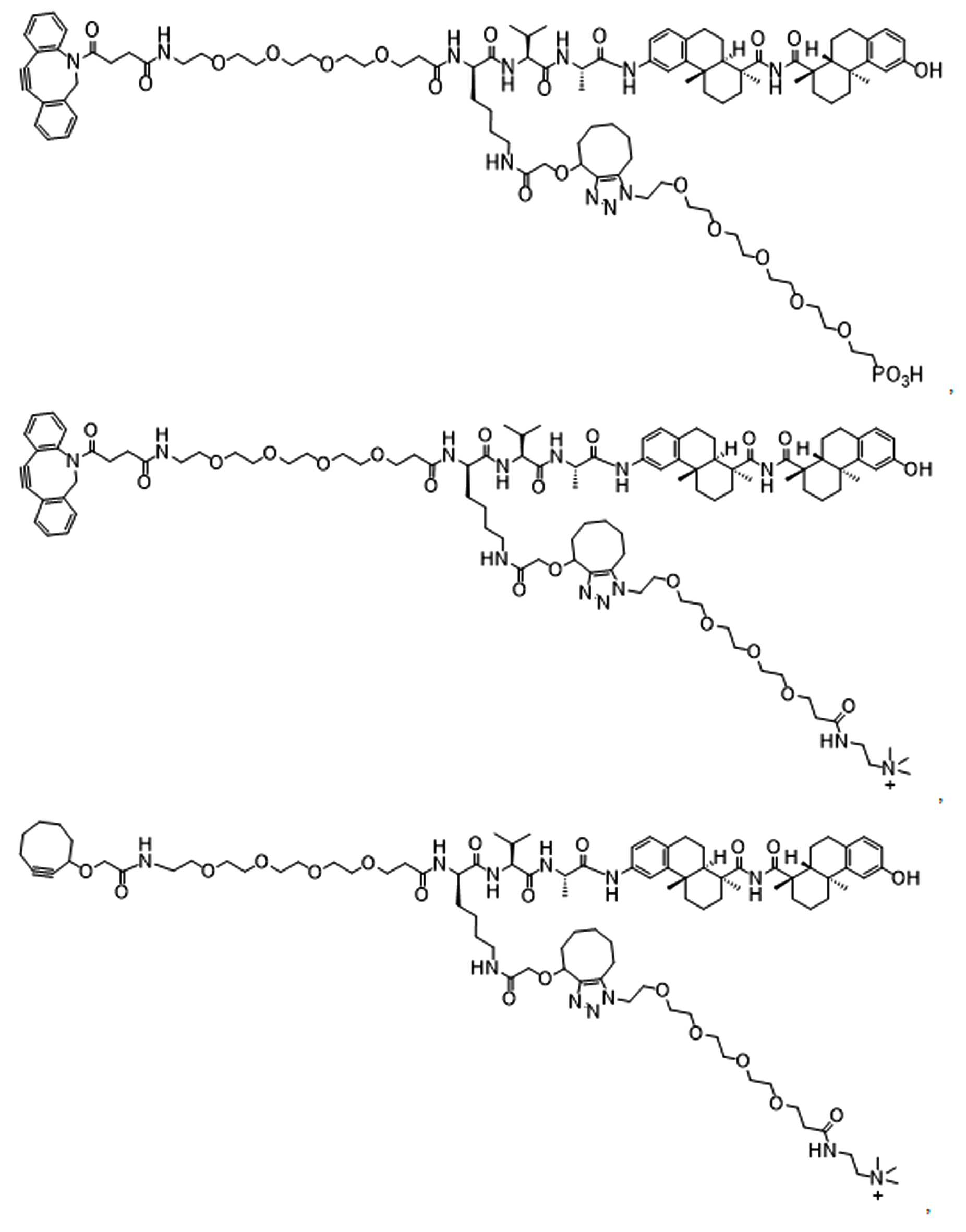
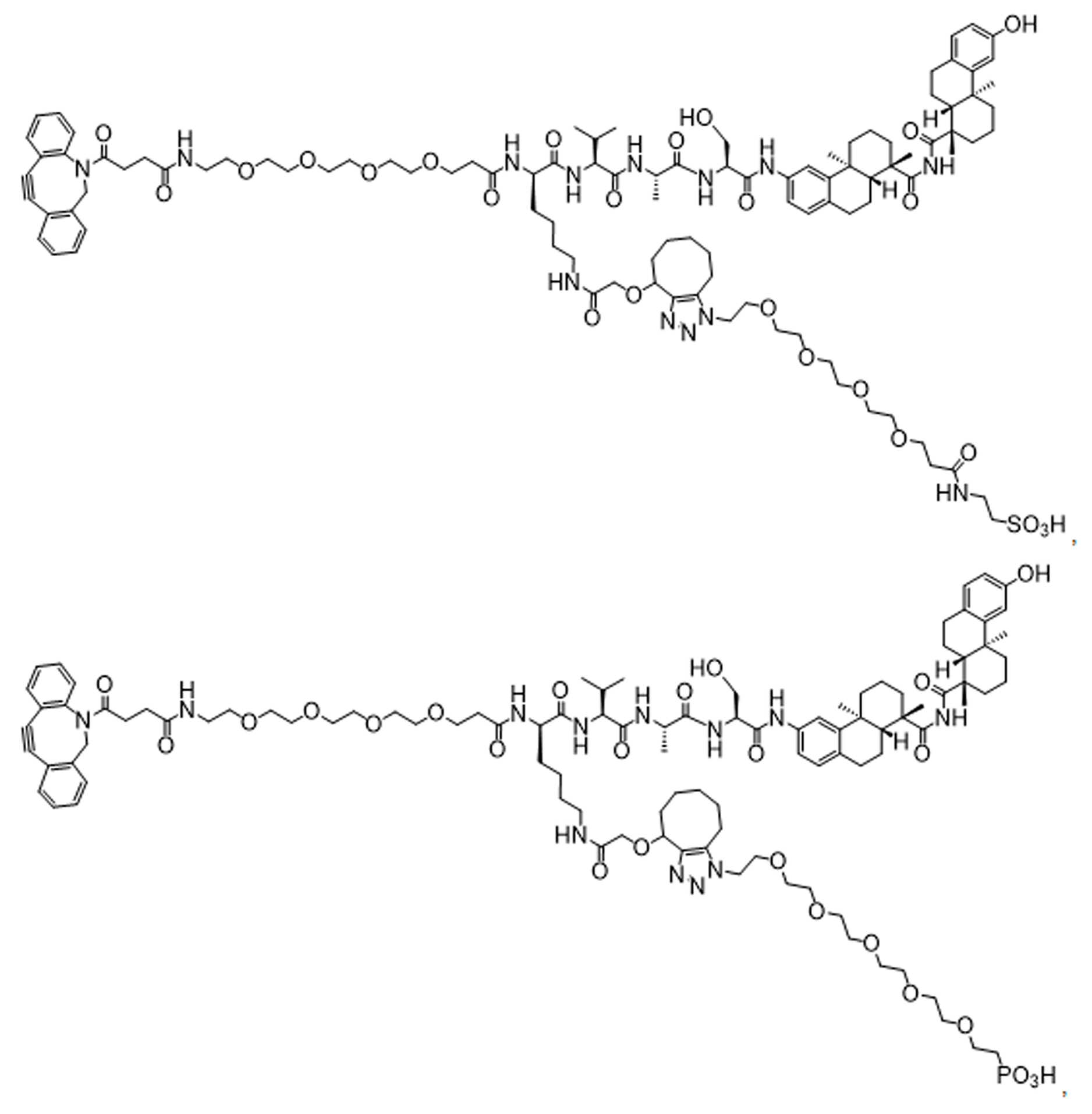
일부 경우에, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물은 항체 약물 접합제(ADC)이다. 여기서 BA는 Ab이고, 및 Ab 는 항체 또는 이의 항원 결합 단편이다. 일부경우에, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물은 하기로 이루어진 군으로부터 선택된 접합제다:
또는 이의 입체 이성질체 형태 또는 이의 위치 이성질체, 또는 위치 이성질체의 혼합물
여기서
각각의 Ab 는 항체 또는 이의 항원-결합 단편이고;
PA 는 페이로드 잔류물이며; 및
아래 첨자 n은 1 내지 30의 정수이다.
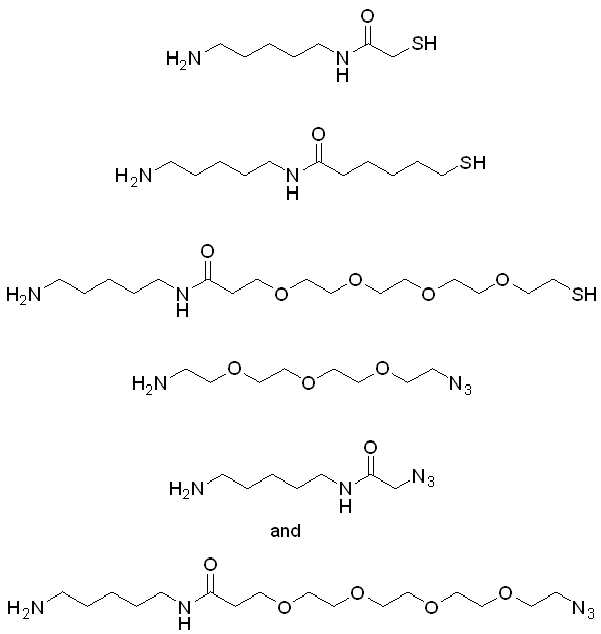
일부 경우에, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물은 항체 약물 접합제(ADC)이며, 여기서 BA 는 Ab이고, 및 Ab 는 다음으로 이루어진 군으로부터 선택된 항원 또는 그의 항원-결합 단편이다:
또는 이의 이성질체 형태, 또는 이의 위치 이성질체, 또는 이의 이성질체 이성질체의 혼합물이고, 여기서 각각의 Ab 는 항체, 또는 이의 항원 결합 단편이고, 및 아래 첨자 n 은 1 내지 30의 정수이다. 일부 실시양태에서, n은 1 내지 4의 정수이다. 일부 실시양태에서, n 은 2이다. 일부 실시양태에서, n 은 4이다.
일부 경우에, BA 는 화학식 (Ab-1)의 변형된 항체이다.
일부 경우에, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물은 항체 약물 접합제(ADC)이며, 여기서 BA는 본 원에 정의된 바와 같은 Ab-1이고, 여기서, Ab 는 다음으로 이루어진 군으로부터 선택된 항원 또는 그의 항원-결합 단편이다:
또는 이의 입체 이성질체 형태, 또는 이의 위치 이성질체, 또는 이의 위치 이성질체의 혼합물이고, 여기서 각각의 Ab는항체, 또는 이의 항원-결합 단편이고, 및 아래 첨자 n 은 1 내지 30의 정수이다. 일부 실시양태에서, n 은 1 내지 4의 정수이다. 일부 실시양태에서, n 은 2이다. 일부 실시양태에서, n 은 4이다.
본 원은 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물, 또는 그의 제약상 허용되는 염, 및 제약상 허용되는 부형제를 포함하는 제약 조성물을 제공한다.
또한, 환자에게 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)중 어느 하나의 화합물을 투여하는 것을 포함하는, 이를 필요로 하는 환자에서 질환 또는 장애를 치료하는 방법, 또는 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물을 포함하는 조성물이 제공된다.
다른 측면에서, 하나 이상의 페이로드 부분에 결합되고 공유 링커를 통해 하나 이상의 친수성 잔기에 결합된 반응성 링커를 포함하는 화합물이 제공되며, 상기 공유 링커는 각각의 반응성 링커, 페이로드 부분 및 친수성 잔기에 직접 또는 간접적으로 결합된다.
추가 측면에 있어서, 화학식 (VI)에 따른 화합물:
(VI)
또는 그의 제약상 허용되는 염, 용매화물, 입체 이성질체 또는 그의 유도체,
여기서:
RG'는 반응성 그룹 이고;
L은 3가 링커이고;
HL은 친수성 잔기이고;
PA는 페이로드 잔기이다.
하나의 경우에, 화학식 (VI)의 화합물은 하기 화학식 (VII)에 따른다:
(VII)
여기서:
LL은 3가 링커이고;
RG'는 반응성 그룹 이고;
RG 2 는 반응성 그룹 잔기이고;
SP 1 및 SP 2 는 독립적으로, 각 경우에, 존재하지 않거나 스페이서기 잔기이고;
HG는 친수성 잔기이고;
PA는 페이로드 잔기이며; 및
아래 첨자 q는 0 또는 1이다.
하나의 경우에, 화학식 (VII)의 화합물은 화학식 (VIII)에 따른 것이다:
여기서
고리 A는 트리아졸에 융합되고 시클로알킬 (cycloalkyl), 시클로알케닐(cycloalkenyl), 헤테로시클로알킬(heterocycloalkyl), 및 헤테로시클로알케닐(heterocycloalkenyl)로 이루어진 군으로부터 선택되고;
여기서 시클로알킬 (cycloalkyl), 시클로알케닐(cycloalkenyl), 헤테로시클로알킬(heterocycloalkyl), 헤테로시클로알케닐(heterocycloalkenyl)은 선택적으로 알킬, -OH, 또는 NR a R b 로 치환되며, 여기서 R a 및 R b 는 각각 알킬 또는 -H이다.
다른 경우에, 화학식 (VII)의 화합물은 화학식 (IX)에 따른다:
(IX)
여기서:
AA 1 은 아미노산 잔기를 포함하는 3가 링커이고;
AA 2 는 디펩티드, 트리펩티드 또는 테트라펩티드 잔기이고; 및
아래 첨자 p 는 0 또는 1이고; 및
아래 첨자 q 는 0 또는 1이다.
특정 경우에, 화학식 (IX)의 화합물은 하기 화학식 (IX)에 따르고: 화학식 (IXa), 화학식 (IXb) 또는 화학식 (IXc)에 따른다:
AA 1 은 아미노산 잔기를 포함하는 3가 링커이며, 항체, 페이로드 및 친수성기에 직접 또는 간접적으로 연결된다. 일부 예에서, AA 1 또는 AA 2 중 어느 하나는독립적으로 각 경우에, 알라닌(alanine), 발린(valine), 류신(leucine), 이소류신(isoleucine), 메티오닌(methionine), 트립토판(tryptophan), 페닐알라닌(phenylalanine), 프롤린(proline), 세린(serine), 트레오닌(threonine), 시스테인(cysteine), 티로신(tyrosine), 아스파라긴(asparagine), 글루타민(glutamine), 아스파르트산(aspartic acid), 글루탐산(glutamic acid), 리신(lysine), 아르기닌(arginine), 히스티딘(histidine), 또는 시트룰린(citrulline), 또는 이의 유도체 또는 이들의 조합으로부터 선택된 아미노산이다. 특정 실시양태에서, AA 1 는 알라닌(alanine), 발린(valine), 류신(leucine), 이소류신(isoleucine), 메티오닌(methionine), 트립토판(tryptophan), 페닐알라닌(phenylalanine), 프롤린(proline), 세린(serine), 트레오닌(threonine), 시스테인(cysteine), 티로신(tyrosine), 아스파라긴(asparagine), 글루타민(glutamine), 아스파르트산(aspartic acid), 글루탐산(glutamic acid), 리신(lysine), 아르기닌(arginine), 히스티딘(histidine), 또는 시트룰린(citrulline), 또는 이의 유도체 또는 이들의 조합으로부터 선택된 아미노산이다.
특정 실시양태에서, AA 1 은 페이로드, 결합제(예를 들어, 이의 항체 또는 항원 결합 단편), 및 친수성기를 포함하는 링커, 예를 들어 리신, 아스파르긴, 글루탐산, 아스파르트산, 글루타민, 시스테인, 트레오닌, 세린, 또는 티로신을 연결하는 3개의 작용기를 갖는 아미노산이다.
특정 실시양태에서, AA 1 은 리신이다. 특정 실시양태에서 AA 1 은 글루타민인다. 특정 실시양태에서, AA 1 은 리신 또는 리신의 유도체이다. 특정 실시양태에서, AA 1 는 L-리신이다. 특정 실시양태에서, 상기 AA 1 은 D-리신이다. 특정 실시양태에서, AA 1 는 글루탐산이다. 특정 실시양태에서, AA 1 는 아스파르트산이다. 특정 실시양태에서, 상기 AA 2 는 발린-시트룰린이다. 일부 실시양태에서, 상기AA 2 는 시트룰린-발린이다. 일부 실시양태에서, 상기 AA 2 는 발린-알라닌이다. 일부 실시양태에서, 상기 AA 2 는 알라닌-발린이다. 일부 실시양태에서, 상기 AA 2 는 발린-글리신이다. 일부 실시양태에서, 상기 AA 2 는 글리신-발린이다. 일부 실시양태에서, 상기 AA 1 -AA 2 는 글루타민-발린-시트룰린이다. 일부 실시양태에서, 상기 AA 1 -AA 2 는 리신-발린-시트룰린이다. 일부 실시양태에서, 상기 AA 1 -AA 2 는 리신-발린-알라닌이다. 일부 실시양태에서, 상기 AA 1 -AA 2 는 글루타민-발린-알라닌이다.
특정 경우에, 화학식 (IXa), 화학식 (IXb) 또는 화학식 (IXc)의 화합물은 화학식 (Xa), (Xb), (Xc) 또는 (Xd)에 따른다:
여기서:
아래 첨자 e 는 독립적으로, 각 경우에, 0 내지 6의 정수, 또는 0 내지 5의 정수이다. 일부 경우에, 아래 첨자 p 는 0이다. 일부 경우에, 아래 첨자 p 는 1이다. 이들 예 중 임의의 경우에, 아래 첨자 e 는 1, 2, 3, 또는 4이다. 일부 예에서, 아래 첨자 e 는 1이다. 일부 예에서, 아래 첨자 e 는 2이다. 일부 예에서, 아래 첨자 e 는 3이다. 일부 예에서, 아래 첨자 e 는 4이다. 일부 예에서, 아래 첨자 e 는 5이다. 일부 예에서, 아래 첨자 e 는 6이다. 특정 실시양태에서, 상기 AA 2 는 발린-시트룰린이다. 일부 실시양태에서, 상기 AA 2 는 시트룰린-발린이다. 일부 실시양태에서, 상기 AA 2 는 발린-알라닌이다. 일부 실시양태에서, 상기 AA 2 는 알라닌-발린이다. 일부 실시양태에서, 상기 AA 2 는 발린-글리신이다. 일부 실시양태에서, 상기 AA 2 는 글리신-발린이다. 일부 실시양태에서, 상기 AA 1 -AA 2 는 글루타민-발린-시트룰린이다. 특정 실시양태에서, 상기 리신 은 L-리신이다. 특정 실시양태에서, 상기 리신은D-리신이다.
특정 실시양태에서, RG' 는, 독립적으로 각 경우에, 클릭 화학 잔기이다. 일부 경우에, RG' 는, 독립적으로 각 경우에, , , , , , , , , , 및 로 이루어진 군으로부터 선택되고, 여기서 는 RG' 가 화학식에서 인접기에 결합되는 원자를 나타낸다.
하나의 경우에, RG'는 이다. 다른 경우에, RG'는 이다. 일부 경우에, RG'는 이다. 일부 경우에, RG'는 이다. 일부 경우에, RG'는 이다. 일부 경우에, RG'는 이다. 일부 경우에, RG'는 이다. 일부 경우에, RG'는 이다. 일부 경우에, RG'는 이다. 일부 경우에, RG'는 이다.
특정 경우에, RG'및 RG 2 는 독립적으로, 각 경우에, 표 R'에 나타낸 바와 같다.
표 R'
본 원에 기재된 바와 같은 표 R'로 부터의 행 및 스페이서 SP2의 임의의 조합은 본 원에 기재된 화학식 (VI)의 화합물에 존재할 수 있다.
특정 경우에, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물에 대해, HG 는
여기서
일부 경우에, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc) 또는 화학식 (Xd)의 화합물에 대해, HG 는 -(CH2)1-5SO3H,
-(CH2)n피-NH-(CH2)1-5SO3H, -(CH2)n피-C(O)NH-(CH2)1-5SO3H,
-(CH2CH2O)m피-C(O)NH-(CH2)1-5SO3H, -(CH2)n피-N((CH2)1-5C(O)NH(CH2)1-5SO3H)2,
-(CH2)n피-C(O)N((CH2)1-5C(O)NH(CH2)1-5SO3H)2, 또는
-(CH2CH2O)m피-C(O)N((CH2)1-5C(O)NH(CH2)1-5SO3H)2이고, 여기서 아래 첨자 n피은 1, 2, 3, 4, 또는 5이고, 및 아래 첨자 m피은 1, 2, 3, 4, 또는 5이다. 한 실시양태에서, HG 는 -(CH2)1-5SO3H이다. 다른 실시양태에서, HG 는 -(CH2)n피-NH-(CH2)1-5SO3H이고, 여기서 아래 첨자 n피 는 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n피-C(O)NH-(CH2)1-5SO3H이고, 여기서 n피 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG는 -(CH2CH2O)m피-C(O)NH-(CH2)1-5SO3H이고, 여기서 아래 첨자 m피 는 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG는 -(CH2)n피-N((CH2)1-5C(O)NH(CH2)1-5SO3H)2이고, 여기서 아래 첨자 n피 는 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n피-C(O)N((CH2)1-5C(O)NH(CH2)1-5SO3H)2이고, 여기서 아래 첨자 n피 는 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2CH2O)m피-C(O)N((CH2)1-5C(O)NH(CH2)1-5SO3H)2이고, 여기서 아래 첨자 m피 은 1, 2, 3, 4, 또는 5이다.
일부 경우에, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물에 대해, HG 는 -(CH2)1-5PO3H,
-(CH2)n-NH-(CH2)1-5PO3H, -(CH2)n-C(O)NH-(CH2)1-5PO3H,
-(CH2CH2O)m-C(O)NH-(CH2)1-5PO3H, -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5PO3H)2,
-(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5PO3H)2, 또는
-(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5PO3H)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이고, 및 m 은 1, 2, 3, 4, 또는 5이다. 한 실시양태에서, HG 는 -(CH2)1-5PO3H이다. 다른 실시양태에서, HG 는 -(CH2)n-NH-(CH2)1-5PO3H이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-C(O)NH-(CH2)1-5PO3H이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는
-(CH2CH2O)m-C(O)NH-(CH2)1-5PO3H이고, 여기서 m 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5PO3H)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5PO3H)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5PO3H)2이고, 여기서 m 은 1, 2, 3, 4, 또는 5이다.
일부 경우에, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc) 또는 화학식 (Xd)의 화합물에 대해, HG 는 -(CH2)1-5N+(R M )3,
-(CH2)n-NH-(CH2)1-5N+(R M )3, -(CH2)n-C(O)NH-(CH2)1-5N+(R M )3,
-(CH2CH2O)m-C(O)NH-(CH2)1-5N+(R M )3, -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5N+(R M )3)2,
-(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+(R M )3)2, 또는
-(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+(R M )3)2이고, 여기서 n 는 1, 2, 3, 4, 또는 5이고, m 는 1, 2, 3, 4, 또는 5이고, 및 R M 은, 각각의 경우에, 독립적으로, H이고, C1-6알킬, C3-7시클로알킬 또는 C1-6알킬-C3-7시클로알킬, 또는, 2개의 R M 은 이들이 부착되어 있는 질소 원자와 함께 3내지 7원 헤테로시클로 알킬고리를 형성한다. 한 실시양태에서, HG 는 -(CH2)1-5N+(R M )3이다. 다른 실시양태에서, HG 는 -(CH2)n-NH-(CH2)1-5N+(R M )3이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-C(O)NH-(CH2)1-5N+(R M )3이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는
-(CH2CH2O)m-C(O)NH-(CH2)1-5N+(R M )3이고, 여기서 m 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5N+(R M )3)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+(R M )3)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+(R M )3)2이고, 여기서 m 은 1, 2, 3, 4, 또는 5이다.
일부 경우에, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 임의의 화합물에 대해, HG 는 -(CH2)1-5N+Me3,
-(CH2)n-NH-(CH2)1-5N+Me3, -(CH2)n-C(O)NH-(CH2)1-5N+Me3,
-(CH2CH2O)m-C(O)NH-(CH2)1-5N+Me3, -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5N+Me3)2,
-(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+Me3)2, 또는
-(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+Me3)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이고, 및 m 은 1, 2, 3, 4, 또는 5이다. 한 실시양태에서, HG 는 -(CH2)1-5N+Me3이다. 다른 실시양태에서, HG 는 -(CH2)n-NH-(CH2)1-5N+Me3이고, 여기서 n 는 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-C(O)NH-(CH2)1-5N+Me3이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는
-(CH2CH2O)m-C(O)NH-(CH2)1-5N+Me3이고, 여기서 m 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-N((CH2)1-5C(O)NH(CH2)1-5N+Me3)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2)n-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+Me3)2이고, 여기서 n 은 1, 2, 3, 4, 또는 5이다. 다른 실시양태에서, HG 는 -(CH2CH2O)m-C(O)N((CH2)1-5C(O)NH(CH2)1-5N+Me3)2이고, 여기서 m 은 1, 2, 3, 4, 또는 5이다.
특정 경우에, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물에 대해, HG 는 이고, 또는 이의 염이다. 특정 경우에, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물에 대해, HG 는 이고, 또는 이의 염이다. 하나의 경우에 HG 는 이고, 또는 이의 염이다. 다른 경우에, HG 는 이고, 또는 이의 염이다.
일부 예에서, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물에 대해, HG는 아민, 또는 이의 염, 예를 들어 4가아민, 예를 들어,이고, 여기서 는 HG가 화학식에서 인접기에 결합되는 원자를 나타내는 4가아민이다.
다른 예에서, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물에 대해, HG 는 포스폰산, 또는 이의 염, 예를 들어, 이고, 여기서 는 HG가 화학식에서 인접기에 결합되는 원자를 나타낸다. 다른 예에서, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물에 대해, HG 는 포스폰산, 또는 이의 염, 예를 들어,이고, 여기서 는HG가 화학식에서 인접기에 결합되는 원자를 나타낸다.
또다른 예에서, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물에 대해, HG는 당 잔기, 예를 들어, (갈락토오스), (글루카민), 또는 (말토오스)이고, 여기서 는 HG가 화학식에서 인접기에 결합되는 원자를 나타낸다.
특정 경우에, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물에 대해, SP 1 및 SP 2 는 독립적으로, 각 경우에, 존재하지 않거나, 또는 C1-6 알킬렌, -NH-, -C(O)-, (-CH2-CH2-O)e, -NH-CH2-CH2-(-O-CH2-CH2)e-C(O)-, -C(O)-(CH2)u-C(O)-, -C(O)-NH-(CH2)v-, 폴리글리신(예를 들어, ((글리신)4-세린) f 이고, 여기서 아래 첨자 f 는 1 내지 6의 정수이다), 및 이들의 조합이고, 여기서 아래 첨자 e 는 0 내지 4의 정수이며, 아래 첨자 u 는1 내지 8의 정수, 및 아래 첨자 v 는 1 내지 8의 정수이다. 특정 경우에, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물에 대해, SP 1 및 SP 2 는독립적으로, 각 경우에, 표S에 나타낸 바와 같다. 특정 실시양태에서, ((글리신)4-세린) f 은 (글리신)4-세린.
일부 경우에, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 임의의 화합물에 대해,
또는 이의 입체 이성질체 형태, 또는 이의 위치 이성질체, 또는 이의 위치 이성질체의 혼합물이고 , 여기서
일부 경우에, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물에 대해,
또는 이의 입체 이성질체 형태, 또는 이의 위치 이성질체, 또는 이의 위치 이성질체의 혼합물이고 , 여기서
일부 경우에, 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물에 대해, LL 은 화학식 (LL1)에 따른다:
여기서 R AA1 , R AA2 , 및 R AA3 는 각각, 독립적으로, 아미노산 측쇄이며, 이들 중 적어도 하나는 -(RG 2 ) q -SP 2 -HG에 직접 또는 간접적으로 결합된다. 일부 경우에, R AA1 은 HG에 직접 또는 간접적으로 결합된 리신, 글루타민, 글루탐산 또는 아스파르트산 측쇄이고, 및 R AA2 및 R AA3 는 각각 발린 및 알라닌 또는 발린 및 시트룰린 측쇄이다.
일부 경우에, 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물에 대해, AA 2 는
여기서 R AA2 , R AA3 , R AA4 , 및 R AA5 는 각각, 독립적으로, 아미노산 측쇄이며, 이들 중 적어도 하나는 -(RG 2 ) q -SP 2 -HG에 직접 또는 간접적으로 연결되고, 여기서 는 AA 2 가 화학식의 인접기에 결합되는 원자를 나타낸다. 일부 예에서, R AA2 , R AA3 , R AA4 , 및 R AA5 는 독립적으로 각 경우에, 알라닌, 발린, 류신, 이소류신, 메티오닌, 트립토판, 페닐알라닌, 프롤린, 세린, 트레오닌, 시스테인, 티로신, 아스파라긴, 글루타민, 아스파르트산, 글루탐산, 리신, 아르기닌, 히스티딘, 또는 시트룰린의 측쇄로부터 선택된 아미노산 측쇄이며, 이들의 유도체 또는 이들의 조합이다.
일부 경우에, 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물에 대해, AA 2 는
일부 경우에, 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 임의의 화합물에 대해, 아래 첨자 e 는 4이다. 일부 경우에, 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물에 대해, 아래 첨자 e 는 5이다.
일부 경우에, 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 임의의 화합물에 대해, PA는 돌라스타틴, 아우린스타틴, 메이탄시노이드, 식물알칼로이드, 탁산, 빈카알칼로이드, 스테로이드 및 간X수용체 (LXR)조절제로 이루어진 군으로부터 선택된 그룹의 잔기이다. 어떤 경우에는, PA 는 둘라스타틴이다. 어떤 경우에는, PA 는 돌라스타틴이다. 어떤 경우에는, PA 가 아우린스타틴이다. 어떤 경우에는, PA 가 메이탄신노이드이다. 어떤 경우에는, PA가 도플랜 알칼로이드(doplant alkaloid)이다. 어떤 경우에는, PA 는 탁산(taxane)이다. 어떤 경우에는, PA 가 빈카 알칼로이드(vinca alkaloid)이다. 어떤 경우에는, PA는 스테로이드이다. 어떤 경우에는, PA 가 LXR조절제 이다. 어떤 경우에는, LXR 조절제는 LXR 작용제이다. 어떤 경우에는, LXR 조절제는 LXR 길항제이다.
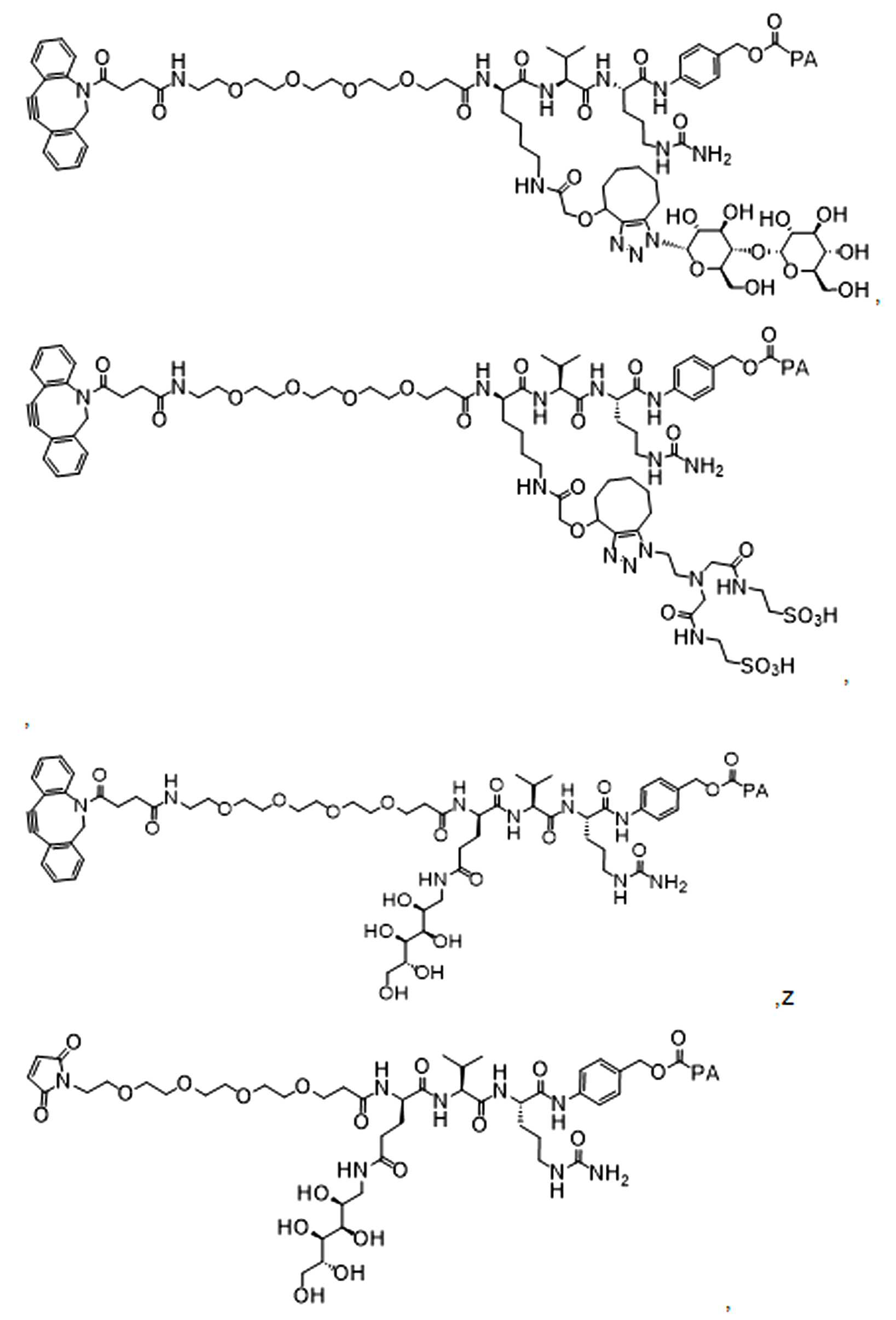
특정 경우에, 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 임의의 화합물은, 다음으로 구성된 그룹에서 선택된다:
또는 이의 입체 이성질체 형태, 또는 이의 위치 이성질체, 또는 이의 위치 이성질체의 혼합물이고, 여기서 PA 는 페이로드의 잔기이다.
일부 경우에, 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 임의의 화합물은, 다음으로 구성된 그룹에서 선택된다:
또는 이의 입체 이성질체 형태, 또는 이의 위치 이성질체, 또는 이의 위치 이성질체의 혼합물이다.
결합제 (BA)를 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)에 따른 화합물과 접속시키는 단계를 포함하고, 결합제와 화합물 사이의 결합을 형성하기에 적합한 조건하에서 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)에 따른 화합물을 사용하는 제조방법 또한 제공된다.
링커에 결합된 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc) 또는 화학식 (Xd)중 임의의 화합물을 포함하는 링커-페이로드가 본 원에 제공된다.
페이로드 산소 또는 1차 또는 2차 질소에 결합된 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)중 임의의 화합물을 포함하는 링커-페이로드가 제공된다.
본 원에 추가로 항체에 결합된 상기 기재된 화합물 또는 링커-페이로드, 또는 이의 항원 결합 단편을 포함하는 항체-약물-접합제가 제공된다.
한 측면에서, 대상체에게 유효 치료량의 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물을 투여하는 단계를 포함하는, 대상체에서 증식성 질환, 대사성 질환, 염증 또는 신경 퇴행성 질환을 치료하는 방법, 또는 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc) 또는 화학식 (Vd)의 화합물을 포함하는 약학 조성물이 제공된다.
한 측면에서, 대상체에게 유효 처리량의 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)에 따른 화합물을 투여하는 단계를 포함하는 대상체에서의 질환, 장애 또는 상태의 치료 방법, 또는 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물을 포함하는 약학 조성물이 제공된다.
한 측면에서, 대상체에게 유효처리량의 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)에 따른 화합물을 투여하는 것을 포함하는, 대상체에서 증식성 질환의 치료방법, 또는 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물을 포함하는 약학 조성물이 제공된다.
한 측면에서, 대상체에게 유효 처리량의 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물을 투여하는 단계를 포함하는 대상체에게 대사 질환의 치료 방법, 또는 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물을 포함하는 약학 조성물이 제공된다.
한 측면에서, 대상체에게 유효 처리량의 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)에 따른 화합물을 투여하는 단계를 포함하는 대상체에서의 염증 치료 방법, 또는 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc) 또는 화학식 (Vd)의 화합물을 포함하는 약학 조성물이 제공된다.
한 측면에서, 대상체에게 유효 처리량의 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물을 투여하는 단계를 포함하는 대상체에서 신경 퇴행성질환의 치료 방법, 또는 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물을 포함하는 약학 조성물이 제공된다.
일부 예에서, 본 원에 상기 언급된 화합물 중 임의의것을 포함하여 본 원에 기재된 화합물 또는 그의 제약상 허용되는 염 및 제약상 허용되는 부형제를 포함하는 약학 조성물이 제공된다.
당업자는 아미노산 잔기가 아키랄(achiral) 또는 키랄(chiral)일 수 있음을 인식할 것이며, 예를 들어, L-아미노산 또는 D-아미노산이다. 아미노산은 일반적으로 아미노산 측쇄를 포함한다. 측쇄는 당업자에게 공지된 임의의 아미노산의 측쇄일 수 있다. 특정 실시양태에서, 측쇄는히스티딘, 알라닌, 이소류신, 아르기닌, 류신, 아스파라긴, 리신, 아스파르트산, 메티오닌, 시스테인, 페닐알라닌, 글루탐산, 트레오닌, 글루타민, 트립토판, 발린, 오르니틴, 셀레노시스테인, 세린, 글리신, 호모글리신(예를 들어, β-호모글리신) 또는 티로신이다. 당업자는 펩티드가 아키랄 또는 키랄일 수 있음을 인식할 것이며, 예를 들어, 라세미DL-아미노산 또는 비라세미D 또는 L-아미노산 및 이들의 부분 입체 이성질체 혼합물을 포함한다. 펩티드의 측쇄는 상기 아미노산과 관련하여 기술된 바와 같다.
당업자는 N-알킬아미노산 잔기가 아미노산의 말단 아미노기 또는 펩티드의 말단 아미노기에 본 원에 정의된 바와 같은 알킬 치환기를 포함한다는 것을 인식할 것이다.
일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 정수1 내지 30의 정수이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 1이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 2이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 3이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 4이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 5이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 6이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 7이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 8이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 9이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 10이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 11이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 12이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 13이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 14이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 15이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 16이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 17이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 18이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 19이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 20이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 21이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 22이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 23이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 24이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 25이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 26이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 27이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 28이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 29이다. 일부 예에서, 전술한 것 중 임의의 것을 포함하여, 아래 첨자 n 은 30이다.
결합제(BA)
본 개시 내용에 제공된 임의의 접합제에 적합한 결합제는 항체, 림포카인, 호르몬, 성장인자, 바이러스 수용체, 인터루킨, 또는 임의의 다른 세포 결합 또는 펩티드 결합 분자 또는 물질을 포함하지만, 이에 제한되지는 않는다. 적합한 결합제는 또한 폴리펩티드를 포함한다.
상기 중 임의의 것을 포함하는 일부 예에서, 결합제(BA)는 임의의 폴리펩티드로부터 선택된다. 예시적인 폴리펩티드는 천연 폴리펩티드 및 비천연 폴리펩티드를 포함하지만 이에 제한되지 않는다. 예시적인 폴리펩티드는 유전자 변형 유기체로부터 생성된 것을 포함하나, 이에 제한되지는 않는다.
상기 중 임의의 것을 포함하는 일부 예에서, BA는 수용체, 사이토 카인, 단백질, 효소, 결합제, 우유펩티드, 리보솜 펩티드, 비리보솜 펩티드, 펩톤 및 펩티드 단편으로부터 선택된다. 상기 중 임의의 것을 포함하는 일부 예에서, BA는 항균성 펩타이드, 타키키닌펩타이드, 혈관활성장펩타이드, 췌장폴리펩타이드 관련 펩타이드, 오피오이드 펩타이드 및 칼시토닌 펩타이드로부터 선택된다. 상기 중 임의의 것을 포함하는 일부 예에서, BA는 B형 나틂 이뇨 펩티드(BNP), 락토트리펩티드, 뉴로펩티드, 리포펩티드, 단백질 또는 호르몬으로 선택된다.
상기 중 임의의 것을 포함하는 일부 예에서, BA는 함께 결합된 2개 이상의 아미노산을 포함하는 짧은 아미노산 사슬로부터 선택된다. 상기 중 임의의 것을 포함하는 일부 예에서, BA는 각각 함께 결합된 2개, 3개 또는 4개의 아미노산을 갖는 디펩티드(Val-Cit), 트리펩티드 및 테트라펩티드(예를 들어, Val-Gly-Ser-Ala)로부터 선택된다.
상기 중 임의의 것을 포함하는 일부 예에서, BA는 디펩티드, 트리펩티드, 테트라펩티드, 펩타펩티드, 헥사펩티드, 헵타펩티드, 옥타펩티드, 비펩티드, 데카펩티드, 운데카펩티드 및 이코사펩티드로부터 선택된다.
상기 중 임의의 것을 포함하는 일부 예에서, BA는 임의의 단백질로부터 선택된다. 일부 예에서, 단백질은 천연 아미노산만을 포함한다. 일부 예에서, 단백질은 비 천연 아미노산을 추가로 포함한다. 일부 표식에서, 결합제는 이의 항원 단편의 항체이다. 항체는 당업자에게 공지된 임의의 형태일 수 있다. 본 원에 사용된 용어 "항체"는 특정 항원에 특이적으로 결합하거나 상호작용하는 하나 이상의 상보성 결정 영역(CDR)을 포함하는 임의의 항원-결합 분자 또는 분자 복합체를 의미한다. 용어 "항체"는 이황화 결합에 의해 상호연결된 4개의 폴리펩티드 사슬, 2개의 중쇄(H) 및 2개의 경쇄(L) 및 이의 다량체(예를 들어, lgM)를 포함하는 면역 글로불린 분자를 포함한다. 각각의 중쇄는 중쇄 가변 영역(본 명세서에서 HCVR 또는 VH로 약칭됨) 및 중쇄 불변 영역을 포함한다.
중쇄 불변 영역은 3개의 도메인 CH1, CH2 및 CH3을 포함한다. 각각의 경쇄는 경쇄 가변 영역(본 명세서에서 LCVR 또는 VL 로 약칭 됨) 및 경쇄 불변 영역을 포함한다. 경쇄 불변 영역은 하나의 도메인((CL1)을 포함한다. VH및 VL영역은 프레임 워크 영역(FR)으로 불리는 보다 보존된 영역과 산재된 상보성 결정 영역(CDRs)으로 지칭되는 초 가변성 영역으로 추가로 세분될 수 있다. 각각의 VH 및 VL 은 3개의 CDR 및 4개의 FR로 구성되며, FR1, CDR1, FR2, CDR2, FR3, CDR3, FR4의 순서로 아미노-말단에서 카르복시-말단으로 배열된다. 본 발명의 다른 실시양태에서, 본 원의 화합물(또는 이의 항원 결합 부분)에 적합한 안티보이드의 FR은 인간 생식계열 서열과 동일하거나 자연적으로 또는 인공적으로 변형될 수 있다.
아미노산 컨센서스 서열은 둘 이상의 CDR의 단계별 분석에 기초하여 정의될 수 있다. 본 원에 사용된 용어 "항체"는 또한 완전한 항체 분자의 항원-결합 단편을 포함한다. 본 원에 사용된 항체의 "항원-결합 부분", 항체의 "항원-결합 단편"등은 자연적으로 발생하거나, 효소적으로 얻을 수 있는, 합성 또는 항원에 특이적으로 결합하여 복합체를 형성하는 유전자 조작된 폴리펩티드 또는 당단백질에 특이적으로 결합하는 것을 포함한다.
항체의 항원-결합 단편은 예를 들어 단백질 가변성 소화법 또는 항체 가변성 및 선택적으로 불변 도메인을 코딩하는 DNA의 조작 및 발현을 포함하는 재조합 유전공학 기술과 같은 임의의 적합한 표준 기술을 사용하는 완전한 항체 분자로부터 유래될 수 있다.
이러한 DNA는 공지된 및/또는 예를 들어 상업적 공급원, DNA라이브러리(예를 들어, 파지-항체 라이브러리 포함)로부터 입수하거나 합성 될 수 있다.
DNA는 화학적으로 또는 분자 생물학 기술을 사용하여, 예를 들어, 하나 이상의 가변 및/또는 불변 도메인을 적합한 구성으로 배열하거나, 코돈을 도입하거나, 시스테인 잔기를 생성하거나, 아미노산을 변형, 등 첨가 도는 결실시키기 위해 서열 분석되고 조작될 수 있다.
항원-결합 단편의 비 제한적 예는 다음을 포함한다: (i) Fab 단편; (ii) F(ab')2 단편; (iii) Fd 단편; (iv) Fv 단편; (v) 단일-사슬 Fv (scFv) 분자; (vi) dAb 단편; 및 (vii) 항체(예를 들어, CDR3 펩티드와 같은 단리된 상보성 결정 영역(CDR))의 초 가변 영역, 또는 제한된 FR3-CDR3-FR4펩티드를 모방하는 아미노산 잔기로 구성된 최소 인식단위이다.
도메인-특이적 항체, 단일 도메인 항체, 도메인-삭제된 항체, 키메라 항체, CDR-그래프팅된 항체, 디아바디, 트리아바디, 테트라바디, 미니바디, 나노바디(예를 들어, 1가 나노 바디, 2가 나노바디 등), 소형 모듈 형 면역 약제 (SMIPs) 및 상어와 같은 기타 조작된 분자 가변 IgNAR 도메인은 또한 본 원에 사용된 "항원-결합 단편"이라는 표현내에 포함된다.
항체의 항원-결합 단편은 전형적으로 하나 이상의 가변 도메인을 포함할 것이다. 가변 도메인은 임의의 크기 또는 아미노산 조성일 수 있고 일반적으로 하나 이상의 프레임 워크 서열에 인정하거나 하나 이상의 프레임 워크 서열을 갖는 하나 이상의 CDR을 포함할 것이다. VL도메인과 관련된 VH도메인을 갖는 항원-결합 단편에서, VH 및 VL 도메인은 임의의 적합한 배열로 서로에 대해 위치될 수 있다. 예를 들어, 가변 영역은 이량체일 수 있고, VH-VH, VH-VL, VL-VL이량체를 함유할 수 있다. 대안적으로, 항체의 항원-결합 단편은 단량체 VH 또는 VL도메인을 함유할 수 있다.
특정 실시양태에서, 항체의 항원-결합 단편은 단량체 VH 또는 VL 도메인을 함유할 수 있다. 대안적으로, 항체의 항원-결합 단편은 단량체 VH 또는 VL도메인을 함유할 수 있다. 특정 실시양태에서, 항체의 항원-결합 단편은 하나 이상의 불변도메인에 공유 결합된 하나 이상의 가변 도메인을 함유할 수 있다. 본 발명의 항체의 항원-결합단편 내에서 발견될 수 있는 가변 및 불변 도메인의 비제한적, 예시적 구성은 다음을 포함한다: (i) VH-CH1; (ii) VH-CH2; (iii) VH-CH3; (iv) VH-CH1-CH2; (v) VH-CH1-CH2-CH3; (vi) VH-CH2-CH3; (vii) VH-CL; (viii) VL-CH1; (ix) VL-CH2; (x) VL-CH3; (xi) VL-CH1-CH2; (xii) VL-CH1-CH2-CH3; (xiii) VL-CH2-CH3; 및 (xiv) VL-CL.
상기 열거된 예시적인 구성 중 임의의 것을 포함하는 가변 및 불변 도메인의 임의의 구성에서, 가변 및 불변 도메인은 서로 직접 연결되거나 전체 또는 부분 힌지 또는 링커 영역에 의해 연결될 수 있다.
힌지 영역은 단일 폴리펩티드에서 인접한 가변 및/또는 불변 도메인 사이에 가요성 또는 반-가요성 연결을 야기하는 적어도 2개(예를 들어, 5, 10, 15, 20, 40, 60 또는 그 이상)이상의 아미노산으로 구성될 수 있다.
완전한 항체 분자와 마찬가지로, 항원-결합 단편은 단일특이적 또는 다중특이적(예를 들어, 이중 특이적)일 수 있다.
항체의 다중 특이적 항원-결합 단편은 전형적으로 2개 이상의 상이한 가변 도메인을 포함할 것이며, 여기서 각각의 가변 도메인은 별개의 항원 또는 동일한 항원상의 상이한 에피토프에 특이적으로 결합할 수 있다.
본 원에 개시된 예시적인 이중특이적 항체 형식을 포함하는 임의의 다중 특이적 항체 형식은 관련 기술분야에서 이용 가능한 통상적인 기술을 사용하여 본 발명의 항체의 항원-결합 단편의 맥락에서 사용하기에 적합할 수 있다. 본 발명의 특정 실시양태에서, 본 발명의 항체는 인간 항체이다. 본 원에 사용된 용어 "인간 항체"는 인간 생식 계열 면역 글로불린 서열로부터 유래된 가변 및 불변 영역을 갖는 항체를 포함하는 것으로 의도된다. 본 발명의 인간항체는 인간 생식 계열 면역 글로불린 서열(예를 들어, 시험관내 무작위 또는 부위-특이적 돌연변이 유발 또는 생체 내 체세포 돌연변이에 의해 도입된 돌연변이), 예를 들어 CDR및 특히 CDR3에 의해 코딩되지 않은 아미노산 잔기를 포함할 수 있다.
그러나, 본 원에 사용된 용어 "인간 항체"는 다른 포유 동물종, 예컨대 마우스의 생식선으로부터 유래된 CDR서열이 인간 프레임 워크 서열에 이식된 항체를 포함하는 거으로 의도되지 않는다. 용어 "인간 항체"는 자연발생의 비변형 생물체에서 일반적으로 변형 또는 인간의 개입/조작없이 존재하는 자연 발생 분자를 포함하지 않는다. 본 발명의 항체는 일부 실시양태에서 재조합 인간 항체일 수 있다. 본 원에 사용된 용어 "재조합 인간 항체"는 숙주 세포로 형질 감염된 재조합 발현 백터를 사용하여 발현된 항체, 재조합 조합 인간 항체 라이브러리(아래에 더 설명)로부터 단리된 항체, 동물(예를 들어, 마우스)로부터 단리된 항체, 인간 면역 글로불린 유전자에 대해 유전자 인식된 동물로부터 단리된 항체(예를 들어, Taylor et al. (1992) Nucl. Acids Res. 20:6287-6295) 또는 인간 면역 글로불린 유전자 서열을 다른 DNA서열에 접합시키는 것을 포함하는 임의의 다른 수단에 의해 제조, 발현, 생성 또는 단리된 항체와 같은 재조합 수단에 의해 제조, 발현, 생성 또는 단리된 모든 인간 항체를 포함하는 것으로 의도된다.
이러한 재조합 인간 항체는 인간 생식 계열 면역 글로불린 서열로부터 유래된 가변 및 불변 영역을 갖는다. 그러나, 특정 실시양태에서, 이러한 재조합 인간 항체는 시험관내 돌연변이 유발(또는, 인간 lg 서열에 대해 유전자 이식된 동물이 사용되는 경우, 생체내 체세포 돌연변이 유발)에 제공되고, 따라서 재조합 항체의 VH 및 VL 영역의 아미노산 서열은, 인간 생식계열 VH 및 VL서열로부터 유래되고 이와 관련되어 있지만, 생체 내에서 인간 항체 생식계 레퍼토리 내에 자연적으로 존재하지 않을 수 있는 서열일 수 있다.
인간 항체는 힌지 이종성과 관련된 2가지 형태로 존재할 수 있다. 한 형태에서, 면역 글로불린 분자는 이량체가 쇄간 중쇄 이황화 결합에 의해 함께 유지되는 대략 150-160kDa의 안정한 4쇄 작제물을 포함한다. 두번째 형태에서, 이량체는 쇄간 이황화 결합을 통해 연결되지 않으며, 약 75-80kDa의 분자가 공유 결합된 경쇄 및 중쇄(반-항체)로 구성되어 형성된다.
이들 형태는 친화성 정제 후에도 분리하기가 매우어렵다. 다양한 온전한 lgG이소 타입에서 제2형태의 출현빈도는 항체의 힌지 영역 이소 타입과 관련된 구조적 차이에 기인하지만 이에 제한되지 않는다. 인간 lgG4 힌지의 힌지 영역에서 단일 아미노산 치환은 제2 형태(Angal et al. (1993) Molecular Immunology 30:105)의 외관을 인간 lgG1 힌지를 사용하여 전형적으로 관찰되는 수준으로 상당히 감소시킬 수 있다. 본 발명은 힌지, CH2 또는 CH3 영역에 하나 이상의 돌연변이를 갖는 항체를 포함하는데, 이를 예를 들어 생산에서 원하는 항체 형태의 수율을 개선시키는 것이 바람직 할 수 있다. 본 발명의 항체는 단리된 항체일 수 있다. 본 원에 사용된 "단리된 항체"는 그의 자연 환경의 하나 이상의 성분으로부터 확인 및 분리 및/또는 회수된 항체를 의미한다. 예를 들어, 유기체의 하나 이상의 성분, 또는 항체가 자연적으로 존재하거나 자연적으로 생성되는 조직 또는 세포로부터 분리 또는 제거된 항체는 본 발명의 목적 상 "단리된 항체"이다. 단리된 항체는 또한 재조합 세포 내의 인 시츄 항체를 포함한다. 단리된 항체는 적어도 하나의 정제 또는 단리 단계를 거친 항체이다. 특정 실시양태에 따르면, 단리된 항체에는 다른 세포 물질 및/또는 화학물질이 실질적으로 없을 수 있다.
본 원에 사용된 항체는 항체가 유래된 상응하는 생식계 서열과 비교하여 중쇄 및 경쇄 가변 도메인의 프레임 워크 및/또는 CDR영역에서 하나 이상의 아미노산 치환, 삽입 및/또는 결실을 포함할 수 있다. 이러한 돌연변이는 본 원에 개시된 아미노산 서열을 예를 들어 공개 항체 서열 데이터 베이스로부터 입수가능한 생식선 서열과 비교함으로써 용이하게 확인할 수 있다. 본 발명은 본원에 개시된 임의의 아미노산 서열로부터 유래된 항체 및 그의 항원-결합 단편을 포함하며, 여기서 하나 이상의 프레임 워크 및/또는 CDR 영역 내의 하나 이상의 아미노산은 항체가 유래된 생식계열 서열의 상응하는 잔기, 또는 다른 인간 생식 계열 서열의 상응하는 잔기(들) 또는 상응하는 생식선 잔기(들)의 보존적 아미노산 치환(이러한 서열변화는 본 원에서 총괄적으로 "생식선 돌연변이"로 지칭됨)에 대응되도록 변이된다.
본 원에 개시된 중쇄 및 경쇄 가변 영역 서열로 시작하여 당업자는 하나 이상의 개별 생식선 돌연변이 또는 이들의 조합을 포함하는 수많은 항체 및 항원-결합 단편을 쉽게 생성할 수 있다. 특정 실시양태에서, VH 및/또는 VL도메인 내의 모든 골격 및/또는 CDR잔기는 항체가 유래된 원래 생식계열 서열에서 발견된 잔기로 다시 돌연변이된다. 다른 실시양태에서, 특정 잔기만이 원래 생식선 서열로 다시 돌연변이되고, 예를 들어, FR1의 처음 8개 아미노산 또는 FR4의 마지막 8개 아미노산 내에서 발견된 돌연변이된 잔기만, 또는 CDR1, CDR2 또는 CDR3 내에서 발견된 돌연변이된 잔기만. 다른 실시양태에서, 하나 이상의 프레임워크 및/또는 CDR잔기(들)는 상이한 생식 계열 서열의 상응하는 잔기(들)로 돌연변이 된다. (예를 들어, 항체가 원래 유래된 생식 계열 서열과 상이한 생식 계열 서열). 또한, 본 발명의 항체는 프레임 워크 및/또는 CDR 영역 내에 2개 이상의 생식선 서열 돌연변이의 임의의 조합을 포함한다, 예를 들어, 특정 개별 잔기는 특정 생식선 서열의 상응하는 잔기로 돌연변이되는 반면, 원래 생식선 서열과 상이한 특정 다른 잔기는 유지되거나 또는 상이한 생식선 서열의 상응하는 잔기로 돌연변이된다.
일단 수득되면, 하나 이상의 생식 계열 돌연변이를 함유하는 항체 및 항원-결합 단편은 개선된 결합 특이성, 증가된 결합 친화성, 개선 또는 강화된 길항적 또는 작용적 생물학적 특성(경우에 따라), 면역 원성 감소등과 같은 하나 이상의 원하는 특성에 대해 용이하게 시험 될 수 있다.
이러한 일반적인 방식으로 수득된 항체 및 항원-결합단편은 본 발명에 포함된다. 본 원의 화합물에 유용한 항체는 또한 하나 이상의 보존적 치환을 갖는 본 원에 개시된 HCVR, LCVR 및/또는 CDR 아미노산 서열 중 어느 하나의 변이체를 포함하는 항체를 포함한다.
용어 "에피토프(epitope)"는 파라토프(paratope)로 알려진 항체 분자의 가변 영역에서 특정 항원 결합 부위와 상호 작용하는 항원 결정기를 의미한다. 단일 항원은 하나 이상의 에피토프를 가질 수 있다. 따라서, 상이한 항체는 항원상의 상이한 영역에 결합할 수 있고 상이한 생물학적 효과를 가질 수 있다. 에피토프는 형태적이거나 선형일 수 있다. 구조적 에피토프는 선형 폴리펩티드 사슬의 상이한 분절로부터 공간적으로 병치된 아미노산에 의해 생성된다. 선형 에피토프는 폴리펩티드 사슬에서 인접한 아미노산 잔기에 의해 생성된 것이다. 특정 상황에서, 에피토프는 항원상의 당류, 포스포릴기 또는 설포닐기의 잔기를 포함할 수 있다.
특정 실시양태에서, 항체는 경쇄를 포함한다. 특정 실시양태에서, 경쇄는 카파(kappa) 경쇄이다. 특정 실시양태에서, 상기 경쇄는 람다(lambda) 경쇄이다. 특정 실시양태에서, 상기 항체는 중쇄를 포함한다. 일부 측면에서, 상기 중쇄는 IgA이다. 일부 측면에서, 상기 중쇄는 IgD이다. 일부 측면에서, 상기 중쇄는IgE이다. 일부 측면에서, 상기 중쇄는 IgG이다. 일부 측면에서, 상기 중쇄는IgM이다. 일부 측면에서, 상기 중쇄는IgG1이다. 일부 측면에서, 상기 중쇄는 IgG2이다. 일부 측면에서, 상기 중쇄는 IgG3이다. 일부 측면에서, 상기 중쇄는 IgG4이다. 일부 측면에서, 상기 중쇄는 IgA1이다. 일부 측면에서, 상기 중쇄는IgA2이다.
일부 실시양태에서, 상기 항체는 항체 단편이다. 일부 측면에서, 상기 항체 단편은 Fv단편이다. 일부 측면에서, 상기 항체 단편은 Fab단편이다. 일부 측면에서, 상기 항체 단편은 F(ab')2 단편이다. 일부 측면에서, 상기 항체단편은Fab' 단편이다. 일부 측면에서, 상기 항체 단편은scFv (sFv)단편이다. 일부 측면에서, 상기 항체 단편은 scFv-Fc 단편이다.
일부 실시양태에서, 항체는 모노클로날 항체이다. 일부 싱시 양태에서, 항체는 폴리클로날 항체이다.
일부 실시양태에서, 항체는 키메라 항체이다. 일부 실시양태에서, 항체는 인간화 항체이다. 일부 실시양태에서, 항체는 인간 항체이다.
항체는 당업자에게 적합한 것으로 간주되는 임의의 항원에 대한 결합 특이성을 가질 수 있다. 특정 실시양태에서, 항원은 막 관통분자(예를 들어, 수용체) 또는 성장인자 이다.
예시적인 항원은 레니과 같은 분자; 인간성장호르몬을 포함하는 성장호르몬; 성장호르몬 방출인자; 부갑상선 호르몬; 갑상선 자극 호르몬; 지단백질; 알파 1-항 트립신; 인슐린 A-사슬; 인슐린 B-사슬; 프로 인슐린; 여포 자극 호르몬; 칼시토닌; 황체 형성 호르몬; 글루카곤; 인자 vcm, 인자 IX, 조직인지(TF) 및 폰 빌레 브란트 인자와 같은 응고인자; 단백질C와 같은 항 응고 인자; 심방 나트륨 이뇨인자; 폐 계면 활성제; 플라스미노겐 활성제; 예컨대 우로키나제 또는 인간 소변 또는 조직형 플라스미노겐 활성제(t-PA);
봄베신; 트롬빈; 조혈 성장 인자; 종양 괴사 인자-알파 및 베타; 엔켈팔리나제; RANTES (통상적으로 T-세포가 발현되고 분비되는 활성화로 조절됨); 인간 대식세포 염증성 단백질 (MIP-I-알파); 인간혈청 알부민과 같은 혈청알부민; 뮬러-억제 물질; 릴렉신 A-사슬; 릴렉신 B-사슬; 프롤락신; 마우스 성선자극 호르몬 관련 펩티드; 베탈락타마제와 같은 미생물 단백질; DNase; 19E; CTLA-4와 같은 세포 독성 T-림프구 관련 항원(CTLA); 인히빈; 액티빈; 혈관내피성장인자(VEGF); 호르몬 또는 성장인자에 대한 수용체; 단백질 A 또는 D; 류마티스 인자; 골 유래 신경 영양 인자(BDNF), 신경 영양 인자-3, -4, -5, 또는 -6 (NT-3, NT4, NT-5, 또는 NT-6), 또는 NGF-β와 같은 신경 성장 인자; 혈소판 유래 성장인자 (PDGF); aFGF 및 bFGF와 같은 섬유아세포 성장인자; 섬유 모세포 성장인자 수용체 2 (FGFR2), 표피 성장인자 (EGF); TGF-β1, TGF-β2, TGF- β3, TGF-β4, 또는 TGF- β5를 포함하는 TGF-알파 및 TGF-베타,와 같은 형질 전환 성장인자 (TGF); 인슐린유사 성장인자-l 및 -II (IGF-l 및 IGF-II); des(I-3)-IGF-l (뇌 IGF-l), 인슐린 유사 성장 인자 결합 단백질, EpCAM, GD3, FLT3, PSMA, PSCA, MUCI, MUCI6, STEAP, CEA, TENB2, EphA 수용체, EphB 수용체, 염산 수용체, FOLRI, 메조 텔린, 크립토, 알파v베타6, 인테그린, VEGF, VEGFR, EGFR, 트렌스퍼린 수용체, IRTA1, IRTA2, IRTA3, IRTA4, IRTA5; CD2, CD3, CD4, CD5, CD6, CD8, CD11, CD14, CD19, CD20, CD21, CD22, CD25, CD26, CD28, CD30, CD33, CD36, CD37, CD38, CD40, CD44, CD52, CD55, CD56, CD59, CD70, CD79, CD80. CD81, CD103, CD105, CD134, CD137, CD138, CDI52, 또는 미국 공개번호. 2008/0171040 또는 미국 공개번호. 2008/0305044 에 개시된 하나 이상의 종양 관련 항원 또는 세포 표면 수용체에 결합하고 참조에 의해 전체가 통합된 항체와 같은 CD 단백질;
에이트리포이에틴; 골유도 인자; 면역 독소; 골 형성 단백질 (BMP); 인터페론-알파, -베타, 및 -감마와 같은 인터페론; 콜로니자극인자 (CSFs), 예를 들어, M-CSF, GM-CSF, 및 G-CSF; 인터루킨 (ILs), 예를 들어, IL-1 내지 IL-10; 슈퍼 옥사이드 디스뮤타제; T-세포 수용체; 표면 막단백질; 붕괴 촉진 인자; 예를 들어, HIV외피의 일부와 같은 바이러스항원; 수송 단백질; 귀환 수용체; 어드레스린; 조절 단백질; CDlla, CDllb, CDllc, CDI8, ICAM, VLA-4 및 VCAM와 같은 인테그린; AFP, ALK, B7H4, BAGE 단백질, β-카테닌(catenin), brc-abl, BRCA1, BORIS, CA9 (탄소 무수물 IX), 카스파제-8(caspase-8), CD20, CD40, CD123, CDK4, CEA, CLEC12A, c-kit, cMET, CTLA4, cyclin-B1, CYP1B1, EGFR, EGFRvIII, endoglin, Epcam, EphA2, ErbB2/Her2, ErbB3/Her3, ErbB4/Her4, ETV6-AML, Fra-1, FOLR1, GAGE 단백질 (e.g., GAGE-1, -2), GD2, GD3, GloboH, glypican-3, GM3, gp100, Her2, HLA/B-raf, HLA/EBNA1, HLA/k-ras, HLA/MAGE-A3, hTERT, IGF1R, LGR5, LMP2, MAGE 단백질 (예를 들어, MAGE-1, -2, -3, -4, -6, and -12), MART-1, 메조텔린(mesothelin), ML-IAP, Muc1, Muc16 (CA-125), MUM1, NA17, NGEP, NY-BR1, NY-BR62, NY-BR85, NY-ESO1, OX40, p15, p53, PAP, PAX3, PAX5, PCTA-1, PDGFR-α, PDGFR-, PDGF-A, PDGF-B, PDGF-C, PDGF-D, PLAC1, PRLR, PRAME, PSCA, PSGR, PSMA (FOLH1), RAGE 단백질, Ras, RGS5, Rho, SART-1, SART-3, Steap-1, Steap-2, STn, 서바이빈(surviving), TAG-72, TGF-β, TMPRSS2, Tn, TNFRSF17, TRP-1, TRP-2, 티로시나제(tyrosinase), 및 유로플라킨-3(uroplakin-3), 및 상기 열거된 폴리펩티드의 단편과 같은 종양 관련 항원, 일부 실시양태에서, 항원은 종양 유형에 특이적인 항원 또는 특정 유형의 종양에서 공유, 과발현 또는 변형된 항원을 포함하는 종양 항원이다.
예를 들면 다음과 같다: 폐암이 있는 알파-액티닌-4(alpha-actinin-4), 흑색종이 있는 ARTC1, 만성 골수성 백혈병이 있는BCR-ABL융합단백질, B-RAF, 흑색 종을 가지는CLPP 또는 Cdc27, 편평 세포 암종을 갖는CASP-8, 및 신장 세포 암종 및 하기 공유 종양-특이적 항원을 갖는hsp70-2 예를 들어: BAGE-1, GAGE, GnTV, KK-LC-1, MAGE-A2, NA88-A, TRP2-INT2 일부 실시양태에서, 항원은 PRLR 또는 HER2이다. 일부 실시양태에서, 항체는 anti-PRLR 또는 anti HER2 항체이다.
본 개시 내용의 이러한 측면의 맥락에서 사용될 수 있는 예시적인 아미노산 부착은 예를 들어 리신(예를 들어, US 5,208,020; US 2010/0129314; Hollander et al., Bioconjugate Chem., 2008, 19:358-361; WO 2005/089808; US 5,714,586; US 2013/0101546; and US 2012/0585592 참조), 시스테인(예를 들어,US 2007/0258987; WO 2013/055993; WO 2013/055990; WO 2013/053873; WO 2013/053872; WO 2011/130598; US 2013/0101546; and US 7,750,116 참조), 셀레노시스테인(예를 들어, WO 2008/122039; and Hofer et al., Proc. Natl. Acad. Sci., USA, 2008, 105:12451-12456 참조), 포르밀글리신(예를 들어, Carrico et al., Nat. Chem. Biol., 2007, 3:321-322; Agarwal et al., Proc. Natl. Acad. Sci., USA, 2013, 110:46-51, and Rabuka et al., Nat. Protocols, 2012, 10:1052-1067 참조), 비천연 아미노산(예를 들어, WO 2013/068874, and WO 2012/166559 참조), 및 산성 아미노산(예를 들어, WO 2012/05982 참조)이다. 링커는 또한 탄수화물(예를 들어, US 2008/0305497, WO 2014/065661, and Ryan et al., Food & Agriculture Immunol., 2001, 13:127-130참조)에 부착을 통해 항원-결합 단백질에 접합될 수 있다.
일부 예에서, 결합제는 항체 또는 항원 또는 항원 결합 분자이고, 항체는 리신 잔기를 통해 링커에 결합된다. 일부 실시양태에서, 항체 또는 항원 결합 분자는 시스테인 잔기를 통해 링커에 결합된다.
링커는 또한 트랜스 글루타미나제-기반 화학효소 접합을 통해 하나 이상의 글루타민 잔기에 접합 될 수 있다(예를 들어, Dennler et al., Bioconjugate Chem. 2014, 25, 569-578 참조). 예를 들어, 트랜스 글루타미나아제의 존재 하에, 항체의 하나 이상의 글루타민 잔기가 1차 아민 화합물에 커플링 될 수 있다. 1차 아민 화합물은 페이로드 또는 링커-페이로드를 포함하여, 이는 트랜스 글루타미나제-매개 커플링을 통해 항체 약물 접합제를 직접 제공한다. 1차 아민 화합물은 또한 항체 약물 접합제의 합성을 향한 추가의 화합물과 후속 반응할 수 있는 반응성 그룹으로 작용화된 링커 및 스페이서를 포함한다. 글루타민잔기를 포함하는 항체는 천연 공급원으로부터 단리되거나 하나 이상의 글루타민 잔기를 포함하도록 조작될 수 있다. 글루타민 잔기를 항체 폴리펩티드 사슬(글루타미닐-개질된 항체 또는 항원 결합분자)로 조작하는 기술은 당업자의 기술 범위내에 있다. 특정 실시양태에서, 항체는 당화된다.
특정 실시양태에서, 항체 또는 글루타미닐-개질된 항체 또는 항원 결합 분자는 하나 이상의 폴리 펩티드 사슬 사열에서 하나 이상의 글루타민 잔기를 포함한다. 항체 또는 항원 결합 단백질의 특정 잔기로 접합을 유도하기 위해 부위 특이적 접합 기술이 사용될 수도 있다(예를 들어, Schumacher et al. J Clin Immunol (2016) 36(Suppl 1): 100참조). 부위 특이적 접합 기술은 트랜스 글루타미나제를 통한 글루타민 접합을 포함하지만 이에 제한되지 않는다(예를 들어, Schibli, Angew Chemie Inter Ed. 2010, 49 ,9995참조). 특정 실시양태에서, 항체 또는 글루타미닐-개질된 항체 또는 항원 결합 분자는 각각 하나의 Gln295 잔기를 갖는 2개의 중쇄 폴리펩티드를 포함한다. 추가의 실시양태에서, 항체 또는 글루타미닐-개질된 항체 또는 항원 결합 분자는 중쇄 295이외의 부위 예를 들어, Gln55(Q55)에서 하나 이상의 글루타민 잔기를 포함한다. 본 원에 기재된 N297Q 돌연변이(들)를 갖는 이 섹션의 항체가 본 원에 포함된다. 간략하게, 일부 실시양태에서, 글루타민 잔기를 포함하는 항체는 효소 트랜스 글루타미나아제의 존재 하에 보다 상세히 후술되는 1차 아민 화합물로 처리된다. 예시적인 N297 돌연변이 체는 Asn297Gln(N297Q)돌연변이체이다. 예를 들어, 일부 실시양태에서, 이러한 항체는 서열을 제거 또는 비활성화 하거나 임의의 간섭 구조와는 다른 부위에 글루타민 잔기를 삽입하기 위해 부위 지향적 돌연변이 유발에 의해 제조될 수 있다. 이러한 항체는 또한 천연 또는 인공 공급원으로부터 단리될 수 있다. 삽입된 글루타민 잔기에서 아미드 기는 본 원에 기재된 클릭화학반응에 적합한 아지도기에 연결될 수 있다 유리하게는, 삽입된 글루타민잔기의 수를 제어할 수 있고, 결과적으로 항체 또는 글루타미닐-개질된 항체 또는 항원 결합 분자의 아지도 그룹의 수를 제어할 수 있어 항체-약물비(ADR)의 제어를 개선할 수 있다. 예를 들어, 실시예 29 및 표 5를 참조.
특정 예에서, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물에 대해, 본 원에 기술된 임의의 항체 약물 접합제 샘풀에서 약물 항체 비율 (DAR)는 약 2(예를 들어, n 은 2이다)이다. 이런한 경우에, 항체 또는 결합 분자는 각각 하나의 Gln295잔기를 갖는 2개의 중쇄 폴리펩티드를 포함하고, 각각의 Gln295잔기는 본 원에 기재된 클릭화학 반응에 적합한 아지도기에 연결되어 약 2의 DAR을 허용한다.
다른 특정 예에서, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc) 또는 화학식 (Vd)의 화합물에 대해, 본 원에 기술된 임의의 항체 약물 접합제 샘풀에서 약물 항체 비율은 약4 (즉, n 은 4이다)이다. 이러한 경우에, 항체 또는 항원 결합 분자는 각각 하나의 Gln295잔기를 갖는 2개의 중쇄 폴리펩티드를 포함하고, 각각의 Gln295잔기는 본 원에 기재된 클릭 화학 반응에 적합한 아지도기에 연결된다. 또한, 항체 또는 항원 결합 분자는 부위-지정 돌연변이 유발에 의해 접합되기 전에 추가로 변형되어 서열을 제거 또는 불능화 시키거나 임의의 간섭 구조와는 다른 부위에 글루타민 잔기를 삽입한다. 예를 들어, 각각의 중쇄에서 N297 돌연변이체, Asn297Gln (N297Q) 돌연변이체는 아지도 그룹에 연결된다. 따라서, 글루타미닐-개질된 항체 또는 항원 결합 분자는 본 원에 기재된 클릭 화학 반응에 적합한 4개의 아지도그룹을포함하여 약 4의 DAR을 허용한다. 도 19 참조.
다른 특정 예에서, 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc) 또는 화학식 (Vd)의 화합물에 대해, 본 원에 기술된 임의의 항체 약물 접합제 샘플에서의 약물 항체 비율은 약 5 또는 약 6 (예를 들어, n 은 5 또는 6이다)이다. 이러한 경우에, 항체 또는 항원 결합 분자는 각각 하나의 Gln295잔기를 갖는 2개의 중쇄 폴리펩티드를 포함하고, 각각의 Gln295잔기는 본 원에 기재된 클릭 화학반응에 적합한 아지도기에 연결된다. 또한, 항체 또는 항원 결합 분자는 부위-지정 돌연변이 유발에 의해 접합되기 전에 추가로 변형되어 서열을 제거 또는 불능화 시키거나 임의의 간섭 구조와는 다른 부위에 글루타민 잔기를 삽입한다. 예를 들어, 각각의 중쇄에서 N297돌연변이체, Asn297Gln (N297Q) 돌연변이체는 아지도 그룹에 연결된다. 특정 경우에, 접합될 항체는 그의 가변 영역에 하나이상의 추가의 자연 발생 글루타민 잔기를 함유하며, 이는 트랜스 글루타미나제에 접근할 수 있고 따라서 접합될 수 있다 예를 들어 Gln55 (Q55)이다. 이러한 경우에 트랜스글루타미나제를 통한 접합후의 항체는 4보다 큰 DAR값을 가질 것이다. 따라서, 글루타미닐-개질된 항체 또는 항원 결합 분자는 본 원에 기재된 클릭 화학 반응에 적합한 5개 또는 6개의 아지도 그룹을 포함하여 약 5 또는 약 6의 DAR을 허용 할 수 있다.
일부 실시양태에서, 본 원에 기재된 접합제의 BA는 항체 또는 그의 항원-결합 단편이다.
일부 예에서, 본 원에 기재된 화학식 (VI), 화학식 (VII), 화학식 (VIII), 화학식 (IX), 화학식 (IXa), 화학식 (IXb), 화학식 (IXc), 화학식 (Xa), 화학식 (Xb), 화학식 (Xc), 또는 화학식 (Xd)의 화합물과 반응하는 결합제는 항체 또는 이의 항원 결합 단편이다. 이러한 경우에, 결합제는 항체 또는 이의 항원 결합 단편이거나, 임의로 아지도기로 변형되거나, 또는 결합제는 본 원에 기재된 화학식 Ab-1의 변형된 항체 또는 이의 항원 결합 단편, 또는 이들의 조합이다.
일부 실시양태에서, 본 원에 기재된 접합제는 아지도-관능화된 항체 또는 이의 항원 결합 단편으로부터 유래된다. 일부 실시양태에서, 본 원에 기재된 접합제는 PEG-관능화된 항체 또는 그의 항원-결합 프래그먼트로부터 유래된다. 일부 실시양태에서, 본 원에 기재된 접합제는 아지도 및 PEG작용기화 항체 또는 이의 항원 결합 단편으로부터 유래된다. 여기서 PEG는 제1 말단에서 항체 또는 이의 항원 결합 단편에 부착되고 PEG는 제 2말단에서 본 원에 기재된 클릭 화학 반응에 적합한 아지도기에 부착된다. 특정 실시양태에서, 본 원에 기재된 접합제 BA는:
일부 예에서, 본 원의 d-Lys는 도 20에 제시된 시약으로 대체될 수 있다.
1차 아민 화합물
글루타민을 포함하는 항체(또는 항원 결합 화합물)의 트랜스 글루타미나제 매개 커플링에 유용한 1차 아민 화합물은 당업자에게 유용한 것으로 간주되는 임의의 1차 아민 화합물일 수 있다. 일반적으로, 1차 아민화합물은 화학식 H2N-R을 가지며, 여기서 R은 항체 및 반응 조건에 적합한 임의의 기일 수 있다. 특정 실시양태에서, R은 알킬, 치환된 알킬, 헤테로알킬, 또는 치환된 헤테로알킬이다.
일부 실시양태에서, 1차 아민 화합물은 반응성 그룹 또는 보호된 반응성 그룹을 포함한다. 유용한 반응성 그룹은 아지드, 알킨, 시클로알킨, 티올, 알코올, 케톤, 알데히드, 산, 에스테르, 히드로지드, 아날린 및 아민을 포함한다. 특정 실시양태에서, 반응성 그룹은 아지드, 알킨, 술프히드릴, 시클로알킨, 알데히드 및 카르복실로 이루어진 군으로부터 선택된다.
특정 실시양태에서, 1차 아민화합물은 화학식H2N-LL-X에 따르며, 여기서 LL은 2가 스페이서이고 X는 반응성 그룹 또는 보호된 반응성 그룹이다. 특정 실시양태에서, LL은 2가 폴리에틸렌글리콜(PEG)기이다. 특정 실시양태에서, X 는 -SH, -N3, 알킨(alkyne), 알데히드(aldehyde), 및 테트라졸(tetrazole)로 이루어진 군으로부터 선택된다. 특정 실시양태에서, X 는 -N3이다.
특정 실시양태에서, 1차 아민 화합물은 하기 화학식 중 하나에 따른다:
H2N-(CH2)n'-X;
H2N-(CH2CH2O)n'-(CH2)p'-X;
H2N-(CH2)n'-N(H)C(O)-(CH2)m'-X;
H2N-(CH2CH2O)n'-N(H)C(O)-(CH2CH2O)m'-(CH2) p'-X;
H2N-(CH2)n'-C(O)N(H)-(CH2)m'-X;
H2N-(CH2CH2O)n'-C(O)N(H)-(CH2CH2O)m'-(CH2) p'-X;
H2N-(CH2)n'-N(H)C(O)-(CH2CH2O)m'-(CH2) p'-X;
H2N-(CH2CH2O)n'-N(H)C(O)-(CH2)m'-X;
H2N-(CH2)n'-C(O)N(H)-(CH2CH2O)m'-(CH2) p'-X; and
H2N-(CH2CH2O)n'-C(O)N(H)-(CH2)m'-X;
여기서 아래 첨자 n'는 1 내지 12로부터 선택된 정수이며;
아래 첨자 m' 는0 내지 12로부터 선택된 정수이며;
아래 첨자 p' 는0 내지 2로부터 선택된 정수이며;
및 X 는 -SH, -N3, -C≡CH,-C(O)H, 테트라졸(tetrazole), 및 임의의
상기에서, 임의의 상기 알킬 또는 알킬렌(예를 들어, -CH2-)기는 예를 들어, C1-8알킬, 메틸포르밀 또는 -SO3H로 선택적으로 치환될 수 있다. 특정 실시양태에서, 상기 알킬기는 비치환된다.
특정 실시양태에서, 1차 아민 화합물은 다음으로 이루어진 군으로부터 선택된다:
특정 실시양태에서, 1차 아민 화합물은
상기 반응에 대한 예시적인 조건은 하기 실시예에 제공된다.
본 원에 기재된 접합제의 링커 LL부분은 결합제를 본 원에 기재된 페이로드 화합물에 공유적으로 연결하는 부분, 예를 들어 2가 부분이다. 다른 경우에, 링커 LL은 결합제를 본 원에 기재된 페이로드 화합물에 공유적으로 연결하는 3가 또는 다가 부분이다. 적합한 링커는 예를 들어 항체-약물 접합제 및 면역 독소; Phillips, G. L., Ed.; Springer Verlag: New York, 2013; Antibody-Drug Conjugates; Ducry, L., Ed.; Humana Press, 2013; Antibody-Drug Conjugates; Wang, J., Shen, W.-C., and Zaro, J. L., Eds.; Springer International Publishing, 2015, 각각의 내용은 전체적으로 본 명세서에 참고로 포함된다.
페이로드 화합물은 도 1의 화합물을 포함한다. 및 링커 LL과의 결합 또는 혼입 후의 잔기이다. 당업자는 페이로드 부분의 특정 작용기가 링커 및/또는 결합제에 연결 또는 결합하기에 편리하다는 것을 인식할 것이다. 이들 기는 아민, 히드록실, 포스페이트 및 당을 포함한다.
특정 실시양태에서, 링커는 생리학적 조건에서 안정하다. 특정 실시양태에서, 링커는 절단 가능하며, 예를 들어, 효소의 존재 또는 특정 pH범위 또는 값에서 적어도 페이로드 부분을 방출할 수 있다. 일부 실시양태에서, 링커는 효소-절단 가능한 부분을 포함한다. 예시적인 효소-절단 가능한 부분은 펩타이드 결합, 에스테르 결합, 히드라존 및 이황화 결합을 포함하나, 이에 제한되지는 않는다. 일부 실시양태에서, 링커는 카텝신-절단가능한링커를 포함한다.
일부 실시양태에서, 링커는 절단 불가능한 부분을 포함한다. 일부 실시양태에서, 비절단성 링커는 또는 이의 잔기로부터 유래된다. 일부 실시양태에서, 비절단성링커-페이로드는 , 또는 이의 위치 이성질체이다. 일부 실시양태에서, 비절단성링커는 또는 이의 잔기로부터 유래된다. 일부 실시양태에서, 비절단성 링커-페이로드는 , 또는 그의 위치 이성질체이다. 한 실시양태에서, 링커는 말레이미드 시클로 헥산 카르복실 레이트 또는 4-(N-말레이미도메틸)시클로헥산카르복실산(MCC)이다. 구조에서, 는 예를 들어 결합제 및 링커 페이로드의 반응으로부터 생성되는 클릭 화학잔류물을 나타낸다.
일부 실시양태에서, 적합한 링커는 단일 결합제, 예를 들어 항체의 2개의 시스테인 잔기에 화학적으로 결합된 것들을 포함하나, 이에 제한되지는 않는다.
이러한 링커는 접합 과정의 결과로 파괴된 항체의 이황화 결합을 모방하는 역할을 할 수 있다.
일부 실시양태에서, 링커는 하나 이상의 아미노산을 포함한다. 적합한 아미노산은 천연, 비천연, 표준, 비표준, 단백질 생성, 비단백질 생성, 및 L-, 또는 D- a-아미노산을 포함한다. 일부 실시양태에서, 링커는 알라닌, 발린, 류신, 이소류신, 메티오닌, 트립토판, 페닐알라닌, 프롤린, 글리신, 세린, 트레오닌, 시스테인, 티로신, 아스파라긴, 글루타민, 아스파르트산, 글루탐산, 리신, 아르기닌, 히스티딘, 또는 시트룰린, 이의 유도체 또는 이들의 조합이다. 특정 실시양태에서, 아미노산의 하나 이상의 측쇄는 후술되는 측쇄기에 연결된다. 일부 실시양태에서, 상기 링커는 발린 및 시트룰린을 포함한다. 일부 실시양태에서, 상기 링커는 리신, 발린, 및 시트룰린을 포함한다. 일부 실시양태에서, 링커는 리신, 발린, 및 알라닌을 포함한다. 일부 실시양태에서, 링커는 발린 및 알라닌을 포함한다.
일부 실시양태에서, 링커는 자기-희생기를 포함한다. 자기 제모 그룹은 당업자에게 알려진 임의의 그룹일 수 있다. 특정 실시양태에서, 자기-희생기는 p-아미노벤질 (PAB), 또는 이의 유도체이다. 유용한 유도체는 p-아미노벤질옥시카르보닐(PABC)을 포함한다. 당업자는 자기-희생기가 페이로드로부터 링커의 나머지 원자를 방출하는 화학 반응을 수행할 수 있음을 인식할 것이다.
특정 실시양태에서, 반응성 그룹은 알킨을 포함하지만 이로 제한되지는 않는다. 특정 실시양태에서, 알킨은 스트레인드알킨과 같은 구리 촉매 부재하에서 1,3-시클로 첨가 반응을 수행할 수 있는 알킨이다. 변형된 알킨은 변형 촉진된 알킨-아지드시클로첨가 (SPAAC), 시클로 알킨, 예를 들어, 시클로옥틴, 아네벤질화된 알킨에 적합하다. 적합한 알킬은 다음을 포함한다, 그러나 이에 제한되지 않는다, 디벤조아자시클로옥틴 또는 (DIBAC), 디벤조시클로옥틴 또는 (DIBO), 바이아릴라시클로옥토논 또는 (BARAC), 디플루오르화시클로옥틴 또는 , 또는 , 또는 (DIFO), 치환된, 예를들어, 플루오르화 알킨, 아자-시클로알킨, 비시클로[6.1.0]노니 또는 (BCN), 및 이들의 유도체이다. 특히 유용한 알킬은 , , 및 을 포함한다.
특정 실시양태에서, 결합제는 반응성 그룹 RG에 직접 결합된다. 특정 실시양태에서, 결합제는 스페이서를 통해 반응성 그룹 RG에 결합된다. 특정 실시양태에서, 결합제는 PEG 스페이서를 통해 반응성 그룹에 결합된다. 특정 실시양태에서, 결합제는 하나 이상의 아지도 그룹으로 작용화함으로써 제조된다. 각각의 아지도 그룹은 RG에서 알킨과 반응하여 RG 1 또는 RG'를 형성할 수 있다. 특정 실시양태에서, 결합제는 글루타민 잔기에 연결된 -PEG-N3으로 유도체화 된다. 예시적인 -N3 유도체화된 결합제, 이의 제조방법 및 RG와의 반응에 사용하는 방법이 본 원에 제공된다. 특정 실시양태에서, RG 는 1,3-시클로첨가에 참여하기에 적합한 알킨이고, 및 RG 1 또는 RG' 는 RG와 아지도-작용기 결합제와의 반응으로부터 형성된 1,2,3-트리아졸리부분이다. 추가의 예로서, 특정 실시양태에서, RG 는 또는 , 또는 각각의 위치 이성질체의 혼합물에 도시된 바와 같이 결합제에 연결된다. 각각의 R 및 R' 는 본 원에 기재된 바와 같다.
유사한 방식으로, 본 원에 기술되 각각의 HG는 RG에서 알킨과 반응하여
RG 2 를 형성하는 아지도-관능화된 친수성 그룹일 수 있다.
특정 실시양태에서, RG 1 , 또는 RG' 는 반응성 그룹과 항체 또는 이의 항원 결합 단편의 시스테인 또는 리신 잔기와의 반응의 반응으로부터 유도된다.
특정 실시양태에서, RG 1 , 또는 RG' 는 클릭 화학반응 으로부터 유래된다. 상기 클릭 화학 반응의 일부 실시양태에서, RG 1 , 또는 RG'는 알킨 및 아지드 사이의 1,3시클로첨가반응에서 유래된다. 이러한 RG 1 , 또는 RG'의 비제한적 예에는 변형 알킨으로부터 유래된 것, 예를 들어 변형 촉진 알킨 아지드 시클로 첨가(SPAAC)에 적합한 것, 시클로알킨, 예를 들어, 시클로옥틴, 벤질화된 알킨 및 구리촉매의 부재하에서 아지드와의 1,3시클로 첨가 반응을 겪을 수 있는 알킨이 포함된다. 적합한 RG 1 , 또는 RG'는 또한 DIBAC, DIBO, BARAC로부터 유도된 것, 치환된, 예를 들어, 플루오르화알킨, 아자-시클로알킨, BCN, 및 이들의 유도체. 이러한 RG 1 , 또는 RG'기를 함유하는 접합제는 아지도기로 기능화된 항체로부터 유래될 수 있다. 이러한 기능화된 항체는 아지도-폴리에틸렌글리콜기로 기능화된 항체를 포함한다. 특정 실시양태에서, 이러한 작용화된 항체는 하나이상의 글루타민 잔기를 포함하는 항체를 화학식 H2N- LL' 3에 따른 화합물과 반응시켜 유도되며, 여기서 LL'효소 트랜스 글루미나아제의 존재 하에 2가 폴리에틸렌 글리콜기이다. 예를 들어, 미생물 트랜스글루타미나제이다. 항체의 접합한 글루타민 잔기는 Q295 또는 Q55, 또는 삽입 또는 돌연변이, 예를 들어, N297Q돌연변이에 의해 유도된 것들을 포함한다.
당업자는 PAB 및 PABC를 각각하기 구조를 갖는 p-아미노벤질옥시카르보닐 및 p-아미노벤질카르바메이트의 잔기로서 인식할 것이다:
PAB 및 PABC잔기는 시험관내(in vivo) 및 생체 내에서 특정 링커의 절단을 촉진하는 것으로 나타났다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dLys(COT-PEG6)-VC-PAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dLys(COT-PEGe-taurine)-VC-PAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는DIBAC-PEGe-dLys(COT-PEGe-taurine)-VC-PAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-dualtaurine)-VC-PAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dGlu(taurine)-VC-PAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dLys(COT-PEG4-taurine)-VC-PAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dLys(COT-PEG4-taurine)-VA이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dLys(COT-PEG4-taurine)-VC이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dGlu(taurine)-VC이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dLys(COT-PEGe-taurine)-VA이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dLys(COT-PEGe-taurine)-VC이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dLys(COT-PEGe-N+Me3)-vcPAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dLys(COT-PEGe-phosphate)-vcPAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dLys(COT-galactose)-vcPAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 MAL-PEGe-dLys(COT-galactose)-vcPAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dGlu(glucamide)-vcPAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는MAL-PEGe-dGlu(glucamide)-vcPAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dLys(COT-PEGe-N+Me3)-vcPAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 COT-PEGe-dLys(COT-PEGe-N+Me3)-vcPAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 BCN-PEGe-dLys(COT-PEGe-N+Me3)-vcPAB이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEGe-dLys(COT-PEGe-N+Me3)-VA이다. 아래 첨자 e 는 0 내지 4의 정수이다. 일부 예에서 아래 첨자 e는 0이다. 일부 예에서 아래 첨자 e 는 1이다. 일부 예에서 아래 첨자 e 는 2이다. 일부 예에서 아래 첨자 e 는 3이다. 일부 예에서 아래 첨자 e 는 4이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-PEG6)-VC-PAB이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-PEG4-taurine)-VC-PAB이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-PEG4-taurine)-VC-PAB 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-dualtaurine)-VC-PAB 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dGlu(taurine)-VC-PAB 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-PEG4-taurine)-VC-PAB 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-PEG4-taurine)-VA 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-PEG4-taurine)-VC 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dGlu(taurine)-VC 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-PEG4-taurine)-VA 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-PEG4-taurine)-VC 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-PEG4-N+Me3)-vcPAB 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-PEG5-phosphate)-vcPAB 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-galactose)-vcPAB 이다.
일부 실시양태에서, 링커는 MAL-PEG4-dLys(COT-galactose)-vcPAB 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dGlu(glucamide)-vcPAB 이다.
일부 실시양태에서, 링커는 MAL-PEG4-dGlu(glucamide)-vcPAB 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-PEG4-N+Me3)-vcPAB 이다.
일부 실시양태에서, 링커는 COT-PEG4-dLys(COT-PEG4-N+Me3)-vcPAB 이다.
일부 실시양태에서, 링커는 BCN-PEG4-dLys(COT-PEG4-N+Me3)-vcPAB 이다.
일부 실시양태에서, 링커는 DIBAC-PEG4-dLys(COT-PEG4-N+Me3)-VA 이다.
반응성 링커-페이로드
본 원에 제공된 접합제는 상기 기재된 바와 같이 반응성 그룹 RG 1 또는 RG , 또는 RG 2 를 포함하는 반응성 링커-페이로드로부터 제조될 수 있다. 반응성 링커 페이로드는 본 원에 기재된 친수성기 및/또는 하기 기재된 방법에 따른 결합제에 연결될 수 있다.
일부 실시양태에서, 하나 이상의 페이로드 부분에 연결되고 공유 링커를 통해 하나 이상의 친수성 부분에 연결된 반응성 그룹을 포함하는 반응성 링커-페이로드가 본 원에 기재되며, 여기서 상기 공유 링커는 각각의 반응성 그룹, 페이로드 부분, 친수성 부분에 직접 또는 간접적으로 결합된다.
본 원에 예시된 바와 같이, 일부 예에서, 반응성 그룹은 리신 아미노산과 같은 공유 링커에 직접 결합된다. 이는 반응성 그룹이 공유 링커로부터 떨어진 하나의 결합 위치임을 의미한다. 이들 예 중 일부에서, 공유 링커는 또한 페이로드 부분에 직접 결합된다. 이는 공유 링커가 MMAE, 스테로이드, LXR조절제 또는 본 원에 제시된 임의의 페이로드와 같은 페이로드로부터 떨어져 있는 하나의 결합 위치임을 의미한다. 이들 예 중 일부에서, 공유 링커는 또한 친수성 부분에 직접 결합된다. 이는 공유 링커가 친수성 잔기, 예컨대 본 원에 제시된 친수성 잔기로부터 떨어진 하나의 결합 위치임을 의미한다. 이들 예 중 일부에서, 공유 링커는 리신 아미노산 또는 이의 유도체이다.
다른 예에서, 반응성 그룹은 공유 링커에 간접적으로 결합된다. 이는 반응성 그룹이 공유 링커로부터 하나 이상의 결합 위치로부터 떨어져 있음을 의미한다. 이는 또한 반응성 그룹이 다른 부분를 통해 공유 링커에 결합됨을 의미한다. 예를 들어, 반응성 그룹은 공유 링커에 결합된 폴리에틸렌 글리콜기에 결합될 수 있다. 이들 예 중 일부에서, 공유 링커는 또한 페이로드 부분에 가점적으로 결합된다. 이는 공유 링커가 MMAE 또는 스테로이드와 같은 페이로드로부터 떨어져있는 하나 이상의 결합 위치 또는 본 명세서에 제시된 임의의 페이로드임을 의미한다. 이것은 또한 공유 링커가 다른 부분을 통해 페이로드에 결합됨을 의미한다. 예를 들어, 공유 링커는 페이로드에 결합될 수 있는 PAB에 결합될 수 있는 Val-Ala 또는 Val-Cit와 같은 다이펩타이드에 결합될 수 있다. 이들 예 중 일부에서, 공유 링커는 또한 친수성 부분에 간접적으로 결합된다. 이는 공유 링커가 친수성 잔기, 예를 들어 본원에 기재된 친수성 잔기로부터 떨어진 하나 이상의 결합 위치임을 의미한다. 이것은 또한 공유 링커가 다른 부분을 통해 친수성 잔기에 결합됨을 의미한다. 예를 들어, 공유 링커는 친수성 잔기에 결합될 수 있는 반응성 그룹에 결합될 수 있는 폴리에틸렌 글리콜기에 결합될 수 있다. 이들 예 중 일부에서, 공유 링커는 리신 아미노산 또는 이의 유도체이다.
본 원의 화학식에서, 각각의 AA 1 는 아미노산이다. 본 원의 화학식 중 일부 예에서, 각각 AA 2 는 아미노산이다. 본 원의 화학식중 일부 예에서, 각각의 AA 2 는 디-펩타이드이다. 본 원의 화학식중 일부 예에서, 각각의 AA 2 는 트라이-펩타이드이다. 각각의 AA 1 또는 AA 2 에 적합한 아미노산은 천연, 비천연, 표준, 비표준, 단백질 생성, 및 L-, 또는 D-아미노산을 포함한다. 일부 실시양태에서, 링커는 알라닌, 발린, 류신, 이소류신, 메티오닌, 트립토판, 페닐알라닌, 프롤린, 글리신, 세린, 트레오닌, 시스테인, 티로신, 아스파라긴, 글루타민, 아스파르트산, 글루탐산, 리신, 아르기닌, 히스티딘, 또는 시트룰린, 이의 유도체 또는 이들의 조합이다. 특정 실시양태에서, 아미노산의 하나 이상의 측쇄는 후술하는 측쇄기에 연결된다. 특정 실시양태에서, AA 1 는 알라닌, 발린, 류신, 이소류신, 메티오닌, 트립토판, 페닐알라닌, 프롤린, 글리신, 세린, 트레오닌, 시스테인, 티로신, 아스파라긴, 글루타민, 아스파르트산, 글루탐산, 리신, 아르기닌, 히스티딘, 또는 시트룰린, 이의 유도체 또는 이들의 조합이다. 특정 실시양태에서, AA 1 는 페이로드, 결합제(예를 들어, 이의 항체 또는 항원의 결합 단편) 및 친수성기를 포함하는 링커, 예를 들어 리신, 아스파르긴, 글루탐산, 아스파르트산, 글루타민, 시스테인, 트레오닌, 세린, 또는 티로신이다. 특정 실시양태에서, AA 1 는 리신이다. 특정 실시양태에서, AA 1 는 글루타민이다. 특정 실시양태에서, AA 1 리신 또는 리신의 유도체이다. 특정 실시양태에서, AA 1 는 L-리신이다. 특정 실시양태에서, AA 1 는 D-리신이다. 특정 실시양태에서, AA 1 는 글루탐산이다. 특정 실시양태에서, AA 2 는 발린-시트룰린이다. 일부 실시양태에서, AA 2 는 시트룰린-발린이다. 일부 실시양태에서, AA 2 는 발린-알라닌이다. 일부 실시양태에서, AA 2 는 알라닌-발린이다. 일부 실시양태에서, AA 2 는 발린-글리신이다. 일부 실시양태에서, AA 2 는 글리신-발린이다. 일부 실시양태에서, AA 1 -AA 2 는 글루타민-발린-시트룰린이다. 일부 실시양태에서, AA 1 -AA 2 는 리신-발린-시트룰린이다. 일부 실시양태에서, AA 1 -AA 2 는 리신-발린-알라닌이다. 일부 실시양태에서, AA 1 -AA 2 는 글루타민-발린-알라닌이다.
일부 실시양태에서, AA 2 는 발린-시트룰린, 시트룰린-발린, 리신-페닐알라닌, 페닐알라닌-리신, 발린-아스파라긴, 아스파라긴-발린, 트레오닌-아스파라긴, 아스파라긴-트레오닌, 세린-아스파라긴, 아스파라긴-세린, 페닐알라닌-아스파라긴, 아스파라긴-페닐알라닌, 류신-아스파라긴, 아스파라긴-류신, 이소류신-아스파라긴, 아스파라긴-이소류신, 글리신-아스파라긴, 아스파라긴-글리신, 글루탐산-아스파라긴, 아스파라긴-글루탐산, 시트룰린-아스파라긴, 아스파라긴-시트룰린, 알라닌-아스파라긴, 또는 아스파라긴-알라닌으로부터 선택된 디펩티드이다.
일부 예에서, AA 1 -AA 2 는 리신-발린-알라닌 또는 알라닌-발린-리신이다.
일부 예에서, AA 1 -AA 2 는 리신-발린-시트룰린 또는 시트룰린-발린-리신이다.
일부 예에서, AA 2 는 발린-시트룰린 또는 시트룰린-발린이다.
일부 예에서, AA 2 는 발린-알라닌 또는 알라닌-발린이다.
일부 예에서, AA 1 -AA 2 는 이다. 이들 예 중 일부 에서, R AA1 는 아미노산 측쇄이고, R AA2 는 아미노산 측쇄이고, 및 R AA3 는 친수성 부분에 직접 또는 간접적으로 결합된 아미노산 측쇄이다.
일부 예에서, R AA1 는 발린 측쇄이다.
일부 예에서 R AA2 는 알라닌 측쇄이다.
일부 예에서, R AA2 는 시트룰린 측쇄이다.
일부 예에서, 본 원에 제시된 화합물을 포함하는 링커-페이로드가 본 원에 제시된다.
일부 예에서, 본 원에는 본 원에 기재된 임의의 화합물의 산소 또는 1차 또는 2차 질소에 결합된 본 워네 기재된 화합물을 포함하는 링커-페이로드가 제시된다.
일부 예에서, 본 원에는 항체에 결합된 화합물 또는 링커-페이로드 또는 이의 항원 결합 단편을 포함하는 항체-약물-접합제가 본 원에 기재되어 있다.
본 원에 제공된 접합제는 상기 기술된 바와 같이 및 실시예 섹션 및 도면에서 반응성 그룹 RG를 갖는 반응성 링커-페이로드로부터 제조될 수 있다. 반응성 링커-페이로드는 본 원에, 예를 들어, 실시예 섹션 및 도면에 기재된 방법에 따라 친수성기 및/또는 결합제에 연결될 수 있다.
일부 실시양태에서, 반응성 링커-페이로드는:
또는 그의 제약상 허용되는 염, 용매화물 또는 입체 이성질체 형태 또는 이의 위치 이성질체 여기서, PAB 1 는 PAB 또는 PABC 이고; p 는 0 또는 1이며; R AA9 는 메틸 또는-(CH2)3-NH-C(=O)-NH2이고; 및 RG', RG 2 , PA, SP 2 및 HG는 본 원에 정의된 바와 같다.
일부 실시양태에서, 반응성 링커 페이로드는:
또는 그의 제약상 허용되는 염, 용매화물 또는 입체 이성질체 형태 또는 이의 위치 이성질체, 여기서 PAB 1 는 PAB 또는 PABC 이고; p 는 0 또는 1이며; R AA9 는 메틸 또는 -(CH2)3-NH-C(=O)-NH2이고; 및 PA, SP 2 및 HG는 본 원에 정의된 바와 같다. 이들 실시양태 중 일부에서, HG 는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA 는 도 1의 페이로드A이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 B이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 C이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 D이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 E이다.
일부 실시양태에서, 반응성 링커 페이로드는:
또는 그의 제약상 허용되는 염, 용매화물 또는 입체 이성질체 형태 또는 이의 위치 이성질체 여기서, PAB 1 는 PAB 또는 PABC 이고; p 는 0 또는 1이며; R AA9 는 메틸 또는 -(CH2)3-NH-C(=O)-NH2이고; 및 PA, SP 2 및 HG는 본 원에 정의된 바와 같다. 이들 실시양태 중 일부에서, HG 는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA 는 도 1의 페이로드A이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 B이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 C이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 D이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 E이다.
일부 실시양태에서, 반응성 링커 페이로드는:
또는 그의 제약상 허용되는 염, 용매화물 또는 입체 이성질체 형태 또는 이의 위치 이성질체 여기서, PAB 1 는 PAB 또는 PABC 이고; p 는 0 또는 1이며; R AA9 는 메틸 또는 -(CH2)3-NH-C(=O)-NH2이고; 및 PA, SP 2 및 HG는 본 원에 정의된 바와 같다. 이들 실시양태 중 일부에서, HG 는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA 는 도 1의 페이로드A이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 B이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 C이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 D이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 E이다.
일부 실시양태에서, 반응성 링커 페이로드는:
또는 그의 제약상 허용되는 염, 용매화물 또는 입체 이성질체 형태 또는 이의 위치 이성질체 여기서, PAB 1 는 PAB 또는 PABC 이고; p 는 0 또는 1이며; R AA9 는 메틸 또는 -(CH2)3-NH-C(=O)-NH2이고; 및 PA, SP 2 및 HG는 본 원에 정의된 바와 같다. 이들 실시양태 중 일부에서, HG 는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA 는 도 1의 페이로드A이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 B이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 C이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 D이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 E이다.
일부 실시양태에서, 반응성 링커 페이로드는:
또는 그의 제약상 허용되는 염, 용매화물 또는 입체 이성질체 형태 또는 이의 위치 이성질체 여기서, PAB 1 는 PAB 또는 PABC 이고; p 는 0 또는 1이며; R AA9 는 메틸 또는 -(CH2)3-NH-C(=O)-NH2이고; 및 PA, SP 2 및 HG는 본 원에 정의된 바와 같다. 이들 실시양태 중 일부에서, HG 는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA 는 도 1의 페이로드A이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 B이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 C이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 D이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 E이다.
일부 실시양태에서, 반응성 링커 페이로드는:
또는 그의 제약상 허용되는 염, 용매화물 또는 입체 이성질체 형태 또는 이의 위치 이성질체 여기서, PAB 1 는 PAB 또는 PABC 이고; p 는 0 또는 1이며; R AA9 는 메틸 또는 -(CH2)3-NH-C(=O)-NH2이고; 및 PA, SP 2 및 HG는 본 원에 정의된 바와 같다. 이들 실시양태 중 일부에서, HG 는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA 는 도 1의 페이로드A이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 B이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 C이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 D이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 E이다.
일부 실시양태에서, 반응성 링커 페이로드는:
또는 그의 제약상 허용되는 염, 용매화물 또는 입체 이성질체 형태 또는 이의 위치 이성질체 여기서, PAB 1 는 PAB 또는 PABC 이고; p 는 0 또는 1이며; R AA9 는 메틸 또는 -(CH2)3-NH-C(=O)-NH2이고; 및 PA, SP 2 및 HG는 본 원에 정의된 바와 같다. 이들 실시양태 중 일부에서, HG 는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA 는 도 1의 페이로드A이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 B이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 C이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 D이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 E이다.
일부 실시양태에서, 반응성 링커 페이로드는:
또는 그의 제약상 허용되는 염, 용매화물 또는 입체 이성질체 형태 또는 이의 위치 이성질체 여기서, PAB 1 는 PAB 또는 PABC 이고; p 는 0 또는 1이며; R AA9 는 메틸 또는 -(CH2)3-NH-C(=O)-NH2이고; 및 PA, SP 2 및 HG는 본 원에 정의된 바와 같다. 이들 실시양태 중 일부에서, HG 는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA 는 도 1의 페이로드A이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 B이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 C이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 D이다. 이들 실시양태 중 일부에서, HG는 본 원에 정의된 바와 같은 타우린 또는 이중 타우린이고 PA는 도 1의 페이로드 E이다.
본 원에 기재된 반응성 링커 페이로드의 임의의 예에서, 반응성 링커 페이로드는 아지드(예를 들어, 클릭 화학에 의한)와 변형된 알킨의 반응을 통해 결합제(예를 들어, 본 원에 정의된 Ab 또는 Ab-1)에 연결된다.
다른 실시양태에서, 반응성 링커 페이로드는 반응성 링커 페이로드에서 석신 이미드 부분에 대한 친 핵성 공격을 통해 결합제(예를 들어, 본 원에 정의된 Ab 또는 Ab-1)dp 연결된다.
일부 실시양태에서, 반응성 링커 페이로드는:
또는 그의 제약상 허용되는 염, 용매화물 또는 입체 이성질체 형태 또는 이의 위치 이성질체, 여기서 PAB 1 는 PAB 또는 PABC이고; p 는 0 또는 1이고; R AA9 는 메틸 또는 -(CH2)3-NH-C(=O)-NH2이고; 및 PA 는 본 원에 정의된 바와 같다. 이러한 경우에, 아지드를 포함하는 친수성 링커는 아지드(예를 들어, 클릭 화학에 의해)와 변형된 알킨의 반응을 통해 반응성 링커 페이로드로 연결된다.
본 원에 제공된 화합물은 당업자에게 명백한 임의의 방법에 의해 제조, 단리 또는 수득될 수 있다. 예시적인 제조방법은 하기 실시예에 상세히 기재되어있다. 특정 실시양태에서, 본 원에 제공된 화합물은 실시예 및 도 1 내지 19에 기재된 방법에 따라 제조될 수 있다.
본 원에 기재된 접합제는 본 원에 기재된 링커-페이로드를 결합제, 예를 들어 표준 접합 조건하의 항체와 커플링함으로써 합성될 수 있다(예를 들어, Doronina et al. Nature Biotechnology 2003, 21, 7, 778, 이는 그 전문이 본원에 참조로 포함됨). 결합제가 항체인 경우, 항체는 항체의 하나 이상의 시스테인 또는 리신 잔기를 통해 링커-페이로드에 결합될 수 있다. 링커-페이로드는 시스테인 잔기에 결합될 수 있으며, 예를 들어, 항체를 환원제, 예를 들어 디티오스테리톨에 적용시켜 항체의 이황화 결합을 절단함으로써, 환원된 항체를 정제함으로써, 예를 들어, 겔 여과에 의해, 이어서 항체를 적합한 반응성 부분, 예를 들어 말레이미도그룹을 함유하는 링커-페이로드로 처리한다. 적합한 용매는 물, DMA, DMF 및 DMSO를 포함하지만 이에 제한되지는 않는다. 반응성 그룹, 예를 들어 활성화된 에스테르 또는 산 할라이드기를 함유하는 링커-페이로드는 항체의 리신잔기에 커플링될 수 있다. 적합한 용매는 물, DMA, DMF 및 DMSO를 포함하지만 이에 제한되지는 않는다. 접합제는 예를 들어 크기 배제 크로마토 그래피, 투석 및 한외여과/정용여과를 포함하는 공지된 단백질 기술을 사용하여 정제될 수 있다.
결합제, 예를 들어 항체는 또한 클릭 화학 반응을 통해 접합될 수 있다. 상기 클릭 화학 반응의 일부 실시양태에서, 링커-페이로드는 반응성 그룹, 예를 들어 알킨을 포함하고, 이는 아지드와 1,3-시클로부가 반응을 겪을 수 있다. 이러한 적합한 반응성 그룹은 상기 기재되어 있다. 항체는 하나 이상의 아지드기를 포함한다. 이러한 항체는 예를 들어 아지도-폴리에틸렌글리콜기로 작용화된 항체를 포함한다. 특정 싱시 양태에서, 이러한 작용화된 항체는 하나 이상의 글루타민 잔기, 예를 들어, 중쇄 Gln295를 갖는 항체를 처리함으로써 유도된다. 이러한 항체는 또한 Asn297Gln (N297Q) 돌연변이체를 포함할 수 있다. 특정 실시양태에서, 이러한 작용화된 항체는 효소 트랜스 글루타미나아제의 존재 하에 2개 이상의 글루타민 잔기, 예를 들어 중쇄 Gln295및 중쇄 Gln297을 갖는 항체를 1차 아민화합물로 처리함으로써 유도된다. 이러한 항체는 Asn297Gln(N297Q)돌연변이 체를 포함한다. 특정 실시양태에서, 항체는 총 2개 또는 총 4개의 글루타민 잔기에 대해 본 단락에 기재된 바와 같은 2개의 중쇄를 갖는다. 특정 예에서, 접합될 항체는 가변 영역에 하나 이상의 추가의 자연 발생 글루타민 잔기를 함유하며, 이는 트랜스 글루타미나제에 접근할 수 있고 따라서 접합될 수 있다(예를 들어, Gln 55(Q55)). 이러한 경우에, 트랜스글루타미나제를 통한 접합 후의 항체는 4보다 큰 DAR값을 가질 수 있다. 이러한 항체는 Asn297Gln(N297Q)돌연변이체를 포함한다. 일부 실시양태에서, 항체는 이 단락에 기재된 바와 같이 총 2개 또는 총 4개 또는 총 5개 또는 6개의 글루타민 잔기에 대해 2개의 중쇄를 갖는다.
특정 실시양태에서, 항체는 EU 넘버링 시스템에서 295로 번호가 매겨진 하나 이상의 중쇄 위치에 글루타민 잔기를 포함한다. 본 개시에서, 이 위치는 글루타민 295, Gln295 또는 Q295로 지칭된다. 당업자는 이것이 많은 항체의 야생형 서열에서 보존된 글루타민 잔기임을 인식할 것이다. 다른 유용한 실시양태에서, 항체는 글루타민 잔기를 포함하도록 조작될 수 있다. 글루타민 잔기를 포함하도록 항체 서열을 변형시키는 기술은 당업자의 기술 번위 내에 있다(예를 들어, Ausubel et al. Current Protoc. Mol. Biol.참조).
특정 실시양태에서, 항체는 각각의 중쇄에 하나씩 2개의 글루타민 잔기를 포함한다. 특정 실시양태에서, 항체는 각각의 중쇄에 Q295잔기를 포함한다. 추가의 실시양태에서, 항체는 1, 2, 3, 4, 5, 6, 7, 8 또는 그 이상의 글루타민 잔기를 포함한다. 이들 글루타민 잔기는 중쇄, 경쇄, 또는 중쇄 및 경쇄 둘다 있을 수 있다. 이들 글루타민 잔기는 야생형 잔기 또는 조작된 잔기일 수 있다. 항체는 표준 기술에 따라 제조될 수 있다. 특정 실시양태에서, 항체는 Q55 잔기를 포함한다.
당업자는 항체가 종종 중쇄 서열에서 잔기 Q295 근처의 잔기 N297에서 글리코실화됨을 인식할 것이다. 잔기N297에서 글리코 실화됨을 인식할 것이다. 잔기 N297에서 글리코 실화는 잔기 Q295에서 트랜스 글루타미나제를 방해할 수 있다(Dennler et al., supra) 따라서, 유리한 실시양태에서, 항체는 글리코 실화되지 않는다. 특정 실시양태에서, 항체는 탈당화 또는 당화 된다. 특정 실시양태에서, 항체 중쇄는 N297돌연변이를 갖는다. 대안적으로, 항체는 더 이상 위치 297에 아스파라긴잔기를 갖지 않도록돌연변이된다. 특정 실시양태에서, 항체 중쇄는 N297Q돌연변이를 갖는다. 이러한 항체는 글리코 실화 서열을 제거 또는 비활성화하기 위해 부위 지향적 돌연변이 유발에 의해, 또는 임의의 간섭 글리코 실화 부위 또는 임의의 다른 간섭구조로부터 분리된 부위에 글루타민 잔기를 삽입하기 위해 부위 지향적 돌연변이 유발에 의해 제조될 수 있다. 이러한 항체는 또한 천연 또는 인공 공급원으로부터 단리될 수 있다.
이어서 글리코실화를 방해하지 않는 항체를 1차 아민 화합물로 처리한다. 특정 실시양태에서, 당화 항체는 1차 아민 화합물로 처리되어 글루타미닐-개질된 항체를 생성한다. 특정 실시양태에서, 탈당화된 항체는 1차 아민 화합물과 반응하여 글루타미닐-개질된 항체를 생성한다.
1차 아민은 트랜스 글루타미나아제의 존재 하에 글루타민 잔기와 공유결합을 형성할 수 있는 임의의 1차 아민일 수 있다. 유용한 1차 아민이 본원에 기재되어 있다. 트랜스 글루타미나제는 당업자에게 적합한 것으로 여겨지는 임의의 트랜스 글루타미나제일 수 있다. 특정 실시양태에서, 트랜스 글루타미나제는 1차 아민 화합물상의 유리 아민기 및 글루타민 잔기의 측쇄상의 아실기 사이에 이소 펩티드 결합의 형성을 촉매하는 효소이다. 트랜스 글루타미나제는 단백질-글루타민-γ-글루타민트랜스퍼라제로도알려져 있다.
특정 실시양태에서, 트랜스 글루타미나제는 EC 2.3.2.13으로 분류된다. 트랜스 글루타미나제는 적합한 것으로 여겨지는 임의의 공급원으로부터 유래될 수 있다. 특정 실시양태에서, 트랜스 글루타미나제는 미생물이다. 유용한 트랜스 글루타미나제는 스트렙토 마이세스모바라센스(Streptomyces mobaraense),스트렙토 마이세스신나모네움(Streptomyces cinnamoneum), 스트렙토마이세스그리세오카르네움(Streptomyces griseo-carneum), 스트렙토마이세스 라벤둘레(Streptomyces lavendulae), 및 바실러스 서브틸리스(Bacillus subtilis)로부터 단리되었다. 포유 동물 트랜스 글루타미나제를 포함하는 비미생물 트랜스글루타미나제는 또한 사용될 수 있다. 특정 실시양태에서, 트랜스 글루타미나제는 임의의 기술에 의해 제조되거나 당업자에 의해 적합한 것으로 여겨지는 임의의 공급원으로부터 수득될 수 있다. 특정 실시양태에서, 트랜스 글루타미나제는 상업적 공급원으로부터 수득된다.
특정 실시양태에서, 1차 아민 화합물은 트랜스 글루타미네이션 후 추가 반응이 가능한 반응성 그룹을 포함한다. 이들 실시양태에서, 글루타미닐-개질된 항체는 반은성 페이로드 화합물 또는 반응성 링커-페이로드 화합물과 반응 또는 처리되어 항체-페이로드 접합제를 형성할 수 있다. 특정 실시양태에서, 1차 아민 화합물은 본 우너에 기재된 바와 같은 아지들르 포함한다.
특정 실시양태에서, 글루타미닐-개질된 항체는 반응성 링커-페이로드와 반응 또는 처리되어 항체-페이로드 접합제를 형성한다. 반응은 당업자에게 적합한 것으로 간주되는 조건 하에서 진행될 수 있다. 특정 실시양태에서, 글루타미닐-변형된 항체는 글루타미닐―변형된 항체와 링커-페이로드 화합물 사이의 결합을 형성하기에 적합한 조건 하에서 반응성 링커-페이로드 화합물과 접촉된다. 접합한 반응 조건은 당업자에게 잘 알려져있다.
이러한 반응의 예는 하기 실시예에서 제공된다.
일부 예에서, 커플링 조건 하에서 화합물을 결합제와 처리 또는 접촉시키는 단계를 포함하는 접합제의 제조방법이 본 원에 제시되며, 여기서 화합물은 하나 이상의 페이로드 부분에 결합되고 공유 링커를 통해 하나 이상의 시클로덱스트린 부분에 연결된 반응성 링커를 포함하고, 여기서 상기 공유 링커는 각각의 반응성 링커, 페이로드 부분, 시클로 덱스트린 부분에 직접 또는 간접적으로 결합된다. 일부 예에서, 결합제와 반응하는 화합물은 화학식 화학식 (VI)에 따른 화합물이다:
(VI)
또는 그의 제약상 허용되는 염, 용매화물, 입체 이성질체 또는 그의 유도체, 여기서 RG' 는 반응성 그룹 이고; L은 3가 링커이고; HL은 친수성 잔기이고 PA는 페이로드 잔기이다.
일부 예에서, 화학식(II)의 화합물과 반응하는 결합제는 항체 또는 이의 항원 결합 단편이다.
일부 예에서, 본 원의 D-Lys는 도 20에 제시된 시약으로 대체될 수 있다.
일부 예에서, 시클로 덱스트린-함유 부분은[3+2]클릭 반응, 딜스-알더 반응, 환원성 아민화, 광 클릭 반응 또는 다른 반응으로부터 선택된 생물 직교 반응에서 반응할 수 있다.
본 원의 방법과 함께 사용하기에 적합한 다른 유용한 생체 직교 반응은 슈타우딩거(Staudinger)결찰, 클릭 반응, 테트라진 결찰 및 광-클릭 반응을 포함하지만, 이에 제한되지는 않는다.
하기 참고 문헌은 본 원에 제시된 생체 직교 반응과 함께 사용될 수 있는 예시적인 반응 및 시약을 보여준다: Zheng, Mengmeng, et al., Molecules 2015, 20, 3190-3205, 그 내용은 모든 목적을 위해 그 전문이 본 원에 참조로 포함됨.
약제학적 조성물 및 치료방법
치료적 또는 예방적 유효랑의 본 원에 개시된 하나 이상의 화합물, 예를 들어 본 원에 제공된 화학식의 화합물 중 하나 이상을 투여하는 것을 포함하는 질환, 병태 또는 장애의 치료 및 예방 방법이 본 원에 제공된다. 당업자는 질환, 장애 및/또는 병태가 본 원에 열거된 항원과 관련된 것들을 포함하나 이에 제한되지 않는 다는 것을 이해할 것이다.
본 원에 기재된 화합물은 단독으로 또는 하나 이상의 추가 치료제와 함께 투여될 수 있다. 하나 이상의 추가의 치료제는 본 원에 기재된 화합물의 투여 직전, 병행 또는 직후에 투여될 수 있다. 본 개시 내용은 또한 하나 이상의 추가 치료제와 조합하여 본 원에 기재된 임의의 화합물을 포함하는 제약 조성물, 및 이러한 조합물을 이를 필요로하는 대상체에게 투여하는 것을 포함하는 치료방법을 포함한다.
적합한 추가 치료제는 제2글루코코르티코이드, 자가 면역 치료제, 호르몬, 생물학적 제제 또는 단일클론 항체를 포함하지만, 이에 제한되지는 않는다. 적합한 치료제는 또한 본 원에 제시된 임의의 약학적으로 허용 가능한 염, 산 또는 유도체를 포함하지만 이에 제한되지는 않는다.
본 원에 기재된 방법의 일부 실시양태에서, 본 원에 기재된 화합물(또는 본 원에 기재된 화합물 및 본 원에 언급된 임의의 추가의 치료제의 조합을 포함하는 제약 조성물)의 다중 용량은 정의된 시간 경과에 걸쳐 대상체에게 투여될 수 있다. 본 개시 내용의 이러한 측면에 따른 방법은 대상체에게 다중 용량의 본 원에 기재된 화합물을 순차적으로 투여하는 것을 포함한다. 본 원에 사용된 "순차 투여"는 화합물의 각 용량이 상이한 시점에서, 예를 들어, 미리 결정된 간격(예를 들어, 시간, 일, 주 또는 월)으로 분리된 다른날에 대상에 투여됨을 의미한다. 본 개시 내용은 환자에게 단일 초기 용량의 본원에 기재된 화합물, 이어서 하나 이상의 이차 용량의 화합물, 및 선택적으로 하나 이상의 삼차 용량의 화합물을 순차적으로 투여하는 것을 포함하는 방법을 포함한다.
용어 "초기 용량(initial dose)", "2차 용량(secondary doses)", "3차 용량(tertiary doses)"은 본 원에 기재된 화합물의 일시적 투여 순서를 지칭한다. 따라서, "초기용량"은 치료 요법의 시작시에 투여되는 용량("베이스 라인 용량"으로도 지칭됨); "2차 용량"은 초기 용량 후 투여되는 용량이고; "3차 용량"은 2차 용량 후에 투여되는 용량이다.
초기, 2차 및 3차 용량은 모두 본 원에 기재된 화합물과 동일한 양을 함유할 수 있지만, 일반적으로 투여빈도의 관점에서 서로 상이할 수 있다. 특정 실시양태에서, 초기 2차 및/또는 3차 용량에 함유된 화합물의 양은 치료 과정 동안 서로 상이하다(예를 들어, 적절하게 상향 또는 하향 조정). 특정 실시양태에서, 2개 이상의(예를 들어, 2, 3, 4 또는 5)용량은 치료 요법의 시작시에 "부하 용량(loading doses)"으로서 투여되고, 이어서 덜 빈번하게 투여되는 후속 용량(예를 들어, "유지용량(maintenance doses)")이 투여된다.
본 개시 내용의 특정 예시적인 실시양태에서, 각각의 2차 및/또는 3차 용량은 직전 용량 후1 내지 26(예를 들어, 1, 1½, 2, 2½, 3, 3½, 4, 4½, 5, 5½, 6, 6½, 7, 7½, 8, 8½, 9, 9½, 10, 10½, 11, 11½, 12, 12½, 13, 13½, 14, 14½, 15, 15½, 16, 16½, 17, 17½, 18, 18½, 19, 19½, 20, 20½, 21, 21½, 22, 22½, 23, 23½, 24, 24½, 25, 25½, 26, 26½, 또는 그이상)에 투여된다. 본 원에 사용된 어구 "직접적인 투여 량(the immediately preceding dose),"은 다수의 투여 순서에서, 중간 투여량 없이 서열에서 바로 다음 투여량을 투여하기 전에 환자에게 투여되는 화합물의 투여량을 의미한다.
본 개시 내용의 이러한 측면에 따른 방법은 환자에게 임의의 수의 2차 및/또는 3차 용량의 화합물을 투여하는 것을 포함할 수 있다. 예를 들어, 특정 실시양태에서, 단일 2차 용량만이 환자에게 투여된다. 다른 실시양태에서, 2회 이상의(예를 들어, 2, 3, 4, 5, 6, 7, 8개 이상의)2차 용량이 환자에게 투여된다. 마찬가지로, 특정 실시양태에서, 단일 3차 용량 만이 환자에게 투여된다. 다른 실시양태에서, 둘 이상의(예를 들어, 2, 3, 4, 5, 6, 7, 8 이상) 3차 용량이 환자에게 투여된다. 투여 요법은 특정 대상의 수명 동안 또는 그러한 치료가 더 이상 치료적으로 필요하거나 유리하지 않을때까지 무기한으로 수행될 수 있다.
다수의 이차 용량을 수반하는 실시양태에서, 각각의 이차 용량은 다른 이차 용량과 동일한 빈도로 투여될 수 있다. 예를 들어, 각각의 2차 용량은 직전 용량 후 1 내지 2주 또는 1 내지 2개월에 환자에게 투여될 수 있다. 유사하게, 다수의 3차 용량을 포함하는 실시양태에서, 각각의 3차 용량은 다른 3차 용량과 동일한 빈도로 투여될 수 있다. 예를 들어, 각각의 3차 용량은 직전 용량 후 2 내지 12주에 환자에게 투여될 수 있다. 본 개시 내용의 특정 실시양태에서, 2차 및/또는 3차 용량이 환자에게 투여되는 빈도는 치료 요법의 과정에 따라 달라질 수 있다. 임상시험 후 개별 환자의 필요에 따라 의사가 치료 과정동안 투여 빈도를 조정할 수도 있다.
본 개시 내용은 2내지 6개의 로딩 용량이 제1빈도(예를 들어, 일주일에 한 번, 2주에 한 번, 3주에 한 번, 한 달에 한 번, 두 달에 한 번 등)로, 환자에게 투여된 후, 덜 빈번하게 환자에게 2개 이상의 유지 용량을 투여하는 투여 요법을 포함한다. 예를 들어, 본 개시의 이러한 측면에 다르면, 로딩 용량이 한 달에 한번의 빈도로 투여되는 경우, 유지 용량은 6주마다 한 번씩, 2개월 마다 한 번, 3개월 마다 한 번씩, 등 환자에게 투여될 수 있다.
본 개시 내용은 본 원에 기재된 화합물 및/또는 접합제의 제약 조성물, 예를 들어 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물, 예를 들어, 본 원에 기재된 화합물, 그의 염, 입체 이성질체, 다형체, 및 약제학적으로 허용되는 담체, 희석제 및/또는 부형제를 포함하는 조성물. 적합한 담체, 희석제 및 부형제의 예는 적절한 조성물 pH(예를 들어, 시트레이트 완충제, 숙시네이트 완충제, 아세테이트 완충제, 포스페이트 완충제, 락테이트 완충제, 옥살레이트 완충제 등), 담체 단백질(예르 들어, 인간 혈청 알부민), 식염수, 폴리올(예를 들어, 트레할로스, 수크로스, 자일리톨, 소르비톨 등), 계면활성제(예를 들어, 폴리소르베이트 20, 폴리소르베이트 80, 폴리옥소레이트 등), 항균제 및 항산화제의 유지를 위한 완충제를 포함하지만, 이에 제한되지는 않는다.
일부 예에서, 치료적 유효량의 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물 또는 그의 제약 조성물을 상기 장애를 갖는 환자에게 투여하는 단계를 포함하는 질환, 장애 또는 병태의 치료 방법이 본 원에 제시된다.
일부 예에서, 본 발명은 상기 장애를 갖는 환자에게 예방 유효량의 화학식 (I), 화학식 (II), 화학식 (III), 화학식 (IV), 화학식 (IVa), 화학식 (IVb), 화학식 (IVc), 화학식 (Va), 화학식 (Vb), 화학식 (Vc), 또는 화학식 (Vd)의 화합물 또는 그의 제약 조성물을 투여하는 단계를 포함하는 질환, 장애 또는 상태를 예방하는 방법을 제공한다.
일부 예에서, 본 원에서 증식성 장애, 신경 퇴행성 장애, 면역 학적 장애, 자가 면역 질환, 염증성 장애, 피부병, 신진 대사 질환, 심혈관 질환 및 위장질환으로 이루어진 군으로부터 선택된 질환, 장애 또는 상태를 치료 또는 예방하는 방법이 본 원에 기재된다.
상기 세포를 항체 약물 접합제 (ADC)와 접촉시키는 단계를 포함하는 세포에서 LDLR(저밀도 지단백질 수용체) 단백질 발현 또는 콜레스테롤 유출을 조절하는 방법이 본 원에 제공되며, 여기서 ADC는 상기 세포, 친수성 잔기 및 LXR작용제를 표적으로 하는 항체를 포함한다.
증식성 장애는 당업자에게 공지된 임의의 증식성 장애일 수 있다. 특정 실시양태에서, 증식성 장애에는 종양학 장애가 포함되나, 종양학 장애는 당업자에게 공지된 임의의 암 장애 일 수 있다. 특정 실시양태에서, 흑색 종을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 전이성 흑색 종을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 폐암을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, EGFR-티로신키나제 억제제 내성 폐암의 치료 또는 예방 방법이 본 원에 제공된다. 특정 실시양태에서, 구강암을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 구강편평 세포 암종을 치료 또는 예방하는 방법이 본 운에 제공된다. 특정 실시양태에서, 전립선 암의 치료 또는 예방 방법이 본 원에 제공된다. 특정 실시양태에서, 호지킨 림프종을 치료또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 유방암을 치료 또는 예방하는 방법이 분 원에 제공된다.
신경퇴행성 장애는 당업자에게 공지된 임의의 신경 퇴행서 장애일 수 있다. 특정 실시양태에서, 알츠하이머 병을 치료 또는 예방 하는 방법이 본 원에 제공된다. 특정 실시양태에서, 파킨슨병을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 헌팅턴병을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 근 위축성 측삭 경화증을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 미엘린 유전자 발현을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 골수화 및 재수초화 상태, 질환 또는 장애를 치료 또는 예방하는 방법이 본 원에 제공된다.
면역 장애는 당업자에게 공지된 임의의 면역 장애 일수 있다. 특정 실시양태에서, 염증성 장 질환을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 궤양성 대장염을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 크론병을 치료 또는 예방하는 방법이 본 원에 제공된다.
염증성 장애는 당업자에게 공지된 임의의 염증성 장애일 수 있다. 특정 실시양태에서, 관절염을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 류마티스 관절염을 치료 또는 예방하는 방법이 본 원에 제공된다.
대사 질환은 당업자에게 공지된 임의의 대사 질환일 수 있다. 특정 실시양태에서, 이상 지질 혈증은 고지혈증, 고콜레스테롤 혈증, 고트리글리세라이드혈증, 고지단백질 혈증, HDL결핍, ApoA-1결핍 및 관상 동맥 질환(예를 들어, 협심증의 치료 및 예방, 심근경색 및 갑작스런 심장 사멸을 포함)과 같은 심혈관 질환; 죽상 동맥 경화증(예를 들어, 죽상 동맥 경화증의 치료 및 예방 포함); 및 재협착(예를 들어, 풍선 혈관 성형술과 같은 의학적 절차의 결과로 발생하는 죽상 경화성 플라크에 예방 또는 치료 포함)으로 이루어진 군으로부터 선택된다. 특정 실시양태에서, 당뇨병을 치료 또는 예방하는 방법이 본 원에 제공된다.
심혈관 질환은 당업자에게 공지된 임의의 심혈관 질환일 수 있다. 특정 실시양태에서, 죽상 동맥 결환증을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 비정상 대식세포 처리로부터 유래된 죽상 동맥 경화증을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 마이크로파지가 oxLDL을 처리하지 못하는 산화된 저밀도 지단백질(oxLDL)의 형성으로부터 유도된 죽상 동맥 경화증을 치료 또는 예방하는 방법이 본원에 제공된다. 특정 실시양태에서, 허혈성 심장 질환을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 뇌졸중을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 고혈압성 심장 질환을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 대동맥 동맥류의 치료 또는 예방 방법이 본 원에 제공된다. 특정 실시양태에서, 심내막염을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 말초 동맥 질환을 치료 또는 예방하는 방법이 본 원에 제공된다. 특정 실시양태에서, 본 단락에 제공된 임의의 질환의 치료 또는 예방 방법이 본 원에 제공된다.
일부 예에서, 핵 수용체의 기능을 조절하는 방법이 본 원에 개시된다. 비 제한적인 예로서, 기능은 염증 매개체(예를들어, 사이토 카인, 케모카인)의 발현/분비, 콜레스테롤 조절, 콜레스테롤 섭취, 콜레스테롤 유출, 콜레스테롤 산화, 이동, 화학 주성, 아포토시스 및 괴사, 염증 활성, 지질 조절, 아포토시스, 이동, 화학주성, 유전자 전사 및 단백질 발현으로부터 선택될 수 있다.
일부 예에서, 본 원에 제시된 화합물 또는 약제 학적 조성물을 환자에게 투여하는 것을 포함하는, 필요로하는 환자에서 질환 또는 장애를 치료하는 방법이 본 원에 제시된다. 일부 예에서, 투여된 화합물은 본 원에 제시된 항체-약물 접합제다.
일부 예에서, 결합제와 화합물 사이의 결합을 형성하기에 적합한 조건 하에서 결합제를 링커-페이로드 화합물과 접촉시키는 단계를 포함하는 항체-약물 접합제의 방법이 본 원에 제시된다.
일부 예에서, 본 원에 기재된 유효 치료량의 화합물 또는 제약 조성물을 대상체에게 투여하는 것을 포함하는, 대상체에서 즉식성 질환, 대사성 질환, 염증 또는 신경 퇴행성 질환을 치료하는 방법이 본 원에 기재된다. 일부 예에서, 투여된 화합물은 본 원에 제시된 항체-약물 접합제다.
일부 예에서, 본 원에 제시된 유효 처리량의 화합물 또는 약제학적 조성물을 대상체에게 투여하는 것을 포함하는, 대상체에서 질환, 장애 또는 병태를 치료하는 방법이 본 원에 제시된다. 일부 예에서, 투여된 화합물은 본 원에 제시된 항체-약물 접합제다.
일부 예에서, 본 원에 제시된 유효 치료량의 화합물 또는 약제학적 조성물을 대상에게 투여하는 것을 포함하는, 대상체에서 증식성 질환을 치료하는 방법이 본 원에 제시된다. 일부 예에서, 투여 된 화합물은 본 원에 제시된 항체-약물 접합제다.
일부 예에서, 본 원에 제시된 유효 치료량의 화합물 또는 약제학적 조성물을 대상체에게 투여하는 것을 포함하는, 대상체에서 대사성 질환을 치료하는 방법이 본 원에 제시된다. 일부 예에서, 투여된 화합물은 본 원에 제시된 항체-약물 접합제다.
일부 예에서, 본 원에 제시된 유효 처리량의 화합물은 본 원에 제시된 유효 처리량의 화합물 또는 약제학적 조성물을 대상체에게 투여하는 것을 포함하는, 대상체에서 대상성 질환을 치료하는 방법이 본 원에 제시된다. 일부 예에서, 투여된 화합물은 본 원에 제시된 항체-약물 접합제다.
일부 예에서, 본 원에 제시된 유효 처리량의 화합물 또는 약제학적 조성물을 대상체에게 투여 함을 포함하여, 대상체에서 신경 퇴행성 질환을 치료하는 방법이 본 원에 제시된다.
도 1은 3가지 상이한 유형의 페이로드 화합물을 도시한다.
도 2는 화합물 1a, 1c, 1e, 1f, 1i, 1j, 1k, 1m, 1q, Ib, Id, Ie-1, If-1, IIb, IIId, IIIe, 및 IVb를 제조하기 위한 합성 공정을 도시한다.
도 3은 화합물 1h, 1l, Ig, 및 Ih-1을 제조하기 위한 합성 공정을 도시한다.
도 4는 페이로드 B 및 C를 제조하기 위한 합성 공정을 도시한다.
도 5는 페이로드 D를 제조하기 위한 합성 공정을 도시한다.
도 6은 중간체 3a, 3b, 3c, 및 3g를 제조하기 위한 일반적인 합성 절차 A를 도시한다.
도 7은 중간체 3d 및 3f를 제조하기 위한 일반적인 합성 절차를 도시한다.
도 8은 중간체 3e의 제조를 위한 합성 공정을 도시한다.
도 9는 중간체 4a의 제조를 위한 합성 공정을 도시한다.
도 10은 중간체 4b의 제조를 위한 합성 공정을 도시한다.
도 11은 중간체 5a-g의 제조를 위한 합성 공정을 도시한다.
도 11A는 중간체 10a의 제조를 위한 합성 공정을 도시한다.
도 11B는 중간체 10b의 제조를 위한 합성 공정을 도시한다.
도 11C는 중간체 10a, 10b, 10c 및 10d의 제조를 위한 합성 공정을 도시한다.
도 12는 중간체 6c의 제조를 위한 합성 공정을 도시한다.
도 13은 중간체 6d의 제조를 위한 합성 공정을 도시한다.
도 13A는 중간체 6b의 제조를 위한 합성 공정을 도시한다.
도 14는 중간체 7a, 7c, 7e, 7f, 7i, 7k, 7m, 7q, 7ab, 7ad, 7ae, 7bb, 7cb, 및 7fb를 제조하기 위한 일반적인 합성 절차를 보여준다.
도 15는 중간체 7h 및 7I의 제조를 위한 합성 공정을 도시한다.
도 15A는 중간체 7ah 을 제조하기 위한 일반적인 합성 절차를 보여준다.
도 15B는 중간체 8c를 제조하기 위한 합성 절차를 도시한다.
도 16은 중간체 1a를 제조하기 위한 일반적인 합성 절차G를 도시한다.
도 17은 중간체 1a, 1c, 1e, 1f, 1h, 1i, 1j, 1k, 1l, 1m, 1q, Ib, Id, If-1, IIb, IIId, IIIe, 및 IVb를 제조하기 위한 일반적인 합성 절차H를 도시한다.
도 18은 자유 페이로드를 방출하기 위한 링커-페이로드 카텝신 B(cathepsin B) 절단을 위한 절단 가능한 조각을 도시한다.
도 18A는 lg 및 lh-1을 제조하기 위한 합성 절차를 도시한다.
도 18B는 자유 페이로드를 방출하기 위한 링커-페이로드의 카텝신 B 절단을 위한 절단 가능한 조각을 도시한다.
도 19는 항체 약물 접합을 위한 일반적인 합성 절차의 예를 도시한다.
도 20은 본원에 제시된 방법에서 d-Lys대신에 사용될 수 있는 시약을 도시한다.
도 2는 화합물 1a, 1c, 1e, 1f, 1i, 1j, 1k, 1m, 1q, Ib, Id, Ie-1, If-1, IIb, IIId, IIIe, 및 IVb를 제조하기 위한 합성 공정을 도시한다.
도 3은 화합물 1h, 1l, Ig, 및 Ih-1을 제조하기 위한 합성 공정을 도시한다.
도 4는 페이로드 B 및 C를 제조하기 위한 합성 공정을 도시한다.
도 5는 페이로드 D를 제조하기 위한 합성 공정을 도시한다.
도 6은 중간체 3a, 3b, 3c, 및 3g를 제조하기 위한 일반적인 합성 절차 A를 도시한다.
도 7은 중간체 3d 및 3f를 제조하기 위한 일반적인 합성 절차를 도시한다.
도 8은 중간체 3e의 제조를 위한 합성 공정을 도시한다.
도 9는 중간체 4a의 제조를 위한 합성 공정을 도시한다.
도 10은 중간체 4b의 제조를 위한 합성 공정을 도시한다.
도 11은 중간체 5a-g의 제조를 위한 합성 공정을 도시한다.
도 11A는 중간체 10a의 제조를 위한 합성 공정을 도시한다.
도 11B는 중간체 10b의 제조를 위한 합성 공정을 도시한다.
도 11C는 중간체 10a, 10b, 10c 및 10d의 제조를 위한 합성 공정을 도시한다.
도 12는 중간체 6c의 제조를 위한 합성 공정을 도시한다.
도 13은 중간체 6d의 제조를 위한 합성 공정을 도시한다.
도 13A는 중간체 6b의 제조를 위한 합성 공정을 도시한다.
도 14는 중간체 7a, 7c, 7e, 7f, 7i, 7k, 7m, 7q, 7ab, 7ad, 7ae, 7bb, 7cb, 및 7fb를 제조하기 위한 일반적인 합성 절차를 보여준다.
도 15는 중간체 7h 및 7I의 제조를 위한 합성 공정을 도시한다.
도 15A는 중간체 7ah 을 제조하기 위한 일반적인 합성 절차를 보여준다.
도 15B는 중간체 8c를 제조하기 위한 합성 절차를 도시한다.
도 16은 중간체 1a를 제조하기 위한 일반적인 합성 절차G를 도시한다.
도 17은 중간체 1a, 1c, 1e, 1f, 1h, 1i, 1j, 1k, 1l, 1m, 1q, Ib, Id, If-1, IIb, IIId, IIIe, 및 IVb를 제조하기 위한 일반적인 합성 절차H를 도시한다.
도 18은 자유 페이로드를 방출하기 위한 링커-페이로드 카텝신 B(cathepsin B) 절단을 위한 절단 가능한 조각을 도시한다.
도 18A는 lg 및 lh-1을 제조하기 위한 합성 절차를 도시한다.
도 18B는 자유 페이로드를 방출하기 위한 링커-페이로드의 카텝신 B 절단을 위한 절단 가능한 조각을 도시한다.
도 19는 항체 약물 접합을 위한 일반적인 합성 절차의 예를 도시한다.
도 20은 본원에 제시된 방법에서 d-Lys대신에 사용될 수 있는 시약을 도시한다.
실시예
달리 명시되지 않는 한, 시너팜 화학 시약 주식회사(SCRC), 시그마-알드리치, 알파 또는 다른 공급 업체와 같은 상업적 공급원으로부터 시약 및 용매를 수득하였다.
1H NMR 및 다른 NMR 스펙트럼은 Bruker AVIII 400 또는 Bruker AVIII 500에서 기록되었다. 데이터는 Nuts 소프트웨어 또는 MestReNova 소프트웨어로 처리하여 내부 표준 테트라 메틸 실란(TMS)에서 백만 분의 일(ppm) 다운 필드로 양자 이동을 측정했다.
HPLC-MS 측정은 하기 조건을 사용하여 Agilent 1200 HPLC/6100 SQ시스템에서 수행하였다:
이동상으로서 HPLC-MS 측정을 위한 방법 A: 물(0.01% 트리플루오로아세트산(TFA)), B:아세토니트릴(0.01% TFA); 구배단계: 15분(min) 내에 B의 5%가 B의 95%로 증가함; 유속: 1.0Ml/min; 칼럼: SunFire C18, 4.6x50 mm, 3.5 μm; 칼럼 온도: 50℃. 검출기: Analog to Digital Converter (ADC) 증발 광 산란 검출기(ELSD), 다이오드 어레이 검출기(DAD) (214 nm and 254 nm), 전기 분무 이온화 대기 이온화(ES-API).
HPLC-MS측정을 위한 방법 B는 이동상으로서:A : 물(10 mM NH4HCO3), B : 아세토니트릴; 구배상: 15분 내에 B의 5% 내지 95%; 유속:1.0 mL/min; 칼럼: XBridge C18, 4.6x50 mm, 3.5 μm; 칼럼 온도: 50 ℃. Detectors: ADC ELSD, DAD (214 nm 및 254 nm), mass selective detector (MSD) (ES-API).
LC-MS 측정을 다음 조건을 사용하여 Agilent 1200 HPLC/6100 SQ 시스템에서 수행하였다:
LC-MS 측정을 위한 방법 A는 기기로서 물 2767; 칼럼: Shimadzu Shim-Pack, PRC-ODS, 20x250mm, 15 μm, 2개 직렬 연결; 이동상: A: 물 (0.01% TFA), B: 아세토니트릴 (0.01% TFA); 구배단계: 3분 내에 5% B의 95%로 증가하고; 유량: 1.8 - 2.3 mL/min; 칼럼: SunFire C18, 4.6x50 mm, 3.5 μm; 칼럼 온도: 50 ℃. 검출기: ADC ELSD, DAD (214 nm and 254 nm), ES-API.
LC-MS측정을 위한 방법 B는 기기로서: Gilson GX-281; 칼럼: Xbridge Prep C18 10 μm OBD, 19x250 mm; 이동상: A: 물 (10 mM NH4HCO3), B: 아세토니트릴; 구배상: 3분 내에 B의 5% 내지 95%; 유량: 1.8 - 2.3 mL/min; 칼럼: XBridge C18, 4.6x50 mm, 3.5 μm; 칼럼 온도: 50 ℃. 검출기: ADC ELSD, DAD (214 nm and 254 nm), MSD (ES-API).
산성(방법A) 또는 염기성(방법B) 용매 시스템에서 제조용 고압 액체 크로마토그래피(Prep-HPLC)를 Gilson GX-281기기에서 사용하였다. 산성 용매 시스템은 Waters SunFire 10 μm C18 column (100Å, 250x19 mm) 을 사용하였고, Prep-HPLC를 위한 용매 A는 물/0.05% TFA이고 용매 B는 아세토니트릴이었다. 용리조건은 30 mL/min의 유속에서 20분의 시간에 걸쳐 용매B의 선형 구배 증가가 5%에서 100%로 증가하였다. 기본 용매 시스템은 Waters Xbridge 10 μm C18 컬럼 (100Å, 250x19 mm)을 포함하고, 및 예비-HPLC에 사용된 용매 A는 물/10 mM 중탄산 암모늄 (NH4HCO3)이고 용매 B는 아세토니트릴이었다. 용리 조건은 30 mL/min의 유속에서 20분의 시간에 걸쳐 용매 B의 선형 구배 증가가 5%에서 100%로 증가 하였다.
플래시 크로마토그래피는 Agela Flash Column silica-CS 카트리지를 사용하여 Biotage기기에서 수행되었으며; 역상 플래쉬 크로마토 그래피는 보스턴 ODS 또는 Agela C18 카트리지와 함께 Bioatage 기기에서 수행되었다.
분석적 키랄 HPLC방법-SFC조건
기기: SFC방법 스테이션(Thar, Waters)
칼럼: CHIRALPAK AD-H/AS-H/OJ-H/OD-H 4.6Х100mm, 5 μm (Daicel)
칼럼 온도: 40 ℃
이동상: CO2/ IPA(0.1% DEA)= 55/45
유량: 4.0 ml/min
배압: 120 Bar
주입량: 2 μL
제조용 키랄 HPLC 방법 - SFC 조건
기기: SFC-80 (Thar, Waters)
칼럼: CHIRALPAK AD-H/AS-H/OJ-H/OD-H 20Х250mm, 10 μm (Daicel)
칼럼온도: 35 ℃
이동상: CO2/ IPA(0.2% Methanol Ammonia)= 30/70
유량: 80 g/min
배압: 100 bar
검출 파장: 214 nm
사이클 시간: 6.0 min
샘플 용액: 1500 mg dissolved in 70 mL Methanol
주입 부피: 2 mL (loading: 42.86 mg/injection)
본 원에 사용된 바와 같이, 특정 약어가 구체적으로 정의되는지 여부에 관계없이 이들 과정, 계획 및 예에서 사용된 기호 및 관례는 현대 과학 문헌, 예를 들어 Journal of the American에 사용된 것과 일치한다. 화학 학회 또는 생물학 화학 저널. 구체적으로, 비 제한적으로, 하기 약어가 실시예 및 명세서 전체에서 사용될 수 있다.
구체적으로, 비 제한적으로, 하기 약어가 실시예 및 명세서 전체에서 사용될 수 있다:
구체적으로, 비 제한적으로, 하기 약어가 실시예 및 명세서 전체에서 사용될 수 있다:
준비방법
표 1
페이로드 목록
표 2
유료링커페이로드 목록
실시예 1
링커페이로드의 일반적인 준비 (도 2 참조)
페이로드 AD를 갖는 Fmoc-vcPAB-PNP (2a), Fmoc-Val-Ala-OH (2b) 및 Fmoc-Val-Cit-OH (2c)로부터 출발하는 링커-페이로드1(1h 및 1l 제외)의 합성 카바메이트(3a-g)를 제공하였다. 아미드 (5a-h)는 Fmoc-D-Lys-COT (4a)로 3a-f로부터 합성되었다. 5a-f를 아지드(6a-d)로 고리화하여 7을 제공하였다. 최종적으로 7은 산 8a 또는 그의 활성 에스테르 8b와 반응하여 링커-페이로드 1(1h 및 1l 제외)을 제공하였다.
링커 페이로드 I, II, III 및 IV (Ig-1, Ih-1, 1h 및 1l 제외)의 합성은 AD를 갖는 Fmoc-vcPAB-PNP (2a), Fmoc-Val-Ala-OH (2b) 및 Fmoc-Val-Cit-OH (2c) 로부터 시작되었다. 페이로드A-E와 함께 카바메이트(3a-g)를 제공하였다. 아미드(5a-g)를 Fmoc-D-Lys-COT (4a)로부터 합성 하였다. 5a-g 를 아지드(6a-d)로 고리화하여 7을 제공하였다. 최종적으로 7은 산 8a 또는 그의 활성 에스테르 8b-e와 반응하여 링커-페이로드 I, II, III 및 IV (Ig-1, Ih-1, 1h 및 1l 제외)를 제공하였다.
실시예 2
탑재량 1h 및 1l의 준비( 도 3 참고)
링커-페이로드 1h 및 1l의 합성은 EDCI의 축합 조건하에 Fmoc-dGlu-taurine (4b)으로 3b 및 3e에서 시작하여 de-Fmoc 반응 및 최종적으로 활성 에스테르 8b로 아미드화 되었다.
링커-페이로드 1h 및 1l의 합성은 Fmoc-dGlu-taurine (4b)과 3b 및 3e의 축합으로부터 개별적으로 시작된 후, Fmoc를 제거하는 반응 및 최종적으로 활성에스테르 8b로 아미드화 되었다.
링커-페이로드 lg-1 및 lh-1의 합성은 3a의 Fmoc-dGlu-acetal glucamide (4c)와의 아미드 커플링 반응에 이어서 8e와의 축합, 및 최종적으로 TFA에 의한 탈 보호 및 이어서 8b와의 응축 으로부터 시작되었다.
실시예 3
링커 페이로드 B 및 C의 준비(도 4 참조)
상업적인 플루오로시놀론 아세토 나이드 9(CAS: 67-73-2)에서 출발하여 4에 따라 제조하였다. 과염소산의 존재 하에 부티르알데히드로 케탈-교환에 의해 9로부터 수득된 화합물 10을 메실레이트 11로 전환한 다음, 메실레이트기를 아지드 잔기로 대체하여 아민 B로 추가로 환원된 12를 형성하였다. 그렇지 않으면, 11의 메실레이트 잔기 4-아미노-페놀로 대체하여 아닐린C를 수득 하였다.
(1S,2S,4R,8S,9S,11S,12R,13S,19S)-12,19-디플로로-11-하이드록시-8-(2-하이드록시아세틸)-9,13-디메틸-6-propyl-5,7-디옥사펜타시클로[10.8.0.02,9.0⁴,8.013.18]이코사-14,17-디엔-16-온 (10)((1S,2S,4R,8S,9S,11S,12R,13S,19S)-12,19-Difluoro-11-hydroxy-8-(2-hydroxyacetyl)-9,13-dimethyl-6-propyl-5,7-dioxapentacyclo[10.8.0.02,9.0⁴,8.013.18]icosa-14,17-dien-16-one (10))
헵탄(90mL)중 플루오로놀론아세토나이드(9, 0.90 g, 2.0 mmol) 및 실리카겔(18g)의 혼합물에 10℃에서 부티르알데히드(0.27 mL, 3.0 mmol)를 첨가하고 현탁액을 10-20℃에서 10분 동안 교반하였다. 혼합물에 과염소산(70%, 0.68 mL, 8.3 mmol)을 0℃에서 적가하였다. 이어서, 반응 혼합물을 10-20℃에서 밤새 교반하였다. 대부분의 플루오로놀론아세토나이드 9는 TLC 및 LCMS에 따라 소비되었다. 반응 혼합물을 석유 에테르로 희석하고 sat. aq. Na2CO3로 켄칭하였다. 현탁액을 여과하고 고체를 DCM/메탄올(v/v = 1)로 세척하였다. 합한 여액을 진공에서 농축시켰다. 잔류물을 실리카겔상에서 플래쉬 크로마토그래피(석유 에테르 중 0-100% 에틸 아세테이트)로 정제하여 화합물10 (0.15 g, 16% 수율) 을 백색 고체로서 수득하였다. ESI m/z: 467.1 (M + H)+.
2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0²
,9
.0
4,8
.0
13,18
]이코사-14,17-디엔-8-일]-2-옥소에틸 메탄설포네이트 (11)(2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-Difluoro-11-hydroxy-9,13-dimethyl-16-oxo-6-propyl-5,7-dioxapentacyclo[10.8.0.0²
,9
.0
4,8
.0
13,18
]icosa-14,17-dien-8-yl]-2-oxoethyl methanesulfonate (11))
DCM(3mL)중 화합물 10 (0.28 g, 0.65 mmol) 및 트리에틸아민(0.13 g, 1.3 mmol)의 용액에 메탄 설포닐클로라이드(89mg, 0.78mmol)를 0℃에서 첨가하였다. 0℃에서 0.5시간동안 교반한 후, 반응 혼합물을 DCM(20mL)으로 희석하였다. 혼합물을 H2O (20 mLХ2)로 세척하고, 무수 Na2SO4로 건조하고, 여과하고 진공에서 농축했다. 잔류물을 실리카겔의 실리카겔 컬럼 크로마토그래피(석유에테르 0-50% 에틸 아세테이트)로 정제하여 화합물 11 (0.26 g, >99% 수율)을 백색 고체로서 수득하였다. ESI m/z: 545 (M + H)+.
(1S,2S,4R,8S,9S,11S,12R,13S,19S)-8-(2-아지도아세틸)-12,19-디플로로-11-하이드록시-9,13-디메틸-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-16-온 (12)
아세톤(15mL) 중 화합물 11 (1.0 g, 1.8 mmol) 및 소듐아지드(1.2 g, 18 mmol)의 현탁액을 50℃에서 밤새 교반하였다. 혼합물을 실온으로 냉각시키고 물 (80mL)에 부었다. 수성 혼합물을 에틸 아세테이트(50mLx3)로 추출하였다. 합한 유기층을 염수 (30 mL)로 세척하고, 무수 Na2SO4상에서 건조시키고, 여과하고 진공에서 농축하여 조 화합물 12 (0.90 g, > 99% 수율)를 황색 고체로서 수득하고, 이를 다음 단계에 사용하지 않고 사용하였다: 추가정제. ESI m/z: 492 (M + H)+.
(1S,2S,4R,6R,8S,9S,11S,12R,13S,19S)-8-(2-아미노아세틸)-12,19-디플로로-11-하이드록시-9,13-디메틸-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-16-온; 트리플루오로아세트산 염 (화합물 B)
THF(20mL)중 화합물 12 (0.85 g, 1.7 mmol)의 용액에 수용액 히드로 클로라이드(1N, 10mL)첨하 하였다. 혼합물이 투명해질 때까지 28-32℃에서 교반한 후, 혼합물에 트리페닐 포스핀(0.68 g, 2.6 mmol)을 첨가하였다. 생성된 황색 투명 용액을 실온에서 18시간 동안 교반하였다. 혼합물을 진공에서 농축시키고 잔류 물을 역상 플래쉬 크로마토그래피(수성중 0-50% 아세토니트릴)로 정제하였다. TFA(0.05%)에 의해 화합물 B(0.56g, 57% 아세토니트릴)로 정제하였다. TFA(0.05%)에 의해 화합물 B(0.56g, 57% 수율, TFA염)를 회백색 고체로서 수득하였다. ESI m/z: 466 (M + H)+. 1H NMR (400 MHz, MeOD d4 ) δ 7.33 (d, J = 9.9 Hz, 1H), 6.40-6.29 (m, 2H), 5.69-5.45 (m, 1H), 4.93-4.92 (m, 1H), 4.71 (t, J = 4.3 Hz, 1H), 4.35-4.27 (m, 2H), 3.90-3.84 (m, 1H), 2.81-2.54 (m, 1H), 2.42-2.06 (m, 3H), 1.82-1.32 (m, 11H), 1.09-0.87 (m, 6H) ppm. 19F NMR (376 MHz, CD3OD) δ -77.01, -166.24, -166.92, -188.81, -188.83 ppm. Anal. HPLC: 100%, 체류시간: 6.86 min (method A).
페이로드 C
(1S,2S,4R,8S,9S,11S,12R,13S,19S)-8-[2-(4-아미노페녹시)아세틸]-12,19-디플로로-11-하이드록시-9,13-디메틸-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-16-온 (C)
아세톤(0.5mL)중 화합물 11 (93 mg, 0.17 mmol) 4-아미노페놀(4-aminophenol) (37 mg, 0.34 mmol) 및 탄산세슘(cesium carbonate) (0.11 g, 0.34 mmol)의 혼합물을 2시간 동안 환류시켰다. 혼합물을 실온으로 냉각시키고 H2O (10 Ml)로 희석하였다. 혼합물을 에틸아세테이트(ethyl acetate) (10 mLХ3)로 추출하였다. 합한 유기층을 물(20mL) 및 염소(20mL)로 세척하고, Na2SO4상에서 건조시키고, 여과하고 진공에서 농축시켰다. 잔류물을 예비-HPLC로 정제하여 페이로드 C (6.0 mg, 6.3% 수율)를 백생고체로서 수득하였다. ESI m/z: 298 (M/2 + H)+, 558 (M + H)+ (10%). 1H NMR (500 MHz, MeOD d4 ) δ 7.34 (d, J = 10.0 Hz, 1H), 6.78-6.71 (m, 4H), 6.37-6.33 (m, 2H), 5.63-5.49 (m, 1H), 5.10-4.99 (m, 1H), 4.77-4.63 (m, 2H), 4.33 (d, J = 9.1 Hz, 1H), 2.74-2.57 (m, 1H), 2.39-2.13 (m, 3H), 1.98-1.31 (m, 12H), 1.03-0.93 (m, 6H) ppm. Anal. HPLC: 순도 97.4%, 체류시간: 7.55 min (method B)
실시예 4
페이로드 D의 준비(도 5 참조)
메틸(1S,4aS,10aR)-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르복실레이트 (14)
메탄올 (200mL)및 톨루엔 (600mL)중 포도카르프산(13, 90 g, 0.33 mol)의 용액에 (트리메틸실릴)디아조메탄(헥산 중 2M, 200mL)을 첨가하였다. 반응 혼합물을 실온에서 2시간동안 교반하였다. 이어서, 포도카르프산을 LCMS에 따라 완전히 소모하였다. 휘발 물을 진공에서 제거하고, 잔류물을 석유 에테르(2L)로부터 연화 처리하여 화합물14 (91 g, 96% 수율)를 백색고체로서 수득하였다. ESI m/z: 289 (M + H)+. 1H NMR (400 MHz, DMSO d6 ) δ 8.95 (s, 1H), 6.79 (d, J = 8.2 Hz, 1H), 6.63 (d, J = 2.4 Hz, 1H), 6.48 (dd, J = 8.2, 2.4 Hz, 1H), 3.58 (s, 3H), 2.80-2.55 (m, 2H), 2.20-2.02 (m, 3H), 1.96-1.71 (m, 2H), 1.56-1.45 (m, 2H), 1.27 (t, J = 13.5 Hz, 1H), 1.21 (s, 3H), 1.09 (td, J = 13.5, 4.1 Hz, 1H), 0.91 (s, 3H) ppm.
메틸(1S,4aS,10aR)-6-(벤질옥시)-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르복실레이트 (20)
DMF(100mL)중 화합물 14 (12 g, 40 mmol) 및 탄산세슘(14 g, 44 mmol)의 혼합물을 20-25℃에서 15분 동안 교반하였다. 혼합물에 벤질 브로마이드(7.1 mL, 60 mmol)를 실온에 첨가하였다. 실온에서 4시간 동안 교반한 후, 생성된 혼합물을 냉수에 붓고 에틸 아세테이트로 추출하였다. 합한 유기 용액을 물 및 염수로 세척하고, 황산나트륨으로 건조시키고 진공에서 농축시켰다. 조 생성물을 플래쉬 크로마토그래피(석유 에테르 중 0-10% 에틸아세테이트)로 정제하여 표제 화합물20 (13 g, 89% 수율)을 백색 고체로서 수득하였다. ESI m/z: 379 (M + H)+. 1H NMR (500 MHz, MeOD d4 ) δ 7.60-7.20 (m, 5H), 7.00-6.82 (m, 2H), 6.73 (d, J = 7.1 Hz, 1H), 5.03 (s, 2H), 3.66 (s, 3H), 2.95-2.58 (m, 2H), 2.36-2.10 (m, 3H), 2.10-1.85 (m, 2H), 1.70-1.48 (m, 2H), 1.44-1.21 (m, 4H), 1.15 (t, J = 17.2 Hz, 1H), 1.01 (s, 3H) ppm.
(1S,4aS,10aR)-6-(벤질옥시)-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르복실산 (21)
DMSO(0.19 L) 중 화합물20 (11 g, 29 mmol)및 칼륨 tert-부톡사이드(potassium tert-butoxide) (33 g, 0.29 mol)의 혼합물을 메틸기가 완전히 제거될 때까지 100℃에서 1시간 동안 교반하였다. LCMS 및 TLC에 의해 모니터링 되었다. 25℃로 냉각한 후, 혼합물을 수성 하이드로 클로라이드(1N)로 켄칭하고 에틸 아세테이트로 추출하였다. 합한 유기용액을 염수로 세척하고, 황산나트륨으로 건조시키고 진공에서 농축시켰다. 잔류물을 실리카겔 칼럼크로마토그래피(석유 에테르중 0-24% 에틸아세테이트)로 정제하여 화합물 21 (7.5 g, 71% 수율)을 백색 고체로서 수득하였다. ESI m/z: 365 (M + H)+. 1H NMR (500 MHz, MeOD d4 ) δ 7.42 (d, J = 7.4 Hz, 2H), 7.36 (t, J = 7.5 Hz, 2H), 7.30 (t, J = 7.3 Hz, 1H), 6.92 (d, J = 8.4 Hz, 1H), 6.87 (d, J = 2.5 Hz, 1H), 6.72 (dd, J = 8.4, 2.5 Hz, 1H), 5.02 (s, 2H), 2.82 (dd, J = 16.3, 4.4 Hz, 1H), 2.77-2.65 (m, 1H), 2.24 (d, J = 13.2 Hz, 2H), 2.19 (dd, J = 13.8, 6.0 Hz, 1H), 2.11-1.96 (m, 2H), 1.64-1.56 (m, 1H), 1.53 (d, J = 11.0 Hz, 1H), 1.35 (td, J = 13.3, 3.7 Hz, 1H), 1.30 (s, 3H), 1.13 (s, 3H), 1.11-1.05 (m, 1H) ppm.
펜타플루오로페닐 (1S,4aS,10aR)-6-(벤질옥시)-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르복실레이트 (22)
DMF(100mL)중 21 (9.6 g, 26 mmol)의 용액에 DIPEA (14 mL, 79 mmol) 및 퍼플루오로페닐 2,2,2-트리플루오로아세테이트(15g, 53mmol)를 첨가하였다. 이 혼합물을 실온에서 밤새 교반하였고, 이를 LCMS로 모니터링 하였다. 이어서, 반응 혼합물을 에테르 (200 mL)로 희석하고 물(300 mL) 및 염수(200 mL)로 세척하였다. 유기용액을 황산나트륨으로 건조시키고 진공에서 농축시켰다. 잔류물을 플래쉬크로마토그래피(석유에테르중 0-10% 에틸아세테이트)로 정제하여 화합물22 (12 g, 88% 수율)를 백색 고체로서 수득하였다. ESI m/z: 531 (M + H)+. 1H NMR (500 MHz, DMSO d6 ) δ 7.43 (d, J = 7.1 Hz, 2H), 7.38 (t, J = 7.4 Hz, 2H), 7.31 (t, J = 7.2 Hz, 1H), 6.93 (dd, J = 10.2, 5.5 Hz, 2H), 6.76 (dd, J = 8.4, 2.5 Hz, 1H), 5.05 (s, 2H), 2.81 (dd, J = 16.3, 4.5 Hz, 1H), 2.77-2.68 (m, 1H), 2.28-2.19 (m, 2H), 2.18 (dd, J = 13.4, 5.6 Hz, 1H), 2.00-1.83 (m, 2H), 1.74 (d, J = 11.8 Hz, 1H), 1.65 (d, J = 14.1 Hz, 1H), 1.47 (s, 3H), 1.38-1.27 (m, 2H), 1.08 (s, 3H) ppm.
tert-부틸 N-[(4bS,8S,8aR)-8-({[(1S,4aS,10aR)-6-(벤질옥시)-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타히드로페난트렌-1-일]포름아미도}카르보닐)-4b,8-디메틸-4b,5,6,7,8,8a,9,10-옥타히드로페난트렌-3-일]카르바메이트 (23)
THF(20mL)중 화합물18 (2.3 g, 6.2 mmol)의 용액에 -78℃에서 n-BuLi (헥산 중2.5 M, 5.5 mL, 14 mmol) 를 적가하였다. 반응물을 이 온도에서 1시간 동안 교반하였다. 혼합물에 THF(20Ml)중 22 (3.0 g, 5.6 mmol)의 용액을 첨가하고, 이어서 생성된 혼합물을 화합물 22가 소모될때까지 밤새 10-20℃에서 교반하였고, 이를 LCMS에 의해 모니터링하였다. 반응물을 sat. aq. 암모늄클로라이드로 켄칭하고 에틸아세테이트로 추출 하였다. 합한 유기 용액을 물 및 염수로 세척하고, 황산나트륨으로 건조시키고 진공에서 농축시켰다. 잔류물을 플래쉬 크로마토그래피(석유 에테르 중 0-30%에틸아세테이트)로 정제하여 화합물 23 (1.59 g, 51% 수율)을 백색고체로서 수득하였다. ESI m/z: 719 (M + 1)+.
tert-부틸 N-[(4bS,8S,8aR)-8-({[(1S,4aS,10aR)-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타히드로페난트렌-1-일]포름아미도}카르보닐)-4b,8-디메틸-4b,5,6,7,8,8a,9,10-옥타히드로페난트렌-3-일]카르바메이트 (24)
에틸아세테이트(40mL)중 23 (2.0 g, 2.78 mmol)의 용액에 질소 보호하에서 탄소(10% Pd, 0.9 g)상의 습식 팔라듐을 첨가하였다. 혼합물을 탈기시키고 수소로 처리하고 23이 완전히 소모될때까지 수소 벌룬하에서 밤새 실온에서 교반하였고, 이를 LCMS에 의해 모니터링 하였다. 혼합물을 셀라이트를 통해 여과하고, 여과를 진공에서 농축시켰다. 잔류물을 실리카겔 칼럼크로마토그래피(석유 에테르 중 0-55% 에틸에테르)로 정제하여 24 (1.06 g, 61% 수율)를 백색 고체로서 제공하였다. ESI m/z: 629 (M + H)+. 1H NMR (500 MHz, DMSO d6 ) δ 9.10 (s, 1H), 8.98 (s, 1H), 8.11 (s, 1H), 7.40 (s, 1H), 7.15 (d, J = 7.5 Hz, 1H), 6.90 (d, J = 8.4 Hz, 1H), 6.81 (d, J = 8.3 Hz, 1H), 6.63 (d, J = 2.3 Hz, 1H), 6.50 (dd, J = 8.2, 2.4 Hz, 1H), 2.84 (td, J = 16.3, 3.8 Hz, 2H), 2.77-2.64 (m, 2H), 2.30-2.22 (m, 2H), 2.14 (t, J = 10.9 Hz, 4H), 2.00-1.80 (m, 4H), 1.65-1.54 (m, 4H), 1.45 (s, 9H), 1.34-1.28 (m, 2H), 1.27 (d, J = 2.5 Hz, 6H), 1.15-1.08 (m, 2H), 0.99 (s, 6H) ppm.
페이로드 D
(1S,4aS,10aR)-N-[(1S,4aS,10aR)-6-아미노-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르보닐]-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르복스아미드 (D)
DCM(10mL)중 화합물 24 (0.17 g, 0.27 mmol) 의 용액에 TFA(3mL)를 실온에서 적가 하였다. LCMS에 따라 Boc가 제거될 때 까지 반응 혼합물을 실온에서 1시간동안 교반하였다. 휘발물을 진공에서 제거하고 잔류물을 분취-HPLC(방법 B(method B))로 정제하여 D(0.10 g, 70% 수율)를 백색 고체로서 수득하였다.
ESI m/z: 529.3 (M + 1)+.
1H NMR (400 MHz, CDCl3) δ 8.14 (s, 1H), 6.92 (d, J = 8.3 Hz, 1H), 6.86 (d, J = 8.1 Hz, 1H), 6.73 (d, J = 2.5 Hz, 1H), 6.65-6.57 (m, 2H), 6.50 (dd, J = 8.1, 2.3 Hz, 1H), 4.75 (s, 1H), 3.49 (s, 1H), 2.99-2.85 (m, 2H), 2.79 (tt, J = 11.6, 5.8 Hz, 2H), 2.34-2.14 (m, 6H), 2.15-1.95 (m, 4H), 1.74-1.51 (m, 5H), 1.46-1.34 (m, 2H), 1.30 (s, 6H), 1.21-1.06 (m, 8H) ppm.
1H NMR (400 MHz, DMSO d6 ) δ 8.99 (s, 1H), 8.09 (s, 1H), 6.81 (d, J = 8.0 Hz, 1H), 6.68 (d, J = 8.0 Hz, 1H), 6.63 (d, J = 2.5 Hz, 1H), 6.50 (dd, J = 8.0, 2.5 Hz, 1H), 6.48 (d, J = 2.5 Hz, 1H), 6.34 (dd, J = 8.0, 2.5 Hz, 1H), 4.69 (s, 2H), 2.86-2.60 (m, 4H), 2.28-2.10 (m, 6H), 1.94-1.75 (m, 4H), 1.65-1.53 (m, 4H), 1.35-1.20 (m, 8H), 1.20-1.06 (m, 2H), 0.98 (s, 6H) ppm.
13C NMR (100 MHz, DMSO d6 ) δ 174.03, 173.92, 155.34, 148.39, 147.63, 146.43, 129.56, 129.09, 124.60, 121.65, 113.23, 112.58, 111.81, 110.77, 52.32, 52.09, 45.56, 45.52, 39.20, 39.36, 38.23, 38.17, 37.18, 37.12, 31.08, 31.00, 27.65, 27.64, 23.08, 23.03, 21.43, 21.27, 19.64, 19.61 ppm.
HPLC (method B): Retention time: 8.92 min, purity: 99.4%. chiral HPLC: >99.9% (in column AD, AS, OD and OJ).
Optical rotation (α): +2.53o (1.7 g/100 mL THF, 25 oC).
페이로드 E
(1S,4aS,10aR)-6-((S)-2-아미노-3-하이드록시프로판아미도)-N-((1S,4aS,10aR)-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르보닐)-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르복스아미드 (E)
DMF(1mL)중 Fmoc-Ser-OH (30 mg, 0.1 mmol)의 용액에 25℃에서 HATU (38 mg, 0.1 mmol) 및 DIPEA (39 mg, 0.3 mmol)를 첨가하였다. 생성된 혼합물을이 온도에서 1시간동안 교반하였다. 이어서 혼합물 D (30 mg, 0.06 mmol)를 첨가하고, 반응 혼합물 25℃에서 16시간 동안 교반하였다. 혼합물에 피페리딘(0.2mL)을 첨가하고, 생성된 혼합물을 실온에서 추가로 30분 동안 교반하였다. 휘발물을 진공에서 제거하고 잔류물을 예비-HPLC(방법 B)에 의해 직접 정재하여 원하는 생성물 (18 mg, 51% 수율)을 백색 고체로서 수득하였다. ESI m/z: 616 (M + 1)+. 1H NMR (500 MHz, DMSO- d6 ) δ 9.74 (br s, 1H, CONH-Ph), 9.00 (s, 1H, OH), 8.11 (s, 1H, NH of imidine), 7.58 (s, 1H), 7.41 (dd, J = 8.2, 2.0 Hz, 1H), 6.96 (d, J = 8.4 Hz, 1H), 6.82 (d, J = 8.3 Hz, 1H), 6.63 (d, J = 2.3 Hz, 1H), 6.50 (dd, J = 8.2, 2.4 Hz, 1H), 4.82 (t, J = 5.5 Hz, 1H, OH on Ser), 3.62-3.45 (m, 3H), 2.97-2.61 (m, 4H), 2.33-2.21 (m, 2H), 2.21-2.03 (m, 4H), 1.96-1.77 (m, 4H), 1.70-1.50 (m, 4H), 1.36-1.20 (m, 8H), 1.23-1.06 (m, 2H), 1.06-0.93 (m, 6H) ppm.
실시예 5
중간체 3a-c, 3g 의 제조 (도 6 참조)
일반절차 A: DMF(10mg의 페이로드 당 0.3mL)중 페이로드(A, B, C, 또는 E 1.0 eq.)의 용액에 Fmoc-vcPAB-PNP 2a (1.1 eq.)를 첨가 하였다. RT에서 HOBt (1.5 eq.) 및 DIPEA (2.0 eq.). 페이로드가 완전히 소비될 때 까지 혼합물을 실온에서 3시간동안 교반하였고, 이를 LCMS에 의해 모니터링 하였다. 반응 혼합물에 디에틸아민(10 mg의 페이로드당 0.03 mL)을 첨가하고 혼합물을 Fmoc가 제거될 때 까지 1시간 동안 상온(18-30℃)에서 교반하였다. 혼합물을 여과하고 여액을 진공에서 농축시켰다. 잔류물을 역상 플래쉬크로마토그래피 또는 prep-HPLC로 표제화합물 (3a, 3b, 3c 또는 3g)로 정제 하였다.
4-((S)-2-((S)-2-아미노-3-메틸부탄아미도)-5-우레이도펜탄아미도)벤질 (S)-1-((S)-1-(((3R,4S,5S)-1-((S)-2-((1R,2R)-3-((1S,2R)-1-하이드록시-1-페닐프로판-2-일아미노)-1-메톡시-2-메틸-3-옥소프로필)피롤리딘-1-일)-3-메톡시-5-메틸-1-옥소헵탄-4-일)(메틸)아미노)-3-메틸-1-옥소부탄-2-일아미노)-3-메틸-1-옥소부탄-2-일(메틸)카르바메이트 (3a) (vcPAB-MMAE)
[참고: WO2012/166560] 페이로드 A (45 mg, 63 μmol), 화합물 3a (28 mg, 40% 수율)를 갖는 화합물 2a (90 mg, purity 75%, 88 μmol)로 부터의 일반적인 절차A에 따라 백색 분말로서 수득하였다. ESI m/z: 1123.5 (M + H)+. 1H NMR (DMSO d 6, 500 MHz): δ 10.12 (br s, 1H), 8.25-8.05 (m, 2H), 7.89-7.58 (m, 3H), 7.34-7.16 (m, 7H), 5.98 (t, J = 5.5 Hz, 1H), 5.42-5.34 (m, 3H), 5.06-4.95 (m, 2H), 4.78-4.57 (m, 1H), 4.51-4.26 (m, 3H), 3.80-3.40 (m, 2H), 3.28-3.18 (m, 7H), 3.12-2.84 (m, 10H), 2.43-2.40 (m, 1H), 2.30-2.27 (m, 1H), 2.15-1.91 (m, 5H), 1.96-1.68 (m, 4H), 1.59-1.34 (m, 6H), 1.06-0.93 (m, 6H), 0.90-0.70 (m, 26H) ppm.
{4-[(2S)-2-[(2S)-2-아미노-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸N-{2-[(1S,2S,4R,8S,9S,11S,12R,13S,19S)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-8-일]-2-옥소에틸}카르바메이트 (3b)
페이로드 B를 갖는 화합물 2a (93 mg, 0.20 mmol)의 일반적인 절차 A에 따라, 역상 플래쉬크로마토그래피(수성중탄산암모늄(10mM)중 50-80%아세토니트릴)에 의한 정제 후 화합물 3b를 백색고체로 수득하였다. ESI m/z: 871 (M + H)+.
{4-[(2S)-2-[(2S)-2-아미노-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸N-(4-{2-[(1S,2S,4R,8S,9S,11S,12R,13S,19S)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-8-yl]-2- 옥소에톡시}페닐)카르바메이트 (3c)
페이로드 C를 갖는 화합물 2a (0.10 g, 0.22 mmol)로부터의 일반적인 절차 A에 따라, 역상 플래쉬 크로마토그래피(수중 50-80%아세토 니트릴)로 정제한 후 화합물 3c(160 mg, 76%수율)를 수득하였다. 암모늄 바이카보네이트(10mM)를 백색고체로 제공하였다. ESI m/z: 963.4 (M + H)+.
{4-[(2S)-2-[(2S)-2-아미노-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸N-[(1S)-1-{[(4bS,8S,8aR)-8-({[(1S,4aS,10aR)-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타히드로페난트렌-1-일]포름아미도}카르보닐)-4b,8-디메틸-4b,5,6,7,8,8a,9,10-옥타히드로페난트렌-3-일]카바모일}-2-하이드록시에틸]카르바메이트 (3g)
DMF(3mL)중 Fmoc-vc-PAB-PNP (58 mg, 76 μmol) 및 E (36 mg, 58 μmol)의 용액에 HOBt (7.9 mg, 58 μmol) 및 DIPEA (15 mg, 0.12 mmol)를 첨가하고, 혼합물을 30℃에서 16시간 동안 교반하였다. 이어서, LCMS에 따라 화합물 E를 완전히 소모하였다. 생성된 혼합물에 디에틸아민(0.1mL)를 첨가하고 Fmoc가 제거될 때 까지 실온에서 1시간 동안 교반하였고, 이를 LCMS에의해 모니터링 하였다. 여과 후, 여액을 예비-HPLC(방법 B)로 직접 정제하여 화합물 3g (36 mg, 48% 수율)을 담황색 고체로서 수득하였다. ESI m/z: 1021 (M + 1)+. 1H NMR (400 MHz, DMSO d6 ) δ 10.02 (s, 1H), 9.82 (s, 1H), 9.00 (s, 1H), 8.69-8.65 (m, 1H), 8.11-8.00 (m, 4H), 7.65-7.53 (m, 3H), 7.40-7.30 (m, 3H), 7.30-7.20 (m, 1H), 6.96 (d, J = 8.0 Hz, 1H), 6.81 (d, J = 8.0 Hz, 1H), 6.65-6.61 (m, 1H), 6.50 (dd, J = 8.0 Hz, 2.0 Hz, 1H), 6.00-5.95 (m, 1H), 5.48 (s, 2H), 5.00-4.95 (m, 3H), 4.60-4.40 (m, 1H), 4.25-4.20 (m, 1H), 3.65-3.55 (m, 4H), 3.15-2.55 (m, 10H), 2.40-2.20 (m, 3H), 2.20-2.00 (m, 5H), 2.00-1.80 (m, 4H), 1.86-1.55 (m, 6H), 1.27 (d, J = 4.8 Hz, 9H), 1.20-1.10 (m, 2H), 0.97-0.90 (m, 6H) ppm.
실시예 6
중간체 3d 및 3f의 제조(도 7 참조)
일반절차 B: DMF(페이로드 그램당 25mL)중 Fmoc-Val-Ala-OH (2b, 1.2 eq.)의 용액에 HATU (1.5 eq.) 및 DIPEA (3.0 eq.)를 실온에서 첨가하였다. 혼합물을 실온에서 5분 동안 교반한 후 페이로드(C 또는 D, 1.0 eq.)를 첨가하였다. 혼합물을 추가로 2시간 동안 교반하고 LCMS가 반응의 완료를 나타냈다. 반응 혼합물에 디에틸아민(5 eq.)을 첨가하였다. LCMS에 따라 Fmoc가 완전히 제거될 때까지 혼합물을 실온에서 2시간동안 교반하였다. 혼합물을 여과하고 여액을 진공에서 농축시켰다. 잔류물을 역상 플래쉬 크로마토그래피(수성 중탄산암모늄(10Mm)중 0-100%아세토니트릴)또는 예비-HPLC(방법B)에 의해 정제하여 원하는 생성물(3d 또는 3f, 페이로드부터 64-72% 수율).
)을 수득하였다.
(2
S
)-2-아미노-
N
-[(1
S
)-1-[(4-{2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9
.0
4,8
.0
13,18
]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카바모일]에틸]-3-메틸부탄아미드 (3d)
페이로드 C를 갖는 화합물 2b (0.50 g, 0.90 mmol)로부터의 일반적인 절차 B에 따라, 역상 플래쉬 크로마토그래피 (수중 0-100% 아세토니트릴)에 의해 정제한 후 화합물 3d (0.69 g, 72% 수율)를 점성 황색오일로서 암모늄 바이카보네이트(10mM)로 수득하였다. ESI m/z: 728 (M + H)+.
(1
S
,4a
S
,10a
R
)-6-((
S
)-2-((
S
)-2-아미노-3-메틸부탄아미도)프로판아미도)-
N
-((1
S
,4a
S
,10a
R
)-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르보닐)-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르복스아미드 (3f)
페이로드 D (53 mg, 0.10 mmol)를 갖는 화합물 2b로부터의 일반적인 절차 B에 따라, 화합물 3f (45 mg, 64% 수율)를 정제한 후 HPLC(방법 B)에 의해 백색 고체로서 수득한 후 수득 하였다. ESI m/z: 699 (M + 1)+. 1H NMR (500 MHz, MeOD d4 ) δ 8.40 (s, 1H), 7.47 (s, 1H), 7.32 (d, J = 8.0 Hz, 1H), 7.03 (d, J = 8.3 Hz, 1H), 6.88 (d, J = 8.2 Hz, 1H), 6.72 (d, J = 2.4 Hz, 1H), 6.56 (dd, J = 8.3, 2.4 Hz, 1H), 4.60-4.48 (m, 1H), 3.22-3.11 (m, 1H), 3.02-2.93 (m, 1H), 2.92-2.76 (m, 3H), 2.74-2.70 (m, 1H), 2.43-2.31 (m, 3H), 2.28 (d, J = 14.1 Hz, 3H), 2.16-1.96 (m, 3H), 1.81 (s, 1H), 1.78-1.65 (m, 4H), 1.53-1.42 (m, 4H), 1.38 (d, J = 5.3 Hz, 6H), 1.33-1.22 (m, 2H), 1.14 (d, J = 6.6 Hz, 6H), 1.09 (d, J = 18.6 Hz, 6H) ppm.
실시예 7
중간체 3e의 제조(도 8 참조)
(2
S
)-2-[(2
S
)-2-아미노-3-메틸부탄아미도]-5-(카바모일아미노)-
N
-(4-{2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9
.0
4,8
.0
13,18
]코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)펜탄아미드 (3e)
DMF(5ml)중 Fmoc-Val-Cit-OH (0.23 g, 0.43 mmol)의 용액에 실온에서 HATU (0.38 g, 0.43 mmol) 및 DIPEA (93 mg, 0.72 mmol)를 첨가하였다. 혼합물을 실온에서 5분 동안 교반한 후 페이로드 C (0.20 g, 0.36 mmol)를 첨가하였다. 혼합물을 추가로 2시간 동안 교반하고 LCMS가 반응의 완료를 나타냈다. 반응 혼합물에 디에틸아민(0.5ml)을 첨가하였다. LCMS에 따라 Fmoc가 완전히 제거될 때까지 혼합물을 실온에서 1시간동안 교반하였다. 혼합물을 여과하고 여액을 진공에서 농축하였다. 잔류물을 역상 플래쉬크로마토그래피(수성중탄산암모늄(10mM)중 0-100% 아세토니트릴 및 이어서 메탄올) 로 정제하여 화합물 3e (페이로드 C로부터 38% 수율). ESI m/z: 814 (M + 1)+.
실시예 8
중간체 4의 제조(도 9 참조)
중간체 4a는 Fmoc-(D)-Lys-OH로부터 상업용 활성화된 에스테르 25로 아미드화하여 합성 하였다.
(2R)-6-[2-(시클로옥트-2-인-1-일옥시)acet아미도]-2-{[(9H-플루오렌-9-yl메톡시)카르보닐]아미노}헥산 산 (4a)
DMF(2ml)중 화합물25 (65 mg, 0.23 mmol, CAS: 1425803-45-7)의 혼합물에 Fmoc-D-Lys-OH (85 mg, 0.23 mmol) 및 트리에틸아민(52 mg, 0.51 mmol)을 첨가하였다. 반응 혼합물을 실온에서 30분동안 교반 하였다. 혼합물을 역상 플래쉬 크로마토 그래피(물 중 0-100% 아세토니트릴 (0.05% TFA))로 직접 분리하여 중간체 4a를 백색 고체로서 수득하였다. ESI m/z: 533 (M + H)+. 1H NMR (MeODd4, 500 MHz): δ 7.70 (d, J = 7.5 Hz, 2H), 7.59 (t, J = 8.0 Hz, 2H), 7.30 (t, J = 7.5 Hz, 2H), 7.22 (t, J = 7.4 Hz, 2H), 4.35-4.22 (m, 2H), 4.22-4.09 (m, 2H), 4.09-3.99 (m, 1H), 3.94-3.81 (m, 1H), 3.79-3.67 (m, 1H), 3.15 (t, J = 6.9 Hz, 2H), 2.17-1.96 (m, 3H), 1.96-1.86 (m, 1H), 1.85-1.66 (m, 4H), 1.66-1.41 (m, 5H), 1.41-1.25 (m, 3H) ppm.
실시예 9
중간체 4b의 제조(도 10 참조)
중간체 4b를 Fmoc-(D)-Glu-O t Bu (26)로부터 합성하였다. 화합물 26을 HOSu로 활성화시킨 후 타우린으로 아미드화하여 화합물 27을 제공하고, 이를 화합물 TFA로 가수분해 하여 중간체 4b를 수득하였다.
2-[(4R)-5-(tert-부톡시)-4-{[(9H-플루오렌-9-일메톡시)카르보닐]아미노}-5-옥소펜탄아미도]에탄-1-술폰 산(27)
DCM(20ml)중 of Fmoc-(D)-Glu-O t Bu (26) (2.0 g, 4.7 mmol)의 용액에 HOSu (1.1 g, 9.6 mmol) 및EDCI (1.8 g, 9.4 mmol)을 실온에서 첨가하였다. 혼합물을 실온에서 밤새 교반하였고, 이를 LCMS로 모니터링하였다. 반응 혼합물 DCM(100ml)으로 희석하고, 물(50 mL x 2) 및 염수(50ml)로 세척하고, 무수 소듐 설페이트로 건조하고 진공에서 농축하였다. 잔류물을 DMF(2ml)에 용해시키고 용액에 타우린(1.2 g, 9.6 mmol) 및 DIPEA (1.4 g, 14 mmol)를 첨가하였다. LCMS에 따라 반응이 완료될 때까지 생성된 혼합물을 실온에서 밤새 교반하였다. 반응 혼합물을 예비-HPLC(방법 B)에 의해 직접 정제하여 화합물27 (2.0 g, 81% 수율)을 백색 고체로서 수득하였다. ESI m/z: 477 (M - 55 + H)+.
(2
R
)-2-{[(9
H
-플루오렌-9-yl메톡시)카르보닐]아미노}-4-[(2-설포에틸)카바모일]부탄 산 (4b)
DCM(2ml)중 화합물27 (0.52 g, 0.98 mmol)의 용액에 TFA(2ml)를 첨가하였다. LCMS에 따라 가수분해가 완료될 때까지 반응 혼합물을 실온에서 3시간 동안 교반하였다. 휘발물을 진공에서 제거하고 잔류물을 역상 플래쉬크로마토그래피(수성중탄산암모늄(10mM)중 0-100%아세토니트릴)로 정제하여 중간체 4b (0.45 g, 97% 수율)를 백색고체로서 수득하였다. ESI m/z: 477 (M + H)+. 1H NMR (DMSO d6 , 500 MHz) δ 7.89 (d, J = 7.5 Hz, 2H), 7.72 (d, J = 7.5 Hz, 2H), 7.42 (t, J = 7.5 Hz, 2H), 7.34 (t, J = 7.5 Hz, 2H), 7.21-7.17 (br s, 1H), 4.27-4.23 (m, 2H), 3.82-3.79 (m, 1H), 3.27-3.19 (m, 1H), 2.71-2.67 (m, 1H), 2.54 (t, J = 7.5 Hz, 2H), 2.13-1.89 (m, 2H), 1.80-1.75 (m, 1H), 1.07-1.06 (m, 4H) ppm (양성자 COOH는 나타나지 않았다).
J. Org. Chem. 2010, 75, 3685-3691로 약술한 합성 절차에 따라 화합물 4c를 제조하고, 화합물 4c를 25%총 수율로 수득하였다. ESI m/z: 613.3 (M + H)+.
실시예 10
충간체 5a-g의 제조(도 11 참조)
일반절차 D: DMF중 화합물 4a (1.2 eq.)의 용액 (4a의 10 mg당 0.2 mL)에 RT에서 HATU (1.4 eq.) 및DIPEA (3 eq.)를 첨가 하였다. 화합물 3을 첨가하기 전에 혼합물을 실온에서 5분 동안 교반 하였다(1.0 당량). 이어서, 화합물 3a-g가 완전히 소비될 때 까지 반응 혼합물을 실온에서 2시간 동안 교반하고, 이를 LCMS에 의해 모니터링 하였다. 반응 혼합물에 디에틸아민(5.0 eq.)을 첨가하였다. 혼합물을 실온에서 2시간 동안 교반하였다. 혼합물을 여과하고 여액을 농축했다. 잔류물을 역상 플래쉬크로마토그래피(수성중탄산암모늄(10mM)중 0-100%아세토니트릴) 또는 예비-HPLC(방법 B)에 의해 정제하여 화합물 5a-g를 수득 하였다.
4-((2
S
)-2-((2
S
)-2-((2
R
)-2-아미노-6-(2-(시클로옥트-2-이닐옥시)아세트아미도)헥산아미도)-3-메틸부탄아미도)-5-우레이도펜탄아미도)벤질 (
S
)-1-((
S
)-1-(((3
R
,4
S
,5
S
)-1-((
S
)-2-((1
R
,2
R
)-3-((1
S
,2
R
)-1-하이드록시-1-페닐프로판-2-일아미노)-1-메톡시-2-메틸-3-옥소프로필)피롤리딘-1-일)-3-메톡시-5-메틸-1-옥소헵탄-4-일)(메틸)아미노)-3-메틸-1-옥소부탄-2-일아미노)-3-메틸-1-옥소부탄-2-일(메틸)카르바메이트 (5a)
화합물 3a (38 mg, 34 μmol)로부터 화합물4 (34 mg, 64 μmol)의 일반적인 절차 D에 따라, 화합물 5a (17 mg, 35% 수율)를 백색 고체로서 수득하였다. ESI m/z: 1415 (M + 1)+. 1H NMR (DMSO d6 , 400 MHz) δ 10.09-10.02 (m, 1H), 8.54 (d, J = 8.4 Hz, 1H), 8.38 (d, J = 7.5 Hz, 1H), 8.35-8.26 (m, 0.5H), 8.12-8.02 (m, 3H), 7.94-7.85 (m, 0.5H), 7.66-7.54 (m, 3H), 7.34-7.23 (m, 6H), 7.20-7.13 (m, 1H), 6.08-5.97 (m, 1H), 5.54-5.37 (m, 3H), 5.13-4.94 (m, 2H), 4.52-4.21 (m, 6H), 4.03-3.70 (m, 4H), 3.63-3.51 (m, 1H), 3.25-3.17 (m, 8H), 3.13-2.82 (m, 10H), 2.31-1.91 (m, 10H), 1.85-1.64 (m, 9H), 1.64-1.25 (m, 15H), 1.07-0.96 (m, 6H), 0.90-0.74 (m, 26H) ppm.
{4-[(2
S
)-2-[(2
S
)-2-[(2
S
)-2-아미노-6-[2-(시클로옥트-2-인-1-일옥시)아세트아미도]헥산아미도]-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸
N
-{2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9.
0
4,8.
0
13,18
]이코사-14,17-디엔-8-일]-2-옥소에틸}카르바메이트 (5b)
3b (0.20 g, 0.23 mmol)로 부터의 일반적인 절차 D에 따라, 화합물 5b (0.12 g, 45% 수율)를 예비-HPLC(방법B)후에 백색 고체로서 수득하였다. ESI m/z: 1385 (M + 1)+. 1H NMR (400 MHz, MeOD d4 ) δ 7.65-7.55 (m, 2H), 7.40-7.26 (m, 3H), 6.39-6.27 (m, 2H), 5.65-5.45 (m, 1H), 5.13-5.01 (m, 2H), 4.71-4.50 (m, 2H), 4.40-4.14 (m, 4H), 4.11-3.82 (m, 3H), 3.46-3.39 (m, 1H), 3.29-3.09 (m, 4H), 2.76-2.54 (m, 1H), 2.41-2.10 (m, 7H), 2.09-1.99 (m, 1H), 1.96-1.80 (m, 5H), 1.78-1.21 (m, 23H), 1.06-0.82 (m, 12H) ppm.
{4-[(2
S
)-2-[(2
S
)-2-[(2
R
)-2-아미노-6-[2-(시클로옥트-2-인-1-일옥시)아세트아미도]헥산아미도]-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸
N
-(4-{2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9
.0
4,8
.0
13,18
]이코사-14,17-디엔-8-yl]-2-옥소에톡시}페닐)카르바메이트 (5c)
4a에 의한 3c (55 mg, 54 μmol)의 일반적인 절차 D에 따라, 화합물5c (0.10 g, 수율57%)를 백색 고체로서 수득하였다. ESI m/z: 1255.5 (M + 1)+. 1H NMR (400 MHz, MeOD d4 ) δ 7.61 (d, J = 8.4 Hz, 2H), 7.32-7.39 (m, 5H), 6.84-6.88 (m, 2H), 6.31-6.36 (m, 2H), 5.05-5.16 (m, 3H), 4.71-4.83 (m ,1H), 4.50-4.54 (m,1H), 4.18-4.33 (m 3H), 3.00-2.85 (m, 2H), 3.40-3.51 (m, 1H), 3.00-3.29 (m, 6H), 1.31-2.35 (m, 34 H), 1.29 (t, J =7.2 Hz, 2H), 0.93-1.02 (m ,12H) ppm.
(2
R
)-2-아미노-6-[2-(시클로옥트-2-yn-1-yl옥시)아세트아미도]-
N
-[(1
S
)-1-{[(1
S
)-1-[(4-{2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9
.0
4,8
.0
13,18
]이코사-14,17-디엔-8-yl]-2-옥소에톡시}페닐)카바모일]에틸]카바모일}-2-메틸프로필]헥산아미드 (5d)
3d (0.28 g, 0.38 mmol)로부터 일반적인 절차 D에 따라, 화합물5d (0.21 g, 46% 수율)를 예비-HPLC(방법 B)후백색 고체로서 수득하였다. ESI m/z: 1021.5 (M + 1)+. 1H NMR (400 MHz, MeOD d4 ) δ 7.33-7.60 (m, 3H), 6.87-6.91 (m ,2H), 6.32-6.37 (m, 2H), 5.47-5.65 (m, 1H), 5.07-5.30 (m, 1H), 4.72-4.86 (m, 3H), 4.34-4.51 (m, 3H), 3.83-4.20 (m, 3H), 3.33-3.49 (m, 1H), 3.14-3.27 (m, 3H), 2.59-2.75 (m, 1H), 1.31-2.39 (m, 33 H), 0.93-1.05 (m, 12H) ppm.
(2
R
)-2-아미노-
N
-[(1
S
)-1-{[(1
S
)-4-(카바모일아미노)-1-[(4-{2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9
.0
4,8
.0
13,18
]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카바모일]부틸]카바모일}-2-메틸프로필]-6-[2-(시클로옥트-2-인-1-일옥시)아세트아미도]헥산아미드 (5e)
3e (0.10 g, 0.12 mmol)의 일반적인 절차 D에 따라, 역상 플래쉬 크로마토그래피(수성중탄산암모늄(10 mM) 0-100%아세토니트릴)에 의해 정제한 후 화합물 5d (0.12 g, 88% 수율)를 백색 고체로서 수득하였다. ESI m/z: 553.7 (M/2 + 1)+.
(1
S
,4a
S
,10a
R
)-6-((2
S
)-2-((2
S
)-2-((2
R
)-2-아미노-6-(2-(시클로옥트-2-이닐옥시)아세트아미도)헥산아미도)-3-메틸부탄아미도)프로판아미도)-
N
-((1
S
,4a
S
,10a
R
)-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르보닐)-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르복스아미드 (5f)
3f (80 mg, 0.11 mmol)로부터 일반적인 절차 D에 따라, 화합물 5f (48 mg, 84% 수율)를 예비-HPLC(방법B)후에 백색 고체로서 수득하였다. ESI m/z: 991.5 (M + 1)+.
{4-[(2 S )-2-[(2 S )-2-[(2 R )-2-아미노-6-[2-(시클로옥트-2-인-1-일옥시)아세트아미도]헥산아미도]-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸 N -[(1 S )-1-{[(4b S ,8 S ,8a R )-8-({[(1 S ,4a S ,10a R )-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타히드로페난트렌-1-일]포름아미도}카르보닐)-4b,8-디메틸-4b,5,6,7,8,8a,9,10-옥타히드로페난트렌-3-일]카바모일}-2-하이드록시에틸]카르바메이트 (5g)
DMF(2ml)중 화합물 4a (24 mg, 44 μmol)의 용액에 후속적으로 실온에서 HATU (17 mg, 44 μmol) 및 화합물3g (35 mg, 34 μmol)을 첨가하였다. 혼합물이 균질해질 때까지 혼합물을 실온에서 몇 분 동안 교반하였다. 이 혼합물에 DIPEA (8.8 mg, 68 μmol)를 실온에서 주사기로 첨가하였다. LCG에 따라 3g이 대부분 소비될 때 까지 생성된 혼합물을 실온에서 2시간 동안 교반 하였다. 이어서, 이 반응 혼합물에 디에틸아민 또는 피페리딘(0.1 mL, excess)[1] 을 실온에서 적가하고 Fmoc기가 제거될때까지 혼하물을 1시간 동안 교반하고, 이를 LCMS로 모니터링 하였다. 반응 혼합물을 예비-HPLC(방법B)로 직접 정제하여 화합물 5g (15 mg, 33% 수율)을 백색 고체로서 수득하였다. ESI m/z: 1313.6 (M + H)+. 1H NMR (500 MHz, MeOD d4 ) δ 7.59 (d, J = 8.5 Hz, 2H), 7.51 (s, 1H), 7.36-7.26 (m, 3H), 7.01 (d, J = 8.5 Hz, 1H), 6.88 (d, J = 8.0 Hz, 1H), 6.72-6.71 (m, 1H), 6.57-6.54 (m, 1H), 5.09 (s, 2H), 4.64-4.52 (m, 1H), 4.35-4.28 (m, 2H), 4.21 (d, J = 7.0 Hz, 1H), 4.01-3.98 (m, 1H), 3.88-3.84 (m, 3H), 3.43 (t, J = 6.5 Hz, 1H), 3.26-3.10 (m, 4H), 3.00-2.76 (m, 3H), 2.38-2.24 (m, 7H), 2.19-2.02 (m, 9H), 1.98-1.78 (m, 4H), 1.74-1.54 (m, 12H), 1.45-1.26 (m, 14H), 1.13 (s, 6H), 1.00 (t, J = 7.5 Hz, 6H) ppm.
실시예 10-1
화합물 10a-d의 제조(도 11C)
도 11C에 따른 아미드 커플링 절차에 의해 화합물 10a-d를 제조하였다.
화합물 10a-d에 대한 일반적인 절차 D2: DMF(1 mL per 5-10 mg of 8a) 중 DIBAC-suc-PEG4-acid 8a (1.1-1.3 eq.)의 용액에 실온에서 HATU (1.5 eq.) 및 DIPEA (5.0 eq.)를 첨가하였다. 혼합물을 실온에서 30분동안 교반한 후 화합물 3(1.0 eq.)을 첨가하였다.
화합물 3이 소모될때까지 생성된 혼합물을 실온에서 교반하였고, 이를 LCMS에 의해 모니터링하였다. 여과 후, 여액을 예비-HPLC로 직접 정제하여 화합물 10a-d를 수득하였다.
실시예 10A
화합물 10a의 제조(도 11A 참조)
{4-[(2
S
)-2-[(2
S
)-2-아미노-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸
N
-{2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2
,
9
.0
4
,
8
.0
13
,
18
]이코사-14,17-디엔-8-일]-2-옥소에틸}카르바메이트 10a
DMF(3ml) 중 of Fmoc-VC-PAB-PNP (10-1, 0.17 g, 0.22 mmol) 및 화합물 B의 용액에, DMF (3 mL)중 (93 mg, 0.20 mmol)을 실온에서 시린지에 의해 DIPEA (51 mg, 0.40 mmol)와 함께 첨가하였다. 혼합물을 실온에서 3시간 동안 교반하고 LCMS에 따라 대부분의 물질을 소비하였다. 생성된 혼합물에 피페리딘(0.3ml, 과량)을 첨가하고 Fmoc가 완전히 제거될 때까지 실온에서 1시간 동안 교반하였고, 이를 LCMS에 의해 모니터링 하였다. 막을 통한 여과 후, 여액을 예비-HPLC(방법 B)에 의해 직접 정제하여 화합물 3b (0.13 g, 73% yield) 를 백색고체로서 수득하였다. ESI m/z: 871 (M + 1)+.
{4-[(2
S
)-2-[(2
S
)-2-[1-(4-{2-Azatri시클로[10.4.0.0
4
,
9
]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸
N
-{2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2
,
9
.0
4
,
8
.0
13
,
18
]이코사-14,17-디엔-8-yl]-2-옥소에틸}카르바메이트 10a
DMF (5 mL)중 산8a (30 mg, 54 μmol)의 용액에 DIPEA (13 mg, 0.10 mmol) 및 HATU (31 mg, 81 μmol)를 실온에서 연속적으로 첨가하였다. 생성된 혼합물을 이 온도에서 0.5시간동안 교반한 후에 아민 3b (43 mg, 50 μmol)를 첨가하였다. 아민이 완전히 소모될때까지 반응 혼합물을 실온에서 3시간 동안 교반하였고, 이를 LCMS에 의해 모니터링 하였다. 반응 혼합물을 막을 통해 여과하고, 이어서 여액을 예비-HPLC(방법 B)로 분리하여 화합물 10a(16mg, 23%수율)를 백색고체로서 수득하였다. ESI m/z: 1406 (M + H)+. 1H NMR (500 MHz, DMSO d6 ) δ 9.99 (s, 1H), 8.11 (d, J = 7.5 Hz, 1H), 7.88 (d, J = 8.5 Hz, 1H), 7.80-7.75 (m, 1H), 7.70-7.66 (m, 1H), 7.65-7.60 (m, 3H), 7.53-7.33 (m, 6H), 7.33-7.28 (m, 3H), 6.30 (dd, J = 10.0 Hz, 1.5 Hz, 1H), 6.11 (s, 1H),6.10-6.00 (m, 1H), 5.72-5.55 (m, 2H), 5.41 (s, 2H), 5.05-5.01 (m, 1H), 4.97 (s, 2H), 4.80-4.72 (m, 1H), 4.60-4.58 (m, 1H), 4.43-4.33 (m, 1H), 4.25-4.10 (m,3H), 3.88-3.80 (m,1H), 3.65-3.55 (m, 3H), 3.50-3.40 (m, 12H), 3.30-3.25 (m, 2H), 3.12-2.90 (m, 4H), 2.70-2.55 (m, 2H), 2.48-2.35 (m, 2H), 2.30-2.20 (m, 2H),2.15-1.95 (m, 4H), 1.86-1.65 (m, 3H), 1.64-1.54 (m, 5H), 1.49 (s, 4H), 1.46-1.34 (m, 5H), 0.90-0.80 (m, 12H) ppm. Anal. HPLC: 100%, 유지 시간: 7.40 min (방법 B). Solubility: 0.02 mg/mL water.
실시예 10B
준비중인1-(4-{2-아자트리시클로[10.4.0.0 4,9 ]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)- N -[(1 S )-1-{[(1 S )-1-{[(4b S ,8 S ,8a R )-8-{[(1 S ,4a S ,10a R )-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르보닐]카바모일}-4b,8-디메틸-4b,5,6,7,8,8a,9,10-옥타히드로페난트렌-3-yl]카바모일}에틸]카바모일}-2-메틸프로필]-3,6,9,12-테트라옥사펜타데칸-15-아미드 10b (도. 11B 참조)
도 11B에 따른 아미드 커플링 절차에 의해 제조하였다. 일반적인 절차 D2에 따라, 아민3f (20 mg, 29 νmol), 산8a (18 mg, 33 νmol), HATU (33 mg, 87 νmol), 및 DIPEA (33 mg, 87 νmol)를 교반하였다. 1-20ml의 DMF중 15-20℃에서 16시간 동안, prep-HPLC (방법 B)로 정제하였다. 10b의 수율 :10 mg, 28%. ESI m/z: 1234 (M + H)+.
[01] 1H NMR (500 MHz, methanol d4 ) δ 7.65 (d, J = 7.4 Hz, 1H), 7.62-7.51 (m, 2H), 7.48-7.28 (m, 6H), 7.27-7.21 (m, 1H), 7.00 (d, J = 8.5 Hz, 1H), 6.88 (d, J = 8.0 Hz, 1H), 6.72 (d, J = 2.4 Hz, 1H), 6.56 (dd, J = 8.3, 2.4 Hz, 1H), 5.15-5.10 (m, 1H), 4.52-4.43 (m, 1H), 4.20 (d, J = 6.5 Hz, 0.5H), 4.04 (d, J = 7.9 Hz, 0.5H), 3.77-3.64 (m, 3H), 3.63-3.49 (m, 12H), 3.47-3.39 (m, 2H), 3.24 (t, J = 5.5 Hz, 2H), 2.99-2.66 (m, 5H), 2.57-2.42 (m, 2H), 2.42-1.94 (m, 14H), 1.76-1.63 (m, 4H), 1.48-1.21 (m, 13H), 1.14-1.10 (m, 6H), 1.05-0.97 (m, 6H) ppm.
Anal. HPLC: >99%, Retention time: 9.21 min (method B).
Solubility: <0.1 mg/mL water.
실시예 10C
{4-[(2S)-2-[(2S)-2-[1-(4-{2-아자트리시클로[10.4.0.04,9]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸N-(4-{2-[(1S,2S,4R,8S,9S,11S,12R,13S,19S)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카르바메이트 (10c)
화합물 3c (58 mg, 60 μmol)로부터 화합물 8a를 사용한 일반적인 절차 D2에 따라, 화합물 10c (20 mg, 22% 수율)를 백색 고체로서 수득하였다. ESI m/z: 1499 (M + H)+. 1H NMR (400 MHz, DMSO d6 ) δ 10.02 (s, 1H), 9.59 (s, 1H), 8.14 (d, J = 7.6 Hz, 1H), 7.88 (d, J = 8.8 Hz, 1H), 7.80-7.75 (m, 1H), 7.70-7.66 (m, 1H), 7.65-7.60 (m, 3H), 7.53-7.45 (m, 3H), 7.40-7.28 (m, 7H), 6.84 (d, J = 9.2 Hz, 2H), 6.30 (dd, J = 10.4 Hz, 1.6 Hz, 1H), 6.11 (s, 1H), 6.10-6.00 (m, 1H), 5.72-5.55 (m,1H), 5.52 (s, 1H), 5.43 (s, 2H), 5.16-5.05 (m, 4H), 4.88-4.70 (m, 3H), 4.43-4.33 (m, 1H), 4.25-4.20 (m, 2H), 3.65-3.55 (m, 3H), 3.50-3.40 (m, 12H), 3.30-3.25 (m, 2H), 3.12-2.90 (m, 4H), 2.70-2.55 (m, 2H), 2.48-2.43 (m, 1H), 2.40-2.35 (m, 1H), 2.30-2.20 (m, 2H), 2.15-1.95 (m, 4H), 1.86-1.75 (m, 2H), 1.64-1.54 (m, 5H), 1.49 (s, 4H), 1.46-1.34 (m, 4H), 1.23 (s, 2H), 0.90-0.80 (m, 12H) ppm. Solubility: <0.01 mg/mL water.
실시예 D
{4-[(2S)-2-[(2S)-2-[1-(4-{2-아자트리시클로[10.4.0.04,9]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸N-[(1S)-1-{[(1S)-1-{[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-2-{[(1S,2R)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필]-N-메틸카르바메이트 (10d)
화합물 8a를 사용한 vcPAB-MMAE 3a (6.9 mg, 6.1 μmol)의 일반적인 절차 D2에 따라, 화합물 10d (2.0 mg, 20% 수율)를 백색 고체로서 수득하였다. ESI m/z: 830 (M/2 + H)+. 1H NMR (500 MHz, DMSO d6 ) δ 9.98 (s, 1H), 8.29 (s, 1H), 8.11 (d, J = 7.3 Hz, 1H), 8.04 (s, 1H), 7.92-7.82 (m, 2H), 7.75 (t, J = 5.1 Hz, 1H), 7.68 (d, J = 7.2 Hz, 1H), 7.65-7.53 (m, 3H), 7.53-7.42 (m, 3H), 7.41-7.22 (m, 9H), 7.22-7.10 (m, 1H), 6.06-5.91 (m, 1H), 5.75 (s, 1H), 5.40 (s, 2H), 5.33 (d, J = 4.8 Hz, 1H), 5.15-4.91 (m, 3H), 4.79-4.57 (m, 1H), 4.54-4.46 (m, 1H), 4.46-4.32 (m, 2H), 4.32-4.17 (m, 2H), 4.08-3.88 (m, 2H), 3.67-3.53 (m, 4H), 3.50-3.40 (m, 12H), 3.27-3.15 (m, 8H), 3.14-2.91 (m, 8H), 2.91-2.80 (m, 3H), 2.62-2.53 (m, 1H), 2.41-2.33 (m, 2H), 2.32-2.19 (m, 2H), 2.17-2.05 (m, 2H), 2.05-1.90 (m, 4H), 1.86-1.65 (m, 5H), 1.64-1.52 (m, 2H), 1.52-1.40 (m, 2H), 1.39-1.27 (m, 2H), 1.07-0.95 (m, 6H), 0.90-0.67 (m, 26H) ppm.
실시예 11
중간체 6c의 제조 (도 12 참조)
아지도-중간체 6c는 도 12에 기술된 바와 같이 타우린으로 활성화된 에스테르 30으로부터의 아미드화에 의해 합성되었다.
1-아지도-15-옥소-3,6,9,12-테트라옥사-16-아자옥타데칸-18-설폰산(6c)
2,5-디옥소피롤리딘-1-일 1-아지도-3,6,9,12-테트라옥사펜타데칸-15-오에이트 30 (0.10 g, 0.26 mmol) 및 타우린 (39 mg, 0.31 mmol)의 용액에 무수 DMF(4ml)에 디이소프로필에틸아민 (15 mg, 0.52 mmol)을 첨가하였다. 혼합물을 25℃에서 밤새 교반하였다. 반응 혼합물을 여과하고 용액을 예비-HPLC(방법 A)로 정제하여 중간체 6c (0.80 g, 수율 78%)를 무색 오일로서 수득하였다. ESI m/z: 399.1 (M + H)+. 1H NMR (500 MHz, D2O) δ 3.69 (t, J = 6.0 Hz, 2H), 3.64-3.59 (m, 14H), 3.49 (t, J = 6.5 Hz, 2H), 3.41 (t, J = 4.5 Hz, 2H), 3.00 (t, J = 7.0 Hz, 2H), 2.45 (t, J = 6.0 Hz, 2H) ppm.
실시예 11A
아지도-중간체 6b는 도 13A에 기술된 바와 같이 활성화된 에스테르 30으로부터 화합물 6b-1을 사용한 아미드 화에 의해 합성되었다.
[2-(1-아지도-3,6,9,12-테트라옥사펜타데칸-15-아미도)에틸]트리메틸아자늄 클로라이드 (6b)
무수 DMF(4ml)중 아지도-PEG4-NHS 30 (0.19 g, 0.50 mmol)의 용액에 화합물6b-1 (83 mg, 0.60 mmol) 및 DIPEA (19 g, 1.5 mmol)를 첨가하였다. 혼합물을 25℃에서 밤새 교반하였다. 혼합물을 여과하고 여액을 예비-HPLC(방법 A)로 정제하여 화합물6b (0.13 g, 64% 수율)를 무색 오일로서 수득하였다. ESI m/z: 376 (M + H)+. 1H NMR (500 MHz, DMSO d6 ) δ 3.65-3.58 (m, 4H), 3.58-3.45 (m, 16H), 3.45-3.30 (m, 12H), 2.35 (t, J = 6.5 Hz, 2H) ppm.
실시예 11B
아지도-중간체 6a는 CAS 86770-69-6과 함께 상업적으로 입수 가능하였다.
실시예 11C
[2-(1-아지도-3,6,9,12-테트라옥사펜타데칸-15
아지드-중간체 6f는 브롬을 아지드부분으로 치환한 후 가수분해 함으로써 화합물 6d-1로부터 합성되었다.
17-아지도-3,6,9,12,15-펜타옥사헵타데실포스폰 산(6f) (도 13B 참조)
10mL 둥근바닥플라스크에 6d-1 (50 mg, 0.11 mmol), 소듐아지드 (28 mg, 0.43 mmol), 아세토니트릴 (2 mL) 및 물(2 mL)을 첨가 하였다. 혼합물을 80℃에서 16시간 동안 교반하였다. LCMS는 6d-1이 완전히 소모되었음을 보여주었다. 반응물을 실온으로 냉각시키고 아세토 니트릴을 진공에서 제거하였다. 잔류물을 에틸아세테이트(20ml)와 H2O (20 mL)사이에 분배시켰다. 유기층을 H2O (15 mL x 2), 염수 (15 mL)로 세척하고, 무수 Na2SO4로 건조시키고, 여과하고 농축하여 6d-2 (35 mg, yield:76%, ESI m/z: 428.2 (M + H)+)를 적색오일로서, 무수 DMF (2 mL)에 용해시켰다. 이 용액에 브로모 트리메틸실란(TMSBr, 0.12 g, 0.32 mmol)을 0 oC에서 첨가 하였다. 혼합물을 0℃에서 30분 동안, 이어서 실온에서 16시간 동안 교반하였다. 휘발물을 진공에서 제거하고 잔류물을 건조 톨루엔과 함께 증발시켰다(3회). 잔류물을 물에 용해시키고 동결 건조시켜 추가 정제 없이 다음 단계에 대한 오일로서 조질의 6f(조악한 수율>100%)를 수득하였다.
실시예 11E
아지도-중간체 6e는 CAS 35899-89-9와 함께 상업적으로 입수 가능하였다.
실시예 11F
아지도 중간체 말토오스-N3(6g)은 Tetrahedron Letters, 2001, 42 (7), 1325-1328에 따라 합성되었다.
실시예 12
중간체 6d의 제조(도 13 참조)
이중 설보네이트를 갖는 아지도-중간체 6d를 도 13에 기재된 바와 같이 합성하였다. 아지도에탄아민31은 2당량의 브로모아세테이트 32와 반응한 다음 가수분해하여 이중산 33을 얻었고, 이를 펜타 플루오로페놀 34를 사용하여 활성화된 에스테르 35로 전환시켰다. 화합물 35를 타우린으로 아미드화하여 중간체 6d를 제공하였다.
2-{2-[(2-아지도에틸)({[(2-설포에틸)카바모일]메틸})아미노]아세트아미도}에탄-1-술폰 산(6d)
아세토니트릴(50ml)중 2-아지도에탄아민 31 (0.52 g, 6.0 mmol)의 용액에 tert-부틸 2-브로모아세테이트 32 (2.6 g, 13 mmol) 및 탄산나트륨 (3.2 g, 30 mmol)을 첨가하였다. 현탁액을 16시간동안 환류시켰다. 실온으로 냉각 한 후, 혼합물을 여과하고 여액을 진공에서 농축시켜 황색 오일(1.6 g, ESI m/z: 315 (M + H)+)을 수득하였다. 유성 생성물 0.62g을 디옥산 (4 N, 10 mL)중 히드로 클로라이드 용액에 용해시켰다. 혼합물을 25℃에서 밤새 교반하고 LCMS가 반응 완료를 나타냈다. 휘발물을 진공에서 제거하여 화합물 33 (0.39 g, ESI m/z: 203 (M + H)+)을 히드로클로라이드염으로서 수득하였으며, 0.20g을 추가 정제없이 다음 단계동안 DCM(5ml)에 용해시켰다. 용액에 DIC (0.38 g, 3.0 mmol), DIPEA (0.77 g, 6.0 mmol) 및 펜타플루오로페놀 34 (0.55 g, 3.0 mol)를 첨가하였다. 반응 혼합물을 실온에서 밤새 교반하였다. LCMS는 반응이 완료되었음을 나타냈다. 혼합물을 진공에서 농축시켜 조 35 (ESI m/z: 289 (M/2 + Na)+)를 얻었고, 이것을 DMF(5ml)에 용해시켰다. 용액에 타우린(0.38 g, 3.0 mmol) 및 DIPEA (0.52 g, 4.0 mmol)를 첨가하였다. 혼합물 25℃에서 밤새 교반하고 생성된 혼합물을 역상 플래쉬크로마토그래피(물 중 0-10% 아세토니트릴(0.01% TFA))로 직접 정제하여 화합물 6d (0.18 g, 2-아지도에탄아민으로부터 34% 수율)를 백색고체로서 수득하였다. ESI m/z: 417 (M + H)+.
실시예 13
중간체 7a, 7c, 7e, 7f, 7j, 7k, 7l, 7m, 7q, 7ab, 7ad, 7ae, 7bb, 7cb, 7fb의 제조 (도 14 참조)
일반절차 E: DMF (0.5 mL per 10 mg of 5)중의 화합물 5의 용액에 실오넹서 아지도 중간체 6 (1.5 eq) 및 DIPEA (0.1 mL per 10 mg of 5)를 첨가하였다. 반응물을 실온에서 24시간 동안 교반하였고, LCMS는 반응의 완료를 나타냈다. 반응 혼합물을 예비-HPLC로 직접 정제하여 화합물 7을 백색고체로서 수득하였다.
{4-[(2
S
)-2-[(2
S
)-2-[(2
R
)-2-아미노-6-(2-{[1-(17-하이드록시-3,6,9,12,15-펜타옥사헵타데칸-1-일)-1
H
,4
H
,5
H
,6
H
,7
H
,8
H
,9
H
-시클로옥트a[d][1,2,3]트리아졸-4-yl]옥시}아세트아미도)헥산아미도]-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸
N
-[(1
S
)-1-{[(1
S
)-1-{[(3
R
,4
S
,5
S
)-1-[(2
S
)-2-[(1
R
,2
R
)-2-{[(1
S
,2
R
)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필]-
N
-메틸카르바메이트 (7a)
화합물 5a (30 mg, 21 μmol)로부터 화합물 6a (20 mg, 64 μmol)의 일반적인 절차 E에 따라, 화합물 7a (30 mg, 74% 수율)를 백색고체로서 수득하였다. ESI m/z: 862 (M/2 + H)+. 1H NMR (MeOD d4 , 500MHz): δ 7.66-7.57 (m, 2H), 7.44-7.29 (m, 6H), 7.26-7.18 (m, 1H), 5.25-5.04 (m, 2H), 4.88-4.74 (m, 2H), 4.70-4.47 (m, 2H), 4.59-4.48 (m, 4H), 4.29-4.17 (m, 4H), 4.00-3.95 (m, 2H), 3.93-3.88 (m, 2H), 3.76-3.70 (m, 1H), 3.69-3.64 (m, 10H), 3.62-3.59 (m, 2H), 3.59-3.55 (m, 8H), 3.49-3.42 (m, 2H), 3.38-3.36 (m, 4H), 3.31-3.28 (m, 3H), 3.27-3.17 (m, 3H), 3.15-3.06 (m, 3H), 3.00-2.87 (m, 4H), 2.57-2.46 (m, 2H), 2.41-2.18 (m, 2H), 2.17-1.99 (m, 5H), 1.98-1.86 (m, 3H), 1.85-1.68 (m, 6H), 1.67-1.54 (m, 9H), 1.50-1.36 (m, 4H), 1.34-1.25 (m, 1H), 1.22-1.12 (m, 6H), 1.06-0.98 (m, 11H), 0.96-0.93 (m, 3H), 0.92-0.84 (m, 9H), 0.79 (m, 2H). ppm.
2-{1-[4-({[(5
R
)-5-아미노-5-{[(1
S
)-1-{[(1
S
)-4-(카바모일아미노)-1-({4-[({[(1
S
)-1-{[(1
S
)-1-{[(3
R
,4
S
,5
S
)-1-[(2
S
)-2-[(1
R
,2
R
)-2-{[(1
S
,2
R
)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필](메틸)카바모일}옥시)메틸]페닐}카바모일)부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1
H
,4
H
,5
H
,6
H
,7
H
,8
H
,9
H
-시클로옥트a[d][1,2,3]트리아졸-1-일]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에탄-1-술폰 산(7c)
화합물 5a (28 mg, 20 μmol)로부터 화합물6c (20 mg, 50 μmol)의 일반적인 절차 E에 따라, 화합물 7c (20 mg, 56% 수율)를 백색 고체로서 수득하였다. ESI m/z: 907.3 (M/2 + H)+.
2-{1-[4-({[(5
R
)-5-아미노-5-{[(1
S
)-1-{[(1
S
)-4-(카바모일아미노)-1-[(4-{[({2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9
.0
4,8
.0
13,18
]이코사-14,17-디엔-8-yl]-2-옥소에틸}카바모일)옥시]메틸}페닐)카바모일]부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1
H
,4
H
,5
H
,6
H
,7
H
,8
H
,9
H
-시클로옥트a[d][1,2,3]트리아졸-1-yl]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에탄-1-술폰 산(7e)
6c를 갖는 5b (60 mg, 52 μmol)의 일반적인 절차 E에 따라, 화합물 7e (60 mg, 74% 수율)를 백색 고체로서 수득하였다. ESI m/z: 781 (M/2 + H)+. 1H NMR (400 MHz, MeOD d4 ) δ 7.61 (d, J = 8.5 Hz, 2H), 7.39-7.28 (m, 3H), 6.39-6.30 (m, 2H), 5.66-5.46 (m, 1H), 5.29-5.13 (m, 1H), 5.12-5.04 (m, 3H), 4.72-4.60 (m, 2H), 4.56-4.49 (m, 2H), 4.36-3.84 (m, 8H), 3.76-3.70 (m, 2H), 3.66-3.54 (m, 14H), 3.30-3.23 (m, 2H), 3.21-3.04 (m, 3H), 3.03-2.97 (m, 2H), 2.96-2.84 (m, 1H), 2.75-2.52 (m, 1H), 2.50-2.42 (m, 2H), 2.39-2.01 (m, 6H), 1.99-1.78 (m, 6H), 1.74-1.22(m, 22H), 1.03-0.87 (m, 12H) ppm.
2-[2-({2-[4-({[(5
R
)-5-아미노-5-{[(1
S
)-1-{[(1
S
)-4-(카바모일아미노)-1-[(4-{[({2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9
.0
4,8
.0
13,18
]이코사-14,17-디엔-8-yl]-2-옥소에틸}카바모일)옥시]메틸}페닐)카바모일]부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1
H
,4
H
,5
H
,6
H
,7
H
,8
H
,9
H
-시클로옥트a[d][1,2,3]트리아졸-1-일]에틸}({[(2-설포에틸)카바모일]메틸})아미노)아세트아미도]에탄-1-술폰 산(7f)
6d에 의한 5b (0.10 g, 86 μmol)의 일반적인 절차 E에 따라, 화합물 7f (65 mg, 48% 수율)를 백색고체로서 수득하였다. ESI m/z: 790 (M/2 + H)+. 1H NMR (500MHz, DMSO d6 ) δ 10.1-10.0 (m, 1H), 8.60-8.50 (m, 1H), 8.40-8.30 (m, 1H), 8.30-8.20 (m, 2H), 8.15-8.00 (m, 4H), 7.60-7.55 (m, 2H), 7.50-7.40 (m, 1H), 7.30-7.20 (m, 4H), 6.30 (d, J = 10.5 Hz, 1H), 6.15-6.00 (m, 2H), 5.70-5.55 (m, 3H), 4.98 (s, 2H), 4.80-4.70 (m, 1H), 4.59 (t, J = 4.0 Hz, 1H), 4.50-4.45 (m, 1H), 4.40-4.35 (m, 2H), 4.25-4.10 (m, 2H), 3.95-3.80 (m, 4H), 3.20-2.90 (m, 10H), 2.85-2.75 (m, 2H), 2.70-2.60 (m, 4H), 2.31-2.10 (m, 3H), 2.10-1.95 (m, 6H), 1.80-1.65 (m, 6H), 1.65-1.55 (m, 7H), 1.40-1.20 (m, 12H), 1.20-1.10 (m, 1H), 1.06 (t, J = 7.0 Hz, 1H), 1.02-1.00 (m, 1H), 0.90-0.80 (m, 16H) ppm.
2-{1-[4-({[(5
R
)-5-아미노-5-{[(1
S
)-1-{[(1
S
)-4-(카바모일아미노)-1-{[4-({[(4-{2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9
.0
4,8
.0
13,18
]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카바모일]옥시}메틸)페닐]카바모일}부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1
H
,4
H
,5
H
,6
H
,7
H
,8
H
,9
H
-시클로옥트a[d][1,2,3]트리아졸-1-yl]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에탄-1-술폰 산(7i)
6c를 갖는 5c (55 mg, 54 μmol)의 일반적인 절차 E에 따라, 화합물 7i (53 mg, 수율 43%)를 백색고체로서 수득하였다. ESI m/z: 827.6 (m/2 + H)+. 1HNMR (400 MHz, MeOD d4 ) δ 7.63-7.61 (m, 2H), 7.40-7.29 (m, 5H), 6.89-6.85 (m, 2H), 6.38-6.33 (m, 2H), 5.65-5.48 (m, 1H), 5.31-5.06 (m, 4H), 4.91-4.70 (m, 4H), 4.65-4.22 (m, 5H), 4.07-3.86 (m, 5H), 3.74-3.63 (m, 16H), 3.33-2.82 (m, 4H), 2.76-1.21 (m, 39H), 1.06-0.93 (m ,12H) ppm.
2-{1-[4-({[(5
R
)-5-아미노-5-{[(1
S
)-1-{[(1
S
)-1-[(4-{2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9
.0
4,8
.0
13,18
]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카바모일]에틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1
H
,4
H
,5
H
,6
H
,7
H
,8
H
,9
H
-시클로옥트a[d][1,2,3]트리아졸-1-yl]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에탄-1-술폰 산(7j)
6c를 갖는 5d (55 mg, 54 μmol)로부터의 일반적인 절차 E에 따라, 화합물 7j (70 mg, 67% 수율)를 백색 고체로서 수득하였다. ESI m/z: 709.9 (M/2 + H)+. 1H NMR (400 MHz, MeOD d4 ) δ 7.58-7.48 (m, 2H), 7.35 (d, J = 8.8 Hz, 1H), 6.92-6.88 (m, 2H), 6.38-6.34 (m, 1H), 6.33 (s, 1H), 5.65-5.46 (m ,1H), 5.31-5.07 (m, 2H), 4.87-4.44 (m, 7H), 4.36-4.13 (m ,2H), 4.06-3.87 (m, 5H), 3.75-3.55 (m, 16H), 3.33-2.60 (m, 6H), 2.47-1.79 (m, 13H), 1.72-1.43 (m, 21H), 1.03-0.94 (m, 12H) ppm.
2-{1-[4-({[(5
R
)-5-아미노-5-{[(1
S
)-1-{[(1
S
)-4-(카바모일아미노)-1-[(4-{2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9
.0
4,8
.0
13,18
]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카바모일]부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1
H
,4
H
,5
H
,6
H
,7
H
,8
H
,9
H
-시클로옥타[d][1,2,3]트리아졸-1-일]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에탄-1-술폰 산(7k)
6c를 갖는 5e (60 mg, 54 μmol)로부터의 일반적인 절차 E에 따라, 화합물7k (50 mg, 61% 수율)를 백색 고체로서 수득하였다. ESI m/z: 753 (M/2 + H)+.
2-{1-[4-({[(5
R
)-5-아미노-5-{[(1
S
)-1-{[(1
S
)-1-({4-[({[(1
S
)-1-{[(4b
S
,8
S
,8a
R
)-8-({[(1
S
,4a
S
,10a
R
)-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타히드로페난트렌-1-일]포름아미도}카르보닐)-4b,8-디메틸-4b,5,6,7,8,8a,9,10-옥타히드로페난트렌-3-일]카바모일}-2-하이드록시에틸]카바모일}옥시)메틸]페닐}카바모일)-4-(카바모일아미노)부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1
H
,4
H
,5
H
,6
H
,7
H
,8
H
,9
H
-시클로옥타[d][1,2,3]트리아졸-1-yl]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에탄-1-술폰 산(7q)
물(1 mL) 중 화합물 6c (20 mg, 50 μmol)의 . pH ~ 7까지 0℃에서 중탄산나트륨용액에 적가하였다. 이어서 교반된 용액에 화합물 5? (28 mg, 21 μmol)의 아세토니트릴(1ml)용액에 첨가하였다. 혼합물 25℃에서 밤새 교반하였다. 화합물 5?가 완전히 소비될 때까지 반응 혼합물을 LCMS로 모니터링 하였다. 반응 혼합물을 여과하고 예비-HPLC(방법 A)에 의해 정제하여 화합물 7q (15 mg, 41% 수율)를 백색고체로서 수득하였다. ESI m/z: 856.5 (M/2 + 1)+.
(2-{1-[4-({[(5R)-5-아미노-5-{[(1S)-1-{[(1S)-4-(카바모일아미노)-1-({4-[({[(1S)-1-{[(1S)-1-{[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-2-{[(1S,2R)-1-하이드록시-1-페닐프로판-2-yl]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필](메틸)카바모일}옥시)메틸]페닐}카바모일)부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-1-일]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에틸)트리메틸아자늄 클로라이드 (7ab)
밤새 50℃에서 교반한 것을 제외하고 5a (55 mg, 39 μmol)로부터 6b까지 일반적인 절차에 따라, 화합물 7ab (50 mg, 70% 수율)를 백색 고체로서 수득하였다. ESI m/z: 896 [(M + H)/2]+. 1H NMR (400 MHz, DMSO d4 ) δ 9.35 (s, 1H), 8.95 (s, 1H), 8.43-8.34 (m, 1H), 8.07-8.00 (m, 1H), 7.91-7.83 (m, 1H), 7.79-7.60 (m, 4H), 7.33-7.23 (m, 6H), 7.20-7.13 (m, 1H), 6.30-5.80 (m, 1H), 5.49-5.34 (m, 1H), 5.12-4.83 (m, 3H), 4.77-4.71 (m, 1H), 4.54-4.38 (m, 4H), 4.27 (t, J = 11.6 Hz, 1H), 4.03-3.93 (m, 4H), 3.85-3.75 (m, 5H), 3.59 (t, J = 6.2 Hz, 3H), 3.50-3.40 (m, 15H), 3.38-3.35 (m, 2H), 3.26-3.16 (m, 7H), 3.13-3.03 (m, 14H), 2.99-2.92 (m, 4H), 2.89-2.78 (m, 4H), 2.44-2.38 (m, 1H), 2.34 (t, J = 6.2 Hz, 2H), 2.30-2.22 (m, 2H), 2.15-1.93 (m, 6H), 1.85-1.42 (m, 19H), 1.37-1.23 (m, 3H), 1.06-0.96 (m, 7H), 0.94-0.71 (m, 27H) ppm.
{17-[4-({[(5R)-5-아미노-5-{[(1S)-1-{[(1S)-4-(카바모일아미노)-1-({4-[({[(1S)-1-{[(1S)-1-{[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-2-{[(1S,2R)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-yl]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필](메틸)카바모일}옥시)메틸]페닐}카바모일)부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-1-yl]-3,6,9,12,15-펜타옥사헵타데칸-1-일}포스폰 산 (7ad)
화합물 5a (18 mg, 13 μmol)로부터 화합물6f (14 mg, 38 μmol)를 사용한일반적인 절차에 따라, 화합물 7ad (15 mg, 58% 수율)를 백색고체로서 수득하였다. ESI m/z: 893.9 (M/2 + H)+. 1H NMR (MeOD d4 , 500MHz): δ 7.98-7.91 (m, 1H), 7.79-7.59 (m, 2H), 7.41-7.20 (m, 6H), 5.51-5.06 (m, 2H), 4.78-4.53 (m, 6H), 4.29-3.88 (m, 9H), 3.78-3.75 (m, 3H), 3.64-3.58 (m, 16H), 3.47-3.36 (m, 6H), 3.29-3.07 (m, 8H), 3.01-2.80 (m, 4H), 2.58-2.05 (m, 10H), 1.96-1.32 (m, 26H), 1.21-1.14 (m, 6H), 1.02-0.71 (m, 25H) ppm.
{4-[(2S)-2-[(2S)-2-[(2R)-2-아미노-6-[2-({1-[(2R,3R,4S,5R,6R)-3,4,5-트리하이드록시-6-(하이드록시메틸)옥산-2-일]-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-4-일}옥시)아세트아미도]헥산아미도]-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸N-[(1S)-1-{[(1S)-1-{[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-2-{[(1S,2R)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필]-N-메틸카르바메이트 (7ae)
화합물 5a (6.0 mg, 4.2 μmol)로부터 화합물6e (3.0 mg, 15 μmol)의 일반적인 절차에 따라, 화합물 7ae의 반응 용액을 얻고 다음 단계에 직접 사용하다. ESI m/z: 811 (M/2 + H)+.
(2-{1-[4-({[(5R)-5-아미노-5-{[(1S)-1-{[(1S)-4-(카바모일아미노)-1-[(4-{[({2-[(1S,2S,4R,8S,9S,11S,12R,13S,19S)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-8-yl]-2-옥소에틸}카바모일)옥시]메틸}페닐)카바모일]부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-1-yl]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에틸)트리메틸아자늄 클로라이드 (7bb)
밤새 50℃에서 교반한 것을 제외하고 6b로 5b (40 mg, 34 μmol)의 일반적인 절차 E에 따라, 화합물7bb (40 mg, 76% 수율)를 예비-HPLC(방법 B)에 의해 정제한 후 백색고체를 수득하였다. ESI m/z: 770 [(M + 18)/2]+. 1H NMR (400 MHz, DMSO d6 ) δ 10.13-8.87 (m, 2H), 8.58-8.21 (m, 2H), 8.09-7.85 (m, 2H), 7.82-7.64 (m, 3H), 7.63-7.55 (m, 1H), 7.49-7.37 (m, 1H), 7.34-7.16 (m, 3H), 6.34-6.21 (m, 1H), 6.15-5.99 (m, 2H), 5.78-5.42 (m, 3H), 5.01-4.83 (m, 3H), 4.81-4.69 (m, 2H), 4.63-4.47 (m, 2H), 4.45-4.34 (m, 2H), 4.27-4.07 (m, 3H), 4.04-3.96 (m, 1H), 3.91-3.70 (m, 6H), 3.60 (t, J = 6.2 Hz, 2H), 3.53-3.40 (m, 14H), 3.15-3.01 (m, 11H), 3.00-2.88 (m, 3H), 2.83-2.73 (m, 1H), 2.68-2.56 (m, 1H), 2.38-2.19 (m, 4H), 2.13-1.93 (m, 4H), 1.87-1.74 (m, 2H), 1.71-1.64 (m, 2H), 1.62-1.18 (m, 22H), 1.14-1.02 (m, 1H), 0.97-0.70 (m, 12H) ppm.
(2-{1-[4-({[(5R)-5-아미노-5-{[(1S)-1-{[(1S)-4-(카바모일아미노)-1-{[4-({[(4-{2-[(1S,2S,4R,8S,9S,11S,12R,13S,19S)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카바모일]옥시}메틸)페닐]카바모일}부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-1-yl]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에틸)트리메틸아자늄 (7cb)
실온에서 24시간동안 교반하면서 6b (44 mg, 35 μmol)의 일반적인 절차에 따라, 역상 플래쉬크로마토그래피(수성 TFA(0.03%)중 0-100% 아세토니트릴)에 의해 정제한 후 화합물 7cb (44 mg, 수율 77%)를 백색고체로서 수득하였다. ESI m/z: 816.0 (m/2 + H)+; 544.5 (M/3 + H)+.
1-(4-(2-(((R)-5-아미노-6-(((S)-1-(((S)-1-(((4bS,8S,8aR)-8-(((1S,4aS,10aR)-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타하이드로페난트렌-1-카르보닐)카바모일)-4b,8-디메틸-4b,5,6,7,8,8a,9,10-옥타히드로페난트렌-3-일)아미노)-1-옥소프로판-2-yl)아미노)-3-메틸-1-옥소부탄-2-일)아미노)-6-옥소헥실)아미노)-2-옥소에톡시)-4,5,6,7,8,9-헥사하이드로-1H-시클로옥타[d][1,2,3]트리아졸-1-일)-N,N,N-트리메틸-15-옥소-3,6,9,12-테트라옥사-16-아자옥타데칸-18-아미늄 (7fb)
실온에서 24시간 동안 교반하는 6b (50 mg, 50 μmol)의 일반적인 절차에 따라, 역상 플래쉬 크로마토그래피(0-30% 수성 TFA(0.03%)중 아세토니트릴)로 정제한 후 화합물 7fb (50 mg, 73% 수율)를 백색 고체로서 수득 하였다. ESI m/z: 684 (M/2 + H)+.
실시예 14
중간체 7h, 7l의 제조(도 15 참조)
일반 절차 F: DMF(화합물 3의 그램당 40 mL)중 화합물4b (1.2 eq.)의 용액에 EDCI (1.5 eq.), HOBt (2.0 eq.), 화합물 3 (3b 또는 3e, 1.0 eq.) 및 트리에틸아민 (3.0 eq.)을 실온에서 연속적으로 첨가하였다. 생성된 혼합물을 실온에서 밤새 교반하였다. LCMS는 화합물 4b가 완전히 소모되었음을 나타냈다(화합물 3은 소모되지 않음). 반응물에 디에틸아민(화합물 3 그램당 6ml, 과량)을 첨가하였다. LCMS에 따라 Fmoc가 제거될 때까지 반응 혼합물을 실온에서 2시간동안 교반하였다. 반응 혼합물을 역상 플래쉬 크로마토그래피(수성 중탄산 암모늄 (10mM)중 0-100% 아세토니트릴)로 직접 정제하여 화합물 7(7h 또는 7l, 25-26% 수율)을 백색 고체로 수득하고 반응하지 않은 화합물 3을 회수할 수 있었다.
2-[(4
R
)-4-아미노-4-{[(1
S
)-1-{[(1
S
)-4-(카바모일아미노)-1-[(4-{[({2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9
.0
4,8
.0
13,18
]이코사-14,17-디엔-8-yl]-2-옥소에틸}카바모일)옥시]메틸}페닐)카바모일]부틸]카바모일}-2-메틸프로필]카바모일}부탄아미도]에탄-1-술폰 산(7h)
4b를 갖는 3b (50 mg, 57 μmol)로부터의 일반적인 절차 F에 따라, 역상 플래쉬 크로마토그래피(물 중 0-100% 아세토니트릴, 17 mg의 화합물 3b를 재순환시켰다(재순환 수율 34%)로 정제한 후 화합물 7h (17 mg, 26% 수율)를 백색 고체로서 수득하였다. ESI m/z: 1107 (M + H)+. 1H NMR (500 MHz, DMSO d6 ) δ 10.07 (s, 1H), 8.31 (d, J = 7.0 Hz, 2H), 7.81 (t, J = 5.5 Hz, 1H), 7.61-7.60 (m, 2H), 7.45-7.42 (m, 1H), 7.30-7.27 (m, 3H), 6.30 (d, J = 10 Hz, 1H), 6.11-6.03 (m, 2H), 5.86-5.82 (m, 1H), 5.70-5.57 (m, 2H), 5.46 (s, 2H), 4.97 (s, 2H), 4.78-4.76 (m, 1H), 4.59 (t, J = 4.5 Hz, 1H), 4.41-4.12 (m, 4H), 3.86-3.80 (m, 1H), 3.64-3.58 (m, 1H), 3.21-3.16 (m, 1H), 3.01-2.90 (m, 6H), 2.56 (t, J = 7.5 Hz, 2H), 2.35-2.32 (m, 2H), 2.17-2.14 (m, 2H), 2.09-1.28 (m, 18H), 1.17-1.14 (m, 1H), 0.97 (t, J = 6.5 Hz, 2H), 0.89-0.84 (m, 10H) ppm.
2-[(4
R
)-4-아미노-4-{[(1
S
)-1-{[(1
S
)-4-(카바모일아미노)-1-[(4-{2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9
.0
4,8
.0
13,18
]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카바모일]부틸]카바모일}-2-메틸프로필]카바모일}부탄아미도]에탄-1-술폰 산(7l)
4b의 3e (80 mg, 98 μmol)로부터의 일반적인 절차 F에 따라, 역상 플래쉬 크로마토그래피(수중0-100% 아세토니트릴)로 정제한 후 화합물7l (26 mg, 25% 수율)을 백색 고체로서 수득하였다. ESI m/z: 525.8 (M/2 + H)+.
{4-[(2S)-2-[(2S)-2-[(2R)-2-아미노-4-{[(2S)-2-[(4R,5R)-5-[(4R)-2,2-디메틸-1,3-디옥솔란-4-일]-2,2-디메틸-1,3-디옥솔란-4-일]-2-하이드록시에틸]카바모일}부탄아미도]-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸N-[(1S)-1-{[(1S)-1-{[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-2-{[(1S,2R)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필]-N-메틸카르바메이트 (7ah)
DMF (1 mL)중 중간체 4c (25 mg, 41 μmol)의 용액에 실온에서 HATU (23 mg, 61 μmol)를 첨가하였다. 수득한 용액을 실온에서 1시간 동안 교반하였다. 이 현탁액에 DMF (1 mL)중 vcPAB-MMAE 3a (28 mg, 25 μmol)의 용액에 이어서 NMM (1 drop, excess)을 첨가하였다. 반응 혼합물을 실온에서 3시간 동안 교반하고 투명해졌다. 화합물 3a가 완전히 소비될 때까지 LCMS에 의해 반응을 모니터링 하였다. 이어서, 반응 혼합물에 디에틸아민(과량)을 첨가하고, 생성된 혼합물을 실온에서 밤새 교반하였다. LCMS에 따라 반응을 완료하였다. 휘발물을 진공에서 제거하고 잔류물을 역상 플래쉬 크로마토그래피(수성 TFA(0.5%)중 0-100%아세토니트릴)로 정제하여 화합물 7ah (25 mg, 67% 수율)를 백색 고체로서 수득하였다. ESI m/z: 1495 (M + H)+. 1H NMR (MeOD d4 , 500 MHz): δ 7.65-7.55 (m, 2H), 7.46-7.28 (m, 6H), 7.23 (t, J = 7.1 Hz, 1H), 5.27-5.02 (m, 2H), 4.72-4.47 (m, 4H), 4.30-4.05 (m, 6H), 4.03-3.78 (m, 4H), 3.78-3.65 (m, 1H), 3.61-3.40 (m, 4H), 3.39-3.27 (m, 5H), 3.26-3.16 (m, 2H), 3.17-3.08 (m, 3H), 3.00-2.91 (m, 3H), 2.58-2.11 (m, 7H), 2.10-1.52 (m, 12H), 1.50-1.25 (m, 15H), 1.24-1.11 (m, 6H), 1.05-0.69 (m, 26H) ppm.
실시예 14A
중간체 8c의 제조(도 15B 참조)
1-[2-(시클로옥트-2-인-1-일옥시)아세트아미도]-3,6,9,12-테트라옥사펜타데칸-15-옥시 산 (8c)
DMF (3 mL)중 화합물 36 (0.50 g, 1.8 mmol) 및 37 (0.65 g, 1.8 mmol)의 혼합물에 실온에서 DIPEA (1.2 g, 9.0 mmol)를 첨가하였다 혼합물을 실온에서 30분 동안 교반하였다. 반응 혼합물을 예비-HPLC(방법 A)에 의해 직접 정제하여 OCT-PEG4-산 (8c) (0.70 g, 91% 수율)을 담황색 오일로서 수득하였다. ESI m/z: 430 (M + H)+.
8d 및 8e는 당업자에게 공지된 적합한 출발물질을 사용하여 8c의 제조방법과 유사한 방법을 사용하여 제조하였다.
실시예 15
1a의 제조(도 16 참조)
DMF (1 mL per 10 mg of 8a)중의 DIBAC-suc-PEG4-acid 8a (1.2-1.3 eq.)의 용액에 실온에서 HATU (1.3 eq.) 및 DIPEA (5.0 eq.)를 첨가하였다. 혼합물을 실온에서 30분 동안 교반한 후, DMF(0.6 mg per 10 mg of 7a)중 화합물7a (1.0 eq.)의 용액을 첨가하였다. 화합물 7이 소모될때까지 생성된 혼합물을 실온에서 교반하였고, 이를 LCMS에 의해 모니터링하였다. 여과 후, 여액을 예비-HPLC로 직접 정제하여 화합물 1a를 수득하였다.
일반절차 G( 8a , 8c 또는 8d ): DMF (1 mL per 10 mg of 8)중 산8 (8a, 8c 또는 8d, 1.2-1.3 eq.)의 용액에 HATU (1.3 eq.) 및 DIPEA (5.0 eq.)을 실온에서 첨가하였다. 혼합물을 실온에서 30분동안 교반한 후, DMF(0.6 mg per 10 mg of 7)중 화합물 7 (1.0 eq.)의 용액을 첨가하였다. 화합물 7이 소모될때까지 생성된 혼합물을 실온에서 교반하였고, 이를 LCMS에 의해 모니터링 하였다. 여과 후, 여과액을 예비-HPLC로 직접 정제하여 링커-페이로드 1, 및 II-V를 제공하였다.
실시예 16
1a, 1c, 1e, 1f, 1h, 1i, 1j, 1k, 1l, 1m 1q의 제조(도 17 참조)
일반 절차 H(8b 또는 8e): DMF (1 mL per 50 mg)중 화합물7 (1.0 eq.)의 용액으로 실온에서 화합물 DIBAC-PEG4-NHS 8b (1.1-1.2 eq.) 및 DIPEA (5.0 eq.)를 실온에서 첨가하였다. 반응 혼합물을 실온에서 3시간 동안 교반하였다. 반응 혼합물을 예비-HPLC로 직접 정제하여 화합물 1을 수득하였다.
실시예 17
1a의 제조(도 17 참조)
{4-[(2
S
)-2-[(2
S
)-2-[(2
R
)-2-[1-(4-{2-아자트리시클로[10.4.0.0
4,9
]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-6-(2-{[1-(17-하이드록시-3,6,9,12,15-펜타옥사헵타데칸-1-일)-1
H
,4
H
,5
H
,6
H
,7
H
,8
H
,9
H
-시클로옥타[d][1,2,3]트리아졸-4-yl]옥시}아세트아미도)헥산아미도]-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도] 페닐}메틸
N
-[(1
S
)-1-{[(1
S
)-1-{[(3
R
,4
S
,5
S
)-1-[(2
S
)-2-[(1
R
,2
R
)-2-{[(1
S
,2
R
)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필]-
N
-메틸카르바메이트 (1a)
화합물 7a (25 mg, 15 μmol)로부터 화합물 8a (10 mg, 18 μmol)의 일반적인 절차 G에 따라, 링커 페이로드 1a (24 mg, 73% 수율)를 백색고체로서 수득하였다. ESI: 753 (M/3 + H)+. 1H NMR (500 MHz, MeOD d4 ) δ 7.74-7.69 (m, 2H), 7.67-7.64 (m, 1H), 7.63-7.59 (m, 1H), 7.53-7.45 (m, 3H), 7.42-7.29 (m, 9H), 7.25-7.20 (m, 1H), 5.22-5.05 (m, 3H), 4.70-4.49 (m, 4H), 4.47-4.43 (m, 1H), 4.33-4.29 (m, 1H), 4.27-4.16 (m, 4H), 4.00-3.95 (m, 2H), 3.92-3.87 (m, 2H), 3.77-3.69 (m, 2H), 3.68-3.63 (m, 10H), 3.61-3.52 (m, 21H), 3.49-3.41 (m, 5H), 3.38-3.36 (m, 4H), 3.30-3.27 (m, 3H), 3.27-3.22 (m, 3H), 3.20-3.14 (m, 2H), 3.12 (s, 1H), 3.10-3.03 (m, 1H), 2.99-2.86 (m, 4H), 2.82-2.68 (m, 2H), 2.56-2.12 (m, 10H), 2.11-1.97 (m, 5H), 1.91-1.79 (m, 5H), 1.76-1.53 (m, 10H), 1.48-1.37 (m, 3H), 1.34-1.26 (m, 1H), 1.21-1.12 (m, 14H), 1.06-0.93 (m, 14H), 0.92-0.81 (m, 10H) ppm.
실시예 17A
1b의 제조(도 17 참조)
(2-{1-[4-({[(5R)-5-[1-(4-{2-아자트리시클로[10.4.0.04,9]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-5-{[(1S)-1-{[(1S)-4-(카바모일아미노)-1-({4-[({[(1S)-1-{[(1S)-1-{[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-2-{[(1S,2R)-1-하이드록시-1-페닐프로판-2-yl]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-yl](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필](메틸)카바모일}옥시)메틸]페닐}카바모일)부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-1-일]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에틸)트리메틸아자늄 (Ib)
화합물 7ab (45 mg, 25 μmol) 로부터 화합물 8a (16 mg, 29 μmol)의 일반적인 절차 G에 따라, 링커-페이로드 Ib (16 mg, 27% 수율)를 백색고체로서 수득하였다. ESI m/z: 766 [(M+H)/3]+. 1H NMR (500MHz, DMSO d6 ): δ 9.78 (s, 1H), 8.34-8.04 (m, 5H), 7.95-7.83 (m, 2H), 7.79-7.74 (m, 1H), 7.70-7.56 (m, 5H), 7.52-7.43 (m, 3H), 7.40-7.11 (m, 12H), 6.08 (s, 1H), 5.43 (s, 2H), 5.06-5.00 (m, 2H), 4.76-4.71 (m, 1H), 4.54-4.39 (m, 4H), 4.35-4.15 (m, 4H), 4.03-3.92 (m, 2H), 3.85-3.73 (m, 5H), 3.64-3.55 (m, 5H), 3.46-3.43 (m, 20H), 3.25-3.16 (m, 11H), 3.13-3.05 (m, 15H), 3.00-2.93 (m, 5H), 2.89-2.82 (m, 4H), 2.80-2.73 (m, 2H), 2.61-2.55 (m, 1H), 2.42-2.32 (m, 5H), 2.31-2.20 (m, 4H), 2.15-2.04 (m, 4H), 2.03-1.95 (m, 4H), 1.83-1.65 (m, 8H), 1.57-1.38 (m, 11H), 1.30-1.19 (m, 10H), 1.06-0.96 (m, 7H), 0.87-0.76 (m, 20H) ppm.
실시예 18
1c의 제조(도 17 참조)
2-{1-[4-({[(5R)-5-[1-(4-{2-아자트리시클로[10.4.0.04,9]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-5-{[(1S)-1-{[(1S)-4-(카바모일아미노)-1-({4-[({[(1S)-1-{[(1S)-1-{[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-2-{[(1S,2R)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필](메틸)카바모일}옥시)메틸]페닐}카바모일)부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-1-yl]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에탄-1-술폰 산(1c)
화합물 7c (20 mg, 11 μmol)로부터 화합물 8b (7.1 mg, 11 μmol)의 일반적인 절차 H에 따라, 링커-페이로드 1c (5.0 mg, 19%수율)를 백색고체로서 수득하였다. ESI m/z: 1174.7 (M/2 + H)+. 1H NMR (MeOD d4 , 500MHz): δ 8.38-8.17 (m, 2H), 7.99-7.87 (m, 2H), 7.77-7.56 (m, 4H), 7.49-7.20 (m, 9H), 5.36 (t, J = 4.5 Hz, 1H), 5.21 -5.07 (m, 4H), 4.71-4.18 (m, 9H), 3.98-3.88 (m, 5H), 3.74-3.43 (m, 37H), 3.37-3.36 (m, 6H), 3.29-3.12 (m, 6H), 3.00-2.88 (m, 6H), 2.75 -2.33 (m, 5H), 2.32-1.78 (m, 17H), 1.64-1.34 (m, 15H), 1.20-1.13 (m, 6H), 1.03-0.76 (m, 30H) ppm.
실시예 18A
Id 의 제조(도 17 참조)
{4-[(2S)-2-[(2S)-2-[(2R)-2-[1-(4-{2-아자트리시클로[10.4.0.04,9]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-6-(2-{[1-(14-{[(1S)-1-{[(1S)-4-(카바모일아미노)-1-({4-[({[(1S)-1-{[(1S)-1-{[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-2-{[(1S,2R)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-yl]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필](메틸)카바모일}옥시)메틸]페닐}카바모일)부틸]카바모일}-2-메틸프로필]카바모일}-3,6,9,12-테트라옥사테트라데칸-1-yl)-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-4-yl]옥시}아세트아미도)헥산아미도]-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸N-[(1S)-1-{[(1S)-1-{[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-2-{[(1S,2R)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필]-N-메틸카르바메이트 (Id)
화합물 8a (4.4 mg, 8.0 μmol)를 갖는 화합물 7ad (12 mg, 6.7 μmol) 로부터의 일반적인 절차 G에 따라, 링커-페이로드 Id (3.0 mg, 19% 수율)를 백색고체로서 수득하였다. ESI m/z: 774.7 (M/3 + H)+. 1H NMR (MeOD d4 , 500MHz): δ 8.00-7.90 (m, 1H), 7.94-7.61 (m, 4H), 7.49-7.47(m, 3H), 7.41-7.14 (m, 9H), 5.37-5.03 (m, 5H), 4.70-4.44 (m, 6H), 4.34-3.90 (m, 7H), 3.77-3.42 (m, 38H), 3.37-3.35 (m, 4H), 3.29 (s, 3H), 3.27-3.01 (m, 9H), 2.97-2.87 (m, 6H), 2.75-2.59 (m, 2H), 2.53-2.16 (m, 9H), 2.06-1.81 (m, 12H), 1.64-1.32 (m, 19H), 1.20-1.13 (m, 6H), 1.03-0.79 (m, 21H) ppm. Anal. HPLC: 95%, Retention time: 5.56 and 6.64 min (method B).
실시예 18B
Ie-1 의 제조(도 17 참조)
{4-[(2S)-2-[(2S)-2-[(2R)-2-[1-(4-{2-아자트리시클로[10.4.0.04,9]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-6-[2-({1-[(2R,3R,4S,5R,6R)-3,4,5-트리하이드록시-6-(하이드록시메틸)옥산-2-일]-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-4-일}옥시)아세트아미도]헥산아미도]-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐}메틸N-[(1S)-1-{[(1S)-1-{[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-2-{[(1S,2R)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필]-N-메틸카르바메이트 (Ie-1) (트리아졸이성질체와 함께)
화합물 8a 를 갖는 화합물 7ae로부터의 일반적인 절차 H에 따라, 트리아졸이성질체(HPLC에 의해 3/2의 비)(13 mg, 5a로부터 수율 30%)를 갖는 화합물 Ie-1을 예비-HPLC(방법B)에 의한 정제 후 백색고체로서 수득하였다. ESI m/z: 1078 (M/2 + H)+ (100%), 2156.9 (M + H)+ (10%). 1H NMR (DMSO d6 , 500 MHz): δ 9.69 (m, 1H), 8.08-8.30 (m, 4H), 7.84-7.89 (m, 1H), 7.61-7.75 (m, 6H), 7.45-7.49 (m, 2H), 7.16-7.37 (m, 10H), 5.96 (m, 1H), 5.34-5.51 (m, 4H), 4.97-5.16 (m, 5H), 4.62-4.75 (m, 4H), 3.92-4.49(m, 9H), 3.77-3.80 (m, 3H), 3.40-3.72 (m, 18H), 3.24 (s, 3H), 3.23 (s, 2H), 3.18-3.20 (m, 4H), 2.88-3.17 (m, 17H), 2.54-2.83 (m, 2H), 2.35-2.42 (m, 2H), 2.22-2.29 (m, 3H), 1.96-2.15 (m, 7H), 1.72-1.82 (m, 5H), 1.28-1.65 (m, 16H), 0.87-1.05 (m, 6H), 0.75-0.87 (m, 27H). Anal. HPLC: isomer 1: 60.3%, Retention time: 7.34 min; isomer 2: 39.7%, Retention time: 7.41 min (method B).
실시예 18C
If-1 의 제조(도 17 참조)
{4-[(2S)-5-(카바모일아미노)-2-[(2S)-2-[(2R)-2-[1-(2,5-디옥소-2,5-디하이드로-1H-피롤-1-일)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-6-[2-({1-[(2R,3R,4S,5R,6R)-3,4,5-트리하이드록시-6-(하이드록시메틸)옥산-2-yl]-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-4-yl}옥시)아세트아미도]헥산아미도]-3-메틸부탄아미도]펜탄아미도]페닐}메틸N-[(1S)-1-{[(1S)-1-{[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-2-{[(1S,2R)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필]-N-메틸카르바메이트 (If-1)
7ae (반응 용액) 및 8e로부터의 일반적인 절차 H에 따라, 트리아졸이성질체(HPLC에 의해 3/2의 비)( 1.5 mg, 5a로부터 수율 18%)를 갖는 화합물 If-1 을 예비-HPLC(방법A)에 의한 정제 후 백색고체로서 수득하였다. ESI m/z: 974.7 (M/2 + H)+ (100%), 1972 (M + Na)+ (20%). 1H NMR (DMSO d6 , 500 MHz): δ 9.69 (s, 1H), 8.19-7.97 (m, 4H), 7.92-7.83 (m, 1H), 7.66-7.54 (m, 3H), 7.36-7.23 (m, 6H), 7.22-7.12 (m, 2H), 7.01 (s, 2H), 6.87 (s, 2H), 6.68-6.59 (m, 2H), 6.03-5.93 (m, 1H), 5.47-5.26 (m, 5H), 5.20-5.11 (m, 1H), 5.07-4.95 (m, 2H), 4.80-4.58 (m, 3H), 4.53-4.38 (m, 2H), 4.36-4.12 (m, 5H), 4.04-3.94 (m, 2H), 3.84-3.76 (m, 3H), 3.68-3.37 (m, 21H), 3.26-3.17 (m, 7H), 3.13-2.96 (m, 7H), 2.90-2.81 (m, 3H), 2.44-2.34 (m, 2H), 2.31-2.21 (m, 2H), 2.18 (s, 3H), 2.15-1.94 (m, 9H), 1.77-1.74 (m, 2H), 1.69-1.59 (m, 4H), 1.56-1.42 (m, 9H), 1.32-1.27 (m, 2H), 1.06-0.96 (m, 6H), 0.90-0.72 (m, 26H) ppm. Anal. HPLC: isomer 1: 76.0%, Retention time: 7.19 min; isomer 2: 24.0%, Retention time: 7.28 min (method A).
실시예 18D
Ig 의 제조(도 18 참조)
{4-[(2S)-2-[(2S)-2-[(2R)-2-[1-(4-{2-아자트리시클로[10.4.0.04,9]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-4-{[(2S,3R,4R,5R)-2,3,4,5,6-펜타하이드록시헥실]카바모일}부탄아미도]-3-메틸부탄아미도]-5-(카바모일아미노)펜탄아미도]페닐} 메틸N-[(1S)-1-{[(1S)-1-{[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-2-{[(1S,2R)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필]-N-메틸카르바메이트 (Ig)
DCM(3ml)중 중간체 7ah (40 mg, 27 μmol)의 혼합물에 TFA (0.25 mL)를 0℃에서 적가하였다. 혼합물을 실온에서 1시간동안 7ah가 소비될 때까지 교반하였다. LCMS에 따라 탈보호가 완료되었다. 휘발물을 진공에서 제거하고 잔류물(ESI m/z: 708 (M/2 + H)+)에 용해시켰다. 용액에 중간체 8b (17 mg, 27 μmol) 및 트리에틸아민(8.2 mg, 81 μmol)을 첨가하였다. 혼합물을 실온에서 밤새 교반하였다. 반응 혼합물을 예비-HPLC(방법B)로 직접 정제하여 Ig (8.0 mg, 7ah 로부터 15%수율)를 백색 고체로서 수득하였다. ESI m/z: 650.8 (M/3 + H)+ (100%), 975 (M/2 + H)+ (40%). 1H NMR (DMSO d6 , 500 MHz): δ 9.75 (s, 1H), 8.31-8.06 (m, 5H), 7.91-7.88 (m, 1H), 7.75-7.74 (m, 2H), 7.68-7.61 (m, 5H), 7.50-7.46 (m, 3H), 7.39-7.24 (m, 11H), 7.17-7.15 (m, 1H), 5.99 (s, 1H), 5.41-5.34 (m, 3H), 5.04-5.01 (m, 2H), 4.77-4.75 (m, 1H), 4.48-4.18 (m, 11H), 4.05-3.95 (m, 3H), 3.62-3.55 (m, 7H), 3.47-3.17 (m, 14H), 3.12-2.97 (m, 10H), 2.88-2.83 (m, 3H), 2.60-2.54 (m, 1H), 2.53-2.51 (m, 2H), 2.42-2.36 (m, 2H), 2.29-2.21 (m, 3H), 2.17-1.99 (m, 8H), 1.79-1.71 (m, 7H), 1.54-1.44 (m, 3H), 1.36-1.28 (m, 2H), 1.05-0.97 (m, 8H), 0.88-0.75 (m, 28H) ppm. Anal. HPLC: 96.9%, 유지 시간: 7.58 min (방법 B).
실시예 18E
Ih-1의 제조(도 18 참조)
{4-[(2S)-5-(카바모일아미노)-2-[(2S)-2-[(2R)-2-[1-(2,5-di옥소-2,5-디하이드로-1H-피롤-1-일)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-4-{[(2R,3S,4S,5S)-2,3,4,5,6-펜타하이드록시헥실]카바모일}부탄아미도]-3-메틸부탄아미도]펜탄아미도]페닐}메틸N-[(1S)-1-{[(1S)-1-{[(3R,4S,5S)-1-[(2S)-2-[(1R,2R)-2-{[(1S,2R)-1-하이드록시-1-페닐프로판-2-일]카바모일}-1-메톡시-2-메틸에틸]피롤리딘-1-일]-3-메톡시-5-메틸-1-옥소헵탄-4-일](메틸)카바모일}-2-메틸프로필]카바모일}-2-메틸프로필]-N-메틸카르바메이트 (Ih-1)
DMF (1 mL)중 중간체 7ah (10 mg, 6.7 μmol)의 용액에 중간체8e (5.9 mg, 13 μmol) 및DIPEA (1.7 mg, 13 μmol)를 첨가하였다. LCMS에 따라 10a의 대부분이 소모될때까지 혼합물을 실온에서 24시간 동안 교반하였다. 반응 혼합물을 막을 통해 여과하고 여과를 예비-HPLC(방법A) (ESI m/z: 912 (M/2 + H)+)에 의해 정제하였다. 동결건조 후의 잔류물을 아세토니트릴(2ml)에 용해시키고 용액에 염화구리(II) 탈수물(19 mg, 0.12 mmol)을 첨가하였다. 혼합물을 실온에서 2일동안 교반하였다. 원하는 질량의 lh가 LCMS에 의해 주요 생성물로서 검출되었다. 무기염을 제거하기 위해 여과한 후, 용액을 예비-HPLC(방법A)로 직접 정제하여 Ih-1 (2.0 mg, 7ah로부터 2단계로 17%수율)을 백색고체로서 수득하였다. ESI m/z: 1742.7 (M + H)+, 1764.8 (M + Na)+. 1H NMR (DMSO d6 , 500 MHz): δ 9.75 (s, 1H), 8.42-7.84 (m, 5H), 7.79-7.70 (m, 1H), 7.68-7.52 (m, 3H), 7.44-7.11 (m, 8H), 7.02 (s, 2H), 6.04-5.93 (m, 1H), 5.45-5.31 (m, 3H), 5.15-4.57 (m, 5H), 4.53-3.91 (m, 14H), 3.84-3.74 (m, 1H), 3.63-3.53 (m, 8H), 3.52-3.09 (m, 9H), 3.04-2.92 (m, 4H), 2.90-2.82 (m, 3H), 2.42-2.36 (m, 2H), 2.32-2.21 (m, 2H), 2.19-1.92 (m, 8H), 1.90-1.15 (m, 23H), 1.06-0.97 (m, 6H), 0.90-0.71 (m, 26H) ppm. Anal. HPLC: 99.4%, 유지 시간: 6.09 min (방법 A).
실시예 19
1e의 제조(도 17 참조)
2-{1-[4-({[(5
R
)-5-[1-(4-{2-아자트리시클로[10.4.0.0
4,9
]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-5-{[(1
S
)-1-{[(1
S
)-4-(카바모일아미노)-1-[(4-{[({2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0²
,
.0
,
8.0¹³
,
¹8]이코사-14,17-디엔-8-일]-2-옥소에틸}카바모일)옥시]메틸}페닐)카바모일]부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1
H
,4
H
,5
H
,6
H
,7
H
,8
H
,9
H
-시클로옥타[d][1,2,3]트리아졸-1-일]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에탄-1-술폰 산(1e)
화합물 7e (47 mg, 30 μmol)로부터 8b의 일반적인 절차H에 따라, 화합물 1e (28 mg, 45% 수율)를 백색 고체로서 수득하였다. ESI m/z: 1049 (M/2 + H)+. 1H NMR (500 MHz, MeODd4) δ 7.75-7.57 (m, 4H), 7.48-7.43 (m, 3H), 7.38-7.23 (m, 6H), 6.37-6.28 (m, 2H), 5.65-5.43 (m, 1H), 5.17-5.03 (m, 3H), 4.69-4.59 (m, 2H), 4.52-4.47 (m, 1H), 4.45-4.41 (m, 1H), 4.34-4.25(m, 2H), 4.23-4.13 (m, 2H), 4.07-3.86 (m, 5H), 3.77-3.68 (m, 4H), 3.64-3.54 (m, 22H), 3.52-3.47 (s, 3H), 3.46-3.40 (m, 4H), 3.29-3.21 (m, 4H), 3.20-3.14 (m, 2H), 3.10-3.01 (m, 1H), 3.00-2.95 (m, 2H), 2.92-2.84 (m, 1H), 2.76-2.60 (m, 2H), 2.47-2.42 (m, 2H), 2.40-2.25 (m, 5H), 2.23-2.13 (m, 3H), 2.07-1.97 (m, 3H), 1.90-1.79 (m, 4H), 1.71-1.55 (m, 14H), 1.52-1.42 (m, 3H), 1.40-1.29 (m, 8H), 1.07-0.85 (m, 12H) ppm. Anal. HPLC: 98%, Retention time: 5.88 min (method B).
실시예 19A
Ilb 제조(도 17 참조)
(2-{1-[4-({[(5R)-5-[1-(4-{2-아자트리시클로[10.4.0.04,9]헥사데카-1(12),4(9),5,7,13,15-헥센-10-yn-2-yl}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-5-{[(1S)-1-{[(1S)-4-(카바모일아미노)-1-[(4-{[({2-[(1S,2S,4R,8S,9S,11S,12R,13S,19S)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-8-yl]-2-옥소에틸}카바모일)옥시]메틸}페닐)카바모일]부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-1-일]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에틸)트리메틸아자늄 클로라이드 (IIb)
8a의 화합물 7bb (35 mg, 23 μmol)로부터 일반적인 절차G에 따라, 수성암모늄바이카보네이트(10mM 및 이어서 100% 메탄올)중의 역상 플래쉬 크로마토그래피 0-100% 아세토니트릴로 정제한 후 화합물 IIb (25 mg, 52% 수율)를 백색 고체로서 수득하였다. ESI m/z: 1037 [(M + 18)/2]+. 1H NMR (400 MHz, DMSO d6 ) δ 9.82-9.74 (m, 1H), 8.30 (s, 1H), 8.21-8.08 (m, 2H), 7.92-7.82 (m, 1H), 7.76 (t, J = 5.5 Hz, 1H), 7.69-7.58 (m, 3H), 7.53-7.18 (m, 9H), 6.34-6.26 (m, 1H), 6.15-6.03 (m, 2H), 5.71-5.53 (m, 1H), 5.43 (s, 2H), 5.31 (t, J = 12.4, 7.8 Hz, 1H), 5.10-4.90 (m, 3H), 4.79-4.72 (m, 1H), 4.58 (t, J = 4.2 Hz, 1H), 4.52 (t, 1H), 4.44-4.28 (m, 3H), 4.25-4.11 (m, 3H), 3.88-3.74 (m, 4H), 3.64-3.55 (m, 3H), 3.49-3.42 (m, 20H), 3.13-3.02 (m, 12H), 3.00-2.91 (m, 3H), 2.81-2.73 (m, 1H), 2.61-2.54 (m, 1H), 2.41-2.32 (m, 3H), 2.29-2.19 (m, 3H), 2.12-1.93 (m, 7H), 1.83-1.73 (m, 3H), 1.70-1.62 (m, 3H), 1.60-1.31 (m, 20H), 1.31-1.19 (m, 17H), 1.15-1.04 (m, 3H), 0.89-0.79 (m, 12H) ppm.
실시예 20
If의 제조(도 17 참조)
2-[2-({2-[4-({[(5 R )-5-[1-(4-{2-아자트리시클로[10.4.0.0 , ]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-5-{[(1 S )-1-{[(1 S )-4-(카바모일아미노)-1-[(4-{[({2-[(1 S ,2 S ,4 R ,8 S ,9 S ,11 S ,12 R ,13 S ,19 S )-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-8-일]-2-옥소에틸}카바모일)옥시]메틸}페닐)카바모일]부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1 H ,4 H ,5 H ,6 H ,7 H ,8 H ,9 H -시클로옥타[d][1,2,3]트리아졸-1-일]에틸}({[(2-설포에틸)카바모일]메틸})아미노)아세트아미도]에탄-1-술폰 산(1f)
화합물 7f (60 mg, 38 μmol)로부터 8b를 사용한 일반적인 절차 H에 따라, 화합물 1f (25 mg, 31% 수율)를 백색 고체로서 수득하였다. ESI m/z: 1058 (M/2 + H)+. 1H NMR (500 MHz, DMSO d6 ) δ 9.62-9.58 (m, 1H), 8.25-8.00 (m, 6H), 7.90-7.80 (m, 1H), 7.77 (t, J = 5.5 Hz, 1H), 7.70-7.60 (m, 4H),7.55-7.25 (m, 12H), 6.30 (d, J = 10.5 Hz, 1H), 6.10 (s, 1H), 6.05-5.95 (m, 1H), 5.70-5.55 (m, 2H), 5.40 (s, 2H), 5.10-4.90 (m, 4H), 4.80-4.70 (m, 1H), 4.59 (t, J = 4.0 Hz, 1H), 4.50-4.35 (m, 2H), 4.35-4.25 (m, 2H), 4.25-4.10 (m, 3H), 3.90-3.75 (m, 3H), 3.65-3.50 (m, 5H), 3.50-3.40 (m, 16H), 3.20-3.05 (m, 12H), 3.00-2.80 (m, 6H), 2.65-2.55 (m, 6H), 2.40-2.35 (m, 1H), 2.30-2.20 (m, 5H), 2.10-1.95 (m, 5H), 1.85-1.70 (m, 4H), 1.65-1.30 (m, 18H), 0.90-0.80 (m, 12H) ppm. Anal. HPLC: 97%, 유지 시간: 6.82 min (방법 B).
실시예 21
1h의 제조(도 17 참조)
2-[(4R)-4-[1-(4-{2-아자트리시클로[10.4.0.04,9]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-4-{[(1S)-1-{[(1S)-4-(카바모일아미노)-1-[(4-{[({2-[(1S,2S,4R,8S,9S,11S,12R,13S,19S)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-8-yl]-2-옥소에틸}카바모일)옥시]메틸}페닐)카바모일]부틸]카바모일}-2-메틸프로필]카바모일}부탄아미도]에탄-1-술폰 산(1h)
8b의 화합물 7h (20 mg, 18 μmol) 로부터의 일반적인 절차 H에 따라, 수용성 암모늄 바이카보네이트(10 mM)중 역상 플래쉬 크로마토그래피 0-100% 아세토 니트릴로 정제한 후 화합물 1h (11 mg, 37% yield) 를 백색고체로서 수득하였다. ESI m/z: 821.3 (M/2 + H)+. 1H NMR (500 MHz, DMSO d6 ) δ 9.70 (s, 1H), 8.22 (d, J = 7.0 Hz, 1H), 8.10 (d, J = 7.0 Hz, 2H), 7.95-7.61 (m, 7H), 7.51-7.26 (m, 11H), 6.30 (d, J = 10 Hz, 1H), 6.11 (s, 1H), 6.01-5.99 (m, 1H), 5.69-5.57 (m, 2H), 5.41 (s, 2H), 5.22-4.92 (m, 4H), 4.78-4.58 (m, 1H), 4.35-4.13 (m, 5H), 3.86-3.80 (m, 1H), 3.62-3.40 (m, 14H), 3.30-3.28 (m, 4H), 3.10-2.73 (m, 5H), 2.63-2.53 (m, 2H), 2.41-2.20 (m, 3H), 2.09-1.57 (m, 13H), 1.48-1.12 (m, 15H), 0.90-0.84 (m, 10H) ppm. Anal. HPLC: 96%, 유지 시간: 7.28 min (방법 B).
실시예 22
1i의 제조(도 17 참조)
2-(1-{4-[({5-[1-(4-{2-아자트리시클로[10.4.0.0
4,9
]헥사데카-1(12),4(9),5,7,13,15-헥센-10-yn-2-yl}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-5-{[(1
S
)-1-{[(1
S
)-4-(카바모일아미노)-1-{[4-({[(4-{2-[(1
S
,2
S
,4
R
,8
S
,9
S
,11
S
,12
R
,13
S
,19
S
)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.0
2,9
.0
4,8
.0
13,18
]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카바모일]옥시}메틸)페닐]카바모일}부틸]카바모일}-2-메틸프로필]카바모일}펜틸}카바모일)메톡시]-1
H
,4
H
,5
H
,6
H
,7
H
,8
H
,9
H
-시클로옥타[d][1,2,3]트리아졸-1-yl}-3,6,9,12-테트라옥사펜타데칸-15-아미도)에탄-1-술폰 산(1i)
화합물 7i (46 mg, 28 μmol)로부터 화합물 8b를 사용한 일반적인 절차 H에 따라, 화합물 1i (28 mg, 46% 수율)을 백색 고체로서 수득하였다. ESI m/z: 1095.0 (M/2 + H)+. 1H NMR (400 MHz, MeOD d4 ) δ 7.42-7.23 (m, 15H), 6.87-6.83 (m, 2H), 6.36-6.31 (m, 2H), 5.64-5.47 (m, 1H), 5.29-5.05 (m, 5H), 4.94-4.90 (m, 1H), 4.84-4.59 (m, 2H), 4.49-4.41 (m, 2H), 4.34-4.26 (m, 2H), 4.16-4.13 (m ,1H), 4.02-3.86 (m, 4H), 3.72-3.68 (m, 3H), 3.66-3.34 (m, 31H), 3.24-3.14 (m, 5H), 3.08-2.83 (m, 4H), 2.73-2.60 (m, 2H), 2.46-2.36 (m, 9H), 2.12-1.19 (m, 32H), 1.05-0.90 (m ,12H) ppm. Anal. HPLC: 100%, 유지 시간: 7.62 min (방법 B).
실시예 23
1j의 제조(도 17 참조)
2-{1-[4-({[(5R)-5-[1-(4-{2-아자트리시클로[10.4.0.04,9]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-5-{[(1S)-1-{[(1S)-1-[(4-{2-[(1S,2S,4R,8S,9S,11S,12R,13S,19S)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카바모일]에틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-1-일]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에탄-1-술폰 산(1j)
화합물 7j (66 mg, 47 μmol)로부터 화합물 8b를 사용한 일반적인 절차H에 따라, 화합물 1j (40 mg, 44% 수율)를 백색 고체로서 수득하였다. ESI m/z: 977.5 (M/2 + H)+. 1H NMR (400 MHz, MeOD d4 ) δ 7.66-7.55 (m, 4H), 7.48-7.24 (m, 7H), 6.90-6.85 (m, 2H), 6.35 (d, J = 10.0 Hz, 1H), 6.32 (s, 1H), 5.64-5.47 (m, 1H), 5.28-5.07 (m, 3H), 4.85-4.60 (m, 3H), 4.50-4.44 (m, 2H), 4.34-4.25 (m, 2H), 4.12-3.88 (m, 5H), 3.73-3.49 (m, 29H), 3.45-3.39 (m, 3H), 3.25-3.20 (m, 3H), 3.14-2.86 (m, 5H), 2.74-2.63 (m, 2H), 2.46-1.27 (m, 41H), 1.05-0.92 (m, 12H) ppm. Anal. HPLC: 95%, 유지 시간: 7.55 min (방법 B).
실시예 24
1k의 제조(도 17 참조)
2-{1-[4-({[(5 R )-5-[1-(4-{2-아자트리시클로[10.4.0.04,9]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-5-{[(1 S )-1-{[(1 S )-4-(카바모일아미노)-1-[(4-{2-[(1 S ,2 S ,4 R ,8 S ,9 S ,11 S ,12 R ,13 S ,19 S )-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카바모일]부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1 H ,4 H ,5 H ,6 H ,7 H ,8 H ,9 H -시클로옥타[d][1,2,3]트리아졸-1-일]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에탄-1-술폰 산(1k
화합물 7k (50 mg, 33 μmol) 로부터 화합물 8b를 사용한 일반적인 절차H에 따라, 화합물 1k (30 mg, 44% 수율)를 백색 고체로서 수득하였다. ESI m/z: 680 (M/3 + H)+. 1H NMR (500 MHz, DMSO d6 ) δ 9.51 (s, 1H), 8.30-7.97 (m, 3H), 7.92-7.84 (m, 1H), 7.80-7.73 (m, 2H), 7.68 (d, J = 7.5 Hz, 1H), 7.62 (d, J = 7.9 Hz, 1H), 7.50-7.45 (m, 4H), 7.38-7.26 (m, 4H), 7.08 (br s, 3H), 6.90-6.78 (m, 2H), 6.30 (d, J = 10.5 Hz, 1H), 6.11 (s, 1H), 6.01-5.94 (m, 1H), 5.72-5.55 (m, 1H), 5.52 (s, 1H), 5.39 (s, 2H), 5.12 (d, J = 18.5 Hz, 1H), 5.03 (d, J = 14.5 Hz, 1H), 4.84 (d, J = 18.5 Hz, 1H), 4.80-4.71 (m, 2H), 4.55-4.49 (m, 1H), 4.42 (t, J = 5.5 Hz, 1H), 4.38-4.12 (m, 4H), 3.81-3.76 (m, 4H), 3.62-3.53 (m, 4H), 3.46-3.39 (m, 21H), 3.33-3.25 (m, 4H), 3.09-2.93 (m, 7H), 2.81-2.78 (m, 1H), 2.64-2.52 (m, 8H), 2.40-2.36 (m, 2H), 2.27-2.20 (m, 5H), 2.09-1.98 (m, 5H), 1.61-1.35 (m, 29H), 0.89-0.83 (m, 11H) ppm.
실시예 24A
llld의 제조(도 17 참조)
(2-{1-[4-({[(5R)-5-{[(1S)-1-{[(1S)-4-(카바모일아미노)-1-{[4-({[(4-{2-[(1S,2S,4R,8S,9S,11S,12R,13S,19S)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카바모일]옥시}메틸)페닐] 카바모일}부틸]카바모일}-2-메틸프로필]카바모일}-5-{1-[2-(시클로옥트-2-인-1-일옥시)아세트아미도]-3,6,9,12-테트라옥사펜타데칸-15-아미도}펜틸]카바모일}메톡시)-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-1-일]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에틸)트리메틸아자늄 (IIId)
화합물 7cb (20 mg, 12 μmol)로부터 화합물 8c (5.2 mg, 12 μmol)를 사용한 일반적인 절차 G에 따라, 역상 플래쉬 크로마토그래피(수성 TFA중 0-100% 아세토니트릴(0.01%))로 정제한 후 화합물 IIId (8 mg, 32% 수율) 를 황색 고체로서 수득하였다. ESI m/z: 681.7 (M/3 + H)+; 1021.7 (M/2 + H)+. 1H NMR (400 MHz, DMSO d6 ) δ 9.73-9.67 (m, 1H), 9.61-9.54 (m, 1H), 8.26-8.20 (m, 1H), 8.19-8.04 (m, 2H), 7.91-7.77 (m, 1H), 7.66-7.57 (m, 3H), 7.40-7.26 (m, 4H), 6.84-6.78 (m, 2H), 6.30 (d, J = 10 Hz, 1H), 6.12 (s, 1H), 6.01-5.99 (m, 1H), 5.72-5.42 (m, 4H), 5.24-5.06 (m, 3H), 4.91-4.73 (m, 3H), 4.55-4.16 (m, 7H), 3.89-3.73 (m, 5H), 3.58 (t, J = 10.4 Hz, 3H), 3.49-3.41 (m, 29H), 3.26-3.22 (m, 4H), 3.08 (s, 9H), 3.04-2.93 (m, 4H), 2.77-2.62 (m, 3H), 2.40-1.98 (m, 13H), 1.89-1.02 (m, 41H), 0.89-0.84 (m, 9H) ppm.
실시예 24B
llle의 제조(도 17 참조)
(2-{1-[4-({[(5R)-5-[1-({[(1R,8S,9S)-Bi시클로[6.1.0]non-4-인-9-일메톡시]카르보닐}아미노)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-5-{[(1S)-1-{[(1S)-4-(카바모일아미노)-1-{[4-({[(4-{2-[(1S,2S,4R,8S,9S,11S,12R,13S,19S)-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카바모일]옥시}메틸) 페닐]카바모일}부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-1-일]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에틸)트리메틸아자늄 (IIIe)
화합물 7cb (25 mg, 15 μmol)로부터 화합물 8d (6.8 mg, 15 μmol)를 사용한 일반적인 절차 G에 따라, 역상 플래쉬 크로마토그래피(수성 TFA중 0-100% 아세토니트릴(0.01%))로 정제한 후 화합물 IIIe (4 mg, 13% 수율) 를 황색 고체로서 수득하였다. ESI m/z: 685.6 (M/3 + H)+. 1H NMR (400 MHz, MeOD d4 ) δ 7.77-7.71 (m, 2H), 7.40-7.34 (m, 5H), 6.90-6.86 (m, 2H), 6.38-6.33 (m, 2H), 5.66-5.47 (m, 1H), 5.38-5.24 (m, 1H), 5.14-5.02 (m, 2H), 4.76-4.58 (m, 4H), 4.52-4.27 (m, 6H), 4.19-4.11 (m, 3H), 3.99-3.86 (m, 4H), 3.75-3.42 (m, 37H), 3.30-3.27 (m, 3H), 3.17 (s, 9H), 3.16-3.00 (m, 2H), 3.0-2.84 (m, 1H), 2.72-2.46 (m, 4H), 2.38-2.04 (m, 15H), 1.83-1.31 (m, 27H), 1.06-0.90 (m, 13H) ppm.
실시예 25
1l의 제조(도 17 참조)
2-[(4 R )-4-[1-(4-{2-아자트리시클로[10.4.0.0 4,9 ]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-4-{[(1 S )-1-{[(1 S )-4-(카바모일아미노)-1-[(4-{2-[(1 S ,2 S ,4 R ,8 S ,9 S ,11 S ,12 R ,13 S ,19 S )-12,19-디플로로-11-하이드록시-9,13-디메틸-16-옥소-6-프로필-5,7-디옥사펜타시클로[10.8.0.02,9.04,8.013,18]이코사-14,17-디엔-8-일]-2-옥소에톡시}페닐)카바모일]부틸]카바모일}-2-메틸프로필]카바모일}부탄아미도]에탄-1-술폰 산(1l)
화합물 7l (20 mg, 19 μmol) 로부터 화합물 8b를 사용한 일반적인 절차 H에따라, 화합물 1l (6.0 mg, 20% 수율)을 백색 고체로서 수득하였다. ESI m/z: 793 (M/2 + H)+. 1H NMR (400 MHz, DMSO d6 ) δ 9.81-9.48 (m, 1H), 8.32-8.18 (m, 1H), 8.12-7.96 (m, 2H), 7.81-7.60 (m, 4H), 7.58-7.43 (m, 5H), 7.41-7.25 (m, 5H), 7.18-6.98 (m, 2H), 6.88-6.81 (m, 2H), 6.30 (d, J = 10.3 Hz, 1H), 6.11 (s, 1H), 6.02-5.95 (m, 1H), 5.71-5.52 (m, 2H), 5.40 (s, 2H), 5.15-5.00 (m, 2H), 4.86-4.74 (m, 2H), 4.34-4.13 (m, 4H), 3.63-3.54 (m, 2H), 3.48-3.42 (m, 9H), 3.30-3.28 (m, 2H), 3.12-3.05 (m, 2H), 3.01-2.92 (m, 2H), 2.62-2.56 (m, 1H), 2.42-2.37 (m, 1H), 2.29-2.20 (m, 3H), 2.12-1.95 (m, 7H), 1.86-1.70 (m, 5H), 1.64-1.56 (m, 4H), 1.52-1.22 (m, 14H), 0.92-0.81 (m, 14H) ppm.
실시예 26
1m의 제조(도 17 참조)
2-{1-[4-({[(5
R
)-5-[1-(4-{2-아자트리시클로[10.4.0.0
4,9
]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-5-{[(1
S
)-1-{[(1
S
)-1-{[(4b
S
,8
S
,8a
R
)-8-({[(1
S
,4a
S
,10a
R
)-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타히드로페난트렌-1-일]포름아미도}카르보닐)-4b,8-디메틸-4b,5,6,7,8,8a,9,10-옥타히드로페난트렌-3-일]카바모일}에틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1
H
,4
H
,5
H
,6
H
,7
H
,8
H
,9
H
-시클로옥타[d][1,2,3]트리아졸-1-일]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에탄-1-술폰 산(1m)
화합물 7m (30 mg, 22 μmol) 로부터 화합물 8b를 사용한 일반적인 절차 H에따라, 화합물 1m (15 mg, 37% 수율) 을 백색 고체로서 수득하였다. ESI m/z: 642 (M/3 + H)+. 1H NMR (400 MHz, DMSO d6 ) δ 9.68-9.27 (m, 1H), 8.99 (s, 1H), 8.23-7.85 (m, 4H), 7.79-7.71 (m, 2H), 7.76-7.42 (m ,6H), 7.39-7.28 (m, 3H), 7.21 (s, 1H), 7.09 (s, 1H), 6.96-6.93 (m, 2H), 6.81 (d, J = 8.4 Hz, 1H), 6.63 (d, J = 2.4 Hz, 1H), 6.50 (dd, J = 8.4 Hz, 2.4 Hz, 1H), 5.02 (d, J = 14.0 Hz, 1H), 4.93-4.72 (m, 1H), 4.53-4.09 (m, 5H), 3.82-3.75 (m, 4H), 3.62-3.53 (m, 3H), 3.51-3.38 (m, 23H), 3.30-3.27 (m, 6H), 3.12-2.67 (m, 10H), 2.61-2.54 (m, 4H), 2.39-1.52 (m, 31H), 1.45-1.08 (m, 18H), 1.01-0.98 (m, 6H), 0.90-0.82 (m, 6H) ppm.
실시예 26A
lVb의 제조(도 17 참조)
(2-{1-[4-({[(5R)-5-{[(1S)-1-{[(1S)-1-{[(4bS,8S,8aR)-8-({[(1S,4aS,10aR)-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타히드로페난트렌-1-일]포름아미도}카르보닐)-4b,8-디메틸-4b,5,6,7,8,8a,9,10-옥타히드로페난트렌-3-일]카바모일}에틸]카바모일}-2-메틸프로필]카바모일}-5-{1-[2-(시클로옥트-2-인-1-일옥시)아세트아미도]-3,6,9,12-테트라옥사펜타데칸-15-아미도}펜틸]카바모일}메톡시)-1H,4H,5H,6H,7H,8H,9H-시클로옥타[d][1,2,3]트리아졸-1-일]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에틸)트리메틸아자늄 (IVb)
화합물 7fb (20 mg, 15 μmol )로부터 8c를 사용한 일반적인 절차 G에따라, 예비-HPLC로 정제한 후 화합물 IVb (6 mg, 23% yield)를 황색고체로서 수득하였다. ESI m/z: 889.8 (M/2 + H)+, 593.5 (M/3 + H)+. 1H NMR (500 MHz, DMSO d6 ) δ 9.30 (d, J = 8.5 Hz, 1H), 9.02 (s, 1H), 8.76 (d, J = 5.5 Hz, 1H), 8.54-8.48 (m, 1H), 8.32-7.76 (m, 6H), 7.62-7.60 (m, 2H), 7.53-7.51 (m, 2H), 7.44 (d, J = 8.0 Hz, 1H), 6.95 (d, J = 8.5 Hz, 1H), 6.81 (d, J = 8.5 Hz, 1H), 6.63 (s, 1H), 6.50 (d, J = 8.0 Hz, 1H), 5.33-4.71 (m, 2H), 4.55-4.05 (m, 7H), 3.88-3.74 (m, 6H), 3.61-3.58 (m, 4H), 3.50-3.42 (m, 44H), 3.26-3.24 (m, 4H), 3.08 (s, 9H), 2.84-2.65 (m, 3H), 2.44 (t, J = 6.5 Hz, 2H), 2.35-1.26 (m, 35H), 1.16-1.13 (m, 2H), 1.02-0.98 (m, 6H), 0.89-0.84 (m, 6H) ppm.
실시예 27
1h의 제조(도 17 참조)
2-{1-[4-({[(5
R
)-5-[1-(4-{2-아자트리시클로[10.4.0.0
4,9
]헥사데카-1(12),4(9),5,7,13,15-헥센-10-인-2-일}-4-옥소부탄아미도)-3,6,9,12-테트라옥사펜타데칸-15-아미도]-5-{[(1
S
)-1-{[(1
S
)-1-({4-[({[(1
S
)-1-{[(4b
S
,8
S
,8a
R
)-8-({[(1
S
,4a
S
,10a
R
)-6-하이드록시-1,4a-디메틸-1,2,3,4,4a,9,10,10a-옥타히드로페난트렌-1-일]포름아미도}카르보닐)-4b,8-디메틸-4b,5,6,7,8,8a,9,10-옥타히드로페난트렌-3-일]카바모일}-2-하이드록시에틸]카바모일}옥시)메틸]페닐}카바모일)-4-(카바모일아미노)부틸]카바모일}-2-메틸프로필]카바모일}펜틸]카바모일}메톡시)-1
H
,4
H
,5
H
,6
H
,7
H
,8
H
,9
H
-시클로옥타[d][1,2,3]트리아졸-1-일]-3,6,9,12-테트라옥사펜타데칸-15-아미도}에탄-1-술폰 산(1q)
DMF (1 mL)중 화합물 7q (15 mg, 8.8 μmol) 및 상업적 DIBAC-Suc-PEG4-OSu (5.7 mg, 8.8 μmol, CAS 1427004-19-0)의 용액에 DIPEA (2.3 mg, 18 μmol)를 첨가하고 혼합물을 실온에서 2시간 동안 교반하였다. 휘발성 물질의 대부분을 진공에서 제거하고 잔류물을 예비-HPLC(방법 B)로 정제하여 1q (6.0 mg, 30% 수율)를 백색 고체로 얻었다. ESI m/z: 1123.8 (M/2 + H)+, 749.5 (M/3 + H)+. 1H NMR (500 MHz, MeOD d4 ) δ 7.76-7.16 (m, 14H), 7.06-7.00 (m, 1H), 6.88 (d, J = 8.5 Hz, 1H), 6.72-6.71 (m, 1H), 6.56-6.55 (m, 1H), 5.39-5.33 (m, 1H), 5.14-5.09 (m, 5H), 4.61 (s, 18H), 4.50-4.43 (m, 2H), 4.33-4.30 (m, 1H), 3.99 (s, 2H), 3.89-3.85 (m, 3H), 3.73-3.42 (m, 28H), 3.25-2.72 (m, 8H), 2.45 (t, J = 7.5 Hz, 2H), 2.36-1.96 (m, 18H), 1.81-1.51 (m, 12H), 1.45-1.32 (m, 15H), 1.12-0.89 (m, 12H) ppm.
표 2B 및 표 2B-1은 링커-페이로드에 대한 결과를 요약한다: HPLC에서 HPLC순도 및 LC 체류시간, 질량 스펙트럼으로부터 M/Z. 분석용 HPLC 및 MS방법은 일반절차에 설명되어 있다.
표 2B. 링커-페이로드의 화학적-물리적 특성
1.
There might be COT-isomers. COT이성질체가 있을 수 있다.
표 2B-1. 링커-페이로드의 화학적-물리적 특성
1.
There might be two regioisomers. 2개의 위치 이성질체가 있을 수 있다.
실시예28
이 실시예는 시험관 내 지질다당류(LPS)에 매게된 IL-1β 방출분석에서 SO3H부분을 포함하는 항-MSR1 항체 스테로이드 비세포 독성 ADC의 활성을 예시한다.
분석을 위해, THP-1세포를 10% FBS 및 펜슬린/스트렙토마이신이 보충된 RPMI를 함유하는 배지에서 40,000세포/웰로 96웰 플레이트 상에 시딩하고, 200 nM Phorbol Myristate Acetate (PMA)로 3일 동안 분화되었다. 3일 분화 후, 항체 약물 접합제 및 비 접합 항체 신선한 배지의 3배 연속 희석액을 100 nM 내지 0.01 nM 범위의 최종 농도로 세포에 첨가하였다. 마지막 유정은 배지만을 포함하는 빈 대조군으로 남았다. 72시간 후, 세포를 5 μg/mL 의 LPS (InVivoGen, Cat# tlrl-eklps)로 5시간동안 처리하였다. 이어서 세포 배지를 수집하고, 제조업체의 지시에 따라 V-PLEX전 염증 패널 1 인간키트(Meso Scale Diagnostics, Cat # 15049D-2)를 사용하여 IL-1β 를 측정하였다. 이어서, 플레이트 MSD 플레이트 판독기((Meso Scale Discovery)에서 판독하였다. IC50 값은 10-포인트 응답 곡선(GraphPad Prism)에 걸친 4-파라미터로지스틱 방정식으로부터 결정되었다. 모든 IC50 값은 몰 농도 (M)로 표시된다.
표 1A에 나타낸 바와 같이, SO3H부분(H1H21234N-N297Q- 실시예 10A)없이 스테로이드 링커 페이로드와 접합된 H1H21234N-N297Q는 IC50 값이 1.73 nM 이고 IL-1β방출이 97.2 pg/Ml이하로 감소된 THP1 세포로부터 LPS매개된 IL-1β 방출의 억제를 나타냈다.
SO3H 부분 (H1H21234N-N297Q- 실시예 19)을 가진 스테로이드 링커 페이로드와 접합된 H1H21234N-N297Q는 1.97 nM의 IC50값으로 97.17 pg/mL까지 방출된 IL-1β의 감소를 갖는 THP1세포로부터 LPS매개된 IL-1β방출의 유사한 억제를 보여주었다. 비접합 항체는 IC50 값이 22.9 nM이고 IL-1β방출이 343.7 pg/Ml로 감소된 THP1 세포로부터 LPS매개 IL-1β방출의 억제가 접합된 것과 비교하여 효능이 없음을 보여 주었다.
표 1A: THP1세포로부터 LPS-유도된 IL-1β 방출에 대한 항-MSR1 Ab-스테로이드 ncADC의 활성
pH 안정성
pH안정성은 다음과 같이 평가되었다. 0.1mg의 샘플을 0.2-0.3ml의 DMSO에 용해시키고, 생성된 용액을 시험 기간 동안 투명한 용액을 유지하면서 상이한 pH완충제(1ml)에 적가하였다. 여러시점(예를 들어, 72시간 이상)으로부터 샘플을 수집하고 pH안정성을 LC-MS에 의해 결정하였다. pH완충액은 다음과 같이 제조하였다: pH8.0 붕산나트륨 완충액: 붕산 나트륨 10 수화물, 1.461g 염화나트륨 및 0.393g DTPA를 900ml증류수에 첨가하고, 모든 힘이 완전히 용해되었는지 확인한 다음 물을 추가하여 최종 부치를 1L로 만들었다. pH 5.0숙시네이트산완충액: 증류수 150ml에 10mM숙시네이트산을 첨가한 다음 0.5M NaOH를 첨가하여 pH 를 Ph5.0으로 변경한 다음, 물을 첨가하여 최종 부피를 250ml로 만든다. pH 7.4 PBS완충제: 시판된 것으로 사용가능하다. LCMS에 의해 72시간에 안정성을 평가하였다.
용해도
용해도 시험 절차: 1mg의 시험 샘플을 1ml DMSO에 용해시키고 표준 용액 A (4.5 mL, 100 μg/mL), B (4.5 mL, 10 μg/mL), C (4.5 mL, 1 μg/mL), D (5 mL, 0.1 μg/mL)를 제조한다.
DMSO 용액 (1 mg/mL, 0.5 mL)을 물(4.5ml)로 희석하여 용액 A (0.1 mg/mL, 5 mL, 0.5 mg)를 생성하였다. 용액 A (0.1 mg/mL, 0.5 mL)를 물 (4.5ml)로 희석하여 용액 B (0.01 mg/mL, 5 mL, 0.05 mg)를 생성하였다. 용액 B (0.01 mg/mL, 0.5 mL)를 물(4.5ml)로 희석하여 용액 solution C (1 μg/mL, 5 mL, 5 μg)를 물(4.5ml)로 희석하여 용액 D (0.1 μg/mL, 5 mL, 0.5 μg)를 생성하였다.
시험 샘플(0.05mg)을 물(1ml)에 현탁시키고, 샘플을 용해시키기 위해 5-30분 동안 초음파 처리하였다. 시험샘플(0.05mg)을 물(1ml)에 현탁시키고, 샘플을 용해시키기 위해 5-30분 동안 초음파 처리하였다. 맑은 용액이 관찰되지 않으면, 생성된 현탁액을 원심분리하고 맑은 상청액을 수집하여 분석하였다. 모든 표준 솔루션 A, B, C, D 및 샘플 솔루션은 동일한 LC-MS기기에서 동일한 방법을 사용하여 테스트 되었다. LCMS에 의해 용해도를 평가하고 표준 곡선에 기초하여 계산하였다. 표 3 및 표 3-1은 이러한 실험의 데이터를 보여준다.
표 3. 링커-페이로드에 대한 pH안정성, 용해도 데이터
Y: 3일 이상 동안 실온에서 pH7.4또는 8완충액에서 안정함;
표 3-1. 링커-페이로드에 대한 pH안정성, 용해도 데이터
Y:3일 이상 실온에서 pH7.4및 8완충액에서 안정함
실시예 29
ADC 접합(도 19 참조)
이 실시예는 일반적으로 항체 또는 이의 항원 결합 단편에 대한 페이로드의 부위-특이적 접합 방법을 설명한다.
하기 실시예는 접합제를 제조하는 방법을 설명한다. BupHTM (pH 7-8)에서 인간 IgG1이소타입을 갖는 당화 항체를 ≥200몰 당량의 아지도-dPEG3-아민 (MW. 218.26 g/mol)과 혼합하였다. 생성된 용액을 트랜스 글루타미나제(25 U/mL; 5U MTG per mg of antibody)와 혼합하여 0.5-10mg/ml에서 최종 농도의 항체를 생성한 다음, 용액을 37℃에서 4-24동안 부드럽게 흔들면서 배양하였다. 반응은 SDS-PAGE 또는 ESI-MS에서 분석되었다. 아지도-dPEG3-아민은 항체의 2개 부위- Q295및Q297-에 첨가되어 4DAR응집화된 항체-PEG3-아지드 접합제에 대해 804Da 증가를 초래하였다.
접합 부위를 확인하고 트립신 소화 중쇄의 펩티드 서열 맴핑을 통해 4DAR아지도 기능화 항체에 대한 EEQLinkerYQLinkerSTYR에서 확인 하였다.
MSR1, HER2 (또는 PRLR)에 대해 생성되고 N297Q돌연변이를 함유하는 인간 IgG1 또는 IgG4를 갖는 부위-특이적글리코실화된 항체 약물접합제(ADCs)는 아지도-작용화된 사이의[2+3]클릭반응에 의해 제조되었다. 알킨 함유 링커-페이로드(LP)를 갖는 항체(mAb-N3). FelD1은 비결합 대조군 항체이다.
표 5에 나타낸 바와 같이, N297Q돌연변이를 함유하는 부위-특이적 글리코실화된 항체를 아민-PEG3-N3 과 접합하여 항 MSR1 Ab-PEG3-N3, 항 Fel D1 Ab-PEG3-N3, 항 HER2 Ab-PEG3-N3, 항 PRLR Ab-PEG3-N3을 포함한 아지도-관능화된 항체 접합제(mAb-N3)를 생성시켰다.
링커-페이로드(LP)를 갖는 부위-특이적 항체 접합제는 적합한 유기용매, 예컨대 DMSO, DMF 또는 DMA(예를 들어, 반응 혼합물은5-20% 유기용매 v/v를 함유함)에 용해된 ≥6몰 당량 LP를 갖는수성매질(예를 들어, PBS, 5%글리세롤을 함유하는 PBS, HBS)에서 mAb-PEG 3 -N 3 (1-12 mg / mL)를 24℃ 내지 37℃에서 30분 내지 24시간 동안 배양함으로써 제조된다.
반응 진행은 ESI-MS에 의해 모니터링 되었고 mAb-PEG 3 -N 3 의 부제는접합의 완료를 나타내었다. 과량의 LP및 유기 용매는 PBS로의 용리를 통해 SEC에 의해, 도는 산성 완충액으로의 용리에 의해 단백질A 칼럼 크로마토그래피를 통해 트리스(pH 8.0)로 중화하여 제거하였다. 정제된 접합제는 SEC, SDS-PAGE 및 ESI-MS에 의해 분석되었다. 표 5에는 상응하는 LP로부터의 MMAE항체 접합제, 스테로이드 항체 접합제 및 LXR작용제 항체 접합제, 그들의 분자량 및 ESI-DAR값의 목록이 제시되어있다.
특정 예에서, 0.800 ml PBSg(PBS, 5% 글리세롤, pH 7.4)중 아지도-관능화된 항체(1mg)를 실온에서 2시간 동안 표 2(농도. 10 mg/mL in DMSO)로부터 6몰 당량의 링커-페이로드(LP)로 처리하고 과량의 링커페이로드(LP)를 크기배제 크로마토그래피(SEC, Superdex 200 HR, GE Healthcare)로 제거하였다. 최종 생성물을 초원심분리에 의해 농축시키고 UV, SEC, SDS-PAGE 및 ESI-MS를 특징으로 한다.
LC-ESI-MS를 통한 ADC 특성 분석
LC-ESI-MS에 의한 ADC샘플에 대한 온전한 질량의 측정을 수행하여 약물-페이로드 분포 프로파일을 결정하고 평균 DAR을 계산하였다. 각각의 시험 샘플(20-50 ng, 5uL)을 Acquity UPLC Protein BEH C4 컬럼(10K psi, 300 Å, 1.7 μm, 75μm Х 100 mm; Cat No. 186003810)에 로드했다. 3분의 탈염 후, 단백질을 용출시키고 Waters Synapt G2-Si질량분석기로 질량 스펙트럼을 획득하였다. 네이키드항체, 아지도-관능화된 항체 접합제(mAb-N3), LP및 ADC의 MW는 표 5에 열거되어 있다. 표 5에 요약된 바와 같이, 대부분의 부위-특이적 ADC는 부위-특이적 접합제에 대해 3.9-4ADR을 갖는다.
표 5. 접합제 목록
| LP | Ex | MW (LP) | Ab, Ab-N 3 , 또는 ncADC | Target | MS m/z (ncADC) | DAR (ESI-MS) |
| 1q | 27 | 2246.7 | H1H21234N-Ex 27 | MSR1 | 155570 | 3.9 |
| 1e | 19 | 2096.4 | H1H21234N-Ex 19 | MSR1 | 154964 | 3.9 |
| 1q | 27 | 2246.2 | H1H1238N-N297Q-Ex 27 | FeID1(isotype control) | 155245 | 4 |
| 1e | 19 | 2096.4 | H1H1238N-N297Q -Ex 19 | FeID1(isotype control) | 154641 | 3.9 |
| 1j | 23 | 1953.2 | H1H6958N2-N297Q -Ex 23 | Anti-PRLRmAb1 | 154070 | 4 |
| 1i | 22 | 2188.5 | H1H6958N2-N297Q -Ex 22 | Anti-PRLRmAb2 | 155011 | 3.9 |
| 1e | 19 | 2096.4 | H1H6958N2-N297Q -Ex 19 | Anti-PRLRmAb3 | 153792 | 4 |
| 1f | 20 | 2114.4 | H1H6958N2-N297Q -Ex 20 | Anti-PRLRmAb4 | 152301 | 3.7 |
| 1j | 23 | 1953.2 | H1H6958N2-N297Q -Ex 23 | Anti-PRLRmAb5 | 153227 | 3.9 |
| 1i | 22 | 2188.5 | H1H6958N2-N297Q -Ex 22 | Anti-PRLRmAb6 | 154168 | 3.9 |
| 1k | 24 | 2039.3 | H1H6958N2-N297Q-Ex 24 | Anti-PRLRmAb7 | 153555 | 3.9 |
| 1c | 18 | 2348.9 | Anti-HER-N297Q-Ex 18 | HER2 | 155358 | 3.9 |
| 1q | 27 | 2246.7 | Anti-HER-N297Q-Ex 27 | HER2 | 154945 | 3.9 |
실시예 30
이 실시예는 SO3H부분, N+Me3 부분, 포스페이트 부분 또는 갈라토스 부분이 카텝신B절단 분석법을 사용하여 링커에 존재할 때 스테로이드 또는 LXR작용제 페이로드에 대한 절단 효율에 대한 효과를 입증한다.
분석을 위해, 링커-페이로드 스톡용액(DMSO 중 10Mm의 링커-페이로드)을 pH5에서 100 mM NaOAc 10mM디티오트레이톨의 용액에 첨가하여 50 μM기질 용액을 수득하였다. pH5에서 50mM NaOAc, 1mM EDTA중 인간 간 카텝신 B(Athens Research & Technology, Cat# 16-12-030102)를 기질 용액에 첨가하였다. 카텝신 B 및 기질 용액을 10mM의 카텝신 B억제제(CA074; APE Bio, Cat# A1926)와 함께하거나 없이 혼합하고, 37℃에서 4시간 동안 배양하였다. 4시간 인큐베이션 후, 아세트산 및 아세토니트릴을 첨가하여 반응을 정지시켰다. 이어서 켄칭된 샘플을 14,000rpm에서 원심분리하였다. 이어서, 생성된 상청액의 분취액을 동일한 부피의 물로 희석하고 LC/MS에 의해 분석하여 방출된 페이로드의 양을 결정하였다. 카텝신 B의 안정성 및 활성은 카텝신B(Santa Cruz Biotechnology, Cat# 207975) (340 nm /425 nm의 방출에서 형광) 200μM형광 기질과 함께 배양함으로써 확인되었다.
표 1B에 나타낸 바와 같이, SO3H부분이 없는 LXR작용제 링커 페이로드는 4시간 동안 카텝신B로 처리될 때 자유 페이로드 방출의 13.6%를 갖는 반면, SO3H부분을 갖는 LXR작용제 링커 페이로드는 44.2%를 가졌다. 카텝신B로 4시간동안 치료할 때 무료 탑재량 방출. SO3H부분이 없는 스테로이드 링커 페이로드는 4시간 동안 카텝신 B로 처리될 때 자유 페이로드 방출의 7.5-17.2%사이에 있는 반면, SO3H부분이 있는 스테로이드 링커 페이로드는 카텝신 B로 4시간동안 처리될 때 무료 페이로드 방출의 79.6%를 가졌다. 표 1C 및 표 1D는 링커 페이로드가 카텝신 B로 처리될 때 무료 페이로드 해제에 대한 추가 데이터를 보여준다.
표 1B: 카텝신 B 분석에서 SO3H 부분을 갖거나 갖지 않는 링커-페이로드로부터 방출된 페이로드의 양(도 18 참조)
표 1C:카텝신 B분석에서 상이한 SO3H링커를 갖는 링커-페이로드로부터 방출된 페이로드의 양(도 18 참조)
표 1D: 카텝신 B분석에서 링커-페이로드(도 19)로부터 방출된 페이로드의 %.
실시예 31
이 실험은 시간에 따른 리소좀 절단을 측정함으로써 친수성 링커가 항-MSR1항체 스테로이드 비세포성 ADC(ncADC)에 존재할 때 스테로이드 페이로드의 절단 효율에 대한 효과를 입증한다.
분석을 위해, ncADC를 1x이화 완충액(Xenotech Cat#K5200) 및 0.125mg/ml인간 간 리소좀 단백질(Xenotech Cat#H0610.L)을 함유하는 새로제조된 리소좀 작업 용액에 첨가하였다. 0.25 μM ncADC를 함유하는 200 μMdml 생성된 혼합물을 24시간에 걸쳐 부드럽게 진탕하면서 37℃에서 인큐베이션 하였다. 20 μL 분취량을 0, 0.5, 1.0, 2.0, 4.0, 8.0 및24시간에 취한 다음, 리소좀을 불활성화시키고 단백질을 침전시키기 위해 80 μL의 냉 아세토니트릴을 함유하는 플레이트로 옮겼다. 2,000 rpm에서 5분 동안 원심 분리한 후, 상청액의 분취액을 동일한 부피의 물로 희석한 후 LC-MS에 의해 분석하여 페이로드 방출량을 결정하였다.
표 1E에 나타낸 바와 같이, 친수성 링커가 없는 ncADC스테로이드 접합 (H1H21234N-N297Q-실시예 10A)는 24시간 시점에서 548nM스테로이드를 방출하였다. 친수성 링커(H1H21234N-N297Q-실시예 19)와의 ncADC스테로이드 접합제는 24시간 시점에서 760nM을 방출하였다.
표 1E: 친수성 링커가 있거나 없는 스테로이드 방출량
전술한 실시예 및 예는 단지 예시적이고 비제한적인 것으로 의도된다. 당엄자는 일상적인 실험, 다수의 등가의 특정 화합물, 재료 및 절차를 사용하여 인식하거나 확인할 수 있을 것이다. 이러한 모든 등가물은 범위 내에 있는 것으로 간주되며 첨부된 청구 범위에 포함된다.
Claims (73)
- 하나 이상의 페이로드 부분(payload moiety)에 연결되고 공유 링커(covalent linker)를 통해 하나 이상의 친수성 잔기(hydrophilic residue)에 연결된 결합제를 포함하고,
상기 공유 링커는 상기 결합제, 상기 페이로드 부분, 및 상기 친수성 잔기 각각에 직접적으로 또는 간접적으로 결합되는, 화합물 또는 그의 제약상 허용되는 용매화물, 입체 이성질체 또는 유도체.
- 제1항에 있어서, 상기 친수성 잔기가 말단 친수성기(hydrophilic group)를 포함하는 화합물.
- 제1항 또는 제2항에 있어서, 상기 친수성 잔기가 술폰산기(sulfonic acid group) 또는 그의 염을 포함하는 화합물.
- 제1항 또는 제2항에 있어서, 상기 친수성 잔기가4차 아민(quarternary amine) 또는 이의 염, 포스폰산기(phosphonic acid group) 또는 이의 염 또는 당잔기(sugar residue)를 포함하는 화합물.
- 제5항 또는 제6항에 있어서, 아래 첨자 n이 1, 2, 3, 또는 4인 화합물.
- 제5항에 있어서, 화학식(III)에 따른 화합물:
(III)
여기서
고리A는 트리아졸에 융합되고 시클로알킬(cycloalkyl), 시클로알케닐(cycloalkenyl), 헤테로시클로알킬(heterocycloalkyl), 및 헤테로시클로알케닐(heterocycloalkenyl)로 이루어진 군으로부터 선택되고;
여기서 시클로알킬(cycloalkyl), 시클로알케닐(cycloalkenyl), 8헤테로시클로알킬(heterocycloalkyl) 및 헤테로시클로알케닐(heterocycloalkenyl)은 알킬, -OH, 또는 -NRaRb로 선택적으로 치환되며, 여기서 Ra 및 Rb는 각각 알킬 또는 H이다.
- 제10항에 있어서, AA1이 리신( lysine), 글루타민(glutamine), 글루탐산(glutamic acid), 또는 아스파르트산(aspartic acid)인 화합물.
- 제9항 내지 제12항 중 어느 한 항에 있어서, RG 1 및 RG2가 독립적으로, 각 경우에, 클릭 화학 잔기(click chemistry residue)인 화합물.
- 제9항 내지 제 12항 중 어느 한 항에 있어서, RG 1 및 RG2가 각각의 경우 독립적으로 트리아자올(triazaole) 또는 융합된 트리아졸(fused triazole)을 포함하는 것인 화합물.
- 제9항 내지 제19항 중 어느 한 항에 있어서, SP 1 및 SP 2 가 독립적으로, 각 경우에, 부재하거나, 또는 C1-6 알킬렌(alkylene), -NH-, -C(O)-, (-CH2-CH2-O)e, -NH-CH2-CH2-(-O-CH2-CH2)e-C(O)-, -C(O)-(CH2)u-C(O)-, -C(O)-NH-(CH2)v-, (글리신)4-세린((glycine)4-serine) 및 이들의 조합이고, 여기서 아래 첨자 e는 0 내지 4의 정수이고, 아래 첨자 u는 1 내지 8의 정수이고, 첨자 v는 1 내지 8정수인 화합물.
- 제23항에 있어서, R AA1 이 HG에 직접 또는 간접적으로 결합된 리신(lysine), 글루타민(glutamine), 글루탐산(glutamic acid) 또는 아스파르트산 측쇄(aspartic acid side chain)이고, R AA2 및 R AA3 이 각각 발린(valine) 및 알라닌(alanine) 또는 시트룰린 측쇄(citrulline sidechains)인 화합물.
- 제12항 내지 제26항 중 어느 한 항에 있어서, 아래 첨자 e가 4인 화합물.
- 제1항 내지 제27항 중 어느 한 항에 있어서, 상기 결합제(BA)가 항체 또는 이의 항원 결합 단편인 화합물.
- 제1항 내지 제27항 중 어느 한 항에 있어서, 결합제 (BA)가 AXL, BAFFR, BCMA, BCR-목록 구성 요소, BDCA2, BDCA4, BTLA, BTNL2, BTNL3, BTNL8, BTNL9, C10 또는 f54, CCR1, CCR3, CCR4, CCR5, CCR6, CCR7, CCR9, CCR10, CD11c, CD137, CD138, CD14, CD168, CD177, CD19, CD20, CD209, CD209L, CD22, CD226, CD248, CD25, CD27, CD274, CD276, CD28, CD30, CD300A, CD33, CD37, CD38, CD4, CD40, CD44, CD45, CD46, CD48, CD5, CD52, CD55, CD56, CD59, CD62E, CD68, CD69, CD70, CD74, CD79a, CD79b, CD8, CD80, CD86, CD90.2, CD96, CLEC12A, CLEC12B, CLEC7A, CLEC9A, CR1, CR3, CRTAM, CSF1R, CTLA4, CXCR1/2, CXCR4, CXCR5, DDR1, DDR2, DEC-205, DLL4, DR6, FAP, FCamR, FCMR, FcR's, Fire, GITR, HHLA2, HLA class II, HVEM, ICOSLG, IFNLR1, IL10R1, IL10R2, IL12R, IL13RA1, IL13RA2, IL15R, IL17RA, IL17RB, IL17RC, IL17RE, IL20R1, IL20R2, IL21R, IL22R1, IL22RA, IL23R, IL27R, IL29R, IL2Rg, IL31R, IL36R, IL3RA, IL4R, IL6R, IL5R, IL7R, IL9R, Integrins, LAG3, LIFR, MAG/Siglec-4, MMR, MSR1, NCR3LG1, NKG2D, NKp30, NKp46, PDCD1, PROKR1, PVR, PVRIG, PVRL2, PVRL3, RELT, SIGIRR, Siglec-1, Siglec-10, Siglec-5, Siglec-6, Siglec-7, Siglec-8, Siglec-9, SIRPA, SLAMF7, TACI, TCR-목록 구성요소/assoc, PTCRA, TCRb, CD3z, CD3, TEK, TGFBR1, TGFBR2, TGFBR3, TIGIT, TLR2, TLR4, TROY, TSLPR, TYRO, VLDLR, VSIG4, 및 VTCN1로 이루어진 군으로부터 선택된 항원에 대해 선택적인 항체 또는 그의 항원 결합 단편인 화합물.
- 제1항 내지 제29항 중 어느 한 항에 있어서, PA가 돌라스타린(a dolastatin), 아우리스타틴(an auristatin), 메이탄시노이드(a maytansinoid), 식물 알칼로이드(a plant alkaloid), 탁산(a taxane), 빈카 알칼로이드(a vinca alkaloid), 스테로이드(a steroid), 및 간 X수용체 (a liver X receptor (LXR)) 조절제로 이루어진 군으로부터 선택된 그룹의 잔기인 화합물.
- 제1항 내지 제34항 중 어느 한 항의 화합물 또는 그의 제약상 허용되는 염, 및 제약상 허용되는 부형제를 포함하는 제약 조성물.
- 제1항 내지 제34항 중 어느 한 항의 화합물 또는 제35항의 조성물을 환자에게
투여하는 단계를 포함하는, 환자에게 질환 또는 장애를 치료하는 방법.
- 하나 이상의 페이로드(payload) 부분에 결합되고 공유 링커를 통해 하나 이상의 친수성 잔기에 결합된 반응성 링커를 포함하고, 상기 공유 링커는 상기 반응성 링커, 상기 페이로드 부분, 및 상기 친수성 잔기 각각에 직접 또는 간접적으로 결합되는 화합물.
- 제33항에 있어서, 화학식 (VIII)에 따른 화합물:
(VIII)
여기서
고리 A는 트리아졸에 융합되고 시클로알킬 (cycloalkyl), 시클로알케닐(cycloalkenyl), 헤테로시클로알킬(heterocycloalkyl), 및 헤테로시클로알케닐(heterocycloalkenyl)로 이루어진 군으로부터 선택되고;
여기서 시클로알킬 (cycloalkyl), 시클로알케닐(cycloalkenyl), 헤테로시클로알킬(heterocycloalkyl), 헤테로시클로알케닐(heterocycloalkenyl)은, 선택적으로 알킬 -OH, 또는 NR a R b 로 치환되며, 여기서 Ra 및 Rb는 각각 알킬 또는 -H이다.
- 제42항에 있어서, AA 1 이 리신(lysine), 글루타민(glutamine), 글루탐산(glutamic acid), 또는 아스파르트산(aspartic acid)인 화합물.
- 제38항 내지 제 44항 중 어느 한 항에 있어서, RG'가 독립적으로, 각 경우에, 클릭 화학 잔기인 화합물.
- 제39항 내지 제 51항 중 어느 한 항에 있어서, SP 1 및 SP 2 가 독립적으로, 각 경우에, 부재하거나, 또는 C1-6 알킬렌(alkylene), -NH-, -C(O)-, (-CH2-CH2-O)e, -NH-CH2-CH2-(-O-CH2-CH2)e-C(O)-, -C(O)-(CH2)u-C(O)-, -C(O)-NH-(CH2)v-, (글리신)4-세린((glycine)4-serine), 및 이들의 조합으로 이루어진 군으로부터 선택되고, 여기서 아래 첨자 e는 0 내지 4의 정수이고, 아래 첨자 u는 1 내지 8의 정수이고, 첨자 v는 1 내지 8의 정수인 화합물.
- 제55항에 있어서, R AA1 이 HG에 직접 또는 간접적으로 결합된 리신, 글루타민, 글루탐산 또는 아스파르트산 측쇄이고, R AA2 및 R AA3 이 각각 발린 및 알라닌 또는 발린 및 시트룰린(citrulline) 측쇄인 화합물.
- 제44항 내지 제52항 중 어느 한 항에 있어서, 아래 첨자 e가 4인 화합물.
- 제37항 내지 제59항 중 어느 한 항에 있어서, PA가 돌라스타린(a dolastatin), 아우리스타틴(an auristatin), 메이탄시노이드(a maytansinoid), 식물 알칼로이드(a plant alkaloid), 탁산(a taxane), 빈카 알칼로이드(a vinca alkaloid), 스테로이드(a steroid), 및 간 X수용체 (a liver X receptor (LXR)) 조절제로 이루어진 군으로부터 선택된 그룹의 잔기인 화합물.
- 제1항에 있어서, 결합제와 화합물 사이의 결합을 형성하기에 적합한 조건 하에서 결합제를 제37항 내지 제62항에 따른 화합물과 접촉시키는 단계를 포함하는, 제1항의 화합물의 제조방법.
- 제37항 내지 제62항 중 어느 한 항의 화합물을 포함하고 링커에 결합된 링커-페이로드.
- 제37항 내지 제62항중 어느 한항의 화합물을 포함하고 페이로드의 산소 또는 1차 또는 2차 질소에 결합된 링커-페이로드.
- 전술한 청구항 중 어느 한 항의 화합물 또는 링커-페이로드를 항체에 결합한 항체-약물-접합제 또는 그의 항원 결합 단편.
- 제1항 내지 제35항 중 어느 한 항의 화합물 또는 약제학적 조성물의 유효 치료량을 대상체에게 투여하는 것을 포함하는, 대상체에서 증식성 질환, 대사성 질환, 염증, 또는 신경 퇴행성 질환을 치료하는 방법.
- 제1항 내지 제35항 중 어느 한 항의 화합물 또는 약제학적 조성물의 유효 치료량을 대상체에게 투여하는 것을 포함하는, 대상체에서의 질환, 장애, 또는 병태의 치료방법.
- 제1항 내지 제35항 중 어느 한 항의 화합물 또는 약제학적 조성물의 유효 치료량을 대상체에게 투여하는 것을 포함하는, 대상체에서 증식성 질환의 치료방법.
- 제1항 내지 제35항 중 어느 한 항의 화합물 또는 약제학적 조성물의 유효 치료량을 대상체에 투여하는 것을 포함하는, 대상체에서 대사 질환의 치료방법.
- 제1항 내지 제35항 중 어느 한 항의 화합물 또는 약제학적 조성물의 유효 치료량을 대상체에 투여하는 것을 포함하는, 대상체에서의 염증 치료방법.
- 제1항 내지 제35항 중 어느 한 항의 화합물 또는 약제학적 조성물의 유효 치료량을 대상체에 투여하는 것을 포함하는, 대상체에서 신경 퇴행성 질환의 치료방법.
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US15/806,197 | 2017-11-07 | ||
| USPCT/US2017/060434 | 2017-11-07 | ||
| US15/806,197 US10711032B2 (en) | 2016-11-08 | 2017-11-07 | Steroids and protein-conjugates thereof |
| PCT/US2017/060434 WO2018089373A2 (en) | 2016-11-08 | 2017-11-07 | Steroids and protein-conjugates thereof |
| US201862669034P | 2018-05-09 | 2018-05-09 | |
| US62/669,034 | 2018-05-09 | ||
| PCT/US2018/059495 WO2019094395A2 (en) | 2017-11-07 | 2018-11-06 | Hydrophilic linkers for antibody drug conjugates |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20200085807A true KR20200085807A (ko) | 2020-07-15 |
Family
ID=66439032
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020207015856A KR20200085807A (ko) | 2017-11-07 | 2018-11-06 | 항체 약물 접합제용 친수성 링커 |
Country Status (11)
| Country | Link |
|---|---|
| EP (1) | EP3706805A2 (ko) |
| JP (2) | JP7426931B2 (ko) |
| KR (1) | KR20200085807A (ko) |
| CN (1) | CN111601619A (ko) |
| AU (1) | AU2018365946A1 (ko) |
| CA (1) | CA3080857A1 (ko) |
| EA (1) | EA202091135A1 (ko) |
| IL (1) | IL274427A (ko) |
| MX (1) | MX2020004691A (ko) |
| SG (1) | SG11202004151YA (ko) |
| WO (1) | WO2019094395A2 (ko) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018089373A2 (en) | 2016-11-08 | 2018-05-17 | Regeneron Pharmaceuticals, Inc. | Steroids and protein-conjugates thereof |
| MX2019013690A (es) | 2017-05-18 | 2020-01-27 | Regeneron Pharma | Conjugados de farmaco-proteina con ciclodextrina. |
| CA3098453A1 (en) * | 2018-05-09 | 2019-11-14 | Regeneron Pharmaceuticals, Inc. | Anti-msr1 antibodies and methods of use thereof |
| AU2021296449A1 (en) * | 2020-06-24 | 2023-01-19 | Regeneron Pharmaceuticals, Inc. | Tubulysins and protein-tubulysin conjugates |
| WO2022029420A1 (en) * | 2020-08-03 | 2022-02-10 | Bicycletx Limited | Peptide-based linkers |
| CN113248436A (zh) * | 2021-04-13 | 2021-08-13 | 南京工业大学 | 一种用于蛋白靶向运输的新型交联分子及其制备方法和应用 |
| KR20240016287A (ko) | 2021-06-01 | 2024-02-06 | 아지노모토 가부시키가이샤 | 항체 및 기능성 물질의 콘쥬게이트 또는 이의 염, 및 이의 제조에 사용되는 화합물 또는 이의 염 |
| TW202400266A (zh) * | 2022-05-18 | 2024-01-01 | 大陸商成都百利多特生物藥業有限責任公司 | 配體藥物偶聯物及其應用 |
| WO2024020164A2 (en) | 2022-07-21 | 2024-01-25 | Firefly Bio, Inc. | Glucocorticoid receptor agonists and conjugates thereof |
Family Cites Families (38)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5208020A (en) | 1989-10-25 | 1993-05-04 | Immunogen Inc. | Cytotoxic agents comprising maytansinoids and their therapeutic use |
| US5714586A (en) | 1995-06-07 | 1998-02-03 | American Cyanamid Company | Methods for the preparation of monomeric calicheamicin derivative/carrier conjugates |
| US20070258987A1 (en) | 2000-11-28 | 2007-11-08 | Seattle Genetics, Inc. | Recombinant Anti-Cd30 Antibodies and Uses Thereof |
| TW200539855A (en) | 2004-03-15 | 2005-12-16 | Wyeth Corp | Calicheamicin conjugates |
| NZ551180A (en) | 2004-06-01 | 2009-10-30 | Genentech Inc | Antibody drug conjugates and methods |
| US7541330B2 (en) * | 2004-06-15 | 2009-06-02 | Kosan Biosciences Incorporated | Conjugates with reduced adverse systemic effects |
| WO2006065533A2 (en) | 2004-11-29 | 2006-06-22 | Seattle Genetics, Inc. | Engineered antibodies and immunoconjugates |
| WO2006135371A1 (en) * | 2005-06-09 | 2006-12-21 | Kosan Biosciences Incorporated | Conjugates with reduced adverse systemic effects |
| US7750116B1 (en) | 2006-02-18 | 2010-07-06 | Seattle Genetics, Inc. | Antibody drug conjugate metabolites |
| WO2008122039A2 (en) | 2007-04-02 | 2008-10-09 | The Government Of The United States Of America, As Represented By The Secretary, Department Of Health And Human Services | Selenocysteine mediated hybrid antibody molecules |
| ES2731432T3 (es) | 2007-05-23 | 2019-11-15 | Ventana Med Syst Inc | Transportadores poliméricos para inmunohistoquímica e hibridación in situ |
| SG189817A1 (en) | 2008-04-30 | 2013-05-31 | Immunogen Inc | Potent conjugates and hydrophilic linkers |
| KR101738203B1 (ko) | 2010-04-15 | 2017-05-19 | 메디뮨 리미티드 | 피롤로벤조디아제핀 및 그의 컨주게이트 |
| US20130244905A1 (en) | 2010-07-06 | 2013-09-19 | Ed Grabczyk | Reporter for RNA Polymerase II Termination |
| MX371526B (es) | 2011-05-27 | 2020-01-31 | Ambrx Inc | Composiciones que contienen, metodos que incluyen, y usos de derivados de dolastatina enlazados a aminoacidos no naturales. |
| MX359217B (es) | 2011-05-27 | 2018-09-19 | Ambrx Inc | Composiciones que contienen, métodos que involucran, y usos de derivados de dolastatina unidos a aminoácidos no naturales. |
| US8815226B2 (en) | 2011-06-10 | 2014-08-26 | Mersana Therapeutics, Inc. | Protein-polymer-drug conjugates |
| KR101891859B1 (ko) | 2011-10-14 | 2018-08-24 | 메디뮨 리미티드 | 피롤로벤조디아제핀 |
| EA036202B1 (ru) | 2011-10-14 | 2020-10-14 | Сиэтл Дженетикс, Инк. | Пирролбензодиазепины и конъюгаты направленного действия |
| US9526798B2 (en) | 2011-10-14 | 2016-12-27 | Seattle Genetics, Inc. | Pyrrolobenzodiazepines and targeted conjugates |
| AU2012322933B2 (en) | 2011-10-14 | 2017-02-02 | Medimmune Limited | Synthesis method and intermediates useful in the preparation of pyrrolobenzodiazepines |
| WO2013068874A1 (en) | 2011-11-11 | 2013-05-16 | Pfizer Inc. | Antibody-drug conjugates |
| JP6855661B2 (ja) | 2012-10-23 | 2021-04-07 | シンアフィックス ビー.ブイ. | 修飾抗体、抗体コンジュゲート及びそれらを調製する方法 |
| MY183572A (en) * | 2013-03-15 | 2021-02-26 | Regeneron Pharma | Biologically active molecules, conjugates thereof, and therapeutic uses |
| CA2921412A1 (en) | 2013-08-26 | 2015-03-05 | Regeneron Pharmaceuticals, Inc. | Pharmaceutical compositions comprising macrolide diastereomers, methods of their synthesis and therapeutic uses |
| US11103593B2 (en) * | 2013-10-15 | 2021-08-31 | Seagen Inc. | Pegylated drug-linkers for improved ligand-drug conjugate pharmacokinetics |
| CA2950155C (en) * | 2014-06-02 | 2021-11-23 | Regeneron Pharmaceuticals, Inc. | Biologically active molecule conjugates, reagents and methods of manufacture, and therapeutic uses |
| KR20170086536A (ko) * | 2014-12-03 | 2017-07-26 | 제넨테크, 인크. | 항-스타필로코커스 아우레우스 항체 리파마이신 접합체 및 이의 용도 |
| JP6751393B2 (ja) * | 2014-12-03 | 2020-09-02 | ジェネンテック, インコーポレイテッド | 抗staphylococcus aureus抗体リファマイシン抱合体及びその使用 |
| CA2970155A1 (en) * | 2014-12-09 | 2016-06-16 | Abbvie Inc. | Bcl-xl inhibitory compounds having low cell permeability and antibody drug conjugates including the same |
| JP2018502839A (ja) * | 2014-12-09 | 2018-02-01 | アッヴィ・インコーポレイテッド | Bcl−xL阻害性化合物およびこれを含む抗体薬物コンジュゲート |
| EA034950B1 (ru) | 2015-03-27 | 2020-04-09 | Регенерон Фармасьютикалз, Инк. | Производные майтанзиноида, их конъюгаты и способы использования |
| CN114478801A (zh) | 2016-01-25 | 2022-05-13 | 里珍纳龙药品有限公司 | 美登素类化合物衍生物、其偶联物和使用方法 |
| AU2017237186A1 (en) | 2016-03-25 | 2018-11-01 | Seagen Inc. | Process for the preparation of PEGylated drug-linkers and intermediates thereof |
| EP3468599A2 (en) * | 2016-06-08 | 2019-04-17 | AbbVie Inc. | Anti-cd98 antibodies and antibody drug conjugates |
| WO2018089373A2 (en) * | 2016-11-08 | 2018-05-17 | Regeneron Pharmaceuticals, Inc. | Steroids and protein-conjugates thereof |
| MX2019013690A (es) * | 2017-05-18 | 2020-01-27 | Regeneron Pharma | Conjugados de farmaco-proteina con ciclodextrina. |
| AU2018269568B2 (en) * | 2017-05-18 | 2022-03-24 | Regeneron Pharmaceuticals, Inc. | Bis-octahydrophenanthrene carboxamides and protein conjugates thereof |
-
2018
- 2018-11-06 KR KR1020207015856A patent/KR20200085807A/ko unknown
- 2018-11-06 MX MX2020004691A patent/MX2020004691A/es unknown
- 2018-11-06 JP JP2020524502A patent/JP7426931B2/ja active Active
- 2018-11-06 AU AU2018365946A patent/AU2018365946A1/en active Pending
- 2018-11-06 CA CA3080857A patent/CA3080857A1/en active Pending
- 2018-11-06 CN CN201880085150.3A patent/CN111601619A/zh active Pending
- 2018-11-06 EA EA202091135A patent/EA202091135A1/ru unknown
- 2018-11-06 SG SG11202004151YA patent/SG11202004151YA/en unknown
- 2018-11-06 WO PCT/US2018/059495 patent/WO2019094395A2/en unknown
- 2018-11-06 EP EP18803845.9A patent/EP3706805A2/en active Pending
-
2020
- 2020-05-04 IL IL274427A patent/IL274427A/en unknown
-
2024
- 2024-01-23 JP JP2024007898A patent/JP2024045283A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| JP2021502341A (ja) | 2021-01-28 |
| WO2019094395A2 (en) | 2019-05-16 |
| JP2024045283A (ja) | 2024-04-02 |
| WO2019094395A3 (en) | 2019-08-22 |
| AU2018365946A1 (en) | 2020-05-14 |
| EA202091135A1 (ru) | 2020-10-14 |
| JP7426931B2 (ja) | 2024-02-02 |
| IL274427A (en) | 2020-06-30 |
| SG11202004151YA (en) | 2020-06-29 |
| MX2020004691A (es) | 2020-08-20 |
| CA3080857A1 (en) | 2019-05-16 |
| EP3706805A2 (en) | 2020-09-16 |
| CN111601619A (zh) | 2020-08-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20210332080A1 (en) | Hydrophilic linkers for antibody drug conjugates | |
| KR20200085807A (ko) | 항체 약물 접합제용 친수성 링커 | |
| US20230035898A1 (en) | Cyclodextrin protein drug conjugates | |
| AU2018269568B2 (en) | Bis-octahydrophenanthrene carboxamides and protein conjugates thereof | |
| KR20200108002A (ko) | 스테로이드 및 이의 항체-접합체 | |
| WO2016094509A1 (en) | Bcl xl inhibitory compounds having low cell permeability and antibody drug conjugates including the same | |
| KR20210114008A (ko) | 흔적이 없는 링커 및 이의 단백질-접합체 | |
| CN113382985A (zh) | 用作lxr激动剂的双八氢菲羧酰胺类衍生物及其蛋白质偶联物 | |
| US20210260208A1 (en) | Tubulysins and protein-tubulysin conjugates | |
| US20230119539A1 (en) | Traceless linkers and protein-conjugates thereof |