KR20200083528A - 파르네소이드 x 수용체 조정제로서의 스피로시클릭 화합물 - Google Patents
파르네소이드 x 수용체 조정제로서의 스피로시클릭 화합물 Download PDFInfo
- Publication number
- KR20200083528A KR20200083528A KR1020207015273A KR20207015273A KR20200083528A KR 20200083528 A KR20200083528 A KR 20200083528A KR 1020207015273 A KR1020207015273 A KR 1020207015273A KR 20207015273 A KR20207015273 A KR 20207015273A KR 20200083528 A KR20200083528 A KR 20200083528A
- Authority
- KR
- South Korea
- Prior art keywords
- alkyl
- independently
- cyclopropyl
- azaspiro
- mmol
- Prior art date
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 368
- 102100038495 Bile acid receptor Human genes 0.000 title abstract description 253
- 101000603876 Homo sapiens Bile acid receptor Proteins 0.000 title abstract description 253
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 80
- 238000000034 method Methods 0.000 claims abstract description 73
- 150000003839 salts Chemical class 0.000 claims abstract description 57
- 208000035475 disorder Diseases 0.000 claims abstract description 50
- 239000012453 solvate Substances 0.000 claims abstract description 39
- 206010016654 Fibrosis Diseases 0.000 claims abstract description 25
- 230000004761 fibrosis Effects 0.000 claims abstract description 23
- 239000008194 pharmaceutical composition Substances 0.000 claims abstract description 23
- 206010028980 Neoplasm Diseases 0.000 claims abstract description 16
- 208000027866 inflammatory disease Diseases 0.000 claims abstract description 13
- 201000011510 cancer Diseases 0.000 claims abstract description 11
- 230000001575 pathological effect Effects 0.000 claims abstract description 5
- -1 cyano, hydroxyl Chemical group 0.000 claims description 203
- 125000000217 alkyl group Chemical group 0.000 claims description 82
- 125000000623 heterocyclic group Chemical group 0.000 claims description 60
- 229910052760 oxygen Inorganic materials 0.000 claims description 53
- 229910052717 sulfur Inorganic materials 0.000 claims description 53
- 125000003118 aryl group Chemical group 0.000 claims description 52
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 44
- 125000005842 heteroatom Chemical group 0.000 claims description 43
- 125000004432 carbon atom Chemical group C* 0.000 claims description 38
- 125000004076 pyridyl group Chemical group 0.000 claims description 38
- 229910052799 carbon Inorganic materials 0.000 claims description 37
- 125000002947 alkylene group Chemical group 0.000 claims description 36
- 125000001072 heteroaryl group Chemical group 0.000 claims description 36
- 229910052757 nitrogen Inorganic materials 0.000 claims description 36
- 125000003545 alkoxy group Chemical group 0.000 claims description 35
- 208000008338 non-alcoholic fatty liver disease Diseases 0.000 claims description 34
- 125000001188 haloalkyl group Chemical group 0.000 claims description 28
- 125000004452 carbocyclyl group Chemical group 0.000 claims description 27
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 claims description 26
- 229910052739 hydrogen Inorganic materials 0.000 claims description 25
- 125000004103 aminoalkyl group Chemical group 0.000 claims description 24
- 125000004438 haloalkoxy group Chemical group 0.000 claims description 24
- 125000005843 halogen group Chemical group 0.000 claims description 24
- 125000004435 hydrogen atom Chemical class [H]* 0.000 claims description 22
- 239000001257 hydrogen Substances 0.000 claims description 21
- 125000002768 hydroxyalkyl group Chemical group 0.000 claims description 21
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 19
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 claims description 18
- 206010053219 non-alcoholic steatohepatitis Diseases 0.000 claims description 18
- 125000003282 alkyl amino group Chemical group 0.000 claims description 17
- 229910052801 chlorine Inorganic materials 0.000 claims description 17
- 125000004433 nitrogen atom Chemical group N* 0.000 claims description 16
- 125000004183 alkoxy alkyl group Chemical group 0.000 claims description 15
- 125000004429 atom Chemical group 0.000 claims description 15
- 125000004994 halo alkoxy alkyl group Chemical group 0.000 claims description 15
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 14
- 229910052731 fluorine Inorganic materials 0.000 claims description 14
- 239000003937 drug carrier Substances 0.000 claims description 13
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 claims description 12
- 125000002950 monocyclic group Chemical group 0.000 claims description 11
- 125000004043 oxo group Chemical group O=* 0.000 claims description 11
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 claims description 10
- 208000008439 Biliary Liver Cirrhosis Diseases 0.000 claims description 9
- 125000001041 indolyl group Chemical group 0.000 claims description 9
- 208000036971 interstitial lung disease 2 Diseases 0.000 claims description 9
- 238000002560 therapeutic procedure Methods 0.000 claims description 9
- 125000001313 C5-C10 heteroaryl group Chemical group 0.000 claims description 8
- 201000009794 Idiopathic Pulmonary Fibrosis Diseases 0.000 claims description 8
- 125000004414 alkyl thio group Chemical group 0.000 claims description 8
- 208000019425 cirrhosis of liver Diseases 0.000 claims description 8
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 claims description 8
- 125000004474 heteroalkylene group Chemical group 0.000 claims description 8
- 125000004450 alkenylene group Chemical group 0.000 claims description 7
- 125000004446 heteroarylalkyl group Chemical group 0.000 claims description 7
- 125000003373 pyrazinyl group Chemical group 0.000 claims description 7
- 125000000714 pyrimidinyl group Chemical group 0.000 claims description 7
- 125000004104 aryloxy group Chemical group 0.000 claims description 6
- 125000002183 isoquinolinyl group Chemical group C1(=NC=CC2=CC=CC=C12)* 0.000 claims description 6
- 125000002098 pyridazinyl group Chemical group 0.000 claims description 6
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 claims description 6
- 208000007342 Diabetic Nephropathies Diseases 0.000 claims description 5
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 5
- 125000004419 alkynylene group Chemical group 0.000 claims description 5
- 238000004132 cross linking Methods 0.000 claims description 5
- 208000033679 diabetic kidney disease Diseases 0.000 claims description 5
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 claims description 5
- 125000001567 quinoxalinyl group Chemical group N1=C(C=NC2=CC=CC=C12)* 0.000 claims description 5
- 208000010157 sclerosing cholangitis Diseases 0.000 claims description 5
- 125000004767 (C1-C4) haloalkoxy group Chemical group 0.000 claims description 4
- 125000004765 (C1-C4) haloalkyl group Chemical group 0.000 claims description 4
- 125000002102 aryl alkyloxo group Chemical group 0.000 claims description 4
- 125000005873 benzo[d]thiazolyl group Chemical group 0.000 claims description 4
- 125000005884 carbocyclylalkyl group Chemical group 0.000 claims description 4
- 208000020832 chronic kidney disease Diseases 0.000 claims description 4
- 125000003147 glycosyl group Chemical group 0.000 claims description 4
- 125000005553 heteroaryloxy group Chemical group 0.000 claims description 4
- 125000004415 heterocyclylalkyl group Chemical group 0.000 claims description 4
- 125000000171 (C1-C6) haloalkyl group Chemical group 0.000 claims description 3
- 125000006555 (C3-C5) cycloalkyl group Chemical group 0.000 claims description 3
- 206010004664 Biliary fibrosis Diseases 0.000 claims description 3
- 125000005083 alkoxyalkoxy group Chemical group 0.000 claims description 3
- 125000001691 aryl alkyl amino group Chemical group 0.000 claims description 3
- 125000001769 aryl amino group Chemical group 0.000 claims description 3
- 230000001587 cholestatic effect Effects 0.000 claims description 3
- 125000000000 cycloalkoxy group Chemical group 0.000 claims description 3
- 125000006310 cycloalkyl amino group Chemical group 0.000 claims description 3
- 125000004992 haloalkylamino group Chemical group 0.000 claims description 3
- 125000005114 heteroarylalkoxy group Chemical group 0.000 claims description 3
- 125000005844 heterocyclyloxy group Chemical group 0.000 claims description 3
- 125000006431 methyl cyclopropyl group Chemical group 0.000 claims description 3
- 201000002793 renal fibrosis Diseases 0.000 claims description 3
- 125000006570 (C5-C6) heteroaryl group Chemical group 0.000 claims description 2
- 206010004659 Biliary cirrhosis Diseases 0.000 claims description 2
- 230000002503 metabolic effect Effects 0.000 claims description 2
- 150000003018 phosphorus compounds Chemical class 0.000 claims 1
- 201000010099 disease Diseases 0.000 abstract description 28
- 230000000694 effects Effects 0.000 abstract description 15
- 239000000556 agonist Substances 0.000 abstract description 5
- 230000008482 dysregulation Effects 0.000 abstract description 3
- 206010052779 Transplant rejections Diseases 0.000 abstract description 2
- 208000001132 Osteoporosis Diseases 0.000 abstract 1
- 238000005481 NMR spectroscopy Methods 0.000 description 280
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 211
- 238000002360 preparation method Methods 0.000 description 203
- 238000007429 general method Methods 0.000 description 189
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 129
- 239000011541 reaction mixture Substances 0.000 description 103
- 235000019439 ethyl acetate Nutrition 0.000 description 102
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical class OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 100
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 93
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 88
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 79
- 239000000203 mixture Substances 0.000 description 77
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 71
- 229910004298 SiO 2 Inorganic materials 0.000 description 66
- 239000000243 solution Substances 0.000 description 60
- 238000003818 flash chromatography Methods 0.000 description 59
- 239000007787 solid Substances 0.000 description 55
- 239000000543 intermediate Substances 0.000 description 53
- 238000006243 chemical reaction Methods 0.000 description 50
- DMIYKWPEFRFTPY-UHFFFAOYSA-N 2,6-dichlorobenzaldehyde Chemical compound ClC1=CC=CC(Cl)=C1C=O DMIYKWPEFRFTPY-UHFFFAOYSA-N 0.000 description 48
- 239000002904 solvent Substances 0.000 description 44
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 42
- JCZHXUDTUVKJFH-UHFFFAOYSA-N ethyl 2-bromo-4-fluoro-1,3-benzothiazole-6-carboxylate Chemical compound BrC=1SC2=C(N=1)C(=CC(=C2)C(=O)OCC)F JCZHXUDTUVKJFH-UHFFFAOYSA-N 0.000 description 42
- OKKJLVBELUTLKV-MZCSYVLQSA-N Deuterated methanol Chemical compound [2H]OC([2H])([2H])[2H] OKKJLVBELUTLKV-MZCSYVLQSA-N 0.000 description 41
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 36
- DTQVDTLACAAQTR-UHFFFAOYSA-N trifluoroacetic acid Substances OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 36
- 239000003814 drug Substances 0.000 description 33
- 239000011734 sodium Substances 0.000 description 32
- 239000012267 brine Substances 0.000 description 28
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 28
- ZDVRPKUWYQVVDX-UHFFFAOYSA-N 2-(trifluoromethyl)benzaldehyde Chemical compound FC(F)(F)C1=CC=CC=C1C=O ZDVRPKUWYQVVDX-UHFFFAOYSA-N 0.000 description 26
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical group CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 25
- 239000012044 organic layer Substances 0.000 description 25
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 24
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 23
- 239000000047 product Substances 0.000 description 23
- 239000002253 acid Substances 0.000 description 22
- 239000012071 phase Substances 0.000 description 22
- 230000001629 suppression Effects 0.000 description 22
- 239000002585 base Substances 0.000 description 21
- 239000000460 chlorine Substances 0.000 description 21
- 238000005859 coupling reaction Methods 0.000 description 21
- 238000010438 heat treatment Methods 0.000 description 21
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 20
- 150000002148 esters Chemical class 0.000 description 20
- 125000001424 substituent group Chemical group 0.000 description 20
- 238000003786 synthesis reaction Methods 0.000 description 20
- 229940124597 therapeutic agent Drugs 0.000 description 20
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium Chemical compound [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 19
- 230000015572 biosynthetic process Effects 0.000 description 19
- 230000008878 coupling Effects 0.000 description 19
- 238000010168 coupling process Methods 0.000 description 19
- 229920006395 saturated elastomer Polymers 0.000 description 19
- RBFNWOINNIOZKR-UHFFFAOYSA-N 3,5-dichloropyridine-4-carbaldehyde Chemical compound ClC1=CN=CC(Cl)=C1C=O RBFNWOINNIOZKR-UHFFFAOYSA-N 0.000 description 18
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 18
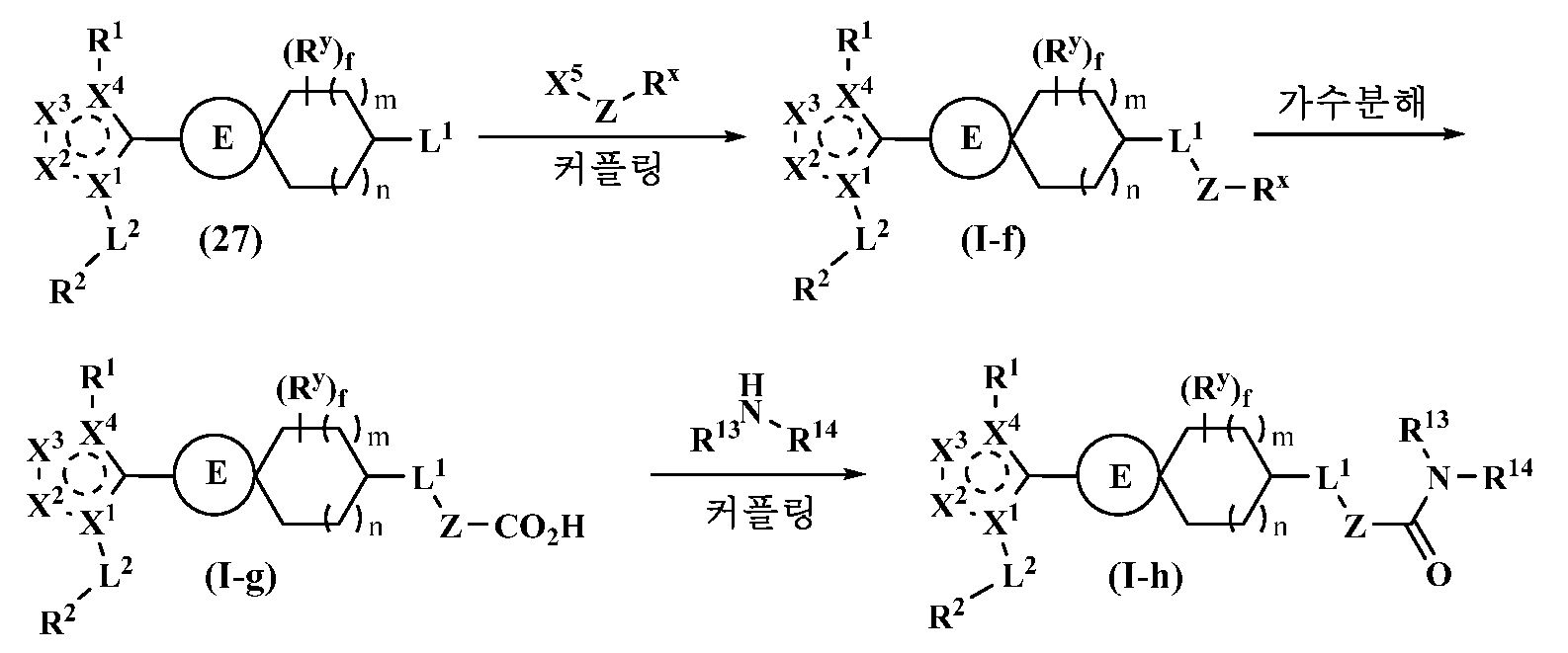
- 230000007062 hydrolysis Effects 0.000 description 18
- 238000006460 hydrolysis reaction Methods 0.000 description 18
- 239000000651 prodrug Substances 0.000 description 18
- 229940002612 prodrug Drugs 0.000 description 18
- 239000003153 chemical reaction reagent Substances 0.000 description 17
- 125000006239 protecting group Chemical group 0.000 description 17
- 238000003756 stirring Methods 0.000 description 17
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Natural products CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 16
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 16
- JZWYSYPKWGGCNQ-UHFFFAOYSA-N methyl 6-chloro-1-methylpyrrolo[2,3-b]pyridine-3-carboxylate Chemical compound ClC1=CC=C2C(C(=O)OC)=CN(C)C2=N1 JZWYSYPKWGGCNQ-UHFFFAOYSA-N 0.000 description 16
- SOWRUJSGHKNOKN-UHFFFAOYSA-N 2,6-difluorobenzaldehyde Chemical compound FC1=CC=CC(F)=C1C=O SOWRUJSGHKNOKN-UHFFFAOYSA-N 0.000 description 15
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 15
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 15
- 239000003112 inhibitor Substances 0.000 description 15
- 239000010410 layer Substances 0.000 description 15
- 230000005764 inhibitory process Effects 0.000 description 14
- 239000004480 active ingredient Substances 0.000 description 13
- 239000003613 bile acid Substances 0.000 description 13
- 239000000725 suspension Substances 0.000 description 13
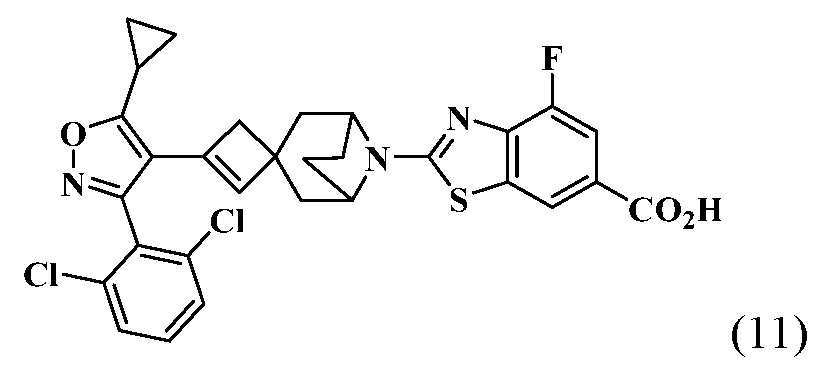
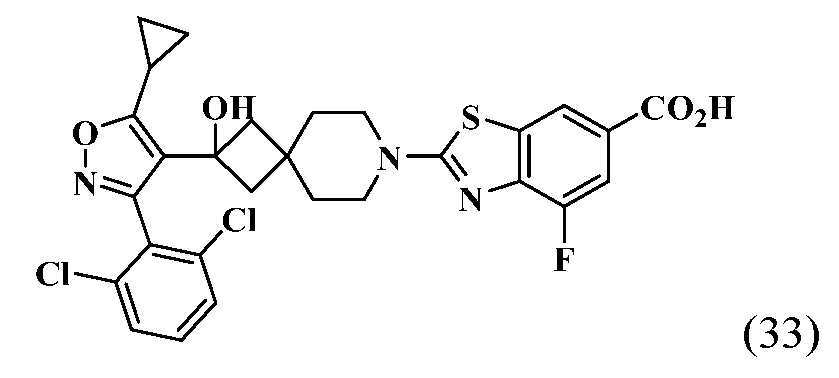
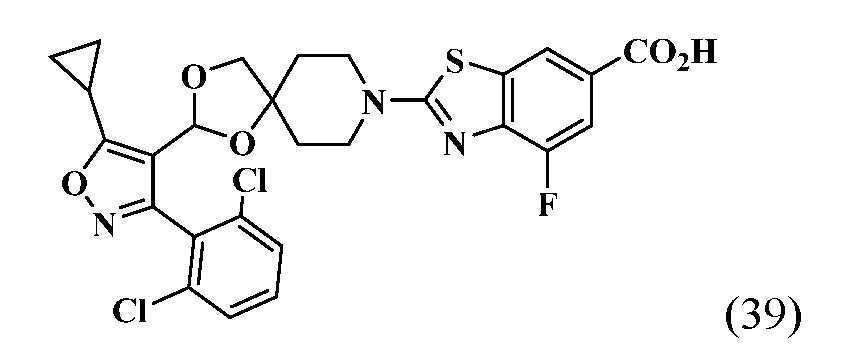
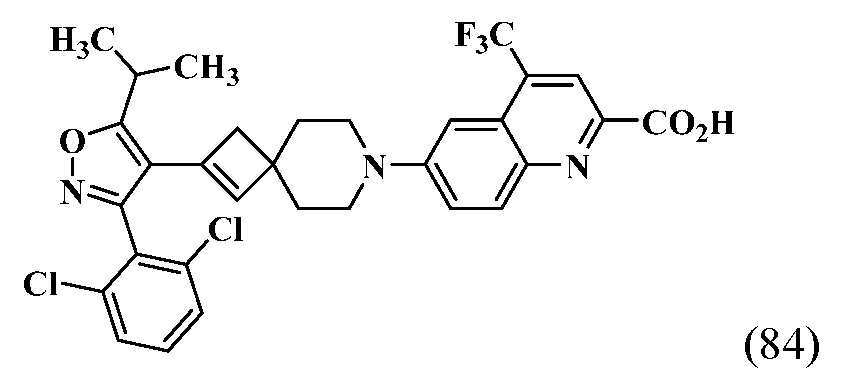
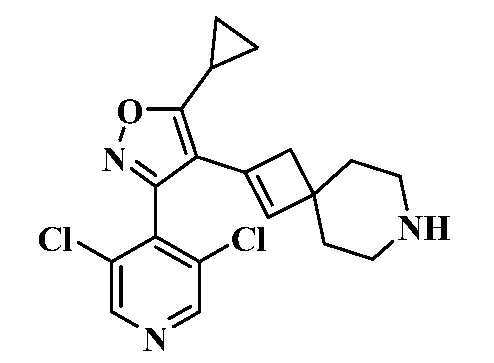
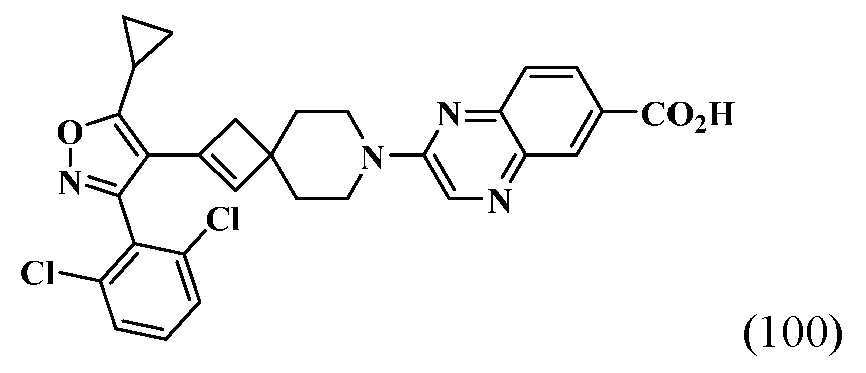
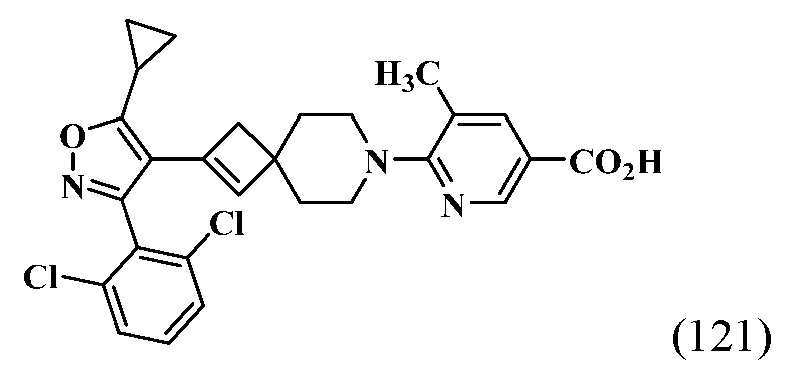
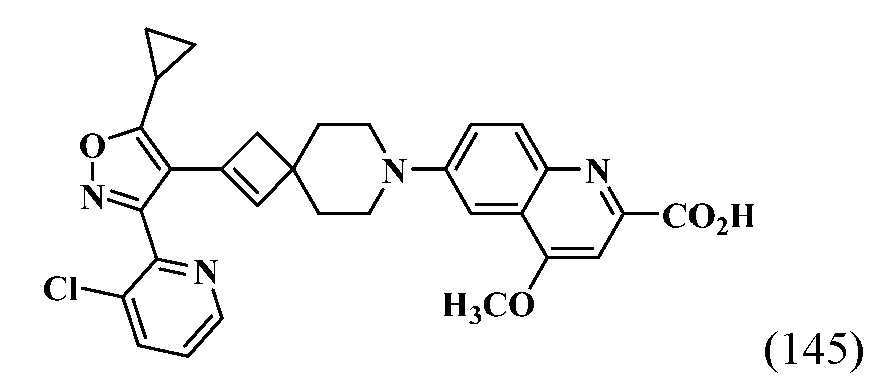
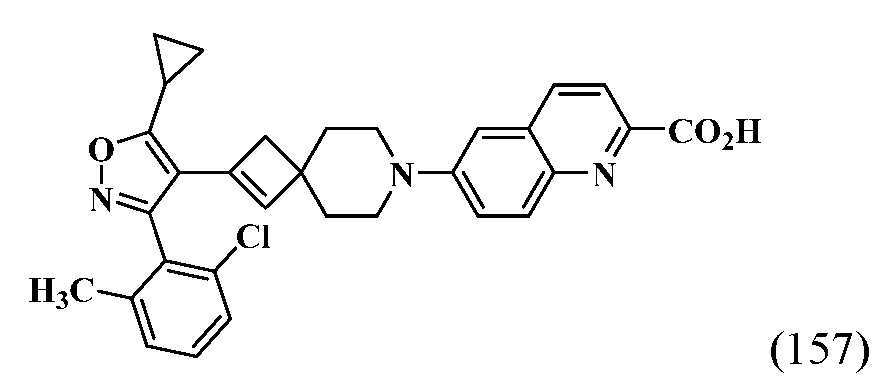
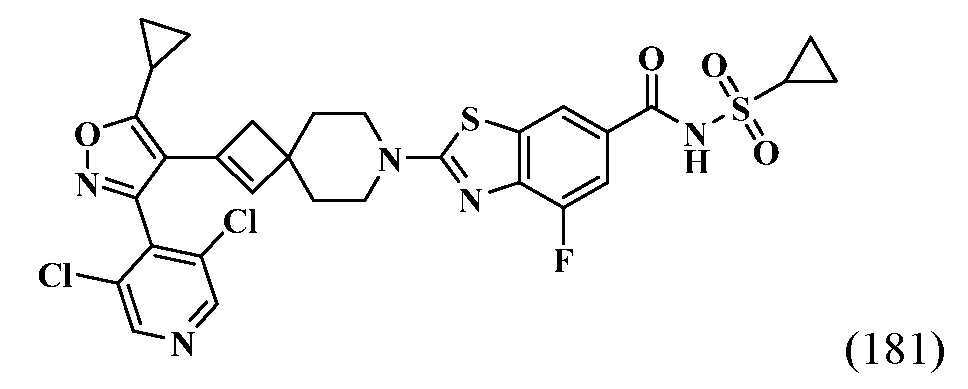
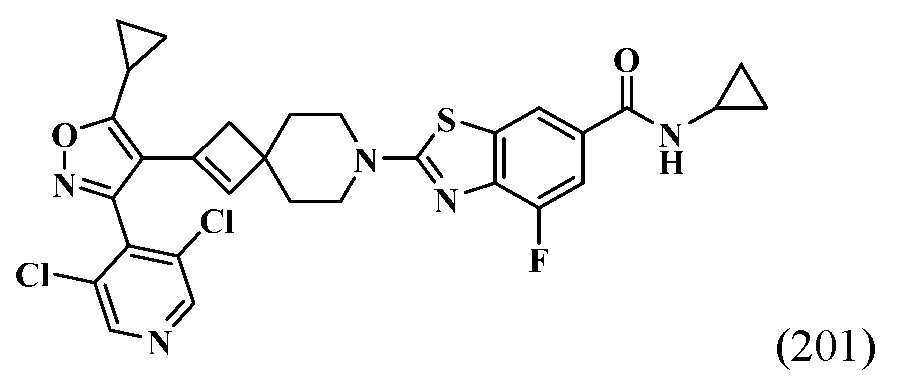
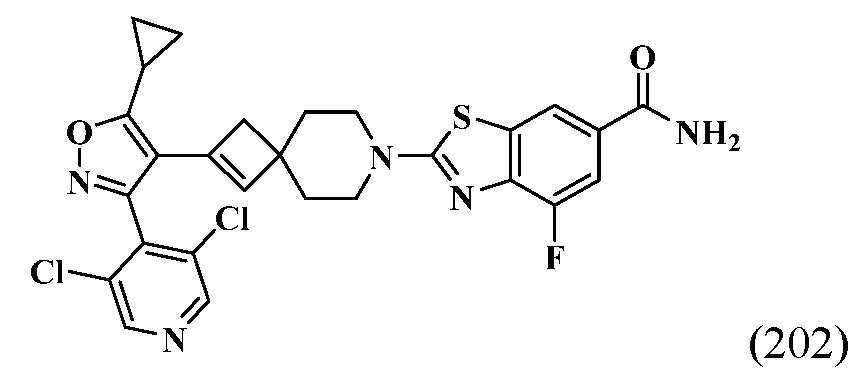
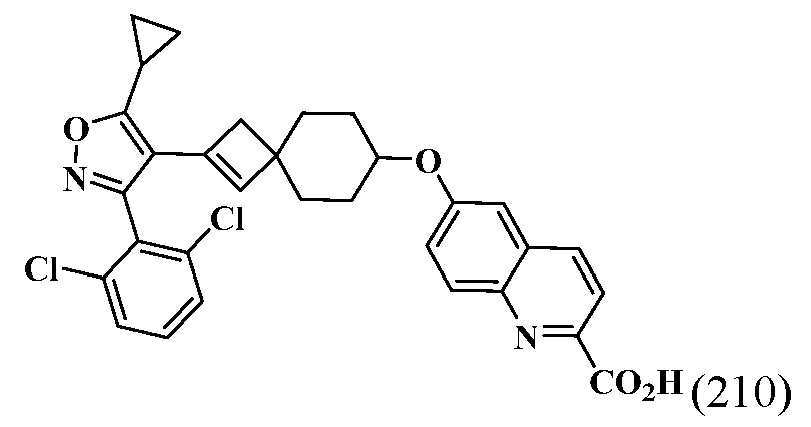
- HSWCABTYQVCNCT-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F HSWCABTYQVCNCT-UHFFFAOYSA-N 0.000 description 12
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 12
- 239000005695 Ammonium acetate Substances 0.000 description 12
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 12
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 12
- 235000019257 ammonium acetate Nutrition 0.000 description 12
- 229940043376 ammonium acetate Drugs 0.000 description 12
- 150000001721 carbon Chemical group 0.000 description 12
- 239000003795 chemical substances by application Substances 0.000 description 12
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 12
- 230000001404 mediated effect Effects 0.000 description 12
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 12
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 11
- PAQZWJGSJMLPMG-UHFFFAOYSA-N 2,4,6-tripropyl-1,3,5,2$l^{5},4$l^{5},6$l^{5}-trioxatriphosphinane 2,4,6-trioxide Chemical compound CCCP1(=O)OP(=O)(CCC)OP(=O)(CCC)O1 PAQZWJGSJMLPMG-UHFFFAOYSA-N 0.000 description 11
- LNHXJOJOYYLHIW-UHFFFAOYSA-N 4-(trifluoromethyl)pyridine-3-carbaldehyde Chemical compound FC(F)(F)C1=CC=NC=C1C=O LNHXJOJOYYLHIW-UHFFFAOYSA-N 0.000 description 11
- 229940121360 farnesoid X receptor (fxr) agonists Drugs 0.000 description 11
- 210000004185 liver Anatomy 0.000 description 11
- 238000004519 manufacturing process Methods 0.000 description 11
- MZRVEZGGRBJDDB-UHFFFAOYSA-N n-Butyllithium Substances [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 11
- 238000000746 purification Methods 0.000 description 11
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 10
- 239000000284 extract Substances 0.000 description 10
- 239000006260 foam Substances 0.000 description 10
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 10
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 9
- PVNIIMVLHYAWGP-UHFFFAOYSA-N Niacin Chemical compound OC(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-N 0.000 description 9
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 9
- 125000004093 cyano group Chemical group *C#N 0.000 description 9
- WMSPXQIQBQAWLL-UHFFFAOYSA-N cyclopropanesulfonamide Chemical compound NS(=O)(=O)C1CC1 WMSPXQIQBQAWLL-UHFFFAOYSA-N 0.000 description 9
- MLUQDYXYTIQLLY-UHFFFAOYSA-N ethyl 6-chloro-4-(trifluoromethyl)quinoline-2-carboxylate Chemical compound C1=C(Cl)C=CC2=NC(C(=O)OCC)=CC(C(F)(F)F)=C21 MLUQDYXYTIQLLY-UHFFFAOYSA-N 0.000 description 9
- NPTDXPDGUHAFKC-UHFFFAOYSA-N ethynylcyclopropane Chemical group C#CC1CC1 NPTDXPDGUHAFKC-UHFFFAOYSA-N 0.000 description 9
- 230000003176 fibrotic effect Effects 0.000 description 9
- 125000004404 heteroalkyl group Chemical group 0.000 description 9
- 238000004128 high performance liquid chromatography Methods 0.000 description 9
- 150000002576 ketones Chemical class 0.000 description 9
- HSINOMROUCMIEA-FGVHQWLLSA-N (2s,4r)-4-[(3r,5s,6r,7r,8s,9s,10s,13r,14s,17r)-6-ethyl-3,7-dihydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-17-yl]-2-methylpentanoic acid Chemical compound C([C@@]12C)C[C@@H](O)C[C@H]1[C@@H](CC)[C@@H](O)[C@@H]1[C@@H]2CC[C@]2(C)[C@@H]([C@H](C)C[C@H](C)C(O)=O)CC[C@H]21 HSINOMROUCMIEA-FGVHQWLLSA-N 0.000 description 8
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 8
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 8
- JRNVZBWKYDBUCA-UHFFFAOYSA-N N-chlorosuccinimide Chemical compound ClN1C(=O)CCC1=O JRNVZBWKYDBUCA-UHFFFAOYSA-N 0.000 description 8
- 230000002378 acidificating effect Effects 0.000 description 8
- 150000001336 alkenes Chemical class 0.000 description 8
- 230000005587 bubbling Effects 0.000 description 8
- 150000001732 carboxylic acid derivatives Chemical group 0.000 description 8
- QTMDXZNDVAMKGV-UHFFFAOYSA-L copper(ii) bromide Chemical compound [Cu+2].[Br-].[Br-] QTMDXZNDVAMKGV-UHFFFAOYSA-L 0.000 description 8
- KVFDZFBHBWTVID-UHFFFAOYSA-N cyclohexanecarbaldehyde Chemical compound O=CC1CCCCC1 KVFDZFBHBWTVID-UHFFFAOYSA-N 0.000 description 8
- 239000000706 filtrate Substances 0.000 description 8
- 150000004820 halides Chemical class 0.000 description 8
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 8
- 239000003446 ligand Substances 0.000 description 8
- 239000000463 material Substances 0.000 description 8
- 229910052763 palladium Inorganic materials 0.000 description 8
- 239000002245 particle Substances 0.000 description 8
- 108090000623 proteins and genes Proteins 0.000 description 8
- LPXPTNMVRIOKMN-UHFFFAOYSA-M sodium nitrite Chemical compound [Na+].[O-]N=O LPXPTNMVRIOKMN-UHFFFAOYSA-M 0.000 description 8
- 229940086542 triethylamine Drugs 0.000 description 8
- UOQMGQYMDHYXTB-UHFFFAOYSA-N 2,6-dichloro-4-fluorobenzaldehyde Chemical compound FC1=CC(Cl)=C(C=O)C(Cl)=C1 UOQMGQYMDHYXTB-UHFFFAOYSA-N 0.000 description 7
- CPHXLFKIUVVIOQ-UHFFFAOYSA-N 2-(trifluoromethoxy)benzaldehyde Chemical compound FC(F)(F)OC1=CC=CC=C1C=O CPHXLFKIUVVIOQ-UHFFFAOYSA-N 0.000 description 7
- QXNVCYJXFQPEKQ-UHFFFAOYSA-N 3-chloropyridine-2-carbaldehyde Chemical compound ClC1=CC=CN=C1C=O QXNVCYJXFQPEKQ-UHFFFAOYSA-N 0.000 description 7
- 208000033222 Biliary cirrhosis primary Diseases 0.000 description 7
- 208000012654 Primary biliary cholangitis Diseases 0.000 description 7
- 238000009472 formulation Methods 0.000 description 7
- 229910052736 halogen Inorganic materials 0.000 description 7
- 150000002367 halogens Chemical class 0.000 description 7
- 238000001727 in vivo Methods 0.000 description 7
- CTAPFRYPJLPFDF-UHFFFAOYSA-N isoxazole Chemical compound C=1C=NOC=1 CTAPFRYPJLPFDF-UHFFFAOYSA-N 0.000 description 7
- HNQIVZYLYMDVSB-UHFFFAOYSA-N methanesulfonimidic acid Chemical compound CS(N)(=O)=O HNQIVZYLYMDVSB-UHFFFAOYSA-N 0.000 description 7
- 238000005457 optimization Methods 0.000 description 7
- 125000003367 polycyclic group Polymers 0.000 description 7
- XGVXKJKTISMIOW-ZDUSSCGKSA-N simurosertib Chemical compound N1N=CC(C=2SC=3C(=O)NC(=NC=3C=2)[C@H]2N3CCC(CC3)C2)=C1C XGVXKJKTISMIOW-ZDUSSCGKSA-N 0.000 description 7
- 239000002002 slurry Substances 0.000 description 7
- 239000000126 substance Substances 0.000 description 7
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 7
- ABDDQTDRAHXHOC-QMMMGPOBSA-N 1-[(7s)-5,7-dihydro-4h-thieno[2,3-c]pyran-7-yl]-n-methylmethanamine Chemical compound CNC[C@@H]1OCCC2=C1SC=C2 ABDDQTDRAHXHOC-QMMMGPOBSA-N 0.000 description 6
- COMFXXABDQGVSV-UHFFFAOYSA-N 2-(trifluoromethyl)pyridine-3-carbaldehyde Chemical compound FC(F)(F)C1=NC=CC=C1C=O COMFXXABDQGVSV-UHFFFAOYSA-N 0.000 description 6
- 101150075266 CYP7A1 gene Proteins 0.000 description 6
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 6
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 6
- WTDHULULXKLSOZ-UHFFFAOYSA-N Hydroxylamine hydrochloride Chemical compound Cl.ON WTDHULULXKLSOZ-UHFFFAOYSA-N 0.000 description 6
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 6
- 101100390675 Mus musculus Fgf15 gene Proteins 0.000 description 6
- PXIPVTKHYLBLMZ-UHFFFAOYSA-N Sodium azide Chemical compound [Na+].[N-]=[N+]=[N-] PXIPVTKHYLBLMZ-UHFFFAOYSA-N 0.000 description 6
- 239000000654 additive Substances 0.000 description 6
- 125000005605 benzo group Chemical group 0.000 description 6
- 229910052794 bromium Inorganic materials 0.000 description 6
- 239000003054 catalyst Substances 0.000 description 6
- NVVXJVMOIGXUGC-UHFFFAOYSA-M chloropalladium(1+);dicyclohexyl-[2-[2,6-di(propan-2-yloxy)phenyl]phenyl]phosphane;2-phenylaniline Chemical compound [Pd+]Cl.NC1=CC=CC=C1C1=CC=CC=[C-]1.CC(C)OC1=CC=CC(OC(C)C)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 NVVXJVMOIGXUGC-UHFFFAOYSA-M 0.000 description 6
- 239000012043 crude product Substances 0.000 description 6
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Substances CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 6
- 125000000524 functional group Chemical group 0.000 description 6
- HLYBWNNPVXFCPZ-UHFFFAOYSA-N methyl 6-fluoropyridine-3-carboxylate Chemical compound COC(=O)C1=CC=C(F)N=C1 HLYBWNNPVXFCPZ-UHFFFAOYSA-N 0.000 description 6
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 6
- NLKNQRATVPKPDG-UHFFFAOYSA-M potassium iodide Chemical compound [K+].[I-] NLKNQRATVPKPDG-UHFFFAOYSA-M 0.000 description 6
- 230000002829 reductive effect Effects 0.000 description 6
- 125000001544 thienyl group Chemical group 0.000 description 6
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 6
- AQRLNPVMDITEJU-UHFFFAOYSA-N triethylsilane Chemical compound CC[SiH](CC)CC AQRLNPVMDITEJU-UHFFFAOYSA-N 0.000 description 6
- OACPOWYLLGHGCR-UHFFFAOYSA-N 2-chloro-6-fluorobenzaldehyde Chemical compound FC1=CC=CC(Cl)=C1C=O OACPOWYLLGHGCR-UHFFFAOYSA-N 0.000 description 5
- USCSRAJGJYMJFZ-UHFFFAOYSA-N 3-methyl-1-butyne Chemical group CC(C)C#C USCSRAJGJYMJFZ-UHFFFAOYSA-N 0.000 description 5
- XCTRBUACYHIAOV-UHFFFAOYSA-N 4-(7-azaspiro[3.5]non-2-en-2-yl)-5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazole Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCNCC2 XCTRBUACYHIAOV-UHFFFAOYSA-N 0.000 description 5
- AQOJZGXBMHLUFA-UHFFFAOYSA-N 4-bromo-5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazole Chemical compound BrC=1C(=NOC=1C1CC1)C1=C(C=CC=C1Cl)Cl AQOJZGXBMHLUFA-UHFFFAOYSA-N 0.000 description 5
- 241000699666 Mus <mouse, genus> Species 0.000 description 5
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 5
- 239000013543 active substance Substances 0.000 description 5
- 125000003342 alkenyl group Chemical group 0.000 description 5
- 150000001412 amines Chemical class 0.000 description 5
- 125000002619 bicyclic group Chemical group 0.000 description 5
- 125000002618 bicyclic heterocycle group Chemical group 0.000 description 5
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 5
- 229910000024 caesium carbonate Inorganic materials 0.000 description 5
- 125000002837 carbocyclic group Chemical group 0.000 description 5
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 description 5
- 238000001023 centrifugal evaporation Methods 0.000 description 5
- 239000010949 copper Substances 0.000 description 5
- 239000002552 dosage form Substances 0.000 description 5
- 229940079593 drug Drugs 0.000 description 5
- 238000005755 formation reaction Methods 0.000 description 5
- 230000014509 gene expression Effects 0.000 description 5
- 206010073071 hepatocellular carcinoma Diseases 0.000 description 5
- 231100000844 hepatocellular carcinoma Toxicity 0.000 description 5
- 150000002430 hydrocarbons Chemical class 0.000 description 5
- 210000000936 intestine Anatomy 0.000 description 5
- 125000000842 isoxazolyl group Chemical group 0.000 description 5
- 235000001968 nicotinic acid Nutrition 0.000 description 5
- 239000011664 nicotinic acid Substances 0.000 description 5
- 229960003512 nicotinic acid Drugs 0.000 description 5
- 125000004430 oxygen atom Chemical group O* 0.000 description 5
- 125000003226 pyrazolyl group Chemical group 0.000 description 5
- 150000003254 radicals Chemical class 0.000 description 5
- 239000000376 reactant Substances 0.000 description 5
- SIMIIXFMGJYGLR-UHFFFAOYSA-N tert-butyl 2-oxo-7-azaspiro[3.5]nonane-7-carboxylate Chemical compound C1CN(C(=O)OC(C)(C)C)CCC11CC(=O)C1 SIMIIXFMGJYGLR-UHFFFAOYSA-N 0.000 description 5
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 5
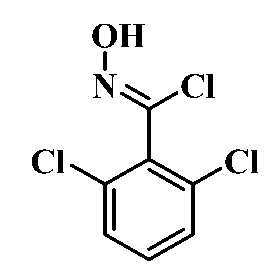
- LXWQVTNZUIURFE-XFFZJAGNSA-N (1z)-2,6-dichloro-n-hydroxybenzenecarboximidoyl chloride Chemical compound O\N=C(/Cl)C1=C(Cl)C=CC=C1Cl LXWQVTNZUIURFE-XFFZJAGNSA-N 0.000 description 4
- 238000005160 1H NMR spectroscopy Methods 0.000 description 4
- BDJKMQQQYNTTMI-UHFFFAOYSA-N 2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]spiro[3.5]nonane-2,7-diol Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1(CC2(C1)CCC(CC2)O)O BDJKMQQQYNTTMI-UHFFFAOYSA-N 0.000 description 4
- CCYFXIJPJFSTSU-UHFFFAOYSA-N 2-chloro-6-methylbenzaldehyde Chemical compound CC1=CC=CC(Cl)=C1C=O CCYFXIJPJFSTSU-UHFFFAOYSA-N 0.000 description 4
- YEDUAINPPJYDJZ-UHFFFAOYSA-N 2-hydroxybenzothiazole Chemical compound C1=CC=C2SC(O)=NC2=C1 YEDUAINPPJYDJZ-UHFFFAOYSA-N 0.000 description 4
- HCDMJFOHIXMBOV-UHFFFAOYSA-N 3-(2,6-difluoro-3,5-dimethoxyphenyl)-1-ethyl-8-(morpholin-4-ylmethyl)-4,7-dihydropyrrolo[4,5]pyrido[1,2-d]pyrimidin-2-one Chemical compound C=1C2=C3N(CC)C(=O)N(C=4C(=C(OC)C=C(OC)C=4F)F)CC3=CN=C2NC=1CN1CCOCC1 HCDMJFOHIXMBOV-UHFFFAOYSA-N 0.000 description 4
- 229960000549 4-dimethylaminophenol Drugs 0.000 description 4
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 4
- 229910021590 Copper(II) bromide Inorganic materials 0.000 description 4
- GSNUFIFRDBKVIE-UHFFFAOYSA-N DMF Natural products CC1=CC=C(C)O1 GSNUFIFRDBKVIE-UHFFFAOYSA-N 0.000 description 4
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 4
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 4
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 4
- 102000003816 Interleukin-13 Human genes 0.000 description 4
- 108090000176 Interleukin-13 Proteins 0.000 description 4
- FXHOOIRPVKKKFG-UHFFFAOYSA-N N,N-Dimethylacetamide Chemical compound CN(C)C(C)=O FXHOOIRPVKKKFG-UHFFFAOYSA-N 0.000 description 4
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 4
- 125000001931 aliphatic group Chemical group 0.000 description 4
- 125000004448 alkyl carbonyl group Chemical group 0.000 description 4
- 125000000304 alkynyl group Chemical group 0.000 description 4
- 238000003556 assay Methods 0.000 description 4
- 150000001540 azides Chemical class 0.000 description 4
- 230000009286 beneficial effect Effects 0.000 description 4
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 4
- 125000001164 benzothiazolyl group Chemical group S1C(=NC2=C1C=CC=C2)* 0.000 description 4
- 125000004541 benzoxazolyl group Chemical group O1C(=NC2=C1C=CC=C2)* 0.000 description 4
- 125000002527 bicyclic carbocyclic group Chemical group 0.000 description 4
- 239000013058 crude material Substances 0.000 description 4
- 125000004122 cyclic group Chemical group 0.000 description 4
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 4
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 4
- 238000010511 deprotection reaction Methods 0.000 description 4
- 150000002009 diols Chemical class 0.000 description 4
- PHDNOFTVHXOAJB-UHFFFAOYSA-N ethyl 7-chlorocinnoline-3-carboxylate Chemical compound C1=C(Cl)C=C2N=NC(C(=O)OCC)=CC2=C1 PHDNOFTVHXOAJB-UHFFFAOYSA-N 0.000 description 4
- PQVSTLUFSYVLTO-UHFFFAOYSA-N ethyl n-ethoxycarbonylcarbamate Chemical compound CCOC(=O)NC(=O)OCC PQVSTLUFSYVLTO-UHFFFAOYSA-N 0.000 description 4
- 239000011737 fluorine Substances 0.000 description 4
- 125000003709 fluoroalkyl group Chemical group 0.000 description 4
- 125000002541 furyl group Chemical group 0.000 description 4
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 4
- 229910052737 gold Inorganic materials 0.000 description 4
- 239000010931 gold Substances 0.000 description 4
- 208000006454 hepatitis Diseases 0.000 description 4
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 4
- 239000005457 ice water Substances 0.000 description 4
- 125000002883 imidazolyl group Chemical group 0.000 description 4
- 125000003392 indanyl group Chemical group C1(CCC2=CC=CC=C12)* 0.000 description 4
- 208000002551 irritable bowel syndrome Diseases 0.000 description 4
- 210000003734 kidney Anatomy 0.000 description 4
- GLXDVVHUTZTUQK-UHFFFAOYSA-M lithium hydroxide monohydrate Substances [Li+].O.[OH-] GLXDVVHUTZTUQK-UHFFFAOYSA-M 0.000 description 4
- 229940040692 lithium hydroxide monohydrate Drugs 0.000 description 4
- 238000004949 mass spectrometry Methods 0.000 description 4
- YKUCHDXIBAQWSF-UHFFFAOYSA-N methyl 3-hydroxybenzoate Chemical compound COC(=O)C1=CC=CC(O)=C1 YKUCHDXIBAQWSF-UHFFFAOYSA-N 0.000 description 4
- RMFMMYKCHSPFSV-UHFFFAOYSA-N methyl 6-bromo-4-(difluoromethoxy)quinoline-2-carboxylate Chemical compound BrC=1C=C2C(=CC(=NC2=CC=1)C(=O)OC)OC(F)F RMFMMYKCHSPFSV-UHFFFAOYSA-N 0.000 description 4
- 239000002808 molecular sieve Substances 0.000 description 4
- 125000002757 morpholinyl group Chemical group 0.000 description 4
- 150000002825 nitriles Chemical class 0.000 description 4
- 125000002971 oxazolyl group Chemical group 0.000 description 4
- KJIFKLIQANRMOU-UHFFFAOYSA-N oxidanium;4-methylbenzenesulfonate Chemical compound O.CC1=CC=C(S(O)(=O)=O)C=C1 KJIFKLIQANRMOU-UHFFFAOYSA-N 0.000 description 4
- 239000001301 oxygen Substances 0.000 description 4
- 125000003386 piperidinyl group Chemical group 0.000 description 4
- 239000004033 plastic Substances 0.000 description 4
- 229920003023 plastic Polymers 0.000 description 4
- 229910052700 potassium Inorganic materials 0.000 description 4
- 239000011591 potassium Substances 0.000 description 4
- 230000008569 process Effects 0.000 description 4
- 238000004007 reversed phase HPLC Methods 0.000 description 4
- 230000002441 reversible effect Effects 0.000 description 4
- 229910052708 sodium Inorganic materials 0.000 description 4
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 4
- 235000010288 sodium nitrite Nutrition 0.000 description 4
- 125000004434 sulfur atom Chemical group 0.000 description 4
- 238000004808 supercritical fluid chromatography Methods 0.000 description 4
- 238000013268 sustained release Methods 0.000 description 4
- 239000012730 sustained-release form Substances 0.000 description 4
- 238000010189 synthetic method Methods 0.000 description 4
- IOGXOCVLYRDXLW-UHFFFAOYSA-N tert-butyl nitrite Chemical compound CC(C)(C)ON=O IOGXOCVLYRDXLW-UHFFFAOYSA-N 0.000 description 4
- 239000012414 tert-butyl nitrite Substances 0.000 description 4
- 125000003831 tetrazolyl group Chemical group 0.000 description 4
- 125000000335 thiazolyl group Chemical group 0.000 description 4
- 238000004809 thin layer chromatography Methods 0.000 description 4
- 125000004306 triazinyl group Chemical group 0.000 description 4
- QAEDZJGFFMLHHQ-UHFFFAOYSA-N trifluoroacetic anhydride Chemical compound FC(F)(F)C(=O)OC(=O)C(F)(F)F QAEDZJGFFMLHHQ-UHFFFAOYSA-N 0.000 description 4
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 4
- CXNIUSPIQKWYAI-UHFFFAOYSA-N xantphos Chemical compound C=12OC3=C(P(C=4C=CC=CC=4)C=4C=CC=CC=4)C=CC=C3C(C)(C)C2=CC=CC=1P(C=1C=CC=CC=1)C1=CC=CC=C1 CXNIUSPIQKWYAI-UHFFFAOYSA-N 0.000 description 4
- 229910052725 zinc Inorganic materials 0.000 description 4
- 239000011701 zinc Substances 0.000 description 4
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 description 3
- WTMHKFNOVQHTAJ-UHFFFAOYSA-N 1-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]ethane-1,2-diol Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C(CO)O WTMHKFNOVQHTAJ-UHFFFAOYSA-N 0.000 description 3
- LIISZMRTGKWIFN-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-1,3-dioxa-8-azaspiro[4.5]decan-8-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1OC2(CO1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F LIISZMRTGKWIFN-UHFFFAOYSA-N 0.000 description 3
- LUPWLIXDLUZHQX-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-2-hydroxyspiro[3.5]nonan-7-yl]oxy-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1(CC2(C1)CCC(CC2)OC=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F)O LUPWLIXDLUZHQX-UHFFFAOYSA-N 0.000 description 3
- PKZVONDTIGQAGS-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoxaline-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC2=CC=C(C=C2N=C1)C(=O)O PKZVONDTIGQAGS-UHFFFAOYSA-N 0.000 description 3
- BVCHNJAOSWWXCL-UHFFFAOYSA-N 3,5-dichloro-N-hydroxypyridine-4-carboximidoyl chloride Chemical compound ON=C(Cl)C1=C(Cl)C=NC=C1Cl BVCHNJAOSWWXCL-UHFFFAOYSA-N 0.000 description 3
- GTILZJWOOZGFHW-UHFFFAOYSA-N 4-(7-azaspiro[3.5]non-2-en-2-yl)-5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazole Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCNCC2 GTILZJWOOZGFHW-UHFFFAOYSA-N 0.000 description 3
- YFCIFWOJYYFDQP-PTWZRHHISA-N 4-[3-amino-6-[(1S,3S,4S)-3-fluoro-4-hydroxycyclohexyl]pyrazin-2-yl]-N-[(1S)-1-(3-bromo-5-fluorophenyl)-2-(methylamino)ethyl]-2-fluorobenzamide Chemical compound CNC[C@@H](NC(=O)c1ccc(cc1F)-c1nc(cnc1N)[C@H]1CC[C@H](O)[C@@H](F)C1)c1cc(F)cc(Br)c1 YFCIFWOJYYFDQP-PTWZRHHISA-N 0.000 description 3
- XXHKQNFPSVYHBJ-UHFFFAOYSA-N 5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazole Chemical compound C1(CC1)C1=CC(=NO1)C1=C(C=CC=C1Cl)Cl XXHKQNFPSVYHBJ-UHFFFAOYSA-N 0.000 description 3
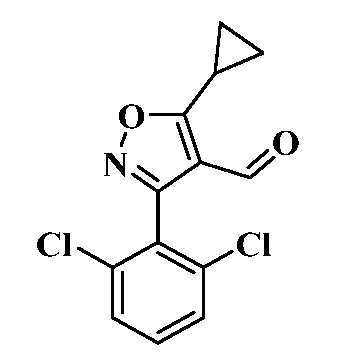
- WVULOKZMQJKUIQ-UHFFFAOYSA-N 5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazole-4-carbaldehyde Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C=O WVULOKZMQJKUIQ-UHFFFAOYSA-N 0.000 description 3
- MOBQAZDFHBZTTN-UHFFFAOYSA-N 5-cyclopropyl-3-(2,6-dichlorophenyl)-4-ethenyl-1,2-oxazole Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C=C MOBQAZDFHBZTTN-UHFFFAOYSA-N 0.000 description 3
- HGMBUIIXCULYSX-UHFFFAOYSA-N 5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazole Chemical compound C1(CC1)C1=CC(=NO1)C1=C(C=NC=C1Cl)Cl HGMBUIIXCULYSX-UHFFFAOYSA-N 0.000 description 3
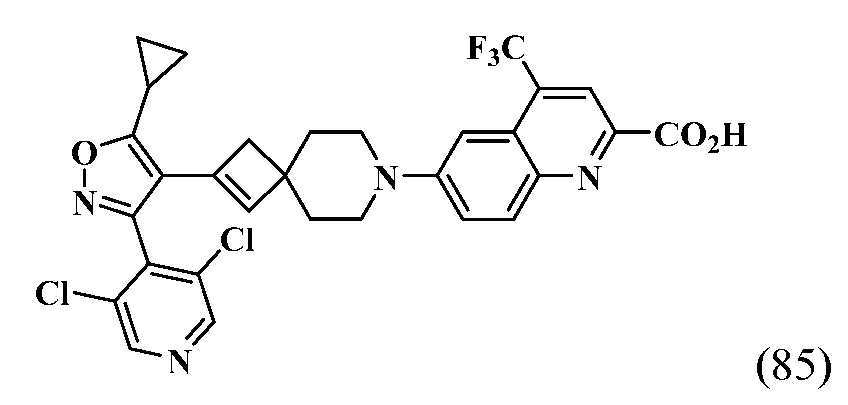
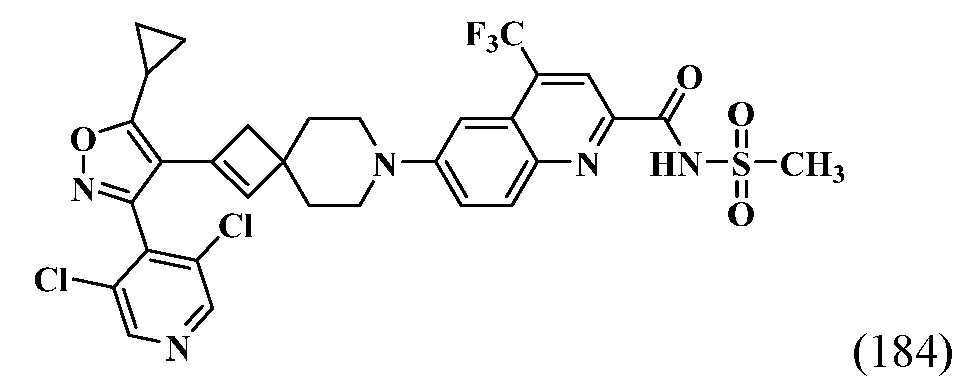
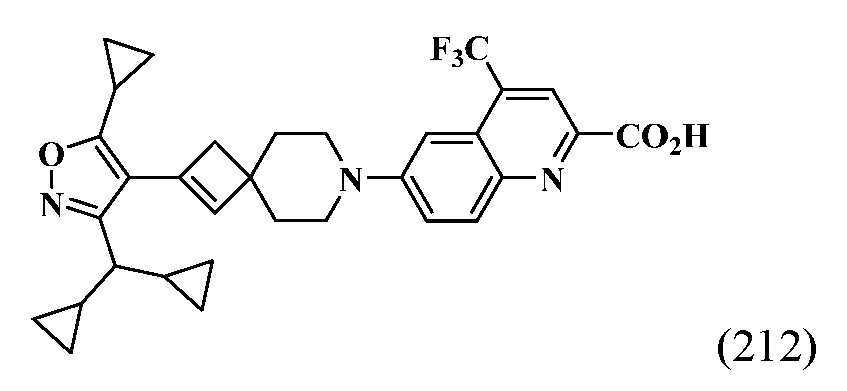
- WPGAVSDZYIRUGE-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F WPGAVSDZYIRUGE-UHFFFAOYSA-N 0.000 description 3
- CCYCOMKSZGNPTO-UHFFFAOYSA-N 7-[tert-butyl(dimethyl)silyl]oxyspiro[3.5]nonan-2-one Chemical compound [Si](C)(C)(C(C)(C)C)OC1CCC2(CC(C2)=O)CC1 CCYCOMKSZGNPTO-UHFFFAOYSA-N 0.000 description 3
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 3
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 3
- 239000004475 Arginine Substances 0.000 description 3
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 3
- 238000006443 Buchwald-Hartwig cross coupling reaction Methods 0.000 description 3
- 208000032928 Dyslipidaemia Diseases 0.000 description 3
- 206010061218 Inflammation Diseases 0.000 description 3
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 3
- 208000017170 Lipid metabolism disease Diseases 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Malonic acid Chemical compound OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
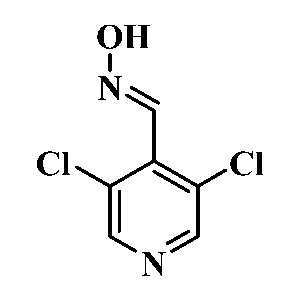
- GURQDWMTFXFSLW-UHFFFAOYSA-N N-[(3,5-dichloropyridin-4-yl)methylidene]hydroxylamine Chemical compound ON=CC1=C(Cl)C=NC=C1Cl GURQDWMTFXFSLW-UHFFFAOYSA-N 0.000 description 3
- 102000007399 Nuclear hormone receptor Human genes 0.000 description 3
- 108020005497 Nuclear hormone receptor Proteins 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 206010035226 Plasma cell myeloma Diseases 0.000 description 3
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical group [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 3
- 238000006069 Suzuki reaction reaction Methods 0.000 description 3
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 3
- KRGFOUGVZFEEBW-UHFFFAOYSA-N [5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]methanol Chemical compound OCC1=C(C2CC2)ON=C1C1=C(Cl)C=CC=C1Cl KRGFOUGVZFEEBW-UHFFFAOYSA-N 0.000 description 3
- 150000007513 acids Chemical class 0.000 description 3
- 150000001299 aldehydes Chemical class 0.000 description 3
- 150000001345 alkine derivatives Chemical group 0.000 description 3
- 125000003368 amide group Chemical group 0.000 description 3
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 3
- 125000005110 aryl thio group Chemical group 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 3
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 3
- 230000033228 biological regulation Effects 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 description 3
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 3
- 239000002775 capsule Substances 0.000 description 3
- 150000007942 carboxylates Chemical class 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 238000007796 conventional method Methods 0.000 description 3
- 229910052802 copper Inorganic materials 0.000 description 3
- NLUNLVTVUDIHFE-UHFFFAOYSA-N cyclooctylcyclooctane Chemical compound C1CCCCCCC1C1CCCCCCC1 NLUNLVTVUDIHFE-UHFFFAOYSA-N 0.000 description 3
- 230000008034 disappearance Effects 0.000 description 3
- AWAJIVUCZYNHEH-UHFFFAOYSA-N ethyl 1-oxido-7-(trifluoromethyl)quinolin-1-ium-5-carboxylate Chemical compound C(C)OC(=O)C1=C2C=CC=[N+](C2=CC(=C1)C(F)(F)F)[O-] AWAJIVUCZYNHEH-UHFFFAOYSA-N 0.000 description 3
- KDZJRTRPRYLILE-UHFFFAOYSA-N ethyl 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)triazol-4-yl]-2-hydroxy-7-azaspiro[3.5]nonan-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylate Chemical compound C1(CC1)C=1N=NN(C=1C1(CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)OCC)F)O)C1=C(C=CC=C1Cl)Cl KDZJRTRPRYLILE-UHFFFAOYSA-N 0.000 description 3
- FIONIWABJPVJSO-UHFFFAOYSA-N ethyl 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylate Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)OCC)C(F)(F)F FIONIWABJPVJSO-UHFFFAOYSA-N 0.000 description 3
- KKPHOPJTCKGVDH-UHFFFAOYSA-N ethyl 6-bromo-3-(trifluoromethyl)imidazo[1,5-a]pyridine-1-carboxylate Chemical compound BrC=1C=CC=2N(C=1)C(=NC=2C(=O)OCC)C(F)(F)F KKPHOPJTCKGVDH-UHFFFAOYSA-N 0.000 description 3
- GGQJJDYISGXYCU-UHFFFAOYSA-N ethyl 7-(trifluoromethyl)quinoline-5-carboxylate Chemical compound FC(C=1C=C(C=2C=CC=NC=2C=1)C(=O)OCC)(F)F GGQJJDYISGXYCU-UHFFFAOYSA-N 0.000 description 3
- 125000004428 fluoroalkoxy group Chemical group 0.000 description 3
- 210000001035 gastrointestinal tract Anatomy 0.000 description 3
- 229930195733 hydrocarbon Natural products 0.000 description 3
- 125000002632 imidazolidinyl group Chemical group 0.000 description 3
- 230000004054 inflammatory process Effects 0.000 description 3
- 229910052740 iodine Inorganic materials 0.000 description 3
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 3
- 150000002545 isoxazoles Chemical class 0.000 description 3
- 208000017169 kidney disease Diseases 0.000 description 3
- 208000032839 leukemia Diseases 0.000 description 3
- 229910052751 metal Inorganic materials 0.000 description 3
- 239000002184 metal Substances 0.000 description 3
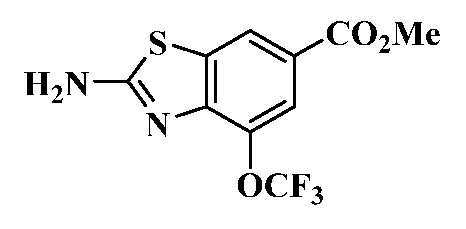
- NOGRCFNAGABAAM-UHFFFAOYSA-N methyl 2-amino-6-methoxy-1,3-benzothiazole-4-carboxylate Chemical compound COC(=O)c1cc(OC)cc2sc(N)nc12 NOGRCFNAGABAAM-UHFFFAOYSA-N 0.000 description 3
- BOIWWTOADPGDKC-UHFFFAOYSA-N methyl 2-bromo-1,3-benzoxazole-5-carboxylate Chemical compound COC(=O)C1=CC=C2OC(Br)=NC2=C1 BOIWWTOADPGDKC-UHFFFAOYSA-N 0.000 description 3
- VPTDWPQJGPAIEO-UHFFFAOYSA-N methyl 6-bromo-4-(2-hydroxyethoxy)quinoline-2-carboxylate Chemical compound BrC=1C=C2C(=CC(=NC2=CC=1)C(=O)OC)OCCO VPTDWPQJGPAIEO-UHFFFAOYSA-N 0.000 description 3
- NJJQNTABCJHZBM-UHFFFAOYSA-N methyl 6-bromo-4-methoxyquinoline-2-carboxylate Chemical compound C1=C(Br)C=CC2=NC(C(=O)OC)=CC(OC)=C21 NJJQNTABCJHZBM-UHFFFAOYSA-N 0.000 description 3
- NMRCOWOPRPIBPQ-UHFFFAOYSA-N methyl 6-fluoropyridine-2-carboxylate Chemical compound COC(=O)C1=CC=CC(F)=N1 NMRCOWOPRPIBPQ-UHFFFAOYSA-N 0.000 description 3
- BYPWKAWWQMTHKE-UHFFFAOYSA-N methyl 8-methoxyquinoline-5-carboxylate Chemical compound C1=CC=C2C(C(=O)OC)=CC=C(OC)C2=N1 BYPWKAWWQMTHKE-UHFFFAOYSA-N 0.000 description 3
- YBSXDWIAUZOFFV-UHFFFAOYSA-N n-[(2,6-dichlorophenyl)methylidene]hydroxylamine Chemical compound ON=CC1=C(Cl)C=CC=C1Cl YBSXDWIAUZOFFV-UHFFFAOYSA-N 0.000 description 3
- 125000001624 naphthyl group Chemical group 0.000 description 3
- PXHVJJICTQNCMI-UHFFFAOYSA-N nickel Substances [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 3
- 238000007339 nucleophilic aromatic substitution reaction Methods 0.000 description 3
- 125000001715 oxadiazolyl group Chemical group 0.000 description 3
- 125000000160 oxazolidinyl group Chemical group 0.000 description 3
- 239000000123 paper Substances 0.000 description 3
- XHXFXVLFKHQFAL-UHFFFAOYSA-N phosphoryl trichloride Chemical compound ClP(Cl)(Cl)=O XHXFXVLFKHQFAL-UHFFFAOYSA-N 0.000 description 3
- 125000004193 piperazinyl group Chemical group 0.000 description 3
- 229920000642 polymer Polymers 0.000 description 3
- 229910000027 potassium carbonate Inorganic materials 0.000 description 3
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 3
- LOAUVZALPPNFOQ-UHFFFAOYSA-M quinaldate Chemical compound C1=CC=CC2=NC(C(=O)[O-])=CC=C21 LOAUVZALPPNFOQ-UHFFFAOYSA-M 0.000 description 3
- IVYZWJPQNNZOHV-UHFFFAOYSA-N quinoxaline-2-carbonitrile Chemical compound C1=CC=CC2=NC(C#N)=CN=C21 IVYZWJPQNNZOHV-UHFFFAOYSA-N 0.000 description 3
- 230000037390 scarring Effects 0.000 description 3
- 239000011877 solvent mixture Substances 0.000 description 3
- 241000894007 species Species 0.000 description 3
- 125000003003 spiro group Chemical group 0.000 description 3
- 238000000967 suction filtration Methods 0.000 description 3
- 239000011593 sulfur Substances 0.000 description 3
- WTYPJRMUPPUMJU-UHFFFAOYSA-N tert-butyl 2-[5-cyclopropyl-3-(2,6-dichlorophenyl)triazol-4-yl]-2-hydroxy-7-azaspiro[3.5]nonane-7-carboxylate Chemical compound C1(CC1)C=1N=NN(C=1C1(CC2(C1)CCN(CC2)C(=O)OC(C)(C)C)O)C1=C(C=CC=C1Cl)Cl WTYPJRMUPPUMJU-UHFFFAOYSA-N 0.000 description 3
- PVVIBQJEDGJHKH-UHFFFAOYSA-N tert-butyl 2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-2-hydroxy-7-azaspiro[3.5]nonane-7-carboxylate Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1(CC2(C1)CCN(CC2)C(=O)OC(C)(C)C)O PVVIBQJEDGJHKH-UHFFFAOYSA-N 0.000 description 3
- PXGDSDBBBJTNAE-UHFFFAOYSA-N tert-butyl 3'-oxospiro[8-azabicyclo[3.2.1]octane-3,1'-cyclobutane]-8-carboxylate Chemical compound O=C1CC2(C1)CC1CCC(C2)N1C(=O)OC(C)(C)C PXGDSDBBBJTNAE-UHFFFAOYSA-N 0.000 description 3
- BKZFMSPPZXDTJL-UHFFFAOYSA-N tert-butyl 4-hydroxy-4-(hydroxymethyl)piperidine-1-carboxylate Chemical compound CC(C)(C)OC(=O)N1CCC(O)(CO)CC1 BKZFMSPPZXDTJL-UHFFFAOYSA-N 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- 125000003718 tetrahydrofuranyl group Chemical group 0.000 description 3
- CXWXQJXEFPUFDZ-UHFFFAOYSA-N tetralin Chemical compound C1=CC=C2CCCCC2=C1 CXWXQJXEFPUFDZ-UHFFFAOYSA-N 0.000 description 3
- 230000001225 therapeutic effect Effects 0.000 description 3
- 230000009466 transformation Effects 0.000 description 3
- 125000001425 triazolyl group Chemical group 0.000 description 3
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 2
- 125000004514 1,2,4-thiadiazolyl group Chemical group 0.000 description 2
- DMPZJACLHDWUFS-UHFFFAOYSA-N 1,3-benzothiazole-6-carboxylic acid Chemical compound OC(=O)C1=CC=C2N=CSC2=C1 DMPZJACLHDWUFS-UHFFFAOYSA-N 0.000 description 2
- DDITYYPIADDMFF-UHFFFAOYSA-N 1-benzothiophen-3-amine;hydrochloride Chemical compound Cl.C1=CC=C2C(N)=CSC2=C1 DDITYYPIADDMFF-UHFFFAOYSA-N 0.000 description 2
- 125000005955 1H-indazolyl group Chemical group 0.000 description 2
- OZEZBKUHAGFQME-UHFFFAOYSA-N 2-(4-ethoxyphenyl)-2-methylpropan-1-ol Chemical compound CCOC1=CC=C(C(C)(C)CO)C=C1 OZEZBKUHAGFQME-UHFFFAOYSA-N 0.000 description 2
- ZZWWXIBKLBMSCS-FQEVSTJZSA-N 2-[1-[(2r)-2-(2-methoxyphenyl)-2-(oxan-4-yloxy)ethyl]-5-methyl-6-(1,3-oxazol-2-yl)-2,4-dioxothieno[2,3-d]pyrimidin-3-yl]-2-methylpropanoic acid Chemical compound COC1=CC=CC=C1[C@@H](OC1CCOCC1)CN1C(=O)N(C(C)(C)C(O)=O)C(=O)C2=C1SC(C=1OC=CN=1)=C2C ZZWWXIBKLBMSCS-FQEVSTJZSA-N 0.000 description 2
- ZOUZHZUQFXBCFZ-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1,3-benzoxazole-5-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1OC2=C(N=1)C=C(C=C2)C(=O)O ZOUZHZUQFXBCFZ-UHFFFAOYSA-N 0.000 description 2
- GRXIUVFREHQJNT-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-[1,3]thiazolo[4,5-b]pyridine-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC=2C(=NC=C(C=2)C(=O)O)N=1 GRXIUVFREHQJNT-UHFFFAOYSA-N 0.000 description 2
- TXSMUNYTYONBAF-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]pyrrolo[2,1-f][1,2,4]triazine-5-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NN2C(C=N1)=C(C=C2)C(=O)O TXSMUNYTYONBAF-UHFFFAOYSA-N 0.000 description 2
- KYWLJQVWQCNDKU-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]spiro[3.5]non-2-en-7-yl]oxy-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCC(CC2)OC=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F KYWLJQVWQCNDKU-UHFFFAOYSA-N 0.000 description 2
- IQJYMTOLMAUPLN-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)triazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C=1N=NN(C=1C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F)C1=C(C=CC=C1Cl)Cl IQJYMTOLMAUPLN-UHFFFAOYSA-N 0.000 description 2
- OKQCZNGBKUMOQU-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethoxy)-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)OC(F)(F)F OKQCZNGBKUMOQU-UHFFFAOYSA-N 0.000 description 2
- AWMVITFYNBJOTG-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F AWMVITFYNBJOTG-UHFFFAOYSA-N 0.000 description 2
- JIBVIIUUPKEJRZ-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-5-methoxy-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C=C(C(=C2)C(=O)O)OC JIBVIIUUPKEJRZ-UHFFFAOYSA-N 0.000 description 2
- AVSAGQFUILFWFR-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-6-methoxy-1,3-benzothiazole-4-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC=2C(N=1)=C(C=C(C=2)OC)C(=O)O AVSAGQFUILFWFR-UHFFFAOYSA-N 0.000 description 2
- XKVTUDWQLKQMDX-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-[1,3]thiazolo[5,4-b]pyridine-5-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=NC(=CC=C2N=1)C(=O)O XKVTUDWQLKQMDX-UHFFFAOYSA-N 0.000 description 2
- HSDPPMZJZQVODQ-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]nonan-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F HSDPPMZJZQVODQ-UHFFFAOYSA-N 0.000 description 2
- YAQKEYXGXVYKFQ-UHFFFAOYSA-N 2-[3-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-1,4-dioxa-8-azaspiro[4.5]decan-8-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1OC2(OC1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F YAQKEYXGXVYKFQ-UHFFFAOYSA-N 0.000 description 2
- DUAHEGBEXYZBER-UHFFFAOYSA-N 2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-1,3-dioxa-8-azaspiro[4.5]decane Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1OC2(CO1)CCNCC2 DUAHEGBEXYZBER-UHFFFAOYSA-N 0.000 description 2
- PFCBHXKWQVABKT-UHFFFAOYSA-N 2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-2-hydroxyspiro[3.5]nonan-7-one Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1(CC2(C1)CCC(CC2)=O)O PFCBHXKWQVABKT-UHFFFAOYSA-N 0.000 description 2
- HVFJVRRQMWMZAP-UHFFFAOYSA-N 2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]spiro[3.5]non-2-en-7-ol Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCC(CC2)O HVFJVRRQMWMZAP-UHFFFAOYSA-N 0.000 description 2
- BGGGBJXUNUESFD-UHFFFAOYSA-N 2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]spiro[3.5]non-2-en-7-one Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCC(CC2)=O BGGGBJXUNUESFD-UHFFFAOYSA-N 0.000 description 2
- BYRWOSJFHWKXET-UHFFFAOYSA-N 2-azido-1,3-dichlorobenzene Chemical compound ClC1=CC=CC(Cl)=C1N=[N+]=[N-] BYRWOSJFHWKXET-UHFFFAOYSA-N 0.000 description 2
- LDLCZOVUSADOIV-UHFFFAOYSA-N 2-bromoethanol Chemical compound OCCBr LDLCZOVUSADOIV-UHFFFAOYSA-N 0.000 description 2
- RLAOKDGTZKSUJB-UHFFFAOYSA-N 3,5-difluoropyridine-4-carbaldehyde Chemical compound FC1=CN=CC(F)=C1C=O RLAOKDGTZKSUJB-UHFFFAOYSA-N 0.000 description 2
- XQRBBNBJCFYTDX-UHFFFAOYSA-N 3-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-2-hydroxyspiro[3.5]nonan-7-yl]oxybenzoic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1(CC2(C1)CCC(CC2)OC=1C=C(C(=O)O)C=CC=1)O XQRBBNBJCFYTDX-UHFFFAOYSA-N 0.000 description 2
- WNEODWDFDXWOLU-QHCPKHFHSA-N 3-[3-(hydroxymethyl)-4-[1-methyl-5-[[5-[(2s)-2-methyl-4-(oxetan-3-yl)piperazin-1-yl]pyridin-2-yl]amino]-6-oxopyridin-3-yl]pyridin-2-yl]-7,7-dimethyl-1,2,6,8-tetrahydrocyclopenta[3,4]pyrrolo[3,5-b]pyrazin-4-one Chemical compound C([C@@H](N(CC1)C=2C=NC(NC=3C(N(C)C=C(C=3)C=3C(=C(N4C(C5=CC=6CC(C)(C)CC=6N5CC4)=O)N=CC=3)CO)=O)=CC=2)C)N1C1COC1 WNEODWDFDXWOLU-QHCPKHFHSA-N 0.000 description 2
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 2
- LTDQVLLWTFGAKG-UHFFFAOYSA-N 4-[7-(5-chloro-[1,3]thiazolo[5,4-b]pyridin-2-yl)-7-azaspiro[3.5]non-2-en-2-yl]-5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazole Chemical compound ClC1=CC=C2C(=N1)SC(=N2)N1CCC2(CC(=C2)C=2C(=NOC=2C2CC2)C2=C(C=NC=C2Cl)Cl)CC1 LTDQVLLWTFGAKG-UHFFFAOYSA-N 0.000 description 2
- BVXZODICWAICGR-UHFFFAOYSA-N 4-[7-(6-bromo-[1,3]thiazolo[4,5-b]pyridin-2-yl)-7-azaspiro[3.5]non-2-en-2-yl]-5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazole Chemical compound BrC=1C=C2C(=NC=1)N=C(S2)N1CCC2(CC(=C2)C=2C(=NOC=2C2CC2)C2=C(C=CC=C2Cl)Cl)CC1 BVXZODICWAICGR-UHFFFAOYSA-N 0.000 description 2
- KVCQTKNUUQOELD-UHFFFAOYSA-N 4-amino-n-[1-(3-chloro-2-fluoroanilino)-6-methylisoquinolin-5-yl]thieno[3,2-d]pyrimidine-7-carboxamide Chemical compound N=1C=CC2=C(NC(=O)C=3C4=NC=NC(N)=C4SC=3)C(C)=CC=C2C=1NC1=CC=CC(Cl)=C1F KVCQTKNUUQOELD-UHFFFAOYSA-N 0.000 description 2
- ZRSOFPIYYNLSDC-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-(2-trimethylsilylethoxymethyl)indole-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=CC=C2C(=CN(C2=C1)COCC[Si](C)(C)C)C(=O)O ZRSOFPIYYNLSDC-UHFFFAOYSA-N 0.000 description 2
- DMEXKGDWMCFTLU-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylpyrrolo[2,3-b]pyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=CC=C2C(=N1)N(C=C2C(=O)O)C DMEXKGDWMCFTLU-UHFFFAOYSA-N 0.000 description 2
- ZXNZTGRBXJYLGG-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-3-(trifluoromethyl)imidazo[1,5-a]pyridine-1-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=CC=2N(C=1)C(=NC=2C(=O)O)C(F)(F)F ZXNZTGRBXJYLGG-UHFFFAOYSA-N 0.000 description 2
- VRWKDDVSCHBDGE-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-3-methylimidazo[1,5-a]pyridine-1-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=CC=2N(C=1)C(=NC=2C(=O)O)C VRWKDDVSCHBDGE-UHFFFAOYSA-N 0.000 description 2
- SMXCWZQTGSMHFQ-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(2-hydroxyethoxy)quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OCCO SMXCWZQTGSMHFQ-UHFFFAOYSA-N 0.000 description 2
- FOKYWJFRYPLJJP-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethoxy)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylindazole-3-carbonitrile Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)OC(F)(F)F)C1=CC2(C1)CCN(CC2)C1=CC=C2C(=NN(C2=C1)C)C#N FOKYWJFRYPLJJP-UHFFFAOYSA-N 0.000 description 2
- SDPRBFSOTHXFGV-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethoxy)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylindazole-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)OC(F)(F)F)C1=CC2(C1)CCN(CC2)C1=CC=C2C(=NN(C2=C1)C)C(=O)O SDPRBFSOTHXFGV-UHFFFAOYSA-N 0.000 description 2
- SLFHKAYGYSSRIL-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(difluoromethoxy)quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC(F)F SLFHKAYGYSSRIL-UHFFFAOYSA-N 0.000 description 2
- KDHDWEZUYPKULD-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]pyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C1=NC=C(C(=O)O)C=C1 KDHDWEZUYPKULD-UHFFFAOYSA-N 0.000 description 2
- WKFMTQUWGVGIDH-UHFFFAOYSA-N 7-[tert-butyl(dimethyl)silyl]oxy-2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]spiro[3.5]nonan-2-ol Chemical compound [Si](C)(C)(C(C)(C)C)OC1CCC2(CC(C2)(O)C=2C(=NOC=2C2CC2)C2=C(C=CC=C2Cl)Cl)CC1 WKFMTQUWGVGIDH-UHFFFAOYSA-N 0.000 description 2
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 2
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 2
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 2
- 241000894006 Bacteria Species 0.000 description 2
- 102100031151 C-C chemokine receptor type 2 Human genes 0.000 description 2
- 101710149815 C-C chemokine receptor type 2 Proteins 0.000 description 2
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 description 2
- KXDHJXZQYSOELW-UHFFFAOYSA-M Carbamate Chemical compound NC([O-])=O KXDHJXZQYSOELW-UHFFFAOYSA-M 0.000 description 2
- 201000009030 Carcinoma Diseases 0.000 description 2
- 206010008609 Cholangitis sclerosing Diseases 0.000 description 2
- 206010008635 Cholestasis Diseases 0.000 description 2
- 206010008909 Chronic Hepatitis Diseases 0.000 description 2
- 206010009944 Colon cancer Diseases 0.000 description 2
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 2
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 2
- QUSNBJAOOMFDIB-UHFFFAOYSA-N Ethylamine Chemical compound CCN QUSNBJAOOMFDIB-UHFFFAOYSA-N 0.000 description 2
- GISRWBROCYNDME-PELMWDNLSA-N F[C@H]1[C@H]([C@H](NC1=O)COC1=NC=CC2=CC(=C(C=C12)OC)C(=O)N)C Chemical compound F[C@H]1[C@H]([C@H](NC1=O)COC1=NC=CC2=CC(=C(C=C12)OC)C(=O)N)C GISRWBROCYNDME-PELMWDNLSA-N 0.000 description 2
- 108050007372 Fibroblast Growth Factor Proteins 0.000 description 2
- 102000018233 Fibroblast Growth Factor Human genes 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- 208000010412 Glaucoma Diseases 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- 206010019708 Hepatic steatosis Diseases 0.000 description 2
- 241000282412 Homo Species 0.000 description 2
- MHAJPDPJQMAIIY-UHFFFAOYSA-N Hydrogen peroxide Chemical compound OO MHAJPDPJQMAIIY-UHFFFAOYSA-N 0.000 description 2
- 206010022489 Insulin Resistance Diseases 0.000 description 2
- 102000004388 Interleukin-4 Human genes 0.000 description 2
- 108090000978 Interleukin-4 Proteins 0.000 description 2
- 208000029523 Interstitial Lung disease Diseases 0.000 description 2
- 108010055717 JNK Mitogen-Activated Protein Kinases Proteins 0.000 description 2
- 208000007766 Kaposi sarcoma Diseases 0.000 description 2
- 206010023421 Kidney fibrosis Diseases 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- 102100027159 Membrane primary amine oxidase Human genes 0.000 description 2
- 101710132836 Membrane primary amine oxidase Proteins 0.000 description 2
- 206010027406 Mesothelioma Diseases 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical group CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- 102100033127 Mitogen-activated protein kinase kinase kinase 5 Human genes 0.000 description 2
- 101710164337 Mitogen-activated protein kinase kinase kinase 5 Proteins 0.000 description 2
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 2
- 241000699670 Mus sp. Species 0.000 description 2
- RRVJPDRJBYQHCF-UHFFFAOYSA-N N#CC1=CN=C2N=CSC2=C1 Chemical compound N#CC1=CN=C2N=CSC2=C1 RRVJPDRJBYQHCF-UHFFFAOYSA-N 0.000 description 2
- 150000001204 N-oxides Chemical class 0.000 description 2
- 238000012565 NMR experiment Methods 0.000 description 2
- 208000008589 Obesity Diseases 0.000 description 2
- 101150003085 Pdcl gene Proteins 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 108010038512 Platelet-Derived Growth Factor Proteins 0.000 description 2
- 102000010780 Platelet-Derived Growth Factor Human genes 0.000 description 2
- 208000002158 Proliferative Vitreoretinopathy Diseases 0.000 description 2
- 206010060862 Prostate cancer Diseases 0.000 description 2
- 208000000236 Prostatic Neoplasms Diseases 0.000 description 2
- SMWDFEZZVXVKRB-UHFFFAOYSA-N Quinoline Chemical compound N1=CC=CC2=CC=CC=C21 SMWDFEZZVXVKRB-UHFFFAOYSA-N 0.000 description 2
- 102000034527 Retinoid X Receptors Human genes 0.000 description 2
- 108010038912 Retinoid X Receptors Proteins 0.000 description 2
- 206010038934 Retinopathy proliferative Diseases 0.000 description 2
- 241000283984 Rodentia Species 0.000 description 2
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- 201000009594 Systemic Scleroderma Diseases 0.000 description 2
- 206010042953 Systemic sclerosis Diseases 0.000 description 2
- KKEYFWRCBNTPAC-UHFFFAOYSA-N Terephthalic acid Chemical compound OC(=O)C1=CC=C(C(O)=O)C=C1 KKEYFWRCBNTPAC-UHFFFAOYSA-N 0.000 description 2
- 102000011016 Type 5 Cyclic Nucleotide Phosphodiesterases Human genes 0.000 description 2
- 108010037581 Type 5 Cyclic Nucleotide Phosphodiesterases Proteins 0.000 description 2
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 description 2
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 description 2
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 description 2
- LXRZVMYMQHNYJB-UNXOBOICSA-N [(1R,2S,4R)-4-[[5-[4-[(1R)-7-chloro-1,2,3,4-tetrahydroisoquinolin-1-yl]-5-methylthiophene-2-carbonyl]pyrimidin-4-yl]amino]-2-hydroxycyclopentyl]methyl sulfamate Chemical compound CC1=C(C=C(S1)C(=O)C1=C(N[C@H]2C[C@H](O)[C@@H](COS(N)(=O)=O)C2)N=CN=C1)[C@@H]1NCCC2=C1C=C(Cl)C=C2 LXRZVMYMQHNYJB-UNXOBOICSA-N 0.000 description 2
- 230000002159 abnormal effect Effects 0.000 description 2
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 2
- 150000001241 acetals Chemical class 0.000 description 2
- CSCPPACGZOOCGX-WFGJKAKNSA-N acetone d6 Chemical compound [2H]C([2H])([2H])C(=O)C([2H])([2H])[2H] CSCPPACGZOOCGX-WFGJKAKNSA-N 0.000 description 2
- 230000004913 activation Effects 0.000 description 2
- 231100000354 acute hepatitis Toxicity 0.000 description 2
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 2
- 239000000853 adhesive Substances 0.000 description 2
- 230000001070 adhesive effect Effects 0.000 description 2
- OQIQSTLJSLGHID-WNWIJWBNSA-N aflatoxin B1 Chemical compound C=1([C@@H]2C=CO[C@@H]2OC=1C=C(C1=2)OC)C=2OC(=O)C2=C1CCC2=O OQIQSTLJSLGHID-WNWIJWBNSA-N 0.000 description 2
- 206010064930 age-related macular degeneration Diseases 0.000 description 2
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 2
- 125000004390 alkyl sulfonyl group Chemical group 0.000 description 2
- 238000005576 amination reaction Methods 0.000 description 2
- 125000003277 amino group Chemical group 0.000 description 2
- 235000019270 ammonium chloride Nutrition 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000005557 antagonist Substances 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 150000004945 aromatic hydrocarbons Chemical class 0.000 description 2
- 125000004658 aryl carbonyl amino group Chemical group 0.000 description 2
- 125000005129 aryl carbonyl group Chemical group 0.000 description 2
- 150000001502 aryl halides Chemical class 0.000 description 2
- 125000005135 aryl sulfinyl group Chemical group 0.000 description 2
- 239000012298 atmosphere Substances 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 125000002393 azetidinyl group Chemical group 0.000 description 2
- 125000004604 benzisothiazolyl group Chemical group S1N=C(C2=C1C=CC=C2)* 0.000 description 2
- 125000004603 benzisoxazolyl group Chemical group O1N=C(C2=C1C=CC=C2)* 0.000 description 2
- 125000000499 benzofuranyl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 2
- 125000004196 benzothienyl group Chemical group S1C(=CC2=C1C=CC=C2)* 0.000 description 2
- 125000005512 benztetrazolyl group Chemical group 0.000 description 2
- 238000006795 borylation reaction Methods 0.000 description 2
- 229940045348 brown mixture Drugs 0.000 description 2
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 125000000609 carbazolyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3NC12)* 0.000 description 2
- 125000001589 carboacyl group Chemical group 0.000 description 2
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 2
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical compound OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 2
- 239000011111 cardboard Substances 0.000 description 2
- 210000004027 cell Anatomy 0.000 description 2
- 210000003679 cervix uteri Anatomy 0.000 description 2
- 231100000359 cholestasis Toxicity 0.000 description 2
- 230000007870 cholestasis Effects 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 125000003016 chromanyl group Chemical group O1C(CCC2=CC=CC=C12)* 0.000 description 2
- 238000004587 chromatography analysis Methods 0.000 description 2
- BLFJCJKTSCOLEY-UHFFFAOYSA-N cinnoline-3-carboxylic acid Chemical compound C1=CC=C2N=NC(C(=O)O)=CC2=C1 BLFJCJKTSCOLEY-UHFFFAOYSA-N 0.000 description 2
- 230000007882 cirrhosis Effects 0.000 description 2
- 210000001072 colon Anatomy 0.000 description 2
- 239000012230 colorless oil Substances 0.000 description 2
- 239000013066 combination product Substances 0.000 description 2
- 229940127555 combination product Drugs 0.000 description 2
- 238000009833 condensation Methods 0.000 description 2
- 230000005494 condensation Effects 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 239000007819 coupling partner Substances 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 239000013078 crystal Substances 0.000 description 2
- 125000000392 cycloalkenyl group Chemical group 0.000 description 2
- 125000001162 cycloheptenyl group Chemical group C1(=CCCCCC1)* 0.000 description 2
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 125000000640 cyclooctyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])C1([H])[H] 0.000 description 2
- NNBZCPXTIHJBJL-UHFFFAOYSA-N decalin Chemical compound C1CCCC2CCCCC21 NNBZCPXTIHJBJL-UHFFFAOYSA-N 0.000 description 2
- 238000013461 design Methods 0.000 description 2
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 2
- ARNYROQVENUCIA-UHFFFAOYSA-N ethyl 2-(5-bromopyridin-2-yl)-2-hydroxyiminoacetate Chemical compound BrC=1C=CC(=NC=1)C(C(=O)OCC)=NO ARNYROQVENUCIA-UHFFFAOYSA-N 0.000 description 2
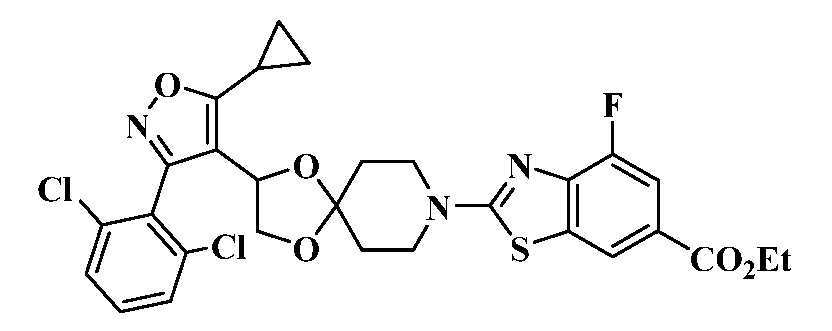
- DFVZFWXHEQYHMW-UHFFFAOYSA-N ethyl 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-1,3-dioxa-8-azaspiro[4.5]decan-8-yl]-4-fluoro-1,3-benzothiazole-6-carboxylate Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1OC2(CO1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)OCC)F DFVZFWXHEQYHMW-UHFFFAOYSA-N 0.000 description 2
- CDMUBPXLXPQQOO-UHFFFAOYSA-N ethyl 2-bromo-5-methoxy-1,3-benzothiazole-6-carboxylate Chemical compound BrC=1SC2=C(N=1)C=C(C(=C2)C(=O)OCC)OC CDMUBPXLXPQQOO-UHFFFAOYSA-N 0.000 description 2
- XYILGOWGHVVTLY-UHFFFAOYSA-N ethyl 2-chloro-7-(trifluoromethyl)quinoline-5-carboxylate Chemical compound ClC1=NC=2C=C(C=C(C=2C=C1)C(=O)OCC)C(F)(F)F XYILGOWGHVVTLY-UHFFFAOYSA-N 0.000 description 2
- RQDFJQFFIITXEV-UHFFFAOYSA-N ethyl 2-chloropyrrolo[2,1-f][1,2,4]triazine-5-carboxylate Chemical compound ClC1=NN2C(C=N1)=C(C=C2)C(=O)OCC RQDFJQFFIITXEV-UHFFFAOYSA-N 0.000 description 2
- KKOWWOLSWGIACP-UHFFFAOYSA-N ethyl 4-fluoro-2-(4-oxopiperidin-1-yl)-1,3-benzothiazole-6-carboxylate Chemical compound FC1=CC(=CC2=C1N=C(S2)N1CCC(CC1)=O)C(=O)OCC KKOWWOLSWGIACP-UHFFFAOYSA-N 0.000 description 2
- FOXNLKXTOCXVPV-UHFFFAOYSA-N ethyl 5-amino-1-[2-(trifluoromethyl)phenyl]pyrazole-4-carboxylate Chemical compound NC1=C(C(=O)OCC)C=NN1C1=CC=CC=C1C(F)(F)F FOXNLKXTOCXVPV-UHFFFAOYSA-N 0.000 description 2
- SPQPXOPWSWGTLK-UHFFFAOYSA-N ethyl 5-bromo-1-[2-(trifluoromethyl)phenyl]pyrazole-4-carboxylate Chemical compound BrC1=C(C=NN1C1=C(C=CC=C1)C(F)(F)F)C(=O)OCC SPQPXOPWSWGTLK-UHFFFAOYSA-N 0.000 description 2
- NUVBSKCKDOMJSU-UHFFFAOYSA-N ethylparaben Chemical compound CCOC(=O)C1=CC=C(O)C=C1 NUVBSKCKDOMJSU-UHFFFAOYSA-N 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 229940126864 fibroblast growth factor Drugs 0.000 description 2
- 206010016629 fibroma Diseases 0.000 description 2
- 210000000232 gallbladder Anatomy 0.000 description 2
- 210000002216 heart Anatomy 0.000 description 2
- 238000004896 high resolution mass spectrometry Methods 0.000 description 2
- 230000013632 homeostatic process Effects 0.000 description 2
- 238000005984 hydrogenation reaction Methods 0.000 description 2
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 2
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 2
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 2
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 2
- 125000003387 indolinyl group Chemical group N1(CCC2=CC=CC=C12)* 0.000 description 2
- 238000001802 infusion Methods 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 239000007972 injectable composition Substances 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 229940028885 interleukin-4 Drugs 0.000 description 2
- 230000000968 intestinal effect Effects 0.000 description 2
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 2
- 238000002955 isolation Methods 0.000 description 2
- 125000001786 isothiazolyl group Chemical group 0.000 description 2
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 2
- 229910052744 lithium Inorganic materials 0.000 description 2
- 208000019423 liver disease Diseases 0.000 description 2
- 208000002780 macular degeneration Diseases 0.000 description 2
- 159000000003 magnesium salts Chemical class 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- 239000002609 medium Substances 0.000 description 2
- JMQPOLIPYXKPMU-UHFFFAOYSA-N methyl 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-2-hydroxyspiro[3.5]nonan-7-yl]oxy-4-fluoro-1,3-benzothiazole-6-carboxylate Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1(CC2(C1)CCC(CC2)OC=1SC2=C(N=1)C(=CC(=C2)C(=O)OC)F)O JMQPOLIPYXKPMU-UHFFFAOYSA-N 0.000 description 2
- KNMMDKTVKFJHMH-UHFFFAOYSA-N methyl 2-amino-4-(trifluoromethoxy)-1,3-benzothiazole-6-carboxylate Chemical compound COC(=O)C1=CC(OC(F)(F)F)=C2N=C(N)SC2=C1 KNMMDKTVKFJHMH-UHFFFAOYSA-N 0.000 description 2
- SGWVZBCLQAXEJM-UHFFFAOYSA-N methyl 2-bromo-4-fluoro-1,3-benzothiazole-6-carboxylate Chemical compound COC(=O)C1=CC(F)=C2N=C(Br)SC2=C1 SGWVZBCLQAXEJM-UHFFFAOYSA-N 0.000 description 2
- YVEDWWBAPREOBF-UHFFFAOYSA-N methyl 2-bromo-4-methoxy-1,3-benzothiazole-6-carboxylate Chemical compound COC(=O)C1=CC(OC)=C2N=C(Br)SC2=C1 YVEDWWBAPREOBF-UHFFFAOYSA-N 0.000 description 2
- BHSNYMWZEPLVSR-UHFFFAOYSA-N methyl 2-chloro-8-methoxyquinoline-5-carboxylate Chemical compound ClC1=NC=2C(=CC=C(C=2C=C1)C(=O)OC)OC BHSNYMWZEPLVSR-UHFFFAOYSA-N 0.000 description 2
- 229940120152 methyl 3-hydroxybenzoate Drugs 0.000 description 2
- VOZICRAZVBGCNM-UHFFFAOYSA-N methyl 4-amino-3-(trifluoromethoxy)benzoate Chemical compound COC(=O)C1=CC=C(N)C(OC(F)(F)F)=C1 VOZICRAZVBGCNM-UHFFFAOYSA-N 0.000 description 2
- IPBRHVDRTRBACF-UHFFFAOYSA-N methyl 5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazole-4-carboxylate Chemical compound COC(=O)C1=C(C2CC2)ON=C1C1=C(Cl)C=CC=C1Cl IPBRHVDRTRBACF-UHFFFAOYSA-N 0.000 description 2
- VWWFDWFVYGOGOK-UHFFFAOYSA-N methyl 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]spiro[3.5]non-2-en-7-yl]oxyquinoline-2-carboxylate Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCC(CC2)OC=1C=C2C=CC(=NC2=CC=1)C(=O)OC VWWFDWFVYGOGOK-UHFFFAOYSA-N 0.000 description 2
- WQTOJVQWGGIHKI-UHFFFAOYSA-N methyl 6-bromo-1-(2-trimethylsilylethoxymethyl)indole-3-carboxylate Chemical compound BrC1=CC=C2C(=CN(C2=C1)COCC[Si](C)(C)C)C(=O)OC WQTOJVQWGGIHKI-UHFFFAOYSA-N 0.000 description 2
- SKZJYJMYLUQJPG-UHFFFAOYSA-N methyl 6-bromo-1h-indole-3-carboxylate Chemical compound BrC1=CC=C2C(C(=O)OC)=CNC2=C1 SKZJYJMYLUQJPG-UHFFFAOYSA-N 0.000 description 2
- ANUOLSUYNCMOIQ-UHFFFAOYSA-N methyl 6-bromo-4-ethoxyquinoline-2-carboxylate Chemical compound CCOc1cc(nc2ccc(Br)cc12)C(=O)OC ANUOLSUYNCMOIQ-UHFFFAOYSA-N 0.000 description 2
- DUKAAWDFGPMTJT-UHFFFAOYSA-N methyl 6-bromo-4-oxo-1h-quinoline-2-carboxylate Chemical compound BrC1=CC=C2NC(C(=O)OC)=CC(=O)C2=C1 DUKAAWDFGPMTJT-UHFFFAOYSA-N 0.000 description 2
- KDMTVIVGDHCOAH-UHFFFAOYSA-N methyl 6-chloro-5-fluoropyridine-3-carboxylate Chemical compound COC(=O)C1=CN=C(Cl)C(F)=C1 KDMTVIVGDHCOAH-UHFFFAOYSA-N 0.000 description 2
- FPKXYXKLOWAIOX-UHFFFAOYSA-N methyl 6-chloropyridazine-3-carboxylate Chemical compound COC(=O)C1=CC=C(Cl)N=N1 FPKXYXKLOWAIOX-UHFFFAOYSA-N 0.000 description 2
- CKYVMSOADNWBFX-UHFFFAOYSA-N methyl 8-methoxy-1-oxidoquinolin-1-ium-5-carboxylate Chemical compound COC=1C=CC(=C2C=CC=[N+](C=12)[O-])C(=O)OC CKYVMSOADNWBFX-UHFFFAOYSA-N 0.000 description 2
- LSEFCHWGJNHZNT-UHFFFAOYSA-M methyl(triphenyl)phosphanium;bromide Chemical compound [Br-].C=1C=CC=CC=1[P+](C=1C=CC=CC=1)(C)C1=CC=CC=C1 LSEFCHWGJNHZNT-UHFFFAOYSA-M 0.000 description 2
- 201000000050 myeloid neoplasm Diseases 0.000 description 2
- OQJBFFCUFALWQL-UHFFFAOYSA-N n-(piperidine-1-carbonylimino)piperidine-1-carboxamide Chemical compound C1CCCCN1C(=O)N=NC(=O)N1CCCCC1 OQJBFFCUFALWQL-UHFFFAOYSA-N 0.000 description 2
- 210000002850 nasal mucosa Anatomy 0.000 description 2
- 208000021971 neovascular inflammatory vitreoretinopathy Diseases 0.000 description 2
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 2
- 201000004071 non-specific interstitial pneumonia Diseases 0.000 description 2
- 235000020824 obesity Nutrition 0.000 description 2
- 125000004930 octahydroisoquinolinyl group Chemical group C1(NCCC2CCCC=C12)* 0.000 description 2
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 2
- 210000001672 ovary Anatomy 0.000 description 2
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 2
- 239000000546 pharmaceutical excipient Substances 0.000 description 2
- XNGIFLGASWRNHJ-UHFFFAOYSA-N phthalic acid Chemical compound OC(=O)C1=CC=CC=C1C(O)=O XNGIFLGASWRNHJ-UHFFFAOYSA-N 0.000 description 2
- SIOXPEMLGUPBBT-UHFFFAOYSA-N picolinic acid Chemical compound OC(=O)C1=CC=CC=N1 SIOXPEMLGUPBBT-UHFFFAOYSA-N 0.000 description 2
- HYAFETHFCAUJAY-UHFFFAOYSA-N pioglitazone Chemical compound N1=CC(CC)=CC=C1CCOC(C=C1)=CC=C1CC1C(=O)NC(=O)S1 HYAFETHFCAUJAY-UHFFFAOYSA-N 0.000 description 2
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 2
- 229910000160 potassium phosphate Inorganic materials 0.000 description 2
- 235000011009 potassium phosphates Nutrition 0.000 description 2
- 201000000742 primary sclerosing cholangitis Diseases 0.000 description 2
- 230000006785 proliferative vitreoretinopathy Effects 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 102000004169 proteins and genes Human genes 0.000 description 2
- 125000000561 purinyl group Chemical group N1=C(N=C2N=CNC2=C1)* 0.000 description 2
- LEHBURLTIWGHEM-UHFFFAOYSA-N pyridinium chlorochromate Chemical compound [O-][Cr](Cl)(=O)=O.C1=CC=[NH+]C=C1 LEHBURLTIWGHEM-UHFFFAOYSA-N 0.000 description 2
- 125000006513 pyridinyl methyl group Chemical group 0.000 description 2
- 125000002294 quinazolinyl group Chemical group N1=C(N=CC2=CC=CC=C12)* 0.000 description 2
- IFIJAECRUMYOAH-UHFFFAOYSA-N quinoxaline-6-carbonitrile Chemical compound N1=CC=NC2=CC(C#N)=CC=C21 IFIJAECRUMYOAH-UHFFFAOYSA-N 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 238000010992 reflux Methods 0.000 description 2
- 230000000717 retained effect Effects 0.000 description 2
- 238000007363 ring formation reaction Methods 0.000 description 2
- 125000006413 ring segment Chemical group 0.000 description 2
- PEGQOIGYZLJMIB-UHFFFAOYSA-N setogepram Chemical compound CCCCCC1=CC=CC(CC(O)=O)=C1 PEGQOIGYZLJMIB-UHFFFAOYSA-N 0.000 description 2
- BNRNXUUZRGQAQC-UHFFFAOYSA-N sildenafil Chemical compound CCCC1=NN(C)C(C(N2)=O)=C1N=C2C(C(=CC=1)OCC)=CC=1S(=O)(=O)N1CCN(C)CC1 BNRNXUUZRGQAQC-UHFFFAOYSA-N 0.000 description 2
- 229910052709 silver Inorganic materials 0.000 description 2
- 239000004332 silver Substances 0.000 description 2
- 210000003491 skin Anatomy 0.000 description 2
- 210000000813 small intestine Anatomy 0.000 description 2
- 239000001632 sodium acetate Substances 0.000 description 2
- 235000017281 sodium acetate Nutrition 0.000 description 2
- 238000004611 spectroscopical analysis Methods 0.000 description 2
- 210000002784 stomach Anatomy 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 2
- 229940124530 sulfonamide Drugs 0.000 description 2
- 150000003456 sulfonamides Chemical class 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 239000006188 syrup Substances 0.000 description 2
- 235000020357 syrup Nutrition 0.000 description 2
- MKHIHFPXOGUAJT-UHFFFAOYSA-N tert-butyl 2-(7-bromoquinoxalin-2-yl)oxyacetate Chemical compound BrC1=CC=C2N=CC(=NC2=C1)OCC(=O)OC(C)(C)C MKHIHFPXOGUAJT-UHFFFAOYSA-N 0.000 description 2
- LOIXEKPLULXYIL-UHFFFAOYSA-N tert-butyl 2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-1,3-dioxa-8-azaspiro[4.5]decane-8-carboxylate Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1OC2(CO1)CCN(CC2)C(=O)OC(C)(C)C LOIXEKPLULXYIL-UHFFFAOYSA-N 0.000 description 2
- QAZRAEOOPUIXGM-UHFFFAOYSA-N tert-butyl 2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-2-hydroxy-7-azaspiro[3.5]nonane-7-carboxylate Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1(CC2(C1)CCN(CC2)C(=O)OC(C)(C)C)O QAZRAEOOPUIXGM-UHFFFAOYSA-N 0.000 description 2
- 150000003509 tertiary alcohols Chemical class 0.000 description 2
- FPGGTKZVZWFYPV-UHFFFAOYSA-M tetrabutylammonium fluoride Chemical compound [F-].CCCC[N+](CCCC)(CCCC)CCCC FPGGTKZVZWFYPV-UHFFFAOYSA-M 0.000 description 2
- 125000003039 tetrahydroisoquinolinyl group Chemical group C1(NCCC2=CC=CC=C12)* 0.000 description 2
- 125000001712 tetrahydronaphthyl group Chemical group C1(CCCC2=CC=CC=C12)* 0.000 description 2
- 125000000147 tetrahydroquinolinyl group Chemical group N1(CCCC2=CC=CC=C12)* 0.000 description 2
- 125000004525 thiadiazinyl group Chemical group S1NN=C(C=C1)* 0.000 description 2
- 125000001113 thiadiazolyl group Chemical group 0.000 description 2
- ZMZDMBWJUHKJPS-UHFFFAOYSA-N thiocyanic acid Chemical compound SC#N ZMZDMBWJUHKJPS-UHFFFAOYSA-N 0.000 description 2
- 150000003573 thiols Chemical class 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- 238000000844 transformation Methods 0.000 description 2
- 238000002054 transplantation Methods 0.000 description 2
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 2
- GTLDTDOJJJZVBW-UHFFFAOYSA-N zinc cyanide Chemical compound [Zn+2].N#[C-].N#[C-] GTLDTDOJJJZVBW-UHFFFAOYSA-N 0.000 description 2
- VCGRFBXVSFAGGA-UHFFFAOYSA-N (1,1-dioxo-1,4-thiazinan-4-yl)-[6-[[3-(4-fluorophenyl)-5-methyl-1,2-oxazol-4-yl]methoxy]pyridin-3-yl]methanone Chemical compound CC=1ON=C(C=2C=CC(F)=CC=2)C=1COC(N=C1)=CC=C1C(=O)N1CCS(=O)(=O)CC1 VCGRFBXVSFAGGA-UHFFFAOYSA-N 0.000 description 1
- IDTWYHVEGJBGPT-UHFFFAOYSA-N (2,6-dichlorophenyl)hydrazine Chemical compound NNC1=C(Cl)C=CC=C1Cl IDTWYHVEGJBGPT-UHFFFAOYSA-N 0.000 description 1
- OUPXSLGGCPUZJJ-SARDKLJWSA-N (2s)-2-[[(2s)-1-[(2s)-6-amino-2-[[(2s)-1-[(2s)-2-amino-5-(diaminomethylideneamino)pentanoyl]pyrrolidine-2-carbonyl]amino]hexanoyl]pyrrolidine-2-carbonyl]amino]-n-[(2s)-5-amino-1-[[(2s)-1-[[(2s)-1-[[2-[[(2s)-1-[[(2s)-1-amino-4-methylsulfonyl-1-oxobutan-2-y Chemical compound C([C@@H](C(=O)N(C)CC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCS(C)(=O)=O)C(N)=O)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCCCN)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](N)CCCN=C(N)N)C1=CC=CC=C1 OUPXSLGGCPUZJJ-SARDKLJWSA-N 0.000 description 1
- AEMPUAWUDAMJBV-QFIPXVFZSA-N (2s)-4-(4-methylphenyl)-5-(2h-tetrazol-5-yl)-2-[4-(4,4,4-trifluorobutoxy)phenyl]-2-(trifluoromethyl)-1,3-dihydropyridin-6-one Chemical compound C1=CC(C)=CC=C1C(C[C@](NC1=O)(C=2C=CC(OCCCC(F)(F)F)=CC=2)C(F)(F)F)=C1C1=NN=NN1 AEMPUAWUDAMJBV-QFIPXVFZSA-N 0.000 description 1
- LDQKDRLEMKIYMC-XMMPIXPASA-N (3R)-1'-(9-anthrylcarbonyl)-3-(morpholin-4-ylcarbonyl)-1,4'-bipiperidine Chemical compound O=C([C@H]1CN(CCC1)C1CCN(CC1)C(=O)C=1C2=CC=CC=C2C=C2C=CC=CC2=1)N1CCOCC1 LDQKDRLEMKIYMC-XMMPIXPASA-N 0.000 description 1
- MAYZWDRUFKUGGP-VIFPVBQESA-N (3s)-1-[5-tert-butyl-3-[(1-methyltetrazol-5-yl)methyl]triazolo[4,5-d]pyrimidin-7-yl]pyrrolidin-3-ol Chemical compound CN1N=NN=C1CN1C2=NC(C(C)(C)C)=NC(N3C[C@@H](O)CC3)=C2N=N1 MAYZWDRUFKUGGP-VIFPVBQESA-N 0.000 description 1
- SHKXZIQNFMOPBS-OOMQYRRCSA-N (4r)-4-[(3s,5s,7r,8r,9s,10s,12s,13r,14s,17r)-7,12-dihydroxy-3-(icosanoylamino)-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-17-yl]pentanoic acid Chemical compound O[C@H]1C[C@@H]2[C@@]3(C)CC[C@H](NC(=O)CCCCCCCCCCCCCCCCCCC)C[C@H]3C[C@@H](O)[C@H]2[C@@H]2CC[C@H]([C@H](C)CCC(O)=O)[C@]21C SHKXZIQNFMOPBS-OOMQYRRCSA-N 0.000 description 1
- YCHYFHOSGQABSW-RTBURBONSA-N (6ar,10ar)-1-hydroxy-6,6-dimethyl-3-(2-methyloctan-2-yl)-6a,7,10,10a-tetrahydrobenzo[c]chromene-9-carboxylic acid Chemical compound C1C(C(O)=O)=CC[C@H]2C(C)(C)OC3=CC(C(C)(C)CCCCCC)=CC(O)=C3[C@@H]21 YCHYFHOSGQABSW-RTBURBONSA-N 0.000 description 1
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 description 1
- 125000006832 (C1-C10) alkylene group Chemical group 0.000 description 1
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 1
- 125000003161 (C1-C6) alkylene group Chemical group 0.000 description 1
- 125000004737 (C1-C6) haloalkoxy group Chemical group 0.000 description 1
- 125000006716 (C1-C6) heteroalkyl group Chemical group 0.000 description 1
- 125000006645 (C3-C4) cycloalkyl group Chemical group 0.000 description 1
- 125000006272 (C3-C7) cycloalkyl group Chemical group 0.000 description 1
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- ZGYIXVSQHOKQRZ-COIATFDQSA-N (e)-n-[4-[3-chloro-4-(pyridin-2-ylmethoxy)anilino]-3-cyano-7-[(3s)-oxolan-3-yl]oxyquinolin-6-yl]-4-(dimethylamino)but-2-enamide Chemical compound N#CC1=CN=C2C=C(O[C@@H]3COCC3)C(NC(=O)/C=C/CN(C)C)=CC2=C1NC(C=C1Cl)=CC=C1OCC1=CC=CC=N1 ZGYIXVSQHOKQRZ-COIATFDQSA-N 0.000 description 1
- MOWXJLUYGFNTAL-DEOSSOPVSA-N (s)-[2-chloro-4-fluoro-5-(7-morpholin-4-ylquinazolin-4-yl)phenyl]-(6-methoxypyridazin-3-yl)methanol Chemical compound N1=NC(OC)=CC=C1[C@@H](O)C1=CC(C=2C3=CC=C(C=C3N=CN=2)N2CCOCC2)=C(F)C=C1Cl MOWXJLUYGFNTAL-DEOSSOPVSA-N 0.000 description 1
- FIARMZDBEGVMLV-UHFFFAOYSA-N 1,1,2,2,2-pentafluoroethanolate Chemical group [O-]C(F)(F)C(F)(F)F FIARMZDBEGVMLV-UHFFFAOYSA-N 0.000 description 1
- 125000004605 1,2,3,4-tetrahydroisoquinolinyl group Chemical group C1(NCCC2=CC=CC=C12)* 0.000 description 1
- 125000004607 1,2,3,4-tetrahydroquinolinyl group Chemical group N1(CCCC2=CC=CC=C12)* 0.000 description 1
- 125000004502 1,2,3-oxadiazolyl group Chemical group 0.000 description 1
- 125000004511 1,2,3-thiadiazolyl group Chemical group 0.000 description 1
- 125000001399 1,2,3-triazolyl group Chemical group N1N=NC(=C1)* 0.000 description 1
- 125000004504 1,2,4-oxadiazolyl group Chemical group 0.000 description 1
- 125000001376 1,2,4-triazolyl group Chemical group N1N=C(N=C1)* 0.000 description 1
- 125000004506 1,2,5-oxadiazolyl group Chemical group 0.000 description 1
- 125000004517 1,2,5-thiadiazolyl group Chemical group 0.000 description 1
- LYPXTDXYEQEIIN-UHFFFAOYSA-N 1,2-oxazole-4-carboxylic acid Chemical compound OC(=O)C=1C=NOC=1 LYPXTDXYEQEIIN-UHFFFAOYSA-N 0.000 description 1
- 125000001781 1,3,4-oxadiazolyl group Chemical group 0.000 description 1
- 125000004520 1,3,4-thiadiazolyl group Chemical group 0.000 description 1
- IQFCJGFQUZORLM-UHFFFAOYSA-N 1,3-benzothiazole-6-carboxamide Chemical compound NC(=O)C1=CC=C2N=CSC2=C1 IQFCJGFQUZORLM-UHFFFAOYSA-N 0.000 description 1
- LVEYOSJUKRVCCF-UHFFFAOYSA-N 1,3-bis(diphenylphosphino)propane Chemical compound C=1C=CC=CC=1P(C=1C=CC=CC=1)CCCP(C=1C=CC=CC=1)C1=CC=CC=C1 LVEYOSJUKRVCCF-UHFFFAOYSA-N 0.000 description 1
- APWRZPQBPCAXFP-UHFFFAOYSA-N 1-(1-oxo-2H-isoquinolin-5-yl)-5-(trifluoromethyl)-N-[2-(trifluoromethyl)pyridin-4-yl]pyrazole-4-carboxamide Chemical compound O=C1NC=CC2=C(C=CC=C12)N1N=CC(=C1C(F)(F)F)C(=O)NC1=CC(=NC=C1)C(F)(F)F APWRZPQBPCAXFP-UHFFFAOYSA-N 0.000 description 1
- NDMFETHQFUOIQX-UHFFFAOYSA-N 1-(3-chloropropyl)imidazolidin-2-one Chemical compound ClCCCN1CCNC1=O NDMFETHQFUOIQX-UHFFFAOYSA-N 0.000 description 1
- GQBRZBHEPUQRPL-LJQANCHMSA-N 1-[4-[4-[3-methyl-4-[[(1r)-1-phenylethoxy]carbonylamino]-1,2-oxazol-5-yl]phenyl]phenyl]cyclopropane-1-carboxylic acid Chemical compound O([C@H](C)C=1C=CC=CC=1)C(=O)NC=1C(C)=NOC=1C(C=C1)=CC=C1C(C=C1)=CC=C1C1(C(O)=O)CC1 GQBRZBHEPUQRPL-LJQANCHMSA-N 0.000 description 1
- DLXBUAFBLMXVMT-UHFFFAOYSA-N 1-ethynyl-1-methylcyclopropane Chemical compound C#CC1(C)CC1 DLXBUAFBLMXVMT-UHFFFAOYSA-N 0.000 description 1
- 125000006432 1-methyl cyclopropyl group Chemical group [H]C([H])([H])C1(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 1
- 125000006017 1-propenyl group Chemical group 0.000 description 1
- QWENRTYMTSOGBR-UHFFFAOYSA-N 1H-1,2,3-Triazole Chemical compound C=1C=NNN=1 QWENRTYMTSOGBR-UHFFFAOYSA-N 0.000 description 1
- 125000004206 2,2,2-trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 1
- VJDWLGLJZNWMFB-UHFFFAOYSA-N 2,2-dicyclopropylacetaldehyde Chemical compound C1CC1C(C=O)C1CC1 VJDWLGLJZNWMFB-UHFFFAOYSA-N 0.000 description 1
- ZFFMLCVRJBZUDZ-UHFFFAOYSA-N 2,3-dimethylbutane Chemical group CC(C)C(C)C ZFFMLCVRJBZUDZ-UHFFFAOYSA-N 0.000 description 1
- SYOANZBNGDEJFH-UHFFFAOYSA-N 2,5-dihydro-1h-triazole Chemical compound C1NNN=C1 SYOANZBNGDEJFH-UHFFFAOYSA-N 0.000 description 1
- JDMFXJULNGEPOI-UHFFFAOYSA-N 2,6-dichloroaniline Chemical compound NC1=C(Cl)C=CC=C1Cl JDMFXJULNGEPOI-UHFFFAOYSA-N 0.000 description 1
- BPXKZEMBEZGUAH-UHFFFAOYSA-N 2-(chloromethoxy)ethyl-trimethylsilane Chemical compound C[Si](C)(C)CCOCCl BPXKZEMBEZGUAH-UHFFFAOYSA-N 0.000 description 1
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 1
- OPKSRSICFGPFJR-NNCDRQEWSA-N 2-[(1'R,5'S)-2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]spiro[1,3-dioxolane-4,3'-8-azabicyclo[3.2.1]octane]-8'-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1OCC2(O1)C[C@H]1CC[C@@H](C2)N1C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F OPKSRSICFGPFJR-NNCDRQEWSA-N 0.000 description 1
- UWRCWLXYNLAUAI-UHFFFAOYSA-N 2-[2-[3-(2,6-dichlorophenyl)-5-propan-2-yl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound ClC1=C(C(=CC=C1)Cl)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F)C(C)C UWRCWLXYNLAUAI-UHFFFAOYSA-N 0.000 description 1
- LYVPDXCHQNZONE-UHFFFAOYSA-N 2-[2-[3-(2-chloro-6-fluorophenyl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound ClC1=C(C(=CC=C1)F)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F)C1CC1 LYVPDXCHQNZONE-UHFFFAOYSA-N 0.000 description 1
- QEPOHZWOLPXQMZ-UHFFFAOYSA-N 2-[2-[3-(2-chloro-6-methylphenyl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound ClC1=C(C(=CC=C1)C)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F)C1CC1 QEPOHZWOLPXQMZ-UHFFFAOYSA-N 0.000 description 1
- OLQSHPAFFXHZHZ-UHFFFAOYSA-N 2-[2-[3-(3,5-dichloropyridin-4-yl)-5-propan-2-yl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound ClC=1C=NC=C(C=1C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F)C(C)C)Cl OLQSHPAFFXHZHZ-UHFFFAOYSA-N 0.000 description 1
- WWRFHHWIFULLSF-UHFFFAOYSA-N 2-[2-[3-(3-chloropyridin-2-yl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound ClC=1C(=NC=CC=1)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F)C1CC1 WWRFHHWIFULLSF-UHFFFAOYSA-N 0.000 description 1
- MYZPXNREXDHGIQ-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichloro-4-fluorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=C(C=C1Cl)F)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F MYZPXNREXDHGIQ-UHFFFAOYSA-N 0.000 description 1
- TTWBXUXKEORCTA-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-2-hydroxy-7-azaspiro[3.5]nonan-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1(CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F)O TTWBXUXKEORCTA-UHFFFAOYSA-N 0.000 description 1
- ZIWDUYVXURUKBR-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C=CC(=C2)C(=O)O ZIWDUYVXURUKBR-UHFFFAOYSA-N 0.000 description 1
- SHIZQXZRYCJGMX-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1,3-benzoxazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1OC2=C(N=1)C=CC(=C2)C(=O)O SHIZQXZRYCJGMX-UHFFFAOYSA-N 0.000 description 1
- BSLDHPKNJLYGFT-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylbenzimidazole-5-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC2=C(N1C)C=CC(=C2)C(=O)O BSLDHPKNJLYGFT-UHFFFAOYSA-N 0.000 description 1
- GNJZLGXRZOTUGE-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)pyrimidine-5-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC=C(C(=N1)C(F)(F)F)C(=O)O GNJZLGXRZOTUGE-UHFFFAOYSA-N 0.000 description 1
- ZZJAJFNADZSURZ-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methyl-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)C ZZJAJFNADZSURZ-UHFFFAOYSA-N 0.000 description 1
- ZYJBEGYNUPPPFA-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-6-methylpyrimidine-4-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC(=CC(=N1)C(=O)O)C ZYJBEGYNUPPPFA-UHFFFAOYSA-N 0.000 description 1
- KDWAQUZOLNXTKG-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-7-methylpyrrolo[2,3-d]pyrimidine-5-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1N=CC2=C(N=1)N(C=C2C(=O)O)C KDWAQUZOLNXTKG-UHFFFAOYSA-N 0.000 description 1
- RRGATMQOHYKZSX-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-N-cyclopropylsulfonyl-4-fluoro-1,3-benzothiazole-6-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)NS(=O)(=O)C1CC1)F RRGATMQOHYKZSX-UHFFFAOYSA-N 0.000 description 1
- PPJRJSPHYHVKNR-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-[1,3]thiazolo[4,5-b]pyridine-6-carbonitrile Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC=2C(=NC=C(C=2)C#N)N=1 PPJRJSPHYHVKNR-UHFFFAOYSA-N 0.000 description 1
- RBBJHCYUAQPSCM-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]pyrimidine-5-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC=C(C=N1)C(=O)O RBBJHCYUAQPSCM-UHFFFAOYSA-N 0.000 description 1
- BGAPLXQQSROBRZ-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoline-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC2=CC=C(C=C2C=C1)C(=O)O BGAPLXQQSROBRZ-UHFFFAOYSA-N 0.000 description 1
- SRVWJMQQFOTYMZ-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]nonan-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F SRVWJMQQFOTYMZ-UHFFFAOYSA-N 0.000 description 1
- DWEUKVKIBLPATL-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(2,6-difluorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1F)F)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F DWEUKVKIBLPATL-UHFFFAOYSA-N 0.000 description 1
- XKMCMGOHWRBXSK-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C=CC(=C2)C(=O)O XKMCMGOHWRBXSK-UHFFFAOYSA-N 0.000 description 1
- OKGCUSLQEZKNIG-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)N)F OKGCUSLQEZKNIG-UHFFFAOYSA-N 0.000 description 1
- JTPWRAMENPUBLY-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-N-methyl-1,3-benzothiazole-6-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)NC)F JTPWRAMENPUBLY-UHFFFAOYSA-N 0.000 description 1
- BBGOFXSSFTUWHZ-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-N-methylsulfonyl-1,3-benzothiazole-6-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)NS(=O)(=O)C)F BBGOFXSSFTUWHZ-UHFFFAOYSA-N 0.000 description 1
- WJZIUTAYTYKRHK-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-N-propan-2-yl-1,3-benzothiazole-6-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)NC(C)C)F WJZIUTAYTYKRHK-UHFFFAOYSA-N 0.000 description 1
- VSSRJYHXEFICFJ-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-N-sulfamoyl-1,3-benzothiazole-6-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)NS(N)(=O)=O)F VSSRJYHXEFICFJ-UHFFFAOYSA-N 0.000 description 1
- RLYHIMDAXHMJPE-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methoxy-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)OC RLYHIMDAXHMJPE-UHFFFAOYSA-N 0.000 description 1
- HZFPOWLMPFSUOB-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methyl-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)C HZFPOWLMPFSUOB-UHFFFAOYSA-N 0.000 description 1
- JEHUKZVMXJYQAA-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-7-(trifluoromethyl)quinoline-5-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC=2C=C(C=C(C=2C=C1)C(=O)O)C(F)(F)F JEHUKZVMXJYQAA-UHFFFAOYSA-N 0.000 description 1
- AXZGMIBDRYHJGG-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-8-methoxyquinoline-5-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC=2C(=CC=C(C=2C=C1)C(=O)O)OC AXZGMIBDRYHJGG-UHFFFAOYSA-N 0.000 description 1
- OLUCEJHCIDASIR-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-N-cyclopropylsulfonyl-4-fluoro-1,3-benzothiazole-6-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)NS(=O)(=O)C1CC1)F OLUCEJHCIDASIR-UHFFFAOYSA-N 0.000 description 1
- UUSDSGBPWJJVMZ-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-N-ethyl-4-fluoro-1,3-benzothiazole-6-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)NCC)F UUSDSGBPWJJVMZ-UHFFFAOYSA-N 0.000 description 1
- DLGUEYSYYUGGQZ-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoline-5-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC=2C=CC=C(C=2C=C1)C(=O)O DLGUEYSYYUGGQZ-UHFFFAOYSA-N 0.000 description 1
- NPBTUYCXWNKOQF-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-(3-fluoro-5-methoxypyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1OC)F)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F NPBTUYCXWNKOQF-UHFFFAOYSA-N 0.000 description 1
- AHBXJXIQDITTRI-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-[2-(trifluoromethoxy)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)OC(F)(F)F)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F AHBXJXIQDITTRI-UHFFFAOYSA-N 0.000 description 1
- UISPRMNEZHHHKK-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-[2-(trifluoromethoxy)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoline-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)OC(F)(F)F)C1=CC2(C1)CCN(CC2)C1=NC2=CC=C(C=C2C=C1)C(=O)O UISPRMNEZHHHKK-UHFFFAOYSA-N 0.000 description 1
- LUYOTEBFELJFAE-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F LUYOTEBFELJFAE-UHFFFAOYSA-N 0.000 description 1
- RYUJZMGRKURZEN-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methoxy-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)OC RYUJZMGRKURZEN-UHFFFAOYSA-N 0.000 description 1
- ZRMNEGMKVZOPDP-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-6-methylpyrimidine-4-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C1=NC(=CC(=N1)C(=O)O)C ZRMNEGMKVZOPDP-UHFFFAOYSA-N 0.000 description 1
- VZAPQGMVTYZJLN-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-[1,3]thiazolo[5,4-b]pyridine-5-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1SC2=NC(=CC=C2N=1)C(=O)O VZAPQGMVTYZJLN-UHFFFAOYSA-N 0.000 description 1
- DRIKTUWIXBRLRM-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C=1C(=NC=CC=1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F DRIKTUWIXBRLRM-UHFFFAOYSA-N 0.000 description 1
- DZXZBNSNTAMGMH-UHFFFAOYSA-N 2-[2-[5-cyclopropyl-3-[4-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C=1C=NC=CC=1C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F DZXZBNSNTAMGMH-UHFFFAOYSA-N 0.000 description 1
- CYHXRQJQWYSXQQ-UHFFFAOYSA-N 2-[3'-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]spiro[8-azabicyclo[3.2.1]octane-3,1'-cyclobutane]-8-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1CC2(C1)CC1CCC(C2)N1C=1SC2=C(N=1)C(=CC(=C2)C(=O)O)F CYHXRQJQWYSXQQ-UHFFFAOYSA-N 0.000 description 1
- KZSKGLFYQAYZCO-UHFFFAOYSA-N 2-[3-[2-chloro-4-[[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]methoxy]phenyl]-3-hydroxyazetidin-1-yl]pyridine-4-carboxylic acid Chemical compound OC(=O)C1=CC=NC(N2CC(O)(C2)C=2C(=CC(OCC=3C(=NOC=3C3CC3)C=3C(=CC=CC=3Cl)Cl)=CC=2)Cl)=C1 KZSKGLFYQAYZCO-UHFFFAOYSA-N 0.000 description 1
- YPKNBCIPYKYYAU-UHFFFAOYSA-N 2-[5-cyclopropyl-3-(2,6-dichlorophenyl)triazol-4-yl]-7-azaspiro[3.5]nonan-2-ol Chemical compound C1(CC1)C=1N=NN(C=1C1(CC2(C1)CCNCC2)O)C1=C(C=CC=C1Cl)Cl YPKNBCIPYKYYAU-UHFFFAOYSA-N 0.000 description 1
- BHDJUAFZNIWISJ-UHFFFAOYSA-N 2-[6-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-2-azaspiro[3.3]hept-6-en-2-yl]-4-fluoro-1,3-benzothiazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(CN(C2)C=2SC3=C(N=2)C(=CC(=C3)C(=O)O)F)C1 BHDJUAFZNIWISJ-UHFFFAOYSA-N 0.000 description 1
- DOTNAYPZESZCJR-UHFFFAOYSA-N 2-[7-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoxalin-2-yl]oxyacetic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=CC=C2N=CC(=NC2=C1)OCC(=O)O DOTNAYPZESZCJR-UHFFFAOYSA-N 0.000 description 1
- YWLYUPVCYYWFCJ-UHFFFAOYSA-N 2-[[2-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carbonyl]amino]acetic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)NCC(=O)O)F YWLYUPVCYYWFCJ-UHFFFAOYSA-N 0.000 description 1
- BVAHPPKGOOJSPU-UHFFFAOYSA-N 2-[[5-chloro-2-[(5-methyl-2-propan-2-ylpyrazol-3-yl)amino]pyridin-4-yl]amino]-n-methoxybenzamide Chemical compound CONC(=O)C1=CC=CC=C1NC1=CC(NC=2N(N=C(C)C=2)C(C)C)=NC=C1Cl BVAHPPKGOOJSPU-UHFFFAOYSA-N 0.000 description 1
- QBRBVIHGBQDOTD-UHFFFAOYSA-N 2-[[6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]pyridine-3-carbonyl]amino]acetic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C1=NC=C(C(=O)NCC(=O)O)C=C1 QBRBVIHGBQDOTD-UHFFFAOYSA-N 0.000 description 1
- 101710186725 2-acylglycerol O-acyltransferase 2 Proteins 0.000 description 1
- HUDIKDNPUIYAKF-UHFFFAOYSA-N 2-bromo-5-chloro-[1,3]thiazolo[5,4-b]pyridine Chemical compound ClC1=CC=C2N=C(Br)SC2=N1 HUDIKDNPUIYAKF-UHFFFAOYSA-N 0.000 description 1
- WKORTIVWOCMGLV-UHFFFAOYSA-N 2-bromo-6-methoxy-1,3-benzothiazole-4-carboxylic acid Chemical compound BrC=1SC=2C(N=1)=C(C=C(C=2)OC)C(=O)O WKORTIVWOCMGLV-UHFFFAOYSA-N 0.000 description 1
- 125000004974 2-butenyl group Chemical group C(C=CC)* 0.000 description 1
- FPYUJUBAXZAQNL-UHFFFAOYSA-N 2-chlorobenzaldehyde Chemical compound ClC1=CC=CC=C1C=O FPYUJUBAXZAQNL-UHFFFAOYSA-N 0.000 description 1
- 125000006040 2-hexenyl group Chemical group 0.000 description 1
- 125000006022 2-methyl-2-propenyl group Chemical group 0.000 description 1
- VNJOEUSYAMPBAK-UHFFFAOYSA-N 2-methylbenzenesulfonic acid;hydrate Chemical compound O.CC1=CC=CC=C1S(O)(=O)=O VNJOEUSYAMPBAK-UHFFFAOYSA-N 0.000 description 1
- 125000001622 2-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C(*)C([H])=C([H])C2=C1[H] 0.000 description 1
- 125000006024 2-pentenyl group Chemical group 0.000 description 1
- KRTGJZMJJVEKRX-UHFFFAOYSA-N 2-phenylethan-1-yl Chemical group [CH2]CC1=CC=CC=C1 KRTGJZMJJVEKRX-UHFFFAOYSA-N 0.000 description 1
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 1
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- WMKYKQWKLILFBM-UHFFFAOYSA-N 2h-pyridine-1-carboxylic acid Chemical group OC(=O)N1CC=CC=C1 WMKYKQWKLILFBM-UHFFFAOYSA-N 0.000 description 1
- ZEBBWYNHVLBCIC-UHFFFAOYSA-N 3-(3,5-dichloropyridin-4-yl)-1,2-oxazole Chemical compound ClC=1C=NC=C(C=1C1=NOC=C1)Cl ZEBBWYNHVLBCIC-UHFFFAOYSA-N 0.000 description 1
- BYHQTRFJOGIQAO-GOSISDBHSA-N 3-(4-bromophenyl)-8-[(2R)-2-hydroxypropyl]-1-[(3-methoxyphenyl)methyl]-1,3,8-triazaspiro[4.5]decan-2-one Chemical compound C[C@H](CN1CCC2(CC1)CN(C(=O)N2CC3=CC(=CC=C3)OC)C4=CC=C(C=C4)Br)O BYHQTRFJOGIQAO-GOSISDBHSA-N 0.000 description 1
- UHDSCTIGBYQNSV-UHFFFAOYSA-N 3-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylindazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NN(C2=CC(=CC=C12)C(=O)O)C UHDSCTIGBYQNSV-UHFFFAOYSA-N 0.000 description 1
- UWAUOLUWECSAFZ-UHFFFAOYSA-N 3-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]benzoic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C(C(=O)O)C=CC=1 UWAUOLUWECSAFZ-UHFFFAOYSA-N 0.000 description 1
- REIQTABSJJZWOQ-UHFFFAOYSA-N 3-[2-[5-cyclopropyl-3-[2-(trifluoromethoxy)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylpyrazolo[4,3-b]pyridine-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)OC(F)(F)F)C1=CC2(C1)CCN(CC2)C1=NN(C=2C1=NC=C(C=2)C(=O)O)C REIQTABSJJZWOQ-UHFFFAOYSA-N 0.000 description 1
- YAXCQRUOIDBASP-UHFFFAOYSA-N 3-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylindazole-6-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C1=NN(C2=CC(=CC=C12)C(=O)O)C YAXCQRUOIDBASP-UHFFFAOYSA-N 0.000 description 1
- SRVXSISGYBMIHR-UHFFFAOYSA-N 3-[3-[3-(2-amino-2-oxoethyl)phenyl]-5-chlorophenyl]-3-(5-methyl-1,3-thiazol-2-yl)propanoic acid Chemical compound S1C(C)=CN=C1C(CC(O)=O)C1=CC(Cl)=CC(C=2C=C(CC(N)=O)C=CC=2)=C1 SRVXSISGYBMIHR-UHFFFAOYSA-N 0.000 description 1
- AKJRHNHVTAAUQL-UHFFFAOYSA-N 3-[[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-2-hydroxyspiro[3.5]nonan-7-yl]oxymethyl]benzoic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1(CC2(C1)CCC(CC2)OCC=1C=C(C(=O)O)C=CC=1)O AKJRHNHVTAAUQL-UHFFFAOYSA-N 0.000 description 1
- FDGAEAYZQQCBRN-UHFFFAOYSA-N 3-amino-4-methoxybenzoic acid Chemical compound COC1=CC=C(C(O)=O)C=C1N FDGAEAYZQQCBRN-UHFFFAOYSA-N 0.000 description 1
- WBTHOSZMTIPJLR-UHFFFAOYSA-N 3-amino-5-(trifluoromethyl)benzoic acid Chemical compound NC1=CC(C(O)=O)=CC(C(F)(F)F)=C1 WBTHOSZMTIPJLR-UHFFFAOYSA-N 0.000 description 1
- 125000004975 3-butenyl group Chemical group C(CC=C)* 0.000 description 1
- 125000006041 3-hexenyl group Chemical group 0.000 description 1
- 125000001541 3-thienyl group Chemical group S1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- ZULJZXHYOZIPFE-UHFFFAOYSA-N 4-(7-azaspiro[3.5]non-2-en-2-yl)-5-cyclopropyl-3-[2-(trifluoromethoxy)phenyl]-1,2-oxazole Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)OC(F)(F)F)C1=CC2(C1)CCNCC2 ZULJZXHYOZIPFE-UHFFFAOYSA-N 0.000 description 1
- YYPAQEMYOCBWOI-UHFFFAOYSA-N 4-(7-azaspiro[3.5]non-2-en-2-yl)-5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazole Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCNCC2 YYPAQEMYOCBWOI-UHFFFAOYSA-N 0.000 description 1
- IMBBXSASDSZJSX-UHFFFAOYSA-N 4-Carboxypyrazole Chemical compound OC(=O)C=1C=NNC=1 IMBBXSASDSZJSX-UHFFFAOYSA-N 0.000 description 1
- OQDQIFQRNZIEEJ-UHFFFAOYSA-N 4-[1-(1,3-benzothiazol-6-ylsulfonyl)-5-chloroindol-2-yl]butanoic acid Chemical compound C1=C2N=CSC2=CC(S(=O)(=O)N2C3=CC=C(Cl)C=C3C=C2CCCC(=O)O)=C1 OQDQIFQRNZIEEJ-UHFFFAOYSA-N 0.000 description 1
- AQFAKTHAOLWCDG-UHFFFAOYSA-N 4-[2-[3-(2-chlorophenyl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]benzoic acid Chemical compound ClC1=C(C=CC=C1)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C1=CC=C(C(=O)O)C=C1)C1CC1 AQFAKTHAOLWCDG-UHFFFAOYSA-N 0.000 description 1
- WHVKNPGPTFPWEQ-UHFFFAOYSA-N 4-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-2-hydroxyspiro[3.5]nonan-7-yl]oxybenzoic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1(CC2(C1)CCC(CC2)OC1=CC=C(C(=O)O)C=C1)O WHVKNPGPTFPWEQ-UHFFFAOYSA-N 0.000 description 1
- FSJONNQIJMENSS-UHFFFAOYSA-N 4-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]benzoic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=CC=C(C(=O)O)C=C1 FSJONNQIJMENSS-UHFFFAOYSA-N 0.000 description 1
- OEJGRKSNCOUDHU-UHFFFAOYSA-N 4-[7-(6-bromoquinoxalin-2-yl)-7-azaspiro[3.5]non-2-en-2-yl]-5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazole Chemical compound BrC=1C=C2N=CC(=NC2=CC=1)N1CCC2(CC(=C2)C=2C(=NOC=2C2CC2)C2=C(C=CC=C2Cl)Cl)CC1 OEJGRKSNCOUDHU-UHFFFAOYSA-N 0.000 description 1
- HKFSVCDCBWQOGS-UHFFFAOYSA-N 4-bromo-5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazole Chemical compound BrC=1C(=NOC=1C1CC1)C1=C(C=NC=C1Cl)Cl HKFSVCDCBWQOGS-UHFFFAOYSA-N 0.000 description 1
- LUUMLYXKTPBTQR-UHFFFAOYSA-N 4-chloro-n-[5-methyl-2-(7h-pyrrolo[2,3-d]pyrimidine-4-carbonyl)pyridin-3-yl]-3-(trifluoromethyl)benzenesulfonamide Chemical compound C=1C(C)=CN=C(C(=O)C=2C=3C=CNC=3N=CN=2)C=1NS(=O)(=O)C1=CC=C(Cl)C(C(F)(F)F)=C1 LUUMLYXKTPBTQR-UHFFFAOYSA-N 0.000 description 1
- GMHIVWZXNHOUEX-UHFFFAOYSA-N 4-cyclopropyl-1-(2,6-dichlorophenyl)-5-iodotriazole Chemical compound C1(CC1)C=1N=NN(C=1I)C1=C(C=CC=C1Cl)Cl GMHIVWZXNHOUEX-UHFFFAOYSA-N 0.000 description 1
- 125000006042 4-hexenyl group Chemical group 0.000 description 1
- 125000004217 4-methoxybenzyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1OC([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000003119 4-methyl-3-pentenyl group Chemical group [H]\C(=C(/C([H])([H])[H])C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- VRJHQPZVIGNGMX-UHFFFAOYSA-N 4-piperidinone Chemical compound O=C1CCNCC1 VRJHQPZVIGNGMX-UHFFFAOYSA-N 0.000 description 1
- 125000004608 5,6,7,8-tetrahydroquinolinyl group Chemical group N1=C(C=CC=2CCCCC12)* 0.000 description 1
- IRPVABHDSJVBNZ-RTHVDDQRSA-N 5-[1-(cyclopropylmethyl)-5-[(1R,5S)-3-(oxetan-3-yl)-3-azabicyclo[3.1.0]hexan-6-yl]pyrazol-3-yl]-3-(trifluoromethyl)pyridin-2-amine Chemical compound C1=C(C(F)(F)F)C(N)=NC=C1C1=NN(CC2CC2)C(C2[C@@H]3CN(C[C@@H]32)C2COC2)=C1 IRPVABHDSJVBNZ-RTHVDDQRSA-N 0.000 description 1
- QLTYREDSJFUKOW-UHFFFAOYSA-N 5-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]pyrazine-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1N=CC(=NC=1)C(=O)O QLTYREDSJFUKOW-UHFFFAOYSA-N 0.000 description 1
- DVMXXSLSGKLUKP-UHFFFAOYSA-N 5-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]pyridine-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=CC(=NC=1)C(=O)O DVMXXSLSGKLUKP-UHFFFAOYSA-N 0.000 description 1
- CNOVSDYVNGGDOR-UHFFFAOYSA-N 5-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]pyrimidine-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=NC(=NC=1)C(=O)O CNOVSDYVNGGDOR-UHFFFAOYSA-N 0.000 description 1
- VPJJJVTYBPWFBR-UHFFFAOYSA-N 5-[2-[5-cyclopropyl-3-[2-(trifluoromethoxy)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylindazole-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)OC(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=NN(C2=CC=1)C)C(=O)O VPJJJVTYBPWFBR-UHFFFAOYSA-N 0.000 description 1
- BLZHNGJZBLBXEX-UHFFFAOYSA-N 5-[2-[5-cyclopropyl-3-[2-(trifluoromethoxy)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylpyrrolo[2,3-c]pyridine-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)OC(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CN=1)N(C(=C2)C(=O)O)C BLZHNGJZBLBXEX-UHFFFAOYSA-N 0.000 description 1
- 125000006043 5-hexenyl group Chemical group 0.000 description 1
- 125000006163 5-membered heteroaryl group Chemical group 0.000 description 1
- XVMSFILGAMDHEY-UHFFFAOYSA-N 6-(4-aminophenyl)sulfonylpyridin-3-amine Chemical compound C1=CC(N)=CC=C1S(=O)(=O)C1=CC=C(N)C=N1 XVMSFILGAMDHEY-UHFFFAOYSA-N 0.000 description 1
- KCBWAFJCKVKYHO-UHFFFAOYSA-N 6-(4-cyclopropyl-6-methoxypyrimidin-5-yl)-1-[[4-[1-propan-2-yl-4-(trifluoromethyl)imidazol-2-yl]phenyl]methyl]pyrazolo[3,4-d]pyrimidine Chemical compound C1(CC1)C1=NC=NC(=C1C1=NC=C2C(=N1)N(N=C2)CC1=CC=C(C=C1)C=1N(C=C(N=1)C(F)(F)F)C(C)C)OC KCBWAFJCKVKYHO-UHFFFAOYSA-N 0.000 description 1
- CEMCQYVNKVSQTD-UHFFFAOYSA-N 6-[2-(3-cyclohexyl-5-cyclopropyl-1,2-oxazol-4-yl)-7-azaspiro[3.5]non-2-en-7-yl]-1-methylindole-3-carboxylic acid Chemical compound C1(CCCCC1)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C1=CC=C2C(=CN(C2=C1)C)C(=O)O)C1CC1 CEMCQYVNKVSQTD-UHFFFAOYSA-N 0.000 description 1
- GKJRHBGSJYIOLZ-UHFFFAOYSA-N 6-[2-(3-cyclohexyl-5-cyclopropyl-1,2-oxazol-4-yl)-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound C1(CCCCC1)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F)C1CC1 GKJRHBGSJYIOLZ-UHFFFAOYSA-N 0.000 description 1
- AUKHRVOPBVAYTH-UHFFFAOYSA-N 6-[2-(3-cyclohexyl-5-cyclopropyl-1,2-oxazol-4-yl)-7-azaspiro[3.5]non-2-en-7-yl]-4-ethoxyquinoline-2-carboxylic acid Chemical compound C1(CCCCC1)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OCC)C1CC1 AUKHRVOPBVAYTH-UHFFFAOYSA-N 0.000 description 1
- ODCDUDICXHWLRS-UHFFFAOYSA-N 6-[2-(3-cyclohexyl-5-cyclopropyl-1,2-oxazol-4-yl)-7-azaspiro[3.5]non-2-en-7-yl]-4-methoxyquinoline-2-carboxylic acid Chemical compound C1(CCCCC1)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC)C1CC1 ODCDUDICXHWLRS-UHFFFAOYSA-N 0.000 description 1
- MOFPIIUDBMDJSN-UHFFFAOYSA-N 6-[2-[3-(2,6-dichlorophenyl)-5-propan-2-yl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound ClC1=C(C(=CC=C1)Cl)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F)C(C)C MOFPIIUDBMDJSN-UHFFFAOYSA-N 0.000 description 1
- LFYXCXFOZYAZGI-UHFFFAOYSA-N 6-[2-[3-(2-chloro-4-fluorophenyl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound ClC1=C(C=CC(=C1)F)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F)C1CC1 LFYXCXFOZYAZGI-UHFFFAOYSA-N 0.000 description 1
- JNHCLLGYVWBUIT-UHFFFAOYSA-N 6-[2-[3-(2-chloro-6-fluorophenyl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound ClC1=C(C(=CC=C1)F)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F)C1CC1 JNHCLLGYVWBUIT-UHFFFAOYSA-N 0.000 description 1
- UJYCBZKDVGIEPD-UHFFFAOYSA-N 6-[2-[3-(2-chloro-6-fluorophenyl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoline-2-carboxylic acid Chemical compound ClC1=C(C(=CC=C1)F)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C=CC(=NC2=CC=1)C(=O)O)C1CC1 UJYCBZKDVGIEPD-UHFFFAOYSA-N 0.000 description 1
- OCPSXWOMCOFBGV-UHFFFAOYSA-N 6-[2-[3-(2-chloro-6-methylphenyl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound ClC1=C(C(=CC=C1)C)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F)C1CC1 OCPSXWOMCOFBGV-UHFFFAOYSA-N 0.000 description 1
- BLKIDVGDNKMSMJ-UHFFFAOYSA-N 6-[2-[3-(2-chloro-6-methylphenyl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoline-2-carboxylic acid Chemical compound ClC1=C(C(=CC=C1)C)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C=CC(=NC2=CC=1)C(=O)O)C1CC1 BLKIDVGDNKMSMJ-UHFFFAOYSA-N 0.000 description 1
- MUMBFDCDONXXQU-UHFFFAOYSA-N 6-[2-[3-(3,5-dichloropyridin-4-yl)-5-(1-methylcyclopropyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound ClC=1C=NC=C(C=1C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F)C1(CC1)C)Cl MUMBFDCDONXXQU-UHFFFAOYSA-N 0.000 description 1
- AFOOMDKFFNXGIW-UHFFFAOYSA-N 6-[2-[3-(3,5-dichloropyridin-4-yl)-5-propan-2-yl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound ClC=1C=NC=C(C=1C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F)C(C)C)Cl AFOOMDKFFNXGIW-UHFFFAOYSA-N 0.000 description 1
- IVTPNQSYGVMWNP-UHFFFAOYSA-N 6-[2-[3-(3-chloropyridin-2-yl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(difluoromethoxy)-N-methylsulfonylquinoline-2-carboxamide Chemical compound ClC=1C(=NC=CC=1)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C)OC(F)F)C1CC1 IVTPNQSYGVMWNP-UHFFFAOYSA-N 0.000 description 1
- ZHLIDCKSNLBMRJ-UHFFFAOYSA-N 6-[2-[3-(3-chloropyridin-2-yl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(difluoromethoxy)quinoline-2-carboxylic acid Chemical compound ClC=1C(=NC=CC=1)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC(F)F)C1CC1 ZHLIDCKSNLBMRJ-UHFFFAOYSA-N 0.000 description 1
- KQBATTWANJDQJT-UHFFFAOYSA-N 6-[2-[3-(3-chloropyridin-2-yl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound ClC=1C(=NC=CC=1)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F)C1CC1 KQBATTWANJDQJT-UHFFFAOYSA-N 0.000 description 1
- FJEGASLQTFTAPW-UHFFFAOYSA-N 6-[2-[3-(3-chloropyridin-2-yl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methoxyquinoline-2-carboxylic acid Chemical compound ClC=1C(=NC=CC=1)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC)C1CC1 FJEGASLQTFTAPW-UHFFFAOYSA-N 0.000 description 1
- JVVIKDGFQLGJML-UHFFFAOYSA-N 6-[2-[3-(3-chloropyridin-2-yl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-N-cyclopropylsulfonyl-4-(difluoromethoxy)quinoline-2-carboxamide Chemical compound ClC=1C(=NC=CC=1)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C1CC1)OC(F)F)C1CC1 JVVIKDGFQLGJML-UHFFFAOYSA-N 0.000 description 1
- AZZFFTCKDXYLKD-UHFFFAOYSA-N 6-[2-[3-(3-chloropyridin-2-yl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]pyridine-3-carboxylic acid Chemical compound ClC=1C(=NC=CC=1)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C1=NC=C(C(=O)O)C=C1)C1CC1 AZZFFTCKDXYLKD-UHFFFAOYSA-N 0.000 description 1
- VRLNJABARCNNFT-UHFFFAOYSA-N 6-[2-[3-(3-chloropyridin-2-yl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoline-2-carboxylic acid Chemical compound ClC=1C(=NC=CC=1)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C=CC(=NC2=CC=1)C(=O)O)C1CC1 VRLNJABARCNNFT-UHFFFAOYSA-N 0.000 description 1
- CILKRDHHPWGVPC-UHFFFAOYSA-N 6-[2-[3-(3-chloropyridin-4-yl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(difluoromethoxy)quinoline-2-carboxylic acid Chemical compound ClC=1C=NC=CC=1C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC(F)F)C1CC1 CILKRDHHPWGVPC-UHFFFAOYSA-N 0.000 description 1
- LRKCLTZXYNXEIZ-UHFFFAOYSA-N 6-[2-[3-(3-chloropyridin-4-yl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methoxyquinoline-2-carboxylic acid Chemical compound ClC=1C=NC=CC=1C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC)C1CC1 LRKCLTZXYNXEIZ-UHFFFAOYSA-N 0.000 description 1
- XGCFMWFNEYKHMZ-UHFFFAOYSA-N 6-[2-[3-(3-chloropyridin-4-yl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoline-2-carboxylic acid Chemical compound ClC=1C=NC=CC=1C1=NOC(=C1C1=CC2(C1)CCN(CC2)C=1C=C2C=CC(=NC2=CC=1)C(=O)O)C1CC1 XGCFMWFNEYKHMZ-UHFFFAOYSA-N 0.000 description 1
- AZVNKEPVQILRDX-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichloro-4-fluorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=C(C=C1Cl)F)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F AZVNKEPVQILRDX-UHFFFAOYSA-N 0.000 description 1
- VRFMOSIMQZRRPA-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichloro-4-fluorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methoxyquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=C(C=C1Cl)F)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC VRFMOSIMQZRRPA-UHFFFAOYSA-N 0.000 description 1
- HDWKXTMKQRXZSE-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichloro-4-fluorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-propan-2-yloxyquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=C(C=C1Cl)F)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC(C)C HDWKXTMKQRXZSE-UHFFFAOYSA-N 0.000 description 1
- JIXPFKJUUAJASB-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichloro-4-fluorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]pyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=C(C=C1Cl)F)Cl)C1=CC2(C1)CCN(CC2)C1=NC=C(C(=O)O)C=C1 JIXPFKJUUAJASB-UHFFFAOYSA-N 0.000 description 1
- DNHONPYJPUPDJP-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichloro-4-fluorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=C(C=C1Cl)F)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C=CC(=NC2=CC=1)C(=O)O DNHONPYJPUPDJP-UHFFFAOYSA-N 0.000 description 1
- ABEUFSGCMAZWCF-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylindazole-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=CC=C2C(=NN(C2=C1)C)C(=O)O ABEUFSGCMAZWCF-UHFFFAOYSA-N 0.000 description 1
- DDERFKUXIPUURA-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylindole-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=CC=C2C=C(N(C2=C1)C)C(=O)O DDERFKUXIPUURA-UHFFFAOYSA-N 0.000 description 1
- SUOMEPOKHNAXGW-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylindole-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=CC=C2C(=CN(C2=C1)C)C(=O)O SUOMEPOKHNAXGW-UHFFFAOYSA-N 0.000 description 1
- NZTGHGFYTUJHRB-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylpyrrolo[3,2-c]pyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=CC2=C(C=N1)C(=CN2C)C(=O)O NZTGHGFYTUJHRB-UHFFFAOYSA-N 0.000 description 1
- RMBBYDDTYRGNSX-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-2-methylpyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC(=C(C(=O)O)C=C1)C RMBBYDDTYRGNSX-UHFFFAOYSA-N 0.000 description 1
- SFZIEFMCGDMPOA-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)pyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC=C(C(=O)O)C(=C1)C(F)(F)F SFZIEFMCGDMPOA-UHFFFAOYSA-N 0.000 description 1
- GGRMLXXEGGRNKV-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F GGRMLXXEGGRNKV-UHFFFAOYSA-N 0.000 description 1
- UVMLOYUOUYENNN-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methylpyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC=C(C(=O)O)C(=C1)C UVMLOYUOUYENNN-UHFFFAOYSA-N 0.000 description 1
- BRIBZUXKBZLRME-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-5-methylpyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC=C(C(=O)O)C=C1C BRIBZUXKBZLRME-UHFFFAOYSA-N 0.000 description 1
- FSHKAVWPRZLJCP-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-N-cyclopropylsulfonylquinoline-2-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C1CC1 FSHKAVWPRZLJCP-UHFFFAOYSA-N 0.000 description 1
- ZUMMCSRHDYOXBN-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-N-methylsulfonylquinoline-2-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C ZUMMCSRHDYOXBN-UHFFFAOYSA-N 0.000 description 1
- SZECPXXSQKYPKM-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]pyridazine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=CC=C(N=N1)C(=O)O SZECPXXSQKYPKM-UHFFFAOYSA-N 0.000 description 1
- RZXAEHFPVGAJRG-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]pyridine-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=CC=CC(=N1)C(=O)O RZXAEHFPVGAJRG-UHFFFAOYSA-N 0.000 description 1
- UXZHKRXZCXSKGC-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C=CC(=NC2=CC=1)C(=O)O UXZHKRXZCXSKGC-UHFFFAOYSA-N 0.000 description 1
- RROZJZRXMBPCTL-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]spiro[3.5]non-2-en-7-yl]oxyquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCC(CC2)OC=1C=C2C=CC(=NC2=CC=1)C(=O)O RROZJZRXMBPCTL-UHFFFAOYSA-N 0.000 description 1
- KWEDVRBXRXNSQB-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-difluorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F KWEDVRBXRXNSQB-UHFFFAOYSA-N 0.000 description 1
- YIMJXCNDELXBMU-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(2,6-difluorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C=CC(=NC2=CC=1)C(=O)O YIMJXCNDELXBMU-UHFFFAOYSA-N 0.000 description 1
- FYTWHVHQZGNBER-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(difluoromethoxy)-N-methylsulfonylquinoline-2-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C)OC(F)F FYTWHVHQZGNBER-UHFFFAOYSA-N 0.000 description 1
- YIRPELGNXFSRBN-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(difluoromethoxy)quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC(F)F YIRPELGNXFSRBN-UHFFFAOYSA-N 0.000 description 1
- LAHZVBUOKWIPNU-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-ethoxyquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OCC LAHZVBUOKWIPNU-UHFFFAOYSA-N 0.000 description 1
- NOVKUUQLGBTQOQ-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methoxy-N-methylsulfonylquinoline-2-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C)OC NOVKUUQLGBTQOQ-UHFFFAOYSA-N 0.000 description 1
- GCLRCFQQGUPZBQ-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methoxypyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC=C(C(=O)O)C(=C1)OC GCLRCFQQGUPZBQ-UHFFFAOYSA-N 0.000 description 1
- AUKUERAKBLFUKO-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methoxyquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC AUKUERAKBLFUKO-UHFFFAOYSA-N 0.000 description 1
- TVAUJLNXTLXMOE-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methylquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C TVAUJLNXTLXMOE-UHFFFAOYSA-N 0.000 description 1
- LZSXRQCQUMGJBV-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-propan-2-yloxyquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC(C)C LZSXRQCQUMGJBV-UHFFFAOYSA-N 0.000 description 1
- HTHPAACRKWVYKH-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-N-cyclopropylsulfonyl-4-(trifluoromethyl)quinoline-2-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C1CC1)C(F)(F)F HTHPAACRKWVYKH-UHFFFAOYSA-N 0.000 description 1
- SWWUUKFAGLEZQU-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-N-methylsulfonyl-4-(trifluoromethyl)quinoline-2-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C)C(F)(F)F SWWUUKFAGLEZQU-UHFFFAOYSA-N 0.000 description 1
- HHKLZVUXGCULKP-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]pyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=NC=C(C(=O)O)C=C1 HHKLZVUXGCULKP-UHFFFAOYSA-N 0.000 description 1
- GVLBROJHBALOBD-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1C=C2C=CC(=NC2=CC=1)C(=O)O GVLBROJHBALOBD-UHFFFAOYSA-N 0.000 description 1
- NGWJWIVLKRWULX-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethoxy)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-3-(trifluoromethyl)imidazo[1,5-a]pyridine-1-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)OC(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=CC=2N(C=1)C(=NC=2C(=O)O)C(F)(F)F NGWJWIVLKRWULX-UHFFFAOYSA-N 0.000 description 1
- RXGBUMPSDSTQLN-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethoxy)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-ethoxyquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)OC(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OCC RXGBUMPSDSTQLN-UHFFFAOYSA-N 0.000 description 1
- ZDOHBTSUKXSISZ-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethoxy)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-propan-2-yloxyquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)OC(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC(C)C ZDOHBTSUKXSISZ-UHFFFAOYSA-N 0.000 description 1
- MJLCYGLEBHWUTA-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethoxy)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-5-fluoropyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)OC(F)(F)F)C1=CC2(C1)CCN(CC2)C1=NC=C(C(=O)O)C=C1F MJLCYGLEBHWUTA-UHFFFAOYSA-N 0.000 description 1
- YCFOXYIBSKKZQM-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethoxy)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]pyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)OC(F)(F)F)C1=CC2(C1)CCN(CC2)C1=NC=C(C(=O)O)C=C1 YCFOXYIBSKKZQM-UHFFFAOYSA-N 0.000 description 1
- OORYFBQCBVYDDN-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylindazole-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C1=CC=C2C(=NN(C2=C1)C)C(=O)O OORYFBQCBVYDDN-UHFFFAOYSA-N 0.000 description 1
- XZYGXULQBKRWJR-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-1-methylindole-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C1=CC=C2C(=CN(C2=C1)C)C(=O)O XZYGXULQBKRWJR-UHFFFAOYSA-N 0.000 description 1
- GXLJPSVMLCCDAC-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(2-hydroxyethoxy)quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OCCO GXLJPSVMLCCDAC-UHFFFAOYSA-N 0.000 description 1
- AUPWJOWJEIXYGR-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(difluoromethoxy)-N-methylsulfonylquinoline-2-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C)OC(F)F AUPWJOWJEIXYGR-UHFFFAOYSA-N 0.000 description 1
- QLJTXDLVICXBJC-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)pyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C1=NC=C(C(=O)O)C(=C1)C(F)(F)F QLJTXDLVICXBJC-UHFFFAOYSA-N 0.000 description 1
- BQHPKGXDMXWAFX-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F BQHPKGXDMXWAFX-UHFFFAOYSA-N 0.000 description 1
- LAAAIMKHZIWJNX-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-ethoxyquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OCC LAAAIMKHZIWJNX-UHFFFAOYSA-N 0.000 description 1
- YPSXJLGVLXNDIL-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methoxy-N-methylsulfonylquinoline-2-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C)OC YPSXJLGVLXNDIL-UHFFFAOYSA-N 0.000 description 1
- ZDZISTYHQOHAQA-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methoxyquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC ZDZISTYHQOHAQA-UHFFFAOYSA-N 0.000 description 1
- CZTHZXZBAROPOC-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-propan-2-yloxyquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC(C)C CZTHZXZBAROPOC-UHFFFAOYSA-N 0.000 description 1
- JUQHQWKGLUOANY-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoxaline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2N=CC(=NC2=CC=1)C(=O)O JUQHQWKGLUOANY-UHFFFAOYSA-N 0.000 description 1
- RBECXVZPUIITBO-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(difluoromethoxy)-N-methylsulfonylquinoline-2-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C=1C(=NC=CC=1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C)OC(F)F RBECXVZPUIITBO-UHFFFAOYSA-N 0.000 description 1
- DIIMGTLVNLLGMO-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(difluoromethoxy)quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C=1C(=NC=CC=1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC(F)F DIIMGTLVNLLGMO-UHFFFAOYSA-N 0.000 description 1
- HPXCMEOZVXGGKD-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C=1C(=NC=CC=1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F HPXCMEOZVXGGKD-UHFFFAOYSA-N 0.000 description 1
- WCZQFYCWZSAXOG-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methoxyquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C=1C(=NC=CC=1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC WCZQFYCWZSAXOG-UHFFFAOYSA-N 0.000 description 1
- PITMUNLGAKZVCL-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C=1C(=NC=CC=1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C=CC(=NC2=CC=1)C(=O)O PITMUNLGAKZVCL-UHFFFAOYSA-N 0.000 description 1
- ZPQLHRWNBILWPG-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[4-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(difluoromethoxy)-N-methylsulfonylquinoline-2-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C=1C=NC=CC=1C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C)OC(F)F ZPQLHRWNBILWPG-UHFFFAOYSA-N 0.000 description 1
- LSDHZZRAOQCKRH-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[4-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(difluoromethoxy)quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C=1C=NC=CC=1C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC(F)F LSDHZZRAOQCKRH-UHFFFAOYSA-N 0.000 description 1
- XJPBZFHKCYPANE-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[4-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(trifluoromethyl)quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C=1C=NC=CC=1C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)C(F)(F)F XJPBZFHKCYPANE-UHFFFAOYSA-N 0.000 description 1
- GUAUOYQZZPVHTR-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[4-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-methoxyquinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C=1C=NC=CC=1C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)O)OC GUAUOYQZZPVHTR-UHFFFAOYSA-N 0.000 description 1
- SVMUGGLJOVPKJH-UHFFFAOYSA-N 6-[2-[5-cyclopropyl-3-[4-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]quinoline-2-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C=1C=NC=CC=1C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C=CC(=NC2=CC=1)C(=O)O SVMUGGLJOVPKJH-UHFFFAOYSA-N 0.000 description 1
- NZXJXRSUHMWMID-UHFFFAOYSA-N 6-[6-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-2-azaspiro[3.3]hept-6-en-2-yl]pyridine-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(CN(C2)C2=NC=C(C(=O)O)C=C2)C1 NZXJXRSUHMWMID-UHFFFAOYSA-N 0.000 description 1
- VPPCXQLDCBPZGQ-UHFFFAOYSA-N 6-bromo-1-methylindazole-3-carbonitrile Chemical compound BrC1=CC=C2C(=NN(C2=C1)C)C#N VPPCXQLDCBPZGQ-UHFFFAOYSA-N 0.000 description 1
- QKBMJZODSYDEFC-UHFFFAOYSA-N 6-bromo-2-chloro-[1,3]thiazolo[4,5-b]pyridine Chemical compound C1=C(Br)C=C2SC(Cl)=NC2=N1 QKBMJZODSYDEFC-UHFFFAOYSA-N 0.000 description 1
- XDJDRCGDVKTDHY-UHFFFAOYSA-N 6-bromo-2-chloroquinoxaline Chemical compound C1=C(Br)C=CC2=NC(Cl)=CN=C21 XDJDRCGDVKTDHY-UHFFFAOYSA-N 0.000 description 1
- OPYRIRRTVBXVRH-UHFFFAOYSA-N 6-bromo-3-methylimidazo[1,5-a]pyridine-1-carboxylic acid Chemical compound C1=CC(Br)=CN2C(C)=NC(C(O)=O)=C21 OPYRIRRTVBXVRH-UHFFFAOYSA-N 0.000 description 1
- DODHNLBNENVQDI-UHFFFAOYSA-N 6-chloroquinoxaline-2-carbonitrile Chemical compound ClC=1C=C2N=CC(=NC2=CC=1)C#N DODHNLBNENVQDI-UHFFFAOYSA-N 0.000 description 1
- TWTJIUIXSVEUST-UHFFFAOYSA-N 7-[2-[3-(2,6-dichlorophenyl)-5-propan-2-yl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]cinnoline-3-carboxylic acid Chemical compound ClC1=C(C(=CC=C1)Cl)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C1=CC=C2C=C(N=NC2=C1)C(=O)O)C(C)C TWTJIUIXSVEUST-UHFFFAOYSA-N 0.000 description 1
- FBPFLCYWDQZAGA-UHFFFAOYSA-N 7-[2-[3-(2-chloro-6-fluorophenyl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]isoquinoline-3-carboxylic acid Chemical compound ClC1=C(C(=CC=C1)F)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C1=CC=C2C=C(N=CC2=C1)C(=O)O)C1CC1 FBPFLCYWDQZAGA-UHFFFAOYSA-N 0.000 description 1
- VCEZXCNWDVZXKF-UHFFFAOYSA-N 7-[2-[3-(2-chloro-6-methylphenyl)-5-cyclopropyl-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]cinnoline-3-carboxylic acid Chemical compound ClC1=C(C(=CC=C1)C)C1=NOC(=C1C1=CC2(C1)CCN(CC2)C1=CC=C2C=C(N=NC2=C1)C(=O)O)C1CC1 VCEZXCNWDVZXKF-UHFFFAOYSA-N 0.000 description 1
- JRLDPVKQZIVJHC-UHFFFAOYSA-N 7-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-8-methylquinoline-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=CC=C2C=C(C=NC2=C1C)C(=O)O JRLDPVKQZIVJHC-UHFFFAOYSA-N 0.000 description 1
- KTRGJFHLXZMCBX-UHFFFAOYSA-N 7-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]cinnoline-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=CC=C2C=C(N=NC2=C1)C(=O)O KTRGJFHLXZMCBX-UHFFFAOYSA-N 0.000 description 1
- YQBJIOUMWBWRCM-UHFFFAOYSA-N 7-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]isoquinoline-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C1=CC=C2C=C(N=CC2=C1)C(=O)O YQBJIOUMWBWRCM-UHFFFAOYSA-N 0.000 description 1
- SRSJZDUTBADUGN-UHFFFAOYSA-N 7-[2-[5-cyclopropyl-3-(2,6-difluorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]cinnoline-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1F)F)C1=CC2(C1)CCN(CC2)C1=CC=C2C=C(N=NC2=C1)C(=O)O SRSJZDUTBADUGN-UHFFFAOYSA-N 0.000 description 1
- PSVAAPLAQYYMRC-UHFFFAOYSA-N 7-[2-[5-cyclopropyl-3-(2,6-difluorophenyl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]isoquinoline-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1F)F)C1=CC2(C1)CCN(CC2)C1=CC=C2C=C(N=CC2=C1)C(=O)O PSVAAPLAQYYMRC-UHFFFAOYSA-N 0.000 description 1
- JQSYSNUNDVELBP-UHFFFAOYSA-N 7-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-8-methylquinoline-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C1=CC=C2C=C(C=NC2=C1C)C(=O)O JQSYSNUNDVELBP-UHFFFAOYSA-N 0.000 description 1
- IYOJOLBRPNAFJA-UHFFFAOYSA-N 7-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)phenyl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]isoquinoline-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C1=CC=C2C=C(N=CC2=C1)C(=O)O IYOJOLBRPNAFJA-UHFFFAOYSA-N 0.000 description 1
- OUWOROJKWNONRI-UHFFFAOYSA-N 7-[2-[5-cyclopropyl-3-[4-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]cinnoline-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C=1C=NC=CC=1C(F)(F)F)C1=CC2(C1)CCN(CC2)C1=CC=C2C=C(N=NC2=C1)C(=O)O OUWOROJKWNONRI-UHFFFAOYSA-N 0.000 description 1
- VNPDFVQAJUCYMR-UHFFFAOYSA-N 7-[2-[5-cyclopropyl-3-[4-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]isoquinoline-3-carboxylic acid Chemical compound C1(CC1)C1=C(C(=NO1)C=1C=NC=CC=1C(F)(F)F)C1=CC2(C1)CCN(CC2)C1=CC=C2C=C(N=CC2=C1)C(=O)O VNPDFVQAJUCYMR-UHFFFAOYSA-N 0.000 description 1
- PXVQWJPOMIRXQL-UHFFFAOYSA-N 7-bromo-1h-quinoxalin-2-one Chemical compound C1=CC(Br)=CC2=NC(O)=CN=C21 PXVQWJPOMIRXQL-UHFFFAOYSA-N 0.000 description 1
- WCKFHJYQFLFMKN-UHFFFAOYSA-N 7-hydroxyspiro[3.5]nonan-2-one Chemical compound C1CC(O)CCC11CC(=O)C1 WCKFHJYQFLFMKN-UHFFFAOYSA-N 0.000 description 1
- 125000005330 8 membered heterocyclic group Chemical group 0.000 description 1
- CYJRNFFLTBEQSQ-UHFFFAOYSA-N 8-(3-methyl-1-benzothiophen-5-yl)-N-(4-methylsulfonylpyridin-3-yl)quinoxalin-6-amine Chemical compound CS(=O)(=O)C1=C(C=NC=C1)NC=1C=C2N=CC=NC2=C(C=1)C=1C=CC2=C(C(=CS2)C)C=1 CYJRNFFLTBEQSQ-UHFFFAOYSA-N 0.000 description 1
- IYTXKIXETAELAV-UHFFFAOYSA-N Aethyl-n-hexyl-keton Natural products CCCCCCC(=O)CC IYTXKIXETAELAV-UHFFFAOYSA-N 0.000 description 1
- 208000007082 Alcoholic Fatty Liver Diseases 0.000 description 1
- 102100024296 Alpha-1,6-mannosyl-glycoprotein 2-beta-N-acetylglucosaminyltransferase Human genes 0.000 description 1
- 229940122849 Autotaxin inhibitor Drugs 0.000 description 1
- 208000010839 B-cell chronic lymphocytic leukemia Diseases 0.000 description 1
- 206010070545 Bacterial translocation Diseases 0.000 description 1
- 206010004446 Benign prostatic hyperplasia Diseases 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- LSNNMFCWUKXFEE-UHFFFAOYSA-M Bisulfite Chemical compound OS([O-])=O LSNNMFCWUKXFEE-UHFFFAOYSA-M 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 description 1
- 102000001902 CC Chemokines Human genes 0.000 description 1
- 108010040471 CC Chemokines Proteins 0.000 description 1
- JOYFKPKVJJGAMO-UHFFFAOYSA-N CCOC(=O)C1=C2N(C=C1)N=C(Cl)N=C2Cl Chemical compound CCOC(=O)C1=C2N(C=C1)N=C(Cl)N=C2Cl JOYFKPKVJJGAMO-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 108010078791 Carrier Proteins Proteins 0.000 description 1
- 102000011727 Caspases Human genes 0.000 description 1
- 108010076667 Caspases Proteins 0.000 description 1
- 229930186147 Cephalosporin Natural products 0.000 description 1
- 206010008111 Cerebral haemorrhage Diseases 0.000 description 1
- 238000006964 Chan-Lam coupling reaction Methods 0.000 description 1
- 208000008964 Chemical and Drug Induced Liver Injury Diseases 0.000 description 1
- 108010083647 Chemokine CCL24 Chemical class 0.000 description 1
- 102000006383 Chemokine CCL24 Human genes 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- 208000006545 Chronic Obstructive Pulmonary Disease Diseases 0.000 description 1
- AEMZEDNMNLIDSL-YGCVIUNWSA-N Cl.CC(C)(C)NC(=O)C1=CC=C(OC\C(CN)=C\F)C=C1 Chemical compound Cl.CC(C)(C)NC(=O)C1=CC=C(OC\C(CN)=C\F)C=C1 AEMZEDNMNLIDSL-YGCVIUNWSA-N 0.000 description 1
- 238000006066 Comins reaction Methods 0.000 description 1
- 102000015225 Connective Tissue Growth Factor Human genes 0.000 description 1
- 108010039419 Connective Tissue Growth Factor Proteins 0.000 description 1
- 208000011231 Crohn disease Diseases 0.000 description 1
- HTJDQJBWANPRPF-UHFFFAOYSA-N Cyclopropylamine Chemical compound NC1CC1 HTJDQJBWANPRPF-UHFFFAOYSA-N 0.000 description 1
- 102000004127 Cytokines Human genes 0.000 description 1
- 108090000695 Cytokines Proteins 0.000 description 1
- JVHXJTBJCFBINQ-ADAARDCZSA-N Dapagliflozin Chemical compound C1=CC(OCC)=CC=C1CC1=CC([C@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)O)=CC=C1Cl JVHXJTBJCFBINQ-ADAARDCZSA-N 0.000 description 1
- 238000006646 Dess-Martin oxidation reaction Methods 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 206010012689 Diabetic retinopathy Diseases 0.000 description 1
- SNRUBQQJIBEYMU-UHFFFAOYSA-N Dodecane Natural products CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 1
- 206010072268 Drug-induced liver injury Diseases 0.000 description 1
- 102100021977 Ectonucleotide pyrophosphatase/phosphodiesterase family member 2 Human genes 0.000 description 1
- 108050004000 Ectonucleotide pyrophosphatase/phosphodiesterase family member 2 Proteins 0.000 description 1
- 229940118365 Endothelin receptor antagonist Drugs 0.000 description 1
- 102000004190 Enzymes Human genes 0.000 description 1
- 108090000790 Enzymes Proteins 0.000 description 1
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 1
- 239000005977 Ethylene Substances 0.000 description 1
- 229940124783 FAK inhibitor Drugs 0.000 description 1
- 229940125634 FPR2 agonist Drugs 0.000 description 1
- 101710153363 Fibroblast growth factor 15 Proteins 0.000 description 1
- 108090000376 Fibroblast growth factor 21 Proteins 0.000 description 1
- 102000003973 Fibroblast growth factor 21 Human genes 0.000 description 1
- 208000007212 Foot-and-Mouth Disease Diseases 0.000 description 1
- 241000710198 Foot-and-mouth disease virus Species 0.000 description 1
- 108010001517 Galectin 3 Proteins 0.000 description 1
- 102100039558 Galectin-3 Human genes 0.000 description 1
- 229940089838 Glucagon-like peptide 1 receptor agonist Drugs 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 206010019280 Heart failures Diseases 0.000 description 1
- 206010019663 Hepatic failure Diseases 0.000 description 1
- 101000966782 Homo sapiens Lysophosphatidic acid receptor 1 Proteins 0.000 description 1
- 101001043352 Homo sapiens Lysyl oxidase homolog 2 Proteins 0.000 description 1
- 101001092910 Homo sapiens Serum amyloid P-component Proteins 0.000 description 1
- 241000243251 Hydra Species 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- 208000010159 IgA glomerulonephritis Diseases 0.000 description 1
- 206010021263 IgA nephropathy Diseases 0.000 description 1
- 102000008070 Interferon-gamma Human genes 0.000 description 1
- 108010074328 Interferon-gamma Proteins 0.000 description 1
- 208000002260 Keloid Diseases 0.000 description 1
- 206010023330 Keloid scar Diseases 0.000 description 1
- PWKSKIMOESPYIA-BYPYZUCNSA-N L-N-acetyl-Cysteine Chemical compound CC(=O)N[C@@H](CS)C(O)=O PWKSKIMOESPYIA-BYPYZUCNSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- 108010014552 LY2405319 Proteins 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 238000006633 Ley oxidation reaction Methods 0.000 description 1
- 229910010082 LiAlH Inorganic materials 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- 208000005777 Lupus Nephritis Diseases 0.000 description 1
- 208000031422 Lymphocytic Chronic B-Cell Leukemia Diseases 0.000 description 1
- 206010025323 Lymphomas Diseases 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 102000004137 Lysophosphatidic Acid Receptors Human genes 0.000 description 1
- 108090000642 Lysophosphatidic Acid Receptors Proteins 0.000 description 1
- 102100040607 Lysophosphatidic acid receptor 1 Human genes 0.000 description 1
- 102100021948 Lysyl oxidase homolog 2 Human genes 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 208000001145 Metabolic Syndrome Diseases 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- UCHDWCPVSPXUMX-TZIWLTJVSA-N Montelukast Chemical compound CC(C)(O)C1=CC=CC=C1CC[C@H](C=1C=C(\C=C\C=2N=C3C=C(Cl)C=CC3=CC=2)C=CC=1)SCC1(CC(O)=O)CC1 UCHDWCPVSPXUMX-TZIWLTJVSA-N 0.000 description 1
- 208000034578 Multiple myelomas Diseases 0.000 description 1
- 229940121948 Muscarinic receptor antagonist Drugs 0.000 description 1
- AYCPARAPKDAOEN-LJQANCHMSA-N N-[(1S)-2-(dimethylamino)-1-phenylethyl]-6,6-dimethyl-3-[(2-methyl-4-thieno[3,2-d]pyrimidinyl)amino]-1,4-dihydropyrrolo[3,4-c]pyrazole-5-carboxamide Chemical compound C1([C@H](NC(=O)N2C(C=3NN=C(NC=4C=5SC=CC=5N=C(C)N=4)C=3C2)(C)C)CN(C)C)=CC=CC=C1 AYCPARAPKDAOEN-LJQANCHMSA-N 0.000 description 1
- ZSNGMDJGTIYZCO-UHFFFAOYSA-N N-cyclopropyl-2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-fluoro-1,3-benzothiazole-6-carboxamide Chemical compound C1(CC1)NC(=O)C1=CC2=C(N=C(S2)N2CCC3(CC(=C3)C=3C(=NOC=3C3CC3)C3=C(C=NC=C3Cl)Cl)CC2)C(=C1)F ZSNGMDJGTIYZCO-UHFFFAOYSA-N 0.000 description 1
- GEIBJOVDVZOQQQ-UHFFFAOYSA-N N-cyclopropylsulfonyl-6-[2-[5-cyclopropyl-3-[2-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(difluoromethoxy)quinoline-2-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C=1C(=NC=CC=1)C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C1CC1)OC(F)F GEIBJOVDVZOQQQ-UHFFFAOYSA-N 0.000 description 1
- YKSJZAMESDEFAJ-UHFFFAOYSA-N N-cyclopropylsulfonyl-6-[2-[5-cyclopropyl-3-[4-(trifluoromethyl)pyridin-3-yl]-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-4-(difluoromethoxy)quinoline-2-carboxamide Chemical compound C1(CC1)C1=C(C(=NO1)C=1C=NC=CC=1C(F)(F)F)C1=CC2(C1)CCN(CC2)C=1C=C2C(=CC(=NC2=CC=1)C(=O)NS(=O)(=O)C1CC1)OC(F)F YKSJZAMESDEFAJ-UHFFFAOYSA-N 0.000 description 1
- 108010049175 N-substituted Glycines Proteins 0.000 description 1
- 108010082699 NADPH Oxidase 4 Proteins 0.000 description 1
- 102100021872 NADPH oxidase 4 Human genes 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- 208000000693 Neurogenic Urinary Bladder Diseases 0.000 description 1
- 206010029279 Neurogenic bladder Diseases 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- VYLOOGHLKSNNEK-PIIMJCKOSA-N OC(=O)c1cc(F)c2nc(sc2c1)N1[C@H]2CC[C@@H]1C[C@@H](C2)OCc1c(onc1-c1ccccc1OC(F)(F)F)C1CC1 Chemical compound OC(=O)c1cc(F)c2nc(sc2c1)N1[C@H]2CC[C@@H]1C[C@@H](C2)OCc1c(onc1-c1ccccc1OC(F)(F)F)C1CC1 VYLOOGHLKSNNEK-PIIMJCKOSA-N 0.000 description 1
- IDRGFNPZDVBSSE-UHFFFAOYSA-N OCCN1CCN(CC1)c1ccc(Nc2ncc3cccc(-c4cccc(NC(=O)C=C)c4)c3n2)c(F)c1F Chemical compound OCCN1CCN(CC1)c1ccc(Nc2ncc3cccc(-c4cccc(NC(=O)C=C)c4)c3n2)c(F)c1F IDRGFNPZDVBSSE-UHFFFAOYSA-N 0.000 description 1
- 208000012868 Overgrowth Diseases 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 108700027412 Pegbelfermin Proteins 0.000 description 1
- 229930182555 Penicillin Natural products 0.000 description 1
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 1
- 102000003728 Peroxisome Proliferator-Activated Receptors Human genes 0.000 description 1
- 108090000029 Peroxisome Proliferator-Activated Receptors Proteins 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 208000004403 Prostatic Hyperplasia Diseases 0.000 description 1
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- 229940127472 RNA Synthetase Inhibitors Drugs 0.000 description 1
- 208000032056 Radiation Fibrosis Syndrome Diseases 0.000 description 1
- 108091005682 Receptor kinases Proteins 0.000 description 1
- 108020004511 Recombinant DNA Proteins 0.000 description 1
- 208000001647 Renal Insufficiency Diseases 0.000 description 1
- 108091027981 Response element Proteins 0.000 description 1
- 206010039491 Sarcoma Diseases 0.000 description 1
- 206010039710 Scleroderma Diseases 0.000 description 1
- DLSWIYLPEUIQAV-UHFFFAOYSA-N Semaglutide Chemical compound CCC(C)C(NC(=O)C(Cc1ccccc1)NC(=O)C(CCC(O)=O)NC(=O)C(CCCCNC(=O)COCCOCCNC(=O)COCCOCCNC(=O)CCC(NC(=O)CCCCCCCCCCCCCCCCC(O)=O)C(O)=O)NC(=O)C(C)NC(=O)C(C)NC(=O)C(CCC(N)=O)NC(=O)CNC(=O)C(CCC(O)=O)NC(=O)C(CC(C)C)NC(=O)C(Cc1ccc(O)cc1)NC(=O)C(CO)NC(=O)C(CO)NC(=O)C(NC(=O)C(CC(O)=O)NC(=O)C(CO)NC(=O)C(NC(=O)C(Cc1ccccc1)NC(=O)C(NC(=O)CNC(=O)C(CCC(O)=O)NC(=O)C(C)(C)NC(=O)C(N)Cc1cnc[nH]1)C(C)O)C(C)O)C(C)C)C(=O)NC(C)C(=O)NC(Cc1c[nH]c2ccccc12)C(=O)NC(CC(C)C)C(=O)NC(C(C)C)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CCCNC(N)=N)C(=O)NCC(O)=O DLSWIYLPEUIQAV-UHFFFAOYSA-N 0.000 description 1
- GIIZNNXWQWCKIB-UHFFFAOYSA-N Serevent Chemical compound C1=C(O)C(CO)=CC(C(O)CNCCCCCCOCCCCC=2C=CC=CC=2)=C1 GIIZNNXWQWCKIB-UHFFFAOYSA-N 0.000 description 1
- 102100036202 Serum amyloid P-component Human genes 0.000 description 1
- 206010050207 Skin fibrosis Diseases 0.000 description 1
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 1
- 229940123518 Sodium/glucose cotransporter 2 inhibitor Drugs 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 238000006859 Swern oxidation reaction Methods 0.000 description 1
- 108091005735 TGF-beta receptors Proteins 0.000 description 1
- QJJXYPPXXYFBGM-LFZNUXCKSA-N Tacrolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1\C=C(/C)[C@@H]1[C@H](C)[C@@H](O)CC(=O)[C@H](CC=C)/C=C(C)/C[C@H](C)C[C@H](OC)[C@H]([C@H](C[C@H]2C)OC)O[C@@]2(O)C(=O)C(=O)N2CCCC[C@H]2C(=O)O1 QJJXYPPXXYFBGM-LFZNUXCKSA-N 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 1
- KPWYNAGOBXLMSE-UHFFFAOYSA-N Tipelukast Chemical compound CCCC1=C(O)C(C(C)=O)=CC=C1SCCCOC1=CC=C(C(C)=O)C(OCCCC(O)=O)=C1CCC KPWYNAGOBXLMSE-UHFFFAOYSA-N 0.000 description 1
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 1
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 1
- 102000016715 Transforming Growth Factor beta Receptors Human genes 0.000 description 1
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- OKJPEAGHQZHRQV-UHFFFAOYSA-N Triiodomethane Natural products IC(I)I OKJPEAGHQZHRQV-UHFFFAOYSA-N 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 238000006887 Ullmann reaction Methods 0.000 description 1
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 1
- 206010046798 Uterine leiomyoma Diseases 0.000 description 1
- 241000700605 Viruses Species 0.000 description 1
- 229910001115 Zinc-copper couple Inorganic materials 0.000 description 1
- QAVZYXJEQFVQRY-UHFFFAOYSA-N [1,3]thiazolo[5,4-b]pyridine-5-carboxylic acid Chemical compound OC(=O)C1=CC=C2N=CSC2=N1 QAVZYXJEQFVQRY-UHFFFAOYSA-N 0.000 description 1
- JSWQDLBFVSTSIW-UHFFFAOYSA-N [2-(trifluoromethyl)phenyl]hydrazine Chemical compound NNC1=CC=CC=C1C(F)(F)F JSWQDLBFVSTSIW-UHFFFAOYSA-N 0.000 description 1
- CKUAXEQHGKSLHN-UHFFFAOYSA-N [C].[N] Chemical group [C].[N] CKUAXEQHGKSLHN-UHFFFAOYSA-N 0.000 description 1
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 description 1
- 229950005008 abituzumab Drugs 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- 229940121373 acetyl-coa carboxylase inhibitor Drugs 0.000 description 1
- 229960004308 acetylcysteine Drugs 0.000 description 1
- 239000003377 acid catalyst Substances 0.000 description 1
- 125000000641 acridinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3C=C12)* 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 210000004100 adrenal gland Anatomy 0.000 description 1
- 239000000614 adrenergic beta-2 receptor agonist Substances 0.000 description 1
- NDAUXUAQIAJITI-UHFFFAOYSA-N albuterol Chemical compound CC(C)(C)NCC(O)C1=CC=C(O)C(CO)=C1 NDAUXUAQIAJITI-UHFFFAOYSA-N 0.000 description 1
- 230000001476 alcoholic effect Effects 0.000 description 1
- 208000026594 alcoholic fatty liver disease Diseases 0.000 description 1
- 229960000548 alemtuzumab Drugs 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 229910001413 alkali metal ion Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 229910001420 alkaline earth metal ion Inorganic materials 0.000 description 1
- 125000005236 alkanoylamino group Chemical group 0.000 description 1
- 150000003973 alkyl amines Chemical class 0.000 description 1
- 125000000278 alkyl amino alkyl group Chemical group 0.000 description 1
- 125000004457 alkyl amino carbonyl group Chemical group 0.000 description 1
- 125000003806 alkyl carbonyl amino group Chemical group 0.000 description 1
- 125000005196 alkyl carbonyloxy group Chemical group 0.000 description 1
- 150000005215 alkyl ethers Chemical class 0.000 description 1
- 230000029936 alkylation Effects 0.000 description 1
- HSFWRNGVRCDJHI-UHFFFAOYSA-N alpha-acetylene Natural products C#C HSFWRNGVRCDJHI-UHFFFAOYSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 235000001014 amino acid Nutrition 0.000 description 1
- 150000001413 amino acids Chemical class 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- SOIFLUNRINLCBN-UHFFFAOYSA-N ammonium thiocyanate Chemical compound [NH4+].[S-]C#N SOIFLUNRINLCBN-UHFFFAOYSA-N 0.000 description 1
- 150000001450 anions Chemical class 0.000 description 1
- 230000003042 antagnostic effect Effects 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 230000003510 anti-fibrotic effect Effects 0.000 description 1
- 229940124599 anti-inflammatory drug Drugs 0.000 description 1
- 239000003429 antifungal agent Substances 0.000 description 1
- 229940121375 antifungal agent Drugs 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000007900 aqueous suspension Substances 0.000 description 1
- 235000009697 arginine Nutrition 0.000 description 1
- 229910052786 argon Inorganic materials 0.000 description 1
- 125000005018 aryl alkenyl group Chemical group 0.000 description 1
- 125000004659 aryl alkyl thio group Chemical group 0.000 description 1
- 125000005100 aryl amino carbonyl group Chemical group 0.000 description 1
- 125000005199 aryl carbonyloxy group Chemical group 0.000 description 1
- 125000005160 aryl oxy alkyl group Chemical group 0.000 description 1
- 125000004657 aryl sulfonyl amino group Chemical group 0.000 description 1
- 125000005164 aryl thioalkyl group Chemical group 0.000 description 1
- 238000006254 arylation reaction Methods 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 229960003852 atezolizumab Drugs 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- 230000001580 bacterial effect Effects 0.000 description 1
- 230000007375 bacterial translocation Effects 0.000 description 1
- 210000004082 barrier epithelial cell Anatomy 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 125000004618 benzofuryl group Chemical group O1C(=CC2=C1C=CC=C2)* 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- 125000003354 benzotriazolyl group Chemical group N1N=NC2=C1C=CC=C2* 0.000 description 1
- KTLFENNEPHBKJD-UHFFFAOYSA-K benzyl(trimethyl)azanium;tribromide Chemical compound [Br-].[Br-].[Br-].C[N+](C)(C)CC1=CC=CC=C1.C[N+](C)(C)CC1=CC=CC=C1.C[N+](C)(C)CC1=CC=CC=C1 KTLFENNEPHBKJD-UHFFFAOYSA-K 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 210000000941 bile Anatomy 0.000 description 1
- 210000000013 bile duct Anatomy 0.000 description 1
- 210000003445 biliary tract Anatomy 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 239000012867 bioactive agent Substances 0.000 description 1
- SIPUZPBQZHNSDW-UHFFFAOYSA-N bis(2-methylpropyl)aluminum Chemical compound CC(C)C[Al]CC(C)C SIPUZPBQZHNSDW-UHFFFAOYSA-N 0.000 description 1
- 230000017531 blood circulation Effects 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 238000006664 bond formation reaction Methods 0.000 description 1
- 210000000988 bone and bone Anatomy 0.000 description 1
- 150000001642 boronic acid derivatives Chemical class 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 210000000481 breast Anatomy 0.000 description 1
- 230000031709 bromination Effects 0.000 description 1
- 238000005893 bromination reaction Methods 0.000 description 1
- 244000309464 bull Species 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 125000000480 butynyl group Chemical group [*]C#CC([H])([H])C([H])([H])[H] 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 208000035269 cancer or benign tumor Diseases 0.000 description 1
- 125000003917 carbamoyl group Chemical group [H]N([H])C(*)=O 0.000 description 1
- 125000004623 carbolinyl group Chemical group 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 230000009787 cardiac fibrosis Effects 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 229940124587 cephalosporin Drugs 0.000 description 1
- 150000001780 cephalosporins Chemical class 0.000 description 1
- 206010008118 cerebral infarction Diseases 0.000 description 1
- 208000026106 cerebrovascular disease Diseases 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- IBGLGMOPHJQDJB-IHRRRGAJSA-N chembl1950289 Chemical compound C1C[C@@H](O)CC[C@@H]1NC1=NC=C(N=C(NC=2C(=CC(F)=CC=2F)F)N2[C@@H]3COCC3)C2=N1 IBGLGMOPHJQDJB-IHRRRGAJSA-N 0.000 description 1
- 125000003636 chemical group Chemical group 0.000 description 1
- 239000013626 chemical specie Substances 0.000 description 1
- 230000035605 chemotaxis Effects 0.000 description 1
- FOCAUTSVDIKZOP-UHFFFAOYSA-N chloroacetic acid Chemical compound OC(=O)CCl FOCAUTSVDIKZOP-UHFFFAOYSA-N 0.000 description 1
- 229940106681 chloroacetic acid Drugs 0.000 description 1
- 208000006990 cholangiocarcinoma Diseases 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 125000004230 chromenyl group Chemical group O1C(C=CC2=CC=CC=C12)* 0.000 description 1
- 208000032852 chronic lymphocytic leukemia Diseases 0.000 description 1
- 235000015165 citric acid Nutrition 0.000 description 1
- 239000011248 coating agent Substances 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 238000002648 combination therapy Methods 0.000 description 1
- 239000000470 constituent Substances 0.000 description 1
- 230000001276 controlling effect Effects 0.000 description 1
- TVZPLCNGKSPOJA-UHFFFAOYSA-N copper zinc Chemical compound [Cu].[Zn] TVZPLCNGKSPOJA-UHFFFAOYSA-N 0.000 description 1
- YRNNKGFMTBWUGL-UHFFFAOYSA-L copper(ii) perchlorate Chemical compound [Cu+2].[O-]Cl(=O)(=O)=O.[O-]Cl(=O)(=O)=O YRNNKGFMTBWUGL-UHFFFAOYSA-L 0.000 description 1
- NHELIHXBJRANPL-UHFFFAOYSA-L copper;diperchlorate;hexahydrate Chemical compound O.O.O.O.O.O.[Cu+2].[O-]Cl(=O)(=O)=O.[O-]Cl(=O)(=O)=O NHELIHXBJRANPL-UHFFFAOYSA-L 0.000 description 1
- 239000003246 corticosteroid Substances 0.000 description 1
- 229960001334 corticosteroids Drugs 0.000 description 1
- 125000001316 cycloalkyl alkyl group Chemical group 0.000 description 1
- 125000001047 cyclobutenyl group Chemical group C1(=CCC1)* 0.000 description 1
- XSYZCZPCBXYQTE-UHFFFAOYSA-N cyclodecylcyclodecane Chemical compound C1CCCCCCCCC1C1CCCCCCCCC1 XSYZCZPCBXYQTE-UHFFFAOYSA-N 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- 125000000522 cyclooctenyl group Chemical group C1(=CCCCCCC1)* 0.000 description 1
- 125000002433 cyclopentenyl group Chemical group C1(=CCCC1)* 0.000 description 1
- AIMMVWOEOZMVMS-UHFFFAOYSA-N cyclopropanecarboxamide Chemical compound NC(=O)C1CC1 AIMMVWOEOZMVMS-UHFFFAOYSA-N 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 229960003834 dapagliflozin Drugs 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 125000004856 decahydroquinolinyl group Chemical group N1(CCCC2CCCCC12)* 0.000 description 1
- ACUZDYFTRHEKOS-UHFFFAOYSA-N decan-2-ol Chemical compound CCCCCCCCC(C)O ACUZDYFTRHEKOS-UHFFFAOYSA-N 0.000 description 1
- 230000007423 decrease Effects 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 230000007850 degeneration Effects 0.000 description 1
- 238000005695 dehalogenation reaction Methods 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- 230000002939 deleterious effect Effects 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 230000005595 deprotonation Effects 0.000 description 1
- 238000010537 deprotonation reaction Methods 0.000 description 1
- 239000002274 desiccant Substances 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 150000001991 dicarboxylic acids Chemical class 0.000 description 1
- 235000014113 dietary fatty acids Nutrition 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- 125000004177 diethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000001028 difluoromethyl group Chemical group [H]C(F)(F)* 0.000 description 1
- 102000038379 digestive enzymes Human genes 0.000 description 1
- 108091007734 digestive enzymes Proteins 0.000 description 1
- 238000005906 dihydroxylation reaction Methods 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- WJJMNDUMQPNECX-UHFFFAOYSA-N dipicolinic acid Chemical compound OC(=O)C1=CC=CC(C(O)=O)=N1 WJJMNDUMQPNECX-UHFFFAOYSA-N 0.000 description 1
- 230000006806 disease prevention Effects 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000009510 drug design Methods 0.000 description 1
- 238000009509 drug development Methods 0.000 description 1
- 238000007876 drug discovery Methods 0.000 description 1
- 201000008865 drug-induced hepatitis Diseases 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 230000004064 dysfunction Effects 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 230000013931 endocrine signaling Effects 0.000 description 1
- 210000004696 endometrium Anatomy 0.000 description 1
- 239000002308 endothelin receptor antagonist Substances 0.000 description 1
- DRKYTUDHOKREMS-UHFFFAOYSA-N ent 27,313 Chemical group ClC1=C(Cl)C2(Cl)C3CCC(Cl)C3C1(Cl)C2(Cl)Cl DRKYTUDHOKREMS-UHFFFAOYSA-N 0.000 description 1
- 239000002702 enteric coating Substances 0.000 description 1
- 238000009505 enteric coating Methods 0.000 description 1
- 230000004890 epithelial barrier function Effects 0.000 description 1
- 210000003238 esophagus Anatomy 0.000 description 1
- KTMGNAIGXYODKQ-VOTSOKGWSA-N ethyl (e)-2-cyano-3-ethoxyprop-2-enoate Chemical compound CCO\C=C(/C#N)C(=O)OCC KTMGNAIGXYODKQ-VOTSOKGWSA-N 0.000 description 1
- QFKXJOMCJPISBG-UHFFFAOYSA-N ethyl 2-(5-bromopyridin-2-yl)acetate Chemical compound CCOC(=O)CC1=CC=C(Br)C=N1 QFKXJOMCJPISBG-UHFFFAOYSA-N 0.000 description 1
- NGPPRFDHTRVGEK-UHFFFAOYSA-N ethyl 2-[3-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-1,4-dioxa-8-azaspiro[4.5]decan-8-yl]-4-fluoro-1,3-benzothiazole-6-carboxylate Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1OC2(OC1)CCN(CC2)C=1SC2=C(N=1)C(=CC(=C2)C(=O)OCC)F NGPPRFDHTRVGEK-UHFFFAOYSA-N 0.000 description 1
- UHDNIMBKAKKJPM-UHFFFAOYSA-N ethyl 2-amino-4-methoxybenzoate Chemical compound CCOC(=O)C1=CC=C(OC)C=C1N UHDNIMBKAKKJPM-UHFFFAOYSA-N 0.000 description 1
- JQZQKEZCRZNJPC-UHFFFAOYSA-N ethyl 2-bromo-1,3-benzothiazole-6-carboxylate Chemical compound CCOC(=O)C1=CC=C2N=C(Br)SC2=C1 JQZQKEZCRZNJPC-UHFFFAOYSA-N 0.000 description 1
- XISSCVMIXDMKLH-UHFFFAOYSA-N ethyl 2-chloro-1,3-benzothiazole-6-carboxylate Chemical compound CCOC(=O)C1=CC=C2N=C(Cl)SC2=C1 XISSCVMIXDMKLH-UHFFFAOYSA-N 0.000 description 1
- UDDSDBJYAMHCCW-UHFFFAOYSA-N ethyl 2-chloro-4-(trifluoromethyl)pyrimidine-5-carboxylate Chemical compound CCOC(=O)C1=CN=C(Cl)N=C1C(F)(F)F UDDSDBJYAMHCCW-UHFFFAOYSA-N 0.000 description 1
- CCCRTSRGFBFALE-UHFFFAOYSA-N ethyl 2-chloro-5-(trifluoromethyl)quinoline-7-carboxylate Chemical compound ClC1=NC2=CC(=CC(=C2C=C1)C(F)(F)F)C(=O)OCC CCCRTSRGFBFALE-UHFFFAOYSA-N 0.000 description 1
- QAUASTLEZAPQTB-UHFFFAOYSA-N ethyl 3-bromobenzoate Chemical group CCOC(=O)C1=CC=CC(Br)=C1 QAUASTLEZAPQTB-UHFFFAOYSA-N 0.000 description 1
- XZIAFENWXIQIKR-UHFFFAOYSA-N ethyl 4-bromobenzoate Chemical group CCOC(=O)C1=CC=C(Br)C=C1 XZIAFENWXIQIKR-UHFFFAOYSA-N 0.000 description 1
- BNAPMVMYMCOTEI-UHFFFAOYSA-N ethyl 6-bromo-4-methylquinoline-2-carboxylate Chemical compound C1=C(Br)C=CC2=NC(C(=O)OCC)=CC(C)=C21 BNAPMVMYMCOTEI-UHFFFAOYSA-N 0.000 description 1
- 239000002024 ethyl acetate extract Substances 0.000 description 1
- 235000010228 ethyl p-hydroxybenzoate Nutrition 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 230000005713 exacerbation Effects 0.000 description 1
- 239000000194 fatty acid Substances 0.000 description 1
- 229930195729 fatty acid Natural products 0.000 description 1
- 150000004665 fatty acids Chemical class 0.000 description 1
- 208000010706 fatty liver disease Diseases 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 229940126374 fipaxalparant Drugs 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- 125000001153 fluoro group Chemical group F* 0.000 description 1
- 125000004216 fluoromethyl group Chemical group [H]C([H])(F)* 0.000 description 1
- MGNNYOODZCAHBA-GQKYHHCASA-N fluticasone Chemical compound C1([C@@H](F)C2)=CC(=O)C=C[C@]1(C)[C@]1(F)[C@@H]2[C@@H]2C[C@@H](C)[C@@](C(=O)SCF)(O)[C@@]2(C)C[C@@H]1O MGNNYOODZCAHBA-GQKYHHCASA-N 0.000 description 1
- 229960002714 fluticasone Drugs 0.000 description 1
- 201000005206 focal segmental glomerulosclerosis Diseases 0.000 description 1
- 231100000854 focal segmental glomerulosclerosis Toxicity 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 238000001640 fractional crystallisation Methods 0.000 description 1
- 238000004108 freeze drying Methods 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 125000003838 furazanyl group Chemical group 0.000 description 1
- 239000007903 gelatin capsule Substances 0.000 description 1
- 210000004392 genitalia Anatomy 0.000 description 1
- 230000014101 glucose homeostasis Effects 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 125000004995 haloalkylthio group Chemical group 0.000 description 1
- LVASCWIMLIKXLA-LSDHHAIUSA-N halofuginone Chemical compound O[C@@H]1CCCN[C@H]1CC(=O)CN1C(=O)C2=CC(Cl)=C(Br)C=C2N=C1 LVASCWIMLIKXLA-LSDHHAIUSA-N 0.000 description 1
- 229950010152 halofuginone Drugs 0.000 description 1
- 125000001475 halogen functional group Chemical group 0.000 description 1
- 230000026030 halogenation Effects 0.000 description 1
- 238000005658 halogenation reaction Methods 0.000 description 1
- 210000003128 head Anatomy 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 210000003494 hepatocyte Anatomy 0.000 description 1
- 125000006343 heptafluoro propyl group Chemical group 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000004447 heteroarylalkenyl group Chemical group 0.000 description 1
- 125000005368 heteroarylthio group Chemical group 0.000 description 1
- 125000004366 heterocycloalkenyl group Chemical group 0.000 description 1
- 125000000592 heterocycloalkyl group Chemical group 0.000 description 1
- 239000000833 heterodimer Substances 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000005980 hexynyl group Chemical group 0.000 description 1
- 150000004677 hydrates Chemical class 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-M hydrogensulfate Chemical compound OS([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-M 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- 238000003384 imaging method Methods 0.000 description 1
- UTCSSFWDNNEEBH-UHFFFAOYSA-N imidazo[1,2-a]pyridine Chemical compound C1=CC=CC2=NC=CN21 UTCSSFWDNNEEBH-UHFFFAOYSA-N 0.000 description 1
- 125000002636 imidazolinyl group Chemical group 0.000 description 1
- 125000004857 imidazopyridinyl group Chemical group N1C(=NC2=C1C=CC=N2)* 0.000 description 1
- 229960003444 immunosuppressant agent Drugs 0.000 description 1
- 239000003018 immunosuppressive agent Substances 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 125000004926 indolenyl group Chemical group 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000008595 infiltration Effects 0.000 description 1
- 238000001764 infiltration Methods 0.000 description 1
- 210000004969 inflammatory cell Anatomy 0.000 description 1
- 230000004941 influx Effects 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 108010021309 integrin beta6 Proteins 0.000 description 1
- 108010044426 integrins Proteins 0.000 description 1
- 102000006495 integrins Human genes 0.000 description 1
- 229960003130 interferon gamma Drugs 0.000 description 1
- 210000004347 intestinal mucosa Anatomy 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 238000001990 intravenous administration Methods 0.000 description 1
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 1
- INQOMBQAUSQDDS-UHFFFAOYSA-N iodomethane Chemical compound IC INQOMBQAUSQDDS-UHFFFAOYSA-N 0.000 description 1
- 150000002500 ions Chemical class 0.000 description 1
- 229960005386 ipilimumab Drugs 0.000 description 1
- 229960001361 ipratropium bromide Drugs 0.000 description 1
- KEWHKYJURDBRMN-ZEODDXGYSA-M ipratropium bromide hydrate Chemical compound O.[Br-].O([C@H]1C[C@H]2CC[C@@H](C1)[N@@+]2(C)C(C)C)C(=O)C(CO)C1=CC=CC=C1 KEWHKYJURDBRMN-ZEODDXGYSA-M 0.000 description 1
- 230000007794 irritation Effects 0.000 description 1
- 125000004936 isatinoyl group Chemical group N1(C(=O)C(=O)C2=CC=CC=C12)C(=O)* 0.000 description 1
- 125000001977 isobenzofuranyl group Chemical group C=1(OC=C2C=CC=CC12)* 0.000 description 1
- 125000003384 isochromanyl group Chemical group C1(OCCC2=CC=CC=C12)* 0.000 description 1
- 125000004491 isohexyl group Chemical group C(CCC(C)C)* 0.000 description 1
- 125000005438 isoindazolyl group Chemical group 0.000 description 1
- 125000004594 isoindolinyl group Chemical group C1(NCC2=CC=CC=C12)* 0.000 description 1
- QRXWMOHMRWLFEY-UHFFFAOYSA-N isoniazide Chemical compound NNC(=O)C1=CC=NC=C1 QRXWMOHMRWLFEY-UHFFFAOYSA-N 0.000 description 1
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003253 isopropoxy group Chemical group [H]C([H])([H])C([H])(O*)C([H])([H])[H] 0.000 description 1
- JJWLVOIRVHMVIS-UHFFFAOYSA-N isopropylamine Chemical compound CC(C)N JJWLVOIRVHMVIS-UHFFFAOYSA-N 0.000 description 1
- 125000005956 isoquinolyl group Chemical group 0.000 description 1
- 210000001117 keloid Anatomy 0.000 description 1
- 208000011379 keloid formation Diseases 0.000 description 1
- 201000006370 kidney failure Diseases 0.000 description 1
- 230000003907 kidney function Effects 0.000 description 1
- 229940043355 kinase inhibitor Drugs 0.000 description 1
- 239000004310 lactic acid Substances 0.000 description 1
- 235000014655 lactic acid Nutrition 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 210000002429 large intestine Anatomy 0.000 description 1
- 206010023841 laryngeal neoplasm Diseases 0.000 description 1
- 229950002183 lebrikizumab Drugs 0.000 description 1
- 201000010260 leiomyoma Diseases 0.000 description 1
- 229940065725 leukotriene receptor antagonists for obstructive airway diseases Drugs 0.000 description 1
- 239000003199 leukotriene receptor blocking agent Substances 0.000 description 1
- 125000005647 linker group Chemical group 0.000 description 1
- 230000037356 lipid metabolism Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- YNESATAKKCNGOF-UHFFFAOYSA-N lithium bis(trimethylsilyl)amide Chemical compound [Li+].C[Si](C)(C)[N-][Si](C)(C)C YNESATAKKCNGOF-UHFFFAOYSA-N 0.000 description 1
- DLEDOFVPSDKWEF-UHFFFAOYSA-N lithium butane Chemical compound [Li+].CCC[CH2-] DLEDOFVPSDKWEF-UHFFFAOYSA-N 0.000 description 1
- 229910001416 lithium ion Inorganic materials 0.000 description 1
- 238000012317 liver biopsy Methods 0.000 description 1
- 230000005976 liver dysfunction Effects 0.000 description 1
- 231100000835 liver failure Toxicity 0.000 description 1
- 208000007903 liver failure Diseases 0.000 description 1
- 230000003908 liver function Effects 0.000 description 1
- 230000033001 locomotion Effects 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 238000003468 luciferase reporter gene assay Methods 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 235000018977 lysine Nutrition 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- MMIPFLVOWGHZQD-UHFFFAOYSA-N manganese(3+) Chemical compound [Mn+3] MMIPFLVOWGHZQD-UHFFFAOYSA-N 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 238000002483 medication Methods 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 208000030159 metabolic disease Diseases 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229910021645 metal ion Inorganic materials 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 description 1
- YMVXSWUSOFRJQK-UHFFFAOYSA-N methyl 2-[2-[5-cyclopropyl-3-(3,5-dichloropyridin-4-yl)-1,2-oxazol-4-yl]-7-azaspiro[3.5]non-2-en-7-yl]-[1,3]thiazolo[5,4-b]pyridine-5-carboxylate Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=NC=C1Cl)Cl)C1=CC2(C1)CCN(CC2)C=1SC2=NC(=CC=C2N=1)C(=O)OC YMVXSWUSOFRJQK-UHFFFAOYSA-N 0.000 description 1
- SEHSCLRSDPFRSB-UHFFFAOYSA-N methyl 2-amino-1,3-benzoxazole-5-carboxylate Chemical compound COC(=O)C1=CC=C2OC(N)=NC2=C1 SEHSCLRSDPFRSB-UHFFFAOYSA-N 0.000 description 1
- MOVBJUGHBJJKOW-UHFFFAOYSA-N methyl 2-amino-5-methoxybenzoate Chemical compound COC(=O)C1=CC(OC)=CC=C1N MOVBJUGHBJJKOW-UHFFFAOYSA-N 0.000 description 1
- ZBTAAEPRTBQKSF-UHFFFAOYSA-N methyl 2-bromo-1-methylbenzimidazole-5-carboxylate Chemical compound COC(=O)C1=CC=C2N(C)C(Br)=NC2=C1 ZBTAAEPRTBQKSF-UHFFFAOYSA-N 0.000 description 1
- YKSROYWRMVHXCA-UHFFFAOYSA-N methyl 2-bromo-4-(trifluoromethoxy)-1,3-benzothiazole-6-carboxylate Chemical compound COC(=O)C1=CC(OC(F)(F)F)=C2N=C(Br)SC2=C1 YKSROYWRMVHXCA-UHFFFAOYSA-N 0.000 description 1
- XSEAGAYSAHNOQI-UHFFFAOYSA-N methyl 2-bromo-4-methyl-1,3-benzothiazole-6-carboxylate Chemical compound COC(=O)C1=CC(C)=C2N=C(Br)SC2=C1 XSEAGAYSAHNOQI-UHFFFAOYSA-N 0.000 description 1
- SHGGYZPEYZOZRZ-UHFFFAOYSA-N methyl 2-bromo-6-methoxy-1,3-benzothiazole-4-carboxylate Chemical compound BrC=1SC=2C(N=1)=C(C=C(C=2)OC)C(=O)OC SHGGYZPEYZOZRZ-UHFFFAOYSA-N 0.000 description 1
- ZZMHBFGSQVJSER-UHFFFAOYSA-N methyl 2-chloro-1,3-benzoxazole-6-carboxylate Chemical compound COC(=O)C1=CC=C2N=C(Cl)OC2=C1 ZZMHBFGSQVJSER-UHFFFAOYSA-N 0.000 description 1
- BOLDVAFZLUCRKJ-UHFFFAOYSA-N methyl 2-chloro-4-methyl-1,3-benzothiazole-6-carboxylate Chemical compound COC(=O)C1=CC(C)=C2N=C(Cl)SC2=C1 BOLDVAFZLUCRKJ-UHFFFAOYSA-N 0.000 description 1
- ZNPORLVPCMFKOR-UHFFFAOYSA-N methyl 2-chloro-6-methylpyrimidine-4-carboxylate Chemical compound COC(=O)C1=CC(C)=NC(Cl)=N1 ZNPORLVPCMFKOR-UHFFFAOYSA-N 0.000 description 1
- VJOKXLBQCKCWLV-UHFFFAOYSA-N methyl 2-chloropyrimidine-5-carboxylate Chemical compound COC(=O)C1=CN=C(Cl)N=C1 VJOKXLBQCKCWLV-UHFFFAOYSA-N 0.000 description 1
- KDYIUQAXLBVZEE-UHFFFAOYSA-N methyl 2-chloroquinoline-5-carboxylate Chemical group ClC1=CC=C2C(C(=O)OC)=CC=CC2=N1 KDYIUQAXLBVZEE-UHFFFAOYSA-N 0.000 description 1
- UOUBEKSUNCCLDY-UHFFFAOYSA-N methyl 2-chloroquinoline-6-carboxylate Chemical compound N1=C(Cl)C=CC2=CC(C(=O)OC)=CC=C21 UOUBEKSUNCCLDY-UHFFFAOYSA-N 0.000 description 1
- YUHSMQQNPRLEEJ-UHFFFAOYSA-N methyl 3-(bromomethyl)benzoate Chemical compound COC(=O)C1=CC=CC(CBr)=C1 YUHSMQQNPRLEEJ-UHFFFAOYSA-N 0.000 description 1
- SUNUGKUYIMWNOI-UHFFFAOYSA-N methyl 3-[2-[5-cyclopropyl-3-(2,6-dichlorophenyl)-1,2-oxazol-4-yl]-2-hydroxyspiro[3.5]nonan-7-yl]oxybenzoate Chemical compound C1(CC1)C1=C(C(=NO1)C1=C(C=CC=C1Cl)Cl)C1(CC2(C1)CCC(CC2)OC=1C=C(C(=O)OC)C=CC=1)O SUNUGKUYIMWNOI-UHFFFAOYSA-N 0.000 description 1
- RIJWDPRXCXJDPK-UHFFFAOYSA-N methyl 3-cyclopropyl-3-oxopropanoate Chemical compound COC(=O)CC(=O)C1CC1 RIJWDPRXCXJDPK-UHFFFAOYSA-N 0.000 description 1
- JEURNBCYNWNADN-UHFFFAOYSA-N methyl 5-bromopyridine-2-carboxylate Chemical group COC(=O)C1=CC=C(Br)C=N1 JEURNBCYNWNADN-UHFFFAOYSA-N 0.000 description 1
- XILAKTMDKMVJQV-UHFFFAOYSA-N methyl 5-bromopyrimidine-2-carboxylate Chemical compound COC(=O)C1=NC=C(Br)C=N1 XILAKTMDKMVJQV-UHFFFAOYSA-N 0.000 description 1
- RCDWEKOOOHATJC-UHFFFAOYSA-N methyl 6-bromo-1-methylindole-2-carboxylate Chemical group C1=C(Br)C=C2N(C)C(C(=O)OC)=CC2=C1 RCDWEKOOOHATJC-UHFFFAOYSA-N 0.000 description 1
- RLMWPNDSVWJWHA-UHFFFAOYSA-N methyl 6-bromo-1-methylindole-3-carboxylate Chemical group BrC1=CC=C2C(C(=O)OC)=CN(C)C2=C1 RLMWPNDSVWJWHA-UHFFFAOYSA-N 0.000 description 1
- IBUVANPFSYRKJV-UHFFFAOYSA-N methyl 6-bromo-3-methylimidazo[1,5-a]pyridine-1-carboxylate Chemical compound COC(=O)c1nc(C)n2cc(Br)ccc12 IBUVANPFSYRKJV-UHFFFAOYSA-N 0.000 description 1
- YTGMHMBVKBJVLL-UHFFFAOYSA-N methyl 6-bromo-4-propan-2-yloxyquinoline-2-carboxylate Chemical compound COC(=O)c1cc(OC(C)C)c2cc(Br)ccc2n1 YTGMHMBVKBJVLL-UHFFFAOYSA-N 0.000 description 1
- BBXGEZRYRMLKTJ-UHFFFAOYSA-N methyl 6-chloro-2-methylpyridine-3-carboxylate Chemical compound COC(=O)C1=CC=C(Cl)N=C1C BBXGEZRYRMLKTJ-UHFFFAOYSA-N 0.000 description 1
- CFJDLJIDLYBQQY-UHFFFAOYSA-N methyl 6-chloro-4-(trifluoromethyl)pyridine-3-carboxylate Chemical compound COC(=O)C1=CN=C(Cl)C=C1C(F)(F)F CFJDLJIDLYBQQY-UHFFFAOYSA-N 0.000 description 1
- CRTSQMSTPZTUDW-UHFFFAOYSA-N methyl 6-chloro-4-methoxypyridine-3-carboxylate Chemical compound COC(=O)C1=CN=C(Cl)C=C1OC CRTSQMSTPZTUDW-UHFFFAOYSA-N 0.000 description 1
- ZAXVCGWNLQTDRU-UHFFFAOYSA-N methyl 6-fluoro-4-methylpyridine-3-carboxylate Chemical compound COC(=O)c1cnc(F)cc1C ZAXVCGWNLQTDRU-UHFFFAOYSA-N 0.000 description 1
- ALCBYUWDBOVTGN-UHFFFAOYSA-N methyl 6-fluoro-5-methylpyridine-3-carboxylate Chemical compound COC(=O)C1=CN=C(F)C(C)=C1 ALCBYUWDBOVTGN-UHFFFAOYSA-N 0.000 description 1
- SKPXRQNAFGKDDC-UHFFFAOYSA-N methyl 7-bromo-8-methylquinoline-3-carboxylate Chemical compound BrC1=CC=C2C=C(C=NC2=C1C)C(=O)OC SKPXRQNAFGKDDC-UHFFFAOYSA-N 0.000 description 1
- 244000005706 microflora Species 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 229960005127 montelukast Drugs 0.000 description 1
- 210000002200 mouth mucosa Anatomy 0.000 description 1
- 230000004682 mucosal barrier function Effects 0.000 description 1
- 210000004400 mucous membrane Anatomy 0.000 description 1
- 239000003149 muscarinic antagonist Substances 0.000 description 1
- 210000003205 muscle Anatomy 0.000 description 1
- 206010028537 myelofibrosis Diseases 0.000 description 1
- ZUHZZVMEUAUWHY-UHFFFAOYSA-N n,n-dimethylpropan-1-amine Chemical compound CCCN(C)C ZUHZZVMEUAUWHY-UHFFFAOYSA-N 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000000740 n-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000003506 n-propoxy group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])O* 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 125000004923 naphthylmethyl group Chemical group C1(=CC=CC2=CC=CC=C12)C* 0.000 description 1
- 125000004593 naphthyridinyl group Chemical group N1=C(C=CC2=CC=CN=C12)* 0.000 description 1
- 210000003928 nasal cavity Anatomy 0.000 description 1
- 230000001338 necrotic effect Effects 0.000 description 1
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 208000004296 neuralgia Diseases 0.000 description 1
- 208000021722 neuropathic pain Diseases 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 125000000627 niacin group Chemical group 0.000 description 1
- 229910052759 nickel Inorganic materials 0.000 description 1
- PVNIIMVLHYAWGP-UHFFFAOYSA-M nicotinate Chemical compound [O-]C(=O)C1=CC=CN=C1 PVNIIMVLHYAWGP-UHFFFAOYSA-M 0.000 description 1
- 229960003301 nivolumab Drugs 0.000 description 1
- 125000006574 non-aromatic ring group Chemical group 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 1
- 108020004017 nuclear receptors Proteins 0.000 description 1
- 102000027507 nuclear receptors type II Human genes 0.000 description 1
- 108091008686 nuclear receptors type II Proteins 0.000 description 1
- 239000002773 nucleotide Substances 0.000 description 1
- 125000003729 nucleotide group Chemical group 0.000 description 1
- ZXERDUOLZKYMJM-ZWECCWDJSA-N obeticholic acid Chemical compound C([C@@]12C)C[C@@H](O)C[C@H]1[C@@H](CC)[C@@H](O)[C@@H]1[C@@H]2CC[C@]2(C)[C@@H]([C@H](C)CCC(O)=O)CC[C@H]21 ZXERDUOLZKYMJM-ZWECCWDJSA-N 0.000 description 1
- 229960001601 obeticholic acid Drugs 0.000 description 1
- 230000000414 obstructive effect Effects 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000002674 ointment Substances 0.000 description 1
- 229920001542 oligosaccharide Polymers 0.000 description 1
- 150000002482 oligosaccharides Chemical class 0.000 description 1
- ACSQLTBPYZSGBA-GMXVVIOVSA-N olorinab Chemical compound C([C@@H]1C[C@@H]1C=12)C=1C(C(=O)N[C@H](CO)C(C)(C)C)=NN2C1=C[N+]([O-])=CC=N1 ACSQLTBPYZSGBA-GMXVVIOVSA-N 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 239000007935 oral tablet Substances 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 239000012074 organic phase Substances 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 229910000489 osmium tetroxide Inorganic materials 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 125000003566 oxetanyl group Chemical group 0.000 description 1
- 239000007800 oxidant agent Substances 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 230000001590 oxidative effect Effects 0.000 description 1
- 150000002923 oximes Chemical class 0.000 description 1
- LXNAVEXFUKBNMK-UHFFFAOYSA-N palladium(II) acetate Substances [Pd].CC(O)=O.CC(O)=O LXNAVEXFUKBNMK-UHFFFAOYSA-N 0.000 description 1
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- WYMSBXTXOHUIGT-UHFFFAOYSA-N paraoxon Chemical compound CCOP(=O)(OCC)OC1=CC=C([N+]([O-])=O)C=C1 WYMSBXTXOHUIGT-UHFFFAOYSA-N 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 229940049954 penicillin Drugs 0.000 description 1
- 125000006340 pentafluoro ethyl group Chemical group FC(F)(F)C(F)(F)* 0.000 description 1
- 125000005981 pentynyl group Chemical group 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 208000033808 peripheral neuropathy Diseases 0.000 description 1
- 239000008024 pharmaceutical diluent Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 230000003285 pharmacodynamic effect Effects 0.000 description 1
- 230000006611 pharmacological activation Effects 0.000 description 1
- 125000004625 phenanthrolinyl group Chemical group N1=C(C=CC2=CC=C3C=CC=NC3=C12)* 0.000 description 1
- 125000001791 phenazinyl group Chemical group C1(=CC=CC2=NC3=CC=CC=C3N=C12)* 0.000 description 1
- 125000001484 phenothiazinyl group Chemical group C1(=CC=CC=2SC3=CC=CC=C3NC12)* 0.000 description 1
- 125000001644 phenoxazinyl group Chemical group C1(=CC=CC=2OC3=CC=CC=C3NC12)* 0.000 description 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- RLOWWWKZYUNIDI-UHFFFAOYSA-N phosphinic chloride Chemical compound ClP=O RLOWWWKZYUNIDI-UHFFFAOYSA-N 0.000 description 1
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 1
- 125000004592 phthalazinyl group Chemical group C1(=NN=CC2=CC=CC=C12)* 0.000 description 1
- 125000001557 phthalyl group Chemical group C(=O)(O)C1=C(C(=O)*)C=CC=C1 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 229940081066 picolinic acid Drugs 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- KASDHRXLYQOAKZ-ZPSXYTITSA-N pimecrolimus Chemical compound C/C([C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@]2(O)O[C@@H]([C@H](C[C@H]2C)OC)[C@@H](OC)C[C@@H](C)C/C(C)=C/[C@H](C(C[C@H](O)[C@H]1C)=O)CC)=C\[C@@H]1CC[C@@H](Cl)[C@H](OC)C1 KASDHRXLYQOAKZ-ZPSXYTITSA-N 0.000 description 1
- 229960005330 pimecrolimus Drugs 0.000 description 1
- 229960005095 pioglitazone Drugs 0.000 description 1
- 229960005235 piperonyl butoxide Drugs 0.000 description 1
- 125000004591 piperonyl group Chemical group C(C1=CC=2OCOC2C=C1)* 0.000 description 1
- LYKMMUBOEFYJQG-UHFFFAOYSA-N piperoxan Chemical compound C1OC2=CC=CC=C2OC1CN1CCCCC1 LYKMMUBOEFYJQG-UHFFFAOYSA-N 0.000 description 1
- 229960003073 pirfenidone Drugs 0.000 description 1
- ISWRGOKTTBVCFA-UHFFFAOYSA-N pirfenidone Chemical compound C1=C(C)C=CC(=O)N1C1=CC=CC=C1 ISWRGOKTTBVCFA-UHFFFAOYSA-N 0.000 description 1
- 125000006684 polyhaloalkyl group Polymers 0.000 description 1
- 150000004033 porphyrin derivatives Chemical class 0.000 description 1
- 208000007232 portal hypertension Diseases 0.000 description 1
- 235000011056 potassium acetate Nutrition 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- 230000035755 proliferation Effects 0.000 description 1
- 108010042589 prolyl T RNA synthetase Proteins 0.000 description 1
- 125000002568 propynyl group Chemical group [*]C#CC([H])([H])[H] 0.000 description 1
- 210000002307 prostate Anatomy 0.000 description 1
- 235000018102 proteins Nutrition 0.000 description 1
- 125000001042 pteridinyl group Chemical group N1=C(N=CC2=NC=CN=C12)* 0.000 description 1
- 208000005069 pulmonary fibrosis Diseases 0.000 description 1
- 125000004309 pyranyl group Chemical group O1C(C=CC=C1)* 0.000 description 1
- 125000003072 pyrazolidinyl group Chemical group 0.000 description 1
- 125000002755 pyrazolinyl group Chemical group 0.000 description 1
- 125000001422 pyrrolinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- UBDIMPWXBMWVTC-UHFFFAOYSA-N quinoline-2-carboxylic acid Chemical compound C1=CC=CC2=NC(C(=O)O)=CC=C21.C1=CC=CC2=NC(C(=O)O)=CC=C21 UBDIMPWXBMWVTC-UHFFFAOYSA-N 0.000 description 1
- RAYMXZBXQCGRGX-UHFFFAOYSA-N quinoline-5-carboxylic acid Chemical compound C1=CC=C2C(C(=O)O)=CC=CC2=N1 RAYMXZBXQCGRGX-UHFFFAOYSA-N 0.000 description 1
- 125000005493 quinolyl group Chemical group 0.000 description 1
- 125000004262 quinoxalin-2-yl group Chemical group [H]C1=NC2=C([H])C([H])=C([H])C([H])=C2N=C1* 0.000 description 1
- 125000004621 quinuclidinyl group Chemical group N12C(CC(CC1)CC2)* 0.000 description 1
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 description 1
- 230000007420 reactivation Effects 0.000 description 1
- 229940044551 receptor antagonist Drugs 0.000 description 1
- 239000002464 receptor antagonist Substances 0.000 description 1
- 231100000272 reduced body weight Toxicity 0.000 description 1
- 230000009467 reduction Effects 0.000 description 1
- 238000006722 reduction reaction Methods 0.000 description 1
- 238000005932 reductive alkylation reaction Methods 0.000 description 1
- 238000006268 reductive amination reaction Methods 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 208000023504 respiratory system disease Diseases 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 229960004641 rituximab Drugs 0.000 description 1
- 238000011808 rodent model Methods 0.000 description 1
- 229960002052 salbutamol Drugs 0.000 description 1
- 229960004017 salmeterol Drugs 0.000 description 1
- MRWFZSLZNUJVQW-DEOSSOPVSA-N saroglitazar Chemical compound C1=CC(C[C@H](OCC)C(O)=O)=CC=C1OCCN1C(C=2C=CC(SC)=CC=2)=CC=C1C MRWFZSLZNUJVQW-DEOSSOPVSA-N 0.000 description 1
- 229950006544 saroglitazar Drugs 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- XIIOFHFUYBLOLW-UHFFFAOYSA-N selpercatinib Chemical compound OC(COC=1C=C(C=2N(C=1)N=CC=2C#N)C=1C=NC(=CC=1)N1CC2N(C(C1)C2)CC=1C=NC(=CC=1)OC)(C)C XIIOFHFUYBLOLW-UHFFFAOYSA-N 0.000 description 1
- 229950011186 semaglutide Drugs 0.000 description 1
- 108010060325 semaglutide Proteins 0.000 description 1
- 239000008299 semisolid dosage form Substances 0.000 description 1
- 210000002966 serum Anatomy 0.000 description 1
- RGYQPQARIQKJKH-UHFFFAOYSA-N setanaxib Chemical compound CN(C)C1=CC=CC(C2=C3C(=O)N(C=4C(=CC=CC=4)Cl)NC3=CC(=O)N2C)=C1 RGYQPQARIQKJKH-UHFFFAOYSA-N 0.000 description 1
- 229960003310 sildenafil Drugs 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- 229950009513 simtuzumab Drugs 0.000 description 1
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 description 1
- 229960002930 sirolimus Drugs 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- WRIKHQLVHPKCJU-UHFFFAOYSA-N sodium bis(trimethylsilyl)amide Chemical compound C[Si](C)(C)N([Na])[Si](C)(C)C WRIKHQLVHPKCJU-UHFFFAOYSA-N 0.000 description 1
- 239000012312 sodium hydride Substances 0.000 description 1
- 229910000104 sodium hydride Inorganic materials 0.000 description 1
- JEZLFWXSKCTMPN-ILCIQDJASA-M sodium;2-[(2s,3r,4e,6e,10e,12s)-13-(4-fluorophenoxy)-2,3,12-trihydroxytrideca-4,6,10-trien-8-ynoxy]acetate Chemical compound [Na+].[O-]C(=O)COC[C@H](O)[C@H](O)/C=C/C=C/C#C/C=C/[C@H](O)COC1=CC=C(F)C=C1 JEZLFWXSKCTMPN-ILCIQDJASA-M 0.000 description 1
- MRTAVLDNYYEJHK-UHFFFAOYSA-M sodium;2-chloro-2,2-difluoroacetate Chemical compound [Na+].[O-]C(=O)C(F)(F)Cl MRTAVLDNYYEJHK-UHFFFAOYSA-M 0.000 description 1
- 239000007909 solid dosage form Substances 0.000 description 1
- 238000007614 solvation Methods 0.000 description 1
- 230000003595 spectral effect Effects 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 206010062261 spinal cord neoplasm Diseases 0.000 description 1
- 208000005198 spinal stenosis Diseases 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 239000007921 spray Substances 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 230000000087 stabilizing effect Effects 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 239000012258 stirred mixture Substances 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 125000000446 sulfanediyl group Chemical group *S* 0.000 description 1
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 150000003468 sulfuric acid diamides Chemical class 0.000 description 1
- YBBRCQOCSYXUOC-UHFFFAOYSA-N sulfuryl dichloride Chemical compound ClS(Cl)(=O)=O YBBRCQOCSYXUOC-UHFFFAOYSA-N 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 1
- 239000003826 tablet Substances 0.000 description 1
- 239000002466 tachykinin receptor agonist Substances 0.000 description 1
- 229960001967 tacrolimus Drugs 0.000 description 1
- QJJXYPPXXYFBGM-SHYZHZOCSA-N tacrolimus Natural products CO[C@H]1C[C@H](CC[C@@H]1O)C=C(C)[C@H]2OC(=O)[C@H]3CCCCN3C(=O)C(=O)[C@@]4(O)O[C@@H]([C@H](C[C@H]4C)OC)[C@@H](C[C@H](C)CC(=C[C@@H](CC=C)C(=O)C[C@H](O)[C@H]2C)C)OC QJJXYPPXXYFBGM-SHYZHZOCSA-N 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- KSXZBUYSCNIFKW-UHFFFAOYSA-N tert-butyl 2-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)-7-azaspiro[3.5]non-2-ene-7-carboxylate Chemical compound CC1(OB(OC1(C)C)C1=CC2(C1)CCN(CC2)C(=O)OC(C)(C)C)C KSXZBUYSCNIFKW-UHFFFAOYSA-N 0.000 description 1
- APXVQWZQBPJTLO-UHFFFAOYSA-N tert-butyl 2-[4-ethoxycarbonyl-2-[2-(trifluoromethyl)phenyl]pyrazol-3-yl]-7-azaspiro[3.5]non-2-ene-7-carboxylate Chemical compound C(C)OC(=O)C=1C=NN(C=1C1=CC2(C1)CCN(CC2)C(=O)OC(C)(C)C)C1=C(C=CC=C1)C(F)(F)F APXVQWZQBPJTLO-UHFFFAOYSA-N 0.000 description 1
- BNWCETAHAJSBFG-UHFFFAOYSA-N tert-butyl 2-bromoacetate Chemical compound CC(C)(C)OC(=O)CBr BNWCETAHAJSBFG-UHFFFAOYSA-N 0.000 description 1
- ZYNYREKPRWPYDC-UHFFFAOYSA-N tert-butyl 3-methylidene-8-azabicyclo[3.2.1]octane-8-carboxylate Chemical compound C1C(=C)CC2CCC1N2C(=O)OC(C)(C)C ZYNYREKPRWPYDC-UHFFFAOYSA-N 0.000 description 1
- HQHRAGXKFOTSQE-UHFFFAOYSA-N tert-butyl 6-oxo-2-azaspiro[3.3]heptane-2-carboxylate Chemical compound C1N(C(=O)OC(C)(C)C)CC21CC(=O)C2 HQHRAGXKFOTSQE-UHFFFAOYSA-N 0.000 description 1
- BCNZYOJHNLTNEZ-UHFFFAOYSA-N tert-butyldimethylsilyl chloride Chemical compound CC(C)(C)[Si](C)(C)Cl BCNZYOJHNLTNEZ-UHFFFAOYSA-N 0.000 description 1
- 210000001550 testis Anatomy 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 125000001412 tetrahydropyranyl group Chemical group 0.000 description 1
- CZDYPVPMEAXLPK-UHFFFAOYSA-N tetramethylsilane Chemical compound C[Si](C)(C)C CZDYPVPMEAXLPK-UHFFFAOYSA-N 0.000 description 1
- 125000004627 thianthrenyl group Chemical group C1(=CC=CC=2SC3=CC=CC=C3SC12)* 0.000 description 1
- 125000005309 thioalkoxy group Chemical group 0.000 description 1
- 125000004001 thioalkyl group Chemical group 0.000 description 1
- 125000005403 thiohaloalkoxy group Chemical group 0.000 description 1
- BRNULMACUQOKMR-UHFFFAOYSA-N thiomorpholine Chemical compound C1CSCCN1 BRNULMACUQOKMR-UHFFFAOYSA-N 0.000 description 1
- 210000001685 thyroid gland Anatomy 0.000 description 1
- 229950004996 tipelukast Drugs 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 229950000835 tralokinumab Drugs 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 238000012250 transgenic expression Methods 0.000 description 1
- 230000001052 transient effect Effects 0.000 description 1
- 229910052723 transition metal Inorganic materials 0.000 description 1
- 150000003624 transition metals Chemical class 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 229960005294 triamcinolone Drugs 0.000 description 1
- GFNANZIMVAIWHM-OBYCQNJPSA-N triamcinolone Chemical compound O=C1C=C[C@]2(C)[C@@]3(F)[C@@H](O)C[C@](C)([C@@]([C@H](O)C4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 GFNANZIMVAIWHM-OBYCQNJPSA-N 0.000 description 1
- DLMDGLJCWXETIS-UHFFFAOYSA-N triazine-5-carboxylic acid Chemical compound OC(=O)C1=CN=NN=C1 DLMDGLJCWXETIS-UHFFFAOYSA-N 0.000 description 1
- IMFACGCPASFAPR-UHFFFAOYSA-N tributylamine Chemical group CCCCN(CCCC)CCCC IMFACGCPASFAPR-UHFFFAOYSA-N 0.000 description 1
- PVFOMCVHYWHZJE-UHFFFAOYSA-N trichloroacetyl chloride Chemical compound ClC(=O)C(Cl)(Cl)Cl PVFOMCVHYWHZJE-UHFFFAOYSA-N 0.000 description 1
- 125000003866 trichloromethyl group Chemical group ClC(Cl)(Cl)* 0.000 description 1
- 150000008648 triflates Chemical class 0.000 description 1
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 description 1
- COIOYMYWGDAQPM-UHFFFAOYSA-N tris(2-methylphenyl)phosphane Chemical compound CC1=CC=CC=C1P(C=1C(=CC=CC=1)C)C1=CC=CC=C1C COIOYMYWGDAQPM-UHFFFAOYSA-N 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- 230000004614 tumor growth Effects 0.000 description 1
- 125000002948 undecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 210000003932 urinary bladder Anatomy 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 239000003981 vehicle Substances 0.000 description 1
- PXXNTAGJWPJAGM-UHFFFAOYSA-N vertaline Natural products C1C2C=3C=C(OC)C(OC)=CC=3OC(C=C3)=CC=C3CCC(=O)OC1CC1N2CCCC1 PXXNTAGJWPJAGM-UHFFFAOYSA-N 0.000 description 1
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 230000029663 wound healing Effects 0.000 description 1
- 125000001834 xanthenyl group Chemical group C1=CC=CC=2OC3=CC=CC=C3C(C12)* 0.000 description 1
- REQQVBGILUTQNN-UHFFFAOYSA-N ziritaxestat Chemical compound CCC=1N=C2C(C)=CC(N3CCN(CC(=O)N4CC(O)C4)CC3)=CN2C=1N(C)C(SC=1C#N)=NC=1C1=CC=C(F)C=C1 REQQVBGILUTQNN-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing three or more hetero rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/42—Oxazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/428—Thiazoles condensed with carbocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/429—Thiazoles condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4523—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems
- A61K31/454—Non condensed piperidines, e.g. piperocaine containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. pimozide, domperidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4709—Non-condensed quinolines and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/498—Pyrazines or piperazines ortho- and peri-condensed with carbocyclic ring systems, e.g. quinoxaline, phenazine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/50—Pyridazines; Hydrogenated pyridazines
- A61K31/502—Pyridazines; Hydrogenated pyridazines ortho- or peri-condensed with carbocyclic ring systems, e.g. cinnoline, phthalazine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D261/00—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings
- C07D261/02—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings not condensed with other rings
- C07D261/06—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings not condensed with other rings having two or more double bonds between ring members or between ring members and non-ring members
- C07D261/08—Heterocyclic compounds containing 1,2-oxazole or hydrogenated 1,2-oxazole rings not condensed with other rings having two or more double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D263/00—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings
- C07D263/02—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings
- C07D263/30—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members
- C07D263/32—Heterocyclic compounds containing 1,3-oxazole or hydrogenated 1,3-oxazole rings not condensed with other rings having two or three double bonds between ring members or between ring members and non-ring members with only hydrogen atoms, hydrocarbon or substituted hydrocarbon radicals, directly attached to ring carbon atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/08—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a carbon chain containing alicyclic rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/14—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing three or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D417/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00
- C07D417/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings
- C07D417/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for by group C07D415/00 containing two hetero rings linked by a chain containing hetero atoms as chain links
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D487/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00
- C07D487/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, not provided for by groups C07D451/00 - C07D477/00 in which the condensed system contains two hetero rings
- C07D487/10—Spiro-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/10—Spiro-condensed systems
- C07D491/107—Spiro-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/10—Spiro-condensed systems
- C07D491/113—Spiro-condensed systems with two or more oxygen atoms as ring hetero atoms in the oxygen-containing ring
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/12—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains three hetero rings
- C07D491/20—Spiro-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D513/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00
- C07D513/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00 in which the condensed system contains two hetero rings
- C07D513/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H15/00—Compounds containing hydrocarbon or substituted hydrocarbon radicals directly attached to hetero atoms of saccharide radicals
- C07H15/26—Acyclic or carbocyclic radicals, substituted by hetero rings
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Urology & Nephrology (AREA)
- Rheumatology (AREA)
- Pain & Pain Management (AREA)
- Pulmonology (AREA)
- Gastroenterology & Hepatology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
Abstract
본 발명은 화학식 (I)의 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물을 제공하며, 여기서 모든 가변기는 본원에 정의된 바와 같다. 이들 화합물은, 예를 들어 효능제로서 파르네소이드 X 수용체 (FXR)의 활성을 조정한다. 본 발명은 또한 이들 화합물을 포함하는 제약 조성물, 및 화합물 및 제약 조성물을 사용하여 FXR 조절이상과 연관된 질환, 장애 또는 상태, 예컨대 병리학적 섬유증, 이식 거부, 암, 골다공증 및 염증성 장애를 치료하는 방법에 관한 것이다.
Description
상호 참조
본 출원은 2017년 11월 1일에 출원된 미국 가출원 일련 번호 62/580068을 우선권 주장하며, 상기 가출원은 그 전문이 본원에 참조로 포함된다.
본 발명은 일반적으로 파르네소이드 X 수용체 (FXR) 조정제로서 유용한 화합물, 이러한 화합물을 포함하는 제약 조성물, 및 요법에서, 특히 FXR 조정제가 지시되는 질환, 장애 및 상태의 치료 또는 예방에서의 그의 용도에 관한 것이다.
FXR 또는 NR1H4 (핵 수용체 서브패밀리 1, 군 H, 구성원 4)는 리간드-의존성 방식으로 특이적 표적 유전자의 발현을 활성화시킬 수 있는 핵 수용체이다. FXR은 인간에서 간에서, 위장관, 결장, 난소, 부신, 신장 전반에 걸쳐, 및 담낭 및 담도계에서 발현된다. FXR은 레티노이드 X 수용체 (RXR)와 이종이량체를 형성하고, 표적 유전자 내의 특이적 반응 요소에 결합하여 유전자 전사를 조절한다 (B. M. Forman et al., Cell 1995; 81: 687; W. Seol et al., Mol. Endocrinol. 1995; 9: 72). FXR/RXR 이종이량체는 전형적으로 단일 뉴클레오티드에 의해 분리된 컨센서스 헥사뉴클레오티드 서열 (AGGTCA)의 역전된 반복부, 즉 IR-1 서열에 결합한다. FXR의 관련 생리학적 리간드는 케노데옥시콜산 및 그의 타우린-접합체를 포함한 담즙산이다 (D. J. Parks et al., Science 1999; 284: 1365; M. Makishima et al., Science 1999; 284: 1362). FXR 활성화는 간 및 장으로부터의 담즙산 합성, 유입 및 유출에 관여하는 효소 및 수송체를 코딩하는 다수의 유전자의 발현을 조절하여 음성 피드백 루프에서 총 내인성 담즙산의 순 감소를 유발한다. FXR은 시토카인 섬유모세포 성장 인자 15 (설치류) 또는 19 (영장류)의 발현을 상향조절함으로써 주변분비 및 내분비 신호전달에 관여하며, 이는 또한 담즙산 농도의 조절에 기여할 수 있다 (Holt et al., Genes Dev. 2003; 17: 1581; Inagaki et al., Cell Metab 2005; 2: 217). 따라서, FXR은 담즙산 항상성의 마스터 조절제인 것으로 간주된다.
FXR 효능제의 한 용도는 섬유증, 간경변증, 담관암종, 간세포성 암종, 간부전 및 사망을 초래할 수 있는 담즙정체성 질환 (예를 들어 원발성 담즙성 간경변증 및 원발성 경화성 담관염)을 포함한, 담즙산이 이상조절되는 질환의 치료를 위한 것이다. 간 내의 상승된 담즙산 농도가 유해 효과를 갖지만, 담즙산은 또한 소장의 미생물총 및 완전성에 영향을 미친다. 인간 또는 설치류에서 담즙 유동의 폐쇄는 장 박테리아의 증식 및 점막 손상을 야기하며, 이는 점막 장벽을 가로지르는 박테리아 전위 및 전신 감염을 초래할 수 있다 (Berg, Trends Microbiol. 1995; 3: 149-154). FXR이 결여된 마우스는 박테리아의 증가된 회장 수준 및 손상된 상피 장벽을 가지며, 한편 장 FXR의 활성화는 박테리아 과도성장을 방지하고 장 상피의 완전성을 유지하는데 중요한 역할을 한다 (Inagaki et al., Proc Natl Acad Sci 2006; 103: 3920-3925). 시간이 경과함에 따라, FXR 결손 마우스는 자발적으로 간세포성 암종이 발생하고, 이는 장에서 FXR의 선택적 재-활성화에 의해 제거될 수 있다 (Degirolamo et al., Hepatology 61: 161-170). 소분자 효능제에 의한 FXR의 약리학적 활성화 또는 장 내의 FXR의 트랜스제닉 발현은 담즙산 농도를 정상화시키고, 간 담관에서 세포 증식을 감소시키며, 담즙정체의 설치류 모델에서 염증 세포 침윤, 괴사 면적 및 간 섬유증을 감소시킬 수 있다 (Liu et al., J. Clin. Invest. 2003; 112:1678-1687; Modica et al., Gastroenterology. 2012; 142: 355-365). 담즙정체의 전임상 모델에서 관찰된 이들 유익한 효과 중 일부는 인간 환자에 대해서도 적용되었고, FXR 효능제인 오베티콜산 (OCA 또는 오칼리바(OCALIVA)™)은 원발성 담즙성 간경변증의 치료를 위해 승인되었다 (https://www.fda.gov/newsevents/newsroom/pressannouncements/ucm503964.htm).
담즙산 항상성을 제어하는 것 이외에, FXR 효능제는 다른 경로 중에서도 특히 콜레스테롤 및 지질 대사 및 수송, 글루코스 항상성, 염증, 화학주성, 및 아폽토시스에 관여하는 단백질을 코딩하는 수백개의 유전자의 간 발현을 조절한다 (Zhan et al., PLoS One 2014; 9: e105930; Ijssennagger et al., J Hepatol 2016; 64: 1158-1166). 유전자 발현에 대한 이들 광범위한 효과와 일치하게, FXR 효능제는 또한 섬유증, 암, 염증성 질환, 및 이상지혈증, 비만, 제2형 당뇨병, 비알콜성 지방간 질환 (NAFLD) 및 대사 증후군을 포함한 대사 장애의 전임상 모델에서 연구되었다 (Crawley, Expert Opin. Ther. Patents 2010; 20:1047-1057).
FXR 효능제는 또한 NAFLD, 지방간 질환의 보다 진행된 형태인 비알콜성 지방간염 (NASH) 및 연관 합병증의 치료를 위해 인간 임상 시험에서 연구되고 있다. NAFLD는 오늘날 세계에서 만성 간 질환의 가장 흔한 원인 중 하나이다 (Vernon et al., Aliment Pharmacol Ther 2011;34:274-285). NAFLD를 발생시키는 위험 인자는 비만, 제2형 당뇨병 (T2DM), 인슐린 저항성, 고혈압 및 이상지혈증을 포함한다. NAFLD를 갖는 T2DM 환자에서의 6-주 임상 시험에서, FXR 효능제인 OCA는 통계적으로 유의하게 인슐린 감수성을 개선시키고 체중을 감소시켰으며, 이는 이들 위험 인자 중 일부에 대한 유익한 효과를 나타낸다 (Mudaliar et al., Gastroenterology 2013; 145: 574-582). NASH는 NAFLD의 가장 중증 및 진행성 형태이고, 간 지방증, 염증 및 다양한 양의 세포주위 섬유증을 갖는 풍선화 변성의 조직학적 소견을 포함한다 (Sanyal et al., Hepatology 2015; 61:1392-1405). NASH를 갖는 환자에서의 72-주 임상 시험에서, 간 생검의 조직학적 분석에 의해 평가된 바와 같이, OCA는 간 지방증, 소엽 염증, 간세포 풍선화 및 섬유증을 통계적으로 유의하게 개선시켰다 (Neuschwander-Tetri et al., Lancet 2015; 385: 956-965). 이들 데이터는 또한 NASH가 미국에서 간세포성 암종 (HCC) 및 간 이식의 제2 주요 원인이라는 것을 고려하여 임상 결과에 대한 이익을 나타내는 FXR 효능제의 잠재력을 시사한다 (Wong et al., Hepatology 2014; 59: 2188-2195).
본 발명은 파르네소이드 X 수용체 (FXR) 활성과 연관된 질환, 장애 또는 상태의 치료를 필요로 하는 환자에서 이러한 질환, 장애 또는 상태를 치료하기 위한 신규 화합물을 제공한다.
한 측면에서, 본 발명은 FXR 조정제로서 유용한, 화학식 (I), 화학식 (II) 및 화학식 (III)의 화합물 뿐만 아니라 그의 입체이성질체, 호변이성질체, 제약상 허용되는 염 및 용매화물을 포함한 그의 아속 및 종을 제공한다.
또 다른 측면에서, 본 발명은 또한 본 발명의 화합물을 제조하기 위한 방법 및 중간체를 제공한다.
또 다른 측면에서, 본 발명은 또한 제약상 허용되는 담체 및 본 발명의 화합물 중 적어도 1종 또는 그의 입체이성질체, 호변이성질체, 제약상 허용되는 염 또는 용매화물을 포함하는 제약 조성물을 제공한다.
또 다른 측면에서, 본 발명의 화합물은 요법에서 단독으로 또는 1종 이상의 추가의 치료제와 조합되어 사용될 수 있다.
본 발명의 화합물은 파르네소이드 X 수용체 (FXR)의 활성과 연관된 질환, 장애 또는 상태의 치료를 필요로 하는 환자에게 치료 유효량의 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물을 투여함으로써 상기 환자에서 FXR의 활성과 연관된 질환, 장애 또는 상태의 치료에 사용될 수 있다. 질환, 장애 또는 상태는 병리학적 섬유증과 관련될 수 있다. 본 발명의 화합물은 단독으로, 본 발명의 1종 이상의 화합물과 조합되어, 또는 1종 이상, 예를 들어 1 내지 2종의 다른 치료제와 조합되어 사용될 수 있다.
본 발명의 화합물은 비알콜성 지방간염 (NASH), 비-알콜성 지방간 질환 (NAFLD), 만성 신장 질환, 당뇨병성 신장 질환, 원발성 경화성 담관염 (PSC) 및 원발성 담즙성 간경변증 (PBC)으로부터 선택된 질환, 장애 또는 상태의 치료에서 단일 작용제로서 또는 다른 작용제와 조합되어 사용될 수 있다. 본 발명의 화합물은 특발성 폐 섬유증 (IPF)의 치료에서 단일 작용제로서 또는 다른 작용제와 조합되어 사용될 수 있다.
본 발명의 화합물은 질환, 장애 또는 상태의 치료를 필요로 하는 환자에서 질환, 장애 또는 상태의 치료를 위한 의약의 제조를 위해 사용될 수 있다.
본 발명의 다른 특색 및 이점은 하기 상세한 설명 및 청구범위로부터 분명해질 것이다.
본 출원은 화학식 (I)에 따른, 그의 모든 입체이성질체, 용매화물, 전구약물 및 제약상 허용되는 염 및 용매화물 형태를 포함한 화합물을 제공한다. 본 출원은 또한 화학식 (I)에 따른 적어도 1종의 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물 및 임의로 적어도 1종의 추가의 치료제를 함유하는 제약 조성물을 제공한다. 추가적으로, 본 출원은 FXR-조정 질환 또는 장애, 예컨대, 예를 들어 담도 섬유증, 간 섬유증, 신섬유증, 비-알콜성 지방간 질환 (NAFLD), 비-알콜성 지방간염 (NASH), 원발성 경화성 담관염 (PSC), 원발성 담즙성 간경변증 (PBC) 및 췌장 섬유증의 치료를 필요로 하는 환자에게 치료 유효량의 본 발명의 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물을 임의로 적어도 1종의 추가의 치료제와 조합하여 투여함으로써 상기 질환 또는 장애를 앓고 있는 환자를 치료하는 방법을 제공한다.
I. 본 발명의 화합물
한 실시양태에서, 본 발명은 하기 화학식 (I)의 화합물을 제공한다:
여기서,
X1 및 X4는 각각 독립적으로 C 또는 N이고;
X2 및 X3은 각각 독립적으로 CR5, N, NR6, O 또는 S이고;
E 고리는 4- 내지 6-원 카르보시클릴 또는 헤테로시클릴이고, 여기서 카르보시클릴 및 헤테로시클릴은 각각 독립적으로 0 내지 3개의 R3으로 치환되고;
*은 스피로 탄소 원자를 나타내고;
Y는 CR7 또는 N이고;
m 및 n은 각각 독립적으로 0, 1 또는 2의 정수이고;
f는 0, 1, 2 또는 3의 정수이고;
Z는 6- 내지 10-원 아릴, N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 5- 내지 10-원 헤테로아릴, 3- 내지 10-원 카르보시클릴, 또는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 4- 내지 10-원 헤테로시클릴이고, 여기서 아릴, 헤테로아릴, 카르보시클릴, 및 헤테로시클릴은 독립적으로 0 내지 5개의 R8로 치환되고;
L1은 공유 결합, O, S, NR16, -S(O)2-, C1-3 알킬렌, C1-3 헤테로알킬렌, C2-4 알케닐렌, C2-4 알키닐렌, 아릴, 또는 N, O 및 S로부터 독립적으로 선택된 1 내지 4개의 헤테로원자를 함유하는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 5- 내지 6-원 헤테로아릴이고; 여기서 알킬렌, 알케닐렌, 아릴, 헤테로알킬렌 및 헤테로아릴은 각각 독립적으로 0 내지 3개의 R11로 치환되고;
L2는 공유 결합, O, S, NR17, C1-3 알킬렌 또는 C1-3 헤테로알킬렌이고, 여기서 알킬렌 및 헤테로알킬렌은 독립적으로 0 내지 3개의 R15로 치환되고;
RX는 -L3-RZ이고;
L3은 공유 결합, C1-3 알킬렌, -C(O)NR12-CH2- 또는 -OCH2-이고, 여기서 C1-3 알킬렌은 0 내지 3개의 R4로 치환되고;
RZ는 -CN, -C(O)OR13, -C(O)NR14aR14b,
Re는 C1-6 알킬, C3-6 시클로알킬, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬 또는 할로알콕시알킬이고;
각각의 RY는 독립적으로 수소, 할로, 시아노, 히드록실, 아미노, C1-6 알킬, 알킬아미노, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬, 할로알콕시알킬, 알콕시 또는 할로알콕시이거나; 또는 대안적으로 2개의 RY는 이들이 부착되어 있는 탄소 원자와 함께 가교 모이어티를 형성하고; 단 Y가 N이고 RY가 Y에 인접한 탄소 원자에 부착되는 경우에, RY는 할로, 시아노, 히드록실, 아미노, 알콕시 또는 할로알콕시가 아니고;
R1은 C1-6 알킬, C3-5 시클로알킬 또는 C4-6 헤테로시클릴이고, 여기서 알킬 또는 시클로알킬은 0 내지 3개의 R9로 치환되고;
R2는 6- 내지 10-원 아릴, N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 5- 내지 10-원 헤테로아릴, 3- 내지 10-원 카르보시클릴, 또는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 4- 내지 10-원 헤테로시클릴이고, 여기서 아릴, 헤테로아릴, 카르보시클릴, 및 헤테로시클릴은 독립적으로 0 내지 5개의 R10으로 치환되고;
R3, R5 및 R7은 각각 독립적으로 수소, 할로, 시아노, 히드록실, 아미노, C1-6 알킬, 알킬아미노, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬, 할로알콕시알킬, 알콕시 또는 할로알콕시이고;
R4는 각각 독립적으로 할로, 옥소, 시아노, 히드록실, 아미노, 알킬, 알콕시 또는 알킬아미노이거나; 또는 대안적으로, 2개의 R4는 이들이 부착되어 있는 원자(들)와 함께 카르보시클릴 또는 헤테로시클릴 모이어티를 형성하고;
R6, R16 및 R17은 각각 독립적으로 수소, C1-6 알킬, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬 또는 할로알콕시알킬이고;
R8 및 R10은 각각 독립적으로 할로, 시아노, 히드록실, 아미노, 옥소, -ORa, -SRa, =S, -NRcRc, =NH, =N-OH, =NRa, =N-ORa, -NO2, -S(O)2Ra, -S(O)2NHRb, -S(O)2NRcRc, -S(O)2ORb, -OS(O)2Rb, -OS(O)2ORb, -P(O)(ORb)(ORb), -C(O)Rb, -C(NRb)Rb, -C(O)ORb, -C(O)NRcRc, -C(NRb)NRcRc, -OC(O)Rb, -NRbC(O)Rb, -OC(O)ORb, -NRbC(O)ORb, -OC(O)NRcRc, -NRbC(O)NRcRc, -NRbC(NRb)Rb, -NRbC(NRb)NRcRc, C1-6 알킬, C1-6 할로알킬, 아릴, 아릴알킬, 헤테로아릴, 카르보시클릴 또는 헤테로시클릴이고; 여기서 알킬, 아릴, 헤테로아릴, 카르보시클릴 및 헤테로시클릴은, 그 자체로서 또는 또 다른 기의 일부로서, 각각 독립적으로 0 내지 5개의 Rd로 치환되고;
Ra는 각각 독립적으로 C1-6 알킬, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬, 할로알콕시알킬, 아릴, 아릴알킬, 헤테로아릴, 헤테로아릴알킬, 카르보시클릴, 카르보시클릴알킬, 헤테로시클릴 또는 헤테로시클릴알킬이고;
Rb는 각각 독립적으로 수소 또는 Ra이고;
Rc는 각각 독립적으로 Rb이거나, 또는 대안적으로, 2개의 Rc는 이들이 결합되어 있는 질소 원자와 함께, N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 4-, 5-, 6- 또는 7-원 헤테로시클릴을 형성하고;
Rd는 각각 독립적으로 Ra, 알콕시, 할로알콕시, 알킬아미노, 시클로알킬아미노, 헤테로시클릴아미노, 할로알킬, 히드록시알킬, 아미노알킬, 시클로알콕시, 헤테로시클릴옥시, 할로알콕시, 알콕시알콕시, 할로알킬아미노, 알콕시알킬아미노, 할로알콕시알킬아미노, 아릴아미노, 아르알킬아미노, 아릴옥시, 아르알킬옥시, 헤테로아릴옥시, 헤테로아릴알킬옥시, 알킬티오, 할로, 시아노, 히드록실, 아미노, 옥소, -ORa, -SRa, =S, -NRcRc, =NH, =N-OH, =NRa, =N-ORa, -NO2, -S(O)2Ra, -S(O)2NHRb, -S(O)2NRcRc, -S(O)2ORb, -OS(O)2Rb, -OS(O)2ORb, -P(O)(ORb)(ORb), -C(O)Rb, -C(NRb)Rb, -C(O)ORb, -C(O)NRcRc, -C(NRb)NRcRc, -OC(O)Rb, -NRbC(O)Rb, -OC(O)ORb, -NRbC(O)ORb, -NRbC(O)NRcRc, -NRbC(NRb)Rb 및 -NRbC(NRb)NRcRc로부터 선택되고;
R9는 각각 독립적으로 할로, 시아노, 히드록실, 아미노 또는 C1-6 알킬이고;
R11 및 R15는 각각 독립적으로 할로, 옥소, 시아노, 히드록실, 아미노, C1-6 알킬, C3-6 시클로알킬, C4-6 헤테로시클릴, 알킬아미노, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬, 할로알콕시알킬, 알콕시 또는 할로알콕시이고;
R12는 수소 또는 C1-4 알킬이고;
R13은 수소, C1-10 알킬, 글리코실 또는 카르복시(트리히드록시)테트라히드로피라닐이고;
R14a 및 R14b는 각각 독립적으로 수소, C1-6 알킬, C3-6 시클로알킬, C4-6 헤테로시클릴, 알킬아미노, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬, 할로알콕시알킬, 알콕시 또는 할로알콕시이다.
관련 기술분야의 통상의 기술자는 파선 원이 X1, X2, X3, X4 및 탄소 원자에 의해 형성된 방향족 고리를 나타내고; 파선 직선은 각각 독립적으로 임의적인 공유 결합이라는 것을 이해할 것이다.
화학식 (I)의 한 실시양태에서, X2는 N 또는 NR6이다.
화학식 (I)의 한 실시양태에서, 2개의 RY는 함께 C1-3 알킬렌 가교 모이어티를 형성한다. (RY)f는 임의의 적합한 고리원 원자 상의 1개 이상의 임의적인 치환기를 나타내고, 각각의 RY는 독립적이고 동일하거나 상이할 수 있다.
화학식 (I)의 상기 실시양태 중 어느 하나에서, L1은 공유 결합, O, S, NH, C1-3 알킬렌, -(C1-3 알킬렌)a-O-(C1-3 알킬렌)b-, -(C1-3 알킬렌)a-S-(C1-3 알킬렌)b- 또는 -(C1-3 알킬렌)a-NH-(C1-3 알킬렌)b-이고, 여기서 C1-3 알킬렌은 0 내지 3개의 R11로 치환되고; a는 0 또는 1의 정수이고; b는 0 또는 1의 정수이고; 단 a 및 b 둘 다가 1은 아니고; L2는 공유 결합이다.
화학식 (I)의 상기 실시양태 중 어느 하나에서, E 고리는 하기로부터 선택된 모이어티이고:
E1 및 E2는 독립적으로 CR3, CHR3, N, NR3, O 또는 S이고;
파선은 임의적인 공유 결합이고; 즉, 파선은 존재하거나 부재한 공유 결합을 나타내고;
t는 0, 1 또는 2이고;
각각의 R3은 독립적으로 수소, 할로, 시아노, 히드록실, 아미노, C1-6 알킬, 알킬아미노, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬, 할로알콕시알킬, 알콕시 또는 할로알콕시이다.
화학식 (I)의 상기 실시양태 중 어느 하나에서,
여기서 질소 원자는 L1에 부착된다.
화학식 (I)의 상기 실시양태 중 어느 하나에서, Z는 페닐, 또는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 5- 내지 10-원 헤테로아릴이고, 여기서 페닐 및 헤테로아릴은 독립적으로 0 내지 5개의 R8로 치환되고, 여기서 R8은 상기 정의된 바와 동일하다.
화학식 (I)의 상기 실시양태 중 어느 하나에서, L1은 공유 결합이다.
화학식 (I)의 상기 실시양태 중 어느 하나에서, -Z-Rx는
이고,
여기서 Z 모이어티는 추가로 0 내지 3개의 R8로 치환되고, R8은 상기 정의된 바와 동일하다.
화학식 (I)의 상기 실시양태 중 어느 하나에서, Y는 N이다.
화학식 (I)의 상기 실시양태 중 어느 하나에서, Y는 CH이고; L1은 공유 결합, O, S, NH, -O-(C1-3 알킬렌)-, -S-(C1-3 알킬렌)- 또는 -NH-(C1-3 알킬렌)-이다.
화학식 (I)의 상기 실시양태 중 어느 하나에서, R2는 페닐, 또는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 6-원 헤테로아릴이고, 여기서 페닐 또는 헤테로아릴은 0 내지 3개의 R10으로 치환된다.
화학식 (I)의 상기 실시양태 중 어느 하나에서, L2는 공유 결합이다.
화학식 (I)의 한 실시양태에서, 화합물은 하기 화학식 (II)에 의해 나타내어지고:
X1은 C 또는 N이고;
X2 및 X3은 각각 독립적으로 CH, N, O 또는 S이고;
Z는 페닐, 또는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 5- 내지 10-원 헤테로아릴이고, 여기서 페닐 및 헤테로아릴은 0 내지 3개의 R8로 치환되고;
RX는 -C(O)OR13 또는 -C(O)NH-S(O)2Re이고;
Re는 C1-6 알킬 또는 C3-6 시클로알킬이고;
R1은 C1-6 알킬 또는 C3-5 시클로알킬이고, 여기서 알킬 또는 시클로알킬은 0 내지 3개의 R9로 치환되고;
R2는 페닐, 또는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 6-원 헤테로아릴이고, 여기서 페닐 또는 헤테로아릴은 0 내지 3개의 R10으로 치환되고;
R8, R9, R10 및 R13은 상기 정의된 바와 동일하다.
화학식 (II)의 상기 실시양태 중 어느 하나에서, R2는 페닐 또는 피리디닐이고, 이들 각각은 독립적으로 0 내지 3개의 R10으로 치환된다.
화학식 (I)의 상기 실시양태 중 어느 하나에서,
화학식 (I)의 상기 실시양태 중 어느 하나에서, Z는 8- 내지 10-원 비시클릭 헤테로아릴이고, 여기서 헤테로아릴은 독립적으로 0 내지 3개의 R8로 치환된다.
화학식 (I)의 상기 실시양태 중 어느 하나에서, RX는 -C(O)OH이다.
한 실시양태에서, 본 발명의 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물은 하기 화학식 (III)에 의해 나타내어지고:
여기서,
Z는 1 또는 2개의 질소 원자를 함유하는 6-원 모노시클릭 헤테로아릴, 또는 N, O 및 S로부터 독립적으로 선택된 1 또는 3개의 헤테로원자를 함유하는 9- 내지 10-원 비시클릭 헤테로아릴이고, 여기서 모노시클릭 또는 비시클릭 헤테로아릴은 독립적으로 0 내지 3개의 R8로 치환되고;
R2는 페닐 또는 피리디닐이고, 여기서 페닐 및 피리디닐은 각각 독립적으로 0 내지 2개의 R10으로 치환되고;
R8은 각각 독립적으로 할로, 시아노, 히드록실, C1-4 알킬, C1-4 할로알킬, C1-4 알콕시 또는 C1-4 할로알콕시이고;
R10은 각각 독립적으로 할로, C1-4 알킬, C1-4 할로알킬, C1-4 알콕시 또는 C1-4 할로알콕시이고;
RX는 -C(O)OH 또는 -C(O)NH-S(O)2Re이고;
Re는 C1-6 알킬 또는 C3-6 시클로알킬이다.
화학식 (III)의 일부 실시양태에서, Z는 피리디닐, 벤즈티아졸릴, 피롤로피리디닐, 피롤로피리미디닐, 인돌릴, 퀴놀리닐, 이미다조피리디닐, 피라졸로피리미디닐 및 피롤로트리아지닐로부터 선택된 헤테로아릴이고, 여기서 헤테로아릴은 독립적으로 0 내지 3개의 R8로 치환된다. 일부 실시양태에서, 헤테로아릴은 독립적으로 0, 1 또는 2개의 R8로 치환된다.
화학식 (III)의 일부 실시양태에서, R2는 페닐 또는 피리디닐이고, 여기서 페닐 및 피리디닐은 각각 독립적으로 1 또는 2개의 R10으로 치환된다.
화학식 (III)의 일부 실시양태에서, R8은 각각 독립적으로 F, -CH3, -OCH3, -OCH2CH3, -OCH(CH3)2, -CF3, -OCF3 또는 -OCHF2이다.
화학식 (III)의 일부 실시양태에서, R10은 각각 독립적으로 Cl, -CH3, -CF3 또는 -OCF3이다.
화학식 (III)의 일부 실시양태에서, RX는 -C(O)OH 또는 -C(O)NH-S(O)2Re이고; Re는 메틸, 에틸, 이소프로필 또는 시클로프로필이다.
화학식 (I) 또는 화학식 (II)의 한 실시양태에서, X1은 C이다.
화학식 (I) 또는 화학식 (II)의 한 실시양태에서, X2는 N이다.
화학식 (I) 또는 화학식 (II)의 한 실시양태에서, X3은 O이다.
화학식 (I)의 한 실시양태에서, X4는 C이다.
화학식 (I)의 한 실시양태에서, X1은 C이고 X4는 C이다.
화학식 (I) 또는 화학식 (II)의 한 실시양태에서, X2 및 X3 중 1개는 N이고 X2 및 X3 중 다른 것은 O이다.
화학식 (I) 또는 화학식 (II)의 한 실시양태에서, X2는 N이고 X3은 O이다.
화학식 (I) 또는 화학식 (II)의 한 실시양태에서, X2는 O이고 X3은 N이다.
화학식 (I) 또는 화학식 (II)의 한 실시양태에서, X1은 C이고; X2는 N이고; X3은 O이다.
화학식 (I)의 한 실시양태에서, X1은 C이고; X2 및 X3 중 1개는 N이고 X2 및 X3 중 다른 것은 O이고; X4는 C이다.
화학식 (I)의 한 실시양태에서, X1은 C이고; X2는 N이고; X3은 O이고; X4는 C이다.
화학식 (I)의 한 실시양태에서, X1은 C이고; X2는 O이고; X3은 N이고; X4는 C이다.
화학식 (I) 또는 화학식 (II)의 한 실시양태에서, X1은 N이고; X2는 N이고; X3은 N이다.
화학식 (I)의 한 실시양태에서, L1은 공유 결합, O, -CH2-, -CH2CH2-, -OCH2-, -CH2OCH2- 또는 -NR16-이다. 이러한 실시양태에, L1이 공유 결합, O 또는 -OCH2-인 화합물이 포함된다. 또한 이러한 실시양태에, L1이 공유 결합인 화합물이 포함된다.
L1은 공유 결합, O, -CH2-, -CH2CH2-, -OCH2-, -CH2OCH2- 또는 -NR16-이다. 이러한 실시양태에, L1이 공유 결합, O 또는 -OCH2-인 화합물이 포함된다. 또한 이러한 실시양태에, L1이 공유 결합인 화합물이 포함된다.
L1은 공유 결합, -CH2-, -CH2CH2- 또는 -CH2OCH2-이다. 이러한 실시양태에, L1이 공유 결합인 화합물이 포함된다.
L1은 공유 결합, O, -CH2-, -CH2CH2-, -OCH2-, -CH2OCH2- 또는 -NR16-이다. 이러한 실시양태에, L1이 공유 결합, O 또는 -OCH2-인 화합물이 포함된다. 또한 이러한 실시양태에, L1이 공유 결합인 화합물이 포함된다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, Z는 아릴, 또는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 5- 내지 10-원 헤테로아릴이고, 여기서 페닐 및 헤테로아릴은 독립적으로 0 내지 5개의 R8로 치환된다. 이러한 실시양태에, Z가 페닐, 피리디닐, 피리다지닐, 피리미디닐, 피라지닐, 벤조[d]이미다졸릴, 벤조[d]이속사졸릴, 벤조[d]옥사디아졸릴, 벤조[d]티아졸릴, 이미다졸로[1,5-a]피리디닐, 인다졸릴, 인돌릴, 피라졸로[4,3-b] 피리디닐, 피롤로[2,1-f][1,2,4]트리아지닐, 피롤로[2,3-b]피리디닐, 피롤로[2,3-c]피리디닐, 피롤로[2,3-d]피리미디닐, 피롤로[3,2-c]피리디닐, 티아졸로[4,5-b]피리디닐, 티아졸로[5,4-b]피리디닐, 신놀리닐, 이소퀴놀리닐, 퀴놀리닐 또는 퀴녹살리닐이고, 이들 각각은 0 내지 1개의 R8로 치환되는 것인 화합물이 포함된다.
L1은 공유 결합, O 또는 -OCH2-이고;
Z는 페닐, 피리디닐, 피리다지닐, 피리미디닐, 피라지닐, 벤조[d]이미다졸릴, 벤조[d]이속사졸릴, 벤조[d]옥사디아졸릴, 벤조[d]티아졸릴, 이미다졸로[1,5-a] 피리디닐, 인다졸릴, 인돌릴, 피라졸로[4,3-b]피리디닐, 피롤로[2,1-f][1,2,4]트리아지닐, 피롤로[2,3-b]피리디닐, 피롤로[2,3-c]피리디닐, 피롤로[2,3-d]피리미디닐, 피롤로[3,2-c]피리디닐, 티아졸로[4,5-b]피리디닐, 티아졸로[5,4-b]피리디닐, 신놀리닐, 이소퀴놀리닐, 퀴놀리닐 또는 퀴녹살리닐이고, 이들 각각은 0 내지 1개의 R8로 치환된다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, L3은 공유 결합, -CH2-, -CH2CH2-, -C(O)NHCH2- 또는 -OCH2-이다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, L3은 공유 결합이다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, L3은 -CH2-, -CH2CH2-, -C(O)NHCH2- 또는 -OCH2-이다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, L3은 공유 결합 또는 -C(O)NHCH2-이다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, RZ는 -CN, -C(O)OR13, -C(O)NR14aR14b,
이러한 실시양태에서, L3이 공유 결합인 화합물이 포함된다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, Rx는 -CN, -C(O)OH, -C(O)O(C1-3 알킬), -C(O)NH2, -C(O)NH(C1-3 알킬), -C(O)NH(C3-6 시클로프로필), -C(O)NHCH2C(O)OH, -C(O)NHS(O)2(C1-3 알킬), -C(O)NHS(O)2(C3-6 시클로프로필), -OCH2C(O)OH 또는 -C(O)O(카르복시(트리히드록시)테트라히드로피라닐)이다. 이러한 실시양태에, Rx가 -CN, -C(O)OH, -C(O)OCH2CH3, -C(O)NH2, -C(O)NH(CH3), -C(O)NHCH2CH3, -C(O)NHCH(CH3)2, -C(O)NH(시클로프로필), -C(O)NHCH2C(O)OH, -C(O)NHS(O)2CH3, -C(O)NHS(O)2(시클로프로필), -OCH2C(O)OH 또는 -C(O)O(카르복시(트리히드록시)테트라히드로피라닐)인 화합물이 포함된다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, L2는 공유 결합 또는 -CH(시클로프로필)-이다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, L2는 공유 결합이다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, L2는 -CH(시클로프로필)-이고, R2는 시클로프로필이다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, R2는 C3-6 시클로알킬, 페닐 또는 피리디닐이고, 여기서 페닐 및 피리디닐은 독립적으로 1 내지 3개의 R10으로 치환된다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, R2는 시클로프로필, 시클로헥실, 페닐 또는 피리디닐이고, 여기서 페닐 및 피리디닐은 독립적으로 1 내지 3개의 R10으로 치환된다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, R2는 시클로헥실, 페닐 또는 피리디닐이고, 여기서 페닐 및 피리디닐은 독립적으로 1 내지 3개의 R10으로 치환되고; L2는 공유 결합이다.
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, R1은 C1-3 알킬, C3-4 시클로알킬 또는 C4-5 헤테로시클릴이고, 여기서 알킬, 시클로알킬 및 헤테로시클릴은 각각 0 내지 3개의 R9로 치환되고;
화학식 (I), 화학식 (II) 또는 화학식 (III)의 한 실시양태에서, R1은 -CHF2, -CH(CH3)2, 시클로프로필 또는 메틸시클로프로필이다.
한 실시양태는 하기와 같은 화학식 (I)에 따른 화합물을 제공한다:
X1은 C이고, X2는 N이고, X3은 O이고, X4는 C이거나; 또는 X1은 N이고, X2는 N이고, X3은 C이고, X4는 C이고;
Y는 CH 또는 N이고;
L1은 공유 결합, O 또는 -OCH2-이고, 단 Y가 N인 경우에 L1은 공유 결합이고;
Z는 페닐, 피리디닐, 피리다지닐, 피리미디닐, 피라지닐, 벤조[d]이미다졸릴, 벤조[d]이속사졸릴, 벤조[d]옥사디아졸릴, 벤조[d]티아졸릴, 이미다졸로[1,5-a] 피리디닐, 인다졸릴, 인돌릴, 피라졸로[4,3-b]피리디닐, 피롤로[2,1-f][1,2,4]트리아지닐, 피롤로[2,3-b] 피리디닐, 피롤로[2,3-c]피리디닐, 피롤로[2,3-d]피리미디닐, 피롤로[3,2-c]피리디닐, 티아졸로[4,5-b]피리디닐, 티아졸로[5,4-b]피리디닐, 신놀리닐, 이소퀴놀리닐, 퀴놀리닐 또는 퀴녹살리닐이고, 이들 각각은 0 내지 1개의 R8로 치환되고;
R8은 F, -CH3, -CF3, -OCH3, -OCH2CH3, -OCH(CH3)2, -OCHF2, -OCF3, -OCH2CH2OH 또는 -CH2OCH2CH2Si(CH3)3이고;
Rx는 -CN, -C(O)OH, -C(O)OCH2CH3, -C(O)NH2, -C(O)NH(CH3), -C(O)NHCH2CH3, -C(O)NHCH(CH3)2, -C(O)NH(시클로프로필), -C(O)NHCH2C(O)OH, -C(O)NHS(O)2CH3, -C(O)NHS(O)2(시클로프로필), -OCH2C(O)OH 또는 -C(O)O(카르복시(트리히드록시)테트라히드로피라닐)이고;
L2는 공유 결합이고;
R1은 -CHF2, -CH(CH3)2, 시클로프로필 또는 메틸시클로프로필이고;
R2는 시클로헥실, 페닐 또는 피리디닐이고, 여기서 페닐 및 피리디닐은 독립적으로 1 내지 3개의 R10으로 치환되고;
R10은 각각 독립적으로 F, Cl, -CH3, -CF3, -OCH3 또는 -OCF3이다.
한 실시양태에서, 본 발명의 화합물은 화학식 (III)으로 나타내어지거나, 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물이고; 여기서:
Z는 N, O 및 S로부터 독립적으로 선택된 1 또는 3개의 헤테로원자를 함유하는 9- 내지 10-원 비시클릭 헤테로아릴이고, 여기서 비시클릭 헤테로아릴은 독립적으로 0 내지 3개의 R8로 치환되고;
R2는 페닐 또는 피리디닐이고, 여기서 페닐 및 피리디닐은 각각 독립적으로 0 내지 2개의 R10으로 치환되고;
R8은 각각 독립적으로 F, Cl, 시아노, 히드록실, C1-3 알킬, C1-2 할로알킬, C1-3 알콕시 또는 C1-2 할로알콕시이고;
R10은 각각 독립적으로 F, Cl, C1-3 알킬, C1-2 플루오로알킬, C1-4 알콕시 또는 C1-2 플루오로알콕시이고;
RX는 -C(O)OH이다.
한 실시양태에서, 본 발명의 화합물은 화학식 (III)으로 나타내어지거나, 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물이고; 여기서:
Z는 N, O 및 S로부터 독립적으로 선택된 1 또는 3개의 헤테로원자를 함유하는 9-원 비시클릭 헤테로아릴이고, 여기서 비시클릭 헤테로아릴은 독립적으로 0 내지 3개의 R8로 치환되고;
R2는 페닐 또는 피리디닐이고, 여기서 페닐 및 피리디닐은 각각 독립적으로 0 내지 2개의 R10으로 치환되고;
R8은 각각 독립적으로 F, Cl, 시아노, 히드록실, C1-3 알킬, C1-2 할로알킬, C1-3 알콕시 또는 C1-2 할로알콕시이고;
R10은 각각 독립적으로 F, Cl, C1-3 알킬, C1-2 플루오로알킬, C1-4 알콕시 또는 C1-2 플루오로알콕시이고;
RX는 -C(O)OH이다.
한 실시양태에서, 본 발명은 하기로부터 선택되는 화합물을 제공한다:
한 실시양태에서, 본 발명은 하기로부터 선택되는 화합물을 제공한다:
한 실시양태에서, 본 발명은 하기로부터 선택되는 화합물을 제공한다:
한 실시양태에서, 본 발명은 하기로부터 선택되는 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물을 제공한다:
한 실시양태에서, 본 발명은, 특히, 명세서에 기재된 바와 같은 실시예 중 어느 하나로부터 선택된 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물을 제공한다.
한 실시양태에서, 본 발명의 화합물은, 일시적 인간 FXR/Gal4-루시페라제 리포터 검정을 이용할 때, ≤ 5000 nM의 FXR EC50 값을 가지며; 또 다른 실시양태에서, 본 발명의 화합물은 ≤ 1000 nM의 FXR EC50 값을 가지며; 또 다른 실시양태에서, 본 발명의 화합물은 ≤ 500 nM의 FXR EC50 값을 가지며; 또 다른 실시양태에서, 본 발명의 화합물은 ≤ 200 nM의 FXR EC50 값을 가지며; 또 다른 실시양태에서, 본 발명의 화합물은 ≤ 100 nM의 FXR EC50 값을 가지며; 또 다른 실시양태에서, 본 발명의 화합물은 ≤ 50 nM의 FXR EC50 값을 갖는다.
II. 제약 조성물, 치료 유용성 및 조합
또 다른 실시양태에서, 본 발명은 본 발명의 화합물 중 적어도 1종 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물을 포함하는 조성물을 제공한다.
또 다른 실시양태에서, 본 발명은 제약상 허용되는 담체 및 본 발명의 화합물 중 적어도 1종 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물을 포함하는 제약 조성물을 제공한다.
또 다른 실시양태에서, 본 발명은 제약상 허용되는 담체 및 치료 유효량의 본 발명의 화합물 중 적어도 1종 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물을 포함하는 제약 조성물을 제공한다.
또 다른 실시양태에서, 본 발명은 본 발명의 화합물의 제조 방법을 제공한다.
또 다른 실시양태에서, 본 발명은 본 발명의 화합물을 제조하기 위한 중간체를 제공한다.
또 다른 실시양태에서, 본 발명은 1종 이상의 추가의 치료제를 추가로 포함하는 상기 정의된 바와 같은 제약 조성물을 제공한다.
또 다른 실시양태에서, 본 발명은 담즙산의 조절이상과 연관된 질환, 장애 또는 상태의 치료를 필요로 하는 환자에게 치료 유효량의 본 발명의 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물을 투여하는 것을 포함하는, 상기 환자에서의 담즙산의 조절이상과 연관된 질환, 장애 또는 상태의 치료 방법을 제공한다.
또 다른 실시양태에서, 본 발명은 파르네소이드 X 수용체 (FXR)의 활성과 연관된 질환, 장애 또는 상태의 치료를 필요로 하는 환자에게 치료 유효량의 본 발명의 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물을 투여하는 것을 포함하는, 상기 환자에서의 FXR의 활성과 연관된 질환, 장애 또는 상태의 치료 방법을 제공한다.
또 다른 실시양태에서, 본 발명은 질환, 장애 또는 상태의 치료를 필요로 하는 환자에게 치료 유효량의 본 발명의 화합물 중 적어도 1종을 단독으로 또는 임의로 본 발명의 또 다른 화합물 및/또는 적어도 1종의 다른 유형의 치료제와 조합하여 투여하는 것을 포함하는, 질환, 장애 또는 상태의 치료 방법을 제공한다.
또 다른 실시양태에서, 본 발명은 환자에게 치료 유효량의 본 발명의 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물을 투여하는 것을 포함하는, 환자에서 파르네소이드 X 수용체 (FXR) 길항작용 효과를 도출하는 방법을 제공한다.
일부 실시양태에서, 질환, 장애 또는 상태는 병리학적 섬유증, 암, 염증성 장애, 대사 또는 담즙정체성 장애를 포함한 FXR 기능장애와 연관된다.
일부 실시양태에서, 질환, 장애 또는 상태는 간, 담도, 신장, 심장, 피부, 안구 및 췌장 섬유증을 포함한 섬유증과 연관된다.
다른 실시양태에서, 질환, 장애 또는 상태는 세포-증식성 장애, 예컨대 암과 연관된다. 일부 실시양태에서, 암은 고형 종양 성장 또는 신생물을 포함한다. 다른 실시양태에서, 암은 종양 전이를 포함한다. 일부 실시양태에서, 암은 간, 담낭, 소장, 대장, 신장, 전립선, 방광, 혈액, 골, 뇌, 유방, 중추 신경계, 자궁경부, 결장, 자궁내막, 식도, 생식기, 비뇨생식관, 두부, 후두, 폐, 근육 조직, 경부, 구강 또는 비강 점막, 난소, 췌장, 피부, 비장, 위, 고환 또는 갑상선의 암이다. 다른 실시양태에서, 암은 암종, 육종, 림프종, 백혈병, 흑색종, 중피종, 다발성 골수종 또는 정상피종이다.
본 발명에 따라 예방, 조정 또는 치료될 수 있는, FXR의 활성과 연관된 질환, 장애 또는 상태의 예는 이식 거부, 섬유화 장애 (예를 들어, 간 섬유증, 신장 섬유증), 염증성 장애 (예를 들어, 급성 간염, 만성 간염, 비-알콜성 지방간염 (NASH), 과민성 장 증후군 (IBS), 염증성 장 질환 (IBD)), 뿐만 아니라 세포-증식성 장애 (예를 들어, 암, 골수종, 섬유종, 간세포성 암종, 결장직장암, 전립선암, 백혈병, 카포시 육종, 고형 종양)를 포함하나 이에 제한되지는 않는다.
본 발명의 화합물에 의해 예방 또는 치료되기에 적합한 섬유화 장애, 염증성 장애, 뿐만 아니라 세포-증식성 장애는 비-알콜성 지방간 질환 (NAFLD), 알콜성 또는 비-알콜성 지방간염 (NASH), 급성 간염, 만성 간염, 간 경변증, 원발성 담즙성 간경변증, 원발성 경화성 담관염, 약물-유발 간염, 담즙성 간경변증, 문맥 고혈압, 재생 부전, 간 기능저하, 간 혈류 장애, 신병증, 과민성 장 증후군 (IBS), 염증성 장 질환 (IBD), 비정상적 췌장 분비, 양성 전립선 비대증, 신경병증성 방광 질환, 당뇨병성 신병증, 초점성 분절성 사구체경화증, IgA 신병증, 약물 또는 이식에 의해 유발된 신병증, 자가면역 신병증, 루푸스 신염, 간 섬유증, 신장 섬유증, 만성 신장 질환 (CKD), 당뇨병성 신장 질환 (DKD), 피부 섬유증, 켈로이드, 전신 경화증, 경피증, 바이러스-유발 섬유증, 특발성 폐 섬유증 (IPF), 간질성 폐 질환, 비-특이적 간질성 폐렴 (NSIP), 통상성 간질성 폐렴 (UIP), 방사선-유발 섬유증, 가족성 폐 섬유증, 기도 섬유증, 만성 폐쇄성 폐 질환 (COPD), 척수 종양, 추간판의 헤르니아, 척추관 협착, 심부전, 심장 섬유증, 혈관 섬유증, 혈관주위 섬유증, 구제역, 암, 골수종, 섬유종, 간세포성 암종, 결장직장암, 전립선암, 백혈병, 만성 림프구성 백혈병, 카포시 육종, 고형 종양, 뇌경색, 뇌출혈, 신경병증성 통증, 말초 신경병증, 연령-관련 황반 변성 (AMD), 녹내장, 안구 섬유증, 각막 반흔형성, 당뇨병성 망막병증, 증식성 유리체망막병증 (PVR), 반흔성 유천포창 녹내장 여과 수술 반흔형성, 크론병 또는 전신 홍반성 루푸스; 비정상적 상처 치유로부터 유발된 켈로이드 형성; 기관 이식 후 발생하는 섬유증, 골수섬유증 및 유섬유종을 포함하나 이에 제한되지는 않는다. 한 실시양태에서, 본 발명은 섬유화 장애, 염증성 장애 또는 세포-증식성 장애의 치료를 필요로 하는 환자에게 치료 유효량의 본 발명의 화합물 중 적어도 1종을 단독으로 또는 임의로 본 발명의 또 다른 화합물 및/또는 적어도 1종의 다른 유형의 치료제와 조합하여 투여하는 것을 포함하는, 섬유화 장애, 염증성 장애 또는 세포-증식성 장애의 치료 방법을 제공한다.
또 다른 실시양태에서, 본 발명은 요법에 사용하기 위한 본 발명의 화합물을 제공한다.
또 다른 실시양태에서, 본 발명은 섬유화 장애, 염증성 장애 또는 세포-증식성 장애의 치료를 위한 요법에 사용하기 위한 본 발명의 화합물을 제공한다.
또 다른 실시양태에서, 본 발명은 또한 섬유화 장애, 염증성 장애 또는 세포-증식성 장애의 치료를 위한 의약의 제조를 위한 본 발명의 화합물의 용도를 제공한다.
또 다른 실시양태에서, 본 발명은 섬유화 장애, 염증성 장애 또는 세포-증식성 장애의 치료를 필요로 하는 환자에게 치료 유효량의 제1 및 제2 치료제를 투여하는 것을 포함하며, 여기서 제1 치료제는 본 발명의 화합물인, 섬유화 장애, 염증성 장애 또는 세포-증식성 장애의 치료 방법을 제공한다.
또 다른 실시양태에서, 본 발명은 요법에서의 동시, 개별 또는 순차적 사용을 위한 본 발명의 화합물 및 추가의 치료제(들)의 조합 제제를 제공한다.
또 다른 실시양태에서, 본 발명은 섬유화 장애, 염증성 장애 또는 세포-증식성 장애의 치료에서의 동시, 개별 또는 순차적 사용을 위한 본 발명의 화합물 및 추가의 치료제(들)의 조합 제제를 제공한다.
본 발명의 화합물은 추가의 치료제(들), 예컨대 1종 이상의 항섬유화 및/또는 항염증 치료제와 조합되어 사용될 수 있다.
한 실시양태에서, 조합 제약 조성물 또는 조합 방법 또는 조합 용도에 사용되는 추가의 치료제(들)는 하기 치료제 중 1종 이상, 바람직하게는 1 내지 3종으로부터 선택된다: TGFβ 수용체 억제제 (예를 들어, 갈루니세르팁), TGFβ 합성의 억제제 (예를 들어, 피르페니돈), 혈관 내피 성장 인자 (VEGF), 혈소판-유래 성장 인자 (PDGF) 및 섬유모세포 성장 인자 (FGF) 수용체 키나제의 억제제 (예를 들어, 닌테다닙), 인간화 항-αVβ6 인테그린 모노클로날 항체 (예를 들어, 3G9), 인간 재조합 펜트락신-2, 재조합 인간 혈청 아밀로이드 P, TGFβ-1, -2 및 -3에 대한 재조합 인간 항체, 엔도텔린 수용체 길항제 (예를 들어, 마시텐탄), 인터페론 감마, c-Jun 아미노-말단 키나제 (JNK) 억제제 (예를 들어, 4-[[9-[(3S)-테트라히드로-3-푸라닐]-8-[(2,4,6-트리플루오로페닐)아미노]-9H-퓨린-2-일]아미노]-트랜스-시클로헥산올, 3-펜틸벤젠아세트산 (PBI-4050), 망가니즈 (III) 함유 테트라-치환된 포르피린 유도체, 에오탁신-2 표적화 모노클로날 항체, 인터류킨-13 (IL-13) 항체 (예를 들어, 레브리키주맙, 트랄로키누맙), 인터류킨 4 (IL-4) 및 인터류킨 13 (IL-13) 표적화 이중특이적 항체, NK1 타키키닌 수용체 효능제 (예를 들어, Sar9, Met(O2)11-물질 P), 신트레데킨 베수도톡스, 결합조직 성장 인자에 대한 인간 재조합 DNA-유도된, IgG1 카파 모노클로날 항체, 및 CC-케모카인 리간드 2에 대해 선택적인 완전 인간 IgG1 카파 항체 (예를 들어, 카를루맙, CCX140), 항산화제 (예를 들어, N-아세틸시스테인), 포스포디에스테라제 5 (PDE5) 억제제 (예를 들어, 실데나필), 폐쇄성 기도 질환의 치료를 위한 작용제, 예컨대 무스카린성 길항제 (예를 들어, 티오트로피움, 이프라트로피움 브로마이드), 아드레날린성 β2 효능제 (예를 들어, 살부타몰, 살메테롤), 코르티코스테로이드 (예를 들어, 트리암시놀론, 덱사메타손, 플루티카손), 면역억제제 (예를 들어, 타크롤리무스, 라파마이신, 피메크롤리무스), 및 섬유화 상태, 예컨대 간, 담도 및 신장 섬유증, 비-알콜성 지방간 질환 (NALFD), 비-알콜성 지방간염 (NASH), 심장 섬유증, 특발성 폐 섬유증 (IPF) 및 전신 경화증의 치료에 유용한 치료제. 이러한 섬유화 상태의 치료에 유용한 치료제는 FXR 효능제 (예를 들어, OCA, GS-9674 및 LJN452), LOXL2 억제제 (예를 들어, 심투주맙), LPA1 길항제 (예를 들어, BMS-986020 및 SAR 100842), PPAR 조정제 (예를 들어, 엘라피브라노르, 피오글리타존, 및 사로글리타자르, IVA337), SSAO/VAP-1 억제제 (예를 들어, PXS-4728A 및 SZE5302), ASK-1 억제제 (예를 들어, GS-4997 또는 세론세르팁), ACC 억제제 (예를 들어, CP-640186 및 NDI-010976 또는 GS-0976), FGF21 모방체 (예를 들어, LY2405319 및 BMS-986036), 카스파제 억제제 (예를 들어, 엠리카산), NOX4 억제제 (예를 들어, GKT137831), MGAT2 억제제 (예를 들어, BMS-963272), αV 인테그린 억제제 (예를 들어, 아비투주맙) 및 담즙산/지방산 접합체 (예를 들어, 아람콜)를 포함하나 이에 제한되지는 않는다. 본 발명의 다양한 실시양태의 FXR 효능제는 또한 1종 이상의 치료제, 예컨대 CCR2/5 억제제 (예를 들어, 세니크리비록), 갈렉틴-3 억제제 (예를 들어, TD-139, GR-MD-02), 류코트리엔 수용체 길항제 (예를 들어, 티펠루카스트, 몬테루카스트), SGLT2 억제제 (예를 들어, 다파글리플로진, 레모글리플로진), GLP-1 수용체 효능제 (예를 들어, 리라글루티드 및 세마글루티드), FAK 억제제 (예를 들어, GSK-2256098), CB1 역 효능제 (예를 들어, JD-5037), CB2 효능제 (예를 들어, APD-371 및 JBT-101), 오토탁신 억제제 (예를 들어, GLPG1690), 프롤릴 t-RNA 신테타제 억제제 (예를 들어, 할로푸기논), FPR2 효능제 (예를 들어, ZK-994), 및 THR 효능제 (예를 들어, MGL:3196)와 조합되어 사용될 수 있다. 또 다른 실시양태에서, 조합 제약 조성물 또는 조합 방법 또는 조합 용도에 사용되는 추가의 치료제(들)는 면역종양학 작용제, 예컨대 알렘투주맙, 아테졸리주맙, 이필리무맙, 니볼루맙, 오파투무맙, 펨브롤리주맙 및 리툭시맙 중 1종 이상, 바람직하게는 1 내지 3종으로부터 선택된다.
본 발명의 화합물은 본원에 기재된 임의의 용도를 위해 임의의 적합한 수단에 의해, 예를 들어 경구로, 예컨대 정제, 캡슐 (이들 각각은 지속 방출 또는 지효성 방출 제제를 포함함), 환제, 분말, 과립, 엘릭시르, 팅크제, 현탁액, 시럽 및 에멀젼; 설하로; 협측으로; 비경구로, 예컨대 피하, 정맥내, 근육내 또는 흉골내 주사 또는 주입 기술에 의해 (예를 들어, 멸균 주사가능한 수성 또는 비-수성 용액 또는 현탁액으로서); 코 점막으로의 투여를 포함한 비강으로, 예컨대 흡입 스프레이에 의해; 국소로, 예컨대 크림 또는 연고 형태로; 또는 직장으로, 예컨대 좌제 형태로 투여될 수 있다. 이들은 단독으로 투여될 수 있지만, 일반적으로 선택된 투여 경로 및 표준 제약 실시에 기초하여 선택된 제약 담체와 함께 투여될 것이다.
용어 "제약 조성물"은 본 발명의 화합물을 적어도 1종의 추가의 제약상 허용되는 담체와 조합하여 포함하는 조성물을 의미한다. "제약상 허용되는 담체"는 투여 방식 및 투여 형태의 성질에 따라, 생물학적 활성제를 동물, 특히 포유동물에게 전달하기 위해 관련 기술분야에서 일반적으로 허용되는 매질, 예컨대, 즉 아주반트, 부형제 또는 비히클, 예컨대 희석제, 보존제, 충전제, 유동 조절제, 붕해제, 습윤제, 유화제, 현탁화제, 감미제, 향미제, 퍼퓸제, 항박테리아제, 항진균제, 윤활제 및 분배제를 지칭한다. 제약상 허용되는 담체는 충분히 다수의 인자에 따라 관련 기술분야의 통상의 기술자의 이해범위 내에서 제제화된다. 이들은 비제한적으로, 제제화될 활성제의 유형 및 성질; 작용제-함유 조성물이 투여될 대상체; 조성물의 의도된 투여 경로; 및 표적화될 치료 적응증을 포함한다. 제약상 허용되는 담체는 수성 및 비-수성 액체 매질 둘 다, 뿐만 아니라 다양한 고체 및 반-고체 투여 형태를 포함한다. 이러한 담체는 활성제에 더하여 다수의 상이한 성분 및 첨가제를 포함할 수 있고, 이러한 추가의 성분은 관련 기술분야의 통상의 기술자에게 널리 공지된 다양한 이유, 예를 들어 활성제, 결합제 등의 안정화를 위해 제제에 포함될 수 있다. 적합한 제약상 허용되는 담체 및 이들의 선택에 수반되는 인자에 대한 기재는, 예를 들어 문헌 [Remington's Pharmaceutical Sciences, 18th Edition (1990)]과 같은 용이하게 입수가능한 다양한 공급원에서 발견된다.
본원에 사용된 용어 "치료하는" 또는 "치료"는 본 발명의 화합물 또는 조성물을 사용하여 임상 결과를 포함한 유익하거나 목적하는 결과를 얻기 위한 접근법을 지칭한다. 본 발명의 목적상, 유익하거나 목적하는 임상 결과는 하기 중 하나 이상을 포함하나 이에 제한되지는 않는다: 질환, 장애 또는 상태로부터 유발되는 1종 이상의 증상의 중증도 및/또는 빈도를 감소시키는 것; 질환, 장애 또는 상태의 정도를 감소시키거나 그의 퇴행을 유발하는 것; 질환, 장애 또는 상태를 안정화시키는 것 (예를 들어, 질환, 장애 또는 상태의 악화를 예방하거나 지연시키는 것); 질환, 장애 또는 상태의 진행을 지연시키거나 느리게 하는 것; 질환, 장애 또는 상태를 호전시키는 것; 질환, 장애 또는 상태를 치료하는데 요구되는 1종 이상의 다른 의약의 용량을 감소시키는 것; 및/또는 삶의 질을 증가시키는 것.
물론, 본 발명의 화합물에 대한 투여 요법은 공지된 인자, 예컨대 특정한 작용제의 약역학적 특징 및 그의 투여 방식 및 경로; 수용자의 종, 연령, 성별, 건강, 의학적 상태 및 체중; 증상의 성질 및 정도; 공동 치료의 종류; 치료 빈도; 투여 경로, 환자의 신장 및 간 기능, 및 목적하는 효과에 따라 달라질 것이다.
일반적 지침에 따라, 각각의 활성 성분의 1일 경구 투여량은, 나타낸 효과를 위해 사용될 경우, 1일에 약 0.01 내지 약 5000 mg, 바람직하게는 1일에 약 0.01 내지 약 1000 mg, 가장 바람직하게는 1일에 약 0.01 내지 약 250 mg 범위일 것이다. 정맥내로, 가장 바람직한 용량은 일정 속도 주입 동안 약 0.01 내지 약 10 mg/kg/분 범위일 것이다. 본 발명의 화합물은 단일 1일 용량으로 투여될 수 있거나, 또는 총 1일 투여량이 1일 2, 3 또는 4회의 분할 용량으로 투여될 수 있다.
화합물은 전형적으로, 의도된 투여 형태, 예를 들어 경구 정제, 캡슐, 엘릭시르 및 시럽에 대해 적합하게 선택되며 통상적인 제약 실시와 부합하는 적합한 제약 희석제, 부형제 또는 담체 (집합적으로 본원에서 제약 담체로 지칭됨)와 혼합되어 투여된다.
투여에 적합한 투여 형태 (제약 조성물)는 투여 단위당 약 0.1 밀리그램 내지 약 2000 밀리그램의 활성 성분을 함유할 수 있다. 이들 제약 조성물에서, 활성 성분은 통상적으로 조성물의 총 중량을 기준으로 하여 약 0.1-95 중량%의 양으로 존재할 것이다.
경구 투여를 위한 전형적인 캡슐은 본 발명의 화합물 중 적어도 1종 (250 mg), 락토스 (75 mg) 및 스테아르산마그네슘 (15 mg)을 함유한다. 혼합물을 60 메쉬 체에 통과시키고, 1번 젤라틴 캡슐 내에 패킹한다.
전형적인 주사가능한 제제는 본 발명의 화합물 중 적어도 1종 (250 mg)을 바이알 내에 무균 상태로 넣고, 무균 상태로 동결-건조시키고, 밀봉함으로써 제조된다. 사용을 위해, 바이알의 내용물을 2 mL의 생리 염수와 혼합하여 주사가능한 제제를 제조한다.
본 발명은 활성 성분으로서 치료 유효량의 본 발명의 화합물 중 적어도 1종을 단독으로 또는 제약 담체와 조합하여 포함하는 제약 조성물을 그의 범주 내에 포함한다. 임의로, 본 발명의 화합물은 단독으로, 본 발명의 다른 화합물과 조합되어, 또는 1종 이상, 바람직하게는 1 내지 3종의 다른 치료제(들), 예를 들어 ASK-1 억제제, CCR2/5 길항제, 오토탁신 억제제, LPA1 수용체 길항제 또는 다른 제약 활성 물질과 조합되어 사용될 수 있다.
상기 다른 치료제는, 본 발명의 화합물과 조합되어 사용되는 경우에, 예를 들어 문헌 [Physicians' Desk Reference]에 나타낸 양으로, 상기 제시된 특허에서와 같이, 또는 관련 기술분야의 통상의 기술자에 의해 달리 결정된 바와 같이 사용될 수 있다.
특히 단일 투여 단위로서 제공되는 경우에, 조합된 활성 성분들 사이의 화학적 상호작용에 대한 가능성이 존재한다. 이러한 이유로, 본 발명의 화합물 및 제2 치료제가 단일 투여 단위로 조합되는 경우에, 이들은 활성 성분이 단일 투여 단위로 조합될지라도, 활성 성분들 사이의 물리적 접촉은 최소화 (즉, 감소)되도록 제제화된다. 예를 들어, 1종의 활성 성분은 장용 코팅될 수 있다. 활성 성분 중 1종을 장용 코팅함으로써, 조합된 활성 성분들 사이의 접촉을 최소화하는 것이 가능할 뿐만 아니라, 이들 성분 중 1종이 위에서 방출되는 것이 아니라 장에서 방출되도록 위장관에서 이들 성분 중 1종의 방출을 제어하는 것이 가능하다. 또한, 활성 성분 중 1종은 위장관 전체에 걸친 지속-방출에 영향을 미치고 또한 조합된 활성 성분들 사이의 물리적 접촉을 최소화하는 역할을 하는 물질로 코팅될 수 있다. 추가로, 지속-방출 성분은 이 성분의 방출이 장에서만 발생하도록 추가적으로 장용 코팅될 수 있다. 또 다른 접근법은, 활성 성분을 추가로 분리하기 위해, 1종의 성분이 지속 및/또는 장용 방출 중합체로 코팅되고 다른 성분이 또한 중합체, 예컨대 저점도 등급의 히드록시프로필 메틸셀룰로스 (HPMC) 또는 관련 기술분야에 공지된 바와 같은 다른 적절한 물질로 코팅되는 조합 생성물의 제제화를 수반할 것이다. 중합체 코팅은 다른 성분과의 상호작용에 대한 추가의 장벽을 형성하는 역할을 한다.
단일 투여 형태로 투여되든지 또는 개별 형태이지만 동일한 방식에 의해 동일한 시간에 투여되든지, 본 발명의 조합 생성물의 성분들 사이의 접촉을 최소화하는 이들 방식 뿐만 아니라 다른 방식은 본 개시내용을 숙지한 관련 기술분야의 통상의 기술자에게 자명할 것이다.
본 발명의 화합물은 단독으로 또는 1종 이상, 바람직하게는 1 내지 3종의 추가의 치료제와 조합되어 투여될 수 있다. "조합되어 투여되는" 또는 "조합 요법"이란 본 발명의 화합물 및 1종 이상, 바람직하게는 1 내지 3종의 추가의 치료제가 치료될 포유동물에게 공동으로 투여되는 것을 의미한다. 조합되어 투여되는 경우에, 각각의 성분은 동일한 시간에 또는 상이한 시점에 임의의 순서로 순차적으로 투여될 수 있다. 따라서, 각각의 성분은 개별적으로, 그러나 목적하는 치료 효과를 제공하도록 충분히 가까운 시간 내에 투여될 수 있다.
본 발명의 화합물은 또한 FXR 효능제를 수반하는 시험 또는 검정에서 표준물 또는 참조 화합물로서, 예를 들어 품질 표준물 또는 대조군으로서 유용하다. 이러한 화합물은, 예를 들어 FXR 효능제 활성을 수반하는 제약 연구에 사용하기 위한 상업용 키트에 제공될 수 있다. 예를 들어, 본 발명의 화합물은 그의 공지된 활성을 비공지된 활성을 갖는 화합물과 비교하기 위한 검정에서 참조물로서 사용될 수 있다. 이는 실험자가 검정을 적절하게 수행하였음을 보장하고, 특히 시험 화합물이 참조 화합물의 유도체였던 경우에 비교의 기준을 제공할 것이다. 새로운 검정 또는 프로토콜을 개발하는 경우에, 본 발명에 따른 화합물은 그의 유효성을 시험하기 위해 사용될 수 있다.
본 발명은 또한 제조 물품을 포괄한다. 본원에 사용된 제조 물품은 키트 및 패키지를 포함하나 이에 제한되지는 않는 것으로 의도된다. 본 발명의 제조 물품은 다음을 포함한다: (a) 제1 용기; (b) 제1 용기 내에 배치된, 본 발명의 화합물 또는 그의 제약상 허용되는 염 형태를 포함하는 제1 치료제를 포함하는 제약 조성물; 및 (c) 제약 조성물이 이상지혈증 및 그의 후유증의 치료에 사용될 수 있다는 것을 명시한 패키지 삽입물. 또 다른 실시양태에서, 패키지 삽입물은 제약 조성물이 섬유증 및 그의 후유증의 치료를 위한 제2 치료제와 조합되어 (상기 정의된 바와 같이) 사용될 수 있다는 것을 명시한다. 제조 물품은 추가로 (d) 제2 용기를 포함할 수 있으며, 여기서 성분 (a) 및 (b)는 제2 용기 내부에 배치되고, 성분 (c)는 제2 용기 내부에 또는 외부에 배치된다. 제1 및 제2 용기 내부에 배치된다는 것은 각각의 용기가 그의 경계 내에 품목을 보유한다는 것을 의미한다.
제1 용기는 제약 조성물을 보유하는데 사용되는 리셉터클이다. 이러한 용기는 제조, 저장, 수송 및/또는 개별/벌크 판매를 위한 것일 수 있다. 제1 용기는 제약 제품의 제조, 보유, 저장 또는 분배를 위해 사용되는 병, 단지, 바이알, 플라스크, 시린지, 튜브 (예를 들어, 크림 제제용) 또는 임의의 다른 용기를 포괄하는 것으로 의도된다.
제2 용기는 제1 용기 및 임의로 패키지 삽입물을 보유하는데 사용되는 것이다. 제2 용기의 예는 박스 (예를 들어, 카드보드 또는 플라스틱), 크레이트, 카톤, 백 (예를 들어, 종이 또는 플라스틱 백), 파우치 및 봉지를 포함하나 이에 제한되지는 않는다. 패키지 삽입물은 테이프, 접착제, 스테이플 또는 또 다른 부착 방법을 통해 제1 용기의 외부에 물리적으로 부착될 수 있거나, 또는 제1 용기에 대한 임의의 물리적 부착 수단 없이 제2 용기의 내부에 놓일 수 있다. 대안적으로, 패키지 삽입물은 제2 용기의 외부에 배치된다. 제2 용기의 외부에 배치되는 경우에, 패키지 삽입물은 테이프, 접착제, 스테이플 또는 또 다른 부착 방법을 통해 물리적으로 부착되는 것이 바람직하다. 대안적으로, 이는 물리적으로 부착되지 않으면서 제2 용기의 외부에 인접해 있거나 또는 접촉되어 있을 수 있다.
패키지 삽입물은 제1 용기 내에 배치된 제약 조성물에 관한 정보를 열거하는 라벨, 태그, 마커 등이다. 기재되는 정보는 통상적으로 제조 물품이 판매되는 지역을 관할하는 규제 기관 (예를 들어, 미국 식품 의약품국)에 의해 결정될 것이다. 바람직하게는, 패키지 삽입물은 제약 조성물이 승인되었다는 표시를 구체적으로 열거한다. 패키지 삽입물은 사람이 그 안에 또는 그 위에 담긴 정보를 읽을 수 있는 임의의 물질로 제조될 수 있다. 바람직하게는, 패키지 삽입물은 그 위에 목적하는 정보가 형성 (예를 들어, 인쇄 또는 적용)된 인쇄가능한 물질 (예를 들어, 종이, 플라스틱, 카드보드, 호일, 접착성-이면 종이 또는 플라스틱 등)이다.
III. 정의
명세서 및 첨부된 청구범위 전반에 걸쳐, 주어진 화학식 또는 명칭은 이성질체가 존재하는 경우에 모든 입체 및 광학 이성질체 및 그의 라세미체를 포괄할 것이다. 달리 나타내지 않는 한, 모든 키랄 (거울상이성질체 및 부분입체이성질체) 및 라세미 형태는 본 발명의 범주 내이다. C=C 이중 결합, C=N 이중 결합, 고리계 등의 많은 기하 이성질체가 화합물에 또한 존재할 수 있으며, 모든 이러한 안정한 이성질체가 본 발명에서 고려된다. 본 발명의 화합물의 시스- 및 트랜스- (또는 E- 및 Z-) 기하 이성질체가 기재되며, 이성질체들의 혼합물로서 또는 분리된 이성질체 형태로서 단리될 수 있다. 본 발명의 화합물은 광학 활성 또는 라세미 형태로 단리될 수 있다. 광학 활성 형태는 라세미 형태의 분해에 의해 또는 광학 활성 출발 물질로부터의 합성에 의해 제조될 수 있다. 본 발명의 화합물을 제조하기 위해 사용되는 모든 방법 및 도중에 제조된 중간체는 본 발명의 일부인 것으로 간주된다. 거울상이성질체 또는 부분입체이성질체 생성물이 제조되는 경우에, 이들은 통상적인 방법에 의해, 예를 들어 크로마토그래피 또는 분별 결정화에 의해 분리될 수 있다. 방법 조건에 따라, 본 발명의 최종 생성물은 유리 (중성) 또는 염 형태로 수득된다. 이들 최종 생성물의 유리 형태 및 염 둘 다는 본 발명의 범주 내이다. 목적하는 경우에, 화합물의 한 형태는 또 다른 형태로 전환될 수 있다. 유리 염기 또는 산은 염으로 전환될 수 있고; 염은 유리 화합물 또는 또 다른 염으로 전환될 수 있고; 본 발명의 이성질체 화합물들의 혼합물은 개별 이성질체로 분리될 수 있다. 본 발명의 화합물, 그의 유리 형태 및 염은, 수소 원자가 분자의 다른 부분으로 전위되고 결과적으로 분자의 원자들 사이의 화학 결합이 재배열된 다중 호변이성질체 형태로 존재할 수 있다. 모든 호변이성질체 형태는 존재할 수 있는 한, 본 발명 내에 포함되는 것으로 이해되어야 한다. 본원에 사용된 "본 발명의 화합물" 또는 "본 발명의 화합물들"은 화학식 (I), (IIa) 또는 (IIb) 중 어느 하나에 의해 포괄되는 1종 이상의 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물을 의미한다.
본원에 사용된 용어 "알킬" 또는 "알킬렌"은 명시된 수의 탄소 원자를 갖는 분지쇄 및 직쇄 포화 지방족 탄화수소 기 둘 다를 포함하는 것으로 의도된다. "알킬"이 1가 포화 지방족 라디칼 (예컨대 에틸)을 나타내는 반면, "알킬렌"은 2가 포화 지방족 라디칼 (예컨대 에틸렌)을 나타낸다. 예를 들어, "C1 내지 C10 알킬" 또는 "C1-10 알킬"은 C1, C2, C3, C4, C5, C6 C7, C8, C9 및 C10 알킬 기를 포함하는 것으로 의도된다. 예를 들어, "C1 내지 C10 알킬렌" 또는 "C1-10 알킬렌"은 C1, C2, C3, C4, C5, C6, C7, C8, C9 및 C10 알킬렌 기를 포함하는 것으로 의도된다. 추가적으로, 예를 들어 "C1 내지 C6 알킬" 또는 "C1-6 알킬"은 1 내지 6개의 탄소 원자를 갖는 알킬을 나타내고; "C1 내지 C6 알킬렌" 또는 "C1-6 알킬렌"은 1 내지 6개의 탄소 원자를 갖는 알킬렌을 나타낸다. 알킬 기는 비치환되거나, 또는 적어도 1개의 수소가 또 다른 화학적 기에 의해 대체됨으로써 치환될 수 있다. 알킬 기의 예는 메틸 (Me), 에틸 (Et), 프로필 (예를 들어, n-프로필 및 이소프로필), 부틸 (예를 들어, n-부틸, 이소부틸, t-부틸), 및 펜틸 (예를 들어, n-펜틸, 이소펜틸, 네오펜틸)을 포함하나 이에 제한되지는 않는다. "C0 알킬" 또는 "C0 알킬렌"이 사용되는 경우에, 직접 결합을 나타내는 것으로 의도된다.
달리 나타내지 않는 한, 본원에 단독으로 또는 또 다른 기의 부분으로서 사용된 용어 "저급 알킬"은 1 내지 8개의 탄소를 함유하는 직쇄 및 분지쇄 탄화수소 둘 다를 포함하고, 본원에 단독으로 또는 또 다른 기의 부분으로서 사용된 용어 "알킬" 및 "알크"는 노르말 쇄 내에 1 내지 20개의 탄소, 바람직하게는 1 내지 10개의 탄소, 보다 바람직하게는 1 내지 8개의 탄소를 함유하는 직쇄 및 분지쇄 탄화수소 둘 다, 예컨대 메틸, 에틸, 프로필, 이소프로필, 부틸, t-부틸, 이소부틸, 펜틸, 헥실, 이소헥실, 헵틸, 4,4-디메틸펜틸, 옥틸, 2,2,4-트리메틸펜틸, 노닐, 데실, 운데실, 도데실, 그의 다양한 분지쇄 이성질체 등을 포함한다.
"헤테로알킬"은 1개 이상의 탄소 원자가 헤테로원자, 예컨대 O, N 또는 S로 대체된 알킬 기를 지칭한다. 예를 들어, 모 분자에 부착된 알킬 기의 탄소 원자가 헤테로원자 (예를 들어, O, N 또는 S)로 대체된 경우에, 생성된 헤테로알킬 기는, 각각, 알콕시 기 (예를 들어, -OCH3 등), 알킬아미노 (예를 들어, -NHCH3, -N(CH3)2 등), 또는 티오알킬 기 (예를 들어, -SCH3)이다. 모 분자에 부착되지 않은 알킬 기의 비-말단 탄소 원자가 헤테로원자 (예를 들어, O, N 또는 S)로 대체된 경우에, 생성된 헤테로알킬 기는, 각각, 알킬 에테르 (예를 들어, -CH2CH2-O-CH3 등), 알킬아미노알킬 (예를 들어, -CH2NHCH3, -CH2N(CH3)2 등), 또는 티오알킬 에테르 (예를 들어, -CH2-S-CH3)이다. 알킬 기의 말단 탄소 원자가 헤테로원자 (예를 들어, O, N 또는 S)로 대체된 경우에, 생성된 헤테로알킬 기는, 각각, 히드록시알킬 기 (예를 들어, -CH2CH2-OH), 아미노알킬 기 (예를 들어, -CH2NH2), 또는 알킬 티올 기 (예를 들어, -CH2CH2-SH)이다. 헤테로알킬 기는, 예를 들어 1 내지 20개의 탄소 원자, 1 내지 10개의 탄소 원자, 또는 1 내지 6개의 탄소 원자를 가질 수 있다. C1-C6 헤테로알킬 기는 1 내지 6개의 탄소 원자를 갖는 헤테로알킬 기를 의미한다.
"알케닐" 또는 "알케닐렌"은 명시된 수의 탄소 원자 및 쇄를 따라 임의의 안정한 지점에서 발생할 수 있는 1개 이상, 바람직하게는 1 내지 2개의 탄소-탄소 이중 결합을 갖는 직쇄형 또는 분지형 배위 중 어느 하나의 탄화수소 쇄를 포함하는 것으로 의도된다. "알케닐"이 1가 라디칼을 나타내는 반면, "알케닐렌"은 2가 라디칼을 나타낸다. 예를 들어, "C2 내지 C6 알케닐" 또는 "C2-6 알케닐" (또는 알케닐렌)은 C2, C3, C4, C5 및 C6 알케닐 기를 포함하는 것으로 의도된다. 알케닐의 예는 에테닐, 1-프로페닐, 2-프로페닐, 2-부테닐, 3-부테닐, 2-펜테닐, 3-펜테닐, 4-펜테닐, 2-헥세닐, 3-헥세닐, 4-헥세닐, 5-헥세닐, 2-메틸-2-프로페닐 및 4-메틸-3-펜테닐을 포함하나 이에 제한되지는 않는다.
"알키닐" 또는 "알키닐렌"은 쇄를 따라 임의의 안정한 지점에서 발생할 수 있는 1개 이상, 바람직하게는 1 내지 3개의 탄소-탄소 삼중 결합을 갖는 직쇄형 또는 분지형 배위 중 어느 하나의 탄화수소 쇄를 포함하는 것으로 의도된다. "알키닐"이 1가 라디칼을 나타내는 반면, "알키닐렌"은 2가 라디칼을 나타낸다. 예를 들어, "C2 내지 C6 알키닐" 또는 "C2-6 알키닐" (또는 알키닐렌)은 C2, C3, C4, C5 및 C6 알키닐 기; 예컨대 에티닐, 프로피닐, 부티닐, 펜티닐 및 헥시닐을 포함하는 것으로 의도된다.
본원에 사용된 "아릴알킬" (일명 아르알킬), "헤테로아릴알킬", "카르보시클릴알킬" 또는 "헤테로시클릴알킬"은 탄소 원자, 전형적으로 말단 또는 sp3 탄소 원자에 결합된 수소 원자 중 1개가 각각 아릴, 헤테로아릴, 카르보시클릴 또는 헤테로시클릴 라디칼로 대체된 비-시클릭 알킬 라디칼을 지칭한다. 전형적인 아릴알킬 기는 벤질, 2-페닐에탄-1-일, 나프틸메틸, 2-나프틸에탄-1-일, 나프토벤질, 2-나프토페닐에탄-1-일 등을 포함하나 이에 제한되지는 않는다. 아릴알킬, 헤테로아릴알킬, 카르보시클릴알킬 또는 헤테로시클릴알킬 기는 4 내지 20개의 탄소 원자 및 0 내지 5개의 헤테로원자를 포함할 수 있고, 예를 들어 알킬 모이어티는 1 내지 6개의 탄소 원자를 함유할 수 있다.
본원에 사용된 용어 "벤질"은 수소 원자 중 1개가 페닐 기에 의해 대체된 메틸 기를 지칭하며, 여기서 상기 페닐 기는 1 내지 5개의 기, 바람직하게는 1 내지 3개의 기, -OH, -OCH3, Cl, F, Br, I, -CN, -NO2, -NH2, -NH(CH3), -N(CH3)2, -CF3, -OCF3, -C(=O)CH3, -SCH3, -S(=O)CH3, -S(=O)2CH3, -CH3, -CH2CH3, -CO2H 및 -CO2CH3으로 임의로 치환될 수 있다. "벤질"은 또한 화학식 "Bn"에 의해 나타내어질 수 있다.
용어 "저급 알콕시", "알콕시" 또는 "알킬옥시", "아릴옥시" 또는 "아르알콕시"는 산소 원자에 연결된 임의의 상기 알킬, 아르알킬 또는 아릴 기를 지칭한다. "C1 내지 C6 알콕시" 또는 "C1-6 알콕시" (또는 알킬옥시)는 C1, C2, C3, C4, C5 및 C6 알콕시 기를 포함하는 것으로 의도된다. 알콕시 기의 예는 메톡시, 에톡시, 프로폭시 (예를 들어, n-프로폭시 및 이소프로폭시), 및 t-부톡시를 포함하나 이에 제한되지는 않는다. 유사하게, "저급 알킬티오", "알킬티오", "티오알콕시", "아릴티오" 또는 "아르알킬티오"는 황 가교를 통해 부착된, 나타낸 수의 탄소 원자를 갖는 상기 정의된 바와 같은 알킬, 아릴 또는 아르알킬 기; 예를 들어 메틸-S- 및 에틸-S-를 나타낸다.
본원에서 단독으로 또는 또 다른 기의 부분으로서 사용된 용어 "알카노일" 또는 "알킬카르보닐"은 카르보닐 기에 연결된 알킬을 지칭한다. 예를 들어, 알킬카르보닐은 알킬-C(O)-에 의해 나타내어질 수 있다. "C1 내지 C6 알킬카르보닐" (또는 알킬카르보닐)은 C1, C2, C3, C4, C5 및 C6 알킬-C(O)- 기를 포함하는 것으로 의도된다.
본원에서 단독으로 또는 또 다른 기의 부분으로서 사용된 용어 "알킬술포닐" 또는 "술폰아미드"는 술포닐 기에 연결된 알킬 또는 아미노를 지칭한다. 예를 들어, 알킬술포닐은 -S(O)2R'에 의해 나타내어질 수 있으며, 반면 술폰아미드는 -S(O)2NRcRd에 의해 나타내어질 수 있다. R'는 C1 내지 C6 알킬이고, Rc 및 Rd는 "아미노"에 대해 하기 정의된 바와 동일하다.
본원에서 단독으로 또는 또 다른 기의 부분으로서 사용된 용어 "카르바메이트"는 아미도 기에 연결된 산소를 지칭한다. 예를 들어, 카르바메이트는 N(RcRd)-C(O)-O-에 의해 나타내어질 수 있고, Rc 및 Rd는 "아미노"에 대해 하기 정의된 바와 동일하다.
본원에서 단독으로 또는 또 다른 기의 부분으로서 사용되는 용어 "아미도"는 카르보닐 기에 연결된 아미노를 지칭한다. 예를 들어, 아미도는 N(RcRd)-C(O)-에 의해 나타내어질 수 있고, Rc 및 Rd는 "아미노"에 대해 하기 정의된 바와 동일하다.
용어 "아미노"는 -NRc1Rc2로 정의되며, 여기서 Rc1 및 Rc2는 독립적으로 H 또는 C1-6 알킬이거나; 또는 대안적으로, Rc1 및 Rc2는 이들이 부착되어 있는 원자와 함께, 할로, 시아노, 히드록실, 아미노, 옥소, C1-6 알킬, 알콕시 및 아미노알킬로부터 선택된 1개 이상의 기로 임의로 치환된 3- 내지 8-원 헤테로시클릭 고리를 형성한다. Rc1 또는 Rc2 (또는 이들 둘 다)가 C1-6 알킬인 경우에, 아미노 기는 또한 알킬아미노로 지칭될 수 있다. 알킬아미노 기의 예는 비제한적으로 -NH2, 메틸아미노, 에틸아미노, 프로필아미노, 이소프로필아미노 등을 포함한다.
용어 "아미노알킬"은 수소 원자 중 1개가 아미노 기에 의해 대체된 알킬 기를 지칭한다. 예를 들어, 아미노알킬은 N(Rc1Rc2)-알킬렌-에 의해 나타내어질 수 있다. "C1 내지 C6" 또는 "C1-6" 아미노알킬 (또는 아미노알킬)은 C1, C2, C3, C4, C5 및 C6 아미노알킬 기를 포함하는 것으로 의도된다.
본원에서 단독으로 또는 또 다른 기의 부분으로서 사용된 용어 "할로겐" 또는 "할로"는 염소, 브로민, 플루오린 및 아이오딘을 지칭하며, 염소 또는 플루오린이 바람직하다.
"할로알킬"은 1개 이상의 할로겐으로 치환된, 명시된 수의 탄소 원자를 갖는 분지쇄 및 직쇄 포화 지방족 탄화수소 기 둘 다를 포함하는 것으로 의도된다. "C1 내지 C6 할로알킬" 또는 "C1-6 할로알킬" (또는 할로알킬)은 C1, C2, C3, C4, C5 및 C6 할로알킬 기를 포함하는 것으로 의도된다. 할로알킬의 예는 플루오로메틸, 디플루오로메틸, 트리플루오로메틸, 트리클로로메틸, 펜타플루오로에틸, 펜타클로로에틸, 2,2,2-트리플루오로에틸, 헵타플루오로프로필 및 헵타클로로프로필을 포함하나 이에 제한되지는 않는다. 할로알킬의 예는 1개 이상의 플루오린 원자로 치환된, 명시된 수의 탄소 원자를 갖는 분지쇄 및 직쇄 포화 지방족 탄화수소 기 둘 다를 포함하는 것으로 의도된 "플루오로알킬"을 또한 포함한다. 본원에 사용된 용어 "폴리할로알킬"은 2 내지 9개, 바람직하게는 2 내지 5개의 할로 치환기, 예컨대 F 또는 Cl, 바람직하게는 F를 포함하는 상기 정의된 바와 같은 "알킬" 기, 예컨대 폴리플루오로알킬, 예를 들어 CF3CH2, CF3 또는 CF3CF2CH2를 지칭한다.
"할로알콕시" 또는 "할로알킬옥시"는 산소 가교를 통해 부착된, 나타낸 수의 탄소 원자를 갖는 상기 정의된 바와 같은 할로알킬 기를 나타낸다. 예를 들어, "C1 내지 C6 할로알콕시" 또는 "C1-6 할로알콕시"는 C1, C2, C3, C4, C5 및 C6 할로알콕시 기를 포함하는 것으로 의도된다. 할로알콕시의 예는 트리플루오로메톡시, 2,2,2-트리플루오로에톡시 및 펜타플루오로에톡시를 포함하나 이에 제한되지는 않는다. 할로알콕시의 다른 예는 또한, 산소 가교를 통해 부착된, 나타낸 수의 탄소 원자를 갖는 상기 정의된 바와 같은 플루오로알킬 기를 나타내는 "플루오로알콕시"를 포함한다. 유사하게, "할로알킬티오" 또는 "티오할로알콕시"는 황 가교를 통해 부착된, 나타낸 수의 탄소 원자를 갖는 상기 정의된 바와 같은 할로알킬 기; 예를 들어, 트리플루오로메틸-S- 및 펜타플루오로에틸-S-를 나타낸다. 본원에 사용된 용어 "폴리할로알콕시"는 2 내지 9개, 바람직하게는 2 내지 5개의 할로 치환기, 예컨대 F 또는 Cl, 바람직하게는 F를 포함하는 상기 정의된 바와 같은 "알콕시" 또는 "알킬옥시" 기, 예컨대 폴리플루오로알콕시, 예를 들어 -OCH2CF3, -ΟCF3 또는 -ΟCH2CF2CF3을 지칭한다.
"히드록시알킬"은 1개 이상의 히드록실 (OH)로 치환된, 명시된 수의 탄소 원자를 갖는 분지쇄 및 직쇄 포화 지방족 탄화수소 기 둘 다를 포함하는 것으로 의도된다. "C1 내지 C6 히드록시알킬" (또는 히드록시알킬)은 C1, C2, C3, C4, C5 및 C6 히드록시알킬 기를 포함하는 것으로 의도된다.
용어 "시클로알킬"은 모노-, 비- 또는 폴리-시클릭 고리계를 포함한 고리화 알킬 기를 지칭한다. "C3 내지 C7 시클로알킬" 또는 "C3-7 시클로알킬"은 C3, C4, C5, C6 및 C7 시클로알킬 기를 포함하는 것으로 의도된다. 시클로알킬 기의 예는 시클로프로필, 시클로부틸, 시클로펜틸, 시클로헥실 및 노르보르닐을 포함하나 이에 제한되지는 않는다. 분지형 시클로알킬 기, 예컨대 1-메틸시클로프로필 및 2-메틸시클로프로필은 "시클로알킬"의 정의에 포함된다.
용어 "시클로헤테로알킬"은 모노-, 비- 또는 폴리-시클릭 고리계를 포함한 고리화 헤테로알킬 기를 지칭한다. "C3 내지 C7 시클로헤테로알킬" 또는 "C3-7 시클로헤테로알킬"은 C3, C4, C5, C6 및 C7 시클로헤테로알킬 기를 포함하는 것으로 의도된다. 시클로헤테로알킬 기의 예는 옥세타닐, 테트라히드로푸라닐, 테트라히드로피라닐, 아제티디닐, 피롤리디닐, 피페리디닐, 모르폴리닐 및 피페라지닐을 포함하나 이에 제한되지는 않는다. 분지형 시클로헤테로알킬 기, 예컨대 피페리디닐메틸, 피페라지닐메틸, 모르폴리닐메틸, 피리디닐메틸, 피리디질메틸, 피리미딜메틸 및 피라지닐메틸은 "시클로헤테로알킬"의 정의에 포함된다.
본원에 사용된 용어 "아자시클릴"은 고리에 1개 이상의 질소 원자를 함유하는 시클로헤테로알킬을 지칭한다. 아자시클릴 기의 예는 피롤리디닐, 피페리디닐, 모르폴리닐 및 피페라지닐을 포함하나 이에 제한되지는 않는다.
본원에 사용된 "카르보사이클", "카르보시클릴" 또는 "카르보시클릭"은 임의의 안정한 3-, 4-, 5-, 6-, 7- 또는 8-원 모노시클릭 또는 5-, 6-, 7-, 8-, 9-, 10-, 11-, 12- 또는 13-원 폴리시클릭 (비시클릭 또는 트리시클릭 포함) 탄화수소 고리 (이들 중 임의의 것은 포화 또는 부분 불포화일 수 있음)를 의미하는 것으로 의도된다. 즉, 용어 "카르보사이클", "카르보시클릴" 또는 "카르보시클릭"은 비제한적으로 시클로알킬 및 시클로알케닐을 포함한다. 이러한 카르보사이클의 예는 시클로프로필, 시클로부틸, 시클로부테닐, 시클로펜틸, 시클로펜테닐, 시클로헥실, 시클로헵테닐, 시클로헵틸, 시클로헵테닐, 아다만틸, 시클로옥틸, 시클로옥테닐, 시클로옥타디에닐, [3.3.0]비시클로옥탄, [4.3.0]비시클로노난, [4.4.0]비시클로데칸 (데칼린), [2.2.2]비시클로옥탄, 플루오레닐, 인다닐, 아다만틸, 및 테트라히드로나프틸 (테트랄린)을 포함하나 이에 제한되지는 않는다. 상기 제시된 바와 같이, 가교된 고리가 또한 카르보사이클의 정의에 포함된다 (예를 들어, [2.2.2]비시클로옥탄). 바람직한 카르보사이클은, 달리 명시되지 않는 한, 시클로프로필, 시클로부틸, 시클로펜틸, 시클로헥실, 인다닐 및 테트라히드로나프틸이다. 가교된 고리는 1개 이상, 바람직하게는 1 내지 3개의 탄소 원자가 2개의 비-인접 탄소 원자를 연결하는 경우에 발생한다. 바람직한 가교는 1 또는 2개의 탄소 원자이다. 가교는 항상 모노시클릭 고리를 트리시클릭 고리로 전환시킨다는 것에 주목한다. 고리가 가교된 경우에, 고리에 대해 열거된 치환기가 또한 가교 상에 존재할 수 있다.
추가로, 본원에서 단독으로 또는 또 다른 기의 부분으로서 사용된 용어 "시클로알킬" 및 "시클로알케닐"을 포함한 "카르보시클릴"은 고리를 형성하는 총 3 내지 20개의 탄소, 바람직하게는 고리를 형성하는 3 내지 10개의 탄소 또는 3 내지 6개의 탄소를 함유하는, 1 내지 3개의 고리를 함유하는 포화 또는 부분 불포화 (1 또는 2개의 이중 결합을 함유함) 시클릭 탄화수소 기, 예를 들어 모노시클릭알킬, 비시클릭알킬 및 트리시클릭알킬을 포함하고, 이들은 아릴에 대해 기재된 바와 같은 1 또는 2개의 방향족 고리에 융합될 수 있고, 이들은 시클로프로필, 시클로부틸, 시클로펜틸, 시클로헥실, 시클로헵틸, 시클로옥틸, 시클로데실 및 시클로도데실, 시클로헥세닐,
를 포함하고, 이들 기 중 임의의 것은 1 내지 4개의 치환기, 예컨대 할로겐, 알킬, 알콕시, 히드록시, 아릴, 아릴옥시, 아릴알킬, 시클로알킬, 알킬아미도, 알카노일아미노, 옥소, 아실, 아릴카르보닐아미노, 니트로, 시아노, 티올 및/또는 알킬티오 및/또는 임의의 알킬 치환기로 임의로 치환될 수 있다.
본원에 사용된 용어 "비시클릭 카르보사이클" 또는 "비시클릭 카르보시클릭 기"는, 2개의 융합된 고리를 함유하고 탄소 원자로 이루어진 안정한 9- 또는 10-원 카르보시클릭 고리계를 의미하는 것으로 의도된다. 2개의 융합된 고리 중, 1개의 고리는 제2 고리에 융합된 벤조 고리이고; 제2 고리는 포화 또는 부분 불포화인 5- 또는 6-원 탄소 고리이다. 비시클릭 카르보시클릭 기는 안정한 구조를 생성하는 임의의 탄소 원자에서 그의 펜던트 기에 부착될 수 있다. 본원에 기재된 비시클릭 카르보시클릭 기는 생성된 화합물이 안정한 경우에 임의의 탄소 상에서 치환될 수 있다. 비시클릭 카르보시클릭 기의 예는 1,2-디히드로나프틸, 1,2,3,4-테트라히드로나프틸 및 인다닐이나 이에 제한되지는 않는다.
본원에서 단독으로 또는 또 다른 기의 부분으로서 본원에 사용된 용어 "아릴"은, 예를 들어 페닐, 나프틸, 안트라세닐 및 페난트라닐을 포함한 모노시클릭 또는 폴리시클릭 (비시클릭 및 트리시클릭 포함) 방향족 탄화수소를 지칭한다. 아릴 모이어티는 널리 공지되어 있고, 예를 들어 문헌 [Lewis, R.J., ed., Hawley's Condensed Chemical Dictionary, 13th Edition, John Wiley & Sons, Inc., New York (1997)]에 기재되어 있다. 한 실시양태에서, 용어 "아릴"은 고리 부분에 6 내지 10개의 탄소를 함유하는 모노시클릭 및 비시클릭 방향족 기를 나타낸다 (예컨대 페닐, 또는 1-나프틸 및 2-나프틸을 포함한 나프틸). 예를 들어, "C6 또는 C10 아릴" 또는 "C6-10 아릴"은 페닐 및 나프틸을 지칭한다. 달리 명시되지 않는 한, "아릴", "C6 또는 C10 아릴", "C6-10 아릴" 또는 "방향족 잔기"는 비치환되거나, 또는 -OH, -OCH3, F, Cl, Br, I, -CN, -NO2, -NH2, -N(CH3)H, -N(CH3)2, -CF3, -OCF3, -C(O)CH3, -SCH3, -S(O)CH3, -S(O)2CH3, -CH3, -CH2CH3, -CO2H 및 -CO2CH3으로부터 선택된 1 내지 5개의 기, 바람직하게는 1 내지 3개의 기로 치환될 수 있다.
본원에 사용된 용어 "헤테로사이클", "헤테로시클릴" 또는 "헤테로시클릭 기"는 포화 또는 부분 불포화이고, 탄소 원자, 및 N, O 및 S로 이루어진 군으로부터 독립적으로 선택된 1, 2, 3 또는 4개의 헤테로원자를 함유하는 안정한 3-, 4-, 5-, 6- 또는 7-원 모노시클릭 또는 5-, 6-, 7-, 8-, 9-, 10-, 11-, 12-, 13- 또는 14-원 폴리시클릭 (비시클릭 및 트리시클릭 포함) 헤테로시클릭 고리를 의미하는 것으로 의도되며; 상기 정의된 헤테로시클릭 고리 중 임의의 것이 카르보시클릭 또는 아릴 (예를 들어, 벤젠) 고리에 융합된 임의의 폴리시클릭 기를 포함한다. 즉, 용어 "헤테로사이클", "헤테로시클릴" 또는 "헤테로시클릭 기"는 비-방향족 고리계, 예컨대 헤테로시클로알킬 및 헤테로시클로알케닐을 포함한다. 질소 및 황 헤테로원자는 임의로 산화될 수 있다 (즉, N→O 및 S(O)p, 여기서 p는 0, 1 또는 2임). 질소 원자는 치환 또는 비치환될 수 있다 (즉, N 또는 NR, 여기서 R은 H, 또는 정의된 경우에는 또 다른 치환기임). 헤테로시클릭 고리는 안정한 구조를 생성하는 임의의 헤테로원자 또는 탄소 원자에서 그의 펜던트 기에 부착될 수 있다. 본원에 기재된 헤테로시클릭 고리는 생성된 화합물이 안정한 경우에 탄소 상에서 또는 질소 원자 상에서 치환될 수 있다. 헤테로사이클 내의 질소는 임의로 4급화될 수 있다. 헤테로사이클 내의 S 및 O 원자의 총수가 1개 초과인 경우에는, 이들 헤테로원자가 서로 인접하지 않는 것이 바람직하다. 헤테로사이클 내의 S 및 O 원자의 총수가 1개 이하인 것이 바람직하다. 헤테로시클릴의 예는 비제한적으로 아제티디닐, 피페라지닐, 피페리디닐, 피페리도닐, 피페로닐, 피라닐, 모르폴리닐, 테트라히드로푸라닐, 테트라히드로이소퀴놀리닐, 테트라히드로퀴놀리닐, 모르폴리닐, 디히드로푸로[2,3-b]테트라히드로푸란을 포함한다.
본원에 사용된 용어 "비시클릭 헤테로사이클" 또는 "비시클릭 헤테로시클릭 기"는 2개의 융합된 고리를 함유하고, 탄소 원자, 및 N, O 및 S로 이루어진 군으로부터 독립적으로 선택된 1, 2, 3 또는 4개의 헤테로원자로 이루어진 안정한 9- 또는 10-원 헤테로시클릭 고리계를 의미하는 것으로 의도된다. 2개의 융합된 고리 중, 1개의 고리는, 제2 고리에 각각 융합된 5-원 헤테로아릴 고리, 6-원 헤테로아릴 고리 또는 벤조 고리를 포함하는 5- 또는 6-원 모노시클릭 방향족 고리이다. 제2 고리는 포화, 부분 불포화 또는 불포화인 5- 또는 6-원 모노시클릭 고리이며, 5-원 헤테로사이클, 6-원 헤테로사이클 또는 카르보사이클 (단, 제2 고리가 카르보사이클인 경우에, 제1 고리는 벤조가 아님)을 포함한다.
비시클릭 헤테로시클릭 기는 안정한 구조를 생성하는 임의의 헤테로원자 또는 탄소 원자에서 그의 펜던트 기에 부착될 수 있다. 본원에 기재된 비시클릭 헤테로시클릭 기는 생성된 화합물이 안정한 경우에 탄소 상에서 또는 질소 원자 상에서 치환될 수 있다. 헤테로사이클 내의 S 및 O 원자의 총수가 1개 초과인 경우에는, 이들 헤테로원자가 서로 인접하지 않는 것이 바람직하다. 헤테로사이클 내의 S 및 O 원자의 총수가 1개 이하인 것이 바람직하다. 비시클릭 헤테로시클릭 기의 예는 1,2,3,4-테트라히드로퀴놀리닐, 1,2,3,4-테트라히드로이소퀴놀리닐, 5,6,7,8-테트라히드로-퀴놀리닐, 2,3-디히드로-벤조푸라닐, 크로마닐, 1,2,3,4-테트라히드로-퀴녹살리닐 및 1,2,3,4-테트라히드로-퀴나졸리닐이나 이에 제한되지는 않는다.
가교된 고리는 또한 헤테로사이클의 정의에 포함된다. 가교된 고리는 1개 이상, 바람직하게는 1 내지 3개의 원자 (즉, C, O, N 또는 S)가 2개의 비-인접 탄소 또는 질소 원자를 연결하는 경우에 발생한다. 가교된 고리의 예는 1개의 탄소 원자, 2개의 탄소 원자, 1개의 질소 원자, 2개의 질소 원자, 및 탄소-질소 기를 포함하나 이에 제한되지는 않는다. 가교는 항상 모노시클릭 고리를 트리시클릭 고리로 전환시킨다는 것에 주목한다. 고리가 가교된 경우에, 고리에 대해 열거된 치환기가 또한 가교 상에 존재할 수 있다.
본원에 사용된 용어 "헤테로아릴"은 적어도 1개의 헤테로원자 고리원, 예컨대 황, 산소 또는 질소를 포함하는 안정한 모노시클릭 및 폴리시클릭 (비시클릭 및 트리시클릭 포함) 방향족 탄화수소를 의미하는 것으로 의도된다. 헤테로아릴 기는 비제한적으로 피리디닐, 피리미디닐, 피라지닐, 피리다지닐, 트리아지닐, 푸릴, 퀴놀릴, 이소퀴놀릴, 티에닐, 이미다졸릴, 티아졸릴, 인돌릴, 피로일, 옥사졸릴, 벤조푸릴, 벤조티에닐, 벤즈티아졸릴, 이속사졸릴, 피라졸릴, 트리아졸릴, 테트라졸릴, 인다졸릴, 1,2,4-티아디아졸릴, 이소티아졸릴, 퓨리닐, 카르바졸릴, 벤즈이미다졸릴, 인돌리닐, 벤조디옥솔라닐 및 벤조디옥산을 포함한다. 헤테로아릴 기는 치환 또는 비치환된다. 질소 원자는 치환 또는 비치환된다 (즉, N 또는 NR, 여기서 R은 H, 또는 정의된 경우에는 또 다른 치환기임). 질소 및 황 헤테로원자는 임의로 산화될 수 있다 (즉, N→O 및 S(O)p, 여기서 p는 0, 1 또는 2임).
헤테로아릴의 예는 아크리디닐, 아조시닐, 벤즈이미다졸릴, 벤조푸라닐, 벤조티오푸라닐, 벤조티오페닐, 벤족사졸릴, 벤족사졸리닐, 벤즈티아졸릴, 벤즈트리아졸릴, 벤즈테트라졸릴, 벤즈이속사졸릴, 벤즈이소티아졸릴, 벤즈이미다졸리닐, 카르바졸릴, 4aH-카르바졸릴, 카르볼리닐, 크로마닐, 크로메닐, 신놀리닐, 데카히드로퀴놀리닐, 2H,6H-1,5,2-디티아지닐, 푸라닐, 푸라자닐, 이미다졸리디닐, 이미다졸리닐, 이미다졸릴, 1H-인다졸릴, 이미다졸로피리디닐, 인돌레닐, 인돌리닐, 인돌리지닐, 인돌릴, 3H-인돌릴, 이사티노일, 이소벤조푸라닐, 이소크로마닐, 이소인다졸릴, 이소인돌리닐, 이소인돌릴, 이소퀴놀리닐, 이소티아졸릴, 이소티아졸로피리디닐, 이속사졸릴, 이속사졸로피리디닐, 메틸렌디옥시페닐, 나프티리디닐, 옥타히드로이소퀴놀리닐, 옥사디아졸릴, 1,2,3-옥사디아졸릴, 1,2,4-옥사디아졸릴, 1,2,5-옥사디아졸릴, 1,3,4-옥사디아졸릴, 옥사졸리디닐, 옥사졸릴, 옥사졸로피리디닐, 옥사졸리디닐페리미디닐, 옥스인돌릴, 피리미디닐, 페난트리디닐, 페난트롤리닐, 페나지닐, 페노티아지닐, 페녹사티아닐, 페녹사지닐, 프탈라지닐, 프테리디닐, 퓨리닐, 피라지닐, 피라졸리디닐, 피라졸리닐, 피라졸로피리디닐, 피라졸릴, 피리다지닐, 피리도옥사졸릴, 피리도이미다졸릴, 피리도티아졸릴, 피리디닐, 피리미디닐, 피롤리디닐, 피롤리닐, 2-피롤리도닐, 2H-피롤릴, 피롤릴, 퀴나졸리닐, 퀴놀리닐, 4H-퀴놀리지닐, 퀴녹살리닐, 퀴누클리디닐, 테트라졸릴, 테트라히드로푸라닐, 테트라히드로이소퀴놀리닐, 테트라히드로퀴놀리닐, 6H-1,2,5-티아디아지닐, 1,2,3-티아디아졸릴, 1,2,4-티아디아졸릴, 1,2,5-티아디아졸릴, 1,3,4-티아디아졸릴, 티안트레닐, 티아졸릴, 티에닐, 티아졸로피리디닐, 티에노티아졸릴, 티에노옥사졸릴, 티에노이미다졸릴, 티오페닐, 트리아지닐, 1,2,3-트리아졸릴, 1,2,4-트리아졸릴, 1,2,5-트리아졸릴, 1,3,4-트리아졸릴 및 크산테닐을 포함하나 이에 제한되지는 않는다.
5- 내지 10-원 헤테로아릴의 예는 피리디닐, 푸라닐, 티에닐, 피라졸릴, 이미다졸릴, 이미다졸리디닐, 인돌릴, 테트라졸릴, 이속사졸릴, 옥사졸릴, 옥사디아졸릴, 옥사졸리디닐, 티아디아지닐, 티아디아졸릴, 티아졸릴, 트리아지닐, 트리아졸릴, 벤즈이미다졸릴, 1H-인다졸릴, 벤조푸라닐, 벤조티오푸라닐, 벤즈테트라졸릴, 벤조트리아졸릴, 벤즈이속사졸릴, 벤족사졸릴, 옥스인돌릴, 벤족사졸리닐, 벤즈티아졸릴, 벤즈이소티아졸릴, 이사티노일, 이소퀴놀리닐, 옥타히드로이소퀴놀리닐, 이속사졸로피리디닐, 퀴나졸리닐, 퀴놀리닐, 이소티아졸로피리디닐, 티아졸로피리디닐, 옥사졸로피리디닐, 이미다졸로피리디닐 및 피라졸로피리디닐을 포함하나 이에 제한되지는 않는다. 5- 내지 6-원 헤테로사이클의 예는 피리디닐, 푸라닐, 티에닐, 피롤릴, 피라졸릴, 피라지닐, 이미다졸릴, 이미다졸리디닐, 인돌릴, 테트라졸릴, 이속사졸릴, 옥사졸릴, 옥사디아졸릴, 옥사졸리디닐, 티아디아지닐, 티아디아졸릴, 티아졸릴, 트리아지닐 및 트리아졸릴을 포함하나 이에 제한되지는 않는다.
달리 나타내지 않는 한, "카르보시클릴" 또는 "헤테로시클릴"은 카르보시클릭 고리 또는 헤테로시클릭 고리에 융합된 1 내지 3개의 추가의 고리, 예컨대 아릴, 시클로알킬, 헤테로아릴 또는 시클로헤테로알킬 고리, 예를 들어
를 포함하고, 수소, 할로, 할로알킬, 알킬, 할로알킬, 알콕시, 할로알콕시, 알케닐, 트리플루오로메틸, 트리플루오로메톡시, 알키닐, 시클로알킬-알킬, 시클로헤테로알킬, 시클로헤테로알킬알킬, 아릴, 헤테로아릴, 아릴알킬, 아릴옥시, 아릴옥시알킬, 아릴알콕시, 알콕시카르보닐, 아릴카르보닐, 아릴알케닐, 아미노카르보닐아릴, 아릴티오, 아릴술피닐, 아릴라조, 헤테로아릴알킬, 헤테로아릴알케닐, 헤테로아릴헤테로아릴, 헤테로아릴옥시, 히드록시, 니트로, 시아노, 티올, 알킬티오, 아릴티오, 헤테로아릴티오, 아릴티오알킬, 알콕시아릴티오, 알킬카르보닐, 아릴카르보닐, 알킬아미노카르보닐, 아릴아미노카르보닐, 알콕시카르보닐, 아미노카르보닐, 알킬카르보닐옥시, 아릴카르보닐옥시, 알킬카르보닐아미노, 아릴카르보닐아미노, 아릴술피닐, 아릴술피닐알킬, 아릴술포닐아미노 및 아릴술폰아미노카르보닐 및/또는 본원에 제시된 임의의 알킬 치환기로부터 선택된 1, 2 또는 3개의 기로 이용가능한 탄소 원자를 통해 임의로 치환될 수 있다.
용어 알킬, 알케닐, 알키닐, 시클로알킬, 카르보시클릴, 헤테로시클릴, 아릴 및 헤테로아릴 중 임의의 것이 또 다른 기의 부분으로서 사용되는 경우에, 탄소 원자 및 고리원의 수는 상기 용어 자체에서 정의된 것과 동일하다. 예를 들어, 알콕시, 할로알콕시, 알킬아미노, 할로알킬, 히드록시알킬, 아미노알킬, 할로알콕시, 알콕시알콕시, 할로알킬아미노, 알콕시알킬아미노, 할로알콕시알킬아미노, 알킬티오 등은 각각 독립적으로 용어 "알킬"에 대해 정의된 바와 동일한 탄소 원자의 수, 예컨대 1 내지 4개의 탄소 원자, 1 내지 6개의 탄소 원자, 1 내지 10개의 탄소 원자 등을 함유한다. 유사하게, 시클로알콕시, 헤테로시클릴옥시, 시클로알킬아미노, 헤테로시클릴아미노, 아르알킬아미노, 아릴아미노, 아릴옥시, 아르알킬옥시, 헤테로아릴옥시, 헤테로아릴알킬옥시 등은 각각 독립적으로 용어 "시클로알킬", "헤테로시클릴", "아릴" 및 "헤테로아릴"에 대해 정의된 바와 동일한 고리원, 예컨대 3 내지 6-원, 4 내지 7-원, 6 내지 10-원, 5 내지 10-원, 5- 또는 6-원 등을 함유한다.
관련 기술분야에 사용된 규정에 따라, 본원의 구조 화학식에 사용된 와 같이, 볼드 선을 가리키는 결합은 코어 또는 백본 구조에 대한 모이어티 또는 치환기의 부착 지점인 결합을 도시한다.
관련 기술분야에 사용된 규정에 따라, 구조 화학식, 예컨대 에서의 파상 또는 물결 결합은 X', Y' 및 Z'가 부착된 탄소 원자의 입체생성 중심을 도시하는데 사용되고, 두 거울상이성질체를 단일 도면에서 나타내기 위해 의도된다. 즉, 예컨대 파상 결합을 갖는 구조 화학식은 각각의 거울상이성질체를 개별적으로, 예컨대 로 나타낼 뿐만 아니라 그의 라세미 혼합물을 나타낸다. 파상 또는 물결 결합이 이중 결합 (예컨대 C=C 또는 C=N) 모이어티에 부착되는 경우에, 시스- 또는 트랜스- (또는 E- 및 Z-) 기하 이성질체 또는 그의 혼합물을 포함한다.
카르보시클릭 또는 헤테로시클릭 모이어티가 결합되거나 또는 달리 구체적 부착 지점을 나타내지 않고 상이한 고리 원자를 통해 지정된 기재에 부착되는 경우에, 탄소 원자를 통하든지 또는 예를 들어 3가 질소 원자를 통하든지 모든 가능한 지점이 의도되는 것으로 본원에서 이해된다. 예를 들어, 용어 "피리디닐" 또는 "피리딜"은 2-, 3- 또는 4-피리디닐을 의미하고, 용어 "티에닐"은 2- 또는 3-티에닐을 의미하는 등이다.
치환기에 대한 결합이 고리 내의 2개의 원자를 연결하는 결합을 가로지르는 것으로 제시된 경우에, 이러한 치환기는 고리 상의 임의의 원자에 결합될 수 있다. 치환기가 주어진 화학식의 화합물의 나머지에 결합된 원자를 나타내지 않으면서 이러한 치환기가 열거된 경우에, 이러한 치환기는 이러한 치환기 내의 임의의 원자를 통해 결합될 수 있다. 치환기 및/또는 가변기의 조합은, 이러한 조합이 안정한 화합물을 생성하는 경우에만 허용가능하다.
관련 기술분야의 통상의 기술자는 본 발명의 화합물의 치환기 및 다른 모이어티가 허용가능하게 안정한 제약 조성물로 제제화될 수 있는 제약상 유용한 화합물을 제공하기 위해 충분히 안정한 화합물을 제공하도록 선택되어야 한다는 것을 인식할 것이다. 이러한 안정성을 갖는 본 발명의 화합물은 본 발명의 범주 내에 속하는 것으로 고려된다.
용어 "반대 이온"은 음으로 하전된 종, 예컨대 클로라이드, 브로마이드, 히드록시드, 아세테이트 및 술페이트를 나타내는데 사용된다. 용어 "금속 이온"은 알칼리 금속 이온, 예컨대 나트륨, 칼륨 또는 리튬, 및 알칼리 토금속 이온, 예컨대 마그네슘 및 칼슘, 뿐만 아니라 아연 및 알루미늄을 지칭한다.
본원에 언급된 용어 "치환된"은, 정상 원자가가 유지되고 치환이 안정한 화합물을 생성하는 것을 조건으로, (탄소 원자 또는 헤테로원자에 부착된) 적어도 1개의 수소 원자가 비-수소 기로 대체된 것을 의미한다. 치환기가 옥소 (즉, =O)인 경우에, 원자 상의 2개의 수소가 대체된다. 옥소 치환기는 방향족 모이어티 상에 존재하지 않는다. 고리계 (예를 들어, 카르보시클릭 또는 헤테로시클릭)가 카르보닐 기 또는 이중 결합으로 치환된 것으로 언급된 경우에, 카르보닐 기 또는 이중 결합이 고리의 부분인 것으로 (즉, 내부에 있는 것으로) 의도된다. 본원에 사용된 고리 이중 결합은 2개의 인접한 고리 원자 사이에 형성된 이중 결합 (예를 들어, C=C, C=N, 또는 N=N)이다. 알킬, 시클로알킬, 헤테로알킬, 시클로헤테로알킬, 알킬렌, 아릴, 아릴알킬, 헤테로아릴, 헤테로아릴알킬, 카르보시클릴 및 헤테로시클릴에 관한 용어 "치환된"은, 각각 탄소 또는 헤테로원자에 부착된 1개 이상의 수소 원자가 각각 독립적으로 1개 이상의 비-수소 치환기(들)로 대체된 알킬, 시클로알킬, 헤테로알킬, 시클로헤테로알킬, 알킬렌, 아릴, 아릴알킬, 헤테로아릴, 헤테로아릴알킬, 카르보시클릴 및 헤테로시클릴을 의미한다.
본 발명의 화합물 상에 질소 원자 (예를 들어, 아민)가 존재하는 경우에, 이들은 산화제 (예를 들어, mCPBA 및/또는 과산화수소)로의 처리에 의해 N-옥시드로 전환되어 본 발명의 다른 화합물을 제공할 수 있다. 따라서, 제시되고 청구된 질소 원자는 제시된 질소 및 그의 N-옥시드 (N→O) 유도체 둘 다를 포괄하는 것으로 간주된다.
임의의 가변기가 화합물에 대한 임의의 구성성분 또는 화학식에서 1회 초과로 발생하는 경우에, 각각의 경우에서의 그의 정의는 모든 다른 경우에서의 그의 정의와 독립적이다. 따라서, 예를 들어, 기가 0, 1, 2 또는 3개의 R 기로 치환되는 것으로 제시되는 경우에, 상기 기는 0개의 R 기로 치환되는 경우에 비치환되거나 또는 3개 이하의 R 기로 치환되고, 각각의 경우에 R은 R의 정의로부터 독립적으로 선택된다.
또한, 치환기 및/또는 가변기의 조합은 이러한 조합이 안정한 화합물을 생성하는 경우에만 허용가능하다.
본원에 사용된 용어 "호변이성질체"는 평형 상태에서 함께 존재하고 분자 내의 원자 또는 기의 이동에 의해 용이하게 상호교환되는 화합물의 2종 이상의 이성질체 각각을 지칭한다. 예를 들어, 관련 기술분야의 통상의 기술자는 1,2,3-트리아졸이 상기 정의된 바와 같은 2종의 호변이성질체 형태로 존재한다는 것을 용이하게 이해할 것이다:
따라서, 본 개시내용은, 심지어 구조가 이들 중 단지 1종만을 도시하는 경우에도, 모든 가능한 호변이성질체를 포괄하는 것으로 의도된다.
어구 "제약상 허용되는"은 타당한 의학적 판단의 범주 내에서, 합리적인 이익/위험 비에 상응하는, 과도한 독성, 자극, 알레르기 반응, 및/또는 다른 문제 또는 합병증 없이 인간 및 동물의 조직과 접촉시켜 사용하기에 적합한 이들 화합물, 물질, 조성물 및/또는 투여 형태를 지칭하기 위해 본원에 사용된다.
본 발명의 화합물은 또한 본 발명의 범주 내에 있는 염으로서 존재할 수 있다. 제약상 허용되는 염이 바람직하다. 본원에 사용된 "제약상 허용되는 염"은 모 화합물이 그의 산 또는 염기 염을 제조함으로써 변형된 개시된 화합물의 유도체를 지칭한다. 본 발명의 제약상 허용되는 염은 통상적인 화학적 방법에 의해 염기성 또는 산성 모이어티를 함유하는 모 화합물로부터 합성될 수 있다. 일반적으로, 이러한 염은 물 중에서 또는 유기 용매 중에서, 또는 둘의 혼합물 중에서 이들 화합물의 유리 산 또는 염기 형태를 화학량론적 양의 적절한 염기 또는 산과 반응시킴으로써 제조될 수 있으며; 일반적으로, 비수성 매질, 예컨대 에테르, 에틸 아세테이트, 에탄올, 이소프로판올 또는 아세토니트릴이 바람직하다. 적합한 염의 목록은 문헌 [Remington's Pharmaceutical Sciences, 18th Edition, Mack Publishing Company, Easton, PA (1990)]에서 발견되며, 이의 개시내용은 본원에 참조로 포함된다.
본 발명의 화합물이, 예를 들어 적어도 1개의 염기성 중심을 갖는 경우에, 이들은 산 부가염을 형성할 수 있다. 이들은, 예를 들어 강한 무기 산, 예컨대 미네랄 산, 예를 들어 황산, 인산 또는 할로겐화수소산과 함께, 유기 카르복실산, 예컨대 1 내지 4개의 탄소 원자의 알칸카르복실산, 예를 들어 비치환되거나 또는 예를 들어 할로겐에 의한 치환된 아세트산, 예컨대 클로로아세트산, 예컨대 포화 또는 불포화 디카르복실산, 예를 들어 옥살산, 말론산, 숙신산, 말레산, 푸마르산, 프탈산 또는 테레프탈산, 예컨대 히드록시카르복실산, 예를 들어 아스코르브산, 글리콜산, 락트산, 말산, 타르타르산 또는 시트르산, 예컨대 아미노산 (예를 들어, 아스파르트산 또는 글루탐산 또는 리신 또는 아르기닌), 또는 벤조산과 함께, 또는 유기 술폰산, 예컨대 비치환되거나 또는 예를 들어 할로겐에 의해 치환된 (C1-C4) 알킬 또는 아릴술폰산, 예를 들어 메틸- 또는 p-톨루엔-술폰산과 함께 형성된다. 목적하는 경우 추가적으로 존재하는 염기성 중심을 갖는 상응하는 산 부가염이 또한 형성될 수 있다. 적어도 1종의 산 기 (예를 들어, COOH)를 갖는 본 발명의 화합물은 또한 염기와 함께 염을 형성할 수 있다. 적합한 염기와의 염은, 예를 들어 금속 염, 예컨대 알칼리 금속 또는 알칼리 토금속 염, 예를 들어 나트륨, 칼륨 또는 마그네슘 염, 또는 암모니아 또는 유기 아민, 예컨대 모르폴린, 티오모르폴린, 피페리딘, 피롤리딘, 모노, 디 또는 트리-저급 알킬아민, 예를 들어 에틸, tert-부틸, 디에틸, 디이소프로필, 트리에틸, 트리부틸 또는 디메틸-프로필아민, 또는 모노, 디 또는 트리히드록시 저급 알킬아민, 예를 들어 모노, 디 또는 트리에탄올아민과의 염이다. 추가로, 상응하는 내부 염이 형성될 수 있다. 제약 용도에는 부적합하지만, 예를 들어 화학식 (I)의 유리 화합물 또는 그의 제약상 허용되는 염의 단리 또는 정제에 사용될 수 있는 염이 또한 포함된다.
염기성 기를 함유하는 화학식 (I)의 화합물의 바람직한 염은 모노히드로클로라이드, 히드로겐술페이트, 메탄술포네이트, 포스페이트, 니트레이트 또는 아세테이트를 포함한다.
산 기를 함유하는 화학식 (I)의 화합물의 바람직한 염은 나트륨, 칼륨 및 마그네슘 염 및 제약상 허용되는 유기 아민을 포함한다.
추가로, 본 발명의 화합물은 전구약물 형태를 가질 수 있다. 생체내에서 전환되어 생물활성제를 제공할 임의의 화합물이 본 발명의 범주 및 취지 내에 있는 전구약물이다. 본원에 사용된 용어 "전구약물"은 카르복실산 잔기를 기재로 하는 전구약물, 즉 "전구약물 에스테르" 및 아르기닌 모방체 모이어티를 기재로 하는 전구약물, 즉 "아르기닌 모방체의 전구약물" 둘 다를 포괄한다. 가수분해는 다수의 경우에서 주로 소화 효소의 영향 하에 일어나기 때문에, 이러한 전구약물은 바람직하게는 경구로 투여된다. 비경구 투여는 에스테르가 그 자체로 활성인 경우에, 또는 가수분해가 혈액 내에서 일어나는 경우에 사용될 수 있다.
본 발명의 화합물은 신체 내에서 가수분해됨으로써 본 발명의 화합물 그 자체를 생성하는 전구약물, 즉 "전구약물 에스테르"로서의 역할을 하는 생리학상 가수분해성 에스테르를 형성할 수 있는 카르복시 기를 함유한다. 본 발명의 화합물의 생리학상 가수분해성 에스테르의 예는 C1 내지 C6 알킬, C1 내지 C6 알킬벤질, 4-메톡시벤질, 인다닐, 프탈릴, 메톡시메틸, C1-6 알카노일옥시-C1-6 알킬 (예를 들어, 아세톡시메틸, 피발로일옥시메틸 또는 프로피오닐옥시메틸), C1 내지 C6 알콕시카르보닐옥시-C1 내지 C6 알킬 (예를 들어, 메톡시카르보닐-옥시메틸 또는 에톡시카르보닐옥시메틸, 글리실옥시메틸, 페닐글리실옥시메틸, (5-메틸-2-옥소-1,3-디옥솔렌-4-일)-메틸), 및 예를 들어 페니실린 및 세팔로스포린 기술분야에서 사용되는 다른 널리 공지된 생리학상 가수분해성 에스테르를 포함한다. 이러한 에스테르는 관련 기술분야에 공지된 통상적인 기술에 의해 제조될 수 있다. "전구약물 에스테르"는 관련 기술분야의 통상의 기술자에게 공지된 절차를 사용하여 본 발명의 화합물의 카르복실산 모이어티를 알킬 또는 아릴 알콜, 할라이드 또는 술포네이트와 반응시킴으로써 형성될 수 있다. 추가로, 전구약물의 다양한 형태는 관련 기술분야에 널리 공지되어 있다. 이러한 전구약물 유도체의 예에 대해서는 하기 문헌을 참조한다:
[Bundgaard, H., ed., Design of Prodrugs, Elsevier (1985), and Widder, K. et al., eds., Methods in Enzymology, 112:309-396, Academic Press (1985)];
[Bundgaard, H., Chapter 5, "Design and Application of Prodrugs", Krosgaard-Larsen, P. et al., eds., A Textbook of Drug Design and Development, pp. 113-191, Harwood Academic Publishers (1991)];
[Bundgaard, H., Adv. Drug Deliv. Rev., 8:1-38 (1992)];
[Bundgaard, H. et al., J. Pharm. Sci., 77:285 (1988)]; 및
[Kakeya, N. et al., Chem. Pharm. Bull., 32:692 (1984)].
전구약물의 제조는 관련 기술분야에 널리 공지되어 있고, 예를 들어 문헌 [King, F.D., ed., Medicinal Chemistry: Principles and Practice, The Royal Society of Chemistry, Cambridge, UK (1994); Testa, B. et al., Hydrolysis in Drug and Prodrug Metabolism. Chemistry, Biochemistry and Enzymology, VCHA and Wiley-VCH, Zurich, Switzerland (2003); Wermuth, C.G., ed., The Practice of Medicinal Chemistry, Academic Press, San Diego, CA (1999); Rautio, J. et al., Nature Review Drug Discovery, 17, 559-587, (2018)]에 기재되어 있다.
본 발명은 본 발명의 화합물에서 발생하는 원자의 모든 동위원소를 포함하는 것으로 의도된다. 동위원소는 동일한 원자 번호를 갖지만 상이한 질량수를 갖는 원자를 포함한다. 일반적 예로서 및 비제한적으로, 수소의 동위원소는 중수소 (기호 D 또는 2H) 및 삼중수소 (기호 T 또는 3H)를 포함한다. 탄소의 동위원소는 13C 및 14C를 포함한다. 동위원소-표지된 본 발명의 화합물은 일반적으로 관련 기술분야의 통상의 기술자에게 공지된 통상적인 기술에 의해 또는 본원에 기재된 것들과 유사한 방법에 의해, 달리 사용되는 비-표지된 시약 대신에 적절한 동위원소-표지된 시약을 사용하여 제조될 수 있다. 이러한 화합물은, 예를 들어 잠재적인 제약 화합물이 표적 단백질 또는 수용체에 결합하는 능력을 결정함에 있어서 표준물 및 시약으로서, 또는 생체내 또는 시험관내에서 생물학적 수용체에 결합된 본 발명의 화합물을 영상화하기 위한 다양한 잠재적 용도를 갖는다.
"안정한 화합물" 및 "안정한 구조"는 반응 혼합물로부터 유용한 정도의 순도로의 단리 및 효과적인 치료제로의 제제화에서 살아남기에 충분히 강건한 화합물을 나타내는 것으로 의도된다. 본 발명의 화합물이 N-할로, S(O)2H 또는 S(O)H 기를 함유하지 않는 것이 바람직하다.
용어 "용매화물"은 유기 또는 무기에 관계 없이, 본 발명의 화합물과 1개 이상의 용매 분자의 물리적 회합을 의미한다. 이러한 물리적 회합은 수소 결합을 포함한다. 용매화물 중의 용매 분자는 규칙적 배열 및/또는 비-규칙적 배열로 존재할 수 있다. 용매화물은 화학량론적 또는 비화학량론적 양의 용매 분자를 포함할 수 있다. "용매화물"은 용액 상 및 단리가능한 용매화물 둘 다를 포괄한다. 예시적인 용매화물은 수화물, 에탄올레이트, 메탄올레이트 및 이소프로판올레이트를 포함하나 이에 제한되지는 않는다. 용매화 방법은 일반적으로 관련 기술분야에 공지되어 있다.
용어 "글리코실"은 헤미아세탈 히드록실 기를 시클릭 형태의 모노사카라이드 및 더 나아가 저급 올리고사카라이드로부터 제거함으로써 얻어지는 1가 자유 라디칼 또는 치환기 모이어티를 의미한다. 한 실시양태에서, 글리코실 기는 하기 구조를 갖는다:
본원에 사용된 약어는 하기와 같이 정의된다: "1 x"는 1회, "2 x"는 2회, "3 x"는 3회, "℃"는 섭씨 온도, "eq"는 당량, "g"는 그램, "mg"는 밀리그램, "L"은 리터, "mL"은 밀리리터, "μL"은 마이크로리터, "N"은 노르말, "M"은 몰, "mmol"은 밀리몰, "min"은 분, "h"는 시간, "rt"는 실온, "RBF"는 둥근 바닥 플라스크, "atm"은 기압, "psi"는 제곱 인치당 파운드, "conc."는 진한, "RCM"은 폐환 복분해, "sat" 또는 "sat'd"는 포화, "SFC"는 초임계 유체 크로마토그래피, "MW"는 분자량, "mp"는 융점, "ee"는 거울상이성질체 과잉률, "MS" 또는 "Mass Spec"는 질량 분광측정법, "ESI"는 전기분무 이온화 질량 분광분석법, "HR"은 고해상도, "HRMS"는 고해상도 질량 분광측정법, "LCMS"는 액체 크로마토그래피 질량 분광측정법, "HPLC"는 고압 액체 크로마토그래피, "RP HPLC"는 역상 HPLC, "TLC" 또는 "tlc"는 박층 크로마토그래피, "NMR"은 핵 자기 공명 분광분석법, "nOe"는 핵 오버하우저 효과 분광분석법, "1H"는 양성자, "δ"는 델타, "s"는 단일선, "d"는 이중선, "t"는 삼중선, "q"는 사중선, "m"은 다중선, "br"은 넓은, "Hz"는 헤르츠, 및 "α", "β", "R", "S", "E" 및 "Z"는 관련 기술분야의 통상의 기술자에게 친숙한 입체화학적 명칭이다.
약어
본원에 사용된 약어는 하기와 같이 정의된다: "1 x"는 1회, "2 x"는 2회, "3 x"는 3회, "℃"는 섭씨 온도, "eq"는 당량, "g"는 그램, "mg"는 밀리그램, "L"은 리터, "mL"은 밀리리터, "μL"은 마이크로리터, "N"은 노르말, "M"은 몰, "mmol"은 밀리몰, "min"은 분, "h"는 시간, "rt"는 실온, "RBF"는 둥근 바닥 플라스크, "atm"은 기압, "psi"는 제곱 인치당 파운드, "conc."는 진한, "RCM"은 폐환 복분해, "sat" 또는 "sat'd"는 포화, "SFC"는 초임계 유체 크로마토그래피, "MW"는 분자량, "mp"는 융점, "ee"는 거울상이성질체 과잉률, "MS" 또는 "Mass Spec"는 질량 분광측정법, "ESI"는 전기분무 이온화 질량 분광분석법, "HR"은 고해상도, "HRMS"는 고해상도 질량 분광측정법, "LCMS"는 액체 크로마토그래피 질량 분광측정법, "HPLC"는 고압 액체 크로마토그래피, "RP HPLC"는 역상 HPLC, "TLC" 또는 "tlc"는 박층 크로마토그래피, "NMR"은 핵 자기 공명 분광분석법, "nOe"는 핵 오버하우저 효과 분광분석법, "1H"는 양성자, "δ"는 델타, "s"는 단일선, "d"는 이중선, "t"는 삼중선, "q"는 사중선, "m"은 다중선, "br"은 넓은, "Hz"는 헤르츠, 및 "α", "β", "R", "S", "E" 및 "Z"는 관련 기술분야의 통상의 기술자에게 친숙한 입체화학적 명칭이다.
또한, 하기 약어가 반응식, 실시예 및 본원의 다른 곳에서 사용된다:
IV. 제조 방법
본 발명의 화합물은 합성 유기 화학 기술분야에 공지된 합성 방법과 함께 하기 기재된 방법, 또는 관련 기술분야의 통상의 기술자에 의해 인지되는 바와 같은 그에 대한 변형법을 사용하여, 유기 합성 기술분야의 통상의 기술자에게 널리 공지되어 있는 다수의 방식으로 제조될 수 있다. 바람직한 방법은 하기 기재된 방법을 포함하나 이에 제한되지는 않는다. 본원에 인용된 모든 참고문헌은 그 전문이 본원에 참조로 포함된다. 반응은 사용되는 시약 및 물질에 적절하고 변환을 실시하기에 적합한 용매 또는 용매 혼합물 중에서 수행된다. 유기 합성 기술분야의 통상의 기술자는 분자 상에 존재하는 관능기가 제안된 변환과 부합해야 함을 이해할 것이다. 이는 때때로 본 발명의 목적 화합물을 수득하기 위해 합성 단계의 순서를 변형하거나, 또는 하나의 특정한 공정 반응식을 또 다른 공정 반응식에 비해 선택하는 것에 대한 판단을 필요로 할 것이다. 반응 조건과 상용성인 치환기에 대한 제한은 관련 기술분야의 통상의 기술자에게 자명할 것이며, 이에 따라 대안적 방법이 사용되어야 한다. 또한, 본 분야의 임의의 합성 경로의 계획시 또 다른 주요 고려사항은 본 발명에 기재된 화합물에 존재하는 반응성 관능기의 보호에 사용되는 보호기의 신중한 선택인 것으로 인식될 것이다. 본 발명의 화합물의 제조에 적용가능할 수 있는 합성 방법의 특히 유용한 일람은 문헌 [Larock, R.C., Comprehensive Organic Transformations, VCH, New York (1989)]에서 찾아볼 수 있다.
본 발명의 화합물은 본 섹션에 기재된 반응 및 기술을 사용하여 제조될 수 있다. 반응은 사용된 시약 및 물질에 적절하고 변환을 실시하기에 적합한 용매 중에서 수행된다. 또한, 하기 기재된 합성 방법의 설명에서, 용매, 반응 분위기, 반응 온도, 실험 지속기간 및 후처리 절차를 포함한 모든 제안된 반응 조건은 해당 반응에 대한 표준 조건이 되도록 선택되며, 이는 관련 기술분야의 통상의 기술자에 의해 용이하게 인식되는 것으로 이해되어야 한다. 유기 합성 기술분야의 통상의 기술자는 포고 분자의 다양한 부분 상에 존재하는 관능기가 제안된 시약 및 반응물과 상용성이어야 한다는 것을 이해한다. 주어진 부류에 속하는 화학식 (I)의 모든 화합물이 기재된 일부 방법에서 요구되는 일부 반응 조건과 상용성일 수는 없다. 반응 조건과 상용성인 치환기에 대한 제한은 관련 기술분야의 통상의 기술자에게 자명할 것이며, 대안적 방법이 사용되어야 한다. 본 발명의 화합물의 제조에 적용가능할 수 있는 합성 방법의 특히 유용한 일람은 문헌 [Larock, R.C., Comprehensive Organic Transformations, VCH, New York (1989)]에서 찾아볼 수 있다.
일반적 반응식
화학식 (I), 화학식 (II), 화학식 (III), 또는 그의 임의의 하위식 또는 종에 의해 나타내어지는 본 발명의 화합물은 하기 반응식 1 내지 13에 제시된 일반적 경로에 따라 제조될 수 있다.
<반응식 1>
반응식 1은 화학식 I-a, I-b 및 I-c의 화합물 (화학식 I의 하위세트)의 제조 방법을 기재한다. 중간체 1은 관련 기술분야의 통상의 기술자에게 널리 공지된 조건 하에 X5-L1-Z-Rx (X5는 할로겐, 트리플레이트 또는 다른 적합한 이탈기이고, 상업적으로 입수가능하거나 또는 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 용이하게 제조됨)과의 커플링을 통해 생성물 I-a로 전환될 수 있다. L1이 공유 결합을 나타내는 예에서, 생성물 I-a는 중간체 1과 적합한 아릴 할라이드, 트리플레이트 또는 등가물 사이의 다양한 C-N 결합 형성 반응을 통해 수득될 수 있다. 일부 예는 Pd-촉매된 부흐발트-하르트비히(Buchwald-Hartwig) 반응, Cu-매개 울만(Ullmann) 커플링, Ni-매개 아미노화 또는 친핵성 방향족 치환 (SNAr)을 포함하나, 이에 제한되지는 않는다. 대안적으로, 보론산 또는 에스테르 커플링 파트너를 이용한 Cu-촉매된 챈-에반스-람(Chan-Evans-Lam) 커플링이 이용될 수 있다. 각 경우에, 촉매, 리간드, 용매, 염기, 첨가제 및 온도와 같은 변수의 최적화가 필요할 수 있다. 다른 예에서, L1은 CO 또는 SO2와 같은 (이에 제한되지는 않음) 링커를 나타낸다. 이러한 예에서, 생성물 I-a는 적합한 염기, 예를 들어 트리에틸아민, 휘니그 염기 또는 피리딘의 존재 하에 적합한 용매, 예컨대 디클로로메탄, 에틸 아세테이트, DMF 또는 THF 중에서 첨가제, 예컨대 HOBT 또는 DMAP를 사용하거나 사용하지 않으면서 T3P, EDC, DCC 또는 CDI와 같은 (이에 제한되지는 않음) 커플링 시약을 사용하여 중간체 1과 적합한 카르복실산을 커플링시킴으로써 수득할 수 있다. 일부 예에서는, I-a를 수득하기 위해, 카르복실산 클로라이드 또는 술포닐 클로라이드를 트리에틸아민 또는 휘니그 염기와 같은 염기의 존재 하에 디클로로메탄과 같은 적절한 용매 중에서 교반함으로써 중간체 1과 반응시킬 수 있다. 각각의 경우에, 온도를 비롯한 사용되는 특정 조건이, 관련 기술분야의 통상의 기술자에게 명백한 최적화를 필요로 할 수 있다. I-a가 에스테르 또는 니트릴을 함유하는 경우, 이는 MeOH, THF 및 물로 이루어진 용매 중에서 가수분해를 가능하게 하기에 적합한 온도에서 NaOH 또는 LiOH를 사용하여 I-a를 처리하는 것과 같은 (이에 제한되지는 않음) 조건 하에 상응하는 카르복실산 I-b로 가수분해될 수 있다. 특정 에스테르, 예컨대 tert-부틸 에스테르의 산-매개 가수분해는 일부 경우에 I-b를 수득하는데 필요할 수 있다. 실시예 I-c는 적합한 염기, 예를 들어 트리에틸아민, 휘니그 염기 또는 피리딘의 존재 하에 적절한 용매, 예컨대 디클로로메탄, 에틸 아세테이트, DMF 또는 THF 중에서 첨가제, 예컨대 HOBT 또는 DMAP를 사용하거나 사용하지 않으면서 커플링 시약, 예컨대 이에 제한되지 않는 T3P, EDC, DCC 또는 CDI를 사용하여 중간체 I-b와 R13-NH-R14를 커플링시킴으로써 수득할 수 있다. 각 경우에 온도 및 농도를 비롯한, I-c를 수득하기 위해 사용되는 특정 조건이 최적화를 필요로 할 수 있다.
<반응식 2>
반응식 2는 중간체 1a, 1b 및 1c (중간체 1의 하위세트)의 제조 방법을 기재한다. 중간체 2 (여기서, X6은 Cl, Br 또는 I임) 및 케톤 3의 커플링은, 2의 아릴 그리냐르, 아릴 리튬, 아릴 아연 또는 다른 아릴 금속 종의 형성과, 케톤 3에의 후속 첨가와 같은 다양한 조건을 통해 달성되어, 3급 알콜 생성물 4를 제공할 수 있다. 케톤 3은 상업적으로 입수가능하거나 관련 기술분야의 통상의 기술자에게 널리 공지된 방법에 의해 제조될 수 있다. 아미노 보호기 (예를 들어, 여기서 P* = Boc)의 제거 동안 적절하게 산성인 조건 (특히 HCl, TFA)이 사용되는 경우, 알켄 1a가 주요 단리물로서 수득될 수 있다 (탈보호 A). P* = Boc인 다른 경우에, 희석 또는 DCM 중 TFA와 같은 약산성 조건이 사용되는 경우, 히드록실이 유지되어 중간체 1b를 수득할 수 있다 (탈보호 B). 추가로, P* = Cbz인 경우, 탄소 상 팔라듐 매개된 수소화를 이용하여, 히드록실의 제거 없이 보호기를 제거하여 1b를 제공할 수 있다 (탈보호 B). 알켄 중간체 1a는, 용매로서의 TFA 중에서 과량의 트리에틸실란을 가열하는 것과 같은 (이에 제한되지는 않음) 조건 하에 환원되어, 중간체 1c를 제공할 수 있다. 관능기 상용성을 위해 대안적 보호기가 필요한 경우, 이들은 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 제거될 수 있다. 보호기 제거를 위한 추가의 방법은 문헌 [Greene, T. and Wuts, P. G. M., Protecting Groups in Organic Synthesis, John Wiley & Sons, Inc., New York, NY, 2006] 및 그의 참고문헌에서 찾을 수 있다.
<반응식 3>
반응식 3은 중간체 1a의 합성을 위한 대안적 방법을 기재한다. 케톤 3을 에놀 트리플레이트 형성 및 후속적인 미야우라(Miyaura) 보릴화로 이루어진 2 단계로 상응하는 보론산 또는 에스테르로 전환시킬 수 있다. 트리플레이트 형성은, 3을 THF 중 저온에서 염기, 예컨대 LiHMDS로 처리하고, 이어서 코민(Comin) 시약 또는 또 다른 적합한 트리플레이트 공여자 공급원을 첨가함으로써 달성할 수 있다. 미야우라 보릴화에 대한 전형적인 조건은 적합한 용매, 예컨대 THF 또는 디옥산 중에서 중간체 트리플레이트를 비스 (피나콜레이토) 디보론 (B2Pin2), 아세트산칼륨 및 팔라듐 촉매, 예컨대 PdCl2(dppf)2와 가열하는 것을 포함하나, 이에 제한되지는 않는다. 헤테로아릴 할라이드 중간체 2는 보론산 또는 보론산 에스테르 5와 스즈키 커플링하여 알켄 6을 생성할 수 있다. 스즈키 커플링에 대한 전형적인 조건은, 탈산소화 용매 또는 용매 혼합물 중 적합한 온도에서 중간체 2 및 5를 팔라듐 촉매, 리간드 및 염기와 함께 가열하는 것을 포함하나, 이에 제한되지는 않는다. 구체적인 조건은 90℃에서의 디옥산/물 중 Pd(OAc)2, DPEPhos, K3PO4를 포함하나, 이에 제한되지는 않는다. 각각의 경우에, 화학량론, 팔라듐 공급원, 리간드, 염기, 용매, 온도 및 농도를 비롯한, 6을 수득하기 위해 사용되는 특정 조건이 독립적인 최적화를 필요로 할 수 있다. 보호기 P*의 제거는 반응식 2에 기재된 바와 같이 달성되어 중간체 1a를 제공할 수 있다.
<반응식 4>
반응식 4는 중간체 1d (중간체 1의 하위세트)의 제조 방법을 기재한다. 중간체 7을 온화하게 산성인 탈수 조건 하에 디올 8 (상업적으로 입수가능하거나 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 용이하게 제조됨)과 축합시켜 아세탈 9를 수득할 수 있다. 7에서 9로의 전환을 위한 조건은 톨루엔과 같은 용매 중에서 4Å 분자체 및 촉매 p-TSA의 존재 하에 7 및 8을 환류시키는 것을 포함하나, 이에 제한되지 않는다. P* = Boc인 경우에, 보호기 P*의 제거에서, 아세탈 보유를 위해 희석 또는 약산성 조건, 예컨대 DCM 중 TFA가 사용될 수 있다. 관능기 상용성을 위해 대안적 보호기가 필요한 경우, 이들은 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 제거될 수 있다. 보호기 제거를 위한 추가의 방법은 문헌 [Greene, T. and Wuts, P. G. M., Protecting Groups in Organic Synthesis, John Wiley & Sons, Inc., New York, NY, 2006] 및 그의 참고문헌에서 찾을 수 있다.
<반응식 5>
반응식 5는 중간체 1e (중간체 1의 하위세트)의 제조 방법을 기재한다. 중간체 알데히드 7을 알케닐화 및 디히드록실화를 포함하는 2 단계로 디올 10으로 전환시킬 수 있다. 알케닐화 단계는 용매, 예컨대 THF 중에서 시약, 예컨대 메틸 트리페닐포스포늄 브로마이드 및 적합한 염기, 예컨대 KOtBu 또는 NaHMDS (이에 제한되지는 않음)을 사용해 달성할 수 있다. 생성된 알켄을 적합한 용매 중에서 OsO4 및 NMO와 같은 (이에 제한되지는 않음) 조건에 적용하여 디올 10을 제공한다. 4Å 분자체와 같은 건조제와 함께 환류 톨루엔 중에서의 촉매 p-TSA와 같은 조건 하에 10을 케톤 11 (상업적으로 입수가능하거나 또는 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 용이하게 제조됨)과 축합시켜 케탈 12를 수득한다. 보호기 P*를 제거하여 중간체 1e를 수득하는 것은 반응식 4에 기재된 바와 같이 수행될 수 있다.
<반응식 6>
대안적으로, 반응식 6은 화합물 I-d 및 I-e (화학식 I의 하위세트)의 제조 방법을 기재한다. 중간체 14는 아미노 케톤 13 (상업적으로 입수가능하거나 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 용이하게 제조됨)과 적합한 아릴 할라이드, 트리플레이트 또는 등가물 X5-L1-Z-Rx (여기서, X5는 할라이드 또는 트리플레이트를 나타냄) 사이의 다양한 커플링 반응을 통해 수득할 수 있다. 이러한 커플링 반응의 일부 예는, 중간체 14를 제공하는 Pd-촉매된 부흐발트-하르트비히 반응, Cu-매개 울만 커플링, Ni-매개 아미노화 또는 친핵성 방향족 치환 (SNAr)을 포함하나, 이에 제한되지는 않는다. DCE와 같은 용매 중에서 p-TSA와 같은 산 촉매의 존재 하에 반응물을 혼합하는 것을 포함하는 조건 하에서의 케톤 14와 디올 10 사이의 후속 축합 (반응식 5)에 의해 생성물 I-d를 수득할 수 있다. 생성물 I-d가 에스테르 또는 니트릴을 함유하는 경우, 이는 MeOH, THF 및 물로 이루어진 용매 중에서 가수분해를 가능하게 하기에 적합한 온도에서 NaOH 또는 LiOH를 사용하여 I-d를 처리하는 것과 같은 (이에 제한되지는 않음) 조건 하에 상응하는 카르복실산 I-e로 가수분해될 수 있다. 특정 에스테르, 예컨대 tert-부틸 에스테르의 산-매개 가수분해가 일부 경우에 I-e를 수득하는데 필요할 수 있다.
<반응식 7>
반응식 7은 중간체 2a (중간체 2의 하위세트)의 제조 방법을 기재한다. 알데히드 15 (상업적으로 입수가능하거나 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 용이하게 제조됨)를 히드록실아민 히드로클로라이드와, 다양한 조건, 예컨대, 실온에서의 피리딘 중에서 상기 두 반응물을 교반하는 것, 또는 에탄올과 같은 적합한 용매 중에서 수산화나트륨 또는 아세트산나트륨과 같은 염기의 존재 하에 반응물을 온화하게 가열하는 것을 포함하는 (이에 제한되지는 않음) 다양한 조건 하에 축합시킬 수 있다. 생성된 옥심을 DMF와 같은 적합한 용매 중에서 NCS 또는 NBS와 같은 (이에 제한되지는 않음) 시약에 의한 할로겐화를 통해 상응하는 히드록시모일 할라이드 16으로 전환시킬 수 있다. 히드록시모일 할라이드 16은 실온에서의 디클로로메탄 중 트리에틸 아민과 같은 (이에 제한되지는 않음) 조건 하에 말단 알킨 (상업적으로 입수가능하거나 관련 기술분야의 통상의 기술자에 의해 용이하게 제조됨)에 의해 환화되어 3,5-치환된 이속사졸 17을 제공한다. 이속사졸의 4-위치를 DMF와 같은 적합한 용매 중에서 NBS 또는 NCS와 같은 (이에 제한되지는 않음) 시약에 의해 할로겐화하여, 3,4,5-치환된 이속사졸 중간체 2a를 수득할 수 있다.
<반응식 8>
반응식 8은 중간체 2b (중간체 2의 하위세트)의 제조 방법을 기재한다. 합성은, 산성 매질 (H2O/TFA) 중 아질산나트륨을 사용하여 처리한 후, 적합한 온도에서 적절한 용매 중 아지드화나트륨을 첨가하는 것과 같은 (이에 제한되지는 않음) 조건 하에서의 아민 18a (상업적으로 입수가능하거나 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 쉽게 제조됨)의 아지드화로 시작하여 아지드 19를 수득할 수 있다. 대안적으로, 아지드 19는 적절한 온도에서의 DMSO/물의 혼합물 중 할라이드 18b (상업적으로 입수가능하거나 또는 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 용이하게 제조됨)와 아지드 염, 예컨대 아지드화나트륨의 반응에 의해 수득할 수 있다. 생성된 아지드 19를, 실온에서 THF 중 과염소산구리 (II), 아이오딘화칼륨 및 DBU와 같은 (이에 제한되지는 않음) 조건 하에, 상업적으로 입수가능한 말단 알킨에 의해 환화시켜, 아이오도트리아졸 중간체 2b를 수득할 수 있다.
<반응식 9>
반응식 9는 중간체 2c (중간체 2의 하위세트)의 제조 방법을 기재한다. 상업적으로 입수가능하거나 용이하게 제조되는 N-치환된 글리신 20을, 문헌 [Fang, Y.; Wu, C.; Larock, R. C.; Shi, F. J. Org. Chem. 2011, 76, 8840]에서 찾을 수 있는 조건 하에 아질산나트륨, HCl ?? 아세트산 무수물로 처리하면 시드논 21을 수득할 수 있다. 시드논 21을, 문헌 [Decuypere, E.; Specklin, S.; Gabillet, S.; Audisio, D.; Liu, H.; Plougastel, L.; Kolodych S.; Taran, F. Org. Lett. 2015, 17, 362]에 기재된 바와 같이 NBS를 사용한 브로민화에 이어서 알킨을 이용한 구리 촉매된 고리화첨가를 포함하는 2단계 공정으로 피리미딘 중간체 2c로 전환시킬 수 있다.
<반응식 10>
반응식 10은 중간체 4a (중간체 4의 하위세트)의 제조 방법을 기재한다. 적절하게 치환된 보론산 또는 에스테르 22 (상업적으로 입수가능하거나 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 용이하게 제조됨) 및 적합하게 반응성인 할로겐 또는 등가물 X를 보유하는 피라졸 23 (상업적으로 입수가능하거나 또는 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 용이하게 제조됨)을 Pd-촉매된 스즈키 반응을 통해 커플링시켜 중간체 24를 수득할 수 있다. 스즈키 커플링에 대한 전형적인 조건은 적합한 온도에서 탈산소화 용매 또는 용매 혼합물 중에서 팔라듐 촉매, 리간드 및 염기와 함께 반응물 22 및 23을 가열하는 것을 포함하나, 이에 제한되지는 않는다. 구체적인 조건은 120℃에서의 THF/물 중 PdCl2(dppf)2, Na2CO3을 포함하나, 이에 제한되지는 않는다. 각각의 경우에, 화학량론, 팔라듐 공급원, 리간드, 염기, 용매, 온도 및 농도를 비롯한, 24를 수득하기 위해 사용되는 특정 조건이 독립적인 최적화를 필요로 할 수 있다. 커플링 파트너 22 및 23은 상업적으로 입수가능하거나, 또는 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 용이하게 제조될 수 있다. 중간체 24는 적합한 용매, 예컨대 THF 또는 Et2O 중에서 n-BuLi 또는 LDA와 같은 (이에 제한되지는 않음) 충분히 강한 염기에 의해 피라졸의 5-위치에서 탈양성자화될 수 있다. 24의 탈양성자화로부터 생성된 음이온을, 케톤 3을 이용해 계내 포획하여 중간체 2a를 수득할 수 있다.
<반응식 11>
반응식 11은 중간체 7a (중간체 7의 하위세트)의 제조 방법을 기재한다. 히드록시모일 할라이드 16 (반응식 6에 기재된 제조)을, DCM과 같은 (이에 제한되지는 않음) 용매 중 트리에틸 아민 또는 또 다른 적합한 염기의 존재 하에 β-케토에스테르 (상업적으로 입수가능하거나 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 용이하게 제조됨)와 반응시켜 3,4,5-치환된 이속사졸 에스테르 25를 수득할 수 있다. 에스테르의 환원은 적절한 용매 중에서 LiAlH4, DIBAL-H 또는 LiBH4를 포함하지만 이에 제한되지 않는 다수의 시약에 의해 달성될 수 있다. 생성된 이속사졸 26의 히드록실을, DCM 또는 DCE와 같은 (이에 제한되지는 않음) 적절한 용매 중에서 PCC 산화, 데스-마르틴 산화, 스웸(Swern) 산화, 레이(Ley) 산화를 포함하는 (이에 제한되지는 않음) 산화성 조건 하에 알데히드 중간체 7a로 전환시킬 수 있다.
<반응식 12>
반응식 12는 화합물 I-f, I-g, I-h (화학식 I의 하위세트)를 제조하는 방법을 기재한다. 일부 예에서, L1은 O 또는 N과 같은 (이에 제한되지는 않음) 링커 원자를 나타내고, 생성물 I-f는 친핵성 방향족 치환 (SNAr), 전이 금속 매개 아릴화 (즉, Pd, Cu, Ni), 미츠노부 커플링, 환원성 아민화 또는 알킬화를 포함하나 이에 제한되지는 않는 조건 하에 중간체 27과 X5-Z-Rx (X5는 할라이드 또는 트리플레이트를 나타냄)의 커플링을 통해 수득될 수 있다. I-f가 에스테르 또는 니트릴을 함유하는 경우, 이는 가수분해를 가능하게 하기에 적합한 온도에서 MeOH, THF 및 물로 이루어진 용매 중에서 NaOH 또는 LiOH를 사용한 처리와 같은 (이에 제한되지는 않음) 조건 하에 상응하는 카르복실산 I-g로 가수분해될 수 있다. 특정 에스테르, 예컨대 tert-부틸 에스테르의 산-매개 가수분해가 일부 경우에 I-g를 수득하는데 필요할 수 있다. 실시예 I-h는 적절한 용매, 예컨대 디클로로메탄, 에틸 아세테이트, DMF 또는 THF 중에서 적합한 염기, 예를 들어 트리에틸아민, 휘니그 염기 또는 피리딘의 존재 하에 첨가제, 예컨대 HOBT 또는 DMAP를 사용하거나 사용하지 않고 T3P, EDC, DCC 또는 CDI와 같은 (이에 제한되지는 않음) 커플링 시약을 사용하여 I-g를 R13-NH-R14와 커플링시킴으로써 수득할 수 있다. 각각의 경우에, 온도 및 농도를 비롯한, I-f, I-g 및 I-h를 수득하기 위해 사용되는 특정 조건은 최적화를 필요로 할 수 있다.
<반응식 13>
반응식 13은 화합물 I-i, I-j, I-k (화학식 I의 하위세트)를 제조하는 방법을 기재한다. 생성물 I-i는, X5-Z-Rx의 아릴 그리냐르 또는 아릴 아연 또는 다른 아릴 화학종의 형성과 28에의 후속 첨가를 포함하는 조건 하에 중간체 28을 X5-Z-Rx (X5는 할라이드 또는 트리플레이트를 나타냄)과 커플링시킴으로써 수득할 수 있다. I-i가 에스테르 또는 니트릴을 함유하는 경우, 이는 가수분해를 가능하게 하기에 적합한 온도에서 MeOH, THF 및 물로 이루어진 용매 중에서 NaOH 또는 LiOH로의 처리를 포함하는 (이에 제한되지는 않음) 조건 하에 상응하는 카르복실산 I-j로 가수분해될 수 있다. 특정 에스테르, 예컨대 tert-부틸 에스테르의 산-매개 가수분해가 일부 경우에 I-j를 수득하는데 필요할 수 있다. 실시예 I-k는 적절한 용매, 예컨대 디클로로메탄, 에틸 아세테이트, DMF 또는 THF 중에서 첨가제, 예컨대 HOBT 또는 DMAP를 사용하거나 사용하지 않으면서 적합한 염기, 예를 들어 트리에틸아민, 휘니그 염기 또는 피리딘의 존재 하에 T3P, EDC, DCC 또는 CDI와 같은 (이에 제한되지는 않음) 커플링 시약을 사용하여 I-j를 R13-NH-R15와 커플링시킴으로써 수득할 수 있다. 각각의 경우에, 온도 및 농도를 비롯한, I-i, I-j 및 I-k를 수득하기 위해 사용되는 특정 조건이 최적화를 필요로 할 수 있다.
<반응식 14>
반응식 14는 중간체 27a, 27b 및 27c (중간체 27의 하위세트)를 제조하는 방법을 기재한다. 헤테로아릴 할라이드 중간체 2 및 케톤 29 (상업적으로 입수가능하거나 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 용이하게 제조됨)의 커플링은, 2의 아릴 그리냐르, 아릴 리튬, 아릴 아연 또는 다른 아릴 금속 화학종의 형성과 케톤 29에의 후속 첨가와 같은 다양한 조건을 통해 달성되어, 3급 알콜 생성물 30을 제공할 수 있다. 아미노 보호기의 제거 동안 적절한 산성 조건 (즉, HCl, TFA)이 사용되는 경우, 예를 들어 P* = Boc인 경우, 알켄 27a가 주요 단리물로서 수득될 수 있다 (탈보호 A). P* = Boc인 다른 경우에, 희석 또는 약산성 조건, 예컨대 DCM 중 TFA가 사용되는 경우, 히드록실이 보유되어 중간체 27b를 수득할 수 있다. 추가로, P* = Cbz인 경우, 탄소 상 팔라듐 매개된 수소화를 이용하여 히드록실의 제거 없이 보호기를 제거하여 27b를 수득할 수 있다. 알켄 중간체 27a는, 용매로서의 TFA 중에서 과량의 트리에틸실란을 가열하는 것과 같은 (이에 제한되지는 않음) 조건 하에 환원되어, 중간체 27c를 제공할 수 있다. 관능기 상용성을 위해 대안적 보호기가 필요한 경우, 이들은 관련 기술분야의 통상의 기술자에게 공지된 방법에 의해 제거될 수 있다. 보호기 제거를 위한 추가의 방법은 문헌 [Greene, T. and Wuts, P. G. M., Protecting Groups in Organic Synthesis, John Wiley & Sons, Inc., New York, NY, 2006] 및 그의 참고문헌에서 찾을 수 있다.
실시예
하기 실시예는 예시로서, 본 발명의 부분적 범주 및 특정한 실시양태로서 제공되며, 본 발명의 범주를 제한하는 것으로 의도되지 않는다. 달리 나타내지 않는 한 약어 및 화학적 기호는 그의 통상적 및 관습적 의미를 갖는다. 달리 나타내지 않는 한, 본원에 기재된 화합물은 본원에 개시된 반응식 및 다른 방법을 사용하여 제조, 단리 및 특징화되었거나 또는 그를 사용하여 제조될 수 있다.
적절한 경우에, 반응을 건조 질소 (또는 아르곤)의 분위기 하에 수행하였다. 무수 반응의 경우, EM으로부터의 드리솔브(DRISOLV)® 용매를 사용하였다. 다른 반응의 경우, 시약 등급 또는 HPLC 등급 용매를 이용하였다. 달리 언급되지 않는 한, 모든 상업적으로 입수한 시약은 제공받은 대로 사용하였다.
실시예의 특성화 또는 정제에 사용된 HPLC/MS 및 정제용/분석용 HPLC 방법
NMR (핵 자기 공명) 스펙트럼은 전형적으로 나타낸 용매 중에서 브루커 또는 JEOL 400 MHz 및 500 MHz 기기로 수득하였다. 모든 화학적 이동은 내부 표준으로서 용매 공명을 사용하여 테트라메틸실란으로부터의 ppm으로 보고하였다. 1H NMR 스펙트럼 데이터는 전형적으로 하기와 같이 보고하였다: 화학적 이동, 다중도 (s = 단일선, br s = 넓은 단일선, d = 이중선, dd = 이중선의 이중선, t = 삼중선, q = 사중선, sep = 칠중선, m = 다중선, app = 겉보기), 커플링 상수 (Hz), 및 적분값.
용어 HPLC는 하기 방법 중 하나에서 시마즈 고성능 액체 크로마토그래피 기기를 지칭한다:
일반적 방법 A
실시예 1
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
단계 1. 2,6-디클로로벤즈알데히드 옥심
히드록실아민 히드로클로라이드 (6.6 g, 95 mmol)를 피리딘 (31.7 mL) 중 2,6-디클로로벤즈알데히드 (11.1 g, 63.4 mmol)의 실온 용액에 첨가하였고, 이때 약한 발열이 나타났다. 10분 후, 과량의 피리딘을 진공 하에 제거하고, 잔류물을 Et2O와 물 사이에 분배하였다. 유기 층을 순차적으로 포화 수성 NH4Cl, 염수로 세척하고, 합한 수성 층을 여러 소량의 Et2O로 역추출하였다. 합한 유기 추출물을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 2,6-디클로로벤즈알데히드 옥심 (12.4 g, 65.3 mmol, 100% 수율)을 백색 고체로서 수득하였다. 생성물을 후속 단계에 추가의 정제 없이 사용하였다.
1H NMR (400MHz, CDCl3) δ 8.39 (s, 1H), 7.92 (s, 1H), 7.40-7.36 (m, 2H), 7.27-7.22 (m, 1H).
단계 2. 2,6-디클로로-N-히드록시벤즈이미도일 클로라이드
2,6-디클로로벤즈알데히드 옥심 (12.0 g, 63.1 mmol)을 DMF (45.9 mL) 중에 용해시키고, 40℃로 가열하였다. 이어서, DMF (38.3 mL) 중에 용해시킨 NCS (10.1 g, 76.0 mmol)를 따뜻한 용액에 대략 3분의 기간에 걸쳐 첨가하였다. 40℃에서 밤새 교반한 후, 반응 혼합물을 실온으로 냉각시키고, 얼음에 붓고, Et2O로 추출하였다. 유기 층을 수집하고, 염수로 세척하였다. 합한 수성 층을 Et2O로 역추출하였다. 합한 유기 층을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축 건조시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-50% EtOAc/헥산, 이스코 120 g 칼럼)에 의해 정제하여 2,6-디클로로-N-히드록시벤즈이미도일 클로라이드 (13.3 g, 59.3 mmol, 94% 수율)을 왁스상 백색 고체로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 8.02 (s, 1H), 7.43-7.37 (m, 2H), 7.37-7.30 (m, 1H).
단계 3. 5-시클로프로필-3-(2,6-디클로로페닐)이속사졸
시클로프로필아세틸렌 (2.8 mL, 33.4 mmol)에 이어서 Et3N (3.7 mL, 26.7 mmol)을 DCM (111 mL) 중 2,6-디클로로-N-히드록시벤즈이미도일 클로라이드 (5.0 g, 22.3 mmol)의 실온 용액에 첨가하였다. 반응 혼합물을 실온에서 밤새 교반하고, 정제를 위해 SiO2 상에 농축시켰다. 생성된 혼합물을 SiO2 상 플래쉬 크로마토그래피 (0-45% EtOAc/헥산, 이스코 120 g 칼럼)에 의해 정제하여 5-시클로프로필-3-(2,6-디클로로페닐)이속사졸 (4.8 g, 18.9 mmol, 85% 수율)을 백색 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 7.43-7.39 (m, 2H), 7.34-7.28 (m, 1H), 6.01 (s, 1H), 2.13 (tt, J=8.2, 5.3 Hz, 1H), 1.16-1.07 (m, 4H).
단계 4. 4-브로모-5-시클로프로필-3-(2,6-디클로로페닐)이속사졸
N-브로모숙신이미드 (0.81 g, 4.6 mmol)를 DMF (14.6 mL) 중 5-시클로프로필-3-(2,6-디클로로페닐)이속사졸 (0.93 g, 3.7 mmol)의 실온 용액에 첨가하였다. 반응 혼합물을 50℃로 가열하였다. 밤새 가열한 후, 추가의 N-브로모숙신이미드 (0.81 g, 4.6 mmol)를 첨가하고, 가열을 계속하였다. 추가로 24시간 동안 가열한 후, 반응을 실온으로 냉각시키고, 대략 100 mL의 빙수에 부었다. 생성된 고체를 흡인 여과에 의해 수집하고, 고진공 하에 건조시켜 4-브로모-5-시클로프로필-3-(2,6-디클로로페닐) 이속사졸 (1.14 g, 3.42 mmol, 94% 수율)을 백색 분말로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 7.49-7.36 (m, 3H), 2.19 (tt, J=8.4, 5.1 Hz, 1H), 1.36-1.29 (m, 2H), 1.24-1.16 (m, 2H).
단계 5. tert-부틸 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시-7-아자스피로[3.5]노난-7-카르복실레이트
n-부틸리튬 (8.1 mL, 20.3 mmol)을 THF (64.9 mL) 중 4-브로모-5-시클로프로필-3-(2,6-디클로로페닐)이속사졸 (5.4 g, 16.2 mmol)의 -78℃ 용액에 천천히 첨가하여 담갈색 용액을 수득하였다. 10분 후, tert-부틸 2-옥소-7-아자스피로[3.5]노난-7-카르복실레이트 (3.9 g, 16.2 mmol)를 THF 3 mL 중 용액으로서 첨가하였다. 온도를 -78℃에서 3시간 동안 유지하였다. 차가운 반응 혼합물을 메탄올 5 mL의 느린 첨가에 의해 켄칭한 다음, SiO2 상에 농축시키고, SiO2 상 플래쉬 크로마토그래피 (0-80% EtOAc/헥산, 이스코 120 g 칼럼)에 의해 정제하여 tert-부틸 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시-7-아자스피로[3.5]노난-7-카르복실레이트 (5.4 g, 10.9 mmol, 67% 수율)을 백색 분말로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 7.47-7.35 (m, 3H), 3.32-3.25 (m, 2H), 3.23-3.16 (m, 2H), 2.30 (s, 1H), 2.07-2.00 (m, 2H), 1.70 (br d, J=1.4 Hz, 2H), 1.46 (br t, J=3.0 Hz, 2H), 1.43 (s, 8H), 1.41-1.35 (m, 2H), 1.32-1.24 (m, 3H), 1.18-1.12 (m, 2H).
단계 6. 5-시클로프로필-3-(2,6-디클로로페닐)-4-(7-아자스피로[3.5]논-1-엔-2-일)이속사졸
트리플루오로아세트산 (8.6 mL, 111.0 mmol)을 tert-부틸 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시-7-아자스피로[3.5]노난-7-카르복실레이트 (5.5 g, 11.2 mmol)가 들은 플라스크에 첨가하였다. 혼합물을 실온에서 1시간 동안 교반하고, 과량의 TFA를 진공 하에 제거하였다. 잔류물을 EtOAc로 희석하고, 포화 수성 K2CO3에 이어서 염수로 세척하였다. 합한 수성 층을 EtOAc로 역추출하고, 합한 유기 추출물을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축 건조시켜 5-시클로프로필-3-(2,6-디클로로페닐)-4-(7-아자스피로[3.5]논-1-엔-2-일)이속사졸 (4.2 g, 11.2 mmol, 100% 수율)을 백색 고체로서 수득하였다.
1H NMR (400 MHz, DMSO-d6) δ 8.43-8.24 (m, 1H), 7.71-7.57 (m, 3H), 5.89 (s, 1H), 3.33 (br s, 2H), 3.06 (br s, 2H), 3.00-2.88 (m, 2H), 2.35 (s, 1H), 2.34-2.25 (m, 1H), 1.72-1.63 (m, 3H), 1.27-1.11 (m, 4H).
실시예 1. 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
탄산세슘 (0.1 g, 0.33 mmol) 및 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트 (60.8 mg, 0.20 mmol)를 DMA (0.38 mL) 중 5-시클로프로필-3-(2,6-디클로로페닐)-4-(7-아자스피로[3.5]논-1-엔-2-일)이속사졸 (50 mg, 0.13 mmol)의 실온 용액에 첨가하고, 반응 혼합물을 90℃로 가열하였다. 2시간 동안 가열한 후, 반응 혼합물을 THF (1.0 mL), 물 (0.2 mL) 및 MeOH (0.1mL)로 희석하였다. 수산화리튬 1수화물 (0.02 g, 0.40 mmol)을 혼합물에 첨가하고, 반응 용기를 밀봉하고, 90℃로 밤새 가열하였다. 이어서, 반응물을 1.0 N HCl 0.5 mL의 첨가에 의해 켄칭하였다. 생성된 혼합물을 이스코 건조 로드 카트리지 내 셀라이트 패트 상에 로딩하고, C-18 역상 플래쉬 크로마토그래피 (A 중 B 10-100%, A = 10:90:0.1 MeCN:H2O:TFA, B = 90:10:0.1 MeCN:H2O:TFA, 18분 선형 구배, 이스코 50 g C-18 골드 칼럼)에 의해 정제하고, 목적 분획을 합하고, 농축시켜 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (69 mg, 0.1 mmol, 88% 수율)을 황갈색 고체로서 수득하였다.
MS (ESI) m/z: 570.6 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.12 (d, J=1.5 Hz, 1H), 7.74 (dd, J=11.1, 1.4 Hz, 1H), 7.47-7.40 (m, 2H), 7.39-7.33 (m, 1H), 5.78 (s, 1H), 3.78 (dt, J=13.1, 5.1 Hz, 2H), 3.63-3.51 (m, 2H), 2.43 (s, 2H), 2.18 (tt, J=8.4, 5.0 Hz, 1H), 1.80-1.74 (m, 4H), 1.38-1.28 (m, 2H), 1.21-1.11 (m, 2H); FXR EC50 = 7 nM; 마우스 생체내 (3 mg/kg, @ 6h): Cyp7a1 = -99%, Fgf15 = +18x; (30 mg/kg, @ 6h): Cyp7a1 = -99%, Fgf15 = +31x.
실시예 2
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-플루오로피콜리네이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 496.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.57 (d, J=1.8 Hz, 1H), 7.87 (dd, J=9.0, 2.3 Hz, 1H), 7.68-7.61 (m, 2H), 7.61-7.54 (m, 1H), 6.81 (d, J=9.2 Hz, 1H), 5.85 (s, 1H), 3.86-3.75 (m, 2H), 3.42-3.30 (m, 1H), 2.38-2.25 (m, 3H), 1.58-1.46 (m, 4H), 1.27-1.16 (m, 2H), 1.15-1.07 (m, 2H); FXR EC50 = 31 nM.
실시예 3
2-(3-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1-옥사-8-아자스피로[4.5]데스-3-엔-8-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, tert-부틸 2-옥소-7-아자스피로[3.5우]노난-7-카르복실레이트를 tert-부틸 3-옥소-1-옥사-8-아자스피로[4.5]데칸-8-카르복실레이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 586.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.14 (s, 1H), 7.70-7.51 (m, 4H), 5.67 (s, 1H), 4.57 (s, 2H), 3.74 (br s, 1H), 3.50 (br t, J=10.8 Hz, 2H), 2.34-2.23 (m, 1H), 1.78-1.66 (m, 2H), 1.59 (br d, J=13.4 Hz, 2H), 1.25-1.16 (m, 2H), 1.13-1.06 (m, 2H); FXR EC50 = 240 nM.
실시예 4
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 피콜린산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-플루오로피콜리네이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 495.8 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.70-7.57 (m, 4H), 7.24 (d, J=7.0 Hz, 1H), 7.02 (d, J=8.9 Hz, 1H), 5.85 (s, 1H), 3.85-3.69 (m, 2H), 3.41-3.23 (m, 1H), 2.38-2.27 (m, 3H), 1.54 (br s, 4H), 1.28-1.17 (m, 3H), 1.17-1.09 (m, 3H); FXR EC50 = 712 nM.
실시예 5
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)피리다진-3-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-클로로피리다진-3-카르복실레이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 497.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.76 (br d, J=9.5 Hz, 1H), 7.70-7.61 (m, 2H), 7.61-7.53 (m, 1H), 7.21 (br d, J=9.8 Hz, 1H), 5.86 (s, 1H), 3.88 (br d, J=13.1 Hz, 1H), 3.44 (br d, J=4.6 Hz, 1H), 2.34 (s, 3H), 1.91 (s, 1H), 1.57 (br s, 4H), 1.29-1.16 (m, 2H), 1.13 (br d, J=2.1 Hz, 2H) FXR EC50 = 313 nM.
실시예 6
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-7-메틸-7H-피롤로[2,3-d]피리미딘-5-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-클로로-7-메틸-7H-피롤로[2,3-d]피리미딘-5-카르복실레이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 550.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.78 (s, 1H), 7.75 (s, 1H), 7.67-7.60 (m, 2H), 7.61-7.53 (m, 1H), 5.85 (s, 1H), 3.99 (br d, J=13.4 Hz, 1H), 3.81-3.67 (m, 2H), 3.53-3.39 (m, 1H), 2.40-2.22 (m, 3H), 1.89 (s, 1H), 1.52 (br s, 4H), 1.29-1.16 (m, 2H), 1.11 (br d, J=2.4 Hz, 2H) DMSO 하의 추가의 피크 및 H2O 피크; FXR EC50 = 47 nM.
일반적 방법 B
실시예 7
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실산
디옥산 중 5-시클로프로필-3-(2,6-디클로로페닐)-4-(7-아자스피로[3.5]논-1-엔-2-일)이속사졸 (0.13 g, 0.34 mmol, 일반적 방법 A에 기재된 합성), 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트 (77 mg, 0.34 mmol) 및 Cs2CO3 (0.22 g, 0.69 mmol)의 슬러리 (3.4 mL)를 5분 동안 혼합물을 통해 질소를 버블링시킴으로써 탈기시켰다. 이어서, 클로로(2-디시클로헥실포스피노-2',6'-디이소프로폭시-1,1'-비페닐)[2-(2'-아미노-1,1'-비페닐)]팔라듐(II) (RuPhos-Pd-G2) (13.3 mg, 0.02 mmol)을 첨가하고, 반응 혼합물을 밀봉하고, 90℃로 가열하였다. 밤새 가열한 후, 추가의 RuPhos-Pd-G2 (13.3 mg, 0.02 mmol)를 첨가하고, 질소를 혼합물을 통해 버블링하고, 이것을 다시 밀봉하고, 100℃로 가열하였다. 1시간 후, 반응 혼합물을 농축 건조시키고, 잔류물을 THF (1.0 mL), 물 (0.4 mL), 및 MeOH의 혼합물 (0.1 mL) 중에 용해시켰다. 수산화리튬 1수화물 (27.9 mg, 0.67 mmol)을 혼합물에 첨가하고, 반응 용기를 밀봉하고, 90℃로 가열하였다. 2시간 동안 가열한 후, 반응을 1N HCl로 켄칭한 다음, 진공 하에 농축시켜 최소량의 부피를 수득하였다. 잔류물을 MeOH에 녹이고, 여과하고, 조 물질을 하기 조건으로 정제용 LC/MS를 통해 정제하였다: 칼럼: 엑스브리지 C18, 19 x 200 mm, 5-μm 입자; 이동상 A: 5:95 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 이동상 B: 95:5 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 구배: 24분에 걸쳐 45-100% B, 이어서 100% B에서 10-분 유지; 유량: 20 mL/분. 목적 생성물을 함유하는 분획을 합하고, 원심 증발을 통해 건조시켜 6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실산을 수득하였다.
MS (ESI) m/z: 549.2 [M+H]+;
1H NMR (400 MHz, DMSO-d6) δ 8.00 (d, J=8.8 Hz, 1H), 7.80 (s, 1H), 7.67 (d, J=1.8 Hz, 1H), 7.65 (d, J=0.7 Hz, 1H), 7.62-7.56 (m, 1H), 6.79 (d, J=8.8 Hz, 1H), 5.84 (s, 1H), 3.81-3.71 (m, 3H), 3.31 (td, J=8.5, 3.5 Hz, 2H), 2.38-2.27 (m, 5H), 1.66-1.51 (m, 5H), 1.25-1.17 (m, 2H), 1.16-1.07 (m, 3H); FXR EC50 = 24 nM.
실시예 8
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인돌-3-카르복실산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 메틸 6-브로모-1-메틸-1H-인돌-3-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 548.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.86-7.75 (m, 2H), 7.71-7.63 (m, 2H), 7.63-7.55 (m, 1H), 6.97-6.86 (m, 2H), 5.87 (s, 1H), 3.75 (s, 3H), 3.30-3.20 (m, 1H), 2.96 (br t, J=9.2 Hz, 2H), 2.40-2.28 (m, 3H), 1.77-1.68 (m, 2H), 1.68-1.57 (m, 2H), 1.28-1.16 (m, 3H), 1.14 (br d, J=2.7 Hz, 2H); FXR EC50 = 45 nM.
실시예 9
3-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 벤조산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 에틸 3-브로모벤조에이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 495.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.66 (d, J=7.6 Hz, 2H), 7.63-7.54 (m, 1H), 7.45 (br s, 1H), 7.38-7.26 (m, 2H), 7.19 (br d, J=7.0 Hz, 1H), 5.85 (s, 1H), 3.30 (br d, J=12.5 Hz, 1H), 3.06-2.96 (m, 2H), 2.37-2.25 (m, 3H), 1.72-1.51 (m, 4H), 1.26-1.16 (m, 2H), 1.14 (br d, J=2.7 Hz, 2H); FXR EC50 = 4200 nM.
실시예 10
4-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 벤조산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 에틸 4-브로모벤조에이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 495.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.72 (br d, J=8.9 Hz, 2H), 7.68-7.52 (m, 3H), 6.91 (br d, J=8.9 Hz, 2H), 5.83 (s, 1H), 3.42 (br d, J=12.8 Hz, 1H), 3.12 (br t, J=9.2 Hz, 2H), 2.39-2.24 (m, 3H), 1.63-1.49 (m, 4H), 1.26-1.15 (m, 4H), 1.12 (br s, 2H); FXR EC50 = 135 nM.
실시예 11
2-(3'-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-8-아자스피로[비시클로[3.2.1]옥탄-3,1'-시클로부탄]-2'-엔-8-일)-4-플루오로벤조[d]티아졸-6-카르복실산
단계 1. tert-부틸 3'-옥소-8-아자스피로[비시클로[3.2.1]옥탄-3,1'-시클로부탄]-8-카르복실레이트
아연-구리 커플 (28.3 g, 219 mmol)을 디에틸 에테르 (43.0 mL) 중 tert-부틸 3-메틸렌-8-아자비시클로[3.2.1]옥탄-8-카르복실레이트 (4.9 g, 21.9 mmol)의 용액에 첨가하였다. DME (21.5 mL) 중 트리클로로아세틸 클로라이드 (13.6 mL, 121 mmol)를 첨가하고, 반응 혼합물을 실온에서 36시간 동안 교반하였다. 반응물을 1M 수성 K2HPO4 (격렬한 버블링)로 조심스럽게 켄칭한 다음, 셀라이트를 통해 여과하였다 (Et2O 세척액). 여과물을 진공 하에 농축시키고, MeOH (65.6 mL)로 희석하였다. 염화암모늄 (4.49 g, 84 mmol)을 급속하게 교반하는 혼합물에 첨가하고, 이어서 아연 분진 (8.0 g, 122 mmol)을 2개의 동일한 분량으로 첨가하였다. 40분 동안 교반한 후, 반응 혼합물을 셀라이트 (MeOH 세척액)을 통해 여과하고, 농축 건조시켰다. 잔류물을 EtOAc에 녹이고, 물 및 염수로 세척하였다. 수성 층을 EtOAc로 역추출하고, 합한 유기부를 Na2SO4 상에서 건조시키고, 여과하고, SiO2로 상으로 농축 건조시켰다. 생성된 혼합물을 SiO2 상 플래쉬 크로마토그래피 (0-50% EtOAc/hex, 이스코 80 g 칼럼, ELS 검출기 사용됨)에 의해 정제하여 tert-부틸 3'-옥소-8-아자스피로[비시클로[3.2.1]옥탄-3,1'-시클로부탄]-8-카르복실레이트 (1.1 g, 4.2 mmol, 20% 수율)을 백색 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 4.50-4.13 (m, 2H), 3.12 (d, J=1.8 Hz, 2H), 2.85 (br s, 2H), 2.23-1.87 (m, 4H), 1.86-1.66 (m, 4H), 1.48 (s, 9H).
실시예 11. 2-(3'-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-8-아자스피로[비시클로[3.2.1]옥탄-3,1'-시클로부탄]-2'-엔-8-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, tert-부틸 2-옥소-7-아자스피로[3.5]노난-7-카르복실레이트를, tert-부틸 3'-옥소-8-아자스피로[비시클로[3.2.1]옥탄-3,1'-시클로부탄]-8-카르복실레이트로 대체하여, 실시예 1의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 596.5 [M+H]+; 올레핀 이성질체의 ~6:4 혼합물:
1H NMR (400 MHz, DMSO-d6) δ 8.21 (dd, J=3.6, 1.4 Hz, 1H), 7.75-7.46 (m, 5H), 6.28 (s, 1H), 5.25 (s, 1H), 4.49-4.29 (m, 2H), 2.84 (s, 1H), 2.17-1.89 (m, 7H), 1.85-1.59 (m, 3H), 1.31-1.07 (m, 5H); FXR EC50 = 189 nM.
실시예 12
6-(3'-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-8-아자스피로[비시클로[3.2.1]옥탄-3,1'-시클로부탄]-2'-엔-8-일)니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-플루오로니코티네이트로 대체하여, 실시예 11의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 522.6 [M+H]+;
1H NMR은 올레핀 이성질체의 ~6:4 혼합물에 대한 것임:
1H NMR (400 MHz, DMSO-d6) δ 8.66-8.51 (m, 1H), 7.99-7.78 (m, 1H), 7.71-7.48 (m, 3H), 6.71-6.64 (m, 1H), 6.24 (s, 1H), 5.18 (s, 1H), 4.57 (br d, J=3.5 Hz, 2H), 2.80 (s, 1H), 2.37-2.23 (m, 2H), 2.01-1.82 (m, 5H), 1.83-1.65 (m, 3H), 1.63-1.45 (m, 3H), 1.30-1.06 (m, 7H); FXR EC50 = 182 nM.
실시예 13
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]노난-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
트리에틸실란 (70.0 μL, 0.44 mmol)을 TFA (175 μL) 중 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (실시예 1) (10 mg, 0.02 mmol)의 용액에 첨가하였다. 반응 바이알을 밀봉하고, 80℃로 가열하였다. 30분 후, 반응 혼합물을 농축 건조시키고, 잔류물을 1:1 DMF 및 MeOH의 ~2 mL에 녹이고, 여과하고, 하기 조건으로 정제용 LC/MS를 통해 정제하였다: 칼럼: 엑스브리지 C18, 19 x 200 mm, 5-μm 입자; 이동상 A: 5:95 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 이동상 B: 95:5 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 구배: 20분에 걸쳐 30-70% B, 이어서 100% B에서 5-분 유지; 유량: 20 mL/분. 목적 생성물을 함유하는 분획을 합하고, 원심 증발을 통해 건조시켜 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐) 이속사졸-4-일)-7-아자스피로[3.5]노난-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산을 수득하였다.
MS (ESI) m/z: 572.0 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.16 (s, 1H), 7.71-7.52 (m, 4H), 3.45-3.34 (m, 1H), 2.28-2.17 (m, 1H), 2.12-1.99 (m, 2H), 1.78 (br t, J=10.7 Hz, 2H), 1.74-1.65 (m, 2H), 1.36-1.26 (m, 2H), 1.22 (s, 2H), 1.12 (br d, J=7.9 Hz, 3H), 1.08-0.99 (m, 3H); FXR EC50 = 202 nM.
실시예 14
4-(2-(3-(2-클로로페닐)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)벤조산
표제 화합물을, 실시예 10의 제조 동안 부흐발트 아미노화 단계 동안의 Pd-매개 탈할로겐화로부터 수득하였다. 대안적으로, 표제 화합물을, 2,6-디클로로벤즈알데히드를 2-클로로벤즈알데히드로 대체하여, 실시예 10에 대하여 기재된 바와 같이 제조할 수 있었다.
MS (ESI) m/z: 461.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.72 (br d, J=8.9 Hz, 2H), 7.66-7.60 (m, 1H), 7.59-7.52 (m, 1H), 7.47 (br d, J=4.0 Hz, 2H), 6.92 (br d, J=8.9 Hz, 2H), 5.86 (s, 1H), 3.49-3.38 (m, 1H), 3.21-3.06 (m, 2H), 2.92 (q, J=7.1 Hz, 1H), 2.35 (s, 2H), 2.32-2.22 (m, 1H), 1.67-1.49 (m, 4H), 1.23 (s, 3H), 1.19-1.12 (m, 4H), 1.10 (br d, J=2.4 Hz, 2H); FXR EC50 = 885 nM.
실시예 15
2-(3'-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-8-아자스피로[비시클로[3.2.1]옥탄-3,1'-시클로부탄]-8-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (실시예 1)을 2-(3'-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-8-아자스피로[비시클로[3.2.1]옥탄-3,1'-시클로부탄]-2'-엔-8-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (실시예 11)로 대체하여, 실시예 13의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 598.0 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.17 (s, 1H), 7.68-7.52 (m, 4H), 4.48-4.12 (m, 1H), 3.89 (s, 1H), 3.58-3.34 (m, 1H), 2.23-2.13 (m, 2H), 2.11-2.03 (m, 1H), 2.03-1.86 (m, 3H), 1.83-1.72 (m, 1H), 1.72-1.54 (m, 4H), 1.33 (br d, J=13.7 Hz, 1H), 1.10 (br d, J=8.2 Hz, 2H), 1.01 (br d, J=2.4 Hz, 2H); FXR EC50 = 301 nM.
실시예 16
6-(3'-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-8-아자스피로[비시클로[3.2.1]옥탄-3,1'-시클로부탄]-8-일)니코틴산
표제 화합물을, 2-(3'-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-8-아자스피로[비시클로[3.2.1]옥탄-3,1'-시클로부탄]-2'-엔-8-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (실시예 11)을 6-(3'-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-8-아자스피로[비시클로[3.2.1]옥탄-3,1'-시클로부탄]-2'-엔-8-일)니코틴산 (실시예 12)로 대체하여, 실시예 15의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 523.9 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.57 (d, J=1.5 Hz, 1H), 7.86 (dd, J=9.0, 2.0 Hz, 1H), 7.70-7.51 (m, 3H), 6.63 (br d, J=8.9 Hz, 1H), 4.66-4.48 (m, 1H), 4.40 (br s, 1H), 2.62-2.57 (m, 1H), 2.25-2.12 (m, 1H), 2.12-1.98 (m, 2H), 1.97-1.77 (m, 3H), 1.59 (br t, J=10.1 Hz, 4H), 1.45 (br d, J=11.6 Hz, 1H), 1.20 (br d, J=13.4 Hz, 1H), 1.10 (br d, J=8.2 Hz, 2H), 1.01 (br d, J=2.4 Hz, 2H); FXR EC50 = 646 nM.
실시예 17
2-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메톡시)벤즈알데히드로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 585.9 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.18 (br s, 1H), 7.73-7.63 (m, 1H), 7.63-7.46 (m, 4H), 5.92 (s, 1H), 3.70 (br d, J=2.2 Hz, 1H), 3.64 (br s, 2H), 3.55-3.43 (m, 1H), 2.47-2.37 (m, 2H), 2.37-2.26 (m, 1H), 1.63 (br s, 4H), 1.25-1.12 (m, 3H), 1.10 (br s, 2H); FXR EC50 = 50 nM.
실시예 18
6-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)피리다진-3-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-클로로피리다진-3-카르복실레이트로 대체하여, 실시예 17의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 513.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.78 (br d, J=9.4 Hz, 1H), 7.71-7.60 (m, 1H), 7.59-7.44 (m, 3H), 7.30 (br s, 1H), 7.36-7.05 (m, 1H), 5.88 (s, 1H), 3.55-3.38 (m, 2H), 2.38 (s, 2H), 2.33-2.22 (m, 1H), 1.55 (br s, 4H), 1.25-1.10 (m, 4H), 1.06 (br s, 2H), 0.98 (d, J=6.2 Hz, 1H); FXR EC50 = 1500 nM.
실시예 19
5-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 피라진-2-카르복실산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 메틸 5-브로모피라진-2-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 497.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.59 (br s, 1H), 8.28 (br s, 1H), 7.70-7.52 (m, 3H), 5.85 (s, 1H), 4.18-3.95 (m, 4H), 3.53-3.35 (m, 2H), 2.33 (br s, 3H), 1.55 (br s, 4H), 1.21 (br d, J=5.0 Hz, 3H), 1.11 (br s, 2H), 1.00 (br d, J=6.1 Hz, 1H); FXR EC50 = 110 nM.
실시예 20
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 퀴놀린-2-카르복실산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 메틸 6-브로모퀴놀린-2-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 546.3 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.19 (d, J=8.5 Hz, 1H), 7.95 (d, J=8.5 Hz, 1H), 7.91 (d, J=9.4 Hz, 1H), 7.72-7.65 (m, 3H), 7.63-7.55 (m, 1H), 7.22 (d, J=2.2 Hz, 1H), 5.86 (s, 1H), 3.59-3.46 (m, 2H), 3.20 (br t, J=9.4 Hz, 2H), 2.40-2.30 (m, 3H), 1.78-1.58 (m, 4H), 1.29-1.23 (m, 2H), 1.16-1.09 (m, 2H); FXR EC50 = 63 nM; 마우스 생체내 (3 mg/kg, @ 6h): Cyp7a1 = -98%, Fgf15 = +30x.
실시예 21
6-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-플루오로니코티네이트로 대체하여, 실시예 17의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 511.9 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.54 (d, J=1.8 Hz, 1H), 7.94-7.82 (m, 1H), 7.72-7.60 (m, 1H), 7.55-7.41 (m, 3H), 6.80 (br d, J=9.2 Hz, 1H), 5.87 (s, 1H), 3.81 (br d, J=15.3 Hz, 2H), 3.46-3.27 (m, 2H), 2.36 (s, 2H), 2.31-2.20 (m, 1H), 1.60-1.42 (m, 4H), 1.23-1.11 (m, 4H), 1.10-1.00 (m, 2H); FXR EC50 = 770 nM.
실시예 22
5-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 피리미딘-2-카르복실산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 메틸 5-브로모피리미딘-2-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 497.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.46 (br s, 2H), 7.75-7.50 (m, 3H), 5.85 (s, 1H), 3.68 (br d, J=13.7 Hz, 1H), 3.51 (br s, 1H), 3.21 (br s, 2H), 2.32 (s, 3H), 1.71-1.51 (m, 4H), 1.27-1.16 (m, 2H), 1.12 (br s, 2H); FXR EC50 = 1500 nM.
실시예 23
5-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 피콜린산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 메틸 5-브로모피콜리네이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 496.0 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.29 (br s, 1H), 7.83 (d, J=8.9 Hz, 1H), 7.70-7.54 (m, 3H), 7.37-7.26 (m, 1H), 5.84 (s, 1H), 3.83-3.68 (m, 1H), 3.49 (br d, J=13.1 Hz, 1H), 3.24-3.11 (m, 2H), 2.31 (s, 3H), 1.68-1.50 (m, 4H), 1.27-1.15 (m, 2H), 1.11 (br d, J=2.1 Hz, 2H), 1.00 (d, J=6.4 Hz, 1H); FXR EC50 = 340 nM.
실시예 24
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 벤조[d]티아졸-6-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 에틸 2-브로모벤조[d]티아졸-6-카르복실레이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 552.0 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.32 (s, 1H), 7.83 (br d, J=7.9 Hz, 1H), 7.72-7.56 (m, 3H), 7.43 (br d, J=8.2 Hz, 1H), 5.89 (s, 1H), 3.90 (s, 1H), 3.71 (br d, J=11.0 Hz, 1H), 3.17 (s, 1H), 2.41-2.29 (m, 3H), 1.64 (br s, 4H), 1.30-1.17 (m, 4H), 1.14 (br d, J=2.4 Hz, 2H); FXR EC50 = 17 nM.
실시예 25
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-벤조[d]이미다졸-5-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-브로모-1-메틸-1H-벤조[d]이미다졸-5-카르복실레이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 549.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.94 (s, 1H), 7.78 (br d, J=8.2 Hz, 1H), 7.73-7.65 (m, 2H), 7.65-7.57 (m, 1H), 7.45 (br d, J=8.5 Hz, 1H), 5.89 (s, 1H), 3.63 (s, 3H), 3.24-3.11 (m, 1H), 2.36 (s, 3H), 1.82-1.72 (m, 2H), 1.70 (br s, 2H), 1.28-1.18 (m, 4H), 1.15 (br d, J=2.1 Hz, 2H); FXR EC50 = 1020 nM.
실시예 26
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)벤조[d]옥사졸-5-카르복실산
단계 1. 메틸 2-브로모벤조[d]옥사졸-5-카르복실레이트
tert-부틸 니트라이트 (0.28 g, 2.7 mmol)를 아세토니트릴 (11.3 mL) 중 브로민화구리 (II) (0.55 g, 2.5 mmol)의 0℃ 현탁액에 천천히 첨가하였다. 5분 후, 메틸 2-아미노벤조[d]옥사졸-5-카르복실레이트 (0.43 g, 2.3 mmol)를 첨가하고, 반응 혼합물을 실온으로 만들었다. 밤새 교반한 후, 혼합물을 SiO2 상으로 농축시켜 정제하였다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-60% EtOAc/헥산, 이스코 40 g 칼럼)에 의해 정제하여 메틸 2-브로모벤조[d]옥사졸-5-카르복실레이트 (0.16 g, 0.60 mmol, 27% 수율)을 백색 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.44-8.35 (m, 1H), 8.13 (dd, J=8.6, 1.8 Hz, 1H), 7.58 (d, J=8.6 Hz, 1H), 3.97 (s, 3H).
실시예 26. 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)벤조[d]옥사졸-5-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-브로모벤조[d]옥사졸-5-카르복실레이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 536.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.75 (s, 1H), 7.71-7.63 (m, 3H), 7.63-7.57 (m, 1H), 7.45 (d, J=8.2 Hz, 1H), 5.89 (s, 1H), 3.82-3.66 (m, 2H), 3.47 (br d, J=8.2 Hz, 1H), 2.40-2.29 (m, 3H), 1.72-1.56 (m, 4H), 1.28-1.18 (m, 3H), 1.15 (br d, J=2.4 Hz, 2H); FXR EC50 = 157 nM.
실시예 27
6-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-5-플루오로니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-클로로-5-플루오로니코티네이트로 대체하여, 실시예 17의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 530.0 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.46 (br s, 1H), 7.78-7.64 (m, 2H), 7.63-7.47 (m, 3H), 5.91 (s, 1H), 3.78 (br d, J=13.7 Hz, 2H), 2.41 (s, 2H), 2.35-2.25 (m, 1H), 1.73-1.54 (m, 4H), 1.24 (s, 1H), 1.18 (br d, J=7.6 Hz, 2H), 1.11 (br s, 2H); FXR EC50 = 1100 nM.
실시예 28
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-5-플루오로니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-클로로-5-플루오로니코티네이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 514.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.45 (br s, 1H), 7.81-7.69 (m, 1H), 7.68-7.63 (m, 2H), 7.62-7.56 (m, 1H), 5.86 (s, 1H), 3.76 (br s, 1H), 2.34 (br s, 3H), 1.60 (br s, 4H), 1.29-1.17 (m, 3H), 1.14 (br s, 2H) 1H NMR 실험에서의 물 억제로 인해 추가의 피크가 소실되었음; FXR EC50 = 453 nM.
실시예 29
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 570.1 [M+H]+;
1H NMR (400 MHz, DMSO-d6) δ 8.20 (d, J=1.5 Hz, 1H), 7.96-7.90 (m, 1H), 7.87-7.73 (m, 2H), 7.63-7.53 (m, 2H), 5.79 (s, 1H), 3.81-3.63 (m, 3H), 2.33 (s, 4H), 1.69-1.54 (m, 4H), 1.23-1.15 (m, 3H), 1.13 (dt, J=5.4, 2.8 Hz, 2H); FXR EC50 = 14 nM.
실시예 30
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-플루오로니코티네이트로 대체하여, 실시예 29의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 496.1 [M+H]+;
1H NMR (400 MHz, DMSO-d6) δ 8.58 (d, J=2.0 Hz, 1H), 7.96-7.90 (m, 1H), 7.88 (dd, J=9.0, 2.4 Hz, 1H), 7.85-7.73 (m, 2H), 7.57 (d, J=7.0 Hz, 1H), 6.83 (d, J=9.2 Hz, 1H), 5.76 (s, 1H), 3.86-3.78 (m, 2H), 3.44-3.33 (m, 2H), 2.32-2.24 (m, 3H), 1.51 (br t, J=5.5 Hz, 4H), 1.24-1.15 (m, 2H), 1.15-1.08 (m, 2H); FXR EC50 = 110 nM.
실시예 31
(6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 니코티노일)글리신
단계 A. T3P (45.2 μL, 0.08 mmol) 및 Et3N (21.4 μL, 0.15 mmol)을 DCE (0.19 mL) 중 6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)니코틴산 (실시예 30) (19 mg, 0.04 mmol) 및 메틸 2-아미노아세테이트, HCl (9.6 mg, 0.08 mmol)의 용액에 첨가하였다. 반응 혼합물을 실온에서 교반하고, 조 반응 혼합물을 SiO2 카트리지 상에 직접 로딩하고 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/hex, 이스코 4 g 칼럼)에 의해 정제하여 메틸 2-(6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐) 이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)니코틴아미도)아세테이트 (10 mg, 0.018 mmol, 46.0% 수율)을 백색 발포체로서 수득하였다.
단계 B. 메틸 2-(6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)니코틴아미도)아세테이트 (10 mg, 0.02 mmol)를 THF (136 μL), 물 (27.2 μL), MeOH (13.6 μL) 중에 용해시키고, 이어서 수산화리튬 1수화물 (3.7 mg, 0.09 mmol)을 혼합물에 첨가하였다. 반응 용기를 밀봉하고, 60℃로 가열하였다. 2시간 동안 가열한 후, 반응을 1N HCl로 켄칭한 다음, 질소의 스트림 하에 농축시켜 최소 부피를 수득하였다. 잔류물을 DMF에 녹이고, 여과하고, 조 물질을 하기 조건으로 정제용 LC/MS를 통해 정제하였다: 칼럼: 엑스브리지 C18, 19 x 200 mm, 5-μm 입자; 이동상 A: 5:95 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 이동상 B: 95:5 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 구배: 19분에 걸쳐 20-60% B, 이어서 100% B에서 5-분 유지; 유량: 20 mL/분. 목적 생성물을 함유하는 분획을 합하고, 원심 증발을 통해 건조시켜 (6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)니코티노일)글리신 (7.7 mg, 0.01 mmol, 79% 수율)을 수득하였다.
MS (ESI) m/z: 552.9 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.78 (br d, J=1.2 Hz, 1H), 8.70 (br s, 1H), 8.13 (br t, J=6.6 Hz, 2H), 8.05-7.92 (m, 2H), 7.78 (br d, J=7.3 Hz, 1H), 7.04 (br d, J=9.2 Hz, 1H), 5.96 (s, 1H), 4.06 (br d, J=5.5 Hz, 2H), 4.02-3.90 (m, 2H), 1.71 (br s, 4H), 1.45 (s, 2H), 1.42-1.35 (m, 2H), 1.33 (br d, J=2.4 Hz, 2H), 1.21 (d, J=6.4 Hz, 2H); FXR EC50 = 5300 nM.
실시예 32
(2-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르보닐)글리신
표제 화합물을, 6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)니코틴산 (실시예 30)을, 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (실시예 29)로 대체하여, 실시예 31의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 627.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.80 (br s, 1H), 8.11 (s, 1H), 7.93 (br d, J=7.3 Hz, 1H), 7.86-7.72 (m, 2H), 7.62 (br d, J=11.9 Hz, 1H), 7.57 (br d, J=7.3 Hz, 1H), 5.78 (s, 1H), 3.92 (br s, 1H), 3.69 (br d, J=13.7 Hz, 1H), 2.37-2.25 (m, 3H), 1.71-1.55 (m, 4H), 1.27-1.16 (m, 3H), 1.12 (br d, J=2.4 Hz, 2H); 1H NMR 실험에서의 물 억제로 인해 추가의 1H NMR 피크가 소실되었음; FXR EC50 = 1500 nM.
실시예 33
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시-7-아자스피로[3.5]노난-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을 일반적 방법 A의 실시예 1의 제조 동안 소량의 단리물로서 수득하였고, 하기 조건을 이용한 정제용 LC/MS에 의해 정제하였다:
칼럼: 엑스브리지 C18, 19 × 200 mm, 5-μm 입자; 이동상 A: 5:95 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 이동상 B: 95:5 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 구배: 19분에 걸쳐 25-65% B, 이어서 100% B에서 5-분 유지; 유량: 20 mL/분.
목적 생성물을 함유하는 분획을 합하고, 원심 증발을 통해 건조시켰다.
MS (ESI) m/z: 588.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.18 (br s, 1H), 7.67-7.48 (m, 3H), 6.38 (s, 1H), 3.67 (br s, 1H), 3.54 (br s, 1H), 2.90 (s, 1H), 2.74 (s, 1H), 2.38 (br d, J=12.8 Hz, 2H), 2.31-2.18 (m, 1H), 1.98 (br s, 2H), 1.54 (br s, 2H), 1.18-1.06 (m, 2H), 1.01-0.90 (m, 2H); FXR EC50 = 4800 nM.
실시예 34
2-(6-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-2-아자스피로[3.3]헵트-5-엔-2-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, tert-부틸 2-옥소-7-아자스피로[3.5]노난-7-카르복실레이트를 tert-부틸 6-옥소-2-아자스피로[3.3]헵탄-2-카르복실레이트로 대체하여, 실시예 29의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 542.6 [M+H]+;
1H NMR (400 MHz, DMSO-d6) δ 12.96 (br s, 1H), 8.23 (d, J=1.5 Hz, 1H), 7.99-7.89 (m, 1H), 7.87-7.74 (m, 2H), 7.65-7.51 (m, 2H), 5.67 (s, 1H), 4.34 (d, J=9.2 Hz, 2H), 4.24 (d, J=9.2 Hz, 2H), 2.83 (s, 2H), 2.37-2.21 (m, 1H), 1.17-1.09 (m, 2H), 0.92-0.79 (m, 2H); FXR EC50 = 400 nM.
실시예 35
6-(6-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-2-아자스피로[3.3]헵트-5-엔-2-일)니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-플루오로니코티네이트로 대체하여, 실시예 34의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 468.6 [M+H]+;
1H NMR (400 MHz, DMSO-d6) δ 8.56 (d, J=2.0 Hz, 1H), 7.97-7.87 (m, 2H), 7.86-7.74 (m, 2H), 7.59 (d, J=6.6 Hz, 1H), 6.35 (d, J=9.2 Hz, 1H), 5.64 (s, 1H), 4.17 (d, J=9.2 Hz, 2H), 4.06 (d, J=9.2 Hz, 2H), 2.78 (s, 2H), 2.36-2.26 (m, 1H), 1.24-1.17 (m, 2H), 1.17-1.09 (m, 2H); FXR EC50 = 4300 nM.
실시예 36
2-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]노난-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (실시예 1)을 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (실시예 29)로 대체하여, 실시예 13의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 572.4 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.12 (s, 1H), 7.91 (d, J=7.6 Hz, 1H), 7.85-7.72 (m, 2H), 7.60-7.53 (m, 3H), 3.90 (s, 1H), 3.39 (br d, J=9.2 Hz, 2H), 2.27-2.14 (m, 1H), 2.09-1.96 (m, 2H), 1.91 (s, 2H), 1.77 (br t, J=10.8 Hz, 2H), 1.73-1.62 (m, 2H), 1.45-1.34 (m, 2H), 1.17-1.08 (m, 2H), 1.07-0.97 (m, 2H); FXR EC50 = 116 nM.
실시예 37
2-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]노난-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (실시예 29)를 6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)니코틴산 (실시예 30)으로 대체하여, 실시예 36의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 498.4 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.55 (br s, 1H), 7.90 (d, J=7.9 Hz, 1H), 7.85 (br s, 1H), 7.82-7.68 (m, 2H), 7.55 (d, J=7.3 Hz, 1H), 6.76 (br d, J=8.9 Hz, 1H), 3.65-3.50 (m, 1H), 3.46-3.29 (m, 2H), 2.26-2.15 (m, 1H), 2.04-1.93 (m, 2H), 1.90 (s, 1H), 1.72 (br t, J=10.8 Hz, 2H), 1.61-1.48 (m, 2H), 1.32-1.20 (m, 2H), 1.15-1.08 (m, 2H), 1.04-0.95 (m, 2H); FXR EC50 = 1400 nM.
일반적 방법 C
실시예 38
(±)-2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸-8-일)-4-플루오로벤조[d]티아졸-6-카르복실산
단계 1. 메틸 5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-카르복실레이트
메틸 3-시클로프로필-3-옥소프로파노에이트 (1.3 g, 8.9 mmol)가 들은 50 mL 둥근 바닥 플라스크에 트리에틸아민 (2.5 mL, 17.8 mmol)을 첨가하였다. 생성된 투명한 용액을 실온에서 15분 동안 교반하고, 빙수조에서 냉각시켰다. 교반하는 용액에 EtOH (4 mL) 중 2,6-디클로로-N-히드록시벤즈이미도일 클로라이드 (2.0 g, 8.9 mmol, 일반적 방법 A에 기재된 합성)의 용액을 10분의 기간에 걸쳐 첨가하여 백색 현탁액을 수득하였다. 첨가한 후, 생성된 현탁액을 실온에서 밤새 교반하였다. 반응 혼합물을 진공 하에 농축시키고, 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-10% EtOAc/헥산, 이스코 80 g 칼럼)에 의해 정제하여 메틸 5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-카르복실레이트 (2.4 g, 7.7 mmol, 87% 수율)을 백색 고체로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 7.45-7.39 (m, 2H), 7.39-7.33 (m, 1H), 3.71 (s, 3H), 2.93 (tt, J=8.5, 5.2 Hz, 1H), 1.47-1.40 (m, 2H), 1.34-1.27 (m, 2H).
단계 2. (5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)메탄올
0℃에서 톨루엔 중 THF (11.1 mL) 중 메틸 5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-카르복실레이트 (3.0 g, 9.6 mmol)에 1 M 디이소부틸 알루미늄 히드라이드 (20.2 mL, 20.2 mmol)의 용액을 첨가하였다. 반응 혼합물을 실온으로 가온하고, 2시간 동안 교반하였다. 반응물을 0℃로 냉각시키고, MeOH (2 mL) 및 1 M 수성 HCl (~75 mL)을 첨가하여 켄칭하였다. 이어서, 혼합물을 EtOAc로 추출하고, 유기 층을 염수로 세척하였다. 유기 층을 MgSO4 상에서 건조시키고, 농축시켜 (5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)메탄올 (2.5 g, 8.9 mmol, 92% 수율)을 백색 고체로서 수득하였으며, 이를 추가의 정제 없이 사용하였다.
1H NMR (500MHz, CDCl3) δ 7.46 (d, J=1.1 Hz, 1H), 7.45 (s, 1H), 7.41-7.36 (m, 1H), 4.44 (s, 2H), 2.22 (tt, J=8.5, 5.2 Hz, 1H), 1.42 (br s, 1H), 1.35-1.25 (m, 2H), 1.23- 1.11 (m, 2H).
단계 3. 5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-카르브알데히드
DCM (37.0 mL) 중 (5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)메탄올 (2.1 g, 7.4 mmol)의 용액에 피리디늄 클로로크로메이트 (6.4 g, 29.6 mmol) 및 미분된 3Å 분자체의 혼합물 (6.1 g)을 첨가하였다. 생성된 혼합물을 실온에서 30분 동안 교반한 다음, 셀라이트의 패드를 통해 여과하였다. 패드를 MeOH/DCM으로 세척하였다. 여과물을 증발시키고, 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 80 g 칼럼)에 의해 정제하여 5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-카르브알데히드 (1.9 g, 6.8 mmol, 93% 수율)을 백색 고체로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 9.67 (s, 1H), 7.49-7.44 (m, 2H), 7.43-7.37 (m, 1H), 2.82 (tt, J=8.3, 5.2 Hz, 1H), 1.52-1.45 (m, 2H), 1.40-1.33 (m, 2H).
단계 4. (±)-tert-부틸 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸-8-카르복실레이트
4-메틸벤젠술폰산 (1.7 mg, 10.0 μmol)에 이어서 tert-부틸 4-히드록시-4-(히드록시메틸)피페리딘-1-카르복실레이트 (23.1 mg, 0.10 mmol) 및 오븐-건조된 3Å 분자체 100 mg을 톨루엔 (0.5 mL) 중 5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-카르브알데히드 (28.2 mg, 0.1 mmol)의 실온 현탁액에 첨가하였다. 생성된 현탁액을 150℃로 밤새 가열하였다. 고체를 여과하고, DCM (~10 mL)로 세척하였다. 여과물을 농축시키고, 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/DCM, 이스코 40 g 칼럼)에 의해 정제하여 tert-부틸 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸-8-카르복실레이트 (12.0 mg, 0.02 mmol, 23% 수율)을 백색 고체로서 수득하였다.
MS (ESI) m/z: 495.1 [M+H]+;
1H NMR (500MHz, CDCl3) δ 7.45-7.37 (m, 2H), 7.36-7.30 (m, 1H), 5.95 (s, 1H), 3.76 (br. s., 1H), 3.61 (d, J=8.0 Hz, 2H), 3.47 (d, J=6.9 Hz, 1H), 3.14 (br. s., 1H), 2.94 (br. s., 1H), 2.37-2.14 (m, 1H), 1.85-1.65 (m, 1H), 1.46 (s, 10H), 1.38-1.23 (m, 3H), 1.22-1.12 (m, 2H), 1.04 (br. s., 1H); FXR EC50 = 4.8 μM.
단계 5. (±)-2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸
트리플루오로아세트산 (0.10 mL, 1.2 mmol)을 DCM (2 mL) 중 (±)-tert-부틸 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸-8-카르복실레이트 (60 mg, 0.12 mmol)의 실온 용액에 첨가하였다. 반응 혼합물을 실온에서 밤새 교반하였다. 과량의 트리플루오로아세트산을 진공 하에 제거하고, 잔류물을 EtOAc (5 mL)와 1M 수성 K2HPO4 (5 mL) 사이에 분배하였다. 유기 층을 Na2SO4 상에서 건조시키고, 여과하고, 농축 건조시켰다. 조 생성물을 직접 후속 단계에 사용하였다.
실시예 38. (±)-에틸 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸-8-일)-4-플루오로벤조[d]티아졸-6-카르복실레이트
탄산세슘 (74.2 mg, 0.23 mmol) 및 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트 (41.5 mg, 0.14 mmol)를 N,N-디메틸아세트아미드 (0.26 mL) 중 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸 (36 mg, 0.09 mmol)의 실온 용액에 첨가하였다. 실온에서의 교반 10분 후, 반응 혼합물을 50℃로 가열하였다. 3시간 후, 반응 혼합물을 부분적으로 농축시키고, 잔류물을 SiO2 상 플래쉬 크로마토그래피 (5-100% EtOAc/헥산, 이스코 24 g 칼럼)에 의해 정제하여 (±)-에틸 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸-8-일)-4-플루오로벤조[d]티아졸-6-카르복실레이트 (23 mg, 0.04 mmol, 39% 수율)을 백색 고체로서 수득하였다.
MS (ESI) m/z: 618.0 [M+H]+;
1H NMR (500MHz, CDCl3) δ 8.10 (d, J=1.4 Hz, 1H), 7.74 (dd, J=11.3, 1.4 Hz, 1H), 7.50-7.40 (m, 2H), 7.39-7.33 (m, 1H), 6.03 (s, 1H), 4.40 (q, J=7.1 Hz, 2H), 4.01 (d, J=12.4 Hz, 1H), 3.91 (d, J=11.8 Hz, 1H), 3.66 (d, J=8.3 Hz, 1H), 3.59-3.46 (m, 2H), 3.40-3.16 (m, 1H), 2.34-2.16 (m, 1H), 1.93 (dd, J=13.8, 2.5 Hz, 1H), 1.81-1.66 (m, 1H), 1.64-1.52 (m, 2H), 1.42 (t, J=7.2 Hz, 3H), 1.34 (dd, J=5.0, 2.2 Hz, 2H), 1.24-1.05 (m, 2H); FXR EC50 = 620 nM.
실시예 39
(±)-2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸-8-일)-4-플루오로벤조[d]티아졸-6-카르복실산
수성 LiOH 1.0 M (130 μL, 0.13 mmol)을 1:1 MeOH: THF (260 μL) 중 에틸 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸-8-일)-4-플루오로벤조[d]티아졸-6-카르복실레이트 (16 mg, 0.03 mmol, 실시예 38)의 실온 용액에 첨가하였다. 반응 혼합물을 실온에서 밤새 교반한 다음, 과량의 용매를 제거하였다. ~pH 5가 달성될 때까지 아세트산을 첨가하고, 혼합물을 디클로로메탄 (10 mL)으로 추출하였다. 유기 층을 수집하고, MgSO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 생성물을 헥산: DCM의 5:1 혼합물로 연화처리하여 (±)-2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸-8-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (12.3 mg, 0.02 mmol, 81% 수율)을 백색 고체로서 수득하였다.
MS (ESI) m/z: 590.0 [M+H]+;
1H NMR (400MHz, CDCl3) δ 8.04 (s, 1H), 7.67 (d, J=11.0 Hz, 1H), 7.39-7.31 (m, 2H), 7.30-7.22 (m, 1H), 5.93 (s, 1H), 3.92 (d, J=11.4 Hz, 1H), 3.79 (br. s., 1H), 3.57 (d, J=8.1 Hz, 1H), 3.46 (d, J=8.1 Hz, 2H), 3.19 (t, J=11.4 Hz, 1H), 2.22-2.09 (m, 1H), 1.83 (d, J=13.0 Hz, 1H), 1.59 (td, J=12.6, 4.5 Hz, 1H), 1.53-1.41 (m, 1H), 1.31-1.20 (m, 2H), 1.15-0.95 (m, 3H); FXR EC50 = 230 nM.
실시예 40
에틸 2-((1R,3S,5S)-2'-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-8-아자스피로[비시클로[3.2.1]옥탄-3,4'-[1,3]디옥솔란]-8-일)-4-플루오로벤조[d]티아졸-6-카르복실레이트
표제 화합물을, tert-부틸 4-히드록시-4-(히드록시메틸) 피페리딘-1-카르복실레이트를 tert-부틸 (1R,3S,5S)-3-히드록시-3-(히드록시메틸)-8-아자비시클로[3.2.1]옥탄-8-카르복실레이트로 대체하여, 실시예 38의 제조에 대하여 일반적 방법 C에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 644.1 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.13 (d, J=1.54 Hz, 1H), 7.76 (dd, J=1.54, 11.22 Hz, 1H), 7.37-7.45 (m, 2H), 7.29-7.35 (m, 1H), 5.87 (s, 1H), 4.41 (q, J=7.04 Hz, 4H), 3.98 (d, J=7.70 Hz, 1H), 3.54 (d, J=7.70 Hz, 1H), 2.12-2.39 (m, 5H), 2.07 (br d, J=13.20 Hz, 1H), 1.78 (br t, J=9.35 Hz, 1H), 1.37-1.49 (m, 4H), 1.22-1.32 (m, 2H), 1.12 (dd, J=1.76, 8.36 Hz, 2H); FXR EC50 = 3400 nM.
실시예 41
2-((1R,5S)-2'-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-8-아자스피로[비시클로[3.2.1]옥탄-3,4'-[1,3]디옥솔란]-8-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을 tert-부틸 4-히드록시-4-(히드록시메틸) 피페리딘-1-카르복실레이트를, tert-부틸 (1R,3S,5S)-3-히드록시-3-(히드록시메틸)-8-아자비시클로[3.2.1]옥탄-8-카르복실레이트로 대체하여, 실시예 39의 제조에 대하여 일반적 방법 C에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 616.6 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.19 (s, 1H), 7.80 (br d, J=11.00 Hz, 1H), 7.37-7.47 (m, 2H), 7.30-7.36 (m, 1H), 5.71-6.01 (m, 1H), 4.29-4.64 (m, 2H), 3.98 (d, J=7.70 Hz, 1H), 3.78 (s, 1H), 3.54 (d, J=7.70 Hz, 2H), 1.99-2.39 (m, 7H), 1.88 (s, 1H), 1.78 (s, 1H), 1.58-1.68 (m, 1H), 1.41-1.52 (m, 1H), 1.20-1.35 (m, 3H), 1.12 (dd, J=1.65, 8.47 Hz, 2H), 0.82-1.04 (m, 2H); FXR EC50 = 1700 nM.
실시예 42
2-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸-8-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메톡시) 벤즈알데히드로 대체하여, 실시예 39의 제조에 대하여 일반적 방법 C에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 606.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.11 (s, 1H), 7.70-7.62 (m, 1H), 7.59-7.48 (m, 4H), 5.94 (s, 1H), 3.84-3.67 (m, 1H), 3.64-3.37 (m, 1H), 3.24-3.15 (m, 1H), 2.94-2.89 (m, 1H), 2.46-2.39 (m, 1H), 1.90 (s, 1H), 1.85 (br d, J=13.1 Hz, 1H), 1.75-1.64 (m, 1H), 1.64-1.53 (m, 1H), 1.22-1.05 (m, 7H); FXR EC50 = 1000 nM.
실시예 43
6-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸-8-일)니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-플루오로니코티네이트로 대체하여, 실시예 42의 제조에 대하여 일반적 방법 C에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 532.4 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.58 (s, 1H), 7.92-7.86 (m, 2H), 7.69-7.63 (m, 2H), 7.58-7.48 (m, 7H), 6.83 (d, J=9.2 Hz, 4H), 5.94 (s, 6H), 3.96 (br d, J=14.0 Hz, 1H), 3.93-3.83 (m, 1H), 3.67-3.50 (m, 1H), 3.41-3.29 (m, 1H), 3.17 (s, 1H), 3.16-3.08 (m, 1H), 2.48-2.41 (m, 1H), 1.75 (br d, J=13.1 Hz, 1H), 1.61-1.50 (m, 1H), 1.47-1.38 (m, 1H), 1.17 (br d, J=7.0 Hz, 2H), 1.14-1.07 (m, 2H); FXR EC50 = 5300 nM.
실시예 44
6-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-1,3-디옥사-8-아자스피로[4.5]데칸-8-일)피콜린산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-플루오로피콜리네이트로 대체하여, 실시예 42의 제조에 대하여 일반적 방법 C에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 532.4 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.72-7.63 (m, 1H), 7.63-7.43 (m, 5H), 7.21 (d, J=7.3 Hz, 1H), 6.96 (d, J=8.5 Hz, 1H), 5.93 (s, 1H), 3.90-3.72 (m, 2H), 3.64-3.44 (m, 2H), 3.33 (br t, J=9.9 Hz, 1H), 3.13 (br t, J=10.7 Hz, 1H), 1.74 (br d, J=13.4 Hz, 1H), 1.58 (br t, J=9.8 Hz, 1H), 1.50-1.39 (m, 1H), 1.17 (br d, J=7.0 Hz, 4H), 1.14-1.07 (m, 2H); FXR EC50 = 5000 nM.
실시예 45
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메틸벤조[d]티아졸-6-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-클로로-4-메틸벤조[d]티아졸-6-카르복실레이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 566.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.14 (br s, 1H), 7.67 (br d, J=1.2 Hz, 2H), 7.66 (s, 1H), 7.62-7.57 (m, 1H), 5.88 (s, 1H), 3.71 (br d, J=11.9 Hz, 1H), 3.59-3.41 (m, 1H), 2.45 (s, 3H), 2.39-2.29 (m, 3H), 1.91 (s, 1H), 1.72-1.55 (m, 4H), 1.30-1.18 (m, 4H), 1.16-1.10 (m, 2H); FXR EC50 = 11 nM.
실시예 46
2-(2-(3-(3-클로로피리딘-2-일)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 3-클로로피콜린알데히드로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 537.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.69 (d, J=4.6 Hz, 1H), 8.20 (s, 1H), 8.15 (d, J=8.2 Hz, 1H), 7.64 (dd, J=8.2, 4.6 Hz, 1H), 7.59 (d, J=11.6 Hz, 1H), 5.91 (s, 1H), 3.82-3.64 (m, 1H), 3.56-3.40 (m, 1H), 2.37 (s, 2H), 2.35-2.27 (m, 1H), 1.74-1.56 (m, 4H), 1.28-1.17 (m, 2H), 1.17-1.09 (m, 2H); FXR EC50 = 200 nM.
실시예 47
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 3,5-디클로로이소니코틴알데히드로 대체하여, 실시예 1에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 571.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.86 (s, 2H), 8.17 (s, 1H), 7.58 (br d, J=11.4 Hz, 1H), 6.02 (s, 1H), 3.73 (br d, J=13.8 Hz, 2H), 3.66-3.44 (m, 2H), 2.42 (s, 2H), 2.40-2.28 (m, 1H), 1.69 (br s, 4H), 1.32-1.20 (m, 4H), 1.19-1.10 (m, 2H); FXR EC50 = 25 nM.
실시예 48
2-(2-(5-시클로프로필-3-(2,6-디클로로-4-플루오로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2,6-디클로로-4-플루오로벤즈알데히드로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 588.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.22 (s, 1H), 7.78 (d, J=8.5 Hz, 2H), 7.60 (br d, J=11.3 Hz, 1H), 5.96 (s, 1H), 3.74 (br s, 1H), 3.55 (br d, J=8.2 Hz, 1H), 3.33-3.14 (m, 1H), 3.04-2.95 (m, 1H), 2.41 (s, 2H), 2.39-2.29 (m, 1H), 1.68 (br s, 4H), 1.23 (br d, J=7.9 Hz, 2H), 1.16 (br d, J=2.4 Hz, 2H); FXR EC50 = 115 nM.
실시예 49
2-(2-(3-(2,6-디클로로페닐)-5-이소프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 시클로프로필아세틸렌을 이소프로필아세틸렌으로 대체하여, 실시예 1에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 572.1 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.13 (s, 1H), 7.75 (d, J=11.1 Hz, 1H), 7.46-7.39 (m, 2H), 7.39-7.32 (m, 1H), 5.78 (s, 1H), 3.83-3.71 (m, 2H), 3.57 (ddd, J=13.0, 7.9, 4.7 Hz, 2H), 3.40-3.29 (m, 1H), 2.63 (s, 1H), 2.36 (s, 2H), 1.84-1.71 (m, 4H), 1.45 (d, J=6.9 Hz, 6H); FXR EC50 = 57 nM.
실시예 50
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메톡시)벤조[d]티아졸-6-카르복실산
단계 1. 메틸 2-아미노-4-(트리플루오로메톡시)벤조[d]티아졸-6-카르복실레이트
아세트산 (2.8 mL) 중에 용해시킨 브로민 (0.22 mL, 4.2 mmol)을 아세트산 (5.7 mL) 중 메틸 4-아미노-3-(트리플루오로메톡시)벤조에이트 (1.0 g, 4.2 mmol) 및 티오시안산나트륨 (1.4 g, 17.0 mmol)의 0℃ 용액에 첨가하였다. 반응 혼합물을 실온이 되도록 하고, 밤새 교반하였다. 브로민 (0.22 mL, 4.2 mmol)을 더 첨가하고, 반응 혼합물을 50℃로 가열하였다. 주말에 걸쳐 가열한 후, 반응 혼합물을 EtOAc와 물 사이에 분배하였다. 유기 층을 수집하고, Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 24 g 칼럼)에 의해 정제하여 메틸 2-아미노-4-(트리플루오로메톡시)벤조[d]티아졸-6-카르복실레이트 (0.21 g, 0.72 mmol, 17% 수율)을 황색 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.27 (d, J=1.5 Hz, 1H), 7.94 (t, J=1.5 Hz, 1H), 5.85 (br s, 2H), 3.96 (s, 3H).
단계 2. 메틸 2-브로모-4-(트리플루오로메톡시)벤조[d]티아졸-6-카르복실레이트
tert-부틸 니트라이트 (0.11 mL, 0.86 mmol)를 아세토니트릴 (3.6 mL) 중 브로민화구리 (II) (0.18 g, 0.79 mmol)의 급속하게 교반하는 현탁액에 첨가하였다. 5분 후, 생성된 암갈색 혼합물을 아세토니트릴 (0.5 mL) 중에 현탁된 메틸 2-아미노-4-(트리플루오로메톡시)벤조[d]티아졸-6-카르복실레이트 (0.21 g, 0.72 mmol)가 들은 플라스크에 첨가하였다. 반응 혼합물을 실온에서 2.5시간 동안 교반한 다음, EtOAc로 희석하고, SiO2을 첨가하였다. 혼합물을 농축시켜 자유-유동 고체를 수득하였으며, 이를 SiO2 상 플래쉬 크로마토그래피 (0-40% EtOAc/헥산, 이스코 24 g 칼럼)에 의해 정제하여 메틸 2-브로모-4-(트리플루오로메톡시) 벤조[d]티아졸-6-카르복실레이트 (0.13 g, 0.37 mmol, 51% 수율)을 백색 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.50 (d, J=1.5 Hz, 1H), 8.06 (quin, J=1.4 Hz, 1H), 4.01 (s, 3H); 19F NMR (377 MHz, CDCl3) δ -57.69 (s).
실시예 50. 2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메톡시)벤조[d]티아졸-6-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-브로모-4-(트리플루오로메톡시)벤조[d]티아졸-6-카르복실레이트로 대체하여, 실시예 47의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 637.2 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.62 (s, 2H), 8.24 (s, 1H), 7.90 (s, 1H), 5.83 (s, 1H), 3.83-3.74 (m, 2H), 3.62-3.51 (m, 2H), 2.43 (s, 2H), 2.22-2.11 (m, 1H), 1.83-1.69 (m, 5H), 1.30 (br d, J=4.6 Hz, 2H), 1.18 (br d, J=7.6 Hz, 2H); FXR EC50 = 11 nM.
실시예 51
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-5-메톡시벤조[d]티아졸-6-카르복실산
단계 1. 에틸 2-브로모-5-메톡시벤조[d]티아졸-6-카르복실레이트
표제 화합물을, 메틸 4-아미노-3-(트리플루오로메톡시)벤조에이트를 에틸 2-아미노-4-메톡시벤조에이트로 대체하여, 메틸 2-브로모-4-(트리플루오로메톡시)벤조[d]티아졸-6-카르복실레이트의 제조에 대하여 실시예 50에 기재된 2-단계 절차에 의해 제조할 수 있었다.
1H NMR (500 MHz, CDCl3) δ 8.23 (s, 1H), 7.55 (s, 1H), 4.40 (q, J=7.2 Hz, 2H), 3.98 (s, 3H), 1.41 (t, J=7.0 Hz, 3H).
실시예 51. 2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-5-메톡시벤조[d]티아졸-6-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 에틸 2-브로모-5-메톡시벤조[d]티아졸-6-카르복실레이트로 대체하여, 실시예 47의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 583.1 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.62 (s, 2H), 8.36 (s, 1H), 7.13 (s, 1H), 5.83 (s, 1H), 4.07 (s, 3H), 3.81-3.68 (m, 3H), 3.60-3.47 (m, 2H), 2.59 (s, 2H), 2.43 (s, 2H), 2.20-2.09 (m, 1H), 1.85-1.67 (m, 4H), 1.30 (br d, J=4.6 Hz, 2H), 1.18 (br d, J=7.7 Hz, 2H); FXR EC50 = 72 nM.
실시예 52
2-(2-(3-(3,5-디클로로피리딘-4-일)-5-이소프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 시클로프로필아세틸렌을 이소프로필아세틸렌으로 대체하여, 실시예 47의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 573.3 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.65 (s, 2H), 8.13 (s, 1H), 7.75 (br d, J=11.0 Hz, 1H), 5.83 (s, 1H), 3.84-3.75 (m, 2H), 3.66-3.50 (m, 2H), 3.36 (dquin, J=13.8, 6.9 Hz, 1H), 2.39 (s, 2H), 1.88-1.69 (m, 4H), 1.46 (br d, J=6.9 Hz, 6H); FXR EC50 = 58 nM.
실시예 53
7-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)신놀린-3-카르복실산
표제 화합물을, 에틸 7-클로로신놀린-3-카르복실레이트를 HCl을 포함하는 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 547.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.54 (br s, 1H), 8.02 (br d, J=9.16 Hz, 1H), 7.83 (br d, J=8.85 Hz, 1H), 7.67-7.75 (m, 2H), 7.59-7.66 (m, 2H), 5.91 (s, 1H), 3.69 (br s, 2H), 3.32-3.46 (m, 1H), 3.21 (s, 1H), 2.40 (m, 3H), 1.61-1.83 (m, 4H), 1.14-1.36 (m, 4H); FXR EC50 = 46 nM.
실시예 54
7-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)신놀린-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 53의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 547.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.52 (s, 1H), 7.99 (d, J=9.16 Hz, 1H), 7.94 (br d, J=7.63 Hz, 1H), 7.81 (br dd, J=7.63, 14.04 Hz, 3H), 7.59 (br d, J=6.41 Hz, 2H), 5.72-5.87 (m, 1H), 3.66 (br d, J=13.73 Hz, 2H), 3.33 (br t, J=8.39 Hz, 1H), 3.17 (dd, J=5.49, 10.38 Hz, 1H), 2.33 (m, 3H), 1.65 (br dd, J=3.36, 12.51 Hz, 4H), 1.08-1.30 (m, 4H); FXR EC50 = 177 nM.
실시예 55
7-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)신놀린-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 3,5-디클로로이소니코틴알데히드로 대체하여, 실시예 53의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 548.0 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.92 (s, 1H), 8.74 (s, 2H), 8.14 (d, J=9.63 Hz, 1H), 7.90-8.07 (m, 1H), 7.15-7.32 (m, 1H), 5.94 (s, 1H), 3.96 (br d, J=13.75 Hz, 2H), 3.53-3.76 (m, 2H), 2.56 (s, 2H), 2.36 (s, 1H), 1.84 (br t, J=4.13 Hz, 4H), 1.19-1.47 (m, 4H); FXR EC50 = 191 nM.
실시예 56
7-(2-(3-(2-클로로-6-플루오로페닐)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)신놀린-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-클로로-6-플루오로벤즈알데히드로 대체하여, 실시예 53의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 531.0 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.54 (s, 1H), 8.01 (d, J = 9.2 Hz, 1H), 7.82 (d, J = 9.8 Hz, 1H), 7.70-7.53 (m, 3H), 7.45 (t, J = 8.7 Hz, 1H), 5.93 (s, 1H), 3.69 (br s, 2H), 2.42 (s, 2H), 2.35 (br s, 1H), 1.68 (br s, 4H), 1.27-1.08 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 194 nM.
실시예 57
7-(2-(3-(2-클로로-6-메틸페닐)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)신놀린-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-클로로-6-메틸벤즈알데히드로 대체하여, 실시예 53의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 527.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.54 (s, 1H), 8.00 (d, J = 9.2 Hz, 1H), 7.86-7.77 (m, 1H), 7.59 (s, 1H), 7.49-7.43 (m, 2H), 7.39-7.33 (m, 1H), 5.77 (s, 1H), 3.72-3.65 (m, 2H), 3.37-3.23 (m, 2H), 2.43-2.30 (m, 3H), 2.11 (s, 3H), 1.71-1.59 (m, 4H), 1.26-1.08 (m, 4H); FXR EC50 = 227 nM.
실시예 58
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(디플루오로메톡시)퀴놀린-2-카르복실산
단계 1. 메틸 6-브로모-4-(디플루오로메톡시)퀴놀린-2-카르복실레이트
0℃에서 DMF (5 mL) 중 Cs2CO3 (0.98 g, 3.0 mmol)의 교반하는 현탁액에 메틸 6-브로모-4-히드록시퀴놀린-2-카르복실레이트 (0.28 g, 1.0 mmol) 및 소듐 클로로디플루오로아세테이트 (0.46 g, 3.0 mmol)를 첨가하였다. 반응 혼합물을 가열하면서 80℃에서 30분 동안 교반하였다. 반응 혼합물을 실온으로 냉각시킨 후, 물 (25 mL)을 첨가하고, 생성된 현탁액을 1시간 동안 교반하였다. 고체를 흡인 여과에 의해 수집하고, 물 (2 x 5 mL)로 세척하였다. 밤새 진공 하에 건조시킨 후, 메틸 6-브로모-4-(디플루오로메톡시)퀴놀린-2-카르복실레이트 (0.28 g, 0.81 mmol, 81% 수율)을 백색 고체로서 수득하였다.
MS (ESI) m/z: 333.9 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.38 (d, J=2.20 Hz, 1H), 8.16 (d, J=9.02 Hz, 1H), 7.91 (dd, J=2.20, 9.24 Hz, 1H), 7.85 (t, J=1.10 Hz, 1H), 6.61-7.17 (m, 1H), 4.09 (s, 3H).
실시예 58. 6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(디플루오로메톡시)퀴놀린-2-카르복실산
표제 화합물을, 에틸 7-클로로신놀린-3-카르복실레이트, HCl를 메틸 6-브로모-4-(디플루오로메톡시)퀴놀린-2-카르복실레이트로 대체하여, 실시예 54의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 612.1 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 7.95 (br d, J=9.24 Hz, 1H), 7.77-7.84 (m, 1H), 7.74 (s, 1H), 7.54-7.68 (m, 3H), 7.43 (br d, J=6.60 Hz, 1H), 7.25 (br d, J=2.20 Hz, 1H), 6.69-7.12 (m, 1H), 5.64 (s, 1H), 3.45-3.63 (m, 2H), 3.27 (ddd, J=4.18, 8.14, 12.54 Hz, 2H), 2.37 (s, 2H), 2.15 (ddd, J=3.30, 5.01, 8.42 Hz, 1H), 1.65-1.86 (m, 4H), 1.10-1.33 (m, 4H); FXR EC50 = 2.3 nM.
실시예 59
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메톡시벤조[d]티아졸-6-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-브로모-4-메톡시벤조[d]티아졸-6-카르복실레이트로 대체하여, 실시예 47의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 583.1 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.74 (s, 2H), 7.99 (d, J=1.54 Hz, 1H), 7.55 (d, J=1.32 Hz, 1H), 5.90-6.01 (m, 1H), 4.01 (s, 3H), 3.72-3.88 (m, 2H), 3.59 (s, 2H), 2.51 (s, 2H), 2.25-2.40 (m, 1H), 1.78 (br d, J=4.18 Hz, 4H), 1.12-1.37 (m, 4H); FXR EC50 = 4.1 nM.
실시예 60
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-7-(트리플루오로메틸)퀴놀린-5-카르복실산
단계 1. 에틸 7-(트리플루오로메틸)퀴놀린-5-카르복실레이트
75% H2SO4 (5.9 mL) 중 3-아미노-5-(트리플루오로메틸)벤조산 (0.51g, 2.5 mmol), 글리세롤 (0.36 mL, 5.0 mmol), 및 3-니트로벤젠술폰산 나트륨 염 (1.679 g, 7.46 mmol)의 용액을 100℃로 1.5시간 동안 가열한 다음, 140℃로 1시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시킨 다음, EtOH (10 mL)를 첨가하고, 반응 혼합물을 85℃로 밤새 가열하였다. 반응 혼합물을 실온으로 냉각시키고, 3.3g NaOH를 갖는 빙수 40 mL에 부었다. 1M K2HPO4을 용액이 pH~7에 도달할 때까지 첨가하였다. 용액을 EtOAc로 추출하였다. 유기 층을 염수로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 24g 칼럼)에 의해 정제하여 에틸 7-(트리플루오로메틸) 퀴놀린-5-카르복실레이트 및 에틸 5-(트리플루오로메틸)퀴놀린-7-카르복실레이트 (0.34 g, 1.3 mmol, 51% 수율)의 혼합물을 베이지색 고체로서 수득하였다.
MS (ESI) m/z: 270.0 [M+H]+.
단계 2. 5-(에톡시카르보닐)-7-(트리플루오로메틸)퀴놀린 1-옥시드
m-클로로퍼옥시벤조산 (0.2 g, 0.87 mmol)을 디클로로메탄 (5.1 mL) 중 에틸 7-(트리플루오로메틸)퀴놀린-5-카르복실레이트 (0.18 g, 0.67 mmol)의 용액에 조금씩 첨가하였다. 반응물을 실온에서 밤새 교반하였다. 용매 부피를 ~25% 감소시키고, 조 반응 혼합물을 SiO2 칼럼 상에 직접 로딩하고, SiO2 상 플래쉬 크로마토그래피 (0-10% MeOH/DCM, 이스코 24 g 칼럼)에 의해 정제하여 5-(에톡시카르보닐)-7-(트리플루오로메틸)퀴놀린 1-옥시드 (0.20 g, 0.68 mmol, 100% 수율)을 황색 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 9.36 (s, 1H), 8.97 (d, J=9.0 Hz, 1H), 8.64 (d, J=5.5 Hz, 1H), 8.53 (d, J=2.0 Hz, 1H), 7.53 (dd, J=9.1, 6.1 Hz, 1H), 4.53 (q, J=7.3 Hz, 2H), 1.50 (t, J=7.2 Hz, 3H); 19F NMR (377 MHz, CDCl3) δ -62.91 (s).
단계 3. 에틸 2-클로로-7-(트리플루오로메틸)퀴놀린-5-카르복실레이트
옥시염화인 (0.039 mL, 0.42 mmol)에 이어서 DMF (0.014 mL, 0.18 mmol)를 디클로로메탄 (3.5 mL) 중 5-(에톡시카르보닐)-7-(트리플루오로메틸) 퀴놀린 1-옥시드 (0.1 g, 0.35 mmol)의 0℃ 용액에 첨가하였다. 5분 후, 반응 혼합물을 실온으로 만들었다. 실온에서 30시간 동안 교반한 후, 조 반응 혼합물을 SiO2 상 플래쉬 크로마토그래피 (0-70% EtOAc/hex, 이스코 12 g 칼럼, 약 20% EtOAc에서 용리된 생성물)에 의해 정제하여 에틸 2-클로로-7-(트리플루오로메틸)퀴놀린-5-카르복실레이트 및 에틸 2-클로로-5-(트리플루오로메틸)퀴놀린-7-카르복실레이트의 혼합물을 백색 고체로서 수득하였다. 혼합물을 후속 단계에 사용하였다.
실시예 60. 2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-7-(트리플루오로메틸)퀴놀린-5-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 에틸 2-클로로-7-(트리플루오로메틸)퀴놀린-5-카르복실레이트로 대체하여, 실시예 47의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 615.1 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 9.06 (br d, J=9.2 Hz, 1H), 8.64 (s, 2H), 8.18 (br s, 1H), 8.15 (br s, 1H), 7.15 (br d, J=9.6 Hz, 1H), 5.86 (s, 1H), 4.07-3.83 (m, 2H), 3.66-3.49 (m, 2H), 2.45 (s, 2H), 2.30-2.12 (m, 1H), 1.73 (br s, 4H), 1.38-1.26 (m, 2H), 1.20 (br d, J=7.9 Hz, 2H); FXR EC50 = 7.2 nM.
실시예 61
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메틸벤조[d]티아졸-6-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-브로모-4-메틸벤조[d]티아졸-6-카르복실레이트로 대체하여, 실시예 47의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 566.9 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.64 (s, 2H), 8.09 (d, J=1.10 Hz, 1H), 7.74 (d, J=0.66 Hz, 1H), 7.67 (s, 1H), 5.67-6.00 (m, 1H), 3.76 (s, 2H), 3.54 (br d, J=8.36 Hz, 2H), 2.49 (s, 3H), 2.45 (s, 2H), 2.25 (s, 1H), 2.00 (s, 1H), 1.64-1.89 (m, 4H), 1.05-1.44 (m, 5H); FXR EC50 = 7.2 nM.
실시예 62
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)티아졸로[5,4-b]피리딘-5-카르복실산
단계 1. 4-(7-(5-클로로티아졸로[5,4-b]피리딘-2-일)-7-아자스피로[3.5]논-1-엔-2-일)-5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸
DMA 중 5-시클로프로필-3-(3,5-디클로로피리딘-4-일)-4-(7-아자스피로[3.5]논-1-엔-2-일)이속사졸 (150 mg, 0.40 mmol), 2-브로모-5-클로로티아졸로[5,4-b]피리딘 (119 mg, 0.48 mmol), 및 탄산세슘 (325 mg, 1.0 mmol)의 현탁액 (1.2 mL)을 50℃에서 3시간 동안 가열하였다. 조 반응 혼합물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 40 g 칼럼)에 의해 직접 정제하여 4-(7-(5-클로로티아졸로[5,4-b]피리딘-2-일)-7-아자스피로[3.5]논-1-엔-2-일)-5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸 (166 mg, 0.29 mmol, 73% 수율)을 검으로서 수득하였다.
MS (ESI) m/z: 543.9 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.63 (s, 2H), 7.60 (d, J=8.36 Hz, 1H), 7.19 (d, J=8.36 Hz, 1H), 5.81 (s, 1H), 3.73 (td, J=5.06, 13.42 Hz, 2H), 3.49 (ddd, J=4.62, 8.03, 13.09 Hz, 2H), 2.44 (s, 2H), 2.10-2.25 (m, 1H), 1.70-1.81 (m, 4H), 1.13-1.36 (m, 4H).
단계 2. 메틸 2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)티아졸로[5,4-b]피리딘-5-카르복실레이트
DMF 중 4-(7-(5-클로로티아졸로[5,4-b]피리딘-2-일)-7-아자스피로[3.5]논-1-엔-2-일)-5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸 (100 mg, 0.18 mmol), 메탄올 (5 mL, 0.18 mmol), 1,3-비스(디페닐포스파닐)프로판 (9.1 mg, 0.022 mmol), 아세트산팔라듐 (II) (4.9 mg, 0.022 mmol), 및 탄산칼륨 (40.6 mg, 0.29 mmol)의 혼합물 (2.5 mL)을 압력 병에서 CO (48 psi) 하에 85℃에서 1일 동안 가열하였다. 혼합물을 에틸 아세테이트 (10 mL)로 희석하고, 셀라이트를 통해 여과하였다. 여과물을 진공 하에 농축 건조시켰다. 잔류물을 에틸 아세테이트 (20 mL) 중에 용해시키고, 물 (10 mL)로 세척하였다. 유기 층을 무수 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축 건조시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 40 g 칼럼)에 의해 정제하여 메틸 2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)티아졸로[5,4-b]피리딘-5-카르복실레이트를 대략 85% 순도로 수득하였다. 물질을 후속 단계에 추가의 정제 없이 사용하였다.
MS (ESI) m/z: 568.0 [M+H]+.
실시예 62. 2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)티아졸로[5,4-b]피리딘-5-카르복실산
1:1 메탄올/THF (0.35 mL) 중 메틸 2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)티아졸로[5,4-b]피리딘-5-카르복실레이트 (20 mg, 0.04 mmol)의 용액에 1N NaOH (0.11 mL, 0.11 mmol)를 첨가하였다. 반응 혼합물을 60℃로 15분 동안 가열하였다. 조 반응 혼합물을 TFA를 사용하여 산성화시키고, C-18 역상 플래쉬 크로마토그래피 (A 중 10-100% B, A = 10:90:0.1 MeCN:H2O:TFA, B = 90:10:0.1 MeCN:H2O:TFA, 18분 선형 구배, 이스코 12 g C-18 골드 칼럼)에 의해 직접 정제하여 2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)티아졸로[5,4-b]피리딘-5-카르복실산 (11 mg, 0.019 mmol, 54% 수율)을 적색 고체로서 수득하였다.
MS (ESI) m/z: 554.0 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.67 (s, 2H), 8.17 (d, J=8.36 Hz, 1H), 7.83 (s, 1H), 5.74-5.95 (m, 1H), 3.75-3.98 (m, 2H), 3.48-3.69 (m, 2H), 2.48 (s, 2H), 2.11-2.26 (m, 1H), 1.82 (br t, J=4.95 Hz, 4H), 1.14-1.51 (m, 4H); FXR EC50 = 24 nM.
실시예 63
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 벤조[d]티아졸-6-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 에틸 2-클로로벤조[d]티아졸-6-카르복실레이트로 대체하여, 실시예 47의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 552.9 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.67 (s, 2H), 8.31 (d, J=1.54 Hz, 1H), 7.99 (dd, J=1.76, 8.58 Hz, 1H), 7.69 (s, 1H), 7.46 (d, J=8.58 Hz, 1H), 5.76-5.99 (m, 1H), 3.79 (br d, J=13.64 Hz, 2H), 3.48-3.68 (m, 2H), 2.50 (s, 2H), 2.15-2.34 (m, 1H), 2.04 (s, 1H), 1.70-1.89 (m, 4H), 1.16-1.40 (m, 4H); FXR EC50 = 62 nM.
실시예 64
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-8-메톡시퀴놀린-5-카르복실산
단계 1. 메틸 8-메톡시퀴놀린-5-카르복실레이트
75% H2SO4 (47.0 mL) 중 3-아미노-4-메톡시벤조산 (3.3 g, 19.7 mmol), 글리세롤 (2.9 mL, 39.5 mmol), 및 3-니트로벤젠술폰산 나트륨 염 (13.3 g, 59.2 mmol)의 용액을 100℃로 2시간 동안, 이어서 140℃로 1시간 동안 가열하였다. 반응 혼합물을 실온으로 냉각시킨 다음, MeOH (40 mL)를 첨가하고, 반응 혼합물을 60℃로 밤새 가열하였다. 반응 혼합물을 실온으로 냉각시키고, 빙수에 붓고, 12 M NH4OH을 사용하여 염기성화시켰다. 생성된 혼합물을 EtOAc로 추출하였다. 층을 분리하고, 수성 층을 추가로 EtOAc (2x)로 추출하였다. 합한 유기 층을 염수로 세척하고, MgSO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 생성물을 SiO2 상에 건조 로딩하고, SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산)에 의해 정제하여 메틸 8-메톡시퀴놀린-5-카르복실레이트 (2.2 g, 9.9 mmol, 50% 수율)을 백색 고체로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 9.50 (dd, J=8.8, 1.7 Hz, 1H), 9.00 (dd, J=3.9, 1.7 Hz, 1H), 8.37 (d, J=8.3 Hz, 1H), 7.59 (dd, J=8.8, 4.1 Hz, 1H), 7.08 (d, J=8.3 Hz, 1H), 4.19 (s, 3H), 4.00 (s, 3H).
단계 2. 8-메톡시-5-(메톡시카르보닐)퀴놀린 1-옥시드
m-클로로퍼옥시벤조산 (0.97 g, 4.3 mmol)을 디클로로메탄 (25.5 mL) 중 메틸 8-메톡시퀴놀린-5-카르복실레이트 (0.72 g, 3.3 mmol)의 용액에 조금씩 첨가하였다. 반응물을 실온에서 밤새 교반하였다. 용매 부피를 ~25% 감소시키고, 조 반응 혼합물을 SiO2 칼럼 상에 직접 로딩하고, SiO2 상 플래쉬 크로마토그래피 (0-10% MeOH/DCM, 이스코 40 g 칼럼)에 의해 정제하여 8-메톡시-5-(메톡시카르보닐)퀴놀린 1-옥시드 (0.6 g, 2.6 mmol, 78% 수율)을 황색 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 9.02 (dd, J=8.9, 1.0 Hz, 1H), 8.47 (dd, J=6.2, 1.1 Hz, 1H), 8.31 (d, J=8.8 Hz, 1H), 7.34 (dd, J=8.9, 6.1 Hz, 1H), 7.07 (d, J=8.8 Hz, 1H), 4.11 (s, 3H), 3.99 (s, 3H).
단계 3. 메틸 2-클로로-8-메톡시퀴놀린-5-카르복실레이트
옥시염화인 (0.29 mL, 3.1 mmol)에 이어서 DMF (0.10 mL, 1.3 mmol)를 디클로로메탄 (26 mL) 중 8-메톡시-5-(메톡시카르보닐)퀴놀린 1-옥시드 (0.6 g, 2.6 mmol)의 0℃ 용액에 첨가하였다. 5분 후, 반응 혼합물을 실온으로 만들었다. 24시간 후, 조 반응 혼합물을 SiO2 상 플래쉬 크로마토그래피 (0-85% EtOAc/헥산에 이어서 0-10% DCM/MeOH, 이스코 40 g 칼럼)에 의해 정제하여 메틸 2-클로로-8-메톡시퀴놀린-5-카르복실레이트 (0.58 g, 2.3 mmol, 90% 수율)을 백색 고체로서 수득하였다.
1H NMR (400 MHz, DMSO-d6) δ 9.35 (d, J=9.0 Hz, 1H), 8.34 (d, J=8.4 Hz, 1H), 7.78 (d, J=9.0 Hz, 1H), 7.38 (d, J=8.6 Hz, 1H), 4.07 (s, 3H), 3.92 (s, 3H).
실시예 64. 2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-8-메톡시퀴놀린-5-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-클로로-8-메톡시퀴놀린-5-카르복실레이트로 대체하여, 실시예 47의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 577.0 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 9.16 (br d, J=9.6 Hz, 1H), 8.61 (s, 2H), 8.08 (br d, J=8.3 Hz, 1H), 7.09 (br d, J=9.5 Hz, 1H), 6.92 (br d, J=8.2 Hz, 1H), 5.85 (s, 1H), 4.06 (s, 3H), 4.02-3.83 (m, 2H), 3.71 (s, 1H), 3.62-3.47 (m, 2H), 2.41 (s, 2H), 2.26-2.11 (m, 1H), 1.73 (br s, 4H), 1.29 (br d, J=4.6 Hz, 2H), 1.17 (br d, J=7.9 Hz, 2H); FXR EC50 = 49 nM.
실시예 65
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴놀린-5-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-클로로퀴놀린-5-카르복실레이트로 대체하여, 실시예 47의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 547.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.92-8.86 (m, 1H), 8.85 (s, 2H), 7.79 (br d, J=7.0 Hz, 1H), 7.73 (br d, J=7.9 Hz, 1H), 7.57 (br t, J=7.8 Hz, 1H), 7.31 (br d, J=9.5 Hz, 1H), 5.98 (s, 1H), 3.98-3.85 (m, 2H), 3.48 (br d, J=7.3 Hz, 1H), 2.39 (br s, 3H), 1.59 (br s, 4H), 1.33-1.19 (m, 3H), 1.16 (br s, 2H); FXR EC50 = 65 nM.
실시예 66
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-플루오로니코티네이트로 대체하여, 실시예 47의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 497.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.88 (s, 2H), 8.60 (d, J=1.8 Hz, 1H), 7.89 (dd, J=9.2, 2.1 Hz, 1H), 6.84 (d, J=9.2 Hz, 1H), 5.98 (s, 1H), 3.93-3.74 (m, 2H), 2.44-2.30 (m, 3H), 1.56 (br s, 4H), 1.32-1.20 (m, 4H), 1.17 (br d, J=2.7 Hz, 2H); FXR EC50 = 342 nM.
실시예 67
6-(2-(5-시클로프로필-3-(2,6-디클로로-4-플루오로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)니코틴산
표제 화합물을, 3,5-디클로로이소니코틴알데히드를 2,6-디클로로-4-플루오로벤즈알데히드로 대체하여, 실시예 66의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 514.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 1H NMR; FXR EC50 = 493 nM 중 8.61 (s, 1H), 7.91 (br d, J=8.9 Hz, 1H), 7.78 (br d, J=8.2 Hz, 2H), 6.85 (br d, J=9.2 Hz, 1H), 5.94 (s, 1H), 3.95-3.80 (m, 2H), 2.44-2.29 (m, 3H), 1.94 (s, 2H), 1.57 (br s, 4H), 1.29-1.18 (m, 2H), 1.17 (br s, 2H) 물 억제로 인해 추가의 신호 소실.
실시예 68
2-(2-(5-시클로프로필-3-(3,5-디플루오로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 3,5-디플루오로이소니코틴알데히드로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 539.0 [M+H]+;
1H NMR (400 MHz, DMSO-d6) δ 8.81 (s, 2H), 8.21 (d, J = 1.5 Hz, 1H), 7.59 (dd, J = 1.5, 11.5 Hz, 1H), 6.15 (s, 1H), 3.88-3.40 (m, 4H), 2.51 (s, 2H), 2.40-2.28 (m, 1H), 1.70 (dd, J = 4.7, 7.0 Hz, 4H), 1.30-1.06 (m, 4H); FXR EC50 = 442 nM.
실시예 69
2-(2-(5-시클로프로필-3-(3-플루오로-5-메톡시피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 1개의 플루오린을 MeOH로 치환하여, 실시예 68의 제조 동안 추가의 단리물로서 수득하였다.
MS (ESI) m/z: 551.0 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.40 (s, 1H), 8.34 (s, 1H), 8.15 (d, J = 1.5 Hz, 1H), 7.66 (dd, J = 1.5, 11.6 Hz, 1H), 5.99 (s, 1H), 4.00 (s, 3H), 3.84 (dt, J = 4.9, 13.7 Hz, 2H), 3.61 (ddd, J = 4.2, 8.2, 13.0 Hz, 2H), 2.53 (s, 2H), 2.32 (tt, J = 5.4, 8.0 Hz, 1H), 1.79 (dt, J = 5.0, 10.2 Hz, 4H), 1.22 (ddd, J = 2.5, 6.3, 7.7 Hz, 4H); FXR EC50 = 730 nM.
실시예 70
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-6-메톡시벤조[d]티아졸-4-카르복실산
단계 1. 메틸 2-아미노-6-메톡시벤조[d]티아졸-4-카르복실레이트
메틸 2-아미노-5-메톡시벤조에이트 (190 mg, 1.0 mmol)를 아세토니트릴 (5.2 mL) 중에 용해시켰다. 티오시안산암모늄 (120 mg, 1.6 mmol)을 첨가한 후, 벤질트리메틸암모늄 트리브로마이드 (409 mg, 1.0 mmol)를 첨가하고, 3.5시간 후, 반응 혼합물을 EtOAc로 희석하고, 포화 NaHCO3에 이어서 염수로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 물질을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 17분 구배, 이스코 12 g 칼럼)에 의해 정제하여 메틸 2-아미노-6-메톡시벤조[d]티아졸-4-카르복실레이트 (100 mg, 0.42 mmol, 40% 수율)을 수득하였다.
1H NMR (400MHz, CDCl3) δ 7.51 (d, J=2.6 Hz, 1H), 7.35 (d, J=2.6 Hz, 1H), 5.89 (br. s., 2H), 3.99 (s, 3H), 3.88 (s, 3H).
단계 2. 메틸 2-브로모-6-메톡시벤조[d]티아졸-4-카르복실레이트
브로민화구리 (II) (159 mg, 0.71 mmol) 및 tert-부틸 니트라이트 (85 μL, 0.71 mmol)을 MeCN (1.7 mL) 중에 용해시키고, 10분 동안 교반되게 하였다. 메틸 2-아미노-6-메톡시벤조[d]티아졸-4-카르복실레이트 (100 mg, 0.42 mmol)를 MeCN (2.5 mL) 중에 용해시키고, 구리 용액을 첨가하였다. 2시간 후, 반응 혼합물을 EtOAc로 희석하고, 1 N HCl, 포화 NaHCO3에 이어서 염수로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 메틸 2-브로모-6-메톡시벤조[d]티아졸-4-카르복실레이트를 수득하였다. 생성물을 추가의 정제 없이 사용하였다.
1H NMR (400MHz, CDCl3) δ 7.68 (d, J=2.6 Hz, 1H), 7.46 (d, J=2.6 Hz, 1H), 4.05 (s, 3H), 3.93 (s, 3H).
실시예 70. 2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-6-메톡시벤조[d]티아졸-4-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 2-브로모-6-메톡시벤조[d]티아졸-4-카르복실산로 대체하여, 실시예 47의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 583.0 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.88 (s, 2H), 7.74 (d, J = 2.7 Hz, 1H), 7.39 (d, J = 2.7 Hz, 1H), 6.00 (s, 1H), 3.81 (s, 3H), 3.73-3.62 (m, 2H), 3.56-3.45 (m, 2H), 2.43 (s, 2H), 2.36 (td, J = 4.3, 8.5 Hz, 1H), 1.70 (br t, J = 6.2 Hz, 4H), 1.28-1.13 (m, 4H); FXR EC50 = 4400 nM.
실시예 71
2-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메톡시벤조[d]티아졸-6-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-브로모-4-메톡시벤조[d]티아졸-6-카르복실레이트로 대체하여, 실시예 29의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 582.2 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 7.98 (d, J=1.54 Hz, 1H), 7.86-7.93 (m, 1H), 7.75 (br d, J=1.98 Hz, 2H), 7.54 (d, J=1.54 Hz, 1H), 7.48-7.53 (m, 1H), 5.74 (s, 1H), 4.00 (s, 3H), 3.70-3.89 (m, 2H), 3.56 (br d, J=8.36 Hz, 2H), 2.43 (s, 2H), 2.30 (s, 1H), 1.62-1.83 (m, 4H), 1.11-1.30 (m, 4H); FXR EC50 = 9.4 nM.
실시예 72
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-에톡시퀴놀린-2-카르복실산
표제 화합물을, 에틸 7-클로로신놀린-3-카르복실레이트, HCl를 메틸 6-브로모-4-에톡시퀴놀린-2-카르복실레이트로 대체하여, 실시예 54의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 590.1 [M+H]+;
1H NMR (400 MHz, CDCl3-d) δ 8.57-8.80 (m, 1H), 7.71-7.88 (m, 3H), 7.56-7.68 (m, 2H), 7.42-7.48 (m, 1H), 7.38 (d, J=2.64 Hz, 1H), 5.64 (s, 1H), 4.58 (d, J=7.04 Hz, 2H), 3.47-3.70 (m, 2H), 3.33 (br dd, J=4.18, 9.02 Hz, 2H), 2.38 (s, 2H), 2.09-2.21 (m, 1H), 1.76 (br t, J=4.95 Hz, 4H), 1.67 (t, J=7.04 Hz, 3H), 1.28 (dd, J=2.53, 4.95 Hz, 2H), 1.15 (dd, J=2.64, 8.36 Hz, 2H); FXR EC50 = 10 nM.
실시예 73
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(디플루오로메톡시)퀴놀린-2-카르복실산
표제 화합물을, 2-(트리플루오로메틸)벤즈알데히드를 3,5-디클로로이소니코틴알데히드로 대체하여, 실시예 58의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 613.0 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.63 (s, 2H), 7.95 (d, J=9.24 Hz, 1H), 7.75 (s, 1H), 7.59 (dd, J=2.75, 9.57 Hz, 1H), 7.28 (d, J=2.64 Hz, 1H), 6.90 (s, 1H), 5.83 (s, 1H), 3.44-3.64 (m, 2H), 3.29 (br s, 2H), 2.44 (s, 2H), 2.19 (ddd, J=3.30, 5.01, 8.42 Hz, 1H), 1.68-1.93 (m, 5H), 1.31-1.37 (m, 2H), 1.18 (s, 2H); FXR EC50 = 16 nM.
실시예 74
6-(2-(3-(3-클로로피리딘-4-일)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(디플루오로메톡시)퀴놀린-2-카르복실산
표제 화합물을 실시예 73의 제조로부터 소량의 단리물로서 수득하였다.
MS (ESI) m/z: 579.1 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.78 (s, 1H), 8.65 (d, J=4.95 Hz, 1H), 8.19 (d, J=9.63 Hz, 1H), 7.95 (dd, J=2.48, 9.63 Hz, 1H), 7.91 (s, 1H), 7.51-7.59 (m, 2H), 7.36-7.46 (m, 1H), 5.97 (s, 1H), 3.65-3.75 (m, 2H), 3.44 (ddd, J=3.71, 8.60, 12.72 Hz, 2H), 2.55 (s, 2H), 2.29-2.37 (m, 1H), 1.77-1.89 (m, 4H), 1.17-1.27 (m, 4H); FXR EC50 = 38 nM.
실시예 75
6-(2-(5-시클로프로필-3-(4-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(디플루오로메톡시)퀴놀린-2-카르복실산
표제 화합물을, 2-(트리플루오로메틸)벤즈알데히드를 4-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 58의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 613.1 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.94-8.82 (m, 1H), 8.12-7.98 (m, 2H), 7.84-7.70 (m, 3H), 7.58-7.18 (m, 2H), 5.77 (s, 1H), 3.65-3.53 (m, 2H), 3.37-3.23 (m, 2H), 2.46 (s, 2H), 2.32 (tt, J = 5.5, 8.0 Hz, 1H), 1.78 (dt, J = 4.9, 10.3 Hz, 4H), 1.29-1.15 (m, 4H); FXR EC50 = 35 nM.
실시예 76
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메톡시니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-클로로-4-메톡시니코티네이트로 대체하여, 실시예 47의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 527.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.83 (s, 2H), 8.32 (s, 1H), 6.33 (s, 1H), 5.94 (s, 1H), 3.83-3.70 (m, 6H), 3.48-3.36 (m, 2H), 2.40-2.31 (m, 3H), 1.57 (br s, 4H), 1.28-1.19 (m, 2H), 1.16-1.09 (m, 2H); FXR EC50 = 2149 nM.
실시예 77
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(디플루오로메톡시)퀴놀린-2-카르복실산
표제 화합물을, 2-(트리플루오로메틸)벤즈알데히드를 2-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 58의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 613.2 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 9.02-8.93 (m, 1H), 8.77 (s, 1H), 8.09 (d, J = 9.5 Hz, 1H), 7.91 (d, J = 5.3 Hz, 1H), 7.83-7.76 (m, 2H), 7.60-7.20 (m, 2H), 5.78 (s, 1H), 3.72-3.49 (m, 2H), 3.38-3.29 (m, 2H), 2.46 (s, 2H), 2.33 (tt, J = 5.6, 7.9 Hz, 1H), 1.78 (dt, J = 4.8, 10.1 Hz, 4H), 1.35-1.10 (m, 4H); FXR EC50 = 68 nM.
실시예 78
6-(2-(3-(3-클로로피리딘-2-일)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(디플루오로메톡시)퀴놀린-2-카르복실산
표제 화합물을, 2-(트리플루오로메틸)벤즈알데히드를 3-클로로피콜린알데히드로 대체하여, 실시예 58의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 579.1 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.65 (dd, J = 1.4, 4.8 Hz, 1H), 8.14 (d, J = 9.5 Hz, 1H), 8.09 (dd, J = 1.4, 8.3 Hz, 1H), 7.89-7.85 (m, 2H), 7.66-7.27 (m, 3H), 5.89 (s, 1H), 3.71-3.60 (m, 2H), 3.44-3.34 (m, 2H), 2.46 (s, 2H), 2.34 (tt, J = 5.7, 7.6 Hz, 1H), 1.81 (dt, J = 4.5, 9.5 Hz, 4H), 1.23 (ddq, J = 2.4, 5.1, 7.3 Hz, 4H); FXR EC50 = 121 nM.
실시예 79
7-(2-(5-시클로프로필-3-(2,6-디플루오로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)신놀린-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2,6-디플루오로벤즈알데히드로 대체하여, 실시예 53의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 515.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.56 (s, 1H), 8.02 (d, J = 9.2 Hz, 1H), 7.83 (d, J = 9.5 Hz, 1H), 7.69 (ddd, J = 6.6, 8.4, 15.1 Hz, 1H), 7.61 (s, 1H), 7.33 (t, J = 8.0 Hz, 2H), 6.00 (s, 1H), 3.76-3.67 (m, 2H), 2.48 (s, 2H), 2.35 (td, J = 4.0, 8.2 Hz, 1H), 1.76-1.63 (m, 4H), 1.18 (ddt, J = 2.7, 5.4, 25.3 Hz, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 733 nM.
실시예 80
7-(2-(3-(3-클로로피리딘-4-일)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)신놀린-3-카르복실산
표제 화합물을, Pd-촉매된 부흐발트 커플링 단계 동안 하나의 염소를 환원시켜 실시예 55의 제조 동안 소량의 단리물로서 수득하였다.
MS (ESI) m/z: 514.0 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.88 (s, 1H), 8.78 (s, 1H), 8.65 (d, J=4.95 Hz, 1H), 8.13 (d, J=9.63 Hz, 1H), 8.00 (s, 2H), 7.55 (d, J=4.95 Hz, 1H), 7.26 (d, J=1.93 Hz, 1H), 5.95-6.01 (m, 1H), 3.90-4.09 (m, 2H), 3.67 (br dd, J=5.36, 8.12 Hz, 2H), 3.02 (s, 2H), 2.34 (s, 1H), 1.85 (br s, 4H), 1.17-1.41 (m, 4H); FXR EC50 = 1360 nM.
실시예 81
7-(2-(5-시클로프로필-3-(4-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)신놀린-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 4-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 53의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 548.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 9.04 (d, J = 5.1 Hz, 1H), 8.86 (s, 1H), 8.50 (s, 1H), 8.02-7.94 (m, 2H), 7.78 (d, J = 9.8 Hz, 1H), 7.57 (s, 1H), 5.84 (s, 1H), 3.69-3.61 (m, 2H), 2.39-2.26 (m, 3H), 1.70-1.58 (m, 4H), 1.18 (dt, J = 5.1, 38.7 Hz, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 1540 nM.
실시예 82
6-(2-(5-시클로프로필-3-(2,6-디플루오로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 에틸 7-클로로신놀린-3-카르복실레이트, HCl을 에틸 6-클로로-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트로 대체하여, 실시예 79의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 582.0 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.21 (s, 1H), 8.08 (d, J = 9.5 Hz, 1H), 7.88 (d, J = 9.5 Hz, 1H), 7.69 (q, J = 7.4 Hz, 1H), 7.33 (t, J = 8.1 Hz, 2H), 7.09 (s, 1H), 6.01 (s, 1H), 3.67-3.59 (m, 2H), 2.48 (s, 2H), 2.40-2.30 (m, 1H), 1.77-1.65 (m, 4H), 1.24-1.12 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 356 nM.
실시예 83
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디플루오로벤즈알데히드를 2,6-디클로로벤즈알데히드로 대체하여, 실시예 82의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 614.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.22 (br s, 1H), 8.09 (br s, 1H), 7.79 (br d, J=8.85 Hz, 1H), 7.62-7.68 (m, 2H), 7.49-7.62 (m, 2H), 7.06 (br s, 1H), 5.87 (s, 1H), 3.55 (br s, 1H), 3.31-3.51 (m, 1H),2.55 (s, 2H), 2.35 (s, 3H), 1.66 (br s, 4H), 1.17-1.25 (m, 2H), 1.13 (br s, 2H); FXR EC50 = 38 nM.
실시예 84
6-(2-(3-(2,6-디클로로페닐)-5-이소프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 시클로프로필아세틸렌을 이소프로필아세틸렌으로 대체하여, 실시예 83의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 612.2 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.46-8.30 (m, 1H), 8.06-7.95 (m, 1H), 7.56 (td, J=4.1, 2.6 Hz, 1H), 7.44-7.36 (m, 2H), 7.35-7.29 (m, 1H), 7.23-7.17 (m, 1H), 5.77 (s, 1H), 3.61-3.46 (m, 2H), 3.40-3.19 (m, 4H), 2.33 (br s, 3H), 1.43 (d, J=6.9 Hz, 8H), 1.26 (s, 1H); FXR EC50 = 127 nM.
실시예 85
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
단계 1. 3,5-디클로로이소니코틴알데히드 옥심
히드록실아민 히드로클로라이드 (11.8 g, 170 mmol)를 피리딘 (50 mL) 중 3,5-디클로로이소니코틴알데히드 (20 g, 114 mmol)의 실온 용액에 첨가하였다. 10분 후, 반응 혼합물을 진공 하에 농축시켜 과량의 피리딘을 제거하였다. 고체를 흡인 여과에 의해 수집하고, 물로 세척하고, 진공 하에 건조시켜 3,5-디클로로이소니코틴알데히드 옥심 (21.7 g, 114 mmol, 100% 수율)을 백색 고체로서 수득하였다.
1H NMR (400 MHz, DMSO-d6) δ 12.32 (s, 1H), 8.71 (s, 2H), 8.28 (s, 1H).
단계 2. 3,5-디클로로-N-히드록시이소니코틴이미도일 클로라이드
3,5-디클로로이소니코틴알데히드 옥심 (21.7 g, 114 mmol)을 DMF (114 mL) 중에 현탁시켰다. N-클로로숙신이미드 (16.7 g, 125 mmol)를 세 부분으로 첨가하여 투명한 황색 용액을 제공하였다. 3시간 동안 교반한 후, 반응 혼합물을 얼음에 붓고, Et2O로 추출하였다. 유기 층을 염수로 세척하고, 합한 수성 층을 Et2O로 역추출하였다. 합한 유기부를 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-60% EtOAc/hex, 이스코 120 g 칼럼)에 의해 정제하여 3,5-디클로로-N-히드록시이소니코틴이미도일 클로라이드 (24.8 g, 110 mmol, 97% 수율)을 회백색 결정으로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.72 (s, 1H), 8.62 (s, 2H).
단계 3. 5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸
에티닐시클로프로판 (12.1 mL, 143 mmol)에 이어서 Et3N (18.4 mL, 132 mmol)을 DCM (440 mL) 중 3,5-디클로로-N-히드록시이소니코틴이미도일 클로라이드 (24.8 g, 110 mmol)의 실온 용액에 첨가하였다. 실온에서 밤새 교반한 후, 반응 혼합물을 진공 하에 농축 건조시킨 다음, EtOAc/물에 녹였다. 유기 층을 염수로 세척하고, 합한 수성 층을 EtOAc로 역추출하였다. 합한 유기 층을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸 (27.3 g, 107 mmol, 97% 수율)을 황색 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.63 (s, 2H), 6.09 (s, 1H), 2.24-2.11 (m, 1H), 1.23-1.07 (m, 4H).
단계 4. 4-브로모-5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸
N-브로모숙신이미드 (24.8 g, 139 mmol)를 DMF (143 mL) 중 5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸 (27.3 g, 107 mmol)의 실온 용액에 첨가하였다. 반응 혼합물을 실온에서 주말 동안 교반하였다. 반응 혼합물을 얼음에 붓고, Et2O로 추출하였다. 유기 층을 염수로 세척하고, 수성 층을 Et2O로 역추출하였다. 합한 유기 추출물을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 황색 고체를 수득하였다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-30% EtOAc/hex, 이스코 220 g 칼럼)에 의해 정제하여 4-브로모-5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸 (29.0 g, 74.9 mmol, 81% 수율)을 백색 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.65 (s, 2H), 2.19 (tt, J=8.4, 5.1 Hz, 1H), 1.36-1.28 (m, 2H), 1.25-1.17 (m, 2H).
단계 5. tert-부틸 2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-2-히드록시-7-아자스피로[3.5]노난-7-카르복실레이트
n-부틸리튬 (22.5 mL, 56.1 mmol)을 천천히 (~30 분의 기간에 걸쳐) THF (150 mL) 중 4-브로모-5-시클로프로필-3-(3,5-디클로로피리딘-4-일) 이속사졸 (15 g, 44.9 mmol)의 -78℃ 용액에 첨가하였다. 10분 후, THF 8 mL 중 용액으로서의 tert-부틸 2-옥소-7-아자스피로[3.5]노난-7-카르복실레이트 (10.8 g, 44.9 mmol)를 차가운 교반하는 혼합물에 천천히 첨가하였다. 2.5시간 후, 반응물을 15 mL 포화 수성 NH4Cl의 느린 첨가에 의해 켄칭하였다. 혼합물을 EtOAc로 추출하고, 유기 층을 염수로 세척하였다. 합한 수성 층을 추가로 EtOAc로 추출하고, 합한 유기 추출물을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 오렌지색 고체 잔류물을 수득하였다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/DCM, 이스코 220 g 칼럼, 넓고 낮은 피크로서 용리된 생성물)에 의해 정제하여 tert-부틸 2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일) 이속사졸-4-일)-2-히드록시-7-아자스피로[3.5]노난-7-카르복실레이트 (6.6 g, 13.4 mmol, 30% 수율)을 황갈색 발포체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.65 (s, 2H), 3.34-3.25 (m, 2H), 3.24-3.17 (m, 2H), 2.25-2.11 (m, 4H), 2.09 (s, 1H), 1.78-1.65 (m, 2H), 1.49-1.42 (m, 11H), 1.42-1.35 (m, 2H), 1.34-1.28 (m, 2H), 1.22-1.11 (m, 2H).
단계 6. 5-시클로프로필-3-(3,5-디클로로피리딘-4-일)-4-(7-아자스피로[3.5]논-1-엔-2-일)이속사졸
트리플루오로아세트산 (5.8 mL, 76 mmol)을 tert-부틸 2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-2-히드록시-7-아자스피로[3.5]노난-7-카르복실레이트 (3.8 g, 7.6 mmol)가 들은 플라스크에 첨가하였다. 3시간 후, 반응 혼합물을 농축 건조시켰다. 잔류물을 EtOAc에 녹이고, 포화 수성 K2CO3으로 염기성화시켰다. 유기 층을 염수로 세척하고, 합한 수성 층을 EtOAc로 역추출하였다. 유기 추출물을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 5-시클로프로필-3-(3,5-디클로로피리딘-4-일)-4-(7-아자스피로[3.5]논-1-엔-2-일)이속사졸을 황갈색 발포체로서 수득하였으며, 이를 추가의 정제 없이 사용하였다.
단계 7. 에틸 6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트
디옥산 중 5-시클로프로필-3-(3,5-디클로로피리딘-4-일)-4-(7-아자스피로[3.5]논-1-엔-2-일)이속사졸 (2.0 g, 5.3 mmol), 에틸 6-클로로-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트 (1.9 g, 6.4 mmol) 및 Cs2CO3 (3.5 g, 10.6 mmol)의 슬러리 (35 mL)를 교반하는 혼합물을 통해 10분 동안 N2 버블링시켜 탈기시켰다. 클로로(2-디시클로헥실포스피노-2',6'-디이소프로폭시-1,1'-비페닐)[2-(2'-아미노-1,1'-비페닐)] 팔라듐(II) (RuPhos-Pd-G2) (0.20 g, 0.27 mmol)을 첨가하고, 반응 용기를 밀봉하고, 70℃로 가열하였다. 밤새 가열한 후, 반응 혼합물을 EtOAc로 희석하고, 셀라이트를 통해 여과하고, 진공 하에 농축 건조시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/hex, 이스코 80 g 칼럼)에 의해 정제하여 에틸 6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트 (1.2 g, 1.8 mmol, 34% 수율)을 황색 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.64 (s, 2H), 8.36 (s, 1H), 8.20 (d, J=9.5 Hz, 1H), 7.60 (dd, J=9.5, 2.6 Hz, 1H), 7.22 (s, 1H), 5.84 (s, 1H), 4.56 (q, J=7.2 Hz, 2H), 3.63-3.53 (m, 2H), 3.32 (ddd, J=12.8, 8.5, 3.9 Hz, 2H), 2.45 (s, 2H), 2.20 (tt, J=8.4, 5.1 Hz, 1H), 1.89-1.72 (m, 4H), 1.49 (t, J=7.2 Hz, 3H), 1.36-1.29 (m, 2H), 1.24-1.14 (m, 2H); 19F NMR (377 MHz, CDCl3) δ -62.65 (s, 3F).
실시예 85. 6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
에틸 6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트 (1.2 g, 1.8 mmol)를 THF (12 mL), 물 (4.8 mL), 및 MeOH (1.2 mL)에 녹인 다음, 수산화리튬 (0.43 g, 18.0 mmol)을 혼합물에 첨가하였다. 반응물을 밀봉하고, 50℃로 가열하였다. 30분 동안 가열한 후, 조 반응 혼합물을 셀라이트 상에 로딩하고, C-18 역상 플래쉬 크로마토그래피 (A 중 10-100% B, A = 10:90:0.1 MeCN:H2O:TFA, B = 90:10:0.1 MeCN:H2O:TFA, 18분 선형 구배, 이스코 100 g C-18 골드 칼럼)에 의해 정제하고, 목적 분획을 합하고, 농축시켜 6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산, 실시예 85 (1.0 g, 1.6 mmol, 89% 수율)을 적색 고체로서 수득하였다.
MS (ESI) m/z: 615.1 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.66 (s, 2H), 8.45 (s, 1H), 8.06 (d, J=9.5 Hz, 1H), 7.65 (dd, J=9.7, 2.6 Hz, 1H), 7.27-7.24 (m, 1H), 5.86 (s, 1H), 3.65-3.58 (m, 2H), 3.41-3.32 (m, 2H), 2.47 (s, 2H), 2.25-2.16 (m, 1H), 1.89-1.76 (m, 4H), 1.37-1.31 (m, 2H), 1.25-1.17 (m, 2H); 19F NMR (377 MHz, CDCl3) δ -62.85 (s, 3F); FXR EC50 = 53 nM; 마우스 생체내 (3 mg/kg, @ 6h): Cyp7a1 = -94%, Fgf15 = +19x.
실시예 86
6-(2-(5-시클로프로필-3-(2,6-디클로로-4-플루오로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디플루오로벤즈알데히드를 2,6-디클로로-4-플루오로벤즈알데히드로 대체하여, 실시예 82의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 632.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.21 (s, 1H), 8.08 (br d, J=9.5 Hz, 1H), 7.88 (br d, J=8.5 Hz, 1H), 7.77 (d, J=8.5 Hz, 2H), 7.08 (br s, 1H), 5.94 (s, 1H), 3.91 (s, 1H), 3.70-3.56 (m, 2H), 3.36-3.23 (m, 3H), 2.40 (s, 1H), 2.38-2.28 (m, 1H), 1.76-1.60 (m, 4H), 1.28-1.18 (m, 2H), 1.16 (br d, J=2.7 Hz, 2H); FXR EC50 = 68 nM.
실시예 87
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메틸퀴놀린-2-카르복실산
표제 화합물을, 에틸 6-클로로-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트를 에틸 6-브로모-4-메틸퀴놀린-2-카르복실레이트로 대체하여, 실시예 85의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 561.0 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.63 (s, 2H), 7.90-8.14 (m, 2H), 7.57 (s, 1H), 7.11 (br s, 1H), 5.79-5.91 (m, 1H), 3.45-3.61 (m, 2H), 3.27 (ddd, J=3.74, 8.58, 12.54 Hz, 2H), 2.69 (s, 3H), 2.44 (s, 2H), 2.19 (s, 1H), 1.78-2.03 (m, 4H), 1.27-1.39 (m, 4H); FXR EC50 = 76 nM.
실시예 88
6-(2-(3-(2-클로로-6-플루오로페닐)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디플루오로벤즈알데히드를 2-클로로-6-플루오로벤즈알데히드로 대체하여, 실시예 82의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 597.9 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.21 (s, 1H), 8.07 (d, J = 9.4 Hz, 1H), 7.80 (d, J = 9.2 Hz, 1H), 7.63 (td, J = 6.1, 8.3 Hz, 1H), 7.52 (d, J = 8.1 Hz, 1H), 7.41 (t, J = 8.7 Hz, 1H), 7.09 (s, 1H), 5.94 (s, 1H), 3.63-3.52 (m, 2H), 3.34-3.25 (m, 2H), 2.40 (s, 2H), 2.32 (td, J = 4.3, 8.5 Hz, 1H), 1.76-1.63 (m, 4H), 1.26-1.09 (m, 4H); FXR EC50 = 150 nM.
실시예 89
6-(2-(3-(2-클로로-6-메틸페닐)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디플루오로벤즈알데히드를 2-클로로-6-메틸벤즈알데히드로 대체하여, 실시예 82의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 594.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.21 (s, 1H), 8.07 (d, J = 9.5 Hz, 1H), 7.83 (dd, J = 2.6, 9.5 Hz, 1H), 7.50-7.40 (m, 2H), 7.36 (dd, J = 2.9, 5.8 Hz, 1H), 7.07 (s, 1H), 5.78 (s, 1H), 3.63-3.55 (m, 2H), 3.31-3.22 (m, 2H), 2.42-2.31 (m, 3H), 2.11 (s, 3H), 1.74-1.59 (m, 4H), 1.25-1.10 (m, 4H); FXR EC50 = 202 nM.
실시예 90
6-(2-(5-시클로프로필-3-(4-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디플루오로벤즈알데히드를 4-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 82의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 615.0 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 9.05 (d, J = 5.1 Hz, 1H), 8.87 (s, 1H), 8.22 (s, 1H), 8.06 (d, J = 9.5 Hz, 1H), 7.99 (d, J = 5.2 Hz, 1H), 7.82-7.76 (m, 1H), 7.07 (s, 1H), 5.85 (s, 1H), 3.58-3.50 (m, 2H), 3.28-3.21 (m, 2H), 2.40-2.30 (m, 3H), 1.73-1.61 (m, 4H), 1.28-1.11 (m, 4H); FXR EC50 = 195 nM.
실시예 91
6-(2-(3-(3-클로로피리딘-2-일)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디플루오로벤즈알데히드를 3-클로로피콜린알데히드로 대체하여, 실시예 82의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 581.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.69 (d, J=4.0 Hz, 1H), 8.20 (s, 1H), 8.15 (d, J=8.2 Hz, 1H), 8.07 (br d, J=9.5 Hz, 1H), 7.86 (br d, J=8.5 Hz, 1H), 7.63 (dd, J=8.2, 4.6 Hz, 1H), 7.07 (br s, 1H), 5.89 (s, 1H), 3.70-3.52 (m, 1H), 3.31 (br t, J=8.9 Hz, 1H), 2.42-2.27 (m, 3H), 1.75-1.57 (m, 4H), 1.27-1.17 (m, 2H), 1.14 (br d, J=2.7 Hz, 2H); FXR EC50 = 219 nM.
실시예 92
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디플루오로벤즈알데히드를 2-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 82의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 615.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.93 (dd, J = 1.5, 4.8 Hz, 1H), 8.24 (s, 1H), 8.20-8.13 (m, 1H), 8.09 (d, J = 9.5 Hz, 1H), 7.89 (dd, J = 4.7, 7.9 Hz, 1H), 7.83-7.72 (m, 1H), 7.06 (s, 1H), 5.83 (s, 1H), 3.56-3.48 (m, 2H), 3.26-3.17 (m, 2H), 2.40-2.29 (m, 3H), 1.65 (ddd, J = 6.0, 11.1, 18.2 Hz, 4H), 1.27-1.08 (m, 4H); FXR EC50 = 253 nM.
실시예 93
6-(2-(5-시클로프로필-3-(3,5-디플루오로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디플루오로벤즈알데히드를 3,5-디플루오로이소니코틴알데히드로 대체하여, 실시예 82의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 583.0 [M+H]+;
1H NMR (400 MHz, DMSO-d6) δ 8.80 (s, 2H), 8.21 (s, 1H), 8.08 (d, J = 9.5 Hz, 1H), 7.89 (dd, J = 2.6, 9.7 Hz, 1H), 7.08 (d, J = 2.4 Hz, 1H), 6.14 (s, 1H), 3.66-3.57 (m, 2H), 3.43-3.27 (m, 2H), 2.51 (s, 2H), 2.41-2.30 (m, 1H), 1.72 (q, J = 4.9, 5.4 Hz, 4H), 1.27-1.10 (m, 4H); FXR EC50 = 511 nM.
실시예 94
6-(2-(3-(3,5-디클로로피리딘-4-일)-5-(1-메틸시클로프로필)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 시클로프로필아세틸렌을 1-에티닐-1-메틸시클로프로판으로 대체하여, 실시예 85의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 629.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.87 (s, 2H), 8.22 (br s, 1H), 8.08 (br d, J=9.2 Hz, 1H), 7.85 (br d, J=7.9 Hz, 1H), 7.09 (br s, 1H), 6.07 (s, 1H), 3.67-3.54 (m, 1H), 3.39-3.25 (m, 1H), 3.02-2.88 (m, 1H), 2.36 (s, 2H), 1.78-1.61 (m, 4H), 1.45 (s, 3H), 1.32-1.21 (m, 2H), 1.18 (br t, J=7.3 Hz, 2H), 1.08 (br s, 2H), 0.99 (br s, 2H); FXR EC50 = 507 nM.
실시예 95
6-(2-(3-(3,5-디클로로피리딘-4-일)-5-이소프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 시클로프로필아세틸렌을 이소프로필아세틸렌으로 대체하여, 실시예 85의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 617.2 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.90-8.52 (m, 2H), 8.42 (br d, J=1.0 Hz, 1H), 8.18-7.93 (m, 1H), 7.70-7.45 (m, 1H), 5.83 (s, 1H), 3.56 (br s, 2H), 3.42-3.25 (m, 3H), 2.37 (s, 2H), 1.78 (br s, 4H), 1.44 (br d, J=6.9 Hz, 6H), 산 OH가 관찰되지 않음, CDCl3 피크 하의 하나의 퀴놀린 C-H; FXR EC50 = 37 nM.
실시예 96
6-(2-(3-(2-클로로-4-플루오로페닐)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, Pd-촉매된 부흐발트 커플링 단계 동안 하나의 염소를 환원시켜 실시예 86의 제조 동안 소량의 단리물로서 수득하였다.
MS (ESI) m/z: 598.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 1H NMR 실험; FXR EC50 = 869 nM 중 8.21 (br s, 1H), 8.08 (br s, 1H), 7.86 (br d, J=9.9 Hz, 1H), 7.63 (br d, J=8.8 Hz, 1H), 7.56 (br dd, J=8.3, 6.1 Hz, 1H), 7.42-7.31 (m, 1H), 7.11 (br s, 1H), 5.96 (s, 1H), 3.61 (br d, J=13.8 Hz, 2H), 3.44-3.24 (m, 1H), 2.43 (s, 1H), 2.37-2.24 (m, 1H), 1.83-1.63 (m, 3H), 1.35-1.05 (m, 5H) 물 억제로 인해 추가의 신호 사라짐.
실시예 97
6-(2-(5-시클로프로필-3-(3-플루오로-5-메톡시피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 가수 분해 단계 동안 1개의 플루오린을 MeOH로 치환하여, 실시예 93의 제조 동안 추가의 단리물로서 수득하였다.
MS (ESI) m/z: 595.1 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.40 (d, J = 3.2 Hz, 1H), 8.34 (t, J = 3.2 Hz, 2H), 8.18 (br s, 1H), 7.86-7.77 (m, 1H), 7.25 (s, 1H), 5.98 (d, J = 3.3 Hz, 1H), 3.99 (s, 3H), 3.72-3.62 (m, 2H), 3.45-3.36 (m, 2H), 2.52 (s, 2H), 2.37-2.28 (m, 1H), 1.88-1.72 (m, 4H), 1.21 (q, J = 3.5, 6.1 Hz, 4H); FXR EC50 = 1940 nM.
실시예 98
6-(2-(3-시클로헥실-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디플루오로벤즈알데히드를 시클로헥산카르브알데히드로 대체하여, 실시예 82의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 552.4 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.23 (s, 1H), 8.10 (d, J = 9.3 Hz, 1H), 7.91 (d, J = 9.9 Hz, 1H), 7.13 (s, 1H), 6.41 (s, 1H), 3.76-3.65 (m, 2H), 2.78-2.67 (m, 3H), 2.21 (dq, J = 5.3, 8.6 Hz, 1H), 1.97-1.22 (m, 8H), 1.47-1.19 (m, 6H), 1.12-0.94 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 1720 nM.
실시예 99
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디플루오로벤즈알데히드를 2-(트리플루오로메틸) 벤즈알데히드로 대체하여, 실시예 82의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 614.1 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.33 (s, 1H), 8.13 (d, J=9.35 Hz, 1H), 7.89 (d, J=7.15 Hz, 1H), 7.68-7.81 (m, 3H), 7.51 (d, J=7.15 Hz, 1H), 7.21 (br s, 1H), 5.67-5.86 (m, 1H), 3.60 (br s, 2H), 3.36 (br d, J=3.58 Hz, 2H), 2.42 (s, 2H), 2.31 (s, 1H), 1.66-1.94 (m, 4H), 1.11-1.40 (m, 4H); FXR EC50 = 92 nM.
일반적 방법 D
실시예 100
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-6-카르복실산
단계 1. 4-(7-(6-브로모퀴녹살린-2-일)-7-아자스피로[3.5]논-1-엔-2-일)-5-시클로프로필-3-(2,6-디클로로페닐)이속사졸
디옥산 중 5-시클로프로필-3-(2,6-디클로로페닐)-4-(7-아자스피로[3.5]논-1-엔-2-일)이속사졸 (25 mg, 0.07 mmol, 일반적 방법 A에 기재된 합성), 6-브로모-2-클로로퀴녹살린 (19.5 mg, 0.08 mmol) 및 Cs2CO3 (43.4 mg, 0.13 mmol)의 슬러리 (0.3 mL)를 5분 동안 혼합물을 통해 질소를 버블링시킴으로써 탈기시켰다. 클로로(2-디시클로헥실포스피노-2',6'-디이소프로폭시-1,1'-비페닐)[2-(2'-아미노-1,1'-비페닐)] 팔라듐(II) (RuPhos-Pd-G2) (2.59 mg, 3.33 μmol)을 첨가하고, 반응 혼합물을 밀봉하고, 90℃로 6시간 동안 가열하였다. 조 반응 혼합물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 12 g 칼럼)에 의해 직접 정제하여 4-(7-(6-브로모퀴녹살린-2-일)-7-아자스피로[3.5]논-1-엔-2-일)-5-시클로프로필-3-(2,6-디클로로페닐)이속사졸 (26 mg, 0.04 mmol, 64% 수율)을 검으로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.57 (s, 1H), 8.03 (d, J=2.2 Hz, 1H), 7.64 (dd, J=8.8, 2.2 Hz, 1H), 7.53 (d, J=8.8 Hz, 1H), 7.46-7.42 (m, 2H), 7.40-7.34 (m, 1H), 5.80 (s, 1H), 3.94 (dt, J=13.5, 5.1 Hz, 2H), 3.66-3.50 (m, 2H), 2.44 (s, 2H), 2.21 (tt, J=8.4, 5.1 Hz, 1H), 1.76 (t, J=5.6 Hz, 4H), 1.36-1.30 (m, 2H), 1.22-1.15 (m, 2H).
단계 2. 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-6-카르보니트릴
4-(7-(6-브로모퀴녹살린-2-일)-7-아자스피로[3.5]논-1-엔-2-일)-5-시클로프로필-3-(2,6-디클로로페닐)이속사졸 (20 mg, 0.03 mmol), Xantphos (4.0 mg, 6.9 μmol), Pd2(dba)3 (6.3 mg, 6.9 μmol), 및 시안화아연 (4.0 mg, 0.03 mmol)을 함유하는 마이크로웨이브 바이알을 질소로 3회 퍼징하고, 무수 DMF (0.5 mL)를 첨가하였다. 반응 혼합물을 마이크로웨이브 조사 하에 110℃에서 1.5시간 동안 가열하였다. 반응 혼합물을 EtOAc (10 mL)로 희석하고, 염수 (10 mL)로 세척하였다. 유기 층을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축 건조시켰다. 조 생성물을 SiO2 상 플래쉬 크로마토그래피 (0 → 100% EtOAc/헥산, 이스코 12 g 칼럼)에 의해 정제하여 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-6-카르보니트릴 (11.5 mg, 0.02 mmol, 60% 수율)을 검으로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.65 (s, 1H), 8.19 (d, J=1.8 Hz, 1H), 7.74-7.68 (m, 1H), 7.67-7.62 (m, 1H), 7.48-7.42 (m, 2H), 7.40-7.34 (m, 1H), 5.79 (s, 1H), 4.02 (dt, J=13.5, 5.0 Hz, 2H), 3.68-3.59 (m, 2H), 2.46 (s, 2H), 2.20 (tt, J=8.4, 5.1 Hz, 1H), 1.77 (t, J=5.6 Hz, 4H), 1.37-1.31 (m, 2H), 1.24-1.15 (m, 2H).
실시예 100. 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-6-카르복실산
EtOH (72.5 μL) 중 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-6-카르보니트릴 (11.5 mg, 0.02 mmol)의 용액에 NaOH (21.8 μL, 0.11 mmol)을 첨가하였다. 반응 혼합물을 밀봉하고, 90℃로 2시간 동안 가열하였다. 조 반응 혼합물을 C-18 역상 플래쉬 크로마토그래피 (A 중 10-100% B, A = 10:90:0.1 MeCN:H2O:TFA, B = 90:10:0.1 MeCN:H2O:TFA, 18분 선형 구배, 이스코 24 g C-18 골드 칼럼)에 의해 정제하고, 목적 분획을 합하고, 농축시켜 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐) 이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-6-카르복실산 (9.6 mg, 0.017 mmol, 79% 수율)을 황색 고체로서 수득하였다.
MS (ESI) m/z: 546.9 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.69 (s, 1H), 8.44 (d, J=1.98 Hz, 1H), 8.11 (dd, J=1.87, 8.69 Hz, 1H), 7.59 (d, J=8.58 Hz, 1H), 7.37-7.52 (m, 3H), 5.80 (s, 1H), 4.03 (td, J=4.98, 13.59 Hz, 2H), 3.52-3.73 (m, 2H), 2.43 (s, 2H), 2.18-2.32 (m, 1H), 1.72 (br t, J=5.50 Hz, 4H), 1.07-1.40 (m, 6H); FXR EC50 = 33 nM.
실시예 101
2-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 100의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 547.0 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.81-8.91 (m, 1H), 8.50 (d, J=1.76 Hz, 1H), 8.20 (dd, J=1.98, 8.80 Hz, 1H), 7.85-7.99 (m, 1H), 7.71-7.80 (m, 2H), 7.68 (d, J=8.80 Hz, 1H), 7.46-7.57 (m, 1H), 5.75 (s, 1H), 3.96-4.35 (m, 2H), 3.60-3.89 (m, 2H), 2.46 (s, 1H), 2.31 (s, 1H), 1.63-1.90 (m, 4H), 1.10-1.44 (m, 4H); FXR EC50 = 17 nM.
실시예 102
2-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)티아졸로[5,4-b]피리딘-5-카르복실산
표제 화합물을, 3,5-디클로로이소니코틴알데히드를 2-(트리플루오로메틸) 벤즈알데히드로 대체하여, 실시예 62의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 553.2 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.15 (br d, J=8.25 Hz, 1H), 7.83 (br d, J=7.43 Hz, 1H), 7.76 (br d, J=8.25 Hz, 1H), 7.62-7.73 (m, 2H), 7.46 (br d, J=6.60 Hz, 1H), 5.57-5.82 (m, 1H), 3.78 (br d, J=11.55 Hz, 2H), 3.46-3.65 (m, 2H), 2.42 (s, 2H), 2.15 (br d, J=4.68 Hz, 1H), 1.24-1.38 (m, 4H), 1.18 (m, 4H); FXR EC50 = 18 nM.
실시예 103
2-(2-(3-(2-클로로-6-메틸페닐)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-클로로-6-메틸벤즈알데히드로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 549.9 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.21 (s, 1H), 7.60 (d, J = 11.5 Hz, 1H), 7.48-7.42 (m, 2H), 7.40-7.33 (m, 1H), 5.80 (s, 1H), 3.78-3.69 (m, 2H), 3.53-3.45 (m, 2H), 2.43-2.29 (m, 3H), 2.12 (s, 3H), 1.66 (br s, 4H), 1.24-1.10 (m, 4H); FXR EC50 = 19 nM.
실시예 104.
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-이소프로폭시퀴놀린-2-카르복실산
표제 화합물을, 에틸 6-클로로-4-(트리플루오로메틸) 퀴놀린-2-카르복실레이트를 메틸 6-브로모-4-이소프로폭시퀴놀린-2-카르복실레이트로 대체하여, 실시예 99의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 604.2 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.08-8.36 (m, 1H), 7.83-8.03 (m, 2H), 7.64-7.82 (m, 3H), 7.51 (br d, J=6.60 Hz, 1H), 7.43 (br s, 1H), 5.63-5.84 (m, 1H), 5.20-5.46 (m, 1H), 3.62 (br s, 4H), 2.42 (br s, 2H), 2.29 (br d, J=4.40 Hz, 1H), 1.75 (br s, 4H), 1.60 (br s, 6H), 1.20 (br s, 4H); FXR EC50 = 59 nM.
실시예 105
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메톡시퀴놀린-2-카르복실산
표제 화합물을, 에틸 6-클로로-4-(트리플루오로메틸) 퀴놀린-2-카르복실레이트를 메틸 6-브로모-4-메톡시퀴놀린-2-카르복실레이트로 대체하여, 실시예 99의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 576.1 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.10 (d, J=9.46 Hz, 1H), 7.86-7.93 (m, 1H), 7.72-7.85 (m, 3H), 7.71 (s, 1H), 7.47-7.60 (m, 1H), 7.43 (d, J=2.64 Hz, 1H), 5.61-5.86 (m, 1H), 4.31 (s, 3H), 3.51-3.68 (m, 2H), 3.21-3.31 (m, 2H), 2.41 (s, 2H), 2.23-2.36 (m, 1H), 1.72-1.89 (m, 4H), 1.11-1.22 (m, 4H); FXR EC50 = 62 nM.
실시예 106
6-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-이소프로폭시퀴놀린-2-카르복실산
표제 화합물을, 2-(트리플루오로메틸)벤즈알데히드를 2-(트리플루오로메톡시)벤즈알데히드로 대체하여, 실시예 104의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 620.2 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.65 (br d, J=9.63 Hz, 1H), 7.83 (br d, J=7.70 Hz, 1H), 7.77 (s, 1H), 7.54-7.59 (m, 1H), 7.52 (dd, J=1.38, 7.70 Hz, 1H), 7.42 (br d, J=7.15 Hz, 3H), 5.87 (s, 1H), 5.16-5.27 (m, 1H), 3.53-3.66 (m, 2H), 3.39 (td, J=3.78, 12.52 Hz, 2H), 2.52 (s, 2H), 2.19 (br t, J=4.95 Hz, 1H), 1.79-1.93 (m, 4H), 1.62 (d, J=6.05 Hz, 6H), 1.30 (dd, J=2.34, 4.81 Hz, 2H), 1.17 (dd, J=2.61, 8.39 Hz, 2H); FXR EC50 = 21 nM.
실시예 107
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-에톡시퀴놀린-2-카르복실산
표제 화합물을, 2-(트리플루오로메틸)벤즈알데히드를 3,5-디클로로이소니코틴알데히드로 대체하여, 실시예 72의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 591.1 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.68 (br d, J=9.46 Hz, 1H), 8.65 (s, 1H), 7.79-7.87 (m, 1H), 7.76 (s, 1H), 7.39 (d, J=2.42 Hz, 1H), 5.84 (s, 1H), 4.59 (d, J=7.04 Hz, 2H), 3.57 (br s, 2H), 3.35 (br s, 2H), 2.45 (s, 2H), 2.14-2.27 (m, 1H), 1.82 (br s, 4H), 1.67 (t, J=7.04 Hz, 3H), 1.06-1.50 (m, 4H); FXR EC50 = 31 nM.
실시예 108
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메톡시퀴놀린-2-카르복실산
표제 화합물을, 메틸 6-브로모-4-에톡시퀴놀린-2-카르복실레이트를 메틸 6-브로모-4-메톡시퀴놀린-2-카르복실레이트로 대체하여, 실시예 107의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 577.0 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.68 (s, 2H), 8.11 (d, J=9.46 Hz, 1H), 7.78 (dd, J=2.53, 9.57 Hz, 1H), 7.72 (d, J=2.64 Hz, 1H), 7.44 (d, J=2.42 Hz, 1H), 5.89 (s, 1H), 4.30 (s, 3H), 3.57 (br s, 2H), 3.22-3.32 (m, 2H), 2.48 (s, 2H), 2.13-2.36 (m, 1H), 1.81 (br d, J=4.18 Hz, 4H), 1.17-1.34 (m, 4H); FXR EC50 = 32 nM; 마우스 생체내 (3 mg/kg, @ 6h): Cyp7a1 = -97%, Fgf15 = +14x.
실시예 109
6-(2-(3-(3-클로로피리딘-4-일)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메톡시퀴놀린-2-카르복실산
표제 화합물을, Pd-촉매된 부흐발트 커플링 단계 동안 하나의 염소를 환원시켜 실시예 108의 제조 동안 소량의 단리물로서 수득하였다.
MS (ESI) m/z: 543.1 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.65 (s, 2H), 8.03 (d, J=9.24 Hz, 1H), 7.61 (s, 2H), 7.40 (d, J=2.64 Hz, 1H), 5.86 (s, 1H), 4.16 (s, 3H), 3.44-3.59 (m, 2H), 3.12-3.37 (m, 2H), 2.45 (s, 2H), 1.82 (br d, J=2.42 Hz, 7H), 1.13-1.44 (m, 8H), 0.91 (s, 3H); FXR EC50 = 140 nM.
실시예 110
6-(2-(5-시클로프로필-3-(2,6-디클로로-4-플루오로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-이소프로폭시퀴놀린-2-카르복실산
표제 화합물을, 2-(트리플루오로메틸)벤즈알데히드를 2,6-디클로로-4-플루오로벤즈알데히드로 대체하여, 실시예 104의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 622.0 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 7.96 (br d, J=8.9 Hz, 1H), 7.53 (br s, 2H), 7.43-7.27 (m, 1H), 7.24-7.16 (m, 2H), 5.84 (s, 1H), 5.02-4.88 (m, 1H), 3.46 (br s, 3H), 3.36-3.15 (m, 2H), 2.40 (s, 2H), 2.21-2.12 (m, 1H), 1.81 (br d, J=10.2 Hz, 4H), 1.50 (br s, 6H), 1.28 (br s, 2H), 1.14 (br d, J=7.4 Hz, 2H); FXR EC50 = 37 nM.
실시예 111
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-이소프로폭시퀴놀린-2-카르복실산
표제 화합물을, 2-(트리플루오로메틸)벤즈알데히드를 2,6-디클로로-4-플루오로벤즈알데히드로 대체하여, 실시예 104의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 605.1 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.73 (s, 2H), 8.18 (d, J=9.63 Hz, 1H), 7.98 (br d, J=2.75 Hz, 1H), 7.77 (s, 1H), 7.46 (d, J=2.75 Hz, 1H), 5.87-6.03 (m, 1H), 5.28-5.46 (m, 1H), 3.56-3.78 (m, 2H), 3.40 (td, J=4.47, 8.67 Hz, 2H), 2.51 (s, 2H), 2.25-2.36 (m, 1H), 1.71-1.94 (m, 4H), 1.61 (d, J=6.05 Hz, 6H), 1.03-1.34 (m, 4H); FXR EC50 = 47 nM.
실시예 112
6-(2-(5-시클로프로필-3-(2,6-디클로로-4-플루오로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메톡시퀴놀린-2-카르복실산
표제 화합물을, 3,5-디클로로이소니코틴알데히드를 2,6-디클로로-4-플루오로벤즈알데히드로 대체하여, 실시예 108의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 594.2 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 7.96 (br d, J=9.2 Hz, 1H), 7.58 (s, 1H), 7.54 (br d, J=9.1 Hz, 1H), 7.40 (br s, 1H), 7.21 (br d, J=8.0 Hz, 2H), 5.85 (s, 1H), 4.14 (s, 3H), 3.74 (s, 1H), 3.61-3.39 (m, 2H), 3.39-3.19 (m, 2H), 2.42 (s, 2H), 2.18 (br d, J=4.6 Hz, 1H), 1.83 (br d, J=12.4 Hz, 4H), 1.30 (br d, J=3.7 Hz, 2H), 1.17 (br d, J=7.0 Hz, 2H); FXR EC50 = 54 nM.
실시예 113
6-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-에톡시퀴놀린-2-카르복실산
표제 화합물을, 2-(트리플루오로메틸)벤즈알데히드를 2-(트리플루오로메톡시)벤즈알데히드로 대체하여, 실시예 72의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 606.2 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.68 (br d, J=9.35 Hz, 1H), 7.72-8.01 (m, 2H), 7.47-7.66 (m, 2H), 7.35-7.44 (m, 3H), 5.70-5.99 (m, 1H), 4.60 (q, J=6.97 Hz, 2H), 3.53-3.77 (m, 3H), 3.37-3.43 (m, 2H), 2.51 (s, 2H), 2.13-2.23 (m, 1H), 1.78-1.88 (m, 4H), 1.66-1.78 (m, 3H), 1.25-1.35 (m, 2H), 1.11-1.23 (m, 2H); FXR EC50 = 116 nM.
실시예 114
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)벤조[d]옥사졸-6-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-클로로벤조[d]옥사졸-6-카르복실레이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 536.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.78-7.92 (m, 2H), 7.63-7.67 (m, 2H), 7.53-7.63 (m, 1H), 7.28 (d, J=8.16 Hz, 1H), 5.91 (s, 1H), 3.65-3.81 (m, 2H), 3.46-3.57 (m, 2H), 2.37 (s, 2H), 2.23-2.36 (m, 1H), 1.59-1.71 (m, 4H), 1.11-1.29 (m, 4H); FXR EC50 = 127 nM.
실시예 115
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메틸니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-플루오로-4-메틸니코티네이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 510.0 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.55 (s, 1H), 7.63-7.70 (m, 2H), 7.61 (s, 1H), 6.65 (s, 1H), 5.71-6.02 (m, 1H), 3.81 (br d, J=13.43 Hz, 2H), 3.26-3.40 (m, 2H), 2.43 (s, 3H), 2.32 (s, 3H), 1.52 (br s, 4H), 1.08-1.34 (m, 4H); FXR EC50 = 132 nM.
실시예 116
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-클로로-4-(트리플루오로메틸)니코티네이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 564.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.63 (s, 1H), 7.64-7.68 (m, 2H), 7.60 (dd, J=7.02, 8.85 Hz, 1H), 7.03 (s, 1H), 5.77-6.14 (m, 1H), 3.88 (br d, J=13.43 Hz, 2H), 2.55 (s, 3H), 2.35 (s, 2H), 1.56 (br s, 4H), 1.21 (br d, J=8.24 Hz, 2H), 1.11-1.17 (m, 2H); FXR EC50 = 135 nM.
실시예 117
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-피롤로[3,2-c]피리딘-3-카르복실산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 메틸 6-클로로-1-메틸-1H-피롤로[3,2-c]피리딘-3-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 549.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.64 (s, 1H), 8.00 (s, 1H), 7.64-7.70 (m, 2H), 7.60 (br d, J=7.02 Hz, 1H), 7.14-7.34 (m, 1H), 6.97-7.09 (m, 1H), 5.74-5.99 (m, 1H), 3.75 (s, 3H), 3.67 (br s, 1H), 3.29 (br s, 1H), 2.89 (s, 1H), 2.73 (s, 1H), 2.35 (s, 3H), 1.64 (br d, J=16.48 Hz, 4H), 1.05-1.36 (m, 4H); FXR EC50 = 139 nM.
실시예 118
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)피리미딘-5-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-클로로피리미딘-5-카르복실레이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 497.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.73 (s, 2H), 7.64-7.71 (m, 2H), 7.62 (s, 1H), 5.80-5.92 (m, 1H), 3.94-4.27 (m, 2H), 2.35 (m, 3H), 1.54 (br s, 4H), 1.08-1.30 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 171 nM.
실시예 119
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)피리미딘-5-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 에틸 2-클로로-4-(트리플루오로메틸)피리미딘-5-카르복실레이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 565.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.80 (s, 1H), 7.64 (s, 2H), 7.60 (br d, J=7.02 Hz, 1H), 5.79-5.92 (m, 1H), 4.01 (br s, 2H), 2.34 (m, 3H), 1.55 (m, 4H), 1.09-1.30 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 316 nM.
실시예 120
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-6-메틸피리미딘-4-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-클로로-6-메틸피리미딘-4-카르복실레이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 511.4 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.63-7.71 (m, 2H), 7.60 (br d, J=7.32 Hz, 1H), 6.84 (s, 1H), 5.84-5.90 (m, 1H), 3.99 (br d, J=12.82 Hz, 2H), 2.32 (m, 3H), 2.29 (s, 3H), 1.50 (br s, 4H), 1.07-1.26 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 1390 nM.
실시예 121
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-5-메틸니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-플루오로-5-메틸니코티네이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 510.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.55 (br s, 1H), 7.87 (br s, 1H), 7.52-7.76 (m, 3H), 5.74-5.94 (m, 1H), 3.08-3.45 (m, 2H), 3.02 (m, 2H), 2.32 (m, 3H), 2.23 (s, 3H), 1.52-1.85 (m, 4H), 1.18-1.35 (m, 4H); FXR EC50 = 2590 nM.
실시예 122
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴놀린-6-카르복실산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 메틸 2-클로로퀴놀린-6-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 546.1 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.52-8.61 (m, 1H), 8.45 (d, J=9.63 Hz, 1H), 8.38 (dd, J=1.51, 8.67 Hz, 1H), 7.93 (d, J=8.80 Hz, 1H), 7.55-7.62 (m, 3H), 7.50-7.55 (m, 1H), 5.87 (s, 1H), 4.11 (br d, J=14.03 Hz, 2H), 3.65-3.90 (m, 2H), 2.56 (s, 2H), 2.34 (s, 1H), 2.06 (s, 1H), 1.90 (br t, J=4.26 Hz, 4H), 1.14-1.33 (m, 4H); FXR EC50 = 40 nM.
실시예 123
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)피롤로[2,1-f][1,2,4]트리아진-5-카르복실산
단계 1. 에틸 2-클로로피롤로[2,1-f][1,2,4]트리아진-5-카르복실레이트
EtOAc (80 mL) 및 2-프로판올 (16 mL)의 혼합물 중 에틸 2,4-디클로로피롤로[2,1-f][1,2,4]트리아진-5-카르복실레이트 (1.3 g, 3.4 mmol) 및 아세트산나트륨 (3.8 g, 45.9 mmol)의 혼합물을 수소 분위기 (풍선 압력) 하에 실온에서 교반하였다. 2.5시간 후, 생성된 혼합물을 셀라이트의 패드를 통해 여과하고, 여과물을 감압 하에 증발시켰다. 조 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 80 g 칼럼)에 의해 정제하여 에틸 2-클로로피롤로[2,1-f][1,2,4]트리아진-5-카르복실레이트 (470 mg, 2.1 mmol, 61% 수율)을 황색 고체로서 수득하였다.
MS (ESI) m/z: 226.1 [M+H]+;
1H NMR (600 MHz, CDCl3) δ 9.46 (s, 1H), 7.77 (d, J=2.6 Hz, 1H), 7.45 (d, J=2.8 Hz, 1H), 4.43 (d, J=7.2 Hz, 2H), 1.44 (t, J=7.1 Hz, 3H).
실시예 123. 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)피롤로[2,1-f][1,2,4]트리아진-5-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 에틸 2-클로로피롤로[2,1-f][1,2,4]트리아진-5-카르복실레이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 535.9 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 9.19 (br s, 1H), 7.57-7.69 (m, 4H), 7.04 (br s, 1H), 5.87 (s, 1H), 3.75-3.96 (m, 2H), 2.34 (m, 3H), 1.56 (br s, 4H), 1.17-1.27 (m, 2H), 1.09-1.17 (m, 2H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 40 nM.
실시예 124
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-2-메틸니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-클로로-2-메틸니코티네이트로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 510.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.90 (br d, J=9.00 Hz, 1H), 7.64-7.72 (m, 2H), 7.54-7.63 (m, 1H), 6.65 (br d, J=8.92 Hz, 1H), 5.76-5.97 (m, 1H), 3.78-3.96 (m, 2H), 3.34 (br s, 1H), 2.55 (m, 3H), 2.33 (br s, 3H), 1.52 (br s, 4H), 1.10-1.25 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 78 nM.
실시예 125
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인다졸-3-카르복실산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 메틸 6-브로모-1-메틸-3a,7a-디히드로-1H-인다졸-3-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 549.0 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.19-8.31 (m, 1H), 7.95 (d, J=1.38 Hz, 1H), 7.53-7.70 (m, 3H), 7.49 (d, J=9.35 Hz, 1H), 5.97 (s, 1H), 4.53 (s, 3H), 3.52-3.85 (m, 5H), 2.61 (s, 2H), 2.36 (s, 1H), 1.97-2.22 (m, 5H), 1.09-1.51 (m, 5H); FXR EC50 = 96 nM.
실시예 126
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-3-(트리플루오로메틸)이미다조[1,5-a]피리딘-1-카르복실산
단계 1. 에틸 2-(5-브로모피리딘-2-일)-2-(히드록시이미노)아세테이트
물 (0.5 mL) 중 아질산나트륨 (28.3 mg, 0.41 mmol)을 0℃에서 AcOH (0.5 mL) 중 에틸 2-(5-브로모피리딘-2-일)아세테이트 (100 mg, 0.41 mmol)의 혼합물에 첨가하였다. 반응 혼합물을 실온에서 1시간 동안 교반하고, 물 (0.5 mL)을 첨가하였다. 교반을 1시간 동안 유지하였고, 반응 혼합물을 1M 수성 K2HPO4을 사용하여 pH 8-9로 염기성화시켰다. 수성 층을 EtOAc로 추출하고, 유기 층을 MgSO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 생성물을 직접 후속 단계에 사용하였다.
단계 2. 에틸 6-브로모-3-(트리플루오로메틸)이미다조[1,5-a]피리딘-1-카르복실레이트
에틸 2-(5-브로모피리딘-2-일)-2-(히드록시이미노)아세테이트 (4.5 g, 16.5 mmol)를 THF (50 mL) 중에 현탁시켰다. TFA (6.2 mL)를 첨가하고, 이어서 아연 분진 (2.2 g, 33.0 mmol)을 조금씩 첨가하였다. 트리플루오로아세트산 무수물 (4.7 mL, 33.0 mmol)을 첨가하고, 반응 혼합물을 1시간 동안 교반하였다. 혼합물을 셀라이트를 통해 여과하고, 진공 하에 농축시켰다. 피리딘 (25 mL)을 잔류물에 첨가하고, 이어서 트리플루오로아세트산 무수물 (4.7 mL, 33.0 mmol)을 천천히 첨가하였다. 1시간 후, 반응 혼합물을 진공 하에 농축시키고, SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 80 g 칼럼)에 의해 정제하여 에틸 6-브로모-3-(트리플루오로메틸) 이미다조[1,5-a]피리딘-1-카르복실레이트 (5 g, 14.8 mmol, 90% 수율)을 황색 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.38 (s, 1H), 8.24 (dd, J=9.7, 0.9 Hz, 1H), 7.36 (dd, J=9.6, 1.4 Hz, 1H), 4.50 (q, J=7.3 Hz, 2H), 1.46 (t, J=7.2 Hz, 3H).
실시예 126. 6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-3-(트리플루오로메틸)이미다조[1,5-a]피리딘-1-카르복실산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 에틸 6-브로모-3-(트리플루오로메틸)이미다조[1,5-a]피리딘-1-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 603.2 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.11-8.18 (m, 1H), 7.61 (s, 1H), 7.50-7.59 (m, 3H), 7.46 (dd, J=1.79, 10.04 Hz, 1H), 5.85 (s, 1H), 3.06 (ddd, J=3.30, 8.60, 12.04 Hz, 2H), 2.43 (s, 2H), 2.33 (s, 1H), 2.06 (s, 1H), 1.59-1.91 (m, 4H), 1.05-1.37 (m, 5H); FXR EC50 = 102 nM.
실시예 127
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-3-메틸이미다조[1,5-a]피리딘-1-카르복실산
단계 1. 메틸 6-브로모-3-메틸이미다조[1,5-a]피리딘-1-카르복실레이트
탄산칼륨 (0.14 g, 0.98 mmol)을 DMF (0.78 mL) 중 6-브로모-3-메틸이미다조[1,5-a]피리딘-1-카르복실산 (0.1 g, 0.39 mmol)의 용액에 첨가하였다. 5분 후, 아이오도메탄 (0.04 mL, 0.59 mmol)을 농후한 슬러리에 첨가하고, 반응 혼합물을 실온에서 밤새 교반하였다. 반응 혼합물을 Et2O 및 물로 희석하였다. 유기 층을 염수로 세척하고, 합한 수성 층을 Et2O로 역추출하였다. 합한 유기 추출물을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 적합한 순도의 백색 결정을 수득하여 후속 단계로 보냈다.
1H NMR (400 MHz, CDCl3) δ 8.08 (dd, J=9.6, 1.0 Hz, 1H), 8.00-7.97 (m, 1H), 7.14 (dd, J=9.7, 1.5 Hz, 1H), 3.98 (s, 3H), 2.70 (s, 3H).
실시예 127. 6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-3-메틸이미다조[1,5-a]피리딘-1-카르복실산
표제 화합물을, 에틸 6-브로모-3-(트리플루오로메틸) 이미다조[1,5-a]피리딘-1-카르복실레이트를 메틸 6-브로모-3-메틸이미다조[1,5-a] 피리딘-1-카르복실레이트로 대체하여, 실시예 126의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 549.2 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 7.96-8.14 (m, 1H), 7.41-7.70 (m, 5H), 5.86 (s, 1H), 3.35-3.49 (m, 2H), 3.13 (ddd, J=3.58, 8.73, 12.17 Hz, 2H), 2.86 (s, 3H), 2.44 (s, 2H), 2.25-2.37 (m, 1H), 2.06 (s, 2H), 1.66-1.90 (m, 4H); FXR EC50 = 267 nM.
실시예 128
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인돌-2-카르복실산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 메틸 6-브로모-1-메틸-1H-인돌-2-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 548.2 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.10-8.23 (m, 1H), 8.04 (d, J=8.53 Hz, 1H), 7.93 (d, J=9.35 Hz, 1H), 7.44-7.67 (m, 3H), 7.18 (d, J=2.20 Hz, 1H), 5.85 (s, 1H), 4.87 (s, 3H), 3.48 (br dd, J=5.09, 11.97 Hz, 2H), 3.33 (br s, 2H), 3.04-3.25 (m, 2H), 2.42 (s, 2H), 2.18-2.35 (m, 1H), 1.61-1.97 (m, 4H), 1.04-1.36 (m, 4H); FXR EC50 = 287 nM.
실시예 129
7-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)이소퀴놀린-3-카르복실산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 메틸 7-클로로이소퀴놀린-3-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 546.3 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 9.19-8.84 (m, 1H), 8.66-8.34 (m, 1H), 8.05-7.69 (m, 1H), 7.66-7.50 (m, 1H), 7.49-7.29 (m, 3H), 5.78 (s, 1H), 3.52 (br d, J=2.6 Hz, 3H), 3.39-3.21 (m, 2H), 2.99 (s, 1H), 2.47-2.32 (m, 2H), 2.26-2.10 (m, 1H), 1.78 (br s, 4H), 1.38-1.23 (m, 2H), 1.22-1.09 (m, 2H); FXR EC50 = 341 nM.
실시예 130
2-((7-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-2-일)옥시)아세트산
단계 1. tert-부틸 2-((7-브로모퀴녹살린-2-일)옥시)아세테이트
탄산칼륨 (0.10 g, 0.75 mmol)을 아세톤 (5 mL) 중 7-브로모퀴녹살린-2-올 (11 g, 0.5 mmol)의 실온 용액에 첨가하였다. 5 분 후, tert-부틸 2-브로모아세테이트 (0.15 g, 0.75 mmol)를 첨가하고, 반응 혼합물을 25℃에서 밤새 교반하였다. 포화 수성 NH4Cl (20 mL)을 첨가하고, 생성된 혼합물을 Et2O (3 x 10 mL)로 추출하였다. 합한 유기 층을 MgSO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 조 생성물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 40 g 칼럼)에 의해 정제하여 tert-부틸 2-((7-브로모퀴녹살린-2-일)옥시)아세테이트 (26 mg, 0.07 mmol, 15% 수율)을 수득하였다.
MS (ESI) m/z: 340.9 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.48-8.67 (m, 1H), 7.98 (d, J=1.98 Hz, 1H), 7.91 (d, J=8.80 Hz, 1H), 7.68 (dd, J=2.20, 8.80 Hz, 1H), 4.94 (s, 2H), 1.51 (s, 9H).
실시예 130. 2-((7-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-2-일)옥시)아세트산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 tert-부틸 2-((7-브로모퀴녹살린-2-일)옥시)아세테이트로 대체하고, tert-부틸 에스테르를 LiOH 대신에 TFA로 가수분해시키며, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 577.0 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.37 (s, 1H), 7.90 (d, J=9.02 Hz, 1H), 7.48-7.61 (m, 4H), 7.37 (d, J=2.64 Hz, 1H), 5.88 (s, 1H), 5.08 (s, 2H), 3.50-3.65 (m, 2H), 3.39 (dt, J=4.29, 8.53 Hz, 2H), 2.48 (s, 2H), 2.34 (s, 1H), 1.76-1.96 (m, 4H), 1.16-1.30 (m, 4H); FXR EC50 = 373 nM.
실시예 131
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-((2-(트리메틸실릴)에톡시)메틸)-1H-인돌-3-카르복실산
단계 1. 메틸 6-브로모-1-((2-(트리메틸실릴)에톡시)메틸)-1H-인돌-3-카르복실레이트
수소화나트륨 (48.0 mg, 1.2 mmol)을 THF (50 mL) 중 메틸 6-브로모-1H-인돌-3-카르복실레이트 (0.25 g, 1.0 mmol)의 실온 용액에 첨가하였다. 15분 동안 교반한 후, SEM-Cl (0.21 mL, 1.2 mmol)을 첨가하고, 생성된 현탁액을 25℃에서 밤새 교반하였다. 물 (50 mL)을 반응 혼합물에 첨가하여 점착성 침전물을 제공하였다. 용매를 가만히 따르고, 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-30% EtOAc/헥산, 이스코 24 g 칼럼)에 의해 정제하여 메틸 6-브로모-1-((2-(트리메틸실릴)에톡시)메틸)-1H-인돌-3-카르복실레이트 (0.36 g, 0.83 mmol)를 검으로서 수득하였다.
MS (ESI) m/z: 384.0 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.06 (d, J=8.53 Hz, 1H), 7.86 (s, 1H), 7.72 (d, J=1.65 Hz, 1H), 7.43 (dd, J=1.65, 8.53 Hz, 1H), 5.48 (s, 2H), 4.80 (s, 1H), 3.94 (s, 3H), 1.29 (br t, J=7.15 Hz, 3H), -0.23-0.22 (m, 11H).
실시예 131. 6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-((2-(트리메틸실릴)에톡시)메틸)-1H-인돌-3-카르복실산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 메틸 6-브로모-1-((2-(트리메틸실릴)에톡시)메틸)-1H-인돌-3-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 664.2 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.10-8.23 (m, 1H), 8.04 (d, J=8.53 Hz, 1H), 7.93 (d, J=9.35 Hz, 1H), 7.44-7.67 (m, 3H), 7.18 (d, J=2.20 Hz, 1H), 5.85 (s, 1H), 4.87 (s, 3H), 3.48 (br dd, J=5.09, 11.97 Hz, 2H), 3.33 (br s, 2H), 3.04-3.25 (m, 2H), 2.42 (s, 2H), 2.18-2.35 (m, 1H), 1.61-1.97 (m, 4H), 1.04-1.36 (m, 4H); FXR EC50 = 445 nM.
실시예 132
7-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-8-메틸퀴놀린-3-카르복실산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 메틸 7-브로모-8-메틸퀴놀린-3-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 560.0 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 9.11-9.45 (m, 2H), 8.14 (d, J=9.08 Hz, 1H), 7.76 (d, J=9.08 Hz, 1H), 7.42-7.65 (m, 3H), 5.83-6.00 (m, 1H), 3.35-3.45 (m, 2H), 3.10-3.30 (m, 2H), 2.66 (s, 3H), 2.48 (s, 2H), 2.34 (s, 1H), 1.66-1.94 (m, 4H), 1.18-1.43 (m, 4H); FXR EC50 = 958 nM.
실시예 133
3-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인다졸-6-카르복실산
표제 화합물을, 메틸 6-클로로-1-메틸-1H-피롤로[2,3-b]피리딘-3-카르복실레이트를 메틸 3-브로모-1-메틸-1H-인다졸-6-카르복실레이트로 대체하여, 실시예 7의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 549.0 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.19-8.31 (m, 1H), 7.95 (d, J=1.38 Hz, 1H), 7.53-7.70 (m, 3H), 7.49 (d, J=9.35 Hz, 1H), 5.97 (s, 1H), 4.53 (s, 3H), 3.52-3.85 (m, 5H), 2.61 (s, 2H), 2.36 (s, 1H), 1.97-2.22 (m, 5H), 1.09-1.51 (m, 5H); FXR EC50 = 1175 nM.
실시예 134
3-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인다졸-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 133의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 549.1 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.07-8.17 (m, 1H), 7.86-7.96 (m, 1H), 7.72-7.85 (m, 3H), 7.69 (br d, J=8.80 Hz, 1H), 7.52 (d, J=6.88 Hz, 1H), 5.74 (s, 1H), 3.95 (s, 3H), 3.43-3.71 (m, 4H), 3.12-3.28 (m, 2H), 2.41 (s, 2H), 2.31 (s, 1H), 1.58-1.97 (m, 5H), 1.06-1.33 (m, 5H); FXR EC50 = 3314 nM.
실시예 135
2-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)피롤로[2,1-f][1,2,4]트리아진-5-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 123의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 536.1 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 9.00-9.33 (m, 2H), 8.10 (d, J=9.46 Hz, 1H), 7.87 (d, J=1.76 Hz, 1H), 7.67-7.83 (m, 3H), 7.51 (dd, J=1.65, 7.15 Hz, 1H), 7.14 (d, J=2.20 Hz, 1H), 5.73 (s, 1H), 3.76-4.07 (m, 2H), 3.58 (br dd, J=6.05, 13.75 Hz, 2H), 2.46 (s, 2H), 2.31 (s, 1H), 2.05 (s, 1H), 1.76 (t, J=5.61 Hz, 4H), 1.10-1.38 (m, 5H); FXR EC50 = 87 nM.
실시예 136
2-(2-(3-(2-클로로-6-플루오로페닐)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-클로로-6-플루오로벤즈알데히드로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 554.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.18 (d, J = 1.5 Hz, 1H), 7.68-7.61 (m, 1H), 7.58 (d, J = 11.5 Hz, 1H), 7.53 (d, J = 8.2 Hz, 1H), 7.42 (t, J = 8.7 Hz, 1H), 5.93 (s, 1H), 3.54-3.45 (m, 2H), 2.40 (s, 2H), 2.33 (dt, J = 3.4, 8.3 Hz, 1H), 1.65 (q, J = 4.8, 5.3 Hz, 4H), 1.25-1.08 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 37 nM.
실시예 137
2-(2-(5-시클로프로필-3-(2,6-디플루오로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2,6-디플루오로벤즈알데히드로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 538.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.20 (br s, 1H), 7.75-7.50 (m, 2H), 7.33 (t, J = 8.1 Hz, 2H), 6.02 (s, 1H), 3.79-3.67 (m, 2H), 2.47 (s, 2H), 2.38-2.27 (m, 1H), 1.71-1.65 (m, 1H), 1.18 (dtd, J = 3.6, 6.5, 29.1 Hz, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 155 nM.
실시예 138
2-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 571.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.92 (d, J = 4.8 Hz, 1H), 8.17 (d, J = 1.5 Hz, 1H), 8.12 (d, J = 7.9 Hz, 1H), 7.87 (dd, J = 4.8, 7.9 Hz, 1H), 7.57 (dd, J = 1.5, 11.4 Hz, 1H), 5.83 (s, 1H), 3.69 (br s, 2H), 3.54-3.40 (m, 2H), 2.38-2.26 (m, 3H), 1.64-1.57 (m, 4H), 1.28-1.06 (m, 4H); FXR EC50 = 319 nM.
실시예 139
2-(2-(5-시클로프로필-3-(4-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 4-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 1의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 571.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 9.01 (d, J = 5.2 Hz, 1H), 8.79 (s, 1H), 8.14 (d, J = 1.6 Hz, 1H), 7.94 (d, J = 5.2 Hz, 1H), 7.61-7.51 (m, 1H), 5.84 (s, 1H), 3.76-3.65 (m, 2H), 2.33 (s, 2H), 2.32-2.26 (m, 1H), 1.63 (br s, 4H), 1.25-1.08 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 482 nM.
실시예 140
2-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴놀린-6-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메톡시)벤즈알데히드로 대체하여, 실시예 122의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 562.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.30 (s, 1H), 8.09 (d, J=9.34 Hz, 1H), 7.88-8.05 (m, 1H), 7.68 (br t, J=7.70 Hz, 1H), 7.49-7.57 (m, 4H), 7.25 (br d, J=9.34 Hz, 1H), 5.79-6.01 (m, 1H), 3.95 (br d, J=12.79 Hz, 2H), 3.75 (br s, 2H), 3.43-3.64 (m, 1H), 2.40 (s, 2H), 2.21-2.37 (m, 1H), 1.57 (br s, 4H), 1.12-1.27 (m, 4H); FXR EC50 = 133 nM.
실시예 141
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인돌-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 8의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 548.1 [M+H]+; H NMR (400 MHz, 메탄올-d4) δ 8.27 (d, J=8.58 Hz, 1H), 8.12 (s, 1H), 7.89-7.96 (m, 1H), 7.87 (d, J=1.98 Hz, 1H), 7.75-7.82 (m, 2H), 7.51-7.58 (m, 1H), 7.46 (dd, J=2.20, 8.80 Hz, 1H), 5.55-6.26 (m, 1H), 3.95 (s, 3H), 3.59-3.82 (m, 4H), 2.59 (s, 2H), 2.34 (s, 1H), 2.01-2.21 (m, 5H), 1.01-1.45 (m, 4H); FXR EC50 = 142 nM.
실시예 142
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(2-히드록시에톡시)퀴놀린-2-카르복실산
단계 1. 메틸 6-브로모-4-(2-히드록시에톡시)퀴놀린-2-카르복실레이트
아세토니트릴 (15 mL) 중 메틸 6-브로모-4-히드록시퀴놀린-2-카르복실레이트 (0.25 g, 0.87 mmol), 2-브로모에탄-1-올 (0.19 mL, 2.7 mmol) 및 탄산칼륨 (0.37 g, 2.7 mmol)을 80℃로 가열하였다. 16시간 후, 추가의 2-브로모에탄-1-올 (0.19 mL, 2.7 mmol)을 첨가하였다. 16시간 후, 반응 혼합물을 물 (25 mL)로 희석하고, 에틸 아세테이트 (2 x 25 mL)로 추출하였다. 유기 층을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 실리카 겔 크로마토그래피를 이용하여 정제하여 메틸 6-브로모-4-(2-히드록시에톡시)퀴놀린-2-카르복실레이트 (0.25 g, 0.78 mmol, 88% 수율)을 단리하였다.
1H NMR (400 MHz, DMSO-d6) δ 8.51 (d, J=2.2 Hz, 1H), 8.06-8.01 (m, 1H), 8.00-7.93 (m, 1H), 7.58 (s, 1H), 4.48 (s, 1H), 4.35 (t, J=4.5 Hz, 2H), 3.95 (s, 3H), 3.91-3.84 (m, 2H).
실시예 142. 6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(2-히드록시에톡시)퀴놀린-2-카르복실산
표제 화합물을, 에틸 6-클로로-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트를 메틸 6-브로모-4-(2-히드록시에톡시)퀴놀린-2-카르복실레이트로 대체하여, 실시예 85의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 606.2 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.74 (s, 2H), 8.13 (d, J=9.63 Hz, 1H), 7.83-7.93 (m, 1H), 7.73 (s, 1H), 7.56-7.65 (m, 1H), 5.89-5.97 (m, 1H), 4.52-4.66 (m, 2H), 4.11 (br d, J=3.85 Hz, 2H), 3.66 (s, 2H), 3.41 (s, 2H), 2.50 (s, 2H), 2.30-2.38 (m, 1H), 1.73-1.91 (m, 4H), 1.28-1.55 (m, 4H); FXR EC50 = 147 nM.
실시예 143
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(2-히드록시에톡시)퀴놀린-2-카르복실산
표제 화합물을, 3,5-디클로로이소니코틴알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 142의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 606.2 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 7.84-7.99 (m, 2H), 7.76 (t, J=8.12 Hz, 2H), 7.48-7.58 (m, 4H), 5.65-5.90 (m, 1H), 4.36 (t, J=4.54 Hz, 2H), 3.97-4.14 (m, 2H), 3.42-3.48 (m, 2H), 3.12-3.19 (m, 2H), 2.39 (s, 2H), 2.24-2.36 (m, 1H), 1.63-1.89 (m, 4H), 1.00-1.33 (m, 4H); FXR EC50 = 159 nM.
실시예 144
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메톡시퀴놀린-2-카르복실산
표제 화합물을, 3,5-디클로로이소니코틴알데히드를 2-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 108의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 577.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.88 (d, J = 4.7 Hz, 1H), 8.13-7.96 (m, 2H), 7.85 (dd, J = 4.7, 7.9 Hz, 1H), 7.67 (br s, 1H), 7.49 (s, 1H), 7.22 (br s, 1H), 5.76 (s, 1H), 4.08 (s, 3H), 3.42 (br s, 2H), 3.13 (br s, 2H), 2.29 (br s, 3H), 1.59 (br s, 4H), 1.23-1.05 (m, 4H); FXR EC50 = 156 nM.
실시예 145
6-(2-(3-(3-클로로피리딘-2-일)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메톡시퀴놀린-2-카르복실산
표제 화합물을, 3,5-디클로로이소니코틴알데히드를 3-클로로피콜린알데히드로 대체하여, 실시예 108의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 543.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.69 (d, J = 4.6 Hz, 1H), 8.15 (d, J = 8.2 Hz, 1H), 7.95 (d, J = 9.4 Hz, 1H), 7.68 (dd, J = 2.8, 9.4 Hz, 1H), 7.63 (dd, J = 4.7, 8.3 Hz, 1H), 7.47 (s, 1H), 7.26 (d, J = 2.7 Hz, 1H), 5.87 (s, 1H), 4.09 (s, 3H), 3.18 (br t, J = 9.4 Hz, 2H), 2.34 (br s, 3H), 1.74-1.59 (m, 4H), 1.24-1.09 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 160 nM.
실시예 146
6-(2-(5-시클로프로필-3-(4-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메톡시퀴놀린-2-카르복실산
표제 화합물을, 3,5-디클로로이소니코틴알데히드를 4-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 108의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 577.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 9.02 (d, J = 5.2 Hz, 1H), 8.82 (s, 1H), 8.02-7.87 (m, 2H), 7.63 (dd, J = 2.8, 9.4 Hz, 1H), 7.46 (s, 1H), 7.27 (d, J = 2.8 Hz, 1H), 5.83 (s, 1H), 4.08 (s, 3H), 2.32 (br s, 3H), 1.71-1.59 (m, 4H), δ 1.25-1.08 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 185 nM.
실시예 147
6-(2-(3-시클로헥실-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메톡시퀴놀린-2-카르복실산
표제 화합물을, 3,5-디클로로이소니코틴알데히드를 시클로헥산카르브알데히드로 대체하여, 실시예 108의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 514.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.97 (d, J = 9.2 Hz, 1H), 7.78-7.68 (m, 1H), 7.49 (s, 1H), 7.33 (d, J = 2.8 Hz, 1H), 6.41 (s, 1H), 4.12 (s, 3H), 3.58-3.66 (m, 2H), 3.34-3.26 (m, 2H), 2.73 (br s, 3H), 2.24-2.17 (m, 1H), 2.00-1.62 (m, 8H), 1.48-1.18 (m, 6H), 1.11-0.95 (m, 4H); FXR EC50 = 1063 nM.
실시예 148
7-(2-(3-(2,6-디클로로페닐)-5-이소프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 신놀린-3-카르복실산
표제 화합물을, 시클로프로필아세틸렌을 이소프로필아세틸렌으로 대체하여, 실시예 53의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 549.1 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.52 (br dd, J=4.8, 1.3 Hz, 1H), 7.85-7.74 (m, 1H), 7.72-7.62 (m, 1H), 7.62-7.52 (m, 1H), 7.49-7.37 (m, 2H), 7.37-7.28 (m, 1H), 5.77 (s, 1H), 3.69-3.58 (m, 1H), 3.46-3.37 (m, 1H), 3.37-3.25 (m, 2H), 2.59 (s, 2H), 2.35 (s, 1H), 1.78 (br s, 4H), 1.43 (br d, J=6.9 Hz, 6H); FXR EC50 = 548 nM.
실시예 149
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 3,5-디클로로이소니코틴알데히드로 대체하여, 실시예 20의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 547.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.86 (s, 2H), 8.18 (d, J=8.5 Hz, 1H), 7.94 (dd, J=12.7, 9.0 Hz, 2H), 7.75-7.57 (m, 1H), 7.21 (br d, J=1.5 Hz, 1H), 6.00 (s, 1H), 3.63-3.46 (m, 2H), 3.00 (s, 1H), 2.40 (s, 2H), 2.39-2.31 (m, 1H), 1.79-1.61 (m, 4H), 1.31-1.21 (m, 4H), 1.17 (br d, J=2.6 Hz, 2H); FXR EC50 = 205 nM.
실시예 150
6-(2-(3-(3-클로로피리딘-4-일)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴놀린-2-카르복실산
표제 화합물을, Pd-촉매된 부흐발트 커플링 단계 동안 하나의 염소를 환원시켜 실시예 149의 제조 동안 소량의 단리물로서 수득하였다.
MS (ESI) m/z: 513.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.84 (s, 1H), 8.69 (br d, J=4.9 Hz, 1H), 8.20 (br d, J=8.4 Hz, 1H), 7.94 (br dd, J=12.1, 9.0 Hz, 2H), 7.68 (br d, J=6.9 Hz, 1H), 7.60 (d, J=4.8 Hz, 1H), 7.22 (br s, 1H), 7.14 (br s, 2H), 6.01 (s, 1H), 3.65-3.44 (m, 3H), 2.46-2.39 (m, 2H), 2.39-2.27 (m, 2H), 1.80-1.61 (m, 3H), 1.28-1.17 (m, 2H), 1.19-1.09 (m, 2H); FXR EC50 = 4345 nM.
실시예 151
6-(2-(5-시클로프로필-3-(2,6-디플루오로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2,6-디플루오로벤즈알데히드로 대체하여, 실시예 20의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 514.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.22 (d, J = 8.6 Hz, 1H), 7.95 (dd, J = 9.0, 13.8 Hz, 2H), 7.74-7.63 (m, 2H), 7.33 (t, J = 8.1 Hz, 2H), 7.23 (d, J = 2.6 Hz, 1H), 6.00 (s, 1H), 3.59-3.51 (m, 2H), 3.22 (dd, J = 12.1, 22.7 Hz, 2H), 2.46 (s, 2H), 2.35 (ddd, J = 5.2, 8.5, 13.2 Hz, 1H), 1.80-1.60 (m, 4H), 1.28-1.09 (m, 4H); FXR EC50 = 1991 nM.
실시예 152
6-(2-(3-(3-클로로피리딘-2-일)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 3-클로로피콜린알데히드로 대체하여, 실시예 20의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 513.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.68 (br d, J=4.0 Hz, 1H), 8.21 (br s, 1H), 8.13 (br d, J=8.0 Hz, 1H), 7.95 (br s, 1H), 7.68 (br d, J=5.7 Hz, 1H), 7.62 (dd, J=8.0, 4.6 Hz, 1H), 7.22 (br s, 1H), 5.91 (br s, 1H), 3.51 (br s, 1H), 3.26 (br d, J=5.7 Hz, 2H), 2.41-2.25 (m, 3H), 1.69 (br s, 4H), 1.20 (br d, J=7.7 Hz, 2H), 1.14 (br d, J=2.0 Hz, 2H) DMSO 신호 하에 추가의 피크 소실; FXR EC50 = 1633 nM.
실시예 153
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 20의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 547.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.89 (d, J = 4.8 Hz, 1H), 8.19 (d, J = 8.6 Hz, 1H), 8.09 (d, J = 7.9 Hz, 1H), 7.94 (d, J = 8.7 Hz, 2H), 7.85 (dd, J = 4.8, 7.9 Hz, 1H), 7.65 (d, J = 9.4 Hz, 1H), 7.17 (s, 1H), 5.78 (s, 1H), 3.52-3.42 (m, 2H), 3.20-3.12 (m, 2H), 2.29 (br s, 3H), 1.67-1.53 (m, 4H), 1.26-1.06 (m, 4H); FXR EC50 = 1282 nM.
실시예 154
6-(2-(5-시클로프로필-3-(4-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 4-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 20의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 547.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 9.03 (d, J = 5.1 Hz, 1H), 8.85 (s, 1H), 8.18 (d, J = 8.6 Hz, 1H), 7.99-7.88 (m, 3H), 7.66 (dd, J = 2.5, 9.4 Hz, 1H), 7.19 (d, J = 2.7 Hz, 1H), 5.82 (s, 1H), 3.22-3.16 (m, 2H), 2.36-2.19 (m, 3H), 1.70-1.58 (m, 4H), 1.24-1.11 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 554 nM.
실시예 155
6-(2-(5-시클로프로필-3-(2,6-디클로로-4-플루오로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2,6-디클로로-4-플루오로벤즈알데히드로 대체하여, 실시예 20의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 564.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 1H NMR 실험; FXR EC50 = 523 nM 중 8.20 (br d, J=8.5 Hz, 1H), 7.96 (br t, J=9.6 Hz, 2H), 7.77 (d, J=8.5 Hz, 2H), 7.69 (br d, J=9.8 Hz, 1H), 7.22 (br s, 1H), 5.93 (s, 1H), 3.91 (s, 1H), 3.54 (br d, J=8.2 Hz, 1H), 3.35-3.07 (m, 2H), 2.42-2.28 (m, 3H), 1.81-1.61 (m, 4H), 1.22 (br d, J=7.9 Hz, 2H), 1.15 (br d, J=2.7 Hz, 2H) 물 억제로 인해 추가의 신호 소실.
실시예 156
6-(2-(3-(2-클로로-6-플루오로페닐)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-클로로-6-플루오로벤즈알데히드로 대체하여, 실시예 20의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 530.4 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.20 (d, J = 8.6 Hz, 1H), 7.95 (dd, J = 9.0, 15.1 Hz, 2H), 7.66 (q, J = 7.4, 10.2 Hz, 2H), 7.55 (d, J = 8.1 Hz, 1H), 7.45 (t, J = 8.7 Hz, 1H), 7.22 (s, 1H), 5.92 (s, 1H), 3.57-3.48 (m, 2H), 3.21 (br s, 2H), 2.40 (s, 2H), 2.39-2.28 (m, 1H), 1.76-1.60 (m, 4H), 1.26-1.08 (m, 4H); FXR EC50 = 326 nM.
실시예 157
6-(2-(3-(2-클로로-6-메틸페닐)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-클로로-6-메틸벤즈알데히드로 대체하여, 실시예 20의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 526.4 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.21 (d, J = 8.7 Hz, 1H), 8.01-7.88 (m, 2H), 7.68 (d, J = 9.4 Hz, 1H), 7.47-7.41 (m, 2H), 7.35 (t, J = 4.5 Hz, 1H), 7.21 (s, 1H), 5.76 (s, 1H), 3.24-3.14(m, 2H), 2.35 (q, J = 12.5 Hz, 3H), 2.10 (s, 3H), 1.72-1.58 (m, 4H), 1.25-1.08 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 223 nM.
실시예 158
7-(2-(3-(2-클로로-6-플루오로페닐)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)이소퀴놀린-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-클로로-6-플루오로벤즈알데히드로 대체하여, 실시예 129의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 530.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 9.09 (s, 1H), 8.40 (s, 1H), 7.96 (d, J = 9.1 Hz, 1H), 7.73-7.59 (m, 2H), 7.54 (d, J = 8.2 Hz, 1H), 7.50-7.36 (m, 2H), 5.91 (s, 1H), 3.28-3.20 (m, 2H), 2.40 (s, 2H), 2.34 (tt, J = 5.0, 8.2 Hz, 1H), 1.73-1.59 (m, 4H), 1.27-1.09 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 459 nM.
실시예 159
7-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)이소퀴놀린-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 129의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 546.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 9.09 (s, 1H), 8.39 (s, 1H), 7.93 (dd, J=13.4, 8.4 Hz, 2H), 7.85-7.73 (m, 2H), 7.66 (dd, J=9.2, 2.3 Hz, 1H), 7.56 (d, J=7.3 Hz, 1H), 7.39 (d, J=1.7 Hz, 1H), 5.78 (s, 1H), 3.52 (br dd, J=12.6, 5.2 Hz, 2H), 2.36-2.20 (m, 3H), 1.75-1.56 (m, 4H), 1.26-1.17 (m, 2H), 1.16-1.08 (m, 2H), 1.02 (d, J=6.2 Hz, 1H) 물 억제로 인해 추가의 양성자 신호가 소실됨; FXR EC50 = 254 nM.
실시예 160
7-(2-(5-시클로프로필-3-(4-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)이소퀴놀린-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 4-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 129의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 547.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 9.08 (s, 1H), 9.03 (d, J = 5.2 Hz, 1H), 8.85 (s, 1H), 8.38 (s, 1H), 7.97 (d, J = 5.2 Hz, 1H), 7.94 (d, J = 9.2 Hz, 1H), 7.70-7.64 (m, 1H), 7.39 (s, 1H), 5.82 (s, 1H), 3.26-3.18 (m, 2H), 2.37-2.29 (m, 3H), 1.72-1.57 (m, 4H), 1.25-1.10 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 1608 nM.
실시예 161
7-(2-(3-(3-클로로피리딘-2-일)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 이소퀴놀린-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 4-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 129의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 513.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 9.10 (s, 1H), 8.69 (br d, J=4.6 Hz, 1H), 8.40 (s, 1H), 8.15 (br d, J=7.9 Hz, 1H), 7.96 (br d, J=9.2 Hz, 1H), 7.69 (br d, J=8.2 Hz, 1H), 7.63 (dd, J=8.2, 4.6 Hz, 1H), 7.41 (s, 1H), 5.88 (s, 1H), 3.67-3.41 (m, 1H), 3.37-3.12 (m, 2H), 2.41-2.22 (m, 3H), 1.81-1.55 (m, 5H), 1.21 (br d, J=7.9 Hz, 2H), 1.14 (br d, J=2.4 Hz, 2H); FXR EC50 = 2324 nM.
실시예 162
7-(2-(5-시클로프로필-3-(2,6-디플루오로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)이소퀴놀린-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2,6-디플루오로벤즈알데히드로 대체하여, 실시예 129의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 514.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 9.10 (s, 1H), 8.41 (s, 1H), 7.96 (d, J = 9.1 Hz, 1H), 7.70 (q, J = 6.7, 7.3 Hz, 2H), 7.42 (s, 1H), 7.33 (t, J = 8.2 Hz, 2H), 6.00 (s, 1H), 3.61-3.53 (m, 2H), 3.29-3.21 (m, 2H), 2.46 (s, 2H), 2.39-2.28 (m, 1H), 1.77-1.57 (m, 4H), 1.28-1.08 (m, 4H); FXR EC50 = 2824 nM.
실시예 163
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)니코틴산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 116의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 564.4 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.63 (s, 1H), 7.92 (br d, J=7.93 Hz, 1H), 7.79 (br dd, J=7.63, 11.90 Hz, 2H), 7.56 (br d, J=7.02 Hz, 1H), 7.02 (s, 1H), 5.75 (s, 1H), 3.72-4.11 (m, 2H), 2.55 (s, 2H), 2.29 (s, 1H), 1.41-1.64 (m, 4H), 1.15-1.24 (m, 2H), 1.11 (br d, J=2.44 Hz, 2H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 344 nM.
실시예 164
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인다졸-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 125의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 549.1 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.27 (d, J=8.58 Hz, 1H), 8.12 (s, 1H), 7.89-7.96 (m, 1H), 7.87 (d, J=1.98 Hz, 1H), 7.75-7.82 (m, 2H), 7.51-7.58 (m, 1H), 7.46 (dd, J=2.20, 8.80 Hz, 1H), 5.55-6.26 (m, 1H), 3.95 (s, 3H), 3.59-3.82 (m, 4H), 2.59 (s, 2H), 2.34 (s, 1H), 2.01-2.21 (m, 5H), 1.01-1.45 (m, 4H); FXR EC50 = 392 nM.
실시예 165
6-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인다졸-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메톡시)벤즈알데히드로 대체하여, 실시예 125의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 565.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.74-7.67 (m, 1H), 7.65 (br d, J=9.2 Hz, 1H), 7.62-7.47 (m, 4H), 7.38 (br d, J=8.5 Hz, 1H), 5.95 (s, 1H), 4.09 (s, 3H), 3.27 (br d, J=4.6 Hz, 1H), 3.03 (br s, 1H), 2.41 (s, 2H), 2.37-2.27 (m, 1H), 1.82-1.64 (m, 4H), 1.24 (s, 2H), 1.21-1.15 (m, 2H), 1.12 (br d, J=2.4 Hz, 2H); FXR EC50 = 2975 nM.
실시예 166
6-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-3-(트리플루오로메틸)이미다조[1,5-a]피리딘-1-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메톡시)벤즈알데히드로 대체하여, 실시예 126의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 619.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.04 (d, J=9.77 Hz, 1H), 7.70 (s, 1H), 7.47-7.61 (m, 5H), 5.82-5.99 (m, 1H), 3.20-3.50 (m, 2H), 3.00 (br s, 2H), 2.39 (s, 2H), 2.23-2.35 (m, 1H), 1.56-1.86 (m, 4H), 1.05-1.33 (m, 4H); FXR EC50 = 494 nM.
실시예 167
6-(2-(3-시클로헥실-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-에톡시퀴놀린-2-카르복실산
표제 화합물을, 2-(트리플루오로메틸)벤즈알데히드를 시클로헥산카르브알데히드로 대체하여, 실시예 72의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 528.4 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.99 (d, J = 9.3 Hz, 1H), 7.76 (d, J = 9.2 Hz, 1H), 7.48 (s, 1H), 7.34 (d, J = 2.8 Hz, 1H), 6.41 (s, 1H), 4.41 (q, J = 6.9 Hz, 2H), 3.66-3.55 (m, 2H), 3.33-3.23 (m, 2H), 2.73 (br s, 3H), 2.24-2.16 (m, 1H), 1.17-1.61(m, 8H), 1.51 (t, J = 6.9 Hz, 3H), 1.47-1.16 (m, 6H), 1.11-0.94 (m, 4H); FXR EC50 = 3096 nM.
실시예 168
6-(2-(3-시클로헥실-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인돌-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 시클로헥산카르브알데히드로 대체하여, 실시예 8의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 486.4 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.94 (d, J = 7.4 Hz, 2H), 7.31 br (s, 1H), 7.19 (br s, 1H), 6.43 (s, 1H), 3.83 (s, 3H), 3.50 (br s, 2H), 2.77-2.69 (m, 3H), 2.20 (tt, J = 5.1, 8.7 Hz, 1H), 2.04-1.64 (m, 8H), 1.52-1.19 (m, 6H), 1.12-0.94 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 3972 nM.
실시예 169
2-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-6-메틸피리미딘-4-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 120의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 511.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.92 (br d, J=7.63 Hz, 1H), 7.70-7.87 (m, 2H), 7.56 (br d, J=7.32 Hz, 1H), 6.82 (s, 1H), 5.64-5.92 (m, 1H), 3.97 (br d, J=13.12 Hz, 2H), 2.55 (m, 2H), 2.28 (s, 3H), 1.91 (s, 1H), 1.47 (br s, 4H), 1.15-1.26 (m, 2H), 1.11 (br d, J=2.14 Hz, 2H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 1300 nM.
실시예 170
7-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-8-메틸퀴놀린-3-카르복실산
표제 화합물을, 2,6-디클로로벤즈알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 132의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 560.0 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.10-8.23 (m, 1H), 8.04 (d, J=8.53 Hz, 1H), 7.93 (d, J=9.35 Hz, 1H), 7.44-7.67 (m, 3H), 7.18 (d, J=2.20 Hz, 1H), 5.85 (s, 1H), 4.87 (s, 3H), 3.48 (br dd, J=5.09, 11.97 Hz, 2H), 3.33 (br s, 2H), 3.04-3.25 (m, 2H), 2.42 (s, 2H), 2.18-2.35 (m, 1H), 1.61-1.97 (m, 4H), 1.04-1.36 (m, 4H); FXR EC50 = 1747 nM.
실시예 171
6-(2-(3-(3-클로로피리딘-2-일)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)니코틴산
표제 화합물을, 2,6-디클로로벤즈알데히드를 3-클로로피콜린알데히드로 대체하여, 실시예 2의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 463.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.68 (d, J=4.6 Hz, 1H), 8.58 (d, J=1.5 Hz, 1H), 8.13 (d, J=8.2 Hz, 1H), 7.89 (dd, J=9.2, 1.8 Hz, 1H), 7.62 (dd, J=8.2, 4.9 Hz, 1H), 6.82 (d, J=9.2 Hz, 1H), 5.86 (s, 1H), 3.88-3.76 (m, 1H), 3.45-3.33 (m, 1H), 3.27 (dd, J=10.5, 6.0 Hz, 1H), 3.21-3.11 (m, 1H), 2.41-2.24 (m, 3H), 1.53 (br t, J=5.2 Hz, 4H), 1.29-1.16 (m, 2H), 1.16-1.08 (m, 2H), 1.01 (d, J=6.1 Hz, 1H); FXR EC50 = 1871 nM.
실시예 172
5-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-피롤로[2,3-c]피리딘-2-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 에틸 5-클로로-1-메틸-1H-피롤로[2,3-c]피리딘-2-카르복실레이트로 대체하여, 실시예 17의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 565.9 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.46 (s, 1H), 7.66-7.77 (m, 1H), 7.47-7.64 (m, 3H), 6.78 (s, 1H), 6.62 (s, 1H), 5.91 (s, 1H), 4.02 (s, 3H), 3.52-3.68 (m, 2H), 3.15 (br d, J=9.16 Hz, 2H), 2.38 (m, 3H), 1.52-1.78 (m, 4H), 1.09-1.37 (m, 4H); FXR EC50 = 2366 nM.
실시예 173
3-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-피라졸로[4,3-b]피리딘-6-카르복실산
표제 화합물을, 메틸 6-브로모-4-에톡시퀴놀린-2-카르복실레이트를 메틸 3-브로모-1-메틸-1H-피라졸로[4,3-b]피리딘-6-카르복실레이트로 대체하여, 실시예 113의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 566.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.78 (s, 1H), 8.40 (s, 1H), 7.65-7.74 (m, 2H), 7.40-7.63 (m, 3H), 5.91 (s, 1H), 3.83-3.84 (m, 2H), 3.88 (s, 3H), 2.36-2.44 (m, 2H), 2.32 (br s, 1H), 1.59-1.77 (m, 4H), 1.15-1.23 (m, 2H), 1.11 (br d, J=2.44 Hz, 2H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 2791 nM.
실시예 174
5-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인다졸-3-카르복실산
표제 화합물을, 실시예 100의 제조에 대하여 일반적 방법 D에 기재된 조건 하에서의 5-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인다졸-3-카르보니트릴의 가수분해를 통해 수득하였다.
MS (ESI) m/z: 565.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.67-7.76 (m, 1H), 7.65 (br d, J=9.16 Hz, 1H), 7.48-7.61 (m, 3H), 7.38 (br d, J=8.54 Hz, 1H), 7.02-7.31 (m, 1H), 5.95 (s, 1H), 3.27 (br d, J=4.58 Hz, 2H), 3.03 (br s, 2H), 2.55 (s, 3H), 2.37-2.45 (m, 2H), 2.33 (br s, 1H), 1.59-1.89 (m, 4H), 1.05-1.21 (m, 4H); FXR EC50 = 236 nM.
실시예 175
6-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인다졸-3-카르보니트릴
디옥산 (154 μL) 중 5-시클로프로필-4-(7-아자스피로[3.5]논-1-엔-2-일)-3-(2-(트리플루오로메톡시)페닐)이속사졸 (18 mg, 0.046 mmol), 6-브로모-1-메틸-1H-인다졸-3-카르보니트릴 (16.3 mg, 0.069 mmol) 및 Cs2CO3 (30.0 mg, 0.092 mmol)의 슬러리를 5분 동안 혼합물을 통해 질소를 버블링시킴으로써 탈기시켰다. 클로로(2-디시클로헥실포스피노-2',6'-디이소프로폭시-1,1'-비페닐)[2-(2'-아미노-1,1'-비페닐)]팔라듐(II) (RuPhos-Pd-G2) (1.791 mg, 2.305 μmol)을 첨가하고, 반응 혼합물을 밀봉하고, 90℃로 가열하였다. 24시간 후, 메탄올 2 mL를 첨가하고, 고체를 여과하고, 여과물을 하기 조건으로 정제용 LC/MS를 통해 정제하였다: 칼럼: 엑스브리지 C18, 19 x 200 mm, 5-μm 입자; 이동상 A: 5:95 아세토니트릴: 물, 0.1% 트리플루오로아세트산 포함; 이동상 B: 95:5 아세토니트릴: 물, 0.1% 트리플루오로아세트산 포함; 구배: 25분에 걸쳐 35-75% B, 이어서 100% B에서 5-분 유지; 유량: 20 mL/분. 목적 생성물을 함유하는 분획을 합하고, 건조시켜 6-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인다졸-3-카르보니트릴 (11.1 mg, 0.019 mmol, 42% 수율)을 수득하였다.
MS (ESI) m/z: 545.9 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.63-7.80 (m, 4H), 7.48-7.62 (m, 3H), 7.32 (br d, J=9.77 Hz, 1H), 6.85 (s, 1H), 5.80-6.18 (m, 1H), 4.23 (s, 3H), 3.19-3.51 (m, 2H), 3.04 (br t, J=9.16 Hz, 2H), 2.35-2.42 (m, 2H), 2.31 (br s, 1H), 1.54-1.81 (m, 4H), 1.03-1.33 (m, 4H); FXR EC50 = 3244 nM.
실시예 176
6-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인다졸-3-카르복실산
표제 화합물을, 실시예 100의 제조에 대하여 일반적 방법 D에 기재된 조건 하에서의 6-(2-(5-시클로프로필-3-(2-(트리플루오로메톡시)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인다졸-3-카르보니트릴 (실시예 175)의 가수분해를 통해 수득하였다.
MS (ESI) m/z: 565.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.82 (br d, J=8.85 Hz, 1H), 7.64-7.75 (m, 1H), 7.49-7.62 (m, 4H), 7.08 (br d, J=8.54 Hz, 1H), 6.94 (br s, 1H), 5.80-6.02 (m, 1H), 4.01 (br s, 3H), 3.08 (br t, J=9.16 Hz, 2H), 2.39 (s, 2H), 2.22-2.35 (m, 1H), 1.59-1.74 (m, 4H), 1.18 (br d, J=7.93 Hz, 2H), 1.11 (br d, J=2.14 Hz, 2H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 2975 nM.
실시예 177
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일) 티아졸로[4,5-b]피리딘-6-카르복실산
단계 1. 4-(7-(6-브로모티아졸로[4,5-b]피리딘-2-일)-7-아자스피로[3.5]논-1-엔-2-일)-5-시클로프로필-3-(2,6-디클로로페닐)이속사졸
탄산세슘 (83 mg, 0.26 mmol)을 DMA (0.25 mL) 중 5-시클로프로필-3-(2,6-디클로로페닐)-4-(7-아자스피로[3.5]논-1-엔-2-일)이속사졸 (50 mg, 0.102 mmol, 일반적 방법 A에 기재된 합성) 및 6-브로모-2-클로로티아졸로[4,5-b]피리딘 (38.2 mg, 0.15 mmol)의 실온 용액에 첨가하였다. 반응 혼합물을 50℃로 4시간 동안 가열하고, 조 반응 혼합물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 12g 칼럼)에 의해 정제하여 4-(7-(6-브로모티아졸로[4,5-b]피리딘-2-일)-7-아자스피로[3.5]논-1-엔-2-일)-5-시클로프로필-3-(2,6-디클로로페닐)이속사졸 (51 mg, 0.082 mmol, 81% 수율)을 수득하였다.
1H NMR (500 MHz, CDCl3) δ 8.40 (d, J=2.20 Hz, 1H), 7.93 (d, J=1.93 Hz, 1H), 7.41-7.50 (m, 2H), 7.33-7.39 (m, 1H), 5.78 (s, 1H), 3.68-3.94 (m, 2H), 3.40-3.63 (m, 2H), 2.42 (s, 2H), 2.14-2.28 (m, 1H), 1.67-1.85 (m, 5H), 1.28-1.39 (m, 3H), 1.10-1.22 (m, 2H).
단계 2. 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)티아졸로[4,5-b]피리딘-6-카르보니트릴
4-(7-(6-브로모티아졸로[4,5-b]피리딘-2-일)-7-아자스피로[3.5]논-1-엔-2-일)-5-시클로프로필-3-(2,6-디클로로페닐)이속사졸 (30 mg, 0.051 mmol), Xantphos (5.9 mg, 10.2 μmol), Pd2(dba)3 (9.3 mg, 10.2 μmol), 및 시안화아연 (6.0 mg, 0.051 mmol)을 함유하는 마이크로웨이브 바이알을 질소로 3회 퍼징한 다음, 무수 DMF (0.5 mL)를 첨가하였다. 반응 혼합물을 마이크로웨이브 조사 하에 110℃에서 1.5시간 동안 가열하였다. 반응 혼합물을 EtOAc로 희석하고, 염수로 세척하였다. 유기 층을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축 건조시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 12g 칼럼)에 의해 정제하여 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)티아졸로[4,5-b]피리딘-6-카르보니트릴 (15.5 mg, 0.028 mmol, 54% 수율)을 검으로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.54-8.79 (m, 1H), 7.87-8.19 (m, 1H), 7.42-7.49 (m, 2H), 7.29-7.41 (m, 2H), 5.71-5.87 (m, 1H), 3.75-4.02 (m, 2H), 3.63 (br d, J=3.96 Hz, 2H), 2.44 (s, 2H), 2.12-2.36 (m, 2H), 1.79 (t, J=5.72 Hz, 4H), 1.62 (br s, 3H), 1.29-1.38 (m, 2H), 1.09-1.25 (m, 3H), 0.88 (dd, J=3.30, 7.92 Hz, 1H).
실시예 177. 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)티아졸로[4,5-b]피리딘-6-카르복실산
표제 화합물을, 실시예 100의 제조에 대하여 일반적 방법 D에 기재된 조건 하에서의 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)티아졸로[4,5-b]피리딘-6-카르보니트릴의 가수분해를 통해 수득하였다.
MS (ESI) m/z: 552.9 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.93 (d, J=1.76 Hz, 1H), 8.81 (d, J=1.76 Hz, 1H), 7.45-7.70 (m, 4H), 5.87 (s, 1H), 3.58-4.43 (m, 5H), 2.52 (s, 2H), 2.33 (s, 1H), 1.83 (t, J=5.72 Hz, 4H), 1.10-1.43 (m, 5H); FXR EC50 = 121 nM.
실시예 178
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-2-카르복실산
단계 1. 6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-2-카르보니트릴
디옥산 중 5-시클로프로필-4-(7-아자스피로[3.5]논-1-엔-2-일)-3-(2-(트리플루오로메틸)페닐)이속사졸 (30 mg, 0.08 mmol, 일반적 방법 A에 기재된 합성), 6-클로로퀴녹살린-2-카르보니트릴 (18.7 mg, 0.10 mmol) 및 Cs2CO3 (52.2 mg, 0.16 mmol)의 슬러리 (0.40 mL)를 5분 동안 혼합물을 통해 질소를 버블링시킴으로써 탈기시켰다. 이어서, 클로로(2-디시클로헥실포스피노-2',6'-디이소프로폭시-1,1'-비페닐)[2-(2'-아미노-1,1'-비페닐)]팔라듐(II) (RuPhos-Pd-G2) (3.11 mg, 4.01 μmol)을 첨가하고, 반응 혼합물을 밀봉하고, 90℃로 6시간 동안 가열하였다. 조 혼합물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 12g 칼럼)에 의해 직접 정제하여 6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-2-카르보니트릴 (31 mg, 0.056 mmol, 70% 수율)을 검으로서 수득하였다.
MS (ESI) m/z: 528.1 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.83 (s, 1H), 7.89 (d, J=9.7 Hz, 1H), 7.84-7.77 (m, 1H), 7.68-7.60 (m, 2H), 7.58 (dd, J=9.6, 2.8 Hz, 1H), 7.44 (dd, J=7.0, 1.8 Hz, 1H), 7.18 (d, J=2.9 Hz, 1H), 5.63 (s, 1H), 3.61 (dt, J=13.4, 5.0 Hz, 2H), 3.38 (ddd, J=13.0, 8.1, 4.4 Hz, 2H), 2.39 (s, 2H), 2.15 (tt, J=8.4, 5.1 Hz, 1H), 1.80-1.69 (m, 4H), 1.32-1.26 (m, 2H), 1.19-1.12 (m, 2H).
실시예 178. 6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-2-카르복실산
표제 화합물을, 실시예 100의 제조에 대하여 일반적 방법 D에 기재된 조건 하에서의 6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)퀴녹살린-2-카르보니트릴의 가수분해를 통해 수득하였다.
MS (ESI) m/z: 547.1 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 9.45 (s, 1H), 7.93 (d, J=9.35 Hz, 1H), 7.82 (br d, J=7.43 Hz, 1H), 7.55-7.74 (m, 3H), 7.39-7.55 (m, 1H), 7.31 (d, J=1.93 Hz, 1H), 5.65 (s, 1H), 3.51-3.66 (m, 2H), 3.31-3.51 (m, 2H), 2.41 (s, 2H), 1.98-2.20 (m, 1H), 1.62-1.81 (m, 4H), 1.24-1.37 (m, 2H), 1.09-1.24 (m, 2H); FXR EC50 = 172 nM.
일반적 방법 E
실시예 179
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-N-(시클로프로필술포닐)-4-플루오로벤조[d]티아졸-6-카르복스아미드
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (실시예 1, 15 mg, 0.03 mmol, 일반적 방법 A에 기재된 합성)을, 교반용 자석이 구비된 5 mL 둥근 바닥 플라스크 내 THF (0.26 mL) 중에 질소 하에 용해시켰다. CDI (12.8 mg, 0.08 mmol)를 첨가하고, 혼합물을 60℃에서 1시간 동안 가열한 후, 시클로프로판술폰아미드 (12.7 mg, 0.10 mmol) 및 DBU (11.9 μL, 0.08 mmol)를 첨가하였다. 반응 혼합물을 실온에서 6시간 동안 교반하였다. 조 혼합물을 하기 조건으로 정제용 LC/MS를 통해 정제하였다: 칼럼: 엑스브리지 C18, 19 x 200 mm, 5-μm 입자; 이동상 A: 5:95 아세토니트릴: 물, 0.1% TFA 포함; 이동상 B: 95:5 아세토니트릴: 물, 0.1% TFA 포함; 구배 포함: 20분에 걸쳐 5-100% B, 이어서 100% B에서 유지; 유량: 20 mL/분. 목적 생성물을 함유하는 분획을 합하고, 건조시켜 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐) 이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-N-(시클로프로필술포닐)-4-플루오로벤조[d]티아졸-6-카르복스아미드 (12.0 mg, 0.02 mmol, 64% 수율)을 수득하였다.
MS (ESI) m/z: 673.0 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.11 (d, J=1.54 Hz, 1H), 7.65 (dd, J=1.43, 11.99 Hz, 1H), 7.36 (d, J=1.76 Hz, 1H), 7.34 (d, J=0.66 Hz, 1H), 7.30 (s, 1H), 5.69 (s, 1H), 3.64-3.74 (m, 2H), 3.27-3.35 (m, 2H), 2.06-2.18 (s, 2H), 1.88-1.93 (m, 2H), 1.04-1.16 (m, 4H), 0.64-0.92 (m, 8H); FXR EC50 = 13 nM.
실시예 180
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로-N-(메틸술포닐)벤조[d]티아졸-6-카르복스아미드
표제 화합물을, 시클로프로판술폰아미드를 메탄술폰아미드로 대체하여, 실시예 179의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 646.9 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.11 (s, 1H), 7.67 (s, 2H), 7.54-7.65 (m, 2H), 6.94-7.35 (m, 1H), 5.91 (s, 1H), 2.90 (s, 2H), 2.55 (s, 3H), 2.28-2.44 (s, 2H), 1.92 (m, 1H), 1.60-1.71 (m, 4H), 1.22 (br d, J=7.93 Hz, 2H), 1.12-1.18 (m, 2H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 35 nM.
실시예 181
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-N-(시클로프로필술포닐)-4-플루오로벤조[d]티아졸-6-카르복스아미드
표제 화합물을, 2,6-디클로로벤즈알데히드를 3,5-디클로로이소니코틴알데히드로 대체하여, 실시예 179의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 674.0 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.68 (br s, 1H), 8.66 (s, 2H), 7.92 (d, J=1.38 Hz, 1H), 7.53 (dd, J=1.24, 10.87 Hz, 1H), 5.84 (s, 1H), 3.71-3.94 (m, 2H), 3.58 (ddd, J=4.54, 7.84, 12.93 Hz, 2H), 2.47 (s, 2H), 2.07-2.30 (m, 2H), 1.73-1.88 (m, 4H), 1.47 (dd, J=1.93, 4.68 Hz, 2H), 1.34 (dd, J=2.34, 4.81 Hz, 2H), 1.10-1.29 (m, 4H); FXR EC50 = 60 nM.
실시예 182
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로-N-(메틸술포닐)벤조[d]티아졸-6-카르복스아미드
표제 화합물을, 시클로프로판술폰아미드를 메탄술폰아미드로 대체하여, 실시예 181의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 648.0 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.65 (s, 2H), 8.03 (d, J=9.24 Hz, 1H), 7.61 (s, 2H), 7.40 (d, J=2.64 Hz, 1H), 5.86 (s, 1H), 4.16 (s, 3H), 3.44-3.59 (m, 2H), 3.12-3.37 (m, 2H), 2.45 (s, 2H), 1.82 (br d, J=2.42 Hz, 7H), 1.13-1.44 (m, 8H), 0.91 (s, 3H); FXR EC50 = 688 nM.
실시예 183
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-N-(시클로프로필술포닐)-4-(트리플루오로메틸)퀴놀린-2-카르복스아미드
표제 화합물을, 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (실시예 1)를 6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산 (실시예 85)로 대체하여, 실시예 179의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 718.2 [M+H]+;
1H NMR (400 MHz, 아세톤-d6) δ 8.62-8.83 (m, 1H), 8.43 (br d, J=1.76 Hz, 1H), 8.11 (br dd, J=1.87, 8.69 Hz, 1H), 7.88 (s, 2H), 7.32-7.69 (m, 2H), 3.89-4.29 (m, 2H), 3.47-3.80 (m, 2H), 2.38-2.62 (m, 2H), 2.13-2.28 (m, 1H), 1.65-1.78 (m, 1H), 0.95-1.34 (m, 5H); FXR EC50 = 55 nM.
실시예 184
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-N-(메틸술포닐)-4-(트리플루오로메틸)퀴놀린-2-카르복스아미드
표제 화합물을, 시클로프로판술폰아미드를 메탄술폰아미드로 대체하여, 실시예 183의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 691.1 [M+H]+;
1H NMR (400 MHz, 아세톤-d6) δ 8.62-8.83 (m, 1H), 8.43 (br d, J=1.76 Hz, 1H), 8.11 (br dd, J=1.87, 8.69 Hz, 1H), 7.88 (s, 2H), 7.32-7.69 (m, 2H), 3.89-4.29 (m, 2H), 3.47-3.80 (m, 2H), 2.38-2.62 (m, 2H), 2.13-2.28 (m, 1H), 1.65-1.78 (m, 1H), 0.95-1.34 (m, 5H); FXR EC50 = 73 nM; 마우스 생체내 (3 mg/kg, @ 6h): Cyp7a1 = -99%, Fgf15 = +28x.
실시예 185
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(디플루오로메톡시)-N-(메틸술포닐)퀴놀린-2-카르복스아미드
표제 화합물을, 에틸 6-클로로-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트를 메틸 6-브로모-4-(디플루오로메톡시)퀴놀린-2-카르복실레이트로 대체하여, 실시예 184의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 690.0 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.75 (br s, 2H), 8.14 (br d, J=8.53 Hz, 1H), 7.83 (br s, 2H), 7.10-7.65 (m, 2H), 5.81-6.14 (m, 1H), 3.67 (br d, J=5.50 Hz, 2H), 3.42 (br s, 2H), 2.68 (br s, 2H), 2.54 (br s, 3H), 2.23-2.48 (m, 1H), 1.70-1.93 (m, 4H), 1.11-1.56 (m, 4H); FXR EC50 = 16 nM.
실시예 186
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(디플루오로메톡시)-N-(메틸술포닐)퀴놀린-2-카르복스아미드
표제 화합물을, 3,5-디클로로이소니코틴알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 185의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 689.0 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.03 (d, J=9.35 Hz, 1H), 7.88 (s, 1H), 7.67-7.81 (m, 4H), 7.51 (d, J=7.15 Hz, 1H), 7.20-7.49 (m, 1H), 7.32 (d, J=2.75 Hz, 1H), 5.73 (s, 1H), 3.50-3.68 (m, 1H), 3.23-3.32 (m, 2H), 2.42 (s, 2H), 2.31 (s, 1H), 2.05 (s, 3H), 1.67-1.87 (m, 4H), 1.14-1.29 (m, 4H); FXR EC50 = 13 nM.
실시예 187
6-(2-(5-시클로프로필-3-(4-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(디플루오로메톡시)-N-(메틸술포닐)퀴놀린-2-카르복스아미드
표제 화합물을, 3,5-디클로로이소니코틴알데히드를 4-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 185의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 690.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.93 (d, J = 4.7 Hz, 1H), 8.15 (d, J = 7.9 Hz, 1H), 8.02 (d, J = 9.4 Hz, 1H), 7.89 (dd, J = 4.8, 7.9 Hz, 1H), 7.86-7.55 (m, 3H), 7.15 (d, J = 2.7 Hz, 1H), 3.35 (s, 3H), 3.29-3.21 (m, 2H), 2.38-2.28 (m, 3H).1.66 (q, J = 7.1, 7.7 Hz, 4H), 1.25-1.08 (m, 4H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 63 nM.
실시예 188
6-(2-(5-시클로프로필-3-(4-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-N-(시클로프로필술포닐)-4-(디플루오로메톡시)퀴놀린-2-카르복스아미드
표제 화합물을, 메탄술폰아미드를 시클로프로판술폰아미드로 대체하여, 실시예 187의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 716.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.92 (d, J = 4.6 Hz, 1H), 8.13 (d, J = 7.9 Hz, 1H), 8.02 (d, J = 9.4 Hz, 1H), 7.88 (dd, J = 4.7, 8.0 Hz, 1H), 7.84-7.49 (m, 3H), 7.15 (d, J = 2.7 Hz, 1H), 5.82 (s, 1H), 3.38-3.19 (m, 2H), 3.14-3.06 (m, 1H), 2.36-2.28 (m, 3H), 1.70-1.59 (m, 4H), 1.25-1.01 (m, 8H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 43 nM.
실시예 189
6-(2-(3-(3-클로로피리딘-2-일)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-N-(시클로프로필술포닐)-4-(디플루오로메톡시)퀴놀린-2-카르복스아미드
표제 화합물을, 4-(트리플루오로메틸)니코틴알데히드를 3-클로로피콜린알데히드로 대체하여, 실시예 188의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 682.0 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.68 (d, J = 4.6 Hz, 1H), 8.14 (d, J = 8.2 Hz, 1H), 7.98 (d, J = 9.2 Hz, 1H), 7.84-7.45 (m, 4H), 7.15 (s, 1H), 5.88 (s, 1H), 3.26-3.16 (m, 2H), 3.04 (br s, 1H), 2.38-2.28 (m, 3H), 1.73-1.61 (m, 4H), 1.26-0.87 (m, 8H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 48 nM.
실시예 190
6-(2-(3-(3-클로로피리딘-2-일)-5-시클로프로필이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(디플루오로메톡시)-N-(메틸술포닐)퀴놀린-2-카르복스아미드
표제 화합물을, 시클로프로판술폰아미드를 메탄술폰아미드로 대체하여, 실시예 189의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 655.8 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.69 (d, J = 4.6 Hz, 1H), 8.15 (d, J = 8.2 Hz, 1H), 8.02 (d, J = 9.5 Hz, 1H), 7.90-7.55 (m, 4H), 7.16 (d, J = 2.7 Hz, 1H), 5.89 (s, 1H), 3.61-3.53 (m, 2H), 3.38 (s, 3H), 3.30-3.22 (m, 2H), 2.39-2.29 (m, 3H), 1.74-1.61 (m, 4H), 1.23-1.10 (m, 4H); FXR EC50 = 168 nM.
실시예 191
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-N-(시클로프로필술포닐)-4-(디플루오로메톡시)퀴놀린-2-카르복스아미드
표제 화합물을, 4-(트리플루오로메틸)니코틴알데히드를 2-(트리플루오로메틸)니코틴알데히드로 대체하여, 실시예 188의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 716.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 9.04 (d, J = 5.2 Hz, 1H), 8.87 (s, 1H), 8.04-7.96 (m, 2H), 7.88-7.54 (m, 3H), 7.15 (d, J = 2.7 Hz, 1H), 5.83 (s, 1H), 3.27-3.18 (m, 2H), 3.09 (dq, J = 3.6, 4.2, 8.1 Hz, 1H), 2.39-2.29 (m, 3H), 1.73-1.58 (m, 4H), 1.26-0.97 (m, 8H), 물 신호 억제로 인해 추가의 신호 사라짐; FXR EC50 = 140 nM.
실시예 192
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)피리딘-3-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(디플루오로메톡시)-N-(메틸술포닐)퀴놀린-2-카르복스아미드
표제 화합물을, 시클로프로판술폰아미드를 메탄술폰아미드로 대체하여, 실시예 191의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 690.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 9.03 (d, J = 5.2 Hz, 1H), 8.84 (s, 1H), 8.01-7.90 (m, 2H), 7.77-7.42 (m, 3H), 7.13 (d, J = 2.7 Hz, 1H), 5.81 (d, J = 2.4 Hz, 1H), 3.51-3.40 (m, 2H), 3.19-3.09 (m, 2H), 2.96 (s, 3H), 2.39-2.27 (m, 3H), 1.74-1.57 (m, 4H), 1.26-1.07 (m, 4H); FXR EC50 = 238 nM.
실시예 193
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-N-(시클로프로필술포닐)퀴놀린-2-카르복스아미드
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-브로모퀴놀린-2-카르복실레이트로 대체하여, 실시예 179의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 649.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.26 (d, J=8.58 Hz, 1H), 7.94-8.05 (m, 2H), 7.73 (br d, J=9.51 Hz, 1H), 7.65-7.69 (m, 2H), 7.60 (dd, J=7.24, 8.92 Hz, 1H), 7.18-7.33 (m, 1H), 5.76-6.04 (m, 1H), 3.55 (br d, J=12.79 Hz, 2H), 2.55 (s, 2H), 2.27-2.41 (m, 2H), 1.56-1.74 (m, 4H), 1.05-1.27 (m, 8H) 물 신호 억제로 인해 추가의 신호 사라짐;; FXR EC50 = 178 nM.
실시예 194
6-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-N-(메틸술포닐)퀴놀린-2-카르복스아미드
표제 화합물을, 시클로프로판술폰아미드를 메탄술폰아미드로 대체하여, 실시예 193의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 623.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.28 (d, J=8.54 Hz, 1H), 7.94-8.07 (m, 2H), 7.75 (dd, J=2.14, 9.46 Hz, 1H), 7.65-7.71 (m, 2H), 7.57-7.64 (m, 1H), 7.26 (d, J=2.14 Hz, 1H), 5.88 (s, 1H), 3.47-3.69 (m, 2H), 3.06-3.39 (m, 2H), 2.56 (s, 3H), 2.37 (m, 3H), 1.53-1.84 (m, 4H), 0.93-1.29 (m, 4H); FXR EC50 = 255 nM.
실시예 195
6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메톡시-N-(메틸술포닐)퀴놀린-2-카르복스아미드
표제 화합물을, 에틸 6-클로로-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트를 메틸 6-브로모-4-메톡시퀴놀린-2-카르복실레이트로 대체하여, 실시예 184의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 653.9 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.73 (s, 2H), 8.15 (d, J=9.35 Hz, 1H), 7.83-7.98 (m, 1H), 7.77 (s, 1H), 7.65-7.74 (m, 1H), 5.85-6.07 (m, 1H), 4.28 (s, 3H), 3.59-3.80 (m, 2H), 3.47 (br d, J=13.20 Hz, 2H), 3.39 (s, 3H), 2.54 (s, 2H), 2.34 (s, 1H), 1.74-2.02 (m, 4H), 1.19-1.32 (m, 4H); FXR EC50 = 75 nM.
실시예 196
6-(2-(5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메톡시-N-(메틸술포닐)퀴놀린-2-카르복스아미드
표제 화합물을, 3,5-디클로로이소니코틴알데히드를 2-(트리플루오로메틸)벤즈알데히드로 대체하여, 실시예 195의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 653.1 [M+H]+;
1H NMR (500 MHz, 메탄올-d4) δ 8.08 (d, J=9.35 Hz, 1H), 7.89 (br d, J=7.15 Hz, 1H), 7.69-7.83 (m, 4H), 7.42-7.57 (m, 2H), 5.63-5.98 (m, 1H), 4.24 (s, 3H), 3.51-3.63 (m, 2H), 3.33-3.38 (m, 2H), 3.35 (s, 3H), 2.44 (s, 2H), 2.31 (m, 1H), 1.79 (m, 4H), 1.21 (m, 4H); FXR EC50 = 155 nM.
실시예 197
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로-N-술파모일벤조[d]티아졸-6-카르복스아미드
표제 화합물을, 시클로프로판술폰아미드를 황산 디아미드로 대체하여, 실시예 181의 제조에 대하여 일반적 방법 E에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 649.0 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.58 (s, 2H), 7.92 (s, 1H), 7.53 (br d, J=11.28 Hz, 1H), 5.77 (s, 1H), 3.66-3.84 (m, 2H), 3.44-3.59 (m, 2H), 2.40 (s, 2H), 2.07-2.21 (m, 1H), 1.72 (br s, 4H), 1.21-1.34 (m, 2H), 1.16 (br d, J=6.05 Hz, 2H); FXR EC50 = 381 nM.
일반적 방법 F
실시예 198
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로-N-메틸벤조[d]티아졸-6-카르복스아미드
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (15 mg, 0.03 mmol)을 DCE (1 mL) 중에 용해시켰다. 2,4,6-트리프로필-1,3,5,2,4,6-트리옥사트리포스피난 2,4,6-트리옥시드 (T3P) (0.03 mL, 0.05 mmol)에 이어서 메틸아민 (1.6 mg, 0.05 mmol) 및 피리딘 (6.4 μL, 0.08 mmol)을 반응 혼합물에 첨가하고, 생성된 용액을 실온에서 6시간 동안 교반하였다. 조 반응 혼합물을 직접 정제된 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 12 g 칼럼)에 의해 직접 정제하여 2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로-N-메틸벤조[d]티아졸-6-카르복스아미드 (10 mg, 0.016 mmol, 62% 수율)을 백색 고체로서 수득하였다.
MS (ESI) m/z: 584.0 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.63 (s, 2H), 7.85 (d, J=1.54 Hz, 1H), 7.38 (dd, J=1.54, 11.22 Hz, 1H), 6.04 (br d, J=4.62 Hz, 1H), 5.81 (s, 1H), 3.65-3.88 (m, 2H), 3.42-3.60 (m, 2H), 3.01 (d, J=4.84 Hz, 3H), 2.44 (s, 2H), 2.06-2.24 (m, 1H), 1.66-1.89 (m, 4H), 1.32 (dd, J=2.53, 4.95 Hz, 2H), 1.07-1.21 (m, 2H); FXR EC50 = 311 nM.
실시예 199
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로-N-이소프로필벤조[d]티아졸-6-카르복스아미드
표제 화합물을, 메틸아민를 이소프로필아민로 대체하여, 실시예 198의 제조에 대하여 일반적 방법 F에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 612.0 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.63 (s, 2H), 7.76-7.95 (m, 1H), 7.38 (d, J=11.22 Hz, 1H), 5.81 (s, 1H), 4.29 (m, 2H), 3.64-3.93 (m, 2H), 3.53 (m, 1H), 2.44 (s, 2H), 2.18 (s, 1H), 1.73-1.94 (m, 4H), 1.32 (m, 2H), 1.26 (d, J=6.60 Hz, 6H), 1.20 (m, 2H); FXR EC50 = 431 nM.
실시예 200
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-N-에틸-4-플루오로벤조[d]티아졸-6-카르복스아미드
표제 화합물을, 메틸아민를 에틸아민로 대체하여, 실시예 198의 제조에 대하여 일반적 방법 F에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 598.0 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.56 (s, 2H), 7.78 (d, J=1.76 Hz, 1H), 7.33 (dd, J=1.54, 11.22 Hz, 1H), 6.02 (s, 1H), 5.74 (s, 1H), 3.60-3.80 (m, 2H), 3.30-3.56 (m, 5H), 2.37 (s, 2H), 1.98-2.21 (m, 2H), 1.45-1.77 (m, 7H), 0.74-1.33 (m, 13H); FXR EC50 = 68 nM.
실시예 201
N-시클로프로필-2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복스아미드
표제 화합물을, 메틸아민를 시클로프로필아민로 대체하여, 실시예 198의 제조에 대하여 일반적 방법 F에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 610.0 [M+H]+;
1H NMR (400 MHz, 클로로포름-d) δ 8.63 (s, 2H), 7.83 (d, J=1.54 Hz, 1H), 7.36 (dd, J=1.54, 11.22 Hz, 1H), 6.20 (br d, J=2.64 Hz, 1H), 3.76 (td, J=5.06, 13.20 Hz, 2H), 3.45-3.64 (m, 2H), 2.89 (dt, J=3.30, 6.93 Hz, 1H), 2.44 (s, 2H), 2.18 (tt, J=5.03, 8.39 Hz, 1H), 1.69-1.81 (m, 4H), 1.31 (dd, J=2.53, 4.95 Hz, 2H), 1.13-1.24 (m, 2H), 0.87 (br d, J=5.50 Hz, 2H), 0.55-0.69 (m, 2H); FXR EC50 = 150 nM.
실시예 202
2-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복스아미드
표제 화합물을, 메틸아민를 염화암모늄로 대체하여, 실시예 198의 제조에 대하여 일반적 방법 F에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 570.0 [M+H]+;
1H NMR (400 MHz, 메탄올-d4) δ 8.63 (s, 2H), 7.92 (d, J=1.76 Hz, 1H), 7.50 (dd, J=1.54, 11.66 Hz, 1H), 5.72-5.99 (m, 1H), 3.72 (br d, J=13.64 Hz, 2H), 3.43-3.57 (m, 2H), 2.41 (s, 2H), 2.18-2.28 (m, 1H), 1.60-1.79 (m, 4H), 1.08-1.17 (m, 4H); FXR EC50 = 155 nM.
실시예 203
에틸 6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트
디옥산 중 5-시클로프로필-3-(3,5-디클로로피리딘-4-일)-4-(7-아자스피로[3.5]논-1-엔-2-일)이속사졸 (0.1 g, 0.27 mmol, 일반적 방법 A에 기재된 합성), 에틸 6-클로로-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트 (0.097 g, 0.32 mmol) 및 Cs2CO3 (0.17 g, 0.53 mmol)의 슬러리 (1.8 mL)를 5분 동안 혼합물을 통해 질소를 버블링시킴으로써 탈기시켰다. 이어서, 클로로(2-디시클로헥실포스피노-2',6'-디이소프로폭시-1,1'-비페닐)[2-(2'-아미노-1,1'-비페닐)]팔라듐(II) (RuPhos-Pd-G2) (10.3 mg, 0.013 mmol)을 첨가하고, 반응 혼합물을 밀봉하고, 70℃로 가열하였다. 3시간 동안 가열한 후, 반응 혼합물을 EtOAc, 여과된으로 희석하고, 여과물을 진공 하에 농축시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-80% EtOAc/헥산, 이스코 40 g 칼럼)에 의해 정제하여 에틸 6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트 (61.7 mg, 0.095 mmol, 36% 수율)을 적색 고체로서 수득하였다.
MS (ESI) m/z: 643.1 [M+H]+;
1H NMR (400 MHz, CDCl3) δ 8.67 (s, 2H), 8.38 (s, 1H), 8.21 (d, J=9.7 Hz, 1H), 7.63 (dd, J=9.7, 2.6 Hz, 1H), 7.25 (br s, 1H), 5.86 (s, 1H), 4.57 (q, J=7.0 Hz, 2H), 3.66-3.53 (m, 2H), 3.34 (ddd, J=12.8, 8.6, 4.3 Hz, 2H), 2.47 (s, 2H), 2.29-2.18 (m, 2H), 1.87-1.77 (m, 4H), 1.50 (t, J=7.2 Hz, 3H), 1.39-1.31 (m, 2H), 1.26-1.18 (m, 2H); FXR EC50 = 946 nM.
일반적 방법 G
실시예 204
2-(2-(4-시클로프로필-1-(2,6-디클로로페닐)-1H-1,2,3-트리아졸-5-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
단계 1. (2,6-디클로로페닐)히드라진
TFA (50 mL) 중 2,6-디클로로아닐린 (5.0 g, 30.9 mmol)의 용액에 물 (10 mL)을 첨가하였다. 반응 혼합물을 0℃로 냉각시키고, 아질산나트륨 (2.1 g, 30.9 mmol)을 0.5시간에 걸쳐 첨가한 후, 물의 최소량의 부피 중에 용해시킨 아지드화나트륨 (5.1 g, 78.0 mmol)를 서서히 첨가하였다. 혼합물을 0℃에서 10분 동안 교반하고, 실온으로 가온되도록 하였다. 2시간 후, 반응 혼합물을 여과하고, 고체를 물로 세척하고, 공기 건조시키고, 수집하였다. 여과물을 EtOAc로 희석하고, 포화 수성 NaHCO3 및 염수로 세척하고, MgSO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-20% EtOAc/헥산) 상에서 플래쉬 크로마토그래피에 의해 정제하였다. 고체를 사전에 단리하고, 크로마토그래피로부터의 생성물을 합하여 2-아지도-1,3-디클로로벤젠 (5.6 g, 29.9 mmol, 97% 수율)을 황갈색 고체로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 7.31 (d, J=8.3 Hz, 2H), 7.06 (t, J=8.1 Hz, 1H).
단계 2. 4-시클로프로필-1-(2,6-디클로로페닐)-5-아이오도-1H-1,2,3-트리아졸
THF (120 mL) 중 2-아지도-1,3-디클로로벤젠 (4.5 g, 23.7 mmol)의 실온 용액에 아이오딘화칼륨 (15.8 g, 95 mmol) 및 구리 (II) 퍼클로레이트 6수화물 (15.8 g, 42.7 mmol)을 첨가하였다. 반응 혼합물을 50℃에서 5분 동안 교반하고, 이어서 DBU (3.9 mL, 26.1 mmol) 및 시클로프로필아세틸렌 (2.3 mL, 27.3 mmol)을 첨가하였다. 생성된 갈색 혼합물을 실온에서 밤새 교반하였다. 반응 혼합물을 SiO2의 패드를 통해 여과하고, 진공 하에 농축 건조시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-20% EtOAc/헥산)에 의해 정제하여 4-시클로프로필-1-(2,6-디클로로페닐)-5-아이오도-1H-1,2,3-트리아졸 (1.8 g, 4.8 mmol, 20% 수율)을 백색 고체로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 7.51-7.55 (m, 2H), 7.45-7.50 (m, 1H), 1.85-1.94 (m, 1H), 1.14-1.21 (m, 2H), 1.03-1.10 (m, 2H).
단계 3. tert-부틸 2-(4-시클로프로필-1-(2,6-디클로로페닐)-1H-1,2,3-트리아졸-5-일)-2-히드록시-7-아자스피로[3.5]노난-7-카르복실레이트
n-부틸리튬 (헥산, 0.26 mL 중 2.5 M, 0.66 mmol)을 THF (2.1 mL) 중 4-시클로프로필-1-(2,6-디클로로페닐)-5-아이오도-1H-1,2,3-트리아졸 (0.2 g, 0.53 mmol)의 -78℃ 용액에 천천히 첨가하여 암갈색 용액을 제공하였다. 5분 후, THF 0.25 mL 중 tert-부틸 2-옥소-7-아자스피로[3.5]노난-7-카르복실레이트 (0.15 g, 0.63 mmol)의 용액을 시린지를 통해 천천히 첨가하였다. 반응을 -78℃에서 2시간 동안 계속하고, 45분 동안 0℃로 만들었다. 반응물을 MeOH 대략 1 mL의 느린 첨가에 의해 켄칭한 다음, 정제를 위해 SiO2 상에 농축시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 24 g 칼럼)에 의해 정제하여 tert-부틸 2-(4-시클로프로필-1-(2,6-디클로로페닐)-1H-1,2,3-트리아졸-5-일)-2-히드록시-7-아자스피로[3.5]노난-7-카르복실레이트 (75 mg, 0.15 mmol, 29% 수율)을 백색 발포체로서 수득하였다.
단계 4. 2-(4-시클로프로필-1-(2,6-디클로로페닐)-1H-1,2,3-트리아졸-5-일)-7-아자스피로[3.5]노난-2-올
tert-부틸 2-(4-시클로프로필-1-(2,6-디클로로페닐)-1H-1,2,3-트리아졸-5-일)-2-히드록시-7-아자스피로[3.5]노난-7-카르복실레이트 (75 mg, 0.152 mmol)를 TFA (117 μL, 1.520 mmol)에 녹였다. 1시간 후, 과량의 TFA를 진공 하에 제거하였다. 고체를 진공 하에 밤새 건조시킨 다음, 직접 후속 단계에 사용하였다.
MS (ESI) m/z: 393.1 [M+H]+.
단계 5. 에틸 2-(2-(4-시클로프로필-1-(2,6-디클로로페닐)-1H-1,2,3-트리아졸-5-일)-2-히드록시-7-아자스피로[3.5]노난-7-일)-4-플루오로벤조[d]티아졸-6-카르복실레이트
탄산세슘 (61.9 mg, 0.19 mmol)에 이어서 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트 (34.7 mg, 0.11 mmol)를 DMA (0.22 mL) 중 2-(4-시클로프로필-1-(2,6-디클로로페닐)-1H-1,2,3-트리아졸-5-일)-7-아자스피로[3.5]노난-2-올, TFA (38.6 mg, 0.08 mmol)의 실온 용액에 첨가하고, 반응 혼합물을 90℃로 가열하였다. 가열 2시간 후, 조 반응 혼합물을 12 g 이스코 SiO2 카트리지 상에 로딩하고 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 12 g 칼럼)에 의해 정제하여 에틸 2-(2-(4-시클로프로필-1-(2,6-디클로로페닐)-1H-1,2,3-트리아졸-5-일)-2-히드록시-7-아자스피로[3.5]노난-7-일)-4-플루오로벤조[d]티아졸-6-카르복실레이트 (48 mg, 0.08 mmol, 100% 수율)을 수득하였다.
MS (ESI) m/z: 616.2 [M+H]+.
실시예 204. 2-(2-(4-시클로프로필-1-(2,6-디클로로페닐)-1H-1,2,3-트리아졸-5-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
옥시염화인(V) (45.4 μL, 0.49 mmol)에 이어서 Et3N (22.6 μL, 0.16 mmol)을 에틸 2-(2-(4-시클로프로필-1-(2,6-디클로로페닐)-1H-1,2,3-트리아졸-5-일)-2-히드록시-7-아자스피로[3.5]노난-7-일)-4-플루오로벤조[d]티아졸-6-카르복실레이트 (중간체 33, 10 mg, 0.02 mmol)을 함유하는 바이알에 첨가하였다. 반응 혼합물을 60℃로 5시간 동안 가열하고, 진공 하에 농축시켜 과량의 POCl3을 제거하였다. 잔류물을 THF (133 μL), 물 (53.3 μL) 중에 용해시키고, MeOH (13.33 μL) 및 수산화리튬 1수화물 (8.4 mg, 0.20 mmol)을 혼합물에 첨가하였다. 반응 용기를 밀봉하고, 80℃로 가열하고, 주말 동안의 가열 후, 1N HCl로 켄칭하고, MeOH로 희석하고, 여과하였다. 용액을 하기 조건으로 정제용 LC/MS를 통해 정제하였다: 칼럼: 엑스브리지 C18, 19 x 200 mm, 5-μm 입자; 이동상 A: 5:95 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 이동상 B: 95:5 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 구배: 19분에 걸쳐 10-60% B, 이어서 100% B에서 5-분 유지; 유량: 20 mL/분. 목적 생성물을 함유하는 분획을 합하고, 원심 증발을 통해 건조시켜 2-(2-(4-시클로프로필-1-(2,6-디클로로페닐)-1H-1,2,3-트리아졸-5-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (4.6 mg, 8.1 mmol, 40% 수율)을 수득하였다.
MS (ESI) m/z: 570.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.19 (s, 1H), 7.85-7.77 (m, 2H), 7.75-7.67 (m, 1H), 7.58 (br d, J=11.6 Hz, 1H), 6.22 (s, 1H), 3.73 (br d, J=13.4 Hz, 1H), 3.53 (br d, J=11.9 Hz, 1H), 2.36 (s, 2H), 2.13-2.00 (m, 1H), 1.77-1.59 (m, 4H), 1.10-1.02 (m, 2H), 0.99 (br d, J=2.7 Hz, 2H); FXR EC50 = 26 nM.
일반적 방법 H
실시예 205
2-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3,5]노난-7-일)옥시)-4-플루오로벤조[d]티아졸-6-카르복실산
단계 1. 7-(tert-부틸디메틸실릴옥시)스피로[3,5]노난-2-온
DCM (3 mL) 중 tert-부틸디메틸클로로실란 (0.28 g, 1.9 mmol)의 용액을 DCM (5 mL) 중 7-히드록시스피로[3.5]노난-2-온 (0.25 g, 1.6 mmol) 및 이미다졸 (0.22 g, 3.2 mmol)의 0℃ 용액에 천천히 첨가하였다. 빙조를 제거하고, 반응 혼합물을 실온에서 밤새 교반하였다. 반응 혼합물을 진공 하에 농축시키고, 잔류물을 EtOAc와 포화 수성 NaHCO3 사이에 분배하였다. 유기 상을 단리시키고, 염수로 세척하고, MgSO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켜 7-((tert-부틸디메틸실릴)옥시)스피로[3.5]노난-2-온 (0.408 g, 1.520 mmol, 94% 수율)을 무색 오일로서 수득하였다.
MS (ESI) m/z: 269.2 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 3.90-3.56 (m, 1H), 2.75 (br d, J=5.5 Hz, 4H), 1.94-1.80 (m, 2H), 1.77-1.64 (m, 2H), 1.62-1.40 (m, 4H), 0.90 (s, 9H), 0.07 (s, 6H).
단계 2. 7-((tert-부틸디메틸실릴)옥시)-2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]노난-2-올
n-부틸리튬 (0.74 mL, 1.8 mmol)을 THF (5.9 mL) 중 4-브로모-5-시클로프로필-3-(2,6-디클로로페닐)이속사졸 (0.49 g, 1.5 mmol, 일반적 방법 A에 기재된 합성)의 -78℃ 용액에 천천히 첨가하여 담갈색 용액을 제공하였다. 10분 후, 7-((tert-부틸디메틸실릴)옥시)스피로[3.5]노난-2-온 (0.40 g, 1.5 mmol)을 THF의 ~3 mL 중 용액으로서 첨가하였다. 반응을 -78℃에서 계속하고, 30분 후, MeOH 5 mL의 느린 첨가에 의해 켄칭한 다음, 진공 하에 농축시켰다. 생성된 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-30% EtOAc/헥산, 40g 이스코 SiO2 카트리지)에 의해 정제하여 7-((tert-부틸디메틸실릴)옥시)-2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]노난-2-올 (0.48 g, 0.92 mmol, 62% 수율)을 백색 발포체로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 7.47-7.41 (m, 2H), 7.40-7.34 (m, 1H), 3.61-3.47 (m, 1H), 2.25 (s, 1H), 2.21-2.08 (m, 3H), 2.04-1.88 (m, 3H), 1.60 (br d, J=12.1 Hz, 2H), 1.45-1.36 (m, 1H), 1.34-1.18 (m, 6H), 1.17-1.08 (m, 2H), 0.87 (s, 9H), 0.03 (s, 6H).
단계 3. 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]노난-2,7-디올
THF (2 mL) 중 7-((tert-부틸디메틸실릴)옥시)-2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]노난-2-올 (0.23 g, 0.43 mmol)의 실온 용액에 테트라부틸암모늄 플루오라이드 (THF, 0.86 mL 중 1 M, 0.86 mmol)을 첨가하였다. 반응 혼합물을 밤새 교반하고, 1.5 M 수성 인산칼륨으로 켄칭하고, EtOAc로 2회 추출하였다. 합한 유기 추출물을 염수로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (24g, 7분에 걸쳐 0-100% EtOAc/헥산, 이어서 100%에서 5분 동안 유지, 이스코 24 g SiO2 칼럼)에 의해 정제하여 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]노난-2,7-디올 (0.16 g, 0.39 mmol, 91% 수율)을 백색 발포체로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 7.47-7.42 (m, 2H), 7.41-7.35 (m, 1H), 3.57 (br s, 1H), 2.27 (s, 1H), 2.22-2.09 (m, 3H), 2.04-1.92 (m, 3H), 1.80-1.63 (m, 2H), 1.52-1.50 (m, 1H), 1.48-1.36 (m, 1H), 1.36-1.23 (m, 6H), 1.18-1.08 (m, 3H).
단계 4. 메틸 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3,5]노난-7-일옥시)-4-플루오로벤조[d]티아졸-6-카르복실레이트
실온에서 무수 THF (1 mL) 중 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일) 스피로[3.5]노난-2,7-디올 (33 mg, 0.081 mmol)의 용액에 KOtBu (19.0 mg, 0.17 mmol)를 첨가하였다. 5분 후, 메틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트 (28.1 mg, 0.097 mmol)를 첨가하고, 반응 혼합물을 실온에서 5분 동안 교반하였다. 반응물을 포화 수성 NH4Cl로 켄칭하고, 생성된 혼합물을 EtOAc로 3회 추출하였다. 합한 유기 추출물을 염수로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-50% EtOAc/헥산, 이스코 12 g 칼럼)에 의해 정제하여 메틸 2-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3.5]노난-7-일)옥시)-4-플루오로벤조[d]티아졸-6-카르복실레이트 (33 mg, 0.053 mmol, 66% 수율)을 백색 발포체로서 수득하였다.
MS (ESI) m/z: 617.2 [M+H]+.
실시예 205. 2-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3,5]노난-7-일)옥시)-4-플루오로벤조[d]티아졸-6-카르복실산
메틸 2-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3.5]노난-7-일)옥시)-4-플루오로벤조[d]티아졸-6-카르복실레이트의 혼합물 (33 mg, 0.053 mmol)에 MeOH (0.1 mL), 물 (0.40 mL) 및 THF (0.50 mL)에 이어서 수산화리튬 1수화물 (9.1 mg, 0.22 mmol)을 첨가하였다. 반응 혼합물을 70℃에서 30분 동안 교반하고, 진공 하에 농축시켜 THF 및 MeOH을 제거하였다. 반응 혼합물을 1 N 수성 HCl을 사용해 ~pH 4로 중화시키고, 생성된 현탁액을 EtOAc로 3회 추출하였다. 합한 EtOAc 추출물을 진공 하에 농축시키고, 조 물질을 하기 조건으로 정제용 LC/MS를 사용하여 정제하였다: 칼럼: 엑스브리지 C18, 19 x 200 mm, 5-μm 입자; 이동상 A: 5:95 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 이동상 B: 95:5 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 구배: 19분에 걸쳐 20-100% B, 이어서 100% B에서 5-분 유지. 목적 분획을 합하고, 농축시켜 2-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3,5]노난-7-일)옥시)-4-플루오로벤조[d]티아졸-6-카르복실산 (5 mg, 8.2 μmol, 15% 수율)을 회백색 고체로서 수득하였다.
MS (ESI) m/z: 603.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.31 (br s, 1H), 7.72-7.65 (m, 1H), 7.64-7.58 (m, 2H), 7.58-7.51 (m, 1H), 5.18-5.02 (m, 1H), 3.60-3.42 (m, 1H), 2.38-2.30 (m, 1H), 2.17-2.06 (m, 2H), 2.00-1.85 (m, 3H), 1.85-1.75 (m, 1H), 1.65-1.51 (m, 2H), 1.50-1.40 (m, 1H), 1.40-1.32 (m, 1H), 1.31-1.17 (m, 2H), 1.17-1.02 (m, 4H); GAL-FXR EC50 = 2618 nM.
실시예 206
3-(((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3.5]노난-7-일)옥시)메틸)벤조산
표제 화합물을, 메틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 3-(브로모메틸)벤조에이트로 대체하여, 실시예 205의 제조에 대하여 일반적 방법 H에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 542.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.90-7.78 (m, 2H), 7.65-7.59 (m, 2H), 7.58-7.52 (m, 1H), 7.50 (br d, J=7.3 Hz, 1H), 7.46-7.40 (m, 1H), 5.26 (s, 1H), 4.49 (s, 2H), 3.20-3.10 (m, 1H), 2.39-2.29 (m, 1H), 2.12-2.01 (m, 2H), 1.95-1.82 (m, 3H), 1.73-1.55 (m, 2H), 1.41-1.17 (m, 4H), 1.16-1.03 (m, 5H); GAL-FXR EC50 = 4711 nM.
일반적 방법 I
실시예 207
3-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3.5]노난-7-일)옥시)벤조산
단계 1. 메틸 3-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3.5]노난-7-일)옥시)벤조에이트
2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]노난-2,7-디올 (30 mg, 0.073 mmol, 일반적 방법 H에 기재된 합성), 메틸 3-히드록시벤조에이트 (12.3 mg, 0.081 mmol), Bu3P (0.029 mL, 0.12 mmol) 및 1,1'-(아조디카르보닐)디피페리딘 (29.7 mg, 0.12 mmol)을 밀봉된 바이알 중 건조 디옥산 (0.3 mL)중에 용해시켰다. 반응 혼합물을 110℃에서 교반하면서 2시간 동안 가열하였다. 실온으로 냉각시킨 후, 혼합물을 물로 희석하고, EtOAc로 3회 추출하였다. 합한 유기 추출물을 염수로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-50% EtOAc/헥산, 이스코 12 g 칼럼)에 의해 정제하여 메틸 3-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3.5]노난-7-일)옥시)벤조에이트 (10 mg, 0.018 mmol, 25% 수율)을 백색 발포체로서 수득하였다.
MS (ESI) m/z: 542.2 [M+H]+.
실시예 207. 3-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3.5]노난-7-일)옥시)벤조산
메틸 3-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3.5]노난-7-일)옥시)벤조에이트의 가수분해를, 실시예 206의 제조에 대하여 일반적 방법 H에 기재된 바와 같이 달성하였다.
MS (ESI) m/z: 528.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.64-7.58 (m, 2H), 7.57-7.51 (m, 1H), 7.46 (br d, J=7.9 Hz, 1H), 7.39-7.32 (m, 2H), 7.12 (br d, J=6.4 Hz, 1H), 5.35 (s, 1H), 4.35-4.21 (m, 1H), 2.42-2.27 (m, 1H), 2.16-2.02 (m, 2H), 1.96-1.83 (m, 3H), 1.79-1.68 (m, 1H), 1.68-1.59 (m, 1H), 1.54-1.43 (m, 1H), 1.41-1.30 (m, 2H), 1.30-1.20 (m, 2H), 1.15-1.02 (m, 4H); FXR EC50 = 4473 nM.
실시예 208
4-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3.5]노난-7-일)옥시)벤조산
표제 화합물을, 메틸 3-히드록시벤조에이트를 에틸 4-히드록시벤조에이트로 대체하여, 실시예 207의 제조에 대하여 일반적 방법 I에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 528.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.82 (br d, J=8.5 Hz, 2H), 7.63-7.60 (m, 2H), 7.58-7.52 (m, 1H), 6.92 (br d, J=8.5 Hz, 2H), 5.33 (s, 1H), 4.32-4.21 (m, 1H), 2.39-2.30 (m, 1H), 2.16-2.04 (m, 2H), 1.97-1.84 (m, 3H), 1.80-1.60 (m, 2H), 1.55-1.44 (m, 1H), 1.43-1.31 (m, 2H), 1.30-1.18 (m, 2H), 1.15-1.03 (m, 4H); GAL-FXR EC50 = 6660 nM.
실시예 209
2-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]논-1-엔-7-일)옥시)-4-플루오로벤조[d]티아졸-6-카르복실산
단계 1. 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-8,11-디옥사디스피로[3.2.47.24]트리데칸-2-올
n-부틸리튬 (헥산, 1.2 mL 중 2.5 M, 3.0 mmol)을 THF (9.6 mL) 중 4-브로모-5-시클로프로필-3-(2,6-디클로로페닐)이속사졸 (0.80 g, 2.4 mmol, 일반적 방법 A에 기재된 합성)의 -78℃ 용액에 천천히 첨가하였다. 10분 후, 8,11-디옥사디스피로[3.2.47.24]트리데칸-2-온 (0.47 mg, 2.4 mmol)을 THF의 ~0.5 mL 중 용액으로서 첨가하였다. 30분 후, 반응물을 MeOH 대략 5 mL의 느린 첨가에 의해 켄칭한 다음, 진공 하에 농축 건조시켰다. 생성된 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-60% EtOAc/헥산, 이스코 40g 칼럼)에 의해 정제하여 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-8,11-디옥사디스피로[3.2.47.24]트리데칸-2-올 (0.76 g, 1.69 mmol, 70% 수율)을 백색 발포체로서 수득하였다.
단계 2. 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3.5]노난-7-온
실온에서 MeOH (4 mL) 및 물 중 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-8,11-디옥사디스피로[3.2.47.24]트리데칸-2-올 (0.40 g, 0.89 mmol)의 혼합물 (4 mL)에 p-톨루엔술폰산 1수화물 (84 mg, 0.44 mmol)을 첨가하였다. 반응 혼합물을 실온에서 16시간 동안 교반하고, 추가의 p-톨루엔술폰산 1수화물 (84 mg, 0.44 mmol)을 첨가하였다. 1시간 후, 반응물을 1M K2HPO4 (20 mL)로 켄칭하고, EtOAc로 2회 추출하였다. 합한 유기 추출물을 염수로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/hex, 이스코 24g 칼럼)에 의해 정제하여 2-(5-시클로프로필-3-(2,6-디클로로페닐) 이속사졸-4-일)-2-히드록시스피로[3.5]노난-7-온 (0.32 g, 0.79 mmol, 89% 수율)을 회백색 발포체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 7.48-7.43 (m, 2H), 7.41-7.35 (m, 1H), 2.36-2.33 (m, 1H), 2.33-2.30 (m, 1H), 2.30-2.22 (m, 2H), 2.21-2.12 (m, 5H), 2.10-2.02 (m, 2H), 1.75 (t, J=6.6 Hz, 2H), 1.33-1.24 (m, 3H), 1.19-1.10 (m, 2H).
단계 3. 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]논-1-엔-7-온
2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3.5]노난-7-온 (0.37 g, 0.91 mmol)이 들은 반응 플라스크에 TFA (1 mL, 13.0 mmol)를 첨가하였다. 반응 혼합물을 실온에서 30분 동안 교반하고, 진공 하에 농축시켰다. 잔류물을 EtOAc로 희석하고, 1M K2HPO4, 염수로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-30% EtOAc/헥산, 이스코 24 g 카트리지)에 의해 정제하여 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]논-1-엔-7-온 (0.28 g, 0.73 mmol, 80% 수율)을 백색 발포체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 7.45-7.40 (m, 2H), 7.39-7.33 (m, 1H), 5.82 (s, 1H), 2.47 (s, 2H), 2.39-2.28 (m, 4H), 2.18 (tt, J=8.4, 5.0 Hz, 1H), 1.99-1.82 (m, 4H), 1.34-1.28 (m, 2H), 1.21-1.12 (m, 2H).
단계 4. 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]논-1-엔-7-올
0℃에서 MeOH (2.1 mL) 중 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일) 스피로[3.5]논-1-엔-7-온 (165 mg, 0.42 mmol)의 용액에 NaBH4 (17.7 mg, 0.47 mmol)을 여러 부분으로 첨가하였다. 반응 혼합물을 0℃에서 30분 동안 교반하고, 진공 하에 농축시켰다. 잔류물을 EtOAc로 희석하고, H2O 및 염수로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/헥산, 이스코 12 g 칼럼)에 의해 정제하여 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]논-1-엔-7-올 (0.14 g, 0.36 mmol, 84% 수율)을 백색 고체로서 수득하였다.
실시예 209. 2-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]논-1-엔-7-일)옥시)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]노난-2,7-디올을 2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]논-1-엔-7-올로 대체하여, 실시예 205의 제조에 대하여 일반적 방법 H에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 585.1 [M+H]+;
이성질체의 NMR은 1:1 혼합물을 나타낸다.
1H NMR (500 MHz, DMSO-d6) δ 8.35 (s, 2H), 7.78-7.56 (m, 8H), 6.00 (s, 1H), 5.77 (s, 1H), 5.29-5.11 (m, 2H), 2.99 (s, 2H), 2.38-2.19 (m, 4H), 2.09-1.74 (m, 8H), 1.69-1.47 (m, 8H), 1.23-1.17 (m, 4H), 1.13-1.08 (m, 4H); FXR EC50 = 1281 nM.
실시예 210
6-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]논-1-엔-7-일)옥시)퀴놀린-2-카르복실산
단계 1. 메틸 6-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]논-1-엔-7-일)옥시)퀴놀린-2-카르복실레이트
2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]논-1-엔-7-올) (32 mg 0.082 mmol), 메틸 6-히드록시퀴놀린-2-카르복실레이트 (20 mg, 0.098 mmol), 1,1'-(아조디카르보닐)디피페리딘 (33 mg, 0.13 mmol) 및 Bu3P (32 μL, 0.13 mmol)을 건조 디옥산 (0.41 mL) 중에 용해시켰다. 반응 혼합물을 밀봉된 압력 바이알 중에서 100℃에서 밤새 교반하였다. 실온으로 냉각시킨 후, 물을 첨가하고, 생성된 혼합물을 EtOAc로 2회 추출하였다. 합한 유기 층을 염수로 세척하고, Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-60% EtOAc/헥산, 10분 구배, 이어서 60%에서 5분 동안 유지, 이스코 12g 카트리지)에 의해 정제하여 메틸 6-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]논-1-엔-7-일)옥시)퀴놀린-2-카르복실레이트 (24 mg, 0.042 mmol, 51% 수율, 부분입체이성질체의 혼합물)을 무색 오일로서 수득하였다.
실시예 210. 6-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]논-1-엔-7-일)옥시)퀴놀린-2-카르복실산
표제 화합물을, 메틸 2-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-2-히드록시스피로[3.5]노난-7-일)옥시)-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-((2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)스피로[3.5]논-1-엔-7-일)옥시)퀴놀린-2-카르복실레이트로 대체하여, 실시예 205의 제조에 대하여 일반적 방법 H에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 560.9 [M+H]+;
1H NMR은 1:1 혼합물을 나타낸다.
1H NMR (500 MHz, DMSO-d6) δ 8.41-8.32 (m, 2H), 8.03 (d, J=8.5 Hz, 4H), 7.70-7.56 (m, 6H), 7.50-7.38 (m, 4H), 6.00 (s, 1H), 5.76 (s, 1H), 4.64-4.43 (m, 2H), 3.16 (s, 1H), 2.88 (s, 1H), 2.35-2.29 (m, 2H), 2.27 (s, 1H), 2.21 (s, 1H), 2.02-1.80 (m, 4H), 1.71-1.41 (m, 12H), 1.24-1.18 (m, 4H), 1.12-1.07 (m, 4H); FXR EC50 = 485 nM.
실시예 211
2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,4-디옥사-8-아자스피로[4.5]데칸-8-일)-4-플루오로벤조[d]티아졸-6-카르복실산
단계 1. 5-시클로프로필-3-(2,6-디클로로페닐)-4-비닐이속사졸
0℃에서 THF (7.5 mL) 중 메틸트리페닐포스포늄 브로마이드 (1.1 g, 3.2 mmol)의 용액에 KOtBu (THF, 3.8 mL 중 1M, 3.8 mmol)을 10분에 걸쳐 적가하였다. 반응 혼합물을 30분 동안 교반하고, 이어서 5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-카르브알데히드 (0.6 g, 2.1 mmol, 일반적 방법 C에 기재된 합성)을 첨가하였다. 반응 혼합물을 0℃에서 30분 동안 교반하고, SiO2 상 플래쉬 크로마토그래피 (0-25% EtOAc/헥산)에 의해 직접 정제하여 5-시클로프로필-3-(2,6-디클로로페닐)-4-비닐이속사졸 (0.59 g, 2.1 mmol, 99% 수율)을 백색 결정질 고체로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 7.45-7.40 (m, 2H), 7.40-7.32 (m, 1H), 6.39 (dd, J=17.9, 11.6 Hz, 1H), 5.11 (d, J=11.6 Hz, 1H), 5.07-4.98 (m, 1H), 2.21-2.04 (m, 1H), 1.32-1.24 (m, 2H), 1.15 (br dd, J=8.1, 2.3 Hz, 2H).
단계 2. 1-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)에탄-1,2-디올
THF (5.3 mL) 및 물 (5.3 mL) 중 5-시클로프로필-3-(2,6-디클로로페닐)-4-비닐이속사졸 (0.50 g, 1.8 mmol)의 0℃ 용액에 4-메틸모르폴린 n-옥시드 (0.31 g, 2.7 mmol)에 이어서 사산화오스뮴 (tBuOH, 0.36 mL 중 2.5%, 0.036 mmol)을 첨가하였다. 반응 혼합물을 0℃에서 2시간 동안 교반한 다음, 실온으로 가온되도록 하였다. 밤새 교반한 후, 반응 혼합물을 EtOAc로 희석하고, 물로 세척하였다. 유기부를 조 고체로 농축시키고, 이를 이어서 SiO2 상 플래쉬 크로마토그래피 (0-75% EtOAc/헥산)에 의해 정제하여 1-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)에탄-1,2-디올 (0.49 g, 1.5 mmol, 87% 수율)을 회백색 결정질 고체로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 7.40-7.45 (m, 2H), 7.33-7.39 (m, 1H), 4.49-4.68 (m, 1H), 3.71-3.78 (m, 1H), 3.61-3.69 (m, 1H), 2.42 (br d, J=1.93 Hz, 1H), 2.34 (ddd, J=3.58, 5.02, 8.46 Hz, 1H), 2.05 (s, 1H), 1.29-1.36 (m, 1H), 1.21-1.28 (m, 1H), 1.09-1.17 (m, 2H).
단계 3. 에틸 4-플루오로-2-(4-옥소피페리딘-1-일)벤조[d]티아졸-6-카르복실레이트
DMF (1.5 mL) 중 피페리딘-4-온 (48.9 mg, 0.49 mmol), 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트 (150 mg, 0.49 mmol) 및 Cs2CO3 (402 mg, 1.2 mmol)의 혼합물을 60℃에서 1시간 동안 가열하였다. 반응 혼합물을 EtOAc로 희석하고, 물로 세척하였다. 유기 층을 진공 하에 농축시키고, 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-60% EtOAc/헥산)에 의해 정제하여 에틸 4-플루오로-2-(4-옥소피페리딘-1-일)벤조[d]티아졸-6-카르복실레이트 (41 mg, 0.13 mmol, 26% 수율)을 황갈색 고체로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 8.14 (d, J=0.8 Hz, 1H), 7.80-7.68 (m, 1H), 4.46-4.32 (m, 2H), 4.09-3.94 (m, 4H), 2.67 (t, J=6.3 Hz, 4H), 1.47-1.34 (m, 3H).
단계 4. 에틸 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,4-디옥사-8-아자스피로[4.5]데칸-8-일)-4-플루오로벤조[d]티아졸-6-카르복실레이트
DCE (0.5 mL) 중 1-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)에탄-1,2-디올 (20.0 mg, 0.064 mmol, 단계 2로부터임) 및 에틸 4-플루오로-2-(4-옥소피페리딘-1-일)벤조[d]티아졸-6-카르복실레이트 (20.5 mg, 0.064 mmol, 단계 3으로부터임)의 혼합물에 p-톨루엔술폰산 1수화물 (24.2 mg, 0.13 mmol)을 첨가하였다. 반응 혼합물을 실온에서 밤새 교반하였다. 반응 혼합물을 SiO2 상 플래쉬 크로마토그래피 (0-30% EtOAc/hex)에 의해 직접 정제하여 에틸 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,4-디옥사-8-아자스피로[4.5]데칸-8-일)-4-플루오로벤조[d]티아졸-6-카르복실레이트 (19.0 mg, 0.031 mmol, 48% 수율)을 황갈색 고체로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 8.11-8.07 (m, 1H), 7.72 (dd, J=11.3, 1.4 Hz, 1H), 7.47-7.41 (m, 2H), 7.40 (d, J=8.0 Hz, 1H), 5.31 (s, 1H), 5.09-5.03 (m, 1H), 4.41-4.34 (m, 2H), 4.16 (dd, J=8.3, 6.1 Hz, 1H), 3.86-3.67 (m, 4H), 3.60-3.52 (m, 1H), 2.21-2.15 (m, 1H), 1.87-1.81 (m, 2H), 1.44-1.37 (m, 3H), 1.30 (br dd, J=5.0, 2.2 Hz, 3H), 1.20-1.13 (m, 2H).
실시예 211. 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,4-디옥사-8-아자스피로[4.5]데칸-8-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을 제공하기 위한 에틸 2-(2-(5-시클로프로필-3-(2,6-디클로로페닐)이속사졸-4-일)-1,4-디옥사-8-아자스피로[4.5]데칸-8-일)-4-플루오로벤조[d]티아졸-6-카르복실레이트의 가수분해를, 실시예 39의 제조에 대하여 일반적 방법 C에 기재된 바와 같이 수행하였다.
MS (ESI) m/z: 590.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.12-8.21 (m, 1H), 7.64-7.68 (m, 2H), 7.56-7.62 (m, 2H), 5.23 (br t, J=7.36 Hz, 1H), 4.24 (t, J=7.15 Hz, 1H), 3.51 (br d, J=9.51 Hz, 1H), 3.21-3.40 (m, 1H), 2.55 (s, 2H), 2.34-2.40 (m, 1H), 1.68-1.83 (m, 2H), 1.37 (br s, 1H), 1.17 (br d, J=8.25 Hz, 2H), 1.09 (br s, 2H), 0.93-1.07 (m, 2H); FXR EC50 = 1360 nM.
실시예 212
6-(2-(5-시클로프로필-3-(디시클로프로필메틸)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 2,6-디플루오로벤즈알데히드를 2,2-디시클로프로필아세트알데히드로 대체하여, 실시예 82의 제조에 대하여 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 564.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.14 (s, 1H), 8.03 (br d, J=9.5 Hz, 1H), 7.83 (br d, J=9.5 Hz, 1H), 7.04 (br s, 1H), 6.37 (s, 1H), 3.60 (br s, 2H), 2.63 (s, 2H), 2.49-2.46 (m, 2H), 2.14 (br s, 1H), 1.82 (br t, J=8.7 Hz, 1H), 1.70 (br s, 4H), 1.15 (br s, 2H), 1.10 (br d, J=7.9 Hz, 2H), 1.01 (br d, J=7.9 Hz, 2H), 0.93 (br s, 2H), 0.43 (br d, J=3.7 Hz, 2H), 0.32-0.24 (m, 2H), 0.21 (br dd, J=9.0, 4.4 Hz, 2H); FXR EC50 = 1546 nM.
실시예 213
2-(2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
단계 1. 에틸 5-아미노-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-4-카르복실레이트
에탄올 (8.52 mL) 중 에틸 (E)-2-시아노-3-에톡시아크릴레이트 (1.6 g, 9.4 mmol) 및 (2-(트리플루오로메틸)페닐)히드라진 (1.5 g, 8.5 mmol)의 용액을 밀봉된 튜브에서 85℃로 가열하였다. 가열을 밤새 계속하고, 반응 혼합물을 최소량의 부피로 농축시키고, 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/hex, 이스코 40 g 칼럼)에 의해 정제하여 에틸 5-아미노-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-4-카르복실레이트 (2.6 g, 8.5 mmol, 100% 수율)을 갈색 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 7.89 (dd, J=7.6, 1.2 Hz, 1H), 7.82 (s, 1H), 7.78-7.71 (m, 1H), 7.71-7.64 (m, 1H), 7.48 (d, J=7.7 Hz, 1H), 5.00 (br s, 2H), 4.32 (q, J=7.3 Hz, 2H), 1.38 (t, J=7.2 Hz, 3H). 19F NMR (377 MHz, CDCl3) δ -60.60 (s).
단계 2. 에틸 5-브로모-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-4-카르복실레이트
tert-부틸 니트라이트 (0.14 mL, 1.0 mmol)를 아세토니트릴 (8.4 mL) 중 브로민화구리 (II) (0.20 g, 0.92 mmol) 및 에틸 5-아미노-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-4-카르복실레이트 (0.25 g, 0.84 mmol)의 실온 현탁액에 천천히 첨가하였다. 1시간 후, 반응물을 포화 수성 NaHCO3으로 켄칭하였다. 혼합물을 EtOAc에 녹이고, 물 및 염수로 세척하였다. 합한 수성 층을 EtOAc로 역추출하고, 합한 유기부를 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축 건조시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-50% EtOAc/hex, 이스코 12 g 칼럼)에 의해 정제하여 에틸 5-브로모-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-4-카르복실레이트 (0.19 g, 0.52 mmol, 62% 수율)을 백색 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.17 (s, 1H), 7.92-7.86 (m, 1H), 7.80-7.69 (m, 2H), 7.43 (dd, J=7.4, 1.4 Hz, 1H), 4.40 (q, J=7.3 Hz, 2H), 1.42 (t, J=7.2 Hz, 3H). 19F NMR (377 MHz, CDCl3) δ -60.52 (s).
단계 3. tert-부틸 2-(4-(에톡시카르보닐)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트
트리-o-톨릴포스핀 (15.8 mg, 0.05 mmol), tert-부틸 2-(4,4,5,5-테트라메틸-1,3,2-디옥사보롤란-2-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트 (0.20 g, 0.57 mmol), 에틸 5-브로모-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-4-카르복실레이트 (0.19 g, 0.52 mmol) 및 2.0 M 수성 인산칼륨 (0.85 mL, 1.7 mmol)을 디옥산 (3.3 mL) 중에 용해시키고, 혼합물을 질소를 20분 동안 버블링시켜 탈기하였다. PdOAc2 (5.8 mg, 0.03 mmol)를 첨가하고, 질소를 생성된 혼합물을 통해 10분 동안 버블링하였다. 반응 용기를 밀봉하고, 80℃로 가열하였다. 3시간 후, 반응 혼합물을 EtOAc로 희석하고, 물 및 염수로 세척하였다. 합한 수성 층을 EtOAc로 역추출하였다. 유기 층을 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축 건조시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-80% EtOAc/hex, 이스코 12 g 칼럼)에 의해 정제하여 tert-부틸 2-(4-(에톡시카르보닐)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트 (0.24 g, 0.48 mmol, 92% 수율)을 점착성 고체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 8.07 (s, 1H), 7.88-7.81 (m, 1H), 7.75-7.65 (m, 2H), 7.47-7.39 (m, 1H), 6.39 (br s, 1H), 4.34 (q, J=7.0 Hz, 2H), 3.47 (dt, J=13.2, 5.1 Hz, 2H), 3.20-3.09 (m, 2H), 2.18 (br s, 2H), 1.55-1.44 (m, 4H), 1.43 (s, 9H), 1.40 (t, J=7.0 Hz, 3H). 19F NMR (377 MHz, CDCl3) δ -60.51 (s, 1F).
단계 4. tert-부틸 2-(4-(히드록시메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트
수소화알루미늄리튬 (2.5 mL, 2.5 mmol, THF 중 1M 용액)을 THF (8.3 mL) 중 tert-부틸 2-(4-(에톡시카르보닐)-1-(2-(트리플루오로메틸) 페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트 (1.1 g, 2.1 mmol)의 -50℃ 용액에 적가하였다. 혼합물을 35분 동안 -10℃로 가온하고, 이어서 40분 동안 0℃가 되게 하였다. 반응물을 0℃에서 켄칭하고, 물 0.1 mL, 15% 수성 NaOH 0.1 mL, 물 0.3 mL를 순차적으로 첨가하였다. 혼합물을 0℃에서 10분 동안 및 실온에서 30분 동안 교반하였다. 층을 분리하고, 유기 층을 물 및 염수로 세척하였다. 수성 층을 EtOAc로 역추출하고, 합한 유기부를 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축 건조시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/hex, 이스코 24 g 칼럼)에 의해 정제하여 tert-부틸 2-(4-(히드록시메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트 (0.78 g, 1.7 mmol, 81% 수율)을 회백색 발포체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 7.88-7.83 (m, 1H), 7.81 (s, 1H), 7.75-7.64 (m, 2H), 7.44-7.38 (m, 1H), 4.64 (d, J=5.7 Hz, 2H), 1.59 (t, J=5.8 Hz, 1H). 19F NMR (377 MHz, CDCl3) δ -60.46 (s).
단계 5. tert-부틸 2-(4-포르밀-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트
트리에틸아민 (97 μL, 0.69 mmol)에 이어서 1-프로판포스폰산 무수물 (0.41 mL, 0.69 mmol, EtOAc 중 50% 용액)을 디클로로메탄 (1.3 mL) 및 DMSO (1.0 mL) 중 tert-부틸 2-(4-(히드록시메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트 (0.11 g, 0.23 mmol)의 0℃ 용액에 첨가하였다. 20분 후, 반응물을 염수로 켄칭하고, EtOAc로 희석하였다. 수성 층을 EtOAc로 역추출하고, 합한 유기부를 Na2SO4 상에서 건조시키고, 여과하고, 진공 하에 농축 건조시켰다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/hex, 이스코 12 g 칼럼)에 의해 정제하여 tert-부틸 2-(4-포르밀-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트 (0.085 g, 0.18 mmol, 80% 수율)을 백색 발포체로서 수득하였다.
1H NMR (500 MHz, CDCl3) δ 10.05 (s, 1H), 8.14 (s, 1H), 7.91-7.84 (m, 1H), 7.78-7.70 (m, 2H), 7.49-7.44 (m, 1H), 6.27 (br d, J=2.2 Hz, 1H), 3.56-3.43 (m, 2H), 3.16 (ddd, J=13.2, 8.9, 3.7 Hz, 2H), 2.22 (s, 2H), 1.44 (m, 13H).
단계 6. tert-부틸 2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트
디에틸아미노설퍼 트리플루오라이드 (73.0 μL, 0.55 mmol)을 디클로로메탄 (1.8 mL) 중 tert-부틸 2-(4-포르밀-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트 (85 mg, 0.18 mmol)의 실온 용액에 첨가하였다. 주말 동안 교반한 후, 반응 혼합물을 SiO2 상 플래쉬 크로마토그래피 (0-80% EtOAc/hex, 이스코 12 g 칼럼)에 의해 직접 정제하여 tert-부틸 2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트 (66 mg, 0.14 mmol, 74% 수율)을 백색 발포체로서 수득하였다.
1H NMR (400 MHz, CDCl3) δ 7.91-7.83 (m, 2H), 7.78-7.68 (m, 2H), 7.51-7.45 (m, 1H), 6.98-6.61 (m, 1H), 5.80 (s, 1H), 3.61-3.45 (m, 2H), 3.16 (ddd, J=13.2, 8.7, 4.1 Hz, 2H), 2.21 (s, 2H), 1.55-1.48 (m, 4H), 1.46 (s, 9H).
단계 7. 2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔
트리플루오로아세트산 (0.21 mL, 2.7 mmol)을 디클로로메탄 (1.4 mL) 중 tert-부틸 2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트 (66 mg, 0.14 mmol)의 실온 용액에 첨가하였다. 2시간 후, 반응 혼합물을 농축 건조시켜 2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔, TFA를 수득하였다. 생성물을 후속 단계에 추가의 정제 또는 특징화 없이 사용하였다.
실시예 213. 2-(2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
디옥산 중 2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔, TFA (30 mg, 0.06 mmol, 단계 7로부터임), 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트 (19 mg, 0.06 mmol) 및 Cs2CO3 (59 mg, 0.18 mmol로부터임)의 슬러리 (0.3 mL)를 밀봉된 플라스크에서 80℃로 가열하였다. 1.5시간 후, 반응 혼합물을 실온으로 냉각시키고, THF/H2O/MeOH (10:4:1, 0.6 mL) 및 LiOH 1수화물 (13 mg, 0.3 mmol)을 첨가하였다. 반응 혼합물을 밀봉하고, 80℃로 2시간 동안 가열하였다. 반응물을 AcOH 0.5 mL의 첨가에 의해 켄칭하고, 진공 하에 농축 건조시켰다. 잔류물을 MeOH 2 mL 중에 용해시키고, 여과하고, 조 물질을 하기 조건으로 정제용 LC/MS를 통해 정제하였다: 칼럼: 엑스브리지 C18, 200 mm x 19 mm, 5-μm 입자; 이동상 A: 5:95 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 이동상 B: 95:5 아세토니트릴: 물, 10-mM 아세트산암모늄 포함; 구배: 19% B에서 0-분 유지, 20분에 걸쳐 19-59% B, 이어서 100% B에서 4-분 유지; 유량: 20 mL/분; 칼럼 온도: 25℃. 분획 수집은 MS 신호에 의해 촉발되었다. 목적 생성물을 함유하는 분획을 합하고, 원심 증발을 통해 건조시켜 2-(2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산 (23 mg, 0.04 mmol, 67% 수율)을 수득하였다.
MS (ESI) m/z: 579.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.17 (s, 1H), 8.03-7.93 (m, 2H), 7.93-7.81 (m, 2H), 7.66 (d, J=7.6 Hz, 1H), 7.57 (d, J=11.6 Hz, 1H), 7.30-7.02 (m, 1H), 5.95 (s, 1H), 3.76-3.65 (m, 1H), 3.62-3.49 (m, 1H), 3.50-3.40 (m, 1H), 2.22 (br s, 2H), 1.69-1.48 (m, 4H) 물 억제로 인해 추가의 피크 사라짐; EC50 = 48 nM.
실시예 214
6-(2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산
표제 화합물을, 5-시클로프로필-3-(2,6-디플루오로페닐)-4-(7-아자스피로[3.5]논-1-엔-2-일)이속사졸을 2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔으로 대체하여, 실시예 82의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 623.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.20 (s, 1H), 8.07 (d, J=9.4 Hz, 1H), 8.04-7.93 (m, 2H), 7.93-7.80 (m, 3H), 7.73-7.65 (m, 1H), 7.33-7.02 (m, 2H), 5.98-5.92 (m, 1H), 3.33-3.22 (m, 1H), 2.23 (br s, 2H), 1.72-1.62 (m, 2H), 1.60 (br s, 2H) 물 억제로 인해 추가의 피크 사라짐; EC50 = 26 nM.
실시예 215
2-(2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]노난-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
단계 1. 2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]노난
MeOH (0.69 mL) 중 tert-부틸 2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-카르복실레이트 (23.4 mg, 0.048 mmol)의 용액을 5분 동안 혼합물을 통해 질소를 버블링시켜 산소제거시켰다. 혼합물에 탄소 상 팔라듐 (10wt%, 25.8 mg, 0.024 mmol)을 첨가하고, 반응 플라스크를 수소로 폭기하였다. 수소 풍선을 부착시키고, 혼합물을 실온에서 교반하였다. 2시간 후, 반응 혼합물을 셀라이트 (EtOAc 세척액)을 통해 여과하고, 진공 하에 농축시켰다. 잔류물을 디클로로메탄 (0.47 mL) 중에 용해시키고, 트리플루오로아세트산 (46.8 μL)을 용액에 첨가하였다. 1시간 후, 용매를 진공 하에 제거하고, 생성된 물질을 직접 후속 단계에 사용하였다.
실시예 215. 2-(2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]노난-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, 2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔을 2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]노난으로 대체하여, 실시예 213의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 581.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.16 (s, 1H), 8.01-7.91 (m, 1H), 7.90-7.84 (m, 2H), 7.83-7.77 (m, 1H), 7.62 (br d, J=7.9 Hz, 1H), 7.56 (br d, J=11.3 Hz, 1H), 7.33-7.06 (m, 1H), 2.88 (s, 1H), 2.72 (s, 1H), 2.11-2.02 (m, 1H), 1.97 (br t, J=10.4 Hz, 1H), 1.86 (br d, J=8.2 Hz, 2H), 1.63 (br d, J=1.5 Hz, 2H), 1.50 (br s, 2H) 물 피크 하에 추가의 피크 소실; EC50 = 995 nM.
실시예 216
2-(2-(1-(3,5-디클로로피리딘-4-일)-4-(디플루오로메틸)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, (2-(트리플루오로메틸)페닐)히드라진을 3,5-디클로로-4-히드라진일피리딘으로 대체하여, 실시예 213의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 580.1 [M+H]+;
1H NMR (500 MHz, CDCl3) δ 8.74 (s, 2H), 8.15 (s, 1H), 7.97 (s, 1H), 7.76 (br d, J=11.0 Hz, 1H), 7.01-6.62 (m, 1H), 6.03 (s, 1H), 3.91-3.78 (m, 2H), 3.74 (s, 1H), 3.61-3.46 (m, 2H), 2.42 (s, 2H), 1.89-1.68 (m, 4H); EC50 = 88 nM.
실시예 217
2-(2-(4-(디플루오로메틸)-1-(2-(트리플루오로메톡시)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-플루오로벤조[d]티아졸-6-카르복실산
표제 화합물을, (2-(트리플루오로메틸)페닐)히드라진을 (2-(트리플루오로메톡시)페닐)히드라진로 대체하여, 실시예 213의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 559.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.16 (s, 1H), 7.98 (s, 1H), 7.74 (t, J = 7.8 Hz, 1H), 7.69 (d, J = 7.6 Hz, 1H), 7.66 - 7.54 (m, 3H), 7.15 (t, J = 55.0 Hz, 1H), 6.06 (s, 1H), 3.67 - 3.44 (m, 4H), 2.31 (s, 2H), 1.63 (dt, J = 4.9, 17.0 Hz, 4H); EC50 = 230 nM.
실시예 218
6-(2-(4-(디플루오로메틸)-1-(2-(트리플루오로메톡시)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-일)니코틴산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 6-플루오로니코티네이트로 대체하여, 실시예 217의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 521.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.58 (s, 1H), 7.99 (s, 1H), 7.89 (d, J = 8.9 Hz, 1H), 7.78 - 7.68 (m, 2H), 7.67 - 7.57 (m, 2H), 7.16 (t, J = 55.1 Hz, 1H), 6.83 (d, J = 9.2 Hz, 1H), 6.04 (s, 1H), 3.86 - 7.78 (m, 2H), 3.45 - 3.36 (m, 2H), 2.29 (s, 2H), 1.59 - 1.45 (m, 2H),); EC50 = 1085 nM.
실시예 219
6-(2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-일)-1-메틸-1H-인돌-3-카르복실산
표제 화합물을, 에틸 6-브로모-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트를 메틸 6-브로모-1-메틸-1H-인돌-3-카르복실레이트로 대체하여, 실시예 214의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 557.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.01 (d, J = 7.5 Hz, 1H), 7.96 (s, 1H), 7.94 - 7.83 (m, 2H), 7.81 (s, 1H), 7.77 (d, J = 8.5 Hz, 1H), 7.68 (d, J = 7.7 Hz, 1H), 7.18 (t, J = 55.1 Hz, 1H), 6.95 - 6.89 (m, 2H), 5.93 (s, 1H), 3.75 (s, 3H), 3.27 - 3.19 (m, 2H), 2.91 (br t, J = 10.4 Hz, 2H), 2.18 (s, 2H), 1.72 - 1.63 (m, 2H), 1.60 - 1.53 (m, 2H); EC50 = 180 nM.
실시예 220
2-(2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]노난-7-일)-4-메틸벤조[d]티아졸-6-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-브로모-4-메틸벤조[d]티아졸-6-카르복실레이트로 대체하여, 실시예 215의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 577.2 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.12 (s, 1H), 7.98 (d, J = 7.6 Hz, 1H), 7.91-7.79 (m, 3H), 7.66 (s, 1H), 7.62 (d, J = 7.8 Hz, 1H), 7.19 (t, J = 55.6 Hz, 1H), 3.70-3.40 (m, 5H), 2.44 (s, 3H), 2.11-2.02 (m, 2H), 2.01-1.92 (m, 2H), 1.86 (br d, J = 9.3 Hz, 2H), 1.63 (br s, 2H), 1.50 (br s, 2H); EC50 = 378 nM.
실시예 221
2-(2-(4-(디플루오로메틸)-1-(2-(트리플루오로메톡시)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-메틸벤조[d]티아졸-6-카르복실산
표제 화합물을, 에틸 2-브로모-4-플루오로벤조[d]티아졸-6-카르복실레이트를 메틸 2-브로모-4-메틸벤조[d]티아졸-6-카르복실레이트로 대체하여, 실시예 217의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 591.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.14 (s, 1H), 7.99 (s, 1H), 7.78-7.56 (m, 5H), 7.16 (t, J = 55.0 Hz, 1H), 6.07 (s, 1H), 3.63-3.43 (m, 4H), 2.45 (s, 3H), 2.32 (s, 2H), 1.71-1.56 (m, 4H); EC50 = 182 nM.
실시예 222
6-(2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]노난-7-일)-1-메틸-1H-인돌-3-카르복실산
표제 화합물을, 2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔, TFA를, 2-(4-(디플루오로메틸)-1-(2-(트리플루오로메틸)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]노난, TFA로 대체하여, 실시예 219의 제조에 대하여 일반적 방법 B에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 559.1 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 7.98 (d, J = 7.8 Hz, 1H), 7.91-7.85 (m, 2H), 7.84-7.79 (m, 2H), 7.76 (d, J = 8.7 Hz, 1H), 7.64 (d, J = 7.8 Hz, 1H), 7.19 (t, J = 55.5 Hz, 1H), 6.94-6.84 (m, 2H), 3.73 (s, 2H), 3.03 (br s, 2H), 2.93 (br s, 2H), 2.07-1.99 (m, 2H), 1.96-1.89 (m, 2H), 1.81 (br d, J = 9.5 Hz, 2H), 1.65 (br s, 2H), 1.52 (br s, 2H), 물 억제로 인해 추가의 피크 사라짐; EC50 = 275 nM.
실시예 223
6-(2-(4-(디플루오로메틸)-1-(2-(트리플루오로메톡시)페닐)-1H-피라졸-5-일)-7-아자스피로[3.5]논-1-엔-7-일)니코틴산
표제 화합물을, (2-(트리플루오로메톡시)페닐)히드라진을 (2-(트리플루오로메틸)페닐)히드라진로 대체하여, 실시예 218의 제조에 대하여 일반적 방법 A에 기재된 바와 같이 제조하였다.
MS (ESI) m/z: 505.3 [M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 8.56 (d, J = 2.4 Hz, 1H), 7.98 (d, J = 7.6 Hz, 1H), 7.95 (s, 1H), 7.92 - 7.81 (m, 3H), 7.64 (d, J = 7.6 Hz, 1H), 7.14 (t, J = 55.0 Hz, 1H), 6.80 (d, J = 9.0 Hz, 1H), 5.91 (s, 1H), 3.83-3.74 (m, 2H), 3.39-3.31 (m, 2H), 2.19 (s, 2H), 1.60-1.39 (m, 4H); EC50 = 205 nM.
실시예 224
(2S,3S,4S,5R,6S)-6-((6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르보닐)옥시)-3,4,5-트리히드록시테트라히드로-2H-피란-2-카르복실산
단계 1. (2S,3R,4S,5S,6S)-6-((알릴옥시)카르보닐)-3,4,5-트리히드록시테트라히드로-2H-피란-2-일 6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트
아세토니트릴 (0.5 mL) 중 6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실산 (실시예 85, 36.5 mg, 0.059 mmol) 및 HATU (24.8 mg, 0.065 mmol)의 혼합물에 실온에서 N-메틸모르폴린 (0.013 mL, 0.12 mmol)을 첨가하였다. 반응 혼합물을 실온에서 25분 동안 교반하고, 이어서 알릴 (2S,3S,4S,5R,6R)-3,4,5,6-테트라히드록시테트라히드로-2H-피란-2-카르복실레이트 (16.7 mg, 0.071 mmol)를 첨가하였다. 생성된 혼합물을 실온에서 1.5시간 동안 교반하고, 질소로 퍼징하여 용매를 제거하였다. 잔류물을 SiO2 상 플래쉬 크로마토그래피 (0-100% EtOAc/CH2Cl2, 이스코 12 g 칼럼)에 의해 정제하여 (2S,3R,4S,5S,6S)-6-((알릴옥시)카르보닐)-3,4,5-트리히드록시테트라히드로-2H-피란-2-일 6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일)이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트 (31.8 mg, 0.038 mmol, 64% 수율)을 오렌지색 고체로서 수득하였다.
MS (ESI) m/z: 831.5[M+H]+.
단계 2. 실시예 224.
0℃에서 THF (8.0 mL) 중 (2S,3R,4S,5S,6S)-6-((알릴옥시)카르보닐)-3,4,5-트리히드록시테트라히드로-2H-피란-2-일 6-(2-(5-시클로프로필-3-(3,5-디클로로피리딘-4-일) 이속사졸-4-일)-7-아자스피로[3.5]논-1-엔-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르복실레이트 (0.50 g, 0.60 mmol) 및 테트라키스(트리페닐포스핀)팔라듐(0) (69.5 mg, 0.060 mmol)의 혼합물에 Et3N (0.13 mL, 0.96 mmol)을 첨가하였다. 0℃에서 40분 동안 교반한 후, 아세토니트릴을 첨가하고, 이어서 셀라이트를 첨가하였다. 이어서, 혼합물을 증발시켜 용매를 제거하고, 카트리지 상에 로딩한 다음, C-18 역상 플래쉬 크로마토그래피 (100 g 이스코 HP C-18 칼럼, A 중 10-100% B, 이동상 A = 10:90 아세토니트릴: 물, 0.05% 트리플루오로아세트산 포함; 이동상 B = 90:10 아세토니트릴: 물, 0.05% 트리플루오로아세트산 포함)에 의해 정제하였다. 목적 생성물을 함유하는 수집된 분획을 질소로 퍼징하여 용매를 제거하고, 잔류물을 동결건조시켜 (2S,3S,4S,5R,6S)-6-((6-(2-((5-시클로프로필-3-(2-(트리플루오로메틸)페닐)이속사졸-4-일)메틸)-7-아자스피로[3.5]노난-7-일)-4-(트리플루오로메틸)퀴놀린-2-카르보닐)옥시)-3,4,5-트리히드록시테트라히드로-2H-피란-2-카르복실산 (0.34 g, 0.43 mmol, 67% 수율)을 담갈색 고체로서 수득하였다.
MS (ESI) m/z: 791.2[M+H]+;
1H NMR (500 MHz, DMSO-d6) δ 12.98-12.86 (m, 1H), 8.87 (s, 2H), 8.26 (s, 1H), 8.11 (d, J=9.5 Hz, 1H), 7.89 (br dd, J=9.8, 2.5 Hz, 1H), 7.06 (br s, 1H), 5.99 (s, 1H), 5.76 (d, J=7.6 Hz, 1H), 3.90 (d, J=9.5 Hz, 1H), 3.68-3.57 (m, 2H), 3.46-3.43 (m, 1H), 3.43-3.41 (m, 1H), 3.40-3.38 (m, 1H), 3.33 (s, 2H), 2.41 (s, 2H), 2.37-2.33 (m, 1H), 1.72-1.63 (m, 4H), 1.26-1.19 (m, 2H), 1.19-1.12 (m, 2H); FXR EC50 = 73 nM.
생물학적 검정
본 발명의 예시된 화합물을 일시적 인간 FXR/Gal4-루시페라제 리포터 검정에서 시험하였고, 검정 결과와 다른 분석 데이터를 실시예 섹션에 보고하였다.
Gal4-hFXR 융합 구축물 리포터 시스템을 1차 검정으로서 사용하여 화합물 활성을 특징화하였다. 반딧불이 루시페라제 리포터 cDNA의 상류에 5 카피의 Gal4 프로모터 반응 요소를 포함하는 구축물을 HEK293 세포에서 안정하게 발현시켰다. 이러한 리포터 세포주를 가습 5% CO2 분위기 하에 37℃에서 1% 페니실린-스트렙토마이신 (P/S) 용액, 500 μg/mL 제오신 및 10% 목탄/덱스트란-처리된 태아 소 혈청 (cs-FBS)이 보충된 둘베코 변형 이글 배지 (DMEM; 깁코(Gibco))에서 유지시켰다. pcDNA3.1 벡터 내의 인간 시토메갈로바이러스 프로모터가 인간 FXR로부터의 리간드 결합 도메인에 융합된 Gal4 전사 인자로부터의 DNA 결합 도메인으로 구성된 융합 단백질을 코딩하는 cDNA의 발현을 지시하는 또 다른 플라스미드를 구축하였다.
형질감염 전날, 배양물 중의 리포터 세포를 트립신에 의해 플레이트로부터 탈착시키고, 다음날 아침 대략 90% 전면생장률을 달성하기에 충분한 밀도로 T75 플라스크 내에 플레이팅하였다. 25 μg의 pcDNA3.1-Gal4-FXR 플라스미드를 1.87 mL의 Opti-MEM (써모-피셔(Thermo-Fisher)) 내로 및 40 μL의 리포펙타민 2000 (써모-피셔)을 1.87 mL의 Opti-MEM 내로 개별적으로 희석한 다음, 희석된 DNA 용액을 희석된 리포펙타민 2000 용액 내로 첨가하고, 실온에서 15-20분 동안 인큐베이션함으로써 형질감염 시약을 제조하였다. 혼합물을 세포로 전달하기 직전에 DMEM, 10% cs-FBS 및 1% P/S로 구성된 용액 10 mL로 추가로 희석하였다. 유지 배양 배지를 세포로부터 흡인하고, 최종 형질감염 혼합물을 첨가한 후에, 세포를 가습 5% CO2 분위기 하에 37℃에서 밤새 인큐베이션하였다. 이러한 프로토콜은 규모 확대될 수 있고, 일시적으로 형질감염된 세포는 검정-준비 포맷으로 동결보존될 수 있다.
화합물 시험을 위해, 100 nL의 화합물 (DMSO 중 연속 희석물)을 코닝(Corning)/코스타(Costar) 투명 바닥 384-웰 백색 플레이트의 웰 내로 에코 음향 분배기 (랩사이트(Labcyte))에 의해 분배하였다. 형질감염된 세포를 수거하고, 계수하고, 25 μL 중 10-25,000개의 세포가 384-웰 화합물 검정 플레이트의 각각의 웰에 플레이팅되도록 희석하였다. 화합물-처리된 세포를 가습 5% CO2 분위기 하에 37℃에서 밤새 인큐베이션하였다. 다음날 아침 25 μL의 스테디-글로 (프로메가(Promega))를 플레이트의 각각의 웰에 첨가하고, 혼합물을 진탕시키면서 15분 동안 인큐베이션하고, 엔비전 (퍼킨 엘머(Perkin Elmer)) 플레이트 판독기 상에서 발광을 측정하였다. DMSO 단독으로 처리된 세포로부터의 배경 수를 모든 미가공 수로부터 차감하고, 보정된 값을 8 μM GW-4064로 달성된 대조군 반응의 백분율로 전환시켰다. 이들 데이터를 4-파라미터 로그 효능제-반응 방정식에 피팅하여 EC50 값을 계산하였다.
급성 마우스 생체내 검정:
체중 25-28g의 수컷 C57BL6/NTac 마우스를 타코닉 랩스(Taconic Labs) (뉴욕주 허드슨)로부터 구입하고, 테크라드 글로벌 18% 단백질 설치류 식이 (하를란 래보러토리즈(Harlan Laboratories))를 유지하였다. 1주 순응 후, 마우스를 체중 기준으로 군으로 분류하였다. 마우스에게 단일 경구 용량의 비히클 또는 실험 화합물을 투여하였다. 투여 1시간 후 및 연구 종료시 (6시간)에 악하 정맥을 통해 수집된 혈액으로부터 유래된 혈장에서 전신 화합물 노출을 평가하였다. 연구 종료시, 동물을 안락사시키고 신속하게 해부하였다. 간의 내측엽을 분할하고, 이 중 한 절반은 균질화시켜 화합물 노출에 대해 분석하고, 다른 절반은 RNA레이터 (써모-피셔 사이언티픽(Thermo-Fisher Scientific))에 저장하였다. 회장을 또한 해부하고 RNA레이터에 보존하였다. RNA레이터 중의 조직 샘플을 엠피 바이오메디칼스(MP Biomedicals)의 비드로 균질화시켰다. 매그맥스-96 총 RNA 단리 키트 (써모-피셔 사이언티픽)를 제조업체의 프로토콜에 따라 사용하여 RNA를 추출하였다. 나노-드롭 8000 분광광도계 (써모 피셔)로 RNA 농도를 결정하였다. 인비트로젠(Invitrogen)의 슈퍼스크립트(SuperScript)® VILO cDNA 합성 키트를 제조업체의 프로토콜에 따라 사용하여 역전사를 수행하였다. 어플라이드 바이오시스템즈(Applied Biosystems)의 택맨 PCR 마스터 혼합물을 제조업체의 프로토콜에 따라 사용하여 실시간 PCR을 수행하였다. 모든 프라이머는 써모-피셔 사이언티픽으로부터 구입하였다. 분석된 마우스 유전자는 간에서의 Nr0b2 (이는 소형 이종이량체 파트너, SHP를 코딩함), Abcb11 (이는 담즙 염 배출 펌프, BSEP를 코딩함), Cyp7a1 및 Cyp8b1을 포함하고, 회장에서의 Fgf15, Fabp6 (이는 회장 담즙산 결합 단백질, I-BABP를 코딩함), Slc51a (이는 유기 용질 수송체 알파 서브유닛, OSTA를 코딩함), 및 Slc51b (이는 유기 용질 수송체 베타 서브유닛, OSTB를 코딩함)를 포함하였다. FGF15 유전자 발현에서의 통계적으로 유의한 변화는 배수 증가로서 표현하고, CYP7A1 발현은 비히클 대조군 대비 퍼센트 감소로서 표현하였다.
본 발명의 다른 특색은, 본 발명의 예시를 위해 제공되고 그에 제한되지 않는 것으로 의도되는 상기 예시적 실시양태의 기재에 따라 분명해질 것이다. 본 발명은 그의 취지 또는 본질적인 속성으로부터 벗어나지 않으면서 다른 구체적 형태로 구현될 수 있다. 본 발명은 본원에 언급된 본 발명의 바람직한 측면의 모든 조합을 포괄한다. 본 발명의 임의의 및 모든 실시양태는 임의의 다른 실시양태 또는 실시양태들과 함께 추가의 실시양태를 기재할 수 있는 것으로 이해된다. 또한, 실시양태의 각각의 개별 요소는 그 자체의 독립적 실시양태인 것으로 이해된다. 추가로, 한 실시양태의 임의의 요소는 임의의 실시양태로부터의 임의의 및 모든 다른 요소와 조합되어 추가의 실시양태를 기재하는 것으로 의도된다.
Claims (15)
- 하기 화학식 (I)의 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물.
여기서,
X1 및 X4는 각각 독립적으로 C 또는 N이고;
X2 및 X3은 각각 독립적으로 CR5, N, NR6, O 또는 S이고;
E 고리는 4- 내지 6-원 카르보시클릴 또는 헤테로시클릴이고, 여기서 카르보시클릴 및 헤테로시클릴은 각각 독립적으로 0 내지 3개의 R3으로 치환되고;
*은 스피로 탄소 원자를 나타내고;
Y는 CR7 또는 N이고;
m 및 n은 각각 독립적으로 0, 1 또는 2의 정수이고;
f는 0, 1, 2 또는 3의 정수이고;
Z는 6- 내지 10-원 아릴, N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 5- 내지 10-원 헤테로아릴, 3- 내지 10-원 카르보시클릴, 또는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 4- 내지 10-원 헤테로시클릴이고, 여기서 아릴, 헤테로아릴, 카르보시클릴 및 헤테로시클릴은 독립적으로 0 내지 5개의 R8로 치환되고;
L1은 공유 결합, O, S, -NR16-, -S(O)2-, C1-3 알킬렌, C1-3 헤테로알킬렌, C2-4 알케닐렌, C2-4 알키닐렌, 아릴, 또는 N, O 및 S로부터 독립적으로 선택된 1 내지 4개의 헤테로원자를 함유하는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 5- 내지 6-원 헤테로아릴이고; 여기서 알킬렌, 알케닐렌, 아릴, 헤테로알킬렌 및 헤테로아릴은 각각 독립적으로 0 내지 3개의 R11로 치환되고;
L2는 공유 결합, O, S, -NR17-, C1-3 알킬렌 또는 C1-3 헤테로알킬렌이고, 여기서 알킬렌 및 헤테로알킬렌은 독립적으로 0 내지 3개의 R15로 치환되고;
RX는 -L3-RZ이고;
L3은 공유 결합, C1-3 알킬렌, -C(O)NR12-CH2- 또는 -OCH2-이고, 여기서 C1-3 알킬렌은 0 내지 3개의 R4로 치환되고;
RZ는 -CN, -C(O)OR13, -C(O)NR14aR14b,
또는 이고;
Re는 C1-6 알킬, C3-6 시클로알킬, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬, 할로알콕시알킬 또는 아릴이고;
RY는 각각 독립적으로 수소, 할로, 시아노, 히드록실, 아미노, C1-6 알킬, 알킬아미노, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬, 할로알콕시알킬, 알콕시 또는 할로알콕시이거나; 또는 대안적으로 2개의 RY는 이들이 부착되어 있는 탄소 원자와 함께 가교 모이어티를 형성하고; 단 Y가 N이고 RY가 Y에 인접한 탄소 원자에 부착되는 경우에, RY는 할로, 시아노, 히드록실, 아미노, 알콕시 또는 할로알콕시가 아니고;
R1은 C1-6 알킬, C3-5 시클로알킬 또는 C4-6 헤테로시클릴이고, 여기서 알킬, 시클로알킬 및 헤테로시클릴은 각각 0 내지 3개의 R9로 치환되고;
R2는 6- 내지 10-원 아릴, N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 5- 내지 10-원 헤테로아릴, 3- 내지 10-원 카르보시클릴, 또는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 4- 내지 10-원 헤테로시클릴이고, 여기서 아릴, 헤테로아릴, 카르보시클릴 및 헤테로시클릴은 독립적으로 0 내지 5개의 R10으로 치환되고;
R3, R5, 및 R7은 각각 독립적으로 수소, 할로, 시아노, 히드록실, 아미노, C1-6 알킬, 알킬아미노, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬, 할로알콕시알킬, 알콕시 또는 할로알콕시이고;
R4는 각각 독립적으로 할로, 옥소, 시아노, 히드록실, 아미노, 알킬, 알콕시 또는 알킬아미노이거나; 또는 대안적으로, 2개의 R4는 이들이 부착되어 있는 원자(들)와 함께 카르보시클릴 또는 헤테로시클릴 모이어티를 형성하고;
R6, R16 및 R17은 각각 독립적으로 수소, C1-6 알킬, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬 또는 할로알콕시알킬이고;
R8 및 R10은 각각 독립적으로 할로, 시아노, 히드록실, 아미노, 옥소, -ORa, -SRa, =S, -NRcRc, =NH, =N-OH, =NRa, =N-ORa, -NO2, -S(O)2Ra, -S(O)2NHRb, -S(O)2NRcRc, -S(O)2ORb, -OS(O)2Rb, -OS(O)2ORb, -P(O)(ORb)(ORb), -C(O)Rb, -C(NRb)Rb, -C(O)ORb, -C(O)NRcRc, -C(NRb)NRcRc, -OC(O)Rb, -NRbC(O)Rb, -OC(O)ORb, -NRbC(O)ORb, -NRbC(O)NRcRc, -NRbC(NRb)Rb, -NRbC(NRb)NRcRc, C1-6 알킬, C1-6 할로알킬, 아릴, 아릴알킬, 헤테로아릴, 카르보시클릴 또는 헤테로시클릴이고; 여기서 알킬, 아릴, 헤테로아릴, 카르보시클릴 및 헤테로시클릴은, 그 자체로서 또는 또 다른 기의 일부로서, 각각 독립적으로 0 내지 5개의 Rd로 치환되고;
Ra는 각각 독립적으로 C1-6 알킬, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬, 할로알콕시알킬, 아릴, 아릴알킬, 헤테로아릴, 헤테로아릴알킬, 카르보시클릴, 카르보시클릴알킬, 헤테로시클릴 또는 헤테로시클릴알킬이고;
Rb는 각각 독립적으로 수소 또는 Ra이고;
Rc는 각각 독립적으로 Rb이거나, 또는 대안적으로, 2개의 Rc는 이들이 결합되어 있는 질소 원자와 함께, N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 4-, 5-, 6- 또는 7-원 헤테로시클릴을 형성하고;
Rd는 각각 독립적으로 Ra, 알콕시, 할로알콕시, 알킬아미노, 시클로알킬아미노, 헤테로시클릴아미노, 할로알킬, 히드록시알킬, 아미노알킬, 시클로알콕시, 헤테로시클릴옥시, 할로알콕시, 알콕시알콕시, 할로알킬아미노, 알콕시알킬아미노, 할로알콕시알킬아미노, 아릴아미노, 아르알킬아미노, 아릴옥시, 아르알킬옥시, 헤테로아릴옥시, 헤테로아릴알킬옥시, 알킬티오, 할로, 시아노, 히드록실, 아미노, 옥소, -ORa, -SRa, =S, -NRcRc, =NH, =N-OH, =NRa, =N-ORa, -NO2, -S(O)2Ra, -S(O)2NHRb, -S(O)2NRcRc, -S(O)2ORb, -OS(O)2Rb, -OS(O)2ORb, -P(O)(ORb)(ORb), -C(O)Rb, -C(NRb)Rb, -C(O)ORb, -C(O)NRcRc, -C(NRb)NRcRc, -OC(O)Rb, -NRbC(O)Rb, -OC(O)ORb, -NRbC(O)ORb, -NRbC(O)NRcRc, -NRbC(NRb)Rb 또는 -NRbC(NRb)NRcRc이고;
R9는 각각 독립적으로 할로, 시아노, 히드록실, 아미노 또는 C1-6 알킬이고;
R11 및 R15는 각각 독립적으로 할로, 옥소, 시아노, 히드록실, 아미노, C1-6 알킬, C3-6 시클로알킬, C4-6 헤테로시클릴, 알킬아미노, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬, 할로알콕시알킬, 알콕시 또는 할로알콕시이고;
R12는 수소 또는 C1-4 알킬이고;
R13은 수소, C1-10 알킬, 글리코실 또는 카르복시(트리히드록시)테트라히드로피라닐이고;
R14a 및 R14b는 각각 독립적으로 수소, C1-6 알킬, C3-6 시클로알킬, C4-6 헤테로시클릴, 알킬아미노, 할로알킬, 히드록시알킬, 아미노알킬, 알콕시알킬, 할로알콕시알킬, 알콕시 또는 할로알콕시이다. - 제1항 또는 제2항에 있어서,
L1이 공유 결합, O, S, NH, C1-3 알킬렌, -(C1-3 알킬렌)a-O-(C1-3 알킬렌)b-, -(C1-3 알킬렌)a-S-(C1-3 알킬렌)b- 또는 -(C1-3 알킬렌)a-NH-(C1-3 알킬렌)b-이고, 여기서 C1-3 알킬렌은 0 내지 3개의 R11로 치환되고;
a가 0 또는 1의 정수이고;
b가 0 또는 1의 정수이고; 단 a 및 b 둘 다가 1은 아니고;
L2가 공유 결합인
화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물. - 제1항 내지 제4항 중 어느 한 항에 있어서, Z가 페닐, 또는 N, O 및 S로부터 독립적으로 선택된 1 내지 3개의 헤테로원자를 함유하는 5- 내지 10-원 헤테로아릴이고, 여기서 페닐 및 헤테로아릴은 독립적으로 0 내지 5개의 R8로 치환된 것인 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물.
- 제1항에 있어서, 하기 화학식 (III)에 의해 나타내어지는 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물.
여기서,
Z는 1 또는 2개의 질소 원자를 함유하는 6-원 모노시클릭 헤테로아릴, 또는 N, O 및 S로부터 독립적으로 선택된 1 또는 3개의 헤테로원자를 함유하는 9- 내지 10-원 비시클릭 헤테로아릴이고, 여기서 모노시클릭 또는 비시클릭 헤테로아릴은 독립적으로 0 내지 3개의 R8로 치환되고;
R2는 페닐 또는 피리디닐이고, 여기서 페닐 및 피리디닐은 각각 독립적으로 0 내지 2개의 R10으로 치환되고;
R8은 각각 독립적으로 할로, 시아노, 히드록실, C1-4 알킬, C1-4 할로알킬, C1-4 알콕시 또는 C1-4 할로알콕시이고;
R10은 각각 독립적으로 할로, C1-4 알킬, C1-4 할로알킬, C1-4 알콕시 또는 C1-4 할로알콕시이고;
RX는 -C(O)OH 또는 -C(O)NH-S(O)2Re이고;
Re는 C1-6 알킬 또는 C3-6 시클로알킬이다. - 제1항에 있어서,
X1이 C이고, X2는 N이고, X3은 O이고, X4는 C이거나; 또는 X1이 N이고, X2는 N이고, X3은 C이고, X4는 C이고;
Y가 CH 또는 N이고;
모이어티가 하기로부터 선택되고:
및 ;
L1이 공유 결합, O 또는 -OCH2-이고, 단 Y가 N인 경우에 L1은 공유 결합이고;
Z가 페닐, 피리디닐, 피리다지닐, 피리미디닐, 피라지닐, 벤조[d]이미다졸릴, 벤조[d]이속사졸릴, 벤조[d]옥사디아졸릴, 벤조[d]티아졸릴, 이미다졸로[1,5-a] 피리디닐, 인다졸릴, 인돌릴, 피라졸로[4,3-b]피리디닐, 피롤로[2,1-f][1,2,4]트리아지닐, 피롤로[2,3-b]피리디닐, 피롤로[2,3-c]피리디닐, 피롤로[2,3-d]피리미디닐, 피롤로[3,2-c]피리디닐, 티아졸로[4,5-b]피리디닐, 티아졸로[5,4-b]피리디닐, 신놀리닐, 이소퀴놀리닐, 퀴놀리닐 또는 퀴녹살리닐이고, 이들 각각은 0 내지 1개의 R8로 치환되고;
R8이 F, -CH3, -CF3, -OCH3, -OCH2CH3, -OCH(CH3)2, -OCHF2, -OCF3, -OCH2CH2OH 또는 -CH2OCH2CH2Si(CH3)3이고;
Rx가 -CN, -C(O)OH, -C(O)OCH2CH3, -C(O)NH2, -C(O)NH(CH3), -C(O)NHCH2CH3, -C(O)NHCH(CH3)2, -C(O)NH(시클로프로필), -C(O)NHCH2C(O)OH, -C(O)NHS(O)2CH3, -C(O)NHS(O)2(시클로프로필), -OCH2C(O)OH 또는 -C(O)O(카르복시(트리히드록시)테트라히드로피라닐)이고;
L2가 공유 결합이고;
R1이 -CHF2, -CH(CH3)2, 시클로프로필 또는 메틸시클로프로필이고;
R2가 시클로헥실, 페닐 또는 피리디닐이고, 여기서 페닐 및 피리디닐은 독립적으로 1 내지 3개의 R10으로 치환되고;
R10이 각각 독립적으로 F, Cl, -CH3, -CF3, -OCH3 또는 -OCF3인
화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물. - 제1항에 있어서, 본 명세서에 기재된 바와 같은 실시예 중 어느 하나로부터 선택된 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물.
- 제약상 허용되는 담체 및 제1항 내지 제9항 중 어느 한 항에 따른 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물을 포함하는 제약 조성물.
- 제1항 내지 제9항 중 어느 한 항에 있어서, 요법에 사용하기 위한 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물.
- 제1항 내지 제9항 중 어느 한 항에 있어서, 병리학적 섬유증, 암, 염증성 장애, 대사 또는 담즙정체성 장애를 치료하는 요법에 사용하기 위한 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물.
- 제12항에 있어서, 병리학적 섬유증이 간 섬유증, 신섬유증, 담도 섬유증 또는 췌장 섬유증인 화합물.
- 제1항 내지 제9항 중 어느 한 항에 있어서, 비알콜성 지방간염 (NASH), 비-알콜성 지방간 질환 (NAFLD), 만성 신장 질환, 당뇨병성 신장 질환, 원발성 경화성 담관염 (PSC) 또는 원발성 담즙성 간경변증 (PBC)을 치료하는 요법에 사용하기 위한 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물.
- 제1항 내지 제9항 중 어느 한 항에 있어서, 특발성 폐 섬유증 (IPF)을 치료하는 요법에 사용하기 위한 화합물 또는 그의 입체이성질체, 호변이성질체 또는 제약상 허용되는 염 또는 용매화물.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762580068P | 2017-11-01 | 2017-11-01 | |
| US62/580,068 | 2017-11-01 | ||
| PCT/US2018/058326 WO2019089672A1 (en) | 2017-11-01 | 2018-10-31 | Spirocyclic compounds as farnesoid x receptor modulators |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20200083528A true KR20200083528A (ko) | 2020-07-08 |
Family
ID=64332185
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020207015273A KR20200083528A (ko) | 2017-11-01 | 2018-10-31 | 파르네소이드 x 수용체 조정제로서의 스피로시클릭 화합물 |
Country Status (19)
| Country | Link |
|---|---|
| US (1) | US11078198B2 (ko) |
| EP (1) | EP3704114B1 (ko) |
| JP (1) | JP7228595B2 (ko) |
| KR (1) | KR20200083528A (ko) |
| CN (1) | CN111278821B (ko) |
| AR (1) | AR113819A1 (ko) |
| AU (1) | AU2018357878A1 (ko) |
| BR (1) | BR112020008157A2 (ko) |
| CA (1) | CA3081424A1 (ko) |
| CL (1) | CL2020001140A1 (ko) |
| CO (1) | CO2020005486A2 (ko) |
| EA (1) | EA202091101A1 (ko) |
| ES (1) | ES2933184T3 (ko) |
| IL (1) | IL274322A (ko) |
| MX (1) | MX2020004400A (ko) |
| PE (1) | PE20201184A1 (ko) |
| SG (1) | SG11202003825TA (ko) |
| TW (1) | TW201922737A (ko) |
| WO (1) | WO2019089672A1 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022240213A1 (ko) * | 2021-05-12 | 2022-11-17 | 에이치케이이노엔 주식회사 | 신규한 벤조티아졸 유도체, 이의 제조방법 및 이의 간질환 예방 또는 치료 용도 |
Families Citing this family (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2023504427A (ja) * | 2019-11-29 | 2023-02-03 | ▲広▼▲東▼▲東▼▲陽▼光▲薬▼▲業▼有限公司 | 三環式含窒素化合物の非晶質及びその用途 |
| AU2021207253A1 (en) | 2020-01-15 | 2022-06-09 | Centre National De La Recherche Scientifique | Use of FXR agonists for treating an infection by hepatitis D virus |
| CN111592557A (zh) * | 2020-05-09 | 2020-08-28 | 河北合佳医药科技集团股份有限公司 | 一种7-氨基-3-乙烯基头孢烷酸的一步法环保制备方法 |
| WO2022152770A1 (en) | 2021-01-14 | 2022-07-21 | Enyo Pharma | Synergistic effect of a fxr agonist and ifn for the treatment of hbv infection |
| WO2022229302A1 (en) | 2021-04-28 | 2022-11-03 | Enyo Pharma | Strong potentiation of tlr3 agonists effects using fxr agonists as a combined treatment |
Family Cites Families (38)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO1993013101A1 (en) | 1991-12-27 | 1993-07-08 | Yoshitomi Pharmaceutical Industries, Ltd. | Pyridonecarboxylate compound, pharmaceutical use thereof, and spiro compound |
| WO1998017276A1 (en) | 1996-10-25 | 1998-04-30 | Merck & Co., Inc. | Heteroaryl spiroethercycloalkyl tachykinin receptor antagonists |
| WO2006006490A1 (ja) | 2004-07-08 | 2006-01-19 | Ono Pharmaceutical Co., Ltd. | スピロ化合物 |
| CN101248049B (zh) * | 2005-06-27 | 2013-08-28 | 埃克塞利希斯专利有限责任公司 | 咪唑类lxr调节剂 |
| EP1962838B1 (en) | 2005-12-19 | 2011-09-28 | GlaxoSmithKline LLC | Farnesoid x receptor agonists |
| CN101679297B (zh) * | 2006-12-08 | 2012-01-11 | 埃克塞利希斯股份有限公司 | Lxr和fxr调节剂 |
| US20100035918A1 (en) | 2007-01-30 | 2010-02-11 | Biogen Idec Ma Inc | Imidazolone Compounds and Methods of Making and Using the Same |
| WO2009005998A1 (en) | 2007-07-02 | 2009-01-08 | Smithkline Beecham Corporation | Farnesoid x receptor agonists |
| WO2009009059A1 (en) | 2007-07-09 | 2009-01-15 | Biogen Idec Ma Inc. | Spiro compounds as antagonists of tgf-beta |
| TW200906823A (en) | 2007-07-16 | 2009-02-16 | Lilly Co Eli | Compounds and methods for modulating FXR |
| CN101910151A (zh) | 2007-10-22 | 2010-12-08 | 先灵公司 | 双环杂环衍生物及其作为gpr119活性调节剂的用途 |
| CA2741839A1 (en) | 2008-11-21 | 2010-05-27 | Pfizer Inc. | 1-oxa-8-azaspiro [4,5] decane-8-carboxamide compounds as faah inhibitors |
| US8440710B2 (en) | 2009-10-15 | 2013-05-14 | Hoffmann-La Roche Inc. | HSL inhibitors useful in the treatment of diabetes |
| CU24152B1 (es) | 2010-12-20 | 2016-02-29 | Irm Llc | 1,2 oxazol-8-azabiciclo[3,2,1]octano 8 il como moduladores de fxr |
| JO3154B1 (ar) | 2011-06-17 | 2017-09-20 | Glaxosmithkline Llc | عوامل مضادة لـ trpv4 |
| EP2545964A1 (en) | 2011-07-13 | 2013-01-16 | Phenex Pharmaceuticals AG | Novel FXR (NR1H4) binding and activity modulating compounds |
| AU2013209958B2 (en) | 2012-01-16 | 2017-09-07 | Vertex Pharmaceuticals Incorporated | Pyran-spirocyclic piperidine amides as modulators of ion channels |
| MA37756B1 (fr) | 2012-06-13 | 2018-09-28 | Hoffmann La Roche | Nouveaux composés diazaspirocycloalcane et azaspirocycloalcane |
| JP6099753B2 (ja) | 2012-10-03 | 2017-03-22 | アドビナス セラピューティクス リミテッド | スピロ環化合物、その組成物及びその医薬応用 |
| TW201946921A (zh) * | 2014-05-14 | 2019-12-16 | 瑞士商諾華公司 | 甲醯胺衍生物 |
| WO2015172747A1 (en) | 2014-05-16 | 2015-11-19 | Zhaoyin Wang | Spirocyclic molecules as mth1 inhibitors |
| EP3034499A1 (en) | 2014-12-17 | 2016-06-22 | Gilead Sciences, Inc. | Novel FXR (NR1H4) modulating compounds |
| EP3034501A1 (en) * | 2014-12-17 | 2016-06-22 | Gilead Sciences, Inc. | Hydroxy containing FXR (NR1H4) modulating compounds |
| WO2016097933A1 (en) | 2014-12-18 | 2016-06-23 | Novartis Ag | Azabicyclooctane derivatives as fxr agonists for use in the treatment of liver and gastrointestinal diseases |
| CN106146483A (zh) | 2015-04-23 | 2016-11-23 | 上海迪诺医药科技有限公司 | 杂环类法尼酯衍生物x受体调节剂 |
| CN106946867B (zh) | 2016-01-06 | 2019-11-12 | 广州市恒诺康医药科技有限公司 | Fxr受体调节剂及其制备方法和用途 |
| CN108602811B (zh) | 2016-02-01 | 2021-11-16 | 轩竹生物科技有限公司 | Fxr受体激动剂 |
| CN107021958A (zh) | 2016-02-01 | 2017-08-08 | 山东轩竹医药科技有限公司 | Fxr受体激动剂 |
| JP6941109B2 (ja) | 2016-02-22 | 2021-09-29 | ノバルティス アーゲー | Fxrアゴニストを使用するための方法 |
| SI3419625T1 (sl) | 2016-02-22 | 2021-08-31 | Novartis Ag | Postopki za uporabo agonistov FXR |
| US10080741B2 (en) | 2016-04-26 | 2018-09-25 | Enanta Pharmaceuticals, Inc. | Isoxazole derivatives as FXR agonists and methods of use thereof |
| US10080742B2 (en) | 2016-04-26 | 2018-09-25 | Enanta Pharmaceuticals, Inc. | Isoxazole derivatives as FXR agonists and methods of use thereof |
| WO2017189663A1 (en) | 2016-04-26 | 2017-11-02 | Enanta Pharmaceuticals, Inc. | Isoxazole derivatives as fxr agonists and methods of use thereof |
| WO2017201155A1 (en) | 2016-05-18 | 2017-11-23 | Enanta Pharmaceuticals, Inc. | lSOXAZOLE DERIVATIVES AS FXR AGONISTS AND METHODS OF USE THEREOF |
| JP6678779B2 (ja) | 2016-06-13 | 2020-04-08 | ギリアード サイエンシーズ, インコーポレイテッド | Fxr(nr1h4)調節化合物 |
| AR108711A1 (es) | 2016-06-13 | 2018-09-19 | Gilead Sciences Inc | Compuestos moduladores de fxr (nr1h4) |
| CN108430998B (zh) | 2016-09-28 | 2021-07-09 | 四川科伦博泰生物医药股份有限公司 | 氮杂双环衍生物及其制备方法和用途 |
| CN106632294A (zh) | 2016-12-15 | 2017-05-10 | 宁波百纳西药业有限公司 | 一种螺环化合物及其药物用途 |
-
2018
- 2018-10-31 EA EA202091101A patent/EA202091101A1/ru unknown
- 2018-10-31 US US16/175,910 patent/US11078198B2/en active Active
- 2018-10-31 MX MX2020004400A patent/MX2020004400A/es unknown
- 2018-10-31 PE PE2020000676A patent/PE20201184A1/es unknown
- 2018-10-31 JP JP2020544335A patent/JP7228595B2/ja active Active
- 2018-10-31 KR KR1020207015273A patent/KR20200083528A/ko not_active Application Discontinuation
- 2018-10-31 EP EP18804190.9A patent/EP3704114B1/en active Active
- 2018-10-31 AR ARP180103176A patent/AR113819A1/es unknown
- 2018-10-31 CN CN201880069863.0A patent/CN111278821B/zh active Active
- 2018-10-31 ES ES18804190T patent/ES2933184T3/es active Active
- 2018-10-31 WO PCT/US2018/058326 patent/WO2019089672A1/en unknown
- 2018-10-31 TW TW107138488A patent/TW201922737A/zh unknown
- 2018-10-31 AU AU2018357878A patent/AU2018357878A1/en not_active Abandoned
- 2018-10-31 BR BR112020008157-4A patent/BR112020008157A2/pt not_active IP Right Cessation
- 2018-10-31 SG SG11202003825TA patent/SG11202003825TA/en unknown
- 2018-10-31 CA CA3081424A patent/CA3081424A1/en active Pending
-
2020
- 2020-04-28 IL IL274322A patent/IL274322A/en unknown
- 2020-04-29 CL CL2020001140A patent/CL2020001140A1/es unknown
- 2020-04-30 CO CONC2020/0005486A patent/CO2020005486A2/es unknown
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2022240213A1 (ko) * | 2021-05-12 | 2022-11-17 | 에이치케이이노엔 주식회사 | 신규한 벤조티아졸 유도체, 이의 제조방법 및 이의 간질환 예방 또는 치료 용도 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA3081424A1 (en) | 2019-05-09 |
| WO2019089672A1 (en) | 2019-05-09 |
| ES2933184T3 (es) | 2023-02-02 |
| CL2020001140A1 (es) | 2020-08-21 |
| US20190127362A1 (en) | 2019-05-02 |
| CN111278821B (zh) | 2023-10-03 |
| EP3704114A1 (en) | 2020-09-09 |
| JP2021501806A (ja) | 2021-01-21 |
| US11078198B2 (en) | 2021-08-03 |
| EP3704114B1 (en) | 2022-11-23 |
| MX2020004400A (es) | 2020-08-06 |
| SG11202003825TA (en) | 2020-05-28 |
| BR112020008157A2 (pt) | 2020-10-06 |
| AR113819A1 (es) | 2020-06-17 |
| TW201922737A (zh) | 2019-06-16 |
| PE20201184A1 (es) | 2020-11-03 |
| JP7228595B2 (ja) | 2023-02-24 |
| CN111278821A (zh) | 2020-06-12 |
| CO2020005486A2 (es) | 2020-05-15 |
| AU2018357878A1 (en) | 2020-06-18 |
| IL274322A (en) | 2020-06-30 |
| EA202091101A1 (ru) | 2020-08-06 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11078198B2 (en) | Spirocyclic compounds as farnesoid X receptor modulators | |
| KR102506327B1 (ko) | αV 인테그린 길항제로서의 인다졸 유도체 | |
| US11168079B2 (en) | Alkene compounds as farnesoid x receptor modulators | |
| EP3704112B1 (en) | Alkene spirocyclic compounds as farnesoid x receptor modulators | |
| JP7264905B2 (ja) | ファルネソイドx受容体モジュレーターとしての多環化合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| E902 | Notification of reason for refusal |