KR20180057636A - 반려 동물 치료용 aav-epo - Google Patents
반려 동물 치료용 aav-epo Download PDFInfo
- Publication number
- KR20180057636A KR20180057636A KR1020187008958A KR20187008958A KR20180057636A KR 20180057636 A KR20180057636 A KR 20180057636A KR 1020187008958 A KR1020187008958 A KR 1020187008958A KR 20187008958 A KR20187008958 A KR 20187008958A KR 20180057636 A KR20180057636 A KR 20180057636A
- Authority
- KR
- South Korea
- Prior art keywords
- epo
- sequence
- raav
- aav
- promoter
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N7/00—Viruses; Bacteriophages; Compositions thereof; Preparation or purification thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/475—Growth factors; Growth regulators
- C07K14/505—Erythropoietin [EPO]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
- C12N15/864—Parvoviral vectors, e.g. parvovirus, densovirus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/01—Fusion polypeptide containing a localisation/targetting motif
- C07K2319/02—Fusion polypeptide containing a localisation/targetting motif containing a signal sequence
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14141—Use of virus, viral particle or viral elements as a vector
- C12N2750/14143—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2800/00—Nucleic acids vectors
- C12N2800/22—Vectors comprising a coding region that has been codon optimised for expression in a respective host
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- Biophysics (AREA)
- Wood Science & Technology (AREA)
- Epidemiology (AREA)
- General Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Toxicology (AREA)
- Dermatology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Virology (AREA)
- Microbiology (AREA)
- Urology & Nephrology (AREA)
- Physics & Mathematics (AREA)
- Plant Pathology (AREA)
- Immunology (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Peptides Or Proteins (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
반려 동물을 치료하기 위한 조성물 및 방법이 제시된다. 에리트로포에틴(EPO)을 인코드하는 서열이 포함된 핵산 분자가 포함된 아데노-연합된 바이러스 벡터가 제시된다. 바람직한 구체예들에서, 상기 대상은 고양이 또는 개이다.
Description
전자형태로 제출된 편입된 참고 자료들
출원인은 여기에 전자 형식으로 제출된 서열 목록 자료를 참조서류에 편입시킨다. 이 화일은 "15-7472PCT_Seq_Listing.txt"로 명명한다.
발명의 배경
에리트로포에틴 (EPO)은 주로 신장의 관주위(peritubular) 세포에서 만들어지는 호르몬이다. 이것은 골수에 작용하여, 적혈구생성(erythropoiesis)을 자극한다. 에리트로포에틴은 또한 성숙한 적혈구의 세포자멸(apoptosis) (프로그램된 세포 사멸)을 조절한다. 신장 질환은 적혈구생성을 감소시킨다. 인간에서 만성 신장 질환의 빈혈 관리는 재조합 인간 에리스로포이에틴(에포에틴(epoetin))의 개발에 의해 혁명을 일으켰다. 빈혈이 치료되면, 만성 신장 질환으로 발생되는 삶의 질에 좋지 않은 영향을 주는 많은 증상, 이를 테면, 피로, 기면, 졸림, 호흡곤란이 해결되었거나 또는 현저히 개선되었다.
만성 신장 질환 (CKD)으로 고통받는 고양이 2 백만 마리와 개 35 만 마리가 있다. CKD 관련 신부전을 겪는 반려 동물도 비슷한 방식으로 고통받는다. 이들 동물은 충분한 EPO를 보유하지 못하고, 결국 심각한 빈혈을 겪게 된다. 과거 수의사는 동물에게 주입된 EPO에 대한 면역 반응을 나타낼 때까지 인간 재조합 EPO를 제공했다. 이것은 매우 잘 이해된 생리학적 과정에 대한 시장에서의 장기적 치료를 효과적으로 제시하지 않았는데, 임상에서는 분명히 필요하다.
따라서, 대상, 특히 반려 동물에서 EPO를 발현하는데 유용한 조성물이 필요하다.
발명의 요약
신규한 조작된 에리트로포에틴 (EPO) 구조체들이 본 명세서에서 제시된다. 이러한 구조체들은 다수의 경로를 통해, 특히 재조합 아데노-연합된 바이러스 (rAAV) 벡터와 같은 재조합 벡터에 의해 매개되는 생체 내 발현에 의해 이를 필요로 하는 대상에게 전달될 수 있다.
일부 구체예들에서, 상기 EPO는 내생성 서열에 인코드된다. 즉, 상기 EPO 서열은 궁극적으로 투여하기로 의도된 대상과 동일한 종으로부터 유래된다.
일부 구체예들에서, 본 명세서에서 기술된 바와 같이, 약학적으로 수용가능한 운반체 및 재조합 벡터가 포함된 약학 조성물이 제시된다. 발현 카세트를 갖는 본원에서 기술된 재조합 벡터를 이를 필요로 하는 대상에게 투여함으로써 만성 신장질환을 치료하는 방법이 또한 제시되는데, 여기에서 전술한 발현 카세트는 상기 대상에서 EPO 구조체의 발현을 지시하는 조정 제어(regulatory control) 서열을 더 포함한다. 일부 구체예들에서, 치료되는 대상은 반려 동물이다. 한 구체예에서, 상기 대상은 고양이다. 또다른 구체예에서, 상기 대상은 개이다. 본 명세서에서 이용된 바와 같이, 용어 "환자"와 "대상(subject)"은 호환될 수 있고, 인간 또는 동물 대상을 지칭할 수 있다.
여전히 또다른 구체예에서, 대상에게서 순환 EPO의 양을 증가시키는 방법은 EPO를 인코드하는 발현 카세트를 갖는 본원에서 기술된 재조합 벡터를 제공하는 것을 포함한다.
상기 기술된 재조합 벡터는 만성 신장 질환 및 순환 적혈구 양의 감소를 특징으로 하는 다른 증상을 치료하기 위한 요법(regimen)에 이용될 수 있다.
본 발명의 다른 측면들 및 이점은 이하의 본 발명의 상세한 설명으로부터 바로 명백해질 것이다.
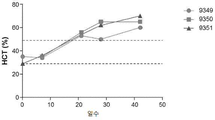
도 1은 고양이 에리트로포에틴을 발현시키는 AAV8로 처리된 고양이의 헤마토크릿(hematocrits)을 나타내는 그래프다. 점선은 정상 범위를 나타낸다.
도 2는 개의 에리트로포에틴을 발현시키는 AAV8로 처리된 개의 헤마토크릿을 나타내는 그래프다. 점선은 정상 범위를 나타낸다.
도 3a는 밑줄친 리더 서열과 함께, 개의 EPO 프로펩티드 서열을 나타낸다. 도 3b는 밑줄친 리더 서열과 함께, 고양이의 EPO 프로펩티드 서열을 나타낸다.
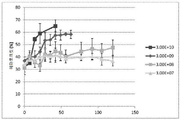
도 4는 고양이 에리트로포에틴을 발현시키는 AAV8로 처리된 고양이의 헤마토크릿을 나타내는 그래프다. 고양이는 3.0 x107 GC, 3.0 x108 GC, 3.0 x109 GC, 또는 3.0 x1010 GC AAV8f.EPO로 처리되었다.
도 2는 개의 에리트로포에틴을 발현시키는 AAV8로 처리된 개의 헤마토크릿을 나타내는 그래프다. 점선은 정상 범위를 나타낸다.
도 3a는 밑줄친 리더 서열과 함께, 개의 EPO 프로펩티드 서열을 나타낸다. 도 3b는 밑줄친 리더 서열과 함께, 고양이의 EPO 프로펩티드 서열을 나타낸다.
도 4는 고양이 에리트로포에틴을 발현시키는 AAV8로 처리된 고양이의 헤마토크릿을 나타내는 그래프다. 고양이는 3.0 x107 GC, 3.0 x108 GC, 3.0 x109 GC, 또는 3.0 x1010 GC AAV8f.EPO로 처리되었다.
발명의 상세한 설명
EPO 발현 구조체를 운반하는 아데노-연합된 바이러스 벡터는 반려 동물 (가령, 고양이 및 개)을 포함하는 대상에서 사용하기 위하여 개발되었다. 비록 효과가 있을지라도, 재조합 개과 고양이 특이적 EPO 단백질 치료제는 질환을 앓고 있는 동물에게 EPO를 전달하기 위한 바이러스 벡터 매개 시스템보다 개발하고 제조하는데 훨씬 많은 비용이 든다. 바이러스 벡터 치료제를 사용하면, 재조합 EPO를 자주 주사하는 것과 달리, 동물을 한 번 치료할 수 있는 편리함이 있다. EPO의 안정적인 발현은 빈혈을 치료하고, 동물의 삶의 질을 향상시킨다. 본원에 기재된 EPO 구조체들은 또한 대상에 있어서 내생성이 아닌 않은 EPO 서열을 제공하고, 이로써 비-고유 단백질에 대한 면역 반응이 대상에서 발달될 위험을 감소시키는 것을 특징으로 한다.
또한 여기에 설명된 구조에 대한 용도가 제공된다. 이들 구조체는 다수의 경로를 통하여 이를 필요로 하는 대상에게 전달될 수 있고, 구체적으로 재조합 벡터 이를 테면, rAAV 벡터에 의해 생체내에서 매개된 발현에 의해 전달될 수 있다. 한 구체예에서, 만성 신장 질환을 치료할 필요가 있는 대상에서 이를 치료하고, 대상에서 EPO를 증가시키기 위한 요법에 구조체를 사용하는 방법이 또한 제공된다. 한 구체예에서, 이를 필요로 하는 대상에서 빈혈을 치료하기 위한 요법에 이들 구조체를 사용하는 방법이 제공된다. 또다른 구체예에서, 대상의 빈혈은 다른 약물의 사용과 관련된다. 빈혈증에 영향을 줄 가능성이 있는 약물로는 HIV/AIDS 치료 (AZT 포함) 및 화학요법을 포함한 암 치료제가 있지만, 이에 국한되지 않는다. 또다른 구체예에서, 대상의 빈혈은 의학적 상태와 관련이 있다. 빈혈에 영향을 줄 수 있는 의학적 증상으로는 암, HIV/AIDS, 류마티스 관절염, 크론(Crohn) 병 및 기타 만성 염증성 질환 및 기능장애 골수 (가령, 재생 불량성 빈혈, 백혈병, 골수이형성증 또는 골수섬유증), 다발성 골수종, 골수증식성 장애 및 림프종, 용혈성 빈혈, 겸상적혈구 빈혈 및 지중해 증후군을 포함하나, 이에 국한되지 않는다. 또한, 대상에게서 EPO의 활성을 강화시키는 방법이 제공된다.
EPO는 프로펩티드(propeptide)로 생체 내에서 발현되며, 리더 서열은 종 (species)에 걸쳐 약간의 상동성을 공유한다. 서열 번호 3은 개의 EPO 프로펩티드의 서열을 나타내며, 성숙 단백질은 아미노산 41에서 시작한다. 리더 서열은 도 3a에서 밑줄로 표시된다. 서열 번호:4는 고양이의 EPO 프로펩티드의 서열을 나타내며, 성숙 단백질은 아미노산 27에서 시작한다. 리더 서열은 도 3b에서 밑줄로 표시된다.
한 구체예에서, EPO의 기능적 변이체는 본원에서 기술된 또는 당분야에 공지된 EPO 핵산 또는 아미노산 서열로부터 최대 약 10% 변이를 함유하지만, 여전히 상기 야생형 서열의 기능을 유지하는 변이체들을 포함한다. 일부 구체예에서 EPO 변이체의 기반 서열은 프로펩티드 리더 서열 (가령, 서열 번호: 3 및 서열 번호: 4에서 나타낸 바와 같이)을 포함한다. 또다른 구체예에서, 본 명세서에서 기술된 EPO 변이체는 단지 성숙한 펩티드 (가령, 서열 번호: 3의 아미노산 41-206, 또는 서열 번호: 4의 아미노산 27-192)를 지칭한다. 본 명세서에서 이용된 바와 같이, "기능의 유지(retain function)"에서 이것은 발현 또는 활성이 반드시 동일한 수준일 필요는 없지만, 상기 핵산 또는 아미노산이 이의 야생형 서열과 동일한 방식으로 기능을 한다는 것을 의미한다. 예를 들면, 한 구체예에서, 기능적 변이체는 야생형 서열과 비교하였을 때, 발현 또는 활성이 증가된다. 또다른 구체예에서, 상기 기능적 변이체는 야생형 서열과 비교하였을 때, 발현 또는 활성이 감소된다. 한 구체예에서, 상기 기능적 변이체는 야생형 서열과 비교하였을 때, 발현 또는 활성이 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90% 또는 그 이상으로 증가 또는 감소된다. 개의 EPO의 아미노산 서열은 본 명세서에서 서열 번호: 3으로 제시된다. 고양이의 EPO의 아미노산 서열은 본 명세서에서 서열 번호: 4로 제시된다.
또다른 구체예에서, EPO의 기능적 변이체는 본원에서 기술된 또는 당분야에 공지된 EPO 핵산 또는 아미노산 서열로부터 최대 약 20% 변이를 함유하지만, 여전히 상기 야생형 서열의 기능을 유지하는 변이체들을 포함한다. 한 구체예에서, EPO의 기능적 변이체는 본원에서 기술된 또는 당분야에 공지된 EPO 핵산 또는 아미노산 서열로부터 최대 약 30% 변이를 함유하지만, 여전히 상기 야생형 서열의 기능을 유지하는 변이체들을 포함한다. 다음과 같은 정렬은 개의 서열를 상단에, 고양이 서열을 하단에, 콘센수스 서열을 가운데에 표시한다.
개의 (의문(query); 서열 번호: 3의 일부분) v. 고양이 (대상, 서열 번호: 4의 일부분)
한 구체예에서, 용어 EPO는 야생형 서열(서열 번호: 3 또는 서열 번호: 4, 리더 펩티드 서열이 있거나, 또는 없거나)과 비교하였을 때, 하나 또는 그 이상의 아미노산 치환이 있는 활성 EPO를 말한다. 한 구체예에서, 잔기에서 하나 또는 그 이상의 아미노산 치환이 있으며, 상기 배열에서와 같이, 종간의 변이로 나타난다. 또다른 구체예에서, 잔기에서 하나 또는 그 이상의 아미노산 치환이 만들어지고, 이는 종간에 보존된다. 비록 EPO는 종간에 높은 정도의 동일성을 공유하지만, 한 구체예에서, 벡터를 궁극적으로 투여하게 되는 대상의 종에 근거하여 상기 EPO 서열을 선택하는 것이 바람직할 수 있다. 한 실시예에서, 상기 대상은 포유류다. 예를 들면, 한 구체예에서, 상기 대상이 고양이라면, 상기 EPO 서열은 고양이 단백질로부터 유래된다. 또다른 구체예에서, 상기 EPO 서열은 개의 단백질로부터 유래된다. 또다른 구체예에서, 상기 EPO 서열은 비-인간 영장류 단백질로부터 유래된다. 또다른 구체예에서, 상기 EPO은 소, 양 또는 돼지 단백질로부터 유래된다. 또다른 구체예에서, 상기 EPO 서열은 서열 번호: 3이다. 또다른 구체예에서, 상기 EPO 서열은 서열 번호: 4이다.
EPO 펩티드 또는 핵산 코딩 서열은 EPO 성숙 단백질 서열과 함께, 이종성 리더 서열을 포함할 수 있다. 단백질 또는 핵산과 관련하여 사용되는 경우 "이종성(heterologous)"이라는 용어는 단백질 또는 핵산이 본질상 서로 동일한 관계에 있지 않는 2 개 또는 그 이상의 서열 또는 하위서열을 포함한다는 것을 나타낸다. 예를 들어, 발현 카세트는 전형적으로 새로운 기능성 핵산을 만들도록 배열된 비-관련 유전자로부터의 2 개 또는 그 이상의 서열을 갖도록 재조합적으로 생산된다. 예로써, 한 구체예에서, 상기 리더 서열은 EPO와는 다른 유전자로부터 유래될 수 있다. 따라서, EPO 코딩 서열에 있어서, 상기 리더는 이종성이다. 한 구체예에서, 상기 리더 서열은 EPO 서열과는 상이한 종으로부터 유래된다.
한 구체예에서, 상기 서열은 EPO 성숙 폴리펩티드의 상류에 융합된 IL-2 리더 펩티드를 인코드한다. 한 구체예에서, 상기 리더 서열은 서열 번호: 9: M Y R M Q L L S C I A L S L A L V T N S이다. 그러나, 또다른 이종성 리더 서열은 IL-2 신호/리더 펩티드에서 치환될 수 있다. 상기 리더는 사이토킨 (예: IL-2, IL12, IL18 또는 유사한 것들), 면역글로블린, 인슐린, 알부민, β-글루쿠로니다아제, 알칼리성 프로테아제 또는 피브로넥틴 분비 신호 펩티드 또는 조직 특이적 분비 단백질의 서열일 수 있다. 한 구체예에서, 상기 리더 서열은 EPO 프로펩티드로부터 유래된 내생성 리더 서열이다.
본 명세서에서 이용된 바와 같이, 용어 "유래된(derived)" 또는 "~로부터 유래된"이란 서열 또는 단백질은 특정 대상 종으로부터 유래되거나, 또는 특정 대상 종으로부터 유래된 단백질 또는 서열과 동일한 서열을 공유한다는 것을 의미한다. 예를 들면, 개로부터 "유래된" 프로펩티드 서열은 개에서 발현되는 동일한 프로펩티드 서열과 동일한 서열 (또는 본원에서 정의된 바와 같은, 이의 변이체)을 공유한다. 그러나, 특정 핵산 또는 아미노산은 실제로 개로부터 기원될 필요는 없다. 유사한 단백질 (가령, 동족체)의 돌연변이 유발 또는 핵산 또는 아미노산 서열의 인위적 생산을 비롯한, 원하는 서열을 생성할 수 있는 다양한 기술이 당업계에 공지되어 있다. "유래된" 핵산 또는 아미노산은 유래된 서열의 실제 공급원과는 무관하게, 그것이 "유래된" 종에서의 동일한 핵산 또는 아미노산 기능을 보유한다.
본 명세서에서 이용된 바와 같이, 용어 "EPO 구조체", "EPO 발현 구조체" 및 동의어는 본원에서 기술된 EPO 서열을 포함한다. 용어 "EPO 구조체", "EPO 발현 구조체" 및 동의어는 EPO (내인성 또는 이종성 리더를 갖는 EPO 성숙 단백질 또는 프로펩티드 포함)를 인코드하는 핵산 서열 또는 이의 발현 산물을 지칭할 때 이용될 수 있다.
용어 "아미노산 치환(substitution)" 및 이의 동의어는 아미노산을 다른 아미노산으로 대체함으로써, 아미노산 서열을 변형시키는 것을 포함한다. 상기 치환은 보존적 치환일 수 있다. 또는 비-보존적 치환일 수도 있다. 2 개의 아미노산을 언급할 때, 보존적(conservative)이라는 용어는 아미노산이 당업자에 의해 인식되는 공통적인 특성을 공유함을 의미한다. 예를 들면, 소수성 비-산성 측쇄를 갖는 아미노산, 소수성 산성 측쇄를 갖는 아미노산, 친수성 비-산성 측쇄를 갖는 아미노산, 친수성 산성 측쇄를 갖는 아미노산 그리고 친수성 염기성 측쇄를 갖는 아미노산이 포함된다. 공통적인 특성은 소수성 측쇄를 갖는 아미노산, 지방족 소수성 측쇄를 갖는 아미노산, 방향족 소수성 측쇄를 갖는 아미노산, 극성 중성 측쇄를 갖는 아미노산, 전기적으로 하전된 측쇄를 갖는 아미노산, 전기적으로 하전된 산성 측쇄 그리고 전기적으로 하전된 염기성 측쇄를 가진 아미노산일 수도 있다. 자연 발생적, 그리고 비-자연 발생적 아미노산은 당업계에 공지되어 있고, 구체예에서 아미노산을 대체하는데 사용될 수 있다. 아미노산을 치환하는 방법은 당해 기술 분야의 숙련자에게 잘 알려져 있으며, 아미노산 서열을 코딩하는 뉴클레오티드 서열의 돌연변이를 포함하나, 이에 한정되지 않는다. 본 명세서에서의 "하나 또는 그 이상"에 대한 언급은 예를 들어 1, 2, 3, 4, 5, 6개 또는 그 이상의 개별적인 구체예를 포함하는 것으로 의도된다.
또한, 본원에 기재된 어셈블리된(assembled) EPO 단백질이 제공된다. 한 구체예에서, EPO 단백질은 기술된 AAV 구조체에 의해 만들어진다. 한 구체예에서, EPO 단백질은 성숙한 EPO 단백질과 조합된, 이종성 리더를 포함한다. 한 구체예에서, 상기 이종성 리더는 IL-2로부터 유래된다. 어셈블리된 EPO 단백질은 진단 분석을 비롯한, 많은 용도를 갖는다. 따라서, 한 구체예에서, 상기 EPO 단백질은 라벨된다. 본원에 사용된 바와 같이, "라벨(labels)"은 EPO 단백질을 표지하는데 유용한 화학적 또는 생화학적 잔기이다. "라벨"은 형광제, 화학발광제, 발색제, 담금질제, 방사성핵종, 효소, 기질, 보조인자, 억제제, 방사성 동위원소, 자성 입자 및 당해 분야에 공지된 다른 모이어티를 포함한다. "라벨" 또는 "리포터 분자(reporter molecules)"는 측정가능한 신호를 생성할 수 있고, 올리고뉴클레오티드 또는 뉴클레오티드 (예 : 비-천연 뉴클레오티드) 또는 리간드에 공유 결합 또는 비공유 결합될 수 있다. 가장 바람직하게는, 라벨은 시각적으로, 가령, 비색(colorimetrically)에 의해 검출 가능하다. 이러한 많은 라벨은 당업계에 공지되어 있으며, FITC (플루오레신 이소티오시아네이트), PE (피코에리트린), APC (코인포스핀-O) 또는 CPD (텐덤 염료), PE-시아닌-5 (PC5) 및 PE-텍사스 레드(Texas Red) (ECD)를 포함하나, 이에 국한되지 않는다. 일반적으로 사용되는 형광색소(fluorochromes)에는 플루오레신 이소티오시아네이트(FITC), 피코에리트린 (PE), 알로피코시아닌(APC) 등이 있으며, 또한 탠덤 염료인 PE-시아닌-5 (PC5), PE-시아닌-7 (PC7), PE-시아닌-5.5, PE-텍사스 레드 (ECD), 로다민, PerCP, 플루오레신 이소티오시아네이트 (FITC) 및 알렉사(Alexa) 염료가 포함된다. 분석 방법에 따라, 텍사스 레드 및 로다민 (rhodamine), FITC + PE, FITC + PECy5 및 PE + PECy7과 같은 그러한 라벨들의 조합이 사용될 수 있다. 다른 바람직한 라벨 또는 태그(tags)는 단백질의 기질 상에 물리적 분리 또는 고정화를 허용하는 것들을 포함한다. 이러한 라벨에는 바이오틴이 포함된다. 다른 적합한 라벨 또는 태그는 예를 들어, 본 명세서에 참고로 포함된 미국 2011-0177967 A1에 기재되어 있다.
또다른 구체예에서, EPO 펩티드는 상기 EPO 서열로부터 최대 10% 변이를 함유하는 변이체들을 포함한다. 즉, 상기 EPO 펩티드는 본원에서 제시된 및/또는 당분야에 공지된 EPO 서열에 대하여 약 90% 동일성 내지 약 99.9 % 동일성, 약 95% 내지 약 99% 동일성 또는 약 97% 내지 약 98% 동일성을 공유한다.
본원에서 제공되는 EPO 펩티드에 추가하여, 이들 펩티드를 인코드하는 핵산 서열들이 제시된다. 한 구체예에서, 본 명세서에서 기술된 EPO 펩티드를 인코드하는 핵산 서열이 제시된다. 또다른 구체예에서, 여기에는 서열 번호: 3의 개 EPO 단백질 또는 서열 번호: 3과 최소한 90% 동일성을 공유하는 서열을 인코드하는 임의의 핵산이 포함된다. 또다른 구체예에서, 여기에는 서열 번호: 4의 고양이 EPO 단백질 또는 서열 번호: 4와 최소한 90% 동일성을 공유하는 서열을 인코드하는 임의의 핵산이 포함된다.
한 구체예에서, 개의 EPO를 인코드하는 핵산 서열은 서열 번호: 5이다. 한 구체예에서, 고양이의 EPO를 인코드하는 핵산 서열은 서열 번호: 6이다. 여전히 또다른 구체예에서, EPO 핵산은 본 명세서에서 기술된 또는 당분야에 공지된 EPO 서열로부터 최대 10% 변이를 함유하는 변이체들을 포함한다. 여전히 또다른 구체예에서, EPO 핵산은 본 명세서에서 기술된 또는 당분야에 공지된 EPO 서열로부터 최대 20% 변이를 함유하는 변이체들을 포함한다. 여전히 또다른 구체예에서, EPO 핵산은 본 명세서에서 기술된 또는 당분야에 공지된 EPO 서열로부터 최대 30% 변이를 함유하는 변이체들을 포함한다. 또다른 구체예에서, EPO 핵산은 본 명세서에서 기술된 또는 당분야에 공지된 EPO 서열로부터 최대 40% 변이를 함유하는 변이체들을 포함한다.
한 구체예에서, EPO을 코딩하는 핵산 서열은 기술된 서열과 최소한 90% 동일성을 공유하는 서열을 포함한, 본원에 기재된 EPO 펩티드 중 임의의 것을 코딩하는 코돈 최적화 서열이다. 한 구체예에서, 핵산 서열은 투여가 요구되는 대상에서 발현되도록 코돈 최적화된다. 한 구체예에서, 개의 EPO를 인코드하는 핵산 서열은 서열 번호: 7이다. 한 구체예에서, 고양이의 EPO를 인코드하는 핵산 서열은 서열 번호: 8이다.
EPO 펩티드의 변이체가 바람직한 경우, 이들 펩티드의 코딩 서열은 야생형 핵산 서열의 부위-지향된(site-directed) 돌연변이유발을 이용하여 생성될 수 있다. 웹 기반 또는 상업적으로 이용가능한 컴퓨터 프로그램 뿐만 아니라, 서비스 기반 회사는 아미노산 서열을 RNA 및/또는 cDNA 둘 모두를 포함하는 핵산 코딩 서열로 역-해독하는데 사용될 수 있다. 가령 , backtranseq by EMBOSS, http://www.ebi.ac.uk/Tools/st/ ; Gene Infinity (http://www.geneinfinity.org/sms-/sms_backtranslation.html); ExPasy (http://www.expasy.org/tools/) 참고. 한 구체예에서, RNA 및/또는 cDNA 코딩 서열은 본원에서 논의된 바와 같이, 궁극적으로 투여하기로 의도된 대상 종에서 최적 발현되도록 기획된다. 따라서, 한 구체예에서, 상기 코딩 서열은 고양이에서 최적 발현되도록 기획된다. 또다른 구체예에서, 상기 코딩 서열은 개에서 최적 발현되도록 기획된다. 또다른 구체예에서, 상기 코딩 서열은 영장류에서 최적 발현되도록 기획된다.
상기 코딩 서열은 코돈 최적화(optimization)를 이용한 최적 발현을 위하여 기획된다. 상이한 다양한 방법에 의해 코돈-최적화된 코딩 영역이 기획될 수 있다. 이러한 최적화는 온라인, 공개된 방법 또는 코돈 최적화 서비스를 제공하는 회사에서 이용가능한 방법을 사용하여 수행될 수 있다. 하나의 코돈 최적화 방법은 예를 들어, 본 명세서에 참고자료에 편입된 국제 특허 공개 번호 WO 2015/012924에 기술되어있다. 간략하게 설명하자면, 생성물을 코딩하는 핵산 서열은 유사한 코돈 서열로 변형된다. 적합하게는, 산물의 개방 판독 틀 (ORF)의 전체 길이가 변경된다. 그러나, 일부 구체예들에서, ORF의 단편만 변경될 수 있다. 이들 방법 중 하나를 사용함으로써, 주어진 폴리펩티드 서열에 빈도를 적용하고, 이 폴리펩티드를 인코딩하는 코돈-최적화된 코딩 영역의 핵산 단편을 생성할 수 있다.
핵산 서열의 문맥에서 "동일성 백분율(%)", "서열 동일성", "서열 동일성 백분율" 또는 "동일 백분율"이란 용어는 대응하도록 정렬될 때, 두 서열에서 동일한 두 서열의 염기를 의미한다. 서열 동일성 비교 길이는 게놈의 전장, 유전자 코딩 서열의 전장, 또는 적어도 약 100 내지 150개의 뉴클레오티드의 단편, 또는 원하는 데로 될 수 있다. 그러나, 더 작은 단편들 사이의 동일성, 가령, 적어도 약 9 개 뉴클레오티드, 보통 약 20 내지 24개 뉴클레오티드, 약 28 내지 32 뉴클레오티드, 약 36 개 또는 그 이상의 뉴클레오티드가 또한 바람직할 수 있다. 다중 서열 정렬 프로그램은 핵산 서열에도 이용 가능하다. 이러한 프로그램의 예로는 인터넷상의 웹 서버를 통해 액세스할 수 있는 "Clustal W", "CAP Sequence Assembly", "BLAST", "MAP" 및 "MEME"가 있다. 그러한 프로그램의 다른 원천은 당업자에게 공지되어 있다. 또는 Vector NTI 유틸리티도 사용된다. 상기 기술된 프로그램에 포함된 것을 포함하여, 뉴클레오티드 서열 동일성을 측정하는데 사용될 수 있는 당업계에 공지된 다수의 알고리즘이 또한 존재한다. 다른 예로서, 폴리뉴클레오티드 서열은 GCG 버젼 6.1의 프로그램인 Fasta ™를 사용하여 비교될 수 있다. Fasta ™는 의문(query) 서열과 검색 서열 사이의 가장 잘 겹쳐지는 영역의 정렬 및 서열 동일성 백분율을 제공한다. 예를 들어, 핵산 서열 간의 서열 동일성 백분율은 참조로 포함된 GCG 버전 6.1에 제공된 바와 같이, 그의 디폴트 매개변수 (워드 크기 6 및 스코어링 매트릭스에 대한 NOPAM 인자)를 갖는 Fasta™를 사용하여 결정될 수 있다.
아미노산 서열의 문맥에서 "동일성 백분율(%)", "서열 동일성", "서열 동일성 백분율" 또는 "동일 백분율"이란 용어는 대응하도록 정렬될 때, 두 서열에서 동일한 잔기를 의미한다. 동일성 백분율은 전장의 단백질, 폴리펩티드, 약 70개 아미노산 내지 약 100개의 아미노산, 또는 이의 펩티드 단편 또는 상응하는 핵산 서열 코딩 서열에 걸친 아미노산 서열에 대해 용이하게 결정될 수 있다. 적합한 아미노산 단편은 적어도 약 8개 아미노산 길이 일 수 있고, 최대 약 150개 아미노산일 수 있다. 일반적으로, 두 개의 다른 서열 사이의 "동일성", "상동성(homology)" 또는 "유사성(similarity)"을 언급할 때, "동일성", "상동성" 또는 "유사성"은 "정렬된(aligned)"서열과 관련하여 결정된다. "정렬된" 서열 또는 "정렬(alignments)"은 다수의 핵산 서열 또는 단백질 (아미노산) 서열을 말하며, 종종 참조 서열과 비교하여 누락 또는 추가 염기 또는 아미노산에 대한 보정을 포함한다. 정렬은 공개적으로 또는 상업적으로 이용가능한 다양한 다중 서열 정렬 프로그램 중 임의의 것을 사용하여 수행된다. 서열 정렬 프로그램은 가령, "Clustal X", "MAP", "PIMA", "MSA", "BLOCKMAKER", "MEME" 및 "Match-Box" 프로그램과 같은 아미노산 서열에 사용할 수 있다. 일반적으로, 이들 프로그램 중 임의의 것은 디폴트 설정에서 사용되지만, 당업자는 필요에 따라 이들 설정을 변경할 수 있다. 대안적으로, 당업자는 적어도 참조된 알고리즘 및 프로그램에 의해 제공되는 것과 동일성 수준 또는 정렬 수준을 제공하는 다른 알고리즘 또는 컴퓨터 프로그램을 이용할 수 있다. 가령 , J. D. Thomson et al, Nucl. Acids. Res., "A comprehensive comparison of multiple sequence alignments", 27(13):2682-2690 (1999) 참고.
한 구체예에서, 본원에서 기술된 EPO 구조체를 인코드하는 핵산 서열은 임의의 적합한 유전적 요소, 가령, 네이키드 DNA, 파아지, 트랜스포존, 코스미드, RNA 분자 (가령, mRNA), 에피좀 등등의 안으로 조작될 수 있고, 이것은 패키징 숙주 세포에서 DNA 또는 RNA, 바이러스 벡터를 운반하는 나노입자를 만들거나 및/또는 대상의 숙주 세포로 전달하기 위하여, 숙주 세포로 EPO 서열을 전달한다. 한 구체예에서, 상기 유전 요소는 플라스미드다. 선택된 유전 요소는 형질 감염, 전기천공, 리포좀 전달, 막 융합 기술, 고속 DNA-코팅된 펠렛, 바이러스 감염 및 원형질체 융합을 포함하는 임의의 적합한 방법에 의해 전달될 수 있다. 이러한 구조체를 제조하는 데 사용되는 방법은 유전 공학, 재조합 공학 및 합성 기술을 포함하는 핵산 조작 기술이 있는 사람들에게 공지되어 있다. 가령 , Green and Sambrook, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Press, Cold Spring Harbor, NY (2012) 참고.
본 명세서에서 이용된 바와 같이, "발현 카세트(expression cassette)"는 EPO 펩티드의 코딩 서열, 프로모터, 프로모터를 포함하는 핵산 분자를 지칭하며, 그리고 이를 위한 임의의 다른 조정 서열을 포함할 수 있고, 이 카세트는 유전자 요소로 조작되거나, 또는 바이러스 벡터의 캡시드 (capsid)(예: 바이러스 입자)에 패키징된다. 전형적으로, 바이러스 벡터를 생성하기 위한 이러한 발현 카세트는 바이러스 벡터 게놈의 패키징 서열과 본원에 기술된 것과 같은 다른 발현 제어 서열 측면에 위치하는 본원에 기술된 EPO 구조체 서열을 함유한다. 당분야에 공지된 기술, 본원에서 기술된 바와 같이 가령, 코돈 최적화를 포함하는 기술을 이용하여 특정 종에 대하여 최적화될 수 있다.
상기 발현 카세트는 발현 제어 서열의 일부분으로써 프로모터 서열을 전형적으로 포함한다. 한 구체예에서, CB7 프로모터가 이용된다. CB7은 사이토메갈로바이러스 인헨서 요소와 함께, 병아리 β-액틴 프로모터다. 대안으로, 다른 간-특이적 프로모터들이 이용된다[가령, The Liver Specific Gene Promoter Database, Cold Spring Harbor, http://rulai.schl.edu/LSPD, alpha 1 anti-trypsin(A1AT); human albumin Miyatake et al., J. Virol., 71:5124 32 (1997), humAlb; and hepatitis B virus core promoter, Sandig et al., Gene Ther., 3:1002 9 (1996)]. TTR 최소 인헨서/프로모터, 알파-안티트립신 프로모터, LSP (845 nt)25(인트론이-적은 scAAV를 요구함). 한 구체예에서, 간-특이적 프로모터 티록신 결합 글로불린(TBG)이 이용된다. 다른 프로모터, 이를 테면, 바이러스 프로모터, 구성 프로모터, 규제가능한 프로모터 [가령, WO 2011/126808 및 WO 2013/04943 참고], 또는 생리학적 신호에 반응성이 있는 프로모터가 본원에서 기술된 백터에 사용될 수 있다.
프로모터에 추가하여, 발현 카세트 및/또는 벡터는 다른 적합한 전사 개시, 종료, 인헨서 서열, 효과적인 RNA 프로세싱 신호, 이를 테면, 스플라이싱 및 폴리아데닐화(polyA) 신호; TATA 서열; 세포질 mRNA를 안정화시키는 서열; 해독 효과를 강화시키는 서열(가령, Kozak 콘센수스 서열); 인트론; 단백질 안정성을 강화시키는 서열; 그리고 바람직한 경우, 인코드된 산물의 분비를 강화시키는 서열을 포함할 수 있다. 발현 카세트 또는 벡터는 본원에 기재된 임의의 요소, 하나 이상의 요소를 함유할 수 있거나, 또는 함유하지 않을 수 있다. 적합한 polyA 서열의 예로는 가령, SV40, 소 성장 호르몬 (bGH), 및 TK poly A를 포함한다. 적합한 인헨서의 예로는 그중에서도 가령, CMV 인헨서, RSV 인헨서, 알파 훼토단백질 인헨서, TTR 최소 프로모터/인헨서, LSP (TH-결합 글로불린 프로모터/알파 1-마이크로글로불린/비쿠민 인헨서)를 포함한다.
한 구체예에서, 상기 바이러스 벡터는 다음을 포함하는 핵산 발현 카세트를 함유한다: 5' AAV 역전된 말단 반복 서열 (ITR), 임의선택적 인헨서와 함께 프로모터, EPO 서열, poly A 서열, 그리고 3' AAV ITR, 이때 전술한 발현 카세트는 숙주 세포에서 기능 EPO를 발현한다.
이들 제어 서열은 상기 EPO 구조체 서열에 "작동가능하도록 연계된다(operably linked)". 본 명세서에서 이용된 바와 같이, 용어 "작동가능하도록 연계된(operably linked)"이란 관심대상 유전자와 연접하는 발현 조절 서열과 관심대상 유전자를 조절하기 위해 트랜스(trans) 또는 먼 거리에서 작용하는 발현 제어 서열 모두를 지칭한다.
상기 발현 카세트는 바이러스 벡터의 생산에 사용되는 플라스미드 상에서 조작될 수 있다. 상기 발현 카세트를 AAV 바이러스 입자 안으로 패키지하는데 요구되는 최소 서열은 AAV 5' 및 3' ITRs이며, 이들은 캡시드와 동일한 AAV 기원이거나, 또는 상이한 AAV 기원 (AAV 위형(pseudotype)을 만들기 위하여)일 수 있다. 한 구체예에서, AAV2의 ITR 서열, 또는 이의 결손된 형태(△ITR)는 조정 승인을 가속화시키기 위하여 편리하게 이용된다. 그러나, 다른 AAV 원천의 ITRs이 선택될 수 있다. ITRs의 원천이 AAV2이고, 그리고 AAV 캡시드는 또다른 AAV 원천인 경우, 생성된 벡터는 위형(pseudotype)이라고 부를 수 있다. 전형적으로, AAV 벡터의 발현 카세트는 AAV 5' ITR, 상기 프로펩티드-EPO 활성 펩티드 코딩 서열 및 임의의 조정 서열, 그리고 AAV 3' ITR을 포함한다. 그러나, 이들 요소들의 다른 배위(configurations)가 적합할 수 있다. D-서열 및 말단 해리 부위 (trs)이 결손된 단축된 형태의 5' ITR(ΔITR로 명명)이 기술되었다. 다른 구체예들에서, 전장의 AAV 5' 및 3' ITRs이 이용된다.
예시적인 플라스미드가 서열 목록에서 제시된다. 서열 번호: 1은 pn1044.CB7.caEPO으로 명명된, 개의 EPO 구조체를 인코드하는 플라스미드 서열이다. 한 구체예에서, 상기 발현 카세트는 서열 번호: 1의 플라스미드로 조작된다. 서열 번호: 2는 pn1044.CB7.feEPO로 명명된, 고양이의 EPO 구조체를 인코드하는 플라스미드 서열이다. 한 구체예에서, 상기 발현 카세트는 서열 번호: 2의 플라스미드로 조작된다. 서열 번호: 1 및 서열 번호: 2에 나타낸 바와 같은 플라스미드는 본원에 기재된 바와 같은 하나 이상의 추가 성분을 포함하도록, 또는 필요에 따라 성분을 제거 또는 대체하도록 변형될 수 있다. 한 구체예에서, 상기 플라스미드는 서열 번호: 1의 서열 또는 이와 최소한 80% 동일성을 공유하는 서열을 갖는다. 또다른 구체예에서, 상기 플라스미드는 서열 번호: 2의 서열 또는 이와 최소한 80% 동일성을 공유하는 서열을 갖는다.
약어 "sc"는 자가-상보성을 나타낸다. "자가-상보성(self-complementary) AAV"는 재조합 AAV 핵산 서열에 의해 운반되는 코딩 영역이 분자내 이중-가닥 DNA 주형을 형성하도록 기획된, 발현 카세트를 갖는 플라스미드 또는 벡터를 말한다. 감염시, 제2 가닥의 세포 매개된 합성을 기다리기보다는, scAAV의 두 개의 상보적인 절반은 연관되어 즉시 복제 및 전사가 가능한 한 개의 이중 가닥 DNA (dsDNA) 유닛을 형성할 것이다. 가령 , D M McCarty et al, "Self-complementary recombinant adeno-associated virus (scAAV) vectors promote efficient transduction independently of DNA synthesis", Gene Therapy, (August 2001), Vol 8, Number 16, Pages 1248-1254 참고. 자가-상보성 AAVs는 가령, 미국 특허 번호 6,596,535; 7,125,717; 및 7,456,683에 기술되어 있으며, 이들 각각은 모두 전문이 본 명세서의 참고자료에 편입된다.
아데노-연합된 바이러스 (AAV) 바이러스 벡터는 표적 세포로 운반을 위하여 패키지된 핵산 서열인, AAV 단백질 캡시드를 갖는 AAV DNase-저항성 입자다. AAV 캡시드는 60개의 캡시드 (cap) 단백질 소단위, VP1, VP2, 및 VP3로 구성되며, 이들은 선택된 AAV에 따라, 대략적으로 1:1:10 내지 1:1:20의 비율의 정이십면체 대칭으로 정렬된다. AAV 혈청형(serotypes)은 AAV 바이러스 벡터 (DNase 저항성 바이러스 입자)의 캡시드의 원천으로 선택될 수 있는데, 가령, AAV1, AAV2, AAV3, AAV4, AAV5, AAV6, AAV6.2, AAV7, AAV8, AAV9, rh10, AAVrh64R1, AAVrh64R2, rh8, rh.10, 임의의 공지의 또는 언급된 AAVs 또는 AAVs의 앞으로 발견될 변이체들이다. 한 구체예에서, 상기 AAV는 AAV8 캡시드 또는 이의 변이체다. 가령 , 미국 공개된 특허 출원 번호 2007-0036760-A1; 미국 공개된 특허 출원 번호. 2009-0197338-A1; EP 1310571 참고. WO 2003/042397 (AAV7 및 다른 유사한 AAV), 미국 특허 7790449 및 미국 특허 7282199 (AAV8), WO 2005/033321 및 미국 7,906,111 (AAV9), 그리고 WO 2006/110689, 그리고 WO 2003/042397 (rh.10) 참고. 대안으로, 임의의 언급된 AAVs를 바탕으로 재조합 AAV는 AAV 캡시드의 원천으로 이용될 수 있다. 이 문서는 또한 AAV를 생성하기 위해 선택될 수 있는 다른 AAV를 기술하며, 이들은 참고자료에 편입된다. 일부 구체예들에서, 바이러스 벡터에서 이용되는 AAV cap는 전술한 AAV Caps 또는 이를 인코드하는 핵산의 돌연변이생성(가령, 삽입, 결손 또는 치환에 의해)에 의해 생성될 수 있다. 일부 구체예들에서, 상기 AAV 캡시드는 전술한 AAV 캡시드 단백질중 2개 또는 3개 또는 4개 또는 그 이상으로부터 유래된 도메인을 포함하는, 키메라다. 일부 구체예들에서, 상기 AAV 캡시드는 상이한 2개 또는 3개의 AAVs 또는 재조합 AAVs로부터 Vp1, Vp2, 및 Vp3 단량체의 모자이크다. 일부 구체예들에서, rAAV 조성물은 전술한 Caps중 하나 이상을 포함한다. 또다른 구체예에서, 상기 AAV 캡시드는 임의의 기술된 또는 공지의 AAV 캡시드 서열로부터 최대 10% 변이를 함유하는 변이체들을 포함한다. 즉, 상기 AAV 캡시드는 본원에서 제시된 및/또는 당분야에 공지된 AAV 캡시드에 대하여 약 90% 동일성 내지 약 99.9 % 동일성, 약 95% 내지 약 99% 동일성 또는 약 97% 내지 약 98% 동일성을 공유한다. 한 구체예에서, 상기 AAV 캡시드는 AAV 캡시드와 최소한 95% 동일성을 공유한다. AAV 캡시드의 동일성을 결정할 때, 임의의 가변 단백질 (예를 들어, vp1, vp2 또는 vp3)에 대해 비교할 수 있다. 한 구체예에서, 상기 AAV 캡시드는 상기 AAV8 vp3과 최소한 95% 동일성을 공유한다. 또다른 구체예에서, 자가-상보성 AAV가 이용된다.
발현 카세트를 비리온(virions)으로 패키징하기 위하여, 상기 ITRs는 동일한 구조체 안에서 이 유전자와 동일한 cis 형태로 요구되는 유일한 AAV 성분들이다. 한 구체예에서, AAV 벡터를 만들기 위하여, 복제 (rep) 및/또는 캡시드 (cap)를 위한 코딩 서열은 AAV 게놈으로부터 제거되고, trans로 공급되거나, 또는 패키징 세포 계통에 의해 공급된다. 예를 들면, 상기와 같이, 위형의(pseudotyped) AAV는 상기 AAV 캡시드의 원천과는 상이한 원천으로부터 유래된 ITRs을 함유할 수 있다. 추가적으로, 또는 대안으로, 키메라 AAV 캡시드를 이용할 수 있다. 여전히 다른 AAV 성분들이 선택될 수 있다. 그러한 AAV 서열의 출처는 여기에 기술되어 있으며, 학술, 상업 또는 공공 출처로부터 단리되거나 획득될 수도 있다(가령, American Type Culture Collection, Manassas, VA). 대안으로, 상기 AAV 서열은 문헌, 또는 예를 들어 GenBank®, PubMed®, 등과 같은 데이터베이스에서 이용가능한 공개된 서열을 참조하여 합성 또는 다른 적절한 수단을 통해 수득할 수 있다.
대상에게 전달하기에 적합한 AAV 바이러스 벡터를 생성하고 단리하는 방법은 당업계에 공지되어 있다. 가령 , 미국 특허 7790449; 미국 특허 7282199; WO 2003/042397; WO 2005/033321, WO 2006/110689; 미국 7588772 B2 참고]. 한 시스템에서, 생산자 세포주는 ITR에 의해 측면에 위치하는 이식유전자(transgene) 및 rep와 cap을 인코딩하는 구조체 (들)에 의해 일시적으로 형질감염된다. 제 2 시스템에서, rep 및 cap을 안정적으로 공급하는 패키징 세포계통은 ITRs의 측면에 있는 이식유전자를 인코딩하는 구조체로 일시적으로 형질감염된다. 이들 각 시스템에서, AAV 비리온은 헬퍼(helper) 아데노바이러스 또는 헤르페스바이러스의 감염에 반응하여 생성되는데, 오염 바이러스로부터 상기 rAAVs의 분리가 필요하다. 더욱 최근에, AAV를 회수시키기 위하여, 헬퍼 바이러스를 이용한 감염이 요구되지 않는 시스템이 개발되었는데, 요구되는 헬퍼 기능 (가령, 아데노바이러스 E1, E2a, VA, 및 E4 또는 헤르페스바이러스 UL5, UL8, UL52, 및 UL29, 그리고 헤르페스바이러스 중합효소)이 이 시스템에 의해 trans로 또한 공급된다. 이들 신규 시스템에서, 헬퍼 기능은 요구되는 헬퍼 기능을 인코드하는 구조체로 이 세포의 일시적 형질감염에 의해 공급될 수 있거나, 또는 이 세포들은 헬퍼 기능을 인코드하는 유전자를 안정적으로 함유하도록 조작될 수 있고, 이의 발현은 전사 또는 전사후 수준에서 제어될 수 있다. 또다른 시스템에서, ITRs의 측면에 있는 이식유전자와 rep/cap 유전자는 베큘로바이러스-기반 벡터을 이용한 감염에 의해 곤충 세포로 도입된다. 이들 생산 시스템에 대한 검토는 일반적으로 가령, Zhang et al., 2009, "Adenovirus-adeno-associated virus hybrid for large-scale recombinant adeno-associated virus production," Human Gene Therapy 20:922-929를 참고하며, 이의 각 내용은 본 명세서의 참고자료에 전문이 편입된다. 이들 및 기타 AAV 생산 시스템을 만들고 이용하는 방법은 다음의 미국 특허에서 또한 설명되어 있으며, 이의 각 내용은 본 명세서의 참고자료에 전문이 편입된다: 5,139,941; 5,741,683; 6,057,152; 6,204,059; 6,268,213; 6,491,907; 6,660,514; 6,951,753; 7,094,604; 7,172,893; 7,201,898; 7,229,823; 및 7,439,065. 가령, Grieger & Samulski, 2005, "Adeno-associated virus as a gene therapy vector: Vector development, production and clinical applications," Adv. Biochem. Engin/Biotechnol. 99: 119-145; Buning et al., 2008, "Recent developments in adeno-associated virus vector technology," J. Gene Med. 10:717-733; 그리고 하기에서 언급된 문헌들을 참고하며, 이의 각 내용은 본 명세서의 참고자료에 전문이 편입된다: 본 발명의 임의의 구체예를 구축하는데 이용되는 방법은 유전 공학, 재조합 공학 및 합성 기술을 포함하는 핵산 조작 기술이 있는 사람들에게 공지되어 있다. 가령 , Green and Sambrook et al, Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Press, Cold Spring Harbor, NY (2012) 참고. 유사하게, rAAV 비리온을 생성하는 방법은 잘 알려져 있으며, 본 발명에서 적합한 방법의 선택은 제한되는 것은 아니다. 가령, K. Fisher et al, (1993) J. Virol., 70:520-532 및 미국 특허 번호 5,478,745 참고.
본원에서 기술된 바이러스 벡터 구조체를 포함하는 조성물이 또한 제시된다. 본원에서 기술된 약학 조성물은 임의의 적합한 경로 또는 상이한 경로의 조합에 의해 이를 필요로 하는 대상에게 전달되도록 기획된다. 간으로 직접 전달 (임의선택적으로 정맥을 경유하여, 간 동맥을 경유하여, 또는 이식에 의해), 경구, 흡입, 비강내, 기관내(intratracheal), 동맥내, 안구내, 정맥내, 근육내, 피하, 피내, 그리고 다른 비경구 투여. 본원에서 기술된 바이러스 벡터는 단일 조성물 또는 다중 조성물로 전달될 수 있다. 임의선택적으로, 2개 또는 그 이상의 상이한 AAV가 전달될 수 있거나, 또는 다중 바이러스[가령, WO 2011/126808 및 WO 2013/049493 참고]. 또다른 구체예에서, 다중 바이러스는 상이한 복제-결함성 바이러스(가령, AAV 및 아데노바이러스)를 함유할 수 있다.
상기 복제-결함성 바이러스는 유전자 전달 및 유전자 치료 응용에 사용하기 위해 생리학적으로 수용가능한 담체와 함께 제형화될 수 있다. AAV 바이러스 벡터의 경우, 게놈 복사체 ("GC")의 정량화는 제형 또는 현탁액에 포함된 용량(dose)의 척도로 사용될 수 있다. 당업계에 공지된 임의의 방법을 사용하여 본 발명의 복제-결함성 바이러스 조성물의 게놈 복사체 (GC) 수를 결정할 수 있다. AAV GC 수 적정을 실행하는 한 가지 방법은 다음과 같다: 정제된 AAV 벡터 시료를 우선 DNase로 처리하여, 캡슐화되지 않은 AAV 게놈 DNA 또는 생산 과정에서 오염된 플라스미드 DNA를 제거한다. 그런 다음 DNase 저항성 입자는 열처리하여, 캡시드에서 게놈을 방출시킨다. 그런 다음 방출된 게놈은 바이러스 게놈의 특정 영역(통상적으로 poly A 신호)을 표적으로 하는 프라이머/프로브 세트를 사용하여 실시간 PCR로 정량된다.
또한, 복제-결함성 바이러스 조성물은 약 1.0 × 109 GC 내지 약 1.0 × 1015 GC의 범위에 있는 복제-결함성 바이러스의 양을 함유하는 투약 단위로 제형화될 수 있다. 또다른 구체예에서, 이 양의 바이러스 게놈은 분할된 용량으로 전달될 수 있다. 한 구체예에서, 상기 투여량(dosage)은 평균 5kg의 고양이 또는 작은 개를 대상으로 하는 경우, 약 1.0 x 1010 GC 내지 약 1.0 x 1012 GC이다. 한 구체예에서, 평균 약 20 kg의 중간 개의 대상를 대상으로 하는 경우, 상기 투여량은 약 1.0 x 1011 GC 내지 약 1.0 x 1013 GC이다. 평균적으로 개의 체중은 약 5 내지 약 50 kg이다. 한 구체예에서, 대상의 투여량은 약 1.0 x 1011 GC 내지 1.0 x 1013 GC이다. 또다른 구체예에서, 용량 약 3 x 1012 GC이다. 예를 들면, AAV 바이러스의 용량은 약 1 x 1011 GC, 약 5 X 1011 GC, 약 1 X 1012 GC, 약 5 X 1012 GC, 또는 약 1 X 1013 GC일 수 있다. 한 구체예에서, 투약량은 약 3 X 1010 GC/kg이다. 또다른 실시예에서, 상기 구조체는 mL당 약 0.001 mg 내지 약 10 mg의 양으로 전달될 수 있다. 한 구체예에서, 상기 구조체는 수의과 동물 대상의 경우 1 μL 내지 약 100 mL 용적으로 전달될 수 있다. 가령, 다양한 수의과 동물에 물질을 투여하기 위한 양호한 실행에 대한 논의는 Diehl et al, J. Applied Toxicology, 21:15-23 (2001) 참고. 이 문헌은 본 명에서의 참고자료에 편입된다. 본 명세서에서 이용된 바와 같이, 용어 "투여량(dosage)"이란 용어는 치료 과정에서 대상에게 전달되는 총 투여 량 또는 단일 투여 (다중 투여)로 전달되는 양을 지칭할 수 있다.
상기 기술된 재조합 벡터는 공지된 방법에 따라 숙주 세포에 전달될 수 있다. 바람직하게는 생리학적으로 양립가능한 운반체, 희석제, 부형제 및/또는 어쥬번트에 현탁된 rAAV는 고양이, 개, 또는 비-인간 포유동물 대상을 포함하나, 이에 국한되지 않는 원하는 대상에게 투여될 수 있다. 적합한 운반체는 전달 바이러스에 의해 지시되는 관점을 고려하여, 당업자에 의해 용이하게 선택될 수 있다. 예를 들면, 한 가지 적합한 운반체는 염수를 포함하는데, 이는 다양한 완충 용액 (가령, 인산염 완충된 염수)로 제형화될 수 있다. 다른 예시적인 운반체는 염수, 락토스, 슈크로스, 인산 칼슘, 젤라틴, 덱스트린, 한천, 펙틴, 땅콩유, 참깨유, 및 물을 포함한다. 운반체의 선택은 본 발명에서 제한되지 않는다.
임의선택적으로, 본 발명의 조성물은 상기 rAAV 및/또는 변이체 및 운반체(들)에 추가하여, 다른 통상적인 약학 성분들, 이를 테면, 보존제 또는 화학적 안정제를 포함한다. 적절한 예시적인 보존제는 클로로부탄올, 소르빈산 칼륨, 소르 브산, 이산화황, 프로필 갈레이트, 파라벤, 에틸 바닐린, 글리세린, 페놀 및 파라클로로페놀을 포함한다. 적합한 화학적 안정제는 젤라틴 및 알부민을 포함한다.
본원에서 기술된 바이러스 벡터 및 다른 구조체는 EPO 구조체를 이를 필요로 하는 대상에게 전달하기 위하여 및/또는 대상의 만성 신장 질환을 치료하기 위한 약물 제조에 이용될 수 있다. 따라서, 또다른 측면에서, 만성 신장 질환을 치료하는 방법이 제시된다. 상기 방법은 이를 필요로 하는 대상에게 본원에서 기술된 바와 같은 조성물을 투여하는 것을 포함한다. 한 구체예에서, 상기 조성물은 본원에서 기술된 바와 같이, EPO 발현 카세트가 함유된 바이러스 벡터를 포함한다. 한 구체예에서, 상기 대상은 포유류다. 또다른 구체예에서, 상기 대상은 고양이 또는 개이다. 따라서, 또다른 측면에서, 빈혈을 치료하는 방법이 제시된다. 상기 방법은 이를 필요로 하는 대상에게 본원에서 기술된 바와 같은 조성물을 투여하는 것을 포함한다. 한 구체예에서, 상기 조성물은 본원에서 기술된 바와 같이, EPO 발현 카세트가 함유된 바이러스 벡터를 포함한다. 한 구체예에서, 상기 대상은 포유류다. 또다른 구체예에서, 상기 대상은 고양이 또는 개이다.
또다른 구체예에서, 고양이의 만성 신장 질환을 치료하는 방법이 제시된다. 상기 방법은 고양이 EPO를 인코드하는 서열이 포함된 핵산 분자가 포함된 바이러스 벡터를 상기 대상에게 투여하는 것을 포함한다. 또다른 구체예에서, 개의 만성 신장 질환을 치료하는 방법이 제시된다 상기 방법은 개의 EPO를 인코드하는 서열이 포함된 핵산 분자가 포함된 바이러스 벡터를 상기 대상에게 투여하는 것을 포함한다.
치료 과정은 임의선택적으로 동일한 바이러스 벡터 (가령, AAV8 벡터) 또는 상이한 바이러스 벡터 (가령, AAV8 및 AAVrh10)의 반복 투여를 포함할 수 있다. 또 다른 조합은 본원에 기재된 바이러스 벡터를 사용하여 선택될 수 있다. 임의선택적으로, 본원에서 기술된 조성물은 가령, 재조합 EPO를 포함하는, 다른 약물 또는 단백질-기반의 요법이 관련된 요법과 복합될 수 있다. 임의선택적으로, 본원에 기재된 조성물은 식이 요법 및 운동 요법을 포함하는 생활 습관 변화를 포함하는 요법과 조합될 수 있다.
용어 "a" 또는 "an"은 하나 이상을 지칭한다는 것을 유의해야 한다. 이와 같이, 용어 "하나"("a" (또는 "an")), "하나 이상"및 "적어도 하나"는 여기서 상호 교환 적으로 사용된다.
단어 "포함한다", "포함한다" 및 "포함하는"이란 배타적이지 않고 포괄적으로 해석되어야 한다. 단어 "구성하다", "구성하는" 및 그 변형은 포괄적인 것이 아니라 배타으로 해석되어야 한다. 본 명세서의 다양한 구체예가 "포함하는(comprising)" 언어를 사용하여 제공되는 동안, 다른 상황 하에서, 관련된 구체예는 또한 "구성된(consisting of)" 또는 "본질적으로 구성된(consisting essentially of)"의 언어를 사용하는 것으로 해석되고, 설명되도록 의도된다.
본 명세서에서 이용된 바와 같이, 용어 "약(about)"은 달리 언급하지 않는 한, 주어진 기준으로부터 10 %의 변동성을 의미한다.
본원에서 사용된 용어 "조절(regulation)" 또는 이의 변형은 생물학적 경로의 하나 또는 그 이상의 성분을 저해하는 조성물의 능력을 지칭한다.
"대상(subject)"은 인간, 마우스, 렛, 기니아 피그, 개, 고양이, 말, 소, 돼지 또는 비-인간 영장류, 가령, 원숭이, 침팬지, 비비 또는 고릴라와 같은 포유 동물이다. 본 명세서에서 이용된 바와 같이, 용어 "대상"은 "환자"와 호환사용된다.
본 명세서에서 이용된 바와 같이, "질병", "장애" 및 "상태"는 상호 호환적으로 사용되어, 대상의 비정상 상태를 나타낸다.
본 명세서에서 다르게 정의되지 않는 한, 본 명세서에서 사용되는 기술적 및 과학적 용어는 당업자가 일반적으로 이해하는 것과 동일한 의미를 가지며, 그리고 본 출원에서 이용된 많은 용어들에 대한 일반적인 지침을 당업자에게 제공하는 출판된 텍스트를 참조한다.
다음의 실시예들은 오직 설명을 위한 것이며, 본 명세서의 범위를 제한하려는 의도는 아니다.
실시예 1 - EPO 벡터의 구축
개 및 고양이 에리트로포에틴의 아미노산 서열은 Genbank에서 구하였다. 상기 아미노산 서열은 역-해독되고, 코돈 최적화되고, kozak 콘센수스 서열, 정지 코돈, 및 클로닝 부위가 추가된다. 이 서열은 GeneArt에서 만들었으며, CMV 인헨서 (p1044)와 함께, 병아리-베타 액틴 프로모터를 함유하는 발현 벡터 안에 클론되었다. 상기 발현 구조체는 AAV2 ITRs 측면에 있다. 개 및 고양이 구조체는 삼중 형질감염 및 이딕사놀(iodixanol) 구배 정제에 의해, 그리고 Taqman 정량적 PCR에 의해 적정되어, AAV 혈청형 8 캡시드 안에 패키지되었다.
실시예 2 - 고양이에서 고양이 에리트로포에틴의 AAV-매개된 발현
3 마리의 고양이에게 고양이 에리트로포에틴을 발현시키는 AAV8를 체중 킬로그램 (GC/kg) 당 3 x 1010 게놈 복사체를 단일 근육 주사하였다. (도 1). 혈액 샘플은 주입시 및 헤마토크릿 측정을 위해 주기적으로 수집하였다. 치료를 위한 정맥 절개는 벡터 주입 후 42 일에 시작되었다. 지금까지 EPO의 발현은 100 일 이상 지속된 결과가 나타났다.
실시예 3 - 개에서 개의 에리트로포에틴의 AAV-매개된 발현
3 마리의 개에게 개의 에리트로포에틴을 발현시키는 AAV8을 3 x 1010 의 단일 근육 주사하였다. 혈액 샘플은 주입시 그리고 헤마토크릿 측정을 위해 주기적으로 수집하였다 (도 2). 미처리된 새끼의 혈액 샘플을 대조군으로 포함시켰다. 치료를 위한 정맥 절개는 벡터 주입 후 60 일에 시작되었다.
실시예 4 - 고양이에서 고양이 에리트로포에틴의 AAV-매개된 발현의 투여량 연구
고양이에게 고양이 에리트로포에틴을 발현시키는 AAV8를 최대 3 x 107, 3 x 108, 3 x 109, 또는 3 x 1010 게놈 복사체(GC/kg)를 단일 근육 주사하였다. 이 3개 코호트는 투여량 당 4 마리의 고양이다. 모든 고양이는 정상/야생형으로 무작위로 선택되었다. 이 연구의 목적은 장기간의 안전성과 효능을 보여줌으로써, 고객이 소유한 동물 연구를 위한 임상적 가능한 후보가 될 수 있음을 강조하는 것이다. 도 4.
실시예 5 - 고양이에서 고양이 에리트로포에틴의 AAV-매개된 발현
고양이의 좌 또는 우측 사두근에 최대 400μL 용적으로 고양이 에리트로포에틴을 발현시키는 AAV8를 체중 kg 당 최대 3 x 109 (GC/kg)의 게놈 복사체를 단일 근육 주사하였다. 혈액 샘플은 주입시 그리고 헤마토크릿 측정을 위해 주기적으로 수집하였다. 동일한 기준을 사용하여 최초 벡터 투여 후 28 일 시점 또는 그 이후에 벡터를 다시 투여할 수 있다.
이 연구는 단계 III 만성 신장 질환과 관련된 빈혈증이 있는 최대 9 마리의 고양이를 포함할 것이다. CKD 관련 빈혈은 최소한 1 개월 간격으로 2 번, 빈혈의 또 다른 명백한 원인이 없이, 29 % 미만의 헤마토크릿으로 정의될 것이다. 등록된 대상은 고양이 에리스로포이에틴 이식유전자(AAV8.fEpo)를 갖는 아데노연합된 바이러스 벡터의 단일 근육 내 주사를 맞는다. 대상은 벡터 투여 시 그리고 투여 후 2, 4, 6 및 8 주 시점에 연구센터에서 평가될 것이다. 각 방문 시에 에리트로포에틴 농도, 헤마토크릿, 망상적혈구수, 평균 적혈구 용적, 평균 미립자 헤모글로빈 및 평균 미립자 헤모글로빈 농도를 평가하기 위해 채혈하게 될 것이다. 헤마토크릿 측정을 위해 연구 약물 투여 후 3 개월, 6 개월 및 12 개월 시점에 환자는 연구 센터를 다시 방문하거나 또는 주치 수의사에게서 후속 조치를 취하게 된다. 연구 약물은 정상적인 고양이 4 마리에서 최대 3E8 게놈 복사체/kg의 용량이 안전하다는 사실은 이미 밝혀진 바 있다. 이 임상 시험에 등록된 처음 3 마리의 대상에게 1E8 게놈 복사체를/kg AAV8.fEpo의 용량으로 투여할 것이다. 처음 3 마리의 대상에게 벡터가 투여된 후 8 주 시점에 도달 한 후, 안전성 및 벡터 활동의 초기 평가가 이루어질 것이다. 이들 최초 3 마리 동물 코호트에서의 8 주 분석 결과에 따라, 3 마리 동물의 제 2 코호트의 투여는 다음 과정을 사용하여 진행될 것이다 :
1. 최초 코호트에서 심각한 이상 반응이 발생하거나 또는 헤마토크릿이 55 %에 도달하면, 용량은 3 배 감소시키고, 3 마리의 추가 동물은 감소된 용량으로 등록될 것이다 (전체 연구에는 6마리의 대상이 등록).
2. 부작용이 없고, 모든 고양이의 헤마토크릿이 최소한 5 % 증가하거나 또는 정상적인 헤마토크릿 범위에 도달하면, 3 마리의 추가 고양이는 출발 용량으로 치료될 것이다 (전체 연구에는 6마리 대상이 등록)
3. 부작용이 없고, 모든 고양이의 헤마토크릿이 최소한 5 % 증가하지 못하거나 또는 정상 범위에 도달하지 않으면, 3 마리의 추가 고양이는 3배 더 높은 용량의 3E8 게놈 복사체/kg로 치료될 것이다. 이 코호트에서 3 마리의 동물 모두 벡터 투여 후 6 주 시점에 도달한 후, 다시 안전성과 활성에 대한 중간 평가를 받을 것이다. 부작용이 없고, 모든 고양이의 헤마토크릿이 최소한 5 % 증가하거나 또는 정상적인 헤마토크릿 범위에 도달하면, 3 마리의 추가 고양이는 이 용량으로 치료될 것이다 부작용이 없고, 모든 고양이의 헤마토크릿이 최소한 5 % 증가하지 못하거나 또는 정상 범위에 도달하지 않으면, 3 마리의 추가 고양이는 3배 더 높은 용량의 6E8 게놈 복사체/kg로 치료될 것이다.(전체 연구에는 9마리의 대상이 등록). 따라서, 이 연구는 안전 및 헤마토크릿 변화의 중간 분석 결과에 따라, 최소 6 마리에서 최대 9 마리까지 등록할 수 있다. 주요 평가목표(endpoints)에는 벡터 발현의 안전성과 평가가 포함된다.
2 차 평가목표에는 동물의 삶의 질과 벡터의 장기 지속적 발현이 포함된다.
포함 기준:
3 단계의 신부전 (혈청 크레아티닌 2.95mg/dL)을 가진 고양이
최소한 1 개월 간격으로 2 번, 29 % 미만의 헤마토크릿
동물 소유주가 연구 약물 투여 후 2 주, 4 주, 6 주 및 8 주에 연구 센터에 방문하고, 연구 약물 투여 후 3 개월, 6 개월 및 12 개월 시점에 연구 센터 또는 주치 수의차의 병원을 방문하려는 의지가 있는 경우
배제 기준:
기대 수명이 3 개월 미만인 경우
신장 이식
재조합 에리트로포에틴 (에포에틴, 다르베포에틴)으로 치료 후
선입 연구자의 의견에 따르면, 연구 약물의 안전성과 활동성을 평가할 수 없는 임의의 다른 상태
AAV8에 대한 중화 항체가 이미 존재
첫 방문시에 적격 고양이들이 선별될 것이다. 여기에는 완전한 병력 및 임상 시험, CBC/화학 요법, AAV8에 대한 기존 항체 및 동의서 정식 제시 등이 포함될 것이다.
연구 프로토콜의 조건에 적합한 모든 적격 고양이는 연구에 승인을 받은 후, 최소 일주일에 최대 3E9 게놈 복사체/kg의 AAV8.fEPO 단일 근육 주사를 맞게 될 것이다.
벡터 투여 후, 고양이는 8 주간 격주로 평가될 것이다. 이러한 임상 검사에는 CBC retic/chem, 완전한 임상 평가 및 혈청 수집이 포함될 것이다. 8 주 후, 이 임상 평가는 벡터 투여 후 90 일 시점에 시작하여, 매 3 개월마다 시행될 것이다. 3 개월, 6 개월, 9 개월, 및 1 년 평가가 실행될 것이다.
있을 수 있는 합병증
65 % 헤마토크릿의 적혈구증가증을 나타내는 모든 동물은 매 3 주마다 최대 10 % 혈액량의 치료 절개술을 받게 될 것이다.
본 명세서에 인용된 모든 출판물 뿐만 아니라, 미국 특허 가출원 62/212,144 및 62/336,211은 본원에 참고자료에 편입되어 있다. 유사하게, 본원에서 언급되고, 첨부된 서열 목록에 나타나는 서열 번호는 참고 문헌에 편입되어 있다. 본 발명은 특정 구체예를 참조하여 설명되었지만, 본 발명의 사상을 벗어나지 않고 수정이 이루어질 수 있음을 알 수 있을 것이다. 이러한 변형은 첨부된 청구범위의 범위 안에 속하는 것으로 의도된다.
SEQUENCE LISTING
<110> The Trustees of the University of Pennsylvania
<120> AAV-EPO FOR TREATING COMPANION ANIMALS
<130> UPN-15-7472PCT
<150> US 62/212,144
<151> 2015-08-31
<150> US 62/336,211
<151> 2016-05-13
<160> 9
<170> PatentIn version 3.5
<210> 1
<211> 5791
<212> DNA
<213> Artificial Sequence
<220>
<223> constructed sequence
<220>
<221> misc_feature
<222> (12)..(629)
<223> Epo
<220>
<221> polyA_signal
<222> (696)..(822)
<223> Rabbit\globin\poly\A
<220>
<221> repeat_region
<222> (911)..(1040)
<223> 3' ITR (complement)
<220>
<221> rep_origin
<222> (1217)..(1672)
<223> f1/ori (complement)
<220>
<221> misc_feature
<222> (1803)..(2660)
<223> AP(R)
<220>
<221> rep_origin
<222> (2834)..(3422)
<223> origin of replication
<220>
<221> repeat_region
<222> (3862)..(3991)
<223> 5' ITR
<220>
<221> repeat_region
<222> (4059)..(4440)
<223> CMV\IE\promoter
<220>
<221> promoter
<222> (4443)..(4724)
<223> CB promoter
<220>
<221> TATA_signal
<222> (4697)..(4700)
<220>
<221> Intron
<222> (4819)..(5791)
<223> chicken\beta-actin\intron
<400> 1
aattcgccac catgtgcgag cctgcccccc ctaagcctac acagtctgcc tggcacagct 60
tccccgagtg tcctgctctc ctgctgctgc tgagtttgct gctgctgcct ctgggcctgc 120
ctgtgctggg agcacctcct agactgatct gcgacagccg ggtgctggaa cggtacatcc 180
tggaagcccg cgaggccgag aatgtgacca tgggatgtgc ccagggctgc agcttcagcg 240
agaacatcac cgtgcccgac accaaagtga acttctacac ctggaagaga atggacgtgg 300
gccagcaggc cctggaagtg tggcagggac tggccctgct gtctgaggcc atcctgagag 360
gacaggctct gctggccaat gccagccagc ctagcgagac acctcagctg cacgtggaca 420
aggccgtgtc ctccctgaga agcctgacca gcctgctgag agcactggga gcccagaaag 480
aagccatgag cctgcctgag gaagccagcc ctgcccctct gagaaccttc accgtggaca 540
ccctgtgcaa gctgttccgg atctacagca acttcctgcg gggcaagctg accctgtaca 600
ccggcgaggc ttgtcggaga ggcgacagat gatgaggtac ctctagagtc gacccgggcg 660
gcctcgagga cggggtgaac tacgcctgag gatccgatct ttttccctct gccaaaaatt 720
atggggacat catgaagccc cttgagcatc tgacttctgg ctaataaagg aaatttattt 780
tcattgcaat agtgtgttgg aattttttgt gtctctcact cggaagcaat tcgttgatct 840
gaatttcgac cacccataat acccattacc ctggtagata agtagcatgg cgggttaatc 900
attaactaca aggaacccct agtgatggag ttggccactc cctctctgcg cgctcgctcg 960
ctcactgagg ccgggcgacc aaaggtcgcc cgacgcccgg gctttgcccg ggcggcctca 1020
gtgagcgagc gagcgcgcag ccttaattaa cctaattcac tggccgtcgt tttacaacgt 1080
cgtgactggg aaaaccctgg cgttacccaa cttaatcgcc ttgcagcaca tccccctttc 1140
gccagctggc gtaatagcga agaggcccgc accgatcgcc cttcccaaca gttgcgcagc 1200
ctgaatggcg aatgggacgc gccctgtagc ggcgcattaa gcgcggcggg tgtggtggtt 1260
acgcgcagcg tgaccgctac acttgccagc gccctagcgc ccgctccttt cgctttcttc 1320
ccttcctttc tcgccacgtt cgccggcttt ccccgtcaag ctctaaatcg ggggctccct 1380
ttagggttcc gatttagtgc tttacggcac ctcgacccca aaaaacttga ttagggtgat 1440
ggttcacgta gtgggccatc gccctgatag acggtttttc gccctttgac gttggagtcc 1500
acgttcttta atagtggact cttgttccaa actggaacaa cactcaaccc tatctcggtc 1560
tattcttttg atttataagg gattttgccg atttcggcct attggttaaa aaatgagctg 1620
atttaacaaa aatttaacgc gaattttaac aaaatattaa cgcttacaat ttaggtggca 1680
cttttcgggg aaatgtgcgc ggaaccccta tttgtttatt tttctaaata cattcaaata 1740
tgtatccgct catgagacaa taaccctgat aaatgcttca ataatattga aaaaggaaga 1800
gtatgagtat tcaacatttc cgtgtcgccc ttattccctt ttttgcggca ttttgccttc 1860
ctgtttttgc tcacccagaa acgctggtga aagtaaaaga tgctgaagat cagttgggtg 1920
cacgagtggg ttacatcgaa ctggatctca acagcggtaa gatccttgag agttttcgcc 1980
ccgaagaacg ttttccaatg atgagcactt ttaaagttct gctatgtggc gcggtattat 2040
cccgtattga cgccgggcaa gagcaactcg gtcgccgcat acactattct cagaatgact 2100
tggttgagta ctcaccagtc acagaaaagc atcttacgga tggcatgaca gtaagagaat 2160
tatgcagtgc tgccataacc atgagtgata acactgcggc caacttactt ctgacaacga 2220
tcggaggacc gaaggagcta accgcttttt tgcacaacat gggggatcat gtaactcgcc 2280
ttgatcgttg ggaaccggag ctgaatgaag ccataccaaa cgacgagcgt gacaccacga 2340
tgcctgtagc aatggcaaca acgttgcgca aactattaac tggcgaacta cttactctag 2400
cttcccggca acaattaata gactggatgg aggcggataa agttgcagga ccacttctgc 2460
gctcggccct tccggctggc tggtttattg ctgataaatc tggagccggt gagcgtgggt 2520
ctcgcggtat cattgcagca ctggggccag atggtaagcc ctcccgtatc gtagttatct 2580
acacgacggg gagtcaggca actatggatg aacgaaatag acagatcgct gagataggtg 2640
cctcactgat taagcattgg taactgtcag accaagttta ctcatatata ctttagattg 2700
atttaaaact tcatttttaa tttaaaagga tctaggtgaa gatccttttt gataatctca 2760
tgaccaaaat cccttaacgt gagttttcgt tccactgagc gtcagacccc gtagaaaaga 2820
tcaaaggatc ttcttgagat cctttttttc tgcgcgtaat ctgctgcttg caaacaaaaa 2880
aaccaccgct accagcggtg gtttgtttgc cggatcaaga gctaccaact ctttttccga 2940
aggtaactgg cttcagcaga gcgcagatac caaatactgt tcttctagtg tagccgtagt 3000
taggccacca cttcaagaac tctgtagcac cgcctacata cctcgctctg ctaatcctgt 3060
taccagtggc tgctgccagt ggcgataagt cgtgtcttac cgggttggac tcaagacgat 3120
agttaccgga taaggcgcag cggtcgggct gaacgggggg ttcgtgcaca cagcccagct 3180
tggagcgaac gacctacacc gaactgagat acctacagcg tgagctatga gaaagcgcca 3240
cgcttcccga agggagaaag gcggacaggt atccggtaag cggcagggtc ggaacaggag 3300
agcgcacgag ggagcttcca gggggaaacg cctggtatct ttatagtcct gtcgggtttc 3360
gccacctctg acttgagcgt cgatttttgt gatgctcgtc aggggggcgg agcctatgga 3420
aaaacgccag caacgcggcc tttttacggt tcctggcctt ttgctggcct tttgctcaca 3480
tgttctttcc tgcgttatcc cctgattctg tggataaccg tattaccgcc tttgagtgag 3540
ctgataccgc tcgccgcagc cgaacgaccg agcgcagcga gtcagtgagc gaggaagcgg 3600
aagagcgccc aatacgcaaa ccgcctctcc ccgcgcgttg gccgattcat taatgcagct 3660
ggcacgacag gtttcccgac tggaaagcgg gcagtgagcg caacgcaatt aatgtgagtt 3720
agctcactca ttaggcaccc caggctttac actttatgct tccggctcgt atgttgtgtg 3780
gaattgtgag cggataacaa tttcacacag gaaacagcta tgaccatgat tacgccagat 3840
ttaattaagg ccttaattag gctgcgcgct cgctcgctca ctgaggccgc ccgggcaaag 3900
cccgggcgtc gggcgacctt tggtcgcccg gcctcagtga gcgagcgagc gcgcagagag 3960
ggagtggcca actccatcac taggggttcc ttgtagttaa tgattaaccc gccatgctac 4020
ttatctacca gggtaatggg gatcctctag aactatagct agtcgacatt gattattgac 4080
tagttattaa tagtaatcaa ttacggggtc attagttcat agcccatata tggagttccg 4140
cgttacataa cttacggtaa atggcccgcc tggctgaccg cccaacgacc cccgcccatt 4200
gacgtcaata atgacgtatg ttcccatagt aacgccaata gggactttcc attgacgtca 4260
atgggtggac tatttacggt aaactgccca cttggcagta catcaagtgt atcatatgcc 4320
aagtacgccc cctattgacg tcaatgacgg taaatggccc gcctggcatt atgcccagta 4380
catgacctta tgggactttc ctacttggca gtacatctac gtattagtca tcgctattac 4440
catggtcgag gtgagcccca cgttctgctt cactctcccc atctcccccc cctccccacc 4500
cccaattttg tatttattta ttttttaatt attttgtgca gcgatggggg cggggggggg 4560
gggggggcgc gcgccaggcg gggcggggcg gggcgagggg cggggcgggg cgaggcggag 4620
aggtgcggcg gcagccaatc agagcggcgc gctccgaaag tttcctttta tggcgaggcg 4680
gcggcggcgg cggccctata aaaagcgaag cgcgcggcgg gcggggagtc gctgcgacgc 4740
tgccttcgcc ccgtgccccg ctccgccgcc gcctcgcgcc gcccgccccg gctctgactg 4800
accgcgttac tcccacaggt gagcgggcgg gacggccctt ctcctccggg ctgtaattag 4860
cgcttggttt aatgacggct tgtttctttt ctgtggctgc gtgaaagcct tgaggggctc 4920
cgggagggcc ctttgtgcgg ggggagcggc tcggggggtg cgtgcgtgtg tgtgtgcgtg 4980
gggagcgccg cgtgcggctc cgcgctgccc ggcggctgtg agcgctgcgg gcgcggcgcg 5040
gggctttgtg cgctccgcag tgtgcgcgag gggagcgcgg ccgggggcgg tgccccgcgg 5100
tgcggggggg gctgcgaggg gaacaaaggc tgcgtgcggg gtgtgtgcgt gggggggtga 5160
gcagggggtg tgggcgcgtc ggtcgggctg caaccccccc tgcacccccc tccccgagtt 5220
gctgagcacg gcccggcttc gggtgcgggg ctccgtacgg ggcgtggcgc ggggctcgcc 5280
gtgccgggcg gggggtggcg gcaggtgggg gtgccgggcg gggcggggcc gcctcgggcc 5340
ggggagggct cgggggaggg gcgcggcggc ccccggagcg ccggcggctg tcgaggcgcg 5400
gcgagccgca gccattgcct tttatggtaa tcgtgcgaga gggcgcaggg acttcctttg 5460
tcccaaatct gtgcggagcc gaaatctggg aggcgccgcc gcaccccctc tagcgggcgc 5520
ggggcgaagc ggtgcggcgc cggcaggaag gaaatgggcg gggagggcct tcgtgcgtcg 5580
ccgcgccgcc gtccccttct ccctctccag cctcggggct gtccgcgggg ggacggctgc 5640
cttcgggggg gacggggcag ggcggggttc ggcttctggc gtgtgaccgg cggctctaga 5700
gcctctgcta accatgttca tgccttcttc tttttcctac agctcctggg caacgtgctg 5760
gttattgtgc tgtctcatca ttttggcaaa g 5791
<210> 2
<211> 5749
<212> DNA
<213> Artificial Sequence
<220>
<223> constructed sequence
<220>
<221> polyA_signal
<222> (56)..(182)
<223> Rabbit\globin\poly\A
<220>
<221> repeat_region
<222> (271)..(400)
<223> 3' ITR (complement)
<220>
<221> rep_origin
<222> (577)..(1032)
<223> F1 ori
<220>
<221> misc_feature
<222> (1163)..(2020)
<223> AP(R)
<220>
<221> rep_origin
<222> (2194)..(2782)
<223> Origin\of\replication
<220>
<221> repeat_region
<222> (3222)..(3351)
<223> 5' ITR
<220>
<221> repeat_region
<222> (3419)..(3800)
<223> CMV\IE\promoter
<220>
<221> promoter
<222> (3803)..(4084)
<223> CB promoter
<220>
<221> TATA_signal
<222> (4057)..(4060)
<220>
<221> Intron
<222> (4179)..(5151)
<223> chicken\beta-actin\intron
<220>
<221> misc_feature
<222> (5163)..(5738)
<223> Epo
<400> 2
ctctagagtc gacccgggcg gcctcgagga cggggtgaac tacgcctgag gatccgatct 60
ttttccctct gccaaaaatt atggggacat catgaagccc cttgagcatc tgacttctgg 120
ctaataaagg aaatttattt tcattgcaat agtgtgttgg aattttttgt gtctctcact 180
cggaagcaat tcgttgatct gaatttcgac cacccataat acccattacc ctggtagata 240
agtagcatgg cgggttaatc attaactaca aggaacccct agtgatggag ttggccactc 300
cctctctgcg cgctcgctcg ctcactgagg ccgggcgacc aaaggtcgcc cgacgcccgg 360
gctttgcccg ggcggcctca gtgagcgagc gagcgcgcag ccttaattaa cctaattcac 420
tggccgtcgt tttacaacgt cgtgactggg aaaaccctgg cgttacccaa cttaatcgcc 480
ttgcagcaca tccccctttc gccagctggc gtaatagcga agaggcccgc accgatcgcc 540
cttcccaaca gttgcgcagc ctgaatggcg aatgggacgc gccctgtagc ggcgcattaa 600
gcgcggcggg tgtggtggtt acgcgcagcg tgaccgctac acttgccagc gccctagcgc 660
ccgctccttt cgctttcttc ccttcctttc tcgccacgtt cgccggcttt ccccgtcaag 720
ctctaaatcg ggggctccct ttagggttcc gatttagtgc tttacggcac ctcgacccca 780
aaaaacttga ttagggtgat ggttcacgta gtgggccatc gccctgatag acggtttttc 840
gccctttgac gttggagtcc acgttcttta atagtggact cttgttccaa actggaacaa 900
cactcaaccc tatctcggtc tattcttttg atttataagg gattttgccg atttcggcct 960
attggttaaa aaatgagctg atttaacaaa aatttaacgc gaattttaac aaaatattaa 1020
cgcttacaat ttaggtggca cttttcgggg aaatgtgcgc ggaaccccta tttgtttatt 1080
tttctaaata cattcaaata tgtatccgct catgagacaa taaccctgat aaatgcttca 1140
ataatattga aaaaggaaga gtatgagtat tcaacatttc cgtgtcgccc ttattccctt 1200
ttttgcggca ttttgccttc ctgtttttgc tcacccagaa acgctggtga aagtaaaaga 1260
tgctgaagat cagttgggtg cacgagtggg ttacatcgaa ctggatctca acagcggtaa 1320
gatccttgag agttttcgcc ccgaagaacg ttttccaatg atgagcactt ttaaagttct 1380
gctatgtggc gcggtattat cccgtattga cgccgggcaa gagcaactcg gtcgccgcat 1440
acactattct cagaatgact tggttgagta ctcaccagtc acagaaaagc atcttacgga 1500
tggcatgaca gtaagagaat tatgcagtgc tgccataacc atgagtgata acactgcggc 1560
caacttactt ctgacaacga tcggaggacc gaaggagcta accgcttttt tgcacaacat 1620
gggggatcat gtaactcgcc ttgatcgttg ggaaccggag ctgaatgaag ccataccaaa 1680
cgacgagcgt gacaccacga tgcctgtagc aatggcaaca acgttgcgca aactattaac 1740
tggcgaacta cttactctag cttcccggca acaattaata gactggatgg aggcggataa 1800
agttgcagga ccacttctgc gctcggccct tccggctggc tggtttattg ctgataaatc 1860
tggagccggt gagcgtgggt ctcgcggtat cattgcagca ctggggccag atggtaagcc 1920
ctcccgtatc gtagttatct acacgacggg gagtcaggca actatggatg aacgaaatag 1980
acagatcgct gagataggtg cctcactgat taagcattgg taactgtcag accaagttta 2040
ctcatatata ctttagattg atttaaaact tcatttttaa tttaaaagga tctaggtgaa 2100
gatccttttt gataatctca tgaccaaaat cccttaacgt gagttttcgt tccactgagc 2160
gtcagacccc gtagaaaaga tcaaaggatc ttcttgagat cctttttttc tgcgcgtaat 2220
ctgctgcttg caaacaaaaa aaccaccgct accagcggtg gtttgtttgc cggatcaaga 2280
gctaccaact ctttttccga aggtaactgg cttcagcaga gcgcagatac caaatactgt 2340
tcttctagtg tagccgtagt taggccacca cttcaagaac tctgtagcac cgcctacata 2400
cctcgctctg ctaatcctgt taccagtggc tgctgccagt ggcgataagt cgtgtcttac 2460
cgggttggac tcaagacgat agttaccgga taaggcgcag cggtcgggct gaacgggggg 2520
ttcgtgcaca cagcccagct tggagcgaac gacctacacc gaactgagat acctacagcg 2580
tgagctatga gaaagcgcca cgcttcccga agggagaaag gcggacaggt atccggtaag 2640
cggcagggtc ggaacaggag agcgcacgag ggagcttcca gggggaaacg cctggtatct 2700
ttatagtcct gtcgggtttc gccacctctg acttgagcgt cgatttttgt gatgctcgtc 2760
aggggggcgg agcctatgga aaaacgccag caacgcggcc tttttacggt tcctggcctt 2820
ttgctggcct tttgctcaca tgttctttcc tgcgttatcc cctgattctg tggataaccg 2880
tattaccgcc tttgagtgag ctgataccgc tcgccgcagc cgaacgaccg agcgcagcga 2940
gtcagtgagc gaggaagcgg aagagcgccc aatacgcaaa ccgcctctcc ccgcgcgttg 3000
gccgattcat taatgcagct ggcacgacag gtttcccgac tggaaagcgg gcagtgagcg 3060
caacgcaatt aatgtgagtt agctcactca ttaggcaccc caggctttac actttatgct 3120
tccggctcgt atgttgtgtg gaattgtgag cggataacaa tttcacacag gaaacagcta 3180
tgaccatgat tacgccagat ttaattaagg ccttaattag gctgcgcgct cgctcgctca 3240
ctgaggccgc ccgggcaaag cccgggcgtc gggcgacctt tggtcgcccg gcctcagtga 3300
gcgagcgagc gcgcagagag ggagtggcca actccatcac taggggttcc ttgtagttaa 3360
tgattaaccc gccatgctac ttatctacca gggtaatggg gatcctctag aactatagct 3420
agtcgacatt gattattgac tagttattaa tagtaatcaa ttacggggtc attagttcat 3480
agcccatata tggagttccg cgttacataa cttacggtaa atggcccgcc tggctgaccg 3540
cccaacgacc cccgcccatt gacgtcaata atgacgtatg ttcccatagt aacgccaata 3600
gggactttcc attgacgtca atgggtggac tatttacggt aaactgccca cttggcagta 3660
catcaagtgt atcatatgcc aagtacgccc cctattgacg tcaatgacgg taaatggccc 3720
gcctggcatt atgcccagta catgacctta tgggactttc ctacttggca gtacatctac 3780
gtattagtca tcgctattac catggtcgag gtgagcccca cgttctgctt cactctcccc 3840
atctcccccc cctccccacc cccaattttg tatttattta ttttttaatt attttgtgca 3900
gcgatggggg cggggggggg gggggggcgc gcgccaggcg gggcggggcg gggcgagggg 3960
cggggcgggg cgaggcggag aggtgcggcg gcagccaatc agagcggcgc gctccgaaag 4020
tttcctttta tggcgaggcg gcggcggcgg cggccctata aaaagcgaag cgcgcggcgg 4080
gcggggagtc gctgcgacgc tgccttcgcc ccgtgccccg ctccgccgcc gcctcgcgcc 4140
gcccgccccg gctctgactg accgcgttac tcccacaggt gagcgggcgg gacggccctt 4200
ctcctccggg ctgtaattag cgcttggttt aatgacggct tgtttctttt ctgtggctgc 4260
gtgaaagcct tgaggggctc cgggagggcc ctttgtgcgg ggggagcggc tcggggggtg 4320
cgtgcgtgtg tgtgtgcgtg gggagcgccg cgtgcggctc cgcgctgccc ggcggctgtg 4380
agcgctgcgg gcgcggcgcg gggctttgtg cgctccgcag tgtgcgcgag gggagcgcgg 4440
ccgggggcgg tgccccgcgg tgcggggggg gctgcgaggg gaacaaaggc tgcgtgcggg 4500
gtgtgtgcgt gggggggtga gcagggggtg tgggcgcgtc ggtcgggctg caaccccccc 4560
tgcacccccc tccccgagtt gctgagcacg gcccggcttc gggtgcgggg ctccgtacgg 4620
ggcgtggcgc ggggctcgcc gtgccgggcg gggggtggcg gcaggtgggg gtgccgggcg 4680
gggcggggcc gcctcgggcc ggggagggct cgggggaggg gcgcggcggc ccccggagcg 4740
ccggcggctg tcgaggcgcg gcgagccgca gccattgcct tttatggtaa tcgtgcgaga 4800
gggcgcaggg acttcctttg tcccaaatct gtgcggagcc gaaatctggg aggcgccgcc 4860
gcaccccctc tagcgggcgc ggggcgaagc ggtgcggcgc cggcaggaag gaaatgggcg 4920
gggagggcct tcgtgcgtcg ccgcgccgcc gtccccttct ccctctccag cctcggggct 4980
gtccgcgggg ggacggctgc cttcgggggg gacggggcag ggcggggttc ggcttctggc 5040
gtgtgaccgg cggctctaga gcctctgcta accatgttca tgccttcttc tttttcctac 5100
agctcctggg caacgtgctg gttattgtgc tgtctcatca ttttggcaaa gaattcgcca 5160
ccatgggcag ctgcgagtgt cctgctctcc tgctgctgct gagtttgctg ctgctgcctc 5220
tgggcctgcc tgtgctggga gcacctccta gactgatctg cgacagccgg gtgctggaac 5280
ggtacatcct ggaagcccgc gaggccgaga atgtgaccat gggatgtgcc gagggctgca 5340
gcttcagcga gaacatcacc gtgcccgaca ccaaagtgaa cttctacacc tggaagagaa 5400
tggacgtggg ccagcaggcc gtggaagtgt ggcagggact ggccctgctg tctgaggcca 5460
tcctgagagg acaggctctg ctggccaaca gcagccagcc tagcgaaacc ctgcagctgc 5520
acgtggacaa ggccgtgtcc tccctgagaa gcctgaccag cctgctgaga gcactgggag 5580
cccagaaaga ggccacctct ctgcctgagg ccacatctgc cgcccctctg agaaccttca 5640
ccgtggacac cctgtgcaag ctgttccgga tctacagcaa cttcctgcgg ggcaagctga 5700
ccctgtacac cggcgaggct tgtcggagag gcgacagatg atgaggtac 5749
<210> 3
<211> 206
<212> PRT
<213> Canis familiaris
<400> 3
Met Cys Glu Pro Ala Pro Pro Lys Pro Thr Gln Ser Ala Trp His Ser
1 5 10 15
Phe Pro Glu Cys Pro Ala Leu Leu Leu Leu Leu Ser Leu Leu Leu Leu
20 25 30
Pro Leu Gly Leu Pro Val Leu Gly Ala Pro Pro Arg Leu Ile Cys Asp
35 40 45
Ser Arg Val Leu Glu Arg Tyr Ile Leu Glu Ala Arg Glu Ala Glu Asn
50 55 60
Val Thr Met Gly Cys Ala Gln Gly Cys Ser Phe Ser Glu Asn Ile Thr
65 70 75 80
Val Pro Asp Thr Lys Val Asn Phe Tyr Thr Trp Lys Arg Met Asp Val
85 90 95
Gly Gln Gln Ala Leu Glu Val Trp Gln Gly Leu Ala Leu Leu Ser Glu
100 105 110
Ala Ile Leu Arg Gly Gln Ala Leu Leu Ala Asn Ala Ser Gln Pro Ser
115 120 125
Glu Thr Pro Gln Leu His Val Asp Lys Ala Val Ser Ser Leu Arg Ser
130 135 140
Leu Thr Ser Leu Leu Arg Ala Leu Gly Ala Gln Lys Glu Ala Met Ser
145 150 155 160
Leu Pro Glu Glu Ala Ser Pro Ala Pro Leu Arg Thr Phe Thr Val Asp
165 170 175
Thr Leu Cys Lys Leu Phe Arg Ile Tyr Ser Asn Phe Leu Arg Gly Lys
180 185 190
Leu Thr Leu Tyr Thr Gly Glu Ala Cys Arg Arg Gly Asp Arg
195 200 205
<210> 4
<211> 192
<212> PRT
<213> Felis catus
<400> 4
Met Gly Ser Cys Glu Cys Pro Ala Leu Leu Leu Leu Leu Ser Leu Leu
1 5 10 15
Leu Leu Pro Leu Gly Leu Pro Val Leu Gly Ala Pro Pro Arg Leu Ile
20 25 30
Cys Asp Ser Arg Val Leu Glu Arg Tyr Ile Leu Glu Ala Arg Glu Ala
35 40 45
Glu Asn Val Thr Met Gly Cys Ala Glu Gly Cys Ser Phe Ser Glu Asn
50 55 60
Ile Thr Val Pro Asp Thr Lys Val Asn Phe Tyr Thr Trp Lys Arg Met
65 70 75 80
Asp Val Gly Gln Gln Ala Val Glu Val Trp Gln Gly Leu Ala Leu Leu
85 90 95
Ser Glu Ala Ile Leu Arg Gly Gln Ala Leu Leu Ala Asn Ser Ser Gln
100 105 110
Pro Ser Glu Thr Leu Gln Leu His Val Asp Lys Ala Val Ser Ser Leu
115 120 125
Arg Ser Leu Thr Ser Leu Leu Arg Ala Leu Gly Ala Gln Lys Glu Ala
130 135 140
Thr Ser Leu Pro Glu Ala Thr Ser Ala Ala Pro Leu Arg Thr Phe Thr
145 150 155 160
Val Asp Thr Leu Cys Lys Leu Phe Arg Ile Tyr Ser Asn Phe Leu Arg
165 170 175
Gly Lys Leu Thr Leu Tyr Thr Gly Glu Ala Cys Arg Arg Gly Asp Arg
180 185 190
<210> 5
<211> 576
<212> DNA
<213> Canis familiaris
<400> 5
atgggggcgt gcgaatgtcc tgccctgttc cttttgctgt ctttgctgct gcttcctctg 60
ggcctcccag tcctgggcgc cccccctcgc ctcatttgtg acagccgggt cctggagaga 120
tacatcctgg aggccaggga ggccgaaaat gtcacgatgg gctgtgctca aggctgcagc 180
ttcagtgaga atatcaccgt cccagacacc aaggttaatt tctatacctg gaagaggatg 240
gatgttgggc agcaggcctt ggaagtctgg cagggcctgg cactgctctc agaagccatc 300
ctgcggggtc aggccctgtt ggccaacgcc tcccagccat ctgagactcc gcagctgcat 360
gtggacaaag ccgtcagcag cctgcgcagc ctcacctctc tgcttcgggc gctgggagcc 420
cagaaggagg ccatgtccct tccagaggaa gcctctcctg ctccactccg aacattcact 480
gttgatactt tgtgcaaact tttccgaatc tactccaatt tcctccgtgg aaagctgaca 540
ctgtacacag gggaggcctg cagaagagga gacagg 576
<210> 6
<211> 579
<212> DNA
<213> Felis catus
<400> 6
atggggtcgt gcgaatgtcc tgccctgctg cttctgctat ctttgctgct gcttcccctg 60
ggcctcccag tcctgggcgc cccccctcgc ctcatctgtg acagccgagt cctggagagg 120
tacattctgg gggccaggga ggccgaaaat gtcacgatgg gctgtgctga aggctgcagc 180
ttcagtgaga atatcactgt cccagacacc aaggtcaact tctatacctg gaagaggatg 240
gacgtcgggc agcaggctgt ggaagtctgg cagggcctcg ccctgctctc agaagccatc 300
ctgcggggcc aggccctgct ggccaactcc tcccagccat ctgagaccct gcagctgcat 360
gtggataaag ccgtcagcag cctgcgcagc ctcacctccc tgcttcgggc actgggagcc 420
cagaaggaag ccacctccct tccagaggca acctctgctg ctccactccg aacattcact 480
gtcgatactt tgtgcaaact tttccgaatc tactccaact tcctgcgggg aaagctgacg 540
ctgtacacag gggaggcctg ccgaagagga gacaggtga 579
<210> 7
<211> 618
<212> DNA
<213> Artificial Sequence
<220>
<223> codon optimized sequence
<400> 7
atgtgcgagc ctgccccccc taagcctaca cagtctgcct ggcacagctt ccccgagtgt 60
cctgctctcc tgctgctgct gagtttgctg ctgctgcctc tgggcctgcc tgtgctggga 120
gcacctccta gactgatctg cgacagccgg gtgctggaac ggtacatcct ggaagcccgc 180
gaggccgaga atgtgaccat gggatgtgcc cagggctgca gcttcagcga gaacatcacc 240
gtgcccgaca ccaaagtgaa cttctacacc tggaagagaa tggacgtggg ccagcaggcc 300
ctggaagtgt ggcagggact ggccctgctg tctgaggcca tcctgagagg acaggctctg 360
ctggccaatg ccagccagcc tagcgagaca cctcagctgc acgtggacaa ggccgtgtcc 420
tccctgagaa gcctgaccag cctgctgaga gcactgggag cccagaaaga agccatgagc 480
ctgcctgagg aagccagccc tgcccctctg agaaccttca ccgtggacac cctgtgcaag 540
ctgttccgga tctacagcaa cttcctgcgg ggcaagctga ccctgtacac cggcgaggct 600
tgtcggagag gcgacaga 618
<210> 8
<211> 576
<212> DNA
<213> Artificial Sequence
<220>
<223> codon optimized sequence
<400> 8
atgggcagct gcgagtgtcc tgctctcctg ctgctgctga gtttgctgct gctgcctctg 60
ggcctgcctg tgctgggagc acctcctaga ctgatctgcg acagccgggt gctggaacgg 120
tacatcctgg aagcccgcga ggccgagaat gtgaccatgg gatgtgccga gggctgcagc 180
ttcagcgaga acatcaccgt gcccgacacc aaagtgaact tctacacctg gaagagaatg 240
gacgtgggcc agcaggccgt ggaagtgtgg cagggactgg ccctgctgtc tgaggccatc 300
ctgagaggac aggctctgct ggccaacagc agccagccta gcgaaaccct gcagctgcac 360
gtggacaagg ccgtgtcctc cctgagaagc ctgaccagcc tgctgagagc actgggagcc 420
cagaaagagg ccacctctct gcctgaggcc acatctgccg cccctctgag aaccttcacc 480
gtggacaccc tgtgcaagct gttccggatc tacagcaact tcctgcgggg caagctgacc 540
ctgtacaccg gcgaggcttg tcggagaggc gacaga 576
<210> 9
<211> 20
<212> PRT
<213> Artificial Sequence
<220>
<223> IL-2 leader
<400> 9
Met Tyr Arg Met Gln Leu Leu Ser Cys Ile Ala Leu Ser Leu Ala Leu
1 5 10 15
Val Thr Asn Ser
20
Claims (33)
- 벡터 게놈을 패키지하고 있는 AAV(adeno-associated virus) 캡시드를 포함하는 재조합 아데노-연합된 바이러스(rAAV)에 있어서, 이때 전술한 벡터 게놈은 고양이 에리트로포에틴 (EPO)을 인코드하는 핵산 서열, 역전된 말단 반복 서열 및 숙주 세포에서 EPO의 발현을 지시하는 발현 제어 서열을 포함하는, 재조합 아데노-연합된 바이러스(rAAV).
- 벡터 게놈을 패키지하고 있는 AAV 캡시드를 포함하는 재조합 아데노-연합된 바이러스(rAAV)에 있어서, 이때 전술한 벡터 게놈은 개의 에리트로포에틴 (EPO)을 인코드하는 핵산 서열, 역전된 말단 반복 서열 및 숙주 세포에서 EPO의 발현을 지시하는 발현 제어 서열을 포함하는, 재조합 아데노-연합된 바이러스(rAAV).
- 청구항 1 또는 2에 있어서, 이때 상기 EPO 서열은 전장(full length)의 EPO 단백질을 인코드하는, rAAV.
- 청구항 1 또는 2에 있어서, 이때 상기 EPO 서열은 이종성 리더 서열이 복합된 성숙 EPO 단백질을 인코드하는, rAAV.
- 청구항 1에 있어서, 이때 상기 EPO 서열은 서열 번호: 4의 단백질 서열을 인코드하는, rAAV.
- 청구항 2에 있어서, 이때 상기 EPO 서열은 서열 번호: 3의 단백질 서열을 인코드하는, rAAV.
- 청구항 1에 있어서, 이때 상기 EPO 서열은 서열 번호: 6 또는 이의 변이체의 핵산 서열을 포함하는, rAAV.
- 청구항 7에 있어서, 이때 상기 변이체는 서열 번호: 6의 코돈 최적화된 변이체인, rAAV.
- 청구항 8에 있어서, 이때 코돈 최적화된 변이체는 서열 번호: 8인, rAAV.
- 청구항 2에 있어서, 이때 상기 EPO 서열은 서열 번호: 5 또는 이의 변이체의 핵산 서열을 포함하는, rAAV.
- 청구항 10에 있어서, 이때 상기 변이체는 서열 번호: 5의 코돈 최적화된 변이체인, rAAV.
- 청구항 11에 있어서, 이때 코돈 최적화된 변이체는 서열 번호: 7인, rAAV.
- 청구항 1 또는 2에 있어서, 이때 상기 발현 제어 서열은 프로모터를 포함하는, rAAV.
- 청구항 13에 있어서, 이때 상기 프로모터는 CB7 프로모터인, rAAV.
- 청구항 13에 있어서, 이때 상기 프로모터는 TBG 프로모터인, rAAV.
- 청구항 13에 있어서, 이때 상기 발현 제어 서열은 조직-특이적 프로모터를 포함하는, rAAV.
- 청구항 16에 있어서, 이때 상기 조직-특이적 프로모터는 신장-특이적 프로모터인, rAAV.
- 청구항 16에 있어서, 이때 상기 조직-특이적 프로모터는 Nkcc2 프로모터, 우로모둘린 프로모터, Ksp-캐드헤린 프로모터 및 THP 유전자 프로모터로부터 선택된, rAAA.
- 청구항 1 또는 청구항 2에 있어서, 인트론, Kozak 서열, poly A, 및 전사-후 조정 요소들중 하나 또는 그 이상을 더 포함하는, rAAA.
- 청구항 1 또는 청구항 2에 있어서, 이때 AAV 캡시드는 AAV8, rh64R1, AAV9, AAVhu.37, 또는 rh10 및 이의 변이체로부터 선택되는, 재조합 벡터.
- 청구항 1 또는 청구항 2에 있어서, 이때 상기 캡시드는 AAV8 캡시드인, 바이러스 벡터.
- 청구항 1 또는 청구항 2에 있어서, AAV 역전된 말단 반복 서열을 더 포함하는, 바이러스 벡터.
- 벡터 게놈을 패키지하고 있는 AAV8 캡시드를 포함하는 재조합 아데노-연합된 바이러스(rAAV)에 있어서, 이때 전술한 벡터 게놈은 고양이 에리트로포에틴 (EPO)을 인코드하는 핵산 서열, 역전된 말단 반복 서열 및 숙주 세포에서 EPO의 발현을 지시하는 발현 제어 서열을 포함하는, 재조합 아데노-연합된 바이러스(rAAV).
- 약학적으로 수용가능한 운반체와 청구항 1 내지 23중 임의의 한 항에 따른 바이러스 벡터를 포함하는 약학 조성물.
- 만성 신장 질환을 치료하는 방법에 있어서, 전술한 방법은 약학적으로 수용가능한 운반체와 청구항 1 또는 청구항 2에 따른 바이러스 벡터를 포함하는 약학 조성물을 투여하는 것을 포함하는 방법.
- 청구항 25에 있어서, 이때 전술한 조성물은 정맥으로 투여되는, 방법.
- 청구항 25에 있어서, 이때 전술한 대상은 고양이 또는 개인, 방법.
- 청구항 25에 있어서, 이때 전술한 대상은 고양이이고, 상기 EPO는 고양이 서열인, 방법.
- 청구항 25에 있어서, 이때 전술한 조성물은 또다른 요법과 병용 투여되는, 방법.
- 청구항 26에 있어서, 이때 전술한 조성물은 약 3x1010 GC/kg의 투여량으로 투여되는, 방법.
- 청구항 27에 있어서, 이때 전술한 조성물은 1회 초과로 투여되는, 방법.
- 만성 신장 질환을 치료하는데 사용되는 청구항 1 내지 23중 임의의 하나에 따른 재조합 AAV의 용도.
- 만성 신장 질환을 치료하는데 사용하는데 적합한 청구항 1 내지 23중 임의의 하나에 따른 rAAV.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562212144P | 2015-08-31 | 2015-08-31 | |
| US62/212,144 | 2015-08-31 | ||
| US201662336211P | 2016-05-13 | 2016-05-13 | |
| US62/336,211 | 2016-05-13 | ||
| PCT/US2016/049487 WO2017040524A1 (en) | 2015-08-31 | 2016-08-30 | Aav-epo for treating companion animals |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20180057636A true KR20180057636A (ko) | 2018-05-30 |
Family
ID=58188403
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020187008958A KR20180057636A (ko) | 2015-08-31 | 2016-08-30 | 반려 동물 치료용 aav-epo |
Country Status (9)
| Country | Link |
|---|---|
| US (2) | US11117942B2 (ko) |
| EP (1) | EP3344650A4 (ko) |
| JP (1) | JP6877408B2 (ko) |
| KR (1) | KR20180057636A (ko) |
| CN (1) | CN108137664B (ko) |
| AU (1) | AU2016315699B2 (ko) |
| CA (1) | CA2995733A1 (ko) |
| HK (1) | HK1257024A1 (ko) |
| WO (1) | WO2017040524A1 (ko) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US11890329B2 (en) * | 2017-07-06 | 2024-02-06 | The Trustees Of The University Of Pennsylvania | AAV9-mediated gene therapy for treating mucopolysaccharidosis type I |
| BR112021001498A2 (pt) * | 2018-07-27 | 2021-04-27 | Regenxbio Inc. | vírus adeno-associado recombinante (raav), composição farmacêutica, polinucleotídeo, plasmídeo de raav, célula ex vivo, método de produção de um raav e métodos para tratar um sujeito humano diagnosticado com mucopolissacaridose tipo iva (mps iva) |
| CN113423721A (zh) * | 2018-12-12 | 2021-09-21 | 金德雷德生物科学股份有限公司 | 兽用促红细胞生成素类似物 |
| US20230355712A1 (en) * | 2020-09-28 | 2023-11-09 | ScoutBio, Inc. | Composition and uses thereof |
| AU2022214429A1 (en) | 2021-02-01 | 2023-09-14 | Regenxbio Inc. | Gene therapy for neuronal ceroid lipofuscinoses |
| CN118475612A (zh) | 2021-08-31 | 2024-08-09 | 斯科特生物公司 | 抗原结合分子及其用途 |
Family Cites Families (36)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5139941A (en) | 1985-10-31 | 1992-08-18 | University Of Florida Research Foundation, Inc. | AAV transduction vectors |
| US5436146A (en) | 1989-09-07 | 1995-07-25 | The Trustees Of Princeton University | Helper-free stocks of recombinant adeno-associated virus vectors |
| US6268213B1 (en) | 1992-06-03 | 2001-07-31 | Richard Jude Samulski | Adeno-associated virus vector and cis-acting regulatory and promoter elements capable of expressing at least one gene and method of using same for gene therapy |
| US5869305A (en) | 1992-12-04 | 1999-02-09 | The University Of Pittsburgh | Recombinant viral vector system |
| US5478745A (en) | 1992-12-04 | 1995-12-26 | University Of Pittsburgh | Recombinant viral vector system |
| US6204059B1 (en) | 1994-06-30 | 2001-03-20 | University Of Pittsburgh | AAV capsid vehicles for molecular transfer |
| US5741683A (en) | 1995-06-07 | 1998-04-21 | The Research Foundation Of State University Of New York | In vitro packaging of adeno-associated virus DNA |
| US6093570A (en) | 1995-06-07 | 2000-07-25 | The University Of North Carolina At Chapel Hill | Helper virus-free AAV production |
| US5846528A (en) * | 1996-01-18 | 1998-12-08 | Avigen, Inc. | Treating anemia using recombinant adeno-associated virus virions comprising an EPO DNA sequence |
| CA2287478C (en) | 1997-04-14 | 2007-06-19 | Richard J. Samulski | Methods for increasing the efficiency of recombinant aav product |
| US6696411B1 (en) * | 1998-04-22 | 2004-02-24 | Cornell Research Foundation, Inc. | Canine erythropoietin gene and recombinant protein |
| WO1999061643A1 (en) | 1998-05-27 | 1999-12-02 | University Of Florida | Method of preparing recombinant adeno-associated virus compositions by using an iodixananol gradient |
| AU5755399A (en) * | 1998-09-16 | 2000-04-03 | Nexia Biotechnologies, Inc. | Recombinant protein production in urine |
| ES2340230T3 (es) | 1998-11-10 | 2010-05-31 | University Of North Carolina At Chapel Hill | Vectores viricos y sus procedimientos de preparacion y administracion. |
| EP1520589A1 (en) * | 1998-12-17 | 2005-04-06 | Pfizer Products Inc. | Erythropoietin in the treatment of domestic and livestock animals for anaemia |
| CA2288341C (en) * | 1998-12-17 | 2005-01-04 | Pfizer Products Inc. | Erythropoietin in the treatment of domestic and livestock animals for anemia |
| ES2308989T3 (es) | 1999-08-09 | 2008-12-16 | Targeted Genetics Corporation | Aumento de la expresion de una secuencia nucleotidica heterologa a partir de vectores viricos recombinantes que contienen una secuencia que forman pares de bases intracatenarios. |
| US7201898B2 (en) | 2000-06-01 | 2007-04-10 | The University Of North Carolina At Chapel Hill | Methods and compounds for controlled release of recombinant parvovirus vectors |
| NZ578982A (en) | 2001-11-13 | 2011-03-31 | Univ Pennsylvania | A method of detecting and/or identifying adeno-associated virus (AAV) sequences and isolating novel sequences identified thereby |
| ES2975413T3 (es) | 2001-12-17 | 2024-07-05 | Univ Pennsylvania | Secuencias de serotipo 8 de virus adenoasociado (AAV), vectores que las contienen y usos de las mismas |
| US20070015238A1 (en) | 2002-06-05 | 2007-01-18 | Snyder Richard O | Production of pseudotyped recombinant AAV virions |
| ES2648241T3 (es) | 2003-09-30 | 2017-12-29 | The Trustees Of The University Of Pennsylvania | Clados de virus adenoasociados (AAV), secuencias, vectores que contienen el mismo, y usos de los mismos |
| US8999678B2 (en) * | 2005-04-07 | 2015-04-07 | The Trustees Of The University Of Pennsylvania | Method of increasing the function of an AAV vector |
| US9988427B2 (en) * | 2005-05-13 | 2018-06-05 | Charite Universitaetsmedizen-Berlin | Erythropoietin variants |
| EP1736481A1 (en) | 2005-05-13 | 2006-12-27 | Charite Universitätsmedizin-Berlin | Erythropoietin variants |
| US7456683B2 (en) | 2005-06-09 | 2008-11-25 | Panasonic Corporation | Amplitude error compensating device and quadrature skew error compensating device |
| US7588772B2 (en) | 2006-03-30 | 2009-09-15 | Board Of Trustees Of The Leland Stamford Junior University | AAV capsid library and AAV capsid proteins |
| US9127078B2 (en) | 2008-07-21 | 2015-09-08 | The Trustees Of The University Of Pennsylvania | Methods and compositions using splicing regulatory proteins involved in tumor suppression |
| KR101647164B1 (ko) * | 2008-09-26 | 2016-08-09 | 암브룩스, 인코포레이티드 | 변형된 동물 에리트로포이에틴 폴리펩티드 및 이의 용도 |
| CA2759801C (en) * | 2009-05-02 | 2019-04-02 | Marco A. Passini | Gene therapy for neurodegenerative disorders |
| CA2793633A1 (en) * | 2010-03-29 | 2011-10-13 | The Trustees Of The University Of Pennsylvania | Pharmacologically induced transgene ablation system |
| US9315825B2 (en) | 2010-03-29 | 2016-04-19 | The Trustees Of The University Of Pennsylvania | Pharmacologically induced transgene ablation system |
| FR2977562B1 (fr) | 2011-07-06 | 2016-12-23 | Gaztransport Et Technigaz | Cuve etanche et thermiquement isolante integree dans une structure porteuse |
| EP2900275A4 (en) | 2012-09-29 | 2016-05-25 | Univ Pennsylvania | VETERINARY COMPOSITION AND METHOD FOR NONOPERATIVE CASTRATION |
| WO2015012924A2 (en) | 2013-04-29 | 2015-01-29 | The Trustees Of The University Of Pennsylvania | Tissue preferential codon modified expression cassettes, vectors containing same, and use thereof |
| EP2994483A4 (en) * | 2013-05-06 | 2017-02-08 | Cell Machines, Inc. | Methods and compositions related to large scale production of proteins |
-
2016
- 2016-08-30 JP JP2018510981A patent/JP6877408B2/ja active Active
- 2016-08-30 WO PCT/US2016/049487 patent/WO2017040524A1/en active Application Filing
- 2016-08-30 EP EP16842817.5A patent/EP3344650A4/en active Pending
- 2016-08-30 AU AU2016315699A patent/AU2016315699B2/en active Active
- 2016-08-30 KR KR1020187008958A patent/KR20180057636A/ko unknown
- 2016-08-30 US US15/754,931 patent/US11117942B2/en active Active
- 2016-08-30 CN CN201680049590.4A patent/CN108137664B/zh active Active
- 2016-08-30 CA CA2995733A patent/CA2995733A1/en not_active Abandoned
-
2018
- 2018-12-17 HK HK18116145.0A patent/HK1257024A1/zh unknown
-
2021
- 2021-09-10 US US17/472,037 patent/US20220056090A1/en active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| HK1257024A1 (zh) | 2019-10-11 |
| US11117942B2 (en) | 2021-09-14 |
| US20180251508A1 (en) | 2018-09-06 |
| US20220056090A1 (en) | 2022-02-24 |
| CA2995733A1 (en) | 2017-03-09 |
| AU2016315699A1 (en) | 2018-03-08 |
| EP3344650A1 (en) | 2018-07-11 |
| WO2017040524A1 (en) | 2017-03-09 |
| JP2018526994A (ja) | 2018-09-20 |
| AU2016315699B2 (en) | 2021-09-09 |
| CN108137664A (zh) | 2018-06-08 |
| CN108137664B (zh) | 2021-11-26 |
| JP6877408B2 (ja) | 2021-05-26 |
| EP3344650A4 (en) | 2019-04-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CN108137664B (zh) | 用于治疗伴侣动物的aav-epo | |
| AU2021261838A1 (en) | Gene therapy for juvenile batten disease | |
| CN111518175B (zh) | Sars-cov-2抗原多肽及其重组腺相关病毒和在制备疫苗中的应用 | |
| US11446395B2 (en) | AAV vector for treatment of Friedreich's ataxia | |
| US20240344071A1 (en) | Products and Methods for Treatment of Amyotrophic Lateral Sclerosis | |
| US11046957B2 (en) | AAV treatment of Huntington's disease | |
| AU2016302335A1 (en) | GLP-1 and use thereof in compositions for treating metabolic diseases | |
| CN113943749B (zh) | 一种基于crispr基因编辑系统提高同源重组效率的方法 | |
| CN111575248A (zh) | 一种慢病毒、重组间充质干细胞及其构建方法和应用 | |
| US20220330533A1 (en) | Systems and methods for batch cultivation of non-transgenic heterogametes | |
| AU2023241362A1 (en) | Chimeric opsin GPCR proteins | |
| CN115074369B (zh) | 表达全长abca4基因的腺相关病毒载体及应用 | |
| KR102570821B1 (ko) | 재조합 바이러스 벡터 및 이를 이용한 약학 조성물 | |
| CN110423776B (zh) | 表达重组凝血因子fix的载体及其构建方法和应用 | |
| TW202302858A (zh) | 治療糖尿病之胰島素基因療法 | |
| TW202227634A (zh) | 表現γ—肌聚醣之腺相關病毒載體之全身性遞送及肌肉失養症之治療 | |
| JP2002034559A (ja) | 遺伝子発現単位 |