KR20170123637A - 항체, 용도 및 방법 - Google Patents
항체, 용도 및 방법 Download PDFInfo
- Publication number
- KR20170123637A KR20170123637A KR1020177025436A KR20177025436A KR20170123637A KR 20170123637 A KR20170123637 A KR 20170123637A KR 1020177025436 A KR1020177025436 A KR 1020177025436A KR 20177025436 A KR20177025436 A KR 20177025436A KR 20170123637 A KR20170123637 A KR 20170123637A
- Authority
- KR
- South Korea
- Prior art keywords
- antibody
- antibodies
- seq
- fragment
- ox40l
- Prior art date
Links
- 238000000034 method Methods 0.000 title claims abstract description 258
- 102000004473 OX40 Ligand Human genes 0.000 claims abstract description 121
- 108010042215 OX40 Ligand Proteins 0.000 claims abstract description 121
- 239000012634 fragment Substances 0.000 claims description 565
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 273
- 241000282414 Homo sapiens Species 0.000 claims description 263
- 201000010099 disease Diseases 0.000 claims description 259
- 210000004027 cell Anatomy 0.000 claims description 251
- 230000001404 mediated effect Effects 0.000 claims description 204
- 101000764263 Homo sapiens Tumor necrosis factor ligand superfamily member 4 Proteins 0.000 claims description 143
- 102000051450 human TNFSF4 Human genes 0.000 claims description 142
- 239000000203 mixture Substances 0.000 claims description 141
- 239000003814 drug Substances 0.000 claims description 118
- 229940124597 therapeutic agent Drugs 0.000 claims description 99
- 210000001744 T-lymphocyte Anatomy 0.000 claims description 96
- 239000003795 chemical substances by application Substances 0.000 claims description 78
- 108090000623 proteins and genes Proteins 0.000 claims description 78
- 238000011282 treatment Methods 0.000 claims description 73
- 208000022559 Inflammatory bowel disease Diseases 0.000 claims description 69
- QJJXYPPXXYFBGM-LFZNUXCKSA-N Tacrolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1\C=C(/C)[C@@H]1[C@H](C)[C@@H](O)CC(=O)[C@H](CC=C)/C=C(C)/C[C@H](C)C[C@H](OC)[C@H]([C@H](C[C@H]2C)OC)O[C@@]2(O)C(=O)C(=O)N2CCCC[C@H]2C(=O)O1 QJJXYPPXXYFBGM-LFZNUXCKSA-N 0.000 claims description 69
- 229960001967 tacrolimus Drugs 0.000 claims description 69
- QJJXYPPXXYFBGM-SHYZHZOCSA-N tacrolimus Natural products CO[C@H]1C[C@H](CC[C@@H]1O)C=C(C)[C@H]2OC(=O)[C@H]3CCCCN3C(=O)C(=O)[C@@]4(O)O[C@@H]([C@H](C[C@H]4C)OC)[C@@H](C[C@H](C)CC(=C[C@@H](CC=C)C(=O)C[C@H](O)[C@H]2C)C)OC QJJXYPPXXYFBGM-SHYZHZOCSA-N 0.000 claims description 69
- 125000003275 alpha amino acid group Chemical group 0.000 claims description 68
- 206010052779 Transplant rejections Diseases 0.000 claims description 64
- 230000027455 binding Effects 0.000 claims description 64
- PMATZTZNYRCHOR-CGLBZJNRSA-N Cyclosporin A Chemical compound CC[C@@H]1NC(=O)[C@H]([C@H](O)[C@H](C)C\C=C\C)N(C)C(=O)[C@H](C(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](CC(C)C)N(C)C(=O)[C@@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)N(C)C(=O)CN(C)C1=O PMATZTZNYRCHOR-CGLBZJNRSA-N 0.000 claims description 63
- 108010036949 Cyclosporine Proteins 0.000 claims description 63
- 229960001265 ciclosporin Drugs 0.000 claims description 63
- 229930182912 cyclosporin Natural products 0.000 claims description 63
- QFJCIRLUMZQUOT-HPLJOQBZSA-N sirolimus Chemical compound C1C[C@@H](O)[C@H](OC)C[C@@H]1C[C@@H](C)[C@H]1OC(=O)[C@@H]2CCCCN2C(=O)C(=O)[C@](O)(O2)[C@H](C)CC[C@H]2C[C@H](OC)/C(C)=C/C=C/C=C/[C@@H](C)C[C@@H](C)C(=O)[C@H](OC)[C@H](O)/C(C)=C/[C@@H](C)C(=O)C1 QFJCIRLUMZQUOT-HPLJOQBZSA-N 0.000 claims description 63
- 102100022153 Tumor necrosis factor receptor superfamily member 4 Human genes 0.000 claims description 58
- 101710165473 Tumor necrosis factor receptor superfamily member 4 Proteins 0.000 claims description 58
- FBOZXECLQNJBKD-ZDUSSCGKSA-N L-methotrexate Chemical compound C=1N=C2N=C(N)N=C(N)C2=NC=1CN(C)C1=CC=C(C(=O)N[C@@H](CCC(O)=O)C(O)=O)C=C1 FBOZXECLQNJBKD-ZDUSSCGKSA-N 0.000 claims description 55
- 229960000485 methotrexate Drugs 0.000 claims description 53
- 230000002265 prevention Effects 0.000 claims description 50
- 102100036301 C-C chemokine receptor type 7 Human genes 0.000 claims description 49
- 101000716065 Homo sapiens C-C chemokine receptor type 7 Proteins 0.000 claims description 49
- CMSMOCZEIVJLDB-UHFFFAOYSA-N Cyclophosphamide Chemical compound ClCCN(CCCl)P1(=O)NCCCO1 CMSMOCZEIVJLDB-UHFFFAOYSA-N 0.000 claims description 47
- 229960004397 cyclophosphamide Drugs 0.000 claims description 47
- 150000001413 amino acids Chemical class 0.000 claims description 42
- VHRSUDSXCMQTMA-PJHHCJLFSA-N 6alpha-methylprednisolone Chemical compound C([C@@]12C)=CC(=O)C=C1[C@@H](C)C[C@@H]1[C@@H]2[C@@H](O)C[C@]2(C)[C@@](O)(C(=O)CO)CC[C@H]21 VHRSUDSXCMQTMA-PJHHCJLFSA-N 0.000 claims description 40
- 229960004584 methylprednisolone Drugs 0.000 claims description 40
- 239000003246 corticosteroid Substances 0.000 claims description 39
- 101000611023 Homo sapiens Tumor necrosis factor receptor superfamily member 6 Proteins 0.000 claims description 36
- 102100040403 Tumor necrosis factor receptor superfamily member 6 Human genes 0.000 claims description 36
- 208000011231 Crohn disease Diseases 0.000 claims description 35
- 229960005027 natalizumab Drugs 0.000 claims description 35
- 108010065637 Interleukin-23 Proteins 0.000 claims description 34
- 102000006395 Globulins Human genes 0.000 claims description 32
- 108010044091 Globulins Proteins 0.000 claims description 32
- 230000001494 anti-thymocyte effect Effects 0.000 claims description 32
- 238000002054 transplantation Methods 0.000 claims description 32
- 108010008165 Etanercept Proteins 0.000 claims description 31
- 229960000403 etanercept Drugs 0.000 claims description 31
- 229960000598 infliximab Drugs 0.000 claims description 31
- -1 methylprednisolone) Chemical compound 0.000 claims description 31
- ZAHRKKWIAAJSAO-UHFFFAOYSA-N rapamycin Natural products COCC(O)C(=C/C(C)C(=O)CC(OC(=O)C1CCCCN1C(=O)C(=O)C2(O)OC(CC(OC)C(=CC=CC=CC(C)CC(C)C(=O)C)C)CCC2C)C(C)CC3CCC(O)C(C3)OC)C ZAHRKKWIAAJSAO-UHFFFAOYSA-N 0.000 claims description 31
- 229960002930 sirolimus Drugs 0.000 claims description 31
- 206010046851 Uveitis Diseases 0.000 claims description 29
- 230000002391 anti-complement effect Effects 0.000 claims description 28
- 108010008730 anticomplement Proteins 0.000 claims description 28
- 201000000596 systemic lupus erythematosus Diseases 0.000 claims description 28
- 102100022005 B-lymphocyte antigen CD20 Human genes 0.000 claims description 27
- 101000897405 Homo sapiens B-lymphocyte antigen CD20 Proteins 0.000 claims description 27
- 229960002806 daclizumab Drugs 0.000 claims description 27
- 210000001519 tissue Anatomy 0.000 claims description 27
- 206010009900 Colitis ulcerative Diseases 0.000 claims description 26
- 201000006704 Ulcerative Colitis Diseases 0.000 claims description 26
- 210000004369 blood Anatomy 0.000 claims description 25
- 239000008280 blood Substances 0.000 claims description 25
- 238000002513 implantation Methods 0.000 claims description 24
- 208000023275 Autoimmune disease Diseases 0.000 claims description 23
- 230000000735 allogeneic effect Effects 0.000 claims description 23
- 206010012601 diabetes mellitus Diseases 0.000 claims description 22
- 208000027866 inflammatory disease Diseases 0.000 claims description 21
- 206010039073 rheumatoid arthritis Diseases 0.000 claims description 21
- 229960002964 adalimumab Drugs 0.000 claims description 20
- 229960000390 fludarabine Drugs 0.000 claims description 20
- GIUYCYHIANZCFB-FJFJXFQQSA-N fludarabine phosphate Chemical compound C1=NC=2C(N)=NC(F)=NC=2N1[C@@H]1O[C@H](COP(O)(O)=O)[C@@H](O)[C@@H]1O GIUYCYHIANZCFB-FJFJXFQQSA-N 0.000 claims description 20
- 102000006495 integrins Human genes 0.000 claims description 20
- 108010044426 integrins Proteins 0.000 claims description 20
- RTGDFNSFWBGLEC-SYZQJQIISA-N mycophenolate mofetil Chemical compound COC1=C(C)C=2COC(=O)C=2C(O)=C1C\C=C(/C)CCC(=O)OCCN1CCOCC1 RTGDFNSFWBGLEC-SYZQJQIISA-N 0.000 claims description 20
- 229960004866 mycophenolate mofetil Drugs 0.000 claims description 20
- 230000009885 systemic effect Effects 0.000 claims description 20
- 238000011134 hematopoietic stem cell transplantation Methods 0.000 claims description 19
- 230000000069 prophylactic effect Effects 0.000 claims description 19
- 230000004083 survival effect Effects 0.000 claims description 19
- 238000004519 manufacturing process Methods 0.000 claims description 18
- 101001055144 Homo sapiens Interleukin-2 receptor subunit alpha Proteins 0.000 claims description 17
- 102100026878 Interleukin-2 receptor subunit alpha Human genes 0.000 claims description 17
- 229960004641 rituximab Drugs 0.000 claims description 17
- 230000000779 depleting effect Effects 0.000 claims description 16
- HPNSFSBZBAHARI-UHFFFAOYSA-N micophenolic acid Natural products OC1=C(CC=C(C)CCC(O)=O)C(OC)=C(C)C2=C1C(=O)OC2 HPNSFSBZBAHARI-UHFFFAOYSA-N 0.000 claims description 16
- 101001057504 Homo sapiens Interferon-stimulated gene 20 kDa protein Proteins 0.000 claims description 15
- 229940014456 mycophenolate Drugs 0.000 claims description 15
- HPNSFSBZBAHARI-RUDMXATFSA-N mycophenolic acid Chemical compound OC1=C(C\C=C(/C)CCC(O)=O)C(OC)=C(C)C2=C1C(=O)OC2 HPNSFSBZBAHARI-RUDMXATFSA-N 0.000 claims description 15
- 229960001334 corticosteroids Drugs 0.000 claims description 14
- 201000006417 multiple sclerosis Diseases 0.000 claims description 14
- 201000001320 Atherosclerosis Diseases 0.000 claims description 13
- 208000035475 disorder Diseases 0.000 claims description 13
- 210000004072 lung Anatomy 0.000 claims description 13
- 239000008194 pharmaceutical composition Substances 0.000 claims description 13
- 210000000130 stem cell Anatomy 0.000 claims description 13
- 241000282560 Macaca mulatta Species 0.000 claims description 12
- 208000010247 contact dermatitis Diseases 0.000 claims description 12
- 230000001965 increasing effect Effects 0.000 claims description 12
- 229930105110 Cyclosporin A Natural products 0.000 claims description 11
- 229960000548 alemtuzumab Drugs 0.000 claims description 11
- 239000002260 anti-inflammatory agent Substances 0.000 claims description 11
- 239000011886 peripheral blood Substances 0.000 claims description 11
- 102000004274 CCR5 Receptors Human genes 0.000 claims description 10
- 108010017088 CCR5 Receptors Proteins 0.000 claims description 10
- 101150097493 D gene Proteins 0.000 claims description 10
- 206010061818 Disease progression Diseases 0.000 claims description 10
- 230000005750 disease progression Effects 0.000 claims description 10
- 238000011321 prophylaxis Methods 0.000 claims description 10
- 238000002965 ELISA Methods 0.000 claims description 9
- 210000005259 peripheral blood Anatomy 0.000 claims description 9
- 206010068051 Chimerism Diseases 0.000 claims description 8
- 206010028980 Neoplasm Diseases 0.000 claims description 8
- 239000003018 immunosuppressive agent Substances 0.000 claims description 8
- 230000001225 therapeutic effect Effects 0.000 claims description 8
- 108010029697 CD40 Ligand Proteins 0.000 claims description 7
- 102100032937 CD40 ligand Human genes 0.000 claims description 7
- 230000002238 attenuated effect Effects 0.000 claims description 7
- 201000011510 cancer Diseases 0.000 claims description 7
- 230000003247 decreasing effect Effects 0.000 claims description 7
- 230000006798 recombination Effects 0.000 claims description 7
- 238000005215 recombination Methods 0.000 claims description 7
- 229960003444 immunosuppressant agent Drugs 0.000 claims description 6
- 230000001861 immunosuppressant effect Effects 0.000 claims description 6
- 238000009097 single-agent therapy Methods 0.000 claims description 6
- FWMNVWWHGCHHJJ-SKKKGAJSSA-N 4-amino-1-[(2r)-6-amino-2-[[(2r)-2-[[(2r)-2-[[(2r)-2-amino-3-phenylpropanoyl]amino]-3-phenylpropanoyl]amino]-4-methylpentanoyl]amino]hexanoyl]piperidine-4-carboxylic acid Chemical compound C([C@H](C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCCCN)C(=O)N1CCC(N)(CC1)C(O)=O)NC(=O)[C@H](N)CC=1C=CC=CC=1)C1=CC=CC=C1 FWMNVWWHGCHHJJ-SKKKGAJSSA-N 0.000 claims description 5
- 108010003723 Single-Domain Antibodies Proteins 0.000 claims description 5
- 229940122739 Calcineurin inhibitor Drugs 0.000 claims description 4
- 101710192106 Calcineurin-binding protein cabin-1 Proteins 0.000 claims description 4
- 102100024123 Calcineurin-binding protein cabin-1 Human genes 0.000 claims description 4
- 241000288906 Primates Species 0.000 claims description 4
- 210000001185 bone marrow Anatomy 0.000 claims description 4
- 239000003085 diluting agent Substances 0.000 claims description 4
- 229940124302 mTOR inhibitor Drugs 0.000 claims description 4
- 239000003628 mammalian target of rapamycin inhibitor Substances 0.000 claims description 4
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 4
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 claims description 4
- 206010002556 Ankylosing Spondylitis Diseases 0.000 claims description 3
- 230000001028 anti-proliverative effect Effects 0.000 claims description 3
- 210000000936 intestine Anatomy 0.000 claims description 3
- 210000004185 liver Anatomy 0.000 claims description 3
- 108010054477 Immunoglobulin Fab Fragments Proteins 0.000 claims description 2
- 102000001706 Immunoglobulin Fab Fragments Human genes 0.000 claims description 2
- 208000012868 Overgrowth Diseases 0.000 claims description 2
- 210000001015 abdomen Anatomy 0.000 claims description 2
- 210000002216 heart Anatomy 0.000 claims description 2
- 210000003734 kidney Anatomy 0.000 claims description 2
- 210000000056 organ Anatomy 0.000 claims description 2
- 230000009870 specific binding Effects 0.000 claims description 2
- 229960005322 streptomycin Drugs 0.000 claims description 2
- JAZBEHYOTPTENJ-JLNKQSITSA-N all-cis-5,8,11,14,17-icosapentaenoic acid Chemical compound CC\C=C/C\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O JAZBEHYOTPTENJ-JLNKQSITSA-N 0.000 claims 7
- 229960005135 eicosapentaenoic acid Drugs 0.000 claims 7
- JAZBEHYOTPTENJ-UHFFFAOYSA-N eicosapentaenoic acid Natural products CCC=CCC=CCC=CCC=CCC=CCCCC(O)=O JAZBEHYOTPTENJ-UHFFFAOYSA-N 0.000 claims 7
- 235000020673 eicosapentaenoic acid Nutrition 0.000 claims 7
- 241000269328 Amphibia Species 0.000 claims 4
- 229960004914 vedolizumab Drugs 0.000 claims 4
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 claims 1
- 229940121363 anti-inflammatory agent Drugs 0.000 claims 1
- 208000009329 Graft vs Host Disease Diseases 0.000 description 136
- 208000024908 graft versus host disease Diseases 0.000 description 136
- 239000000523 sample Substances 0.000 description 80
- 206010057190 Respiratory tract infections Diseases 0.000 description 73
- 238000006467 substitution reaction Methods 0.000 description 70
- 235000001014 amino acid Nutrition 0.000 description 63
- 102000004127 Cytokines Human genes 0.000 description 50
- 108090000695 Cytokines Proteins 0.000 description 50
- 239000002773 nucleotide Substances 0.000 description 47
- 125000003729 nucleotide group Chemical group 0.000 description 47
- 229940024606 amino acid Drugs 0.000 description 40
- 230000028327 secretion Effects 0.000 description 36
- 241000282412 Homo Species 0.000 description 35
- 150000007523 nucleic acids Chemical class 0.000 description 33
- 102000039446 nucleic acids Human genes 0.000 description 33
- 108020004707 nucleic acids Proteins 0.000 description 33
- 210000000265 leukocyte Anatomy 0.000 description 26
- 230000035755 proliferation Effects 0.000 description 26
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 24
- 102100040247 Tumor necrosis factor Human genes 0.000 description 24
- 210000002919 epithelial cell Anatomy 0.000 description 24
- 108010074328 Interferon-gamma Proteins 0.000 description 23
- 102000008070 Interferon-gamma Human genes 0.000 description 22
- 229960003130 interferon gamma Drugs 0.000 description 22
- 102000005962 receptors Human genes 0.000 description 22
- 108020003175 receptors Proteins 0.000 description 22
- 108010002350 Interleukin-2 Proteins 0.000 description 21
- 102000000588 Interleukin-2 Human genes 0.000 description 21
- 230000004048 modification Effects 0.000 description 21
- 238000012986 modification Methods 0.000 description 21
- 230000009467 reduction Effects 0.000 description 20
- 102000013264 Interleukin-23 Human genes 0.000 description 19
- 102000004890 Interleukin-8 Human genes 0.000 description 19
- 108090001007 Interleukin-8 Proteins 0.000 description 19
- 101001037140 Homo sapiens Immunoglobulin heavy variable 3-23 Proteins 0.000 description 18
- 102100040220 Immunoglobulin heavy variable 3-23 Human genes 0.000 description 18
- 208000024891 symptom Diseases 0.000 description 18
- 210000004443 dendritic cell Anatomy 0.000 description 17
- 210000003819 peripheral blood mononuclear cell Anatomy 0.000 description 17
- 230000001154 acute effect Effects 0.000 description 15
- 239000000090 biomarker Substances 0.000 description 15
- 238000000338 in vitro Methods 0.000 description 15
- 230000002757 inflammatory effect Effects 0.000 description 15
- 239000000556 agonist Substances 0.000 description 14
- 238000000099 in vitro assay Methods 0.000 description 14
- 230000008859 change Effects 0.000 description 13
- 210000001072 colon Anatomy 0.000 description 13
- 230000000694 effects Effects 0.000 description 13
- 238000007799 mixed lymphocyte reaction assay Methods 0.000 description 13
- 230000007423 decrease Effects 0.000 description 12
- 210000001508 eye Anatomy 0.000 description 12
- 238000000684 flow cytometry Methods 0.000 description 12
- 239000013598 vector Substances 0.000 description 12
- 241001465754 Metazoa Species 0.000 description 11
- 210000002889 endothelial cell Anatomy 0.000 description 11
- 230000002496 gastric effect Effects 0.000 description 11
- 230000003993 interaction Effects 0.000 description 11
- 108050003558 Interleukin-17 Proteins 0.000 description 10
- 102000013691 Interleukin-17 Human genes 0.000 description 10
- 229940124599 anti-inflammatory drug Drugs 0.000 description 10
- 235000018102 proteins Nutrition 0.000 description 10
- 102000004169 proteins and genes Human genes 0.000 description 10
- 238000002198 surface plasmon resonance spectroscopy Methods 0.000 description 10
- 108010055166 Chemokine CCL5 Proteins 0.000 description 9
- 102000001327 Chemokine CCL5 Human genes 0.000 description 9
- 208000007465 Giant cell arteritis Diseases 0.000 description 9
- 102000003814 Interleukin-10 Human genes 0.000 description 9
- 108090000174 Interleukin-10 Proteins 0.000 description 9
- 206010047115 Vasculitis Diseases 0.000 description 9
- 208000037883 airway inflammation Diseases 0.000 description 9
- 208000006673 asthma Diseases 0.000 description 9
- 230000000875 corresponding effect Effects 0.000 description 9
- 210000001842 enterocyte Anatomy 0.000 description 9
- 210000004698 lymphocyte Anatomy 0.000 description 9
- 208000011580 syndromic disease Diseases 0.000 description 9
- 206010043207 temporal arteritis Diseases 0.000 description 9
- 101100112922 Candida albicans CDR3 gene Proteins 0.000 description 8
- 108010002335 Interleukin-9 Proteins 0.000 description 8
- 102000000585 Interleukin-9 Human genes 0.000 description 8
- 238000003556 assay Methods 0.000 description 8
- 230000001363 autoimmune Effects 0.000 description 8
- 230000005779 cell damage Effects 0.000 description 8
- 208000037887 cell injury Diseases 0.000 description 8
- 210000001035 gastrointestinal tract Anatomy 0.000 description 8
- 238000002868 homogeneous time resolved fluorescence Methods 0.000 description 8
- 208000015181 infectious disease Diseases 0.000 description 8
- 230000002458 infectious effect Effects 0.000 description 8
- 230000002401 inhibitory effect Effects 0.000 description 8
- 230000000968 intestinal effect Effects 0.000 description 8
- 230000002829 reductive effect Effects 0.000 description 8
- 102000003816 Interleukin-13 Human genes 0.000 description 7
- 108090000176 Interleukin-13 Proteins 0.000 description 7
- 108090000978 Interleukin-4 Proteins 0.000 description 7
- 108010002616 Interleukin-5 Proteins 0.000 description 7
- 102000000743 Interleukin-5 Human genes 0.000 description 7
- 241000699670 Mus sp. Species 0.000 description 7
- 201000004681 Psoriasis Diseases 0.000 description 7
- 230000003042 antagnostic effect Effects 0.000 description 7
- 230000004054 inflammatory process Effects 0.000 description 7
- 230000035772 mutation Effects 0.000 description 7
- 210000002966 serum Anatomy 0.000 description 7
- 102000017420 CD3 protein, epsilon/gamma/delta subunit Human genes 0.000 description 6
- 108050005493 CD3 protein, epsilon/gamma/delta subunit Proteins 0.000 description 6
- 206010016654 Fibrosis Diseases 0.000 description 6
- 101001008313 Homo sapiens Immunoglobulin kappa variable 1D-39 Proteins 0.000 description 6
- 102100027404 Immunoglobulin kappa variable 1D-39 Human genes 0.000 description 6
- 206010061218 Inflammation Diseases 0.000 description 6
- 239000004698 Polyethylene Substances 0.000 description 6
- 206010039705 Scleritis Diseases 0.000 description 6
- 208000027585 T-cell non-Hodgkin lymphoma Diseases 0.000 description 6
- 238000001574 biopsy Methods 0.000 description 6
- 229940079593 drug Drugs 0.000 description 6
- 230000004761 fibrosis Effects 0.000 description 6
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 6
- 230000014509 gene expression Effects 0.000 description 6
- 210000001616 monocyte Anatomy 0.000 description 6
- 210000004296 naive t lymphocyte Anatomy 0.000 description 6
- 238000011287 therapeutic dose Methods 0.000 description 6
- 238000002560 therapeutic procedure Methods 0.000 description 6
- 206010001052 Acute respiratory distress syndrome Diseases 0.000 description 5
- 108010047041 Complementarity Determining Regions Proteins 0.000 description 5
- 101000679851 Homo sapiens Tumor necrosis factor receptor superfamily member 4 Proteins 0.000 description 5
- 102000014150 Interferons Human genes 0.000 description 5
- 108010050904 Interferons Proteins 0.000 description 5
- 108091028043 Nucleic acid sequence Proteins 0.000 description 5
- 208000012654 Primary biliary cholangitis Diseases 0.000 description 5
- 241000700159 Rattus Species 0.000 description 5
- 208000013616 Respiratory Distress Syndrome Diseases 0.000 description 5
- 241000283984 Rodentia Species 0.000 description 5
- 206010042971 T-cell lymphoma Diseases 0.000 description 5
- 208000011341 adult acute respiratory distress syndrome Diseases 0.000 description 5
- 201000000028 adult respiratory distress syndrome Diseases 0.000 description 5
- 230000010056 antibody-dependent cellular cytotoxicity Effects 0.000 description 5
- 238000011161 development Methods 0.000 description 5
- 230000018109 developmental process Effects 0.000 description 5
- 125000002485 formyl group Chemical group [H]C(*)=O 0.000 description 5
- 230000004927 fusion Effects 0.000 description 5
- 102000050320 human TNFRSF4 Human genes 0.000 description 5
- 210000000987 immune system Anatomy 0.000 description 5
- 229940079322 interferon Drugs 0.000 description 5
- 230000003449 preventive effect Effects 0.000 description 5
- 238000011002 quantification Methods 0.000 description 5
- 239000002464 receptor antagonist Substances 0.000 description 5
- 229940044551 receptor antagonist Drugs 0.000 description 5
- 208000032671 Allergic granulomatous angiitis Diseases 0.000 description 4
- 241000251730 Chondrichthyes Species 0.000 description 4
- 208000006344 Churg-Strauss Syndrome Diseases 0.000 description 4
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical group [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 4
- 208000018428 Eosinophilic granulomatosis with polyangiitis Diseases 0.000 description 4
- 241000287828 Gallus gallus Species 0.000 description 4
- 206010017711 Gangrene Diseases 0.000 description 4
- 101001091242 Homo sapiens Immunoglobulin kappa joining 1 Proteins 0.000 description 4
- 102100034892 Immunoglobulin kappa joining 1 Human genes 0.000 description 4
- 208000011200 Kawasaki disease Diseases 0.000 description 4
- 206010025323 Lymphomas Diseases 0.000 description 4
- 108010060408 Member 25 Tumor Necrosis Factor Receptors Proteins 0.000 description 4
- 102000008166 Member 25 Tumor Necrosis Factor Receptors Human genes 0.000 description 4
- 241000283973 Oryctolagus cuniculus Species 0.000 description 4
- 241001494479 Pecora Species 0.000 description 4
- 208000017442 Retinal disease Diseases 0.000 description 4
- 206010038923 Retinopathy Diseases 0.000 description 4
- 208000021386 Sjogren Syndrome Diseases 0.000 description 4
- 125000000539 amino acid group Chemical group 0.000 description 4
- 238000013475 authorization Methods 0.000 description 4
- 235000013330 chicken meat Nutrition 0.000 description 4
- 230000001684 chronic effect Effects 0.000 description 4
- 229910052802 copper Inorganic materials 0.000 description 4
- 239000010949 copper Substances 0.000 description 4
- 210000003162 effector t lymphocyte Anatomy 0.000 description 4
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 4
- 239000007943 implant Substances 0.000 description 4
- 230000000977 initiatory effect Effects 0.000 description 4
- 210000003071 memory t lymphocyte Anatomy 0.000 description 4
- 208000001725 mucocutaneous lymph node syndrome Diseases 0.000 description 4
- 239000000092 prognostic biomarker Substances 0.000 description 4
- 229910052717 sulfur Inorganic materials 0.000 description 4
- 239000003053 toxin Substances 0.000 description 4
- 231100000765 toxin Toxicity 0.000 description 4
- 108700012359 toxins Proteins 0.000 description 4
- 208000009137 Behcet syndrome Diseases 0.000 description 3
- 208000008439 Biliary Liver Cirrhosis Diseases 0.000 description 3
- 208000033222 Biliary cirrhosis primary Diseases 0.000 description 3
- 241000283690 Bos taurus Species 0.000 description 3
- 210000001266 CD8-positive T-lymphocyte Anatomy 0.000 description 3
- 241000282832 Camelidae Species 0.000 description 3
- 208000030836 Hashimoto thyroiditis Diseases 0.000 description 3
- 101000914514 Homo sapiens T-cell-specific surface glycoprotein CD28 Proteins 0.000 description 3
- 102000008394 Immunoglobulin Fragments Human genes 0.000 description 3
- 108010021625 Immunoglobulin Fragments Proteins 0.000 description 3
- 206010062016 Immunosuppression Diseases 0.000 description 3
- 208000032514 Leukocytoclastic vasculitis Diseases 0.000 description 3
- 241000699666 Mus <mouse, genus> Species 0.000 description 3
- 230000006052 T cell proliferation Effects 0.000 description 3
- 102100027213 T-cell-specific surface glycoprotein CD28 Human genes 0.000 description 3
- 230000004913 activation Effects 0.000 description 3
- 210000000612 antigen-presenting cell Anatomy 0.000 description 3
- 206010003246 arthritis Diseases 0.000 description 3
- 230000009286 beneficial effect Effects 0.000 description 3
- 229940046731 calcineurin inhibitors Drugs 0.000 description 3
- 210000003169 central nervous system Anatomy 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 206010009887 colitis Diseases 0.000 description 3
- 238000007796 conventional method Methods 0.000 description 3
- 239000012636 effector Substances 0.000 description 3
- 210000005260 human cell Anatomy 0.000 description 3
- 230000028993 immune response Effects 0.000 description 3
- 230000001506 immunosuppresive effect Effects 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 201000002364 leukopenia Diseases 0.000 description 3
- 231100001022 leukopenia Toxicity 0.000 description 3
- 239000003446 ligand Substances 0.000 description 3
- 206010025135 lupus erythematosus Diseases 0.000 description 3
- 210000002540 macrophage Anatomy 0.000 description 3
- 210000004379 membrane Anatomy 0.000 description 3
- 239000012528 membrane Substances 0.000 description 3
- 238000012544 monitoring process Methods 0.000 description 3
- 210000005087 mononuclear cell Anatomy 0.000 description 3
- 230000008506 pathogenesis Effects 0.000 description 3
- 229910052700 potassium Inorganic materials 0.000 description 3
- 238000009117 preventive therapy Methods 0.000 description 3
- 230000002062 proliferating effect Effects 0.000 description 3
- 102200072304 rs1057519530 Human genes 0.000 description 3
- 150000003839 salts Chemical class 0.000 description 3
- 208000010157 sclerosing cholangitis Diseases 0.000 description 3
- 230000011664 signaling Effects 0.000 description 3
- 210000003491 skin Anatomy 0.000 description 3
- 229960003989 tocilizumab Drugs 0.000 description 3
- 230000003442 weekly effect Effects 0.000 description 3
- TVZRAEYQIKYCPH-UHFFFAOYSA-N 3-(trimethylsilyl)propane-1-sulfonic acid Chemical compound C[Si](C)(C)CCCS(O)(=O)=O TVZRAEYQIKYCPH-UHFFFAOYSA-N 0.000 description 2
- 208000003343 Antiphospholipid Syndrome Diseases 0.000 description 2
- 206010069002 Autoimmune pancreatitis Diseases 0.000 description 2
- 201000001178 Bacterial Pneumonia Diseases 0.000 description 2
- 206010008609 Cholangitis sclerosing Diseases 0.000 description 2
- 206010012689 Diabetic retinopathy Diseases 0.000 description 2
- 206010018612 Gonorrhoea Diseases 0.000 description 2
- WZUVPPKBWHMQCE-UHFFFAOYSA-N Haematoxylin Chemical compound C12=CC(O)=C(O)C=C2CC2(O)C1C1=CC=C(O)C(O)=C1OC2 WZUVPPKBWHMQCE-UHFFFAOYSA-N 0.000 description 2
- 208000007514 Herpes zoster Diseases 0.000 description 2
- 101001055222 Homo sapiens Interleukin-8 Proteins 0.000 description 2
- 241000713772 Human immunodeficiency virus 1 Species 0.000 description 2
- 108010002386 Interleukin-3 Proteins 0.000 description 2
- 102100026236 Interleukin-8 Human genes 0.000 description 2
- 102000015696 Interleukins Human genes 0.000 description 2
- 108010063738 Interleukins Proteins 0.000 description 2
- 208000000209 Isaacs syndrome Diseases 0.000 description 2
- 201000010743 Lambert-Eaton myasthenic syndrome Diseases 0.000 description 2
- 208000034624 Leukocytoclastic Cutaneous Vasculitis Diseases 0.000 description 2
- 241000282553 Macaca Species 0.000 description 2
- 108091092878 Microsatellite Proteins 0.000 description 2
- 208000003250 Mixed connective tissue disease Diseases 0.000 description 2
- 206010028424 Myasthenic syndrome Diseases 0.000 description 2
- 108010057466 NF-kappa B Proteins 0.000 description 2
- 102000003945 NF-kappa B Human genes 0.000 description 2
- JYDNKGUBLIKNAM-UHFFFAOYSA-N Oxyallobutulin Natural products C1CC(=O)C(C)(C)C2CCC3(C)C4(C)CCC5(CO)CCC(C(=C)C)C5C4CCC3C21C JYDNKGUBLIKNAM-UHFFFAOYSA-N 0.000 description 2
- 206010034277 Pemphigoid Diseases 0.000 description 2
- 241000721454 Pemphigus Species 0.000 description 2
- 208000027190 Peripheral T-cell lymphomas Diseases 0.000 description 2
- 208000009052 Precursor T-Cell Lymphoblastic Leukemia-Lymphoma Diseases 0.000 description 2
- 101100412401 Rattus norvegicus Reg3a gene Proteins 0.000 description 2
- 230000010799 Receptor Interactions Effects 0.000 description 2
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 2
- 201000010848 Schnitzler Syndrome Diseases 0.000 description 2
- 206010040070 Septic Shock Diseases 0.000 description 2
- 108020004459 Small interfering RNA Proteins 0.000 description 2
- 206010072148 Stiff-Person syndrome Diseases 0.000 description 2
- 208000031672 T-Cell Peripheral Lymphoma Diseases 0.000 description 2
- 208000029052 T-cell acute lymphoblastic leukemia Diseases 0.000 description 2
- 230000029662 T-helper 1 type immune response Effects 0.000 description 2
- 210000000447 Th1 cell Anatomy 0.000 description 2
- 108060008683 Tumor Necrosis Factor Receptor Proteins 0.000 description 2
- 101710187743 Tumor necrosis factor receptor superfamily member 1A Proteins 0.000 description 2
- 102100033732 Tumor necrosis factor receptor superfamily member 1A Human genes 0.000 description 2
- 239000013543 active substance Substances 0.000 description 2
- 208000002552 acute disseminated encephalomyelitis Diseases 0.000 description 2
- 208000024340 acute graft versus host disease Diseases 0.000 description 2
- 235000004279 alanine Nutrition 0.000 description 2
- 208000004631 alopecia areata Diseases 0.000 description 2
- 150000001408 amides Chemical class 0.000 description 2
- 230000033115 angiogenesis Effects 0.000 description 2
- 208000027625 autoimmune inner ear disease Diseases 0.000 description 2
- 206010071578 autoimmune retinopathy Diseases 0.000 description 2
- 201000004982 autoimmune uveitis Diseases 0.000 description 2
- 210000003719 b-lymphocyte Anatomy 0.000 description 2
- 230000001580 bacterial effect Effects 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- JYDNKGUBLIKNAM-CNRMHUMKSA-N betulone Chemical compound C1CC(=O)C(C)(C)[C@@H]2CC[C@@]3(C)[C@]4(C)CC[C@@]5(CO)CC[C@@H](C(=C)C)[C@@H]5[C@H]4CC[C@@H]3[C@]21C JYDNKGUBLIKNAM-CNRMHUMKSA-N 0.000 description 2
- 230000000903 blocking effect Effects 0.000 description 2
- 206010006451 bronchitis Diseases 0.000 description 2
- 210000004970 cd4 cell Anatomy 0.000 description 2
- 208000010353 central nervous system vasculitis Diseases 0.000 description 2
- 239000003067 chemokine receptor CCR5 antagonist Substances 0.000 description 2
- 210000000349 chromosome Anatomy 0.000 description 2
- 208000037976 chronic inflammation Diseases 0.000 description 2
- 238000002648 combination therapy Methods 0.000 description 2
- 150000001875 compounds Chemical class 0.000 description 2
- 230000004940 costimulation Effects 0.000 description 2
- 230000003111 delayed effect Effects 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 206010014599 encephalitis Diseases 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 102000037865 fusion proteins Human genes 0.000 description 2
- 108020001507 fusion proteins Proteins 0.000 description 2
- 201000011587 gastric lymphoma Diseases 0.000 description 2
- 208000007565 gingivitis Diseases 0.000 description 2
- 125000000291 glutamic acid group Chemical group N[C@@H](CCC(O)=O)C(=O)* 0.000 description 2
- 230000013595 glycosylation Effects 0.000 description 2
- 238000006206 glycosylation reaction Methods 0.000 description 2
- 208000001786 gonorrhea Diseases 0.000 description 2
- 210000000224 granular leucocyte Anatomy 0.000 description 2
- 230000033687 granuloma formation Effects 0.000 description 2
- 230000012010 growth Effects 0.000 description 2
- 230000036541 health Effects 0.000 description 2
- 201000006362 hypersensitivity vasculitis Diseases 0.000 description 2
- 210000002865 immune cell Anatomy 0.000 description 2
- 230000001900 immune effect Effects 0.000 description 2
- 229940127121 immunoconjugate Drugs 0.000 description 2
- 229940124589 immunosuppressive drug Drugs 0.000 description 2
- 230000001976 improved effect Effects 0.000 description 2
- 230000006698 induction Effects 0.000 description 2
- 238000011221 initial treatment Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 230000021995 interleukin-8 production Effects 0.000 description 2
- 238000001990 intravenous administration Methods 0.000 description 2
- 230000009545 invasion Effects 0.000 description 2
- 229910052740 iodine Inorganic materials 0.000 description 2
- 125000001909 leucine group Chemical group [H]N(*)C(C(*)=O)C([H])([H])C(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- 230000003211 malignant effect Effects 0.000 description 2
- 208000020968 mature T-cell and NK-cell non-Hodgkin lymphoma Diseases 0.000 description 2
- 238000005259 measurement Methods 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 108020004999 messenger RNA Proteins 0.000 description 2
- 238000010172 mouse model Methods 0.000 description 2
- 230000002232 neuromuscular Effects 0.000 description 2
- 210000000440 neutrophil Anatomy 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 230000001575 pathological effect Effects 0.000 description 2
- 210000004976 peripheral blood cell Anatomy 0.000 description 2
- 229910052698 phosphorus Inorganic materials 0.000 description 2
- 210000002381 plasma Anatomy 0.000 description 2
- 208000005987 polymyositis Diseases 0.000 description 2
- 208000015768 polyposis Diseases 0.000 description 2
- 108090000765 processed proteins & peptides Proteins 0.000 description 2
- 230000005855 radiation Effects 0.000 description 2
- 208000002574 reactive arthritis Diseases 0.000 description 2
- 201000000306 sarcoidosis Diseases 0.000 description 2
- 230000036303 septic shock Effects 0.000 description 2
- 239000004055 small Interfering RNA Substances 0.000 description 2
- 238000010186 staining Methods 0.000 description 2
- 230000001629 suppression Effects 0.000 description 2
- 230000002195 synergetic effect Effects 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 206010043778 thyroiditis Diseases 0.000 description 2
- 239000013638 trimer Substances 0.000 description 2
- 102000003298 tumor necrosis factor receptor Human genes 0.000 description 2
- 229910052720 vanadium Inorganic materials 0.000 description 2
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 1
- NFGXHKASABOEEW-UHFFFAOYSA-N 1-methylethyl 11-methoxy-3,7,11-trimethyl-2,4-dodecadienoate Chemical compound COC(C)(C)CCCC(C)CC=CC(C)=CC(=O)OC(C)C NFGXHKASABOEEW-UHFFFAOYSA-N 0.000 description 1
- 208000030090 Acute Disease Diseases 0.000 description 1
- 206010048998 Acute phase reaction Diseases 0.000 description 1
- 208000026872 Addison Disease Diseases 0.000 description 1
- 102100034540 Adenomatous polyposis coli protein Human genes 0.000 description 1
- 208000016683 Adult T-cell leukemia/lymphoma Diseases 0.000 description 1
- 208000022309 Alcoholic Liver disease Diseases 0.000 description 1
- 208000024827 Alzheimer disease Diseases 0.000 description 1
- 108091093088 Amplicon Proteins 0.000 description 1
- 206010073478 Anaplastic large-cell lymphoma Diseases 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 206010003267 Arthritis reactive Diseases 0.000 description 1
- DCXYFEDJOCDNAF-UHFFFAOYSA-N Asparagine Natural products OC(=O)C(N)CC(N)=O DCXYFEDJOCDNAF-UHFFFAOYSA-N 0.000 description 1
- 230000003844 B-cell-activation Effects 0.000 description 1
- 208000027496 Behcet disease Diseases 0.000 description 1
- 208000014644 Brain disease Diseases 0.000 description 1
- 206010006458 Bronchitis chronic Diseases 0.000 description 1
- 102100036848 C-C motif chemokine 20 Human genes 0.000 description 1
- 241000282836 Camelus dromedarius Species 0.000 description 1
- 208000005623 Carcinogenesis Diseases 0.000 description 1
- 102000019034 Chemokines Human genes 0.000 description 1
- 108010012236 Chemokines Proteins 0.000 description 1
- 108010019670 Chimeric Antigen Receptors Proteins 0.000 description 1
- 208000017667 Chronic Disease Diseases 0.000 description 1
- 206010010356 Congenital anomaly Diseases 0.000 description 1
- 206010010904 Convulsion Diseases 0.000 description 1
- 201000003883 Cystic fibrosis Diseases 0.000 description 1
- 102100025621 Cytochrome b-245 heavy chain Human genes 0.000 description 1
- 201000004624 Dermatitis Diseases 0.000 description 1
- 108700022150 Designed Ankyrin Repeat Proteins Proteins 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 208000032274 Encephalopathy Diseases 0.000 description 1
- 208000024658 Epilepsy syndrome Diseases 0.000 description 1
- 208000002877 Epileptic Syndromes Diseases 0.000 description 1
- 208000016937 Extranodal nasal NK/T cell lymphoma Diseases 0.000 description 1
- 102000009109 Fc receptors Human genes 0.000 description 1
- 108010087819 Fc receptors Proteins 0.000 description 1
- 208000024160 Fuchs heterochromic iridocyclitis Diseases 0.000 description 1
- 201000010479 Fuchs' heterochromic uveitis Diseases 0.000 description 1
- WHUUTDBJXJRKMK-UHFFFAOYSA-N Glutamic acid Natural products OC(=O)C(N)CCC(O)=O WHUUTDBJXJRKMK-UHFFFAOYSA-N 0.000 description 1
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 1
- 206010072579 Granulomatosis with polyangiitis Diseases 0.000 description 1
- 102000012153 HLA-B27 Antigen Human genes 0.000 description 1
- 108010061486 HLA-B27 Antigen Proteins 0.000 description 1
- 208000001204 Hashimoto Disease Diseases 0.000 description 1
- 208000035186 Hemolytic Autoimmune Anemia Diseases 0.000 description 1
- 241000238631 Hexapoda Species 0.000 description 1
- 101000924577 Homo sapiens Adenomatous polyposis coli protein Proteins 0.000 description 1
- 101000713099 Homo sapiens C-C motif chemokine 20 Proteins 0.000 description 1
- 101000746373 Homo sapiens Granulocyte-macrophage colony-stimulating factor Proteins 0.000 description 1
- 101001018097 Homo sapiens L-selectin Proteins 0.000 description 1
- 101000738771 Homo sapiens Receptor-type tyrosine-protein phosphatase C Proteins 0.000 description 1
- 101000713602 Homo sapiens T-box transcription factor TBX21 Proteins 0.000 description 1
- 206010020751 Hypersensitivity Diseases 0.000 description 1
- 206010020850 Hyperthyroidism Diseases 0.000 description 1
- 206010053574 Immunoblastic lymphoma Diseases 0.000 description 1
- 102100022297 Integrin alpha-X Human genes 0.000 description 1
- 102100037850 Interferon gamma Human genes 0.000 description 1
- 102100020881 Interleukin-1 alpha Human genes 0.000 description 1
- 102000003777 Interleukin-1 beta Human genes 0.000 description 1
- 108090000193 Interleukin-1 beta Proteins 0.000 description 1
- 108010082786 Interleukin-1alpha Proteins 0.000 description 1
- 208000026492 Isaac syndrome Diseases 0.000 description 1
- QNAYBMKLOCPYGJ-REOHCLBHSA-N L-alanine Chemical compound C[C@H](N)C(O)=O QNAYBMKLOCPYGJ-REOHCLBHSA-N 0.000 description 1
- DCXYFEDJOCDNAF-REOHCLBHSA-N L-asparagine Chemical compound OC(=O)[C@@H](N)CC(N)=O DCXYFEDJOCDNAF-REOHCLBHSA-N 0.000 description 1
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 1
- WHUUTDBJXJRKMK-VKHMYHEASA-N L-glutamic acid Chemical compound OC(=O)[C@@H](N)CCC(O)=O WHUUTDBJXJRKMK-VKHMYHEASA-N 0.000 description 1
- AGPKZVBTJJNPAG-WHFBIAKZSA-N L-isoleucine Chemical compound CC[C@H](C)[C@H](N)C(O)=O AGPKZVBTJJNPAG-WHFBIAKZSA-N 0.000 description 1
- ROHFNLRQFUQHCH-YFKPBYRVSA-N L-leucine Chemical compound CC(C)C[C@H](N)C(O)=O ROHFNLRQFUQHCH-YFKPBYRVSA-N 0.000 description 1
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 description 1
- COLNVLDHVKWLRT-QMMMGPOBSA-N L-phenylalanine Chemical compound OC(=O)[C@@H](N)CC1=CC=CC=C1 COLNVLDHVKWLRT-QMMMGPOBSA-N 0.000 description 1
- 102100033467 L-selectin Human genes 0.000 description 1
- QIVBCDIJIAJPQS-VIFPVBQESA-N L-tryptophane Chemical compound C1=CC=C2C(C[C@H](N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-VIFPVBQESA-N 0.000 description 1
- OUYCCCASQSFEME-QMMMGPOBSA-N L-tyrosine Chemical compound OC(=O)[C@@H](N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-QMMMGPOBSA-N 0.000 description 1
- KZSNJWFQEVHDMF-BYPYZUCNSA-N L-valine Chemical compound CC(C)[C@H](N)C(O)=O KZSNJWFQEVHDMF-BYPYZUCNSA-N 0.000 description 1
- ROHFNLRQFUQHCH-UHFFFAOYSA-N Leucine Natural products CC(C)CC(N)C(O)=O ROHFNLRQFUQHCH-UHFFFAOYSA-N 0.000 description 1
- 101710177649 Low affinity immunoglobulin gamma Fc region receptor III Proteins 0.000 description 1
- 101710099301 Low affinity immunoglobulin gamma Fc region receptor III-A Proteins 0.000 description 1
- 102100029185 Low affinity immunoglobulin gamma Fc region receptor III-B Human genes 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 101710125418 Major capsid protein Proteins 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 201000009906 Meningitis Diseases 0.000 description 1
- 206010027476 Metastases Diseases 0.000 description 1
- 208000019695 Migraine disease Diseases 0.000 description 1
- 206010060880 Monoclonal gammopathy Diseases 0.000 description 1
- 206010051787 Multiple organ transplant rejection Diseases 0.000 description 1
- 241001529936 Murinae Species 0.000 description 1
- 101000764258 Mus musculus Tumor necrosis factor ligand superfamily member 4 Proteins 0.000 description 1
- 201000003793 Myelodysplastic syndrome Diseases 0.000 description 1
- 201000002481 Myositis Diseases 0.000 description 1
- 206010072359 Neuromyotonia Diseases 0.000 description 1
- 208000021384 Obsessive-Compulsive disease Diseases 0.000 description 1
- 108091008606 PDGF receptors Proteins 0.000 description 1
- 102100026450 POU domain, class 3, transcription factor 4 Human genes 0.000 description 1
- 101710133389 POU domain, class 3, transcription factor 4 Proteins 0.000 description 1
- 208000002774 Paraproteinemias Diseases 0.000 description 1
- 208000018737 Parkinson disease Diseases 0.000 description 1
- 241000577979 Peromyscus spicilegus Species 0.000 description 1
- 241000235648 Pichia Species 0.000 description 1
- 102000011653 Platelet-Derived Growth Factor Receptors Human genes 0.000 description 1
- 206010035664 Pneumonia Diseases 0.000 description 1
- 206010036105 Polyneuropathy Diseases 0.000 description 1
- 201000001263 Psoriatic Arthritis Diseases 0.000 description 1
- 208000036824 Psoriatic arthropathy Diseases 0.000 description 1
- 208000012322 Raynaud phenomenon Diseases 0.000 description 1
- 102100037422 Receptor-type tyrosine-protein phosphatase C Human genes 0.000 description 1
- 102000018210 Recoverin Human genes 0.000 description 1
- 108010076570 Recoverin Proteins 0.000 description 1
- 208000033464 Reiter syndrome Diseases 0.000 description 1
- 241000235070 Saccharomyces Species 0.000 description 1
- 206010039710 Scleroderma Diseases 0.000 description 1
- 206010040047 Sepsis Diseases 0.000 description 1
- MTCFGRXMJLQNBG-UHFFFAOYSA-N Serine Natural products OCC(N)C(O)=O MTCFGRXMJLQNBG-UHFFFAOYSA-N 0.000 description 1
- 208000009359 Sezary Syndrome Diseases 0.000 description 1
- 208000021388 Sezary disease Diseases 0.000 description 1
- 201000009594 Systemic Scleroderma Diseases 0.000 description 1
- 206010042953 Systemic sclerosis Diseases 0.000 description 1
- 102100036840 T-box transcription factor TBX21 Human genes 0.000 description 1
- 208000000389 T-cell leukemia Diseases 0.000 description 1
- 208000028530 T-cell lymphoblastic leukemia/lymphoma Diseases 0.000 description 1
- 230000030429 T-helper 17 type immune response Effects 0.000 description 1
- 210000000662 T-lymphocyte subset Anatomy 0.000 description 1
- 208000001106 Takayasu Arteritis Diseases 0.000 description 1
- 210000000068 Th17 cell Anatomy 0.000 description 1
- 210000004241 Th2 cell Anatomy 0.000 description 1
- AYFVYJQAPQTCCC-UHFFFAOYSA-N Threonine Natural products CC(O)C(N)C(O)=O AYFVYJQAPQTCCC-UHFFFAOYSA-N 0.000 description 1
- 239000004473 Threonine Substances 0.000 description 1
- 206010043540 Thromboangiitis obliterans Diseases 0.000 description 1
- 208000031981 Thrombocytopenic Idiopathic Purpura Diseases 0.000 description 1
- QIVBCDIJIAJPQS-UHFFFAOYSA-N Tryptophan Natural products C1=CC=C2C(CC(N)C(O)=O)=CNC2=C1 QIVBCDIJIAJPQS-UHFFFAOYSA-N 0.000 description 1
- 102100026890 Tumor necrosis factor ligand superfamily member 4 Human genes 0.000 description 1
- 206010054094 Tumour necrosis Diseases 0.000 description 1
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 1
- 108091005956 Type II transmembrane proteins Proteins 0.000 description 1
- 208000001445 Uveomeningoencephalitic Syndrome Diseases 0.000 description 1
- KZSNJWFQEVHDMF-UHFFFAOYSA-N Valine Natural products CC(C)C(N)C(O)=O KZSNJWFQEVHDMF-UHFFFAOYSA-N 0.000 description 1
- 208000034705 Vogt-Koyanagi-Harada syndrome Diseases 0.000 description 1
- 208000027207 Whipple disease Diseases 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- 230000003187 abdominal effect Effects 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000004658 acute-phase response Effects 0.000 description 1
- 201000006966 adult T-cell leukemia Diseases 0.000 description 1
- 125000003295 alanine group Chemical group N[C@@H](C)C(=O)* 0.000 description 1
- 208000026935 allergic disease Diseases 0.000 description 1
- 230000000172 allergic effect Effects 0.000 description 1
- 230000007815 allergy Effects 0.000 description 1
- 231100000360 alopecia Toxicity 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 230000008485 antagonism Effects 0.000 description 1
- 239000005557 antagonist Substances 0.000 description 1
- 239000000427 antigen Substances 0.000 description 1
- 108091007433 antigens Proteins 0.000 description 1
- 102000036639 antigens Human genes 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 238000013459 approach Methods 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 229960001230 asparagine Drugs 0.000 description 1
- 235000009582 asparagine Nutrition 0.000 description 1
- 235000003704 aspartic acid Nutrition 0.000 description 1
- 208000010668 atopic eczema Diseases 0.000 description 1
- 201000000448 autoimmune hemolytic anemia Diseases 0.000 description 1
- 201000003710 autoimmune thrombocytopenic purpura Diseases 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- OQFSQFPPLPISGP-UHFFFAOYSA-N beta-carboxyaspartic acid Natural products OC(=O)C(N)C(C(O)=O)C(O)=O OQFSQFPPLPISGP-UHFFFAOYSA-N 0.000 description 1
- 239000002981 blocking agent Substances 0.000 description 1
- 201000009267 bronchiectasis Diseases 0.000 description 1
- 230000036952 cancer formation Effects 0.000 description 1
- 231100000504 carcinogenesis Toxicity 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 208000007451 chronic bronchitis Diseases 0.000 description 1
- 208000016532 chronic granulomatous disease Diseases 0.000 description 1
- 230000006020 chronic inflammation Effects 0.000 description 1
- 208000037893 chronic inflammatory disorder Diseases 0.000 description 1
- 208000025302 chronic primary adrenal insufficiency Diseases 0.000 description 1
- DQLATGHUWYMOKM-UHFFFAOYSA-L cisplatin Chemical compound N[Pt](N)(Cl)Cl DQLATGHUWYMOKM-UHFFFAOYSA-L 0.000 description 1
- 230000008951 colonic inflammation Effects 0.000 description 1
- 208000022136 colorectal lymphoma Diseases 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 230000003750 conditioning effect Effects 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 230000002596 correlated effect Effects 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000006378 damage Effects 0.000 description 1
- 238000013016 damping Methods 0.000 description 1
- 230000034994 death Effects 0.000 description 1
- 230000007812 deficiency Effects 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- 201000001981 dermatomyositis Diseases 0.000 description 1
- 238000002405 diagnostic procedure Methods 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 230000009266 disease activity Effects 0.000 description 1
- 230000003828 downregulation Effects 0.000 description 1
- 230000009977 dual effect Effects 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- YQGOJNYOYNNSMM-UHFFFAOYSA-N eosin Chemical compound [Na+].OC(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C(O)=C(Br)C=C21 YQGOJNYOYNNSMM-UHFFFAOYSA-N 0.000 description 1
- 206010015037 epilepsy Diseases 0.000 description 1
- 230000001747 exhibiting effect Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000013604 expression vector Substances 0.000 description 1
- 210000004700 fetal blood Anatomy 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 210000004475 gamma-delta t lymphocyte Anatomy 0.000 description 1
- 235000013922 glutamic acid Nutrition 0.000 description 1
- 239000004220 glutamic acid Substances 0.000 description 1
- ZDXPYRJPNDTMRX-UHFFFAOYSA-N glutamine Natural products OC(=O)C(N)CCC(N)=O ZDXPYRJPNDTMRX-UHFFFAOYSA-N 0.000 description 1
- PCHJSUWPFVWCPO-UHFFFAOYSA-N gold Chemical compound [Au] PCHJSUWPFVWCPO-UHFFFAOYSA-N 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 210000000777 hematopoietic system Anatomy 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- 210000003630 histaminocyte Anatomy 0.000 description 1
- 230000002962 histologic effect Effects 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 208000003532 hypothyroidism Diseases 0.000 description 1
- 230000002989 hypothyroidism Effects 0.000 description 1
- 238000010166 immunofluorescence Methods 0.000 description 1
- 238000003364 immunohistochemistry Methods 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000001727 in vivo Methods 0.000 description 1
- 230000001524 infective effect Effects 0.000 description 1
- 208000000509 infertility Diseases 0.000 description 1
- 230000036512 infertility Effects 0.000 description 1
- 231100000535 infertility Toxicity 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 229940096397 interleukin-8 Drugs 0.000 description 1
- XKTZWUACRZHVAN-VADRZIEHSA-N interleukin-8 Chemical compound C([C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@@H](NC(C)=O)CCSC)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CCSC)C(=O)N1[C@H](CCC1)C(=O)N1[C@H](CCC1)C(=O)N[C@@H](C)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC=1C=CC(O)=CC=1)C(=O)N[C@H](CO)C(=O)N1[C@H](CCC1)C(N)=O)C1=CC=CC=C1 XKTZWUACRZHVAN-VADRZIEHSA-N 0.000 description 1
- 230000004609 intestinal homeostasis Effects 0.000 description 1
- 210000004347 intestinal mucosa Anatomy 0.000 description 1
- 230000006662 intracellular pathway Effects 0.000 description 1
- 238000007913 intrathecal administration Methods 0.000 description 1
- 208000028867 ischemia Diseases 0.000 description 1
- 229960000310 isoleucine Drugs 0.000 description 1
- AGPKZVBTJJNPAG-UHFFFAOYSA-N isoleucine Natural products CCC(C)C(N)C(O)=O AGPKZVBTJJNPAG-UHFFFAOYSA-N 0.000 description 1
- 230000002147 killing effect Effects 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 210000001821 langerhans cell Anatomy 0.000 description 1
- 239000008141 laxative Substances 0.000 description 1
- 230000002475 laxative effect Effects 0.000 description 1
- 230000003902 lesion Effects 0.000 description 1
- 231100000518 lethal Toxicity 0.000 description 1
- 230000001665 lethal effect Effects 0.000 description 1
- 208000032839 leukemia Diseases 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 230000004807 localization Effects 0.000 description 1
- 210000001165 lymph node Anatomy 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 210000004962 mammalian cell Anatomy 0.000 description 1
- GSNHKUDZZFZSJB-QYOOZWMWSA-N maraviroc Chemical compound CC(C)C1=NN=C(C)N1[C@@H]1C[C@H](N2CC[C@H](NC(=O)C3CCC(F)(F)CC3)C=3C=CC=CC=3)CC[C@H]2C1 GSNHKUDZZFZSJB-QYOOZWMWSA-N 0.000 description 1
- 229960004710 maraviroc Drugs 0.000 description 1
- 239000003550 marker Substances 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 201000001441 melanoma Diseases 0.000 description 1
- 230000009401 metastasis Effects 0.000 description 1
- 229930182817 methionine Natural products 0.000 description 1
- 206010027599 migraine Diseases 0.000 description 1
- 230000005012 migration Effects 0.000 description 1
- 238000013508 migration Methods 0.000 description 1
- 239000000178 monomer Substances 0.000 description 1
- 206010065579 multifocal motor neuropathy Diseases 0.000 description 1
- 208000037890 multiple organ injury Diseases 0.000 description 1
- 206010028417 myasthenia gravis Diseases 0.000 description 1
- 201000005962 mycosis fungoides Diseases 0.000 description 1
- 208000025113 myeloid leukemia Diseases 0.000 description 1
- 210000000822 natural killer cell Anatomy 0.000 description 1
- 230000002956 necrotizing effect Effects 0.000 description 1
- 201000008383 nephritis Diseases 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 230000003472 neutralizing effect Effects 0.000 description 1
- 230000011242 neutrophil chemotaxis Effects 0.000 description 1
- 230000000414 obstructive effect Effects 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 235000019198 oils Nutrition 0.000 description 1
- 208000005963 oophoritis Diseases 0.000 description 1
- 201000005737 orchitis Diseases 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 238000002823 phage display Methods 0.000 description 1
- 238000011422 pharmacological therapy Methods 0.000 description 1
- COLNVLDHVKWLRT-UHFFFAOYSA-N phenylalanine Natural products OC(=O)C(N)CC1=CC=CC=C1 COLNVLDHVKWLRT-UHFFFAOYSA-N 0.000 description 1
- 208000008423 pleurisy Diseases 0.000 description 1
- 230000007824 polyneuropathy Effects 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 238000011324 primary prophylaxis Methods 0.000 description 1
- 201000000742 primary sclerosing cholangitis Diseases 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 239000003805 procoagulant Substances 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 238000000159 protein binding assay Methods 0.000 description 1
- 238000002331 protein detection Methods 0.000 description 1
- 238000002818 protein evolution Methods 0.000 description 1
- 238000003753 real-time PCR Methods 0.000 description 1
- 210000003289 regulatory T cell Anatomy 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 230000008439 repair process Effects 0.000 description 1
- 230000010410 reperfusion Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 238000002702 ribosome display Methods 0.000 description 1
- 238000009118 salvage therapy Methods 0.000 description 1
- 238000005070 sampling Methods 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 208000017520 skin disease Diseases 0.000 description 1
- 150000003384 small molecules Chemical class 0.000 description 1
- 210000000329 smooth muscle myocyte Anatomy 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 210000000952 spleen Anatomy 0.000 description 1
- 238000003153 stable transfection Methods 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 230000008093 supporting effect Effects 0.000 description 1
- 238000001356 surgical procedure Methods 0.000 description 1
- 210000005222 synovial tissue Anatomy 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- 230000002992 thymic effect Effects 0.000 description 1
- 230000000451 tissue damage Effects 0.000 description 1
- 231100000827 tissue damage Toxicity 0.000 description 1
- 230000009261 transgenic effect Effects 0.000 description 1
- 208000035408 type 1 diabetes mellitus 1 Diseases 0.000 description 1
- OUYCCCASQSFEME-UHFFFAOYSA-N tyrosine Natural products OC(=O)C(N)CC1=CC=C(O)C=C1 OUYCCCASQSFEME-UHFFFAOYSA-N 0.000 description 1
- 239000004474 valine Substances 0.000 description 1
- 230000004580 weight loss Effects 0.000 description 1
- 210000005253 yeast cell Anatomy 0.000 description 1
- 229910052727 yttrium Inorganic materials 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
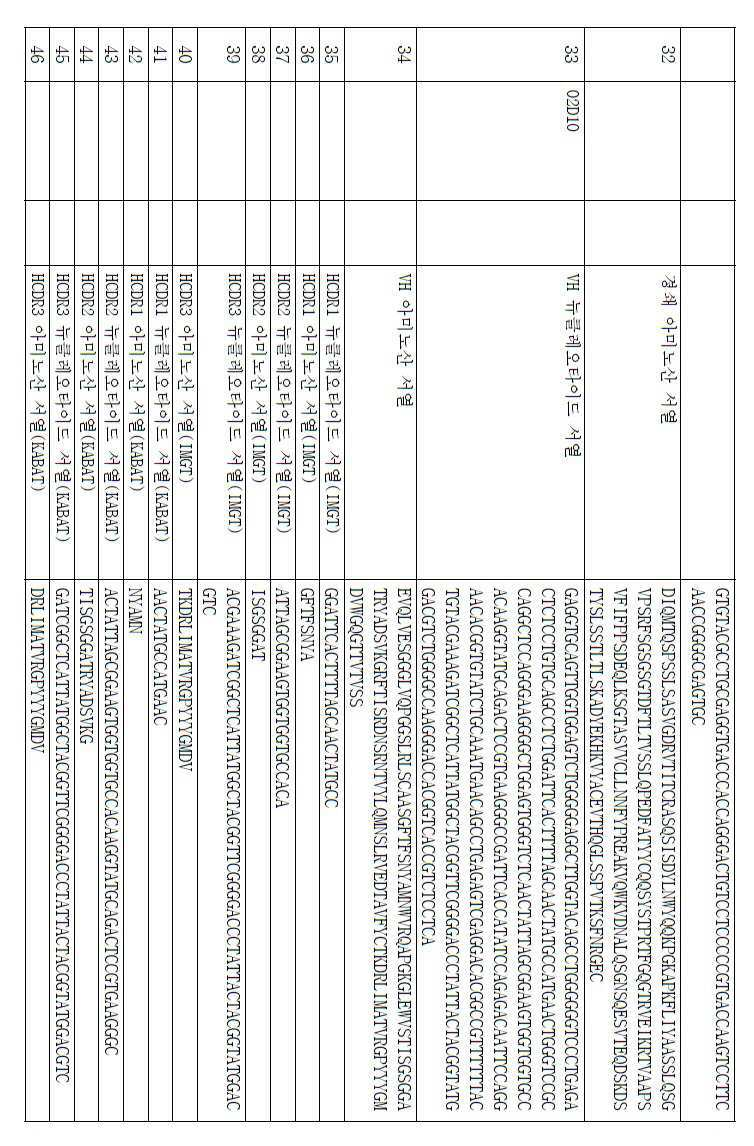
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/365—Lactones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/436—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a six-membered ring having oxygen as a ring hetero atom, e.g. rapamycin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/57—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone
- A61K31/573—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone substituted in position 21, e.g. cortisone, dexamethasone, prednisone or aldosterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/66—Phosphorus compounds
- A61K31/675—Phosphorus compounds having nitrogen as a ring hetero atom, e.g. pyridoxal phosphate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/12—Cyclic peptides, e.g. bacitracins; Polymyxins; Gramicidins S, C; Tyrocidins A, B or C
- A61K38/13—Cyclosporins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/177—Receptors; Cell surface antigens; Cell surface determinants
- A61K38/1793—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
- A61K39/39533—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals
- A61K39/3955—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum against materials from animals against proteinaceous materials, e.g. enzymes, hormones, lymphokines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P27/00—Drugs for disorders of the senses
- A61P27/02—Ophthalmic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/06—Immunosuppressants, e.g. drugs for graft rejection
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2875—Immunoglobulins [IGs], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the NGF/TNF superfamily, e.g. CD70, CD95L, CD153, CD154
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/20—Immunoglobulins specific features characterized by taxonomic origin
- C07K2317/21—Immunoglobulins specific features characterized by taxonomic origin from primates, e.g. man
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/73—Inducing cell death, e.g. apoptosis, necrosis or inhibition of cell proliferation
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/94—Stability, e.g. half-life, pH, temperature or enzyme-resistance
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/30—Non-immunoglobulin-derived peptide or protein having an immunoglobulin constant or Fc region, or a fragment thereof, attached thereto
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2319/00—Fusion polypeptide
- C07K2319/32—Fusion polypeptide fusions with soluble part of a cell surface receptor, "decoy receptors"
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Immunology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Gastroenterology & Hepatology (AREA)
- Endocrinology (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Rheumatology (AREA)
- Transplantation (AREA)
- Diabetes (AREA)
- Pain & Pain Management (AREA)
- Biophysics (AREA)
- Zoology (AREA)
- Cell Biology (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Pulmonology (AREA)
- Physical Education & Sports Medicine (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Emergency Medicine (AREA)
- Ophthalmology & Optometry (AREA)
- Obesity (AREA)
- Hematology (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
본 발명은 항-인간 OX40L 항체, 신규한 의약 용도 및 방법에 관한 것이다.
Description
본 발명은 항-인간 OX40L 항체, 신규 의학 용도 및 방법에 관한 것이다.
OX40 리간드(OX40L)는 TNF 패밀리 구성원; 34 kDa 유형 II 막관통 단백질이다. 인간 OX40 및 OX40L의 결정화된 복합체는 하나의 OX40L 및 3개의 OX40 단량체의 삼량체 구성(삼량체)이다. 인간 세포외 도메인은 마우스 OX40L에 대해서 42% 상동성이다.
OX40L은 본질적으로 발현되지 않고, 프로페셔널(professional) APC, 예컨대 B-세포, 수지상 세포(DC) 및 대식세포 상에 유도될 수 있다. 상이한 세포 유형, 예컨대 랑게르한스 세포, 내피 세포, 평활근 세포, 비만 세포 및 자연 킬러(NK) 세포가 유도되어 OX40L을 발현할 수 있다. T-세포가 또한 OX40L을 발현할 수 있다. OX40L 수용체, OX40은 활성화의 부재 시에도, 활성화된 T-세포(CD4 및 CD8 T-세포, Th2, Th1 및 Th17 세포) 및 CD4+Foxp3+ 세포 상에서 발현된다.
OX40과 OX40L 간의 상호작용은 항원 인식 2일 또는 3일 후에 T-세포-DC 상호작용 동안 일어난다. DC를 떠난 후에, OX40-발현 T-세포는 DC가 아닌 OX40L-발현 세포와 상호작용하여, 이 세포로부터의 OX40 신호를 받아들일 수 있는데, 이것이 기억 T-세포의 생성, Th2 반응의 향상 및 염증 반응의 연장을 위한 본질적인 신호를 제공할 수 있다. 응답기(responder) T-세포로의 OX40 신호는 그것을 Treg 매개된 억제에 대해서 저항성이게 한다.
이식편대숙주병(graft versus host disease)이 동종이형 골수 치료 이후의 사망률의 주요 원인이다. 급성 버전의 질환에서, 골수 이식편 중에 존재하는 성숙 T-세포는 공여자 조직을 손상된 조직의 환경에서 외부 물질로서 인식하는데, 이것은 숙주 APC를 통해서 공여자 T-세포의 활성화 및 증식을 유발하고, 그 다음 T-세포가 간, 비장, 장, 피부 및 폐로 이동하여, CTL 이펙터 반응 및 염증 사이토카인/케모카인 방출에 의해서 조직 손상을 유발한다. 급성 질환의 발병은 통상적으로 이식 후 첫 번째 100일 내에 일어난다(Hill-Ferrara, Blood May 1, 2000 vol. 95 no. 9 2754-275, Reddy-Ferrara Blood, Volume 17, Issue 4, December 2003).
만성 GvHD는 통상적으로 이식 후 100일에 보이며, 병원성 T-세포의 클리어런스(clearance) 감쇠를 유발하는 사전 급성 GvHD에 의해서 유발되는 흉선 손상(Zhang et al, September 1, 2007 vol. 179 no. 5 3305-3314), 섬유증을 유발하는 TGF-β의 하향조절(McCormick et al J Immuno, November 15, 1999 vol. 163 no. 10 5693-5699), 및 상승된 B-세포 활성화 인자(BAFF)에 의해서 유도되는 B-세포 성분(Sarantopoulos et al, Clin Cancer Res October 15, 2007 13; 6107)뿐만 아니라 혈소판 유래된 성장 인자 수용체에 대한 자기-항체(Svegliati et al, Blood July 1, 2007 vol. 110 no. 1 237-241)를 비롯한 몇몇 인자가 포함된다고 생각된다.
임상 연구에서는 OX40이 급성(Morante et al, Clinical and Experimental Immunology, 145:36-43) 및 만성(Kotani et al, Blood November 15, 2001 vol. 98 no. 10 3162-3164) GvHD 모두에서 상향조절된다고 밝혀져 있다. 길항작용적인 항-OX40L은 GvHD의 급성 치사 마우스 모델에서 생존을 향상시켰는데, 43일에 모두 사망한 치료되지 않은 군에 비해서 치료된 군에서는 70%가 생존한 반면(Tsukada et al, Blood, 1 April 2000, Volume 95, Number 7), 효능작용적인 항-OX40 Ab로의 치료는 질환 및 사망률을 가속화하였다(Blazar et al Blood May 1, 2003 vol. 101 no. 9 3741-3748). OX40-OX40L 상호작용의 봉쇄가 몇몇 상이한 염증 질환에서 효능이 있는 것으로 밝혀져 있는데, 항-OX40L Ab는 대장염의 마우스 모델을 치료하는 데 사용되고(Totsuka et al., AJP - GI April 1, 2003 vol. 284 no. 4 G595-G603), 항-OX40L Ab는 NOD 마우스에서 당뇨병의 전개를 차단할 수 있다(Pakala et al European Journal of Immunology Volume 34, Issue 11, pages 3039-3046, November 2004).
Lamb, L.S., Abhyankar, S.A., Hazlett, L., O'Neal, W., Folk, R.S., Vogt, S., Parrish, R.S., Bridges, K., Henslee-Downey, P.J. and Gee, A. P. (1999), Expression of CD134 (0X-40) on T-cells during the first 100 days following allogeneic bone marrow transplantation as a marker for lymphocyte activation and therapy-resistant graft-versus-host disease. Cytometry, 38: 238-243.
Xupeng Ge, Julia Brown, Megan Sykes, Vassiliki A. Boussiotis, CD134-Allodepletion Allows Selective Elimination of Alloreactive Human T-cells without Loss of Virus-Specific and Leukemia-Specific Effectors, Biology of Blood and Marrow Transplantation, Volume 14, Issue 5, May 2008, Pages 518-530.
Naoto Ishii, Takeshi Takahashi, Pejman Soroosh, Kazuo Sugamura, Chapter 3 - OX40-OX40 Ligand Interaction in T-Cell-Mediated Immunity and Immunopathology, In: Frederick W. Alt, Editor(s), Advances in Immunology, Academic Press, 2010, Volume 105, Pages 63-98.
Croft, M., So, T., Duan, W. and Soroosh, P. (2009), The significance of OX40 and OX40L to T-cell biology and immune disease. Immunological Reviews, 229: 173-191.
본 발명은 항-인간 OX40L(hOX40L) 항체 및 단편, 및 인간에서 hOX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한 신규 의학 응용을 제공한다. 이를 위해서, 본 발명은 다음을 제공한다:-
제1 구성
항체 또는 단편이 인간에게 투여되는 방법에서 상기 인간에서 hOX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위해서 hOX40L에 특이적으로 결합하는 항체 또는 이의 단편이되, 여기서 항체 또는 단편은 하기 중 하나, 그 초과 또는 전부를 감소시킴으로써 상기 hOX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한 것인, hOX40L에 특이적으로 결합하는 항체 또는 이의 단편:
a. 인간에서 TNF 알파, IL-2, IL-3, IL-4, IL-5, IL-6, IL-8, IL-9,IL-10, IL-13, IL-17, RANTES 및 인터페론 감마로부터 선택된 사이토카인의 분비;
b. 인간의 백혈구의 증식; 및
c. 인간 T-세포에 의해서 발현된 hOX40 수용체와 내피 세포 발현된 hOX40L의 결합.
제2 구성에서
hOX40L에 특이적으로 결합하고, 상기 hOX40L에 대한 결합을 위해서 02D10, 10A07, 09H04 및 19H01로 이루어진 군으로부터 선택된 항체와 경쟁하는 항체 또는 이의 단편.
제3 구성에서
하기 중 하나, 그 초과 또는 전부를 감소시킴으로써 인간에서 hOX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한, 인간에게 투여하기 위한 의약의 제조에서의 hOX40L에 특이적으로 결합하는 항체 또는 이의 단편의 용도:
a. 인간에서 TNF 알파, IL-2, IL-3, IL-4, IL-5, IL-6, IL-8, IL-9,IL-10, IL-13, IL-17, RANTES 및 인터페론 감마로부터 선택된 사이토카인의 분비;
b. 인간의 백혈구의 증식; 및
c. 인간 T-세포에 의해서 발현된 hOX40 수용체와 내피 세포 발현된 hOX40L의 결합.
제4 구성에서
하기 중 하나, 그 초과 또는 전부를 감소시킴으로써 hOX40L-매개된 질환 또는 병태를 치료 또는 예방하는 방법이되:
a. 인간에서 TNF 알파, IL-2, IL-3, IL-4, IL-5, IL-6, IL-8, IL-9,IL-10, IL-13, IL-17, RANTES 및 인터페론 감마로부터 선택된 사이토카인의 분비;
b. 인간의 백혈구의 증식; 및
c. 인간 T-세포에 의해서 발현된 hOX40 수용체와 내피 세포 발현된 hOX40L의 결합;
여기서 상기 인간에게 치료 유효량의 hOX40L에 특이적으로 결합하는 항체 또는 단편을 투여하는 것을 포함하는, 치료 또는 예방 방법.
제5 구성에서
hOX40L에 특이적으로 결합하고 상기 hOX40L에 대한 결합을 위해서 항체 02D10과 경쟁하는 항체 또는 이의 단편이되, 여기서 항체 또는 단편은 모티프 VRGXYYY를 포함하는 HCDR3을 포함하는 VH 도메인을 포함하고, 여기서 X는 임의의 아미노산인, 항체 또는 이의 단편.
제6 구성에서
hOX40L에 특이적으로 결합하고 상기 hOX40L에 대한 결합을 위해서 항체 02D10과 경쟁하는 항체 또는 이의 단편이되, 여기서 항체 또는 단편은 5개 미만의 아미노산 치환기를 포함하는 서열번호 40 또는 46의 HCDR3 서열 또는 서열번호 40 또는 46의 HCDR3 서열을 포함하는 VH 도메인을 포함하는, 항체 또는 이의 단편.
제7 구성에서
자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택된 자가면역 질환을 치료 또는 예방하기 위한, hOX40L에 특이적으로 결합하는, 16 내지 27개의 아미노산의 HCDR3을 포함하고, 인간 VH 유전자 조각, 인간 D 유전자 조각 및 인간 JH 유전자 조각의 재조합으로부터 유래된 인간 항체 또는 이의 단편이되, 여기서 인간 JH 유전자 조각은 IGHJ6인, 인간 항체 또는 이의 단편.
제8 구성에서
자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택된 인간에서 hOX40L 매개된 질환 또는 병태를 치료 또는 예방하기 위해서 인간에게 투여하기 위한 의약의 제조에서의, hOX40L에 특이적으로 결합하는, 16 내지 27개의 아미노산의 HCDR3을 포함하고, 인간 VH 유전자 조각, 인간 D 유전자 조각 및 인간 JH 유전자 조각의 재조합으로부터 유래된 인간 항체 또는 이의 단편의 용도이되, 여기서 인간 JH 유전자 조각은 IGHJ6인, 인간 항체 또는 이의 단편의 용도.
제9 구성에서
상기 인간에게 치료 유효량의, hOX40L에 특이적으로 결합하는, 16 내지 27개의 아미노산의 HCDR3을 포함하고, 인간 VH 유전자 조각, 인간 D 유전자 조각 및 인간 JH 유전자 조각의 재조합으로부터 유래된 인간 항체 또는 이의 단편을 투여하는 것을 포함하는, 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택된 hOX40L 매개된 질환 또는 병태의 치료 또는 예방 방법이되, 여기서 인간 JH 유전자 조각은 IGHJ6이고, 여기서 이에 의해서 hOX40L 매개된 질환 또는 병태가 치료 또는 예방되는, 치료 또는 예방 방법.
본 발명은 또한 약제학적 조성물, 키트, 핵산, 벡터 및 숙주를 제공한다.
도 1: HTRF 리간드/수용체 중화 검정법에서 완전 인간 재조합 항-OX40L 항체의 프로파일링. 데이터는 3회의 반복 실험을 대표한다.
도 2: 동종이형 PBMC/T 혼합 림프구 반응에서 항-OX40L 항체의 측정 효과. 3개의 공여자 짝지움으로부터의 데이터를 나타내며, 각각의 공여자는 상이한 개체라고 추정된다.
도 3: 동종이형 HCT 이후의 Tscm 세포의 확장. 플롯은 CD4+ CD45RA+CCR7+ T-세포에 대해서 의존적이다.
도 4: OX40L 봉쇄는 동종이형 HCT 이후에 CD4+ T 나이브(naive) 세포를 보존하면서 CD4+ Tscm 세포의 확장을 제어한다. 대조군 동물 및 2D10 IgG4PE 치료된 동물에서 동종이형 HCT 이후의 말초 혈액 CD4+ Tscm(좌측) 및 T나이브(우측)의 절대 수치.
도 5: 동종이형 HCT 이후에 대표 동물에서 나이브 CD4+ T 및 기억 줄기 T-세포 상에서의 OX40 발현. 좌측 및 중앙 FACS 플롯은 CD3+CD4+CD45RA+CCR7+에 대해서 의존성이었다. 우측 히스토그램은 CD4+ T-세포의 상이한 T-세포 하위세트: 나이브(CD45RA+CCR7+CD95-), 기억 줄기(SCM: CD45RA+CCR7+CD95+), 중앙 기억(CM: CD45RA-CCR7+), 이펙터 기억(EM: CD45RA-CCR7-) 및 최종 분화 이펙터-기억 세포 재-발현 CD45RA(TEMRA: CD45RA+CCR7-)에서의 OX40 발현을 나타낸다.
도 6a: SCM CD4+ T-세포 상에서의 OX40L 봉쇄의 효과. 02D10 Ig4PE에 대한 데이터 포인트는 원으로 표시되어 있고, 라파마이신에 대한 데이터 포인트는 채워진 사각형으로 표시되어 있고, 타크롤리무스와 메토트렉세이트(Tac/MTX)에 대한 데이터 포인트는 빈 사각형으로 표시되어 있다.
도 6a: SCM CD8+ T-세포 상에서의 OX40L 봉쇄의 효과. 02D10 Ig4PE에 대한 데이터 포인트는 원으로 표시되어 있고, 라파마이신에 대한 데이터 포인트는 채워진 사각형으로 표시되어 있고, Tac/MTX에 대한 데이터 포인트는 채워지지 않은 사각형으로 표시되어 있다.
도 7: 동종 반-형제(half-sibling) 공여자의 말초 혈액으로부터 유래된 조혈 줄기 세포 이식의 레서스(rhesus) 원숭이 수용자에 대한 카플란-마이어(Kaplan-Meier) 생존 곡선. 결과는, 이식 후 예방 치료 요법이 제공되지 않은 동물(치료받지 않은 대조군; 중간 생존 시간, MST= 8일; n=4), 및 라파마이신 단일 요법을 제공받은 것(MST= 17일; n=4), 2D10 단일 요법을 제공받은 것(MST= 19일; n=4) 또는 라파마이신과 2D10을 제공받은 것(MST >82일; n=3)에 대한 것을 보여준다. 도면에 나타내어진 동물 2 및 3은 드래프팅(drafting) 시기에서 시험 중이었음을 주목하기 바라며: 각각 이식 후 82일 또는 41일 모두에서 GVHD의 징후를 나타내지 않았다. 치료되지 않은 대조군 및 라파마이신 단일 요법 군에 대한 별표*는 문헌[Furlan et al., 2015, Science Translational Medicine, vol 7(315), 315ra191]로부터 취한 데이터이다.
도 2: 동종이형 PBMC/T 혼합 림프구 반응에서 항-OX40L 항체의 측정 효과. 3개의 공여자 짝지움으로부터의 데이터를 나타내며, 각각의 공여자는 상이한 개체라고 추정된다.
도 3: 동종이형 HCT 이후의 Tscm 세포의 확장. 플롯은 CD4+ CD45RA+CCR7+ T-세포에 대해서 의존적이다.
도 4: OX40L 봉쇄는 동종이형 HCT 이후에 CD4+ T 나이브(naive) 세포를 보존하면서 CD4+ Tscm 세포의 확장을 제어한다. 대조군 동물 및 2D10 IgG4PE 치료된 동물에서 동종이형 HCT 이후의 말초 혈액 CD4+ Tscm(좌측) 및 T나이브(우측)의 절대 수치.
도 5: 동종이형 HCT 이후에 대표 동물에서 나이브 CD4+ T 및 기억 줄기 T-세포 상에서의 OX40 발현. 좌측 및 중앙 FACS 플롯은 CD3+CD4+CD45RA+CCR7+에 대해서 의존성이었다. 우측 히스토그램은 CD4+ T-세포의 상이한 T-세포 하위세트: 나이브(CD45RA+CCR7+CD95-), 기억 줄기(SCM: CD45RA+CCR7+CD95+), 중앙 기억(CM: CD45RA-CCR7+), 이펙터 기억(EM: CD45RA-CCR7-) 및 최종 분화 이펙터-기억 세포 재-발현 CD45RA(TEMRA: CD45RA+CCR7-)에서의 OX40 발현을 나타낸다.
도 6a: SCM CD4+ T-세포 상에서의 OX40L 봉쇄의 효과. 02D10 Ig4PE에 대한 데이터 포인트는 원으로 표시되어 있고, 라파마이신에 대한 데이터 포인트는 채워진 사각형으로 표시되어 있고, 타크롤리무스와 메토트렉세이트(Tac/MTX)에 대한 데이터 포인트는 빈 사각형으로 표시되어 있다.
도 6a: SCM CD8+ T-세포 상에서의 OX40L 봉쇄의 효과. 02D10 Ig4PE에 대한 데이터 포인트는 원으로 표시되어 있고, 라파마이신에 대한 데이터 포인트는 채워진 사각형으로 표시되어 있고, Tac/MTX에 대한 데이터 포인트는 채워지지 않은 사각형으로 표시되어 있다.
도 7: 동종 반-형제(half-sibling) 공여자의 말초 혈액으로부터 유래된 조혈 줄기 세포 이식의 레서스(rhesus) 원숭이 수용자에 대한 카플란-마이어(Kaplan-Meier) 생존 곡선. 결과는, 이식 후 예방 치료 요법이 제공되지 않은 동물(치료받지 않은 대조군; 중간 생존 시간, MST= 8일; n=4), 및 라파마이신 단일 요법을 제공받은 것(MST= 17일; n=4), 2D10 단일 요법을 제공받은 것(MST= 19일; n=4) 또는 라파마이신과 2D10을 제공받은 것(MST >82일; n=3)에 대한 것을 보여준다. 도면에 나타내어진 동물 2 및 3은 드래프팅(drafting) 시기에서 시험 중이었음을 주목하기 바라며: 각각 이식 후 82일 또는 41일 모두에서 GVHD의 징후를 나타내지 않았다. 치료되지 않은 대조군 및 라파마이신 단일 요법 군에 대한 별표*는 문헌[Furlan et al., 2015, Science Translational Medicine, vol 7(315), 315ra191]로부터 취한 데이터이다.
본 발명은 하기 양상 1 내지 양상 113을 제공한다.
본 발명은 예를 들어, 이식 거부, 예를 들어, 이식편대숙주병(GvHD) 또는 동종이형 이식 거부의 치료 또는 예방에 유용하다. 본 발명은 또한 예를 들어, 염증성 장 질환, 예를 들어 UC 또는 CD의 치료 또는 예방에 유용하거나, 또는 기도 염증 질환 또는 병태의 치료 또는 예방에 유용하다. 예에서 이러한 양상은 천식의 치료 또는 예방에 유용하다. 본 발명은 또한 예를 들어, 섬유증의 치료 또는 예방에 유용하다. 본 발명은 또한 예를 들어, 당뇨병의 치료 또는 예방에 유용하다. 본 발명은 또한 예를 들어, 포도막염의 치료 또는 예방에 유용하다. 본 발명은 또한 예를 들어, 괴저성 농피증의 치료 또는 예방에 유용하다. 본 발명은 또한 예를 들어, 거대 세포성 동맥염의 치료 또는 예방에 유용하다. 본 발명은 또한 예를 들어, 슈니츨러 증후군(Schnitzler syndrome)의 치료 또는 예방에 유용하다. 본 발명은 또한 예를 들어, 비-감염성 공막염의 치료 또는 예방에 유용하다.
1. 항체 또는 단편이 인간에게 투여되는 방법에서 상기 인간에서 hOX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위해서 hOX40L에 특이적으로 결합하는 항체 또는 이의 단편이되, 여기서 항체 또는 단편은 하기 중 하나, 그 초과 또는 전부를 감소시킴으로써 상기 hOX40L을 치료 또는 예방하기 위한 것인, 항체 또는 이의 단편:
a. 인간에서 TNF 알파, IL-2, IL-3, IL-4, IL-5, IL-6, IL-8, IL-9,IL-10, IL-13, IL-17, RANTES 및 인터페론 감마로부터 선택된 사이토카인의 분비;
b. 인간의 백혈구의 증식; 및
c. 인간 T-세포에 의해서 발현된 hOX40 수용체와 내피 세포 발현된 hOX40L의 결합.
따라서, 본 발명자들은 인간에서 OX40L-매개된 질환 및 병태를 치료 및/또는 예방하는 방식으로서 (a), (b) 및 (c)를 감소시키는 것을 처음으로 발견하였고, 본 발명자들은 이러한 목적을 위해서 항체 및 항체 단편을 제공한다.
예에서, 분비는 백혈구 분비이다. 예에서, (a)는 인간 혈액, 혈장 또는 혈청에서 사이토카인(들)의 상당히 증가된 수준에 의해서 나타내어진다.
예에서, 사이토카인은 (i) TNF 알파, (ii) IL-2 및 (iii) 인터페론 감마로부터 선택된다. 예에서, 사이토카인은 TNF 알파이다. 예에서, 사이토카인은 IL-2이다. 예에서, 사이토카인은 인터페론 감마이다. 예에서, 사이토카인은 (i)과 (ii); 또는 (i)과 (iii); 또는 (ii)와 (iii); 또는 (i) 내지 (iii)이다.
예에서, (a), (b) 또는 (c)의 감소 또는 본 명세서에 개시된 임의의 다른 감소는 hOX40L-매개된 질환 또는 병태의 위험이 있거나 또는 그것으로부터 고통을 받는 인간에서의 수준에 비해서 적어도 10 또는 20%의 감소이다. 예에서, 후자는 항체 또는 단편의 투여 이전에 양상 1에서 언급된 인간이고; 상이한 예에서 후자 인간은 상이한 인간이다. 예에서, 상기 감소는 적어도 10, 20, 30, 40, 50 또는 60%이다.
(i) 예에서, 항체 또는 단편은 시험관내 검정법(하기에 추가로 설명된 바와 같음)에서 백혈구(예를 들어, 인간 T-세포)로부터 관련된 사이토카인의 분비의 감소를 달성할 수 있고, 따라서 인간에게 그러한 항체 또는 단편의 투여는 (a)의 감소로 이어진다.
(ii) 예에서, 항체 또는 단편은 시험관내 검정법(하기에 추가로 설명된 바와 같음)에서 백혈구(예를 들어, 인간 PBMC 및/또는 인간 T-세포)의 증식의 감소를 달성할 수 있고, 따라서 인간에게 그러한 항체 또는 단편의 투여는 (b)의 감소로 이어진다.
(iii) 예에서, 항체 또는 단편은 시험관내 검정법(하기에 추가로 설명된 바와 같음)에서 인간 T-세포에 의해서 발현된 hOX40 수용체와 내피 세포 발현된 hOX40L의 결합의 감소를 달성할 수 있고, 따라서 인간에게 그러한 항체 또는 단편의 투여는 (C)의 감소로 이어진다.
예에서, (i)과 (ii); 또는 (i)과 (iii); 또는 (ii)과 (iii); 또는 (i) 내지 (iii)이 적용한다.
추가로 또는 대안적으로, 상기 감소의 평가는 치료된 인간으로부터의 샘플을 사용하여 수행될 수 있다. 예를 들어, 문헌[J. Clin. Immunol., 2004 Jan, 24(1):74-85; "Increased expression of CCL20 in human inflammatory bowel disease"; Kaser A et al.]을 참고한다. 이러한 공개물은 생체내에서 항체로 치료된 후 조직 생체검사를 사용하여, 사이토카인 분비를 감소시키는 것을 나타내는 감소된 사이토카인 수준을 판독하는 일반적으로-적용 가능한 기술의 예를 제공한다. 유사한 방법을 사용하여 본 발명의 항체가 제공된 인간에서 하나 이상의 사이토카인의 분비의 감소를 측정할 수 있다. 통상의 기술자는 예를 들어, 조직 생체검사, 조직 생체검사, 면역조직화학법, 면역형광법, 조직 염색법, 사이토카인 mRNA 정량화(예를 들어, PCR, 예컨대 타크만(Taqman)(상표명) PCR 사용), 사이토카인 단백질 검출법 및 정량화(예를 들어, 예컨대 ELISA에 의한 사이토카인-특이적인 툴(tool) 항체 및 정량화, 또는 또 다른 표준 단백질 정량화 기술) 중 하나 이상을 사용함으로써 환자 또는 환자 샘플에서 사이토카인 수준을 평가하기 위한 기술에 친숙할 것이다. 예를 들어, 질환 또는 병태가 GI관(예를 들어, IBD) 중 하나에 존재하는 경우, 본 발명의 항체가 제공된 환자로부터의 관련된 장 조직의 생체검사를 수행하고, 그 후에 사이토카인 mRNA 및/또는 사이토카인 단백질(예를 들어, 정량 PCR 사용)의 정량화를 수행할 수 있다. 그 결과를, 항체 투여 전의 동일한 환자로부터의 생체검사된 관련된 조직 중의 사이토카인 정량화와 비교하거나, 또는 동일한 질환 또는 병태로부터 고통을 받지만 질환 또는 병태를 위해서 항-OX40L 치료가 제공되지 않거나 어떠한 치료도 제공되지 않은 동일한 질환 또는 병태로부터 고통을 받는 또 다른 인간 환자와 비교할 수 있다. 이러한 방식으로, 통상의 기술자는 본 발명의 항체가 인간 수용자에서 사이토카인의 분비를 감소시키는지를 결정할 수 있다. 장 조직 수준을 평가하는 것 대신에, 질환 또는 병태의 본성 및 위치에 따라서 인간 환자로부터의 상이한 조직 또는 샘플을 대신 사용할 수 있다. 예를 들어, 질환 또는 병태가 기도(예를 들어, 폐) 중 하나에 존재하는 경우, 사이토카인 평가를 위해서 폐 또는 상이한 기도 조직 샘플을 취할 수 있다. 대안적으로는, 통상의 기술자에게 자명할 바와 같이, 기관지 폐포 세척(Bronchoalveolar lavage: BAL) 샘플을 사용할 수 있다. 또 다른 예에서, 일부 질환 또는 병태의 경우, 본 발명의 항체가 제공된 인간으로부터 취한 혈액, 혈청 또는 혈장 샘플 중의 사이토카인의 감소를 평가하고, 그 다음 상기에 논의된 바와 같이, 항체가 제공되기 전의 수준을 비교하거나 또는 치료되지 않은 인간에서의 수준을 비교할 수 있다.
관련 기술에서 논의된 바와 같이, 용어 "백혈구"는 예를 들어, 림프구, 다형핵 백혈구 및 단핵구 중 하나 이상을 포함한다. 또한 통상의 기술자에게 자명한 바와 같이, 용어 "단핵구"는 예를 들어, 말초 혈액 단핵 세포(PBMC) 또는 단핵구 유래 세포, 예를 들어, 수지상 세포(DC)를 포함한다. 예를 들어, 문헌[Immunobiology, 2013 Nov, 218(11):1392-401. doi: 10.1016/j.imbio.2013.07.005. Epub 2013 Jul 25; "Leukoreduction system chambers are an efficient, valid, and economic source of functional monocyte-derived dendritic cells and lymphocytes", Pfeiffer IA et al.]을 참고하기 바란다.
백혈구, 예를 들어, 프로프리아층 림프구(LPL)의 증식은 통상의 기술자에게 자명할 바와 같이 조직 생체검사, 염색, 및 조직학을 사용하여 평가될 수 있다. 헤마톡실린 및 에오신 스테인(stain)(H&E 스테인 또는 HE 스테인)이 예를 들어, 전체 범위의 인간 조직에서 침윤성 림프구를 찾기 위해서 조직학에서 일반적으로 사용되며, 그것은 조직학에서 주요 스테인 중 하나이다. 그것은 의학 진단에서 가장 널리 사용되는 스테인이고, 흔히 금 표준(gold standard)이고, 그와 같이 본 발명에 따라서 백혈구의 증식을 평가하는 데 사용될 수 있다. 예를 들어, hOX40L-매개된 질환 또는 병태로부터 고통을 받거나 그것의 위험이 있는 인간으로부터의 GI관 조직(예를 들어, 장 조직)을 얻고, 착색시키고, LPL의 침윤 정도를 평가할 수 있다. 항체를 투여하기 전의 동일한 인간 또는 치료가 제공되지 않고 질환 또는 병태의 위험이 있거나 그것으로부터 고통을 받는 또 다른 인간으로부터 얻어진 조직에서의 침윤 정도와 비교하여 본 발명의 항체가 제공된 인간으로부터의 그러한 조직을 비교할 수 있다. 예를 들어, 비교는 IBD로부터 고통을 받는 동일한(또는 상이한)인간으로부터 취한 인간 장 조직들 간의 비교이다.
예를 들어, ELISA 또는 SPR을 사용하여 통상의 기술자에게 친숙한 표준 결합 검정법을 사용하여 항체 또는 단편이 인간 T-세포에 의해서 발현된 hOX40 수용체와 내피 세포 발현된 hOX40L의 결합을 감소시킬 수 있는지를 결정할 수 있다.
염증성 장 질환(IBD)은 명백하게 계속 증가하는 발생률로 위장관에 영향을 미치는 만성 염증 장애이고, 보다 중증의 임상 표현형인 경향이 있다. 그러한 질환은 내강 세균총(flora)에 대한 과장된 면역 반응을 특징으로 하는데, 이는 장내 세균총의 장벽 기능의 결핍이 포함될 수 있다는 것을 제안하고, 이러한 개념을 연구들이 지지한다([Cucchiara et al., 2012; Jostins et al., 2012; Manichanh et al., 2012]; [Salzman et al., 2007, all cited in Deuring et al., "The cell biology of the intestinal epithelium and its relation to inflammatory bowel disease], [The International Journal of Biochemistry & Cell Biology 45 (2013) 798-806]). IBD는 2개의 주요 군을 포함한다: 크론병(CD) 및 궤양성 대장염(UC). CD 환자는 그의 전체 위장관에서 염증 병변을 가질 수 있는 반면, UC 환자에서의 염증은 결장에 제한된다. 또한 히사마추(Hisamatsu) 등의 문헌("Immune aspects of the pathogenesis of inflammatory bowel disease", Pharmacology & Therapeutics 137 (2013) 283-297) 및 그 문헌에 인용된 문헌을 참고한다.
육아종 형성은 인간 크론병의 가장 중요한 병리학적 특징 중 하나이다. 미조구치(Mizoguchi) 등은 F4/80-양성 미성숙 CD11c+ 수지상 세포(DC)가 IL-23을 생성하고, 뮤린 대장염 모델에서 육아종 형성에 기여한다는 것을 보여주었다(Mizoguchi et al., 2007). Th1 면역 반응은 크론병에서 우세하다. 사실, 크론병의 LP에서 CD4+ T-세포는 T-bet를 발현하였고, 다량의 인터페론(IFN)-γ를 생성하였다(Matsuoka et al., 2004). 사쿠라바(Sakuraba) 등은 크론병을 갖는 환자의 창자간막 림프절에서 DC가 Th1 및 Th17 면역 반응을 강하게 촉진시켰다는 것을 보여주었다(Sakuraba et al., 2009). 창자간막 림프절 DC는 IBD 병인, 특히 크론병의 IBD 병인에 기여한다.
질환 및
병태에서의
사이토카인의 역할
문헌[Muzes et al, World J Gastroenterol 2012 November 7; 18(41): 5848-5861ISSN 1007-9327 (인쇄판) ISSN 2219-2840 (온라인판), "Changes of the cytokine profile in inflammatory bowel Diseases"]을 참고한다.
사이토카인은 정상 장 항상성을 유지시키기 위한 점막-관련 면역계의 필수적인 신호이다. 염증 개시를 지지하는 그의 프로파일의 불균형이 예컨대 염증성 장 질환(IBD)에서 관찰되는 질환 상태, 예를 들어, 크론병(CD) 및 궤양성 대장염(UC)으로 이어질 수 있다. IBD에서 염증전(pro-inflammation) 사이토카인, 예컨대 IL-1α, IL-1β, IL-2, -6, -8, -12, -17, -23, IFN-감마, 또는 TNF 알파의 역할은 UC 및 CD의 발병 및 진행과 연관된다. CD는 종종 T-헬퍼(Th) 1-매개된 질환의 원형(prototype)으로서 기술되는데, 그 이유는 1차 염증 매개체가 Th1 사이토카인, 예컨대 인터류킨(IL)-12, 인터페론(IFN)-γ, 및 종양 괴사 인자(TNF)-α이기 때문이다.
TNF-유사 리간드의 그의 수용체에 대한 결합은 세포 증식, 분화, 및 생존에 직접 포함된 세포내 경로를 촉발한다. TNF/TNF-수용체 단백질 슈퍼패밀리의 대부분의 구성원은 면역 세포 상에서 발현되고, 면역 반응의 다중 성분에서 중요한 역할을 한다. TNF-α는 IBD의 병인에서 마스터 사이토카인이다. 그것은 부착 분자, 섬유 모세포 증식, 응혈 촉진성 인자의 발현, 뿐만 아니라 세포독성, 세포사멸 및 급성기 반응의 개시를 통해서 그의 다면발현 효과를 행사한다. IBD에서 TNF-α의 공급원은 부분적으로 선천성 면역 세포, 예컨대 대식세포 또는 단핵구, 및 또한 분화된 Th1 세포이다. TNF-α의 혈청 수준은 UC 및 CD[31]의 임상 활성과 상관관계가 있다. 그것은 IBD에서의 결장성 염증에서 조정 역할을 한다. CD에서 TNF-α의 역할이 폭넓게 연구되었다. 혈청 용해성 TNF 수용체 1 및 2(sTNFR1 및 2)에 TNF-α을 결합시키는 것은 염증전 신호전달을 개시한다. sTNFR1 및 2의 수준은 CD에서 상승된다.
종양 괴사 인자-유사 인자(TL1A), TNF 패밀리의 또 다른 구성원은 사멸 수용체 3(DR3)에 대한 결합에 의해서 IFN-γ 분비를 자극한다. DR3은 UC 및 CD의 점막 생체검사로부터의 높은 백분율의 세포에 의해서 발현되고, IFN-γ의 증가는 IBD 환자에서 질환 활성으로 관찰되었다. TL1A/DR3 시스템은 CD의 병인에 포함된다. 프로프리아층의 대식세포는 TL1A의 주 생산자인데, 발현이 CD에서 상당히 향상된다. TL1A 및 IL-23은 점막 T-세포에 의한 IFN-γ의 생성은 상승작용적으로 촉진시키는 것을 발견하였다. FN-Y:는 TH1 T-세포에 의해서 생성된다. 염증이 개시되면, IFN-γ가 생성되고, 그 다음 면역계의 다양한 분자 및 경로를 통해서 작용하여 염증 과정을 강화시킨다. IFN-γ가 염증 및 자가면역 질환에서 주된 염증전 사이토카인이라는 주류 견해로 이어지는 IFN-γ의 염증전 본성을 광범위하게 서술하는 강력한 문헌이 존재한다. 인터페론-감마는 마우스에서 실험적인 염증성 장 질환에 원인으로 포함된다(Ito et al, Clinical and Experimental Immunology (2006), 146:330-338). 그러한 연구는 IFN-γ-/- 마우스가 DSS로의 자극 이후에 약화된 대장염(체중 감소 정도, DAI, 조직학적 점수 및 MPO 활성 측면에서)을 나타내었다는 것을 명백하게 예증하였다. IFN-γ는 중증의 IBD-유사 증상을 나타낸 DSS-치료된 WT 마우스의 결장에서 증가하게 생성되었다.
인터류킨-2(IL-2)은 T-세포에 의해서 생성되고, T-세포가 이펙터 T-세포로 분화하는 데 가장 중요하다. IL-2는 또한 T-세포 증식에 중요하다. 이것은 IBD에 대해서 중요한데, 그 이유는 이펙터 T-세포가 IBD에서 위험을 유발하기 위한 중요한 세포 유형이라고 생각되기 때문이다.
IL-8(인터류킨-8; aka CXCL8)은 호중구의 활성화 및 호중구의 말초 혈액으로부터의 조직으로의 이동 및 염증 부위로의 이동을 주로 매개한다. IL-8의 조직 수준은 정상 결장 조직에 비교할 때 활성 UC에서 더 높다는 것이 발견되었고, 그의 혈청 농도는 UC에서 내시경적 중증도 및 조직학적 중증도에 연관되었다. IL-8은 염증 설정 및 암에 대해서 중요하다(예를 들어, 문헌[The Chemokine CXCL8 in Carcinogenesis and Drug Response", ISRN Oncol. 2013 Oct 9;2013:859154; Gales D et al.] 및 [Future Oncol., 2010 Jan;6(1):111-6. doi: 10.2217/fon.09.128; "CXCL8 and its cognate receptors in melanoma progression and metastasis", Singh S et al.] 참고). 특히 암에서, IL-8이 또한 혈관신생을 지지함으로써 기여한다고 생각된다.
본 명세서에서 임의의 구성, 양상, 개념 또는 실시예에서, 항체 또는 단편은 OX40 수용체에 대한 hOX40L의 결합에 길항작용한다.
본 명세서에서 임의의 구성, 양상, 개념 또는 실시예에서, 항체 또는 단편은 OX40에 대한 hOX40L의 결합에 길항작용한다.
본 명세서에서 임의의 구성, 양상, 개념 또는 실시예에서, OX40L 수용체는 인간 OX40일 수 있다.
본 명세서에서 임의의 구성, 양상, 개념 또는 실시예에서, 인간은 천식으로부터 고통을 받거나 그것의 위험이 있고, 항체 또는 단편은 인간에서 IgE를 감소시킨다.
본 명세서에서 임의의 구성, 양상, 개념 또는 실시예에서, 인간은 천식으로부터 고통을 받거나 그것의 위험이 있고, 항체 또는 단편은 인간에서 IgE를 감소시키기 위함이다.
2. 양상 1의 항체 또는 단편으로서, 항체 또는 단편은 인간 T-세포에 의해서 발현된 hOX40 수용체와 내피 세포 발현된 hOX40L의 결합을 감소시키고, 인간 T-세포의 증식을 감소시키고; 항체 또는 단편은 TNF 알파, IL-2, IL-3, IL-4, IL-5, IL-6, IL-8, IL-9,IL-10, IL-13, IL-17, RANTES 및 인터페론 감마로부터 선택된 사이토카인의 분비를 감소시킴으로써, 상기 hOX40L-매개된 질환 또는 병태의 치료 또는 예방하기 위함인, 항체 또는 단편.
예에서, 사이토카인은 (i) TNF 알파, (ii) IL-2 및 (iii) 인터페론 감마로부터 선택된다. 예에서, 사이토카인은 TNF 알파이다. 예에서, 사이토카인은 IL-2이다. 예에서, 사이토카인은 인터페론 감마이다. 예에서, 사이토카인은 (i)과 (ii); 또는 (i)과 (iii); 또는 (ii)와 (iii); 또는 (i) 내지 (iii)이다.
3. 양상 1의 항체 또는 단편으로서, 백혈구는 다형핵 백혈구, 단핵구, 말초 혈액 단핵 세포(PBMC), 림프구, T-세포, 항원 제시 세포(APC), 수지상 세포(DC 세포) 및 자연 킬러 세포(NK 세포)로 이루어진 군으로부터 선택되는, 항체 또는 단편.
일 실시형태에서, 백혈구는 말초 혈액 단핵 세포(PBMC) 및 T-세포(예를 들어, PBMC)이다.
4. 양상 3의 항체 또는 단편으로서, 백혈구는 프로프리아층 림프구(LPL)를 포함하고, 질환 또는 병태는 위장관(GI관)의 질환 또는 병태인, 항체 또는 단편.
5. 임의의 상기 양상의 항체 또는 단편으로서, 상피 세포는 위장 세포, 결장 세포, 장 세포 및 기도(예를 들어, 폐) 상피 세포로 이루어진 군으로부터 선택된 세포를 포함하는, 항체 또는 단편.
또 다른 실시형태에서, 상피 세포는 위장 세포, 결장 세포, 장 세포, 눈 세포 및 기도(예를 들어, 폐) 상피 세포로 이루어진 군으로부터 선택된 세포를 포함한다. 또 다른 실시형태에서, 상피 세포는 위장 세포, 결장 세포, 장 세포 및 눈 세포로 이루어진 군으로부터 선택된 세포를 포함한다. 추가 실시형태에서, 상피 세포는 눈 세포를 포함한다.
6. 상기 인간에서 T-세포의 증식을 감소시킴으로써 상기 인간에서 상기 hOX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한, 임의의 상기 양상의 항체 또는 단편.
예에서, 항체 또는 단편은 시험관내 검정법에서(예를 들어, 인간 DC 세포/T-세포 시험관내 검정법에서, 예를 들어 하기에 추가로 설명된 바와 같음) T-세포의 증식의 감소를 달성할 수 있고, 따라서 그러한 항체 또는 단편을 인간에게 투여하는 것은 상기 인간에서 T-세포의 증식의 감소로 이어진다.
7. 인간의 hOX40L과 백혈구 간의 상호작용을 길항작용함으로써 상기 인간에서 상기 hOX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한, 임의의 상기 양상의 항체 또는 단편으로서, 백혈구의 증식이 감소되는, 항체 또는 단편.
예에서, 항체 또는 단편은 시험관내 검정법에서(예를 들어, MLR 시험관내 검정법에서, 예를 들어 하기에 추가로 설명된 바와 같음) 백혈구(예를 들어, 단핵 세포)의 증식의 감소를 달성할 수 있고, 따라서 그러한 항체 또는 단편을 인간에게 투여하는 것은 상기 인간에서 백혈구의 증식의 감소로 이어진다.
8. 상기 인간에서 T-세포에 의해서 매개되는 OX40L/OX40L 수용체를 길항작용함으로써 인간의 백혈구의 증식을 감소시킴으로써 상기 인간에서 상기 hOX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한, 임의의 상기 양상의 항체 또는 단편.
예에서, 항체 또는 단편은 시험관내 검정법에서 백혈구(예를 들어, 단핵 세포)의 증식의 감소를 달성할 수 있고, 여기서 항체 또는 단편은 상기 검정법에서 T-세포에 의해서 매개된 OX40L/OX40L 수용체 상호작용을 길항작용하고, 따라서 그러한 항체 또는 단편을 인간에게 투여하는 것은 상기 인간에서 백혈구의 증식의 감소로 이어진다.
9. 인간에서 TNF 알파, IL-2 및 인터페론 감마로부터 선택된 사이토카인의 분비를 감소시킴으로써 상기 인간에서 상기 hOX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한, 임의의 상기 양상의 항체 또는 단편.
예에서, 항체 또는 단편은 인간에서 (i) IL-2 및 인터페론 감마, (ii) IL-2 및 TNF 알파 또는 (iii) 인터페론 감마 및 TNF 알파의 분비를 감소시킴으로써 상기 인간에서 상기 hOX40L-매개된 질환, 병태 또는 상피 세포 손상을 치료 또는 예방하기 위함이다.
예에서, 항체 또는 단편은 시험관내 검정법에서(예를 들어, MLR 시험관내 검정법에서, 예를 들어 하기에 추가로 설명된 바와 같음), IL-2, TNF 알파 및 인터페론 감마로부터 선택된 사이토카인의 분비의 감소를 달성하고, 따라서 그러한 항체 또는 단편을 인간에게 투여하는 것을 상기 인간에서 상기 선택된 사이토카인(들)의 분비의 감소로 이어진다.
예에서, 항체 또는 단편은 시험관내 검정법(예를 들어, MLR 시험관내 검정법에서, 예를 들어 하기에 추가로 설명된 바와 같음)에서 IL-8의 분비의 감소를 달성할 수 있고, 따라서 인간에게 그러한 항체 또는 단편을 투여하는 것은 상기 인간에서 IL-8의 분비의 감소로 이어진다.
10. 인간에서 수지상 세포(DC 세포)와 T-세포의 상호작용에 의해서 매개된 상기 사이토카인의 분비를 감소시킴으로써 상기 질환 또는 병태를 치료 또는 예방하기 위한, 양상 9의 항체 또는 단편.
예에서, 항체 또는 단편은 DC 세포/T-세포 시험관내 검정법(예를 들어 하기에 추가로 설명된 바와 같음)에서 상기 사이토카인(들) 분비의 감소를 달성할 수 있고, 따라서 인간에게 그러한 항체 또는 단편을 투여하는 것은 상기 인간에서 상기 사이토카인(들)의 분비의 감소로 이어진다.
11. 임의의 상기 양상의 항체 또는 단편으로서, 위장 세포, 결장 세포, 장 세포 또는 기도(예를 들어, 폐) 세포 손상은 인간에서 상기 질환 또는 병태의 증상 또는 원인인, 항체 또는 단편.
또 다른 실시형태에서, 상피 세포는 위장 세포, 결장 세포, 장 세포, 눈 세포 및 기도(예를 들어, 폐) 상피 세포로 이루어진 군으로부터 선택된 세포를 포함한다. 또 다른 실시형태에서, 상피 세포는 위장 세포, 결장 세포, 장 세포 및 눈 세포로 이루어진 군으로부터 선택된 세포를 포함한다. 추가 실시형태에서, 상피 세포는 눈 세포를 포함한다.
12. 임의의 상기 양상의 항체 또는 단편으로서, 인간은 염증성 장 질환(IBD), 동종이형 이식 거부, 이식편대숙주병(GvHD), 당뇨병 또는 기도 염증으로부터 고통을 받거나 그것의 위험이 있고, 상기 방법은 인간에서 IBD, 동종이형 이식 거부, GvHD, 당뇨병 또는 기도 염증을 치료 또는 예방하는, 항체 또는 단편.
12a. 임의의 상기 양상의 항체 또는 단편으로서, 인간은 염증성 장 질환(IBD), 동종이형 이식 거부, 이식편대숙주병(GvHD), 포도막염, 괴저성 농피증, 거대 세포성 동맥염, 슈니츨러 증후군, 비-감염성 공막염, 당뇨병 또는 기도 염증으로부터 고통을 받거나 그것의 위험이 있고, 상기 방법은 인간에서 IBD, 동종이형 이식 거부, GvHD, 포도막염, 괴저성 농피증, 거대 세포성 동맥염, 슈니츨러 증후군, 비-감염성 공막염, 당뇨병 또는 기도 염증을 치료 또는 예방하는, 항체 또는 단편.
임의의 상기 양상의 예에서, 인간은 염증 또는 자가면역 질환 또는 병태로부터 고통을 받거나 그것의 위험이 있거나, 그와 같이 진단된다.
예에서, 자가면역 질환 또는 병태는 하기로부터 선택된다:-
급성 파종성 뇌척수염(Acute disseminated encephalomyelitis: ADEM)
에디슨병(Addison's disease)
알레르기성 육아종증 및 혈관염 또는 척-스트라우스 증후군(Churg-Strauss syndrome: CSS)
탈모증 또는 원형 탈모증(AA)
강직성 척수염
자가면역 만성 활동 간염(CAH)
자가면역 용혈성 빈혈
자가면역 췌장염(AIP)
자가면역 망막증(AR), 망막증 참고
자가면역 혈소판감소성 자반증
자가면역 백혈구 감소증
자가면역 내이 질환(AIED)
항인지질 증후군(APS)
자가면역 림프세포증식 증후군(ALPS)
베체트 증후군(Behcet's syndrome)
수포성 유천포창(Bullus pemphigoid)
셀리악병
척-스트라우스 증후군(CSS) 또는 알레르기성 육아종증 혈관염
어린이의 만성 수포성 질환
만성 염증 탈수초성 다발신경병증(CIDP)
씨크리티칼 유천포창(Cictricial pemphigoid: CP)
중추 신경계 혈관염
크론병
한랭글로불린혈증
포진형 피부염(DH)
원반상 홍반성 난창(DLE)
뇌척수염
후천성 표피 수포증(EBA)
거대 세포성 동맥염, 측두 동맥염 참고
이식편대숙주병
그레이브즈병(Graves' diease)
길랑-바레 증후군(Gullain-Barre syndrome)
하노트 증후군(Hanot Syndrome), 원발성 담즙성 간경화증 참고
자가면역 갑상선염 및 만성 림프구성 갑상선염라고도 불리는 하시모토병(Hashimoto's thyroiditis)
과민성 혈관염(HV) 또는 작은 혈관염
면역-매개된 불임
염증성 장 질환
인슐린-의존성 진성 당뇨병
중추 신경계의 고립성 혈관염 또는 CNS 혈관염
이삭 증후군(Isaacs' Syndrome): 신경근긴장증
가와사키병(Kawasaki diease: KD)
람베르트-이튼 근무력 증후군(Lambert-Eaton myasthenic syndrome: LEMS)
선상 IgA 질환
루프스 - 전신 홍반 루푸스 참고
메니에르병(Meniere's diease)
현미경적 다발혈관염(MPA)
혼합 결합 조직병 또는 MCTD
단클론 감마병증
중증 근무력증
다발성 경화증
다초점 운동 신경병증
신경근긴장증 또는 이삭 증후군
백혈구 감소증, 자가면역 백혈구 감소증 참고
난소염
안구간대경련-근간대경련 증후군
고환염
방종양성 신경 장애
심창성 천포창
펨피거스 폴라세우스(Pemphigus follaceus: PF)
유천포창 포진(PG)
악성 빈혈
종양수반성 천포창(PNP)
다발혈관염 - 현미경적 다발혈관염 참고
결절설 다발동맥염(PAN)
다발성근염/피부근염
류마티스성 다발근통
하노트 증후근(Hanot Syndrome)이라고도 지칭되는 원발성 담즙성 간경화증(PBC)
원발 경화성 담관염(PSC)
레이노 증후군(Raynaud's phenomenon)
레코베린-연관 망막증(Recoverin-associated retinopathy: RAR), 망막증 참고
라이터 증후군(Reiter's syndrome)이라 이미 알려진 반응성 관절염
망막증
류마티스 관절염(RA)
사르코이드증
경화성 담관염, 원발 경화성 담관염 참고
쇼그렌 증후군(Sjogren's syndrome)
전신 괴사성 맥관염(systemic necrotizing vascolitides)
강직 증후군(Stiff man syndrome) 또는 머셔-울트만 증후군(Moersch-Woltmann syndrome)
전신 홍반 루푸스
전신 경화증(경피증)
측두 동맥염 또는 거대 세포성 동맥염(GCV)
타카야수 동맥염(Takayasu's arteritis)
폐색성 혈전 혈관염 또는 버거씨병(Buerger's disease)
갑상선 기능 저하증을 동반한 갑상선염
갑상선 기능 항진증을 동반한 갑상선염
유형 I 자가면역 다분비성 증후군(PAS)
유형 II 자가면역 다분비성 증후군
혈관염
베게너 육아종증
임의의 양상, 구성, 개념 또는 실시형태의 예에서, 인간은 포도막염으로부터 고통을 받는다. 예를 들어, 포도막염은 본래 비-감염성 및/또는 자가면역성이고, 즉, 비-감염성 포도막염이거나, 자가면역성 포도막염이다. 예를 들어, 비-감염성/자가면역성 포도막염은 베체트병, 푸크스 이색성홍체 모양체염(Fuchs heterochromic iridocyclitis), 다발혈관염을 동반한 육아종증, HLA-B27 관련 포도막염, 소아 특발성 관절염, 사르코이드증, 척추관절염, 교감성 안염, 요세관간질 신장염 또는 포도막염 증후군에 의해서 유발되고/되거나 그와 연관된다. 예에서, 포도막염은 본래 전신성이고, 즉, 전신성 포도막염이다. 예를 들어, 전신성 포도막염은 강직성 척추염, 베체트병, 만성 육아종성 질환, 착부염, 염증성 장 질환, 소아 류마티스 관절염, 가와사키병, 다발성 경화증, 결절설 다발동맥염, 건선 관절염, 반응성 관절염, 사르코이드증, 전신 홍반 루푸스, 보그트-코야나기-하라다 증후군(Vogt-Koyanagi-Harada syndrome) 또는 휘플병(Whipple's disease)에 의해서 유발되고/되거나 그와 연관된다.
임의의 양상, 구성, 개념 또는 실시형태의 예에서, 인간은 괴저성 농피증, 거대 세포성 동맥염, 슈니츨러 증후군 또는 비-감염성 공막염으로부터 고통을 받는다. 예에서, 인간은 괴저성 농피증으로부터 고통을 받는다. 예에서, 인간은 거대 세포성 동맥염으로부터 고통을 받는다. 예에서, 인간은 슈니츨러 증후군으로부터 고통을 받는다. 예에서, 인간은 비-감염성 공막염으로부터 고통을 받는다.
임의의 양상, 구성, 개념 또는 실시형태의 예에서, 인간은 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택된 ahOX40L 매개된 질환 또는 병태; 예를 들어 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염,접촉 과민증, 다발성 경화증 및 죽상동맥경화증, 특히 GvHD로부터 고통을 받는다. 또 다른 실시형태에서, 인간은 다장기 기관 이식 거부로부터 고통을 받거나 그것으로부터의 위험이 있다.
13. hOX40L에 특이적으로 결합하고 상기 hOX40L에 대한 결합을 위해서 02D10, 10A07, 09H04 및 19H01로 이루어진 군으로부터 선택된 항체와 경쟁하는, 항체 또는 이의 단편.
임의의 양상, 구성, 개념 또는 실시형태의 예에서, 경쟁은 표면 플라즈몬 공명(SPR)에 의해서 측정되고, 그러한 기술은 통상의 기술자에게 보통 자명하다. SPR은 비아코어(Biacore)(상표명), 프로테온(Proteon)(상표명) 또는 또 다른 표준 SPR 기술을 사용하여 수행될 수 있다. 그러한 경쟁은 예를 들어, 동일하거나 중첩된 hOX40L의 에피토프에 대한 항체/단편 결합으로 인한 것일 수 있다. 임의의 양상, 구성, 개념 또는 실시형태의 예에서, 경쟁은 ELISA에 의해서 측정되고, 그러한 기술은 통상의 기술자에게 보통 자명하다. 임의의 양상, 구성, 개념 또는 실시형태의 예에서, 경쟁은 균일 시간 분해 형광(homogenous time resolved fluorescence: HTRF)에 의해서 측정되고, 그러한 기술은 통상의 기술자에게 보통 자명하다. 임의의 양상, 구성, 개념 또는 실시형태의 예에서, 경쟁은 형광 활성화 세포 분류(fluorescence activated cell sorting: FACS)에 의해서 측정되고, 그러한 기술은 통상의 기술자에게 보통 자명하다. 일 양상에서, HTRF, ELISA 및/또는 FACS 방법은 본 명세서 하기의 실시예에 기술된 바와 같이 수행된다.
14. 양상 13의 항체 또는 단편으로서, 항체 또는 단편은 양상 1 내지 12 중 임의의 것에 따른, 항체 또는 단편.
15. 람다 경쇄 가변 도메인(임의로는 인간임)을 포함하는, 임의의 상기 양상의 항체 또는 단편.
본 발명의 임의의 양상, 구성, 개념 또는 실시형태의 예에서, 항체 또는 단편의 가변 도메인은 인간이거나 또는 인간화된다. 추가로, 임의로 항체 또는 단편은 인간 또는 인간화 불변 영역(예를 들어, 인간 Fc 및/또는 인간 CL)을 추가로 포함한다. 본 발명의 임의의 양상의 예에서, 항체 또는 단편의 가변 도메인은 형질전환 동물(예를 들어, 설치류, 마우스, 래트, 토끼, 닭, 양, 낙타 또는 상어)에 의해서 생성된다. 본 발명의 임의의 양상의 예에서, 항체 또는 단편의 가변 도메인은 파지 전시법, 리보솜 전시법 또는 효모 전시법에 의해서 생성되거나 또는 식별된다.
본 발명의 임의의 양상, 구성, 개념 또는 실시형태의 예에서, 항체 또는 단편은 재조합성이다.
본 발명의 임의의 양상, 구성, 개념 또는 실시형태의 예에서, 항체 또는 단편은 재조합 포유동물, 박테리아, 곤충, 식물 또는 효모 세포에 의해서 생성된다. 예에서, 포유동물 세포는 CHO 또는 HEK293 세포이고, 항체 또는 단편은 CHO 또는 HEK293 세포 글리코실화를 포함한다.
본 발명의 임의의 양상, 구성, 개념 또는 실시형태의 예에서, 항체 또는 단편은 단리된다.
16. 하기의 HCDR1로 이루어진 군으로부터 선택된 HCDR1 서열을 포함하는 VH 도메인을 포함하는 임의의 상기 양상의 항체 또는 단편:
a. 02D10(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 02D10과 경쟁함);
b. 10A07(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 10A07과 경쟁함);
c. 09H04(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 09H04와 경쟁함); 및
d. 19H01(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 19H01와 경쟁함).
17.
하기의 HCDR2로 이루어진 군으로부터 선택된 HCDR2 서열을 포함하는 VH 도메인을 포함하는 임의의 상기 양상의 항체 또는 단편:
a. 02D10(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 02D10과 경쟁함);
b. 10A07(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 10A07과 경쟁함);
c. 09H04(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 09H04와 경쟁함); 및
d. 19H01(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 19H01과 경쟁함).
18. 하기의 HCDR3으로 이루어진 군으로부터 선택된 HCDR3 서열을 포함하는 VH 도메인을 포함하는 임의의 상기 양상의 항체 또는 단편:
a. 02D10(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 02D10과 경쟁함);
b. 10A07(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 10A07과 경쟁함);
c. 09H04(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 09H04와 경쟁함); 및
d. 19H01(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 19H01과 경쟁함).
19. a. 양상 16 내지 18의 (a)에 언급되거나(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 02D10과 경쟁함);
b. 양상 16 내지 18의 (b)에 언급되거나(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 10A07과 경쟁함);
c. 양상 16 내지 18의 (c)에 언급되거나(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 09H04와 경쟁함);
d. 양상 16 내지 18의 (d)에 언급된(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 19H01과 경쟁함)
(i) CDR1 및 CDR2, (ii) CDR1 및 CDR3, (iii) CDR2 및 CDR3 또는 (iv) CDR1, CDR2 및 CDR3 서열을 포함하는 VH 도메인을 포함하는 임의의 상기 양상의 항체 또는 단편.
20. 서열 목록의 VH 아미노산 서열로 이루어진 군으로부터 선택된 아미노산 서열을 포함하는 VH 도메인을 포함하는 임의의 상기 양상의 항체 또는 단편.
양상에서, 본 발명은 서열 목록의 VH 아미노산 서열로 이루어진 군으로부터 선택된 아미노산을 포함하는 VH 도메인을 포함하는 항-hOX40L 항체 또는 단편(본 명세서에 언급된 임의의 다른 양상을 임의로 따름)을 제공한다. 양상에서, VH 도메인은 서열번호 2, 서열번호 34, 서열번호 66, 서열번호 94, 서열번호 122, 서열번호 124, 서열번호 126, 서열번호 128, 서열번호 132 또는 서열번호 134로부터 선택된 아미노산 서열을 포함한다.
본 발명의 또 다른 예에서, 항체 또는 단편은 하기에 열거된 서열로 설정된 VH 도메인 아미노산 서열을 포함한다. 추가로 또는 대안적으로, 항체 또는 단편은 하기 서열 목록(즉, 서열번호 4, 서열번호 10, 서열번호 36, 서열번호 42, 서열번호 68, 서열번호 74, 서열번호 96 또는 서열번호 102, 특히, 서열번호 36 또는 서열번호 42)으로 설정된 HCDR1 도메인 아미노산 서열을 포함한다. 추가로 또는 대안적으로, 항체 또는 단편은 하기 서열 목록(즉, 서열번호 6, 서열번호 12, 서열번호 38, 서열번호 44, 서열번호 70, 서열번호 76, 서열번호 98 또는 서열번호 104, 특히 서열번호 38 또는 서열번호 44)으로 설정된 HCDR2 도메인 아미노산 서열을 포함한다. 추가로 또는 대안적으로, 항체 또는 단편은 하기 서열 목록(즉, 서열번호 8, 서열번호 14, 서열번호 40, 서열번호 46, 서열번호 72, 서열번호 78, 서열번호 100 또는 서열번호 106, 특히 서열번호 40 또는 서열번호 46)으로 설정된 HCDR3 도메인 아미노산 서열을 포함한다.
본 발명의 예에서, 항체 또는 단편은 하기 서열 목록으로 설정된 VL 도메인 아미노산 서열을 포함한다. 추가로 또는 대안적으로, 항체 또는 단편은 하기 서열 목록(즉, 서열번호 18, 서열번호 24, 서열번호 50, 서열번호 56, 서열번호 82, 서열번호 88, 서열번호 110 또는 서열번호 116, 특히 서열번호 50 또는 서열번호 56)으로 설정된 LCDR1 도메인 아미노산 서열을 포함한다. 추가로 또는 대안적으로, 항체 또는 단편은 하기 서열 목록 (즉, 서열번호 20, 서열번호 26, 서열번호 52, 서열번호 58, 서열번호 84, 서열번호 90, 서열번호 112 또는 서열번호 118, 특히 서열번호 52 또는 서열번호 58)으로 설정된 LCDR2 도메인 아미노산 서열을 포함한다. 추가로 또는 대안적으로, 항체 또는 단편은 하기 서열 목록(즉, 서열번호 22, 서열번호 28, 서열번호 54, 서열번호 60, 서열번호 86, 서열번호 92, 서열번호 114 또는 서열번호 120, 특히 서열번호 54 또는 서열번호 60)으로 설정된 LCDR3 도메인 아미노산 서열을 포함한다.
본 명세서에서 임의의 양상의 예에서, 항체 또는 단편은 서열 목록에서 중쇄 불변 영역 서열번호(즉, 서열번호 126, 128, 132, 또는 134 중 임의의 것, 특히 서열번호 128의 불변 영역)로 이루어진 군으로부터 선택된 불변 영역; 및 임의로 양상 19 또는 20에 언급된 바와 같은 VH 도메인을 포함하는 중쇄를 포함한다. 예에서, 항체 또는 단편은 그러한 중쇄의 2개의 복사체를 포함한다. 또 다른 예에서, 중쇄는 설치류, 래트, 마우스, 인간, 토끼, 닭, 낙타, 양, 소, 비-인간 영장류 또는 상어 불변 영역(예를 들어, Fc), 특히 마우스 불변 영역을 포함한다.
본 명세서에서 임의의 양상의 예에서, 항체 또는 단편은 감마(예를 들어, 인간 감마) 불변 영역, 예를 들어, 인간 감마 불변 영역을 포함하는 중쇄를 포함한다. 또 다른 본 명세서에서 임의의 양상의 예에서, 항체 또는 단편은 인간 감마 4 불변 영역을 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 Fc-γ 수용체를 결합하지 않고, 예를 들어, Leu235Glu 돌연변이(즉, 야생형 류신 잔기가 글루탐산 잔기로 돌연변이됨)를 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 안정성을 증가시키기 위해서 Ser228Pro 돌연변이를 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 Leu235Glu 돌연변이 및 Ser228Pro 돌연변이 둘 다를 포함하는 IgG4이다. 이러한 중쇄 불변 영역을 본 명세서에서 "IgG4-PE"라 칭한다.
본 명세서에서 임의의 양상의 예에서, 항체 또는 단편은 키메릭이고, 예를 들어, 그것은 인간 가변 도메인 및 비-인간(예를 들어, 설치류, 마우스 또는 래트, 예컨대 마우스) 불변 영역을 포함한다.
21. 상기 VH 도메인의 제1 복사체 및 제2 복사체를 포함하는, 양상 16 내지 양상 20의 임의의 하나의 항체 또는 단편.
22. 하기의 LCDR1로 이루어진 군으로부터 선택된 LCDR1 서열을 포함하는 VL 도메인을 포함하는 임의의 상기 양상의 항체 또는 단편:
a. 02D10(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 02D10과 경쟁함);
b. 10A07(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 10A07과 경쟁함);
c. 09H04(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 09H04와 경쟁함); 및
d. 19H01(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 19H01과 경쟁함).
23. 하기의 LCDR2로 이루어진 군으로부터 선택된 LCDR2 서열을 포함하는 VL 도메인을 포함하는 임의의 상기 양상의 항체 또는 단편:
a. 02D10(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 02D10과 경쟁함;
b. 10A07(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 10A07과 경쟁함;
c. 09H04(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 09H04와 경쟁함); 및
d. 19H01(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 19H01과 경쟁함.
24. 하기의 LCDR3으로 이루어진 군으로부터 선택된 LCDR3 서열을 포함하는 VL 도메인을 포함하는, 임의의 상기 양상의 항체 또는 단편:
a. 02D10(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 02D10과 경쟁함);
b. 10A07(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 10A07과 경쟁함);
c. 09H04(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 09H04와 경쟁함); 및
d. 19H01(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 19H01과 경쟁함).
25. a. 양상 22 내지 24의 (a)에 언급되거나(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 02D10과 경쟁함);
b. 양상 22 내지 24의 (b)에 언급되거나(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 10A07과 경쟁함);
c. 양상 22 내지 24의 (c)에 언급되거나(여기서 항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 09H04와 경쟁함);
d. 양상 22 내지 24의 (d)에 언급된(항체 또는 단편은 상기 hOX40L에 대한 결합을 위해서 19H01과 경쟁함)
(i) CDR1 및 CDR2, (ii) CDR1 및 CDR3, (iii) CDR2 및 CDR3 또는 (iv) CDR1, CDR2 및 CDR3 서열을 포함하는 VL 도메인을 포함하는 임의의 상기 양상의 항체 또는 단편.
26. 서열 목록의 VL 아미노산 서열로 이루어진 군으로부터 선택된 아미노산 서열을 포함하는 VL 도메인을 포함하는, 임의의 상기 양상의 항체 또는 단편.
본 발명의 양상에서, 서열 목록의 VL 아미노산 서열로 이루어진 군으로부터 선택된 아미노산 서열(즉, 서열번호 16, 서열번호 48, 서열번호 80 또는 서열번호 108, 특히 서열번호 48)을 포함하는 VL 도메인을 포함하는, 항-hOX40L 항체 또는 단편(임의로 본 명세서의 임의의 다른 양상에 따름)이 제공된다.
본 명세서에서 임의의 양상의 예에서, 항체 또는 단편은 서열 목록(즉, 서열번호 136, 서열번호 138, 서열번호 140, 서열번호 142, 서열번호 144, 서열번호 146, 서열번호 148, 서열번호 152, 서열번호 154, 서열번호 156, 서열번호 158, 서열번호 160, 서열번호 162, 서열번호 164 또는 서열번호 166)의 경쇄 불변 영역 서열로 이루어진 군으로부터 선택된 불변 영역; 및 임의로 양상 25 또는 26에 언급된 바와 같은 VL 도메인(예를 들어, 람다 VL)을 포함하는 경쇄(예를 들어, 람다 경쇄)를 포함한다. 예에서, 항체 또는 단편은 그러한 경쇄의 2개의 복사체(임의로 또한 상기에 기술된 중쇄의 2개의 복사체)를 포함한다. 또 다른 예에서, 경쇄는 설치류, 래트, 마우스, 인간, 토끼, 닭, 낙타, 양, 소, 비-인간 영장류 또는 상어 불변 영역을 포함한다.
본 명세서에서 임의의 양상의 예에서, 항체 또는 단편은 서열 목록(즉, 서열번호 136, 서열번호 138, 서열번호 140, 서열번호 142, 서열번호 144, 서열번호 146, 서열번호 148, 서열번호 152, 서열번호 154, 서열번호 156, 서열번호 158, 서열번호 160, 서열번호 162, 서열번호 164 또는 서열번호 166)의 경쇄 불변 영역 서열로 이루어진 군으로부터 선택된 불변 영역; 및 임의로 양상 25 또는 26에서 언급된 바와 같은 VL 도메인(예를 들어, 카파 VL)을 포함하는 경쇄(예를 들어, 카파 경쇄)를 포함한다. 예에서, 항체 또는 단편은 그러한 경쇄의 2개의 복합체(임의로 또한 상기에 기술된 중쇄의 2개의 복사체)를 포함한다. 또 다른 예에서, 경쇄는 설치류, 래트, 마우스, 인간, 토끼, 닭, 낙타, 양, 소, 비-인간 영장류 또는 상어 불변 영역을 포함한다.
예에서, 항체 또는 단편은 서열 목록(즉, 서열번호 146, 서열번호 148, 서열번호 152, 서열번호 154, 서열번호 156, 서열번호 158, 서열번호 160, 서열번호 162, 서열번호 164 또는 서열번호 166)의 경쇄 불변 영역 서열로 이루어진 군으로부터 선택된 불변 영역; 및 임의로 람다 VL 도메인을 포함하는 람다 경쇄를 포함한다.
예에서, 항체 또는 단편은 서열 목록(즉, 즉, 서열번호 136, 서열번호 138, 서열번호 140, 서열번호 142 또는 서열번호 144)의 경쇄 불변 영역 서열로 이루어진 군으로부터 선택된 불변 영역; 및 임의로 카파 VL 도메인을 포함하는 카파 경쇄를 포함한다.
예에서, 항체 또는 단편의 VL 도메인은 람다 경쇄 가변 도메인이다. 예에서, 항체 또는 단편의 VL 도메인은 카파 경쇄 가변 도메인이다.
27. 상기 VL 도메인의 제1 복사체 및 제2 복사체를 포함하는, 양상 22 내지 26 중 임의의 하나의 항체 또는 단편.
28. 임의의 상기 양상의 항체 또는 단편으로서, hOX40L은 예를 들어, 내피 세포(예를 들어, 기도 또는 GI관 내피 세포) 상에서 인간 세포 표면-발현된 hOX40L인, 항체 또는 단편.
또 다른 실시형태에서, 상피 세포는 위장 세포, 결장 세포, 장 세포, 눈 세포 및 기도(예를 들어, 폐) 상피 세포로 이루어진 군으로부터 선택된 세포를 포함한다. 또 다른 실시형태에서, 상피 세포는 위장 세포, 결장 세포, 장 세포 및 눈 세포로 이루어진 군으로부터 선택된 세포를 포함한다. 추가 실시형태에서, 상피 세포는 눈 세포를 포함한다.
29.
임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 시험관내 혼합 림프구 반응(MLR) 검정법에서 hOX40L의 존재 하에서의 인간 PBMC 또는 T-세포의 증식을, hOX40L에 대해서 특이적인 항체의 부재하의 시험관내 대조군 MLR 검정법에서 hOX40L의 존재 하에서의 인간 PBMC 또는 T-세포의 증식에 비해서 적어도 20, 30, 40, 50 또는 60%만큼 감소시키는, 항체 또는 단편. 적합한 검정법의 예가 하기 실시예에 제공되어 있다.
30. 양상 29의 항체 또는 단편으로서, 검정법에서 hOX40L은 인간 수지상 세포(DC 세포) 상에서 표면-발현된, 항체 또는 단편.
적합한 검정법의 예가 하기 실시예에 제공되어 있다.
31. 임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 hOX40L의 존재 하에서 시험관내에서 hOX40 수용체를 발현하는 인간 HT-1080 세포에서 NF-κB 활성을 감소시키는, 항체 또는 단편.
예에서, 항체 또는 단편, NF-κB 활성의 감소는 시험관내에서 (hOX40의 존재 하에서, hOX40 수용체로 임의로 형질주입된) HT-1080 세포(ATCC(등록상표) CCL-121)에 의한 IL-8 분비의 감소를 검출함으로써 측정된다.
32. 임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 시험관내에서 hOX40L의 존재 하에서 hOX40 수용체를 발현하는 인간 HT-1080 세포로부터의 IL-8 분비를 감소시키는, 항체 또는 단편.
33. 양상 32의 항체 또는 단편으로서, 항체 또는 단편은 hOX40L에 대해서 특이적인 항체의 부재 하에서 시험관내에서 hOX40L의 존재 하에서 hOX40 수용체를 발현하는 HT-1080 세포에 의한 IL-8 생성에 비해서 적어도 20, 30, 40, 50 또는 60%만큼 IL-8 분비를 감소시키는, 항체 또는 단편.
34. 임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 시험관내에서 hOX40L-자극된 인간 T-세포 증식을 감소시키는, 항체 또는 단편.
35. 임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 시험관내에서 인간 T-세포로부터의 hOX40L-자극된 IL-2 분비를 감소시키는, 항체 또는 단편.
36. 임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 인간 수지상 세포(DC 세포)와 인간 T-세포의 상호작용에 의해서 매개된 사이토카인 분비를 감소시키고, 사이토카인은 TNF 알파, IL-2, IL-3, IL-4, IL-5, IL-6, IL-8, IL-9,IL-10, IL-13, IL-17, RANTES 및 인터페론 감마 중 1개, 2개, 그 초과 또는 전부로부터 선택된, 항체 또는 단편.
이것은 예를 들어, MLR 시험관내 검정법(예를 들어, DC/T-세포 MLR 시험관내 검정법)을 사용하여 평가될 수 있다. 적합한 검정법의 예가 하기 실시예에 제공되어 있다.
예에서, 예를 들어, DC 세포가 T-세포 인간 공급원과 상이한 인간으로부터의 것인 경우 가능한 바와 같이, DC 세포는 T-세포에 미스매칭되고, 예를 들어, MHC 미스-매칭된다. 예에서, DC 세포는 GMCSF 및 IL-4를 사용한 인간 단핵구의 시험관내 유도에 의해서 생성된다.
37. 임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 hOX40L에 대해서 특이적인 항체의 부재 하에서 인간 수지상 세포(DC 세포)와 인간 T-세포의 상호작용에 의해서 매개된 인터페론 감마의 생성에 비해서 인터페론 감마 분비를 적어도 20, 30, 40, 50 또는 60%만큼 감소시키는, 항체 또는 단편.
38. 임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 hOX40L에 대해서 특이적인 항체의 부재 하에서 인간 수지상 세포(DC 세포)와 인간 T-세포의 상호작용에 의해서 매개된 TNF 알파의 생성에 비해서 TNF 알파 분비를 적어도 20, 30, 40, 50 또는 60%만큼 감소시키는, 항체 또는 단편.
39. 임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 hOX40L에 대해서 특이적인 항체의 부재 하에서 인간 수지상 세포(DC 세포)와 인간 T-세포의 상호작용에 의해서 매개된 IL-2의 생성에 비해서 IL-2 분비를 적어도 10, 20, 30, 40, 50 또는 60%만큼 감소시키는, 항체 또는 단편.
40. 임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 인간 말초 혈액 단핵 세포(PBMC) 혼합 림프구(MLR) 검정법에서 사이토카인 분비(예를 들어, 백혈구 사이토카인 분비)를 감소시키고, 사이토카인은 TNF 알파, IL-2, IL-4, IL-3, IL-6, IL-8, IL-10, IL-17, RANTES 및 인터페론 감마 중 1개, 2개, 그 초과 또는 전부로부터 선택되는, 항체 또는 단편.
41. 임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 인간 PBMC MLR 검정법에서 hOX40L에 대해서 특이적인 항체의 부재 하에서의 인터페론 감마의 생성에 비해서 인터페론 감마 분비를 적어도 20, 30, 40, 50 또는 60%만큼 감소시키는, 항체 또는 단편.
일 실시형태에서, 비교는 인간 PBMC MLR 검정법에서 항체의 부재 하에서의 인터페론 감마의 생성에 대한 것이다.
42. 임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 인간 PBMC MLR 검정법에서 hOX40L에 대해서 특이적인 항체의 부재 하에서의 TNF 알파의 생성에 비해서 TNF 알파 분비를 적어도 20, 30, 40, 50 또는 60%만큼 감소시키는, 항체 또는 단편.
43. 임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 인간 PBMC MLR 검정법에서 hOX40L에 대해서 특이적인 항체의 부재 하에서의 IL-2의 생성에 비해서 IL-2 분비를 적어도 10, 20, 30, 40, 50 또는 60%만큼 감소시키는, 항체 또는 단편.
44. 양상 36 내지 43 중 임의의 하나의 항체 또는 단편으로서, 세포는 1차 세포인, 항체 또는 단편.
"1차 세포"는 시험관내에서 본 발명의 항체 또는 단편에 결합시키기 위해서 환자로부터 취한 인간의 세포 또는 그러한 세포를 나타낸다(예를 들어, 인간에서 OX40L 상태 또는 질환/병태 상태의 진단 방법에서 유용할 수 있는 바와 같음). 본 명세서에서 사용되는 바와 같은 1차 세포는 인간 세포주의 세포가 아니고, 그것은 전형적으로는 시험관내에서 여러번 배양된 것이다. 본 실시형태에서 수용체에 대한 hOX40L 결합을 특이적으로 억제하는 본 발명의 항체 또는 단편의 능력은 이로운데, 그 이유는 그것이 hOX40L-매개된 질환 또는 병태의 고통을 받거나 또는 그것의 위험이 있는 인간 환자에게 세포를 전달하기 위한 직접적인 유용성을 제공하기 때문이다.
45. 임의의 상기 양상의 항체 또는 단편으로서, 항체 또는 단편은 HTRF(균일 시간 분해 형광) 검정법에서 IC50 1x10-8 이하로 hOX40L 수용체(예를 들어, hOX40)에 대한 hOX40L의 결합을 억제하는, 항체 또는 단편.
예에서, IC50는 1x10-8 내지 1x10-11 범위 또는 1x10-9 내지 1x10-10 범위이다.
46. OX40L-매개된 병태 또는 질환을 예방 및/또는 치료하기 위한 약제학적 조성물로서, 조성물은 임의의 상기 양상의 항체 또는 단편 및 희석제, 부형제 또는 담체를 포함하고; 임의로 항-염증 약물을 추가로 포함하는, 약제학적 조성물.
예에서, 항-염증 약물은 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-VLA4항체(예를 들어, 나탈리주맙), 항-LFA1항체, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R항체(예를 들어, 바실릭수맙) 또는 항-TNFa항체/TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙, 세르톨리주맙 페골)로 이루어진 군으로부터 독립적으로 선택된다. 예에서, 항-염증 약물은 코르티코스테로이드(예를 들어, 메틸프레드니솔론) 및 항-LFA1 항체로 이루어진 군으로부터 독립적으로 선택된다.
47. OX40L-매개된 병태 또는 질환을 치료 및/또는 예방하기 위한 약제학적 조성물 또는 키트로서, 조성물 또는 키트는 임의로 인간에서 상기 질환 또는 병태를 치료 및/또는 예방하는 데 사용하기 위한 레이블 또는 지시서와 함께 본 발명의 항체 또는 단편(및 임의로 항-염증 약물)을 포함하고; 임의로 레이블 및 지시서는 마켓팅 인증 번호(marketing authorisation number)(예를 들어, FDA 또는 EMA 인증 번호)를 포함하고; 임의로 키트는 항체 또는 단편을 포함하는 IV 또는 주사 장치를 포함하는, 조성물 또는 키트.
48. 양상 1 내지 45 중 임의의 하나에 언급된 항체의 HCDR3을 코딩하는 핵산.
일 실시형태에서, 본 명세서에서 HCDR은 카바트 명명법(Kabat nomenclature)에 따른다. 또 다른 실시형태에서, 본 명세서에서 HCDR은 IMGT 명명법에 따른다.
49. 서열 목록의 HCDR3 서열과 적어도 80, 85, 90, 95, 96, 97, 98 또는 99% 동일하거나 또는 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 48의 핵산.
양상에서, 본 발명은 항-hOX40L 항체의 VH 도메인을 코딩하는 뉴클레오타이드 서열을 포함하는 핵산을 제공하며, 여기서 뉴클레오타이드 서열은 서열 목록의 HCDR3 서열과 적어도 80, 85, 90, 95, 96, 97, 98 또는 99% 동일하거나 또는 100% 동일한 HCDR3 서열을 포함한다. 임의로, 항체는 본 명세서에서 임의의 다른 양상에 따른다.
또 다른 실시형태에서, 1, 2 또는 3개의 뉴클레오타이드 치환을 제외하고, 서열 목록의 HCDR3 서열과 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 48의 핵산이 제공되고, 여기서 각각의 치환은 상응하는 단백질 서열에서 아미노산 변화를 생성하지 않거나 또는 보존적 아미노산 변화(즉, 뉴클레오타이드 치환은 동의 치환임)를 생성한다. 통상의 기술자는 보존적 아미노산 변화에 친숙할 것이다.
아미노산 치환은 아미노산이 상이한 자연-발생 아미노산 잔기로 치환되는 변경을 포함한다. 그러한 치환은 "보존적"으로서 분류될 수 있고, 이러한 경우 폴리펩타이드 중에 함유된 아미노산 잔기는 극성, 측쇄 관능성 또는 크기와 관련하여 유사한 특징을 갖는 또 다른 자연 발생 아미노산으로 대체된다. 그러한 보존적 치환은 관련 기술 분야에 널리 공지되어 있다. 본 발명에 포함되는 치환은 또한 "비-보존적"일 수 있는데, 여기서는 펩타이드 중에 존재하는 아미노산 잔기가 상이한 특성을 갖는 아미노산, 예컨대 상이한 기를 갖는 자연-발생 아미노산으로 치환되고(예를 들어, 하전되거나 소수성인 아미노산을 알라닌으로 치환함), 또는 대안적으로는, 자연-발생 아미노산이 비-통상적인 아미노산으로 치환된다.
추가로 또는 대안적으로, 1, 2, 3, 4, 5, 6 또는 7개의 동의 뉴클레오타이드 치환 및 상응하는 단백질 서열에서 보존적 아미노산 변화를 생성하는 0, 1, 2 또는 3개의 뉴클레오타이드 치환을 제외하고, 서열 목록의 HCDR3 서열과 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 49의 핵산이 제공된다.
50. 양상 1 내지 45 중 임의의 하나에 언급된 항체의 HCDR2를 코딩하는 핵산으로서, 임의로 핵산은 양상 48 또는 49에 따르는, 핵산.
51. 서열 목록의 HCDR2 서열과 적어도 80, 85, 90, 95, 96, 97, 98 또는 99% 동일하거나 또는 100% 동일한 뉴클레오타이드 서열을 포함하는, 양상 50의 핵산.
양상에서, 본 발명은 항-hOX40L 항체의 VH 도메인을 코딩하는 뉴클레오타이드 서열을 포함하는 핵산을 제공하며, 여기서 뉴클레오타이드 서열은 서열 목록의 HCDR2 서열과 적어도 80, 85, 90, 95, 96, 97, 98 또는 99% 동일하거나 또는 100% 동일한 HCDR2 서열을 포함한다. 임의로, 항체는 본 명세서에서 임의의 다른 양상에 따른다.
또 다른 실시형태에서, 1, 2 또는 3개의 뉴클레오타이드 치환을 제외하고, 서열 목록의 HCDR2 서열과 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 51의 핵산을 제공하고, 여기서 각각의 치환은 상응하는 단백질 서열에서 아미노산 변화를 생성하지 않거나 또는 보존적 아미노산 변화(즉, 뉴클레오타이드 치환은 동의 치환임)를 생성한다. 통상의 기술자는 보존적 아미노산 변화에 친숙할 것이다.
추가로 또는 대안적으로, 1, 2, 3, 4, 5, 6 또는 7개의 동의 뉴클레오타이드 치환 및 상응하는 단백질 서열에서 보존적 아미노산 변화를 생성하는 0, 1, 2 또는 3개의 뉴클레오타이드 치환을 제외하고, 서열 목록의 HCDR2 서열과 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 50의 핵산이 제공된다.
52. 양상 1 내지 45 중 임의의 하나에 언급된 바와 같은 항체의 HCDR1을 코딩하는 핵산으로서, 임의로 핵산은 양상 48 내지 51 중 임의의 하나에 따르는, 핵산.
53. 서열 목록의 HCDR1 서열과 적어도 80, 85, 90, 95, 96, 97, 98 또는 99% 동일하거나 또는 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 52의 핵산.
양상에서, 본 발명은 항-hOX40L 항체의 VH 도메인을 코딩하는 뉴클레오타이드 서열을 포함하는 핵산을 제공하고, 여기서 뉴클레오타이드 서열은 서열 목록의 HCDR1 서열과 적어도 80, 85, 90, 95, 96, 97, 98 또는 99% 동일하거나 또는 100% 동일한 HCDR1 서열을 포함한다. 임의로, 항체는 본 명세서에서 임의의 다른 양상에 따른다.
또 다른 실시형태에서, 1, 2 또는 3개의 뉴클레오타이드 치환을 제외하고, 서열 목록의 HCDR1 서열과 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 52의 핵산이 제공되고, 여기서 각각의 치환은 상응하는 단백질 서열에서 아미노산 변화를 생성하지 않거나 또는 보존적 아미노산 변화(즉, 뉴클레오타이드 치환은 동의 치환임)를 생성한다. 통상의 기술자는 보존적 아미노산 변화에 친숙할 것이다.
추가로 또는 대안적으로, 1, 2, 3, 4, 5, 6 또는 7개의 동의 뉴클레오타이드 치환 및 상응하는 단백질 서열에서 보존적 아미노산 변화를 생성하는 0, 1, 2 또는 3개의 뉴클레오타이드 치환을 제외하고, 서열 목록의 HCDR1 서열과 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 52의 핵산이 제공된다.
54. 양상 1 내지 45의 임의의 하나에 언급된 바와 같은 항체의 VH 도메인 및/또는 VL 도메인을 코딩하는 핵산.
55. 서열 목록의 VH 도메인 뉴클레오타이드 서열과 적어도 80, 85, 90, 95, 96, 97, 98 또는 99% 동일하거나 또는 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 54의 핵산.
또 다른 실시형태에서, 1, 2 또는 3개의 뉴클레오타이드 치환을 제외하고, 서열 목록의 VH 도메인 뉴클레오타이드 서열과 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 54의 핵산이 제공되고, 여기서 각각의 치환은 상응하는 단백질 서열에서 아미노산 변화를 생성하지 않거나 또는 보존적 아미노산 변화(즉, 뉴클레오타이드 치환은 동의 치환임)를 생성한다. 통상의 기술자는 보존적 아미노산 변화에 친숙할 것이다.
추가로 또는 대안적으로, 1, 2, 3, 4, 5, 6 또는 7개의 동의 뉴클레오타이드 치환 및 상응하는 단백질 서열에서 보존적 아미노산 변화를 생성하는 0, 1, 2 또는 3개의 뉴클레오타이드 치환을 제외하고, 서열 목록의 VH 도메인 뉴클레오타이드 서열과 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 54의 핵산이 제공된다.
56. 서열 목록의 VL 도메인 뉴클레오타이드 서열과 적어도 80, 85, 90, 95, 96, 97, 98 또는 99% 동일하거나 또는 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 54 또는 55의 핵산.
또 다른 실시형태에서, 1, 2 또는 3개의 뉴클레오타이드 치환을 제외하고, 서열 목록의 VL 도메인 뉴클레오타이드 서열과 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 54 또는 55의 핵산이 제공되고, 여기서 각각의 치환은 상응하는 단백질 서열에서 아미노산 변화를 생성하지 않거나 또는 보존적 아미노산 변화(즉, 뉴클레오타이드 치환은 동의 치환임)를 생성한다. 통상의 기술자는 보존적 아미노산 변화에 친숙할 것이다.
추가로 또는 대안적으로, 1, 2, 3, 4, 5, 6 또는 7개의 동의 뉴클레오타이드 치환 및 상응하는 단백질 서열에서 보존적 아미노산 변화를 생성하는 0, 1, 2 또는 3개의 뉴클레오타이드 치환을 제외하고, 서열 목록의 VL 도메인 뉴클레오타이드 서열과 100% 동일한 뉴클레오타이드 서열을 포함하는 양상 54 또는 55의 핵산이 제공된다.
57. 양상 1 내지 45 중 임의의 하나에 언급된 바와 같은 항체의 중쇄 또는 경쇄를 코딩하는 핵산.
58. 양상 48 내지 56 중 임의의 하나에 언급된 바와 같은 뉴클레오타이드 서열을 포함하는 양상 57의 핵산.
59. 양상 48 내지 58 중 임의의 하나의 핵산을 포함하는 벡터(예를 들어, 포유동물 발현 벡터)로서; 임의로 벡터는 CHO 또는 HEK293 벡터인, 벡터. 예에서, 벡터는 효모 벡터, 예를 들어, 사카로마이세스(Saccharomyces) 또는 피치아(Pichia) 벡터이다.
60. 양상 48 내지 58 중 임의의 하나의 핵산 또는 양상 59의 벡터를 포함하는 숙주. 예에서, 숙주는 포유동물(예를 들어, 인간, 예를 들어, CHO 또는 HEK293) 세포주 또는 효모 또는 박테리아 세포주이다.
61. 하기 중 하나, 그 초과 또는 전부를 감소시킴으로써 hOX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한, 인간에게 투여하기 위한 의약의 제조에서 hOX40L에 특이적으로 결합하는 항체 또는 이의 단편의 용도:
a. 인간에서 TNF 알파, IL-2, IL-3, IL-4, IL-5, IL-6, IL-8, IL-9,IL-10, IL-13, IL-17, RANTES 및 인터페론 감마로부터 선택된 사이토카인의 분비;
b. 인간의 백혈구의 증식; 및
c. 인간 T-세포에 의해서 발현된 hOX40 수용체와 내피 세포 발현된 hOX40L의 결합.
상기 양상, 구성, 개념, 예 또는 실시형태 중 임의의 것의 특징부가 이러한 용도에 필요한 부분만 약간 수정하여 임의로 적용된다.
예에서, 인간은 천식으로부터 고통을 받거나 그것의 위험이 있고, 항체 또는 단편은 인간에서 IgE를 감소시키기 위함이고, 따라서 인간에서 천식을 치료, 예방 또는 감쇠시킨다.
62. 하기 중 하나, 그 초과 또는 전부를 감소시킴으로써 인간에서 hOX40L-매개된 질환 또는 병태를 치료 또는 예방하는 방법으로서:
a. 인간에서 TNF 알파, IL-2, IL-3, IL-4, IL-5, IL-6, IL-8, IL-9,IL-10, IL-13, IL-17, RANTES 및 인터페론 감마로부터 선택된 사이토카인의 분비;
b. 인간의 백혈구의 증식; 및
c. 인간 T-세포에 의해서 발현된 hOX40 수용체와 내피 세포 발현된 hOX40L의 결합;
방법은 상기 인간에게 치료 유효량의 hOX40L에 특이적으로 결합하는 항체 또는 단편을 투여하는 것을 포함하는, 치료 또는 예방하는 방법.
상기 양상, 예 또는 실시형태 중 임의의 것의 특징부가 이러한 방법에 필요한 부분만 약간 수정하여 임의로 적용된다.
본 발명의 방법은 인간에서 상기 질환 또는 병태를 치료 또는 예방한다. "치료 유효량"의 항체 또는 단편은 상기 치료 또는 예방을 제공하기에 효과적인 양(단회 투여 또는 다회 투여로 투여되고, 이것은 시간 간격이 있을 수 있고, 예를 들어, 실질적으로 매월 투여됨)이다. 이는 통상의 기술자에게 보통 자명할 것이고, 다루는 특정 인간 환자 및 질환 또는 병태에 따라서 달라질 수 있다.
예에서, 인간은 천식으로부터 고통을 받거나 그것의 위험이 있고, 항체 또는 단편은 인간에서 IgE를 감소시키고, 이에 의해서 인간에서 천식을 치료, 예방 또는 감쇠시킨다.
63. 상기 인간에서 T-세포의 증식을 감소시킴으로써 상기 인간에서 상기 hOX40L-매개된 질환, 병태 또는 상피 세포 손상을 치료 또는 예방하기 위한, 양상 61 또는 62의 방법.
64. 인간의 hOX40L과 백혈구 간의 상호작용을 길항작용함으로써 상기 인간에서 상기 hOX40L-매개된 질환, 병태 또는 상피 세포 손상을 치료 또는 예방하기 위한, 양상 61 내지 63 중 임의의 하나의 방법 또는 용도로서, 백혈구의 증식이 감소되는, 방법 또는 용도.
65. 상기 인간에서 T-세포에 의해서 매개된 OX40L/OX40L 수용체 상호작용을 길항작용함으로써 인간의 백혈구의 증식을 감소시킴으로써 상기 인간에서 상기 hOX40L-매개된 질환, 병태 또는 상피 세포 손상을 치료 또는 예방하기 위한, 양상 61 내지 64 중 임의의 하나의 방법 또는 용도.
66. 인간에서 IL-8 사이토카인의 분비를 감소시킴으로써 상기 인간에서 상기 hOX40L-매개된 질환, 병태 또는 상피 세포 손상을 치료 또는 예방하기 위한, 양상 61 내지 65 중 임의의 하나의 방법 또는 용도.
67. 인간에서 수지상 세포(DC 세포)와 T-세포의 상호작용에 의해서 매개된 상기 IL-8의 분비를 감소시킴으로써 상기 질환, 병태 또는 상피 세포 손상을 치료 또는 예방하기 위한, 양상 66의 방법.
68. 양상 61 내지 67의 임의의 하나의 방법 또는 용도로서, 위장 세포, 결장 세포, 장 세포 또는 기도(예를 들어, 폐) 세포 손상이 인간에서 상기 질환 또는 병태의 증상 또는 원인인, 방법 또는 용도.
또 다른 실시형태에서, 상피 세포는 위장 세포, 결장 세포, 장 세포, 눈 세포 및 기도(예를 들어, 폐) 상피 세포로 이루어진 군으로부터 선택된 세포를 포함한다. 또 다른 실시형태에서, 상피 세포는 위장 세포, 결장 세포, 장 세포 및 눈 세포로 이루어진 군으로부터 선택된 세포를 포함한다. 추가 실시형태에서, 상피 세포는 눈 세포를 포함한다.
69. 양상 61 내지 68 중 임의의 하나의 방법 또는 용도로서, 인간은 염증성 장 질환(IBD), 동종이형 이식 거부, 이식편대숙주병(GvHD), 당뇨병 또는 기도 염증으로부터 고통을 받거나 그것의 위험이 있고, 상기 방법은 인간에서 IBD, 동종이형 이식 거부, GvHD, 당뇨병 또는 기도 염증을 치료 또는 예방하는, 방법 또는 용도.
69a. 양상 61 내지 68 중 임의의 하나의 방법 또는 용도로서, 인간은 염증성 장 질환(IBD), 동종이형 이식 거부, 이식편대숙주병(GvHD), 포도막염, 괴저성 농피증, 거대 세포성 동맥염, 슈니츨러 증후군, 비-감염성 공막염, 당뇨병 또는 기도 염증으로부터 고통을 받거나 그것의 위험이 있고, 상기 방법은 인간에서 IBD, 동종이형 이식 거부, GvHD, 포도막염, 괴저성 농피증, 거대 세포성 동맥염, 슈니츨러 증후군, 비-감염성 공막염, 당뇨병 또는 기도 염증을 치료 또는 예방하는, 방법 또는 용도.
임의의 양상, 구성, 개념 또는 실시형태에서, 인간은 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택된 hOX40L-매개된 질환 또는 병태; 예를 들어 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염, 접촉 과민증, 다발성 경화증 및 죽상동맥경화증, 특히 GvHD로부터 고통을 받거나 그것의 위험이 있다.
70. 양상 61 내지 69a 중 임의의 하나의 방법 또는 용도로서, 항체 또는 단편은 양상 1 내지 45 중 임의의 하나 또는 본 명세서 기술된 임의의 예, 구성, 개념, 양상 또는 실시형에 따르는, 방법 또는 용도.
71. 인간에서 염증 또는 자가면역 질환 또는 병태를 치료 또는 예방하거나, 또는 인간에서 혈관신생을 감쇠 또는 예방하기 위한, 임의의 상기 양상의 항체, 단편, 조성물, 키트, 방법 또는 용도.
72. 임의의 상기 양상의 항체, 단편, 조성물, 키트, 방법 또는 용도로서, 질환 또는 병태는 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 건선, 모세기관지염, 치은염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 천식, 성인 호흡 곤란 증후군(ARDS), 패혈성 쇼크, 궤양성 대장염, 쇼그렌 증후군, 기도 염증, 전신 홍반 루푸스(SLE), 당뇨병, 접촉 과민증, 다발성 경화증 및 죽상동맥경화증으로 이루어진 군으로부터 선택된, 항체, 단편, 조성물, 키트, 방법 또는 용도.
72a. 임의의 상기 양상의 항체, 단편, 조성물, 키트, 방법 또는 용도로서, 질환 또는 병태는 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 건선, 모세기관지염, 치은염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 천식, 성인 호흡 곤란 증후군(ARDS), 패혈성 쇼크, 궤양성 대장염, 쇼그렌 증후군, 기도 염증, 전신 홍반 루푸스(SLE), 포도막염, 괴저성 농피증, 거대 세포성 동맥염, 슈니츨러 증후군, 비-감염성 공막염,당뇨병, 접촉 과민증, 다발성 경화증 및 죽상동맥경화증으로 이루어진 군으로부터 선택된, 항체, 단편, 조성물, 키트, 방법 또는 용도.
임의의 양상, 구성, 개념 또는 실시형태에서, 인간은 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택된 hOX40L-매개된 질환 또는 병태; 예를 들어 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염, 접촉 과민증, 다발성 경화증 및 죽상동맥경화증, 특히 GvHD로부터 고통을 받거나 그것의 위험이 있다.
예에서, 질환 또는 병태는 미국 특허 제7812133호 또는 유럽 특허 제1791869호에 개시된 OX40L-매개된 질환 또는 병태이다.
예에서, 질환 또는 병태는 염증 또는 자가면역 질환 또는 병태이다. 예에서, 질환 또는 병태는 이식 거부이다.
본 명세서에서 사용되는 바와 같이, 염증 질환 또는 병태는 염증을 유발하는 병리학적 상태, 예를 들어 호중구 주화성에 의해서 유발되는 병리학적 상태를 나타낸다. 그러한 장애의 예는 건선을 비롯한 염증 피부 질환; 염증성 장 질환(예컨대 크론병 및 궤양성 대장염)과 관련된 반응; 허혈 재관류; 성인 호흡 곤란 증후군; 피부염; 뇌수막염; 뇌염; 포도막염; 자가면역 질환, 예컨대 류마티스 관절염, 쇼그렌 증후군, 혈관염; 백혈구 누출을 포함하는 질환; 중추 신경계(CNS) 염증 장애, 패혈증 또는 외상 이후의 다발성 기관 손상 증후군(multiple organ injury syndrome); 알코올성 간질환, 박테리아 폐렴, 항원-항체 복합체 매개된 질환; 흉막염, 폐포염, 혈관염, 폐렴, 만성 기관지염, 기관지 확장증, 및 낭성 섬유증을 비롯한 폐의 염증 등을 포함한다. 바람직한 적응증은 박테리아 폐렴 및 염증성 장 질환, 예컨대 궤양성 대장염이다. 따라서 본 발명은 예에서 그러한 병태 중 임의의 하나 이상의 치료 또는 예방을 위해서 제공된다.
예에서, 질환 또는 병태는 암이다.
예에서, 질환은 포도막염, 예컨대 전신성 포도막염 또는 자가면역/비-감염성 포도막염이다.
73. hOX40L에 특이적으로 결합하고 상기 hOX40L에 대한 결합을 위해서 항체 02D10과 경쟁하는 항체 또는 이의 단편으로서, 항체 또는 단편은 모티프 VRGXYYY를 포함하는 HCDR3을 포함하는 VH 도메인을 포함하고, X는 임의의 아미노산인, 항체 또는 이의 단편.
본 명세서에 기술된 양상, 구성, 개념, 예 또는 실시형태 중 임의의 것의 항체의 특징부가 이러한 항체에 필요한 부분만 약간 수정하여 임의로 적용되고, 예를 들어, 항체는 본 명세서에서 기술된 바와 같은 기능성 특징부를 갖는 인간 항체 또는 키메릭 항체일 수 있다. 경쟁은 본 명세서에 기술된 임의의 양상, 실시형태, 예, 개념 또는 구성에 기술된 바와 같이, 예를 들어, SPR, ELISA, HTRF 또는 FACS에 의해서 측정되는 바와 같이 측정될 수 있다.
일 실시형태에서, 항체 또는 단편은 02D10의 가변 영역과 경쟁한다(예를 들어, 서열번호 34의 중쇄 가변 영역 및 서열번호 48의 경쇄 가변 영역을 포함하는 항체와 경쟁한다). 또 다른 실시형태에서, 항체 또는 단편은 서열번호 62의 중쇄 아미노산 서열 및 서열번호 64의 경쇄 아미노산 서열을 갖는 02D10 IgG4-PE와 경쟁한다.
또 다른 실시형태에서, 항체 또는 단편은 추가로 또는 대안적으로 10A7과 경쟁한다. 일 실시형태에서, 항체 또는 단편은 10A7의 가변 영역과 경쟁한다(예를 들어, 서열번호 2의 중쇄 가변 영역 및 서열번호 16의 경쇄 가변 영역을 포함하는 항체와 경쟁한다). 또 다른 실시형태에서, 항체 또는 단편은 서열번호 30의 중쇄 아미노산 서열 및 서열번호 32의 경쇄 아미노산 서열을 갖는 02D10 IgG4-PE와 경쟁한다
일 실시형태에서, 아미노산은 임의의 자연-발생 아미노산이다.
74. 양상 73에 따른 항체 또는 단편으로서, X는 중성 아미노산, 임의로 P 또는 G인, 항체 또는 단편.
실시형태에서, X는 P 또는 G이다. 실시형태에서, X는 P, N, A 또는 G로부터 선택된다. 또 다른 실시형태에서, X는 P, G 또는 N으로부터 선택된다. 또 다른 실시형태에서, X는 P, G 또는 A로부터 선택된다.
75. hOX40L에 특이적으로 결합하고 상기 hOX40L에 대한 결합을 위해서 항체 02D10과 경쟁하는 임의로 양상 73 또는 74에 따른 항체 또는 이의 단편으로서, 항체 또는 단편은 서열번호 40 또는 46의 HCDR3 서열 또는 5개 미만의 아미노산 치환을 포함하는 서열번호 40 또는 46의 HCDR3 서열을 포함하는 VH 도메인을 포함하는, 항체 또는 이의 단편.
본 명세서에 기술된 양상, 구성, 개념, 예 또는 실시형태 중 임의의 것의 항체의 특징부가 이러한 항체에 필요한 부분만 약간 수정하여 임의로 적용되고, 예를 들어, 항체는 본 명세서에서 기술된 바와 같은 기능성 특징부를 갖는 인간 항체 또는 키메릭 항체일 수 있다. 경쟁은 예를 들어, SPR, ELISA, HTRF 또는 FACS에 의해서 측정되는 바와 같이, 본 명세서에 기술된 임의의 양상, 실시형태, 개념, 예 또는 구성에서 기술된 바와 같이 측정될 수 있다.
실시형태에서, 서열번호 40 또는 46의 HCDR3 서열은 4개 미만(즉, 3개 이하)의 아미노산 치환을 포함한다. 실시형태에서, 서열번호 40 또는 46의 HCDR3 서열은 3개 미만(즉, 2개 또는 1개의 치환)의 아미노산 치환을 포함한다. 실시형태에서, 서열번호 40 또는 46의 HCDR3 서열은 2개 미만의 아미노산 치환(즉, 1개의 치환)을 포함한다.
일 실시형태에서, 항체 또는 단편은 02D10의 가변 영역과 경쟁한다(예를 들어, 서열번호 34의 중쇄 가변 영역 및 서열번호 48의 경쇄 가변 영역을 포함하는 항체와 경쟁한다). 또 다른 실시형태에서, 항체 또는 단편은 서열번호 62의 중쇄 아미노산 서열 및 서열번호 64의 경쇄 아미노산 서열을 갖는 02D10 IgG4-PE와 경쟁한다
또 다른 실시형태에서, 항체 또는 단편 추가로 또는 대안적으로 10A7과 경쟁한다. 일 실시형태에서, 항체 또는 단편은 10A7의 가변 영역과 경쟁한다(예를 들어, 서열번호 2의 중쇄 가변 영역 및 서열번호 16의 경쇄 가변 영역을 포함하는 항체와 경쟁한다). 또 다른 실시형태에서, 항체 또는 단편은 서열번호 30의 중쇄 아미노산 서열 및 서열번호 32의 경쇄 아미노산 서열을 갖는 02D10 IgG4-PE와 경쟁한다.
76. 양상 73 내지 75 중 임의의 하나에 따른 항체 또는 단편으로서, VH 도메인은 16 내지 27개의 아미노산의 HCDR3을 포함하고, 인간 VH 유전자 조각, 인간 D 유전자 조각 및 인간 JH 유전자 조각으로부터 유래되고, 인간 JH 유전자 조각은 IGHJ6(예를 들어, IGHJ6*02)인, 항체 또는 단편.
실시형태에서, 인간 JH 유전자 조각은 IGHJ6*01, IGHJ6*02, IGHJ6*03 및 HJ6*04로부터 선택된다. 또 다른 실시형태에서, 인간 JH 유전자 조각은 IGHJ6*01, IGHJ6*02 및 IGHJ6*04로부터 선택된다. 또 다른 실시형태에서, JH 유전자 조각은 IGHJ6*02이다.
추가 실시형태에서, 인간 VH 유전자 조각은 IGHV3-23, 예를 들어 IGHV3-23*01, IGHV3-23*02,IGHV3-23*03, IGHV3-23*04 또는 IGHV3-23*05로부터 선택된다. 또 다른 실시형태에서, 인간 VH 유전자 조각은 IGHV3-23*01 또는 IGHV3-23*04, 특히 IGHV3-23*04이다.
추가 실시형태에서, 인간 DH 유전자 조각은 IGHD3-10, 예를 들어 IGHD3-10*01 또는 IGHD3-10*02로부터 선택된다. 일 실시형태에서, 인간 DH 유전자 조각은 IGHD3-10*01이다. 일 실시형태에서, 인간 DH 유전자 조각은 IGHD3-10*02이다.
77. 양상 73 내지 76 중 임의의 하나에 따른 항체 또는 단편으로서, VH 도메인은 서열번호 36 또는 42의 HCDR1 서열 또는 4개 미만의 아미노산 치환을 포함하는 서열번호 36 또는 42의 HCDR1 서열을 포함하는, 항체 또는 단편.
실시형태에서, 서열번호 36 또는 42의 HCDR1 서열은 3개 미만(즉, 2개 또는 1개의 치환)의 아미노산 치환을 포함한다. 실시형태에서, 서열번호 36 또는 42의 HCDR1 서열은 2개 미만의 아미노산 치환(즉, 1개의 치환)을 포함한다.
78. 양상 73 내지 77 중 임의의 하나에 따른 항체 또는 단편으로서, VH 도메인은 서열번호 38 또는 44의 HCDR2 서열, 또는 5개 미만의 아미노산 치환을 포함하는 서열번호 38 또는 44의 HCDR2 서열을 포함하는, 항체 또는 단편.
실시형태에서, 서열번호 38 또는 44의 HCDR2 서열은 4개 미만(즉, 3개 이하)의 아미노산 치환을 포함한다. 실시형태에서, 서열번호 38 또는 44의 HCDR2 서열은 3개 미만(즉, 2개 또는 1개의 치환)의 아미노산 치환을 포함한다. 실시형태에서, 서열번호 38 또는 44의 HCDR2 서열은 2개 미만의 아미노산 치환(즉, 1개의 치환)을 포함한다.
79. 양상 73 내지 78 중 임의의 하나에 따른 항체 또는 단편으로서, VH 도메인은 서열번호 34의 아미노산 서열, 또는 서열번호 34와 적어도 80%(예를 들어, 적어도 85%) 동일한 중쇄 가변 도메인 아미노산 서열을 포함하는, 항체 또는 단편.
실시형태에서, 중쇄 가변 도메인 아미노산 서열은 서열번호 34와 적어도 85%, 적어도 90%, 적어도 95%, 적어도 96% 적어도 97% 적어도 98% 또는 적어도 99% 동일하다.
80. 상기 VH 도메인의 제1 복사체 및 제2 복사체를 포함하는 양상 73 내지 79 중 임의의 하나에 따른 항체 또는 단편.
81. 서열번호 54 또는 60의 LCDR1 서열, 또는 5개 미만의 아미노산 치환을 포함하는 서열번호 54 또는 60의 LCRD3 서열을 포함하는 VL 도메인을 포함하는, 양상 73 내지 80 중 임의의 하나에 따른 항체 또는 단편.
실시형태에서, 서열번호 54 또는 60의 LCRD3 서열은 4개 미만(즉, 3개 이하)의 아미노산 치환을 포함한다. 실시형태에서, 서열번호 54 또는 60의 LCRD3 서열은 3개 미만(즉, 2개 또는 1개의 치환)의 아미노산 치환을 포함한다. 실시형태에서, 서열번호 54 또는 60의 LCRD3 서열은 2개 미만의 아미노산 치환(즉, 1개의 치환)을 포함한다.
82. VL 도메인 또는 상기 VL 도메인을 포함하는 양상 73 내지 81 중 임의의 하나에 따른 항체 또는 단편으로서, VL 도메인은 서열번호 52 또는 58의 LCDR2 서열, 또는 2개 미만의 아미노산 치환을 포함하는 서열번호 52 또는 58의 LCRD2 서열을 포함하는, 항체 또는 단편.
83. VL 도메인 또는 상기 VL 도메인을 포함하는 양상 73 내지 82 중 임의의 하나에 따른 항체 또는 단편으로서, VL 도메인은 서열번호 54 또는 60의 LCDR1 서열, 또는 4개 미만의 아미노산 치환을 포함하는 서열번호 54 또는 60의 LCRD1 서열을 포함하는, 항체 또는 단편.
실시형태에서, 서열번호 54 또는 60의 LCDR1 서열은 3개 미만(즉, 2개 또는 1개의 치환)의 아미노산 치환을 포함한다. 실시형태에서, 서열번호 54 또는 60의 LCDR1 서열은 2개 미만의 아미노산 치환(즉, 1개의 치환)을 포함한다.
84. VL 도메인 또는 상기 VL 도메인을 포함하는 양상 73 내지 83 중 임의의 하나에 따른 항체 또는 단편으로서, VL 도메인은 서열번호 48의 아미노산 서열, 또는 서열번호 48과 적어도 80%(예를 들어, 적어도 85%) 동일한 경쇄 가변 도메인 아미노산 서열을 포함하는, 항체 또는 단편.
실시형태에서, 경쇄 가변 도메인 아미노산 서열은 서열번호 48과 적어도 85%, 적어도 90%, 적어도 95%, 적어도 96%, 적어도 97% 적어도 98% 또는 적어도 99% 동일하다.
85. 상기 VL 도메인의 제1 복사체 및 제2 복사체를 포함하는, 양상 81 내지 84 중 임의의 하나에 따른 항체 또는 단편.
86. 양상 81 내지 85 중 임의의 하나에 따른 항체 또는 단편으로서, 항체 또는 단편은 카파 경쇄를 포함하는, 항체 또는 단편.
또 다른 실시형태에서, VL 도메인은 카파 VL 도메인이다. 실시형태에서, 카파 VL 도메인은 인간 VL 유전자 조각, 및 인간 JL 유전자 조각의 재조합으로부터 유래되고, 인간 VL 유전자 조각은 IGKV1D-39이다. 또 다른 실시형태에서, VL 유전자 조각은 IGKV1D-39*01이다.
추가 실시형태에서, 인간 JL 유전자 조각은 IGKJ1 또는 IGKJ3이다. 또 다른 실시형태에서, JL 유전자 조각은 IGKJ1*01이다. 또 다른 실시형태에서, JL 유전자 조각은 IGKJ3*01이다.
87. 양상 75 내지 86 중 임의의 하나에 따른 항체 또는 단편으로서, 아미노산 치환은 보존적 아미노산 치환이고, 임의로 보존적 치환은 하기로부터 선택된 6개의 군(각각의 군은 서로에 대해서 보존적 치환인 아미노산을 함유함) 중 하나로부터인, 항체 또는 단편:
1) 알라닌(A), 세린(S), 트레오닌(T);
2) 아스파트산(D), 글루탐산(E);
3) 아스파라긴(N), 글루타민(Q);
4) 아르기닌(R), 라이신(K);
5) 아이소류신(I), 류신(L), 메티오닌(M), 발린(V); 및
6) 페닐알라닌(F), 티로신(Y), 트립토판(W)
실시형태에서, 보존적 아미노산 치환은 본 명세서에서 기술된 바와 같다. 예를 들어, 치환은 Y의 F로의 치환, T의 S 또는 K로의 치환, P의 A로의 치환, E의 D 또는 Q로의 치환, N의 D 또는 G로의 치환, R의 K로의 치환, G의 N 또는 A로의 치환, T의 S 또는 K로의 치환, D의 N 또는 E로의 치환, I의 L 또는 V로의 치환, F의 Y로의 치환, S의 T 또는 A로의 치환, R의 K로의 치환, G의 N 또는 A로의 치환, K의 R로의 치환, A의 S, K 또는 P로의 치환일 수 있다. 또 다른 실시형태에서, 보존적 아미노산 치환은, Y가 F로 치환되고, T가 A 또는 S로 치환되고, I가 L 또는 V로 치환되고, W가 Y로 치환되고, M이 L로 치환되고, N이 D로 치환되고, G가 A로 치환되고, T가 A 또는 S로 치환되고, D가 N으로 치환되고, I가 L 또는 V로 치환되고, F가 Y 또는 L로 치환되고, S가 A 또는 T로 치환되고, A가 S, G, T 또는 V로 치환될 수 있다.
88. 양상 73 내지 87 중 임의의 하나에 따른 항체 또는 단편으로서, 항체 또는 단편은 불변 영역, 예를 들어, IgG4 불변 영역을 포함하고, 임의로 불변 영역은 IgG4-PE(서열번호 128)인, 항체 또는 단편.
또 다른 본 명세서에서 임의의 양상의 예에서, 단편의 항체는 인간 감마 4 불변 영역을 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 Fc-γ 수용체를 결합하지 않고, 예를 들어, Leu235Glu 돌연변이(즉, 야생형 류신 잔기가 글루탐산 잔기로 변형된 경우)를 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 안정성을 증가시키기 위해서 Ser228Pro 돌연변이를 포함한다.
89. 양상 73 내지 88 중 임의의 하나에 따른 항체로서, 항체는 중쇄 및 경쇄를 포함하고, 중쇄 아미노산 서열은 서열번호 62의 서열로 이루어지고, 경쇄 아미노산 서열은 서열번호 64의 서열로 이루어진, 항체.
90. 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부; 예를 들어 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염, 접촉 과민증, 다발성 경화증 또는 죽상동맥경화증, 특히 GvHD로부터 선택된 hOX40L-매개된 질환 또는 병태를 치료 또는 예방하는 데 사용하기 위한 양상 73 내지 89, 98, 99, 101 또는 102 중 임의의 하나에 정의된 바와 같은 항체 또는 단편.
본 명세서에 기술된 양상, 구성, 개념, 예 또는 실시형태 중 임의의 것의 항체 및 hOX40L-매개된 질환의 특징부가 이러한 용도에 필요한 부분만 약간 수정하여 임의로 적용된다. 본 명세서에서 임의의 양상, 구성, 개념, 예 또는 실시형태에 기술된 바와 같은 조성물, 투여 스케줄 또는 투여 모드 중 임의의 것이 이러한 용도에 필요한 부분만 약간 수정하여 임의로 적용된다.
91. 인간에서 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식/숙주 거부; 예를 들어 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염, 접촉 과민증, 다발성 경화증 또는 죽상동맥경화증, 특히 GvHD로부터 선택된 hOX40L 매개된 질환 또는 병태를 치료 또는 예방하기 위해서 인간에게 투여하기 위한 의약의 제조에서의, 양상 73 내지 89, 98, 99, 101 또는 102 중 임의의 하나에 정의된 바와 같은 항체 또는 단편의 용도.
본 명세서에 기술된 양상, 구성, 개념, 예 또는 실시형태 중 임의의 것의 항체 및 hOX40L-매개된 질환의 특징부가 이러한 용도에 필요한 부분만 약간 수정하여 임의로 적용된다. 본 명세서에서 임의의 양상, 구성, 개념, 예 또는 실시형태에 기술된 바와 같은 조성물, 투여 스케줄 또는 투여 모드 중 임의의 것이 이러한 용도에 필요한 부분만 약간 수정하여 임의로 적용된다.
92. 인간에게 치료 유효량의 양상 73 내지 89, 98, 99, 101 또는 102 중 임의의 하나에 정의된 바와 같은 항체 또는 단편을 투여하는 것을 포함하는, 인간에서 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택된 hOX40L 매개된 질환 또는 병태; 예를 들어 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염, 접촉 과민증, 다발성 경화증 또는 죽상동맥경화증, 특히 GvHD를 치료 또는 예방하는 방법으로서, 이에 의해서 hOX40L 매개된 질환 또는 병태가 치료 또는 예방되는, 치료 또는 예방하는 방법.
본 명세서에 기술된 양상, 구성, 개념, 예 또는 실시형태 중 임의의 것의 항체 및 hOX40L-매개된 질환의 특징부가 이러한 방법에 필요한 부분만 약간 수정하여 임의로 적용된다. 본 명세서에서 임의의 양상, 구성, 개념, 예 또는 실시형태에 기술된 바와 같은 조성물, 투여 스케줄 또는 투여 모드 중 임의의 것이 이러한 방법에 필요한 부분만 약간 수정하여 임의로 적용된다.
93. 양상 90에 따른 항체 또는 단편, 양상 91에 따른 용도, 또는 양상 92에 따른 방법으로서, hOX40L-매개된 질환 또는 병태가 GvHD인, 항체 또는 단편, 용도, 또는 방법.
또 다른 실시형태에서, 항체 또는 단편은 GvHD를 치료 또는 예방할 수 있다.
94. 항체 또는 단편, 양상 90 내지 93 중 임의의 하나에 따른 용도 또는 방법으로서, 항체는 예방적으로 투여되는, 항체 또는 단편, 용도 또는 방법.
실시형태에서, 예방조치는 질환 또는 병태의 발병 또는 질환 또는 병태의 증상의 발병을 예방한다. 일 실시형태에서, 예방 치료는 질환 또는 병태의 악화 또는 발병을 예방한다. 일 실시형태에서, 예방 치료는 질환 또는 병태의 악화를 예방한다.
또 다른 실시형태에서, 상기 항체는 정맥내로 투여된다. 또 다른 실시형태에서, 상기 항체는 약 5 내지 10mg/kg(예를 들어, 약 8mg/kg)의 용량으로 투여된다. 또 다른 실시형태에서, 상기 항체는 약 0.1mg/kg, 약 0.5mg/kg, 약 1mg/kg, 3mg/kg, 5mg/kg, 약 10mg/kg, 약 15mg/kg, 약 20mg/kg, 약 25mg/kg, 약 30mg/kg, 약 40mg/kg, 약 50mg/kg, 약 60mg/kg, 약 70mg/kg, 약 80mg/kg 약 90mg/kg 또는 약 100mg/kg, 특히 약 1mg/kg, 또는 약 3mg/kg으로부터 선택된 용량으로 투여된다.
또 다른 실시형태에서, 상기 항체는 이식 1 내지 4일 전, 예를 들어, 이식 1 내지 3일 전 또는 이식 1 내지 2일 전에 투여된다. 또 다른 실시형태에서, 상기 항체는 이식 이후에 매주, 격주 또는 매달, 예를 들어, 격주에 투여된다. 추가 실시형태에서, 상기 항체는 이식 1 내지 3일 전에 약 5 내지 10mg/kg(예를 들어, 약 8mg/kg)의 용량으로 예방적으로 정맥내 투여되고, 그 다음 약 5 내지 10mg/kg(예를 들어, 약 8mg/kg)의 용량으로 격주로 정맥내 투여된다.
또 다른 실시형태에서, 환자는 GvHD(예를 들어, 급성 GvHD)의 전개에 대한 예측성 바이오마커의 존재 하에서 이식 이후에 주기적으로 모니터링되고, 바이오마커 수준이 환자가 GvHD(예를 들어, 급성 GvHD) 전개 위험이 있다고 결정되도록 하는 수준이 되면 본 발명의 항-OX40L 항체가 투여된다. 이러한 전략은 약물의 불필요한 투여 및 면역계의 불필요한 억제를 방지할 것이다. 급성 GvHD의 예측성 바이오마커로서 유용할 수 있는 바이오마커의 예는 문헌[Levine et al., "A prognostic score for acute graft-versus-host disease based on biomarkers : a multicentre study", Lancet Haematol 2015; 2:e21-29]에서 식별된 것일 수 있다. 이러한 바이오마커는 TNFR1, ST-2, 엘라핀 및 IL2Rα 및 Reg3α를 포함하지만, 이들로 제한되는 것은 아니다.
95. 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택된 ahOX40L-매개된 질환 또는 병태; 예를 들어 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염, 접촉 과민증, 다발성 경화증 또는 죽상동맥경화증, 특히 GvHD(예를 들어, 항체는 GvHD의 예방을 위해서임)의 치료 또는 예방을 위한 16 내지 27개의 아미노산의 HCDR3을 포함하고, 인간 VH 유전자 조각, 인간 D 유전자 조각 및 인간 JH 유전자 조각의 재조합으로부터 유래된 인간 항체 또는 이의 단편으로서, 인간 JH 유전자 조각은 IGHJ6(예를 들어, IGHJ6*02)이고, hOX40L에 특이적으로 결합하는, 인간 항체 또는 이의 단편.
양상, 구성, 개념, 예 또는 실시형태 중 임의의 것의 항체 및 hOX40L-매개된 질환의 특징부가 이러한 용도에 필요한 부분만 약간 수정하여 임의로 적용된다. 본 명세서에서 임의의 양상, 구성, 개념, 예 또는 실시형태에 기술된 바와 같은 조성물, 투여 스케줄 또는 투여 모드 중 임의의 것이 이러한 용도에 필요한 부분만 약간 수정하여 임의로 적용된다.
96. 인간에서 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택된 hOX40L 매개된 질환 또는 병태; 예를 들어 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염, 접촉 과민증, 다발성 경화증 또는 죽상동맥경화증, 특히 GvHD의 치료 또는 예방을 위해서 인간에게 투여하기 위한 의약의 제조에서의 16 내지 27개의 아미노산의 HCDR3을 포함하고, 인간 VH 유전자 조각, 인간 D 유전자 조각 및 인간 JH 유전자 조각의 재조합으로부터 유래된 인간 항체 또는 이의 단편의 용도로서, 인간 JH 유전자 조각은 IGHJ6(예를 들어, IGHJ6*02)이고, hOX40L에 특이적으로 결합하는, 인간 항체 또는 이의 단편의 용도.
양상, 구성, 개념, 예 또는 실시형태 중 임의의 것의 항체 및 hOX40L-매개된 질환의 특징부가 이러한 용도에 필요한 부분만 약간 수정하여 임의로 적용된다. 본 명세서에서 임의의 양상, 구성, 개념, 예 또는 실시형태에 기술된 바와 같은 조성물, 투여 스케줄 또는 투여 모드 중 임의의 것이 이러한 용도에 필요한 부분만 약간 수정하여 임의로 적용된다.
97. 인간에게 치료 유효량의 16 내지 27개의 아미노산의 HCDR3을 포함하고, 인간 VH 유전자 조각, 인간 D 유전자 조각 및 인간 JH 유전자 조각의 재조합으로부터 유래된 인간 항체 또는 이의 단편을 투여하는 것을 포함하는, 인간에서 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택된 hOX40L 매개된 질환 또는 병태; 예를 들어 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염, 접촉 과민증, 다발성 경화증 또는 죽상동맥경화증, 특히 GvHD를 치료 또는 예방하는 방법으로서, 인간 JH 유전자 조각은 IGHJ6(예를 들어, IGHJ6*02)이고, hOX40L에 특이적으로 결합하고, 이에 의해서 hOX40L 매개된 질환 또는 병태가 치료 또는 예방되는, 치료 또는 예방하는 방법.
양상, 구성, 개념, 예 또는 실시형태 중 임의의 것의 항체 및 hOX40L-매개된 질환의 특징부가 이러한 방법에 필요한 부분만 약간 수정하여 임의로 적용된다. 본 명세서에서 임의의 양상, 구성, 개념, 예 또는 실시형태에 기술된 바와 같은 조성물, 투여 스케줄 또는 투여 모드 중 임의의 것이 이러한 방법에 필요한 부분만 약간 수정하여 임의로 적용된다.
양상 95 내지 97 중 임의의 하나의 실시형태에서, 인간 JH 유전자 조각은 IGHJ6*01, IGHJ6*02, IGHJ6*03 및 IGHJ6*04로부터 선택된다. 양상 95 내지 97 중 임의의 하나의 또 다른 실시형태에서, 인간 JH 유전자 조각은 IGHJ6*01, IGHJ6*02 및 IGHJ6*04로부터 선택된다. 양상 95 내지 97의 임의의 하나의 또 다른 실시형태에서, JH 유전자 조각은 IGHJ6*02이다.
양상 95 내지 97의 임의의 하나의 추가 실시형태에서, 인간 VH 유전자 조각은 IGHV3-23, 예를 들어 IGHV3-23*01, IGHV3-23*02, IGHV3-23*03, IGHV3-23*04 또는 IGHV3-23*05로부터 선택된다. 양상 95 내지 97 중 임의의 하나의 또 다른 실시형태에서 인간 VH 유전자 조각은 IGHV3-23*01 또는 IGHV3-23*04, 특히 IGHV3-23*04이다.
양상 95 내지 97 중 임의의 하나의 추가 실시형태에서, 인간 DH 유전자 조각은 IGHD3-10, 예를 들어 IGHD3-10*01 또는 IGHD3-10*02로부터 선택된다. 양상 95 내지 97 중 임의의 하나의 실시형태에서, 인간 DH 유전자 조각은 IGHD3-10*01이다. 양상 95 내지 97 중 임의의 하나의 실시형태에서, 인간 DH 유전자 조각은 IGHD3-10*02이다.
양상 90 내지 97 중 임의의 하나의 실시형태에서, 항체는 GvHD를 치료 또는 예방할 수 있다. 양상 90 내지 97 중 임의의 하나의 또 다른 실시형태에서, 항체 또는 단편은 GvD가 아닌 질환의 치료 또는 예방을 위해서 사용되지만, 항체 또는 단편은 GvHD를 치료 또는 예방할 수 있다.
98. 양상 86에 따른 항체 또는 단편, 또는 양상 95에 따른 항체 또는 단편, 양상 96에 따른 용도, 또는 양상 97에 따른 방법으로서, 항체 또는 단편은 카파 경쇄를 포함하고, 예를 들어, 경쇄의 VL 도메인은 인간 VL 유전자 조각, 및 인간 JL 유전자 조각의 재조합으로부터 유래되고, 인간 VL 유전자 조각은 IGKV1D-39(예를 들어, IGKV1D-39*01)이고, 임의로 인간 JL 유전자 조각은 IGKJ1(예를 들어, IGKJ1*01) 또는 IGKJ3(예를 들어, IGKJ3*01)인, 항체 또는 단편, 용도, 또는 방법.
또 다른 실시형태에서, VL 도메인은 카파 VL 도메인이다. 실시형태에서, 카파 VL 도메인은 인간 VL 유전자 조각, 및 인간 JL 유전자 조각의 재조합으로부터 유래되고, 인간 VL 유전자 조각은 IGKV1D-39이다. 또 다른 실시형태에서, VL 유전자 조각은 IGKV1D-39*01이다.
추가 실시형태에서, 인간 JL 유전자 조각은 IGKJ1이다. 또 다른 실시형태에서, JL 유전자 조각은 IGKJ1*01이다. 추가 실시형태에서, 인간 JL 유전자 조각은 IGKJ3이다. 또 다른 실시형태에서, JL 유전자 조각은 IGKJ3*01이다.
99. 양상 73 내지 89, 98, 101 또는 102 중 임의의 하나에 따른 항체 또는 단편, 또는 양상 90 내지 98 중 임의의 하나에 따른 항체 또는 단편 용도 또는 방법으로서, 항체 또는 단편은 동종 조혈 줄기 세포 이식의 레서스 마카크 모델에서 12일에 80%를 초과하는 줄기 세포 공여자 키메리즘을 가능하게 하고, 임의로 항체는 GvHD의 예방을 위한 것인, 항체 또는 단편, 항체 또는 단편 용도 또는 방법.
또 다른 양상에서, 양상 95 내지 98 중 임의의 하나에 따른 항체 또는 단편, 용도 또는 방법이 제공되며, 여기서 항체 또는 단편은 공여자 인간 조혈 줄기 세포 이식 이후에 상기 인간에서 12일에 80%를 초과하는 줄기 세포 공여자 키메리즘을 가능하게 함으로써 인간에서 이식 거부(예를 들어, GvHD)를 치료 또는 예방하기 위함이다.
또 다른 실시형태에서, 양상 73 내지 89, 98, 101 또는 102 중 임의의 하나에 따른 항체 또는 단편이 제공되며, 여기서 항체 또는 단편은 동종 조혈 줄기 세포 이식의 레서스 마카크 모델에서 12일에 80%를 초과하는 줄기 세포 공여자 키메리즘을 가능하게 한다.
일 실시형태에서, 키메리즘은 T 세포(CD3+/CD20-) 키메리즘이다. 또 다른 실시형태에서, 키메리즘은 말초 혈액 키메리즘이다. 또 다른 실시형태에서, 키메리즘은 말초 혈액 또는 T 세포(CD3+/CD20-) 키메리즘이다.
일 실시형태에서, 줄기 세포 공여자 키메리즘(예를 들어, 말초 혈액 또는 T 세포(CD3+/CD20-)키메리즘)은 공여자-특이적인 앰플리콘(amplicon)과 수용자-특이적인 앰플리콘의 최대 높이를 비교함으로써, 대립적인 공여자-특이적인 MHC-연결된 미소부수체(microsatellite) 마커 및 수용자-특이적인 MHC-연결된 미소부수체 마커를 사용하여 측정된다. 또 다른 실시형태에서, 줄기 세포 공여자 키메리즘은 문헌[Kean, LS, et al., "Induction of chimerism in rhesus macaques through stem cell transplant and costimulation blockade-based immunosuppression", Am J Transplant. 2007 Feb;7(2):320-35]에 기술된 바와 같이 측정된다. 또 다른 실시형태에서, 줄기 세포 공여자 키메리즘은 실시예 7에 기술된 바와 같이 측정된다.
일 실시형태에서, 동종 조혈 줄기 세포의 레서스 마카크 모델은 항-OX40L 항체가 투여되고, 그 다음 반-형제 공여자 동물로부터 단리된 말초 혈액이 주입되고, 컨디셔닝 절차를 겪은 이식(HSCT) 수용자 동물에 의해서 수행되며, 그 다음에 동물은 1주 용량의 본 발명의 항-OX40L 항체를 계속 제공받으며, 혈액 샘플을 키메리즘을 위해서 취하고 분석한다.
또 다른 실시형태에서, HSCT 모델에서, 수용자 동물에게 본 발명의 항-OX40L 항체를 정맥내 투여하기 전에(-2일, 그 다음에 5일, 12일, 19일, 26일, 33일, 40일, 47일에 정맥내 투여) 숙주 조혈계를 제거하기 위해서 4회 분할 용량으로 2일(실험 -2일 및 -1일)에 걸쳐서 1020 cGy의 컨디셔닝 방사선 용량을 제공하며, 연속적인 지지 치료를 제공하면서 수용자의 면역계를 재구성하기 위해서 MHC 하프-매치트(반-형제) 공여자 동물로부터 백혈구- 및 줄기 세포-풍부 말초 혈액을 이식하며, GVHD의 징후를 위해서 혈액을 샘플링하고, 모니터링한다.
일 실시형태에서, 항체 또는 단편, 용도 또는 방법은 GvHD의 예방을 위함이다.
실시형태에서, 본 발명의 항-hOX40L 항체는 예방적으로 투여된다. 일 실시형태에서, 예방 치료는 질환 또는 병태의 악화 또는 발병을 예방한다.
또 다른 실시형태에서, 상기 항체는 정맥내로 투여된다. 또 다른 실시형태에서, 상기 항체는 약 5 내지 10mg/kg(예를 들어, 약 8mg/kg)의 용량으로 투여된다. 또 다른 실시형태에서, 상기 항체는 정맥내로 투여된다. 또 다른 실시형태에서, 상기 항체는 약 5 내지 10mg/kg(예를 들어, 약 8mg/kg)의 용량으로 투여된다. 또 다른 실시형태에서, 상기 항체는 약 0.1mg/kg, 약 0.5mg/kg, 약 1mg/kg, 3mg/kg, 5mg/kg, 약 10mg/kg, 약 15mg/kg, 약 20mg/kg, 약 25mg/kg, 약 30mg/kg, 약 40mg/kg, 약 50mg/kg, 약 60mg/kg, 약 70mg/kg, 약 80mg/kg 약 90mg/kg 또는 약 100mg/kg, 특히 약 1mg/kg, 또는 약 3mg/kg으로부터 선택된 용량으로 투여된다.
또 다른 실시형태에서, 상기 항체는 이식 전 1 내지 4일, 예를 들어, 이식 전 1 내지 3일 또는 이식 전 1 내지 2일에 투여된다. 또 다른 실시형태에서, 상기 항체는 이식 이후에 매주, 격주 또는 매달, 예를 들어, 격주에 투여된다. 추가 실시형태에서, 상기 항체는 이식 1 내지 3일 전에 약 5 내지 10mg/kg(예를 들어, 약 8mg/kg)의 용량으로 예방적으로 정맥내 투여되고, 그 다음 약 5 내지 10mg/kg(예를 들어, 약 8mg/kg)의 용량으로 격주로 정맥내 투여된다.
또 다른 실시형태에서, 환자는 GvHD(예를 들어, 급성 GvHD)의 전개에 대한 예측성 바이오마커의 존재 하에서 이식 이후에 주기적으로 모니터링되고, 바이오마커 수준이 환자가 GvHD(예를 들어, 급성 GvHD) 전개 위험이 있다고 결정되도록 하는 수준이 되면 본 발명의 항-OX40L 항체가 투여된다. 이러한 전략은 약물의 불필요한 투여 및 면역계의 불필요한 억제를 방지할 것이다. 급성 GvHD의 예측성 바이오마커로서 유용할 수 있는 바이오마커의 예는 문헌[Levine et al., "A prognostic score for acute graft-versus-host disease based on biomarkers : a multicentre study", Lancet Haematol 2015; 2:e21-29]에서 식별된 것일 수 있다. 이러한 바이오마커는 TNFR1, ST-2, 엘라핀 및 IL2Rα 및 Reg3α를 포함하지만, 이들로 제한되는 것은 아니다.
추가 실시형태에서, HSCT 모델은 문헌[Miller, Weston P., et al. "GVHD after haploidentical transplantation: a novel, MHC-defined rhesus macaque model identifies CD28 - CD8 + T cells as a reservoir of breakthrough T-cell proliferation during costimulation blockade and sirolimus-based immunosuppression." Blood, 116, 24(2010):5403-5418]에 기술된 바와 같이 수행된다. 추가 실시형태에서, HSCT 모델은 실시예 7에 기술된 바와 같이 수행된다.
100. 양상 95 내지 99 중 임의의 하나에 따른 항체 또는 단편, 용도 또는 방법으로서, 항체는 양상 73 내지 89, 98, 99, 101 또는 102 중 임의의 하나에 정의된 바와 같은, 항체 또는 단편, 용도 또는 방법.
101. 양상 73 내지 89, 98, 99 또는 102 중 임의의 하나에 따른 항체 또는 단편, 또는 양상 90 내지 100 중 임의의 하나에 따른 항체 또는 단편, 용도 또는 방법으로서, 항체 또는 단편은 14일의 과성장 기간으로 론자 버전 8 공급 시스템을 사용하여 유가 과성장 배양액(fed batch overgrow culture) 중에서 1.5g/L를 초과하는 수준으로 론자 지에스-엑스시드(Lonza GS-Xceed)(상표명) 중에서 안정하게 형질주입된 풀로서 발현하는, 항체 또는 단편, 용도 또는 방법.
일 실시형태에서, 발현 수준은 1.0g/L 초과, 1.1g/L 초과, 1.2g/L 초과, 1.3g/L 초과 또는 1.4g/L 초과이다.
102. 양상 73 내지 89, 98, 99 또는 101 중 임의의 하나에 따른 항체 또는 단편, 또는 양상 90 내지 101 중 임의의 하나에 따른 항체 또는 단편, 용도 또는 방법으로서, 항체 또는 단편은 동종 조혈 줄기 세포 이식의 레서스 마카크 모델에서 제12일에 총 CD4+ T 세포 집단의 20%를 초과하는 CD4+ T-세포의 나이브 개체군을 유지하는, 항체 또는 단편, 또는 용도 또는 방법.
또 다른 양상에서, 항체 또는 단편은 공여자 인간 조혈 줄기 세포 이식 이후에 상기 인간에서 제12일에 총 CD4+ T 세포 집단의 20%를 초과하는 공여자 CD4+ T-세포의 나이브 개체군을 유지함으로써 인간에서 이식 거부를 치료 또는 예방하기 위한 것인, 양상 73 내지 89, 98, 99 또는 101 중 임의의 하나에 따른 항체 또는 단편, 또는 양상 90 내지 101 중 임의의 하나에 따른 항체 또는 단편, 용도 또는 방법이 제공된다.
일 실시형태에서, HSCT 모델은 상기 본 명세서에서 고려된 임의의 실시양태에 기술된 바와 같고, 예를 들어 양상 99와 관련하여 기술된 바와 같다.
또 다른 실시형태에서, 나이브 개체군은 유세포 분석법(flow cytometry)을 사용하여 특이적인 T 세포 표현형의 상대적인 비율을 평가함으로써 측정되는데, 여기서는 세포 하위세트가 형광성 항체 프로브로 표지됨으로써 식별되고, 그로 인해서 나이브 CD4 또는 CD8 T-세포는 각각 표지된 CD4+/CD28+/CD95- 또는 CD8+/CD28+/CD95-이고, 중앙 기억 CD4 또는 CD8 T-세포는 각각 표지된 CD4+/CD28+/CD95+ 또는 CD8+/CD28+/CD95+이고, 이펙터 기억 CD4 또는 CD8 T-세포는 각각 표지된 CD4+/CD28-/CD95+ 또는 CD8+/CD28-/CD95+이다.
103. 인간에게 추가 치료제를 투여하는 것을 추가로 포함하는 양상 90 내지 102 중 임의의 하나에 따른 항체 또는 단편, 용도 또는 방법으로서, 임의로 추가 치료제는 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록(maraviroc)), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트, 특히 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, CTLA4-Fc 분자(예를 들어, 아바타셉트), 항-CD40L 항체, 항-LFA1 항체, 항-CD52 항체(예를 들어, 알렘투주맙), 사이클로포스파미드 및 항-흉선세포 글로불린으로 이루어진 군으로부터 독립적으로 선택된, 항체 또는 단편, 용도 또는 방법.
일 실시형태에서, 추가 치료제는 항-염증 약물이다. 또 다른 실시형태에서, 항-염증 약물은 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙) 또는 항-TNFa 항체/TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙, 세르톨리주맙 페골)로 이루어진 군으로부터 독립적으로 선택된다. 예에서, 항-염증 약물은 코르티코스테로이드(예를 들어, 메틸프레드니솔론) 및 항-LFA1 항체로 이루어진 군으로부터 독립적으로 선택된다.
일 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와, 칼시뉴린 억제제(예를 들어, 타크롤리무스, 사이클로스포린), mTOR 억제제(예를 들어, 라파마이신(시롤리무스)), 및 항증식제(예를 들어, 마이코페놀레이트 모페틸, 사이클로포스파미드)로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 포함한다.
일 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와, IL-2 신호전달을 조절하는 면역억제제(예를 들어, 타크롤리무스, 사이클로스포린, 라파마이신(시롤리무스), 및 항-CD25 항체(예를 들어, 바실릭수맙, 다클리주맙)로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 포함한다.
일 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 라파마이신(시롤리무스)을 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 타크롤리무스를 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 타크롤리무스 및 메토트렉세이트를 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 사이클로스포린을 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 사이클로스포린 및 메토트렉세이트를 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 사이클로포스파미드를 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 마이코페놀레이트 모페틸을 포함한다
104. 양상 103에 따른 항체 또는 단편, 용도 또는 방법으로서, 추가 치료제는 항-hOX40L 항체 또는 단편과 순차적으로 또는 동시에 투여되는, 항체 또는 단편, 용도 또는 방법.
105. 양상 73 내지 89, 98, 99, 101 또는 102 중 임의의 하나에 정의된 바와 같은 항체 또는 단편 및 약제학적으로 허용 가능한 부형제, 희석제 또는 담체를 포함하고, 임의로 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트, 특히 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, CTLA4-Fc 분자(예를 들어, 아바타셉트), 항-CD40L 항체, 항-LFA1 항체, 항-CD52 항체(예를 들어, 알렘투주맙), 사이클로포스파미드 및 항-흉선세포 글로불린으로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 추가로 포함하는 약제학적 조성물.
본 명세서에 기술된 바와 같은 약제학적으로 허용 가능한 부형제, 희석제 또는 담체가 이러한 조성물에 필요한 부분만 약간 수정하여 적용된다.
일 실시형태에서, 추가 치료제는 항-염증 약물이다. 또 다른 실시형태에서, 항-염증 약물은 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙) 또는 항-TNFa 항체/TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙, 세르톨리주맙 페골)로 이루어진 군으로부터 독립적으로 선택된다. 예에서, 항-염증 약물은 코르티코스테로이드(예를 들어, 메틸프레드니솔론) 및 항-LFA1 항체로 이루어진 군으로부터 독립적으로 선택된다.
일 실시형태에서, 추가 치료제는 칼시뉴린 억제제(예를 들어, 타크롤리무스, 사이클로스포린), mTOR 억제제(예를 들어, 라파마이신(시롤리무스)), 및 항증식제(예를 들어, 마이코페놀레이트 모페틸, 사이클로포스파미드)로 이루어진 군으로부터 독립적으로 선택된다.
일 실시형태에서, 추가 치료제는 IL-2 신호전달을 조절하는 면역억제제(예를 들어, 타크롤리무스, 사이클로스포린, 라파마이신(시롤리무스), 및 항-CD25 항체(예를 들어, 바실릭수맙, 다클리주맙)로 이루어진 군으로부터 독립적으로 선택된다.
일 실시형태에서, 추가 치료제는 라파마이신(시롤리무스)이다. 또 다른 실시형태에서, 추가 치료제는 타크롤리무스이다. 또 다른 실시형태에서, 추가 치료제는 타크롤리무스와 메토트렉세이트의 조합물이다. 또 다른 실시형태에서, 추가 치료제는 사이클로스포린이다. 또 다른 실시형태에서, 추가 치료제는 사이클로스포린과 메토트렉세이트의 조합물이다. 또 다른 실시형태에서, 추가 치료제는 사이클로포스파미드이다. 또 다른 실시형태에서, 추가 치료제는 마이코페놀레이트 모페틸이다.
106. 양상 105에 따른 약제학적 조성물, 또는 양상 105에 정의된 바와 같은 약제학적 조성물을 포함하는 키트로서, 조성물은 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택된 hOX40L-매개된 병태 또는 질환; 예를 들어 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염, 접촉 과민증, 다발성 경화증 및 죽상동맥경화증, 특히 GvHD를 치료 및/또는 예방하기 위한 것인, 약제학적 조성물 또는 키트.
양상, 구성, 개념, 예 또는 실시형태 중 임의의 것의 hOX40L-매개된 질환이 이러한 조합에 필요한 부분만 약간 수정하여 임의로 적용된다.
107. 인간에서 상기 질환 또는 병태를 치료 및/또는 예방하는 데 사용하기 위한 레이블 또는 지시서와 조합된 양상 105 또는 양상 106에 따른 약제학적 조성물, 또는 그것을 포함하는 양상 106에 따른 키트로서; 임의로 레이블 및 지시서는 마켓팅 인증 번호(예를 들어, FDA 또는 EMA 인증 번호)를 포함하고; 임의로 키트는 항체 또는 단편을 포함하는 IV 또는 주사 장치를 포함하는, 약제학적 조성물 또는 키트.
본 명세서에 기술된 양상, 구성, 개념, 예 또는 실시형태 중 임의의 것의 레이블, 지시서, hOX40L-매개된 질환 및 조건이 이러한 조합에 필요한 부분만 약간 수정하여 임의로 적용된다.
108. 양상 73 내지 89, 98, 99, 101 또는 102 중 임의의 하나에 정의된 바와 같은 항체 또는 단편의 HCDR3을 코딩하는 핵산.
109. 양상 73 내지 89, 98, 99, 101 또는 102 중 임의의 하나에 정의된 바와 같은 항체 또는 단편의 VH 도메인 및/또는 VL 도메인을 코딩하는 핵산.
110. 서열번호 33 및/또는 서열번호 47의 서열과 적어도 80% 동일한 뉴클레오타이드 서열을 포함하는, 양상 109에 따른 핵산.
예에서, 뉴클레오타이드 서열은 서열번호 33 및/또는 서열번호 47의 서열과 적어도 85% 동일하거나, 적어도 90% 동일하거나, 적어도 95% 동일하거나, 적어도 96% 동일하거나,적어도 97% 동일하거나, 적어도 98% 동일하거나 적어도 99% 동일하다.
111. 양상 73 내지 89, 98, 99, 101 또는 102 중 임의의 하나에 언급된 항체의 중쇄 또는 경쇄를 코딩하는 핵산.
112. 양상 108 내지 111 중 임의의 하나의 핵산을 포함하는 벡터로서, 벡터는 CHO 또는 HEK293 벡터인 벡터.
113. 양상 108 내지 111 중 임의의 하나의 핵산 또는 양상 112의 벡터를 포함하는 숙주.
본 발명은 추가로 하기 개념에 관한 것이다:
개념 1.
CD45RA+CCR7+CD95+OX40+ 기억 줄기 T-세포(Tscm)를, Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제(예컨대 항-OX40 또는 항-OX40L 항체 또는 이의 단편)와 조합하는 것을 포함하는 CD45RA+CCR7+CD95+OX40+ 기억 줄기 T-세포의 비율을 감쇠시키는(예를 들어, 수준을 고갈 또는 감소시키는) 방법으로서, 이에 의해서 상기 Tscm 세포의 비율이 감쇠되는(예를 들어, 이에 의해서 상기 Tscm 세포의 수준이 감소 또는 고갈되는) 방법.
CD45RA+CCR7+CD95+OX40+ 기억 줄기 T-세포(Tscm)는 수명이 길고, 자기-재생 능력을 갖는 줄기 세포 기억 T-세포의 새로-정의된 하위세트인 것으로 생각된다. 따라서, 이러한 세포는 다양한 질환, 예컨대 GvHD 및 자가면역 장애에서 해로울 수 있는데, 그 이유는 그것이 잠재적으로 자가-반응성인 이펙터 T-세포의 지속적인 공급원 및 다능성 집단이기 때문이다. 문헌[inGattinoni and Restifo (2013), Inside Blood, 121(4), 567-568]에 기술된 바와 같이, T-세포는 나이브 T-세포(Tn)로 시작하는 경로를 통해서, 줄기 세포 기억 T-세포(Tscm)를 지나고, 중앙 기억 T-세포(Tcm) 및 이펙터 기억 T-세포(Tem)를 지나고, 그 후에 단수명 이펙터 T-세포(Teff)로 발달한다고 공지되어 있다. 이러한 다양한 단계에서, 상이한 마커가 T-세포의 표면 상에서 발현되는데, 이것은 T-세포의 활성 상태, 그의 조직 위치결정 및 다양한 자극, 예컨대 염증 사이토카인에 대한 그의 감응성을 반영한다.
Tscm 세포는 본 명세서에서 정의된 바와 같이 CD45RA+CCR7+CD95+OX40+로서 특성 규명된다. 상이한 T-세포 유형의 대안적인 선행 기술 분류법에 대해서는, 문헌[Gattinoni and Restifo (2013)]의 도면을 참고하기 바란다. 추가 마커가 존재하거나 존재하지 않을 수 있지만, Tscm 세포는 최소한 CD45RA+CCR7+CD95+OX40+여야 한다. 다양한 세포-표면 마커는 일 실시형태에서 관련 기술 분야의 통상의 기술자에게 널리 공지된 방법을 사용하여 유세포 분석법을 사용하여 식별된다. 일 실시형태에서, Tscm 세포는 추가로 CD8+일 수 있다. 또 다른 실시형태에서, Tscm 세포는 추가로 CD62L+일 수 있다. 유세포 분석법 기술은 관련 기술 분야의 통상의 기술자에게 널리 공지되어 있다. 유세포 분석법 기술에서 사용될 수 있는 작용제는 하기 실시예 7에 정의되어 있다. 일 실시형태에서, 유세포 분석법은 하기 실시예 7에 기술된 바와 같이 수행된다. 또 다른 실시형태에서, 유세포 분석법은 문헌[Baumgarth & Roederer (2000), Journal of Immunological Methods, 243, 77-97]에 기술된 바와 같이 수행된다(하기 본 명세서의 개념 25 참고).
특정 실시형태에서, Tscm 세포는 CD4+CD45RA+CCR7+CD95+OX40+인 것으로 특성 규명된다.
이론에 얽매이고자 함은 아니지만, 이러한 Tscm 집단은 본 명세서에서 언급된 바와 같이 다양한 질환에서 다수의 이익을 가질 것이다. 일 실시형태에서, Tscm 세포는 활성 Tscm 세포이다.
본 명세서에서 개념 1 내지 83 전체에서, Tscm 세포의 비율 또는 수준은 샘플에서 또는 실제로 대상체의 혈액(의 샘플)에서 감쇠될 수 있다. Tscm 세포의 비율 또는 수준은 샘플 중의 전체 T-세포 집단에 대해서 측정될 수 있다. 일 실시형태에서, Tscm 세포의 비율 또는 수준은 샘플 중의 다른 T-세포에 대해서 측정된다. T-세포는 일반적으로 CD3+와 동일할 수 있고, Tn 세포, Tscm 세포, Tcm 세포, Tem 세포 및 Teff 세포를 포함한다. 특정 실시형태에서, Tscm 세포의 비율 또는 수준은 샘플 중의 Tn 세포(하기 본 명세서에서 정의된 바와 같음)에 대해서 측정된다. Tscm 세포의 비율 또는 수준은 고갈 또는 감소에 의해서 변경될 수 있다. 일 실시형태에서, 세포 유형의 수준은 Tscm 세포(예를 들어, 하기 본 명세서의 개념 2 관련)의 비율과 동일할 수 있다. 또 다른 실시형태에서, T-세포 유형의 수준은 Tscm 세포의 비율과 동일할 수 있다. 일 실시형태에서, Tscm:Tn의 비 또는 비율은 50:50 초과이다. 특정 비 및 비율은 개념 23 및 24에 기술된 바와 같다.
본 명세서에서 개념 1 내지 83에서 사용되는 바와 같이 "고갈" 및 "고갈시킨다"는 표적 세포(예를 들어, Tscm 세포)를 사멸 또는 제거하기 위한 목적하는 표적에 대한 작용제(예컨대 항체)와의 조합 이후의 활성 효과를 기술한다. 작용제가 항체인 경우, 이것은 통상적으로 이펙터 기능, 예컨대 ADC, ADCC 또는 CDC를 통해서 달성된다. 대안적으로, 표적은 약물 또는 표적화된 모이어티(예컨대 항-OX40 또는 항-OX40L 항체)에 컨쥬게이팅될 수 있는 독소에 의해서 사멸 또는 제거될 수 있다. 그러한 독소는 선택적으로 그것이 표적화된 세포를 선택적으로 사멸 또는 제거할 것이다. 적합한 면역컨쥬게이트는 본 명세서 제90면, 제114면 내지 제118면, 및 제134면(특히 제114면 내지 제116면)에 기술되어 있다.
본 명세서에서 개념 1 내지 83에서 사용되는 바와 같이 "감소시키는" 또는 "감소시킨다"는 고갈이 아닌 기전을 말하며, 이것은 주어진 집단에서 세포의 절대적인 수를 감소시킨다. 이것은 예를 들어, 차단제 또는 중화제(예컨대 항체)를 통해서 표적에 대해서 간접적으로 달성될 수 있으며, 이것은 표적 세포(예컨대 Tscm)의 사멸을 간접적으로 유발하거나, 또는 표적 세포의 확장 또는 성장을 예방하여, 세포의 또 다른 유형(예컨대 Tn 세포)에 대한 상대적인 비율을 현저히 감소시킨다.
개념 1 내지 83에서 사용되는 바와 같이 본 명세서에서, T-세포 집단의 "수준"은 T-세포의 유형의 절대적인 수치 또는 상대적인 비율을 말할 수 있다.
본 명세서에 기술된 개념 다양한 개념 1 내지 83 전체에서, Tscm 세포의 비율을 감쇠시키는 작용제는 예를 들어 항체 또는 이의 단편, 짧은 간섭 RNA(SiRNA), 아연 집게, DARPin, 압타머, 스피겔머(Spiegelmer), 앤트-칼린(ant-calin), 수용체-Fc 융합, 리간드-Fc 융합 또는 소분자일 수 있다. 일 실시형태에서, 작용제는 OX40(예를 들어, 인간 OX40), 또는 OX40의 리간드를 표적화한다. 또 다른 실시형태에서, 작용제는 OX40L(예를 들어, 인간 OX40L), 또는 OX40L의 수용체를 표적화한다. 일례에서, 작용제는 OX40-Fc 융합 단백질(예를 들어, hOX40-Fc 융합체)일 수 있거나, OX40L-Fc 융합 단백질(예를 들어, hOX40L-Fc 융합체)일 수 있고, 둘 다는 OX40 및 OX40L의 단편을 포함한다. 이들 유형의 구축물은 관련 기술 분야의 통상의 기술자에게 공지되어 있다. 또 다른 실시형태에서, 작용제는 OX40(예를 들어, 인간 OX40)을 표적화한다. 또 다른 실시형태에서, 작용제는 OX40L(예를 들어, 인간 OX40L)을 표적화한다.
특정 실시형태에서, 작용제는 항체 또는 이의 단편이다. 항체 및 단편의 포맷 및 구조는 본 명세서에서 다른 곳에 기술되어 있고, 본 명세서에 개시된 개념 중 임의의 것에 적용될 수 있다. 항체 또는 단편은 본 명세서에서 기술된 바와 같은(예를 들어, 본 명세서의 개념 52 내지 64 중 임의의 하나) 구축물 중 임의의 것일 수 있다. 특정 실시형태에서, 작용제는 항-인간 OX40 항체 또는 이의 단편이다. 또 다른 측정 실시형태에서, 작용제는 항-인간 OX40L 항체, 예컨대 본 명세서에 기술된 02D10의 아미노산 서열을 포함하는 항체 또는 옥셀루맙의 아미노산 서열을 포함하는 항체이다.
개념 2. 샘플 중의 T-세포 집단의 세포 유형의 비를 변경하는 방법으로서, 방법은
a. 상기 집단을 제공하는 단계이되, 집단은 상이한 T-세포 유형의 혼합물을 포함하고, 집단은 CD45RA+CCR7+CD95+OX40+ Tscm 세포를 포함하는, 단계,
b. Tscm 세포의 비율을 감쇠시키는 작용제를 제공하는 단계(또는 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 제공하는 단계); 및
c. 상기 세포 집단을, 상기 집단 중의 Tscm 세포의 비를 변경(예를 들어, 비율을 감소)하기에 효과적인 상기 작용제(예를 들어, 항체 또는 이의 단편)의 양과 배합하는 단계를 포함하는, 샘플 중의 T-세포 집단의 세포 유형의 비를 변경하는 방법.
본 명세서에서 개념 1 내지 83 전체에서, T-세포 유형의 비는 예를 들어, 나이브 T-세포(Tn, 하기 본 명세서에서 정의된 바와 같음)의 비율을 증가시킴으로써 샘플 중에서 변경될 수 있다. 또 다른 실시형태에서, T-세포 유형의 비는 Tscm 세포의 비율을 감소시킴으로써 변경될 수 있다. Tscm 세포의 비는 전체 샘플에 대해서 측정될 수 있다. 일 실시형태에서, T-세포의 비는 샘플 중의 다른 T-세포에 대해서 나이브 T-세포 또는 Tscm 세포의 비율을 비교함으로써 측정된다. T-세포는 일반적으로 CD3+인 것으로서 식별될 수 있고, Tn 세포, Tscm 세포, Tcm 세포, Tem 세포 및 Teff 세포를 포함한다. 특정 실시형태에서, T-세포의 비는 샘플 중의 나이브 T-세포에 대한 Tscm 세포의 비로서 측정된다. T-세포의 비는 Tscm 세포의 고갈 또는 감소에 의해서 변경될 수 있다. T-세포의 비는 나이브 T-세포의 증가 또는 확장에 의해서 변경될 수 있다.
개념 3. 개념 2에 따른 방법으로서, 단계 a)에서, 집단이 CD45RA+CCR7+CD95- 나이브 T-세포(Tn)를 추가로 포함하는, 방법.
본 명세서에서 개념 1 내지 83에 정의된 바와 같은 나이브 T-세포(Tn)는 CD45RA+CCR7+CD95-로서 특성 규명된다. 추가 마커가 존재하거나 또는 존재하지 않을 수 있지만, Tn 세포는 최소한 CD45RA+CCR7+CD95-여야 한다. 일 실시형태에서, Tn 세포는 추가로 CD8+ 또는 CD4+, 특히 CD4+일 수 있다. Tn이 이롭다고 여겨지는데, 그 이유는 이것이 T-세포의 전체 풀을 대표하며, 그로부터 조정 T-세포 면역 반응이 잠재적으로 위험한 병원체 및 악성 세포에 노출되는 경우 개체를 보호하도록 발전할 수 있기 때문이다.
개념 4. 개념 3에 따른 방법으로서, 단계 a)의 집단 중의 Tscm:Tn의 비는 50:50을 초과하는, 방법.
개념 5. 개념 1 내지 4 중 임의의 하나에 따른 방법으로서, 방법은 생체외에서 인간 공여자 대상체로부터 추출된 혈액의 샘플 중에서 수행되는, 방법.
개념 6. 개념 5에 따른 방법으로서, 상기 방법에 의해서 생성된 혈액이 수용자 인간 대상체에 다시 도입되는, 방법.
일 실시형태에서, 수용자 인간 대상체는 샘플이 제거된 동일한 공여자 인간 대상체이다. 또 다른 실시형태에서, 수용자 인간 대상체는 공여자 인간 대상체와는 상이하다. 수용자가 공여자와 상이한 경우, 공여자는 수용자 대상체와 동일한 성별인 것이 바람직하다. 또 다른 실시형태에서, 공여자는 수용자 대상체와 유사한 연령 및 인종성을 가질 수 있다. 또 다른 실시형태에서, 공여자는 수용자 대상체와 동일하거나 유사한 동종이인자형(allotype) 마커를 가질 수 있다.
또 다른 실시형태에서, 수용자 인간 공여자는 치료될 질환의 중증도에 따라서, 공여자 혈액을 1회를 초과하게 수혈받을 수 있다.
개념 7. 개념 1 내지 4 중 임의의 하나의 방법으로서, 방법은 인간 대상체에서 생채내에서 수행되는, 방법.
개념 8. 개념 7에 따른 방법으로서, 대상체는 Tscm-매개된 질환 또는 병태를 갖거나 그것의 위험이 있는, 방법.
본 명세서에서 사용되는 바와 같이, 대상체는 그의 T-세포 집단에서의 세포 변화가 일어나기 시작하지만, 대상체에서 증상이 아직 나타나지 않거나 또는 대상체가 임의의 종래의 방법에 의해서 그러한 질환을 갖는 것으로서 진단되지 않은 경우, "Tscm-매개된 질환 또는 병태"의 위험이 있다고 식별될 수 있다. 따라서, 본 명세서에 개시된 방법 및 용도는 그러한 질환이 발전할 환자의 조기 식별에 도움을 줄 수 있다. 일 실시형태에서, 질환은 예방된다(즉, 치료는 예방적이다).
특정 실시형태에서, 대상체는 그가 이식을 위해서 사전 수술된 경우 GvHD 또는 이식 거부의 위험이 있다. 잠재적인 이식 요법은 하기 본 명세서에서 개념 78에서 예상된다.
본 명세서에 기술된 개념 1 내지 83 중 임의의 것에서, Tscm-매개된 질환은 하기 본 명세서의 개념 71 내지 80 중 임의의 것에 정의된 바와 같을 수 있다.
개념 9. 대상체에서 Tscm-매개된 질환 또는 병태의 위험을 치료 또는 감쇠시키는 방법으로서, 방법은 T-세포의 집단을 Tscm 세포의 비율을 감소시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제(예를 들어, 항-OX40 또는 항-OX40L 항체 또는 이의 단편)와 조합하는 단계를 포함하고, 이에 의해서 CD45RA+CCR7+CD95+OX40+ Tscm 세포의 비율이 집단에서 감쇠되는(예를 들어, 이에 의해서 상기 Tscm 세포의 수준이 상기 집단에서 감소 또는 고갈되는), 방법.
개념 1 내지 83에서 사용되는 바와 같이 본 명세서에서, Tscm-매개된 질환의 "치료"는 상기 Tscm-매개된 질환 중 하나 이상의 증상(들)의 감쇠를 포함한다. Tscm-매개된 질환의 "예방"은 상기 Tscm-매개된 질환 중 하나 이상의 증상(들)의 예방을 포함한다.
개념 10. 개념 7 내지 9 중 임의의 하나에 따른 방법으로서, 작용제는 상기 작용제(예를 들어, 항체 또는 단편)를 상기 대상체에게 치료 유효량으로 투여함으로써 배합되고, 이에 의해서 상기 Tscm-매개된 질환 또는 병태가 치료되거나 또는 상기 Tscm-매개된 질환 또는 병태의 위험이 상기 대상체에서 감쇠되는, 방법.
일 실시형태에서, 투여는 Tscm-매개된 질환의 위험을 감쇠시키기 위한 예방적인 것이다.
본 명세서에 기술된 개념 중 임의의 것에서, 치료 유효량 또는 예방 유효량의 항체 또는 단편은 다른 곳에 기술된 바와 같다(치료의 경우 명세서 제29면, 제73면, 제105면 내지 제107면, 및 예방조치의 경우 명세서 제72면, 및 제102면 내지 제103면). 본 명세서에 기술된 개념 중 임의의 것에서, 투여 모드 및 조성물은 다른 곳에 기술된 바와 같다(본 명세서에서 118 내지 142 참고). 일 실시형태에서, 항체 또는 단편은 (예를 들어, 정맥내로) 볼러스(bolus) 주입에 의해서 투여된다.
개념 11. 상기 대상체에게 치료 유효량의 Tscm 세포의 비율을 감소시키는(예를 들어 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제(예를 들어, 항-OX40 또는 항-OX40L 항체 또는 이의 단편)를 투여하는 것을 포함하는 대상체에서 Tscm-매개된 질환 또는 병태의 위험을 치료 또는 감쇠시키는 방법으로서, 이에 의해서 CD45RA+CCR7+CD95+OX40+ Tscm 세포의 비율이 감쇠되고(예를 들어, 이에 의해서 상기 Tscm 세포의 수준이 감소 또는 고갈되고), Tscm-매개된 질환 또는 병태가 따라서 치료되거나 상기 Tscm-매개된 질환 또는 병태의 위험이 감쇠되는, 방법.
개념 12a. 대상체에서 Tscm-매개된 질환 또는 병태의 위험을 치료 또는 감쇠시키는 데 사용하기 위한 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제(예를 들어, 항-OX40 또는 항-OX40L 항체 또는 이의 단편); 또는 개념 12b. 대상체에서 Tscm-매개된 질환 또는 병태의 위험을 치료 또는 감쇠시키는 데 사용하기 위한 항-OX40 또는 항-OX40L 항체 또는 이의 단편.
개념 13a. 대상체에서 Tscm-매개된 질환 또는 병태의 치료 또는 예방을 위한 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제(예를 들어, 항-OX40 또는 항-OX40L 항체 또는 이의 단편)의 용도; 또는 개념 13b. 대상체에서 Tscm-매개된 질환 또는 병태의 치료 또는 예방을 위한 항-OX40 또는 항-OX40L 항체 또는 이의 단편의 용도.
개념 14a. 대상체에서 Tscm-매개된 질환 또는 병태의 치료 또는 예방을 위한 의약의 제조에서의 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제(예를 들어, 항-OX40 또는 항-OX40L 항체 또는 이의 단편)의 용도; 또는 개념 14b. 대상체에서 Tscm-매개된 질환 또는 병태의 치료 또는 예방을 위한 의약의 제조에서의 항-OX40 또는 항-OX40L 항체 또는 이의 단편의 용도.
개념 15a. 대상체에서 Tscm-매개된 질환 또는 병태의 치료 또는 예방을 위한 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제(예를 들어, 항-OX40 또는 항-OX40L 항체 또는 이의 단편)를 포함하는 조성물; 또는 개념 15b. 대상체에서 Tscm-매개된 질환 또는 병태의 치료 또는 예방을 위한 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 포함하는 조성물.
개념 16. 질환 또는 병태의 치료가 필요한 대상체에서 질환 또는 병태를 치료하는 방법으로서,
a. 대상체로부터 수득된 샘플 중의 CD45RA+CCR7+CD95- Tn 세포의 수준 및 CD45RA+CCR7+CD95+OX40+ Tscm 세포의 수준을 측정하기 위한 검정법을 수행하는 단계; 및
b. 샘플 중의 Tscm:Tn 세포의 비가 검정법에서 50:50을 초과하는 것으로 측정되는 경우 대상체에게 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제(예를 들어, 항-OX40 또는 항-OX40L 항체 또는 이의 단편), 예컨대 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 투여하는 단계를 포함하는, 방법.
개념 17a. 대상체의 치료에서 사용하기 위한 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제(예를 들어, 항-OX40 또는 항-OX40L 항체 또는 이의 단편)로서, 작용제는 50:50을 초과하는 D45RA+CCR7+CD95+OX40+ Tscm 세포:CD45RA+CCR7+CD95- Tn 세포의 비를 갖거나 또는 그러한 비를 갖는다고 측정된 대상체에게 투여되는, 작용제; 또는 개념 17b. 대상체의 치료에서 사용하기 위한 항-OX40 또는 항-OX40L 항체 또는 이의 단편으로서, 항체 또는 이의 단편은 50:50을 초과하는 D45RA+CCR7+CD95+OX40+ Tscm 세포:CD45RA+CCR7+CD95- Tn 세포의 비를 갖거나 또는 그러한 비를 갖는다고 측정된 대상체에게 투여되려는 것인, 작용제.
개념 18a. 50:50을 초과하는 CD45RA+CCR7+CD95+OX40+ Tscm 세포: CD45RA+CCR7+CD95- Tn 세포의 비를 갖거나 또는 그러한 비를 갖는다고 측정된 대상체의 치료를 위한 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제(예를 들어, 항-OX40 또는 항-OX40L 항체 또는 이의 단편)의 용도; 또는 개념 18b. 50:50을 초과하는 CD45RA+CCR7+CD95+OX40+ Tscm 세포: CD45RA+CCR7+CD95- Tn 세포의 비를 갖거나 또는 그러한 비를 갖는다고 측정된 대상체의 치료를 위한 항-OX40 또는 항-OX40L 항체 또는 이의 단편의 용도.
개념 19a. 대상체의 치료에서 사용하기 위한 의약의 제조에서의 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제(예를 들어, 항-OX40 또는 항-OX40L 항체 또는 이의 단편)의 용도로서, 작용제는 50:50을 초과하는 CD45RA+CCR7+CD95+OX40+ Tscm 세포:CD45RA+CCR7+CD95- Tn 세포의 비를 갖거나 또는 그러한 비를 갖는다고 측정된 대상체에게 투여되는, 용도; 또는 개념 19b. 대상체의 치료에서 사용하기 위한 의약의 제조에서의 항-OX40 또는 항-OX40L 항체 또는 이의 단편의 용도로서, 항체 또는 이의 단편은 50:50을 초과하는 CD45RA+CCR7+CD95+OX40+ Tscm 세포:CD45RA+CCR7+CD95- Tn 세포의 비를 갖거나 또는 그러한 비를 갖는다고 측정된 대상체에게 투여되려는 것인, 용도.
개념 17 내지 19 중 임의의 것에서, 비는 샘플 중에서, 예를 들어 상기 대상체로부터 수득된 혈액의 샘플 중에서 측정된다.
개념 20. 개념 16a 또는 b에 따른 방법, 개념 17a 또는 b에 따라서 사용하기 위한 작용제 또는 항체 또는 단편, 또는 개념 18a 또는 b 또는 개념 19a 또는 b에 따른 용도로서, 요법은 Tscm-매개된 질환 또는 병태의 치료 또는 예방이고, 바람직하게는 요법은 Tscm-매개된 질환 또는 병태의 치료인, 방법, 작용제 또는 항체 또는 단편, 또는 용도.
또 다른 실시형태에서, 대상체는 Tscm-매개된 질환 또는 병태를 갖거나 그것의 위험이 있다. Tscm-매개된 질환 또는 병태는 하기 본 명세서의 개념 71 내지 80 중 중 임의의 하나에 정의된 바와 같을 수 있다.
개념 21. 하기 단계를 포함하는 대상체를 Tscm-매개된 질환 또는 병태(예를 들어, 질환 또는 병태는 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 사용하여 치료하기에 적합함)를 갖거나 그것의 위험이 있는 것으로서 분류하는 방법:
a. 상기 대상체로부터 수득된 샘플 중의 (i) CD45RA+CCR7+CD95+OX40+ Tscm 세포, 및 (ii) CD45RA+CCR7+CD95- Tn 세포를 검출하는 검정법을 수행하는 단계; 및
b. 샘플 중의 Tscm:Tn 세포의 비가 50:50을 초과하는 경우 대상체를 Tscm-매개된 질환 또는 병태를 갖거나 그것의 위험이 있는 것으로서 분류하는 단계.
개념 22. 하기 단계를 포함하는 개념 21에 따른 방법:
c. 상기 대상체가 단계 b)에서 Tscm-매개된 질환 또는 병태를 갖거나 그것의 위험이 있는 것으로서 분류된 경우 상기 대상체에게 상기 대상체의 혈액 중의 상기 Tscm 세포의 비율을 감소시키는, (예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 투여하는 단계.
항-OX40 또는 항-OX40L 항체 또는 이의 단편을 사용하여 치료하기에 적합한 Tscm-매개된 질환 또는 병태는 하기 본 명세서에서 개념 71 내지 80 중 임의의 하나에 기술된 바와 같다.
개념 23. 개념 4, 16, 또는 20 내지 22 중 임의의 하나에 따른 방법, 개념 17 또는 20에 따라서 사용하기 위한 작용제 또는 항체 또는 단편, 또는 개념 18 내지 20 중 임의의 하나에 따른 용도로서, Tscm:Tn 세포의 비는 60:40 초과, 또는 70:30 초과, 또는 75:25 초과, 예컨대 70:30초과인 (또는 그렇게 측정되거나 또는 그렇다고 분류된), 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 또는 용도.
또 다른 실시형태에서, 비는 55:45 초과이다(또는 그렇게 측정되거나 또는 그렇다고 분류된다). 또 다른 실시형태에서, 비는 65:35 초과이다 (또는 그렇게 측정되거나 또는 그렇다고 분류된다).
개념 24. 개념 23에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 또는 용도로서, Tscm:Tn 세포의 비는 80:20 초과, 또는 85:15 초과, 예를 들어 90:10 초과, 예를 들어, 95:5 초과인 (또는 그렇게 측정되거나 또는 그렇다고 분류된), 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 또는 용도.
개념 25. 개념 4, 16, 또는 20 내지 24 중 임의의 하나에 따른 방법, 개념 17, 20, 23 또는 24 중 임의의 하나에 따라서 사용하기 위한 작용제 또는 항체 또는 단편, 또는 개념 18 내지 20, 23 또는 24 중 임의의 하나에 따른 용도로서, Tscm:Tn 세포의 비는 유세포 분석법에 의해서 측정된(측정 가능한), 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 또는 용도.
유세포 분석법 기술은 상기에 논의된 바와 같이, 관련 기술 분야의 통상의 기술자에게 널리 공지되어 있다. 유세포 분석법 기술에서 사용될 수 있는 작용제는 하기 실시예 7에 정의되어 있다. 일 실시형태에서, 유세포 분석법은 하기 실시예 7에 기술된 바와 같이 수행된다. 또 다른 실시형태에서, 유세포 분석법은 문헌 [Baumgarth & Roederer(2000)]에 기술된 바와 같이 수행된다.
개념 26. 하기 단계를 포함하는, Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제(예를 들어, 항-OX40 또는 항-OX40L 항체 또는 이의 단편)를 사용하거나, 또는 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 사용하여 Tscm-매개된 질환 또는 병태의 위험을 치료 또는 감쇠시키는 방법:
a. 대상체로부터의 샘플로부터 수득된 CD45RA+CCR7+CD95+ Tscm 세포의 표면 상에서 OX40의 존재를 검출함으로써 대상체가 치료를 위한 후보자인지를 결정하는 단계; 및
b. 대상체가 치료를 위한 후보자인 것으로서 식별된 경우 대상체에게 상기 작용제, 예컨대 상기 항체 또는 단편을 투여하는 단계.
개념 27. 개념 26에 따른 방법으로서, Tscm 세포의 표면 상에서의 OX40의 존재는 유세포 분석법을 사용하여 측정되는, 방법.
일 실시형태에서, 대상체는 인간이고, OX40는 인간 OX40이다.
개념 28. 하기 단계를 포함하는 방법:
a. Tscm-매개된 질환 또는 병태를 갖거나 또는 그것의 위험이 있는 대상체로부터 유도된 적어도 2개의 T-세포 샘플을 수득하는 단계이되, 상기 적어도 2개의 샘플은 제1 샘플 및 제2 샘플을 포함하는, 단계,
b. 상기 제1 샘플 및 제2 샘플 중의 CD45RA+CCR7+CD95+OX40+ Tscm 세포의 수준을 측정하는 단계; 및
c. 상기 제2 샘플 중의 Tscm 세포의 수준이 상기 제1 샘플에 비해서 상승된 경우, 상기 Tscm-매개된 질환 또는 병태의 위험을 치료 또는 감쇠시키기 위해서, Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제를 투여하거나, 또는 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 투여함으로써 상기 대상체를 치료하여 CD45RA+CCR7+CD95+OX40+ Tscm 세포의 비율을 감쇠시키는(예를 들어, Tscm 세포의 수준을 고갈 또는 감소시키는) 단계.
단계 b.에서 상기 제1 샘플 및 제2 샘플 중의 Tscm의 수준은 Tscm 세포의 절대 수치일 수 있거나, Tscm의 상대적인 비율(예를 들어, Tscm:Tn, 또는 Tacm:총 T-세포 수의 비)일 수 있다. Tscm 세포의 수준은, 그것이 제1 샘플 중의 수준보다 통계학적으로 유의하게 더 높은 경우 제2 샘플 중에서 상승될 수 있다.
개념 29. 개념 28에 따른 방법으로서, 상기 제1 샘플은
i. 상기 질환 또는 병태의 발병 이전에; 또는
ii. 상기 질환 또는 병태의 발병 이후에 수집되고;
임의로 상기 제2 샘플은 제1 샘플보다 1개월 이하, 예를 들어 1주 늦게 수집된다.
본 명세서에서 개념에서 사용되는 바와 같이, 대상체는 대상체에게 통상적으로 상기 질환 또는 병태와 관련된 증상이 나타나지 않거나 또는 대상체가 임의의 종래의 방법에 의해서 그러한 질환 또는 병태를 갖는 것으로서 진단되지 않은 경우, "Tscm-매개된 질환 또는 병태의 발병 이전"인 것으로 결정될 수 있다. 예를 들어, 급성 GvHD의 징후 및 증상의 존재는 예컨대 문헌[Przepiorka et al. (1995), 1994 Consensus Conference on Acute GvHD GradingBone Marrow Transplant 1995; 15, 825-828]에 기술된 표준화된 규모에 따라서 단계화 및 등급화될 수 있다. 유사한 질환 등급 규모가 또한 다른 관련 질환, 예컨대 류마티스 관절염 및 염증성 장 질환을 위한 일상적인 임상 용도로 존재한다.
개념 30.
개념 28 또는 개념 29에 따른 방법으로서, Tscm-매개된 질환 또는 병태는 이식이고, 단계 c)에서 치료는 이식 거부의 위험을 감쇠시키기 위해서 이고, 임의로 제1 샘플은 이식 이전에 취해진 것이고, 제2 샘플은 이식 이후에 취해진 것인, 방법.
제1 샘플은 수술 전에, 예를 들어 대상체가 치료를 위한 후보자로서 식별된 이후에 취해질 수 있다. 제2 샘플은 이식 이후에 취해져서, 이식의 수용을 모니터링하는 방법으로서 의료진에 의해서 사용될 수 있다. 따라서, 의료진은 이식 이후에 하나를 초과하는 샘플을 취할 수 있고, 예를 들어 매일 혈액 샘플을 취하여 샘플 중의 Tscm:Tn의 비율 변화 또는 Tscm의 수준에 대해서 대상체를 모니터링할 수 있다. 샘플은 이식 거부 가능성에 따라서 격일로, 매주, 매달 또는 더 긴 주기(매년 포함)에 취해질 수 있다. 예를 들어, 이식이 자가형인 경우, 이식 거부 가능성은 동종이형 이식에 비해서 감쇠될 수 있고, 따라서 이식 후 샘플 수집 간의 시간 간격은 거부 위험이 더 높은 동종이형 이식보다 더 길 수 있다.
개념 31. 개념 30에 따른 방법으로서, 단계 a)에서, 제1 샘플은 상기 이식을 수행하기 1주일 이하 이전에, 예를 들어 6일 이하 이전에, 5일 이하 이전에, 4일 이하 이전에, 또는 3일 이하 이전에, 예컨대 2일 이하 이전에 수집된, 방법.
개념 32. 개념 28 내지 31 중 임의의 하나에 따른 방법으로서, 제2 샘플은 제1 샘플 또는 상기 이식을 수행하고 6일 이하 이후에, 5일 이하 이후에, 4일 이하 이후에, 또는 3일 이하 이후에, 예컨대 2일 이하 이후에 수집된, 방법.
개념 33. 개념 28 내지 32 중 임의의 하나에 따른 방법으로서, 단계 c)에서, 상기 제2 샘플 중의 Tscm 세포의 수준은 상기 제1 샘플에 비해서 2배 높은 수준이고, 예를 들어 3배 높은 수준이거나, 바람직하게는 상기 제1 샘플에 비해서 4배 높은 수준인, 방법.
일 실시형태에서, 단계 c)에서, 상기 제2 샘플 중의 Tscm 세포의 수준은 상기 제1 샘플에 비해서 4배를 초과하는(예를 들어, 4.5배를 초과하는) 수준이다. 또 다른 실시형태에서, 단계 c)에서, 상기 제2 샘플 중의 Tscm 세포의 수준은 상기 제1 샘플에 비해서 5배를 초과한다.
개념 34. 개념 30 내지 33 중 임의의 하나에 따른 방법으로서, 대상체는 상기 이식 이전에 예방 용량의 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제를 제공받거나, 예방 용량의 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 제공받고, 제1 샘플은 상기 작용제, 또는 항체 또는 이의 단편의 투여 이전에 취해지고, 제2 샘플은 이식 이후에 또는 작용제, 또는 항체 또는 이의 단편의 투여 이후에 취해지는(바람직하게는, 제2 샘플은 이식 이후에 취해짐), 방법.
일 실시형태에서, 예방 용량은 유효 예방 용량이다. "유효"라는 것은, 그 용량이 본 명세서에 기술된 바와 같은 Tscm의 비율 또는 수준을 감쇠시키기에 유효하거나, Tscm-매개된 질환 또는 병태의 위험을 예방 또는 감쇠시키기에 유효하다는 것을 의미한다.
이식 이후에 이식 거부의 위험을 감쇠시키기 위해서, 본 명세서에서 기술된 바와 같은 방법을 사용하여, 이식 이전에 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제를 투여함으로써, 또는 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 투여함으로써, Tscm 세포의 이미-일탈한 수준을 수정할 수 있다. 따라서, 작용제(또는 항-OX40 또는 항-OX40L 항체 또는 이의 단편)의 투여 이후에, 그러나 이식 이전에 다수의 샘플을 취할 수 있다. 수집된 샘플과 건강한 공여자로부터의 샘플을 비교할 수 있다.
개념 35. 개념 30 내지 33 중 임의의 하나에 따른 방법으로서, 대상체는 이식 이후에 치료 용량의 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제를 제공받거나, 또는 치료 용량의 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 제공받고, 제1 샘플은 상기 이식 이전에 취해지고, 제2 샘플은 이식 이후에 취해지는, 방법.
일 실시형태에서, 치료 용량은 유효 치료 용량이다. "유효"라는 것은, 그 용량이 본 명세서에 기술된 바와 같은 Tscm의 비율 또는 수준을 감쇠시키기에 유효하거나, Tscm-매개된 질환 또는 병태의 위험을 치료하기에 유효하다는 것을 의미한다.
일 실시형태에서, 제2 샘플은 작용제, 또는 항체 또는 이의 단편의 투여 이후에 취해진다. 이것은 Tscm 세포의 수준 또는 비율이 즉 제1 샘플 또는 건강한 공여자로부터 수득된 샘플에 비해서 "정상"으로 유지되는지를 체크하는 것을 가능하게 할 것이다.
개념 36. 개념 30 내지 33 중 임의의 하나에 따른 방법으로서, 대상체는 이식 이후에 치료 용량의 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제를 제공받거나, 치료 용량의 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 제공받고, 제1 샘플은 상기 이식 이전에 취해지고, 제2 샘플은 상기 작용제, 또는 상기 항체 또는 이의 단편의 투여 이후에 취해지는, 방법.
개념 37. 하기 단계를 추가로 포함하는 개념 34 내지 36 중 임의의 하나에 따른 방법:
d. 상기 대상체로부터 유래된 제3 샘플을 수득하는 단계;
e. 상기 제3 샘플 중의 CD45RA+CCR7+CD95+OX40+ Tscm 세포의 수준을 측정하는 단계;
f. 상기 제3 샘플 중의 Tscm 세포의 수준이 상기 제2 샘플 또는 상기 제1 샘플에 비해서 상승된 경우, Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제를 투여함으로써, 또는 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 투여함으로써, 상기 대상체를 치료하여 Tscm 세포의 CD45RA+CCR7+CD95+OX40+ Tscm 세포의 비율을 감쇠시키는(예를 들어, 수준을 고갈 또는 감소시키는) 단계.
수준은 상기 본 명세서에서 기술된 바와 같이 "상승된"것으로 간주된다(예를 들어, 개념 28 또는 33와 관련됨).
개념 38. 개념 37에 따른 방법으로서, 단계 d) 내지 f)는 Tscm 세포의 수준이 치료-유효량 또는 예방-유효량, 예를 들어, 상기 대상체에서 실질적으로 일정한 수준으로 유지될 때까지 필요에 따라서 반복되는, 방법.
본 명세서에서 개념에서 사용되는 바와 같이, "실질적으로 일정한 수준"은 샘플들 간의 30% 이내의 변화인 것으로 기술될 수 있다. 일 실시형태에서, 실질적으로 일정한 수준은 샘플들 간의 20% 이내의 변화인 것으로 기술될 수 있다. 또 다른 실시형태에서, 실질적으로 일정한 수준은 샘플들 간의 15% 이내의 변화, 예컨대 샘플들 간의 10% 이내의 변화, 예를 들어, 샘플들 간의 5% 이내의 변화이다.
개념 39. 개념 28 내지 38 중 임의의 하나에 따른 방법으로서, 제2 샘플은 제1 샘플을 취하고 1개월 이하 이후에, 예컨대 1주일 이하, 6일 이하, 5일 이하, 4일 이하, 또는 3일 이하 이후에, 예를 들어, 제1 샘플을 취하고 2일 이하 이후에 취해지고, 임의로 제3 샘플은 제2 샘플을 취하고 1개월 이하 이후에, 예컨대 1주일 이하, 6일 이하, 5일 이하, 4일 이하, 또는 3일 이하, 예를 들어, 제2 샘플을 취하고 2일 이하 이후에 취해진다.
이러한 개념에 기술된 샘플 중 임의의 것을 취하는 시간 지점은 다수의 인자, 예컨대 Tscm-매개된 질환(예를 들어, GvHD 또는 이식 거부)의 위험을 갖거나 그것의 위험이 있는 대상체의 가능성, 이전 샘플 중에서 측정된 수준, 이식의 유형 등에 좌우될 것이다. 관련 기술 분야의 통상의 기술자는 필요에 따라서 또는 목적하는 바에 따라서 적절한 시간 지점을 결정할 수 있을 것이다. 시간 지점은 목적에 따라서 매달, 2개월 마다, 3개월 마다, 6개월 마다 또는 매년일 수 있다.
개념 40. 대상체에서 Tscm-매개된 질환 또는 병태(예를 들어, 질환 또는 병태는 대상체에서 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제를 사용하거나 또는 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 사용하여 치료 또는 예방될 수 있음)를 위한 진단법으로서의 CD45RA+CCR7+CD95+OX40+ Tscm 세포의 시험관내 용도.
일 실시형태에서, 자가면역 질환, HIV-1, 및 T-세포 악성종양의 바이오마커가 제공되며, 여기서 바이오마커는 CD45RA+CCR7+CD95+OX40+ Tscm 세포이다. 또 다른 실시형태에서, 바이오마커는 하기 본 명세서에서 개념 71 내지 80에 기술된 질환 중 임의의 것의 바이오마커이다. 또 다른 실시형태에서, Tscm 세포는 CD4+CD45RA+CCR7+CD95+OX40+ Tscm 세포이다.
개념 41. Tscm-매개된 질환 또는 병태의 바이오마커의 용도로서, 바이오마커는 CD45RA+CCR7+CD95+OX40+ Tscm 세포인, Tscm-매개된 질환 또는 병태(예를 들어, 질환 또는 병태는 대상체에서 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제를 사용하거나, 또는 항-OX40 또는 항-OX40L 항체 또는 이의 단편을 사용하여 치료 또는 예방될 수 있음)를 위한 진단법으로서의 시험관내에서의 용도.
일 실시형태에서, Tscm-매개된 질환은 하기 본 명세서에서 개념 71 내지 80에 기술된 것 중 임의의 것이다.
개념 42. 샘플 중의 T-세포의 집단에서 CD45RA+CCR7+CD95+OX40+ Tscm 세포를 감소시키면서, CD45RA+CCR7+CD95- Tn 세포를 유지시키는 방법으로서, 상기 방법은 상기 샘플을 유효량의 Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 작용제 또는 항-OX40 또는 항-OX40L 항체 또는 이의 단편과 접촉시키는 단계를 포함하는, 방법.
개념 1 내지 83에서 사용되는 바와 같이 본 명세서에서, 수준 또는 비율과 관련하여 "유지시킨다" 또는 "유지시키는"은 실질적으로 일정한 것으로서 기술될 수 있다. 실질적으로 일정한 수준은 샘플들 간의 30% 이내일 수 있다. 일 실시형태에서, 실질적으로 일정한 수준은 샘플들 간의 20% 이내의 변화이다. 일 실시형태에서, 실질적으로 일정한 수준은 샘플들 간의 15% 이내의 변화, 예컨대 샘플들 간의 10% 이내의 변화, 예를 들어, 샘플들 간의 5% 이내의 변화이다. 또 다른 실시형태에서, 실질적으로 일정한 수준은 수준이 통계학적으로 유의한 변화를 나타내지 않는 것이다. 일 실시형태에서, 실질적으로 일정한 수준은 95% 신뢰 수준(예를 들어, 97% 초과 또는 99% 초과)에 도달하는 것이다. "통계학적으로 유의한"은 본 명세서에서 개념 28에서 상기에 정의된 바와 같을 수 있다.
개념 43. 개념 42에 따른 방법으로서, 상기 Tscm 세포의 수준이 상기 샘플 중에서 감소되면서, 상기 Tn 세포의 수준이 적어도 유지되고, 임의로 샘플은 대상체로부터의 것인, 방법.
개념 44. 개념 2 내지 8, 10, 16, 20, 21, 23 내지 39, 42 또는 43 중 임의의 하나에 따른 방법, 개념 12, 17, 20, 21 또는 23 내지 25 중 임의의 하나에 따라서 사용하기 위한 작용제 또는 항체 또는 이의 단편, 개념 13, 14, 18 내지 20 또는 23 내지 25 중 임의의 하나에 따른 용도, 또는 개념 15에 따른 조성물로서, 작용제(예를 들어, 항체 또는 이의 단편)는 CD45RA+CCR7+CD95+OX40+ Tscm 세포의 비율을 감소시키는(예를 들어, Tscm 세포의 수준을 고갈 또는 감소시키는), 방법, 사용하기 위한 작용제 또는 항체 또는 이의 단편, 용도, 또는 조성물.
개념 45. 개념 1 내지 8, 10, 16, 20, 21, 23 내지 39 또는 42 내지 44 중 임의의 하나에 따른 방법 또는 이의 단편, 개념 12, 17, 20, 21, 23 내지 25, 또는 44 중 임의의 하나에 따라서 사용하기 위한 작용제 또는 항체 또는 이의 단편, 개념 13, 14, 18 내지 20 또는 23 내지 25 또는 44 중 임의의 하나에 따른 용도, 또는 개념 15 또는 개념 44에 따른 조성물로서, 작용제(예를 들어, 항체 또는 이의 단편)는 CD45RA+CCR7+CD95- Tn 세포를 유지시키는, 방법 또는 이의 단편, 사용하기 위한 작용제 또는 항체 또는 이의 단편, 용도 또는 조성물.
개념 46. 개념 42 또는 45에 따른 방법, 개념 45에 따라서 사용하기 위한 작용제 또는 항체 또는 이의 단편, 개념 45에 따른 용도, 또는 개념 45에 따른 조성물로서, Tn 세포는 건강한 공여자 또는 질환의 발병 이전의 상기 대상체로부터의 샘플 중의 상기 Tn 세포의 수준의 50% 이상의 수준에서 유지되는, 방법, 사용하기 위한 작용제 또는 항체 또는 이의 단편, 용도, 또는 조성물.
건강한 공여자는 바람직하게는 대상체에서 동일한 종이고, 예를 들어, 여기서 대상체는 인간이고, 가장 바람직하게는 공여자 또한 인간이다. 공여자는 또한 바람직하게는 대상체와 동일한 성별이다. 공여자는 바람직하게는 대상체와 유사한 연령 및 및 인종성을 갖는다.
개념 47. 개념 46에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tn 세포는 55% 이상(예컨대 60% 이상, 예를 들어 65% 이상, 예를 들어, 70% 이상)의 수준에서 유지되는, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 48. 개념 47에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tn 세포는 75% 이상(예컨대 80% 이상, 예를 들어 85% 이상, 예를 들어, 90% 이상)의 수준에서 유지되는, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 49. 개념 1 내지 8, 또는 42 내지 48 중 임의의 하나에 따른 방법, 개념 44 내지 48중 임의의 하나에 따라서 사용하기 위한 작용제 또는 항체 또는 이의 단편, 개념 38 내지 41 중 임의의 하나에 따른 용도, 또는 개념 44 내지 48 중 임의의 하나에 따른 조성물로서, Tscm 세포는 건강한 공여자 또는 질환의 발병 이전의 상기 대상체로부터의 샘플 중의 상기 Tscm 세포의 수준의 50% 미만의 수준으로 고갈 또는 감소되는, 방법, 사용하기 위한 작용제 또는 항체 또는 이의 단편, 용도, 또는 조성물.
개념 50. 개념 49에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, Tscm 세포는 45% 미만(예컨대 40% 미만, 예를 들어 35% 미만, 예를 들어, 30% 미만 또는 25% 미만)의 수준으로 고갈 또는 감소되는, 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물.
개념 51. 개념 50에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, Tscm 세포는 20% 미만(예컨대 15% 미만, 예를 들어 10% 미만의 수준으로 고갈 또는 감소되는, 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물.
개념 52. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, 항체 또는 단편은 OX40(특히 인간 OX40)을 특이적으로 결합하는 고갈성 항체 또는 단편이고, 임의로 항체는 향상된 ADC, ADCC 및/또는 CDC를 위해서 조작된, 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물.
Fc-매개된 효과의 효력은 다양한 설정된 기술에 의해서 Fc 도메인을 조작함으로써 향상될 수 있다. 그러한 방법은 특정 Fc-수용체에 대한 친화도를 증가시키고, 따라서 활성 향상의 잠재적인 다양한 프로파일을 생성한다. 이는 하나 또는 몇몇 아미노산 잔기의 변형에 의해서(예를 들어, 문헌[Lazar et al., 2006, Proc. Natl. Acad. Sci. U.S.A., Mar 14; 103(11):4005-10]에 기술된 바와 같음) 또는 Fc 도메인의 자연적인 글리코실화 프로파일을 변경함으로써, 예를 들어 푸코실화되거나 탈-푸코실화된 변이체(문헌[Natsume et al., 2009,Drug Des Devel Ther.,3:7-16]에 기술된 바와 같음) 하에서 생성함으로써 달성될 수 있다. 예를 들어, ADCC를 증가시키기 위해서, 경첩(hinge) 영역에서 잔기는 Fc-감마 RIII에 대한 결합을 증가시키도록 변경될 수 있다(예를 들어, 문헌[Shields et al, 2001,J Biol Chem., Mar 2; 276(9):6591-604] 참고).
동일하게, CDC의 향상은 전통적인 보체 활성화 케시케이드의 제1 성분인 C1q에 대한 친화도를 증가시키는 아미노산 변화에 의해서 달성될 수 있다(문헌 [Idusogie et al.,J. Immunol., 2001;166:2571-2575] 참고). 또 다른 접근법은 C1q에 대한 IgG3의 더 높은 친화도를 활용하는 인간 IgG1 및 인간 IgG3 조각으로부터 생성된 키메릭 Fc 도메인을 생성하는 것이다(Natsume et al., 2008, Cancer Res., 68: 3863-3872).
항체는 항체가 컨쥬게이팅될 수 있는 독소를 통해서 그의 효과를 나타내는 표적화 항체(예컨대 항-OX40 또는 항-OX40L 항체)일 수 있다. 그러한 독소는 그것이 표적화한 세포를 선택적으로 사멸 또는 제거할 것이다. 적합한 면역컨쥬게이트가 본 명세서 제90면, 및 제114면 내지 제118면, 및 제134면(특히 제114면 내지 제116면)에 기술되어 있다.
따라서, 일 실시형태에서, 항체 또는 이의 단편은 탈-푸코실화된다. 또 다른 실시형태에서, 항체 또는 이의 단편은 ADCC 및/또는 CDC 기능성을 향상시키는 경첩 또는 Fc 영역에서 하나 이상의 돌연변이를 함유한다.
고갈 및/또는 ADCC 및/또는 CDC 기능성을 측정하는 방법은 본 명세서에서 기술된 바와 같을 수 있거나, 관련 기술 분야의 통상의 기술자에게 널리 공지된 바와 같다.
OX40 항체는 WO2014/148895(바이오세록스 프로덕츠 앤드 얀센 파마슈티컬즈(Biocerox Products & Janssen Pharmaceuticals); 본 명세서에 참고로 포함된 구체적인 서열에 대해서는 제138면 내지 제139면을 참고하기 바람), WO2013/068563 (바이오세록스 프로덕츠 앤드 얀센 파마슈티컬즈; 본 명세서에 참고로 포함된 구체적인 서열에 대해서는 제138면 내지 제139면을 참고하기 바람), WO2013/130102 및 WO2013/119202(프로비던스 헬쓰 앤드 서비스즈(Providence Health & Services) - 오레곤(Oregon), 문헌[Weinberg, A.D., et al., J. Immunother., 29, 575-585 (2006)]에 기술된 바와 같은 mAb 9B12 및 본 명세서에 참고로 포함된 IL-2을 갖는 융합체), WO2013/038191(바이오세로스 비.브이.(Bioceros B.V.); 본 명세서에 참고로 포함된 구체적인 서열에 대해서는 청구항 4 내지 11을 참고하기 바람), WO2013/028231(보드 오브 레전츠, 더 유니버시티 오브 텍사스 시스템(Board of Regents, the University of Texas System); 본 명세서에 참고로 포함된 구체적인 항체 서열에 대해서는 청구항 1 내지 12을 참고하기 바람), WO2013/008171(글렌마크 파마슈티컬즈 에스.에이.(Glenmark Pharmaceuticals S.A.); 본 명세서에 참고로 포함된 구체적인 서열에 대해서는 청구항 1, 2, 5 내지 12, 16 내지 21 및 28 내지 29를 참고하기 바람), WO2012/027328(보드 오브 레전츠, 더 유니버시티 오브 텍사스 시스템; 본 명세서에 참고로 포함된 구체적인 서열에 대해서는 청구항 1 내지 11을 참고하기 바람), WO2010/096418(유씨비 파마 에스.에이.(UCB Pharma S.A.); 본 명세서에 참고로 포함된 구체적인 서열에 대해서는 청구항 1 내지 9 및 11 내지 14를 참고하기 바람), WO2009/079335(메다렉스, 인코퍼레이티드(Medarex, Inc) 및 파이자, 인코퍼레이티드(Pfizer, Inc); 본 명세서에 참고로 포함된 구체적인 서열에 대해서는 청구항 1 내지 9 및 14 내지 17을 참고하기 바람), WO2008/106116(제넨테크, 인코퍼레이티드(Genentech, Inc); 본 명세서에 참고로 포함된 구체적인 서열에 대해서는 청구항 1 내지 12를 참고하기 바람), WO2007/062245(기린 비어 가부시끼 가이샤(Kirin Beer Kabushiki Kaisha) 및 라 욜라 인스티튜트 포 알러지 앤드 이뮤놀로지(La Jolla Institute for Allergy and Immunology)); 본 명세서에 참고로 포함된 구체적인 항체 기탁 번호에 대해서는 청구항 12 및 구체적인 항체 서열에 대해서는 청구항 16을 참고하기 바람), WO03/106498(크루셀 홀란드 비.브이.(Crucell Holland B.V.); 본 명세서에 참고로 포함된 구체적인 서열에 대해서는 청구항 3 및 4를 참고하기 바람)에 기술된 바와 같을 수 있다.
보다 일반적으로 항-OX40 항체는 WO99/42585, WO95/21251, WO95/21915 및 WO95/12673에 기술되어 있다.
개념 53. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, 항체는 길항작용적 항체 또는 차단 항체인, 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물.
길항작용 또는 차단 기능의 측정 방법은 본 명세서에서 기술된 바와 같을 수 있거나, 관련 기술 분야의 통상의 기술자에게 널리 공지된 바와 같다. 예를 들어, 시험관내 기술은 SPR 및/또는 ELISA를 포함하고, 이것은 본 명세서에 다른 곳에 기술되어 있다.
개념 54. 개념 53에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, 항체는 OX40L(특히 인간 OX40L)에 특이적으로 결합하는, 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물.
OX40L 항체는 본 명세서에서 기술된 바와 같은 임의의 항체 또는 단편일 수 있다. 일 실시형태에서, OX40L 항체는 문헌[Matsumura et al., J Immunol.(1999), 163:3007]에 기술된 길항제 항-인간 OX40L(gp34) 항체 ik-1이다.
개념 55. 개념 56에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, 항체는 예를 들어, SPR 또는 ELISA를 사용하여 측정되는 바와 같이 OX40L에 대한 OX40의 특이적인 결합에 길항작용하는, 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물.
SPR 및 ELIS 방법은 명세서에서 다른 부분에 기술된 바와 같을 수 있다.
개념 56. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, 항체는 인간화 항체, 인간 항체 또는 완전 인간 항체인 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물.
다른 항체 구축물은 본 명세서에서 기술된 바와 같을 수 있다.
개념 57. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, 항체는 다중특이적인 항체(예를 들어, 이중-특이적인 항체), 인트라바디, 단일-쇄 Fv 항체(scFv), 낙타화 항체, Fab 단편, F(ab') 단편, 다이설파이드-연결된 Fv(sdFv), 항-이디오타입(항-Id) 항체, 및 이의 에피토프-결합 단편의 목록으로부터 선택된 항체의 단편인, 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물.
개념 58. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, 항체 또는 단편은 동종 조혈 줄기 세포 이식의 레서스 마카크 모델에서 12일에 80%를 초과하는 줄기 세포 공여자 키메리즘을 가능하게 하는, 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물.
개념 59. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, 항체 또는 단편은 14일의 과성장 기간으로 론자 버전 8 공급 시스템을 사용하여 유가 과성장 배양액 중에서 1.5g/L를 초과하는 수준으로 론자 지에스-엑스시드(상표명) 중에서 안정하게 형질주입된 풀로서 발현하는, 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물.
개념 60. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, 항체 또는 이의 단편은 16 내지 27개의 아미노산의 HCDR3을 포함하고, 인간 VH 유전자 조각, 인간 D 유전자 조각 및 인간 JH 유전자 조각의 재조합으로부터 유래되고, 인간 JH 유전자 조각은 IGHJ6(예를 들어, IGHJ6*02)인, 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물.
개념 61. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, 항체 또는 이의 단편은 하기로부터 선택된 HCDR3을 포함하는, 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물:
a. 항체 2D10의 HCDR3(서열번호 40 또는 서열번호 46);
b. 항체 10A7의 HCDR3(서열번호 8 또는 서열번호 14);
c. 항체 09H04의 HCDR3(서열번호 72 또는 서열번호 78);
d. 항체 19H01의 HCDR3(서열번호 100 또는 서열번호 106);
e. WO2011/073180(아블링스(Ablynx), 그것에서 서열번호 161 내지 167, 이것은 본 명세서에 참고로 포함됨)에 개시된 나노바디 중 임의의 것의 CDR3;
f. WO2006/029879(로슈(Roche)/제넨테크, 그것에서 서열번호 33 내지 38, 이것은 본 명세서에 참고로 포함됨)에 개시된 항체 중 임의의 것의 HCDR3; 또는
g. US7,812,133(제넨테크, 그것에서 서열번호 11 또는 12, 이것은 본 명세서에 참고로 포함됨)에 개시된 항체 중 임의의 것의 HCDR3.
개념 62. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, 항체 또는 이의 단편은 하기를 포함하는 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물:
a. 항체 2D10의 CDR(CDRH3의 경우 서열번호 40 또는 서열번호 46, CDRH2의 경우 서열번호 38 또는 서열번호 44, CDRH1의 경우 서열번호 36 또는 서열번호 42, CDRL1의 경우 서열번호 50 또는 서열번호 56, CDRL2의 경우 서열번호 52 또는 서열번호 58 및 CDRL3의 경우 서열번호 54 또는 서열번호 60);
b. 항체 10A7의 CDR(CDRH3의 경우 서열번호 8 또는 서열번호 14, CDRH2의 경우 서열번호 6 또는 서열번호 12, CDRH1의 경우 서열번호 4 또는 서열번호 10, CDRL1의 경우 서열번호 18 또는 서열번호 24, CDRL2의 경우 서열번호 20 또는 서열번호 26 및 CDRL3의 경우 서열번호 22 또는 서열번호 28);
c. 항체 09H04의 CDR(CDRH3의 경우 서열번호 72 또는 서열번호 78, CDRH2의 경우 서열번호 70 또는 서열번호 76, CDRH1의 경우 서열번호 68 또는 서열번호 74, CDRL1의 경우 서열번호 82 또는 서열번호 88, CDRL2의 경우 서열번호 84 또는 서열번호 90 및 CDRL3의 경우 서열번호 86 또는 서열번호 92);
d. 항체 19H01의 CDR(CDRH3의 경우 서열번호 100 또는 서열번호 106, CDRH2의 경우 서열번호 98 또는 서열번호 104, CDRH1의 경우 서열번호 96 또는 서열번호 102, CDRL1의 경우 서열번호 110 또는 서열번호 116, CDRL2의 경우 서열번호 112 또는 서열번호 118 및 CDRL3의 경우 서열번호 114 또는 서열번호 120);
e. WO2011/073180(아블링스: CDR3의 경우 그것에서 서열번호 161 내지 167; CDR2의 경우 그것에서 서열번호 147 내지 153; 및 CDR1의 경우 그것에서 서열번호 133 내지 139, 서열은 본 명세서에 참고로 포함됨)에 개시된 나노바디 중 임의의 것의 CDR;
f. WO2006/029879(로슈/제넨테크: CDRH3의 경우 그것에서 서열번호 33 내지 38; CDRH1의 경우 그것에서 서열번호 21 내지 25 및 CDRH2의 경우 그것에서 서열번호 26 내지 32; CDRL1의 경우 그것에서 서열번호 39 내지 44; CDRL2의 경우 그것에서 서열번호 45 내지 50; 및 CDRL3의 경우 그것에서 서열번호 51 내지 57, 서열은 본 명세서에 참고로 포함됨)에 개시된 항체 중 임의의 것의 CDR; 또는
g. US7,812,133(제넨테크: CDRH3의 경우 그것에서 서열번호 11 또는 12; CDRH1의 경우 그것에서 서열번호 7 또는 8 및 CDRH2의 경우 그것에서 서열번호 9 또는 10; CDRL1의 경우 그것에서 서열번호 1 또는 2; CDRL2의 경우 그것에서 서열번호 3 또는 4; 및 CDRL3의 경우 그것에서 서열번호 5 또는 6, 서열은 본 명세서에 참고로 포함됨)에 개시된 항체 중 임의의 것의 CDR.
개념 63. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, 항체 또는 이의 단편은 하기로부터 선택된 VH 및/또는 VL 도메인을 포함하는, 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물:
a. 항체 2D10의 VH 및/또는 VL 도메인(VH의 경우 서열번호 34 및/또는 VL의 경우 서열번호 48);
b. 항체 10A7의 VH 및/또는 VL 도메인(VH의 경우 서열번호 2 및/또는 VL의 경우 서열번호 16);
c. 항체 09H04의 VH 및/또는 VL 도메인(VH의 경우 서열번호 66 및/또는 VL의 경우 서열번호 80);
d. 항체 19H01의 VH 및/또는 VL 도메인(VH의 경우 서열번호 94 및/또는 VL의 경우 서열번호 108);
e. WO2011/073180(아블링스, 그것에서 서열번호 177 내지 185, 199 내지 226, 서열은 본 명세서에 참고로 포함됨 [본 명세서에서 서열번호 177 내지 213으로서 재생산됨];
f. WO2006/029879(로슈/제넨테크, VH 도메인의 경우 그것에서 서열번호 2, 4, 6, 8, 10, 12, 17, 19 및 20; 및 VL 도메인의 경우 그것에서 서열번호 1, 3, 5, 7, 9, 11, 16 및 18, 서열은 본 명세서에 참고로 포함됨 [본 명세서에서 서열번호 214 내지 230으로서 재생산됨])에 개시된 항체 중 임의의 것의 VH 및/또는 VL 도메인; 또는
g. US7,812,133(제넨테크, VH 도메인의 경우 그것에서 서열번호 15 및 16; 및 VL 도메인의 경우 그것에서 서열번호 13 및 14, 서열은 본 명세서에 참고로 포함됨 [본 명세서에서 서열번호 231 내지 234로서 재생산됨])에 개시된 항체 중 임의의 것의 VH 및/또는 VL 도메인.
개념 64.
임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물로서, 항체는 옥셀루맙인, 방법, 사용하기 위한 항체 또는 단편, 용도 또는 조성물.
개념 65. 임의의 상기 개념에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tscm 세포 및/또는 Tn 세포는 CD4+인, 임의의 상기 개념에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
또 다른 실시형태에서, Tscm 세포 및/또는 Tn 세포는 CD8+이다.
개념 66. 개념 64에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tscm 세포 및/또는 Tn 세포는 순환 T-세포인, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 67. 개념 65에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tscm 세포 및/또는 Tn 세포는 혈액, 예를 들어, 말초 혈액 중의 샘플 중에 존재하는, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
혈액 중에 존재하는 T-세포는 단리 및 특징분석이 비교적 간단하지만, 대상체의 조직 중에 존재하는 T-세포는 일반적으로 단리시키기가 더 어렵다. 즉, 다양한 조직(예컨대 피부, GI관, 예를 들어, 장의 조직, 및 염증 관절, 예를 들어, 활막의 조직)으로부터 T-세포를 단리시키는 것이 가능할 수 있다.
개념 68. 개념 9 내지 11, 16, 20 내지 39 또는 43 내지 67 중 임의의 하나에 따른 방법, 개념 12, 17, 20, 21, 23 내지 25 또는 44 내지 67 중 임의의 하나에 따라서 사용하기 위한 작용제 또는 항체 또는 단편, 개념 13, 14, 18 내지 20 또는 23 내지 25 또는 44 내지 67 중 임의의 하나에 따른 용도, 또는 개념 15 또는 44 내지 67 중 임의의 하나에 따른 조성물로서, 대상체는 인간 환자인, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도, 또는 조성물.
개념 69. 개념 68에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, 대상체는 Tscm-매개된 질환 또는 병태의 위험이 있는, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 70. 개념 68에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, 대상체는 Tscm-매개된 질환 또는 병태를 갖는, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 71. 임의의 상기 개념에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tscm-매개된 질환 또는 병태는 CD45RA+CCR7+CD95+OX40+ Tscm 세포에 의해서 매개된, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 72. 개념 68 내지 70 중 임의의 하나에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tscm-매개된 질환 또는 병태는 50:50을 초과하는 CD45RA+CCR7+CD95+OX40+ Tscm 세포:CD45RA+CCR7+CD95- Tn 세포의 비를 갖는 것을 특징으로 하는, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
또 다른 실시형태에서, 질환 또는 병태는 개념 23 내지 25 중 임의의 것에 언급된 바와 같은 Tscm 세포:Tn 세포의 비를 갖는 것을 특징으로 한다.
개념 73. 개념 72에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tscm-매개된 질환 또는 병태는 60:40 초과, 또는 70:30 초과, 또는 75:25 초과, 예컨대 70:30 초과의 Tscm:Tn의 비를 갖는 것을 특징으로 하는, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 74. 개념 73에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tscm-매개된 질환 또는 병태는 80:20 초과, 또는 85:15 초과, 예를 들어 90:10 초과, 예를 들어, 95:5 초과의 Tscm:Tn의 비를 갖는 것을 특징으로 하는, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 75. 임의의 상기 개념에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tscm-매개된 질환 또는 병태는 자가면역 질환, HIV-1, 및 T-세포 악성종양으로부터 선택되는, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 76. 개념 75에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tscm-매개된 질환 또는 병태는 GvHD, 이식 거부, 건선, 류마티스 관절염, 전신 홍반 루푸스, 다발성 경화증, 소아 피부근염, T-세포 림프종 및 T-세포 백혈병으로부터 선택되는, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 77. 개념 76에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tscm-매개된 질환 또는 병태는 GvHD 또는 이식 거부인, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 78. 개념 76에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, 이식은 세포, 조직 또는 기관 이식(예를 들어, 간, 폐, 심장, 신장 또는 장), 또는 혈액 이식(예를 들어, 자가형 또는 동종이형)이고, 예를 들어 혈액은 골수-유래되거나, 제대혈(배꼽) 유래되거나, 또는 말초-혈액 유래된, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
일 실시형태에서, 이식은 CAR T-세포 이식(키메릭 항원 수용체)이다.
개념 79. 개념 76에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tscm-매개된 질환 또는 병태는 T-세포 비-호지킨 림프종, 말초 T-세포 림프종(PTCL), 역형성 큰세포 림프종(ALCL), 혈액면역아세포성 림프종, 피부 T-세포 림프종, 성인 T-세포 백혈병/림프종, 아세포성 NK-세포 림프종, 장질환-유형 T-세포 림프종, 헤마토스플렌(hematosplenic) 감마-델타 T-세포 림프종, 림프아구 림프종(T-LBL) 및 코 NK/T-세포 림프종으로부터 선택된 T-세포 림프종인, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 80. 개념 76에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, Tscm-매개된 질환 또는 병태는 대형 과립 림프구성 백혈병(LGLL), T-세포 전림프구성 백혈병(T-PLL), T-세포 급성 림프아구 백혈병(T-ALL) 및 세자리 증후군(Sezary syndrome)으로부터 선택된 T-세포 백혈병인, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 81. 인간에게 추가 치료제를 투여하는 것을 추가로 포함하는 임의의 상기 개념에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물로서, 임의로 추가 치료제는 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트, 특히 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, CTLA4-Fc 분자(예를 들어, 아바타셉트), 항-CD40L 항체, 항-LFA1 항체, 항-CD52 항체(예를 들어, 알렘투주맙), 사이클로포스파미드 및 항-흉선세포 글로불린으로 이루어진 군으로부터 독립적으로 선택되는, 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
일 실시형태에서, 추가 치료제는 칼시뉴린 억제제(예를 들어, 타크롤리무스, 사이클로스포린), mTOR 억제제(예를 들어, 라파마이신(시롤리무스)), 및 항증식제(예를 들어, 마이코페놀레이트 모페틸, 사이클로포스파미드)로 이루어진 군으로부터 독립적으로 선택된다.
일 실시형태에서, 추가 치료제는 IL-2 신호전달을 조절하는 면역억제제(예를 들어, 타크롤리무스, 사이클로스포린, 라파마이신(시롤리무스), 및 항-CD25 항체(예를 들어, 바실릭수맙, 다클리주맙)로 이루어진 군으로부터 독립적으로 선택된다.
일 실시형태에서, 추가 치료제는 라파마이신(시롤리무스)이다. 또 다른 실시형태에서, 추가 치료제는 타크롤리무스이다. 또 다른 실시형태에서, 추가 치료제는 타크롤리무스와 메토트렉세이트의 조합물이다. 또 다른 실시형태에서, 추가 치료제는 사이클로스포린이다. 또 다른 실시형태에서, 추가 치료제는 사이클로스포린과 메토트렉세이트의 조합물이다. 또 다른 실시형태에서, 추가 치료제는 사이클로포스파미드이다. 또 다른 실시형태에서, 추가 치료제는 마이코페놀레이트 모페틸이다.
개념 82. 인간에게 치료 유효량의 라파마이신을 투여하는 것을 추가로 포함하는 임의의 상기 개념에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
개념 83. 인간에게 치료 유효량의 타크롤리무스를 투여하는 것을 추가로 포함하는 임의의 상기 개념에 따른 방법, 사용하기 위한 작용제 또는 항체 또는 단편, 용도 또는 조성물.
본 발명은 놀랍게도 항-OX40L 항체가 추가 치료제와의 조합 요법의 일부로서 투여되는 경우 상승작용적 효과를 제공할 수 있다는 것을 발견하였다. 이를 위해서, 추가 개념이 하기에 제공된다:
개념 101. 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제와 조합하여 대상체에서 OX40L-매개된 질환 또는 병태의 위험을 치료 또는 감쇠시키는 데 사용하기 위한 항-OX40L 항체 또는 이의 단편.
개념 102. 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제와 조합하여 대상체에서 OX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한 항-OX40L 항체 또는 이의 단편의 용도.
개념 103. 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제와 조합하여 대상체에서 OX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한 의약의 제조에서의 항-OX40L 항체 또는 이의 단편의 용도.
개념 104. 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제와 조합하여 대상체에서 OX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한 항-OX40L 항체 또는 이의 단편을 포함하는 조성물.
개념 105. 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제와 조합하여 치료 유효량의 항-OX40L 항체 또는 이의 단편을 상기 인간에게 투여하는 것을 포함하는 대상체에서 OX40L-매개된 질환 또는 병태를 치료 또는 예방하는 방법으로서, 이에 의해서 OX40L-매개된 질환 또는 병태가 치료 또는 예방되는, 방법.
본 명세서에서 개념의 임의의 것에서, 조합물은 OX40L-매개된 질환의 예방에서 사용될 수 있다. 개념 중 임의의 것에서, 조합물은 OX40L-매개된 질환의 위험을 감쇠시키기 위해서 사용될 수 있다. 개념 중 임의의 것은 OX40L-매개된 질환의 치료에서 사용될 수 있다.
본 명세서에서 기술된 바와 같이 "조합"은 본 명세서에 다른 곳, 예를 들어 명세서 제100면, 제105면 내지 제107면, 및 제119면 내지 제120면에 정의된 바와 같을 수 있다. 일 실시형태에서, 질환은 류마티스 관절염 또는 건선이고, 추가 치료제는 항-IL-17 항체(예컨대 브로달루맙, 세쿠키누맙 및 익세키주맙)이다. 조합물은 부수적으로 또는 순차적으로 투여될 수 있다. 투여는 본 명세서에 개시된 방법 중 임의의 것을 통해서, 예를 들어 본 명세서 제130면 전반부의 "투여 및 투약 방법"이라는 제목의 단락에 논의된 바와 같이 일어날 수 있다.
본 명세서에서 개념의 임의의 것에서 사용되는 바와 같이, OX40L-매개된 질환의 "치료"는 상기 OX40L-매개된 질환 중의 하나 이상의 증상(들)의 감쇠를 포함한다. 치료는 명세서에서 다른 부분 예를 들어 명세서 제107면, 및 "키트"라는 제목의 단락(명세서 제149면, 특히 제152면의 전반부)에 기술된 바와 같이 이해될 수 있다.
조혈 줄기 세포 이식(HSCT)과 관련된 GvHD의 조절에서 면역억제 약물 중재는 만성 질환을 갖는 환자를 치료하기 위해서 투여될 수 있다. GvHD 등급화는 하기에 기술된 바와 같이 결정될 수 있다.
일 실시형태에서, 투여는 OX40L-매개된 질환의 위험을 예방 또는 감쇠시킨다. 본 명세서에서 개념에서 사용되는 바와 같이, OX40L-매개된 질환의 "예방"(또는 "예방하다" 또는 "예방하는" 등)은 상기 OX40L-매개된 질환의 하나 이상의 증상(들)의 예방을 포함한다. 예방은 본 명세서에 제공된 치료제의 투여 조합물(예를 들어, 예방제 및/또는 치료제의 조합물)로부터 유발되는, OX40L-매개된 질환 및/또는 이에 관련된 증상의 전개, 재발, 발병 또는 퍼짐의 전체 억제 또는 부분적인 억제를 말할 수 있다. 예방은 본 명세서에 다른 부분에 개시된 바와 같이 해석될 수 있다.
조혈 줄기 세포 이식(HSCT)과 관련된 GvHD의 조절에서 면역억제 약물 중재는 위험이 있다고 알려진 환자에서 질환을 예방하기 위해서 투여될 수 있다.
따라서, 일 실시형태에서, OX40L-매개된 질환 또는 병태의 발병 이전에 예방-유효 용량이 투여된다. 본 명세서에서 개념에서 사용되는 바와 같이, 대상체가 상기 질환 또는 병태와 통상적으로 관련된 증상이 나타나지 않거나 또는 대상체가 임의의 종래의 방법에 의해서 그러한 질환 또는 병태를 갖는 것으로서 진단되지 않은 경우, 대상체는 "OX40L-매개된 질환 또는 병태의 발병 이전"인 것으로 결정될 수 있다. 또 다른 실시형태에서, 질환의 발병 이전의 투여는 "선취(pre-emptive) 치료"라 지칭될 수 있는데, 이는 질환을 전개의 위험이 있는 개체에서 추가 치료제(예컨대 면역억제제) 및/또는 본 발명의 항-OX40L 항체의 사용을 말하며, 여기서 임상적으로 관련된 GvHD의 출현이 임박한 조기 징후가 존재할 수 있다. 예를 들어, 실험 또는 예측 혈청 또는 세포 바이오마커가 선취 GvHD 치료의 개시를 위한 최적의 시간을 나타낼 수 있다.
예를 들어, 인간에서 급성 GvHD의 징후 및 증상의 존재는 예컨대 프르제피오카(Przepiorka) 등의 문헌에 기술된 표준화된 규모에 따라서 단계화 및 등급화될 수 있다. 영장류, 예컨대 레서스 마카크 원숭이에서, 급성 GvHD의 징후 및 증상의 존재는 예컨대 본 명세서 실시예 7에 기술된 표준화된 규모에 따라서 단계화 및 등급화될 수 있다. 유사한 질환 등급 규모가 또한 다른 관련 질환, 예컨대 류마티스 관절염 및 염증성 장 질환을 위한 일상적인 임상 용도로 존재한다.
"예방" 또는 "예방조치"는 기술된 바와 같은 항-OX40L 항체의 투여량 및 투여 형태와 함께 본 명세서에서 양상 94에 기술된 바와 같을 수 있다. 예방제는 명세서 제102면 내지 제103면에 기술된 방법 중 임의의 것에서 사용될 수 있다.
OX40L-매개된 질환 또는 병태는 Tscm-매개된 질환 또는 병태(상기 본 명세서에서 개념 75 내지 80 참고)로서 본 명세서 다른 곳에 정의된 것을 비롯하여, 본 명세서에 언급된 질환 또는 병태 중 임의의 것일 수 있다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 본 명세서에서 기술된 바와 같은 양상 12, 12a, 69, 69a, 71, 72, 72a, 90 내지 93 중 임의의 것에 기술된 바와 같다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 본 명세서에서 기술된 바와 같은 양상 12, 12a, 69, 69a, 71, 72, 72a, 90 내지 93 중 임의의 것에 기술된 바와 같다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 본 명세서, 예를 들어 명세서 제103면 내지 제104면, 또는 제131면에서 기술된 바와 같은 hOX40L-매개된 질환 또는 병태이다. 또 다른 실시형태에서, OX40L-매개된 질환 또는 병태는 본 명세서 제130면 전반부의 "투여 및 투약 방법"이라는 제목의 단락에 기술된 바와 같다. 바람직한 실시형태에서, 질환 또는 병태는 GvHD 또는 이식 거부, 특히, GvHD이다. 또 다른 실시형태에서, OX40L-매개된 질환 또는 병태는 크론병이다. 또 다른 실시형태에서, OX40L-매개된 질환 또는 병태는 염증성 장 질환(IBD)이다. 또 다른 실시형태에서, OX40L-매개된 질환 또는 병태는 궤양성 대장염이다. 또 다른 실시형태에서, OX40L-매개된 질환 또는 병태는 건선이다.
명세서에 기술된 개념 중 임의의 것에서, 항-OX40L 항체 및/또는 추가 치료제가 대상체에 투여된다. 투여는 본 명세서에 기술된 임의의 방법에 의해서, 예를 들어 각각 명세서 제93면 또는 제118면 및 제130면 전반부의 "약제학적 조성물" 및 "투여 및 투약 방법"의 제목 부분에 기술된 바와 같이 일어날 수 있다. 일 실시형태에서, 본 발명의 항-OX40L 항체는 정맥내로 투여된다. 일 실시형태에서, 본 발명의 항-OX40L 항체는 피하로 투여된다.
일 실시형태에서, 추가 치료제는 라파마이신(시롤리무스)이고, 경구 투여된다. 일 실시형태에서, 추가 치료제는 타크롤리무스이고, 경구 투여된다. 일 실시형태에서, 추가 치료제는 메토트렉세이트이고, 경구 및/또는 정맥내로 투여된다. 일 실시형태에서, 추가 치료제는 사이클로스포린이고, 정맥내 및/또는 경구 투여된다. 일 실시형태에서, 추가 치료제는 사이클로포스파미드이고, 정맥내 및/또는 경구 투여된다. 일 실시형태에서, 추가 치료제는 메틸 프레드니솔론이고, 경구 및/또는 정맥내로 투여된다.
개념 106. 개념 101 내지 105 중 임의의 하나에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 대상체는 적어도 14일, 또는 적어도 21일, 또는 적어도 28일, 또는 적어도 40일, 또는 적어도 50일, 또는 적어도 60일의 치료후 또는 예방조치후 생존 시간을 갖는, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 107. 개념 101 내지 105 중 임의의 하나에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 예방조치후, 대상체는 적어도 7일, 또는 적어도 14일, 또는 적어도 21일, 또는 적어도 28일, 또는 적어도 40일, 또는 적어도 50일, 또는 적어도 60일의 무병 기간을 갖는, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 108. 개념 101 내지 105 중 임의의 하나에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 치료후, 대상체는 적어도 7일, 또는 적어도 14일, 또는 적어도 21일, 또는 적어도 28일, 또는 적어도 40일, 또는 적어도 50일, 또는 적어도 60일의 질환 무진행 기간을 갖는, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 109. 개념 106 내지 108 중 임의의 하나에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 생존일수, 무질환일수, 또는 질환 무진행일수는 적어도 2개월, 또는 적어도 3개월, 또는 적어도 4개월, 예를 들어, 적어도 5개월, 예컨대 적어도 6개월인, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 110. 개념 109에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 생존일수, 무질환일수, 또는 질환 무진행일수는 적어도 9개월, 또는 적어도 1년인 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 111. 예방-유효량의 항-OX40L 항체를 투여하고, 예방-유효량의 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여함으로써, 대상체에서 OX40L-매개된 질환 또는 병태의 발병을 예방하는 방법으로서, OX40L-매개된 질환 또는 병태의 발병이 예방되는, 방법.
"예방-유효"라는 것은, 그 용량이 X40L-매개된 질환 또는 병태의 위험을 예방 또는 감쇠시키기에 유효한 것을 의미한다.
일 실시형태에서, OX40L-매개된 질환 또는 병태의 위험을 감쇠시키기 위해서 조합물이 사용될 수 있다. 개념 111에서, 본 발명의 항-OX40L 항체 및 추가 치료제는 환자에게 예방적으로 투여될 수 있고, 투여는 순차적으로 또는 동시에 일어날 수 있다. 투여 요법 및 투여 모드는 추가 치료제를 위해서 의료진에 의해서 일반적으로 또는 전통적으로 투여되는 것일 수 있다. 투여 요법 및 투여 모드는 본 발명의 항-OX40L 항체를 위해서 의료진에 의해서 일반적으로 또는 전통적으로 투여되는 것일 수 있다. 그러나, 두 작용제의 병행 사용은 작용제를 단독으로 사용하는 것에 비해서 개선된 예방 조치를 유발할 것이라고 예상된다.
개념 112. 예방-유효량의 항-OX40L 항체를 투여하고, 치료-유효량의 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여함으로써 대상체에서 OX40L-매개된 질환 또는 병태를 치료하는 방법으로서, OX40L-매개된 질환 또는 병태의 발병이 치료되는, 방법.
"치료 유효"라는 것은, OX40L-매개된 질환 또는 병태를 치료하기에 유효한 용량을 의미한다. 유효는 본 명세서 제96면 내지 제97면, 또는 제152면에 정의된 바와 같을 수 있고, 본 명세서에서 제118면 전반부의 "약제학적 조성물"이라는 제목 단락에 기술된 바와 같은 혈청 농도를 제공할 수 있다.
개념 112에서, 본 발명의 항-OX40L 항체는 환자에게 투여될 수 있지만, 예방조치임에도, OX40L-매개된 질환 또는 병태의 발병(발병은 본 발명의 항체가 제공되지 않은 환자에 비해서 수일 또는 수주 지연될 수 있음)이 일어난다. 이 경우, 치료-유효량의 추가 치료제가 질환 또는 병태를 치료하기 위해서 투여될 수 있다.
개념 113. 치료-유효량의 항-OX40L 항체를 투여하고, 예방-유효량의 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여함으로써, 대상체에서 OX40L-매개된 질환 또는 병태를 치료하는 방법으로서, OX40L-매개된 질환 또는 병태가 치료되는, 방법.
개념 113에서, 추가 치료제는 환자에게 투여될 수 있지만, 예방조치임에도, OX40L-매개된 질환 또는 병태의 발병(발병은 본 발명의 항체가 제공되지 않은 환자에 비해서 수일 또는 수주 지연될 수 있음)이 일어난다. 이 경우, 치료-유효량의 본 발명의 항-OX40L 항체가 질환 또는 병태를 치료하기 위해서 투여될 수 있다.
개념 114. 치료-유효량의 항-OX40L 항체를 투여하고, 치료-유효량의 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여함으로써, 대상체에서 OX40L-매개된 질환 또는 병태를 치료하는 방법으로서, X40L-매개된 질환 또는 병태가 치료되는, 방법.
개념 114에서, 본 발명의 항-OX40L 항체 및 추가 치료제 둘 다는 OX40L-매개된 질환 또는 병태의 임상적 징후가 존재할 때까지 투여되지 않는다. 두 작용제의 조합 치료는 작용제 단독에 비해서 추가 이익을 제공할 수 있다.
개념 115. 개념 111 또는 개념 113에 따른 방법으로서, 추가 치료제는 라파마이신(시롤리무스), 타크롤리무스, 타크롤리무스와 메토트렉세이트의 조합물, 사이클로포스파미드, 사이클로스포린, 및 사이클로스포린과 메토트렉세이트의 조합물로부터 독립적으로 선택되는, 방법.
일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 라파마이신(시롤리무스)이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 타크롤리무스이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 타크롤리무스와 메토트렉세이트의 조합물이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 사이클로포스파미드이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 사이클로스포린이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 사이클로스포린과 메토트렉세이트의 조합물이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 마이코페놀레이트 모페틸이다.
일 실시형태에서, 라파마이신(시롤리무스)이 이미 제공된 환자에게 항-OX40L 항체가 투여된다. 또 다른 실시형태, 실시형태에서, 타크롤리무스가 이미 제공된 환자에게 항-OX40L 항체가 투여된다. 또 다른 실시형태에서, 타크롤리무스와 메토트렉세이트의 조합물이 이미 제공된 환자에게 항-OX40L 항체가 투여된다. 또 다른 실시형태에서, 사이클로스포린과 메토트렉세이트의 조합물이 이미 제공된 환자에게 항-OX40L 항체가 투여된다. 또 다른 실시형태에서, 사이클로스포린이 이미 제공된 환자에게 항-OX40L 항체가 투여된다. 또 다른 실시형태에서, 사이클로포파미드가 이미 제공된 환자에게 항-OX40L 항체가 투여된다. 또 다른 실시형태에서, 마이코페놀레이트 모페틸이 이미 제공된 환자에게 항-OX40L 항체가 투여된다.
이들 추가 치료제는 OX40L-매개된 질환 또는 병태의 치료에서 예방적으로 사용될 수 있다. 예를 들어, GvHD에서, 예방 요법(예방조치)은 전형적으로 HSCT 시기 근처에 투여되고, 급성 GvHD 전개의 위험이 가장 높은 기간 동안 이식 이후의 시간 동안 계속된다. 특정 약물 요법은 이식 중심에 따라서 상이하지만, 예로서 칼시뉴린 억제제, 예컨대 사이클로스포린 또는 타크롤리무스, 또는 라파마이신(시롤리무스)으로의 예방조치가 이식 전 7일 기간 이내(예컨대 HSCT 이전 -3일, 또는 -1일)에 개시될 수 있거나, 또는 HSCT 절차 직후(예를 들어, 이식 후 0일, 또는 +1일)에 개시될 수 있다. 마이코페놀레이트 모페틸로의 예방조치는 전형적으로는 HSCT 이후에 투약되고, 예를 들어 이식 이후 +1일 내지 +5일에 시작된다. 이러한 작용제로의 예방조치는 예를 들어 이식 이후에 28 내지 180일 또는 더 긴 기간 동안 계속될 수 있고, 1일 투여량은 부작용을 제한하지 않으면서 유효한 면역억제를 성취하는 범위로 혈청 수준을 유지시키도록 계산된다. 칼시뉴린 억제제에 더하여, 메토트렉세이트가 종종 예방조치에 대한 부가물로서 사용되는데, 이것은 전형적으로는 이식 이후 +1일, +3일, +6일, 및 +11일에 투여된다.
본 발명의 항-OX40L 항체는 타크롤리무스, 사이클로스포린, 타크롤리무스와 메토트렉세이트의 조합물, 사이클로스포린과 메토트렉세이트의 조합물, 사이클로포스파미드, 마이코페놀레이트 모페틸 또는 라파마이신과 조합되어 예방조치로서 사용될 수 있고, 이러한 작용제 중 임의의 것으로의 예방조치는 HSCT 시기 이전에 또는 근처에, 또는 이식 절차 직후에, 예를 들어 이식 7일 전 내지 이식 7일 후의 기간 사이에 시작된다. 이어서, 타크롤리무스, 또는 사이클로스포린, 또는 라파마이신이 치료 유효량 용량으로, 자주, 예를 들어 이식 이후에 180일까지 매일 투여될 수 있다. 본 발명의 항-OX40L 항체는 동시에 투여될 수 있고, HSCT 시기 이전에 또는 근처에, 또는 이식 절차 직후에, 예를 들어 이식 7일 전 내지 이식 7일 후의 기간 사이에 시작된다. 이어서, 항-OX40L 항체가 치료 유효량 용량으로, 자주, 예를 들어 이후에 180일까지 격주로 또는 매달 투여된다. 이러한 상황하에서, 항-OX40L 항체와 추가 예방제의 조합 활성은 GvHD의 발병 및/또는 중증도를 예방하는 데 상승작용적 효과를 나타낸다고 예견될 것이다.
개념 116. 개념 112 또는 개념 114에 따른 방법으로서, 추가 치료제는 코르티코스테로이드(예를 들어, 메틸프레드니솔론)인, 방법.
일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 메틸프레드니솔론이다.
브레이크쓰루(breakthrough) GvHD가 발생한 경우(예를 들어, 심지어는 예방조치임에도 불구하고), 치료는 등급 II 또는 더 중증 GvHD 질환의 식별 후에 즉시 개시될 수 있다. 예를 들어, 칼시뉴린 억제제, 예컨대 사이클로스포린 또는 타크롤리무스로의 계속적인 예방조치와 함께 동시에 투여되는 전신성 코르티코스테로이드, 예컨대 메틸프레드니솔론이 1차 치료 선택이다.
1차 치료 또는 예방조치가 GvHD를 제어하는 데 실패한 경우, "구제 요법(salvage therapy)"이 시도될 수 있고, 이러한 경우에 이전에 사용되지 않은 면역억제제, 예컨대 라파마이신 또는 마이코페놀레이트 모페틸이 투여될 수 있다. 따라서, 일 실시형태에서, 치료 유효량의 본 발명의 항-OX40L 항체는 메토트렉세이트, 사이클로포스파미드, 사이클로스포린, 사이클로스포린과 조합된 라파마이신, 타크롤리무스, 타크롤리무스 중 임의의 것으로의 예방조치 또는 치료에 난치성인 환자에게 메토트렉세이트, 또는 코르티코스테로이드(예를 들어, 메틸프레드니솔론)와 조합되어 투여된다. 또 다른 실시형태에서, 치료 유효량의 본 발명의 항-OX40L 항체는 본 명세서에 언급된 추가 치료제 중 임의의 것으로의 예방조치 또는 치료에 난치성인 환자에게 투여된다. 또 다른 실시형태에서, 본 발명의 항-OX40L 항체는 구제 요법으로서 투여된다.
개념 117. 항-OX40L 항체와, 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제의 치료 조합물 또는 예방 조합물을 투여함으로써 OX40L-매개된 질환 또는 병태를 갖거나 이의 위험을 갖는 생존 대상체에서 생존을 연장시키는 방법.
일 실시형태에서, 이제 OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이다. 다수의 인자, 예컨대 이식 이전 컨디셔닝 요법(예를 들어, 방사선에 의한 마이오어블레이션(myeoablation), 예비 화학요법), 공여자-수용자 조직 매칭(HLA 매칭, 및/또는 공여자-수용자의 관계) 정도, 및 치료 또는 예방 치료 요법이 GvHD에서 중증도 및 질환 진행에 영향을 미친다.
그러나, 일반적으로, 불일치 줄기 세포가 이식된 영장류, 예컨대 레서스 마카크에서, 치료를 하지 않은 이식 이후 평균 생존 시간(MST)은 8일이다.
개념 118. 개념 117에 따른 방법으로서, 생존은 적어도 7일, 또는 적어도 14일, 또는 적어도 20일, 또는 적어도 30일 또는 적어도 40일, 또는 적어도 50일, 또는 적어도 60일, 또는 적어도 70일이 증가되는, 방법.
개념 119. 항-OX40L 항체와, 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제의 치료 조합물 또는 예방 조합물을 투여함으로써 OX40L-매개된 질환 또는 병태를 갖거나 이의 위험을 갖는 대상체에서 무병일수, 또는 질환 무진행일수를 증가시키는 방법.
일 실시형태에서, 이제 OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이다. 인간에서, 급성 GvHD의 징후 및 증상의 존재는 예컨대 프르제피오카 등의 문헌에 기술된 표준화된 규모에 따라서 단계화 및 등급화될 수 있다. 영장류, 예컨대 레서스 마카크 원숭이에서, 급성 GvHD의 징후 및 증상의 존재는 예컨대 본 명세서 실시예 7에 기술된 표준화된 규모에 따라서 단계화 및 등급화될 수 있다.
따라서, 무질환일수는 임상 등급 증상의 부재에 의해서 측정될 수 있다. 질환 무진행일수는 임상 등급 점수에 변화가 없는 일수로서 측정될 수 있다.
개념 120. 개념 119에 따른 방법으로서, 무병일수, 또는 질환 무진행일수는 적어도 7일, 또는 적어도 14일, 또는 적어도 21일, 또는 적어도 28 또는 적어도 40일, 또는 적어도 50일, 또는 적어도 60일, 또는 적어도 70일인, 방법.
개념 121. 개념 120에 따른 방법으로서, 무질환일수 또는 질환 무진행일수는 적어도 90일, 적어도 180일 또는 적어도 365일인, 방법.
개념 122. 항-OX40L 항체와, 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제의 치료 조합물 또는 예방 조합물을 투여함으로써 대상체에서 이식 거부 또는 GvHD의 위험을 치료 또는 감쇠시키는 방법으로서, 조합물은 동종 조혈 줄기 세포 이식의 레서스 마카크 모델에서 단일 요법으로서의 항체 또는 추가 치료제에 비해서 증가된 생존을 유발하는, 방법.
일 실시형태에서, 방법은 OX40L-매개된 질환 또는 병태의 예방 방법이다.
일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 라파마이신(시롤리무스)이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 타크롤리무스이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 타크롤리무스와 메토트렉세이트의 조합물이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 사이클로포스파미드이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 사이클로스포린이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 사이클로스포린과 메토트렉세이트의 조합물이다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 추가 치료제는 마이코페놀레이트 모페틸이다.
동종 조혈 줄기 세포 이식의 레서스 마카크 모델은 또한 본 명세서에서 양상 99에서 기술된 바와 같을 수 있다.
개념 123. 개념 106, 109, 110, 117, 119, 또는 122 중 임의의 하나에 따른 방법으로서, 생존은 단일 요법으로서의 항체 또는 추가 치료제에 비해서 적어도 7일, 또는 적어도 14일, 또는 적어도 21일, 또는 적어도 28일, 또는 적어도 40일, 또는 적어도 50일, 또는 적어도 60일, 또는 적어도 70일이 증가되는, 방법.
개념 124. 개념 106, 109, 110, 117, 119, 또는 122 중 임의의 하나에 따른 방법으로서, 생존은 단일 요법으로서의 항체 또는 추가 치료제에 비해서 적어도 2배, 예를 들어 3배인, 방법.
개념 125. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항체는 인간 OX40L(hOX40L)에 특이적으로 결합하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
hOX40L은 본 명세서에 기술된 양상 28 또는 양상 30에 기술된 바와 같을 수 있다.
본 명세서에 제공된 개념 중 임의의 것에서, 항-OX40L 항체는 명세서에서 다른 부분에 기술된 바와 같을 수 있다. 일 실시형태에서, 항-OX40L 항체는 본 명세서에 기술된 양상 1 내지 11, 13 내지 27, 29, 31 내지 43 또는 45 중 임의의 것에 기술된 바와 같다. 또 다른 실시형태에서, 항-OX40L 항체는 양상 73 내지 89에 기술된 바와 같고, 본 명세서에 기술된 양상 95 내지 102 중 임의의 것에서와 같다. 또 다른 실시형태에서, 항-OX40L 항체는 상기 본 명세서에서 개념 53 내지 64 중 임의의 것에 기술된 바와 같다. 본 명세서 제86면 내지 제89면, 제90면 전반부의 "이중특이성"이라는 제목의 단락, 본 명세서에서 제108면 전반부의 "항체"라는 제목의 단락, 본 명세서에서 제130면 전반부의 "투여 및 투약 방법"이라는 제목의 단락에 기술되어 있다.
개념 126. 개념 125에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 상기 hOX40L에 대한 결합을 위해서 02D10, 10A07, 09H04 및 19H01로 이루어진 군으로부터 선택된 항체와 경쟁하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
항체들 간의 경쟁은 양상 13 또는 양상 73에 기술된 바와 같이, 예를 들어 SPR, ELISA, HTRF 또는 FACS에 의해서 측정되는 바와 같이 측정될 수 있다. 측정 방법에 관련된 방법은 실시예를 비롯하여 본 명세서에 개시되어 있다.
개념 127. 상기 hOX40L에 대한 결합을 위해서 항체 02D10과 경쟁하는 개념 126에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항체 또는 단편은 모티프 VRGXYYY를 포함하는 HCDR3을 포함하는 VH 도메인을 포함하고, X는 임의의 아미노산인, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 128. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항체는 예를 들어, SPR 또는 ELISA를 사용하여 측정되는 바와 같이 OX40L에 대한 OX40의 특이적인 결합에 길항작용하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
길항작용 및 억제는 제94면 내지 제95에 정의된 바와 같이 수행될 수 있다.
개념 129. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항체는 인간화 항체, 인간 항체 또는 완전 인간 항체인, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 130. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항체는 다중특이적인 항체(예를 들어, 이중-특이적인 항체), 인트라바디, 단일-쇄 Fv 항체(scFv), 낙타화 항체, Fab 단편, F(ab') 단편, 다이설파이드-연결된 Fv(sdFv), 항-이디오타입(항-Id) 항체, 및 이의 에피토프-결합 단편의 목록으로부터 선택된 항체의 단편인, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 131. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항체 또는 단편은 동종 조혈 줄기 세포 이식의 레서스 마카크 모델에서 12일에 80%를 초과하는 줄기 세포 공여자 키메리즘을 가능하게 하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 132. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항체 또는 단편은 14일의 과성장 기간으로 론자 버전 8 공급 시스템을 사용하여 유가 과성장 배양액 중에서 1.5g/L를 초과하는 수준으로 론자 지에스-엑스시드(상표명) 중에서 안정하게 형질주입된 풀로서 발현하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 133. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항체 또는 이의 단편은 16 내지 27개의 아미노산의 HCDR3을 포함하고, 인간 VH 유전자 조각, 인간 D 유전자 조각 및 인간 JH 유전자 조각의 재조합으로부터 유래되고, 인간 JH 유전자 조각은 IGHJ6(예를 들어, IGHJ6*02)인, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 134. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항체 또는 이의 단편은 하기로부터 선택된 CDR을 포함하는, 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도:
a. 항체 2D10의 HCDR3(서열번호 40 또는 서열번호 46);
b. 항체 10A7의 HCDR3(서열번호 8 또는 서열번호 14);
c. 항체 09H04의 HCDR3(서열번호 72 또는 서열번호 78);
d. 항체 19H01의 HCDR3(서열번호 100 또는 서열번호 106);
e. 서열번호 177 내지 213의 가변 영역 아미노산 서열을 갖는 나노바디 중 임의의 것의 CDR3;
f. 서열번호 215, 217, 219, 221, 223, 225, 227, 229 또는 230의 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 HCDR3; 또는
g. 서열번호 232 또는 234의 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 HCDR3.
개념 135. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항체 또는 이의 단편은 하기를 포함하는, 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도:
a. 항체 2D10의 CDR(CDRH3의 경우 서열번호 40 또는 서열번호 46, CDRH2의 경우 서열번호 38 또는 서열번호 44, CDRH1의 경우 서열번호 36 또는 서열번호 42, CDRL1의 경우 서열번호 50 또는 서열번호 56, CDRL2의 경우 서열번호 52 또는 서열번호 58 및 CDRL3의 경우 서열번호 54 또는 서열번호 60);
b. 항체 10A7의 CDR(CDRH3의 경우 서열번호 8 또는 서열번호 14, CDRH2의 경우 서열번호 6 또는 서열번호 12, CDRH1의 경우 서열번호 4 또는 서열번호 10, CDRL1의 경우 서열번호 18 또는 서열번호 24, CDRL2의 경우 서열번호 20 또는 서열번호 26 및 CDRL3의 경우 서열번호 22 또는 서열번호 28);
c. 항체 09H04의 CDR(CDRH3의 경우 서열번호 72 또는 서열번호 78, CDRH2의 경우 서열번호 70 또는 서열번호 76, CDRH1의 경우 서열번호 68 또는 서열번호 74, CDRL1의 경우 서열번호 82 또는 서열번호 88, CDRL2의 경우 서열번호 84 또는 서열번호 90 및 CDRL3의 경우 서열번호 86 또는 서열번호 92);
d. 항체 19H01의 CDR(CDRH3의 경우 서열번호 100 또는 서열번호 106, CDRH2의 경우 서열번호 98 또는 서열번호 104, CDRH1의 경우 서열번호 96 또는 서열번호 102, CDRL1의 경우 서열번호 110 또는 서열번호 116, CDRL2의 경우 서열번호 112 또는 서열번호 118 및 CDRL3의 경우 서열번호 114 또는 서열번호 120);
e. 서열번호 177 내지 213의 가변 영역 아미노산 서열을 갖는 나노바디 중 임의의 것의 CDR;
f. 서열번호 215, 217, 219, 221, 223, 225, 227, 229 또는 230의 중쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 중쇄 CDR, 및 서열번호 214, 216, 218, 220, 222, 224, 226 또는 228의 경쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 경쇄 CDR; 또는
g. 서열번호 232 또는 234의 중쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 중쇄 CDR, 및 서열번호 231 또는 233의 경쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 경쇄 CDR.
개념 136. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항체 또는 이의 단편은 하기로부터 선택된 VH 및/또는 VL 도메인을 포함하는, 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도:
a. 항체 2D10의 VH 및/또는 VL 도메인(VH의 경우 서열번호 34 및/또는 VL의 경우 서열번호 48);
b. 항체 10A7의 VH 및/또는 VL 도메인(VH의 경우 서열번호 2 및/또는 VL의 경우 서열번호 16);
c. 항체 09H04의 VH 및/또는 VL 도메인(VH의 경우 서열번호 66 및/또는 VL의 경우 서열번호 80);
d. 항체 19H01의 VH 및/또는 VL 도메인(VH의 경우 서열번호 94 및/또는 VL의 경우 서열번호 108);
e. 서열번호 177 내지 213의 가변 영역 아미노산 서열을 갖는 나노바디 중 임의의 것의 VH 도메인;
f. 서열번호 215, 217, 219, 221, 223, 225, 227, 229 또는 230의 중쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 VH 도메인, 및 서열번호 214, 216, 218, 220, 222, 224, 226 또는 228의 경쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 VL 도메인; 또는
g. 서열번호 232 또는 234의 중쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 VH 도메인, 및 서열번호 231 또는 233의 경쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 VL 도메인.
개념 137. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항체는 옥셀루맙인, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 138. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 대상체는 영장류인 방법, 항체 또는 단편, 조성물, 또는 용도.
용어 "대상체"는 본 명세서에서 기술된 바와 같은, 예를 들어, 제104면에 기술된 바와 같은 다른 대상체일 수 있다. 일 실시형태에서, 영장류는 레서스 마카크 원숭이이다.
개념 139. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 대상체는 인간인, 방법, 항체 또는 단편, 조성물, 또는 용도.
일 실시형태에서, 대상체는 인간 환자이다.
개념 140. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 대상체는 OX40L-매개된 질환 또는 병태의 위험이 있는, 방법, 항체 또는 단편, 조성물, 또는 용도.
일 실시형태에서, 대상체가 예를 들어, 유전형분석(genotyping) 및/또는 표현형분석(phenotyping)에 의해서, 증가된 위험을 갖는 것으로서 이미 식별되었지만, 대상체에게 증상이 아직 나타나지 않았거나 또는 임의의 종래의 방법에 의해서 그러한 질환 또는 병태를 갖는 것으로서 진단되지 않은 경우, 대상체는 "OX40L-매개된 질환 또는 병태의 위험"이 있는 것으로서 식별될 수 있다. 따라서, 본 명세서에 개시된 방법 및 용도는 그러한 질환 또는 병태가 전개될 환자의 조기 식별에 도움이 될 수 있다. 일 실시형태에서, 질환 또는 병태가 예방된다(즉, 치료는 예방적이다).
일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이다. 특정 실시형태에서, 대상체는 그가 이식을 위해서 사전 수술된 경우 GvHD 또는 이식 거부의 위험이 있다. 특히, 대상체는 그에게 이식 이전 컨디셔닝 요법(예를 들어, 방사선에 의한 마이오어블레이션, 예비 화학요법)을 시작하는 경우, 공여자-수용자 조직 매칭(HLA 매칭, 및/또는 공여자-수용자의 관계) 정도가 100%가 아닌 경우에 GvHD 또는 이식 거부의 위험이 있다. 잠재적인 이식 요법은 상기 본 명세서에서 개념 78에서 예상된다.
개념 141. 개념 40에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 방법, 사용하기 위한 항체 또는 단편 또는 조성물은 OX40L-매개된 질환 또는 병태의 예방을 위한 것인, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 142. 개념 101 내지 139 중 임의의 하나에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 대상체는 OX40L-매개된 질환 또는 병태를 갖는, 방법, 항체 또는 단편, 조성물, 또는 용도.
대상체에게 통상적으로 상기 질환 또는 병태와 관련된 증상이 나타나거나 또는 대상체가 임의의 종래의 방법에 의해서 그러한 질환 또는 병태를 갖는 것으로서 진단된 경우 대상체는 OX40L-매개된 질환 또는 병태를 갖는다. 일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이고, 대상체는 상기 본 명세서에서 개념 101 내지 105 및 119에 언급된 방법 중 임의의 것에 의해서 질환을 갖는다고 결정될 수 있다.
개념 143. 개념 142에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도는 OX40L-매개된 질환 또는 병태의 치료를 위한 것인, 방법, 항체 또는 단편, 조성물, 또는 용도.
일 실시형태에서, 치료는 OX40L-매개된 질환 또는 병태가 만성 질환 또는 병태로서 진단되는 경우 시작된다.
일 실시형태에서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부, 특히 GvHD이다. GvHD 등급화는 본 명세서에서 기술된 바와 같이 결정될 수 있다(상기 본 명세서에서 개념 101 내지 105 및 119 참고). 일 실시형태에서, 대상체는 GvHD의 등급 II 임상 증상을 갖는 인간이다.
개념 144. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, OX40L-매개된 질환 또는 병태는 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 145. 개념 144에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, OX40L-매개된 질환 또는 병태는 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염, 접촉 과민증, 다발성 경화증 및 죽상동맥경화증으로부터 선택되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 146. 개념 145에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부인, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 147. 개념 146에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, OX40L-매개된 질환 또는 병태는 GvHD인, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 148. 개념 146에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 이식은 세포, 조직 또는 기관 이식(예를 들어, 간, 폐, 심장, 신장 또는 장), 또는 혈액 이식(예를 들어, 자가형 또는 동종이형)이고, 예를 들어 혈액은 골수-유래되거나, 제대혈(배꼽) 유래되거나, 또는 말초-혈액 유래된, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 149. 개념 146 내지 148에 따른 임의의 하나에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항-OX40L 항체 또는 이의 단편은 이식 이전에 투여되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 150. 개념 146 내지 148 중 임의의 하나에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 항-OX40L 항체 또는 이의 단편은 이식 이후에 투여되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
개념 151. 개념 149 또는 개념 150에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 추가 치료제는 이식 이후에 투여되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
일 실시형태에서, 추가 치료제는 라파마이신(시롤리무스)이다. 일 실시형태에서, 추가 치료제는 타크롤리무스이다. 일 실시형태에서, 추가 치료제는 타크롤리무스와 메토트렉세이트의 조합물이다. 일 실시형태에서, 추가 치료제는 사이클로포스파미드이다. 일 실시형태에서, 추가 치료제는 사이클로스포린이다. 일 실시형태에서, 추가 치료제는 사이클로스포린과 메토트렉세이트의 조합물이다. 일 실시형태에서, 추가 치료제는 마이코페놀레이트 모페틸이다. 일 실시형태에서, 추가 치료제는 메틸 프레딘솔로넬이다.
개념 152. 개념 149 또는 개념 150에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 또는 용도로서, 추가 치료제는 이식 이전에 투여되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
일 실시형태에서, 추가 치료제는 라파마이신(시롤리무스)이다. 일 실시형태에서, 추가 치료제는 타크롤리무스이다. 일 실시형태에서, 추가 치료제는 타크롤리무스와 메토트렉세이트의 조합물이다. 일 실시형태에서, 추가 치료제는 사이클로포스파미드이다. 일 실시형태에서, 추가 치료제는 사이클로스포린이다. 일 실시형태에서, 추가 치료제는 사이클로스포린과 메토트렉세이트의 조합물이다. 일 실시형태에서, 추가 치료제는 마이코페놀레이트 모페틸이다.
개념 153. 항-OX40L 항체 또는 이의 단편 및 약제학적으로 허용 가능한 부형제, 희석제 또는 담체를 포함하고, 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 추가로 포함하는 약제학적 조성물.
일 실시형태에서, OX40L-매개된 병태 또는 질환을 치료 및/또는 예방하기 위한 조성물 또는 키트가 제공되며, 조성물 또는 키트는 임의로 인간에서 상기 질환 또는 병태를 치료 및/또는 예방하기 위해서 사용하기 위한 레이블 또는 지시서와 조합으로 추가 치료제와 조합하여 본 발명의 항체 또는 단편을 포함하고; 임의로 레이블 또는 지시서는 마켓팅 인증 번호(예를 들어, FDA 또는 EMA 인증 번호)를 포함하고; 임의로 키트는 항체 또는 단편을 포함하는 IV 또는 주사 장치를 포함한다.
조성물은 본 명세서에서 양상 105, 106 또는 107에 기술된 바와 같을 수 있다. 약제학적 제제에서 사용하기 위한 부형제는 통상의 기술자에게 널리 공지되어 있고, 본 명세서에서 제97면, 또는 본 명세서에서 제118면 전반부의 "약제학적 조성물"이라는 제목의 단락, 또는 본 명세서에서 제130면 전반부의 "투여 및 투약 방법"이라는 제목의 단락에 정의된 바와 같을 수 있다.
개념 154. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물로서, 추가 치료제는 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, CTLA4-Fc 분자(예를 들어, 아바타셉트), 항-CD40L 항체, 항-LFA1 항체, 항-CD52 항체(예를 들어, 알렘투주맙), 사이클로포스파미드 및 항-흉선세포 글로불린으로 이루어진 군으로부터 독립적으로 선택되는, 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물.
다른 조합물은 본 명세서에서 양상 46에 기술되거나 또는 양상 103에 기술된 바와 같은 항-염증 약물을 가질 수 있다. 다른 조합물은 상기 본 명세서에서 개념 81 내지 83, 또는 상기 본 명세서에서 개념 101 내지 153 중 임의의 것에 기술된 바와 같다.
개념 155. 인간에게 치료 유효량, 또는 예방 유효량의 라파마이신, 타크롤리무스, 사이클로스포린, 사이클로포스파미드,코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트 또는 마이코페놀레이트 모페틸, 항-CD28 항체, CTLA4-Fc 분자(예를 들어, 아바타셉트) 및 항-흉선세포 글로불린으로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여하는 것을 추가로 포함하는, 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물.
개념 156. 인간에게 치료 유효량, 또는 예방 유효량의 라파마이신, 타크롤리무스, 사이클로스포린, 사이클로포스파미드,코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트 및 마이코페놀레이트 모페틸로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여하는 것을 추가로 포함하는, 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물
개념 157. 인간에게 치료 유효량, 또는 예방 유효량의 IL-2 신호전달을 조절하는 면역억제제(예를 들어, 타크롤리무스, 사이클로스포린, 라파마이신(시롤리무스)), 및 항-CD25 항체(예를 들어, 바실릭수맙, 다클리주맙)로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여하는 것을 추가로 포함하는, 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물.
개념 158. 인간에게 치료 유효량, 또는 예방 유효량의 칼시뉴린 억제제(예를 들어, 타크롤리무스, 사이클로스포린), mTOR 억제제(예를 들어, 라파마이신(시롤리무스)), 및 항증식제(예를 들어, 마이코페놀레이트 모페틸, 사이클로포스파미드)로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여하는 것을 추가로 포함하는, 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물.
개념 159. 인간에게 치료 유효량, 또는 예방 유효량의 라파마이신을 투여하는 것을 추가로 포함하는, 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물
개념 160. 인간에게 치료 유효량, 또는 예방 유효량의 타크롤리무스를 투여하는 것을 추가로 포함하는, 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물.
개념 161. 인간에게 치료 유효량, 또는 예방 유효량의 타크롤리무스 및 메토트렉세이트를 투여하는 것을 추가로 포함하는, 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물.
개념 162. 인간에게 치료 유효량, 또는 예방 유효량의 사이클로스포린을 투여하는 것을 추가로 포함하는, 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물.
개념 163. 인간에게 치료 유효량, 또는 예방 유효량의 사이클로스포린 및 메토트렉세이트를 투여하는 것을 추가로 포함하는, 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물.
개념 164. 인간에게 치료 유효량, 또는 예방 유효량의 사이클로포스파미드를 투여하는 것을 추가로 포함하는, 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물.
개념 165. 인간에게 치료 유효량, 또는 예방 유효량의 마이코페놀레이트 모페틸을 투여하는 것을 추가로 포함하는, 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물.
개념 166. 인간에게 치료 유효량, 또는 예방 유효량의 코르티코스테로이드(예를 들어, 메틸 프레드니솔론)를 투여하는 것을 추가로 포함하는, 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물.
개념 167. 임의의 상기 개념에 따른 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물로서, 추가 치료제가 항-hOX40L 항체 또는 단편과 순차적으로 또는 동시에 투여되는, 방법, 사용하기 위한 항체 또는 단편, 사용하기 위한 조성물, 용도 또는 조성물.
실시예에 설명된 바와 같이, 본 발명자들은 본 발명의 항체 및 단편을 식별하는 데 특히 유용한 기준 세트를 고안하였는데, 이러한 기준은 하기와 같다:-
(a) HTRF 검정법에서 CHO-S 세포(임의로 전장 인간 OX40L 내로 형질주입됨) 상의 세포-표면 hOX40L을 결합하고/하거나 재조합 hOX40L을 결합하는 항체 또는 단편의 능력;
(b) 수용체 중화 HTRF 검정법 및/또는 유세포 분석법 수용체 중화 검정법에서 인간 OX40을 중화시키는(예를 들어, 인간 OX40 수용체에 대한 인간 OX40L 결합을 중화시키는) 항체 또는 단편의 능력; 및
(c) 인간 및 레서스 원숭이 OX40L 둘 모두를 특이적으로 결합하는 항체 또는 단편의 능력(항체 또는 단편의 PK, PD, 효능 및 다른 파라미터가 인간에 대한 대용품으로서의 레서스 모델에서 평가될 수 있기 때문에 유용함).
따라서, 본 발명의 예에서 항체 또는 단편은 기준 (a), (b) 및 (c)를 충족한다.
예에서, 기준 (a)는 항체 또는 단편이 CHO-S 세포에 의해서 발현된 hOX40L에 대한 수용체 결합이 FACS에 의해서 70% 미만을 나타내도록 설정된다.
예에서, 기준 (a)는 항체 또는 단편이 HTRF 검정법에서 OX40L에 대한 수용체 결합이 90% 미만을 나타내도록 설정된다.
예에서, 기준 (a)는 항체 또는 단편이 HTRF 검정법에서 적어도 20% 효과를 나타내도록 설정된다.
예에서, OX40이 기준 (b)에서 사용된다.
실시형태에서, 본 발명의 항체 또는 단편의 검정 또는 시험은 pH7에서 또는 실질적으로 pH7에서(예를 들어, 시험관내 시험 및 검정법의 경우) 그리고 실온에서 또는 실질적으로 실온에서 수행된다.
임의로, 항체 또는 단편은 예를 들어, 본 명세서에 개시된 조건 하에서, SPR에 의해서 측정되는 경우 1μM 미만, 1000nM 내지 100nM, 100nM 내지 10nM, 10nM 내지 1nM, 1000pM 내지 500pM, 500pM 내지 200pM, 200pM 미만, 200pM 내지 150pM, 200pM 내지 100pM, 100pM 내지 10pM, 10pM 내지 1 pM, 예를 들어, 1mM 내지 1pM(예를 들어, 1mM 내지 100pM; 10nM 내지 100pM; 1nM 내지 10pM; 또는 100pM 내지 1pM) 범위의 친화도(겉보기 친화도, Kd)로 hOX40L을 특이적으로 결합한다. 추가로 또는 대안적으로, 항체 또는 단편은 예를 들어, 본 명세서에 개시된 조건 하에서, SPR에 의해서 측정되는 경우 1μM 미만, 1000nM 내지 100nM, 100nM 내지 10nM, 10nM 내지 1nM, 1000pM 내지 500pM, 500pM 내지 200pM, 200pM 미만, 200pM 내지 150pM, 200pM 내지 100pM, 100pM 내지 10pM, 10pM 내지 1pM, 예를 들어, 1mM 내지 1pM(예를 들어, 1mM 내지 100pM; 10nM 내지 100pM; 1nM 내지 10pM; 또는 100pM 내지 1pM) 범위의 친화도(겉보기 친화도, Kd)로 레서스 원숭이 OX40L을 특이적으로 결합한다. 그러한 결합 측정은 관련 기술 분야에 공지된 다양한 결합 검정법을 사용하여, 예컨대 비아코어(상표명)에 의해서 또는 프로테온 XPR36(상표명)(바이오-라드(Bio-Rad)(등록상표))을 사용하거나, 킨엑스에이(KinExA)(등록상표)(사피다인 인스트루먼츠, 인코퍼레이티드(Sapidyne Instruments, Inc))를 사용하거나, 포르테바이오 옥테트(ForteBio Octet)(폴 포르테바이오 코퍼레이션(Pall ForteBio Corp.))를 사용하여, 예를 들어 표면 플라즈몬 공명(SPR)을 사용하여, 수행될 수 있다.
OX40L 결합 능력, 특이성 및 친화도(Kd, K오프 및/또는 K온)는 관련 기술 분야에서 임의의 일상적인 방법에 의해서, 예를 들어 표면 플라즈몬 공명(SPR)에 의해서 측정될 수 있다. 용어 "Kd"는 본 명세서에서 사용되는 바와 같이 특정 항체-항원 상호작용의 평형 해리 상수를 지칭하도록 의도된다.
일 실시형태에서, 표면 플라즈몬 공명(SPR)은 25℃에서 수행된다. 또 다른 실시형태에서, SPR은 37℃에서 수행된다.
일 실시형태에서, SPR은 생리학적 pH, 예컨대 약 pH7 또는 pH7.6(예를 들어, pH7.6에서 헤페스 완충 식염수(Hepes buffered saline)(또한 HBS-EP라 지칭됨)를 사용함)에서 수행된다.
일 실시형태에서, SPR은 생리학적 염 수준, 예를 들어, 150mM NaCl에서 수행된다.
일 실시형태에서, SPR은 예를 들어, 0.05%의 P20(폴리소르베이트 20; 예를 들어, 트윈(Tween)-20(상표명)) 및 3mM의 EDTA의 존재 하에서 0.05부피% 이하의 세제 수준에서 수행된다.
일례에서, SPR은 pH7.6, 150mM NaCl, 0.05% 세제(예를 들어, P20) 및 3mM EDTA에서 완충액에서 25℃ 또는 37℃에서 수행된다. 완충액은 10mM의 헤페스를 함유할 수 있다. 일례에서, SPR은 HBS-EP 중에서 25℃ 또는 37℃에서 수행된다. HBS-EP는 테크노바 인코퍼레이티드(Teknova Inc)(미국 캘리포니아소재; 카탈로그 번호 H8022)로부터 입수 가능하다.
예에서, 항체 또는 단편의 친화도는 하기에 의해서 SPR을 사용하여 측정된다:
1. 항-마우스(또는 다른 관련 인간, 래트 또는 비-인간 척추동물 항체 불변 영역 종-매칭된) IgG(예를 들어, 비아코어(상표명) BR-1008-38)를 예컨대 1차 아민 커플링에 의해서 바이오센서 칩(예를 들어, GLM 칩)에 커플링시킴;
2. 항-마우스 IgG(또는 다른 매칭된 종 항체)를 IgG 항체에 노출시켜서 칩 상에 시험 항체를 포획함;
3. 시험 항원을 1024nM, 256nM, 64nM, 16nM, 4nM 및 0nM(즉, 완충액 단독)에서 칩의 포획 표면을 통해서 통과시킴;
4. 그리고 예를 들어, 상기에 논의된 조건하에서(예를 들어, 생리학적 완충액 중에서 25℃에서), 표면 플라즈몬 공명을 사용하여 시험 항원에 대한 시험 항체의 결합 친화도를 측정함. SPR은 예컨대 비아코어(상표명)에 의해서 또는 프로테온 XPR36(상표명)(바이오-라드(등록상표))을 사용하여 임의의 표준 SPR 장치를 사용하여 수행될 수 있다.
포획 표면의 재생은 pH 1.7에서 10mM 글리신으로 수행될 수 있다. 이것은 포획된 항체를 제거하여, 표면이 또 다른 상호작용을 위해서 사용되도록 한다. 결합 데이터는 표준 기술을 사용하여, 예를 들어, 프로테온 XPR36(상표명) 분석 소프트웨어에 대한 고유 모델을 사용하는 1:1 고유 모델에 피팅될 수 있다.
예에서, 본 발명의 항체 또는 단편은 의료 용기, 예를 들어 바이알, 주사기, IV 용기 또는 주사 장치(예를 들어, 안구내(intraocular) 또는 유리체내(intravitreal) 주사 장치) 내에 함유된다. 예에서, 항체 또는 단편은 시험관내에, 예를 들어, 무균 용기 내에 존재한다. 예에서, 본 발명은 본 발명의 항체 또는 단편, 포장재 및 인간에서 OX40L에 의해서 매개된 질환 또는 병태를 치료 또는 예방 또는 진단하는 데 사용하기 위한 지시서를 포함하는 키트를 제공한다. 예에서, 지시서는 인간에게 항체 또는 단편을 투여하기 전에 인간은 본 발명의 OX40L 변이체 서열에 대해서 유전형분석되어야 한다는 것을 지적한다. 예에서, 지시서는 인간에게 항체 또는 단편을 투여하기 전에 인간이 본 발명의 OX40L 변이체에 대해서 표현형분석되어야 한다는 것을 지적한다. 예에서, 인간은 중국(예를 들어, Han 또는 CHS) 인종성을 갖고, 그 지시서는 중국어(예를 들어, 만다린(Mandarin))로 쓰여져 있다.
예에서 항체 또는 단편의 결합 부위(들)는 복수의(예를 들어, 라이브러리) 결합 부위로부터 선택된다. 예를 들어, 복수의 결합 부위는 복수의 4-쇄 항체 또는 그의 단편, 예를 들어, dAb, Fab 또는 scFv를 포함하거나 그것으로 이루어진다. 스크리닝을 위해서 복수의 결합 부위를 생성하는 적합한 방법은 파지 전시법(항체 결합 부위의 파지 전시법 라이브러리를 생성함), 리보솜 전시법(항체 결합 부위의 리보솜 전시법 라이브러리를 생성함), 효모 전시법(항체 결합 부위의 효모 전시법 라이브러리를 생성함), 또는 비-인간 척추동물(예를 들어, 설치류, 예를 들어, 마우스 또는 래트, 예를 들어, 벨로시마우스(Velocimouse)(상표명), 키마우스(Kymouse)(상표명), 제노마우스(Xenomouse)(상표명), 알리바 마우스(Aliva mouse)(상표명), 후맙 마우스(HuMab mouse)(상표명), 옴니마우스(Omnimouse)(상표명), Omnirat(상표명) 또는 메모 마우스(MeMo mouse)(상표명))의 hOX40L 또는 hOX40L 에피토프로의 면역화 및 항체-생성 세포(예를 들어, B-세포, 혈장 세포 또는 형질모세포 레퍼토리)의 레퍼토리 및/또는 단리된 항체, 단편 또는 결합 부위의 레퍼토리의 단리를 포함한다.
용어 "에피토프"는 항체 또는 단편에 의해서 결합된 항원의 영역이다. 에피토프는 구조성 또는 기능성으로서 정의될 수 있다. 기능성 에피토프는 일반적으로 구조성 에피토프의 하위세트이며, 상호작용의 친화도에 직접 기여하는 그러한 잔기를 갖는다. 에피토프는 또한 컨포메이션성(conformational)일 수 있고, 즉 비-선형 아미노산으로 구성될 수 있다. 특정 실시형태에서, 에피토프는 분자의 화학적 활성 표면 그룹핑인 결정자, 예컨대 아미노산, 당 측쇄, 포스포릴기, 또는 설포닐기를 포함할 수 있고, 특정 실시형태에서는, 특이적인 3차원 구조 특징부 및/또는 특이적인 전하 특징부를 가질 수 있다.
본 발명의 임의의 양상, 예를 들어, 항체 또는 단편과 관련하여 용어 "단리된"은, 대상체 항체 또는 단편 등이 (1) 그것과 함께 일반적으로 발견되는 적어도 일부의 다른 단백질을 갖지 않거나, (2) 동일한 공급원으로부터, 예를 들어, 동일한 종으로부터의 다른 단백질을 본질적으로 갖지 않거나, (3) 상이한 종으로부터의 세포에 의해서 발현되거나, (4) 적어도 약 50%의 폴리뉴클레오타이드, 지질, 탄수화물, 또는 그것이 본래 회합된 다른 물질로부터 분리되었거나, (5) 자연에서는 회합되지 않는 폴리펩타이드와 (공유 또는 비공유 상호작용에 의해서) 작동 가능하게 관련되거나, 또는 (6) 자연에서 존재하지 않는 것을 의미힌다. 전형적으로, "단리된" 항체, 단편 등은 특정 샘플의 적어도 약 5%, 적어도 약 10%, 적어도 약 25%, 또는 적어도 약 50%, 60%, 70%, 80%, 85%, 90%, 92%, 95%, 97%, 98%, 99% 또는 99% 초과를 구성한다. 합성 기원의 게놈 DNA, cDNA, mRNA 또는 다른 RNA 또는 이의 임의의 조합이 그러한 단리된 항체, 단편 등을 코딩할 수 있다. 바람직하게는, 단리된 항체, 단편 등은 단백질 또는 폴리펩타이드 또는 그의 치료, 진단, 예방, 연구 또는 다른 용도를 방해할 그의 자연 환경에서 발견되는 다른 오염물을 실질적으로 함유하지 않는다.
예를 들어, "단리된" 항체는 그의 제조 환경(예를 들어, 자연적 또는 재조합적)의 성분으로부터 식별, 분리 및/또는 회수된 것이다. 바람직하게는 단리된 폴리펩타이드는 예를 들어, 항체가 FDA-승인 가능하거나 승인된 표준으로 단리되도록 단리된 그의 제조 환경으로부터의 모든 다른 성분과 관련되지 않는다. 예컨대 재조합의 형질주입된 세포로부터 생성된 그의 제조 환경의 오염 성분은 항체를 위한 연구, 진단법 또는 치료 용도를 전형적으로 방해할 물질이고, 효소, 호르몬 및 다른 단백질 또는 비-단백질 용질을 포함할 수 있다. 바람직한 실시형태에서, 폴리펩타이드는 (1) 예를 들어, 로우리(Lowry) 방법에 의해서 측정되는 경우 95 중량% 초과, 일부 실시형태에서는 99 중량% 초과의 항체로; (2) 예를 들어 스피닝 컵 시쿼네이터(spinning cup sequenator)를 사용하여 N-말단 또는 내부 아미노산 서열의 적어도 15개의 잔기를 얻기에 충분한 정도로, 또는 (3) 쿠마시 블루(Coomassie blue) 또는 바람직하게는 은 염색을 이용하여 환원 또는 비환원 조건하에 SDS-PAGE에 의해 균일한 것으로 나타날 정도로 정제될 것이다. 단리된 항체는 재조합 세포 내의 계내에 항체를 포함하는데, 이는 항체의 자연 환경의 적어도 하나의 성분이 존재하지 않을 것이기 때문이다. 그러나, 통상적으로 단리된 폴리펩타이드 또는 항체는 적어도 하나의 정제 단계에 의해 제조될 것이다.
면역컨쥬게이트
본 발명은 치료 모이어티("면역컨쥬게이트"), 예컨대 세포 독소, 화학요법 약물, 면역억제제 또는 방사성 동위 원소에 컨쥬게이팅된 항체 또는 단편을 포함한다. 세포 독소제는 세포에 해로운 임의의 작용제를 포함한다. 면역컨쥬게이트를 형성하는 데 적합한 세포 독소제 및 화학치료제의 예는 관련 기술 분야에 공지되어 있고, 예를 들어, 그의 전문이 본 명세서에 참고로 포함된 WO 05/103081을 참고하기 바란다.
이중특이성
본 발명의 항체 및 단편은 단일특이적이거나, 이중특이적이거나, 또는 다중특이적일 수 있다. 다중특이적인 mAb는 하나의 표적 폴리펩타이드의 상이한 에피토프들에 대해서 특이적일 수 있거나 또는 하나를 초과하는 표적 폴리펩타이드에 대해서 특이적인 항원-결합 도메인을 함유할 수 있다. 예를 들어, 문헌[Tutt et al., (1991) J. Immunol. 147:60-69]을 참고하기 바란다. 인간 항-hOX40L 항체 또는 단편은 또 다른 기능성 분자, 예를 들어 또 다른 펩타이드 또는 단백질에 연결될 수 있거나 또는 그것과 공동-발현될 수 있다. 예를 들어, 항체 또는 이의 단편은 (예를 들어, 화학적 커플링, 유전적 융합, 비공유 회합 등에 의해서) 하나 이상의 다른 분자 엔티티, 예컨대 또 다른 항체 또는 항체 단편에 기능적으로 연결되어 제2 결합 특이성을 갖는 이중특이적이거나 또는 다중특이적인 항체를 생성할 수 있다.
본 발명의 내용에서 사용될 수 있는 예시적인 이중-특이적인 항체 포맷은 제1 면역글로불린(Ig) CH3 도메인 및 제2 Ig CH3 도메인의 사용을 포함하는데, 여기서 제1 및 제2 Ig CH3 도메인은 적어도 하나의 아미노산에 의해서 서로와 상이하고, 여기서 적어도 하나의 아미노산 차이가 아미노산 차이가 없는 이중-특이적인 항체에 비해서 단백질 A에 대해서 이중특이적인 항체의 결합을 감쇠시킨다. 일 실시형태에서, 제1 Ig CH3 도메인은 단백질 A를 결합하고, 제2 Ig CH3 도메인은 단백질 A 결합을 감쇠 또는 없앤 돌연변이, 예컨대 H95R 변형(IMGT 엑손 넘버링에 의함; EU 넘버링에 의하면 H435R)을 함유한다. 제2 CH3은 Y96F 변형(IMGT에 의함; EU에 의하면 Y436F)을 추가로 포함할 수 있다. 제2 CH3 내에서 발견될 수 있는 추가 변형은 IgG1 항체의 경우 D16E, L18M, N44S, K52N, V57M, 및 V821(IMGT에 의함; EU에 의하면 D356E, L358M, N384S, K392N, V397M, 및 V422I)을 포함하고; IgG2 항체의 경우 N44S, K52N, 및 V82I(IMGT; EU에 의하면 N384S, K392N, 및 V422I); 및 IgG4 항체의 경우 Q15R, N44S, K52N, V57M, R69K, E79Q, 및 V82I(IMGT에 의함; EU에 의하면 Q355R, N3845, K392N, V397M, R409K, E419Q, 및 V422I)를 포함한다. 상기에 기술된 이중-특이적인 항체 포맷에 대한 변이가 또한 본 발명의 범주 내에서 고려된다.
특정 실시형태에서, 항체 또는 이의 OX40L 결합 단편은 6개 미만의 CDR을 포함한다. 일부 실시형태에서, 이의 항체 또는 항원 결합 단편은 HCDR1, HCDR2, HCDR3, LCDR1, LCDR2, 및 LCDR3으로 이루어진 군으로부터 선택된 1개, 2개, 3개, 4개, 또는 5개의 CDR을 포함하거나 그것으로 이루어진다. 구체적인 실시형태에서, 이의 항체 또는 항원 결합 단편은 서열 목록 (즉, HCDR1의 경우 서열번호 4, 서열번호 10, 서열번호 36, 서열번호 42, 서열번호 68, 서열번호 74, 서열번호 96 또는 서열번호 102, 특히, 서열번호 36 또는 서열번호 42; HCDR2의 경우 서열번호 6, 서열번호 12, 서열번호 38, 서열번호 44, 서열번호 70, 서열번호 76, 서열번호 98 또는 서열번호 104, 특히 서열번호 38 또는 서열번호 44; HCDR3의 경우 서열번호 8, 서열번호 14, 서열번호 40, 서열번호 46, 서열번호 72, 서열번호 78, 서열번호 100 또는 서열번호 106, 특히 서열번호 40 또는 서열번호 46; LCDR1의 경우 서열번호 18, 서열번호 24, 서열번호 50, 서열번호 56, 서열번호 82, 서열번호 88, 서열번호 110 또는 서열번호 116, 특히 서열번호 50 또는 서열번호 56; LCDR2의 경우 서열번호 20, 서열번호 26, 서열번호 52, 서열번호 58, 서열번호 84, 서열번호 90, 서열번호 112 또는 서열번호 118, 특히 서열번호 52 또는 서열번호 58; 및 서열번호 22, 서열번호 28, 서열번호 54, 서열번호 60, 서열번호 86, 서열번호 92, 서열번호 114 또는 서열번호 120, 특히 서열번호 54 또는 서열번호 60 for LCDR3)의 HCDR1, HCDR2, HCDR3, LCDR1, LCDR2, 및 LCDR3으로 이루어진 군으로부터 선택된 1개, 2개, 3개, 4개, 또는 5개의 CDR을 포함하거나 그것으로 이루어진다.
구체적인 실시형태에서, 본 발명의 항체는 완전 인간 항체, 단클론성 항체, 재조합 항체, 길항제 항체, hOX40L-중화 항체 또는 이의 임의의 조합이거나, 또는 본 발명은 이의 hOX40L 결합 단편을 제공한다. 예에서, 항체는 인간 가변 도메인 및 비-인간(예를 들어, 마우스 또는 래트 또는 토끼) 불변 도메인을 포함하는 키메릭 항체이다. 특정 실시형태에서, 항체는 hOX40L에 특이적으로 결합하는 완전 인간 항체, 예컨대 완전 인간 단클론성 항체, 또는 이의 항원 결합 단편이다. 바람직한 실시형태에서, 항체는 길항제 항체이다. 바람직한 실시형태에서, 항체는 중화 항체이다.
예에서, 항체 또는 단편은 람다-유형 항체 또는 단편(즉, 그의 가변 도메인은 람다 가변 도메인임)이다. 임의로, 항체 또는 단편은 또한 람다 불변 도메인을 포함한다.
특정 실시형태에서, 항체는 hOX40L, 예컨대 세포 표면-발현된 hOX40L 또는 가용성 hOX40L에 대한 결합을 위해서, OX40 또는 이의 융합 단백질(예를 들어, Fc:OX40)과 (예를 들어, 용량 의존적인 방식으로) 경쟁한다. 예시적인 경쟁적인 차단 시험은 본 명세서에서 실시예에 제공되어 있다.
또 다른 양상에서, 본 명세서에서 hOX40L 폴리펩타이드(예를 들어, 세포 표면-발현된 hOX40L 또는 가용성 hOX40L), hOX40L 폴리펩타이드 단편, 또는 hOX40L 에피토프에 특이적으로 결합하는 항체를 코딩하는 단리된 핵산이 제공된다. 특정 실시형태에서, 핵산은 서열 목록(즉, VH 쇄의 경우 서열번호 30 또는 서열번호 62; VL 쇄의 경우 서열번호 32 또는 서열번호 64; VH 도메인의 경우 서열번호 서열번호 2, 서열번호 34, 서열번호 66 또는 서열번호 94, 특히 서열번호 34 도메인; VL 도메인의 경우 서열번호 16, 서열번호 48, 서열번호 80, 또는 서열번호 108, 특히 서열번호 48 도메인; HCDR1의 경우 서열번호 4, 서열번호 10, 서열번호 36, 서열번호 42, 서열번호 68, 서열번호 74, 서열번호 96 또는 서열번호 102, 특히, 서열번호 36 또는 서열번호 42; HCDR2의 경우 서열번호 6, 서열번호 12, 서열번호 38, 서열번호 44, 서열번호 70, 서열번호 76, 서열번호 98 또는 서열번호 104, 특히 서열번호 38 또는 서열번호 44; HCDR3의 경우 서열번호 8, 서열번호 14, 서열번호 40, 서열번호 46, 서열번호 72, 서열번호 78, 서열번호 100 또는 서열번호 106, 특히 서열번호 40 또는 서열번호 46; LCDR1의 경우 서열번호 18, 서열번호 24, 서열번호 50, 서열번호 56, 서열번호 82, 서열번호 88, 서열번호 110 또는 서열번호 116, 특히 서열번호 50 또는 서열번호 56; LCDR2의 경우 서열번호 20, 서열번호 26, 서열번호 52, 서열번호 58, 서열번호 84, 서열번호 90, 서열번호 112 또는 서열번호 118, 특히 서열번호 52 또는 서열번호 58; 및 LCDR3의 경우 서열번호 22, 서열번호 28, 서열번호 54, 서열번호 60, 서열번호 86, 서열번호 92, 서열번호 114 또는 서열번호 120, 특히 서열번호 54 또는 서열번호 60)에 개시된 바와 같은 VH 쇄, VL 쇄, VH 도메인, VL 도메인, HCDR1, HCDR2, HCDR3, LCDR1, LCDR2, 및 LCDR3을 코딩한다.
또 다른 양상에서, 본 명세서에서 본 발명의 항체 또는 단편을 코딩하는 핵산을 포함하는 벡터 및 숙주-세포가 제공된다.
특정 실시형태에서, 항체는 hOX40L의 하나 이상의 단일 염기 다형성(single nucleotide polymorphism: SNP) 변이체에 특이적으로 결합한다. 본 발명의 임의의 양상의 예에서, hOX40L은 단량체의 삼량체이다.
양상에서, 본 명세서에서 대상체에게 유효량의 hOX40L(예를 들어, 세포 표면-발현된 hOX40L 또는 가용성 hOX40L)에 특이적으로 결합하는 본 발명의 항체 또는 단편을 투여하는 것을 포함하는, 대상체(예를 들어, 인간 대상체)에서 OX40에 대한 hOX40L의 결합을 감소(예를 들어, 적어도 20, 30, 40 50 또는 60%, 또는 70%, 80%, 90%, 95% 또는 90% 초과만큼) 또는 완전히 억제하는 방법이 제공된다.
양상에서, 본 명세서에서 hOX40L-매개된 질환 또는 병태 대상체(예를 들어, 인간 대상체)의 치료 또는 예방 방법이 제공되며, 방법은 대상체에게 유효량의 hOX40L(예를 들어, 세포 표면-발현된 hOX40L 또는 가용성 hOX40L)에 특이적으로 결합하는 본 발명의 항체 또는 이의 단편을 투여하는 것을 포함하고, 여기서 질환 또는 병태가 항체 또는 단편에 의해서 예방된다. 예에서, 방법은 대상체에서 hOX40L생물학적 활성, 예컨대 IL-2, IL-8, TNF 알파 및 인터페론 감마 중 하나, 그 초과 또는 전부의 분비를 감소 또는 억제하는 것을 포함한다. 예에서, 생물학적 활성은 IL-2, TNF 알파 및 인터페론 감마 중 하나, 그 초과 또는 전부의 분비로부터 선택된다. 예에서, 생물학적 활성은 IL-8, CCL20 및 RANTES 중 하나, 그 초과 또는 전부의 분비로부터 선택된다.
양상에서, 본 명세서에서 대상체(예를 들어, 인간 대상체)에서 hOX40L 생물학적 활성, 예컨대 TNF 알파 및 인터페론 감마 중 하나, 그 초과 또는 전부의 분비를 감소 또는 억제하는 방법이 제공되며, 방법은 대상체에게 유효량의 hOX40L(예를 들어, 세포 표면-발현된 hOX40L 또는 가용성 hOX40L)에 특이적으로 결합하는 본 발명의 항체 또는 이의 단편을 투여하는 것을 포함하고, 여기서 hOX40L 생물학적 활성은 항체 또는 단편에 의해서 감소된다. 예에서, 생물학적 활성은 IL-2, TNF 알파 및 인터페론 감마 중 하나, 그 초과 또는 전부의 분비로부터 선택된다. 예에서, 생물학적 활성은 IL-8, CCL20 및 RANTES 중 하나, 그 초과 또는 전부의 분비로부터 선택된다.
용어 "약" 또는 "대략"은 주어진 값 또는 범위의 20% 이내, 바람직하게는 10% 이내, 보다 바람직하게는 5%(또는 4%, 또는 3% 또는 2%, 또는, 예에서, 1% 이하) 이내를 의미한다.
본 명세서에서 사용되는 바와 같이, "투여하다" 또는 "투여"는 체세포 외부에 존재하는 바와 같은 물질(예를 들어, 본 명세서에 제공된 항-hOX40L 항체)을 예컨대 점막, 피부내, 정맥내, 근육내 전달 및/또는 본 명세서에 기술되거나 관련 기술 분야에 공지된 임의의 다른 물리적인 전달 방법에 의해서 환자에게 투여 또는 달리 물리적으로 전달하는 행동을 나타낸다. 질환 또는 이의 증상이 치료되려는 경우, 물질의 투여는 전형적으로 이의 질환 또는 증상의 발병 이후에 일어난다. 이의 질환 또는 증상이 예방되려는 경우, 물질의 투여는 전형적으로 이의 질환 또는 증상의 발병 이전에 일어난다.
두 아미노산 서열 또는 두 핵산 서열의 % 동일성을 결정하기 위해서, 서열을 최적의 비교 목적을 위해서 정렬시킨다(예를 들어, 제2 아미노산 서열 또는 핵산 서열과의 최적의 정렬을 위해서 제1 아미노산의 서열 또는 핵산 서열에 갭(gap)을 도입할 수 있다). 그 다음, 상응하는 아미노산 위치 또는 뉴클레오타이드 위치에서 에서 아미노산 잔기 또는 뉴클레오타이드를 비교한다. 제1 서열 내의 위치가 제2 서열 내의 상응하는 위치와 동일한 아미노산 잔기 또는 뉴클레오타이드에 의해서 차지된 경우, 그 분자는 그 위치에서 동일하다. 두 서열들 간의 % 동일성은 서열들이 공유하는 동일한 위치의 수의 함수이다(즉, % 동일성=동일한 중첩 위치의 수/위치의 총 수×100%). 일 실시형태에서, 두 서열은 동일한 길이이다.
두 서열들(예를 들어, 아미노산 서열 또는 핵산 서열) 간의 % 동일성의 결정은 또한 수학적 알고리즘을 사용하여 달성될 수 있다. 두 서열들의 비교를 위해서 사용되는 수학적 알고리즘의 비제한적인 예는 문헌[Karlin and Altschul, 1993, Proc. Natl. Acad. Sci. U.S.A. 90:5873 5877]에서와 같이 변형된 문헌[Karlin and Altschul, 1990, Proc. Natl. Acad. Sci. U.S.A. 87:2264 2268]의 알고리즘이다. 그러한 알고리즘은 문헌[Altschul et al., 1990, J. Mol. Biol. 215:403]의 NBLAST 및 XBLAST 프로그램에 도입되어 있다. BLAST 뉴클레오타이드 탐색은 본 발명의 핵산 분자에 상동성인 뉴클레오타이드 서열을 얻기 위해서 예를 들어, 스코어=100, 단어길이=12에 대한 NBLAST 뉴클레오타이드 프로그램 세트를 사용하여 수행할 수 있다. BLAST 단백질 탐색은 본 발명의 단백질 분자에 상동성인 아미노산 서열을 얻기 위해서, 예를 들어 스코어 50, 단어길이=3에 대한 XBLAST 프로그램 파라미터 세트를 사용하여 수행할 수 있다. 비교 목적을 위해서 갭을 도입한(gapped) 정렬을 얻기 위해서, 문헌[Altschul et al., 1997, Nucleic Acids Res. 25:3389 3402]에 기술된 바와 같은 갭트(Gapped) BLAST가 사용될 수 있다. 대안적으로, 분자들 간의 먼 관계를 검출하는 반복 탐색을 수행하기 위해서 PSI BLAST를 사용할 수 있다(Id.). BLAST, 갭트 BLAST, 및 PSI Blast 프로그램을 사용하는 경우, (예를 들어, XBLAST 및 NBLAST의) 각각의 프로그램의 디폴트 파라미터를 사용할 수 있다(예를 들어, 월드와이드웹, ncbi.nlm.nih.gov 상의 국립 생물 정보 센터(National Center for Biotechnology Information: NCBI)를 참고하기 바란다). 서열의 비교를 위해서 사용되는 수학적 알고리즘의 또 다른 바람직한 비제한적인 예는 문헌[Myers and Miller, 1988, CABIOS 4:11 17]의 알고리즘이다. 그러한 알고리즘은 GCG 서열 정렬 소프트웨어 패키지의 일부인 ALIGN 프로그램(버전 2.0)에 도입되어 있다. 아미노산 서열을 비교하기 위해서 ALIGN 프로그램을 사용하는 경우, PAM120 중량 잔기 표, 12의 갭 길이 패널티, 및 4의 갭 패널티를 사용할 수 있다.
두 서열들 간의 % 동일성은 갭을 허용하거나 또는 갭을 허용하지 않으면서 상기에 기술된 것과 유사한 기술을 사용하여 측정될 수 있다. % 동일성의 계산 시, 전형적으로는 정확한 매치만을 카운팅한다.
본 명세서에서 사용되는 바와 같이, hOX40L의 "길항제" 또는 "억제제"는 예컨대 hOX40L을 발현하는 세포 또는 hOX40L 리간드를 발현하는 세포에서 hOX40L의 생물학적 활성 중 하나 이상을 억제 또는 달리 감소시킬 수 있는 리간드(예를 들어, 항체 또는 단편)를 나타낸다. 예를 들어, 특정 실시형태에서, 본 발명의 항체는, 상기 항체가 상기 세포와 접촉할 때 세포 표면-발현된 OX40을 갖는 세포로부터 CCL20, IL-8 및/또는 RANTES의 분비를 억제 또는 달리 감소시키는 길항제 항체이다. 일부 실시형태에서, hOX40L의 길항제(예를 들어, 본 발명의 길항성 항체)는 예를 들어, OX40L을 발현하는 세포의 활성화 및/또는 세포 신호전달 경로를 억제 또는 달리 감소시키고, 이에 의해서 길항제의 부재 하에서의 hOX40L-매개된 생물학적 활성에 비해서 세포의 hOX40L-매개된 생물학적 활성을 억제함으로써 작용할 수 있다. 특정 실시형태에서, 본 명세서에서 제공된 항체는 완전 인간, 길항성 항-hOX40L 항체, 바람직하게는 와전 인간, 단클론성, 길항성 항-hOX40L 항체이다.
용어 "항체" 및 "면역글로불린" 또는 "Ig"는 본 명세서에서 상호교환 가능하게 사용될 수 있다. hOX40L 항원에 특이적으로 결합하는 항체 또는 이의 단편은 관련된 항원과 교차-반응할 수 있다. 바람직하게는, hOX40L 항원에 특이적으로 결합하는 항체 또는 이의 단편은 다른 항원과 교차-반응하지 않는다(그러나 상이한 종, 예를 들어 레서스 또는 뮤린의 OX40L과 임의의 교차 반응할 수 있다). hOX40L 항원에 특이적으로 결합하는 항체 또는 이의 단편은 예를 들어, 면역검정법, 비아코어(상표명), 또는 관련 기술 분야의 통상의 기술자에게 공지된 다른 기술에 의해서 식별될 수 있다. 항체 또는 이의 단편은, 그것이 실험 기술, 예컨대 방사성면역검정법(RIA) 및 효소-연결된 면역흡착성 검정법(ELISA)을 사용하여 측정되는 바와 같은 임의의 교차 반응성 항원에 대한 것보다 더 높은 친화도로 hOX40L 항원에 결합할 때, hOX40L 항원에 대해서 특이적으로 결합한다. 전형적으로 특이적인 또는 선택적인 반응은 배경 신호 또는 노이즈의 적어도 2배, 보다 전형적으로는 배경의 10배 초과일 것이다. 예를 들어, 항체 특이성에 관련된 논의에 대해서는 문헌[Paul, ed., 1989, Fundamental Immunology Second Edition, Raven Press, New York at pages 332-336]을 참고하기 바란다.
본 발명의 항체는 합성 항체, 단클론성 항체, 재조합 방식으로 제조된 항체, 다중특이적인 항체(이중-특이적인 항체 포함), 인간 항체, 인간화 항체, 키메릭 항체, 인트라바디, 단일-쇄 Fv(scFv)(예를 들어, 단일특이성, 이중특이성 등), 낙타화 항체, Fab 단편, F(ab') 단편, 다이설파이드-연결된 Fv(sdFv), 항-이디오타입(항-Id) 항체, 및 상기 중 임의의 것의 에피토프-결합 단편을 포함하지만, 이들로 제한되는 것은 아니다. 특히, 본 발명의 항체는 면역글로불린 분자 및 면역글로불린 분자의 면역학적 활성 부분, 즉 hOX40L 항원에 특이적으로 결합하는 항원-결합 부위(항-hOX40L 항체의 하나 이상의 상보성 결정 영역(CDR))를 함유하는 항원 결합 도메인 또는 분자를 포함한다. 본 발명의 항체는 면역글로불린 분자의 임의의 유형(예를 들어, IgG, IgE, IgM, IgD, IgA 및 IgY), 임의의 부류(예를 들어, IgG1, IgG2, IgG3, IgG4, IgA1 및 IgA2, 특히 IgG4), 또는 임의의 하위부류(예를 들어, IgG2a 및 IgG2b)를 가질 수 있다. 바람직한 실시형태에서, hOX40L 항체는 완전 인간, 예컨대 완전 인간 단클론성 hOX40L 항체이다. 특정 실시형태에서, 본 발명의 항체는 IgG 항체, 또는 이의 부류(예를 들어, 인간 IgG1 또는 IgG4) 또는 하위부류이다. 특정 실시형태에서, 본 발명의 항체는 인간 감마 4 불변 영역을 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 Fc-γ 수용체를 결합하지 않고, 예를 들어, Leu235Glu 돌연변이를 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 안정성을 증가시키기 위해서 Ser228Pro 돌연변이를 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 IgG4-PE이다.
용어 "항원 결합 도메인," "항원 결합 영역," "항원 결합 단편," 및 유사한 용어는 항원과 상호작용하고, 결합제 상에 항원에 대한 그의 특이성 및 친화도를 부여하는 아미노산 잔기를 포함하는 항체의 부분(예를 들어, 상보성 결정 영역(CDR))을 나타낸다. 항원 결합 영역은 임의의 동물 종, 예컨대 설치류(예를 들어, 토끼, 래트 또는 햄스터) 및 인간으로부터 유래될 수 있다. 바람직하게는, 항원 결합 영역은 인간 기원일 것이다.
본 명세서에서 사용되는 바와 같이, 용어 "조성물"은 명시된 구성 성분(예를 들어, 본 발명의 항체)을, 임의로, 명시된 양으로, 그리고 명시된 구성 성분의 조합물로부터 직접적으로 또는 간접적으로 유래한 임의의 생성물을, 임의로, 명시된 양으로 함유하는 생성물을 포함하도록 의도된다.
폴리펩타이드와 관련하여, 용어 "유도체"는 본 명세서에서 사용되는 바와 같이 아미노산 잔기 치환, 결손 또는 부가에 의한 도입에 의해서 변경된 hOX40L 폴리펩타이드, hOX40L 폴리펩타이드의 단편, 또는 hOX40L 폴리펩타이드에 특이적으로 결합하는 항체의 아미노산 서열을 포함하는 폴리펩타이드를 나타낸다. 용어 "유도체"는 본 명세서에서 사용되는 바와 같이 또한 예를 들어, 폴리펩타이드에 대한 임의의 유형의 공유 부착에 의해서, 화학적으로 변형된 hOX40L 폴리펩타이드, hOX40L 폴리펩타이드의 단편, 또는 hOX40L 폴리펩타이드에 특이적으로 결합하는 항체를 나타낸다. 예를 들어, 그렇지만 제한이 아니게, hOX40L 폴리펩타이드, hOX40L 폴리펩타이드의 단편, 또는 hOX40L 항체는 예를 들어, 글리코실화, 아세틸화, 페길화, 인산화, 아마이드화, 공지된 보호/차단 기에 의한 유도체화, 단백질분해성 절단, 세포 리간드 또는 다른 단백질에 대한 연결 등에 의해서 화학적으로 변형될 수 있다. 유도체는 부착된 분자의 유형 또는 위치에서, 자연 발생 또는 출발 펩타이드 또는 폴리펩타이드와 상이한 방식으로 변형된다. 유도체는 펩타이드 또는 폴리펩타이드 상에 자연적으로 존재하는 하나 이상의 화학기의 결손을 추가로 포함한다. hOX40L 폴리펩타이드, hOX40L 폴리펩타이드의 단편, 또는 hOX40L 항체의 유도체는 특이적인 화학 절단, 아세틸화, 제제화, 튜니카마이신의 대사 합성을 포함하지만 이에 제한되지 않는 관련 기술 분야의 통상의 기술자에게 공지된 기술을 사용한 화학적 변형에 의해서 화학적으로 변형될 수 있다. 추가로, hOX40L 폴리펩타이드, hOX40L 폴리펩타이드의 단편, 또는 hOX40L 항체의 유도체는 하나 이상의 비-전통적인 아미노산을 함유할 수 있다. 폴리펩타이드 유도체는 본 명세서에 기술된 hOX40L 폴리펩타이드, hOX40L 폴리펩타이드의 단편, 또는 hOX40L 항체와 유사하거나 동일한 기능을 갖는다.
용어 "유효량"은 본 명세서에서 사용되는 바와 같이 특정 질환 및/또는 이에 관련된 증상의 중증도 및/또는 기간을 감쇠 및/또는 완화시키기에 충분한 치료제(예를 들어, 본 명세서에 제공된 항체 또는 약제학적 조성물)의 양을 나타낸다. 이 용어는 또한 특정 질환의 발전 또는 진행의 감쇠 또는 완화, 재발의 감쇠 또는 완화, 특정 질환의 전개 또는 발병, 및/또는 또 다른 요법(예를 들어 본 명세서에 제공된 항-hOX40L 항체 이외의 요법)의 예방 또는 치료 효과(들)를 개선 또는 향상시키는 데 필요한 양을 포함한다. 일부 실시형태에서, 본 발명의 항체의 유효량은 약 0.1mg/kg(대상체 체중 당 항체 mg) 내지 약 100mg/kg이다. 특정 실시형태에서, 본 명세서에 제공된 항체의 유효량은 약 0.1mg/kg, 약 0.5mg/kg, 약 1mg/kg, 3mg/kg, 5mg/kg, 약 10mg/kg, 약 15mg/kg, 약 20mg/kg, 약 25mg/kg, 약 30mg/kg, 약 35mg/kg, 약 40mg/kg, 약 45mg/kg, 약 50mg/kg, 약 60mg/kg, 약 70mg/kg, 약 80mg/kg 약 90mg/kg 또는 약 100mg/kg(또는 그 내의 범위)이다. 일부 실시형태에서, "유효량"은 본 명세서에서 사용되는 바와 같이 또한 명시된 결과(예를 들어, 세포의 hOX40L 생물학적 활성의 억제, 예컨대 세포로부터의 CCL20, IL-8 또는 RANTES, 또는 INF-γ, TNF-α 또는 IL-2, 특히 INF-γ의 억제)를 달성하기 위한 본 발명의 항체의 양을 나타낸다.
용어 "에피토프"는 본 명세서에서 사용되는 바와 같이 항체의 하나 이상의 항원 결합 영역에 결합할 수 있고, 동물, 바람직하게는 포유동물, 가장 바람직하게는 인간에서 면역 반응을 일으킬 수 있는, 항원 활성 또는 면역성 활성을 갖는 항원 표면 상의 국지적인 영역, 예컨대 hOX40L 폴리펩타이드 또는 hOX40L 폴리펩타이드 단편을 나타낸다. 면역성 활성을 갖는 에피토프는 동물에서 항체 반응을 일으키는 폴리펩타이드의 부분이다. 항원 활성을 갖는 에피토프는 관련 기술 분야에 널리 공지된 임의의 방법에 의해서, 예를 들어 본 명세서에 기술된 면역검정법에 의해서 측정되는 바와 같이 항체가 특이적으로 결합하는 폴리펩타이드의 부분이다. 항원성 에피토프는 반드시 면역성일 필요는 없다. 에피토프는 통상적으로 분자, 예컨대 아미노산 또는 당 측쇄의 화학 활성 표면 그룹으로 이루어지고, 특이적인 3차원 구조 특징뿐만 아니라 특이적인 전하 특징을 갖는다. 에피토프에 기여하는 폴리펩타이드의 영역은 폴리펩타이드의 인접 아미노산일 수 있거나, 에피토프는 폴리펩타이드의 둘 이상의 비-인접 영역으로부터 함께 형성될 수 있다. 에피토프는 항원의 3차원 표면 특징부이거나 그것이 아닐 수 있다. 특정 실시형태에서, hOX40L 에피토프는 (예를 들어, hOX40L 폴리펩타이드의 삼량체 형태에서) hOX40L 폴리펩타이드의 3차원 표면 특징부이다. 다른 실시형태에서, hOX40L 에피토프는 (예를 들어, hOX40L 폴리펩타이드의 삼량체 형태 또는 단량체 형태에서) hOX40L 폴리펩타이드의 선형 특징부이다. 본 명세서에서 제공된 항체는 hOX40L의 단량체(변성) 형태의 에피토프, hOX40L의 삼량체(네이티브) 형태의 에피토프, 또는 hOX40L의 단량체(변성) 형태와 삼량체(네이티브) 형태 둘 모두에 특이적으로 결합할 수 있다. 구체적인 실시형태에서, 본 명세서에 제공된 항체는 hOX40L의 삼량체 형태의 에피토프에 특이적으로 결합하지만, hOX40L의 단량체 형태에는 특이적으로 결합하지 않는다.
용어 "부형제"는 본 명세서에서 사용되는 바와 같이 약물을 위해서 희석제, 비히클, 방부제, 결합제 또는 안정제로서 일반적으로 사용되는 불활성 물질을 말하고, 단백질(예를 들어, 혈청 알부민 등), 아미노산(예를 들어, 아스파트산, 글루탐산, 라이신, 아르기닌, 글리신, 히스티딘 등), 지방산 및 인지질(예를 들어, 알킬 설포네이트, 카프릴레이트 등), 계면활성제(예를 들어, SDS, 폴리소르베이트, 비이온성 계면활성제 등), 당류(예를 들어, 수크로스, 말토스, 트레할로스 등) 및 폴리올(예를 들어, 만니톨, 소르비톨 등)을 포함하지만, 이들로 제한되는 것은 아니다. 예를 들어, 또한 전문이 참고로 본 명세서에 포함된 문헌[Remington's Pharmaceutical Sciences (1990)](미국 펜실베니아주 소재의 백 퍼플리싱, 코퍼레이션(Mack Publishing Co.)을 참고하기 바란다.
펩타이드 또는 폴리펩타이드와 관련하여, 용어 "단편"은 본 명세서에서 사용되는 바와 같이 전장보다 작은 아미노산 서열을 포함하는 펩타이드 또는 폴리펩타이드를 나타낸다. 그러한 단편은 예를 들어, 아미노산 말단에서의 절단, 카복시 말단에서의 절단 및/또는 아미노산 서열로부터의 잔기(들)의 내부 결손으로부터 일어날 수 있다. 단편은 예를 들어, 대안적인 RNA 스플라이싱(splicing)으로부터 또는 생체내 프로테아제 활성으로부터 발생될 수 있다. 특정 실시형태에서, hOX40L 단편은 hOX40L 폴리펩타이드 또는 hOX40L 폴리펩타이드에 특이적으로 결합하는 항체의 아미노산 서열의 적어도 5개의 인접 아미노산 잔기, 적어도 10개의 인접 아미노산 잔기, 적어도 15개의 인접 아미노산 잔기, 적어도 20개의 인접 아미노산 잔기, 적어도 25개의 인접 아미노산 잔기, 적어도 40개의 인접 아미노산 잔기, 적어도 50개의 인접 아미노산 잔기, 적어도 60 인접한 아미노 잔기, 적어도 70개의 인접 아미노산 잔기, 적어도 80개의 인접 아미노산 잔기, 적어도 90개의 인접 아미노산 잔기, 적어도 인접한 100개의 아미노산 잔기, 적어도 125개의 인접 아미노산 잔기, 적어도 150개의 인접 아미노산 잔기, 적어도 175개의 인접 아미노산 잔기, 적어도 200개의 인접 아미노산 잔기, 또는 적어도 250개의 인접 아미노산 잔기의 아미노산 서열을 포함하는 폴리펩타이드를 포함한다. 구체적인 실시형태에서, hOX40L 폴리펩타이드의 단편 또는 hOX40L 항원에 특이적으로 결합하는 항체는 폴리펩타이드 또는 항체의 적어도 1개, 적어도 2개, 또는 적어도 3개의 기능을 보유한다.
용어 "완전 인간 항체" 또는 "인간 항체"는 본 명세서에서 상호 교환 가능하게 사용되고, 인간 가변 영역, 가장 바람직하게는 인간 불변 영역을 포함하는 항체를 나타낸다. 구체적인 실시형태에서, 그 용어는 인간 기원의 가변 영역 및 불변 영역을 포함하는 항체를 나타낸다. "완전 인간" 항-hOX40L 항체는 특정 실시형태에서 hOX40L 폴리펩타이드를 결합하고, 인간 생식계열 면역글로불린 핵산 서열의 자연 발생 체세포 변이체인 핵산 서열에 의해서 코딩되는 항체를 또한 포함한다. 구체적인 실시형태에서, 본 명세서에 제공된 항-hOX40L 항체는 완전 인간 항체이다. 용어 "완전 인간 항체"는 카바트(문헌[Kabat et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242]를 참고하기 바람) 등에 의해서 기술된 바와 같이 인간 생식계열 면역글로불린 서열에 상응하는 가변 영역 및 불변 영역을 갖는 항체를 포함한다. 완전 인간 항체를 생성하는 예시적인 방법이 예를 들어 본 명세서에서 실시예에 제공되지만, 관련 기술 분야에 공지된 임의의 방법이 사용할 수 있다.
구 "재조합 인간 항체"는 재조합 수단에 의해 제조되거나, 발현되거나, 생성되거나, 단리된 인간 항체, 예컨대 숙주 세포 내로 형질주입된 재조합 발현 벡터를 사용하여 발현된 항체, 재조합, 조합 인간 항체 라이브러리로부터 단리된 항체, 인간 면역글로불린 유전자에 대해서 형질전환되고/되거나 트랜스크로모조멀(transchromosomal)인 동물(예를 들어, 마우스 또는 소)로부터 단리된 항체(예를 들어, 문헌[Taylor, L. D. et al. (1992) Nucl. Acids Res. 20:6287-6295] 참조) 또는 인간 면역글로불린 유전자 서열의 다른 DNA 서열에 대한 스플라이싱을 수반하는 임의의 다른 수단에 의해 제조되거나, 발현되거나, 생성되거나, 단리된 항체를 포함한다. 그러한 재조합 인간 항체는 인간 생식계열 면역글로불린 서열로부터 유도된 가변 영역 및 불변 영역을 가질 수 있다([Kabat, E. A. et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242] 참조). 그러나, 특정 실시양태에서, 그러한 재조합 인간 항체는 시험관내 돌연변이 유발(또는, 인간 Ig 서열에 대해서 형질전환된 동물이 사용되는 경우, 생체내 체세포 돌연변이 유발)에 적용되고, 따라서, 재조합 항체의 VH 및 VL 영역의 아미노산 서열은, 인간 생식계열 VH 및 VL 서열로부터 유도되고 이와 관련되지만 자연 상태에서는 생체내에서 인간 항체 생식계열 레퍼토리 내에 존재하지 않을 수 있는 서열이다.
용어 "융합 단백질"은 본 명세서에서 사용되는 바와 같이 항체의 아미노산 서열 및 이종성 폴리펩타이드 또는 단백질의 아미노산 서열을 포함하는 폴리펩타이드를 나타낸다(즉, 폴리펩타이드 또는 단백질은 정상적으로 항체의 일부가 아니다(예를 들어, 비-항-hOX40L 항원 항체)). 용어 hOX40L 또는 항-hOX40L 항체와 관련하여 사용되는 경우 "융합"은 펩타이드 또는 폴리펩타이드, 또는 이의 단편, 변이체 및/또는 유도체와 이종성 펩타이드 또는 폴리펩타이드의 결합을 나타낸다. 바람직하게는, 융합 단백질은 hOX40L 또는 항-hOX40L 항체의 생물학적 활성을 보유한다. 특정 실시형태에서, 융합 단백질은 hOX40L 항체 VH 도메인, VL 도메인, VH CDR(1, 2 또는 3개의 VH CDR), 및/또는 VL CDR(1, 2 또는 3개의 VL CDR)을 포함하고, 여기서 융합 단백질은 hOX40L 에피토프에 특이적으로 결합한다.
항체에 관련하여 사용되는 경우 용어 "중쇄"는 중쇄 불변 도메인의 아미노산 서열을 기초로 하는, 즉 알파(α), 델타(δ), 엡실론(ε), 감마(γ) 및 뮤(μ)라 불리는 5개의 특유한 유형을 나타낸다. 이러한 특유한 유형의 중쇄는 널리 공지되어 있고, IgG의 4개의 하위부류, 즉 IgG1, IgG1, IgG3 및 IgG4를 포함하여 항체의 5개의 부류, 즉 IgA, IgD, IgE, IgG 및 IgM을 형성한다. 바람직하게는, 중쇄는 인간 중쇄이다. 일례에서, 중쇄는 장애를 갖는 IgG 동종형, 예를 들어, 장애를 갖는 IgG4이다. 특정 실시형태에서, 본 발명의 항체는 인간 감마 4 불변 영역을 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 Fc-γ 수용체를 결합하지 않고, 예를 들어, Leu235Glu 돌연변이를 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 안정성을 증가시키기 위해서 Ser228Pro 돌연변이를 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 IgG4-PE이다.
용어 "숙주"는 본 명세서에서 사용되는 바와 같이 동물, 바람직하게는 포유동물, 가장 바람직하게는 인간을 나타낸다.
용어 "숙주 세포"는 본 명세서에서 사용되는 바와 같이 핵산 분자 내로 형질주입된 특정 대상체 세포 및 그러한 세포의 자손체 또는 잠재적인 자손체를 나타낸다. 그러한 세포의 자손체는 후속 세대에서 발생할 수 있는 돌연변이 또는 환경적인 영향 또는 핵산 분자의 숙주 세포 게놈 내로의 통합으로 인해서 핵산 분자 내로 형질주입된 모 세포와 동일하지 않을 수 있다.
용어 "면역조절제" 및 면역조절제들을 포함하고 이로 제한되지 않는 변형 표현은 본 명세서에서 사용되는 바와 같이 숙주의 면역계를 조절하는 작용제를 나타낸다. 특정 실시형태에서, 면역조절제는 면역억제제이다. 다른 특정 실시형태에서, 면역조절제는 면역자극제이다. 본 발명에 따르면, 본 발명의 조합 요법에 사용되는 면역조절제는 항-hOX40L 항체 또는 항원-결합 단편을 포함하지 않는다. 면역조절제는 소분자, 펩타이드, 폴리펩타이드, 단백질, 융합 단백질, 항체, 무기 분자, 모방제(mimetic agent), 및 유기 분자를 포함하지만 이에 제한되는 것은 아니다.
본 명세서에서 사용되는 바와 같이, 다른 치료제 투여와 관련하여 용어 "조합으로"는 하나를 초과하는 치료제의 사용을 의미한다. 용어 "조합으로"의 사용이, 치료제가 질환을 갖는 대상에게 투여되는 순서를 제한하는 것은 아니다. 제1 치료제는 hOX40L-매개된 질환이 발병한 적이 있거나 개시된 상태이거나 발병에 취약한 대상체에게 제2 치료제의 투여 전에 (예를 들어, 1분, 45분, 30분, 45분, 1시간, 2시간, 4시간, 6시간, 12시간, 24시간, 48시간, 72시간, 96시간, 1주, 2주, 3주, 4주, 5주, 6주, 8주 또는 12주 전에), 투여와 동시에 또는 투여 이후에 (예를 들어, 1분, 45분, 30분, 45분, 1시간, 2시간, 4시간, 6시간, 12시간, 24시간, 48시간, 72시간, 96시간, 1주, 2주, 3주, 4주, 5주, 6주, 8주, 또는 12주 후에) 투여될 수 있다. 임의의 추가의 치료제가 다른 추가의 치료제와 함께 임의의 순서로 투여될 수 있다. 특정 실시형태에서, 본 발명의 항체는 1종 이상의 치료제(예를 들어, hOX40L-매개된 질환의 예방, 치료, 관리 및/또는 완화를 위해 동시에 투여되는 본 발명의 항체가 아닌 치료제)와 조합으로 투여될 수 있다. 본 발명의 항체와 조합으로 투여될 수 있는 치료제의 비제한적인 예는 진통제, 마취제, 항생제, 또는 면역조절제 또는 미국 약전(U.S. Pharmacopoeia) 및/또는 의사 처방 참고서(Physician's Desk Reference)에 열거된 임의의 다른 작용제를 포함한다.
"단리된" 또는 "정제된" 항체에는 항체가 유도되는 세포 또는 조직 공급원으로부터의 세포 물질 또는 다른 오염 단백질이 실질적으로 존재하지 않거나, 또는 화학적으로 합성된 경우 화학적 전구체 또는 다른 화학물질이 실질적으로 존재하지 않는다. 용어 "세포 물질이 실질적으로 존재하지 않는"은 그로부터 항체가 단리되는 세포의 세포 성분으로부터 분리되거나 재조합 방식으로 생산된 항체의 제제를 포함한다. 따라서, 세포 물질이 실질적으로 존재하지 않는 항체는 약 30%, 20%, 10%, 또는 5% 미만(건조 중량 기준)의 이종성 단백질(본 명세서에서 "오염 단백질"이라고도 칭함)을 갖는 항체의 제제를 포함한다. 항체가 재조합 방식으로 생산되는 경우, 배양 배지가 실질적으로 존재하지 않는 것이 또한 바람직하며, 즉, 배양 배지는 단백질 제제 부피의 약 20%, 10%, 또는 5% 미만을 나타낸다. 항체가 화학 합성에 의해 생산되는 경우, 항체에 화학 전구체 또는 다른 화학물질이 실질적으로 존재하지 않는 것이 바람직하고, 즉, 항체는 단백질 합성에 관련되는 화학적 전구체 또는 다른 화학물질로부터 분리된다. 따라서, 그러한 항체 제제는 관심 항체 이외의 다른 화학 전구체 또는 화합물을 약 30%, 20%, 10%, 5% 미만 (건조 중량 기준)으로 포함한다. 바람직한 실시형태에서, 본 발명의 항체는 단리되거나 정제된 것이다.
"단리된" 핵산 분자는 핵산 분자의 자연 공급원에 존재하는 다른 핵산 분자로부터 분리된 것이다. 또한, "단리된" 핵산 분자, 예컨대 cDNA 분자에는 재조합 기술에 의해 생산되는 경우 다른 세포 물질, 또는 배양 배지가 실질적으로 존재하지 않거나, 또는 화학적으로 합성되는 경우 화학 전구체 또는 다른 화학물질이 실질적으로 존재하지 않을 수 있다. 구체적인 실시형태에서, 본 발명의 항체를 코딩하는 핵산 분자(들)는 단리되거나 정제된 것이다
용어 "인간 OX40L", "hOX40L" 또는 "hOX40L 폴리펩타이드" 및 유사한 용어는 서열 목록의 아미노산 서열을 포함하는 폴리펩타이드("폴리펩타이드", "펩타이드" 및 "단백질"은 본 명세서에서 상호 교환 가능하게 사용됨) 및 그의 SNP 변이체를 비롯한 관련 폴리펩타이드를 나타낸다. 관련 폴리펩타이드는 바람직하게는 hOX40L 활성을 보유하고/하거나 항-hOX40L 면역 반응을 생성하기에 충분한 대립유전자 변이체(예를 들어, SNP 변이체); 스플라이스 변이체; 단편; 유도체; 치환, 결손, 및 삽입 변이체; 융합 폴리펩타이드; 및 종간 상동체를 포함한다. 또한, 항-hOX40L 면역학적 반응을 생성하기기에 충분한 가용성 형태의 hOX40L이 또한 포함된다. 관련 기술 분야의 통상의 기술자가 이해할 바와 같이, 본 발명의 항-hOX40L 항체는 hOX40L 폴리펩타이드, 폴리펩타이드 단편, 항원, 및/또는 에피토프에 결합할 수 있는데, 이는 에피토프가 보다 큰 항원의 일부이고, 이 항원은 보다 큰 폴리펩타이드 단편의 일부이고, 이 단편은 다시 보다 큰 폴리펩타이드의 일부이기 때문이다. hOX40L는 삼량체(네이티브) 또는 단량체(변성) 형태로 존재할 수 있다.
용어 "카바트 넘버링" 및 유사한 용어는 관련 기술 분야에서 인식되고, 항체의 중쇄 가변 영역 또는 이의 항원 결합 부분 내의 다른 아미노산 잔기보다 더 가변성(즉, 초가변성)인 아미노산 잔기를 넘버링하는 시스템을 나타낸다([Kabat et al. (1971) Ann. NY Acad. Sci. 190:382-391] 및 [Kabat et al. (1991) Sequences of Proteins of Immunological Interest, Fifth Edition, U.S. Department of Health and Human Services, NIH Publication No. 91-3242]). 중쇄 가변 영역에서, 초가변 영역은 전형적으로 CDR1의 경우 아미노산 위치 31 내지 35, CDR2의 경우 아미노산 위치 50 내지 65, 및 CDR3의 경우 아미노산 위치 95 내지 102 범위이다.
용어 "단클론성 항체"는 균일한 또는 실질적으로 균일한 항체 집단으로부터 얻은 항체를 말하며, 각각의 단클론성 항체는 전형적으로 항원 상의 단일 에피토프를 인식할 것이다. 바람직한 실시형태에서, 본 명세서에서 사용되는 바와 같이 "단클론성 항체"는 단일 하이브리도마 또는 다른 세포에 의해 생산된 항체이고, 여기서 항체는 예를 들어 ELISA 또는 관련 기술 분야에서 공지되거나 본 명세서에 제공된 실시예의 다른 항원-결합 또는 경쟁적 결합 검정법에 의해서 결정되는 바와 같이 hOX40L 에피토프에만 특이적으로 결합한다. 용어 "단클론성"은 항체를 제조하기 위한 임의의 특정 방법으로 제한되지 않는다. 예를 들어, 본 발명의 단클론성 항체는 문헌[Kohler et al.; Nature, 256:495 (1975)]에 기술된 바와 같은 하이브리도마 방법에 의해 제조되거나 또는 예를 들어 본 명세서에서 기술된 바와 같은 기술을 사용하여 파지 라이브러리로부터 단리될 수 있다. 클론성 세포주 및 이에 의해 발현된 단클론성 항체의 제조를 위한 다른 방법은 관련 기술 분야에 널리 공지되어 있다(예를 들어, [Chapter 11 in: Short Protocols in Molecular Biology, (2002) 5th Ed., Ausubel et al., eds., John Wiley and Sons, New York] 참조). 다른 단클론성 항체를 생산하는 다른 예시적인 방법이 본 명세서의 실시예에서 제공된다.
생물학적 물질, 예컨대 핵산 분자, 폴리펩타이드, 숙주 세포 등과 관련하여 사용되는 경우 용어 "자연 발생" 또는 "네이티브"는 자연에서 발견되는 것으로서 인간에 의해 조작되지 않은 것을 나타낸다.
용어 "약제학적으로 허용 가능한"은 본 명세서에서 사용되는 바와 같이 미국 연방 또는 미국 주 정부의 감독 기관에 의해 승인되거나, 또는 미국 약전, 유럽 약전 또는 동물에서, 보다 특히 인간에서 사용하기 위한 일반적으로 인정되는 다른 약전에 열거되었음을 의미한다.
"다클론성 항체" 본 명세서에서 사용되는 바와 같이 많은 에피토프를 갖는 단백질에 대한 면역성 반응에서 생성되는 항체 집단을 말하고, 따라서 단백질 내의 동일한 에피토프 및 상이한 에피토프에 대해 작용하는 다양한 상이한 항체를 포함한다. 다클론성 항체를 생산하는 방법은 관련 기술 분야에 공지되어 있다(예를 들어, [Chapter 11 in: Short Protocols in Molecular Biology, (2002) 5th Ed., Ausubel et al., eds., John Wiley and Sons, New York] 참조).
본 명세서에서 사용되는 바와 같이, 용어 "폴리뉴클레오타이드", "뉴클레오타이드," 핵산" "핵산 분자" 및 다른 유사한 용어는 상호 교환 가능하게 사용되고, DNA, RNA, mRNA 등을 포함한다.
본 명세서에서 사용되는 바와 같이, 용어 "예방하다", "예방하는" 및 "예방"은 본 명세서에 제공된 치료제 또는 치료제 조합물(예를 들어, 예방제 또는 치료제, 예컨대 본 발명의 항체의 조합물)의 투여에 의한, hOX40L-매개된 질환 및/또는 이와 관련된 증상의 전개, 재발, 발병 또는 확산의 완전한 또는 부분적인 억제를 나타낸다.
본 명세서에서 사용되는 바와 같이, 용어 "예방제"는 대상체에서 hOX40L-매개된 질환 및/또는 이와 관련된 증상의 전개, 재발, 발병 또는 확산을 완전히 또는 부분적으로 억제할 수 있는 임의의 작용제를 나타낸다. 특정 실시형태에서, 용어 "예방제"는 본 발명의 항체를 나타낸다. 다른 특정 실시형태에서, 용어 "예방제"는 본 발명의 항체 이외의 작용제를 나타낸다. 바람직하게는, 예방제는 hOX40L-매개된 질환 및/또는 이와 관련된 증상을 예방하거나 또는 hOX40L-매개된 질환 및/또는 이와 관련된 증상의 발병, 전개, 진행 및/또는 중증도를 지연시키기 위해 유용한 것으로 공지되어 있거나, 사용되었거나, 현재 사용되고 있는 작용제이다. 구체적인 실시형태에서, 예방제는 완전 인간 항-hOX40L 항체, 예를 들어 완전 인간 항-hOX40L 단클론성 항체이다
실시형태에서, 예방조치는 질환 또는 병태의 발병 또는 질환 또는 병태의 증상을 예방한다. 일 실시형태에서, 예방 치료는 질환 또는 병태의 악화 또는 발병을 예방한다. 일 실시형태에서, 예방 치료는 질환 또는 병태의 악화를 예방한다.
또 다른 실시형태에서, 본 발명의 항-OX40L 항체는 이식, 예를 들어 혈액 또는 기관 이식 이전에 또는 부수적으로) 정맥내로 투여된다. 또 다른 실시형태에서, 상기 항체는 약 5 내지 10mg/kg(예를 들어, 약 8mg/kg)의 용량으로 투여된다. 또 다른 실시형태에서, 상기 항체는 약 0.1mg/kg, 약 0.5mg/kg, 약 1mg/kg, 3mg/kg, 5mg/kg, 약 10mg/kg, 약 15mg/kg, 약 20mg/kg, 약 25mg/kg, 약 30mg/kg, 약 40mg/kg, 약 50mg/kg, 약 60mg/kg, 약 70mg/kg, 약 80mg/kg 약 90mg/kg 또는 약 100mg/kg, 특히 약 1mg/kg, 또는 약 3mg/kg으로부터 선택된 용량으로 투여된다
또 다른 실시형태에서, 상기 항체는 (예를 들어, 혈액 또는 기관의) 이식 1 내지 4일 이전에, 예를 들어 이식 1 내지 3일 이전에 또는 이식 1 내지 2일 이전에 투여된다. 또 다른 실시형태에서, 상기 항체는 이식 이후에 매주, 격주 또는 매달, 예를 들어, 격주로 투여된다. 추가 실시형태에서, 상기 항체는 이식 이전에 약 5 내지 10mg/kg(예를 들어, 약 8mg/kg)의 용량으로 이식 1 내지 3일 전에 정맥내로 예방적으로 투여되고, 그 다음 약 5 내지 10mg/kg(예를 들어, 약 8mg/kg)의 용량으로 격주로 정맥내로 투여된다.
또 다른 실시형태에서, 환자는 GvHD(예를 들어, 급성 GvHD)의 전개에 대한 예측성 바이오마커의 존재 하에서 이식 이후에 주기적으로 모니터링되고, 바이오마커 수준이 환자가 GvHD(예를 들어, 급성 GvHD) 전개 위험이 있다고 결정되도록 하는 수준이 되면 본 발명의 항-OX40L 항체가 투여된다. 이러한 전략은 약물의 불필요한 투여 및 면역계의 불필요한 억제를 방지할 것이다. 급성 GvHD의 예측성 바이오마커로서 유용할 수 있는 바이오마커의 예는 문헌[Levine et al., "A prognostic score for acute graft-versus-host disease based on biomarkers : a multicentre study", Lancet Haematol 2015; 2:e21-29]에서 식별된 것일 수 있다. 이러한 바이오마커는 TNFR1, ST-2, 엘라핀 및 IL2Rα 및 Reg3α를 포함하지만, 이들로 제한되는 것은 아니다.
에피토프에 기여하는 hOX40L의 영역은 폴리펩타이드의 인접 아미노산일 수 있거나, 에피토프는 폴리펩타이드의 둘 이상의 비-인접 영역으로부터 함께 형성될 수 있다. 에피토프는 항원의 3차원 표면 특징부이거나 그것이 아닐 수 있다. 면역 반응을 일으킬 수 있는 hOX40L 항원의 표면 상의 국지적인 영역은 hOX40L 에피토프이다. 에피토프는 항원의 3차원 표면 특징부이거나 그것이 아닐 수 있다.
"hOX40L-매개된 질환" 및 "hOX40L-매개된 병태"는 상호 교환 가능하게 사용되고, 완전히 또는 부분적으로 hOX40L에 의해 야기되거나 hOX40L의 결과인 임의의 질환 또는 병태를 나타낸다. 특정 실시형태에서, hOX40L은 세포의 표면 상에서 비정상적으로(예를 들어, 고도로) 발현된다. 일부 실시형태에서, hOX40L은 특정 세포 유형에서 비정상적으로 상향조절될 수 있다. 다른 실시형태에서, 정상적인, 비정상적인 또는 과도한 세포 신호전달은 hOX40L 리간드에 대한 hOX40L의 결합에 의해 야기된다. 특정 실시형태에서, hOX40L 리간드는 예를 들어 세포, 예컨대 결장 상피 세포의 표면 상에서 발현되는 OX40이다. 특정 실시형태에서, hOX40L-매개된 질환은 염증성 장 질환(IBD), 예컨대 크론병(CD) 또는 궤양성 대장염(UC)이다. 다른 실시형태에서, hOX40L-매개된 질환은 이식편대숙주병(GVHD)이다. 다른 실시형태에서, hOX40L-매개된 질환은 괴저성 농피증, 거대 세포성 동맥염, 슈니츨러 증후군, 비-감염성 공막염 및 포도막염(비-감염성/자가면역 및/또는 전신성)로부터 선택된다. 다른 실시형태에서, hOX40L 매개된 질환 또는 병태는 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부; 예를 들어 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염, 접촉 과민증, 다발성 경화증 및 죽상동맥경화증, 특히 GvHD로부터 선택된다.
용어 "hOX40L 수용체" 또는 "hOX40L 결합 수용체"는 본 명세서에서 상호 교환 가능하게 사용되고, hOX40L에 결합하는 수용체 폴리펩타이드를 나타낸다. 구체적인 실시형태에서, hOX40L 수용체는 Hox40이다. 일부 실시형태에서, hOX40L 수용체는 세포의 표면, 예컨대 결장 상피 세포; 또는 이식편 또는 이식 조직 또는 숙주 조직 상에서 발현된다.
본 명세서에서 사용되는 바와 같이, 용어 "대상체" 및 "환자"는 상호 교환 가능하게 사용된다. 본 명세서에서 사용되는 바와 같이, 대상체는 바람직하게는 포유동물, 예컨대 비-영장류(예를 들어, 소, 돼지, 말, 고양이, 개, 래트 등) 또는 영장류(예를 들어, 원숭이 및 인간), 가장 바람직하게는 인간이다. 일 실시형태에서, 대상체는 hOX40L-매개된 질환을 갖는 포유동물, 바람직하게는 인간이다. 또 다른 실시형태에서, 대상체는 hOX40L-매개된 질환이 전개할 위험이 있는 포유동물, 바람직하게는 인간이다.
본 명세서에서 사용되는 바와 같이 "실질적으로 전부"는 적어도 약 60%, 적어도 약 70%, 적어도 약 75%, 적어도 약 80%, 적어도 약 85%, 적어도 약 90%, 적어도 약 95%, 적어도 약 98%, 적어도 약 99%, 또는 약 100%를 나타낸다.
용어 "계면활성제가 실질적으로 존재하지 않는"은 본 명세서에서 사용되는 바와 같이 hOX40L 항원에 특이적으로 결합하는 항체의 제제가 0.0005% 미만, 0.0003% 미만, 또는 0.0001% 미만의 계면활성제 및/또는 0.0005% 미만, 0.0003% 미만, 또는 0.0001% 미만의 계면활성제를 함유함을 나타낸다.
용어 "염이 실질적으로 존재하지 않는"은 본 명세서에서 사용되는 바와 같이 hOX40L 항원에 특이적으로 결합하는 항체의 제제가 0.0005% 미만, 0.0003% 미만, 또는 0.0001% 미만의 무기 염을 함유함을 나타낸다.
용어 "계면활성제"는 본 명세서에서 사용되는 바와 같이 양친매성 구조를 갖는 유기 물질을 말하며; 즉, 계면활성제는 반대되는 용해도 경향을 갖는 기, 전형적으로 지용성 탄화수소쇄 및 수용성 이온기로 구성된다. 계면활성제는 표면-활성 모이어티의 전하에 따라서 음이온성, 양이온성 및 비이온성 계면활성제로 분류될 수 있다. 계면활성제는 종종 생물학적 물질의 다양한 약제학적 조성물 및 제제의 습윤제, 유화제, 가용화제, 및 분산제로서 사용된다.
본 명세서에서 사용되는 바와 같이, 용어 "태그"는 예를 들어 폴리펩타이드 및/또는 hOX40L 또는 hOX40L 항체 또는 이의 항원 결합 단편을 코딩하는 폴리뉴클레오티드에 부착된 임의의 유형의 모이어티를 나타낸다. 예를 들어, hOX40L, hOX40L 항체 항체 또는 이의 항원 결합 단편을 코딩하는 폴리뉴클레오티드는 예를 들어 검출 가능한 모이어티 또는 친화도 정제를 돕는 모이어티를 코딩하는 하나 이상의 추가적인 태그-코딩 뉴클레오티드 서열을 함유할 수 있다. 번역될 때, 태그 및 항체는 융합 단백질의 형태일 수 있다. 태그와 관련하여 용어 "검출 가능한" 또는 "검출"은 임의의 태그가 가시화될 수 있거나 태그의 존재를 다른 방식으로 (예를 들어, 정량화에 의해서) 결정 및/또는 측정할 수 있음을 나타낸다. 검출 가능한 태그의 비제한적인 예는 형광성 태그이다.
본 명세서에서 사용되는 바와 같이, 용어 "치료제"는 hOX40L-매개 질병 및/또는 이와 관련된 증상의 치료, 관리 또는 완화에 사용될 수 있는 임의의 작용제를 나타낸다. 특정 실시형태에서, 용어 "치료제"는 본 발명의 항체를 나타낸다. 다른 특정 실시형태에서, 용어 "치료제"는 본 발명의 항체 이외의 다른 작용제를 나타낸다. 바람직하게는, 치료제는 hOX40L-매개된 질환 또는 이와 관련된 하나 이상의 증상의 치료, 관리 또는 완화를 위해 유용한 것으로 공지되거나, 사용되었거나, 현재 사용되고 있는 작용제이다. 구체적인 실시형태에서, 치료제는 완전 인간 항-hOX40L 항체, 예컨대 완전 인간 항-hOX40L 단클론성 항체이다.
치료제들의 조합물(예를 들어, 예방제 또는 치료제의 사용)은 임의의 2종 이상의 단일 치료제의 부가 효과보다 더 효과적이다. 예를 들어, 예방 및/또는 치료제의 조합물의 상승작용적 효과는 hOX40L-매개된 질환이 존재하는 대상체에 대한 작용제의 보다 낮은 투여량의 사용 및/또는 상기 작용제의 보다 적은 투여 횟수를 허용한다. 예방 또는 치료적인 치료제의 보다 낮은 투여량의 이용 및/또는 상기 치료제의 보다 적은 투여 횟수에 대한 능력은 hOX40L-매개된 질환의 예방, 관리, 치료 또는 완화시에 상기 치료제의 효능을 감쇠시키지 않으면서, 대상체에 대한 상기 치료제의 투여와 관련된 독성을 감쇠시킨다. 또한, 상승작용적 효과는 hOX40L-매개된 질환의 예방, 또는 관리, 치료 또는 완화에서 치료제의 효능을 개선할 수 있다. 마지막으로, 치료제(예를 들어, 예방제 또는 치료제)의 조합물의 상승작용적 효과는 임의의 단일 요법의 사용과 관련된 유해하거나 원치 않는 부작용을 방지하거나 감쇠시킬 수 있다.
일 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와, 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 포함한다. 또 다른 실시형태에서 조합물은 본 발명의 항-OX40L 항체와, 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, CTLA4-Fc 분자(예를 들어, 아바타셉트), 항-CD40L 항체, 항-LFA1 항체, 항-CD52 항체(예를 들어, 알렘투주맙), 사이클로포스파미드 및 항-흉선세포 글로불린으로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 포함한다.
일부 실시형태에서 조합물은 본 발명의 항-OX40L 항체와, 칼시뉴린 억제제(예를 들어, 타크롤리무스, 사이클로스포린), mTOR 억제제(예를 들어, 라파마이신(시롤리무스)), 및 항증식제(예를 들어, 마이코페놀레이트 모페틸, 사이클로포스파미드)로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 포함한다.
추가 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와, IL-2 신호전달을 조절하는 면역억제제(예를 들어, 타크롤리무스, 사이클로스포린, 라파마이신(시롤리무스), 및 항-CD25 항체(예를 들어, 바실릭수맙, 다클리주맙)로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 포함한다.
이론에 얽매이고자 함은 아니지만, 본 발명의 항-OX40L 항체의 작용 기전은 면역 기능을 조절하는 추가 치료제와 상호 보완적이라고 생각된다. 특히, IL-2 신호전달을 조절하거나, IL-2/IL-2R-매개된 T 세포 증식을 억제하는 작용제는 항-OX40L 항체와 상승작용적으로 조합될 수 있어서, 작용제 단독에서 관찰될 것보다 더 높은 면역 조절을 유발한다. 하기 본 명세서에서 실시예 7 및 9에 나타내어진 바와 같이, 타크롤리무스 및 라파마이신 둘 모두는 면역 조절 활성을 나타낸다. 타크롤리무스 및 라파마이신 둘 모두는 IL-2 신호전달을 조절한다고 공지된 작용제이다. 특히, 라파마이신은 IL-2 및 IL2R 전사를 감쇠시키고, IL2R 활성화에 의해서 유발되는 세포 주기 진행을 억제하는 mTOR 억제제로서 작용한다고 공지되어 있지만, mTOR 억제제가 기능할 수 있는 T 세포의 증식에 대해서 다른 기전이 존재할 수 있다.(Thomson et al, Nat. Rev. Immunol., 2009, 9(5), 324-337; Scheffert & Raza, J. Thorac. Dis., 2014, 6(8), 1039-1053). 본 명세서의 도 6은 항-OX40L 항체의 기전이 이러한 두 작용제 모두에 대한 Tscm 집단과 관련하여 상이하다는 것을 나타내고, 도 7은 라파마이신과 조합된 본 발명의 항-OX40L 항체의 생존에 대한 상승작용적 효과를 나타낸다. 따라서, 라파마이신 및/또는 타크롤리무스에 대해서 유사한 작용 기전을 갖는 다른 작용제가 또한 본 발명의 항-OX40L 항체와 조합으로 사용되는 경우 상승작용적 효과를 유발할 것이라고 생각된다.
일 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 라파마이신(시롤리무스)을 포함한다.
일 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 타크롤리무스를 포함한다. 일 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 타크롤리무스 및 메토트렉세이트의 조합물을 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 사이클로스포린을 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 사이클로스포린 및 메토트렉세이트를 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 사이클로포스파미드를 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 마이코페놀레이트 모페틸을 포함한다.
본 명세서에서 사용되는 바와 같이, 용어 "요법"은 hOX40L-매개된 질환(예를 들어, IBD 또는 GVHD)의 예방, 관리, 치료 및/또는 완화에 사용될 수 있는 임의의 프로토콜, 방법 및/또는 작용제를 나타낸다. 특정 실시형태에서, 용어 "요법들" 및 "요법"은 생물학적 요법, 지지 요법, 및/또는 관련 기술 분야의 통상의 기술자, 예를 들어 의료인에게 공지된 hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에 유용한 다른 요법을 나타낸다.
본 명세서에서 사용되는 바와 같이, 용어 "치료하다", "치료" 및 "치료하는"은 1종 이상의 치료제의 투여(1종 이상의 예방제 또는 치료제, 예를 들어 본 발명의 항체의 투여를 포함하지만, 이들로 제한되는 것은 아님)에 의한 hOX40L-매개된 질환(예를 들어, IBD 또는 GVHD)의 진행, 중증도, 및/또는 시간의 감쇠 또는 완화를 나타낸다. 구체적인 실시형태에서, 그러한 용어는 OX40에 대한 hOX40L의 결합의 감쇠 또는 억제, hOX40 또는 hOX40L을 발현하는 세포로부터의 CCL20의 생산 또는 분비의 감쇠 또는 억제, hOX40 또는 hOX40L을 발현하는 세포로부터의 IL-8의 생산 또는 분비의 감소 또는 억제, hOX40 또는 hOX40L을 발현하는 세포로부터의 RANTES의 생산 또는 분비의 감소 또는 억제, 및/또는 hOX40L-매개된 질환, 예컨대 IBD 또는 GVHD와 연관된 하나 이상의 증상의 억제 또는 감소를 나타낸다. 구체적인 실시형태에서, 그러한 용어는 OX40에 대한 hOX40L의 결합의 감쇠 또는 억제, hOX40 또는 hOX40L을 발현하는 세포로부터의 INF-γ의 생산 또는 분비의 감쇠 또는 억제, hOX40 또는 hOX40L을 발현하는 세포로부터의 TNF-α의 분비의 생산 또는 분비의 감쇠 또는 억제, hOX40 또는 hOX40L을 발현하는 세포로부터의 IL-2의 생산 또는 분비의 감쇠 또는 억제, 및/또는 hOX40L-매개된 질환, 예컨대 IBD 또는 GVHD(특히 GvHD)과 관련된 하나 이상의 증상의 억제 또는 감쇠를 나타낸다. 예에서, 세포는 인간 세포이다. 구체적인 실시형태에서, 예방제는 완전 인간 항-hOX40L 항체, 예컨대 완전 인간 항-hOX40L 단클론성 항체이다.
용어 "가변 영역" 또는 "가변 도메인"은 OX40L 및 중쇄의 일부, 전형적으로 중쇄의 대략 아미노-말단의 120 내지 130개 아미노산 및 경쇄의 약 100 내지 110개 아미노산을 나타내고, 이것은 항체 사이에서 그 서열이 크게 상이하고, 그의 특정 항원에 대한 각각의 특정 항체의 결합 및 특이성에서 사용된다. 서열의 가변성은 상보성 결정 영역(CDR)으로 불리는 그러한 영역에 집중되고, 가변 도메인 내의 보다 고도로 보존된 역역은 프레임워크 영역(FR)으로 불린다. OX40L 및 중쇄의 CDR은 주로 항체와 항원의 상호작용을 책임진다. 본 명세서에서 사용되는 아미노산 위치의 넘버링은 문헌[Kabat et al. (1991) Sequences of proteins of immunological interest. (U.S. Department of Health and Human Services, Washington, D. C.) 5th ed. ("Kabat et al.")]에서와 같은 EU 인덱스(Index)에 따른다. 바람직한 실시형태에서, 가변 영역은 인간 가변 영역이다.
항체
본 발명의 항체는 합성 항체, 단클론성 항체, 제조합으로 생산된 항체, 다중특이적인 항체(이중-특이적인 항체 포함), 인간 항체, 인간화 항체, 키메릭 항체, 인트라바디, 단일-쇄 Fv(scFv)(예를 들어, 단일특이적, 이중특이적 등), 낙타화 항체, Fab 단편, F(ab') 단편, 다이설파이드-연결된 Fv(sdFv), 항-이디오타입(항-Id) 항체, 및 상기 중 임의의 것의 에피토프-결합 단편을 포함하지만, 이들로 제한되는 것은 아니다.
특히, 본 명세서에 제공된 항체는 면역글로불린 분자 및 면역글로불린 분자의 면역학적 활성 부분, 즉, hOX40L 항원에 특이적으로 결합하는 항원 결합 부위를 함유하는 분자를 포함한다. 본 명세서에 제공된 면역글로불린 분자는 임의의 유형(예를 들어, IgG, IgE, IgM, IgD, IgA 및 IgY), 부류(예를 들어, IgG1, IgG2, IgG3, IgG4, IgA1 및 IgA2) 또는 하위부류의 면역글로불린 분자일 수 있다. 구체적인 실시형태에서, 본 명세서에 제공된 항체는 IgG 항체, 바람직하게는 IgG1 또는 IgG4이다. 특정 실시형태에서, 본 발명의 항체는 인간 감마 4 불변 영역을 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 Fc-γ 수용체를 결합하지 않고, 예를 들어, Leu235Glu 돌연변이를 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 안정성을 증가시키기 위해서 Ser228Pro 돌연변이를 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 IgG4-PE이다.
항체의 변이체 및 유도체는 에피토프에 특이적으로 결합하는 능력을 보유하는 항체 단편을 포함한다. 바람직한 단편은 Fab 단편; Fab'(Fab 및 경첩 영역을 통해서 중쇄의 추가 부분을 포함하는 단일 항-결합 도메인을 함유하는 항체 단편); F(ab')2(중쇄의 경첩 영역에서 쇄내 다이설파이드 결합에 의해서 결합된 2개의 Fab' 분자; Fab' 분자는 동일하거나 상이한 에피토프에 대해 지향될 수 있음); 이중특이적인 Fab(각각 상이한 에피토프에 대해 지향될 수 있는 2개의 항원 결합 도메인을 갖는 Fab 분자); sFv로서도 공지된 가변 영역을 포함하는 단일 쇄 Fab 쇄; 다이설파이드-연결된 Fv, 또는 dsFv; 낙타화 VH(VH 계면(interface)에서 일부 아미노산이 자연 발생 낙타 항체의 중쇄에서 발견되는 것인, 항체의 단일 중쇄의 가변, 항원 결합 결정 영역); 이중특이적인 sFv(각각 상이한 에피토프에 대해 지향될 수 있는 2개의 항원 결합 도메인을 갖는 sFv 또는 dsFv 분자); 다이아바디(diabody)(제1 sFv의 VH 도메인이 제2 sFv의 VL 도메인과 조립하고, 제1 sFv의 VL 도메인이 제2 sFv의 VH 도메인과 조립할 때 형성된 이량체화 sFv; 다이아바디의 2개의 항원 결합 영역은 동일하거나 상이한 에피토프에 대해 지향될 수 있음); 및 트라아바디(triabody)(다이아바디와 유사한 방식으로 형성되지만, 3개의 항원-결합 도메인이 단일 복합체 내에 생성되는 삼량체화 sFv; 3개의 항원 결합 도메인은 동일하거나 상이한 에피토프에 대해 지향될 수 있음)를 포함한다. 항체의 유도체는 또한 항체 조합 부위의 하나 이상의 CDR 서열을 포함한다. CDR 서열은 2개 이상의 CDR 서열이 존재할 때 스캐폴드(scaffold) 상에서 함께 연결될 수 있다. 특정 실시형태에서, 본 발명과 함께 사용될 항체는 단일-쇄 Fv("scFv")를 포함한다. scFv는 항체의 VH 및 VL 도메인을 포함하는 항체 단편이고, 여기서 이들 도메인은 단일 폴리펩타이드 쇄 내에 존재한다. 일반적으로, scFv 폴리펩타이드는 VH 도메인과 VL 도메인 사이에 폴리펩타이드 링커(linker)를 추가로 포함하고, 이는 scFv가 항원 결합을 위해 목적하는 구조를 형성할 수 있도록 한다. scFv의 내용에 대해서 문헌[Pluckthun in The Pharmacology of Monoclonal Antibodies, vol. 113, Rosenburg and Moore eds. Springer-Verlag, New York, pp. 269-315 (1994)]을 참고한다.
본 발명의 항체는 새 및 포유동물(예를 들어, 인간, 뮤린, 당나귀, 양, 토끼, 염소, 기니아 피그, 낙타, 말 또는 닭)을 비롯한 임의의 동물 기원의 것일 수 있다. 특정 실시형태에서, 본 발명의 항체는 인간 또는 인간화 단클론성 항체이다. 본 명세서에서 사용되는 바와 같이, "인간" 항체는 인간 면역글로불린의 아미노산 서열을 갖는 항체를 포함하고, 인간 면역글로불린 라이브러리로부터 또는 인간 유전자로부터의 항체를 발현하는 마우스로부터 단리된 항체를 포함한다.
바람직한 실시형태에서, 본 발명의 항체는 완전 인간 항체, 예컨대 hOX40L 폴리펩타이드, hOX40L 폴리펩타이드 단편, 또는 hOX40L 에피토프에 특이적으로 결합하는 완전 인간 항체이다. 그러한 완전 인간 항체는 원치않거나 불필요한 부작용, 예컨대, 대상체에게 투여될 때 비-완전 인간 항체(예를 들어, 다른 종으로부터 유도된 항-hOX40L 항체)에 대해 지향된 면역 반응의 전개를 최소화하기 위해 완전 마우스(또는 다른 완전 또는 부분 비-인간 종 항체), 인간화 항체, 또는 키메릭 항체에 비해 유익할 것이다.
본 발명의 항체는 일특이적, 이중특이적, 삼중특이적 또는 보다 고차의 다중특이적일 수 있다. 다중특이적인 항체는 hOX40L 폴리펩타이드의 상이한 에피토프에 대해 특이적일 수 있거나, hOX40L 폴리펩타이드 및 이종성 에피토프, 예컨대 이종성 폴리펩타이드 또는 고체 지지체 물질 둘 모두에 대해서 특이적일 수 있다. 바람직한 실시형태에서, 본 명세서에서 제공되는 항체는 hOX40L 폴리펩타이드의 특정 에피토프에 일특이적이고, 다른 에피토프에 특이적으로 결합하지 않는다.
또한 본 명세서에서 본 명세서에 기술된 항-hOX40L 항체 또는 단편을 생산하는 B-세포(예를 들어, 영생(immortalised) B-세포) 또는 하이브리도마가 제공된다.
특정 실시형태에서, hOX40L 에피토프에 특이적으로 결합하는 단리된 항체가 본 명세서에서 제공되며, 여기서 항체에 의한 hOX40L 에피토프에 대한 결합이 본 발명의 항체 또는 단편에 의해서 (예를 들어, 용량-의존적인 방식으로) 경쟁적으로 차단된다. 항체는 완전 인간 항체일 수 있거나 이것이 아닐 수 있다. 바람직한 실시형태에서, 항체는 완전 인간 단클론성 항-hOX40L 항체, 보다 더 바람직하게는 완전 인간, 단클론성, 길항제 항-hOX40L 항체이다. 사용될 수 있는 예시적인 경쟁적인 차단 시험은 본 명세서에서 실시예에 제공된다.
일부 실시형태에서, 본 발명의 항체 또는 단편은 세포 표면-발현된 hOX40L에 대한 결합을 위해서 (예를 들어, 용량-의존적인 방식으로) OX40 수용체(또는 이의 융합 단백질)와 경쟁한다. 다른 실시형태에서, 본 발명의 항체 또는 단편은 가용성 hOX40L에 대한 결합을 위해서 (예를 들어, 용량-의존적인 방식으로) OX40 수용체(또는 이의 융합 단백질)와 경쟁한다. 사용될 수 있는 예시적인 경쟁적인 차단 시험은 본 명세서에서 실시예에 제공된다. 일 실시형태에서, 항체 또는 단편은 세포 표면-발현된 OX40L, 예컨대 hOX40L에 대한 hOX40의 결합을 부분적으로 또는 완전히 억제한다. 또 다른 실시형태에서, 항체는 가용성 hOX40L에 대한 hOX40의 결합을 부분적으로 또는 완전히 억제한다. 일부 실시형태에서, 항체 또는 단편은 세포 표면-발현된 OX40을 갖는 세포로부터의 CCL20, IL-8, 및/또는 RANTES, 또는 INF-γ, TNF-α 또는 IL-2, 특히 INF-γ의 분비를 부분적으로 또는 완전히 억제한다. 특정 실시형태에서, OX40을 발현하는 세포는 결장 상피 세포이다.
바람직하게는, 본 발명의 항체는 hOX40L에 특이적으로 결합하는 완전 인간, 단클론성 항체, 예컨대 완전 인간, 단클론성 길항제 항체이다.
일부 실시형태에서, 본 명세서에서 제공된 항체 또는 단편은 (예를 들어, hOX40L 폴리펩타이드의 삼량체 형태에서) hOX40L 폴리펩타이드의 3차원 표면 특징부인 hOX40L 에피토프에 결합한다. 에피토프에 기여하는 hOX40L 폴리펩타이드의 영역은 폴리펩타이드의 인접 아미노산일 수 있거나, 에피토프는 폴리펩타이드의 2개 이상의 비-인접 영역으로부터 함께 형성될 수 있다. hOX40L 에피토프는 (a) hOX40L의 삼량체 형태("삼량체 hOX40L 에피토프"), (b) hOX40L의 단량체 형태("단량체 hOX40L 에피토프"), (c) hOX40L의 삼량체 형태 및 단량체 형태 모두 내에 존재할 수 있거나, (d) hOX40L의 삼량체 형태 내에 존재하지만 단량체 형태 내에 존재하지 않거나, (e) hOX40L의 단량체 형태 내에 존재하지만 삼량체 형태 내에 존재하지 않을 수 있다.
예를 들어, 일부 실시형태에서, 에피토프는 삼량체(네이티브) 형태 내에만 존재하거나 삼량체(네이티브) 형태 내에서 항-hOX40L 항체에 의한 결합을 위해 이용 가능하지만, 단량체(변성) 형태 내에 존재하지 않거나 단량체(변성) 형태 내에서결합을 위해서 이용 가능하지 않다. 다른 실시형태에서, hOX40L 에피토프는 hOX40L 폴리펩타이드(예를 들어, hOX40L 폴리펩타이드의 삼량체 형태 또는 단량체 형태에서)의 선형 특징부이다. 본 명세서에서 제공된 항체는 (a) hOX40L의 단량체 형태의 에피토프에, (b) hOX40L의 삼량체 형태의 에피토프에, (c) hOX40L의 삼량체 형태가 아닌 단량체의 에피토프에, (d) hOX40L의 단량체 형이 아닌 삼량체의 에피토프에, 또는 (e) hOX40L의 단량체 형태와 삼량체 형태 둘 모두에 특이적으로 결합할 수 있다. 바람직한 실시형태에서, 본 명세서에서 제공된 항체는 hOX40L의 삼량체 형태의 에피토프에 특이적으로 결합하지만, hOX40L의 단량체 형태의 에피토프에 특이적으로 결합하지 않는다.
본 발명은 또한 hOX40L 항원에 특이적으로 결합하는 본 명세서에 기술된 VH 도메인, VH CDR, VL 도메인, 및 VL CDR의 유도체를 포함하는, hOX40L 에피토프에 특이적으로 결합하는 항체를 제공한다. 본 발명은 또한 실시예에 개시된 항체의 유도체를 포함하는 항체를 제공하고, 여기서 상기 항체는 X40L 에피토프에 특이적으로 결합한다. 예를 들어, 아미노산 치환을 유발하는 부위-지정 돌연변이 유발 및 PCR-매개 돌연변이 유발을 비롯한 관련 기술 분야의 통상의 기술자에게 공지된 표준 기술을 사용하여 본 발명의 분자를 코딩하는 뉴클레오타이드 서열 내에 돌연변이를 도입할 수 있다. 바람직하게는, 유도체는 본래 분자에 비해 25개 미만의 아미노산 치환, 20개 미만의 아미노산 치환, 15개 미만의 아미노산 치환, 10개 미만의 아미노산 치환, 5개 미만의 아미노산 치환, 4개 미만의 아미노산 치환, 3개 미만의 아미노산 치환, 또는 2개 미만의 아미노산 치환을 포함한다. 또 다른 실시형태에서, 유도체는 보존적 아미노산 치환을 갖는다. 바람직한 실시형태에서, 유도체는 하나 이상의 예측된 비-필수 아미노산 잔기에서 이루어지는 보존적 아미노산 치환을 갖는다. 대안적으로, 돌연변이는 예컨대 포화 돌연변이 유발에 의해서 코딩 서열의 전체 또는 일부를 따라 무작위로 도입될 수 있고, 생성되는 돌연변이체는 활성을 보유하는 돌연변이체를 식별하기 위해서 생물학적 활성에 대해 스크리닝될 수 있다. 돌연변이 유발 후, 코딩된 단백질이 발현될 수 있고, 단백질 활성을 결정할 수 있다.
또 다른 실시형태에서, hOX40L 에피토프에 특이적으로 결합하는 항체는 서열 목록의 가변 도메인 아미노산 서열과 적어도 35%, 적어도 40%, 적어도 45%, 적어도 50%, 적어도 55%, 적어도 60%, 적어도 65%, 적어도 70%, 적어도 75%, 적어도 80%, 적어도 85%, 적어도 90%, 적어도 95%, 또는 적어도 99% 동일한 가변 도메인 아미노산 서열을 포함한다.
구체적인 실시형태에서, 항체는 완전 인간 항-인간 항체, 예컨대 완전 인간 단클론성 항체이다. 완전 인간 항체는 관련 기술 분야에 공지된 임의의 방법에 의해서 생산할 수 있다. 예시적인 방법은 hOX40L 항원(면역 반응을 일으킬 수 있고, 임의로 담체에 컨쥬게이팅된 임의의 hOX40L 폴리펩타이드)을 사용하여 내인성 면역글로불린 생산의 부재하에 인간 항체의 레퍼토리를 생산할 수 있는 형질전환 동물(예를 들어, 마우스)을 면역화시키는 것을 포함한다(예를 들어, 문헌[Jakobovits et al., (1993) Proc. Natl. Acad. ScL, 90:2551]; [Jakobovits et al., (1993) Nature, 362:255 258(1993)]; [Bruggermann et al., (1993) Year in Immunol., 7:33] 참고). 완전 인간 항-hOX40L 항체를 생산하는 다른 방법은 본 명세서의 실시예에서 찾을 수 있다.
대안적으로, 완전 인간 항체는 파지 전시법 항체 라이브러리의 시험관내 스크리닝을 통해서 생성될 수 있다(예를 들어, 본 명세서에 참고로 포함된 문헌([Hoogenboom et al., J. Mol. Biol., 227:381(1991)]; [Marks et al., J. Mol. Biol., 222:581(1991)]) 참고). 다양한 항체-함유 파지 전시법 라이브러리가 기술되었고, 관련 기술 분야의 통상의 기술자가 쉽게 제조할 수 있다. 라이브러리는 적절한 표적에 대해 스크리닝될 수 있는 다양한 인간 항체 서열, 예컨대 인간 Fab, Fv 및 scFv 단편을 함유할 수 있다.
본 발명의 항체 및 단편은 즉, 항체에 임의의 유형의 분자의 공유 부착에 의해서 화학적으로 변형된 항체 및 단편을 포함한다. 제한의 방식이 아닌 예를 들어, 항체 유도체는 예를 들어, 글리코실화, 아세틸화, 페길화, 인산화, 아마이드화, 공지된 보호/차단기에 의한 유도체화, 단백분해성 절단, 세포 리간드 또는 다른 단백질에 대한 연결 등에 의해서 화학적으로 변형된 항체를 포함한다. 임의의 많은 화학적 변형은 특이적인 화학 절단, 아세틸화, 제제화, 튜니카마이신의 대사 합성 등을 포함하고 이에 제한되지 않는 공지된 기술에 의해서 수행할 수 있다. 추가로, 항체는 하나 이상의 비-전통적인 아미노산을 함유할 수 있다.
본 발명은 또한 관련 기술 분야의 통상의 기술자에게 공지된 프레임워크 영역을 포함하는 hOX40L 항원(예를 들어, 인간 또는 비-인간 단편)에 특이적으로 결합하는 항체를 제공한다. 프레임워크 영역은 예를 들어, 자연 발생 또는 컨센서스 프레임워크 영역일 수 있다. 가장 바람직하게는, 본 발명의 항체의 프레임워크 영역은 인간(인간 프레임워크 영역에 대한 목록은 예를 들어, 전문이 본 명세서에 참고로 포함된 문헌[Chothia et al., 1998, J. Mol. Biol. 278:457-479]을 참고하기 바람)이다. 또한 문헌[Kabat et al. (1991) Sequences of Proteins of Immunological Interest (U.S. Department of Health and Human Services, Washington, D.C.) 5th ed.]을 참고하기 바란다.
구체적인 실시형태에서, 본 발명은 hOX40L 항원에 특이적으로 결합하는 항체를 제공하고, 상기 항체는 서열 목록(즉, HCDR1의 경우 서열번호 4, 서열번호 10, 서열번호 36, 서열번호 42, 서열번호 68, 서열번호 74, 서열번호 96 또는 서열번호 102, 특히, 서열번호 36 또는 서열번호 42; HCDR2의 경우 서열번호 6, 서열번호 12, 서열번호 38, 서열번호 44, 서열번호 70, 서열번호 76, 서열번호 98 또는 서열번호 104, 특히 서열번호 38 또는 서열번호 44; HCDR3의 경우 서열번호 8, 서열번호 14, 서열번호 40, 서열번호 46, 서열번호 72, 서열번호 78, 서열번호 100 또는 서열번호 106, 특히 서열번호 40 또는 서열번호 46; LCDR1의 경우 서열번호 18, 서열번호 24, 서열번호 50, 서열번호 56, 서열번호 82, 서열번호 88, 서열번호 110 또는 서열번호 116, 특히 서열번호 50 또는 서열번호 56; LCDR2의 경우 서열번호 20, 서열번호 26, 서열번호 52, 서열번호 58, 서열번호 84, 서열번호 90, 서열번호 112 또는 서열번호 118, 특히 서열번호 52 또는 서열번호 58; 및 LCDR3의 경우 서열번호 22, 서열번호 28, 서열번호 54, 서열번호 60, 서열번호 86, 서열번호 92, 서열번호 114 또는 서열번호 120, 특히 서열번호 54 또는 서열번호 60)의 CDR 중 하나 이상의 아미노산 서열, 및 a) 뮤린 항체 프레임워크(즉, 공여 항체 프레임워크)와 인간 항체 프레임워크(즉, 수용 항체 프레임워크) 사이에서 상이한 희귀(rare) 프레임워크 잔기; (b) 공여 항체 프레임워크와 수용 항체 프레임워크 사이에서 상이한 비니어(Venier) 대역 잔기; (c) 공여 항체 프레임워크와 수용 항체 프레임워크 사이에서 상이한, VH/VL 계면에서 쇄내 패킹(packing) 잔기; (d) 공여 항체 프레임워크와 수용 항체 프레임워크 서열 사이에서 상이한, 정규(canonical) 잔기, 특히 정규 부류의 뮤린 항체 CDR 루프의 정의에 중요한 프레임워크 영역; (e) CDR에 인접한 잔기; (g) 항원과 상호작용할 수 있는 잔기; (h) CDR과 상호작용할 수 있는 잔기; 및 (i) VH 도메인과 VL 도메인 사이의 접촉 잔기 중 1, 2 또는 3개 이상의 잔기에서 하나 이상의 아미노산 치환을 갖는 인간 프레임워크 영역을 포함한다.
본 발명은 hOX40L 항원에 특이적으로 결합하는 항체를 포함하며, 상기 항체는 서열 목록(즉, VH 도메인의 경우 서열번호 2, 서열번호 34, 서열번호 66 또는 서열번호 94, 특히 서열번호 34; VL 도메인의 경우 서열번호 16, 서열번호 48, 서열번호 80, 또는 서열번호 108, 특히 서열번호 48) 내에 VH 도메인 및/또는 VL 도메인의 아미노산 서열을 포함하지만, 프레임워크 영역 내에 돌연변이(예를 들어, 하나 이상의 아미노산)를 갖는다. 특정 실시형태에서, hOX40L 항원에 특이적으로 결합하는 항체는 VH 도메인 및/또는 VL 도메인의 프레임워크 내에 하나 이상의 아미노산 잔기 치환을 갖는 실시예에 개시된 항체의 VH 도메인 및/또는 VL 도메인 또는 이의 항원-결합 단편의 아미노산 서열을 포함한다.
일부 실시형태에서, 본 명세서에 제공된 항체는 hOX40L hOX40의 결합을 감소 또는 감소/억제하거나, 대상체(예를 들어, 인간 대상체)에서 hOX40L 생물학적 활성, 예컨대 CCL20, IL8 및/또는 RANTES, 또는 INF-γ, TNF-α 또는 IL-2, 특히 INF-γ의 분비를 감소 또는 억제한다. 특정 실시형태에서, 본 명세서에 제공된 항체, 예컨대 인간 단클론성 항-hOX40L 항체는 hOX40에 대한 가용성 또는 세포 표면-발현된 hOX40L의 결합을 감소 또는 억제하고/하거나 대상체에서 가용성 또는 세포 표면-발현된 hOX40L과 접촉한 후 CCL20 및/또는 RANTES, 또는 INF-γ, TNF-α 또는 IL-2, 특히 INF-γ의 분비를 감소 또는 억제한다. 본 명세서에 제공된 항체의 hOX40에 대한 hOX40L 결합의 차단 활성은 실시예에 기술된 바와 같은 검정법을 사용하여 검출될 수 있다. 본 명세서에 제공된 hOX40L 항체에 의한 OX40L을 발현하는 세포의 생물학적 활성의 억제는 실시예에 기술된 바와 같은 검정법을 사용하여 검출될 수 있다.
본 발명은 또한 hOX40L 항원에 특이적으로 결합하는 본 명세서에서 제공된 항체 및 이종성 폴리펩타이드를 포함하는 융합 단백질을 제공한다. 일부 실시형태에서, 항체가 융합되는 이종성 폴리펩타이드는 항체를 세포 표면-발현된 hOX40L을 갖는 세포에 표적화하기 위해 유용하다.
항체
컨쥬게이트
및 융합 단백질
컨쥬게이트 및 융합 단백질에 대한 하기 논의는 항체를 언급한 개시 내용이 또한 본 발명의 단편에 필요한 부분만 약간 수정하여 적용될 수 있도록 단편에 적용된다.
일부 실시형태에서, 본 발명의 항체는 진단제, 검출 가능한 물질 또는 치료제 또는 임의의 다른 분자에 컨쥬게이팅되거나 재조합 방식으로 융합된다. 컨쥬게이팅 또는 재조합 방식으로 융합된 항체는 예컨대, 특정 요법의 효능을 결정하는 것과 같은 임상 시험 절차의 일부로서 hOX40L-매개된 질환의 발병, 전개, 진행 및/또는 중증도를 모니터링 또는 예측하는 데 유용할 수 있다.
그러한 진단 및 검출은 예를 들어 항체를 다양한 효소, 제한적이지 않은 예컨대 호스래디시 퍼옥시다제, 알칼린 포스파타제, 베타-갈락토시다제 또는 아세틸콜린에스터라제; 보조군, 제한적이지 않은 예컨대 스트렙타비딘(Streptavidin)/비오틴 및 아비딘/비오틴; 형광 물질, 제한적이지 않은 예컨대 움벨리페론, 플루오레세인, 플루오레세인 아이소티오시아네이트, 로다민, 다이클로로트라이아지닐아민 플루오레세인, 단실 클로라이드 또는 피코에리트린; 발광 물질, 제한적이 아닌 예컨대 루미놀; 생체발광 물질, 제한적이지 않은 예컨대 루시퍼라제, 루시페린 및 에쿠오린; 방사성 물질, 비제한적인 예컨대 비제한적인 예를 들어 아이오딘(131I, 125I, 123I 및 121I), 탄소(14C), 황(35S), 삼중수소(3H), 인듐(115In, 113In, 112In 및 111In), 테크네튬(99Tc), 탈륨(201Ti), 갈륨(68Ga, 67Ga), 팔라듐(103Pd), 몰리브데넘(99Mo), 제논(133Xe), 플루오린(18F), 153Sm, 177Lu, 159Gd, 149Pm, 140La, 175Yb, 166Ho, 90Y, 47Sc, 186Re, 188Re, 142Pr, 105Rh, 97Ru, 68Ge, 57Co, 65Zn, 85Sr, 32P, 153Gd, 169Yb, 51Cr, 54Mn, 75Se, 113Sn 및 117Sn; 및 다양한 양전자 방출 단층 촬영을 이용하는 양전자 방출 금속, 및 비-방사성 상자성 금속 이온을 포함하지만 이에 제한되지 않는 검출 가능한 물질에 커플링시켜 달성할 수 있다.
본 발명은 치료 모이어티(또는 하나 이상의 치료 모이어티)에 컨쥬게이팅되거나 재조합 방식으로 융합된 본 발명의 항체의 용도를 추가로 포함한다. 항체는 치료 모이어티, 예컨대 세포독소, 예를 들어, 세포증식 억제제 또는 세포파괴제, 치료제 또는 방사성 금속 이온, 예를 들어, 알파 방사체에 컨쥬게이팅되거나 재조합 방식으로 융합될 수 있다. 세포독소제 또는 세포독성제는 세포에 해로운 임의의 작용제를 포함한다. 치료 모이어티는 항대사체(예를 들어, 메토트렉세이트, 6-머캅토퓨린, 6-티오구아닌, 시타라빈, 5-플루오로우라실 데카르바진); 알킬화제(예를 들어, 메클로르에타민, 티오에파 클로람부실, 멜팔란, 카르무스틴(BCNU) 및 로무스틴(CCNU), 사이클로토스파미드, 부술판, 다이브로모만니톨, 스트렙토조토신, 미토마이신 C 및 시스다이클로로다이아민 백금(II)(DDP) 및 시스플라틴); 안트라사이클린(예를 들어, 다우노루비신(이전에 다우노마이신) 및 독소루비신); 항생제(예를 들어, 닥티노마이신(이전에 액티노마이신), 블레오마이신, 미트라마이신 및 안트라마이신(AMC)); 오리스타틴 분자(예를 들어, 오리스타틴 PHE, 브리오스타틴 1 및 솔라스타틴 10; 모두 본 명세서 참고로 포함된 문헌[Woyke et al., Antimicrob. Agents Chemother. 46:3802-8 (2002)], [Woyke et al., Antimicrob. Agents Chemother. 45:3580-4 (2001)], [Mohammad et al., Anticancer Drugs 12:735-40 (2001)], [Wall et al., Biochem. Biophys. Res. Commun 266:76-80 (1999)], [Mohammad et al., Int. J. Oncol. 15:367-72 (1999)] 참고; 호르몬(예를 들어, 글루코코르티코이드, 프로게스틴, 안드로겐 및 에스트로겐), DNA-복구 효소 억제제(예를 들어, 에토포시드 또는 토포테칸), 키나제 억제제(예를 들어, 화합물 ST1571, 이마티닙 메실레이트(문헌[Kantarjian et al., Clin Cancer Res. 8(7):2167-76(2002)]); 세포독성제(예를 들어, 파클리탁셀, 사이토칼라신 B, 그라미시딘 D, 에티듐 브로마이드, 에메틴, 미토마이신, 에토포시드, 테노포시드, 빈크리스틴, 빈블라스틴, 콜히친, 독소루비신, 다우노루비신, 다이하이드록시 안트라신 다이온, 미톡산트론, 미트라마이신, 액티노마이신 D, 1데하이드로테스토스테론, 글루코르티코이드, 프로카인, 테트라카인, 리도카인, 프로프라놀올 및 푸로마이신 및 이의 유사체 또는 상동체, 및 미국 특허 6,245,759, 6,399,633, 6,383,790, 6,335,156, 6,271,242, 6,242,196, 6,218,410, 6,218,372, 6,057,300, 6,034,053, 5,985,877, 5,958,769, 5,925,376, 5,922,844, 5,911,995, 5,872,223, 5,863,904, 5,840,745, 5,728,868, 5,648,239, 5,587,459에 개시된 화합물); 파르네실 트랜스퍼라제 억제제(예를 들어, R115777, BMS-214662, 예를 들어, 미국 특허 6,458,935, 6,451,812, 6,440,974, 6,436,960, 6,432,959, 6,420,387, 6,414,145, 6,410,541, 6,410,539, 6,403,581, 6,399,615, 6,387,905, 6,372,747, 6,369,034, 6,362,188, 6,342,765, 6,342,487, 6,300,501, 6,268,363, 6,265,422, 6,248,756, 6,239,140, 6,232,338, 6,228,865, 6,228,856, 6,225,322, 6,218,406, 6,211,193, 6,187,786, 6,169,096, 6,159,984, 6,143,766, 6,133,303, 6,127,366, 6,124,465, 6,124,295, 6,103,723, 6,093,737, 6,090,948, 6,080,870, 6,077,853, 6,071,935, 6,066,738, 6,063,930, 6,054,466, 6,051,582, 6,051,574, 및 6,040,305에 개시된 것); 토포아이소머라제 억제제(예를 들어, 캄프토테신; 이리노테칸; SN-38; 토포테칸; 9-아미노캄포테신; GG-211(GI 147211); DX-8951f; IST-622; 루비테칸; 피라졸로아크리딘; XR-5000; 사인토핀; UCE6; UCE1022; TAN-1518A; TAN 1518B; KT6006; KT6528; ED-110; NB-506; ED-110; NB-506; 및 레베카마이신); 불가레인; DNA 소 그루브 바인더(minor groove binder), 예컨대 호쉐트(Hoescht) 염료 33342 및 호치스트(Hoechst) 염료 33258; 니티딘; 파가로닌; 에피베르베린; 코랄린; 베타-라파콘; BC-4-1; 비스포스포네이트(예를 들어, 알렌드로네이트, 시마드로네이트, 클로드로네이트, 틸루드로네이트, 에티드로네이트, 이반드로네이트, 네리드로네이트, 올판드로네이트, 리세드로네이트, 피리드로네이트, 파미드로네이트, 졸렌드로네이트), HMG-CoA 리덕타제 억제제(예를 들어, 로바스타틴, 심바스타틴, 아토르바스타틴, 프라바스타틴, 플루바스타틴, 스타틴, 세리바스타틴, 레스콜, 루피터, 로수바스타틴 및 아토르바스타틴); 안티센스 올리고뉴클레오타이드(예를 들어, 미국 특허 6,277,832, 5,998,596, 5,885,834, 5,734,033, 및 5,618,709에 개시된 것); 아데노신 데아미나제 억제제(예를 들어, 플루다라빈 포스페이트 및 2-클로로데옥시아데노신); 이브리투모맙 티욱세탄(제발린(Zevalin)(등록상표)); 토시투모맙(벡사르(Bexxar)(등록상표)) 및 이의 약제학적으로 허용 가능한 염, 용매화물, 포접화합물 및 전구약물을 포함하지만 이에 제한되는 것은 아니다.
추가로, 본 발명의 항체는 특정 생물학적 반응을 변형시키는 치료 모이어티 또는 약물 모이어티에 컨쥬게이팅되거나 재조합 방식으로 융합될 수 있다. 치료 모이어티 또는 약물 모이어티는 전통적인 화학 치료제로 제한되는 것으로 해석하지 않아야 한다. 예를 들어, 약물 모이어티는 목적하는 생물학적 활성을 갖는 단백질, 펩타이드 또는 폴리펩타이드이다. 그러한 단백질은 예를 들어 독소, 예를 들어 아브린, 리신 A, 슈도모나스(pseudomonas) 외독소, 콜레라 독소 또는 디프테리아 독소; 단백질, 예를 들어 종양 괴사 인자, γ-인터페론, α-인터페론, 신경 성장 인자, 혈소판 유래 성장 인자, 조직 플라스미노겐 활성화 인자, 세포사멸제, 예를 들어, TNF-γ, TNF-γ, AIM I(국제 특허 출원 공개 WO 97/33899 참고), AIM II(국제 특허 출원 공개 WO 97/34911 참고), Fas 리간드(문헌[Takahashi et al., 1994, J. 면역l., 6:1567-1574]), 및 VEGF(국제 특허 출원 공개 WO 99/23105 참고), 항-혈관신생제, 예를 들어, 안지오스타틴, 엔도스타틴 또는 응고 경로의 성분(예를 들어, 조직 인자); 또는 생물학적 반응 변형제, 예컨대, 예를 들어 림포카인(예를 들어, 인터페론 감마, 인터류킨-1("IL-1"), 인터류킨-2("IL-2"), 인터류킨-5("IL-5"), 인터류킨-6("IL-6"), 인터류킨-7("IL-7"), 인터류킨 9("IL-9"), 인터류킨-10("IL-1O"), 인터류킨-12("IL-12"), 인터류킨-15("IL-15"), 인터류킨-23("IL-23"), 과립구 대식세포 콜로니 자극 인자("GM-CSF") 및 과립구 콜로니 자극 인자("G-CSF")), 또는 성장 인자(예를 들어, 성장 호르몬("GH")) 또는 응고제(예를 들어, 칼슘, 비타민 K, 조직 인자, 제한이 아닌 예컨대 하게만(Hageman) 인자(인자 XII), 고분자량 키니노겐(HMWK), 프레칼리크레인(PK), 응고 단백질-인자 II(프로트롬빈), 인자 V, XIIa, VIII, XIIIa, XI, XIa, IX, IXa, X, 인지질 및 피브린 단량체)를 포함할 수 있다.
본 발명은 융합 단백질을 생성하도록 이종성 단백질 또는 폴리펩타이드(또는 이의 단편, 바람직하게는 약 10, 약 20, 약 30, 약 40, 약 50, 약 60, 약 70, 약 80, 약 90 또는 약 100개 아미노산의 폴리펩타이드)에 재조합 방식으로 융합되거나 화학적으로 컨쥬게이팅(공유 또는 비-공유 컨쥬게이션)된 본 발명의 항체를 포함한다. 특히, 본 발명은 본 발명의 항체의 항원 결합 단편(예를 들어, Fab 단편, Fd 단편, Fv 단편, F(ab)2 단편, VH 도메인, VH CDR, VL 도메인 또는 VL CDR) 및 이종성 단백질, 폴리펩타이드 또는 펩타이드를 포함하는 융합 단백질을 제공한다. 일 실시형태에서, 항체가 융합되는 이종성 단백질, 폴리펩타이드 또는 펩타이드는 항체를 특정 세포 유형, 예컨대 hOX40L 또는 hOX40L 수용체를 발현하는 세포에 표적화하기에 유용하다. 예를 들어, 특정 세포 유형(예를 들어, 면역 세포)에 의해서 발현된 세포 표면 수용체에 특이적으로 결합하는 항체는 본 발명의 변형된 항체에 융합되거나 컨쥬게이팅될 수 있다.
본 발명의 컨쥬게이팅된 단백질 또는 융합 단백질은 본 명세서에 기술된 임의의 본 발명의 항체 및 이종성 폴리펩타이드를 포함한다. 일 실시형태에서, 본 발명의 컨쥬게이팅된 단백질 또는 융합 단백질은 실시예에 개시된 항체의 가변 도메인 및 이종성 폴리펩타이드를 포함한다.
또한, 본 발명의 항체는 치료 모이어티, 예컨대 방사성 금속 이온, 예를 들어 알파 방사체, 예를 들어 213Bi, 또는 131In, 131LU, 131Y, 131Ho, 131Sm을 포함하지만 이에 제한되지 않는 방사성 금속 이온을 폴리펩타이드에 컨쥬게이팅하기 위해 유용한 마크로사이클릭 킬레이터에 컨쥬게이팅될 수 있다. 특정 실시형태에서, 마크로사이클릭 킬레이터는 링커 분자를 통해 항체에 부착될 수 있는 1,4,7,10-테트라아자사이클로도데칸-N,N',N",N'"-테트라아세트산(DOTA)이다. 그러한 링커 분자는 관련 기술 분야에 일반적으로 공지되어 있고, 각각 전문이 참고로 포함된 문헌([Denardo et al., 1998, Clin Cancer Res. 4(10):2483-90]; [Peterson et al., 1999, Bioconjug. Chem. 10(4):553-7]; 및 [Zimmerman et al., 1999, Nucl. Med. Biol. 26(8):943-50])에 설명되어 있다.
또한, 본 발명의 항체는 마커 서열, 예컨대 정제를 용이하게 하기 위해 펩타이드에 융합될 수 있다. 바람직한 실시형태에서, 마커 아미노산 서열은 헥사-히스티딘 펩타이드, 예컨대 특히 pQE 벡터(퀴아겐, 인코퍼레이티드(QIAGEN, Inc.)) 내에 제공된 태그이고, 이 중 많은 것은 상업적으로 입수 가능하다. 예를 들어, 문헌[Gentz et al., 1989, Proc. Natl. Acad. Sci. USA 86:821-824]에 기술된 바와 같이, 헥사-히스티딘은 융합 단백질의 간편한 정제를 제공한다. 정제에 유용한 다른 펩타이드 태그는 헤마글루티닌("HA") 태그(이는 인플루엔자 헤마글루티닌 단백질로부터 유도된 에피토프에 대응함(문헌[Wilson et al., 1984, Cell 37:767]) 및 "FLAG" 태그를 포함하지만 이에 제한되는 것은 아니다.
항체에 치료 모이어티(폴리펩타이드 포함)를 융합 또는 컨쥬게이팅하는 방법은 널리 공지되어 있고, 예를 들어, 전문이 본 명세서에 참고로 포함된 문헌[Arnon et al., "Monoclonal Antibodies For Immunotargeting Of Drugs In Cancer Therapy", in Monoclonal Antibodies And Cancer Therapy], [Reisfeld et al. (eds.), pp. 243-56 (Alan R. Liss, Inc. 1985)]; [Hellstrom et al., "Antibodies For Drug Delivery", in Controlled Drug Delivery (2nd Ed.), Robinson et al. (eds.), pp. 623-53 (Marcel Dekker, Inc. 1987)]; [Thorpe, "Antibody Carriers Of Cytotoxic Agents In Cancer Therapy: A Review", in Monoclonal Antibodies 84]: [Biological And Clinical Applications, Pinchera et al. (eds.), pp. 475-506 (1985)]; ["Analysis, Results, And Future Prospective Of The Therapeutic Use Of Radiolabeled Antibody In Cancer Therapy", in Monoclonal Antibodies For Cancer Detection And Therapy, Baldwin et al. (eds.), pp. 303-16 (Academic Press 1985)], [Thorpe et al., 1982, Immunol. Rev. 62:119-58]; 미국 특허 5,336,603, 5,622,929, 5,359,046, 5,349,053, 5,447,851, 5,723,125, 5,783,181, 5,908,626, 5,844,095, 및 5,112,946; EP 307,434; EP 367,166; EP 394,827; PCT 공개 WO 91/06570, WO 96/04388, WO 96/22024, WO 97/34631, 및 WO 99/04813; 문헌[Ashkenazi et al., Proc. Natl. Acad. Sci. USA, 88: 10535-10539, 1991]; [Traunecker et al., Nature, 331:84-86, 1988]; [Zheng et al., J. Immunol., 154:5590-5600, 1995]; [Vil et al., Proc. Natl. Acad. Sci. USA, 89:11337-11341, 1992]를 참고하기 바란다.
융합 단백질은 예를 들어, 유전자-셔플링(shuffling), 모티프-셔플링, 엑손-셔플링 및/또는 코돈-셔플링("DNA 셔플링"으로서 총칭함)의 기술을 통해 생성될 수 있다. DNA 셔플링은 본 발명의 항체의 활성(예를 들어, 보다 높은 친화도 및 보다 낮은 해리율을 갖는 항체)을 변경시키기 위해 사용될 수 있다. 일반적으로, 미국 특허 5,605,793, 5,811,238, 5,830,721, 5,834,252, 및 5,837,458; 문헌[Patten et al., 1997, Curr. Opinion Biotechnol. 8:724-33]; [Harayama, 1998, Trends Biotechnol. 16(2):76-82]; [Hansson et al., 1999, J. Mol. Biol. 287:265-76]; 및 [Lorenzo and Blasco, 1998, Biotechniques 24(2):308-313](이들 특허 및 공개물 각각은 그의 전문이 참고로 포함됨)을 참고하기 바란다. 항체 또는 코딩된 항체는 재조합 전에 오류-빈발(error-prone PCR), 랜덤 뉴클레오티드 삽입 또는 다른 방법에 의해서 랜덤 돌연변이 유발됨으로써 변경될 수 있다. 본 발명의 항체를 코딩하는 폴리뉴클레오티드는 하나 이상의 이종성 분자의 하나 이상의 성분, 모티프, 섹션, 부분, 도메인, 단편 등과 재조합될 수 있다.
본 발명의 항체는 또한 전문이 본 명세서에 참고로 포함된 미국 특허 4,676,980에 기술된 바와 같이 제2 항체에 컨쥬게이팅되어 항체 헤테로컨쥬게이트를 형성할 수 있다.
hOX40L 항원에 특이적으로 결합하는 본 발명의 항체에 컨쥬게이팅되거나 재조합 방식으로 융합된 치료 모이어티 또는 약물은 목적하는 예방 또는 치료 효과(들)를 달성하도록 선택되어야 한다. 특정 실시형태에서, 항체는 변형된 항체이다. 임상의 또는 다른 의료 관련자는 본 발명의 항체에 컨쥬게이팅되거나 재조합 방식으로 융합되는 치료 모이어티 또는 약물을 결정할 때 다음을 고려해야 한다: 질환의 본성, 질환의 중증도, 및 대상체의 상태.
본 발명의 항체는 또한 고체 지지체에 부착될 수 있고, 이는 표적 항원의 면역검정법 또는 정제에 특히 유용하다. 그러한 고체 지지체는 유리, 셀룰로스, 폴리아크릴아마이드, 나일론, 폴리스타이렌, 폴리염화비닐 또는 폴리프로필렌을 포함하지만 이에 제한되는 것은 아니다
약제학적 조성물
조성물에 대한 하기 논의는 항체를 언급한 개시 내용이 또한 본 발명의 단편에 필요한 부분만 약간 수정하여 적용될 수 있도록 단편에 적용된다.
본 발명의 본 명세서에 제공된 하나 이상의 항체를 함유하는 치료 제제는 목적하는 정도의 순도를 갖는 항체를 동결건조 제제 또는 수용액 형태로 선택적인 생리학적으로 허용 가능한 담체, 부형제 또는 안정제(문헌[Remington's Pharmaceutical Sciences(1990)](미국 펜실베니아주 소재의 백 퍼플리싱, 코퍼레이션) 참고)와 혼합함으로써 저장을 위해 제조될 수 있다. 허용 가능한 담체, 부형제, 또는 안정제는 사용되는 투여량 및 농도에서 수용자에게 무독성이고, 완충액, 예를 들어 포스페이트, 시트레이트 및 다른 유기산; 항산화제, 예를 들어 아스코르브산 및 메티오닌; 방부제(예컨대 옥타데실다이메틸벤질 암모늄 클로라이드; 헥사메토늄 클로라이드; 벤즈알코늄 클로라이드, 벤조토늄 클로라이드; 페놀, 부틸 또는 벤질 알코올; 알킬 파라벤, 예컨대 메틸 또는 프로필 파라벤; 카테콜; 레소르시놀; 사이클로헥산올; 3-펜탄올; 및 m-크레졸); 저분자량(약 10개 미만의 잔기) 폴리펩타이드; 단백질, 예컨대 혈청 알부민, 젤라틴 또는 면역글로불린; 친수성 중합체, 예컨대 폴리비닐피롤리돈; 아미노산, 예컨대 글리신, 글루타민, 아스파라긴, 히스티딘, 아르기닌 또는 라이신; 단당류, 이당류 및 다른 탄수화물, 예를 들어 글루코스, 만노스 또는 덱스트린; 킬레이팅제, 예컨대 EDTA; 당, 예컨대 수크로스, 만니톨, 트레할로스 또는 소르비톨; 염-형성 반대-이온, 예를 들어 나트륨; 금속 착물(예를 들어, Zn-단백질 착물); 및/또는 -이온성 계면활성제, 예컨대 트윈(상표명), 플루로닉스(PLURONICS)(상표명) 또는 폴리에틸렌 글리콜(PEG)을 포함한다.
본 명세서에 제공된 본 발명의 항체는 또한 예를 들어 리포좀 내에 제제화될 수 있다. 관심 분자를 함유하는 리포좀은 문헌([Epstein et al(1985) Proc. Natl. Acad, Sci. USA 82:3688]; [Hwang et al.(1980) Proc. Natl. Acad. Sci. USA 77:4030]); 및 미국 특허 4,485,045 및 4,544,545에 기술된 것과 같은 관련 기술 분야에 공지된 방법에 의해서 제조된다. 순환 시간이 향상된 리포좀은 미국 특허 5,013,556에 개시되어 있다.
특히 유용한 면역리포좀은 포스파티딜콜린, 콜레스테롤 및 PEG-유도체화된 포스파티딜에탄올아민(PEG-PE)을 함유하는 지질 조성물을 사용하는 역상 증발 방법에 의해서 생성될 수 있다. 리포좀은 규정된 공극 크기의 필터를 통해 압출되어 목적하는 직경의 리포좀이 생성된다. 본 명세서에 제공된 항체의 Fab' 단편은 문헌 [Martin et al.(1982) J. Biol. Chem. 257:286-288]에 설명된 바와 같이 다이설파이드 교환 반응을 통해 리포좀에 컨쥬게이팅될 수 있다. 화학치료제(예컨대 독소루비신)가 임의로 리포좀 내에 함유된다([Gabizon et al., (1989) J. National Cancer Inst. 81(19):1484] 참고).
또한, 본 명세서에 기술된 것과 같은 제제는 치료되는 특정 적응증에 대해 필요할 때 1종 초과의 활성 화합물을 함유할 수 있다. 특정 실시형태에서, 제제는 본 발명의 항체 및 서로 불리한 영향을 미치지 않는 상호 보완적인 활성을 갖는 1종 이상의 활성 화합물을 포함한다. 그러한 분자는 적합하게는 의도되는 목적에 효과적인 양으로 조합하여 존재한다. 예를 들어, 본 발명의 항체는 1종 이상의 다른 치료제와 조합될 수 있다. 상기 조합 요법은 환자에게 연속적으로 또는 동시에 또는 순서대로 투여될 수 있다.
일 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와, 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와, 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, CTLA4-Fc 분자(예를 들어, 아바타셉트), 항-CD40L 항체, 항-LFA1 항체, 항-CD52 항체(예를 들어, 알렘투주맙), 사이클로포스파미드 및 항-흉선세포 글로불린으로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 포함한다.
일부 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와, 칼시뉴린 억제제(예를 들어, 타크롤리무스, 사이클로스포린), mTOR 억제제(예를 들어, 라파마이신(시롤리무스)), 및 항증식제(예를 들어, 마이코페놀레이트 모페틸, 사이클로포스파미드)로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 포함한다.
추가 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와, IL-2 신호전달을 조절하는 면역억제제(예를 들어, 타크롤리무스, 사이클로스포린, 라파마이신(시롤리무스), 및 항-CD25 항체(예를 들어, 바실릭수맙, 다클리주맙)로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 포함한다.
일 실시형태에서, 조성물은 본 발명의 항-OX40L 항체와 라파마이신(시롤리무스)을 포함한다. 일 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 타크롤리무스를 포함한다. 일 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와, 타크롤리무스 및 메토트렉세이트의 조합물을 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 사이클로스포린을 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와, 사이클로스포린 및 메토트렉세이트를 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 사이클로포스파미드를 포함한다. 또 다른 실시형태에서, 조합물은 본 발명의 항-OX40L 항체와 마이코페놀레이트 모페틸을 포함한다.
본 발명의 항체는 또한 예를 들어, 액적 형성 기술 또는 계면 중합에 의해서 제조된 마이크로캡슐 내에, 예를 들어, 각각 하이드록시메틸셀룰로스 또는 젤라틴-마이크로캡슐 및 폴리(메틸메타크릴레이트) 마이크로캡슐, 콜로이드성 약물 전달계(예를 들어, 리포좀, 알부민 미세구, 마이크로에멀전, 나노-입자 및 나노캡슐) 내에 또는 마크로에멀전 내에 포획될 수 있다. 그러한 기술은 문헌 [Remington's Pharmaceutical Sciences(1990)](미국 펜실베니아주 소재의 백 퍼플리싱, 코퍼레이션)에 개시되어 있다.
생체내 투여를 위해 사용될 제제는 멸균될 수 있다. 이는 예를 들어, 멸균 여과막을 통한 여과에 의해서 쉽게 달성된다.
지속-방출 제제가 또한 제조될 수 있다. 지속-방출 제제의 적합한 예는 길항제를 함유하는 고체 소수성 중합체의 반투과성 매트릭스를 포함하는데, 매트릭스는 성형된 용품, 예를 들어, 필름 또는 마이크로캡슐 형태로 존재한다. 지속-방출 매트릭스의 예는 폴리에스터, 하이드로겔(예를 들어, 폴리(2-하이드록시에틸-메타크릴레이트) 또는 폴리(비닐알코올)), 폴리락티드(미국 특허 3,773,919), L-글루탐산 및 에틸-L-글루타메이트의 공중합체, 비-분해성 에틸렌-비닐 아세테이트, 분해성 락트산-글리콜산 공중합체, 예컨대 루프론 데포트(LUPRON DEPOT)(상표명)(락트산-글리콜산 공중합체 및 류프롤리드 아세테이트로 이루어진 주사 가능 미세구) 및 폴리-D-(-)-3-하이드록시부티르산을 포함한다. 에틸렌-비닐 아세테이트 및 락트산-글리콜산과 같은 중합체는 100일이 넘는 동안 분자의 방출을 가능하게 하는 반면, 특정 하이드로겔은 보다 짧은 시간 동안 단백질을 방출한다. 캡슐화된 항체가 장시간 동안 체내에 남아있으면, 37℃에서 습기에 노출된 결과로서 변성하거나 응집될 수 있어서, 생물학적 활성의 손실 및 면역성의 가능한 변화를 일으킨다. 관여된 기전에 따라 안정화를 위한 합리적인 전략이 고안될 수 있다. 예를 들어, 응집 기전이 티오-다이설파이드 교환을 통한 분자간 S―S 결합 형성인 것으로 발견되면, 안정화는 설프하이드릴 잔기를 변형시키고, 산성 용액으로부터 동결건조시키고, 적절한 첨가제를 사용하여 함습량을 제어하고, 특수한 중합체 매트릭스 조성물을 개발함으로써 달성될 수 있다.
본 명세서에 제공된 약제학적 조성물은 치료 유효량의 본 명세서에 제공된 하나 이상의 본 발명의 항체, 및 임의로 하나 이상의 추가의 예방제 또는 치료제를 약제학적으로 허용 가능한 담체 내에 함유한다. 그러한 제약 조성물은 hOX40L-매개된 질환, 예를 들어 염증 장 질환, 이식 거부, GvHD 또는 이의 하나 이상의 증상의 예방, 치료, 관리 또는 완화에 유용하다.
본 명세서에 제공된 화합물의 투여에 적합한 약제학적 담체는 특정 투여 모드에 적합한 것으로 관련 기술 분야의 통상의 기술자에게 공지된 임의의 그러한 담체를 포함한다.
또한, 본 발명의 항체는 조성물 내에 약제학적 활성 성분 단독으로서 제제화될 수 있거나, 다른 활성 성분(예컨대, 하나 이상의 다른 예방제 또는 치료제)과 조합될 수 있다.
조성물은 본 발명의 하나 이상의 항체를 함유할 수 있다. 일 실시형태에서, 항체는 적합한 약제학적 제제, 예를 들어 경구 투여를 위해 용액, 현탁액, 정제, 분산가능 정제, 알약, 캡슐, 분말, 지속 방출 제제 또는 엘릭시르로 또는 비경구 투여를 위해 멸균 용액 또는 현탁액으로, 그리고 경피 패치 제제 및 건조 분말 흡입기로 제제화된다. 일 실시형태에서, 상기에 기술된 항체는 관련 기술 분야에 널리 공지된 기술 및 절차를 사용하여 약제학적 조성물로 제제화된다(예를 들어, 문헌[Ansel(1985) Introduction to Pharmaceutical Dosage Forms, 4th Ed., p.126] 참고).
조성물 내에서, 유효 농도의 하나 이상의 항체 또는 이의 유도체는 적합한 약제학적 담체와 혼합된다. 조성물 내의 화합물의 농도는 투여 시에 hOX40L-매개된 질환 또는 이의 증상을 치료, 예방, 또는 완화하는 양의 전달을 위해 효과적이다.
일 실시형태에서, 조성물은 단일 용량 투여를 위해 제제화된다. 조성물을 제제화하기 위해, 화합물의 중량 분획을 치료되는 병태가 경감되거나, 예방되거나, 하나 이상의 증상이 완화되도록 하는 유효 농도로 선택된 담체 내에 용해시키거나, 현탁시키거나, 분산시키거나, 또는 달리 혼합한다.
본 발명의 항체는 치료받는 환자에 대해 바람직하지 않은 부작용이 없이 치료상 유용한 효과를 발휘하기에 충분한 유효량으로 약제학적으로 허용 가능한 담체 내에 포함된다. 치료 유효 농도를 일상적인 방법을 사용하여 화합물을 시험관내 및 생체내 시스템 내에서 시험한 후, 인간에 대한 투여량에 대해 그로부터 외삽함으로써 경험적으로 결정할 수 있다.
약제학적 조성물 내의 항체의 농도는 예를 들어, 항체의 물리화학적 특징, 투여량 스케줄 및 투여되는 양과 관련 기술 분야의 통상의 기술자에게 공지된 다른 인자에 따를 것이다.
일 실시형태에서, 치료 유효 투여량은 약 0.1ng/ml 내지 약 50 내지 100μg/ml의 항체 혈청 농도를 생성시킨다. 또 다른 실시형태에서, 약제학적 조성물은 약 0.001mg 내지 약 2000mg의 항체/kg 체중/일의 투여량을 제공한다. 약제학적 투여량 단위 형태는 약 0.01mg, 0.1mg 또는 1mg 내지 약 500mg, 1000mg 또는 2000mg 및 일 실시형태에서 약 10mg 내지 약 500mg의 항체 및/또는 다른 선택적인 필수 성분의 조합물/투여량 단위 형태를 제공하도록 제조될 수 있다.
항체는 1회 투여될 수 있거나, 시간 간격을 두고 투여되는 많은 보다 적은 용량으로 분할될 수 있다. 정확한 투여량 및 치료의 지속시간은 치료되는 질환의 함수이고, 공지의 시험 프로토콜을 사용하여 경험적으로 또는 생체내 또는 시험관내 시험 데이타로부터 외삽법에 의해서 결정될 수 있음이 이해된다. 농도 및 투여량 값은 경감시킬 병태의 중증도에 따라 또한 변할 수 있음을 알아야 한다. 임의의 특정 대상체에 대해, 구체적인 투여량 용법은 개체의 필요성 및 조성물을 투여하거나 투여를 감독하는 사람의 전문적인 판단에 따라 시간이 지남에 따라 조정될 수 있고, 본 명세서에 기재된 농도 범위는 단지 예시적인 것이고 청구된 조성물의 범위 또는 실시를 제한하는 것으로 의도되지 않음을 또한 이해해야 한다.
항체의 혼합 또는 첨가 시에, 생성되는 혼합물은 용액, 현탁액, 에멀전 등일 수 있다. 생성되는 혼합물의 형태는 의도된 투여 모드 및 선택된 담체 또는 비히클 내의 화합물의 용해도를 포함한 많은 인자에 따른다. 유효 농도는 치료되는 질환, 장애 또는 병태의 증상을 완화시키기 위해 충분하고, 경험적으로 결정될 수 있다.
약제학적 조성물은 인간 및 동물에 투여하기 위해 적합한 양의 화합물 또는 약제학적으로 허용 가능한 이의 유도체를 함유하는 단위 투여 형태, 예를 들어 정제, 캡슐, 알약, 분말, 과립, 멸균 비경구 용액 또는 현탁액, 및 경구 용액 또는 현탁액, 및 오일-물 에멀전으로 제공된다. 일 실시형태에서, 항체는 단위 투여 형태 또는 다중 투여 형태로 제제화되고 투여된다. 본 명세서에서 사용되는 바와 타이 단위-투여 형태는 인간 및 동물 대상체에 적합하고 관련 기술 분야에 공지된 바와 같이 개별 포장된 물리적으로 구분되는 단위를 나타낸다. 각각의 단위-투여형은 필요한 약제학적 담체, 비히클 또는 희석제와 연합시킨 목적하는 치료 효과를 생성하기 위해 충분한 소정량의 항체를 함유한다. 단위-투여 형태의 예는 앰플 및 주사기 및 개별 포장된 정제 또는 캡슐을 포함한다. 단위-투여 형태는 이의 분획 또는 다수로 투여될 수 있다. 다중-투여 형태는 분리된 단위-투여 형태로 투여될 단일 용기 내에 포장된 복수의 동일한 단위-투여 형태이다. 다중-투여 형태의 예는 바이알, 정제 또는 캡슐의 병, 또는 파인트 또는 갤런의 병을 포함한다. 따라서, 다중 투여 형태는 포장 내에 분리되지 않은 다수의 단위-투여형이다.
바람직한 실시형태에서, 본 발명의 하나 이상의 항-hOX40L 항체는 액체 약제학적 제제로 존재한다. 액체의 약제학적 투여 가능 조성물은 예를 들어, 상기에 규정된 바와 같은 활성 화합물 및 임의적인 약제학적 아주반트(adjuvant)를, 담체, 예컨대, 예를 들어 물, 염수, 수성 덱스트로스, 글리세롤, 글리콜, 에탄올 등 내에 용해시키거나, 분산시키거나, 달리 혼합하여 용액 또는 현탁액을 형성함으로써 제조할 수 있다. 원하는 경우에, 투여될 약제학적 조성물은 또한 미량의 무독성 보조 물질, 예를 들어 습윤제, 유화제, 가용화제, pH 완충액 등, 예를 들어 아세테이트, 시트르산 나트륨, 사이클로덱스트린 유도체, 소르비탄 모노라우레이트, 트라이에탄올아민 아세트산나트륨, 트라이에탄올아민 올레에이트 및 다른 그러한 물질을 함유할 수 있다.
그러한 투여 형태를 제조하는 실제 방법은 공지되어 있거나, 관련 기술 분야의 통상의 기술자에게 자명할 것이다; 예를 들어, 문헌[Remington's Pharmaceutical Sciences(1990)](미국 펜실베니아주 소재의 백 퍼플리싱, 코퍼레이션)을 참고하기 바란다.
0.005% 내지 100%의 범위의 항체와 나머지 범위의 무독성 담체를 함유하는 투여 형태 또는 조성물이 제조될 수 있다. 이들 조성물의 제조 방법은 관련 기술 분야의 통상의 기술자에게 공지되어 있다.
경구 약제학적 투여 형태는 고체, 겔 또는 액체이다. 고체 투여 형태는 정제, 캡슐, 과립 및 벌크(bulk) 분말이다. 경구 정제의 예는 장용-코팅되거나, 당-코팅되거나, 필름-코팅될 수 있는 압축 츄어블 로젠지(lozenge) 및 정제를 포함한다. 캡슐은 경질 또는 연질 젤라틴 캡슐일 수 있는 한편, 과립 및 분말은 관련 기술 분야의 통상의 기술자에게 공지된 다른 성분들의 조합으로 비-발포형 또는 발포형으로 제공될 수 있다.
특정 실시형태에서, 제제는 고체 투여 형태이다. 특정 실시형태에서, 제제는 캡슐 또는 정제이다. 정제, 알약, 캡슐, 트로키(troche) 등은 하나 이상의 다음 성분 또는 유사한 본성의 화합물을 함유할 수 있다: 결합제; 윤활제; 희석제; 유동화제(glidant); 붕해제; 착색제; 감미제; 향미제; 습윤제; 최토제 코팅; 및 필름 코팅을 함유할 수 있다. 바인더의 예는 미세결정질 셀룰로스, 검 트라가칸트, 글루코스 용액, 아카시아 점액, 젤라틴 용액, 당밀, 폴리비닐피롤리딘, 포비돈, 크로스포비돈, 수크로스 및 전분 페이스트를 포함한다. 윤활제는 탈크, 전분, 스테아르산 마그네슘 또는 스테아르산 칼슘, 리코포듐 및 스테아르산을 포함한다. 희석제는 예를 들어 락토스, 수크로스, 전분, 카올린, 염, 만니톨 및 인산 이칼슘을 포함한다. 유동화제는 콜로이드성 이산화규소를 포함하지만 이에 제한되는 것은 아니다. 붕해제는 크로스카르멜로스 나트륨, 나트륨 전분 글리콜레이트, 알긴산, 옥수수 전분, 감자 전분, 벤토나이트, 메틸셀룰로스, 아가 및 카복시메틸셀룰로스를 포함한다. 착색제는 예를 들어 임의의 승인 인증된 수용성 FD 및 C 염료, 이의 혼합물; 및 알루미나 수화물 상에 현탁된 수불용성 FD 및 C 염료를 포함한다. 감미제는 수크로스, 락토스, 만니톨 및 인공 감미제, 예를 들어 사카린 및 임의의 많은 분무 건조된 향료를 포함한다. 향미제는 과일과 같은 식물로부터 추출한 자연 향료 및 비제한적으로 박하 및 메틸 살리실레이트와 같은 즐거운 미각을 생성시키는 화합물의 합성 블렌드를 포함한다. 습윤제는 프로필렌 글리콜 모노스테아레이트, 소르비탄 모노올레에이트, 다이에틸렌 글리콜 모노라우레이트 및 폴리옥시에틸렌 라우릴 에터를 포함한다. 최토제 코팅은 지방산, 지방, 왁스, 셀락(shellac), 암모니아처리 셀락 및 셀룰로스 아세테이트 프탈레이트를 포함한다. 필름 코팅은 히드록시에틸셀룰로스, 나트륨 카복시메틸셀룰로스, 폴리에틸렌 글리콜 4000 및 셀룰로스 아세테이트 프탈레이트를 포함한다.
본 발명의 항체는 위의 산성 환경으로부터 그를 보호하는 조성물 내에 제공될 수 있다. 예를 들어, 조성물은 위에서 이의 완전성을 유지하고 장에서 활성 화합물을 방출하는 장용 코팅 내에 제제화될 수 있다. 조성물은 또한 제산제 또는 다른 그러한 성분과 조합으로 제제화될 수 있다.
투여 단위 형태가 캡슐일 때 상기한 유형의 물질에 추가로 액체 담체, 예를 들어 지방 오일을 함유할 수 있다. 또한, 투여 단위 형태는 투여 단위의 물리적 형태를 변형시키는 다양한 다른 물질, 예를 들어, 당 및 다른 장용제의 코팅을 함유할 수 있다. 화합물은 또한 엘릭시르, 현탁액, 시럽, 웨이퍼(wafer), 스프링클(sprinkle), 츄잉 검 등의 성분으로서 투여될 수 있다. 시럽은 활성 화합물에 추가로 감미제로서 수크로스 및 특정 방부제, 염료 및 착색제 및 향료를 함유할 수 있다.
항체는 또한 목적하는 작용을 저해하지 않는 다른 활성 물질, 또는 목적하는 작용을 보충하는 물질, 예를 들어 제산제, H2 차단제 및 이뇨제와 혼합될 수 있다. 활성 성분은 본 명세서에서 설명된 항체 또는 이의 약제학적으로 허용 가능한 유도체이다. 보다 고농도, 약 98 중량% 이하의 활성 성분이 포함될 수 있다.
모든 실시형태에서, 정제 및 캡슐 제제는 활성 성분의 분해를 변형 또는 지속시키기 위해 관련 기술 분야의 통상의 기술자에게 공지된 바와 같이 코팅될 수 있다. 따라서, 예를 들어, 이들은 통상적인 장용 코팅, 예를 들어 페닐살리실레이트, 왁스 및 셀룰로스 아세테이트 프탈레이트로 코팅될 수 있다.
바람직한 실시형태에서, 제제는 액체 투여 형태이다. 액체 경구 투여 형태는 수용액, 에멀전, 현탁액, 용액 및/또는 비-발포성 과립으로부터 재구성된 현탁액 및 발포성 과립으로부터 재구성된 발포성 제제를 포함한다. 수용액은 예를 들어, 엘릭시르 및 시럽을 포함한다. 에멀전은 수-중-유형 또는 유-중-수형이다.
엘릭시르는 투명한 감미 수성알코올 제제이다. 엘릭시르에 사용되는 약제학적으로 허용 가능한 담체는 용매를 포함한다. 시럽은 당, 예를 들어 수크로스의 농축 수용액이고, 방부제를 함유할 수 있다. 에멀전은 하나의 액체가 작은 구형으로 다른 액체 전체에 분산된 2상계이다. 에멀전에 사용되는 약제학적으로 허용 가능한 담체는 비-수성 액체, 유화제 및 방부제이다. 현탁액은 약제학적으로 허용 가능한 현탁제 및 방부제를 사용한다.
액체 경구 투여 형태로 재구성되는 비-발포성 과립에 사용되는 약제학적으로 허용 가능한 물질은 희석제, 감미료 및 습윤제를 포함한다. 액체 경구 투여 형태로 재구성되는 발포성 과립에 사용되는 약제학적으로 허용 가능한 물질은 유기산 및 이산화탄소원을 포함한다. 착색제 및 향미제는 상기 투여 형태 모두에 사용된다.
용매는 글리세린, 소르비톨, 에틸 알코올 및 시럽을 포함한다. 방부제의 예는 글리세린, 메틸 및 프로필파라벤, 벤조산, 벤조산 나트륨 및 알코올을 포함한다. 에멀전에 사용되는 비-수성 액체의 예는 광유 및 면실유를 포함한다. 유화제의 예는 젤라틴, 아카시아, 트라가칸트, 벤토나이트 및 계면활성제, 예를 들어 폴리옥시에틸렌 소르비탄 모노올레에이트를 포함한다. 현탁제는 나트륨 카복시메틸셀룰로스, 펙틴, 트라가칸트, 비검(Veegum) 및 아카시아를 포함한다. 감미제는 수크로스, 시럽, 글리세린 및 인공 감미제, 예를 들어 사카린을 포함한다. 습윤제는 프로필렌 글리콜 모노스테아레이트, 소르비탄 모노올레에이트, 디에틸렌 글리콜 모노라우레이트 및 폴리옥시에틸렌 라우릴 에터를 포함한다. 유기산은 시트르산 및 타르타르산을 포함한다. 이산화탄소원은 중탄산나트륨 및 탄산나트륨을 포함한다. 착색제는 임의의 승인 인증된 수용성 FD 및 C 염료와 이의 혼합물을 포함한다. 향미제는 과일과 같은 식물로부터 추출한 자연 향료, 및 즐거운 미각을 생성시키는 화합물의 합성 블렌드를 포함한다.
고체 투여 형태를 위해, 예를 들어 프로필렌 카보네이트, 식물유 또는 트라이글리세리드 중의 용액 또는 현탁액은 일 실시형태에서 젤라틴 캡슐 내에 캡슐화된다. 그러한 용액 및 이의 제조 및 캡슐화는 미국 특허 4,328,245; 4,409,239; 및 4,410,545에 개시되어 있다. 액체 투여 형태를 위해, 예를 들어, 폴리에틸렌 글리콜 중의 용액은 투여를 위해 쉽게 측정되도록 충분한 양의 약제학적으로 허용 가능한 액체 담체, 예를 들어, 물로 희석될 수 있다.
대안적으로, 액체 또는 반-고체 경구 제제는 활성 화합물 또는 염을 식물유, 글리콜, 트리글리세리드, 프로필렌 글리콜 에스터(예를 들어, 프로필렌 카보네이트) 및 다른 그러한 담체에 용해 또는 분산시키고, 상기 용액 또는 현탁액을 경질 또는 연질 젤라틴 캡슐 외피에 캡슐화함으로써 제조될 수 있다. 다른 유용한 제제는 미국 특허 RE28,819와 4,358,603에 기재된 것을 포함한다. 간단히 설명하면, 상기 제제는 본 명세서에 제공된 화합물, 다이알킬화 모노- 또는 폴리-알킬렌 글리콜, 비제한적인 예를 들어 1,2-다이메톡시메탄, 다이글라임, 트라이글라임, 테트라글라임, 폴리에틸렌 글리콜-350-다이메틸 에터, 폴리에틸렌 글리콜-550-다이메틸 에터, 폴리에틸렌 글리콜-750-다이메틸 에터(여기서 350, 550 및 750은 폴리에틸렌 글리콜의 대략적인 평균 분자량을 나타낸다) 및 하나 이상의 항산화제, 예를 들어 부틸화 히드록시톨루엔(BHT), 부틸화 히드록시아니솔(BHA), 프로필 갈레이트, 비타민 E, 하이드로퀴논, 히드록시쿠마린, 에탄올아민, 레시틴, 세팔린, 아스코르브산, 말산, 소르비톨, 인산, 티오다이프로피온산과 이의 에스터 및 다이티오카바메이트를 함유하는 것을 포함하지만 이에 제한되는 것은 아니다.
다른 제제는 약제학적으로 허용 가능한 아세탈을 포함하는 수성 알코올 용액을 포함하지만 이에 제한되는 것은 아니다. 이들 제제에 사용되는 알코올은 프로필렌 글리콜 및 에탄올을 포함하고 이로 제한되지 않는, 하나 이상의 하이드록실기를 갖는 임의의 약제학적으로 허용 가능한 수-혼화성 용매이다. 아세탈은 저급 알킬 알데하이드의 다이(저급 알킬)아세탈, 예를 들어 아세트알데하이드 다이에틸 아세탈을 포함하지만 이에 제한되는 것은 아니다.
일 실시형태에서, 피하, 근육내 또는 정맥내의 주사를 특징으로 하는 비경구 투여가 또한 본 명세서에서 고려된다. 주사 가능 물질은 통상적인 형태로, 액체 용액 또는 현탁액, 주사 전에 액체 중의 용액 또는 현탁액에 적합한 고체 형태로 또는 에멀전으로서 제조될 수 있다. 주사 가능 물질, 용액 및 에멀전은 또한 하나 이상의 부형제를 함유한다. 적합한 부형제는 예를 들어 물, 염수, 덱스트로스, 글리세롤 또는 에탄올이다. 또한, 원하는 경우에, 투여될 약제학적 조성물은 또한 미량의 무독성 보조 물질, 예를 들어 습윤제 또는 유화제, pH 완충액, 안정화제, 용해도 강화제 및 다른 그러한 물질, 예를 들어 아세트산 나트륨, 소르비탄 모노라우레이트, 트라이에탄올아민 올레에이트 및 사이클로덱스트린을 함유할 수 있다.
일정안 수준의 투여량을 유지시키는 서방 또는 지속-방출 시스템(예를 들어, 미국 특허 3,710,795 참고)의 이식이 또한 본 명세서에서 고려된다. 간단히 설명하면, 본 명세서에 제공된 화합물은 체액에 불용성인 외부 중합체 막, 예를 들어 폴리에틸렌, 폴리프로필렌, 에틸렌/프로필렌 공중합체, 에틸렌/에틸 아크릴레이트 공중합체, 에틸렌/비닐아세테이트 공중합체, 실리콘 고무, 폴리디메틸 실록산, 네오프렌 고무, 염소화 폴리에틸렌, 폴리염화비닐, 비닐클로라이드의 비닐 아세테이트, 비닐리덴 클로라이드, 에틸렌 및 프로필렌과의 공중합체, 이오노머 폴리에틸렌 테레프탈레이트, 부틸 고무 에피클로로히드린 고무, 에틸렌/비닐 알코올 공중합체, 에틸렌/비닐 아세테이트/비닐 알코올 3원 공중합체 및 에틸렌/비닐옥시에탄올 공중합체에 의해서 둘러싸인 고체 내부 매트릭스, 예를 들어 폴리메틸메타크릴레이트, 폴리부틸메타크릴레이트, 가소성 또는 비가소성 폴리염화비닐, 가소성 나일론, 가소성 폴리에틸렌테레프탈레이트, 자연 고무, 폴리이소프렌, 폴리이소부틸렌, 폴리부타다이엔, 폴리에틸렌, 에틸렌-비닐아세테이트 공중합체, 실리콘 고무, 폴리다이메틸실록산, 실리콘 카보네이트 공중합체, 친수성 중합체, 예를 들어 아크릴산 및 메타크릴산의 에스터의 하이드로겔, 콜라겐, 가교결합된 폴리비닐알코올 및 가교결합된 부분적으로 가수분해된 폴리비닐 아세테이트 내에 분산된다. 항체는 방출 속도 제어 단계에 외부 중합체 막을 통해 확산한다. 상기 비경구 조성물 내에 함유된 항체의 양은 이의 구체적인 성질 및 화합물의 활성과 대상체의 필요에 매우 의존적이다.
비경구 투여를 위한 제제는 즉시 주사하기 위한 멸균 용액, 사용 직전에 용매와 조합하기 위한 멸균 건조 가용성 산물, 예를 들어 동결건조 분말, 예를 들어 피하 정제, 즉시 주사하기 위한 멸균 현탁액, 사용 직전에 비히클과 조합하기 위한 멸균 건조 불용성 산물 및 멸균 에멀전을 포함한다. 용액은 수성 또는 비수성일 수 있다.
정맥내 투여되는 경우에, 적합한 담체는 생리 염수 또는 포스페이트 완충 식염수(PBS), 및 농후제 및 가용화제, 예를 들어 글루코스, 폴리에틸렌 글리콜 및 폴리프로필렌 글리콜 및 이의 혼합물을 함유하는 용액을 포함한다.
비경구 제제에 사용되는 약제학적으로 허용 가능한 담체는 수성 비히클, 비수성 비히클, 항미생물제, 등장제, 완충액, 항산화제, 국소 마취제, 현탁 및 분산제, 유화제, 격리(sequestering) 또는 킬레이팅제 및 다른 약제학적으로 허용 가능한 물질을 포함한다.
수성 비히클의 예는 염화나트륨 주사액, 링거(Ringers) 주사액, 등장성 덱스트로스 주사액, 멸균수 주사액, 덱스트로스 및 유산 첨가(lactated) 링거 주사액을 포함한다. 비수성 비경구 비히클은 식물 기원의 고정유, 면실유, 옥수수유, 참기름 및 땅콩유를 포함한다. 정균 또는 정진균 농도의 항미생물제가 다수-용량 용기에 포장된 비경구 제제에 첨가될 수 있고, 이는 페놀 또는 크레졸, 수은제, 벤질 알코올, 클로로부탄올, 메틸 및 프로필 p-하이드록시벤조산 에스터, 치메로살, 벤즈알코늄 클로라이드 및 벤조토늄 클로라이드를 포함한다. 등장제는 염화나트륨 및 덱스트로스를 포함한다. 완충액은 포스페이트 및 시트레이트를 포함한다. 항산화제는 중황산나트륨을 포함한다. 국소 마취제는 염산프로카인을 포함한다. 현탁 및 분산제는 나트륨 카복시메틸셀룰로스, 하이드록시프로필 메틸셀룰로스 및 폴리비닐피롤리돈을 포함한다. 유화제는 폴리소르베이트 80(트윈(등록상표) 80)을 포함한다. 금속 이온의 격리 또는 킬레이팅제는 EDTA를 포함한다. 약제학적 담체는 또한 수혼화성 비히클을 위한 에틸 알코올, 폴리에틸렌 글리콜 및 프로필렌 글리콜; 및 pH 조정을 위한 수산화 나트륨, 염산, 시트르산 또는 락트산을 포함한다.
약제학적 활성 화합물의 농도는 주사가 목적하는 약물학적 효과를 제공하기 위해 유효량을 제공하도록 조정된다. 정확한 용량은 관련 기술 분야에 논의 바와 같이 환자 또는 동물의 연령, 체중 및 상태에 좌우된다.
단위-용량 비경구 제제는 앰플, 바이알 또는 바늘이 있는 주사기 내에 포장될 수 있다. 비경구 투여를 위한 모든 제제는 관련 기술 분야에 공지되고 실시되는 바와 같이 멸균될 수 있다.
예시적으로, 활성 화합물을 함유하는 멸균 수용액의 정맥내 또는 동맥내 주입이 효과적인 투여 모드이다. 또 다른 실시형태는 목적하는 약물학적 효과를 생성하기 위해 필요한 만큼 주사되는 활성 물질을 함유하는 멸균 수용액 또는 유성 용액 또는 현탁액이다.
주사 가능 물질은 국소 및 전신 투여를 위해 설계된다. 일 실시형태에서, 치료 유효 투여량은 처리된 조직(들)에 적어도 약 0.1% w/w 내지 약 90% w/w 이상, 특정 실시형태에서 1% w/w 초과의 활성 화합물의 농도를 함유하도록 제제화된다.
항체는 미소화 또는 다른 적합한 형태로 현탁될 수 있다. 생성되는 혼합물의 형태는 의도되는 투여 방식 및 선택된 담체 또는 비히클 내의 화합물의 용해도를 포함한 많은 인자에 의해서 좌우된다. 효과적인 농도는 병태의 증상을 완화시키기 위해 충분하고, 경험적으로 결정될 수 있다.
다른 실시형태에서, 약제학적 제제는 투여를 위해 용액, 에멀전 및 다른 혼합물로서 재구성될 수 있는 동결건조 분말이다. 이들은 또한 고체 또는 겔로서 재구성되거나 제제화될 수 있다.
동결건조 분말은 본 명세서에 제공된 항체 또는 약제학적으로 허용 가능한 이의 유도체를 적합한 용매에 용해시킴으로써 제조된다. 일부 실시형태에서, 동결건조 분말은 무균이다. 용매는 안정성을 향상시키는 부형제 또는 분말, 또는 분말로부터 제조된 재구성된 용액의 다른 약물학적 성분을 함유할 수 있다. 사용될 수 있는 부형제는 덱스트로스, 소르비탈, 프룩토스, 옥수수 시럽, 자일리톨, 글리세린, 글루코스, 수크로스 또는 다른 적합한 물질을 포함하지만 이에 제한되는 것은 아니다. 일 실시형태에서, 용매는 또한 완충액, 예를 들어 시트레이트, 인산 나트륨 또는 인산 칼륨 또는 관련 기술 분야의 통상의 기술자에게 공지된 다른 그러한 완충액을 하나의 실시형태에서 약 중성 pH에서 함유할 수 있다. 용액을 후속적으로 멸균 여과한 후, 관련 기술 분야의 통상의 기술자에게 공지된 표준 조건 하에 동결건조하여 목적하는 제제를 제공한다. 일 실시형태에서, 생성되는 용액은 동결건조를 위해 바이알 내로 배분될 것이다. 각각의 바이알은 단일 투여량 또는 다중 투여량의 화합물을 함유할 것이다. 동결건조 분말은 적절한 조건, 예를 들어 약 4℃ 내지 실온하에 저장될 수 있다.
주사용수를 사용하여 이러한 동결건조 분말을 재구성하여 비경구 투여에 사용하기 위한 제제를 제공한다. 재구성을 위해, 동결건조 분말을 멸균수 또는 다른 적합한 담체에 첨가한다. 정확한 양은 선택된 화합물에 좌우된다. 그러한 양은 경험적으로 결정될 수 있다.
국소 혼합물은 국소 및 전신 투여를 위해 기술된 바와 같이 제조된다. 생성되는 혼합물은 용액, 현탁액, 에멀전 등일 수 있고, 크림, 젤, 연고, 에멀전, 용액, 엘릭시르, 로션, 현탁액, 팅크제(tincture), 페이스트, 포움, 에어로졸, 세척액(irrigation), 스프레이, 좌제, 밴드, 피부 패치 또는 국소 투여에 적합한 임의의 다른 제제로서 제제화될 수 있다.
본 발명의 항체는 예를 들어 흡입에 의한 국소 적용을 위한 에어로졸로서 제제화될 수 있다(예를 들어, 미국 특허 4,044,126, 4,414,209 및 4,364,923 참고하고, 이는 염증 질환, 특히 천식의 치료에 유용한 스테로이드의 전달을 위한 에어로졸을 기술한다). 기도로 투여하기 위한 이들 제제는 네불라이저(nebulizer)용 에어로졸 또는 용액의 형태, 또는 통기법(insufflation)을 위한 미세 분말로서 단독으로 또는 락토스와 같은 불활성 담체와 조합으로 존재할 수 있다. 그러한 경우에, 하나의 실시형태에서, 제제의 입자는 직경이 50 마이크로미터 미만, 일 실시형태에서 10 마이크로미터 미만이다.
화합물은 국지 또는 국소 적용하기 위해, 예컨대, 예컨대 눈에서 피부 및 점막에 국소 적용하기 위해 젤, 크림 및 로션의 형태로 및 눈에 적용하기 위해 또는 뇌수조내 또는 척수강내 적용을 위해 제제화될 수 있다. 국소 투여는 경피 전달을 위해 및 또한 눈 또는 점막에 투여하기 위해 또는 흡입 요법을 위해 고려된다. 활성 화합물 단독 또는 다른 약제학적으로 허용 가능한 부형제와의 조합으로의 비강 용액이 또한 투여될 수 있다.
이러한 용액, 특히 안과 용도로 의도되는 용액은 적절한 염을 사용하여 0.01% 내지 10% 등장성 용액, pH 약 5 내지 7로서 제제화될 수 있다.
다른 투여 경로, 예를 들어 이온영동 및 전기영동 장치를 포함한 경피 패치 및 직장 투여가 또한 본 명세서에서 고려된다.
이온영동 및 전기영동 장치를 포함한 경피 패치는 관련 기술 분야의 통상의 기술자에게 널리 공지되어 있다. 예를 들어, 그러한 패치는 미국 특허 6,267,983, 6,261,595, 6,256,533, 6,167,301, 6,024,975, 6,010715, 5,985,317, 5,983,134, 5,948,433 및 5,860,957에 개시되어 있다.
예를 들어, 직장 투여를 위한 약제학적 투여 형태는 전신 효과를 위한 직장 좌제, 캡슐 및 정제이다. 본 명세서에서 사용되는 직장 좌제는 체온에서 용융하거나 연화되어 하나 이상의 약리학상 또는 치료상 활성 성분을 방출하는, 직장 내로 삽입하기 위한 고체를 의미한다. 직장 좌제에 사용되는 약제학적으로 허용 가능한 물질은 베이스(base) 또는 비히클 및 용융점을 상승시키는 물질이다. 베이스의 예는 코코아 버터(코코아 오일(theobroma oil)), 글리세린-젤라틴, 카보왁스(폴리옥시에틸렌 글리콜) 및 지방산의 모노-, 다이- 및 트라이글리세리드의 적절한 혼합물을 포함한다. 다양한 베이스의 조합을 사용할 수 있다. 좌제의 용융점을 상승시키는 작용제는 스퍼마세티(spermaceti) 및 왁스를 포함한다. 직장 좌제는 압축법 또는 성형에 의해서 제조할 수 있다. 일 실시형태에서 직장 좌제의 중량은 약 2 내지 3gm이다.
직장 투여를 위한 정제 및 캡슐은 경구 투여용 제제를 위한 것과 동일한 약제학적으로 허용 가능한 물질을 사용하여 동일한 방법에 의해서 제조될 수 있다.
본 명세서에 제공된 항체 및 다른 조성물은 또한 치료되는 대상체의 신체의 특정 조직, 수용체 또는 다른 영역에 표적화되도록 제제화될 수 있다. 많은 그러한 표적화 방법이 관련 기술 분야의 통상의 기술자에게 널리 공지되어 있다. 모든 그러한 표적화 방법이 본 발명의 조성물에서 사용하기 위해 본 명세서에서 고려된다. 표적화 방법의 비제한적인 예에 대해서는 예를 들어, 미국 특허 6,316,652, 6,274,552, 6,271,359, 6,253,872, 6,139,865, 6,131,570, 6,120,751, 6,071,495, 6,060,082, 6,048,736, 6,039,975, 6,004,534, 5,985,307, 5,972,366, 5,900,252, 5,840,674, 5,759,542 및 5,709,874를 참고하기 바란다. 일부 실시형태에서, 본 발명의 항-hOX40L 항체는 예컨대 IBD를 갖거나 또는 그것을 가질 위험이 있는 환자에서 결장에 표적화된다(또는 달리 투여된다). 일부 실시형태에서, 본 발명의 항-hOX40L 항체는 예컨대 포도막염을 갖거나 또는 그것을 가질 위험이 있는 환자에서 눈에 표적화된다(또는 달리 투여된다).
일 실시형태에서, 조직-표적화 리포좀, 예를 들어 종양-표적화 리포좀을 포함하는 리포좀 현탁액이 또한 약제학적으로 허용 가능한 담체로서 적합할 수 있다. 이들은 관련 기술 분야의 통상의 기술자에게 공지된 방법에 따라 제조할 수 있다. 예를 들어, 리포좀 제제는 미국 특허 4,522,811에 기재된 바와 같이 제조될 수 있다. 간단히 설명하면, 리포좀, 예를 들어 다층판 소포(multilamellar vesicle: MLV)는 플라스크의 내부 상에서 난(egg) 포스파티딜 콜린과 뇌 포스파티딜 세린(7:3 몰비)을 건조시킴으로써 형성할 수 있다. 2가 양이온이 결핍되는 포스페이트 완충 식염수(PBS) 내의 본 명세서에 제공된 화합물의 용액을 첨가하고, 액체 필름이 분산될 때까지 플라스크를 진탕시킨다. 생성되는 소포를 세척하여 캡슐화되지 않은 화합물을 제거하고, 원심분리에 의해서 펠렛화한 후, PBS 중에 재현탁시킨다.
투여 및 투약 방법
본 발명은 hOX40L-매개된 질환(또는 이의 증상)의 예방, 관리, 치료 및/또는 완화에 사용하기 위한 본 발명의 하나 이상의 항체 또는 단편을 포함하는 조성물을 추가로 제공한다. 항체와 관련된 논의는 또한 본 발명의 단편에 필요한 부분만 약간 수정하여 적용된다. 대안적으로, 본 발명은 대상체에서 OX40L-매개된 질환(또는 이의 증상)의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 하나 이상의 본 발명의 항체 또는 단편을 포함하는 조성물을 추가로 제공하고, 여기서, OX40L은 비-인간(예를 들어, 캐닌(canine), 펠린(feline), 에퀸(equine), 소, 오바인(ovine) 또는 포사인(porcine))이고, 대상체는 각각 개, 고양이, 말, 소, 양 또는 돼지이다.
특정 실시형태에서, 본 명세서에서 hOX40L-매개된 질환, 예를 들어 IBD(예를 들어, 궤양성 대장염 또는 크론병) 또는 이의 증상의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 본 발명의 하나 이상의 항체를 포함하는 조성물이 제공된다. IBD 증상은 경증에서 중증에 이를 수 있고, 일반적으로 관여된 장관의 부분에 의해서 좌우된다. IBD의 예시적인 증상은 복부 경련 및 복통, 혈성 설사, 중증 배변 절박, 열, 식욕 상실, 체중 감소, 빈혈, 피로, 및/또는 하지, 발목, 종아리, 허벅지 및 팔의 궤양을 포함한다. IBD의 예시적인 장 합병증은 장의 궤양, 천공 또는 파열로부터 많은 출혈, 협착 및 폐쇄, 누공(fistulae)(비정상 통로) 및 항문주위 질환, 독성 거대결장증(예를 들어, 결장의 급성 비폐쇄성 확장) 및/또는 악성종양(예를 들어, 결장 또는 소장의 암)을 포함한다. IBD의 예시적인 장외 합병증은 관절염, 피부 병태, 눈의 염증, 간 및 신장 질환 및/또는 뼈 손실을 포함한다. 이들 증상의 임의의 조합이 본 명세서에 제공된 조성물 및 방법을 사용하여 예방되고/되거나 관리되고/되거나 치료되고/되거나 완화될 수 있다.
특정 실시형태에서, 본 명세서에서 hOX40L-매개된 질환, 예를 들어 GVHD 또는 이의 증상의 예방, 관리, 치료 및/또는 완화에 사용하기 위한 본 발명의 하나 이상의 항체를 포함하는 조성물이 제공된다. GVHD는 일반적으로 동종이형 또는 매칭된 비관련 골수 이식(BMT) 이후에 일어난다.
일부 실시형태에서, GVHD는 급성 GVHD이다. 급성 GVHD의 증상은 빠르게 일어날 수 있고, 경증 또는 중증일 수 있다. 특정한 경우에, 급성 GVHD는 이식 후 약 3개월 이내에, 예를 들어 이식 후 혈구수가 회복될 때 발병한다. 특정한 경우에, 급성 GVHD는 피부, 위장관(GI) 및/또는 간에 침범한다. 예를 들어, 일부 환자에서, 급성 피부 GVHD는 예를 들어, 환자의 손바닥, 발바닥 또는 어깨에서 발진으로 시작한다. 그러나, 발진은 확산될 수 있고, 가렵고 아플 수 있고/있거나 물집이 생기고 벗겨질 수도 있다. 급성 간 GVHD는 간, 예를 들어 간 효소의 정상 기능을 해칠 수 있고, 이는 다시 황달을 일으킬 수 있다. 급성 간 GVHD는 또한 간이 팽대되면 환자의 복부를 팽창시키고 아프게 할 수 있다. 마지막으로, 급성 장 GVHD(또는 소화계 GVHD)의 증상은 설사, 대변 내 점액 또는 혈액, 경련 또는 복통, 소화불량, 오심 및/또는 식욕 상실을 포함할 수 있다. 급성 GVHD의 다른 일반적인 증상은 빈혈, 미열 및/또는 감염 가능성 증가를 포함할 수 있다. 급성 GVHD의 이들 증상의 임의의 조합이 본 명세서에 제공된 조성물 및 방법을 사용하여 예방되고/되거나 관리되고/되거나 치료되고/되거나 완화될 수 있다.
다른 실시형태에서, GVHD는 만성 GVHD이다. 만성 GVHD는 이식 후 약 3개월 내지 약 1년 또는 그 후 발생할 수 있다. 만성 GVHD는 경증 또는 중증일 수 있고, 일반적으로 급성 GVHD와 유사한 증상을 포함한다. 만성 GVHD는 피부 및 소화계, 예를 들어 간에 침범할 수 있지만, 또한 다른 장기 및 면역계(예를 들어, 환자의 감염 가능성을 증가시킴) 및/또는 결합 조직에 관련될 수 있다. 만성 피부 GVHD의 증상은 발진, 피부 건조, 피부 당김, 피부 가려움, 어두운 피부색, 피부 비후를 포함하고/하거나 모발(예를 들어 탈모, 백발) 또는 손발톱(예를 들어 딱딱하거나 부서지기 쉬운 손발톱)에 침범할 수 있다. 만성 장 GVHD는 소화계, 입, 식도, 위 내벽 및/또는 장 내벽에 침범할 수 있고, 증상은 설사, 구갈 또는 구내염, 연하 통증, 위에 의한 영양 흡수 저하, 고창, 위 경련을 포함할 수 있다. 만성 간 GVHD는 간 손상 및 흉터형성(경화증)을 일으킬 수 있다. 눈의 만성 GVHD는 눈물샘에 침범할 수 있어서, 눈을 건조하고 작열하고 아프게 하거나 밝은 빛에 견디기 어렵게 한다. 만성 폐 GVHD는 호흡 곤란, 천명, 지속적인 기침 및/또는 흉부 감염 가능성 증가를 일으킬 수 있다. 만성 GVHD는 근육을 뼈에 연결시키는 건(예를 들어, 염증)에 침범할 수 있어서, 팔과 다리를 뻗거나 굽히기 어렵게 한다. 만성 GVHD의 이들 증상의 임의의 조합은 본 명세서에 제공된 조성물 및 방법을 사용하여 예방되고/되거나 관리되고/되거나 치료되고/되거나 완화될 수 있다.
특정 실시형태에서 본 명세서에서 hOX40L-매개된 질환, 예컨대 포도막염, 또는 이의 증상의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 하나 이상의 본 발명의 항체를 포함하는 조성물이 제공된다.
특정 실시형태에서 본 명세서에서 hOX40L-매개된 질환, 예컨대 예컨대 괴저성 농피증, 거대 세포성 동맥염, 슈니츨러 증후군 또는 비-감염성 공막의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 하나 이상의 본 발명의 항체를 포함하는 조성물이 제공된다.
특정 실시형태에서 본 명세서에서 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택된 hOX40L 매개된 질환 또는 병태; 예를 들어 염증성 장 질환(IBD), 크론병, 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염, 접촉 과민증, 다발성 경화증 및 죽상동맥경화증, 특히 GvHD의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 하나 이상의 본 발명의 항체를 포함하는 조성물이 제공된다.
구체적인 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 조성물은 본 발명의 항체, 예를 들어, 실시예에 개시된 항체의 OX40L 결합 부위를 포함한다.
또 다른 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 조성물은 서열 목록(즉, 서열번호 2, 서열번호 34, 서열번호 66 또는 서열번호 94, 특히 서열번호 34)의 VH 도메인 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VH 도메인을 포함하는 하나 이상의 항체를 포함한다. 또 다른 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 조성물은 서열 목록(즉, 서열번호 4, 서열번호 10, 서열번호 36, 서열번호 42, 서열번호 68, 서열번호 74, 서열번호 96 또는 서열번호 102, 특히, 서열번호 36 또는 서열번호 42)의 VH CDR1 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VH CDR1을 포함하는 하나 이상의 항체를 포함한다. 또 다른 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 조성물은 서열 목록(즉, 서열번호 6, 서열번호 12, 서열번호 38, 서열번호 44, 서열번호 70, 서열번호 76, 서열번호 98 또는 서열번호 104, 특히 서열번호 38 또는 서열번호 44)의 VH CDR2 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VH CDR2를 포함하는 하나 이상의 항체를 포함한다. 바람직한 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 조성물은 서열 목록(즉, 서열번호 8, 서열번호 14, 서열번호 40, 서열번호 46, 서열번호 72, 서열번호 78, 서열번호 100 또는 서열번호 106, 특히 서열번호 40 또는 서열번호 46)의 VH CDR3 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VH CDR3을 포함하는 하나 이상의 항체를 포함한다.
또 다른 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 조성물은 서열 목록(즉, 서열번호 16, 서열번호 48, 서열번호 80, 또는 서열번호 108, 특히 서열번호 48)(임의로 서열 목록(즉, 서열번호 2/16, 서열번호 34/48, 서열번호 66/80 또는 서열번호 94/108, 특히 서열번호 34/48)에 언급된 유사한 VH 도메인을 또한 포함함))의 VL 도메인 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VL 도메인을 포함하는 하나 이상의 항체를 포함한다. 또 다른 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 조성물은 서열 목록(즉, 서열번호 18, 서열번호 24, 서열번호 50, 서열번호 56, 서열번호 82, 서열번호 88, 서열번호 110 또는 서열번호 116, 특히 서열번호 50 또는 서열번호 56)의 VL CDR1 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VL CDR1을 포함하는 하나 이상의 항체를 포함한다. 또 다른 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 조성물은 서열 목록(즉, 서열번호 20, 서열번호 26, 서열번호 52, 서열번호 58, 서열번호 84, 서열번호 90, 서열번호 112 또는 서열번호 118, 특히 서열번호 52 또는 서열번호 58)의 VL CDR2 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VL CDR2를 포함하는 하나 이상의 항체를 포함한다. 바람직한 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 조성물은 서열 목록(즉, 서열번호 22, 서열번호 28, 서열번호 54, 서열번호 60, 서열번호 86, 서열번호 92, 서열번호 114 또는 서열번호 120, 특히 서열번호 54 또는 서열번호 60)의 VL CDR3 중 임의의 하나의 아미노산 서열을 갖는 VL CDR3 중 임의의 하나의 아미노산 서열을 갖는 VL CDR3을 포함하는 하나 이상의 항체를 포함한다
또 다른 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 조성물은 서열 목록(즉, 서열번호 2, 서열번호 34, 서열번호 66 또는 서열번호 94, 특히 서열번호 34)의 VH 도메인 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VH 도메인, 및 서열 목록(즉, 서열번호 16, 서열번호 48, 서열번호 80, 또는 서열번호 108, 특히 서열번호 48)의 VL 도메인 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VL 도메인을 포함하는 하나 이상의 항체를 포함한다.
또 다른 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 조성물은 서열 목록(즉, 서열번호 4, 서열번호 10, 서열번호 36, 서열번호 42, 서열번호 68, 서열번호 74, 서열번호 96 또는 서열번호 102, 특히, 서열번호 36 또는 서열번호 42)의 VH CDR1 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VH CDR1, 및 서열 목록(즉, 서열번호 18, 서열번호 24, 서열번호 50, 서열번호 56, 서열번호 82, 서열번호 88, 서열번호 110 또는 서열번호 116, 특히 서열번호 50 또는 서열번호 56)의 VL CDR1 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VL CDR1을 포함하는 하나 이상의 항체를 포함한다. 또 다른 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 조성물은 서열 목록(즉, 서열번호 4, 서열번호 10, 서열번호 36, 서열번호 42, 서열번호 68, 서열번호 74, 서열번호 96 또는 서열번호 102, 특히, 서열번호 36 또는 서열번호 42)의 VH CDR1 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VH CDR1, 및 서열 목록(즉, 서열번호 20, 서열번호 26, 서열번호 52, 서열번호 58, 서열번호 84, 서열번호 90, 서열번호 112 또는 서열번호 118, 특히 서열번호 52 또는 서열번호 58)의 VL CDR2 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VL CDR2를 포함하는 하나 이상의 항체를 포함한다. 또 다른 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에서 사용하기 위한 조성물은 서열 목록(즉, 서열번호 4, 서열번호 10, 서열번호 36, 서열번호 42, 서열번호 68, 서열번호 74, 서열번호 96 또는 서열번호 102, 특히, 서열번호 36 또는 서열번호 42)의 VH CDR1 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VH CDR1, 및 서열 목록(즉, 서열번호 22, 서열번호 28, 서열번호 54, 서열번호 60, 서열번호 86, 서열번호 92, 서열번호 114 또는 서열번호 120, 특히 서열번호 54 또는 서열번호 60)의 VL CDR3 중 임의의 하나의 아미노산 서열을 갖는 하나 이상의 VL CDR3을 포함하는 하나 이상의 항체를 포함한다.
본 명세서의 다른 곳에서 보다 상세히 논의된 바와 같이, 본 발명의 조성물은 단독으로 또는 다른 화합물 또는 조성물과 조합으로 사용될 수 있다. 또한, 항체는 추가로 N- 또는 C-말단에서 이종성 폴리펩타이드에 재조합 방식으로 융합될 수 있거나, 폴리펩타이드 또는 다른 조성물에 화학적으로 컨쥬게이팅될 수 있다(공유 및 비-공유 컨쥬게이션 포함). 예를 들어, 본 발명의 항체는 검출 검정법에서 표지로서 유용한 분자 및 이펙터 분자, 예를 들어 이종성 폴리펩타이드, 약물, 방사성 뉴클레오티드 또는 독소에 재조합 방식으로 융합되거나 컨쥬게이팅될 수 있다. 예를 들어, PCT 공개 WO 92/08495; WO 91/14438; WO 89/12624; 미국 특허 5,314,995; 및 EP 396,387를 참고하기 바란다.
일부 실시형태에서, 본 명세서에서 대상체에게 hOX40L 폴리펩타이드(예를 들어, 세포 표면-발현된 hOX40L 또는 가용성 hOX40L)에 특이적으로 결합하는 항체의 유효량을 투여하는 것을 포함하는, 대상체(예를 들어, 인간 대상체)에서 OX40L 수용체 또는 유사한 리간드(예를 들어, OX40)에 대한 hOX40L의 결합을 감소 또는 억제하기 위한 방법이 제공된다. 일부 실시형태에서, hOX40L 생물학적 활성, 예컨대 CCL20, IL8 및/또는 RANTES, 또는 INF-γ, TNF-α 또는 IL-2, 특히 INF-γ 또는 본 명세서에 개시된 또 다른 사이토카인이 또한 대상체에서 감소되고, 예를 들어 적어도 10, 20, 30, 40, 50 또는 60%, 또는 70%, 또는 80%, 또는 90% 또는 95% 또는 >95%만큼 감소된다.
특정 실시형태에서, 본 명세서에서 대상체에게 유효량의 hOX40L 폴리펩타이드(예를 들어, 세포 표면-발현된 hOX40L)에 특이적으로 결합하는 항체를 투여하는 것을 포함하는, 대상체(예를 들어, 인간 대상체)에서 hOX40L 생물학적 활성, 예컨대 인터페론 감마, IL-2, CCL20, IL8 및/또는 RANTES 또는 다른 사이토카인, 또는 INF-γ, TNF-α 또는 IL-2, 특히 INF-γ의 분비를 감소 또는 억제하는 방법이 제공되며, 여기서 hOX40L 생물학적 활성은 항체에 의해서 감소된다.
다른 실시형태에서, 본 명세서에서 세포를 유효량의 hOX40L 폴리펩타이드(예를 들어, 세포 표면-발현된 hOX40L 또는 가용성 hOX40L), 예컨대 hOX40L 폴리펩타이드, hOX40L 폴리펩타이드 단편, 또는 hOX40L 에피토프에 특이적으로 결합하는 항체와 접촉시키는, 세포 표면-발현된 hOX40L을 갖는 세포에서 OX40L 수용체 또는 유사한 리간드(예를 들어, OX40)에 대한 hOX40L의 결합을 감소 또는 억제하는 방법이 제공된다. 일부 실시형태에서, hOX40L 생물학적 활성, 예컨대 인터페론 감마, IL-2, CCL20, IL8 및/또는 RANTES, 또는 INF-γ, TNF-α 또는 IL-2, 특히 INF-γ 또는 본 명세서에 개시된 다른 사이토카인의 분비는 또한 세포에서 감소된다.
특정 실시형태에서, 본 명세서에서 세포를 유효량의 hOX40L 폴리펩타이드(예를 들어, 세포 표면-발현된 hOX40L 또는 가용성 hOX40L)에 특이적으로 결합하는 항체와 접촉시키는, 세포 표면-발현된 hOX40L 수용체(예컨대 OX40)를 갖는 세포에서, hOX40L 생물학적 활성, 예컨대 인터페론 감마, IL-2, CCL20, IL8 및/또는 RANTES 또는 본 명세서에 개시된 다른 사이토카인의 분비를 감소 또는 억제하는 방법이 제공되고, 여기서 hOX40L 생물학적 활성이 항체에 의해서 감소된다.
본 발명의 항체는 예를 들어, 시험관내 및 생체내 진단법 및 치료 방법 모두에서 hOX40L 항원을 정제하고, 검출하고, 표적화하기 위해 사용될 수 있다. 예를 들어, 변형된 항체는 생물학적 샘플 내의 hOX40L의 수준을 정성적 및 정량적으로 측정하기 위한 면역검정법에서 사용된다. 예를 들어, 문헌[Harlow et al., Antibodies: A Laboratory Manual, (Cold Spring Harbor Laboratory Press, 2nd ed. 1988)] (전문이 본 명세서에 참고로 포함됨)을 참고하기 바란다.
본 발명은 또한 대상체에게 유효량의 본 발명의 항체 또는 항체를 포함하는 약제학적 조성물을 투여함으로써, hOX40L-매개된 질환을 예방 및/또는, 관리 및/또는, 치료 및/또는 완화하는 방법을 제공한다. 일 양상에서, 항체는 실질적으로 정제된다(즉, 이의 효과를 제한하거나 바람직하지 않은 부작용을 일으키는 물질이 실질적으로 없다). 바람직한 실시형태에서, 항체는 완전 인간 단클론성 항체, 예를 들어 완전 인간 단클론성 길항제 항체이다. 치료제가 투여되는 대상체는 바람직하게는 포유동물, 예를 들어 비-영장류(예를 들어, 소, 돼지, 말, 고양이, 개, 래트 등) 또는 영장류(예를 들어, 원숭이, 예를 들어 레서스 또는 사이노몰거스 원숭이 또는 인간)이다. 바람직한 실시형태에서, 대상체는 인간이다. 또 다른 바람직한 실시형태에서, 대상체는 인간 유아 또는 인간 조산아이다. 또 다른 실시형태에서, 대상체는 hOX40L-매개된 질환을 갖는 인간이다.
리포좀, 마이크로입자, 마이크로캡슐 내의 캡슐화, 항체를 발현할 수 있는 재조합 세포, 수용체-매개된 세포내이입(예를 들어 문헌 [Wu and Wu, J. Biol. Chem. 262:4429-4432(1987)] 참고), 레트로바이러스 벡터 또는 다른 벡터의 일부로서 핵산의 구축 등을 포함하지만 이에 제한되지 않는 다양한 전달계가 공지되어 있고, 예방제 또는 치료제(예를 들어, 본 발명의 항체)를 투여하기 위해 사용될 수 있다. 예방 또는 치료제(예를 들어, 본 발명의 항체) 또는 약제학적 조성물을 투여하는 방법은 비경구 투여(예를 들어, 피부내, 근육내, 복강내, 정맥내 및 피하), 경막외 및 점막(예를 들어, 코 안 및 구강 경로)을 포함하지만 이에 제한되는 것은 아니다. 구체적인 실시형태에서, 예방제 또는 치료제(예를 들어, 본 발명의 항체) 또는 약제학적 조성물은 코 안, 근육내, 정맥내 또는 피하 투여된다. 예방제 또는 치료제 또는 조성물은 예를 들어 주입 또는 볼러스 주사에 의해, 상피 또는 점막피부 내층(예를 들어 구강 점막, 코 안 점막, 직장 및 장 점막 등)을 통한 흡수에 의해서 임의의 편리한 경로로 투여될 수 있고, 다른 생물학적 활성제와 함께 투여될 수 있다. 투여는 전신 또는 국지일 수 있다. 또한, 예를 들어, 흡입기 또는 네불라이저, 및 에어로졸화제를 사용한 제제화의 사용에 의해서 폐 투여가 또한 사용될 수 있다. 예를 들어 각각 전문이 본 명세서에 참고로 포함된 미국 특허 6,019,968, 5,985,320, 5,985,309, 5,934,272, 5,874,064, 5,855,913, 5,290,540, 및 4,880,078; 및 PCT 공개 WO 92/19244, WO 97/32572, WO 97/44013, WO 98/31346, 및 WO 99/66903을 참고하기 바란다.
구체적인 실시형태에서, 본 발명의 예방제 또는 치료제 또는 약제학적 조성물을 치료가 필요한 구역에 국소로 투여하는 것이 바람직할 수 있다. 이는 예를 들어 비제한적으로 국소 주입에 의해, 국소 투여에 의해(예를 들어, 코 안 스프레이에 의해), 주사에 의해, 또는 임플란트(implant)(상기 임플란트는 다공성, 비-다공성 또는 젤라틴성 물질, 예를 들어 실라스틱(sialastic) 막과 같은 막, 또는 섬유로 이루어짐)에 의해서 달성할 수 있다. 바람직하게는, 본 발명의 항체를 투여할 때, 항체가 흡수되지 않는 물질을 사용하도록 주의해야 한다.
또 다른 실시형태에서, 예방제 또는 치료제, 또는 본 발명의 조성물은 소포, 특히 리포좀 내에서 전달될 수 있다(문헌 [Langer, 1990, Science 249:1527-1533]; [Treat et al., in Liposomes in the Therapy of Infectious Disease and Cancer, Lopez-Berestein and Fidler(eds.), Liss, New York, pp. 353-365(1989)]; [Lopez-Berestein, 동일 문헌, pp. 317 내지 327]; 일반적으로 동일 문헌 참고).
또 다른 실시형태에서, 예방제 또는 치료제, 또는 본 발명의 조성물은 제어 방출 또는 지속 방출 시스템으로 전달될 수 있다. 일 실시형태에서, 제어 또는 지속 방출을 달성하기 위해 펌프(pump)를 사용할 수 있다(상기 랭거(Langer) 문헌; [Sefton, 1987, CRC Crit. Ref. Biomed. Eng. 14:20]; [Buchwald et al., 1980, Surgery 88:507]; [Saudek ef al., 1989, N. Engl. J. Med. 321:574] 참고). 또 다른 실시형태에서, 예방제 또는 치료제(예를 들어, 본 발명의 항체) 또는 본 발명의 조성물의 제어 또는 지속 방출을 달성하기 위해 중합체 물질을 사용할 수 있다(예를 들어, 문헌[Medical Applications of Controlled Release, Langer and Wise (eds.), CRC Pres., Boca Raton, Fla. (1974)]; [Controlled Drug Bioavailability, Drug Product Design and Performance, Smolen and Ball (eds.), Wiley, New York (1984)]; [Ranger and Peppas, 1983, J., Macromol. Sci. Rev. Macromol. Chem. 23:61]; 또한 [Levy et al., 1985, Science 228:190]; [During et al., 1989, Ann. Neurol. 25:351]; [Howard et al., 1989, J. Neurosurg. 7 1:105] 참고); 또한 미국 특허 5,679,377; 미국 특허 5,916,597; 미국 특허 5,912,015; 미국 특허 5,989,463; 미국 특허 5,128,326; PCT 공개 WO 99/15154; 및 PCT 공개 WO 99/20253). 지속 방출 제제에 사용되는 중합체의 예는 폴리(2-하이드록시 에틸 메타크릴레이트), 폴리(메틸 메타크릴레이트), 폴리(아크릴산), 폴리(에틸렌-코-비닐 아세테이트), 폴리(메타크릴산), 폴리글리콜리드(PLG), 폴리안하이드라이드, 폴리(N-비닐 피롤리돈), 폴리(비닐 알코올), 폴리아크릴아마이드, 폴리(에틸렌 글리콜), 폴리락티드(PLA), 폴리(락티드-코-글리콜리드)(PLGA) 및 폴리오르토에스터를 포함하지만 이에 제한되는 것은 아니다. 바람직한 실시형태에서, 지속 방출 제제에서 사용되는 중합체는 불활성이고, 용출가능한(leachable) 불순물이 없고, 저장 시에 안정하고, 무균성이고, 생분해성이다. 또 다른 실시형태에서, 제어 또는 지속 방출 시스템은 치료 표적, 즉, 비도 또는 폐에 근접하게 놓일 수 있어서, 전신 용량의 일부 분획만을 필요로 한다(예를 들어, 문헌[Goodson, in Medical Applications of Controlled Release, supra, vol. 2, pp. 115-138(1984)] 참고). 제어 방출 시스템은 문헌[Langer, 1990, Science 249: 1527-1533]의 리뷰에서 논의된다. 본 발명의 하나 이상의 항체를 포함하는 지연 방출 제제를 제조하기 위해 관련 기술 분야의 통상의 기술자에게 공지된 임의의 기술을 사용할 수 있다. 예를 들어, 본 명세서에 참고로 포함된 미국 특허 4,526,938, PCT 공개 WO 91/05548, PCT 공개 WO 96/20698, 문헌[Ning et al., 1996, "Intratumoral Radioimmunotherapy of a Human Colon Cancer Xenograft Using a Sustained-Release Gel," Radiotherapy & Oncology 39:179-189], [Song et al., 1995, "Antibody Mediated Lung Targeting of Long-Circulating Emulsions," PDA Journal of Pharmaceutical Science & Technology 50:372-397], [Cleek et al., 1997, "Biodegradable Polymeric Carriers for a bFGF Antibody for Cardiovascular Application," Pro. Int'l. Symp. Control. Rel. Bioact. Mater. 24:853-854], 및 [Lam et al., 1997, "Microencapsulation of Recombinant Humanized Monoclonal Antibody for Local Delivery," Proc. Int'l. Symp. Control Rel. Bioact. Mater. 24:759-760]을 참고하기 바란다.
구체적인 실시형태에서, 본 발명의 조성물이 예방제 또는 치료제(예를 들어, 본 발명의 항체)를 코딩하는 핵산인 경우에, 핵산은 그를 적절한 핵산 발현 벡터의 일부로서 구축하고, 예를 들어, 레트로바이러스 벡터(미국 특허 4,980,286 참고)의 사용에 의해서 또는 직접 주사에 의해서 또는 마이크로입자 폭격(예를 들어, 유전자 총(gun); 비올리스틱(Biolistic), 듀퐁(Dupont))의 사용에 의해서 또는 지질 또는 세포 표면 수용체 또는 형질주입제를 사용한 코팅 또는 핵 내로 도입하는 것으로 공지된 호메오박스(homeobox)-유사 펩타이드에 연결하여 투여함으로써(예를 들어, [Joliot et al., 1991, Proc. Natl. Acad. Sci. USA 88:1864-1868] 참고) 등에 의해서 그를 세포 내에 존재하도록 투여함으로써 이의 코딩된 예방 또는 치료제의 발현을 촉진하도록 생체내 투여될 수 있다. 대안적으로, 핵산은 세포내 도입되고 동종 재조합에 의해서 발현을 위해 숙주 세포 DNA 내에 도입될 수 있다.
구체적인 실시형태에서, 본 발명의 조성물은 1개, 2개 또는 그 초과의 본 발명의 항체 또는 단편을 포함한다. 또 다른 실시형태에서, 본 발명의 조성물은 1개, 2개 또는 그 초과의 본 발명의 항체 또는 단편 및 본 발명의 항체 이외의 예방제 또는 치료제를 포함한다. 바람직하게는, 작용제는 hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화를 위해 유용한 것으로 공지되거나 사용되었거나 현재 사용되고 있다. 예방제 또는 치료제에 추가로, 본 발명의 조성물은 또한 담체를 포함할 수 있다.
본 발명의 조성물은 단위 투여 형태의 제조에 사용될 수 있는 약제학적 조성물(예를 들어, 대상체 또는 환자에게 투여하기 적합한 조성물)의 제조에 유용한 벌크 약물 조성물을 포함한다. 바람직한 실시형태에서, 본 발명의 조성물은 약제학적 조성물이다. 그러한 조성물은 예방 또는 치료 유효량의 하나 이상의 예방제 또는 치료제(예를 들어, 본 발명의 항체 또는 다른 예방제 또는 치료제) 및 약제학적으로 허용 가능한 담체를 포함한다. 바람직하게는, 약제학적 조성물은 대상체에 대한 투여 경로에 적합하도록 제제화된다.
구체적인 실시형태에서, 용어 "담체"는 그와 함께 치료제가 투여되는 희석제,아주반트(예를 들어, 프로인트(Freund) 아주반트(완전 및 불완전)), 부형제 또는 비히클을 나타낸다. 그러한 약제학적 담체는 멸균 액체, 예를 들어 물 및 오일, 예를 들어 석유, 동물, 식물 또는 합성 기원의 것, 예를 들어 땅콩유, 대두유, 광유, 참기름 등일 수 있다. 물이 약제학적 조성물을 정맥내 투여할 때 바람직한 담체이다. 염수 용액 및 수성 덱스트로스 및 글리세롤 용액을 또한 특히 주사가능 용액에 대한 액체 담체로서 사용할 수 있다. 적합한 약제학적 부형제는 전분, 글루코스, 락토스, 수크로스, 젤라틴, 엿기름, 쌀, 밀가루, 호분(chalk), 실리카겔, 스테아르산나트륨, 글리세롤 모노스테아레이트, 탈크, 염화나트륨, 건조 탈지유, 글리세롤, 프로필렌, 글리콜, 물, 에탄올 등을 포함한다. 원하는 경우에, 조성물은 또한 소량의 습윤 또는 유화제 또는 pH 완충액을 함유할 수 있다. 이러한 조성물은 용액, 현탁액, 에멀전, 정제, 알약, 캡슐, 분말, 지속-방출 제제 등의 형태를 취할 수 있다. 경구 제제는 표준 담체, 예를 들어 약제학적 등급의 만니톨, 락토스, 전분, 스테아르산 마그네슘, 나트륨 사카린, 셀룰로스, 탄산 마그네슘 등을 포함할 수 있다. 적합한 약제학적 담체의 예는 문헌[Remington's Pharmaceutical Sciences(1990) Mack Publishing Co., Easton, PA]에 기술되어 있다. 이러한 조성물은 예방 또는 치료 유효량의 항체를 바람직하게는 정제된 형태로 환자에 대한 적절한 투여를 제공하도록 적합한 양의 담체와 함께 함유할 것이다. 제제는 투여 모드에 적합해야 한다.
바람직한 실시형태에서, 조성물은 인간에게 정맥내 투여하도록 개작된 약제학적 조성물로서 일상적인 절차에 따라 제제화된다. 전형적으로, 정맥내 투여용 조성물은 멸균 등장성 수성 완충액 중의 용액이다. 필요한 경우, 조성물은 또한 가용화제 및 주사 부위에서 통증을 완화시키기 위해 국소 마취제, 예를 들어 리그노카인을 포함할 수 있다. 그러나, 그러한 조성물은 정맥내 이외의 경로로 투여될 수 있다.
일반적으로, 본 발명의 조성물의 구성 성분은 별개로 또는 함께 혼합되어 단위 투여 형태로, 예를 들어 건조 동결건조 분말 또는 무수 농축물로서 활성제의 양을 나타내는 밀폐 용기, 예를 들어 앰플 또는 샤세(sachette) 내에 공급된다. 조성물이 주입에 의해서 투여되어야 하는 경우에, 멸균 약제학적 등급의 물 또는 염수를 함유하는 주입병과 함께 분배할 수 있다. 조성물이 주사에 의해서 투여되는 경우, 투여 전에 구성 성분을 혼합할 수 있도록 주사용 멸균수 또는 염수의 앰플을 제공할 수 있다.
본 발명은 또한 항체의 양을 나타내는 밀폐 용기, 예를 들어 앰플 또는 샤세 내에 포장된 본 발명의 항체를 제공한다. 일 실시형태에서, 항체는 건조 멸균 동결건조 분말 또는 무수 농축물로서 밀폐 용기 내에 공급되고, 예를 들어, 물 또는 염수를 사용하여 대상체에 투여하기 적절한 농도로 재구성될 수 있다. 바람직하게는, 항체는 건조 멸균 동결건조 분말로서 밀폐 용기 내에 적어도 0.1mg, 적어도 0.5mg, 적어도 1mg, 적어도 2mg, 또는 적어도 3mg, 보다 바람직하게는 적어도 5mg, 적어도 10mg, 적어도 15mg, 적어도 25mg, 적어도 30mg, 적어도 35mg, 적어도 45mg, 적어도 50mg, 적어도 60mg, 적어도 75mg, 적어도 80mg, 적어도 85mg, 적어도 90mg, 적어도 95mg, 또는 적어도 100mg의 단위 투여량으로 공급된다. 동결건조 항체는 이의 본래 용기 내에서 2 내지 8℃에서 저장될 수 있고, 항체는 재구성된 후 12시간 내에, 바람직하게는 6시간 내에, 5시간 내에, 3시간 내에, 또는 1시간 내에 투여될 수 있다. 대안적인 실시형태에서, 항체는 액체 형태로 항체의 양 및 농도를 나타내는 밀폐 용기 내에 공급된다. 바람직하게는, 액체 형태의 항체는 밀폐 용기 내에 적어도 0.1mg/ml, 적어도 0.5 mg/ml, 또는 적어도 1mg/ml, 보다 바람직하게는 적어도 5mg/ml, 적어도 10mg/ml, 적어도 15mg/ml, 적어도 25mg/ml, 적어도 30mg/ml, 적어도 40mg/ml, 적어도 50mg/ml, 적어도 60mg/ml, 적어도 70mg/ml, 적어도 80mg/ml, 적어도 90mg/ml, 또는 적어도 100mg/ml로 공급된다.
본 발명의 조성물은 중성 또는 염 형태로서 제제화될 수 있다. 약제학적으로 허용 가능한 염은 음이온과 함께 형성된 것, 예를 들어 염산, 인산, 아세트산, 옥살산, 타르타르산 등으로부터 유래된 것 및 양이온과 함께 형성된 것, 예를 들어 나트륨, 칼륨, 암모늄, 칼슘, 수산화철, 이소프로필아민, 트리에틸아민, 2-에틸아미노 에탄올, 히스티딘, 프로카인 등으로부터 유래한 것을 포함한다.
hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화에 효과적일 예방제 또는 치료제(예를 들어, 본 발명의 항체), 또는 본 발명의 조성물의 양은 표준 임상 기술에 의해서 결정될 수 있다.
따라서, 약 0.1μg/ml 내지 약 450μg/ml, 일부 실시형태에서 적어도 0.1μg/ml, 적어도 0.2μg/ml, 적어도 0.4μg/ml, 적어도 0.5μg/ml, 적어도 0.6μg/ml, 적어도 0.8μg/ml, 적어도 1μg/ml, 적어도 1.5μg/ml, 바람직하게는 적어도 2μg/ml, 적어도 5μg/ml, 적어도 10μg/ml, 적어도 15μg/ml, 적어도 20μg/ml, 적어도 25μg/ml, 적어도 30μg/ml, 적어도 35μg/ml, 적어도 40μg/ml, 적어도 50μg/ml, 적어도 75μg/ml, 적어도 100μg/ml, 적어도 125μg/ml, 적어도 150μg/ml, 적어도 200μg/ml, 적어도 250μg/ml, 적어도 300μg/ml, 적어도 350μg/ml, 적어도 400μg/ml, 또는 적어도 450μg/ml의 혈청 역가를 생성하는 항체 또는 조성물의 투여량이 hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화를 위해서 인간에게 투여될 수 있다. 또한, 최적 투여량 범위의 식별을 돕기 위해 시험관내 검정법을 임의로 사용할 수 있다. 제제에 사용될 정확한 용량은 또한 투여 경로 및 hOX40L-매개된 질환의 중대성에 따라 좌우될 것이고, 실시자의 판단 및 각각의 환자의 상황에 따라 결정되어야 한다.
유효 용량은 시험관내 또는 동물 모델 시험 시스템으로부터 유래된 용량-반응 곡선으로부터 외삽될 수 있다.
본 발명의 항체의 경우, 환자에게 투여되는 투여량은 전형적으로 0.1mg/kg 내지 100mg/kg 환자 체중이다. 일부 실시형태에서, 환자에게 투여되는 투여량은 약 1mg/kg 내지 약 75mg/kg 환자 체중이다. 바람직하게는, 환자에게 투여되는 투여량은 1mg/kg 내지 20mg/kg 환자 체중, 보다 바람직하게는 1mg/kg 내지 5mg/kg 환자 체중이다. 일반적으로, 인간 항체는 외래 폴리펩타이드에 대한 면역 반응때문에 다른 종으로부터의 항체보다 인체 내 반감기가 더 길다. 따라서, 보다 낮은 투여량의 인간 항체 및 덜 빈번한 투여가 종종 가능하다. 또한, 본 발명의 항체의 투여량 및 투여 빈도는 예를 들어, 지질화(lipidation)와 같은 변형에 의해서 항체의 섭취 및 조직 관통을 향상시킴으로써 감소시킬 수 있다.
일 실시형태에서, hOX40L-매개된 질환을 관리하기 위해 대략 100 mg/kg 이하, 대략 75 mg/kg 이하, 대략 50 mg/kg 이하, 대략 25 mg/kg 이하, 대략 10 mg/kg 이하, 대략 5 mg/kg 이하, 대략 1 mg/kg 이하, 대략 0.5 mg/kg 이하 또는 대략 0.1 mg/kg 이하의 본 발명의 항체 또는 단편을 5회, 4회, 3회, 2회 또는 바람직하게는 1회 투여한다. 일부 실시형태에서, 본 발명의 항체는 약 1 내지 12회 투여되고, 용량은 의료진이 결정할 때 필요한 만큼, 예를 들어, 매주, 격주, 매월, 격월, 3달마다 등으로 투여될 수 있다. 일부 실시형태에서, 보다 저용량(예를 들어, 1 내지 15 mg/kg)을 보다 빈번하게(예를 들어, 3 내지 6회) 투여할 수 있다. 다른 실시형태에서, 보다 고용량(예를 들어, 25 내지 100 mg/kg)을 덜 빈번하게(예를 들어, 1 내지 3회) 투여할 수 있다. 그러나, 관련 기술 분야의 통상의 기술자에게 명백할 바와 같이, 다른 투여량 및 스케줄은 쉽게 결정될 수 있고, 본 발명의 범위 내에 있다.
구체적인 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화를 위해서, 대략 100mg/kg, 대략 75mg/kg 이하, 대략 50mg/kg 이하, 대략 25mg/kg 이하, 대략 10mg/kg 이하, 대략 5mg/kg 이하, 대략 1mg/kg 이하, 대략 0.5mg/kg 이하, 대략 0.1mg/kg 이하의 본 발명의 항체 또는 단편이 대상체, 바람직하게는 인간에게 투여된다. 또 다른 구체적인 실시형태에서, hOX40L-매개된 질환의 예방, 관리, 치료 및/또는 완화를 위해서, 대략 100mg/kg, 대략 75mg/kg 이하, 대략 50mg/kg 이하, 대략 25mg/kg 이하, 대략 10mg/kg 이하, 대략 5mg/kg 이하, 대략 1mg/kg 이하, 대략 0.5mg/kg 이하, 또는 대략 0.1mg/kg 이하의 지속 방출 제제가 아닌 본 발명의 항체의 볼러스가 대상체, 바람직하게는 인간에게 투여되고, 특정 기간 후에, 대략 100mg/kg, 대략 75mg/kg 이하, 대략 50mg/kg 이하, 대략 25mg/kg 이하, 대략 10mg/kg 이하, 대략 5mg/kg 이하, 대략 1mg/kg 이하, 대략 0.5mg/kg 이하, 또는 대략 5mg/kg 이하의 본 발명의 항체가 지속 방출제로 상기 대상체에게 (예를 들어, 코 안 또는 근육내) 2, 3 또는 4회(바람직하게는 1회) 투여된다. 본 실시형태에 따라, 특정 기간은 1 내지 5일, 1주, 2주 또는 1개월일 수 있다.
일부 실시형태에서, hOX40L-매개된 질환을 예방 및/또는 관리 및/또는 치료 및/또는 완화하기 위해서 단일 용량의 본 발명의 항체 또는 단편이 환자에게 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12회, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25 또는 26회로 격주(예를 들어, 약 14일) 간격으로 1년에 걸쳐 투여되고, 여기서 용량은 약 0.1mg/kg, 약 0.5mg/kg, 약 1mg/kg, 약 5mg/kg, 약 10mg/kg, 약 15mg/kg, 약 20mg/kg, 약 25mg/kg, 약 30mg/kg, 약 35mg/kg, 약 40mg/kg, 약 45mg/kg, 약 50mg/kg, 약 55mg/kg, 약 60mg/kg, 약 65mg/kg, 약 70mg/kg, 약 75mg/kg, 약 80mg/kg, 약 85mg/kg, 약 90mg/kg, 약 95mg/kg, 약 100mg/kg, 또는 이의 조합으로 이루어진 군으로부터 선택된다(즉, 각각의 용량 매달 용량은 동일할 수 있거나 동일하지 않을 수 있다).
또 다른 실시형태에서, hOX40L-매개된 질환을 예방 및/또는 관리 및/또는 치료 및/또는 완화하기 위해서 단일 용량의 본 발명의 항체 또는 단편이 환자에게 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 또는 12회로 매달(예를 들어, 약 30일) 간격으로 1년에 걸쳐 투여되고, 여기서 용량은 약 0.1mg/kg, 약 0.5mg/kg, 약 1mg/kg, 약 5mg/kg, 약 10mg/kg, 약 15mg/kg, 약 20mg/kg, 약 25mg/kg, 약 30 mg/kg, 약 35mg/kg, 약 40mg/kg, 약 45mg/kg, 약 50mg/kg, 약 55mg/kg, 약 60mg/kg, 약 65mg/kg, 약 70mg/kg, 약 75mg/kg, 약 80mg/kg, 약 85mg/kg, 약 90mg/kg, 약 95mg/kg, 약 100mg/kg, 또는 이의 조합으로 이루어진 군으로부터 선택된다(즉, 각각의 격월 용량은 동일할 수 있거나 동일하지 않을 수 있다(각각의 용량 매달 용량은 동일할 수 있거나 동일하지 않을 수 있다).
일 실시형태에서, hOX40L-매개된 질환을 예방 및/또는 관리 및/또는 치료 및/또는 완화하기 위해서 단일 용량의 본 발명의 항체 또는 단편이 환자에게 2, 3, 4, 5 또는 6회로 대략 격월(예를 들어, 약 60일) 간격으로 1년에 걸쳐 투여되고, 여기서 용량은 약 0.1mg/kg, 약 0.5mg/kg, 약 1mg/kg, 약 5mg/kg, 약 10mg/kg, 약 15mg/kg, 약 20mg/kg, 약 25mg/kg, 약 30mg/kg, 약 35mg/kg, 약 40mg/kg, 약 45mg/kg, 약 50mg/kg, 약 55mg/kg, 약 60mg/kg, 약 65mg/kg, 약 70mg/kg, 약 75mg/kg, 약 80mg/kg, 약 85mg/kg, 약 90mg/kg, 약 95mg/kg, 약 100mg/kg, 또는 이의 조합으로 이루어진 군으로부터 선택된다(즉, 각각의 격월 용량은 동일할 수 있거나 동일하지 않을 수 있다).
일부 실시형태에서, hOX40L-매개된 질환을 예방 및/또는 관리 및/또는 치료 및/또는 완화하기 위해서 단일 용량의 본 발명의 항체 또는 단편이 환자에게 2, 3 또는 4회로 대략 3달(예를 들어, 약 120일) 간격으로 1년에 걸쳐 투여하고, 여기서 용량은 약 0.1mg/kg, 약 0.5mg/kg, 약 1mg/kg, 약 5mg/kg, 약 10mg/kg, 약 15mg/kg, 약 20mg/kg, 약 25mg/kg, 약 30mg/kg, 약 35mg/kg, 약 40mg/kg, 약 45mg/kg, 약 50mg/kg, 약 55mg/kg, 약 60mg/kg, 약 65mg/kg, 약 70mg/kg, 약 75mg/kg, 약 80mg/kg, 약 85mg/kg, 약 90mg/kg, 약 95mg/kg, 약 100mg/kg, 또는 이의 조합으로 이루어진 군으로부터 선택된다(즉, 각각의 3달 용량은 동일할 수 있거나 동일하지 않을 수 있다).
특정 실시형태에서, 환자에게 본 발명의 항체 또는 단편의 용량의 투여 경로는 코 안, 근육내, 정맥내 또는 이의 조합이지만, 본 명세서에 기술된 다른 경로도 또한 허용 가능하다. 각각의 용량은 동일한 투여 경로로 투여될 수 있거나 투여되지 않을 수 있다. 특정 실시형태에서, 투여 경로는 눈안이다. 각각의 용량은 동일한 투여 경로에 의해서 투여될 수 있거나 투여되지 않을 수 있다. 일부 실시형태에서, 본 발명의 항체는 다수 투여 경로로 본 발명의 동일하거나 또는 상이한 항체 또는 단편의 다른 용량과 동시에 또는 후속적으로 투여될 수 있다.
특정 실시형태에서, 본 발명의 항체 또는 단편은 대상체에게 예방적으로 또는 치료적으로 투여된다. 본 발명의 항체 또는 단편은 hOX40L-매개된 질환 또는 이의 증상을 예방, 경감, 완화하도록 대상체에게 예방적으로 또는 치료적으로 투여될 수 있다.
유전자 요법
구체적인 실시형태에서, 본 발명의 핵산 또는 뉴클레오타이드 서열은 유전자 요법에 의해서 hOX40L-매개된 질환을 예방, 관리, 치료 및/또는 완화하기 위해 투여된다. 유전자 요법은 발현되거나 또는 발현 가능한 핵산을 대상체에 투여하여 수행되는 요법을 나타낸다. 본 발명의 실시형태에서, 핵산은 그의 코딩된 항체를 생산하고, 항체는 예방 또는 치료 효과를 매개한다.
관련 기술 분야에 이용 가능한 유전자 요법을 위한 임의의 방법을 본 발명에 따라 사용할 수 있다.
항체의 진단 용도
항체가 진단 용도와 관련하여 언급되어 있지만, 본 개시 내용은 또한 본 발명의 단편에 필요한 부분만 약간 수정하여 적용되는 것으로서 이해되어야 한다.
hOX40L 항원에 특이적으로 결합하는 본 발명의 표지된 항체 및 이의 유도체 및 유사체는 hOX40L-매개된 질환을 검출, 진단, 또는 모니터링하기 위해 진단 목적을 위해 사용될 수 있다. 본 발명은 (a) hOX40L 항원에 특이적으로 결합하는 본 발명의 하나 이상의 항체를 사용하여 대상체의 세포 또는 조직 샘플 내의 hOX40L 항원의 발현을 검정하고; (b) hOX40L 항원의 수준을 대조 수준, 예를 들어, 정상 조직 샘플(예를 들어, hOX40L-매개된 질환을 갖지 않은 환자로부터의, 또는 질환 발병 전의 동일한 환자로부터의) 내의 수준과 비교하는 것을 포함하는, hOX40L-매개된 질환의 검출 방법을 제공하고, 이에 의해서 hOX40L 항원의 대조 수준에 비해 검정된 hOX40L 항원 수준의 증가는 hOX40L-매개된 질환의 지표이다.
본 발명은 (a) hOX40L 항원에 특이적으로 결합하는 본 발명의 하나 이상의 항체를 사용하여 개체의 세포 또는 조직 샘플 내의 hOX40L 항원의 수준에 대해 검정하고; (b) hOX40L 항원의 수준을 대조 수준, 예를 들어, 정상 조직 샘플 내의 수준과 비교하는 것을 포함하는, hOX40L-매개된 질환을 진단하기 위한 진단 검정법을 제공하고, 이에 의해서 hOX40L 항원의 대조 수준에 비해 검정된 hOX40L 항원 수준의 증가는 hOX40L-매개된 질환의 지표이다. hOX40L-매개된 질환을 보다 명확하게 진단하면, 의료 종사자는 예방 대책 또는 적극적 치료를 보다 일찍 사용하여 hOX40L-매개된 질환의 발생 또는 추가의 진행을 방지할 수 있다.
본 발명의 항체는 본 명세서에 기술된 바와 같은 또는 관련 기술 분야의 통상의 기술자에게 공지된 전통적인 면역조직학적 방법을 이용하여 생물학적 샘플 내의 hOX40L 항원 수준을 검정하기 위해 사용될 수 있다(예를 들어, 문헌[Jalkanen et al., 1985, J. Cell. Biol. 101:976-985]; 및 [Jalkanen et al., 1987, J. Cell. Biol. 105:3087-3096] 참고). 단백질 유전자 발현을 검출하기 위한 다른 항체-기반 방법은 면역검정법, 예를 들어 효소 연결 면역흡착성 검정법(ELISA) 및 방사성면역검정법(RIA)을 포함한다. 적합한 항체 검정법 표지는 관련 기술 분야에 공지되어 있고, 효소 표지, 예를 들어, 글루코스 옥시다제; 방사성 동위원소, 예를 들어 아이오딘(125I, 121I), 탄소(14C), 황(35S), 삼중수소(3H), 인듐(121In) 및 테크네튬(99Tc); 발광 표지, 예를 들어 루미놀; 및 형광 표지, 예를 들어 플루오레세인 및 로다민, 및 비오틴을 포함한다.
본 발명의 한 양상은 인간에서 hOX40L-매개된 질환의 검출 및 진단이다. 일 실시형태에서, 진단은 a) 대상체에게 유효량의 hOX40L 항원에 특이적으로 결합하는 표지된 항체를 투여하고(예를 들어, 비경구, 피하 또는 복강내); b) 표지된 항체가 대상체에서 hOX40L 항원이 발현되는 부위에 우선적으로 농축되는 것을 허용하기 위해(그리고 결합되지 않은 표지된 분자가 배경 수준으로 제거되도록 하기 위해)투여 후 일정 시간 간격 동안 기다리고; c) 배경 수준을 결정하고; d) 대상체에서 표지된 항체를 검출하는 것을 포함하고, 여기서 배경 수준을 초과하는 표지된 항체의 검출은 대상체가 hOX40L-매개된 질환에 걸린 것을 나타낸다. 배경 수준은 검출된 표지된 분자의 양을 특정 시스템에 대해 미리 결정된 표준 값에 비교하는 것을 포함하는 다양한 방법에 의해서 결정할 수 있다.
대상체의 크기 및 사용되는 영상화 시스템이 진단법 영상을 생성하기 위해 필요한 영상화 모이어티의 양을 결정할 것임이 관련 기술 분야에서 이해될 것이다. 인간 대상체를 위한 방사성 동위원소 모이어티의 경우에, 주사된 방사성의 양은 보통 약 5 내지 20밀리퀴리의 99Tc일 것이다. 이어서, 표지된 항체는 특정 단백질을 함유하는 세포의 위치에 우선적으로 축적될 것이다. 생체내 종양 영상화는 문헌 [S.W. Burchiel et al., "Immunopharmacokinetics of Radiolabeled Antibodies and Their Fragments."(Chapter 13 in Tumor Imaging: The Radiochemical Detection of Cancer, S. W. Burchiel and B.A. Rhodes, eds., Masson Publishing Inc.(1982)]에 기술되어 있다.
사용된 표지의 유형 및 투여 모드를 비롯한 몇몇 변수에 따라, 표지된 항체가 대상체에서 부위에 우선적으로 농축되는 것을 허용하고 결합되지 않은 표지된 항체가 배경 수준으로 제거되도록 하기 위한 투여 후 시간 간격은 6 내지 48시간 또는 6 내지 24시간 또는 6 내지 12시간이다. 또 다른 실시형태에서, 투여 후 시간 간격은 5 내지 20일 또는 5 내지 10일이다.
일 실시형태에서, hOX40L-매개된 질환의 모니터링은 hOX40L-매개된 질환을 진단하는 방법을, 예를 들어 초기 진단 1개월 후, 초기 진단 6개월 후, 초기 진단 1년 후 등에 반복함으로써 수행한다.
표지된 분자의 존재를 생체내 스캐닝을 위한 관련 기술 분야에 공지된 방법을 사용하여 대상체에서 검출할 수 있다. 이들 방법은 사용된 표지의 유형에 의해서 좌우된다. 숙련된 기술자는 특정 표지를 검출하기 위한 적절한 방법을 결정할 수 있을 것이다. 본 발명의 진단 방법에서 사용할 수 있는 방법 및 장치는 컴퓨터 단층촬영(CT), 전신 스캔, 예를 들어 양성자 방출 단층촬영(PET), 자기 공명 영상(MRI) 및 초음파 검사를 포함하지만 이에 제한되는 것은 아니다.
구체적인 실시형태에서, 분자는 방사성 동위 원소로 표지되고, 방사선 반응성 외과 기구를 사용하여 환자에서 검출된다(투르스톤(Thurston) 등의 미국 특허 5,441,050). 또 다른 실시형태에서, 분자는 형광성 화합물로 표지되고, 형광 반응성 스캐닝 기구를 사용하여 환자에서 검출된다. 또 다른 실시형태에서, 분자는 양전자 방출 금속으로 표지되고, 양전자 방출 단층촬영을 사용하여 환자에서 검출된다. 또 다른 실시형태에서, 분자는 상자성 표지로 표지되고, 자기 공명 영상(MRI)을 이용하여 환자에서 검출된다.
항체의 생산 방법
항원(OX40L)에 특이적으로 결합하는 본 발명의 항체 및 단편은 항체의 합성을 위해 관련 기술 분야에 공지된 임의의 방법에 의해서, 특히, 화학 합성 또는 바람직하게는 재조합 발현 기술에 의해서 생산될 수 있다. 본 발명의 실시에는 달리 지시하지 않으면 분자 생물학, 미생물학, 유전자 분석, 재조합 DNA, 유기 화학, 생화학, PCR, 올리고뉴클레오타이드 합성 및 변형, 핵산 혼성화 및 관련 기술 분야의 기술 범위 내의 관련 분야의 통상적인 기술을 사용한다. 이러한 기술은 본 명세서에서 인용된 참고문헌에 기술되어 있고 문헌에 충분히 설명되어 있다. 예를 들어, [Maniatis et al. (1982) Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press]; [Sambrook et al. (1989), Molecular Cloning: A Laboratory Manual, Second Edition, Cold Spring Harbor Laboratory Press]; [Sambrook et al. (2001) Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y.]; [Ausubel et al., Current Protocols in Molecular Biology, John Wiley & Sons (1987 and annual updates)]; [Current Protocols in Immunology, John Wiley & Sons (1987 and annual updates) Gait (ed.) (1984) Oligonucleotide Synthesis: A Practical Approach, IRL Press]; [Eckstein (ed.) (1991) Oligonucleotides and Analogues: A Practical Approach, IRL Press]; [Birren et al. (eds.) (1999) Genome Analysis: A Laboratory Manual, Cold Spring Harbor Laboratory Press]을 참고하기 바란다.
항원에 특이적으로 결합하는 다클론성 항체는 관련 기술 분야에 널리 공지된 다양한 절차에 의해서 생산될 수 있다. 예를 들어, 인간 항원은 인간 항원에 특이적인 다클론성 항체를 함유하는 혈청의 생산을 유도하기 위해 비제한적으로 토끼, 마우스, 래트 등을 포함하는 다양한 숙주 동물에 투여될 수 있다. 다양한 아주반트가 숙주 종에 따라 면역학적 반응을 증가시키기 위해 사용될 수 있고, 프로인트(완전 및 불완전), 광물젤, 예를 들어 수산화 알루미늄, 표면 활성 물질, 예를 들어 리소레시틴, 플루로닉(pluronic) 폴리올, 다중음이온, 펩타이드, 오일 에멀전, 키홀 림펫 헤모시아닌, 다이나이트로페놀 및 잠재적으로 유용한 인간 아주반트, 예를 들어 BCG(bacille Calmette-Guerin) 및 코리네박테리움 파르븀(Corynebacterium parvum)을 포함하지만 이에 제한되는 것은 아니다. 상기 아주반트는 또한 관련 기술 분야에 널리 공지되어 있다.
단클론성 항체는 하이브리도마, 재조합 및 파지 전시법 기술 또는 이의 조합의 사용을 포함하는 관련 기술 분야에 공지된 매우 다양한 기술을 사용하여 제조될 수 있다. 예를 들어, 단클론성 항체는 관련 기술 분야에 공지되고 예를 들어, 문헌([Harlow et al., Antibodies: A Laboratory Manual, (Cold Spring Harbor Laboratory Press, 2nd ed. 1988)]; [Hammerling et al., in: Monoclonal Antibodies and T-Cell Hvbridomas 563 681(Elsevier, N.Y., 1981)](상기 문헌은 전문이 참고로 포함됨)]에 교시된 것을 포함하는 하이브리도마 기술을 사용하여 생산할 수 있다. 용어 "단클론성 항체"는 본 명세서에서 사용되는 바와 같이 하이브리도마 기술을 통해 생산된 항체에 제한되지 않는다. 단클론성 항체를 생산하는 다른 예시적인 방법은 예를 들어 KM 마우스(상표명)의 사용과 같은 본 명세서의 다른 곳에서 논의된다. 단클론성 항체를 생산하는 또 다른 예시적인 방법은 본 명세서의 실시예에 제공된다.
하이브리도마 기술을 이용하여 특이적인 항체를 생산하고 스크리닝하기 위한 방법은 일상적이고 관련 기술 분야에 잘 공지되어 있다. 간단히 설명하면, 마우스를 hOX40L 항원을 사용하여 면역화시킬 수 있고, 일단 면역 반응이 검출되면, 예를 들어, hOX40L 항원에 특이적인 항체가 마우스 혈청 내에 검출되면, 마우스 비장을 수거하고 비장세포를 단리시킨다. 이어서, 비장세포를 잘 공지된 기술에 의해서 임의의 적합한 골수종 세포, 예를 들어 ATCC로부터 이용 가능한 세포주 SP20으로부터의 세포에 융합시킨다. 하이브리도마는 제한 희석에 의해서 선택하고 클로닝한다.
추가로, RIMMS(반복 면역화 다수 부위) 기술을 사용하여 동물을 면역화시킬 수 있다(문헌 [Kilptrack et al., 1997 Hybridoma 16:381-9](전문이 참고로 포함됨)). 이어서, 하이브리도마 클론을 관련 기술 분야에 공지된 방법에 의해서 본 발명의 폴리펩타이드에 결합할 수 있는 항체를 분비하는 세포에 대해 분석한다. 일반적으로 고수준의 항체를 함유하는 복수액은 마우스를 양성 하이브리도마 클론으로 면역화시킴으로써 생성될 수 있다.
따라서, 본 발명은 본 발명의 변형된 항체를 분비하는 하이브리도마 세포를 배양함으로써 항체를 생성하는 방법을 제공하고, 여기서 바람직하게는 하이브리도마는 hOX40L 항원으로 면역화된 마우스로부터 단리된 비장세포를 골수종 세포와 융합시킨 후, 융합으로부터 생성된 하이브리도마를 hOX40L 항원에 결합할 수 있는 항체를 분비하는 하이브리도마 클론에 대해 스크리닝함으로써 생성된다.
특이적인 hOX40L 항원을 인식하는 항체 단편은 관련 기술 분야의 통상의 기술자에게 공지된 임의의 기술에 의해서 생성될 수 있다. 예를 들어, 본 발명의 Fab 및 F(ab')2 단편은 효소, 예컨대 파파인(Fab 단편을 생산하기 위해) 또는 펩신(F(ab')2 단편을 생산하기 위해)을 사용한 면역글로불린 분자의 단백분해성 절단에 의해서 생산될 수 있다. F(ab')2 단편은 가변 영역, 경쇄 불변 영역 및 중쇄의 CH1 도메인을 함유한다. 추가로, 본 발명의 항체는 또한 관련 기술 분야에 공지된 다양한 파지 전시법 방법을 사용하여 생성될 수 있다.
예를 들어, 항체는 또한 다양한 파지 전시법 방법을 이용하여 생성될 수 있다. 파지 전시법 방법에서, 기능적 항체 도메인은 그를 코딩하는 폴리뉴클레오타이드 서열을 보유하는 파지 입자의 표면 상에 전시된다. 특히, VH 및 VL 도메인을 코딩하는 DNA 서열을 동물 cDNA 라이브러리(예를 들어, 침범된 조직의 인간 또는 뮤린 cDNA 라이브러리)로부터 증폭시킨다. VH 및 VL 도메인을 코딩하는 DNA를 PCR에 의해서 scFv 링커와 함께 재조합하고, 파지미드 벡터 내로 클로닝한다. 벡터를 이. 콜라이(E. coli) 내에서 전기천공하고, 이. 콜라이를 헬퍼(helper) 파지로 형질주입시킨다. 이러한 방법에 사용되는 파지는 전형적으로 fd 및 M13을 포함하는 필라멘트성 파지이고, VH 및 VL 도메인은 대체로 파지 유전자 III 또는 유전자 VIII에 재조합 방식으로 융합된다. 특정 항원에 결합하는 항원 결합 도메인을 발현하는 파지는 항원, 예를 들어, 표지된 항원 또는 고체 표면 또는 비드에 결합되거나 포획된 항원을 사용하여 선택 또는 식별될 수 있다. 본 발명의 항체 제조에 사용될 수 있는 파지 전시법 방법의 예는 각각 전문이 본 명세서에 참고로 포함된 문헌[Brinkman et al., 1995, J. Immunol. Methods 182:41-50]; [Ames et al., 1995, J. Immunol. Methods 184:177-186]; [Kettleborough et al., 1994, Eur. J. Immunol. 24:952-958]; [Persic et al., 1997, Gene 187:9-18; Burton et al., 1994, Advances in Immunology 57:191-280]; PCT 출원 PCT/GB91/01134; 국제 공개 WO 90/02809, WO 91/10737, WO 92/01047, WO 92/18619, WO 93/1 1236, WO 95/15982, WO 95/20401, 및 WO97/13844; 및 미국 특허 5,698,426, 5,223,409, 5,403,484, 5,580,717, 5,427,908, 5,750,753, 5,821,047, 5,571,698, 5,427,908, 5,516,637, 5,780,225, 5,658,727, 5,733,743 및 5,969,108에 개시된 것을 포함하고; 이들 각각은 이의 전문이 참고로 본 명세서에 포함된다.
상기 문헌에 기술된 바와 같이, 파지 선택 후에, 파지로부터의 항체 코딩 영역을 단리시키고 사용하여 인간 항체 또는 임의의 다른 목적하는 항원 결합 단편을 포함하는 전체 항체를 생성할 수 있고, 예를 들어, 하기에 기술된 바와 같이 포유동물 세포, 곤충 세포, 식물 세포, 효모 및 박테리아를 포함하는 임의의 목적하는 숙주 내에서 발현시킬 수 있다. 또한, Fab, Fab' 및 F(ab')2 단편을 재조합 방식으로 생산하는 기술은 관련 기술 분야에 공지된 방법, 예컨대 PCT 공개 WO 92/22324; 문헌[Mullinax et al., 1992, BioTechniques 12(6):864-869]; [Sawai et al., 1995, AJRI 34:26-34]; 및 [Better et al., 1988, Science 240:1041-1043](상기 문헌은 이의 전문이 참고로 포함됨)에 개시된 것을 사용하여 이용될 수 있다.
전체 항체를 생성하기 위해, VH 또는 VL 뉴클레오티드 서열, 제한 부위, 및 제한 부위를 보호하기 위해 플랭킹(flanking) 서열을 포함하는 PCR 프라이머를 사용하여 scFv 클론 내에서 VH 또는 VL 서열을 증폭시킬 수 있다. 관련 기술 분야의 통상의 기술자에게 공지된 클로닝 기술을 이용하여, PCR 증폭된 VH 도메인을 VH 불변 영역, 예를 들어, 인간 감마 4 불변 영역을 발현하는 벡터 내로 클로닝할 수 있고, PCR 증폭된 VL 도메인을 VL 불변 영역, 예를 들어, 인간 카파 또는 람다 불변 영역을 발현하는 벡터 내로 클로닝할 수 있다. VH 및 VL 도메인은 또한 필요한 불변 영역을 발현하는 하나의 벡터 내로 클로닝될 수 있다. 이어서, 중쇄 전환 벡터 및 경쇄 전환 벡터를 관련 기술 분야의 통상의 기술자에게 공지된 기술을 이용하여 세포주 내로 동시-형질주입시켜, 전장 항체, 예를 들어, IgG를 발현하는 안정한 세포주 또는 일시적인 세포주를 생성한다.
인간 내에서 항체의 생체내 사용 및 시험관내 검출 검정법을 비롯한 일부 용도에 대해, 인간 또는 키메릭 항체를 사용하는 것이 바람직할 수 있다. 인간 대상체의 치료적 치료를 위해 완전 인간 항체가 특히 바람직하다. 인간 항체는 인간 면역글로불린 서열로부터 유래된 항체 라이브러리를 사용하여 상기 설명된 파지 전시법 방법을 포함하는 관련 기술 분야에 공지된 다양한 방법에 의해서 제조할 수 있다. 또한 미국 특허 4,444,887 및 4,716,111; 및 국제 특허 출원 공개 WO 98/46645, WO 98/50433, WO 98/24893, WO 98/16654, WO 96/34096, WO 96/33735, 및 WO 91/10741을 참고하기 바라며; 이들 각각은 이의 전문이 참고로 본 명세서에서 포함된다.
바람직한 실시형태에서, 인간 항체가 생산된다. 인간 항체 및/또는 완전 인간 항체는 본 명세서에 제공된 실시예를 포함하는 관련 기술 분야에 공지된 임의의 방법을 이용하여 생산될 수 있다. 예를 들어, 기능적 내인성 면역글로불린을 발현할 수 없지만, 인간 면역글로불린 유전자를 발현할 수 있는 형질전환 마우스를 이용할 수 있다. 예를 들어, 인간 중쇄 및 경쇄 면역글로불린 유전자 복합체를 무작위로 또는 동종 재조합에 의해서 마우스 배아 줄기 세포 내로 도입할 수 있다. 대안적으로, 인간 가변 영역, 불변 영역 및 다양성 영역을 인간 중쇄 및 경쇄 유전자에 추가로 마우스 배아 줄기 세포 내로 도입할 수 있다. 마우스 중쇄 및 경쇄 면역글로불린 유전자는 별개로 또는 동종 재조합에 의한 인간 면역글로불린 로커스의 도입과 동시에 비기능적으로 될 수 있다. 특히, JH 영역의 동종접합성 결손은 내인성 항체 생산을 방지한다. 변형된 배아 줄기 세포를 팽창시키고, 포배 내로 마이크로주사하여 키메릭 마우스를 생산한다. 이어서, 키메릭 마우스를 번식시켜 인간 항체를 발현하는 동종접합성 자손을 생성한다. 형질전환 마우스를 정상적인 방식으로 선택된 항원, 예를 들어, 본 발명의 폴리펩타이드의 전부 또는 일부를 사용하여 면역화시킨다. 항원에 대한 단클론성 항체는 통상적인 하이브리도마 기술을 사용하여 면역화된 형질전환 마우스로부터 얻을 수 있다. 형질전환 마우스에 보유된 인간 면역글로불린 트랜스젠은 B-세포 분화 동안 재배열하고, 후속적으로 클래스 교체 및 체세포 돌연변이를 겪는다. 따라서, 그러한 기술을 사용하여, 치료적으로 유용한 IgG, IgA, IgM 및 IgE 항체를 생산하는 것이 가능하다. 인간 항체를 생산하기 위한 상기 기술의 개요에 대해서는 문헌[Lonberg and Huszar, 1995, Int. Rev. Immunol. 13:65-93]을 참고한다. 인간 항체 및 인간 단클론성 항체를 생산하기 위한 이러한 기술 및 그러한 항체를 생산하기 위한 프로토콜의 상세한 논의에 대해서는, 예를 들어, 전문이 본 명세서에 참고로 포함된 PCT 공개 WO 98/24893, WO 96/34096, 및WO 96/33735; 및 미국 특허 5,413,923, 5,625,126, 5,633,425, 5,569,825, 5,661,016, 5,545,806, 5,814,318, 및 5,939,598을 참고하기 바란다. 다른 방법은 본 명세서의 실시예에 설명되어 있다. 또한, 압제닉스, 인코퍼레이티드(Abgenix Inc./암젠.(Amgen.)(미국 캘리포니아주 싸우전드 오크스 소재) 오엠티(OMT)(미국 캘리포니아주 파올로 알토 소재), 아르젠-엑스(Argen-x)(네덜란드 브레다 소재), 아블렉시스(Ablexis)(미국 캘리포니아주 샌프란시스코 소재) 또는 하버 앤티바디즈(Harbour Antibodies)(미국 매사추세스주 캠브리지 소재)와 같은 회사는 상기에 기술된 것과 유사한 기술을 사용하여 선택된 항원에 대해 지향되는 인간 항체를 제공하기 위해 참여할 수 있다.
키메릭 항체는 항체의 상이한 부분이 상이한 면역글로불린 분자로부터 유래되는 분자이다. 키메릭 항체를 생산하는 방법은 관련 기술 분야에 공지되어 있다. 예를 들어, 전문이 본 명세서에 참고로 포함된 문헌[Morrison, 1985, Science 229:1202]; [Oi et al., 1986, BioTechniques 4:214]; [Gillies et al., 1989, J. Immunol. Methods 125:191-202]; 및 미국 특허 5,807,715, 4,816,567, 4,816,397 및 6,331,415를 참고하기 바란다.
인간화 항체는 소정의 항원에 결합할 수 있고, 실질적으로 인간 면역글로불린의 아미노산 서열을 갖는 프레임워크 영역 및 실질적으로 비-인간 면역글로불린의 아미노산 서열을 갖는 CDR을 포함하는 항체 또는 이의 변이체 또는 이의 단편이다. 인간화 항체는 적어도 하나 및 전형적으로 2개의 가변 도메인(Fab, Fab', F(ab')2, Fabc, Fv)을 실질적으로 모두 포함하고, 여기서 모든 또는 실질적으로 모든 CDR 영역은 비-인간 면역글로불린의 것(즉, 공여 항체)에 대응하고, 모든 또는 실질적으로 모든 프레임워크 영역은 인간 면역글로불린 컨센서스 서열의 것이다. 바람직하게는, 인간화 항체는 또한 면역글로불린 불변 영역(Fc)의 적어도 일부, 전형적으로 인간 면역글로불린의 것을 포함한다. 통상적으로, 항체는 경쇄 및 적어도 중쇄의 가변 도메인 둘 모두를 함유할 것이다. 항체는 또한 중쇄의 CH1, 경첩, CH2, CH3 및 CH4 영역을 포함할 수 있다. 인간화 항체는 IgM, IgG, IgD, IgA 및 IgE를 포함하는 임의의 클래스 및 IgG1, IgG2, IgG3 및 IgG4를 포함하는 임의의 동종형의 면역글로불린으로부터 선택될 수 있다. 대체로, 불변 도메인은 인간화 항체가 세포독성 활성을 나타내는 것을 목적하는 경우에 보체 고정 불변 도메인이고, 클래스는 대개 IgG1이다. 그러한 세포독성 활성이 요망되지 않는 경우에, 불변 도메인은 IgG2 클래스의 것일 수 있다. 특정 실시형태에서, 본 발명의 항체는 인간 감마 4 불변 영역을 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 Fc-γ 수용체를 결합하고, 예를 들어, Leu235Glu 돌연변이를 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은 안정성을 증가시키기 위해서 Ser228Pro 돌연변이를 포함한다. 또 다른 실시형태에서, 중쇄 불변 영역은IgG4-PE이다. 본 발명의 특정 실시형태에서 사용될 수 있는 VL 및 VH 불변 도메인의 예는 문헌[Johnson et al(1997) J. Infect. Dis. 176, 1215-1224]에 기술된 C-카파 및 C-감마-1(nG1m) 및 미국 특허 5,824,307에 기술된 것을 포함하지만 이에 제한되는 것은 아니다. 인간화 항체는 하나를 초과하는 클래스 또는 동종형으로부터의 서열을 포함할 수 있고, 목적하는 이펙터 기능을 최적화하기 위해 특정 불변 도메인을 선택하는 것은 관련 기술 분야의 통상의 기술 내에 있다. 인간화 항체의 프레임워크 및 CDR 영역은 모 서열에 정확하게 대응할 필요가 없고, 예를 들어, 공여 CDR 또는 컨센서스 프레임워크는 적어도 하나의 잔기의 치환, 삽입 또는 결손에 의해서 돌연변이될 수 있어서, 그 부위에서 CDR 또는 프레임워크 잔기가 컨센서스 또는 도입 항체에 대응하지 않는다. 그러나, 그러한 돌연변이는 광범하지 않을 것이다. 대체로, 인간화 항체 잔기의 적어도 75%, 보다 종종 90%, 가장 바람직하게는 95% 초과가 모 FR 및 CDR 서열의 잔기에 대응할 것이다. 인간화 항체는 CDR-그래프팅(grafting)((유럽 특허 EP 239,400; 국제 특허 출원 공개 WO 91/09967; 및 미국 특허 5,225,539, 5,530,101, 및 5,585,089), 베니어링(veneering) 또는 리서피싱(resurfacing)(유럽 특허 EP 592,106 및 EP 519,596; 문헌[Padlan, 1991, Molecular Immunology 28(4/5):489-498]; [Studnicka et al., 1994, Protein Engineering 7(6):805-814]; 및 [Roguska et al., 1994, PNAS 91:969-973]);, 쇄 셔플링(미국 특허 5,565,332), 및 예를 들어, 미국 특허 6,407,213, 미국 특허 5,766,886, WO 9317105, 문헌[Tan et al., J. Immunol. 169:1119 25 (2002)], [Caldas et al., Protein Eng. 13(5):353-60 (2000)], [Morea et al., Methods 20(3):267 79 (2000)], [Baca et al., J. Biol. Chem. 272(16):10678-84 (1997)], [Roguska et al., Protein Eng. 9(10):895 904 (1996)], [Couto et al., Cancer Res. 55 (23 Supp):5973s-5977s (1995)], [Couto et al., Cancer Res. 55(8):1717-22 (1995)], [Sandhu J S, Gene 150(2):409-10 (1994)], 및 [Pedersen et al., J. Mol. Biol. 235(3):959-73 (1994)]에 개시된 기술을 포함하지만 이에 제한되지 않는 관련 기술 분야에 공지된 다양한 기술을 사용하여 생산될 수 있다. 또한 전문이 참고로 본 명세서에 포함된 미국 특허 공개 US 2005/0042664 A1(2005년 2월 24일)을 참고하기 바란다. 종종, 프레임워크 영역 내의 프레임워크 잔기는 항원 결합을 변경시키고, 바람직하게는 향상시키기 위해 CDR 공여 항체로부터의 상응하는 잔기로 치환될 것이다. 이러한 프레임워크 치환은 관련 기술 분야에 널리 공지된 방법에 의해, 예를 들어, 항원 결합에 중요한 프레임워크 잔기를 식별하기 위해 CDR 및 프레임워크 잔기의 상호작용의 모델링, 및 특정 위치에서 드문 프레임워크 잔기를 식별하기 위해 서열 비교에 의해서 식별된다(예를 들어, 전문이 본 명세서에 참고로 포함된 미국 특허 5,585,089(퀸(Queen) 등); 및 문헌[Reichmann et al., 1988, Nature 332:323] 참고).
단일 도메인 항체, 예를 들어, 경쇄가 결핍되는 항체는 관련 기술 분야에 잘 공지된 방법에 의해서 생산될 수 있다. 전문이 본 명세서에 참고로 포함된 문헌[Riechmann et al., 1999, J. Immunol. 231:25-38]; [Nuttall et al., 2000, Curr. Pharm. Biotechnol. 1(3):253-263]; [Muylderman, 2001, J. Biotechnol. 74(4): 277302]); 미국 특허 6,005,079; 및 국제 특허 출원 공개 WO 94/04678, WO 94/25591 및 WO 01/44301 참고하기 바란다.
또한, hOX40L 항원에 특이적으로 결합하는 항체는 다시 관련 기술 분야의 통상의 기술자에게 잘 공지된 기술을 사용하여 항원을 "모방하는" 항-개별특이형 항체를 생성하기 위해 이용될 수 있다(예를 들어, 문헌[Greenspan & Bona, 1989, FASEB J. 7(5):437-444]; 및 [Nissinoff, 1991, J. Immunol. 147(8):2429-2438] 참고).
키트
본 발명은 또한 본 발명의 약제학적 조성물의 하나 이상의 구성 성분, 예를 들어 본 명세서에 제공된 하나 이상의 항체 또는 단편으로 채워진 하나 이상의 용기를 포함하는 약제학적 또는 진단 팩(pack) 또는 키트를 제공한다. 약제학적 또는 생물학적 산물의 제조, 사용 또는 판매를 규제하는 정부 기관에 의해서 규정된 형태의 공지문(notice)이 임의로 상기 용기(들)에 연합될 수 있고, 공지문은 기관에 의한 인간 투여를 위한 제조, 사용 또는 판매의 승인, 예를 들어 인증 번호를 반영한다.
본 발명은 상기 방법에서 사용될 수 있는 키트를 제공한다. 일 실시형태에서, 키트는 하나 이상의 용기 내에 본 발명의 항체, 바람직하게는 정제된 항체를 포함한다. 구체적인 실시형태에서, 본 발명의 키트는 대조군으로서 실질적으로 단리된 hOX40L 항원을 함유한다. 바람직하게는, 본 발명의 키트는 hOX40L 항원과 반응하지 않는 대조군 항체를 추가로 포함한다. 또 다른 구체적인 실시형태에서, 본 발명의 키트는 hOX40L 항원에 대한 변형된 항체의 결합을 검출하기 위한 수단을 함유한다(예를 들어, 항체는 검출 가능한 기질, 예를 들어 형광성 화합물, 효소 기질, 방사성 화합물 또는 발광 화합물에 컨쥬게이팅될 수 있거나, 제1 항체를 인식하는 제2 항체가 검출 가능한 기질에 컨쥬게이팅될 수 있다). 구체적인 실시형태에서, 키트는 재조합 방식으로 생산되거나 또는 화학적으로 합성된 hOX40L 항원을 포함할 수 있다. 키트 내에 제공되는 hOX40L 항원은 또한 고체 지지체에 부착될 수 있다. 보다 구체적인 실시형태에서, 상기에 기술된 키트의 검출 수단은 hOX40L 항원이 부착되는 고체 지지체를 포함한다. 상기 키트는 또한 비-부착된 리포터(reporter)-표지된 항-인간 항체를 포함할 수 있다. 이러한 실시형태에서, hOX40L 항원에 대한 항체의 결합은 상기 리포터-표지된 항체의 결합에 의해서 검출될 수 있다.
"보존적 아미노산 치환"은 임의의 아미노산 잔기를 유사한 구조 및/또는 화학적 특성을 갖는 또 다른 것으로 대체함으로써, 예컨대 류신을 아이소류신 또는 발린으로, 아스파테이트를 글루타메이트로, 또는 트레오닌을 세린으로 대체함으로써 일어난다. 따라서 특정 아미노산 서열의 "보존적 치환"은 폴리펩타이드 활성에 중요하지 않은 아미노산의 치환 또는 유사한 특성(예를 들어, 산성, 염기성, 양성 또는 음성 전하를 띤, 극성 또는 비극성, 등)을 지니는 다른 아미노산으로의 치환을 나타내며, 매우 중요한 아미노산의 치환이 펩타이드의 활성(즉, 혈뇌장벽(BBB)를 통과할 수 있는 펩타이드의 활성)을 감소시키지는 않는다. 기능적으로 유사한 아미노산을 제공하는 보존적 치환 표는 관련 기술 분야에 널리 공지되어 있다. 예를 들어, 다음 여섯 군은 각각 서로에 대해 보존적 치환인 아미노산을 함유한다: 1) 알라닌(A), 세린(S), 트레오닌(T); 2) 아스파트산(D), 글루탐산(E); 3) 아스파라긴(N), 글루타민(Q); 4) 아르기닌(R), 라이신(K); 5) 아이소류신(I), 류신(L), 메티오닌(M), 발린(V); 및 6) 페닐알라닌(F), 티로신(Y), 트립토판(W). (또한 전문이 참고로 포함된 문헌[Creighton, Proteins, W. H. Freeman and Company (1984)] 참고). 일부 실시형태에서, 단일 아미노산 또는 작은 범위의 아미노산을 변경, 부가 또는 결손시키는 개개의 치환, 결손 또는 부가는, 그 변화가 펩타이드의 활성을 감소시키지 않는다면 "보존적 치환"으로서 고려될 수 있다. 삽입 또는 결손은 전형적으로 약 1 내지 5개의 아미노산의 범위에서 이루어진다. 보존적 아미노산의 선택은 펩타이드 내에서 치환될 아미노산의 위치(예를 들어, 그 아미노산이 펩타이드의 외부에 존재하여 용매에 노출되거나 또는 아미노산이 펩타이드의 내부에 존재하여 용매에 노출되지 않는 경우)를 기초로 선택될 수 있다.
대안적인 실시형태에서, 기존의 아미노산의 위치, 즉 용매에 대한 그의 노출을 기초로 하여(즉, 그 아미노산이 용매에 노출되지 않거나, 또는 용매에 노출되지 않은 내부에 존재하는 아미노산에 비해서 펩타이드 또는 폴리펩타이드의 외부 표면 상에 존재하는 경우) 기존의 아미노산을 대체할 아미노산을 선택할 수 있다. 그러한 보존적 아미노산 치환의 선택은 예를 들어 문헌[Dordo et al, J. Mol Biol, 1999, 217, 721-739] 및 [Taylor et al., J. Theor. Biol. 119 (1986); 205-218] 및 [S. French and B. Robson, J. Mol. Evol., 19(1983)171]에 개시된 바와 같이 관련 기술 분야에 널리 공지되어 있다. 따라서, 단백질 또는 펩타이드의 외부에 존재하는 아미노산(즉, 용매에 노출된 아미노산)에 적합한 보존적 아미노산 치환을 선택할 수 있고, 제한이 아닌 예를 들어, 하기 치환이 사용될 수 있다: F에 의한 Y의 치환, S 또는 K에 의한 T의 치환, A에 의한 P의 치환, D 또는 Q에 의한 E의 치환, D 또는 G에 의한 N의 치환, K에 의한 R의 치환, N 또는 A에 의한 G의 치환, S 또는 K에 의한 T의 치환, N 또는 E에 의한 D의 치환, L 또는 V에 의한 I의 치환, Y에 의한 F의 치환, T 또는 A에 의한 S의 치환, K에 의한 R의 치환, N 또는 A에 의한 G의 치환, R에 의한 K의 치환, 또는 S, K 또는 P에 의한 A의 치환.
대안적인 실시형태에서, 또한 단백질 또는 펩타이드의 내부에 존재하는 아미노산에 적합하게 포함되는 보존적 아미노산 치환을 선택할 수 있고, 예를 들어 단백질 또는 펩타이드의 내부에 존재하는 경우(즉, 아미노산이 용매에 내출되지 않음) 아미노산에 대해서 적합한 보존적 치환을 사용할 수 있고, 제한이 아닌 예를 들어, 하기 보존적 치환을 사용할 수 있다: Y는 F로, T는 A 또는 S로, I는 L 또는 V로, W는 Y로, M은 L로, N은 D로, G는 A로, T는 A 또는 S로, D는 N으로, I는 L 또는 V로, F는 Y 또는 L로, S는 A 또는 T로, A는 S, G, T 또는 V로 치환된다. 일부 실시형태에서, 비-보존적 아미노산 치환이 또한 그 용어의 변형에 포함된다.
본 명세서에서 사용되는 바와 같이 "항체"는 IgG, IgM, IgA, IgD 또는 IgE 분자 또는 이의 항원-특이적인 항체 단편(Fab, F(ab')2, Fv, 다이설파이드 연결된 Fv, scFv, 단일 도메인 항체, 클로즈드 컨포메이션(closed conformation) 다중특이적인 항체, 다이설파이드-연결된 scfv, 다이아바디를 포함하지만 이에 제한되지 않음)을 나타내며, 자연적으로 항체를 생산하거나, 재조합 DNA 기술에 의해서 생성된 임의의 종으로부터 유래된 것인지; 혈청, B-세포, 하이브리도마, 트랜스퍼펙토마(transfectoma), 효모 또는 박테리아로부터 단리된 것인지에 관계없다. 항체는 일상적인 기술을 사용하여 인간화될 수 있다.
본 명세서에서 기술된 바와 같이, "항원"은 항체 작용제 상의 결합 부위에 의해서 결합되는 분자이다. 전형적으로, 항원은 항체 리간드에 의해서 결합되고, 생체내에서 항체 반응을 상승시킬 수 있다. 항원은 폴리펩타이드, 단백질, 핵산 또는 다른 분자 또는 이의 부분일 수 있다. 용어 "항원 결정자"는 항원-결합 분자에 의해서, 보다 특히 상기 분자의 항원-결합 부위에 의해서 인식되는 항원 상의 에피토프를 나타낸다.
본 명세서에서 사용되는 바와 같이, 용어 "항체 단편"은 적어도 하나의 면역글로불린 가변 도메인 또는 면역글로불린 가변 도메인 서열을 포함하고, 주어진 항원에 특이적으로 결합하는 폴리펩타이드를 나타낸다. 항체 단편은 항체 또는 항체의 항원-결합 도메인을 포함하는 폴리펩타이드를 포함할 수 있다. 일부 실시형태에서, 항체 단편은 단클론성 항체 또는 단클론성 항체의 항원-결합 도메인을 포함하는 폴리펩타이드를 포함할 수 있다. 예를 들어, 항체는 중(H)쇄 가변 영역(본 명세서에서 VH라 약칭됨) 및 OX40L(L)쇄 가변 영역(본 명세서에서 VL이라 약칭됨)을 포함할 수 있다. 또 다른 예에서, 항체는 2개의 중(H)쇄 가변 영역 및 2개의 OX40L(L)쇄 가변 영역을 포함한다. 용어 "항체 단편"은 항체의 항원-결합 단편(예를 들어, 단쇄 항체, Fab 및 sFab 단편, F(ab')2, Fd 단편, Fv 단편, scFv, 및 도메인 항체(dAb) 단편(예를 들어, 전문이 본 명세서에 참고로 포함된 문헌[de Wildt et al., Eur J. Immunol., 1996; 26(3):629-39] 참고) 뿐만 아니라 완전 항체를 포함한다. 항체는 IgA, IgG, IgE, IgD, IgM(뿐만 아니라 하위유형 및 이의 조합)의 구조적 특징부를 가질 수 있다. 항체는 마우스, 토끼, 돼지, 래트 및 영장류(인간 및 비-인간 영장류) 및 영장류화된 항체를 비롯한 임의의 공급원으로부터 유래할 수 있다. 항체는 또한 미디바디(midibody), 인간화 항체, 키메릭 항체 등을 포함한다.
본 명세서에서 사용되는 바와 같이, "항체 가변 도메인"은 OX40L 및 상보성 결정 영역(CDR; 즉, CDR1, CDR2, 및 CDR3) 및 프레임워크 영역(FR)의 아미노산 서열을 포함하는 항체 분자의 중쇄의 부분을 말한다. VH는 중쇄의 가변 도메인을 나타낸다. VL은 경쇄의 가변 도메인을 나타낸다. 본 발명에서 사용되는 방법에 따라서, CDR 및 FR에서 할당된 아미노산 위치는 카바트(문헌[Sequences of Proteins of Immunological Interest (National Institutes of Health, Bethesda, Md., 1987 and 1991]) 또는 IMGT 명명법에 따라서 정의될 수 있다.
본 명세서에서 사용되는 바와 같이, 용어 "항체 결합 부위"는 항체의 하나 이상의 CDR을 포함하고, 항원을 결합할 수 있는 폴리펩타이드 또는 도메인을 나타낸다. 예를 들어, 폴리펩타이드는 CDR3(예를 들어, HCDR3)을 포함한다. 예를 들어 폴리펩타이드는 항체의 가변 도메인의 CDR 1 및 2(예를 들어, HCDR1 및 2) 또는 CDR 1 내지 3(예를 들어, HCDR1-3)을 포함한다. 예에서, 항체 결합 부위는 단일 가변 도메인(예를 들어, VH 또는 VL 도메인)에 의해서 제공된다. 또 다른 예에서, 결합 부위는 VH/VL 쌍 또는 그러한 쌍의 둘 이상을 포함한다.
본 명세서에서 사용되는 바와 같이, "유전형분석"은 예를 들어, 그 위치에서의 핵산 서열을 측정함으로써, 게놈 내의 하나 이상의 위치에서 세포 및/또는 대상체의 특이적인 대립유전자 조성을 측정하는 방법을 나타낸다. 유전형분석은 핵산 분석 및/또는 핵산 수준에서의 분석을 나타낸다. 본 명세서에서 사용되는 바와 같이, "표현형분석"은 예를 들어, 발현 산물의 폴리펩타이드 서열을 측정함으로써, 세포 및/또는 대상체의 발현 산물의 동일성 및/또는 조성을 측정하는 방법을 나타낸다. 표현형분석은 단백질 분석 및/또는 단백질 수준에서의 분석을 나타낸다.
본 명세서에서 사용되는 바와 같이, 용어 "치료하다", "치료", "치료하는" 또는 "완화"는 치료적 치료를 나타내고, 여기서 목적은 질환 또는 장애와 관련된 병태의 진행 또는 중증도의 역전, 경감, 완화, 억제, 늦춤 또는 중단이다. 용어 "치료하는"은 병태, 질환 또는 장애의 적어도 하나의 부작용 또는 증상의 감쇠 또는 경감을 포함한다. 치료는 일반적으로 하나 이상의 증상 또는 임상적인 마커가 감쇠되는 경우 "효과적"이다. 대안적으로, 치료는 질환의 진행이 감쇠 또는 정지되는 경우 "효과적"이다. 즉, "치료"는 단지 증상 또는 마커의 개선을 포함하지 않고, 또한 치료 부재 하에서 예상될 것에 비해서 증상의 진행 또는 악화가 중지되거나 또는 적어도 느려지는 것을 포함한다. 유익하거나 목적하는 임상 결과는 하나 이상의 증상(들)의 경감, 질환 정도의 약화, 질환 상태의 안정화(즉, 악화되지 않음), 질환 진행의 연장 또는 느려짐, 질환 상태의 완화 또는 일시적 완화, 차도(부분적 또는 전체적), 및/또는 감소된 사망률을 포함하지만 이에 제한되는 것은 아니며, 이것은 검출되든 검출되지 않든 관계없다. 용어 질환의 "치료"는 또한 질환의 증상 또는 부작용으로부터의 경감(완화적 치료 포함)을 제공하는 것을 포함한다. 효과적인 치료의 경우 완전한 치유가 고려되지 않는다. 방법은 마찬가지로 특정 양상에서 치유를 포함할 수 있다.
본 명세서에서 사용되는 바와 같이, 용어 "약제학적 조성물"은 약제학적으로 허용 가능한 담체 예를 들어, 약제학적 산업에서 일반적으로 사용되는 담체와 조합되는 활성제를 나타낸다. 구 "약제학적으로 허용 가능한"은 본 명세서에서 정통한 의학적 판단의 범주에서 과도한 독성, 자극, 알레르기성 반응 또는 다른 문제 또는 합병증 없이 타당한 이익/위험 비로의 보상으로 인간 및 동물 조직과 접촉하는 데 사용하기에 적합한 그러한 화합물, 물질, 조성물 및/또는 투여 형태를 나타낸다.
본 명세서에서 사용되는 바와 같이, 용어 "투여하는"은 목적하는 부위에서 그 작용제의 적어도 부분적인 전달을 유발하는 방법 또는 경로에 의한 본 명세서에 개시된 바와 같은 화합물의 대상체 내의 배치를 나타낸다. 본 명세서에 개시된 화합물을 포함하는 약제학적 조성물은 대상체에서 효과적인 치료를 유발하는 임의의 적절한 경로에 의해서 투여될 수 있다.
다수의 조성물이 별개로 또는 동시에 투여될 수 있다. 별개 투여는 두 조성물을 상이한 시기에, 예를 들어 적어도 10, 20, 30, 또는 10 내지 60분 간격으로, 또는 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 12시간 간격으로 투여하는 것을 나타낸다. 또한 조성물을 24시간 간격 또는 심지어는 더 긴 간격으로 투여할 수 있다. 대안적으로, 2종 이상의 조성물은 동시에, 예를 들어 10분 미만 또는 5분 미만의 간격으로 투여될 수 있다. 동시에 투여되는 조성물은 일부 양상에서 성분 각각에 대해서 동일한 또는 상이한 시간 방출 메커니즘을 갖거나 또는 갖지 않는 혼합물로서 투여될 수 있다.
본 명세서에서 사용되는 바와 같이, "인증 번호" 또는 "마켓팅 인증 번호"는, 기관이 특정 의료 제품 및/또는 조성물이 기관의 관할 지역 하에서 광고되고/되거나 판매를 위해서 제공될 수 있는지를 결정한 후에 감독 기관에 의해서 부여되는 번호를 나타낸다. 본 명세서서에서 사용되는 바와 같이 "감독 기관"은 예를 들어, 의료 제품 및/또는 조성물의 안전성 및 효능을 평가하는 책임이 있고, 주어진 지역에서 그러한 제품 및/또는 조성물의 판매/광고를 제어하는 기관 중 하나를 나타낸다. 미국의 식품 의약국(FDA) 및 유럽의 유럽 의약청(EPA)이 그러한 감독 기관의 두 예이다. 다른 비제한적인 예는 SDA, MPA, MHPRA, IMA, ANMAT, 건강-의약국의 홍콩 지부(Hong Kong Department of Health-Drug Office), CDSCO, 메드세이프(Medsafe), 및 KFDA를 포함할 수 있다.
본 명세서에서 사용되는 바와 같이, "주사 장치"는 주사를 수행하기 위해서 설계된 장치를 나타내고, 주사는 주사 장치를 인간의 조직, 전형적으로는 피하 조직에 일시적으로 유체 커플링시키는 단계를 포함한다. 주사는 일정량의 액체 약물을 조직에 투여하고, 조직으로부터 주입 장치를 디커플링 또는 제거하는 것을 추가로 포함한다. 일부 실시형태에서, 주사 장치는 정맥내 장치 또는 IV일 수 있고, 이것은 표적 조직이 순환계 내의 혈액, 예를 들어 정맥 혈액인 경우에 사용되는 주사 장치의 유형이다. 주사 장치의 일반적이지만 비제한적인 예는 니들 또는 주사기이다.
본 명세서에서 사용되는 바와 같이, "완충액"은 pH를 상당히 변화시키지 않으면서 산 또는 염기의 특정량을 흡수할 수 있는 화학 작용제를 말한다.
본 명세서에서 사용되는 바와 같이, "패키징"은 분포 및/또는 사용을 위해서 성분을 단위 핏(fit)에 조직화하고/하거나 구속시키는 방법을 나타낸다. 패키징은 예를 들어, 박스, 백, 주사기, 앰플, 바이알, 튜브, 클램쉘(clamshell) 패키징, 멸균성을 유지시키기 위한 장벽 및/또는 용기, 레이블 등을 포함할 수 있다.
본 명세서에서 사용되는 바와 같이, "지시서"는 물품의 직접 용기 상의 필사물, 인쇄물 또는 그래픽의 디스플레이, 예를 들어 약제학적 활성제를 함유하는 바이알 상에 디스플레이된 필사물, 또는 관심 조성물을 함유하는 키트에 포함된 관심 제품의 조성 및 용도의 상세사항의 디스플레이를 나타낸다. 지시서는 투여 또는 수행될 고려되는 바와 같은 치료 방법을 언급한다.
본 명세서에 사용되는 바와 같이, 용어 "포함하는" 또는 "포함하다"는 항체, 단편, 용도, 조성물, 방법, 및 그 방법 또는 조성물에 본질적인 이들의 각각의 성분(들)과 관련하여 사용되면서도 여전히, 본질적이든 그렇지 않든 명시되지 않은 요소들의 포함에 대해 개방되어 있다.
용어 "이루어진"은 본 명세서에 기술된 바와 같은 항체, 단편, 용도, 조성물, 방법 및 이들의 각각의 성분을 나타내며, 이들은 그 실시형태의 그러한 설명에서 언급되지 않은 어떠한 요소도 배제한다.
본 명세서에 사용되는 바와 같이, 용어 "본질적으로 이루어진"은 주어진 실시형태에 필요한 그러한 요소들을 나타낸다. 이 용어는 그러한 실시형태의 기본적이고 신규하거나 기능적인 특질(들)에 실질적으로 영향을 주지 않는 요소들의 존재를 허용한다.
단수형 표현은 문맥이 달리 명백히 나타내지 않는 한 복수의 지시대상을 포함한다. 유사하게, 단어 "또는"은 그 문맥이 달리 명백히 나타내지 않는 한 "및"을 포함하도록 의도된다. 본 명세서에 기술된 것과 유사하거나 등가인 방법 및 물질이 본 개시 내용의 실시 또는 시험에서 사용될 수 있지만, 적합한 방법 및 물질이 하기에 기술되어 있다. 약어 "예를 들어(e.g.)"는 라틴어(exempli gratia)에서 유래되며, 비제한적인 예를 나타내기 위해 본 명세서에서 사용된다. 따라서, 약어 "예를 들어"는 용어 "예컨대"와 동의어이다.
세포 생물학 및 분자 생물학에서 공통된 용어의 정의는 문헌["The Merck Manual of Diagnosis and Therapy", 19th Edition, published by Merck Research Laboratories, 2006 (ISBN 0-911910-19-0)]; [Robert S. Porter et al. (eds.), The Encyclopedia of Molecular Biology, published by Blackwell Science Ltd., 1994 (ISBN 0-632-02182-9)]; [Benjamin Lewin, Genes X, published by Jones & Bartlett Publishing, 2009 (ISBN-10: 0763766321)]; [Kendrew et al. (eds.), Molecular Biology and Biotechnology: a Comprehensive Desk Reference, published by VCH Publishers, Inc., 1995 (ISBN 1-56081-569-8)] 및 [Current Protocols in Protein Sciences 2009, Wiley Intersciences, Coligan et al., eds.]에서 찾아볼 수 있다.
달리 언급되지 않는 한, 본 발명은 예를 들어, 모두 전문이 참고로 본 명세서에 포함된 문헌[Sambrook et al., Molecular Cloning: A Laboratory Manual (4 ed.), Cold Spring Harbor Laboratory Press, Cold Spring Harbor, N.Y., USA (2012)]; [Davis et al., Basic Methods in Molecular Biology, Elsevier Science Publishing, Inc., New York, USA (1995)]; 또는 [Methods in Enzymology: Guide to Molecular Cloning Techniques Vol.152, S. L. Berger and A. R. Kimmel Eds., Academic Press Inc., San Diego, USA (1987)]; [Current Protocols in Protein Science (CPPS) (John E. Coligan, et al., ed., John Wiley and Sons, Inc.)], [Current Protocols in Cell Biology (CPCB) (Juan S. Bonifacino et al. ed., John Wiley and Sons, Inc.)], 및 [Culture of Animal Cells: A Manual of Basic Technique by R. Ian Freshney, Publisher: Wiley-Liss; 5th edition (2005)], [Animal Cell Culture Methods (Methods in Cell Biology, Vol. 57, Jennie P. Mather and David Barnes editors, Academic Press, 1st edition, 1998)]에 기술된 바와 같은 표준 절차를 사용하여 수행되었다.
다른 용어들은 본 발명의 다양한 양상의 설명에서 본 명세서에 정의되어 있다.
본 출원 전체에서 인용된 공표 특허, 공개 특허 출원 및 공계류 중인 특허 출원을 포함한 모든 특허 및 다른 간행물은, 예를 들어 본 명세서에 기술된 기술과 관련하여 사용될 수 있는 그러한 간행물들에 기술된 방법론을 설명 및 개시하려는 목적을 위하여 명시적으로 본 명세서에 참고로 포함된다. 이들 간행물은 본 출원의 출원일 전에 오로지 그들의 개시를 위해서만 제공된다. 이에 관하여 어떤 것도, 본 발명자들이 종래 발명에 의해 또는 임의의 다른 이유로 그러한 개시 내용보다 선행하지 않음을 인정하는 것으로 해석되어서는 안 된다. 이들 문헌의 내용에 관한 표현 및 날짜에 관한 모든 진술은 본 출원인들이 이용 가능한 정보에 기초하며, 이들 문헌의 내용 또는 날짜의 정확함에 대해 어떠한 것도 인정하는 것으로 여겨지지 않는다.
본 개시 내용의 실시형태의 설명은 본 발명을 망라하거나 개시된 정확한 형태로 본 개시 내용을 제한하는 것을 의도하지 않는다. 본 개시 내용의 구체적인 실시형태 및 그를 위한 실시예가 예시적인 목적으로 본 명세서에 기술되어 있지만, 관련 기술분야의 통상의 기술자가 인식하는 바와 같이, 다양한 등가의 변형이 본 개시 내용의 범주 내에서 가능하다. 예를 들어, 방법 단계 또는 기능이 주어진 순서로 제시되어 있지만, 대안적인 실시형태가 상이한 순서로 기능을 수행할 수 있거나, 또는 기능이 실질적으로 동시에 수행될 수 있다. 본 명세서에 제공된 본 개시 내용의 교시는 적절한 경우에 다른 절차 또는 방법에 적용될 수 있다. 본 명세서에 기술된 다양한 실시형태를 조합하여 추가의 실시형태를 제공할 수 있다. 본 발명의 양상은, 필요하다면, 상기 문헌 및 출원의 조성물, 기능 및 개념을 사용하여 본 개시 내용의 또 다른 추가의 실시형태를 제공하기 위하여 변형될 수 있다. 또한, 생물학적 기능성 등가성 고려 사항으로 인해서, 일부 변화는 부류 또는 양에서 생물학적 또는 화학적 행동에 영향을 미치지 않으면서 단백질 구조에서 행해질 수 있다. 이러한 변화 및 다른 변화는 상세한 설명의 OX40L에서 본 개시 내용에서 행해질 수 있다. 모든 그러한 변형은 첨부된 청구범위의 범주 내에 포함되는 것이 의도된다.
전술된 실시형태 중 임의의 것의 구체적인 요소는 조합되거나 다른 실시형태 내의 요소를 위해서 치환될 수 있다. 더욱이, 본 발명의 특정 실시형태와 관련된 이점이 이들 실시형태와 관련하여 기술되어 있지만, 다른 실시형태가 또한 그러한 이점을 나타낼 수 있으며, 본 발명의 범주 내에 속하기 위하여 모든 실시형태가 반드시 그러한 이점을 나타낼 필요는 없다.
본 명세서에 기술된 특정 구성, 개념, 양상, 예, 조항은 본 발명의 제한이 아니라 설명의 방식으로 제시된다는 것을 이해할 것이다. 본 발명의 원칙적인 특징부는 본 발명의 범주로부터 벗어나지 않으면서 다양한 실시형태에서 사용될 수 있다. 관련 기술 분야의 통상의 기술자는 단지 일상적인 연구를 사용하여 본 명세서에 기술된 특정 절차에 대한 다수의 등가물을 인식할 것이고, 확인할 수 있을 것이다. 그러한 등가물은 본 발명의 범주에 포함되고, 청구범위에 의해서 보호되는 것으로 간주된다. 본 명세서에 언급된 모든 공개물 및 특허 출원은 본 발명이 속한 관련 기술 분야의 통상의 기술자의 기술 수준을 대표한다. 모든 공개물 및 특허 출원은 각각의 개별 공개물 또는 특허 출원이 구체적으로 그리고 개별적으로 참고로 포함됨을 나타내는 동일한 정도로 본 명세서에 참고로 포함된다. 청구항 및/또는 명세서에서 용어 "포함하는"과 함께 사용되는 경우 용어 단수 표현의 사용은 하나를 의미할 수 있지만, 그것은 또한 "하나 이상", "적어도 하나" 및 "하나 또는 하나 초과"의 의미와 일치한다. 청구항에서 용어 "또는"의 사용은 대안만을 명확하게 나타내지 않는 한 또는 그 대안이 서로 배타적이지 않는 한 "및/또는"을 의미하도록 사용되지만, 본 개시 내용은 "대안"과 관련되고 "및/또는"과 관련된 정의를 지지한다. 본 출원 전체에서, 용어 "약"은 값이 장치에 대한 본질적인 오차 변화, 그 값을 측정하기 위해서 사용되는 방법 또는 연구 대상들 간에 존재하는 차이의 본질적인 오차 변화를 포함하는 것을 나타내기 위해서 사용된다.
본 명세서 및 청구범위(들)에서 사용되는 바와 같이, 용어 "포함하는"(및 포함하는의 임의의 형태, 예컨대 "포함하다", 및 "포함한다"), "갖는"(및 갖는의 임의의 형태, 예컨대 "갖는다" 및 "갖고 있다"), "포함하는"(및 포함하는의 임의의 형태, 예컨대 "포함하다" 및 "포함한다") 또는 "함유하는"(및 함유하는의 임의의 형태, 예컨대 "함유하다" 및 "함유한다")는 포괄적이거나 개방된 표현이며, 추가적인 언급되지 않은 요소 또는 방법 단계를 배제하지 않는다.
본 개시 내용의 임의의 부분은 문맥으로부터 명백하게 다르지 않는 한 본 개시내용의 임의의 다른 부분과 조합되어 검토될 수 있다.
본 명세서에 개시되고, 청구된 조성물 및/또는 방법 모두는 본 개시 내용의 OX40L에서 과도한 실험 없이 실시되고 실행될 수 있다. 본 발명의 조성물 및 방법이 바람직한 실시형태와 관련하여 기술되지 않더라도, 본 발명의 개념, 사상 및 범주로부터 벗어나지 않고 본 명세서에 기술된 조성물 및/또는 방법에, 그리고 방법의 단계에서 또는 방법의 단계의 순서에서 변경이 적용될 수 있다는 것은 관련 기술 분야의 통상의 기술자에게 명백할 것이다. 관련 기술 분야의 통상의 기술자에게 명백한 모든 그러한 유사한 치환 및 변형은 첨부된 청구범위에 의해서 정의된 바와 같은 본 발명의 사상, 범주 및 개념에 포함되는 것으로 생각된다.
실시예
실시예
1
항원 제조, 면역화 절차, 및
하이브리도마
생성
하기 실시예는 키마우스(상표명) 시스템을 사용한 항-인간 OX40L 단클론성 항체의 패널의 생성 및 식별의 상세한 설명을 제공한다(예를 들어, WO2011/004192 참고). 이를 위해서, 다량의 인간 면역글로불린 유전자를 함유하는 유전자 조작된 마우스를 가용성 재조합 인간 OX40L(시판되거나 실험실에서 생산됨) 또는 마우스 배아 섬유 모세포(MEF) 세포 상에 디스플레이된 표면 발현된 인간 OX40L로 면역화시켰다. 종래의 복강내 주사를 비롯한 다양한 면역화 방법뿐만 아니라 많은 부위에서의 신속한 면역화를 설정하고, 몇 주에 걸쳐서 동물을 키웠다. 각각의 방법의 마지막에, 2차 림프 조직, 예컨대 비장, 및 일부 경우에, 림프절을 제거하였다. 단일 세포 현탁액 중에서 조직을 제조하고, SP2/0 세포와 융합시켜 안정한 하이브리도마 세포주를 생성하였다.
물질 및 방법
재조합
레서스
및 인간
OX40L의
클로닝
발현 및 정제
인간 OX40L의 세포외 도메인을 코딩하는 cDNA를 표준 분자 생물학 기술을 사용하여 pREP4 발현 플라스미드(인비트로젠(Invitrogen)) 내로 클로닝하였다. 구축물은 또한 정제에 도움을 주기 위해서 FLAG 펩타이드 모티프를 함유하였고, 삼량체화에 도움을 주기 위해서 아이소류신 지퍼(zipper) 모이어티를 함유하였다. 그의 올바른 서열 조성을 보장하기 위해서 구축물을 시퀀싱하였다.
아미노산 변화를 도입하기 위해서 템플레이트로서 상기에서 생성된 인간 OX40L 플라스미드를 사용하고, 부위 지향된 돌연변이 유발을 사용하여 레서스(마카카 물라타(Macaca mulatta)) OX40L을 생성하였다.
레서스 원숭이 OX40L로서 인간 OX40L 웰을 일시적으로 발현시켜 인비트로젠의 프리스타일(FreeStyle)(상표명) CHO-S 현탁액 개작된 세포주를 사용하여 재조합 단백질을 생산하였다. 플라스미드를 PEI(폴리에틸렌이민 MW 40000)를 사용하여 세포 내로 형질주입시켰고, 13일의 기간 동안 과성장하도록 방치한 후 정제를 위해서 상청액을 수확하였다. 과성장 과정 동안 세포에 지이 헬쓰케어(GE Healthcare)로부터의 액티(Acti)CHO(상표명) 공급물 A 및 B를 공급하여 생산성을 상승시키고 세포의 수명을 증가시키는 것을 도왔다. 과성장 과정 동안, 샘플을 주기적으로 취하여 세포 성장 및 생존 능력을 모니터링하였다.
FLAG-태깅된 OX40L 단백질을 하기 2-단계 과정으로 정제하였다; 먼저 CHO-S 발현으로부터의 규명된 조직 배양 상충액을 M2 항-FLAG 친화도 크로마토그래피를 사용하여 정제하였다. 이어서, OX40L 단백질을 함유하는 용리된 분획을 크기 배제 크로마토크래피에 적용하고, SDS-PAGE 분석에 의해서 순도에 대해서 평가하고, OD280nm에서의 분광광도계 판독에 의해서 정량화하였다.
재조합 인간 OX40 수용체의
클로닝
발현 및 정제
인간 OX40 수용체의 세포외 도메인을 코딩하는 cDNA를 표준 제한 효소 소화 및 결찰을 사용하여 pREP4 발현 플라스미드(인비트로젠) 내로 클로닝하였다. 구축물은 정제를 돕기 위해서 인간 Fc 부분을 함유하였다. 그의 올바른 서열 조성을 보장하기 위해서 구축물을 시퀀싱하였다.
인간 OX40 수용체를 일시적으로 발현시켜 인비트로젠의 프리스타일(상표명) CHO-S 현탁액 개작된 세포주를 사용하여 재조합 단백질을 생산하였다. 플라스미드를 PEI(폴리에틸렌이민 MW 40000)를 사용하여 세포 내로 형질주입시켰고, 13일의 기간 동안 과성장하도록 방치한 후 정제를 위해서 상청액을 수확하였다. 과성장 과정 동안 세포에 지이 헬쓰케어(GE Healthcare)로부터의 액티(Acti)CHO(상표명) 공급물 A 및 B를 공급하여 생산성을 상승시키고 세포의 수명을 증가시키는 것을 도왔다. 과성장 과정 동안, 샘플을 주기적으로 취하여 세포 성장 및 생존 능력을 모니터링하였다.
Fc 태깅된 OX40 수용체 단백질을 하기 2-단계 과정으로 정제하였다; 먼저 CHO-S 발현으로부터의 규명된 조직 배양 상청액을 단백질 G 친화도 크로마토그래피를 사용하여 정제하였다. 이어서, OX40 수용체 단백질을 함유하는 용리된 분획을 크기 배제 크로마토크래피에 적용하고, SDS-PAGE 분석에 의해서 순도에 대해서 평가하고, OD280nm에서의 분광광도계 판독에 의해서 정량화하였다.
안정하게 형질주입된
MEF
및
CHO
-S 세포 발현 인간
OX40L의
생성
완전 인간 OX40L 서열을 포유동물 발현을 위해서 코돈 최적화하였고(서열번호 173), 3' 및 5' 피기백(piggyBac) 특이적인 말단 반복 서열에 의해서 플랭킹된 CMV 프로모터 하에서 발현 벡터 내로 클로닝하여 세포 게놈 내로의 안정한 통합을 용이하게 하였다(문헌["A hyperactive piggyBac transposase for mammalian applications"; Yusa K, Zhou L, Li MA, Bradley A, Craig NL. Proc Natl Acad Sci U S A. 2011 Jan 25] 참고). 추가로, 발현 벡터는 안정한 세포주 생성을 용이하게 하기 위해서 푸로마이신 또는 네오마이신 선택 카세트를 함유하였다. hOX40L 발현 플라스미드를 제조사 지시서에 따라서 프리스타일 맥스(FreeStyle Max) 형질주입제(인비트로젠)를 사용하여 플라스미드 코딩 피기백 트랜스포사제로 실험실 내에서 유래된 마우스 배아 섬유 모세포(MEF) 세포주(이 세포주를 생성하는 데 사용된 배아는 C57BL6 암컷 마우스에 이종 교배된 129S5로부터 입수함) 및 CHO-S 세포 내로 공동 형질주입시켰다. 형질주입 24시간 후에, 배지에 G418 또는 네오마이신을 보충하고, 배지를 3 내지 4일마다 교환하면서 적어도 2주 동안 성장시켜서 안정한 세포주를 선택하였다. 항-인간 OX40L-PE 컨쥬게이팅된 항체(이바이오사이언스)를 사용하여 유세포 분석법에 의해서 hOX40L의 발현을 평가하였다. 완전 MEF 배지는 10% v/v 태아 소 혈청(fetal bovine serum)(깁코(Gibco))이 보충된 둘베코 모디파이드 이글 배지(Dulbecco's Modified Eagle's Medium)(깁코)로 구성되었다. 완전 CHO-S 배지는 8mM 글루타맥스(깁코)가 보충된 CD-CHO 배지로 구성되었다.
HT1080 발현
OX40R
및
NF
-
카파
리포터 유전자의 생성
완전 인간 OX40 수용체 서열을 포유동물 발현을 위해서 코돈 최적화하였고(서열번호 175), 3' 및 5' 피기백 특이적인 말단 반복 서열에 의해서 플랭킹된 CMV 프로모터 하에서 발현 벡터 내로 클로닝하여 세포 게놈 내로의 안정한 통합을 용이하게 하였다(문헌["A hyperactive piggyBac transposase for mammalian applications"; Yusa K, Zhou L, Li MA, Bradley A, Craig NL. Proc Natl Acad Sci U S A. 2011 Jan 25] 참고). 추가로, 발현 벡터는 안정한 세포주 생성을 용이하게 하기 위해서 푸로마이신 선택 카세트를 함유하였다. hOX40 수용체 발현 플라스미드를 제조사 지시서에 따라서 프리스타일 맥스 형질주입제(인비트로젠)를 사용하여 플라스미드 코딩 피기백 트랜스포사제로 HT1080 세포(ATCC(등록상표) CCL-121) 내로 공동 형질주입시켰다. 형질주입 24시간 후에, 배지에 푸로마이신을 보충하고, 배지를 3 내지 4일마다 교환하면서 적어도 2주 동안 성장시켜서 안정한 세포주를 선택하였다. 항-인간 OX40 수용체-PE 컨쥬게이팅된 항체(알앤디(R&D), 클론 443318)를 사용하여 유세포 분석법에 의해서 OX40 수용체의 발현을 평가하였다. OX40 수용체를 발현하는 안정한 세포주 생성 이후에, 세포를 5개의 반복된 NFkB 전사 인자 결합 부위를 함유하는 pNiFty-2-SEAP 플라스미드(인비보겐(invivogen)) 내로 형질주입시키고, 알칼린 포스파타제를 분비시켰다. 안정한 세포를 선택하고, 배지에 제오신을 첨가하고, 3 내지 4일마다 새로운 배지를 추가하였다. 완전 HT1080 배지는 10% 우태아 혈청(fetal calf serum)이 보충된 MEM으로 구성되었다.
마우스 면역화를 위한
MEF
세포의 제조:
세포 배양 배지를 제거하고, 세포를 1×PBS로 1회 세척하였다. 세포를 트립신으로 5분 동안 처리하여 세포를 조직 배양 표면으로부터 느슨하게 하였다. 세포를 수집하고, 10% 태아 소 혈청(FCS)을 함유하는 완전 배지를 첨가하여 트립신을 중화시켰다. 이어서, 세포를 300xg에서 10분 동안 원심분리하고, 1×PBS 25 mL로 세척하였다. 세포를 카운팅하고, 1XPBS 중에 적절한 농도로 재현탁시켰다.
면역화 절차:
형질전환 키마우스를 hOX40L을 사용하여 CHO-S 세포에 의해서 발현된 가용성 재조합 형태 또는 안정하게 형질주입된 MEF 세포에 의해서 발현된 막 결합 형태로 면역화시켰다.
세포를 사용한 면역화의 경우, 아주반트를 1:1 v/v 비로 세포와 혼합하고, 파이펫팅으로 온화하게 혼합한 후에 복강내로 주사하였다. 단백질을 사용한 면역화의 경우, 아주반트를 1:1 v/v 비로 단백질과 혼합하고, 반복적으로 보텍싱(vortexing)하였다. 모든 마우스를 프라임(primed) 전에 채혈하였고, 이어서 3주 마다 부스팅하였다. 적어도 2주 간격의 적어도 3개의 연속적인 혈액을 수집하였고, ELISA 또는 유세포 분석법 기반 검정법을 사용하여 hOX40L 특이적인 IgG 타이터에 대해서 분석하였다.
CHO
-S 발현된
hOX40L을
사용하여
FACS에
의해서 혈청
타이터를
측정함
FACS 완충액(PBS + 1% w/v BSA + 0.1% w/v NaN3) 중에 용해된, CHO-S hOX40L을 발현하는 세포 또는 비형질주입된 CHO-S 세포를 웰 당 1x105세포 밀도로 96 웰 V-바텀 플레이트(그레이너(Greiner))에 분포시켰다. 세포를 PBS 150μL로 세척하고, 300xg로 3분 동안 원심분리하였다. 상청액을 흡입시키고, PBS 150μL를 첨가하였다. 이러한 세척 단계를 반복하였다. 마우스 혈청의 적정액을 제조하였고, 샘플을 FACS 완충액 중에서 희석하였다. 이어서 이러한 적정액 50μL/웰을 세포 플레이트에 첨가하였다. 면역화로 인한 활성 수준 변화를 측정하기 위해서, 면역화 이전에 각각의 동물로부터의 혈청을 FACS 완충액 중에서 100분의 1로 희석하고, 50μL/웰을 세포에 첨가하였다. 적합한 참고군 항체(항-OX40L 항체MAB10541, 알앤디 시스템즈(R&D systems)) 또는 마우스 IgG1 대조군 항체(시그마(Sigma))를 FACS 완충액(1 내지 9μg/ml) 중에서 희석하고, 세포에 50μL를 첨가하였다. 세포를 4℃에서 30분 동안 인큐베이션시켰다. 세포를 PBS 150μL로 2회 세척하고, 각각의 세척 단계 이후에 원심분리하고, 상청액을 흡입시켰다(300xg으로 3분 동안), 항체 결합을 검출하기 위해서, APC 고트(goat)-항-마우스 IgG(잭슨 이뮤노리서치(Jackson ImmunoResearch))를 FACS 완충액 중에서 500분의 1로 희석하고, 50μL를 세포에 첨가하였다. 세포를 30분 동안 4℃에서 암실에서 인큐베이션시켰다. 세포를 PBS 150μL로 2회 세척하고, 각각의 세척 단계 이후에 원심분리하고, 상청액을 흡입시켰다(300xg으로 3분 동안). 세포를 고정시키기 위해서, 2% v/v 파라폼알데하이드 100μL를 첨가하고, 세포를 30분 동안 4℃에서 인큐베이션시키고, 세포를 300xg에서의 원심분리에 의해서 펠렛화하고, 플레이트를 FACS 완충액 50μL 중에 재현탁시켰다. BD FACS 어레이 장비를 사용하여 유세포 분석법에 의해서 APC 신호 강도(지오민(geomean))를 측정하였다.
재조합
hOX40L을
사용하여
델피아
(
DELFIA
) 면역검정법에 의해서 혈청
타이터를
측정함
반전 OX40L ELISA 프로토콜을 사용하여 마우스 혈청 샘플 중의 타이터를 측정하였다. 항-마우스 IgG 캡쳐 항체(써던 바이오테크(Southern Biotech))(PBS 중에 희석된 4μg/ml, 50μL/웰)를 96웰 저 자가-형광성, 고 단백질 결합 플레이트(코스타(Costar))에 밤새 4℃에서 흡착시켰다. PBS-트윈(0.1% v/v)으로의 세척에 의해서 과량의 IgG를 제거하였고, 웰을 PBS 중의 1% w/v 소 혈청 알부민(BSA, 시그마)으로 1시간 동안 실온에서 차단하였고, 그 후 플레이트를 상기에 기술된 바와 같이 세척하였다. 마우스 혈청의 적정액을 제조하였고, 샘플을 시약 희석제(0.1% w/v BSA/PBS) 중에서 희석하였다. 이어서, 이러한 적정액 50μL/웰을 ELISA 플레이트에 첨가하였다. 면역화로 인한 활성 수준 변화를 측정하기 위해서, 면역화 이전에 각각의 동물로부터의 혈청을 시약 희석제 중에서 100분의 1로 희석하고, 50μL/웰을 ELISA 플레이트에 첨가하였다. 바이오티닐화된 OX40L 결합에 대한 양성 대조군으로서, 1μg/ml로 희석된 항-OX40L 항체(MAB10541, 알앤디 시스템즈)를 50μL로 플레이트에 첨가하였다. 마우스 IgG1 동종형 대조군(시그마)을 음성 대조군으로서 포함시켰고, 시약 희석제 중에서 1μg/ml로 희석시켰고, 50μL/웰을 ELISA 플레이트에 첨가하였다. 일부 예에서, 비-관련 항원으로 면역화된 마우스로부터의 혈청 샘플을 1000분의 1로 희석시켰고, 50μL/웰을 ELISA 플레이트에 첨가하였다. 플레이트를 실온에서 적어도 1시간 동안 인큐베이션시켰다. 인큐베이션 후, 플레이트를 비결합 단백질을 제거하기 위해서 상기에 같이 세척하였다. 이어서, 바이오티닐화된 OX40L(시약 희석제 중의 100ng/mL; 50μL/웰)을 플레이트에 첨가하고, 실온에서 1시간 동안 인큐베이션시켰다. PBS-트윈(0.1% v/v)으로의 세척에 의해서 비결합 바이오티닐화된 OX40L을 제거하였고, 델피아(등록상표) 검정 완충액(퍼킨 엘머(Perkin Elmer)) 중에 희석된 스트렙타비딘-유로퓸3+컨쥬게이트(델피아(등록상표) 검출, 퍼킨 엘머)에 의해서, 또는 시약 희석제 중에 희석된 스트렙타비딘-HRP에 의해서 남아있는 바이오티닐화된 OX40L을 검출하였다.
스트렙타비딘-HRP의 경우, 플레이트를 상기에 기술된 바와 같이 세척하였고, 플레이트에 TMB(시그마) 50μL를 첨가하였다. 이어서, 1M 황산(플루카 아날리티칼(Fluka analytical))을 50μL를 첨가함으로써 반응을 중단시켰다. 앤비젼 플레이트 판독기(EnVision plate reader)(퍼킨엘머) 상에서 450nm에서의 OD를 측정하였다.
스트렙타비딘-유로퓸3의 경우, TBS(트리스 완충 식염수)-트윈(0.1% v/v)으로 플레이트를 세척하였고, 200μL/웰 델피아 향상 용액(DELFIA Enhancement solution)(퍼킨엘머)을 플레이트에 첨가하였다. 엔비젼 플레이트 판독기(퍼킨엘머) 상에서 615nm에서 시간-분해 형광을 측정하였다. 유로퓸 수로서 형광 데이터를 플로팅하였다.
뮤린
조직 단리 및 제조:
면역화된 마우스로부터 비장을 절제하고, 1×PBS 중에서 세척하고, 추가 가공까지 얼음에서 유지시켰다. 1×PBS(인비트로젠) 및 3% 열-불활성화 FBS(인비트로젠)를 함유하는 완충액 중에서 조직을 제조하였다. 45μm 스트레인너(strainer)(비디 팔콘(BD Falcon))를 통해서 조직을 담그고, 30mL 3%FBS/PBS 완충액으로 헹구고, 그 후에 700g으로 10분 동안 4℃에서 원심분리함으로써 비장세포를 분산시켰다. 적혈구를 제거하기 위해서, 펠렛화된 비장세포를 적혈구 용해 완충액(시그마) 4mL 중에 재현탁시켰다. 4분의 인큐베이션 후에, 3%FBS/1×PBS 완충액의 첨가에 의해서 용해 반응을 중단시켰다. 세포 덩어리를 45μm 스트레인너로 여과하였다. 남아있는 비장세포를 추가 절차를 위해서 펠렛화하였다.
하이브리도마
융합
KM055 실험의 경우, 펠렛화된 비장세포를 임의의 선택 또는 밤새 CpG 자극 없이 직접 융합으로 진행시켰다. KM040 실험의 경우, B-세포를 MACS(등록상표) 분리 시스템을 사용하여 양성 선택 방법에 적용하였다. 세포를 1×107세포 당 80μL 3% FBS/PBS 완충액 중에 재현탁시켰고, 그 후에 항-마우스 IgG1 및 항-마우스 IgG2a+b 마이크로비드(MicroBead)(밀테니이 바이오테크(Miltenyi Biotec))를 첨가하고 15분 동안 4℃에서 인큐베이션시켰다. 이어서, 세포/마이크로비드 혼합물을 자기 MACS 분리기 중에 놓인 미리 습윤된 LS 칼럼에 적용하고, 3% FBS/PBS 완충액으로 세척하였다. IgG 양성 세포를 3% FBS/PBS 완충액 중의 표지된 칼럼-결합 분획 중에 수집하였다.
KM040 실험의 경우, 풍부해진 B-세포를 CpG로 밤새(최종 농도 25μM) 처리하고, 다음 날 BSA 융합 완충액(0.3M D-소르비톨, 0.11mM 아세트산 칼슘 수화물, 0.5mM 아세트산 마그네슘 사수화물 및 0.1% BSA(v/w), pH 7.2로 조정) 중에서 1회 세척하였다. KM055 실험의 경우, 적혈구 용해로부터의 펠렛화된 비장세포를 조직을 제조한 같은 날에 BSA 융합 완충액 중에서 1회 세척하였다. 이 시점 이후에 두 실험 모두에 대해서 동일한 방식으로 융합을 진행하였다. 세척된 세포를 BSA 융합 완충액 200μL 중에 재현탁시키고, 세포 수를 측정하였다. BSA 융합 완충액으로 2회 세척한 것을 제외하고는 SP2/0 세포를 동일한 방식으로 처리하였다. B-세포를 BTX ECM 2001 일렉트로 셀 매니퓰레이터(Electro Cell Manipulator)(하바드 어패러터스(Harvard Apparatus))를 사용하여 전기융합에 의해서 3:1의 비로 SP2/0 골수종 세포와 융합시켰다. 각각의 융합체를 회수 배지(둘베코 모디파이드 이글 배지 - 고 글루코스(페놀 레드 없음, L-G 없음), OPI(시그마), L-글루타맥스(깁코), 20% FBS(깁코, 하이브리도마를 위해서 배취-시험됨) 및 2-머캅토에탄올 함유) 중에서 밤새 유지시켰다. 마지막 날에, 세포를 펠렛화하고, 9부의 반-고체 배지(클로나셀-HY-하이브리도마 선택 배지 D(ClonaCell-HY Hybridoma Selection Medium D), 스템셀 테크놀로지스(Stemcell Technologies))에 1부의 회수 배지로 재현탁시키고, 이어서 10cm 페트리 디쉬 상에 시딩하였다. 결장을 12일 이후에 96-웰 플레이트에 피킹(picking)하고, 스크리닝 전에 추가 2 내지 3일 동안 배양시켰다.
실시예
2
하이브리도마
상청액
스크리닝
하이브리도마 클론의 생성 후에, 하이브리도마 상청액을 순차적인 1차 및 2차 스크린으로 평가하였고, CHO 발현된 hOX40L에 대한 항체 결합 및 수용체 중화 활성을 기초로 적절한 하이브리도마 클론을 선택하였다(물질 및 방법의 상세사항 참고)(표 1).
1차 스크린을 위해서, 본 발명자들은 하기 선택 기준을 고안하였다: 상청액 중에 존재하는 항체가 세포 표면 상에 발현된 네이티브 디스플레이된 hOX40L에 결합할 수 있는 경우 하이브리도마 클론을 함유하는 웰을 선택하였다. 이러한 검정법은 세포 표면 상에 hOX40L을 발현하는 CHO-S 세포를 플레이팅하고, 이어서 하이브리도마 상청액과 함께, 그 다음 형광성 검출 항체와 함께 인큐베이션시킴으로써 설정될 수 있다. 상청액 중의 항-OX40L 항체의 존재는 적절한 형광을 판독할 수 있는 플레이트 판독기를 사용하여 판독될 수 있다. 추가로, 본 발명자들은 HTRF(균일 시간 분해 형광) 검정법을 사용하여 재조합 방식으로 발현된 인간 OX40L에 대한 결합에 대해서 하이브리도마 상청액을 평가하였다. 본 발명자들은 또한 하이브리도마 상청액이 인간 OX40R Fc에 대한 인간 재조합 OX40L의 결합을 감쇠시키는 능력을 갖는지를 측정하였다. 이어서, 상기에 언급된 3회의 1차 스크린 검정법으로부터의 데이터를 사용하여, 특정 선택 기준(추가로 하기 상세한 설명 참고)을 충족시키는 클론을 체리-피킹하고, 2차 스크린으로 옮겼는데, 여기서는 그의 수용체, OX40 수용체(aka CD134)에 대한 hOX40L 결합을 중화시키는 각각의 항체의 능력이 측정되었다. 본 발명자들은 수용체 중화 HTRF 검정법 및 유세포 분석법-기반 수용체 중화 검정법을 사용하여 이를 평가하기로 결정하였다. 마지막으로, 본 발명자들은 재조합 삼량체 인간 OX40L에 대한 항체의 겉보기 친화도뿐만 아니라 레서스 원숭이 OX40L에 대한 교차-반응성을 평가하기 위해서 SPR에 의해서 하이브리도마 상청액을 분석하기로 결정하였다.
하이브리도마 상청액 중의 항체가 높은 겉보기 친화도를 갖고, 재조합 레서스 원숭이 OX40L과 교차-반응되면서, hOX40L에 결합하는 경우 항체를 제2 히트로서 정의하였다. 추가로, 상청액 중의 항체는 HTRF 또는 유세포 분석법 기반 검정법에서 그의 수용체, 즉, OX40 수용체(aka CD134)에 대한 OX40L 결합을 중화시키는 능력을 나타내야만 했다.
물질 및 방법
1차 스크린 - 세포 발현된 인간
OX40L에
대한 결합
하이브리도마 세포로부터 수집된 상청액을 시험하여 CHO-S 세포의 표면 상에서 발현된 hOX40L에 결합하는 분비된 항체의 능력을 평가하였다. CHO-S hOX40L 결합을 측정하기 위해서, 세포를 10% v/v FBS(깁코)가 보충된 F12 배지(깁코) 중에서 투명한 바닥의 조직 배양액 처리된 384-웰 플레이트(코스타 또는 브랜드(BRAND)) 중에 2×104세포/웰로 플레이팅하고, 밤새 배양하였다. 배양 배지를 384-웰 검정법 플레이트로부터 제거하였다. 하이브리도마 유지 배지(HMM) 중에 희석된 적어도 40μL의 하이브리도마 상청액 또는 양성 대조 항-인간 OX40L 참고군 항체(최종 농도 1μg/ml) 또는 동종형 IgG1 대조군 항체(일부 예에서 Cm7이라 칭함, 시그마 M9269, 최종 농도 1μg/ml)를 각각의 웰에 첨가하였다. 하이브리도마 유지 배지는 1× 글루타맥스(깁코), 20% v/v FBS(깁코), 0.05mM β-머캅토에탄올, 1×HT 보충액(깁코), 및 1×페니실린/스트렙토마이신(깁코)이 보충된 어드밴스트(Advanced) DMEM(깁코)로 구성되었다. 플레이트를 1시간 동안 4℃에서 인큐베이션시켰다. 배양 배지를 흡입시키고, FACS 완충액(PBS+1% w/v BSA+0.1% w/v NaN3) 중에 용해된, 0.2μM DRAQ5(바이오스타터스(Biostatus))가 보충된 1000ng/mL에서, 50μL의 고트 항-마우스 알렉사 플로어(Alexa Fluor) 790(잭슨 이뮤노리서치, 115-655-071)을 첨가하였다. 플레이트를 1시간 동안 4℃에서 다시 인큐베이션시켰다. 상청액을 흡입시키고, 25μL의 4% v/v 파라폼알데하이드를 첨가하고, 플레이트를 실온에서 15분 동안 인큐베이션시켰다. 플레이트를 100μL PBS로 2회 세척하고, 이어서, 세척 완충액을 완전히 제거하였다. 오디세이 인프라레드 이미징 시스템(Odyssey Infrared Imaging System(LI-COR(등록상표))을 사용하여 플레이트를 스캐닝하여 형광 강도를 판독하였다. 항-마우스 결합(800nm 채널)을 LI-COR(등록상표) 추천 알고리즘에 따라서 세포수(700nm 채널)에 대해서 정규화하였다. % 효과를 하기에 상술된 바와 같이 계산하였다(식 1). 1μg/ml의 최종 검정 농도에서 참고군 항체를 사용하여 총 결합을 정의하였다. 1μg/ml의 최종 검정 농도에서 마우스 IgG1 동종형 대조군(시그마)을 사용하여 비 특이적인 결합을 정의하였다. % 효과가 5% 이상인 경우 웰을 히트로서 정의하였다.
식
1: 1차
스크린(LI-
COR
) 및
HTRF로부터의
%
효과의 계산
(800% 흡입값(LI-COR) 또는 665/620nm 비(식 2 참고)(HTRF) 사용
비-특이적인 결합 = 동종형 대조군 마우스 IgG1 또는 HMM 또는 완충액을 함유하는 웰로부터의 값
총 결합(결합 HTRF 및 LICOR) = 참고군 항체를 함유하는 웰로부터의 값
총 결합(OX40L/OX40RFc 검정법) = OX40L 및 OX40RFc
1차 스크린: 재조합 인간
OX40L에
대한 결합:
CHO-S 발현된 OX40L에 대한 결합에 대한 스크리닝과 동시에, 하이브리도마 웰로부터 수집된 상청액을 또한 재조합 단백질로서 발현된 hOX40L(실험실에서 제조됨, 실시예 1의 상세사항 참고)에 결합하는 분비된 항체의 능력을 평가하기 위해서 시험하였다. 재조합 hOX40L에 대한 분비된 항체의 결합은 바이오티닐화된 hOX40L을 사용하여 HTRF(등록상표)(균일 시간 분해 형광, 시스바이오(CISBIO)) 검정법 포맷에 의해서 식별하였다. 5μL의 하이브리도마 상청액을 백색 384 웰 저 부피 비결합 표면 폴리스타이렌 플레이트(그레이너)에 옮겼다. 이어서, HTRF 완충액(PBS(시그마) + 0.53M KF(시그마) + 0.1% w/v BSA(시그마) 중에 희석된 5μL의 바이오티닐화된 hOX40L(작업 농도 20nM)을 첨가하였다. 최종 희석 1:400을 위해서 HTRF 검정 완충액 중에 1:100 희석된 스트렙타비딘 D2(시스바이오) 및 최종 희석 1:400을 위해서 HTRF 검정 완충액 중에 1:100 희석된 유로퓸 크립테이트(europium cryptate)(시스바이오)로 표지된 고트 항-마우스 IgG(써던 바이오테크)의 조합된 검출 시약 5μL를 첨가하였다. 유로퓸 크립테이트로 표지된 고트 항-마우스 IgG(써던 바이오테크)의 농도는 배취 의존적이었고, 일부 경우에 1:1000의 희석을 수행하여 1:4000의 최종 검정 농도를 달성하였다. 총 검정 부피를 20μL로 조정하기 위해서, HTRF 검정 완충액 5μL를 모든 웰에 첨가하였다. 비-특이적인 결합을 정의하기 위해서 양성 대조군 항체 또는 하이브리도마 배지의 첨가를 HTRF 검정 완충액 또는 HMM으로 대체하였다. 플레이트를 암실에서 3시간 동안 인큐베이션시켰고, 그 후에 엔비젼 플레이트 판독기(퍼킨 엘머)를 사용하여 620nM 및 665nm 방출 파장에서 시간 분해 형광을 판독하였다. HTRF(등록상표) 검정법 기술의 보다 상세한 내용은 문헌[Mathis(1995) Clinical Chemistry 41(9), 1391-1397]에서 찾아볼 수 있다. 각각 식 2 및 식 1에 따라서 각각의 샘플에 대한 665/620 비 및 % 효과를 계산함으로써 데이터를 분석하였다.
식
2: 665
/620 비
665/620 비 = (샘플 665/620nM 값) x 10000
KM040-1 및 KM055-1로부터 유래된 클론의 경우, 본 발명자들은 20% 효과 이상의 선택 기준을 적용하여 표 1에 기술된 바와 같은 재조합 hOX40L 결합으로부터 히트를 또한 정의하였다.
1차 스크린: 인간
OX40L
/인간
OX40R
Fc
결합 검정법:
하이브리도마 웰로부터 수집된 상청액이 OX40RFc에 대한 OX40L의 결합을 억제하였지를 측정하기 위해서, 분비된 항체를 OX40L/OX40RFc 결합 HTRF 검정법으로 시험하였다. 하이브리도마 상청액 5μL를 백색 384 웰 저 부피 비-결합 표면 폴리스타이렌 플레이트(그레이너)로 옮겼다. 바이오티닐화된 OX40L을 HTRF 검정 완충액 중에 2.4nM의 작업 농도로 희석하고, 5μL를 첨가하였다. 이어서, OX40RFc를 4.8nM의 작업 농도로 희석하고, 5μL를 첨가하였다. OX40RFc를 검정 완충액 또는 HMM으로 대체함으로써 비-특이적인 결합을 정의하였다. 스트렙타비딘 크립테이트(시스바이오) 및 항-인간 Fc D2(시스바이오)를 HTRF 검정 완충액 중에 각각 1:100 및 5nM의 작업 농도로 희석하였다. 플레이트를 밀폐하고, 광으로부터 보호하고, 실온에서 3시간 동안 인큐베이션시키고, 그 후에 엔비젼 플레이트 판독기(퍼킨 엘머)를 사용하여 620nM 및 665nm 방출 파장에서 시간 분해 형광을 판독하였다. 각각 식 2 및 식 5에 따라서 각각의 샘플에 대해서 665/620 비 및 % 효과를 계산함으로써 데이터를 분석하였다.
KM040-1 및 KM055-1로부터 유래된 클론의 경우, 본 발명자들은 90% 이하의 OX40L에 대한 OX40 수용체 Fc 결합의 검정법 신호의 선택 기준을 적용하여 웰을 표 1에 기술된 바와 같은 히트로서 또한 정의하였다.
2차 스크린: 세포 발현된 인간
OX40L
및 재조합 인간
OX40L에
대한 결합
1차 스크린 선택 기준을 사용하여 선택된 웰이 본 발명자들이 설정한 요구되는 특징을 갖는지를 측정하기 위해서, 다수의 검정법을 수행하였다. 1차 스크리닝으로부터 히트로서 선택된 하이브리도마 클론을 3일 동안 배양하고, 하이브리도마 세포로부터 수집된 상청액을 시험하여 분비된 항체가 CHO-S 발현된 hOX40L에 결합하는지, 일부 경우에는 비형질주입된 CHO-S 세포에 결합하는지를 평가하였고, 그리고 그들이 CHO-S hOX40L에 대한 재조합 OX40R Fc 결합을 중화시키는지를 평가하였고, 재조합 바이오티닐화된 hOX40L에 대한 OX40R 결합을 중화시키는 능력을 평가하였다.
CHO
-S 발현된
hOX40L의
결합 및 수용체 중화:
FACS 완충액(PBS + 1% w/v BSA + 0.1% w/v NaN3) 중에 희석된, hOX40L을 발현하는 CHO-S 세포 또는 비형질주입된 CHO-S 세포를 웰 당 1x105세포 밀도로 96 웰 V-바텀 플레이트(그레이너)에 분포시켰다. 세포를 PBS 150μL로 세척하고, 300xg로 3분 동안 원심분리하였다. 상청액을 흡입시키고, PBS 150μL를 첨가하였다. 이러한 세척 단계를 반복하였다.
하이브리도마 상청액 또는 FACS 완충액 중에 희석된 하이브리도마 상청액으로부터의 정제된 항체 25μL를 세척된 세포에 첨가하고, 10 내지 15분 동안 인큐베이션시켰다. 참고군 항체 또는 마우스 IgG1 대조군 항체(시그마)를 FACS 완충액 중에 20μg/ml로 희석하고, 25μL를 세포에 첨가하였다. 이어서, FACS 완충액 중에 1000ng/mL로 희석된 인간 OX40R Fc(실험실 생산) 25μL를 웰에 첨가하였다. 세포를 4℃에서 30분 동안 인큐베이션시켰다.
세포를 PBS 150μL로 2회 세척하고, 각각의 세척 단계 이후에 원심분리하고, 상청액을 흡입시켰다(300xg으로 3분 동안 원심분리),
항체 및 수용체 결합을 검출하기 위해서, FACS 완충액 중에 500분의 1로 희석된, 고트 항-인간 IgG-PE(잭슨 이뮤노리서치) 및 APC 항-마우스 IgG(잭슨 이뮤노리서치) 50μL를 세포에 첨가하였다. 세포를 30분 동안 4℃에서 암실에서 인큐베이션시켰다.
세포를 PBS 150μL로 2회 세척하고, 각각의 세척 단계 이후에 원심분리하고, 상청액을 흡입시켰다(300xg으로 3분 동안 원심분리).
세포를 고정시키기 위해서, 2% v/v 파라폼알데하이드 100μL를 첨가하고, 세포를 30분 동안 4℃에서 인큐베이션시키고, 세포를 300xg에서의 원심분리에 의해서 펠렛화하고, 플레이트를 FACS 완충액 50μL 중에 재현탁시켰다. BD FACS 어레이 장비를 사용하여 유세포 분석법에 의해서 PE 및 APC 신호 강도(지오민)를 측정하였다.
식 1에 기술된 바와 같이 지오민 형광을 사용하여 대조군 결합 %를 계산하였고, 여기서 총 결합은 참고군 항체로서 10μg/ml에서 정의되었고, 비-특이적인 결합은 마우스 IgG1 항체로서 10μg/ml에서 정의되었다. 식 3을 사용하여 % 수용체 결합을 계산하였다.
식 3: 수용체 결합(
FACS
)
%
지오민 형광 기준
비-특이적인 결합 = 항체 없음, 수용체 없음
총 결합 = 수용체(OX40R)만 결합(억제제 없음) + 10μg/ml에서의 동종형 대조군
2차 스크린 -
HTRF
리간드/수용체 중화
1차 스크린으로부터 식별된 항체가 OX40RFc에 대한 OX40L 결합을 중화시키는지를 측정하기 위해서, 인간 OX40L/인간 OX40R Fc 결합 검정법을 1차 스크린에 대해서 기술된 바와 같이 수행하였다.
플레이트를 암실에서 3시간 동안 인큐베이션시켰고, 그 후에 엔비젼 플레이트 판독기(퍼킨 엘머)를 사용하여 620nM 및 665nm 방출 파장에서 시간 분해 형광을 판독하였다. HTRF(등록상표) 검정법 기술의 보다 상세한 내용은 문헌[Mathis(1995) Clinical Chemistry 41(9), 1391-1397]에서 찾아볼 수 있다. 식 4에 기술된 바와 같이 델타 F를 계산하고, 식 5에 따라서 각각의 샘플에 대해서 수용체 %를 계산함으로써 데이터를 분석하였다.
식 4:
%
델타F의
계산
식 5: 수용체 결합(
HTRF
)
%
% 델타F(식 4) 또는 665/620 비(식 2)의 계산 기준
비 특이적인 결합 = HMM 또는 완충액 + OX40L(수용체 없음)
총 결합 = 수용체(OX40R) 및 OX40L(억제제 없음)
2차 스크리닝으로부터의 히트 기준 선택:
히트의 패널을 결합 및 중화 검정법을 기준으로 선택하였다. 본 발명자들은 FACS에 의해서 CHO-S OX40L 세포에 대한 유의한 결합 및 CHO-S 세포에 대한 비결합으로서 CHO-S OX40L 결합 검정법에서의 히트를 정의하였다. 히트는 재조합 OX40L(HTRF)에 대한 OX40RFc 결합을 유의하게 감쇠시키고, CHO 세포 상에 발현된 hOX40L에 대한 OX40RFc 결합을 유의하게 감쇠시키는 능력을 갖는 것으로서 추가로 정의되었다. 데이터를 표 1에 요약한다. SPR에 의한 겉보기 친화도 측정법을 또한 고려하였다.
실시예
3
항체 리드(lead) 특징
스크리닝을 기초로, 선택된 웰을 확장시키고, 뮤린/인간 키메릭 항체를 표준 단백질 G 기반 친화도 크로마토그래피 정제(하기 방법 참고)를 사용하여 정제하였다. 항체를 다양한 검정법에 적용하여 그 수용체 OX40R에 대한 hOX40L 결합을 차단하는 그의 능력, 뿐만 아니라 높은 겉보기 친화도로 인간과 레서스 원숭이 OX40L에 결합하는 각각의 항체의 능력을 평가하였다. 어느 항체가 가장 우수한지를 해독하기 위해서, 선택된 클론을 OX40L/OX40RFc HTRF 검정법을 사용하여 시험하였고, OX40L은 1차 인간 T-세포로부터의 IL2 방출을 유도하였다.
물질 및 방법:
하이브리도마
상청액으로부터의
항체의 정제:
항체를 단백질 G 친화도 크로마토그래피를 사용하여 정제하였다. 항체를 IgG 용리 시약(피어스(Pierce))을 사용하여 단백질 G 배지로부터 용리하고, 용리된 항체를 사용 전에 PBS로 완충액 교체하였다. SDS-PAGE 분석에 의해서 항체 순도를 평가하고, OD280nm에서의 분광광도계 판독에 의해서 정량화하였다.
하이브리도마 상청액으로부터 정제된 항체의 결합을 본 명세서에서 기술된 바와 같이 수행하였다.
HTRF
리간드/수용체 중화:
검정법에서 IC50 값에 의해서 측정되는 바와 같은 클론 효력을 설정하기 위해서 억제제의 적정과 함께 하기 방법을 수행하였다. 하이브리도마로부터 정제된 항체를 HTRF 검정 완충액 중에서 용해시킴으로써 적정하고, 이 적정액 5μL를 백색 384 웰 저 부피 비결합 표면 폴리스타이렌 플레이트(그레이너)에 옮겼다. 바이오티닐화된 OX40L을 HTRF 검정 완충액 중에 2.4nM의 작업 농도로 희석하고, 5μL를 첨가하였다. 이어서, OX40RFc를 4.8nM의 작업 농도로 희석하고, 5μL를 첨가하였다. OX40RFc를 검정 완충액 또는 HMM으로 대체함으로써 비-특이적인 결합을 정의하였다. 스트렙타비딘 크립테이트(시스바이오) 및 항-인간 Fc D2(시스바이오)를 HTRF 검정 완충액 중에 각각 1:100 및 5nM의 작업 농도로 희석하였다. 플레이트를 밀폐하고, 광으로부터 보호하고, 실온에서 3시간 동안 인큐베이션시키고, 그 후에 엔비젼 플레이트 판독기(퍼킨 엘머)를 사용하여 620nM 및 665nm 방출 파장에서 시간 분해 형광을 판독하였다. 식 4에 기술된 바와 같이 델타 F를 계산하고, 식 5 또는 일부 경우에는 식 6에 따라서 각각의 샘플에 대해서 수용체 %를 계산함으로써 데이터를 분석하였다. 4-파라미터 로지스틱식(식 7)을 사용한 곡선 피팅에 의해서 그래프패드 프리즘(GraphPad Prism) 소프트웨어를 사용하여 IC50 값을 측정하였다.
식 6: 수용체 결합(
HTRF
)
%
% 델타F(식 8)의 계산 기준
총 결합 = 수용체(OX40R) 및 OX40L(억제제 없음)
식
7: 4
파라미터
로지스틱
계산
Y = 하부 +(상부-하부)/(1+10^((로그IC50-X)*힐슬로프(HillSlope)))
X = 농도의 로그값
Y = 특이적인 결합(식 6)
상부 및 하부 = Y와 동일한 단위의 편평부(특이적인 결합)
X와 동일한 단위의 로그 IC50. Y는 S자 형상으로 하부에서 시작하여 상부로 상승함. 특이적인 결합은 X가 증가함에 따라서 감소함.
HTRF
리간드/수용체 중화 검정법에서의 완전 인간 재조합 항-
OX40L
항체의 프로파일링
재조합 방식으로 발현된 완전 인간 정제된 IgG가 OX40RFc에 대한 인간 OX40L 결합을 억제하는지를 측정하기 위해서, 하기 방법을 수행하였다. 검정법에서 IC50 값에 의해서 측정되는 바와 같은 클론 효력을 설정하기 위해서 완전 인간 정제된 IgG 또는 다른 억제제를 시험하였다. 재조합 방식으로 발현되고 정제된 항체를 HTRF 검정 완충액 중에 희석함으로써 적정하고, 이러한 적정액 5μL를 백색 384 웰 저 부피 비-결합 표면 폴리스타이렌 플레이트(그레이너)로 옮겼다. 바이오티닐화된 OX40L을 HTRF 검정 완충액 중에 2.4nM의 작업 농도로 희석하고, 5μL를 첨가하였다. 이어서, AF647로 직접 표지된 OX40RFc를 10nM의 작업 농도로 희석하고, 5μL를 첨가하였다. OX40RFc-AF647을 검정 완충액 또는 HMM으로 대체함으로써 비-특이적인 결합을 정의하였다. 스트렙타비딘 크립테이트(시스바이오)를 HTRF 검정 완충액 중에 1:100의 작업 농도로 희석하고, 플레이트의 모든 웰에 5μL를 첨가하였다. 플레이트를 밀폐하고, 광으로부터 보호하고, 실온에서 3시간 동안 인큐베이션시키고, 그 후에 엔비젼 플레이트 판독기(퍼킨 엘머)를 사용하여 620nM 및 665nm 방출 파장에서 시간 분해 형광을 판독하였다. 식 4에 기술된 바와 같인 델타 F를 계산하고, 식 5 또는 일부 경우에는 식 6에 따라서 각각의 샘플에 대해서 수용체 %를 계산함으로써 데이터를 분석하였다. 4-파라미터 로지스틱식(식 7)을 사용한 곡선 피팅에 의해서 그래프패드 프리즘 소프트웨어를 사용하여 IC50 값을 측정하였다(도 1).
1차
단리된
T-세포로부터의 재조합
OX40L
유도된 IL2 방출에 대한 항-OX40L 항체의 효과를 측정함
재조합 인간 OX40L(실험실 생산)을 배양 배지 중에 400ng/mL 농도로 희석하고, 50μL를 조직 배양액 처리된 96 웰 플레이트(코스타)에 첨가하였다. 항-OX40L 항체 또는 적절한 종의 동종형 대조군(시그마 또는 실험실 생산)을 배양 배지 중에서 96 웰 플레이트(그레이너) 내에서 적정하고, 적정액 50μL를 OX40L 50μL를 함유하는 96 웰 플레이트로 옮겼다. 항체 적정액을 재조합 OX40L과 함께 30분 동안 실온에서 인큐베이션시킨 후 CD3 양성 T-세포를 첨가하였다.
밀도 구배 원심분리에 의해서 피콜-플라크 플러스(Ficoll-Paque plus)(지이 헬쓰케어)를 사용하여 PBMC를 류코리덕션 시스템 챔버(leukoreduction system chamber: NHSBT)로부터 단리시켰다. CD3 양성 세포(T-세포)를 제조사의 제안에 따른 자기 마이크로비드(밀테니이 바이오테크)를 사용하여 음성 선택에 의해서 인간 PBMC로부터 단리시켰다. 단리된 세포를 300xg/5분으로 원심분리하고, 배양 배지(배양 배지는 RPMI(깁코) + 10% v/v FBS 또는 RPMI + 5% v/v 인간 AB 혈청으로서 정의되었음) 중에 재현탁시키고, 세포 현탁액 50μL를 재조합 OX40L을 함유하는 96 웰 플레이트에 첨가하고, 항체를 적정하여 2×105세포/웰의 최종 농도를 달성하였다.
이어서, 8μg/ml의 PHA 50μL를 모든 웰에 첨가하여 최종 검정 농도 2μg/ml를 달성하였다. 세포를 37℃에서 3일 동안 인큐베이션시키고, 그 후에 상청액을 수확하고, IL-2 농도에 대해서 분석하였다. 억제제의 부재 하에서 OX40L 자극에 의해서 최대 IL-2 방출이 정의되었다. 배양 배지 단독(OX40L 없음)에 의해서 최대 IL-2 방출이 정의되었다.
상청액 중의 IL-2 수준을 제조사의 제안에 따라서 인간 IL-2 듀오세트 ELISA(Duoset ELISA) 키트(알앤디 시스템즈)를 사용하여 측정하였다. IL-2 포획 항체(PBS 중에 희석된 4μg/ml, 50μL/웰)를 96웰 저 자가-형광성, 고 단백질 결합 플레이트(코스타)에 밤새 4℃에서 흡착시켰다. PBS-트윈으로의 세척에 의해서 과량의 IgG를 제거하였고, 웰을 PBS 중의 1% 소 혈청 알부민(BSA)으로 1시간 동안 실온에서 차단하였고, 그 후 플레이트를 상기에 기술된 바와 같이 세척하였다. 이어서, 컨디셔닝된 배양 배지 50μL/웰을 첨가하고, IL-2 표준품(2000pg/mL로부터, 1:2 희석)을 또한 ELISA 대조군으로서 ELISA 플레이트에 첨가하고, 플레이트를 실온에서 적어도 1시간 동안 인큐베이션시켰다.
인큐베이션 후, 플레이트를 상기에서와 같이 비결합 단백질을 제거하기 위해서 세척하였다. 이어서, 바이오티닐화된 IL-2 검출 Ab(시약 희석제(0.1% BSA/PBS) 중의 200ng/mL; 50μL/웰)를 플레이트에 첨가하고, 실온에서 1시간 동안 인큐베이션시켰다. PBS-트윈(0.1% v/v)으로의 세척에 의해서 비결합 검출 항체를 제거하였고, 스트렙타비딘-유로퓸3+컨쥬게이트(델피아(등록상표) 검출, 퍼킨엘머)에 의해서 남아있는 바이오티닐화된 항체를 검출하였다. 엔비젼 플레이트 판독기(퍼킨엘머) 상에서 615nm에서 시간-분해 형광을 측정하였다. 유로퓸 수 또는 제조사의 제안에 따른 선형 회귀에 의해서 표준 곡선으로부터 계산된 IL-2 방출의 농도로서 형광을 플로팅하였다. 4-파라미터 로지스틱식(식 7)을 사용한 곡선 피팅에 의해서 그래프패드 프리즘 소프트웨어를 사용하여 IC50 값을 측정하였다.
표면
플라즈몬
공명 분석:
프로테온(상표명) XPR36 어레이 시스템(바이오라드)을 사용하여 SPR을 수행하였다. 항-마우스 IgG(지이 헬쓰케어 BR-1008-38)를 아민 커플링을 사용하여 GLM 바이오 센서 표면 상에 고정화시키고, 이어서 표면을 1M 에탄올아민을 사용하여 차단시켰다. 시험 항체를 이 표면 상에 포획하고, 재조합 hOX40L(인간 및 레서스)를 256nM의 단일 농도로 사용하였고, 완충액 주입(즉, 0nM)을 사용하여 참고로 결합 센서그램(sensorgram)을 2배로 하여 기준선 드리프트(drift) 및 주사 아트팩트(artefact)를 제거하였다. 프로테온 XPR36 분석 소프트웨어에 고유한 1:1 모델을 사용하여 OX40L-항체 상호작용에 대한 겉보기 친화도를 측정하였다. 유동 완충액으로서 HBS-EP(테크노바(Teknova))를 사용하여 검정법을 진행하였고, 25℃에서 수행하였다.
실시예
4
리드 항체 후보군의 서열 회수
리드 후보군의 선택 및 특징분석 후에, 포워드 프라이머와 리버스 프라이머의 혼합물을 사용하는 RT-PCR을 사용하여 이의 완전 인간 가변 도메인을 회수하였다. 항체를 인간 IgG4 골격(IgG4-PE)으로 재포맷팅하고, CHO-S 세포 중에서 일시적 발현 시스템을 사용하여 발현시켰다. 모든 서열의 요약이 서열 목록에 나타나 있다.
하이브리도마
세포로부터의 RNA 단리:
트라이졸(TRIzol)(상표명) 시약(인비트로젠)을 사용하여 하이브리도마 세포로부터 전체 RNA를 추출하였다. 단리된 RNA의 양 및 질을 분광광도계로 분석하였다.
RT-
PCR에
의한 항체 가변 도메인 회수:
선택된 클론을 전체 RNA의 제조를 위해서 사용하였고, 전체 RNA를 RT-PCR 반응에서 사용하여 중쇄 V-영역을 회수하였다. IgG 특이적인 리버스 프라이머 및 Ig 리더 서열 특이적인 포워드 프라이머 세트 또는 대안적으로 IgG 특이적인 리버스 프라이머 및 Ig 5' 미번역 영역(UTR) 서열 특이적인 포워드 프라이머 세트를 중쇄를 위해서 사용하였다. 카파 불변 영역 특이적인 리버스 프라이머 및 카파 리더 서열 특이적인 포워드 프라이머 세트 또는 대안적으로 카파 불변 영역 특이적인 리버스 프라이머 및 카파 5'UTR 서열 특이적인 포워드 프라이머 세트를 카파 OX40L 쇄를 위해서 사용하였다. 아가로스 겔 전기영동에 의해서 RT-PCR 산물을 분리하였고, 예측된 크기의 DNA를 포워드 및 리버스 방향에서 시퀀싱하였다. 대안적으로, RT-PCR 산물을 클로닝 벡터 내로 서브클로닝하고, 개별 집단의 DNA를 시퀀싱을 위해서 제출하였다.
재조합 항체의
클로닝
표준 제한 효소 소화 및 결찰을 사용하여 mAb 10A7의 중쇄 가변 영역을 코딩하는 DNA를 인간 IgG1 불변 영역을 갖는 프레임의 pREP4 발현 플라스미드(인비트로젠) 내로 클로닝하고, mAb 10A7의 경쇄 가변 영역을 코딩하는 DNA를 인간 카파 불변 영역을 갖는 프레임의 pREP4 발현 플라스미드 내로 클로닝하였다.
표준 제한 효소 소화 및 결찰을 사용하여 인간 IgG4-PE 불변 영역을 갖는 프레임의 mAb 10A7 및 2D10의 서열을 코딩하는 중쇄 가변 영역을 포유동물 발현을 위해서 코돈 최적화하고, pXC-18.4 발현 플라스미드(론자) 내로 클로닝하고, 인간 카파 불변 영역을 갖는 프레임의 mAb 10A7 및 2D10의 경쇄 코딩 서열을 포유동물 발현을 위해서 코돈 최적화하고, pXC-17.4 발현 플라스미드(론자) 내로 클로닝하였다. 중쇄 및 경쇄의 동시 발현을 위해서, 표준 제한 효소 소화 및 결찰을 사용하여 벡터 pXC-17.4 및 pXC-18.4를 하나의 단일 벡터로 융합시켰다.
모든 구축물을 시퀀싱하여 이의 올바른 서열 조성을 보장하였다.
OX40L
항체의 일시적인 발현
항체를 일시적으로 발현시켜서 인비트로젠의 프리스타일(상표명) CHO-S 현탁액 개작된 세포주를 사용하여 재조합 단백질을 생산하였다. PEI(폴리에틸렌이민 MW 40000)를 사용하여 플라스미드를 세포 내로 형질주입시키고, 13일의 기간 동안 과성장하도록 방치한 후 정제를 위해서 상청액을 수확하였다. 과성장 과정 동안 세포에 지이 헬쓰케어로부터의 액티CHO(상표명) 공급물 A 및 B를 공급하여 생산성을 상승시키고 세포의 수명을 증가시키는 것을 도왔다. 과성장 과정 동안, 샘플을 주기적으로 취하여 세포 성장 및 생존 능력을 모니터링하였다.
안정한
론자
풀의 생성
독성 연구를 위해서 필요한 그램 단위의 양을 생산하기 위해서, 10A7 및 2D10 OX40L 항체를 안정한 발현을 위해서 론자 GS 엑시드 시스템으로 옮겼다. 각각의 항체에 대한 HC 및 LC를 먼저 젠위즈(Genewiz)에 의해서 CHO 세포 중에서 발현을 위해서 코돈 최적화하였다. 이어서, 표준 제한 효소 소화 및 결찰을 사용하여 HC 카세트(최적화된 IgG4PE 불변 영역 함유)를 론자의 pXC18.4 벡터 내로 클로닝하고, LC 카세트(최적화된 카파 불변 영역 함유)를 론자의 pXC17.4 벡터 내로 클로닝하였다. 이어서, HC 및 LC 서열 둘 모두를 코딩하는 더블 유전자 벡터(DGV)를 제한 효소 소화 및 결찰에 의해서 생성하고, 발현 전에 서열을 확인하였다.
안정한 풀 생성 전에; HC 및 LC를 별개로 코딩하는 단일 유전자 벡터, 뿐만 아니라 둘 모두를 함유하는 DGV를 PEI(폴리에틸렌이민 MW 40000)를 사용하여 일시적으로 론자 CHOK1SVKO 세포주 중에서 발현시켰다. 세포를 13일의 기간 동안 과성장하도록 방치한 후 정제를 위해서 상청액을 수확하였다. 과성장 과정 동안 세포에 지이 헬쓰케어로부터의 액티CHO(상표명) 공급물 A 및 B를 공급하여 생산성을 상승시키고 세포의 수명을 증가시키는 것을 도왔다. 과성장 과정 동안, 샘플을 주기적으로 취하여 세포 성장 및 생존 능력을 모니터링하였다. 일단 일시적인 발현이 확인되고, 정제된 물질이 분석되면, 항체를 안정한 풀로서 발현시켰다.
안정한 풀을 론자 소유의 방법 및 배지를 사용하여 생성하였다. 항체 당 4개의 풀을 생성하였고, 10 내지 15일의 기간에 걸쳐서 회수되도록 하였다. 세포를 회수한 후, 세포의 프리-시드 스톡(pre-seed stock: PSS)을 MCB의 추후 회수 및 생성을 위해서 동결시켰다. 이어서, 소규모(50mL) 진탕 플라스크 공급 배취 과성장을 론자 소유의 배지를 사용하여 설정하였다. 세포를 14일의 기간 동안 과성장하게 하였다. 이 기간 동안, 세포를 성장, 생존 능력 및 글루코스 수준에 대해서 모니터링하였다. 따라서 세포에 론자 소유의 공급물 및 400g/L 글루코스를 보충하였다. 샘플을 또한 조 샘플 정량화를 위해서 방법 전체에서 취하였다. 과성장 방법 마지막에, 상청액을 정제를 위해서 수확하였다.
안정한 풀을 론자 소유의 방법 및 배지를 사용하여 생성하였다. 항체 당 4개의 풀을 생성하였고, 10 내지 15일의 기간에 걸쳐서 회수되도록 하였다. 세포를 회수한 후, 세포의 프리-시드 스톡을 MCB의 추후 회수 및 생성을 위해서 동결시켰다. 이어서, 소규모(50mL) 진탕 플라스크 공급 배취 과성장물을 론자 소유의 배지를 사용하여 설정하였다. 세포를 14일의 기간 동안 과성장하게 하였다. 이 기간 동안, 세포를 성장, 생존 능력 및 글루코스 수준에 대해서 모니터링하였다. 따라서 세포에 론자 소유의 공급물 및 400g/L 글루코스를 보충하였다. 샘플을 또한 조 샘플 정량화를 위해서 방법 전체에서 취하였다. 과성장 방법 마지막에, 상청액을 정제를 위해서 수확하였다.
2D10 및 10A07은 서열이 유사하였지만, 안정한 론자 풀 중의 발현 프로파일이 상이하였는데, 4개의 별개의 생성된 안정한 풀에서 진탕 플라스크를 사용한 경우 최적의 조건하에서 10A07은 매우 낮은 타이터로 발현한 반면, 2D10은 훨씬 더 높은 타이터로 발현하였다(표 2 참고).
발현 후, 레서스 마카크 GvHD 모델에서 사용될 항체를 2-단계 정제 방법을 사용하여 정제하였다. 항체를 먼저 맵셀렉트 수레(MabSelect SuRe)(지이 헬쓰케어) 친화도 크로마토그래피를 사용하여 정제하였다. 항체를 IgG 용리 시약(피어스)을 사용하여 맵셀렉트 수레 배지로부터 용리하고, 용리된 항체를 제2 정제 단계 전에 아세트산 나트륨(pH 5.5) 중에서 투석하였다. 이어서, 항체를 양이온 교환에 의해서 정제하고, 아세트산 나트륨 완충액 중에서 염화나트륨과 함께 용리하였다. 용리된 항체를 PBS 중에서 투석하였다. 항체를 OD280nm에서의 분광광도계 판독에 의해서 정량하고, 목적하는 농도(10mg/ml)로 조정하였다. SDS-PAGE 분석 및 크기 배제 크로마토그래피에 의해서 항체 순도를 평가하였다. 엔도톡신 농도를 엔도세이프(Endosafe) PTS 및 LAL 시험 카트리지(샤를즈 리버 레보러토리즈(Charles River Laboratories))를 사용하여 측정하였다.
실시예
5
동종이형
PBMC
혼합 림프구 반응에서 항-
OX40L
항체의 효과를 측정함
밀도 구배 원심분리에 의해서 피콜-플라크 플러스(지이 헬쓰케어)를 사용하여 PBMC를 류코리덕션 시스템 챔버(NHSBT)로부터 단리시켰다. PBMC를 PBS 중의 10μg/ml에서 미토마이신 C(시그마)과 1시간 동안 37℃에서 미리 인큐베이션시킨다. 이어서, 세포를 PBS 중에서 3회 세척하고, 각각의 세척 후에 300xg로 3분 동안 원심분리하고, 상청액을 흡입하였다. 동종이형 PBMC(미토마이신 C로 처리되지 않음)를 2×106/m의 농도 및 50μL/웰로 10% v/v FBS가 보충된 RPMI 중의 96-웰 플레이트에 첨가하였다. 항-OX40L 항체를 배양 배지 중에서 희석하고, PBMC(처리된 미토마이신 C 없음)를 함유하는 96 웰 플레이트에 50μL/웰로 첨가하였다. 이어서, 미토마이신 C 처리된 PBMC를 세포/웰의 수를 기준으로 처리된 미토마이신 C 대 비 미토마이신 C의 1:1 내지 4:1 범의의 최종 세포 비로 96-웰 플레이트 중의 동종이형 PBMC(미토마이신 C로 처리되지 않음)에 첨가하였다. 세포를 5일 동안 37℃/5% CO2에서 인큐베이션시켰다. 5일 후에, TNF-α, IFN-γ, 및 IL-2를 제조사의 제안에 따라서 듀오세트 ELISA(알앤디 시스템즈)에 의해서 측정하였다. 제조사의 제안에 따라서 CFSE 희석에 의해서 증식을 측정하였다.
밀도 구배 원심분리에 의해서 피콜-플라크 플러스(지이 헬쓰케어)를 사용하여 PBMC를 류코리덕션 시스템 챔버(NHSBT)로부터 단리시켰다. PBMC를 PBS 중의 10μg/ml에서 미토마이신 C(시그마)와 1시간 동안 37℃에서 미리 인큐베이션시켰다. 이어서, 세포를 PBS 중에서 3회 세척하고, 각각의 세척 후에 300xg로 3분 동안 원심분리하고, 상청액을 흡입하였다. 일부 경우에 CD3 양성인 T-림프구(T-세포), 및 다른 경우에는 CD4 및 CD8 양성인 T-림프구(T-세포)를 제조사의 제안에 따라서 자기 마이크로비드(밀테니이 바이오테크)를 사용한 음성 선택에 의해서 동종이형 PBMC로부터 단리시켰다. 일부 경우에, 비-마이토마이신 C 처리된 PBMC를 T-세포 대신에 사용하였다. 단리된 세포를 300xg/5분에서 원심분리하고, 배양 배지(배양 배지는 RPMI(깁코) + 10% v/v FBS 또는 RPMI + 5% v/v 인간 AB 혈청으로서 정의되었음) 중에 재현탁시키고, 세포 현탁액 50μL를 재조합 OX40L 및 항체 적정액을 함유하는 96 웰 플레이트에 첨가하여 2×105 세포/웰의 최종 농도를 달성하였다. 항-OX40L 항체를 배양 배지 중에서 최종 검정 농도 100nM로 희석하거나, 일부 경우에는 항체의 적정액을 사용하였다. 항체를 T-세포 또는 비-마이토마이신 C 처리된 PBMC를 함유하는 96 웰 플레이트에 50μL/웰로 첨가하였다. 이어서, 미토마이신 C 처리된 PBMC를 세포/웰의 수를 기준으로 미토마이신 C 처리된 PBMC 대 T-세포(또는 PBMC)의 1:1 내지 4:1 범의의 최종 세포 비로 96-웰 플레이트 내의 T세포 또는 비 마이토마이신 C 처리된 PBMC에 첨가하였다. 세포를 5일 동안 37℃/5% CO2에서 인큐베이션시켰다. 5일 후에, IFN-γ를 제조사의 제안에 따라서 듀오세트 ELISA(알앤디 시스템즈)에 의해서 측정하였다.
항체의 부재 하에서의 대조군 웰과 비교하여 >20%의 인자 방출(IFN-γ,) 억제(식 8 참고)가 관찰되는 경우 항-OX40L 항체를 동종이형 PBMC/T 세포 MLR 또는 PBMC/PBMCl MLR에서 억제제로서 정의하였다. 수행된 4개의 실험으로부터, 하나의 실험은 기술적인 실패였는데, 이것은 동종이형 공여자 중에서 검출된 MLR 반응(IFN-γ 방출)이 전혀 없는 것으로 정의되었다. 나머지 3개의 실험 중에서, 3개의 실험 전부가 2D10, 10A07 및 양성 대조군 1을 사용하여 억제를 나타내었지만(항체의 부재하의 대조군 웰에 비해서 >20%의 인자 방출(IFN-γ,) 억제가 관찰됨), 3개의 실험 중 하나에서, 유의한 억제가 또한 동종형 대조군 항체를 사용하여 관찰되었다(도 2). PBMC/PBMC MLR을 위해서, 3개의 실험을 수행하였다. 3개의 실험 중에서, 2개는 기술적인 실패로서 간주되었는데, 그 이유는 IFN-γ 방출이 없거나 낮았기 때문이었다. 그러나, 또 다른 실험에서, 10A07는 동종형 대조군과 비교하는 경우 IFN-γ 방출을 억제하였다.
식 8:
%
억제(
MLR
)
기술된 바와 같이 측정된 IFN-γ 또는 IL2 방출로부터의 값(pg/mL)을 기준으로 함
자극 없음 = T-세포 또는 비-마이토마이신 C 처리된 PBMC 만 첨가된 웰(미토마이신 C 처리된 PBMC 없음)
IgG 없음 = 마이토마이신 C 처리된 PBMC와 함께 T-세포 또는 일부 경우에 비-마이토마이신 C 처리된 PBMC가 첨가되지만, IgG는 없음
실시예
6
CD3
프라임
1차 인간 T 림프구에 대한 항-
OX40L
항체의 효과를 측정함
항-OX40L이 OX40L의 부재 하에서 T-세포 반응을 유도하는 능력을 갖는지를 측정하기 위해서, 문헌[Wang et al.,Hybridoma (Larchmt)., 2009 Aug;28(4):269-76]으로부터 개작된 방법을 사용하여 하기 검정법을 수행하는데, 이 문헌은 길항제 항-OX40L 항체가 기술되어 있다.
마우스 항-인간 CD3 항체(베크톤 디킨슨(Becton Dickinson))를 멸균 PBS 중에서 0.5μg/ml로 희석하고, 50μL/웰을 96 웰 고 결합 멸균 플레이트에 첨가하고, 밤새 4℃에서 인큐베이션시켰다.
밤새 인큐베이션시킨 후, 플레이트를 멸균 PBS 100μL로 3회 세척하였다.
T-세포(CD3 양성)를 실시예 3에 기술된 바와 같이 류코리덕션 시스템 챔버(NHSBT)로부터 유래된 PBMC로부터 단리시켰다. 단리 후, 세포를 100μL로 웰에 첨가하여 1×105 세포/웰의 최종 농도를 달성하였다.
시험 항체를 RPMI+ 10% FBS 중에 희석하고, 50μL 또는 100μL/웰을 세포 플레이트에 첨가하여 10μg/ml의 최종 검정 농도를 달성하였다. 일부 경우에, 마우스 항-인간 CD28 항체(베크톤 디킨슨)를 또한 1μg/ml의 최종 농도로 웰에 첨가하였다.
검정 물질을 5일 동안 인큐베이션시켰다. 5일 후에, 수확 상청액 및 상청액 중의 IFN-γ 수준을 실시예 5에 기술된 바와 같이 측정하였다.
검정법을 4명의 독립적인 공여자에서 수행하였고, 인간 IgG4PE 동종형 대조군에서 관찰된 것과 비교할 경우 IgG4PE 포맷의 10A07 또는 2D10을 첨가하는 것은 어떤 효과도 없었다(IFN-γ 방출).
실시예
7
레서스
마카크
이식편대숙주병
(
GvHD
) 모델
GvHD의 예방에 대한 단일 요법 예방제로서의 항체 2D10 IgG4PE의 효과를 동종 조혈 줄기 세포 이식(HSCT)의 레서스 마카크 모델에서 관찰하였다. 이러한 모델에서 HSCT를 겪은 원숭이는 6 내지 8일의 생존 시간을 갖는다고 이미 기술되어 있다(Miller, Weston P., et al. "GVHD after haploidentical transplantation: a novel, MHC -defined rhesus macaque model identifies CD28 - CD8 + Tcells as a reservoir of breakthrough Tcell proliferation during costimulation blockade and sirolimus-based immunosuppression." Blood, 116, 24(2010):5403-5418).
모든 이식은 하나의 MHC 하플로타입(haplotype)("동종-HCT")에서 미스매칭된 반-형제 쌍 간에 수행되었다. 수용자 동물은 선형 가속기를 사용하여 사전-골수파괴 이식 전 컨디셔닝을 기초로 방사선 조사되었다. 선량률: 7cGy/분. 4회 분획으로 선량 1020cGy가 제공됨. 류카페레시스(leukapheresis) 공여자 동물을 GCSF 고정화에 적용하고, 스펙트라 옵티아 어페레레시스 머신(Spectra Optia apheresis machine)에 적용하였다. 하기 표는 4개의 성공적인 실험에 대한 총 유핵 세포(TNC) kg 당 CD3+ 세포, 및 CD34+ 세포의 용량을 제공한다.
이식-후 -2일, +5일, +12일, +19일, +26일, +33일, +40일, +47일에 수행하기 위해서 2D10 IgG4PE를 계획된 투약 스케줄에 따라서 10mg/kg i.v로 투약하였다. 2D10 IgG4PE를 투여한 결과로서 동물 중 어떤 것에서도 심각한 부정적인 투약 부작용이 관찰되지 않았다.
샘플을 연구 기간 동안 취하여 공여자 키메리즘(표 4) 및 백혈구 수를 모니터링하였다. 제1 최종 지점은 생존을 기준으로 하였고, 15일까지 생존하면 성공적인 예방 요법의 징후인 것으로 생각하였다(예방조치가 없을 경우 6 내지 8일의 서류화된 생존에 비교됨; 상기 문헌[Miller et al 2010]). GvHD 등급 스코어, T-세포 증식의 마커 및 활성화(예컨대 Ki-67 및 그랜자임 B)를 갖는 완전 병리학 및 조직학 및 유전자 어레이 분석법을 계획하였지만, 그것은 드래프팅 시간에서 포함을 위해서 사용 가능하지 않았다.
이러한 연구를 위한 방법은 본질적으로 문헌[Miller WPet al., (2010) "GVHD after haploidentical transplantation: a novel, MHC -defined rhesus macaque model identifies CD28- CD8+ T cells as a reservoir of breakthrough T-cell proliferation during costimulation blockade and sirolimus -based immunosuppression", Blood 116:5403-5418]에 기술된 바와 같다.
GvHD의
임상 단계
임상 증상의 스코어화는 하기 표 5에 언급된 기준에 따라서 분류된 관측 평가 및 임상 화학을 기초로 하였다.
조직병리학
부검시에 폐, 간, 피부 및 위장관을 비롯한 조직을 수집하였고, 포르말린 중에 고정시키고, 파라핀-포매(paraffin-embedded)하였다. 섹션을 절단하고, 슬라이드-장착하고, 림프구에 의한 조직 침윤의 가시화를 위해서 해마톡실린/에오신으로 또는 T-세포 마커로 염색하였다. 제조된 슬라이드를 반정량적 스코어화 시스템을 사용하여 GvHD에서 특정 전문지식을 가진 조직병리학자에 의해서 판독한다.
유세포
분석법
림프구 하위세트의 유세포 분석기 분석을 위해서 조혈 줄기 세포 이식 전 및 후에, 그리고 부검시에 종(longitudinal) 말초 혈액 샘플을 수집하였다. 폐, 간, 결장 비장 및 림프절(겨드랑이 및 서혜부) 조직을 부검시에 수집하였고, 유세포 분석법에 의해서 림프구 침윤물의 후속 분석을 위해서 적절한 경우 해리 또는 효소에 의해서 소화시켰다. 샘플을 하기 T 림프구 마커 프로브를 사용하여 LSR포르테사(LSRFortessa) 세포 분석기(비디 바이오사이언시스(BD Biosciences))를 사용하여 멀티컬러 유세포 분석법에 의해서 분석하였다: CD3(APC-Cy7 표지; 클론 SP34-2, 비디 바이오사이언시스), CD4(BV786 표지; 클론 L200, 비디 바이오사이언시스), CD8(BUV395 표지; 클론 RPA-T8, 비디 바이오사이언시스), CD28(PE-Cy7 표지; 클론 CD28.2, 이바이오사이언스), CD95(BV605 표지; 클론 DX2, 바이오레전드(Biolegend)). 증식 세포 집단을 Ki-67(FITC 표지, 다코(Dako))을 사용하여 식별하였다. CD4+ 또는 CD8+ T 세포 하위조직체(subcompartment)를 하기와 같이 표지하였다: 나이브 T-세포(CD28+/CD95-), 중앙 기억 T-세포(CD28+/CD95+), 이펙터 기억 T-세포(CD28-/CD95+).
혈액을 나트륨 EDTA를 사용하여 튜브에 수집하였고, 이어서 적혈구를 염화암모늄을 함유하는 용해 완충액으로 용해시켰다. 남아있는 백혈구를 FACS 완충액(2% FBS를 갖는 PBS)로 세척하고, 항체 칵테일(표 7)로 30분 동안 4℃에서 염색하였다. 염색 후, 세포를 세척하고, 1x BD 안정화 고정액(Stabilizing Fixative) 중에서 고정시켰다. 유동 데이터의 수집을 BD LSR 포르테사 사이토미터(BD LSR Fortessa cytometer) 상에서 수행하였다. 데이터를 플로조(FloJo)를 사용하여 분석하였다. T-세포를 CD3+ CD14/CD20- 림프구로서 정의하였다.
결과:
1: 이식 후 기억 줄기 T-세포의 확장
급성 이식편대숙주병(GVHD)의 비-인간 영장류 모델에서, 동종이형 조혈 세포 이식(HCT)은 진정한(bona fide) 나이브 T-세포(Tn: CD45RA+CCR7+CD95-)의 재구성을 희생시켜서 CD4 및 CD8 기억 줄기 T-세포(Tscm: CD45RA+CCR7+CD95+) 둘 모두의 조기 확장을 유발한다(도 3). 이러한 Tscm 세포가 혈액 중에서 순환하고, 또한 림프(림프절, 비장) 및 비-림프 기관(폐, 간 및 결장)에 존재한다.
2: 2D10
IgG4PE는
Tscm의
확장을
제한한다
차단 항-OX40L 항체, 2D10 IgG4PE로의 치료는, 동종이형 HCT 이후에 동물의 생존을 연장하고, 급성 GVHD의 임상적인 증상을 감소시킨다. GVHD 진행에서의 이러한 지연은 제한된 CD4+ Tscm 확장 및 CD4+ Tn 세포의 보존과 연관된다(도 4).
3: CD4
Tscm
세포는 그의
표면 상에서
OX40을
발현시킨다
도 5에 도시된 바와 같이, CD4+ Tscm은 그의 표면 상에서 OX40을 발현시키지만, 나이브 T-세포는 그렇지 않다. 또한, OX40 발현 수준은 CD4+ Tscm과 중앙 기억 세포(Tcm) 간에 대등하였다. 중요하게는, OX40 발현은 CD4+ Tscm 세포 상에서 광범위하게 검출되었다. 이것은 이식 전에 나이브 원숭이에서(혈액 및 림프 기관 둘 모두에서), 뿐만 아니라 류코페레시스(leukopheresis) 산물에서 검출되었다. 이러한 발현은 또한 이식 이후에 동종이형 HCT 수용자에서 종으로 관찰된다.
4: 표준
GvHD
요법과 비교한
02D10
Ig4PE
치료된 동물에서의
Tscm의
비교 분석
02D10 IgG4PE가 제공된 레서스 원숭이의 말초 혈액에서 명백한 HCT 이후 Tscm 세포의 비율을 시롤리무스(라파마이신) 또는 타크롤리무스와 메토트렉세이트의 조합물(Tac/MTX)이 투여된 별개의 동물 군으로부터의 Tscm과 비교하였다. CD4+ Tscm 세포에 대한 결과를 도 6a에 나타내고, CD8+ Tscm 세포에 대한 결과를 도 6b에 나타낸다. 데이터는 항-OX40L 항체 02D10 IgG4PE로의 치료가 시롤리무스 및 Tac/MTX 치료에 비해서 Tscm 세포의 비율을 지속적으로 억제한다는 것을 나타낸다.
결론:
Tscm의 OX40-발현 하위세트는 2D10 IgG4PE-매개된 OX40L-봉쇄에 민감할 수 있다. 이러한 봉쇄는 Tscm 확장을 제어할 수 있고, 따라서 급성 GVHD의 진행을 제한할 수 있다. OX40 경로는 Tscm 조절의 잠재적으로 신규한 기전이고, 이것을 임상 실시에서 사용하여 면역-매개된 질환을 치료하거나 입양 면역 요법의 결과를 개선시킬 수 있다.
키메리즘
공여자-특이적인 앰플리콘과 수용자-특이적인 앰플리콘의 최대 높이를 비교함으로써, 대립적인 공여자-특이적인 MHC-연결된 미소부수체 마커 및 수용자-특이적인 MHC-연결된 미소부수 마커를 사용하여 말초 혈액 또는 T 세포(CD3+/CD20-) 키메리즘을 측정하였다(문헌[Penedo MC et al., (2005) "Microsatellite typing of the rhesus macaque MHC region", Imunogenetics 57:198-209]).
총 6마리의 동물을 선택하여 HSCT를 제공하였다. 이들 6마리의 동물 중에서, 실험 중 둘은 기술적인 실패라고 여겨졌는데, 한 동물은 햄퍼드 생착(hampered engraftment)을 가질 수 있는 바이러스 재활성화를 경험하였고, 그것은 공여자 키메리즘이 초기에 상승하였지만, 그 다음 강하한 것이라고 판단되었고, 이는 제2 재구성이 자가형 재증식이었음을 나타낸다. 단일 고 거대세포바이러스(cytomegalovirus: CMV) 및 레서스 마카크 림포크립토바이러스(Lymphocryptovirus: rhLCV) 판독은 키메리즘 및 자가형 재증식의 강하가 동시에 일어나는 것을 보여주었다. 제2의 기술적인 실패는 이식에 적합한 산물을 생성하기 위한 분반법(apheresis) 기계의 실패 결과였다. 수용자 동물은 이미 방사능 조사되었기 때문에, 그것을 희생시켜야 했다. 4마리의 다른 동물 모두는 15일의 1차 최종 지점까지 생존하였는데, 이는 전통적인 비-예방조치 대조군 및 동시적인 비-예방조치 대조군 둘 모두와 비교하여 연장된 생존을 나타내었다. 하기 표 6은 본 연구에서 각각의 동물의 요약을 서술한다.
실시예
8
약동학
레서스 마카크에게 2D10 또는 적절한 비-기능성 동종형 대조군 항체 10mg/kg을 0일에 투약하였다. 샘플을 +15분, +1시간, +8시간, +24 내지 36시간, +72시간, +96시간, +8일, +11일, +15일, +18일, +22일, +25일 후에 취하였다. 29일에, 동물에게 2D10 또는 적절한 비-기능성 동종형 대조군 항체 3mg/kg을 투약하였다. 샘플을 29일에 +15분, +1시간, +8시간 후에, 그리고 후속으로 29일 이후 24 내지 36시간에 취하였다. 샘플을 +32일, +33일, +36일, +39일, +43일, +46일, +50일, +53일, +57일, +60일, +64일, +67일 및 +71일에 계속적으로 취하였다.
PK를 측정하기 위해서, 항-인간 IgG를 PBS 중에 8μg/ml로 희석하고, 96웰 저 자가-형광성, 고 단백질 결합 플레이트(코스타)에 밤새 4℃에서 흡착시켰다. PBS-트윈으로의 세척에 의해서 과량의 IgG를 제거하고, 웰을 5%w/v 탈지분유(차단 완충액)로 1시간 동안 실온에서 차단하였다. 인큐베이션 기간 이후에, 플레이트를 세척하였다. 혈장 샘플을 차단 완충액 중에서 희석하였다(다수의 희석). 10μg/ml로부터의 차단 완충액 중에 희석된 양성 대조군 항-OX40L 항체의 적정액을 사용하여 표준 곡선을 또한 생성한다(3회의 희석중 1회). 적정액 또는 희석된 혈장 샘플을 플레이트에 첨가하고, 1시간 동안 실온에서 인큐베이션시킨다. 이어서, 플레이트를 세척하고, 바이오티닐화된 인간 OX40L을 차단 완충액 중에 500ng/mL로 희석하고, 1시간 동안 실온에서 첨가하였다. 이어서 플레이트를 세척하고, 델피아(등록상표) 검정 완충액(퍼킨 엘머) 중에 희석된 스트렙타비딘-유로퓸3+컨쥬게이트(델피아(등록상표) 검출, 퍼킨엘머)를 첨가한다. 이어서, 플레이트를 트리스 완충 식염수 +0.1% 트윈 중에서 3회 세척한다. 이어서, 델피아 향상 용액(퍼킨 엘머)을 플레이트에 첨가하고, 엔비젼 플레이트 판독기(퍼킨엘머) 상에서 615nm에서 시간-분해 형광을 측정하였다. 4 파라미터 로지스틱 곡선 피팅 알고리즘을 사용하여 샘플 웰로부터의 형광 값을 양성 대조군 항-OX40L 항체의 적정액으로부터 생성된 표준 곡선으로부터 얻은 값에 외삽함으로써 혈장 중의 항-OX40L 항체의 농도를 계산한다.
실시예
9
레서스
마카크
(
GvHD
) 모델:
2D10
IgG4PE
+
라파마이신으로의
조합된 예방조치의 효과
2D10 IgG4PE와 라파마이신을 사용한 HSCT 이후 예방조치의 조합된 효과를 측정하기 위해서 추가의 레서스 마카크 GvHD 연구를 수행하였다. 연구는 실시예 7에 기술된 바와 같이 수행하였고, 투약은 하기와 같다: 2D10 IgG4PE를 이식 후 -2일, +5일, +12일, +19일, +26일, +33일, +40일, +47일 및 +56일에 10mg/kg으로 i.v. 투여하였다. 라파마이신을 -14일에 0.1mg/kg의 로딩 용량으로 i.m.으로 투여하였고, 그 후에 +100일의 본 연구의 계획된 종결까지 0.025mg/kg의 유지 용량을 매일 i.m.으로 투여하였다. 라파마이신 용량을 조정하여 최저 수준(trough level)을 5 내지 15ng/mL 범위로 유지시켰다.
결과:
라파마이신과 함께 2D10 IgG4PE를 HSCT 이후에 투여하면 HSCT 이후 실험 치료가 제공되지 않은 전통적인 대조군 동물(MST=8일; n=4; 문헌[Furlan et al, Science Translational Medicine, Vol 7 (315); 315ra1910])과 비교하여 연장된 GvHD-부재 및 절대 생존(중간 생존 시간, MST >82일; n=3)을 유발하였다. 2D10 IgG4PE + 라파마이신 조합 투약 효과는 또한 단독으로 투여되는 경우 각각의 분자의 부가적인 효과보다 더 큰 것 같았다(도 7: HSCT 이후 2D10 IgG4PE 및 라파마이신에 대한 MST는 각각 19일 및 17일이었음; 둘 모두 n-4). 또한, 퍼란(Furlan) 등은 타크롤리무스 + 메토트렉세이트로의 조합된 예방조치의 경우 MST가 49일이라고 개시한 것이 또한 주목된다. 타크롤리무스 + 메토트렉세이트와 항-OX40L 항체(예컨대 2D10)의 조합물, 또는 실제로 타크롤리무스와 항-OX40L 항체(예컨대 2D10)의 조합물이 또한 본 실시예에서 인지되는 바와 같이 상승작용적 결과를 제공할 것이라고 예상된다.
| 2D10 IgG4PE 레서스 GvHD 연구 | |
| 동물 | 상세사항 |
| #1 | 24일까지 생존. 4회 투여량의 2D10 IgG4PE를 제공하였다. 2상 조혈 재구성(biphasic hematopoietic reconstitution); 말초 혈액 키메리즘 데이터는 초기 공여자 생착 이후에 CMV 및 rhLCV 감염의 증거와 동시에 자가형 재증식을 보여주었다. 바이러스 감염은 이식 실패의 가능한 원인으로 간주하였다. 기술적인 실패라 기록하였다. |
| #2 | 16일까지 생존. 3회 투여량의 2D10 IgG4PE를 제공하였다. 15일에 88%의 최대 말초 혈액 공여자 키메리즘. CMV 또는 rhLCV 감염 증거 없음. 카테터 부위에서의 상처로 인한 수의학적 조언에 따라서 연구를 중단하였다(치료 또는 GvHD 관련된다고 여겨지지 않음). 부검시 GvHD 단계: 피부 1(발진 < 25%); 간 0(빌리루빈 상승 없음); GI 0(설사 없음). |
| #3 | 기술적인 실패라 기록하였다. 분반법 장비 실패가 상당한 최적값 미만의 공여자 혈액 산물을 유발하였다. |
| #4 | 26일까지 생존. 4회 투여량의 2D10 IgG4PE를 제공하였다. 23일에 99%의 최대 말초 혈액 공여자 키메리즘으로 깨끗한 조혈 재구성. CMV 또는 rhLCV 감염 증거 없음. 음낭 부종으로 인한 수의학적 조언에 따라서 연구를 중단하였다. 부검시 GvHD 단계: 피부 2(발진 25 내지 50%); 간 0(빌리루빈 상승 없음); GI 0(설사 없음). 전체 부검시 명시적인 내장 GvHD가 없음을 확인하였다. |
| #5 | 22일까지 생존. 4회 투여량의 2D10 IgG4PE를 제공하였다. 12일에 99%의 최대 말초 혈액 공여자 키메리즘으로 깨끗한 조혈 재구성. CMV 또는 rhLCV 감염 증거 없음. 지속적인 낮은 혈소판 수로 인해서 연구를 중단하였는데, 이는 높은 출혈 위험을 가지며, 급성 전신성 GVHD의 전개 징후이다. 부검시 GvHD 단계: 피부 3(발진>50%); 간 1(4 내지 8 x 빌리루빈 상승); GI 3(중증 설사). |
| #6 | 16일까지 생존. 3회 투여량의 2D10 IgG4PE를 제공하였다. 12일에 100%의 최대 말초 혈액 공여자 키메리즘으로 깨끗한 조혈 재구성. CMV 또는 rhLCV 감염 증거 없음. 부검시 GvHD 단계: 피부 2(발진 25 내지 50%); 간 1(4 내지 8 x 빌리루빈 상승); GI 2(중등도의 설사). |
SEQUENCE LISTING
<110> Kymab Limited
<120> ANTIBODIES, USES & METHODS
<130> KYMBT/P60284PC
<140> GBPCT/GB2016/050565
<141> 2016-03-03
<150> US14/955843
<151> 2015-12-01
<150> US14/935937
<151> 2015-11-09
<150> GB1516008.8
<151> 2015-09-09
<150> US14/811163
<151> 2015-07-28
<150> US14/700896
<151> 2015-04-30
<150> PCT/GB2015/050614
<151> 2015-03-03
<160> 234
<170> BiSSAP 1.3.6
<210> 1
<211> 384
<212> DNA
<213> Homo Sapiens
<400> 1
gaggtgcaac tggtggagtc tgggggagtc ttggtacagc cgggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacctttagc agttatatta tgacttgggt ccgccaggct 120
ccagggaagg ggctggagtg ggtctcaggt attagtggta gtggtggtgg tacatactac 180
gcagactcca tgaagggccg gttcaccatc tccagagaca attccaagaa cacgctgtat 240
ctgcagatga acagcctgag agtcgaggac acggccgtat attactgtgc gaaagatcgg 300
ttaggtccga ttactttggt tcgggggggc tattactacg gtatggacgt ctggggccaa 360
gggaccacgg tcaccgtctc ctca 384
<210> 2
<211> 128
<212> PRT
<213> Homo Sapiens
<400> 2
Glu Val Gln Leu Val Glu Ser Gly Gly Val Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ile Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Gly Ser Gly Gly Gly Thr Tyr Tyr Ala Asp Ser Met
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Val Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Leu Gly Pro Ile Thr Leu Val Arg Gly Gly Tyr Tyr
100 105 110
Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 3
<211> 24
<212> DNA
<213> Homo Sapiens
<400> 3
ggattcacct ttagcagtta tatt 24
<210> 4
<211> 8
<212> PRT
<213> Homo Sapiens
<400> 4
Gly Phe Thr Phe Ser Ser Tyr Ile
1 5
<210> 5
<211> 24
<212> DNA
<213> Homo Sapiens
<400> 5
attagtggta gtggtggtgg taca 24
<210> 6
<211> 8
<212> PRT
<213> Homo Sapiens
<400> 6
Ile Ser Gly Ser Gly Gly Gly Thr
1 5
<210> 7
<211> 63
<212> DNA
<213> Homo Sapiens
<400> 7
gcgaaagatc ggttaggtcc gattactttg gttcgggggg gctattacta cggtatggac 60
gtc 63
<210> 8
<211> 21
<212> PRT
<213> Homo Sapiens
<400> 8
Ala Lys Asp Arg Leu Gly Pro Ile Thr Leu Val Arg Gly Gly Tyr Tyr
1 5 10 15
Tyr Gly Met Asp Val
20
<210> 9
<211> 15
<212> DNA
<213> Homo Sapiens
<400> 9
agttatatta tgact 15
<210> 10
<211> 5
<212> PRT
<213> Homo Sapiens
<400> 10
Ser Tyr Ile Met Thr
1 5
<210> 11
<211> 51
<212> DNA
<213> Homo Sapiens
<400> 11
ggtattagtg gtagtggtgg tggtacatac tacgcagact ccatgaaggg c 51
<210> 12
<211> 17
<212> PRT
<213> Homo Sapiens
<400> 12
Gly Ile Ser Gly Ser Gly Gly Gly Thr Tyr Tyr Ala Asp Ser Met Lys
1 5 10 15
Gly
<210> 13
<211> 57
<212> DNA
<213> Homo Sapiens
<400> 13
gatcggttag gtccgattac tttggttcgg gggggctatt actacggtat ggacgtc 57
<210> 14
<211> 19
<212> PRT
<213> Homo Sapiens
<400> 14
Asp Arg Leu Gly Pro Ile Thr Leu Val Arg Gly Gly Tyr Tyr Tyr Gly
1 5 10 15
Met Asp Val
<210> 15
<211> 321
<212> DNA
<213> Homo Sapiens
<400> 15
gacatccaga tgacccagtc tccatcctcc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgcc gggcaagtca gagcattagc gactatttaa attggtatca gcagaaacca 120
gggaaagccc ctaagttcct gatctatgct gcatccagtt tgcaaagtgg agtcccatca 180
aggttcagtg gcagtggatc tgggacagat ttcactctca ccgtcagcag tctgcaacct 240
gaagattttg caacttacta ctgtcaacag agttacagta cccctcggac gttcggccaa 300
gggaccaggg tggaaatcaa a 321
<210> 16
<211> 107
<212> PRT
<213> Homo Sapiens
<400> 16
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Asp Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Arg Val Glu Ile Lys
100 105
<210> 17
<211> 18
<212> DNA
<213> Homo Sapiens
<400> 17
cagagcatta gcgactat 18
<210> 18
<211> 6
<212> PRT
<213> Homo Sapiens
<400> 18
Gln Ser Ile Ser Asp Tyr
1 5
<210> 19
<211> 9
<212> DNA
<213> Homo Sapiens
<400> 19
gctgcatcc 9
<210> 20
<211> 3
<212> PRT
<213> Homo Sapiens
<400> 20
Ala Ala Ser
1
<210> 21
<211> 27
<212> DNA
<213> Homo Sapiens
<400> 21
caacagagtt acagtacccc tcggacg 27
<210> 22
<211> 9
<212> PRT
<213> Homo Sapiens
<400> 22
Gln Gln Ser Tyr Ser Thr Pro Arg Thr
1 5
<210> 23
<211> 33
<212> DNA
<213> Homo Sapiens
<400> 23
cgggcaagtc agagcattag cgactattta aat 33
<210> 24
<211> 11
<212> PRT
<213> Homo Sapiens
<400> 24
Arg Ala Ser Gln Ser Ile Ser Asp Tyr Leu Asn
1 5 10
<210> 25
<211> 21
<212> DNA
<213> Homo Sapiens
<400> 25
gctgcatcca gtttgcaaag t 21
<210> 26
<211> 7
<212> PRT
<213> Homo Sapiens
<400> 26
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 27
<211> 27
<212> DNA
<213> Homo Sapiens
<400> 27
caacagagtt acagtacccc tcggacg 27
<210> 28
<211> 9
<212> PRT
<213> Homo Sapiens
<400> 28
Gln Gln Ser Tyr Ser Thr Pro Arg Thr
1 5
<210> 29
<211> 1365
<212> DNA
<213> Homo Sapiens
<400> 29
gaggtccagc tcgtggaaag cggaggagtg ctcgtgcagc ctggaggcag cctcaggctg 60
tcctgtgccg cctccggctt caccttcagc agctacatca tgacctgggt gaggcaggct 120
cccggaaaag gcctggagtg ggtgtccggc atctccggat ccggaggagg cacatactac 180
gccgacagca tgaagggccg gttcaccatc agccgggaca atagcaagaa taccctctac 240
ctgcaaatga acagcctgcg ggtggaggat accgccgtgt actactgcgc caaagatagg 300
ctgggcccca ttaccctcgt gaggggaggc tattactacg gcatggatgt gtggggccag 360
ggcaccaccg tgacagtgtc cagcgccagc accaagggcc cttccgtgtt ccccctggcc 420
ccttgcagca ggagcacctc cgaatccaca gctgccctgg gctgtctggt gaaggactac 480
tttcccgagc ccgtgaccgt gagctggaac agcggcgctc tgacatccgg cgtccacacc 540
tttcctgccg tcctgcagtc ctccggcctc tactccctgt cctccgtggt gaccgtgcct 600
agctcctccc tcggcaccaa gacctacacc tgtaacgtgg accacaaacc ctccaacacc 660
aaggtggaca aacgggtcga gagcaagtac ggccctccct gccctccttg tcctgccccc 720
gagttcgaag gcggacccag cgtgttcctg ttccctccta agcccaagga caccctcatg 780
atcagccgga cacccgaggt gacctgcgtg gtggtggatg tgagccagga ggaccctgag 840
gtccagttca actggtatgt ggatggcgtg gaggtgcaca acgccaagac aaagccccgg 900
gaagagcagt tcaactccac ctacagggtg gtcagcgtgc tgaccgtgct gcatcaggac 960
tggctgaacg gcaaggagta caagtgcaag gtcagcaata agggactgcc cagcagcatc 1020
gagaagacca tctccaaggc taaaggccag ccccgggaac ctcaggtgta caccctgcct 1080
cccagccagg aggagatgac caagaaccag gtgagcctga cctgcctggt gaagggattc 1140
tacccttccg acatcgccgt ggagtgggag tccaacggcc agcccgagaa caattataag 1200
accacccctc ccgtcctcga cagcgacgga tccttctttc tgtactccag gctgaccgtg 1260
gataagtcca ggtggcagga aggcaacgtg ttcagctgct ccgtgatgca cgaggccctg 1320
cacaatcact acacccagaa gtccctgagc ctgtccctgg gaaag 1365
<210> 30
<211> 455
<212> PRT
<213> Homo Sapiens
<400> 30
Glu Val Gln Leu Val Glu Ser Gly Gly Val Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ile Met Thr Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Gly Ile Ser Gly Ser Gly Gly Gly Thr Tyr Tyr Ala Asp Ser Met
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Val Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Leu Gly Pro Ile Thr Leu Val Arg Gly Gly Tyr Tyr
100 105 110
Tyr Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
130 135 140
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
145 150 155 160
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
165 170 175
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
180 185 190
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
195 200 205
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
210 215 220
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
225 230 235 240
Glu Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
245 250 255
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
260 265 270
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
275 280 285
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
290 295 300
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
305 310 315 320
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
325 330 335
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
340 345 350
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
355 360 365
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
370 375 380
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
385 390 395 400
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
405 410 415
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
420 425 430
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
435 440 445
Leu Ser Leu Ser Leu Gly Lys
450 455
<210> 31
<211> 642
<212> DNA
<213> Homo Sapiens
<400> 31
gacatccaga tgacccagtc cccttcctcc ctgtccgcct ccgtgggaga cagggtgacc 60
atcacctgcc gggccagcca gtccatcagc gactacctga actggtatca gcagaagccc 120
ggcaaggccc ctaagttcct gatctacgcc gcttcctccc tgcagtccgg agtgcccagc 180
aggttttccg gctccggatc cggcaccgac ttcaccctga ccgtgtccag cctgcagccc 240
gaggacttcg ccacctacta ctgccagcag agctacagca cccccaggac atttggccag 300
ggcacccggg tggagatcaa gaggaccgtc gctgccccct ccgtgtttat cttccccccc 360
agcgacgagc agctgaaatc cggcaccgcc tccgtggtct gcctgctgaa taacttctac 420
cctcgggagg ccaaggtgca gtggaaggtg gacaacgccc tgcagagcgg aaactcccag 480
gagagcgtga ccgagcagga ctccaaggac tccacatact ccctgtcctc caccctgaca 540
ctgtccaagg ccgattacga gaagcacaag gtgtacgcct gcgaggtgac ccaccaggga 600
ctgtcctccc ccgtgaccaa gtccttcaac cggggcgagt gc 642
<210> 32
<211> 214
<212> PRT
<213> Homo Sapiens
<400> 32
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Asp Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Phe Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Val Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser Tyr Ser Thr Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Arg Val Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 33
<211> 381
<212> DNA
<213> Homo Sapiens
<400> 33
gaggtgcagt tggtggagtc tgggggaggc ttggtacagc ctggggggtc cctgagactc 60
tcctgtgcag cctctggatt cacttttagc aactatgcca tgaactgggt ccgccaggct 120
ccagggaagg ggctggagtg ggtctcaact attagcggaa gtggtggtgc cacaaggtat 180
gcagactccg tgaagggccg attcaccata tccagagaca attccaggaa cacggtgtat 240
ctgcaaatga acagcctgag agtcgaggac acggccgttt tttactgtac gaaagatcgg 300
ctcattatgg ctacggttcg gggaccctat tactacggta tggacgtctg gggccaaggg 360
accacggtca ccgtctcctc a 381
<210> 34
<211> 127
<212> PRT
<213> Homo Sapiens
<400> 34
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Thr Ile Ser Gly Ser Gly Gly Ala Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Val Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Val Glu Asp Thr Ala Val Phe Tyr Cys
85 90 95
Thr Lys Asp Arg Leu Ile Met Ala Thr Val Arg Gly Pro Tyr Tyr Tyr
100 105 110
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120 125
<210> 35
<211> 24
<212> DNA
<213> Homo Sapiens
<400> 35
ggattcactt ttagcaacta tgcc 24
<210> 36
<211> 8
<212> PRT
<213> Homo Sapiens
<400> 36
Gly Phe Thr Phe Ser Asn Tyr Ala
1 5
<210> 37
<211> 24
<212> DNA
<213> Homo Sapiens
<400> 37
attagcggaa gtggtggtgc caca 24
<210> 38
<211> 8
<212> PRT
<213> Homo Sapiens
<400> 38
Ile Ser Gly Ser Gly Gly Ala Thr
1 5
<210> 39
<211> 60
<212> DNA
<213> Homo Sapiens
<400> 39
acgaaagatc ggctcattat ggctacggtt cggggaccct attactacgg tatggacgtc 60
<210> 40
<211> 20
<212> PRT
<213> Homo Sapiens
<400> 40
Thr Lys Asp Arg Leu Ile Met Ala Thr Val Arg Gly Pro Tyr Tyr Tyr
1 5 10 15
Gly Met Asp Val
20
<210> 41
<211> 15
<212> DNA
<213> Homo Sapiens
<400> 41
aactatgcca tgaac 15
<210> 42
<211> 5
<212> PRT
<213> Homo Sapiens
<400> 42
Asn Tyr Ala Met Asn
1 5
<210> 43
<211> 51
<212> DNA
<213> Homo Sapiens
<400> 43
actattagcg gaagtggtgg tgccacaagg tatgcagact ccgtgaaggg c 51
<210> 44
<211> 17
<212> PRT
<213> Homo Sapiens
<400> 44
Thr Ile Ser Gly Ser Gly Gly Ala Thr Arg Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 45
<211> 54
<212> DNA
<213> Homo Sapiens
<400> 45
gatcggctca ttatggctac ggttcgggga ccctattact acggtatgga cgtc 54
<210> 46
<211> 18
<212> PRT
<213> Homo Sapiens
<400> 46
Asp Arg Leu Ile Met Ala Thr Val Arg Gly Pro Tyr Tyr Tyr Gly Met
1 5 10 15
Asp Val
<210> 47
<211> 321
<212> DNA
<213> Homo Sapiens
<400> 47
gacatccaga tgacccagtc tccatcctcc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgcc gggcaagtca gagcattagc agctatttaa attggtatca gcagaaacca 120
gggaaagccc ctaacctcct gatctatgct gcatccagtt tgcaaagtgg ggtcccatca 180
aggttcagtg gcagtggatc tgagacagat ttcactctca ccatcagcag tctgcaacct 240
gaagattttg caacttacta ctgtcaacag agtcacagtg tctcattcac tttcggccct 300
gggaccaaag tggatatcaa a 321
<210> 48
<211> 107
<212> PRT
<213> Homo Sapiens
<400> 48
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Glu Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser His Ser Val Ser Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 49
<211> 18
<212> DNA
<213> Homo Sapiens
<400> 49
cagagcatta gcagctat 18
<210> 50
<211> 6
<212> PRT
<213> Homo Sapiens
<400> 50
Gln Ser Ile Ser Ser Tyr
1 5
<210> 51
<211> 9
<212> DNA
<213> Homo Sapiens
<400> 51
gctgcatcc 9
<210> 52
<211> 3
<212> PRT
<213> Homo Sapiens
<400> 52
Ala Ala Ser
1
<210> 53
<211> 27
<212> DNA
<213> Homo Sapiens
<400> 53
caacagagtc acagtgtctc attcact 27
<210> 54
<211> 9
<212> PRT
<213> Homo Sapiens
<400> 54
Gln Gln Ser His Ser Val Ser Phe Thr
1 5
<210> 55
<211> 33
<212> DNA
<213> Homo Sapiens
<400> 55
cgggcaagtc agagcattag cagctattta aat 33
<210> 56
<211> 11
<212> PRT
<213> Homo Sapiens
<400> 56
Arg Ala Ser Gln Ser Ile Ser Ser Tyr Leu Asn
1 5 10
<210> 57
<211> 21
<212> DNA
<213> Homo Sapiens
<400> 57
gctgcatcca gtttgcaaag t 21
<210> 58
<211> 7
<212> PRT
<213> Homo Sapiens
<400> 58
Ala Ala Ser Ser Leu Gln Ser
1 5
<210> 59
<211> 27
<212> DNA
<213> Homo Sapiens
<400> 59
caacagagtc acagtgtctc attcact 27
<210> 60
<211> 9
<212> PRT
<213> Homo Sapiens
<400> 60
Gln Gln Ser His Ser Val Ser Phe Thr
1 5
<210> 61
<211> 1362
<212> DNA
<213> Homo Sapiens
<400> 61
gaagtgcaac tggtggagtc cggaggaggc ctggtgcagc ctggaggaag cctgaggctg 60
agctgtgccg ccagcggctt caccttcagc aactacgcca tgaactgggt gaggcaggcc 120
cctggcaagg gactggagtg ggtctccacc atcagcggct ccggaggcgc tacacggtac 180
gccgatagcg tgaagggccg gtttaccatt tcccgggaca actcccggaa caccgtgtac 240
ctccagatga acagcctgag ggtggaggat accgccgtgt tctactgcac caaggacagg 300
ctgattatgg ccaccgtgag gggaccttac tactatggca tggatgtgtg gggccagggc 360
acaaccgtca ccgtgtcctc cgcctccacc aagggaccta gcgtgttccc tctcgccccc 420
tgttccaggt ccacaagcga gtccaccgct gccctcggct gtctggtgaa agactacttt 480
cccgagcccg tgaccgtctc ctggaatagc ggagccctga cctccggcgt gcacacattt 540
cccgccgtgc tgcagagcag cggactgtat agcctgagca gcgtggtgac cgtgcccagc 600
tccagcctcg gcaccaaaac ctacacctgc aacgtggacc acaagccctc caacaccaag 660
gtggacaagc gggtggagag caagtacggc cccccttgcc ctccttgtcc tgcccctgag 720
ttcgagggag gaccctccgt gttcctgttt ccccccaaac ccaaggacac cctgatgatc 780
tcccggacac ccgaggtgac ctgtgtggtc gtggacgtca gccaggagga ccccgaggtg 840
cagttcaact ggtatgtgga cggcgtggag gtgcacaatg ccaaaaccaa gcccagggag 900
gagcagttca attccaccta cagggtggtg agcgtgctga ccgtcctgca tcaggattgg 960
ctgaacggca aggagtacaa gtgcaaggtg tccaacaagg gactgcccag ctccatcgag 1020
aagaccatca gcaaggctaa gggccagccg agggagcccc aggtgtatac cctgcctcct 1080
agccaggaag agatgaccaa gaaccaagtg tccctgacct gcctggtgaa gggattctac 1140
ccctccgaca tcgccgtgga gtgggagagc aatggccagc ccgagaacaa ctacaaaaca 1200
acccctcccg tgctcgatag cgacggcagc ttctttctct acagccggct gacagtggac 1260
aagagcaggt ggcaggaggg caacgtgttc tcctgttccg tgatgcacga ggccctgcac 1320
aatcactaca cccagaagag cctctccctg tccctgggca ag 1362
<210> 62
<211> 454
<212> PRT
<213> Homo Sapiens
<400> 62
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Thr Ile Ser Gly Ser Gly Gly Ala Thr Arg Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Asn Thr Val Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Val Glu Asp Thr Ala Val Phe Tyr Cys
85 90 95
Thr Lys Asp Arg Leu Ile Met Ala Thr Val Arg Gly Pro Tyr Tyr Tyr
100 105 110
Gly Met Asp Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser Ala
115 120 125
Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg Ser
130 135 140
Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr Phe
145 150 155 160
Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser Gly
165 170 175
Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser Leu
180 185 190
Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr Tyr
195 200 205
Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys Arg
210 215 220
Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro Glu
225 230 235 240
Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp
245 250 255
Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp
260 265 270
Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp Gly
275 280 285
Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe Asn
290 295 300
Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp
305 310 315 320
Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu Pro
325 330 335
Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu
340 345 350
Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys Asn
355 360 365
Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile
370 375 380
Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr
385 390 395 400
Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Arg
405 410 415
Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser Cys
420 425 430
Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu
435 440 445
Ser Leu Ser Leu Gly Lys
450
<210> 63
<211> 642
<212> DNA
<213> Homo Sapiens
<400> 63
gacatccaga tgacccagtc cccttcctcc ctgagcgcta gcgtgggaga tagggtgacc 60
atcacctgca gggcctccca aagcatctcc tcctacctga actggtacca gcagaaaccc 120
ggcaaggccc ccaacctgct gatctacgct gcctcctccc tccagtccgg cgtgcctagc 180
aggtttagcg gctccggaag cgagaccgac ttcaccctga ccatctcctc cctgcagccc 240
gaggacttcg ccacctacta ctgccagcaa tcccacagcg tgtccttcac cttcggcccc 300
ggcaccaagg tggacatcaa gaggaccgtg gccgccccct ccgtgttcat ctttcccccc 360
tccgatgaac agctgaagag cggcaccgct agcgtggtgt gcctgctgaa caacttctac 420
cccagggagg ccaaggtgca gtggaaggtg gacaatgccc tgcagtccgg caacagccag 480
gagagcgtga ccgagcagga ctccaaggac agcacctaca gcctgtcctc caccctgacc 540
ctgtccaagg ccgactacga gaagcacaaa gtgtacgcct gcgaagtgac ccatcagggc 600
ctgagctccc ccgtgaccaa gtcctttaac aggggcgagt gc 642
<210> 64
<211> 214
<212> PRT
<213> Homo Sapiens
<400> 64
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Ser Ile Ser Ser Tyr
20 25 30
Leu Asn Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Asn Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Glu Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Ser His Ser Val Ser Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 65
<211> 372
<212> DNA
<213> Homo Sapiens
<400> 65
caggtgcagc tggtggagtc tgggggaggc ttggtcaagc ctggagggtc cctgagactc 60
tcctgtgcag cctctcgatt caccctcagt gactactaca tgacctggat ccgccaggct 120
ccagggaagg ggctggagtg ggtttcatac attagtagta gtggtaatac catatactac 180
gcagactctg tgaagggccg attcaccatc tccagggaca acgccaagaa ctcactgtat 240
ctgcaaatga acagcctgag agccgaggac acggccgtgt attactgtgc gagagatctg 300
agtgggagct actgggacta ctactacggt atggacgtct ggggccaagg gaccacggtc 360
accgtctcct ca 372
<210> 66
<211> 124
<212> PRT
<213> Homo Sapiens
<400> 66
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Phe Thr Leu Ser Asp Tyr
20 25 30
Tyr Met Thr Trp Ile Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Tyr Ile Ser Ser Ser Gly Asn Thr Ile Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Ser Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Leu Ser Gly Ser Tyr Trp Asp Tyr Tyr Tyr Gly Met Asp
100 105 110
Val Trp Gly Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 67
<211> 24
<212> DNA
<213> Homo Sapiens
<400> 67
cgattcaccc tcagtgacta ctac 24
<210> 68
<211> 8
<212> PRT
<213> Homo Sapiens
<400> 68
Arg Phe Thr Leu Ser Asp Tyr Tyr
1 5
<210> 69
<211> 24
<212> DNA
<213> Homo Sapiens
<400> 69
attagtagta gtggtaatac cata 24
<210> 70
<211> 8
<212> PRT
<213> Homo Sapiens
<400> 70
Ile Ser Ser Ser Gly Asn Thr Ile
1 5
<210> 71
<211> 51
<212> DNA
<213> Homo Sapiens
<400> 71
gcgagagatc tgagtgggag ctactgggac tactactacg gtatggacgt c 51
<210> 72
<211> 17
<212> PRT
<213> Homo Sapiens
<400> 72
Ala Arg Asp Leu Ser Gly Ser Tyr Trp Asp Tyr Tyr Tyr Gly Met Asp
1 5 10 15
Val
<210> 73
<211> 15
<212> DNA
<213> Homo Sapiens
<400> 73
gactactaca tgacc 15
<210> 74
<211> 5
<212> PRT
<213> Homo Sapiens
<400> 74
Asp Tyr Tyr Met Thr
1 5
<210> 75
<211> 51
<212> DNA
<213> Homo Sapiens
<400> 75
tacattagta gtagtggtaa taccatatac tacgcagact ctgtgaaggg c 51
<210> 76
<211> 17
<212> PRT
<213> Homo Sapiens
<400> 76
Tyr Ile Ser Ser Ser Gly Asn Thr Ile Tyr Tyr Ala Asp Ser Val Lys
1 5 10 15
Gly
<210> 77
<211> 45
<212> DNA
<213> Homo Sapiens
<400> 77
gatctgagtg ggagctactg ggactactac tacggtatgg acgtc 45
<210> 78
<211> 15
<212> PRT
<213> Homo Sapiens
<400> 78
Asp Leu Ser Gly Ser Tyr Trp Asp Tyr Tyr Tyr Gly Met Asp Val
1 5 10 15
<210> 79
<211> 321
<212> DNA
<213> Homo Sapiens
<400> 79
gccatccagt tgacccagtc tccatcctcc ctgtctacat ctgtaggaga cagagtcacc 60
atcgcttgcc gggcaagtca gggcattaac aatgctttag cctggtatca gcagaaacca 120
gggaaagctc ctaagctcct gatctatgat gcctccagtt tggaaagtgg ggtcccatca 180
aggttcagcg gcagtggatc tgggacagat ttcactctca ccatcagcag cctgcagcct 240
gaagattttg caacttatta ctgtcaacag tttaatagtt accctcggac gttcggccaa 300
gggaccaagg tggaaatcaa a 321
<210> 80
<211> 107
<212> PRT
<213> Homo Sapiens
<400> 80
Ala Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Thr Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Ala Cys Arg Ala Ser Gln Gly Ile Asn Asn Ala
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Asn Ser Tyr Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 81
<211> 18
<212> DNA
<213> Homo Sapiens
<400> 81
cagggcatta acaatgct 18
<210> 82
<211> 6
<212> PRT
<213> Homo Sapiens
<400> 82
Gln Gly Ile Asn Asn Ala
1 5
<210> 83
<211> 9
<212> DNA
<213> Homo Sapiens
<400> 83
gatgcctcc 9
<210> 84
<211> 3
<212> PRT
<213> Homo Sapiens
<400> 84
Asp Ala Ser
1
<210> 85
<211> 27
<212> DNA
<213> Homo Sapiens
<400> 85
caacagttta atagttaccc tcggacg 27
<210> 86
<211> 9
<212> PRT
<213> Homo Sapiens
<400> 86
Gln Gln Phe Asn Ser Tyr Pro Arg Thr
1 5
<210> 87
<211> 33
<212> DNA
<213> Homo Sapiens
<400> 87
cgggcaagtc agggcattaa caatgcttta gcc 33
<210> 88
<211> 11
<212> PRT
<213> Homo Sapiens
<400> 88
Arg Ala Ser Gln Gly Ile Asn Asn Ala Leu Ala
1 5 10
<210> 89
<211> 21
<212> DNA
<213> Homo Sapiens
<400> 89
gatgcctcca gtttggaaag t 21
<210> 90
<211> 7
<212> PRT
<213> Homo Sapiens
<400> 90
Asp Ala Ser Ser Leu Glu Ser
1 5
<210> 91
<211> 27
<212> DNA
<213> Homo Sapiens
<400> 91
caacagttta atagttaccc tcggacg 27
<210> 92
<211> 9
<212> PRT
<213> Homo Sapiens
<400> 92
Gln Gln Phe Asn Ser Tyr Pro Arg Thr
1 5
<210> 93
<211> 369
<212> DNA
<213> Homo Sapiens
<400> 93
gaggtgcagc tggtggagtc tgggggaggc ttggtaaagc ctggggggtc ccttagactc 60
tcctgtgcag cctctggatt cactttcagt aacgcctgga tgagctgggt ccgccaggct 120
ccagggaagg ggctggagtg ggttggccgt attaaaagca aaactgaagg tgggacaaca 180
gactacgctg cacccgtgaa aggcagattc accatctcaa gagatgattc aaaaaacacg 240
ctgtatctgc aaatgaacag cctgaaaacc gaggacacag ccgtgtatta ctgtaccaca 300
gattttctat ggttcgggga gttccctttt gactactggg gccagggaac cctggtcacc 360
gtctcctca 369
<210> 94
<211> 123
<212> PRT
<213> Homo Sapiens
<400> 94
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Lys Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Ala
20 25 30
Trp Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Gly Arg Ile Lys Ser Lys Thr Glu Gly Gly Thr Thr Asp Tyr Ala Ala
50 55 60
Pro Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asp Ser Lys Asn Thr
65 70 75 80
Leu Tyr Leu Gln Met Asn Ser Leu Lys Thr Glu Asp Thr Ala Val Tyr
85 90 95
Tyr Cys Thr Thr Asp Phe Leu Trp Phe Gly Glu Phe Pro Phe Asp Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 95
<211> 24
<212> DNA
<213> Homo Sapiens
<400> 95
ggattcactt tcagtaacgc ctgg 24
<210> 96
<211> 8
<212> PRT
<213> Homo Sapiens
<400> 96
Gly Phe Thr Phe Ser Asn Ala Trp
1 5
<210> 97
<211> 30
<212> DNA
<213> Homo Sapiens
<400> 97
attaaaagca aaactgaagg tgggacaaca 30
<210> 98
<211> 10
<212> PRT
<213> Homo Sapiens
<400> 98
Ile Lys Ser Lys Thr Glu Gly Gly Thr Thr
1 5 10
<210> 99
<211> 42
<212> DNA
<213> Homo Sapiens
<400> 99
accacagatt ttctatggtt cggggagttc ccttttgact ac 42
<210> 100
<211> 14
<212> PRT
<213> Homo Sapiens
<400> 100
Thr Thr Asp Phe Leu Trp Phe Gly Glu Phe Pro Phe Asp Tyr
1 5 10
<210> 101
<211> 15
<212> DNA
<213> Homo Sapiens
<400> 101
aacgcctgga tgagc 15
<210> 102
<211> 5
<212> PRT
<213> Homo Sapiens
<400> 102
Asn Ala Trp Met Ser
1 5
<210> 103
<211> 57
<212> DNA
<213> Homo Sapiens
<400> 103
cgtattaaaa gcaaaactga aggtgggaca acagactacg ctgcacccgt gaaaggc 57
<210> 104
<211> 19
<212> PRT
<213> Homo Sapiens
<400> 104
Arg Ile Lys Ser Lys Thr Glu Gly Gly Thr Thr Asp Tyr Ala Ala Pro
1 5 10 15
Val Lys Gly
<210> 105
<211> 36
<212> DNA
<213> Homo Sapiens
<400> 105
gattttctat ggttcgggga gttccctttt gactac 36
<210> 106
<211> 12
<212> PRT
<213> Homo Sapiens
<400> 106
Asp Phe Leu Trp Phe Gly Glu Phe Pro Phe Asp Tyr
1 5 10
<210> 107
<211> 321
<212> DNA
<213> Homo Sapiens
<400> 107
gacatccaga tgacccagtc tccatcctcc ctgtctgcat ctgtaggaga cagagtcacc 60
atcacttgcc gggcgagtca gggcattagc aattatttag cctggtatca gcagaaacca 120
gggaaaattc ctaagctcct gatctatgct gcatccactt tgcaatcagg ggtcccatct 180
cggttcagtg gcagtggatc tgggacagat ttcactctca ccatcagcag cctgcagcct 240
gaagatgttg caacttatta ctgtcaaaag tataacagtg cccctcggac gttcggccaa 300
gggaccaagg tggaaatcaa a 321
<210> 108
<211> 107
<212> PRT
<213> Homo Sapiens
<400> 108
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Asn Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ile Pro Lys Leu Leu Ile
35 40 45
Tyr Ala Ala Ser Thr Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Val Ala Thr Tyr Tyr Cys Gln Lys Tyr Asn Ser Ala Pro Arg
85 90 95
Thr Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 109
<211> 18
<212> DNA
<213> Homo Sapiens
<400> 109
cagggcatta gcaattat 18
<210> 110
<211> 6
<212> PRT
<213> Homo Sapiens
<400> 110
Gln Gly Ile Ser Asn Tyr
1 5
<210> 111
<211> 9
<212> DNA
<213> Homo Sapiens
<400> 111
gctgcatcc 9
<210> 112
<211> 3
<212> PRT
<213> Homo Sapiens
<400> 112
Ala Ala Ser
1
<210> 113
<211> 27
<212> DNA
<213> Homo Sapiens
<400> 113
caaaagtata acagtgcccc tcggacg 27
<210> 114
<211> 9
<212> PRT
<213> Homo Sapiens
<400> 114
Gln Lys Tyr Asn Ser Ala Pro Arg Thr
1 5
<210> 115
<211> 33
<212> DNA
<213> Homo Sapiens
<400> 115
cgggcgagtc agggcattag caattattta gcc 33
<210> 116
<211> 11
<212> PRT
<213> Homo Sapiens
<400> 116
Arg Ala Ser Gln Gly Ile Ser Asn Tyr Leu Ala
1 5 10
<210> 117
<211> 21
<212> DNA
<213> Homo Sapiens
<400> 117
gctgcatcca ctttgcaatc a 21
<210> 118
<211> 7
<212> PRT
<213> Homo Sapiens
<400> 118
Ala Ala Ser Thr Leu Gln Ser
1 5
<210> 119
<211> 27
<212> DNA
<213> Homo Sapiens
<400> 119
caaaagtata acagtgcccc tcggacg 27
<210> 120
<211> 9
<212> PRT
<213> Homo Sapiens
<400> 120
Gln Lys Tyr Asn Ser Ala Pro Arg Thr
1 5
<210> 121
<211> 981
<212> DNA
<213> Homo Sapiens
<400> 121
gcttccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagccg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccatgccc atcatgccca gcacctgagt tcctgggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtcc tccatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggctcct tcttcctcta cagcaggcta accgtggaca agagcaggtg gcaggagggg 900
aatgtcttct catgctccgt gatgcatgag gctctgcaca accactacac acagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 122
<211> 327
<212> PRT
<213> Homo Sapiens
<400> 122
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 123
<211> 981
<212> DNA
<213> Homo Sapiens
<400> 123
gcttccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagccg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccgtgccc atcatgccca gcacctgagt tcctgggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcgtgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtcc tccatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggctcct tcttcctcta cagcaggcta accgtggaca agagcaggtg gcaggagggg 900
aatgtcttct catgctccgt gatgcatgag gctctgcaca accactacac gcagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 124
<211> 327
<212> PRT
<213> Homo Sapiens
<400> 124
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Val His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 125
<211> 981
<212> DNA
<213> Homo Sapiens
<400> 125
gcttccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacagccg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccatgccc atcatgccca gcacctgagt tcctgggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtcc tccatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggctcct tcttcctcta cagcaagctc accgtggaca agagcaggtg gcaggagggg 900
aacgtcttct catgctccgt gatgcatgag gctctgcaca accactacac gcagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 126
<211> 327
<212> PRT
<213> Homo Sapiens
<400> 126
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Ser Cys Pro Ala Pro
100 105 110
Glu Phe Leu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 127
<211> 981
<212> DNA
<213> Homo Sapiens
<400> 127
gcctccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacggccg ccctgggctg cctggtcaag gactacttcc ccgaaccagt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccatgccc accatgccca gcgcctgaat ttgagggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtca tcgatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggatcct tcttcctcta cagcaggcta accgtggaca agagcaggtg gcaggagggg 900
aatgtcttct catgctccgt gatgcatgag gctctgcaca accactacac acagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 128
<211> 327
<212> PRT
<213> Homo Sapiens
<400> 128
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Glu Phe Glu Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 129
<211> 981
<212> DNA
<213> Homo Sapiens
<400> 129
gcctccacca agggacctag cgtgttccct ctcgccccct gttccaggtc cacaagcgag 60
tccaccgctg ccctcggctg tctggtgaaa gactactttc ccgagcccgt gaccgtctcc 120
tggaatagcg gagccctgac ctccggcgtg cacacatttc ccgccgtgct gcagagcagc 180
ggactgtata gcctgagcag cgtggtgacc gtgcccagct ccagcctcgg caccaaaacc 240
tacacctgca acgtggacca caagccctcc aacaccaagg tggacaagcg ggtggagagc 300
aagtacggcc ccccttgccc tccttgtcct gcccctgagt tcgagggagg accctccgtg 360
ttcctgtttc cccccaaacc caaggacacc ctgatgatct cccggacacc cgaggtgacc 420
tgtgtggtcg tggacgtcag ccaggaggac cccgaggtgc agttcaactg gtatgtggac 480
ggcgtggagg tgcacaatgc caaaaccaag cccagggagg agcagttcaa ttccacctac 540
agggtggtga gcgtgctgac cgtcctgcat caggattggc tgaacggcaa ggagtacaag 600
tgcaaggtgt ccaacaaggg actgcccagc tccatcgaga agaccatcag caaggctaag 660
ggccagccga gggagcccca ggtgtatacc ctgcctccta gccaggaaga gatgaccaag 720
aaccaagtgt ccctgacctg cctggtgaag ggattctacc cctccgacat cgccgtggag 780
tgggagagca atggccagcc cgagaacaac tacaaaacaa cccctcccgt gctcgatagc 840
gacggcagct tctttctcta cagccggctg acagtggaca agagcaggtg gcaggagggc 900
aacgtgttct cctgttccgt gatgcacgag gccctgcaca atcactacac ccagaagagc 960
ctctccctgt ccctgggcaa g 981
<210> 130
<211> 981
<212> DNA
<213> Homo Sapiens
<400> 130
gccagcacca agggcccttc cgtgttcccc ctggcccctt gcagcaggag cacctccgaa 60
tccacagctg ccctgggctg tctggtgaag gactactttc ccgagcccgt gaccgtgagc 120
tggaacagcg gcgctctgac atccggcgtc cacacctttc ctgccgtcct gcagtcctcc 180
ggcctctact ccctgtcctc cgtggtgacc gtgcctagct cctccctcgg caccaagacc 240
tacacctgta acgtggacca caaaccctcc aacaccaagg tggacaaacg ggtcgagagc 300
aagtacggcc ctccctgccc tccttgtcct gcccccgagt tcgaaggcgg acccagcgtg 360
ttcctgttcc ctcctaagcc caaggacacc ctcatgatca gccggacacc cgaggtgacc 420
tgcgtggtgg tggatgtgag ccaggaggac cctgaggtcc agttcaactg gtatgtggat 480
ggcgtggagg tgcacaacgc caagacaaag ccccgggaag agcagttcaa ctccacctac 540
agggtggtca gcgtgctgac cgtgctgcat caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtca gcaataaggg actgcccagc agcatcgaga agaccatctc caaggctaaa 660
ggccagcccc gggaacctca ggtgtacacc ctgcctccca gccaggagga gatgaccaag 720
aaccaggtga gcctgacctg cctggtgaag ggattctacc cttccgacat cgccgtggag 780
tgggagtcca acggccagcc cgagaacaat tataagacca cccctcccgt cctcgacagc 840
gacggatcct tctttctgta ctccaggctg accgtggata agtccaggtg gcaggaaggc 900
aacgtgttca gctgctccgt gatgcacgag gccctgcaca atcactacac ccagaagtcc 960
ctgagcctgt ccctgggaaa g 981
<210> 131
<211> 981
<212> DNA
<213> Homo Sapiens
<400> 131
gcctccacca agggcccatc cgtcttcccc ctggcgccct gctccaggag cacctccgag 60
agcacggccg ccctgggctg cctggtcaag gactacttcc ccgaaccagt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacgaagacc 240
tacacctgca acgtagatca caagcccagc aacaccaagg tggacaagag agttgagtcc 300
aaatatggtc ccccatgccc accatgccca gcgcctccag ttgcgggggg accatcagtc 360
ttcctgttcc ccccaaaacc caaggacact ctcatgatct cccggacccc tgaggtcacg 420
tgcgtggtgg tggacgtgag ccaggaagac cccgaggtcc agttcaactg gtacgtggat 480
ggcgtggagg tgcataatgc caagacaaag ccgcgggagg agcagttcaa cagcacgtac 540
cgtgtggtca gcgtcctcac cgtcctgcac caggactggc tgaacggcaa ggagtacaag 600
tgcaaggtct ccaacaaagg cctcccgtca tcgatcgaga aaaccatctc caaagccaaa 660
gggcagcccc gagagccaca ggtgtacacc ctgcccccat cccaggagga gatgaccaag 720
aaccaggtca gcctgacctg cctggtcaaa ggcttctacc ccagcgacat cgccgtggag 780
tgggagagca atgggcagcc ggagaacaac tacaagacca cgcctcccgt gctggactcc 840
gacggatcct tcttcctcta cagcaggcta accgtggaca agagcaggtg gcaggagggg 900
aatgtcttct catgctccgt gatgcatgag gctctgcaca accactacac acagaagagc 960
ctctccctgt ctctgggtaa a 981
<210> 132
<211> 327
<212> PRT
<213> Homo Sapiens
<400> 132
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Cys Ser Arg
1 5 10 15
Ser Thr Ser Glu Ser Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Lys Thr
65 70 75 80
Tyr Thr Cys Asn Val Asp His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Arg Val Glu Ser Lys Tyr Gly Pro Pro Cys Pro Pro Cys Pro Ala Pro
100 105 110
Pro Val Ala Gly Gly Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys
115 120 125
Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys Val Val Val
130 135 140
Asp Val Ser Gln Glu Asp Pro Glu Val Gln Phe Asn Trp Tyr Val Asp
145 150 155 160
Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Phe
165 170 175
Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu His Gln Asp
180 185 190
Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn Lys Gly Leu
195 200 205
Pro Ser Ser Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg
210 215 220
Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Gln Glu Glu Met Thr Lys
225 230 235 240
Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp
245 250 255
Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys
260 265 270
Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser
275 280 285
Arg Leu Thr Val Asp Lys Ser Arg Trp Gln Glu Gly Asn Val Phe Ser
290 295 300
Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser
305 310 315 320
Leu Ser Leu Ser Leu Gly Lys
325
<210> 133
<211> 990
<212> DNA
<213> Homo Sapiens
<400> 133
gcctccacca agggcccatc ggtcttcccc ctggcaccct cctccaagag cacctctggg 60
ggcacagcgg ccctgggctg cctggtcaag gactacttcc ccgaaccggt gacggtgtcg 120
tggaactcag gcgccctgac cagcggcgtg cacaccttcc cggctgtcct acagtcctca 180
ggactctact ccctcagcag cgtggtgacc gtgccctcca gcagcttggg cacccagacc 240
tacatctgca acgtgaatca caagcccagc aacaccaagg tggacaagaa agtggagccc 300
aaatcttgtg acaaaactca cacatgccca ccgtgcccag cacctgaact cgcgggggca 360
ccgtcagtct tcctcttccc cccaaaaccc aaggacaccc tcatgatctc ccggacccct 420
gaggtcacat gcgtggtggt ggacgtgagc cacgaagacc ctgaggtcaa gttcaactgg 480
tacgtggacg gcgtggaggt gcataatgcc aagacaaagc cgcgggagga gcagtacaac 540
agcacgtacc gtgtggtcag cgtcctcacc gtcctgcacc aggactggct gaatggcaag 600
gagtacaagt gcaaggtctc caacaaagcc ctcccagccc ccatcgagaa aaccatctcc 660
aaagccaaag ggcagccccg agaaccacag gtgtacaccc tgcccccatc ccgggatgag 720
ctgaccaaga accaggtcag cctgacctgc ctggtcaaag gcttctatcc cagcgacatc 780
gccgtggagt gggagagcaa tgggcagccg gagaacaact acaagaccac gcctcccgtg 840
ctggactccg acggctcctt cttcctctac agcaagctca ccgtggacaa gagcaggtgg 900
cagcagggga acgtcttctc atgctccgtg atgcatgagg ctctgcacaa ccactacacg 960
cagaagagcc tctccctgtc tccgggtaaa 990
<210> 134
<211> 330
<212> PRT
<213> Homo Sapiens
<400> 134
Ala Ser Thr Lys Gly Pro Ser Val Phe Pro Leu Ala Pro Ser Ser Lys
1 5 10 15
Ser Thr Ser Gly Gly Thr Ala Ala Leu Gly Cys Leu Val Lys Asp Tyr
20 25 30
Phe Pro Glu Pro Val Thr Val Ser Trp Asn Ser Gly Ala Leu Thr Ser
35 40 45
Gly Val His Thr Phe Pro Ala Val Leu Gln Ser Ser Gly Leu Tyr Ser
50 55 60
Leu Ser Ser Val Val Thr Val Pro Ser Ser Ser Leu Gly Thr Gln Thr
65 70 75 80
Tyr Ile Cys Asn Val Asn His Lys Pro Ser Asn Thr Lys Val Asp Lys
85 90 95
Lys Val Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys Pro Pro Cys
100 105 110
Pro Ala Pro Glu Leu Ala Gly Ala Pro Ser Val Phe Leu Phe Pro Pro
115 120 125
Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu Val Thr Cys
130 135 140
Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys Phe Asn Trp
145 150 155 160
Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys Pro Arg Glu
165 170 175
Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu Thr Val Leu
180 185 190
His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys Val Ser Asn
195 200 205
Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys Ala Lys Gly
210 215 220
Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser Arg Asp Glu
225 230 235 240
Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys Gly Phe Tyr
245 250 255
Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln Pro Glu Asn
260 265 270
Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly Ser Phe Phe
275 280 285
Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln Gln Gly Asn
290 295 300
Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn His Tyr Thr
305 310 315 320
Gln Lys Ser Leu Ser Leu Ser Pro Gly Lys
325 330
<210> 135
<211> 321
<212> DNA
<213> Homo Sapiens
<400> 135
cgtacggtgg ccgctccctc cgtgttcatc ttcccacctt ccgacgagca gctgaagtcc 60
ggcaccgctt ctgtcgtgtg cctgctgaac aacttctacc cccgcgaggc caaggtgcag 120
tggaaggtgg acaacgccct gcagtccggc aactcccagg aatccgtgac cgagcaggac 180
tccaaggaca gcacctactc cctgtcctcc accctgaccc tgtccaaggc cgactacgag 240
aagcacaagg tgtacgcctg cgaagtgacc caccagggcc tgtctagccc cgtgaccaag 300
tctttcaacc ggggcgagtg t 321
<210> 136
<211> 107
<212> PRT
<213> Homo Sapiens
<400> 136
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 137
<211> 321
<212> DNA
<213> Homo Sapiens
<400> 137
cgaactgtgg ctgcaccatc tgtcttcatc ttcccgccat ctgatgagca gttgaaatct 60
ggaactgcct ctgttgtgtg cctgctgaat aacttctatc ccagagaggc caaagtacag 120
tggaaggtgg ataacgccct ccaatcgggt aactcccagg agagtgtcac agagcaggag 180
agcaaggaca gcacctacag cctcagcagc accctgacgc tgagcaaagc agactacgag 240
aaacacaaag tctacgccgg cgaagtcacc catcagggcc tgagctcgcc cgtcacaaag 300
agcttcaaca ggggagagtg t 321
<210> 138
<211> 107
<212> PRT
<213> Homo Sapiens
<400> 138
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Glu Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Gly Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 139
<211> 321
<212> DNA
<213> Homo Sapiens
<400> 139
cgaactgtgg ctgcaccatc tgtcttcatc ttcccgccat ctgatgagca gttgaaatct 60
ggaactgcct ctgttgtgtg cctgctgaat aacttctatc ccagagaggc caaagtacag 120
cggaaggtgg ataacgccct ccaatcgggt aactcccagg agagtgtcac agagcaggag 180
agcaaggaca gcacctacag cctcagcagc accctgacgc tgagcaaagc agactacgag 240
aaacacaaag tctacgcctg cgaagtcacc catcagggcc tgagctcgcc cgtcacaaag 300
agcttcaaca ggggagagtg t 321
<210> 140
<211> 107
<212> PRT
<213> Homo Sapiens
<400> 140
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Arg Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Glu Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 141
<211> 321
<212> DNA
<213> Homo Sapiens
<400> 141
cgaactgtgg ctgcaccatc tgtcttcatc ttcccgccat ctgatgagca gttgaaatct 60
ggaactgcct ctgttgtgtg cctgctgaat aacttctatc ccagagaggc caaagtacag 120
tggaaggtgg ataacgccct ccaatcgggt aactcccagg agagtgtcac agagcaggac 180
agcaaggaca gcacctacag cctcagcagc accctgacgc tgagcaaagc agactacgag 240
aaacacaaac tctacgcctg cgaagtcacc catcagggcc tgagctcgcc cgtcacaaag 300
agcttcaaca ggggagagtg t 321
<210> 142
<211> 107
<212> PRT
<213> Homo Sapiens
<400> 142
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Leu Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 143
<211> 321
<212> DNA
<213> Homo Sapiens
<400> 143
cgaactgtgg ctgcaccatc tgtcttcatc ttcccgccat ctgatgagca gttgaaatct 60
ggaactgcct ctgttgtgtg cctgctgaat aacttctatc ccagagaggc caaagtacag 120
tggaaggtgg ataacgccct ccaatcgggt aactcccagg agagtgtcac agagcaggac 180
agcaaggaca gcacctacag cctcagcaac accctgacgc tgagcaaagc agactacgag 240
aaacacaaag tctacgcctg cgaagtcacc catcagggcc tgagctcgcc cgtcacaaag 300
agcttcaaca ggggagagtg c 321
<210> 144
<211> 107
<212> PRT
<213> Homo Sapiens
<400> 144
Arg Thr Val Ala Ala Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu
1 5 10 15
Gln Leu Lys Ser Gly Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe
20 25 30
Tyr Pro Arg Glu Ala Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln
35 40 45
Ser Gly Asn Ser Gln Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser
50 55 60
Thr Tyr Ser Leu Ser Asn Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu
65 70 75 80
Lys His Lys Val Tyr Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser
85 90 95
Pro Val Thr Lys Ser Phe Asn Arg Gly Glu Cys
100 105
<210> 145
<211> 312
<212> DNA
<213> Homo Sapiens
<400> 145
cccaaggcca accccacggt cactctgttc ccgccctcct ctgaggagct ccaagccaac 60
aaggccacac tagtgtgtct gatcagtgac ttctacccgg gagctgtgac agtggcttgg 120
aaggcagatg gcagccccgt caaggcggga gtggagacga ccaaaccctc caaacagagc 180
aacaacaagt acgcggccag cagctacctg agcctgacgc ccgagcagtg gaagtcccac 240
agaagctaca gctgccaggt cacgcatgaa gggagcaccg tggagaagac agtggcccct 300
acagaatgtt ca 312
<210> 146
<211> 104
<212> PRT
<213> Homo Sapiens
<400> 146
Pro Lys Ala Asn Pro Thr Val Thr Leu Phe Pro Pro Ser Ser Glu Glu
1 5 10 15
Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr
20 25 30
Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro Val Lys
35 40 45
Ala Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn Lys Tyr
50 55 60
Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His
65 70 75 80
Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys
85 90 95
Thr Val Ala Pro Thr Glu Cys Ser
100
<210> 147
<211> 318
<212> DNA
<213> Homo Sapiens
<400> 147
ggtcagccca aggccaaccc cactgtcact ctgttcccgc cctcctctga ggagctccaa 60
gccaacaagg ccacactagt gtgtctgatc agtgacttct acccgggagc tgtgacagtg 120
gcctggaagg cagatggcag ccccgtcaag gcgggagtgg agaccaccaa accctccaaa 180
cagagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcccga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 148
<211> 106
<212> PRT
<213> Homo Sapiens
<400> 148
Gly Gln Pro Lys Ala Asn Pro Thr Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 149
<211> 318
<212> DNA
<213> Homo Sapiens
<400> 149
ggtcagccca aggccaaccc cactgtcact ctgttcccgc cctcctctga ggagctccaa 60
gccaacaagg ccacactagt gtgtctgatc agtgacttct acccgggagc tgtgacagtg 120
gcctggaagg cagatggcag ccccgtcaag gcgggagtgg agaccaccaa accctccaaa 180
cagagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcccga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 150
<211> 318
<212> DNA
<213> Homo Sapiens
<400> 150
ggccagccta aggccgctcc ttctgtgacc ctgttccccc catcctccga ggaactgcag 60
gctaacaagg ccaccctcgt gtgcctgatc agcgacttct accctggcgc cgtgaccgtg 120
gcctggaagg ctgatagctc tcctgtgaag gccggcgtgg aaaccaccac cccttccaag 180
cagtccaaca acaaatacgc cgcctcctcc tacctgtccc tgacccctga gcagtggaag 240
tcccaccggt cctacagctg ccaagtgacc cacgagggct ccaccgtgga aaagaccgtg 300
gctcctaccg agtgctcc 318
<210> 151
<211> 318
<212> DNA
<213> Homo Sapiens
<400> 151
ggccagccta aagctgcccc cagcgtcacc ctgtttcctc cctccagcga ggagctccag 60
gccaacaagg ccaccctcgt gtgcctgatc tccgacttct atcccggcgc tgtgaccgtg 120
gcttggaaag ccgactccag ccctgtcaaa gccggcgtgg agaccaccac accctccaag 180
cagtccaaca acaagtacgc cgcctccagc tatctctccc tgacccctga gcagtggaag 240
tcccaccggt cctactcctg tcaggtgacc cacgagggct ccaccgtgga aaagaccgtc 300
gcccccaccg agtgctcc 318
<210> 152
<211> 106
<212> PRT
<213> Homo Sapiens
<400> 152
Gly Gln Pro Lys Ala Asn Pro Thr Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 153
<211> 318
<212> DNA
<213> Homo Sapiens
<400> 153
ggtcagccca aggctgcccc ctcggtcact ctgttcccgc cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcata agtgacttct acccgggagc cgtgacagtg 120
gcctggaagg cagatagcag ccccgtcaag gcgggagtgg agaccaccac accctccaaa 180
caaagcaaca acaagtacgc ggccagcagc tatctgagcc tgacgcctga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 154
<211> 106
<212> PRT
<213> Homo Sapiens
<400> 154
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 155
<211> 312
<212> DNA
<213> Homo Sapiens
<400> 155
cccaaggctg ccccctcggt cactctgttc ccaccctcct ctgaggagct tcaagccaac 60
aaggccacac tggtgtgtct cataagtgac ttctacccgg gagccgtgac agttgcctgg 120
aaggcagata gcagccccgt caaggcgggg gtggagacca ccacaccctc caaacaaagc 180
aacaacaagt acgcggccag cagctacctg agcctgacgc ctgagcagtg gaagtcccac 240
aaaagctaca gctgccaggt cacgcatgaa gggagcaccg tggagaagac agttgcccct 300
acggaatgtt ca 312
<210> 156
<211> 104
<212> PRT
<213> Homo Sapiens
<400> 156
Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser Glu Glu
1 5 10 15
Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp Phe Tyr
20 25 30
Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro Val Lys
35 40 45
Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn Lys Tyr
50 55 60
Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys Ser His
65 70 75 80
Lys Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val Glu Lys
85 90 95
Thr Val Ala Pro Thr Glu Cys Ser
100
<210> 157
<211> 318
<212> DNA
<213> Homo Sapiens
<400> 157
ggtcagccca aggctgcccc ctcggtcact ctgttcccac cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcata agtgacttct acccggggcc agtgacagtt 120
gcctggaagg cagatagcag ccccgtcaag gcgggggtgg agaccaccac accctccaaa 180
caaagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcctga gcagtggaag 240
tcccacaaaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacgg aatgttca 318
<210> 158
<211> 106
<212> PRT
<213> Homo Sapiens
<400> 158
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Pro Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Lys Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 159
<211> 318
<212> DNA
<213> Homo Sapiens
<400> 159
ggtcagccca aggctgcccc ctcggtcact ctgttcccac cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcata agtgacttct acccgggagc cgtgacagtg 120
gcctggaagg cagatagcag ccccgtcaag gcgggagtgg agaccaccac accctccaaa 180
caaagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcctga gcagtggaag 240
tcccacaaaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 160
<211> 106
<212> PRT
<213> Homo Sapiens
<400> 160
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Lys Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 161
<211> 318
<212> DNA
<213> Homo Sapiens
<400> 161
ggtcagccca aggctgcccc ctcggtcact ctgttcccgc cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcata agtgacttct acccgggagc cgtgacagtg 120
gcctggaagg cagatagcag ccccgtcaag gcgggagtgg agaccaccac accctccaaa 180
caaagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcctga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctacag aatgttca 318
<210> 162
<211> 106
<212> PRT
<213> Homo Sapiens
<400> 162
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Ser Ser Pro
35 40 45
Val Lys Ala Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Thr Glu Cys Ser
100 105
<210> 163
<211> 318
<212> DNA
<213> Homo Sapiens
<400> 163
ggtcagccca aggctgcccc atcggtcact ctgttcccgc cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgcctgatc agtgacttct acccgggagc tgtgaaagtg 120
gcctggaagg cagatggcag ccccgtcaac acgggagtgg agaccaccac accctccaaa 180
cagagcaaca acaagtacgc ggccagcagc tacctgagcc tgacgcctga gcagtggaag 240
tcccacagaa gctacagctg ccaggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctgcag aatgttca 318
<210> 164
<211> 106
<212> PRT
<213> Homo Sapiens
<400> 164
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Ile Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Lys Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Asn Thr Gly Val Glu Thr Thr Thr Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Gln Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Ala Glu Cys Ser
100 105
<210> 165
<211> 318
<212> DNA
<213> Homo Sapiens
<400> 165
ggtcagccca aggctgcccc atcggtcact ctgttcccac cctcctctga ggagcttcaa 60
gccaacaagg ccacactggt gtgtctcgta agtgacttct acccgggagc cgtgacagtg 120
gcctggaagg cagatggcag ccccgtcaag gtgggagtgg agaccaccaa accctccaaa 180
caaagcaaca acaagtatgc ggccagcagc tacctgagcc tgacgcccga gcagtggaag 240
tcccacagaa gctacagctg ccgggtcacg catgaaggga gcaccgtgga gaagacagtg 300
gcccctgcag aatgctct 318
<210> 166
<211> 106
<212> PRT
<213> Homo Sapiens
<400> 166
Gly Gln Pro Lys Ala Ala Pro Ser Val Thr Leu Phe Pro Pro Ser Ser
1 5 10 15
Glu Glu Leu Gln Ala Asn Lys Ala Thr Leu Val Cys Leu Val Ser Asp
20 25 30
Phe Tyr Pro Gly Ala Val Thr Val Ala Trp Lys Ala Asp Gly Ser Pro
35 40 45
Val Lys Val Gly Val Glu Thr Thr Lys Pro Ser Lys Gln Ser Asn Asn
50 55 60
Lys Tyr Ala Ala Ser Ser Tyr Leu Ser Leu Thr Pro Glu Gln Trp Lys
65 70 75 80
Ser His Arg Ser Tyr Ser Cys Arg Val Thr His Glu Gly Ser Thr Val
85 90 95
Glu Lys Thr Val Ala Pro Ala Glu Cys Ser
100 105
<210> 167
<211> 615
<212> DNA
<213> Homo Sapiens
<400> 167
atgggctggt cctgcatcat cctgtttctg gtggccaccg ccaccggcgt gcacagcgat 60
tacaaggatg acgacgataa gcgtatgaaa cagatcgaag ataaaattga agagatcttg 120
agcaaaatct atcatatcga aaacgaaatt gcgcgtatca aaaagctgat tggcgaacgt 180
ggcggtggca gcggtggcgg tagcggcggt ggcagccagg tgtcccaccg ataccccagg 240
atccagtcca tcaaggtcca gttcaccgag tacaaaaagg agaagggatt catcctgacc 300
tcccaaaagg aggacgagat catgaaggtg caaaacaact ccgtgatcat caactgcgac 360
ggcttctacc tgatctccct gaagggctac ttctcccagg aggtgaacat ctccctgcac 420
taccagaagg acgaggagcc cctgttccag ctgaagaagg tgaggtccgt gaattccctg 480
atggtggcca gcctgaccta caaggacaag gtctacctga acgtgaccac cgacaacacc 540
agcctggacg acttccatgt caacggcggc gagctgatcc tgatccatca gaaccccggc 600
gagttttgcg tcctg 615
<210> 168
<211> 205
<212> PRT
<213> Homo Sapiens
<400> 168
Met Gly Trp Ser Cys Ile Ile Leu Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Asp Tyr Lys Asp Asp Asp Asp Lys Arg Met Lys Gln Ile
20 25 30
Glu Asp Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile Glu Asn
35 40 45
Glu Ile Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly Gly Gly Ser
50 55 60
Gly Gly Gly Ser Gly Gly Gly Ser Gln Val Ser His Arg Tyr Pro Arg
65 70 75 80
Ile Gln Ser Ile Lys Val Gln Phe Thr Glu Tyr Lys Lys Glu Lys Gly
85 90 95
Phe Ile Leu Thr Ser Gln Lys Glu Asp Glu Ile Met Lys Val Gln Asn
100 105 110
Asn Ser Val Ile Ile Asn Cys Asp Gly Phe Tyr Leu Ile Ser Leu Lys
115 120 125
Gly Tyr Phe Ser Gln Glu Val Asn Ile Ser Leu His Tyr Gln Lys Asp
130 135 140
Glu Glu Pro Leu Phe Gln Leu Lys Lys Val Arg Ser Val Asn Ser Leu
145 150 155 160
Met Val Ala Ser Leu Thr Tyr Lys Asp Lys Val Tyr Leu Asn Val Thr
165 170 175
Thr Asp Asn Thr Ser Leu Asp Asp Phe His Val Asn Gly Gly Glu Leu
180 185 190
Ile Leu Ile His Gln Asn Pro Gly Glu Phe Cys Val Leu
195 200 205
<210> 169
<211> 615
<212> DNA
<213> Homo Sapiens
<400> 169
atgggctggt cctgcatcat cctgtttctg gtggccaccg ccaccggcgt gcacagcgat 60
tacaaggatg acgacgataa gcgtatgaaa cagatcgaag ataaaattga agagatcttg 120
agcaaaatct atcatatcga aaacgaaatt gcgcgtatca aaaagctgat tggcgaacgt 180
ggcggtggca gcggtggcgg tagcggcggt ggcagccagg tgtcccacca ataccccagg 240
atccagtcca tcaaggtcca gttcaccgag tacaaaaagg aggagggatt catcctgacc 300
tcccaaaagg aggacgagat catgaaggtg caaaacaact ccgtgatcat caactgcgac 360
ggcttctacc tgatctccct gaagggctac ttctcccagg aggtgaacat ctccctgcac 420
taccagaagg acgaggagcc cctgttccag ctgaagaagg tgaggtccgt gaattccctg 480
atggtggcca gcctgaccta caaggacaag gtctacctga acgtgaccac cgacaacacc 540
agcctggacg acttccatgt caacggcggc gagctgatcc tgatccatca gaaccccggc 600
gagttttgcg tcctg 615
<210> 170
<211> 205
<212> PRT
<213> Homo Sapiens
<400> 170
Met Gly Trp Ser Cys Ile Ile Leu Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Asp Tyr Lys Asp Asp Asp Asp Lys Arg Met Lys Gln Ile
20 25 30
Glu Asp Lys Ile Glu Glu Ile Leu Ser Lys Ile Tyr His Ile Glu Asn
35 40 45
Glu Ile Ala Arg Ile Lys Lys Leu Ile Gly Glu Arg Gly Gly Gly Ser
50 55 60
Gly Gly Gly Ser Gly Gly Gly Ser Gln Val Ser His Gln Tyr Pro Arg
65 70 75 80
Ile Gln Ser Ile Lys Val Gln Phe Thr Glu Tyr Lys Lys Glu Glu Gly
85 90 95
Phe Ile Leu Thr Ser Gln Lys Glu Asp Glu Ile Met Lys Val Gln Asn
100 105 110
Asn Ser Val Ile Ile Asn Cys Asp Gly Phe Tyr Leu Ile Ser Leu Lys
115 120 125
Gly Tyr Phe Ser Gln Glu Val Asn Ile Ser Leu His Tyr Gln Lys Asp
130 135 140
Glu Glu Pro Leu Phe Gln Leu Lys Lys Val Arg Ser Val Asn Ser Leu
145 150 155 160
Met Val Ala Ser Leu Thr Tyr Lys Asp Lys Val Tyr Leu Asn Val Thr
165 170 175
Thr Asp Asn Thr Ser Leu Asp Asp Phe His Val Asn Gly Gly Glu Leu
180 185 190
Ile Leu Ile His Gln Asn Pro Gly Glu Phe Cys Val Leu
195 200 205
<210> 171
<211> 1332
<212> DNA
<213> Homo Sapiens
<400> 171
atgggctggt cctgcatcat cctgtttctg gtggccaccg ccaccggcgt gcacagcctg 60
cattgcgtgg gcgacaccta tccctccaac gacaggtgct gccacgagtg caggcctgga 120
aacggcatgg tgagcaggtg cagccggtcc cagaataccg tgtgtaggcc ctgcggcccc 180
ggcttttaca acgacgtggt gtcctccaag ccctgcaagc cctgcacatg gtgcaacctg 240
cggtccggca gcgagaggaa gcagctctgc acagccaccc aggacaccgt ctgtaggtgt 300
agggctggca cccagcctct ggactcctac aagcccggcg tggattgtgc tccttgccct 360
cccggccatt tctcccctgg cgacaaccag gcttgcaagc cctggaccaa ctgtaccctg 420
gccggcaagc atacactgca gcctgcttcc aactcctccg acgctatctg cgaggatagg 480
gacccccctg ccacacaacc ccaggagaca cagggccctc ctgctaggcc catcacagtc 540
caacccaccg aagcctggcc caggacatcc caaggccctt ccaccaggcc tgtggaagtg 600
cctggaggaa gggctgtggc cattgaaggt cgtatggatg aacccaagtc ctgcgacaag 660
acccacacct gtcccccttg tcctgcccct gaactgctgg gcggaccttc cgtgttcctg 720
ttccccccaa agcccaagga caccctgatg atctcccgga cccccgaagt gacctgcgtg 780
gtggtggatg tgtcccacga ggaccctgaa gtgaagttca attggtacgt ggacggcgtg 840
gaagtgcaca acgccaagac caagcctaga gaggaacagt acaactccac ctaccgggtg 900
gtgtccgtgc tgaccgtgct gcaccaggat tggctgaacg gcaaagagta caagtgcaag 960
gtgtccaaca aggccctgcc tgcccccatc gaaaagacca tctccaaggc caagggccag 1020
ccccgggaac cccaggtgta cacactgccc cctagcaggg acgagctgac caagaaccag 1080
gtgtccctga cctgtctcgt gaaaggcttc tacccctccg atatcgccgt ggaatgggag 1140
tccaacggcc agcctgagaa caactacaag accacccccc ctgtgctgga ctccgacggc 1200
tcattcttcc tgtacagcaa gctgacagtg gacaagtccc ggtggcagca gggcaacgtg 1260
ttctcctgct ccgtgatgca cgaggccctg cacaaccact acacccagaa gtccctgtcc 1320
ctgagcccct ga 1332
<210> 172
<211> 443
<212> PRT
<213> Homo Sapiens
<400> 172
Met Gly Trp Ser Cys Ile Ile Leu Phe Leu Val Ala Thr Ala Thr Gly
1 5 10 15
Val His Ser Leu His Cys Val Gly Asp Thr Tyr Pro Ser Asn Asp Arg
20 25 30
Cys Cys His Glu Cys Arg Pro Gly Asn Gly Met Val Ser Arg Cys Ser
35 40 45
Arg Ser Gln Asn Thr Val Cys Arg Pro Cys Gly Pro Gly Phe Tyr Asn
50 55 60
Asp Val Val Ser Ser Lys Pro Cys Lys Pro Cys Thr Trp Cys Asn Leu
65 70 75 80
Arg Ser Gly Ser Glu Arg Lys Gln Leu Cys Thr Ala Thr Gln Asp Thr
85 90 95
Val Cys Arg Cys Arg Ala Gly Thr Gln Pro Leu Asp Ser Tyr Lys Pro
100 105 110
Gly Val Asp Cys Ala Pro Cys Pro Pro Gly His Phe Ser Pro Gly Asp
115 120 125
Asn Gln Ala Cys Lys Pro Trp Thr Asn Cys Thr Leu Ala Gly Lys His
130 135 140
Thr Leu Gln Pro Ala Ser Asn Ser Ser Asp Ala Ile Cys Glu Asp Arg
145 150 155 160
Asp Pro Pro Ala Thr Gln Pro Gln Glu Thr Gln Gly Pro Pro Ala Arg
165 170 175
Pro Ile Thr Val Gln Pro Thr Glu Ala Trp Pro Arg Thr Ser Gln Gly
180 185 190
Pro Ser Thr Arg Pro Val Glu Val Pro Gly Gly Arg Ala Val Ala Ile
195 200 205
Glu Gly Arg Met Asp Glu Pro Lys Ser Cys Asp Lys Thr His Thr Cys
210 215 220
Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly Pro Ser Val Phe Leu
225 230 235 240
Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile Ser Arg Thr Pro Glu
245 250 255
Val Thr Cys Val Val Val Asp Val Ser His Glu Asp Pro Glu Val Lys
260 265 270
Phe Asn Trp Tyr Val Asp Gly Val Glu Val His Asn Ala Lys Thr Lys
275 280 285
Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg Val Val Ser Val Leu
290 295 300
Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys Glu Tyr Lys Cys Lys
305 310 315 320
Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu Lys Thr Ile Ser Lys
325 330 335
Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr Thr Leu Pro Pro Ser
340 345 350
Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu Thr Cys Leu Val Lys
355 360 365
Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp Glu Ser Asn Gly Gln
370 375 380
Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val Leu Asp Ser Asp Gly
385 390 395 400
Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp Lys Ser Arg Trp Gln
405 410 415
Gln Gly Asn Val Phe Ser Cys Ser Val Met His Glu Ala Leu His Asn
420 425 430
His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440
<210> 173
<211> 552
<212> DNA
<213> Homo Sapiens
<400> 173
atggagaggg tgcagcccct cgaggagaac gtgggaaacg ccgccaggcc taggttcgag 60
aggaacaagc tgctgctggt ggcttccgtg atccaaggac tcggcctgct gctctgcttc 120
acctacatct gcctccactt cagcgccctg caggtgtccc accgataccc caggatccag 180
tccatcaagg tccagttcac cgagtacaaa aaggagaagg gattcatcct gacctcccaa 240
aaggaggacg agatcatgaa ggtgcaaaac aactccgtga tcatcaactg cgacggcttc 300
tacctgatct ccctgaaggg ctacttctcc caggaggtga acatctccct gcactaccag 360
aaggacgagg agcccctgtt ccagctgaag aaggtgaggt ccgtgaattc cctgatggtg 420
gccagcctga cctacaagga caaggtctac ctgaacgtga ccaccgacaa caccagcctg 480
gacgacttcc atgtcaacgg cggcgagctg atcctgatcc atcagaaccc cggcgagttt 540
tgcgtcctgt aa 552
<210> 174
<211> 181
<212> PRT
<213> Homo Sapiens
<400> 174
Met Glu Arg Val Gln Pro Leu Glu Glu Asn Val Gly Asn Ala Ala Arg
1 5 10 15
Pro Arg Phe Glu Arg Asn Lys Leu Leu Leu Val Ala Ser Val Ile Gln
20 25 30
Gly Leu Gly Leu Leu Leu Cys Phe Thr Tyr Ile Cys Leu His Phe Ser
35 40 45
Ala Leu Gln Val Ser His Arg Tyr Pro Arg Ile Gln Ser Ile Lys Val
50 55 60
Gln Phe Thr Glu Tyr Lys Lys Glu Lys Gly Phe Ile Leu Thr Ser Gln
65 70 75 80
Lys Glu Asp Glu Ile Met Lys Val Gln Asn Asn Ser Val Ile Ile Asn
85 90 95
Cys Asp Gly Phe Tyr Leu Ile Ser Leu Lys Gly Tyr Phe Ser Gln Glu
100 105 110
Val Asn Ile Ser Leu His Tyr Gln Lys Asp Glu Glu Pro Leu Phe Gln
115 120 125
Leu Lys Lys Val Arg Ser Val Asn Ser Leu Met Val Ala Ser Leu Thr
130 135 140
Tyr Lys Asp Lys Val Tyr Leu Asn Val Thr Thr Asp Asn Thr Ser Leu
145 150 155 160
Asp Asp Phe His Val Asn Gly Gly Glu Leu Ile Leu Ile His Gln Asn
165 170 175
Pro Gly Glu Phe Cys
180
<210> 175
<211> 834
<212> DNA
<213> Homo Sapiens
<400> 175
atgtgcgtgg gggctcggcg gctgggccgc gggccgtgtg cggctctgct cctcctgggc 60
ctggggctga gcaccgtgac ggggctccac tgtgtcgggg acacctaccc cagcaacgac 120
cggtgctgcc acgagtgcag gccaggcaac gggatggtga gccgctgcag ccgctcccag 180
aacacggtgt gccgtccgtg cgggccgggc ttctacaacg acgtggtcag ctccaagccg 240
tgcaagccct gcacgtggtg taacctcaga agtgggagtg agcggaagca gctgtgcacg 300
gccacacagg acacagtctg ccgctgccgg gcgggcaccc agcccctgga cagctacaag 360
cctggagttg actgtgcccc ctgccctcca gggcacttct ccccaggcga caaccaggcc 420
tgcaagccct ggaccaactg caccttggct gggaagcaca ccctgcagcc ggccagcaat 480
agctcggacg caatctgtga ggacagggac cccccagcca cgcagcccca ggagacccag 540
ggccccccgg ccaggcccat cactgtccag cccactgaag cctggcccag aacctcacag 600
ggaccctcca cccggcccgt ggaggtcccc gggggccgtg cggttgccgc catcctgggc 660
ctgggcctgg tgctggggct gctgggcccc ctggccatcc tgctggccct gtacctgctc 720
cggagggacc agaggctgcc ccccgatgcc cacaagcccc ctgggggagg cagtttccgg 780
acccccatcc aagaggagca ggccgacgcc cactccaccc tggccaagat ctga 834
<210> 176
<211> 277
<212> PRT
<213> Homo Sapiens
<400> 176
Met Cys Val Gly Ala Arg Arg Leu Gly Arg Gly Pro Cys Ala Ala Leu
1 5 10 15
Leu Leu Leu Gly Leu Gly Leu Ser Thr Val Thr Gly Leu His Cys Val
20 25 30
Gly Asp Thr Tyr Pro Ser Asn Asp Arg Cys Cys His Glu Cys Arg Pro
35 40 45
Gly Asn Gly Met Val Ser Arg Cys Ser Arg Ser Gln Asn Thr Val Cys
50 55 60
Arg Pro Cys Gly Pro Gly Phe Tyr Asn Asp Val Val Ser Ser Lys Pro
65 70 75 80
Cys Lys Pro Cys Thr Trp Cys Asn Leu Arg Ser Gly Ser Glu Arg Lys
85 90 95
Gln Leu Cys Thr Ala Thr Gln Asp Thr Val Cys Arg Cys Arg Ala Gly
100 105 110
Thr Gln Pro Leu Asp Ser Tyr Lys Pro Gly Val Asp Cys Ala Pro Cys
115 120 125
Pro Pro Gly His Phe Ser Pro Gly Asp Asn Gln Ala Cys Lys Pro Trp
130 135 140
Thr Asn Cys Thr Leu Ala Gly Lys His Thr Leu Gln Pro Ala Ser Asn
145 150 155 160
Ser Ser Asp Ala Ile Cys Glu Asp Arg Asp Pro Pro Ala Thr Gln Pro
165 170 175
Gln Glu Thr Gln Gly Pro Pro Ala Arg Pro Ile Thr Val Gln Pro Thr
180 185 190
Glu Ala Trp Pro Arg Thr Ser Gln Gly Pro Ser Thr Arg Pro Val Glu
195 200 205
Val Pro Gly Gly Arg Ala Val Ala Ala Ile Leu Gly Leu Gly Leu Val
210 215 220
Leu Gly Leu Leu Gly Pro Leu Ala Ile Leu Leu Ala Leu Tyr Leu Leu
225 230 235 240
Arg Arg Asp Gln Arg Leu Pro Pro Asp Ala His Lys Pro Pro Gly Gly
245 250 255
Gly Ser Phe Arg Thr Pro Ile Gln Glu Glu Gln Ala Asp Ala His Ser
260 265 270
Thr Leu Ala Lys Ile
275
<210> 177
<211> 117
<212> PRT
<213> Homo sapiens
<400> 177
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Thr Gly Glu Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Ile Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Asn Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Gln
100 105 110
Val Thr Val Ser Ser
115
<210> 178
<211> 128
<212> PRT
<213> Homo sapiens
<400> 178
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Val Ala Ser Gly Arg Ser Phe Ser Thr Tyr
20 25 30
Ile Met Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ala Thr Ile Ser Arg Ser Gly Ile Thr Ile Arg Ser Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ala Gly Pro Tyr Val Glu Gln Thr Leu Gly Leu Tyr Gln Thr Leu
100 105 110
Gly Pro Trp Asp Tyr Trp Gly Gln Gly Thr Gln Val Thr Val Ser Ser
115 120 125
<210> 179
<211> 124
<212> PRT
<213> Homo sapiens
<400> 179
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Thr Phe Ser Ser Ile
20 25 30
Tyr Ala Lys Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe
35 40 45
Val Ala Ala Ile Ser Arg Ser Gly Arg Ser Thr Ser Tyr Ala Asp Ser
50 55 60
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Ala Val Gly Gly Ala Thr Thr Val Thr Ala Ser Glu Trp Asp
100 105 110
Tyr Trp Gly Leu Gly Thr Gln Val Thr Val Ser Ser
115 120
<210> 180
<211> 125
<212> PRT
<213> Homo sapiens
<400> 180
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Asp
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Leu Thr Phe Ser Ser Phe
20 25 30
Ala Met Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ala Ala Ile Ser Arg Ser Gly Tyr Gly Thr Ser Glu Ala Asp Ser Val
50 55 60
Arg Asp Arg Phe Ile Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Thr
65 70 75 80
Leu His Leu Ser Arg Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ala Glu His Thr Leu Gly Arg Pro Ser Arg Ser Gln Ile Asn Tyr
100 105 110
Leu Tyr Trp Gly Gln Gly Thr Gln Val Thr Val Ser Ser
115 120 125
<210> 181
<211> 117
<212> PRT
<213> Homo sapiens
<400> 181
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Asn Ile Leu Ser Leu Asn
20 25 30
Thr Met Gly Trp Tyr Arg His Ala Pro Gly Lys Pro Arg Glu Leu Val
35 40 45
Ala Arg Ile Ser Ser Asn Ser Lys Thr Asp Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Leu Leu
65 70 75 80
Gln Met Asn Ser Leu Lys Pro Glu Asp Thr Gly Val Tyr Tyr Cys Asn
85 90 95
Leu Asn Val Trp Arg Thr Ser Ser Asp Tyr Trp Gly Gln Gly Thr Gln
100 105 110
Val Thr Val Ser Ser
115
<210> 182
<211> 128
<212> PRT
<213> Homo sapiens
<400> 182
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Leu Asp Asp Tyr
20 25 30
Ala Ile Ala Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Gly Val
35 40 45
Ser Arg Ile Lys Ile Ser Asn Gly Arg Thr Thr Tyr Ala Gly Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Ser Asp Asn Ala Lys Asn Thr Val Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Asn Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ala Asp Arg Ser Ser Leu Leu Phe Gly Ser Asn Trp Asp Arg Lys
100 105 110
Ala Arg Tyr Asp Tyr Trp Gly Gln Gly Thr Gln Val Thr Val Ser Ser
115 120 125
<210> 183
<211> 125
<212> PRT
<213> Homo sapiens
<400> 183
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Ala
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Arg Phe Ile Ser Asn
20 25 30
Tyr Ala Met Gly Trp Phe Arg Gln Ala Pro Gly Gln Glu Arg Ala Phe
35 40 45
Val Ala Ala Ile Ser Arg Ser Gly Ser Ile Thr Tyr Tyr Thr Asp Ser
50 55 60
Val Lys Gly Arg Phe Ser Ile Ser Arg Asp Tyr Ala Lys Ser Thr Val
65 70 75 80
Tyr Leu Gln Met Asp Asn Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Ala Asp Gly Gly Ala Val Arg Asp Leu Thr Thr Asn Leu Pro
100 105 110
Asp Tyr Trp Gly Arg Gly Thr Gln Val Thr Val Ser Ser
115 120 125
<210> 184
<211> 128
<212> PRT
<213> Homo sapiens
<400> 184
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Ser Phe Ser Thr Tyr
20 25 30
Ile Met Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe Val
35 40 45
Ala Thr Ile Ser Arg Ser Gly Ile Thr Thr Arg Ser Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Ala Gly Pro Tyr Val Glu Gln Thr Leu Gly Leu Tyr Gln Thr Leu
100 105 110
Gly Pro Trp Asp Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120 125
<210> 185
<211> 124
<212> PRT
<213> Homo sapiens
<400> 185
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Thr Phe Ser Ser Ile
20 25 30
Tyr Ala Lys Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe
35 40 45
Val Ala Ala Ile Ser Arg Ser Gly Arg Ser Thr Ser Tyr Ala Asp Ser
50 55 60
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Ala Val Gly Gly Ala Thr Thr Val Thr Ala Ser Glu Trp Asp
100 105 110
Tyr Trp Gly Leu Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 186
<211> 124
<212> PRT
<213> Homo sapiens
<400> 186
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Thr Phe Ser Ser Ile
20 25 30
Tyr Ala Lys Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe
35 40 45
Val Ala Ala Ile Ser Arg Ser Gly Arg Ser Thr Ser Tyr Ala Asp Ser
50 55 60
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Ala Val Gly Gly Ala Thr Thr Val Thr Ala Ser Glu Trp Asp
100 105 110
Tyr Trp Gly Leu Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 187
<211> 124
<212> PRT
<213> Homo sapiens
<400> 187
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Thr Phe Ser Ser Ile
20 25 30
Tyr Ala Lys Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe
35 40 45
Val Ala Ala Ile Ser Arg Ser Gly Arg Ser Thr Ser Tyr Ala Asp Ser
50 55 60
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Ala Val Gly Gly Ala Thr Thr Val Thr Ala Ser Glu Trp Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 188
<211> 124
<212> PRT
<213> Homo sapiens
<400> 188
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Thr Phe Ser Ser Ile
20 25 30
Tyr Ala Lys Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe
35 40 45
Val Ala Ala Ile Ser Arg Ser Gly Arg Ser Thr Ser Tyr Ala Asp Ser
50 55 60
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Ala Val Gly Gly Ala Thr Thr Val Thr Ala Ser Glu Trp Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 189
<211> 124
<212> PRT
<213> Homo sapiens
<400> 189
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Thr Phe Ser Ser Ile
20 25 30
Tyr Ala Lys Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe
35 40 45
Val Ala Ala Ile Ser Arg Ser Gly Arg Ser Thr Ser Tyr Ala Asp Ser
50 55 60
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Ala Val Gly Gly Ala Thr Thr Val Thr Ala Ser Glu Trp Asp
100 105 110
Tyr Trp Gly Leu Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 190
<211> 124
<212> PRT
<213> Homo sapiens
<400> 190
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Arg Thr Phe Ser Ser Ile
20 25 30
Tyr Ala Lys Gly Trp Phe Arg Gln Ala Pro Gly Lys Glu Arg Glu Phe
35 40 45
Val Ala Ala Ile Ser Arg Ser Gly Arg Ser Thr Ser Tyr Ala Asp Ser
50 55 60
Val Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val
65 70 75 80
Tyr Leu Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr
85 90 95
Cys Ala Ala Val Gly Gly Ala Thr Thr Val Thr Ala Ser Glu Trp Asp
100 105 110
Tyr Trp Gly Gln Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 191
<211> 117
<212> PRT
<213> Homo sapiens
<400> 191
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Ala Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Thr Gly Glu Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Ile Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Asn Leu Lys Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Gln
100 105 110
Val Thr Val Ser Ser
115
<210> 192
<211> 117
<212> PRT
<213> Homo sapiens
<400> 192
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Thr Gly Glu Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 193
<211> 117
<212> PRT
<213> Homo sapiens
<400> 193
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Ala Thr Gly Glu Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 194
<211> 117
<212> PRT
<213> Homo sapiens
<400> 194
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Pro Gly Glu Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 195
<211> 117
<212> PRT
<213> Homo sapiens
<400> 195
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Thr Gly Lys Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 196
<211> 117
<212> PRT
<213> Homo sapiens
<400> 196
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Ala Pro Gly Glu Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 197
<211> 117
<212> PRT
<213> Homo sapiens
<400> 197
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Ala Thr Gly Lys Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 198
<211> 117
<212> PRT
<213> Homo sapiens
<400> 198
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Pro Gly Lys Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 199
<211> 117
<212> PRT
<213> Homo sapiens
<400> 199
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Ala Pro Gly Lys Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 200
<211> 117
<212> PRT
<213> Homo sapiens
<400> 200
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Thr Gly Glu Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Ala Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 201
<211> 117
<212> PRT
<213> Homo sapiens
<400> 201
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Thr Gly Glu Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 202
<211> 117
<212> PRT
<213> Homo sapiens
<400> 202
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Thr Gly Glu Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 203
<211> 117
<212> PRT
<213> Homo sapiens
<400> 203
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Thr Gly Glu Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Ile Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 204
<211> 117
<212> PRT
<213> Homo sapiens
<400> 204
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Thr Gly Glu Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ala Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 205
<211> 117
<212> PRT
<213> Homo sapiens
<400> 205
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Thr Gly Glu Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Phe Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Asn Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 206
<211> 117
<212> PRT
<213> Homo sapiens
<400> 206
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Pro Gly Lys Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 207
<211> 117
<212> PRT
<213> Homo sapiens
<400> 207
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Pro Gly Lys Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Ile Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 208
<211> 117
<212> PRT
<213> Homo sapiens
<400> 208
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Pro Gly Lys Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Asn Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 209
<211> 117
<212> PRT
<213> Homo sapiens
<400> 209
Asp Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Pro Gly Lys Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Ala Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Ile Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Asn Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 210
<211> 117
<212> PRT
<213> Homo sapiens
<400> 210
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Pro Gly Glu Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Ile Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 211
<211> 117
<212> PRT
<213> Homo sapiens
<400> 211
Glu Val Gln Leu Val Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Arg Ser Ile Gly Arg Leu Asp
20 25 30
Arg Met Gly Trp Tyr Arg His Arg Pro Gly Lys Pro Arg Glu Leu Val
35 40 45
Ala Thr Ile Thr Gly Gly Ser Ser Ile Asn Tyr Gly Asp Ser Val Lys
50 55 60
Gly Arg Phe Thr Ile Ser Ile Asp Asn Ser Lys Asn Thr Val Tyr Leu
65 70 75 80
Gln Met Asn Ser Leu Arg Pro Glu Asp Thr Ala Val Tyr Tyr Cys Asn
85 90 95
Phe Asn Lys Tyr Val Thr Ser Arg Asp Thr Trp Gly Gln Gly Thr Leu
100 105 110
Val Thr Val Ser Ser
115
<210> 212
<211> 450
<212> PRT
<213> Homo sapiens
<400> 212
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Leu Ile Ser Gly Ser Gly Gly Phe Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Thr Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Leu Val Ala Pro Gly Thr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Ala Leu Val Thr Val Ser Ser Ala Ser Thr Lys Gly Pro Ser Val
115 120 125
Phe Pro Leu Ala Pro Ser Ser Lys Ser Thr Ser Gly Gly Thr Ala Ala
130 135 140
Leu Gly Cys Leu Val Lys Asp Tyr Phe Pro Glu Pro Val Thr Val Ser
145 150 155 160
Trp Asn Ser Gly Ala Leu Thr Ser Gly Val His Thr Phe Pro Ala Val
165 170 175
Leu Gln Ser Ser Gly Leu Tyr Ser Leu Ser Ser Val Val Thr Val Pro
180 185 190
Ser Ser Ser Leu Gly Thr Gln Thr Tyr Ile Cys Asn Val Asn His Lys
195 200 205
Pro Ser Asn Thr Lys Val Asp Lys Lys Val Glu Pro Lys Ser Cys Asp
210 215 220
Lys Thr His Thr Cys Pro Pro Cys Pro Ala Pro Glu Leu Leu Gly Gly
225 230 235 240
Pro Ser Val Phe Leu Phe Pro Pro Lys Pro Lys Asp Thr Leu Met Ile
245 250 255
Ser Arg Thr Pro Glu Val Thr Cys Val Val Val Asp Val Ser His Glu
260 265 270
Asp Pro Glu Val Lys Phe Asn Trp Tyr Val Asp Gly Val Glu Val His
275 280 285
Asn Ala Lys Thr Lys Pro Arg Glu Glu Gln Tyr Asn Ser Thr Tyr Arg
290 295 300
Val Val Ser Val Leu Thr Val Leu His Gln Asp Trp Leu Asn Gly Lys
305 310 315 320
Glu Tyr Lys Cys Lys Val Ser Asn Lys Ala Leu Pro Ala Pro Ile Glu
325 330 335
Lys Thr Ile Ser Lys Ala Lys Gly Gln Pro Arg Glu Pro Gln Val Tyr
340 345 350
Thr Leu Pro Pro Ser Arg Asp Glu Leu Thr Lys Asn Gln Val Ser Leu
355 360 365
Thr Cys Leu Val Lys Gly Phe Tyr Pro Ser Asp Ile Ala Val Glu Trp
370 375 380
Glu Ser Asn Gly Gln Pro Glu Asn Asn Tyr Lys Thr Thr Pro Pro Val
385 390 395 400
Leu Asp Ser Asp Gly Ser Phe Phe Leu Tyr Ser Lys Leu Thr Val Asp
405 410 415
Lys Ser Arg Trp Gln Gln Gly Asn Val Phe Ser Cys Ser Val Met His
420 425 430
Glu Ala Leu His Asn His Tyr Thr Gln Lys Ser Leu Ser Leu Ser Pro
435 440 445
Gly Lys
450
<210> 213
<211> 214
<212> PRT
<213> Homo sapiens
<400> 213
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Glu Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys Arg Thr Val Ala Ala
100 105 110
Pro Ser Val Phe Ile Phe Pro Pro Ser Asp Glu Gln Leu Lys Ser Gly
115 120 125
Thr Ala Ser Val Val Cys Leu Leu Asn Asn Phe Tyr Pro Arg Glu Ala
130 135 140
Lys Val Gln Trp Lys Val Asp Asn Ala Leu Gln Ser Gly Asn Ser Gln
145 150 155 160
Glu Ser Val Thr Glu Gln Asp Ser Lys Asp Ser Thr Tyr Ser Leu Ser
165 170 175
Ser Thr Leu Thr Leu Ser Lys Ala Asp Tyr Glu Lys His Lys Val Tyr
180 185 190
Ala Cys Glu Val Thr His Gln Gly Leu Ser Ser Pro Val Thr Lys Ser
195 200 205
Phe Asn Arg Gly Glu Cys
210
<210> 214
<211> 107
<212> PRT
<213> Homo sapiens
<400> 214
Asp Ile Gln Met Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Trp
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Glu Lys Ala Pro Lys Ser Leu Ile
35 40 45
Tyr Ala Ala Ser Ser Leu Gln Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Tyr Asn Ser Tyr Pro Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile Lys
100 105
<210> 215
<211> 120
<212> PRT
<213> Homo sapiens
<400> 215
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ile Ile Ser Gly Ser Gly Gly Phe Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Thr Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Leu Val Ala Pro Gly Thr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Ala Leu Val Thr Val Ser Ser
115 120
<210> 216
<211> 107
<212> PRT
<213> Homo sapiens
<400> 216
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 217
<211> 120
<212> PRT
<213> Homo sapiens
<400> 217
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Phe
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ala Ile Trp Tyr Asp Gly His Asp Lys Tyr Tyr Ser Tyr Tyr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Ser Ser Trp Tyr Arg Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 218
<211> 107
<212> PRT
<213> Homo sapiens
<400> 218
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Ser
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 219
<211> 120
<212> PRT
<213> Homo sapiens
<400> 219
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Phe
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ala Ile Trp Tyr Asp Gly His Asp Lys Tyr Tyr Ala Tyr Tyr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Ser Ser Trp Tyr Arg Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 220
<211> 120
<212> PRT
<213> Homo sapiens
<400> 220
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Phe
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Ala Ile Trp Tyr Asp Gly His Asp Lys Tyr Tyr Ser Tyr Tyr Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Phe
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Ser Ser Ser Trp Tyr Arg Tyr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 221
<211> 116
<212> PRT
<213> Homo sapiens
<400> 221
Gln Val Gln Leu Val Glu Ser Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Thr Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Tyr Asp Gly Ser Asn Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Lys Asn Trp Ser Phe Asp Phe Trp Gly Gln Gly Thr Leu Val
100 105 110
Thr Val Ser Ser
115
<210> 222
<211> 106
<212> PRT
<213> Homo sapiens
<400> 222
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Gly Val Ser Arg Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Val Ser Gly
50 55 60
Ser Gly Pro Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Asp Tyr Cys Gln Gln Arg Ser Asn Trp Gln Tyr
85 90 95
Thr Phe Gly Gln Gly Thr Lys Leu Glu Ile
100 105
<210> 223
<211> 121
<212> PRT
<213> Homo sapiens
<400> 223
Gln Lys Gln Leu Val Glu Phe Gly Gly Gly Val Val Gln Pro Gly Arg
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Asn Tyr
20 25 30
Gly Met His Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ala Val Ile Trp Asn Asp Gly Ser Asn Lys Tyr Tyr Val Asp Ser Val
50 55 60
Lys Gly Arg Phe Ile Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Arg Asp Arg Met Gly Ile Tyr Tyr Tyr Gly Met Asp Val Trp Gly
100 105 110
Gln Gly Thr Thr Val Thr Val Ser Ser
115 120
<210> 224
<211> 104
<212> PRT
<213> Homo sapiens
<400> 224
Glu Ile Val Leu Thr Gln Ser Pro Ala Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Tyr
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu Ile
35 40 45
Tyr Asp Ala Ser Asn Arg Ala Thr Gly Ile Pro Ala Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Glu Pro
65 70 75 80
Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Arg Ser Asn Trp Thr Phe
85 90 95
Gly Gln Gly Thr Lys Val Glu Ile
100
<210> 225
<211> 120
<212> PRT
<213> Homo sapiens
<400> 225
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Asn Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ile Ile Ser Gly Ser Gly Gly Phe Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Arg Thr Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Arg Leu Val Ala Pro Gly Thr Phe Asp Tyr Trp Gly Gln
100 105 110
Gly Ala Leu Val Thr Val Ser Ser
115 120
<210> 226
<211> 107
<212> PRT
<213> Homo sapiens
<400> 226
Glu Ile Val Leu Thr Gln Ser Pro Gly Thr Leu Ser Leu Ser Pro Gly
1 5 10 15
Glu Arg Ala Thr Leu Ser Cys Arg Ala Ser Gln Ser Val Ser Ser Asn
20 25 30
Tyr Leu Ala Trp Tyr Gln Gln Lys Pro Gly Gln Ala Pro Arg Leu Leu
35 40 45
Ile Tyr Gly Ala Ser Ser Arg Ala Thr Gly Ile Pro Asp Arg Phe Ser
50 55 60
Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Arg Leu Glu
65 70 75 80
Pro Glu Asp Phe Ala Val Tyr Tyr Cys Gln Gln Tyr Gly Ser Ser Phe
85 90 95
Thr Phe Gly Pro Gly Thr Lys Val Asp Ile Lys
100 105
<210> 227
<211> 120
<212> PRT
<213> Homo sapiens
<400> 227
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ile Ile Ser Gly Ser Gly Gly Phe Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Asn Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Arg Leu Arg Ala Glu Asp Thr Ala Ile Tyr Phe Cys
85 90 95
Ala Lys Asp Asp Ile Pro Ala Ala Gly Thr Phe Asp Pro Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 228
<211> 106
<212> PRT
<213> Homo sapiens
<400> 228
Ala Ile Gln Leu Thr Gln Ser Pro Ser Ser Leu Ser Ala Ser Val Gly
1 5 10 15
Asp Arg Val Thr Ile Thr Cys Arg Ala Ser Gln Gly Ile Ser Ser Ala
20 25 30
Leu Ala Trp Tyr Gln Gln Lys Pro Gly Lys Ala Pro Lys Leu Leu Ile
35 40 45
Tyr Asp Val Ser Ser Leu Glu Ser Gly Val Pro Ser Arg Phe Ser Gly
50 55 60
Ser Gly Ser Gly Thr Asp Phe Thr Leu Thr Ile Ser Ser Leu Gln Pro
65 70 75 80
Glu Asp Phe Ala Thr Tyr Tyr Cys Gln Gln Phe Asn Ser Tyr Trp Thr
85 90 95
Phe Gly Gln Gly Thr Lys Val Glu Ile Lys
100 105
<210> 229
<211> 119
<212> PRT
<213> Homo sapiens
<400> 229
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Ser Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Leu Ile Ser Gly Ser Gly Gly Leu Thr Lys Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Arg Thr Leu Tyr
65 70 75 80
Leu Gln Met Asn Ser Leu Arg Ala Glu Asp Thr Ala Val Tyr Tyr Cys
85 90 95
Ala Lys Asp Ile Leu Val Thr Gly Ala Leu Asp Tyr Trp Gly Gln Gly
100 105 110
Thr Leu Val Thr Val Ser Ser
115
<210> 230
<211> 120
<212> PRT
<213> Homo sapiens
<400> 230
Glu Val Gln Leu Leu Glu Ser Gly Gly Gly Leu Val Gln Pro Gly Gly
1 5 10 15
Ser Leu Arg Leu Ser Cys Ala Ala Ser Gly Phe Thr Phe Ser Ser Tyr
20 25 30
Ala Met Asn Trp Val Arg Gln Ala Pro Gly Lys Gly Leu Glu Trp Val
35 40 45
Ser Ile Ile Ser Gly Ser Gly Gly Phe Thr Tyr Tyr Ala Asp Ser Val
50 55 60
Lys Gly Arg Phe Thr Ile Ser Arg Asp Asn Ser Lys Lys Thr Leu Tyr
65 70 75 80
Leu Gln Met Ser Arg Leu Arg Ala Glu Asp Thr Ala Ile Tyr Phe Cys
85 90 95
Ala Lys Asp Asp Ile Pro Ala Ala Gly Thr Phe Asp Pro Trp Gly Gln
100 105 110
Gly Thr Leu Val Thr Val Ser Ser
115 120
<210> 231
<211> 113
<212> PRT
<213> Homo sapiens
<400> 231
Asp Ile Leu Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Ile Ser Cys Arg Ser Ser Gln Ser Ile Val His Gly
20 25 30
Asn Gly Asn Thr Tyr Leu Glu Trp His Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Arg Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Asn Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Tyr Cys Phe Gln Gly
85 90 95
Ser His Val Pro Tyr Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg
<210> 232
<211> 113
<212> PRT
<213> Homo sapiens
<400> 232
Asp Ile Val Met Thr Gln Thr Pro Leu Ser Leu Pro Val Ser Leu Gly
1 5 10 15
Asp Gln Ala Ser Met Tyr Cys Arg Ser Ser Gln Ser Pro Val His Ser
20 25 30
Asn Gly Asn Thr Tyr Leu His Trp Tyr Leu Gln Lys Pro Gly Gln Ser
35 40 45
Pro Lys Leu Leu Ile Tyr Lys Val Ser Asn Arg Phe Ser Gly Val Pro
50 55 60
Asp Arg Phe Ser Gly Ser Gly Ser Gly Thr Asp Phe Thr Leu Lys Ile
65 70 75 80
Ser Arg Val Glu Ala Glu Asp Leu Gly Val Tyr Phe Cys Ser Gln Ser
85 90 95
Thr His Ile Pro Trp Thr Phe Gly Gly Gly Thr Lys Val Glu Ile Lys
100 105 110
Arg
<210> 233
<211> 123
<212> PRT
<213> Homo sapiens
<400> 233
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Arg Pro Gly Ala
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Thr Phe Thr Ser Tyr
20 25 30
Trp Leu Asn Trp Val Lys Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Val Met Ile Asp Pro Ser Asp Ser Glu Thr His Tyr Asn Gln Val Phe
50 55 60
Lys Asp Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Met Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Ile Arg Gly Arg Gly Asn Phe Tyr Gly Gly Ser His Ala Met Glu Tyr
100 105 110
Trp Gly Gln Gly Thr Leu Leu Thr Val Ser Ser
115 120
<210> 234
<211> 118
<212> PRT
<213> Homo sapiens
<400> 234
Gln Val Gln Leu Gln Gln Pro Gly Ala Glu Leu Val Lys Pro Gly Thr
1 5 10 15
Ser Val Lys Leu Ser Cys Lys Ala Ser Gly Tyr Ser Phe Thr Ser Tyr
20 25 30
Trp Met His Gly Val Arg Gln Arg Pro Gly Gln Gly Leu Glu Trp Ile
35 40 45
Gly Glu Ile Asp Pro Ser Asn Gly Arg Thr Asn Tyr Asn Glu Lys Phe
50 55 60
Lys Ser Lys Ala Thr Leu Thr Val Asp Lys Ser Ser Ser Thr Ala Tyr
65 70 75 80
Ile Gln Leu Ser Ser Leu Thr Ser Glu Asp Ser Ala Val Tyr Tyr Cys
85 90 95
Thr Arg Glu Arg Ser Pro Arg Tyr Phe Asp Val Trp Gly Ala Gly Thr
100 105 110
Thr Leu Thr Val Ser Ser
115
Claims (68)
- 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어, 리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록(maraviroc)), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제와 조합하여 대상체에서 OX40L-매개된 질환 또는 병태의 위험을 치료 또는 감쇠시키는 데 사용하기 위한, 항-OX40L 항체 또는 이의 단편.
- 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제와 조합하여 대상체에서 OX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한, 항-OX40L 항체 또는 이의 단편의 용도.
- 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제와 조합하여 대상체에서 OX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한 의약의 제조에서의, 항-OX40L 항체 또는 이의 단편의 용도.
- 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제와 조합하여 대상체에서 OX40L-매개된 질환 또는 병태를 치료 또는 예방하기 위한, 항-OX40L 항체 또는 이의 단편을 포함하는 조성물.
- 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제와 조합으로 치료 유효량의 항-OX40L 항체 또는 이의 단편을 상기 인간에게 투여하는 것을 포함하는 대상체에서 OX40L-매개된 질환 또는 병태를 치료 또는 예방하는 방법으로서, 이에 의해서 상기 OX40L-매개된 질환 또는 병태가 치료 또는 예방되는, 치료 또는 예방하는 방법.
- 제1항 내지 제5항 어느 한 항에 있어서, 상기 대상체가 적어도 14일, 또는 적어도 21일, 또는 적어도 28일, 또는 적어도 40일, 또는 적어도 50일, 또는 적어도 60일의 치료후 또는 예방조치후 생존 시간을 갖는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제5항 중 어느 한 항에 있어서, 예방조치후 상기 대상체가 적어도 7일, 또는 적어도 14일, 또는 적어도 21일, 또는 적어도 28일, 또는 적어도 40일, 또는 적어도 50일, 또는 적어도 60일의 무질환 기간을 갖는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제5항 중 어느 한 항에 있어서, 치료후, 상기 대상체가 적어도 7일, 또는 적어도 14일, 또는 적어도 21일, 또는 적어도 28일, 또는 적어도 40일, 또는 적어도 50일, 또는 적어도 60일의 질환 무진행 기간을 갖는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제6항 내지 제8항 중 어느 한 항에 있어서, 생존일수, 무질환일수, 또는 질환 무진행일수가 적어도 2개월, 또는 적어도 3개월, 또는 적어도 4개월, 예를 들어, 적어도 5개월, 예컨대 적어도 6개월인, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제9항에 있어서, 상기 생존일수, 상기 무질환일수, 또는 상기 질환 무진행일수가 적어도 9개월, 또는 적어도 1년인, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 예방-유효량의 항-OX40L 항체를 투여하고, 예방-유효량의 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여함으로써 대상체에서 OX40L-매개된 질환 또는 병태의 발병을 예방하는 방법으로서, 상기 OX40L-매개된 질환 또는 병태의 상기 발병이 예방되는, OX40L-매개된 질환 또는 병태의 발병을 예방하는 방법.
- 예방-유효량의 항-OX40L 항체를 투여하고, 치료-유효량의 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여함으로써 대상체에서 OX40L-매개된 질환 또는 병태를 치료하는 방법이되, OX40L-매개된 질환 또는 병태의 발병이 치료되는, 대상체에서 OX40L-매개된 질환 또는 병태를 치료하는 방법.
- 치료-유효량의 항-OX40L 항체를 투여하고, 예방-유효량의 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여함으로써 대상체에서 OX40L-매개된 질환 또는 병태를 치료하는 방법으로서, 상기 OX40L-매개된 질환 또는 병태의 발병이 치료되는, 대상체에서 OX40L-매개된 질환 또는 병태를 치료하는 방법.
- 치료-유효량의 항-OX40L 항체를 투여하고, 치료-유효량의 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여함으로써 대상체에서 OX40L-매개된 질환 또는 병태를 치료하는 방법으로서, 상기 OX40L-매개된 질환 또는 병태의 발병이 치료되는, 대상체에서 OX40L-매개된 질환 또는 병태를 치료하는 방법.
- 제11항 또는 제13항에 있어서, 상기 추가 치료제가 라파마이신(시롤리무스), 타크롤리무스, 타크롤리무스와 메토트렉세이트의 조합물, 사이클로포스파미드, 사이클로스포린, 및 사이클로스포린과 메토트렉세이트의 조합물로부터 독립적으로 선택되는, 대상체에서 OX40L-매개된 질환 또는 병태를 치료하는 방법.
- 제12항 또는 제14항에 있어서, 상기 추가 치료제가 코르티코스테로이드(예를 들어, 메틸프레드니솔론)인, 대상체에서 OX40L-매개된 질환 또는 병태를 치료하는 방법.
- 항-OX40L 항체와, 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제의 치료 조합물 또는 예방 조합물을 투여함으로써 OX40L-매개된 질환 또는 병태를 갖거나 또는 이의 위험을 갖는 대상체에서 생존을 연장시키는 방법.
- 제17항에 있어서, 생존이 적어도 7일, 또는 적어도 14일, 또는 적어도 20일, 또는 적어도 30일 또는 적어도 40일, 또는 적어도 50일, 또는 적어도 60일, 또는 적어도 70일 증가되는, 대상체에서 생존을 연장시키는 방법.
- 항-OX40L 항체와, 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제의 치료 조합물 또는 예방 조합물을 투여함으로써 OX40L-매개된 질환 또는 병태를 갖거나 이의 위험을 갖는 대상체에서 무병일수, 또는 질환 무진행일수를 증가시키는 방법.
- 제19항에 있어서, 상기 무병일수, 또는 질환 무진행일수가 적어도 7일, 또는 적어도 14일, 또는 적어도 21일, 또는 적어도 28일, 또는 적어도 40일, 또는 적어도 50일, 또는 적어도 60일, 또는 적어도 70일인, 무병일수, 또는 질환 무진행일수를 증가시키는 방법.
- 제20항에 있어서, 상기 무병일수, 또는 질환 무진행일수가 적어도 90일, 적어도 180일 또는 적어도 365일인, 무병일수, 또는 질환 무진행일수를 증가시키는 방법.
- 항-OX40L 항체와, 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제의 치료 조합물 또는 예방 조합물을 투여함으로써 대상체에서 이식 거부 또는 GvHD의 위험을 치료 또는 감쇠시키는 방법으로서, 상기 조합물은 단일 요법으로서의 상기 항체 또는 상기 추가 치료제에 비해서 동종 조혈 줄기 세포 이식(haploidentical hematopoietic stem cell transplantation)의 레서스 마카크 모델(Rhesus macaque model)에서 증가된 생존을 유발하는, 이식 거부 또는 GvHD의 위험을 치료 또는 감쇠시키는 방법.
- 제6항, 제9항, 제10항, 제17항, 제19항, 또는 제22항 중 어느 한 항에 있어서, 단일 요법으로서의 상기 항체 또는 상기 추가 치료제에 비해서 상기 생존이 적어도 7일, 또는 적어도 14일, 또는 적어도 21일, 또는 적어도 28일, 또는 적어도 40일, 또는 적어도 50일, 또는 적어도 60일, 또는 적어도 70일 증가되는, 방법.
- 제6항, 제9항, 제10항, 제17항, 제19항, 또는 제22항 중 어느 한 항에 있어서, 단일 요법으로서의 상기 항체 또는 상기 추가 치료제에 비해서 상기 생존이 적어도 2배, 예를 들어 3배인, 방법.
- 제1항 내지 제24항 중 어느 한 항에 있어서, 상기 항체는 인간 OX40L(hOX40L)에 특이적으로 결합하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제25항에 있어서, 상기 hOX40L에 결합하기 위해서 02D10, 10A07, 09H04 및 19H01로 이루어진 군으로부터 선택된 항체와 경쟁하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제25항에 있어서, 상기 hOX40L에 결합하기 위해서 상기 항체 02D10과 경쟁하고, 상기 항체 또는 단편은 모티프 VRGXYYY를 포함하는 HCDR3을 포함하는 VH 도메인을 포함하되, X는 임의의 아미노산인, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제27항 중 어느 한 항에 있어서, 상기 항체는 예를 들어, SPR 또는 ELISA를 사용하여 측정되는 바와 같이 OX40L에 대한 OX40의 특이적인 결합에 길항작용하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제28항 중 어느 한 항에 있어서, 상기 항체는 인간화 항체, 인간 항체 또는 완전 인간 항체인, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제29항 중 어느 한 항에 있어서, 상기 항체는 다중특이적인 항체(예를 들어, 이중-특이적인 항체), 인트라바디(intrabody), 단일-쇄 Fv 항체(scFv), 낙타화(camelized) 항체, Fab 단편, F(ab') 단편, 다이설파이드-연결된 Fv(sdFv), 항-이디오타입(idiotypic)(항-Id) 항체, 및 이의 에피토프-결합 단편의 목록으로부터 선택된 항체의 단편인, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제30항 중 어느 한 항에 있어서, 상기 항체 또는 단편은 동종 조혈 줄기 세포 이식의 레서스 마카크 모델에서 12일에 80%를 초과하는 줄기 세포 공여자 키메리즘을 가능하게 하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제31항 중 어느 한 항에 있어서, 상기 항체 또는 단편은 14일의 과성장 기간으로 론자(Lonza) 버전 8 공급 시스템을 사용하여 유가 과성장 배양액(fed batch overgrow culture) 중에서 1.5g/L를 초과하는 수준으로 론자 지에스-엑스시드(Lonza GS-Xceed)(상표명) 중에서 안정하게 형질주입된 풀로서 발현하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제32항 중 어느 한 항에 있어서, 상기 항체 또는 이의 단편은 16 내지 27개의 아미노산이고, 인간 VH 유전자 조각, 인간 D 유전자 조각 및 인간 JH 유전자 조각의 재조합으로부터 유래된 HCDR3을 포함하되, 상기 인간 JH 유전자 조각은 IGHJ6(예를 들어, IGHJ6*02)인, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제33항 중 어느 한 항에 있어서, 상기 항체 또는 이의 단편은,
a. 항체 2D10의 HCDR3(서열번호 40 또는 서열번호 46);
b. 항체 10A7의 HCDR3(서열번호 8 또는 서열번호 14);
c. 항체 09H04의 HCDR3(서열번호 72 또는 서열번호 78);
d. 항체 19H01의 HCDR3(서열번호 100 또는 서열번호 106);
e. 서열번호 177 내지 213의 가변 영역 아미노산 서열을 갖는 나노바디(nanobody) 중 임의의 것의 CDR3;
f. 서열번호 215, 217, 219, 221, 223, 225, 227, 229 또는 230의 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 HCDR3; 또는
g. 서열번호 232 또는 234의 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 HCDR3으로부터 선택된 CDR을 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도. - 제1항 내지 제34항 중 어느 한 항에 있어서, 상기 항체 또는 이의 단편은,
a. 항체 2D10의 CDR(CDRH3의 경우 서열번호 40 또는 서열번호 46, CDRH2의 경우 서열번호 38 또는 서열번호 44, CDRH1의 경우 서열번호 36 또는 서열번호 42, CDRL1의 경우 서열번호 50 또는 서열번호 56, CDRL2의 경우 서열번호 52 또는 서열번호 58 및 CDRL3의 경우 서열번호 54 또는 서열번호 60);
b. 항체 10A7의 CDR(CDRH3의 경우 서열번호 8 또는 서열번호 14, CDRH2의 경우 서열번호 6 또는 서열번호 12, CDRH1의 경우 서열번호 4 또는 서열번호 10, CDRL1의 경우 서열번호 18 또는 서열번호 24, CDRL2의 경우 서열번호 20 또는 서열번호 26 및 CDRL3의 경우 서열번호 22 또는 서열번호 28);
c. 항체 09H04의 CDR(CDRH3의 경우 서열번호 72 또는 서열번호 78, CDRH2의 경우 서열번호 70 또는 서열번호 76, CDRH1의 경우 서열번호 68 또는 서열번호 74, CDRL1의 경우 서열번호 82 또는 서열번호 88, CDRL2의 경우 서열번호 84 또는 서열번호 90 및 CDRL3의 경우 서열번호 86 또는 서열번호 92);
d. 항체 19H01의 CDR(CDRH3의 경우 서열번호 100 또는 서열번호 106, CDRH2의 경우 서열번호 98 또는 서열번호 104, CDRH1의 경우 서열번호 96 또는 서열번호 102, CDRL1의 경우 서열번호 110 또는 서열번호 116, CDRL2의 경우 서열번호 112 또는 서열번호 118 및 CDRL3의 경우 서열번호 114 또는 서열번호 120);
e. 서열번호 177 내지 213의 가변 영역 아미노산 서열을 갖는 나노바디 중 임의의 것의 CDR;
f. 서열번호 215, 217, 219, 221, 223, 225, 227, 229 또는 230의 중쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 중쇄 CDR, 및 서열번호 214, 216, 218, 220, 222, 224, 226 또는 228의 경쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 경쇄 CDR; 또는
g. 서열번호 232 또는 234의 중쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 중쇄 CDR, 및 서열번호 231 또는 233의 경쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 경쇄 CDR을 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도. - 제1항 내지 제35항 중 어느 한 항에 있어서, 상기 항체 또는 이의 단편은,
a. 항체 2D10의 VH 및/또는 VL 도메인(VH의 경우 서열번호 34 및/또는 VL의 경우 서열번호 48);
b. 항체 10A7의 VH 및/또는 VL 도메인(VH의 경우 서열번호 2 및/또는 VL의 경우 서열번호 16);
c. 항체 09H04의 VH 및/또는 VL 도메인(VH의 경우 서열번호 66 및/또는 VL의 경우 서열번호 80);
d. 항체 19H01의 VH 및/또는 VL 도메인(VH의 경우 서열번호 94 및/또는 VL의 경우 서열번호 108);
e. 서열번호 177 내지 213의 가변 영역 아미노산 서열을 갖는 나노바디 중 임의의 것의 VH 도메인;
f. 서열번호 215, 217, 219, 221, 223, 225, 227, 229 또는 230의 중쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 VH 도메인, 및 서열번호 214, 216, 218, 220, 222, 224, 226 또는 228의 경쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 VL 도메인; 또는
g. 서열번호 232 또는 234의 중쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 VH 도메인, 및 서열번호 231 또는 233의 경쇄 가변 영역 아미노산 서열을 갖는 항체 중 임의의 것의 VL 도메인으로부터 선택된 VH 및/또는 VL 도메인을 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도. - 제1항 내지 제36항 중 어느 한 항에 있어서, 상기 항체는, 옥셀루맙인, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제37항 중 어느 한 항에 있어서, 상기 대상체는 영장류인, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제38항 중 어느 한 항에 있어서, 상기 대상체는 인간인, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제39항 중 어느 한 항에 있어서, 상기 대상체는 OX40L-매개된 질환 또는 병태의 위험이 있는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제40항에 있어서, 상기 방법, 상기 사용하기 위한 항체 또는 단편, 상기 용도 또는 상기 조성물은 상기 OX40L-매개된 질환 또는 병태의 상기 예방을 위한 것인, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제39항 중 어느 한 항에 있어서, 상기 대상체는 OX40L-매개된 질환 또는 병태를 갖는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제42항에 있어서, 상기 방법, 상기 사용하기 위한 항체 또는 단편, 상기 사용하기 위한 조성물, 또는 상기 용도는 상기 OX40L-매개된 질환 또는 병태의 치료를 위한 것인, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제43항 중 어느 한 항에 있어서, 상기 OX40L-매개된 질환 또는 병태는 자가면역 질환 또는 병태, 전신 염증 질환 또는 병태, 또는 이식 거부로부터 선택되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제44항에 있어서, 상기 OX40L-매개된 질환 또는 병태는 염증성 장 질환(IBD), 크론병(Crohn's diease), 류마티스 관절염, 이식 거부, 동종이형 이식 거부, 이식편대숙주병(graft-versus-host disease: GvHD), 궤양성 대장염, 전신 홍반 루푸스(SLE), 당뇨병, 포도막염, 강직성 척추염, 접촉 과민증, 다발성 경화증 및 죽상동맥경화증으로부터 선택되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제45항에 있어서, 상기 OX40L-매개된 질환 또는 병태는 GvHD 또는 이식 거부인, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제46항에 있어서, 상기 OX40L-매개된 질환 또는 병태는 GvHD인, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제46항에 있어서, 상기 이식은 세포, 조직 또는 기관 이식(예를 들어, 간, 폐, 심장, 신장 또는 장), 또는 혈액 이식(예를 들어, 자가형 또는 동종이형)이고, 예를 들어 상기 혈액은 골수-유래되거나, 제대혈(배꼽) 유래되거나, 말초-혈액 유래된, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제46항 내지 제48항 중 어느 한 항에 있어서, 상기 항-OX40L 항체 또는 이의 단편은 이식 이전에 투여되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제46항 내지 제48항 중 어느 한 항에 있어서, 상기 항-OX40L 항체 또는 이의 단편은 이식 이후에 투여되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제49항 또는 제50항에 있어서, 상기 추가 치료제는 이식 이후에 투여되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제49항 또는 제50항에 있어서, 상기 추가 치료제는 이식 이전에 투여되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 약제학적 조성물로서, 항-OX40L 항체 또는 이의 단편 및 약제학적으로 허용 가능한 부형제, 희석제 또는 담체를 포함하되, 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, 항-IL12/IL-23 항체(예를 들어, 우스테키누맙), 항-CD20 항체(예를 들어,리툭시맙), 항-CD30 항체(예를 들어, 브렌툭시맙), CTLA4-Fc 분자(예를 들어, 아바타셉트), CCR5 수용체 길항제(예를 들어, 마라비록), 항-CD40L 항체, 항-VLA4 항체(예를 들어, 나탈리주맙), 항-LFA1 항체, 플루다라빈, 항-CD52 항체(예를 들어, 알렘투주맙), 항-CD45 항체, 사이클로포스파미드, 항-흉선세포 글로불린, 항-보체 C5 항체(예를 들어, 에쿨리주맙), 항-a4b7 인테그린 항체(예를 들어, 베돌리주맙), 항-IL6 항체(예를 들어, 토실리주맙), 항-IL2R 항체(예를 들어, 바실릭수맙), 항-CD25 항체(예를 들어, 다클리주맙), 항-TNFa / TNFa-Fc 분자(예를 들어, 에타너셉트, 아달리무맙, 인플릭시맙, 골리무맙 또는 세르톨리주맙 페골) 및 보리노스타트로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 추가로 포함하는, 약제학적 조성물.
- 제1항 내지 제53항 중 어느 한 항에 있어서, 상기 추가 치료제는 라파마이신(시롤리무스), 타크롤리무스, 사이클로스포린, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트, 마이코페놀레이트 모페틸, 항-CD28 항체, CTLA4-Fc 분자(예를 들어, 아바타셉트), 항-CD40L 항체, 항-LFA1 항체, 항-CD52 항체(예를 들어, 알렘투주맙), 사이클로포스파미드 및 항-흉선세포 글로불린으로 이루어진 군으로부터 독립적으로 선택되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제54항 중 어느 한 항에 있어서, 상기 인간에게, 치료 유효량, 또는 예방 유효량의, 라파마이신, 타크롤리무스, 사이클로스포린, 사이클로포스파미드, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트 또는 마이코페놀레이트 모페틸, 항-CD28 항체, CTLA4-Fc 분자(예를 들어, 아바타셉트) 및 항-흉선세포 글로불린으로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 추가로 투여하는 것을 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제55항 중 어느 한 항에 있어서, 상기 인간에게, 치료 유효량, 또는 예방 유효량의, 라파마이신, 타크롤리무스, 사이클로스포린, 사이클로포스파미드, 코르티코스테로이드(예를 들어, 메틸프레드니솔론), 메토트렉세이트 및 마이코페놀레이트 모페틸로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여하는 것을 추가로 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제56항 중 어느 한 항에 있어서, 상기 인간에게, 치료 유효량, 또는 예방 유효량의, IL-2 신호전달을 조절하는 면역억제제(예를 들어, 타크롤리무스, 사이클로스포린, 라파마이신(시롤리무스)), 및 항-CD25 항체(예를 들어, 바실릭수맙, 다클리주맙)로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여하는 것을 추가로 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제57항 중 어느 한 항에 있어서, 상기 인간에게, 치료 유효량, 또는 예방 유효량의, 칼시뉴린 억제제(예를 들어, 타크롤리무스, 사이클로스포린), mTOR 억제제(예를 들어, 라파마이신(시롤리무스)), 및 항증식제(antiproliferative agent)(예를 들어, 마이코페놀레이트 모페틸, 사이클로포스파미드)로 이루어진 군으로부터 독립적으로 선택된 추가 치료제를 투여하는 것을 추가로 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제58항 중 어느 한 항에 있어서, 상기 인간에게 치료 유효량, 또는 예방 유효량의 라파마이신을 투여하는 것을 추가로 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제59항 중 어느 한 항에 있어서, 상기 인간에게 치료 유효량, 또는 예방 유효량의 타크롤리무스를 투여하는 것을 추가로 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제60항 중 어느 한 항에 있어서, 상기 인간에게 치료 유효량, 또는 예방 유효량의 타크롤리무스 및 메토트렉세이트를 투여하는 것을 추가로 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제61항 중 어느 한 항에 있어서, 상기 인간에게 치료 유효량, 또는 예방 유효량의 사이클로스포린을 투여하는 것을 추가로 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제62항 중 어느 한 항에 있어서, 상기 인간에게 치료 유효량, 또는 예방 유효량의 사이클로스포린 및 메토트렉세이트를 투여하는 것을 추가로 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제63항 중 어느 한 항에 있어서, 상기 인간에게 치료 유효량, 또는 예방 유효량의 사이클로포스파미드를 투여하는 것을 추가로 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제64항 중 어느 한 항에 있어서, 상기 인간에게 치료 유효량, 또는 예방 유효량의 마이코페놀레이트 모페틸을 투여하는 것을 추가로 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제65항 중 어느 한 항에 있어서, 상기 인간에게 치료 유효량, 또는 예방 유효량의 코르티코스테로이드(예를 들어, 메틸 프레드니솔론)을 투여하는 것을 추가로 포함하는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- 제1항 내지 제66항 중 어느 한 항에 있어서, 상기 추가 치료제는 항-hOX40L 항체 또는 단편과 순차적으로 또는 동시에 투여되는, 방법, 항체 또는 단편, 조성물, 또는 용도.
- CD45RA+CCR7+CD95+OX40+ 기억 줄기 T-세포(Tscm)를, Tscm 세포의 비율을 감쇠시키는(예를 들어, 상기 Tscm 세포의 수준을 고갈 또는 감소시키는) 항-OX40 또는 항-OX40L 항체 또는 이의 단편과 조합하는 단계를 포함하는 CD45RA+CCR7+CD95+OX40+ 기억 줄기 T-세포의 비율을 감쇠시키는(예를 들어, 수준을 고갈 또는 감소시키는) 방법으로서, 이에 의해서 상기 Tscm 세포의 비율이 감쇠되는(예를 들어, 이에 의해서 상기 Tscm 세포의 수준이 감소 또는 고갈되는), 방법.
Applications Claiming Priority (13)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBPCT/GB2015/050614 | 2015-03-03 | ||
| PCT/GB2015/050614 WO2015132580A1 (en) | 2014-03-04 | 2015-03-03 | Antibodies, uses & methods |
| US14/700,896 US9139653B1 (en) | 2015-04-30 | 2015-04-30 | Anti-human OX40L antibodies and methods of treatment |
| US14/700,896 | 2015-04-30 | ||
| US14/811,163 US9234043B1 (en) | 2015-04-30 | 2015-07-28 | Anti-human OX40L antibodies |
| US14/811,163 | 2015-07-28 | ||
| GBGB1516008.8A GB201516008D0 (en) | 2015-09-09 | 2015-09-09 | OX40L antibodies and uses thereof |
| GB1516008.8 | 2015-09-09 | ||
| US14/935,937 | 2015-11-09 | ||
| US14/935,937 US9434785B1 (en) | 2015-04-30 | 2015-11-09 | Anti-human OX40L antibodies and methods of treating graft versus host disease with the same |
| US201514955843A | 2015-12-01 | 2015-12-01 | |
| US14/955,843 | 2015-12-01 | ||
| PCT/GB2016/050565 WO2016139482A1 (en) | 2015-03-03 | 2016-03-03 | Antibodies, uses & methods |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20170123637A true KR20170123637A (ko) | 2017-11-08 |
Family
ID=56849249
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020177025436A KR20170123637A (ko) | 2015-03-03 | 2016-03-03 | 항체, 용도 및 방법 |
Country Status (23)
| Country | Link |
|---|---|
| EP (2) | EP4137157A1 (ko) |
| JP (2) | JP7094698B2 (ko) |
| KR (1) | KR20170123637A (ko) |
| CN (3) | CN108064169B (ko) |
| AU (2) | AU2016227493B2 (ko) |
| BR (1) | BR112017015880A2 (ko) |
| CA (1) | CA2968642A1 (ko) |
| DE (1) | DE112016001013T5 (ko) |
| DK (1) | DK3265123T5 (ko) |
| ES (1) | ES2937020T3 (ko) |
| FI (1) | FI3265123T3 (ko) |
| HR (1) | HRP20230046T1 (ko) |
| HU (1) | HUE061070T2 (ko) |
| IL (1) | IL252430A0 (ko) |
| LT (1) | LT3265123T (ko) |
| MX (3) | MX2017011194A (ko) |
| PL (1) | PL3265123T3 (ko) |
| PT (1) | PT3265123T (ko) |
| RS (1) | RS63903B1 (ko) |
| RU (1) | RU2725221C2 (ko) |
| SG (2) | SG10201907901XA (ko) |
| SI (1) | SI3265123T1 (ko) |
| WO (1) | WO2016139482A1 (ko) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB201403775D0 (en) | 2014-03-04 | 2014-04-16 | Kymab Ltd | Antibodies, uses & methods |
| US9512229B2 (en) | 2015-03-03 | 2016-12-06 | Kymab Limited | Synergistic combinations of OX40L antibodies for the treatment of GVHD |
| EP3534947A1 (en) * | 2016-11-03 | 2019-09-11 | Kymab Limited | Antibodies, combinations comprising antibodies, biomarkers, uses & methods |
| CN111971052B (zh) | 2018-02-08 | 2024-07-05 | 小利兰.斯坦福大学托管委员会 | 用于异基因造血干细胞移植的方法 |
| WO2019173780A2 (en) * | 2018-03-08 | 2019-09-12 | Magenta Therapeutics, Inc. | Anti-cd252 antibodies, conjugates, and methods of use |
| BR112020023746A2 (pt) * | 2018-05-23 | 2021-02-17 | Beigene, Ltd. | anticorpo, composição farmacêutica, método para tratar câncer, ácido nucleico isolado, vetor, célula hospedeira, processo para a produção de um anticorpo e reagente de diagnóstico |
| GB202012331D0 (en) | 2020-08-07 | 2020-09-23 | Petmedix Ltd | Therapeutic antibodies |
| EP4384270A1 (en) | 2021-08-10 | 2024-06-19 | Kymab Limited | Treatment of atopic dermatitis |
| AU2023219227A1 (en) | 2022-02-09 | 2024-08-01 | Petmedix Ltd | Therapeutic antibodies |
Family Cites Families (236)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3773919A (en) | 1969-10-23 | 1973-11-20 | Du Pont | Polylactide-drug mixtures |
| US3710795A (en) | 1970-09-29 | 1973-01-16 | Alza Corp | Drug-delivery device with stretched, rate-controlling membrane |
| US4044126A (en) | 1972-04-20 | 1977-08-23 | Allen & Hanburys Limited | Steroidal aerosol compositions and process for the preparation thereof |
| GB1429184A (en) | 1972-04-20 | 1976-03-24 | Allen & Hanburys Ltd | Physically anti-inflammatory steroids for use in aerosols |
| USRE28819E (en) | 1972-12-08 | 1976-05-18 | Syntex (U.S.A.) Inc. | Dialkylated glycol compositions and medicament preparations containing same |
| US4444887A (en) | 1979-12-10 | 1984-04-24 | Sloan-Kettering Institute | Process for making human antibody producing B-lymphocytes |
| US4410545A (en) | 1981-02-13 | 1983-10-18 | Syntex (U.S.A.) Inc. | Carbonate diester solutions of PGE-type compounds |
| US4328245A (en) | 1981-02-13 | 1982-05-04 | Syntex (U.S.A.) Inc. | Carbonate diester solutions of PGE-type compounds |
| US4358603A (en) | 1981-04-16 | 1982-11-09 | Syntex (U.S.A.) Inc. | Acetal stabilized prostaglandin compositions |
| US4485045A (en) | 1981-07-06 | 1984-11-27 | Research Corporation | Synthetic phosphatidyl cholines useful in forming liposomes |
| US4409239A (en) | 1982-01-21 | 1983-10-11 | Syntex (U.S.A.) Inc. | Propylene glycol diester solutions of PGE-type compounds |
| DE3378250D1 (en) | 1982-04-22 | 1988-11-24 | Ici Plc | Continuous release formulations |
| US4522811A (en) | 1982-07-08 | 1985-06-11 | Syntex (U.S.A.) Inc. | Serial injection of muramyldipeptides and liposomes enhances the anti-infective activity of muramyldipeptides |
| US4716111A (en) | 1982-08-11 | 1987-12-29 | Trustees Of Boston University | Process for producing human antibodies |
| GB8308235D0 (en) | 1983-03-25 | 1983-05-05 | Celltech Ltd | Polypeptides |
| US4816567A (en) | 1983-04-08 | 1989-03-28 | Genentech, Inc. | Recombinant immunoglobin preparations |
| US4544545A (en) | 1983-06-20 | 1985-10-01 | Trustees University Of Massachusetts | Liposomes containing modified cholesterol for organ targeting |
| US5807715A (en) | 1984-08-27 | 1998-09-15 | The Board Of Trustees Of The Leland Stanford Junior University | Methods and transformed mammalian lymphocyte cells for producing functional antigen-binding protein including chimeric immunoglobulin |
| US5128326A (en) | 1984-12-06 | 1992-07-07 | Biomatrix, Inc. | Drug delivery systems based on hyaluronans derivatives thereof and their salts and methods of producing same |
| US4980286A (en) | 1985-07-05 | 1990-12-25 | Whitehead Institute For Biomedical Research | In vivo introduction and expression of foreign genetic material in epithelial cells |
| US4676980A (en) | 1985-09-23 | 1987-06-30 | The United States Of America As Represented By The Secretary Of The Department Of Health And Human Services | Target specific cross-linked heteroantibodies |
| GB8607679D0 (en) | 1986-03-27 | 1986-04-30 | Winter G P | Recombinant dna product |
| US5225539A (en) | 1986-03-27 | 1993-07-06 | Medical Research Council | Recombinant altered antibodies and methods of making altered antibodies |
| JP3101690B2 (ja) | 1987-03-18 | 2000-10-23 | エス・ビィ・2・インコーポレイテッド | 変性抗体の、または変性抗体に関する改良 |
| US4880078A (en) | 1987-06-29 | 1989-11-14 | Honda Giken Kogyo Kabushiki Kaisha | Exhaust muffler |
| US5336603A (en) | 1987-10-02 | 1994-08-09 | Genentech, Inc. | CD4 adheson variants |
| ATE120454T1 (de) | 1988-06-14 | 1995-04-15 | Cetus Oncology Corp | Kupplungsmittel und sterisch gehinderte, mit disulfid gebundene konjugate daraus. |
| US5223409A (en) | 1988-09-02 | 1993-06-29 | Protein Engineering Corp. | Directed evolution of novel binding proteins |
| EP0768377A1 (en) | 1988-09-02 | 1997-04-16 | Protein Engineering Corporation | Generation and selection of recombinant varied binding proteins |
| KR900005995A (ko) | 1988-10-31 | 1990-05-07 | 우메모또 요시마사 | 변형 인터류킨-2 및 그의 제조방법 |
| US5734033A (en) | 1988-12-22 | 1998-03-31 | The Trustees Of The University Of Pennsylvania | Antisense oligonucleotides inhibiting human bcl-2 gene expression |
| US5530101A (en) | 1988-12-28 | 1996-06-25 | Protein Design Labs, Inc. | Humanized immunoglobulins |
| EP0394827A1 (en) | 1989-04-26 | 1990-10-31 | F. Hoffmann-La Roche Ag | Chimaeric CD4-immunoglobulin polypeptides |
| IE63847B1 (en) | 1989-05-05 | 1995-06-14 | Res Dev Foundation | A novel antibody delivery system for biological response modifiers |
| US5112946A (en) | 1989-07-06 | 1992-05-12 | Repligen Corporation | Modified pf4 compositions and methods of use |
| US5413923A (en) | 1989-07-25 | 1995-05-09 | Cell Genesys, Inc. | Homologous recombination for universal donor cells and chimeric mammalian hosts |
| WO1991005548A1 (en) | 1989-10-10 | 1991-05-02 | Pitman-Moore, Inc. | Sustained release composition for macromolecular proteins |
| US5013556A (en) | 1989-10-20 | 1991-05-07 | Liposome Technology, Inc. | Liposomes with enhanced circulation time |
| WO1991006570A1 (en) | 1989-10-25 | 1991-05-16 | The University Of Melbourne | HYBRID Fc RECEPTOR MOLECULES |
| EP0550436A1 (en) | 1989-11-06 | 1993-07-14 | Alkermes Controlled Therapeutics, Inc. | Protein microspheres and methods of using them |
| GB8928874D0 (en) | 1989-12-21 | 1990-02-28 | Celltech Ltd | Humanised antibodies |
| US5585112A (en) | 1989-12-22 | 1996-12-17 | Imarx Pharmaceutical Corp. | Method of preparing gas and gaseous precursor-filled microspheres |
| AU7247191A (en) | 1990-01-11 | 1991-08-05 | Molecular Affinities Corporation | Production of antibodies using gene libraries |
| US5780225A (en) | 1990-01-12 | 1998-07-14 | Stratagene | Method for generating libaries of antibody genes comprising amplification of diverse antibody DNAs and methods for using these libraries for the production of diverse antigen combining molecules |
| DE69120146T2 (de) | 1990-01-12 | 1996-12-12 | Cell Genesys Inc | Erzeugung xenogener antikörper |
| US5314995A (en) | 1990-01-22 | 1994-05-24 | Oncogen | Therapeutic interleukin-2-antibody based fusion proteins |
| AU654811B2 (en) | 1990-03-20 | 1994-11-24 | Trustees Of Columbia University In The City Of New York, The | Chimeric antibodies with receptor binding ligands in place of their constant region |
| IT1246382B (it) | 1990-04-17 | 1994-11-18 | Eurand Int | Metodo per la cessione mirata e controllata di farmaci nell'intestino e particolarmente nel colon |
| US5427908A (en) | 1990-05-01 | 1995-06-27 | Affymax Technologies N.V. | Recombinant library screening methods |
| US5349053A (en) | 1990-06-01 | 1994-09-20 | Protein Design Labs, Inc. | Chimeric ligand/immunoglobulin molecules and their uses |
| GB9015198D0 (en) | 1990-07-10 | 1990-08-29 | Brien Caroline J O | Binding substance |
| US5633425A (en) | 1990-08-29 | 1997-05-27 | Genpharm International, Inc. | Transgenic non-human animals capable of producing heterologous antibodies |
| DK0814159T3 (da) | 1990-08-29 | 2005-10-24 | Genpharm Int | Transgene, ikke-humane dyr, der er i stand til at danne heterologe antistoffer |
| US5625126A (en) | 1990-08-29 | 1997-04-29 | Genpharm International, Inc. | Transgenic non-human animals for producing heterologous antibodies |
| US5661016A (en) | 1990-08-29 | 1997-08-26 | Genpharm International Inc. | Transgenic non-human animals capable of producing heterologous antibodies of various isotypes |
| US5545806A (en) | 1990-08-29 | 1996-08-13 | Genpharm International, Inc. | Ransgenic non-human animals for producing heterologous antibodies |
| US5814318A (en) | 1990-08-29 | 1998-09-29 | Genpharm International Inc. | Transgenic non-human animals for producing heterologous antibodies |
| US5698426A (en) | 1990-09-28 | 1997-12-16 | Ixsys, Incorporated | Surface expression libraries of heteromeric receptors |
| US5543390A (en) | 1990-11-01 | 1996-08-06 | State Of Oregon, Acting By And Through The Oregon State Board Of Higher Education, Acting For And On Behalf Of The Oregon Health Sciences University | Covalent microparticle-drug conjugates for biological targeting |
| CA2095836C (en) | 1990-11-09 | 1999-04-06 | Stephen D. Gillies | Cytokine immunoconjugates |
| WO1992009690A2 (en) | 1990-12-03 | 1992-06-11 | Genentech, Inc. | Enrichment method for variant proteins with altered binding properties |
| ES2096749T3 (es) | 1990-12-14 | 1997-03-16 | Cell Genesys Inc | Cadenas quimericas para vias de transduccion de señal asociada a un receptor. |
| DK1471142T3 (da) | 1991-04-10 | 2009-03-09 | Scripps Research Inst | Heterodimere receptor-biblioteker under anvendelse af fagemider |
| JPH06507404A (ja) | 1991-05-01 | 1994-08-25 | ヘンリー エム.ジャクソン ファウンデイション フォー ザ アドバンスメント オブ ミリタリー メディスン | 感染性の呼吸性疾患の治療方法 |
| DE69233482T2 (de) | 1991-05-17 | 2006-01-12 | Merck & Co., Inc. | Verfahren zur Verminderung der Immunogenität der variablen Antikörperdomänen |
| LU91067I2 (fr) | 1991-06-14 | 2004-04-02 | Genentech Inc | Trastuzumab et ses variantes et dérivés immuno chimiques y compris les immotoxines |
| CA2110799A1 (en) | 1991-06-14 | 1992-12-23 | Arnold H. Horwitz | Microbially-produced antibody fragments and their conjugates |
| US5844095A (en) | 1991-06-27 | 1998-12-01 | Bristol-Myers Squibb Company | CTLA4 Ig fusion proteins |
| ES2136092T3 (es) | 1991-09-23 | 1999-11-16 | Medical Res Council | Procedimientos para la produccion de anticuerpos humanizados. |
| ES2313867T3 (es) | 1991-12-02 | 2009-03-16 | Medical Research Council | Produccion de anticuerpos anti-auto de repertorios de segmentos de anticuerpo expresados en la superficie de fagos. |
| ES2202310T3 (es) | 1991-12-13 | 2004-04-01 | Xoma Corporation | Metodos y materiales para la preparacion de dominios variables de anticuerpos modificados y sus usos terapeuticos. |
| US5824307A (en) | 1991-12-23 | 1998-10-20 | Medimmune, Inc. | Human-murine chimeric antibodies against respiratory syncytial virus |
| US5622929A (en) | 1992-01-23 | 1997-04-22 | Bristol-Myers Squibb Company | Thioether conjugates |
| US6271242B1 (en) | 1992-02-10 | 2001-08-07 | Bristol-Myers Squibb Co. | Method for treating cancer using a tyrosine protein kinase inhibitor |
| GB9203459D0 (en) | 1992-02-19 | 1992-04-08 | Scotgen Ltd | Antibodies with germ-line variable regions |
| US5912015A (en) | 1992-03-12 | 1999-06-15 | Alkermes Controlled Therapeutics, Inc. | Modulated release from biocompatible polymers |
| US5733743A (en) | 1992-03-24 | 1998-03-31 | Cambridge Antibody Technology Limited | Methods for producing members of specific binding pairs |
| US6010715A (en) | 1992-04-01 | 2000-01-04 | Bertek, Inc. | Transdermal patch incorporating a polymer film incorporated with an active agent |
| US5447851B1 (en) | 1992-04-02 | 1999-07-06 | Univ Texas System Board Of | Dna encoding a chimeric polypeptide comprising the extracellular domain of tnf receptor fused to igg vectors and host cells |
| US6024975A (en) | 1992-04-08 | 2000-02-15 | Americare International Diagnostics, Inc. | Method of transdermally administering high molecular weight drugs with a polymer skin enhancer |
| US6005079A (en) | 1992-08-21 | 1999-12-21 | Vrije Universiteit Brussels | Immunoglobulins devoid of light chains |
| EP2192131A1 (en) | 1992-08-21 | 2010-06-02 | Vrije Universiteit Brussel | Immunoglobulins devoid of light chains |
| US5639641A (en) | 1992-09-09 | 1997-06-17 | Immunogen Inc. | Resurfacing of rodent antibodies |
| US5441050A (en) | 1992-12-18 | 1995-08-15 | Neoprobe Corporation | Radiation responsive surgical instrument |
| US5934272A (en) | 1993-01-29 | 1999-08-10 | Aradigm Corporation | Device and method of creating aerosolized mist of respiratory drug |
| US6274552B1 (en) | 1993-03-18 | 2001-08-14 | Cytimmune Sciences, Inc. | Composition and method for delivery of biologically-active factors |
| US5985307A (en) | 1993-04-14 | 1999-11-16 | Emory University | Device and method for non-occlusive localized drug delivery |
| US5523092A (en) | 1993-04-14 | 1996-06-04 | Emory University | Device for local drug delivery and methods for using the same |
| US6838254B1 (en) | 1993-04-29 | 2005-01-04 | Conopco, Inc. | Production of antibodies or (functionalized) fragments thereof derived from heavy chain immunoglobulins of camelidae |
| AU691820B2 (en) | 1993-07-15 | 1998-05-28 | Cancer Research Campaign Technology Limited | Prodrugs of protein tyrosine kinase inhibitors |
| US6004534A (en) | 1993-07-23 | 1999-12-21 | Massachusetts Institute Of Technology | Targeted polymerized liposomes for improved drug delivery |
| US5821332A (en) | 1993-11-03 | 1998-10-13 | The Board Of Trustees Of The Leland Stanford Junior University | Receptor on the surface of activated CD4+ T-cells: ACT-4 |
| WO1995015982A2 (en) | 1993-12-08 | 1995-06-15 | Genzyme Corporation | Process for generating specific antibodies |
| US5925376C1 (en) | 1994-01-10 | 2001-03-20 | Madalene C Y Heng | Method for treating psoriasis using selected phosphorylase kinase inhibitor and additional compounds |
| US5618709A (en) | 1994-01-14 | 1997-04-08 | University Of Pennsylvania | Antisense oligonucleotides specific for STK-1 and method for inhibiting expression of the STK-1 protein |
| EP1231268B1 (en) | 1994-01-31 | 2005-07-27 | Trustees Of Boston University | Polyclonal antibody libraries |
| US5759546A (en) | 1994-02-04 | 1998-06-02 | Weinberg; Andrew D. | Treatment of CD4 T-cell mediated conditions |
| US6242566B1 (en) | 1994-02-10 | 2001-06-05 | Board Of Trustees Of The Leland Stanford Junior University | Ligand (ACT-4-L) to a receptor on the surface of activated CD4+ T-cells |
| US5605793A (en) | 1994-02-17 | 1997-02-25 | Affymax Technologies N.V. | Methods for in vitro recombination |
| US5837458A (en) | 1994-02-17 | 1998-11-17 | Maxygen, Inc. | Methods and compositions for cellular and metabolic engineering |
| US5834252A (en) | 1995-04-18 | 1998-11-10 | Glaxo Group Limited | End-complementary polymerase reaction |
| US5516637A (en) | 1994-06-10 | 1996-05-14 | Dade International Inc. | Method involving display of protein binding pairs on the surface of bacterial pili and bacteriophage |
| CN1117155C (zh) | 1994-07-29 | 2003-08-06 | 史密丝克莱恩比彻姆有限公司 | 新型化合物 |
| GB9415379D0 (en) | 1994-07-29 | 1994-09-21 | Smithkline Beecham Plc | Novel compounds |
| US5759542A (en) | 1994-08-05 | 1998-06-02 | New England Deaconess Hospital Corporation | Compositions and methods for the delivery of drugs by platelets for the treatment of cardiovascular and other diseases |
| US5911995A (en) | 1994-08-19 | 1999-06-15 | Regents Of The University Of Minnesota | EGF-genistein conjugates for the treatment of cancer |
| US5587459A (en) | 1994-08-19 | 1996-12-24 | Regents Of The University Of Minnesota | Immunoconjugates comprising tyrosine kinase inhibitors |
| US5660854A (en) | 1994-11-28 | 1997-08-26 | Haynes; Duncan H | Drug releasing surgical implant or dressing material |
| EP0805678B1 (en) | 1995-01-05 | 2003-10-29 | THE BOARD OF REGENTS acting for and on behalf of THE UNIVERSITY OF MICHIGAN | Surface-modified nanoparticles and method of making and using same |
| DK1323346T3 (da) | 1995-01-17 | 2006-10-30 | Brigham & Womens Hospital | Receptorspecifik transport af immunogener gennem epitelet |
| US6030613A (en) | 1995-01-17 | 2000-02-29 | The Brigham And Women's Hospital, Inc. | Receptor specific transepithelial transport of therapeutics |
| GB9501567D0 (en) | 1995-01-26 | 1995-03-15 | Pharmacia Spa | Hydrosoluble 3-arylidene-2-oxindole derivatives as tyrosine kinase inhibitors |
| US5998596A (en) | 1995-04-04 | 1999-12-07 | The United States Of America As Represented By The Department Of Health And Human Services | Inhibition of protein kinase activity by aptameric action of oligonucleotides |
| US6019968A (en) | 1995-04-14 | 2000-02-01 | Inhale Therapeutic Systems, Inc. | Dispersible antibody compositions and methods for their preparation and use |
| US5983134A (en) | 1995-04-23 | 1999-11-09 | Electromagnetic Bracing Systems Inc. | Electrophoretic cuff apparatus drug delivery system |
| EP1709970A1 (en) | 1995-04-27 | 2006-10-11 | Abgenix, Inc. | Human antibodies against EGFR, derived from immunized xenomice |
| AU2466895A (en) | 1995-04-28 | 1996-11-18 | Abgenix, Inc. | Human antibodies derived from immunized xenomice |
| ATE332710T1 (de) | 1995-06-01 | 2006-08-15 | Kishimoto Tadamitsu | Wachstumsinhibitor gegen leukämische zellen, der antisense-oligonukleotidderivate gegen das wilms- tumorgen enthält |
| US6316652B1 (en) | 1995-06-06 | 2001-11-13 | Kosta Steliou | Drug mitochondrial targeting agents |
| GB9515975D0 (en) | 1995-08-04 | 1995-10-04 | Zeneca Ltd | Chemical compounds |
| US6167301A (en) | 1995-08-29 | 2000-12-26 | Flower; Ronald J. | Iontophoretic drug delivery device having high-efficiency DC-to-DC energy conversion circuit |
| CA2230494A1 (en) | 1995-08-31 | 1997-03-06 | Alkermes Controlled Therapeutics Inc. | Composition for sustained release of an agent |
| US5863904A (en) | 1995-09-26 | 1999-01-26 | The University Of Michigan | Methods for treating cancers and restenosis with P21 |
| GB9601081D0 (en) | 1995-10-06 | 1996-03-20 | Cambridge Antibody Tech | Specific binding members for human transforming growth factor beta;materials and methods |
| US6039975A (en) | 1995-10-17 | 2000-03-21 | Hoffman-La Roche Inc. | Colon targeted delivery system |
| US6127366A (en) | 1995-11-22 | 2000-10-03 | Merck & Co., Inc. | Inhibitors of farnesyl-protein transferase |
| DE69620445T2 (de) | 1995-12-08 | 2002-12-12 | Janssen Pharmaceutica N.V., Beerse | (imidazol-5-yl)methyl-2-chinolinoderivate als farnesyl protein transferase inhibitoren |
| US5723125A (en) | 1995-12-28 | 1998-03-03 | Tanox Biosystems, Inc. | Hybrid with interferon-alpha and an immunoglobulin Fc linked through a non-immunogenic peptide |
| US5958769A (en) | 1996-01-18 | 1999-09-28 | Fred Hutchinson Cancer Research Center | Compositions and methods for mediating cell cycle progression |
| JP2978435B2 (ja) | 1996-01-24 | 1999-11-15 | チッソ株式会社 | アクリロキシプロピルシランの製造方法 |
| AU703203B2 (en) | 1996-01-30 | 1999-03-18 | Merck & Co., Inc. | Inhibitors of farnesyl-protein transferase |
| JP2000504017A (ja) | 1996-01-30 | 2000-04-04 | メルク エンド カンパニー インコーポレーテッド | ファルネシル―タンパク質転移酵素の阻害剤 |
| DK0885002T3 (da) | 1996-03-04 | 2011-08-22 | Penn State Res Found | Materialer og fremgangsmåder til forøgelse af cellulær internalisering |
| AU5711196A (en) | 1996-03-14 | 1997-10-01 | Human Genome Sciences, Inc. | Apoptosis inducing molecule i |
| AU728657B2 (en) | 1996-03-18 | 2001-01-18 | Board Of Regents, The University Of Texas System | Immunoglobulin-like domains with increased half-lives |
| JP2000508522A (ja) | 1996-03-22 | 2000-07-11 | ヒューマン・ジェノム・サイエンシズ・インコーポレイテッド | アポトーシス誘導分子ii |
| US5891889A (en) | 1996-04-03 | 1999-04-06 | Merck & Co., Inc. | Inhibitors of farnesyl-protein transferase |
| US6063930A (en) | 1996-04-03 | 2000-05-16 | Merck & Co., Inc. | Substituted imidazole compounds useful as farnesyl-protein transferase inhibitors |
| US5883105A (en) | 1996-04-03 | 1999-03-16 | Merck & Co., Inc. | Inhibitors of farnesyl-protein transferase |
| US6080870A (en) | 1996-04-03 | 2000-06-27 | Merck & Co., Inc. | Biaryl substituted imidazole compounds useful as farnesyl-protein transferase inhibitors |
| US6300501B1 (en) | 1996-05-22 | 2001-10-09 | Warner-Lambert Company | Histidine-(N-benzyl glycinamide) inhibitors of protein farnesyl transferase |
| US5985309A (en) | 1996-05-24 | 1999-11-16 | Massachusetts Institute Of Technology | Preparation of particles for inhalation |
| US5855913A (en) | 1997-01-16 | 1999-01-05 | Massachusetts Instite Of Technology | Particles incorporating surfactants for pulmonary drug delivery |
| US5874064A (en) | 1996-05-24 | 1999-02-23 | Massachusetts Institute Of Technology | Aerodynamically light particles for pulmonary drug delivery |
| TW345603B (en) | 1996-05-29 | 1998-11-21 | Gmundner Fertigteile Gmbh | A noise control device for tracks |
| US5648239A (en) | 1996-06-21 | 1997-07-15 | Incyte Pharmaceuticals, Inc. | Human camp-dependent protein kinase inhibitor homolog |
| AU2710597A (en) | 1996-06-27 | 1998-01-14 | Pfizer Inc. | Derivatives of 2-(2-oxo-ethylidene)-imidazolidin-4-one and their use as farnesyl protein transferase inhibitors |
| PT956865E (pt) | 1996-08-12 | 2007-07-30 | Mitsubishi Pharma Corp | Medicamentos compreendendo inibidores da rho cinase. |
| US5985317A (en) | 1996-09-06 | 1999-11-16 | Theratech, Inc. | Pressure sensitive adhesive matrix patches for transdermal delivery of salts of pharmaceutical agents |
| US5945429A (en) | 1996-09-13 | 1999-08-31 | Schering Corporation | Compounds useful for inhibition of farnesyl protein transferase |
| US6030982A (en) | 1996-09-13 | 2000-02-29 | Schering Corporationm | Compounds useful for inhibition of farnesyl protein transferase |
| US6040305A (en) | 1996-09-13 | 2000-03-21 | Schering Corporation | Compounds useful for inhibition of farnesyl protein transferase |
| US5885834A (en) | 1996-09-30 | 1999-03-23 | Epstein; Paul M. | Antisense oligodeoxynucleotide against phosphodiesterase |
| US6139865A (en) | 1996-10-01 | 2000-10-31 | Eurand America, Inc. | Taste-masked microcapsule compositions and methods of manufacture |
| US5916771A (en) | 1996-10-11 | 1999-06-29 | Abgenix, Inc. | Production of a multimeric protein by cell fusion method |
| US6131570A (en) | 1998-06-30 | 2000-10-17 | Aradigm Corporation | Temperature controlling device for aerosol drug delivery |
| CA2273194C (en) | 1996-12-03 | 2011-02-01 | Abgenix, Inc. | Transgenic mammals having human ig loci including plural vh and vk regions and antibodies produced therefrom |
| US6093737A (en) | 1996-12-30 | 2000-07-25 | Merck & Co., Inc. | Inhibitors of farnesyl-protein transferase |
| US6013662A (en) | 1996-12-30 | 2000-01-11 | Rhone-Poulenc Rorer S.A. | Farnesyl transferase inhibitors, their preparation, the pharmaceutical compositions which contain them and their use in the preparation of medicaments |
| US5939439A (en) | 1996-12-30 | 1999-08-17 | Merck & Co., Inc. | Inhibitors of farnesyl-protein transferase |
| WO1998031346A1 (en) | 1997-01-16 | 1998-07-23 | Massachusetts Institute Of Technology | Preparation of particles for inhalation |
| JP2001509156A (ja) | 1997-01-29 | 2001-07-10 | ゼネカ・リミテッド | ファルネシルプロテイントランスフェラーゼの阻害剤 |
| US5860957A (en) | 1997-02-07 | 1999-01-19 | Sarcos, Inc. | Multipathway electronically-controlled drug delivery system |
| ZA981080B (en) | 1997-02-11 | 1998-08-12 | Warner Lambert Co | Bicyclic inhibitors of protein farnesyl transferase |
| TW591030B (en) | 1997-03-10 | 2004-06-11 | Janssen Pharmaceutica Nv | Farnesyl transferase inhibiting 1,8-annelated quinolinone derivatives substituted with N- or C-linked imidazoles |
| US6120751A (en) | 1997-03-21 | 2000-09-19 | Imarx Pharmaceutical Corp. | Charged lipids and uses for the same |
| TR199902553T2 (xx) | 1997-04-14 | 2000-03-21 | Micromet Gesellschaft F�R Biomedizinische Forschung Mbh | �nsan v�cuduna kar�� antijen resept�rlerinin �retimi i�in yeni metod ve kullan�mlar�. |
| US6060082A (en) | 1997-04-18 | 2000-05-09 | Massachusetts Institute Of Technology | Polymerized liposomes targeted to M cells and useful for oral or mucosal drug delivery |
| US6235883B1 (en) | 1997-05-05 | 2001-05-22 | Abgenix, Inc. | Human monoclonal antibodies to epidermal growth factor receptor |
| US6239140B1 (en) | 1997-06-17 | 2001-05-29 | Schering Corporation | Compounds useful for inhibition of farnesyl protein transferase |
| US6228865B1 (en) | 1997-06-17 | 2001-05-08 | Schering Corporation | Compounds useful for inhibition of farnesyl protein transferase |
| US6211193B1 (en) | 1997-06-17 | 2001-04-03 | Schering Corporation | Compounds useful for inhibition of farnesyl protein transferase |
| US6051582A (en) | 1997-06-17 | 2000-04-18 | Schering Corporation | Compounds useful for inhibition of farnesyl protein transferase |
| US6225322B1 (en) | 1997-06-17 | 2001-05-01 | Schering Corporation | Compounds useful for inhibition of farnesyl protein transferase |
| US6159984A (en) | 1997-06-17 | 2000-12-12 | Schering Corporation | Farnesyl protein transferase inhibitors |
| KR100612161B1 (ko) | 1997-08-15 | 2006-08-14 | 세파론, 인코포레이티드 | 전립선암 치료를 위한 티로신 키나아제 억제제 및 화학적거세법의 조합 |
| US5948433A (en) | 1997-08-21 | 1999-09-07 | Bertek, Inc. | Transdermal patch |
| US5989463A (en) | 1997-09-24 | 1999-11-23 | Alkermes Controlled Therapeutics, Inc. | Methods for fabricating polymer-based controlled release devices |
| US6103723A (en) | 1997-10-17 | 2000-08-15 | Merck & Co., Inc. | Inhibitors of farnesyl-protein transferase |
| DE69801590T2 (de) | 1997-10-22 | 2002-07-11 | Astrazeneca Ab, Soedertaelje | Imidazolderivate und ihre verwendung als farnesylproteintransferase inhibitoren |
| WO1999020612A1 (en) | 1997-10-22 | 1999-04-29 | Astrazeneca Uk Limited | Imidazole derivatives and their use as farnesyl protein transferase inhibitors |
| SE512663C2 (sv) | 1997-10-23 | 2000-04-17 | Biogram Ab | Inkapslingsförfarande för aktiv substans i en bionedbrytbar polymer |
| EP0968711B9 (en) | 1997-10-28 | 2008-05-28 | Bando Chemical Industries, Ltd. | Dermatological patch sheet and process for producing base sheet therefor |
| KR20010031713A (ko) | 1997-11-03 | 2001-04-16 | 벤슨 로버트 에이치. | 맥관형성 및 종양 성장 억제제인 맥관 내피 세포 성장억제제 |
| US6124465A (en) | 1997-11-25 | 2000-09-26 | Rhone-Poulenc S.A. | Farnesyl transferase inhibitors, their preparation, the pharmaceutical compositions which contain them and their use in the preparation of medicaments |
| EP1045846B1 (en) | 1997-11-28 | 2003-05-02 | Lg Chemical Limited | Imidazole derivatives having an inhibitory activity for farnesyl transferase and process for preparation thereof |
| US6054466A (en) | 1997-12-04 | 2000-04-25 | Merck & Co., Inc. | Inhibitors of farnesyl-protein transferase |
| US6242196B1 (en) | 1997-12-11 | 2001-06-05 | Dana-Farber Cancer Institute | Methods and pharmaceutical compositions for inhibiting tumor cell growth |
| US6335156B1 (en) | 1997-12-18 | 2002-01-01 | The Johns Hopkins University School Of Medicine | 14-3-3σ arrests the cell cycle |
| ES2185307T3 (es) | 1998-02-02 | 2003-04-16 | Lg Chemical Ltd | Inhibidores de la farnesil transferasa que tienen una estructura piperidinica y procedimiento para su preparacion. |
| EP1997893A1 (en) | 1998-02-24 | 2008-12-03 | Sisters of Providence in Oregon | Compositions containing an OX-40 receptor binding agent or a nucleic acid encoding the same and methods for enhancing antigen-specific immune response |
| US6369034B1 (en) | 1998-04-27 | 2002-04-09 | Warner-Lambert Company | Functionalized alkyl and alenyl side chain derivatives of glycinamides as farnesyl transferase inhibitors |
| US6048736A (en) | 1998-04-29 | 2000-04-11 | Kosak; Kenneth M. | Cyclodextrin polymers for carrying and releasing drugs |
| JP2002518432A (ja) | 1998-06-24 | 2002-06-25 | アドバンスト インハレーション リサーチ,インコーポレイテッド | 吸入器から放出される大多孔性粒子 |
| SI1094815T1 (en) | 1998-07-06 | 2004-04-30 | Janssen Pharmaceutica N.V. | Farnesyl protein transferase inhibitors for treating arthropathies |
| US6034053A (en) | 1998-07-13 | 2000-03-07 | Wayne Hughes Institute | EGF-isoflavone conjugates for the prevention of restenosis |
| US6372747B1 (en) | 1998-12-18 | 2002-04-16 | Schering Corporation | Farnesyl protein transferase inhibitors |
| US6362188B1 (en) | 1998-12-18 | 2002-03-26 | Schering Corporation | Farnesyl protein transferase inhibitors |
| FR2787327B1 (fr) | 1998-12-21 | 2003-01-17 | Aventis Pharma Sa | Compositions contenant des inhibiteurs de farnesyle transferase |
| US6432959B1 (en) | 1998-12-23 | 2002-08-13 | Schering Corporation | Inhibitors of farnesyl-protein transferase |
| WO2000042042A2 (en) | 1999-01-11 | 2000-07-20 | Princeton University | High affinity inhibitors for target validation and uses thereof |
| US6399633B1 (en) | 1999-02-01 | 2002-06-04 | Aventis Pharmaceuticals Inc. | Use of 4-H-1-benzopryan-4-one derivatives as inhibitors of smooth muscle cell proliferation |
| US6245759B1 (en) | 1999-03-11 | 2001-06-12 | Merck & Co., Inc. | Tyrosine kinase inhibitors |
| US6271359B1 (en) | 1999-04-14 | 2001-08-07 | Musc Foundation For Research Development | Tissue-specific and pathogen-specific toxic agents and ribozymes |
| US6143766A (en) | 1999-04-16 | 2000-11-07 | Warner-Lambert Company | Benzopyranone and quinolone inhibitors of ras farnesyl transferase |
| US6256533B1 (en) | 1999-06-09 | 2001-07-03 | The Procter & Gamble Company | Apparatus and method for using an intracutaneous microneedle array |
| US6458935B1 (en) | 1999-06-23 | 2002-10-01 | Merck & Co., Inc. | Radiolabeled farnesyl-protein transferase inhibitors |
| WO2001044301A1 (en) | 1999-11-29 | 2001-06-21 | Unilever Plc | Immobilized single domain antigen-binding molecules |
| US6403581B1 (en) | 2000-01-19 | 2002-06-11 | American Cyanamid Company | Method of inhibition of farnesyl-protein transferase using substituted benz (cd) indol-2-imine and-amine derivatives |
| US6261595B1 (en) | 2000-02-29 | 2001-07-17 | Zars, Inc. | Transdermal drug patch with attached pocket for controlled heating device |
| US20040110226A1 (en) * | 2002-03-01 | 2004-06-10 | Xencor | Antibody optimization |
| CA2489004C (en) | 2002-06-13 | 2013-01-08 | Crucell Holland B.V. | Agonistic binding molecules to the human ox40 receptor |
| US7291331B1 (en) * | 2002-09-11 | 2007-11-06 | La Jolla Institute For Allergy And Immunology | Methods of treating OX40 medicated recall immune responses |
| JP2007528723A (ja) | 2003-08-22 | 2007-10-18 | メディミューン,インコーポレーテッド | 抗体のヒト化 |
| US7850962B2 (en) | 2004-04-20 | 2010-12-14 | Genmab A/S | Human monoclonal antibodies against CD20 |
| CN101023102B (zh) * | 2004-09-17 | 2013-05-29 | 霍夫曼-拉罗奇有限公司 | 抗-ox40l抗体 |
| TWI380996B (zh) | 2004-09-17 | 2013-01-01 | Hoffmann La Roche | 抗ox40l抗體 |
| TWI461436B (zh) | 2005-11-25 | 2014-11-21 | Kyowa Hakko Kirin Co Ltd | 人類cd134(ox40)之人類單株抗體及其製造及使用方法 |
| CN101374865A (zh) * | 2005-12-16 | 2009-02-25 | 健泰科生物技术公司 | 抗ox40l抗体及其使用方法 |
| CN101668776A (zh) * | 2007-02-27 | 2010-03-10 | 健泰科生物技术公司 | 拮抗剂ox40抗体及其在炎性和自身免疫疾病的治疗中的用途 |
| BRPI0820875B1 (pt) | 2007-12-14 | 2021-10-19 | Bristol-Myers Squibb Company | Molécula de ligação isolada, anticorpo monoclonal humano, composição, molécula de ácido nucleico, vetor e célula hospedeira |
| WO2009141239A1 (en) * | 2008-05-20 | 2009-11-26 | F. Hoffmann-La Roche Ag | A pharmaceutical formulation comprising an antibody against ox40l, uses thereof |
| UY32451A (es) | 2009-02-17 | 2010-09-30 | Ucb Pharma Sa | Moléculas de anticuerpo con especifidad por el ox40 humano |
| PT2564695E (pt) | 2009-07-08 | 2015-06-03 | Kymab Ltd | Modelos animais e moléculas terapêuticas |
| EP2513145B1 (en) | 2009-12-14 | 2018-01-24 | Ablynx N.V. | Single variable domain antibodies against ox40l, constructs and therapeutic use |
| WO2013028231A1 (en) | 2011-08-23 | 2013-02-28 | Board Of Regents, The University Of Texas System | Anti-ox40 antibodies and methods of using the same |
| MX339964B (es) | 2010-08-23 | 2016-06-17 | Board Of Regents The Univ Of Texas System * | Anticuerpos anti-ox40 y metodos para usarlos. |
| US20140170157A1 (en) * | 2011-06-15 | 2014-06-19 | Glaxosmithkline Intellectual Property (No.2) Limited | Method of selecting therapeutic indications |
| EA036047B1 (ru) | 2011-07-11 | 2020-09-18 | Икнос Сайенсиз Са | Антитела, которые связываются с ox40, и их применение |
| GB201116092D0 (en) | 2011-09-16 | 2011-11-02 | Bioceros B V | Antibodies and uses thereof |
| UA112203C2 (uk) | 2011-11-11 | 2016-08-10 | Юсб Фарма С.А. | Злитий білок біоспецифічного антитіла, який зв'язується з ox40 людини та сироватковим альбуміном людини |
| WO2013119202A1 (en) | 2012-02-06 | 2013-08-15 | Providence Health & Services - Oregon | Cancer treatment and monitoring methods using ox40 agonists |
| EP2819693A4 (en) | 2012-03-02 | 2015-10-28 | Providence Health & Services Oregon | ANTICANCER BITHERAPY BASED ON OX40 / IL-2 AGONIST |
| ES2774549T3 (es) * | 2013-03-13 | 2020-07-21 | Bioasis Technologies Inc | Fragmentos de P97 y usos de los mismos |
| DK2976361T3 (en) | 2013-03-18 | 2018-10-01 | Biocerox Prod Bv | HUMANIZED ANTI-CD134- (0X40) ANTIBODIES AND APPLICATIONS THEREOF |
| GB201403775D0 (en) * | 2014-03-04 | 2014-04-16 | Kymab Ltd | Antibodies, uses & methods |
-
2016
- 2016-03-03 BR BR112017015880A patent/BR112017015880A2/pt active Search and Examination
- 2016-03-03 PL PL16715337.8T patent/PL3265123T3/pl unknown
- 2016-03-03 RU RU2017118985A patent/RU2725221C2/ru active
- 2016-03-03 EP EP22161983.6A patent/EP4137157A1/en active Pending
- 2016-03-03 CN CN201680008817.0A patent/CN108064169B/zh active Active
- 2016-03-03 KR KR1020177025436A patent/KR20170123637A/ko active IP Right Grant
- 2016-03-03 CN CN202210103585.4A patent/CN114504651A/zh active Pending
- 2016-03-03 WO PCT/GB2016/050565 patent/WO2016139482A1/en active Application Filing
- 2016-03-03 SI SI201631656T patent/SI3265123T1/sl unknown
- 2016-03-03 DK DK16715337.8T patent/DK3265123T5/da active
- 2016-03-03 RS RS20230045A patent/RS63903B1/sr unknown
- 2016-03-03 MX MX2017011194A patent/MX2017011194A/es unknown
- 2016-03-03 SG SG10201907901X patent/SG10201907901XA/en unknown
- 2016-03-03 AU AU2016227493A patent/AU2016227493B2/en active Active
- 2016-03-03 PT PT167153378T patent/PT3265123T/pt unknown
- 2016-03-03 ES ES16715337T patent/ES2937020T3/es active Active
- 2016-03-03 FI FIEP16715337.8T patent/FI3265123T3/fi active
- 2016-03-03 EP EP16715337.8A patent/EP3265123B1/en active Active
- 2016-03-03 JP JP2017537300A patent/JP7094698B2/ja active Active
- 2016-03-03 LT LTEPPCT/GB2016/050565T patent/LT3265123T/lt unknown
- 2016-03-03 DE DE112016001013.3T patent/DE112016001013T5/de active Pending
- 2016-03-03 CN CN202210103864.0A patent/CN114504652A/zh active Pending
- 2016-03-03 HR HRP20230046TT patent/HRP20230046T1/hr unknown
- 2016-03-03 HU HUE16715337A patent/HUE061070T2/hu unknown
- 2016-03-03 CA CA2968642A patent/CA2968642A1/en active Pending
- 2016-03-03 SG SG11201704160XA patent/SG11201704160XA/en unknown
-
2017
- 2017-05-22 IL IL252430A patent/IL252430A0/en unknown
- 2017-08-31 MX MX2023006416A patent/MX2023006416A/es unknown
- 2017-08-31 MX MX2023006415A patent/MX2023006415A/es unknown
-
2022
- 2022-04-19 AU AU2022202539A patent/AU2022202539A1/en active Pending
- 2022-06-22 JP JP2022100443A patent/JP7472198B2/ja active Active
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2020294247B2 (en) | Antibodies, uses & methods | |
| US9234043B1 (en) | Anti-human OX40L antibodies | |
| RU2725221C2 (ru) | Антитела, их применение и способы применения | |
| US9868790B2 (en) | Synergistic combinations of OX40L antibodies for the treatment of GvHD | |
| US10259880B2 (en) | Anti-LIGHT antibodies | |
| US20220372153A1 (en) | Synergistic combinations of ox40l antibodies for the treatment of gvhd | |
| US9434785B1 (en) | Anti-human OX40L antibodies and methods of treating graft versus host disease with the same | |
| Class et al. | Patent application title: ANTIBODIES, USES & METHODS |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| E902 | Notification of reason for refusal | ||
| E90F | Notification of reason for final refusal | ||
| E701 | Decision to grant or registration of patent right |