KR20140006909A - 화염 분무 열분해로부터의 촉매 지지체 및 자가열 프로판 탈수소화를 위한 촉매 - Google Patents
화염 분무 열분해로부터의 촉매 지지체 및 자가열 프로판 탈수소화를 위한 촉매 Download PDFInfo
- Publication number
- KR20140006909A KR20140006909A KR1020137022258A KR20137022258A KR20140006909A KR 20140006909 A KR20140006909 A KR 20140006909A KR 1020137022258 A KR1020137022258 A KR 1020137022258A KR 20137022258 A KR20137022258 A KR 20137022258A KR 20140006909 A KR20140006909 A KR 20140006909A
- Authority
- KR
- South Korea
- Prior art keywords
- catalyst
- pyrolysis
- support
- particles
- zirconium
- Prior art date
Links
- 239000003054 catalyst Substances 0.000 title claims abstract description 66
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N Propane Chemical compound CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 title claims description 20
- 238000006356 dehydrogenation reaction Methods 0.000 title claims description 14
- 239000001294 propane Substances 0.000 title claims description 10
- 238000005118 spray pyrolysis Methods 0.000 title description 6
- 239000002243 precursor Substances 0.000 claims abstract description 44
- 238000000197 pyrolysis Methods 0.000 claims abstract description 38
- 238000000034 method Methods 0.000 claims abstract description 37
- 150000001875 compounds Chemical class 0.000 claims abstract description 36
- 239000002245 particle Substances 0.000 claims abstract description 36
- 239000000443 aerosol Substances 0.000 claims abstract description 17
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims abstract description 15
- RVTZCBVAJQQJTK-UHFFFAOYSA-N oxygen(2-);zirconium(4+) Chemical compound [O-2].[O-2].[Zr+4] RVTZCBVAJQQJTK-UHFFFAOYSA-N 0.000 claims abstract description 11
- MCMNRKCIXSYSNV-UHFFFAOYSA-N ZrO2 Inorganic materials O=[Zr]=O MCMNRKCIXSYSNV-UHFFFAOYSA-N 0.000 claims abstract description 10
- 238000004519 manufacturing process Methods 0.000 claims abstract description 6
- 239000000377 silicon dioxide Substances 0.000 claims abstract description 5
- 235000012239 silicon dioxide Nutrition 0.000 claims abstract description 5
- 229910052814 silicon oxide Inorganic materials 0.000 claims abstract description 4
- BASFCYQUMIYNBI-UHFFFAOYSA-N platinum Chemical compound [Pt] BASFCYQUMIYNBI-UHFFFAOYSA-N 0.000 claims description 24
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 19
- 239000000203 mixture Substances 0.000 claims description 19
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 claims description 15
- 229910052746 lanthanum Inorganic materials 0.000 claims description 13
- 229910052718 tin Inorganic materials 0.000 claims description 13
- QQONPFPTGQHPMA-UHFFFAOYSA-N Propene Chemical compound CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 claims description 12
- 229910052697 platinum Inorganic materials 0.000 claims description 11
- 229910052792 caesium Inorganic materials 0.000 claims description 10
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 10
- 229910004298 SiO 2 Inorganic materials 0.000 claims description 9
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 claims description 8
- TVFDJXOCXUVLDH-UHFFFAOYSA-N caesium atom Chemical compound [Cs] TVFDJXOCXUVLDH-UHFFFAOYSA-N 0.000 claims description 8
- FZLIPJUXYLNCLC-UHFFFAOYSA-N lanthanum atom Chemical compound [La] FZLIPJUXYLNCLC-UHFFFAOYSA-N 0.000 claims description 8
- 239000008096 xylene Substances 0.000 claims description 8
- ATJFFYVFTNAWJD-UHFFFAOYSA-N Tin Chemical compound [Sn] ATJFFYVFTNAWJD-UHFFFAOYSA-N 0.000 claims description 7
- UQEAIHBTYFGYIE-UHFFFAOYSA-N hexamethyldisiloxane Chemical compound C[Si](C)(C)O[Si](C)(C)C UQEAIHBTYFGYIE-UHFFFAOYSA-N 0.000 claims description 7
- 238000001354 calcination Methods 0.000 claims description 6
- OFBQJSOFQDEBGM-UHFFFAOYSA-N n-pentane Natural products CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 claims description 5
- 239000001273 butane Substances 0.000 claims description 3
- 238000001035 drying Methods 0.000 claims description 3
- IJDNQMDRQITEOD-UHFFFAOYSA-N n-butane Chemical compound CCCC IJDNQMDRQITEOD-UHFFFAOYSA-N 0.000 claims description 3
- VXNZUUAINFGPBY-UHFFFAOYSA-N 1-Butene Chemical compound CCC=C VXNZUUAINFGPBY-UHFFFAOYSA-N 0.000 claims 1
- YJZXDFOVSQRRHO-UHFFFAOYSA-N C(CCCCC)(=O)OCC.[Zr+4] Chemical compound C(CCCCC)(=O)OCC.[Zr+4] YJZXDFOVSQRRHO-UHFFFAOYSA-N 0.000 claims 1
- IAQRGUVFOMOMEM-UHFFFAOYSA-N butene Natural products CC=CC IAQRGUVFOMOMEM-UHFFFAOYSA-N 0.000 claims 1
- GBNDTYKAOXLLID-UHFFFAOYSA-N zirconium(4+) ion Chemical compound [Zr+4] GBNDTYKAOXLLID-UHFFFAOYSA-N 0.000 claims 1
- 238000010438 heat treatment Methods 0.000 abstract description 4
- 239000007789 gas Substances 0.000 description 25
- 239000000243 solution Substances 0.000 description 24
- 238000005470 impregnation Methods 0.000 description 12
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 10
- 238000002360 preparation method Methods 0.000 description 9
- 238000001694 spray drying Methods 0.000 description 8
- 230000015572 biosynthetic process Effects 0.000 description 7
- 229910052751 metal Inorganic materials 0.000 description 7
- 239000002184 metal Substances 0.000 description 7
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 7
- 229910052726 zirconium Inorganic materials 0.000 description 7
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- 238000001556 precipitation Methods 0.000 description 6
- QCWXUUIWCKQGHC-UHFFFAOYSA-N Zirconium Chemical compound [Zr] QCWXUUIWCKQGHC-UHFFFAOYSA-N 0.000 description 5
- 230000000694 effects Effects 0.000 description 5
- 229910052757 nitrogen Inorganic materials 0.000 description 5
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 4
- 239000012159 carrier gas Substances 0.000 description 4
- SHZIWNPUGXLXDT-UHFFFAOYSA-N ethyl hexanoate Chemical compound CCCCCC(=O)OCC SHZIWNPUGXLXDT-UHFFFAOYSA-N 0.000 description 4
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 description 4
- 150000003839 salts Chemical class 0.000 description 4
- 239000002904 solvent Substances 0.000 description 4
- 238000003786 synthesis reaction Methods 0.000 description 4
- YOBOXHGSEJBUPB-MTOQALJVSA-N (z)-4-hydroxypent-3-en-2-one;zirconium Chemical compound [Zr].C\C(O)=C\C(C)=O.C\C(O)=C\C(C)=O.C\C(O)=C\C(C)=O.C\C(O)=C\C(C)=O YOBOXHGSEJBUPB-MTOQALJVSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 238000002485 combustion reaction Methods 0.000 description 3
- 239000001257 hydrogen Substances 0.000 description 3
- 229910052739 hydrogen Inorganic materials 0.000 description 3
- 229910000510 noble metal Inorganic materials 0.000 description 3
- 239000012454 non-polar solvent Substances 0.000 description 3
- 239000002798 polar solvent Substances 0.000 description 3
- XPGAWFIWCWKDDL-UHFFFAOYSA-N propan-1-olate;zirconium(4+) Chemical compound [Zr+4].CCC[O-].CCC[O-].CCC[O-].CCC[O-] XPGAWFIWCWKDDL-UHFFFAOYSA-N 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- -1 zirconium propionate Zirconium oxalate Chemical compound 0.000 description 3
- OFYFURKXMHQOGG-UHFFFAOYSA-J 2-ethylhexanoate;zirconium(4+) Chemical compound [Zr+4].CCCCC(CC)C([O-])=O.CCCCC(CC)C([O-])=O.CCCCC(CC)C([O-])=O.CCCCC(CC)C([O-])=O OFYFURKXMHQOGG-UHFFFAOYSA-J 0.000 description 2
- DUFCMRCMPHIFTR-UHFFFAOYSA-N 5-(dimethylsulfamoyl)-2-methylfuran-3-carboxylic acid Chemical compound CN(C)S(=O)(=O)C1=CC(C(O)=O)=C(C)O1 DUFCMRCMPHIFTR-UHFFFAOYSA-N 0.000 description 2
- IJEFAHUDTLUXDY-UHFFFAOYSA-J 7,7-dimethyloctanoate;zirconium(4+) Chemical compound [Zr+4].CC(C)(C)CCCCCC([O-])=O.CC(C)(C)CCCCCC([O-])=O.CC(C)(C)CCCCCC([O-])=O.CC(C)(C)CCCCCC([O-])=O IJEFAHUDTLUXDY-UHFFFAOYSA-J 0.000 description 2
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 2
- YNQLUTRBYVCPMQ-UHFFFAOYSA-N Ethylbenzene Chemical compound CCC1=CC=CC=C1 YNQLUTRBYVCPMQ-UHFFFAOYSA-N 0.000 description 2
- 239000005977 Ethylene Substances 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- LRHPLDYGYMQRHN-UHFFFAOYSA-N N-Butanol Chemical compound CCCCO LRHPLDYGYMQRHN-UHFFFAOYSA-N 0.000 description 2
- DKGAVHZHDRPRBM-UHFFFAOYSA-N Tert-Butanol Chemical compound CC(C)(C)O DKGAVHZHDRPRBM-UHFFFAOYSA-N 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- 150000001298 alcohols Chemical class 0.000 description 2
- 150000007942 carboxylates Chemical class 0.000 description 2
- 238000001816 cooling Methods 0.000 description 2
- 238000000354 decomposition reaction Methods 0.000 description 2
- 229930195733 hydrocarbon Natural products 0.000 description 2
- 150000002430 hydrocarbons Chemical class 0.000 description 2
- 150000002431 hydrogen Chemical class 0.000 description 2
- 238000011068 loading method Methods 0.000 description 2
- 150000001282 organosilanes Chemical class 0.000 description 2
- 229910052700 potassium Inorganic materials 0.000 description 2
- TVCBSVKTTHLKQC-UHFFFAOYSA-M propanoate;zirconium(4+) Chemical compound [Zr+4].CCC([O-])=O TVCBSVKTTHLKQC-UHFFFAOYSA-M 0.000 description 2
- 238000010791 quenching Methods 0.000 description 2
- 229910052710 silicon Inorganic materials 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000012798 spherical particle Substances 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- ZWEHNKRNPOVVGH-UHFFFAOYSA-N 2-Butanone Chemical compound CCC(C)=O ZWEHNKRNPOVVGH-UHFFFAOYSA-N 0.000 description 1
- BGGIUGXMWNKMCP-UHFFFAOYSA-N 2-methylpropan-2-olate;zirconium(4+) Chemical compound CC(C)(C)O[Zr](OC(C)(C)C)(OC(C)(C)C)OC(C)(C)C BGGIUGXMWNKMCP-UHFFFAOYSA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 1
- 229910018072 Al 2 O 3 Inorganic materials 0.000 description 1
- DKPFZGUDAPQIHT-UHFFFAOYSA-N Butyl acetate Natural products CCCCOC(C)=O DKPFZGUDAPQIHT-UHFFFAOYSA-N 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 description 1
- 229910052684 Cerium Inorganic materials 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- MYMOFIZGZYHOMD-UHFFFAOYSA-N Dioxygen Chemical compound O=O MYMOFIZGZYHOMD-UHFFFAOYSA-N 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- NHTMVDHEPJAVLT-UHFFFAOYSA-N Isooctane Chemical compound CC(C)CC(C)(C)C NHTMVDHEPJAVLT-UHFFFAOYSA-N 0.000 description 1
- 229910002422 La(NO3)3·6H2O Inorganic materials 0.000 description 1
- BZLVMXJERCGZMT-UHFFFAOYSA-N Methyl tert-butyl ether Chemical compound COC(C)(C)C BZLVMXJERCGZMT-UHFFFAOYSA-N 0.000 description 1
- BPQQTUXANYXVAA-UHFFFAOYSA-N Orthosilicate Chemical compound [O-][Si]([O-])([O-])[O-] BPQQTUXANYXVAA-UHFFFAOYSA-N 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 229910003902 SiCl 4 Inorganic materials 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 229910002808 Si–O–Si Chemical group 0.000 description 1
- 229910021626 Tin(II) chloride Inorganic materials 0.000 description 1
- 229910007926 ZrCl Inorganic materials 0.000 description 1
- 150000001242 acetic acid derivatives Chemical class 0.000 description 1
- KXKVLQRXCPHEJC-UHFFFAOYSA-N acetic acid trimethyl ester Natural products COC(C)=O KXKVLQRXCPHEJC-UHFFFAOYSA-N 0.000 description 1
- CDXSJGDDABYYJV-UHFFFAOYSA-N acetic acid;ethanol Chemical compound CCO.CC(O)=O CDXSJGDDABYYJV-UHFFFAOYSA-N 0.000 description 1
- CUJRVFIICFDLGR-UHFFFAOYSA-N acetylacetonate Chemical compound CC(=O)[CH-]C(C)=O CUJRVFIICFDLGR-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 239000004480 active ingredient Substances 0.000 description 1
- 150000001335 aliphatic alkanes Chemical class 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 238000000889 atomisation Methods 0.000 description 1
- BSDOQSMQCZQLDV-UHFFFAOYSA-N butan-1-olate;zirconium(4+) Chemical compound [Zr+4].CCCC[O-].CCCC[O-].CCCC[O-].CCCC[O-] BSDOQSMQCZQLDV-UHFFFAOYSA-N 0.000 description 1
- 229910001942 caesium oxide Inorganic materials 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 1
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 230000003197 catalytic effect Effects 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- ZMIGMASIKSOYAM-UHFFFAOYSA-N cerium Chemical compound [Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce][Ce] ZMIGMASIKSOYAM-UHFFFAOYSA-N 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 239000003638 chemical reducing agent Substances 0.000 description 1
- PNOXNTGLSKTMQO-UHFFFAOYSA-L diacetyloxytin Chemical compound CC(=O)O[Sn]OC(C)=O PNOXNTGLSKTMQO-UHFFFAOYSA-L 0.000 description 1
- JVSWJIKNEAIKJW-UHFFFAOYSA-N dimethyl-hexane Natural products CCCCCC(C)C JVSWJIKNEAIKJW-UHFFFAOYSA-N 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 238000007580 dry-mixing Methods 0.000 description 1
- ASBGGHMVAMBCOR-UHFFFAOYSA-N ethanolate;zirconium(4+) Chemical compound [Zr+4].CC[O-].CC[O-].CC[O-].CC[O-] ASBGGHMVAMBCOR-UHFFFAOYSA-N 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 150000004675 formic acid derivatives Chemical class 0.000 description 1
- FUZZWVXGSFPDMH-UHFFFAOYSA-N hexanoic acid Chemical compound CCCCCC(O)=O FUZZWVXGSFPDMH-UHFFFAOYSA-N 0.000 description 1
- KGDJAQAMSDMZCD-UHFFFAOYSA-M hydrogen carbonate lanthanum(3+) oxygen(2-) Chemical compound C([O-])(O)=O.[O-2].[La+3] KGDJAQAMSDMZCD-UHFFFAOYSA-M 0.000 description 1
- 238000005984 hydrogenation reaction Methods 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- 150000004679 hydroxides Chemical class 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 229960004592 isopropanol Drugs 0.000 description 1
- OXHNIMPTBAKYRS-UHFFFAOYSA-H lanthanum(3+);oxalate Chemical compound [La+3].[La+3].[O-]C(=O)C([O-])=O.[O-]C(=O)C([O-])=O.[O-]C(=O)C([O-])=O OXHNIMPTBAKYRS-UHFFFAOYSA-H 0.000 description 1
- JLRJWBUSTKIQQH-UHFFFAOYSA-K lanthanum(3+);triacetate Chemical compound [La+3].CC([O-])=O.CC([O-])=O.CC([O-])=O JLRJWBUSTKIQQH-UHFFFAOYSA-K 0.000 description 1
- PLOSEKHZRPLNLO-UHFFFAOYSA-K lanthanum(3+);triformate Chemical compound [La+3].[O-]C=O.[O-]C=O.[O-]C=O PLOSEKHZRPLNLO-UHFFFAOYSA-K 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- SYSQUGFVNFXIIT-UHFFFAOYSA-N n-[4-(1,3-benzoxazol-2-yl)phenyl]-4-nitrobenzenesulfonamide Chemical class C1=CC([N+](=O)[O-])=CC=C1S(=O)(=O)NC1=CC=C(C=2OC3=CC=CC=C3N=2)C=C1 SYSQUGFVNFXIIT-UHFFFAOYSA-N 0.000 description 1
- VRQWWCJWSIOWHG-UHFFFAOYSA-J octadecanoate;zirconium(4+) Chemical compound [Zr+4].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O VRQWWCJWSIOWHG-UHFFFAOYSA-J 0.000 description 1
- TVMXDCGIABBOFY-UHFFFAOYSA-N octane Chemical compound CCCCCCCC TVMXDCGIABBOFY-UHFFFAOYSA-N 0.000 description 1
- BPYXFMVJXTUYRV-UHFFFAOYSA-J octanoate;zirconium(4+) Chemical compound [Zr+4].CCCCCCCC([O-])=O.CCCCCCCC([O-])=O.CCCCCCCC([O-])=O.CCCCCCCC([O-])=O BPYXFMVJXTUYRV-UHFFFAOYSA-J 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- 150000003891 oxalate salts Chemical class 0.000 description 1
- DAWBXZHBYOYVLB-UHFFFAOYSA-J oxalate;zirconium(4+) Chemical compound [Zr+4].[O-]C(=O)C([O-])=O.[O-]C(=O)C([O-])=O DAWBXZHBYOYVLB-UHFFFAOYSA-J 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- TWNQGVIAIRXVLR-UHFFFAOYSA-N oxo(oxoalumanyloxy)alumane Chemical compound O=[Al]O[Al]=O TWNQGVIAIRXVLR-UHFFFAOYSA-N 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- CHWRSCGUEQEHOH-UHFFFAOYSA-N potassium oxide Chemical compound [O-2].[K+].[K+] CHWRSCGUEQEHOH-UHFFFAOYSA-N 0.000 description 1
- 229910001950 potassium oxide Inorganic materials 0.000 description 1
- ZGSOBQAJAUGRBK-UHFFFAOYSA-N propan-2-olate;zirconium(4+) Chemical compound [Zr+4].CC(C)[O-].CC(C)[O-].CC(C)[O-].CC(C)[O-] ZGSOBQAJAUGRBK-UHFFFAOYSA-N 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 238000000926 separation method Methods 0.000 description 1
- SCPYDCQAZCOKTP-UHFFFAOYSA-N silanol Chemical group [SiH3]O SCPYDCQAZCOKTP-UHFFFAOYSA-N 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 238000005245 sintering Methods 0.000 description 1
- 238000003980 solgel method Methods 0.000 description 1
- 239000011343 solid material Substances 0.000 description 1
- 239000011877 solvent mixture Substances 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 235000011150 stannous chloride Nutrition 0.000 description 1
- 238000003860 storage Methods 0.000 description 1
- 239000006228 supernatant Substances 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 150000003606 tin compounds Chemical class 0.000 description 1
- AXZWODMDQAVCJE-UHFFFAOYSA-L tin(II) chloride (anhydrous) Chemical compound [Cl-].[Cl-].[Sn+2] AXZWODMDQAVCJE-UHFFFAOYSA-L 0.000 description 1
- KSBAEPSJVUENNK-UHFFFAOYSA-L tin(ii) 2-ethylhexanoate Chemical compound [Sn+2].CCCCC(CC)C([O-])=O.CCCCC(CC)C([O-])=O KSBAEPSJVUENNK-UHFFFAOYSA-L 0.000 description 1
- 229910001928 zirconium oxide Inorganic materials 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01G—COMPOUNDS CONTAINING METALS NOT COVERED BY SUBCLASSES C01D OR C01F
- C01G25/00—Compounds of zirconium
- C01G25/02—Oxides
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J21/00—Catalysts comprising the elements, oxides, or hydroxides of magnesium, boron, aluminium, carbon, silicon, titanium, zirconium, or hafnium
- B01J21/06—Silicon, titanium, zirconium or hafnium; Oxides or hydroxides thereof
- B01J21/066—Zirconium or hafnium; Oxides or hydroxides thereof
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J21/00—Catalysts comprising the elements, oxides, or hydroxides of magnesium, boron, aluminium, carbon, silicon, titanium, zirconium, or hafnium
- B01J21/06—Silicon, titanium, zirconium or hafnium; Oxides or hydroxides thereof
- B01J21/08—Silica
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/38—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of noble metals
- B01J23/54—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of noble metals combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/56—Platinum group metals
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/38—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of noble metals
- B01J23/54—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of noble metals combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/56—Platinum group metals
- B01J23/62—Platinum group metals with gallium, indium, thallium, germanium, tin or lead
- B01J23/622—Platinum group metals with gallium, indium, thallium, germanium, tin or lead with germanium, tin or lead
- B01J23/626—Platinum group metals with gallium, indium, thallium, germanium, tin or lead with germanium, tin or lead with tin
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/38—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of noble metals
- B01J23/54—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of noble metals combined with metals, oxides or hydroxides provided for in groups B01J23/02 - B01J23/36
- B01J23/56—Platinum group metals
- B01J23/63—Platinum group metals with rare earths or actinides
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/90—Regeneration or reactivation
- B01J23/96—Regeneration or reactivation of catalysts comprising metals, oxides or hydroxides of the noble metals
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J35/00—Catalysts, in general, characterised by their form or physical properties
- B01J35/60—Catalysts, in general, characterised by their form or physical properties characterised by their surface properties or porosity
- B01J35/61—Surface area
- B01J35/613—10-100 m2/g
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/02—Impregnation, coating or precipitation
- B01J37/03—Precipitation; Co-precipitation
- B01J37/036—Precipitation; Co-precipitation to form a gel or a cogel
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/08—Heat treatment
- B01J37/082—Decomposition and pyrolysis
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/34—Irradiation by, or application of, electric, magnetic or wave energy, e.g. ultrasonic waves ; Ionic sputtering; Flame or plasma spraying; Particle radiation
- B01J37/349—Irradiation by, or application of, electric, magnetic or wave energy, e.g. ultrasonic waves ; Ionic sputtering; Flame or plasma spraying; Particle radiation making use of flames, plasmas or lasers
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J38/00—Regeneration or reactivation of catalysts, in general
- B01J38/04—Gas or vapour treating; Treating by using liquids vaporisable upon contacting spent catalyst
- B01J38/10—Gas or vapour treating; Treating by using liquids vaporisable upon contacting spent catalyst using elemental hydrogen
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J38/00—Regeneration or reactivation of catalysts, in general
- B01J38/04—Gas or vapour treating; Treating by using liquids vaporisable upon contacting spent catalyst
- B01J38/12—Treating with free oxygen-containing gas
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01B—NON-METALLIC ELEMENTS; COMPOUNDS THEREOF; METALLOIDS OR COMPOUNDS THEREOF NOT COVERED BY SUBCLASS C01C
- C01B33/00—Silicon; Compounds thereof
- C01B33/113—Silicon oxides; Hydrates thereof
- C01B33/12—Silica; Hydrates thereof, e.g. lepidoic silicic acid
- C01B33/18—Preparation of finely divided silica neither in sol nor in gel form; After-treatment thereof
- C01B33/187—Preparation of finely divided silica neither in sol nor in gel form; After-treatment thereof by acidic treatment of silicates
- C01B33/193—Preparation of finely divided silica neither in sol nor in gel form; After-treatment thereof by acidic treatment of silicates of aqueous solutions of silicates
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C5/00—Preparation of hydrocarbons from hydrocarbons containing the same number of carbon atoms
- C07C5/32—Preparation of hydrocarbons from hydrocarbons containing the same number of carbon atoms by dehydrogenation with formation of free hydrogen
- C07C5/327—Formation of non-aromatic carbon-to-carbon double bonds only
- C07C5/333—Catalytic processes
- C07C5/3335—Catalytic processes with metals
- C07C5/3337—Catalytic processes with metals of the platinum group
-
- C—CHEMISTRY; METALLURGY
- C01—INORGANIC CHEMISTRY
- C01P—INDEXING SCHEME RELATING TO STRUCTURAL AND PHYSICAL ASPECTS OF SOLID INORGANIC COMPOUNDS
- C01P2006/00—Physical properties of inorganic compounds
- C01P2006/12—Surface area
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2521/00—Catalysts comprising the elements, oxides or hydroxides of magnesium, boron, aluminium, carbon, silicon, titanium, zirconium or hafnium
- C07C2521/06—Silicon, titanium, zirconium or hafnium; Oxides or hydroxides thereof
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2521/00—Catalysts comprising the elements, oxides or hydroxides of magnesium, boron, aluminium, carbon, silicon, titanium, zirconium or hafnium
- C07C2521/06—Silicon, titanium, zirconium or hafnium; Oxides or hydroxides thereof
- C07C2521/08—Silica
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2523/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00
- C07C2523/02—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00 of the alkali- or alkaline earth metals or beryllium
- C07C2523/04—Alkali metals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2523/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00
- C07C2523/10—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00 of rare earths
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2523/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00
- C07C2523/14—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00 of germanium, tin or lead
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2523/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00
- C07C2523/38—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00 of noble metals
- C07C2523/40—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00 of noble metals of the platinum group metals
- C07C2523/42—Platinum
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2523/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00
- C07C2523/38—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00 of noble metals
- C07C2523/54—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group C07C2521/00 of noble metals combined with metals, oxides or hydroxides provided for in groups C07C2523/02 - C07C2523/36
- C07C2523/56—Platinum group metals
- C07C2523/62—Platinum group metals with gallium, indium, thallium, germanium, tin or lead
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/52—Improvements relating to the production of bulk chemicals using catalysts, e.g. selective catalysts
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/584—Recycling of catalysts
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Inorganic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Optics & Photonics (AREA)
- Plasma & Fusion (AREA)
- Toxicology (AREA)
- Thermal Sciences (AREA)
- Dispersion Chemistry (AREA)
- Catalysts (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Low-Molecular Organic Synthesis Reactions Using Catalysts (AREA)
Abstract
본 발명은 (i) 지르코늄 다이옥사이드 및 선택적으로 규소 다이옥사이드의 전구체 화합물을 함유하는 용액을 제조하는 단계, (ii) 상기 용액을 에어로졸로 전환하는 단계, (iii) 상기 에어로졸을 직접 또는 간접적으로 가열된 열분해 대역으로 도입하는 단계, (iv) 열분해를 수행하는 단계, 및 (v) 형성된 촉매 입자를 열분해 기체로부터 분리하는 단계를 포함하는, 지르코늄 다이옥사이드 및 선택적으로 규소 옥사이드를 함유하는 촉매 지지체 입자의 제조 방법에 관한 것이다.
Description
본 발명은 옥사이드 촉매 지지체 및 이로부터 제조된 촉매 입자, 이의 제조 방법 및 상기 촉매 입자의 탈수소화 촉매로서의 용도에 관한 것이다.
함침 방법 또는 분무 건조에 의한 탈수소화 촉매의 제조가 공지되어 있다. 이러한 방법에서, 촉매적 활성 금속은 함침 방법에 의해 옥사이드 지지체 또는 규산염 지지체상에 적용되거나, 촉매가 공침된(coprecipitated) 옥사이드 전구체의 분무 건조에 의해 제조된다.
독일 특허 제 A 196 54 391 호는, 본질적인 단사정계(monoclinic) ZrO2를 Pt(NO3)2 및 Sn(OAc)2의 용액에 의해 함침시키거나, ZrO2를 Pt(NO3)2의 제 1 용액에 의해 함침시키고 이어서 La(NO3)3의 제 2 용액에 의해 함침시킴으로써 탈수소화 촉매를 제조하는 것을 기술한다. 상기 함침된 지지체는 건조되고 이어서 하소된다. 이와 같이 제조된 촉매는, 예컨대 프로판을 프로펜으로 탈수소화하기 위한 탈수소화 촉매로서 사용된다.
상기 촉매 지지체는, 졸-겔(sol-gel) 방법, 염의 침전, 상응하는 산의 탈수소화, 건조 혼합, 슬러리화 또는 분무 건조에 의해 통상적인 방식으로 제조된다. 예컨대, ZrO2·Al2O3·SiO2가 혼합된 옥사이드의 제조를 위해, 우선 높은 수분 함량을 갖는 화학식 ZrO2·xH2O의 지르코늄 옥사이드가 적절한 지르코늄-함유 전구체의 침전에 의해 제조될 수 있다. 적절한 지르코늄의 전구체는, 예컨대 Zr(NO3)4, ZrOCl2 또는 ZrCl4이다. 실제의 침전이 염기, 예컨대 NaOH, KOH, Na2CO3 및 NH3의 첨가에 의해 수행되고, 이는 예컨대 유럽특허 제 A 0 849 224 호에 기술되어 있다.
ZrO2·SiO2가 혼합된 옥사이드를 제조하기 위해, 지르코늄-함유 전구체가 규소-함유 전구체와 혼합될 수 있다. SiO2를 위한 매우 적절한 전구체는, 예컨대 SiO2의 수분-함유 졸, 예컨대 루독스(Ludox, 상표)이다. 상기 두 성분은, 예컨대 간단한 기계적인 혼합 또는 분무 탑내에서의 분무 건조에 의해 혼합될 수 있다.
화염 분무 열분해에 의한 금속 촉매의 공지된 제조 방법이 문헌[Pisduangnawakij et al., Applied Catalysis A: General 370 1-6, 2009]에 기술되어 있다. 상기 문헌에서, 자일렌중에 백금 및 주석의 전구체 화합물 및 지지체인 알루미늄 옥사이드의 전구체 화합물을 함유하는 용액이 에어로졸로 전환되며, 이는 상기 전구체 화합물의 분해 온도를 초과하는 온도에서 열분해 반응기내의 불활성 운반(carrier) 기체중에서 처리되고, 이어서 형성된 미세하게 분해된 금속이 운반 기체로부터 분리된다.
본 발명에 의해 해결될 문제점은 탈수소화 촉매를 위한 옥사이드 지지체의 값싸고 시간-절약적인 제조 방법을 제공하는 것이며, 이때, 제조된 탈수소화 촉매는 함침 방법 또는 분무 건조에 의해 독점적으로 제조된, 종래 기술의 촉매에 대한 활성 및 선택성에 있어 필적할만 해야 한다.
이러한 문제점은 지르코늄 다이옥사이드 및 선택적으로 규소 옥사이드를 함유하는 촉매 지지체 입자의 제조 방법에 의해 해결되며, 상기 제조 방법은 다음의 단계를 포함한다:
(i) 지르코늄 다이옥사이드 및 선택적으로 규소 옥사이드의 전구체 화합물을 함유하는 용액을 제조하는 단계;
(ii) 상기 용액을 에어로졸로 전환하는 단계;
(iii) 상기 에어로졸을 직접 또는 간접적으로 가열된 열분해 대역으로 도입하는 단계;
(iv) 열분해를 수행하는 단계; 및
(v) 형성된 촉매 입자를 열분해 기체로부터 분리하는 단계.
옥사이드-형성 전구체 화합물은 에어로졸로서 열분해 대역으로 공급된다. 열분해 대역으로 공급된 에어로졸이 모든 옥사이드-형성 전구체 화합물을 함유하는 단지 하나의 용액의 분무화에 의해 제조되는 것이 바람직하다. 이러한 방식에서, 제조된 입자의 조성이 균질하고 일정한 것이 항상 보장된다. 따라서, 에어로졸로 전환될 용액을 제조하는 동안, 개별적인 성분은 용액중에 함유된 옥사이드-형성 전구체가 용액이 분무화될 때까지 함께 서로 균질하게 용해되도록 바람직하게 선택된다. 다르게는, 옥사이드-형성 전구체를 함께 함유하는 몇몇의 상이한 용액을 사용하는 것이 또한 가능하다. 상기 용액은 극성 및 비극성 용매 둘 다 또는 용매 화합물을 함유할 수 있다.
열분해 대역에서, 옥사이드의 형성과 함께 옥사이드 전구체의 분해 및/또는 산화가 발생한다. 열분해는 일반적으로 다양한 비표면(specific surface)을 갖는 구형 입자를 생산한다.
열분해 대역내의 온도는 옥사이드를 형성하기에 충분한 온도, 통상적으로 500 내지 2000℃이다. 열분해는 바람직하게는 900 내지 1500℃의 온도에서 수행된다.
열분해 반응기는, 예컨대 전기 로에 의해 외부로부터 간접적으로 가열될 수 있다. 간접적인 가열에서 요구되는 외부로부터 내부로의 온도 구배 때문에, 상기 로는 열분해에 요구되는 상응하는 온도보다 훨씬 더 뜨거워야 한다. 간접적인 가열은 열적으로 안정한 로 물질 및 비싼 반응기 구조물을 요구하지만, 요구되는 기체의 총량은 화염 반응기의 경우보다 더 적다.
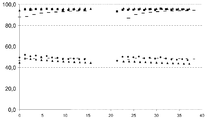
도 1은, 침전 및 분무 건조에 의해 제조된 지지체를 갖는 기준 촉매(-)의 활성 및 선택성, 및 함침에 의해 각각의 경우에 적용된 추가의 원소를 갖고 화염 합성으로부터 유도된 지지체를 갖는 본 발명에 따른 촉매(■)의 활성 및 선택성을 나타낸다. 동일한 조성의 독점적으로 화염-합성된 촉매(▲)의 결과가 또한 나타나 있다.
바람직한 실시양태에서, 열분해 대역은 화염에 의해 가열된다(화염 분무 열분해). 이때, 상기 열분해 대역은 점화 장치를 포함한다. 직접적인 가열을 위해, 바람직하게는 수소, 메탄 또는 에틸렌이 사용되지만, 통상적인 가연성 기체가 사용된다. 상기 열분해 대역내의 온도는 가연성 기체의 양 대 기체의 총량의 비율에 의해 요구되는 바와 같이 조정될 수 있다. 기체의 총량을 낮게 유지하되, 그럼에도 불구하고 가능한한 높은 온도를 달성하기 위해, 상기 열분해 대역은 또한 공기 대신 순수한 산소가 가연성 기체의 연소를 위한 O2 공급원으로서 공급될 수 있다. 기체의 총량은 또한 에어로졸 및 에어로졸의 증발된 용매를 위한 운반 기체를 포함한다. 상기 열분해 대역으로 공급된 에어로졸은 바람직하게는 직접 화염내로 공급된다. 일반적으로 공기가 에어로졸을 위한 운반 기체로서 바람직하지만, 질소, CO2, O2 또는 가연성 기체, 예컨대 수소, 메탄, 에틸렌, 프로판 또는 부탄이 또한 사용될 수 있다.
본 발명에 따른 방법의 또 다른 실시양태에서, 열분해 대역은 전기 플라즈마 또는 유도 플라즈마에 의해 가열된다.
화염 분부 열분해 장치는 일반적으로 분무화될 액체를 위한 저장 컨테이너, 운반 기체를 위한 공급 파이프, 가연성 기체 및 산소-함유 기체, 중앙 에어로졸 노즐 및 이 주위에 배열된 환형 연소기, 필터 요소를 포함하는 기체-고체 분리를 위한 장치, 고체 배출 장치 및 배기 가스 배출구를 포함한다. 입자는 급랭 기체, 예컨대 질소 또는 공기에 의해 냉각된다.
안정된 온도 프로파일을 생성하기 위해, 바람직하게는 관-형상의 연소 공간이 단열된다.
열분해 결과, 다양한 비표면을 갖는 구형 입자를 함유하는 열분해 기체가 제조된다. 제조된 입자의 크기 분포는, 다른 것들중에서, 열분해 대역내로 공급된 에어로졸의 점적 크기 스펙트럼 및 사용된 용액의 농도로부터 기인한다.
바람직하게는, 열분해 기체로부터 형성된 입자가 분리되기 전에, 상기 열분해 기체는 입자의 소결이 제외되도록 냉각된다. 이러한 이유 때문에, 상기 열분해 대역은 바람직하게는 열분해 반응기의 연소 공간에 인접한 냉각 대역을 포함한다. 사용된 필터 요소에 따라, 열분해 기체 및 이에 함유된 촉매 입자를 약 100 내지 500℃의 온도까지 냉각시키는 것이 일반적으로 요구된다. 약 100 내지 150℃까지 냉각시키는 것이 바람직하게 발생한다. 상기 열분해 대역을 떠난 후, 촉매 입자를 함유하고 부분적으로 냉각된 상기 열분해 기체는 상기 입자를 열분해 기체로부터 분리시키기 위한 장치(필터 요소를 포함함)로 들어간다. 냉각을 위해, 급랭 기체, 예컨대 질소, 공기 또는 수분-습윤된 기체가 상기 장치 내로 공급된다.
적절한 지르코늄 다이옥사이드-형성 전구체 화합물은 알콜레이트, 예컨대 지르코늄(IV) 에탄올레이트, 지르코늄(IV) n-프로판올레이트, 지르코늄(IV) 이소프로판올레이트, 지르코늄(IV) n-부탄올레이트 및 지르코늄(IV) tert-부탄올레이트이다. 본 발명에 따른 방법의 바람직한 실시양태에서, 바람직하게는 n-프로판올중의 용액으로서의 지르코늄(IV) 프로판올레이트가 ZrO2 전구체 화합물로서 사용된다.
다른 적절한 지르코늄 다이옥사이드-형성 전구체 화합물은 카복실레이트, 예컨대 지르코늄 아세테이트, 지르코늄 프로피오네이트, 지르코늄 옥살레이트, 지르코늄 옥토에이트, 지르코늄 2-에틸-헥사노에이트, 지르코늄 네오데카노에이트, 지르코늄 아세테이트, 지르코늄 프로피오네이트, 지르코늄 옥살레이트, 지르코늄 옥타노에이트, 지르코늄 2-에틸헥사노에이트, 지르코늄 네오데카노에이트 및/또는 지르코늄 스테아레이트, 지르코늄 프로피오네이트이다. 본 발명에 따른 방법의 또 다른 바람직한 실시양태에서, 지르코늄(IV) 아세틸아세토네이트가 전구체 화합물로서 사용된다.
하나의 실시양태에서, 상기 전구체 화합물은 규소 다이옥사이드 전구체 화합물을 추가로 포함한다. 규소 다이옥사이드를 위한 가능한 전구체는 유기실란, 및 SiCl4와 저급 알콜 또는 저급 카복실산의 반응 생성물이다. 전술된 유기실란 및/또는 -실라놀과 Si-O-Si 단위의 축합물을 사용하는 것이 또한 가능하다. 실록산이 바람직하게 사용된다. 또한, SiO2를 사용하는 것이 가능하다. 본 발명에 따른 방법의 바람직한 실시양태에서, 전구체 화합물은 헥사메틸다이실록산을 실리카-형성 전구체 화합물로서 포함한다.
극성 및 비극성 용매 둘 다 또는 용매 혼합물이 에어로졸 형성에 요구되는 용액을 제조하기 위해 사용될 수 있다.
바람직한 극성 용매는 물, 메탄올, 에탄올, n-프로판올, 이소-프로판올, n-부탄올, tert-부탄올, n-프로판온, n-부탄온, 다이에틸 에터, tert-부틸-메틸 에터, 테트라하이드로퓨란, C1-C8 카복실산, 에틸 아세테이트 및 이들의 혼합물이다.
본 발명에 따른 방법의 바람직한 실시양태에서, 하나 이상의 상기 전구체 화합물, 바람직하게는 상기 모든 전구체 화합물은 아세트산, 에탄올 및 물의 혼합물에 용해된다. 바람직하게는 상기 혼합물은 30 내지 75 중량%의 아세트산, 30 내지 75 중량%의 에탄올 및 0 내지 20 중량%의 물을 함유한다. 특히, 지르코늄(IV) 아세틸아세토네이트 및 헥사메틸다이실록산이 아세트산, 에탄올 및 물의 혼합물에 용해된다.
바람직한 비극성 용매는 톨루엔, 자일렌, n-헵탄, n-펜탄, 옥탄, 이소옥탄, 사이클로헥산, 메틸, 에틸 또는 부틸 아세테이트 또는 이들의 혼합물이다. 5 내지 15개의 탄소 원자를 갖는 탄화수소 또는 탄화수소의 혼합물이 또한 적절하다. 자일렌이 특히 바람직하다.
특히, Zr(IV) 에틸헥사노에이트 및 헥사메틸다이실록산은 자일렌에 용해된다.
분무 열분해에 의해 제조된 촉매 지지체 입자는 바람직하게는 36 내지 70 m2/g의 비표면을 갖는다.
이어서, 제조된 촉매 지지체 입자는, 백금, 주석, 및 란타늄 및 세슘으로부터 선택된 하나 이상의 다른 원소의 화합물을 함유하는 하나 이상의 용액에 의해 함침된다. 함침된 촉매 지지체 입자는 건조되고 하소된다.
따라서, 본 발명은 또한 지르코늄 다이옥사이드-함유 지지체상에 백금 및 주석, 및 란타늄 및 세슘으로부터 선택된 하나 이상의 다른 원소를 포함하는 촉매 입자의 제조 방법에 관한 것으로서, 상기 제조 방법은 상기 (i) 내지 (v)의 단계, 및 추가로 다음의 단계를 포함한다:
(vi) 형성된 촉매 지지체 입자를 백금, 주석, 및 란타늄 및 세슘으로부터 선택된 하나 이상의 다른 원소의 화합물을 함유하는 하나 이상의 용액에 의해 함침시키는 단계; 및
(vii) 상기 함침된 촉매 지지체 입자를 건조시키고 하소시키는 단계.
일반적으로, 사용된 전구체 화합물은 하소에 의해 상응하는 옥사이드로 전환될 수 있는 화합물이다. 예컨대, 하이드록사이드, 카보네이트, 옥살레이트, 아세테이트, 클로라이드 및 상응하는 금속의 혼합된 하이드록시카보네이트가 적절하다.
일반적으로, 탈수소화-활성 성분은 함침에 의해 적용된다. 그러나, 함침 대신, 탈수소화-활성 성분은 또한 다른 방법, 예컨대 금속 염 전구체의 분무에 의해 적용될 수 있다. 백금이 H2PtCl6 또는 Pt(NO3)2로서 바람직하게 사용된다. 물 및 유기 용매 둘 다가 용매로서 적절하다. 물 및 저급 알콜, 예컨대 메탄올 및 에탄올이 특히 적절하다.
또한, 귀금속이 탈수소화-활성 성분으로서 사용될 경우, 적절한 전구체는 상응하는 귀금속 졸이며, 상기 귀금속 졸은 공지된 방법중 하나, 예컨대 환원제와 함께 안정화제, 예컨대 PVP의 존재하에 금속 염의 환원에 의해 제조될 수 있다. 독일특허출원 제 195 00 366 호에 상기 제조 기술의 상세한 설명이 있다.
촉매내의 탈수소화-활성 성분으로서 백금의 함량은 0.01 내지 5 중량%, 바람직하게는 0.05 내지 1 중량%, 특히 바람직하게는 0.05 내지 0.5 중량%이다.
또한, 상기 촉매는 적어도 주석을 0.01 내지 10 중량%, 바람직하게는 0.05 내지 2 중량%의 양으로 함유한다. 적절한 주석 화합물은 카복실레이트, 예컨대 주석(II) 아세테이트, 주석 2-에틸헥사노에이트 또는 주석(II) 클로라이드이다.
바람직한 실시양태에서, Pt의 적재(loading)는 0.05 내지 1 중량%이고, Sn의 적재는 0.05 내지 2 중량%이다.
또한, 활성 질량은 적어도 세슘 및 란타늄을 함유하는 다음의 추가 성분을 함유할 수 있다:
- 세슘 및 선택적으로 0.1 내지 10 중량%의 함량을 갖는 칼륨. 하소에 의해 옥사이드로 전환될 수 있는 화합물, 예컨대 하이드록사이드, 카보네이트, 옥살레이트, 아세테이트 또는 포르메이트가 세슘 또는 칼륨 옥사이드 전구체로서 사용된다.
- 란타늄 및 선택적으로 0.1 내지 10 중량%의 함량을 갖는 세륨. 란타늄이 사용되는 경우, 예컨대 란타늄 옥사이드 카보네이트, La(OH)3, La2(CO3)3, La(NO3)3, 란타늄 포르메이트, 란타늄 아세테이트 및 란타늄 옥살레이트가 전구체 염으로서 적절하다.
활성 성분을 촉매 지지체상에 적용한 후, 하소가 400 내지 1000℃, 바람직하게는 500 내지 700℃, 특히 바람직하게는 550 내지 650℃의 온도에서 수행된다.
또한, 본 발명은 본 발명에 따른 방법에 의해 제조될 수 있는 지지체 및 촉매 입자에 관한 것이다. 이들은 바람직하게는 20 내지 70 m2/g의 비표면을 갖는다.
바람직한 실시양태에서, 상기 촉매 지지체는 다음의 백분율 조성을 갖는다: 30 내지 99.5 중량%의 ZrO2, 0.5 내지 25 중량%의 SiO2. 추가로, 상기 촉매 입자는 지지체의 질량을 기준으로 0.1 내지 1 중량%의 Pt, 0.1 내지 10 중량%의 Sn, La 및/또는 Cs를 함유하며, 이때, 적어도 Sn 및 적어도 La 또는 Cs가 포함된다.
또한, 본 발명은 상기 촉매 입자의 수소화 촉매 또는 탈수소화 촉매로서의 용도에 관한 것이다. 알칸, 예컨대 부탄 및 프로판뿐만 아니라 에틸벤젠이 바람직하게는 탈수소화된다.
프로판을 프로펜으로 탈수소화하기 위한 본 발명에 따른 촉매의 용도가 특히 바람직하다.
본 발명이 하기 실시예로 더욱 상세하게 설명된다.
실시예
사용된 화학약품
지르코늄 아세틸아세토네이트 Zr(acac)2(98%)
지르코늄(IV) 프로폭사이드 Zr(OPr)4(1-프로판올중의 70%)
헥사메틸다이실록산(HMDSO)(98%)
CsNO3
KNO3
SnCl2·2 H2O
La(NO3)3·6 H2O
아세트산(100%), 에탄올(96%) 및 물(탈이온화됨)의 혼합물
자일렌(이성질체의 혼합물)
전구체 화합물 용액의 제조
용매는 4.6 : 4.6 : 1의 중량비의 HoAc : EtOH : H2O이다. 아세트산-에탄올 혼합물을 신선하게 제조하였다. Si 및 Zr을 위한 전구체 화합물을 여기에 용해시켰다.
실시예를 위한 전구체 화합물의 극성 용액의 조성을 하기 표 1에 나타냈다.
| [g] | 물질 | 순도[중량%] |
| 374.40 | Zr[IV] 에틸헥사노에이트 | 97 |
| 10.11 | 헥사메틸다이실록산 | 99 |
화염 분무 열분해에 의한 촉매 지지체 입자의 제조
전구체 화합물을 함유하는 용액을 2-성분 노즐을 통해 피스톤 펌프로 공급하고 상응하는 양의 공기로 원자화하였다. 상응하는 온도를 달성하기 위해, 이따금씩 에틸렌-공기 혼합물로부터의 지지체 화염(노즐 주위에 위치한 환형 연소기를 통해 공급됨)을 사용하였다. 압력 강하를 1.1 바(bar)에서 일정하게 유지시켰다.
화염 합성 조건을 하기 표 2에 요약하였다.
| 용매 | cZr [mol/kg용액] |
전구체 화합물의 유속 [ml/시간] |
총 기체 흐름 [l/시간] |
분산 기체 흐름 [l/시간] |
| 자일렌 | 1 | 310 | 3500 | 1200 |
입자를 분리하기 위해 백하우스(baghouse) 필터를 사용하였다. 5 바 압력의 질소 서지(surge)를 필터 주머니에 적용함으로써 이러한 필터를 청소할 수 있다.
화염-합성된 지지체의
함침
함침을 유럽특허 제 1 074 301 호의 실시예 4와 같이 수행하였다. 에탄올중의 SnCl2 및 H2PtCl6의 용액을 1 내지 2 mm의 체 분획의 화염-합성된 SiO2/ZrO2 지지체상에 부었다. 과량의 용액을 회전 증발기내에서 제거하고, 고체 물질을 건조시키고 하소시켰다. 이를 위해, CsNO3 및 La(NO3)3의 수용액을 첨가하고, 상청액을 제거하였다. 건조 및 하소시킨 후, 23 m2의 BET 표면적을 갖는 촉매를 수득하였다.
기준 촉매
습식-화학적 경로에 의해 실시예 4에 따라 제조한, 유럽특허 제 1 074 301 호에 따른 기준 촉매는 95 중량% ZrO2, 5 중량% SiO2(지지체), 0.5 중량% Pt, 1 중량% Sn, 3% La, 0.5 중량% Cs 및 0.2 중량% K(지지체의 질량을 기준으로, 활성 및 촉진제 금속)로 이루어져 있다. 졸/겔 방법에 따라 침전에 의해 수득된 옥사이드 혼합물을 분무 건조시켜 지지체를 수득하였다.
촉매 측정
프로판 탈수소화를 약 600℃에서 수행하였다: 21 Nl/시간 총 기체(20 Nl/시간 프로판, 내부 표준으로서 1 Nl/시간 질소), 5 g/시간 물. 400℃에서 재생을 수행하였다: 2시간의 21 Nl/시간 N2 + 4 Nl/시간 공기; 2시간의 25 Nl/h 공기; 1시간의 25 Nl/시간 수소.
전환, 장기 안정성 및 프로펜 형성의 선택성을 촉매 시험에서 조사하였다. 이어지는 함침과 함께 화염 합성으로부터 제조된 촉매는, 최적 작동 조건에서, 프로판의 프로펜으로의 자가열 탈수소화에서 48%의 전환 및 95%의 선택성을 나타냈다.
비교를 위한 도 1은, 침전 및 분무 건조에 의해 제조된 지지체를 갖는 기준 촉매(-)의 활성 및 선택성, 및 함침에 의해 각각의 경우에 적용된 추가의 원소를 갖고 화염 합성으로부터 유도된 지지체를 갖는 본 발명에 따른 촉매(■)의 활성 및 선택성을 나타낸다. 동일한 조성의 독점적으로 화염-합성된 촉매(▲)의 결과가 또한 나타나 있다. 시간(시)이 횡좌표상에 나타나 있고, 프로판의 프로펜으로의 자가열 탈수소화에 대한 전환(40 내지 50%) 및 선택성(80% 초과)이 종좌표상에 나타나 있다.
3개의 촉매가 필적할만한 성능을 갖는다는 것을 확인할 수 있다. 기준 촉매는 보다 낮은 초기 선택성을 갖는다. 그러나, 몇 주의 시험 사이클에 걸쳐, 이는 대등해졌다. 따라서, 화염-합성된 촉매 및 화염-합성된 지지체는 (본 발명에 따른) 추가 원소의 습식-화학적 적용 후에 숙성된 촉매(이의 지지체는 분무 건조에 의해 수득됨)와 유사하게 행동하였다.
Claims (16)
- (i) 지르코늄 다이옥사이드 및 선택적으로 규소 다이옥사이드의 전구체 화합물을 함유하는 용액을 제조하는 단계;
(ii) 상기 용액을 에어로졸로 전환하는 단계;
(iii) 에어로졸을 직접 또는 간접적으로 가열된 열분해 대역으로 도입하는 단계;
(iv) 열분해를 수행하는 단계; 및
(v) 형성된 촉매 입자를 열분해 기체로부터 분리하는 단계
를 포함하는, 지르코늄 다이옥사이드 및 선택적으로 규소 옥사이드를 함유하는 촉매 지지체 입자의 제조 방법. - 제 1 항에 있어서,
열분해 대역이 화염에 의해 가열되는 제조 방법. - 제 1 항 또는 제 2 항에 있어서,
지르코늄 다이옥사이드 전구체 화합물이 지르코늄(IV) 에틸헥사노에이트를 포함하는 제조 방법. - 제 1 항 내지 제 3 항중 어느 한 항에 있어서,
규소 다이옥사이드 전구체 화합물이 헥사메틸다이실록산을 포함하는 제조 방법. - 제 1 항 내지 제 4 항중 어느 한 항에 있어서,
지르코늄 다이옥사이드 전구체 화합물이 지르코늄(IV) 프로폭실레이트를 포함하는 제조 방법. - 제 1 항 내지 제 5 항중 어느 한 항에 있어서,
하나 이상의 전구체 화합물이 아세트산, 에탄올 및 물의 혼합물에 용해되는 제조 방법. - 제 1 항 내지 제 6 항중 어느 한 항에 있어서,
하나 이상의 전구체 화합물이 자일렌에 용해되는 제조 방법. - 제 1 항 내지 제 7 항중 어느 한 항에 있어서,
열분해가 900 내지 1500℃의 온도에서 수행되는 제조 방법. - 제 1 항 내지 제 8 항중 어느 한 항에 따른 제조 방법에 의해 제조될 수 있는 촉매 지지체 입자.
- 제 1 항 내지 제 8 항중 어느 한 항에 따른 (i) 내지 (v) 단계를 포함하고, 추가로,
(vi) 형성된 촉매 지지체 입자를 백금, 주석, 및 란타늄 및 세슘으로부터 선택된 하나 이상의 다른 원소의 화합물을 함유하는 하나 이상의 용액에 의해 함침시키는 단계; 및
(vii) 상기 함침된 촉매 지지체 입자를 건조시키고 하소시키는 단계
를 포함하는, 지르코늄 다이옥사이드-함유 지지체상에 백금 및 주석, 및 란타늄 및 세슘으로부터 선택된 하나 이상의 다른 원소를 포함하는 촉매 입자의 제조 방법. - 제 10 항에 따른 제조 방법에 의해 제조될 수 있는 촉매 입자.
- 제 11 항에 있어서,
0.05 내지 1 중량%의 Pt 및 0.05 내지 2 중량%의 Sn을 함유하는 촉매 입자. - 제 11 항 또는 제 12 항에 있어서,
20 내지 70 m2/g의 비표면을 갖는 촉매 입자. - 제 11 항 내지 제 13 항중 어느 한 항에 있어서,
지지체로서 30 내지 99.5 중량%의 ZrO2, 0.5 내지 25 중량%의 SiO2, 및 지지체의 질량을 기준으로 0.1 내지 1 중량%의 Pt, 0.1 내지 10 중량%의 Sn, La 및/또는 Cs를 포함하되, 적어도 Sn 및 적어도 La 또는 Cs를 포함하는 촉매 입자. - 제 11 항 내지 제 14 항중 어느 한 항에 따른 촉매 입자의 탈수소화 촉매로서의 용도.
- 제 15 항에 있어서,
프로판을 프로펜으로 탈수소화하거나 부탄을 부텐으로 탈수소화하기 위한 촉매 입자의 용도.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP11151958 | 2011-01-25 | ||
| EP11151958.3 | 2011-01-25 | ||
| PCT/IB2012/050303 WO2012101567A2 (de) | 2011-01-25 | 2012-01-23 | Katalysatorträger aus der flammen-spraypyrolyse und katalysator für die autotherme propandehydrierung |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20140006909A true KR20140006909A (ko) | 2014-01-16 |
Family
ID=46581216
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020137022258A KR20140006909A (ko) | 2011-01-25 | 2012-01-23 | 화염 분무 열분해로부터의 촉매 지지체 및 자가열 프로판 탈수소화를 위한 촉매 |
Country Status (6)
| Country | Link |
|---|---|
| EP (1) | EP2667968A2 (ko) |
| JP (1) | JP2014511259A (ko) |
| KR (1) | KR20140006909A (ko) |
| CN (1) | CN103379957A (ko) |
| BR (1) | BR112013019047A2 (ko) |
| WO (1) | WO2012101567A2 (ko) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017082564A1 (ko) * | 2015-11-10 | 2017-05-18 | 희성촉매 주식회사 | 안정화 활성금속 복합체를 이용한 직쇄형 경질탄화수소류 탈수소화 촉매 제조방법 |
| WO2017082565A1 (ko) * | 2015-11-10 | 2017-05-18 | 희성촉매 주식회사 | 안정화 활성금속 착체를 이용한 직쇄형 탄화수소류 탈수소화 촉매 제조방법 |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8933262B2 (en) | 2011-05-24 | 2015-01-13 | Basf Se | Process for preparing polyisocyanates from biomass |
| CN103566933B (zh) * | 2012-08-08 | 2016-09-07 | 中国石油化工股份有限公司 | 一种醋酸酯加氢制乙醇用催化剂及其制备方法 |
| CN104248953A (zh) * | 2013-06-28 | 2014-12-31 | 中国石油化工股份有限公司 | 一种醋酸酯加氢制乙醇用催化剂及其制备方法 |
| CN106753391A (zh) * | 2016-11-28 | 2017-05-31 | 新沂市中诺新材料科技有限公司 | 一种用于钝化修复土壤中重金属的纳米材料及制备方法 |
| CN111821996B (zh) * | 2019-04-18 | 2022-11-29 | 清华大学 | 高效抗水热和抗硫性能的脱汞催化剂及其制备方法与应用 |
| CN115069246B (zh) * | 2021-03-15 | 2023-08-15 | 中国石油化工股份有限公司 | 一种负载型银催化剂及其制备方法和应用 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3701805A (en) * | 1971-09-27 | 1972-10-31 | Pfizer | Preparation of citraconic and itaconic acids |
| US6057030A (en) * | 1997-07-21 | 2000-05-02 | Kanebo Ltd. | Porous ceramic body and kiln furniture made from a porous ceramic body |
| DE19937107A1 (de) * | 1999-08-06 | 2001-02-08 | Basf Ag | Katalysator mit bimodaler Porenradienverteilung |
| CN1513600A (zh) * | 2003-08-19 | 2004-07-21 | 丁章云 | 一种催化剂活性载体及其制备 |
| CN101204654A (zh) * | 2006-12-20 | 2008-06-25 | 中国科学院生态环境研究中心 | 一种低温催化氧化苯系物的负载型贵金属催化剂及其制备方法 |
| CN101433863B (zh) * | 2007-11-15 | 2012-08-29 | 中国石油化工股份有限公司 | 一种复合氧化物载体及其制备方法 |
-
2012
- 2012-01-23 WO PCT/IB2012/050303 patent/WO2012101567A2/de active Application Filing
- 2012-01-23 BR BR112013019047A patent/BR112013019047A2/pt not_active IP Right Cessation
- 2012-01-23 KR KR1020137022258A patent/KR20140006909A/ko not_active Application Discontinuation
- 2012-01-23 EP EP12739435.1A patent/EP2667968A2/de not_active Withdrawn
- 2012-01-23 CN CN2012800086618A patent/CN103379957A/zh active Pending
- 2012-01-23 JP JP2013549930A patent/JP2014511259A/ja not_active Withdrawn
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017082564A1 (ko) * | 2015-11-10 | 2017-05-18 | 희성촉매 주식회사 | 안정화 활성금속 복합체를 이용한 직쇄형 경질탄화수소류 탈수소화 촉매 제조방법 |
| WO2017082565A1 (ko) * | 2015-11-10 | 2017-05-18 | 희성촉매 주식회사 | 안정화 활성금속 착체를 이용한 직쇄형 탄화수소류 탈수소화 촉매 제조방법 |
| US11040333B2 (en) | 2015-11-10 | 2021-06-22 | Heesung Catalysts Corporation | Method for preparing dehydrogenation catalyst for straight chain-type light hydrocarbon using stabilized active material complex |
| US11266979B2 (en) | 2015-11-10 | 2022-03-08 | Heesung Catalysts Corporation | Method for preparing dehydrogenation catalyst for straight chain-type light hydrocarbon using stabilized active metal composite |
Also Published As
| Publication number | Publication date |
|---|---|
| EP2667968A2 (de) | 2013-12-04 |
| WO2012101567A3 (de) | 2013-01-03 |
| BR112013019047A2 (pt) | 2017-03-28 |
| WO2012101567A2 (de) | 2012-08-02 |
| JP2014511259A (ja) | 2014-05-15 |
| CN103379957A (zh) | 2013-10-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20140006909A (ko) | 화염 분무 열분해로부터의 촉매 지지체 및 자가열 프로판 탈수소화를 위한 촉매 | |
| TWI511787B (zh) | 整體型觸媒(monolith catalyst)及其用途 | |
| JPH01320214A (ja) | シリカ―アルミナゲル | |
| KR20140010050A (ko) | 자가열 프로판 탈수소화를 위한 화염 분무 열분해에 의해 제조된 촉매 | |
| CN101024196A (zh) | 重油的催化裂解催化剂以及烯烃和燃料油的制造方法 | |
| US10695750B2 (en) | Catalyst for decomposition of nitrous oxide | |
| EP1074299A2 (de) | Multikomponenten-Dehydrierungskatalysatoren | |
| US8680005B2 (en) | Catalyst from flame-spray pyrolysis and catalyst for autothermal propane dehydrogenation | |
| US20120190537A1 (en) | Catalyst support from flame-spray pyrolysis and catalyst for autothermal propane dehydrogenation | |
| US20030101659A1 (en) | Nanoscalar pyrogenically produced yttrium-zirconium mixed oxide | |
| KR101421189B1 (ko) | 개선된 이산화탄소 전환촉매 | |
| Bian et al. | The effect of catalyst preparation on the activity of MoO 3-SiO 2 catalyst in transesterification of diethyl oxalate | |
| CN116920926A (zh) | 贵金属加氢催化剂及其制备方法与应用 | |
| DEVIKA et al. | Selective oxidation of diphenylmethane to benzophenone over CeAlPO-5 molecular sieves | |
| JP6840056B2 (ja) | 脱水素触媒、水素の製造システム、及び水素の製造方法 | |
| WO2021250567A1 (en) | A process for reconstructing a spent dehydrogenation catalyst | |
| CN101147860A (zh) | 由甲醇制备二甲醚的催化剂 | |
| KR102223597B1 (ko) | 아세틸렌의 선택적 수소화용 촉매 및 이의 제조방법 | |
| KR101525943B1 (ko) | 디메틸에테르와 아세트산의 동시 제조용 불균일계 구리촉매 | |
| US11352307B2 (en) | Catalyst, device for manufacturing conjugated diene, and method for manufacturing conjugated diene | |
| Han et al. | Synthesis of C 2 oxygenates from syngas over UiO-66 supported Rh–Mn catalysts: the effect of functional groups | |
| CN116920924A (zh) | 载体组合物及其制备方法与应用 | |
| US7723258B2 (en) | Method and substance for reactive catalytic combustion | |
| KR101839568B1 (ko) | 금속 담지 촉매, 이의 제조방법 및 이를 이용한 탄소수 4의 올레핀 제조 방법 | |
| Kaneda et al. | Hydrogenation of Pyroglutamic Acid into Pyroglutaminol over Ni/SiO2 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WITN | Application deemed withdrawn, e.g. because no request for examination was filed or no examination fee was paid |