KR20100109909A - 신속하게 활성화되는 촉매 - Google Patents
신속하게 활성화되는 촉매 Download PDFInfo
- Publication number
- KR20100109909A KR20100109909A KR1020107013663A KR20107013663A KR20100109909A KR 20100109909 A KR20100109909 A KR 20100109909A KR 1020107013663 A KR1020107013663 A KR 1020107013663A KR 20107013663 A KR20107013663 A KR 20107013663A KR 20100109909 A KR20100109909 A KR 20100109909A
- Authority
- KR
- South Korea
- Prior art keywords
- silica support
- chromium
- aging
- alkali
- silica
- Prior art date
Links
- 239000003054 catalyst Substances 0.000 title claims abstract description 90
- 230000003213 activating effect Effects 0.000 title claims abstract description 12
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 claims abstract description 180
- 239000000377 silicon dioxide Substances 0.000 claims abstract description 97
- 229920000642 polymer Polymers 0.000 claims abstract description 67
- 239000003513 alkali Substances 0.000 claims abstract description 59
- 238000000034 method Methods 0.000 claims abstract description 54
- 230000032683 aging Effects 0.000 claims abstract description 48
- 239000011651 chromium Substances 0.000 claims abstract description 43
- 229910052804 chromium Inorganic materials 0.000 claims abstract description 33
- VYZAMTAEIAYCRO-UHFFFAOYSA-N Chromium Chemical compound [Cr] VYZAMTAEIAYCRO-UHFFFAOYSA-N 0.000 claims abstract description 29
- 230000004913 activation Effects 0.000 claims abstract description 28
- 239000000203 mixture Substances 0.000 claims abstract description 27
- 239000000463 material Substances 0.000 claims abstract description 21
- 239000000178 monomer Substances 0.000 claims abstract description 20
- 150000001336 alkenes Chemical class 0.000 claims abstract description 17
- 239000012670 alkaline solution Substances 0.000 claims abstract description 14
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 claims abstract description 13
- 239000000243 solution Substances 0.000 claims abstract description 11
- 239000002685 polymerization catalyst Substances 0.000 claims abstract description 10
- 238000006243 chemical reaction Methods 0.000 claims abstract description 8
- 238000010923 batch production Methods 0.000 claims abstract description 6
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 claims description 21
- -1 polyethylene Polymers 0.000 claims description 12
- 239000000155 melt Substances 0.000 claims description 10
- 238000010438 heat treatment Methods 0.000 claims description 6
- 238000002360 preparation method Methods 0.000 claims description 6
- 238000000071 blow moulding Methods 0.000 claims description 3
- 239000003960 organic solvent Substances 0.000 claims description 3
- 238000001694 spray drying Methods 0.000 claims description 2
- 239000004698 Polyethylene Substances 0.000 claims 2
- 229920000573 polyethylene Polymers 0.000 claims 2
- 238000011282 treatment Methods 0.000 abstract description 21
- 238000004519 manufacturing process Methods 0.000 abstract description 11
- 238000006116 polymerization reaction Methods 0.000 description 42
- 238000001994 activation Methods 0.000 description 29
- 239000000017 hydrogel Substances 0.000 description 25
- 150000001875 compounds Chemical class 0.000 description 15
- 239000007789 gas Substances 0.000 description 14
- 239000011148 porous material Substances 0.000 description 14
- 230000008569 process Effects 0.000 description 13
- 230000000694 effects Effects 0.000 description 12
- 239000000047 product Substances 0.000 description 12
- 230000002829 reductive effect Effects 0.000 description 11
- 239000003085 diluting agent Substances 0.000 description 9
- 230000014759 maintenance of location Effects 0.000 description 9
- 229920005989 resin Polymers 0.000 description 9
- 239000011347 resin Substances 0.000 description 9
- 239000012190 activator Substances 0.000 description 7
- BFGKITSFLPAWGI-UHFFFAOYSA-N chromium(3+) Chemical class [Cr+3] BFGKITSFLPAWGI-UHFFFAOYSA-N 0.000 description 7
- 239000007788 liquid Substances 0.000 description 7
- 239000012071 phase Substances 0.000 description 7
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 6
- JOPOVCBBYLSVDA-UHFFFAOYSA-N chromium(6+) Chemical compound [Cr+6] JOPOVCBBYLSVDA-UHFFFAOYSA-N 0.000 description 6
- 230000037048 polymerization activity Effects 0.000 description 6
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 6
- 239000002952 polymeric resin Substances 0.000 description 5
- 239000002002 slurry Substances 0.000 description 5
- 229920003002 synthetic resin Polymers 0.000 description 5
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 4
- 239000005977 Ethylene Substances 0.000 description 4
- 230000003197 catalytic effect Effects 0.000 description 4
- 238000001125 extrusion Methods 0.000 description 4
- 229930195733 hydrocarbon Natural products 0.000 description 4
- 150000002430 hydrocarbons Chemical class 0.000 description 4
- NNPPMTNAJDCUHE-UHFFFAOYSA-N isobutane Chemical compound CC(C)C NNPPMTNAJDCUHE-UHFFFAOYSA-N 0.000 description 4
- 239000003607 modifier Substances 0.000 description 4
- 239000002243 precursor Substances 0.000 description 4
- BDERNNFJNOPAEC-UHFFFAOYSA-N propan-1-ol Chemical compound CCCO BDERNNFJNOPAEC-UHFFFAOYSA-N 0.000 description 4
- 229910002028 silica xerogel Inorganic materials 0.000 description 4
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 3
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 3
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 3
- 239000002253 acid Substances 0.000 description 3
- 239000000654 additive Substances 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 230000015572 biosynthetic process Effects 0.000 description 3
- 239000003795 chemical substances by application Substances 0.000 description 3
- PHFQLYPOURZARY-UHFFFAOYSA-N chromium trinitrate Chemical class [Cr+3].[O-][N+]([O-])=O.[O-][N+]([O-])=O.[O-][N+]([O-])=O PHFQLYPOURZARY-UHFFFAOYSA-N 0.000 description 3
- GRWVQDDAKZFPFI-UHFFFAOYSA-H chromium(III) sulfate Chemical class [Cr+3].[Cr+3].[O-]S([O-])(=O)=O.[O-]S([O-])(=O)=O.[O-]S([O-])(=O)=O GRWVQDDAKZFPFI-UHFFFAOYSA-H 0.000 description 3
- 238000010924 continuous production Methods 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 238000012685 gas phase polymerization Methods 0.000 description 3
- 238000002844 melting Methods 0.000 description 3
- 230000008018 melting Effects 0.000 description 3
- 229910052757 nitrogen Inorganic materials 0.000 description 3
- 238000000926 separation method Methods 0.000 description 3
- 238000004904 shortening Methods 0.000 description 3
- 239000011949 solid catalyst Substances 0.000 description 3
- 230000003068 static effect Effects 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 238000012546 transfer Methods 0.000 description 3
- 239000004711 α-olefin Substances 0.000 description 3
- KWKAKUADMBZCLK-UHFFFAOYSA-N 1-octene Chemical compound CCCCCCC=C KWKAKUADMBZCLK-UHFFFAOYSA-N 0.000 description 2
- WSSSPWUEQFSQQG-UHFFFAOYSA-N 4-methyl-1-pentene Chemical compound CC(C)CC=C WSSSPWUEQFSQQG-UHFFFAOYSA-N 0.000 description 2
- XEEYBQQBJWHFJM-UHFFFAOYSA-N Iron Chemical compound [Fe] XEEYBQQBJWHFJM-UHFFFAOYSA-N 0.000 description 2
- CPLXHLVBOLITMK-UHFFFAOYSA-N Magnesium oxide Chemical compound [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 2
- OFBQJSOFQDEBGM-UHFFFAOYSA-N Pentane Chemical compound CCCCC OFBQJSOFQDEBGM-UHFFFAOYSA-N 0.000 description 2
- ATUOYWHBWRKTHZ-UHFFFAOYSA-N Propane Chemical compound CCC ATUOYWHBWRKTHZ-UHFFFAOYSA-N 0.000 description 2
- 239000004115 Sodium Silicate Substances 0.000 description 2
- 229910000831 Steel Inorganic materials 0.000 description 2
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 2
- MCMNRKCIXSYSNV-UHFFFAOYSA-N Zirconium dioxide Chemical compound O=[Zr]=O MCMNRKCIXSYSNV-UHFFFAOYSA-N 0.000 description 2
- 229910052910 alkali metal silicate Inorganic materials 0.000 description 2
- 239000003963 antioxidant agent Substances 0.000 description 2
- 239000007864 aqueous solution Substances 0.000 description 2
- 239000002585 base Substances 0.000 description 2
- 238000009835 boiling Methods 0.000 description 2
- BTANRVKWQNVYAZ-UHFFFAOYSA-N butan-2-ol Chemical compound CCC(C)O BTANRVKWQNVYAZ-UHFFFAOYSA-N 0.000 description 2
- 238000005266 casting Methods 0.000 description 2
- 150000001844 chromium Chemical class 0.000 description 2
- 150000001845 chromium compounds Chemical class 0.000 description 2
- 229910021563 chromium fluoride Inorganic materials 0.000 description 2
- QSWDMMVNRMROPK-UHFFFAOYSA-K chromium(3+) trichloride Chemical compound [Cl-].[Cl-].[Cl-].[Cr+3] QSWDMMVNRMROPK-UHFFFAOYSA-K 0.000 description 2
- SCCNXKACLAJZAP-UHFFFAOYSA-N chromium(3+);pyrrol-1-ide Chemical class [Cr+3].C=1C=C[N-]C=1.C=1C=C[N-]C=1.C=1C=C[N-]C=1 SCCNXKACLAJZAP-UHFFFAOYSA-N 0.000 description 2
- WYYQVWLEPYFFLP-UHFFFAOYSA-K chromium(3+);triacetate Chemical compound [Cr+3].CC([O-])=O.CC([O-])=O.CC([O-])=O WYYQVWLEPYFFLP-UHFFFAOYSA-K 0.000 description 2
- OXMLCJOPQGRRKV-UHFFFAOYSA-K chromium(3+);tribenzoate Chemical class [Cr+3].[O-]C(=O)C1=CC=CC=C1.[O-]C(=O)C1=CC=CC=C1.[O-]C(=O)C1=CC=CC=C1 OXMLCJOPQGRRKV-UHFFFAOYSA-K 0.000 description 2
- XVHFYNOGAFYRJV-UHFFFAOYSA-L chromium(ii) oxalate Chemical compound [Cr+2].[O-]C(=O)C([O-])=O XVHFYNOGAFYRJV-UHFFFAOYSA-L 0.000 description 2
- 239000003426 co-catalyst Substances 0.000 description 2
- 229920001577 copolymer Polymers 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 239000000835 fiber Substances 0.000 description 2
- 239000012530 fluid Substances 0.000 description 2
- 238000005243 fluidization Methods 0.000 description 2
- 238000010528 free radical solution polymerization reaction Methods 0.000 description 2
- ZSIAUFGUXNUGDI-UHFFFAOYSA-N hexan-1-ol Chemical compound CCCCCCO ZSIAUFGUXNUGDI-UHFFFAOYSA-N 0.000 description 2
- 229920001519 homopolymer Polymers 0.000 description 2
- 239000001257 hydrogen Substances 0.000 description 2
- 229910052739 hydrogen Inorganic materials 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 239000003999 initiator Substances 0.000 description 2
- 239000001282 iso-butane Substances 0.000 description 2
- PHTQWCKDNZKARW-UHFFFAOYSA-N isoamylol Chemical compound CC(C)CCO PHTQWCKDNZKARW-UHFFFAOYSA-N 0.000 description 2
- QWTDNUCVQCZILF-UHFFFAOYSA-N isopentane Chemical compound CCC(C)C QWTDNUCVQCZILF-UHFFFAOYSA-N 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 2
- CRSOQBOWXPBRES-UHFFFAOYSA-N neopentane Chemical compound CC(C)(C)C CRSOQBOWXPBRES-UHFFFAOYSA-N 0.000 description 2
- 239000002245 particle Substances 0.000 description 2
- JYVLIDXNZAXMDK-UHFFFAOYSA-N pentan-2-ol Chemical compound CCCC(C)O JYVLIDXNZAXMDK-UHFFFAOYSA-N 0.000 description 2
- 230000000704 physical effect Effects 0.000 description 2
- 229920005638 polyethylene monopolymer Polymers 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 239000002994 raw material Substances 0.000 description 2
- 238000011084 recovery Methods 0.000 description 2
- NTHWMYGWWRZVTN-UHFFFAOYSA-N sodium silicate Chemical compound [Na+].[Na+].[O-][Si]([O-])=O NTHWMYGWWRZVTN-UHFFFAOYSA-N 0.000 description 2
- 229910052911 sodium silicate Inorganic materials 0.000 description 2
- 230000006641 stabilisation Effects 0.000 description 2
- 238000011105 stabilization Methods 0.000 description 2
- 239000010959 steel Substances 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 238000012360 testing method Methods 0.000 description 2
- 238000003856 thermoforming Methods 0.000 description 2
- FTBATIJJKIIOTP-UHFFFAOYSA-K trifluorochromium Chemical compound F[Cr](F)F FTBATIJJKIIOTP-UHFFFAOYSA-K 0.000 description 2
- DURPTKYDGMDSBL-UHFFFAOYSA-N 1-butoxybutane Chemical compound CCCCOCCCC DURPTKYDGMDSBL-UHFFFAOYSA-N 0.000 description 1
- PAWQVTBBRAZDMG-UHFFFAOYSA-N 2-(3-bromo-2-fluorophenyl)acetic acid Chemical compound OC(=O)CC1=CC=CC(Br)=C1F PAWQVTBBRAZDMG-UHFFFAOYSA-N 0.000 description 1
- OBETXYAYXDNJHR-UHFFFAOYSA-N 2-Ethylhexanoic acid Chemical compound CCCCC(CC)C(O)=O OBETXYAYXDNJHR-UHFFFAOYSA-N 0.000 description 1
- YHQXBTXEYZIYOV-UHFFFAOYSA-N 3-methylbut-1-ene Chemical compound CC(C)C=C YHQXBTXEYZIYOV-UHFFFAOYSA-N 0.000 description 1
- OEOIWYCWCDBOPA-UHFFFAOYSA-N 6-methyl-heptanoic acid Chemical compound CC(C)CCCCC(O)=O OEOIWYCWCDBOPA-UHFFFAOYSA-N 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- 235000005039 Brassica rapa var. dichotoma Nutrition 0.000 description 1
- ZTQSAGDEMFDKMZ-UHFFFAOYSA-N Butyraldehyde Chemical compound CCCC=O ZTQSAGDEMFDKMZ-UHFFFAOYSA-N 0.000 description 1
- CYHOFESITORDDD-UHFFFAOYSA-M C(CCC)O[Cr](=O)(=O)O Chemical group C(CCC)O[Cr](=O)(=O)O CYHOFESITORDDD-UHFFFAOYSA-M 0.000 description 1
- 239000004215 Carbon black (E152) Substances 0.000 description 1
- 229910021555 Chromium Chloride Inorganic materials 0.000 description 1
- 229910021556 Chromium(III) chloride Inorganic materials 0.000 description 1
- 229920000089 Cyclic olefin copolymer Polymers 0.000 description 1
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 1
- NTIZESTWPVYFNL-UHFFFAOYSA-N Methyl isobutyl ketone Chemical compound CC(C)CC(C)=O NTIZESTWPVYFNL-UHFFFAOYSA-N 0.000 description 1
- UIHCLUNTQKBZGK-UHFFFAOYSA-N Methyl isobutyl ketone Natural products CCC(C)C(C)=O UIHCLUNTQKBZGK-UHFFFAOYSA-N 0.000 description 1
- 239000006057 Non-nutritive feed additive Substances 0.000 description 1
- BPQQTUXANYXVAA-UHFFFAOYSA-N Orthosilicate Chemical group [O-][Si]([O-])([O-])[O-] BPQQTUXANYXVAA-UHFFFAOYSA-N 0.000 description 1
- 235000002597 Solanum melongena Nutrition 0.000 description 1
- 244000061458 Solanum melongena Species 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 229910021536 Zeolite Inorganic materials 0.000 description 1
- RZMMIPFUKMHZFD-UHFFFAOYSA-N [Cr+3].CCCCCC(=O)OCC(Cl)Cl Chemical compound [Cr+3].CCCCCC(=O)OCC(Cl)Cl RZMMIPFUKMHZFD-UHFFFAOYSA-N 0.000 description 1
- QEIJLYPFVMNNQJ-UHFFFAOYSA-K [Cr+3].[O-][Cl](=O)=O.[O-][Cl](=O)=O.[O-][Cl](=O)=O Chemical compound [Cr+3].[O-][Cl](=O)=O.[O-][Cl](=O)=O.[O-][Cl](=O)=O QEIJLYPFVMNNQJ-UHFFFAOYSA-K 0.000 description 1
- 239000002250 absorbent Substances 0.000 description 1
- 230000002745 absorbent Effects 0.000 description 1
- WDNIVTZNAPEMHF-UHFFFAOYSA-N acetic acid;chromium Chemical compound [Cr].CC(O)=O.CC(O)=O WDNIVTZNAPEMHF-UHFFFAOYSA-N 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 230000029936 alkylation Effects 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 1
- ILRRQNADMUWWFW-UHFFFAOYSA-K aluminium phosphate Chemical compound O1[Al]2OP1(=O)O2 ILRRQNADMUWWFW-UHFFFAOYSA-K 0.000 description 1
- 239000000908 ammonium hydroxide Substances 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 238000000137 annealing Methods 0.000 description 1
- 239000002216 antistatic agent Substances 0.000 description 1
- 150000007514 bases Chemical class 0.000 description 1
- 238000005452 bending Methods 0.000 description 1
- HVURSIGIEONDKB-UHFFFAOYSA-N benzene;chromium Chemical compound [Cr].C1=CC=CC=C1.C1=CC=CC=C1 HVURSIGIEONDKB-UHFFFAOYSA-N 0.000 description 1
- 238000007664 blowing Methods 0.000 description 1
- 244000130745 brown sarson Species 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- OJRZMCPJFSNIJV-UHFFFAOYSA-L butanoate;chromium(2+) Chemical compound [Cr+2].CCCC([O-])=O.CCCC([O-])=O OJRZMCPJFSNIJV-UHFFFAOYSA-L 0.000 description 1
- CNIGXAJYMNFRCZ-UHFFFAOYSA-K butanoate;chromium(3+) Chemical compound [Cr+3].CCCC([O-])=O.CCCC([O-])=O.CCCC([O-])=O CNIGXAJYMNFRCZ-UHFFFAOYSA-K 0.000 description 1
- SHZIWNPUGXLXDT-UHFFFAOYSA-N caproic acid ethyl ester Natural products CCCCCC(=O)OCC SHZIWNPUGXLXDT-UHFFFAOYSA-N 0.000 description 1
- 125000004432 carbon atom Chemical group C* 0.000 description 1
- 239000000969 carrier Substances 0.000 description 1
- 238000006555 catalytic reaction Methods 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- CETPSERCERDGAM-UHFFFAOYSA-N ceric oxide Chemical compound O=[Ce]=O CETPSERCERDGAM-UHFFFAOYSA-N 0.000 description 1
- 229910000422 cerium(IV) oxide Inorganic materials 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 229940117975 chromium trioxide Drugs 0.000 description 1
- WGLPBDUCMAPZCE-UHFFFAOYSA-N chromium trioxide Inorganic materials O=[Cr](=O)=O WGLPBDUCMAPZCE-UHFFFAOYSA-N 0.000 description 1
- UZEDIBTVIIJELN-UHFFFAOYSA-N chromium(2+) Chemical class [Cr+2] UZEDIBTVIIJELN-UHFFFAOYSA-N 0.000 description 1
- HYTFNZKVQXUNQW-UHFFFAOYSA-L chromium(2+);2,2-dimethylpropanoate Chemical compound [Cr+2].CC(C)(C)C([O-])=O.CC(C)(C)C([O-])=O HYTFNZKVQXUNQW-UHFFFAOYSA-L 0.000 description 1
- MFBPBRIDLMRZJL-UHFFFAOYSA-L chromium(2+);2-ethylhexanoate Chemical compound [Cr+2].CCCCC(CC)C([O-])=O.CCCCC(CC)C([O-])=O MFBPBRIDLMRZJL-UHFFFAOYSA-L 0.000 description 1
- RZHZCSBNEIZYNZ-UHFFFAOYSA-L chromium(2+);dibenzoate Chemical compound [Cr+2].[O-]C(=O)C1=CC=CC=C1.[O-]C(=O)C1=CC=CC=C1 RZHZCSBNEIZYNZ-UHFFFAOYSA-L 0.000 description 1
- FFWNKDUCKICKKQ-UHFFFAOYSA-L chromium(2+);dodecanoate Chemical compound [Cr+2].CCCCCCCCCCCC([O-])=O.CCCCCCCCCCCC([O-])=O FFWNKDUCKICKKQ-UHFFFAOYSA-L 0.000 description 1
- KNRWTCHCJZVKSV-UHFFFAOYSA-L chromium(2+);octadecanoate Chemical compound [Cr+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O KNRWTCHCJZVKSV-UHFFFAOYSA-L 0.000 description 1
- MGNZTOJSOXWNCH-UHFFFAOYSA-N chromium(2+);pyrrol-1-ide Chemical compound [Cr+2].C=1C=C[N-]C=1.C=1C=C[N-]C=1 MGNZTOJSOXWNCH-UHFFFAOYSA-N 0.000 description 1
- GOCJWSXBGBQVSO-UHFFFAOYSA-K chromium(3+);2,2-dimethylpropanoate Chemical compound [Cr+3].CC(C)(C)C([O-])=O.CC(C)(C)C([O-])=O.CC(C)(C)C([O-])=O GOCJWSXBGBQVSO-UHFFFAOYSA-K 0.000 description 1
- NMXUZAZJTJAHGK-UHFFFAOYSA-K chromium(3+);dodecanoate Chemical compound [Cr+3].CCCCCCCCCCCC([O-])=O.CCCCCCCCCCCC([O-])=O.CCCCCCCCCCCC([O-])=O NMXUZAZJTJAHGK-UHFFFAOYSA-K 0.000 description 1
- PPUZYFWVBLIDMP-UHFFFAOYSA-K chromium(3+);triiodide Chemical compound I[Cr](I)I PPUZYFWVBLIDMP-UHFFFAOYSA-K 0.000 description 1
- ZKJMJQVGBCLHFL-UHFFFAOYSA-K chromium(3+);triperchlorate Chemical compound [Cr+3].[O-]Cl(=O)(=O)=O.[O-]Cl(=O)(=O)=O.[O-]Cl(=O)(=O)=O ZKJMJQVGBCLHFL-UHFFFAOYSA-K 0.000 description 1
- GAMDZJFZMJECOS-UHFFFAOYSA-N chromium(6+);oxygen(2-) Chemical compound [O-2].[O-2].[O-2].[Cr+6] GAMDZJFZMJECOS-UHFFFAOYSA-N 0.000 description 1
- 239000011636 chromium(III) chloride Substances 0.000 description 1
- 235000007831 chromium(III) chloride Nutrition 0.000 description 1
- 229910000356 chromium(III) sulfate Inorganic materials 0.000 description 1
- 239000011696 chromium(III) sulphate Substances 0.000 description 1
- 235000015217 chromium(III) sulphate Nutrition 0.000 description 1
- XZQOHYZUWTWZBL-UHFFFAOYSA-L chromium(ii) bromide Chemical compound [Cr+2].[Br-].[Br-] XZQOHYZUWTWZBL-UHFFFAOYSA-L 0.000 description 1
- MJSNUBOCVAKFIJ-LNTINUHCSA-N chromium;(z)-4-oxoniumylidenepent-2-en-2-olate Chemical compound [Cr].C\C(O)=C\C(C)=O.C\C(O)=C\C(C)=O.C\C(O)=C\C(C)=O MJSNUBOCVAKFIJ-LNTINUHCSA-N 0.000 description 1
- AWNBGWWVMCBBST-UHFFFAOYSA-N chromium;cumene Chemical compound [Cr].CC(C)C1=CC=CC=C1.CC(C)C1=CC=CC=C1 AWNBGWWVMCBBST-UHFFFAOYSA-N 0.000 description 1
- 239000004927 clay Substances 0.000 description 1
- 229910052570 clay Inorganic materials 0.000 description 1
- 238000000975 co-precipitation Methods 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 238000004891 communication Methods 0.000 description 1
- 238000000748 compression moulding Methods 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000010586 diagram Methods 0.000 description 1
- AFABGHUZZDYHJO-UHFFFAOYSA-N dimethyl butane Natural products CCCC(C)C AFABGHUZZDYHJO-UHFFFAOYSA-N 0.000 description 1
- HNPSIPDUKPIQMN-UHFFFAOYSA-N dioxosilane;oxo(oxoalumanyloxy)alumane Chemical compound O=[Si]=O.O=[Al]O[Al]=O HNPSIPDUKPIQMN-UHFFFAOYSA-N 0.000 description 1
- 239000002612 dispersion medium Substances 0.000 description 1
- 238000005315 distribution function Methods 0.000 description 1
- 239000003623 enhancer Substances 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 238000011049 filling Methods 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 239000003063 flame retardant Substances 0.000 description 1
- 238000001595 flow curve Methods 0.000 description 1
- 229920001973 fluoroelastomer Polymers 0.000 description 1
- 238000005194 fractionation Methods 0.000 description 1
- 239000002828 fuel tank Substances 0.000 description 1
- 239000000499 gel Substances 0.000 description 1
- 230000009477 glass transition Effects 0.000 description 1
- 229920001903 high density polyethylene Polymers 0.000 description 1
- 239000004700 high-density polyethylene Substances 0.000 description 1
- 150000002431 hydrogen Chemical class 0.000 description 1
- XLYOFNOQVPJJNP-UHFFFAOYSA-M hydroxide Chemical compound [OH-] XLYOFNOQVPJJNP-UHFFFAOYSA-M 0.000 description 1
- 238000005470 impregnation Methods 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 238000001746 injection moulding Methods 0.000 description 1
- 229910052809 inorganic oxide Inorganic materials 0.000 description 1
- 229910052742 iron Inorganic materials 0.000 description 1
- JMMWKPVZQRWMSS-UHFFFAOYSA-N isopropanol acetate Natural products CC(C)OC(C)=O JMMWKPVZQRWMSS-UHFFFAOYSA-N 0.000 description 1
- 229940011051 isopropyl acetate Drugs 0.000 description 1
- GWYFCOCPABKNJV-UHFFFAOYSA-M isovalerate Chemical compound CC(C)CC([O-])=O GWYFCOCPABKNJV-UHFFFAOYSA-M 0.000 description 1
- 239000011344 liquid material Substances 0.000 description 1
- 239000007791 liquid phase Substances 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000000395 magnesium oxide Substances 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 238000005259 measurement Methods 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 150000005673 monoalkenes Chemical class 0.000 description 1
- 238000000465 moulding Methods 0.000 description 1
- TVMXDCGIABBOFY-UHFFFAOYSA-N n-Octanol Natural products CCCCCCCC TVMXDCGIABBOFY-UHFFFAOYSA-N 0.000 description 1
- IJDNQMDRQITEOD-UHFFFAOYSA-N n-butane Chemical compound CCCC IJDNQMDRQITEOD-UHFFFAOYSA-N 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 230000036961 partial effect Effects 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 231100000614 poison Toxicity 0.000 description 1
- 238000004184 polymer manufacturing process Methods 0.000 description 1
- 230000000379 polymerizing effect Effects 0.000 description 1
- 229920000098 polyolefin Polymers 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000004886 process control Methods 0.000 description 1
- 239000001294 propane Substances 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 239000012429 reaction media Substances 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 230000000630 rising effect Effects 0.000 description 1
- 238000001175 rotational moulding Methods 0.000 description 1
- 239000012748 slip agent Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 230000035882 stress Effects 0.000 description 1
- 239000013589 supplement Substances 0.000 description 1
- 239000000725 suspension Substances 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 238000007725 thermal activation Methods 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 231100000816 toxic dose Toxicity 0.000 description 1
- 239000003440 toxic substance Substances 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 125000005208 trialkylammonium group Chemical group 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 239000012808 vapor phase Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000001993 wax Substances 0.000 description 1
- 238000004260 weight control Methods 0.000 description 1
- 239000010457 zeolite Substances 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F10/00—Homopolymers and copolymers of unsaturated aliphatic hydrocarbons having only one carbon-to-carbon double bond
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J21/00—Catalysts comprising the elements, oxides, or hydroxides of magnesium, boron, aluminium, carbon, silicon, titanium, zirconium, or hafnium
- B01J21/06—Silicon, titanium, zirconium or hafnium; Oxides or hydroxides thereof
- B01J21/08—Silica
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J23/00—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00
- B01J23/16—Catalysts comprising metals or metal oxides or hydroxides, not provided for in group B01J21/00 of arsenic, antimony, bismuth, vanadium, niobium, tantalum, polonium, chromium, molybdenum, tungsten, manganese, technetium or rhenium
- B01J23/24—Chromium, molybdenum or tungsten
- B01J23/26—Chromium
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/02—Impregnation, coating or precipitation
- B01J37/0201—Impregnation
- B01J37/0207—Pretreatment of the support
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/02—Impregnation, coating or precipitation
- B01J37/03—Precipitation; Co-precipitation
- B01J37/036—Precipitation; Co-precipitation to form a gel or a cogel
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J37/00—Processes, in general, for preparing catalysts; Processes, in general, for activation of catalysts
- B01J37/06—Washing
-
- B01J35/615—
-
- B01J35/638—
-
- B01J35/647—
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F110/00—Homopolymers of unsaturated aliphatic hydrocarbons having only one carbon-to-carbon double bond
- C08F110/02—Ethene
Abstract
알칼리 노화 실리카 지지체를 제조하기 위하여 알칼리 용액에서 실리카 지지체를 노화하고, 건조 실리카 지지체를 제조하기 위해 알칼리 노화 실리카 지지체로부터 알칼리 수용액의 최소 일부를 제거하고, 촉매 조성물을 제조하기 위해 실리카 지지체를 활성화하는 것을 포함하는 촉매 제조방법이 개시되고, 여기에서 알칼리 노화 처리는 최초 값의 약 50%이하로 실리카 지지체의 표면적을 낮추고 실리카 지지체의 활성화는 약 8 시간 이내에서 약 500 lb 이상으로 배치 공정에서 수행될 수 있다. 실리카 지지체 재료를 알칼리 노화하고, 크롬-실리카 지지체 형성하기 위하여 알칼리 노화 이전, 이후 또는 양자 동안 실리카 지지체 재료에 크롬을 추가하고, 활성 올레핀 중합촉매를 제조하기 위하여 크롬-실리카 지지체를 신속하게 활성화시키고, 폴리머 제조에 적절한 조건 하에 반응 구역에서 활성 올레핀 중합촉매를 최소한 하나의 단량체와 접촉시키고, 및 폴리머를 회수하는 것을 포함하는 폴리머 제조방법이 개시된다.
Description
본 개시는 일반적으로 크롬 및 지지체로 구성되는 촉매 및 이의 제조 및 활성화 방법에 관한 것이다.
크롬 지지 촉매는 올레핀 폴리머 중합에 사용된다. 촉매 제조업자는 실리카 또는 실리카-티타니아와 같은 지지체에 크롬을 배치하여 이러한 촉매를 제조한다. 지지체는 크롬의 활성을 안정화시키고, 이로 인하여 촉매는 구매자에게 불활성 형태로 전달될 수 있다. 일단 촉매가 폴리머 제조업자에게 도착되면, 중합 공정에 사용하기 위하여 활성화된다. 이러한 촉매의 활성 과정에서 통상 장시간 고온에서 비활성 조성물을 열적으로 처리하기 위하여 사용되는 대규모의 고가 장비가 사용된다.
폴리머 제조업자의 생산 용량은 여러 요인들에 의해 제한되며, 그 하나가 촉매의 활성에 요구되는 시간이다. 촉매의 촉매 활성에 필요한 시간 및/또는 한번에 활성화될 수 있는 촉매 함량을 개선하면 전체적 폴리머 제조 공정 효율을 개선할 수 있다. 따라서, 개선된 촉매 활성화 처리 방법을 개발할 필요가 있다.
알칼리 노화 실리카 지지체를 제조하기 위하여 알칼리 용액에서 실리카 지지체를 노화하고, 건조 실리카 지지체를 제조하기 위해 알칼리 노화 실리카 지지체로부터 알칼리 수용액의 최소 일부를 제거하고, 촉매 조성물을 제조하기 위해 실리카 지지체를 활성화하는 것을 포함하는 촉매 제조방법이 본원에서 개시되고, 여기에서 알칼리 노화 처리는 최초 값의 약 50%이하로 실리카 지지체의 표면적을 낮추고 실리카 지지체의 활성화는 약 8 시간 이내에서 약 500 lb 이상으로 배치 공정에서 수행될 수 있다.
실리카 지지체 재료를 알칼리 노화하고, 크롬-실리카 지지체 형성하기 위하여 알칼리 노화 이전, 이후 또는 양자 동안 실리카 지지체 재료에 크롬을 추가하고, 활성 올레핀 중합촉매를 제조하기 위하여 크롬-실리카 지지체를 신속하게 활성화시키고, 폴리머 제조에 적절한 조건 하에 반응 구역에서 활성 올레핀 중합촉매를 최소한 하나의 단량체와 접촉시키고, 및 폴리머를 회수하는 것을 포함하는 폴리머 제조방법이 또한 개시된다.
또한, 실리카 지지체 재료를 알칼리 노화하고, 크롬-실리카 지지체 형성하기 위하여 알칼리 노화 이전, 이후 또는 양자 동안 실리카 지지체 재료에 크롬을 추가하고, 활성 올레핀 중합촉매를 제조하기 위하여 크롬-실리카 지지체를 신속하게 활성화시키는 것을 포함하는 폴리머 제조방법이 또한 개시되고, 여기에서 크롬-실리카 지지체를 신속하게 활성화시키는 것은 약 8 시간 이내에 약 700℃ 이상의 온도로 가열시키는 것을 포함한다.
또한, 지지된 크롬 조성물을 제공하고, 융합되는(fused) 지지된 크롬 조성물을 제조하기 위하여 지지체 재료를 화학적으로 융합시키고, 활성 올레핀 중합 촉매를 제조하기 위하여 신속하게 전구체 촉매 조성물을 활성화하는 것을 포함하는 촉매 제조방법이 개시된다.
또한, 알칼리 노화 실리카 하이드로겔을 제조하기 위한 알칼리 수용액에서 실리카 하이드로겔을 노화하고, 실리카 크세로겔을 제조하기 위해 알칼리 노화 실리카 하이드로겔에서 알칼리 수용액의 최소 일부를 제거하고, 촉매 조성물을 생산하기 위해 실리카 크세로겔을 활성화하는 것을 포함하는 촉매 제조 방법이 개시되고, 여기에서 촉매 조성물이 약 300 ㎡/g이하의 표면적을 가지고 실리카 크세로겔의 활성화는 약 8 시간 이내에서 약 500 lb 이상으로 배치 공정에서 수행될 수 있다.
본 개시의 더욱 완전한 이해를 위하여, 첨부 도면에 간단한 설명 및 이하 상세한 설명이 기재되며, 동일 부호는 동일 부분을 표시한다.
도 1은 촉매 제조방법 흐름도이다.
도 2는 실시예 1에서 얻어진 샘플들의 다양한 촉매 함량에 대한 생산성 대 용융지수 그래프이다.
도 3은 실시예 1에서 얻어진 샘플들의 다양한 촉매 함량에 대한 용융지수 대 HLMI/MI 그래프이다.
도 4는 실시예 2에서 얻어진 샘플들의 다양한 촉매 함량에 대한 생산성 대 용융지수 그래프이다.
도 5는 실시예 2에서 얻어진 샘플들의 다양한 촉매 함량에 대한 용융지수 대 HLMI/MI 비율 그래프이다.
도 1은 촉매 제조방법 흐름도이다.
도 2는 실시예 1에서 얻어진 샘플들의 다양한 촉매 함량에 대한 생산성 대 용융지수 그래프이다.
도 3은 실시예 1에서 얻어진 샘플들의 다양한 촉매 함량에 대한 용융지수 대 HLMI/MI 그래프이다.
도 4는 실시예 2에서 얻어진 샘플들의 다양한 촉매 함량에 대한 생산성 대 용융지수 그래프이다.
도 5는 실시예 2에서 얻어진 샘플들의 다양한 촉매 함량에 대한 용융지수 대 HLMI/MI 비율 그래프이다.
하나 이상의 예시적 실시예가 제공될지라도, 본 개시 시스템 및/또는 방법은 현재 공지되거나 존재하는 여러 기술로 구현될 수 있다는 것을 이해하여야 한다. 본 개시는 하기 예시적 설계 및 실시예를 포함하여 기술된 실시예, 도면 및 기술들에 제한되지 않으며 균등한 모든 범위뿐 아니라 첨부된 청구항의 범위로 변형될 수 있다.
본원에서, 알칼리 노화 실리카 지지체를 제조하기 위하여 알칼리 용액에서 실리카 지지체를 노화하고, 건조 실리카 지지체를 제조하기 위해 알칼리 노화 실리카 지지체로부터 알칼리 수용액의 최소 일부를 제거하고, 촉매 조성물을 제조하기 위해 실리카 지지체를 활성화하는 것을 포함하는 촉매 제조방법이 개시된다. 알칼리 처리 없이 제조된 조성물과 비교할 때 상기 실리카 지지체의 활성화 공정은 단축된 시간 동안 수행될 수 있다. 이하, 본원에서 기술되는 방법론에 의해 제조되고 연속적으로 활성화되는 촉매 조성물은 신속하게 활성화된 촉매 조성물 (RACC)로서 언급된다. 다양한 촉매 성분 및 제조 및 활성화 방법들이 더욱 상세히 기술된다.
실시예에서, RACC는 지지체를 포함한다. 지지체는 실리카, 또는 실리카-티타니아와 같은 무기산화물일 수 있다. 지지체는 RACC에 악영향을 미치지 않는 다른 성분을 더욱 포함할 수 있고, 예를들면 알루미나, 인산알루미늄, 보리아, 마그네샤, 토리아, 지르코니아, 세리아, 점토, 제올라이트 또는 이들의 조합을 포함할 수 있다.
실시예에서, 지지체는 실리카를 포함한다. 실리카 지지체는 임의의 적절한 수단을 사용하여 제조될 수 있고, 예를들면 알칼리 금속 실리케이트 수용액 및 산을 접촉시켜 실리카 하이드로겔을 형성하여 실리카 지지체를 제조할 수 있다
선택적 실시예에 있어서, 지지체는 실리카 티타니아를 포함한다. 실리카-티타니아 지지체는 실리카 및 TiCl3 또는 TiCl4와 같은 티타늄-함유 화합물의 공동 겔화, 불균질 공침, 및 표면 함침과 같은 임의의 적절한 방법을 사용하여 제조될 수 있다. 실시예에서, 실리카-티타니아 지지체는 약 250 ㎡/g내지 약 600 ㎡/g 표면적 및 약 1.0 cc/g 내지 약 3.0 cc/g 기공 부피를 가질 수 있다.
지지체 (즉, 실리카 또는 실리카 티타니아)는 RACC 전체 중량에 약 90 퍼센트 (%)의 이상, 선택적으로 약 95% 이상, 선택적으로 약 98% 이상 존재할 수 있다.
실시예에서, RACC는 크롬을 포함하며, 이는 크롬-함유 화합물 및 지지체와의 접촉을 통하여 RACC에 도입된다. 크롬-함유 화합물은 6가 산화 상태 (이하 크롬(VI) )인 크롬을 포함하거나 크롬(VI)로 변환될 수 있는 재료를 포함하는 하나 이상의 화합물일 수 있다. 실시예에서, 크롬-함유 화합물은 수용성 크롬 화합물을 포함한다; 선택적으로 크롬-함유 화합물은 탄화수소 가용성 크롬 화합물을 포함한다. 크롬-함유 화합물은 크롬 (II) 화합물, 크롬 (III) 화합물, 또는 이들의 조합 일 수 있다. 적절한 크롬 (III) 화합물은 크롬 카르복실레이트, 크롬 나프테네이트, 크롬 할로겐화물, 크롬 피롤라이드, 크롬 벤조에이트, 크롬 디오네이트, 크롬 질산염, 크롬 황산염, 또는 이들의 조합을 포함하지만 여기에 한정되지는 않는다. 특정한 크롬 (III) 화합물은 크롬 (III) 아이소옥탄산염, 크롬 (III) 2,2,6,6-테트라메틸헵탄디오네이트, 크롬 (III) 나프테네이트, 크롬 (III) 클로라이드, 크롬 (III) 트리스(2-에틸헥사노에이트), 크롬 플루오라이드, 크롬 (III) 옥시-2-에틸헥사노에이트, 크롬 (III) 디클로로에틸헥사노에이트, 크롬 (III) 아세틸아세토네이트, 크롬 (III) 아세테이트, 크롬 (III) 부티레이트, 크롬 (III) 네오펜타노에이트, 크롬 (III) 라우레이트, 크롬 (III) 설페이트, 크롬 (III) 옥살레이트, 크롬 (III) 벤조에이트, 크롬 (III) 피롤라이드(들), 크롬 (III) 퍼클로레이트, 크롬 (III) 클로레이트, 또는 이들의 조합을 포함하지만 여기에 한정되지는 않는다. 적절한 크롬 (II) 화합물은 불화 제 1 크롬, 염화 제 1 크롬, 크롬 브롬화물, 크롬 요오드화물, 크롬 (II) 비스(2-에틸헥사노에이트), 크롬 (II) 아세테이트, 크롬 (II) 부티레이트, 크롬 (II) 네오펜타노에이트, 크롬 (II) 라우레이트, 크롬 (II) 스테아르산염, 크롬 (II) 옥살레이트, 크롬 (II) 벤조에이트, 크롬 (II) 피롤라이드(들), 크롬 설페이트, 또는 이들의 조합을 포함하지만 여기에 한정되지는 않는다. 다른 적절한 크롬-함유 화합물로는 액상 탄화수소에 녹은 삼차 부틸 크로메이트를 포함한다; 물에 녹은 크롬 삼산화물; 물에 녹은 크롬 아세테이트 ; 알코올 녹은 크롬 질산염; 파이 결합 크롬 복합체, 예를들면, 디쿠멘 크롬 및 다이벤젠 크롬과 같은 0가 크롬유기화합물; 또는 이들의 조합을 포함한다. 파이 결합된 크롬 복합체는 미국 특허 번호 3,976,632에서 기술되며, 본원에서 전체가 참고에 포함된다.
크롬은 RACC 최종 중량에 약 0.1% 내지 약 10%, 선택적으로 약 0.2% 내지 약 2%, 또는 약 1%함량으로 RACC에서 존재할 수 있다.
본원에 개시된 RACC제조 방법 100의 실시예는 도 1에서 기술된다. 도 1을 참고하면, 실시예에서, 방법 100은 하이드로겔을 형성하는 블록 110으로 개시된다. 하이드로겔은 물에서 녹지 않는 실리케이트 사슬망이고, 물이 분산 매질인 교질상 겔이다. 실시예에서, 하이드로겔은 지지체 재료 (즉, 실리카 또는 실리카-티타니아)로 구성된다. 이하에, 단순성을 위해, 실리카 하이드로겔 적용에 초점을 맞출 것일지라도 본원에서 기술된 다른 유형의 하이드로겔( 즉, 실리카-티타니아)도 예상될 수 있다.
실시예에서, 하이드로겔은 실리카로 구성된다. 실리카 하이드로겔은 황산과 같은 산과 규산 나트륨과 같은 알칼리 금속 실리케이트를 접촉시킴으로써 형성될 수 있다. 접촉은 예를들면 혼합 또는 교반과 같은 적절한 조건 하에 실시될 수 있다. 실리카 하이드로겔은 실리카 하이드로겔의 알칼리 금속 함량을 감소시키기 위하여 물로 및/또는 암모늄 염 (즉, 질산 암모늄 등) 또는 희석산과 같은 임의의 적절한 화합물로 더욱 세척될 수 있다. 세척은 바람직한 결과까지 달성될 때까지 수회 수행될 수 있다.
이후 블록 120에서 실리카 하이드로겔은, 약 8 내지 약 13의 pH, 선택적으로 약 9 내지 약 12의 pH, 선택적으로 약 9내지 약 10의 pH를 가지는 하나 이상의 염기성 화합물 (즉, 염기, 버퍼)을 포함한 알칼리 용액과, 약 60℃ 내지 약 90℃, 또는 70℃ 내지 약 85℃, 또는 약 80℃에서 접촉될 수 있다. 본원에 기술된 조건으로 알칼리 용액에 노출시켜 실리카 하이드로겔을 처리하는 것을 알칼리 노화라고 언급된다. 알칼리 용액은 개시된 범위의 pH를 제공하고 조성물 다른 성분과 양립될 수 있는 임의의 성분을 포함될 수 있다. 예를들면, 알칼리 용액은 수산화암모늄, 수산화칼륨, 수산화나트륨, 트리알킬암모늄 수산화물, 규산나트륨 및 기타 등등을 포함할 수 있다. 개시된 pH 범위의 용액을 제공하기에 유효한 다른 적절한 함량의 적절한 화합물이 적용될 수 있다.
실리카 하이드로겔의 알칼리 노화 처리는 알칼리 노화 처리되지 않은 재료의 초기 표면적 대비 약 50%이하, 선택적으로 약 45%이하, 선택적으로 약 40%이하, 선택적으로 약 35%이하로 실리카 지지체의 표면적을 낮추기에 충분한 시간 동안 실시될 수 있다. 베이스 실리카 또는 크롬/실리카의 표면적을 결정하기 위해, 크세로겔은 우선 200-400℃로 건조되어 흡착된 성분을 제거한다. 예를들면 지지체는, (알칼리 노화되지 않은) 순수 상태에서 건조되면, 약 600 ㎡/g의 표면적의 실리카 지지체를 포함할 수 있다. 그러나, 알칼리 노화 처리되면 지지체의 표면적은 약 300 ㎡/g 이하로, 선택적으로 약 280 ㎡/g이하로, 선택적으로 약 250 ㎡/g이하로, 선택적으로 약 225 ㎡/g이하로 감소시킬 수 있다. 실시예에서, 알칼리성 노화는 약 1 시간 내지 약 24 시간, 또는 약 2 시간 내지 약 10 시간으로, 또는 약 3 시간 내지 약 6 시간 동안 실시된다.
실리카 하이드로겔 및 알칼리 수용액을 포함하는 조성물은, 블록 130에서 모든 또는 일부의 수용액을 제거하기 위해 더 처리될 수 있다. 예를들면, 조성물은 열 처리, 분무 건조와 같은 표준 기법을 사용하거나, 휘발성 액체 유기 용매와 접촉하여 건조될 수 있다. 휘발성 액체 유기 용매로는 제한되지는 않지만 메틸 이소부틸케톤, 에틸 아세테이트, sec-부틸 알코올, n-프로필 알코올, 부틸알데히드, 디부틸 에테르, 이소프로필 아세테이트, 3-메틸-1-부탄올, 1-펜타놀, 2-펜타놀, 1-헥사놀 또는 이들의 조합을 포함한다. 실리카를 건조하면 실리카 하이드로겔을 실리카 크세로겔로 변환시킬 수 있고, 생성된 알칼리-노화(alkaline-aged), 건조 실리카 재료는 이하 전구체 촉매 조성물 (PCC)로 언급된다. 블록 140에서 PCC는 RACC를 형성하기 위해 활성화될 수 있다. 전구체 조성물의 활성은 이후 본원에 기술된 것처럼 수행될 수 있다.
크롬은 합성 공정 동안 임의 시간에 전구체 촉매 조성물 (즉, 실리카 지지체, 실리카-티타니아 지지체)에 추가될 수 있다. 실시예에서, 실리카 지지체 (즉, 하이드로겔 및/또는 크세로겔)은, 알칼리 노화 전, 동안, 후에 크롬 함유하는 화합물과 더욱 접촉된다. 실시예에서, 실리카 하이드로겔 및/또는 크세로겔은 알칼리 노화 처리 전에 크롬 함유된 화합물과 접촉된다 ; 선택적으로 알칼리 노화 처리된 실리카 하이드로겔 및/또는 크세로겔은 알칼리 노화 이후 본원에서 이미 기술된 유형의 크롬-함유된 화합물과 접촉될 수 있다 ; 또는 이들의 조합에 의해 접촉될 수 있다. Cr-실리카 재료 또는 지지체는 실리카-함유 지지체 및 크롬-함유된 화합물과의 접촉에 의해 형성된다. 실시예에서, Cr-실리카 하이드로겔은 알칼리 노화되고 실리카-Cr 크세로겔로 변환된다.
실시예에서, PCC는 활성화되어 활성 촉매, 선택적으로 활성 중합 촉매가 형성된다. 본 개시에서 PCC는 여러 유형의 활성화 장비를 사용하여 활성화될 수 있다. 임의의 용기 또는 장치가 PCC를 활성화하기 위해 이용될 수 있으며, 예로는 회전식 하소기, 정적 팬 건조기 또는 유동상을 포함한다. 이와 같은 장비는 정적, 배치 또는 연속 모드에서 수행할 수 있다. 정적 또는 배치 모드에서, 촉매 베드를 포함하는 용기 또는 장치는 활성화 공정의 다양한 단계를 연속적으로 거친다. 연속 모드에서, 공정 단계들은, PCC가 활성화 장치를 통하여 진행되는 일련의 구역에서 수행된다.
실시예에서, PCC는 유동상 활성화기에서 활성화된다. 유동상 활성화기에서, PCC가 배치된 많은 작은 홀을 포함한 그리드 판을 통하여 가스가 상향으로 유동될 수 있다. 가스는 원하는 공정 조건을 형성하기 위한 다양한 화합물을 포함할 수 있다. 가스가 유동될 때 PCC는 가스와 혼합되어 유체-유사 흐름을 생성한다. 이것은 때로 유동화 또는 유체화라고 언급된다.
활성화 공정은 하나 이상의 단계에서 바람직한 온도로 PCC를 가열시키는 것을 더욱 포함할 수 있다. 본원에서 사용되는 용어 "단계:는 바람직한 온도로 PCC를 가열시키고 일정 시간 온도를 유지하는 것을 언급한다. 단계는 PCC가 고정 위치에 있을 때 또는 다양한 위치로 PCC를 이동시킴으로써 수행될 수 있고, 바람직한 온도로의 대기시간 (ramp up time) 및 소정의 보유시간 동안 그 온도에서 PCC를 보유하는 것을 포함한다. 2 이상 단계에서, 2 이상의 대기시간, 2 이상의 바람직한 온도, 및 2 이상의 보유시간이 있을 수 있다. 대기시간이 똑같거나 다른 것일 수 있고, 예를들면 대기시간은 약 3 시간 이하로 순간적일 수 있다 (즉, 예열된 환경).
본원에 기술된 유형의 PCC에 대한 상업적 활성화는 전형적으로 상업적 배치라 불리는 큰 용량의 이들 재료 (100 내지 1500 파운드)를 적용하고, 상승 온도 (즉, 800℃)로 이러한 재료를 오랜 시간에 걸쳐 서서히 가열하는 것이 필요하다. 실시예에서, 알칼리 노화 공정은 상업적 촉매 제조 설비에서 상업적 촉매 제조업자에 의해 실시되고, 촉매는 운반되고, 활성화 공정은 상업적 중합 공정 장치에서 상업적 폴리머 생산자에 의해 실시된다. 실시예에서, PCC는 각각의 배치가 약 500 lb 이상, 선택적으로 약 750 lb 이상, 선택적으로 약 1000 lb 이상, 선택적으로 약 1250 lb 이상을 포함하는 상업적 배치에서 활성화된다. PCC 활성화 온도(들)는 사용자가 원하는 결과를 달성하기 위해 조절될 수 있다. 예를들면, 온도(들)은 400℃ 내지 약 1000℃, 선택적으로 600℃ 내지 약 900℃, 선택적으로 750℃ 내지 약 900℃ 범위일 수 있다. 본원에서 기술된 바와 같은 PCC 활성은 본원에 기술된 처리가 없는 유사한 조성물과 비교하여 짧은 시간에 신속하게 수행될 수 있다. 실시예에서, PCC는 최고 온도에서 약 8 시간 이하, 선택적으로 약 7 시간 이하, 선택적으로 약 6 시간 이하, 선택적으로 약 5 시간 이하, 선택적으로 약 4 시간 이하, 선택적으로 약 3 시간 이하, 선택적으로 약 2 시간 이하, 선택적으로 약 1 시간 이하에서 활성화될 수 있다. 2 이상 단계가 적용되면, 총 보유시간은 최고 온도에 있는 모든 단계에서의 보유시간의 합이다. 열적 활성화는 미국 특허 번호 4,022,580 및 2005년 11월 17일에 공개된 미국 특허 공개 번호 2005/0255987 A1에서 기술되고 이들 각각은 본원에서 전체가 참조로서 포함된다.
이론에 의해 구속되지 않고, PCC 활성화 결과 지지체 재료의 탈수산화 및 어닐링이 동반되어 더 표면적을 낮출 수 있다. 그러므로, 알칼리 노화 단계가 개선되고 적당히 조절되면, 장시간 고온 활성화와 동일한 이익을 달성할 수 있다. 그러므로, 개선된 알칼리 노화처리는 활성화 시간을 줄이고, 활성화 효율을 높이고 장비 생산성을 더 높일 수 있다.
활성화는 또한 크롬 (Cr(III))의 임의 3가 형태를 6가 형태 (크롬(VI))로 산화시키고 Cr(VI) 형태를 안정화시킬 수 있다. 본원에서 사용되는 용어 "안정화"는 촉매의 Cr(VI) 형태에 이르는 활성 공정을 언급한다. 활성 공정은 Cr(III)의 약 10 내지 약 100%, 또는 약 30내지 약 80%, 또는 약 35내지 약 65%를 Cr(VI)로 변환시키고, 약 0.1 내지 약 1%, 약 0.2에서 약 0.9%, 또는 약 0.3에서 약 0.65% 크롬(VI)을 수득할 수 있다.
실시예에서, 본원에 기술된 유형의 RACC는 알칼리 처리가 없이 제조된 유사한 촉매와 비교할 때 표면적이 감소되고 기공 직경이 커진다. 몇몇 실시예에서, 본원에 기술된 유형의 RACC는 알칼리 처리가 없이 제조된 유사한 촉매와 비교할 때 기공 부피가 커진다. 예를들면, RACC의 표면적은 그램당 약 100 평방미터 (㎡/g) 내지 약 600 ㎡/g, 또는 약 200 ㎡/g 내지 약 400 ㎡/g, 또는 약 250 ㎡/g 내지 약 350 ㎡/g범위일 수 있다. 또 다른 실시예에서, RACC의 기공 직경은 약 50 옴스트롱(Å) 내지 약 400 Å+ 또는 약 100 Å 내지 약 350 Å 또는 약 200 Å 내지 약 300 Å범위일 수 있다. 또 다른 실시예에서, RACC의 기공 부피는 그램 당 약 1 세제곱 센티미터(cc/g) 내지 약 3, cc/g 또는 약 1.2 cc/g 내지 약 2.5로, cc/g 또는 약 1.5 cc/g내지 약 2 cc/g 범위일 수 있다.
본 발명에 의한 촉매들 (즉, RACC)은 여러 종류의 중합반응기를 사용하는 임의의 올레핀 중합방법에 적용될 수 있다. 본원에서 사용되는 "중합반응기"는 단일중합체 또는 공중합체를 제조하기 위하여 올레핀 단량체를 중합할 수 있는 임의의 중합반응기를 포함한다. 이러한 단일중합체 및 공중합체는 수지 또는 폴리머라고 언급된다. 여러 종류의 반응기로는 배치, 슬러리, 가스-상, 용액, 고압, 튜브 또는 오토클레이브 반응기라고 칭하는 것들을 포함한다. 가스상 반응기는 유동상 반응기 또는 단형 수평 반응기를 포함한다. 슬러리 반응기는 수직 또는 수평 루프를 포함한다. 고압 반응기는 오토클레이브 또는 튜브 반응기를 포함한다. 반응기 타입으로는 배치 또는 연속 공정을 포함할 수 있다. 연속공정은 단속적 또는 연속 생성물 방출이 적용될 수 있다. 또한 공정은 미-반응 단량체, 비-반응 공단량체 및/또는 희석제의 부분적 또는 완전한 직접 재생단계를 포함할 수 있다.
본 발명의 중합반응기 시스템은 한 종류의 반응기 또는 동종 또는 상이한 종류의 다수의 반응기들을 포함할 수 있다. 다수 반응기에서의 폴리머 제조는, 제1중합반응기에서 생성된 폴리머를 제2 반응기로 이송할 수 있도록 하는 이송장치로 연결된, 최소한 두 개의 분리된 중합반응기들에서의 여러 단계들을 포함할 수 있다. 반응기들 중 하나에서의 원하는 중합조건들은 다른 반응기의 조작 조건들과 다를 수 있다. 달리, 다수 반응기들에서의 중합은 하나의 반응기로부터의 폴리머를 연속 중합을 위한 순차 반응기로의 수동 이송을 포함할 수 있다. 여러 반응기 시스템은 제한적이지는 않지만 다수의 루프 반응기, 다수의 가스 반응기, 루프 및 가스 반응기들 조합, 다수의 고압 반응기 또는 고압 및 루프 및/또는 가스 반응기들의 조합을 포함할 수 있다. 다수 반응기들은 직렬 또는 병렬 작동될 수 있다.
본 발명의 다른 측면에 의하면, 중합반응기 시스템은 수직 또는 수평 루프를 포함하는 최소한 하나의 루프 슬러리 반응기를 포함한다. 이러한 반응기는 수 있다. 단량체, 희석제, 촉매 및 선택적 임의 공단량체는 연속적으로 루프 반응기에 공급되어 여기에서 중합된다. 일반적으로, 연속공정은 단량체, 촉매 및 희석제를 중합 반응기에 연속적으로 투입하고 중합체 입자들 및 희석제로 이루어진 현탁액을 상기 반응기에서 연속적으로 제거하는 단계를 포함한다. 반응기 유출물은 플래시 되어 희석제, 단량체 및/또는 공단량체로 이루어진 액체로부터 고형 폴리머를 제거한다. 여러 기술들이 이러한 분리 단계에서 적용될 수 있으며 제한적이지는 않지만 가열 및 감압의 임의 조합을 포함하는 플래싱; 사이클론 또는 하이드로사이클론 에서의 사이클론 작용에 의한 분리; 또는 원심분리에 의한 분리를 포함할 수 있다.
전형적인 슬러리 중합공정 (입자 형성 공정이라고도 알려짐)은 미국특허번호들 3,248,179, 4,501,885, 5,565,175, 5,575,979, 6,239,235, 6,262,191 및 6,833,415에 개시되며, 이들 각각은 본원에 참조로써 전체가 포함된다.
슬러리 중합에 사용되는 적합한 희석제는 제한적이지는 않지만 중합되는 단량체 및 반응조건 하에서 액상인 탄화수소를 포함한다. 적합한 희석제의 예시로는 제한적이지는 않지만 예를들면 프로판, 사이클로헥산, 이소부탄, n-부탄, n-펜탄, 이소펜탄, 네오펜탄 및 n-헥산과 같은 탄화수소이다. 일부 루프 중합반응은 희석제가 사용되지 않는 벌크 조건 하에서 진행될 수 있다. 일 예로 프로필렌 단량체 중합은 미국특허번호 5,455,314에 개시되며, 본원에 전체가 참조로써 포함된다.
본 발명의 또 다른 측면에 의하면, 중합반응기는 최소한 하나의 가스상 반응기를 포함할 수 있다. 이러한 시스템은 중합조건으로 촉매 존재 하에 유동상을 통하여 연속적으로 순환되는 하나 이상의 단량체를 포함한 연속적인 재순환 스트림을 이용한다. 재순환 스트림은 유동상에서 나와 반응기로 다시 재순환될 수 있다. 동시에, 폴리머 생성물은 반응기로부터 유출되고 새로운 단량체가 중합된 단량체를 대체하여 투여될 수 있다. 이러한 가스상 반응기는 올레핀의 다중-단계 가스상 중합을 위한 공정을 포함할 수 있고, 올레핀은 최소한 두 개의 독립된 가스상 중합 영역들에서 가스상에서 중합되면서 한편 제1 중합 영역에서 형성된 촉매-함유 폴리머는 제2 중합영역으로 공급된다. 가스상 반응기 일 종류는 미국특허번호들 5,352,749, 4588,790 및 5,436,304에 개시되며, 이들 각각은 본원에 참조로써 전체가 포함된다.
본 발명의 또 다른 측면에 의하면, 고압 중합반응기는 튜브 반응기 또는 오토클레이브 반응기를 포함한다. 튜브 반응기는 여러 영역을 가지며, 여기에서 새로운 단량체, 개시제 또는 촉매들이 투입된다. 단량체는 불활성 가스 스트림에 동반되어 반응기 일 영역에 도입된다. 개시제, 촉매 및/또는 성분들은 가스상에 동반되어 반응기 다른 영역으로 도입된다. 가스 스트림은 중합되기 위하여 상호 혼합된다. 열 및 압력이 적당히 인가되어 최적의 중합반응조건을 달성한다.
본 발명의 또 다른 측면에 의하면, 중합반응기는 용액중합반응기를 포함하며, 적당한 교반 또는 기타 수단에 의해 단량체는 촉매와 접촉된다. 불활성 유기 희석제 또는 과잉 단량체를 포함한 운반체가 이용될 수 있다. 원한다면, 액상 물질 존재 또는 부존재 하에서 단량체는 증기상으로 운반되어 촉매 반응생성물과 접촉한다. 중합영역은 반응 매질에서 폴리머 용액을 형성할 수 있는 온도 및 압력이 유지된다. 중합영역을 지나면서 교반되어 더욱 양호한 온도 제어 및 균일한 중합혼합물을 얻을 수 있다. 중합 발열을 분산시키기 위한 적합한 수단이 이용된다.
본 발명에 적합한 중합반응기는 최소한 하나의 원료 공급시스템, 최소한 하나의 촉매 또는 촉매성분들 공급시스템, 및/또는 최소한 하나의 폴리머회수시스템의 임의 조합을 포함한다. 적합한 본 발명의 반응기 시스템은 공급원료 정제, 촉매저장 및 제조, 압출, 반응기 냉각, 폴리머 회수, 분별, 재순환, 저장, 로드아웃, 실험실 분석 및 공정 제어를 위한 시스템을 더욱 포함한다.
중합 효율 및 수지 특성을 제어하는 조건으로는 온도, 압력 및 여러 성분들 농도를 포함한다. 중합온도는 촉매 생산성, 폴리머 분자량 및 분자량 분포에 영향을 준다. 적합한 중합온도는 깁스 자유에너지 공식에 의한 해-중합 온도 이하의 임의 온도이다. 전형적으로는 이것은 예를들면 중합반응기 종류에 따라 약 60℃ 내지 약 280℃, 및 약 70℃ 내지 약 110℃일 수 있다.
또한 적합한 압력 역시 반응기 및 중합 타입에 따라 변동될 수 있다. 루프 반응기에서 전형적인 액상 중합 압력 1000 psig 이하이다. 가스상 중합 압력은 통상 약 200 - 500 psig이다. 튜브 또는 오토클레이브 반응기에서의 고압 중합은 일반적으로 약 20,000 내지 75,000 psig에서 진행될 수 있다. 중합반응기는 또한 대략 더 높은 온도 및 압력에서 발생되는 초임계 영역에서 작동될 수 있다. 압력/온도 선도 상부에서의 작동 (초임계상)은 장점을 제공할 수도 있다.
여러 원료 농도는 특정 물성 및 기계적 성질을 가지는 수지가 생성되도록 제어될 수 있다. 제안되는 최종-사용 제품은 수지에 의해 형성되며 제품 형성 방법은 원하는 수지 특성을 결정한다. 기계적 특성은 인장, 굽힘, 충격, 크리프, 응력 이완 및 경도 시험을 포함한다. 물성은 밀도, 분자량, 분자량 분포, 용융점, 유리전이온도, 결정 용융온도, 밀도, 입체규칙성, 내 균열전진, 장 사슬 분지 및 유동변형 측정을 포함한다.
단량체, 공-단량체, 수소, 공-촉매, 개질제 및 전자주게 농도는 이들 수지 특성 형성에 중요하다. 공단량체는 생성물 밀도 조절에 이용된다. 수소는 생성물 분자량 제어에 이용될 수 있다. 공-촉매는 알킬화, 독성 제거, 분자량 조절을 위하여 사용된다. 개질제는 생성물 특성 제어를 위하여 이용되고 전자주게는 입체규칙성에 영향을 준다. 또한 독성물질은 반응 및 제품 특성에 영향을 주므로 독성 농도는 최소로 유지된다.
폴리머 및 수지는 병, 드럼, 장난감, 가정용 컨테이너, 가정용품, 필름 제품, 드럼, 연료 탱크, 파이프, 지오멤브레인, 및 라이너를 포함한 다양한 제품으로 성형될 수 있으나, 이에 제한되는 것은 아니다. 다양한 가공은 상기 제품들을 형성할 수 있으며, 제한적이지는 않지만 중공 성형, 압축 성형, 회전 성형, 열 성형, 주조 성형 등을 포함한다. 중합 후, 최종 제품에서 원하는 특성을 가지고 제조되는 동안 양호하게 처리되도록 첨가제 및 개질제가 폴리머에 첨가된다. 첨가제는 표면개질제 예를들면 슬립제, 블록킹 방지제, 점착제; 항산화제 예를들면 1차 및 2차 항산화제; 안료; 가공조제 예를들면 왁스/오일 및 플로오로엘라스토머; 및 특수 첨가제 예를들면 난연제, 대전방지제, 포집제, 흡수제, 악취 개선제, 및 분해제를 포함한다.
본 개시에 의해 제조된 촉매들은 올레핀 예를들면 알파-올레핀 중합반응에 사용될 수 있다. 일 실시예에서, RACC는 적합한 반응 조건 (예를들면, 온도, 압력 등)의 반응 구역에서 하나 이상의 올레핀과 접촉하여 올레핀을 중합한다. 2 내지 30개의 탄소원자들을 가지는 선형 또는 분지형 알파-올레핀이 올레핀 원료로 사용될 수 있다. 알파-올레핀의 특정 예로써 에틸렌, 프로필렌, 1-부텐, 1-옥텐, 3-메틸-1-부텐, 4-메틸-1-펜텐 등을 포함할 수 있다.
폴리에틸렌 단일중합체 및 에틸렌 및 기타 모노-올레핀 공중합체와 같은 폴리머는 본원에 기재된 바와 같이 제조된 촉매 (즉, RACC)를 이용하여 상기 방식으로 제조될 수 있다. 일 예에서, RACC는 폴리에틸렌 단일중합체, 선택적으로 고밀도 폴리에틸렌을 제조하기 위하여 사용된다. 본원에 기재된 바와 같이 제조된 폴리머 수지는 예를들면 압출, 중공 성형, 사출 성형, 파이버 스핀, 열 성형 및 주조에 의해 제조물 또는 최종 사용 물품으로 형성될 수 있다. 예를들면, 폴리머 수지는 시트로 압출되고 이것은 열 성형되어 용기, 컵, 접시, 팔레트, 장난감 또는 기타 제품 부분과 같은 최종 물품으로 형성될 수 있다. 폴리머 수지로 형성되는 기타 최종 물품 예시로는 파이프, 필름, 병, 파이버, 기타 등등을 포함한다.
RACC는 알칼리 처리되지 않고 제조된 유사 촉매와 비슷한 중합 활성을 보일 수 있다. 중합 활성은 시간당 충전 고형 촉매 그램당 생성 폴리머 그램으로 정의된다 (g/g-h). 일 예에서, RACC는 약 1000 g/g-h 이상, 또는 약 2000 g/g-h 이상, 또는 약 2500 g/g-h 이상의 중합 활성을 가진다.
이하 개시된 폴리머 특성은 본원에 기재된 알칼리 처리 없이 제조된 유사 촉매를 이용하여 제조된 폴리머에 비하여 특징적이다. 일 실시예에서, RACC는 약 0.1 내지 약 10, 선택적으로 0.2 내지 약 5, 선택적으로 약 0.3 내지 약 1.5의 용융지수를 가지는 폴리머를 제조한다. 용융지수 (MI)는 ASTM D 1238에 따라 결정되는, 2160 그램의 힘이 적용될 때 190℃에서 10분마다 0.0825 인치 직경의 압출 유량계 오리피스를 통하여 밀려나오는 폴리머 함량으로 정의된다. 일 실시예에서, RACC는 0.945 cc/g 이상, 선택적으로 0.950 cc/g 이상, 선택적으로 0.955 cc/g 이상의 밀도를 가지는 폴리머를 제조하기 위하여 사용될 수 잇다.
본원에 기재된 유형의 RACC를 사용하여 제조된 폴리머는 또한 높은 고하중 용융지수를 보인다. 고하중 용융지수 (HLMI)는 ASTM D 1238에 따라 결정되는, 190℃에서 21,600 그램의 힘이 적용될 때 0.0825 인치 직경의 압출 유량계 오리피스를 통하여 밀려나오는 용융 폴리머 수지 유동율로 정의된다. 일 예에서, RACC는 약 10, 선택적으로 약 50 이상의 고하중 용융지수를 가지는 폴리머를 제조할 수 있다.
본원에서 기재된 방법에 의해 제조되는 RACC를 이용하여 제조되는 폴리머는 긴 사슬 분지가 증가되는 특징이 있고 다이 스웰 (die swell)이 감소된다. 다이 스웰이란 폴리머가 압출 출구 포트를 통과할 때 원하지 않는 방향으로 부푸는 현상을 언급한다. 일 예에서, RACC는, 알칼리 처리되지 않고 제조된 유사 촉매와 비교할 때, 약 5% 내지 약 50%, 선택적으로 약 10% 내지 약 30%, 선택적으로 약 10% 내지 약 25%의 다이 스웰을 가지는 폴리머를 제조한다.
본원에 기재된 방법에 의해 제조되는 RACC를 이용하여 제조되는 폴리머는 알칼리 처리되지 않은 촉매를 이용하여 제조되는 폴리머와 비교할 때 유변학적 너비(rheological breath)가 감소된다. 유변학적 너비는 폴리머에 대한 뉴턴적 지수법칙 유형의 전단율 또는 폴리머 점도의 주파수 의존도 간 전이 영역 너비로 정의된다. 유변학적 너비는 폴리머 수지의 이완 시간 분포 함수이고 이는 다시 수지 분자 구조 또는 아키텍처 함수이다. Cox-Merz 법칙을 가정하여, 유변학적 너비는 아래 변형 Carreau-Yasuda (CY) 모델을 적용하여 선형-점탄성 동적 진동 주파수 실험에서 얻어진 유동 곡선을 피팅하여 계산될 수 있다.
모델 피팅을 용이하게 하기 위하여 지수법칙 상수는 일정 수치로 잡는다. CY 모델 및 유도된 인자들의 중요성 및 해석에 관한 상세는: C.A.Hieber and H.H.Chiang, Rheol. Acta, 28, 321(1989); C.A.Hieber and H.H.Chiang, Polym. Eng.Sci., 32, 931(1992); 및 R.B.Bird, R.C.Armstrong and O.Hasseger, Dynamics of Polymeric Liquids, Volume 1, Fluid Mechanics, 2nd Edition, John Wiley & Sons (1987)에서 찾을 수 있으며, 이들은 각각 본원에 참고로 포함된다. 일 예에서, 본원에 기술된 유형의 RACC를 이용하여 제조된 폴리머는 알칼리 처리되지 않고 제조된 촉매를 이용하여 생성된 폴리머와 비교할 때 약 5% 이상, 선택적으로 약 7% 이상, 선택적으로 약 10% 이상 감소된 CY-a 수치를 가진다. 일 예에서, 본원에 기재된 유형의 RACC를 적용하여 제조된 폴리머는 약 0.2 이하, 선택적으로 0.18 이하, 선택적으로 0.16 이하, 선택적으로 0.15 이하의 CY-a 수치를 가진다.
실시예에서, 본원에서 기술된 방법에 의한 RACC의 제조에 의해 촉매 활성화 시간이 감소되므로 제조 효율이 향상된다. 이론에 구속되지 않고, 활성 공정 동안 방출된 수분은 Cr(VI)을 가수분해하여 결과적으로 Cr(VI)을 Cr(III)로 분해시킨다. 이러한 효과를 완화시키기 위하여 상업적 활성 공정은 일반적으로 크롬(VI) 안정화를 달성하기 위하여 장시간 동안 진행된다. 통상의 상업적 활성 공정은 목표 최고 온도를 달성하도록 거의 36 시간이 필요하고, 약 12시간 내지 약 15 시간 이러한 온도에 유지시켜 크롬(III)의 약 40%가 크롬(VI)로 변환된다. 이론에 구애되지 않고, 본원에서 기술된 알칼리 용액 처리는 실리카 입자를 용융하여(fuse) 더 긴 보유시간으로 장기간 활성화에 의해 수득되는 것과 유사한 결과를 얻을 수 있다. 양 공정들은 실리카 입자를 용융하여, 이로 인하여 매트릭스의 강도를 증가시키고, RACC의 기공 반경을 증가시키면서도 표면적을 감소시킨다.
본원에서 기술된 RACC는 알칼리 처리가 결핍된 비슷한 촉매와 비교될 때 활성화 시간이 감소된다. 실시예에서, 본원에서 기술된 RACC를 위한 활성화 시간은, 추가적 알칼리 처리가 없는 유사 촉매와 비교할 때, 약 10% 이상, 또는 약 25% 이상 또는 약 50% 이상, 또는 약 70% 이상 감소될 수 있다.
실시예
본 발명은 개괄적으로 기술되나 이하 실시예는 본 발명의 특정 예로 제공되어 본 발명의 구현 및 장점들을 보인다. 예들은 예시적으로 제공되는 것이며 어떠한 경우에도 이하 청구 범위를 제한하는 것이 아니라는 점을 이해하여야 한다. "Quantachrome Autosorb-6 질소 기공 크기 분포 측정기구"가 지지체 표면적 및 기공부피를 결정하는데 사용되었다. 이러한 측정기구는 뉴욕, Syosset에 있는 Quantachrome사에서 획득되었다.
실시예 1
촉매 활성화기에 로딩되는 추가적인 촉매 함량이 활성화 촉매 최종 함량에 미치는 영향이 조사되었다. 촉매 샘플 1, 2 및 3으로 지정된 촉매 샘플들은 각각 150 파운드 (lb), 450 lb및 1050 lb로 활성화기에 충전되었다. 활성화기는 48-in 활성화기였다. 각각 Inneos및 W. R. Grace로부터 시판중인 촉매 EP 30X 또는 969MPI가 사용되었다.
각각의 샘플이 시간 상승 2.5℉/분, 0.21 ft/초 조건으로 12 시간의 보유시간 동안 1560℉ 내지1575℉ 범위에서 활성화되었다. 결과는 표 1에서 요약된다.
표에 따르면, 충전 촉매 양이 증가되면 Cr(VI) 변환이 감소된다. 촉매 샘플 중합 활성은 소규모 반응기에서 테스트되었다.
중합은 400 rpm으로 회전되는 마린 교반기가 구비된 2.2 리터 철재 반응기에서 진행되었다. 반응기는 비등 메탄올을 가지며 철재 응축기와 연통되는 철재 덮개로 둘러싸인다. 메탄올 비등점은 응축기 및 덮개에 인가되는 질소 압력을 변경시켜 조절되었고 전자제어장치로써 1/2 섭씨 온도까지 제어 가능하였다. 달리 언급되지 않는 한, 소량의 고형 촉매 (통상 0.01 내지 0.10 그램)가 건식 반응기에 질소 하에서 충전되었다. 다음 1.2 리터 이소부탄 액이 충전되고 반응기는 특정 온도 약 105 ℃로 가열되었다. 마지막으로 통상 고정 압력 550 psig이 유지되도록 에틸렌이 반응기에 첨가되었다. 특정 시간, 통상 1시간 정도 교반이 계속되었고, 설정 압력을 유지하기 위하여 반응기에 유입되는 에틸렌 유입(flow)을 기록하여 활성이 측정되었다. 설정 시간 후, 에틸렌 유입이 중지되었고 반응기는 서서히 압력이 낮추어 개방되고 입자 폴리머 분말을 회수하였다. 모든 경우에서, 반응기는 어떠한 벽 스케일, 피복물 또는 기타 오염 형태가 나타나지 않고 청결하였다. 활성은 시간당 충전 고형 촉매 그램당 생성 폴리머 그램으로 정의되었다.
촉매 활성 및 생성된 폴리머의 물성은 도 2와 3에서 도시된다. 도 2는 촉매 생산성 함수로서의 폴리머 용융지수의 플롯이다. 도 2에 도시된 바와 같이, 촉매 충전 양이 감소되면 폴리머 용융지수가 증가된다. 도 3은 폴리머 용융지수 함수로서의 고하중 용융지수 및 용융지수의 비율(HLMI/MI 비율)의 플롯이다. 도 3을 참고하면, 촉매 충전 함량이 증가할수록 수지 탄성도 영향을 받았다. 특히, 충전 촉매 함량이 증가할수록 HLMI/MI 비율이 감소되었다. 전체적으로, 이러한 결과는 활성화기에 촉매를 더욱 충전하여도 활성 촉매를 더욱 생성하지 않는다는 것을 보인다.
실시예 2
촉매 활성 동안 목표 활성 온도로 시간 상승 후 보유시간 단축 영향이 조사되었다. 여러 테스트가 상업용 반응기에서 실시되었고 촉매 샘플이 활성화되는 동안 1450℉에 보유시간이 12 시간에서 2 시간으로 단축되었다. 결과는 도 4에서 도시된다. 연속하여 매 샘플이 폴리머 조성물을 생성하기 위하여 사용되었고 실시예 1에서 기술된 바와 같이 폴리머의 MI 및 HLMI가 결정되었다. 도 4를 참고하면, 목표 활성 온도에서 보유시간이 12 시간에서 2 시간으로 단축되면 폴리머의 용융지수가 감소되는 것으로 관찰되었다.
보유 시간 단축은 도 5에 도시된 바와 같이 탄성에 영향을 주는 것으로 관찰되었고, 목표 활성 온도에서 보유시간이 12 시간에서 2 시간으로 단축되면 폴리머의 HLMI/MI 비율이 감소되었다. 이러한 결과는 목표 활성 온도에서의 보유시간 단축은 완전히 활성화되지 않은 촉매를 생성할 수 있다는 것을 보인다.
실시예 3
알칼리 처리가 촉매 활성 공정에 미치는 영향은 실리카-티타니아 지지체를 포함하는 촉매를 사용하여 조사되었다. 샘플 4, 5 및 6으로 지정된 3개의 실리카-티타니아 하이드로겔 샘플들이 제조되었다. 샘플 4는 알칼리 용액으로 처리되지 않았고, 반면에 샘플 5및 6는 28 시간 동안 80℃에서 NH4OH로 처리되었다. 모든 샘플은 n-프로필 알코올에서 최종 세척되고 이어 6 시간 동안 800℃에서 활성화되었다. 표면적 (SA), 기공 부피 (PV) 및 촉매 샘플의 기공 반경이 결정되었다. 실시예 1에 기재된 바와 같이 촉매들은 폴리머 조성물을 제조하기 위해 사용되었고 촉매의 중합 활성, 폴리머의 용융지수 (MI), 고하중 용융지수 (HLMI) 및 HLMI/MI 비율이 결정되었고 결과가 표 2에서 정리된다.
표 2에 도시된 바와 같이, 실리카-티타니아 하이드로겔을 알칼리 처리하면 표면적은 감소되면서 촉매 기공 반경은 증가된다. 이러한 알칼리 처리 촉매로부터 제조된 폴리머는 용융지수가 증가된다. 용융지수의 큰 증가에도 불과하고 폴리머의 HLMI/MI 비율은 약간 감소된 것이 관찰되었다. 그러므로, 이러한 경향은 폴리머의 탄성 증가를 의미한다.
실시예 4
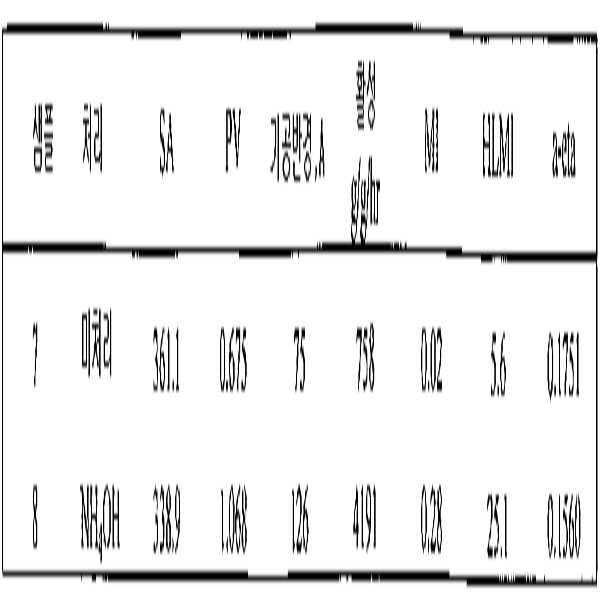
건조 방법 변경이 촉매 활성에 미치는 영향이 조사되었다. 샘플 7 및 8로 지정된 실리카-티타니아 하이드로겔이 준비되었다. 샘플 7은 알칼리 용액으로 처리되지 않았고, 샘플 8은 28 시간 동안 80℃에서 NH4OH로 처리되었다. 양 샘플이 110℃의 오븐에서 8 시간 건조되었고 이어 6 시간 동안 800℃에서 활성화되었다. 표면적 (SA), 기공 부피 (PV), 기공 반경 및 촉매 샘플의 중합 활성이 결정되었다. 촉매는 실시예 1에서 기술된 것처럼 폴리머 조성물을 제조하기 위하여 사용되었고 용융지수 (MI), 고하중 용융지수 (HLMI), HLMI/MI 비율 및 폴리머 조성물의 절대점도(a-eta)가 결정되었다. 이러한 결과는 표 3에 제시된다.
결과에 의하면, 알칼리 처리 (샘플 8)로 제조된 폴리머 샘플의 용융지수는 증가되고 촉매의 표면적 및 기공 반경 및 폴리머 용융지수 경향 은 실시예 3에서 관찰된 것들과 유사하였다.
여러 예들이 도시되고 기술되지만, 본 발명의 사상 및 교시로부터 벗어남이 없이 당 분야 기술자에 의한 이들의 변형이 가능하다. 본원에 기재된 예들은 단지 예시적이고 제한적인 목적이 아니다. 본원에 기재된 발명에 대한 다양한 변형 및 변경이 가능하며 본 발명의 범위에 속할 것이다. 수치 범위 또는 제한이 특별히 언급된 부분에서, 이러한 명백한 범위 또는 제한은 명백하게 언급된 범위 또는 제한 내에 해당되는 유사한 정도의 반복적 범위 또는 제한을 포함하는 것으로 이해되어야 한다 (예를들면 약 1 내지 약 10은 2, 3, 4, 등을 포함; 0.10 이상은 0.11, 0.12, 0.13, 등을 포함).
예를들면, 하한치 RL 및 상한치 RU를 가진 수치 범위가 기술될 때, 본 범위에 포함되는 임의의 수치는 특히 개시된다. 특히, 범위 내에 있는 하기 수치는 특히 개시된다: R=RL+k*(RU-RL), 여기에서 k는 1 퍼센트 증가되는 1 퍼센트 내지 100 퍼센트 범위로 가변되고, 즉 k가 1 퍼센트, 2 퍼센트, 3 퍼센트, 4 퍼센트, 5 퍼센트,... 50 퍼센트, 51퍼센트, 52 퍼센트, 95 퍼센트, 96 퍼센트, 97 퍼센트, 98 퍼센트, 99퍼센트, 또는 100 퍼센트이다. 더욱이, 상기 정의된 바와 같은 두 R 수치들에 의해 규정된 임의의 수치 범위 또한 특히 기술된다.
청구범위에서 임의 요소에 대한 "선택적으로" 라는 용어는 주제적 요소가 필요하거나, 또한 달리 필요하지 않은 것을 의미한다. 두 가지 경우가 청구범위에 속하는 것이다. 구성하는, 포함하는, 가지는 등과 같은 더 넓은 용어를 사용하는 것은 이루어지는, 실질적으로 이루는, 실질적으로 포함하는 등과 같은 더 좁은 용어를 지지하기 위하여 제공되는 것으로 이해되어야 한다.
따라서, 보호 범위는 상기 설명된 명세서에 의하여 제한되지 않으며, 다음에 수반되는 청구항에 의하여만 제한되고, 보호범위에는 청구항의 대상물의 모든 균등물이 포함된다. 각각 그리고 모든 청구항은 본원 발명의 예로서 명세서에 편입된다. 그러므로, 청구항은 또 다른 명세서이며, 본원 발명의 바람직한 예에 추가된다. 본원에서 참고문헌 특히 본원 우선일자 이후 공개일자를 가지는 임의 참고문헌을 언급하는 것은 본 발명에 대한 선행기술로 인정하는 것은 아니다. 본원에 인용된 모든 특허, 특허 출원, 및 간행물들의 개시는 본원에 설명된 발명에 대한 예시, 절차 또는 다른 상세에 관한 보충을 제공하는 정도로 본원에 참고문헌으로 포함된다.
Claims (24)
- 알칼리 노화 실리카 지지체를 제조하기 위하여 알칼리 용액에서 실리카 지지체를 노화하는 단계;
건조 실리카 지지체를 제조하기 위해 알칼리 노화 실리카 지지체로부터 알칼리 용액의 최소 일부를 제거하는 단계; 및
촉매 조성물을 제조하기 위해 실리카 지지체를 활성화하는 단계를 포함하며,
알칼리 노화 단계는 최초 값의 약 50%이하로 실리카 지지체의 표면적을 낮추고 실리카 지지체의 활성화 단계는 약 8 시간 이내에서 약 500 lb 이상으로 배치 공정에서 수행되는, 촉매 제조방법. - 제1항에 있어서, 노화단계는 약 60℃ 내지 약 90℃에서 수행되는, 촉매 제조방법.
- 제1항에 있어서, 알칼리 용액은 pH가 약 8 내지 약 13인, 촉매 제조방법.
- 제1항에 있어서, 노화단계는 약 1 시간 내지 약 24시간 수행되는, 촉매 제조방법.
- 제1항에 있어서, 알칼리 용액의 최소 일부 제거 단계는 알칼리 노화 지지체 및 유기 용매를 접촉, 알칼리 노화 지지체 열적 접촉, 알칼리 노화 지지체 분무 건조 또는 이들의 조합을 더욱 포함하는, 촉매 제조방법.
- 제1항에 있어서, 알칼리 노화 조성물의 상업적 활성화 단계는 약 700℃ 이상으로 조성물을 가열하는 단계를 더욱 포함하는, 촉매 제조방법.
- 제1항에 있어서, 실리카 지지체는 티타니아를 더욱 포함하는, 촉매 제조방법.
- 제1항에 있어서, 실리카 지지체는 약 300㎡/g 이하의 표면적을 가지는, 촉매 제조방법.
- 제1항에 있어서, 노화 단계 전, 동안, 후 또는 이들의 조합에 실리카 지지체에 크롬을 첨가하는 것을 더욱 포함하는, 촉매 제조방법.
- 실리카 지지체 재료를 알칼리 노화하는 단계;
크롬-실리카 지지체 형성하기 위하여 알칼리 노화 이전, 이후 또는 양자 동안 실리카 지지체 재료에 크롬을 첨가하는 단계;
활성 올레핀 중합촉매를 제조하기 위하여 크롬-실리카 지지체를 신속하게 활성화하는 단계;
폴리머 제조에 적절한 조건 하에 반응 구역에서 활성 올레핀 중합촉매를 최소한 하나의 단량체와 접촉시키는 단계; 및
폴리머를 회수하는 단계를 포함하는, 폴리머 제조방법. - 제10항에 있어서, 실리카 지지체 재료는 pH가 약 8 내지 약 13인 용액과 약 60℃ 내지 약 90℃에서 약 1 시간 내지 약 24시간 접촉되어 알칼리 노화되는, 폴리머 제조방법.
- 제10항에 있어서, 크롬-실리카 지지체는 약 500 파운드 이상으로 배치 공정에서 신속하게 활성화되는, 폴리머 제조방법.
- 제10항에 있어서, 실리카 지지체는 티타니아를 더욱 포함하는, 폴리머 제조방법.
- 제10항에 있어서, 알칼리 노화 단계는 최초 값의 약 50%이하로 실리카 지지체의 표면적을 낮추는, 폴리머 제조방법.
- 제10항에 있어서, 크롬-실리카 지지체는 약 8시간 이내로 신속하게 활성화되는, 폴리머 제조방법.
- 제10항에 있어서, 폴리머는 약 0.945g/cc 이상의 밀도를 가지는 폴리에틸렌을 포함하는, 폴리머 제조방법.
- 제16항에 있어서, 폴리머는 약 1 내지 약 10 용융지수를 가지는, 폴리머 제조방법.
- 제17항에 있어서, 폴리머는 약 0.2 이하의 CY-a 수치를 가지는, 폴리머 제조방법.
- 제18항에 있어서, 폴리에틸렌 중공 성형을 더욱 포함하는, 폴리머 제조방법.
- 실리카 지지체 재료를 알칼리 노화하는 단계;
크롬-실리카 지지체 형성하기 위하여 알칼리 노화 이전, 이후 또는 양자 동안 실리카 지지체 재료에 크롬을 첨가하는 단계;
활성 올레핀 중합촉매를 제조하기 위하여 약 8 시간 이내에 약 700℃ 이상의 온도로 가열하는 크롬-실리카 지지체를 신속하게 활성화하는 단계를 포함하는, 폴리머 제조방법. - 제20항에 있어서, 실리카 지지체 재료는 pH가 약 8 내지 약 13인 용액과 약 60℃ 내지 약 90℃에서 약 1 시간 내지 약 24시간 접촉되어 알칼리 노화되는, 폴리머 제조방법.
- 제20항에 있어서, 실리카 지지체는 티타니아를 더욱 포함하는, 폴리머 제조방법.
- 제20항에 있어서, 크롬-실리카 지지체는 약 500 파운드 이상으로 배치 공정에서 신속하게 활성화되는, 폴리머 제조방법.
- 제20항에 있어서, 알칼리 노화 단계는 최초 값의 약 50%이하로 실리카 지지체의 표면적을 낮추는, 폴리머 제조방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US11/963,530 US8183173B2 (en) | 2007-12-21 | 2007-12-21 | Fast activating catalyst |
| US11/963,530 | 2007-12-21 | ||
| PCT/US2008/013497 WO2009085100A2 (en) | 2007-12-21 | 2008-12-09 | Fast activating catalyst |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20100109909A true KR20100109909A (ko) | 2010-10-11 |
| KR101524330B1 KR101524330B1 (ko) | 2015-05-29 |
Family
ID=40517736
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020107013663A KR101524330B1 (ko) | 2007-12-21 | 2008-12-09 | 신속하게 활성화되는 촉매 |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US8183173B2 (ko) |
| EP (2) | EP2231722B1 (ko) |
| KR (1) | KR101524330B1 (ko) |
| CN (1) | CN101903419B (ko) |
| AR (1) | AR069713A1 (ko) |
| AU (1) | AU2008343937A1 (ko) |
| BR (1) | BRPI0821766B1 (ko) |
| CA (1) | CA2710163C (ko) |
| CL (1) | CL2008003747A1 (ko) |
| ES (2) | ES2668368T3 (ko) |
| HU (1) | HUE039190T2 (ko) |
| MX (1) | MX2010006971A (ko) |
| WO (1) | WO2009085100A2 (ko) |
Families Citing this family (22)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8183173B2 (en) | 2007-12-21 | 2012-05-22 | Chevron Phillips Chemical Company Lp | Fast activating catalyst |
| JP5746144B2 (ja) * | 2010-03-17 | 2015-07-08 | 出光興産株式会社 | オレフィンのオリゴマー化反応用触媒 |
| US8396600B2 (en) | 2010-07-23 | 2013-03-12 | Chevron Phillips Chemical Company Lp | Prediction and control solution for polymerization reactor operation |
| US8399580B2 (en) | 2010-08-11 | 2013-03-19 | Chevron Philips Chemical Company Lp | Additives to chromium catalyst mix tank |
| US9023967B2 (en) * | 2011-11-30 | 2015-05-05 | Chevron Phillips Chemical Company Lp | Long chain branched polymers and methods of making same |
| US9096699B2 (en) * | 2011-12-02 | 2015-08-04 | Chevron Phillips Chemical Company Lp | Methods of preparing a catalyst |
| US9376511B2 (en) | 2013-03-13 | 2016-06-28 | Chevron Phillips Chemical Company Lp | Polymerization catalysts and polymers |
| CN105658686A (zh) * | 2013-06-24 | 2016-06-08 | 沙特基础工业公司 | 基于钛酸化的铬的催化剂以制备高密度聚乙烯 |
| US20150050742A1 (en) * | 2013-08-16 | 2015-02-19 | Cdti | Analysis of Occurrence of Corrosion Products with ZPGM and PGM Catalysts Coated on Metallic Substrates |
| US10213766B2 (en) | 2015-09-18 | 2019-02-26 | Chevron Phillips Chemical Company Lp | Methods of preparing a catalyst |
| US9988468B2 (en) | 2016-09-30 | 2018-06-05 | Chevron Phillips Chemical Company Lp | Methods of preparing a catalyst |
| US11267914B2 (en) | 2016-12-29 | 2022-03-08 | Chevron Phillips Chemical Company Lp | Methods of preparing a catalyst |
| US10654953B2 (en) | 2016-12-29 | 2020-05-19 | Chevron Phillips Chemical Company Lp | Methods of preparing a catalyst |
| US20200369803A1 (en) | 2016-12-29 | 2020-11-26 | Chevron Phillips Chemical Company Lp | Methods of Preparing a Catalyst |
| US10287369B2 (en) | 2017-04-24 | 2019-05-14 | Chevron Phillips Chemical Company Lp | Methods of preparing a catalyst |
| US10513570B2 (en) | 2017-11-17 | 2019-12-24 | Chevron Phillips Chemical Company Lp | Methods of preparing a catalyst |
| US10323109B2 (en) | 2017-11-17 | 2019-06-18 | Chevron Phillips Chemical Company Lp | Methods of preparing a catalyst utilizing hydrated reagents |
| US10543480B2 (en) | 2018-04-16 | 2020-01-28 | Chevron Phillips Chemical Company Lp | Methods of preparing a catalyst utilizing hydrated reagents |
| US11266976B2 (en) * | 2018-04-16 | 2022-03-08 | Chevron Phillips Chemical Company Lp | Methods of preparing a catalyst with low HRVOC emissions |
| US10722874B2 (en) | 2018-04-16 | 2020-07-28 | Chevron Phillips Chemical Company Lp | Methods of preparing a catalyst utilizing hydrated reagents |
| WO2020094714A1 (en) * | 2018-11-08 | 2020-05-14 | Rhodia Operations | Precipitated silica and process for its manufacture |
| GB201903452D0 (en) * | 2019-03-13 | 2019-04-24 | Lucite Int Uk Ltd | A catalyst and a process for the production of ethylenically unsaturated carboxylic acids for esters |
Family Cites Families (42)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3248179A (en) | 1962-02-26 | 1966-04-26 | Phillips Petroleum Co | Method and apparatus for the production of solid polymers of olefins |
| US3362946A (en) | 1964-06-01 | 1968-01-09 | Phillips Petroleum Co | Method of treating supported chromium oxide catalyst and polymerization therewith |
| US3281405A (en) | 1964-10-05 | 1966-10-25 | Phillips Petroleum Co | Catalyst and process for polymerizing ethylene |
| US3446754A (en) | 1965-12-03 | 1969-05-27 | Nat Distillers Chem Corp | Catalyst activation |
| US3629216A (en) | 1968-05-14 | 1971-12-21 | Mitsubishi Chem Ind | Process for the polymerization of olefins |
| US3806500A (en) | 1972-07-21 | 1974-04-23 | Union Carbide Corp | Polymerization with thermally aged catalyst |
| US4022580A (en) | 1973-05-07 | 1977-05-10 | Phillips Petroleum Company | Catalyst activation |
| US3976632A (en) | 1974-12-04 | 1976-08-24 | Phillips Petroleum Company | Reactivation of organochromium olefin polymerization catalyst in presence of oxygen |
| US4041224A (en) | 1975-11-19 | 1977-08-09 | Chemplex Company | Catalyst, method and polymerization processes |
| US4151122A (en) | 1977-12-05 | 1979-04-24 | Phillips Petroleum Company | Reduction and reoxidation of cogel or self-reduced catalyst |
| US4296001A (en) | 1980-02-06 | 1981-10-20 | Phillips Petroleum Company | Titanium impregnated silica-chromium catalysts |
| US4397769A (en) | 1981-04-02 | 1983-08-09 | Phillips Petroleum Company | Olefin polymerization catalyst |
| US4501885A (en) | 1981-10-14 | 1985-02-26 | Phillips Petroleum Company | Diluent and inert gas recovery from a polymerization process |
| US4405501A (en) | 1982-01-20 | 1983-09-20 | Phillips Petroleum Company | Aging of chromium-containing gel at high pH |
| US4436882A (en) | 1982-01-20 | 1984-03-13 | Phillips Petroleum Company | Polymerization process utilizing a catalyst prepared by aging of a chromium-containing gel at high pH |
| US4588790A (en) | 1982-03-24 | 1986-05-13 | Union Carbide Corporation | Method for fluidized bed polymerization |
| US5200478A (en) | 1983-04-04 | 1993-04-06 | Solvay S.A. | Method for activating supported chromium oxide catalysts and olefin polymerization process carried out therewith |
| US4547557A (en) * | 1984-07-09 | 1985-10-15 | Phillips Petroleum Company | Silica-titania cogel from two-step hydrolysis |
| US4981831A (en) * | 1988-07-25 | 1991-01-01 | Phillips Petroleum Company | Twice-aged porous inorganic oxides, catalysts, and polymerization processes |
| US5006506A (en) | 1989-12-21 | 1991-04-09 | Mobil Oil Corporation | Modified chromium-containing catalyst composition for polymerizing olefins and method of preparing the catalyst composition |
| US5565175A (en) | 1990-10-01 | 1996-10-15 | Phillips Petroleum Company | Apparatus and method for producing ethylene polymer |
| US5575979A (en) | 1991-03-04 | 1996-11-19 | Phillips Petroleum Company | Process and apparatus for separating diluents from solid polymers utilizing a two-stage flash and a cyclone separator |
| US5183792A (en) | 1991-11-26 | 1993-02-02 | Allied-Signal Inc. | Catalyst for making polyethylene |
| US5352749A (en) | 1992-03-19 | 1994-10-04 | Exxon Chemical Patents, Inc. | Process for polymerizing monomers in fluidized beds |
| US5436304A (en) | 1992-03-19 | 1995-07-25 | Exxon Chemical Patents Inc. | Process for polymerizing monomers in fluidized beds |
| US5576263A (en) * | 1993-12-28 | 1996-11-19 | Phillips Petroleum Company | Chromium catalyst compositions and ethylene polymerization processes therewith |
| US5455314A (en) | 1994-07-27 | 1995-10-03 | Phillips Petroleum Company | Method for controlling removal of polymerization reaction effluent |
| EP0857737A1 (en) | 1997-02-07 | 1998-08-12 | Fina Research S.A. | Production of polyethylene having impact resistance |
| EP0882740A1 (en) | 1997-06-06 | 1998-12-09 | Fina Research S.A. | Titanated chromium-based catalysts to produce polyethylene exhibiting better environmental stress crack resistance |
| US6239235B1 (en) | 1997-07-15 | 2001-05-29 | Phillips Petroleum Company | High solids slurry polymerization |
| KR100531628B1 (ko) | 1998-03-20 | 2005-11-29 | 엑손모빌 케미칼 패턴츠 인코포레이티드 | 연속적인 슬러리 중합반응의 휘발물질 제거 |
| US6204346B1 (en) | 1998-12-17 | 2001-03-20 | Phillips Petroleum Co. | Polymerization process |
| US6262191B1 (en) | 1999-03-09 | 2001-07-17 | Phillips Petroleum Company | Diluent slip stream to give catalyst wetting agent |
| BE1012566A3 (fr) | 1999-03-23 | 2000-12-05 | Solvay | Procede pour la production de polymeres de l'ethylene. |
| DE19914751A1 (de) | 1999-03-31 | 2000-10-05 | Elenac Gmbh | Verfahren und Vorrichtung zur kontinuierlichen Behandlung von Katalysatoren und Katalysatorträger |
| DE19914752A1 (de) | 1999-03-31 | 2000-10-05 | Elenac Gmbh | Verfahren zur diskontinuierlichen, thermischen Behandlung von Katalysatormaterial |
| EP1162210A1 (en) | 2000-06-08 | 2001-12-12 | ATOFINA Research | Multimodal polyethylene obtained with multilayer chromium catalyst |
| US7381778B2 (en) | 2002-06-06 | 2008-06-03 | Exxonmobil Chemical Patents Inc. | Method of preparing a treated support |
| US7223823B2 (en) | 2002-06-06 | 2007-05-29 | Exxon Mobil Chemical Patents Inc. | Catalyst system and process |
| US7384885B2 (en) | 2003-03-31 | 2008-06-10 | Exxonmobil Chemical Patents Inc. | Catalyst activation and resins therefrom |
| US7615510B2 (en) * | 2004-05-12 | 2009-11-10 | Chevron Phillips Chemical Company Lp | Methods of activating chromium catalysts |
| US8183173B2 (en) | 2007-12-21 | 2012-05-22 | Chevron Phillips Chemical Company Lp | Fast activating catalyst |
-
2007
- 2007-12-21 US US11/963,530 patent/US8183173B2/en active Active
-
2008
- 2008-12-09 EP EP08869028.4A patent/EP2231722B1/en active Active
- 2008-12-09 BR BRPI0821766-1A patent/BRPI0821766B1/pt active IP Right Grant
- 2008-12-09 EP EP16153015.9A patent/EP3042919B1/en active Active
- 2008-12-09 ES ES16153015.9T patent/ES2668368T3/es active Active
- 2008-12-09 WO PCT/US2008/013497 patent/WO2009085100A2/en active Application Filing
- 2008-12-09 MX MX2010006971A patent/MX2010006971A/es active IP Right Grant
- 2008-12-09 CN CN2008801219822A patent/CN101903419B/zh active Active
- 2008-12-09 KR KR1020107013663A patent/KR101524330B1/ko active IP Right Grant
- 2008-12-09 AU AU2008343937A patent/AU2008343937A1/en not_active Abandoned
- 2008-12-09 CA CA2710163A patent/CA2710163C/en active Active
- 2008-12-09 HU HUE16153015A patent/HUE039190T2/hu unknown
- 2008-12-09 ES ES08869028.4T patent/ES2573938T3/es active Active
- 2008-12-16 AR ARP080105472A patent/AR069713A1/es active IP Right Grant
- 2008-12-16 CL CL2008003747A patent/CL2008003747A1/es unknown
Also Published As
| Publication number | Publication date |
|---|---|
| AU2008343937A1 (en) | 2009-07-09 |
| BRPI0821766B1 (pt) | 2018-08-14 |
| EP2231722B1 (en) | 2016-03-23 |
| EP3042919A3 (en) | 2016-08-24 |
| CN101903419B (zh) | 2012-12-05 |
| ES2573938T3 (es) | 2016-06-13 |
| ES2668368T3 (es) | 2018-05-17 |
| AR069713A1 (es) | 2010-02-10 |
| WO2009085100A3 (en) | 2009-10-22 |
| MX2010006971A (es) | 2010-10-05 |
| CL2008003747A1 (es) | 2010-12-24 |
| EP3042919A2 (en) | 2016-07-13 |
| KR101524330B1 (ko) | 2015-05-29 |
| CN101903419A (zh) | 2010-12-01 |
| WO2009085100A2 (en) | 2009-07-09 |
| EP3042919B1 (en) | 2018-02-14 |
| EP2231722A2 (en) | 2010-09-29 |
| CA2710163C (en) | 2016-04-05 |
| US8183173B2 (en) | 2012-05-22 |
| BRPI0821766A2 (pt) | 2015-06-16 |
| HUE039190T2 (hu) | 2018-12-28 |
| CA2710163A1 (en) | 2009-07-09 |
| US20090163681A1 (en) | 2009-06-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR101524330B1 (ko) | 신속하게 활성화되는 촉매 | |
| US9879101B2 (en) | Long chain branched polymers and methods of making same | |
| KR101562406B1 (ko) | 중합촉매 제조방법 | |
| US10287369B2 (en) | Methods of preparing a catalyst | |
| KR102533502B1 (ko) | 촉매의 제조 방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| E902 | Notification of reason for refusal | ||
| E701 | Decision to grant or registration of patent right | ||
| GRNT | Written decision to grant | ||
| FPAY | Annual fee payment |
Payment date: 20180510 Year of fee payment: 4 |
|
| FPAY | Annual fee payment |
Payment date: 20190516 Year of fee payment: 5 |