KR102445708B1 - 비피도박테리움 락티스 idcc 4301을 포함하는 체지방감소용 조성물 - Google Patents
비피도박테리움 락티스 idcc 4301을 포함하는 체지방감소용 조성물 Download PDFInfo
- Publication number
- KR102445708B1 KR102445708B1 KR1020210171209A KR20210171209A KR102445708B1 KR 102445708 B1 KR102445708 B1 KR 102445708B1 KR 1020210171209 A KR1020210171209 A KR 1020210171209A KR 20210171209 A KR20210171209 A KR 20210171209A KR 102445708 B1 KR102445708 B1 KR 102445708B1
- Authority
- KR
- South Korea
- Prior art keywords
- idcc
- bifidobacterium lactis
- composition
- fat
- body fat
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- OGQHCUYSWDOIMP-UHFFFAOYSA-N 7-(diethylamino)-n-[2-[(2-iodoacetyl)amino]ethyl]-2-oxochromene-3-carboxamide Chemical compound C1=C(C(=O)NCCNC(=O)CI)C(=O)OC2=CC(N(CC)CC)=CC=C21 OGQHCUYSWDOIMP-UHFFFAOYSA-N 0.000 title claims abstract description 34
- 241000901050 Bifidobacterium animalis subsp. lactis Species 0.000 title claims abstract description 34
- 229940009289 bifidobacterium lactis Drugs 0.000 title claims abstract description 34
- 239000000203 mixture Substances 0.000 title claims abstract description 32
- 210000000577 adipose tissue Anatomy 0.000 title claims abstract description 20
- 230000009467 reduction Effects 0.000 claims abstract description 7
- 210000001789 adipocyte Anatomy 0.000 claims description 21
- 235000013305 food Nutrition 0.000 claims description 19
- 208000008589 Obesity Diseases 0.000 claims description 11
- 235000020824 obesity Nutrition 0.000 claims description 11
- 239000008194 pharmaceutical composition Substances 0.000 claims description 11
- 230000036541 health Effects 0.000 claims description 8
- 102100034808 CCAAT/enhancer-binding protein alpha Human genes 0.000 claims description 5
- 102100030431 Fatty acid-binding protein, adipocyte Human genes 0.000 claims description 5
- 108010016731 PPAR gamma Proteins 0.000 claims description 5
- 210000003608 fece Anatomy 0.000 claims description 5
- 235000013376 functional food Nutrition 0.000 claims description 5
- 101000945515 Homo sapiens CCAAT/enhancer-binding protein alpha Proteins 0.000 claims description 3
- 101710118908 Fatty acid-binding protein, adipocyte Proteins 0.000 claims 1
- 102000000536 PPAR gamma Human genes 0.000 claims 1
- 239000003925 fat Substances 0.000 description 28
- 235000019197 fats Nutrition 0.000 description 27
- 235000009200 high fat diet Nutrition 0.000 description 19
- 210000004027 cell Anatomy 0.000 description 11
- 230000000694 effects Effects 0.000 description 10
- JVTAAEKCZFNVCJ-UHFFFAOYSA-N lactic acid Chemical compound CC(O)C(O)=O JVTAAEKCZFNVCJ-UHFFFAOYSA-N 0.000 description 10
- 235000013361 beverage Nutrition 0.000 description 9
- 239000003814 drug Substances 0.000 description 9
- 238000005259 measurement Methods 0.000 description 8
- 241000894006 Bacteria Species 0.000 description 7
- 230000035508 accumulation Effects 0.000 description 6
- 238000009825 accumulation Methods 0.000 description 6
- 210000004369 blood Anatomy 0.000 description 6
- 239000008280 blood Substances 0.000 description 6
- 230000037396 body weight Effects 0.000 description 6
- 230000004069 differentiation Effects 0.000 description 6
- 238000000034 method Methods 0.000 description 6
- AHLBNYSZXLDEJQ-FWEHEUNISA-N orlistat Chemical compound CCCCCCCCCCC[C@H](OC(=O)[C@H](CC(C)C)NC=O)C[C@@H]1OC(=O)[C@H]1CCCCCC AHLBNYSZXLDEJQ-FWEHEUNISA-N 0.000 description 6
- 102000004169 proteins and genes Human genes 0.000 description 6
- 108090000623 proteins and genes Proteins 0.000 description 6
- 210000001519 tissue Anatomy 0.000 description 6
- 102100036475 Alanine aminotransferase 1 Human genes 0.000 description 5
- 108010082126 Alanine transaminase Proteins 0.000 description 5
- 108010003415 Aspartate Aminotransferases Proteins 0.000 description 5
- 102000004625 Aspartate Aminotransferases Human genes 0.000 description 5
- 238000011746 C57BL/6J (JAX™ mouse strain) Methods 0.000 description 5
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 5
- 230000003013 cytotoxicity Effects 0.000 description 5
- 231100000135 cytotoxicity Toxicity 0.000 description 5
- 229940079593 drug Drugs 0.000 description 5
- 239000000796 flavoring agent Substances 0.000 description 5
- 235000013355 food flavoring agent Nutrition 0.000 description 5
- 235000015203 fruit juice Nutrition 0.000 description 5
- 239000004310 lactic acid Substances 0.000 description 5
- 235000014655 lactic acid Nutrition 0.000 description 5
- 229960001243 orlistat Drugs 0.000 description 5
- 239000000243 solution Substances 0.000 description 5
- 102100022089 Acyl-[acyl-carrier-protein] hydrolase Human genes 0.000 description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 4
- 108010039731 Fatty Acid Synthases Proteins 0.000 description 4
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 4
- WZUVPPKBWHMQCE-UHFFFAOYSA-N Haematoxylin Chemical compound C12=CC(O)=C(O)C=C2CC2(O)C1C1=CC=C(O)C(O)=C1OC2 WZUVPPKBWHMQCE-UHFFFAOYSA-N 0.000 description 4
- 101001062864 Homo sapiens Fatty acid-binding protein, adipocyte Proteins 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- 108010028554 LDL Cholesterol Proteins 0.000 description 4
- 239000004480 active ingredient Substances 0.000 description 4
- 238000010171 animal model Methods 0.000 description 4
- 230000008859 change Effects 0.000 description 4
- 201000010099 disease Diseases 0.000 description 4
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 4
- 210000000918 epididymis Anatomy 0.000 description 4
- 201000010063 epididymitis Diseases 0.000 description 4
- 239000012091 fetal bovine serum Substances 0.000 description 4
- 238000009472 formulation Methods 0.000 description 4
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 4
- 239000002953 phosphate buffered saline Substances 0.000 description 4
- 238000002360 preparation method Methods 0.000 description 4
- 235000018102 proteins Nutrition 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 150000003839 salts Chemical class 0.000 description 4
- 238000010186 staining Methods 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- 229940124597 therapeutic agent Drugs 0.000 description 4
- 239000011782 vitamin Substances 0.000 description 4
- 235000013343 vitamin Nutrition 0.000 description 4
- 229940088594 vitamin Drugs 0.000 description 4
- 229930003231 vitamin Natural products 0.000 description 4
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- NPGIHFRTRXVWOY-UHFFFAOYSA-N Oil red O Chemical compound Cc1ccc(C)c(c1)N=Nc1cc(C)c(cc1C)N=Nc1c(O)ccc2ccccc12 NPGIHFRTRXVWOY-UHFFFAOYSA-N 0.000 description 3
- 102100038825 Peroxisome proliferator-activated receptor gamma Human genes 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 244000299461 Theobroma cacao Species 0.000 description 3
- 239000000090 biomarker Substances 0.000 description 3
- 150000001720 carbohydrates Chemical class 0.000 description 3
- 235000014633 carbohydrates Nutrition 0.000 description 3
- 235000014171 carbonated beverage Nutrition 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 230000003247 decreasing effect Effects 0.000 description 3
- 230000001419 dependent effect Effects 0.000 description 3
- 239000000284 extract Substances 0.000 description 3
- 235000003599 food sweetener Nutrition 0.000 description 3
- -1 for example Substances 0.000 description 3
- 210000004013 groin Anatomy 0.000 description 3
- 231100000304 hepatotoxicity Toxicity 0.000 description 3
- 230000007056 liver toxicity Effects 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 235000015097 nutrients Nutrition 0.000 description 3
- 239000000546 pharmaceutical excipient Substances 0.000 description 3
- 239000000843 powder Substances 0.000 description 3
- 239000003755 preservative agent Substances 0.000 description 3
- 239000003765 sweetening agent Substances 0.000 description 3
- 239000002562 thickening agent Substances 0.000 description 3
- 101710168309 CCAAT/enhancer-binding protein alpha Proteins 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 2
- 229930091371 Fructose Natural products 0.000 description 2
- 239000005715 Fructose Substances 0.000 description 2
- RFSUNEUAIZKAJO-ARQDHWQXSA-N Fructose Chemical compound OC[C@H]1O[C@](O)(CO)[C@@H](O)[C@@H]1O RFSUNEUAIZKAJO-ARQDHWQXSA-N 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- 206010019133 Hangover Diseases 0.000 description 2
- 102000004877 Insulin Human genes 0.000 description 2
- 108090001061 Insulin Proteins 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 239000000020 Nitrocellulose Substances 0.000 description 2
- 229920002230 Pectic acid Polymers 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 244000269722 Thea sinensis Species 0.000 description 2
- 238000002835 absorbance Methods 0.000 description 2
- 235000013334 alcoholic beverage Nutrition 0.000 description 2
- 239000000783 alginic acid Substances 0.000 description 2
- 235000010443 alginic acid Nutrition 0.000 description 2
- 229920000615 alginic acid Polymers 0.000 description 2
- 229960001126 alginic acid Drugs 0.000 description 2
- 150000004781 alginic acids Chemical class 0.000 description 2
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 2
- 229940098773 bovine serum albumin Drugs 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 235000019219 chocolate Nutrition 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- 239000003086 colorant Substances 0.000 description 2
- 235000009508 confectionery Nutrition 0.000 description 2
- 238000012790 confirmation Methods 0.000 description 2
- 235000005911 diet Nutrition 0.000 description 2
- 230000037213 diet Effects 0.000 description 2
- 239000003792 electrolyte Substances 0.000 description 2
- 239000000839 emulsion Substances 0.000 description 2
- YQGOJNYOYNNSMM-UHFFFAOYSA-N eosin Chemical compound [Na+].OC(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C(O)=C(Br)C=C21 YQGOJNYOYNNSMM-UHFFFAOYSA-N 0.000 description 2
- 230000029142 excretion Effects 0.000 description 2
- 230000037406 food intake Effects 0.000 description 2
- 239000008103 glucose Substances 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 235000013402 health food Nutrition 0.000 description 2
- 238000007490 hematoxylin and eosin (H&E) staining Methods 0.000 description 2
- 239000004615 ingredient Substances 0.000 description 2
- 229940125396 insulin Drugs 0.000 description 2
- 229960004592 isopropanol Drugs 0.000 description 2
- 210000003734 kidney Anatomy 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 210000004185 liver Anatomy 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 210000004379 membrane Anatomy 0.000 description 2
- 239000012528 membrane Substances 0.000 description 2
- 229920001220 nitrocellulos Polymers 0.000 description 2
- 150000007524 organic acids Chemical class 0.000 description 2
- 235000005985 organic acids Nutrition 0.000 description 2
- 239000012188 paraffin wax Substances 0.000 description 2
- LCLHHZYHLXDRQG-ZNKJPWOQSA-N pectic acid Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)O[C@H](C(O)=O)[C@@H]1OC1[C@H](O)[C@@H](O)[C@@H](OC2[C@@H]([C@@H](O)[C@@H](O)[C@H](O2)C(O)=O)O)[C@@H](C(O)=O)O1 LCLHHZYHLXDRQG-ZNKJPWOQSA-N 0.000 description 2
- 239000006187 pill Substances 0.000 description 2
- 239000010318 polygalacturonic acid Substances 0.000 description 2
- 210000000229 preadipocyte Anatomy 0.000 description 2
- 230000001681 protective effect Effects 0.000 description 2
- 239000000523 sample Substances 0.000 description 2
- 230000035945 sensitivity Effects 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- UNAANXDKBXWMLN-UHFFFAOYSA-N sibutramine Chemical compound C=1C=C(Cl)C=CC=1C1(C(N(C)C)CC(C)C)CCC1 UNAANXDKBXWMLN-UHFFFAOYSA-N 0.000 description 2
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 2
- 239000007787 solid Substances 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 239000000126 substance Substances 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 239000006228 supernatant Substances 0.000 description 2
- 239000000829 suppository Substances 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 239000003826 tablet Substances 0.000 description 2
- 235000013311 vegetables Nutrition 0.000 description 2
- 150000003722 vitamin derivatives Chemical class 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 230000004584 weight gain Effects 0.000 description 2
- 235000019786 weight gain Nutrition 0.000 description 2
- 238000001262 western blot Methods 0.000 description 2
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 2
- BJEPYKJPYRNKOW-REOHCLBHSA-N (S)-malic acid Chemical compound OC(=O)[C@@H](O)CC(O)=O BJEPYKJPYRNKOW-REOHCLBHSA-N 0.000 description 1
- OWEGMIWEEQEYGQ-UHFFFAOYSA-N 100676-05-9 Natural products OC1C(O)C(O)C(CO)OC1OCC1C(O)C(O)C(O)C(OC2C(OC(O)C(O)C2O)CO)O1 OWEGMIWEEQEYGQ-UHFFFAOYSA-N 0.000 description 1
- APIXJSLKIYYUKG-UHFFFAOYSA-N 3 Isobutyl 1 methylxanthine Chemical compound O=C1N(C)C(=O)N(CC(C)C)C2=C1N=CN2 APIXJSLKIYYUKG-UHFFFAOYSA-N 0.000 description 1
- AZKSAVLVSZKNRD-UHFFFAOYSA-M 3-(4,5-dimethylthiazol-2-yl)-2,5-diphenyltetrazolium bromide Chemical compound [Br-].S1C(C)=C(C)N=C1[N+]1=NC(C=2C=CC=CC=2)=NN1C1=CC=CC=C1 AZKSAVLVSZKNRD-UHFFFAOYSA-M 0.000 description 1
- 108010085238 Actins Proteins 0.000 description 1
- 102000007469 Actins Human genes 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 108010011485 Aspartame Proteins 0.000 description 1
- 238000009010 Bradford assay Methods 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 208000017667 Chronic Disease Diseases 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 206010012335 Dependence Diseases 0.000 description 1
- 229920001353 Dextrin Polymers 0.000 description 1
- 239000004375 Dextrin Substances 0.000 description 1
- 239000004278 EU approved seasoning Substances 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 239000004386 Erythritol Substances 0.000 description 1
- UNXHWFMMPAWVPI-UHFFFAOYSA-N Erythritol Natural products OCC(O)C(O)CO UNXHWFMMPAWVPI-UHFFFAOYSA-N 0.000 description 1
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 1
- 208000004930 Fatty Liver Diseases 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 206010019708 Hepatic steatosis Diseases 0.000 description 1
- 239000012741 Laemmli sample buffer Substances 0.000 description 1
- 206010067125 Liver injury Diseases 0.000 description 1
- GUBGYTABKSRVRQ-PICCSMPSSA-N Maltose Natural products O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@@H]1O[C@@H]1[C@@H](CO)OC(O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-PICCSMPSSA-N 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 102000012132 Peroxisome proliferator-activated receptor gamma Human genes 0.000 description 1
- 229940122907 Phosphatase inhibitor Drugs 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 229940124158 Protease/peptidase inhibitor Drugs 0.000 description 1
- 241000700159 Rattus Species 0.000 description 1
- 102100037486 Reverse transcriptase/ribonuclease H Human genes 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 244000228451 Stevia rebaudiana Species 0.000 description 1
- 235000005764 Theobroma cacao ssp. cacao Nutrition 0.000 description 1
- 235000005767 Theobroma cacao ssp. sphaerocarpum Nutrition 0.000 description 1
- 102000040945 Transcription factor Human genes 0.000 description 1
- 108091023040 Transcription factor Proteins 0.000 description 1
- TVXBFESIOXBWNM-UHFFFAOYSA-N Xylitol Natural products OCCC(O)C(O)C(O)CCO TVXBFESIOXBWNM-UHFFFAOYSA-N 0.000 description 1
- 244000126002 Ziziphus vulgaris Species 0.000 description 1
- 238000010521 absorption reaction Methods 0.000 description 1
- 235000011054 acetic acid Nutrition 0.000 description 1
- 230000011759 adipose tissue development Effects 0.000 description 1
- 210000000593 adipose tissue white Anatomy 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N alpha-hydroxysuccinic acid Natural products OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 230000003579 anti-obesity Effects 0.000 description 1
- 239000000883 anti-obesity agent Substances 0.000 description 1
- 230000036528 appetite Effects 0.000 description 1
- 235000019789 appetite Nutrition 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000003125 aqueous solvent Substances 0.000 description 1
- 239000000605 aspartame Substances 0.000 description 1
- 235000010357 aspartame Nutrition 0.000 description 1
- IAOZJIPTCAWIRG-QWRGUYRKSA-N aspartame Chemical compound OC(=O)C[C@H](N)C(=O)N[C@H](C(=O)OC)CC1=CC=CC=C1 IAOZJIPTCAWIRG-QWRGUYRKSA-N 0.000 description 1
- 229960003438 aspartame Drugs 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- GUBGYTABKSRVRQ-QUYVBRFLSA-N beta-maltose Chemical compound OC[C@H]1O[C@H](O[C@H]2[C@H](O)[C@@H](O)[C@H](O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@@H]1O GUBGYTABKSRVRQ-QUYVBRFLSA-N 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000036765 blood level Effects 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 235000008429 bread Nutrition 0.000 description 1
- 235000014121 butter Nutrition 0.000 description 1
- 235000001046 cacaotero Nutrition 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 235000019577 caloric intake Nutrition 0.000 description 1
- 230000015556 catabolic process Effects 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 238000005119 centrifugation Methods 0.000 description 1
- 235000013351 cheese Nutrition 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000003795 chemical substances by application Substances 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 238000005352 clarification Methods 0.000 description 1
- 235000020940 control diet Nutrition 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 210000000028 corpus adiposum pararenale Anatomy 0.000 description 1
- 238000012258 culturing Methods 0.000 description 1
- 235000013365 dairy product Nutrition 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 238000006731 degradation reaction Methods 0.000 description 1
- 230000018044 dehydration Effects 0.000 description 1
- 238000006297 dehydration reaction Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- UREBDLICKHMUKA-CXSFZGCWSA-N dexamethasone Chemical compound C1CC2=CC(=O)C=C[C@]2(C)[C@]2(F)[C@@H]1[C@@H]1C[C@@H](C)[C@@](C(=O)CO)(O)[C@@]1(C)C[C@@H]2O UREBDLICKHMUKA-CXSFZGCWSA-N 0.000 description 1
- 229960003957 dexamethasone Drugs 0.000 description 1
- 235000019425 dextrin Nutrition 0.000 description 1
- 206010012601 diabetes mellitus Diseases 0.000 description 1
- 235000015872 dietary supplement Nutrition 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- LOKCTEFSRHRXRJ-UHFFFAOYSA-I dipotassium trisodium dihydrogen phosphate hydrogen phosphate dichloride Chemical compound P(=O)(O)(O)[O-].[K+].P(=O)(O)([O-])[O-].[Na+].[Na+].[Cl-].[K+].[Cl-].[Na+] LOKCTEFSRHRXRJ-UHFFFAOYSA-I 0.000 description 1
- 150000002016 disaccharides Chemical class 0.000 description 1
- 230000002124 endocrine Effects 0.000 description 1
- 230000019439 energy homeostasis Effects 0.000 description 1
- 235000019414 erythritol Nutrition 0.000 description 1
- 229940009714 erythritol Drugs 0.000 description 1
- UNXHWFMMPAWVPI-ZXZARUISSA-N erythritol Chemical compound OC[C@H](O)[C@H](O)CO UNXHWFMMPAWVPI-ZXZARUISSA-N 0.000 description 1
- 150000002148 esters Chemical class 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 208000010706 fatty liver disease Diseases 0.000 description 1
- 238000000855 fermentation Methods 0.000 description 1
- 230000004151 fermentation Effects 0.000 description 1
- 235000013373 food additive Nutrition 0.000 description 1
- 239000002778 food additive Substances 0.000 description 1
- 235000011194 food seasoning agent Nutrition 0.000 description 1
- 239000003205 fragrance Substances 0.000 description 1
- 235000011389 fruit/vegetable juice Nutrition 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 235000001727 glucose Nutrition 0.000 description 1
- 239000001963 growth medium Substances 0.000 description 1
- 231100000234 hepatic damage Toxicity 0.000 description 1
- 230000013632 homeostatic process Effects 0.000 description 1
- 235000015243 ice cream Nutrition 0.000 description 1
- 238000010191 image analysis Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- VMPHSYLJUKZBJJ-UHFFFAOYSA-N lauric acid triglyceride Natural products CCCCCCCCCCCC(=O)OCC(OC(=O)CCCCCCCCCCC)COC(=O)CCCCCCCCCCC VMPHSYLJUKZBJJ-UHFFFAOYSA-N 0.000 description 1
- 229940069445 licorice extract Drugs 0.000 description 1
- 230000006372 lipid accumulation Effects 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 239000012669 liquid formulation Substances 0.000 description 1
- 229940057995 liquid paraffin Drugs 0.000 description 1
- 230000008818 liver damage Effects 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 239000012139 lysis buffer Substances 0.000 description 1
- 229960003511 macrogol Drugs 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 239000001630 malic acid Substances 0.000 description 1
- 235000011090 malic acid Nutrition 0.000 description 1
- 235000013372 meat Nutrition 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 210000000713 mesentery Anatomy 0.000 description 1
- HEBKCHPVOIAQTA-UHFFFAOYSA-N meso ribitol Natural products OCC(O)C(O)C(O)CO HEBKCHPVOIAQTA-UHFFFAOYSA-N 0.000 description 1
- 239000002207 metabolite Substances 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 150000002772 monosaccharides Chemical class 0.000 description 1
- 239000006872 mrs medium Substances 0.000 description 1
- 208000010125 myocardial infarction Diseases 0.000 description 1
- 235000021096 natural sweeteners Nutrition 0.000 description 1
- 230000007935 neutral effect Effects 0.000 description 1
- 239000012457 nonaqueous media Substances 0.000 description 1
- 235000012149 noodles Nutrition 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 201000008482 osteoarthritis Diseases 0.000 description 1
- 239000003002 pH adjusting agent Substances 0.000 description 1
- 229920002866 paraformaldehyde Polymers 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 239000002504 physiological saline solution Substances 0.000 description 1
- 235000013550 pizza Nutrition 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 229920001282 polysaccharide Polymers 0.000 description 1
- 239000005017 polysaccharide Substances 0.000 description 1
- 150000004804 polysaccharides Chemical class 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 239000013641 positive control Substances 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 239000006041 probiotic Substances 0.000 description 1
- 235000018291 probiotics Nutrition 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 239000000047 product Substances 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- HELXLJCILKEWJH-NCGAPWICSA-N rebaudioside A Chemical compound O([C@H]1[C@H](O)[C@@H](CO)O[C@H]([C@@H]1O[C@H]1[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O1)O)O[C@]12C(=C)C[C@@]3(C1)CC[C@@H]1[C@@](C)(CCC[C@]1([C@@H]3CC2)C)C(=O)O[C@H]1[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O1)O)[C@@H]1O[C@H](CO)[C@@H](O)[C@H](O)[C@H]1O HELXLJCILKEWJH-NCGAPWICSA-N 0.000 description 1
- BOLDJAUMGUJJKM-LSDHHAIUSA-N renifolin D Natural products CC(=C)[C@@H]1Cc2c(O)c(O)ccc2[C@H]1CC(=O)c3ccc(O)cc3O BOLDJAUMGUJJKM-LSDHHAIUSA-N 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- 235000013580 sausages Nutrition 0.000 description 1
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 1
- 229960004425 sibutramine Drugs 0.000 description 1
- 235000011888 snacks Nutrition 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 229960002920 sorbitol Drugs 0.000 description 1
- 235000010356 sorbitol Nutrition 0.000 description 1
- 235000014347 soups Nutrition 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 231100000240 steatosis hepatitis Toxicity 0.000 description 1
- 235000000346 sugar Nutrition 0.000 description 1
- 150000005846 sugar alcohols Chemical class 0.000 description 1
- 239000000375 suspending agent Substances 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000013616 tea Nutrition 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- UFTFJSFQGQCHQW-UHFFFAOYSA-N triformin Chemical compound O=COCC(OC=O)COC=O UFTFJSFQGQCHQW-UHFFFAOYSA-N 0.000 description 1
- 238000009966 trimming Methods 0.000 description 1
- 239000003656 tris buffered saline Substances 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 238000005303 weighing Methods 0.000 description 1
- 230000004580 weight loss Effects 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 229940002552 xenical Drugs 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
- 239000000811 xylitol Substances 0.000 description 1
- 235000010447 xylitol Nutrition 0.000 description 1
- HEBKCHPVOIAQTA-SCDXWVJYSA-N xylitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)CO HEBKCHPVOIAQTA-SCDXWVJYSA-N 0.000 description 1
- 229960002675 xylitol Drugs 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23L—FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES, NOT OTHERWISE PROVIDED FOR; PREPARATION OR TREATMENT THEREOF
- A23L33/00—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof
- A23L33/10—Modifying nutritive qualities of foods; Dietetic products; Preparation or treatment thereof using additives
- A23L33/135—Bacteria or derivatives thereof, e.g. probiotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/74—Bacteria
- A61K35/741—Probiotics
- A61K35/744—Lactic acid bacteria, e.g. enterococci, pediococci, lactococci, streptococci or leuconostocs
- A61K35/745—Bifidobacteria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms, e.g. protozoa; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
- C12N1/205—Bacterial isolates
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2002/00—Food compositions, function of food ingredients or processes for food or foodstuffs
-
- A—HUMAN NECESSITIES
- A23—FOODS OR FOODSTUFFS; TREATMENT THEREOF, NOT COVERED BY OTHER CLASSES
- A23V—INDEXING SCHEME RELATING TO FOODS, FOODSTUFFS OR NON-ALCOHOLIC BEVERAGES AND LACTIC OR PROPIONIC ACID BACTERIA USED IN FOODSTUFFS OR FOOD PREPARATION
- A23V2200/00—Function of food ingredients
- A23V2200/30—Foods, ingredients or supplements having a functional effect on health
- A23V2200/332—Promoters of weight control and weight loss
-
- A23Y2220/49—
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12R—INDEXING SCHEME ASSOCIATED WITH SUBCLASSES C12C - C12Q, RELATING TO MICROORGANISMS
- C12R2001/00—Microorganisms ; Processes using microorganisms
- C12R2001/01—Bacteria or Actinomycetales ; using bacteria or Actinomycetales
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Genetics & Genomics (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Obesity (AREA)
- Tropical Medicine & Parasitology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Hematology (AREA)
- Nutrition Science (AREA)
- Food Science & Technology (AREA)
- Polymers & Plastics (AREA)
- Diabetes (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Virology (AREA)
- Biomedical Technology (AREA)
- Child & Adolescent Psychology (AREA)
- Epidemiology (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Description
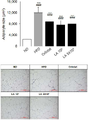
도 2는 3T3-L1 세포를 이용하여 비피도박테리움 락티스 IDCC 4301 처리에 따른 지방 축적량을 Oil red O 염색을 통해 확인한 그래프이고,
도 3은 western blot 방법을 이용하여 3T3-L1 세포 내 비만 관련 바이오마커의 단백질 발현양을 측정한 그래프이고,
도 4는 비피도박테리움 락티스 IDCC 4301 처리에 따른 C57BL/6J 쥐의 12주간 체중 변화를 나타낸 그래프이고,
도 5는 C57BL/6J 쥐의 지방(부고환 주위 지방, 신장 주위 지방, 서혜부 지방, 장간막 주위 지방) 무게를 측정하여 군 별로 비교한 그래프이고,
도 6은 C57BL/6J 쥐의 혈청에서 간 독성(AST, ALT) 및 혈중 지질 마커(TG, TC, LDL-C)를 분석한 그래프이고,
도 7은 비피도박테리움 락티스 IDCC 4301 처리에 따른 부고환 주위 지방 세포 크기 변화를 hematoxylin&eosin(H&E 염색)을 통해 조직병리학적으로 확인한 그래프이다.
| Group | Treatment |
| Normal control diet (ND) |
ND (5.57 kcal % fat) |
| High fat diet (HFD) |
HFD (45 kcal % fat) |
| HFD+Orlistat (Orlistat) |
HFD+Orlistat 50 mg/kg B.W. |
| HFD+Bifidobacterium lactis IDCC 4301 (LA 108) |
HFD+Bifidobacterium lactis IDCC 4301 108 CFU/mL |
| HFD+Bifidobacterium lactis IDCC 4301 (LA 5×108) |
HFD+Bifidobacterium lactis IDCC 4301 5×108 CFU/mL |
Claims (5)
- 체지방 감소 기능을 가지는 조성물에 있어서,
비피도박테리움 락티스 IDCC 4301[기탁번호: ATCC BAA-2848]를 포함하며,
상기 비피도박테리움 락티스 IDCC 4301은 모유를 먹인 유아의 대변에서 분리된 조성물. - 제1항에서,
상기 비피도박테리움 락티스 IDCC 4301는,
지방세포 내에서 PPARγ, CEBP/α, A-FABP 및 FAS의 발현을 감소시키는 조성물. - 제1항 및 제2항 중 어느 한 항에 따른 조성물을 0.1 내지 50중량% 포함하는 식품.
- 제1항 및 제2항 중 어느 한 항에 따른 조성물을 0.1 내지 50중량% 포함하며 체지방 감소 기능이 있는 건강기능식품.
- 비만을 치료하기 위한 약학적 조성물에 있어서,
비피도박테리움 락티스 IDCC 4301을 포함하며,
상기 비피도박테리움 락티스 IDCC 4301은 모유를 먹인 유아의 대변에서 분리된 약학적 조성물.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020210171209A KR102445708B1 (ko) | 2021-12-02 | 2021-12-02 | 비피도박테리움 락티스 idcc 4301을 포함하는 체지방감소용 조성물 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020210171209A KR102445708B1 (ko) | 2021-12-02 | 2021-12-02 | 비피도박테리움 락티스 idcc 4301을 포함하는 체지방감소용 조성물 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR102445708B1 true KR102445708B1 (ko) | 2022-09-23 |
Family
ID=83446083
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020210171209A Active KR102445708B1 (ko) | 2021-12-02 | 2021-12-02 | 비피도박테리움 락티스 idcc 4301을 포함하는 체지방감소용 조성물 |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR102445708B1 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102523776B1 (ko) * | 2022-09-27 | 2023-04-21 | 일동바이오사이언스(주) | 비타민 a 생성능이 우수한 비피도박테리움 락티스 idcc 4301을 포함하는 조성물 및 건강기능식품 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20080267933A1 (en) | 2005-10-07 | 2008-10-30 | Arla Foods Amba | Probiotics to Influence Fat Metabolism and Obesity |
| WO2015121458A2 (fr) * | 2014-02-14 | 2015-08-20 | Vesale Pharma Sa | Composition comprenant du bifidobacterium animalis ssp. lactis |
| US20160354418A1 (en) * | 2014-02-14 | 2016-12-08 | Vesale Pharma Sa | Use of compositions comprising bifidobacterium animalis ssp. lactis lmg p-28149 |
-
2021
- 2021-12-02 KR KR1020210171209A patent/KR102445708B1/ko active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20080267933A1 (en) | 2005-10-07 | 2008-10-30 | Arla Foods Amba | Probiotics to Influence Fat Metabolism and Obesity |
| WO2015121458A2 (fr) * | 2014-02-14 | 2015-08-20 | Vesale Pharma Sa | Composition comprenant du bifidobacterium animalis ssp. lactis |
| US20160354418A1 (en) * | 2014-02-14 | 2016-12-08 | Vesale Pharma Sa | Use of compositions comprising bifidobacterium animalis ssp. lactis lmg p-28149 |
Non-Patent Citations (4)
| Title |
|---|
| Molecules a journal of synthetic chemistry and natural product chemistry, MDPI, Mar. 2020, Vol.25, no.7, pp. 1490 * |
| Molecules a journal of synthetic chemistry and natural product chemistry, MDPI, Mar. 2020, Vol.25, no.7, pp.1490 |
| Wiley Sons, Ltd., Jun. 2020, Vol.100, no.8, pp. 3308-3318 * |
| WileySons, Ltd., Jun. 2020, Vol.100, no.8, pp.3308-3318 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102523776B1 (ko) * | 2022-09-27 | 2023-04-21 | 일동바이오사이언스(주) | 비타민 a 생성능이 우수한 비피도박테리움 락티스 idcc 4301을 포함하는 조성물 및 건강기능식품 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8753694B2 (en) | Anti-angiogenic agents and anti-obesity substances applied with anti-angiogenesis from natural products | |
| KR20120002131A (ko) | 울금 추출물을 함유하는 비만 치료 또는 예방용 조성물 | |
| JP2012149004A (ja) | 核内受容体の賦活剤 | |
| KR102483300B1 (ko) | 진세노사이드 Rf, 진세노사이드 Rf를 포함하는 진세노사이드 조성물, 또는 이들 중 어느 하나 이상의 혼합물을 유효성분으로 포함하는 근감소증 개선용 조성물 | |
| KR102696677B1 (ko) | 찔레나무 뿌리 추출물을 포함하는 비만 및 대사질환의 개선, 예방 또는 치료용 조성물 | |
| KR102445708B1 (ko) | 비피도박테리움 락티스 idcc 4301을 포함하는 체지방감소용 조성물 | |
| KR101888871B1 (ko) | 차전초 잎 추출물을 포함하는 비만 또는 대사성 질환의 예방 및 치료용 조성물 | |
| JP2020188709A (ja) | ペルオキシソーム増殖因子活性化受容体発現抑制用食品組成物 | |
| KR101882492B1 (ko) | 페룰릭산 및 이의 약학적으로 허용가능한 염을 유효성분으로 함유하는 식욕억제용 약학적 조성물 | |
| JP2006298792A (ja) | 脂肪蓄積抑制剤及び飲食品 | |
| KR20170023910A (ko) | 퀘르세틴-3-o-글루코시드를 포함하는 비알콜성 지방간 예방 또는 치료용 약학적 조성물 | |
| KR101534142B1 (ko) | 혼합 생약 추출물을 이용한 대사성질환 예방 및 치료용 조성물 | |
| KR101851639B1 (ko) | 모과 추출물 또는 이의 분획물을 유효성분으로 함유하는 항비만용 조성물 | |
| JP2014185088A (ja) | 経口組成物、脂肪細胞分化抑制剤および飲食品 | |
| KR101160575B1 (ko) | 소맥엽 추출물 또는 이의 분획물을 유효성분으로 함유하는 조성물 | |
| WO2011090265A2 (ko) | 신코닌을 유효성분으로 포함하는 비만, 이상지방혈증, 지방간 또는 인슐린 저항성 증후군의 예방 또는 치료용 조성물 | |
| KR102178199B1 (ko) | 옻나무 및 두충으로 구성된 조합 추출물을 유효성분으로 함유하는 비만증의 예방 및 치료용 조성물 | |
| KR101427253B1 (ko) | 미더덕 추출물을 함유하는 지방산 산화 촉진용 약학 조성물 또는 건강기능 식품 | |
| KR102649974B1 (ko) | 진세노사이드 Rf, 진세노사이드 Rf를 포함하는 진세노사이드 조성물, 또는 이들 중 어느 하나 이상의 혼합물을 유효성분으로 포함하는 근기능 개선용 조성물 | |
| KR102645300B1 (ko) | 다이메틸 이타콘산을 포함하는 인슐린 저항성 증후군의 예방 또는 치료용 조성물 | |
| KR20140093573A (ko) | 디하이드로진저론을 함유하는 비만 치료 또는 예방용 조성물 | |
| KR20160044257A (ko) | 여주의 에틸 아세테이트 분획물을 유효성분으로 포함하는 지질개선 또는 비만 예방 또는 치료용 조성물 | |
| JP2017222715A (ja) | 経口組成物、脂肪細胞分化抑制剤および飲食品 | |
| KR20190118961A (ko) | 구꼬아민 a 및 구꼬아민 b를 유효성분으로 함유하는 골격근 위축 예방 또는 개선용 조성물 | |
| KR20240115524A (ko) | 항염 또는 항비만 효능이 우수한 신품종 단삼 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
Patent event code: PA01091R01D Comment text: Patent Application Patent event date: 20211202 |
|
| PA0201 | Request for examination | ||
| PA0302 | Request for accelerated examination |
Patent event date: 20211203 Patent event code: PA03022R01D Comment text: Request for Accelerated Examination Patent event date: 20211202 Patent event code: PA03021R01I Comment text: Patent Application |
|
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20220211 Patent event code: PE09021S01D |
|
| PE0701 | Decision of registration |
Patent event code: PE07011S01D Comment text: Decision to Grant Registration Patent event date: 20220914 |
|
| PR0701 | Registration of establishment |
Comment text: Registration of Establishment Patent event date: 20220916 Patent event code: PR07011E01D |
|
| PR1002 | Payment of registration fee |
Payment date: 20220919 End annual number: 3 Start annual number: 1 |
|
| PG1601 | Publication of registration |